Перекрестная ссылка на родственные заявки
[0001] Настоящая заявка утверждает приоритет патентной заявки США с регистрационным номером (U.S.S.N.) 62/734,718, поданной 21 сентября 2018 года, U.S.S.N. 62/722,78, поданной 24 августа 2018 года, U.S.S.N. 62/620,095, поданной 22 января 2018 года, U.S.S.N. 62/611,983, поданной 29 декабря 2017 года, и U.S.S.N. 62/610,069, поданной 22 декабря 2017 года, содержание каждой из которых включено здесь ссылкой во всей их полноте.
Область техники, к которой относится изобретение
[0002] Возбудимость головного мозга определяется как уровень активации животного, континуум, который варьирует от комы до конвульсий, и регулируется разнообразными нейромедиаторами. Как правило, нейромедиаторы ответственны за регулирование проводимости ионов через мембраны нейронов. В состоянии покоя мембрана нейрона имеет потенциал (или напряжение на мембране) приблизительно -70 мВ, причем внутренность клетки является отрицательно заряженной относительно окружающей клетку среды. Потенциал (напряжение) является результатом ионного (K+, Na+, Cl-, органические анионы) баланса по обе стороны нейронной полупроницаемой мембраны. Нейромедиаторы содержатся в пресинаптических пузырьках и высвобождаются под влиянием потенциала действия нейрона. Когда они выделяются в синаптическую щель, происходит изменение потенциала от -70 мВ до -50 мВ. Посредниками этого эффекта выступают постсинаптические никотиновые рецепторы, которые стимулируются ацетилхолином для повышения проницаемости мембраны для Na+-ионов. Сниженный мембранный потенциал стимулирует возбудимость нейрона в форме потенциала действия нейрона.
[0003] В случае ГАМК-рецепторного комплекса (GRC), воздействие на возбудимость мозга обусловливается таким нейромедиатором, как γ-аминомасляная кислота (GABA, ГАМК). ГАМК оказывает сильное влияние на общую возбудимость мозга потому, что до 40% нейронов используют ГАМК в качестве нейромедиатора. ГАМК контролирует возбудимость индивидуальных нейронов регулированием проводимости хлорид-ионов через нейронную мембрану. ГАМК взаимодействует с участком ее распознавания на GRC, облегчая течение в клетку хлорид-ионов для снижения электрохимического градиента GRC. Повышение уровней этого аниона внутри клетки вызывает гиперполяризацию трансмембранного потенциала, делая нейроны менее чувствительными к возбуждающим входным сигналам, то есть, снижая возбудимость нейронов. Другими словами, чем выше концентрация хлорид-ионов в нейроне, тем ниже возбудимость мозга и уровень возбуждения.
[0004] Хорошо задокументировано, что GRC ответственна за смягчение беспокойства, судорожной активности, и успокоение. Так, ГАМК и лекарственные препараты, которые действуют подобно ГАМК или усиливают действие ГАМК (например, терапевтически приемлемые барбитураты и бензодиазепины (BZs), такие как Valium®), проявляют свои терапевтически полезные эффекты взаимодействием со специфичными регуляторными участками на GRC. Накопленные к настоящему времени доказательства показывают, что, в дополнение к участкам связывания бензодиазепинов и барбитуратов, GRC содержит отдельный участок для нейроактивных стероидов. Например, смотри работу авторов Lan, N. C. и др., Neurochem. Res., (1991) том 16: стр. 347-356.
[0005] Нейроактивные стероиды могут возникать эндогенно. Наиболее действенными эндогенными нейроактивными стероидами являются 3α—гидрокси-5(Н)-прегнанон-20-он и 3α-21-дигидрокси-5(Н)-прегнанон-20-он, метаболиты стероидных гормонов прогестерона и дезоксикортикостерона, соответственно. Способность этих стероидных метаболитов изменять возбудимость мозга была выявлена в 1986 году (Majewska, M. D. и др., Science, том 232: стр. 1004-1007 (1986); Harrison, N. L. и др., J. Pharmacol. Exp. Ther., том 241: стр. 346-353 (1987))
[0006] Требуются новые и усовершенствованные соединения, которые действуют как модулирующие агенты для возбудимости мозга, а также препараты для профилактики и лечения имеющих к ЦНС отношение заболеваний. На достижение этой цели направлены описываемые здесь соединения, композиции и способы.
Сущность изобретения
[0007] Здесь представлены соединения, предназначенные для действия в качестве ГАМК-модуляторов. В некоторых вариантах исполнения такие соединения представляются пригодными в качестве терапевтических средств для лечения имеющих к ЦНС отношение заболеваний.
[0008] Здесь представлены соединения Формулы (I-X):
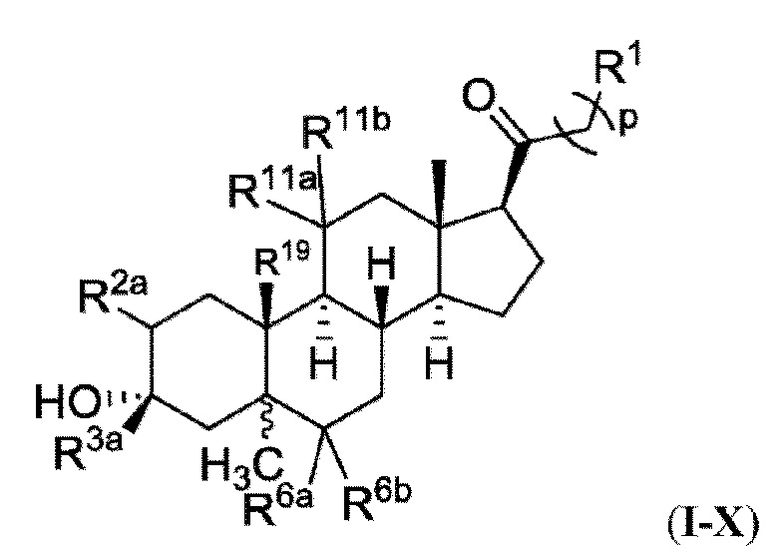
[0009] или фармацевтически приемлемые соли их. Также здесь представлены соединения Формулы (I-I):
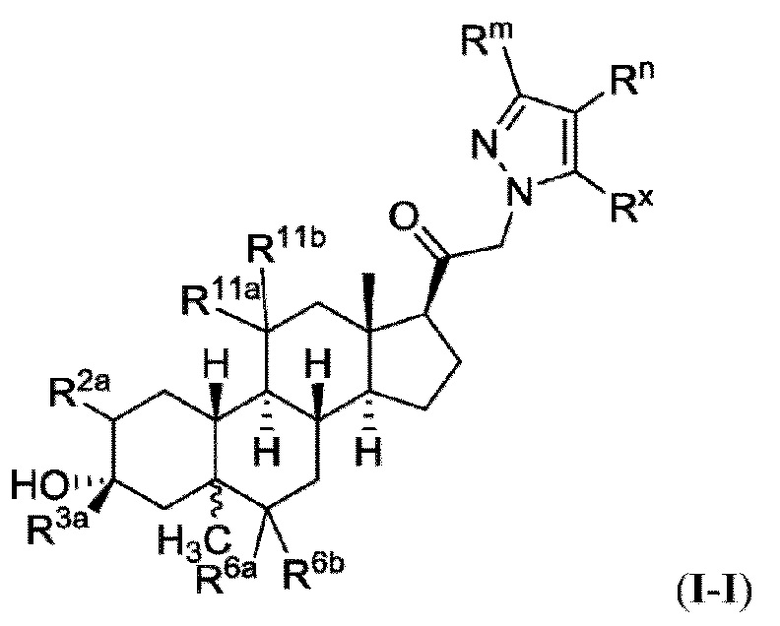
[0010] или фармацевтически приемлемые соли их.
[0011] В некоторых вариантах исполнения здесь представлено соединение Формулы (II-I)
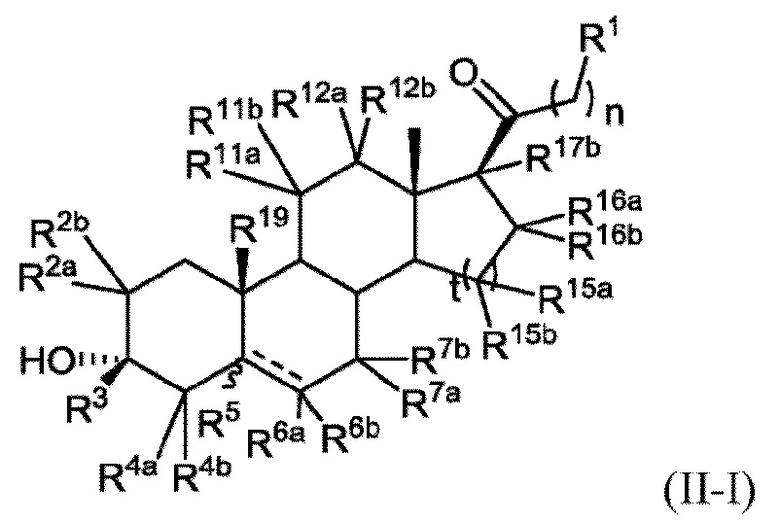
или фармацевтически приемлемая соль его.
[0012] В некоторых вариантах исполнения соединение Формулы (II-I) представляет собой соединение Формулы (II-Ia)
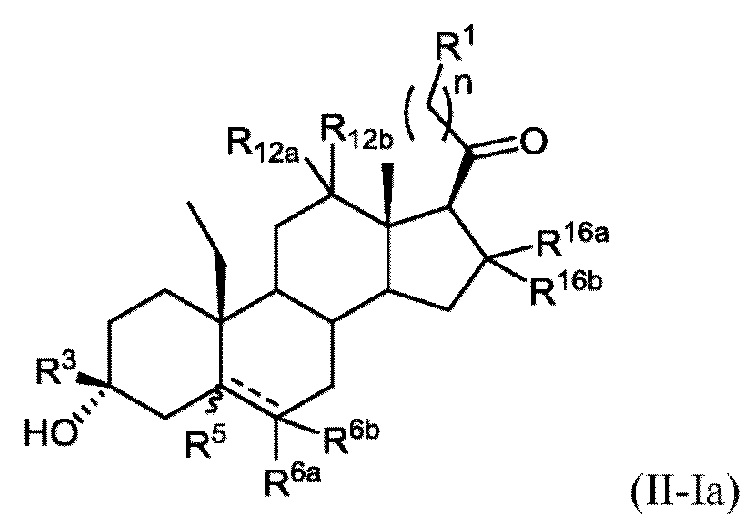
или фармацевтически приемлемую соль его.
[0013] В некоторых вариантах исполнения соединение Формулы (II-I) представляет собой соединение Формулы (II-Ib)
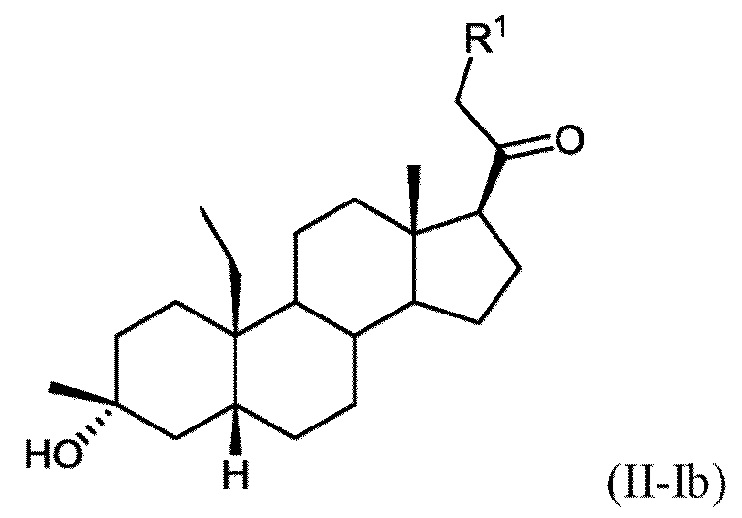
или фармацевтически приемлемую соль его.
[0014] В некоторых вариантах исполнения соединение Формулы (II-I) представляет собой соединение Формулы
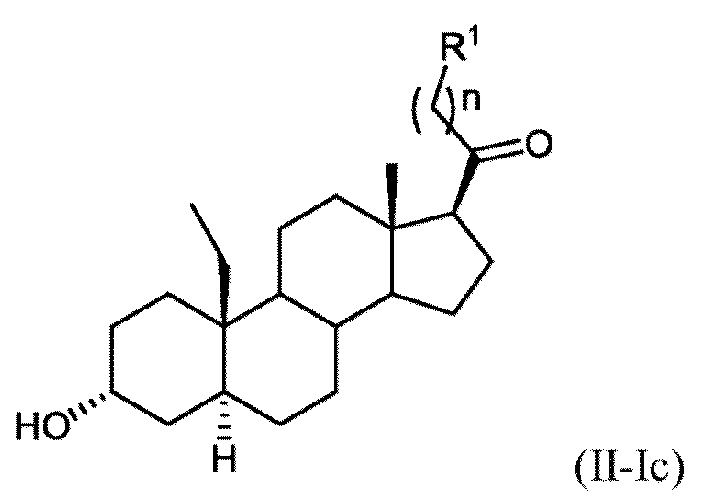
или фармацевтически приемлемую соль его.
[0015] В некоторых вариантах исполнения соединение Формулы (II-I) представляет собой соединение Формулы
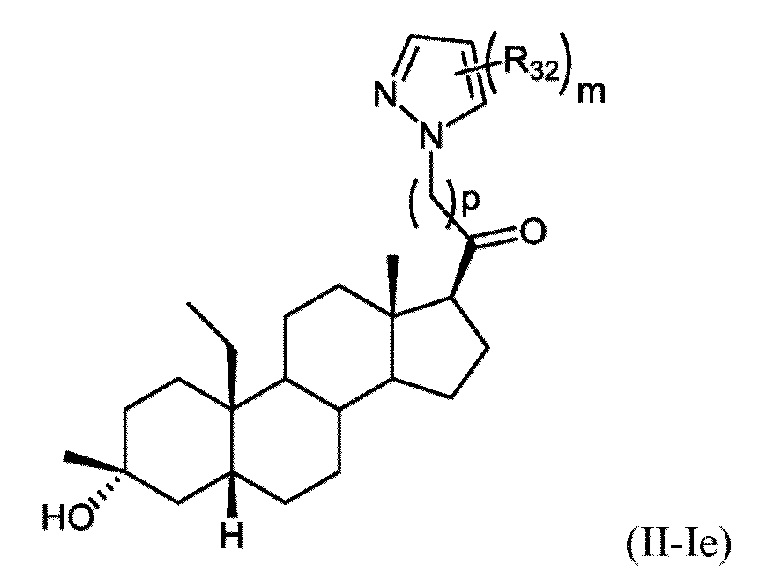
или фармацевтически приемлемую соль его.
[0016] В некоторых вариантах исполнения соединение Формулы (II-I) представляет собой соединение Формулы
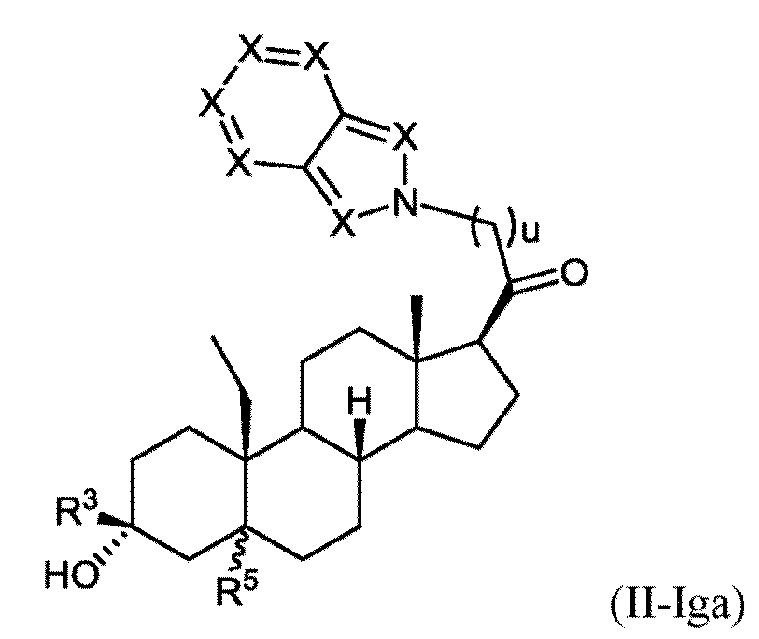
или фармацевтически приемлемую соль его.
[0017] В некоторых вариантах исполнения соединение Формулы (II-I) представляет собой соединение Формулы
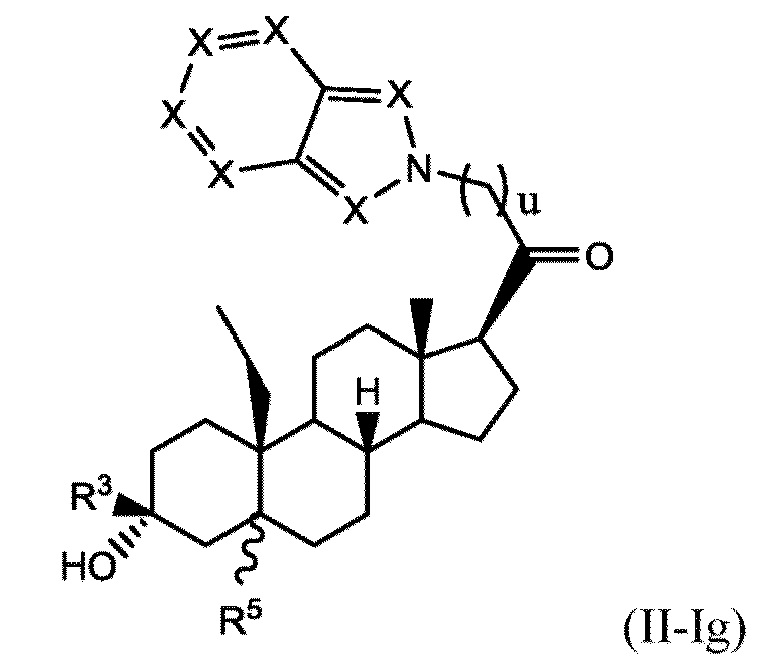
или фармацевтически приемлемую соль его.
[0018] В некоторых вариантах исполнения соединение Формулы (II-I) представляет собой соединение Формулы
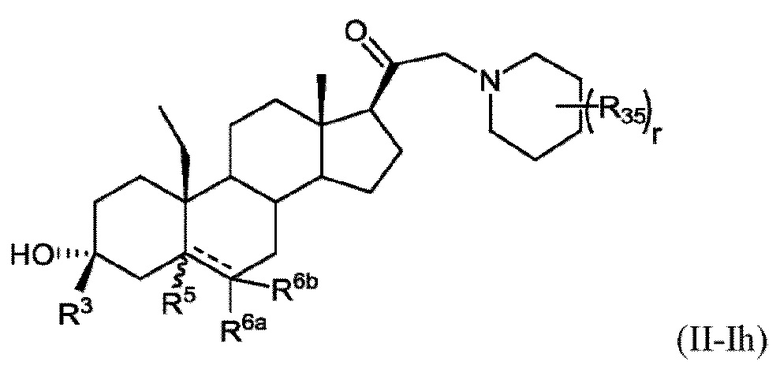
или фармацевтически приемлемую соль его.
[0019] В некоторых вариантах исполнения соединение Формулы (II-I) представляет собой соединение Формулы
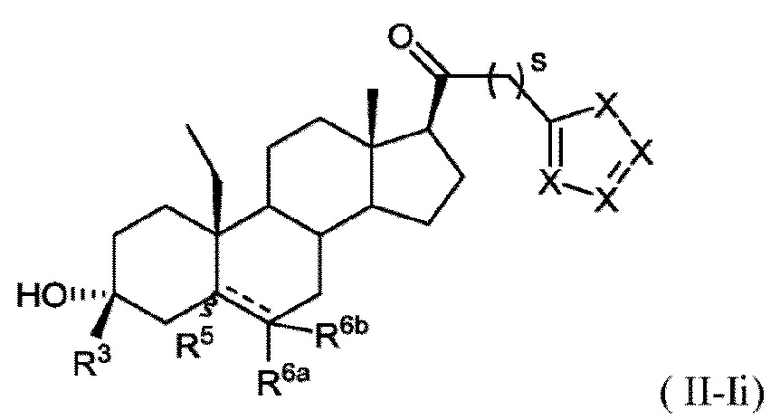
или фармацевтически приемлемую соль его.
[0020] В некоторых вариантах исполнения здесь представлено соединение Формулы (III-I)
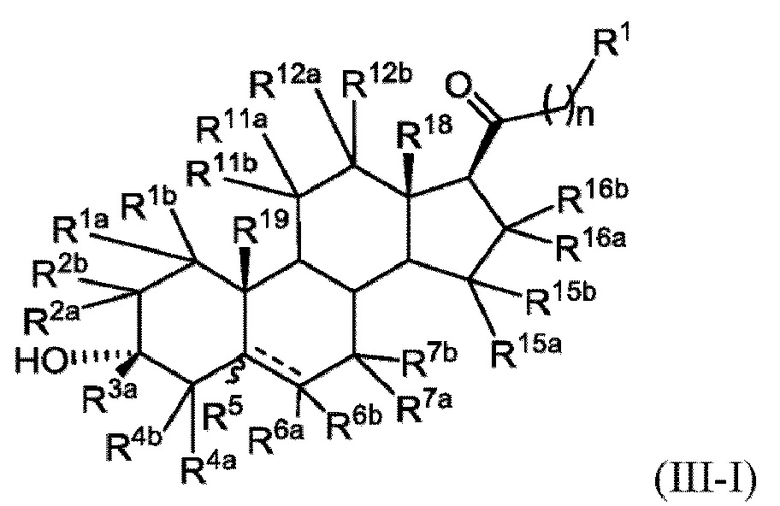
или фармацевтически приемлемая соль его.
[0021] В некоторых вариантах исполнения здесь представлено соединение Формулы (III-II)
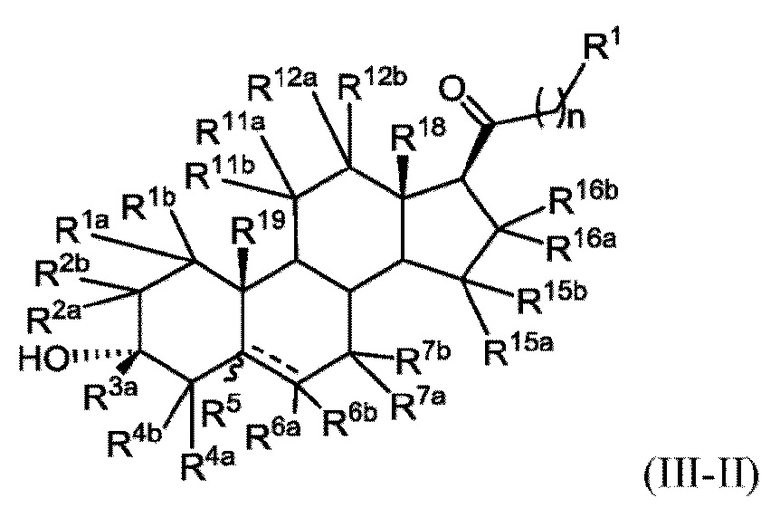
или фармацевтически приемлемая соль его.
[0022] В некоторых вариантах исполнения соединение Формулы (III-I) или (III-II) представляет собой соединение Формулы (III-Ia)
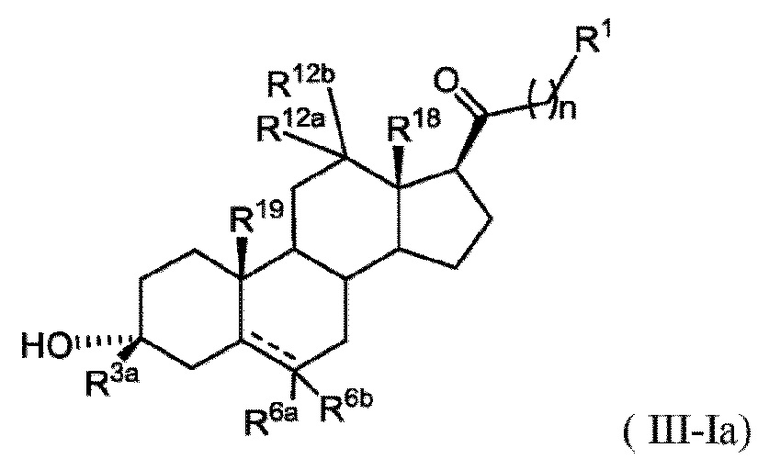
или фармацевтически приемлемую соль его.
[0023] В некоторых вариантах исполнения соединение Формулы (III-I) или (III-II) представляет собой соединение Формулы (III-Ib)
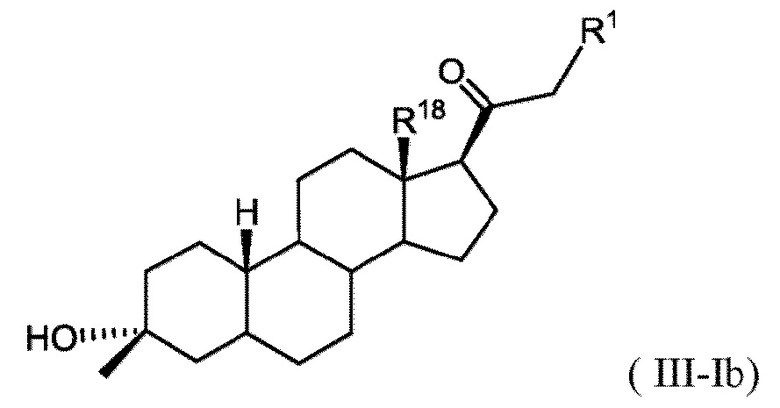
или фармацевтически приемлемую соль его.
[0024] В некоторых вариантах исполнения соединение Формулы (III-I) или (III-II) представляет собой соединение Формулы (III-Ie)
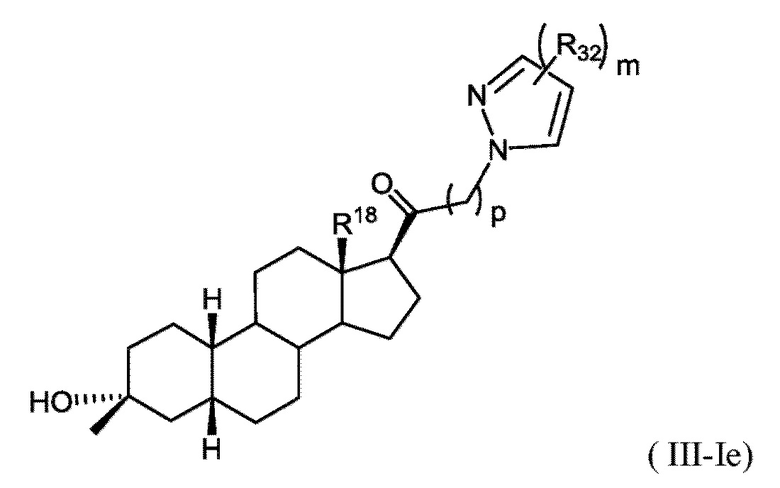
или фармацевтически приемлемую соль его.
[0025] В некоторых вариантах исполнения соединение Формулы (III-I) или (III-II) представляет собой соединение Формулы (III-Ig)
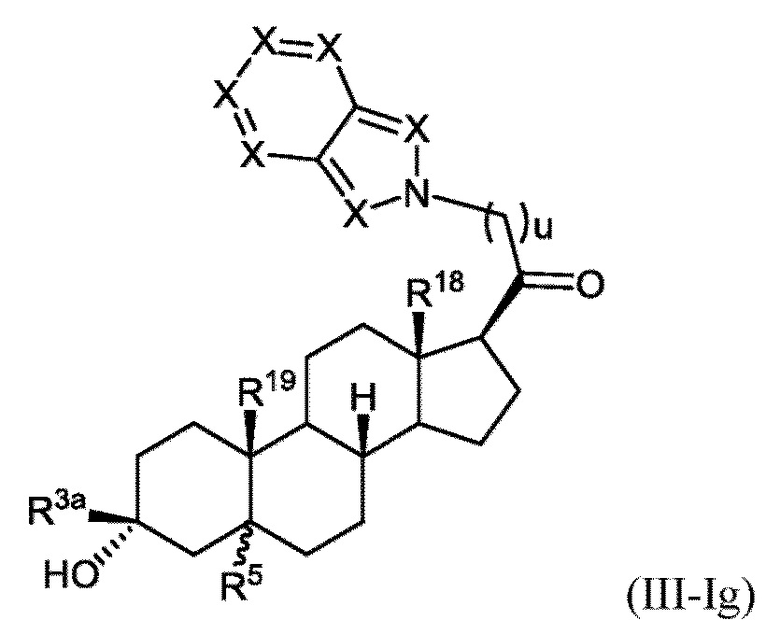
или фармацевтически приемлемую соль его.
[0026] В некоторых вариантах исполнения соединение Формулы (III-I) или (III-II) представляет собой соединение Формулы (III-Ih)
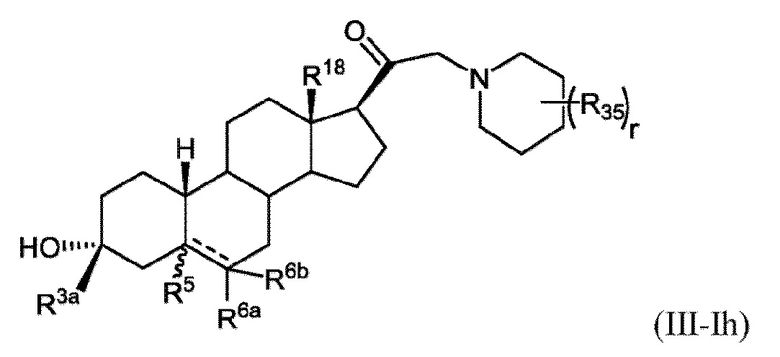
или фармацевтически приемлемую соль его.
[0027] В некоторых вариантах исполнения соединение Формулы (III-I) или (III-II) представляет собой соединение Формулы (III-Ii)
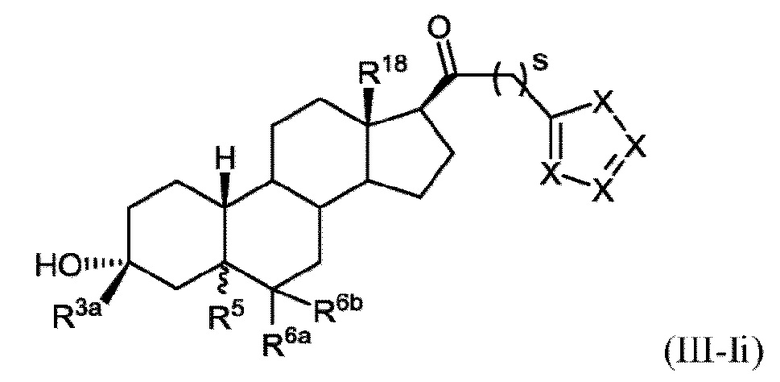
или фармацевтически приемлемую соль его.
[0028] В некоторых вариантах исполнения фармацевтическая композиция включает описываемое здесь соединение или фармацевтически приемлемую соль его, и фармацевтически приемлемый эксципиент.
[0029] В некоторых вариантах исполнения способ лечения связанного с ЦНС заболевания у нуждающегося в этом субъекта включает введение субъекту эффективного количества описываемого здесь соединения или фармацевтически приемлемой соли его. В некоторых вариантах исполнения связанное с ЦНС заболевание представляет собой нарушение сна, расстройство настроения, расстройство шизофренического спектра, судорожный синдром, нарушение памяти и/или познавательной способности, нарушение движений, изменение личности, расстройство аутистического спектра, боль, травматическое повреждение мозга, сосудистые болезни, связанные с наркотической зависимостью расстройства, и/или абстинентный синдром, шум в ушах, или эпилептический статус. В некоторых вариантах исполнения связанное с ЦНС заболевание представляет собой депрессию. В некоторых вариантах исполнения связанное с ЦНС заболевание представляет собой послеродовую депрессию. В некоторых вариантах исполнения связанное с ЦНС заболевание представляет собой большое депрессивное расстройство. В некоторых вариантах исполнения большое депрессивное расстройство представляет собой большое депрессивное расстройство в умеренной форме. В некоторых вариантах исполнения большое депрессивное расстройство представляет собой большое депрессивное расстройство в тяжелой форме.
[0030] В некоторых вариантах исполнения соединение выбирают из группы, состоящей из соединений, указанных здесь в Таблице I-1, Таблице II-1 или Таблице III-1.
[0031] В одном аспекте здесь представлена фармацевтически приемлемая соль описываемого здесь соединения (например, соединения Формулы (I-X, I-I, II-I, III-I, или III-II).
[0032] В одном аспекте здесь представлена фармацевтическая композиция, включающая описываемое здесь соединение (например, соединение Формулы (I-X, I-I, II-I, III-I, или III-II), или фармацевтически приемлемую соль его, и фармацевтически приемлемый эксципиент. В определенных вариантах исполнения соединение согласно настоящему изобретению вносят в фармацевтическую композицию в эффективном количестве. В определенных вариантах исполнения соединение согласно настоящему изобретению вносят в терапевтически эффективном количестве. В определенных вариантах исполнения соединение согласно настоящему изобретению вносят в профилактически эффективном количестве.
[0033] Соединения согласно настоящему изобретению, как описываемые здесь, действуют, в определенных вариантах исполнения, как ГАМК-модуляторы, например, воздействием на ГАМКА-рецептор позитивным или негативным образом. В качестве модуляторов возбудимости центральной нервной системы (ЦНС, CNS) при содействии их способности модулировать ГАМКА-рецептор, такие соединения предполагаются имеющими CNS-активность.
Так, в еще одном аспекте представлены способы лечения связанного с ЦНС заболевания у нуждающегося в этом субъекта, включающие введение субъекту эффективного количества соединения согласно настоящему изобретению. В определенных вариантах исполнения связанное с ЦНС заболевание представляет собой нарушение сна, расстройство настроения, расстройство шизофренического спектра, судорожный синдром, нарушение памяти и/или познавательной способности, нарушение движений, изменение личности, расстройство аутистического спектра, боль, травматическое повреждение мозга, сосудистые болезни, связанные с наркотической зависимостью расстройства, и/или абстинентный синдром, шум в ушах, или эпилептический статус. В определенных вариантах исполнения связанное с ЦНС заболевание представляет собой депрессию. В определенных вариантах исполнения связанное с ЦНС заболевание представляет собой послеродовую депрессию. В определенных вариантах исполнения связанное с ЦНС заболевание представляет собой большое депрессивное расстройство. В определенных вариантах исполнения большое депрессивное расстройство представляет собой большое депрессивное расстройство в умеренной форме. В определенных вариантах исполнения большое депрессивное расстройство представляет собой большое депрессивное расстройство в тяжелой форме. В определенных вариантах исполнения соединение вводят перорально, подкожно, внутривенно или внутримышечно. В определенных вариантах исполнения соединение вводят перорально. В определенных вариантах исполнения соединение вводят хронически. В определенных вариантах исполнения соединение вводят непрерывно, например, непрерывной внутривенной инфузией.
Подробное описание определенных вариантов осуществления изобретения
[0034] Как в общих чертах описано здесь, настоящее изобретение представляет соединения, предназначенные, например, для действия в качестве ГАМК-модуляторов. В определенных вариантах исполнения такие соединения представляются полезными в качестве терапевтических препаратов для лечения связанного с ЦНС заболевания (например, как описанного здесь расстройства, например, депрессии, такой как послеродовая депрессия или большое депрессивное расстройство).
Определения
Химические определения
[0035] Ниже более подробно описаны определения конкретных функциональных групп и химические термины. Химические элементы идентифицируются в соответствии с Периодической Таблицей Элементов, CAS-версией, справочником Handbook of Chemistry and Physics, 75-ое издание, внутренняя обложка, и конкретные функциональные группы в целом определены, как в них описано. Кроме того, общие принципы органической химии, а также конкретные функциональные фрагменты и реакционная способность, описаны в изданиях Thomas Sorrell, Organic Chemistry, University Science Books, Sausalito, 1999; Smith и March, March’s Advanced Organic Chemistry, 5-ое издание, издательство John Wiley & Sons, Inc., Нью-Йорк, 2001; Larock, Comprehensive Organic Transformations, издательство VCH Publishers, Inc., Нью-Йорк, 1989; и Carruthers, Some Modern Methods of Organic Synthesis, 3-е издание, издательство Cambridge University Press, Cambridge, 1987.
[0036] Изомеры, например, стереоизомеры, могут быть выделены из смесей способами, известными квалифицированным специалистам в этой области технологии, в том числе хиральной жидкостной хроматографией высокого давления (HPLC) и образованием и кристаллизацией хиральных солей; или предпочтительные изомеры могут быть получены асимметрическим синтезом. Например, смотри работы авторов Jacques и др., Enantiomers, Racemates and Resolutions (Wiley Interscience, New York, 1981); Wilen и др., Tetrahedron, том 33: стр. 2725 (1977); Eliel, Stereochemistry of Carbon Compounds (McGraw-Hill, NY, 1962); и Wilen, Tables of Resolving Agents and Optical Resolutions, стр. 268 (E.L. Eliel, редактор, Univ. of Notre Dame Press, Notre Dame, IN 1972). Изобретение дополнительно охватывает описываемые здесь соединения как индивидуальные изомеры, по существу не содержащие другие изомеры, и, альтернативно, как смеси различных изомеров.
[0037] Как применяемое здесь, чистое энантиомерное соединение по существу не содержит другие энантиомеры или стереоизомеры соединения (то есть, находится в энантиомерном избытке). Иначе говоря, «S»-форма соединения по существу не содержит «R»-форму соединения, и тем самым находится в энантиомерном избытке относительно «R»-формы. Термин «энантиомерно чистый» или «чистый энантиомер» означает, что соединение включает более 75% по весу, более 80% по весу, более 85% по весу, более 90% по весу, более 91% по весу, более 92% по весу, более 93% по весу, более 94% по весу, более 95% по весу, более 96% по весу, более 97% по весу, более 98% по весу, более 98,5% по весу, более 99% по весу, более 99,2% по весу, более 99,5% по весу, более 99,6% по весу, более 99,7% по весу, более 99,8% по весу, или более 99,9% по весу, энантиомера. В определенных вариантах исполнения весовые количества приводятся в расчете на общий вес всех энантиомеров или стереоизомеров соединения.
[0038] В представляемых здесь композициях энантиомерно чистое соединение может присутствовать с другими активными или неактивными ингредиентами. Например, фармацевтическая композиция, включающая энантиомерно чистое соединение с R-положением центрального атома углерода, может содержать, например, около 90% эксципиента и около 10% энантиомерно чистого R-соединения. В определенных вариантах исполнения энантиомерно чистое R-соединение в таких композициях может включать, например, по меньшей мере около 95% по весу R-соединения и не более, чем около 5% по весу S-соединения, относительно общего веса соединения. Например, фармацевтическая композиция, содержащая энантиомерно чистое S-соединение, может включать, например, около 90% эксципиента и около 10% энантиомерно чистого S-соединения. В определенных вариантах исполнения энантиомерно чистое S-соединение в таких композициях может включать, например, по меньшей мере около 95% по весу S-соединения и не более, чем около 5% по весу R-соединения, относительно общего веса соединения. В определенных вариантах исполнения активный ингредиент может быть составлен с малым количеством эксципиента или носителя или вообще без них.
[0039] Термин «диастереомерно чистый» означает, что соединение включает более 75% по весу, более 80% по весу, более 85% по весу, более 90% по весу, более 91% по весу, более 92% по весу, более 93% по весу, более 94% по весу, более 95% по весу, более 96% по весу, более 97% по весу, более 98% по весу, более 98,5% по весу, более 99% по весу, более 99,2% по весу, более 99,5% по весу, более 99,6% по весу, более 99,7% по весу, более 99,8% по весу, или более 99,9% по весу, одного диастереомера. Методы определения диастереомерной и энантиомерной чистоты являются общеизвестными с технологии. Диастереомерная чистота может быть определена любым аналитическим методом, способным количественно различить соединение и его диастереомеры, таким как высокоэффективная жидкостная хроматография (HPLC).
[0040] «Стереоизомеры»: также должно быть понятно, что соединения, которые имеют одинаковую молекулярную формулу, но различаются по природе или последовательности связей между их атомами, или размещением их атомов в пространстве, называются «изомерами». Изомеры, которые различаются размещением их атомов в пространстве, называются «стереоизомерами». Стереоизомеры, которые не являются зеркальными отражениями друг относительно друга, называются «диастереомерами», и те, которые представляет собой несовпадающие при наложении зеркальные изображения, называются «энантиомерами». Когда соединение имеет асимметрический центр, например, в котором связаны четыре различных группы, возможно образование пары энантиомеров. Энантиомер может быть охарактеризован абсолютной конфигурацией своего асимметрического центра, и описывается правилами R- и S-последовательности Кана и Прелога, или таким образом, в котором молекула вращает плоскость поляризованного света и обозначается как правовращающая или левовращающая (то есть, как (+)- или (-)-изомеры, соответственно). Хиральное соединение может существовать либо как индивидуальный энантиомер, либо как их смесь. Смесь, содержащая равные количества энантиомеров, называется «рацемической смесью».
[0041] Артикли «a» и «an» могут быть использованы здесь для указания на один или более чем один (то есть, по меньшей мере один) грамматический объект артикля. В качестве примера «аналог» означает один аналог или более чем один аналог.
[0042] Когда перечисляется диапазон значений, этим подразумевается включение каждого значения и поддиапазона в пределах диапазона. Например, «C1-6-алкил» предполагается включающим C1, C2, C3, C4, C5, C6, C1-6, C1-5, C1-4, C1-3, C1-2, C2-6, C2-5, C2-4, C2-3, C3-6, C3-5, C3-4, C4-6, C4-5, и C5-6-алкил.
[0043] Нижеследующие термины предполагаются имеющими значения, приведенные для них ниже, и полезны для понимания описания и предполагаемой области настоящего изобретения.
[0044] «Алкил» означает радикал с линейноцепочечной или разветвленной углеводородной группой, имеющей от 1 до 20 атомов углерода («С1-20-алкил»). В некоторых вариантах исполнения алкильная группа имеет от 1 до 12 атомов углерода («С1-12-алкил»). В некоторых вариантах исполнения алкильная группа имеет от 1 до 10 атомов углерода («С1-10-алкил»). В некоторых вариантах исполнения алкильная группа имеет от 1 до 9 атомов углерода («С1-9-алкил»). В некоторых вариантах исполнения алкильная группа имеет от 1 до 8 углеродных атомов («С1-8-алкил»). В некоторых вариантах исполнения алкильная группа имеет от 1 до 7 углеродных атомов («С1-7-алкил»). В некоторых вариантах исполнения алкильная группа имеет от 1 до 6 углеродных атомов («С1-6-алкил», также называемый здесь «низшим алкилом»). В некоторых вариантах исполнения алкильная группа имеет от 1 до 5 углеродных атомов («С1-5-алкил»). В некоторых вариантах исполнения алкильная группа имеет от 1 до 4 углеродных атомов («С1-4-алкил»). В некоторых вариантах исполнения алкильная группа имеет от 1 до 3 углеродных атомов («С1-3-алкил»). В некоторых вариантах исполнения алкильная группа имеет от 1 до 2 углеродных атомов («С1-2-алкил»). В некоторых вариантах исполнения алкильная группа имеет 1 атом углерода («С1-алкил»). В некоторых вариантах исполнения алкильная группа имеет от 2 до 6 углеродных атомов («С2-6-алкил»). Примеры С1-6-алкильных групп включают метил (C1), этил (C2), н-пропил (C3), изопропил (C3), н-бутил (C4), трет-бутил (C4), втор-бутил (C4), изобутил (C4), н-пентил (C5), 3-пентил (C5), амил (C5), неопентил (C5), 3-метил-2-бутил (C5), третичный амил (C5), и н-гексил (C6). Дополнительные примеры алкильных групп включают н-гептил (C7), н-октил (C8) и тому подобные. Если не оговорено иное, алкильная группа в каждом случае независимо является необязательно замещенной, то есть, незамещенной («незамещенный алкил») или замещенной («замещенный алкил») одним или более заместителями; например, от 1 до 5 заместителей, от 1 до 3 заместителей, или 1 заместитель. В определенных вариантах исполнения алкильная группа представляет собой незамещенный C1-10-алкил (например, -CH3). В определенных вариантах исполнения алкильная группа представляет собой замещенный C1-10-алкил. Общепринятые сокращенные обозначения алкильных групп включают Me (-CH3), Et (-CH2CH3), i-Pr (-CH(CH3)2), n-Pr (-CH2CH2CH3), n-Bu (-CH2CH2CH2CH3), или i-Bu (-CH2CH(CH3)2).
[0045] «Алкилен» означает алкильную группу, в которой два атома водорода удалены с образованием двухвалентного радикала, и которая может быть замещенной или незамещенной. Незамещенные алкиленовые группы включают, но без ограничения этим, метилен (-CH2-), этилен (-CH2CH2-), пропилен (-CH2CH2CH2-), бутилен (-CH2CH2CH2CH2-), пентилен (-CH2CH2CH2CH2CH2-), гексилен (-CH2CH2CH2CH2CH2CH2-), и тому подобные. Примерные замещенные алкиленовые группы, например, замещенные одной или многими алкильными (метильными) группами, включают, но без ограничения этим, замещенный метилен (-CH(CH3)-, (-C(CH3)2-), замещенный этилен (-CH(CH3)CH2-,-CH2CH(CH3)-, -C(CH3)2CH2-,-CH2C(CH3)2-), замещенный пропилен (-CH(CH3)CH2CH2-, -CH2CH(CH3)CH2-, -CH2CH2CH(CH3)-, -C(CH3)2CH2CH2-, -CH2C(CH3)2CH2-, -CH2CH2C(CH3)2-), и тому подобные. Когда для конкретной алкиленовой группы приводится число или диапазон атомов углерода, этим подразумевается диапазон или число атомов углерода в линейной двухвалентной углеродной цепи. Алкиленовые группы могут быть замещенными или незамещенными с одним или более заместителями, как здесь описывается.
[0046] «Алкенил» означает радикал с линейноцепочечной или разветвленной углеводородной группой, имеющей от 2 до 20 атомов углерода, с одной или более двойными углерод-углеродными связями (например, с 1, 2, 3 или 4 двойными углерод-углеродными связями), и необязательно с одной или более тройными углерод-углеродными связями (например, с 1, 2, 3 или 4 тройными углерод-углеродными связями) («С2-20-алкенил»). В определенных вариантах исполнения алкенил не содержит никаких тройных связей. В некоторых вариантах исполнения алкенильная группа имеет от 2 до 10 атомов углерода («С2-10-алкенил»). В некоторых вариантах исполнения алкенильная группа имеет от 2 до 9 атомов углерода («С2-9-алкенил»). В некоторых вариантах исполнения алкенильная группа имеет от 2 до 8 атомов углерода («С2-8-алкенил»). В некоторых вариантах исполнения алкенильная группа имеет от 2 до 7 атомов углерода («С2-7-алкенил»). В некоторых вариантах исполнения алкенильная группа имеет от 2 до 6 атомов углерода («С2-6-алкенил»). В некоторых вариантах исполнения алкенильная группа имеет от 2 до 5 атомов углерода («С2-5-алкенил»). В некоторых вариантах исполнения алкенильная группа имеет от 2 до 4 атомов углерода («С2-4-алкенил»). В некоторых вариантах исполнения алкенильная группа имеет от 2 до 3 атомов углерода («С2-3-алкенил»). В некоторых вариантах исполнения алкенильная группа имеет 2 атома углерода («С2-алкенил»). Одна или многие двойные углерод-углеродные связи могут быть внутренними (такими как в 2-бутениле) или концевыми (такими как в 1-бутениле). Примеры C2-4-алкенильных групп включают этенил (C2), 1-пропенил (C3), 2-пропенил (C3), 1-бутенил (C4), 2-бутенил (C4), бутадиенил (C4), и тому подобные. Примеры C2-6-алкенильных групп включают вышеуказанные C2-4-алкенильные группы, а также пентенил (C5), пентадиенил (C5), гексенил (C6), и тому подобные. Дополнительные примеры алкенильных групп включают гептенил (C7), октенил (C8), октатриенил (C8), и тому подобные. Если не оговаривается иное, алкенильная группа в каждом случае независимо является необязательно замещенной, то есть, незамещенной («незамещенный алкенил») или замещенной («замещенный алкенил») одним или более заместителями; например, от 1 до 5 заместителей, от 1 до 3 заместителей, или 1 заместитель. В определенных вариантах исполнения алкенильная группа представляет собой незамещенный C2-10-алкенил. В определенных вариантах исполнения алкенильная группа представляет собой замещенный C2-10-алкенил.
[0047] «Алкинил» означает радикал с линейноцепочечной или разветвленной углеводородной группой, имеющей от 2 до 20 атомов углерода, с одной или более тройными углерод-углеродными связями (например, с 1, 2, 3 или 4 тройными углерод-углеродными связями), и необязательно с одной или более двойными углерод-углеродными связями (например, с 1, 2, 3 или 4 двойными углерод-углеродными связями) («С2-20-алкинил»). В некоторых вариантах исполнения алкинильная группа не содержит никаких двойных связей. В некоторых вариантах исполнения алкинильная группа имеет от 2 до 10 атомов углерода («С2-10-алкинил»). В некоторых вариантах исполнения алкинильная группа имеет от 2 до 9 атомов углерода («С2-9-алкинил»). В некоторых вариантах исполнения алкинильная группа имеет от 2 до 8 атомов углерода («С2-8-алкинил»). В некоторых вариантах исполнения алкинильная группа имеет от 2 до 7 атомов углерода («С2-7-алкинил»). В некоторых вариантах исполнения алкинильная группа имеет от 2 до 6 атомов углерода («С2-6-алкинил»). В некоторых вариантах исполнения алкинильная группа имеет от 2 до 5 атомов углерода («С2-5-алкинил»). В некоторых вариантах исполнения алкинильная группа имеет от 2 до 4 атомов углерода («С2-4-алкинил»). В некоторых вариантах исполнения алкинильная группа имеет от 2 до 3 атомов углерода («С2-3-алкинил»). В некоторых вариантах исполнения алкинильная группа имеет 2 атома углерода («С2-алкинил»). Одна или многие тройные углерод-углеродные связи могут быть внутренними (такими как в 2-бутиниле) или концевыми (такими как в 1-бутиниле). Примеры C2-4-алкинильных групп включают этинил (C2), 1-пропинил (C3), 2-пропинил (C3), 1-бутинил (C4), 2-бутинил (C4), и тому подобные. Примеры C2-6-алкинильных групп включают вышеуказанные C2-4-алкинильные группы, а также пентинил (C5), гексинил (C6), и тому подобные. Дополнительные примеры алкинильных групп включают гептинил (C7), октинил (C8), и тому подобные. Если не оговаривается иное, алкинильная группа в каждом случае независимо является необязательно замещенной, то есть, незамещенной («незамещенный алкинил») или замещенной («замещенный алкинил») одним или более заместителями; например, от 1 до 5 заместителей, от 1 до 3 заместителей, или 1 заместитель. В определенных вариантах исполнения алкинильная группа представляет собой незамещенный C2-10-алкинил. В определенных вариантах исполнения алкинильная группа представляет собой замещенный C2-10-алкинил.
[0048] Термин «гетероалкил», как используемый здесь, подразумевает алкильную группу, как здесь определенную, которая дополнительно включает 1 или более (например, 1, 2, 3 или 4) гетероатомов (например, кислорода, серы, азота, бора, кремния, фосфора) внутри основной цепи, причем один или многие гетероатомы введены между соседними атомами углерода внутри основной цепи, и/или один или многие гетероатомы введены между атомом углерода и основной цепью, то есть, между точками присоединения. В определенных вариантах исполнения гетероалкильная группа имеет отношение к насыщенной группе, имеющей от 1 до 10 атомов углерода и 1, 2, 3 или 4 гетероатома («гетеро-С1-10-алкил»). В некоторых вариантах исполнения гетероалкильная группа представляет собой насыщенную группу, имеющую от 1 до 9 атомов углерода и 1, 2, 3 или 4 гетероатома («гетеро-С1-9-алкил»). В некоторых вариантах исполнения гетероалкильная группа представляет собой насыщенную группу, имеющую от 1 до 8 атомов углерода и 1, 2, 3 или 4 гетероатома («гетеро-С1-8-алкил»). В некоторых вариантах исполнения гетероалкильная группа представляет собой насыщенную группу, имеющую от 1 до 7 атомов углерода и 1, 2, 3 или 4 гетероатома («гетеро-С1-7-алкил»). В некоторых вариантах исполнения гетероалкильная группа представляет собой группу, имеющую от 1 до 6 атомов углерода и 1, 2 или 3 гетероатома («гетеро-С1-6-алкил»). В некоторых вариантах исполнения гетероалкильная группа представляет собой насыщенную группу, имеющую от 1 до 5 атомов углерода и 1 или 2 гетероатома («гетеро-С1-5-алкил»). В некоторых вариантах исполнения гетероалкильная группа представляет собой насыщенную группу, имеющую от 1 до 4 атомов углерода и 1 или 2 гетероатома («гетеро-С1-4-алкил»). В некоторых вариантах исполнения гетероалкильная группа представляет собой насыщенную группу, имеющую от 1 до 3 атомов углерода и 1 гетероатом («гетеро-С1-3-алкил»). В некоторых вариантах исполнения гетероалкильная группа представляет собой насыщенную группу, имеющую от 1 до 2 атомов углерода и 1 гетероатом («гетеро-С1-2-алкил»). В некоторых вариантах исполнения гетероалкильная группа представляет собой насыщенную группу, имеющую 1 атом углерода и 1 гетероатом («гетеро-С1-алкил»). В некоторых вариантах исполнения гетероалкильная группа представляет собой насыщенную группу, имеющую от 2 до 6 атомов углерода и 1 или 2 гетероатома («гетеро-С2-6-алкил»). Если не оговорено иное, гетероалкильная группа в каждом случае независимо является необязательно незамещенной («незамещенный гетероалкил») или замещенной («замещенный гетероалкил») одним или более заместителями. В определенных вариантах исполнения гетероалкильная группа представляет собой незамещенный C1-10-гетероалкил. В определенных вариантах исполнения гетероалкильная группа представляет собой замещенный C1-10-гетероалкил.
[0049] «Арил» означает радикал моноциклической или полициклической (например, бициклической или трициклической) 4n+2-ароматической циклической системы (например, имеющей 6, 10 или 14 π-электронов, обобществленных в кольцевой структуре), имеющей 6-14 атомов углерода в цикле и нулевое количество гетероатомов, введенных в ароматическую циклическую систему («С6-14-арил»). В некоторых вариантах исполнения арильная группа имеет шесть атомов углерода в цикле («С6-арил»; например, фенил). В некоторых вариантах исполнения арильная группа имеет десять атомов углерода в цикле («С10-арил»; например, нафтил, такой как 1-нафтил и 2-нафтил). В некоторых вариантах исполнения арильная группа имеет четырнадцать атомов углерода в цикле («С14-арил»; например, антраценил). «Арил» также включает циклические системы, в которых арильное кольцо, как определенное выше, конденсировано с одной или многими карбоциклическими или гетероциклическими группами, причем радикал или точка присоединения находится на арильном цикле, и в таких случаях число атомов углерода продолжает означать число углеродных атомов в арильной циклической системе. Типичные арильные группы включают, но без ограничения этим, группы, образованные из ацеантрилена, аценафтилена, ацефенантрилена, антрацена, азулена, бензола, хризена, коронена, флуорантена, флуорена, гексацена, гексафена, гексалена, асимм-индацена, симм-индацена, индана, индена, нафталина, октацена, октафена, окталена, овалена, пента-2,4-диена, пентацена, пенталена, пентафена, перилена, феналена, фенантрена, пицена, плейадиена, пирена, пирантрена, рубицена, трифенилена, и тринафталена. Конкретные арильные группы включают фенил, нафтил, инденил, и тетрагидронафтил. Если не оговорено иное, арильная группа в каждом случае независимо является необязательно замещенной, то есть, незамещенной («незамещенный арил») или замещенной (замещенный арил») с одним или более заместителями. В определенных вариантах исполнения арильная группа представляет собой незамещенный С6-14-арил. В определенных вариантах исполнения арильная группа представляет собой замещенный С6-14-арил.
[0050] В определенных вариантах исполнения арильную группу, замещенную одной или многими группами, выбирают из таких групп, как атомы галогена, С1-С8-алкил, С1-С8-галоалкил, цианогруппа, гидроксил, С1-С8-алкоксигруппа, и аминогруппа.
[0051] Примеры показательных замещенных арильных групп включают следующие:
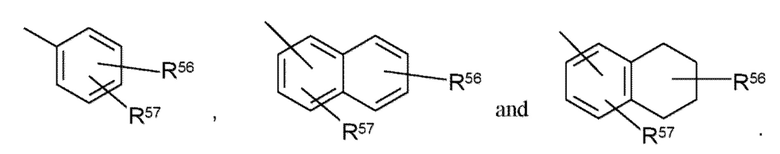
в которых один из R56 и R57 может представлять атом водорода, и по меньшей мере один из R56 и R57, в каждом случае независимо, выбирается из C1-C8-алкила, C1-C8-галоалкила, 4-10-членного гетероциклического фрагмента, алканоила, C1-C8-алкоксигруппы, гетероарилоксигруппы, алкиламиногруппы, ариламиногруппы, гетероариламиногруппы, NR58COR59, NR58SOR59 NR58SO2R59, COO-алкила, COO-арила, CONR58R59, CONR58OR59, NR58R59, SO2NR58R59, S-алкила, SO-алкила, SO2-алкила, S-арила, SO-арила, SO2-арила; или R56 и R57 могут быть объединены с образованием циклической структуры (насыщенной или ненасыщенной) из 5-8 атомов, необязательно содержащей один или многие гетероатомы, выбранные из группы N, O, или S. R60 и R61 независимо представляют атом водорода, C1-C8-алкил, C1-C4-галоалкил, C3-C10-циклоалкил, 4-10-членный гетероциклический фрагмент, C6-C10-арил, замещенный C6-C10-арил, 5-10-членный гетероарил, или замещенный 5-10-членный гетероарил.
[0052] «Конденсированный арил» подразумевает арил, имеющий два из своих атомов углерода в общей структуре со вторым арильным или гетероарильным циклом, или с карбоциклическим или гетероциклическим циклом.
[0053] «Гетероарил» означает радикал 5-10-членной моноциклической или бициклической 4n+2-ароматической циклической системы (например, имеющей 6 или 10 π-электронов, обобществленных в кольцевой структуре), имеющей атомы углерода в цикле и 1-4 гетероатомов в цикле, включенных в ароматическую циклическую систему, в которой каждый гетероатом независимо выбирается из азота, кислорода и серы («5-10-членный гетероарил»). В гетероарильной группе, которая содержит один или более атомов азота, точка присоединения может представлять собой атом углерода или азота, насколько позволяет валентность. Гетероарильные бициклические кольцевые системы могут включать один или многие гетероатомы в одном или обоих циклах. «Гетероарил» включает циклические системы, в которых гетероарильный цикл, как определенный выше, конденсирован с одной или более карбоциклическими или гетероциклическими группами, в которых точка присоединения находится на гетероарильном цикле, и в таких случаях число членов цикла продолжает обозначать число членов цикла в гетероарильной кольцевой системе. «Гетероарил» также включает циклические системы, в которых гетероарильный цикл, как определенный выше, конденсирован с одной или более арильными группами, в которых точка присоединения находится либо на арильном, либо на гетероарильном цикле, и в таких случаях число членов цикла обозначает число членов цикла в конденсированной (арил/гетероарил) кольцевой системе. Бициклические гетероарильные группы, в которых один цикл не содержит гетероатом (например, индолил, хинолинил, карбазолил, и тому подобные), точка присоединения может быть на любом цикле, то есть, либо на кольце, содержащем гетероатом (например, 2-индолил), либо на цикле, который не содержит гетероатом (например, 5-индолил).
[0054] В некоторых вариантах исполнения гетероарильная группа представляет собой 5-10-членную ароматическую циклическую систему, имеющую атомы углерода в цикле и 1-4 гетероатома в цикле, включенные в ароматическую циклическую систему, причем каждый гетероатом независимо выбирается из азота, кислорода и серы («5-10-членный гетероарил»). В некоторых вариантах исполнения гетероарильная группа представляет собой 5-8-членную ароматическую циклическую систему, имеющую атомы углерода в цикле и 1-4 гетероатома в цикле, включенные в ароматическую циклическую систему, причем каждый гетероатом независимо выбирается из азота, кислорода и серы («5-8-членный гетероарил»). В некоторых вариантах исполнения гетероарильная группа представляет собой 5-6-членную ароматическую циклическую систему, имеющую атомы углерода в цикле и 1-4 гетероатома в цикле, включенные в ароматическую циклическую систему, причем каждый гетероатом независимо выбирается из азота, кислорода и серы («5-6-членный гетероарил»). В некоторых вариантах исполнения 5-6-членный гетероарил имеет 1-3 гетероатома в цикле, выбранных из азота, кислорода и серы. В некоторых вариантах исполнения 5-6-членный гетероарил имеет 1-2 гетероатома в цикле, выбранных из азота, кислорода и серы. В некоторых вариантах исполнения 5-6-членный гетероарил имеет 1 гетероатом в цикле, выбранных из азота, кислорода и серы. Если не оговорено иное, гетероарильная группа в каждом случае независимо является необязательно замещенной, то есть, незамещенной («незамещенный гетероарил») или замещенной («замещенный гетероарил») с одним или более заместителями. В определенных вариантах исполнения гетероарильная группа представляет собой незамещенный 5-14-членный гетероарил. В определенных вариантах исполнения гетероарильная группа представляет собой замещенный 5-14-членный гетероарил.
[0055] Примерные 5-членные гетероарильные группы, содержащие один гетероатом, включают, без ограничения, пирролил, фуранил и тиофенил. Примерные 5-членные гетероарильные группы, содержащие два гетероатома, включают, без ограничения, имидазолил, пиразолил, оксазолил, изоксазолил, тиазолил, и изотиазолил. Примерные 5-членные гетероарильные группы, содержащие три гетероатома, включают, без ограничения, триазолил, оксадиазолил, и тиадиазолил. Примерные 5-членные гетероарильные группы, содержащие четыре гетероатома, включают, без ограничения, тетразолил. Примерные 6-членные гетероарильные группы, содержащие один гетероатом, включают, без ограничения, пиридинил. Примерные 6-членные гетероарильные группы, содержащие два гетероатома, включают, без ограничения, пиридазинил, пиримидинил и пиразинил. Примерные 6-членные гетероарильные группы, содержащие три или четыре гетероатома, включают, без ограничения, триазинил и тетразинил, соответственно. Примерные 7-членные гетероарильные группы, содержащие один гетероатом, включают, без ограничения, азепинил, оксепинил и тиепинил. Примерные 5,6-бициклические гетероарильные группы включают, без ограничения, индолил, изоиндолил, индазолил, бензотриазолил, бензотиофенил, изобензотиофенил, бензофуранил, бензоизофуранил, бензимидазолил, бензоксазолил, бензизоксазолил, бензоксадиазолил, бензтиазолил, бензизотиазолил, бензтиадиазолил, индолизинил, и пуринил. Примерные 6,6-бициклические гетероарильные группы включают, без ограничения, нафтиридинил, птеридинил, хинолинил, изохинолинил, циннолинил, хиноксалинил, фталазинил, и хиназолинил.
[0056] Примеры показательных гетероарилов включают следующие:
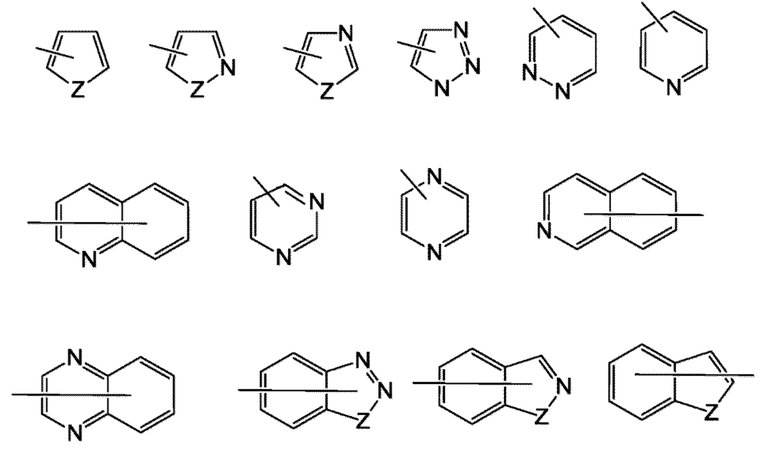
в которых каждый Z выбирается из карбонила, N, NR65, O, и S; и R65 независимо представляет атом водорода, C1-C8-алкил, C3-C10-циклоалкил, 4-10-членный гетероциклил, C6-C10-арил, и 5-10-членный гетероциклический фрагмент.
[0057] «Карбоциклил» или «карбоциклический» имеет отношение к радикалу неароматической циклической углеводородной группы, имеющей от 3 до 10 атомов углерода в цикле («C3-10-карбоциклил»), и не содержащей гетероатомы в неароматической циклической системе. В некоторых вариантах исполнения карбоциклильная группа имеет от 3 до 8 атомов углерода в цикле («C3-8-карбоциклил»). В некоторых вариантах исполнения карбоциклильная группа имеет от 3 до 6 атомов углерода в цикле («C3-6-карбоциклил»). В некоторых вариантах исполнения карбоциклильная группа имеет от 3 до 6 атомов углерода в цикле («C3-6-карбоциклил»). В некоторых вариантах исполнения карбоциклильная группа имеет от 5 до 10 атомов углерода в цикле («C5-10-карбоциклил»). Примерные C3-6-карбоциклильные группы включают, без ограничения, циклопропил (C3), циклопропенил (C3), циклобутил (C4), циклобутенил (C4), циклопентил (C5), циклопентенил (C5), циклогексил (C6), циклогексенил (C6), циклогексадиенил (C6), и тому подобные. Примерные C3-8-карбоциклильные группы включают, без ограничения, вышеупомянутые C3-6-карбоциклильные группы, а также циклогептил (C7), циклогептенил (C7), циклогептадиенил (C7), циклогептатриенил (C7), циклооктил (C8), циклооктенил (C8), бицикло[2.2.1]гептил (C7), бицикло[2.2.2]октил (C8), и тому подобные. Примерные C3-10-карбоциклильные группы включают, без ограничения, вышеупомянутые C3-8-карбоциклильные группы, а также циклононил (C9), циклононенил (C9), циклодецил (C10), циклодеценил (C10), октагидро-1H-инденил (C9), декагидронафталенил (C10), спиро[4.5]децил (C10), и тому подобные. Как иллюстрировано в вышеуказанных примерах, в определенных вариантах исполнения карбоциклильная группа является либо моноциклической («моноциклический карбоциклил»), или же содержит конденсированную, мостиковую или спироциклическую систему, такую как бициклическая система («бициклический карбоциклил»), и может быть насыщенной, или может быть частично ненасыщенной. «Карбоциклил» также включает циклические системы, в которых карбоциклическое кольцо, как определено выше, является конденсированным с одним или многими арильными или гетероарильными группами, причем точка присоединения находится на карбоциклическом кольце, и таких случаях число атомов углерода продолжает обозначать число атомов углерода в карбоциклической циклической системе. Если не оговорено иное, карбоциклическая группа в каждом случае независимо является необязательно замещенной, то есть, незамещенной («незамещенный карбоциклил») или замещенной («замещенный карбоциклил») с одним или многими заместителями. В определенных вариантах исполнения карбоциклильная группа представляет собой незамещенный C3-10-карбоциклил. В определенных вариантах исполнения карбоциклильная группа представляет собой замещенный C3-10-карбоциклил.
[0058] В некоторых вариантах исполнения «карбоциклил» представляет собой моноциклическую, насыщенную карбоциклильную группу, имеющую от 3 до 10 атомов углерода в цикле («C3-10-циклоалкил»). В некоторых вариантах исполнения циклоалкильная группа имеет от 3 до 8 атомов углерода в цикле («C3-8-циклоалкил»). В некоторых вариантах исполнения циклоалкильная группа имеет от 3 до 6 атомов углерода в цикле («C3-6-циклоалкил»). В некоторых вариантах исполнения циклоалкильная группа имеет от 5 до 6 атомов углерода в цикле («C5-6-циклоалкил»). В некоторых вариантах исполнения циклоалкильная группа имеет от 5 до 10 атомов углерода в цикле («C5-10-циклоалкил»). Примеры C5-6-циклоалкильных групп включают циклопентил (C5) и циклогексил (C6). Примеры C3-6-циклоалкильных групп включают вышеупомянутые C5-6-циклоалкильные группы, а также циклопропил (C3) и циклобутил (C4). Примеры C3-8-циклоалкильных групп включают вышеупомянутые C3-6-циклоалкильные группы, а также циклогептил (C7) и циклооктил (C8). Если не оговорено иное, циклоалкильная группа в каждом случае независимо является незамещенной («незамещенный циклоалкил») или замещенной («замещенный циклоалкил») с одним или многими заместителями. В определенных вариантах исполнения циклоалкильная группа представляет собой незамещенный C3-10-циклоалкил. В определенных вариантах исполнения циклоалкильная группа представляет собой замещенный C3-10-циклоалкил.
[0059] «Гетероциклил» или «гетероциклический» имеет отношение к радикалу 3-10-членной неароматической циклической системе, имеющей атомы углерода в цикле и от 1 до 4 гетероатомов в цикле, причем каждый гетероатом независимо выбирается из азота, кислорода, серы, бора, фосфора и кремния («3-10-членный гетероциклил»). В гетероциклических группах, которые содержат один или многие атомы азота, точка присоединения может быть атомом углерода или азота, насколько позволяет валентность. Гетероциклильная группа может быть либо моноциклической («моноциклический гетероциклил»), либо конденсированной, мостиковой или спироциклической системой, такой как бициклическая («бициклический гетероциклил»), и может быть насыщенной или частично ненасыщенной. Гетероциклильные бициклические кольцевые системы могут включать один или многие гетероатомы в одном или обоих циклах. «Гетероциклил» также включает циклические системы, в которых гетероциклильный цикл, как определенный выше, конденсирован с одной или более карбоциклическими группами, в которых точка присоединения находится либо на карбоциклильном, либо на гетероциклильном кольце, или циклические системы, в которых гетероциклильный цикл, как определенный выше, конденсирован с одной или более арильными или гетероарильными группами, причем точка присоединения находится на гетероциклильном кольце, и в таких случаях число членов цикла продолжает обозначать число членов цикла в гетероциклильной кольцевой системе. Если не оговорено иное, гетероциклил в каждом случае независимо является незамещенным («незамещенный гетероциклил») или замещенным («замещенный гетероциклил») с одним или многими заместителями. В определенных вариантах исполнения гетероциклильная группа представляет собой незамещенный 3-10-членный гетероциклил. В определенных вариантах исполнения гетероциклильная группа представляет собой замещенный 3-10-членный гетероциклил.
[0060] В некоторых вариантах исполнения гетероциклильная группа представляет собой 5-10-членную неароматическую циклическую систему, имеющую атомы углерода в цикле и 1-4 гетероатомов в цикле, причем каждый гетероатом независимо выбирается из азота, кислорода, серы, бора, фосфора и кремния («5-10-членный гетероциклил»). В некоторых вариантах исполнения гетероциклильная группа представляет собой 5-8-членную неароматическую циклическую систему, имеющую атомы углерода в цикле и 1-4 гетероатомов в цикле, причем каждый гетероатом независимо выбирается из азота, кислорода и серы («5-8-членный гетероциклил»). В некоторых вариантах исполнения гетероциклильная группа представляет собой 5-6-членную неароматическую циклическую систему, имеющую атомы углерода в цикле и 1-4 гетероатомов в цикле, причем каждый гетероатом независимо выбирается из азота, кислорода и серы («5-6-членный гетероциклил»). В некоторых вариантах исполнения 5-6-членный гетероциклил имеет 1-3 гетероатома в цикле, выбранных из азота, кислорода и серы. В некоторых вариантах исполнения 5-6-членный гетероциклил имеет 1-2 гетероатома в цикле, выбранных из азота, кислорода и серы. В некоторых вариантах исполнения 5-6-членный гетероциклил имеет один гетероатом в цикле, выбранный из азота, кислорода и серы.
[0061] Примерные 3-членные гетероциклильные группы, содержащие один гетероатом, включают, без ограничения, азиридинил, оксиранил, тиоренил. Примерные 4-членные гетероциклильные группы, содержащие один гетероатом, включают, без ограничения, азетидинил, оксетанил и тиетанил. Примерные 5-членные гетероциклильные группы, содержащие один гетероатом, включают, без ограничения, тетрагидрофуранил, дигидрофуранил, тетрагидротиофенил, дигидротиофенил, пирролидинил, дигидропирролил и пирролил-2,5-дион. Примеры 5-членных гетероциклильных групп, содержащих два гетероатома, включают, без ограничения, диоксоланил, оксасульфуранил, дисульфуранил и оксазолидин-2-он. Примерные 5-членные гетероциклильные группы, содержащие три гетероатома, включают, без ограничения, триазолинил, оксадиазолинил и тиадиазолинил. Примеры 6-членных гетероциклильных групп, содержащих один гетероатом, включают, без ограничения, пиперидинил, тетрагидропиранил, дигидропиридинил и тианил. Примеры 6-членных гетероциклильных групп, содержащих два гетероатома, включают, без ограничения, пиперазинил, морфолинил, дитианил, диоксанил. Примеры 6-членных гетероциклильных групп, содержащих два гетероатома, включают, без ограничения, триазинанил. Примеры 7-членных гетероциклильных групп, содержащих один гетероатом, включают, без ограничения, азепанил, оксепанил и тиепанил. Примеры 8-членных гетероциклильных групп, содержащих один гетероатом, включают, без ограничения, азоканил, оксеканил и тиоканил. Примеры 5-членных гетероциклильных групп, конденсированных с С6-арильным циклом (также называемых здесь 5,6-бициклическим гетероциклическим циклом), включают, без ограничения, индолинил, изоиндолинил, дигидробензофуранил, дигидробензотиенил, бензоксазолинонил и тому подобные. Примерные 6-членные гетероциклильные группы, конденсированные с арильным циклом (также называемые здесь 6,6-бициклическим гетероциклическим циклом), включают, без ограничения, тетрагидрохинолинил, тетрагидроизохинолинил, и тому подобные.
[0062] «Азотсодержащая гетероциклильная» группа означает 4-7-членную неароматическую циклическую группу, содержащую по меньшей мере один атом азота, например, но без ограничения, морфолин, пиперидин (например, 2-пиперидинил, 3-пиперидинил и 4-пиперидинил), пирролидин (например, 2-пирролидинил и 3-пирролидинил), азетидин, пирролидон, имидазолин, имидазолидинон, 2-пиразолин, пиразолидин, пиперазин и N-алкилпиперазины, такие как N-метилпиперазин. Конкретные примеры включают азетидин, пиперидон и пиперазон.
[0063] «Гетеро» при использовании для описания соединения или группы, присутствующей в соединении, означает, что один или многие атомы углерода в соединении или группе были замещены гетероатомом азота, кислорода или серы. «Гетеро» можно применить к любой из углеводородных групп, описанных выше, таких как алкил, например, гетероалкил, циклоалкил, например, гетероциклил, арил, например, гетероарил, циклоалкенил, например, циклогетероалкенил, и тому подобных, имеющих от 1 до 5, и в частности, от 1 до 3 гетероатомов.
[0064] «Ацил» относится к радикалу -С(О)R20, где R20 представляет водород, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил или замещенный или незамещенный гетероарил, как здесь определенные. «Алканоил» представляет собой ацильную группу, в которой R20 представляет собой иную группу, нежели водород. Показательные ацильные группы включают, но без ограничения этим, формил (-CHO), ацетил (-C(=O)CH3), циклогексилкарбонил, циклогексилметилкарбонил, бензоил (-C(=O)Ph), бензилкарбонил (-C(=O)CH2Ph), -C(O)-C1-C8-алкил, -C(O)-(CH2)t(C6-C10-арил), -C(O)-(CH2)t(5-10-членный гетероарил), -C(O)-(CH2)t(C3-C10-циклоалкил) и -C(O)-(CH2)t(4-10-членный гетероциклил), в которых t представляет целое число от 0 до 4. В определенных вариантах исполнения R21 представляет собой C1-C8-алкил, замещенный галогеном или гидроксигруппой; или C3-C10-циклоалкил, 4-10-членный гетероциклил, C6-C10-арил, арилалкил, 5-10-членный гетероарил или гетероарилалкил, каждый из которых является замещен незамещенным C1-C4-алкилом, галогеном, незамещенной C1-C4-алкоксигруппой, незамещенным C1-C4-галогеналкилом, незамещенным C1-C4-гидроксиалкилом или незамещенной C1-C4-галогеналкоксигруппой или гидроксигруппой.
[0065] «Алкокси» относится к группе -OR29, где R29 представляет замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил или замещенный или незамещенный гетероарил. Конкретными алкоксигруппами являются метоксигруппа, этоксигруппа, н-пропоксигруппа, изопропоксигруппа, н-бутоксигруппа, трет-бутоксигруппа, втор-бутоксигруппа, н-пентоксигруппа, н-гексоксигруппа и 1,2-диметилбутоксигруппа. Конкретные алкоксигруппы представляют собой низшие алкоксигруппы, то есть, с числом атомов углерода от 1 до 6. Дополнительные конкретные алкоксигруппы имеют от 1 до 4 атомов углерода.
[0066] В определенных вариантах исполнения R29 представляет собой группу, которая имеет 1 или больше заместителей, например, от 1 до 5 заместителей, и в частности, от 1 до 3 заместителей, в частности, 1 заместитель, выбранные из группы, включающей аминогруппу, замещенную аминогруппу, С6-С10-арил, арилоксигруппу, карбоксил, цианогруппу, С3-С10-циклоалкил, 4-10-членный гетероциклил, галоген, 5-10-членный гетероарил, гидроксил, нитрогруппу, тиоалкоксигруппу, тиоарилоксигруппу, тиол, алкил-S(O)-, арил-S(O)-, алкил-S(O)2-, и арил-S(O)2-. Примерные «замещенные алкоксигруппы» включают, но без ограничения этим, -O-(CH2)t(C6-C10-арил), -O-(CH2)t(5-10-членный гетероарил), -O-(CH2)t(C3-C10-циклоалкил) и -O-(CH2)t(4-10-членный гетероциклил), в которых t представляет целое число от 0 до 4, и любые присутствующие арильные, гетероарильные, циклоалкильные или гетероциклильные группы сами могут быть замещены незамещенным С1-С4-алкилом, галогеном, незамещенной С1-С4-алкоксигруппой, незамещенным С1-С4-галогеналкилом, незамещенным С1-С4-гидроксиалкилом или незамещенной С1-С4-галогеналкоксигруппой или гидроксигруппой. Конкретными примерными «замещенными алкоксигруппами» являются -OCF3, -OCH2CF3, -OCH2Ph, -OCH2-циклопропил, -OCH2CH2OH и -OCH2CH2NMe2.
[0067] «Амино» относится к радикалу -NH2.
[0068] «Оксогруппа» подразумевает -С(=О)-.
[0069] «Замещенная аминогруппа» относится к аминогруппе формулы -N(R38)2, где R38 представляет водород, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, замещенный или незамещенный гетероарил, или аминозащитную группу, где по меньшей мере один R38 не является водородом. В определенных вариантах исполнения каждый R38 выбирают независимо из атома водорода, С1-С8-алкила, С3-С8-алкенила, С3-С8-алкинила, С6-С10-арила, 5-10-членного гетероарила, 4-10-членного гетероциклила или С3-С10-циклоалкила; или С1-С8-алкила, замещенного галогеном или гидроксигруппой; С3-С8-алкинила, замещенного галогеном или гидроксигруппой, или -(CH2)t(C6-C10-арила), -(CH2)t(5-10-членного гетероарила), -(CH2)t(C3-C10-циклоалкила) или -(CH2)t(4-10-членного гетероциклила), в которых t представляет целое число от 0 до 8, каждый из которых замещен незамещенным C1-C4-алкилом, галогеном, незамещенной C1-C4-алкоксигруппой, незамещенным C1-C4-галогеналкилом, незамещенным C1-C4-гидроксиалкилом или незамещенной C1-C4-галогеналкоксигруппой или гидроксигруппой; или обе группы R38 объединены с образованием алкиленовой группы.
[0070] Примерные «замещенные аминогруппы» включают, но без ограничения этим, -NR39-C1-C8-алкил, -NR39-(CH2)t(C6-C10-арил),- NR39-(CH2)t(5-10-членный гетероарил), -NR39-(CH2)t(C3-C10-циклоалкил) и -NR39-(CH2)t(4-10-членный гетероциклил), в которых t представляет целое число от 0 до 4, например, 1 или 2, каждый R39 независимо представляет Н или C1-C8-алкил; и любые присутствующие алкильные группы сами могут быть замещены галогеном, замещенной или незамещенной аминогруппой или гидроксигруппой; и любые присутствующие арильные, гетероарильные, циклоалкильные или гетероциклильные группы сами могут быть замещены незамещенным C1-C4-алкилом, галогеном, незамещенной C1-C4-алкоксигруппой, незамещенным C1-C4-галогеналкилом, незамещенным C1-C4-гидроксиалкилом или незамещенной C1-C4-галогеналкоксигруппой или гидроксигруппой. Во избежание сомнений, термин «замещенная аминогруппа» включает алкиламиногруппу, замещенную алкиламиногруппу, алкилариламиногруппу, замещенную алкилариламиногруппу, ариламиногруппу, замещенную ариламиногруппу, диалкиламиногруппу и замещенную диалкиламиногруппу, как определено ниже. Замещенная аминогруппа охватывает как монозамещенные аминогруппы, так и дизамещенные аминогруппы.
[0071] «Карбокси» подразумевает радикал -С(О)ОН.
[0072] «Циано» подразумевает радикал -CN.
[0073] «Гало» или «галоген» относится к фтору (F), хлору (Cl), брому (Br) или иоду (I). В определенных вариантах исполнения галогеногруппа представляет собой либо фтор, либо хлор.
[0074] «Галоалкил» подразумевает алкильный радикал, в котором алкильная группа замещена одним или многими атомами галогенов. Типичные галоалкильные группы включают, но без ограничения этим, трифторметил, дифторметил, фторметил, хлорметил, дихлорметил, дибромэтил, трибромметил, тетрафторэтил, и тому подобные.
[0075] «Гидрокси» относится к радикалу -ОН.
[0076] «Нитро» относится к радикалу -NO2.
[0077] «Тиокето» относится к группе =S.
[0078] Алкильная, алкенильная, алкинильная, карбоциклильная, гетероциклильная, арильная и гетероарильная группы, как здесь определено, необязательно являются замещенными (например, «замещенная» или «незамещенная» алкильная, «замещенная» или «незамещенная» алкенильная, «замещенная» или «незамещенная» алкинильная, «замещенная» или «незамещенная» карбоциклильная, «замещенная» или «незамещенная» гетероциклильная, «замещенная» или «незамещенная» арильная или «замещенная» или «незамещенная» гетероарильная группа). В целом, термин «замещенный», предшествует ли ему термин «необязательно» или нет, означает, что по меньшей мере один присутствующий водород в группе (например, у атома углерода или азота) замещен на допустимый заместитель, например, заместитель, который при замещении дает в результате стабильное соединение, например, соединение, которое спонтанно не подвергается преобразованию, такому как перегруппировка, циклизация, расщепление, или другие реакции. Если не оговорено иное, «замещенная» группа содержит заместитель в одном или более замещаемых положениях группы, и когда более чем одно положение в любой данной структуре замещено, заместитель находится или в том же или в другом положении. Термин «замещенный» рассматривается как включающий замещение всеми допустимыми заместителями органических соединений, любыми из описанных здесь заместителей, которые приводят к образованию стабильного соединения. В настоящем изобретении рассматриваются любые и все такие комбинации, которые приводят к стабильному соединению. Для целей настоящего изобретения гетероатомы, такие как азот, могут иметь в качестве заместителей атомы водорода и/или любой подходящий заместитель, как здесь описано, которые удовлетворяют валентностям гетероатомов и приводят к образованию стабильного остатка.
[0079] Примерные заместители у атома углерода включают, но без ограничения этим, галоген, -CN, -NO2, -N3, -SO2H, -SO3H, -OH, -ORaa, -ON(Rbb)2, -N(Rbb)2, -N(Rbb)3+X-, -N(ORcc)Rbb, -SH, -SRaa, -SSRcc, -C(=O)Raa, -CO2H, -CHO, -C(ORcc)2, -CO2Raa, -OC(=O)Raa, -OCO2Raa, -C(=O)N(Rbb)2, -OC(=O)N(Rbb)2, -NRbbC(=O)Raa, -NRbbCO2Raa, -NRbbC(=O)N(Rbb)2, -C(=NRbb)Raa, -C(=NRbb)ORaa, -OC(=NRbb)Raa, -OC(=NRbb)ORaa, -C(=NRbb)N(Rbb)2, -OC(=NRbb)N(Rbb)2, -NRbbC(=NRbb)N(Rbb)2, -C(=O)NRbbSO2Raa, -NRbbSO2Raa, -SO2N(Rbb)2, -SO2Raa, -SO2ORaa, -OSO2Raa, -S(=O)Raa, -OS(=O)Raa, -Si(Raa)3, -OSi(Raa)3, -C(=S)N(Rbb)2, -C(=O)SRaa, -C(=S)SRaa, -SC(=S)SRaa, -SC(=O)SRaa, -OC(=O)SRaa, -SC(=O)ORaa, -SC(=O)Raa, -P(=O)2Raa, -OP(=O)2Raa, -P(=O)(Raa)2, -OP(=O)(Raa)2, -OP(=O)(ORcc)2, -P(=O)2N(Rbb)2, -OP(=O)2N(Rbb)2, -P(=O)(NRbb)2, -OP(=O)(NRbb)2, -NRbbP(=O)(ORcc)2, -NRbbP(=O)(NRbb)2, -P(Rcc)2, -P(Rcc)3, -OP(Rcc)2, -OP(Rcc)3, -B(Raa)2, -B(ORcc)2, -BRaa(ORcc), C1-10-алкил, C1-10-галогеналкил, C2-10-алкенил, C2-10-алкинил, C3-10-карбоциклил, 3-14-членный гетероциклил, C6-14-арил и 5-14-членный гетероарил, причем каждый алкил, алкенил, алкинил, карбоциклил, гетероциклил, арил и гетероарил независимо замещены 0, 1, 2, 3, 4 или 5 Rdd-группами; или два геминальных атома водорода на атоме углерода замещены группой =О, =S, =NN(Rbb)2, =NNRbbC(=O)Raa, =NNRbbC(=O)ORaa, =NNRbbS(=O)2Raa, =NRbb, или =NORcc;
[0080] Raa в каждом случае независимо выбран из C1-10-алкила, C1-10-галогеналкила, C2-10-алкенила, C2-10-алкинила, C3-10-карбоциклила, 3-14-членного гетероциклила, C6-14-арила и 5-14-членного гетероарила, или две Raa-группы объединены с образованием 3-14-членного гетероциклила или 5-14-членного гетероарильного кольца, где каждый алкил, алкенил, алкинил, карбоциклил, гетероциклил, арил и гетероарил независимо замещены 0, 1, 2, 3, 4 или 5 Rdd-группами;
[0081] Rbb в каждом случае независимо выбран из атома водорода, -OH, -ORaa, -N(Rcc)2, -CN, -C(=O)Raa, -C(=O)N(Rcc)2, -CO2Raa, -SO2Raa, -C(=NRcc)ORaa, -C(=NRcc)N(Rcc)2, -SO2N(Rcc)2, -SO2Rcc, -SO2ORcc, -SORaa, -C(=S)N(Rcc)2, -C(=O)SRcc, -C(=S)SRcc, -P(=O)2Raa, -P(=O)(Raa)2, -P(=O)2N(Rcc)2, -P(=O)(NRcc)2, C1-10-алкила, C1-10-галогеналкила, C2-10-алкенила, C2-10-алкинила, C3-10-карбоциклила, 3-14-членного гетероциклила, C6-14-арила и 5-14-членного гетероарила, или две Rbb-группы объединены с образованием 3-14-членного гетероциклила или 5-14-членного гетероарильного кольца, причем каждый алкил, алкенил, алкинил, карбоциклил, гетероциклил, арил и гетероарил независимо замещены 0, 1, 2, 3, 4 или 5 Rdd-группами;
[0082] Rcc в каждом случае независимо выбран из атома водорода, C1-10-алкила, C1-10-галогеналкила, C2-10-алкенила, C2-10-алкинила, C3-10-карбоциклила, 3-14-членного гетероциклила, C6-14-арила и 5-14-членного гетероарила, или две Rcc-группы объединены с образованием 3-14-членного гетероциклила или 5-14-членного гетероарильного кольца, где каждый алкил, алкенил, алкинил, карбоциклил, гетероциклил, арил и гетероарил независимо замещены 0, 1, 2, 3, 4 или 5 Rdd-группами;
[0083] Rdd в каждом случае независимо выбран из галогена, -CN, -NO2, -N3, -SO2H, -SO3H, -OH, -ORee, -ON(Rff)2, -N(Rff)2, -N(Rff)3+X-, -N(ORee)Rff, -SH, -SRee, -SSRee, -C(=O)Ree, -CO2H, -CO2Ree, -OC(=O)Ree, -OCO2Ree, -C(=O)N(Rff)2, -OC(=O)N(Rff)2, -NRffC(=O)Ree, -NRffCO2Ree, -NRffC(=O)N(Rff)2, -C(=NRff)ORee, -OC(=NRff)Ree, -OC(=NRff)ORee, -C(=NRff)N(Rff)2, -OC(=NRff)N(Rff)2, -NRffC(=NRff)N(Rff)2, -NRffSO2Ree, -SO2N(Rff)2, -SO2Ree, -SO2ORee, -OSO2Ree, -S(=O)Ree, -Si(Ree)3, -OSi(Ree)3, -C(=S)N(Rff)2, -C(=O)SRee, -C(=S)SRee, -SC(=S)SRee, -P(=O)2Ree, -P(=O)(Ree)2, -OP(=O)(Ree)2, -OP(=O)(ORee)2, C1-6-алкила, C1-6-галогеналкила, C2-6-алкенила, C2-6-алкинила, C3-10-карбоциклила, 3-10-членного гетероциклила, C6-10-арила, 5-10-членного гетероарила, где каждый алкил, алкенил, алкинил, карбоциклил, гетероциклил, арил и гетероарил независимо замещены 0, 1, 2, 3, 4 или 5 Rgg-группами, два геминальных Rdd-заместителя могут быть объединены с образованием =О или =S;
[0084] Ree в каждом случае независимо выбран из C1-6-алкила, C1-6-галогеналкила, C2-6-алкенила, C2-6-алкинила, C3-10-карбоциклила, C6-10-арила, 3-10-членного гетероциклила и 3-10-членного гетероарила, причем каждый алкил, алкенил, алкинил, карбоциклил, гетероциклил, арил и гетероарил независимо замещены 0, 1, 2, 3, 4 или 5 Rgg-группами;
[0085] Rff в каждом случае независимо выбран из атома водорода, C1-6-алкила, C1-6-галогеналкила, C2-6-алкенила, C2-6-алкинила, C3-10-карбоциклила, 3-10-членного гетероциклила, C6-10-арила и 5-10-членного гетероарила, или две Rff-группы присоединены с образованием 3-14-членного гетероциклила или 5-14-членного гетероарильного кольца, где каждый алкил, алкенил, алкинил, карбоциклил, гетероциклил, арил и гетероарил независимо замещены 0, 1, 2, 3, 4 или 5 Rgg-группами; и
[0086] Rgg в каждом случае независимо представляет галоген, -CN, -NO2, -N3, -SO2H, -SO3H, -OH, -OC1-6-алкил, -ON(C1-6-алкил)2, -N(C1-6-алкил)2, -N(C1-6-алкил)3+X-, -NH(C1-6-алкил)2+X-, -NH2(C1-6-алкил)+X-, -NH3+X-, -N(OC1-6-алкил)(C1-6-алкил), -N(OH)(C1-6-алкил), -NH(OH), -SH, -SC1-6-алкил, -SS(C1-6-алкил), -C(=O)(C1-6-алкил), -CO2H, -CO2(C1-6-алкил), -OC(=O)(C1-6-алкил), -OCO2(C1-6-алкил), -C(=O)NH2, -C(=O)N(C1-6-алкил)2, -OC(=O)NH(C1-6-алкил), -NHC(=O)(C1-6-алкил), -N(C1-6-алкил)C(=O)(C1-6-алкил), -NHCO2(C1-6-алкил), -NHC(=O)N(C1-6-алкил)2, -NHC(=O)NH(C1-6-алкил), -NHC(=O)NH2, -C(=NH)O(C1-6-алкил),-OC(=NH)(C1-6-алкил), -OC(=NH)OC1-6-алкил, -C(=NH)N(C1-6-алкил)2, -C(=NH)NH(C1-6-алкил), -C(=NH)NH2, -OC(=NH)N(C1-6-алкил)2, -OC(NH)NH(C1-6-алкил), -OC(NH)NH2, -NHC(NH)N(C1-6-алкил)2, -NHC(=NH)NH2, -NHSO2(C1-6-алкил), -SO2N(C1-6-алкил)2, -SO2NH(C1-6-алкил), -SO2NH2, -SO2C1-6-алкил, -SO2OC1-6-алкил, -OSO2C1-6-алкил, -SOC1-6-алкил, -Si(C1-6-алкил)3, -OSi(C1-6-алкил)3 -C(=S)N(C1-6-алкил)2, C(=S)NH(C1-6-алкил), C(=S)NH2, -C(=O)S(C1-6-алкил), -C(=S)SC1-6-алкил, -SC(=S)SC1-6-алкил, -P(=O)2(C1-6-алкил), -P(=O)(C1-6-алкил)2, -OP(=O)(C1-6-алкил)2, -OP(=O)(OC1-6-алкил)2, C1-6-алкил, C1-6-галогеналкил, C2-6-алкенил, C2-6-алкинил, C3-10-карбоциклил, C6-10-арил, 3-10-членный гетероциклил, 5-10-членный гетероарил; или два геминальных Rgg-заместителя могут быть объединены с образованием =О или =S; причем X- представляет противоион.
[0087] «Противоион» или «анионный противоион» представляет собой отрицательно заряженную группу, связанную с катионной четвертичной аминогруппой для того, чтобы поддерживать электронейтральность. Примерные противоионы включают галогенид-ионы (например, F-, Cl-, Br-, I-), NO3-, ClO4-, ОH-, H2PO4-, HSO4-, сульфонатные ионы (например, метансульфонат, трифторметансульфонат, пара-толуолсульфонат, бензолсульфонат, 10-камфорсульфонат, нафталин-2-сульфонат, 5-сульфонат нафталин-1-сульфоновой кислоты, 2-сульфонат этан-1-сульфоновой кислоты, и тому подобные), и карбоксилатные ионы (например, ацетат, этаноат, пропаноат, бензоат, глицерат, лактат, тартрат, гликолят и тому подобные).
[0088] Эти и другие примерные заместители более подробно описываются в разделе «Подробное Описание» и в Пунктах Формулы изобретения. Изобретение никоим образом не предполагается быть ограниченным вышеуказанным примерным списком заместителей.
Другие определения
[0089] Как используемый здесь, термин «модулирование» относится к ингибированию или потенцированию функции ГАМК-рецептора. «Модулятор» (например, модулирующее соединение) может представлять собой, например, агонист, частичный агонист, антагонист или частичный антагонист ГАМК-рецептора.
[0090] «Фармацевтически приемлемый» означает одобренный или одобряемый регулирующим агентством федерального правительства или штата или соответствующим агентством в странах, отличных от Соединенных Штатов Америки, или такой, который перечислен в Фармакопее США или других общепризнанных фармакопеях для применения у животных, и более конкретно, у людей.
[0091] «Фармацевтически приемлемая соль» относится к соли соединения согласно изобретению, которая является фармацевтически приемлемой, и которая обладает желательной фармакологической активностью исходного соединения. В частности, такие соли являются нетоксичными, и могут представлять собой соли присоединения неорганической или органической кислоты и соли присоединения основания. Более конкретно, такие соли включают: (1) соли присоединения кислоты, образованные неорганическими кислотами, такими как соляная кислота, бромистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота, и тому подобные; или образованные органическими кислотами, такими как уксусная кислота, пропионовая кислота, капроновая кислота, циклопентанпропионовая кислота, гликолевая кислота, пировиноградная кислота, молочная кислота, малоновая кислота, янтарная кислота, яблочная кислота, малеиновая кислота, фумаровая кислота, винная кислота, лимонная кислота, бензойная кислота, 3-(4-гидроксибензоил)бензойная кислота, коричная кислота, миндальная кислота, метансульфоновая кислота, этансульфоновая кислота, 1,2-этандисульфоновая кислота, 2-гидроксиэтансульфоновая кислота, бензолсульфоновая кислота, 4-хлорбензолсульфоновая кислота, 2-нафталинсульфоновая кислота, 4-толуолсульфоновая кислота, камфорсульфоновая кислота, 4-метилбицикло[2,2,2]-окт-2-ен-1-карбоновая кислота, глюкогептоновая кислота, 3-фенилпропионовая кислота, триметилуксусная кислота, трет-бутилуксусная кислота, лаурилсерная кислота, глюконовая кислота, глутаминовая кислота, гидроксинафтойная кислота, салициловая кислота, стеариновая кислота, муконовая кислота и тому подобные; или (2) соли, образованные, когда протон кислоты, присутствующий в исходном соединении, также замещен ионом металла, например, ионом щелочного металла, ионом щелочноземельного металла или ионом алюминия; или координирован с органическим основанием, таким как этаноламин, диэтаноламин, триэтаноламин, N-метилглюкамин, и тому подобными. Кроме того, соли включают, только в качестве примера, натрий, калий, кальций, магний, аммоний, тетраалкиламмоний и тому подобные; и когда соединение содержит оснóвную функциональность, соли нетоксичных органических или неорганических кислот, такие как гидрохлорид, гидробромид, тартрат, мезилат, ацетат, малеат, оксалат, и тому подобные. Термин «фармацевтически приемлемый катион» относится к приемлемому катионному противоиону кислотной функциональной группы. Примерами таких катионов являются катионы натрия, калия, кальция, магния, аммония, тетраалкиламмония, и тому подобные. Смотри, например, работу авторов Berge, и др., J. Pharm. Sci., (1977) том 66 (№1): стр. 1-79.
[0092] Термин «пролекарство» предполагается включающим терапевтически неактивные соединения, которые в физиологических условиях преобразуются в терапевтически активные агенты согласно настоящему изобретению. Одним способом получения пролекарства является подбор некоторых фрагментов, которые гидролизуются или расщепляются в целевом in vitro месте под действием физиологических условий с высвобождением желательной молекулы, которая затем проявляет свой терапевтический эффект. В определенных вариантах исполнения пролекарство преобразуется в результате ферментативной активности субъекта.
[0093] В альтернативном варианте осуществления настоящее изобретение представляет пролекарства соединения Формулы (I-X, I-I, II-I, III-I, или III-II), причем пролекарство включает отщепляемый фрагмент на C3-гидроксигруппе, как изображено в соединении Формулы (I-X, I-I, II-I, III-I, или III-II). «Таутомеры» относятся к соединениям, которые представляют собой взаимопревращающиеся формы структуры конкретного соединения, и которые изменяются при перемещении атомов водорода и электронов. Таким образом, две структуры могут находиться в равновесии через движение π-электронов и атома (обычно H). Например, енолы и кетоны являются таутомерами, так как они быстро переходят друг в друга в присутствии кислоты или основания. Еще одним примером таутомерии являются аци- и нитро-формы фенилнитрометана, которые аналогичным образом образуются в присутствии кислоты или основания. Таутомерные формы могут иметь значение для достижения оптимальной химической реакционной способности и биологической активности обсуждаемого соединения.
[0094] «Субъект», которому предполагается введение, включает, но без ограничения этим, людей (то есть, мужского или женского пола любой возрастной группы, например, педиатрический субъект (например, младенцы, дети, подростки) или взрослый субъект (например, молодые взрослые, взрослые среднего возраста или взрослые старшего возраста)), и/или животных, не являющихся людьми, например, млекопитающих, таких как приматы (например, яванский макак, макак-резус), крупный рогатый скот, свиньи, лошади, овцы, козы, грызуны, кошки и/или собаки. В определенных вариантах исполнения субъектом является человек. В определенных вариантах исполнения субъект представляет собой не являющееся человеком животное.
[0095] В определенных вариантах исполнения заместитель, присутствующий на атоме кислорода, представляет собой защитную группу для кислорода (также называемую гидроксилзащитной группой). Защитные группы для кислорода включают, но без ограничения этим, -Raa, -N(Rbb)2, -C(=O)SRaa, -C(=O)Raa, -CO2Raa, -C(=O)N(Rbb)2, -C(=NRbb)Raa, -C(=NRbb)ORaa, -C(=NRbb)N(Rbb)2, -S(=O)Raa, -SO2Raa, -Si(Raa)3, -P(Rcc)2, -P(Rcc)3, -P(=O)2Raa, -P(=O)(Raa)2, -P(=O)(ORcc)2, -P(=O)2N(Rbb)2 и -P(=O)(NRbb)2, где Raa, Rbb и Rcc являются такими, как здесь определено. Защитные группы для кислорода являются общеизвестными в технологии, и включают такие, какие подробно описаны в издании Protecting Groups in Organic Synthesis, T.W. Greene и P.G.M. Wuts, 3-е издание, издательство John Wiley & Sons, 1999, включенном здесь ссылкой.
[0096] Примерные защитные группы для кислорода включают, но не ограничиваются этим, метил, метоксилметил (MOM), 2-метоксиэтоксиметил (MEM), бензил (Bn), триизопропилсилил (TIPS), трет-бутилдиметилсилил (TBDMS), трет-бутилметоксифенилсилил (TBMPS), метансульфонат (мезилат) и тозилат (Ts).
[0097] В определенных вариантах исполнения заместитель, присутствующий на атоме серы, представляет собой защитную группу для серы (также называемую тиолзащитной группой). Защитные группы для серы включают, но не ограничиваются этим, -Raa, -N(Rbb)2, -C(=O)SRaa, -C(=O)Raa, -CO2Raa, -C(=O)N(Rbb)2, -C(=NRbb)Raa, -C(=NRbb)ORaa, -C(=NRbb)N(Rbb)2, -S(=O)Raa, -SO2Raa, -Si(Raa)3, -P(Rcc)2, -P(Rcc)3, -P(=O)2Raa, -P(=O)(Raa)2, -P(=O)(ORcc)2, -P(=O)2N(Rbb)2 и -P(=O)(NRbb)2, в которых Raa, Rbb и Rcc являются такими, как здесь определено. Защитные группы для серы являются общеизвестными в технологии, и включают такие, какие подробно описаны в издании Protecting Groups in Organic Synthesis, T.W. Greene и P.G.M. Wuts, 3-е издание, издательство John Wiley & Sons, 1999, включенном здесь ссылкой.
[0098] В определенных вариантах исполнения заместитель, присутствующий на атоме азота, представляет собой аминозащитную группу (также называемую здесь азотзащитной группой). Аминозащитные группы включают, но не ограничиваются этим, -OH, -ORaa, -N(Rcc)2, -C(=O)Raa, -C(=O)ORaa, -C(=O)N(Rcc)2, -S(=O)2Raa, -C(=NRcc)Raa, -C(=NRcc)ORaa, -C(=NRcc)N(Rcc)2, -SO2N(Rcc)2, -SO2Rcc, -SO2ORcc, -SORaa, -C(=S)N(Rcc)2, -C(=O)SRcc, -C(=S)SRcc, C1-10-алкил, C2-10-алкенил, C2-10-алкинил, C3-10-карбоциклил, 3-14-членный гетероциклил, C6-14-арил и 5-14-членные гетероарильные группы, где каждый алкил, алкенил, алкинил, карбоциклил, гетероциклил, арил и гетероарил независимо замещены 0, 1, 2, 3, 4 или 5 Rdd-группами, и где Raa, Rbb, Rcc и Rdd являются такими, как здесь определено. Аминозащитные группы являются общеизвестными в технологии, и включают такие, какие подробно описаны в издании Protecting Groups in Organic Synthesis, T.W. Greene и P.G.M. Wuts, 3-е издание, издательство John Wiley & Sons, 1999, включенном здесь ссылкой.
[0099] Примерные аминозащитные группы включают, но без ограничения этим, амидные группы (например, -C(=O)Raa), которые включают, но без ограничения этим, формамид и ацетамид; карбаматные группы (например, -C(=O)ORaa), которые включают, но без ограничения этим, 9-флуоренилметилкарбамат (Fmoc), трет-бутилкарбамат (BOC) и бензилкарбамат (Cbz); сульфонамидные группы (например, -S(=O)2Raa), которые включают, но без ограничения этим, p-толуолсульфонамид (Ts), метансульфонамид (Ms) и N-[2-(триметилсилил)этокси]метиламин (SEM).
[0100] Заболевание, расстройство и состояние используются здесь как взаимозаменяемые.
[0101] Как применяемые здесь, и если не оговаривается иное, термины «лечить», «обработка» и «лечение» рассматривают действие, которое происходит в то время, как субъект страдает от указанного заболевания, расстройства или состояния, которое уменьшает тяжесть заболевания, расстройства или состояния, или задерживает или замедляет прогрессирование заболевания, расстройства или состояния. Как правило, «эффективное количество» соединения означает количество, достаточное для достижения желаемого биологического отклика, например, для лечения связанного с ЦНС расстройства, является достаточным, чтобы вызвать анестезию или успокоение. Как будет понятно специалистам с обычной квалификацией в этой области технологии, эффективное количество соединения согласно изобретению может изменяться в зависимости от таких факторов, как желательный биологический конечный результат, фармакокинетика соединения, подлежащее лечению заболевание, способ введения, и возраст, вес, здоровье и состояние субъекта.
[0102] Как применяемое здесь, и если не оговорено иное, «терапевтически эффективное количество» соединения представляет собой количество, достаточное для обеспечения терапевтического эффекта при лечении заболевания, расстройства или состояния, или для задержки или минимизации одного или более симптомов, связанных с заболеванием, расстройством или состоянием. Терапевтически эффективное количество соединения означает количество терапевтического агента, одного или в комбинации с другими видами терапии, которое обеспечивает терапевтический эффект при лечении заболевания, расстройства или состояния. Термин «терапевтически эффективное количество» может включать количество, которое улучшает общую терапию, снижает или позволяет избежать симптомов или причин заболевания или состояния, или повышает терапевтическую эффективность другого терапевтического агента.
[0103] В альтернативном варианте осуществления настоящее изобретение рассматривает введение соединений, или фармацевтически приемлемой соли, или фармацевтически приемлемой композиции его согласно настоящему изобретению, для профилактики, прежде чем субъект начнет страдать от указанных заболевания, расстройства или состояния. Как применяемое здесь, и если не оговорено иное, «профилактически эффективное количество» соединения представляет собой количество, достаточное для предотвращения заболевания, расстройства или состояния, или одного или более симптомов, связанных с заболеванием, расстройством или состоянием, или для предотвращения его рецидива. Профилактически эффективное количество соединения означает количество терапевтического агента, одного или в комбинации с другими агентами, которое обеспечивает профилактический эффект в предотвращении заболевания, расстройства или состояния. Термин «профилактически эффективное количество» может охватывать количество, которое улучшает общую профилактику или усиливает профилактическую эффективность другого профилактического агента.
[0104] Как применяемый здесь, «эпизодический режим дозирования» представляет собой режим дозирования, в котором соединение Формулы (I-X, I-I, II-I, III-I, или III-II) или композиции, включающей соединение Формулы (I-X, I-I, II-I, III-I, или III-II), вводят субъекту в течение ограниченного периода времени в ответ на диагностирование заболевания или его симптома, например, диагноза или симптома депрессии, эпизода большого депрессивного расстройства, биполярной депрессии, беспокойства, или послеродовой депрессии. В некоторых вариантах исполнения большое депрессивное расстройство является умеренным большим депрессивным расстройством. В некоторых вариантах исполнения большое депрессивное расстройство является тяжелым большим депрессивным расстройством. В некоторых вариантах исполнения соединение составляют как индивидуальные дозировки, причем каждая доза включает соединение Формулы (I-X, I-I, II-I, III-I, или III-II) и один или многие фармацевтически приемлемые эксципиенты. В некоторых вариантах исполнения эпизодический режим дозирования имеет продолжительность многих недель, например, около 8 недель. В отличие от хронического введения, как здесь определенного, эпизодическое дозирование соединения проводится на протяжении ограниченного периода времени, например, от около 2 недель до около 8 недель, в ответ на диагностирование заболевания, например, депрессии, или его симптома. В некоторых вариантах исполнения эпизодическое дозирование проводится один раз в день в течение многих недель, например, от около 2 недель до около 6 недель. В одном варианте исполнения эпизодическое дозирование имеет двухнедельную продолжительность. В некоторых вариантах исполнения субъекту прописывают более чем одно эпизодическое дозирование, например, два или более эпизодических дозирования на протяжении жизни субъекта.
Соединения
[0105] Должно быть понятно, что в описываемых здесь формулах могут упоминаться конкретные атомы углерода, такие как С17, С3, С10, и т.д. Эти ссылки основываются на положении атомов углерода согласно номенклатуре стероидов, известной и применяемой в промышленности, как показано ниже:
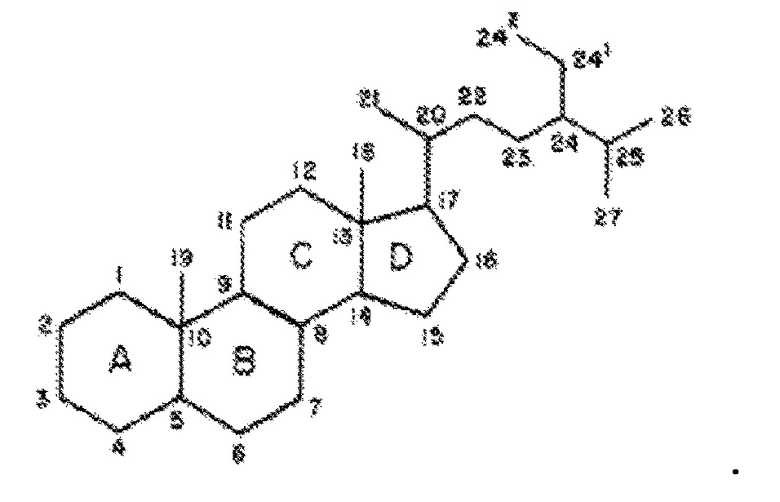
Например, С17 относится к атому углерода в положении 17, и С3 подразумевает атом углерода в положении 3.
[0106] Как здесь описывается, в одном аспекте настоящее изобретение представляет соединения Формулы (I-X):
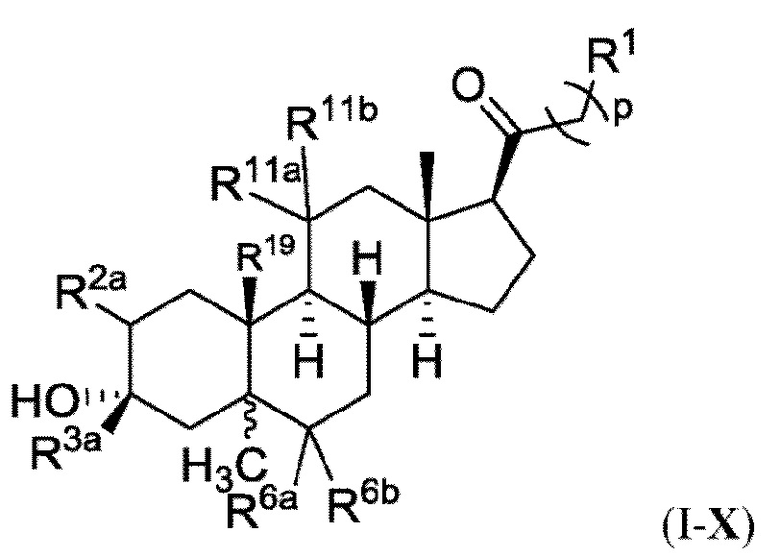
или фармацевтически приемлемые соли их,
в которых: p составляет 0, 1 или 2; R19 представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил; R1 представляет замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил, -SRX1, -N(RX1)2,-OC(=O)RX1, -OC(=O)ORX1, -OC(=O)SRX1, -OC(=O)N(RX1)2, -SC(=O)RX2, -SC(=O)ORX1, -SC(=O)SRX1, -SC(=O)N(RX1)2,-NHC(=O)RX1, -NHC(=O)ORX1, -NHC(=O)SRX1, -NHC(=O)N(RX1)2, -OS(=O)2RX2, -OS(=O)2ORX1, -S-S(=O)2RX2, -S-S(=O)2ORX1, -S(=O)RX2, -SO2RX2, или -S(=O)2ORX1, причем RX1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил, защитную группу для кислорода, когда присоединена к атому кислорода, защитную группу для серы, когда присоединена к атому серы, азотзащитную группу, когда присоединена к атому азота, или две RX1-группы объединены с образованием замещенного или незамещенного гетероциклического или гетероарильного цикла; и RX2, в каждом случае независимо, представляет замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил; R3a представляет замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, или замещенный или незамещенный C3-6-карбоциклил; R2a представляет атом водорода, галоген, замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, или замещенный или незамещенный C3-6-карбоциклил, или -ORA2, причем RA2 представляет атом водорода или замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, или замещенный или незамещенный C3-6-карбоциклил; R11a представляет атом водорода или -ORA3, причем RA3 представляет атом водорода или замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, или замещенный или незамещенный C3-6-карбоциклил, и R11b представляет атом водорода; или R11a и R11b объединены с образованием оксогруппы (=O); и R6a и R6b, в каждом случае независимо, представляют атом водорода или замещенный или незамещенный C1-6-алкил, или галоген.
[0107] Должно быть понятно, что стереохимическая конфигурация при С17 могла бы быть изображена любым из следующих, но эквивалентных путей:
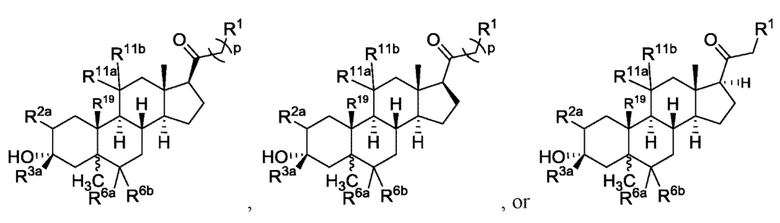
[0108] В определенных вариантах исполнения R19 представляет атом водорода в соединении Формулы (I-X); в определенных вариантах исполнения R19 представляет метил в соединении Формулы (I-X).
[0109] В определенных вариантах исполнения R1 представляет замещенный или незамещенный алкил в соединении Формулы (I-X).
[0110] В определенных вариантах исполнения R1 представляет замещенный или незамещенный гетероарил в соединении Формулы (I-X).
[0111] В определенных вариантах исполнения R1 представляет замещенный или незамещенный гетероарил, причем гетероарил содержит по меньшей мере один атом азота в соединении Формулы (I-X).
[0112] В определенных вариантах исполнения R1 представляет замещенный или незамещенный гетероарил, причем гетероарил является бициклическим в соединении Формулы (I-X).
[0113] В одном аспекте настоящее изобретение представляет соединения незамещенного в положении 19 C3,3-дизамещенного C21-пиразолильного производного Формулы (I-I):
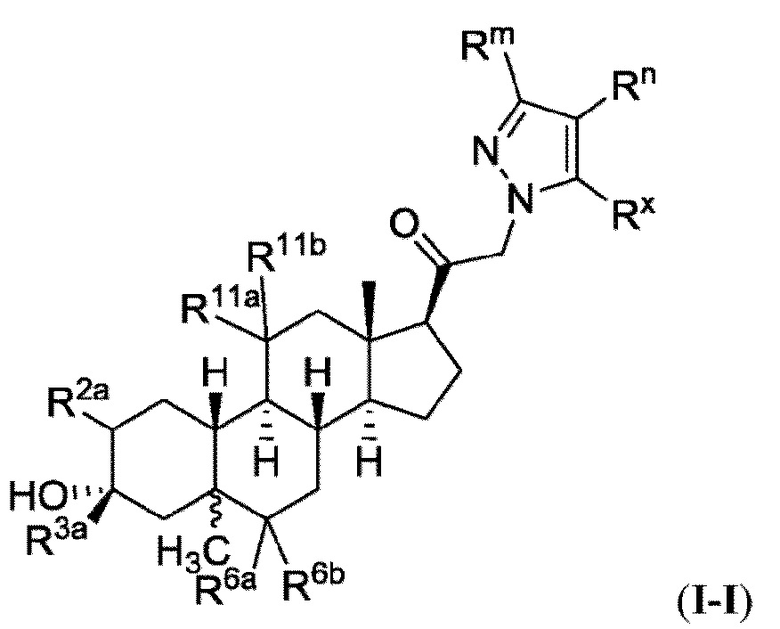
и фармацевтически приемлемую соль его, причем: R3a представляет замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, или замещенный или незамещенный C3-6-карбоциклил; R2a представляет атом водорода, галоген, замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, или замещенный или незамещенный C3-6-карбоциклил, или -ORA2, причем RA2 представляет атом водорода или замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, или замещенный или незамещенный C3-6-карбоциклил; R11a представляет атом водорода или -ORA3, причем RA3 представляет атом водорода или замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, или замещенный или незамещенный C3-6-карбоциклил, и R11b представляет атом водорода; или R11a и R11b объединены с образованием оксогруппы (=O); R6a и R6b, в каждом случае независимо, представляют атом водорода, замещенный или незамещенный C1-6-алкил, или галоген; Rm, Rn, и Rx, в каждом случае независимо, представляет атом водорода, галоген, -NO2, -CN, -ORGA, -N(RGA)2, -C(=O)RGA, -C(=O)ORGA, -OC(=O)RGA, -OC(=O)ORGA, -C(=O)N(RGA)2, -N(RGA)C(=O)RGA, -OC(=O)N(RGA)2, -N(RGA)C(=O)ORGA, -N(RGA)C(=O)N(RGA)2, -SRGA, -S(O)RGA, например,-S(=O)RGA, -S(=O)2RGA, -S(=O)2ORGA, -OS(=O)2RGA, -S(=O)2N(RGA)2, -N(RGA)S(=O)2RGA, замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, или замещенный или незамещенный C3-6-карбоциклил, или замещенный или незамещенный 3-6-членный гетероциклил; и RGA в каждом случае независимо представляет атом водорода, замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, или замещенный или незамещенный C3-6-карбоциклил, или замещенный или незамещенный 3-6-членный гетероциклил, замещенный или незамещенный арил, замещенный или незамещенный гетероарил, защитную группу для кислорода, когда присоединена к атому кислорода, азотзащитную группу, когда присоединена к атому азота; или две RGA-группы связаны общими атомами с образованием замещенного или незамещенного гетероциклического или гетероарильного цикла.
[0114] В определенных вариантах исполнения R3a в незамещенном в положении 19 C3,3-дизамещенном C21-пиразолильном производном Формулы (I-I) представляет C1-6-алкил, необязательно замещенный алкоксигруппой или одним-двумя атомами галогена (например, фтора), или по меньшей мере один из Rm, Rn, и Rx представляет галоген (например, -F, -Cl, -Br), -NO2, -CN, -ORGA, -N(RGA)2, -C(=O)RGA, -C(=O)ORGA, -SRGA, -S(=O) RGA, -S(=O)2RGA, -S(=O)2ORGA, -OS(=O)2RGA, -S(=O)2N(RGA)2, замещенный или незамещенный C1-6-алкил, (например, -CH3, -CH2CH3, галоалкил, например, -CF3), причем RGA представляет замещенный или незамещенный C1-2-алкил.
[0115] На основе приведенного выше описания понятно, что стероиды Формулы (I-I) включают 3,3-дизамещенные незамещенные в положении 19 соединения, в которых А/В-циклическая система соединения имеет цис-конфигурацию (как представлено в Формуле (I-I-A), в которых А/В-циклическая система соединения имеет транс-конфигурацию (как представлено в Формуле (I-I-B):
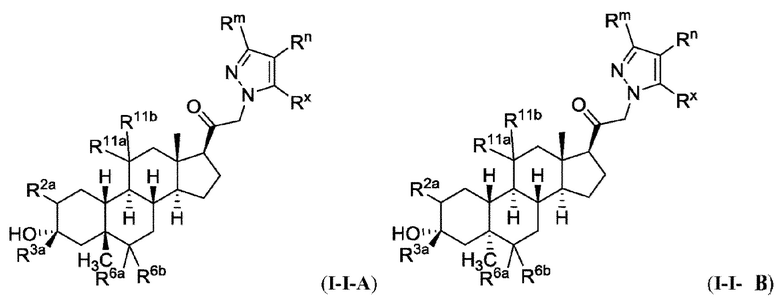
и фармацевтически приемлемые соли их.
Формула ( I-X ) или Формула ( I-I ): группа R 3а
[0116] Как в общих чертах определено здесь, R3a представляет замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, или замещенный или незамещенный C3-6-карбоциклил.
[0117] В определенных вариантах исполнения R3a представляет замещенный или незамещенный C1-6-алкил, например, замещенный или незамещенный C1-2-алкил, замещенный или незамещенный C2-3-алкил, замещенный или незамещенный C3-4-алкил, замещенный или незамещенный C4-5-алкил, или замещенный или незамещенный C5-6-алкил. Примерные R3a как C1-6-алкильные группы включают, но без ограничения этим, замещенный или незамещенный метил (C1), этил (C2), н-пропил (C3), изопропил (C3), н-бутил (C4), трет-бутил (C4), втор-бутил (C4), изобутил (C4), н-пентил (C5), 3-пентил (C5), амил (C5), неопентил (C5), 3-метил-2-бутил (C5), третичный амил (C5), н-гексил (C6), C1-6-алкил, замещенный 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, или более атомами фтора (например, -CF3, -CH2F, -CHF2, дифторэтил, и 2,2,2-трифтор-1,1-диметилэтил), C1-6-алкил, замещенный 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, или более атомами хлора (например, -CH2Cl, -CHCl2), и C1-6-алкил, замещенный алкоксигруппами (например, -CH2OCH3 и -CH2OCH2CH3). В определенных вариантах исполнения R3a представляет замещенный C1-6-алкил, например, R3a представляет галоалкил, алкоксиалкил, или аминоалкил. В определенных вариантах исполнения R3a представляет Me, Et, n-Pr, n-Bu, i-Bu, фторметил, хлорметил, дифторметил, трифторметил, трифторэтил, дифторэтил, 2,2,2-трифтор-1,1-диметилэтил, метоксиметил, метоксиэтил или этоксиметил.
[0118] В определенных вариантах исполнения R3a представляет незамещенный C1-3-алкил, например, R3a представляет -CH3, -CH2CH3, или -CH2CH2CH3.
[0119] В определенных вариантах исполнения R3a представляет C1-6-алкил, замещенный одним или более атомами фтора; например, R3a представляет -CH2F, -CHF2, или -CF3. В определенных вариантах исполнения R3a представляет C1-6-алкил, замещенный одним или двумя атомами фтора; например, R3a представляет -CH2F или -CHF2.
[0120] В определенных вариантах исполнения R3a представляет C1-6-алкил, замещенный одной или более -ORA1-группами, причем RA1 представляет атом водорода или замещенный или незамещенный алкил. В определенных вариантах исполнения R3a представляет -CH2ORA1, например, в котором RA1 представляет атом водорода, -CH3, -CH2CH3, или -CH2CH2CH3, например, для образования группы R3a с формулой -CH2OH, -CH2OCH3, -CH2OCH2CH3, или -CH2OCH2CH2CH3.
[0121] В определенных вариантах исполнения R3a представляет замещенный или незамещенный C2-6-алкенил, например, замещенный или незамещенный C2-3-алкенил, замещенный или незамещенный C3-4-алкенил, замещенный или незамещенный C4-5-алкенил, или замещенный или незамещенный C5-6-алкенил. В определенных вариантах исполнения R3a представляет этенил (C2), пропенил (C3), или бутенил (C4), замещенный или незамещенный одним или более заместителями, выбранными из группы, состоящей из алкила, галогена, галоалкила, алкоксиалкила или гидроксила. В определенных вариантах исполнения R3a представляет этенил, пропенил или бутенил, замещенный или незамещенный алкилом, галогеном, галоалкилом, алкоксиалкилом или гидроксилом. В определенных вариантах исполнения R3a представляет этенил.
[0122] В определенных вариантах исполнения R3a представляет замещенный или незамещенный C2-6-алкинил, например, замещенный или незамещенный C2-3-алкинил, замещенный или незамещенный C3-4-алкинил, замещенный или незамещенный C4-5-алкинил, или замещенный или незамещенный C5-6-алкинил. В определенных вариантах исполнения R3a представляет этинил, пропинил или бутинил, замещенный или незамещенный алкилом, галогеном, галоалкилом (например, CF3), алкоксиалкилом, циклоалкилом (например, циклопропилом или циклобутилом), или гидроксилом. В определенных вариантах исполнения R3a выбирают из группы, состоящей из трифторэтинила, циклопропилэтинила, циклобутилэтинила, и пропинила, фторпропинила и хлорэтинила. В определенных вариантах исполнения R3a представляет этинил (C2), пропинил (C3) или бутинил (C4), замещенный или незамещенный одним или более заместителями, выбранными из группы, состоящей из замещенного или незамещенного арила, замещенного или незамещенного гетероарила, замещенного или незамещенного карбоциклила, и замещенного или незамещенного гетероциклила. В определенных вариантах исполнения R3a представляет этинил (C2), пропинил (C3) или бутинил (C4), замещенный фенилом. В определенных вариантах исполнения фенильный заместитель дополнительно замещен одним или многими заместителями, выбранными из группы, состоящей из галогена, алкила, трифторалкила, алкоксигруппы, ацила, аминогруппы или амидной группы. В определенных вариантах исполнения R3a представляет этинил (C2), пропинил (C3) или бутинил (C4), замещенный замещенным или незамещенным пирролилом, имидазолилом, пиразолилом, оксазолилом, тиазолилом, изоксазолилом, 1,2,3-триазолилом, 1,2,4-триазолилом, оксадиазолилом, тиадиазолилом или тетразолилом.
[0123] В определенных вариантах исполнения R3a представляет этинил, пропинил или бутинил, незамещенный или замещенный алкилом, галогеном, галоалкилом, алкоксиалкилом или гидроксилом. В определенных вариантах исполнения R3a представляет этинил или пропинил, замещенный или незамещенный арилом. В определенных вариантах исполнения R3a представляет этинил или пропинил, замещенный фенилом, незамещенным или замещенным атомом галогена, алкилом, алкоксигруппой, галоалкилом, тригалоалкилом или ацилом. В определенных вариантах исполнения R3a представляет этинил или пропинил, замещенный незамещенным или замещенным карбоциклилом. В определенных вариантах исполнения R11a представляет этинил или пропинил, замещенный фенилом, незамещенным или замещенным циклопропилом, циклобутилом, циклопентилом или циклогексилом. В определенных вариантах исполнения R3a представляет этинил или пропинил, замещенный незамещенным или замещенным гетероарилом. В определенных вариантах исполнения R3a представляет этинил или пропинил, замещенный незамещенным или замещенным пиридинилом или пиримидинилом. В определенных вариантах исполнения R3a представляет этинил или пропинил, замещенный незамещенным или замещенным пирролилом, имидазолилом, пиразолилом, оксазолилом, тиазолилом, изоксазолилом, 1,2,3-триазолилом, 1,2,4-триазолилом, оксадиазолилом, тиадиазолилом, тетразолилом. В определенных вариантах исполнения R3a представляет этинил или пропинил, замещенный незамещенным или замещенным гетероциклилом. В определенных вариантах исполнения R3a представляет этинил или пропинил, замещенный незамещенным или замещенным пирролидинилом, пиперидинилом, пиперазинилом или морфолинилом. В определенных вариантах исполнения R3a представляет пропинил или бутинил, замещенный гидроксильной или алкаксильной группой. В определенных вариантах исполнения R3a представляет пропинил или бутинил, замещенный метоксильной или этоксильной группой. В определенных вариантах исполнения R3a представляет этинил или пропинил, замещенный атомом хлора. В определенных вариантах исполнения R3a представляет этинил или пропинил, замещенный трифторметилом.
[0124] В определенных вариантах исполнения R3a представляет замещенный или незамещенный C3-6-карбоциклил, например, замещенный или незамещенный C3-4-карбоциклил, замещенный или незамещенный C4-5-карбоциклил или замещенный или незамещенный C5-6-карбоциклил. В определенных вариантах исполнения R3a представляет замещенный или незамещенный циклопропил или замещенный или незамещенный циклобутил.
Формула (I-X) или Формула (I-1) группы R2a, R11a, R11b, R6a, и R6b
[0125] Как в общих чертах определено здесь, R2a представляет атом водорода, галоген, замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, замещенный или незамещенный C3-6-карбоциклил, или -ORA2, причем RA2 представляет атом водорода, замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, замещенный или незамещенный C3-6-карбоциклил.
[0126] В определенных вариантах исполнения R2a представляет атом водорода. В определенных вариантах исполнения R2a представляет атом галогена, например, фтора, хлора, брома или иода. В определенных вариантах исполнения R2a представляет фтор или хлор. В определенных вариантах исполнения R2a представляет замещенный или незамещенный C1-6-алкил, например, замещенный или незамещенный C1-2-алкил, замещенный или незамещенный C2-3-алкил, замещенный или незамещенный C3-4-алкил, замещенный или незамещенный C4-5-алкил, или замещенный или незамещенный C5-6-алкил. Например, в некоторых вариантах исполнения R2a представляет C1-6-алкил, необязательно замещенный атомом галогена (например, брома, хлора, фтора (то есть, с образованием группы R2a с формулой -CH2F, -CHF2, -CF3)) или -ORA2. В определенных вариантах исполнения RA2 представляет -CH3, -CH2CH3, или -CH2CH2CH3, то есть, с образованием группы R2a с формулой -OH, -OCH3, -OCH2CH3, или -OCH2CH2CH3. В определенных вариантах исполнения R2a представляет замещенный или незамещенный C2-6-алкенил. В определенных вариантах исполнения R2a представляет замещенный или незамещенный C2-6-алкинил, например, замещенный или незамещенный C2-3-алкинил, замещенный или незамещенный C3-4-алкинил, замещенный или незамещенный C4-5-алкинил, или замещенный или незамещенный C5-6-алкинил. В определенных вариантах исполнения R2a представляет замещенный или незамещенный C3-6-карбоциклил, например, замещенный или незамещенный C3-4-карбоциклил, замещенный или незамещенный C4-5-карбоциклил, или замещенный или незамещенный C5-6-карбоциклил. В определенных вариантах исполнения R2a представляет замещенный или незамещенный циклопропил или замещенный или незамещенный циклобутил. В определенных вариантах исполнения R2a представляет -CH3, -CH2CH3, -CH2CH2CH3, или замещенный или незамещенный циклопропил. В определенных вариантах исполнения R2a представляет -ORA2. В определенных вариантах исполнения RA2 представляет атом водорода. В определенных вариантах исполнения RA2 представляет замещенный или незамещенный алкил, например, замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C1-2-алкил, замещенный или незамещенный C2-3-алкил, замещенный или незамещенный C3-4-алкил, замещенный или незамещенный C4-5-алкил, или замещенный или незамещенный C5-6-алкил. В определенных вариантах исполнения RA2 представляет атом водорода, -CH3, -CH2CH3, или -CH2CH2CH3, то есть, с образованием группы R2a с формулой -OH, -OCH3, -OCH2CH3, или -OCH2CH2CH3. В определенных вариантах исполнения R2a представляет неводородный заместитель в альфа-конфигурации. В определенных вариантах исполнения R2a представляет неводородный заместитель в бета-конфигурации.
[0127] Как в общих чертах определено здесь, R11a представляет атом водорода или -ORA3, причем RA3 представляет атом водорода или замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, замещенный или незамещенный C3-6-карбоциклил, и R11b представляет атом водорода; или R11a и R11b объединены с образованием оксогруппы (=O).
[0128] В определенных вариантах исполнения оба R11a и R11b представляют атом водорода.
[0129] В определенных вариантах исполнения R11a и R11b объединены с образованием оксогруппы (=O).
[0130] В определенных вариантах исполнения R11a представляет -ORA3, и R11b представляет атом водорода. В определенных вариантах исполнения, в которых R11a представляет -ORA3, R11a находится в альфа- или бета-конфигурации. В определенных вариантах исполнения, в которых R11a представляет -ORA3, R11a находится в альфа-конфигурации. В определенных вариантах исполнения, в которых R11a представляет -ORA3, R11a находится в бета-конфигурации. В определенных вариантах исполнения, RA3 представляет атом водорода. В определенных вариантах исполнения RA3 представляет замещенный или незамещенный C1-6-алкил,, например, замещенный или незамещенный C1-2-алкил, замещенный или незамещенный C2-3-алкил, замещенный или незамещенный C3-4-алкил, замещенный или незамещенный C4-5-алкил, или замещенный или незамещенный C5-6-алкил. В определенных вариантах исполнения RA3 представляет атом водорода, -CH3, -CH2CH3, или -CH2CH2CH3, то есть, для образования группы R11a с формулой -OH, -OCH3, -OCH2CH3, или -OCH2CH2CH3.
[0131] Как в общих чертах определено здесь, R6a и R6b в каждом случае независимо представляет атом водорода, замещенный или незамещенный C1-6-алкил, или галоген.
Формула (I-X) группа p
[0132] В некоторых вариантах исполнения p составляет 0, 1, или 2. В некоторых вариантах исполнения p составляет 0. В некоторых вариантах исполнения p составляет 1. В некоторых вариантах исполнения p составляет 2.
Формула (I-1) группы Rm, Rn, и Rx
[0133] Как в общих чертах определено здесь, Rm, Rn, и Rx, в каждом случае независимо, представляет атом водорода, галоген, -NO2, -CN, -ORGA, -N(RGA)2, -C(=O)RGA, -C(=O)ORGA, -OC(=O)RGA, -OC(=O)ORGA, -C(=O)N(RGA)2, -N(RGA)C(=O)RGA, -OC(=O)N(RGA)2, -N(RGA)C(=O)ORGA, -N(RGA)C(=O)N(RGA)2, -SRGA, -S(O)RGA, например, S(=O)RGA, -S(=O)2RGA, -S(=O)2ORGA, -OS(=O)2RGA, -S(=O)2N(RGA)2, -N(RGA)S(=O)2RGA, замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, замещенный или незамещенный C3-6-карбоциклил, или замещенный или незамещенный 3-6-членный гетероциклил.
[0134] Кроме того, как в общих чертах определено здесь, RGA, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, замещенный или незамещенный C3-6-карбоциклил, или замещенный или незамещенный 3-6-членный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил, защитную группу для кислорода, когда присоединена к атому кислорода, азотзащитную группу, когда присоединена к атому азота, или две RGA-группы связаны общими атомами с образованием замещенного или незамещенного гетероциклического или гетероарильного цикла. В определенных вариантах исполнения RGA, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный C1-6-алкил (например, замещенный или незамещенный C1-2-алкил, замещенный или незамещенный C2-3-алкил, замещенный или незамещенный C3-4-алкил, замещенный или незамещенный C4-5-алкил, или замещенный или незамещенный C5-6-алкил), замещенный или незамещенный арил, или замещенный или незамещенный гетероарил. В определенных вариантах исполнения RGA, в каждом случае независимо, представляет атом водорода, -CH3, -CH2CH3, или замещенный или незамещенный фенил.
[0135] В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет атом водорода. В определенных вариантах исполнения по меньшей мере два из Rm, Rn, и Rx представляют атом водорода. В определенных вариантах исполнения все из Rm, Rn, и Rx представляют атом водорода с образованием незамещенного пиразолила.
[0136] В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет неводородный заместитель. Как применяемый здесь, Rm, Rn, и Rx как «неводородный заместитель» означает, что Rm, Rn, и Rx не являются атомами водорода, но представляют любой из галогена, -NO2, -CN, -CF3, -ORGA, -N(RGA)2, -C(=O)RGA, -C(=O)ORGA, -OC(=O)RGA, -OC(=O)ORGA, -C(=O)N(RGA)2, -N(RGA)C(=O)RGA, -OC(=O)N(RGA)2, -N(RGA)C(=O)ORGA, -SRGA, -S(O)RGA, например, S(=O)RGA, -S(=O)2RGA, -S(=O)2ORGA, -OS(=O)2RGA, -S(=O)2N(RGA)2, или -N(RGA)S(=O)2RGA; замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, замещенный или незамещенный C3-6-карбоциклил, замещенный или незамещенный 3-6-членный гетероциклил.
[0137] В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет атом галогена, например, фтора, брома, иода или хлора. В определенных вариантах исполнения один из Rm, Rn, и Rx представляет атом галогена. В определенных вариантах исполнения Rm представляет атом галогена, например, фтора, брома, иода или хлора. В определенных вариантах исполнения Rn представляет атом галогена, например, фтора, брома, иода или хлора. В определенных вариантах исполнения Rx представляет атом галогена, например, фтора, брома, иода или хлора.
[0138] В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет -NO2. В определенных вариантах исполнения один из Rm, Rn, и Rx представляет -NO2. В определенных вариантах исполнения Rm представляет -NO2. В определенных вариантах исполнения Rn представляет -NO2. В определенных вариантах исполнения Rx представляет -NO2.
[0139] В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет -CN. В определенных вариантах исполнения один из Rm, Rn, и Rx представляет -CN. В определенных вариантах исполнения Rm представляет -CN. В определенных вариантах исполнения Rn представляет -CN. В определенных вариантах исполнения Rx представляет -CN.
[0140] В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет -ORGA, например, причем RGA представляет атом водорода или замещенный или незамещенный C1-6-алкил (например, -CH3 или -CF3). В определенных вариантах исполнения один из Rm, Rn, и Rx представляет -ORGA, например, -OH, -OCH3, или -OCF3. В определенных вариантах исполнения Rm представляет -ORGA, например, -OH, -OCH3, или -OCF3. В определенных вариантах исполнения Rn представляет -ORGA. В определенных вариантах исполнения Rx представляет -ORGA, например, -OH, -OCH3, или -OCF3.
[0141] В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет -N(RGA)2, например, причем RGA представляет атом водорода или замещенный или незамещенный C1-6-алкил (например, -CH3 или -CF3). В определенных вариантах исполнения один из Rm, Rn, и Rx представляет -N(RGA)2, e.g., -NH2, -NHCH3, или -N(CH3)2. В определенных вариантах исполнения Rm представляет -N(RGA)2, например, -NH2, -NHCH3, или -N(CH3)2. В определенных вариантах исполнения Rn представляет -N(RGA)2, например, -NH2, -NHCH3, или -N(CH3)2. В определенных вариантах исполнения Rx представляет -N(RGA)2, например, -NH2, -NHCH3, или -N(CH3)2.
[0142] В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет -C(=O)RGA, -C(=O)ORGA, или -C(=O)N(RGA)2, например, в которых RGA представляет атом водорода или замещенный или незамещенный C1-6-алкил (например, -CH3 или -CF3). В определенных вариантах исполнения один из Rm, Rn, и Rx представляет -C(=O)RGA, например, -CHO, -C(=O)CH3, или -C(=O)CH2CH3. В определенных вариантах исполнения Rm представляет -C(=O)RGA, например, -CHO, -C(=O)CH3, или -C(=O)CH2CH3. В определенных вариантах исполнения Rn представляет -C(=O)RGA, например, -CHO, -C(=O)CH3, или -C(=O)CH2CH3. В определенных вариантах исполнения Rx представляет -C(=O)RGA, например, -CHO, -C(=O)CH3, или -C(=O)CH2CH3. В определенных вариантах исполнения один из Rm, Rn, и Rx представляет -C(=O)ORGA, например, -C(=O)OH, -C(=O)OCH3, или -C(=O)OCH2CH3. В определенных вариантах исполнения Rm представляет -C(=O)ORGA, например, -C(=O)OH, -C(=O)OCH3, или -C(=O)OCH2CH3. В определенных вариантах исполнения Rn представляет -C(=O)ORGA, например, -C(=O)OH, -C(=O)OCH3, или -C(=O)OCH2CH3. В определенных вариантах исполнения Rx представляет -C(=O)ORGA, например, -C(=O)OH, -C(=O)OCH3, или -C(=O)OCH2CH3. В определенных вариантах исполнения один из Rm, Rn, и Rx представляет -C(=O)N(RGA)2, например, -C(=O)NH2, -C(=O)NHCH3, или -C(=O)N(CH3)2. В определенных вариантах исполнения Rm представляет -C(=O)N(RGA)2, например, -C(=O)NH2, -C(=O)NHCH3, или -C(=O)N(CH3)2. В определенных вариантах исполнения Rn представляет -C(=O)N(RGA)2, например, -C(=O)NH2, -C(=O)NHCH3, или -C(=O)N(CH3)2. В определенных вариантах исполнения Rx представляет -C(=O)N(RGA)2, например, -C(=O)NH2, -C(=O)NHCH3, или -C(=O)N(CH3)2.
[0143] В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет -OC(=O)RGA, -OC(=O)ORGA, или -OC(=O)N(RGA)2, например, в которых RGA представляет атом водорода или замещенный или незамещенный C1-6-алкил (например, -CH3 или -CF3). В определенных вариантах исполнения один из Rm, Rn, и Rx представляет -OC(=O)RGA, например, -OC(=O)CH3. В определенных вариантах исполнения Rm представляет -OC(=O)RGA, например, -OC(=O)CH3. В определенных вариантах исполнения Rn представляет -OC(=O)RGA, например, -OC(=O)CH3. В определенных вариантах исполнения Rx представляет -OC(=O)RGA, например, -OC(=O)CH3. В определенных вариантах исполнения один из Rm, Rn, и Rx представляет -OC(=O)ORGA, например, -OC(=O)OCH3. В определенных вариантах исполнения Rm представляет -OC(=O)ORGA, например, -OC(=O)OCH3. В определенных вариантах исполнения Rn представляет -OC(=O)ORGA, например, -OC(=O)OCH3. В определенных вариантах исполнения Rx представляет -OC(=O)ORGA, например, -OC(=O)OCH3. В определенных вариантах исполнения один из Rm, Rn, и Rx представляет -OC(=O)N(RGA)2, например, -OC(=O)NHCH3 или -OC(=O)N(CH3)2. В определенных вариантах исполнения Rm представляет -OC(=O)N(RGA)2, например, -OC(=O)NHCH3 или -OC(=O)N(CH3)2. В определенных вариантах исполнения Rn представляет -OC(=O)N(RGA)2, например, -OC(=O)NHCH3 или -OC(=O)N(CH3)2. В определенных вариантах исполнения Rx представляет -OC(=O)N(RGA)2, например, -OC(=O)NHCH3 или -OC(=O)N(CH3)2.
[0144] В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет -N(RGA)C(=O)RGA, -N(RGA)C(=O)ORGA, или -N(RGA)C(=O)N(RGA)2, например, в которых RGA представляет атом водорода или замещенный или незамещенный C1-6-алкил (например, -CH3 или -CF3). В определенных вариантах исполнения один из Rm, Rn, и Rx представляет -N(RGA)C(=O)RGA, например, -NHC(=O)CH3. В определенных вариантах исполнения Rm представляет -N(RGA)C(=O)RGA, например, -NHC(=O)CH3. В определенных вариантах исполнения Rn представляет -N(RGA)C(=O)RGA, например, -NHC(=O)CH3. В определенных вариантах исполнения Rx представляет -N(RGA)C(=O)RGA, например, -NHC(=O)CH3. В определенных вариантах исполнения один из Rm, Rn, и Rx представляет -N(RGA)C(=O)ORGA, например, -NHC(=O)OCH3. В определенных вариантах исполнения Rm представляет -N(RGA)C(=O)ORGA, например, -NHC(=O)OCH3. В определенных вариантах исполнения Rn представляет -N(RGA)C(=O)ORGA, например, -NHC(=O)OCH3. В определенных вариантах исполнения Rx представляет -N(RGA)C(=O)ORGA, например, -NHC(=O)OCH3. В определенных вариантах исполнения один из Rm, Rn, и Rx представляет -N(RGA)C(=O)N(RGA)2, например, -NHC(=O)NH2 или -NHC(=O)N(CH3)2. В определенных вариантах исполнения Rm представляет -N(RGA)C(=O)N(RGA)2, например, -NHC(=O)NH2 или -NHC(=O)N(CH3)2. В определенных вариантах исполнения Rn представляет -N(RGA)C(=O)N(RGA)2, например, -NHC(=O)NH2 или -NHC(=O)N(CH3)2. В определенных вариантах исполнения Rx представляет -N(RGA)C(=O)N(RGA)2, например, -NHC(=O)NH2 или -NHC(=O)N(CH3)2.
[0145] В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет -SRGA, -S(O)RGA, например, -S(=O)RGA, -S(=O)2RGA, -S(=O)2ORGA, -OS(=O)2RGA, -S(=O)2N(RGA)2, или -N(RGA)S(=O)2RGA, например, в которых RGA представляет атом водорода, замещенный или незамещенный C1-6-алкил (например, -CH3 или -CF3), замещенный или незамещенный арил, или замещенный или незамещенный гетероарил. В определенных вариантах исполнения один из Rm, Rn, и Rx представляет -SRGA, например, -SCH3, или -S-Арил, в которых Арил представляет замещенный или незамещенный арил или гетероарил. В определенных вариантах исполнения один из Rm, Rn, и Rx представляет -S(O)RGA, например, -S(=O)RGA, например,-S(=O)CH3, -S(=O)CF3, или -S(=O)-Арил, в которых Арил представляет замещенный или незамещенный арил или гетероарил. В определенных вариантах исполнения один из Rm, Rn, и Rx представляет -S(=O)2RGA, например, -S(=O)2CH3, -S(=O)2CF3, или -S(=O)2-Арил, в которых Арил представляет замещенный или незамещенный арил или гетероарил. В определенных вариантах исполнения Rm представляет -SRGA, например, -SCH3, -SCF3; -S(O)RGA, например, -S(=O)RGA, например, -S(=O)CH3, -S(=O)CF3; -S(=O)2RGA, например, -S(=O)2CH3, -S(=O)2CF3, или -S(=O)2-Арил, в которых Арил представляет замещенный или незамещенный арил или гетероарил. В определенных вариантах исполнения Rn представляет -SRGA, например, -SCH3, -SCF3; -S(O)RGA, например, -S(=O)RGA, например, -S(=O)CH3, -S(=O)CF3; -S(=O)2RGA, например, -S(=O)2CH3, -S(=O)2CF3, или -S(=O)2-Арил, в которых Арил представляет замещенный или незамещенный арил или гетероарил. В определенных вариантах исполнения Rx представляет -SRGA, например, -SCH3, -SCF3; -S(O)RGA, например, S(=O)RGA, например, -S(=O)CH3, -S(=O)CF3; -S(=O)2RGA, например, -S(=O)2CH3, -S(=O)2CF3, или -S(=O)2-Арил, в которых Арил представляет замещенный или незамещенный арил или гетероарил. В определенных вариантах исполнения один из Rm, Rn, и Rx представляет -S(=O)2ORGA. В определенных вариантах исполнения Rm представляет -S(=O)2ORGA, например, -S(=O)2OCH3, -S(=O)2OCF3, или -S(=O)2OАрил, в которых Арил представляет замещенный или незамещенный арил или гетероарил. В определенных вариантах исполнения Rn представляет -S(=O)2ORGA, например, -S(=O)2OCH3, -S(=O)2OCF3, или -S(=O)2OАрил, в которых Арил представляет замещенный или незамещенный арил или гетероарил. В определенных вариантах исполнения Rx представляет -S(=O)2ORGA, например, -S(=O)2OCH3, -S(=O)2OCF3, или -S(=O)2OАрил, в которых Арил представляет замещенный или незамещенный арил или гетероарил. В определенных вариантах исполнения один из Rm, Rn, и Rx представляет -OS(=O)2RGA. В определенных вариантах исполнения Rm представляет -OS(=O)2RGA, например, -OS(=O)2CH3, -OS(=O)2CF3, или -OS(=O)2-Арил, в которых Арил представляет замещенный или незамещенный арил или гетероарил. В определенных вариантах исполнения Rn представляет -OS(=O)2RGA, например, -OS(=O)2CH3, -OS(=O)2CF3, или -OS(=O)2-Арил, в которых Арил представляет замещенный или незамещенный арил или гетероарил. В определенных вариантах исполнения Rx представляет -OS(=O)2RGA, например, -OS(=O)2CH3, -OS(=O)2CF3, или -OS(=O)2-Арил, в которых Арил представляет замещенный или незамещенный арил или гетероарил. В определенных вариантах исполнения один из Rm, Rn, и Rx представляет -S(=O)2N(RGA)2. В определенных вариантах исполнения Rm представляет -S(=O)2N(RGA)2, например, -S(=O)2NHCH3, -S(=O)2NHCF3, или -S(=O)2-NH-Арил, в которых Арил представляет замещенный или незамещенный арил или гетероарил. В определенных вариантах исполнения Rn представляет -S(=O)2N(RGA)2, например, -S(=O)2NHCH3, -S(=O)2NHCF3, или -S(=O)2-NH-Арил, в которых Арил представляет замещенный или незамещенный арил или гетероарил. В определенных вариантах исполнения Rx представляет -S(=O)2N(RGA)2, например, -S(=O)2NHCH3, -S(=O)2NHCF3, или -S(=O)2-NH-Арил, в которых Арил представляет замещенный или незамещенный арил или гетероарил. В определенных вариантах исполнения один из Rm, Rn, и Rx представляет -N(RGA)S(=O)2RGA. В определенных вариантах исполнения Rm представляет -N(RGA)S(=O)2RGA, например, -NHS(=O)2CH3, -NHS(=O)2CF3, или -NHS(=O)2-Арил, в которых Арил представляет замещенный или незамещенный арил или гетероарил. В определенных вариантах исполнения Rn представляет -N(RGA)S(=O)2RGA, например, -NHS(=O)2CH3, -NHS(=O)2CF3, или -NHS(=O)2-Арил, в которых Арил представляет замещенный или незамещенный арил или гетероарил. В определенных вариантах исполнения Rx представляет -N(RGA)S(=O)2RGA, например, -NHS(=O)2CH3, -NHS(=O)2CF3, или -NHS(=O)2-Арил, в которых Арил представляет замещенный или незамещенный арил или гетероарил.
[0146] В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет замещенный или незамещенный C1-6-алкил, например, замещенный или незамещенный C1-2-алкил, замещенный или незамещенный C2-3-алкил, замещенный или незамещенный C3-4-алкил, замещенный или незамещенный C4-5-алкил, или замещенный или незамещенный C5-6-алкил. Примерные C1-2-алкильные группы включают, но без ограничения этим, замещенный или незамещенный метил (C1), этил (C2), н-пропил (C3), изопропил (C3), н-бутил (C4), трет-бутил (C4), втор-бутил (C4), изобутил (C4), н-пентил (C5), 3-пентил (C5), амил (C5), неопентил (C5), 3-метил-2-бутил (C5), третичный амил (C5), н-гексил (C6), C1-6-алкил, замещенный 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, или более атомами фтора (например, -CF3, -CH2F, -CHF2, дифторэтил, и 2,2,2-трифтор-1,1-диметилэтил), C1-6-алкил, замещенный 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, или более атомами хлора (например, -CH2Cl, -CHCl2), и C1-6-алкил, замещенный алкоксигруппами (например, -CH2OCH3 и -CH2OCH2CH3). В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет замещенный C1-6-алкил,, например, по меньшей мере один из Rm, Rn, и Rx представляет галоалкил, алкоксиалкил или аминоалкил. В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет Me, Et, n-Pr, n-Bu, i-Bu, фторметил, хлорметил, дифторметил, трифторметил, трифторэтил, дифторэтил, 2,2,2-трифтор-1,1-диметилэтил, метоксиметил, метоксиэтил или этоксиметил.
[0147] В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет замещенный или незамещенный C2-6-алкенил, например, замещенный или незамещенный C2-3-алкенил, замещенный или незамещенный C3-4-алкенил, замещенный или незамещенный C4-5-алкенил, или замещенный или незамещенный C5-6-алкенил. В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет этенил (C2), пропенил (C3), или бутенил (C4), незамещенный или замещенный одним или более заместителями, выбранными из группы, состоящей из алкила, атома галогена, галоалкила, алкоксиалкила или гидроксила. В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет этенил, пропенил или бутенил, незамещенный или замещенный алкилом, галогеном, галоалкилом, алкоксиалкилом или гидроксилом.
[0148] В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет замещенный или незамещенный C2-6-алкинил, например, замещенный или незамещенный C2-3-алкинил, замещенный или незамещенный C3-4-алкинил, замещенный или незамещенный C4-5-алкинил, или замещенный или незамещенный C5-6-алкинил. В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет этинил, пропинил или бутинил, незамещенный или замещенный алкилом, галогеном, галоалкилом (например, CF3), алкоксиалкилом, циклоалкилом (например, циклопропилом или циклобутилом), или гидроксилом.
[0149] В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет замещенный или незамещенный C3-6-карбоциклил, например, замещенный или незамещенный C3-4-карбоциклил, замещенный или незамещенный C4-5-карбоциклил, или замещенный или незамещенный C5-6-карбоциклил. В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет замещенный или незамещенный циклопропил или замещенный или незамещенный циклобутил.
[0150] В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет замещенный или незамещенный 3-6-членный гетероциклил, например, замещенный или незамещенный 3-4-членный гетероциклил, замещенный или незамещенный 4-5-членный гетероциклил, или замещенный или незамещенный 5-6-членный гетероциклил.
[0151] В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет замещенный или незамещенный C1-2-алкил (например, -CH3, -CF3), -CO2RGA, -C(=O)RGA, -CN, -NO2, или галоген, причем RGA представляет замещенный или незамещенный C1-2-алкил (например, -CH3, -CF3).
[0152] Примерные комбинации Rm, Rn, и Rx как неводородных заместителей рассматриваются здесь.
[0153] Например, в определенных вариантах исполнения С21-пиразолил формулы
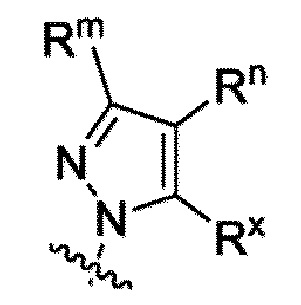
представляет собой монозамещенный пиразолильный цикл формулы
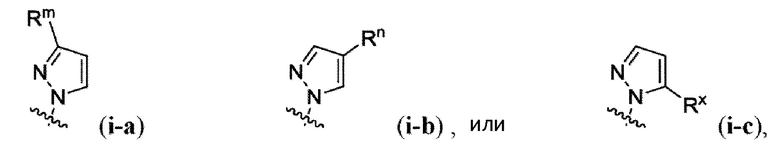
в котором каждый из Rm, Rn, и Rx является неводородным заместителем, как здесь определенным.
[0154] В определенных вариантах исполнения С21-пиразолил формулы
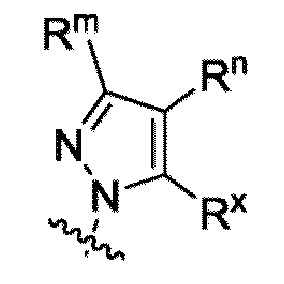
представляет собой дизамещенный пиразолильный цикл формулы
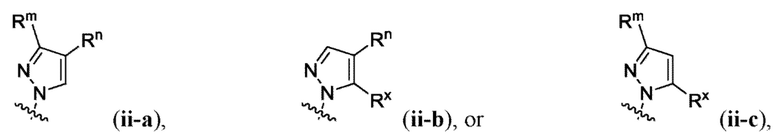
в котором каждый из Rm, Rn, и Rx является неводородным заместителем, как здесь определенным.
[0155] В определенных вариантах исполнения С21-пиразолил формулы
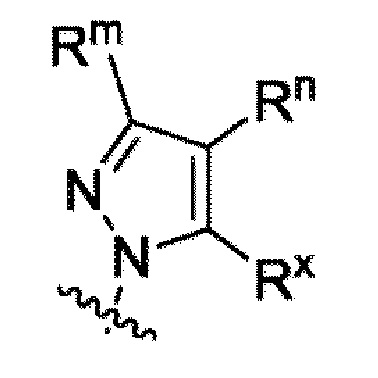
представляет собой тризамещенный пиразолильный цикл, в котором Rm, Rn, и Rx в каждом случае являются неводородными заместителями, как здесь определенными.
[0156] Например, в определенных вариантах исполнения, в которых R2a представляет атом водорода или неводородный альфа-заместитель, представлен стероид Формулы (I-I-A1) или (I-I-B1):
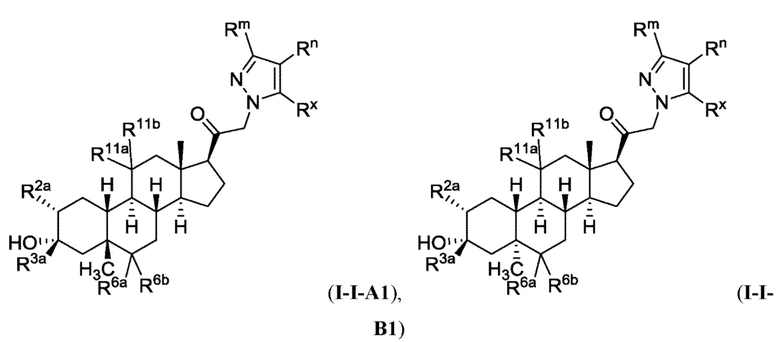
или фармацевтически приемлемая соль его. В определенных вариантах исполнения R3a представляет -CH3, -CH2CH3, -CH2F, -CHF2, -CF3, -CH2OCH3, или замещенный или незамещенный циклопропил. В определенных вариантах исполнения R2a представляет -OH, -OCH3, -OCH2CH3, -OCH2CH2CH3, -CH3, -CH2CH3, -CH2CH2CH3, замещенный или незамещенный циклопропил, атом фтора или хлора. В определенных вариантах исполнения оба R11a и R11b представляют атом водорода. В определенных вариантах исполнения R11a и R11b объединены с образованием =O (оксогруппы). В определенных вариантах исполнения, в которых Цикл B включает двойную C5-C6-связь, R6a представляет атом водорода, атом фтора, -CH3, или -CF3. В определенных вариантах исполнения, в которых Цикл B не содержит двойную C5-C6-связь, оба из R6a и R6b представляют атом водорода. В определенных вариантах исполнения, в которых Цикл B содержит двойную C5-C6-связь, оба из R6a и R6b представляют -CH3 или -CF3. В определенных вариантах исполнения, в которых Цикл B не содержит двойную C5-C6-связь, оба из R6a и R6b представляют фтор. В определенных вариантах исполнения, в которых Цикл B не содержит двойную C5-C6-связь, R6a представляет неводородный заместитель, и R6b представляет атом водорода. В определенных вариантах исполнения C21-пиразолильный цикл представляет собой монозамещенный пиразолил. В определенных вариантах исполнения C21-пиразолильный цикл представляет собой дизамещенный пиразолил. В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет замещенный или незамещенный C1-2-алкил (например, -CH3, -CF3), -CO2RGA, -C(=O)RGA, -CN, -NO2, или галоген, причем RGA представляет замещенный или незамещенный C1-2-алкил (например, -CH3, -CF3). В определенных вариантах исполнения C21-пиразолильный цикл представляет собой незамещенный пиразолил, в котором в каждом случае Rm, Rn, и Rx представляет атом водорода.
[0157] В определенных вариантах исполнения, в которых R2a представляет атом водорода или неводородный бета-заместитель, представлен стероид Формулы (I-I-A2) или (I-I-B2):
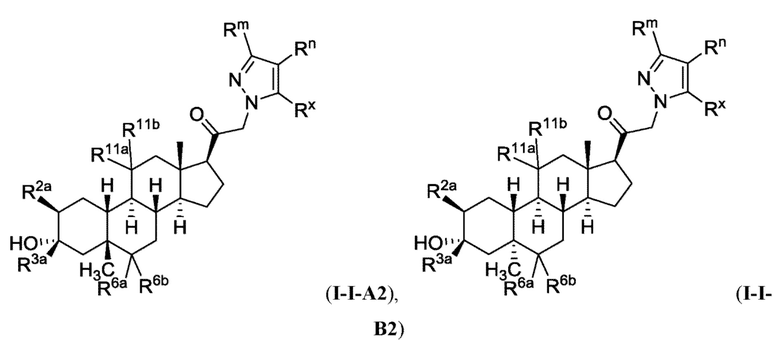
или фармацевтически приемлемая соль его. В определенных вариантах исполнения R3a представляет -CH3, -CH2CH3, -CH2F, -CHF2, -CF3, -CH2OCH3, или замещенный или незамещенный циклопропил. В определенных вариантах исполнения R2a представляет -OH, -OCH3, -OCH2CH3, -OCH2CH2CH3, -CH3, -CH2CH3, -CH2CH2CH3, замещенный или незамещенный циклопропил, атом фтора или хлора. В определенных вариантах исполнения оба R11a и R11b представляют атом водорода. В определенных вариантах исполнения R11a и R11b объединены с образованием =O (оксогруппы). В определенных вариантах исполнения, в которых Цикл B включает двойную C5-C6-связь, R6a представляет атом водорода, атом фтора, -CH3, или -CF3. В определенных вариантах исполнения, в которых Цикл B не содержит двойную C5-C6-связь, оба из R6a и R6b представляют атом водорода. В определенных вариантах исполнения, в которых Цикл B не содержит двойную C5-C6-связь, оба из R6a и R6b представляют -CH3 или -CF3. В определенных вариантах исполнения, в которых Цикл B не содержит двойную C5-C6-связь, оба из R6a и R6b представляют фтор. В определенных вариантах исполнения, в которых Цикл B не содержит двойную C5-C6-связь, R6a представляет неводородный заместитель, и R6b представляет атом водорода. В определенных вариантах исполнения C21-пиразолильный цикл представляет собой монозамещенный пиразолил. В определенных вариантах исполнения C21-пиразолильный цикл представляет собой дизамещенный пиразолил. В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет замещенный или незамещенный C1-2-алкил (например, -CH3, -CF3), -CO2RGA, -C(=O)RGA, -CN, -NO2, или галоген, причем RGA представляет замещенный или незамещенный C1-2-алкил (например, -CH3, -CF3). В определенных вариантах исполнения C21-пиразолильный цикл представляет собой незамещенный пиразолил, в котором в каждом случае Rm, Rn, и Rx представляет атом водорода.
[0158] В определенных вариантах исполнения, в которых R11a представляет атом водорода или неводородный альфа-заместитель, и R11b представляет атом водорода, представлен стероид Формулы (I-I-A3) или (I-I-B3):
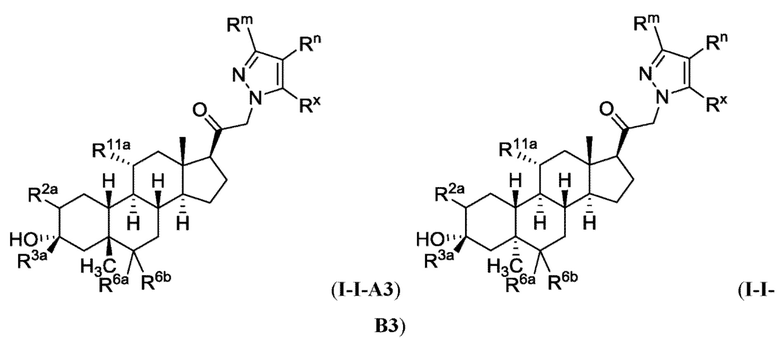
или фармацевтически приемлемая соль его. В определенных вариантах исполнения R3a представляет -CH3, -CH2CH3, -CH2F, -CHF2, -CF3, -CH2OCH3, или замещенный или незамещенный циклопропил. В определенных вариантах исполнения R2a представляет -OH, -OCH3, -OCH2CH3, -OCH2CH2CH3, -CH3, -CH2CH3, -CH2CH2CH3, замещенный или незамещенный циклопропил, атом фтора или хлора. В определенных вариантах исполнения R2a представляет неводородный заместитель в альфа-конфигурации. В определенных вариантах исполнения R2a представляет неводородный заместитель в бета-конфигурации. В определенных вариантах исполнения, в которых Цикл B включает двойную C5-C6-связь, R6a представляет атом водорода, атом фтора, -CH3, или -CF3. В определенных вариантах исполнения, в которых Цикл B не содержит двойную C5-C6-связь, оба из R6a и R6b представляют атом водорода. В определенных вариантах исполнения, в которых Цикл B не содержит двойную C5-C6-связь, оба из R6a и R6b представляют -CH3 или -CF3. В определенных вариантах исполнения, в которых Цикл B не содержит двойную C5-C6-связь, оба из R6a и R6b представляют фтор. В определенных вариантах исполнения, в которых Цикл B не содержит двойную C5-C6-связь, R6a представляет неводородный заместитель, и R6b представляет атом водорода. В определенных вариантах исполнения C21-пиразолильный цикл представляет собой монозамещенный пиразолил. В определенных вариантах исполнения C21-пиразолильный цикл представляет собой дизамещенный пиразолил. В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет замещенный или незамещенный C1-2-алкил (например, -CH3, -CF3), -CO2RGA, -C(=O)RGA, -CN, -NO2, или галоген, причем RGA представляет замещенный или незамещенный C1-2-алкил (например, -CH3, -CF3). В определенных вариантах исполнения C21-пиразолильный цикл представляет собой незамещенный пиразолил, в котором в каждом случае Rm, Rn, и Rx представляет атом водорода.
[0159] В определенных вариантах исполнения, в которых R11a представляет атом водорода или неводородный бета-заместитель, и R11b представляет атом водорода, представлен стероид Формулы (I-I-A4) или (I-I-B4):
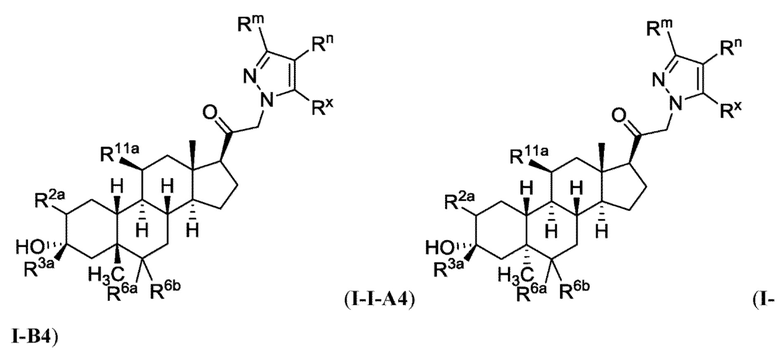
или фармацевтически приемлемая соль его. В определенных вариантах исполнения R3a представляет -CH3, -CH2CH3, -CH2F, -CHF2, -CF3, -CH2OCH3, или замещенный или незамещенный циклопропил. В определенных вариантах исполнения R2a представляет -OH, -OCH3, -OCH2CH3, -OCH2CH2CH3, -CH3, -CH2CH3, -CH2CH2CH3, замещенный или незамещенный циклопропил, атом фтора или хлора. В определенных вариантах исполнения R2a представляет неводородный заместитель в альфа-конфигурации. В определенных вариантах исполнения R2a представляет неводородный заместитель в бета-конфигурации. В определенных вариантах исполнения, в которых Цикл B включает двойную C5-C6-связь, R6a представляет атом водорода, атом фтора, -CH3, или -CF3. В определенных вариантах исполнения, в которых Цикл B не содержит двойную C5-C6-связь, оба из R6a и R6b представляют атом водорода. В определенных вариантах исполнения, в которых Цикл B не содержит двойную C5-C6-связь, оба из R6a и R6b представляют -CH3 или -CF3 В определенных вариантах исполнения, в которых Цикл B не содержит двойную C5-C6-связь, оба из R6a и R6b представляют фтор. В определенных вариантах исполнения, в которых Цикл B не содержит двойную C5-C6-связь, R6a представляет неводородный заместитель, и R6b представляет атом водорода. В определенных вариантах исполнения C21-пиразолильный цикл представляет собой монозамещенный пиразолил. В определенных вариантах исполнения C21-пиразолильный цикл представляет собой дизамещенный пиразолил. В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет замещенный или незамещенный C1-2-алкил (например, -CH3, -CF3), -CO2RGA, -C(=O)RGA, -CN, -NO2, или галоген, причем RGA представляет замещенный или незамещенный C1-2-алкил (например, -CH3, -CF3). В определенных вариантах исполнения C21-пиразолильный цикл представляет собой незамещенный пиразолил, в котором в каждом случае Rm, Rn, и Rx представляет атом водорода.
[0160] В определенных вариантах исполнения, в которых R11a и R11b объединены с образованием оксогруппы, представлен стероид Формулы (I-I-A5) или (I-I-B5):
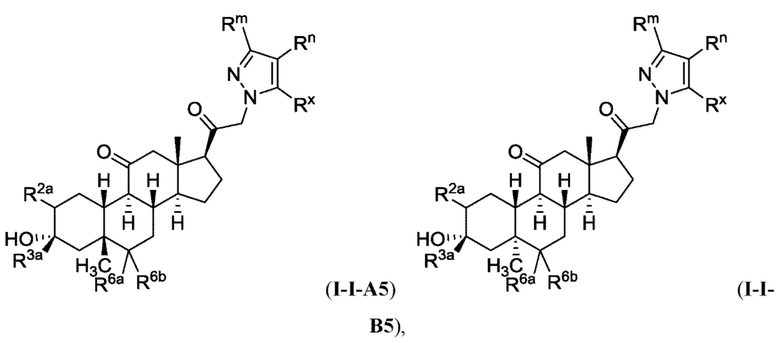
или фармацевтически приемлемая соль его. В определенных вариантах исполнения R3a представляет -CH3, -CH2CH3, -CH2F, -CHF2, -CF3, -CH2OCH3, или замещенный или незамещенный циклопропил. В определенных вариантах исполнения R2a представляет -OH, -OCH3, -OCH2CH3, -OCH2CH2CH3, -CH3, -CH2CH3, -CH2CH2CH3, замещенный или незамещенный циклопропил, атом фтора или хлора. В определенных вариантах исполнения R2a представляет неводородный заместитель в альфа-конфигурации. В определенных вариантах исполнения R2a представляет неводородный заместитель в бета-конфигурации. В определенных вариантах исполнения, в которых Цикл B включает двойную C5-C6-связь, R6a представляет атом водорода, атом фтора, -CH3, или -CF3. В определенных вариантах исполнения, в которых Цикл B не содержит двойную C5-C6-связь, оба из R6a и R6b представляют атом водорода. В определенных вариантах исполнения, в которых Цикл B не содержит двойную C5-C6-связь, оба из R6a и R6b представляют -CH3 или -CF3 В определенных вариантах исполнения, в которых Цикл B не содержит двойную C5-C6-связь, оба из R6a и R6b представляют фтор. В определенных вариантах исполнения, в которых Цикл B не содержит двойную C5-C6-связь, R6a представляет неводородный заместитель, и R6b представляет атом водорода. В определенных вариантах исполнения C21-пиразолильный цикл представляет собой монозамещенный пиразолил. В определенных вариантах исполнения C21-пиразолильный цикл представляет собой дизамещенный пиразолил. В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет замещенный или незамещенный C1-2-алкил (например, -CH3, -CF3), -CO2RGA, -C(=O)RGA, -CN, -NO2, или галоген, причем RGA представляет замещенный или незамещенный C1-2-алкил (например, -CH3, -CF3). В определенных вариантах исполнения C21-пиразолильный цикл представляет собой незамещенный пиразолил, в котором в каждом случае Rm, Rn, и Rx представляет атом водорода.
[0161] В определенных вариантах исполнения, в которых в которых R6a представляет собой неводородный заместитель, представлен стероид Формулы (I-I-A6) или (I-I-B6):
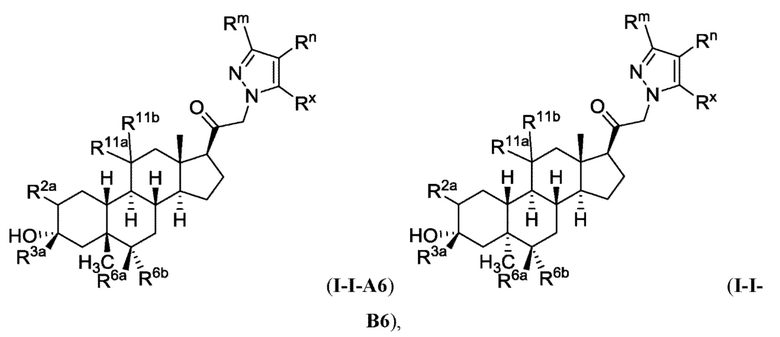
или фармацевтически приемлемая соль его. В определенных вариантах исполнения R3a представляет -CH3, -CH2CH3, -CH2F, -CHF2, -CF3, -CH2OCH3, или замещенный или незамещенный циклопропил. В определенных вариантах исполнения R2a представляет -OH, -OCH3, -OCH2CH3, -OCH2CH2CH3, -CH3, -CH2CH3, -CH2CH2CH3, замещенный или незамещенный циклопропил, атом фтора или хлора. В определенных вариантах исполнения R2a представляет неводородный заместитель в альфа-конфигурации. В определенных вариантах исполнения R2a представляет неводородный заместитель в бета-конфигурации. В определенных вариантах исполнения оба из R11a и R11b представляют атом водорода. В определенных вариантах исполнения R11a и R11b объединены с образованием =O (оксогруппы). В определенных вариантах исполнения R6a представляет атом фтора, -CH3, или -CF3, и R6b представляют атом водорода. В определенных вариантах исполнения R6b представляет атом фтора, -CH3, или -CF3, и R6a представляют атом водорода. В определенных вариантах исполнения оба из R6a и R6b представляют -CH3 или -CF3. В определенных вариантах исполнения оба из R6a и R6b представляют фтор. В определенных вариантах исполнения C21-пиразолильный цикл представляет собой монозамещенный пиразолил. В определенных вариантах исполнения C21-пиразолильный цикл представляет собой дизамещенный пиразолил. В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет замещенный или незамещенный C1-2-алкил (например, -CH3, -CF3), -CO2RGA, -C(=O)RGA, -CN, -NO2, или галоген, причем RGA представляет замещенный или незамещенный C1-2-алкил (например, -CH3, -CF3). В определенных вариантах исполнения C21-пиразолильный цикл представляет собой незамещенный пиразолил, в котором в каждом случае Rm, Rn, и Rx представляет атом водорода.
[0162] В определенных вариантах исполнения представлен стероид Формулы (I-I-A7) или (I-I-B7):
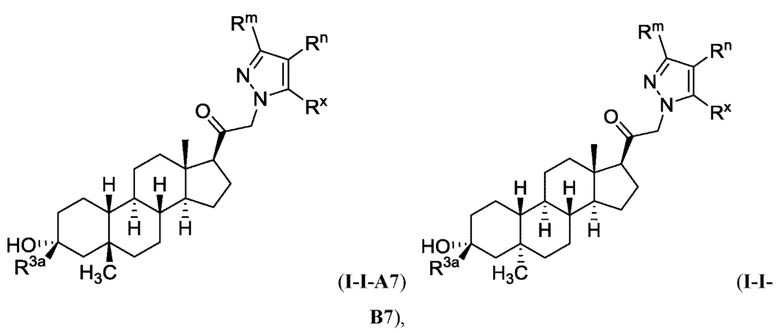
или фармацевтически приемлемая соль его. В определенных вариантах исполнения R3a представляет -CH3, -CH2CH3, -CH2F, -CHF2, -CF3, -CH2OCH3, или замещенный или незамещенный циклопропил. В определенных вариантах исполнения C21-пиразолильный цикл представляет собой монозамещенный пиразолил. В определенных вариантах исполнения C21-пиразолильный цикл представляет собой дизамещенный пиразолил. В определенных вариантах исполнения по меньшей мере один из Rm, Rn, и Rx представляет замещенный или незамещенный C1-2-алкил (например, -CH3, -CF3), -CO2RGA, -C(=O)RGA, -CN, -NO2, или галоген, причем RGA представляет замещенный или незамещенный C1-2-алкил (например, -CH3, -CF3). В определенных вариантах исполнения C21-пиразолильный цикл представляет собой незамещенный пиразолил, в котором в каждом случае Rm, Rn, и Rx представляет атом водорода.
[0163] В некоторых вариантах исполнения соединение представляет собой:
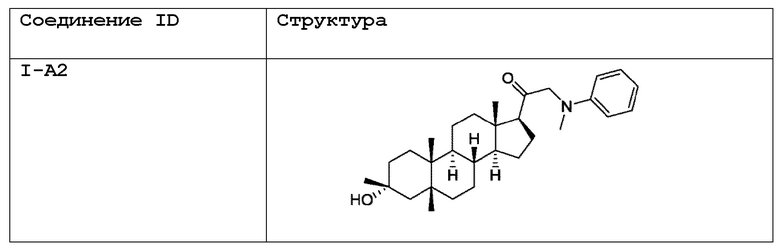
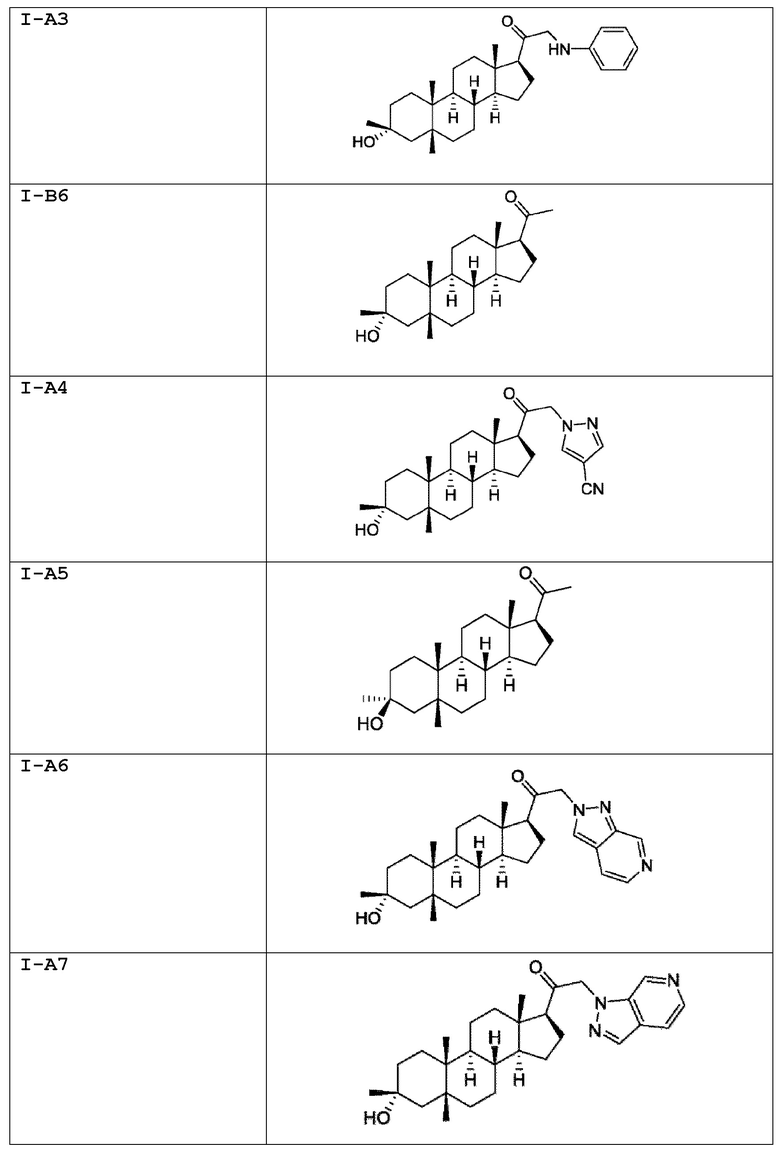
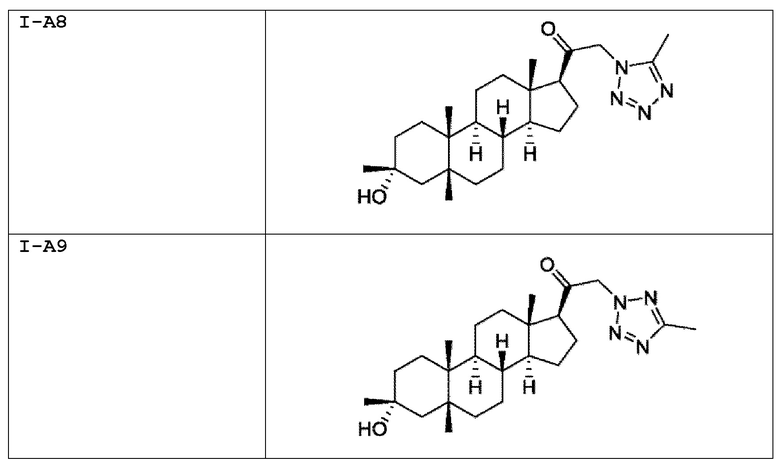
[0164]
[0165] В некоторых вариантах исполнения здесь представлено соединение Формулы (II-I)
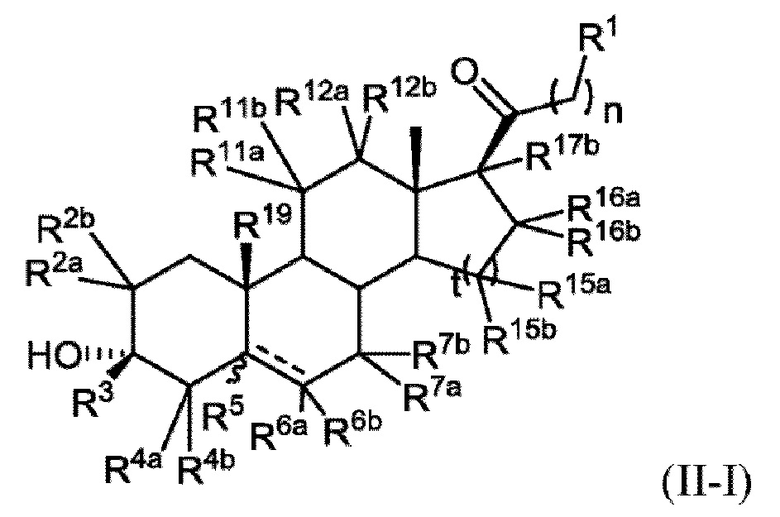
или фармацевтически приемлемая соль его; в котором
t составляет 1, 2, или 3;
n составляет 0, 1 или 2;
R19 представляет замещенный или незамещенный C2-C6-алкил, замещенный или незамещенный C2-C6-алкенил, или замещенный или незамещенный C2-C6-алкинил;
R5 представляет атом водорода или метил, или когда  представляет двойную связь, R5 отсутствует;
представляет двойную связь, R5 отсутствует;
R3 представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил;
каждый из R6a и R6b независимо представляет атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, или замещенный или незамещенный алкинил, или R6a и R6b объединены с образованием оксогруппы (=O);
R1 представляет замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил, -ORA1, -SRA1, -N(RA1)2, -N(RA1), -OC(=O)RA1, -OC(=O)ORA1, -OC(=O)SRA1, -OC(=O)N(RA1)2, -SC(=O)RA2, -SC(=O)ORA1, -SC(=O)SRA1, -SC(=O)N(RA1)2,-NHC(=O)RA1, -NHC(=O)ORA1, -NHC(=O)SRA1, -NHC(=O)N(RA1)2, -OS(=O)2RA2, -OS(=O)2ORA1, -S-S(=O)2RA2, -S-S(=O)2ORA1, -S(=O)RA2, -SO2RA2, или -S(=O)2ORA1, причем RA1, в каждом случае независимо, представляет представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил, защитную группу для кислорода, когда присоединена к атому кислорода, защитную группу для серы, когда присоединена к атому серы, азотзащитную группу, когда присоединена к атому азота, или две RGA-группы объединены с образованием замещенного или незамещенного гетероциклического или гетероарильного цикла; и RA2 представляет замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил;
каждый из R2a, R2b, R4a, R4b, R7a, R7b, R11a, R11b, R12a, R12b или R17b, независимо представляет атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный гетероциклил, или замещенный или незамещенный алкинил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил, защитную группу для кислорода, когда присоединена к атому кислорода, азотзащитную группу, когда присоединена к атому азота, или две RD1-группы объединены с образованием замещенного или незамещенного гетероциклического ядра; или любые из R2a и R2b, R4a и R4b, R7a и R7b, R11a и R11b, и R12a и R12b объединены с образованием оксогруппы (=O);
каждый из R15a, R15b, R16a и R16b, в каждом случае независимо, представляет атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил, -ORA1, -SRA1, -N(RA1)2, -N(RA1), -CN(RA1)2, -C(O)RA1, -OC(=O)RA1, -OC(=O)ORA1, -OC(=O)SRA1, -OC(=O)N(RA1)2, -SC(=O)RA2, -SC(=O)ORA1, -SC(=O)SRA1, -SC(=O)N(RA1)2, -NHC(=O)RA1, -NHC(=O)ORA1, -NHC(=O)SRA1, -NHC(=O)N(RA1)2, -OS(=O)2RA2, -OS(=O)2ORA1, -S-S(=O)2RA2, -S-S(=O)2ORA1, -S(=O)RA2, -SO2RA2, или -S(=O)2ORA1, причем RA1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил, защитную группу для кислорода, когда присоединена к атому кислорода, защитную группу для серы, когда присоединена к атому серы, азотзащитную группу, когда присоединена к атому азота, -SO2RA2, -C(O)RA2, или две RA1-группы объединены с образованием замещенного или незамещенного гетероциклического или гетероарильного цикла; и RA2 представляет замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил; и
причем  представляет одинарную или двойную связь, при условии, что, если в Цикле В присутствует двойная связь, то один из R6a или R6b и R5 отсутствует.
представляет одинарную или двойную связь, при условии, что, если в Цикле В присутствует двойная связь, то один из R6a или R6b и R5 отсутствует.
[0166] Должно быть понятно, что стереохимическая конфигурация при С17 могла бы быть изображена любым из следующих, но эквивалентных путей:
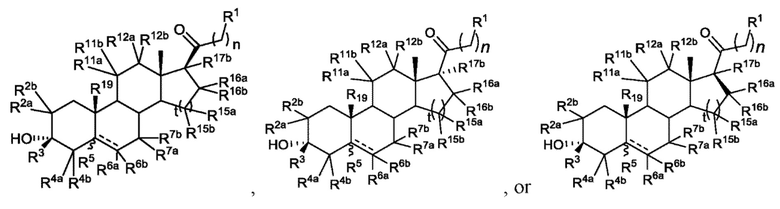
Формула (II-I) Группы R2a и R2b
[0167] В некоторых аспектах R2a и R2b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный гетероциклил, или замещенный или незамещенный алкинил,-ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0168] В некоторых аспектах R2a и R2b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, -ORD1, -OC(=O)RD1, -NH2, или -N(RD1)2, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0169] В некоторых аспектах R2a и R2b, в каждом случае независимо, представляют атом водорода, замещенный или незамещенный алкил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0170] В некоторых аспектах оба R2a и R2b представляют атом водорода.
[0171] В некоторых вариантах исполнения R2a и R2, в каждом случае независимо, представляют атом водорода или замещенный или незамещенный алкил.
[0172] В некоторых вариантах исполнения каждый R2a и R2b независимо представляет атом водорода, С1-С6-алкил, С1-С6-галоалкил, С1-С6-алкоксигруппу, С1-С6-галоалкоксигруппу, или -ОН.
[0173] В некоторых вариантах исполнения R2a или R2b независимо представляют -СН3, -СН2СН3, -ОН, -ОСН3 или -СН(СН3)2.
Формула (II-I): группы R4a и R4b
[0174] В некоторых аспектах R4a и R4b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный гетероциклил, замещенный или незамещенный алкинил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0175] В некоторых аспектах R4a и R4b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, -ORD1, -OC(=O)RD1, -NH2, или -N(RD1)2, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0176] В некоторых аспектах R4a и R4b, в каждом случае независимо, представляют атом водорода, замещенный или незамещенный алкил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0177] В некоторых аспектах оба R4a и R4b представляют атом водорода. В дополнительных вариантах исполнения R16a и R16b, в каждом случае независимо, представляют атом водорода или замещенный или незамещенный алкил.
[0178] В некоторых аспектах R4a и R4b независимо представляют атом водорода, С1-С6-алкил, С1-С6-галоалкил, С1-С6-алкоксигруппу, С1-С6-галоалкоксигруппу, или -ОН. В некоторых других аспектах R4a и R4b представляют -СН3, -СН2СН3, -ОН, -ОСН3 или -СН(СН3)2.
Формула (II-I): группы R11a и R11b
[0179] В некоторых вариантах исполнения R11a и R11b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный гетероциклил, замещенный или незамещенный алкинил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0180] В некоторых дополнительных вариантах исполнения R11a и R11b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, -ORD1, -OC(=O)RD1, -NH2, или -N(RD1)2, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0181] В некоторых аспектах R11a и R11b, в каждом случае независимо, представляют атом водорода, замещенный или незамещенный алкил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил. В некоторых аспектах оба R11a и R11b представляют атом водорода.
[0182] В некоторых аспектах R11a и R11b, в каждом случае независимо, представляют атом водорода или замещенный или незамещенный алкил. В некоторых аспектах R11a и R11b независимо представляют атом водорода, С1-С6-алкил, С1-С6-галоалкил, С1-С6-алкоксигруппу, С1-С6-галоалкоксигруппу, или -ОН.
[0183] В некоторых аспектах R11a и R11b представляет -СН3, -СН2СН3, -ОН, -ОСН3 или -СН(СН3)2.
[0184] В некоторых вариантах исполнения R11a и R11b объединены с образованием оксогруппы (=O).
Формула (II-I): группы R15a и R15b
[0185] В некоторых аспектах R15a и R15b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный гетероциклил, замещенный или незамещенный алкинил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0186] В некоторых вариантах исполнения R15a и R15b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, -ORD1, -OC(=O)RD1, -NH2, или -N(RD1)2, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0187] В некоторых вариантах исполнения R15a и R15b, в каждом случае независимо, представляют атом водорода, замещенный или незамещенный алкил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0188] В некоторых дополнительных вариантах исполнения оба R15a и R15b представляют атом водорода.
[0189] В некоторых аспектах R15a и R15b, в каждом случае независимо, представляют атом водорода или замещенный или незамещенный алкил. В некоторых аспектах R15a и R15b независимо представляют атом водорода, С1-С6-алкил, С1-С6-галоалкил, С1-С6-алкоксигруппу, С1-С6-галоалкоксигруппу, или -ОН. В некоторых аспектах R15a и R15b представляет -СН3, -СН2СН3, -ОН, -ОСН3 или -СН(СН3)2.
Формула (II-I): группы R16a и R16b
[0190] В некоторых аспектах R16a и R16b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный гетероциклил, замещенный или незамещенный алкинил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0191] В некоторых вариантах исполнения R16a и R16b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, -ORD1, -OC(=O)RD1, -NH2, или -N(RD1)2, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0192] В некоторых вариантах исполнения R16a и R16b, в каждом случае независимо, представляют атом водорода, замещенный или незамещенный алкил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0193] В некоторых дополнительных вариантах исполнения оба R16a и R16b представляют атом водорода.
[0194] В некоторых аспектах R16a и R16b, в каждом случае независимо, представляют атом водорода или замещенный или незамещенный алкил. В некоторых аспектах R16a и R16b независимо представляют атом водорода, С1-С6-алкил, С1-С6-галоалкил, С1-С6-алкоксигруппу, С1-С6-галоалкоксигруппу, или -ОН.
[0195] В некоторых аспектах R16a и R16b представляет -СН3, -СН2СН3, -ОН, -ОСН3 или -СН(СН3)2.
Формула (II-I): группы R7a и R7b
[0196] В некоторых аспектах R7a и R7b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный гетероциклил, замещенный или незамещенный алкинил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил, или любые из R7a и R7b объединены с образованием оксогруппы (=O).
[0197] В некоторых дополнительных вариантах исполнения R7a и R7b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, -ORD1, -OC(=O)RD1, -NH2, или -N(RD1)2, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0198] В некоторых аспектах R7a и R7b, в каждом случае независимо, представляют атом водорода, замещенный или незамещенный алкил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0199] В некоторых аспектах все R7a и R7b представляют атом водорода.
[0200] В некоторых аспектах R7a и R7b, в каждом случае независимо, представляют атом водорода или замещенный или незамещенный алкил. В некоторых аспектах R7a и R7b независимо представляют атом водорода, С1-С6-алкил, С1-С6-галоалкил, С1-С6-алкоксигруппу, С1-С6-галоалкоксигруппу, или -ОН.
[0201] В некоторых аспектах R7a и R7b представляет -СН3, -СН2СН3, -ОН, -ОСН3 или -СН(СН3)2.
[0202] В некоторых вариантах исполнения любые из R7a и R7b объединены с образованием оксогруппы (=O).
Формула (II-I): группа R5
[0203] В некоторых аспектах R5 представляет атом водорода в цис-положении относительно С19-положения. В некоторых других аспектах R5 представляет атом водорода в транс-положении относительно С19-положения. В некоторых вариантах исполнения R5 представляет метил в цис-положении относительно С19-положения. В некоторых дополнительных вариантах исполнения R5 представляет метил в транс-положении относительно С19-положения.
Формула (II-I): группа R3
[0204] В некоторых вариантах исполнения R3 представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, или замещенный или незамещенный алкинил.
[0205] В некоторых вариантах исполнения R3 представляет замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0206] В некоторых вариантах исполнения R3 представляет замещенный или незамещенный алкил.
[0207] В некоторых вариантах исполнения R3 представляет атом водорода. В некоторых вариантах исполнения R3 представляет замещенный алкил (например, -CH2OMe или -CH2OEt, и т.д.). В некоторых вариантах исполнения R3 представляет незамещенный алкил. В некоторых вариантах исполнения R3 представляет метил.
Формула (II-I) группа R19
[0208] В некоторых аспектах R19 представляет С2-С6-алкил. В некоторых аспектах R19 представляет С2-С6-алкил с дейтериевым замещением.
[0209] В некоторых вариантах исполнения R19 представляет замещенный С2-С6-алкил. В некоторых вариантах исполнения R19 представляет незамещенный С2-С6-алкил.
[0210] В некоторых вариантах исполнения R19 представляет замещенный С2-С6-алкенил. В некоторых вариантах исполнения R19 представляет незамещенный С2-С6-алкенил.
[0211] В некоторых вариантах исполнения R19 представляет замещенный С2-С6-алкинил. В некоторых вариантах исполнения R19 представляет незамещенный С2-С6-алкинил.
[0212] В некоторых аспектах R19 представляет этил.
Формула (II-I): группа R6a и R6b
[0213] В некоторых вариантах исполнения R6a и R6b независимо представляет атом водорода, галоген, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, или замещенный или незамещенный алкинил.
[0214] В некоторых вариантах исполнения R6a и R6b независимо представляет атом водорода или замещенный или незамещенный алкил.
[0215] В некоторых аспектах R6a и R6b независимо представляет атом водорода или замещенный алкил. В некоторых аспектах R6a и R6b независимо представляет атом водорода или незамещенный алкил.
[0216] В некоторых аспектах оба R6a и R6b представляют атом водорода. В некоторых аспектах R6a представляет галоген или алкил, и R6b представляет атом водорода. В некоторых вариантах исполнения оба R6a и R6b представляют галоген.
[0217] В некоторых аспектах оба R6a и R6b представляют алкил.
[0218] В некоторых вариантах исполнения R6a и R6b объединены с образованием оксогруппы.
Формула (II-I) группа R12a и R12b
[0219] В некоторых аспектах R12a и R12b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный гетероциклил, замещенный или незамещенный алкинил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0220] В некоторых вариантах исполнения R12a и R12b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, -ORD1, -OC(=O)RD1, -NH2, или -N(RD1)2, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0221] В некоторых вариантах исполнения R12a и R12b, в каждом случае независимо, представляют атом водорода, замещенный или незамещенный алкил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0222] В некоторых вариантах исполнения оба R12a и R12b представляют атом водорода.
[0223] В некоторых дополнительных вариантах исполнения R12a и R12b, в каждом случае независимо, представляют атом водорода или замещенный или незамещенный алкил.
[0224] В некоторых вариантах исполнения R12a и R12b объединены между собой с образованием оксогруппы (=O).
Формула (II-I) группа R17b
[0225] В некоторых вариантах исполнения R17b представляет фтор, гидроксил, метил или атом водорода. В некоторых дополнительных вариантах исполнения водород при R17b замещен дейтерием.
Формула (II-I) t и n
[0226] В некоторых вариантах исполнения t составляет 1. В некоторых других вариантах исполнения t составляет 2. В некоторых других вариантах исполнения t составляет 3.
[0227] В некоторых вариантах исполнения n составляет 1. В некоторых других вариантах исполнения n составляет 2.
Формула (II-I) группа R1
[0228] В некоторых вариантах исполнения R1 представляет замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0229] В некоторых вариантах исполнения R1 представляет
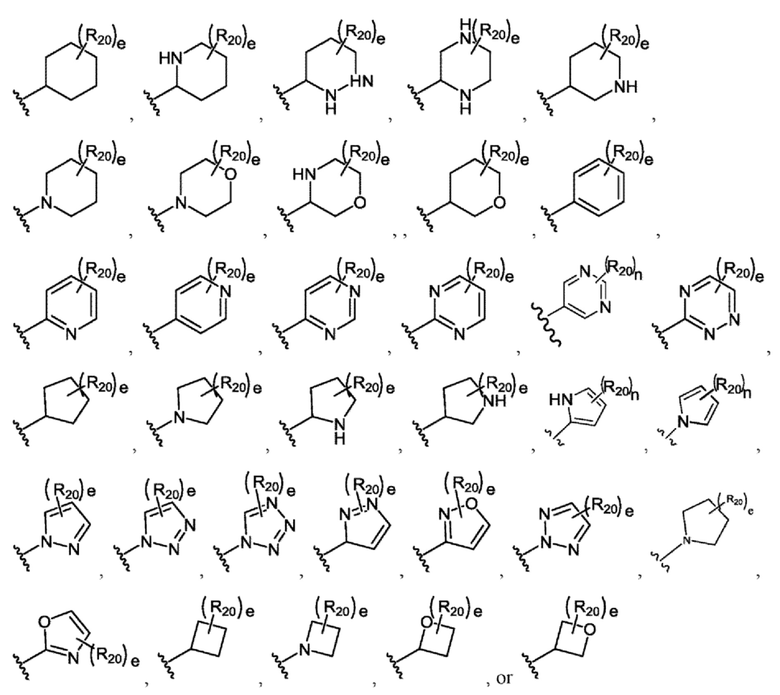
причем R20, в каждом случае независимо, представляет галоген, -NO2, -CN, -ORGA, -N(RGA)2, -C(=O)RGA, -C(=O)ORGA, -OC(=O)RGA, -OC(=O)ORGA, -C(=O)N(RGA)2, -N(RGA)C(=O)RGA, -OC(=O)N(RGA)2, -N(RGA)C(=O)ORGA, -S(=O)2RGA, -S(=O)2ORGA, -OS(=O)2RGA, -S(=O)2N(RGA)2, или -N(RGA)S(=O)2RGA; замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, замещенный или незамещенный C3-4-карбоциклил, замещенный или незамещенный 3-4-членный гетероциклил, замещенный или незамещенный C5-10-арил, замещенный или незамещенный 5-10-членный гетероарил, или необязательно две RGA-группы связаны общими атомами с образованием замещенного или незамещенного 3-4-членного карбоциклического или гетероциклического цикла; причем RGA, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, замещенный или незамещенный C3-6-карбоциклил, замещенный или незамещенный 3-6-членный гетероциклил, замещенный или незамещенный арил, замещенный или незамещенный гетероарил, защитную группу для кислорода, когда присоединена к атому кислорода, азотзащитную группу, когда присоединена к атому азота, или две RGA-группы связаны общими атомами с образованием замещенного или незамещенного карбоциклического или гетероциклического цикла; и e составляет 0, 1, 2, 3, 4, или 5, или n составляет 0, 1, 2, 3, 4, или 5.
[0230] В некоторых вариантах исполнения, в которых R1 представляет
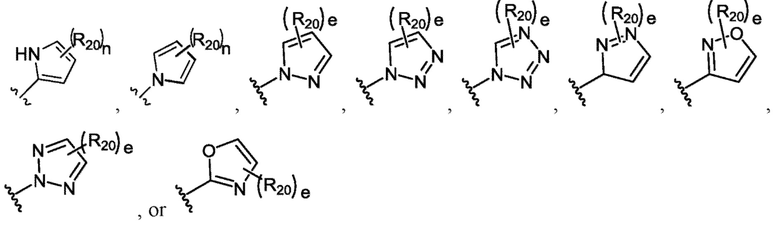
причем R20, в каждом случае независимо, представляет галоген, -NO2, -CN, -ORGA, -N(RGA)2, -C(=O)RGA, -C(=O)ORGA, -OC(=O)RGA, -OC(=O)ORGA, -C(=O)N(RGA)2, -N(RGA)C(=O)RGA, -OC(=O)N(RGA)2, -N(RGA)C(=O)ORGA, -S(=O)2RGA, -S(=O)2ORGA, -OS(=O)2RGA, -S(=O)2N(RGA)2, или -N(RGA)S(=O)2RGA; замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, замещенный или незамещенный C3-4-карбоциклил, замещенный или незамещенный 3-4-членный гетероциклил, замещенный или незамещенный C5-10-арил, замещенный или незамещенный 5-10-членный гетероарил, или необязательно две RGA-группы связаны общими атомами с образованием замещенного или незамещенного 3-4-членного карбоциклического или гетероциклического цикла; причем RGA, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, замещенный или незамещенный C3-6-карбоциклил, замещенный или незамещенный 3-6-членный гетероциклил, замещенный или незамещенный арил, замещенный или незамещенный гетероарил, защитную группу для кислорода, когда присоединена к атому кислорода, азотзащитную группу, когда присоединена к атому азота, или две RGA-группы связаны общими атомами с образованием замещенного или незамещенного карбоциклического или гетероциклического цикла; и e составляет 0, 1, 2, 3, 4, или 5, и n составляет 0, 1, 2, 3, 4, или 5.
[0231] В некоторых вариантах исполнения R1 представляет замещенный карбоциклил, замещенный гетероциклил, замещенный арил, или замещенный гетероарил, причем каждый замещенный карбоциклил, замещенный гетероциклил, замещенный арил, или замещенный гетероарил независимо замещен замещенным или незамещенным карбоциклилом, замещенным или незамещенным гетероциклилом, замещенным или незамещенным арилом, или замещенным или незамещенным гетероарилом.
[0232] В некоторых вариантах исполнения соединение Формулы (II-I) представляет собой соединение Формулы (II-Ia)
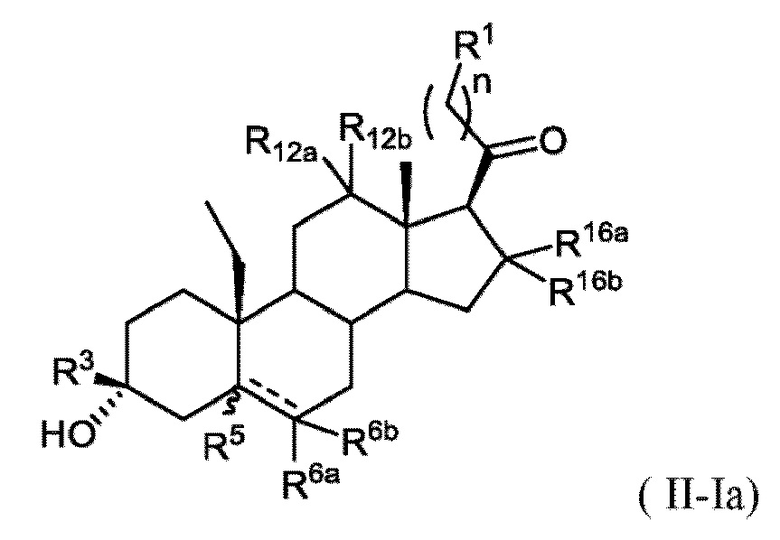
или фармацевтически приемлемую соль его.
[0233] В некоторых вариантах исполнения соединение Формулы (II-I) представляет собой соединение Формулы (II-Ib)
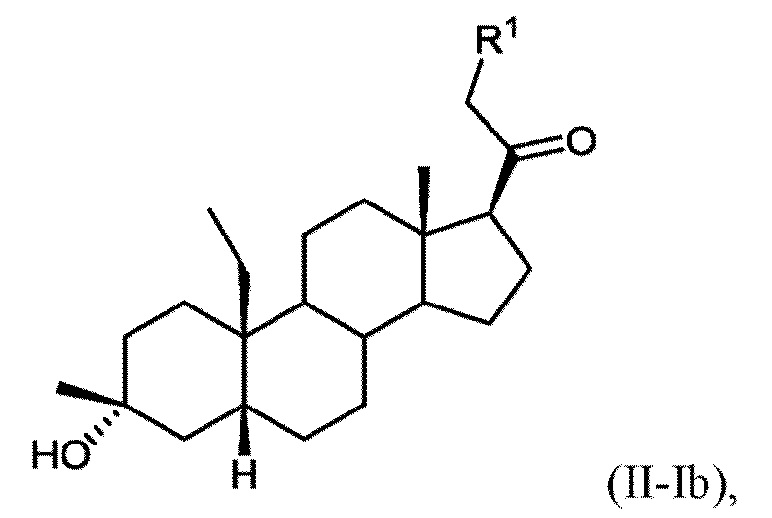
или фармацевтически приемлемую соль его.
[0234] В некоторых вариантах исполнения соединение Формулы (II-I) представляет собой соединение Формулы (II-Ic)
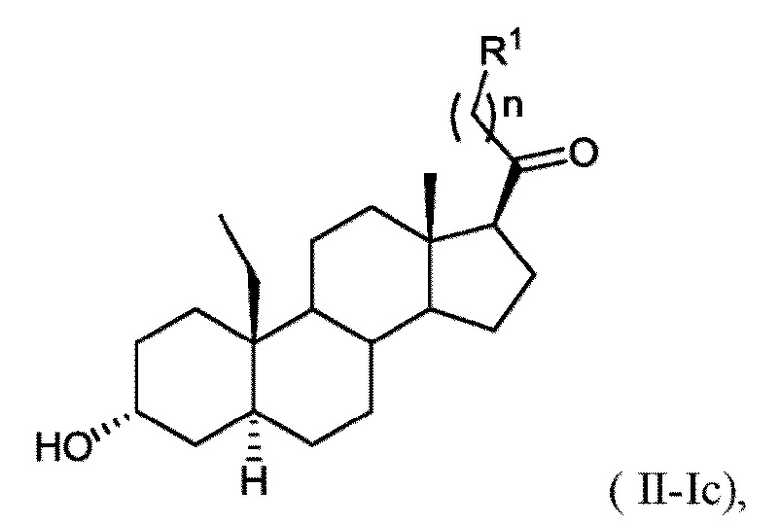
или фармацевтически приемлемую соль его.
[0235] В некоторых вариантах исполнения соединение Формулы (II-I) представляет собой соединение Формулы (II-Ie)
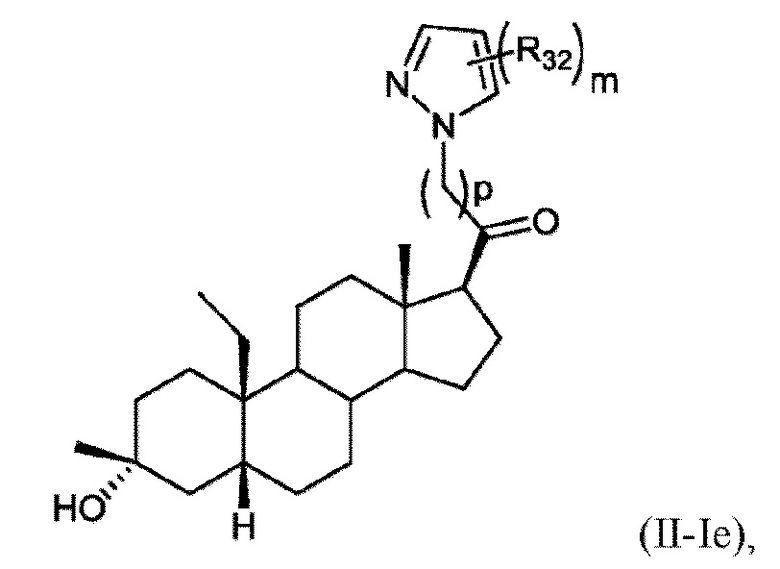
в котором m составляет 0, 1, 2 или 3; p составляет 0, 1, или 3; каждый R32 независимо представляет галоген, алкил, гидроксил или цианогруппу;
или фармацевтически приемлемую соль его.
[0236] В некоторых вариантах исполнения соединение Формулы (II-I) представляет собой соединение Формулы (II-Ig)
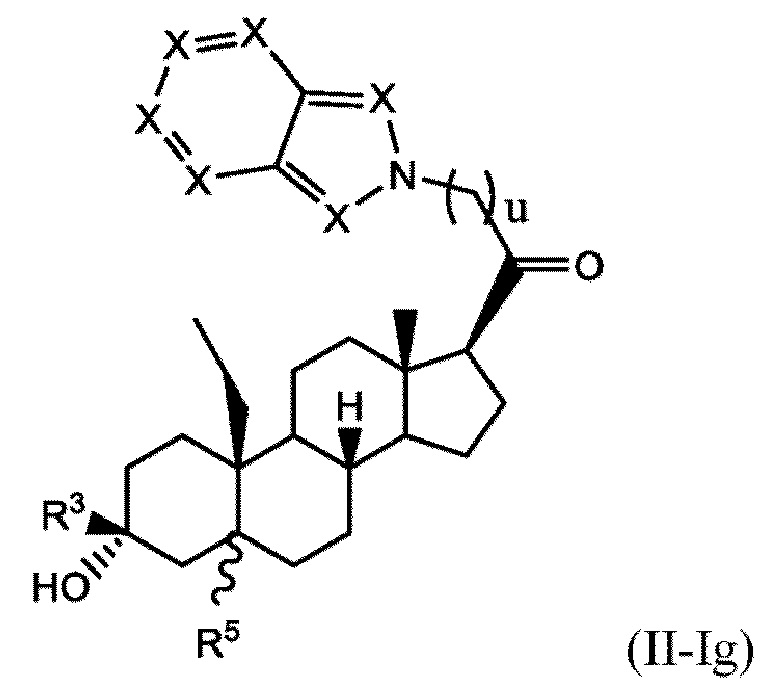
причем u составляет 0, 1, или 2; каждый X независимо представляет -C(RN)-, -C(RN)2-, -O-, -S-, -N-, или N(RN)-, причем RN независимо представляет атом водорода, замещенный или незамещенный C1-6-алкил, C(=O)RGA, -C(=O)ORGA, -C(=O)N(RGA)2, -S(=O)2RGA, или -S(=O)2N(RGA)2; и RGA, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, замещенный или незамещенный C3-6-карбоциклил, замещенный или незамещенный 3-6-членный гетероциклил, замещенный или незамещенный арил, замещенный или незамещенный гетероарил, защитную группу для кислорода, когда присоединена к атому кислорода, азотзащитную группу, когда присоединена к атому азота, или две RGA-группы связаны общими атомами с образованием замещенного или незамещенного гетероциклического или гетероарильного цикла; или фармацевтически приемлемую соль его.
[0237] В некоторых вариантах исполнения соединение Формулы (II-I) представляет собой соединение Формулы (II-Iga)
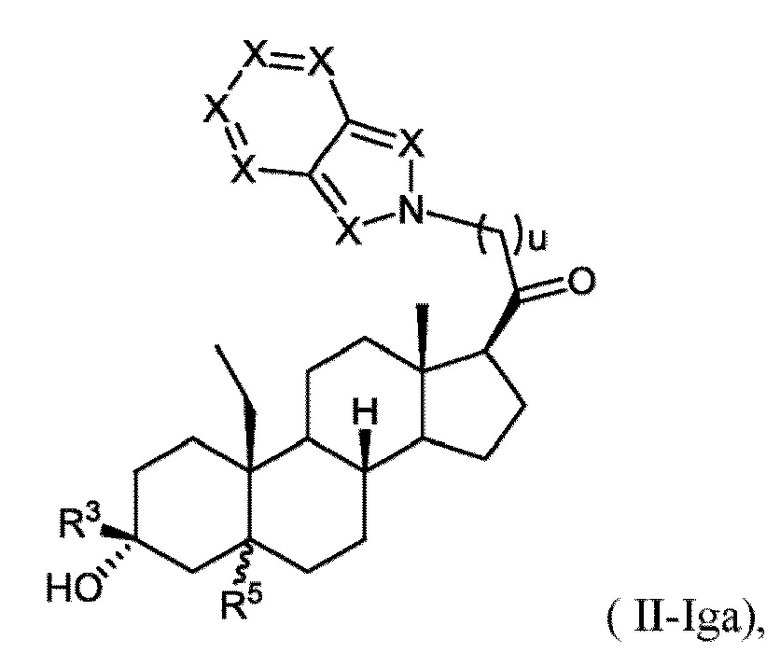
причем u составляет 0, 1, или 2; каждый X независимо представляет -C(RN)-, -C(RN)2-, -O-, -S-, -N-, или N(RN)-, причем RN независимо представляет атом водорода, замещенный или незамещенный C1-6-алкил, C(=O)RGA, -C(=O)ORGA, -C(=O)N(RGA)2, -S(=O)2RGA, или -S(=O)2N(RGA)2; и RGA, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, замещенный или незамещенный C3-6-карбоциклил, замещенный или незамещенный 3-6-членный гетероциклил, замещенный или незамещенный арил, замещенный или незамещенный гетероарил, защитную группу для кислорода, когда присоединена к атому кислорода, азотзащитную группу, когда присоединена к атому азота, или две RGA-группы связаны общими атомами с образованием замещенного или незамещенного гетероциклического или гетероарильного цикла; или фармацевтически приемлемую соль его.
[0238] В некоторых вариантах исполнения соединение Формулы (II-I) представляет собой соединение Формулы (II-Ih)
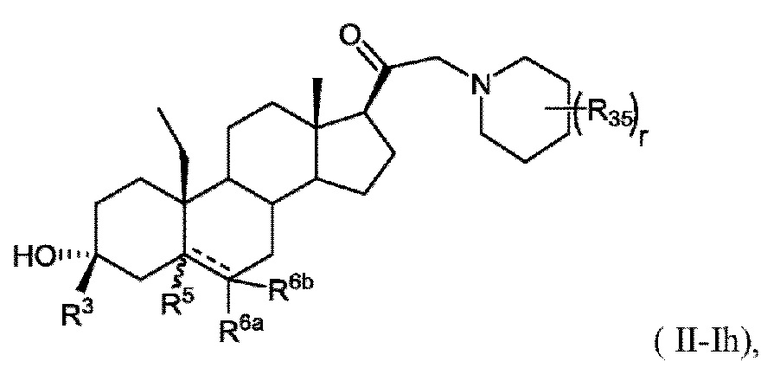
в котором каждый R35 независимо представляет галоген, алкил, гидроксил или цианогруппу; и r составляет 0, 1, 2 или 3; или фармацевтически приемлемую соль его.
[0239] В некоторых вариантах исполнения соединение Формулы (II-I) представляет собой соединение Формулы (II-Ii)
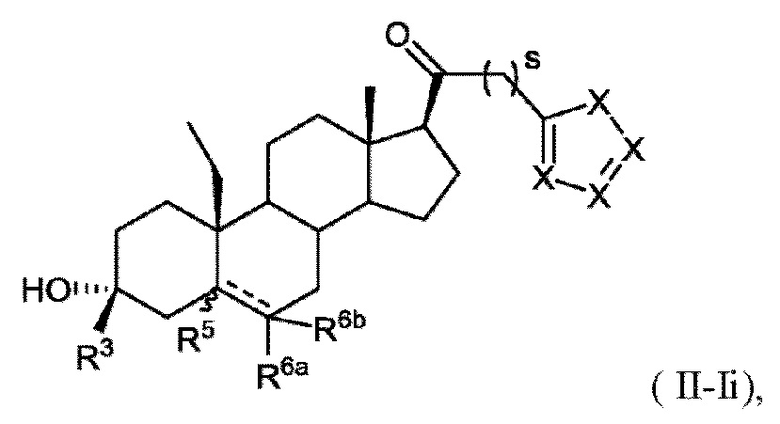
в котором s составляет 0, 1, или 2; каждый X независимо представляет -C(RN)-, -C(RN)2-, -O-, -S-, -N-, или N(RN)-, причем RN независимо представляет атом водорода, замещенный или незамещенный C1-6-алкил, C(=O)RGA, -C(=O)ORGA, -C(=O)N(RGA)2, -S(=O)2RGA, или -S(=O)2N(RGA)2; и
RGA, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, замещенный или незамещенный C3-6-карбоциклил, замещенный или незамещенный 3-6-членный гетероциклил, замещенный или незамещенный арил, замещенный или незамещенный гетероарил, защитную группу для кислорода, когда присоединена к атому кислорода, азотзащитную группу, когда присоединена к атому азота, или две RGA-группы связаны общими атомами с образованием замещенного или незамещенного гетероциклического или гетероарильного цикла; или фармацевтически приемлемую соль его.
[0240] В некоторых вариантах исполнения соединение выбирают из группы, состоящей из соединений, идентифицированных ниже в Таблице II-I:
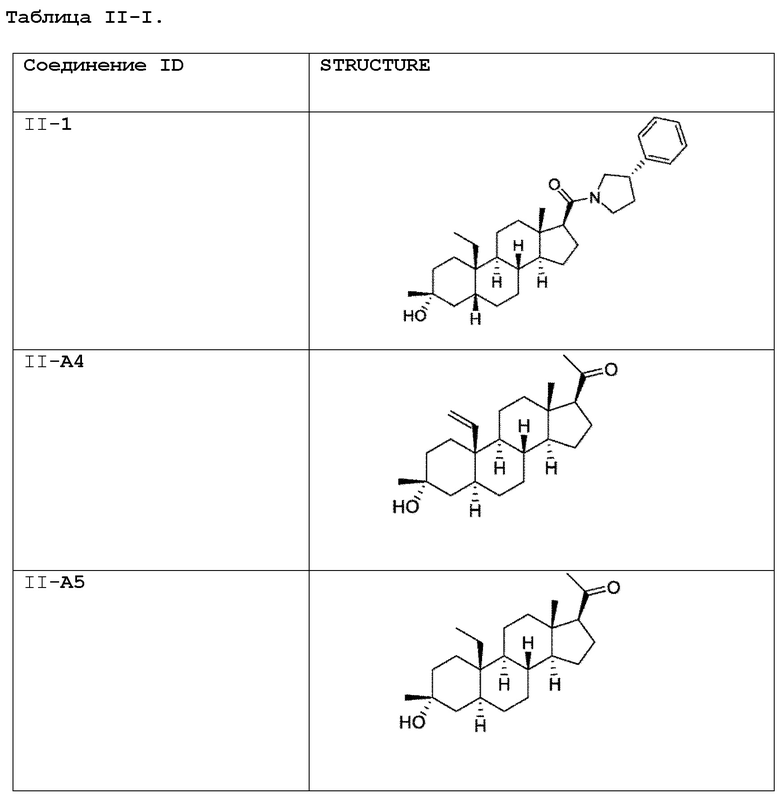
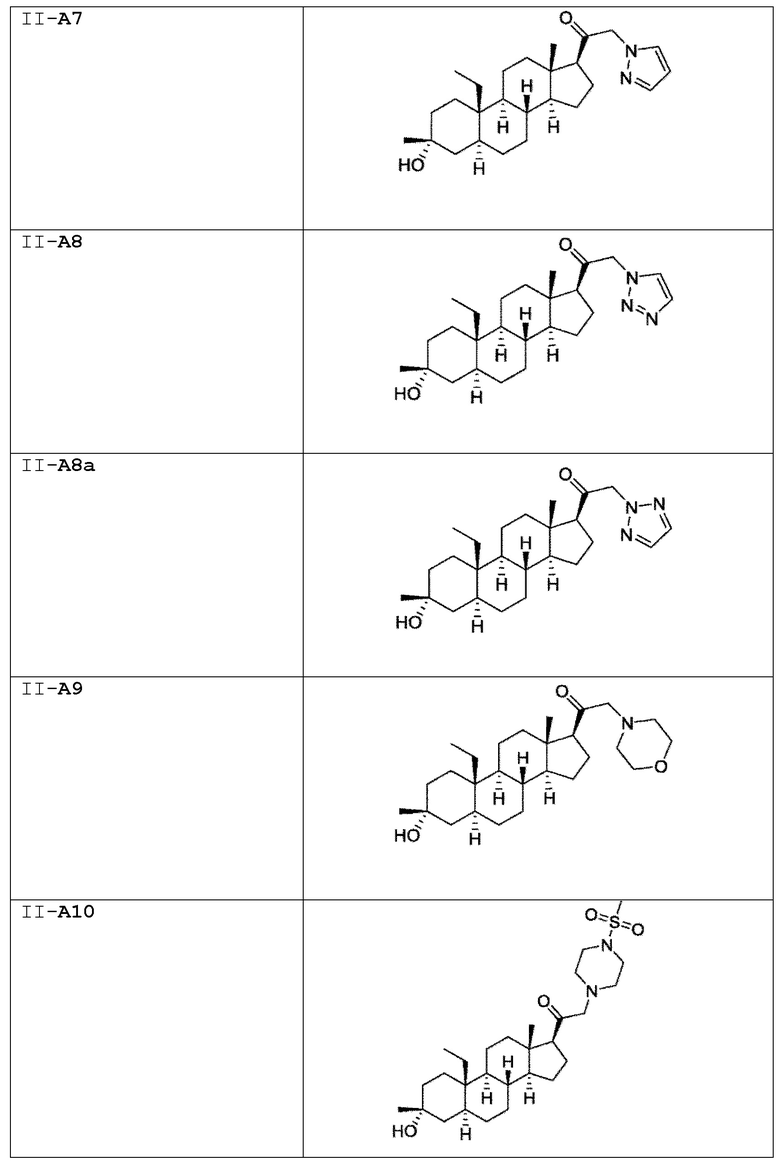
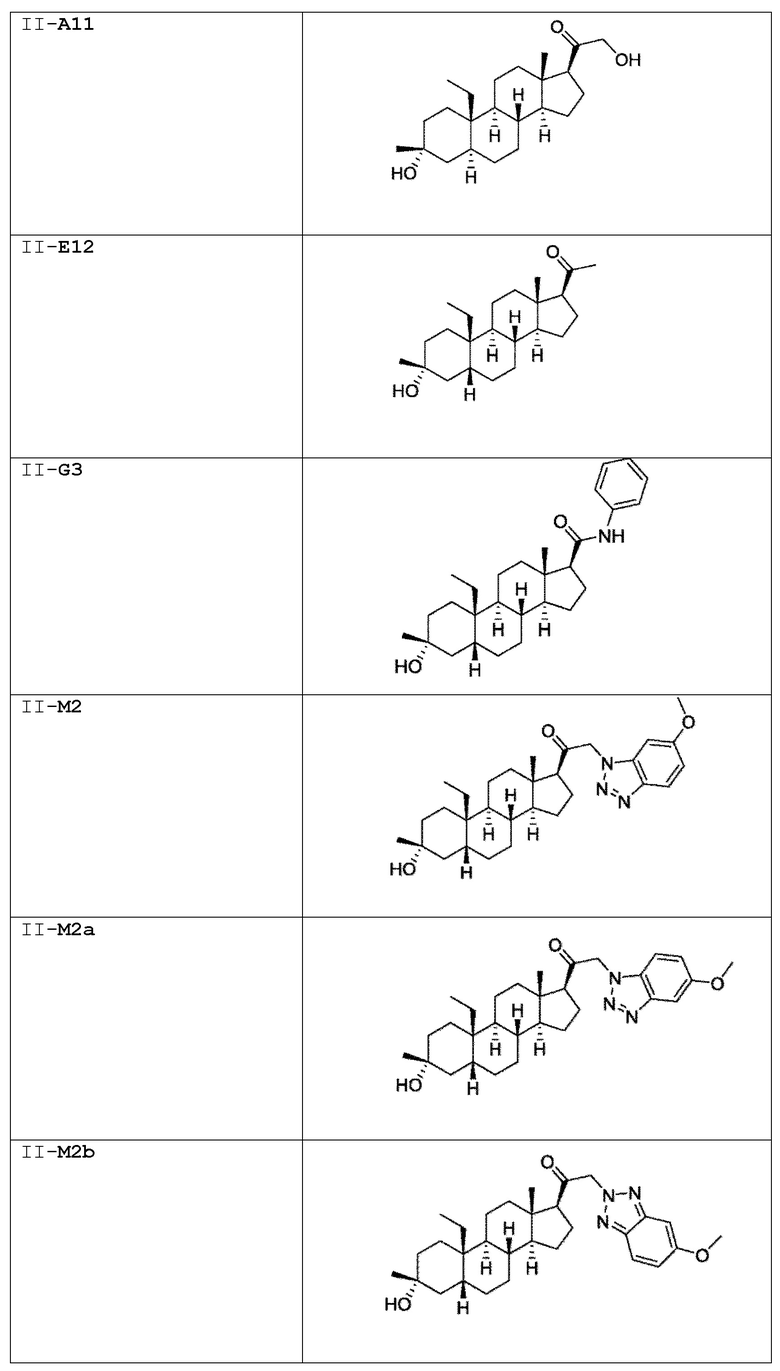
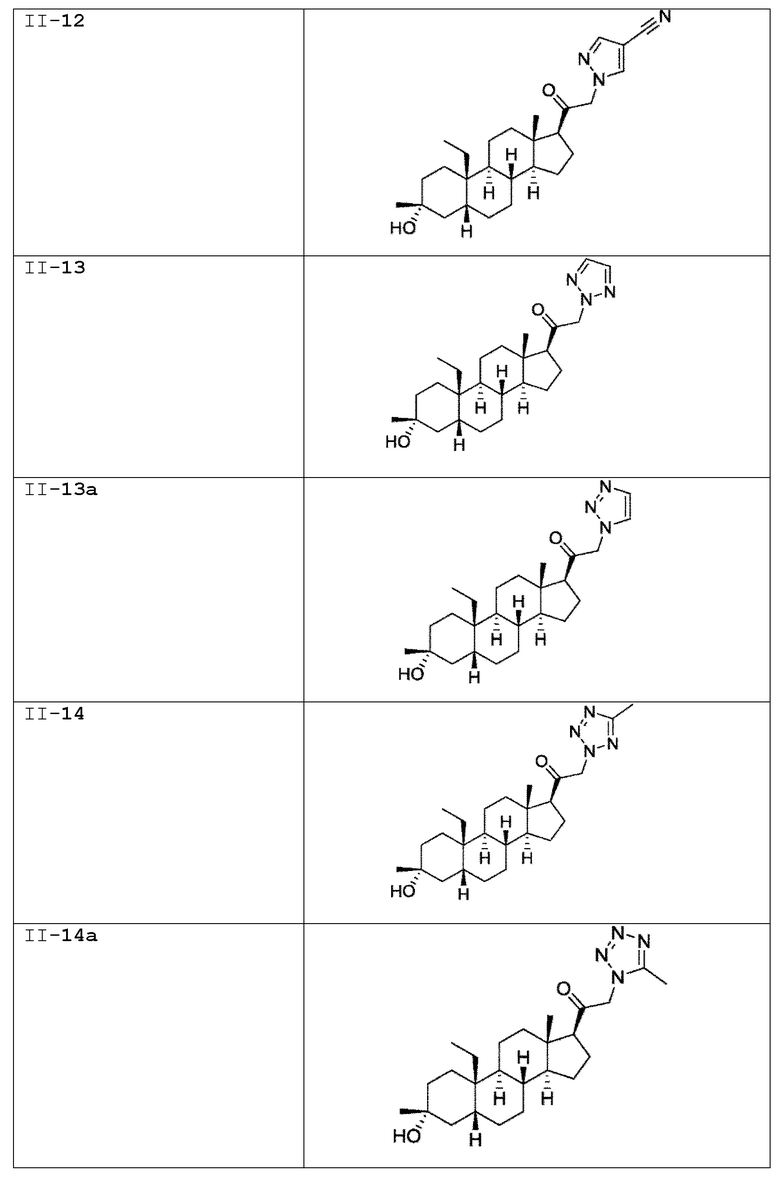
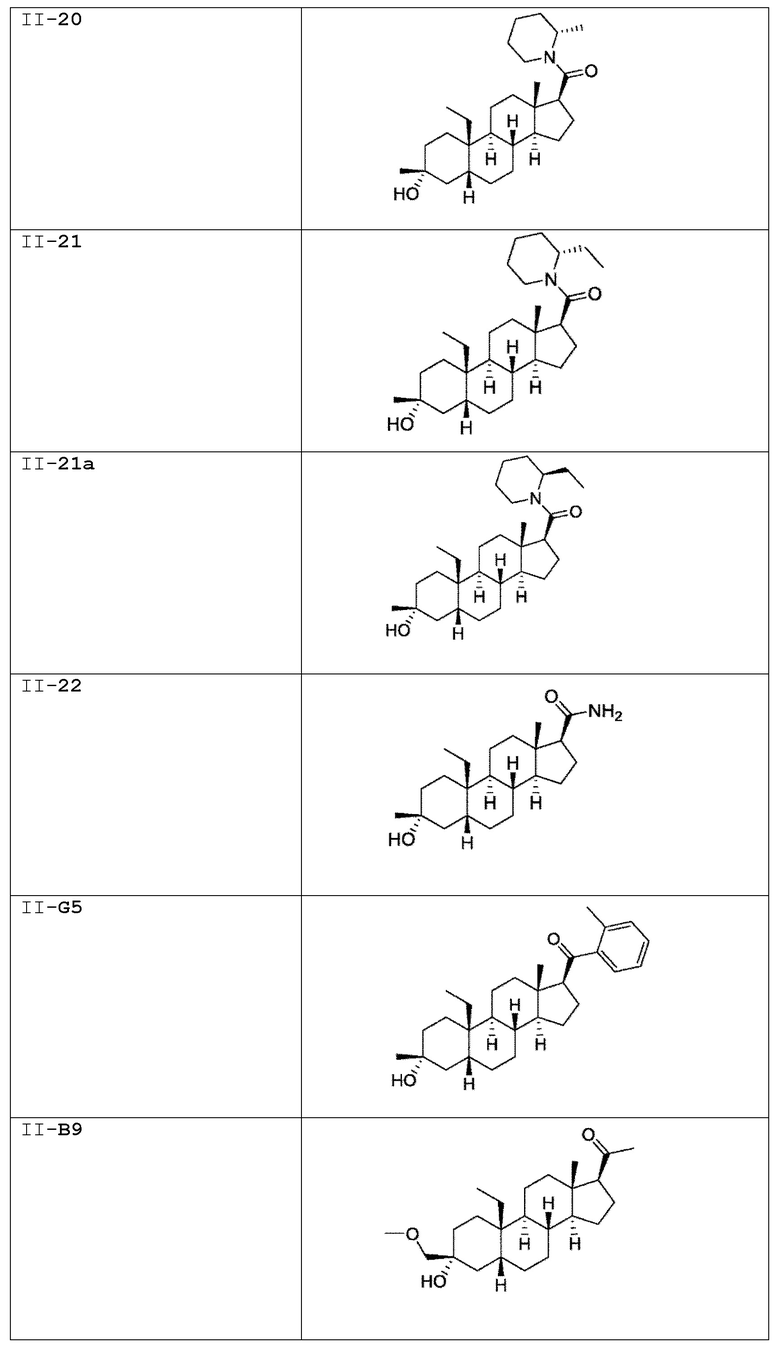
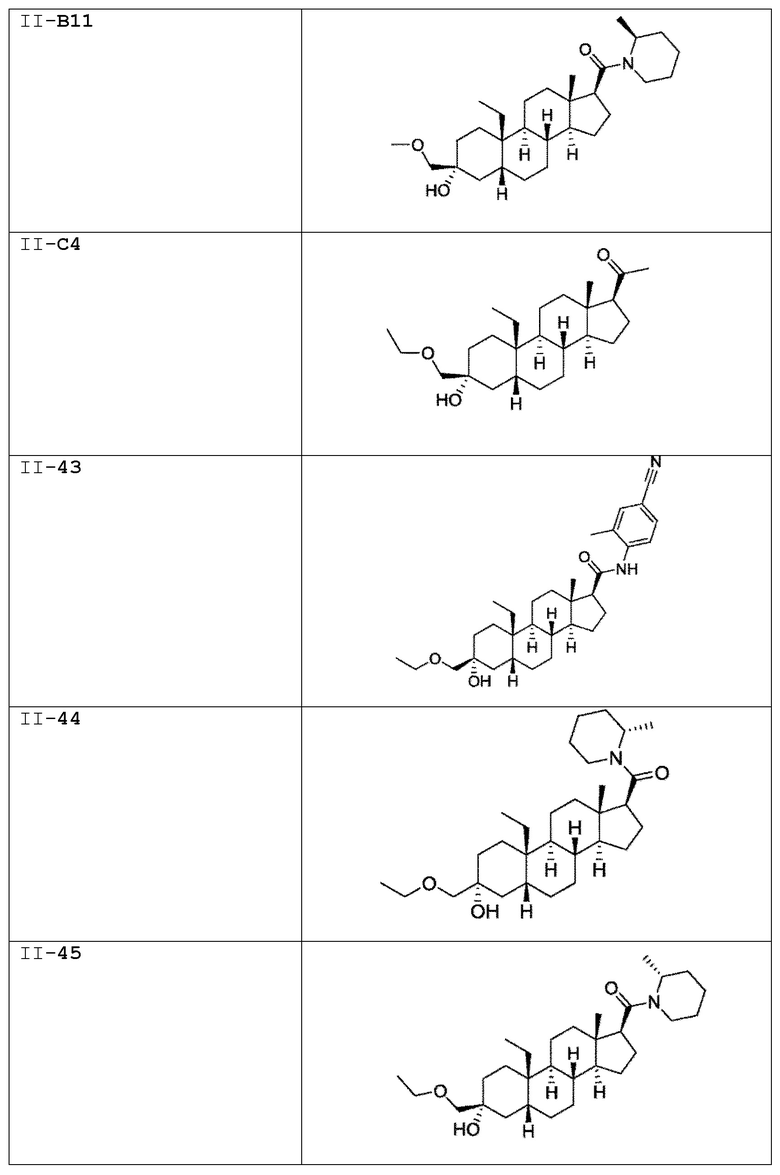
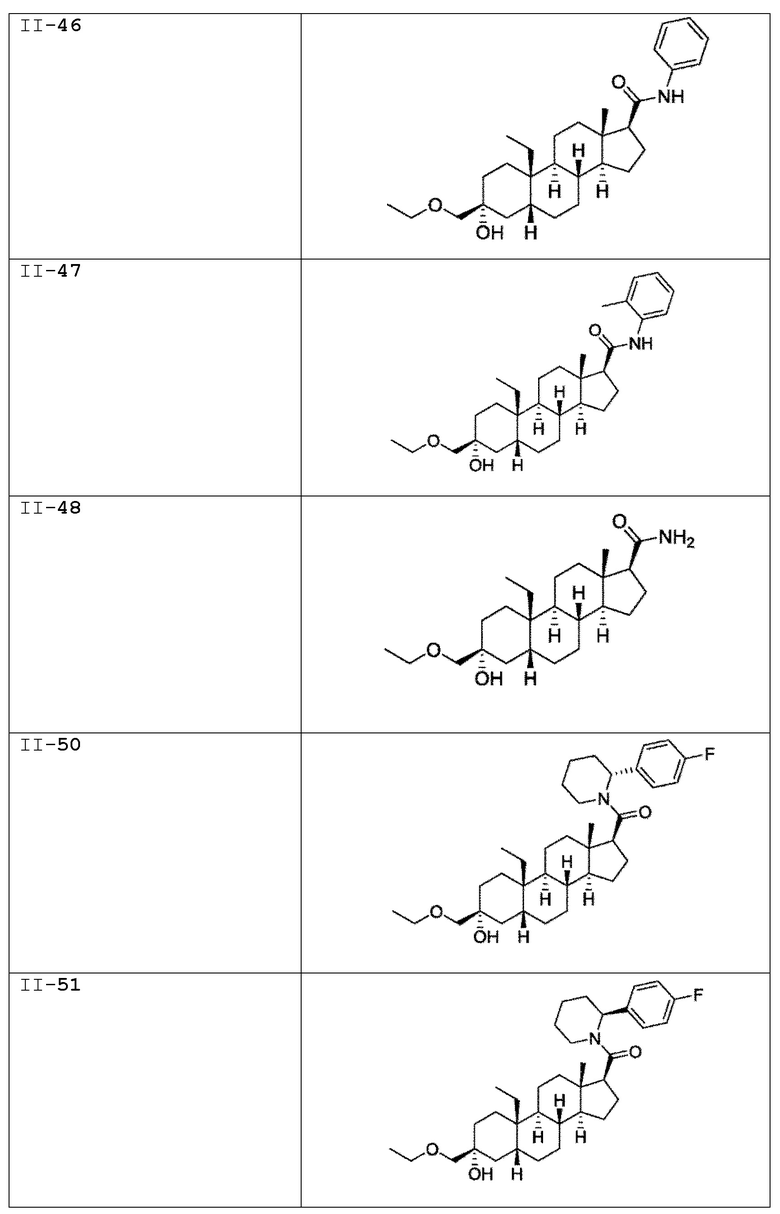
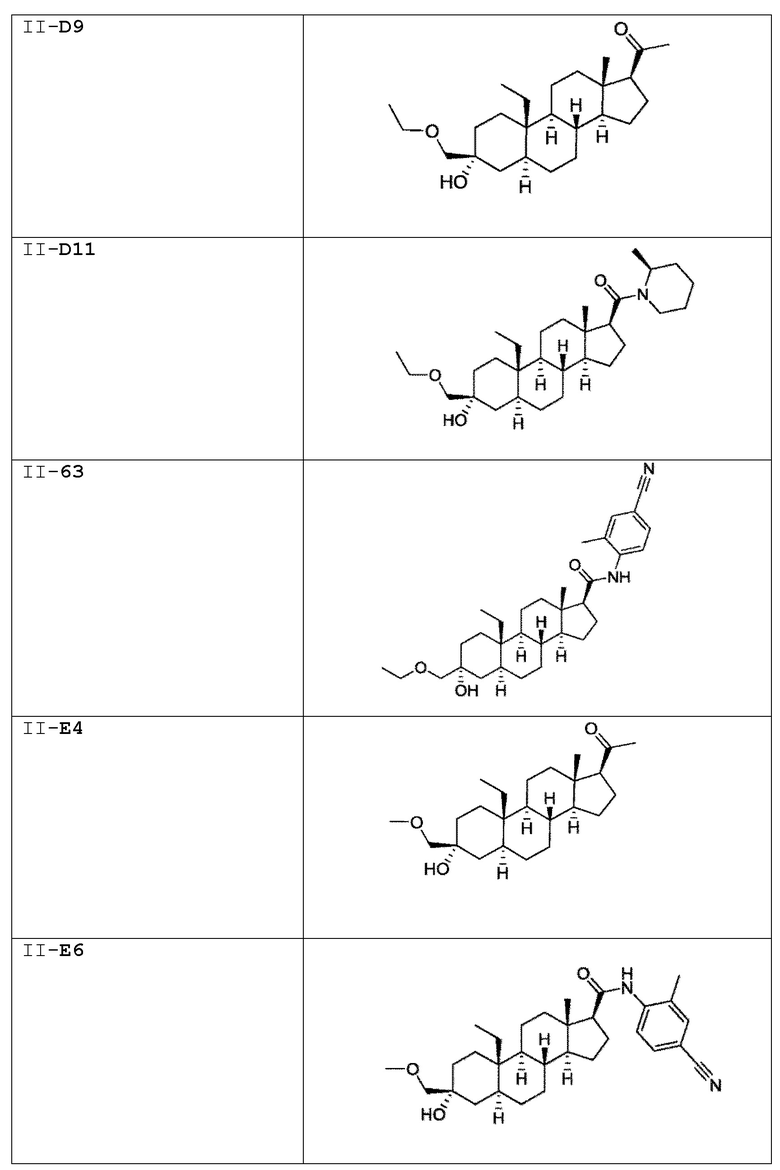
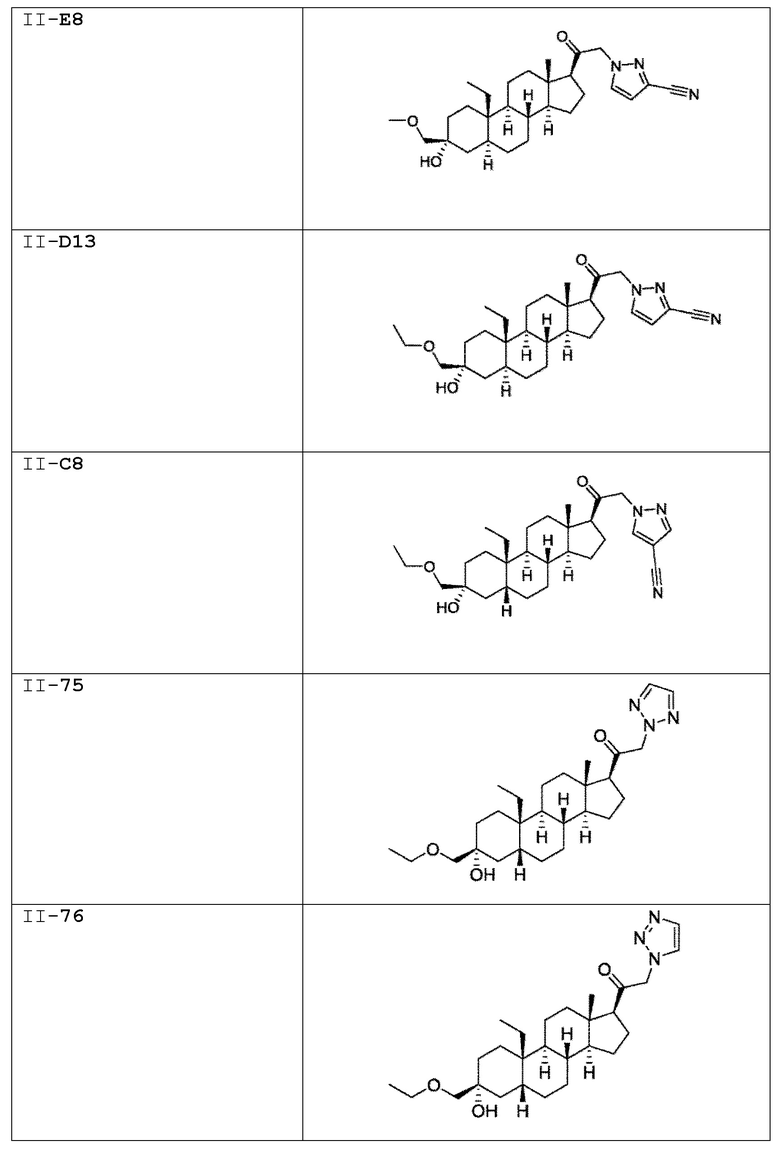
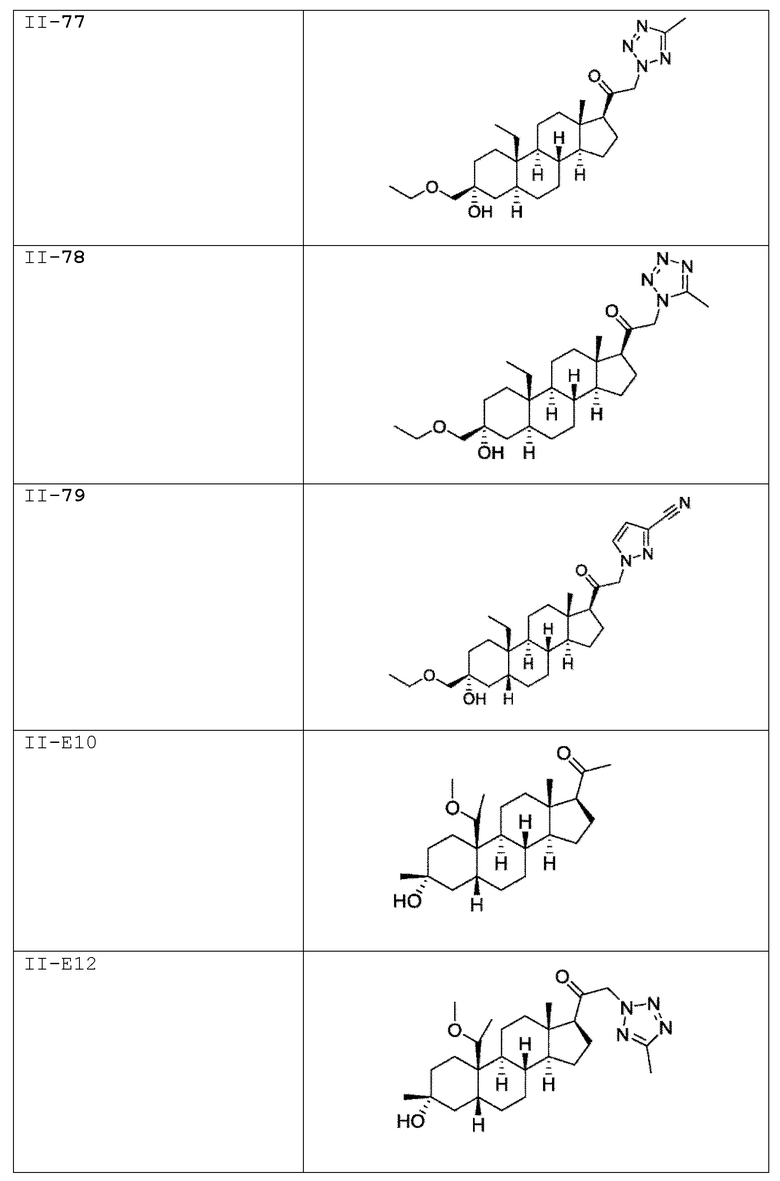
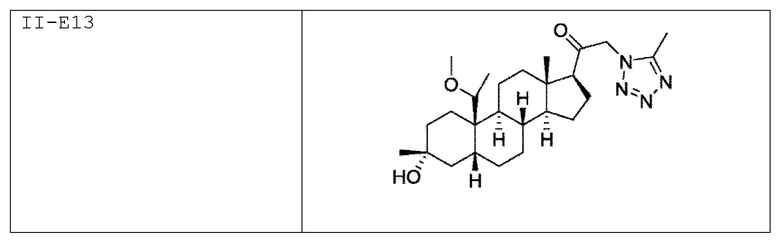
Соединения
[0241] В некоторых вариантах исполнения здесь представлено соединение Формулы (III-I)
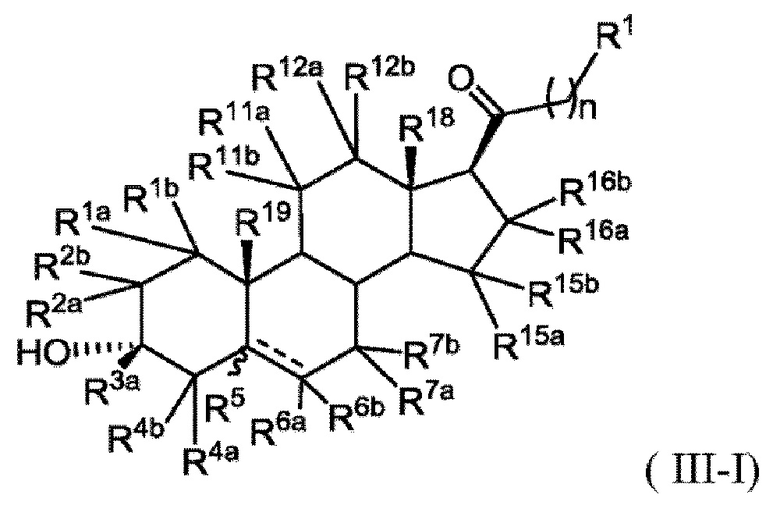
или фармацевтически приемлемая соль его;
в котором:
n составляет 0, 1 или 2;
R3a представляет замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил;
R18 представляет замещенный алкил, или незамещенный C2-C6-алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил;
R19 представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный C2-C6-алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил;
R5 представляет атом водорода или метил, или когда  представляет двойную связь, R5 отсутствует;
представляет двойную связь, R5 отсутствует;
каждый из R6a и R6b независимо представляет атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, или замещенный или незамещенный алкинил, или R6a и R6b объединены с образованием оксогруппы (=O);
R1 представляет замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил, -ORA1, -SRA1, -N(RA1)2, -N(RA1), -OC(=O)RA1, -OC(=O)ORA1, -OC(=O)SRA1, -OC(=O)N(RA1)2, -SC(=O)RA2, -SC(=O)ORA1, -SC(=O)SRA1, -SC(=O)N(RA1)2, -NHC(=O)RA1, -NHC(=O)ORA1, -NHC(=O)SRA1, -NHC(=O)N(RA1)2, -OS(=O)2RA2, -OS(=O)2ORA1, -S-S(=O)2RA2, -S-S(=O)2ORA1, -S(=O)RA2, -SO2RA2, или -S(=O)2ORA1, причем RA1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил, защитную группу для кислорода, когда присоединена к атому кислорода, защитную группу для серы, когда присоединена к атому серы, азотзащитную группу, когда присоединена к атому азота, или две RGA-группы объединены с образованием замещенного или незамещенного гетероциклического или гетероарильного цикла; и RA2 представляет замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил;
каждый из R1a, R1b, R2a, R2b, R4a, R4b, R7a, R7b, R11a, R11b, R12a, R12b, R15a, R15b, R16a, или R16b независимо представляет атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный гетероциклил, или замещенный или незамещенный алкинил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил, защитную группу для кислорода, когда присоединена к атому кислорода, азотзащитную группу, когда присоединена к атому азота, или две RD1-группы объединены с образованием замещенного или незамещенного гетероциклического ядра; или любые из R2a и R2b, R4a и R4b, R7a и R7b, R11a и R11b, и R12a и R12b объединены с образованием оксогруппы (=O); и
причем  представляет одинарную или двойную связь, при условии, что, если в Цикле В присутствует двойная связь, то один из R6a или R6b отсутствует.
представляет одинарную или двойную связь, при условии, что, если в Цикле В присутствует двойная связь, то один из R6a или R6b отсутствует.
[0242] В некоторых вариантах исполнения здесь представлено соединение Формулы (III-II)
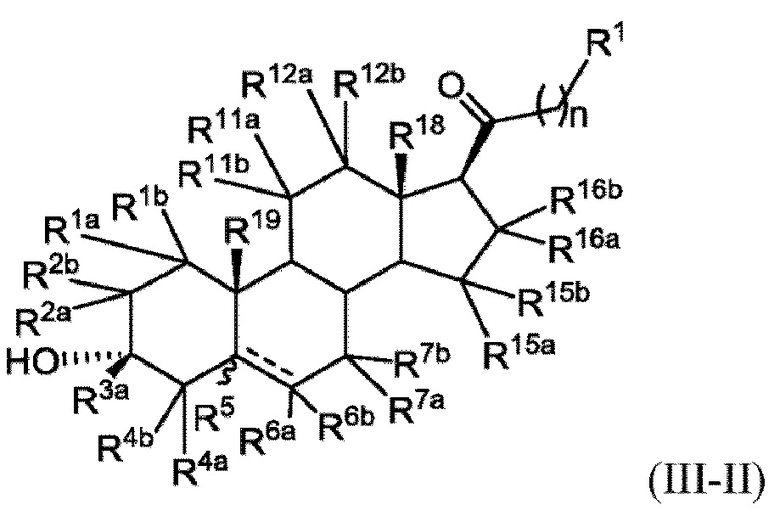
или фармацевтически приемлемая соль его;
причем переменные значения R18, n, R5, R1, R1a, R1b, R2a, R2b, R4a, R4b, R6a, R6b, R7a, R7b, R11a, R11b, R12a, R12b, R15a, R15b, R16a и R16b определены, как выше в Формуле III-I; и
R3a представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил; и
R19 представляет атом водорода, замещенный C1-C6-алкил, незамещенный C2-C6-алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил;
при условии, что, если n составляет 0, R1 представляет метил, и R1a, R1b, R2a, R2b, R4a, R4b, R6a, R6b, R7a, R7b, R11a, R11b, R12a, R12b, R15a, R15b, R16a и R16b представляют атом водорода, тогда R18 представляют замещенный C1-C6-алкил, незамещенный C3-C6-алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, причем, если R18 представляют замещенный метил, то метил замещен атомом галогена, -CN, -NO2,-SO2H, -SO3H, -ORaa, -ON(Rbb)2, -N(Rbb)2,-C(=O)Raa, -C(O)H, -CO2H, карбоциклилом, гетероциклилом, арилом, или гетероарилом, причем Raa, в каждом случае независимо, выбирают из C1-10-алкила, C1-10-галоалкила, C2-10-алкенила, C2-10-алкинила, C3-10-карбоциклила, 3-14-членного гетероциклила, C6-14-арила, и 5-14-членного гетероарила, или две Raa-группы объединены с образованием 3-14-членного гетероциклила, или 5-14-членного гетероарила, и Rbb, в каждом случае независимо, выбирают из атома водорода, -OH, -ORaa, -N(Rcc)2, -CN, -C(=O)Raa, -C(=O)N(Rcc)2, -CO2Raa, -SO2Raa, или -C(=NRcc)ORaa.
Формула (III-I) и Формула (III-II) Группа R18
[0243] В некоторых аспектах R18 представляет алкил, замещенный атомом галогена, цианогруппой, -СО2Н или фенилом.
[0244] В некоторых вариантах исполнения R18 представляет замещенный или незамещенный C2-6-алкил.
[0245] В некоторых вариантах исполнения R18 представляет -CH(CH3)2.
[0246] В некоторых вариантах исполнения R18 представляет замещенный алкил. В некоторых вариантах исполнения алкил замещен группой -OCH3, -CH2CN, или -OCH(CH3)2.
[0247] В некоторых вариантах исполнения R18 представляет пропил, бутил, трет-бутил, или изопропил, или этил.
Формула (III-I) и Формула (III-II) Группы R1a и R1b
[0248] В некоторых аспектах R1a и R1b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный гетероциклил, замещенный или незамещенный алкинил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0249] В некоторых аспектах R1a и R1b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, -ORD1, -OC(=O)RD1, -NH2, или -N(RD1)2, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0250] В некоторых аспектах R1a и R1b, в каждом случае независимо, представляют атом водорода, замещенный или незамещенный алкил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0251] В некоторых аспектах оба R1a и R1b представляют атом водорода.
[0252] В некоторых вариантах исполнения R1a и R1b, в каждом случае независимо, представляют атом водорода или замещенный или незамещенный алкил.
[0253] В некоторых вариантах исполнения R1a и R1b независимо представляют атом водорода, С1-С6-алкил, С1-С6-галоалкил, С1-С6-алкоксигруппу, С1-С6-галоалкоксигруппу, или -ОН.
В некоторых вариантах исполнения R1a и R1b представляют -СН3, -СН2СН3, -ОН, -ОСН3 или -СН(СН3)2.
Формула (III-I) и Формула (III-II) Группы R2a и R2b
[0254] В некоторых аспектах R2a и R2b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный гетероциклил, замещенный или незамещенный алкинил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0255] В некоторых аспектах R2a и R2b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, -ORD1, -OC(=O)RD1, -NH2, или -N(RD1)2, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0256] В некоторых аспектах R2a и R2b, в каждом случае независимо, представляют атом водорода, замещенный или незамещенный алкил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0257] В некоторых аспектах оба R2a и R2b представляют атом водорода.
[0258] В некоторых вариантах исполнения R2a и R2b, в каждом случае независимо, представляют атом водорода или замещенный или незамещенный алкил.
[0259] В некоторых вариантах исполнения R2a и R2b независимо представляют атом водорода, С1-С6-алкил, С1-С6-галоалкил, С1-С6-алкоксигруппу, С1-С6-галоалкоксигруппу, или -ОН.
[0260] В некоторых вариантах исполнения R2a и R2b представляют -СН3, -СН2СН3, -ОН, -ОСН3 или -СН(СН3)2.
Формула (III-I) и Формула (III-II) Группы R4a и R4b
[0261] В некоторых аспектах R4a и R4b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный гетероциклил, или замещенный или незамещенный алкинил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0262] В некоторых аспектах R4a и R4b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, -ORD1, -OC(=O)RD1, -NH2, или -N(RD1)2, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0263] В некоторых аспектах R4a и R4b, в каждом случае независимо, представляют атом водорода, замещенный или незамещенный алкил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0264] В некоторых аспектах оба R4a и R4b представляют атом водорода. В дополнительных вариантах исполнения R4a и R4b, в каждом случае независимо, представляют атом водорода или замещенный или незамещенный алкил.
[0265] В некоторых аспектах R4a и R4b независимо представляют атом водорода, С1-С6-алкил, С1-С6-галоалкил, С1-С6-алкоксигруппу, С1-С6-галоалкоксигруппу, или -ОН. В некоторых других аспектах R4a и R4b представляют -СН3, -СН2СН3, -ОН, -ОСН3 или -СН(СН3)2.
Формула (III-I) и Формула (III-II) Группы R11a и R11b
[0266] В некоторых вариантах исполнения R11a и R11b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный гетероциклил, или замещенный или незамещенный алкинил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0267] В некоторых дополнительных вариантах исполнения R11a и R11b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, -ORD1, -OC(=O)RD1, -NH2, или -N(RD1)2, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0268] В некоторых аспектах R11a и R11b, в каждом случае независимо, представляют атом водорода, замещенный или незамещенный алкил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил. В некоторых аспектах оба R11a и R11b представляют атом водорода.
[0269] В некоторых аспектах R11a и R11b, в каждом случае независимо, представляют атом водорода или замещенный или незамещенный алкил. В некоторых аспектах R11a и R11b независимо представляют атом водорода, С1-С6-алкил, С1-С6-галоалкил, С1-С6-алкоксигруппу, С1-С6-галоалкоксигруппу, или -ОН.
[0270] В некоторых других аспектах R11a и R11b представляют -СН3, -СН2СН3, -ОН, -ОСН3 или -СН(СН3)2.
[0271] В некоторых вариантах исполнения R11a и R11b объединены между собой с образованием оксогруппы (=О).
Формула (III-I) и Формула (III-II) Группы R15a и R15b
[0272] В некоторых вариантах исполнения R15a и R15b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный гетероциклил, или замещенный или незамещенный алкинил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0273] В некоторых вариантах исполнения R15a и R15b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, -ORD1, -OC(=O)RD1, -NH2, или -N(RD1)2, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0274] В некоторых вариантах исполнения R15a и R15b, в каждом случае независимо, представляют атом водорода, замещенный или незамещенный алкил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0275] В некоторых дополнительных вариантах исполнения оба R15a и R15b представляют атом водорода.
[0276] В некоторых аспектах R15a и R15b, в каждом случае независимо, представляют атом водорода или замещенный или незамещенный алкил. В некоторых аспектах R15a и R15b независимо представляют атом водорода, С1-С6-алкил, С1-С6-галоалкил, С1-С6-алкоксигруппу, С1-С6-галоалкоксигруппу, или -ОН. В некоторых аспектах R15a и R15b представляют -СН3, -СН2СН3, -ОН, -ОСН3 или -СН(СН3)2.
Формула (III-I) и Формула (III-II) Группы R16a и R16b
[0277] В некоторых аспектах R16a и R16b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный гетероциклил, или замещенный или незамещенный алкинил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0278] В некоторых вариантах исполнения R16a и R16b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, -ORD1, -OC(=O)RD1, -NH2, или -N(RD1)2, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0279] В некоторых вариантах исполнения R16a и R16b, в каждом случае независимо, представляют атом водорода, замещенный или незамещенный алкил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0280] В некоторых дополнительных вариантах исполнения оба R16a и R16b представляют атом водорода.
[0281] В некоторых аспектах R16a и R16b, в каждом случае независимо, представляют атом водорода или замещенный или незамещенный алкил. В некоторых аспектах R16a и R16b независимо представляют атом водорода, С1-С6-алкил, С1-С6-галоалкил, С1-С6-алкоксигруппу, С1-С6-галоалкоксигруппу, или -ОН.
[0282] В некоторых аспектах R16a и R16b представляют -СН3, -СН2СН3, -ОН, -ОСН3 или -СН(СН3)2.
Формула (III-I) и Формула (III-II) Группы R7a и R7b
[0283] В некоторых вариантах исполнения R7a и R7b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный гетероциклил, или замещенный или незамещенный алкинил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил, или любые из R7a и R7b объединены между собой с образованием оксогруппы (=О).
[0284] В некоторых дополнительных вариантах исполнения R7a и R7b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, -ORD1, -OC(=O)RD1, -NH2, или -N(RD1)2, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0285] В некоторых аспектах R7a и R7b, в каждом случае независимо, представляют атом водорода, замещенный или незамещенный алкил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0286] В некоторых аспектах все R7a и R7b представляют атом водорода.
[0287] В некоторых аспектах R7a и R7b, в каждом случае независимо, представляют атом водорода или замещенный или незамещенный алкил. В некоторых аспектах R7a и R7b независимо представляют атом водорода, С1-С6-алкил, С1-С6-галоалкил, С1-С6-алкоксигруппу, С1-С6-галоалкоксигруппу, или -ОН.
[0288] В некоторых аспектах R7a и R7b представляют -СН3, -СН2СН3, -ОН, -ОСН3 или -СН(СН3)2.
[0289] В некоторых вариантах исполнения любые из R7a и R7b объединены между собой с образованием оксогруппы (=О).
Формула (III-I) и Формула (III-II) Группа R5
[0290] В некоторых аспектах R5 представляет атом водорода в цис-положении относительно С19-положения. В некоторых других аспектах R5 представляет атом водорода в транс-положении относительно С19-положения. В некоторых вариантах исполнения R5 представляет метил в цис-положении относительно С19-положения. В некоторых дополнительных вариантах исполнения R5 представляет метил в транс-положении относительно С19-положения.
Формула (III-I) и Формула (III-II) Группа R3a
[0291] В некоторых вариантах исполнения R3а представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, или замещенный или незамещенный алкинил.
[0292] В некоторых вариантах исполнения R3а представляет замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0293] В некоторых вариантах исполнения R3а представляет замещенный или незамещенный алкил.
[0294] В некоторых вариантах исполнения R3а представляет атом водорода. В некоторых вариантах исполнения R3а представляет замещенный алкил (например, -CH2OMe или -CH2OEt, и т.д.). В некоторых вариантах исполнения R3а представляет незамещенный алкил. В некоторых вариантах исполнения R3а представляет метил.
[0295] В некоторых аспектах R3а не представляет трифторметил.
Формула (III-I) и Формула (III-II) Группа R19
[0296] В некоторых аспектах R19 представляет замещенный алкил. В некоторых аспектах R19 представляет незамещенный алкил.
[0297] В некоторых аспектах R19 представляет С2-С6-алкил. В некоторых вариантах исполнения R19 представляет атом водорода. В некоторых аспектах R19 представляет С2-С6-алкил с дейтериевым замещением.
[0298] В некоторых вариантах исполнения R19 представляет замещенный С2-С6-алкил. В некоторых вариантах исполнения R19 представляет незамещенный С2-С6-алкил.
[0299] В некоторых вариантах исполнения R19 представляет замещенный С2-С6-алкенил. В некоторых вариантах исполнения R19 представляет незамещенный С2-С6-алкенил.
[0300] В некоторых вариантах исполнения R19 представляет замещенный С2-С6-алкинил. В некоторых вариантах исполнения R19 представляет незамещенный С2-С6-алкинил.
[0301] В некоторых аспектах R19 представляет этил.
Формула (III-I) и Формула (III-II) Группы R6a и R6b
[0302] В некоторых вариантах исполнения R6a и R6b независимо представляет атом водорода, галоген, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, или замещенный или незамещенный алкинил.
[0303] В некоторых аспектах R6a и R6b независимо представляет атом водорода или замещенный или незамещенный алкил.
[0304] В некоторых аспектах R6a и R6b независимо представляет атом водорода или замещенный алкил. В некоторых аспектах R6a и R6b независимо представляет атом водорода или незамещенный алкил.
[0305] В некоторых аспектах оба R6a и R6b представляют атом водорода. В некоторых аспектах R6a представляет галоген или алкил, и R6b представляет атом водорода. В некоторых вариантах исполнения оба R6a и R6b представляют галоген.
[0306] В некоторых аспектах оба R6a и R6b представляют алкил.
[0307] В некоторых вариантах исполнения R6a и R6b объединены с образованием оксогруппы.
Формула (III-I) и Формула (III-II) Группы R12a и R12b
[0308] В некоторых аспектах R12a и R12b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный гетероциклил, замещенный или незамещенный алкинил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0309] В некоторых аспектах R12a и R12b, в каждом случае независимо, представляют атом водорода, галоген, цианогруппу, гидроксил, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, -ORD1, -OC(=O)RD1, -NH2, или -N(RD1)2, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0310] В некоторых вариантах исполнения R12a и R12b, в каждом случае независимо, представляют атом водорода, замещенный или незамещенный алкил, -ORD1, -OC(=O)RD1, -NH2, -N(RD1)2, или -NRD1C(=O)RD1, причем RD1, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0311] В некоторых вариантах исполнения оба R12a и R12b представляют атом водорода.
[0312] В некоторых дополнительных вариантах исполнения R12a и R12b, в каждом случае независимо, представляют атом водорода или замещенный или незамещенный алкил.
[0313] В некоторых вариантах исполнения R12a и R12b объединены между собой с образованием оксогруппы (=O).
Формула (III-I) и Формула (III-II) Группы n
[0314] В некоторых вариантах исполнения n составляет 1. В некоторых других вариантах исполнения n составляет 2.
[0315] В некоторых вариантах исполнения n составляет 0. В некоторых вариантах исполнения n составляет 1. В некоторых других вариантах исполнения n составляет 2.
Формула (III-I) и Формула (III-II) Группы R1
[0316] В некоторых вариантах исполнения R1 представляет замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, или замещенный или незамещенный гетероарил.
[0317] В некоторых вариантах исполнения R1 представляет
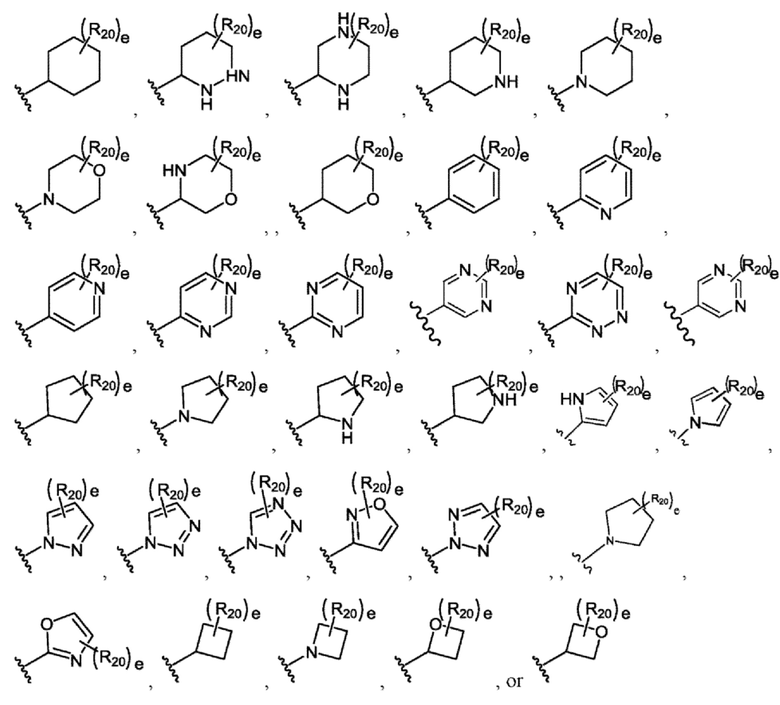
причем R20, в каждом случае независимо, представляет галоген, -NO2, -CN, -ORGA, -N(RGA)2, -C(=O)RGA, -C(=O)ORGA, -OC(=O)RGA, -OC(=O)ORGA, -C(=O)N(RGA)2, -N(RGA)C(=O)RGA, -OC(=O)N(RGA)2, -N(RGA)C(=O)ORGA, -S(=O)2RGA, -S(=O)2ORGA, -OS(=O)2RGA, -S(=O)2N(RGA)2, или -N(RGA)S(=O)2RGA; замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, замещенный или незамещенный C3-6-карбоциклил, замещенный или незамещенный 3-6-членный гетероциклил, замещенный или незамещенный C5-10-арил, замещенный или незамещенный 5-10-членный гетероарил, или необязательно две RGA-группы связаны общими атомами с образованием замещенного или незамещенного 3-4-членного карбоциклического или гетероциклического цикла; причем RGA, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, замещенный или незамещенный C3-6-карбоциклил, замещенный или незамещенный 3-6-членный гетероциклил, замещенный или незамещенный арил, замещенный или незамещенный гетероарил, защитную группу для кислорода, когда присоединена к атому кислорода, азотзащитную группу, когда присоединена к атому азота, или две RGA-группы связаны общими атомами с образованием замещенного или незамещенного карбоциклического или гетероциклического цикла; и e составляет 0, 1, 2, 3, 4, или 5, или n составляет 0, 1, 2, 3, 4, или 5.
[0318] В некоторых вариантах исполнения, в которых R1 представляет
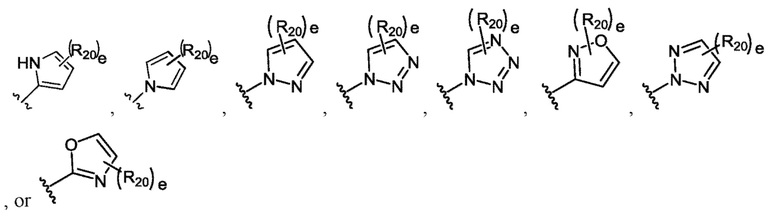
причем R20, в каждом случае независимо, представляет галоген, -NO2, -CN, -ORGA, -N(RGA)2, -C(=O)RGA, -C(=O)ORGA, -OC(=O)RGA, -OC(=O)ORGA, -C(=O)N(RGA)2, -N(RGA)C(=O)RGA, -OC(=O)N(RGA)2, -N(RGA)C(=O)ORGA, -S(=O)2RGA, -S(=O)2ORGA, -OS(=O)2RGA, -S(=O)2N(RGA)2, или -N(RGA)S(=O)2RGA; замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, замещенный или незамещенный C3-6-карбоциклил, замещенный или незамещенный 3-6-членный гетероциклил, замещенный или незамещенный C5-10-арил, замещенный или незамещенный 5-10-членный гетероарил, или необязательно две RGA-группы связаны общими атомами с образованием замещенного или незамещенного 3-4-членного карбоциклического или гетероциклического цикла; причем RGA, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, замещенный или незамещенный C3-6-карбоциклил, замещенный или незамещенный 3-6-членный гетероциклил, замещенный или незамещенный арил, замещенный или незамещенный гетероарил, защитную группу для кислорода, когда присоединена к атому кислорода, азотзащитную группу, когда присоединена к атому азота, или две RGA-группы связаны общими атомами с образованием замещенного или незамещенного карбоциклического или гетероциклического цикла; и e составляет 0, 1, 2, 3, 4, или 5.
[0319] В некоторых вариантах исполнения соединение Формулы (III-I) или (III-II) представляет собой соединение Формулы (III-Ia)
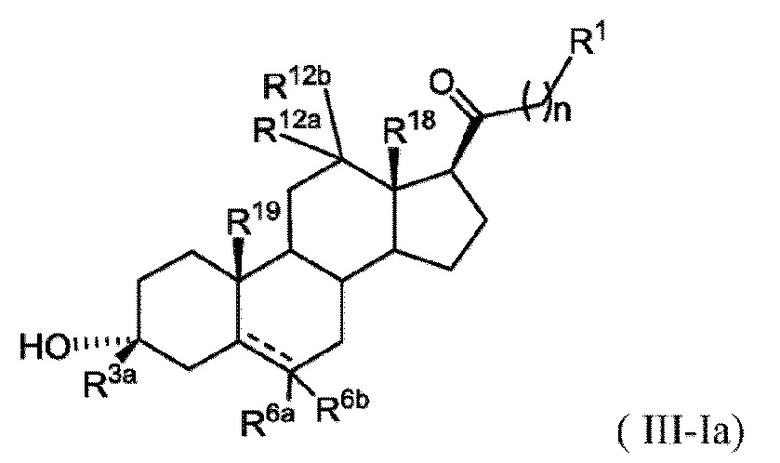
или фармацевтически приемлемую соль его.
[0320] В некоторых вариантах исполнения соединение Формулы (III-I) или (III-II) представляет собой соединение Формулы (III-Ib)
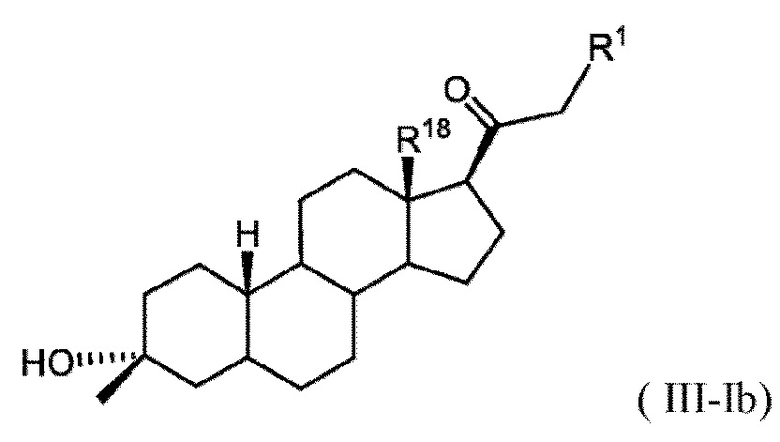
или фармацевтически приемлемую соль его.
В некоторых вариантах исполнения соединение Формулы (III-I) или (III-II) представляет собой соединение Формулы (III-Ie)
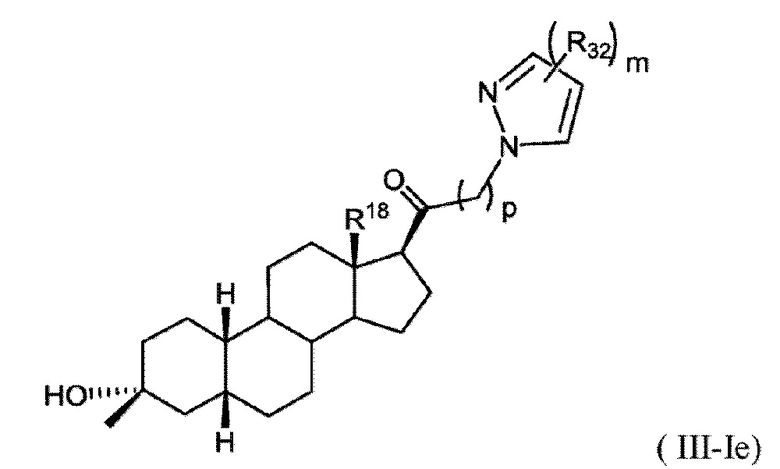
в котором m составляет 0, 1, 2 или 3;
p составляет 0, 1, или 3;
каждый R32 независимо представляет галоген, алкил, гидроксил или цианогруппу;
или фармацевтически приемлемую соль его.
В некоторых вариантах исполнения соединение Формулы (III-I) или (III-II) представляет собой соединение Формулы (III-Ig)
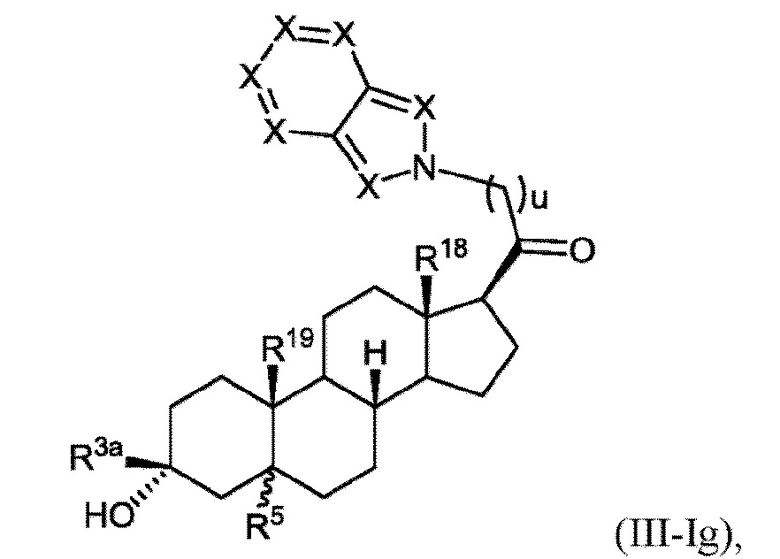
причем u составляет 0, 1, или 2; каждый X независимо представляет -C(RN)-, -C(RN)2-, -O-, -S-, -N-, или N(RN)-, причем RN независимо представляет атом водорода, замещенный или незамещенный C1-6-алкил, C(=O)RGA, -C(=O)ORGA, -C(=O)N(RGA)2, -S(=O)2RGA, или -S(=O)2N(RGA)2; и RGA, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, замещенный или незамещенный C3-6-карбоциклил, замещенный или незамещенный 3-6-членный гетероциклил, замещенный или незамещенный арил, замещенный или незамещенный гетероарил, защитную группу для кислорода, когда присоединена к атому кислорода, азотзащитную группу, когда присоединена к атому азота, или две RGA-группы связаны общими атомами с образованием замещенного или незамещенного гетероциклического или гетероарильного цикла;
или фармацевтически приемлемую соль его.
В некоторых вариантах исполнения соединение Формулы (III-I) или (III-II) представляет собой соединение Формулы (III-Ih)
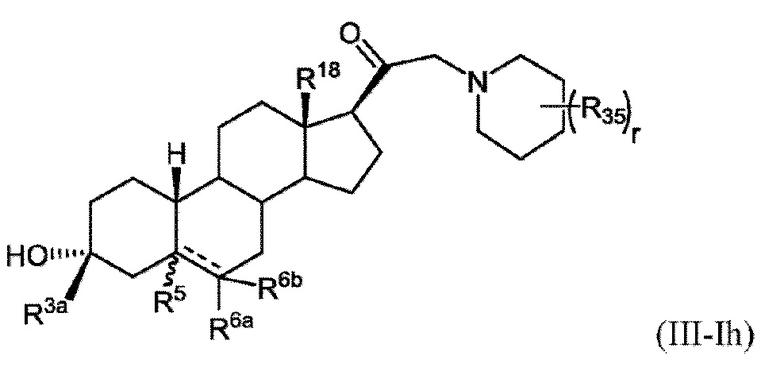
в котором каждый R35 независимо представляет галоген, алкил, гидроксил или цианогруппу; и r составляет 0, 1, 2 или 3;
или фармацевтически приемлемую соль его.
В некоторых вариантах исполнения соединение Формулы (III-I) или (III-II) представляет собой соединение Формулы (III-Ii)
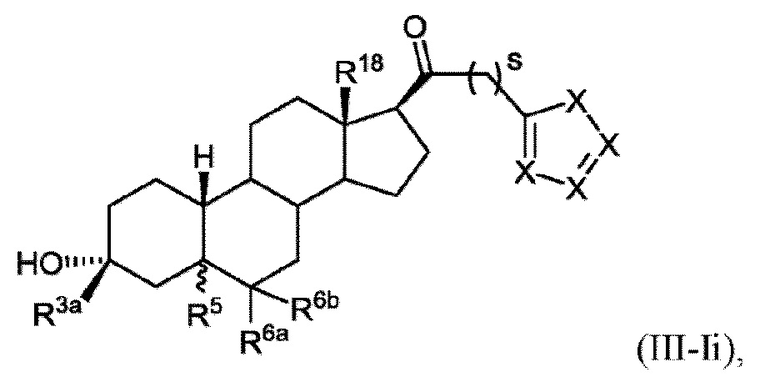
в котором s составляет 0, 1, или 2; каждый X независимо представляет -C(RN)-, -C(RN)2-, -O-, -S-, -N-, или N(RN)-, причем RN независимо представляет атом водорода, замещенный или незамещенный C1-6-алкил, C(=O)RGA, -C(=O)ORGA, -C(=O)N(RGA)2, -S(=O)2RGA, или -S(=O)2N(RGA)2; и
RGA, в каждом случае независимо, представляет атом водорода, замещенный или незамещенный C1-6-алкил, замещенный или незамещенный C2-6-алкенил, замещенный или незамещенный C2-6-алкинил, замещенный или незамещенный C3-6-карбоциклил, замещенный или незамещенный 3-6-членный гетероциклил, замещенный или незамещенный арил, замещенный или незамещенный гетероарил, защитную группу для кислорода, когда присоединена к атому кислорода, азотзащитную группу, когда присоединена к атому азота, или две RGA-группы связаны общими атомами с образованием замещенного или незамещенного гетероциклического или гетероарильного цикла;
или фармацевтически приемлемую соль его.
[0321] В некоторых вариантах исполнения соединение выбирают из группы, состоящей из соединений, идентифицированных здесь ниже в Таблице III-I:
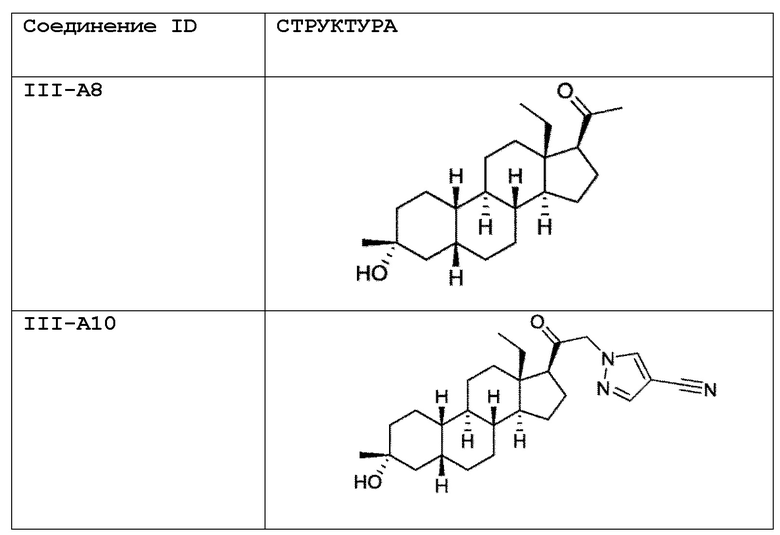
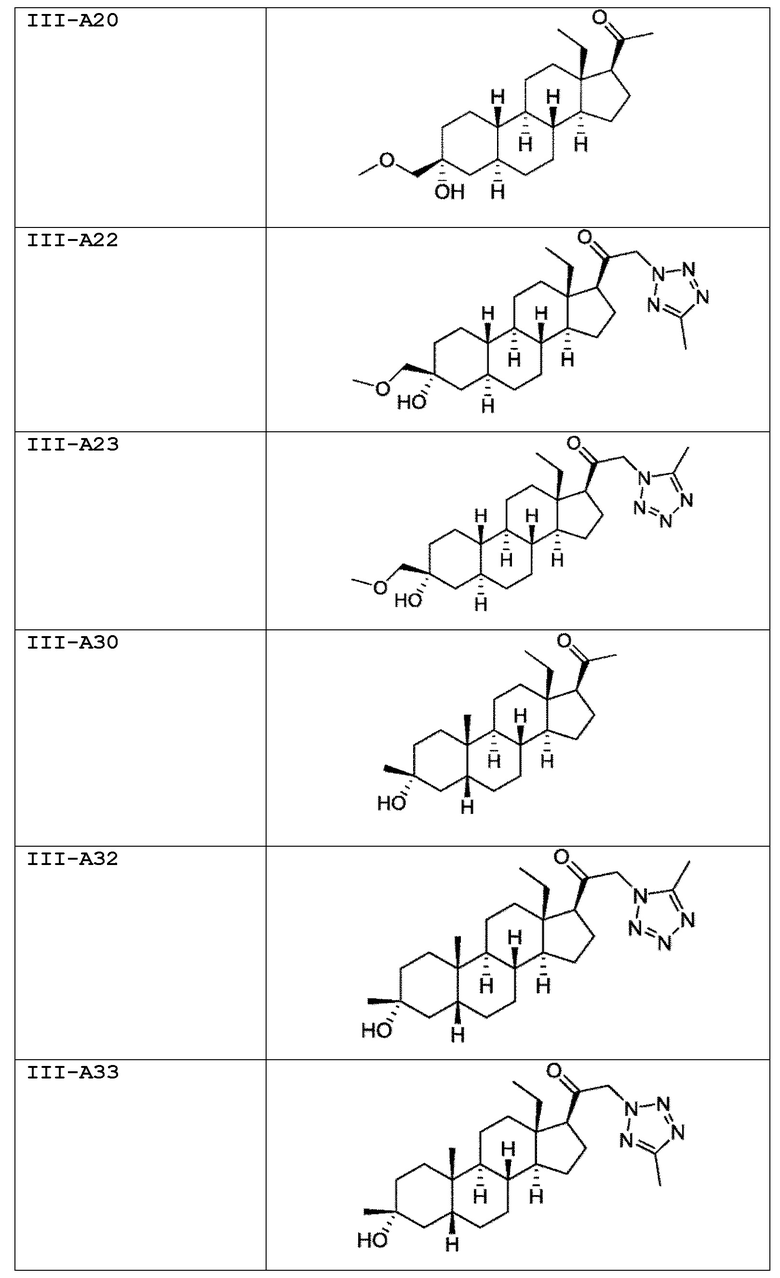
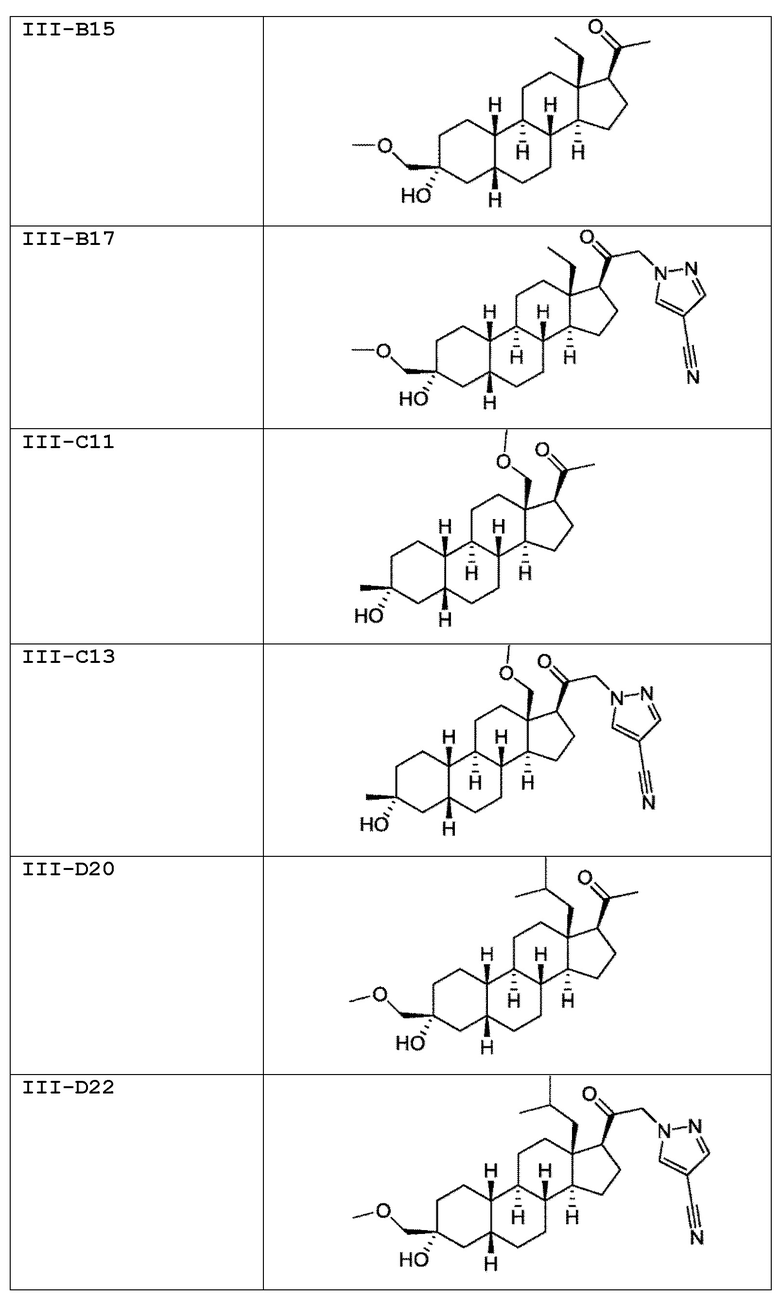
[0322] В одном аспекте здесь представлена фармацевтически приемлемая соль описанного здесь соединения (например, соединения Формулы (I-X, I-I, II-I, III-1 или III-2)
[0323] В одном аспекте здесь представлена фармацевтически приемлемая композиция, включающая описанное здесь соединение (например, соединение Формулы (I-X, I-I, II-I, III-I или III-II), или фармацевтически приемлемую соль его, и и фармацевтически приемлемый эксципиент.
[0324] В определенных вариантах исполнения соединение согласно настоящему изобретению вносят в фармацевтическую композицию в эффективном количестве. В определенных вариантах исполнения соединение согласно настоящему изобретению вводят в терапевтически эффективном количестве. В определенных вариантах исполнения соединение согласно настоящему изобретению вводят в профилактически эффективном количестве.
[0325] Соединения согласно настоящему изобретению, как здесь описанные, действуют, в определенных вариантах исполнения, как ГАМКА-модуляторы, например, воздействием на ГАМКА-рецептор позитивным или негативным образом. В качестве модуляторов возбудимости центральной нервной системы (ЦНС, CNS) при содействии их способности модулировать ГАМКА-рецептор, такие соединения предполагаются имеющими CNS-активность.
[0326] Так, в еще одном аспекте представлены способы лечения связанного с ЦНС заболевания у нуждающегося в этом субъекта, включающие введение субъекту эффективного количества соединения согласно настоящему изобретению. В определенных вариантах исполнения связанное с ЦНС заболевание представляет собой нарушение сна, расстройство настроения, расстройство шизофренического спектра, судорожный синдром, нарушение памяти и/или познавательной способности, нарушение движений, изменение личности, расстройство аутистического спектра, боль, травматическое повреждение мозга, сосудистые болезни, связанные с наркотической зависимостью расстройства, и/или абстинентный синдром, шум в ушах, или эпилептический статус. В определенных вариантах исполнения связанное с ЦНС заболевание представляет собой депрессию. В определенных вариантах исполнения связанное с ЦНС заболевание представляет собой послеродовую депрессию. В определенных вариантах исполнения связанное с ЦНС заболевание представляет собой большое депрессивное расстройство. В определенных вариантах исполнения большое депрессивное расстройство представляет собой большое депрессивное расстройство в умеренной форме. В определенных вариантах исполнения большое депрессивное расстройство представляет собой большое депрессивное расстройство в тяжелой форме. В определенных вариантах исполнения соединение вводят перорально, подкожно, внутривенно или внутримышечно. В определенных вариантах исполнения соединение вводят перорально. В определенных вариантах исполнения соединение вводят хронически. В определенных вариантах исполнения соединение вводят непрерывно, например, непрерывной внутривенной инфузией.
[0327] Примерные соединения согласно изобретению могут быть синтезированы из следующих известных исходных материалов с использованием способов, известных квалифицированному специалисту в этой области технологии, или следуя определенным литературным источникам. В одном аспекте здесь представлена фармацевтически приемлемая соль описанного здесь соединения (например, соединения Формулы (I-X, I-I, II-I, III-I, или III-II).
Альтернативные варианты осуществления изобретения
[0328] В одном альтернативном варианте осуществления описанные здесь соединения могут также включать один или многие изотопные заместители. Например, водород может представлять собой 2Н (D, или дейтерий) или 3Н (Т, или тритий), например, углерод может представлять собой 13С или 14С; например, кислород может быть 18О; например, азот может быть 15N, и тому подобно. В других вариантах исполнения конкретный изотоп (например, 3Н, 13С, 14С, 18О, или 15N) может присутствовать в количестве по меньшей мере 1%, по меньшей мере 5%, по меньшей мере 10%, по меньшей мере 15%, по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 35%, по меньшей мере 40%, по меньшей мере 45%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 99%, или по меньшей мере 99,9% от общего изотопного состава элемента, который занимает заданное место в соединении.
Фармацевтические композиции
[0329] В одном аспекте здесь представлена фармацевтическая композиция, включающая описанное здесь соединение (например, соединение Формулы (I-X, I-I, II-I, III-I, или III-II)), или фармацевтически приемлемую соль его, и фармацевтически приемлемый эксципиент. В определенных вариантах исполнения соединение согласно настоящему изобретению вводят в фармацевтическую композицию в эффективном количестве. В определенных вариантах исполнения соединение согласно настоящему изобретению вводят в терапевтически эффективном количестве. В определенных вариантах исполнения соединение согласно настоящему изобретению вводят в профилактически эффективном количестве.
[0330] В определенных вариантах исполнения фармацевтическая композиция включает эффективное количество активного ингредиента. В определенных вариантах исполнения фармацевтическая композиция включает терапевтически эффективное количество активного ингредиента.
[0331] Представленная здесь фармацевтическая композиция может быть введена разнообразными путями, включающими, но без ограничения этим, пероральное (энтеральное) введение, парентеральное (путем инъекции) введение, ректальное введение, трансдермальное введение, интрадермальное введение, интратекальное введение, подкожное (SC) введение, внутривенное (IV) введение, внутримышечное (IM) введение и интраназальное введение.
[0332] Как правило, представленные здесь соединения вводят в эффективном количестве. Количество соединения, вводимое фактически, обычно будет определяться врачом с учетом релевантных обстоятельств, включая излечиваемое состояние, выбранный путь введения, фактическое вводимое соединение, возраст, вес и реакцию индивидуального пациента, серьезность симптомов у пациента, и тому подобные.
[0333] При использовании для предупреждения начала расстройства ЦНС, представленные здесь соединения будут вводиться субъекту, имеющему опасность развития состояния, типично по совету и под наблюдением врача при уровнях доз, описанных выше. Субъекты с опасностью развития определенного состояния, как правило, включают тех, кто имеет семейный анамнез состояния, или тех, у кого генетическим исследованием или скринингом идентифицирована особая подверженность к развитию состояния.
[0334] Представленные здесь фармацевтические композиции также могут вводиться длительно («хроническое введение»). Хроническое введение относится к введению соединения или его фармацевтической композиции в течение продолжительного периода времени, например, в течение 3 месяцев, 6 месяцев, 1 года, 2 лет, 3 лет, 5 лет и т.д., или может продолжаться неограниченно долго, например, всю остальную жизнь субъекта. В определенных вариантах исполнения предполагается, что хроническое введение обеспечивает постоянный уровень соединения в крови, например, в пределах терапевтического окна, в течение длительного периода времени.
[0335] Кроме того, представленные здесь фармацевтические композиции могут доставляться с использованием различных методов дозирования. Например, в определенных вариантах исполнения фармацевтическая композиция может даваться в виде болюса, например, для того, чтобы повысить концентрацию соединения в крови до эффективного уровня. Размещение болюсной дозы зависит от системных уровней активного ингредиента, желательных для организма, например, внутримышечная или подкожная болюсная доза обеспечивает возможность медленного высвобождения активного ингредиента, тогда как болюсная доставка непосредственно в вену (например, внутривенным (IV) вливанием) делает возможной значительно более быструю доставку, которая быстро повышает концентрацию активного ингредиента в крови до эффективного уровня. В других вариантах исполнения фармацевтическую композицию можно вводить непрерывной инфузией, например, внутривенно через капельницу, для обеспечения поддержания установившейся концентрации активного ингредиента в организме субъекта. Кроме того, в других дополнительных вариантах исполнения фармацевтическую композицию можно вводить сначала в виде болюсной дозы, а затем непрерывной инфузией. Композициям для перорального введения может быть придана форма объемных жидких растворов или суспензий или массы порошка. Однако чаще композиции предоставляют в стандартных лекарственных формах для облегчения точного дозирования. Термин «стандартные лекарственные формы» относится к физически дискретным единицам, подходящим в качестве однократных дозировок для больных людей и других млекопитающих, причем каждая единица содержит предварительно заданное количество активного материала, рассчитанное на получение желательного терапевтического действия, в сочетании с подходящим фармацевтическим эксципиентом. Типичные стандартные лекарственные формы включают предварительно наполненные жидкими композициями предварительно установленного объема ампулы или шприцы, или пилюли, таблетки, капсулы или подобные формы в случае твердых композиций. В таких композициях соединение обычно составляет меньший по содержанию компонент (от около 0,1 до около 50% по весу, или предпочтительно от около 1 до около 40% по весу), где остальное количество составляют различные носители или эксципиенты, и способствующие переработке вспомогательные вещества для формирования желательной лекарственной формы.
[0336] При пероральном приеме характерными схемами являются от одной до пяти, в особенности, от двух до четырех, и обычно три пероральные дозы в сутки. При использовании таких схем приема каждая доза доставляет от около 0,01 до около 20 мг/кг представленного здесь соединения, причем предпочтительные дозы доставляют в каждом случае от около 0,1 до около 10 мг/кг, и в особенности, от около 1 до около 5 мг/кг.
[0337] Трансдермальные дозы, как правило, выбираются для достижения подобных или меньших уровней в крови, чем уровни, достигаемые с использованием инъекций, как правило, в количестве, варьирующем от около 0,01 до около 20% по весу, предпочтительно от около 0,1 до около 20% по весу, предпочтительно от около 0,1 до около 10% по весу, и более предпочтительно от около 0,5 до около 15% по весу.
[0338] Уровни доз, вводимых инъекцией, варьируют от около 0,1 мг/кг/час до по меньшей мере 10 мг/кг/час, все в течение от около 1 часа до около 120 часов, и в особенности от 24 до 96 часов. Также для достижения адекватных установившихся уровней можно вводить предварительно нагружающий болюс от около 0,1 мг/кг до около 10 мг/кг или больше. Предполагается, что максимальная общая доза не превышает около 5 г/день для больного человека весом от 40 до 80 кг.
[0339] Жидкие формы, подходящие для перорального введения, могут включать подходящий водный или неводный носитель с буферами, суспендирующими и диспергирующими веществами, красителями, отдушками, и тому подобными. Твердые формы могут включать, например, любой из следующих ингредиентов или соединений подобной природы: связующий материал, такой как микрокристаллическая целлюлоза, трагакантовая камедь или желатин; эксципиент, такой как крахмал или лактоза, дезинтегратор, такой как альгиновая кислота, примогель или кукурузный крахмал; смазочное средство, такое как стеарат магния; регулятор сыпучести (глидант), такой как коллоидный диоксид кремния; подсластитель, такой как сахароза или сахарин; или вкусо-ароматическую добавку, такую как перечная мята, метилсалицилат или апельсиновая отдушка.
[0340] Инъецируемые композиции обычно имеют основой стерильный физиологический раствор для инъекций или физиологический раствор с фосфатным буфером, или другие известные в технологии инъецируемые эксципиенты. Как и прежде, активное соединение в таких композициях типично является меньшим по содержанию компонентом, часто составляющим от около от 0,05 до 10% по весу, где остальное количество составляет инъецируемый эксципиент и тому подобные.
[0341] Трансдермальные композиции обычно составляют в виде мази или крема для местного применения, содержащих активный(-ные) ингредиент(-ты). При составлении в виде мази активные ингредиенты обычно будут объединены либо в парафиновой, либо в смешивающейся с водой основой мази. В альтернативном варианте, активные ингредиенты могут быть составлены в виде крема, например, крема с основой типа масло-в-воде. Такие трансдермальные препараты являются общеизвестными в технологии и, как правило, включают дополнительные ингредиенты для усиления проникновения в кожу или устойчивости активных ингредиентов или препарата. Все такие известные трансдермальные препараты и ингредиенты включены в область настоящего изобретения.
[0342] Представленные здесь соединения также могут быть введены с помощью трансдермального устройства. Соответственно этому, трансдермальное введение может быть выполнено с использованием пластыря или резервуара, или пористой мембраны или различных твердых матриц.
[0343] Вышеописанные компоненты для композиций, вводимых перорально, инъекцией или местным применением, являются только показательными. Другие материалы, а также методы обработки и тому подобные изложены в Части 8 издания Remington’s Pharmaceutical Sciences, 17-ое издание, 1985, издательство Mack Publishing Company, Истон, Пенсильвания, которое включено здесь ссылкой.
[0344] Соединения согласно настоящему изобретению также могут быть введены в формах с отсроченным высвобождением, или из систем доставки с пролонгированным высвобождением лекарственного средства. Описание типичных материалов для пролонгированного высвобождения можно найти в издании Remington’s Pharmaceutical Sciences.
[0345] Настоящее изобретение также относится к фармацевтически приемлемой образованной присоединением кислоты соли соединения согласно настоящему изобретению. Кислота, которая может быть использована для получения фармацевтически приемлемой соли, является такой, которая образует нетоксичную соль присоединения кислоты, то есть, соль, содержащую фармакологически приемлемые анионы, такие как гидрохлорид, гидроиодид, гидробромид, нитрат, сульфат, бисульфат, фосфат, ацетат, лактат, цитрат, тартрат, сукцинат, малеинат, фумарат, бензоат, пара-толуолсульфонат, и тому подобные.
[0346] В еще одном аспекте изобретение представляет фармацевтическую композицию, включающую соединение согласно настоящему изобретению и фармацевтически приемлемый эксципиент, например, композицию, пригодную для инъекции, такой как внутривенное (IV) введение.
[0347] Фармацевтически приемлемые эксципиенты включают любые и все разбавители или прочие жидкостные носители, диспергаторы или суспендирующие вспомогательные добавки, поверхностно-активные вещества, изотонические растворы, консерванты, смазочные средства, и тому подобные, насколько пригодные для конкретной желательной лекарственной формы, например, для инъекции. Общие соображения в отношении составления и/или получения агентов для фармацевтических композиций можно найти, например, в изданиях Remington’s Pharmaceutical Sciences, шестнадцатое издание, E. W. Martin (Mack Publishing Co., Истон, Пенсильвания, 1980), и Remington: The Science and Practice of Pharmacy, 21-ое издание (Lippincott Williams & Wilkins, 2005).
[0348] Например, инъецируемые препараты, такие как стерильные водные суспензии для инъекций, могут быть составлены согласно известной технологиии с использованием пригодных диспергаторов и смачивателей, и суспендирующих добавок. Примерные эксципиенты, которые могут быть использованы, включают, но без ограничения этим, воду, стерильный физиологический раствор или содержащий фосфатный буфер физиологический раствор, или раствор Рингера.
[0349] В определенных вариантах исполнения фармацевтическая композиция дополнительно включает производное циклодекстрина. Наиболее распространенными циклодекстринами являются α-, β- и γ-циклодекстрины, состоящие из 6, 7 и 8 α-1,4-соединенных глюкозных звеньев, соответственно, необязательно включающие один или многие заместители на соединенных углеводных фрагментах, которые включают, но не ограничиваются этим, заместители, введенные метилированием, гидроксиалкилированием, ацилированием и введением простого сульфоалкилэфира. В определенных вариантах исполнения циклодекстрин представляет собой простой сульфоалкиловый эфир β-циклодекстрина, например, простой сульфобутиловый эфир β-циклодекстрина, также известный как CAPTISOL®. Смотри, например, Патент США 5,376,645. В определенных вариантах исполнения композиция включает гексапропил-β-циклодекстрин. В более конкретном варианте исполнения композиция включает гексапропил-β-циклодекстрин (10-50% в воде).
[0350] Инъецируемая композиция может быть стерилизована, например, фильтрацией через задерживающий бактерии фильтр, или введением стерилизующих агентов в форме стерильных твердых композиций, которые могут быть растворены или диспергированы в стерильной воде или другой стерильной инъецируемой среде перед применением.
[0351] Как правило, представленные здесь соединения вводятся в эффективном количестве. Фактически вводимое количество соединения обычно будет определяться врачом с учетом соответственных обстоятельств, включая излечиваемое состояние, выбранный путь введения, фактическое вводимое соединение, возраст, вес и реакцию индивидуального пациента, серьезность симптомов у пациента, и тому подобные.
[0352] Композиции представлены в стандартных лекарственных формах для облегчения точного дозирования. Термин «стандартные лекарственные формы» относится к физически дискретным единицам, подходящим в качестве однократных дозировок для больных людей и других млекопитающих, причем каждая единица содержит предварительно заданное количество активного материала, рассчитанное на получение желательного терапевтического действия, в сочетании с подходящим фармацевтическим эксципиентом. Типичные стандартные лекарственные формы включают предварительно наполненные жидкими композициями предварительно установленного объема ампулы или шприцы. В таких композициях соединение обычно составляет меньший по содержанию компонент (от около 0,1% до около 50% по весу, или предпочтительно от около 1% до около 40% по весу), где остальное количество составляют различные носители или эксципиенты, и способствующие переработке вспомогательные вещества для формирования желательной лекарственной формы.
[0353] Представленные здесь соединения могут быть введены как единственный активный агент, или они могут быть введены в комбинации с другими активными агентами. В одном аспекте настоящее изобретение представляет комбинацию соединения согласно настоящему изобретению и еще одного фармакологически активного агента. Введение в комбинации может производиться любым способом, очевидным для квалифицированных специалистов в этой области технологии, включающим, например, отдельное, последовательное, одновременное или попеременное введение.
[0354] Хотя описания представленных здесь фармацевтических композиций в принципе направлены на фармацевтические композиции, которые пригодны для введения людям, квалифицированному специалисту будет понятно, что такие композиции в целом пригодны для введения млекопитающим всех видов. Модификация фармацевтических композиций, пригодных для введения людям, чтобы сделать композиции пригодными для введения различным млекопитающим, является общеизвестной, и ветеринарный врач с обычной квалификацией может разработать и/или выполнить такую модификацию простым экспериментированием. Общие сведения в отношении составления и/или получения фармацевтических композиций можно найти, например, в издании Remington: The Science and Practice of Pharmacy, 21-ое издание, Lippincott Williams & Wilkins, 2005.
[0355] В одном аспекте представлен набор, включающий композицию (например, твердую композицию), содержащую соединение Формулы (I-X, I-I, II-I, III-I или III-II).
Способы применения и лечения
[0356] В одном аспекте описываемые здесь соединения, например, соединения Формулы (I-X, I-I, II-I, III-I или III-II), представляются применимыми в качестве терапевтических агентов для лечения связанного с ЦНС заболевания (например, нарушения сна, расстройства настроения, такого как депрессия, расстройства шизофренического спектра, судорожного синдрома, эпилептогенеза, нарушения памяти и/или познавательной способности, нарушения движений, изменения личности, расстройства аутистического спектра, боли, травматического повреждения мозга, сосудистых болезней, связанного с наркотической зависимостью расстройства, и/или абстинентного синдрома, или шума в ушах) у нуждающегося в этом субъекта (например, синдром Ретта, синдром хрупкой Х-хромосомы, или синдром Ангельмана). Примерные ЦНС-состояния, связанные с ГАМК-модуляцией, включают, но не ограничиваются этим, расстройства сна [например, бессонницу], расстройства настроения [например, депрессию (например, большое депрессивное расстройство (MDD)), дистимическое расстройство (например, легкую степень депрессии), биполярное расстройство (например, I и/или II), тревожные расстройства (например, генерализованное тревожное расстройство (GAD), социальное тревожное расстройство), стресс, посттравматическое стрессовое расстройство (PTSD), компульсивные расстройства (например, обсессивно-компульсивное расстройство (OCD))], расстройства шизофренического спектра [например, шизофрению, шизоаффективное расстройство], судорожные синдромы [например, эпилепсию (например, эпилептический статус (SE)), припадки], расстройства памяти и/или познавательной способности [например, расстройства внимания (например, гиперактивное расстройство с дефицитом внимания (ADHD)), деменцию (например, деменцию по типу Альцгеймера, деменцию с тельцами Леви, деменцию сосудистого типа], расстройства движения [например, болезнь Гентингтона, болезнь Паркинсона], расстройства личности [например, антисоциальное расстройство личности, обсессивно-компульсивное расстройство личности], расстройства аутистического спектра (ASD) [например, аутизм, моногенные причины аутизма, такие как синаптопатические, например, синдром Ретта, синдром хрупкой Х-хромосомы, синдром Ангельмана], боль [например, невропатическую боль, болевые синдромы, связанные с травмой, острую боль, хроническую боль], травматическое повреждение головного мозга (TBI), сосудистые расстройства [например, удар, ишемию, пороки сосудов], связанные с наркотической зависимостью расстройства и/или абстинентный синдром [например, привычку к опиатам, кокаину и/или алкоголю] и шум в ушах.
[0357] В определенных вариантах исполнения связанное с ЦНС заболевание представляет собой нарушение сна, расстройство настроения, расстройство шизофренического спектра, судорожный синдром, нарушение памяти и/или познавательной способности, нарушение движений, изменение личности, расстройство аутистического спектра, боль, травматическое повреждение мозга, сосудистые болезни, связанные с наркотической зависимостью расстройства, и/или абстинентный синдром, шум в ушах, или эпилептический статус. В определенных вариантах исполнения связанное с ЦНС заболевание представляет собой депрессию. В определенных вариантах исполнения связанное с ЦНС заболевание представляет собой послеродовую депрессию. В определенных вариантах исполнения связанное с ЦНС заболевание представляет собой большое депрессивное расстройство. В определенных вариантах исполнения большое депрессивное расстройство представляет собой большое депрессивное расстройство в умеренной форме. В определенных вариантах исполнения большое депрессивное расстройство представляет собой большое депрессивное расстройство в тяжелой форме.
[0358] В одном аспекте представлен способ смягчения или предотвращения судорожной активности у субъекта, включающий введение нуждающемуся в таком лечении субъекту эффективного количества соединения согласно настоящему изобретению. В некоторых вариантах исполнения способ смягчает или предотвращает эпилептогенез.
[0359] В еще одном аспекте представлена комбинация соединения согласно настоящему изобретению и еще одного фармакологически активного агента. Представленные здесь соединения могут быть введены в виде единственного активного агента, или же они могут быть введены в комбинации с другими агентами. Введение в комбинации может производиться любым способом, очевидным для квалифицированных специалистов в этой области технологии, включающим, например, отдельное, последовательное, одновременное или попеременное введение.
[0360] В еще одном аспекте представлен способ лечения или профилактики возбудимости головного мозга у субъекта, чувствительного к состоянию, связанному с возбудимостью головного мозга, или страдающего от этого, включающему введение субъекту эффективного количества соединения согласно настоящему изобретению.
[0361] В еще одном дополнительном аспекте настоящее изобретение относится к способу лечения или предупреждения стресса или тревоги у субъекта, включающему введение субъекту, нуждающемуся в таком лечении, эффективного количества соединения согласно настоящему изобретению, или композиции с ним.
[0362] В еще одном дополнительном аспекте представлен способ лечения или профилактики бессонницы у субъекта, включающий введение нуждающемуся в таком лечении субъекту эффективного количества соединения согласно настоящему изобретению, или композиции с ним.
[0363] В еще одном дополнительном аспекте представлен способ вызывания сна и поддержания по существу уровня REM-фазы сна, который обнаруживается при нормальном сне, причем существенное возобновление бессонницы не вызывается, включающий введение эффективного количества соединения согласно настоящему изобретению.
[0364] В еще одном дополнительном аспекте представлен способ лечения или профилактики предменструального синдрома (PMS) или послеродовой депрессии (PND) у субъекта, включающий введение нуждающемуся в таком лечении субъекту эффективного количества соединения согласно настоящему изобретению.
[0365] В еще одном дополнительном аспекте представлен способ лечения или профилактики расстройств настроения у субъекта, включающий введение нуждающемуся в таком лечении субъекту эффективного количества соединения согласно настоящему изобретению. В определенных вариантах исполнения расстройство настроения представляет собой депрессию.
[0366] В еще одном дополнительном аспекте представлен способ улучшения познавательной способности или лечения расстройства памяти введением субъекту терапевтически эффективного количества соединения согласно настоящему изобретению. В определенных вариантах исполнения расстройство представляет собой болезнь Альцгеймера. В определенных вариантах исполнения расстройство представляет собой синдром Ретта.
[0367] В еще одном дополнительном аспекте представлен способ лечения расстройств внимания путем введения субъекту терапевтически эффективного количества соединения согласно настоящему изобретению. В определенных вариантах исполнения расстройство внимания представляет собой ADHD.
[0368] В определенных вариантах исполнения соединение вводят субъекту хронически. В определенных вариантах исполнения соединение вводят субъекту перорально, подкожно, внутримышечно или внутривенно.
Нейроэндокринные заболевания и дисфункция
[0369] Здесь представлены способы, которые могут быть применены для лечения нейроэндокринных заболеваний и дисфункции. Как применяемые здесь, «нейроэндокринное заболевание» или «нейроэндокринная дисфункция» подразумевают различные состояния, обусловленные диспропорциями в продуцировании в организме гормонов, непосредственно связанных с мозгом. Нейроэндокринные заболевания включают взаимодействия между нервной системой и эндокринной системой. Поскольку гипоталамус и гипофиз представляют собой две области мозга, которые регулируют продуцирование гормонов, повреждение гипоталамуса или гипофиза, например, в случае черепно-мозговой травмы, может нарушать продуцирование гормонов и других нейроэндокринных функций мозга. В некоторых вариантах исполнения нейроэндокринное заболевание или дисфункция связаны с расстройством здоровья или состояния у женщин (например, описываемых здесь нарушений здоровья или состояния у женщин). В некоторых вариантах исполнения нейроэндокринное заболевание или дисфункция, связанные с нарушений здоровья или состояния у женщин, представляет собой синдром поликистозных яичников.
[0370] Симптомы нейроэндокринного заболевания включают, но без ограничения этим, поведенческие, эмоциональные и связанные со сном симптомы, связанные с репродуктивной функцией симптомы, и соматические симптомы, включающие, но без ограничения этим, усталость, плохую память, тревогу, депрессию, увеличение или потерю веса, эмоциональную неустойчивость, отсутствие концентрации, трудности с вниманием, снижение либидо, бесплодие, аменорею, снижение мышечной массы, увеличение жировой массы на животе, низкое кровяное давление, снижение частоты сердцебиения, выпадение волос, анемию, запор, непереносимость холода, и сухость кожи.
Нейродегенеративные заболевания и расстройства
[0371] Описываемые здесь способы могут быть применены для лечения нейродегенеративных заболеваний и расстройств. Термин «нейродегенеративное заболевание» включает заболевания и расстройства, которые связаны с прогрессирующей утратой структуры или функции нейронов, или с отмиранием нейронов. Нейродегенеративные заболевания и расстройства включают, но без ограничения этим, болезнь Альцгеймера (в том числе связанные с этим симптомы легкого, умеренного или тяжелого когнитивного нарушения); боковой амиотрофический склероз (ALS), повреждения вследствие гипоксии и ишемические повреждения; атаксию и конвульсии (в том числе для лечения и профилактики припадков, которые вызваны шизоаффективным заболеванием или лекарствами, использованными для лечения шизофрении); доброкачественную забывчивость; отек мозга; мозжечковую атаксию, в том числе синдром нейроакантоцитоза МакЛеода (MLS); закрытую черепно-мозговую травму; сому; контузионные травмы (например, травмы спинного мозга или повреждения головы); деменции, включающие мультиинфарктную деменцию и старческое слабоумие; затемнение сознания; синдром Дауна; вызванный лекарственными средствами или лечением паркинсонизм (такой как обусловленная нейролептиками острая акатизия, острая дистония, паркинсонизм или поздняя дискинезия, нейролептический злокачественный синдром, или вызванный лечением постуральный тремор); эпилепсию; синдром хрупкой Х-хромосомы; синдром Жилль де ла Туретта; травму головы; ухудшение и потерю слуха; болезнь Гентингтона; синдром Леннокса; вызванную леводопой дискинезию; олигофрению; расстройства движения, в том числе акинезии и акинетические (ригидные) синдромы (включая кальцификацию базальных ганглиев, кортикобазальную дегенерацию, мультисистемную атрофию, комплекс паркинсонизм-ALS деменция, болезнь Паркинсона, постэнцефалитный паркинсонизм и прогрессирующий надъядерный паралич); миотонические спазмы и расстройства, связанные с мышечной спастичностью, или слабость, включая хорею (такую как доброкачественная наследственная хорея, вызванная лекарственными средствами хорея, гемибаллизм, болезнь Гентингтона, нейроакантоцитоз, хорею Сиденгама и симптоматическую хорею), дискинезию (включая тики, такие как сложные тики, простые тики и симптоматические тики), миоклонус (включая генерализованный миоклонус и очаговую дистонию), тремор (такой как тремор в покое, ортостатический тремор и интенционный тремор) и дистонию (включая аксиальную дистонию, дистонические спазмы писателей, гемиплегическую дистонию, пароксизмальную дистонию и фокальную дистонию, такую как блефароспазм, оромандибулярная дистония и спастическая дистония и кривошея); повреждение нейронов, включая повреждение глаза, ретинопатию или дегенерацию желтого пятна; нейротоксическое повреждение, которое обусловлено мозговым инсультом, тромбоэмболическим инсультом, геморрагическим инсультом, церебральной ишемией, церебральным спазмом сосудов, гипогликемией, амнезией, гипоксией, аноксией, перинатальной асфиксией и остановкой сердца; болезнь Паркинсона; припадок; эпилептический статус; удар; шум в ушах; тубулярный склероз и вызванную вирусной инфекцией нейродегенерацию (например, вызванную синдромом приобретенного иммунодефицита (СПИДом) и энцефалопатиями). Нейродегенеративные заболевания также включают, но не ограничиваются этим, нейротоксическое повреждение, которое следует за мозговым инсультом, тромбоэмболическим инсультом, геморрагическим инсультом, церебральной ишемией, церебральным спазмом сосудов, гипогликемией, амнезией, гипоксией, аноксией, перинатальной асфиксией и остановкой сердца. Способы лечения или профилактики нейродегенеративного заболевания также включают лечение или предупреждение утраты функции нейронов, характеризующей нейродегенеративное расстройство.
Расстройства настроения
[0372] Здесь также представлены способы лечения расстройства настроения, например, такого как клиническая депрессия, постнатальная депрессия или послеродовая депрессия, перинатальная депрессия, атипичная депрессия, меланхолическая депрессия, психотическая большая депрессия, кататоническая депрессия, сезонное аффективное расстройство, дистимия, двойная депрессия, депрессивное расстройство личности, рекуррентная депрессия, слабое депрессивное расстройство, биполярное расстройство или маниакально-депрессивное расстройство, депрессия, вызванная хроническими заболеваниями, не поддающаяся лечению депрессия, рефрактерная депрессия, суицидальность, суицидальные мысли, или суицидальное поведение. В некоторых вариантах исполнения описываемый здесь способ обеспечивает терапевтическое действие на субъекта, страдающего от депрессии (например, умеренной или тяжелой депрессии). В некоторых вариантах исполнения нарушение настроения связано с описанными здесь болезнью или расстройством (например, нейроэндокринными заболеваниями или расстройствами, нейродегенеративными заболеваниями или расстройствами (например, эпилепсией), нарушениями движения, тремором (например, болезнью Паркинсона), расстройствами здоровья или состояния у женщин).
[0373] Клиническая депрессия также известна как большая депрессия, большое депрессивное расстройство (MDD), тяжелая депрессия, униполярная депрессия, униполярное расстройство и рецидивирующая депрессия, и относится к психическому расстройству, характеризующемуся глубоким и устойчивым плохим настроением, которое сопровождается низкой самооценкой и утратой интереса или удовольствия от нормальной доставляющей удовольствие деятельности. Некоторые люди с клинической депрессией имеют тревожный сон, потерю веса, и обычно чувствуют себя возбужденными и раздраженными. Клиническая депрессия влияет как на чувства и мысли индивидуума, так и на поведение, и может привести к ряду эмоциональных и физических проблем. Индивидуумы с клинической депрессией могут иметь тревогу от повседневной деятельности и приобрести ощущение, что жизнь не стоит того, чтобы жить.
[0374] Периродовая депрессия относится к депрессии во время беременности. Симптомы включают раздражительность, плаксивость, ощущение беспокойства, проблемы со сном, сильное истощение (эмоциональное и/или физическое), изменения аппетита, рассеянность внимания, повышенное беспокойство и/или волнение, ощущение разобщения с ребенком и/или плодом, и потерю интереса к ранее доставляющей удовольствие деятельности.
[0375] Послеродовая депрессия (PND) также относится к периродовой депрессии (PPD), и относится к типу клинической депрессии, которая поражает женщин после родов. Симптомы могут включать уныние, усталость, изменения в сне и пищевых привычках, сниженном сексуальном желании, эпизоды плача, тревогу и раздражительность. В некоторых вариантах исполнения PND представляет собой не поддающуюся лечению депрессию (например, рефрактерную депрессию, как здесь описанную).
[0376] В некоторых вариантах исполнения субъект, имеющий PND, также испытывает депрессию, или симптом депрессии во время беременности. Эта депрессия здесь называется как перинатальная депрессия. В одном варианте исполнения субъект, испытывающий перинатальную депрессию, весьма рискует испытывать PND.
[0377] Атипичная депрессия (AD) характеризуется реактивностью настроения (например, парадоксальной ангедонией) и позитивностью, существенным приростом веса или повышенным аппетитом. Страдающие AD пациенты также могут иметь избыточный сон или сонливость (гиперсомнию), ощущение тяжести в конечностях и существенное социальное ухудшение как следствие гиперчувствительности к ощущаемому отторжению при межличностных отношениях.
[0378] Меланхоличная депрессия характеризуется утратой удовольствия (ангедонией) при большинстве или всех действиях, недостаточностью реакции на приятные стимулы, депрессивным настроением, более выраженным, чем при горе или потере, чрезмерной потерей веса, или чрезмерным чувством вины.
[0379] Психотическая большая депрессия (PMD), или психотическая депрессия, относится к большому депрессивному эпизоду, в частности, меланхолической природы, где индивидуум испытывает психотические симптомы, такие как бред и галлюцинации.
[0380] Кататоническая депрессия относится к большой депрессии, включающей нарушения двигательного поведения и другие симптомы. Индивидуум может стать немым и ступорозным и либо неподвижным, либо совершает бесцельные и странные движения.
[0381] Сезонное аффективное расстройство (SAD) относится к типу сезонной депрессии, при которой индивидуум имеет сезонные картины депрессивных эпизодов, приходящихся на осень или зиму.
[0382] Дистимия относится к состоянию, родственному униполярной депрессии, где очевидны одни и те же физические и познавательные проблемы. Они не являются тяжелыми, и проявляют тенденцию к длительной продолжительности (например, по меньшей мере 2 года).
[0383] Двойная депрессия относится к недостаточному депрессивному настроению (дистимии), которое длится по меньшей мере 2 года и перемежается периодами большой депрессии.
[0384] Депрессивное расстройство личности (DPD) относится к расстройству личности с депрессивными признаками.
[0385] Рецидивирующая кратковременная депрессия (RBD) относится к состоянию, при котором индивидуумы имеют депрессивные эпизоды примерно один раз в месяц, где каждый эпизод длится 2 недели или меньше, и обычно менее 2-3 дней.
[0386] Малое депрессивное расстройство, или малая депрессия, относится к депрессии, при которой по меньшей мере 2 симптома проявляются в течение 2 недель.
[0387] Биполярное расстройство, или маниакально-депрессивное расстройство, вызывает исключительные колебания настроения, которые включают эмоциональные взлеты (мания или гипомания) и падения (депрессия). Во время периодов мании индивидуум может ощущать или действовать анормально счастливо, энергично или раздраженно. Они часто принимают плохие решения, мало заботясь о последствиях. Обычно снижается потребность в сне. Во время периодов депрессии они могут быть плаксивыми, плохо контактировать визуально с другими и отрицательно смотреть на жизнь. Среди людей с таким расстройством является высокой опасность суицида, свыше 6% у людей старше 20 лет, в то время как причинение себе вреда происходит у 30-40%. Другие проблемы с психическим здоровьем, такие как тревожное расстройство и неправильное применение веществ, обычно ассоциируются с биполярным расстройством.
[0388] Депрессия, вызванная условиями хронического лечения, относится к депрессии, вызванной такими хроническими заболеваниями, как рак или хроническая боль, химиотерапия, хронический стресс.
[0389] Не поддающаяся лечению депрессия относится к состоянию, когда индивидуумы подвергаются лечению от депрессии, но симптомы не улучшаются. Например, антидепрессанты или советы психолога (психотерапия) не облегчают симптомы у индивидуумов с терапевтически резистентной депрессией. В некоторых случаях у индивидуумов с терапевтически резистентной депрессией симптомы улучшаются, но возвращаются. Рефрактерная депрессия имеет место у пациентов, страдающих от депрессии, которые резистентны к стандартному фармакологическому лечению, включающему трициклические антидепрессанты, ингибитор моноаминооксидазы (MAOI), ингибиторы обратного захвата серотонина (SSRI), и двойной и тройной прием ингибиторов и/или анксиолитических лекарственных средств, а также к нефармакологическому лечению (например, психотерапии, электросудорожной терапии, стимуляции блуждающего нерва и/или транскраниальной магнитной стимуляции).
[0390] Послеоперационная депрессия относится к ощущению депрессии, которое возникает после хирургического вмешательства (например, в результате того, что пациент стоял на пороге смерти). Например, индивидуумы могут ощущать уныние или настойчиво возвращаться к подавленному настроению, испытывать потерю удовольствия или интереса к увлечениям и действиям, обычно привлекательным, или неотвязное ощущение никчемности или безнадежности.
[0391] Нарушение настроения, связанное с состояниями или расстройствами женского здоровья, имеет отношение к расстройствам настроения (например, депрессии), связанным (например, обусловленным) состоянием или ухудшением женского здоровья (например, как здесь описано).
[0392] Суицидальность, суицидальные мысли, суицидальное поведение относятся к склонности индивидуума совершить самоубийство. Суицидальные мысли касаются размышлений о самоубийстве или необычной увлеченности суицидом. Размах суицидального мышления широко варьирует от, например, быстропроходящих мыслей до пространных мыслей, подробного планирования, обыгрывания, незавершенных попыток. Симптомы включают разговоры о суициде, приобретение средств для совершения суицида, отказ от социального контакта, поглощение мыслями о смерти, ощущение захватывающей или безнадежной ситуации, возрастание употребления алкоголя или лекарственных средств, совершение опасных или самоубийственных поступков, прощальные разговоры с людьми, как будто бы они не увидятся снова.
[0393] Симптомы депрессии включают постоянные ощущения страха или печали, чувство беспомощности, безнадежности, пессимизма, никчемности, слабой энергии, беспокойства, плохого сна, бессонницы, раздраженности, усталости, двигательные проблемы, потерю интереса к приятной деятельности или увлечениям, потерю сосредоточенности, потерю энергии, низкую самооценку, отсутствие позитивных мыслей или планов, избыточную сонливость, переедание, потерю аппетита, инсонмию, причинение вреда себе, мысли о суициде, и попытки самоубийства. Наличие, тяжесть, частота и длительность симптомов могут изменяться от случая к случаю. Симптомы депрессии и их характер может выяснить врач или психолог (например, проверкой психического состояния).
[0394] В некоторых вариантах исполнения терапевтический эффект может быть определен мониторингом субъекта согласно известной шкале депрессии, например, шкале депрессии Гамильтона (HAM-D), улучшенной шкале общего клинического впечатления (CGI), и шкале Монтгомери-Асберга для оценки депрессии (MADRS). В некоторых вариантах исполнения терапевтический эффект может быть определен по снижению общего балла субъекта в шкале депрессии Гамильтона (HAM-D). Снижение общего балла согласно HAM-D может происходить в пределах 4, 3, 2, или 1 дня; или 96, 84, 72, 60, 48, 24, 20, 16, 12, 10, 8 часов или менее. Терапевтический эффект может быть оценен на протяжении заданного периода лечения. Например, терапевтический эффект может быть определен по снижению базовой линии общего балла HAM-D после введения описываемого здесь соединения, например, соединения Формулы (I-X, I-I, II-I, III-I или III-II) (например, через 12, 24, или 48 часов после введения; или спустя 24, 48, 72, или 96 часов или более; или через 1 день, 2 дня, 14 дней, 21 день, или 28 дней; или через 1 неделю, 2 недели, 3 недели, или 4 недели; или спустя 1 месяц, 2 месяца, 6 месяцев, или 10 месяцев; или через 1 год, 2 года, или на протяжении жизни).
[0395] В некоторых вариантах исполнения субъект имеет слабое депрессивное расстройство, например, слабое большое депрессивное расстройство. В некоторых вариантах исполнения субъект имеет умеренное депрессивное расстройство, например, умеренное большое депрессивное расстройство. В некоторых вариантах исполнения субъект имеет тяжелое депрессивное расстройство, например, тяжелое большое депрессивное расстройство. В некоторых вариантах исполнения субъект имеет очень тяжелое депрессивное расстройство, например, очень тяжелое большое депрессивное расстройство. В некоторых вариантах исполнения базовая линия общего балла HAM-D субъекта (то есть, до лечения описанным здесь соединением, например, соединением Формулы (I-X, I-I, II-I, III-I или III-II)), составляет по меньшей мере 24. В некоторых вариантах исполнения базовая линия общего балла HAM-D субъекта составляет по меньшей мере 18. В некоторых вариантах исполнения базовая линия общего балла HAM-D субъекта составляет между 14 и 18 включительно. В некоторых вариантах исполнения базовая линия общего балла HAM-D субъекта составляет между 19 и 22 включительно. В некоторых вариантах исполнения базовая линия общего балла HAM-D субъекта до лечения описанным здесь соединением, например, соединением Формулы (I-X, I-I, II-I, III-I или III-II)), составляет величину, превышающую или равную 23. В некоторых вариантах исполнения базовый балл составляет по меньшей мере 10, 15 или 20. В некоторых вариантах исполнения общий балл HAM-D субъекта после лечения описанным здесь соединением, например, соединением Формулы (I-X, I-I, II-I, III-I или III-II)), составляет от около 0 до 10 (например, менее 10; от 0 до 10, от 0 до 6, от 0 до 4, от 0 до 3, от 0 до 2, или 1,8). В некоторых вариантах исполнения общий балл HAM-D субъекта после лечения описанным здесь соединением, например, соединением Формулы (I-X, I-I, II-I, III-I или III-II)), составляет менее 10, 7, 5 или 3. В некоторых вариантах исполнения снижение общего балла HAM-D от базового балла от около 20 до 30 (например, от 22 до 28, от 23 до 27, от 24 до 27, от 25 до 27, от 26 до 27) до общего балла HAM-D составляет от около 0 до 10 (например, менее 10; от 0 до 10, от 0 до 6, от 0 до 4, от 0 до 3, от 0 до 2, или 1,8) после лечения описанным здесь соединением, например, соединением Формулы (I-X, I-I, II-I, III-I или III-II). В некоторых вариантах исполнения снижение базовой линии общего балла HAM-D после лечения описанным здесь соединением, например, соединением Формулы (I-X, I-I, II-I, III-I или III-II), составляет 1-, 2-, 3-, 4-, 5-, 7-, 10-, 25-, 40-, 50-, или 100-кратную величину). В некоторых вариантах исполнения процентное снижение базовой линии общего балла HAM-D после лечения описанным здесь соединением, например, соединением Формулы (I-X, I-I, II-I, III-I или III-II), составляет по меньшей мере 50% (например, 60%, 70%, 80%, или 90%). В некоторых вариантах исполнения терапевтический эффект, измеренный по снижению общего балла HAM-D после лечения описанным здесь соединением, например, соединением Формулы (I-X, I-I, II-I, III-I или III-II), относительно базовой линии общего балла HAM-D (например, через 12, 24, 48 часов после введения; или спустя 24, 48, 72, 96 часов или более; или через 1 день, 2 дня, 14 дней, или более) составляет по меньшей мере 10, 15, или 20 пунктов.
[0396] В некоторых вариантах исполнения способ лечения депрессивного расстройства, например, большого депрессивного расстройства, обеспечивает терапевтический эффект (например, по измерению оценки депрессии по шкале Гамильтона (HAM-D) в пределах 14, 10, 4, 3, 2, или 1 дня, или 24, 20, 16, 12, 10, или 8 часов или менее. В некоторых вариантах исполнения способ лечения депрессивного расстройства, например, большого депрессивного расстройства, обеспечивает терапевтический эффект (например, определенный по статистически значительному снижению общего балла HAM-D) в пределах первого или второго дня лечения описанным здесь соединением, например, соединением Формулы (I-X, I-I, II-I, III-I или III-II). В некоторых вариантах исполнения способ лечения депрессивного расстройства, например, большого депрессивного расстройства, обеспечивает терапевтический эффект (например, определенный по статистически значительному снижению общего балла HAM-D) в пределах периода, меньшего или равного 14 дням с начала лечения описанным здесь соединением, например, соединением Формулы (I-X, I-I, II-I, III-I или III-II). В некоторых вариантах исполнения способ лечения депрессивного расстройства, например, большого депрессивного расстройства, обеспечивает терапевтический эффект (например, определенный по статистически значительному снижению общего балла HAM-D) в пределах периода, меньшего или равного 21 дню с начала лечения описанным здесь соединением, например, соединением Формулы (I-X, I-I, II-I, III-I или III-II). В некоторых вариантах исполнения способ лечения депрессивного расстройства, например, большого депрессивного расстройства, обеспечивает терапевтический эффект (например, определенный по статистически значительному снижению общего балла HAM-D) в пределах периода, меньшего или равного 28 дням с начала лечения описанным здесь соединением, например, соединением Формулы (I-X, I-I, II-I, III-I или III-II). В некоторых вариантах исполнения терапевтический эффект проявляется как снижение от базовой линии общего балла HAM-D после лечения описанным здесь соединением, например, соединением Формулы (I-X, I-I, II-I, III-I или III-II) (например, лечения описанным здесь соединением, например, соединением Формулы (I-X, I-I, II-I, III-I или III-II) один раз в день в течение 14 дней. В некоторых вариантах исполнения общий балл HAM-D субъекта перед лечением описанным здесь соединением, например, соединением Формулы (I-X, I-I, II-I, III-I или III-II) составляет по меньшей мере 24. В некоторых вариантах исполнения общий балл HAM-D субъекта перед лечением описанным здесь соединением, например, соединением Формулы (I-X, I-I, II-I, III-I или III-II) составляет по меньшей мере 18. В некоторых вариантах исполнения общий балл HAM-D субъекта перед лечением описанным здесь соединением, например, соединением Формулы (I-X, I-I, II-I, III-I или III-II), составляет между 14 и 18 включительно. В некоторых вариантах исполнения снижение общего балла HAM-D после лечения субъекта описанным здесь соединением, например, соединением Формулы (I-X, I-I, II-I, III-I или III-II), относительно базовой линии общего балла HAM-D составляет по меньшей мере 10. В некоторых вариантах исполнения снижение общего балла HAM-D после лечения субъекта описанным здесь соединением, например, соединением Формулы (I-X, I-I, II-I, III-I или III-II), относительно базовой линии общего балла HAM-D составляет по меньшей мере 15 (например, по меньшей мере 17). В некоторых вариантах исполнения общий балл HAM-D, связанный с лечением субъекта описанным здесь соединением, например, соединением Формулы (I-X, I-I, II-I, III-I или III-II), составляет не более, чем число в диапазоне от 6 до 8. В некоторых вариантах исполнения общий балл HAM-D, связанный с лечением субъекта описанным здесь соединением, например, соединением Формулы (I-X, I-I, II-I, III-I или III-II), составляет не более 7.
[0397] В некоторых вариантах исполнения способ обеспечивает терапевтический эффект (например, измеренный по снижению показателя в улучшенной шкале общего клинического впечатления (CGI) в пределах 14, 10, 4, 3, 2, или 1 дня, или 24, 20, 16, 12, 10, или 8 часов или менее. В некоторых вариантах исполнения связанное с ЦНС заболевание представляет собой депрессивное расстройство, например, большое депрессивное расстройство. В некоторых вариантах исполнения способ лечения депрессивного расстройства, например, большого депрессивного расстройства, обеспечивает терапевтический эффект в пределах второго дня периода лечения. В некоторых вариантах исполнения терапевтический эффект проявляется в снижении базовой линии балла CGI в конце периода лечения (например, через 14 дней после введения).
[0398] В некоторых вариантах исполнения способ обеспечивает терапевтический эффект (например, измеренный по снижению показателя в шкале Монтгомери-Асберга для оценки депрессии (MADRS) в пределах 14, 10, 4, 3, 2, или 1 дня, или 24, 20, 16, 12, 10, или 8 часов или менее. В некоторых вариантах исполнения связанное с ЦНС заболевание представляет собой депрессивное расстройство, например, большое депрессивное расстройство. В некоторых вариантах исполнения способ лечения депрессивного расстройства, например, большого депрессивного расстройства, обеспечивает терапевтический эффект в пределах второго дня периода лечения. В некоторых вариантах исполнения терапевтический эффект проявляется в снижении базовой линии балла MADRS в конце периода лечения (например, через 14 дней после введения).
[0399] Терапевтический эффект в отношении большого депрессивного расстройства может быть определен по проявляемому субъектом снижению балла в шкале Монтгомери-Асберга для оценки депрессии (MADRS). Например, балл MADRS может быть снижен в пределах 4, 3, 2, или 1 дня; или 96, 84, 72, 60, 48, 24, 20, 16, 12, 10, 8 часов или менее. Шкала Монтгомери-Асберга для оценки депрессии (MADRS) представляет собой диагностический опросник из десяти пунктов (относительно очевидного уныния, выраженного уныния, внутреннего разлада, сокращенного сна, пониженного аппетита, проблем с концентрацией внимания, апатии, неспособности чувствовать, пессимистических мыслей, и суицидальных мыслей), который врачи применяют для измерения серьезности депрессивных эпизодов у пациентов с расстройствами настроения.
[0400] В некоторых вариантах исполнения способ обеспечивает терапевтический эффект (например, измерением по Эдинбургской шкале послеродовой депрессии (EPDS)) в пределах 4, 3, 2, или 1 дня; 24, 20, 16, 12, 10, 8 часов или менее. В некоторых вариантах исполнения терапевтический эффект проявляется в улучшении, измеренном согласно EPDS.
[0401] В некоторых вариантах исполнения способ обеспечивает терапевтический эффект (например, измерением по опроснику Генерализованного тревожного расстройства из 7 пунктов (GAD-7)) в пределах 4, 3, 2, 1 дня; 24, 20, 16, 12, 10, 8 часов или менее.
Тревожные расстройства
[0402] Здесь представлены способ лечения тревожных расстройств (например, генерализованное тревожное расстройство, паническое расстройство, обсессивно-компульсивное расстройство, фобия, посттравматическое стрессовое расстройство). Тревожное расстройство представляет собой общий термин, охватывающий несколько различных форм аномального и патологического страха и тревоги. Современные врачебные диагностические критерии распознают широкий круг тревожных расстройств.
[0403] Генерализованное тревожное расстройство представляет собой распространенное хроническое расстройство, характеризующееся продолжительной тревогой, которая не сосредоточена на каком-либо одном объекте или ситуации. Лица, страдающие от генерализованной тревоги, испытывают неспецифический упорный страх и беспокойство и становятся чрезмерно обеспокоенными повседневными вещами. Генерализованное тревожное расстройство является наиболее распространенным тревожным расстройством, поражающим пожилых людей.
[0404] При паническом расстройстве человек страдает от кратковременных приступов интенсивного ужаса и мрачного предчувствия, часто отмечаемых дрожью, ознобом, замешательством, головокружением, тошнотой, затрудненным дыханием. Такие панические приступы определяются Американской психологической ассоциацией (APA) как страх или дискомфорт, который внезапно появляется и достигает максимума менее чем за десять минут, может продолжаться в течение нескольких часов, и может запускаться стрессом, страхом или спокойным упражнением, хотя конкретная причина не всегда видна. В дополнение к повторяющимся неожиданным паническим приступам, диагноз панического расстройства также требует, чтобы указанные приступы имели хронические последствия: либо беспокойство в связи с возможными приступами, упорный страх перед будущими приступами, либо существенные изменения в поведении, связанные с приступами. Соответственно этому люди, страдающие от панического расстройства, испытывают симптомы даже вне специфических панических эпизодов. Часто страдающие от паники замечают обычные изменения сердечных сокращений, что приводит их к мысли, что с их сердцем что-то не так, или они задумываются о другом паническом приступе. В некоторых случаях во время панических приступов имеет место повышенная осведомленность (гипервигильность) о функционировании организма, где любое ощущаемое физиологическое изменение интерпретируется как возможная угрожающая жизни болезнь (то есть, крайняя ипохондрия).
[0405] Обсессивно-компульсивное расстройство представляет собой тип тревожного расстройства, характеризующийся главным образом повторяющимися обсессиями (дистрессивные, упорные и навязчивые мысли и образы) и компульсивными побуждениями (побуждения к выполнению специфических действий или ритуалов). Картина мышления при OCD может иметь сходство с суевериями, постольку она включает веру в причинно-следственную взаимосвязь, где в действительности она не существует. Часто процесс полностью нелогичен; например, компульсивное побуждение к ходьбе в определенном режиме может быть использовано для облегчения обсессии приближающейся беды. И во многих случаях компульсивное побуждение совершенно необъяснимо, просто побудительный мотив к завершению ритуала, спровоцированный нервозностью. В меньшинстве случаев страдающие от OCD могут испытывать только обсессии без явных компульсивных побуждений; значительно меньшее число больных испытывает только компульсивные побуждения.
[0406] Отдельной самой большой категорией тревожных расстройств является фобия, которая включает все случаи, в которых страх и тревога провоцируются определенным стимулом или ситуацией. Страдающие от этого типично предчувствуют ужасные последствия от столкновения с объектом их страха, который может представлять собой что угодно от животного до расположения к жидкости организма.
[0407] Посттравматическое стрессовое расстройство, или PTSD, представляет собой тревожное расстройство, которое является результатом перенесенной травмы. Посттравматический стресс может являться результатом экстремальной ситуации, такой как драка, изнасилование, ситуации с взятием заложников, или даже серьезный несчастный случай. Он также может быть результатом длительного (хронического) воздействия тяжелого стрессора, например, как у солдат, которые пережили отдельные сражения, но не могут справиться с непрерывной битвой. Обычные симптомы включают яркие воспоминания о прошедшем, реакции избегания или депрессию.
Расстройства здоровья у женщин
[0408] Здесь представлены способ лечения состояний или расстройств, имеющих отношение к здоровью женщин. Состояния или расстройства, имеющие отношение к здоровью женщин, включают, но без ограничения этим, гинекологическое здоровье и расстройства (например, предменструальный синдром (PMS), предменструальное дисфорическое расстройство (PMDD), проблемы беременности (например, выкидыш, аборт), бесплодие, и родственные расстройства (например, синдром поликистозных яичников (PCOS)), другие расстройства и состояния, и проблемы, связанные с общим здоровьем и самочувствием женщины (например, менопауза).
[0409] Гинекологическое здоровье и расстройства, которые волнуют женщину, включают менструацию и нерегулярности менструального цикла; здоровье мочевых путей, в том числе недержание мочи и расстройства тазового дна; и такие расстройства, как бактериальный вагиноз, вагинит, фибромы матки, и вульводиния.
[0410] Предменструальный синдром (PMS) имеет отношение к физическим и эмоциональным симптомам, которые возникают за одну-две недели до менструального цикла. Симптомы варьируют, но могут включать кровотечение, колебания настроения, припухлые молочные железы, чувство голода, усталость, раздражительность, угри, и депрессию.
[0411] Предменструальное дисфорическое расстройство (PMDD) представляет собой тяжелую форму PMS. Симптомы PMDD подобны PMS, но более серьезны, и могут мешать работе, социальной активности и взаимоотношениям. Симптомы PMDD включают колебания настроения, депрессивное настроение или ощущение безнадежности, гневливость, повышенную межличностную конфликтность, напряженное состояние и тревожность, раздражительность, ощущение контроля над собой или подавления, проблемы со сном, физические проблемы (например, вздутие, болезненность молочных желез, припухлость, головные боли, суставная или мышечная боль).
[0412] Проблемы беременности включают наблюдение перед зачатием и дородовый уход, невынашивание беременности (выкидыш и мертвый плод), преждевременные схватки и преждевременные роды, синдром внезапной смерти младенца (SIDS), кормление грудью, и родовые травмы.
[0413] Выкидыш имеет отношение к беременности, которая самопроизвольно заканчивается в пределах первых 20 недель вынашивания.
[0414] Аборт имеет отношение к преднамеренному прерыванию беременности, которое может быть выполнено в течение первых 28 недель вынашивания.
[0415] Бесплодие и родственные расстройства включают фибромы матки, синдром поликистозных яичников, эндометриоз и первичная недостаточность яичников.
[0416] Синдром поликистозных яичников (PCOS) имеет отношение к расстройствам эндокринной системы среди женщин репродуктивного возраста. PCOS представляет собой комплекс симптомов, обусловленных повышенным уровнем мужских гормонов у женщин. У большинства женщин с PCOS растут многочисленные мелкие кисты на их яичниках. Симптомы PCOS включают нерегулярные или отсутствующие менструальные циклы, обильные менструации, чрезмерный рост волос на теле и лице, угри, тазовые боли, невозможности забеременеть, и лоскуты толстой, темной, бархатистой кожи. PCOS может быть связан с состояниями, включающими диабет 2 типа, ожирение, синдром остановок дыхания во сне, сердечные болезни, расстройства настроения, и рак эндометрия.
[0417] Другие расстройства и состояния, которые касаются только женщин, включают синдром Тернера, синдром Ретта, и раковые заболевания яичников и шейки матки.
[0418] Проблемы, связанные с общим здоровьем и самочувствием женщины включают насилие в отношении женщин, женщин с инвалидностью и их уникальными проблемами, остеопороз и здоровье костей, и менопаузу.
[0419] Менопауза имеет отношение к 12 месяцам после последнего менструального периода женщины, и означает конец менструальных циклов. Менопауза обычно происходит у женщин в возрасте от 40 до 50 лет. Физические симптомы, такие как приливы жара, и эмоциональные симптомы менопаузы могут нарушать сон, снижать энергию, провоцировать беспокойство или ощущения печали или потери. Менопауза включает натуральную менопаузу и хирургическую менопаузу, которая представляет собой тип индуцированной менопаузы вследствие такого события, как операция (например, удаление матки, удаление яичника, рак). Она вызывается, когда яичники серьезно повреждены, например, радиацией, химиотерапией, или другими лечебными воздействиями.
Эпилепсия
[0420] Соединение Формулы (I-X, I-I, II-I, III-I или III-II), или фармацевтически приемлемая соль, или фармацевтически приемлемая композиция его, может быть использовано в описанном здесь способе, например, в лечении описанных здесь расстройств, таких как эпилепсия, эпилептический статус или эпилептический припадок.
[0421] Эпилепсия является расстройством головного мозга, характеризующимся повторяющимися припадками в неустановленное время. Типы эпилепсии могут включать, но без ограничения этим, генерализованную эпилепсию, например, абсансную эпилепсию у детей, юношескую миоклоническую эпилепсию, эпилепсию с большими приступами при пробуждении, синдром Веста, синдром Леннокса-Гасто, парциальную эпилепсию, например, височную эпилепсию, лобную эпилепсию, доброкачественную фокальную эпилепсию детского возраста.
Эпилептогенез
[0422] Описанные здесь соединения и способы могут быть применены для лечения или профилактики эпилептогенеза. Эпилептогенез представляет собой постепенный процесс, при котором в нормальном мозгу развивается эпилепсия (хроническое состояние, в котором возникают эпилептические припадки). Эпилептогенез обусловливается нейрональным повреждением, вызванным начальным проявлением инсульта (например, эпилептический статус).
Эпилептический статус (SE)
[0423] Эпилептический статус (SE) может включать, например, судорожный эпилептический статус, например, ранний эпилептический статус, установившийся эпилептический статус, рефрактерный эпилептический статус, суперрефрактерный эпилептический статус; бессудорожный эпилептический статус, например, генерализованный эпилептический статус, сложный парциальный эпилептический статус; генерализованные периодические эпилептиформные разряды и периодические латерализованные эпилептиформные разряды. Судорожный эпилептический статус характеризуется наличием судорожных эпилептических припадков и может включать ранний эпилептический статус, установившийся эпилептический статус, рефрактерный эпилептический статус, суперрефрактерный эпилептический статус. Ранний эпилептический статус лечат терапией первой линии. Установившийся эпилептический статус характеризуется эпилептическими припадками, которые остаются, несмотря на лечение терапией первой линии, и назначается терапия второй линии. Рефрактерный эпилептический статус характеризуется эпилептическими припадками, которые остаются, несмотря на лечение терапией первой линии и второй линии, и обычно назначаются общие анестетики. Суперрефрактерный эпилептический статус характеризуется эпилептическими припадками, которые остаются, несмотря на лечение терапией первой линии, терапией второй линии и общими анестетиками, в течение 24 часов или дольше.
[0424] Бессудорожный эпилептический статус может включать, например, фокальный бессудорожный эпилептический статус, например, сложный парциальный эпилептический статус; простой парциальный бессудорожный эпилептический статус, едва различимый бессудорожный эпилептический статус; генерализованный бессудорожный эпилептический статус, например, поздний абсансный бессудорожный эпилептический статус, атипичный абсансный бессудорожный эпилептический статус или типичный абсансный бессудорожный эпилептический статус.
[0425] Соединение Формулы (I-X, I-I, II-I, III-I или III-II), или фармацевтически приемлемая соль, или фармацевтически приемлемая композиция его, может быть также введено как профилактическое средство субъекту, имеющему расстройство ЦНС, например, травматическое повреждение головного мозга, эпилептический статус, например, судорожный эпилептический статус, например, ранний эпилептический статус, установившийся эпилептический статус, рефрактерный эпилептический статус, суперрефрактерный эпилептический статус; бессудорожный эпилептический статус, например, генерализованный бессудорожный эпилептический статус, например, сложный частичный эпилептический статус; генерализованные периодические эпилептиформные разряды и периодические летерализованные эпилептиформные разряды, до начала приступа.
Эпилептический припадок
[0426] Припадок представляет собой физические проявления или изменения в поведении, которые происходят после эпизода аномальной электрической активности в головном мозгу. Термин «припадок» часто используют взаимозаменяемо с термином «судорога». Судороги представляют собой состояние, когда тело человека сотрясается быстро и неконтролируемо. Во время судорог мышцы человека многократно сокращаются и расслабляются.
[0427] На основании типа поведения и активности головного мозга, припадки делятся на две больших категории: генерализованные и частичные (также называемые локальными или фокальными). Классификация типа припадка помогает врачам диагностировать, имеет ли пациент эпилепсию или не имеет.
[0428] Генерализованные припадки инициируются электрическими импульсами из всей площади всего головного мозга, в то время как частичные припадки инициируются (по меньшей мере изначально) электрическими импульсами в относительно небольшой части головного мозга. Часть головного мозга, генерирующую припадки, иногда называют фокусом.
[0429] Существуют шесть типов генерализованных припадков. Наиболее частым и драматическим, и, следовательно, наиболее общеизвестным, является генерализованная судорога, также называемая большим судорожным припадком. При таком типе припадка пациент теряет сознание и обычно падает. За потерей сознания следует генерализованное окоченение тела (называемое «тонической» фазой припадка) в течение 30-60 секунд, затем резкое вздрагивание («клоническая» фаза) в течение 30-60 секунд, после чего пациент впадает в глубокий сон («постиктальная», или послеприпадочная фаза). Во время больших припадков могут иметь место повреждения и травмы, такие как прикусывание языка и недержание мочи.
[0430] Абсансные припадки вызывают кратковременную потерю сознания (всего несколько секунд) с немногими симптомами или без них. Пациент, чаще всего ребенок, обычно прерывает деятельность и становится безучастным. Такие припадки начинаются и заканчиваются внезапно и могут происходить несколько раз в день. Пациенты обычно не сознают, что у них происходит припадок, за исключением того, что они могут осознавать «потерю времени».
[0431] Миоклонические припадки заключаются в спорадических подергиваниях, обычно по обеим сторонам тела. Пациенты иногда описывают подергивания как электрические удары. Такие припадки, когда сильные, могут привести к падению или непреднамеренному бросанию предметов.
[0432] Клонические припадки являются повторяющимися ритмическими вздрагиваниями, которые затрагивают обе стороны тела в одно и то же время.
[0433] Тонические припадки характеризуются ригидностью мышц.
[0434] Атонические припадки заключаются во внезапной и общей потере тонуса мышц, особенно рук и ног, которая часто приводит к падению.
[0435] Описанные здесь припадки могут включать эпилептические припадки; острые повторяющиеся припадки; кластерные припадки; непрерывные припадки; упорные припадки; пролонгированные припадки; рецидивирующие припадки; припадки эпилептического статуса, например, рефрактерного судорожного эпилептического статуса, припадки бессудорожного эпилептического статуса; рефрактерные припадки; миоклонические припадки; тонические припадки; тонико-клонические припадки; сложные частичные припадки; вторичные генерализованные припадки; атипичные абсансные припадки; абсансные припадки; атонические припадки; доброкачественные роландические припадки; фебрильные припадки; эмоциональные припадки; фокальные припадки; геластические припадки; генерализованные начальные припадки; инфантильные спазмы; джексоновские припадки; выраженные двусторонние миоклонические припадки; мультифокальные припадки; неонатальные начальные припадки; ночные припадки; затылочные припадки; посттравматические припадки; едва различимые припадки; припадки Сильвана; визуальные рефлекторные припадки или припадки отдергивания. В некоторых вариантах исполнения припадок представляет собой генерализованный начальный припадок, связанный с синдромом Драве, синдромом Леннокса-Гасто, туберозным склерозным комплексом, синдромом Ретта, или женской детской эпилепсией, вызванной мутацией гена PCDH19.
Нарушение движения
[0436] Здесь также описаны способы лечения нарушения движения. Как применяемые здесь, «нарушения движения» относятся к разнообразным заболеваниям и расстройствам, которые связаны с гиперкинетическими нарушениями движения и родственными аномалиями в мышечном контроле. Примерные нарушения движения включают, но без ограничения этим, болезнь Паркинсона и паркинсонизм (определяемый, в частности, по замедленности движений (брадикинезии)), дистонию, хорею и болезнь Хантингтона, атаксию, тремор (например, идиопатическое дрожание), миоклонус и вздрагивание, тики и синдром Туретта, синдром беспокойных ног, синдром мышечной скованности, и нарушения походки.
Тремор
[0437] Описываемые здесь способы могут быть применены для лечения тремора, например, соединения Формулы (I-X, I-I, II-I, III-I или III-II) могут быть использованы для лечения мозжечкового дрожания или динамического тремора, дистонического тремора, эссенциального тремора, ортостатического тремора, паркинсонического тремора, физиологического тремора, психогенного тремора, или рубрального тремора. Тремор включает наследственные, дегенеративные и идиопатические расстройства, такие как болезнь Вильсона, болезнь Паркинсона и эссенциального тремора, соответственно; метаболические расстройства (например, тиреоидные-паратиреоидные-, заболевания печени и гипогликемия); периферические нейропатии (связанные с болезнью Шарко-Мари-Тута, синдромом Русси-Леви, сахарным диабетом, комплексным региональным болевым синдромом); токсины (никотин, ртуть, свинец, CO, марганец, мышьяк, толуол); вызванные лекарствами (нарколептики, трициклические антидепрессанты, литий, кокаин, алкоголь, адреналин, бронхолитические средства, теофиллин, кофеин, стероиды, вальпроат, амиодарон, тиреоидные гормоны, винкристин); и психогенные расстройства. Клиническая картина тремора может быть классифицирована на физиологический тремор, усиленный физиологический тремор, синдромы эссенциального тремора (в том числе классический эссенциальный тремор, первичный ортостатический тремор, и специфический по задаче и положению тремор), дистонический тремор, паркинсонический тремор, мозжечкового дрожания, тремор Холмса (то есть, рубральный тремор), палатальный тремор, нейропатический тремор, вызванный токсинами или лекарствами тремор, и психогенный тремор.
[0438] Тремор представляет собой непроизвольное ритмичное по времени сокращение и расслабление мышц, которое может включать колебания или подергивания одной или нескольких частей тела (например, кистей рук, плеч, глаз, лица, головы, голосовых связок, туловища, ног).
[0439] Мозжечковое дрожание, или интенционный тремор, представляет собой медленный обширный тремор конечностей, который происходит после целенаправленного движения. Мозжечковый тремор вызывается поражениями или повреждением мозжечка в результате, например, опухоли, удара, заболевания (например, рассеянного склероза, наследственного дегенеративного расстройства).
[0440] Дистонический тремор происходит у индивидуумов, пораженных дистонией, расстройством движения, при котором длительные непроизвольные сокращения мышц вызывают скручивающие и повторяющиеся телодвижения и/или болезненные и анормальные положения тела или позиции. Дистонический тремор может поражать любую мышцу тела. Дистонические треморы происходят нерегулярно и часто могут быть ослаблены полноценным отдыхом.
[0441] Эссенциальный тремор, или доброкачественный эссенциальный тремор, является наиболее распространенным типом тремора. Эссенциальный тремор может быть у кого-то умеренным и непрогрессирующим, и может медленно прогрессировать, начинаясь на одной стороне тела, но в пределах 3 лет поражает обе стороны. Кисти рук поражаются наиболее часто, но также могут затрагиваться голова, голос, язык, ноги и туловище. Частотность тремора может снижаться с возрастом человека, но тяжесть может возрастать. Повышенное волнение, стресс, нервное возбуждение, физическое истощение или низкий уровень сахара в крови могут спровоцировать треморы и/или повысить их тяжесть. Симптомы обычно развиваются со временем, и могут быть как видимыми, так и продолжительными после начала.
[0442] Ортостатический тремор характеризуется быстрыми (например, более 12 Гц) ритмическими сокращениями мышц, что происходит в ногах и туловище сразу после вставания. В бедрах и голенях ощущаются спазмы, и пациент может неконтролируемо дрожать, когда его просят стоять на одном месте. Ортостатический тремор может иметь место у пациентов с эссенциальным тремором.
[0443] Паркинсонический тремор вызывается повреждением структур в головном мозгу, которые контролируют движение. Паркинсонический тремор часто является предшественником болезни Паркинсона и типично виден как «круговое» движение кистей рук, которое также может поражать подбородок, губы, ноги и туловище. Типично паркинсонический тремор появляется в возрасте после 60. Движение начинается в одной конечности или на одной стороне тела и может прогрессировать, включая другую сторону.
[0444] Физиологический тремор может происходить у здоровых индивидуумов и не имеет клинического значения. Его можно видеть во всех произвольных группах мышц. Физиологический тремор может быть вызван некоторыми лекарственными средствами, похмельным синдромом или медицинским состоянием, включающим гиперфункцию щитовидной железы и гипогликемию. Тремор классически имеет частоту приблизительно 10 Гц.
[0445] Психогенный тремор, или истерический тремор, может происходить в состоянии покоя или во время постурального или кинетического движения. Пациент с психогенным тремором может иметь конверсионное расстройство или другое психическое заболевание.
[0446] Рубральный тремор характеризуется крупноразмашистым слабым дрожанием, которое может присутствовать в покое, при принятии позы и действии. Тремор ассоциируется с состояниями, поражающими красные ядра в среднем мозгу, классическими необычными припадками.
[0447] Болезнь Паркинсона поражает нервные клетки в мозгу, которые продуцируют допамин. Симптомы включают мышечную ригидность, треморы изменения речи и походки. Паркинсонизм характеризуется тремором, брадикинезией, ригидностью, и постуральной неустойчивостью. Паркинсонизм проявляет общую с болезнью Паркинсона симптоматику, но скорее комплекс симптомов, нежели прогрессирующее нейродегенеративное заболевание.
[0448] Дистония представляет собой нарушение движения, которое характеризуется длительными или перемежающимися сокращениями мышц, приводя к ненормальным, часто повторяющимся движениям или положениям. Дистония часто инициируется или ухудшается преднамеренными действиями, и связана с чрезмерной мышечной активацией.
[0449] Хорея представляет собой неврологическое расстройство, которое характеризуется толчкообразными непроизвольными движениями, обычно возникающими в плечах, бедрах и лице. Болезнь Хантингтона представляет собой врожденное заболевание, которое обусловливает отмирание нервных клеток в мозгу. Симптомы включают неконтролируемые движения, неповоротливость, и проблемы с равновесием. Болезнь Хантингтона может нарушать ходьбу, речь и глотание.
[0450] Атаксия имеет отношение к потере полного контроля над движениями тела, и может поражать пальцы, кисти рук, руки, ноги, тело, нарушать речь и движения глаз.
[0451] Миоклонус и Испуг представляет собой отклик на внезапный и неожиданный стимул, который может быть звуковым, тактильным, визуальным или вестибулярным.
[0452] Тики представляют собой непроизвольное движение, обычно возникающее внезапно, кратковременное, многократное, но неритмичное, обычно имитирующее нормальное поведение, и часто происходящее на фоне обычной активности. Тики могут быть классифицированы как моторные или вокальные моторные тики, связанные с движениями, тогда как вокальные тики связаны со звуком. Тики могут быть охарактеризованы как простые или сложные. Например, простые моторные тики затрагивают только некоторые мышцы, ограниченные конкретной частью тела. Синдром Туретта представляет собой врожденное нейропсихиатрическое заболевание, возникающее в детстве, которое характеризуется множественными моторными тиками и по меньшей мере одним вокальным тиком.
[0453] Синдром беспокойных ног представляет собой неврологическое сенсоримоторное заболевание, которое характеризуется непреодолимым побуждением двигать ногами в состоянии покоя.
[0454] Синдром мышечной скованности представляет собой прогрессирующее нарушение движения, которое характеризуется непроизвольными болезненными спазмами и ригидностью мышц, обычно находящихся в нижней части спины и в ногах. Как правило, это приводит к походке на негнущихся ногах с тяжелым поясничным гиперлордозом. Обычно наблюдается характерная ненормальность на электромиограммах (EMG)с непрерывной моторной активностью параспинальных аксиальных мышц. Варианты включают «синдром ригидности конечностей», создающий фокальную ригидность, обычно поражающую концы ног и ступни.
[0455] Нарушения походки относятся к ненормальности характера и стиля ходьбы, которая обусловливается нервно-мышечными, артритными и прочими изменениями в теле. Походка классифицируется согласно системе, ответственной за аномальное передвижение, и включает гемиплегическую походку, диплегическую походку, нейропатическую походку, миопатическую походку, паркинсоническую походку, хореическую походку, атаксическую походку, и сенсорическую походку.
Анестезия/Седация
[0456] Анестезия представляет собой вызванное фармакологически и обратимое состояние амнезии, анальгезии, потери чувствительности, потери рефлексов скелетных мышц, ослабленной стрессовой реакции, или все из них одновременно. Такие эффекты можно получить от одного лекарственного средства, которое одно обеспечивает правильную комбинацию действий, или иногда с помощью комбинации лекарственных средств (например, снотворных средств, седативных средств, парализующих средств, анальгетиков) для достижения весьма специфической комбинации результатов. Анестезия позволяет пациентам переносить операцию и другие процедуры без дистресса и боли, которые они в противном случае могли бы испытывать.
[0457] Седация представляет собой снижение раздражительности или возбуждения путем введения фармакологического средства, как правило, для облегчения медицинской процедуры или диагностической процедуры.
[0458] Седация и обезболивание включают непрерывный спектр состояний сознания, колеблющихся от минимальной седации (анксиолизис) до общей анестезии.
[0459] Минимальная седация также известна как анксиолизис. Минимальная седация представляет собой вызванное лекарственным средством состояние, во время которого пациент нормально реагирует на словесные команды. Могут ухудшиться когнитивная функция и координация. Дыхательная функция и функция сердечно-сосудистой системы обычно не поражаются.
[0460] Умеренная седация/анальгезия (седация под контролем сознания) представляет собой вызванную лекарственным средством депрессию сознания, во время которой пациент реагирует целенаправленно на словесную команду или одну или сопровождающуюся свето-тактильной стимуляцией. Обычно нет необходимости в поддержании дыхательных путей пациента. Типично самопроизвольное дыхание является адекватным. Обычно функция сердечно-сосудистой системы сохраняется.
[0461] Глубокая седация/анальгезия представляет собой вызванную лекарственным средством депрессию сознания, во время которой пациент не может легко встать, но целенаправленно реагирует (без потери рефлекса на болевой раздражитель) после повторной или болевой стимуляции. Может ухудшиться независимая дыхательная функция, и пациенту может потребоваться помощь для поддержания собственных дыхательных путей. Самопроизвольное дыхание может быть неадекватным. Обычно функция сердечно-сосудистой системы сохраняется.
[0462] Общая анестезия представляет собой вызванную лекарственным средством потерю сознания, во время которой пациент не может реагировать даже на болевой раздражитель. Способность поддерживать независимую дыхательную функцию часто ухудшается, и обычно требуется помощь для поддержания дыхательных путей пациента. Может потребоваться дыхание под положительным давлением из-за угнетенного самопроизвольного дыхания или вызванного лекарственным средством угнетения нейромышечной функции. Может ухудшиться функция сердечно-сосудистой системы.
[0463] Седация в отделении интенсивной терапии (ICU) позволяет подавить осведомленность пациента об окружающей среде и ослабить его реакцию на внешнюю стимуляцию. Это может сыграть роль при лечении тяжелобольного пациента и охватывает широкий спектр контроля за симптомами, который будет изменяться от пациента к пациенту и у отдельных пациентов в течение всего времени течения их болезни. Глубокую седацию при интенсивной терапии применяют для облегчения переносимости эндотрахеальной трубки и синхронизации дыхания, часто с нейромышечными блокаторами.
[0464] В некоторых вариантах исполнения седацию (например, длительную седацию, непрерывную седацию) вызывают и поддерживают в ICU в течение продолжительного периода времени (например, 1 день, 2 дня, 3 дня, 5 дней, 1 неделю, 2 недели, 3 недели, 1 месяц, 2 месяца). Средства для длительной седации могут иметь длительное действие. Седативные средства в ICU могут иметь короткий период полувыведения.
[0465] Процедурная седация и анальгезия, также отнесенная к сознательной седации, представляет собой способ введения седативных средств или диссоциативных средств с анальгетиками или без них для вызывания состояния, которое позволяет субъекту переносить неприятные процедуры с сохранением сердечно-легочной функции.
Примеры
[0466] Для того, чтобы описываемое здесь изобретение могло быть полнее понятным, приводятся нижеследующие примеры. Синтетические и биологические примеры, описанные в настоящей заявке, представлены для иллюстрирования представленных здесь соединений, фармацевтических композиций и способов, и никоим образом не должны толковаться как ограничивающие его объем.
Материалы и способы
[0467] Представленные здесь соединения могут быть получены из легкодоступных исходных материалов с использованием нижеследующих общих способов и методик. Будет понятно, что там, где приводятся типичные или предпочтительные условия процессов (то есть, температуры реакций, продолжительности, молярные отношения реактантов, растворители, давление и т.д.), также могут быть применены другие условия процессов, если не оговорено иное. Оптимальные условия реакций могут изменяться в связи с определенными используемыми реактантами или растворителями, но такие условия могут быть определены квалифицированным специалистом в этой области технологии обычной экспериментальной оптимизацией.
[0468] Кроме того, как будет очевидно квалифицированным специалистам в этой области технологии, могут понадобиться обычные защитные группы для предохранения определенных функциональных групп от участия в нежелательных реакциях. Выбор подходящей защитной группы для конкретной функциональной группы, а также подходящие условия для ее введения и удаления, являются общеизвестными в технологии. Например, многие защитные группы и их введение и удаление описаны в работе авторов T.W. Greene и P.G.M. Wuts, Protecting Groups in Organic Synthesis, второе издание, издательство Wiley, Нью-Йорк, 1991, и в цитированных в ней литературных ссылках.
[0469] Представленные здесь соединения могут быть выделены и очищены известными стандартными процедурами. Такие процедуры включают (но без ограничения этим) колоночную хроматографию, жидкостную хроматографию высокого давления (HPLC, ВЭЖХ) или сверхкритическую флюидную хроматографию (SFC, СФХ). Нижеследующие схемы представлены с подробностями получения показательных оксистеролов, которые были здесь перечислены. Представленные здесь соединения могут быть получены квалифицированным специалистом в области технологии органического синтеза из известных или имеющихся в продаже на рынке исходных материалов и реагентов. Указанные здесь примерные хиральные колонки, доступные для использования при разделении/очистке энантиомеров/диастереомеров, включают, но не ограничиваются этим, CHIRALPAK® AD-10, CHIRALCEL® OB, CHIRALCEL® OB-H, CHIRALCEL® OD, CHIRALCEL® OD-H, CHIRALCEL® OF, CHIRALCEL® OG, CHIRALCEL® OJ и CHIRALCEL® OK.
[0470] Приведенные здесь данные 1Н-ЯМР (например, для области между δ (ppm, млн-1) от около 0,5 до около 4 млн-1) будут подразумевать примерную интерпретацию ЯМР-спектра (например, интегрирование примерного пика) соединения.
[0471] Примерный общий способ препаративной HPLC: колонка: Waters RBridge prep., 10 мкм C18, 19*250 мм. Подвижная фаза: ацетонитрил, вода (NH4HCO3) (30 л воды, 24 г NH4HCO3, 30 мл NH3·H2O). Расход потока: 25 мл/мин.
[0472] Примерный общий способ аналитической HPLC: подвижная фаза: A: вода (10 мМ NH4HCO3), B: ацетонитрил, градиент: 5%-95% B в 1,6 или 2 мин. Расход потока: 1,8 или 2 мл/мин; колонка: XBridge C18, 4,6*50 мм, 3,5 мкм при 45°С.
[0473] Примерный общий способ препаративной HPLC: колонка: Waters Xbridge Column 150*25 5 мкм, условия: вода (10 мМ NH4HCO3)-ACN, начало: B 85, конец: B 100, время градиента (минут) 6,5, время удерживания 100% B (минут) 1, расход потока(мл/мин) 25, впрыски: 4).
[0474] Примерный общий способ для SFC: колонка: CHIRALPAK® AD CSP (250 мм*30 мм, 10 мкм), градиент: 45% B, A=NH3H2O, B=MeOH, расход потока: 60 мл/мин. Например, AD_3_EtOH_DEA_5_40_25 мл обозначали бы: «колонка: Chiralpak AD-3 150×4,6 мм внутреннего диаметра (I.D.), 3 мкм, подвижная фаза: A: CO2 B: этанол (0,05% DEA), градиент: от 5% до 40% B до 5 минут, и выдерживание 40% в течение 2,5 минут, затем 5% B в течение 2,5 минут, расход потока: 2,5 мл/мин, температура колонки: 35°С».
[0475] Примерный общий способ для стандартной LC-ELSD: 30-90AB_2 мин_E. (подвижная фаза: 1,5 мл/4 л TFA в воде (растворитель A) и 0,75 мл/4 л TFA в ацетонитриле (растворитель B), с использованием градиента вымывания 30%-90% (растворитель B) в течение 0,9 минуты и выдерживанием при 90% в течение 0,6 минуты при расходе потока 1,2 мл/мин; колонка: Xtimate C18 2,1*30 мм, 3 мкм; длина волны: UV 220 нм; температура колонки: 50°С; MS-ионизация: ESI; детектор: PDA&ELSD.
[0476] Примерный общий способ для SFC: колонка: CHIRALPAK® AD CSP (250 мм*30 мм, 10 мкм), градиент: 45% B, A=NH3H2O, B=MeOH, расход потока: 60 мл/мин. Например, AD_3_EtOH_DEA_5_40_25 мл обозначали бы: «колонка: Chiralpak AD-3 150×4,6 мм внутреннего диаметра (I.D.), 3 мкм, подвижная фаза: A: CO2 B: этанол (0,05% DEA), градиент: от 5% до 40% B до 5 минут, и выдерживание 40% в течение 2,5 минут, затем 5% B в течение 2,5 минут, расход потока: 2,5 мл/мин, температура колонки: 35°С».
Формула (I-X) или Формула (I-I) Сокращения:
[0477] PE: петролейный эфир; EtOAc: этилацетат; THF: тетрагидрофуран; PCC: хлорхромат пиридиния; TLC: тонкослойная хроматография; PCC: хлорхромат пиридиния; t-BuOK: трет-бутоксид калия; 9-BBN: 9-борабицикло[3.3.1]нонан; Pd(t-Bu3P)2: бис(три-трет-бутилфосфин)палладий(0); AcCl: ацетилхлорид; i-PrMgCl: изопропилмагнийхлорид; TBSCl: трет-бутил(хлор)диметилсилан; (i-PrO)4Ti: тетраизопропоксид титана; BHT: 2,6-ди-трет-бутил-4-метилфеноксид; Me: метил; i-Pr: изопропил; t-Bu: трет-бутил; Ph: фенил; Et: этил; Bz: бензоил; BzCl: бензоилхлорид; CsF: фторид цезия; DAST: трифторид диэтиламиносеры, DCC: дициклогексилкарбодиимид; DCM: дихлорметан; DMAP: 4-диметиламинопиридин; DMP: периодинан Десса-Мартина; EtMgBr: этилмагнийбромид; EtOAc: этилацетат; TEA: триэтиламин; AlaOH: аланин; Boc: трет-бутоксикарбонил; Py: пиридин; TBAF: фторид тетра-н-бутиламмония; THF: тетрагидрофуран; TBS: трет-бутилдиметилсилил; TMS: триметилсилил; TMSCF3: (трифторметил)триметилсилан; Ts: пара-толуолсульфонил; Bu: бутил; Ti(OiPr)4: тетраизопропоксититан; LAH: литийалюминийгидрид; LDA: диизопропиламид лития; LiOH·H2O: гидраты гидроксида лития; MAD: бис(2,6-ди-трет-бутил-4-метилфеноксид) метилалюминия; MeCN: ацетонитрил; NBS: N-бромсукцинимид; Na2SO4: сульфат натрия; Na2S2O3: тиосульфат натрия; PE: петролейный эфир; MeCN: ацетонитрил; MeOH: метанол; Boc: трет-бутоксикарбонил; MTBE: метил-трет-бутиловый простой эфир; K-selectride: три(втор-бутил)боргидрид калия.
[0478] ПРИМЕР I-1: синтез 1-((3R,5R,8S,9S,10R,13S,14S,17S)-3-гидрокси-3,5,10,13-тетраметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-(метил(фенил)амино)этан-1-она (I-A2)
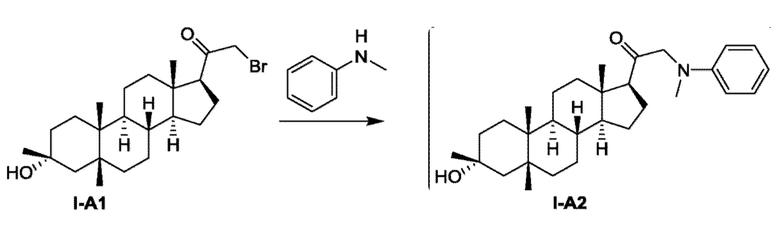
[0479] К раствору DIPEA (78,9 мг, 0,611 ммол) в DMF (10 мл) добавили N-метиланилин (100 мг, 0,94 ммол) при 10°С. После перемешивания при 10°С в течение 10 минут добавили I-A1 (200 мг, 0,47 ммол, описанного ниже в ПРИМЕРЕ I-4). Смесь перемешивали при 40°С в течение 16 часов. Смесь упарили с образованием масла, которое очистили с использованием HPLC с получением I-A2 (21 мг, 10%) в виде твердого вещества.
[0480] 1H-ЯМР (400 МГц, CDCl3) δ 7,24-7,15 (м, 2H), 6,75-6,70 (м, 1H), 6,65-6,55 (м, 2H), 4,13-3,93 (м, 2H), 3,00 (с, 3H), 2,63-2,54 (м, 1H), 2,27-2,09 (м, 2H), 2,03-1,95 (м, 1H), 1,74-1,53 (м, 6H), 1,50-1,42 (м, 6H), 1,38-1,32 (м, 5H), 1,24-1,11 (м, 4H), 1,06-0,98 (м, 1H), 0,93 (с, 3H), 0,81 (с, 3H), 0,65 (с, 3H); LC ELSD чистота 99%, MS ESI рассчитано для C30H46NO2 [M+H]+ 452, найдено 452.
[0481] ПРИМЕР I-2: синтез 1-((3R,5R,8S,9S,10R,13S,14S,17S)-3-гидрокси-3,5,10,13-тетраметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-(фениламино)этан-1-она (I-A3)
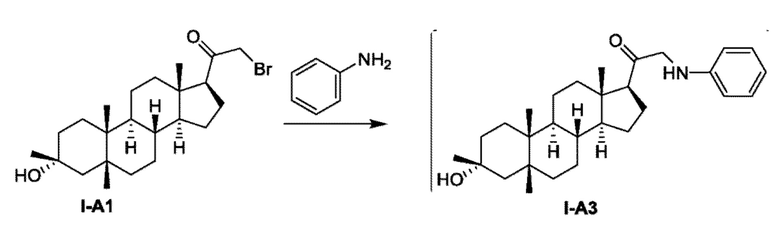
[0482] К раствору DIPEA (78,9 мг, 0,611 ммол) в DMF (10 мл) добавили анилин (100 мг, 0,94 ммол) при 10°С. После перемешивания при 10°С в течение 10 минут добавили I-A1 (200 мг, 0,47 ммол). Смесь перемешивали при 40°С в течение 16 часов. Смесь упарили с образованием масла, которое очистили с использованием HPLC с получением I-A3 (5 мг, 2%) в виде твердого вещества.
[0483] 1H-ЯМР (400 МГц, CDCl3) δH 7,23-7,16 (м, 2H), 6,75-6,70 (м, 1H), 6,63-6,58 (м, 2H), 4,00-3,86 (м, 2H), 2,60-2,56 (м, 1H), 2,29-2,18 (м, 2H), 2,04-1,94 (м, 2H), 1,78-1,71 (м, 2H), 1,52-1,43 (м, 7H), 1,42-1,38 (м, 2H), 1,36 (с, 4H), 1,29-1,23 (м, 3H), 1,20-1,15 (м, 2H), 1,06-0,99 (м, 1H), 0,94 (с, 3H), 0,90-0,85 (м, 1H), 0,80 (с, 3H), 0,62 (с, 3H); LC-ELSD чистота 99%; MS ESI рассчитано для C29H44NO2 [M+H]+ 438, найдено 438.
[0484] ПРИМЕР I-3: синтез 1-((3R,5R,8S,9S,10R,13S,14S,17S)-3-гидрокси-3,5,10,13-тетраметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)этан-1-она (I-B6)
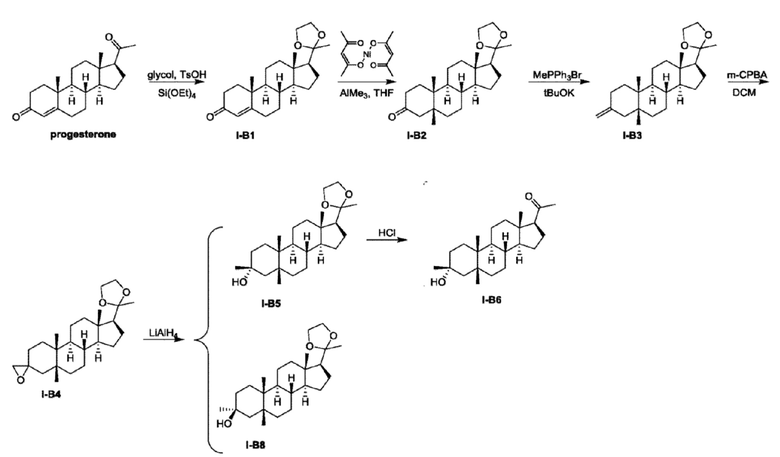
Синтез I-B1
[0485] Si(OEt)4 (132 г, 636 ммол) и каталитическое количество TsOH (4,91 г, 28,6 ммол) добавили к раствору прогестерона (100 г, 318 ммол) в этиленгликоле (2 л). После перемешивания при 25°С в течение 5 часов реакционную смесь залили раствором NaHCO3 (водным, 1,5 л), профильтровали, промыли водой (2 л×3), профильтровали, высушили на воздухе, и растерли с MTBE/PE (50 мл/2,5 л) с образованием I-B1 (95,0 г, 83%) в виде твердого вещества.
[0486] 1H-ЯМР (400 МГц, CDCl3) δH 5,72 (с, 1H), 4,05-3,80 (м, 4H), 2,45-2,25 (м, 4H), 2,10-2,00 (м, 2H), 1,90-1,57 (м, 5H), 1,56-1,40 (м, 3H), 1,29 (с, 3H), 1,22-1,13 (м, 5H), 1,10-0,85 (м, 4H), 0,81 (с, 3H).
Синтез I-B2
[0487] К раствору I-B1 (10 г, 27,8 ммол) и диацетилацетоната никеля (2+) (1,42 г, 5,56 ммол) в THF (300 мл) по каплям добавили AlMe3 (41,7 мл, 83,4 ммол, 2 M в толуоле) при 0°С под N2. После добавления реакционную смесь перемешивали при 0°С в течение 2 часов. Смесь залили 50%-ным раствором NH4Cl (500 мл), разбавили EtOAc (300 мл), и затем профильтровали. Органический слой отделили, и водную фазу экстрагировали EtOAc (200 мл). Объединенную органическую фазу промыли рассолом (500 мл), высушили над Na2SO4, профильтровали, упарили и очистили с использованием Combi-flash (0-15% EtOAc в PE) с образованием I-B2 (6 г, 57%) в виде твердого вещества.
Синтез I-B3
[0488] К суспензии MePh3PBr (17 г, 48 ммол) в THF (80 мл) добавили t-BuOK (5,37 г, 48 ммол). После перемешивания при 40°С в течение 20 минут по каплям при 40°С добавили раствор I-B2 (6 г, 16 ммол) в THF (20 мл). После добавления смесь залили 50%-ным раствором NH4Cl (300 мл) и экстрагировали EtOAc (2×100 мл). Объединенную органическую фазу высушили над Na2SO4, профильтровали, упарили и очистили с использованием Combi-flash (0-5% EtOAc в PE) с образованием I-B3 (5 г, 83%) в виде твердого вещества.
[0489] 1H-ЯМР (400 МГц, CDCl3) δH 4,66-4,61 (м, 1H), 4,58-4,51 (м, 1H), 4,03-3,82 (м, 4H), 2,87-2,79 (м, 1H), 2,20-1,91 (м, 3H), 1,83-1,77 (м, 1H), 1,75-1,58 (м, 5H), 1,54 (с, 3H), 1,48-1,31 (м, 5H), 1,29 (с, 3H), 1,23-1,01 (м, 5H), 0,82-0,78 (м, 5H), 0,74 (с, 3H).
Синтез I-B4
[0490] У раствору I-B3 (5 г, 13,4 ммол) в DCM (100 мл) добавили K2CO3 (9,27 г, 67 ммол) и мета-хлорпероксибензойную кислоту (м-CPBA) (6,91 г, 40,1 ммол). После перемешивания при 20°С в течение 30 минут реакционную смесь залили насыщенным раствором Na2S2O3 (300 мл). После перемешивания при 20°С в течение 10 минут органическую фазу отделили, высушили над Na2SO4, профильтровали и упарили с образованием I-B4 (5 г) в виде твердого вещества.
[0491] 1H-ЯМР (400 МГц, CDCl3) δH 4,03-3,83 (м, 4H), 2,69-2,46 (м, 3H), 2,09-1,89 (м, 2H), 1,82-1,76 (м, 1H), 1,75-1,62 (м, 4H), 1,62-1,47 (м, 2H), 1,46-1,33 (м, 4H), 1,29 (с, 3H), 1,26-0,98 (м, 8H), 0,96-0,93 (м, 2H), 0,89-0,82 (м, 3H), 0,74 (с, 3H), 0,61-0,50 (м, 1H).
Синтез I-B5 и I-B8
[0492] К раствору I-B4 (300 мг, 0,772 ммол) в THF (30 мл) порциями в течение 10 минут добавили LiAlH4 (293 мг, 7,72 ммол). После перемешивания при 20°С в течение 30 минут смесь залили 50%-ным раствором NH4Cl (60 мл) и экстрагировали EtOAc (3×30 мл). Объединенную органическую фазу промыли 50%-ным раствором NH4Cl (100 мл), высушили над Na2SO4, профильтровали, упарили и очистили с использованием Combi-flash (0-15% EtOAc в PE) с образованием I-B5 (210 мг, 69%) и I-B8 (40 мг, 13%) в виде твердого вещества.
[0493] I-B5: 1H-ЯМР (400 МГц, CDCl3) δH 4,04-3,81 (м, 4H), 2,11-2,00 (м, 2H), 1,84-1,58 (м, 5H), 1,52-1,39 (м, 3H), 1,39-1,34 (м, 2H), 1,33-1,29 (м, 4H), 1,28-1,23 (м, 3H), 1,22-1,16 (м, 4H), 1,16-1,02 (м, 7H), 1,00-0,87 (м, 2H), 0,83 (с, 3H), 0,73 (с, 3H).
[0494] I-B8: 1H-ЯМР (400 МГц, CDCl3) δH 4,02-3,82 (м, 4H), 2,26-2,19 (м, 1H), 2,05-2,00 (м, 1H), 1,82-1,75 (м, 1H), 1,74-1,62 (м, 3H), 1,57-1,49 (м, 2H), 1,48-1,37 (м, 7H), 1,33 (с, 3H), 1,28 (с, 3H), 1,24-1,09 (м, 5H), 1,08-0,98 (м, 3H), 0,91 (с, 3H), 0,79 (с, 3H), 0,72 (с, 3H).
Синтез I-B6
[0495] К раствору I-B5 (210 мг, 0,537 ммол) в MeOH (8 мл) добавили HCl (5,35 мл, 10,7 ммол, 2 M в воде). После перемешивания при 20°С в течение 5 минут смесь разбавили водой (50 мл) и профильтровали, высушили в вакууме с образованием I-B6 (150 мг, 80%) в виде твердого вещества. Стереохимическое отнесение было подтверждено рентгеновской кристаллографией.
[0496] 1H-ЯМР (400 МГц, CDCl3) δH 2,56-2,47 (м, 1H), 2,26-2,12 (м, 2H), 2,10 (с, 3H), 2,04-1,97 (м, 1H), 1,74-1,53 (м, 5H), 1,52-1,38 (м, 7H), 1,37-1,33 (м, 4H), 1,29-1,10 (м, 5H), 1,05-0,98 (м, 1H), 0,92 (с, 3H), 0,79 (с, 3H), 0,57 (с, 3H).
[0497] ПРИМЕР I-4: синтез 1-(2-((3R,5R,8S,9S,10R,13S,14S,17S)-3-гидрокси-3,5,10,13-тетраметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-оксоэтил)-1H-пиразол-4-карбонитрила (I-A4)
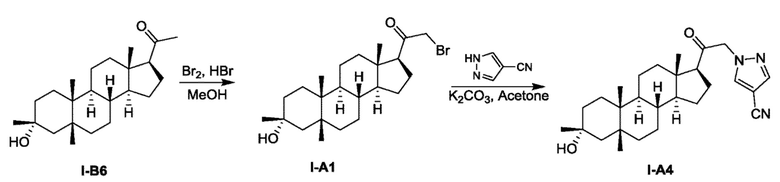
Синтез I-A1
[0498] К раствору I-B6 (1,2 г, 3,46 ммол) в MeOH (30 мл) добавили одну каплю HBr (55,9 мг, 0,692 ммол) и Br2 (829 мг, 5,19 ммол). После перемешивания при 20°С в течение 1 часа смесь залили 50%-ным раствором NaHCO3 (50 мл) и экстрагировали EtOAc (2×30 мл). Объединенный органический слой промыли рассолом (50 мл), высушили над Na2SO4, профильтровали, упарили с образованием I-AI (1,4 г, 95%) в виде твердого вещества.
[0499] 1H-ЯМР (400 МГц, CDCl3) δH 3,95-3,85 (м, 2H), 2,85-2,77 (м, 1H), 2,27-2,12 (м, 2H), 1,96-1,88 (м, 1H), 1,80-1,68 (м, 2H), 1,56-1,39 (м, 10H), 1,35 (с, 3H), 1,34-1,11 (м, 6H), 1,06-0,99 (м, 1H), 0,93 (с, 3H), 0,79 (с, 3H), 0,61 (с, 3H).
Синтез I-A4
[0500] К раствору I-AI (100 мг, 0,235 ммол) в ацетоне (2 мл) добавили 1H-пиразол-4-карбонитрил (32,7 мг, 0,352 ммол) и K2CO3 (64,8 мг, 0,47 ммол). После перемешивания при 20°С в течение 16 часов реакционную смесь профильтровали и очистили препаративной HPLC с образованием I-A4 (46 мг, 45%) в виде твердого вещества.
[0501] 1H-ЯМР (400 МГц, CDCl3) δH 7,85 (с, 1H), 7,81 (с, 1H), 5,05-4,85 (м, 2H), 2,64-2,54 (м, 1H), 2,29-2,15 (м, 2H), 2,09-1,99 (м, 1H), 1,80-1,71 (м, 2H), 1,51-1,38 (м, 9H), 1,38-1,33 (м, 5H), 1,32-1,21 (м, 3H), 1,20-1,12 (м, 2H), 1,07-1,00 (м, 1H), 0,94 (с, 3H), 0,80 (с, 3H), 0,64 (с, 3H); LC-ELSD чистота 99%; MS ESI рассчитано для C27H38N3O [M+H-H2O]+ 420, найдено 420.
[0502] ПРИМЕР I-5: синтез 1-((3S,5R,8S,9S,10R,13S,14S,17S)-3-гидрокси-3,5,10,13-тетраметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-этан-1-она (I-A5)
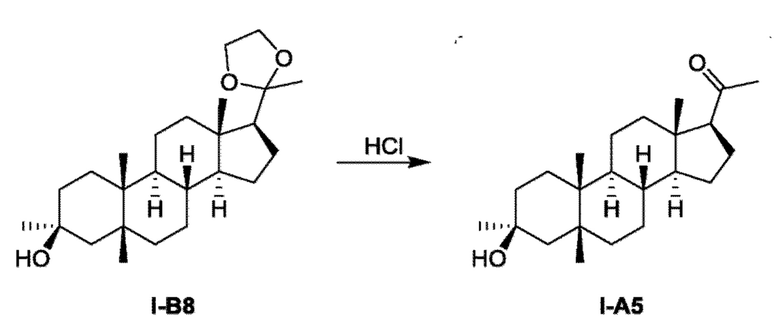
[0503] К раствору I-B8 (40 мг, 0,102 ммол) в MeOH (2 мл) добавили HCl (1,02 мл, 2 M в воде). После перемешивания при 20°С в течение 5 минут смесь разбавили водой (20 мл) и профильтровали, высушили в вакууме с образованием A5 (20 мг, 56%) в виде твердого вещества.
[0504] 1H-ЯМР (400 МГц, CDCl3) δH 2,57-2,48 (м, 1H), 2,20-1,98 (м, 6H), 1,74-1,57 (м, 4H), 1,56-1,42 (м, 5H), 1,41-1,30 (м, 5H), 1,21 (с, 3H), 1,20-1,13 (м, 2H), 1,13-1,03 (м, 6H), 0,98-0,92 (м, 1H), 0,83 (с, 3H), 0,58 (с, 3H).
[0505] ПРИМЕР I-6 и I-7: синтез 1-((3R,5R,8S,9S,10R,13S,14S,17S)-3-гидрокси-3,5,10,13-тетраметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-(2H-пиразоло[3,4-c]пиридин-2-ил)этан-1-она (I-A6) и 1-((3R,5R,8S,9S,10R,13S,14S,17S)-3-гидрокси-3,5,10,13-тетраметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-(1H- пиразоло[3,4-c]пиридин-2-ил)этан-1-она (I-A7)
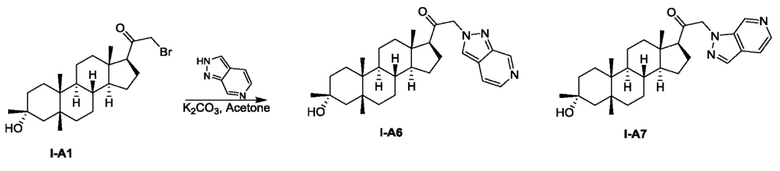
[0506] К смеси I-AI (200 мг, 0,47 ммол) и K2CO3 (129 мг, 0,94 ммол) в ацетоне (5 мл) добавили 1H-пиразоло[3,4-c]пиридин (83,9 мг, 0,705 ммол) при 25°С. После перемешивания при 25°С в течение 16 часов реакционную смесь профильтровали, и фильтрат упарили в вакууме с образованием продукта, который очистили препаративной HPLC, и элюаты промыли насыщенным раствором NaHCO3, высушили над Na2SO4, профильтровали и упарили с образованием I-A6 (25 мг) и I-A7 (40 мг) в виде твердого вещества, которое дополнительно очистили препаративной TLC (DCM:ацетон=2:3) с образованием чистого I-A6 (4 мг, 1,8%) и I-A7 (20 мг, 9%) в виде твердого вещества.
[0507] I-A6: 1H-ЯМР (400 МГц, CDCl3) δ 9,26 (с, 1H), 8,19-8,14 (м, 1H), 7,98 (с, 1H), 7,55-7,50 (м, 1H), 5,35-5,18 (м, 2H), 2,70-2,61 (м, 1H), 2,29-2,09 (м, 3H), 1,84-1,71 (м, 2H), 1,55-1,40 (м, 10H), 1,38-1,35 (м, 4H), 1,31-1,22 (м, 3H), 1,20-1,11 (м, 2H), 1,08-1,00 (м, 1H), 0,94 (с, 3H), 0,81 (с, 3H), 0,70 (с, 3H); LC-ELSD чистота 99%; MS ESI рассчитано для C29H42N3O2 [M+H]+ 464, найдено 464.
[0508] I-A7: 1H-ЯМР (400 МГц, CDCl3) δ 8,79 (с, 1H), 8,36-8,31 (м, 1H), 8,09 (с, 1H), 7,67-7,62 (м, 1H), 5,31-5,19 (м, 2H), 2,70-2,62 (м, 1H), 2,29-2,11 (м, 3H), 1,81-1,69 (м, 2H), 1,64-1,60 (м, 1H), 1,53-1,39 (м, 9H), 1,36 (с, 3H), 1,35-1,21 (м, 4H), 1,20-1,13 (м, 2H), 1,08-1,01 (м, 1H), 0,94 (с, 3H), 0,82 (с, 3H), 0,72 (с, 3H); LC-ELSD чистота 99%; MS ESI рассчитано для C29H42N3O2 [M+H]+ 464, найдено 464.
[0509] ПРИМЕР I-8 и I-9: синтез 1-((3R,5R,8S,9S,10R,13S,14S,17S)-3-гидрокси-3,5,10,13-тетраметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-(5-метил-1H-тетразол-1-ил)этан-1-она (I-A8) и 1-((3R,5R,8S,9S,10R,13S,14S,17S)-3-гидрокси-3,5,10,13-тетраметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-(5-метил-2H-тетразол-2-ил)этан-1-она (I-A9)
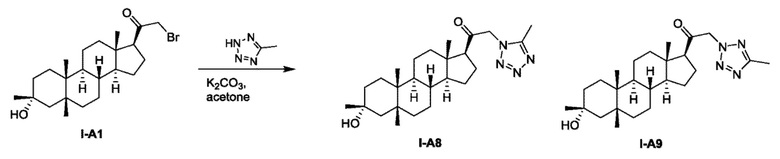
[0510] К смеси I-AI (200 мг, 0,5 ммол) и K2CO3 (129 мг, 0,9 ммол) в ацетоне (5 мл) при 15°С добавили 5-метил-2H-1,2,3,4-тетразол (59,2 мг, 0,7 ммол). Реакционную смесь перемешивали при 15°С в течение 16 часов. Реакционную смесь залили водой (20 мл) и экстрагировали EtOAc (2×20 мл). Объединенный органический слой высушили над безводным Na2SO4, профильтровали и упарили в вакууме с образованием продукта, который очистили на колонке для флэш-хроматографии (EtOAc в PE, 50%~80%) с образованием I-A8 (65 мг, 32%) в виде твердого вещества и I-A9 (45 мг, 22%) в виде твердого вещества.
[0511] I-A8: 1H-ЯМР (400 МГц, CDCl3) δ 5,21-4,97 (м, 2H), 2,68-2,59 (м, 1H), 2,47 (с, 3H), 2,30-2,03 (м, 3H), 1,86-1,67 (м, 2H), 1,65-1,57 (м, 2H), 1,53-1,38 (м, 9H), 1,37 (с, 3H), 1,32-1,11 (м, 5H), 1,08-1,01 (м, 1H), 0,95 (с, 3H), 0,81 (с, 3H), 0,66 (с, 3H); LC ELSD чистота 99%; MS ESI рассчитано для C25H39N4O [M+H-H2O]+ 411, найдено 411
[0512] I-A9: 1H-ЯМР (400 МГц, CDCl3) δ 5,40-5,29 (м, 2H), 2,65-2,53 (м, 4H), 2,29-2,15 (м, 2H), 2,12-2,04 (м, 1H), 1,84-1,71 (м, 2H), 1,66-1,57 (м, 2H), 1,52-1,39 (м, 7H), 1,39-1,33 (м, 5H), 1,29-1,11 (м, 5H), 1,07-0,99 (м, 1H), 0,94 (с, 3H), 0,81 (с, 3H), 0,69 (с, 3H); LC-ELSD чистота 99%; MS ESI рассчитано для C25H39N4O [M+H-H2O]+ 411, найдено 411.
[0513] Формула II, сокращения: PE: петролейный эфир; EtOAc: этилацетат; THF: тетрагидрофуран; PCC: хлорхромат пиридиния; TLC: тонкослойная хроматография; PCC: хлорхромат пиридиния; t-BuOK: трет-бутоксид калия; 9-BBN: 9-борабицикло[3.3.1]нонан; Pd(t-Bu3P)2: бис(три-трет-бутилфосфин)палладий(0); AcCl: ацетилхлорид; i-PrMgCl: изопропилмагнийхлорид; TBSCl: трет-бутил(хлор)диметилсилан; (i-PrO)4Ti: тетраизопропоксид титана; BHT: 2,6-ди-трет-бутил-4-метилфеноксид; Me: метил; i-Pr: изопропил; t-Bu: трет-бутил; Ph: фенил; Et: этил; Bz: бензоил; BzCl: бензоилхлорид; CsF: фторид цезия; DCC: дициклогексилкарбодиимид; DCM: дихлорметан; DMAP: 4-диметиламинопиридин; DMP: периодинан Десса-Мартина; EtMgBr: этилмагнийбромид; EtOAc: этилацетат; TEA: триэтиламин; AlaOH: аланин; Boc: трет-бутоксикарбонил; Py: пиридин; TBAF: фторид тетра-н-бутиламмония; THF: тетрагидрофуран; TBS: трет-бутилдиметилсилил; TMS: триметилсилил; TMSCF3: (трифторметил)триметилсилан; Ts: пара-толуолсульфонил; Bu: бутил; Ti(OiPr)4: тетраизопропоксититан; LAH: литийалюминийгидрид; LDA: диизопропиламид лития; LiOH·H2O: гидраты гидроксида лития; MAD: бис(2,6-ди-трет-бутил-4-метилфеноксид) метилалюминия; MeCN: ацетонитрил; NBS: N-бромсукцинимид; Na2SO4: сульфат натрия; Na2S2O3: тиосульфат натрия; PE: петролейный эфир; MeCN: ацетонитрил; MeOH: метанол; Boc: трет-бутоксикарбонил; MTBE: метил-трет-бутиловый простой эфир; K-selectride: три(втор-бутил)боргидрид калия.
Общие схемы
Схема II-1
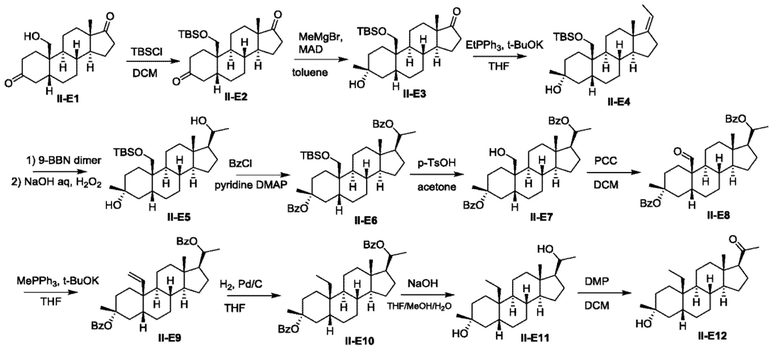
Схема II-2
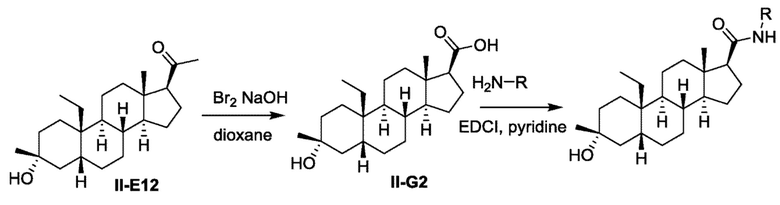
Схема II-3
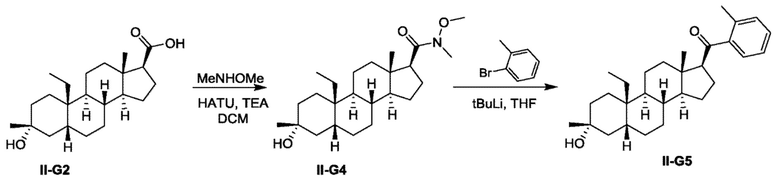
Схема II-4
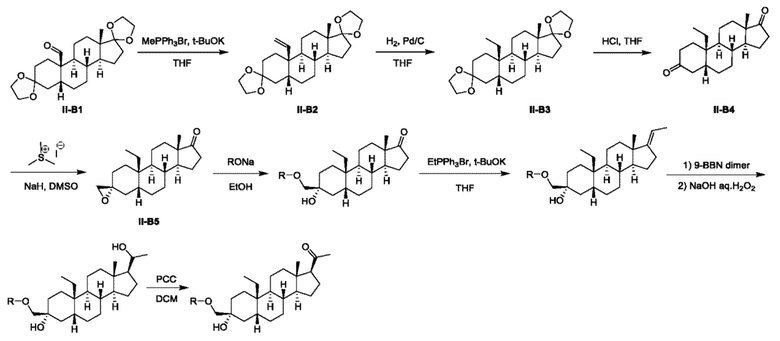
Схема II-5
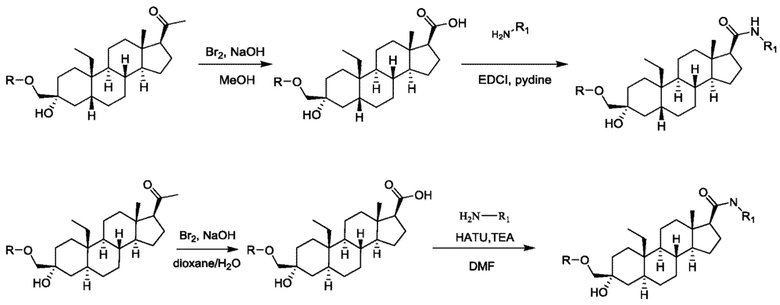
Схема II-6
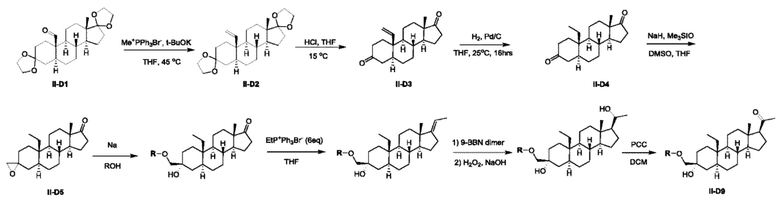
Схема II-7
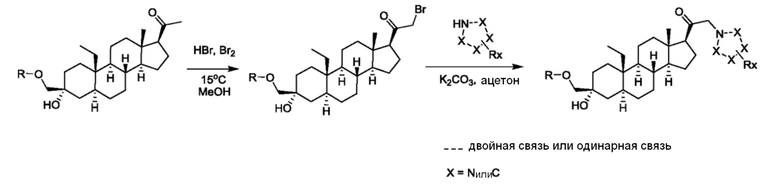
[0514] Пример II-1: синтез ((3R,5R,8S,9S,10S,13S,14S,17S)-10-этил-3-гидрокси-3,13-диметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)((S)-3-фенилпирролидин-1-ил)метанона (II-1)
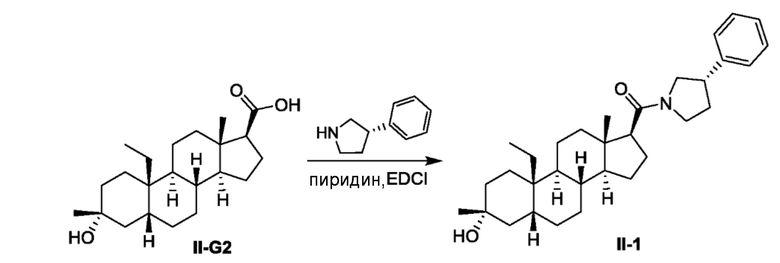
[0515] Экспериментальные данные об интермедиате II-G2 могут быть найдены в Примере II-10.
Раствор II-G2 (50 мг, 0,143 ммол), EDCI (54,9 мг, 0,287 ммол) и (3S)-3-фенилпирролидина (25,3 мг, 0,172 ммол) в пиридине (2 мл) перемешивали при 35°С в течение 18 часов. Смесь обработали водой (5 мл), экстрагировали EtOAc (2×8 мл). Органические слои промыли рассолом (2×10 мл), высушили над Na2SO4, профильтровали, упарили в вакууме с образованием масла (35 мг). Продукт очистили препаративной HPLC (прибор: BF; колонка: Agela DuraShell 150 мм_25 мм_5 мкм; условия: вода (0,225% FA)-ACN, начало B: 69, конец B: 99, время градиента (минут): 8,5, время удерживания 100% B (минут): 2; расход потока (мл/мин): 30; впрыскивания: 7) с образованием II-1 (20 мг, 29%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 7,37-7,29 (м, 2H), 7,26-7,19 (м, 3H), 4,11-3,97 (м, 1H), 3,94-3,85 (м, 0,5H), 3,81-3,71 (м, 0,5H), 3,58-3,26 (м, 3H), 2,60-2,48 (м, 1H), 2,40-2,16 (м, 2H), 2,09-1,88 (м, 2H), 1,87-1,61 (м, 6H), 1,59-1,47 (м, 4H), 1,45-1,28 (м, 8H), 1,27-1,09 (м, 8H), 0,85-0,72 (м, 6H).
LC-ELSD/MS время удерживания (Rt)=1,252 мин в 2-мин хроматографии, 30-90AB_2MIN_E.M, чистота 99%, MS ESI рассчитано для C32H48NO2 [M+H]+ 478, найдено 478.
(Подвижная фаза: 1,5 мл/4 л TFA в воде (растворитель A) и 0,75 мл/4 л TFA в ацетонитриле (растворитель B), с использованием градиента вымывания 30%-90% (растворитель B) в течение 0,9 минуты и выдерживанием при 90% в течение 0,6 минуты при расходе потока 1,2 мл/мин; колонка: Xtimate C18 2,1*30 мм, 3 мкм; длина волны: UV 220 нм; температура колонки: 50oC; MS ионизация: ESI; детектор: PDA&ELSD).
[0516] Пример II-2: синтез 1-((3R,5S,8S,9S,10R,13S,14S,17S)-3-гидрокси-3,13-диметил-10-винилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)этан-1-она (II-A4)
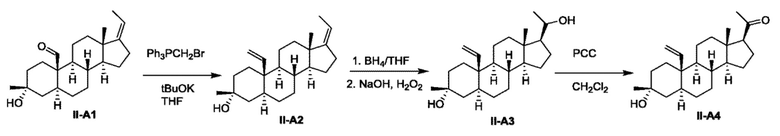
[0517] Синтез II-A2
К суспензии бромида метилтрифенилфосфония (16,27 г, 45,45 ммол) в безводном THF (30 мл) добавили KOtBu (5,15 г, 45,9 ммол) в атмосфере азота (N2). Смесь нагревали при кипячении с обратным холодильником в течение 1 часа. Затем к вышеуказанному кипящему с обратным холодильником раствору добавили соединение II-A1 (5,0 г, 15,15 ммол) в безводном THF (15 мл), и перемешивали при кипячении с обратным холодильником в течение 3 часов. После охлаждения до комнатной температуры раствор вылили в рассол (100 мл). Водный раствор экстрагировали этилацетатом (50 мл×3). Экстракты промыли рассолом (50 мл×2), высушили над Na2SO4, профильтровали, упарили и очистили колоночной хроматографией на силикагеле (петролейный эфир/этилацетат от 20/1 до 10/1) с получением 3,82 г (11,65 ммол, выход 76,90%) II-A2 в виде твердого вещества.
Соединение II-A2:
1H-ЯМР (500 МГц, CDCl3) δH (млн-1): 5,88 (1H, дд, J=11,0 Гц, J=17,0 Гц), 5,33 (1H, дд, J=1,5 Гц, J=11,5 Гц), 5,10 (1H, т×д, J=2,0 Гц, J=7,5 Гц), 5,00 (1H, дд, J=1,5 Гц, J=11,5 Гц), 1,63 (3H, т×д, J=2,0 Гц, 7,0 Гц), 1,15 (3H, с), 0,78 (3H, с).
[0518] Синтез II-A3
К раствору соединения II-A2 (3,82 г, 11,65 ммол) в безводном THF (50 мл) добавили боран-тетрагидрофурановый комплекс (15 мл 1,0 M раствора в THF), и реакционную смесь перемешивали при температуре окружающей среды в течение 3 часов, и медленно добавили 10%-ный водный раствор NaOH (5 мл). Смесь охладили во льду, и медленно добавили 30%-ный водный раствор H2O2 (10 мл). Смесь перемешивали при температуре окружающей среды в течение 1 часа, и затем экстрагировали CH2Cl2 (3×50 мл). Объединенные CH2Cl2-экстракты промыли 10%-ным водным раствором Na2S2O3 (2×20 мл), затем непосредственно использовали в следующей стадии без дополнительной очистки.
[0519] Синтез II-A4
Соединение II-A3 из последней стадии растворили в 100 мл дихлорметана, охлажденного до 0°С, и при 0°С добавили 4,0 г PCC. Затем смесь перемешивали в течение 6 часов. Смесь профильтровали, упарили и очистили флэш-хроматографией на силикагеле вымыванием с использованием (петролейный эфир/этилацетат=12/1~6/1) с образованием 3,15 г (9,15 ммол, 78,54%, две стадии) соединения II-A4 в виде твердого вещества.
1H-ЯМР (500 МГц, CDCl3) δH (млн-1): 5,85 (1H, дд, J=11,5 Гц, J=17,5 Гц), 5,32 (1H, дд, J=2,0 Гц, J=11,5 Гц), 4,98 (1H, дд, J=2,0 Гц, J=11,5 Гц), 2,51 (1H, т, J=9,5 Гц), 2,10 (3H, с), 1,15 (3H, с), 0,51 (3H, с). LC-MS: rt=1,88 мин, m/z=327,0 [M-H2O+H]+, m/z=345,1 [M+H]+.
[0520] Пример II-3: синтез 1-((3R,5S,8S,9S,10S,13S,14S,17S)-10-этил-3-гидрокси-3,13-диметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)этан-1-она (II-A5)
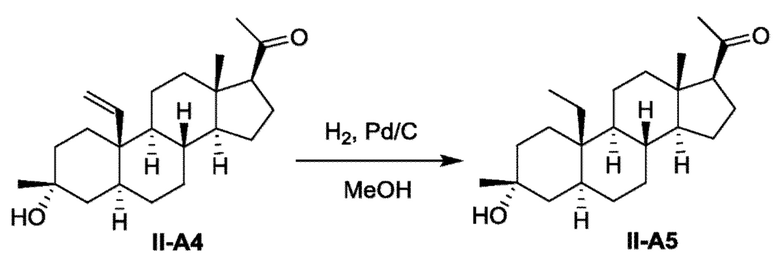
Соединение II-A4 (1,0 г, 2,91 ммол) растворили в 20 мл безводного MeOH, и добавили 100 мг Pd/C. Реакционную смесь перемешивали при комнатной температуре в атмосфере H2 из баллона в течение ночи, профильтровали, полученный раствор упарили и очистили колоночной хроматографией на силикагеле (петролейный эфир/этилацетат от 12/1 до 6/1) с образованием 896 мг (2,59 ммол, выход 89,0%) соединения II-A5 в виде твердого вещества.
1H-ЯМР (500 МГц, CDCl3) δH (млн-1): 2,52 (1H, т, J=8,5 Гц), 2,11 (3H, с), 1,20 (3H, с), 0,93 (3H, т, J=7,0 Гц), 0,63 (3H, с).
[0521] Пример II-4: синтез 1-((3R,5S,8S,9S,10S,13S,14S,17S)-10-этил-3-гидрокси-3,13-диметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-(1H-пиразол-1-ил)этан-1-она (II-A7)
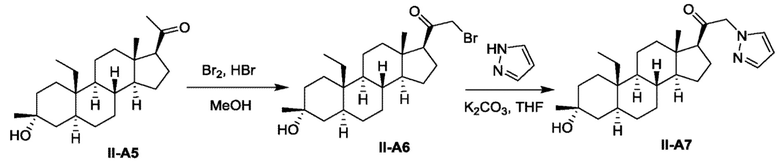
[0522] Синтез II-A6:
Соединение II-A5 (100 мг, 0,29 ммол) растворили в 10 мл безводного MeOH, и добавили 3 капли Br2 и 2 капли водной HBr. Реакционную смесь перемешивали при комнатной температуре три часа, затем раствор вылили в ледяную воду (30 мл). Водный раствор экстрагировали этилацетатом (20 мл×2). Экстракты высушили над MgSO4, профильтровали, упарили с образованием 94 мг соединения II-A6 в виде твердого вещества.
[0523] Синтез II-A7
64 мг (0,15 ммол) соединения I-A6 растворили в 8 мл безводного THF и добавили 100 мг (0,77 ммол) K2CO3, 100 мг (1,47 ммол) пиразола. Реакционную смесь перемешивали при комнатной температуре в течение ночи. Затем раствор разбавили этилацетатом (100 мл). Полученный раствор промыли рассолом (100 мл), высушили над сульфатом натрия и упарили в вакууме. Остаток очистили обратнофазной препаративной HPLC с образованием 20 мг (0,05 ммол, 32,36%) соединения II-A7 в виде твердого вещества.
1H-ЯМР (500 МГц, CDCl3) δH (млн-1): 7,54 (1H, д, J=2,0 Гц), 7,40 (1H, д, J=2,0 Гц), 6,33 (1H, т, J=2,0 Гц), 4,95 (1H, AB, J=18,0 Гц), 4,87 (1H, AB, J=17,5 Гц), 2,57 (1H, т, J=9,0 Гц), 1,20 (3H, с), 0,93 (3H, т, J=7,5 Гц), 0,70 (3H, с).
[0524] Пример II-5: синтез 1-((3R,5S,8S,9S,10S,13S,14S,17S)-10-этил-3-гидрокси-3,13-диметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-(1H-1,2,3-триазол-1-ил)этан-1-она (II-A8) и 1-((3R,5S,8S,9S,10S,13S,14S,17S)-10-этил-3-гидрокси-3,13-диметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-(2H-1,2,3-триазол-1-ил)этан-1-она (II-A8a)
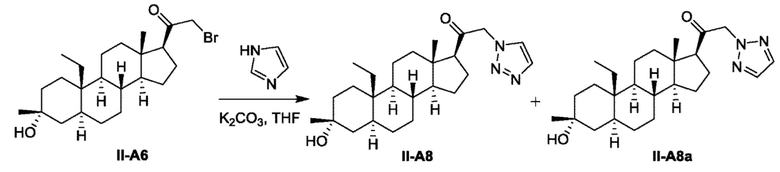
К растворенному в THF (8 мл) II-A6 (120 мг, 0,28 ммол) добавили K2CO3 (200 мг, 1,54 ммол) и 1H-1,2,3-триазол (0,5 мл, 8,6 ммол). Реакционную смесь перемешивали при комнатной температуре в течение ночи. Затем раствор разбавили этилацетатом (100 мл). Полученный раствор промыли рассолом (100 мл), высушили над сульфатом натрия и упарили в вакууме. Остаток очистили обратнофазной препаративной HPLC с образованием II-A8 (24 мг, 0,06 ммол, выход 20,75%) и II-A8a (23 мг, 0,06 ммол, выход 19,89%) в виде твердых веществ.
II-A8:
1H-ЯМР (500 МГц, CDCl3) δH (млн-1): 7,75 (1H, с), 7,64 (1H, с), 5,26 (1H, AB, J=18,0 Гц), 5,13 (1H, AB, J=18,0 Гц), 2,64 (1H, т, J=8,5 Гц), 1,21 (3H, с), 0,94 (3H, т, J=7,5 Гц), 0,69 (3H, с); LC-MS: rt=2,25 мин, m/z=414,4 [M+H]+.
II-A8a:
1H-ЯМР (500 МГц, CDCl3) δH (млн-1): 7,68 (2H, с), 5,25 (1H, AB, J=17,0 Гц), 5,21 (1H, AB, J=17,5 Гц), 2,57 (1H, т, J=9,0 Гц), 1,21 (3H, с), 0,94 (3H, т, J=7,5 Гц), 0,73 (3H, с); LC-MS: rt=2,40 мин, m/z=414,4 [M+H]+.
[0525] Пример II-6: синтез 1-((3R,5S,8S,9S,10S,13S,14S,17S)-10-этил-3-гидрокси-3,13-диметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-морфолиноэтан-1-она (II-A9)
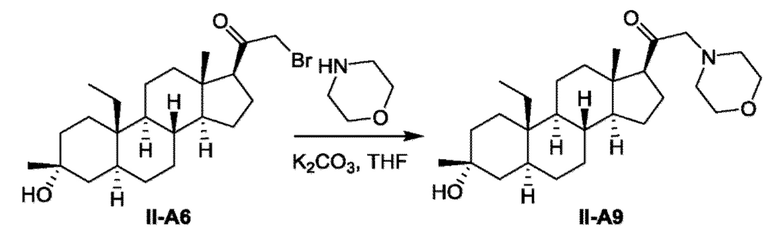
К растворенному в THF (8 мл) соединению II-A6 (90 мг, 0,21 ммол) добавили K2CO3 (100 мг, 0,77 ммол) и морфолин (0,5 мл, 5,74 ммол). Реакционную смесь перемешивали при комнатной температуре в течение ночи. Раствор разбавили этилацетатом (100 мл). Полученный раствор промыли рассолом (100 мл), высушили над сульфатом натрия и упарили в вакууме. Остаток очистили обратнофазной препаративной HPLC с образованием 50 мг (0,11 ммол, 55,24%) продукта II-A9 в виде твердого вещества.
1H-ЯМР (500 МГц, CDCl3) δH (млн-1): 3,75 (4H, т, J=4,5 Гц), 3,18 (1H, AB, J=17,5 Гц), 3,17 (1H, AB, J=17,5 Гц), 2,56 (1H, т, J=8,5 Гц), 2,51-2,45 (4H, м), 1,20 (3H, с), 0,93 (3H, т, J=7,5 Гц), 0,64 (3H, с); LC-MS: rt=2,40 мин, m/z=432,4 [M+H]+.
[0526] Пример II-7: синтез 1-((3R,5S,8S,9S,10S,13S,14S,17S)-10-этил-3-гидрокси-3,13-диметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-(4-(метилсульфонил)пиперазин-1-ил)этан-1-она (II-A10)
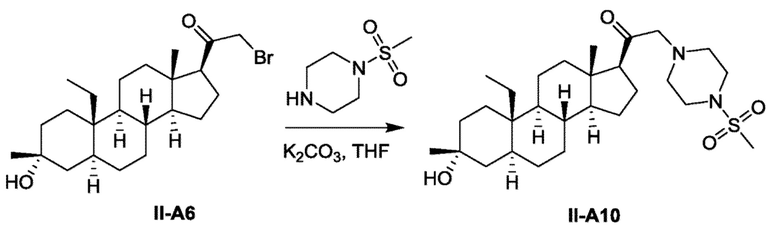
К растворенному в THF (8 мл) соединению II-A6 (150 мг, 0,35 ммол) добавили K2CO3 (160 мг, 1,15 ммол) и 1-(метилсульфонил)пиперазин (150 мг, 0,92 ммол). Реакционную смесь перемешивали при комнатной температуре в течение ночи. Раствор разбавили этилацетатом (100 мл), и полученный раствор промыли рассолом (100 мл), высушили над сульфатом натрия и упарили в вакууме. Остаток очистили обратнофазной препаративной HPLC с образованием 33 мг (0,06 ммол, 18,56%) продукта II-A10 в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH (млн-1): 3,30 (4H, т, J=4,0 Гц), 3,25 (2H, с), 2,78 (3H, с), 2,64~2,57 (4H, м), 2,51 (1H, т, J=9,2 Гц), 1,21 (3H, с), 0,93 (3H, т, J=7,2 Гц), 0,64 (3H, с); LC-MS: rt=2,33 мин, m/z=509,4 [M+H]+.
[0527] Пример II-8: синтез 1-((3R,5S,8S,9S,10S,13S,14S,17S)-10-этил-3-гидрокси-3,13-диметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-гидроксиэтан-1-она (II-A11)
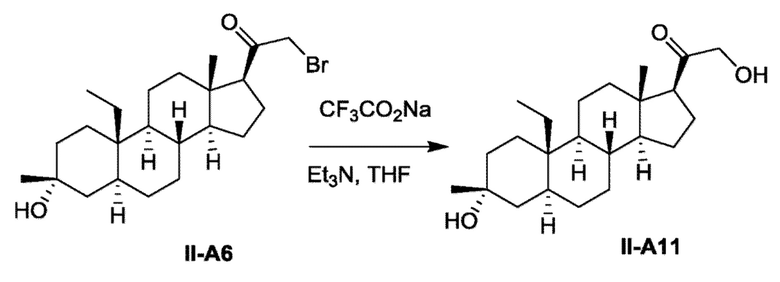
К растворенному в THF (8 мл) соединению II-A6 (300 мг, 0,71 ммол) добавили триэтиламин (1 мл) и 2,2,2-трифторуксусную кислоту (0,5 мл). Смесь нагревали при кипячении с обратным холодильником в течение 1 часа, затем добавили 400 мг (2,9 ммол) 2,2,2-трифторацетата натрия, и полученный раствор кипятили с обратным холодильником в течение ночи, затем раствор вылили в ледяную воду (50 мл). Водный раствор экстрагировали этилацетатом (30 мл×2). Экстракты высушили над MgSO4, и упарили в вакууме. Остаток очистили обратнофазной препаративной HPLC с образованием 88 мг (0,24 ммол, 34,23%) продукта II-A11 в виде твердого вещества.
1H-ЯМР (500 МГц, CDCl3) δH (млн-1): 4,20 (1H, AB×д, J=4,0 Гц, J=19,0 Гц), 4,15 (1H, AB×д, J=4,0 Гц, J=19,0 Гц), 3,28 (1H, т, J=4,0 Гц), 2,44 (1H, т, J=9,0 Гц), 2,20 (1H, дд, J=11,0 Гц, J=20,5 Гц,), 1,20 (3H, с), 0,93 (3H, AB, J=7,5 Гц), 0,68 (3H, с).
[0528] Пример II-9: синтез 1-((3R,5R,8S,9S,10S,13S,14S,17S)-10-этил-3-гидрокси-3,13-диметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)этан-1-она (II-E12)
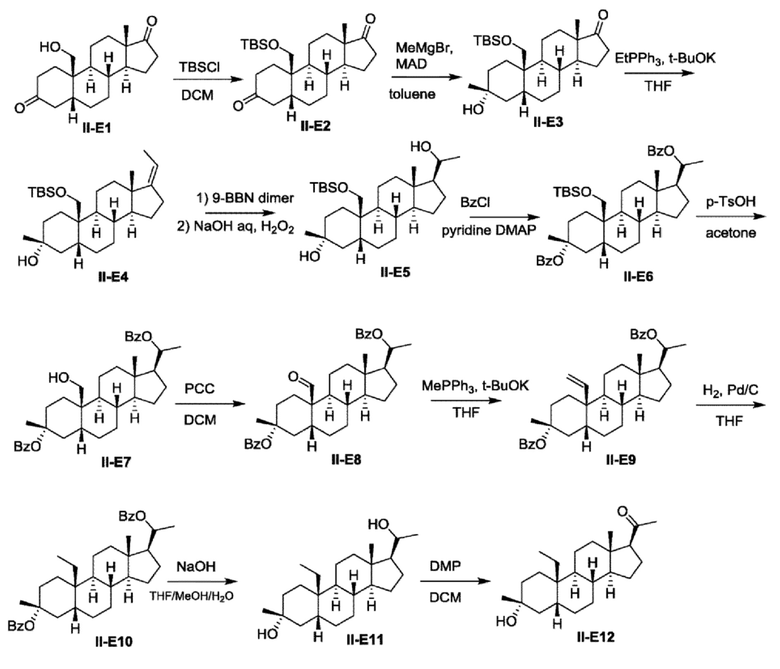
[0529] Синтез II-E2
К раствору II-E1 (226 г, 742 ммол) в DCM (1000 мл) добавили 1H-имидазол (125 г, 1,85 моля) и трет-бутилхлордиметилсилан (200 г, 1,33 моля) при 25°С под N2. После перемешивания при 25°С в течение 4 часов смесь залили водой (500 мл). Органический слой отделили. Водную фазу экстрагировали DCM (2×300 мл). Объединенную органическую фазу промыли насыщенным рассолом (500 мл), высушили над безводным Na2SO4, профильтровали и упарили в вакууме. Остаток очистили хроматографией на силикагеле (PE/EtOAc=100/1 до 20/1) с образованием продукта II-E2 (240 г, 77%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 3,80-3,75 (м, 1H), 3,60-3,50 (м, 1H), 2,65-2,50 (м, 1H), 2,48-2,40 (м, 1H), 2,40-2,25 (м, 3H), 2,20-1,65 (м, 7H), 1,65-1,10 (м, 9H), 0,81-0,80 (м, 13H), 0,00 (м, 6H).
[0530] Синтез II-E3
К раствору BHT (753 г, 3,42 моля) в толуоле (2000 мл) под азотом при 0°С по каплям добавили раствор триметилалюминия (855 мл, 2 M, 1,71 моля). После перемешивания при 0°С в течение 30 минут раствор охладили до -78°С, с последующим добавлением по каплям при -78°С раствора II-E2 (240 г, 573 ммол) в толуоле (500 мл). После перемешивания при -78°С в течение 1 часа по каплям добавили при -78°С раствор MeMgBr (476 мл, 1,43 моля, 3 M в диэтиловом эфире). Полученный раствор перемешивали при температуре от -78°С до -60°С в течение 2 часов. Реакционную смесь вылили при -60°С в насыщенный раствор лимонной кислоты (3000 мл). После перемешивания при 25°С в течение 25 минут водный слой экстрагировали этилацетатом (3×1000 мл). Объединенный органический слой высушили над Na2SO4 и упарили в вакууме с образованием масла, которое очистили на колонке с силикагелем (PE:EtOAc=50:1, 30:1, 15:1, 10:1, 5:1) с образованием II-E3 (60 г, 24%) в виде твердого вещества и II-E3 (1,2 кг).
1H-ЯМР (400 МГц, CDCl3) δH 3,80-3,75 (м, 1H), 3,45-3,35 (м, 1H), 2,55-2,40 (м, 1H), 2,25-1,65 (м, 7H), 1,65-1,35 (м, 6H), 1,35-1,15 (м, 12H), 0,90-0,75 (м, 12H), 0,05 (м, 6H).
[0531] Синтез II-E4
К суспензии MePPh3Br (170 г, 460 ммол) в THF (200 мл) добавили t-BuOK (51,6 г, 460 ммол) при 25°С. После добавления реакционную смесь нагрели до 45°С и перемешивали в течение 1 часа. Затем добавили раствор II-E3 (50 г, 115 ммол) в THF (50 мл), и реакционную смесь перемешивали при 45°С в течение 16 часов. Смесь обработали раствором NH4Cl (100 мл, насыщенным, водным). Органический слой отделили. Водную фазу экстрагировали EtOAc (2×100 мл). Объединенную органическую фазу промыли насыщенным рассолом (2×50 мл), высушили над безводным Na2SO4, профильтровали, упарили. Остаток очистили на колонке для флэш-хроматографии (0~10% EtOAc в PE) с образованием II-E4 (48 г, 93%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 5,25-5,05 (м, 1H), 3,80-3,75 (м, 1H), 3,45-3,35 (м, 1H), 2,45-2,35 (м, 1H), 2,35-2,15 (м, 2H), 2,00-1,80 (м, 2H), 1,75-1,35 (м, 13H), 1,35-1,05 (м, 11H), 0,95-0,80 (м, 9H), 0,80-0,75 (м, 3H), 0,05 (м, 6H).
[0532] Синтез II-E5
К раствору II-E4 (48 г, 107 ммол) в THF (500 мл) при 0°С добавили 9-BBN-димер (104 г, 428 ммол) под N2. Раствор перемешивали при 65°С в течение 2 часов. После охлаждения до 0°С добавили EtOH (49,2 г, 1,07 моля). Затем очень медленно добавили раствор NaOH (214 мл, 5 M, 1,07 моля). После добавления медленно добавили H2O2 (121 г, 1,07 моля, 30% в воде), и внутреннюю температуру поддерживали ниже 10°С. Смесь перемешивали при 75°С под N2 в течение 1 часа. Смесь повторно охладили до 25°С. Затем добавили воду (300 мл). Органический слой отделили. Водную фазу экстрагировали EtOAc (3×100 мл). Объединенную органическую фазу промыли насыщенным рассолом (100 мл), высушили над безводным Na2SO4, профильтровали и упарили в вакууме. Остаток перекристаллизовали из THF/H2O (100 мл/1500 мл) при 25°С и очистили на колонке для флэш-хроматографии (0~20% EtOAc в PE) с образованием II-E5 (45 г, 82%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 3,80-3,75 (м, 1H), 3,75-3,55 (м, 1H), 3,45-3,35 (м, 1H), 2,04 (с, 4H), 2,01-1,75 (м, 4H), 1,75-1,55 (м, 3H), 1,55-1,25 (м, 12H), 1,25-1,05 (м, 8H), 0,89 (с, 9H), 0,63 (с, 3H), 0,05-0,01 (м, 6H).
[0533] Синтез II-E6
К раствору II-E5 (15 г, 32,2 ммол) в пиридине (200 мл) добавили бензоилхлорид (22,6 г, 161 ммол) и DMAP (392 мг, 3,22 ммол). После перемешивания при 80°С в течение 4 часов реакционную смесь вылили в воду (1000 мл). Смесь перемешивали в течение 10 минут, профильтровали, и осадок на фильтре растворили в EtOAc (200 мл). Раствор промыли рассолом (2×50 мл), высушили над Na2SO4, профильтровали, упарили. Остаток очистили на колонке для флэш-хроматографии (0~10% EtOAc в PE) с образованием II-E6 (19 г, 84%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 8,05-8,00 (м, 4H), 7,65-7,50 (м, 2H), 7,45-7,35 (м, 4H), 5,25-5,15 (м, 1H), 3,80-3,75 (м, 1H), 3,45-3,35 (м, 1H), 2,30-2,20 (м, 1H), 2,25-2,00 (м, 2H), 1,95-1,75 (м, 4H), 1,75-1,25 (м, 5H), 1,25-1,00 (м, 13H), 0,95-0,75 (м, 13H), 0,70 (с, 3H), 0,06 (м, 6H).
[0534] Синтез II-E7
К раствору II-E6 (18,9 г, 28,0 ммол) в ацетоне (200 мл) добавили p-TsOH (10,4 г, 56,0 ммол). Реакционную смесь перемешивали при 25°С в течение 5 часов, залили водой (200) и экстрагировали EtOAc (2×200 мл). Объединенные органические экстракты промыли раствором NaHCO3 (50 мл, 10%) и рассолом (50 мл), и высушили над Na2SO4, профильтровали и упарили с образованием II-E7 (15 г) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δН 8,05-8,00 (м, 4H), 7,65-7,50 (м, 2H), 7,45-7,35 (м, 4H), 5,25-5,15 (м, 1H), 4,00-3,90 (м, 1H), 3,65-3,50 (м, 1H), 2,30-2,20 (м, 1H), 2,20-1,75 (м, 7H), 1,75-1,25 (м, 6H), 1,25-1,05 (м, 12H), 0,91 (с, 4H), 0,70 (с, 3H).
[0535] Синтез II-E8
К раствору II-E7 (15 г, 26,8 ммол) в DCM (100 мл) при 25°С добавили PCC (11,5 г, 53,6 ммол) и силикагель (10 г). После перемешивания при 25°С в течение 2 часов реакционную смесь профильтровали, и остаток промыли безводным DCM (2×50 мл). Объединенный фильтрат упарили в вакууме. Остаток очистили на колонке для флэш-хроматографии (0~10% EtOAc в PE) с образованием II-E8 (7 г, 58%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δН 0,97 (с, 1H) 8,05-8,00 (м, 4H), 7,65-7,50 (м, 2H), 7,45-7,35 (м, 4H), 5,25-5,15 (м, 1H), 2,30-2,20 (м, 1H), 2,20-1,75 (м, 12H), 1,75-1,01 (м, 14H), 1,01-0,80 (м, 4H) 0,78 (с, 3H).
[0536] Синтез II-E9
К суспензии PPh3EtBr (17,9 г, 30,8 ммол) в THF (100 мл) при 25°С добавили t-BuOK (3,45 г, 30,8 ммол). После перемешивания при 45°С в течение 1 часа добавили при 40°С раствор II-E8 (7 г, 15,4 ммол) в THF (20 мл). Реакционную смесь перемешивали при 40°С в течение 10 минут и обработали насыщенным раствором NH4Cl (50 мл) и EtOAc (50 мл). Органический слой отделили, и водную фазу экстрагировали EtOAc (2×50 мл). Объединенную органическую фазу промыли насыщенным рассолом (2×30 мл), высушили над безводным Na2SO4, профильтровали и упарили. Остаток очистили на колонке для флэш-хроматографии (0~20% EtOAc в PE) с образованием II-E9 (4,8 г, 90%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 8,05-8,00 (м, 4H), 7,65-7,50 (м, 2H), 7,45-7,35 (м, 4H), 6,40-6,25 (м, 1H), 5,20-4,95 (м, 3H), 2,30-2,20 (м, 1H), 2,15-1,75 (м, 9H), 1,75-1,05 (м, 15H), 1,05-0,80 (м, 4H), 0,69 (с, 3H).
[0537] Синтез II-E10
К раствору II-E9 (2,5 г, 4,50 ммол) в THF (30 мл) добавили Pd-C (сухой, 10%, 0,2 г) под N2. Суспензию дегазировали в вакууме и трижды продули водородом. Смесь перемешивали под H2 (30 psi, (0,21 МПа)) при 25°С в течение 16 часов с образованием суспензии. Реакционную смесь профильтровали через слой Целита и промыли THF (3×20 мл). Фильтрат упарили с образованием II-E10 (2,4 г, 96%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 8,05-8,00 (м, 4H), 7,65-7,50 (м, 2H), 7,45-7,35 (м, 4H), 5,20-5,10 (м, 1H), 2,30-2,20 (м, 1H), 2,10-1,75 (м, 6H), 1,75-1,30 (м, 13H), 1,30-1,05 (м, 11H), 0,85-0,75 (м, 3H), 0,70 (с, 3H).
[0538] Синтез II-E11
К раствору II-E10 (2,4 г, 0,875 ммол) в THF (10 мл) и MeOH (10 мл) добавили NaOH (1,72 г, 43,1 ммол) и H2O (4 мл) при 25°С. раствор перемешивали при 25°С в течение 48 часов. Остаток вылили в воду (30 мл). Смесь экстрагировали EtOAc (2×20 мл). Объединенные органические слои высушили над Na2SO4, профильтровали и упарили в вакууме с образованием продукта, который растерли с MeCN (10 мл) с образованием желательного продукта II-E11 (1,6 г) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 3,75-3,65 (м, 1H), 2,05-1,75 (м, 4H), 1,75-1,35 (м, 13H), 1,35-1,05 (м, 16H), 0,85-0,75 (м, 3H), 0,64 (с, 3H).
[0539] Синтез II-E12
К раствору II-E11 (1,6 г, 4,59 ммол) в DCM (20 мл) добавили PCC (1,97 г, 1,51 ммол) и силикагель (1 г) при 25°С. После перемешивания при 25°С в течение 3 часов реакционную смесь профильтровали, и остаток промыли безводным DCM (2×10 мл). Объединенный фильтрат упарили в вакууме. Остаток очистили на колонке для флэш-хроматографии (0~50% EtOAc в PE) с образованием II-E12 (1,4 г, 88%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 2,60-2,50 (м, 1H), 2,25-2,05 (м, 4H), 2,05-1,90 (м, 2H), 1,80-1,65 (м, 6H), 1,65-0,30 (м, 8H), 1,30-1,05 (м, 11H), 0,85-0,70 (м, 3H), 0,59 (с, 3H).
LC-ELSD/MS Rt=1,223 мин в 2-мин хроматографии, 30-90AB_2MIN_E, чистота 99%, MS ESI рассчитано для C23H37O [M+H-H2O]+ 329, найдено 329.
(Подвижная фаза: 1,5 мл/4 л TFA в воде (растворитель A) и 0,75 мл/4 л TFA в ацетонитриле (растворитель B), с использованием градиента вымывания 30%-90% (растворитель B) в течение 0,9 минуты и выдерживанием при 90% в течение 0,6 минуты при расходе потока 1,2 мл/мин; колонка: Xtimate C18 2,1*30 мм, 3 мкм; длина волны: UV 220 нм; температура колонки: 50°С; MS ионизация: ESI; детектор: PDA&ELSD).
[0540] Пример II-10: синтез (3R,5R,8S,9S,10S,13S,14S,17S)-10-этил-3-гидрокси-3,13-диметил-N-фенилгексадекагидро-1H-циклопента[a]фенантрен-17-карбоксамида (II-G3)
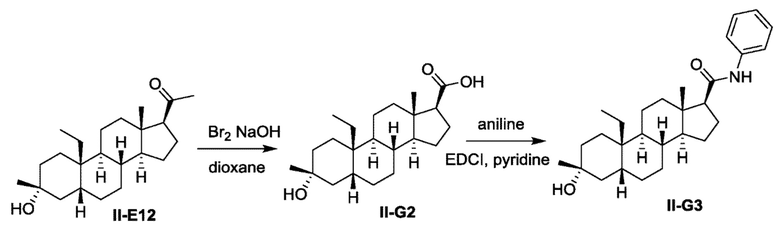
[0541] Экспериментальные данные о II-E12 могут быть найдены в Примере II-8.
[0542] Синтез II-G2
Жидкий бром (2,28 г, 14,3 ммол) медленно добавили к интенсивно перемешиваемому водному раствору гидроксида натрия (5,73 мл, 3 M, 17,2 ммол) при 0°С. Когда весь бром растворился, смесь разбавили холодным диоксаном (10 мл), и медленно добавили к перемешиваемому раствору II-E12 (500 мг, 1,44 ммол) в диоксане (10 мл) и воде (10 мл), и образовался осадок, и реакционную смесь перемешивали при 20°С в течение 16 часов. Оставшийся окислительный реагент погасили водным раствором Na2S2O3 (20 мл), и затем смесь нагревали при 80°С, пока твердый материал не растворился. Подкисление раствора соляной кислотой (3н.) привело к образованию осадка. Твердое вещество отфильтровали и промыли водой (3×20 мл) с образованием твердого вещества, которое высушили в вакууме с получением II-G2 (450 мг) в виде твердого вещества.
[0543] Синтез II-G3
К раствору II-G2 (100 мг, 0,2869 ммол) в пиридине (5 мл) добавили EDCI (82,4 мг, 0,4303 ммол). После перемешивания при 20°С в течение 10 минут добавили анилин (29,3 мг, 0,3155 ммол). Смесь перемешивали при 20°С в течение 16 часов. К реакционной смеси добавили воду (20 мл) и перемешивали в течение 30 минут. Суспензию профильтровали и перекристаллизовали из MeCN (5 мл) при 20°С с образованием II-G3 (63 мг, 52%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 7,60-7,45 (м, 2H), 7,35-7,27 (м, 2H), 7,20-7,05 (м, 1H), 6,93 (с, 1H), 2,35-2,25 (м, 2H), 2,10-1,95 (м, 2H), 1,90-1,50 (м, 6H), 1,50-1,05 (м, 19H), 0,85-0,75 (м, 3H), 0,73 (с, 3H).
LC-ELSD/MS чистота 99%, MS ESI рассчитано для C28H42NO2 [M+H]+ 424, найдено 424.
[0544] Пример II-11: синтез 1-((3R,5R,8S,9S,10S,13S,14S,17S)-10-этил-3-гидрокси-3,13-диметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-(6-метокси-1H-бензо[d][1,2,3]триазол-1-ил)этан-1-она (II-M2), 1-((3R,5R,8S,9S,10S,13S,14S,17S)-10-этил-3-гидрокси-3,13-диметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-(5-метокси-1H-бензо[d][1,2,3]триазол-1-ил)этан-1-она (II-M2a) и 1-((3R,5R,8S,9S,10S,13S,14S,17S)-10-этил-3-гидрокси-3,13-диметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-(5-метокси-2H- бензо[d][1,2,3]триазол-2-ил)этан-1-она (II-M2b)
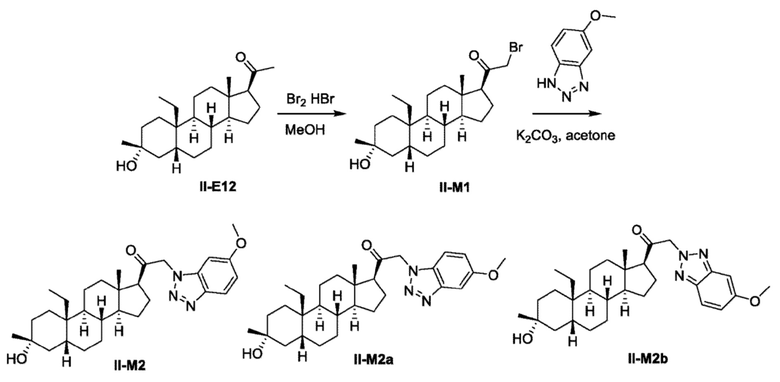
[0545] Экспериментальные данные о II-E12 могут быть найдены в Примере II-8.
Синтез II-M1
[0546] К раствору II-E12 (500 мг, 1,44 ммол) в MeOH (10 мл) добавили HBr (58,2 мг, 0,288 ммол, 40% в воде) и Br2 (241 мг, 1,51 ммол) при 25°С. После перемешивания при 25°С в течение 2 часов смесь залили насыщенным водным раствором NaHCO3 (20 мл). Смесь экстрагировали EtOAc (2×20 мл). Объединенную органическую фазу промыли рассолом (20 мл), высушили над безводным Na2SO4, профильтровали, упарили в вакууме с образованием II-M1 (610 мг) в виде твердого вещества, которое использовали непосредственно в следующей стадии.
Синтез II-M2, II-M2a, II-M2b
[0547] К раствору II-M1 (510 мг, 1,19 ммол) в ацетоне (10 мл) добавили K2CO3 (245 мг, 1,78 ммол) и 5-метил-2H-тетразол (211 мг, 1,42 ммол) при 20°С. Смесь перемешивали при 20°С в течение 16 часов. Реакционную смесь обработали водой (20 мл). Смесь экстрагировали EtOAc (2×20 мл). Объединенную органическую фазу промыли рассолом (20 мл), высушили над безводным Na2SO4, профильтровали, упарили в вакууме. Остаток очистили с использованием HPLC (колонка: YMC-Actus Triart C18 100*30 мм*5 мкм), градиент: 75-95% B (вода (0,05% HCl)-ACN), расход потока: 25 мл/мин) с получением смеси II-M2 и II-M2a (пик 1, 320 мг) в виде твердого вещества, и II-M2b (пик 2, 50 мг) в виде твердого вещества.
Смесь II-M2 и II-M2a (320 мг) очистили с использованием SFC (колонка: DAICEL CHIRALCEL OJ-H (250 мм*30 мм, 5 мкм)), градиент: 35-35% B (0,1% NH3H2O, B=EtOH ), расход потока: 200 мл/мин) с получением II-M2 (пик 1, 49 мг, 8%) в виде твердого вещества, и II-M2a (пик 2, 62 мг, 10%) в виде твердого вещества.
Остаток II-M2b (50 мг) растворили в MeCN (5 мл) при 25°С и упарили в вакууме с образованием II-M2b (45 мг, 8%) в виде твердого вещества.
II-M2:
1H-ЯМР (400 МГц, CDCl3) δH 7,90-7,80 (м, 1H), 7,05-6,95 (м, 1H), 6,75-6,55 (м, 1H), 5,45-5,25 (м, 2H), 3,86 (с, 3H), 2,75-5,60 (м, 1H), 2,25-2,05 (м, 2H), 2,01-1,85 (м, 1H), 1,80-1,50 (м, 6H), 1,50-1,05 (м, 19H), 0,80-0,75 (м, 3H), 0,72 (с, 3H); MS ESI рассчитано для C30H44N3O3 [M+H]+ 494, найдено 494.
II-M2a:
1H-ЯМР (400 МГц, CDCl3) δ 7,40-7,35 (м, 1H), 7,25-7,15 (м, 1H), 7,15-7,05 (м, 1H), 5,40-5,30 (м, 2H), 3,89 (м, 3H), 2,65-2,55 (м, 1H), 2,25-2,05 (м, 3H), 2,05-1,80 (м, 1H), 1,75-1,50 (м, 7H), 1,50-1,30 (м, 7H), 1,30-1,05 (м, 10H), 0,85-0,75 (м, 3H), 0,70 (с, 3H); MS ESI рассчитано для C30H44N3O3 [M+H]+ 494, найдено 494.
II-M2b:
1H-ЯМР (400 МГц, CDCl3) δH 7,5-7,70 (м, 1H), 7,15-7,05 (м, 2H), 5,55-5,35 (м, 2H), 3,88 (м, 3H), 2,65-2,55 (м, 1H), 2,25-2,05 (м, 2H), 2,05-1,80 (м, 1H), 1,80-1,50 (м, 7H), 1,50-1,30 (м, 8H), 1,30-1,05 (м, 10H), 0,85-0,75 (м, 3H), 0,72 (с, 3H); MS ESI рассчитано для C30H44N3O3 [M+H]+ 494, найдено 494.
[0548] Пример II-12-II-14
Нижеследующие примеры были выполнены из II-M1, как в Примере II-11, с заменой 5-метил-2Н-тетразола указанными нуклеофилами.
[0549] Пример II-20-II-22
[0550] Нижеследующие примеры были выполнены из II-G2, как в Примере II-1, с заменой (3S)-3-фенилпирролидина указанным нуклеофилом (амином).
[0551] Пример II-30: синтез ((3R,5R,8S,9S,10S,13S,14S,17S)-10-этил-3-гидрокси-3,13-диметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)(о-толил)метанона (II-G5)
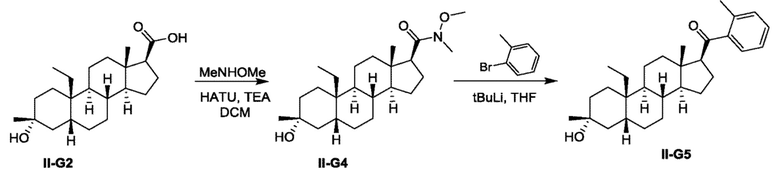
Синтез II-G4
[0552] К раствору II-G2 (100 мг, 0,3 ммол) в DMF (3 мл) добавили HATU (163 мг, 0,4 ммол), TEA (57,9 мг, 0,6 ммол) и гидрохлорид N, O-диметилгидроксиламина (26,2 мг, 0,4 ммол) при 25°С. Смесь перемешивали при 25°С в течение 16 часов. Реакционную смесь вылили в воду (50 мл) и экстрагировали DCM (2×50 мл). Объединенную органическую фазу промыли рассолом (50 мл), высушили над безводным Na2SO4, профильтровали и упарили в вакууме с получением продукта, который промыли раствором LiCl (2×50 мл), рассолом (2×20мл), высушили над безводным Na2SO4, профильтровали, упарили и очистили на колонке для флэш-хроматографии (0~20% EtOAc в PE) с образованием (95 мг, 95%) как II-G4 в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 3,67 (с, 3H), 3,19 (с, 3H), 1,92 (т, J=8,0 Гц, 1H), 1,55-1,45 (м, 7H), 1,45-1,10 (м, 18H), 0,90-0,80 (м, 3H), 0,78 (т, J=8,0 Гц, 3H), 0,72 (с, 3H).
[0553] Синтез II-G5
К раствору 1-бром-2-метилбензола (700 мг, 4,1 ммол) в THF (2 мл) добавили t-BuLi (5,53 мл, 1,3 M, 7,2 ммол) при -70°С. Получилась суспензия. Полученную смесь перемешивали при -70°С в течение 15 минут. К суспензии (2-метилфенил)лития при -70°С добавили II-G4 (80 мг, 0,2 ммол) в THF (2 мл). Реакционную смесь перемешивали при 0°С в течение 10 минут. Смесь экстрагировали этилацетатом (3×50 мл). Объединенную органическую фазу промыли рассолом (50 мл), высушили над безводным Na2SO4, профильтровали и упарили в вакууме с образованием твердого вещества (95 мг). Материал (20 мг) очистили препаративной HPLC с образованием II-G5 (12 мг, 0,028 ммол) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 7,47 (д, 1H), 7,40-7,30 (м, 1H), 7,25-7,20 (м, 2H), 3,30 (т, J=8,0 Гц, 1H), 2,39 (с, 3H), 2,35-2,25 (м, 1H), 1,91 (т, J=8,0 Гц, 1H), 1,75-1,05 (м, 26H), 0,76 (т, J=8,0 Гц, 3H), 0,64 (с, 3H); MS ESI рассчитано для C29H43O2 [M+H]+ 423, найдено 423.
[0554] ПРИМЕР II-35: синтез 1-((3R,5R,8S,9S,10S,13S,14S,17S)-10-этил-3-гидрокси-3-(метоксиметил)-13-метилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)этан-1-она (II-B9)
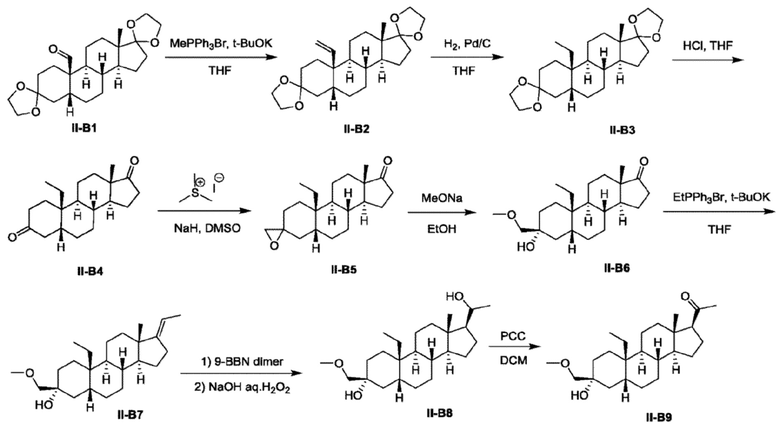
Синтез II-B2
[0555] К суспензии PPh3MeBr (548 г, 1536 ммол) в THF (1000 мл) добавили t-BuOK (172 г, 1536 ммол) при 15°С. После перемешивания при 45°С в течение 1 часа, при 45°С добавили раствор II-B1 (200 г, 512 ммол, описанный в патентном документе «WO2016/134301, 2016, A2») в THF (500 мл), и реакционную смесь перемешивали при 45°С в течение 10 минут. К реакционной смеси добавили насыщенный раствор NH4Cl (500 мл) и EtOAc (500 мл). Органический слой отделили, и водную фазу экстрагировали EtOAc (2×300 мл). Объединенную органическую фазу промыли насыщенным рассолом (2×300 мл), высушили над безводным Na2SO4, профильтровали, упарили и растерли с MeOH/H2O (1000 мл/1000 мл) при 15°С, и очистили хроматографией на силикагеле (PE/EtOAc=50/1 до 20/1) с образованием II-B2 (137 г, 69%) в виде масла.
1H-ЯМР (400 МГц, CDCl3) δ 6,40-6,25 (м, 1H), 5,15-5,00 (м, 2H), 3,95-3,75 (м, 9H), 2,10-1,65 (м, 9H), 1,65-1,25 (м, 5H), 1,25-1,05 (м, 6H), 0,85-0,75 (м, 4H).
Синтез II-B3
[0556] К раствору II-B2 (70 г, 180 ммол) в THF (1000 мл) добавили Pd-C (сухой, 10%, 10 г) под N2. Суспензию дегазировали в вакууме и трижды продули водородом. Смесь перемешивали под H2 (30 psi (0,21 МПа)) при 25°С в течение 16 часов. Реакционную смесь профильтровали через слой Целита и промыли THF (3×500 мл). Фильтрат упарили со 2-ой партией (70 г II-B2) с образованием II-B3 (141 г) в виде масла.
1H-ЯМР (400 МГц, CDCl3) δ 3,95-3,75 (м, 9H), 2,10-1,90 (м, 2H), 1,90-1,65 (м, 8H), 1,65-1,25 (м, 4H), 1,25-1,05 (м, 8H), 0,80-0,45 (с, 7H).
Синтез II-B4
[0557] К раствору II-B3 (141 г, 361 ммол) в THF (1000 мл) добавили водную HCl (361 мл, 4 M, 1444 ммол). Смесь перемешивали при 25°С в течение 16 часов. Смесь вылили в воду (500 мл). Органическую фазу отделили, и водный слой экстрагировали этилацетатом (EA) (2×300 мл). Объединенные органические растворы промыли насыщенным водным раствором NaHCO3 (500 мл), H2O (2×300 мл), рассолом (200 мл), высушили над Na2SO4, профильтровали, упарили в вакууме и растерли с PE (300 мл) при 15°С с образованием II-B4 (82 г, 73%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δ 2,80-2,70 (м, 1H), 2,55-2,45 (м, 3H), 2,45-2,15 (м, 1H), 2,15-2,00 (м, 3H), 2,00-1,90 (м, 1H), 1,90-1,65 (м, 6H), 1,65-1,30 (м, 2H), 1,30-1,10 (м, 7H), 0,88 (с, 3H), 1,85-0,75 (м, 3H).
Синтез II-B5
[0558] К перемешиваемому раствору иодида триметилсульфония (22,2 г, 109 ммол) в DMSO/THF (100 мл/500 мл) добавляли NaH (4,35 г, 109 ммол, 60% в масле) при 0°С в течение 1 часа под N2. Смесь добавляли к раствору II-B4 (30 г, 99,1 ммол) в DMSO (100 мл) при 15°С в течение 4 часов. Реакционную смесь обработали водой (200 мл). Смесь экстрагировали EtOAc (2×100 мл). Объединенную органическую фазу промыли водой (2×100 мл), рассолом (100 мл), высушили над безводным Na2SO4, профильтровали и упарили в вакууме с образованием II-B5 (35 г) в виде масла.
Синтез II-B6
[0559] К безводному метанолу (300 мл) при 15°С десятью порциями добавили Na (9,83 г, 410 ммол). Реакционную смесь перемешивали при 65°С в течение 1 часа. К суспензии метилата натрия при 65°С добавили II-B5 (13 г, 41,0 ммол) в безводном метаноле (50 мл). Реакционную смесь перемешивали при 65°С в течение 16 часов. Добавили воду (500 мл). Реакционную смесь упарили для удаления большей части растворителя. Смесь экстрагировали EtOAc (2×200 мл). Объединенную органическую фазу промыли рассолом (2×100 мл), высушили над безводным Na2SO4, профильтровали, упарили. Остаток очистили на колонке для флэш-хроматографии (0~20% EtOAc в PE) с образованием II-B6 (7 г) в виде масла и II-B6a.
II-B6:
1H-ЯМР (400 МГц, CDCl3) δ 3,45-3,30 (м, 5H), 2,50-2,30 (м, 1H), 2,15-1,95 (м, 2H), 1,95-1,80 (м, 2H), 1,80-1,50 (м, 5H), 1,50-1,30 (м, 7H), 1,30-1,05 (м, 8H), 0,90-0,65 (м, 6H).
Синтез II-B7
[0560] К суспензии бром(этил)трифенилфосфорана (29,6 г, 80,0 ммол) в THF (200 мл) добавили t-BuOK (8,96 г, 80,0 ммол) при 15°С под N2. Смесь нагрели до 45°С и перемешивали в течение 1 часа. Добавили раствор II-B6 (7 г, 20,0 ммол) в THF (50 мл). Смесь перемешивали при 45°С в течение 16 часов. Смесь обработали раствором NH4Cl (100 мл). Органический слой отделили. Водную фазу экстрагировали EtOAc (2×50 мл). Объединенную органическую фазу промыли рассолом (2×30 мл), высушили над безводным Na2SO4, профильтровали, упарили в вакууме. Остаток растерли с MeOH/H2O (50 мл/50 мл) при 15°С с образованием II-B7 (7,5 г) в виде твердого вещества.
Синтез II-B8
[0561] К раствору II-B7 (5 г, 13,8 ммол) в THF (50 мл) добавили 9-BBN-димер (6,73 г, 27,6 ммол) при 15°С. Смесь перемешивали при 15°С в течение 48 часов. После охлаждениия до 0°С к реакционной смеси очень медленно добавили этанол (6,34 г, 138 ммол) и раствор NaOH (27,6 мл, 5 M, 138 ммол). После завершения добавления медленно добавили H2O2 (13,8 мл, 138 ммол, 30%), и внутреннюю температуру поддерживали ниже 15°С. Полученный раствор перемешивали при 75°С в течение 1 часа. Добавили насыщенный водный раствор Na2S2O3 (50 мл), и смесь перемешивали при 0°С в течение дополнительного 1 часа. Реакционную смесь проверили с использованием индикаторной бумаги с иодидом калия и крахмалом, чтобы подтвердить разложение избыточного H2O2. Смесь охладили и добавили к воде (500 мл). Смесь профильтровали. Осадок на фильтре растворили в EtOAc (100 мл). Органическую фазу промыли рассолом (30 мл), высушили над безводным Na2SO4, профильтровали и упарили в вакууме с образованием II-B8 (7 г) в виде масла.
Синтез II-B9
[0562] К раствору II-B8 (7 г, 18,4 ммол) в DCM (100 мл) при 15°С добавили PCC (7,91 г, 36,8 ммол) и силикагель (8 г). Раствор перемешивали при 15°С в течение 3 часов. Реакционную смесь профильтровали, и остаток промыли безводным DCM (2×100 мл). Объединенный фильтрат упарили в вакууме. Остаток очистили на колонке для флэш-хроматографии (0~50% EtOAc в PE) с образованием II-B9 (3,8 г, 55%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δ 3,45-3,30 (м, 5H), 2,63 (с, 1H), 2,60-2,45 (м, 1H), 2,20-2,05 (м, 4H), 2,05-1,80 (м, 2H), 1,80-1,50 (м, 7H), 1,50-1,30 (м, 7H), 1,30-1,05 (м, 7H), 0,80-0,65 (м, 3H), 0,58 (с, 3H); MS ESI рассчитано для C24H39O2 [M+H-H2O]+ 359, найдено 359.
[0563] Пример II-36: синтез ((3R,5R,8S,9S,10S,13S,14S,17S)-10-этил-3-гидрокси-3-(метоксиметил)-13-метилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)((S)-2-метилпиперидин-1-ил)метанона (II-B11)
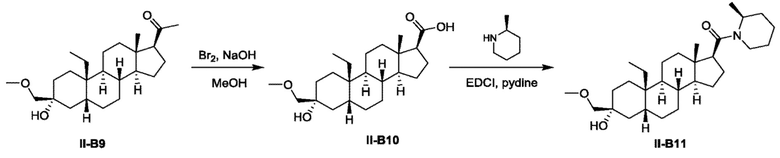
Синтез II-B10
[0564] Жидкий бром (1,05 г, 6,60 ммол) медленно добавляли при 0°С к энергично перемешиваемому водному раствору гидроксида натрия (5,26 мл, 3 M, 15,8 ммол). Когда весь бром растворился, смесь разбавили холодным диоксаном (5 мл) и медленно добавили к перемешиваемому раствору II-B9 (500 мг, 1,32 ммол) в диоксане (10 мл) и воде (5 мл), и образовался осадок, и реакционную смесь перемешивали при 15°С в течение 16 часов. Оставшийся окислительный реагент погасили водным раствором Na2SO3 (30 мл), и смесь затем нагревали при 80°С, пока твердый материал не растворился. Подкисление раствора соляной кислотой (3н.) привело к образованию осадка. К суспензии добавили EtOAc (20 мл). Органическую фазу отделили. Водную фазу экстрагировали EtOAc (2×20 мл). Объединенный органический раствор промыли рассолом (20 мл), высушили над безводным Na2SO4, профильтровали и упарили в вакууме с получением II-B10 (550 мг) в виде твердого вещества.
Синтез II-B11
[0565] К раствору II-B10 (500 мг, 1,32 ммол) в пиридине (10 мл) добавили EDCI (1,01 г, 5,28 ммол) и перемешивали при 25°С в течение 10 минут. Добавили (2S)-2-метилпиперидин (143 мг, 1,45 ммол). Смесь перемешивали при 25°С в течение 16 часов. К реакционной смеси добавили воду (20 мл) и EtOAc (20 мл). Органический слой отделили. Водную фазу экстрагировали EtOAc (2×10 мл). Объединенную органическую фазу промыли рассолом (2×10 мл), высушили над безводным Na2SO4, профильтровали, упарили и очистили с использованием HPLC ((колонка: YMC-Actus Triart C18 100*30 мм*5 мкм), градиент: 85-100% B (A=вода (0,05% HCl)-ACN), B=MeCN), расход потока: 25 мл/мин) с образованием II-B11 (136 мг, 22%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δ 5,00-4,80 (м, 0,7H), 4,65-4,45 (м, 0,3H), 4,35-4,25 (м, 0,3H), 3,80-3,70 (м, 0,7H), 3,40-3,25 (м, 5H), 3,10-2,95 (м, 1H), 2,75-2,60 (м, 2H), 2,35-2,15 (м, 1H), 2,00-1,80 (м, 1H), 1,80-1,55 (м, 12H), 1,55-1,30 (м, 8H), 1,30-1,05 (м, 11H), 0,80-0,65 (м, 6H); MS ESI рассчитано для C29H50NO3 [M+H]+ 460, найдено 460.
[0566] Пример II-40: синтез 1-((3R,5R,8S,9S,10S,13S,14S,17S)-3-(этоксиметил)-10-этил-3-гидрокси-13-метилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)этан-1-она (II-C4)
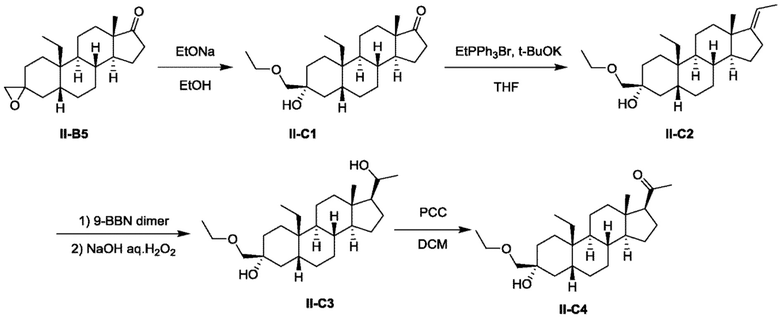
Синтез II-C1
[0567] К безводному EtOH (200 мл) при 15°С десятью порциями добавили Na (25,4 г, 1107 ммол). Реакционную смесь перемешивали при 75°С в течение 1 часа. К суспензии этилата натрия при 75°С добавили II-B5 (22 г, 69,5 ммол) в безводном этаноле (50 мл). Реакционную смесь перемешивали при 75°С в течение 16 часов. Добавили при 15°С воду (500 мл). Реакционную смесь упарили для удаления большей части растворителя. Смесь экстрагировали EtOAc (2×200 мл). Объединенную органическую фазу промыли насыщенным рассолом (2×100 мл), высушили над безводным Na2SO4, профильтровали, упарили. Остаток очистили на колонке для флэш-хроматографии (0~20% EtOAc в PE) с образованием II-C1 (12 г) в виде масла, и II-C1a (7 г, 28%) в виде твердого вещества.
II-C1:
1H-ЯМР (400 МГц, CDCl3) δH 3,60-3,45 (м, 2H), 3,45-3,30 (м, 2H), 2,45-2,30 (м, 1H), 2,10-1,90 (м, 4H), 1,90-1,55 (м, 5H), 1,55-1,30 (м, 7H), 1,30-1,10 (м, 11H), 0,90-0,80 (м, 3H), 0,80-0,60 (м, 3H).
II-C1a:
1H-ЯМР (400 МГц, CDCl3) δH 3,55-3,46 (м, 2H), 3,25-3,15 (м, 2H), 2,47-2,35 (м, 1H), 2,10-1,95 (м, 4H), 1,95-1,85 (м, 1H), 1,85-1,60 (м, 5H), 1,55-1,35 (м, 6H), 1,35-1,15 (м, 11H), 0,90-0,80 (м, 6H)
Синтез II-C2
[0568] К суспензии бром(этил)трифенилфосфорана) (48,9 г, 132 ммол) в THF (200 мл) добавили t-BuOK (14,7 г, 132 ммол) при 15°С под N2. Смесь нагрели до 45°С и перемешивали в течение 1 часа. При 45°С добавили раствор II-C1 (12 г, 33,0 ммол) в THF (20 мл). Смесь перемешивали при 45°С в течение 16 часов. Смесь обработали раствором NH4Cl (100 мл). Органический слой отделили. Водную фазу экстрагировали EtOAc (2×50 мл). Объединенную органическую фазу промыли рассолом (2×40 мл), высушили над безводным Na2SO4, профильтровали, упарили в вакууме. Остаток растерли с MeOH/H2O (50 мл/50 мл) при 20°С с образованием II-C2 (17 г) в виде масла.
Синтез II-C3
[0569] К раствору II-C2 (17 г, 45,3 ммол) в THF (100 мл) добавили 9-BBN-димер (22,1 г, 90,6 ммол) при 15°С. Смесь перемешивали при 15°С в течение 16 часов. После охлаждения до 0°С к реакционной смеси добавили этанол (20,8 г, 453 ммол) и очень медленно раствор NaOH (90,6 мл, 5 M, 453 ммол). После завершения добавления медленно добавили H2O2 (45,3 мл, 453 ммол, 30%), и внутреннюю температуру поддерживали ниже 15°С. Полученный раствор перемешивали при 75°С в течение 1 часа. Добавили насыщенный водный раствор Na2S2O3 (100 мл), и смесь перемешивали при 0°С в течение 1 часа. Реакционную смесь проверили с использованием индикаторной бумаги с иодидом калия и крахмалом, чтобы подтвердить разложение избыточного H2O2. Смесь охладили и добавили к воде (2 л). Смесь профильтровали. Объединенный масляный фильтрат растворили в EtOAc (200 мл). Органическую фазу промыли рассолом (50 мл), высушили над безводным Na2SO4, профильтровали и упарили в вакууме с образованием II-C3 (18 г) в виде масла.
Синтез II-C4
[0570] К раствору II-C3 (18 г, 45,8 ммол) в DCM (200 мл) при 15°С добавили PCC (19,6 г, 91,6 ммол) и силикагель (15 г). Раствор перемешивали при 15°С в течение 3 часов. Реакционную смесь профильтровали, и остаток промыли безводным DCM (2×100 мл). Объединенный фильтрат упарили в вакууме. Остаток очистили на колонке для флэш-хроматографии (0~20% EtOAc в PE) с образованием II-C4 (8 г, 45%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 3,60-3,50 (м, 2H), 3,50-3,30 (м, 2H), 2,74 (с, 1H), 2,60-2,45 (м, 1H), 2,20-2,05 (м, 4H), 2,05-1,75 (м, 2H), 1,75-1,50 (м, 7H), 1,50-1,30 (м, 7H), 1,30-1,05 (м, 10H), 0,80-0,65 (м, 3H), 0,59 (с, 3H); MS ESI рассчитано для C25H41O2 [M+H-H2O]+ 373, найдено 373.
Пример II-43-II-51
[0571] Нижеследующие примеры были выполнены из II-C5, как в Примере II-41, с заменой 1,3-диметил-1H-пиразол-5-амина перечисленными амином и подходящим связующим реагентом (дихлорангидрид щавелевой кислоты, EDCI, HATU, и т.д.).
δF -117,23.
δF -116,27, -117,01
[0572] Пример II-61: синтез 1-((3R,5S,8S,9S,10S,13S,14S,17S)-3-(этоксиметил)-10-этил-3-гидрокси-13-метилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)этан-1-она (II-D9)
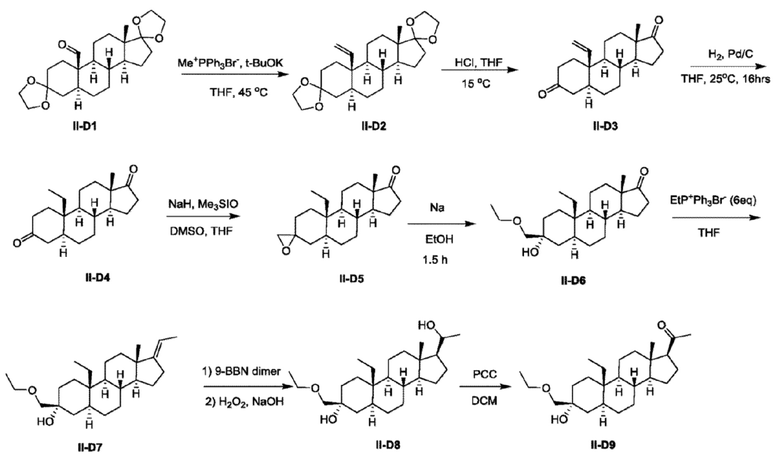
Синтез II-D2
[0573] К суспензии MePPh3Br (50,3 г, 141 ммол) в THF (200 мл) при 15°С добавили t-BuOK (15,8 г, 141 ммол). После перемешивания при 45°С в течение 0,5 часа добавили при 45°С раствор II-D1 (18,5 г, 47,3 ммол) в THF (100 мл), и реакционную смесь перемешивали при 45°С в течение 1 часа. К смеси добавили насыщенный раствор NH4Cl (200 мл), и отделили органический слой. Водный слой экстрагировали EtOAc (2×100 мл). Объединенные органические слои промыли насыщенным рассолом (200 мл), профильтровали и упарили при пониженном давлении. Остаток очистили колоночной хроматографией (PE/EtOAc=10/1~4/1) с получением II-D2 (13,6 г, 74,3%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 5,88 (дд, J=10,8, 17,6 Гц, 1H), 5,35 (дд, J=11,2 Гц, 1H), 5,02 (дд, J=1,2, 18,0 Гц, 1H), 4,00-3,82 (м, 8H), 2,20-2,12 (м, 1H), 2,00-1,90 (м, 1H), 1,85-1,12 (м, 18H), 1,07-0,92 (м, 1H), 0,90-0,80 (м, 1H), 0,74 (с, 3H).
Синтез II-D3
[0574] К раствору II-D2 (13,6 г, 35,0 ммол) в THF (80 мл) добавили 12 M HCl (29,1 мл, 350 ммол). Реакционную смесь перемешивали при 15°С в течение 16 часов. Реакционную смесь разбавили водой (50 мл) и отрегулировали значение рН до pH=9 твердым Na2CO3 (20 г). Водный слой экстрагировали EtOAc (3×200 мл). Объединенные органические слои промыли насыщенным рассолом (200 мл), высушили над безводным Na2SO4, профильтровали и упарили с образованием продукта (10,5 г). Продукт очистили на колонке для флэш-хроматографии (15~20% EtOAc в PE) с образованием II-D3 (8,0 г, 76,9%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 6,03 (дд, J=11,2, 18,0 Гц, 1H), 5,52 (д, J=11,2 Гц, 1H), 5,20 (д, J=18,0 Гц, 1H), 2,55-2,40 (м, 3H), 2,32-1,55 (м, 13H), 1,55-1,15 (м, 4H), 1,10-0,95 (м, 1H), 0,93-0,83 (м, 1H), 0,80 (с, 3H).
Синтез II-D4
[0575] К смеси II-D3 (8,0 г, 26,6 ммол) в THF (200 мл) добавили Pd-C (влажный, 50%, 2,0 г) под Ar. Суспензию дегазировали в вакууме и трижды продули водородом. Над полученным раствором поддерживали давление водорода 30 psi (0,21 МПа) при 25°С в течение 16 часов. Реакционную смесь профильтровали через слой Целита и промыли THF (2×200 мл). Фильтрат упарили при пониженном давлении. Продукт очистили на колонке для флэш-хроматографии (15~20% EtOAc в PE) с образованием II-D4 (8,0 г, 99,5%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 2,55-2,25 (м, 5H), 2,15-1,15 (м, 17H), 1,10 (т, J=8,0 Гц, 3H), 1,05-0,95 (м, 1H), 0,91 (с, 3H), 0,85-0,65 (м, 1H); MS ESI рассчитано для C20H31O2 [M+H]+ 303, найдено 303.
Синтез II-D5
[0576] К перемешиваеому раствору Me3SIO (4,35 г, 19,8 ммол) в DMSO (30 мл) и THF (30 мл) порциями при 0°С добавили NaH (791 мг, 19,8 ммол, 60% в масле). Реакционную смесь перемешивали в течение 1 часа под N2. Смесь добавили к раствору II-D4 (5,0 г, 16,5 ммол) в DMSO (30 мл). Реакционную смесь перемешивали при 15°С в течение 16 часов. Реакционную смесь вылили в ледяную воду (300 мл). Смесь экстрагировали EtOAc (2×100 мл). Объединенную органическую фазу промыли водой (2×100 мл) и рассолом (100 мл), высушили над безводным Na2SO4, профильтровали и упарили с образованием продукта II-D5 (5,0 г) в виде масла (с селективным получением структуры с экваториальным метиленом).
1H-ЯМР (400 МГц, CDCl3) δH 2,61 (с, 2H), 2,42 (дд, J=8,8, 19,6 Гц, 1H), 2,15-1,40 (м, 11H), 1,35-1,05 (м, 8H), 1,02-0,70 (м, 10H).
Синтез II-D6
[0577] К свежеприготовленному раствору этилата натрия (31,5 мл, 31,5 ммол, 1 M в EtOH) при 75°С добавили раствор II-D5 (1,0 г, 3,15 ммол) в безводном этаноле (20 мл). Реакционную смесь перемешивали при 75°С в течение 16 часов. Добавили воду (50 мл). Реакционную смесь упарили для удаления большей части растворителя. Смесь экстрагировали EtOAc (2×30 мл). Объединенную органическую фазу промыли насыщенным рассолом (50 мл), высушили над безводным Na2SO4, профильтровали и упарили. Остаток очистили хроматографией на силикагеле (0-40% EtOAc в PE) с образованием II-D6 (512 мг, 44,9%) в виде масла.
II-D6:
1H-ЯМР (400 МГц, CDCl3) δH 3,52 (кв, J=6,8 Гц, 2H), 3,21 (с, 2H), 2,42 (дд, J=8,8, 19,6 Гц, 1H), 2,15-1,50 (м, 9H), 1,50-1,10 (м, 15H), 1,05-0,99 (м, 1H), 0,95 (т, J=7,6 Гц, 3H), 0,90-0,65 (м, 4H); MS ESI рассчитано для C23H38O3Na [M+Na]+ 385, найдено 385.
[0578] Синтез II-D7
К суспензии бром(этил)трифенилфосфорана (22,4 г, 60,4 ммол) в THF (100 мл) добавили t-BuOK (6,76 г, 60,4 ммол) при 15°С под N2. Смесь нагрели до 45°С и перемешивали в течение 1 часа. Добавили при 45°С раствор II-D6 (5,5 г, 15,1 ммол) в THF (100 мл). Смесь перемешивали при 45°С в течение 16 часов. Смесь обработали раствором NH4Cl (300 мл). Органический слой отделили. Водную фазу экстрагировали EtOAc (2×150 мл). Объединенную органическую фазу промыли рассолом (2×100 мл), высушили над безводным Na2SO4, профильтровали, упарили в вакууме. Остаток очистили на колонке для флэш-хроматографии (0~15% EtOAc в PE) с образованием II-D7 (5,0 г, 88%) в виде масла.
1H-ЯМР (400 МГц, CDCl3) δH 5,15-5,05 (м, 1H), 3,52 (кв, J=6,8 Гц, 2H), 3,21 (с, 2H), 2,40-2,10 (м, 4H), 1,85-1,75 (м, 1H), 1,70-1,40 (м, 7H), 1,35-1,10 (м, 14H), 1,10-0,80 (м, 11H).
[0579] Синтез II-D8
К раствору II-D7 (3,0 г, 8,0 ммол) в THF (50 мл) добавили 9-BBN-димер (3,90 г, 16,0 ммол) при 15°С. Смесь перемешивали при 15°С в течение 16 часов. После охлаждения до 0°С к смеси добавили этанол (3,68 г, 80,0 ммол) и очень медленно раствор NaOH (16 мл, 5 M, 80,0 ммол). После завершения добавления медленно добавили H2O2 (8,01 мл, 80,0 ммол, 30%), и внутреннюю температуру поддерживали ниже 15°С. Полученный раствор перемешивали при 75°С в течение 1 часа. Раствор обработали и очистили вместе с еще одной партией, полученной подобным образом. Добавили насыщенный водный раствор Na2S2O3 (300 мл), и смесь перемешивали при 0°С в течение дополнительнного 1 часа. Реакционную смесь проверили с использованием индикаторной бумаги с иодидом калия и крахмалом, чтобы подтвердить разложение избыточного H2O2. Смесь охладили и добавили к воде (200 мл). Смесь экстрагировали EtOAc (3×100 мл), промыли насыщенным рассолом (200 мл), высушили над безводным Na2SO4, профильтровали и упарили в вакууме с образованием II-D8 (5,0 г) в виде масла.
1H-ЯМР (400 МГц, CDCl3) δH 3,75-3,65 (м, 1H), 3,51 (кв, J=6,8 Гц, 2H), 3,20 (с, 2H), 1,95-1,75 (м, 12H), 1,74-1,40 (м, 13H), 1,39-0,95 (м, 8H), 0,92 (т, J=7,6 Гц, 3H), 0,66 (с, 3H).
Синтез II-D9
[0580] К раствору II-D8 (0,8 г, 2,0 ммол) в DCM (20 мл) при 18°С добавили PCC (872 мг, 4,1 ммол) и силикагель (1 г). Раствор перемешивали при 18°С в течение 3 часов. Реакционную смесь профильтровали, и остаток промыли безводным DCM (2×50 мл). Объединенный фильтрат упарили в вакууме. Остаток очистили на колонке для флэш-хроматографии (0~20% EtOAc в PE) с образованием II-D9 (0,75 г, 94,6%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 3,52 (кв, J=6,8 Гц, 2H), 3,21 (с, 2H), 2,52 (т, J=8,8 Гц, 1H), 2,25-2,10 (м, 5H), 2,05-1,95 (м, 1H), 1,90-1,80 (м, 1H), 1,75-1,65 (м, 4H), 1,55-1,05 (м, 18H), 1,00-0,80 (м, 5H), 0,62 (с, 3H); MS ESI рассчитано для C25H41O2 [M-H2O+H]+ 373, найдено 373.
[0581] Пример II-62: синтез ((3R,5S,8S,9S,10S,13S,14S,17S)-3-(этоксиметил)-10-этил-3-гидрокси-13-метилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)((S)-2-метилпиперидин-1-ил)метанона (II-D11)
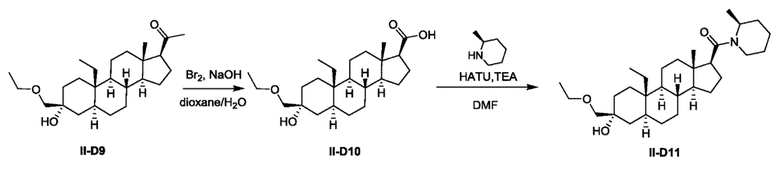
Синтез II-D10
[0582] Жидкий бром (1,22 г, 7,7 ммол) медленно добавляли к энергично перемешиваемому водному раствору гидроксида натрия (10,2 мл, 3 M, 30,7 ммол) при 0°С. Когда весь бром растворился, смесь медленно добавили к перемешиваемому раствору II-D9 (1,0 г, 2,6 ммол) в диоксане (18 мл) и воде (6 мл). Реакционную смесь перемешивали при 15°С в течение 16 часов. Оставшийся окислительный реагент погасили водным раствором Na2SO3 (30 мл). Подкисление раствора соляной кислотой (3н.) привело к образованию осадка. К суспензии добавили EtOAc (50 мл). Отделили органическую фазу. Водную фазу экстрагировали EtOAc (2×50 мл). Объединенные органические слои промыли насыщенным рассолом (50 мл), высушили над безводным Na2SO4, профильтровали и упарили в вакууме с образованием II-D10 (0,8 г, 80%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 3,71 (с, 1H), 3,52 (кв, J=6,8 Гц, 2H), 3,21 (с, 2H), 2,37 (т, J=9,2 Гц, 1H), 2,15-2,00 (м, 3H), 1,90-1,70 (м, 2H), 1,60-1,10 (м, 20H), 1,00-0,65 (м, 5H), 0,74 (с, 3H).
Синтез II-D11
[0583] К раствору II-D10 (200 мг, 0,5 ммол) в DMF (5 мл) добавили HATU (382 мг, 1,0 ммол), TEA (256 мг, 2,5 ммол) и (2S)-2-метилпиперидин (100 мг, 1,0 ммол) при 20°С. Смесь перемешивали при 20°С в течение 16 часов с образованием коричневого раствора. Реакционную смесь вылили в воду (50 мл) и экстрагировали EtOAc (2×20 мл). Объединенную органическую фазу промыли насыщенным рассолом (2×20 мл), высушили над безводным Na2SO4, профильтровали и упарили в вакууме. Остаток очистили на колонке для флэш-хроматографии (10~20% EtOAc в PE) с получением продукта. Продукт очистили препаративной HPLC (колонка: Agela DuraShell 150 мм_25 мм_5 мкм; условия: вода (10 мМ NH4HCO3)-ACN; начало B: 83; конец B: 99; время градиента (минут): 8,5; время удерживания 100% B (минут): 2) с образованием II-D11 (53,3 мг, 22%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 5,00-4,90 (м, 1H), 4,60-4,25 (м, 1H), 3,82 (д, J=11,6 Гц, 1H), 3,52 (кв, J=6,8 Гц, 2H), 3,21 (с, 2H), 3,03 (т, J=12,0 Гц, 1H), 2,63 (т, J=8,8 Гц, 1H), 2,40-2,15 (м, 1H), 2,12 (с, 1H), 1,90-1,80 (м, 2H), 1,65-1,60 (м, 5H), 1,58-1,40 (м, 10H), 1,38-1,00 (м, 15H), 0,95-0,65 (м, 8H); MS ESI рассчитано для C30H52NO3 [M+H]+ 474, найдено 474.
Нижеследующий пример был выполнен из II-D10, как в Примере II-62, с заменой (2S)-2-метилпиперидина перечисленными амином и подходящим связующим реагентом (дихлорангидрид щавелевой кислоты, EDCI, HATU, и т.д.).
[0584] Пример II-70: синтез 1-((3R,5S,8S,9S,10S,13S,14S,17S)-10-этил-3-гидрокси-3-(метоксиметил)-13-метилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)этан-1-она (II-E4)
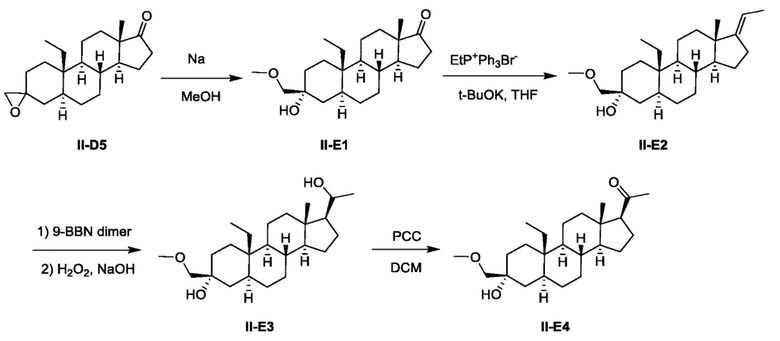
Синтез II-E1
[0585] Свежий Na (1,45 г, 63 ммол) осторожно порциями добавляли к MeOH (63 мл) при 0°С. После перемешивания при 20°С в течение 3 часов Na полностью растворился. К раствору MeONa (63 мл, 63,0 ммол, 1 M в MeOH) добавили II-D5 (2,0 г, 6,3 ммол) в безводном MeOH (40 мл) при 65°С. Реакционную смесь перемешивали при 65°С в течение 2 часов. К вышеуказанной смеси добавили воду (100 мл). Реакционную смесь упарили для удаления большей части растворителя. Водный слой экстрагировали EtOAc (2×100 мл). Объединенную органическую фазу промыли насыщенным рассолом (100 мл), высушили над безводным Na2SO4, профильтровали и упарили при пониженном давлении. Остаток очистили на колонке для флэш-хроматографии (15~20% EtOAc в PE) с получением II-E1 (0,8 г, 37%) в виде масла и II-E1a.
II-E1:
1H-ЯМР (400 МГц, CDCl3) δH 3,39 (с, 3H), 3,18 (с, 2H), 2,43 (дд, J=8,4, 19,2 Гц, 1H), 2,15-1,86 (м, 4H), 1,85-1,75 (м, 3H), 1,75-1,45 (м, 6H), 1,44-1,13 (м, 10H), 1,12-0,93 (м, 4H), 0,92-0,82 (м, 3H).
Синтез II-E2
[0586] К суспензии бром(этил)трифенилфосфорана (3,4 г, 9,2 ммол) в THF (10 мл) добавили t-BuOK (1,0 г, 9,2 ммол) при 15°С под N2. Смесь нагрели до 60°С и перемешивали в течение 1 часа. Добавили при 60°С раствор II-E1 (0,8 г, 2,3 ммол) в THF (5 мл). Смесь перемешивали при 60°С в течение 16 часов. Смесь обработали раствором NH4Cl (20 мл). Органический слой отделили. Водную фазу экстрагировали EtOAc (3×20 мл). Объединенную органическую фазу промыли рассолом (20 мл), высушили над безводным Na2SO4, профильтровали и упарили при пониженном давлении. Остаток очистили на колонке для флэш-хроматографии (0~15% EtOAc в PE) с образованием II-E2 (630 мг, 76%) в виде масла.
1H-ЯМР (400 МГц, CDCl3) δH 5,12 (кв, J=6,8 Гц, 1H), 3,38 (с, 3H), 3,18 (с, 2H), 2,45-2,12 (м, 3H), 1,88 (д, J=12,8 Гц, 1H), 1,77-1,40 (м, 12H), 1,39-1,08 (с, 11H), 0,95 (т, J=7,6 Гц, 3H), 0,93-0,80 (м, 4H).
Синтез II-E3
[0587] К раствору II-E2 (630 мг, 1,7 ммол) в THF (10 мл) добавили 9-BBN-димер (849 мг, 3,5 ммол) при 15°С. Смесь перемешивали при 15°С в течение 16 часов. После охлаждения до 0°С к смеси медленно добавили этанол (800 мг, 17,4 ммол) и 5 M раствор NaOH (3,47 мл, 17,4 ммол). После завершения добавления медленно добавили H2O2 (1,74 мл, 17,4 ммол, 30%), и внутреннюю температуру поддерживали ниже 15°С. Полученный раствор перемешивали при 75°С в течение 1 часа. Водный слой экстрагировали EtOAc (3×20 мл). Объединенный органический слой промыли насыщенным рассолом (20 мл), высушили над безводным Na2SO4, профильтровали и упарили при пониженном давлении. Остаток очистили на колонке для флэш-хроматографии (30%~50% EtOAc в PE) с получением II-E3 (540 мг, 82%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 3,77-3,15 (м, 1H), 3,38 (с, 3H), 3,18 (с, 2H), 1,95-1,80 (м, 3H), 1,70-1,40 (м, 11H), 1,40-1,00 (м, 15H), 0,98-0,90 (м, 3H), 0,89-0,77 (м, 1H), 0,76 (с, 1H), 0,64 (с, 2H).
Синтез II-E4
[0588] К раствору II-E3 (0,54 г, 1,4 ммол) в DCM (10 мл) добавили PCC (610 мг, 2,8 ммол) и силикагель (1 г) при 18°С. Раствор перемешивали при 18°С в течение 1 часа. Реакционную смесь профильтровали, и остаток промыли DCM (2×50 мл). Объединенный фильтрат упарили при пониженном давлении с получением II-E4 (534 мг) в виде масла. Очистка хроматографией дала чистый II-E4.
1H-ЯМР (400 МГц, CDCl3) δH 3,38 (с, 3H), 3,18 (с, 2H), 2,52 (т, J=8,4 Гц, 1H), 2,20-2,08 (м, 4H), 2,05-1,95 (м, 2H), 1,93-1,83 (м, 1H), 1,77-1,55 (м, 4H), 1,54-1,08 (м, 15H), 1,05-0,82 (м, 5H), 0,62 (с, 3H); MS ESI рассчитано для C24H40O3Na [M+Na]+ 399, найдено 399.
[0589] Пример II-71: синтез (3R,5S,8S,9S,10S,13S,14S,17S)-N-(4-циано-2-метилфенил)-10-этил-3-гидрокси-3-(метоксиметил)-13-метилгексадекагидро-1H-циклопента[a]фенантрен-17-карбоксамида (II-E6)
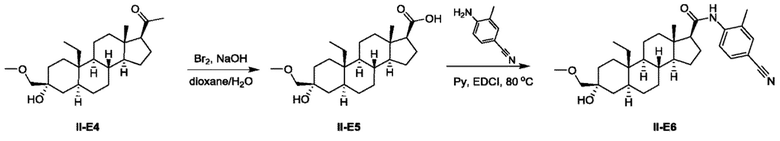
Синтез II-E5
[0590] Жидкий бром (127 мг, 0,8 ммол) медленно добавили к интенсивно перемешиваемому водному раствору гидроксида натрия (1,05 мл, 3 M, 3,2 ммол) при 0°С. Когда весь бром растворился, смесь медленно добавили к перемешиваемому раствору II-E4 (100 мг, 0,3 ммол) в диоксане (6 мл) и воде (2 мл). Реакционную смесь перемешивали при 15°С в течение 16 часов. Оставшийся окислительный реагент погасили водным раствором Na2SO3 (3 мл), и подкисление раствора соляной кислотой (5 мл, 3н.) привело к образованию осадка. К суспензии добавили EtOAc (10 мл). Органический слой отделили. Водную фазу экстрагировали EtOAc (2×10 мл). Объединенную органическую фазу промыли насыщенным рассолом (30 мл), высушили над безводным Na2SO4, профильтровали и упарили в вакууме с образованием II-E5 (120 мг) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 3,38 (с, 3H), 3,18 (с, 2H), 2,37 (т, J=9,2 Гц, 1H), 2,12-1,99 (м, 2H), 1,93-1,64 (м, 5H), 1,62-1,40 (м, 5H), 1,36-1,09 (м, 11H), 1,07-0,79 (м, 6H), 0,73 (с, 3H).
Синтез II-E6
[0591] К раствору II-E5 (110 мг, 0,3 ммол) в пиридине (5 мл) добавили EDCI (167 мг, 0,9 ммол) и перемешивали в течение 10 минут. Добавили 4-амино-3-метилбензонитрил (76,7 мг, 0,6 ммол). Смесь перемешивали при 80°С в течение 16 часов с образованием коричневого раствора. Реакционную смесь вылили в воду (50 мл) и экстрагировали EtOAc (2×20 мл). Объединенную органическую фазу промыли насыщенным рассолом (2×20 мл), высушили над безводным Na2SO4, профильтровали и упарили в вакууме. Остаток очистили хроматографией на силикагеле (0-50% EtOAc в PE) с образованием продукта II-E6 (51,1 мг, 36%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 8,35 (д, J=8,8 Гц, 1H), 7,53-7,48 (м, 1H), 7,45 (с, 1H), 6,95 (с, 1H), 3,39 (с, 3H), 3,19 (с, 2H), 2,36-2,23 (м, 5H), 2,06-1,99 (м, 2H), 1,91-1,67 (м, 5H), 1,65-1,56 (м, 2H), 1,53-1,41 (м, 3H), 1,36-1,13 (м, 10H), 1,02-0,85 (м, 5H), 0,76 (с, 3H); MS ESI рассчитано для C31H45N2O3 [M+H]+ 493, найдено 493.
Пример II-72: синтез 1-(2-((3R,5S,8S,9S,10S,13S,14S,17S)-10-этил-3-гидрокси-3-(метоксиметил)-13-метилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-оксоэтил)-1H-пиразол-3-карбонитрила (II-E8)
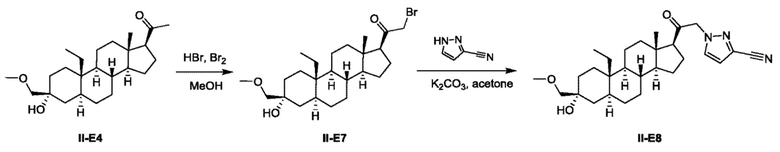
Синтез II-E7
[0592] К раствору II-E4 (100 мг, 0,27 ммол) в MeOH (5 мл) добавили HBr (10,7 мг, 0,05 ммол, 40%) и Br2 (46,6 мг, 0,3 ммол) при 15°С. Реакционную смесь перемешивали при 15°С в течение 1 часа. К смеси добавили насыщенный раствор NaHCO3 (10 мл) и насыщенный раствор Na2SO3 (10 мл). Водный слой экстрагировали EtOAc (3×10 мл). Объединенные органические слои промыли насыщенным рассолом (10 мл), высушили над безводным Na2SO4, профильтровали и упарили с образованием II-E7 (120 мг) в виде масла.
Синтез II-E8
[0593] К раствору II-E7 (120 мг, 0,26 ммол) в ацетоне (3 мл) при 15°С добавили K2CO3 (54,6 мг, 0,4 ммол) и 1H-пиразол-4-карбонитрил (36,7 мг, 0,4 ммол). Реакционную смесь перемешивали при 15°С в течение 16 часов. Реакционную смесь упарили и очистили на колонке для флэш-хроматографии (20-40% EtOAc в PE) с получением II-E8 (46 мг, 39%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 7,46 (д, J=2,4 Гц, 1H), 6,70 (д, J=2,0 Гц, 1H), 4,96 (дд, J=18,0, 42,8 Гц, 2H), 3,37 (с, 3H), 3,17 (с, 2H), 2,58 (т, J=8,8 Гц, 1H), 2,24-2,00 (м, 3H), 1,86 (д, J=12,4 Гц, 1H), 1,80-1,43 (м, 9H), 1,42-1,10 (м, 10H), 1,05-0,85 (м, 5H), 0,66 (с, 3H); MS ESI рассчитано для C28H41N3O3Na [M+Na]+ 490, найдено 490.
[0594] Пример II-73: синтез 1-(2-((3R,5S,8S,9S,10S,13S,14S,17S)-3-(этоксиметил)-10-этил-3-гидрокси-13-метилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-оксоэтил)-1H-пиразол-3-карбонитрила (II-D13)
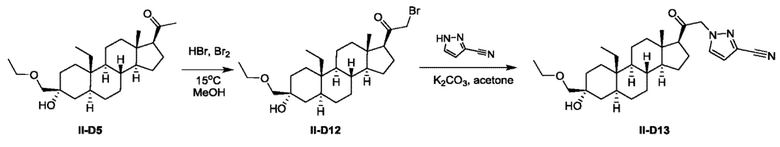
Синтез II-D12
[0595] К раствору II-D5 (150 мг, 0,38 ммол) в MeOH (5 мл) добавили HBr (15,3 мг, 0,077 ммол, 40%) и Br2 (67,5 мг, 0,42 ммол) при 15°С. Реакционную смесь перемешивали при 15°С в течение 16 часов. Реакционную смесь добавили в насыщенный раствор NaHCO3 (20 мл), затем экстрагировали EtOAc (3×20 мл). Объединенный органический слой промыли насыщенным рассолом (50 мл), высушили над Na2SO4, профильтровали и упарили с образованием II-D12 (165 мг) в виде масла.
1H-ЯМР (400 МГц, CDCl3) δH 4,00-3,85 (м, 2H), 3,52 (кв, J=6,8 Гц, 2H), 3,21 (с, 2H), 2,80 (т, J=9,2 Гц, 1H), 2,25-2,10 (м, 1H), 1,90-1,80 (м, 2H), 1,75-1,40 (м, 10H), 1,40-1,10 (м, 12H), 1,00-0,80 (м, 6H), 0,65 (с, 3H).
Синтез II-D13
[0596] К раствору II-D12 (165 мг, 0,4 ммол) в ацетоне (5 мл) при 15°С добавили K2CO3 (96,9 мг, 0,7 ммол) и 1H-пиразол-4-карбонитрил (65,4 мг, 0,7 ммол). Реакционную смесь перемешивали при 15°С в течение 16 часов. Реакционную смесь добавили в насыщенный раствор NH4Cl (20 мл). Водный слой экстрагировали EtOAc (3×20 мл). Объединенный органический слой промыли насыщенным рассолом (50 мл), высушили над безводным Na2SO4, профильтровали и упарили с образованием продукта. Остаток очистили с использованием Combi-flash (0-20% EtOAc в PE) с образованием II-D13 (74,6 мг, 44,1%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 7,47 (д, J=2,4 Гц, 1H), 6,72 (д, J=2,4 Гц, 1H), 4,96 (дд, J=17,6, 51,2 Гц, 2H), 3,52 (кв, J=6,8 Гц, 2H), 3,21 (с, 2H), 2,59 (т, J=8,8 Гц, 1H), 2,25-2,10 (м, 2H), 1,90-1,60 (м, 6H), 1,55-1,10 (м, 18H), 1,05-0,80 (м, 5H), 0,68 (с, 3H); MS ESI рассчитано для C29H42N3O2 [M-H2O+H]+ 464, найдено 464.
[0597] Пример II-74: синтез 1-(2-((3R,5R,8S,9S,10S,13S,14S,17S)-3-(этоксиметил)-10-этил-3-гидрокси-13-метилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-оксоэтил)-1H-пиразол-4-карбонитрила (II-C8)
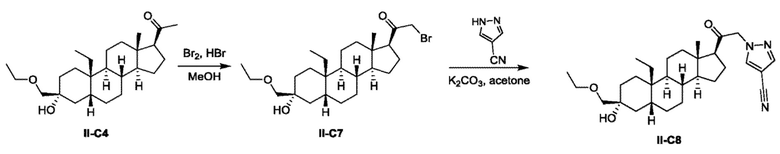
Синтез II-C7
[0598] К раствору II-C4 (500 мг, 1,3 ммол) в MeOH (10 мл) при 15°С добавили HBr (10 мг, 40%) и Br2 (224 мг, 1,4 ммол). Реакционную смесь перемешивали при 15°С в течение 16 часов. Реакционную смесь добавили в насыщенный раствор NaHCO3 (50 мл). Водный слой экстрагировали EtOAc (3×50 мл). Объединенный органический слой промыли насыщенным рассолом (100 мл), высушили над безводным Na2SO4, профильтровали и упарили с образованием II-C7 (220 мг) в виде масла.
1H-ЯМР (400 МГц, CDCl3) δH 3,95-3,88 (м, 2H), 3,54 (кв, J=6,8 Гц, 2H), 3,41 (кв, J=11,2 Гц, 2H), 2,85-2,75 (м, 1H), 2,74-2,60 (м, 1H), 2,25-2,10 (м, 1H), 1,95-1,81 (м, 2H), 1,78-1,59 (м, 9H), 1,38-1,10 (м, 13H), 0,98-0,78 (м, 2H), 0,78 (т, J=6,8 Гц, 3H), 0,62 (с, 3H).
Синтез II-C8
[0599] К раствору II-C7 (70 мг, 0,15 ммол) в ацетоне (5 мл) при 15°С добавили K2CO3 (41 мг, 0,3 ммол) и 1H-пиразол-4-карбонитрил (28 мг, 0,3 ммол). Реакционную смесь перемешивали при 15°С в течение 16 часов. Реакционную смесь добавили в насыщенный раствор NH4Cl (50 мл), и водный слой экстрагировали EtOAc (3×50 мл). Объединенный органический слой промыли насыщенным рассолом (100 мл), высушили над безводным Na2SO4, профильтровали и упарили с образованием продукта. Остаток очистили с использованием Combi-flash (0-20% EtOAc в PE) с образованием II-C8 (45 мг, 63%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 7,85 (с, 1H), 7,81 (с, 1H), 5,02 (д, J=18,0 Гц, 2H), 4,89 (д, J=18,0 Гц, 2H), 3,54 (кв, J=6,8 Гц, 2H), 3,41 (кв, J=9,2 Гц, 2H), 2,75 (с, 1H), 2,63-2,53 (м, 1H), 2,25-2,10 (м, 1H), 2,09-1,85 (м, 2H), 1,80-1,58 (м, 7H), 1,51-1,25 (м, 11H), 1,24-1,10 (м, 6H), 0,78 (т, J=7,2 Гц, 3H), 0,64 (с, 3H); MS ESI рассчитано для C29H42N3O2 [M+H-H2O]+ 464, найдено 464.
Примеры от II-75 до II-79
Примеры II-75-II-76 были выполнены из α-галогенкетона (II-C7), примеры II-77-II-70 были выполнены из α-галогенкетона II-D12), как в Примерах от II-72 до II-74, с заменой 1H-пиразол-4-карбонитрила перечисленными нуклеофилами.
ПРИМЕР II-80: синтез 1-((3R,5R,8S,9S,10R,13S,14S,17S)-3-гидрокси-10-((R)-1-метоксиэтил)-3,13-диметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)этан-1-она (II-E10)
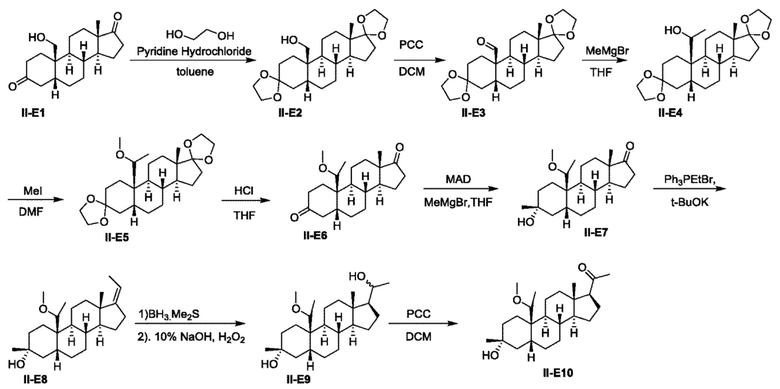
Синтез II-E2
[0600] К раствору II-E2 (6 г, 19,7 ммол) в толуоле (100 мл) добавили гидрохлорид пиридина (453 мг, 3,94 ммол) и этан-1,2-диол (6,1 г, 98,4 ммол). После перемешивания при 130°С в течение 16 часов смесь упарили в вакууме. Остаток очистили на колонке с силикагелем, с вымыванием смесью (PE/EtOAc=5/1) с получением II-E2 (5,4 г, 66%) в виде твердого вещества. 1H-ЯМР (400 МГц, CDCl3) δ 3,98-3,80 (м, 9H), 3,58-3,55 (м, 1H), 2,10-2,01 (м, 1H), 1,99-1,91 (м, 2H), 1,84-1,60 (м, 5H), 1,59-1,33 (м, 10H), 1,30-1,17 (м, 4H), 1,15-1,02 (м, 1H), 0,82 (с, 3H).
Синтез II-E3
[0601] К раствору II-E2 (5,3 г, 13,5 ммол) в DCM (60 мл) при 25°С добавили PCC (4,34 г, 20,2 ммол). После перемешивания при 25°С в течение 30 минут раствор профильтровали, и осадок на фильтре промыли DCM (2×100 мл). Объединенный фильтрат промыли насыщенным раствором NaHCO3 (100 мл) и рассолом (100 мл), высушили над Na2SO4, профильтровали и упарили в вакууме. Остаток очистили на колонке с силикагелем, с вымыванием смесью (PE/EtOAc=8/1) с получением II-E3 (3,1 г, 53%) в виде масла. 1H-ЯМР (400 МГц, CDCl3) δ 9,58 (с, 1H), 4,00-3,84 (м, 8H), 2,25-2,15 (м, 1H), 2,03-1,88 (м, 2H), 1,84-1,59 (м, 7H), 1,56-1,32 (м, 10H), 1,30-1,17 (м, 1H), 1,13-0,99 (м, 1H), 0,92 (с, 3H).
Синтез II-E4
[0602] К раствору II-E4 (3 г, 7,68 ммол) в THF (50 мл) при 0°С добавили MeMgBr (5,1 мл, 15,3 ммол, 3 M в дмэтиловом эфире). После перемешивания при 25°С в течение 2 часов реакционную смесь вылили в воду (100 мл) и экстрагировали EtOAc (2×100 мл). Объединенный органический раствор промыли рассолом (100 мл), высушили над Na2SO4, профильтровали и упарили в вакууме с получением II-E4 (2,8 г, 81%) в виде масла.
1H-ЯМР (400 МГц, CDCl3) δ 4,42 (м, 1H), 3,97-3,81 (м, 8H), 2,03-1,92 (м, 2H), 1,90-1,74 (м, 5H), 1,71-1,64 (м, 1H), 1,60-1,34 (м, 9H), 1,30-1,22 (м, 4H), 1,21-1,11 (м, 5H), 0,87 (с, 3H).
Синтез II-E5
[0603] К раствору II-E4 (2,7 г, 6,64 ммол) в DMF (20 мл) добавили NaH (795 мг, 19,9 ммол, 60%) при 25°С. После перемешивания при 50°С в течение 30 минут к реакционной смеси по каплям добавили MeI (2,82 г, 19,9 ммол). После перемешивания при 50°С в течение 2 часов по каплям добавили дополнительный MeI (2,82 г, 19,9 ммол). После перемешивания при 50°С в течение 1 часа смесь вылили в ледяную воду (50 мл) и экстрагировали EtOAc (2×60 мл). Объединенный органический раствор промыли насыщенным рассолом (100 мл), высушили над безводным Na2SO4, профильтровали и упарили в вакууме. Остаток очистили на колонке с силикагелем (PE/EtOAc=10/1) с получением II-E5 (2 г, 64%) в виде твердого вещества. 1H-ЯМР (400 МГц, CDCl3) δ 3,97-3,83 (м, 8H), 3,79-3,74 (м, 1H), 3,29 (с, 3H), 2,08-1,93 (м, 2H), 1,91-1,75 (м, 3H), 1,73-1,57 (м, 3H), 1,54-1,36 (м, 8H), 1,31-1,05 (м, 9H), 0,88 (с, 3H).
Синтез II-E6
[0604] К раствору II-E5 (2 г, 4,75 ммол) в THF (30 мл) добавили водную HCl (4,75 мл, 4 M, 19 ммол). После перемешивания при 25°С в течение 16 часов смесь вылили в воду (100 мл) и экстрагировали EtOAc (2×50 мл). Объединенный органический раствор промыли насыщенным водным раствором NaHCO3 (50 мл), рассолом (50 мл), высушили над Na2SO4 и упарили в вакууме с получением II-E6 (1,4 г, 80%) в виде твердого вещества. 1H-ЯМР (400 МГц, CDCl3) δ 3,86-3,82 (м, 1H), 3,31 (с, 3H), 2,77-2,67 (м, 1H), 2,54-2,43 (м, 1H), 2,32-2,19 (м, 3H), 2,16-1,94 (м, 4H), 1,91-1,78 (м, 3H), 1,75-1,60 (м, 4H), 1,55-1,35 (м, 2H), 1,30-1,16 (м, 4H), 1,10-1,05 (м, 3H), 0,93 (с, 3H).
Синтез II-E7
[0605] К раствору BHT (5,56 г, 25,2 ммол) в толуоле (50 мл) по каплям при 0°С добавили AlMe3 (6,3 мл, 12,6 ммол, 2 M в толуоле). После перемешивания при 25°С в течение 1 часа к смеси при -65°С по каплям добавили раствор II-E6 (1,4 г, 4,21 ммол) в толуоле (20 мл). После перемешивания при -65°С в течение 1 часа по каплям при -65°С добавили MeMgBr (4,19 мл, 12,6 ммол, 3 M в диэтиловом эфире). После перемешивания при -65°С в течение 3 часов реакционную смесь залили насыщенным водным раствором NH4Cl (50 мл) при -65°С. После перемешивания при 25°С в течение 0,5 часа полученную смесь профильтровали через слой целита, и слой промыли EtOAc (100 мл). Объединенный органический раствор отделили, промыли рассолом (2×100 мл), высушили над Na2SO4 и упарили в вакууме. Остаток очистили на колонке с силикагелем, с вымыванием смесью PE/EtOAc=5/1 с образованием II-E7 (1,1 г, 68%) в виде твердого вещества. 1H-ЯМР (400 МГц, CDCl3) δ 3,80-3,75 (м, 1H), 3,29 (с, 3H), 2,48-2,41 (м, 1H), 2,15-2,02 (м, 1H), 2,00-1,77 (м, 4H), 1,74-1,63 (м, 4H), 1,57-1,33 (м, 7H), 1,29-1,13 (м, 9H), 1,08 (д, J=6,4 Гц, 3H), 0,89 (с, 3H); LC-ELSD/MS чистота 99%, MS ESI рассчитано для C21H31O [M+H-H2O-MeOH]+ 299, найдено 299.
Синтез II-E8
[0606] К раствору PPh3EtBr (3,18 г, 8,58 ммол) в THF (15 мл) добавили t-BuOK (962 мг, 8,58 ммол) при 25°С. После перемешивания при 60°С в течение 1 часа по каплям добавили раствор II-E7 (1 г, 2,86 ммол) в THF (5 мл). После перемешивания при 60°С в течение 16 часов смесь вылили в ледяную воду (100 мл) и экстрагировали EtOAc (2×50 мл). Объединенный органический раствор промыли рассолом (50 мл), высушили над Na2SO4 и профильтровали, упарили в вакууме. Остаток очистили на колонке с силикагелем, с вымыванием смесью PE/EtOAc=15/1 с получением II-E8 (1 г, 78%) в виде твердого вещества. 1H-ЯМР (400 МГц, CDCl3) δ 5,18-4,99 (м, 1H), 3,83-3,71 (м, 1H), 3,30 (с, 3H), 2,45-2,09 (м, 3H), 2,01-1,81 (м, 3H), 1,68-1,58 (м, 6H), 1,58-1,37 (м, 7H), 1,31-1,12 (м, 10H), 1,08-1,03 (м, 3H), 0,91 (с, 3H).
Синтез II-E9
[0607] К раствору II-E8 (1 г, 2,77 ммол) в THF (20 мл) по каплям при 0°С добавили раствор BH3-Me2S (2,77 мл, 27,7 ммол). После перемешивания при 25°С в течение 16 часов раствор охладили до 0°С и очень медленно добавляли раствор NaOH (9,23 мл, 3 M). После завершения добавления медленно добавили H2O2 (4,5 мл, 33%), и внутреннюю температуру поддерживали ниже 10°С. После перемешивания при 25°С в течение 2 часов полученный раствор экстрагировали EtOAc (2×20 мл). Объединенный органический раствор промыли насыщенным водным раствором Na2S2O3 (2×50 мл), рассолом (50 мл), высушили над Na2SO4, профильтровали и упарили в вакууме с образованием II-E9 (0,9 г) в виде твердого вещества, которое использовали для следующей стадии без дополнительной очистки.
Синтез II-E10
[0608] К раствору II-E9 (800 мг, 2,11 ммол) в DCM (10 мл) добавили PCC (907 мг, 4,22 ммол) при 25°С. После перемешивания при 25°С в течение 2 часов раствор профильтровали, и осадок на фильтре промыли DCM (2×50 мл). Объединенный фильтрат упарили в вакууме. Остаток очистили на колонке с силикагелем, с вымыванием смесью (PE/EtOAc=5/1) с получением II-E10 (600 мг, 68%) в виде твердого вещества. 1H-ЯМР (400 МГц, CDCl3) δ 3,78-3,74 (м, 1H), 3,27 (с, 3H), 2,56-2,51 (м, 1H), 2,22-2,16 (м, 1H), 2,12 (с, 3H), 2,06-1,94 (м, 2H), 1,91-1,79 (м, 1H), 1,74-1,61 (м, 6H), 1,50-1,32 (м, 6H), 1,29-1,10 (м, 10H), 1,06 (д, J=6,0 Гц, 3H), 0,64 (с, 3H); LC-ELSD/MS чистота 99%, MS ESI рассчитано для C23H35O [M+H-H2O-MeOH]+ 327, найдено 327.
ПРИМЕР II-81: синтез 1-((3R,5R,8S,9S,10R,13S,14S,17S)-3-гидрокси-10-((R)-1-метоксиэтил)-3,13-диметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-(5-метил-2H-тетразол-2-ил)этан-1-она (II-E12) и 1-((3R,5R,8S,9S,10R,13S,14S,17S)-3-гидрокси-10-((R)-1-метоксиэтил)-3,13-диметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-(5-метил-1H-тетразол-1-ил)этан-1-она (II-E13)
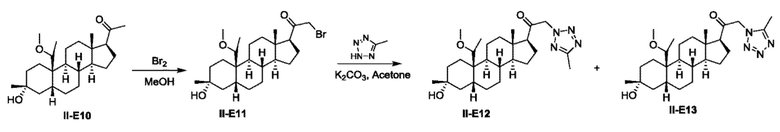
Синтез II-E11
[0609] К раствору II-E10 (300 мг, 0,796 ммол) и HBr (0,1 мл, 48% в воде) в MeOH (5 мл) по каплям добавили бром (190 мг, 1,19 ммол). После перемешивания при 25°С в течение 2 часов реакционную смесь залили насыщенным водным раствором NaHCO3 (20 мл), и отрегулировали значение рН на 7~8. Смесь экстрагировали EtOAc (2×30 мл). Объединенный органический раствор промыли рассолом (50 мл), высушили над Na2SO4, профильтровали и упарили в вакууме. Остаток очистили на колонке с силикагелем, с вымыванием смесью (PE/EtOAc=8/1) с получением II-E11 (240 мг, 60%) в виде твердого вещества. 1H-ЯМР (400 МГц, CDCl3) δ 3,98-3,86 (м, 2H), 3,77-3,73 (м, 1H), 3,26 (с, 3H), 2,85-2,83 (м, 1H), 2,27-2,13 (м, 1H), 2,02-1,83 (м, 3H), 1,77-1,61 (м, 5H), 1,54-1,33 (м, 7H), 1,31-1,11 (м, 8H), 1,08-1,02 (м, 3H), 0,91-0,80 (м, 2H), 0,67 (с, 3H).
Синтез II-E12 и II-E13
[0610] К раствору II-E11 (120 мг, 0,263 ммол) в ацетоне (3 мл) добавили K2CO3 (72,5 мг, 0,526 ммол) и 5-метил-2H-тетразол (44,2 мг, 0,526 ммол) при 25°С. После перемешивания при 25°С в течение 16 часов смесь вылили в воду (30 мл) и экстрагировали EtOAc (2×30 мл). Объединенный органический раствор промыли рассолом (20 мл), высушили над Na2SO4, профильтровали и упарили в вакууме. Остаток очистили с разделением препаративной HPLC (колонка: Boston Green ODS 150*30 5 мкм, градиент: 60-90% B (A=0,05% HCl-ACN, B=ацетонитрил), расход потока: 25 мл/мин) с образованием II-E12 (15 мг, 12%) и II-E12 (32 мг, 27%), оба в виде твердых веществ.
II-E12: 1H-ЯМР (400 МГц, CDCl3) δ 5,43-5,29 (м, 2H), 3,79-3,74 (м, 1H), 3,27 (с, 3H), 2,65-2,60 (м, 1H), 2,57 (с, 3H), 2,30-2,16 (м, 1H), 2,11-2,08 (м, 1H), 2,01-1,95 (м, 1H), 1,76-1,65 (м, 1H), 1,80-1,63 (м, 6H), 1,52-1,34 (м, 6H), 1,33-1,10 (м, 10H), 1,07 (д, J=6,4 Гц, 3H), 0,74 (с, 3H); LC-ELSD/MS чистота 99%, MS ESI рассчитано для C26H41N4O2 [M+H-H2O]+ 441, найдено 441.
II-E13: 1H-ЯМР (400 МГц, CDCl3) δ 5,21-5,02 (м, 2H), 3,79-3,74 (м, 1H), 3,28 (с, 3H), 2,71-2,61 (м, 1H), 2,48 (с, 3H), 2,29-2,17 (м, 1H), 2,09-2,06 (м, 1H), 2,03-1,93 (м, 1H), 1,90-1,87 (м, 1H), 1,83-1,62 (м, 6H), 1,53-1,41 (м, 6H), 1,39-1,11 (м, 10H), 1,07 (д, J=6,4 Гц, 3H), 0,71 (с, 3H); LC-ELSD/MS чистота 99%, MS ESI рассчитано для C26H41N4O2 [M+H-H2O]+ 441, найдено 441.
[0611] Формула III, сокращения: PE: петролейный эфир; EtOAc: этилацетат; THF: тетрагидрофуран; PCC: хлорхромат пиридиния; TLC: тонкослойная хроматография; PCC: хлорхромат пиридиния; t-BuOK: трет-бутоксид калия; 9-BBN: 9-борабицикло[3.3.1]нонан; Pd(t-Bu3P)2: бис(три-трет-бутилфосфин)палладий(0); AcCl: ацетилхлорид; i-PrMgCl: изопропилмагнийхлорид; TBSCl: трет-бутил(хлор)диметилсилан; (i-PrO)4Ti: тетраизопропоксид титана; BHT: 2,6-ди-трет-бутил-4-метилфеноксид; Me: метил; i-Pr: изопропил; t-Bu: трет-бутил; Ph: фенил; Et: этил; Bz: бензоил; BzCl: бензоилхлорид; CsF: фторид цезия; DCC: дициклогексилкарбодиимид; DCM: дихлорметан; DMAP: 4-диметиламинопиридин; DMP: периодинан Десса-Мартина; EtMgBr: этилмагнийбромид; EtOAc: этилацетат; TEA: триэтиламин; AlaOH: аланин; Boc: трет-бутоксикарбонил; Py: пиридин; TBAF: фторид тетра-н-бутиламмония; THF: тетрагидрофуран; TBS: трет-бутилдиметилсилил; TMS: триметилсилил; TMSCF3: (трифторметил)триметилсилан; Ts: пара-толуолсульфонил; Bu: бутил; Ti(OiPr)4: тетраизопропоксититан; LAH: литийалюминийгидрид; LDA: диизопропиламид лития; LiOH·H2O: гидраты гидроксида лития; MAD: бис(2,6-ди-трет-бутил-4-метилфеноксид) метилалюминия; MeCN: ацетонитрил; NBS: N-бромсукцинимид; Na2SO4: сульфат натрия; Na2S2O3: тиосульфат натрия; PE: петролейный эфир; MeCN: ацетонитрил; MeOH: метанол; Boc: трет-бутоксикарбонил; MTBE: метил-трет-бутиловый простой эфир; K-selectride: три(втор-бутил)боргидрид калия.
[0612] ПРИМЕР III-1: синтез 1-((3R,5R,8R,9R,10S,13S,14S,17S)-13-этил-3-гидрокси-3-метилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)этан-1-она (III-A8)
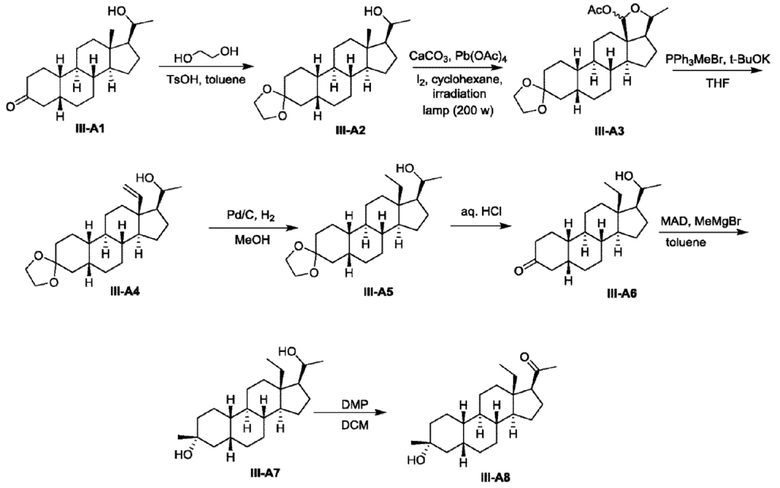
Синтез III-A2
[0613] Раствор III-A1 (описанного в патентном документе WO 2013056181) (14 г, 45,9 ммол), TsOH (787 мг, 4,6 ммол) и этан-1,2-диола (28,4 г, 458 ммол) добавили к толуолу (200 мл) при 25°С под N2. Смесь перемешивали при 120°С в течение 4 часов. Смесь вылили в воду (100 мл) и экстрагировали этилацетатом (2×100 мл). Объединенный органический раствор промыли рассолом (100 мл), высушили над Na2SO4, профильтровали и упарили в вакууме. Остаток очистили на колонке для флэш-хроматографии (5-10% EtOAc в PE) с образованием III-A2 (8 г, 50%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 3,93 (с, 4H), 3,76-3,63 (м, 1H), 2,03-1,95 (м, 1H), 1,93-1,80 (м, 4H), 1,64-1,58 (м, 3H), 1,56-1,48 (м, 2H), 1,44-1,30 (с, 6H), 1,27-0,95 (м, 12H), 0,66 (с, 3H).
Синтез III-A3
[0614] К раствору III-A2 (2 г, 5,7 ммол) в циклогексане (100 мл), перемешиваемому под N2, добавили CaCO3 (1,71 г, 17,1 ммол), Pb(OAc)4 (7,58 г, 17,1 ммол), и I2 (2,89 г, 11,4 ммол), и облучали высокомощной вольфрамовой лампой в течение 130 минут. Во время облучения растворитель кипятили с обратным холодильником. Реакционную смесь оставили остывать до 25°С, профильтровали, и циклогексановый раствор промыли 10%-ным водным раствором Na2S2O3 (30 мл), рассолом (50 мл), высушили над Na2SO4 и упарили. Остаток очистили на колонке для флэш-хроматографии (0-15% EtOAc в PE) с образованием III-A3 (900 мг, 39%) в виде масла.
1H-ЯМР (400 МГц, CDCl3) δH 5,95 (с, 1H), 4,36-4,27 (м, 1H), 3,93 (с, 4H), 2,38-2,35 (м, 1H), 2,08 (с, 3H), 2,05-1,96 (м, 2H), 1,91-1,73 (м, 4H), 1,70-1,60 (м, 2H), 1,41-1,32 (м, 4H), 1,31-1,19 (м, 7H), 1,18-0,98 (м, 4H), 0,89-0,80 (м, 3H).
Синтез III-A4
[0615] К раствору PPh3MeBr (5,28 г, 14,8 ммол) в THF (15 мл) добавили t-BuOK (1,66 г, 14,8 ммол) при 25°С. После перемешивания при 50°С в течение 1 часа по каплям при 50°С добавили раствор III-A3 (600 мг, 1,48 ммол) в THF (5 мл). После перемешивания при 50°С в течение 3 часов смесь вылили в насыщенный раствор NH4Cl (50 мл) и экстрагировали EtOAc (2×50 мл). Органический слой промыли рассолом (100 мл), высушили над Na2SO4 и профильтровали, упарили в вакууме. Остаток очистили на колонке для флэш-хроматографии (0~30% EtOAc в PE) с образованием III-A4 (420 мг, 79%) в виде масла.
1H-ЯМР (400 МГц, CDCl3) δH 5,84-5,70 (м, 1H), 5,34-5,23 (м, 1H), 5,18-5,13 (м, 1H), 3,94 (с, 4H), 3,87-3,75 (м, 1H), 2,39-2,34 (м, 1H), 2,03-1,93 (м, 1H), 1,90-1,73 (м, 5H), 1,63-1,56 (м, 4H), 1,44-1,21 (м, 10H), 1,14-1,09 (м, 4H), 1,16-1,09 (м, 1H), 0,90-0,86 (м, 2H).
Синтез III-A5
[0616] К раствору III-A4 (420 мг, 1,2 ммол) в MeOH (10 мл) добавили Pd/C (200 мг, <1% воды). Затем раствор подвергали гидрированию под давлением водорода 15 psi (0,1 МПа) при 25°С в течение 16 часов. Смесь профильтровали через слой целита, и фильтрат упарили в вакууме с образованием III-A5 (420 мг, 100%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 3,94 (с, 4H), 3,85-3,82 (м, 1H), 2,15-2,11 (м, 1H), 2,03-1,97 (м, 1H), 1,90-1,84 (м, 3H), 1,65-1,51 (м, 10H), 1,45-1,31 (м, 6H), 1,28-1,26 (м, 3H), 1,18-1,06 (м, 3H), 0,98-0,89 (м, 2H), 0,84 (т, J=8 Гц, 3H).
Синтез III-A6
[0617] К раствору III-A5 (420 мг, 1,2 ммол) в THF (10 мл) добавили водную HCl (1,15 мл, 4 M, 4,6 ммол). После перемешивания при 25°С в течение 2 часов смесь вылили в воду (100 мл) и экстрагировали EtOAc (2×50 мл). Объединенный органический раствор промыли насыщенным водным раствором NaHCO3 (50 мл), рассолом (50 мл), высушили над Na2SO4 и упарили в вакууме с получением III-A6 (240 мг, 66%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 3,87-3,84 (м, 1H), 2,60 (т, J=16 Гц, 1H), 2,29-2,14 (м, 4H), 2,11-2,03 (м, 1H), 1,92-1,84 (м, 1H), 1,75-1,64 (м, 4H), 1,61-1,56 (м, 3H), 1,54-1,45 (м, 2H), 1,45-1,31 (м, 4H), 1,29-1,26 (м, 3H), 1,24-1,09 (м, 5H), 1,07-0,92 (м, 2H), 0,87 (т, J=8 Гц, 3H).
Синтез III-A7
[0618] К раствору BHT (1,65 г, 7,52 ммол) в толуоле (10 мл) по каплям при 0°С под азотом добавили AlMe3 (2 M в толуоле, 1,88 мл, 3,76 ммол). Смесь перемешивали при 25°С в течение 1 часа. К раствору по каплям при -65°С добавили III-A6 (240 мг, 0,75 ммол) в толуоле (5 мл). После перемешивания при -65°С в течение 1 часа по каплям при -65°С добавили MeMgBr (1 мл, 3,0 ммол, 3 M в диэтиловом эфире). Полученный раствор перемешивали при -65°С в течение 1 часа. Реакционную смесь залили насыщенным водным раствором NH4Cl (50 мл) при -65°С. После перемешивания при 25°С в течение 0,5 часа полученную смесь профильтровали через слой целита, и слой промыли EtOAc (20 мл). Объединенный органический слой отделили, промыли рассолом (2×20 мл), высушили над Na2SO4, профильтровали и упарили в вакууме. Остаток очистили на колонке для флэш-хроматографии (0-30% EtOAc в PE) с образованием III-A7 (215 мг, 86%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 3,85-3,81 (м, 1H), 2,15-2,11 (м, 1H), 1,92-1,76 (м, 4H), 1,64-1,61 (м, 1H), 1,48-1,18 (м, 20H), 1,11-1,04 (м, 4H), 0,98-0,88 (м, 1H), 0,87-0,79 (м, 4H).
Синтез III-A8
[0619] К раствору III-A7 (215 мг, 0,64 ммол) в DCM (5 мл) добавили DMP (542 мг, 1,28 ммол). Реакционную смесь перемешивали при 30°С в течение 30 минут. Реакционную смесь залили насыщенным водным раствором NaHCO3 (50 мл), пока значение рН водного слоя не достигло примерно 9, и профильтровали. DCM-слой отделили, и водную фазу экстрагировали DCM (10 мл). Объединенную органическую фазу промыли насыщенным водным раствором Na2S2O3 (2×20 мл), насыщенным раствором NaHCO3 (40 мл), рассолом (40 мл), высушили над Na2SO4, профильтровали и упарили. Остаток очистили на колонке для флэш-хроматографии (0-30% EtOAc в PE) с образованием III-A8 (138 мг, 65%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 2,46 (т, J=8 Гц, 1H), 2,33-2,21 (м, 2H), 2,20 (с, 3H), 1,87-1,80 (м, 3H), 1,74-1,59 (м, 4H), 1,52-1,33 (м, 7H), 1,32-1,04 (м, 12H), 0,96-0,81 (м, 1H), 0,62 (т, J=8 Гц, 3H); LC-ELSD/MS чистота 99%, MS ESI рассчитано для C22H35O [M-H2O+H]+ 315, найдено 315.
[0620] ПРИМЕР III-2: синтез 1-(2-((3R,5R,8R,9R,10S,13S,14S,17S)-13-этил-3-гидрокси-3-метилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-оксоэтил)-1H-пиразол-4-карбонитрила (III-A10)
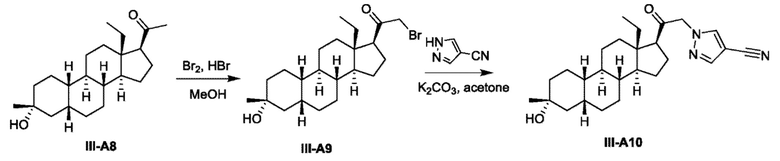
Синтез III-A9
[0621] К раствору III-A8 (107 мг, 0,32 ммол) и концентрированной HBr (0,1 мл, 48% в воде) в MeOH (2 мл) добавили бром (61,5 мг, 0,39 ммол). Реакционную смесь перемешивали при 25°С в течение 2 часов. Реакционную смесь залили насыщенным водным раствором NaHCO3 и отрегулировали значение рН на 7~8, и экстрагировали EtOAc (2×30 мл). Объединенную органическую фазу промыли насыщенным раствором Na2S2O3 (50 мл) и рассолом (50), высушили над безводным Na2SO4, профильтровали и упарили в вакууме с получением III-A9 (130 мг) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 4,01-3,91 (м, 2H), 2,67 (т, J=8 Гц, 1H), 2,26-2,13 (м, 2H), 1,79-1,71 (м, 4H), 1,67-1,56 (м, 4H), 1,43-1,29 (м, 8H), 1,22-1,08 (м, 10H), 0,86-0,73 (м, 1H), 0,52 (т, J=8 Гц, 3H).
Синтез III-A10
[0622] К раствору III-A9 (130 мг, 0,32 ммол) в ацетоне (3 мл) добавили K2CO3 (108 мг, 0,79 ммол) и 1H-пиразол-4-карбонитрил (43,9 мг, 0,47 ммол). Смесь перемешивали при 25°С в течение 3 часов. Смесь вылили в воду (30 мл) и экстрагировали этилацетатом (2×30 мл). Объединенные органические слои промыли рассолом (50 мл), высушили над Na2SO4, профильтровали и упарили в вакууме. Остаток очистили на колонке для флэш-хроматографии (15-35% EtOAc в PE) с образованием III-A10 (43 мг, 32%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 7,86 (с, 1H), 7,81 (с, 1H), 5,20-4,88 (м, 2H), 2,52-2,46 (м, 1H), 2,36-2,25 (м, 2H), 1,89-1,62 (м, 7H), 1,51-1,33 (м, 10H), 1,29-1,07 (м, 9H), 0,98-0,85 (м, 1H), 0,61 (т, J=8 Гц, 3H); LC-ELSD/MS чистота 99%, MS ESI рассчитано для C26H37N3O2Na [M+Na]+ 446, найдено 446.
[0623] ПРИМЕР III-3: синтез 1-((3R,5S,8R,9R,10S,13S,14S,17S)-13-этил-3-гидрокси-3-(метоксиметил)гексадекагидро-1H-циклопента[a]фенантрен-17-ил)этан-1-она (III-A20)
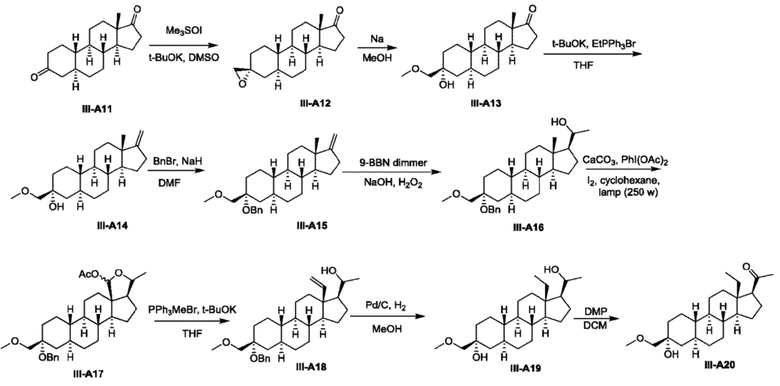
Синтез III-A12
[0624] Перемешиваемый раствор иодида триметилсульфония (880 мг, 4,00 ммол) и t-BuOK (448 мг, 4,00 ммол) в DMSO (10 мл) нагревали при 40°С в течение 1 часа под N2. Реакционную смесь добавили к III-A11 (1 г, 3,64 ммол, CAS № 5696-58-2) в DMSO (10 мл) и перемешивали при 40°С. Через 10 минут реакционную смесь обработали водой (100 мл), экстрагировали EtOAc (3×50 мл). Объединенную органическую фазу промыли водой (100 мл), рассолом (50 мл), высушили над безводным Na2SO4, профильтровали и упарили в вакууме с образованием III-A12 (1,8 г) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 2,43 (дд, J=8,3, 19,3 Гц, 1H), 2,13-2,05 (м, 1H), 2,00-1,73 (м, 5H), 1,66-1,28 (м, 6H), 1,22-0,98 (м, 4H), 0,91-0,72 (м, 4H).
Синтез III-A13
[0625] К раствору III-A12 (1,8 г, 6,24 ммол) в MeOH (20 мл) добавили метилат натрия (1,34 г, 24,9 ммол) при 25°С под N2. После кипячения с обратным холодильником в течение 16 часов смесь залили водой (300 мл) и экстрагировали EtOAc (2×200 мл). Объединенную органическую фазу промыли рассолом (2×200 мл), высушили над Na2SO4, профильтровали, упарили с образованием остатка. Остаток очистили хроматографией на силикагеле (0-20% EtOAc в PE) с образованием III-A13 (900 мг, 45,2%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 3,38 (с, 3H), 3,19 (с, 2H), 2,52-2,32 (м, 1H), 2,16-2,00 (м, 2H), 1,98-1,85 (м, 2H), 1,84-1,70 (м, 4H), 1,68-1,62 (м, 2H), 1,55-1,41 (м, 2H), 1,37-1,18 (м, 5H), 1,15-0,96 (м, 4H), 0,87 (с, 3H), 0,81-0,67 (м, 2H).
Синтез III-A14
[0626] К раствору PPh3EtBr (20,7 г, 56 ммол) в THF (100 мл) добавили t-BuOK (6,28 г, 56 ммол) при 25°С. После перемешивания при 50°С в течение 1 часа по каплям при 50°С добавили раствор III-A13 (9 г, 28 ммол) в THF (50 мл). После перемешивания при 50°С в течение 16 часов смесь вылили в насыщенный раствор NH4Cl (500 мл) и экстрагировали EtOAc (2×100 мл). Органический слой промыли рассолом (300 мл), высушили над Na2SO4, и профильтровали, упарили в вакууме. Остаток очистили на колонке для флэш-хроматографии (0~30% EtOAc в PE) с образованием III-A14 (8,5 г, 91,2%) в виде масла.
1H-ЯМР (400 МГц, CDCl3) δH 5,14-5,07 (м, 1H), 3,38 (с, 3H), 3,18 (с, 2H), 2,38-2,29 (м, 1H), 2,25-2,12 (м, 2H), 1,86-1,67 (м, 3H), 1,60-1,49 (м, 4H), 1,33-0,95 (м, 12H), 0,89-0,83 (м, 6H), 0,75-0,65 (м, 2H).
Синтез III-A15
[0627] К раствору III-A14 (7,5 г, 22,5 ммол) в DMF (100 мл) тремя порциями при 25°С добавили NaH (2,68 г, 67,5 ммол, 60% в минеральном масле). После перемешивания при 25°С в течение 30 минут к раствору добавили BnBr (11,5 г, 67,5 ммол). После перемешивания при 25°С в течение 16 часов смесь вылили в ледяную воду (500 мл) и экстрагировали этилацетатом (2×200 мл). Объединенные органические растворы промыли рассолом (200 мл), высушили над Na2SO4, профильтровали и упарили в вакууме. Остаток очистили на колонке для флэш-хроматографии (5-10% EtOAc в PE) с образованием III-A15 (8 г) в виде масла.
1H-ЯМР (400 МГц, CDCl3) δH 7,30-7,18 (м, 5H), 5,06-5,01 (м, 1H), 4,50 (с, 1H), 4,44-4,38 (м, 2H), 3,32-3,24 (м, 5H), 2,31-2,25 (м, 1H), 2,17-1,92 (м, 3H), 1,80-1,52 (м, 9H), 1,45-0,88 (м, 9H), 0,79-0,76 (м, 4H), 0,67-0,65 (м, 2H).
Синтез III-A16
[0628] К раствору III-A15 (8,0 г, 18,9 ммол) в THF (150 мл) добавили 9-BBN-димер (9,22 г, 37,8 ммол) и перемешивали при 25°С в течение 12 часов. К полученной смеси при 15°С добавили этанол (50 мл), затем при 0°С водный раствор NaOH (37,8 мл, 5,0 M, 189 ммол). По каплям при 0°С добавили пероксид водорода (18,9 мл, 10 M, 189 ммол). Реакционную смесь перемешивали при 78°С в течение 1 часа. После охлаждения до 15°С смесь добавили к воде (100 мл) и экстрагировали EtOAc (2×200 мл). Объединенный органический слой промыли раствором Na2S2O3 (2×100 мл) и рассолом (200 мл), высушили над Na2SO4, профильтровали и упарили в вакууме. Остаток очистили на колонке для флэш-хроматографии (0-15% EtOAc в PE) с образованием III-A16 (8,2 г) в виде масла. III-A16 (8 г) дополнительно очистили на колонке для флэш-хроматографии (0-5% EtOAc в PE) с образованием III-A16 (5,6 г, 70%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 7,39-7,29 (м, 4H), 7,26-7,21 (м, 1H), 4,50-4,45 (м, 2H), 3,75-3,66 (м, 1H), 3,40-3,30 (м, 5H), 2,03-1,96 (м, 1H), 1,93-1,79 (м, 3H), 1,77-1,60 (м, 6H), 1,42-1,18 (м, 8H), 1,17-0,91 (м, 9H), 0,75-0,69 (м, 1H), 0,66 (с, 3H).
Синтез III-A17
[0629] К раствору III-A16 (1 г, 2,26 ммол) в циклогексане (100 мл) при 25°С добавили CaCO3 (677 мг, 6,77 ммол), PhI(OAc)2 (2,18 г, 6,77 ммол), I2 (1,14 мг, 4,52 ммол). Реакционную смесь нагревали при кипячении с обратным холодильником (80°С) при облучении инфракрасной лампой (250 Вт) в течение 15 минут в атмосфере N2, затем охладили до температуры окружающей среды. Реакционную смесь вылили в насыщенный раствор Na2S2O3 в ледяной воде (200 мл) и экстрагировали EtOAc (2×200 мл), объединенные органические слои высушили над Na2SO4, упарили при температуре ниже 35°С с образованием III-A17 (1,1 г) в виде масла, и использовали непосредственно для следующей стадии.
Синтез III-A18
[0630] К смеси MePPh3Br (15,7 г, 44,2 ммол) в THF (100 мл) добавили t-BuOK (4,95 г, 44,2 ммол) при 25°С под N2. После перемешивания при 50°С в течение 30 минут порциями при температуре ниже 50°С добавили III-A17 (2,2 г, 4,42 ммол). Реакционную смесь перемешивали при 50°С в течение 16 часов с образованием суспензии. Реакционную смесь залили 10%-ным водным раствором NH4Cl (500 мл). Водный раствор экстрагировали EtOAc (2×300 мл), и объединенные органические слои промыли рассолом (150 мл), высушили над Na2SO4, профильтровали и упарили. Остаток очистили на колонке для флэш-хроматографии (0~10% EtOAc в PE) с образованием III-A18 (1,3 г, 65%) в виде масла.
1H-ЯМР (400 МГц, CDCl3) δH 7,38-7,30 (м, 4H), 7,26-7,21 (м, 1H), 5,78 (дд, J=11,2, 18,4 Гц, 1H), 5,32-5,12 (м, 2H), 4,47 (с, 2H), 3,86-3,77 (м, 1H), 3,37-3,29 (м, 5H), 2,40-2,31 (м, 1H), 2,01-1,94 (м, 1H), 1,85-1,65 (м, 5H), 1,56-1,23 (м, 9H), 1,22-0,93 (м, 10H), 0,78-0,62 (м, 2H).
Синтез III-A19
[0631] К раствору III-A18 (220 мг, 0,49 ммол) в MeOH (10 мл) добавили Pd/C (500 мг) (10% Pd, 50% воды), смесь перемешивали при 25°С под H2 (15 psi (0,1 МПа)) в течение 15 часов. Реакционную смесь профильтровали через слой Целита и промыли MeOH (3×10 мл). Фильтрат упарили с образованием III-A19 (170 мг, 96%) в виде твердого вещества. Твердое вещество (170 мг) очистили на колонке для флэш-хроматографии (0~20% EtOAc в PE) с образованием III-A19 (140 мг) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δ 3,87-3,78 (м, 1H), 3,38 (с, 3H), 3,18 (с, 2H), 2,15-2,08 (м, 1H), 1,93-1,69 (м, 5H), 1,64-1,58 (м, 5H), 1,46-1,30 (м, 4H), 1,26 (д, J=6,0 Гц, 3H), 1,24-1,15 (м, 3H), 1,13-1,05 (м, 3H), 1,03-0,87 (м, 5H), 0,84 (т, J=8,0 Гц, 3H), 0,75-0,63 (м, 2H).
LC-ELSD/MS чистота 99%, MS ESI рассчитано для C23H37O [M-2H2O+H]+ 329,3, найдено 329,3.
Синтез III-A20
[0632] К раствору III-A19 (1 г, 2,74 ммол) в DCM (20 мл) добавили DMP (2,32 г, 5,48 ммол), смесь перемешивали при 25°С в течение 2 часов. Смесь залили насыщенным водным раствором NaHCO3 (150 мл) и водным раствором Na2S2O3 (150 мл). Водную фазу экстрагировали DCM (3×100 мл). Объединенную органическую фазу промыли рассолом (200 мл), высушили над Na2SO4, профильтровали и упарили. Остаток очистили на колонке для флэш-хроматографии (0~15% EtOAc в PE) с образованием III-A20 (840 мг, 84,5%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δ 3,38 (с, 3H), 3,18 (с, 2H), 2,46 (т, J=8,8 Гц, 1H), 2,36-2,20 (м, 2H), 2,19 (с, 3H), 1,87-1,60 (м, 7H), 1,58-1,08 (м, 11H), 1,05-0,86 (м, 4H), 0,81-0,66 (м, 2H), 0,62 (т, J=7,6 Гц, 3H); LC-ELSD/MS 99%, MS ESI рассчитано для C23H37O2 [M-H2O+H]+ 345,3, найдено 345,3.
[0633] ПРИМЕР III-4: синтез 1-((3R,5S,8R,9R,10S,13S,14S,17S)-13-этил-3-гидрокси-3-(метоксиметил)гексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-(5-метил-2H-тетразол-2-ил)этан-1-она (III-A22) и 1-((3R,5S,8R,9R,10S,13S,14S,17S)-13-этил-3-гидрокси-3-(метоксиметил)гексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-(5-метил-1H-тетразол-1-ил)этан-1-она (III-A23)
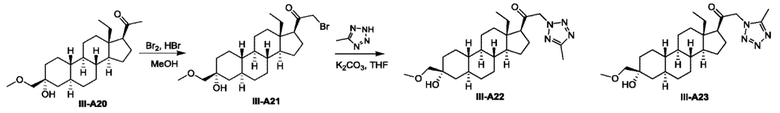
Синтез III-A21
[0634] К раствору III-A20 (150 мг, 0,41 ммол) в MeOH (2 мл) добавили HBr (16,7 мг, 0,08 ммол, 40% в воде) и Br2 (66,1 мг, 0,41 ммол) при 25°С. После перемешивания при 25°С в течение 2 часов смесь залили насыщенным водным раствором NaHCO3 (10 мл), обработали водой (30 мл), экстрагировали EtOAc (2×50 мл). Объединенную органическую фазу промыли рассолом (30 мл), высушили над безводным Na2SO4, профильтровали, упарили с образованием III-A21 (180 мг) в виде масла, и использовали непосредственно для следующей стадии.
1H-ЯМР (400 МГц, CDCl3) δ 4,01 (с, 2H), 3,39 (с, 3H), 3,18 (с, 2H), 2,74 (т, J=8,8 Гц, 1H), 2,32-2,17 (м, 2H), 1,87-1,69 (м, 4H), 1,61-1,54 (м, 1H), 1,47-1,15 (м, 13H), 0,96-0,65 (м, 6H), 0,59 (т, J=7,6 Гц, 3H).
Синтез III-A22 и III-A23
[0635] К раствору III-A21 (180 мг, 0,41 ммол) в THF (3 мл) добавили K2CO3 (168 мг, 1,22 ммол) и 5-метил-2H-1,2,3,4-тетразол (52 мг, 0,62 ммол). После перемешивания при 25°С в течение 14 часов к смеси добавили воду (20 мл) и экстрагировали EtOAc (2×30 мл). Органический слой отделили, высушили над Na2SO4, профильтровали и упарили. Остаток очистили на колонке для флэш-хроматографии (5~90% EtOAc в PE) с образованием III-A22 (50 мг) и III-A23 (50 мг).
III-A22 (50 мг) очистили с использованием HPLC с образованием III-A22 (4 мг, 2,2%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δ 5,54-5,32 (м, 2H), 3,39 (с, 3H), 3,19 (с, 2H), 2,60-2,47 (м, 4H), 2,41-2,23 (м, 2H), 2,09-1,96 (м, 1H), 1,94-1,61 (м, 7H), 1,49-1,17 (м, 9H), 1,07-0,90 (м, 4H), 0,84-0,67 (м, 5H); LC-ELSD/MS чистота 99%, MS ESI рассчитано для C25H40N4O3 [M+H]+ 445,3, найдено 445,3.
III-A23 (50 мг) очистили с использованием HPLC с образованием III-A23 (4 мг, 2,2%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 5,48-4,89 (м, 2H), 3,39 (с, 3H), 3,19 (с, 2H), 2,45 (т, J=8,4 Гц, 1H), 2,49 (с, 3H), 2,43-2,36 (м, 1H), 2,32-2,22 (м, 1H), 1,95-1,64 (м, 8H), 1,48-1,18 (м, 8H), 1,11-0,67 (м, 7H), 0,63 (т, J=7,6 Гц, 3H); LC-ELSD/MS чистота 99%, MS ESI рассчитано для C25H40N4O3 [M+H]+ 445,3, найдено 445,3.
[0636] ПРИМЕР III-6: синтез 1-((3R,5R,8R,9S,10S,13S,14S,17S)-13-этил-3-гидрокси-3,10-диметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)этан-1-она (III-A30)
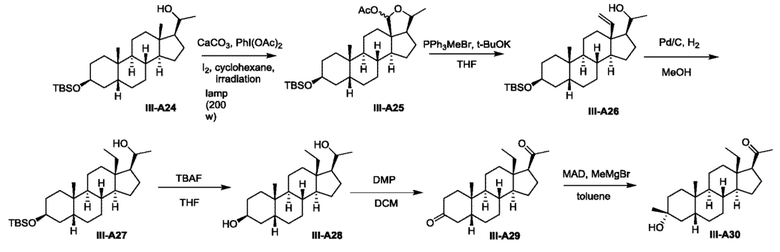
Синтез III-A25
[0637] К раствору III-A24 (1,0 г, 2,3 ммол) в циклогексане (100 мл) при 25°С добавили CaCO3 (688 мг, 6,89 ммол), PhI(OAc)2 (2,21 г, 6,89 ммол), I2 (1,16 г, 4,6 ммол). Реакционную смесь нагревали при кипячении с обратным холодильником (80°С) при облучении инфракрасной лампой (250 Вт) в течение 15 минут в атмосфере N2. Затем реакционную смесь охладили до температуры окружающей среды. Реакционную смесь вылили в насыщенный раствор Na2S2O3 в ледяной воде (100 мл) и разделили. Водный слой экстрагировали EtOAc (2×50 мл), и объединенные органические слои промыли рассолом, высушили над Na2SO4, упарили при температуре ниже 40°С с образованием III-A25 (2,5 г) в виде твердого вещества, и использовали непосредственно для следующей стадии.
Синтез III-A26
[0638] К смеси MePPh3Br (9,07 г, 25,4 ммол) в THF (50 мл) добавили t-BuOK (2,85 г, 25,4 ммол) при 25°С под N2. После перемешивания при 50°С в течение 30 минут порциями при температуре ниже 50°С добавили III-A25 (2,5 г, 5,09 ммол). После перемешивания при 50°С в течение 14 часов реакционную смесь залили насыщенным 10%-ным водным раствором NH4Cl (100 мл) при 15°С. Смесь экстрагировали EtOAc (2×50 мл). Органический слой отделили, высушили над Na2SO4, профильтровали и упарили. Остаток очистили на колонке для флэш-хроматографии (0~10% EtOAc в PE) с образованием III-A26 (410 мг, 18,0%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 5,73-5,57 (м, 1H), 5,36-5,25 (м, 1H), 5,23-5,12 (м, 1H), 3,70-3,48 (м, 2H), 2,54-2,43 (м, 1H), 1,87-1,66 (м, 5H), 1,61-1,44 (м, 6H), 1,40-1,30 (м, 8H), 1,28-1,13 (м, 4H), 1,12-1,08 (м, 3H), 0,90-0,80 (с, 12H), 0,06 (с, 6H).
Синтез III-A27
[0639] К раствору III-A26 (560 мг, 1,25 ммол) в MeOH (20 мл) добавили Pd/C (500 мг, 10%, влажный с 50% воды). Раствор подвергали гидрированию при давлении водорода 15 psi (0,1 МПа) при 25°С в течение 16 часов. Реакционную смесь профильтровали через слой Целита и промыли THF (3×50 мл). Фильтрат упарили с образованием III-A27 (600 мг) в виде твердого вещества и использовали непосредственно для следующей стадии.
1H-ЯМР (400 МГц, CDCl3) δH 3,81-3,71 (м, 1 H), 3,64-3,53 (м, 1H), 2,33-2,18 (м, 1H), 1,90-1,71 (м, 3H), 1,70-1,58 (м, 2H), 1,54-1,14 (м, 14H), 1,14-1,11 (м, 3H), 1,10-1,01 (м, 3H), 1,00-0,92 (м, 5H), 0,91-0,88 (м, 12H), 0,06 (с, 6H).
Синтез III-A28
[0640] III-A27 (562 мг, 1,25 ммол) растворили в TBAF (6,26 мл, 6,26 ммол, 1 М в THF). Смесь перемешивали при 25°С в течение 16 часов. Смесь залили 10%-ным раствором NH4Cl (30 мл) и экстрагировали EtOAc (2×10 мл). Объединенную органическую фазу промыли 10%-ным раствором NH4Cl (3×20 мл), высушили над Na2SO4, профильтровали и упарили с образованием III-A28 (400 мг) в виде масла.
Синтез III-A29
[0641] К раствору III-A28 (300 мг, 0,89 ммол) в DCM (5 мл) при 30°С добавили периодинан Десса-Мартина (1,14 г, 2,69 ммол). После перемешивания при 30°С в течение 10 минут смесь залили насыщенным водным раствором NaHCO3/Na2S2O3 (1:1, 50 мл) при 25°С. Органическую фазу отделили и промыли насыщенным водным раствором NaHCO3/Na2S2O3 (1:1, 50 мл), рассолом (50 мл), высушили над Na2SO4, профильтровали и упарили в вакууме с образованием III-A29 (230 мг) в виде твердого вещества, и использовали непосредственно для следующей стадии.
1H-ЯМР (400 МГц, CDCl3) δH 2,74-2,62 (м, 1H), 2,52-2,43 (м, 1H), 2,41-2,23 (м, 3H), 2,21 (с, 3H), 2,09-0,99 (м, 2H), 1,96-1,78 (м, 2H), 1,72-1,58 (м, 3H), 1,55-1,47 (м, 3H), 1,47-1,37 (м, 1H), 1,37-1,05 (м, 9H), 1,02 (с, 3H), 0,65 (т, J=7,6 Гц, 3H); LC-ELSD/MS чистота 99%, MS ESI рассчитано для C22H34O2 [M+H]+ 331,2, найдено 331,2.
Синтез III-A30
[0642] К раствору MAD (3,38 ммол в 3 мл толуола) по каплям при -70°С добавили раствор III-A29 (280 мг, 0,85 ммол) в DCM (2 мл). После перемешивания при -70°С в течение 1 часа под N2, по каплям при -70°С добавили MeMgBr (0,85 мл, 2,55 ммол, 3 M в диэтиловом эфире). Полученный раствор перемешивали при -70°С в течение дополнительных 4 часов. Реакционную смесь вылили в насыщенный водный раствор лимонной кислоты (50 мл) при температуре ниже 10°С, и экстрагировали EtOAc (2×50 мл). Объединенный органический слой высушили над Na2SO4, профильтровали и упарили в вакууме. Остаток очистили на колонке с силикагелем (PE/EtOAc=0-20%) с образованием III-A30 (110 мг) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 2,49-2,39 (м, 1H), 2,36-2,21 (м, 2H), 2,19 (с, 3H), 2,01-1,92 (м, 1H), 1,91-1,79 (м, 1H), 1,79-1,70 (м, 1H), 1,68-1,57 (м, 3H), 1,53-1,32 (м, 9H), 1,31-1,19 (м, 11H), 1,14-1,00 (м, 3H), 0,93 (с, 3H), 0,62 (т, J=7,6 Гц, 3H); LC-ELSD/MS чистота 99%, MS ESI рассчитано для C23H38O2 [M+H]+ 329,3, найдено 329,3.
[0643] ПРИМЕР III-7 и III-8: синтез 1-((3R,5R,8R,9S,10S,13S,14S,17S)-13-этил-3-гидрокси-3,10-диметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-(5-метил-1H-тетразол-1-ил)этан-1-она (III-A32) и 1-((3R,5R,8R,9S,10S,13S,14S,17S)-13-этил-3-гидрокси-3,10-диметилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-(5-метил-2H-тетразол-2-ил)этан-1-она (III-A33)
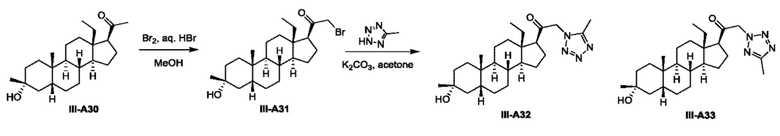
Синтез III-A31
К раствору III-A30 (99 мг, 0,28 ммол) в MeOH (2 мл) добавили HBr (0,01 мл, 40% в воде) и Br2 (54,7 мг, 0,3427 ммол) при 25°С. После перемешивания при 25°С в течение 2 часов смесь залили насыщенным водным раствором NaHCO3 (10 мл), экстрагировали EtOAc (2×30 мл). Объединенную органическую фазу промыли рассолом (30 мл), высушили над безводным Na2SO4, профильтровали и упарили в вакууме с получением III-A31 (100 мг) в виде твердого вещества, и использовали непосредственно для следующей стадии.
Синтез III-A32 и III-A33
[0644] К раствору III-A31 (100 мг, 0,23 ммол) в ацетоне (3 мл) добавили 1H-пиразол-4-карбонитрил (23,7 мг, 0,282 ммол) и K2CO3 (60,2 мг, 0,47 ммол). После перемешивания при 25°С в течение 14 часов к смеси добавили воду (20 мл) и экстрагировали EtOAc (2×30 мл). Органический слой отделили, высушили над Na2SO4, профильтровали и упарили. Остаток очистили на колонке для флэш-хроматографии (20~50% EtOAc в PE) с образованием III-A32 (20 мг, 19,9%) и III-A33 (16,5 мг, 16,5%) в виде твердого вещества.
III-A32: 1H-ЯМР (400 МГц, CDCl3) δH 5,36 (д, J=18,0 Гц, 1H), 4,96 (д, J=18,0 Гц, 1H), 2,57-2,50 (м, 1H), 2,49 (с, 3H), 2,44-2,17 (м, 2H), 2,03-1,81 (м, 2H), 1,81-1,62 (м, 3H), 1,51-1,40 (м, 5H), 1,39-1,22 (м, 12H), 1,22-0,99 (м, 4H), 0,95 (с, 3H), 0,63 (т, J=7,6 Гц, 3H); LC-ELSD/MS чистота 99%, MS ESI рассчитано для C25H40N4O2 [M-H2O +H]+ 411,3, найдено 411,3.
III-A33: 1H-ЯМР (400 МГц, CDCl3) δH 5,48 (д, J=17,6 Гц, 1H) 5,37 (д, J=17,6 Гц, 1H), 2,56 (с, 3H), 2,54-2,47 (м, 1H), 2,41-2,20 (м, 2H), 2,06-1,79 (м, 2H), 1,79-1,63 (м, 3H), 1,52-1,39 (м, 6H), 1,39-1,20 (м, 14H), 1,19-0,99 (м, 4H), 0,95 (с, 3H), 0,71 (т, J=7,6 Гц, 3H); LC-ELSD/MS чистота 99%, MS ESI рассчитано для C25H40N4O2 [M-H2O +H]+ 411,3, найдено 411,3.
ПРИМЕР III-9: синтез 1-((3R,5R,8R,9R,10S,13S,14S,17S)-13-этил-3-гидрокси-3-(метоксиметил)гексадекагидро-1H-циклопента[a]фенантрен-17-ил)этан-1-она (III-B15)
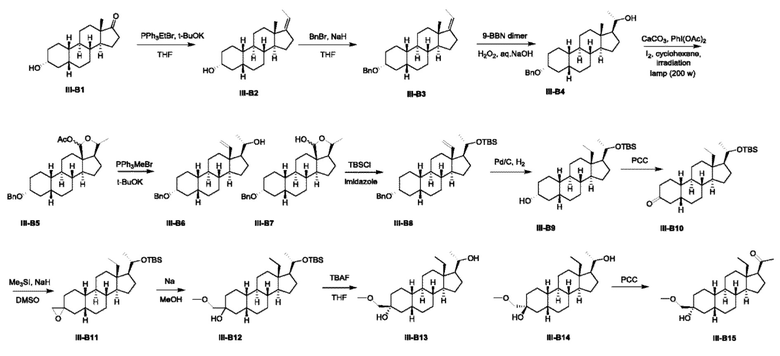
Синтез III-B2
[0645] К суспензии бром(этил)трифенилфосфорана (160 г, 432 ммол) в THF (300 мл) добавили t-BuOK (48,3 г, 432 ммол) при 25°С под N2. После перемешивания при 45°С в течение 1 часа добавили при 45°С раствор III-B1 (30 г, 108 ммол, CAS: 33036-33-8) в THF (100 мл). После перемешивания при 45°С в течение 16 часов смесь охладили, разбавили насыщенным раствором NH4Cl (1000 мл) и экстрагировали EtOAc (2×250 мл). Объединенный органический раствор промыли рассолом (2×250 мл), высушили над безводным Na2SO4, профильтровали, упарили (30 г), и очистили вместе с еще двумя партиями (из 20 г и 30 г). Остаток (80 г) очистили на колонке для флэш-хроматографии (0~25% EtOAc в PE) с образованием III-B2 (50 г, 63%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 5,20-5,05 (м, 1H), 3,70-3,60 (м, 1H), 2,40-2,30 (м, 1H), 2,25-2,10 (м, 2H), 1,95-1,85 (м, 1H), 1,85-1,40 (м, 12H), 1,40-1,05 (м, 11H), 0,87 (с, 3H).
Синтез III-B3
[0646] К раствору III-B2 (15 г, 51,9 ммол) в DMF (100 мл) порциями при 25°С добавили NaH (6,18 г, 155 ммол, 60% в масле). После перемешивания при 25°С в течение 30 минут добавили BnBr (26,5 г, 155 ммол). После перемешивания при 25°С в течение 3 часов смесь вылили в ледяную воду (500 мл) и экстрагировали этилацетатом (2×100 мл). Объединенный органический раствор промыли рассолом (100 мл), высушили над безводным Na2SO4, профильтровали и упарили в вакууме. Остаток очистили на колонке для флэш-хроматографии (PE) с образованием III-B3 (19 г) в виде масла. 1H-ЯМР (400 МГц, CDCl3) δH 7,43-7,26 (м, 5H), 5,20-5,05 (м, 1H), 4,57 (с, 2H), 3,45-3,35 (м, 1H), 2,45-2,10 (м, 4H), 2,00-1,93 (м, 1H), 1,85-1,55 (м, 8H), 1,50-1,00 (м, 13H), 0,88 (с, 3H).
Синтез III-B4
[0647] К раствору III-B3 (10 г, 26,4 ммол) в THF (100 мл) при 25°С добавили 9-BBN-димер (12,8 г, 52,8 ммол). После перемешивания при 25°С в течение 12 часов реакционную смесь охладили до 0°С и очень медленно добавили этанол (12,1 г, 264 ммол) и NaOH (52,8 мл, 5 M, 264 ммол). После завершения добавления медленно добавили H2O2 (26,4 мл, 264 ммол, 30%), поддерживая внутреннюю температуру ниже 15°С. После перемешивания при 75°С в течение 1 часа добавили насыщенный водный раствор Na2S2O3 (500 мл), и смесь перемешивали при 0°С в течение дополнительного 1 часа. Смесь разбавили водой (500 мл) и экстрагировали EtOAc (3×200 мл). Объединенный органический раствор промыли насыщенным рассолом (500 мл), высушили над безводным Na2SO4, профильтровали, упарили (10 г), и очистили на колонке для флэш-хроматографии (0-15% EtOAc в PE) с образованием III-B4 (8 г, 80%) в виде масла. 1H-ЯМР (400 МГц, CDCl3) δH 7,42-7,20 (м, 5H), 4,56 (с, 2H), 3,90-3,80 (м, 2H), 3,75-3,65 (м, 1H), 3,45-3,30 (м, 1H), 2,00-1,75 (м, 9H), 1,70-1,55 (м, 4H), 1,40-0,95 (м, 13H), 0,66 (с, 3H).
Синтез III-B5
[0648] К суспензии III-B4 (2,5 г, 6,3 ммол), PhI(OAc)2 (6,08 г, 18,9 ммол) и CaCO3 (1,89 г, 18,9 ммол) в циклогексане (250 мл) при 25°С добавили элементарный иод (3,19 г, 12,6 ммол). После нагревания до 80°С путем облучения инфракрасной лампой (275 Вт) в течение 10 минут смесь добавили в насыщенный раствор Na2S2O3 (500 мл) и экстрагировали EtOAc (3×50 мл). Объединенный органический раствор промыли насыщенным рассолом (200 мл), высушили над безводным Na2SO4, профильтровали и упарили с образованием III-B5 (2,85 г) в виде масла, которое использовали непосредственно для следующей стадии без дополнительной очистки.
Синтез III-B6 и III-B7
[0649] После перемешивания при 50°С в течение 1 часа суспензию PPh3MeBr (11,2 г, 31,4 ммол) и t-BuOK (3,51 г, 31,4 ммол) в THF (30 мл) добавили к раствору III-B7 (2,85 г, 6,29 ммол) в THF (20 мл). После перемешивания при 50°С в течение 12 часов смесь добавили в насыщенный раствор NH4Cl (100 мл) и экстрагировали EtOAc (3×50 мл). Объединенный органический раствор промыли насыщенным рассолом (100 мл), высушили над безводным Na2SO4, профильтровали и упарили (2,5 г) в виде масла, которое очистили вместе с другими тремя партиями (из 2,85 г, 2,85 г и 2,35 г). Остаток (9,5 г) очистили на колонке для флэш-хроматографии (0-15% EtOAc в PE) с образованием смеси III-B6 и III-B7 (~1:1) (5 г) в виде масла.
Синтез III-B8
[0650] К раствору III-B6 и III-B7 (~1:1) (5,0 г, 12,2 ммол) в DCM (50 мл) добавили имидазол (2,48 г, 36,5 ммол) и TBSCl (5,50 г, 36,5 ммол) при 25°С. После перемешивания при 25°С в течение 12 часов смесь профильтровали, и фильтрат упарили. Продукт растворили в DCM (70 мл), промыли насыщенным водным раствором NH4Cl (50 мл), насыщенным рассолом (50 мл). Органический раствор высушили над сульфатом натрия, профильтровали, и фильтрат упарили и очистили на колонке для флэш-хроматографии (0-15% EtOAc в PE) с образованием III-B8 (3,5 г, 55%) и III-B7 (2 г, 40%), оба в виде масел.
III-B8: 1H-ЯМР (400 МГц, CDCl3) δH 7,40-7,20 (м, 5H), 5,57 (дд, J=11,2, 17,6 Гц, 1H), 5,18 (дд, J=1,6, 12,8 Гц, 1H), 4,98 (дд, J=1,6, 18,0 Гц, 1H), 4,55 (с, 2H), 3,50-3,30 (м, 2H), 2,40-2,25 (м, 1H), 2,05-1,75 (м, 3H), 1,55-1,00 (м, 14H), 0,95-0,75 (м, 12H), 0,02 (с, 3H), 0,01 (с, 3H).
III-B7: 1H-ЯМР (400 МГц, CDCl3) δH 7,40-7,20 (м, 5H), 5,04 (с, 1H), 4,56 (с, 2H), 4,45-4,35 (м, 1H), 3,45-3,30 (м, 1H), 2,55-2,30 (м, 2H), 2,00-1,45 (м, 15H), 1,44-0,95 (м, 12H).
Синтез III-B9
[0651] К раствору III-B8 (3,5 г, 6,7 ммол) в MeOH (30 мл) добавили Pd/C (1 г, 10% Pd, 50% воды). После перемешивания при 25°С под H2 (15 psi (0,1 МПа)) в течение 12 часов реакционную смесь профильтровали через слой Целита и промыли MeOH (3×10 мл). Фильтрат упарили с образованием III-B9 (2,50 г, 86%) в виде масла. 1H-ЯМР (400 МГц, CDCl3) δH 3,80-3,73 (м, 1H), 3,65-3,55 (м, 1H), 2,15-2,05 (м, 1H), 1,95-1,70 (м, 6H), 1,55-1,35 (м, 6H), 1,30-0,95 (м, 15H), 0,90-0,75 (м, 14H), 0,05 (с, 3H), 0,04 (с, 3H).
Синтез III-B10
[0652] К раствору III-B9 (2,5 г, 5,8 ммол) в DCM (20 мл) добавили PCC (2,47 г, 11,5 ммол) и силикагель (5 г) при 25°С. После перемешивания при 25°С в течение 1 часа реакционную смесь профильтровали, и остаток промыли безводным DCM (2×20 мл). Объединенный фильтрат упарили в вакууме с образованием III-B10 (2,2 г, 88%) в виде твердого вещества. 1H-ЯМР (400 МГц, CDCl3) δH 3,85-3,75 (м, 1H), 2,61 (т, J=14,0 Гц, 1H), 2,30-2,10 (м, 6H), 1,95-1,83 (м, 1H), 1,78-1,60 (м, 2H), 1,50-1,25 (м, 7H), 1,25-0,95 (м, 11H), 0,90-0,80 (м, 13H), 0,05 (с, 3H), 0,04 (с, 3H).
Синтез III-B11
К перемешиваемому раствору Me3SI (1,24 г, 6,1 ммол) в DMSO (10 мл) и THF (10 мл) при 0°С добавили NaH (243 мг, 6,1 ммол, 60% в масле). После перемешивания в течение 1 часа под N2 смесь добавили к раствору III-B10 (2,2 г, 5,1 ммол) в DMSO (10 мл). После перемешивания при 25°С в течение 16 часов реакционную смесь вылили в ледяную воду (100 мл) и экстрагировали EtOAc (2×50 мл). Объединенный органический раствор промыли водой (2×50 мл) и рассолом (50 мл), высушили над безводным Na2SO4, профильтровали и упарили с образованием III-B11 (2 г) в виде масла, которое использовали непосредственно для следующей стадии без дополнительной очистки. 1H-ЯМР (400 МГц, CDCl3) δH 3,80-3,70 (м, 1H), 2,65-2,50 (м, 2H), 2,30-2,05 (м, 2H), 2,00-1,80 (м, 3H), 1,55-1,30 (м, 12H), 1,30-0,75 (м, 24H), 0,05 (с, 3H), 0,04 (с, 3H).
Синтез III-B12
Свежий Na (1,02 г, 44,7 ммол) осторожно порциями добавляли к MeOH (44,7 мл). После перемешивания при 25°С в течение 3 часов добавили раствор III-B11 (2 г, 4,47 ммол) в безводном MeOH (30 мл). После перемешивания при 75°С в течение 16 часов реакционную смесь разбавили водой (50 мл), упарили для удаления большей части растворителя, и экстрагировали EtOAc (2×50 мл). Объединенный органический раствор промыли насыщенным рассолом (100 мл), высушили над безводным Na2SO4, профильтровали и упарили. Остаток очистили хроматографией на силикагеле (0-20% EtOAc в PE) с образованием продукта III-B12 (2 г, 93%) в виде масла.
Синтез III-B13 и III-B14
[0653] К раствору III-B12 (2 г, 4,2 ммол) в THF (30 мл) при 25°С добавили TBAF·3H2O (1,95 г, 6,3 ммол). После перемешивания при 55°С в течение 12 часов смесь вылили в воду (50 мл) и экстрагировали EtOAc (2×30 мл). Органический раствор промыли насыщенным рассолом (2×20 мл), высушили над безводным Na2SO4, профильтровали и упарили в вакууме. Остаток очистили хроматографией на силикагеле (0-20% EtOAc в PE) с образованием III-B13 (620 мг, 42%) и III-B14 (570 мг, 38%), оба в виде масел.
III-B13: 1H-ЯМР (400 МГц, CDCl3) δH 3,93-3,76 (м, 1H), 3,48-3,35 (м, 5H), 2,58 (с, 1H), 2,17-2,08 (м, 1H), 1,93-1,60 (м, 8H), 1,55-1,02 (м, 19H), 1,00-0,78 (м, 5H); LC-ELSD/MS чистота 99%, 100% по данным H-ЯМР. MS ESI рассчитано для C23H37O [M-H2O-H2O+H]+ 329,3, найдено 329,3.
III-B14: 1H-ЯМР (400 МГц, CDCl3) δH 3,93-3,76 (м, 1H), 3,39 (с, 3H), 3,20 (с, 2H), 3,18-3,10 (м, 2H), 2,00 (с, 1H), 1,95-1,82 (м, 1H), 1,75-1,58 (м, 5H), 1,54-0,85 (м, 25H); LC-ELSD/MS чистота 99%, 100% по данным H-ЯМР. MS ESI рассчитано для C23H37O [M-H2O-H2O+H]+ 329,3, найдено 329,3.
Синтез III-B15
[0654] К раствору III-B13 (600 мг, 1,6 ммол) в DCM (20 мл) порциями при 25°С добавили силикагель (1,5 г) и PCC (1,05 г, 4,9 ммол). После перемешивания при 25°С в течение 0,5 часа смесь профильтровали, и осадок на фильтре промыли DCM (30 мл). Объединенный фильтрат упарили и очистили хроматографией на силикагеле (0-20% EtOAc в PE) с образованием III-B15 (550 мг, 93%) в виде масла. 1H-ЯМР (400 МГц, CDCl3) δH 3,45-2,35 (м, 5H), 2,61 (с, 1H), 2,53-2,42 (м, 1H), 2,35-2,18 (м, 5H), 1,85-1,10 (м, 22H), 0,96-0,82 (м, 1H), 0,62 (т, J=7,6 Гц, 3H); LC-ELSD/MS чистота 99%, MS ESI рассчитано для C23H37O2 [M-H2O+H]+ 345,3, найдено 345,3.
ПРИМЕР III-10: 1-(2-((3R,5R,8R,9R,10S,13S,14S,17S)-13-этил-3-гидрокси-3-(метоксиметил)гексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-оксоэтил)-1H-пиразол-4-карбонитрила (III-B17)
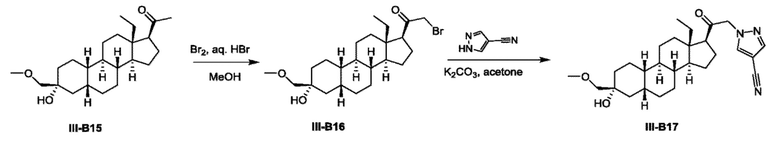
Синтез III-B16
[0655] К раствору III-B15 (80 мг, 0,22 ммол) в MeOH (5 мл) при 25°С добавили HBr (8,80 мг, 0,044 ммол) и Br2 (35,2 мг, 0,22 ммол). После перемешивания при 25°С в течение 2 часов реакционную смесь добавили в насыщенный раствор NaHCO3 (10 мл) и экстрагировали EtOAc (3×10 мл). Объединенный органический раствор промыли насыщенным рассолом (20 мл), высушили над безводным Na2SO4, профильтровали и упарили с образованием III-B16 (90 мг) в виде масла, которое использовали непосредственно в следующей стадии без дополнительной очистки.
Синтез III-B17
[0656] К раствору III-B16 (90 мг, 0,2 ммол) и 1H-пиразол-4-карбонитрила (37,9 мг, 0,4 ммол) в ацетоне (5 мл) добавили K2CO3 (56,2 мг, 0,4 ммол). После перемешивания при 25°С в течение 2 часов реакционную смесь экстрагировали EtOAc (3×30 мл). Объединенный органический раствор промыли насыщенным рассолом (30 мл), высушили над безводным Na2SO4, профильтровали и упарили. Остаток очистили на колонке для флэш-хроматографии (0-30% EtOAc в PE), и затем препаративной HPLC (колонка: Waters Xbridge Prep OBD C18 150*30 5 мкм; условия: вода (10 мМ NH4HCO3)-ACN; начало B: 70; конец B: 90; время градиента (минут): 7; время удерживания 100% B (минут): 1) с образованием III-B17 (32,6 мг, 53%) в виде твердого вещества. 1H-ЯМР (400 МГц, CDCl3) δH 7,86 (с, 1H), 7,81 (с, 1H), 5,04 (дд, J=18,0, 95,6 Гц, 2H), 3,45-3,33 (м, 5H), 2,50 (т, J=8,8 Гц, 1H), 2,40-2,23 (м, 2H), 1,88-1,10 (м, 23H), 1,00-0,83 (м, 1H), 0,60 (т, J=7,6 Гц, 3H); LC-ELSD/MS чистота 99%, MS ESI рассчитано для C27H38N3O2 [M-H2O+H]+ 436,3, найдено 436,3.
ПРИМЕР III-11: синтез 1-((3R,5R,8R,9R,10S,13R,14S,17S)-3-гидрокси-13-(метоксиметил)-3-метилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)этан-1-она (III-C11)
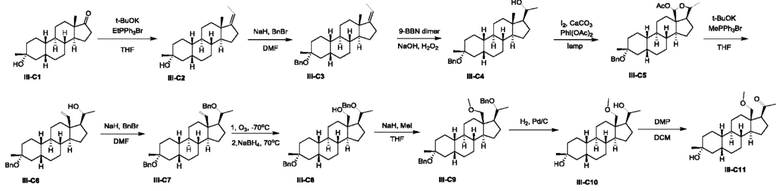
Синтез III-C2
[0657] К раствору EtPh3PBr (63,4 г, 171 ммол) в THF (400 мл) при 25°С добавили t-BuOK (19,1 г, 171 ммол). После перемешивания при 50°С в течение 30 минут добавили III-C1 (20 г, 68,8 ммол). После перемешивания при 50°С в течение 2 часов смесь добавили в насыщенный раствор NH4Cl (400 мл) и экстрагировали EtOAc (3×200 мл). Объединенный органический раствор промыли насыщенным рассолом (500 мл), высушили над безводным Na2SO4, профильтровали и упарили. Остаток перекристаллизовали из MeOH/воды (700 мл, 1:1) с образованием III-C2 (25 г) в виде масла. 1H-ЯМР (400 МГц, CDCl3) δH 5,25-5,05 (м, 1H), 2,42-2,10 (м, 3H), 1,92-1,55 (м, 7H), 1,53-1,25 (м, 14H), 1,24-1,06 (м, 6H), 0,87 (с, 3H).
Синтез III-C3
[0658] К смеси III-C2 (25 г, 82,6 ммол) в DMF (300 мл) добавили NaH (8,23 г, 206 ммол, 60%) при 0°С. После перемешивания при 25°С в течение 1 часа добавили BnBr (35,2 г, 206 ммол). После перемешивания при 60°С в течение 20 часов смесь добавили в воду (500 мл) и экстрагировали EtOAc (3×200 мл). Объединенный органический раствор промыли раствором LiCl (2×500 мл, 4% в воде), насыщенным рассолом (500 мл), высушили над безводным Na2SO4, профильтровали и упарили. Остаток очистили на колонке для флэш-хроматографии (100% PE) с образованием III-C3 (30 г, 93%) в виде твердого вещества.
1H-ЯМР (400 МГц, CDCl3) δH 7,40-7,27 (м, 5H), 5,15-5,05 (м, 1H), 4,50 (с, 2H), 2,40-2,10 (м, 3H), 1,99-1,59 (м, 9H), 1,52-1,34 (м, 6H), 1,33 (с, 3H), 1,32-1,05 (м, 8H), 0,87 (с, 3H).
Синтез III-C4
[0659] К раствору III-C3 (28 г, 71,3 ммол) в THF (300 мл) при 0°С добавили 9-BBN-димер (34,3 г, 142 ммол). После перемешивания при 25°С в течение 1 часа добавили при 25°С этанол (200 мл), и затем по каплям водный раствор NaOH (142 мл, 5 M, 713 ммол), затем H2O2 (121 г, 30%, 1069 ммол). После перемешивания при 70°С в течение 1 часа реакционную смесь разбавили водой (300 мл) и перемешивали при 25°С в течение 1 часа. Твердое вещество отфильтровали и промыли водой (2×300 мл), высушили в вакууме с образованием III-C4 (19,1 г, 65%) в виде твердого вещества. 1H-ЯМР (400 МГц, CDCl3) δH 7,45-7,28 (м, 5H), 4,50 (с, 2H), 3,75-3,62 (м, 1H), 2,00-1,59 (м, 12H), 1,52-1,32 (м, 10H), 1,31-1,00 (м, 9H), 0,67 (с, 3H).
Синтез III-C5
[0660] К раствору III-C4 (3 г, 7,3 ммол) в циклогексане (300 мл) при 25°С под N2 добавили CaCO3 (2,19 г, 21,9 ммол), PhI(OAc)2 (7,05 г, 21,9 ммол), I2 (3,70 г, 14,6 ммол). После нагревания при кипячении с обратным холодильником (80°С) посредством облучения инфракрасной лампой (250 Вт) в течение 30 минут смесь добавили в насыщенный раствор Na2S2O3 (500 мл) и экстрагировали EtOAc (3×100 мл). Объединенный органический раствор промыли насыщенным рассолом (500 мл), высушили над безводным Na2SO4, профильтровали и упарили. Остаток очистили на колонке для флэш-хроматографии (0-5% EtOAc в PE) с образованием III-C5 (4,0 г) в виде масла. 1H-ЯМР (400 МГц, CDCl3) δH 7,40-7,20 (м, 4H), 7,25-7,20 (м, 1H), 6,00 (с, 1H), 5,07 (с, 1H), 4,50 (с, 2H), 4,40-4,25 (м, 2H), 2,20-2,08 (м, 1H), 2,00-1,65 (м, 13H), 1,50-1,40 (м, 10H), 1,25-0,95 (м, 5H), 0,85-0,70 (м, 2H).
Синтез III-C6
[0661] К раствору MePh3PBr (30,5 г, 85,7 ммол) в THF (200 мл) добавили t-BuOK (9,59 г, 85,7 ммол) при 25°C. После перемешивания при 50°С в течение 1 часа добавили раствор III-C5 (4 г, 8,6 ммол) в THF (20 мл). После перемешивания при 50°С в течение 16 часов смесь добавили в насыщенный раствор NH4Cl (200 мл) и экстрагировали EtOAc (3×100 мл). Объединенный органический раствор промыли насыщенным рассолом (200 мл), высушили над безводным Na2SO4, профильтровали и упарили. Остаток растерли со смесью MeOH/воды (400 мл, 1:1) при 25°С с образованием III-C6 (3,6 г) в виде масла. 1H-ЯМР (400 МГц, CDCl3) δH 7,42-7,27 (м, 5H), 5,85-5,70 (м, 1H), 5,35-5,25 (м, 1H), 5,20-5,10 (м, 1H), 4,50 (с, 2H), 3,90-3,75 (м, 1H), 2,40-2,30 (м, 1H), 1,95-1,60 (м, 9H), 1,55-1,30 (м, 14H), 1,28-0,90 (м, 7H).
Синтез III-C7
[0662] К раствору III-C6 (3,6 г, 8,5 ммол) в DMF (20 мл) при 25°С добавили NaH (1,70 г, 42,5 ммол, 60% в масле). После перемешивания при 25°С в течение 1 часа добавили BnBr (4,36 г, 25,5 ммол). После перемешивания при 60°С в течение 16 часов смесь добавили в воду (200 мл) и экстрагировали EtOAc (3×50 мл). Объединенный органический раствор промыли раствором LiCl (2×100 мл, 4% в воде), насыщенным рассолом (100 мл), высушили над безводным Na2SO4, профильтровали и упарили. Остаток очистили на колонке для флэш-хроматографии (0-2% EtOAc в PE) с образованием III-C7 (1 г, 23%) в виде масла. 1H-ЯМР (400 МГц, CDCl3) δH 7,45-7,28 (м, 10H), 5,70-5,55 (м, 1H), 5,25-5,15 (м, 1H), 5,05-4,95 (м, 1H), 4,57-4,45 (м, 3H), 4,33-4,25 (м, 1H), 3,27-3,15 (м, 1H), 2,41-2,32 (м, 1H), 2,15-2,05 (м, 1H), 1,95-1,59 (м, 7H), 1,52-1,25 (м, 11H), 1,20-0,80 (м, 10H).
Синтез III-C8
[0663] К раствору III-C7 (1 г, 1,9 ммол) в DCM/MeOH (10 мл/10 мл) при 25°С добавили NaHCO3 (1 г, 11,9 ммол). После перемешивания под O3 (1 атм) в течение 20 минут при -70°С к смеси при 0°С добавили NaBH4 (296 мг, 7,8 ммол). После перемешивания в течение 1 часа при 70°С смесь добавили в насыщенный раствор NH4Cl (100 мл) и экстрагировали EtOAc (3×50 мл). Объединенный органический раствор промыли насыщенным рассолом (100 мл), высушили над безводным Na2SO4, профильтровали и упарили с образованием III-C8 (300 мг) в виде масла, которое использовали непосредственно для следующей стадии.
Синтез III-C9
[0664] К раствору III-C8 (300 мг, 0,58 ммол) в THF (5 мл) при 0°С добавили NaH (92,6 мг, 2,3 ммол, 60%). После перемешивания при 25°С в течение 1 часа добавили MeI (329 мг, 2,3 ммол). После перемешивания при 25°С в течение 1 часа смесь добавили в насыщенный раствор NH4Cl (100 мл) и экстрагировали EtOAc (3×50 мл). Объединенный органический раствор промыли насыщенным рассолом (100 мл), высушили над безводным Na2SO4, профильтровали и упарили. Остаток очистили на колонке для флэш-хроматографии (0-2% EtOAc в PE) с образованием III-C9 (200 мг) в виде масла. 1H-ЯМР (400 МГц, CDCl3) δH 7,45-7,28 (м, 8H), 7,25-7,21 (м, 2H), 4,65-4,55 (м, 1H), 4,50 (с, 2H), 4,40-4,30 (м, 1H), 3,55-3,43 (м, 1H), 3,40-3,30 (м, 1H), 3,21 (с, 3H), 3,15-3,05 (м, 1H), 2,40-2,30 (м, 1H), 2,20-1,59 (м, 11H), 1,52-1,20 (м, 11H), 1,18-0,80 (м, 7H).
Синтез III-C10
[0665] К раствору III-C9 (200 мг, 0,38 ммол) в MeOH (5 мл) добавили Pd/C (50 мг, 10% в воде) при 25°С. После перемешивания при комнатной температуре в течение 16 часов под H2 (50 psi (0,35 МПа)) смесь профильтровали, и маточную жидкость упарили. Остаток очистили на колонке для флэш-хроматографии (0-30% EtOAc в PE) с образованием III-C10 (50 мг, 38%) в виде масла. 1H-ЯМР (400 МГц, CDCl3) δH 4,20-4,11 (м, 1H), 4,10-4,00 (м, 1H), 3,40-3,25 (м, 5H), 2,35-2,25 (м, 1H), 1,95-1,80 (м, 4H), 1,78-1,59 (м, 4H), 1,52-1,35 (м, 5H), 1,33-1,23 (м, 7H), 1,30-1,00 (м, 6H), 0,98-0,80 (м, 4H).
Синтез III-C11
[0666] Раствор III-C10 (50 мг, 0,14 ммол) и DMP (120 мг, 0,29 ммол) в DCM (2 мл) перемешивали при 25°С в течение 1 часа. Смесь добавили в насыщенный раствор NaHCO3 (50 мл) и экстрагировали DCM (3×20 мл). Объединенный органический раствор промыли насыщенным раствором Na2S2O3 (2×50 мл), насыщенным рассолом (50 мл), высушили над безводным Na2SO4, профильтровали и упарили. Остаток очистили на колонке для флэш-хроматографии (0-30% EtOAc в PE) с образованием III-C11 (30 мг, 60%) в виде твердого вещества. 1H-ЯМР (400 МГц, CDCl3) δH 3,48-3,40 (м, 1H), 3,09 (с, 3H), 2,88-2,80 (м, 1H), 2,65-2,55 (м, 1H), 2,50-2,40 (м, 1H), 2,38-2,28 (м, 1H), 2,15 (с, 3H), 1,95-1,59 (м, 7H), 1,52-1,25 (м, 13H), 1,24-1,00 (м, 5H); LC-ELSD/MS чистота 99%, MS ESI рассчитано для C22H37O3 [M+H]+ 349,3, найдено 349,3.
ПРИМЕР III-12: синтез 1-(2-((3R,5R,8R,9R,10S,13R,14S,17S)-3-гидрокси-13-(метоксиметил)-3-метилгексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-оксоэтил)-1H-пиразол-4-карбонитрила (III-C13)
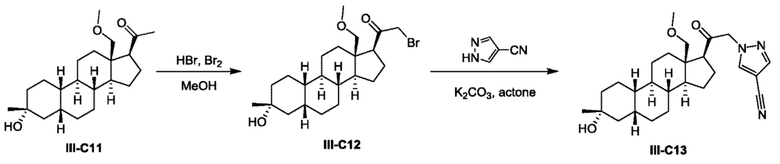
Синтез III-C12
[0667] К раствору III-C11 (25 мг, 0,072 ммол) в MeOH (5 мл) добавили HBr (2 мг, 40%) при 25°С, и затем Br2 (11,4 мг, 0,072 ммол) при 0°С. После перемешивания при 25°С в течение 5 часов смесь добавили в насыщенный раствор NaHCO3 (50 мл) и экстрагировали EtOAc (3×20 мл). Объединенный органический раствор промыли насыщенным рассолом (50 мл), высушили над безводным Na2SO4, профильтровали и упарили с образованием III-C12 (40 мг) в виде масла. 1H-ЯМР (400 МГц, CDCl3) δH 4,05-3,95 (м, 2H), 3,55-3,45 (м, 1H), 3,06 (с, 3H), 2,85-2,75 (м, 2H), 2,52-2,38 (м, 2H), 1,92-1,59 (м, 5H), 1,52-1,30 (м, 12H), 1,27 (с, 3H), 1,25-0,80 (м, 5H).
Синтез III-C13
[0668] Раствор III-C12 (40 мг, 0,094 ммол), K2CO3 (17,4 мг, 0,19 ммол) и 1H-пиразол-4-карбонитрила (25,8 мг, 0,19 ммол) перемешивали при 25°С в течение 2 часов. Смесь добавили в воду (100 мл) и экстрагировали EtOAc (3×20 мл). Объединенный органический раствор промыли водой (2×100 мл), насыщенным рассолом (100 мл), высушили над безводным Na2SO4, профильтровали и упарили. Остаток очистили на колонке для флэш-хроматографии (0-50% EtOAc в PE) с образованием III-C13 (5 мг, 12%) в виде твердого вещества. 1H-ЯМР (400 МГц, CDCl3) δH 7,82 (с, 1H), 7,80 (с, 1H), 5,28-5,20 (м, 1H), 4,92-4,85 (м, 1H), 3,55-3,45 (м, 1H), 3,02 (с, 3H), 2,92-2,82 (м, 1H), 2,65-2,35 (м, 3H), 1,90-1,59 (м, 7H), 1,52-1,30 (м, 11H), 1,28 (с, 3H), 1,25-1,02 (м, 4H); LC-ELSD/MS чистота 99%, MS ESI рассчитано для C26H38N3O3 [M+H]+ 440,3, найдено 440,3.
ПРИМЕР III-13: синтез 1-((3R,5R,8R,9R,10S,13R,14S,17S)-3-гидрокси-13-изобутил-3-(метоксиметил)гексадекагидро-1H-циклопента[a]фенантрен-17-ил)этан-1-она (III-D20)
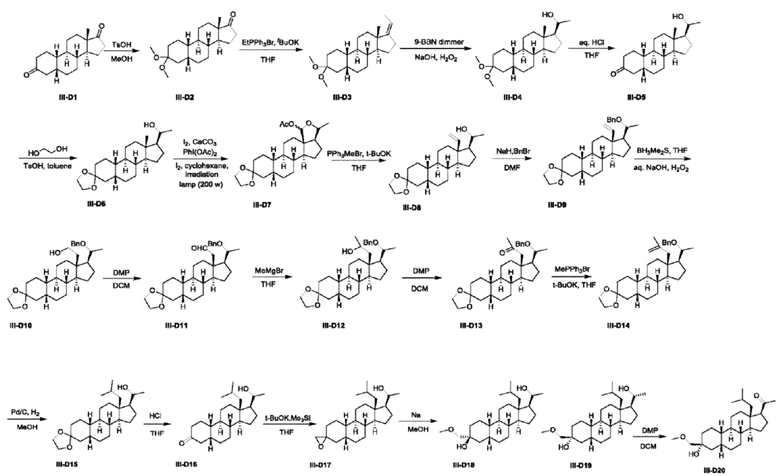
Синтез III-D2
[0669] К раствору III-D1 (300 г, 1093 ммол) в MeOH (2 л) при 25°С добавили 4-метилбензолсульфоновую кислоту (18,7 г, 109 ммол). После перемешивания при 65°С в течение 1 часа реакционную смесь охладили, и осадок выделили фильтрованием, и промыли метанолом (2×300 мл) с образованием III-D2 (230 г) в виде твердого вещества. 1H-ЯМР (400 МГц, CDCl3) δH 3,19 (с, 3H), 3,14 (с, 3H), 2,60-2,39 (м, 2H), 2,25-2,00 (м, 2H), 1,97-1,90 (м, 2H), 1,86-1,75 (м, 6H), 1,70-1,60 (м, 5H), 1,56-1,49 (м, 4H), 1,47-1,35 (м, 10H), 1,30-1,22 (м, 5H), 1,15-1,00 (м, 2H), 0,86 (с, 3H).
Синтез III-D3
[0670] К суспензии EtPPh3Br (798 г, 2,15 моля) в THF (1,5 л) добавили t-BuOK (241 г, 2,15 моля) при 25°С под N2. После перемешивания при 50°С в течение 30 минут добавили при 50°С раствор III-D2 (230 г, 717 ммол) в THF (500 мл). После перемешивания при 50°С в течение 16 часов реакционную смесь охладили до 25°С, разбавили насыщенным раствором NH4Cl (500 мл) и экстрагировали EtOAc (2×500 мл). Объединенный органический раствор промыли рассолом (2×500 мл), высушили над безводным Na2SO4, профильтровали и упарили. Остаток перекристаллизовали из метанола (1 л) и воды (1 л) с образованием III-D3 (290 г) в виде твердого вещества. 1H-ЯМР (400 МГц, CDCl3) δH 3,19 (с, 3H), 3,14 (с, 3H), 2,40-2,10 (м, 4H), 1,95-1,35 (м, 13H), 1,33-1,05 (м, 10H), 0,87 (с, 3H).
Синтез III-D4
[0671] К раствору III-D3 (275 г, 826 ммол) в THF (2 л) добавили 9-BBN-димер (402 г, 1,65 моля) при 25°С. После перемешивания при 50°С в течение 2 часов реакционную смесь охладили до 0°С, и очень медленно добавили этанол (379 г, 8,26 моля) и NaOH (1,65 л, 5 M, 8,26 моля). После завершения добавления медленно добавили H2O2 (825 мл, 8,26 моля, 30%), поддерживая внутреннюю температуру ниже 15°С. После перемешивания при 75°С в течение 1 часа реакционную смесь залили насыщенным водным раствором Na2S2O3 (260 мл) и перемешивали при 0°С в течение 1 часа. Смесь разбавили водой (2 л) и профильтровали. Осадок на фильтре промыли водой (3×700 мл), высушили в вакууме с образованием III-D4 (285 г) в виде твердого вещества. 1H-ЯМР (400 МГц, CDCl3) δH 3,17-3,09 (м, 6H), 1,96-1,77 (м, 8H), 1,64-1,29 (м, 11H), 1,24-0,91 (м, 10H), 0,63 (с, 3H).
Синтез III-D5
[0672] К раствору III-D4 (285 г, 813 ммол) в THF (3 л) при 20°С добавили водную HCl (1,62 л, 1,62 моля, 1 M). После перемешивания в течение 1 часа смесь разбавили водой (700 мл) и экстрагировали DCM (2×500 мл). Объединенный органический раствор промыли рассолом (2×500 мл), высушили над безводным Na2SO4, профильтровали, упарили с получением III-D5 (280 г) в виде твердого вещества. 1H-ЯМР (400 МГц, CDCl3) δH 3,75-3,65 (м, 1H), 2,65-2,55 (м, 1H), 2,30-2,10 (м, 1H), 2,00-1,80 (м, 5H), 1,75-1,42 (м, 10H), 1,40-1,28 (м, 4H), 1,29-1,15 (м, 7H), 0,66 (с, 3H).
Синтез III-D6
[0673] К раствору III-D6 (14 г, 45,9 ммол) в толуоле (200 мл) при 25°С добавили TsOH (787 мг, 4,6 ммол) и этан-1,2-диол (28,4 г, 458 моля) под N2. После перемешивания при 120°С в течение 4 часов смесь вылили в воду (100 мл) и экстрагировали этилацетатом (2×100 мл). Объединенный органический раствор промыли рассолом (100 мл), высушили над безводным Na2SO4, профильтровали и упарили в вакууме. Остаток очистили на колонке для флэш-хроматографии (5-10% EtOAc в PE) с образованием III-D6 (8 г, 50%) в виде твердого вещества. 1H-ЯМР (400 МГц, CDCl3) δH 3,93 (с, 4H), 3,76-3,63 (м, 1H), 2,03-1,95 (м, 1H), 1,93-1,80 (м, 4H), 1,64-1,58 (м, 3H), 1,56-1,48 (м, 2H), 1,44-1,30 (с, 6H), 1,27-0,95 (м, 12H), 0,66 (м, 3H).
Синтез III-D7
[0674] К раствору III-D6 (2,0 г, 5,7 ммол), PhI(OAc)2 (5,50 г, 17,1 ммол) и CaCO3 (1,71 г, 17,1 ммол) в циклогексане (200 мл) при 25°С добавили I2 (2,89 г, 11,4 ммол). Смесь нагрели до 80°С облучением инфракрасной лампой (200 Вт) в течение 10 минут. Смесь очистили вместе с еще одной подобной реакционной смесью (2 г). Смесь добавили в насыщенный раствор Na2S2O3 (1000 мл) и экстрагировали EtOAc (3×300 мл). Объединенный органический раствор промыли насыщенным рассолом (1000 мл), высушили над безводным Na2SO4, профильтровали и упарили с образованием III-D7 (4,6 г) в виде масла. 1H-ЯМР (400 МГц, CDCl3) δH 5,95 (с, 1H), 4,35-4,40 (м, 1H), 3,92 (с, 4H), 2,40-2,30 (м, 1H), 2,25-2,05 (м, 3H), 2,00-1,70 (м, 12H), 1,50-1,35 (м, 7H), 1,30-1,00 (м, 6H), 0,90-0,70 (м, 1H).
Синтез III-D8
[0675] К раствору PPh3MeBr (20,2 г, 56,8 ммол) и t-BuOK (6,36 г, 56,8 ммол) в THF (30 мл), перемешиваемому в течение 1 часа, добавили раствор III-D7 (2,3 г, 5,7 ммол) в THF (20 мл). После перемешивания в течение 12 часов при 50°С раствор очистили вместе с еще одной партией (из 2,3 г). Смесь добавили к насыщенному раствору NH4Cl (200 мл) и экстрагировали EtOAc (3×50 мл). Объединенный органический раствор промыли насыщенным рассолом (100 мл), высушили над безводным Na2SO4, профильтровали и упарили. Остаток очистили хроматографией на силикагеле (0-20% EtOAc в PE) с образованием III-D8 (2,3 г) в виде масла. 1H-ЯМР (400 МГц, CDCl3) δH 5,77 (дд, J=11,2, 18,0 Гц, 1H), 5,28 (д, J=10,8 Гц, 1H), 5,14 (д, J=18,0 Гц, 1H), 3,93 (с, 4H), 3,90-3,85 (м, 1H), 2,40-2,30 (м, 1H), 2,00-1,90 (м, 1H), 1,90-1,65 (м, 6H), 1,60-1,50 (м, 3H), 1,50-1,40 (м, 1H), 1,35-0,80 (м, 16H).
Синтез III-D9
[0676] К раствору III-D8 (2,0 г, 5,5 ммол) в DMF (20 мл) добавили NaH (438 мг, 11,0 ммол, 60% в минеральном масле) при 0°С. После перемешивания при 20°С в течение 1 часа к смеси при 20°С добавили BnBr (2,36 г, 13,8 ммол). После перемешивания при 60°С в течение 10 часов смесь вылили в воду (50 мл) и экстрагировали EtOAc (2×50 мл). Объединенный органический раствор промыли рассолом (3×50 мл), высушили над безводным Na2SO4, профильтровали и упарили. Остаток очистили на колонке для флэш-хроматографии (0-40% EtOAc в PE) с образованием III-D9 (2,0 г, 80,3%) в виде масла. 1H-ЯМР (400 МГц, CDCl3) δH 7,34-7,25 (м, 5H), 5,66-5,56 (м, 1H), 5,27-5,17 (м, 1H), 5,08-5,01 (м, 1H), 4,57-4,26 (м, 2H), 3,93 (с, 4H), 3,27-3,14 (м, 1H), 2,39-2,34 (м, 1H), 1,96 (с, 2H), 1,90-1,78 (м, 3H), 1,61-1,54 (м, 4H), 1,48-1,34 (м, 10H), 1,20-1,14 (м, 5H), 1,06-0,99 (м, 2H).
Синтез III-D10
[0677] К раствору III-D9 (2,0 г, 4,4 ммол) в THF (20 мл) добавили BH3·Me2S (2,21 мл, 10 M, 22,1 ммол). После перемешивания при 25°С в течение 16 часов медленно добавили EtOH (2,55 мл, 44,3 ммол), затем водный раствор NaOH (1,77 г в 8,86 мл воды, 44,3 ммол) и водный раствор H2O2 (4,43 мл, 10 M, 44,3 ммол). После перемешивания при 70°С в течение 1 часа смесь залили раствором Na2SO3 (80 мл, 10%) и экстрагировали EtOAc (2×100 мл). Объединенный органический раствор высушили над Na2SO4, профильтровали и упарили, и очистили на колонке для флэш-хроматографии (0~30% EtOAc в PE) с образованием III-D10 (1,4 г, 67,6%) в виде твердого вещества. 1H-ЯМР (400 МГц, CDCl3) δ 7,37-7,31 (м, 4H), 7,28-7,24 (м, 1H), 4,66 (д, J=11,2 Гц, 1H), 4,32 (д, J=11,2 Гц, 1H), 3,93 (с, 4H), 3,68-3,46 (м, 3H), 2,02-1,74 (м, 6H), 1,70-1,57 (с, 5H), 1,52-1,33 (м, 9H), 1,28-1,23 (м, 2H), 1,21-1,03 (м, 5H), 1,02-0,92 (м, 3H)
Синтез III-D11
[0678] К раствору III-D10 (1,4 г, 2,98 ммол) в DCM (50 мл) добавили DMP (2,52 г, 5,96 ммол). После перемешивания при 20°С в течение 1 часа смесь добавили к насыщенному раствору NaHCO3 (200 мл) и экстрагировали DCM (3×50 мл). Объединенный органический раствор промыли насыщенным раствором Na2S2O3 (2×200 мл), насыщенным рассолом (200 мл), высушили над безводным Na2SO4, профильтровали и упарили с образованием III-D11 (1,4 г) в виде масла. 1H-ЯМР (400 МГц, CDCl3) δH 9,66 (с, 1H), 7,40-7,27 (м, 4H), 7,25-7,15 (м, 1H), 4,56 (д, J=11,6 Гц, 1H), 4,23 (д, J=11,6 Гц, 1H), 3,93 (с, 4H), 3,80-3,70 (м, 1H), 2,55-2,40 (м, 2H), 2,30-2,20 (м, 1H), 2,10-1,60 (м, 9H), 1,52-1,25 (м, 8H), 1,22 (д, J=6,0 Гц, 3H), 1,20-0,92 (м, 6H).
Синтез III-D12
[0679] К раствору III-D11 (1,4 г, 3,0 ммол) в THF (20 мл) при 0°С добавили MeMgBr (5 мл, 3 M в Et2O, 15,0 ммол). После перемешивания при 20°С в течение 1 часа смесь добавили к насыщенному раствору NH4Cl (200 мл) и экстрагировали EtOAc (3×50 мл). Объединенный органический раствор промыли насыщенным рассолом (200 мл), высушили над безводным Na2SO4, профильтровали и упарили с образованием III-D12 (1,3 г) в виде масла. 1H-ЯМР (400 МГц, CDCl3) δH 7,35-7,28 (м, 4H), 7,25-7,16 (м, 1H), 4,61 (д, J=12,0 Гц, 1H), 4,34 (д, J=11,6 Гц, 1H), 3,93 (с, 4H), 3,91-3,75 (м, 1H), 3,54-3,40 (м, 1H), 2,40-2,25 (м, 1H), 2,00-1,60 (м, 8H), 1,52-1,20 (м, 14H), 1,18-0,80 (м, 10H).
Синтез III-D13
[0680] К раствору III-D12 (1,8 г, 3,7 ммол) в DCM (40 мл) добавили периодинан Десса-Мартина (DMP) (3,15 г, 7,4 ммол). После перемешивания при 20°С в течение 1 часа смесь добавили к насыщенному раствору NaHCO3 (300 мл) и экстрагировали DCM (3×50 мл). Объединенный органический раствор промыли насыщенным раствором Na2S2O3 (2×300 мл), насыщенным рассолом (300 мл), высушили над безводным Na2SO4, профильтровали и упарили с образованием III-D13 (1,8 г) в виде масла. 1H-ЯМР (400 МГц, CDCl3) δH 7,40-7,28 (м, 4H), 7,25-7,16 (м, 1H), 4,51 (д, J=12,0 Гц, 1H), 4,11 (д, J=12,0 Гц, 1H), 3,93 (с, 4H), 3,13-3,02 (м, 1H), 2,44 (д, J=18,4 Гц, 1H), 2,29 (д, J=19,2 Гц, 1H), 2,10-1,78 (м, 8H), 1,76 (с, 3H), 1,52-1,11 (м, 15H), 1,10-0,75 (м, 4H).
К раствору MePh3PBr (6,67 г, 18,7 ммол) в THF (30 мл) добавили t-BuOK (2,09 г, 18,7 ммол) при 20°С. После перемешивания при 50°С в течение 1 часа к реакционной смеси при температуре ниже 50°С добавили раствор III-D13 (1,8 г, 3,7 ммол) в THF (20 мл). После перемешивания при 50°С в течение 16 часов смесь добавили к насыщенному раствору NH4Cl (200 мл) и экстрагировали EtOAc (3×50 мл). Объединенный органический раствор промыли насыщенным рассолом (200 мл), высушили над безводным Na2SO4, профильтровали и упарили. Остаток очистили на колонке для флэш-хроматографии (0-5% EtOAc в PE) с образованием III-D14 (1,2 г, 67%) в виде масла. 1H-ЯМР (400 МГц, CDCl3) δH 7,40-7,28 (м, 4H), 7,25-7,16 (м, 1H), 4,77 (с, 1H), 4,71 (с, 1H), 4,57 (д, J=11,6 Гц, 1H), 4,34 (д, J=11,2 Гц, 1H), 3,93 (с, 4H), 3,90-3,75 (м, 1H), 2,36 (д, J=11,6 Гц, 1H), 2,20-1,80 (м, 9H), 1,78-1,59 (м, 4H), 1,52-1,25 (м, 9H), 1,23-1,19 (м, 3H), 1,15-0,80 (м, 6H).
Синтез III-D15 и III-D15a
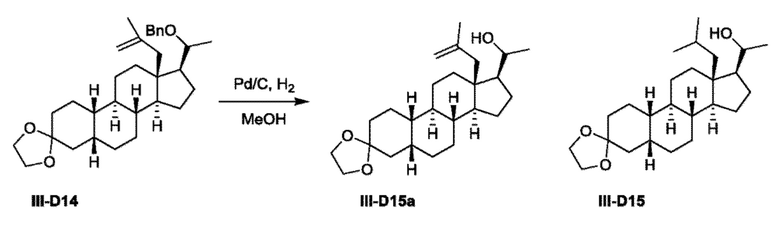
К раствору III-D14 (1,2 г, 2,5 ммол) в MeOH (20 мл) добавили Pd/C (200 мг, 10% в воде) при 25°С. После перемешивания при 25°С в течение 16 часов под H2 (50 psi (0,35 МПа)), смесь профильтровали, и маточную жидкость упарили. Остаток очистили на колонке для флэш-хроматографии (0-10% EtOAc в PE) с образованием III-D15a (400 мг, 41%) и III-D15 (300 мг, 31%), оба в виде масел.
К раствору III-15a (400 мг, 1,0 ммол) в MeOH (10 мл) добавили Pd/C (100 мг, 10% в воде) при 25°С. После перемешивания при 50°С в течение 16 часов под H2 (50 psi (0,35 МПа)), смесь профильтровали, и осадок на фильтре промыли MeOH (3×30 мл). Маточную жидкость упарили с образованием III-D15 (300 мг) в виде масла. 1H-ЯМР (400 МГц, CDCl3) δH 3,93 (с, 4H), 3,84-3,71 (м, 1H), 2,25-2,15 (м, 1H), 2,08-1,60 (м, 8H), 1,52-1,33 (м, 9H), 1,31 (д, J=6,0 Гц, 3H), 1,28-1,02 (м, 10H), 0,97 (д, J=6,4 Гц, 3H), 0,92 (д, J=6,8 Гц, 3H).
Синтез III-D16
[0681] Раствор III-D15 (600 мг, 1,5 ммол) и водной HCl (3 мл, 2 M, 6,0 ммол) в THF (5 мл) перемешивали при 20°С в течение 1 часа. Смесь добавили в насыщенный раствор NaHCO3 (150 мл) и экстрагировали EtOAc (3×50 мл). Объединенный органический раствор промыли насыщенным рассолом (150 мл), высушили над безводным Na2SO4, профильтровали и упарили с образованием III-D16 (500 мг) в виде масла. 1H-ЯМР (400 МГц, CDCl3) δH 3,90-3,75 (м, 1H), 2,59 (т, J=14,0 Гц, 1H), 2,35-2,05 (м, 6H), 2,00-1,60 (м, 5H), 1,50-1,35 (м, 4H), 1,32 (д, J=5,6 гц, 3H), 1,30-1,03 (м, 12H), 1,00 (д, J=6,4 Гц, 3H), 0,94 (д, J=6,8 Гц, 3H).
Синтез III-D17
[0682] К раствору t-BuOK (581 мг, 5,2 ммол) и Me3SI (1,05 г, 5,2 ммол) в THF (15 мл) добавили III-D16 (600 мг, 1,7 ммол). После перемешивания при 20°С в течение 1 часа реакционную смесь разбавили водой (200 мл) и экстрагировали EtOAc (3×50 мл). Объединенный органический раствор промыли насыщенным рассолом (200 мл), высушили над безводным Na2SO4, профильтровали и упарили с образованием III-D17 (540 мг) в виде масла. 1H-ЯМР (400 МГц, CDCl3) δH 3,85-3,70 (м, 1H), 2,65-2,55 (м, 2H), 2,30-2,15 (м, 2H), 2,03-1,59 (м, 9H), 1,52-1,35 (м, 5H), 1,32 (д, J=6,0 Гц, 3H), 1,30-1,02 (м, 10H), 0,99 (д, J=6,4 Гц, 3H), 0,93 (д, J=6,8 Гц, 3H), 0,91-0,80 (м, 2H).
Синтез III-D18 и III-D19
[0683] В MeOH (30 мл) при 20°С добавили Na (716 мг, 29,8 ммол). После перемешивания при 70°С в течение 3 часов добавили раствор III-D17 (540 мг, 1,5 ммол) в MeOH (10 мл). После перемешивания при 70°С в течение 5 часов смесь добавили в насыщенный раствор NH4Cl (150 мл) и экстрагировали EtOAc (3×50 мл). Объединенный органический раствор промыли насыщенным рассолом (150 мл), высушили над безводным Na2SO4, профильтровали и упарили. Остаток очистили на колонке для флэш-хроматографии (0-25% EtOAc в PE) с образованием III-D18 (150 мг, 26%) и III-D19 (250 мг, 43%), оба в виде масел. Стереохимическая конфигурация при C3 была приписана на основе H-ЯМР.
III-D18: 1H-ЯМР (400 МГц, CDCl3) δH 3,90-3,75 (м, 1H), 3,39 (с, 3H), 3,20 (с, 2H), 2,25-2,10 (м, 2H), 1,99 (с, 1H), 1,98-1,58 (м, 8H), 1,52-1,34 (м, 6H), 1,31 (д, J=6,0 гц, 3H), 1,28-1,02 (м, 12H), 0,98 (д, J=6,4 Гц, 3H), 0,92 (д, J=6,8 Гц, 3H).
III-D19: 1H-ЯМР (400 МГц, CDCl3) δH 3,88-3,72 (м, 1H), 3,48-3,30 (м, 5H), 2,57 (с, 1H), 2,19 (д, J=9,2 Гц, 1H), 2,00-1,60 (м, 8H), 1,50-1,34 (м, 6H), 1,31 (д, J=5,6 Гц, 3H), 1,28-1,02 (м, 12H), 0,98 (д, J=6,4 Гц, 3H), 0,92 (д, J=6,4 Гц, 3H), 0,90-0,85 (м, 1H); LC-ELSD/MS чистота 99%, 100% по данным H-ЯМР; MS ESI рассчитано для C25H41O [M-2H2O+H]+ 357,3, найдено 357,3.
Синтез III-D20
[0684] К раствору III-D19 (230 мг, 0,59 ммол) в DCM (10 мл) добавили DMP (496 мг, 1,2 ммол). После перемешивания при 20°С в течение 1 часа смесь добавили в насыщенный раствор NaHCO3 (100 мл) и экстрагировали DCM (3×50 мл). Объединенный органический раствор промыли насыщенным раствором Na2S2O3 (2×100 мл), насыщенным рассолом (100 мл), высушили над безводным Na2SO4, профильтровали и упарили. Остаток очистили на колонке для флэш-хроматографии (0-25% EtOAc в PE) с образованием III-D20 (132 мг, 58%) в виде твердого вещества. 1H-ЯМР (400 МГц, CDCl3) δH 3,45-3,35 (м, 5H), 2,61 (с, 1H), 2,48-2,36 (м, 2H), 2,30-2,15 (м, 4H), 1,90-1,59 (м, 8H), 1,52-1,32 (м, 7H), 1,30-1,05 (м, 9H), 0,93 (д, J=6,4 Гц, 3H), 0,78 (д, J=6,4 Гц, 3H); LC-ELSD/MS чистота 99%, MS ESI рассчитано для C25H41O2 [M-H2O+H]+ 373,3, найдено 373,3.
ПРИМЕР III-14: синтез 1-(2-((3R,5R,8R,9R,10S,13R,14S,17S)-3-гидрокси-13-изобутил-3-(метоксиметил)гексадекагидро-1H-циклопента[a]фенантрен-17-ил)-2-оксоэтил)-1H-пиразол-4-карбонитрила (III-D22)
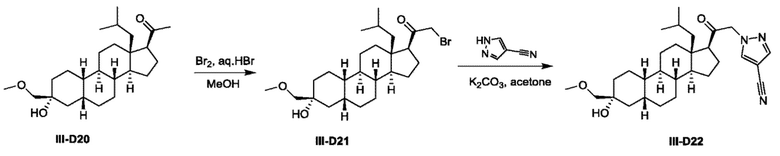
Синтез III-D21
[0685] К раствору III-D21 (117 мг, 0,3 ммол) и HBr (11,9 мг, 0,06 ммол, 40%) в MeOH (5 мл) при 0°С добавили Br2 (47,9 мг, 0,3 ммол). После перемешивания при 20°С в течение 3 часов смесь добавили в насыщенный раствор NaHCO3 (100 мл) и экстрагировали EtOAc (3×50 мл). Объединенный органический раствор промыли насыщенным рассолом (100 мл), высушили над безводным Na2SO4, профильтровали и упарили с образованием III-D21 (180 мг) в виде масла, которое использовали как есть.
Синтез III-D22
[0686] К раствору III-D22 (180 мг, 0,38 ммол) в ацетоне (5 мл) добавили 1H-пиразол-4-карбонитрил (106 мг, 1,1 ммол) и K2CO3 (157 мг, 1,1 ммол). После перемешивания при 20°С в течение 16 часов смесь добавили в насыщенный раствор NH4Cl (100 мл) и экстрагировали EtOAc (3×30 мл). Объединенный органический раствор промыли водой (2×100 мл), насыщенным рассолом (100 мл), высушили над безводным Na2SO4, профильтровали и упарили. Остаток очистили на колонке для флэш-хроматографии (0-40% EtOAc в PE) с образованием III-D2 (24,5 мг, 13%) в виде твердого вещества. 1H-ЯМР (400 МГц, CDCl3) δH 7,86 (с, 1H), 7,80 (с, 1H), 5,22 (д, J=18,0 Гц, 1H), 4,90 (д, J=17,6 Гц, 1H), 3,48-3,35 (м, 5H), 2,50-2,40 (м, 2H), 2,35-2,22 (м, 1H), 1,95-1,55 (м, 13H), 1,53-1,00 (м, 12H), 0,95 (д, J=6,4 Гц, 3H), 0,67 (д, J=6,4 Гц, 3H); LC-ELSD/MS чистота 99%, MS ESI рассчитано для C29H42N3O2 [M-H2O+H]+ 464,3, найдено 464,3.
Ингибирование стероидами связывания TBPS
[0687] Были описаны анализы связывания [35S]-трет-бутилбициклофосфоротионата (TBPS) с использованием кортикальных мембран головного мозга крысы в присутствии 5 мкМ GABA (Gee и др., J. Pharmacol. Exp. Ther., 1987, том 241, стр. 346-353; Hawkinson и др., Mol. Pharmacol., 1994, том 46, стр. 977-985; Lewin A.H. и др., Mol. Pharmacol., 1989, том 35, стр. 189-194).
[0688] Вкратце, после декапитации под наркозом диоксидом углерода у крыс Sprague-Dawley (200-250 г) быстро извлекают кору головного мозга. Кору головного мозга гомогенизируют в 10 объемах охлажденного льдом 0,32 М раствора сахарозы с использованием стеклянного/тефлонового гомогенизатора и центрифугируют при 1500×g в течение 10 мин при 4°С. Полученные супернатанты центрифугируют при 10000×g в течение 20 мин при 4°С с образованием осадков Р2. Осадки Р2 ресуспендируют в смеси 200 мМ NaCl/50 мМ Na-K-фосфатный буфер, рН 7,4, и центрифугируют при 10000×g в течение 10 мин при 4°С. Такую процедуру промывания повторяют дважды, и осадки ресуспендируют в 10 объемах буфера. Аликвоты (100 мкл) мембранных суспензий инкубируют с 3 нМ [35S]-TBPS и 5-мл аликвотами испытуемого лекарственного препарата, растворенного в диметилсульфоксиде (ДМСО) (конечная концентрация 0,5%), в присутствии 5 мкМ GABA. Смесь для инкубации доводят до конечного объема 1,0 мл буфером. Неспецифическое связывание определяют в присутствии 2 мкМ немеченого TBPS и в интервале от 15 до 25%. После 90-мин инкубации при комнатной температуре анализы прерывают фильтрацией через стеклянные фильтры (Schleicher and Schuell, № 32) с использованием харвестера клеток (Brandel) и трижды промывают охлажденным льдом буфером. Радиоактивность, связанную с фильтром, измеряют жидкостной сцинтилляционной спектрометрией. С использованием Prism (GraphPad) осуществляют подбор нелинейной кривой по всем данным для каждого лекарственного средства, усредненных для каждой концентрации. Данные подбирают для частичной модели ингибирования вместо полной, если сумма квадратов является существенно меньшей по F-критерию. Подобным образом, данные подбирают для двухкомпонентной модели ингибирования вместо однокомпонентной, если сумма квадратов является значительно меньшей по F-критерию. Концентрацию испытуемого соединения, создающую 50%-ное ингибирование (IC50) специфического связывания и максимальную степень ингибирования (Imax), определяют для индивидуальных экспериментов с той же моделью, которую используют для всех данных, и затем рассчитывают среднее±SEM в отдельных экспериментах. В качестве положительного контроля для таких исследований служит пикротоксин, так как было продемонстрировано, что он устойчиво ингибирует связывание TBPS.
[0689] Различные соединения скринируют или могут быть скринированы in vitro для определения их потенциала как модуляторов связывания [35S]-TBPS. Такие анализы проводятся или могут быть выполнены в соответствии с вышеизложенным.
[0690] Пример I-10: связывание TBPS
[0691] Ниже в Таблице I-1 А означает TBPS IC50 (мкМ) <0,01 мкМ, B означает TBPS IC50 (мкМ) от 0,01 мкМ до <0,1 мкМ, C означает TBPS IC50 (мкМ) от 0,1 мкМ до <1,0 мкМ, D означает TBPS IC50 (мкМ) от 1,0 мкМ до <10 мкМ, и E означает ≥10 мкМ.
[0692]
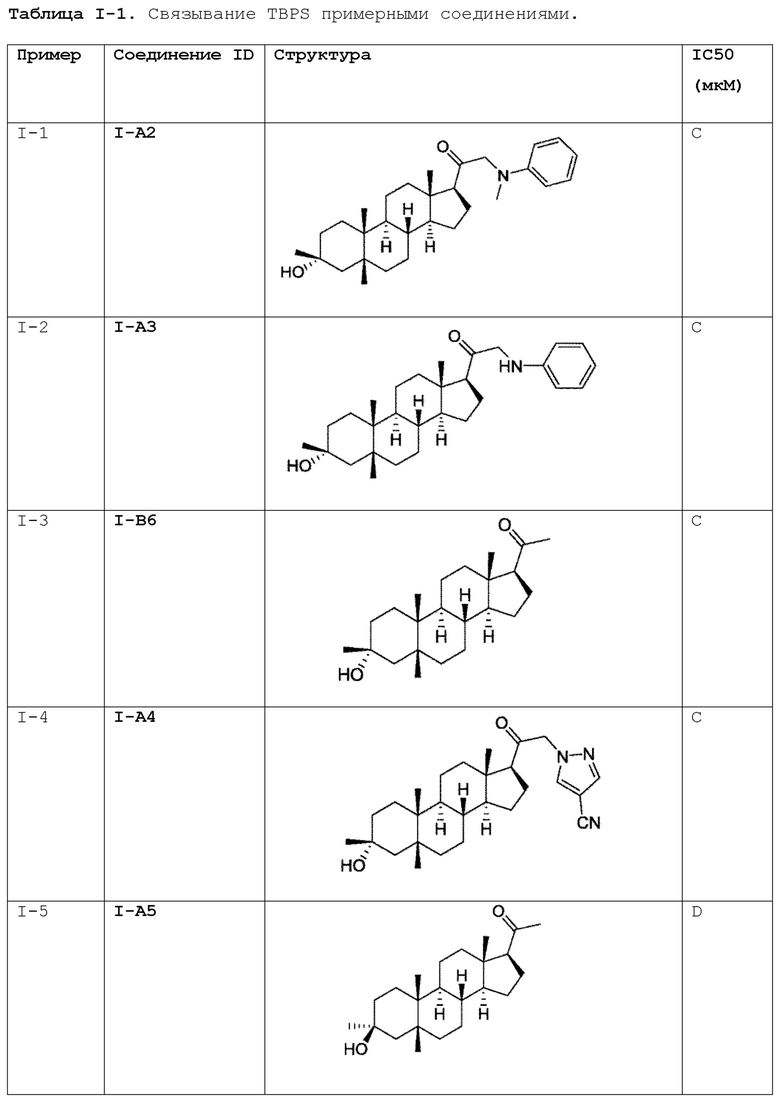
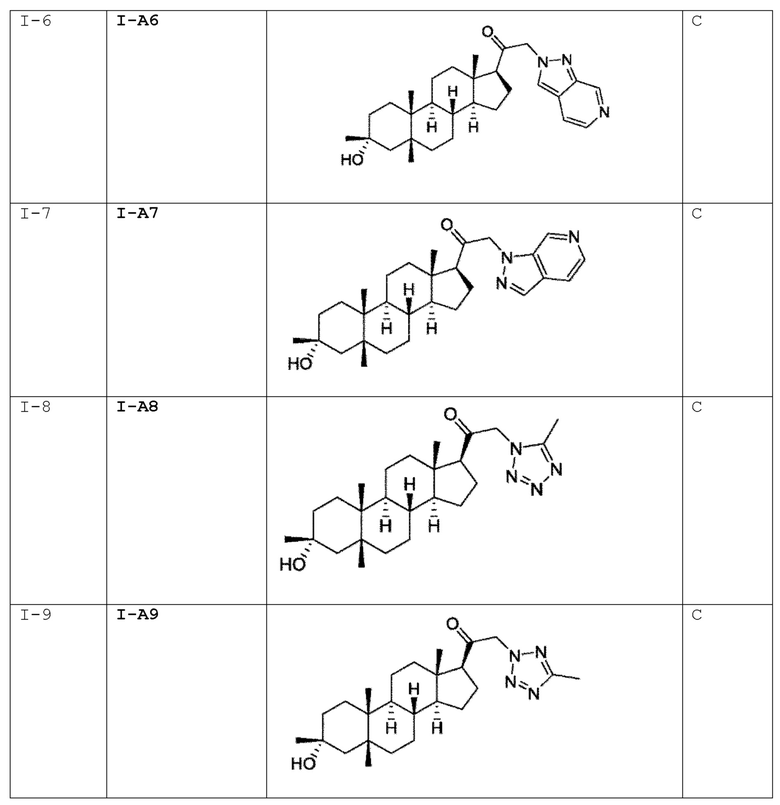
ПРИМЕР II-82
[0693] Ниже в Таблице II-2 А означает TBPS IC50 (мкМ) <0,01 мкМ, B означает TBPS IC50 (мкМ) от 0,01 мкМ до <0,1 мкМ, C означает TBPS IC50 (мкМ) от 0,1 мкМ до <1,0 мкМ, D означает TBPS IC50 (мкМ) от 1,0 мкМ до <10 мкМ, и E означает ≥10 мкМ.
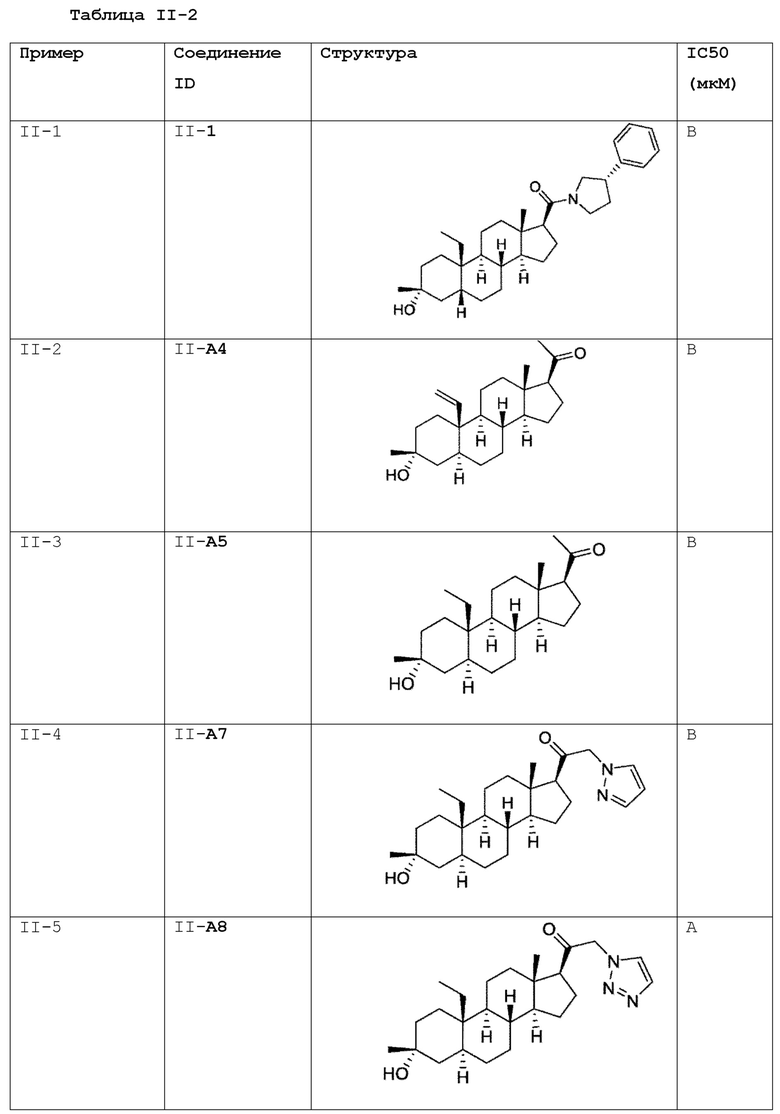
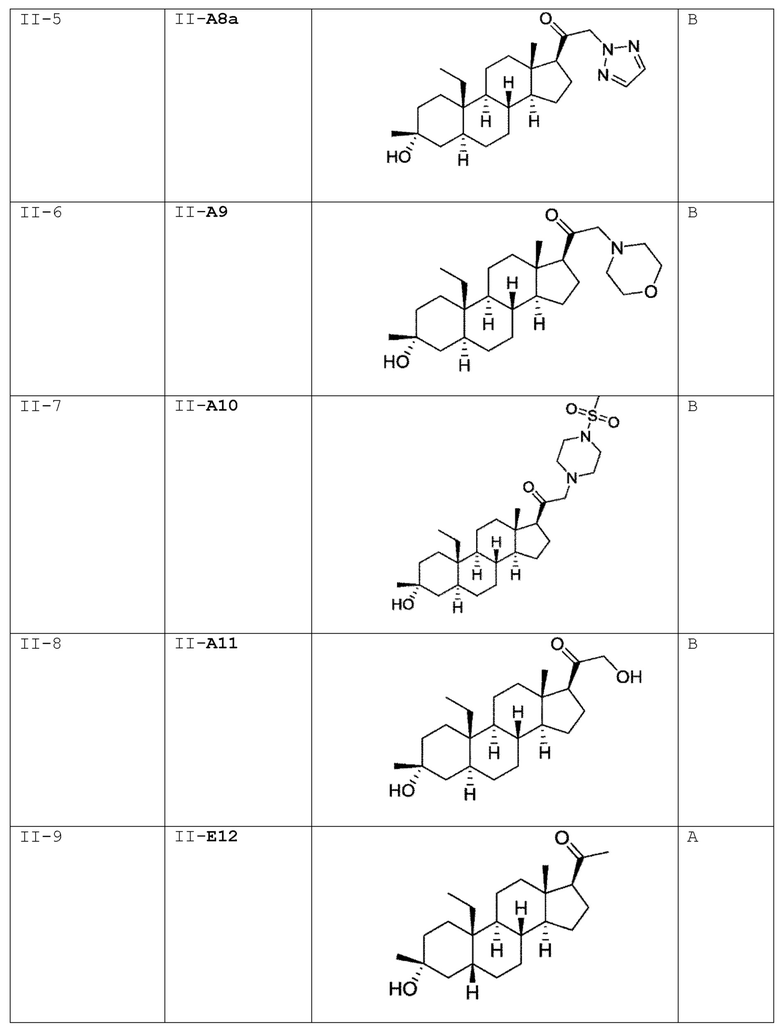
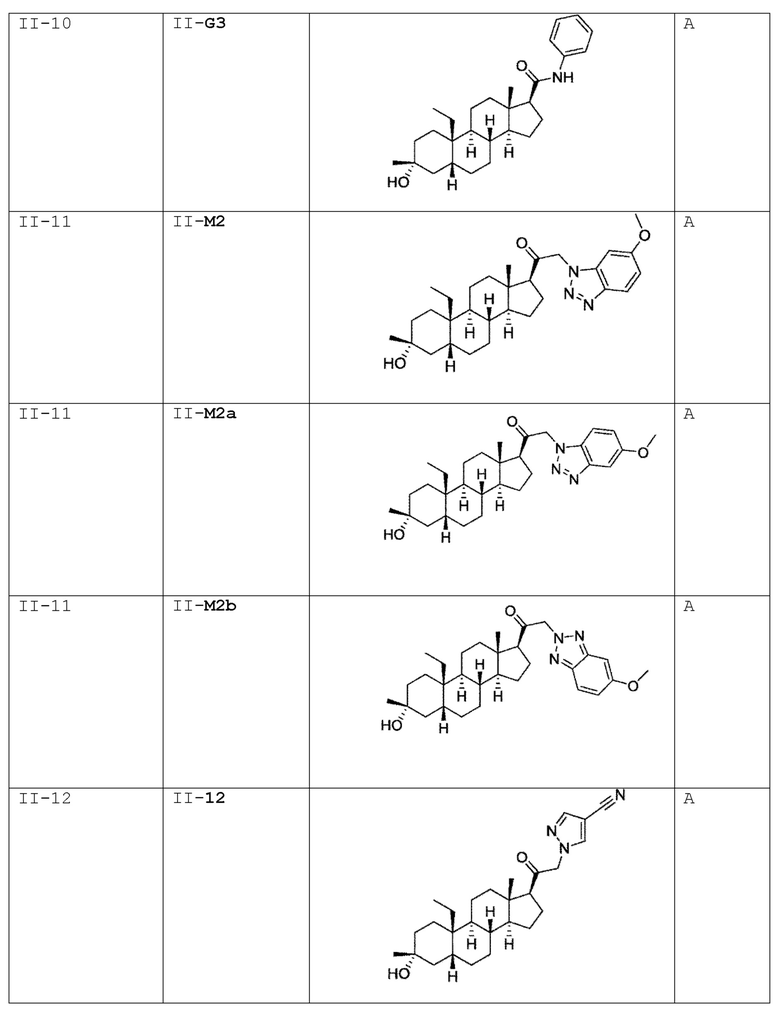
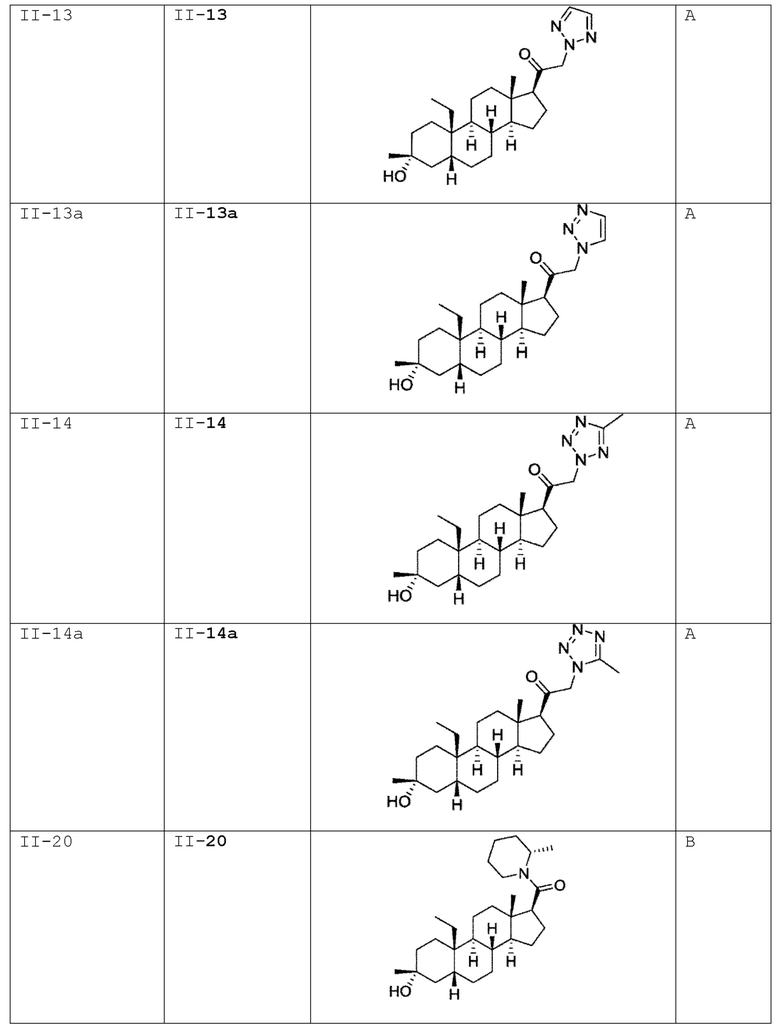
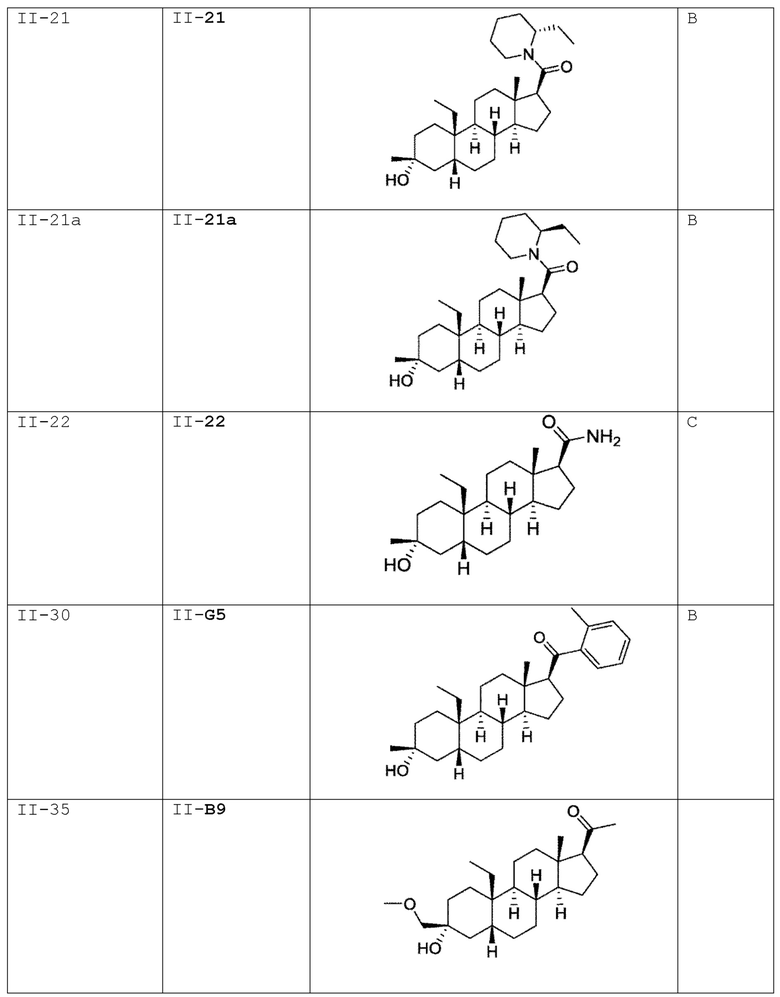
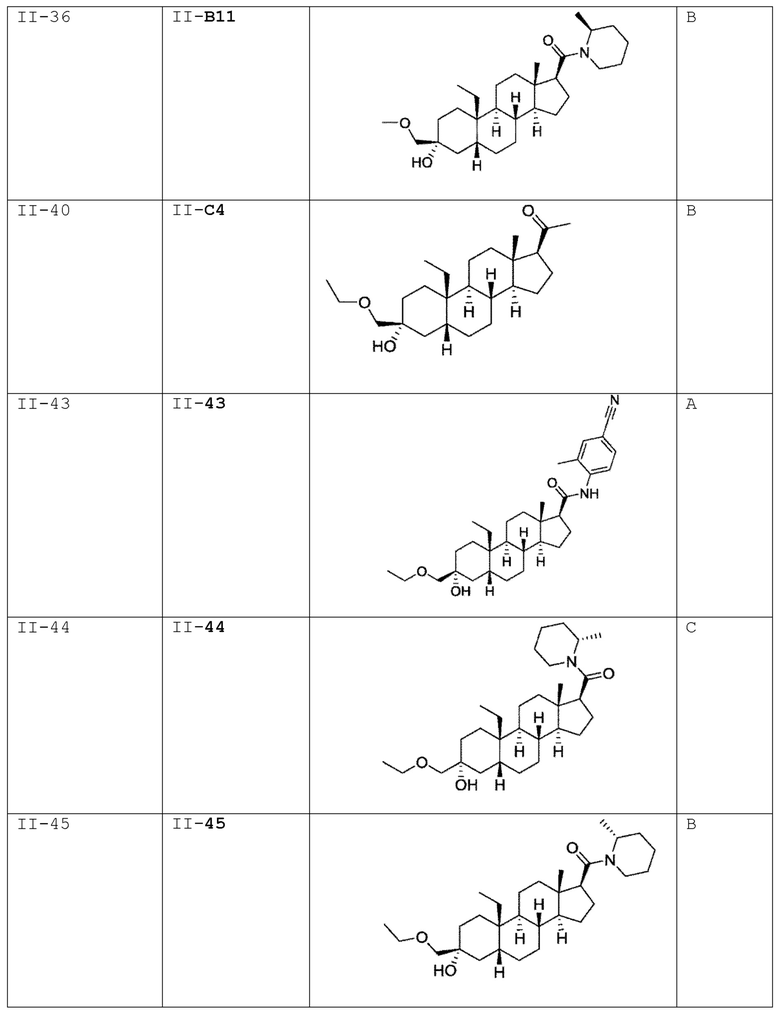
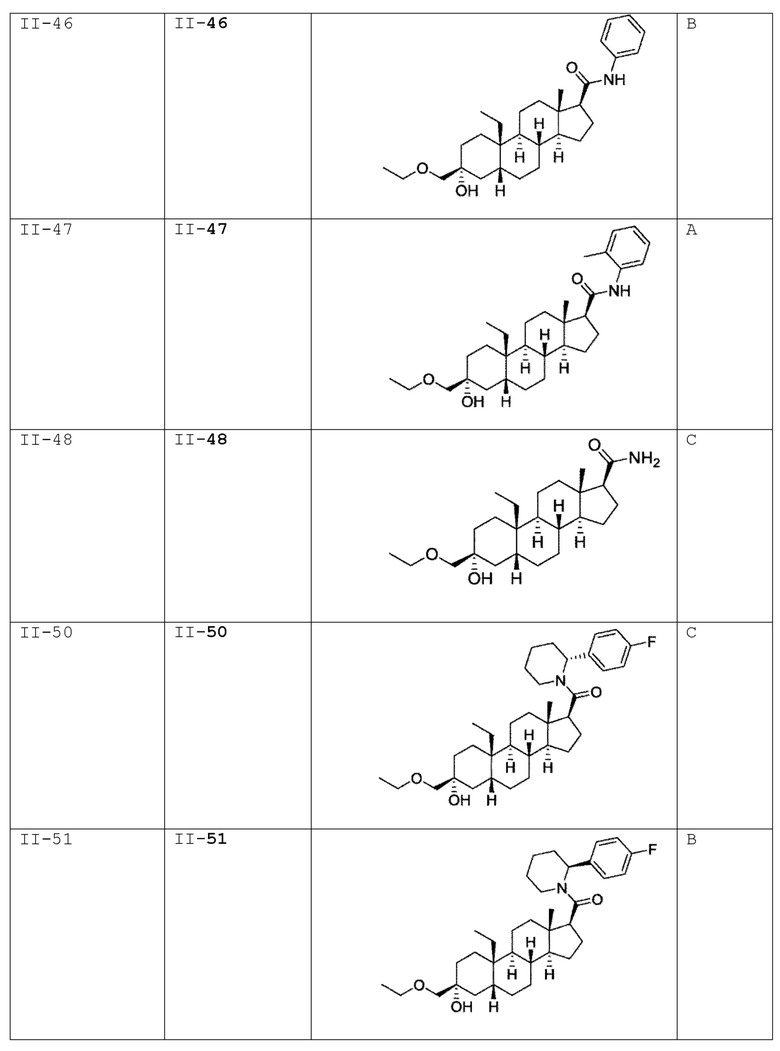
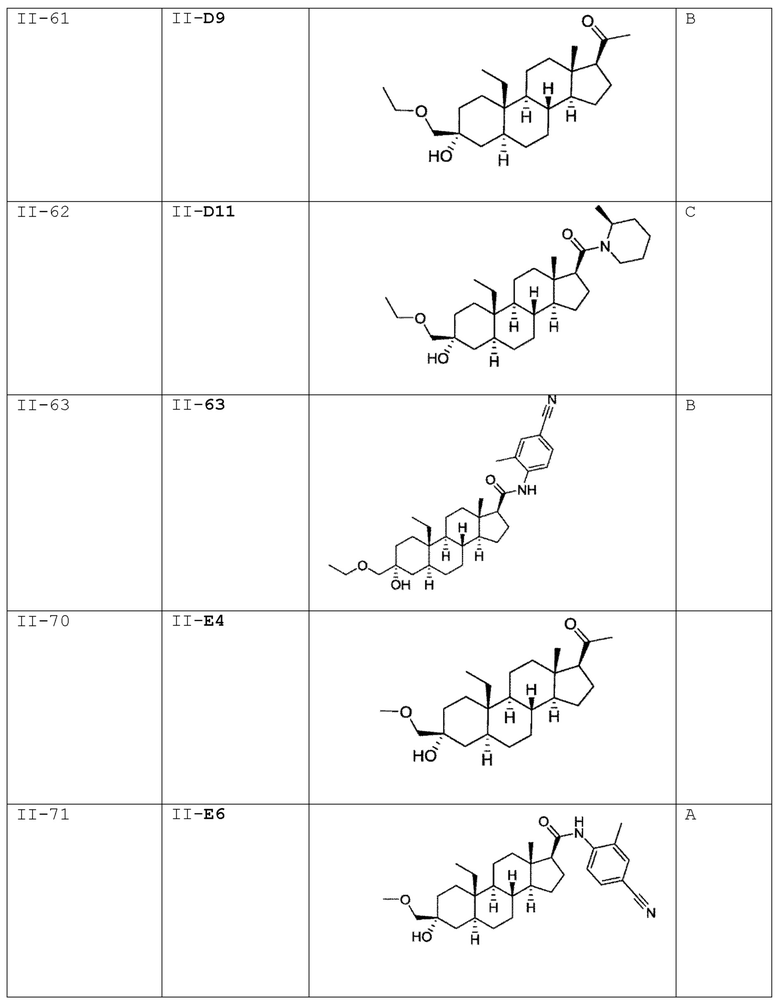
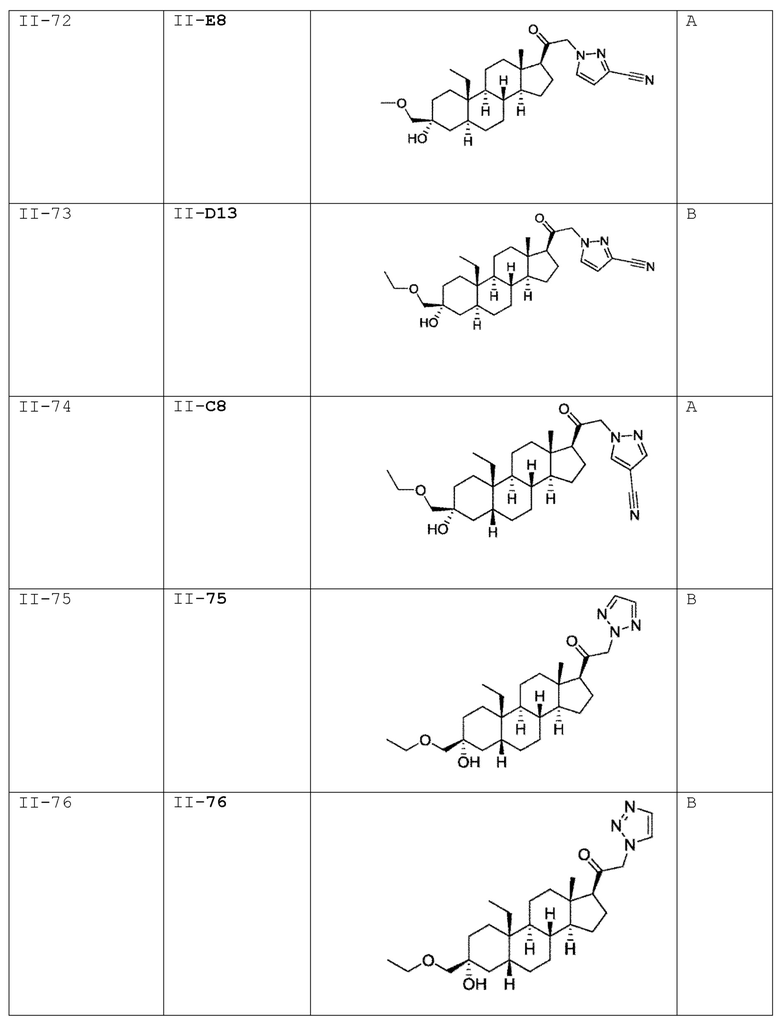
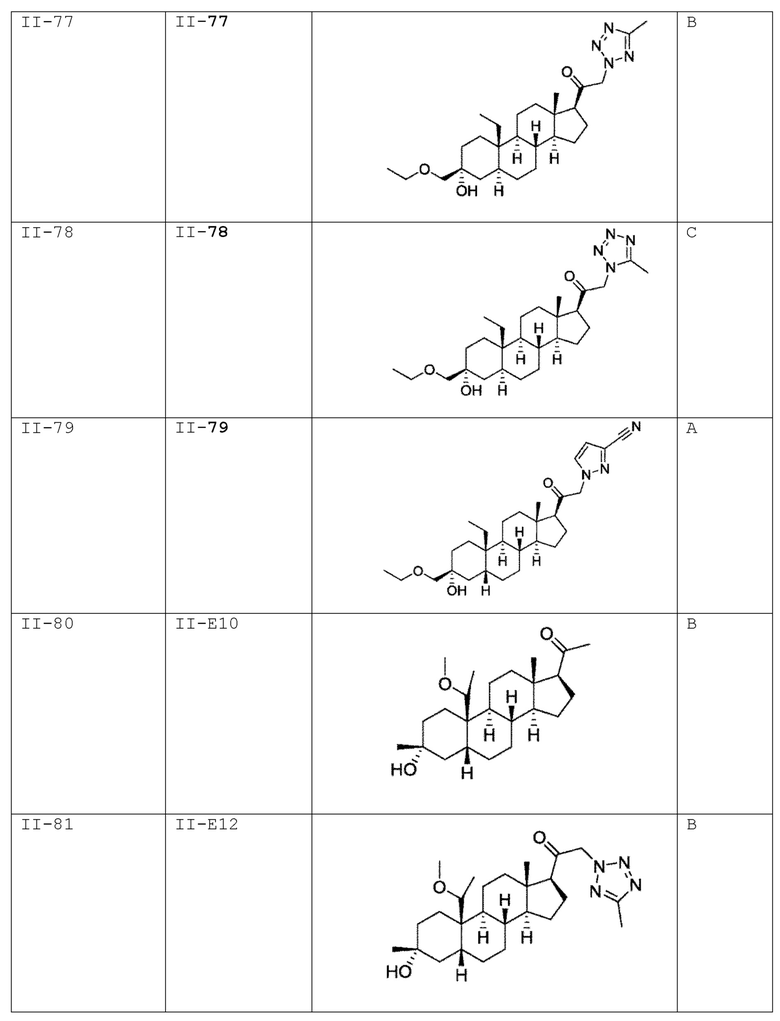
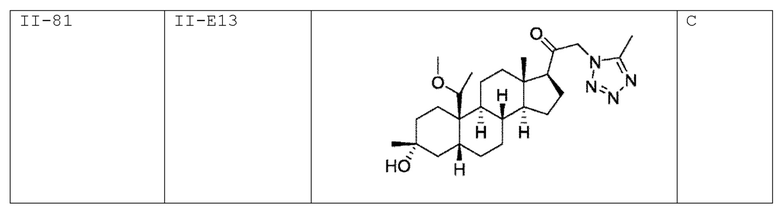
[0694] ПРИМЕР III-14: биологические данные
[0695] Ниже в Таблице III-1 А означает TBPS IC50 (мкМ) <0,01 мкМ, B означает TBPS IC50 (мкМ) от 0,01 мкМ до <0,1 мкМ, C означает TBPS IC50 (мкМ) от 0,1 мкМ до <1,0 мкМ, D означает TBPS IC50 (мкМ) 1,0 мкМ до <10 мкМ, и E означает ≥10 мкМ.
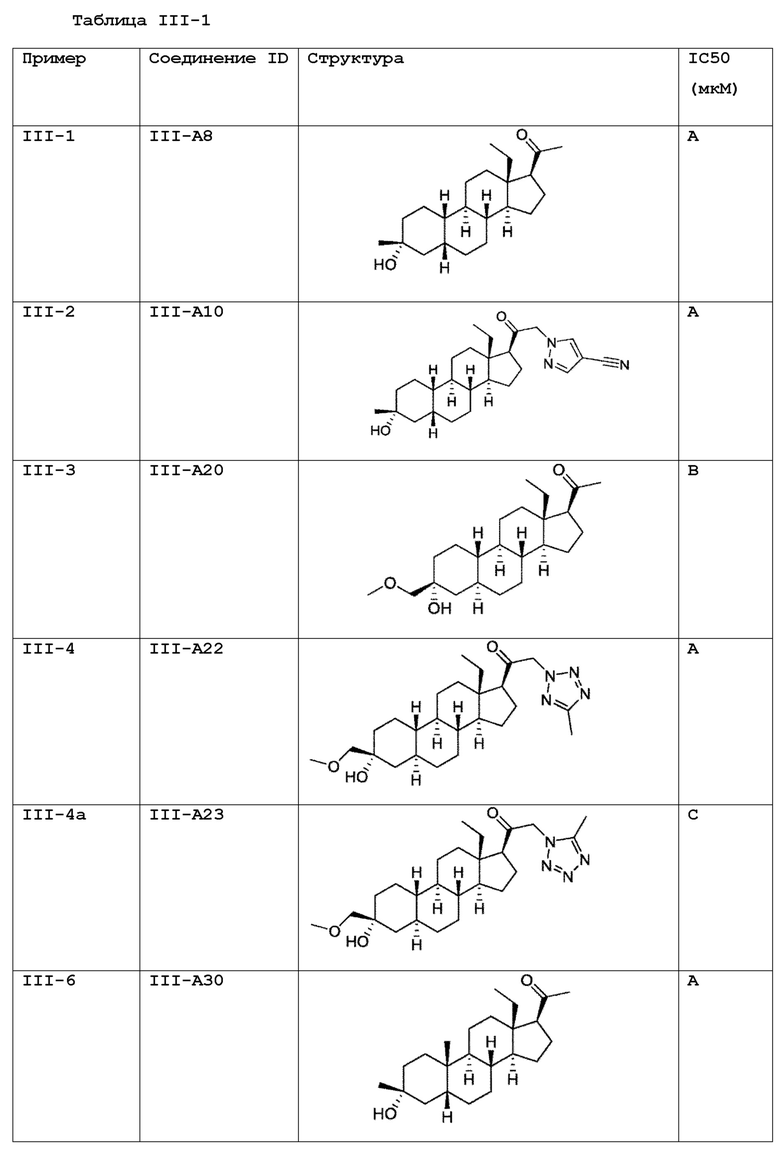
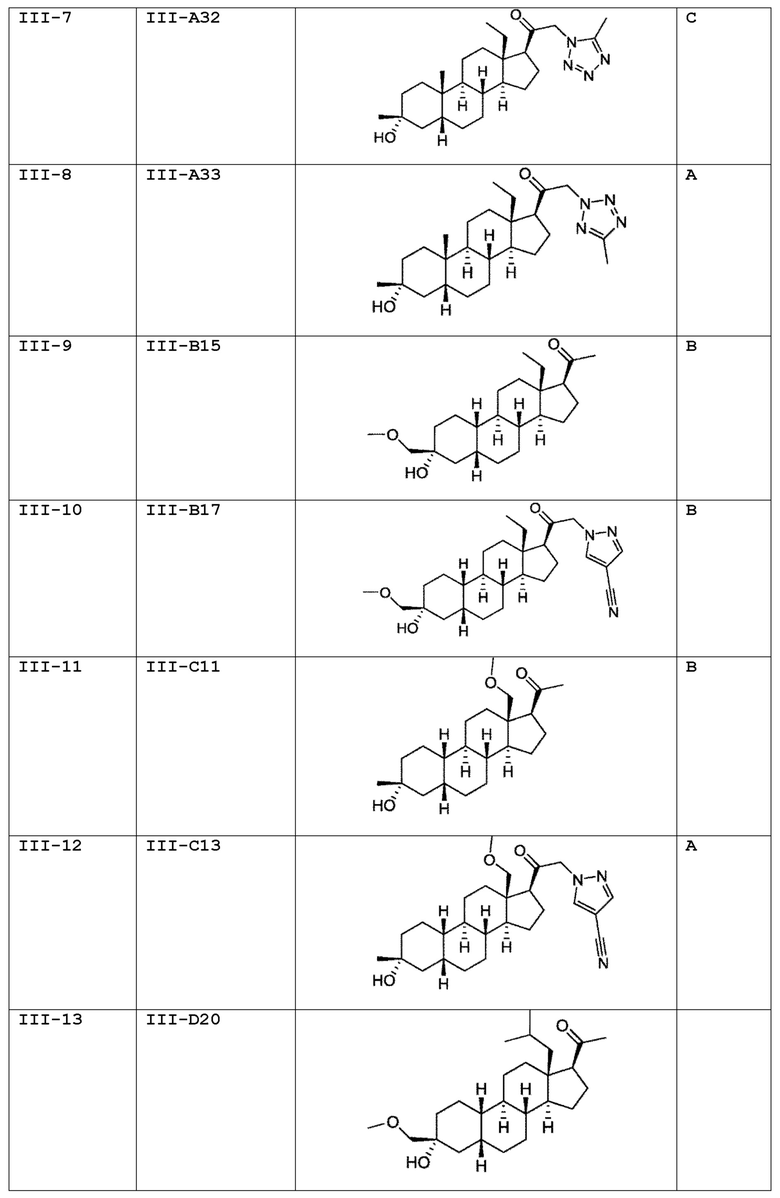
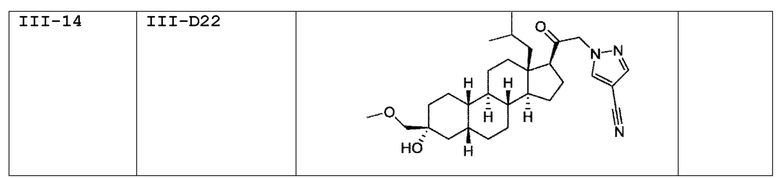
Эквиваленты и область
[0696] В пунктах формулы изобретения такие артикли, как «a», «an» и «the», могут означать один или более чем один объект, если не оговаривается иное, или иным образом не очевидно из контекста. Пункты формулы изобретения или описания, которые включают «или» между одним или более членами группы, рассматриваются как исполняемые, если один, более чем один, или все из членов группы присутствуют, используются или иным образом имеют отношение к данному продукту или процессу, если не оговаривается иное, или иным образом не очевидно из контекста. Изобретение включает варианты осуществления, в которых ровно один член группы присутствует, используется или иным образом имеет отношение к данному продукту или процессу. Изобретение включает варианты осуществления, в которых более чем один, или все из членов группы присутствуют, используются или иным образом имеют отношение к данному продукту или процессу.
[0697] Кроме того, изобретение охватывает все вариации, комбинации и видоизменения, в которых одно или более из ограничений, элементов, статей и описательных терминов из одного или более из перечисленных пунктов формулы изобретения введены в еще один пункт формулы изобретения. Например, любой пункт формулы изобретения, который является зависимым от еще одного пункта формулы изобретения, может быть модифицирован для включения одного или многих ограничений, найденных в любом другом пункте формулы изобретения, который является зависимым от того же основного пункта формулы изобретения. Там, где элементы представлены как списки, например, в формате группы Маркуша, также раскрыта каждая подгруппа элементов, и любой(-ые) элемент(-ты) может(-гут) быть удален(-ны) из группы. Должно быть понятно, что, как правило, где изобретение, или аспект изобретения, приводится(-ятся) как включающий(-щие) конкретные элементы и/или признаки, определенные варианты осуществления изобретения или аспекты изобретения состоят, или по существу состоят из таких элементов и/или признаков. Для целей простоты, те варианты осуществления не были здесь специально изложены этими словами. Также следует отметить, что термины «включающий» и «содержащий» предполагаются открытыми и позволяют включение дополнительных элементов или стадий. Там, где приведены диапазоны, включены конечные точки. Кроме того, если не оговаривается иное, или иным образом не очевидно из контекста, и является понятным для специалиста с обычной квалификацией в этой области технологии, значения, которые выражены как диапазоны, могут допускать любое конкретное значение или поддиапазон в пределах указанных диапазонов в различных вариантах осуществления изобретения, до десятой доли единицы нижнего предела диапазона, если контекст четко не оговаривает иное.
[0698] Эта заявка ссылается на различные выданные патенты, опубликованные патентные заявки, журнальные статьи и прочие публикации, все из которых включены здесь ссылкой. Если имеет место противоречие между любой из включенных литературных ссылок и данным описанием, следует руководствоваться описанием. В дополнение, любой конкретный вариант осуществления настоящего изобретения, который находится в пределах прототипа, может быть определенно исключен из любых одного или более пунктов формулы изобретения. Насколько такие варианты осуществления представляются известными специалисту с обычной квалификацией в этой области технологии, они могут быть исключены, даже если исключение не является здесь четко изложенным. Любой конкретный вариант осуществления изобретения может быть исключен из любого пункта формулы изобретения на любом основании, относится ли он или нет к существующему прототипу.
[0699] Квалифицированным специалистам в этой области технологии будут понятными, или же им не составит труда выяснить с использованием не более чем обычных экспериментов, многие эквивалентные варианты описанных здесь конкретных вариантов осуществления. Область описанных здесь данных вариантов осуществления не предполагается ограниченной приведенным выше Описанием, но, скорее, является такой, как изложено в пунктах прилагаемой формулы изобретения. Квалифицированным специалистам в этой области технологии будет понятно, что разнообразные изменения и модификации этого описания могут быть сделаны без выхода за пределы смысла и области настоящего изобретения, как определенных в пунктах нижеследующей формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ | 2018 |
|
RU2799448C2 |
| 19-НОР НЕЙРОАКТИВНЫЕ СТЕРОИДЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2014 |
|
RU2700264C2 |
| 19-НОР C3,3-ДИЗАМЕЩЕННЫЕ C21-N-ПИРАЗОЛИЛЬНЫЕ СТЕРОИДЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2014 |
|
RU2812930C2 |
| 19-НОР C3, 3-ДИЗАМЕЩЕННЫЕ C21-N-ПИРАЗОЛИЛЬНЫЕ СТЕРОИДЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2014 |
|
RU2675855C2 |
| НЕЙРОАКТИВНЫЕ СТЕРОИДЫ, ЗАМЕЩЕННЫЕ В ПОЛОЖЕНИИ 10 ЦИКЛИЧЕСКОЙ ГРУППОЙ, ДЛЯ ИСПОЛЬЗОВАНИЯ ПРИ ЛЕЧЕНИИ РАССТРОЙСТВ ЦНС | 2019 |
|
RU2796006C2 |
| НЕЙРОАКТИВНЫЕ СТЕРОИДЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2830163C2 |
| С17-, С20- И С21-ЗАМЕЩЕННЫЕ НЕЙРОАКТИВНЫЕ СТЕРОИДЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2828261C2 |
| НЕЙРОАКТИВНЫЕ СТЕРОИДЫ, КОМПОЗИЦИИ И ИХ ПРИМЕНЕНИЯ | 2012 |
|
RU2808165C2 |
| НЕЙРОАКТИВНЫЕ СТЕРОИДЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2014 |
|
RU2808166C2 |
| НЕЙРОАКТИВНЫЕ СТЕРОИДЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2014 |
|
RU2684103C2 |
Группа изобретений относится к области органической химии и фармацевтики, а именно к соединению Формулы (II-I), обладающему свойствами ингибитора функции ГАМК-рецептора, фармацевтической композиция на его основе, способу лечения связанного с ЦНС заболевания, связанного с функцией ГАМК, и способу индуцирования седативного эффекта и/или анестезии с их использованием. В общей формуле (II-I) t составляет 1; n составляет 0 или 1; R19 представляет незамещенный C2-C6-алкил, незамещенный C2-C6-алкенил; R5 представляет атом водорода; R3 представляет атом водорода или С1-6 алкил, необязательно замещенный одним или несколько С1-3 алкокси; каждый из R6a и R6b представляет атом водорода; R1 представляет C1-6 алкил, необязательно замещенный одним или несколько –ОН, 5-6-членный гетероциклил, содержащий 1-2 гетероатома, независимо выбранных из N или O, и необязательно замещенный одним или несколькими заместителями, независимо выбранными из незамещенного C1-6 алкила, фенила, необязательно замещенного одним или несколькими галогенами, или –S(O)2CH3, фенил, необязательно замещенный одним или несколькими незамещенными C1-6 алкилами, 5-10-членный гетероарил, содержащий 1-4 атома N и необязательно замещенный одним или несколькими заместителями, независимо выбранными из незамещенного C1-6 алкила, –CN или C1-6 алкокси, или -N(RA1)2, где RA1 представляет атом водорода или фенил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из незамещенного C1-6 алкила или –CN; каждый из R2a, R2b, R4a, R4b, R7a, R7b, R11a, R11b, R12a, R12b или R17b представляет атом водорода; каждый из R15a, R15b, R16a и R16b представляет атом водорода; и причем  представляет одинарную связь. Использование группы изобретений позволяет эффективно лечить связанные с ЦНС заболевания, связанные с функцией ГАМК, и индуцировать седативный эффект и/или анестезию. 5 н. и 26 з.п. ф-лы, 50 пр.
представляет одинарную связь. Использование группы изобретений позволяет эффективно лечить связанные с ЦНС заболевания, связанные с функцией ГАМК, и индуцировать седативный эффект и/или анестезию. 5 н. и 26 з.п. ф-лы, 50 пр.
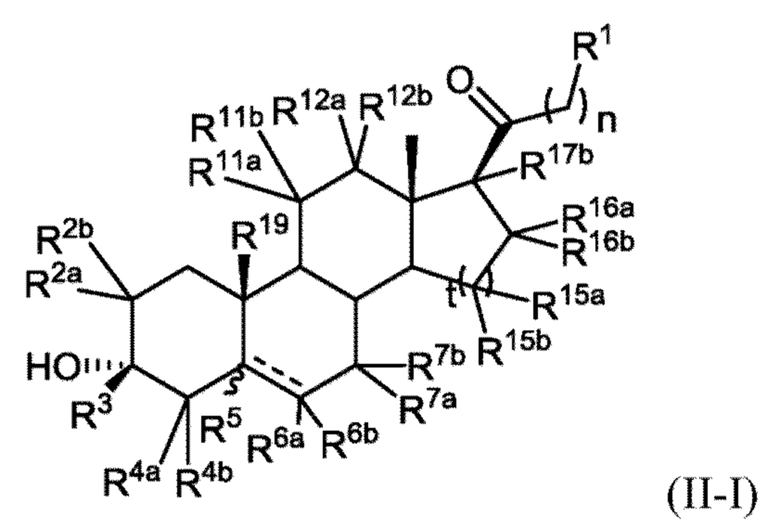
1. Соединение Формулы (II-I):
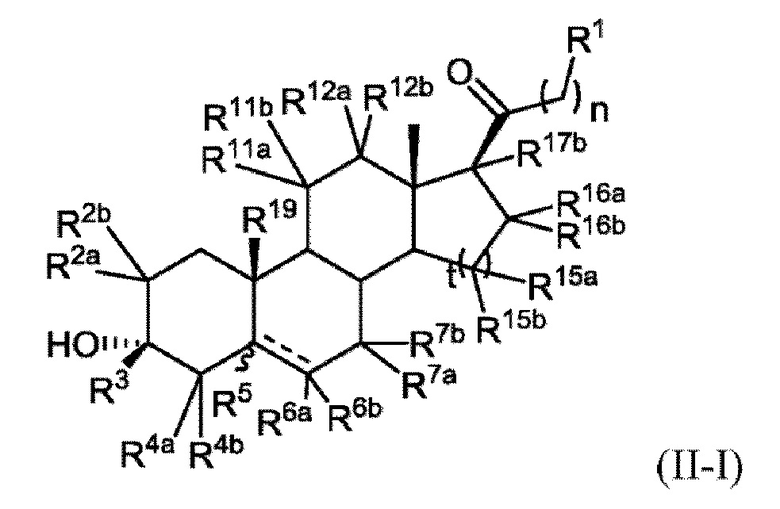
в котором:
t составляет 1;
n составляет 0 или 1;
R19 представляет незамещенный C2-C6-алкил, незамещенный C2-C6-алкенил;
R5 представляет атом водорода;
R3 представляет атом водорода или С1-6 алкил, необязательно замещенный одним или несколько С1-3 алкокси;
каждый из R6a и R6b представляет атом водорода;
R1 представляет C1-6 алкил, необязательно замещенный одним или несколько –ОН, 5-6-членный гетероциклил, содержащий 1-2 гетероатома, независимо выбранных из N или O, и необязательно замещенный одним или несколькими заместителями, независимо выбранными из незамещенного C1-6 алкила, фенила, необязательно замещенного одним или несколькими галогенами, или –S(O)2CH3, фенил, необязательно замещенный одним или несколькими незамещенными C1-6 алкилами, 5-10-членный гетероарил, содержащий 1-4 атома N и необязательно замещенный одним или несколькими заместителями, независимо выбранными из незамещенного C1-6 алкила, –CN или C1-6 алкокси, или -N(RA1)2, где RA1 представляет атом водорода или фенил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из незамещенного C1-6 алкила или –CN;
каждый из R2a, R2b, R4a, R4b, R7a, R7b, R11a, R11b, R12a, R12b или R17b представляет атом водорода;
каждый из R15a, R15b, R16a и R16b представляет атом водорода; и
причем  представляет одинарную связь.
представляет одинарную связь.
2. Соединение по п. 1, в котором R5 представляет атом водорода в цис-положении относительно С19-положения.
3. Соединение по п. 1, в котором R5 представляет атом водорода в транс-положении относительно С19-положения.
4. Соединение по любому из пп. 1-3, в котором n составляет 1.
5. Соединение по любому из пп. 1-4, в котором R3 представляет атом водорода или незамещенный метил.
6. Соединение по любому из пп. 1-5, в котором R19 представляет незамещенный С2-6-алкил.
7. Соединение по любому из пп. 1-6, в котором R19 представляет незамещенный этил.
8. Соединение по любому из пп. 1-7, в котором R1 представляет
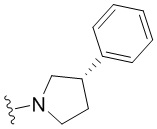 ,
, 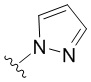 ,
, 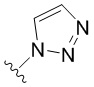 ,
, 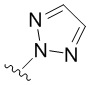 ,
, 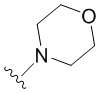 ,
, 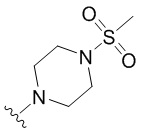 ,
, 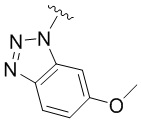 ,
, 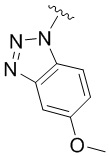 ,
, 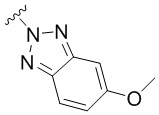 ,
, 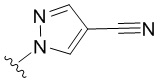 ,
, 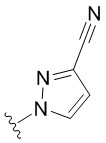 ,
, 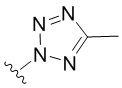 ,
, 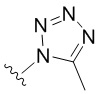 ,
, 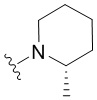 ,
, 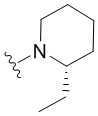 ,
, 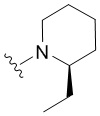 ,
, 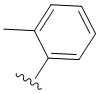 ,
, 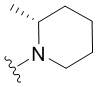 ,
, 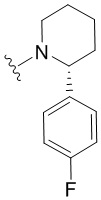 ,
, 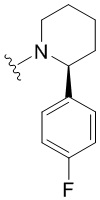 , или
, или  .
.
9. Соединение по п. 1, где соединение Формулы (II-I) имеет Формулу (II-Ia):
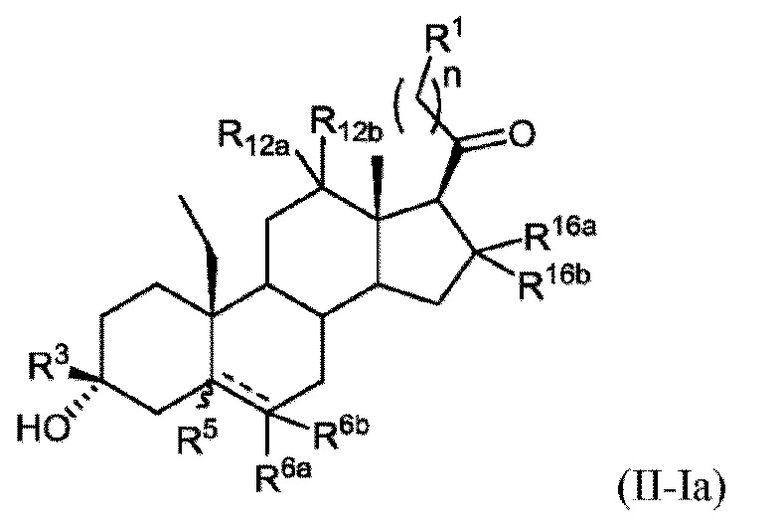
где:
n составляет 0 или 1;
R5 представляет атом водорода;
R3 представляет атом водорода или C1-6 алкил, необязательно замещенный одним или несколькими C1-3 алкокси;
каждый из R6a и R6b представляет атом водорода;
R1 представляет C1-6 алкил, необязательно замещенный одним или несколькими –OH, 5-6-членный гетероциклил, содержащий 1-2 гетероатома, независимо выбранных из N или O, и необязательно замещенный одним или несколькими заместителями, независимо выбранными из незамещенного C1-6 алкила, фенила, необязательно замещенного одним или несколькими галогенами или –S(O)2CH3, фенил, необязательно замещенный одним или несколькими незамещенными C1-6 алкилами, 5-10-членный гетероарил, содержащий 1-4 атома N и необязательно замещенный одним или несколькими заместителями независимо выбранный из незамещенного C1-6 алкила, –CN или C1-6 алкокси, или –N(RA1)2, где каждый RA1 независимо представляет собой водород или фенил, необязательно замещенный одним или несколькими заместителями, независимо выбранными из незамещенного C1-6 алкила или –CN;
каждый из R12a и R12b представляет атом водорода;
каждый из R16a и R16b представляет атом водорода; и
причем  представляет одинарную связь.
представляет одинарную связь.
10. Соединение по п. 9, в котором R5 представляет атом водорода в цис-положении относительно С19-положения.
11. Соединение по п. 9, в котором R5 представляет атом водорода в транс-положении относительно С19-положения.
12. Соединение по любому из пп. 9-11, в котором R3 представляет собой метил, метоксиметил или этоксиметил.
13. Соединение по п. 9, в котором R1 представляет собой
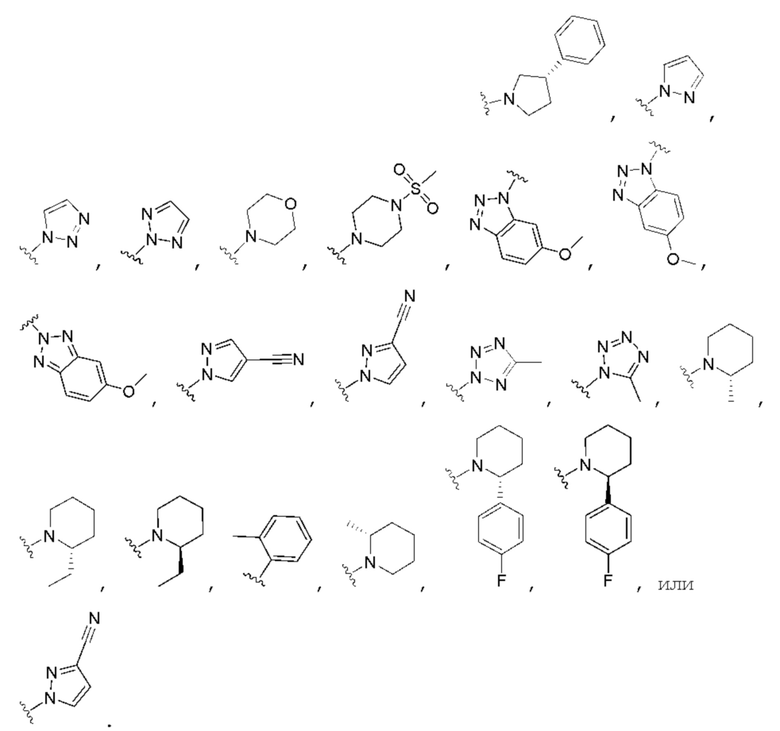
14. Соединение по п. 9, где соединение Формулы (II-Iа) имеет Формулу (II-Ib) или Формулу (II-Ic):
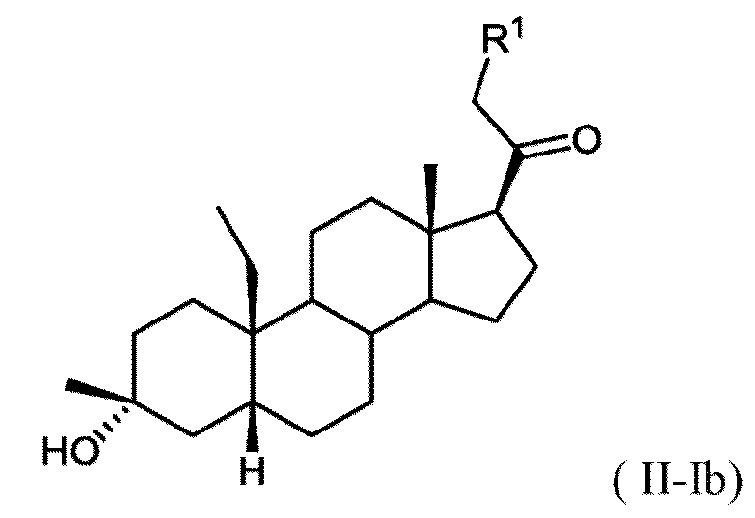
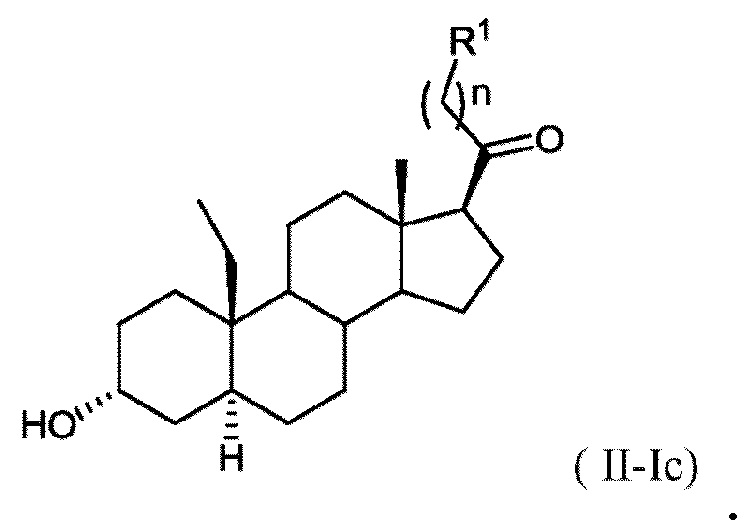
15. Соединение по п. 9, где соединение Формулы (II-Iа) имеет Формулу (II-Ie):
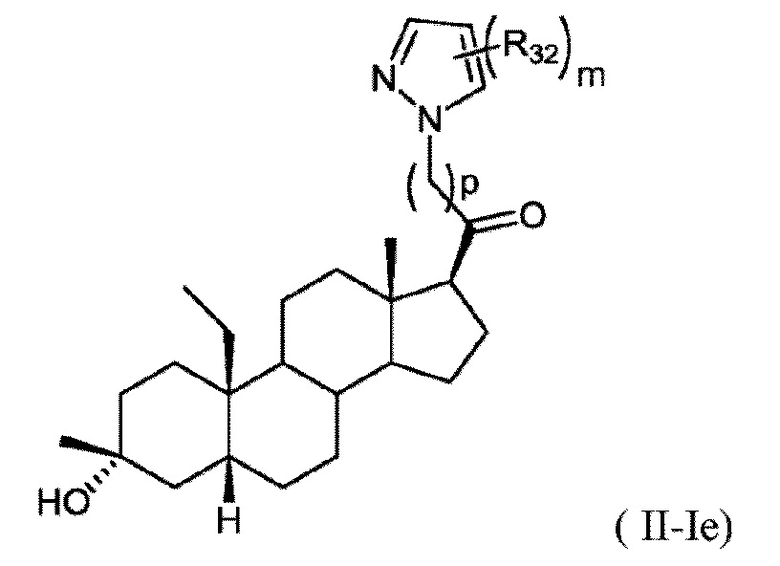
в котором m составляет 0 или 1;
p составляет 0 или 1;
R32 представляет цианогруппу.
16. Соединение по п. 9, где соединение Формулы (II-Iа) имеет Формулу (II-Ig):
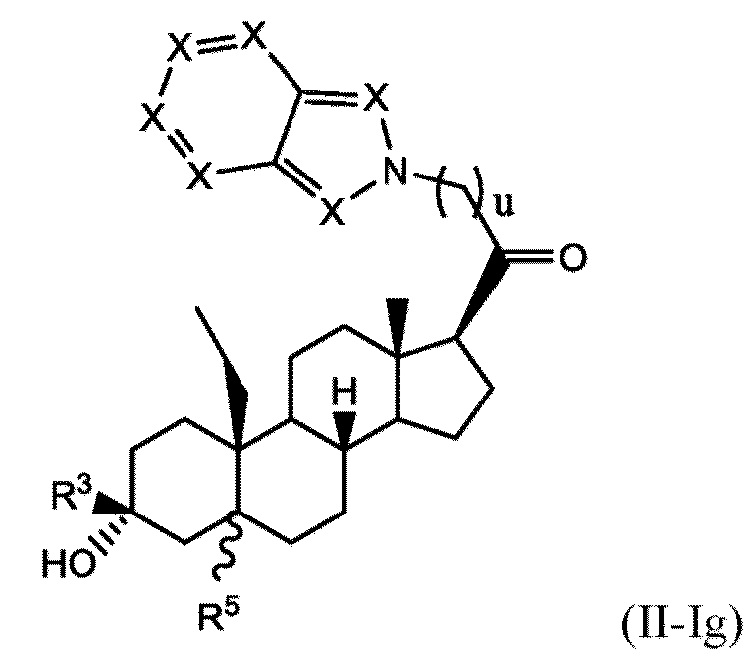
причем u составляет 0 или 1;
каждый X независимо представляет -C(RN)-, -C(RN)2-, -S-, -N- или N(RN)-,
где RN независимо представляет атом водорода или ОСН3.
17. Соединение, выбранное из
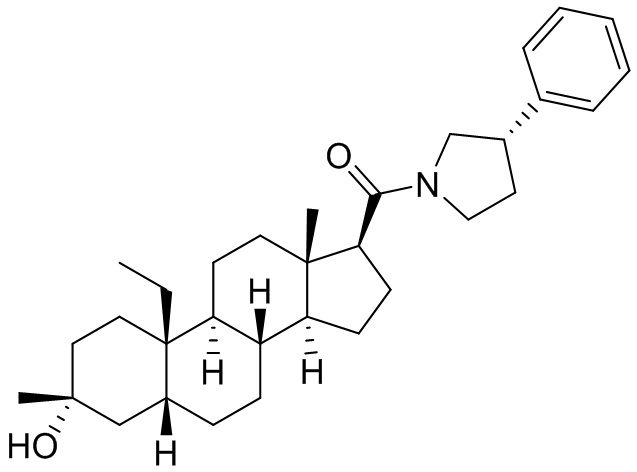
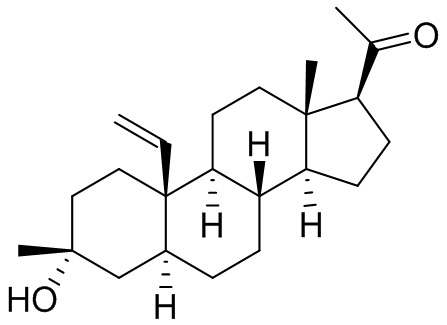
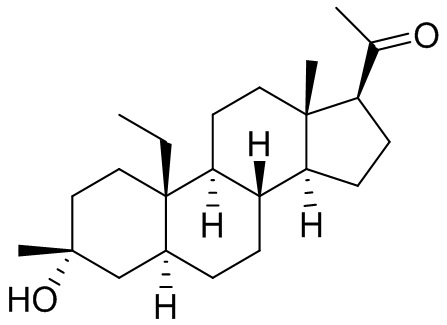
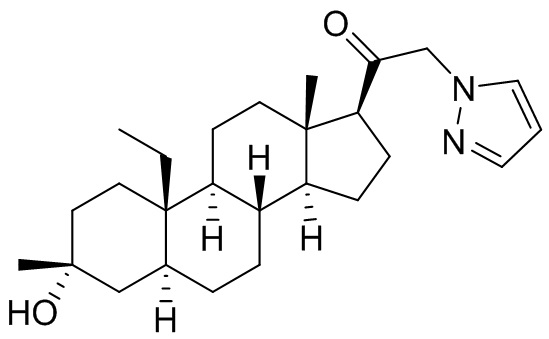
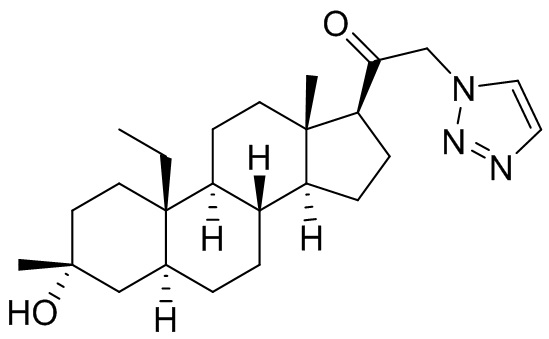
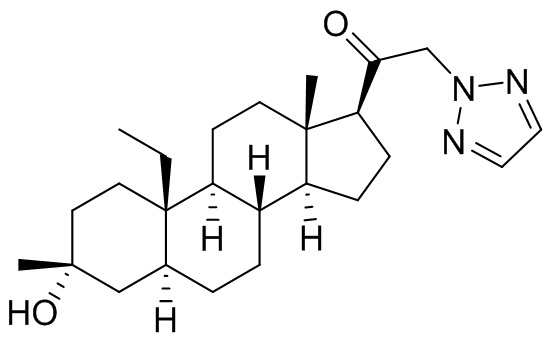
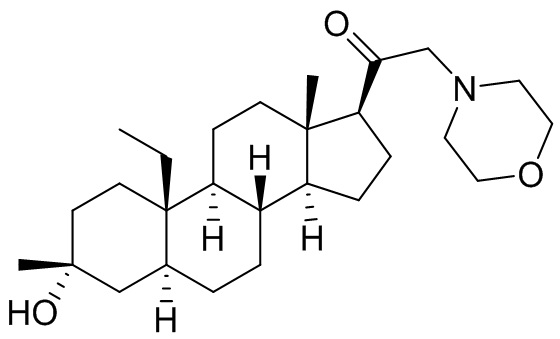
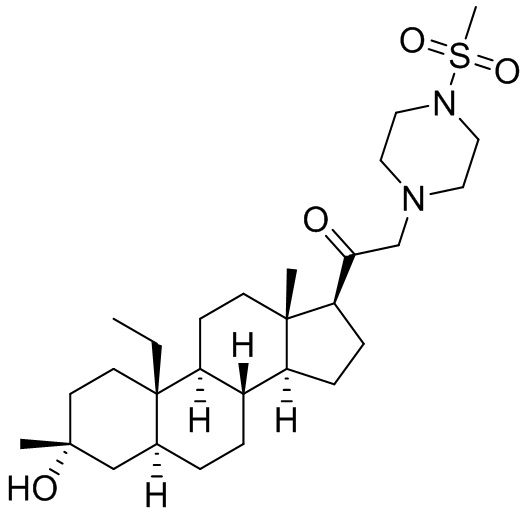
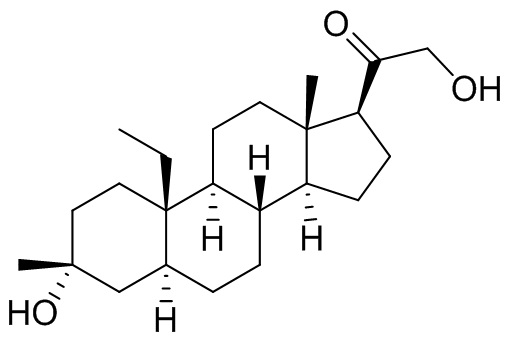
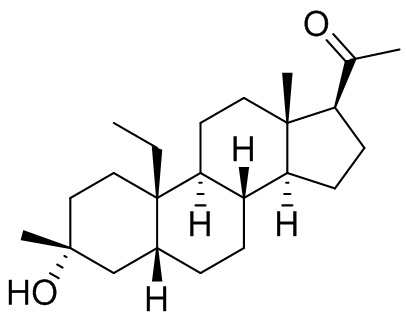
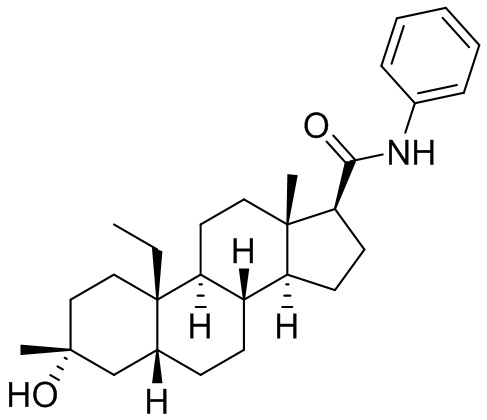
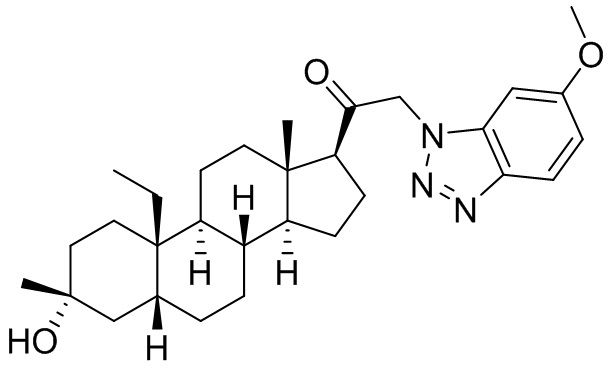
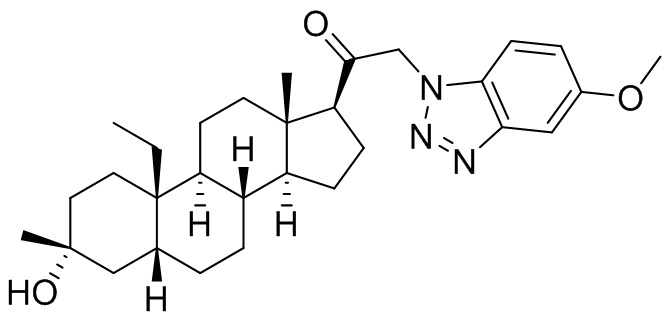
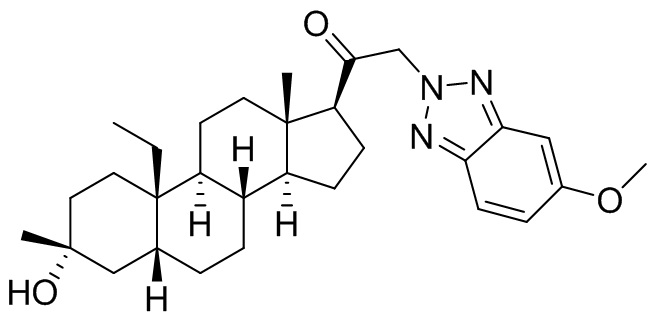
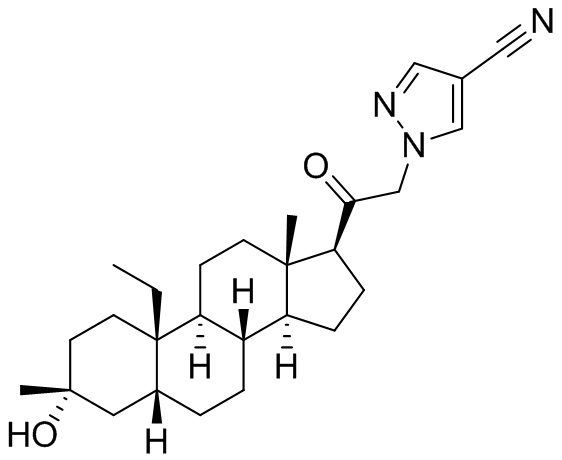
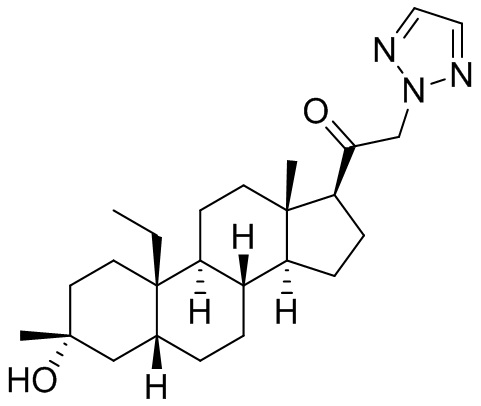
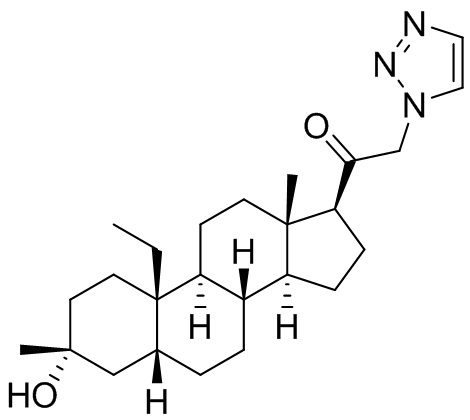
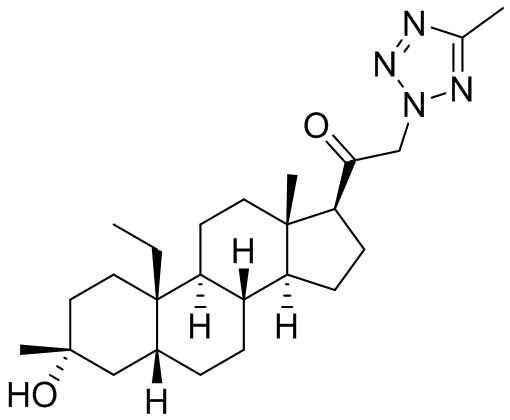
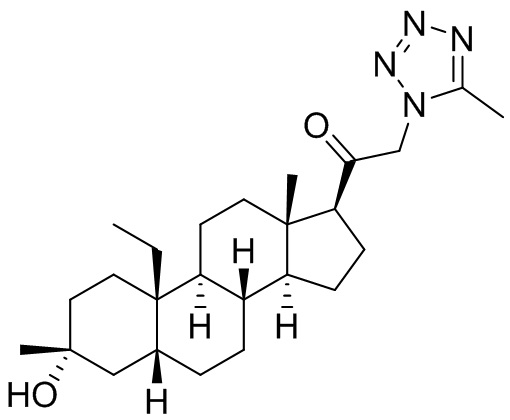
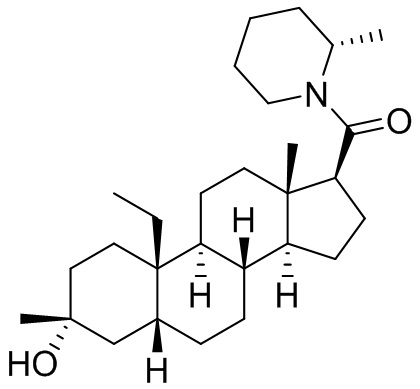
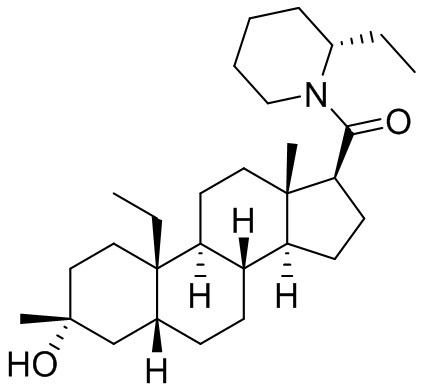
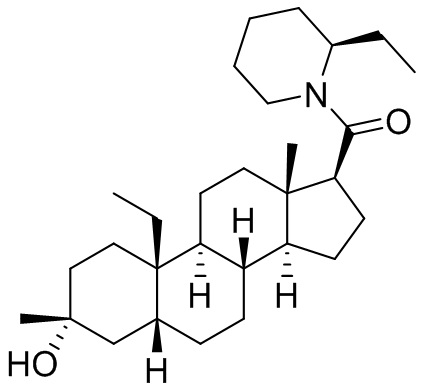
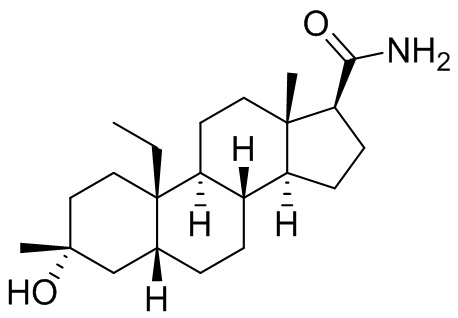
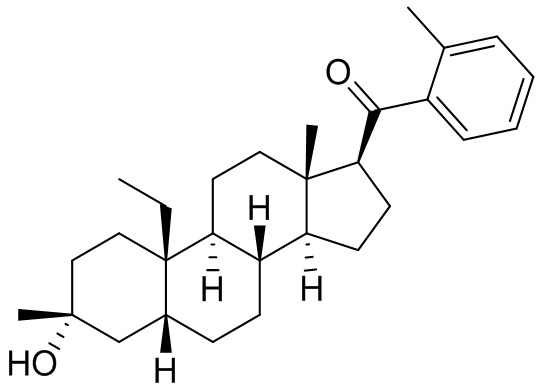
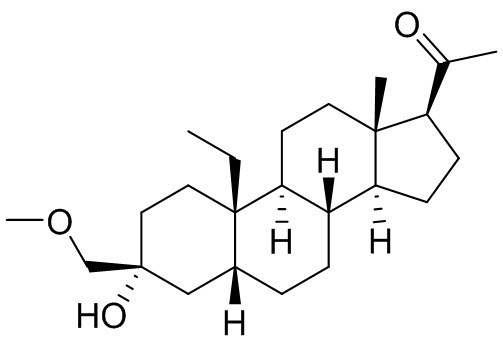
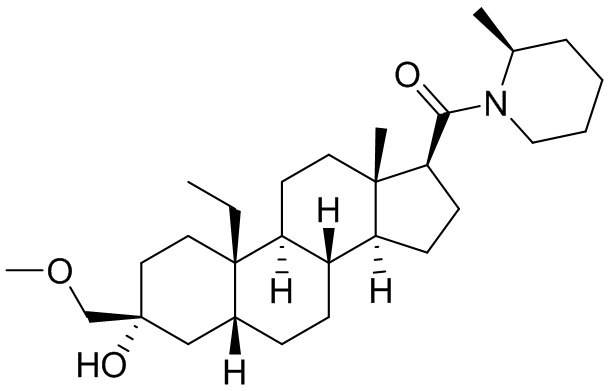
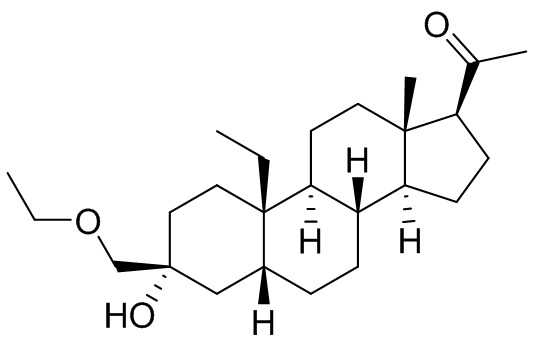
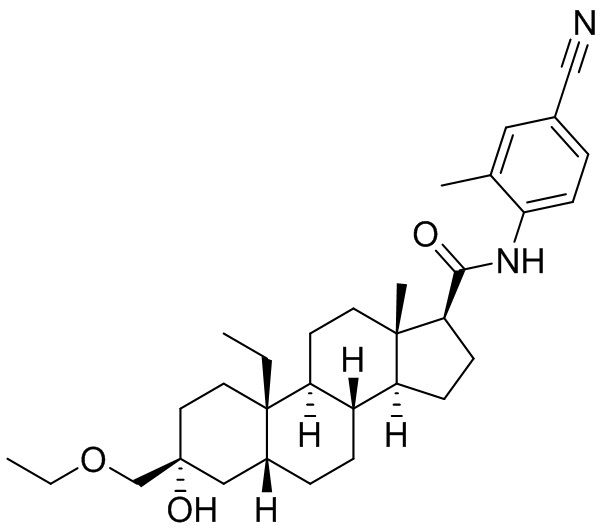
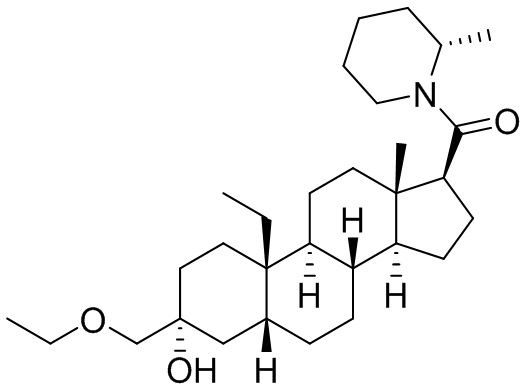
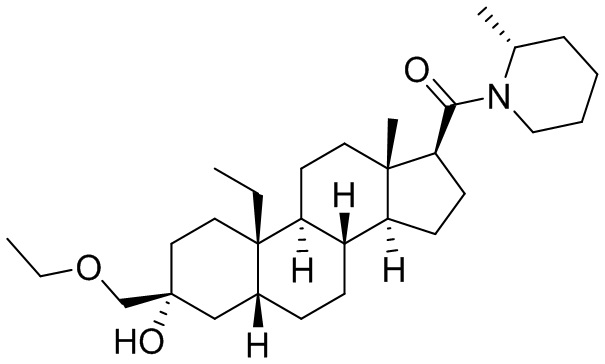
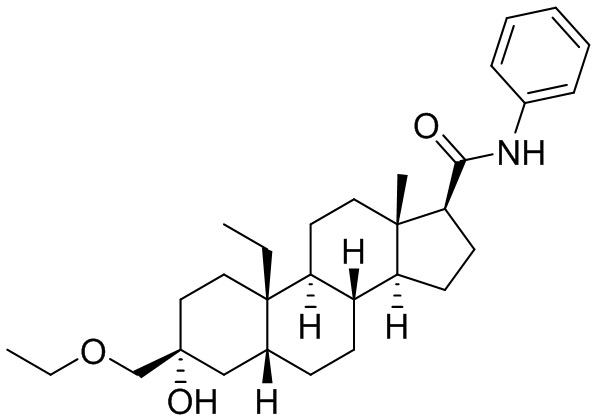
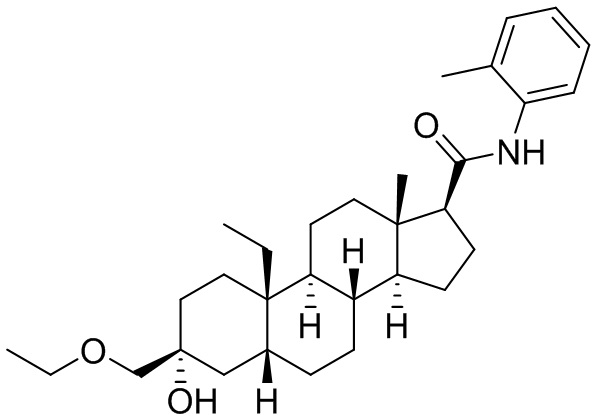
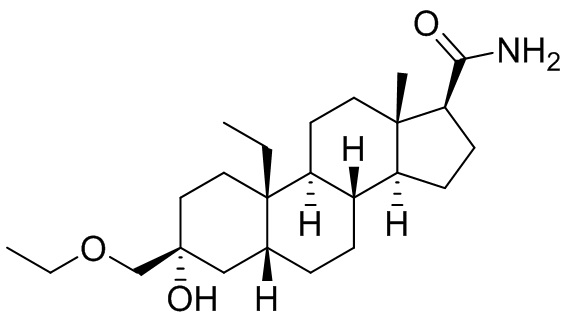
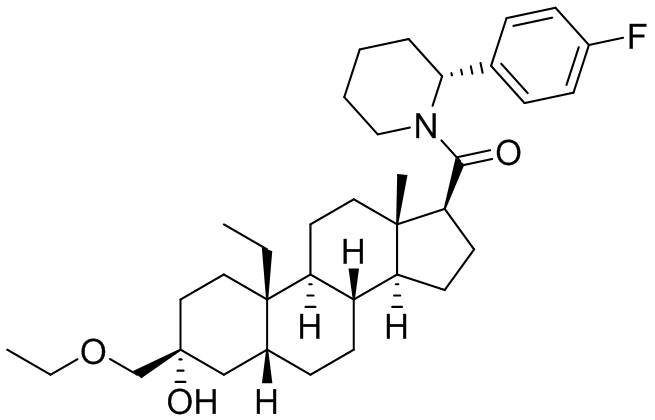
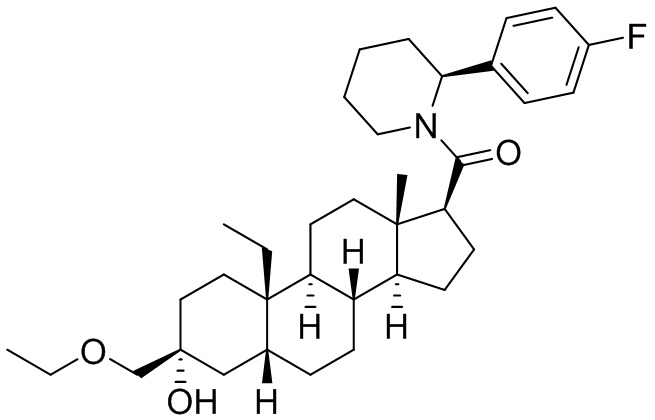
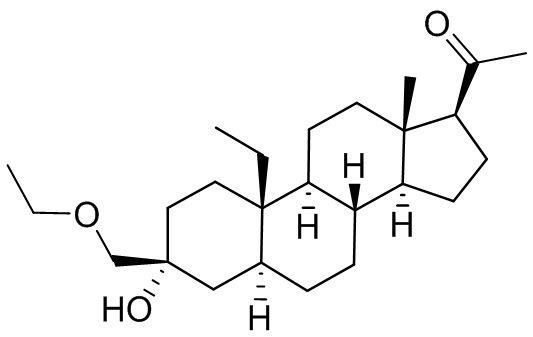
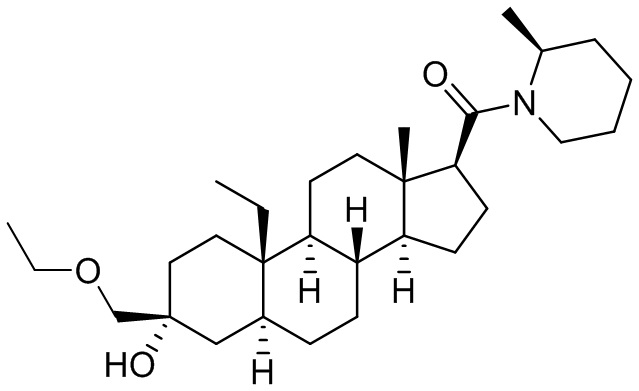
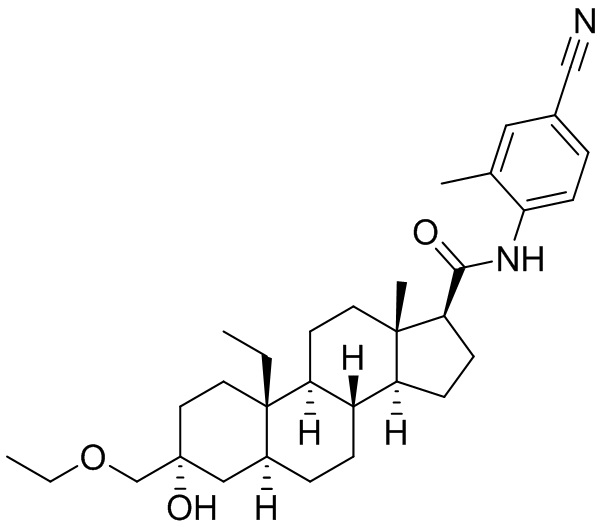
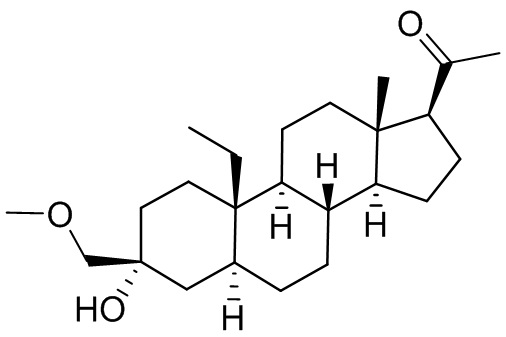
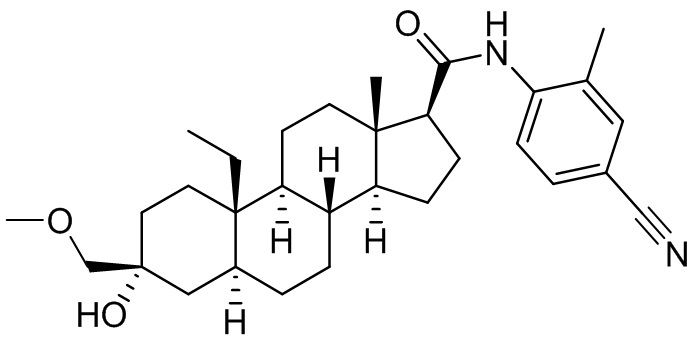
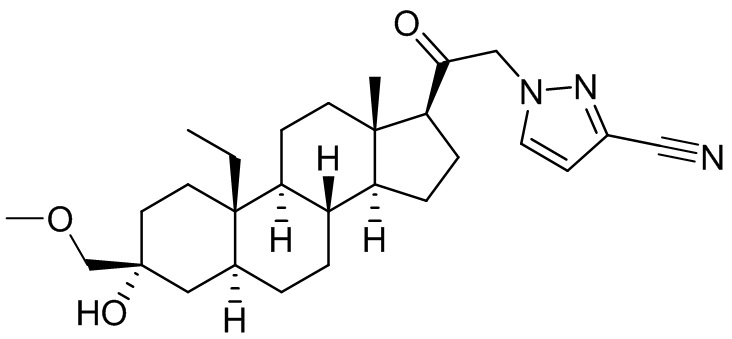
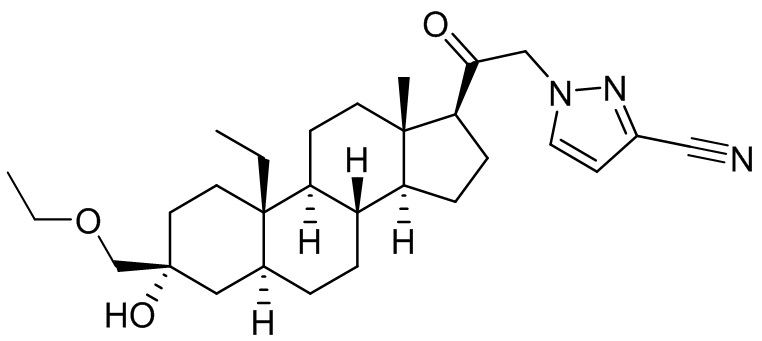
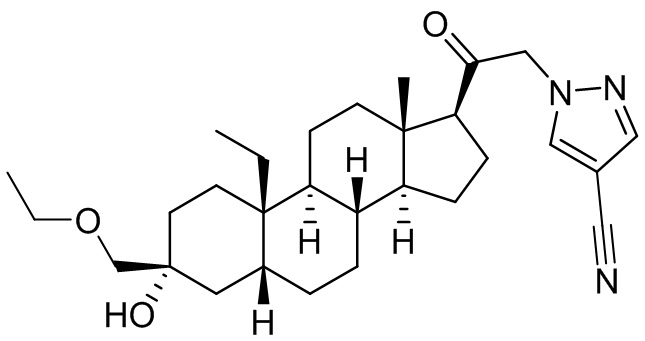
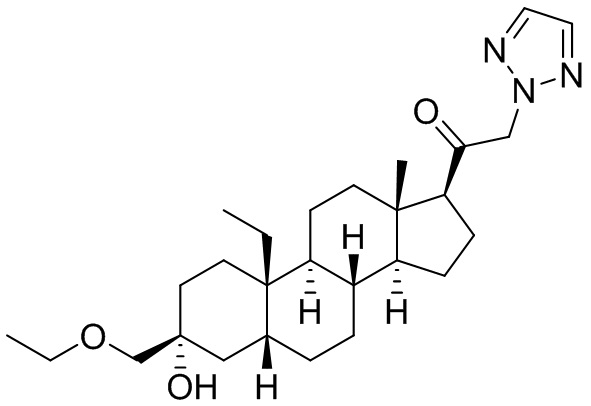
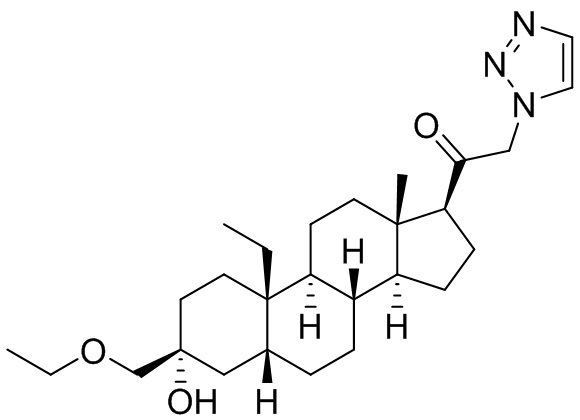
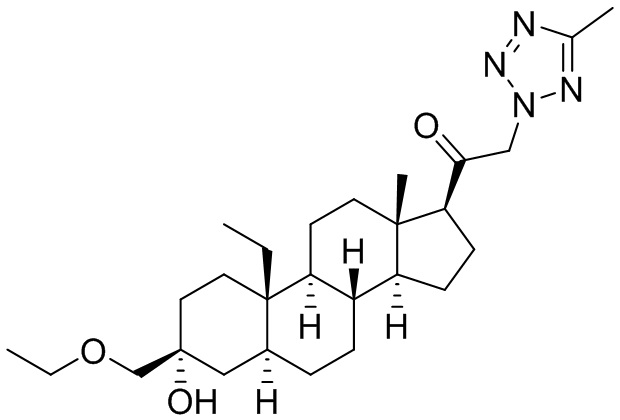
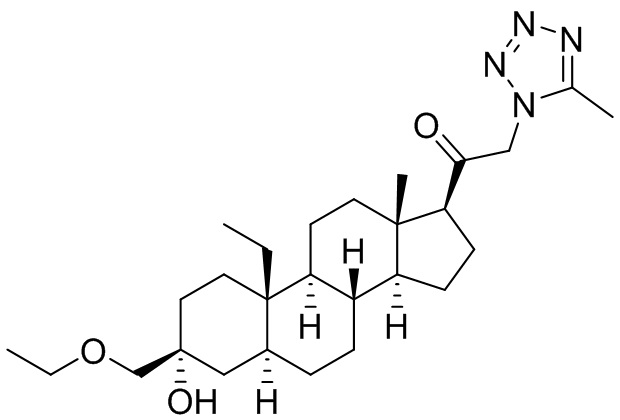
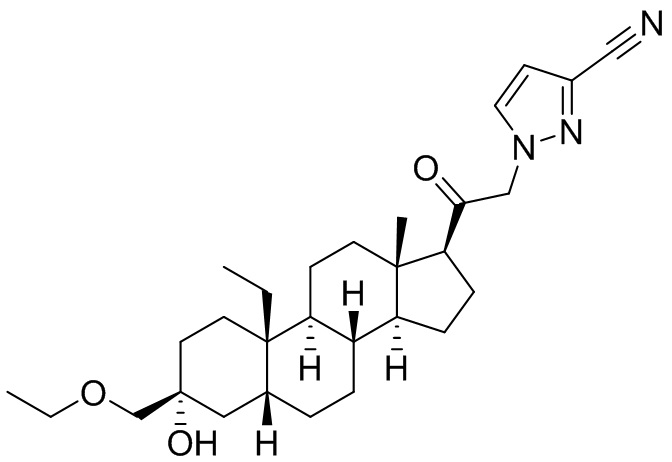
18. Фармацевтическая композиция для лечения расстройства ЦНС, связанного с функцией ГАМК, у субъекта, содержащая эффективное количество соединения по любому из пп. 1-17 и фармацевтически приемлемый эксципиент.
19. Способ лечения связанного с ЦНС заболевания, связанного с функцией ГАМК, у нуждающегося в этом субъекта, включающий введение субъекту эффективного количества соединения по любому из пп. 1-17 или фармацевтической композиции по п. 18.
20. Способ по п. 19, в котором связанное с ЦНС заболевание представляет собой нарушение сна, расстройство настроения, расстройство шизофренического спектра, судорожный синдром, нарушение памяти и/или познавательной способности, нарушение движений, изменение личности, расстройство аутистического спектра, боль, травматическое повреждение мозга, сосудистые болезни, связанное с наркотической зависимостью расстройство и/или абстинентный синдром, шум в ушах или эпилептический статус.
21. Способ по п. 19, в котором связанное с ЦНС заболевание представляет собой депрессию.
22. Способ по п. 20, в котором связанное с ЦНС заболевание представляет собой послеродовую депрессию.
23. Способ по п. 22, в котором связанное с ЦНС заболевание представляет собой большое депрессивное расстройство.
24. Способ по п. 22, в котором связанное с ЦНС заболевание представляет собой большое депрессивное расстройство в умеренной форме.
25. Способ по п. 19, в котором связанное с ЦНС заболевание представляет собой большое депрессивное расстройство в тяжелой форме.
26. Способ по п. 19, в котором расстройство, связанное с ЦНС, представляет собой судороги.
27. Способ по п. 19, в котором расстройством, связанным с ЦНС, является тремор.
28. Способ по п. 27, в котором тремор представляет собой эссенциальный тремор.
29. Способ по любому из пп. 19-28, в котором соединение или фармацевтическую композицию вводят перорально.
30. Способ по любому из пп. 19-29, в котором соединение или фармацевтическую композицию вводят постоянно.
31. Способ индуцирования седативного эффекта и/или анестезии у нуждающегося в этом субъекта, включающий введение субъекту эффективного количества соединения по любому из пп. 1-17.
| CRISTINA SUNOL et al | |||
| Activity of B-Nor Analogues of Neurosteroids on the GABA A Receptor in Primary Neuronal Cultures | |||
| Journal Of Medicinal Chemistry,Vol | |||
| Способ смешанной растительной и животной проклейки бумаги | 1922 |
|
SU49A1 |
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| HAN MINGCHENG et al | |||
| Neurosteroid Analogs | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
Авторы
Даты
2023-12-27—Публикация
2018-12-21—Подача