Изобретение относится к области органической химии, а именно к структуре и противомикробной активности новых индивидуальных соединений класса 3-арил-5-((тозилметил)имино)-5H,6H-бензо[b]фуро[3',4':2,3]пирроло[1,2-d][1,4]оксазин-1,2,6-трионов, которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем и в фармакологии.
Известен способ получения структурного аналога заявляемых соединений: метил 2,3-диоксо-1,4-дифенил-6-((тозилметил)имино)-2,3-дигидро-1H-фуро[3,4-b]пиррол-6а(6H)-карбоксилата 3 из тозилизоцианида 1 и метил 3-бензоил-4,5-диоксо-1-фенил-4,5-дигидро-1H-пиррол-2-карбоксилата 2 (Схема 1) (Moroz A.A. et al. Diversity-oriented synthesis of three skeletally diverse iminolactones from isocyanides, activated acetylenes and 1H-pyrrole-2,3-diones via [3+2] and [4+1] cycloaddition reactions //Tetrahedron. - 2020. - T. 76. - №. 5. - C. 130880), синтезируемого по следующей схеме:
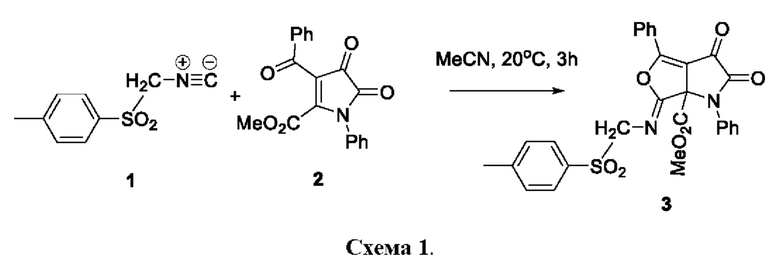
К недостаткам данного способа относится невозможность получения 3-арил-5-((тозилметил)имино)-5H,6H-бензо[b]фуро[3',4':2,3]пирроло[1,2-d][1,4]оксазин-1,2,6-трионов.
Задачей изобретения является разработка простого способа синтеза 3-Арил-5-((тозилметил)имино)-5H,6H-бензо[b]фуро[3',4':2,3]пирроло[1,2-d][1,4]оксазин-1,2,6-трионов и расширение арсенала средств воздействия на живой организм.
Технический результат - получение новых соединений, которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем и в фармакологии как обладающие противомикробной активностью.
Поставленная задача осуществляется путем взаимодействия 3-ароил-1H-бензо[b]пирроло[1,2-d[1,4]оксазин-1,2,4-трионов 4а,b с тозилизоцианидом 5 в среде растворителя (Схема 2) с последующим выделением целевых продуктов 6а,b, по следующей схеме:
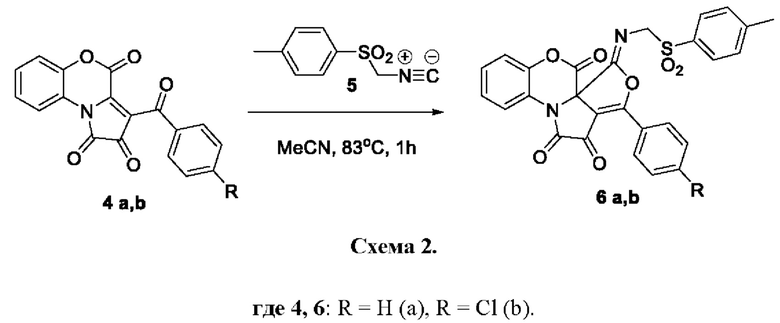
Процесс ведут при температуре 83°С, а в качестве растворителя используют безводный ацетонитрил.
Из патентной и технической литературы не были выявлены способы получения 3-Арил-5-((тозилметил)имино)-5H,6H-бензо[b]фуро[3',4':2,3]пирроло[1,2-d][1,4]оксазин-1,2,6-трионов, имеющие сходные признаки с заявляемым способом, а именно, не использовались исходные продукты, растворители, в которых проходит реакция, и интервал температур.
Изобретение иллюстрируется следующими примерами.
Пример 1. 3-Фенил-5-((тозилметил)имино)-5H,6H-бензо[b]фуро[3',4':2,3]пирроло[1,2-d][1,4]оксазин-1,2,6-трион (6а).
К раствору 0.50 ммоль 3-бензоил-1H-бензо[b]пирроло[1,2-d][1,4]оксазин-1,2,4-триона 4а в 2 мл ацетонитрила приливали раствор 0.50 ммоль тозилизо цианида 5 в 1 мл ацетонитрила, оставляли перемешиваться в течение 1 часа при температуре 83°С, остужали реакционную массу до комнатной температуры, отфильтровывали образовавшийся осадок, промывали 1 мл безводного ацетонитрила. Выход 68%, т. пл. 198-199°С (AN, разл.).
Соединение (6а) C27H18N2O7S.
Найдено, %: С 63.05; Н 3.53; N 5.45.
Вычислено, %: С 63.03; Н 3.53; N 5.44.
Соединение (6а) - бледно-желтое кристаллическое вещество, легкорастворимое в ДМСО и ДМФА, растворимое в 1,4-диоксане, этилацетате и ацетонитриле при нагревании, трудно растворимое в менее полярных органических растворителях, нерастворимое в воде и алканах. Устойчиво при хранении в обычных условиях.
В спектре ЯМР 1H соединения 6а, записанном в растворе в ДМСО-d6, кроме сигналов протонов ароматических колец, присутствует синглет метальной группы тозильного фрагмента при 2.35 м.д.; мультиплеты метиленовой группы тозильного фрагмента при 5.10 и 5.20. м.д.
Спектр ЯМР 1H соединения 6а снят в растворе ДМСО-d6 при частоте 400 МГц: δ=8.28-8.22 (м, 2Н), 7.86-7.80 (м, 1H), 7.74-7.66 (м, 3Н), 7.51-7.45 (м, 1Н), 7.40 (м, 4Н), 7.28 (м, 2Н), 5.20 (м, 1Н), 5.10 (м, 1Н), 2.35 (с, 3Н) м.д.
Спектр ЯМР 13С соединения 6а снят в растворе ДМСО-d6 при частоте 100 МГц: δ=172.72, 162.21, 160.92, 159.26, 155.61, 144.40, 143.22, 135.14, 133.96, 129.90, 129.40, 129.03, 128.36, 127.31, 124.96, 124.85, 123.05, 121.85, 116.72, 106.29, 68.12, 66.11, 20.90 м.д.
Пример 2. 3-(4-Хлорфенил)-5-((тозилметил)имино)-5H,6H-бензо[b]фуро[3',4':2,3]пирроло[1,2-d][1,4]оксазин-1,2,6-трион (6b).
К раствору 0.50 ммоль 3-(4-хлорбензоил)-1H-бензо[b]пирроло[1,2-d][1,4]оксазин-1,2,4-триона 4b в 2 мл ацетонитрила приливали раствор 0.50 ммоль тозилизоцианида 5 в 1 мл ацетонитрила, оставляли перемешиваться в течение 1 часа при температуре 83°С, остужали реакционную массу до комнатной температуры, отфильтровывали образовавшийся осадок, промывали 1 мл безводного ацетонитрила. Выход 43%, т. пл. 210-211°С (AN, разл.).
Соединение (6b) C27H17ClN2O7S.
Найдено, %: С 59.08; Н 3.13; N 5.10.
Вычислено, %: С 59.08; Н 3.12; N 5.10.
Соединение 6b - бежевое кристаллическое вещество, легкорастворимое в ДМСО и ДМФА, растворимое в 1,4-диоксане, этилацетате и ацетонитриле при нагревании, трудно растворимое в менее полярных органических растворителях, нерастворимое в воде и алканах. Устойчиво при хранении в обычных условиях.
В спектре ЯМР 1H соединения 6b, записанном в растворе в ДМСО-d6, кроме сигналов протонов ароматических колец, присутствует синглет метальной группы тозильного фрагмента при 2.36 м.д.; мультиплеты метиленовой группы тозильного фрагмента при 5.10 и 5.20. м.д.
Спектр ЯМР 1H соединения 6b снят в растворе ДМСО-d6 при частоте 400 МГц: δ=8.25 (м, 2Н), 7.80 (м, 2Н), 7.67 (м, 1Н), 7.50-7.45 (м, 1Н), 7.43-7.37 (м, 4Н), 7.29 (м, 2Н), 5.20 (м, 1H), 5.10 (м, 1Н), 2.36 (с, 3Н) м.д.
Спектр ЯМР 13С соединения 6b снят в растворе ДМСО-d6 при частоте 100 МГц: 5=172.79, 161.12, 160.77, 159.16, 155.44, 144.40, 143.19, 140.01, 133.97, 129.40, 129.32, 128.35, 127.34, 124.88, 123.85, 123.02, 121.80, 116.74, 106.72, 68.11, 66.10, 20.91 м.д.
Пример 3. Исследование соединений 6а,b на наличие противомикробной активности.
Для исследований использовали общепринятый метод двукратных серийных разведений в жидкой питательной среде микрометодом [Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ - М.: И-во Медицина, 2005]. Готовили исходные разведения микроорганизмов в физиологическом растворе из суточной агаровой культуры по оптическому стандарту мутности (ОСО) на 5 ME с использованием денситометра. После ряда разведений конечная концентрация клеток в опыте составляла 2,5×105 клеток/мл.
Противомикробные свойства химических веществ изучали на 3-х коллекционных условно-патогенных штаммах микроорганизмов: Staphylococcus aureus (АТСС 25923), Escherichia coli (АТСС 25922), Candida albicans (РКПГУ 1353/1277).
В лунках стерильного 96 луночного плоскодонного микропланшета готовили два параллельных ряда двукратных серийных разведений химических соединений в бульоне РПБ, Сабуро. В каждой лунке содержалось 150 мкл определенной концентрации испытуемого вещества и 150 мклинокулята культуры. В последних рядах содержалась питательная среда и культура в равных объемах (контроль). Максимально испытанная концентрация соответствовала 1000,0 мкг/мл, минимальная - 1,0 мкг/мл. Микропланшет помещали в термостат спектрофотометра Epoch и замеряли оптическую плотности (ОП) при длине волны 540 нм. Через 24 часа и 7 суток вновь регистрировали ОП культуральной жидкости.
Результаты оценивали с помощью программного обеспечения Gen 5 спектрофотометра для микропланшет Epoch. Последняя лунка ряда с задержкой роста и показателями ОП равной оптической плотности контрольной лунки соответствует минимальной подавляющей концентрацией соединения.
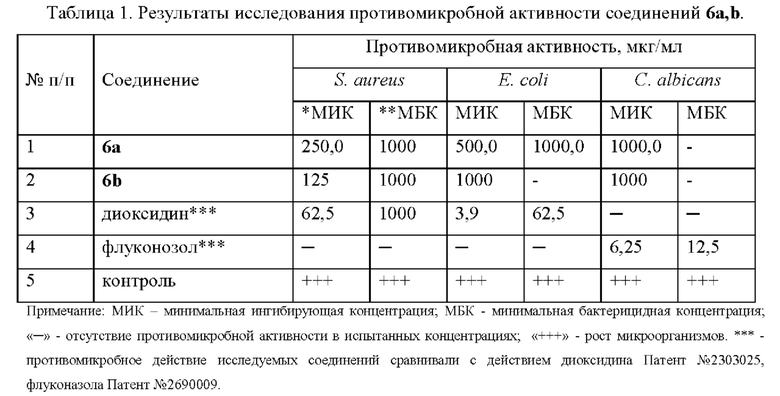
Соединение 6а подавляет рост S. aureus в концентрации 250 мкг/мл, гибель культуры наступает при концентрации 1000 мкг/мл, подавляет рост E. coli в концентрации 500 мкг/мл, гибель культуры наступает при концентрации 1000 мкг/мл, подавляет рост С. albicans в концентрации 1000 мкг/мл; соединение 6b подавляет рост S. aureus в концентрации 125 мкг/мл, гибель культуры наступает при концентрации 1000 мкг/мл, подавляет рост Е. coli в концентрации 1000 мкг/мл, подавляет рост С. albicans в концентрации 1000 мкг/мл.
Результаты исследований приведены в Таблице 1.
Предлагаемый способ прост в осуществлении, одностадиен и позволяет получить с хорошим выходом 3-арил-5-((тозилметил)имино)-5H,6H-бензо[b]фуро[3',4':2,3]пирроло[1,2-d][1,4]оксазин-1,2,6-трионы, которые могут найти применение в качестве исходных продуктов для синтеза гетероциклических систем и в фармакологии в качестве потенциальных лекарственных средств.
Изобретение относится к области органической химии и раскрывает соединения 3-арил-5-((тозилметил)имино)-5H,6H-бензо[b]фуро[3',4':2,3]пирроло[1,2-d][1,4]оксазин-1,2,6-трионов, обладающие противомикробной активностью. Технический результат заключается в получении новых соединений, которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем и в фармакологии как обладающие противомикробной активностью. 1 табл., 3 пр.
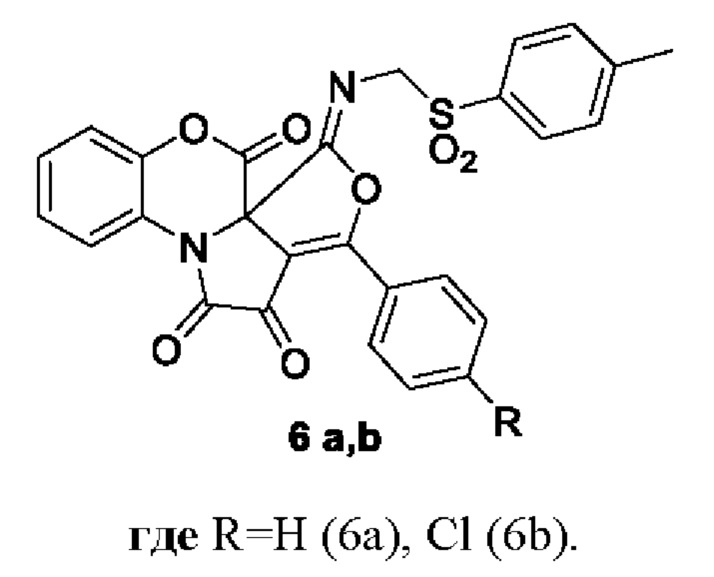
3-Арил-5-((тозилметил)имино)-5H,6H-бензо[b]фуро[3',4':2,3]пирроло[1,2-d][1,4]оксазин-1,2,6-трионы формулы
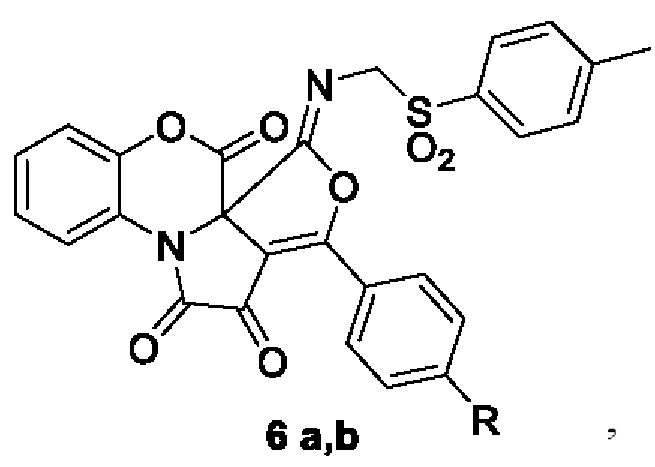
где R=H (6a), Cl (6b), обладающие противомикробной активностью.
| Способ получения 3-арил-7-фенилспиро[фуро[3',4':2,3]пирроло[1,2-a]хиноксалин-5,3'-индолин]-1,2,2',6(7Н)-тетраонов, обладающих противомикробной активностью | 2021 |
|
RU2758379C1 |
| (Z)-5-замещенные-3-(гидрокси(арил)метилен)-3а-(фенилтио)-3,3а-дигидропирроло[1,2-a]хиноксалин-1,2,4(5H)-трионы, обладающие противомикробной активностью | 2021 |
|
RU2759006C1 |
| MOROZ A.A | |||
| et al | |||
| Diversity-oriented synthesis of three skeletally diverse iminolactones from isocyanides, activated acetylenes and lH-pyrrole-2, 3-diones via [3+2] and [4+1] cycloaddition reactions, Tetrahedron | |||
| Способ восстановления спиралей из вольфрамовой проволоки для электрических ламп накаливания, наполненных газом | 1924 |
|
SU2020A1 |
| T | |||
| Аппарат, предназначенный для летания | 0 |
|
SU76A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| WO 2017153919 A1, 14.09.2017. | |||
Авторы
Даты
2023-12-27—Публикация
2023-03-28—Подача