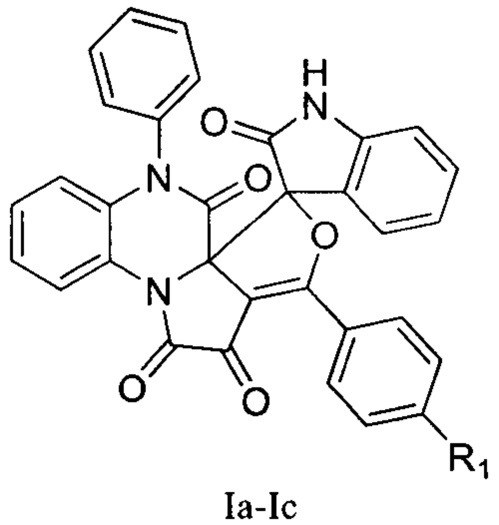
Изобретение относится к области органической химии, а именно к способу получения новых биологически активных веществ класса замещенных спиро[фуро[3',4':2,3]пирроло[1,2-а]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраонов общей формулы:
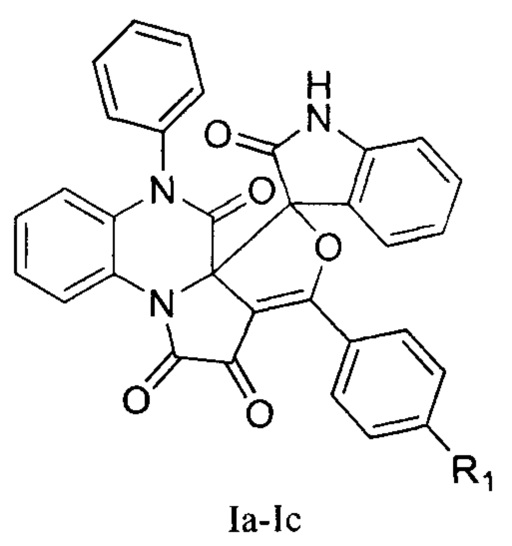
где R1=NO2 (Ia); R1=Cl (Ib); R1=CH3 (Ic),
обладающих противомикробной активностью. Указанное свойство предполагает возможность использования данного ряда соединений в медицине в качестве лекарственных средств (табл. 1).
Ближайшим структурным аналогом заявляемых соединений является метил (1R,31S,4aR,4a1S,10aS,11aR)-1,31,11а-тригидрокси-4,4,9-триметил-2,10-диоксо-1,2,31,4a,5,9,10,11а-октагидро-4H,4a1H-пирролизино[7',1',2':2,3,4]бензофуро[7а,7,6-cd]индол-4а1-карбоксилат [М.С. Nakhla, J.L. Wood, JACS, 2017, 139, p. 18504-18507], синтезируемый по следующей схеме:
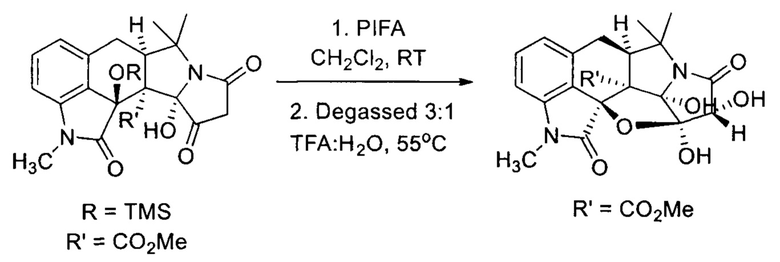
К недостаткам данного способа относится невозможность получения 3-арил-7-дифенилспиро[фуро[3',4':2,3]пирроло[1,2-а]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраонов.
Задачей создания изобретения является разработка простого способа синтеза не описанных в литературе 3-арил-7-дифенилспиро[фуро[3',4':2,3]пирроло[1,2-а]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраонов.
Достигаемый технический результат - разработан способ получения новых соединений, обладающих противомикробным действием.
Технический результат достигается тем, что 3-ароил-5-фенилпирроло[1,2-а]хиноксалин-1,2,4(5H)-трионы подвергают взаимодействию с 3-диазоиндолин-2-оном в среде ацетонитрила с последующим выделением целевых продуктов.
Схема синтеза заявляемых соединений:
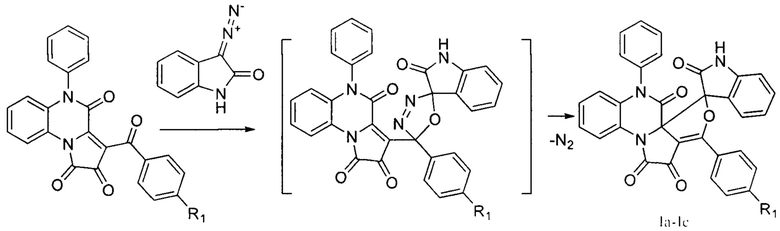
где R1=NO2 (Ia); R1=Cl (Ib); R1=CH3 (Ic).
Процесс ведут при 83°С, в качестве растворителя используют безводный ацетонитрил.
Из патентной и технической литературы не были выявлены способы получения 3-арил-7-дифенилспиро[фуро[3',4':2,3]пирроло[1,2-а]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраонов, имеющие сходные признаки с заявленным способом, а именно не использовались исходные продукты, растворитель, в котором проходит реакция, на основании чего можно сделать вывод о соответствии заявленного технического решения критерию «новизна» и «изобретательский уровень».
Изобретение иллюстрируется следующими примерами.
Пример 1. 3-(4-нитрофенил)-7-фенилспиро[фуро[3',4':2,3]пирроло[1,2-а]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраон (Ia).
Раствор 0.439 г (1.0 ммоль) 3-(4-нитробензоил)-5-фенилпирроло[1,2-а]хиноксалин-1,2,4(5H)-триона и 0,159 г (1.0 ммоль) 3-диазоиндолин-2-она растворяли в 5 мл безводного ацетонитрила и при кипячении перемешивали в течение 4 часов (до исчезновения темно-фиолетовой окраски исходного соединения), охлаждали, образовавшийся осадок соединения Ia отфильтровывали.
Выход 70%, т.пл. 230-232°С (из ацетонитрила).
ИК спектр (вазелиновое масло, см-1): 3192 (N-НСОиндол), 1750 (С1=O), 1730 (С4=O), 1682 (NHC=Оиндол, С2=O).
Спектр ЯМР 1Н (400 МГц, ДМСО-d6) δ, м.д.:
6.34-6.36 д. (1Н, Н6), 6.61-6.63 д. (1Н), 6.83-8.52 гр.с. (15Н), 10.85 с (1Н, NHиндол).
Найдено, %: С 65.79: Н 3.78; N 7.19. C32H18N4O7.
Вычислено, %: С, 67.37; Н, 3.18; N, 9.82.
Соединения Ib-Ic получены аналогично. Характеристики синтезированных соединений приведены в табл. 1.
Пример 2. 3-(4-хлорфенил)-7-дифенилспиро[фуро[3',4':2,3]пирроло[1,2-а]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраон (Ib).
Выход 77%, т.пл. 245-246°С (из ацетонитрила).
ИК спектр (вазелиновое масло, см-1): 3267 (N-HCOиндол), 1751 (С1=O), 1731 (С4=O), 1681 (NHC=Oиндол, С2=О).
Спектр ЯМР 1Н (400 МГц, ДМСО-d6) δ, м.д.:
6.33-6.35 д. (1Н, Н6), 6.61-6.63 д. (1Н), 6.82-8.26 гр.с. (15Н), 10.82 с (1H, NHиндол).
Найдено, %: С 68.67; Н 3.28; N 7.52. C32H18ClN3O5.
Вычислено, %: С, 68.64; Н, 3.24; N, 7.50.
Пример 3. 3-(п-толил)-7-фенилспиро[фуро[3',4':2,3]пирроло[1,2-а]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраон (Ic).
Выход 45%, т.пл. 242-244°С (из ацетонитрила).
ИК спектр (вазелиновое масло, см-1): 3168 (N-HCOиндол), 1752 (С1=O), 1741 (C4=O), 1711 (NHC=Oиндол), 1688 (С2=O).
Спектр ЯМР 1Н (400 МГц, ДМСО-d6) δ, м.д.:
2.47 с (3Н, Me), 6.33-6.35 д. (1Н, Н6), 6.61-6.63 д. (1Н), 6.82-8.16 гр.с. (14Н), 10.80 с (1Н, NHиндол).
Найдено, %: С 73.48; Н 3.93; N 7.81. C33H21N3O5.
Вычислено, %: С, 73.46; Н, 3.92; N, 7.79.
Соединения Ia-d представляют собой желтые кристаллические вещества с высокими температурами плавления, легкорастворимые в ДМФА и ДМСО, труднорастворимые в хлороформе, этилацетате, дихлорэтане, нерастворимые в алканах и воде.
Пример 4. Исследование противомикробной активности 3-арил-7-фенилспиро[фуро[3',4':2,3]пирроло[1,2-а]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраонов.
Для исследований использовали общепринятый метод двукратных серийных разведений в жидкой питательной среде микрометодом [Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ - М.: И-во Медицина, 2005]. Готовили исходные разведения микроорганизмов в физиологическом растворе из суточной агаровой культуры по оптическому стандарту мутности (ОСО) на 5 ME с использованием денситометра. После ряда разведений конечная концентрация клеток в опыте составляла 2,5×105 клеток/мл.
В лунках стерильного 96 луночного плоскодонного микропланшета готовили два параллельных ряда двукратных серийных разведений химических соединений в бульоне РПБ. В каждой лунке содержалось 150 мкл определенной концентрации испытуемого вещества и 150 мкл инокулята культуры. В последних рядах содержалась питательная среда и культура в равных объемах (контроль). Максимально испытанная концентрация соответствовала 1000,0 мкг/мл, минимальная - 2,0 мкг/мл. Микропланшет помещали в термостат спектрофотометра Epoch и замеряли оптическую плотность (ОН) при длине волны 540 нм. Через 24 часа вновь регистрировали ОН культуральной жидкости.
Результаты оценивали с помощью программного обеспечения Gen 5 спектрофотометра для микропланшет Epoch. Последняя лунка ряда с задержкой роста и показателями ОП равной оптической плотности контрольной лунки соответствует минимальной подавляющей концентрацией соединения.
Противомикробные свойства химических веществ изучали на 3-х коллекционных условно-патогенных штаммах микроорганизмов: Staphylococcus aureus (штамм 906). Escherichia coli (штамм 1257), Candida albicans, 1353.
Анализ полученных данных показал, что соединения Ib и Ic проявляют ингибирующее и бактерицидное действие в отношении культуры S. Aureus в концентрации 1000 мкг/мл, а соединение Ia в этой же концентрации проявляет только ингибирующее действие.
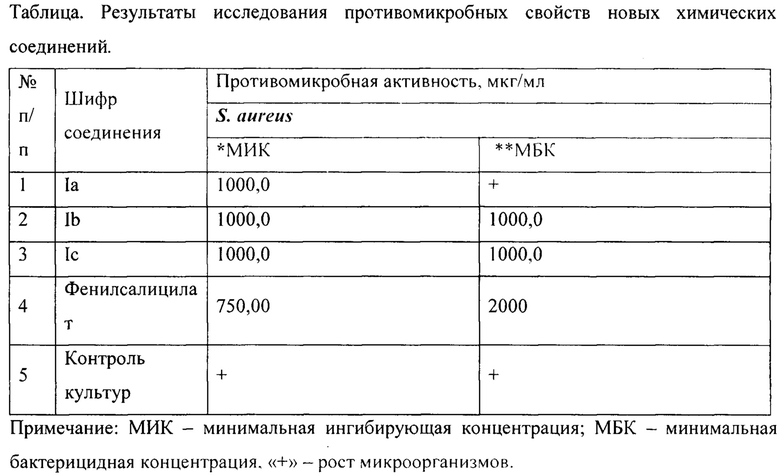
Таким образом, исследуемые соединения Ia-с обладают противомикробным действием, сравнимым или превышающим таковое для эталона - фенилсалицилата.
Изобретение относится к способу получения 3-арил-7-дифенилспиро[фуро[3',4':2,3]пирроло[1,2-а]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраонов, общей формулы
 ,
,
где R1=NO2 (Ia); R1=Cl (Ib); R1=CH3 (Ic), который заключается в том, что 3-ароил-5-фенилпирроло[1,2-а]хиноксалин-1,2,4(5H)-трионы подвергают взаимодействию с 3-диазоиндолин-2-оном в среде ацетонитрила с последующим выделением целевых продуктов. Технический результат – разработан способ получения новых соединений, которые могут найти применение в медицине в качестве противомикробных лекарственных средств. 4 пр., 1 табл.
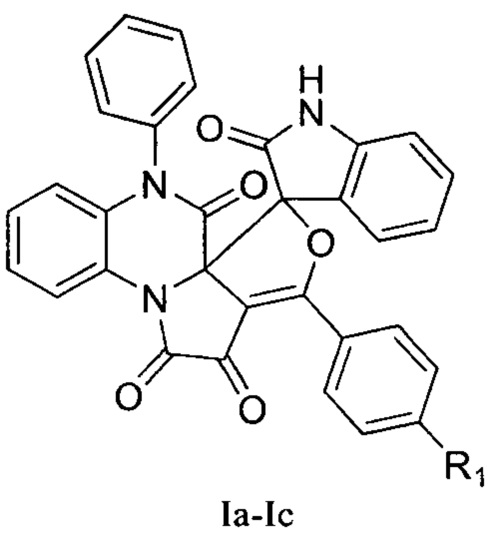
Способ получения 3-арил-7-дифенилспиро[фуро[3',4':2,3]пирроло[1,2-а]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраонов, общей формулы
 ,
,
где R1=NO2 (Ia); R1=Cl (Ib); R1=CH3 (Ic),
обладающих противомикробной активностью,
заключающийся в том, что 3-ароил-5-фенилпирроло[1,2-а]хиноксалин-1,2,4(5H)-трионы подвергают взаимодействию с 3-диазоиндолин-2-оном в среде ацетонитрила с последующим выделением целевых продуктов.
| Mina C | |||
| Nakhla and John L.Wood, J | |||
| Am | |||
| Chem | |||
| Soc., 139, 2017, pp.18504-18507 | |||
| КАСАТКИНА С.О | |||
| и др., Журнал органической химии, т.54, вып | |||
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| 2'-Амино-2,5'-диоксо-5-фенил-1,2,5',6',7',8'-гексагидро-1'Н-спиро[пиррол-3,4'-хинолины] | 2020 |
|
RU2743922C1 |
| 6'-АРИЛ-2'-(2-ГИДРОКСИФЕНИЛ)-11',11'-ДИМЕТИЛ-3',4,4',13'-ТЕТРАОКСОСПИРО[2,5-ЦИКЛОГЕКСАДИЕН-1,9'-(7'-ОКСА-2',12'-ДИАЗАТЕТРАЦИКЛО[6.5.1.0.0]ТЕТРАДЕЦ-5'-ЕН)]-14'-КАРБОКСИЛАТЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2011 |
|
RU2485126C1 |
| 10-Бензил-3,4-дибензоил-2´-оксо-1´,2´,10,10a-тетрагидроспиро[бензо[4,5]имидазо[2,1-b][1,3]оксазин-2,3´-пирролы] | 2017 |
|
RU2668969C1 |
| 1,6'-ДИАРИЛ-3-АРОИЛ-4-ГИДРОКСИ-1',3'-ДИМЕТИЛСПИРО[ПИРРОЛ-2,5'-ПИРРОЛО[2,3-d]ПИРИМИДИН]-2',4',5(1Н,1'Н,3'Н)-ТРИОНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2012 |
|
RU2502738C2 |
Авторы
Даты
2021-10-28—Публикация
2021-03-11—Подача