Изобретение относится к области органической химии, а именно к применению индивидуальных соединений класса 3-арил-6H-спиро[бензо[b]фуро[3',4':2,3]пирроло[1,2-d][1,4]оксазин-5,3'-индолин]-1,2,2',6-тетраонов в качестве средств, обладающих противотуберкулезной активностью, которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем и в фармакологии.
Заявленные соединения 3-арил-6H-спиро[бензо[b]фуро[3',4':2,3]пирроло[1,2-d][1,4]оксазин-5,3'-индолин]-1,2,2',6-тетраоны 3а-с и способ синтеза их производных известны из уровня техники. Заявляемые соединения являются продуктом взаимодействия 3-ароил-1H-бензо[b]пирроло[1,2-d][1,4]оксазин-1,2,4-трионов 1а,b с 3-диазоиндолин-2-онами 2а,b (Схема 1) (A facile approach to spiro[dihydrofuran-2,3'-oxindoles] via formal [4+1] annulation reaction of fused 1H-pyrrole-2,3-diones with diazooxindoles / P.A. Topanov, A.A. Maslivets, M.V. Dmitriev [et al.] // Beilstein Journal of Organic Chemistry. - 2022. - Vol. 18. - P. 1532-1538. - DOI 10.3762/bjoc. 18.162), образуются по следующей схеме:
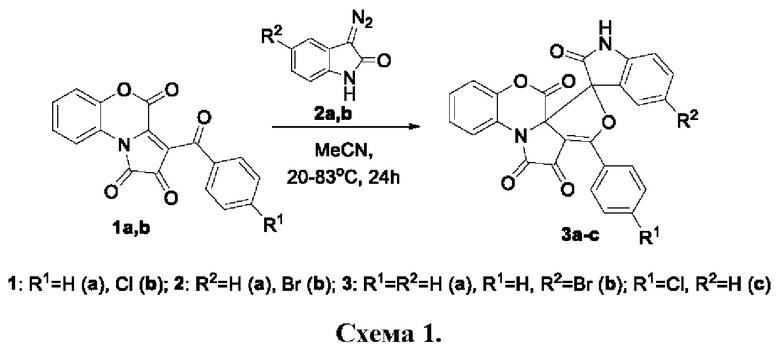
Известна противотуберкулезная активность 1-бензоил-5,5-диметил-5,6-дигидропирроло[2,1-а]изохинолин-2,3-диона 4 (Схема 2) (Патент №2783286 С1 Российская Федерация, МПК C07D 471/04, A61K 31/4745, А61Р 31/06. Применение 1-бензоил-5,5-диметил-5,6-дигидропирроло[2,1-а]изохинолин-2,3-диона в качестве средства, обладающего противотуберкулезной активностью: №2022105252: заявл. 28.02.2022: опубл. 11.11.2022 / И.В. Машевская, П.А. Топанов, С.Ю. Баландина, Ю.В. Шкляев; заявитель Федеральное государственное автономное образовательное учреждение высшего образования "Пермский государственный национальный исследовательский университет").
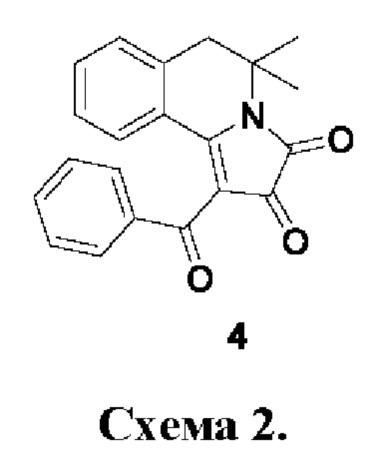
Соединение 4 проявляет ингибирующее действие в отношении культуры М. tuberculosis штамма H37Rv в концентрации 62,5 мкг/мл.
Противотуберкулезная активность 3-арил-6H-спиро[бензо[6]фуро[3',4':2,3]пирроло[1,2-d][1,4]оксазин-5,3'-индолин]-1,2,2',6-тетраонов ранее не известна.
Задачей изобретения является изыскание новых соединений, обладающих противотуберкулезной активностью, и расширение арсенала средств воздействия на живой организм.
Технический результат - получение нового соединения, которое может быть использовано в качестве исходных продуктов для синтеза новых гетероциклических систем и в фармакологии как обладающее противотуберкулезной активностью.
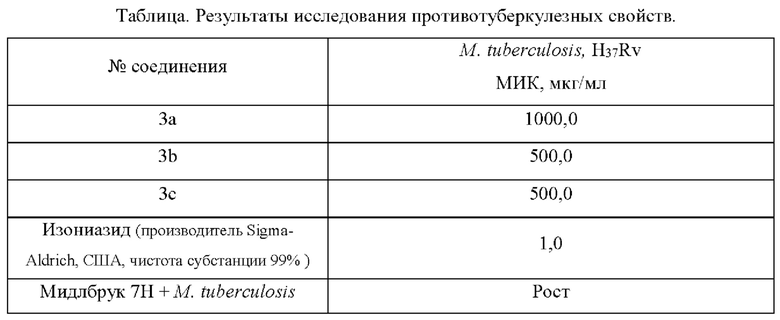
Поставленная задача решается тем, что соединение 3-фенил-6H-спиро[бензо[b]фуро[3',4':2,3]пирроло[1,2-d][1,4]оксазин-5,3'-индолин]-1,2,2',6-тетраон 3а проявляет ингибирующее действие в отношении культуры М. tuberculosis штамма H37Rv в концентрации 1000,0 мкг/мл, соединения 5'-бром-3-фенил-6H-спиро[бензо[b]фуро[3',4':2,3]пирроло[1,2-d][1,4]оксазин-5,3'-индолин]-1,2,2',6-тетраон 3b и 3-(4-хлорфенил)-6H-спиро[бензо[b]фуро[3',4':2,3]пирроло[1,2-d][1,4]оксазин-5,3'-индолин]-1,2,2',6-тетраон 3 с проявляют ингибирующее действие в отношении культуры М. tuberculosis штамма H37Rv в концентрации 500,0 мкг/мл.
Синтезируют заявляемые соединения путем взаимодействия 3-ароил-1H-бензо[b]пирроло[1,2-d][1,4]оксазин-1,2,4-трионов 1а,b с 3-диазоиндолин-2-онами 2а,b в среде растворителя с выделением целевого продукта, по следующей схеме (Схема 3):
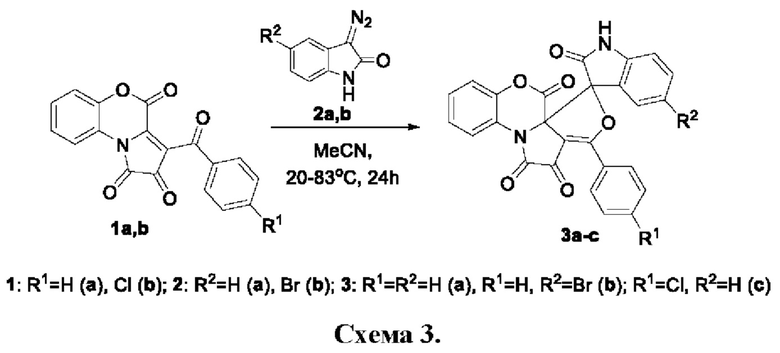
Процесс ведут при температуре 20°С для получения соединений 3а,с и при температуре 83°С для получения соединения 3b, в качестве растворителя используют безводный ацетонитрил.
Изобретение иллюстрируется следующими примерами.
Пример 1. 3-Фенил-6H-спиро[бензо[b]фуро[3',4':2,3]пирроло[1,2-d][1,4]оксазин-5,3'-индолин]-1,2,2',6-тетраон (3а).
К смеси 0.5 ммоль соединения 1а и 0.5 ммоль 3-диазоиндолин-2-она 2а в виале добавляли 3 мл абсолютного ацетонитрила, перемешивали при температуре 20°С в течение 24 ч, образовавшийся осадок отфильтровывали, промывали ацетонитрилом.
Выход 73%, т.пл. 246-247°С (AN, разл.).
Соединение (3а) C26H14N2O6.
Найдено, %: С 69.33; Н 3.14; N 6.23.
Вычислено, %: С 69.33; Н 3.13; N 6.22.
Соединение 3а - бледно-желтое кристаллическое вещество с высокой температурой плавления, плавящееся с разложением, растворимое при нагревании в этилацетате, растворимое в ацетонитриле, 1,4-диоксане, ДМСО, ДМФА, ацетоне, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
Спектр ЯМР 1Н соединения 3а снят в растворе ДМСО-d6 при частоте 400 МГц: δ=10.83 (с, 1H), 8.24 (м, 2Н), 7.86 (м, 1H), 7.72 (м, 2Н), 7.30 (м, 3f), 7.06 (м, 1H), 7.00 - 6.90 (м, 3Н), 6.65 (м, 1H) м.д.
Спектр ЯМР 13С соединения 3а снят в растворе ДМСО-d6 при частоте 100 МГц: δ=173.15, 169.11, 167.41, 160.65, 158.76, 147.02, 143.17, 141.50, 132.59, 130.10 (2С), 129.98 (2С), 127.86, 124.59, 123.95, 123.08, 122.76, 121.77, 121.48, 121.31, 116.67, 110.80, 104.33, 91.02, 70.58, 21.56 м.д.
Пример 2. 5'-Бром-3-фенил-6H-спиро[бензо[b]фуро[3',4':2,3]пирроло[1,2-d][1,4]оксазин-5,3'-индолин]-1,2,2',6-тетраон (3b).
К смеси 0.5 ммоль соединения 1а и 0.5 ммоль 5-бром-3-диазоиндолин-2-она 2b в виале добавляли 3 мл абсолютного ацетонитрила, перемешивали при температуре 83°С в течение 24 ч, образовавшийся осадок отфильтровывали, промывали ацетонитрилом. Выход 60%, т.пл. 225-226°С (AN, разл.).
Соединение (3b) C26H13BrN2O6.
Найдено, %: С 59.01; Н 2.48; N 5.30.
Вычислено, %: С 59.00; Н 2.48; N 5.29.
Соединение 3b - бледно-желтое кристаллическое вещество с высокой температурой плавления, плавящееся с разложением, растворимое при нагревании в этилацетате, ацетонитриле, 1,4-диоксане, ДМСО, ДМФА, ацетоне, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
Спектр ЯМР 1Н соединения 3b снят в растворе ДМСО-d6 при частоте 400 МГц: δ=11.00 (с, 1H), 8.23 (м, 2Н), 7.85 (м, 1H), 7.72 (м, 2Н), 7.50 - 7.44 (м, 1H), 7.36 (м, 1H), 7.29 (м, 2Н), 7.12 - 7.06 (м, 1H), 6.98 (м, 1H), 6.59 (м, 1H) м.д.
Спектр ЯМР 13С соединения 3b снят в растворе ДМСО-d6 при частоте 100 МГц: δ=173.14, 169.01, 166.82, 160.44, 158.35, 143.16, 140.82, 135.44, 135.27, 130.09 (2С), 129.25 (2С), 127.92, 127.27, 125.73, 124.75, 123.40, 121.88, 121.44, 116.72, 114.04, 112.63, 104.46, 90.51, 71.18 м.д.
Пример 3. 3-(4-Хлорфенил)-6H-спиро[бензо[b]фуро[3',4':2,3]пирроло[1,2-d][1,4]оксазин-5,3'-индолин]-1,2,2',6-тетраон (3с).
К смеси 0.5 ммоль соединения 1b и 0.5 ммоль 3-диазоиндолин-2-она 2а в виале добавляли 3 мл абсолютного ацетонитрила, перемешивали при температуре 20°С в течение 24 ч, образовавшийся осадок отфильтровывали, промывали ацетонитрилом.
Выход 71%, т.пл. 225-226°С (AN, разл.).
Соединение (3 с) C26H13ClN2O6.
Найдено, %: С 64.44; Н 2.71; N 5.80.
Вычислено, %: С 64.41; Н 2.70; N 5.78.
Соединение 3с - бледно-желтое кристаллическое вещество с высокой температурой плавления, плавящееся с разложением, растворимое при нагревании в этилацетате, растворимое в ацетонитриле, 1,4-диоксане, ДМСО, ДМФА, ацетоне, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
Спектр ЯМР 1Н соединения 3с снят в растворе ДМСО-d6 при частоте 400 МГц: δ=10.83 (с, 1H), 8.23 (м, 2Н), 7.81 (м, 2Н), 7.28 (м, 3Н), 7.04 (м, 2Н), 6.97 - 6.89 (м, 2Н), 6.64 (м, 1H) м.д.
Спектр ЯМР 13С соединения 3с снят в растворе ДМСО-d6 при частоте 100 МГц: δ=173.38, 168.98, 165.68, 160.31, 158.53, 143.17, 141.46, 140.43, 132.66, 131.49 (2С), 129.65 (2С), 127.95, 124.64, 124.50, 124.24, 122.78, 121.84, 121.40, 121.21, 116.69, 110.75, 105.40, 91.34, 70.65 м.д.
Пример 4. Фармакологическое исследование соединений 3а-с на наличие противотуберкулезной активности.
Для исследований химических веществ использован микрометод двукратных серийных разведений в жидкой питательной среде с использованием индикатора роста резазурина натриевой соли [Palomino J., Martin A., Camacho М. et al. Resazurin Microliter Assay Plate: Simple and Inexpensive Method for Detection of Drug Resistance in Mycobacterium tuberculosis. Resazurin Microtiter Assay Plate: Simple and Inexpensive Method for Detection of Drug Resistance in Mycobacterium tuberculosis // Antimicrobial Agents and Chemotherapy. 2002. Vol. 46, N 8.P. 2720-2722. https://doi.org/10.1128/AAC.46.8.2720].
Исследуемые вещества в количестве 10 мг растворяли в 0,5 мл диметилсульфоксида, после чего добавляли 4,5 мл 0,9% изотонического раствора хлорида натрия, тем самым получая исходный раствор в 2,0 мг/мл.
В лунках стерильного 96-луночного плоскодонного микропланшета готовили два параллельных ряда двукратных серийных разведений химических соединений в питательной жидкой среде Мидлбрук 7Н, содержащую обогатительную добавку ВАСТЕС MGIT OADC (олеиновая кислота, альбумин, декстроза и каталаза). В каждой лунке содержалось 150 мкл определенной концентрации испытуемого вещества.
Из 14-суточной культуры М. tuberculosis штамм H37Rv готовили бактериальную суспензию, которая была стандартизирована по оптическому стандарту мутности Мак-Фарланда №1 с использованием денситометра, после чего инокулят разводили 1:20 в питательной среде Мидлбрук 7Н9 и вносили в каждую лунку планшета по 150 мкл.
В последних рядах содержалась питательная среда и культура в равных объемах (контроль). Максимально испытанная концентрация соответствовала 1000,0 мкг/мл, минимальная - 1,0 мкг/мл.
Планшеты запечатывали в полиэтиленовые пакеты и инкубировали при 37°С в течение 8 суток. Через 8 дней инкубации в каждую лунку добавляли 30 мкл 0,01% раствора натрия резазурината, приготовленного в стерильной дистиллированной воде и культивировали еще 24 часа при 37°С, затем оценивали визуально изменение окраски резазурина. Изменение от синего до розового цвета указывает на снижение резазурина и, следовательно, рост бактерий. МИК - минимальная ингибирующая концентрация химических веществ, при которой не происходило изменение цвета.
Соединение 3а ингибирует рост культуры М. tuberculosis в концентрации 1000,0 мкг/мл, соединения 3b,с ингибируют рост культуры М. tuberculosis в концентрации 500,0 мкг/мл.
Предлагаемые вещества 3-фенил-6H-спиро[бензо[b]фуро[3',4':2,3]пирроло[1,2-d][1,4]оксазин-5,3'-индолин]-1,2,2',6-тетраон 3а, 5'-бром-3-фенил-6H-спиро[бензо[b]фуро[3',4':2,3]пирроло[1,2-d][1,4]оксазин-5,3'-индолин]-1,2,2',6-тетраон 3b, 3-(4-хлорфенил)-6H-спиро[бензо[b]фуро[3',4':2,3]пирроло[1,2-d][1,4]оксазин-5,3'-индолин]-1,2,2',6-тетраон 3с обладают фармакологической активностью, а именно противотуберкулезной активностью, и могут найти применение в фармакологии в качестве потенциального лекарственного средства.
Изобретение относится к области органической химии, а именно к применению 3-арил-6H-спиро[бензо[b]фуро[3',4':2,3]пирроло[1,2-d][1,4]оксазин-5,3'-индолин]-1,2,2',6-тетраонов 3a-c в качестве средств, обладающих противотуберкулезной активностью. 1 табл., 4 пр.
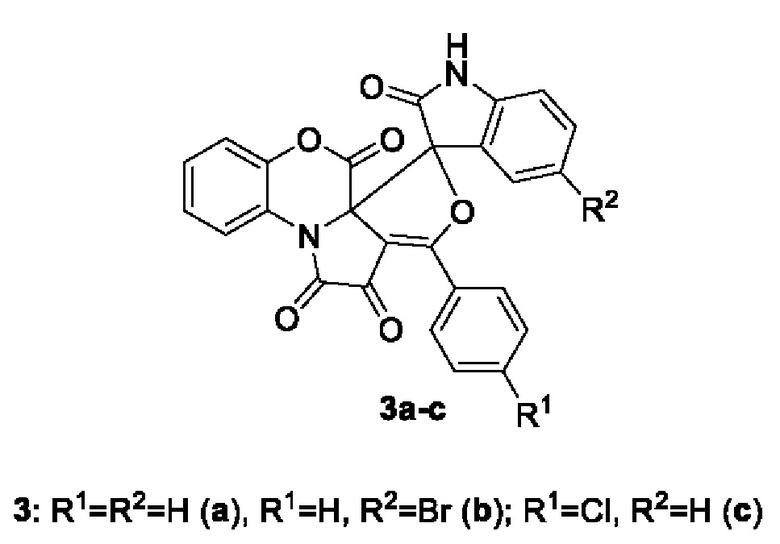
Применение 3-арил-6H-спиро[бензо[b]фуро[3',4':2,3]пирроло[1,2-d][1,4]оксазин-5,3'-индолин]-1,2,2',6-тетраонов 3a-c
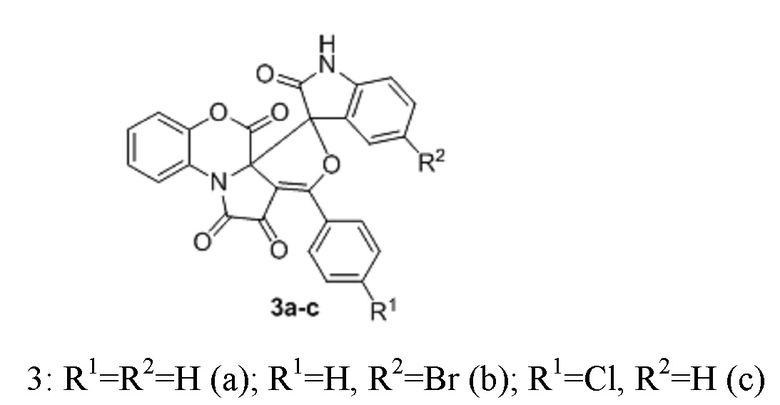
в качестве средств, обладающих противотуберкулезной активностью.
Авторы
Даты
2024-12-04—Публикация
2024-03-27—Подача