1. Перекрестная ссылка на родственные заявки
Данная заявка испрашивает приоритет на основании предварительной заявки на патент США № 62/679611, поданной 1 июня 2018 года, и предварительной заявки на патент США № 62/684046, поданной 12 июня 2018 года, содержание которых включено в данный документ посредством ссылки во всей своей полноте.
2. Перечень последовательностей
Настоящая заявка содержит перечень последовательностей, который был подан в электронном виде в формате ASCII и тем самым включен посредством ссылки во всей своей полноте. Копия в формате ASCII, созданная 10 мая 2019 года, имеет название NOV-003WO_SL, и ее размер составляет 400375 байт.
3. Включение посредством ссылки
Все публикации, патенты, заявки на патенты и другие документы, цитируемые в настоящей заявке, тем самым включены в данный документ посредством ссылки во всей своей полноте для всех целей в той же степени, как если бы каждая отдельная публикация, патент, заявка на патент или другой документ были отдельно указаны как включенные посредством ссылки для всех целей. В случае наличия любых несоответствий между идеями одного или нескольких литературных источников, включенных в данный документ, и настоящего изобретения предполагается, что следует руководствоваться идеями настоящего описания.
4. Уровень техники
BCMA является представителем семейства рецепторов фактора некроза опухоли (TNFR), который экспрессируется на клетках B-клеточной линии дифференцировки. Экспрессия BCMA является наиболее высокой на терминально дифференцированных B-клетках, которые приобретают судьбу долгоживущих плазматических клеток, в том числе на плазматических клетках, плазмобластах и в субпопуляции активированных B-клеток и B-клеток памяти. BCMA участвует в опосредовании выживания плазматических клеток для поддержания длительного гуморального иммунитета. Было показано, что экспрессия BCMA связана с рядом видов рака, аутоиммунных нарушений и инфекционных заболеваний. Виды рака с повышенной экспрессией BCMA включают некоторые формы гематологического рака, такие как множественная миелома, лимфома Ходжкина и неходжкинская лимфома, различные формы лейкоза и глиобластома.
Различные BCMA-связывающие молекулы находятся в клинической разработке, включая конъюгаты антитела к BCMA и лекарственного средства, такие как GSK2857916 (GlaxoSmithkline), и биспецифические BCMA-связывающие молекулы, нацеливающиеся на BMCA и CD3, такие как PF06863135 (Pfizer), EM 901 (EngMab), JNJ-64007957 (Janssen) и AMG 420 (Amgen). См. Cho et al., 2018, Front Immunol. 9:1821; WO 2016/0166629.
Одной из основных проблем безопасности любых лекарственных средств на основе антител, включая CD3-биспецифические молекулы, является их потенциал к индукции опасных для жизни побочных эффектов, таких как синдром высвобождения цитокинов ("CRS"). См. Shimabukuro-Vornhagen, A. et al., 2018, J. Immunother Cancer. 6:56.
Таким образом, существует неудовлетворенная медицинская потребность в полипептидах, например в антителах и полиспецифических связывающих молекулах, которые связывают BCMA и которые имеют улучшенный профиль безопасности (например, снижение высвобождения цитокинов), сохраняя при этом высокую эффективность.
5. Краткое описание
В настоящем изобретении предусмотрены BCMA-связывающие молекулы, которые специфически связываются с ВСМА человека, например антитела, их антигенсвязывающие фрагменты и полиспецифические молекулы, которые специфически связываются с ВСМА человека.
В одном аспекте в настоящем изобретении предусмотрены моноспецифические BCMA-связывающие молекулы (например, антитела и их антигенсвязывающие фрагменты), содержащие антигенсвязывающий домен ВСМА ("ABD"). Иллюстративные BCMA-связывающие молекулы, которые могут быть моноспецифическими, описаны в разделе 7.2 и конкретных вариантах осуществления 1-142 ниже.
В другом аспекте в настоящем изобретении предусмотрены полиспецифические связывающие молекулы ("MBM") (например, биспецифические связывающие молекулы ("BBM")), содержащие первый ABD, который специфически связывается с BCMA человека ("ABD1" или "ABD к BCMA"), и второй ABD, который специфически связывается со вторым антигеном ("ABD2"), например, с CD3 человека или другим компонентом комплекса TCR (иногда называемый в данном документе "ABD к TCR"). Термины ABD1, ABD2, ABD к BCMA и ABD к TCR используются исключительно для удобства и не предполагаются как обозначающие какую-либо конкретную конфигурацию BBM. В некоторых вариантах осуществления ABD к TCR связывается с CD3 (называется в данном документе "ABD к CD3" или т. п.). Соответственно, изобретения, относящиеся к ABD2 и ABD к TCR, также применимы к ABD к CD3. Такие мультиспецифические молекулы можно использовать для направления CD3+ эффекторных Т-клеток к ВСМА+ сайтам, тем самым позволяя CD3+ эффекторным Т-клеткам атаковать и лизировать ВСМА+ клетки и опухоли. Признаки иллюстративных MBM описаны в разделах 7.2-7.6 и конкретных вариантах осуществления 143-716 ниже.
ABD могут быть на основе иммуноглобулинов или на основе, отличной от иммуноглобулинов, и MBM могут включать ABD на основе иммуноглобулинов или любую комбинацию ABD на основе иммуноглобулинов и ABD на основе, отличной от иммуноглобулинов. ABD на основе иммуноглобулинов, которые можно использовать в BCMA-связывающих молекулах, описаны в разделах 7.2 и 7.3.1 и конкретных вариантах осуществления 147-329 ниже. ABD на основе, отличной от иммуноглобулинов, которые можно применять в MBM, описаны в разделе 7.3.2 и конкретных вариантах осуществления 330-331 ниже. Дополнительные признаки иллюстративных ABD, которые связываются с BCMA, описаны в разделе 7.2 и конкретных вариантах осуществления 147-155 ниже. Дополнительные признаки иллюстративных ABD, которые связываются с компонентом комплекса TCR, описаны в разделе 7.3.3 и конкретных вариантах осуществления 156-331 ниже.
ABD BCMA-связывающей молекулы (или их части), могут быть соединены друг с другом, например, посредством коротких пептидных линкеров или посредством Fc-домена. Способы и компоненты для соединения ABD и их частей с образованием BCMA-связывающей молекулы описаны в разделе 7.4 и конкретных вариантах осуществления 332-620 ниже.
В некоторых вариантах осуществления MBM по настоящему изобретению представляет собой BBM. BBM содержат по меньшей мере два ABD (т. е. BBM является по меньшей мере бивалентной), но также могут содержать более двух ABD. Например, BBM может содержать три ABD (т. е. быть тривалентной) или четыре ABD (т. е. быть тетравалентной), при условии, что BBM содержит по меньшей мере один ABD, который способен связывать BCMA, и по меньшей мере один ABD, который способен связывать антиген-мишень, отличный от BCMA. Иллюстративные бивалентные, тривалентные и тетравалентные конфигурации BBM показаны на фиг. 1 и описаны в разделе 7.5 и конкретных вариантах осуществления 621-681 ниже.
В настоящем изобретении дополнительно предусмотрены нуклеиновые кислоты, кодирующие BCMA-связывающие молекулы (либо в виде одной нуклеиновой кислоты, либо в виде совокупности нуклеиновых кислот), и рекомбинантные клетки-хозяева и линии клеток, сконструированные для экспрессии нуклеиновых кислот и BCMA-связывающих молекул. Иллюстративные нуклеиновые кислоты, клетки-хозяева и линии клеток описаны в разделе 7.7 и конкретных вариантах осуществления 1051-1057 ниже.
В настоящем изобретении также предусмотрены BCMA-связывающие молекулы с увеличенным периодом полужизни in vivo. Примеры таких BCMA-связывающих молекул, описаны в разделе 7.8 и конкретных вариантах осуществления 836-845 ниже.
В настоящем изобретении дополнительно предусмотрены конъюгаты лекарственных средств, содержащие ВСМА-связывающие молекулы. Такие конъюгаты для удобства называются в данном документе "конъюгатами антител и лекарственных средств" или "ADC", несмотря на то, что некоторые ABD могут представлять собой домены, отличные от иммуноглобулиновых. Примеры ADC описаны в разделе 7.9 и конкретных вариантах осуществления 851-889 ниже.
В настоящем изобретении также предусмотрены конъюгаты, содержащие ВСМА-связывающие молекулы и полипептид, маркер, диагностическое или выявляемое средство или твердую подложку. Примеры таких конъюгатов описаны в разделах 7.10 и 7.11 и конкретных вариантах осуществления 846-850 и 890-891 ниже.
Также предусмотрены фармацевтические композиции, содержащие BCMA-связывающие молекулы и ADC. Примеры фармацевтических композиций описаны в разделе 7.12 и конкретном варианте осуществления 892 ниже.
В данном документе дополнительно предусмотрены способы применения BCMA-связывающих молекул, ADC и фармацевтических композиций, например, для лечения пролиферативных состояний (например, видов рака), при которых экспрессируется BCMA, для лечения аутоиммунных нарушений и для лечения других заболеваний и состояний, ассоциированных с экспрессией BCMA. Иллюстративные способы описаны в разделе 7.13 и конкретных вариантах осуществления 893-971 и 1012-1050 ниже.
В настоящем изобретении дополнительно предусмотрены способы применения BCMA-связывающих молекул, ADC и фармацевтических композиций в комбинации с другими средствами и видами терапии. Иллюстративные средства, виды терапии и способы комбинированной терапии описаны в разделе 7.14 и конкретных вариантах осуществления 972-1011 ниже.
6. Краткое описание графических материалов
Фиг. 1A-1AG: Иллюстративные конфигурации BBM. На фиг. 1A проиллюстрированы компоненты иллюстративных конфигураций BBM, проиллюстрированных на фиг. 1B-1AG. Не все участки, соединяющие различные домены каждой цепи, проиллюстрированы (например, линкер, соединяющий VH- и VL-домены scFv, шарнирный участок, соединяющий CH2- и CH3-домены Fc-домена, и т. д. пропущены). На фиг. 1B-1F проиллюстрированы бивалентные BBM; на фиг. 1G-1Z проиллюстрированы тривалентные BBM; на фиг. 1AA-1AG проиллюстрированы тетравалентные BBM.
Фиг. 2A-2I: Моноклональный фаговый ELISA с ВСМА-реактивными клонами (пример 1). ФИГ. 2A: PI-26; фиг. 2B: PI-28; фиг. 2C: PI-61; фиг. 2D: PIII-79; фиг. 2E: PIII-78; фиг. 2F: PIV-24; фиг. 2G: PII-55; фиг. 2H: PII-45; фиг. 2I: PI-45.
Фиг. 3A-3I: Титрование растворимого ВСМА на поверхности отдельных клонов дрожжей (пример 2). Фиг. 3A: клон H2/L2-18; фиг. 3B: клон H2/L2-2; фиг. 3C: клон H2/L2-68; фиг. 3D: клон H2/L2-80; фиг. 3E: клон H2/L2-83; фиг. 3F: клон H2/L2-88; фиг. 3G: клон H2/L2-47; фиг. 3H: клон H2/L2-36; фиг. 3I: клон H2/L2-34.
Фиг. 4: Последовательности CDR-H2 исходного PI-61 (SEQ ID NO:113) и выбранных клонов H2/L2-22 (SEQ ID NO:114), H2/L2-88 (SEQ ID NO:115), H2/L2-36 (SEQ ID NO:115), H2/L2-34 (SEQ ID NO:116), H2/L2-68 (SEQ ID NO:117), H2/L2-18 (SEQ ID NO:118), H2/L2-47 (SEQ ID NO:115), H2/L2-20 (SEQ ID NO:112), H2/L2-80 (SEQ ID NO:112), и H2/L2-83 (SEQ ID NO:115).
Фиг. 5: Последовательности CDR-L2 исходного PI-61 (SEQ ID NO:103) и выбранных клонов H2/L2-22 (SEQ ID NO:104), H2/L2-88 (SEQ ID NO:105), H2/L2-36 (SEQ ID NO:105), H2/L2-34 (SEQ ID NO:106), H2/L2-68 (SEQ ID NO:107), H2/L2-18 (SEQ ID NO:106), H2/L2-47 (SEQ ID NO:106), H2/L2-20 (SEQ ID NO:102), H2/L2-80 (SEQ ID NO:108), и H2/L2-83 (SEQ ID NO:105).
Фиг. 6: Формат гетеродимерного биспецифического антитела биспецифических антител из примера 3.
Фиг. 7: Последовательности CDR-H2 исходного PI-61 (SEQ ID NO:113) и выбранных клонов H3-1 (SEQ ID NO:119), H3-2 (SEQ ID NO:120), H3-3 (SEQ ID NO:121), H3-4 (SEQ ID NO:119), H3-5 (SEQ ID NO:122), H3-6 (SEQ ID NO:119), H3-7 (SEQ ID NO:112), H3-8 (SEQ ID NO:119), H3-9 (SEQ ID NO:119), H3-10 (SEQ ID NO:120), H3-11 (SEQ ID NO:123), H3-12 (SEQ ID NO:124), H3-13 (SEQ ID NO:119), H3-14 (SEQ ID NO:119), и H3-15 (SEQ ID NO:125).
Фиг. 8: Последовательности CDR-L2 исходного PI-61 (SEQ ID NO:155) и выбранных клонов H3-1 (SEQ ID NO:157), H3-2 (SEQ ID NO:157), H3-3 (SEQ ID NO:157), H3-4 (SEQ ID NO:156), H3-5 (SEQ ID NO:157), H3-6 (SEQ ID NO:157), H3-7 (SEQ ID NO:157), H3-8 (SEQ ID NO:157), H3-9 (SEQ ID NO:157), H3-10 (SEQ ID NO:157), H3-11 (SEQ ID NO:157), H3-12 (SEQ ID NO:157), H3-13 (SEQ ID NO:156), H3-14 (SEQ ID NO:161), и H3-15 (SEQ ID NO:156).
Фиг. 9: Последовательности CDR-H3 исходного PI-61 (SEQ ID NO:49) и выбранных клонов H3-1 (SEQ ID NO:127), H3-2 (SEQ ID NO:128), H3-3 (SEQ ID NO:127), H3-4 (SEQ ID NO:127), H3-5 (SEQ ID NO:129), H3-6 (SEQ ID NO:127), H3-7 (SEQ ID NO:130), H3-8 (SEQ ID NO:127), H3-9 (SEQ ID NO:127), H3-10 (SEQ ID NO:131), H3-11 (SEQ ID NO:132), H3-12 (SEQ ID NO:133), H3-13 (SEQ ID NO:127), H3-14 (SEQ ID NO:127), и H3-15 (SEQ ID NO:134).
Фиг. 10: Скрининг с помощью ELISA клонов, полученных в примере 4, для тестирования связывания с рекомбинантным полноразмерным hBCMA и cynoBCMA.
Фиг. 11A-11S: Графики биослойной интерферометрии (BLI), демонстрирующие связывание выбранных человеческих антител к ВСМА с hBCMA (пример 4). ФИГ. 11A: R1F2; фиг. 11B: PALF01; фиг. 11C: PALF03; фиг. 11D: PALF04; фиг. 11E: PALF05; фиг. 11F: PALF06; фиг. 11G: PALF07; фиг. 11H: PALF08; фиг. 11I: PALF09; фиг. 11J: PALF11; фиг. 11K: PALF12; фиг. 11L: PALF13; фиг. 11M: PALF14; фиг. 11N: PALF15; фиг. 11O: PALF16; фиг. 11P: PALF17; фиг. 11Q: PALF18; фиг. 11R: PALF19; фиг. 11S: PALF20.
Фиг. 12A-12S: Графики биослойной интерферометрии (BLI), демонстрирующие связывание выбранных человеческих антител к ВСМА с cynoBCMA (пример 4). ФИГ. 12A: R1F2; фиг. 12B: PALF01; фиг. 12C: PALF03; фиг. 12D: PALF04; фиг. 12E: PALF05; фиг. 12F: PALF06; фиг. 12G: PALF07; фиг. 12H: PALF08; фиг. 12I: PALF09; фиг. 12J: PALF11; фиг. 12K: PALF12; фиг. 12L: PALF13; фиг. 12M: PALF14; фиг. 12N: PALF15; фиг. 12O: PALF16; фиг. 12P: PALF17; фиг. 12Q: PALF18; фиг. 12R: PALF19; фиг. 12S: PALF20.
Фиг. 13A-13D: Противоопухолевая активность бивалентного или тривалентного AB1 (фиг. 13A и фиг. 13B) и AB2 (фиг. 13C и фиг. 13D) к BCMA-CD3 в адаптации адоптивного переноса PBMC человека ортотопической модели опухоли KMS11Luc (пример 6). Серый круг: доза 0,03 мг/кг; серый треугольник: доза 0,3 мг/кг; серый ромб: доза 3,0 мг/кг; черный круг: только опухоль; черный квадрат: необработанный контроль. * p < 0,05, критерий множественного сравнения Даннета.
Фиг. 14A-14D: Изменение массы тела после лечения с помощью бивалентного или тривалентного AB1 (фиг. 14A и фиг. 14B) или AB2 (фиг. 14C и фиг. 14D) к BCMA-CD3 в адаптации адоптивного переноса PBMC человека ортотопической модели опухоли KMS11Luc (пример 6). Серый круг: доза 0,03 мг/кг; серый треугольник: доза 0,3 мг/кг; серый ромб: доза 3,0 мг/кг; черный круг: только опухоль; черный квадрат: необработанный контроль.
Фиг. 15A-15F: Противоопухолевая активность бивалентного или тривалентного AB1 (фиг. 15A и фиг. 15B), AB2 (фиг. 15C и фиг. 15D) и AB3 (фиг. 15E и фиг. 15F) к BCMA-CD3 в адаптации адоптивного переноса PBMC человека ортотопической модели опухоли KMS11Luc (пример 7). Серый круг: доза 0,03 мг/кг; серый треугольник: доза 0,3 мг/кг; серый ромб: доза 3,0 мг/кг; черный круг: только опухоль; черный квадрат: необработанный контроль. * p < 0,05, критерий множественного сравнения Даннета.
Фиг. 16A-16F: Изменение массы тела после лечения с помощью бивалентного или тривалентного AB1 (фиг. 16A и фиг. 16B), AB2 (фиг. 16C и фиг. 16D) и AB3 (фиг. 16E и фиг. 16F) к BCMA-CD3 в адаптации адоптивного переноса PBMC человека ортотопической модели опухоли KMS11Luc (пример 7). Серый круг: доза 0,03 мг/кг; серый треугольник: доза 0,3 мг/кг; серый ромб: доза 3,0 мг/кг; черный круг: только опухоль; черный квадрат: необработанный контроль.
Фиг. 17: Экспрессия BCMA на клеточной поверхности в линиях клеток множественной миеломы, оцененная с помощью проточной цитометрии (пример 8). Дельта-показатель средней интенсивности флуоресценции (MFI) определяли посредством вычитания MFI неокрашенных клеток из MFI клеток, окрашенных антителом к BCMA, меченым BV421.
Фиг. 18: Результаты EC50 для RTCC, индуцированной биспецифическим антителом к BCMA-CD3, на линиях клеток BCMA+ MM с использованием размножившихся Т-клеток (пример 8).
Фиг. 19A-19B: Антитело к BCMA-CD3 опосредовало RTCC на линиях клеток BCMA+ MM MM1S (фиг. 19A) и MC116 (фиг. 19B) с использованием свежевыделенных Т-клеток (пример 8).
Фиг. 20A-B: Секреция цитокинов, индуцированная биспецифическими антителами к BCMA-CD3 (пример 9). ФИГ. 20A: IFN-γ; фиг. 20B: TNF-α.
Фиг. 21A-21B: Биспецифическое антитело к ВСМА-CD3 опосредовало пролиферацию Т-клеток в присутствии линий клеток BCMA+ ММ MM1S (фиг. 21A) и MC116 (фиг. 21B) (пример 9).
Фиг. 22A-22B: Временная динамика концентрации растворимого BCMA (sBCMA) (фиг. 22A) и экспрессии связанного с мембраной BCMA (mBCMA) (фиг. 22B) из клеток линии KMS11, обработанных ингибиторами гамма-секретазы LY411575 и PF03084014 (пример 10). Данные для необработанных клеток показаны незакрашенными кругами, данные для клеток, обработанных с помощью LY415575, показаны закрашенными квадратами, а данные для клеток, обработанных с помощью PF03084014, показаны закрашенными ромбами.
Фиг. 23A-23B: Временная динамика концентрации sBCMA (фиг. 23A) и экспрессии mBCMA (фиг. 23B) из клеток линии KMS11, предварительно обработанных ингибитором гамма-секретазы LY411575 в течение 22 часов до измерения временной динамики (пример 10). Данные для необработанных клеток показаны незакрашенными кругами, а данные для клеток, обработанных с помощью LY415575, показаны закрашенными квадратами.
Фиг. 24A-24C: Результаты анализа RTCC комбинаций бивалентного AB3 и ингибиторов гамма-секретазы LY411575 (фиг. 24A), PR03084014 (фиг. 24B) и BMS0708163 (фиг. 24C) (пример 11). Концентрация бивалентного AB3 (нМ) показана на оси X.
Фиг. 25A-C: Результаты анализов, демонстрирующие влияние GSI на локализацию BCMA (фиг. 25A), передачу сигналов NOTCH (фиг. 25B) и активность бивалентного AB3 (фиг. 25C) (пример 12).
Фиг. 26: уровни mBCMA в модели ксенотрансплантата KMS11 после обработки с помощью PFZ03084014, оцененные с помощью проточной цитометрии (пример 13).
Фиг. 27: Уровни sBCMA в модели ксенотрансплантата KMS11 после обработки с помощью PFZ03084014, оцененные с помощью ELISA (пример 13).
Фиг. 28A-C: Уровни цитокинов в супернатантах культур клеток после 48 часов совместного культивирования клеток линии KMS11 и Т-клеток (соотношение 1:3) в присутствии gH (контроль), бивалентного AB3 и h2B4_C29 (пример 14). ФИГ. 28A: Уровни IFN-γ; фиг. 28B: Уровни IL-2; фиг. 28C: Уровни TNF-α.
7. Подробное описание
7.1. Определения
Предполагается, что используемые в данном документе следующие термины имеют приведенные ниже значения.
ADCC: Используемый в данном документе термин "ADCC" или "антителозависимая клеточноопосредованная цитотоксичность" означает клеточноопосредованную реакцию, где неспецифические цитотоксические клетки, которые экспрессируют FcγR, распознают связанное антитело на клетке-мишени и затем вызывают лизис клетки-мишени. ADCC коррелирует со связыванием с FcγRIIIa; повышение связывания с FcγRIIIa приводит к повышению активности ADCC.
ADCP: Используемый в данном документе термин "ADCP" или антителозависимый клеточноопосредованный фагоцитоз означает клеточноопосредованную реакцию, где неспецифические фагоцитарные клетки, которые экспрессируют FcγR, распознают связанное антитело на клетке-мишени и затем вызывают фагоцитоз клетки-мишени.
Дополнительное средство: Для удобства средство, которое применяют в комбинации с антигенсвязывающей молекулой по настоящему изобретению, в данном документе называется "дополнительным" средством.
Антитело: Используемый в данном документе термин "антитело" относится к полипептиду (или к набору полипептидов) из семейства иммуноглобулинов, который способен к связыванию антигена нековалентно, обратимо и специфически. Например, встречающееся в природе "антитело" типа IgG представляет собой тетрамер, содержащий по меньшей мере две тяжелые (H) цепи и две легкие (L) цепи, соединенные между собой посредством дисульфидных связей. Каждая тяжелая цепь состоит из вариабельного участка тяжелой цепи (сокращенно обозначенного в данном документе как VH) и константного участка тяжелой цепи. Константный участок тяжелой цепи состоит из трех доменов - CH1, CH2 и CH3. Каждая легкая цепь состоит из вариабельного участка легкой цепи (сокращенно обозначенного в данном документе как VL) и константного участка легкой цепи. Константный участок легкой цепи состоит из одного домена (сокращенно обозначенного в данном документе как CL). VH- и VL-участки могут быть дополнительно подразделены на участки гипервариабельности, называемые участками, определяющими комплементарность (CDR), которые чередуются с участками, являющимися более консервативными, называемыми каркасными участками (FR). Каждый VH и VL состоит из трех CDR и четырех FR, расположенных от амино-конца к карбокси-концу в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. Вариабельные участки тяжелой и легкой цепей содержат связывающий домен, который взаимодействует с антигеном. Константные участки антител способны опосредовать связывание иммуноглобулина с тканями хозяина или факторами, включая различные клетки иммунной системы (например, эффекторные клетки) и первый компонент (Clq) классического пути активации системы комплемента. Термин "антитело" включает без ограничения моноклональные антитела, человеческие антитела, гуманизированные антитела, камелизированные антитела, химерные антитела, биспецифические или полиспецифические антитела и антиидиотипические (анти-Id) антитела (в том числе, например, анти-Id антитела к антителам по настоящему изобретению). Антитела могут относиться к любому изотипу/классу (например, IgG, IgE, IgM, IgD, IgA и IgY) или подклассу (например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2).
Как легкая, так и тяжелая цепи подразделяются на участки структурной и функциональной гомологии. Термины "константный" и "вариабельный" используются в функциональном смысле. В связи с этим следует понимать, что вариабельные домены из частей как легкой (VL), так и тяжелой (VH) цепей определяют распознавание антигена и специфичность. Напротив, константные домены легкой цепи (CL) и тяжелой цепи (CH1, CH2 или CH3) придают важные биологические свойства, такие как секреция, трансплацентарный переход, связывание с Fc-рецепторами, связывание комплемента и т. п. Принято, что нумерация доменов константных участков возрастает по мере их удаления от антигенсвязывающего сайта или аминоконца антитела. В антителе дикого типа N-конец представляет собой вариабельный участок, и C-конец представляет собой константный участок; CH3- и CL-домены фактически содержат карбоксиконец тяжелой и легкой цепей соответственно.
Фрагмент антитела: Используемый в данном документе термин "фрагмент антитела" из антитела относится к одной или нескольким частям антитела. В некоторых вариантах осуществления эти части представляют собой часть контактного(контактных) домена(доменов) антитела. В некоторых других вариантах осуществления эта(эти) часть(части) представляет(представляют) собой антигенсвязывающие фрагменты, которые сохраняют способность к связыванию антигена нековалентно, обратимо и специфически и иногда называются в данном документе "антигенсвязывающим фрагментом", "его антигенсвязывающим фрагментом", "антигенсвязывающей частью" и т. п. Примеры связывающих фрагментов включают без ограничения одноцепочечные Fv (scFv), Fab-фрагмент, моновалентный фрагмент, состоящий из VL-, VH-, CL- и CH1-доменов; F(ab)2-фрагмент, бивалентный фрагмент, содержащий два Fab-фрагмента, соединенных дисульфидным мостиком в шарнирном участке; Fd-фрагмент, состоящий из VH- и CH1-доменов; Fv-фрагмент, состоящий из VL- и VH-доменов одного плеча антитела; dAb-фрагмент (Ward et al., (1989) Nature 341:544-546), который состоит из VH-домена; и выделенный участок, определяющий комплементарность (CDR). Таким образом, термин "фрагмент антитела" охватывает как протеолитические фрагменты антител (например, Fab- и F(ab)2-фрагменты), так и сконструированные белки, содержащие одну или несколько частей антитела (например, scFv).
Фрагменты антител также могут быть включены в состав однодоменных антител, максиантител, миниантител, интрател, диател, триател, тетрател, v-NAR и бис-scFv (см., например, Hollinger and Hudson, 2005, Nature Biotechnology 23: 1126-1136). Фрагменты антител могут быть привиты на каркасные структуры на основе полипептидов, таких как фибронектин III типа (Fn3) (см. патент США № 6703199, в котором описаны монотела на основе полипептида фибронектина).
Фрагменты антител могут быть включены в состав одноцепочечных молекул, содержащих пару тандемных Fv-сегментов (например, VH-CH1-VH-CH1), которые вместе с комплементарными полипептидами легкой цепи (например, VL-VC-VL-VC) образуют пару антигенсвязывающих участков (Zapata et al., 1995, Protein Eng. 8:1057-1062 и патент США № 5641870).
Система нумерации антител: В настоящем описании ссылки на пронумерованные аминокислотные остатки в доменах антител приводятся на основе системы нумерации EU, если не указано иное (например, в таблицах 1C-1N). Эта система была первоначально разработана Edelman et al., 1969, Proc. Nat'l Acad. Sci. USA 63:78-85 и описана подробно в Kabat et al., 1991, в Sequences of Proteins of Immunological Interest, US Department of Health and Human Services, NIH, USA.
Антигенсвязывающий домен: Термин "антигенсвязывающий домен" или "ABD" относится к части антигенсвязывающей молекулы, которая обладает способностью связываться с антигеном нековалентно, обратимо и специфически. Иллюстративные ABD включают антигенсвязывающие фрагменты и части как каркасных структур на основе иммуноглобулинов, так и каркасных структур на основе молекул, отличных от иммуноглобулинов, которые сохраняют способность к связыванию антигена нековалентно, обратимо и специфически. Используемый в данном документе термин "антигенсвязывающий домен" охватывает фрагменты антител, которые сохраняют способность к связыванию антигена нековалентно, обратимо и специфически.
Цепь антигенсвязывающего домена или цепь ABD: Отдельные ABD могут существовать в виде одной (например, в случае scFv) полипептидной цепи или образовываться посредством ассоциации более чем одной полипептидной цепи (например, в случае Fab). Используемый в данном документе термин "цепь ABD" относится ко всему ABD или его части, которые существуют в виде одной полипептидной цепи. Использование термина "цепь ABD" предполагается только для удобства и описательных целей и не означает конкретную конфигурацию или способ получения.
Антигенсвязывающий фрагмент: Термин "антигенсвязывающий фрагмент" антитела относится к части антитела, которая сохраняет способность связываться с антигеном нековалентно, обратимо и специфически.
Антигенсвязывающая молекула: Термин "антигенсвязывающая молекула" относится к молекуле, содержащей один или несколько антигенсвязывающих доменов, например, к антителу. Антигенсвязывающая молекула может содержать одну или несколько полипептидных цепей, например одну, две, три, четыре или больше полипептидных цепей. Полипептидные цепи в антигенсвязывающей молекуле могут быть ассоциированы друг с другом непосредственно или опосредованно (например, первая полипептидная цепь может быть ассоциирована со второй полипептидной цепью, которая, в свою очередь, может быть ассоциирована с третьей полипептидной цепью с образованием антигенсвязывающей молекулы, в которой первая и вторая полипептидные цепи непосредственно ассоциированы друг с другом, вторая и третья полипептидные цепи непосредственно ассоциированы друг с другом, а первая и третья полипептидные цепи опосредованно ассоциированы друг с другом посредством второй полипептидной цепи).
Ассоциированный: Термин "ассоциированный" применительно к доменам или участкам в антигенсвязывающей молекуле относится к функциональной взаимосвязи между двумя или более полипептидными цепями и/или двумя или более частями одной полипептидной цепи. В частности, термин "ассоциированный" означает, что два или более полипептидов (или частей одного полипептида) ассоциированы друг с другом, например, нековалентно посредством молекулярных взаимодействий и/или ковалентно посредством одного или нескольких дисульфидных мостиков или химических сшивок таким образом, что они образуют функциональный антигенсвязывающий домен. Примеры ассоциаций, которые могут присутствовать в антигенсвязывающей молекуле включают (без ограничения) ассоциации между Fc-участками в Fc-домене, ассоциации между VH- и VL-участками в Fab или Fv и ассоциации между CH1 и CL в Fab.
В-клетка: Используемый в данном документе термин "В-клетка" относится к клетке В-клеточной линии дифференцировки, которая принадлежит к типу белых кровяных клеток и подтипу лимфоцитов. Примеры В-клеток включают плазмобласты, плазматические клетки, лимфоплазмоцитоидные клетки, В-клетки памяти, фолликулярные В-клетки, В-клетки маргинальной зоны, B-1-клетки, B-2-клетки и регуляторные В-клетки.
В-клеточное злокачественное новообразование: Как используется в данном документе, В-клеточное злокачественное новообразование относится к неконтролируемой пролиферации В-клеток. Примеры В-клеточного злокачественного новообразования включают неходжкинские лимфомы (NHL), формы лимфомы Ходжкина, лейкоз и миелому. Например, В-клеточное злокачественное новообразование может представлять собой без ограничения множественную миелому, хронический лимфоцитарный лейкоз (CLL)/мелкоклеточную лимфоцитарную лимфому (SLL), фолликулярную лимфому, мантийноклеточную лимфому (MCL), диффузную крупноклеточную В-клеточную лимфому (DLBCL), формы лимфомы из клеток маргинальной зоны, лимфому Беркитта, лимфоплазмоцитарную лимфому (макроглобулинемию Вальденстрема), волосатоклеточный лейкоз, первичную лимфому центральной нервной системы (CNS), первичную медиастинальную крупноклеточную В-клеточную лимфому, медиастинальную лимфому "серой зоны" (MGZL), B-клеточную лимфому из клеток маргинальной зоны селезенки, внеузловую B-клеточную лимфому из клеток маргинальной зоны MALT, узловую B-клеточную лимфому из клеток маргинальной зоны и первичную эффузионную лимфому, а также новообразования из плазмоцитоидных дендритных клеток.
BCMA: Используемый в данном документе термин "ВСМА" относится к антигену созревания В-клеток. BCMA (также известный как TNFRSF17, BCM или CD269) является представителем семейства рецепторов фактора некроза опухоли (TNFR) и преимущественно экспрессируется на терминально дифференцированных B-клетках, например, B-клетках памяти и плазматических клетках. Его лиганды включают фактор активации В-клеток (BAFF) и лиганд, индуцирующий пролиферацию (APRIL). Белок BCMA кодируется геном TNFRSF17. Иллюстративные последовательности BCMA доступны в базе данных Uniprot под номером доступа Q02223.
Связывающие последовательности: Что касается таблицы 1 (включая ее подразделы), термин "связывающие последовательности" означает ABD, содержащий полный набор CDR, пару VH-VL или scFv, представленные в данной таблице.
Биспецифическая связывающая молекула: Термин "биспецифическая связывающая молекула" или "BBM" относится к молекуле, которая специфически связывается с двумя антигенами и содержит два или более ABD. BBM по настоящему изобретению содержат по меньшей мере один антигенсвязывающий домен, который является специфическим по отношению к BCMA, и по меньшей мере один антигенсвязывающий домен, который является специфическим по отношению к другому антигену, например, компоненту комплекса TCR. Иллюстративные BBM проиллюстрированы на фиг. 1B-1AG. BBM могут содержать одну, две, три, четыре или еще больше полипептидных цепей.
Бивалентный: Используемый в данном документе термин "бивалентный" применительно к антигенсвязывающей молекуле относится к антигенсвязывающей молекуле, которая содержит два ABD. Домены могут быть одинаковыми или разными. Соответственно, бивалентная антигенсвязывающая молекула может быть моноспецифической или биспецифической. Бивалентные BBM содержат ABD, который специфически связывается с BCMA, и другой ABD, который связывается с другим антигеном, например, компонентом комплекса TCR.
Рак. Термин "рак" относится к заболеванию, которое характеризуется неконтролируемым (и часто быстрым) ростом аберрантных клеток. Раковые клетки могут распространяться локально или через кровоток и лимфатическую систему в другие части организма. Примеры различных видов рака описаны в данном документе и включают без ограничения лейкемию, множественную миелому, бессимптомную миелому, лимфому Ходжкина и неходжкинскую лимфому, например, любые BCMA-положительные формы рака любого из вышеуказанных видов. Термин "раковая В-клетка" относится к В-клетке, которая подвергается или подверглась неконтролируемой пролиферации.
CD3: Термин "CD3" или "кластер дифференцировки 3" относится к корецептору Т-клеточного рецептора из кластера дифференцировки 3. CD3 помогает в активации как цитотоксических Т-клеток (например, CD8+ наивных Т-клеток), так и Т-хелперных клеток (например, CD4+ наивных Т-клеток) и состоит из четырех отдельных цепей: одной цепи CD3γ (например, под номерами доступа в Genbank NM_000073 и MP_000064 (человек)), одной цепи CD3δ (например, под номерами доступа в Genbank NM_000732, NM_001040651, NP_00732 и NP_001035741 (человек)) и двух цепей CD3ε (например, под номерами доступа в Genbank NM_000733 и NP_00724 (человек)). Цепи CD3 представляют собой белки клеточной поверхности с высокой степенью родства из суперсемейства иммуноглобулинов, содержащие единственный внеклеточный иммуноглобулиновый домен. Молекула CD3 ассоциирует с Т-клеточным рецептором (TCR) и ζ-цепью с образованием комплекса Т-клеточного рецептора (TCR), функция которого заключается в генерации сигналов активации в Т-лимфоцитах.
Если специально не указано иное, упоминание CD3 в настоящей заявке может относиться к корецептору CD3, корецепторному комплексу CD3 или любой полипептидной цепи корецепторного комплекса CD3.
Химерное антитело: Термин "химерное антитело" (или его антигенсвязывающий фрагмент) представляет собой молекулу антитела (или ее антигенсвязывающий фрагмент), в которой (a) константный участок или его часть изменены, заменены или обменены таким образом, что антигенсвязывающий сайт (вариабельный участок) связан с константным участком, соответствующим другим или измененным классу, эффекторной функции и/или виду, или с совершенно другой молекулой, которая придает новые свойства химерному антителу, например, ферментом, токсином, гормоном, фактором роста, лекарственным средством и т. д.; или (b) вариабельный участок или его часть изменены, заменены или обменены на вариабельный участок, обладающий другой или измененной специфичностью к антигену. Например, мышиное антитело можно модифицировать посредством замены его константного участка на константный участок из человеческого иммуноглобулина. Вследствие замены на человеческий константный участок химерное антитело может сохранять свою специфичность в распознавании антигена и при этом обладать пониженной антигенностью у человека по сравнению с исходным мышиным антителом.
Участок, определяющий комплементарность. Используемые в данном документе термины "участок, определяющий комплементарность" или "CDR" относятся к последовательностям аминокислот в пределах вариабельных участков антитела, которые придают специфичность к антигену и аффинность связывания. Например, как правило, имеются три CDR в каждом вариабельном участке тяжелой цепи (например, CDR-H1, CDR-H2 и CDR-H3) и три CDR в каждом вариабельном участке легкой цепи (CDR-L1, CDR-L2 и CDR-L3). Точные границы аминокислотной последовательности указанного CDR можно определить с применением любой из ряда широко известных схем, в том числе описанных в Kabat et al. (1991), "Sequences of Proteins of Immunological Interest," 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD (схема нумерации по "Kabat"), Al-Lazikani et al., (1997) JMB 273, 927-948 (схема нумерации по "Chothia") или их комбинации и схемы нумерации ImMunoGenTics (IMGT) (Lefranc, M.-P., The Immunologist, 7, 132-136 (1999); Lefranc, M.-P. et al., Dev. Comp. Immunol., 27, 55-77 (2003) (схема нумерации "IMGT"). Согласно комбинированной схеме нумерации по Kabat и Chothia для указанного CDR-участка (например, CDR1 HC, CDR2 HC, CDR3 HC, CDR1 LC, CDR2 LC или CDR3 LC) в некоторых вариантах осуществления CDR соответствуют аминокислотным остаткам, которые определены как часть CDR по Kabat, вместе с аминокислотными остатками, которые определены как часть CDR по Chothia. Как используется в данном документе, CDR, определенные в соответствии со схемой нумерации по "Chothia", также иногда называют "гипервариабельными петлями".
Например, согласно Kabat аминокислотные остатки CDR в вариабельном домене тяжелой цепи (VH) нумеруются как 31-35 (CDR-H1) (например, вставка(вставки) после положения 35), 50-65 (CDR-H2) и 95-102 (CDR-H3); и аминокислотные остатки CDR в вариабельном домене легкой цепи (VL) нумеруются как 24-34 (CDR-L1) (например, вставка(вставки) после положения 27), 50-56 (CDR-L2) и 89-97 (CDR-L3). В качестве другого примера согласно Chothia аминокислоты CDR в VH нумеруются как 26-32 (CDR-H1) (например, вставка(вставки) после положения 31), 52-56 (CDR-H2) и 95-102 (CDR-H3); и аминокислотные остатки в VL нумеруются как 26-32 (CDR-L1) (например, вставка(вставки) после положения 30), 50-52 (CDR-L2) и 91-96 (CDR-L3). В случае объединения определений CDR по Kabat и Chothia CDR содержат, например, аминокислотные остатки 26-35 (CDR-H1), 50-65 (CDR-H2) и 95-102 (CDR-H3) в VH человека и аминокислотные остатки 24-34 (CDR-L1), 50-56 (CDR-L2) и 89-97 (CDR-L3) в VL человека или состоят из них. Согласно IMGT аминокислотные остатки CDR в VH нумеруются как примерно 26-35 (CDR1), 51-57 (CDR2) и 93-102 (CDR3), и аминокислотные остатки CDR в VL нумеруются как примерно 27-32 (CDR1), 50-52 (CDR2) и 89-97 (CDR3) (нумерация в соответствии с "Kabat"). Согласно IMGT CDR-участки антитела можно определять с применением программы IMGT/DomainGapAlign. Как правило, если конкретно не указано иное, молекулы антител могут содержать любую комбинацию одного или нескольких CDR по Kabat и/или CDR по Chothia.
Одновременно: Термин "одновременно" не ограничивается введением средств терапии (например, профилактических или терапевтических средств) точно в одно и то же время, а скорее означает, что фармацевтическую композицию, содержащую антигенсвязывающую молекулу, вводят субъекту последовательно и в течение временного интервала таким образом, чтобы молекулы могли действовать вместе с дополнительным(дополнительными) средством(средствами) терапии с обеспечением большей пользы, чем если бы их вводили иным способом.
Консервативные модификации последовательностей: Термин "консервативные модификации последовательностей" относится к аминокислотным модификациям, которые не оказывают значительного влияния на характеристики связывания BCMA-связывающей молекулы или ее компонента (например, ABD или Fc-участка) или не изменяют их. Такие консервативные модификации включают аминокислотные замены, добавления и делеции. Модификации можно вводить в BBM с помощью стандартных методик, таких как сайт-направленный мутагенез и ПЦР-опосредованный мутагенез. Консервативные аминокислотные замены представляют собой замены, при которых аминокислотный остаток заменяют на аминокислотный остаток, имеющий сходную боковую цепь. Семейства аминокислотных остатков, имеющих сходные боковые цепи, были определены в уровне техники. Эти семейства включают аминокислоты с основными боковыми цепями (например, лизин, аргинин, гистидин), кислыми боковыми цепями (например, аспарагиновая кислота, глутаминовая кислота), незаряженными полярными боковыми цепями (например, глицин, аспарагин, глутамин, серин, треонин, тирозин, цистеин, триптофан), неполярными боковыми цепями (например, аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин), бета-разветвленными боковыми цепями (например, треонин, валин, изолейцин) и ароматическими боковыми цепями (например, тирозин, фенилаланин, триптофан, гистидин). Таким образом, один или несколько аминокислотных остатков в BBM можно заменить другими аминокислотными остатками из того же семейства боковой цепи, и измененную BBM можно тестировать в отношении, например, связывания с молекулами-мишенями и/или эффективной гетеродимеризации и/или эффекторной функции.
Диатело: Используемый в данном документе термин "диатело" относится к небольшим фрагментам антител с двумя антигенсвязывающими сайтами, как правило, образованным посредством спаривания цепей scFv. Каждый scFv содержит вариабельный домен тяжелой цепи (VH), соединенный с вариабельным доменом легкой цепи (VL) в той же полипептидной цепи (VH-VL, где VH расположен либо в N-концевом, либо в C-концевом направлении относительно VL). В отличие от типичного scFv, в котором VH и VL разделены линкером, который обеспечивает для VH и VL в одной и той же полипептидной цепи возможность спаривания и образования антигенсвязывающего домена, диатела, как правило, содержат линкер, который является слишком коротким для обеспечения возможности спаривания между VH- и VL-доменами в одной и той же цепи, что вынуждает VH- и VL-домены спариваться с комплементарными доменами другой цепи и образовывать два антигенсвязывающих сайта. Диатела описаны более подробно, например, в EP 404097; WO 93/11161 и Hollinger et al., 1993, Proc. Natl. Acad. Sci. USA 90:6444-6448.
dsFv: Термин "dsFv" относится к Fv-фрагментам, стабилизированным посредством дисульфидных связей. VH и VL в dsFv соединены междоменной дисульфидной связью. Для получения таких молекул по одной аминокислоте в каждом из каркасных участков VH и VL подвергают мутации по типу замены на цистеин, который в свою очередь образует стабильную межцепочечную дисульфидную связь. Как правило, положение 44 в VH и положение 100 в VL подвергают мутации по типу замены на остатки цистеина. См. Brinkmann, 2010, Antibody Engineering 181-189, DOI:10.1007/978-3-642-01147-4_14. Термин dsFv охватывает как то, что известно как dsFv (молекула, в которой VH и VL соединены межцепочечной дисульфидной связью, но не линкерным пептидом), так и то, что известно как scdsFv (молекула, в которой VH и VL соединены линкером, а также межцепочечной дисульфидной связью).
Эпитоп: Эпитоп или антигенная детерминанта представляет собой часть антигена, распознаваемую антителом или другим антигенсвязывающим фрагментом, описанным в данном документе. Эпитоп может быть линейным или конформационным.
Эффекторная функция: Термин "эффекторная функция" относится к активности молекулы антитела, которая опосредована связыванием посредством домена антитела, отличного от антигенсвязывающего домена, и обычно опосредована связыванием эффекторных молекул. Эффекторная функция включает комплемент-опосредованную эффекторную функцию, которая опосредована, например, связыванием компонента C1 комплемента с антителом. Активация комплемента важна для опсонизации и лизиса клеточных патогенов. Активация комплемента также стимулирует воспалительный ответ и может также участвовать в аутоиммунной гиперчувствительности. Эффекторная функция также включает эффекторную функцию, опосредованную Fc-рецептором (FcR), которая может запускаться при связывании константного домена антитела с Fc-рецептором (FcR). При связывании антитела с Fc-рецепторами на клеточных поверхностях запускается ряд важных и разнообразных биологических реакций, в том числе поглощение и разрушение частиц, покрытых антителами, выведение иммунных комплексов, ADCC, ADCP, высвобождение медиаторов воспаления, перенос через плаценту и контроль образования иммуноглобулинов. Эффекторная функция антитела может быть изменена посредством изменения, например, усиления или снижения аффинности антитела к эффектoрной молекуле, такой как Fc-рецептор или компонент комплемента. Аффинность связывания обычно будет варьироваться при модификации сайта связывания эффектoрной молекулы, и в данном случае целесообразно определить местоположение сайта, представляющего интерес, и модифицировать по меньшей мере часть данного сайта подходящим образом. Также предусматривается, что для изменения в сайте связывания эффекторной молекулы на антителе не является необходимым значительное изменение общей аффинности связывания, но можно изменять геометрию взаимодействия, делая эффекторный механизм неэффективным, как при непродуктивном связывании. Дополнительно предусматривается, что эффекторную функцию также можно изменять посредством модификации сайта, не участвующего непосредственно в связывании эффекторной молекулы, но иным образом участвующего в выполнении эффекторной функции.
Fab: Используемый в данном документе термин "Fab" или "Fab-участок" означает участок полипептида, который содержит VH-, CH1-, VL- и CL-домены иммуноглобулина. Эти термины могут относиться к данному участку в отдельности или к данному участку применительно к антигенсвязывающей молекуле.
Fab-домены образуются посредством ассоциации CH1-домена, присоединенного к VH-домену, с CL-доменом, присоединенным к VL-домену. VH-домен спарен с VL-доменом с образованием Fv-участка, и CH1-домен спарен с CL-доменом для дополнительной стабилизации связывающего модуля. Дисульфидная связь между двумя константными доменами может дополнительно стабилизировать Fab-домен.
Fab-участки можно получать посредством протеолитического расщепления молекул иммуноглобулинов (например, с применением ферментов, таких как папаин) или посредством рекомбинантной экспрессии. В молекулах нативных иммуноглобулинов Fab образуются посредством ассоциации двух разных полипептидных цепей (например, VH-CH1 в одной цепи ассоциирует с VL-CL в другой цепи). Как правило, Fab-участки экспрессируются рекомбинантно, как правило в двух полипептидных цепях, хотя в данном документе также рассматриваются одноцепочечные Fab.
Fc-участок: Используемый в данном документе термин "Fc-участок" или "Fc-цепь" означает полипептид, содержащий CH2-CH3-домены молекулы IgG, в некоторых случаях включая шарнирный участок. В системе нумерации EU в случае человеческого IgG1 CH2-CH3-домен состоит из аминокислот 231-447, а шарнирный участок состоит из аминокислот 216-230. Таким образом, определение "Fc-участок" включает как аминокислоты 231-447 (CH2-CH3), так и аминокислоты 216-447 (шарнирный участок-CH2-CH3), или их фрагменты. "Fc-фрагмент" в данном контексте может содержать меньше аминокислот с одного или обоих N- и C-концов, но все еще сохраняет способность к образованию димера с другим Fc-участком, что можно определить с использованием стандартных способов, как правило основанных на размере (например, хроматография в неденатурирующих условиях, эксклюзионная хроматография). Fc-участки человеческого IgG особенно применимы в настоящем изобретении и могут представлять собой Fc-участок из человеческого IgG1, IgG2 или IgG4.
Fc-домен: Термин "Fc-домен" относится к паре ассоциированных Fc-участков. Два Fc-участка димеризуются с образованием Fc-домена. Два Fc-участка в Fc-домене могут быть одинаковыми (такой Fc-домен упоминается в данном документе как "гомодимер Fc") или могут отличаться друг от друга (такой Fc-домен упоминается в данном документе как "гетеродимер Fc").
Fv: Термин "Fv", "Fv-фрагмент" или "Fv-участок" относится к участку, который содержит VL- и VH-домены фрагмента антитела в тесной нековалентной ассоциации (димер VH-VL). Именно в этой конфигурации три CDR каждого вариабельного домена взаимодействуют для определения сайта связывания мишени. Зачастую шесть CDR придают антигенсвязывающей молекуле специфичность связывания мишени. Однако, в некоторых случаях даже один вариабельный домен (или половина Fv, содержащая только три CDR, специфичных в отношении мишени) может обладать способностью распознавать и связывать мишень. В молекуле нативного иммуноглобулина VH и VL из Fv находятся в отдельных полипептидных цепях, но могут быть сконструированы в виде одноцепочечного Fv (scFv). Термины также включают Fv, которые сконструированы посредством введения дисульфидных связей для обеспечения большей стабильности.
Ссылка на димер VH-VL в данном документе не предполагается как обозначающая какую-либо конкретную конфигурацию. Например, VH в scFv может быть N-концевым или C-концевым по отношению к VL (при этом VH и VL как правило соединены линкером, как обсуждается в данном документе).
Полуантитело: Термин "полуантитело" относится к молекуле, которая содержит по меньшей мере один ABD или одну цепь ABD и способна ассоциировать с другой молекулой, содержащей ABD или цепь ABD, посредством, например, дисульфидного мостика или молекулярных взаимодействий (например, взаимодействий типа "выступ в углубление" между гетеродимерами Fc). Полуантитело может состоять из одной полипептидной цепи или более чем одной полипептидной цепи (например, двух полипептидных цепей Fab). В варианте осуществления полуантитело содержит Fc-участок.
Примером полуантитела является молекула, содержащая тяжелую и легкую цепь антитела (например, антитела IgG). Другим примером полуантитела является молекула, содержащая первый полипептид, содержащий VL-домен и CL-домен, и второй полипептид, содержащий VH-домен, CH1-домен, шарнирный домен, CH2-домен и CH3-домен, где VL- и VH-домены образуют ABD. Еще одним примером полуантитела является полипептид, содержащий scFv-домен, CH2-домен и CH3-домен.
Полуантитело может содержать более одного ABD, например полуантитело, содержащее (в направлении от N-конца к C-концу) scFv-домен, CH2-домен, CH3-домен и другой scFv-домен.
Полуантитела могут также содержать цепь ABD, которая при ассоциации с другой цепью ABD в другом полуантителе образует полный ABD.
Таким образом, BBM может содержать одно, более типично два или даже более двух полуантител, и полуантитело может содержать один или несколько ABD или цепей ABD.
В некоторых BBM первое полуантитело будет ассоциировать, например, гетеродимеризоваться, со вторым полуантителом. В других BBM первое полуантитело будет ковалентно связано со вторым полуантителом, например, посредством дисульфидных мостиков или химического сшивания. В еще одних BBM первое полуантитело будет ассоциировать со вторым полуантителом посредством как ковалентных присоединений, так и нековалентных взаимодействий, например, дисульфидных мостиков и взаимодействий типа "выступ в углубление".
Термин "полуантитело" предполагается только для описательных целей и не означает конкретную конфигурацию или способ получения. Описания полуантитела как "первого" полуантитела, "второго" полуантитела, "левого" полуантитела, "правого" полуантитела или т. п. приведены исключительно для удобства и описательных целей.
Углубление: Применительно к взаимодействию типа "выступ в углубление" "углубление" относится к по меньшей мере одной боковой цепи аминокислоты, которая углублена относительно области контакта первой Fc-цепи и, следовательно, может располагаться в компенсирующем "выступе" в соседней области контакта второй Fc-цепи, чтобы стабилизировать гетеродимер Fc и, таким образом, способствовать, например, образованию гетеродимера Fc вместо образования гомодимера Fc.
Клетка-хозяин или рекомбинантная клетка-хозяин: Термины "клетка-хозяин" или "рекомбинантная клетка-хозяин" относятся к клетке, которая была генетически сконструирована, например, посредством введения гетерологичной нуклеиновой кислоты. Следует понимать, что такие термины предполагаются как обозначающие не только конкретную рассматриваемую клетку, но и потомство такой клетки. Поскольку определенные модификации могут происходить в последующих поколениях либо из-за мутации, либо из-за влияний окружающей среды, такое потомство может в действительности не являться идентичным родительской клетке, но, тем не менее, оно все же включено в объем термина "клетка-хозяин", используемого в данном документе. Клетка-хозяин может нести гетерологичную нуклеиновую кислоту транзиентно, например, во внехромосомном гетерологичном векторе экспрессии, или стабильно, например, посредством интеграции гетерологичной нуклеиновой кислоты в геном клетки-хозяина. Для целей экспрессии антигенсвязывающей молекулы клетка-хозяин может относиться к линии клеток, происходящей от млекопитающих или обладающей характеристиками, сходными с характеристиками клеток млекопитающих, такой как клетки почки обезьяны (COS, например, COS-1, COS-7), HEK293, клетки почки новорожденного хомячка (BHK, например, BHK21), клетки яичника китайского хомячка (CHO), NSO, PerC6, BSC-1, клетки гепатоцеллюлярной карциномы человека (например, Hep G2), SP2/0, HeLa, клетки почки быка Мадин-Дарби (MDBK), клетки миеломы и лимфомы или их производные и/или сконструированные варианты. Сконструированные варианты включают, например, производные с модифицированным профилем гликанов и/или производные, модифицированные по сайтам сайт-специфической интеграции.
Гуманизированный: Термин "гуманизированные" формы антител, отличных от человеческих антител (например, мышиных антител), относится к химерным антителам, которые содержат минимальную последовательность, полученную из иммуноглобулина, отличного от человеческого иммуноглобулина. В большинстве случаев гуманизированные антитела представляют собой человеческие иммуноглобулины (реципиентное антитело), в которых остатки из гипервариабельного участка, полученного от реципиента, заменены остатками из гипервариабельного участка, полученного из вида, отличного от человека (донорное антитело), такого как мышь, крыса, кролик или примат, отличный от человека, обладающего необходимой специфичностью, аффинностью и способностью. В некоторых случаях остатки каркасного участка (FR) человеческого иммуноглобулина заменены соответствующими остатками, отличными от остатков человеческого иммуноглобулина. Кроме того, гуманизированные антитела могут содержать остатки, которые не обнаруживаются в реципиентном антителе или в донорном антителе. Эти модификации осуществляют для дополнительного улучшения характеристик антитела. Как правило, гуманизированное антитело будет содержать по существу все из по меньшей мере одного и, как правило, двух вариабельных доменов, в которых все или по существу все гипервариабельные петли соответствуют гипервариабельным петлям иммуноглобулина, отличного от человеческого иммуноглобулина, и все или по существу все FR представляют собой FR из последовательности lo человеческого иммуноглобулина. Гуманизированное антитело будет также необязательно содержать по меньшей мере часть константного участка иммуноглобулина (Fc), как правило, человеческого иммуноглобулина. Гуманизированные антитела, как правило, менее иммуногенны в отношении людей по сравнению с негуманизированными антителами и, таким образом, обладают терапевтическими преимуществами в определенных ситуациях. Гуманизированные антитела можно получать с применением известных способов. См., например, Hwang et al., 2005, Methods 36:35; Queen et al., 1989, Proc. Natl. Acad. Sci. U.S.A. 86:10029-10033; Jones et al., 1986, Nature 321:522-25, 1986; Riechmann et al., 1988, Nature 332:323-27; Verhoeyen et al.,1988, Science 239:1534-36; Orlandi et al., 1989, Proc. Natl. Acad. Sci. U.S.A. 86:3833-3837; патенты США №№ 5,225,539; 5,530,101; 5,585,089; 5,693,761; 5,693,762; и 6,180,370; и WO 90/07861. См. также следующие обзорные статьи и литературные источники, цитируемые в них: Presta, 1992, Curr. Op. Struct. Biol. 2:593-596; Vaswani and Hamilton, 1998, Ann. Allergy, Asthma & Immunol. 1:105-115; Harris, 1995, Biochem. Soc. Transactions 23:1035-1038; Hurle and Gross, 1994, Curr. Op. Biotech. 5:428-433.
Человеческое антитело: Используемый в данном документе термин "человеческое антитело" включает антитела, имеющие вариабельные участки, в которых как каркасные, так и CDR-участки получены из последовательностей, происходящих от человека. Кроме того, если антитело содержит константный участок, то константный участок также получен из таких человеческих последовательностей, например, человеческих последовательностей зародышевого типа, или мутантных вариантов человеческих последовательностей зародышевого типа, или антитела, содержащего консенсусные каркасные последовательности, полученные посредством анализа человеческих каркасных последовательностей, например, как описано в Knappik et al., 2000, J Mol Biol 296, 57-86. Структуры и местоположения вариабельных доменов иммуноглобулинов, например, CDR, можно определять с применением широко известных схем нумерации, например, схемы нумерации по Kabat, схемы нумерации по Chothia или любой комбинации схем по Kabat и по Chothia (см., например, Lazikani et al., 1997, J. Mol. Bio. 273:927-948; Kabat et al., 1991, Sequences of Proteins of Immunological Interest, 5th edit., NIH Publication no. 91-3242 U.S. Department of Health and Human Services; Chothia et al., 1987, J. Mol. Biol. 196:901-917; Chothia et al., 1989, Nature 342:877-883).
Человеческие антитела могут содержать аминокислотные остатки, которые не кодируются человеческими последовательностями (например, мутации, введенные посредством случайного или сайт-специфического мутагенеза in vitro или посредством соматической мутации in vivo, или консервативную замену, которая способствует стабильности или изготовлению). Однако используемый в данном документе термин "человеческое антитело" не предназначен для включения антител, в которых последовательности CDR, полученные из антитела зародышевого типа другого вида млекопитающих, такого как мышь, были привиты на человеческие каркасные последовательности.
[00100] В комбинации: Как используется в данном документе, вводимый "в комбинации" означает, что два (или более) различных средства для лечения доставляют субъекту в период, когда субъект страдает нарушением, например, два или более средства для лечения доставляют после того, как у субъекта было диагностировано нарушение, и до того, как нарушение было излечено или устранено или лечение было прекращено по другим причинам.
[00101] Выступ: Применительно к взаимодействию типа "выступ в углубление" "выступ" относится к по меньшей мере одной боковой цепи аминокислоты, которая выступает над областью контакта первой Fc-цепи и, следовательно, может располагаться в компенсирующем "углублении" в области контакта второй Fc-цепи, чтобы стабилизировать гетеродимер Fc и, таким образом, способствовать, например, образованию гетеродимера Fc вместо образования гомодимера Fc.
Выступы и углубления (или выступы в углубления): Один механизм гетеродимеризации Fc обычно упоминается в данной области техники как "выступы и углубления" или "выступы в углубления". Эти термины относятся к аминокислотным мутациям, которые создают стерические влияния, способствующие образованию гетеродимеров Fc вместо гомодимеров Fc, как описано, например, в Ridgway et al., 1996, Protein Engineering 9(7):617; Atwell et al., 1997, J. Mol. Biol. 270:26; и патенте США № 8216805. Мутации типа "выступ в углубление" можно комбинировать с другими стратегиями для улучшения гетеродимеризации, например, как описано в разделе 7.4.1.6.
Моноклональное антитело: Используемый в данном документе термин "моноклональное антитело" относится к полипептидам, включая антитела, фрагменты антител, молекулы (включая BBM) и т. д., которые получены из одного и того же генетического источника.
Моновалентный: Используемый в данном документе термин "моновалентный" применительно к антигенсвязывающей молекуле относится к антигенсвязывающей молекуле, которая содержит один антигенсвязывающий домен.
Полиспецифическая связывающая молекула: Термин "полиспецифическая связывающая молекула" или "MBM" относится к антигенсвязывающей молекуле, которая специфически связывается с по меньшей мере двумя антигенами и содержит два или более ABD. Каждый из ABD может независимо представлять собой фрагмент антитела (например, scFv, Fab, нанотело), лиганд или связывающее средство, полученное не из антитела (например, фибронектин, финомер, дарпин).
Мутация или модификация: Применительно к первичной аминокислотной последовательности полипептида термины "модификация" и "мутация" относятся к аминокислотной замене, вставке и/или делеции в полипептидной последовательности относительно эталонного полипептида. Кроме того, термин "модификация" дополнительно охватывает изменение аминокислотного остатка, например, посредством химической конъюгации (например, лекарственного средства или фрагмента полиэтиленгликоля) или посттрансляционной модификации (например, гликозилирования).
Нуклеиновая кислота: Термин "нуклеиновая кислота" используется в данном документе взаимозаменяемо с термином "полинуклеотид" и относится к дезоксирибонуклеотидам или рибонуклеотидам и их полимерам в однонитевой либо двухнитевой форме. Термин охватывает нуклеиновые кислоты, содержащие известные аналоги нуклеотидов или модифицированные остатки или связи в остове, которые являются синтетическими, встречающимися в природе и не встречающимися в природе, которые обладают свойствами связывания, сходными со свойствами эталонной нуклеиновой кислоты, и которые метаболизируются подобно эталонным нуклеотидам. Примеры таких аналогов включают без ограничения фосфотиоаты, фосфорамидаты, метилфосфонаты, хиральные метилфосфонаты, 2-O-метилрибонуклеотиды и пептидные нуклеиновые кислоты (PNA).
Если не указано иное, конкретная последовательность нуклеиновой кислоты также в неявной форме охватывает ее варианты с консервативными модификациями (например, с заменами вырожденными кодонами) и комплементарные последовательности, а также последовательность, указанную явным образом. В частности, как подробно описано ниже, замены вырожденными кодонами можно осуществлять за счет получения последовательностей, в которых третье положение одного или нескольких выбранных (или всех) кодонов заменено на любой из канонических нуклеозидов и/или остатков дезоксиинозина (Batzer et al., (1991) Nucleic Acid Res. 19:5081; Ohtsuka et al., (1985) J. Biol. Chem. 260:2605-2608; и Rossolini et al., (1994) Mol. Cell. Probes 8:91-98).
Функционально связанный: Термин "функционально связанный" относится к функциональной связи между двумя или более доменами пептидов или полипептидов или сегментами нуклеиновой кислоты (например, ДНК). Применительно к слитому белку или другому полипептиду термин "функционально связанный" означает, что два или более аминокислотных сегмента связаны таким образом, что образуют функциональный полипептид. Например, применительно к антигенсвязывающей молекуле отдельные ABM (или цепи ABM) могут быть функционально связаны посредством последовательностей пептидных линкеров. Применительно к нуклеиновой кислоте, кодирующей слитый белок, такой как полипептидная цепь антигенсвязывающей молекулы, "функционально связанный" означает, что две нуклеиновые кислоты соединены таким образом, что аминокислотные последовательности, кодируемые двумя нуклеиновыми кислотами, остаются в одной рамке считывания. Применительно к регуляции транскрипции термин относится к функциональной связи последовательности, регулирующей транскрипцию, с транскрибируемой последовательностью. Например, промоторная или энхансерная последовательность функционально связана с кодирующей последовательностью, если она стимулирует или модулирует транскрипцию кодирующей последовательности в подходящей клетке-хозяине или другой системе экспрессии.
Полипептид и белок: Термины "полипептид" и "белок" используются в данном документе взаимозаменяемо для обозначения полимера из аминокислотных остатков. Данные термины охватывают полимеры из аминокислот, в которых один или несколько аминокислотных остатков представляют собой искусственный химический миметик соответствующей встречающейся в природе аминокислоты, а также полимеры из встречающихся в природе аминокислот и полимер из не встречающихся в природе аминокислот. Кроме того, данные термины охватывают полимеры из аминокислот, которые дериватизируются, например, посредством синтетической дериватизации одной или нескольких боковых цепей или концов, подвергаются гликозилированию, пегилированию, круговой перестановке, циклизации, связыванию с другими молекулами посредством линкеров, слиянию с белками или доменами белков и добавлению пептидных меток или маркеров.
Распознавать: Используемый в данном документе термин "распознавать" относится к ABD, который находит свой эпитоп и взаимодействует (например, связывается) с ним.
Идентичность последовательностей: Идентичность последовательностей двух подобных последовательностей (например, вариабельных доменов антитела) можно измерить с помощью таких алгоритмов, как алгоритм в Smith, TF. & Waterman, M.S. (1981) "Comparison Of Biosequences," Adv. Appl. Math. 2:482 [алгоритм поиска локальной гомологии]; Needleman, S.B. & Wunsch, CD. (1970) "A General Method Applicable To The Search For Similarities In The Amino Acid Sequence Of Two Proteins," J. Mol. Biol.48:443 [алгоритм выравнивания участков гомологии], Pearson, W.R. & Lipman, D.J. (1988) "Improved Tools For Biological Sequence Comparison," Proc. Natl. Acad. Sci. (U.S.A.) 85:2444 [способ поиска сходства]; или Altschul, S.F. et al, (1990) "Basic Local Alignment Search Tool," J. Mol. Biol. 215:403-10, алгоритм "BLAST", см. blast.ncbi.nlm.nih.gov/Blast.cgi. При использовании любого из вышеупомянутых алгоритмов используются параметры по умолчанию (для длины окна, штрафа за гэп и т. д.). В одном варианте осуществления идентичность последовательностей определяется с использованием алгоритма BLAST с использованием параметров по умолчанию.
Идентичность необязательно определяется по участку, длина которого составляет по меньшей мере приблизительно 50 нуклеотидов (или, в случае пептида или полипептида, по меньшей мере приблизительно 10 аминокислот), или в некоторых случаях по участку, длина которого составляет от 100 до 500 или 1000 или больше нуклеотидов (или 20, 50, 200 или больше аминокислот). В некоторых вариантах осуществления идентичность определяется по определенному домену, например VH или VL антитела. Если не указано иное, идентичность двух последовательностей определяется по всей длине более короткой из двух последовательностей.
Одноцепочечный Fab или scFab: Термины "одноцепочечный Fab" и "scFab" означают полипептид, содержащий вариабельный домен тяжелой цепи антитела (VH), константный домен 1 антитела (CH1), вариабельный домен легкой цепи антитела (VL), константный домен легкой цепи антитела (CL) и линкер, так что VH и VL ассоциированы друг с другом, и CH1 и CL ассоциированы друг с другом. В некоторых вариантах осуществления домены антитела и линкер расположены в одном из следующих порядков в направлении от N-конца к C-концу: a) VH-CH1-линкер-VL-CL, b) VL-CL-линкер-VH-CH1, c) VH-CL-линкер-VL-CH1 или d) VL-CH1-линкер-VH-CL. Линкер может представлять собой полипептид из по меньшей мере 30 аминокислот, например, от 32 до 50 аминокислот. Одноцепочечные Fab стабилизированы посредством природной дисульфидной связи между CL-доменом и CH1-доменом.
Одновременная или параллельная доставка: В некоторых вариантах осуществления доставка одного средства для лечения все еще осуществляется, когда начинается доставка второго, поэтому с точки зрения введения имеет место перекрывание. Это иногда упоминается в данном документе как "одновременная" или "параллельная" доставка. В некоторых вариантах осуществления в любом случае лечение является более эффективным благодаря комбинированному введению. Например, второе средство для лечения является более эффективным, например, эквивалентный эффект наблюдается при меньшем количестве второго средства для лечения, или второе средство для лечения обеспечивает снижение интенсивности симптомов в большей степени, чем наблюдалось бы при введении второго средства для лечения в отсутствие первого средства для лечения, или аналогичная ситуация наблюдается с первым средством для лечения. В некоторых вариантах осуществления доставка является такой, при которой снижение интенсивности симптома или другого параметра, связанного с нарушением, является более значительным, чем наблюдалось бы при доставке одного средства для лечения в отсутствие другого. Эффект двух средств для лечения может быть частично аддитивным, полностью аддитивным или превышающим аддитивный. Доставка может быть такой, что эффект от первого доставленного средства для лечения все еще поддается выявлению при доставке второго.
Одноцепочечный Fv или scFv: Под "одноцепочечным Fv" или "scFv" в данном документе подразумевается вариабельный домен тяжелой цепи, ковалентно присоединенный к вариабельному домену легкой цепи, обычно с использованием линкера для ABD, как обсуждается в данном документе, с образованием scFv или scFv-домена. scFv-домен может иметь любую ориентацию от N- к С-концу (VH-линкер-VL или VL-линкер-VH). Для обзора scFv см. Plückthun, The Pharmacology of Monoclonal Antibodies, vol. 113, Rosenburg and Moore eds., (1994) Springer-Verlag, New York, pp. 269-315.
Специфически (или избирательно) связывается: Термин "специфически (или избирательно) связывается" с антигеном или эпитопом относится к реакции связывания, которая определяет наличие когнатного антигена или эпитопа в гетерогенной совокупности белков и других биологических материалов. Антигенсвязывающая молекула или ABD по настоящему изобретению как правило характеризуется константой скорости диссоциации (KD) (koff/kon), составляющей менее 5×10-2 M, менее 10-2 M, менее 5×10-3 M, менее 10-3 M, менее 5×10-4 M, менее 10-4 M, менее 5×10-5 M, менее 10-5 M, менее 5×10-6 M, менее 10-6 M, менее 5×10-7 M, менее 10-7 M, менее 5×10-8 M, менее 10-8 M, менее 5×10-9 M или менее 10-9 M, и связывается с антигеном-мишенью с аффинностью, которая по меньшей мере в два раза больше (а более типично по меньшей мере в 20 раз, по меньшей мере в 50 раз или по меньшей мере в 100 раз больше) его аффинности связывания с неспецифическим антигеном (например, HSA). Аффинность связывания можно измерить с помощью анализа Biacore, SPR или BLI.
Термин "специфически связывает" не исключает межвидовую перекрестную реактивность. Например, антигенсвязывающий модуль (например, антигенсвязывающий фрагмент антитела), который "специфически связывается" с антигеном из одного вида, также способен "специфически связываться" с этим антигеном из одного или нескольких других видов. Таким образом, такая межвидовая перекрестная реактивность сама по себе не изменяет классификацию антигенсвязывающего модуля как "специфичного" связывающего средства. В определенных вариантах осуществления антигенсвязывающий домен, который специфически связывается с антигеном человека, обладает межвидовой перекрестной реактивностью с одним или несколькими видами млекопитающих, отличных от человека, например видами приматов (включая без ограничения один или несколько из Macaca fascicularis, Macaca mulatta и Macaca nemestrina) или видами грызунов, например, Mus musculus. В других вариантах осуществления антигенсвязывающий домен не обладает межвидовой перекрестной реактивностью.
Субъект: Термин "субъект" включает человека и животных, отличных от человека. Животные, отличные от человека, включают всех позвоночных, например, млекопитающих и животных, отличных от млекопитающих, такие как приматы, отличные от человека, овца, собака, корова, куры, амфибии и рептилии. За исключением случаев, когда это отмечено, термины "пациент" или "субъект" используются в данном документе взаимозаменяемо.
Тандем VH-доменов: Используемый в данном документе термин "тандем VH-доменов (или VH)" относится к цепочке VH-доменов, состоящей из множества идентичных VH-доменов антитела. У каждого из VH-доменов, за исключением последнего на конце тандема, C-конец соединен с N-концом другого VH-домена с помощью или без помощи линкера. Тандем содержит по меньшей мере 2 VH-домена, и в некоторых вариантах осуществления BBM содержит 3, 4, 5, 6, 7, 8, 9 или 10 VH-доменов. Тандем VH можно получать посредством соединения нуклеиновых кислот, кодирующих каждый VH-домен, в необходимом порядке с применением рекомбинантных способов с помощью или без помощи линкера (например, описанных в разделе 7.4.3), что позволяет получать их в виде одной полипептидной цепи. N-конец первого VH-домена в тандеме определяется как N-конец тандема, тогда как C-конец последнего VH-домена в тандеме определяется как C-конец тандема.
Тандем VL-доменов: Используемый в данном документе термин "тандем VL-доменов (или VL)" относится к цепочке VL-доменов, состоящей из множества идентичных VL-доменов антитела. У каждого из VL-доменов, за исключением последнего на конце тандема, C-конец соединен с N-концом другого VL с помощью или без помощи линкера. Тандем содержит по меньшей мере 2 VL-домена, и в некоторых вариантах осуществления BBM содержит 3, 4, 5, 6, 7, 8, 9 или 10 VL-доменов. Тандем VL можно получать посредством соединения нуклеиновых кислот, кодирующих каждый VL-домен, в необходимом порядке с применением рекомбинантных способов с помощью или без помощи линкера (например, описанных в разделе 7.4.3), что позволяет получать их в виде одной полипептидной цепи. N-конец первого VL-домена в тандеме определяется как N-конец тандема, тогда как C-конец последнего VL-домена в тандеме определяется как C-конец тандема.
Антиген-мишень: Используемый в данном документе термин "антиген-мишень" означает молекулу, которая нековалентно, обратимо и специфически связывается антигенсвязывающим доменом.
Тетравалентный: Используемый в данном документе термин "тетравалентный" применительно к антигенсвязывающей молекуле (например, BBM) относится к антигенсвязывающей молекуле, которая содержит четыре ABD. Антигенсвязывающие молекулы по настоящему изобретению, которые представляют собой BBM, являются биспецифическими и специфически связываются с BCMA и вторым антигеном, например компонентом комплекса TCR. В определенных вариантах осуществления тетравалентные BBM обычно содержат два ABD, каждый из которых специфически связывается с BCMA, и два ABD, каждый из которых специфически связывается со вторым антигеном, например компонентом комплекса TCR, хотя предполагаются другие конфигурации, где три ABD специфически связываются с одним антигеном (например, BCMA), и один ABD специфически связывается с другим антигеном (например, компонентом комплекса TCR). Примеры тетравалентных конфигураций схематически показаны на фиг. 1AA-1AG.
Терапевтически эффективное количество: "Терапевтически эффективное количество" относится к количеству, эффективному в дозах и в течение периодов времени, необходимых для достижения желаемого терапевтического результата.
Лечить, лечение, осуществление лечения: Применяемые в данном документе термины "лечить", "лечение" и "осуществление лечения" относятся к снижению или ослаблению прогрессирования, тяжести и/или продолжительности пролиферативного нарушения или ослаблению одного или нескольких симптомов (например, одного или нескольких различимых симптомов) пролиферативного нарушения в результате введения одной или нескольких антигенсвязывающих молекул. В некоторых вариантах осуществления термины "лечить", "лечение" и "осуществление лечения" относятся к ослаблению по меньшей мере одного поддающегося измерению физического параметра пролиферативного нарушения, такого как рост опухоли, необязательно различимого для пациента. В других вариантах осуществления термины "лечить", "лечение" и "осуществление лечения" относятся к подавлению прогрессирования пролиферативного нарушения либо физически, например, посредством стабилизации различимого симптома, физиологически, например, посредством стабилизации физического параметра, либо и тем, и другим способом. В других вариантах осуществления термины "лечить", "лечение" и "осуществление лечения" относятся к снижению или стабилизации размера опухоли или количества раковых клеток.
Опухоль: Термин "опухоль" используется в данном документе взаимозаменяемо с термином "рак", например, оба термина охватывают солидные опухоли и опухоли жидких тканей, например, диффузные или циркулирующие. Используемый в данном документе термин "рак" или "опухоль" включает предзлокачественные, а также злокачественные виды рака и опухоли.
Тривалентный: Используемый в данном документе термин "тривалентный" применительно к антигенсвязывающей молекуле (например, BBM) относится к антигенсвязывающей молекуле, которая содержит три ABD. Антигенсвязывающие молекулы по настоящему изобретению, которые представляют собой BBM, являются биспецифическими и специфически связываются с BCMA и вторым антигеном, например компонентом комплекса TCR. Соответственно, тривалентные BBM содержат два ABD, которые связываются с одним антигеном (например, BCMA), и один ABD, который связывается с другим антигеном (например, компонентом комплекса TCR). Примеры тривалентных конфигураций схематически показаны на фиг. 1G-1Z.
Вариабельный участок: Используемый в данном документе термин "вариабельный участок" или "вариабельный домен" означает участок иммуноглобулина, который содержит один или несколько доменов Ig, по существу кодируемых любым из генов Vκ, Vλ и/или VH, которые составляют генетические локусы каппа, лямбда и тяжелой цепи иммуноглобулина соответственно, и содержит CDR, которые придают специфичность к антигену. "Вариабельный домен тяжелой цепи" способен спариваться с "вариабельным доменом легкой цепи" с образованием антигенсвязывающего домена ("ABD"). Кроме того, каждый вариабельный домен содержит три гипервариабельных участка ("участка, определяющих комплементарность", "CDR") (CDR-H1, CDR-H2, CDR-H3 в случае вариабельного домена тяжелой цепи и CDR-L1, CDR-L2, CDR-L3 в случае вариабельного домена легкой цепи) и четыре каркасных (FR) участка, расположенных от аминоконца к карбоксиконцу в следующем порядке: FR1-CDR1-FR2-CDR2-FR3-CDR3-FR4.
Вектор: Термин "вектор" предназначен для обозначения молекулы полинуклеотида, способной транспортировать другой полинуклеотид, с которым она была связана. Одним типом вектора является "плазмида", которая относится к кольцевой двухнитевой петле ДНК, в которую посредством лигирования могут быть встроены дополнительные сегменты ДНК. Другим типом вектора является вирусный вектор, где дополнительные сегменты ДНК могут быть встроены в вирусный геном посредством лигирования. Определенные векторы способны к автономной репликации в клетке-хозяине, в которую их вводят (например, бактериальные векторы, содержащие бактериальную точку начала репликации, и эписомные векторы млекопитающих). Другие векторы (например, неэписомные векторы млекопитающих) могут быть интегрированы в геном клетки-хозяина после введения в клетку-хозяина и благодаря этому реплицируются вместе с геномом хозяина. Более того, определенные векторы способны регулировать экспрессию генов, с которыми они функционально связаны. Такие векторы называются в данном документе "рекомбинантными векторами экспрессии" (или просто "векторами экспрессии"). В целом, векторы экспрессии, применимые в методиках рекомбинантной ДНК, часто представлены в форме плазмид. В настоящем описании "плазмида" и "вектор" могут использоваться взаимозаменяемо, поскольку плазмида является наиболее широко используемой формой вектора. Тем не менее, предполагается, что настоящее изобретение включает такие другие формы векторов экспрессии, как вирусные векторы (например, на основе ретровирусов, аденовирусов и аденоассоциированных вирусов, дефектных по репликации), которые выполняют эквивалентные функции.
VH: Термин "VH" относится к вариабельному участку тяжелой цепи иммуноглобулина антитела, в том числе тяжелой цепи Fv, scFv, dsFv или Fab.
VL: Термин "VL" относится к вариабельному участку легкой цепи иммуноглобулина, в том числе легкой цепи Fv, scFv, dsFv или Fab.
VH-VL или пара VH-VL: Что касается пары VH-VL, независимо от того, находятся ли они на одной и той же полипептидной цепи или на разных полипептидных цепях, термины "VH-VL" и "пара VH-VL" используются для удобства и не предполагаются как обозначающие какую-либо конкретную ориентацию, если в контексте не указано иное. Таким образом, scFv, содержащий "VH-VL" или "пару VH-VL", может содержать VH- и VL-домены в любой ориентации, например, VH, расположенный в N-концевом направлении относительно VL, или VL, расположенный в N-концевом направлении относительно VH.
7.2. BCMA-связывающие молекулы
В одном аспекте в настоящем изобретении предусмотрены ВСМА-связывающие молекулы, включая моноспецифические и полиспецифические молекулы, которые связываются с ВСМА человека. В некоторых вариантах осуществления ВСМА-связывающая молекула представляет собой моноспецифическую связывающую молекулу. Например, моноспецифическая связывающая молекула может представлять собой антитело или его антигенсвязывающий фрагмент (например, фрагмент антитела, scFv, dsFv, Fv, Fab, scFab, (Fab')2 или однодоменное антитело (SDAB). В других вариантах осуществления ВСМА-связывающая молекула представляет собой полиспецифическую (например, биспецифическую) ВСМА-связывающую молекулу (например, биспецифическое антитело).
В некоторых вариантах осуществления ВСМА-связывающие молекулы представляют собой химерные или гуманизированные моноклональные антитела. Химерные и/или гуманизированные антитела могут быть сконструированы для минимизации иммунного ответа пациента-человека на антитела, продуцируемые отличными от человека субъектами, или полученные в результате экспрессии генов, кодирующих антитела, отличные от человеческих антител. Химерные антитела содержат вариабельный участок антитела отличного от человека животного и константный участок человеческого антитела. Такие антитела сохраняют специфичность связывания эпитопа исходного моноклонального антитела, но могут быть менее иммуногенными при введении людям и, следовательно, с большей вероятностью будут переноситься пациентом. Например, один или все (например, один, два или три) из вариабельных участков легкой(легких) цепи(цепей) и/или один или все (например, один, два или три) из вариабельных участков тяжелой(тяжелых) цепи(цепей) мышиного антитела (например, мышиного моноклонального антитела) могут быть присоединены к человеческому константному участку, такому как без ограничения константный участок человеческого IgG1. Химерные моноклональные антитела можно получать с помощью известных методик рекомбинантной ДНК. Например, ген, кодирующий константный участок молекулы антитела, отличного от человеческого, может быть заменен геном, кодирующим человеческий константный участок (см. Robinson et al., публикация патента согласно PCT PCT/US86/02269; Akira, et al., европейская патентная заявка 184187; или Taniguchi, M., европейская патентная заявка 171496). Кроме того, другие подходящие методики, которые можно использовать для получения химерных антител, описаны, например, в патентах США № 4816567; 4,978,775; 4975369; и 4816397.
Химерные или гуманизированные антитела и их антигенсвязывающие фрагменты по настоящему изобретению можно получать на основе последовательности мышиного моноклонального антитела. ДНК, кодирующую тяжелую и легкую цепи иммуноглобулинов, можно получать из представляющей интерес мышиной гибридомы и конструировать таким образом, чтобы она содержала отличные от мышиных последовательности иммуноглобулинов (например, человеческие), с применением стандартных методик молекулярной биологии. Например, для создания химерного антитела мышиные вариабельные участки можно связать с человеческими константными участками с применением известных способов (см., например, патент США № 4816567 за авторством Cabilly et al.). Для создания гуманизированного антитела мышиные CDR-участки можно вставить в человеческий каркасный участок с применением известных способов. См., например, патент США № 5225539 за авторством Winter и патенты США № 5530101; 5585089; 5693762 и 6180370 за авторством Queen et al.
Гуманизированное антитело можно получить с помощью различных известных методик, в том числе без ограничения с помощью прививки CDR (см., например, европейский патент № EP 239400; международную публикацию № WO 91/09967 и патенты США №№ 5225539, 5530101 и 5585089), венирования или изменения поверхности (см., например, европейские патенты №№ EP 592106 и EP 519596; Padlan, 1991, Molecular Immunology, 28(4/5):489-498; Studnicka et al., 1994, Protein Engineering, 7(6):805-814 и Roguska et al., 1994, PNAS, 91:969-973), перетасовки цепей (см., например, патент США № 5565332), и методик, раскрытых, например, в публикации заявки на патент США № US2005/0042664, публикации заявки на патент США № US2005/0048617, патенте США № № 6407213, патенте США № 5766886, международной публикации № WO 9317105, Tan et al., J. Immunol., 169:1119-25 (2002), Caldas et al., Protein Eng., 13(5):353-60 (2000), Morea et al., Methods, 20(3):267-79 (2000), Baca et al., J. Biol. Chem., 272(16):10678-84 (1997), Roguska et al., Protein Eng., 9(10):895-904 (1996), Couto et al., Cancer Res., 55 (23 Supp):5973s-5977s (1995), Couto et al., Cancer Res., 55(8):1717-22 (1995), Sandhu J S, Gene, 150(2):409-10 (1994) и Pedersen et al., J. Mol. Biol., 235(3):959-73 (1994). Часто каркасные остатки в каркасных участках будут заменены соответствующим остатком из CDR донорного антитела для изменения, например, улучшения связывания антигена. Эти каркасные замены, например консервативные замены, идентифицируют с помощью хорошо известных способов, например, посредством моделирования взаимодействий CDR и каркасных остатков с идентификацией каркасных остатков, важных для связывания антигена, и сравнения последовательностей с идентификацией необычных каркасных остатков в конкретных положениях. (См., например, Queen et al., патент США № 5585089; и Riechmann et al., 1988, Nature, 332:323).
Как предусмотрено в данном документе, гуманизированные антитела или фрагменты антител могут содержать один или несколько CDR из молекул иммуноглобулина, отличных от человеческих, и каркасные участки, где аминокислотные остатки, составляющие каркас, получены полностью или по большей части из человеческих иммуноглобулинов зародышевого типа. Множество методик гуманизации антител или фрагментов антител хорошо известны, и их, по существу, можно осуществлять в соответствии со способом Winter и коллег (Jones et al., Nature, 321:522-525 (1986); Riechmann et al., Nature, 332:323-327 (1988); Verhoeyen et al., Science, 239:1534-1536 (1988)) посредством замены CDR или последовательностей CDR грызунов на соответствующие последовательности человеческого антитела, т. е. посредством прививки CDR (ЕР 239400; РСТ-публикация № WO 91/09967 и патенты США №№ 4816567; 6331415; 5225539; 5530101; 5585089; 6548640). В таких гуманизированных антителах и фрагментах антител значительно меньшая часть, чем интактный человеческий вариабельный домен, была заменена соответствующей последовательностью из вида, отличного от человека. Гуманизированные антитела часто представляют собой человеческие антитела, в которых некоторые остатки CDR и, возможно, некоторые каркасные (FR) остатки заменены на остатки из аналогичных сайтов в антителах грызунов. Гуманизация антител и фрагментов антител также может быть достигнута посредством венирования или изменения поверхности (ЕР 592106; ЕР 519596; Padlan, 1991, Molecular Immunology, 28 (4/5):489-498; Studnicka et al., Protein Engineering, 7(6):805-814 (1994) и Roguska et al., PNAS, 91:969-973 (1994)) или перетасовки цепей (патент США № 5565332).
Выбор человеческих вариабельных доменов как легкой, так и тяжелой цепей для использования при создании гуманизированных антител необходим для снижения антигенности. В соответствии с так называемым способом "наилучшего соответствия" последовательность вариабельного домена антитела грызуна подвергают скринингу по всей библиотеке известных последовательностей человеческих вариабельных доменов. Человеческую последовательность, которая является наиболее близкой к последовательности грызуна, затем принимают в качестве человеческого каркасного участка (FR) для гуманизированного антитела (Sims et al., J. Immunol., 151:2296 (1993); Chothia et al., J. Mol. Biol., 196:901 (1987)). В другом способе применяют конкретный каркасный участок, полученный из консенсусной последовательности всех человеческих антител из определенной подгруппы легких или тяжелых цепей. Один и тот же каркасный участок можно использовать для нескольких различных гуманизированных антител (см., например, Nicholson et al. Mol. Immun. 34 (16-17): 1157-1165 (1997); Carter et al., Proc. Natl. Acad. Sci. USA, 89:4285 (1992); Presta et al., J. Immunol., 151:2623 (1993). В некоторых вариантах осуществления каркасный участок, например, все четыре каркасных участка вариабельного участка тяжелой цепи, получены из последовательности VH4_4-59 зародышевого типа. В одном варианте осуществления каркасный участок может содержать одну, две, три, четыре или пять модификаций, например замен, например консервативных замен, например, аминокислоты в соответствующей мышиной последовательности. В одном варианте осуществления каркасный участок, например, все четыре каркасных участка вариабельного участка легкой цепи, получены из последовательности VK3_1.25 зародышевого типа. В одном варианте осуществления каркасный участок может содержать одну, две, три, четыре или пять модификаций, например замен, например консервативных замен, например аминокислоты в соответствующей мышиной последовательности.
В определенных вариантах осуществления BCMA-связывающие молекулы содержат вариабельный участок тяжелой цепи из конкретного гена, кодирующего тяжелую цепь иммуноглобулина зародышевого типа, и/или вариабельный участок легкой цепи из конкретного гена, кодирующего легкую цепь иммуноглобулина зародышевого типа. Например, такие антитела могут содержать человеческое антитело, содержащее вариабельные участки тяжелой или легкой цепи, которые являются "продуктом" или "получены из" конкретной последовательности зародышевого типа, или состоять из него. Человеческое антитело, которое является "продуктом" или "получено из" человеческой последовательности иммуноглобулина зародышевого типа, может быть идентифицировано как таковое посредством сравнения аминокислотной последовательности человеческого антитела с аминокислотными последовательностями человеческих иммуноглобулинов зародышевого типа и выбора человеческой последовательности иммуноглобулина зародышевого типа, которая является наиболее близкой по последовательности (т. е. имеет наибольший % идентичности) к последовательности человеческого антитела (с использованием описанных в данном документе способов). Человеческое антитело, которое является "продуктом" или "получено из" конкретной человеческой последовательности иммуноглобулина зародышевого типа, может содержать аминокислотные различия по сравнению с последовательностью зародышевой линии, возникшие вследствие, например, естественных соматических мутаций или преднамеренного введения сайт-направленной мутации. Однако аминокислотная последовательность гуманизированного антитела обычно на по меньшей мере 90% идентична аминокислотной последовательности, кодируемой геном иммуноглобулина зародышевого типа человека, и содержит аминокислотные остатки, по которым идентифицируют антитело как полученное из человеческих последовательностей при сравнении с аминокислотными последовательностями иммуноглобулинов зародышевого типа других видов (например, мышиными последовательностями зародышевого типа). В определенных случаях аминокислотная последовательность гуманизированного антитела может быть на по меньшей мере 95, 96, 97, 98 или 99%, или даже на по меньшей мере 96%, 97%, 98% или 99% идентична аминокислотной последовательности, кодируемой геном иммуноглобулина зародышевого типа. Как правило, гуманизированное антитело, полученное из конкретной человеческой последовательности зародышевого типа, будет демонстрировать не более 10-20 аминокислотных различий по сравнению с аминокислотной последовательностью, кодируемой геном иммуноглобулина зародышевого типа человека (перед введением в нее каких-либо асимметричных вариантов, вариантов с измененной pI и вариантов с устранением связывания с Fcγ-рецепторами; то есть, количество вариантов перед введением вариантов по настоящему изобретению, как правило, является низким). В определенных случаях гуманизированное антитело может демонстрировать не более 5 или даже не более 4, 3, 2 или 1 аминокислотного различия по сравнению с аминокислотной последовательностью, кодируемой геном иммуноглобулина зародышевого типа (снова, перед введением в нее каких-либо асимметричных вариантов, вариантов с измененной pI и вариантов с устранением связывания с Fcγ-рецепторами; то есть, количество вариантов перед введением вариантов по настоящему изобретению, как правило, является низким).
В одном варианте осуществления исходное антитело было созревшим в отношении аффинности. Способы на основе структуры можно использовать для гуманизации и созревания аффинности, например, как описано в USSN 11/004590. Способы на основе отбора можно использовать для гуманизации и/или созревания аффинности вариабельных участков антител, включая без ограничения способы, описанные в Wu et al., 1999, J. Mol. Biol. 294:151-162; Baca et al., 1997, J. Biol. Chem. 272(16):10678-10684; Rosok et al., 1996, J. Biol. Chem. 271(37): 22611-22618; Rader et al., 1998, Proc. Natl. Acad. Sci. USA 95: 8910-8915; Krauss et al., 2003, Protein Engineering 16(10):753-759. Другие способы гуманизации могут включать прививку только части CDR, включая без ограничения способы, описанные в USSN 09/810510; Tan et al., 2002, J. Immunol. 169:1119-1125; De Pascalis et al., 2002, J. Immunol. 169:3076-3084.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит ABD, который представляет собой Fab. Fab-домены можно получать посредством протеолитического расщепления молекул иммуноглобулинов с применением ферментов, таких как папаин, или посредством рекомбинантной экспрессии. Fab-домены, как правило, содержат CH1-домен, присоединенный к VH-домену, который образует пару с CL-доменом, присоединенным к VL-домену. В иммуноглобулине дикого типа VH-домен спарен с VL-доменом с образованием Fv-участка, и CH1-домен спарен с CL-доменом для дополнительной стабилизации связывающего модуля. Дисульфидная связь между двумя константными доменами может дополнительно стабилизировать Fab-домен.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит ABD, который представляет собой scFab. В одном варианте осуществления домены антитела и линкер в scFab-фрагменте расположены в одном из следующих порядков в направлении от N-конца к C-концу: a) VH-CH1-линкер-VL-CL или b) VL-CL-линкер-VH-CH1. В некоторых случаях используют VL-CL-линкер-VH-CH1.
В другом варианте осуществления домены антитела и линкер в scFab-фрагменте расположены в одном из следующих порядков в направлении от N-конца к C-концу: a) VH-CL-линкер-VL-CH1 или b) VL-CH1-линкер-VH-CL.
В scFab-фрагменте в дополнение к природной дисульфидной связи между CL-доменом и CH1-доменом вариабельный домен тяжелой цепи (VH) антитела и вариабельный домен легкой цепи (VL) антитела также необязательно стабилизированы дисульфидными связями посредством введения дисульфидной связи между следующими положениями: i) положением 44 вариабельного домена тяжелой цепи и положением 100 вариабельного домена легкой цепи, ii) положением 105 вариабельного домена тяжелой цепи и положением 43 вариабельного домена легкой цепи или iii) положением 101 вариабельного домена тяжелой цепи и положением 100 вариабельного домена легкой цепи (нумерация в соответствии с EU-индексом по Kabat).
Такую дополнительную стабилизацию scFab-фрагментов дисульфидными связями осуществляют посредством введения дисульфидной связи между вариабельными доменами VH и VL одноцепочечных Fab-фрагментов. Методики введения неприродных дисульфидных мостиков для стабилизации одноцепочечного Fv описаны, например, в WO 94/029350, Rajagopal et al., 1997, Prot. Engin. 10:1453-59; Kobayashi et al., 1998, Nuclear Medicine & Biology, 25:387-393; и Schmidt, et al., 1999, Oncogene 18:1711-1721. В одном варианте осуществления необязательная дисульфидная связь между вариабельными доменами scFab-фрагментов находится между положением 44 вариабельного домена тяжелой цепи и положением 100 вариабельного домена легкой цепи. В одном варианте осуществления необязательная дисульфидная связь между вариабельными доменами scFab-фрагментов находится между положением 105 вариабельного домена тяжелой цепи и положением 43 вариабельного домена легкой цепи (нумерация в соответствии с EU-индексом по Kabat).
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит ABD, который представляет собой scFv. Фрагменты антител, представляющие собой одноцепочечные Fv, содержат VH- и VL-домены антитела в одной полипептидной цепи, способны экспрессироваться в виде одноцепочечного полипептида и сохраняют специфичность интактного антитела, из которого они получены. Обычно полипептид scFv дополнительно содержит полипептидный линкер между VH- и VL-доменами, который позволяет scFv образовывать необходимую структуру для связывания мишени. Примерами линкеров, подходящих для соединения VH- и VL-цепей scFv, являются линкеры для ABD, идентифицированные в разделе 7.4.3, например, любой из линкеров, обозначенных от L1 до L58.
Если не указано иное, то scFv, как используется в данном документе, может содержать вариабельные VL- и VH-участки в любом порядке, например, по отношению к N-концу и С-концу полипептида scFv может содержать VL-линкер-VH или может содержать VH-линкер-VL.
Для получения кодирующей scFv нуклеиновой кислоты фрагменты ДНК, кодирующие VH и VL, функционально связывают с другим фрагментом, кодирующим линкер, например, кодирующим любой из линкеров, описанных в разделе 7.4.3 (например, аминокислотная последовательность (Gly4˜Ser)3 (SEQ ID NO:1)), таким образом, чтобы последовательности VH и VL можно было экспрессировать в виде непрерывного одноцепочечного белка с VL- и VH-участками, соединенными гибким линкером (см., например, Bird et al., 1988, Science 242:423-426; Huston et al., 1988, Proc. Natl. Acad. Sci. USA 85:5879-5883; McCafferty et al., 1990, Nature 348:552-554).
BCMA-связывающие молекулы также могут содержать ABD, который представляет собой Fv, dsFv, (Fab')2, однодоменное антитело (SDAB), VH- или VL-домен или VHH-домен верблюдовых (также называемый нанотелом).
BCMA-связывающие молекулы могут содержать однодоменное антитело, состоящее из одного VH- или VL-домена, который проявляет достаточную аффинность к BCMA. В одном варианте осуществления однодоменное антитело представляет собой VHH-домен верблюдовых (см., например, Riechmann, 1999, Journal of Immunological Methods 231:25-38; WO 94/04678).
В таблицах с 1A-1 по 1P (в совокупности называемых "таблица 1") перечислены последовательности иллюстративных BCMA-связывающих последовательностей, которые могут быть включены в BCMA-связывающие молекулы.
Консенсусные последовательности CDR легкой цепи семейства AB1/AB2
(консенсусная последовательность AB1/AB2 - по Kabat)
(x=s или t)
(консенсусная последовательность семейства AB1/AB2 - по Kabat)
(X1=S, G, D, Y или A; x2=s, t или A; X3=P или L)
(консенсусная последовательность AB1/AB2 - по Chothia)
(X=S или T)
(консенсусная последовательность семейства AB1/AB2 - по Chothia)
(X1=S, G, D, Y или A; x2=s, t или A; X3=P или L)
(консенсусная последовательность AB1/AB2 - по IMGT)
(X=S или T)
(консенсусная последовательность семейства AB1/AB2 - по IMGT)
(X1=S, G, D, Y или A; x2=s, t или A; X3=P или L)
(консенсусная последовательность AB1/AB2 - по Kabat+Chothia)
(X=S или T)
(консенсусная последовательность семейства AB1/AB2 - по Kabat+Chothia)
(X1=S, G, D, Y или A; x2=s, t или A; X3=P или L)
(консенсусная последовательность AB1/AB2 - по Kabat+IMGT)
(X=S или T)
(консенсусная последовательность семейства AB1/AB2 - по Kabat+IMGT)
(X1=S, G, D, Y или A; x2=s, t или A; X3=P или L)
(консенсусная последовательность AB1/AB2 - по Chothia+IMGT)
(X=S или T)
(консенсусная последовательность семейства AB1/AB2 - по Chothia+IMGT)
(X1=S, G, D, Y или A; x2=s, t или A; X3=P или L)
Консенсусные последовательности CDR тяжелой цепи семейства AB1/AB2
(консенсусная последовательность AB1/AB2 - по Kabat)
(X1=G или E; X2=S или R; X3=T или A; X4=Y или A)
(консенсусная последовательность семейства AB1/AB2 - по Kabat)
(X1=G, E или A; X2=S, A, H или E; X3=G, D, E, H, R или A; X4=S, R, V, T, Y; X5 =
T, A, E, H или R; X6=Y, A или S)
(консенсусная последовательность AB1/AB2 - по Chothia)
(X1=G или E; X2=S или R)
(консенсусная последовательность семейства AB1/AB2 - по Chothia)
(X1=G, E или A; X2=S, A, H или E; X3=G, D, E, H, R или A; X4=S, R, V, T, Y)
(консенсусная последовательность AB1/AB2 - по IMGT)
(X1=G или E; X2=S или R; X3=T или A)
(консенсусная последовательность семейства AB1/AB2 - по IMGT)
(X1=G, E или A; X2=S, A, H или E; X3=G, D, E, H, R или A; X4=S, R, V, T, Y; X5 =
T, A, E, H или R)
(консенсусная последовательность AB1/AB2 - по Kabat+Chothia)
(X1=G или E; X2=S или R; X3=T или A; X4=Y или A)
(консенсусная последовательность семейства AB1/AB2 - по Kabat+Chothia)
(X1=G, E или A; X2=S, A, H или E; X3=G, D, E, H, R или A; X4=S, R, V, T, Y; X5 =
T, A, E, H или R; X6=Y, A или S)
(консенсусная последовательность AB1/AB2 - по Kabat+IMGT)
(X1=G или E; X2=S или R; X3=T или A; X4=Y или A)
(консенсусная последовательность семейства AB1/AB2 - по Kabat+IMGT)
(X1=G, E или A; X2=S, A, H или E; X3=G, D, E, H, R или A; X4=S, R, V, T, Y; X5 =
T, A, E, H или R; X6=Y, A или S)
(консенсусная последовательность AB1/AB2 - по Chothia+IMGT)
(X1=G или E, X2=S или R; X3=T или A)
(консенсусная последовательность семейства AB1/AB2 - по Chothia+IMGT)
(X1=G, E или A; X2=S, A, H или E; X3=G, D, E, H, R или A; X4=S, R, V, T, Y; X5 =
T, A, E, H или R)
Консенсусные последовательности CDR легкой цепи семейства AB3
(консенсусная последовательность AB3/PI-61 - по Kabat)
(X1=l или p; x2=r или s)
(X=A или T)
(консенсусная последовательность семейства AB3 - по Kabat)
(X1=D или E; X2=L, P или A; X3=R, S, G или W)
(X=A или T)
(консенсусная последовательность AB3/PI-61 - по Chothia)
(X=A или T)
(консенсусная последовательность семейства AB3 - по Chothia)
(X=D или E)
(X=A или T)
(консенсусная последовательность AB3/PI-61 - по IMGT, с удлиненным CDR-L2)
(X1=L или P; X2=R или S)
(X=A или T)
(консенсусная последовательность семейства AB3 - по IMGT, с удлиненным CDR-L2)
(X1=D или E; X2=L, P или A; X3=R, S, G или W)
(X=A или T)
(консенсусная последовательность AB3/PI-61 - по Kabat+Chothia)
(X1=L или P; X2=R или S)
(X=A или T)
(консенсусная последовательность семейства AB3 - по Kabat+Chothia)
(X1=D или E; X2=L, P или A; X3=R, S, G или W)
(X=A или T)
(консенсусная последовательность AB3/PI-61 - по Kabat+IMGT)
(X1=L или P; X2=R или S)
(X=A или T)
(консенсусная последовательность семейства AB3 - по Kabat+IMGT)
(X1=D или E; X2=L, P или A; X3=R, S, G или W)
(X=A или T)
(консенсусная последовательность AB3/PI-61 - по Chothia+IMGT, с удлиненным CDR-L2)
(X1=L или P; X2=R или S)
(X=A или T)
(консенсусная последовательность семейства AB3 - по Chothia+IMGT, с удлиненным CDR-L2)
(X1=D или E; X2=L, P или A; X3=R, S, G или W)
(X=A или T)
(консенсусная последовательность AB3/PI-61 - по IMGT)
(X=A или T)
(консенсусная последовательность семейства AB3 - по IMGT)
(X1=D или E)
(X=A или T)
(консенсусная последовательность AB3/PI-61 - по Chothia+IMGT)
(X=A или T)
(консенсусная последовательность семейства AB3 - по Chothia+IMGT)
(X1=D или E)
(X=A или T)
Консенсусные последовательности CDR тяжелой цепи семейства AB3
(консенсусная последовательность AB3/PI-61 - по Kabat)
(X=T или D)
(консенсусная последовательность семейства AB3 - по Kabat)
(X1=H, K, T, R, D, N, S; X2=G, D или E; X3=S, T, F, A, L; X4=H, N или K)
X6X7X8X9DV
(X1=A, N, E; X2=L, F, V или Y; X3=H, Q, R или D; X4=D, E, G или Q; X5=D, Q или F; X6=Y или Q; X7=Y, K или D; X8=G или P; X9=L, Q, V или T)
(консенсусная последовательность AB3/PI-61 - по Chothia)
(X=T или D)
(консенсусная последовательность семейства AB3 - по Chothia)
(X1=H, K, T, R, D, N, S; X2=G, D или E; X3=S, T, F, A, L; X4=H, N или K)
X6X7X8X9DV
(X1=A, N, E; X2=L, F, V или Y; X3=H, Q, R или D; X4=D, E, G или Q; X5=D, Q или F; X6=Y или Q; X7=Y, K или D; X8=G или P; X9=L, Q, V или T)
(консенсусная последовательность AB3/PI-61 - по IMGT)
(консенсусная последовательность семейства AB3 - по IMGT)
(X1=H, K, T, R, D, N, S; X2=G, D или E; X3=S, T, F, A, L; X4=H, N или K)
×5X6X7X8X9DV
(X1=A, N, E; X2=L, F, V или Y; X3=H, Q, R или D; X4=D, E, G или Q; X5=D, Q или F; X6=Y или Q; X7=Y, K или D; X8=G или P; X9=L, Q, V или T)
(консенсусная последовательность AB3/PI-61 - по Kabat+Chothia)
(X=T или D)
(консенсусная последовательность семейства AB3 - по Kabat+Chothia)
(X1=H, K, T, R, D, N, S; X2=G, D или E; X3=S, T, F, A, L; X4=H, N или K)
X6X7X8X9DV
(X1=A, N, E; X2=L, F, V или Y; X3=H, Q, R или D; X4=D, E, G или Q; X5=D, Q или F; X6=Y или Q; X7=Y, K или D; X8=G или P; X9=L, Q, V или T)
(консенсусная последовательность AB3/PI-61 - по Kabat+IMGT)
(X=T или D)
(консенсусная последовательность семейства AB3 - по Kabat+IMGT)
(X1=H, K, T, R, D, N, S; X2=G, D или E; X3=S, T, F, A, L; X4=H, N или K)
×5X6X7X8X9DV
(X1=A, N, E; X2=L, F, V или Y; X3=H, Q, R или D; X4=D, E, G или Q; X5=D, Q или F; X6=Y или Q; X7=Y, K или D; X8=G или P; X9=L, Q, V или T)
(консенсусная последовательность AB3/PI-61 - по Chothia+IMGT)
(X=T или D)
(консенсусная последовательность семейства AB3 - по Chothia+IMGT)
(X1=H, K, T, R, D, N, S; X2=G, D или E; X3=S, T, F, A, L; X4=H, N или K)
×5X6X7X8X9DV
(X1=A, N, E; X2=L, F, V или Y; X3=H, Q, R или D; X4=D, E, G или Q; X5=D, Q или F; X6=Y или Q; X7=Y, K или D; X8=G или P; X9=L, Q, V или T)
(консенсусная последовательность AB3/PI-61 - по IMGT)
(консенсусная последовательность семейства AB3 - по IMGT)
(X1=H, K, T, R, D, N, S; X2=G, D или E; X3=S, T, F, A, L; X4=H, N или K)
×5X6X7X8X9DV
(X1=A, N, E; X2=L, F, V или Y; X3=H, Q, R или D; X4=D, E, G или Q; X5=D, Q или F; X6=Y или Q; X7=Y, K или D; X8=G или P; X9=L, Q, V или T)
(консенсусная последовательность AB3/PI-61 - по Chothia+IMGT)
(X=T или D)
(консенсусная последовательность семейства AB3 - по Chothia+IMGT)
(X1=H, K, T, R, D, N, S; X2=G, D или E; X3=S, T, F, A, L; X4=H, N или K)
×5X6X7X8X9DV
(X1=A, N, E; X2=L, F, V или Y; X3=H, Q, R или D; X4=D, E, G или Q; X5=D, Q или F; X6=Y или Q; X7=Y, K или D; X8=G или P; X9=L, Q, V или T)
Средства, связывающие BCMA, из семейства AB1/AB2 - последовательности CDR легкой цепи в соответствии со схемой нумерации по Kabat
Средства, связывающие BCMA, из семейства AB1/AB2 - последовательности CDR тяжелой цепи в соответствии со схемой нумерации по Kabat
Средства, связывающие BCMA, из семейства AB1/AB2 - последовательности CDR легкой цепи в соответствии со схемой нумерации по Chothia
Средства, связывающие BCMA, из семейства AB1/AB2 - последовательности CDR тяжелой цепи в соответствии со схемой нумерации по Chothia
Средства, связывающие BCMA, из семейства AB1/AB2 - последовательности CDR легкой цепи в соответствии со схемой нумерации IMGT
Средства, связывающие BCMA, из семейства AB1/AB2 - последовательности CDR тяжелой цепи в соответствии со схемой нумерации IMGT
Средства, связывающие BCMA, из семейства AB1/AB2 - последовательности CDR легкой цепи в соответствии с комбинацией схем нумерации по Kabat и Chothia
Средства, связывающие BCMA, из семейства AB1/AB2 - последовательности CDR тяжелой цепи в соответствии с комбинацией схем нумерации по Kabat и Chothia
Средства, связывающие BCMA, из семейства AB1/AB2 - последовательности CDR легкой цепи в соответствии с комбинацией схем нумерации по Kabat и IMGT
Средства, связывающие BCMA, из семейства AB1/AB2 - последовательности CDR тяжелой цепи в соответствии с комбинацией схем нумерации по Kabat и IMGT
Средства, связывающие BCMA, из семейства AB1/AB2 - последовательности CDR легкой цепи в соответствии с комбинацией схем нумерации по Chothia и IMGT
Средства, связывающие BCMA, из семейства AB1/AB2 - последовательности CDR тяжелой цепи в соответствии с комбинацией схем нумерации по Chothia и IMGT
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR легкой цепи в соответствии со схемой нумерации по Kabat
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR тяжелой цепи в соответствии со схемой нумерации по Kabat
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR легкой цепи в соответствии со схемой нумерации по Chothia
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR тяжелой цепи в соответствии со схемой нумерации по Chothia
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR-L1 и CDR-L3 в соответствии со схемой нумерации IMGT и удлиненные последовательности CDR-L2
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR легкой цепи в соответствии со схемой нумерации IMGT
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR тяжелой цепи в соответствии со схемой нумерации IMGT
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR легкой цепи в соответствии с комбинацией схем нумерации по Kabat и Chothia
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR тяжелой цепи в соответствии с комбинацией схем нумерации по Kabat и Chothia
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR легкой цепи в соответствии с комбинацией схем нумерации по Kabat и IMGT
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR тяжелой цепи в соответствии с комбинацией схем нумерации по Kabat и IMGT
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR-L1 и CDR-L3 в соответствии с комбинацией схем нумерации по Chothia и IMGT и удлиненные последовательности CDR-L2
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR легкой цепи в соответствии с комбинацией схем нумерации по Chothia и IMGT
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR тяжелой цепи в соответствии с комбинацией схем нумерации по Chothia и IMGT
Средства, связывающие BCMA, - последовательности вариабельных участков легкой цепи
Средства, связывающие BCMA, - последовательности вариабельных участков тяжелой цепи
Средства, связывающие BCMA, - последовательности scFv
В таблицах с 1A-1 по 1B-2 перечислены консенсусные последовательности CDR, полученные из последовательностей CDR иллюстративных BCMA-связывающих молекул, описанных в примерах. Консенсусные последовательности CDR включают последовательности на основе последовательностей CDR по Kabat иллюстративных BCMA-связывающих молекул, последовательностей CDR по Chothia иллюстративных BCMA-связывающих молекул, последовательностей CDR по IMGT иллюстративных BCMA-связывающих молекул, последовательностей CDR в соответствии с комбинацией по Kabat и Chothia иллюстративных BCMA-связывающих молекул, последовательностей CDR в соответствии с комбинацией по Kabat и IMGT иллюстративных BCMA-связывающих молекул и последовательностей CDR в соответствии с комбинацией по Chothia и IMGT иллюстративных BCMA-связывающих молекул. Конкретные последовательности CDR иллюстративных ВСМА-связывающих молекул, описанных в примерах, перечислены в таблицах 1C1-1N-2. Иллюстративные последовательности VL и VH перечислены в таблицах 1O-1 и 1O-2 соответственно. Иллюстративные последовательности scFv перечислены в таблице 1P.
В некоторых вариантах осуществления ВСМА-связывающие молекулы содержат CDR легкой цепи, имеющий аминокислотную последовательность любой из консенсусных последовательностей CDR, перечисленных в таблице 1A-1 или таблице 1B-1. В конкретных вариантах осуществления в настоящем изобретении предусмотрены ВСМА-связывающие молекулы, содержащие один, два, три или более CDR легкой цепи (или в качестве альтернативы состоящие из них), выбранных из CDR легкой цепи, описанных в таблице 1A-1 или таблице 1B-1.
В некоторых вариантах осуществления ВСМА-связывающие молекулы содержат CDR тяжелой цепи, имеющий аминокислотную последовательность любого из CDR тяжелой цепи, перечисленных в таблице 1A-2 или таблице 1B-2. В конкретных вариантах осуществления в настоящем изобретении предусмотрены ВСМА-связывающие молекулы, содержащие один, два, три или более CDR тяжелой цепи (или в качестве альтернативы состоящие из них), выбранных из CDR тяжелой цепи, описанных в таблице 1A-2 или таблице 1B-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C1, как указано в таблицах 1A-1 и 1A-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C2, как указано в таблицах 1A-1 и 1A-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C3, как указано в таблицах 1A-1 и 1A-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C4, как указано в таблицах 1A-1 и 1A-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C5, как указано в таблицах 1A-1 и 1A-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C6, как указано в таблицах 1A-1 и 1A-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C7, как указано в таблицах 1A-1 и 1A-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C8, как указано в таблицах 1A-1 и 1A-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C9, как указано в таблицах 1A-1 и 1A-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C10, как указано в таблицах 1A-1 и 1A-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C11, как указано в таблицах 1A-1 и 1A-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C12, как указано в таблицах 1A-1 и 1A-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C13, как указано в таблицах 1B-1 и 1B-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C14, как указано в таблицах 1B-1 и 1B-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C15, как указано в таблицах 1B-1 и 1B-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C16, как указано в таблицах 1B-1 и 1B-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C17, как указано в таблицах 1B-1 и 1B-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C18, как указано в таблицах 1B-1 и 1B-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C19, как указано в таблицах 1B-1 и 1B-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C20, как указано в таблицах 1B-1 и 1B-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C21, как указано в таблицах 1B-1 и 1B-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C22, как указано в таблицах 1B-1 и 1B-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C23, как указано в таблицах 1B-1 и 1B-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C24, как указано в таблицах 1B-1 и 1B-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C25, как указано в таблицах 1B-1 и 1B-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C26, как указано в таблицах 1B-1 и 1B-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C27, как указано в таблицах 1B-1 и 1B-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C28, как указано в таблицах 1B-1 и 1B-2.
В некоторых вариантах осуществления BCMA-связывающие молекулы содержат CDR легкой цепи, имеющий аминокислотную последовательность любого из CDR, перечисленных в таблице 1C-1, таблице 1D-1, таблице 1E-1, таблице 1F-1, таблице 1G-1, таблице 1H-1, таблице 1I-1, таблице 1J-1, таблице 1K-1(a), таблице 1K-1(b), таблице 1L-1, таблице 1M-1, таблице 1N-1(a) или таблице 1N-1(b). В конкретных вариантах осуществления в настоящем изобретении предусмотрены ВСМА-связывающие молекулы, содержащие один, два, три или более CDR легкой цепи (или в качестве альтернативы состоящие из них), выбранных из CDR легкой цепи, описанных в таблице 1C-1, таблице 1D-1, таблице 1E-1, таблице 1F-1, таблице 1G-1, таблице 1H-1, таблице 1I-1, таблице 1J-1, таблице 1K-1(a), таблице 1K-1(b), таблице 1L-1, таблице 1M-1, таблице 1N-1(a) и таблице 1N-1(b).
В некоторых вариантах осуществления BCMA-связывающие молекулы содержат CDR тяжелой цепи, имеющий аминокислотную последовательность любого из CDR тяжелой цепи, перечисленных в таблице 1C-2, таблице 1D-2, таблице 1E-2, таблице 1F-2, таблице 1G-2, таблице 1H-2, таблице 1I-2, таблице 1J-2, таблице 1K-2, таблице 1L-2, таблице 1M-2 или таблице 1N-2. В конкретных вариантах осуществления в настоящем изобретении предусмотрены ВСМА-связывающие молекулы, содержащие один, два, три или более CDR тяжелой цепи (или в качестве альтернативы состоящие из них), выбранных из CDR тяжелой цепи, описанных в таблице 1C-2, таблице 1D-2, таблице 1E-2, таблице 1F-2, таблице 1G-2, таблице 1H-2, таблице 1I-2, таблице 1J-2, таблице 1K-2, таблице 1L-2, таблице 1M-2 и таблице 1N-2.
В некоторых вариантах осуществления BCMA-связывающие молекулы содержат VL-домен, имеющий аминокислотную последовательность любого VL-домена, описанного в таблице 1O-1. Другие BCMA-связывающие молекулы могут содержать аминокислоты, которые были подвергнуты мутации, но при этом они характеризуются по меньшей мере 80, 85, 90, 95, 96, 97, 98 или 99 процентами идентичности VL-домена с VL-доменами, показанными в последовательностях, описанных в таблице 1O-1.
В некоторых вариантах осуществления BCMA-связывающие молекулы содержат VH-домен, имеющий аминокислотную последовательность любого VH-домена, описанного в таблице 1O-2. Другие BCMA-связывающие молекулы могут содержать аминокислоты, которые были подвергнуты мутации, но при этом они характеризуются по меньшей мере 80, 85, 90, 95, 96, 97, 98 или 99 процентами идентичности VH-домена с VH-доменами, показанными в последовательностях, описанных в таблице 1O-2.
Другие BCMA-связывающие молекулы содержат аминокислоты, которые были подвергнуты мутации, но при этом они характеризуются по меньшей мере 80, 85, 90, 95, 96, 97, 98 или 99 процентами идентичности CDR-участков с последовательностями CDR, описанными в таблице 1. В некоторых вариантах осуществления такие ВСМА-связывающие молекулы содержат мутантные аминокислотные последовательности, где не более 1, 2, 3, 4 или 5 аминокислот были подвергнуты мутации в CDR-участках по сравнению с последовательностями CDR, описанными в таблице 1.
Другие BCMA-связывающие молекулы содержат VH- и/или VL-домены, содержащие аминокислотные последовательности, характеризующиеся по меньшей мере 80, 85, 90, 95, 96, 97, 98 или 99 процентами идентичности с последовательностями VH- и/или VL, описанными в таблице 1. В некоторых вариантах осуществления BCMA-связывающие молекулы содержат VH- и/или VL-домены, где не более 1, 2, 3, 4 или 5 аминокислот были подвергнуты мутации по сравнению с VH- и/или VL-доменами, показанными в последовательностях, описанных в таблице 1, при этом они сохраняют по существу такую же терапевтическую активность.
Последовательности VH и VL (аминокислотные последовательности и нуклеотидные последовательности, кодирующие аминокислотные последовательности) могут быть подвергнуты "смешиванию и подбору" для создания других BCMA-связывающих молекул. Такие подвергнутые "смешиванию и подбору" BCMA-связывающие молекулы можно тестировать с применением известных анализов связывания (например, разновидностей ELISA, анализов, описанных в примерах). Когда цепи подвергают смешиванию и подбору, последовательность VH из конкретной пары VH/VL следует заменить на структурно подобную последовательность VH. Последовательность VL из конкретной пары VH/VL следует заменить на структурно подобную последовательность VL.
Соответственно, в одном варианте осуществления в настоящем изобретении предусмотрены ВСМА-связывающие молекулы, содержащие: вариабельный участок тяжелой цепи (VH), содержащий аминокислотную последовательность, выбранную из любой из последовательностей VH, описанных в таблице 1-O2; и вариабельный участок легкой цепи (VL), содержащий аминокислотную последовательность, описанную в таблице 1-O1.
В другом варианте осуществления в настоящем изобретении предусмотрены ВСМА-связывающие молекулы, которые содержат CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3, описанные в таблице 1, или любую их комбинацию.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB1, как указано в таблицах 1C-1 и 1C-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB1, как указано в таблицах 1D-1 и 1D-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB1, как указано в таблицах 1E-1 и 1E-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB1, как указано в таблицах 1F-1 и 1F-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB1, как указано в таблицах 1G-1 и 1G-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB1, как указано в таблицах 1H-1 и 1H-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB2, как указано в таблицах 1C-1 и 1C-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB2, как указано в таблицах 1D-1 и 1D-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB2, как указано в таблицах 1E-1 и 1E-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB2, как указано в таблицах 1F-1 и 1F-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB2, как указано в таблицах 1G-1 и 1G-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB2, как указано в таблицах 1H-1 и 1H-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из R1F2, как указано в таблицах 1C-1 и 1C-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из R1F2, как указано в таблицах 1D-1 и 1D-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из R1F2, как указано в таблицах 1E-1 и 1E-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из R1F2, как указано в таблицах 1F-1 и 1F-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из R1F2, как указано в таблицах 1G-1 и 1G-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из R1F2, как указано в таблицах 1H-1 и 1H-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF03, как указано в таблицах 1C-1 и 1C-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF03, как указано в таблицах 1D-1 и 1D-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF03, как указано в таблицах 1E-1 и 1E-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF03, как указано в таблицах 1F-1 и 1F-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF03, как указано в таблицах 1G-1 и 1G-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF03, как указано в таблицах 1H-1 и 1H-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF04, как указано в таблицах 1C-1 и 1C-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF04, как указано в таблицах 1D-1 и 1D-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF04, как указано в таблицах 1E-1 и 1E-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF04, как указано в таблицах 1F-1 и 1F-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF04, как указано в таблицах 1G-1 и 1G-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF04, как указано в таблицах 1H-1 и 1H-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF05, как указано в таблицах 1C-1 и 1C-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF05, как указано в таблицах 1D-1 и 1D-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF05, как указано в таблицах 1E-1 и 1E-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF05, как указано в таблицах 1F-1 и 1F-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF05, как указано в таблицах 1G-1 и 1G-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF05, как указано в таблицах 1H-1 и 1H-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF06, как указано в таблицах 1C-1 и 1C-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF06, как указано в таблицах 1D-1 и 1D-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF06, как указано в таблицах 1E-1 и 1E-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF06, как указано в таблицах 1F-1 и 1F-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF06, как указано в таблицах 1G-1 и 1G-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF06, как указано в таблицах 1H-1 и 1H-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF07, как указано в таблицах 1C-1 и 1C-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF07, как указано в таблицах 1D-1 и 1D-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF07, как указано в таблицах 1E-1 и 1E-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF07, как указано в таблицах 1F-1 и 1F-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF07, как указано в таблицах 1G-1 и 1G-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF07, как указано в таблицах 1H-1 и 1H-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF08, как указано в таблицах 1C-1 и 1C-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF08, как указано в таблицах 1D-1 и 1D-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF08, как указано в таблицах 1E-1 и 1E-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF08, как указано в таблицах 1F-1 и 1F-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF08, как указано в таблицах 1G-1 и 1G-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF08, как указано в таблицах 1H-1 и 1H-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF09, как указано в таблицах 1C-1 и 1C-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF09, как указано в таблицах 1D-1 и 1D-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF09, как указано в таблицах 1E-1 и 1E-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF09, как указано в таблицах 1F-1 и 1F-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF09, как указано в таблицах 1G-1 и 1G-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF09, как указано в таблицах 1H-1 и 1H-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF12, как указано в таблицах 1C-1 и 1C-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF12, как указано в таблицах 1D-1 и 1D-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF12, как указано в таблицах 1E-1 и 1E-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF12, как указано в таблицах 1F-1 и 1F-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF12, как указано в таблицах 1G-1 и 1G-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF12, как указано в таблицах 1H-1 и 1H-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF13, как указано в таблицах 1C-1 и 1C-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF13, как указано в таблицах 1D-1 и 1D-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF13, как указано в таблицах 1E-1 и 1E-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF13, как указано в таблицах 1F-1 и 1F-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF13, как указано в таблицах 1G-1 и 1G-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF13, как указано в таблицах 1H-1 и 1H-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF14, как указано в таблицах 1C-1 и 1C-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF14, как указано в таблицах 1D-1 и 1D-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF14, как указано в таблицах 1E-1 и 1E-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF14, как указано в таблицах 1F-1 и 1F-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF14, как указано в таблицах 1G-1 и 1G-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF14, как указано в таблицах 1H-1 и 1H-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF15, как указано в таблицах 1C-1 и 1C-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF15, как указано в таблицах 1D-1 и 1D-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF15, как указано в таблицах 1E-1 и 1E-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF15, как указано в таблицах 1F-1 и 1F-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF15, как указано в таблицах 1G-1 и 1G-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF15, как указано в таблицах 1H-1 и 1H-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF16, как указано в таблицах 1C-1 и 1C-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF16, как указано в таблицах 1D-1 и 1D-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF16, как указано в таблицах 1E-1 и 1E-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF16, как указано в таблицах 1F-1 и 1F-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF16, как указано в таблицах 1G-1 и 1G-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF16, как указано в таблицах 1H-1 и 1H-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF17, как указано в таблицах 1C-1 и 1C-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF17, как указано в таблицах 1D-1 и 1D-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF17, как указано в таблицах 1E-1 и 1E-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF17, как указано в таблицах 1F-1 и 1F-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF17, как указано в таблицах 1G-1 и 1G-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF17, как указано в таблицах 1H-1 и 1H-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF18, как указано в таблицах 1C-1 и 1C-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF18, как указано в таблицах 1D-1 и 1D-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF18, как указано в таблицах 1E-1 и 1E-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF18, как указано в таблицах 1F-1 и 1F-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF18, как указано в таблицах 1G-1 и 1G-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF18, как указано в таблицах 1H-1 и 1H-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF19, как указано в таблицах 1C-1 и 1C-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF19, как указано в таблицах 1D-1 и 1D-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF19, как указано в таблицах 1E-1 и 1E-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF19, как указано в таблицах 1F-1 и 1F-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF19, как указано в таблицах 1G-1 и 1G-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF19, как указано в таблицах 1H-1 и 1H-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF20, как указано в таблицах 1C-1 и 1C-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF20, как указано в таблицах 1D-1 и 1D-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF20, как указано в таблицах 1E-1 и 1E-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF20, как указано в таблицах 1F-1 и 1F-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF20, как указано в таблицах 1G-1 и 1G-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF20, как указано в таблицах 1H-1 и 1H-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB3, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB3, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB3, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB3, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB3, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB3, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PI-61, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PI-61, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PI-61, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PI-61, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PI-61, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PI-61, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-22, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-22, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-22, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-22, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-22, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-22, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-88, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-88, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-88, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-88, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-88, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-88, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-36, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-36, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-36, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-36, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-36, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-36, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-34, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-34, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-34, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-34, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-34, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-34, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-68, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-68, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-68, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-68, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-68, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-68, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-18, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-18, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-18, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-18, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-18, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-18, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-47, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-47, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-47, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-47, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-47, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-47, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-20, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-20, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-20, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-20, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-20, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-20, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-80, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-80, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-80, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-80, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-80, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-80, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-83, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-83, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-83, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-83, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-83, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-83, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-1, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-1, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-1, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-1, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-1, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-1, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-2, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-2, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-2, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-2, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-2, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-2, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-3, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-3, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-3, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-3, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-3, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-3, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-4, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-4, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-4, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-4, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-4, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-4, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-5, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-5, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-5, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-5, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-5, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-5, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-6, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-6, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-6, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-6, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-6, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-6, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-7, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-7, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-7, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-7, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-7, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-7, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-8, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-8, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-8, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-8, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-8, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-8, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-9, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-9, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-9, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-9, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-9, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-9, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-10, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-10, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-10, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-10, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-10, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-10, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-11, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-11, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-11, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-11, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-11, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-11, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-12, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-12, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-12, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-12, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-12, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-12, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-13, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-13, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-13, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-13, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-13, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-13, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-14, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-14, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-14, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-14, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-14, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-14, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-15, как указано в таблицах 1I-1 и 1I-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-15, как указано в таблицах 1J-1 и 1J-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-15, как указано в таблицах 1K-1 и 1K-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-15, как указано в таблицах 1L-1 и 1L-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-15, как указано в таблицах 1M-1 и 1M-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-15, как указано в таблицах 1N-1 и 1N-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи AB1, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи AB2, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи R1F2, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF03, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF04, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF05, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF06, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF07, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF08, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF09, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF12, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF13, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF14, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF15, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF16, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF17, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF18, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF19, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF20, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи AB3, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PI-61, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-1, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-2, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-3, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-4, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-5, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-6, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-7, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-8, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-9, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-10, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-11, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-12, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-13, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-14, как указано в таблице 1O-1 и таблице 1O-2. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-15, как указано в таблице 1O-1 и таблице 1O-2.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность scFv из H2/L2-88, как указано в таблице 1P. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность scFv из H2/L2-36, как указано в таблице 1P. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность scFv из H2/L2-34, как указано в таблице 1P. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность scFv из H2/L2-68, как указано в таблице 1P. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность scFv из H2/L2-18, как указано в таблице 1P. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность scFv из H2/L2-47, как указано в таблице 1P. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность scFv из H2/L2-20, как указано в таблице 1P. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность scFv из H2/L2-80, как указано в таблице 1P. В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность scFv из H2/L2-83, как указано в таблице 1P.
Учитывая, что каждая ВСМА-связывающая молекула связывает ВСМА, и что специфичность связывания антигена обеспечивается в первую очередь участками CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3, последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 могут быть подвергнуты "смешиванию и подбору". Такие подвергнутые "смешиванию и подбору" BCMA-связывающие молекулы можно тестировать с применением известных анализов связывания и тех анализов, что описаны в примерах (например, разновидностей ELISA). Когда последовательности CDR VH подвергают смешиванию и подбору, последовательность CDR-H1, CDR-H2 и/или CDR-H3 из конкретной последовательности VH следует заменить на структурно сходную(сходные) последовательность(последовательности) CDR. Аналогичным образом, когда последовательности CDR VL подвергают смешиванию и подбору, последовательность CDR-L1, CDR-L2 и/или CDR-L3 из конкретной последовательности VL следует заменить на структурно сходную(сходные) последовательность(последовательности) CDR. Специалисту в данной области техники будет совершенно очевидно, что новые последовательности VH и VL можно создавать посредством замены одной или нескольких последовательностей CDR-участков VH и/или VL на структурно сходные последовательности из последовательностей CDR, показанных в данном документе для моноклональных антител или других BCMA-связывающих молекул по настоящему изобретению.
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит последовательность VL, выбранную из последовательностей VL, указанных в таблице 1O-1, и последовательность VH, выбранную из последовательностей VH, указанных в таблице 1O-2. В некоторых вариантах осуществления BCMA-связывающая молекула содержит последовательность CDR-H1, выбранную из последовательностей CDR-H1, указанных в таблице 1A-2, таблице 1B-2, таблице 1C-2, таблице 1D-2, таблице 1E-2, таблице 1F-2, таблице 1G-2, таблице 1H-2, таблице 1I-2, таблице 1J-2, таблице 1K-2, таблице 1L-2, таблице 1M-2 и таблице 1N-2; последовательность CDR-H2, выбранную из последовательностей CDR-H2, указанных в таблице 1A-2, таблице 1B-2, таблице 1C-2, таблице 1D-2, таблице 1E-2, таблице 1F-2, таблице 1G-2, таблице 1H-2, таблице 1I-2, таблице 1J-2, таблице 1K-2, таблице 1L-2, таблице 1M-2 и таблице 1N-2; последовательность CDR-H3, выбранную из последовательностей CDR-H3, указанных в таблице 1A-2, таблице 1B-2, таблице 1C-2, таблице 1D-2, таблице 1E-2, таблице 1F-2, таблице 1G-2, таблице 1H-2, таблице 1I-2, таблице 1J-2, таблице 1K-2, таблице 1L-2, таблице 1M-2 и таблице 1N-2; последовательность CDR-L1, выбранную из последовательностей CDR-L1, указанных в таблице 1A-1, таблице 1B-1, таблице 1C-1, таблице 1D-1, таблице 1E-1, таблице 1F-1, таблице 1G-1, таблице 1H-1, таблице 1I-1, таблице 1J-1, таблице 1K-1(a), таблице 1K-1(b), таблице 1L-1, таблице 1M-1, таблице 1N-1(a) и таблице 1N-1 (b); последовательность CDR-L2, выбранную из последовательностей CDR-L2, указанных в таблице 1A-1, таблице 1B-1, таблице 1C-1, таблице 1D-1, таблице 1E-1, таблице 1F-1, таблице 1G-1, таблице 1H-1, таблице 1I-1, таблице 1J-1, таблице 1K-1(a), таблице 1K-1(b), таблице 1L-1, таблице 1M-1, таблице 1N-1(a) и таблице 1N-1 (b); и последовательность CDR-L3, выбранную из последовательностей CDR-L3, указанных в таблице 1A-1, таблице 1B-1, таблице 1C-1, таблице 1D-1, таблице 1E-1, таблице 1F-1, таблице 1G-1, таблице 1H-1, таблице 1I-1, таблице 1J-1, таблице 1K-1(a), таблице 1K-1(b), таблице 1L-1, таблице 1M-1, таблице 1N-1(a) и таблице 1N-1(b).
BCMA-связывающие молекулы могут быть слиты или химически конъюгированы (в том числе посредством как ковалентной, так и нековалентной конъюгации) с гетерологичным белком или полипептидом (или его фрагментом, например с полипептидом из по меньшей мере 10, по меньшей мере 20, по меньшей мере 30, по меньшей мере 40, по меньшей мере 50, по меньшей мере 60, по меньшей мере 70, по меньшей мере 80, по меньшей мере 90 или по меньшей мере 100 аминокислот). Например, ВСМА-связывающая молекула может быть непосредственно или опосредованно слита с выявляемым белком, например с ферментом или флуоресцентным белком, таким как те, что описаны в разделе 7.10. Способы слияния или конъюгации белков, полипептидов или пептидов с антителом или фрагментом антитела известны и могут быть использованы для слияния или конъюгации белка или полипептида с ВСМА-связывающей молекулой по настоящему изобретению. См., например, патенты США №№ 5336603, 5622929, 5359046, 5349053, 5447851 и 5112946; европейские патенты №№ EP 307434 и EP 367166; международные публикации №№ WO 96/04388 и WO 91/06570; Ashkenazi et al., (1991) Proc. Natl. Acad. Sci. USA 88:10535-10539; Zheng et al., (1995) J. Immunol. 154:5590-5600; и Vil et al., (1992) Proc. Natl. Acad. Sci. USA 89:11337- 11341.
Дополнительные BCMA-связывающие молекулы можно получать с помощью методик перетасовки генов, перетасовки мотивов, перетасовки экзонов и/или перетасовки кодонов (в совокупности называемых "перетасовкой ДНК"). Перетасовку ДНК можно применять для изменения активностей молекул по настоящему изобретению или их фрагментов (например, молекул или их фрагментов с более высокими уровнями аффинности и более низкими значениями скорости диссоциации). См., в целом патенты США №№ 5605793, 5811238, 5830721, 5834252 и 5837458; Patten et al., (1997) Curr. Opinion Biotechnol. 8:724-33; Harayama, (1998) Trends Biotechnol. 16(2):76-82; Hansson et al., (1999) J. Mol. Biol. 287:265-76; и Lorenzo and Blasco, (1998) Biotechniques 24(2):308- 313. Описанные в данном документе ВСМА-связывающие молекулы или их фрагменты можно изменять посредством воздействия на них случайного мутагенеза с помощью ПЦР с внесением ошибок, случайной вставки нуклеотидов или других способов до проведения рекомбинации. Полинуклеотид, кодирующий фрагмент описанной в данном документе BCMA-связывающей молекулы, может быть подвергнут рекомбинации с одним или несколькими компонентами, мотивами, секциями, частями, доменами, фрагментами и т. д. одной или нескольких гетерологичных молекул.
Более того, BCMA-связывающие молекулы могут быть слиты с маркерными последовательностями, таким как пептид, для облегчения очистки. В некоторых вариантах осуществления маркерная аминокислотная последовательность представляет собой гексагистидиновый пептид (SEQ ID NO:603), такой как, среди прочих, метка, представленная в векторе pQE (QIAGEN, Inc., 9259 Eton Avenue, Чатсворт, Калифорния, 91311), многие из которых являются коммерчески доступными. Как описано в Gentz et al., (1989) Proc. Natl. Acad. Sci. USA 86:821-824, например, гексагистидин (SEQ ID NO:603) обеспечивает удобную очистку слитого белка. Другие пептидные метки, применимые для очистки, включают без ограничения гемагглютининовую ("HA") метку, которая соответствует эпитопу, полученному из белка гемагглютинина вируса гриппа (Wilson et al., (1984) Cell 37:767), и метку "flag".
7.3. Антиген-связывающие домены полиспецифических связывающих молекул
Как правило, один или несколько ABD из МBM содержат антигенсвязывающие домены на основе иммуноглобулинов, например, последовательности фрагментов или производных антител, как описано в разделе 7.2. Эти фрагменты и производные антител, как правило, включают CDR антитела и могут включать фрагменты большего размера и их производные, например, Fab, scFab, Fv и scFv.
7.3.1. ABD на основе иммуноглобулинов
7.3.1.1. Fab
В определенных аспектах MBM содержат один или несколько ABD, которые представляют собой Fab-домены, например, как описано в разделе 7.2.
Для MBM по настоящему изобретению является преимущественным применение стратегий гетеродимеризации Fab для обеспечения надлежащей ассоциации Fab-доменов, входящих в состав одного и того же ABD, и минимизации аберрантного спаривания Fab-доменов, входящих в состав различных ABD. Например, можно применять стратегии гетеродимеризации Fab, показанные в таблице 2 ниже:
Стратегии гетеродимеризации Fab
Соответственно, в определенных вариантах осуществления надлежащей ассоциации между двумя полипептидами Fab способствует обмен VL- и VH-доменов Fab друг на друга или обмен CH1- и CL-доменов друг на друга, например, как описано в WO 2009/080251.
Надлежащему спариванию Fab также может способствовать введение одной или нескольких аминокислотных модификаций в CH1-домен и одной или нескольких аминокислотных модификаций в CL-домен Fab и/или одной или нескольких аминокислотных модификаций в VH-домен и одной или нескольких аминокислотных модификаций в VL-домен. Аминокислоты, которые подвергают модификации, как правило, являются частью области контакта VH:VL и CH1:CL таким образом, что компоненты Fab предпочтительно спариваются друг с другом, а не с компонентами других Fab.
В одном варианте осуществления одна или несколько аминокислотных модификаций ограничены консервативными остатками каркасных участков в вариабельных (VH, VL) и константных (CH1, CL) доменах, которые указаны в нумерации остатков по Kabat. В Almagro, 2008, Frontiers In Bioscience 13:1619-1633 приводится определение остатков каркасных участков на основании схем нумерации по Kabat, Chothia и IMGT.
В одном варианте осуществления модификации, введенные в VH- и CH1-домены и/или VL- и CL-домены, являются комплементарными друг другу. Комплементарности в области контакта тяжелой и легкой цепей можно достигать с использованием стерических и гидрофобных контактов, электростатических взаимодействий/взаимодействий зарядов или любой комбинации разнообразных взаимодействий. Комплементарность между поверхностями белков широко описана в литературе в терминах соответствия "ключ-замок", взаимодействий типа "выступ в углубление", выпячивания и полости, донора и акцептора и т. д., при этом во всех из них подразумевается природа структурного и химического соответствия между двумя взаимодействующими поверхностями.
В одном варианте осуществления посредством одной или нескольких введенных модификаций вводят новую водородную связь в области контакта компонентов Fab. В одном варианте осуществления посредством одной или нескольких введенных модификаций вводят новый солевой мостик в области контакта компонентов Fab. Иллюстративные замены описаны в WO 2014/150973 и WO 2014/082179.
В некоторых вариантах осуществления Fab-домен содержит замену 192E в CH1-домене и замены 114A и 137K в CL-домене, посредством которых вводят солевой мостик между CH1- и CL-доменами (см. Golay et al., 2016, J Immunol 196:3199-211).
В некоторых вариантах осуществления Fab-домен содержит замены 143Q и 188V в CH1-домене и замены 113T и 176V в CL-домене, которые способствуют обмену гидрофобных и полярных участков контакта между CH1- и CL-доменами (см. Golay et al., 2016, J Immunol 196:3199-211).
В некоторых вариантах осуществления Fab-домен может содержать модификации в некоторых или во всех из VH-, CH1-, VL-, CL-доменов для введения ортогональных областей контакта в Fab, которые способствуют надлежащей сборке Fab-доменов (Lewis et al., 2014 Nature Biotechnology 32:191-198). В одном варианте осуществления модификации 39K, 62E вводят в VH-домен, модификации H172A, F174G вводят в CH1-домен, модификации 1R, 38D, (36F) вводят в VL-домен, и модификации L135Y, S176W вводят в CL-домен. В другом варианте осуществления модификацию 39Y вводят в VH-домен, и модификацию 38R вводят в VL-домен.
Fab-домены также можно модифицировать, замещая нативную дисульфидную связь CH1:CL сконструированной дисульфидной связью, за счет чего обеспечивается увеличение эффективности спаривания компонентов Fab. Например, сконструированную дисульфидную связь можно вводить посредством введения 126C в CH1-домен и 121C в CL-домен (см. Mazor et al., 2015, MAbs 7:377-89).
Fab-домены также можно модифицировать посредством замены CH1-домена и CL-домена на альтернативные домены, которые способствуют надлежащей сборке. Например, в Wu et al., 2015, MAbs 7:364-76 описана замена CH1-домена на константный домен T-клеточного рецептора α и замена CL-домена на β-домен T-клеточного рецептора, а также спаривание этих замененных доменов с помощью дополнительного взаимодействия типа "заряд-заряд" между VL- и VH-доменами посредством введения модификации 38D в VL-домен и модификации 39K в VH-домен.
MBM могут содержать один или несколько ABD, которые представляют собой одноцепочечные Fab-фрагменты, например, как описано в разделе 7.2.
7.3.1.2. scFv
В определенных аспектах MBM содержат один или несколько ABD, которые представляют собой scFv, например, как описано в разделе 7.2.
7.3.1.3. Другие ABD на основе иммуноглобулинов
МBM также могут содержать ABD, имеющие формат иммуноглобулина, который отличается от Fab или scFv, например, Fv, dsFv, (Fab')2, однодоменное антитело (SDAB), VH- или VL-домен или VHH-домен верблюдовых (также называемый нанотелом).
ABD может представлять собой однодоменное антитело, состоящее из одного VH- или VL-домена, который проявляет достаточную аффинность к мишени. В одном варианте осуществления однодоменное антитело представляет собой VHH-домен верблюдовых (см., например, Riechmann, 1999, Journal of Immunological Methods 231:25-38; WO 94/04678).
7.3.2. ABD на основе молекул, отличных от иммуноглобулинов
В определенных вариантах осуществления MBM содержат один или несколько ABD, которые получены из отличных от антител каркасных белков (включая без ограничения сконструированные белки с анкириновыми повторами (дарпины), авимеры (что сокращенно обозначает авидные мультимеры), антикалины/липокалины, центирины, домены Куница, аднексины, аффилины, аффитины (также известные как нонфитины), ноттины, пронектины, версатела, дуокалины и финомеры), лигандов, рецепторов, цитокинов или хемокинов.
Каркасные структуры на основе молекул, отличных от иммуноглобулинов, которые можно применять в МBM, включают каркасные структуры, которые перечислены в таблицах 3 и 4 из Mintz and Crea, 2013, Bioprocess International 11(2):40-48; на фигуре 1, в таблице 1 и на фигуре I в Vazquez-Lombardi et al., 2015, Drug Discovery Today 20(10):1271-83; в таблице 1 и боксе 2 в Skrlec et al., 2015, Trends in Biotechnology 33(7):408-18. Содержание таблиц 3 и 4 из Mintz and Crea, 2013, Bioprocess International 11(2):40-48; фигуры 1, таблицы 1 и фигуры I из Vazquez-Lombardi et al., 2015, Drug Discovery Today 20(10):1271-83; таблицы 1 и бокса 2 из Skrlec et al., 2015, Trends in Biotechnology 33(7):408-18 (совместно называемые "раскрытия каркасных структур") включено в данный документ посредством ссылки. В конкретном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении аднексинов. В другом варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении авимеров. В другом варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении аффител. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении антикалинов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении дарпинов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении доменов Куница. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении ноттинов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении пронектинов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении нанофитинов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении аффилинов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении аднектинов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении ABD. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении адгиронов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении аффимеров. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении альфател. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении белков с повторами Armadillo. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении атримеров/тетранектинов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении O-тел/OB-складок. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении центиринов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении репетел. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении антикалинов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении атримеров. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении бициклических пептидов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении цистиновых узлов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении каркасных структур Fn3 (включая аднектины, центирины, пронектины и Tn3).
В одном варианте осуществления ABD может представлять собой сконструированный белок с анкириновым повтором ("дарпин"). Дарпины представляют собой белки-миметики антител, которые, как правило, проявляют высокоспецифическое и высокоаффинное связывание белков-мишеней. Как правило, они являются генетически сконструированными и полученными из природных белков-анкиринов и состоят из по меньшей мере трех, обычно четырех или пяти повторяющихся мотивов этих белков. Их молекулярная масса составляет приблизительно 14 или 18 кДа (килодальтон) для дарпинов, содержащих четыре или пять повторов соответственно. Примеры дарпинов можно найти, например, в патенте США № 7417130. Полиспецифические связывающие молекулы, содержащие связывающие модули на основе дарпинов и связывающие модули на основе иммуноглобулинов, раскрыты, например, в публикации заявки на патент США № 2015/0030596 A1.
В другом варианте осуществления ABD может представлять собой аффитело. Аффитело широко известно и относится к аффинным белкам на основе белкового домена из 58 аминокислотных остатков, полученного из одного из IgG-связывающих доменов стафилококкового белка A.
В другом варианте осуществления ABD может представлять собой антикалин. Антикалины широко известны и относятся к другой технологии с использованием миметиков антител, где специфичность связывания определяется липокалинами. Антикалины также могут существовать в формате белков с двойным нацеливанием, называемых дуокалинами.
В другом варианте осуществления ABD может представлять собой версатело. Версатела широко известны и относятся к другой технологии с использованием миметиков антител. Они представляют собой небольшие белки с молекулярным весом 3-5 кДа с > 15% содержанием остатков цистеина, которые образуют каркасную структуру с высокой плотностью дисульфидных связей, заменяющую гидрофобное ядро типичных белков.
Другие ABD на основе молекул, отличных от иммуноглобулинов, включают олигомеры "A"-доменов (также известные как авимеры) (см., например, публикации заявок на патент США №№ 2005/0164301, 2005/0048512 и 2004/017576), белковые каркасные структуры на основе Fn3 (см., например, публикацию заявки на патент США 2003/0170753), полипептиды VASP, птичий панкреатический полипептид (aPP), тетранектин (на основе CTLD3), аффилин (на основе γB-кристаллина/убиквитина), ноттины, SH3-домены, PDZ-домены, тендамистат, неокарциностатин, домены белка A, липокалины, трансферрин и домены Куница. В одном аспекте ABD, применимые в конструкции МBM, содержат каркасные структуры на основе фибронектина, как проиллюстрировано в WO 2011/130324.
Более того, в определенных аспектах ABD содержит лиганд-связывающий домен рецептора или рецептор-связывающий домен лиганда.
7.3.3. ABD к TCR
MBM содержат ABD, который специфически связывается с BCMA, и по меньшей мере один ABD, который является специфическим по отношению к другому антигену, например, компоненту комплекса TCR. TCR представляет собой стабилизированный дисульфидными связями заякоренный в мембране гетеродимерный белок, обычно состоящий из высоковариабельных альфа- (α-) и бета- (β-) цепей, которые экспрессируются в виде части комплекса с молекулами инвариантных цепей CD3. T-клетки, экспрессирующие этот рецептор, называются α:β- (или αβ-) T-клетками, хотя меньшая часть T-клеток, называемая γδ-T-клетками, экспрессирует альтернативный рецептор, образованный вариабельными гамма- (γ-) и дельта- (δ-) цепями.
В одном варианте осуществления MBM содержат ABD, который специфически связывается с CD3.
7.3.3.1. ABD к CD3
MBM могут содержать ABD, который специфически связывается с CD3. Термин "CD3" относится к корецептору (или корецепторному комплексу, или полипептидной цепи корецепторного комплекса) T-клеточного рецептора, представляющему собой кластер дифференцировки 3. Аминокислотные последовательности полипептидных цепей CD3 человека приведены в NCBI под номерами доступа P04234, P07766 и P09693. Белки CD3 также могут включать варианты. Белки CD3 также могут включать фрагменты. Белки CD3 также содержат посттрансляционные модификации аминокислотных последовательностей CD3. Посттрансляционные модификации включают без ограничения N- и O-связанное гликозилирование.
В некоторых вариантах осуществления MBM может содержать ABD, который представляет собой антитело к CD3 (например, как описано в US 2016/0355600, WO 2014/110601 и WO 2014/145806) или его антигенсвязывающий домен. Иллюстративные последовательности VH, VL и scFV к CD3, которые можно применять в MBM, предусмотрены в таблице 3A.
Средства, связывающие CD3 - последовательности вариабельных доменов
Последовательности CDR для ряда средств, связывающих CD3, которые определены согласно схеме нумерации по Kabat (Kabat et al, 1991, Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, Md.), схеме нумерации по Chothia (Al-Lazikani et al., 1997, J. Mol. Biol 273:927-948) и комбинации схем нумерации по Kabat и по Chothia, предусмотрены в таблицах 3B-3D соответственно.
Средства, связывающие CD3 - последовательности CDR в соответствии со схемой нумерации по Kabat
TNYNQKFKD
CLDY
VSYMN
PFT
ATYYADSVKD
SYVSWFAY
TTSNYAN
NLWV
KYNQKFKD
VYFDY
VSYMH
PPT
NYNQKFKD
YCLDY
YMN
NPLT
NYNQKVKD
YCLDY
VSYMN
NPFT
YYVDSVKG
HFDL
VSSYLA
WPPLT
ATYYAD
SYVSWFAY
TTSNYAN
NLWV
NYNQKFKD
CLDY
SYMN
NPLT
YATYYAD
SYVSWFAY
TTSNYAN
LWV
TYYADSVKD
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWWAY
TSGNYPN
NRWV
TYYADSVKD
YISYWAY
TSGNYPN
NYNQKFKD
YCLDY
SYMN
PFT
TYYADSVKD
YVSWFAY
TTSNYAN
NLWV
TYYADSVKD
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
NYNQKVKD
YCLDY
SYMN
NPFT
NYNQKVKD
YSLDY
SYMN
NPFT
TYNQKFKD
DWYFDV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
RNYLN
LPWT
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFDY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
ATYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TAYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFDY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TSSNYAN
NLWV
TYYADSVKG
YVSWFAY
TSGHYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFDY
TTSNYAN
NLWV
TYYADSVKG
YVSWFDY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NLWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
TYYADSVKG
YVSWFAY
TTSNYAN
NHWV
Средства, связывающие CD3 - последовательности CDR в соответствии со схемой нумерации по Chothia
YVSWFAY
YVSWFA
YVSWFA
YVSWFAY
YVSWWAY
YISYWAY
YVSWFAY
YVSWFAY
YVSWFAY
YVSWFAY
Средства, связывающие CD3 - последовательности CDR в соответствии с комбинацией схем нумерации по Kabat и по Chothia
YTMH
NYNQKFKD
CLDY
SYMN
PFT
YAMN
TYYADSVKD
YVSWFAY
TTSNYAN
LWV
YTMH
KYNQKFKD
YFDY
SYMH
PPT
YTMH
NYNQKFKD
CLDY
SYMN
PLT
YTMH
NYNQKVKD
CLDY
SYMN
PFT
YGMH
YYVDSVKG
FDL
SSYLA
PPLT
YAMN
ATYYADSVK
YVSWFAY
TTSNYAN
LWV
YTMH
NYNQKFKD
CLDY
SYMN
PLT
YAMN
ATYYADSVK
YVSWFAY
TTSNYAN
LWV
YAMN
TYYADSVKD
YVSWFAY
TTSNYAN
LWV
YAMN
TYYADSVKG
YVSWWAY
TSGNYPN
RWV
YAMN
TYYADSVKD
YISYWAY
TSGNYPN
RWV
YTMH
NYNQKFKD
CLDY
SYMN
YAMN
TYYADSVKD
YVSWFAY
TTSNYAN
LWV
YAMN
TYYADSVKD
TTSNYAN
LWV
YAMN
TYYADSVKG
YVSWFAY
TTSNYAN
LWV
YAMN
TYYADSVKG
YVSWFAY
HWV
YTMH
NYNQKVKD
CLDY
SYMN
PFT
YTMH
NYNQKVKD
SLDY
SYMN
PFT
YTMN
TYNQKFKD
DWYFDV
RNYLN
LPWT
В некоторых вариантах осуществления MBM может содержать ABD к CD3, который содержит CDR из любого из CD3-1 - CD3-127, которые определены согласно нумерации по Kabat (например, как указано в таблице 3B). В других вариантах осуществления MBM может содержать ABD к CD3, который содержит CDR из любого из CD3-1 - CD3-127, которые определены согласно нумерации по Chothia (например, как указано в таблице 3C). В других вариантах осуществления MBM может содержать ABD к CD3, который содержит CDR из любого из CD3-1 - CD3-127, которые определены согласно комбинации схем нумерации по Kabat и по Chothia (например, как указано в таблице 3D).
В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-1. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-2. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-3. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-4. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-5. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-6. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-7. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-8. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-9. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-10. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-11. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-12. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-13. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-14. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-15. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-16. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-17. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-18. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-19. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-20. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-21. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-22. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-23. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-24. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-25. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-26. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-27. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-28. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-29. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-30. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-31. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-32. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-33. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-34. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-35. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-36. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-37. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-38. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-39. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-40. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-41. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-42. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-43. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-44. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-45. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-46. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-47. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-48. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-49. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-50. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-51. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-52. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-53. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-54. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-55. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-56. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-57. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-58. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-59. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-60. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-61. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-62. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-63. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-64. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-65. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-66. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-67. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-68. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-69. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-70. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-71. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-72. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-73. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-74. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-75. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-76. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-77. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-78. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-79. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-80. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-81. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-82. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-83. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-84. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-85. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-86. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-87. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-88. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-89. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-90. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-91. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-92. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-93. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-94. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-95. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-96. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-97. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-98. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-99. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-100. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-101. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-102. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-103. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-104. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-105. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-106. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-107. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-108. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-109. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-110. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-111. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-112. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-113. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-114. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-115. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-116. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-117. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-118. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-119. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-120. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-121. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-122. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-123. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-124. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-125. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-126. В некоторых вариантах осуществления ABD к CD3 содержит последовательности CDR из CD3-127.
MBM может содержать полные вариабельные последовательности тяжелых и легких цепей из любого из от CD3-1 до CD3-127. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-1. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-1. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-2. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-3. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-4. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-5. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-6. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-7. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-8. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-9. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-10. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-11. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-12. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-13. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-14. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-15. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-16. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-17. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-18. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-19. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-20. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-21. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-22. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-23. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-24. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-25. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-26. В некоторых вариантах осуществления МBM содержит ABD к CD3, который содержит последовательности VH и VL из CD3-27.
В дополнение к наборам CDR, описанным в таблицах 3B-3D (т. е. набору из шести CDR для каждого из CD3-1 - CD3-127), в настоящем изобретении предусмотрены варианты наборов CDR. В одном варианте осуществления набор из 6 CDR может содержать 1, 2, 3, 4 или 5 аминокислотных изменений по сравнению с набором CDR, описанным в таблицах 3B-3D, при условии, что ABD к CD3 все еще сохраняет способность связываться с антигеном-мишенью, как измерено с помощью по меньшей мере одного из анализа Biacore, анализа поверхностного плазмонного резонанса (SPR) и/или анализа BLI (биослойная интерферометрия, например, анализ Octet).
В дополнение к вариабельным доменам тяжелой цепи и вариабельным доменам легкой цепи, раскрытым в таблице 3A, которые образуют ABD для CD3, в настоящем изобретении предусмотрены варианты VH- и VL-доменов. В одном варианте осуществления каждый вариант VH- и VL-доменов может содержать от 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 аминокислотных изменений по сравнению с VH- и VL-доменом, указанными в таблице 3A, при условии, что ABD все еще сохраняет способность связываться с антигеном-мишенью, как измерено с помощью по меньшей мере одного из анализа Biacore, анализа поверхностного плазмонного резонанса (SPR) и/или анализа BLI (биослойная интерферометрия, например, анализ Octet). В другом варианте осуществления варианты VH и VL по меньшей мере на 90, 95, 97, 98 или 99% идентичны соответствующим VH или VL, раскрытым в таблице 3A, при условии, что ABD все еще сохраняет способность связываться с антигеном-мишенью, как измерено с помощью по меньшей мере одного из анализа Biacore, анализа поверхностного плазмонного резонанса (SPR) и/или анализа BLI (биослойная интерферометрия, например, анализ Octet).
В некоторых вариантах осуществления антигенсвязывающий домен, который специфически связывается с CD3 человека, основан на отличной от иммуноглобулина молекуле, и вместо этого получен из каркасного белка, отличного от антитела, например, из одного из каркасных белков, отличных от антител, описанных в разделе 7.3.2. В одном варианте осуществления антигенсвязывающий домен, который специфически связывается с CD3 человека, включает аффилин-144160, который описан в WO 2017/013136. Аффилин-144160 имеет следующую аминокислотную последовательность:
MQIFVKTLTGKTITLEVEPSDTIENVKAKIQDKEGIPPDQQWLWFAGKQLEDGRTLSDYNIQKESTLKLWLVDKAAMQIFVYTRTGKTITLEVEPSDTIENVKAKIQDKEGIPPDQQRLIWAGKQLEDGRTLSDYNIALESGLHLVLRLRAA (SEQ ID NO:415)
7.3.3.2. ABD к TCR-α/β
MBM могут содержать ABD, который специфически связывается с α-цепью TCR, β-цепью TCR или димером TCR-αβ. Иллюстративные антитела к TCRα/β известны (см., например, US 2012/0034221; Borst et al., 1990, Hum Immunol. 29(3):175-88 (в которых описано антитело BMA031)). Последовательности VH, VL и CDR по Kabat из антитела BMA031 предусмотрены в таблице 4.
Последовательности BMA031
В одном варианте осуществления ABD к TCR может содержать последовательности CDR из антитела BMA031. В других вариантах осуществления ABD к TCR может содержать последовательности VH и VL из антитела BMA031.
7.3.3.3. ABD к TCR-γ/δ
MBM могут содержать ABD, который специфически связывается с γ цепью TCR, δ цепью TCR или димером TCR-γδ. Иллюстративные антитела к TCR-γ/δ известны (см., например, патент США № 5980892 (в котором описано δTCS1, полученное с помощью гибридомы, депонированной в ATCC под номером доступа HB 9578)).
7.4. Соединители
Предполагается, что BCMA-связывающие молекулы в некоторых случаях могут содержать пары ABD или цепей ABD (например, компонент VH-CH1 или VL-CL из Fab), непосредственно соединенные друг с другом, например, в виде слитого белка без линкера. Например, BCMA-связывающие молекулы содержат соединительные фрагменты, связывающие отдельные ABD или цепи ABD. Применение соединительных фрагментов может улучшать связывание мишени, например, посредством повышения гибкости ABD в BCMA-связывающей молекуле и, таким образом, снижения стерического несоответствия. ABD или цепи ABD могут быть соединены друг с другом посредством, например, Fc-доменов (при этом каждый Fc-домен представляет собой пару ассоциированных Fc-участков) и/или линкеров для ABD. При применении Fc-доменов будет, как правило, требоваться применение шарнирных участков в качестве соединителей для ABD или цепей ABD для оптимального связывания антигена. Таким образом, термин "соединитель" охватывает без ограничения Fc-участки, Fc-домены и шарнирные участки.
Соединители могут быть выбраны или модифицированы, например, для увеличения или уменьшения биологического периода полужизни BCMA-связывающей молекулы. Например, для уменьшения биологического периода полужизни одна или несколько аминокислотных мутаций могут быть введены в участок области контакта доменов CH2-CH3 фрагмента Fc-шарнирный фрагмент таким образом, чтобы BCMA-связывающая молекула, содержащая фрагмент, характеризовалась ухудшенным связыванием со стафилококковым белком A (SpA) по сравнению со связыванием нативного домена Fc-шарнирный участок с SpA. Данный подход более подробно описан в патенте США № 6165745 под авторством Ward et al. В качестве альтернативы, BCMA-связывающая молекула может быть модифицирована для увеличения ее биологического периода полужизни. Например, можно вводить одну или несколько из следующих мутаций: T252L, T254S, T256F, как описано в патенте США № 6277375, выданном Ward. В качестве альтернативы, для увеличения биологического периода полужизни BCMA-связывающую молекулу можно изменять в пределах CH1- или CL-участка таким образом, чтобы она содержала эпитоп связывания рецептора реутилизации, взятый из двух петель CH2-домена Fc-участка IgG, как описано в патентах США №№ 5869046 и 6121022 за авторством Presta et al.
Примеры Fc-доменов (образованных посредством спаривания двух Fc-участков), шарнирных участков и линкеров для ABD описаны в разделах 7.4.1, 7.4.2 и 7.4.3 соответственно.
7.4.1. Fc-домены
BCMA-связывающие молекулы могут содержать Fc-домен, полученный из любого подходящего вида. В одном варианте осуществления Fc-домен получен из человеческого Fc-домена.
Fc-домен может быть получен из антитела любого подходящего класса, включая IgA (включая подклассы IgA1 и IgA2), IgD, IgE, IgG (включая подклассы IgG1, IgG2, IgG3 и IgG4) и IgM. В одном варианте осуществления Fc-домен получен из IgG1, IgG2, IgG3 или IgG4. В одном варианте осуществления Fc-домен получен из IgG1. В одном варианте осуществления Fc-домен получен из IgG4.
В нативном антителе Fc-участки, как правило, являются идентичными, но для цели получения полиспецифических связывающих молекул, например, MBM по настоящему изобретению, Fc-участки могут быть преимущественно отличающимися для обеспечения возможности гетеродимеризации, которая описана в разделе 7.4.1.5 ниже.
Как правило, каждый Fc-участок содержит два или три константных домена тяжелой цепи или состоит из них.
В нативных антителах Fc-участок IgA, IgD и IgG состоит из двух константных доменов тяжелой цепи (CH2 и CH3), и Fc-участок IgE и IgM состоит из трех константных доменов тяжелой цепи (CH2, CH3 и CH4). Они димеризуются с образованием Fc-домена.
В настоящем изобретении Fc-участок может содержать константные домены тяжелой цепи из одного или нескольких различных классов антител, например, одного, двух или трех различных классов.
В одном варианте осуществления Fc-участок содержит CH2- и CH3-домены, полученные из IgG1.
В одном варианте осуществления Fc-участок содержит CH2- и CH3-домены, полученные из IgG2.
В одном варианте осуществления Fc-участок содержит CH2- и CH3-домены, полученные из IgG3.
В одном варианте осуществления Fc-участок содержит CH2- и CH3-домены, полученные из IgG4.
В одном варианте осуществления Fc-участок содержит CH4-домен из IgM. CH4-домен IgM, как правило, расположен на C-конце CH3-домена.
В одном варианте осуществления Fc-участок содержит CH2- и CH3-домены, полученные из IgG, и CH4-домен, полученный из IgM.
Следует понимать, что константные домены тяжелой цепи для применения для получения Fc-участка для BCMA-связывающих молекул по настоящему изобретению могут включать варианты встречающихся в природе константных доменов, описанных выше. Такие варианты могут содержать одну или несколько аминокислотных вариаций по сравнению с константными доменами дикого типа. В одном примере Fc-участок по настоящему изобретению содержит по меньшей мере один константный домен, который отличается по последовательности от константного домена дикого типа. Следует понимать, что варианты константных доменов могут быть более длинными или более короткими, чем константный домен дикого типа. Например, варианты константных доменов на по меньшей мере 60% идентичны константному домену дикого типа или сходны с ним. В другом примере варианты константных доменов являются на по меньшей мере 70% идентичными или сходными. В другом примере варианты константных доменов являются на по меньшей мере 75% идентичными или сходными. В другом примере варианты константных доменов являются на по меньшей мере 80% идентичными или сходными. В другом примере варианты константных доменов являются на по меньшей мере 85% идентичными или сходными. В другом примере варианты константных доменов являются на по меньшей мере 90% идентичными или сходными. В другом примере варианты константных доменов являются на по меньшей мере 95% идентичными или сходными. В другом примере варианты константных доменов являются на по меньшей мере 99% идентичными или сходными. Иллюстративные варианты Fc описаны в разделах 7.4.1.1-7.4.1.5 ниже.
IgM и IgA встречаются в природе у людей в виде ковалентных мультимеров общего звена антитела H2L2. IgM встречается в виде пентамера, если он содержит в своем составе J-цепь, или в виде гексамера, если он лишен J-цепи. IgA встречается в виде мономерных и димерных форм. Тяжелые цепи IgM и IgA имеют 18-аминокислотное удлинение C-концевого константного домена, известное как хвостовая часть. Хвостовая часть содержит остаток цистеина, который образует дисульфидную связь между тяжелыми цепями в полимере и, как полагают, играет важную роль при полимеризации. Хвостовая часть также содержит сайт гликозилирования. В определенных вариантах осуществления BCMA-связывающие молекулы по настоящему изобретению не содержат хвостовую часть.
Fc-домены, которые включены в состав BCMA-связывающих молекул по настоящему изобретению, могут содержать одну или несколько модификаций, которые изменяют одно или несколько функциональных свойств белков, таких как период полужизни в сыворотке крови, фиксация комплемента, связывание с Fc-рецепторами и/или антиген-зависимая клеточная цитотоксичность. Кроме того, BCMA-связывающая молекула может быть химически модифицирована (например, к BCMA-связывающей молекуле могут быть присоединены один или несколько химических фрагментов) или быть модифицирована с изменением ее гликозилирования снова для изменения одного или нескольких функциональных свойств BCMA-связывающей молекулы.
Эффекторная функция молекулы антитела включает комплемент-опосредованную эффекторную функцию, которая опосредована, например, связыванием компонента C1 комплемента с антителом. Активация комплемента важна для опсонизации и прямого лизиса патогенов. Кроме того, она стимулирует воспалительный ответ посредством привлечения фагоцитов к месту активации комплемента и их активации. Эффекторная функция включает эффекторную функцию, опосредованную Fc-рецептором (FcR), которая может запускаться при связывании константных доменов антитела с Fc-рецептором (FcR). При опосредованном комплексом антиген-антитело перекрестном связывании Fc-рецепторов на поверхностях эффекторных клеток запускается ряд важных и разнообразных биологических реакций, в том числе поглощение и разрушение частиц, покрытых антителами, выведение иммунных комплексов, лизис клеток-мишеней, покрытых антителами, клетками-киллерами (называемый антителозависимой клеточноопосредованной цитотоксичностью или ADCC), высвобождение медиаторов воспаления, перенос через плаценту и контроль выработки иммуноглобулинов.
Fc-участки могут быть изменены посредством замены по меньшей мере одного аминокислотного остатка на другой аминокислотный остаток для изменения эффекторных функций. Например, одну или несколько аминокислот можно заменить на другой аминокислотный остаток таким образом, чтобы Fc-участок характеризовался измененной аффинностью в отношении эффекторного лиганда. Эффекторный лиганд, аффинность в отношении которого изменяют, может представлять собой, например, Fc-рецептор или компонент C1 комплемента. Данный подход описан, например, в патентах США №№ 5624821 и 5648260, оба под авторством Winter et al. Модифицированные Fc-участки также способны изменять связывание C1q и/или снижать или устранять комплемент-зависимую цитотоксичность (CDC). Данный подход описан, например, в патенте США № 6194551 за авторством Idusogie et al. Модифицированные Fc-участки также способны изменять способность Fc-участка к фиксации комплемента. Данный подход описан, например, в PCT-публикации WO 94/29351 за авторством Bodmer et al. Аллотипические аминокислотные остатки включают без ограничения константный участок тяжелой цепи подклассов IgG1, IgG2 и IgG3, а также константный участок легкой цепи изотипа каппа, как описано в Jefferis et al., 2009, MAbs, 1:332-338.
Fc-участки также могут быть модифицированы для "подавления" эффекторной функции, например, для снижения или устранения способности BCMA-связывающей молекулы опосредовать антителозависимую клеточную цитотоксичность (ADCC) и/или антителозависимый клеточный фагоцитоз (ADCP). Это может быть достигнуто, например, путем введения мутации в Fc-участок. Такие мутации были описаны в данной области техники: LALA и N297A (Strohl, 2009, Curr. Opin. Biotechnol. 20(6):685-691); а также D265A (Baudino et al., 2008, J. Immunol. 181: 6664-69; Strohl, выше). Примеры антител IgG1 с подавленной активностью Fc включают так называемый мутантный вариант LALA, содержащий мутации L234A и L235A в аминокислотной последовательности Fc IgG1. Другой пример антитела IgG1 с подавленной активностью содержит мутацию D265A. Другой пример антитела IgG1 с подавленной активностью включает так называемый мутантный вариант DAPA, содержащий мутации D265A и P329A в аминокислотной последовательности Fc IgG1. Другое антитело IgG1 с подавленной активностью содержит мутацию N297A, которая приводит к образованию агликозилированных/негликозилированных антител.
Fc-участки могут быть модифицированы для повышения способности BCMA-связывающей молекулы, содержащей Fc-участок, опосредовать антителозависимую клеточную цитотоксичность (ADCC) и/или антителозависимый клеточный фагоцитоз (ADCP), например, посредством модификации одного или нескольких аминокислотных остатков с повышением аффинности BCMA-связывающей молекулы в отношении активирующего Fcγ-рецептора или снижением аффинности BCMA-связывающей молекулы в отношении ингибирующего Fcγ-рецептора. Активирующие Fcγ-рецепторы человека включают FcγRIa, FcγRIIa, FcγRIIIa и FcγRIIIb, а ингибирующий Fcγ-рецептор человека включает FcγRIIb. Данный подход описан, например, в PCT-публикации WO 00/42072 авторства Presta. Кроме того, сайты связывания на IgG1 человека для FcγRI, FcγRII, FcγRIII и FcRn были картированы, и были описаны варианты с улучшенным связыванием (см. Shields et al., J. Biol. Chem. 276:6591-6604, 2001). Была описана оптимизация Fc-опосредованных эффекторных функций моноклональных антител, как, например, увеличение функции ADCC/ADCP (см. Strohl, 2009, Current Opinion in Biotechnology 20:685-691). Мутации, которые способны усиливать функцию ADCC/ADCP, включают одну или несколько мутаций, выбранных из G236A, S239D, F243L, P247I, D280H, K290S, R292P, S298A, S298D, S298V, Y300L, V305I, A330L, I332E, E333A, K334A, A339D, A339Q, A339T и P396L (все положения согласно нумерации EU).
Fc-участки также могут быть модифицированы для повышения способности BCMA-связывающей молекулы опосредовать ADCC и/или ADCP, например, посредством модификации одной или нескольких аминокислот с повышением аффинности BCMA-связывающей молекулы в отношении активирующего рецептора, который, как правило, не будет распознаваться исходной BCMA-связывающей молекулой, такого как FcαRI. Данный подход описан, например, в Borrok et al., 2015, mAbs. 7(4):743-751.
Соответственно, в определенных аспектах BCMA-связывающие молекулы по настоящему изобретению могут содержать Fc-домены с измененной эффекторной функцией, такой как, без ограничения, связывание с Fc-рецепторами, такими как FcRn или лейкоцитарные рецепторы (например, как описано выше или в разделе 7.4.1.1), связывание с комплементом (например, как описано выше или в разделе 7.4.1.2), модифицированной архитектурой дисульфидных связей (например, как описано выше или в разделе 7.4.1.3) или измененными паттернами гликозилирования (например, как описано выше или в разделе 7.4.1.4). Fc-домены также можно изменять таким образом, чтобы они содержали модификации, которые улучшают технологичность получения асимметричных BCMA-связывающих молекул, например, посредством обеспечения возможности гетеродимеризации, которая заключается в предпочтительном спаривании неидентичных Fc-участков по сравнению с идентичными Fc-участками. Гетеродимеризация позволяет получать BCMA-связывающие молекулы, в которых различные ABD соединены друг с другом посредством Fc-домена, содержащего Fc-участки, которые отличаются по последовательности. Примеры стратегий гетеродимеризации проиллюстрированы в разделе 7.4.1.5 (и в его подразделах).
Следует понимать, что любые модификации, описанные в разделах 7.4.1.1-7.4.1.5, можно комбинировать любым подходящим образом для достижения необходимых функциональных свойств и/или комбинировать с другими модификациями для изменения свойств BCMA-связывающих молекул.
7.4.1.1. Fc-домены с измененным связыванием FcR
Fc-домены BCMA-связывающих молекул способны демонстрировать измененное связывание с одним или несколькими Fc-рецепторами (FcR) по сравнению с соответствующим нативным иммуноглобулином. Связывание с любым конкретным Fc-рецептором может быть повышенным или пониженным. В одном варианте осуществления Fc-домен содержит одну или несколько модификаций, которые изменяют его профиль связывания с Fc-рецепторами.
Клетки человека могут экспрессировать ряд мембраносвязанных FcR, выбранных из FcαR, FcεR, FcγR, FcRn и гликановых рецепторов. Некоторые клетки также способны к экспрессии растворимого FcR (эктодомена) (Fridman et al., 1993, J Leukocyte Biology 54: 504-512). FcγR могут дополнительно подразделять по аффинности связывания IgG (высокая/низкая) и биологическому эффекту (активирующие/ингибирующие). Общепризнанно, что FcγRI человека представляет собой единственный рецептор с "высокой аффинностью", тогда как все остальные считаются рецепторами с аффинностью от средней до низкой. FcγRIIb представляет собой единственный рецептор с "ингибирующими" функциональными свойствами благодаря своему внутриклеточному ITIM-мотиву, тогда как все остальные считаются "активирующими" рецепторами благодаря ITAM-мотивам или спариванию с общей γ-цепью FcγR. FcγRIIIb также уникален тем, что, хотя он и является активирующим, он ассоциирует с клеткой посредством GPI-якоря. В целом, у людей экспрессируются шесть "стандартных" FcγR: FcγRI, FcγRIIa, FcγRIIb, FcγRIIc, FcγRIIIa и FcγRIIIb. В дополнение к этим последовательностям существует большое количество последовательностей или аллотипических вариантов, распространенных в этих семействах. Было обнаружено, что некоторые из них имеют важное функциональное значение и поэтому иногда считаются самостоятельными подтипами рецепторов. Примеры включают FcγRIIaH134R, FcγRIIbI190T, FcγRIIIaF158V, FcγRIIIbNA1, FcγRIIIbNA2 и FcγRIIISH. Было показано, что каждая последовательность рецептора имеет различные значения аффинности для 4 подклассов IgG: IgG1, IgG2, IgG3 и IgG4 (Bruhns, 1993, Blood 113:3716-3725). Другие виды имеют несколько иные количества и функциональные свойства FcγR, при этом мышиная система является на сегодняшний день наиболее хорошо изученной и содержит 4 FcγR: FcγRI, FcγRIIb, FcγRIII, FcγRIV (Bruhns, 2012, Blood 119:5640-5649). FcγRI человека на клетках обычно считается "занятым" мономерным IgG при нормальных условиях в сыворотке крови вследствие его аффинности к IgG1/IgG3/IgG4 (приблизительно 10-8 M) и концентрации этих IgG в сыворотке крови (приблизительно 10 мг/мл). Следовательно, клетки, несущие FcγRI на своей поверхности, считаются способными к "скринингу" или "отбору образцов" из их антигенного окружения опосредованно с помощью связанного полиспецифического IgG. Другие рецепторы, имеющие более низкие значения аффинности к подклассам IgG (в диапазоне от приблизительно 10-5 до 10-7 M), обычно считаются "незанятыми". Следовательно, низкоаффинные рецепторы по своей природе чувствительны к выявлению иммунных комплексов, образованных при участии антител, и активации ими. Увеличенная плотность Fc в иммунных комплексах антител приводит к увеличению функциональной аффинности авидности связывания с низкоаффинным FcγR. Это было продемонстрировано in vitro с применением ряда способов (Shields et al., 2001, J Biol Chem 276(9):6591-6604; Lux et al., 2013, J Immunol 190:4315-4323). Это также считается одним из основных механизмов действия при применении антител к RhD для лечения ITP у людей (Crow, 2008, Transfusion Medicine Reviews 22:103-116).
Множество типов клеток экспрессируют множество типов FcγR, и поэтому связывание IgG или иммунного комплекса антител с клетками, несущими FcγR, может иметь множественные и сложные результаты в зависимости от биологического контекста. Говоря наиболее просто, клетки могут получать активирующий, ингибирующий либо смешанный сигнал. Это может приводить к таким событиям, как фагоцитоз (например, в случае с макрофагами и нейтрофилами), процессирование антигена (например, в случае с дендритными клетками), снижение выработки IgG (например, в случае с B-клетками) или дегрануляция (например, в случае с нейтрофилами, тучными клетками). Существуют данные, подтверждающие, что ингибирующий сигнал от FcγRIIb может преобладать над активирующими сигналами (Proulx, 2010, Clinical Immunology 135:422-429).
Существует ряд полезных замен в Fc, которые можно осуществлять для изменения связывания с одним или несколькими FcγR-рецепторами. Могут быть полезны замены, которые приводят к повышению степени связывания, а также к снижению степени связывания. Например, известно, что повышение степени связывания с FcγRIIIa обычно приводит к повышению ADCC (антителозависимой клеточноопосредованной цитотоксичности, клеточноопосредованной реакции, где неспецифические цитотоксические клетки, которые экспрессируют FcγR, распознают связанное антитело на клетке-мишени и впоследствии вызывают лизис клетки-мишени). Аналогичным образом, в некоторых обстоятельствах также может быть полезным снижение степени связывания с FcγRIIb (ингибирующий рецептор). Аминокислотные замены, которые находят применение в настоящем изобретении, включают замены, перечисленные в US 2006/0024298 (в частности на фиг. 41), US 2006/0121032, US 2006/0235208 и US 2007/0148170. Конкретные варианты, которые находят применение, включают без ограничения , 236A, 239D, 239E, 332E, 332D, 239D/332E, 267D, 267E, 328F, 267E/328F, 236A/332E, 239D/332E/330Y, 239D, 332E/330L, 243A, 243L, 264A, 264V и 299T.
FcRn играет решающую роль при поддержании длительного периода полужизни IgG в сыворотке крови взрослых и детей. Рецептор связывает IgG в подкисленных везикулах (pH<6,5), защищая молекулу IgG от деградации и затем высвобождая ее в кровь при более высоком pH, составляющем 7,4.
FcRn отличается от лейкоцитарных Fc-рецепторов и вместе с этим имеет структурное сходство с молекулами MHC I класса. Он представляет собой гетеродимер, состоящий из цепи β2-микроглобулина, нековалентно присоединенной к мембраносвязанной цепи, которая содержит три внеклеточных домена. Один из этих доменов, включая углеводную цепь, вместе с β2-микроглобулином взаимодействует с сайтом между CH2- и CH3-доменами Fc. Взаимодействие включает образование солевых мостиков с остатками гистидина в IgG, которые являются положительно заряженными при pH<6,5. При более высоком pH остатки His теряют свои положительные заряды, взаимодействие FcRn-IgG ослабляется, и IgG диссоциирует.
В одном варианте осуществления BCMA-связывающая молекула содержит Fc-домен, который связывается с FcRn человека.
В одном варианте осуществления Fc-домен содержит Fc-участки (например, один или два), содержащие остаток гистидина в положении 310 и в некоторых случаях также в положении 435. Эти остатки гистидина важны для связывания FcRn человека. В одном варианте осуществления остатки гистидина в положениях 310 и 435 представляют собой нативные остатки, т. е. положения 310 и 435 не являются модифицированными. В качестве альтернативы, один или оба из этих остатков гистидина могут присутствовать в результате модификации.
BCMA-связывающие молекулы могут содержать один или несколько Fc-участков, которые изменяют степень связывания Fc с FcRn. Изменение степени связывания может представлять собой повышение степени связывания или снижение степени связывания.
В одном варианте осуществления BCMA-связывающая молекула содержит Fc-домен, в котором по меньшей мере один Fc-участок (и необязательно оба) содержит одну или несколько таких модификаций, при которых он связывается с FcRn с большей аффинностью и авидностью, чем соответствующий нативный иммуноглобулин.
Замены Fc, которые повышают степень связывания с FcRn-рецептором и увеличивают период полужизни в сыворотке крови, описаны в US 2009/0163699, включая без ограничения 434S, 434A, 428L, 308F, 259I, 428L/434S, 259I/308F, 436I/428L, 436I или V/434S, 436V/428L и 259I/308F/428L.
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка треонина в положении 250 на остаток глутамина (T250Q).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка метионина в положении 252 на остаток тирозина (M252Y).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка серина в положении 254 на остаток треонина (S254T).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка треонина в положении 256 на остаток глутаминовой кислоты (T256E).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка треонина в положении 307 на остаток аланина (T307A).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка треонина в положении 307 на остаток пролина (T307P).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка валина в положении 308 на остаток цистеина (V308C).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка валина в положении 308 на остаток фенилаланина (V308F).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка валина в положении 308 на остаток пролина (V308P).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка глутамина в положении 311 на остаток аланина (Q311A).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка глутамина в положении 311 на остаток аргинина (Q311R).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка метионина в положении 428 на остаток лейцина (M428L).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка гистидина в положении 433 на остаток лизина (H433K).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка аспарагина в положении 434 на остаток фенилаланина (N434F).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка аспарагина в положении 434 на остаток тирозина (N434Y).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка метионина в положении 252 на остаток тирозина, остатка серина в положении 254 на остаток треонина и остатка треонина в положении 256 на остаток глутаминовой кислоты (M252Y/S254T/T256E).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка валина в положении 308 на остаток пролина и остатка аспарагина в положении 434 на остаток тирозина (V308P/N434Y).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка метионина в положении 252 на остаток тирозина, остатка серина в положении 254 на остаток треонина, остатка треонина в положении 256 на остаток глутаминовой кислоты, остатка гистидина в положении 433 на остаток лизина и остатка аспарагина в положении 434 на остаток фенилаланина (M252Y/S254T/T256E/H433K/N434F).
Следует понимать, что любые перечисленные выше модификации можно комбинировать для изменения степени связывания FcRn.
В одном варианте осуществления BCMA-связывающая молекула содержит Fc-домен, в котором один или оба Fc-участка содержат одну или несколько таких модификаций, при которых Fc-домен связывается с FcRn с более низкой аффинностью и авидностью, чем соответствующий нативный иммуноглобулин.
В одном варианте осуществления Fc-участок содержит любой аминокислотный остаток, отличный от гистидина, в положении 310 и/или положении 435.
BCMA-связывающая молекула может содержать Fc-домен, в котором один или оба Fc-участка содержат одну или несколько модификаций, которые повышают его степень связывания с FcγRIIb. FcγRIIb является единственным ингибирующим рецептором у людей и единственным Fc-рецептором, обнаруживаемым на B-клетках.
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка пролина в положении 238 на остаток аспарагиновой кислоты (P238D).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка глутаминовой кислоты в положении 258 на остаток аланина (E258A).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка серина в положении 267 на остаток аланина (S267A).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка серина в положении 267 на остаток глутаминовой кислоты (S267E).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка лейцина в положении 328 на остаток фенилаланина (L328F).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка глутаминовой кислоты в положении 258 на остаток аланина и остатка серина в положении 267 на остаток аланина (E258A/S267A).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка серина в положении 267 на остаток глутаминовой кислоты и остатка лейцина в положении 328 на остаток фенилаланина (S267E/L328F).
Следует понимать, что любые перечисленные выше модификации можно комбинировать для повышения степени связывания FcγRIIb.
В одном варианте осуществления предусмотрены BCMA-связывающие молекулы, содержащие Fc-домены, которые проявляют уменьшение степени связывания с FcγR.
В одном варианте осуществления BCMA-связывающая молекула содержит Fc-домен, в котором один или оба Fc-участка содержат одну или несколько модификаций, которые снижают степень связывания Fc с FcγR.
Fc-домен может быть получен из IgG1.
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка лейцина в положении 234 на остаток аланина (L234A).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка лейцина в положении 235 на остаток аланина (L235A).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка глицина в положении 236 на остаток аргинина (G236R).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка аспарагина в положении 297 на остаток аланина (N297A) или остаток глутамина (N297Q).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка серина в положении 298 на остаток аланина (S298A).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка лейцина в положении 328 на остаток аргинина (L328R).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка лейцина в положении 234 на остаток аланина и остатка лейцина в положении 235 на остаток аланина (L234A/L235A).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка фенилаланина в положении 234 на остаток аланина и остатка лейцина в положении 235 на остаток аланина (F234A/L235A).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка глицина в положении 236 на остаток аргинина и остатка лейцина в положении 328 на остаток аргинина (G236R/L328R).
Следует понимать, что любые перечисленные выше модификации можно комбинировать для снижения степени связывания FcγR.
В одном варианте осуществления BCMA-связывающая молекула содержит Fc-домен, в котором один или оба Fc-участка содержат одну или несколько модификаций, которые снижают степень связывания Fc с FcγRIIIa без влияния на связывание Fc с FcγRII.
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка серина в положении 239 на остаток аланина (S239A).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка глутаминовой кислоты в положении 269 на остаток аланина (E269A).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка глутаминовой кислоты в положении 293 на остаток аланина (E293A).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка тирозина в положении 296 на остаток фенилаланина (Y296F).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка валина в положении 303 на остаток аланина (V303A).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка аланина в положении 327 на остаток глицина (A327G).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка лизина в положении 338 на остаток аланина (K338A).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка аспарагиновой кислоты в положении 376 на остаток аланина (D376A).
Следует понимать, что любые перечисленные выше модификации можно комбинировать для снижения степени связывания FcγRIIIa.
Варианты Fc-участков с пониженной степенью связывания с FcR могут быть названы "вариантами с устранением связывания с FcγR", "вариантами с подавлением связывания с FcγR" или вариантами "Fc с нокаутом (FcKO или KO)". Для некоторых путей терапевтического применения желательно снизить степень связывания или устранить нормальное связывание Fc-домена с одним или несколькими или всеми из Fcγ-рецепторов (например, FcγR1, FcγRIIa, FcγRIIb, FcγRIIIa), чтобы избежать дополнительных механизмов действия. То есть, например, во многих вариантах осуществления, особенно при применении BBM, которые моновалентно связывают CD3, обычно желательно устранять связывание FcγRIIIa для элиминирования или значительного снижения активности ADCC. В некоторых вариантах осуществления по меньшей мере один из Fc-участков ВСМА-связывающих молекул, описанных в данном документе, содержит один или несколько вариантов с устранением связывания с Fcγ-рецепторами. В некоторых вариантах осуществления оба Fc-участка содержат один или несколько вариантов с устранением связывания с Fcγ-рецепторами. Эти варианты с устранением связывания с Fcγ-рецепторами показаны в таблице 5, и каждый из них может быть независимо и необязательно включен или исключен, причем в некоторых аспектах используют варианты с устранением связывания с Fcγ-рецепторами, выбранные из группы, состоящей из G236R/L328R, E233P/L234V/L235A/G236del/S239K, E233P/L234V/L235A/G236del/S267K, E233P/L234V/L235A/G236del/S239K/A327G, E233P/L234V/L235A/G236del/S267K/A327G и E233P/L234V/L235A/G236del ("del" означает делецию, например G236del относится к делеции глицина в положении 236). Следует отметить, что варианты с устранением связывания с Fcγ-рецепторами, упоминаемые в данном документе, устраняют связывание FcγR, но, как правило, не связывание FcRn.
Варианты с устранением связывания с Fcγ-рецепторами
В некоторых вариантах осуществления полиспецифическая ВСМА-связывающая молекула по настоящему изобретению содержит первый Fc-участок и второй Fc-участок. В некоторых вариантах осуществления первый Fc-участок и/или второй Fc-участок могут содержать следующие мутации: E233P, L234V, L235A, G236del и S267K.
Fc-домен человеческого IgG1 характеризуется самой высокой степенью связывания с Fcγ-рецепторами и, таким образом, можно использовать варианты с устранением связывания с Fcγ-рецепторами, когда константный домен (или Fc-домен) в остове гетеродимерного антитела представляет собой IgG1.
В качестве альтернативы или в дополнение к вариантам с устранением связывания с Fcγ-рецепторами на фоне IgG1, мутации в положении гликозилирования 297, например замена остатка аспарагина в положении 297 на остаток аланина (N297A) или остаток глутамина (N297Q), способны, например, в значительной степени устранять связывание с FcγRIIIa. Человеческие IgG2 и IgG4 обладают естественной пониженной степенью связывания с Fcγ-рецепторами и, таким образом, эти остовы можно использовать с вариантами с устранением связывания с Fcγ-рецепторами или без них.
7.4.1.2. Fc-домены с изменением степени связывания с комплементом
BCMA-связывающие молекулы могут содержать Fc-домен, в котором один или оба Fc-участка содержат одну или несколько модификаций, которые изменяют степень связывания Fc с комплементом. Изменение степени связывания комплемента может представлять собой повышение степени связывания или снижение степени связывания.
В одном варианте осуществления Fc-участок содержит одну или несколько модификаций, которые снижают его степень связывания с C1q. Инициация классического пути активации системы комплемента начинается со связывания гексамерного белка C1q с CH2-доменом IgG и IgM, связанных с антигеном.
В одном варианте осуществления BCMA-связывающая молекула содержит Fc-домен, в котором один или оба Fc-участка содержат одну или несколько модификаций для снижения степени связывания Fc с C1q.
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка лейцина в положении 234 на остаток аланина (L234A).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка лейцина в положении 235 на остаток аланина (L235A).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка лейцина в положении 235 на остаток глутаминовой кислоты (L235E).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка глицина в положении 237 на остаток аланина (G237A).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка лизина в положении 322 на остаток аланина (K322A).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка пролина в положении 331 на остаток аланина (P331A).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка пролина в положении 331 на остаток серина (P331S).
В одном варианте осуществления BCMA-связывающая молекула содержит Fc-домен, полученный из IgG4. IgG4 по своей природе характеризуется более низким профилем активации комплемента, чем IgG1, но также более слабым связыванием FcγR. Таким образом, в одном варианте осуществления BCMA-связывающая молекула содержит Fc-домен IgG4 и также содержит одну или несколько модификаций, которые повышают степень связывания FcγR.
Следует понимать, что любые перечисленные выше модификации можно комбинировать для снижения степени связывания C1q.
7.4.1.3. Fc-домены с измененной архитектурой дисульфидных связей
BCMA-связывающая молекула может содержать Fc-домен, содержащий одну или несколько модификаций для создания и/или удаления остатка цистеина. Остатки цистеина играют важную роль в самопроизвольной сборке полиспецифических связывающих молекул на основе Fc посредством образования дисульфидных мостиков между отдельными парами полипептидных мономеров. Таким образом, посредством изменения количества и/или положения остатков цистеина возможно модифицировать структуру BCMA-связывающей молекулы для получения белка с улучшенными терапевтическими свойствами.
BCMA-связывающая молекула по настоящему изобретению может содержать Fc-домен, в котором один или оба Fc-участка, например, оба Fc-участка, содержат остаток цистеина в положении 309. В одном варианте осуществления остаток цистеина в положении 309 образован посредством модификации, например, в случае Fc-домена, полученного из IgG1, остаток лейцина в положении 309 заменен на остаток цистеина (L309C) в случае Fc-домена, полученного из IgG2, остаток валина в положении 309 заменен на остаток цистеина (V309C).
В одном варианте осуществления Fc-участок модифицирован посредством замены остатка валина в положении 308 на остаток цистеина (V308C).
В одном варианте осуществления две дисульфидные связи в шарнирном участке удаляют посредством мутации коровой последовательности CPPC шарнирного участка (SEQ ID NO:422) с заменой на SPPS (SEQ ID NO:423).
7.4.1.4. Fc-домены с измененным гликозилированием
В определенных аспектах предусмотрены BCMA-связывающие молекулы с улучшенной технологичностью получения, которые содержат меньше сайтов гликозилирования, чем соответствующий иммуноглобулин. Такие белки характеризуются менее сложными паттернами посттрансляционного гликозилирования, и, таким образом, их получение является более простым и менее дорогостоящим.
В одном варианте осуществления сайт гликозилирования в CH2-домене удален посредством замены остатка аспарагина в положении 297 на остаток аланина (N297A) или остаток глутамина (N297Q). В дополнение к улучшенной технологичности получения эти агликозилированные мутантные варианты также характеризуются пониженной степенью связывания FcγR, как описано в данном документе выше.
В некоторых вариантах осуществления может быть получена BCMA-связывающая молекула, которая характеризуется измененным типом гликозилирования, такая как гипофукозилированное антитело, содержащее пониженные количества фукозильных остатков, или антитело, характеризующееся повышенным содержанием структур с остатком GlcNAc в точке ветвления. Было продемонстрировано, что такие измененные паттерны гликозилирования повышают способность антител к ADCC. Такие модификации углеводов можно осуществлять, например, посредством экспрессии BCMA-связывающей молекулы в клетке-хозяине с измененным механизмом гликозилирования. Клетки с измененным механизмом гликозилирования были описаны в данной области техники, и их можно применять в качестве клеток-хозяев, в которых экспрессируются BCMA-связывающие молекулы, за счет чего обеспечивается получение BCMA-связывающих молекул с измененным гликозилированием. Например, в EP 1176195 под авторством Hang et al. описывается линия клеток с функциональным нарушением гена FUT8, который кодирует фукозилтрансферазу, благодаря чему антитела, которые экспрессируются в такой линии клеток, проявляют гипофукозилирование. В PCT-публикации WO 03/035835 под авторством Presta описывается вариант линии клеток CHO - клетки Lecl3 с пониженной способностью к присоединению фукозы к Asn(297)-связанным углеводам, что также приводит к гипофукозилированию антител, которые экспрессируются в такой клетке-хозяине (см. также Shields et al., 2002, J. Biol. Chem. 277:26733-26740). В PCT-публикации WO 99/54342 под авторством Umana et al. описываются линии клеток, сконструированные для экспрессии гликозилтрансфераз, модифицирующих гликопротеины (например, бета-(1,4)-N-ацетилглюкозаминилтрансферазы III (GnTIII)), благодаря чему антитела, которые экспрессируются в сконструированных линиях клеток, демонстрируют повышенное содержание структур с остатком GlcNAc в точке ветвления, что приводит к повышению активности ADCC у антител (см. также Umana et al., Nat. Biotech. 17:176-180, 1999).
7.4.1.5. Гетеродимеризация Fc
Множество форматов полиспецифических молекул подразумевают димеризацию между двумя Fc-участками, которые, в отличие от нативного иммуноглобулина, функционально связаны с неидентичными антигенсвязывающими доменами (или их частями, например, VH или VH-CH1 в Fab). Ненадлежащая гетеродимеризация двух Fc-участков с образованием Fc-домена всегда была препятствием для увеличения выхода необходимых полиспецифических молекул и представляет трудности для очистки. Множество подходов, доступных в данной области техники, можно применять для усиления димеразации Fc-участков, которые могут присутствовать в ВСМА-связывающих молекулах (и в частности в MBM по настоящему изобретению), например, как раскрыто в EP 1870459A1; патенте США № 5582996; патенте США № 5731168; патенте США № 5910573; патенте США № 5932448; патенте США № 6833441; патенте США № 7183076; публикации заявки на патент США № 2006204493A1 и PCT-публикации № WO2009/089004A1.
В настоящем изобретении предусмотрены ВСМА-связывающие молекулы, содержащие гетеродимеры Fc. Стратегии гетеродимеризации применяют для усиления димеризации Fc-участков, функционально связанных с разными ABD (или их частями, например, VH или VH-CH1 в Fab), и снижения димеризации Fc-участков, функционально связанных с одним и тем же ABD или его частью. Как правило, каждый Fc-участок в гетеродимере Fc содержит CH3-домен антитела. CH3-домены получают из константного участка антитела любого изотипа, класса или подкласса, а в некоторых случаях класса IgG (IgG1, IgG2, IgG3 и IgG4), как описано в предыдущем разделе.
Как правило, ВСМА-связывающие молекулы содержат другие фрагменты антител в дополнение к CH3-доменам, такие как CH1-домены, CH2-домены, шарнирный домен, VH-домен(домены), VL-домен(домены), CDR и/или антигенсвязывающие фрагменты, описанные в данном документе. В некоторых вариантах осуществления два гетерополипептида представляют собой две тяжелые цепи, образующие биспецифические или полиспецифические молекулы. Гетеродимеризация двух различных тяжелых цепей в CH3-доменах приводит к образованию необходимых антитела или антителоподобной молекулы, тогда как гомодимеризация идентичных тяжелых цепей приводит к снижению выхода необходимых антитела или молекулы. В иллюстративном варианте осуществления две или более гетерополипептидные цепи содержат две цепи, содержащие CH3-домены и образующие молекулы в любом из форматов полиспецифических молекул, описанных в настоящем изобретении выше. В одном варианте осуществления две гетерополипептидные цепи, содержащие CH3-домены, содержат модификации, которые содействуют гетеродимерной ассоциации полипептидов по сравнению с немодифицированными цепями. Различные примеры стратегий модификации предусмотрены ниже в таблице 6 и разделах 7.4.1.5.1-7.4.1.5.7.
Стратегии гетеродимеризации Fc
7.4.1.5.1. Стерические варианты
BCMA-связывающие молекулы могут содержать одну или несколько, например, множество модификаций в одном или нескольких константных доменах Fc-домена, например, в CH3-доменах. В одном примере BCMA-связывающая молекула по настоящему изобретению содержит два полипептида, каждый из которых содержит константный домен тяжелой цепи антитела, например, СН2- или СН3-домен. В одном примере два константных домена тяжелой цепи, например, CH2- или CH3-домены BCMA-связывающей молекулы содержат одну или несколько модификаций, которые обеспечивают возможность гетеродимерной ассоциации между двумя цепями. В одном аспекте одна или несколько модификаций расположены в CH2-доменах двух тяжелых цепей. В одном аспекте одна или несколько модификаций расположены в CH3-доменах по меньшей мере двух полипептидов BCMA-связывающей молекулы.
Один механизм гетеродимеризации Fc обычно упоминается в данной области техники как "выступы и углубления" или "выступы в углубления". Эти термины относятся к аминокислотным мутациям, которые создают стерические влияния, способствующие образованию гетеродимеров Fc вместо гомодимеров Fc, как описано, например, в Ridgway et al., 1996, Protein Engineering 9(7):617; Atwell et al., 1997, J. Mol. Biol. 270:26; патенте США № 8216805. Мутации типа "выступ в углубление" можно комбинировать с другими стратегиями для улучшения гетеродимеризации.
В одном аспекте одна или несколько модификаций в первом полипептиде BCMA-связывающей молекулы, содержащем константный домен тяжелой цепи, могут образовывать "выступ", и одна или несколько модификаций во втором полипептиде BCMA-связывающей молекулы образуют "углубление", так что гетеродимеризация полипептида BCMA-связывающей молекулы, содержащего константный домен тяжелой цепи, приводит к тому, что "выступ" вступает в контакт (например, взаимодействует, например, CH2-домен первого полипептида взаимодействует с CH2-доменом второго полипептида, или CH3-домен первого полипептида взаимодействует с CH3-доменом второго полипептида) с "углублением". "Выступ" выступает над областью контакта первого полипептида BCMA-связывающей молекулы, содержащего константный домен тяжелой цепи, и поэтому способен располагаться в компенсирующем "углублении" в области контакта со вторым полипептидом BCMA-связывающей молекулы, содержащим константный домен тяжелой цепи, чтобы таким образом стабилизировать гетеромультимер и, таким образом, способствовать, например, образованию гетеромультимера вместо образования гомомультимера. Выступ может существовать в исходной области контакта или может быть введен синтетически (например, посредством изменения нуклеиновой кислоты, кодирующей область контакта). Вводимыми остатками для образования выступа обычно являются встречающиеся в природе аминокислотные остатки, и они могут быть выбраны из аргинина (R), фенилаланина (F), тирозина (Y) и триптофана (W). В некоторых случаях выбирают триптофан и тирозин. В одном варианте осуществления исходный остаток для образования выпячивания имеет небольшой объем боковой цепи, такой как у аланина, аспарагина, аспарагиновой кислоты, глицина, серина, треонина или валина.
"Углубление" содержит по меньшей мере одну боковую цепь аминокислоты, которая углублена в область контакта второго полипептида BCMA-связывающей молекулы, содержащего константный домен тяжелой цепи и, следовательно, создает условия для размещения соответствующего "выступа" на прилегающей области контакта первого полипептида BCMA-связывающей молекулы, содержащего константный домен тяжелой цепи. Углубление может существовать в исходной области контакта или может быть введено синтетически (например, посредством изменения нуклеиновой кислоты, кодирующей область контакта). Вводимыми остатками для образования углубления обычно являются встречающиеся в природе аминокислотные остатки, и они в некоторых случаях выбраны из аланина (A), серина (S), треонина (T) и валина (V). В одном варианте осуществления аминокислотный остаток представляет собой серин, аланин или треонин. В другом варианте осуществления исходный остаток для образования углубления имеет большой объем боковой цепи, такой как у тирозина, аргинина, фенилаланина или триптофана.
В одном варианте осуществления первый CH3-домен модифицирован по остатку 366, 405 или 407 с образованием либо "выступа", либо "углубления" (как описано выше), и второй CH3-домен, который гетеродимеризуется с первым CH3-доменом, модифицирован по остатку 407, если в первом CH3-домене модифицирован остаток 366, остатку 394, если в первом CH3-домене модифицирован остаток 405, или остатку 366, если в первом CH3-домене модифицирован остаток 407, с образованием "углубления" или "выступа", комплементарных "выступу" или "углублению" первого CH3-домена.
В другом варианте осуществления первый CH3-домен модифицирован по остатку 366, и второй CH3-домен, который гетеродимеризуется с первым CH3-доменом, модифицирован по остаткам 366, 368 и/или 407 с образованием "углубления" или "выступа", комплементарного "выступу" или "углублению" первого CH3-домена. В одном варианте осуществления при модификации в первом CH3-домене вводится остаток тирозина (Y) в положении 366. В одном варианте осуществления модификация в первом CH3 представляет собой T366Y. В одном варианте осуществления при модификации в первом CH3-домене вводится остаток триптофана (W) в положении 366. В одном варианте осуществления модификация в первом CH3 представляет собой T366W. В некоторых вариантах осуществления модификация во втором CH3-домене, который гетеродимеризуется с первым CH3-доменом, модифицированным в положении 366 (например, имеющим тирозин (Y) или триптофан (W), введенный в положение 366, например, содержащим модификацию T366Y или T366W), включает модификацию в положении 366, модификацию в положении 368 и модификацию в положении 407. В некоторых вариантах осуществления при модификации в положении 366 вводится остаток серина (S), при модификации в положении 368 вводится аланин (A), и при модификации в положении 407 вводится валин (V). В некоторых вариантах осуществления модификации включают T366S, L368A и Y407V. В одном варианте осуществления первый CH3-домен полиспецифической молекулы содержит модификацию T366Y, а второй CH3-домен, который гетеродимеризуется с первым CH3-доменом, содержит модификации T366S, L368A и Y407V, или наоборот. В одном варианте осуществления первый CH3-домен полиспецифической молекулы содержит модификацию T366W, а второй CH3-домен, который гетеродимеризуется с первым CH3-доменом, содержит модификации T366S, L368A и Y407V, или наоборот.
Дополнительные стерические или "асимметричные" (например, типа "выступ в углубление") модификации описаны в PCT-публикации № WO2014/145806 (например, на фигуре 3, фигуре 4 и фигуре 12 в WO2014/145806), PCT-публикации № WO2014/110601 и PCT-публикациях №№ WO 2016/086186, WO 2016/086189, WO 2016/086196 и WO 2016/182751. Пример KIH-варианта содержит первый константный домен цепи, содержащий модификации L368D и K370S, спаренный со вторым константным доменом цепи, содержащим модификации S364K и E357Q.
Дополнительные пары модификаций типа "выступ в углубление", подходящие для применения в BCMA-связывающих молекулах по настоящему изобретению, дополнительно описаны, например, в WO1996/027011 и Merchant et al., 1998, Nat. Biotechnol., 16:677-681.
В дополнительных вариантах осуществления CH3-домены могут быть дополнительно модифицированы с введением пары остатков цистеина. Не ограничиваясь какой-либо теорией, полагают, что введение пары остатков цистеина, способной к образованию дисульфидной связи, обеспечивает стабильность гетеродимеризующимся BCMA-связывающим молекулам, содержащим спаренные CH3-домены. В некоторых вариантах осуществления первый CH3-домен содержит цистеин в положении 354, а второй CH3-домен, который гетеродимеризуется с первым CH3-доменом, содержит цистеин в положении 349. В некоторых вариантах осуществления первый CH3-домен содержит цистеин в положении 354 (например, содержит модификацию S354C) и тирозин (Y) в положении 366 (например, содержит модификацию T366Y), а второй CH3-домен, который гетеродимеризуется с первым CH3-доменом, содержит цистеин в положении 349 (например, содержит модификацию Y349C), серин в положении 366 (например, содержит модификацию T366S), аланин в положении 368 (например, содержит модификацию L368A) и валин в положении 407 (например, содержит модификацию Y407V). В некоторых вариантах осуществления первый CH3-домен содержит цистеин в положении 354 (например, содержит модификацию S354C) и триптофан (W) в положении 366 (например, содержит модификацию T366W), а второй CH3-домен, который гетеродимеризуется с первым CH3-доменом, содержит цистеин в положении 349 (например, содержит модификацию Y349C), серин в положении 366 (например, содержит модификацию T366S), аланин в положении 368 (например, содержит модификацию L368A) и валин в положении 407 (например, содержит модификацию Y407V).
Дополнительный механизм, который находит применение при получении гетеродимеров, иногда называют "направленным электростатическим взаимодействием", как описано в Gunasekaran et al., 2010, J. Biol. Chem. 285(25):19637. Это иногда упоминается в данном документе как "пары зарядов". В данном варианте осуществления используют электростатику для обеспечения асимметрии образования в сторону гетеродимеризации. Как будет понятно специалисту в данной области техники, они могут также оказывать влияние на pI и, следовательно, на очистку, и поэтому в некоторых случаях также могут рассматриваться pI-варианты. Однако поскольку их создавали для усиления гетеродимеризации и не использовали в качестве инструментов для очистки, их классифицируют как "стерические варианты". Они включают без ограничения D221E/P228E/L368E в паре с D221R/P228R/K409R и C220E/P228E/368E в паре с C220R/E224R/P228R/K409R.
Дополнительные варианты, которые можно комбинировать с другими вариантами, необязательно и независимо в любом количестве, такие как pI-варианты, описанные в данном документе, или другие стерические варианты, которые показаны на фигуре 37 в US 2012/0149876.
В некоторых вариантах осуществления стерические варианты, описанные в данном документе, могут быть необязательно и независимо включены в любой pI-вариант (или другие варианты, такие как варианты Fc, варианты FcRn) в одном или обоих Fc-участках и могут быть независимо и необязательно включены или исключены из BCMA-связывающих молекул по настоящему изобретению.
Список подходящих асимметричных вариантов представлен в таблице 7, где показаны некоторые пары с конкретной практической применимостью во многих вариантах осуществления. Особенно пригодными во многих вариантах осуществления являются пары наборов, включая без ограничения S364K/E357Q : L368D/K370S; L368D/K370S : S364K; L368E/K370S : S364K; T411T/E360E/Q362E : D401K; L368D/K370S : S364K/E357L; и K370S : S364K/E357Q. В терминах номенклатуры пара "S364K/E357Q : L368D/K370S" означает, что один из Fc-участков имеет двойной набор вариантов S364K/E357Q, а другой имеет двойной набор вариантов L368D/K370S.
Иллюстративные асимметричные варианты
В некоторых вариантах осуществления ВСМА-связывающая молекула содержит первый Fc-участок и второй Fc-участок. В некоторых вариантах осуществления первый Fc-участок содержит следующие мутации: L368D и K370S, а второй Fc-участок содержит следующие мутации: S364K и E357Q. В некоторых вариантах осуществления первый Fc-участок содержит следующие мутации: S364K и E357Q, а второй Fc-участок содержит следующие мутации: L368D и K370S.
7.4.1.5.2. Альтернативные выступы и углубления: Гетеродимеризация IgG
Гетеродимеризацию полипептидных цепей BCMA-связывающей молекулы, содержащих спаренные CH3-домены, можно усиливать посредством введения одной или нескольких модификаций в CH3-домен, который получен из антитела класса IgG1. В одном варианте осуществления модификации включают модификацию K409R в одном CH3-домене в паре с модификацией F405L во втором CH3-домене. Дополнительные модификации также, или в качестве альтернативы, можно осуществлять в положениях 366, 368, 370, 399, 405, 407 и 409. В некоторых случаях гетеродимеризацию полипептидов, содержащих такие модификации, осуществляют в восстанавливающих условиях, например, в 10-100 мМ 2-MEA (например, в 25, 50 или 100 мМ 2-MEA) в течение 1-10, например, 1,5-5, например, 5 часов при 25-37°С, например, 25°С или 37°С.
Аминокислотные замены, описанные в данном документе, можно вводить в CH3-домены с применением методик, которые широко известны (см., например, McPherson, ed., 1991, Directed Mutagenesis: a Practical Approach; Adelman et al., 1983, DNA, 2:183).
Стратегия гетеродимеризации IgG дополнительно описана, например, в WO2008/119353, WO2011/131746 и WO2013/060867.
В любом из вариантов осуществления, описанных в данном разделе, CH3-домены могут быть дополнительно модифицированы с введением пары остатков цистеина, как описано в разделе 7.4.1.3.
7.4.1.5.3. pI-варианты (варианты с измененной изоэлектрической точкой)
В целом, как будет понятно специалисту в данной области техники, существуют две общие категории pI-вариантов: те, которые повышают pI белка (щелочные изменения) и те, которые снижают pI белка (кислотные изменения). Как описано в данном документе, можно осуществлять все комбинации этих вариантов: один Fc-участок может представлять собой Fc-участок дикого типа или представлять собой вариант, который не демонстрирует pI, существенно отличающуюся от дикого типа, а другой может быть либо более щелочным, либо более кислым. В качестве альтернативы, изменяют каждый Fc-участок, один на более щелочной, а другой на более кислый.
Иллюстративные комбинации pI-вариантов показаны в таблице 8. Как описано в данном документе и показано в таблице 8, эти изменения показаны относительно IgG1, но все изотипы можно изменить таким образом, а также гибриды изотипов. В случае, когда константный домен тяжелой цепи получен из IgG2-4, можно также использовать R133E и R133Q.
Иллюстративные комбинации pI-вариантов
В одном варианте осуществления, например, в формате фиг. 1C, G, H, O, P и Q, комбинация pI-вариантов содержит один Fc-участок (отрицательная Fab-сторона), содержащий варианты 208D/295E/384D/418E/421D (N208D/Q295E/N384D/Q418E/N421D, если рассматривать относительно человеческого IgG1), и второй Fc-участок (положительная scFv-сторона), содержащий положительно заряженный линкер для scFv, например, L36 (описанный в разделе 7.4.3). Однако, как будет понятно специалисту в данной области техники, первый Fc-участок содержит CH1-домен, в том числе положение 208. Соответственно, в конструкциях, которые не содержат CH1-домен (например, в случае антител, в которых не используется CH1-домен в качестве одного из доменов, например, в формате двойного scFv или в "одноплечевом" формате, таком как те, что изображены на фиг. 1D, E или F), иллюстративный набор отрицательных pI-вариантов Fc включает варианты 295E/384D/418E/421D (Q295E/N384D/Q418E/N421D, если рассматривать относительно человеческого IgG1).
В некоторых вариантах осуществления первый Fc-участок содержит набор замен из таблицы B, а второй Fc-участок соединен с заряженным линкером (например, выбранным из линкеров, описанных в разделе 7.4.3).
В некоторых вариантах осуществления ВСМА-связывающая молекула по настоящему изобретению содержит первый Fc-участок и второй Fc-участок. В некоторых вариантах осуществления первый Fc-участок содержит следующие мутации: N208D, Q295E, N384D, Q418E и N421D. В некоторых вариантах осуществления второй Fc-участок содержит следующие мутации: N208D, Q295E, N384D, Q418E и N421D.
7.4.1.5.4. Изотипические варианты
Кроме того, многие варианты осуществления настоящего изобретения основаны на "импорте" pI-аминокислот в определенных положениях из одного изотипа IgG в другой, тем самым снижая или устраняя возможность введения нежелательной иммуногенности в варианты. Некоторые из них показаны на фигуре 21 из публикации заявки на патент США 2014/0370013. То есть IgG1 является распространенным изотипом для терапевтических антител по множеству причин, включая высокую эффекторную функцию. Однако константный участок тяжелой цепи IgG1 характеризуется более высокой pI, чем у IgG2 (8,10 по сравнению с 7,31). Посредством введения остатков IgG2 в определенные положения в остов IgG1 pI полученного Fc-участка понижается (или повышается) и дополнительно проявляется более продолжительный период полужизни в сыворотке крови. Например, IgG1 содержит глицин (pI 5,97) в положении 137, а IgG2 содержит глутаминовую кислоту (pI 3,22); импорт глутаминовой кислоты будет влиять на pI полученного белка. Как описано ниже, обычно требуется ряд аминокислотных замен, чтобы оказывать значительное влияние на pI варианта антитела. Однако следует отметить, как обсуждается ниже, что даже изменения в молекулах IgG2 позволяют увеличить период полужизни в сыворотке крови.
В других вариантах осуществления осуществляют неизотипические аминокислотные замены либо для снижения общего зарядового состояния получаемого белка (например, посредством замены аминокислоты с более высокой pI на аминокислоту с более низкой pI), либо для обеспечения приспособлений в структуре для стабильности, как подробнее описано ниже.
Кроме того, с помощью pI-конструирования константных доменов тяжелой и легкой цепей ВСМА-связывающей молекулы, содержащей два полуантитела, можно увидеть значительные изменения в каждом полуантителе. Наличие pI двух полуантител, отличающихся по меньшей мере на 0,5, может позволить разделение с помощью ионообменной хроматографии или изоэлектрического фокусирования, или других способов, чувствительных к изоэлектрической точке.
7.4.1.5.5. Расчет pI
Значение pI полуантитела, содержащего Fc-участок и ABD или цепь ABD, может зависеть от pI варианта константного домена тяжелой цепи и pI полного полуантитела, включая вариант константного домена тяжелой цепи и ABD или цепь ABD. Таким образом, в некоторых вариантах осуществления изменение pI рассчитывают на основе варианта константного домена тяжелой цепи, используя диаграмму, приведенную на фигуре 19 из публикации заявки на патент США 2014/0370013. Как обсуждается в данном документе, выбор полуантитела для конструирования обычно определяется собственной pI полуантител. В качестве альтернативы, можно сравнить pI каждого полуантитела.
7.4.1.5.6. pI-варианты, которые также обеспечивают лучшее связывание FcRn in vivo
В случае, когда pI-вариант снижает pI Fc-участка, он может получить дополнительное преимущество в виде улучшения удержания в сыворотке крови in vivo.
Считается, что pI-варианты Fc-участков обеспечивают антигенсвязывающим молекулам более длительные периоды полужизни in vivo , поскольку связывание с FcRn при pH 6 в эндосоме секвестрирует Fc (Ghetie and Ward, 1997 Immunol Today. 18(12): 592-598). Затем эндосомальный компартмент возвращает Fc на поверхность клетки. Как только компартмент открывается во внеклеточное пространство, более высокий pH ~7,4 индуцирует высвобождение Fc обратно в кровь. Dall' Acqua et al. показали, что у мышей мутантные варианты Fc с повышенной степенью связывания FcRn при pH 6 и pH 7,4 фактически имели пониженные концентрации в сыворотке крови и такой же период полужизни, как у Fc дикого типа (Dall' Acqua et al,. 2002, J. Immunol. 169:5171-5180). Считается, что повышенная аффинность Fc к FcRn при рН 7,4 препятствует высвобождению Fc обратно в кровь. Следовательно, мутации Fc, которые увеличивают период полужизни Fc in vivo, в идеальном случае повышают степень связывания FcRn при более низком рН, в то же время позволяя высвобождать Fc при более высоком рН. Аминокислота гистидин изменяет свое зарядовое состояние в диапазоне рН 6,0-7,4. Поэтому неудивительно обнаруживать остатки His в важных положениях в комплексе Fc/FcRn.
Было высказано предположение, что антитела с вариабельными участками, которые характеризуются более низкими значениями изоэлектрических точек, также могут иметь более длительные периоды полужизни в сыворотке крови (Igawa et al., 2010, PEDS. 23(5): 385-392). Однако механизм этого явления еще слабо понятен. Более того, вариабельные участки различаются от антитела к антителу. Варианты константного участка с пониженным значением pI и увеличенным периодом полужизни обеспечили бы более модульный подход к улучшению фармакокинетических свойств BCMA-связывающих молекул, описанных в данном документе.
7.4.1.5.7. Полярный мостик
Гетеродимеризацию полипептидных цепей BCMA-связывающих молекул, содержащих Fc-домен, можно усиливать посредством введения модификаций на основе "образования полярного мостика", который необходим для того, чтобы остатки в области контакта двух полипептидных цепей взаимодействовали с остатками, имеющими сходные (или дополняющие) физические свойства в гетеродимерной конфигурации, и в то же время с остатками с другими физическими свойствами в гомодимерной конфигурации. В частности, эти модификации сконструированы таким образом, чтобы при образовании гетеродимера полярные остатки взаимодействовали с полярными остатками, а гидрофобные остатки при этом взаимодействовали с гидрофобными остатками. В отличие от этого, при образовании гомодимера остатки модифицируют таким образом, чтобы полярные остатки взаимодействовали с гидрофобными остатками. Благоприятные взаимодействия в гетеродимерной конфигурации и неблагоприятные взаимодействия в гомодимерной конфигурации совместно повышают вероятность того, что Fc-участки будут образовывать гетеродимеры вместо образования гомодимеров.
В иллюстративном варианте осуществления вышеуказанные модификации вводят в одно или несколько положений с остатками 364, 368, 399, 405, 409 и 411 CH3-домена.
В некоторых вариантах осуществления одну или несколько модификаций, выбранных из группы, состоящей из S364L, T366V, L368Q, N399K, F405S, K409F и R411K, вводят в один из двух CH3-доменов. Одну или несколько модификаций, выбранных из группы, состоящей из Y407F, K409Q и T411N, можно вводить во второй CH3-домен.
В другом варианте осуществления одну или несколько модификаций, выбранных из группы, состоящей из S364L, T366V, L368Q, D399K, F405S, K409F и T411K, вводят в один CH3-домен, тогда как одну или несколько модификаций, выбранных из группы, состоящей из Y407F, K409Q и T411D, вводят во второй CH3-домен.
В одном иллюстративном варианте осуществления исходный остаток треонина в положении 366 одного CH3-домена заменен на валин, тогда как исходный остаток тирозина в положении 407 другого CH3-домена заменен на фенилаланин.
В другом иллюстративном варианте осуществления исходный остаток серина в положении 364 одного CH3-домена заменен на лейцин, тогда как исходный остаток лейцина в положении 368 того же CH3-домена заменен на глутамин.
В еще одном иллюстративном варианте осуществления исходный остаток фенилаланина в положении 405 одного CH3-домена заменен на серин, а исходный остаток лизина в положении 409 этого CH3-домена заменен на фенилаланин, тогда как исходный остаток лизина в положении 409 другого CH3-домена заменен на глутамин.
В еще одном иллюстративном варианте осуществления исходный остаток аспарагиновой кислоты в положении 399 одного CH3-домена заменен на лизин, а исходный остаток треонина в положении 411 того же CH3-домена заменен на лизин, тогда как исходный остаток треонина в положении 411 другого CH3-домена заменен на аспарагиновую кислоту.
Аминокислотные замены, описанные в данном документе, можно вводить в CH3-домены с применением методик, которые широко известны (см., например McPherson, ed., 1991, Directed Mutagenesis: a Practical Approach; Adelman et al., 1983, DNA, 2:183). Стратегия с полярным мостиком описана, например, в WO2006/106905, WO2009/089004 и K. Gunasekaran, et al. (2010) JBC, 285:19637-19646.
Дополнительные модификации типа полярных мостиков описаны, например, в PCT-публикации № WO2014/145806 (например, на фигуре 6 в WO2014/145806), PCT-публикации № WO2014/110601 и PCT-публикациях №№ WO 2016/086186, WO 2016/086189, WO 2016/086196 и WO 2016/182751. Пример варианта с полярным мостиком содержит константный домен цепи, содержащий модификации N208D, Q295E, N384D, Q418E и N421D.
В любом из вариантов осуществления, описанных в данном документе, CH3-домены могут быть дополнительно модифицированы с введением пары остатков цистеина, как описано в разделе 7.4.1.3.
Дополнительные стратегии для усиления гетеродимеризации описаны, например, в WO2016/105450, WO2016/086186, WO2016/086189, WO2016/086196, WO2016/141378, WO2014/145806 и WO2014/110601. Любую из стратегий можно использовать в BCMA-связывающей молекуле, описанной в данном документе.
7.4.1.6. Комбинация вариантов гетеродимеризации и других Fc-вариантов
Как будет понятно специалисту в данной области техники, все перечисленные варианты гетеродимеризации (включая асимметричные и/или pI-варианты) можно необязательно и независимо комбинировать любым способом, при условии, что Fc-участки Fc-домена сохраняют свою способность к димеризации. Кроме того, все эти варианты можно комбинировать в любом из форматов гетеродимеризации.
В случае pI-вариантов, в то время как варианты осуществления, находящие конкретное применение, показаны в таблице 8, можно генерировать другие комбинации, следуя основному правилу изменения разности pI между двумя Fc-участками в гетеродимере Fc для облегчения очистки.
Кроме того, любые из вариантов гетеродимеризации, асимметричные и pI, также независимо и необязательно комбинируют с вариантами Fc с устранением связывания с Fcγ-рецепторами, вариантами Fc, вариантами FcRn, как в целом описано в данном документе.
В некоторых вариантах осуществления конкретная комбинация ассиметричных и pI-вариантов, которая находит применение в настоящем изобретении, представляет собой T366S/L368A/Y407V: T366W (необязательно включая мостиковую дисульфидную связь, T366S/L368A/Y407V/Y349C : T366W/S354C) с одним Fc-участком, содержащим Q295E/N384D/Q418E/N481D, и другим, представляющим собой положительно заряженный линкер для scFv (когда формат включает scFv-домен). Как будет понятно специалисту в данной области техники, варианты типа "выступы в углубления" не изменяют pI и, таким образом, могут использоваться в любом из Fc-участков в гетеродимере Fc.
В некоторых вариантах осуществления первый и второй Fc-участки, которые находят применение в настоящем изобретении, включают аминокислотные замены S364K/E357Q : L368D/K370S, где первый и/или второй Fc-участки включают замены варианта с устранением связывания с Fcγ-рецепторами 233P/L234V/L235A/G236del/S267K, и первый и/или второй Fc-участок содержат замены pI-варианта N208D/Q295E/N384D/Q418E/N421D (pl_(-)_изостерический_A).
7.4.2. Шарнирные участки
BCMA-связывающие молекулы могут также содержать шарнирные участки, например, соединяющие антигенсвязывающий домен с Fc-участком. Шарнирный участок может представлять собой нативный или модифицированный шарнирный участок. Шарнирные участки, как правило, находятся на N-концах Fc-участков.
Нативный шарнирный участок представляет собой шарнирный участок, который обычно будет находиться между Fab- и Fc-доменами встречающегося в природе антитела. Модифицированный шарнирный участок представляет собой любой шарнирный участок, который отличается по длине и/или составу от нативного шарнирного участка. Такие шарнирные участки могут включать шарнирные участки из других видов, такие как шарнирные участки человека, мыши, крысы, кролика, акулы, свиньи, хомяка, верблюда, ламы или козы. Другие модифицированные шарнирные участки могут содержать полный шарнирный участок, полученный из антитела класса или подкласса, отличающегося от класса или подкласса Fc-участка. В качестве альтернативы, модифицированный шарнирный участок может содержать часть природного шарнирного участка или повторяющееся звено, в котором каждое звено в повторе получено из природного шарнирного участка. В качестве дополнительной альтернативы, природный шарнирный участок можно изменять посредством превращения одного или нескольких остатков цистеина или других остатков в нейтральные остатки, такие как серин или аланин, или посредством превращения подходящим образом размещенных остатков в остатки цистеина. С помощью этого количество остатков цистеина в шарнирном участке может быть увеличено или уменьшено. Данный подход дополнительно описан в патенте США № 5677425 под авторством Bodmer et al... Изменение количества остатков цистеина в шарнирном участке может, например, облегчать сборку легких и тяжелых цепей или приводить к повышению или снижению стабильности BCMA-связывающей молекулы. Другие модифицированные шарнирные участки могут быть полностью синтетическими и могут быть сконструированы таким образом, чтобы они обладали необходимыми свойствами, такими как длина, состав в отношении остатков цистеина и гибкость.
Ряд модифицированных шарнирных участков был описан, например, в патентах США №№ 5677425, WO9915549, WO2005003170, WO2005003169, WO2005003170, WO9825971 и WO2005003171.
Примеры подходящих последовательностей шарнирных участков показаны в таблице 9.
Последовательности шарнирных участков
В одном варианте осуществления Fc-участок содержит интактный шарнирный участок на своем N-конце.
В одном варианте осуществления Fc-участок и шарнирный участок получены из IgG4, и шарнирный участок содержит модифицированную последовательность CPPC (SEQ ID NO:422). Коровый шарнирный участок человеческого IgG4 содержит последовательность CPSC (SEQ ID NO:432) в отличие от IgG1, который содержит последовательность CPPC (SEQ ID NO:422). Остаток серина, присутствующий в последовательности IgG4, приводит к повышению гибкости данного участка и, следовательно, определенная доля молекул образует дисульфидные связи в пределах одной и той же белковой цепи (внутрицепочечную дисульфидную связь), а не образует мостик с другой тяжелой цепью в молекуле IgG с образованием межцепочечной дисульфидной связи. (Angel et al., 1993, Mol Immunol 30(1):105-108). Изменение остатка серина на пролин с получением той же коровой последовательности, что и у IgG1, обеспечивает возможность завершения образования межцепочечных дисульфидных связей в шарнирном участке IgG4, таким образом снижая гетерогенность очищенного продукта. Этот измененный изотип называется IgG4P.
7.4.3. Линкеры для ABD
В определенных аспектах в настоящем изобретении предусмотрены BCMA-связывающие молекулы, где два или более компонентов ABD (например, VH и VL scFv), два или более ABD или ABD и домен, отличный от ABD (например, домен димеризации, такой как Fc-участок), соединены друг с другом посредством пептидного линкера. Такие линкеры называются в данном документе "линкерами для ABD", в отличие от линкеров для ADC, применяемых для присоединения лекарственных средств к BCMA-связывающим молекулам, как описано, например, в разделе 7.9.2.
Длина пептидного линкера может находиться в диапазоне от 2 аминокислот до 60 или более аминокислот, и в определенных аспектах длина пептидного линкера находится в диапазоне от 3 аминокислот до 50 аминокислот, от 4 до 30 аминокислот, от 5 до 25 аминокислот, от 10 до 25 аминокислот или от 12 до 20 аминокислот. В конкретных вариантах осуществления длина пептидного линкера составляет 2 аминокислоты, 3 аминокислоты, 4 аминокислоты, 5 аминокислот, 6 аминокислот, 7 аминокислот, 8 аминокислот, 9 аминокислот, 10 аминокислот, 11 аминокислот, 12 аминокислот, 13 аминокислот, 14 аминокислот, 15 аминокислот, 16 аминокислот, 17 аминокислот, 18 аминокислот, 19 аминокислот, 20 аминокислот, 21 аминокислоту, 22 аминокислоты, 23 аминокислоты, 24 аминокислоты, 25 аминокислот, 26 аминокислот, 27 аминокислот, 28 аминокислот, 29 аминокислот, 30 аминокислот, 31 аминокислоту, 32 аминокислоты, 33 аминокислоты, 34 аминокислоты, 35 аминокислот, 36 аминокислот, 37 аминокислот, 38 аминокислот, 39 аминокислот, 40 аминокислот, 41 аминокислоту, 42 аминокислоты, 43 аминокислоты, 44 аминокислоты, 45 аминокислот, 46 аминокислот, 47 аминокислот, 48 аминокислот, 49 аминокислот или 50 аминокислот.
Можно применять заряженные и/или гибкие линкеры.
Примеры гибких линкеров для ABD, которые можно применять в BCMA-связывающих молекулах, включают линкеры для ABD, раскрытые в Chen et al., 2013, Adv Drug Deliv Rev. 65(10):1357-1369 и Klein et al., 2014, Protein Engineering, Design & Selection 27(10):325-330. Особенно применимым гибким линкером является (GGGGS)n (также называемый (G4S)n) (SEQ ID NO:445). В некоторых вариантах осуществления n равняется любому числу между 1 и 10, т. е. 1, 2, 3, 4, 5, 6, 7, 8, 9 и 10, или находится в любом диапазоне, ограниченном любыми двумя из вышеуказанных чисел, например, от 1 до 5, от 2 до 5, от 3 до 6, от 2 до 4, от 1 до 4 и т. д. и т. п.
Другие примеры линкеров для ABD, подходящих для применения в BCMA-связывающих молекулах по настоящему изобретению, показаны в таблице 10 ниже:
Последовательности линкеров для ABD
В различных аспектах в настоящем изобретении предусмотрена BCMA-связывающая молекула, которая содержит один или несколько ABD-линкеров. Длина каждого из линкеров для ABD может находиться в диапазоне от 2 аминокислот до 60 аминокислот, например, от 4 до 30 аминокислот, от 5 до 25 аминокислот, от 10 до 25 аминокислот или от 12 до 20 аминокислот, при этом линкер необязательно выбран из таблицы 10 выше. В конкретных вариантах осуществления BCMA-связывающая молекула содержит два, три, четыре, пять или шесть линкеров для ABD. Линкеры для ABD могут находиться в одной, двух, трех, четырех или даже более полипептидных цепях BCMA-связывающей молекулы.
7.5. Конфигурации биспецифической связывающей молекулы
Иллюстративные конфигурации BBM показаны на фиг. 1. На фиг. 1A показаны компоненты конфигураций BBM, показанных на фиг. 1B-1AG. Каждый из доменов scFv, Fab, scFab, ABD на основе молекул, отличных от иммуноглобулинов, и Fc может иметь характеристики, описанные для этих компонентов в разделах 7.2 и 7.3. Компоненты конфигураций BBM, показанных на фиг. 1, могут быть ассоциированы друг с другом посредством любого из средств, описанных в разделе 7.4 (например, с помощью прямых связей, линкеров для ABD, дисульфидных связей, Fc-доменов, модифицированных для взаимодействий типа выступ в углубление, и т. д.). Ориентации и ассоциации различных компонентов, показанных на фиг. 1, являются исключительно иллюстративными; как следует понимать специалисту в данной области техники, другие ориентации и ассоциации могут быть подходящими (например, которые описаны в разделах 7.2 и 7.3).
BBM не ограничены конфигурациями, показанными на фиг. 1. Другие конфигурации, которые можно применять, известны специалистам в данной области техники. См., например, WO 2014/145806; WO 2017/124002; Liu et al., 2017, Front Immunol. 8:38; Brinkmann & Kontermann, 2017, mAbs 9:2, 182-212; US 2016/0355600; Klein et al., 2016, MAbs 8(6):1010-20; и US 2017/0145116.
7.5.1. Иллюстративные бивалентные BBM
BBM могут быть бивалентными, т. е. они могут содержать два антигенсвязывающих домена, один или два из которых связывают BCMA (ABD1), и один из которых связывает второй антиген-мишень (ABD2), например, компонент комплекса TCR.
Иллюстративные бивалентные конфигурации BBM показаны на фиг. 1B-1F.
Как изображено на фиг. 1B-1D, BBM может содержать два полуантитела, одно из которых содержит один ABD, и другое содержит один ABD, и эти две половины спарены посредством Fc-домена.
В варианте осуществления на фиг. 1B первое (или левое) полуантитело содержит Fab и Fc-участок, и второе (или правое) полуантитело содержит Fab и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В варианте осуществления на фиг. 1C первое (или левое) полуантитело содержит Fab и Fc-участок, а второе (или правое) полуантитело содержит scFv и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В варианте осуществления на фиг. 1D первое (или левое) полуантитело содержит scFv и Fc-участок, и второе (или правое) полуантитело содержит scFv и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
Как показано на фиг. 1E-1F, бивалентная BBM может содержать два ABD, присоединенных к одному Fc-участку Fc-домена.
В варианте осуществления, показанном на фиг. 1E, BBM содержит Fab, scFv и Fc-домен, где scFv расположен между Fab и Fc-доменом.
В варианте осуществления, показанном на фиг. 1F (конфигурация "одноплечевой scFv-mAb"), BBM содержит Fab, scFv и Fc-домен, где Fab расположен между scFv и Fc-доменом.
В конфигурации, показанной на фиг. 1B-1F, каждый из X и Y представляет собой либо ABD1, либо ABD2, при условии, что BBM содержит один ABD1 и один ABD2. Соответственно, в настоящем изобретении предусмотрена бивалентная BBM, которая показана на любой из фиг. 1B-1F, где X представляет собой ABD1, и Y представляет собой ABD2 (эта конфигурация ABD обозначена как "B1" для удобства). В настоящем изобретении также предусмотрена бивалентная BBM, которая показана на любой из фиг. 1B-1F, где X представляет собой ABD2, и Y представляет собой ABD1 (эта конфигурация ABD обозначена как "B2" для удобства).
7.5.2. Иллюстративные тривалентные BBM
BBM могут быть тривалентными, т. е. они могут содержать три антигенсвязывающих домена, один или два из которых связывают BCMA (ABD1), и один или два из которых связывают второй антиген-мишень (ABD2), например, компонент комплекса TCR.
Иллюстративные тривалентные конфигурации BBM показаны на фиг. 1G-1Z.
Как изображено на фиг. 1G-1N, 1Q-1W, 1Y-1Z, BBM может содержать два полуантитела, одно из которых содержит два ABD, а другое содержит один ABD, и эти две половины спарены посредством Fc-домена.
В варианте осуществления на фиг. 1G первое (или левое) полуантитело содержит Fab и Fc-участок, а второе (или правое) полуантитело содержит scFv, Fab и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В варианте осуществления на фиг. 1H первое (или левое) полуантитело содержит Fab и Fc-участок, а второе (или правое) полуантитело содержит Fab, scFv и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В варианте осуществления на фиг. 1I первое (или левое) полуантитело содержит scFv и Fc-участок, а второе (или правое) полуантитело содержит два Fab и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В варианте осуществления на фиг. 1J первое (или левое) полуантитело содержит два Fab и Fc-участок, а второе (или правое) полуантитело содержит Fab и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В варианте осуществления на фиг. 1K первое (или левое) полуантитело содержит scFv и Fc-участок, а второе (или правое) полуантитело содержит два scFv и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В варианте осуществления на фиг. 1L первое (или левое) полуантитело содержит scFv и Fc-участок, а второе (или правое) полуантитело содержит scFv, Fab и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В варианте осуществления на фиг. 1M первое (или левое) полуантитело содержит scFv и Fc-участок, а второе (или правое) полуантитело содержит Fab, scFv и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В варианте осуществления на фиг. 1N первое (или левое) полуантитело содержит связывающий домен типа диатела и Fc-участок, а второе (или правое) полуантитело содержит Fab и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В варианте осуществления на фиг. 1Q первое (или левое) полуантитело содержит Fab и Fc-участок, а второе (или правое) полуантитело содержит Fab, Fc-участок и scFv. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В варианте осуществления на фиг. 1R первое (или левое) полуантитело содержит scFv и Fc-участок, а второе (или правое) полуантитело содержит Fab, Fc-участок и scFv. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В варианте осуществления на фиг. 1S первое (или левое) полуантитело содержит scFv и Fc-участок, а второе (или правое) полуантитело содержит scFv, Fc-участок и второй scFv. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В варианте осуществления на фиг. 1T первое (или левое) полуантитело содержит scFv, Fc-участок и Fab, а второе (или правое) полуантитело содержит Fab и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В варианте осуществления на фиг. 1U первое (или левое) полуантитело содержит два Fab и Fc-участок, а второе (или правое) полуантитело содержит ABD на основе молекулы, отличной от иммуноглобулина, и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В варианте осуществления на фиг. 1V первое (или левое) полуантитело содержит Fab, scFv и Fc-участок, а второе (или правое) полуантитело содержит ABD на основе молекулы, отличной от иммуноглобулина, и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В варианте осуществления на фиг. 1W первое (или левое) полуантитело содержит Fab и Fc-участок, а второе (или правое) полуантитело содержит scFv, ABD на основе молекулы, отличной от иммуноглобулина, и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В варианте осуществления на фиг. 1Y первое (или левое) полуантитело содержит scFv и Fc-участок, а второе (или правое) полуантитело содержит Fab, scFv и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В варианте осуществления на фиг. 1Z первое (или левое) полуантитело содержит Fab, Fc-участок и scFab, а второе (или правое) полуантитело содержит Fab и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В качестве альтернативы, как изображено на фиг. 1O и 1P, тривалентная BBM может содержать два полуантитела, при этом каждое из них содержит один полный ABD (Fab на фиг. 1O и 1P) и часть другого ABD (одно содержит VH, а другое содержит VL). Два полуантитела спарены посредством Fc-домена, после чего VH и VL ассоциируют с образованием полного антигенсвязывающего Fv-домена.
BBM может быть одноцепочечной, как показано на фиг. 1X. BBM на фиг. 1X содержит три scFv-домена, соединенных посредством линкеров.
В конфигурации, показанной на фиг. 1G-1Z, каждый из X, Y и A представляет собой либо ABD1, либо ABD2, при условии, что BBM содержит по меньшей мере ABD1 и по меньшей мере один ABD2. Таким образом, тривалентные MBM будут содержать один или два ABD1 и один или два ABD2. В некоторых вариантах осуществления тривалентная BBM содержит два ABD1 и один ABD2. В других вариантах осуществления тривалентная BBM по настоящему изобретению содержит один ABD1 и два ABD2.
Соответственно, в настоящем изобретении предусмотрена тривалентная BBM, которая показана на любой из фиг. 1G-1Z, где X представляет собой ABD1, Y представляет собой ABD1, и A представляет собой ABD2 (эта конфигурация ABD обозначена как "T1" для удобства).
В настоящем изобретении дополнительно предусмотрена тривалентная BBM, которая показана на любой из фиг. 1G-1Z, где X представляет собой ABD1, Y представляет собой ABD2, и A представляет собой ABD1 (эта конфигурация ABD обозначена как "T2" для удобства).
В настоящем изобретении дополнительно предусмотрена тривалентная BBM, которая показана на любой из фиг. 1G-1Z, где X представляет собой ABD2, Y представляет собой ABD1, и A представляет собой ABD1 (эта конфигурация ABD обозначена как "T3" для удобства).
В настоящем изобретении дополнительно предусмотрена тривалентная BBM, которая показана на любой из фиг. 1G-1Z, где X представляет собой ABD1, Y представляет собой ABD2, и A представляет собой ABD2 (эта конфигурация ABD обозначена как "T4" для удобства).
В настоящем изобретении дополнительно предусмотрена тривалентная BBM, которая показана на любой из фиг. 1G-1Z, где X представляет собой ABD2, Y представляет собой ABD1, и A представляет собой ABD2 (эта конфигурация ABD обозначена как "T5" для удобства).
В настоящем изобретении дополнительно предусмотрена тривалентная BBM, которая показана на любой из фиг. 1G-1Z, где X представляет собой ABD2, Y представляет собой ABD2, и A представляет собой ABD1 (эта конфигурация ABD обозначена как "T6" для удобства).
7.5.3. Иллюстративные тетравалентные BBM
BBM могут быть тетравалентными, т. е. они могут иметь четыре антигенсвязывающих домена, один, два или три из которых связывают BCMA (ABD1), и один, два или три из которых связывают второй антиген-мишень (ABD2), например, компонент комплекса TCR.
Иллюстративные тетравалентные конфигурации BBM показаны на фиг. 1AA-1AG.
Как изображено на фиг. 1AA-1AG, тетравалентная BBM может содержать два полуантитела, при этом каждое из них содержит два полных ABD, и эти две половины спарены посредством Fc-домена.
В варианте осуществления на фиг. 1AA первое (или левое) полуантитело содержит Fab, Fc-участок и scFv, а второе (или правое) полуантитело содержит Fab, Fc-участок и scFv. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В варианте осуществления на фиг. 1AB первое (или левое) полуантитело содержит Fab, scFv и Fc-участок, а второе (или правое) полуантитело содержит Fab, scFv и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В варианте осуществления на фиг. 1AC первое (или левое) полуантитело содержит scFv, Fab и Fc-участок, а второе (или правое) полуантитело содержит scFv, Fab и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В варианте осуществления на фиг. 1AD первое (или левое) полуантитело содержит Fab, Fc-участок и второй Fab, а второе (или правое) полуантитело содержит Fab, Fc-участок и второй Fab. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В варианте осуществления на фиг. 1AE первое (или левое) полуантитело содержит scFv, второй scFv и Fc-участок, а второе (или правое) полуантитело содержит scFv, второй scFv и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В варианте осуществления на фиг. 1AF первое (или левое) полуантитело содержит Fab, scFv и Fc-участок, а второе (или правое) полуантитело содержит Fab, scFv и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В варианте осуществления на фиг. 1AG первое (или левое) полуантитело содержит Fab, Fc-участок и scFv, а второе (или правое) полуантитело содержит scFv, Fc-участок и Fab. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
В конфигурации, показанной на фиг. 1AA-1AG, каждый из X, Y, A и B представляет собой ABD1 или ABD2, хоть и не обязательно в таком порядке, при условии, что BBM содержит по меньшей мере один ABD1 и по меньшей мере один ABD2. Таким образом, тетравалентные ABD будут содержать один, два или три ABD1 и один, два или три ABD2. В некоторых вариантах осуществления тетравалентная BBM содержит три ABD1 и один ABD2. В других вариантах осуществления тетравалентная BBM содержит два ABD1 и два ABD2s. В еще других вариантах осуществления тетравалентная BBM содержит один ABD1 и три ABD2.
Соответственно, в настоящем изобретении предусмотрена тетравалентная BBM, которая показана на любой из фиг. 1AA-1AG, где X представляет собой ABD1, и каждый из Y, A и B представляет собой ABD2s (эта конфигурация ABD обозначена как "Tv 1" для удобства).
В настоящем изобретении дополнительно предусмотрена тетравалентная BBM, которая показана на любой из фиг. 1AA-1AG, где Y представляет собой ABD1, и каждый из X, A и B представляет собой ABD2s (эта конфигурация ABD обозначена как "Tv 2" для удобства).
В настоящем изобретении дополнительно предусмотрена тетравалентная BBM, которая показана на любой из фиг. 1AA-1AG, где A представляет собой ABD1, и каждый из X, Y и B представляет собой ABD2s (эта конфигурация ABD обозначена как "Tv 3" для удобства).
В настоящем изобретении дополнительно предусмотрена тетравалентная BBM, которая показана на любой из фиг. 1AA-1AG, где B представляет собой ABD1, и каждый из X, Y и A представляет собой ABD2s (эта конфигурация ABD обозначена как "Tv 4" для удобства).
В настоящем изобретении дополнительно предусмотрена тетравалентная BBM, которая показана на любой из фиг. 1AA-1AG, где оба X и Y представляют собой ABD1, и оба A и B представляют собой ABD2 (эта конфигурация ABD обозначена как "Tv 5" для удобства).
В настоящем изобретении дополнительно предусмотрена тетравалентная BBM, которая показана на любой из фиг. 1AA-1AG, где оба X и A представляют собой ABD1, и оба Y и B представляют собой ABD2 (эта конфигурация ABD обозначена как "Tv 6" для удобства).
В настоящем изобретении дополнительно предусмотрена тетравалентная BBM, которая показана на любой из фиг. 1AA-1AG, где оба X и B представляют собой ABD1, и оба Y и A представляют собой ABD2 (эта конфигурация ABD обозначена как "Tv 7" для удобства).
В настоящем изобретении дополнительно предусмотрена тетравалентная BBM, которая показана на любой из фиг. 1AA-1AG, где оба Y и A представляют собой ABD1, и оба X и B представляют собой ABD2 (эта конфигурация ABD обозначена как "Tv 8" для удобства).
В настоящем изобретении дополнительно предусмотрена тетравалентная BBM, которая показана на любой из фиг. 1AA-1AG, где оба Y и B представляют собой ABD1, и оба X и A представляют собой ABD2 (эта конфигурация ABD обозначена как "Tv 9" для удобства).
В настоящем изобретении дополнительно предусмотрена тетравалентная BBM, которая показана на любой из фиг. 1AA-1AG, где оба A и B представляют собой ABD1, и оба X и Y представляют собой ABD2 (эта конфигурация ABD обозначена как "Tv 10" для удобства).
В настоящем изобретении дополнительно предусмотрена тетравалентная BBM, которая показана на любой из фиг. 1AA-1AG, где каждый из X, Y и A представляет собой ABD1, и B представляет собой ABD2 (эта конфигурация ABD обозначена как "Tv 11" для удобства).
В настоящем изобретении дополнительно предусмотрена тетравалентная BBM, которая показана на любой из фиг. 1AA-1AG, где каждый из X, Y и B представляет собой ABD1, и A представляет собой ABD2 (эта конфигурация ABD обозначена как "Tv 12" для удобства).
В настоящем изобретении дополнительно предусмотрена тетравалентная BBM, которая показана на любой из фиг. 1AA-1AG, где каждый из X, A и B представляет собой ABD1, и Y представляет собой ABD2 (эта конфигурация ABD обозначена как "Tv 13" для удобства).
В настоящем изобретении дополнительно предусмотрена тетравалентная BBM, которая показана на любой из фиг. 1AA-1AG, где каждый из Y, A и B представляет собой ABD1, и X представляет собой ABD2 (эта конфигурация ABD обозначена как "Tv 14" для удобства).
7.6. Иллюстративные BBM
BBM по настоящему изобретению содержат по меньшей мере один ABD, который специфически связывается с BCMA, и по меньшей мере один ABD, который связывается со вторым антигеном-мишенью, таким как CD3. Иллюстративные BBM к BCMA и CD3 представлены в таблицах 11A-11F.
BBM могут содержать, например, последовательности CDR иллюстративной BBM, представленной в таблицах 11A-11F. В некоторых вариантах осуществления BBM содержит последовательности вариабельных участков тяжелой и легкой цепей иллюстративной BBM, приведенной в таблицах 11A-F.
Бивалентное AB1
(формат 1×1 hBCMA Fab/hCD3 scFv)
Тривалентное AB1
(формат 2×1 BCMA Fab/hCD3 scFv)
Бивалентное AB2
(формат 1×1 BCMA Fab/hCD3 scFv)
Тривалентное AB2
(формат 2×1 BCMA Fab/hCD3 scFv)
Бивалентное AB3
(формат 1×1 hBCMA Fab/hCD3 scFv)
Тривалентное AB3
(формат 2×1 BCMA Fab/hCD3 scFv)
7.7. Нуклеиновые кислоты и клетки-хозяева
В другом аспекте в настоящем изобретении предусмотрены нуклеиновые кислоты (т. е. полинуклеотиды), кодирующие BCMA-связывающие молекулы по настоящему изобретению. В некоторых вариантах осуществления BCMA-связывающие молекулы кодируются одной нуклеиновой кислотой. В других вариантах осуществления BCMA-связывающие молекулы кодируются совокупностью (например, двумя, тремя, четырьмя или больше) нуклеиновых кислот.
Одна нуклеиновая кислота может кодировать BCMA-связывающую молекулу, которая содержит одну полипептидную цепь, BCMA-связывающую молекулу, которая содержит две или более полипептидные цепи, или часть BCMA-связывающей молекулы, которая содержит более двух полипептидных цепей (например, одна нуклеиновая кислота может кодировать две полипептидные цепи BCMA-связывающей молекулы, содержащей три, четыре или больше полипептидных цепей, или три полипептидные цепи BCMA-связывающей молекулы, содержащей четыре или больше полипептидных цепей). Для индивидуального контроля экспрессии открытые рамки считывания, кодирующие две или более полипептидные цепи, могут находиться под контролем отдельных элементов, регулирующих транскрипцию (например, промоторов и/или энхансеров). Открытые рамки считывания, кодирующие два или более полипептида, могут также находиться под контролем одних и тех же элементов, регулирующих транскрипцию, и могут быть отделены последовательностями внутреннего участка посадки рибосомы (IRES), что обеспечивает возможность трансляции с образованием отдельных полипептидов.
В некоторых вариантах осуществления BCMA-связывающая молекула, содержащая две или более полипептидных цепей, кодируется двумя или более нуклеиновыми кислотами. Количество нуклеиновых кислот, кодирующих BCMA-связывающую молекулу, может равняться количеству полипептидных цепей в BCMA-связывающей молекуле (например, если более чем одна полипептидная цепь кодируется одной нуклеиновой кислотой) или быть меньшим, чем это количество.
Нуклеиновые кислоты могут представлять собой ДНК или РНК (например, мРНК).
В другом аспекте в настоящем изобретении предусмотрены клетки-хозяева и векторы, содержащие нуклеиновые кислоты по настоящему изобретению. Нуклеиновые кислоты могут присутствовать в одном векторе или отдельных векторах, присутствующих в одной и той же клетке-хозяине или отдельных клетках-хозяевах, как более подробно описано в данном документе ниже.
7.7.1. Векторы
В настоящем изобретении предусмотрены векторы, содержащие нуклеотидные последовательности, кодирующие BCMA-связывающую молекулу или компонент BCMA-связывающей молекулы, описанные в данном документе. В одном варианте осуществления векторы содержат нуклеотиды, кодирующие ABD на основе иммуноглобулина, описанный в данном документе. В одном варианте осуществления векторы содержат нуклеотиды, кодирующие Fc-домен, описанный в данном документе. В одном варианте осуществления векторы содержат нуклеотиды, кодирующие рекомбинантный ABD на основе молекулы, отличной от иммуноглобулина, описанный в данном документе. Вектор может кодировать один или несколько ABD, один или несколько Fc-доменов, один или несколько ABD на основе молекул, отличных от иммуноглобулинов, или любую их комбинацию (например, если несколько компонентов или субкомпонентов кодируются одной полипептидной цепью). В одном варианте осуществления векторы содержат нуклеотидные последовательности, описанные в данном документе. Векторы включают без ограничения вирус, плазмиду, космиду, фаг лямбда или искусственную хромосому дрожжей (YAC).
Можно использовать многочисленные векторные системы. Например, в одном классе векторов используются ДНК-элементы, которые получены из вирусов животных, таких как, например, вирус папилломы крупного рогатого скота, вирус полиомы, аденовирус, вирус осповакцины, бакуловирус, ретровирусы (вирус саркомы Рауса, MMTV или MOMLV) или вирус SV40. В другом классе векторов используются РНК-элементы, полученные из РНК-содержащих вирусов, таких как вирус леса Семлики, вирус восточного энцефалита лошадей и флавивирусы.
Кроме того, клетки, которые стабильно интегрировали ДНК в свои хромосомы, могут быть отобраны посредством введения одного или нескольких маркеров, которые обеспечивают возможность отбора трансфицированных клеток-хозяев. Маркер может обеспечивать, например, прототрофность для ауксотрофного хозяина, устойчивость к биоцидам (например, антибиотикам) или устойчивость к тяжелым металлам, таким как медь и т. п. Селектируемый маркерный ген может быть непосредственно связан с последовательностями ДНК, которые должны экспрессироваться, либо введен в ту же самую клетку путем котрансформации. Дополнительные элементы также могут быть необходимы для оптимального синтеза мРНК. Эти элементы могут включать сигналы сплайсинга, а также промоторы транскрипции, энхансеры и сигналы терминации.
После того, как вектор экспрессии или последовательность ДНК, содержащие конструкции, были подготовлены для экспрессии, векторами экспрессии можно трансфицировать соответствующую клетку-хозяина или векторы экспрессии можно вводить в соответствующую клетку-хозяина. Для достижения этого можно использовать различные методики, такие как, например, слияние протопластов, осаждение фосфатом кальция, электропорация, ретровирусная трансдукция, вирусная трансфекция, генная пушка, трансфекция с использованием липидов или другие общепринятые методики. Способы и условия культивирования полученных в результате трансфицированных клеток и извлечения экспрессированных полипептидов известны специалистам в данной области техники и могут быть изменены или оптимизированы в зависимости от конкретных используемых вектора экспрессии и клетки-хозяина, представляющей собой клетку млекопитающего, исходя из настоящего описания.
7.7.2. Клетки
В настоящем изобретении также предусмотрены клетки-хозяева, содержащие нуклеиновую кислоту по настоящему изобретению.
В одном варианте осуществления клетки-хозяева являются генетически сконструированными таким образом, что они содержат одну или несколько нуклеиновых кислот, описанных в данном документе.
В одном варианте осуществления клетки-хозяева являются генетически сконструированными с применением кассеты экспрессии. Фраза "кассета экспрессии" относится к нуклеотидным последовательностям, которые способны влиять на экспрессию гена у хозяев, совместимых с такими последовательностями. Такие кассеты могут содержать промотор, открытую рамку считывания с интронами или без них и сигнал терминации. Также можно применять дополнительные факторы, необходимые или полезные при осуществлении экспрессии, такие как, например, индуцируемый промотор.
В настоящем изобретении также предусмотрены клетки-хозяева, содержащие векторы, описанные в данном документе.
Клетка может представлять собой без ограничения эукариотическую клетку, бактериальную клетку, клетку насекомого или клетку человека. Подходящие эукариотические клетки включают без ограничения клетки Vero, клетки HeLa, клетки COS, клетки CHO, клетки HEK293, клетки BHK и клетки MDCKII. Подходящие клетки насекомых включают без ограничения клетки Sf9.
7.8. BCMA-связывающие молекулы с увеличенным периодом полужизни in vivo
BCMA-связывающие молекулы по настоящему изобретению могут быть модифицированы так, чтобы иметь увеличенный период полужизни in vivo.
Для увеличения периода полужизни BCMA-связывающих молекул по настоящему изобретению можно применять ряд стратегий. Например, химическое связывание с полиэтиленгликолем (PEG), reCODE PEG, каркасной структурой антитела, полисиаловой кислотой (PSA), гидроксиэтилкрахмалом (HES), альбуминсвязывающими лигандами и углеводными защитными фрагментами; генетическое слияние с белками, связывающимися с белками сыворотки крови, такими как альбумин, IgG, FcRn, и перенос; соединение (генетическое или химическое) с другими связывающими фрагментами, которые связываются с белками сыворотки крови, такими как нанотела, Fab, дарпины, авимеры, аффитела и антикалины; генетическое слияние с rPEG, альбумином, доменом альбумина, альбуминсвязывающими белками и Fc; или включение в наноносители, составы с медленным высвобождением или медицинские устройства.
Для продления циркуляции BCMA-связывающих молекул в сыворотке крови in vivo молекулы инертного полимера, такого как высокомолекулярный PEG, могут быть присоединены к BCMA-связывающим молекулам с помощью полифункционального линкера или без него посредством сайт-специфической конъюгации PEG с N- или С-концом полипептида, содержащего BCMA-связывающую молекулу, либо посредством эпсилон-аминогрупп, присутствующих в остатках лизина. Для пегилирования BCMA-связывающей молекулы можно осуществлять реакцию молекулы с полиэтиленгликолем (PEG), таким как реакционноспособный сложный эфир или альдегидное производное PEG в условиях, при которых одна или несколько PEG-групп присоединяются к BCMA-связывающим молекулам. Пегилирование можно осуществлять посредством реакции ацилирования или реакции алкилирования с реакционноспособной молекулой PEG (или аналогичным реакционноспособным водорастворимым полимером). Предполагается, что используемый в данном документе термин "полиэтиленгликоль" охватывает любую из форм PEG, которые применялись для дериватизации других белков, например, моно(C1-C10)алкокси- или арилоксиполиэтиленгликоль или полиэтиленгликоль-малеимид. В одном варианте осуществления ВСМА-связывающая молекула, подлежащая пегилированию, представляет собой агликозилированное антитело. Будет применяться дериватизация с помощью линейного или разветвленного полимера, которая приводит к минимальной потере биологической активности. Степень конъюгации можно тщательно контролировать с помощью SDS-PAGE и масс-спектрометрии для обеспечения надлежащей конъюгации молекул PEG с антителами. Непрореагировавший PEG можно отделить от конъюгатов антитело-PEG с помощью эксклюзионной или ионообменной хроматографии. PEG-дериватизированные антитела можно тестировать в отношении связывающей активности, а также в отношении эффективности in vivo с применением способов, хорошо известных специалистам в данной области техники, например, с помощью иммуноанализов, описанных в данном документе. Способы пегилирования белков известны и могут применяться по отношению к ВСМА-связывающим молекулам по настоящему изобретению. См., например, EP 0154316 под авторством Nishimura et al. и EP 0401384 под авторством Ishikawa et al.
Другие модифицированные технологии пегилирования включают преобразующую технологию химически ортогонального направленного конструирования (PEG ReCODE), при которой химически определенные боковые цепи включаются в состав биосинтетических белков посредством преобразующей системы, которая содержит тРНК-синтетазу и тРНК. Данная технология позволяет включать более чем 30 новых аминокислот в биосинтетические белки в E. coli, дрожжах и клетках млекопитающих. тРНК включает стандартную аминокислоту в любое место, где расположен амбер-кодон, превращая амбер-кодон из стоп-кодона в кодон, который передает сигнал о включении химически определенной аминокислоты.
Технология рекомбинантного пегилирования (rPEG) также может применяться для увеличения периода полужизни в сыворотке крови. Данная технология предусматривает генетическое слияние неструктурированного белкового хвоста из 300-600 аминокислот с существующим фармацевтическим белком. Поскольку кажущийся молекулярный вес такой неструктурированной белковой цепи в приблизительно 15 раз превышает ее фактический молекулярный вес, период полужизни белка в сыворотке крови значительно увеличивается. В отличие от традиционного пегилирования, для которого требуется химическая конъюгация и повторная очистка, способ изготовления значительно упрощается, и продукт является гомогенным.
Полисиалирование представляет собой другую технологию, в которой используется природный полимер полисиаловая кислота (PSA) для продления срока действия и улучшения стабильности терапевтических пептидов и белков. PSA представляет собой полимер сиаловой кислоты (сахар). При применении для доставки лекарственного средства на основе белка и терапевтического пептида полисиаловая кислота обеспечивает защитную микросреду при конъюгации. Это увеличивает срок действия терапевтического белка в кровотоке и предотвращает его распознавание иммунной системой. Полимер, представляющий собой PSA, в естественных условиях обнаруживается в организме человека. Его начали использовать некоторые бактерии, которые эволюционировали на протяжении миллионов лет, для покрытия им своих клеточных стенок. Эти полисиалированные в естественных условиях бактерии затем были способны благодаря молекулярной мимикрии противодействовать защитной системе организма. PSA, которую можно отнести к совершенной природной технологии малозаметности, можно с легкостью получать из таких бактерий в больших количествах и с заданными физическими характеристиками. Бактериальная PSA является полностью неимуногенной, даже когда связана с белками, так как она является химически идентичной PSA в организме человека.
Другая технология предусматривает применение производных гидроксиэтилкрахмала ("HES"), связанных с BCMA-связывающими молекулами. HES представляет собой модифицированный природный полимер, полученный из крахмала восковидной кукурузы, и может быть метаболизирован ферментами организма. Растворы HES обычно вводят для восполнения недостающего объема крови и улучшения реологических свойств крови. Модификация BCMA-связывающей молекулы с помощью HES позволяет продлить период полужизни в кровотоке за счет повышения стабильности молекулы, а также за счет снижения почечного клиренса, что приводит к повышению биологической активности. Изменяя различные параметры, такие как молекулярный вес HES, можно адаптировать к конкретным требованиям широкий спектр конъюгатов HES-BCMA-связывающая молекула.
BCMA-связывающие молекулы, характеризующиеся увеличенным периодом полужизни in vivo, также можно получать посредством введения одной или нескольких аминокислотных модификаций (т. е. замен, вставок или делеций) в константный домен IgG или его FcRn-связывающий фрагмент (например, Fc или шарнирный фрагмент Fc-домена). См., например, международную публикацию № WO 98/23289; международную публикацию № WO 97/34631 и патент США № 6277375.
Кроме того, ВСМА-связывающие молекулы могут быть конъюгированы с альбумином, доменом альбумина, альбумин-связывающим белком или альбумин-связывающим антителом или фрагментами данного антитела для обеспечения молекулам большей стабильности in vivo или более длительного периода полужизни in vivo. Методики являются хорошо известными, см., например, международные публикации №№ WO 93/15199, WO 93/15200 и WO 01/77137; и европейский патент № EP 413622.
ВСМА-связывающие молекулы по настоящему изобретению также могут быть слиты с одним или несколькими полипептидами человеческого сывороточного альбумина (HSA) или с их частью. Использование альбумина в качестве компонента слитого с альбумином белка в качестве носителя для различных белков было предложено в WO 93/15199, WO 93/15200 и EP 413622. Также было предложено использование N-концевых фрагментов HSA для слияния с полипептидами (EP 399666). Соответственно, посредством генетического или химического слияния или конъюгации молекул с альбумином можно стабилизировать или продлить срок хранения и/или сохранить активность молекулы в течение продолжительных периодов времени в растворе in vitro и/или in vivo. Дополнительные способы, относящиеся к слияниям с HSA, можно найти, например, в WO 2001077137 и WO 200306007. В одном варианте осуществления экспрессия слитого белка осуществляется в линиях клеток млекопитающих, например, в линиях клеток СНО.
ВСМА-связывающие молекулы по настоящему изобретению также могут быть слиты с антителом или фрагментом данного антитела, которые связываются с альбумином, например, с человеческим сывороточным альбумином (HSA). Альбумин-связывающее антитело или фрагмент данного антитела могут представлять собой Fab, scFv, Fv, scFab, (Fab')2, однодоменное антитело, VHH-домен верблюдовых, VH- или VL-домен или полноразмерное моноклональное антитело (mAb).
ВСМА-связывающие молекулы по настоящему изобретению также могут быть слиты с жирной кислотой для увеличения их периода полужизни. Жирные кислоты, подходящие для связывания с биомолекулой, были описаны в данной области техники, например, в WO2015/200078, WO2015/191781, US2013/0040884. Подходящие жирные кислоты, увеличивающие период полужизни, включают жирные кислоты, которые определены как C6-70алкильная, C6-70алкенильная или C6-70алкинильная цепь, каждая из которых замещена по меньшей мере одной карбоновой кислотой (например, 1, 2, 3 или 4 CO2H) и необязательно дополнительно замещена гидроксильной группой. Например, описанные в данном документе ВСМА-связывающие молекулы могут быть связаны с жирной кислотой, имеющей любую из следующих формул A1, A2 или A3:
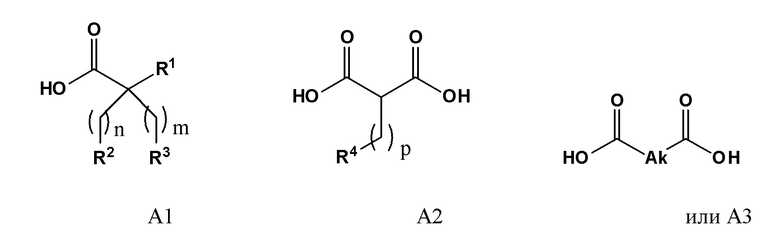
R1 представляет собой CO2H или H;
R2, R3 и R4 независимо друг от друга представляют собой H, OH, CO2H, -CH=CH2 или -C=CH;
Ak представляет собой разветвленный C6-C30алкилен;
n, m и p независимо друг от друга представляют собой целое число от 6 до 30; или амид, сложный эфир или их фармацевтически приемлемую соль.
В некоторых вариантах осуществления жирная кислота имеет формулу A1, например, жирная кислота формулы A1, где n и m независимо представляют собой число от 8 до 20, например, от 10 до 16. В другом варианте осуществления фрагмент жирной кислоты имеет формулу A1, и где по меньшей мере один из R2 и R3 представляет собой CO2H.
В некоторых вариантах осуществления жирная кислота выбрана из следующих формул:
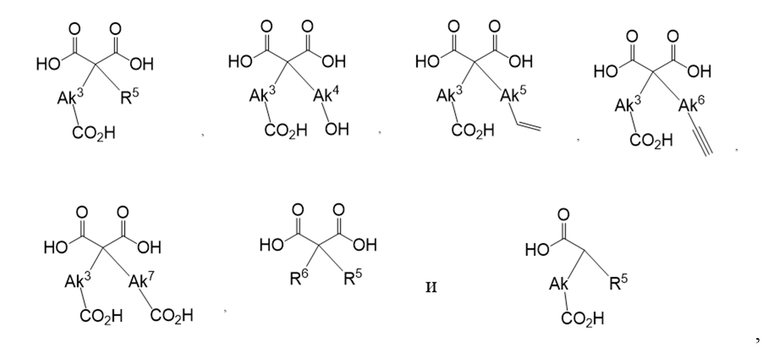
где Ak3, Ak4, Ak5, Ak6 и Ak7 независимо представляют собой (C8-20)алкилен, R5 и R6 независимо представляют собой (C8-20)алкил.
В некоторых вариантах осуществления жирная кислота выбрана из следующих формул:
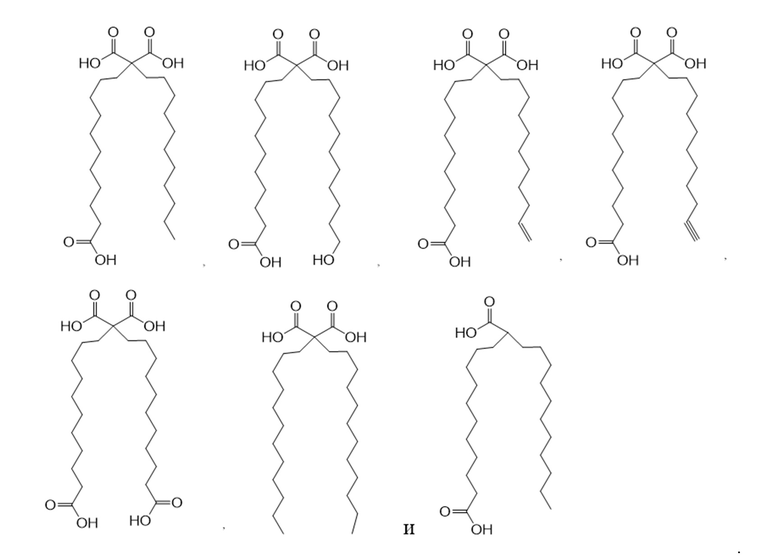
В некоторых вариантах осуществления жирная кислота выбрана из следующих формул:
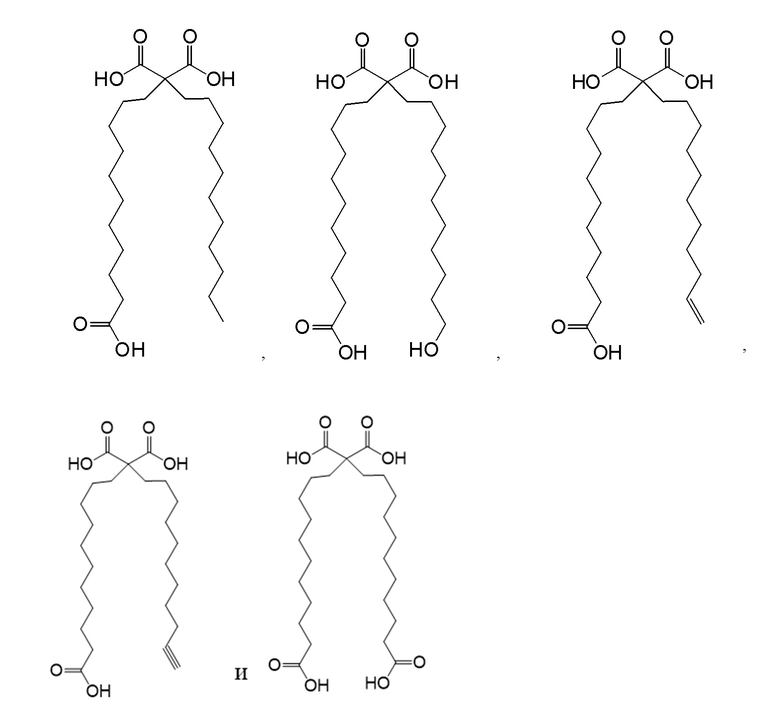
В некоторых вариантах осуществления жирная кислота имеет формулу A2 или A3. В конкретном варианте осуществления конъюгат содержит фрагмент жирной кислоты формулы A2, где p представляет собой число от 8 до 20, или фрагмент жирной кислоты формулы A3, где Ak представляет собой C8-20алкилен.
7.9. Конъюгаты антител и лекарственных средств
BCMA-связывающие молекулы по настоящему изобретению могут быть конъюгированы, например, посредством линкера, с фрагментом, представляющим собой лекарственное средство. Для удобства такие конъюгаты называются в данном документе конъюгатами антител и лекарственных средств (или "ADC"), несмотря на тот факт, что один или несколько ABD могут быть на основе каркасных структур на основе молекул, отличных от иммуноглобулинов, например, MBM, содержащая один или несколько ABD на основе молекул, отличных от иммуноглобулинов, таких как ABD к TCR, содержащие аффилин-144160.
В определенных аспектах фрагмент, представляющий собой лекарственное средство, проявляет цитотоксическую или цитостатическую активность. В одном варианте осуществления фрагмент, представляющий собой лекарственное средство, выбран из майтанзиноида, ингибитора кинезиноподобного белка KIF11, ингибитора V-ATPазы (Н+-ATPазы вакуолярного типа), проапоптотического средства, ингибитора Bcl2 (белка 2 B-клеточной лимфомы), ингибитора MCL1 (белка 1 миелоидноклеточного лейкоза), ингибитора HSP90 (белка теплового шока 90), ингибитора IAP (ингибитора апоптоза), ингибитора mTOR (механистической мишени рапамицина), стабилизатора микротрубочек, дестабилизатора микротрубочек, ауристатина, доластатина, MetAP (метионинаминопептидазы), ингибитора CRM1 (белка 1 поддержания структуры хромосом), ингибитора DPPIV (дипептидилпептидазы IV), ингибитора протеасом, ингибитора реакции переноса фосфорильной группы в митохондриях, ингибитора синтеза белка, ингибитора киназы, ингибитора CDK2 (циклинзависимой киназы 2), ингибитора CDK9 (циклинзависимой киназы 9), ингибитора кинезина, ингибитора HDAC (деацетилазы гистонов), средства, повреждающего ДНК, средства, алкилирующего ДНК, интеркалятора ДНК, средства, связывающегося с малой бороздкой ДНК, ингибитора РНК-полимеразы, ингибитора топоизомеразы или ингибитора DHFR (дигидрофолатредуктазы). В некоторых вариантах осуществления фрагмент, представляющий собой лекарственное средство, представляет собой ион радиоактивного металла, такой как излучатели альфа-частиц, такие как 213Bi, или макроциклические хелаторы, пригодные для конъюгации ионов радиоактивных металлов, включая без ограничения 131In, 131LU, 131Y, 131Ho, 131Sm, с полипептидами. В одном варианте осуществления макроциклический хелатор представляет собой 1,4,7,10-тетраазациклододекан-N, N',N'',N'''-тетрауксусную кислоту (DOTA).
В одном варианте осуществления линкер выбран из расщепляемого линкера, нерасщепляемого линкера, гидрофильного линкера, предварительно заряженного линкера или линкера на основе дикарбоновой кислоты.
В некоторых вариантах осуществления ADC представляют собой соединения в соответствии со структурной формулой (I):
[D-L-XY]n-Ab
или их соли, где каждый "D" представляет собой независимо от других цитотоксическое и/или цитостатическое средство ("лекарственное средство"); каждый "L" представляет собой независимо от других линкер; "Ab" представляет собой BCMA-связывающую молекулу, описанную в данном документе; каждый "XY" представляет собой связь, образованную между функциональной группой Rx в линкере и "комплементарной" функциональной группой Ry в антителе, и n представляет собой количество связанных лекарственных средств или соотношение лекарственное средство: антитело (DAR) в ADC.
Некоторые варианты осуществления различных антител (Ab), которые могут содержаться в ADC, включают различные варианты осуществления BCMA-связывающих молекул, описанных выше.
В некоторых вариантах осуществления ADC и/или солей структурной формулы (I) все D являются одинаковыми, и/или все L являются одинаковыми.
Некоторые варианты осуществления цитотоксических и/или цитостатических средств (D) и линкеров (L), которые могут содержаться в ADC по настоящему изобретению, а также количество цитотоксических и/или цитостатических средств, связанных с ADC, более подробно описаны ниже.
7.9.1. Цитотоксические и/или цитостатические средства
Цитотоксические и/или цитостатические средства могут представлять собой любые средства, которые, как известно, подавляют рост и/или репликацию клеток, и в частности раковых и/или опухолевых клеток, и/или уничтожают их. В литературе известны многочисленные средства, обладающие цитотоксическими и/или цитостатическими свойствами. Неограничивающие примеры классов цитотоксических и/или цитостатических средств включают в качестве примера и без ограничения радионуклиды, алкилирующие средства, ингибиторы топоизомеразы I, ингибиторы топоизомеразы II, средства, интеркалирующие ДНК (например, средства, связывающиеся с бороздками, такие как средства, связывающиеся с малой бороздкой), антиметаболиты РНК/ДНК, модуляторы клеточного цикла, ингибиторы киназ, ингибиторы синтеза белка, ингибиторы деацетилаз гистонов, ингибиторы митохондрий и антимитотические средства.
Ниже приведены конкретные неограничивающие примеры средств в пределах некоторых из этих различных классов.
Алкилирующие средства: асалей ((L-лейцин, N-[N-ацетил-4-[бис-(2-хлорэтил)амино]-D/L-фенилaланил]-, этиловый сложный эфир; NSC 167780; регистрационный № по CAS 3577897)); AZQ ((1,4-циклогексадиен-1,4-дикарбаминовая кислота, 2,5-бис(1-азиридинил)-3,6-диоксо-, диэтиловый сложный эфир; NSC 182986; регистрационный № по CAS 57998682)); BCNU ((N, N'-бис(2-хлорэтил)-N-нитрозомочевина; NSC 409962; регистрационный № по CAS 154938)); бусульфан (1,4-бутандиолдиметансульфонат; NSC 750; регистрационный № по CAS 55981); (карбоксифталато)платина (NSC 27164; регистрационный № по CAS 65296813); CBDCA ((цис-(1,1-циклобутандикарбоксилато)диаминоплатина(II)); NSC 241240; регистрационный № по CAS 41575944)); CCNU ((N-(2-хлорэтил)-N'-циклогексил-N-нитрозомочевина; NSC 79037; регистрационный № по CAS 13010474)); CHIP (ипроплатин; NSC 256927); хлорамбуцил (NSC 3088; регистрационный № по CAS 305033); хлорозотоцин ((2-[[[(2-хлорэтил)нитрозамино]карбонил]амино]-2-дезокси-D-глюкопиранoза; NSC 178248; регистрационный № по CAS 54749905)); цис-платина (цисплатин; NSC 119875; регистрационный № по CAS 15663271); кломезон (NSC 338947; регистрационный № по CAS 88343720); цианоморфолинодоксорубицин (NCS 357704; регистрационный № по CAS 88254073); циклодизон (NSC 348948; регистрационный № по CAS 99591738); диангидрогалактит (5,6-диэпоксидульцит; NSC 132313; регистрационный № по CAS 23261203); фтордопан (5-[(2-хлорэтил)(2-фторэтил)амино]-6-метилурацил; NSC 73754; регистрационный № по CAS 834913); гепсульфам (NSC 329680; регистрационный № по CAS 96892578); гикантон (NSC 142982; регистрационный № по CAS 23255938); мелфалан (NSC 8806; регистрационный № по CAS 3223072); метил-CCNU (1-(2-хлорэтил)-3-(транс-4-метилциклогексан)-1-нитрозомочевина; NSC 95441; 13909096); митомицин C (NSC 26980; регистрационный № по CAS 50077); митозоламид (NSC 353451; регистрационный № по CAS 85622953); азотистый иприт (гидрохлорид бис(2-хлорэтил)метиламина; NSC 762; регистрационный № по CAS 55867); PCNU ((1-(2-хлорэтил)-3-(2,6-диоксо-3-пиперидил)-1-нитрозомочевина; NSC 95466; регистрационный № по CAS 13909029)); пиперазиновый алкилятор (дигидрохлорид (1-(2-хлорэтил)-4-(3-хлорпропил)пиперазина; NSC 344007)); пиперазиндион (NSC 135758; регистрационный № по CAS 41109802); пипоброман ((N, N-бис(3-бромпропионил)пиперазин; NSC 25154; регистрационный № по CAS 54911)); порфиромицин (N-метилмитомицин C; NSC 56410; регистрационный № по CAS 801525); спирогидантоиновый иприт (NSC 172112; регистрационный № по CAS 56605164); тероксирон (триглицидилизоцианурат; NSC 296934; регистрационный № по CAS 2451629); тетраплатин (NSC 363812; регистрационный № по CAS 62816982); тиотепа (N, N',N''-три-1,2-этандиилтиофосфорамид; NSC 6396; регистрационный № по CAS 52244); триэтиленмеламин (NSC 9706; регистрационный № по CAS 51183); урациловый иприт (десметилдопан; NSC 34462; регистрационный № по CAS 66751); Yoshi-864 (гидрохлорид бис(3-мезилоксипропил)амина; NSC 102627; регистрационный № по CAS 3458228).
Ингибиторы топоизомеразы I: камптотецин (NSC 94600; регистрационный № по CAS 7689-03-4); различные производные и аналоги камптотецина (например, NSC 100880, NSC 603071, NSC 107124, NSC 643833, NSC 629971, NSC 295500, NSC 249910, NSC 606985, NSC 74028, NSC 176323, NSC 295501, NSC 606172, NSC 606173, NSC 610458, NSC 618939, NSC 610457, NSC 610459, NSC 606499, NSC 610456, NSC 364830 и NSC 606497); морфолиноизоксорубицин (NSC 354646; регистрационный № по CAS 89196043); SN-38 (NSC 673596; регистрационный № по CAS 86639-52-3).
Ингибиторы топоизомеразы II: доксорубицин (NSC 123127; регистрационный № по CAS 25316409); амонафид (бензизохинолиндион; NSC 308847; регистрационный № по CAS 69408817); m-AMSA ((4'-(9-акридиниламино)-3'-метоксиметансульфонанилид; NSC 249992; регистрационный № по CAS 51264143)); производное антрапиразола (NSC 355644); этопозид (VP-16; NSC 141540; регистрационный № по CAS 33419420); пиразолоакридин (пиразолo[3,4,5-kl]акридин-2(6H)пропанамин, 9-метокси-N, N-диметил-5-нитро-, монометансульфонат; NSC 366140; регистрационный № по CAS 99009219); гидрохлорид бисантрена (NSC 337766; регистрационный № по CAS 71439684); даунорубицин (NSC 821151; регистрационный № по CAS 23541506); дезоксидоксорубицин (NSC 267469; регистрационный № по CAS 63950061); митоксантрон (NSC 301739; регистрационный № по CAS 70476823); меногарил (NSC 269148; регистрационный № по CAS 71628961); N, N-дибензилдауномицин (NSC 268242; регистрационный № по CAS 70878512); оксантразол (NSC 349174; регистрационный № по CAS 105118125); рубидазон (NSC 164011; регистрационный № по CAS 36508711); тенипозид (VM-26; NSC 122819; регистрационный № по CAS 29767202).
Средства, интеркалирующие ДНК: антрамицин (регистрационный № по CAS 4803274); чикамицин A (регистрационный № по CAS 89675376); томаймицин (регистрационный № по CAS 35050556); DC-81 (регистрационный № по CAS 81307246); сибиромицин (регистрационный № по CAS 12684332); производное пирролобензодиазепина (регистрационный № по CAS 945490095); SGD-1882 ((S)-2-(4-аминофенил)-7-метокси-8-(3-4-(S)-7-метокси-2-(4-метоксифенил)-5-оксо-5,11a-дигидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-8-ил)окси)пропокси)-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-5-(11aH)-он); SG2000 (SJG-136; (11aS,11a'S)-8,8'-(пропан-1,3-диилбис(окси)бис(7-метокси-2-метилен-2,3-дигидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-5(11aH)-он); NSC 694501; регистрационный № по CAS 232931576).
Антиметаболиты РНК/ДНК: L-аланозин (NSC 153353; регистрационный № по CAS 59163416); 5-азацитидин (NSC 102816; регистрационный № по CAS 320672); 5-фторурацил (NSC 19893; регистрационный № по CAS 51218); ацивицин (NSC 163501; регистрационный № по CAS 42228922); производное аминоптерина N-[2-хлор-5-[[(2,4-диамино-5-метил-6-хиназолинил)метил]амино]бензоил]-L-аспарагиновая кислота (NSC 132483); производное аминоптерина N-[4-[[(2,4-диамино-5-этил-6-хиназолинил)метил]амино]бензоил]-L-аспарагиновая кислота (NSC 184692); производное аминоптерина моногидрат N-[2-хлор-4-[[(2,4-диамино-6-птеридинил)метил]амино]бензоил]-L-аспарагиновой кислоты (NSC 134033); антифолат ((Nα-(4-амино-4-дезоксиптероил)-N7-гемифталоил-L-орнитин; NSC 623017)); растворимый антифолат Бейкера (NSC 139105; регистрационный № по CAS 41191042); дихлораллиллаусон (2-(3,3-дихлораллил)-3-гидрокси-1,4-нафтохинон; NSC 126771; регистрационный № по CAS 36417160); бреквинар (NSC 368390; регистрационный № по CAS 96201886); фторафур (пролекарство; 5-фтор-1-(тетрагидро-2-фурил)урацил; NSC 148958; регистрационный № по CAS 37076689); 5,6-дигидро-5-азацитидин (NSC 264880; регистрационный № по CAS 62402317); метотрексат (NSC 740; регистрационный № по CAS 59052); производное метотрексата (N-[[4-[[(2,4-диамино-6-птеридинил)метил]метиламино]-1-нафталинил]карбонил]-L-глутаминовая кислота; NSC 174121); PALA (N-(фосфоноацетил)-L-аспартат; NSC 224131; регистрационный № по CAS 603425565); пиразофурин (NSC 143095; регистрационный № по CAS 30868305); триметрексат (NSC 352122; регистрационный № по CAS 82952645).
Антиметаболиты ДНК: 3-HP (NSC 95678; регистрационный № по CAS 3814797); 2'-дезокси-5-фторуридин (NSC 27640; регистрационный № по CAS 50919); 5-HP (NSC 107392; регистрационный № по CAS 19494894); α-TGDR (α-2'-дезокси-6-тиогуанозин; NSC 71851; регистрационный № по CAS 2133815); глицинат афидиколина (NSC 303812; регистрационный № по CAS 92802822); Ara-C (цитозинарабинозид; NSC 63878; регистрационный № по CAS 69749); 5-аза-2'-дезоксицитидин (NSC 127716; регистрационный № по CAS 2353335); β-TGDR (β-2'-дезокси-6-тиогуанозин; NSC 71261; регистрационный № по CAS 789617); циклоцитидин (NSC 145668; регистрационный № по CAS 10212256); гуаназол (NSC 1895; регистрационный № по CAS 1455772); гидроксимочевина (NSC 32065; регистрационный № по CAS 127071); инозингликодиальдегид (NSC 118994; регистрационный № по CAS 23590990); макбецин II (NSC 330500; регистрационный № по CAS 73341738); пиразолоимидазол (NSC 51143; регистрационный № по CAS 6714290); тиогуанин (NSC 752; регистрационный № по CAS 154427); тиопурин (NSC 755; регистрационный № по CAS 50442).
Модуляторы клеточного цикла: силибинин (регистрационный № по CAS 22888-70-6); галлат эпигаллокатехина (EGCG; регистрационный № по CAS 989515); производные процианидина (например, процианидин A1 [регистрационный № по CAS 103883030], процианидин B1 [регистрационный № по CAS 20315257], процианидин B4 [регистрационный № по CAS 29106512], арекатанин B1 [регистрационный № по CAS 79763283]); изофлавоны (например, генистеин [4',5,7-тригидроксиизофлавон; регистрационный № по CAS 446720], дайдзеин [4',7-дигидроксиизофлавон, регистрационный № по CAS 486668]; индол-3-карбинол (регистрационный № по CAS 700061); кверцетин (NSC 9219; регистрационный № по CAS 117395); эстрамустин (NSC 89201; регистрационный № по CAS 2998574); нокодазол (регистрационный № по CAS 31430189); подофиллотоксин (регистрационный № по CAS 518285); тартрат винорелбина (NSC 608210; регистрационный № по CAS 125317397); криптофицин (NSC 667642; регистрационный № по CAS 124689652).
Ингибиторы киназ: афатиниб (регистрационный № по CAS 850140726); акситиниб (регистрационный № по CAS 319460850); ARRY-438162 (биниметиниб) (регистрационный № по CAS 606143899); босутиниб (регистрационный № по CAS 380843754); кабозантиниб (регистрационный № по CAS 1140909483); церитиниб (регистрационный № по CAS 1032900256); кризотиниб (регистрационный № по CAS 877399525); дабрафениб (регистрационный № по CAS 1195765457); дазатиниб (NSC 732517; регистрационный № по CAS 302962498); эрлотиниб (NSC 718781; регистрационный № по CAS 183319699); эверолимус (NSC 733504; регистрационный № по CAS 159351696); фостаматиниб (NSC 745942; регистрационный № по CAS 901119355); гефитиниб (NSC 715055; регистрационный № по CAS 184475352); ибрутиниб (регистрационный № по CAS 936563961); иматиниб (NSC 716051; регистрационный № по CAS 220127571); лапатиниб (регистрационный № по CAS 388082788); ленватиниб (регистрационный № по CAS 857890392); мубритиниб (CAS 366017096); нилотиниб (регистрационный № по CAS 923288953); нинтеданиб (регистрационный № по CAS 656247175); палбоциклиб (регистрационный № по CAS 571190302); пазопаниб (NSC 737754; регистрационный № по CAS 635702646); пегаптаниб (регистрационный № по CAS 222716861); понатиниб (регистрационный № по CAS 1114544318); рапамицин (NSC 226080; регистрационный № по CAS 53123889); регорафениб (регистрационный № по CAS 755037037); AP 23573 (ридафоролимус) (регистрационный № по CAS 572924540); INCB018424 (руксолитиниб) (регистрационный № по CAS 1092939177); ARRY-142886 (селуметиниб) (NSC 741078; регистрационный № по CAS 606143-52-6); сиролимус (NSC 226080; регистрационный № по CAS 53123889); сорафениб (NSC 724772; регистрационный № по CAS 475207591); сунитиниб (NSC 736511; регистрационный № по CAS 341031547); тофацитиниб (регистрационный № по CAS 477600752); темсиролимус (NSC 683864; регистрационный № по CAS 163635043); траметиниб (регистрационный № по CAS 871700173); вандетаниб (регистрационный № по CAS 443913733); вемурафениб (регистрационный № по CAS 918504651); SU6656 (регистрационный № по CAS 330161870); CEP-701 (лесауртиниб) (регистрационный № по CAS 111358884); XL019 (регистрационный № по CAS 945755566); PD-325901 (регистрационный № по CAS 391210109); PD-98059 (регистрационный № по CAS 167869218); АТФ-конкурирующие ингибиторы TORC1/TORC2, включая PI-103 (регистрационный № по CAS 371935749), PP242 (регистрационный № по CAS 1092351671), PP30 (регистрационный № по CAS 1092788094), торин 1 (регистрационный № по CAS 1222998368), LY294002 (регистрационный № по CAS 154447366), XL-147 (регистрационный № по CAS 934526893), CAL-120 (регистрационный № по CAS 870281348), ETP-45658 (регистрационный № по CAS 1198357797), PX 866 (регистрационный № по CAS 502632668), GDC-0941 (регистрационный № по CAS 957054307), BGT226 (регистрационный № по CAS 1245537681), BEZ235 (регистрационный № по CAS 915019657), XL-765 (регистрационный № по CAS 934493762).
Ингибиторы синтеза белка: акрифлавин (регистрационный № по CAS 65589700); амикацин (NSC 177001; регистрационный № по CAS 39831555); арбекацин (регистрационный № по CAS 51025855); астромицин (регистрационный № по CAS 55779061); азитромицин (NSC 643732; регистрационный № по CAS 83905015); беканамицин (регистрационный № по CAS 4696768); хлортетрациклин (NSC 13252; регистрационный № по CAS 64722); кларитромицин (NSC 643733; регистрационный № по CAS 81103119); клиндамицин (регистрационный № по CAS 18323449); кломоциклин (регистрационный № по CAS 1181540); циклогексимид (регистрационный № по CAS 66819); дактиномицин (NSC 3053; регистрационный № по CAS 50760); далфопристин (регистрационный № по CAS 112362502); демеклоциклин (регистрационный № по CAS 127333); дибекацин (регистрационный № по CAS 34493986); дигидрострептомицин (регистрационный № по CAS 128461); диритромицин (регистрационный № по CAS 62013041); доксициклин (регистрационный № по CAS 17086281); эметин (NSC 33669; регистрационный № по CAS 483181); эритромицин (NSC 55929; регистрационный № по CAS 114078); флуритромицин (регистрационный № по CAS 83664208); фрамицетин (неомицин B; регистрационный № по CAS 119040); гентамицин (NSC 82261; регистрационный № по CAS 1403663); глицилциклины, такие как тигециклин (регистрационный № по CAS 220620097); гигромицин B (регистрационный № по CAS 31282049); изепамицин (регистрационный № по CAS 67814760); джозамицин (NSC 122223; регистрационный № по CAS 16846245); канамицин (регистрационный № по CAS 8063078); кетолиды, такие как телитромицин (регистрационный № по CAS 191114484), цетромицин (регистрационный № по CAS 205110481) и солитромицин (регистрационный № по CAS 760981837); линкомицин (регистрационный № по CAS 154212); лимециклин (регистрационный № по CAS 992212); меклоциклин (NSC 78502; регистрационный № по CAS 2013583); метациклин (рондомицин; NSC 356463; регистрационный № по CAS 914001); мидекамицин (регистрационный № по CAS 35457808); миноциклин (NSC 141993; регистрационный № по CAS 10118908); миокамицин (регистрационный № по CAS 55881077); неомицин (регистрационный № по CAS 119040); нетилмицин (регистрационный № по CAS 56391561); олеандомицин (регистрационный № по CAS 3922905); оксазолидиноны, такие как эперезолид (регистрационный № по CAS 165800044), линезолид (регистрационный № по CAS 165800033), посизолид (регистрационный № по CAS 252260029), радезолид (регистрационный № по CAS 869884786), ранбезолид (регистрационный № по CAS 392659380), сутезолид (регистрационный № по CAS 168828588), тедизолид (регистрационный № по CAS 856867555); окситетрациклин (NSC 9169; регистрационный № по CAS 2058460); паромомицин (регистрационный № по CAS 7542372); пенимепициклин (регистрационный № по CAS 4599604); ингибиторы пептидилтрансферазы, например, хлорамфеникол (NSC 3069; регистрационный № по CAS 56757) и его производные, такие как азидамфеникол (регистрационный № по CAS 13838089), флорфеникол (регистрационный № по CAS 73231342) и тиамфеникол (регистрационный № по CAS 15318453), а также плевромутилины, такие как ретапамулин (регистрационный № по CAS 224452668), тиамулин (регистрационный № по CAS 55297955), вальнемулин (регистрационный № по CAS 101312929); пирлимицин (регистрационный № по CAS 79548735); пуромицин (NSC 3055; регистрационный № по CAS 53792); хинупристин (регистрационный № по CAS 120138503); рибостамицин (регистрационный № по CAS 53797356); рокитaмицин (регистрационный № по CAS 74014510); ролитетрациклин (регистрационный № по CAS 751973); рокситромицин (регистрационный № по CAS 80214831); сизомицин (регистрационный № по CAS 32385118); спектиномицин (регистрационный № по CAS 1695778); спирамицин (регистрационный № по CAS 8025818); стрептограмины, такие как пристинамицин (регистрационный № по CAS 270076603), хинупристин/далфопристин (регистрационный № по CAS 126602899) и виргиниамицин (регистрационный № по CAS 11006761); стрептомицин (регистрационный № по CAS 57921); тетрациклин (NSC 108579; регистрационный № по CAS 60548); тобрамицин (регистрационный № по CAS 32986564); тролеандомицин (регистрационный № по CAS 2751099); тилозин (регистрационный № по CAS 1401690); вердамицин (регистрационный № по CAS 49863481).
Ингибиторы деацетилаз гистонов: абексиностат (регистрационный № по CAS 783355602); белиностат (NSC 726630; регистрационный № по CAS 414864009); чидамид (регистрационный № по CAS 743420022); энтиностат (регистрационный № по CAS 209783802); гивиностат (регистрационный № по CAS 732302997); моцетиностат (регистрационный № по CAS 726169739); панобиностат (регистрационный № по CAS 404950807); квизиностат (регистрационный № по CAS 875320299); резминостат (регистрационный № по CAS 864814880); ромидепсин (регистрационный № по CAS 128517077); сульфорафан (регистрационный № по CAS 4478937); тиоуреидобутиронитрил (Kevetrin™; регистрационный № по CAS 6659890); вальпроевая кислота (NSC 93819; регистрационный № по CAS 99661); вориностат (NSC 701852; регистрационный № по CAS 149647789); ACY-1215 (роцилиностат; регистрационный № по CAS 1316214524); CUDC-101 (регистрационный № по CAS 1012054599); CHR-2845 (тефиностат; регистрационный № по CAS 914382608); CHR-3996 (регистрационный № по CAS 1235859138); 4SC-202 (регистрационный № по CAS 910462430); CG200745 (регистрационный № по CAS 936221339); SB939 (прациностат; регистрационный № по CAS 929016966).
Ингибиторы митохондрий: панкратистатин (NSC 349156; регистрационный № по CAS 96281311); родамин-123 (регистрационный № по CAS 63669709); эдельфозин (NSC 324368; регистрационный № по CAS 70641519); сукцинат d-альфа-токоферола (NSC 173849; регистрационный № по CAS 4345033); соединение 11β (регистрационный № по CAS 865070377); аспирин (NSC 406186; регистрационный № по CAS 50782); эллиптицин (регистрационный № по CAS 519233); берберин (регистрационный № по CAS 633658); церуленин (регистрационный № по CAS 17397896); GX015-070 (Obatoclax®; 2-(2-((3,5-диметил-1H-пиррол-2-ил)метилен)-3-метокси-2H-пиррол-5-ил)-1H-индол; NSC 729280; регистрационный № по CAS 803712676); целастрол (триптерин; регистрационный № по CAS 34157830); метформин (NSC 91485; регистрационный № по CAS 1115704); бриллиантовый зеленый (NSC 5011; регистрационный № по CAS 633034); ME-344 (регистрационный № по CAS 1374524556).
Антимитотические средства: аллоколхицин (NSC 406042); ауристатины, такие как MMAE (монометилауристатин E; регистрационный № по CAS 474645-27-7) и MMAF (монометилауристатин F; регистрационный № по CAS 745017-94-1; галихондрин B (NSC 609395); колхицин (NSC 757; регистрационный № по CAS 64868); производное колхицина (N-бензоилдеацетилбензамид; NSC 33410; регистрационный № по CAS 63989753); доластатин 10 (NSC 376128; регистрационный № по CAS 110417-88-4); майтанзин (NSC 153858; регистрационный № по CAS 35846-53-8); розоксин (NSC 332598; регистрационный № по CAS 90996546); таксол (NSC 125973; регистрационный № по CAS 33069624); производное таксола (2'-N-[3-(диметиламино)пропил]глутарамат таксола; NSC 608832); тиоколхицин (3-деметилтиоколхицин; NSC 361792); тритилцистеин (NSC 49842; регистрационный № по CAS 2799077); сульфат винбластина (NSC 49842; регистрационный № по CAS 143679); сульфат винкристина (NSC 67574; регистрационный № по CAS 2068782).
Любое из этих средств, которые содержат или которые могут быть модифицированы таким образом, чтобы они содержали сайт прикрепления к BCMA-связывающей молекуле, может быть включено в ADC, раскрытые в данном документе.
В одном варианте осуществления цитотоксическое и/или цитостатическое средство представляет собой антимитотическое средство.
В другом варианте осуществления цитотоксическое и/или цитостатическое средство представляет собой ауристатин, например, монометилауристатин E ("MMAE") или монометилауристатин F ("MMAF").
7.9.2. Линкеры для ADC
В ADC по настоящему изобретению цитотоксические и/или цитостатические средства связаны с BCMA-связывающей молекулой посредством линкеров для ADC. Линкер для ADC, связывающий цитотоксическое и/или цитостатическое средство с BCMA-связывающей молекулой в ADC, может быть коротким, длинным, гидрофобным, гидрофильным, гибким или жестким или может состоять из сегментов, каждый из которых независимо обладает одним или несколькими из вышеуказанных свойств, так что линкер может содержать сегменты, обладающие различными свойствами. Линкеры могут быть поливалентными, так что они ковалентно связывают более одного средства с одним сайтом в BCMA-связывающей молекуле, или моновалентными, так что они ковалентно связывают одно средство с одним сайтом в BCMA-связывающей молекуле.
Как будет понятно специалисту в данной области техники, линкеры для ADC связывают цитотоксические и/или цитостатические средства с BCMA-связывающей молекулой посредством образования ковалентной связи с цитотоксическим и/или цитостатическим средством в одном местоположении и ковалентной связи с BCMA-связывающей молекулой в другом. Ковалентные связи образуются посредством реакции между функциональными группами в линкере для ADC и функциональными группами в средствах и BCMA-связывающей молекуле. Используемое в данном документе выражение "линкер для ADC" предназначено для включения (i) неконъюгированных форм линкера для ADC, которые содержат функциональную группу, способную ковалентно связывать линкер для ADC с цитотоксическим и/или цитостатическим средством, и функциональную группу, способную ковалентно связывать линкер для ADC с BCMA-связывающей молекулой; (ii) частично конъюгированных форм линкера для ADC, которые содержат функциональную группу, способную ковалентно связывать линкер для ADC с BCMA-связывающей молекулой, и которые при этом являются ковалентно связанными с цитотоксическим и/или цитостатическим средством, или наоборот; и (iii) полностью конъюгированных форм линкера для ADC, которые являются ковалентно связанными как с цитотоксическим и/или цитостатическим средством, так и с BCMA-связывающей молекулой. В некоторых вариантах осуществления линкеров для ADC и ADC по настоящему изобретению, а также синтонов, применяемых для конъюгации линкеров, связанных со средствами, с BCMA-связывающими молекулами, фрагменты, содержащие функциональные группы в линкере для ADC, и ковалентные связи, образованные между линкером для ADC и BCMA-связывающей молекулой, конкретно проиллюстрированы в виде Rx и XY соответственно.
Линкеры для ADC могут являться, хотя и не обязательно должны, химически стабильными в условиях снаружи клетки и могут быть разработаны таким образом, чтобы они расщеплялись, разрушались и/или иным образом специфически деградировали внутри клетки. В качестве альтернативы можно применять линкеры для ADC, которые не разработаны таким образом, чтобы они специфически расщеплялись или деградировали внутри клетки. Выбор стабильного или нестабильного линкера для ADC может зависеть от токсичности цитотоксического и/или цитостатического средства. В случае со средствами, которые являются токсичными для нормальных клеток, можно применять стабильные линкеры. Можно использовать средства, которые являются селективными или нацеливающимися и характеризуются низкой токсичностью в отношении нормальных клеток, при этом химическая стабильность линкера для ADC во внеклеточной среде является менее важной. Известно большое разнообразие линкеров для ADC, применимых для связывания лекарственных средств с BCMA-связывающими молекулами в качестве составной части ADC. Любой из этих линкеров для ADC, а также другие линкеры для ADC можно применять для связывания цитотоксических и/или цитостатических средств с BCMA-связывающей молекулой в ADC по настоящему изобретению.
Иллюстративные поливалентные линкеры для ADC, которые можно применять для связывания множества цитотоксических и/или цитостатических средств с одной BCMA-связывающей молекулой, описаны, например, в WO 2009/073445; WO 2010/068795; WO 2010/138719; WO 2011/120053; WO 2011/171020; WO 2013/096901; WO 2014/008375; WO 2014/093379; WO 2014/093394; WO 2014/093640. Например, технология линкеров Fleximer, разработанная Mersana et al., обладает потенциалом в отношении обеспечения получения ADC с высоким DAR и хорошими физико-химическими свойствами. Как показано ниже, технология от Mersana основана на включении молекул лекарственного средства в солюбилизирующий полиацетальный каркас с помощью последовательности сложноэфирных связей. Данная методика обеспечивает получение ADC с высокой нагрузкой (до 20 DAR) при сохранении в то же время хороших физико-химических свойств.
Дополнительные примеры линкеров дендритного типа можно найти в US 2006/116422; US 2005/271615; de Groot et al., 2003, Angew. Chem. Int. Ed. 42:4490-4494; Amir et al., 2003, Angew. Chem. Int. Ed. 42:4494-4499; Shamis et al., 2004, J. Am. Chem. Soc. 126:1726-1731; Sun et al., 2002, Bioorganic & Medicinal Chemistry Letters 12:2213-2215; Sun et al., 2003, Bioorganic & Medicinal Chemistry 11:1761-1768; King et al., 2002, Tetrahedron Letters 43:1987-1990.
Иллюстративные моновалентные линкеры для ADC, которые можно применять, описаны, например, в Nolting, 2013, Antibody-Drug Conjugates, Methods in Molecular Biology 1045:71-100; Kitson et al., 2013, CROs-MOs--Chemica-ggi--Chemistry Today 31(4):30-38; Ducry et al., 2010, Bioconjugate Chem. 21:5-13; Zhao et al., 2011, J. Med. Chem. 54:3606-3623; патенте США № 7223837; патенте США № 8568728; патенте США № 8535678 и WO2004010957.
В качестве примера и без ограничения некоторые расщепляемые и нерасщепляемые линкеры для ADC, которые могут быть включены в ADC, описаны ниже.
7.9.2.1. Расщепляемые линкеры для ADC
В определенных вариантах осуществления выбранный линкер для ADC является расщепляемым in vivo. Расщепляемые линкеры для ADC могут содержать химически или ферментативно нестабильные или деградируемые связи. В случае с расщепляемыми линкерами для ADC высвобождение лекарственного средства обычно зависит от процессов внутри клетки, таких как восстановление в цитоплазме, воздействие кислых условий в лизосоме или расщепление посредством специфичных протеаз или других ферментов в клетке. Расщепляемые линкеры для ADC обычно содержат одну или несколько химических связей, которые являются химически либо ферментативно расщепляемыми, тогда как остальная часть линкера для ADC является нерасщепляемой. В определенных вариантах осуществления линкер для ADC содержит химически неустойчивую группу, такую как гидразоновые и/или дисульфидные группы. В линкерах, содержащих химически неустойчивые группы, используются различия в свойствах между плазмой крови и некоторыми цитоплазматическими компартментами. Внутриклеточные условия, содействующие высвобождению лекарственного средства гидразонсодержащими линкерами для ADC, представляют собой кислую среду эндосом и лизосом, тогда как дисульфидсодержащие линкеры для ADC восстанавливаются в цитозоле, который содержит высокие концентрации тиолов, например, глутатиона. В определенных вариантах осуществления стабильность линкера для ADC, содержащего химически неустойчивую группу, в плазме крови можно увеличить посредством введения стерического несоответствия с использованием заместителей вблизи химически неустойчивой группы.
Кислотонеустойчивые группы, такие как гидразоновые, остаются интактными в ходе системного кровообращения в среде крови с нейтральным pH (pH 7,3-7,5) и подвергаются гидролизу и высвобождают лекарственное средство после интернализации ADC в слабокислые эндосомальные (pH 5,0-6,5) и лизосомальные (pH 4,5-5,0) компартменты клетки. Было показано, что данный pH-зависимый механизм высвобождения связан с неспецифическим высвобождением лекарственного средства. Для повышения стабильности гидразоновой группы линкера для ADC линкер для ADC можно изменять посредством химической модификации, например, замещения, что обеспечивает возможность перестраивания для достижения более эффективного высвобождения в лизосоме с минимизированными потерями в кровотоке.
Гидразон-содержащие линкеры для ADC могут содержать дополнительные сайты расщепления, такие как дополнительные кислотонеустойчивые сайты расщепления и/или ферментативно неустойчивые сайты расщепления. ADC, содержащие иллюстративные гидразонсодержащие линкеры для ADC, включают следующие структуры:
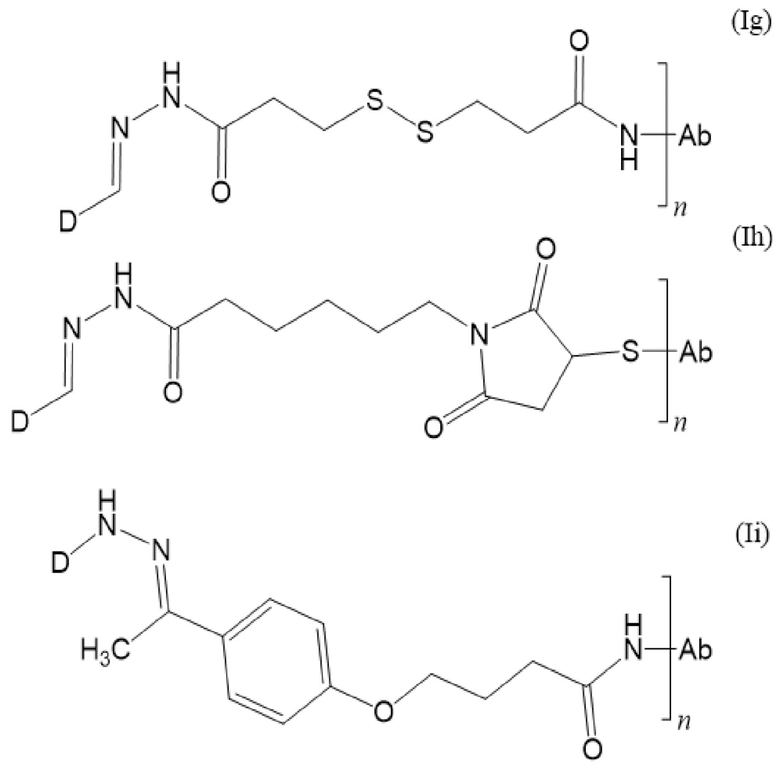
где D и Ab представляют собой цитотоксическое и/или цитостатическое средство (лекарственное средство) и Ab соответственно, и n представляет собой количество линкеров для ADC с лекарственным средством, связанных с BCMA-связывающей молекулой. В определенных линкерах для ADC, таких как линкер (Ig), линкер для ADC содержит две расщепляемые группы - дисульфидный и гидразоновый фрагменты. В случае с такими линкерами для ADC для эффективного высвобождения немодифицированного лекарственного средства в свободной форме требуется кислое значение pH или восстановление дисульфида и кислое значение pH. Было показано, что такие линкеры, как (Ih) и (Ii), являются эффективными с одним гидразоновым сайтом расщепления.
Дополнительные линкеры для ADC, которые остаются интактными в ходе системного кровообращения и подвергаются гидролизу и высвобождают лекарственное средство, когда ADC интернализируется в кислые клеточные компартменты, содержат карбонаты. Такие линкеры для ADC могут быть применимыми в случаях, когда цитотоксическое и/или цитостатическое средство может быть ковалентно присоединено посредством атома кислорода.
Другие кислотонеустойчивые группы, которые могут быть включены в линкеры для ADC, включают цис-аконитил-содержащие линкеры для ADC. Химические свойства цис-аконитила обусловлены карбоновой кислотой, смежной с амидной связью, что обеспечивает ускорение гидролиза амидов в кислых условиях.
Расщепляемые линкеры для ADC могут также содержать дисульфидную группу. Дисульфиды являются термодинамически стабильными при физиологическом значении pH и разработаны таким образом, чтобы они высвобождали лекарственное средство при интернализации внутрь клеток, где цитозоль обеспечивает в значительной степени более восстановительную среду по сравнению с внеклеточной средой. Для разрыва дисульфидных связей обычно требуется присутствие цитоплазматического тиольного кофактора, такого как (восстановленный) глутатион (GSH), так что дисульфидсодержащие линкеры для ADC являются довольно стабильными в кровотоке, избирательно высвобождая лекарственное средство в цитозоле. Внутриклеточный белок-фермент дисульфидизомераза или подобные ферменты, способные расщеплять дисульфидные связи, могут также способствовать предпочтительному расщеплению дисульфидных связей внутри клеток. Сообщалось, что GSH присутствует в клетках в диапазоне концентраций 0,5-10 мМ по сравнению со в значительной степени более низкой концентрацией GSH или цистеина, наиболее широко распространенного низкомолекулярного тиола, в кровотоке при примерно 5 опухолевых клетках, при этом нарушенный ток крови приводит к состоянию гипоксии, в результате чего повышается активность восстановительных ферментов и, следовательно, еще больше возрастают концентрации глутатиона. В определенных вариантах осуществления стабильность дисульфидсодержащего линкера для ADC in vivo можно повысить посредством химической модификации линкера для ADC, например, посредством применения стерического несоответствия рядом с дисульфидной связью.
ADC, содержащие иллюстративные дисульфидсодержащие линкеры для ADC, включают следующие структуры:
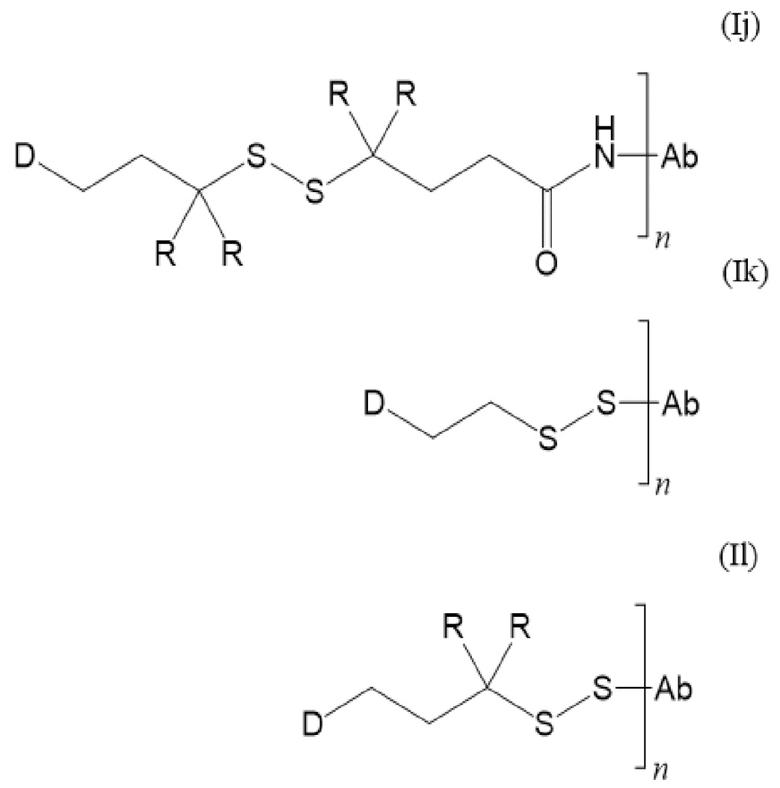
где D и Ab представляют собой лекарственное средство и BCMA-связывающую молекулу соответственно, при этом n представляет собой количество линкеров для ADC с лекарственным средством, связанных с BCMA-связывающей молекулой, и R в каждом случае независимо выбран, например, из водорода или алкила. В определенных вариантах осуществления увеличение стерического несоответствия рядом с дисульфидной связью приводит к увеличению стабильности линкера для ADC. Структуры, такие как (Ij) и (Il), демонстрируют увеличенную стабильность in vivo, если одна или несколько групп R выбраны из низшего алкила, такого как метил.
Другой тип расщепляемого линкера для ADC, который можно применять, представляет собой линкер для ADC, который специфически расщепляется ферментом. Такие линкеры для ADC, как правило, представляют собой линкеры на основе пептидов или содержат пептидные участки, которые выступают в качестве субстратов для ферментов. Линкеры для ADC на основе пептидов оказываются более стабильными в плазме крови и внеклеточной среде, чем химически неустойчивые линкеры для ADC. Пептидные связи обычно характеризуются хорошей стабильностью в сыворотке крови, поскольку лизосомальные протеолитические ферменты обладают очень низкой активностью в крови вследствие наличия эндогенных ингибиторов и неблагоприятно высокого значения pH крови по сравнению с лизосомами. Высвобождение лекарственного средства из BCMA-связывающей молекулы происходит специфически благодаря действию лизосомальных протеаз, например, катепсина и плазмина. Эти протеазы могут присутствовать на повышенных уровнях в определенных опухолевых клетках.
В иллюстративных вариантах осуществления расщепляемый пептид выбран из тетрапептидов, таких как Gly-Phe-Leu-Gly (SEQ ID NO:512), Ala-Leu-Ala-Leu (SEQ ID NO:513) или дипептидов, таких как Val-Cit, Val-Ala, Met-(D)Lys, Asn-(D)Lys, Val-(D)Asp, Phe-Lys, Ile-Val, Asp-Val, His-Val, NorVal-(D)Asp, Ala-(D)Asp 5, Met-Lys, Asn-Lys, Ile-Pro, Me3Lys-Pro, PhenylGly-(D)Lys, Met-(D)Lys, Asn-(D)Lys, Pro-(D)Lys, Met-(D)Lys, Asn-(D)Lys, AM Met-(D)Lys, Asn-(D)Lys, AW Met-(D)Lys и Asn-(D)Lys. В определенных вариантах осуществления дипептиды могут быть выбраны вместо более длинных полипептидов вследствие гидрофобности более длинных пептидов.
Были описаны разнообразные расщепляемые линкеры для ADC на основе дипептидов, применимые для связывания лекарственных средств, таких как доксорубицин, митомицин, камптотецин, пирролобензодиазепин, таллизомицин и ауристатин/представители семейства ауристатинов, с BCMA-связывающими молекулами (см. Dubowchik et al., 1998, J. Org. Chem. 67:1866-1872; Dubowchik et al., 1998, Bioorg. Med. Chem. Lett. 8(21):3341-3346; Walker et al., 2002, Bioorg. Med. Chem. Lett. 12:217-219; Walker et al., 2004, Bioorg. Med. Chem. Lett. 14:4323-4327; Sutherland et al., 2013, Blood 122: 1455-1463; и Francisco et al., 2003, Blood 102:1458-1465). Все эти дипептидные линкеры для ADC или модифицированные варианты этих дипептидных линкеров для ADC можно применять в ADC по настоящему изобретению. Другие дипептидные линкеры для ADC, которые можно применять, включают линкеры, которые можно найти в ADC, таких как брентуксимаб-вендотин SGN-35 от Seattle Genetics (Adcetris™), SGN-75 от Seattle Genetics (антитело к CD-70, Val-Cit-монометилауристатин F (MMAF)), SGN-CD33A от Seattle Genetics (антитело к CD-33, Val-Ala-(SGD-1882)), глембатумумаб от Celldex Therapeutics (CDX-011) (антитело к NMB, Val-Cit-монометилауристатин E (MMAE)) и PSMA-ADC от Cytogen (PSMA-ADC-1301) (антитело к PSMA, Val-Cit-MMAE).
Ферментативно расщепляемые линкеры для ADC могут содержать саморазлагающийся спейсер для пространственного отделения лекарственного средства от сайта ферментативного расщепления. Прямое присоединение лекарственного средства к пептидному линкеру для ADC может в результате приводить к протеолитическому высвобождению аддукта лекарственного средства с аминокислотой, в результате чего, таким образом, ухудшается его активность. Применение саморазлагающегося спейсера обеспечивает возможность элиминирования полностью активного химически немодифицированного лекарственного средства при гидролизе амидных связей.
Один саморазлагающийся спейсер представляет собой бифункциональную группу пара-аминобензилового спирта, которая связана с пептидом посредством аминогруппы, образуя амидную связь, при этом аминосодержащие лекарственные средства могут быть присоединены посредством карбаматных функциональных групп к бензильной гидроксильной группе линкера для ADC (PABC). Полученные в результате пролекарства активируются при расщеплении, опосредованном протеазой, что приводит к реакции 1,6-элиминирования с высвобождением немодифицированного лекарственного средства, диоксида углерода и остатков линкерной группы для ADC. На следующей схеме изображены фрагментация п-амидобензилового эфира и высвобождение лекарственного средства:
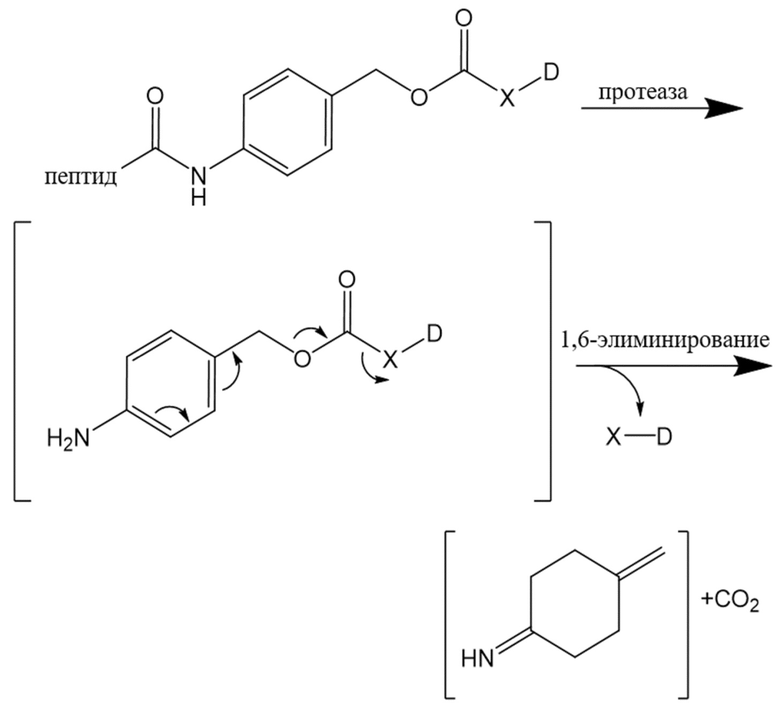
где X-D представляет немодифицированное лекарственное средство.
Гетероциклические варианты данной саморазлагающейся группы также были описаны. См., например, патент США № 7989434.
В некоторых вариантах осуществления ферментативно расщепляемый линкер для ADC представляет собой линкер для ADC на основе β-глюкуроновой кислоты. Легкое высвобождение лекарственного средства можно реализовать посредством расщепления гликозидной связи β-глюкуронида с помощью лизосомального фермента β-глюкуронидазы. Данный фермент в большом количестве присутствует внутри лизосом и сверхэкспрессируется в некоторых типах опухолей, хотя активность фермента снаружи клеток является низкой. Для предотвращения склонности ADC подвергаться агрегации из-за гидрофильной природы β-глюкуронидов можно применять линкеры для ADC на основе β-глюкуроновой кислоты. В некоторых вариантах осуществления линкеры для ADC на основе β-глюкуроновой кислоты можно применять в качестве линкеров для ADC в ADC, связанных с гидрофобными лекарственными средствами. На следующей схеме изображены высвобождение лекарственного средства из линкера для ADC на основе β-глюкуроновой кислоты и ADC, содержащий данный линкер:
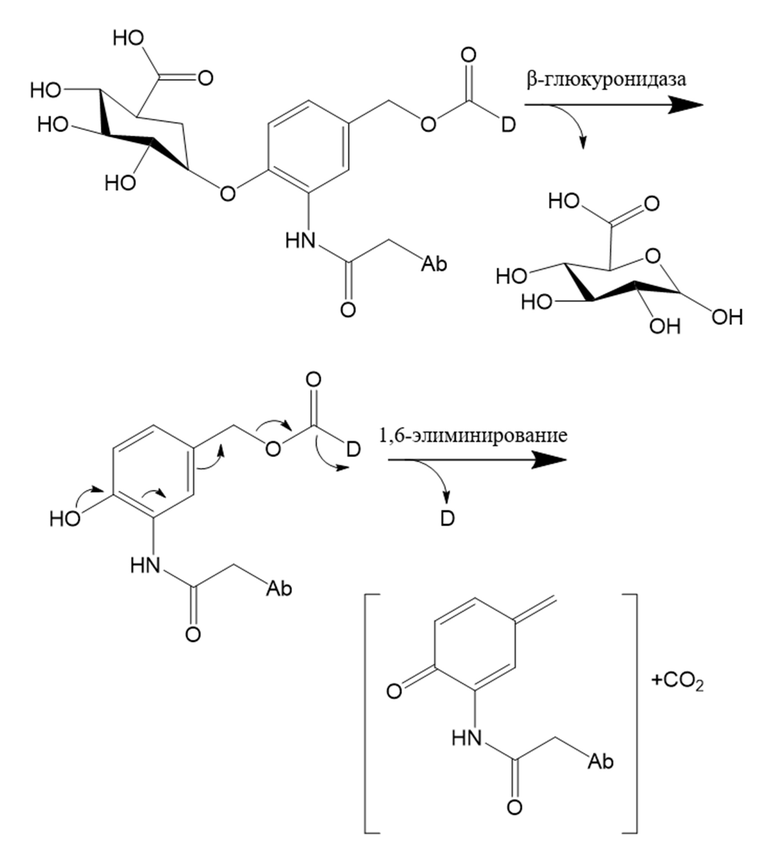
Были описаны разнообразные расщепляемые линкеры для ADC на основе β-глюкуроновой кислоты, применимые для связывания лекарственных средств, таких как аналоги ауристатинов, камптотецина и доксорубицина, средства на основе CBI, связывающиеся с малой бороздкой, и псимберин, с BCMA-связывающими молекулами (см. Nolting, Chapter 5 "Linker Technology in Antibody-Drug Conjugates", в Antibody-Drug Conjugates: Methods in Molecular Biology, vol. 1045, pp. 71-100, Laurent Ducry (Ed.), Springer Science & Business Medica, LLC, 2013; Jeffrey et al., 2006, Bioconjug. Chem. 17:831-840; Jeffrey et al., 2007, Bioorg. Med. Chem. Lett. 17:2278-2280; и Jiang et al., 2005, J. Am. Chem. Soc. 127:11254-11255). Все эти линкеры для ADC на основе β-глюкуроновой кислоты можно применять в ADC по настоящему изобретению.
Кроме того, цитотоксические и/или цитостатические средства, содержащие фенольную группу, могут быть ковалентно связаны с линкером для ADC посредством фенольного атома кислорода. Использование одного такого линкера для ADC, описанного в WO 2007/089149, основывается на методике, в которой диаминоэтан "SpaceLink" применяют совместно с традиционными саморазлагающимися группами на основе "PABO" для доставки фенолов. Расщепление линкера для ADC схематически изображено ниже, где D представляет собой цитотоксическое и/или цитостатическое средство, содержащее фенольную гидроксильную группу.
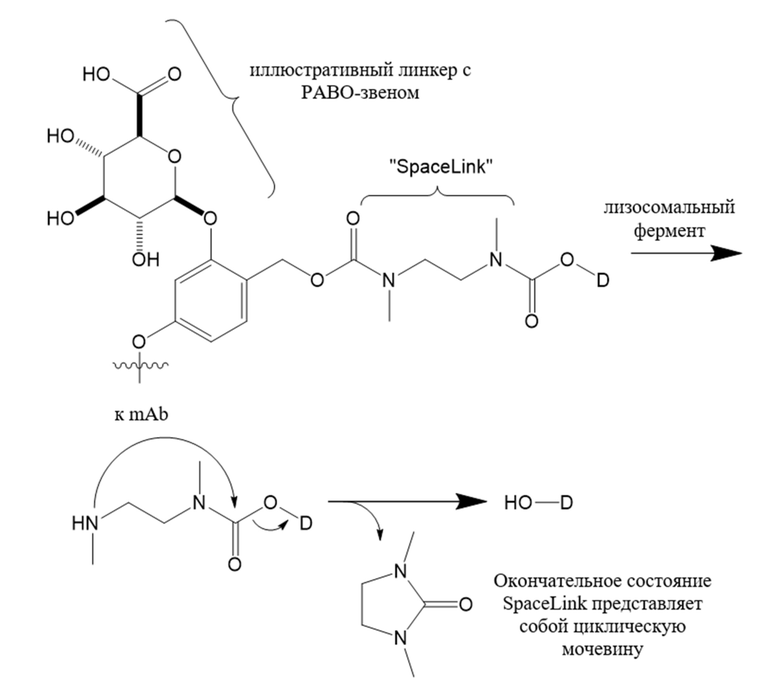
Расщепляемые линкеры для ADC могут содержать нерасщепляемые части или сегменты, и/или расщепляемые сегменты или части могут быть включены в линкер для ADC, в ином случае являющийся нерасщепляемым, чтобы сделать его расщепляемым. Исключительно в качестве примера, полиэтиленгликоль (PEG) и родственные полимеры могут содержать расщепляемые группы в полимерном остове. Например, линкер для ADC на основе полиэтиленгликоля или полимера может содержать одну или несколько расщепляемых групп, таких как дисульфид, гидразон или дипептид.
Другие деградируемые связи, которые могут быть включены в линкеры для ADC, включают сложноэфирные связи, образующиеся посредством реакции PEG, функционализированного группами карбоновых кислот, или PEG, функционализированного активированными группами карбоновых кислот, со спиртовыми группами в биологически активном средстве, где такие сложноэфирные группы обычно гидролизуются при физиологических условиях с высвобождением биологически активного средства. Гидролитически деградируемые связи включают без ограничения карбонатные связи; иминные связи, образующиеся в результате реакции амина и альдегида; фосфатные сложноэфирные связи, образующиеся посредством осуществления реакции спирта с фосфатной группой; ацетальные связи, которые представляют собой продукт реакции альдегида и спирта; ортоэфирные связи, которые представляют собой продукт реакции формиата и спирта; и олигонуклеотидные связи, образуемые фосфорамидитной группой, в том числе без ограничения на конце полимера, и 5'-гидроксильной группой олигонуклеотида.
В определенных вариантах осуществления линкер для ADC содержит ферментативно расщепляемый пептидный фрагмент, например, линкер для ADC, предусматривающий структурную формулу (IVa) или (IVb):
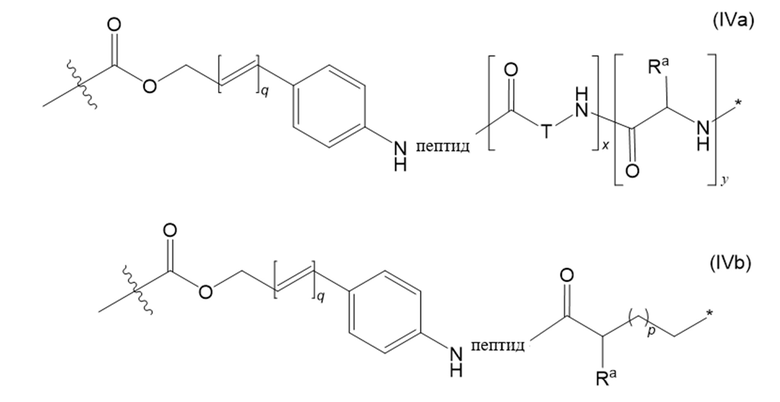
или его соль, где пептид представляет пептид (который проиллюстрирован в направлении C→N и в котором не показаны карбокси- и амино-"концы"), расщепляемый лизосомальным ферментом; T представляет полимер, содержащий одно или несколько этиленгликолевых звеньев или алкиленовую цепь или их комбинации; Ra выбран из водорода, алкила, сульфоната и метилсульфоната; p представляет собой целое число, находящееся в диапазоне от 0 до 5; q равняется 0 или 1; x равняется 0 или 1; y равняется 0 или 1;  представляет точку присоединения линкера для ADC к цитотоксическому и/или цитостатическому средству; и * представляет точку присоединения к остальной части линкера для ADC.
представляет точку присоединения линкера для ADC к цитотоксическому и/или цитостатическому средству; и * представляет точку присоединения к остальной части линкера для ADC.
В определенных вариантах осуществления пептид выбран из трипептида или дипептида. В конкретных вариантах осуществления дипептид выбран из: Val-Cit; Cit-Val; Ala-Ala; Ala-Cit; Cit-Ala; Asn-Cit; Cit-Asn; Cit-Cit; Val-Glu; Glu-Val; Ser-Cit; Cit-Ser; Lys-Cit; Cit-Lys; Asp-Cit; Cit-Asp; Ala-Val; Val-Ala; Phe-Lys; Val-Lys; Ala-Lys; Phe-Cit; Leu-Cit; Ile-Cit; Phe-Arg и Trp-Cit. В определенных вариантах осуществления дипептид выбран из: Cit-Val и Ala-Val.
Конкретные иллюстративные варианты осуществления линкеров для ADC в соответствии со структурной формулой (IVа), которые могут быть включены в ADC, включают линкеры для ADC, проиллюстрированные ниже (как проиллюстрировано, линкеры для ADC содержат группу, подходящую для ковалентного связывания линкера для ADC с BCMA-связывающей молекулой):
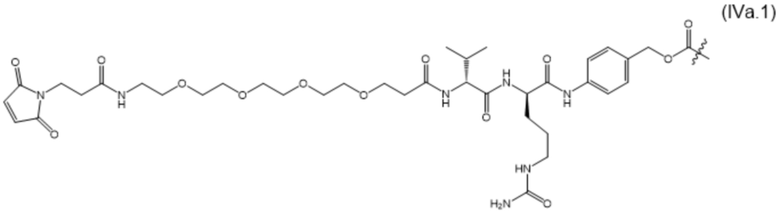
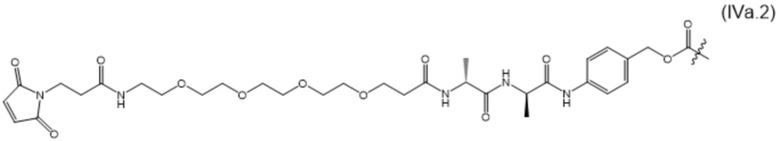
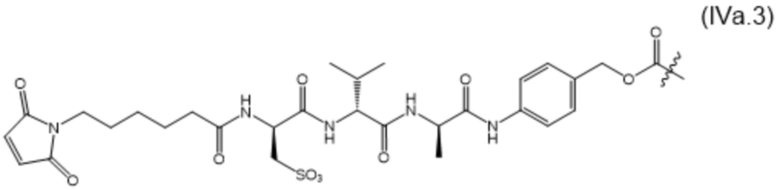

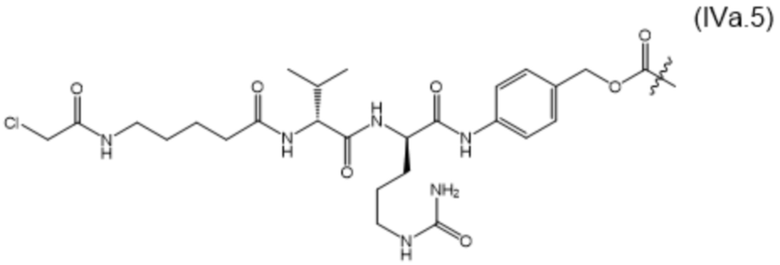
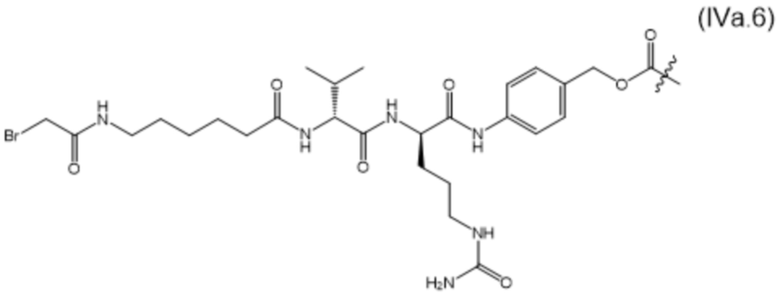
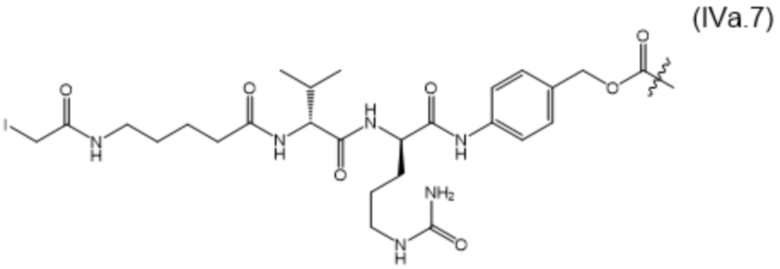
Конкретные иллюстративные варианты осуществления линкеров для ADC в соответствии со структурной формулой (IVb), которые могут быть включены в ADC, включают линкеры для ADC, проиллюстрированные ниже (как проиллюстрировано, линкеры для ADC содержат группу, подходящую для ковалентного связывания линкера для ADC с BCMA-связывающей молекулой):
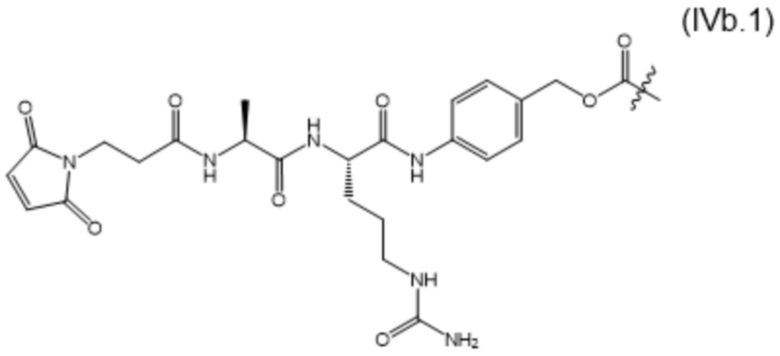
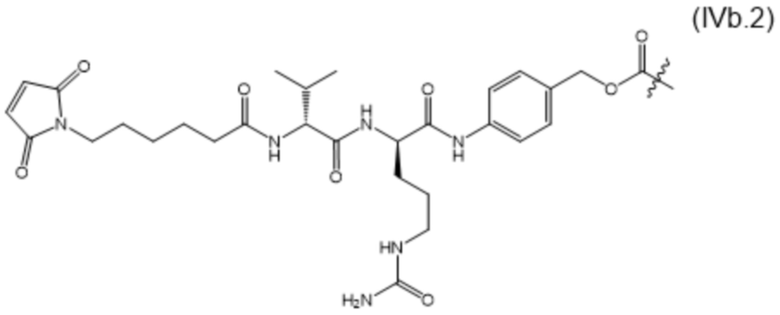
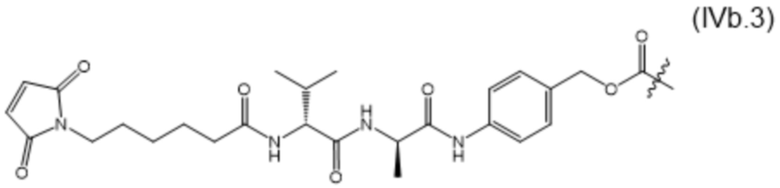
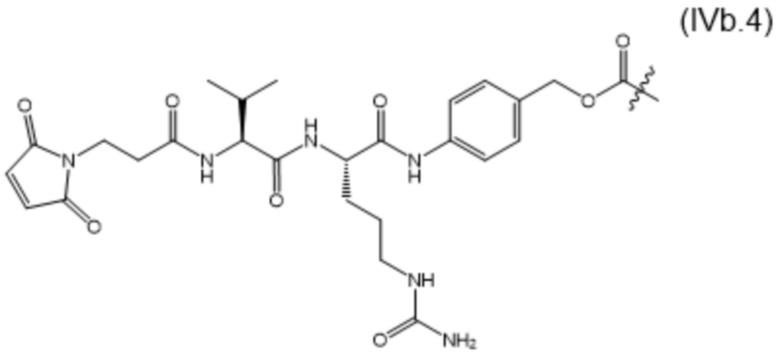
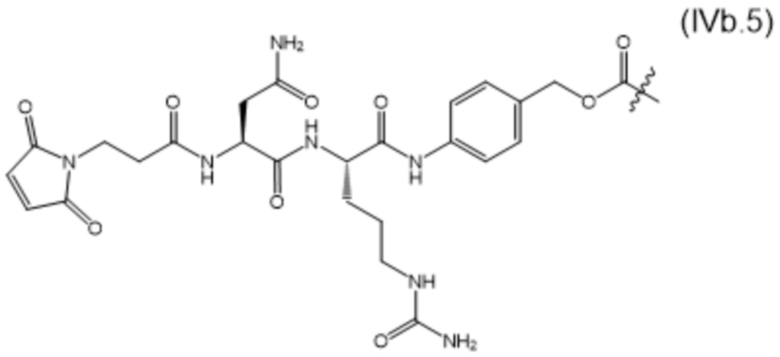
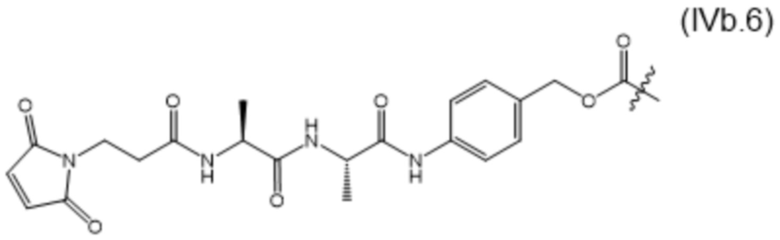
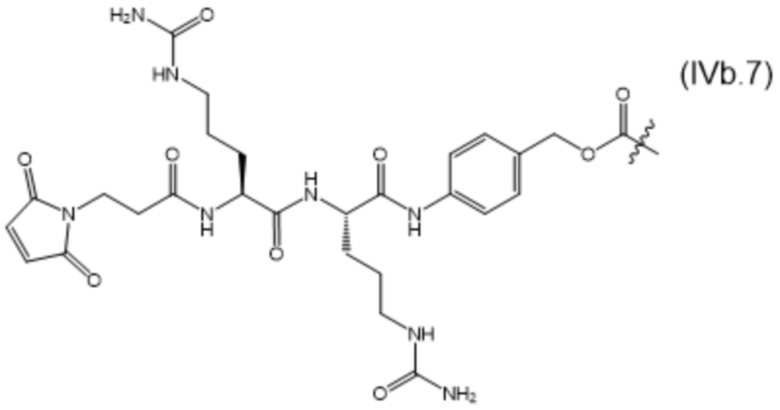
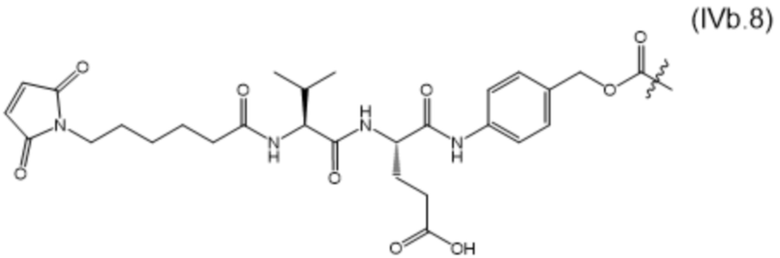
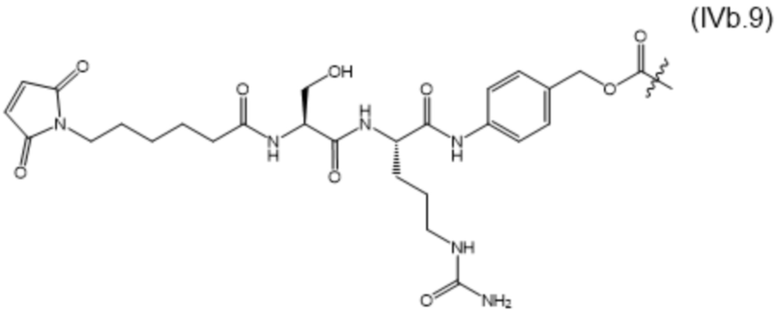
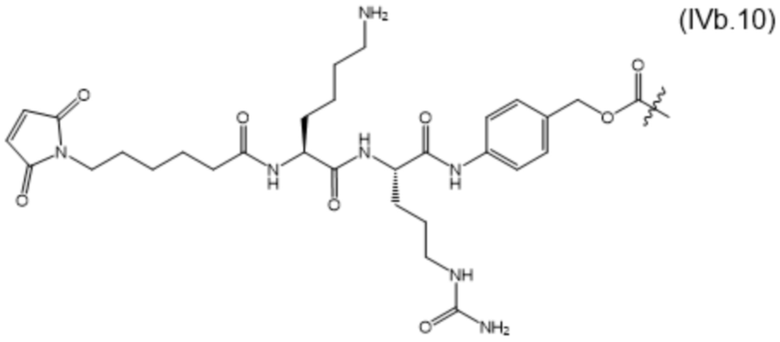
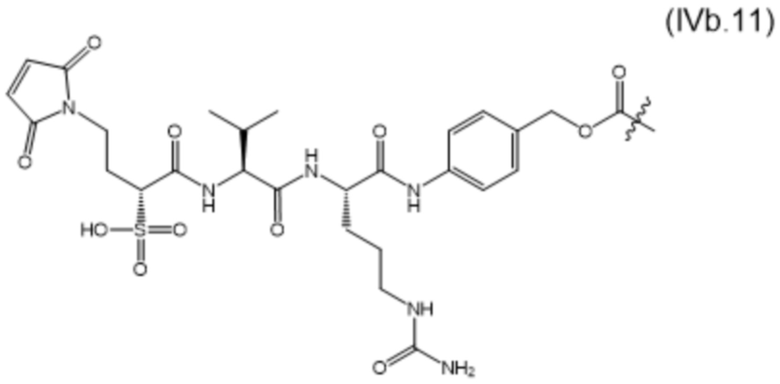
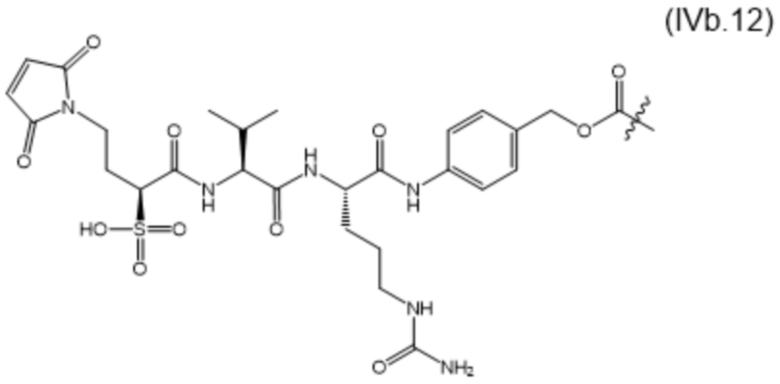
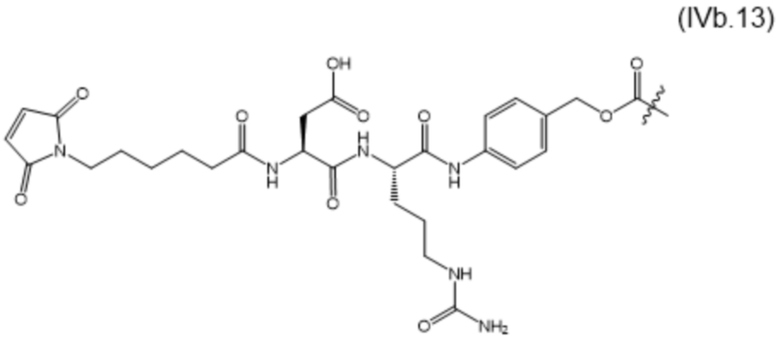
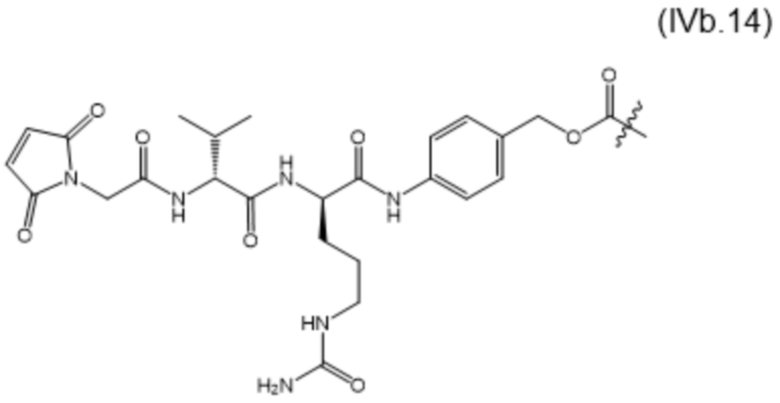
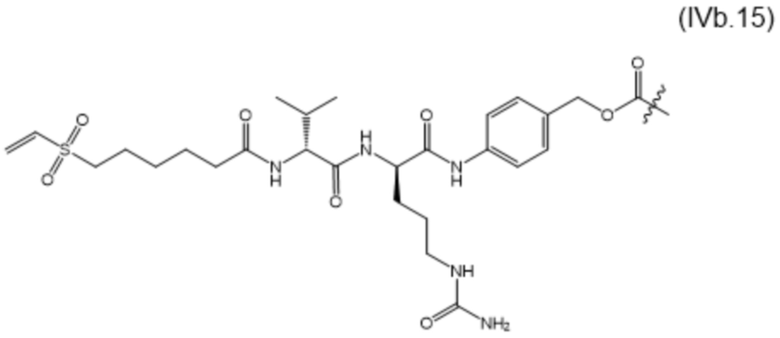
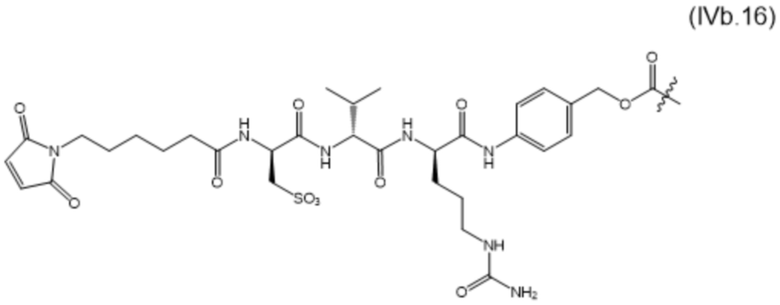
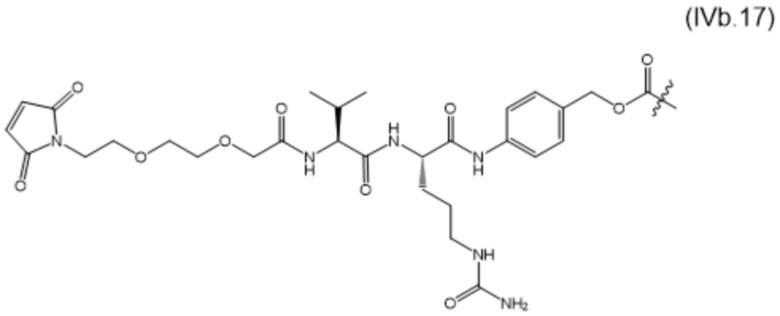
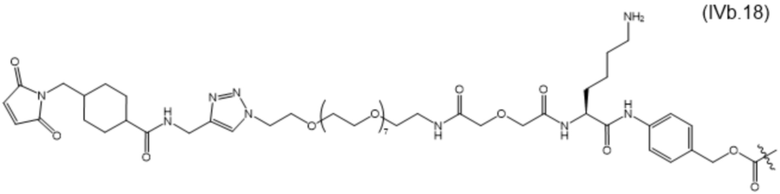
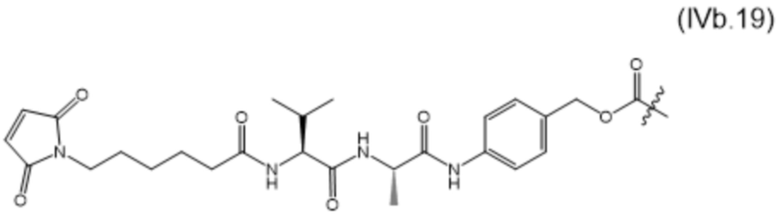
В определенных вариантах осуществления линкер для ADC содержит ферментативно расщепляемый пептидный фрагмент, например, линкер для ADC, предусматривающий структурную формулу (IVc) или (IVd):
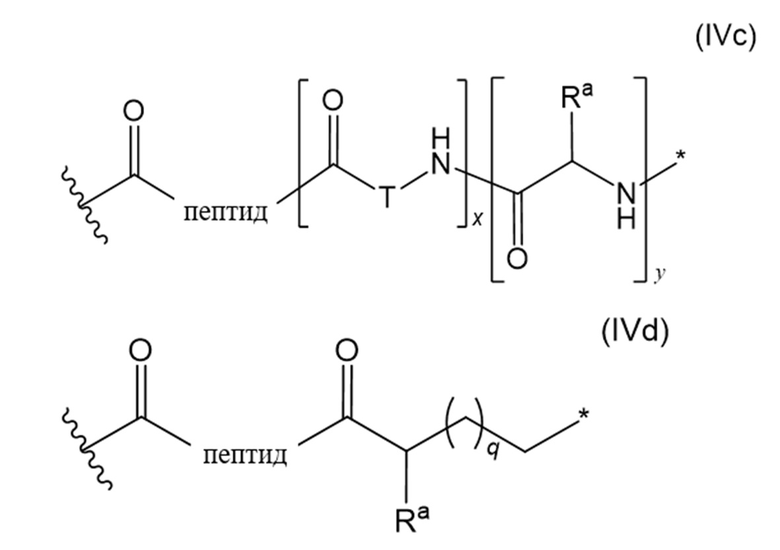
или его соль, где пептид представляет пептид (который проиллюстрирован в направлении C→N и в котором не показаны карбокси- и амино-"концы"), расщепляемый лизосомальным ферментом; T представляет полимер, содержащий одно или несколько этиленгликолевых звеньев или алкиленовую цепь или их комбинации; Ra выбран из водорода, алкила, сульфоната и метилсульфоната; p представляет собой целое число, находящееся в диапазоне от 0 до 5; q равняется 0 или 1; x равняется 0 или 1; y равняется 0 или 1;  x
x 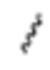 представляет точку присоединения линкера для ADC к цитотоксическому и/или цитостатическому средству; и * представляет точку присоединения к остальной части линкера для ADC.
представляет точку присоединения линкера для ADC к цитотоксическому и/или цитостатическому средству; и * представляет точку присоединения к остальной части линкера для ADC.
Конкретные иллюстративные варианты осуществления линкеров для ADC в соответствии со структурной формулой (IVc), которые могут быть включены в ADC, включают линкеры для ADC, проиллюстрированные ниже (как проиллюстрировано, линкеры для ADC содержат группу, подходящую для ковалентного связывания линкера для ADC с BCMA-связывающей молекулой):
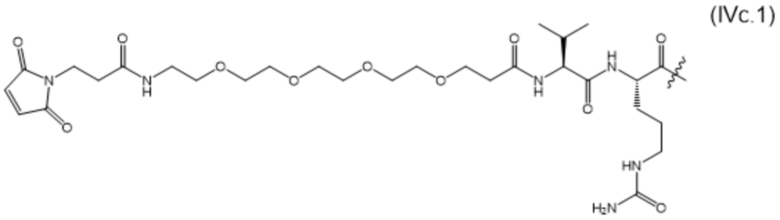
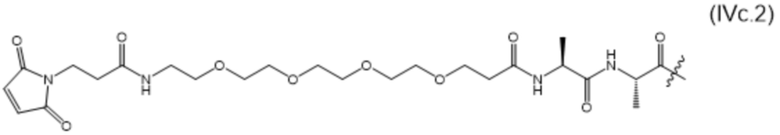
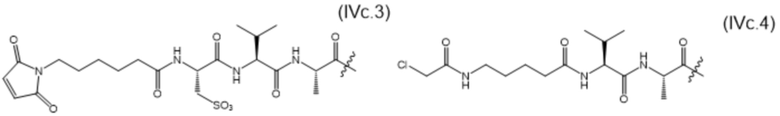
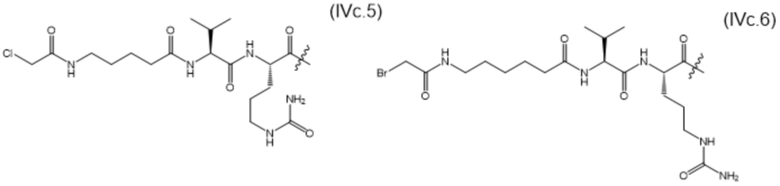
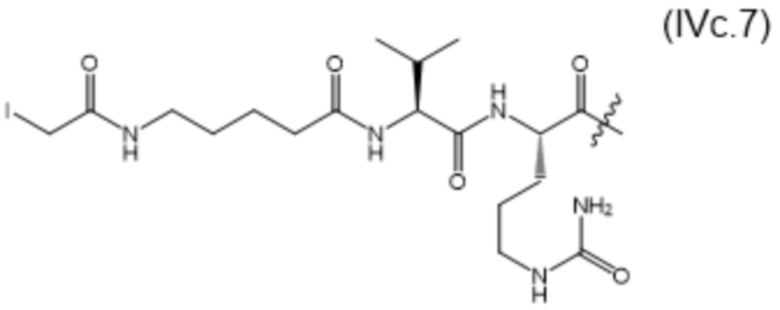
Конкретные иллюстративные варианты осуществления линкеров для ADC в соответствии со структурной формулой (IVd), которые могут быть включены в ADC, включают линкеры для ADC, проиллюстрированные ниже (как проиллюстрировано, линкеры для ADC содержат группу, подходящую для ковалентного связывания линкера для ADC с BCMA-связывающей молекулой):
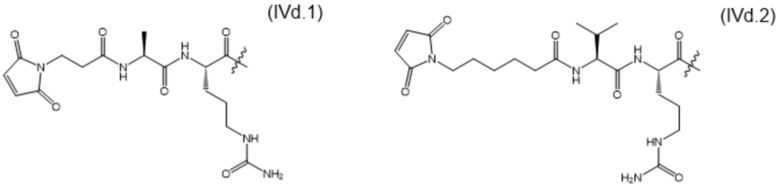
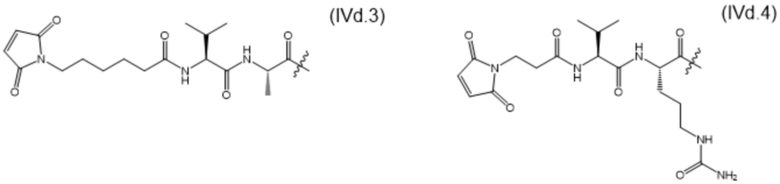
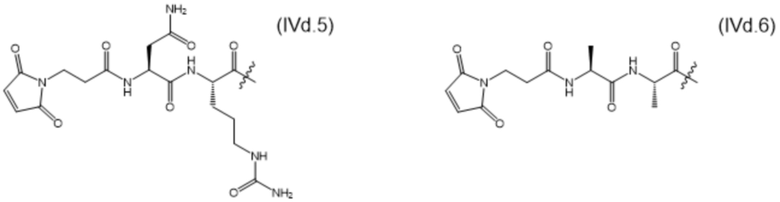
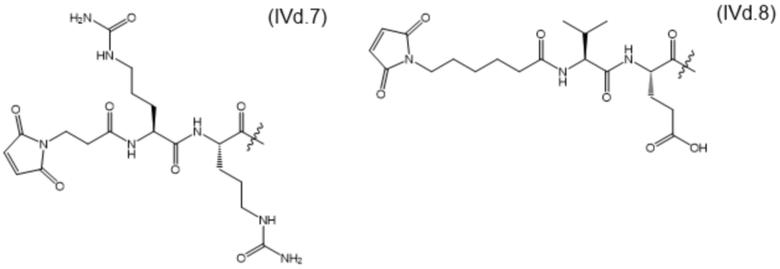
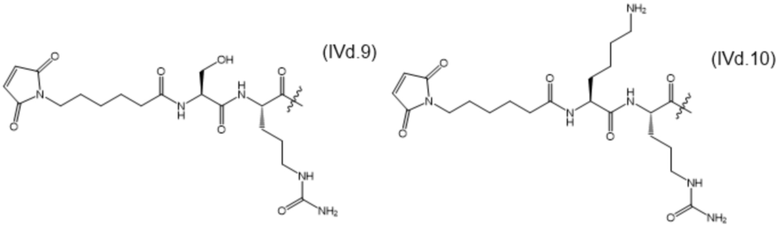
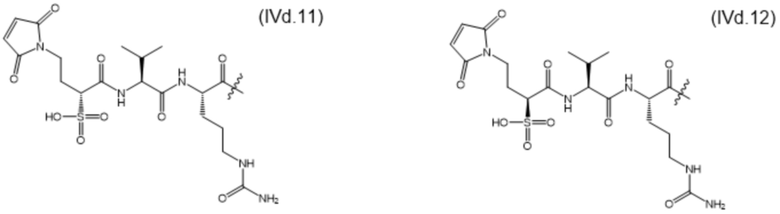
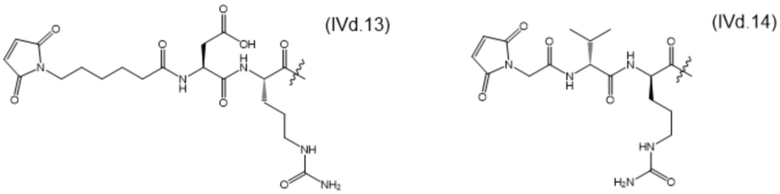
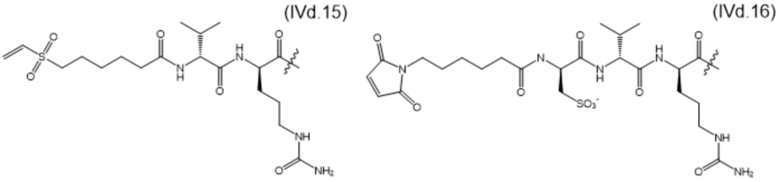
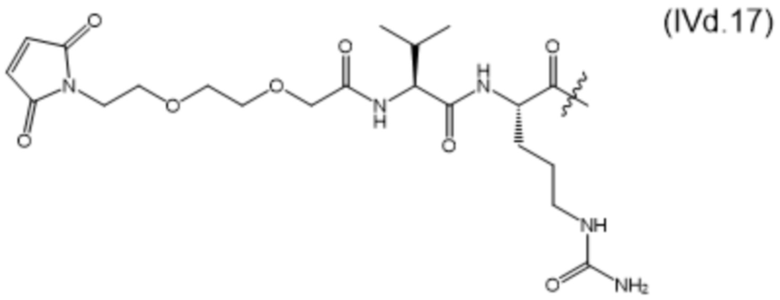
В определенных вариантах осуществления линкер для ADC, предусматривающий структурную формулу (IVa), (IVb), (IVc) или (IVd), дополнительно содержит карбонатный фрагмент, расщепляемый посредством воздействия кислой среды. В конкретных вариантах осуществления линкер для ADC присоединен к цитотоксическому и/или цитостатическому средству посредством атома кислорода.
7.9.2.2. Нерасщепляемые линкеры
Хотя расщепляемые линкеры для ADC могут обеспечивать определенные преимущества, линкеры для ADC, содержащие ADC, не обязательно должны быть расщепляемыми. В случае с нерасщепляемыми линкерами для ADC высвобождение лекарственного средства не зависит от различий в свойствах между плазмой крови и некоторыми цитоплазматическими компартментами. Высказано предположение, что высвобождение лекарственного средства происходит после интернализации ADC посредством антиген-опосредованного эндоцитоза и доставки в лизосомальный компартмент, где BCMA-связывающая молекула деградирует до уровня аминокислот посредством внутриклеточной протеолитической деградации. Данный способ обеспечивает высвобождение производного лекарственного средства, которое образовано лекарственным средством, линкером для ADC и аминокислотным остатком, к которому был ковалентно присоединен линкер для ADC. Аминокислотные метаболиты лекарственных средств из конъюгатов с нерасщепляемыми линкерами для ADC являются более гидрофильными и обычно характеризуются меньшей способностью к проникновению через мембраны, что приводит к менее интенсивным эффектам "свидетеля" и менее интенсивным проявлениям неспецифической токсичности по сравнению с конъюгатами с расщепляемым линкером для ADC. В целом, ADC с нерасщепляемыми линкерами для ADC характеризуются большей стабильностью в кровотоке, чем ADC с расщепляемыми линкерами для ADC. Нерасщепляемые линкеры для ADC могут представлять собой алкиленовые цепи или могут быть полимерными по природе, такими как, например, полимеры на основе полиалкиленгликоля, амидные полимеры, или могут содержать сегменты алкиленовых цепей, полиалкиленгликолей и/или амидных полимеров.
Были описаны разнообразные нерасщепляемые линкеры для ADC, применяемые для связывания лекарственных средств с BCMA-связывающими молекулами. См. Jeffrey et al., 2006, Bioconjug. Chem. 17; 831-840; Jeffrey et al., 2007, Bioorg. Med. Chem. Lett. 17:2278-2280; и Jiang et al., 2005, J. Am. Chem. Soc. 127:11254-11255. Все эти линкеры для ADC могут быть включены в ADC по настоящему изобретению.
В определенных вариантах осуществления линкер для ADC является нерасщепляемым in vivo, например, линкер для ADC в соответствии со структурной формулой (VIa), (VIb), (VIc) или (VId) (как проиллюстрировано, линкеры для ADC содержат группу, подходящую для ковалентного связывания линкера для ADC с BCMA-связывающей молекулой:
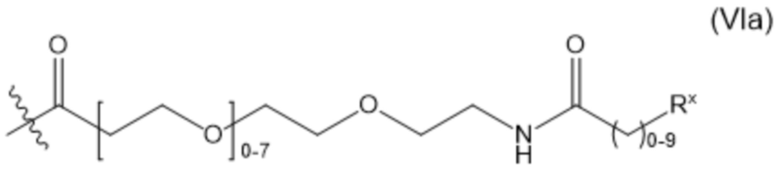


или его соли, где: Ra выбран из водорода, алкила, сульфоната и метилсульфоната; Rx представляет собой фрагмент, содержащий функциональную группу, способную ковалентно связывать линкер для ADC с BCMA-связывающей молекулой; и  представляет точку присоединения линкера для ADC к цитотоксическому и/или цитостатическому средству.
представляет точку присоединения линкера для ADC к цитотоксическому и/или цитостатическому средству.
Конкретные иллюстративные варианты осуществления линкеров для ADC в соответствии со структурной формулой (VIa)-(VId), которые могут быть включены в ADC, включают линкеры для ADC, проиллюстрированные ниже (как проиллюстрировано, линкеры для ADC содержат группу, подходящую для ковалентного связывания линкера для ADC с BCMA-связывающей молекулой, и  представляет собой точку присоединения к цитотоксическому и/или цитостатическому средству):
представляет собой точку присоединения к цитотоксическому и/или цитостатическому средству):

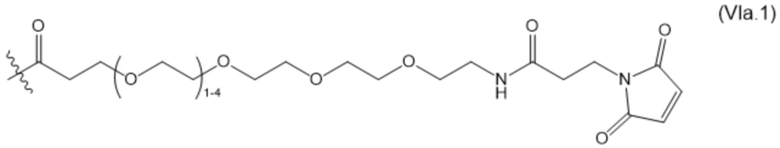

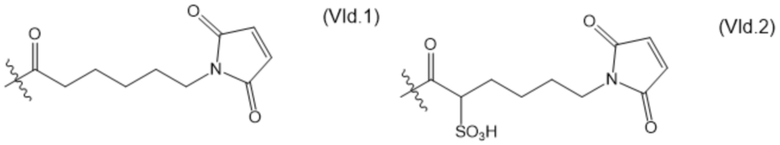
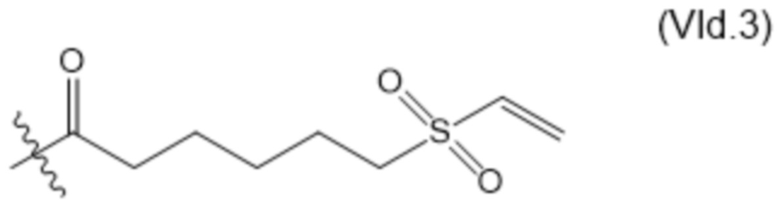
7.9.2.3. Группы, применяемые для присоединения линкеров к BCMA-связывающим молекулам
Для присоединения синтонов ADC-линкер-лекарственное средство к BCMA-связывающим молекулам с получением ADC можно применять разнообразные группы. Группы для присоединения могут являться электрофильными по своей природе и включают малеимидные группы, активированные дисульфидные группы, активные сложноэфирные группы, такие как NHS-сложноэфирные группы и HOBt-сложноэфирные группы, галогенформиатные группы, галогенангидридные группы, алкил- и бензилгалогенидные группы, такие как галогенацетамидные группы. Как обсуждается ниже, существуют также перспективные технологии, связанные с "самостабилизирующимися" малеимидами и "мостикообразующими дисульфидами", которые можно применять в соответствии с настоящим изобретением. Выбор конкретной применяемой группы будет частично зависеть от сайта присоединения к BCMA-связывающей молекуле.
Один пример "самостабилизирующейся" малеимидной группы, которая самопроизвольно гидролизуется в условиях конъюгации BCMA-связывающей молекулы с получением молекул ADC с улучшенной стабильностью, изображен на схеме ниже. См. US20130309256 A1; также Lyon et al., Nature Biotech, опубликованный в режиме онлайн, doi:10.1038/nbt.2968.
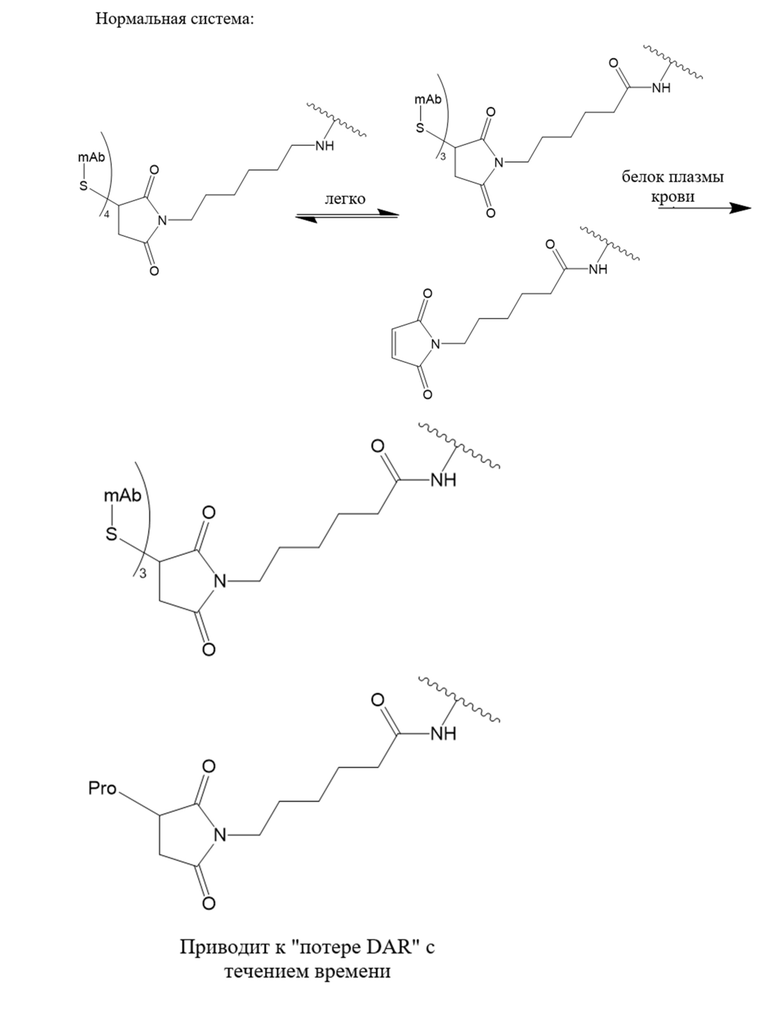
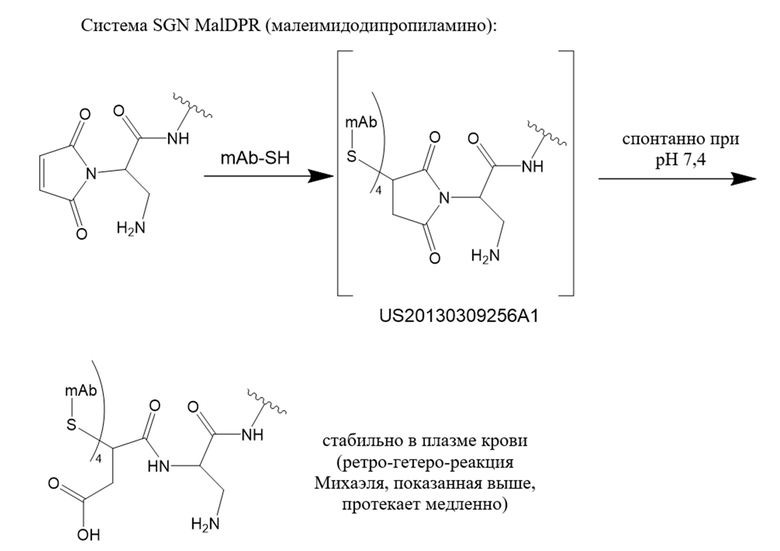
PolyTherics раскрыли способ образования мостика между парой сульфгидрильных групп, полученных в результате восстановления нативной дисульфидной связи в шарнирном участке. См. Badescu et al., 2014, Bioconjugate Chem. 25:1124-1136. Реакция изображена на схеме ниже. Преимущество данной методики состоит в возможности синтезировать обогащенные ADC с DAR4 посредством полного восстановления молекул IgG (с получением 4 пар сульфгидрильных групп) с последующей реакцией с 4 эквивалентами алкилирующего средства. ADC, содержащие "мостиковые дисульфиды", обладают увеличенной стабильностью.
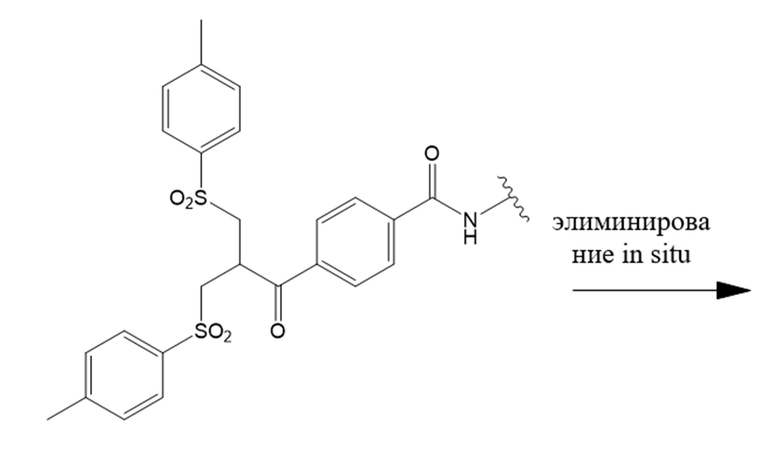
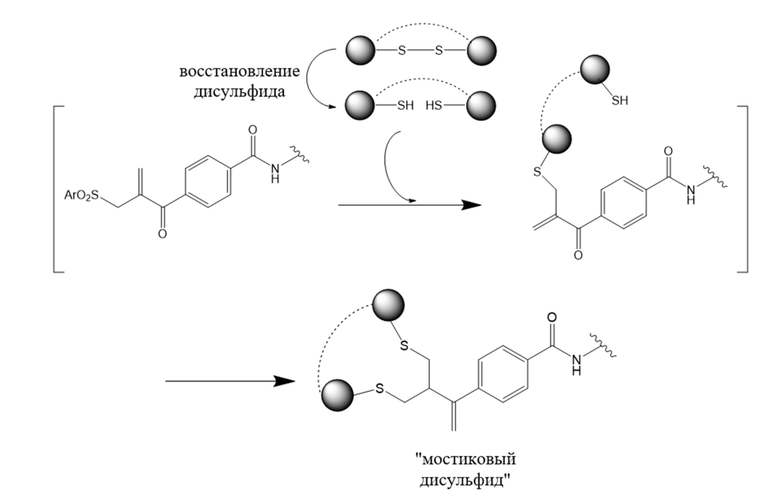
Аналогичным образом, как изображено ниже, было разработано малеимидное производное (1, ниже), которое способно к образованию мостика между парой сульфгидрильных групп. См. WO2013/085925.
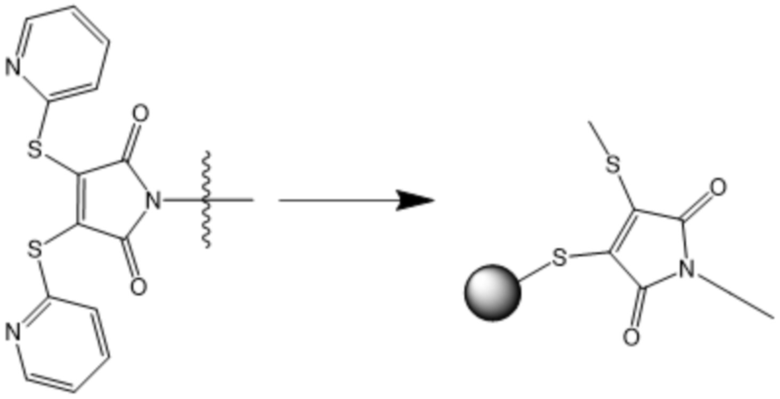
7.9.2.4. Критерии выбора линкеров для ADC
Как известно специалистам в данной области техники, на выбор линкера для ADC для конкретного ADC могут влиять разнообразные факторы, в том числе без ограничения сайт присоединения к BCMA-связывающей молекуле (например, Lys, Cys или другие аминокислотные остатки), структурные ограничения фармакофора лекарственного средства и липофильность лекарственного средства. Конкретный линкер для ADC, выбранный для ADC, должен стремиться сбалансировать эти различные факторы для конкретной комбинации BCMA-связывающая молекула/лекарственное средство. Для обзора факторов, которые влияют на выбор линкеров для ADC в ADC, см. Nolting, Chapter 5 "Linker Technology in Antibody-Drug Conjugates", в Antibody-Drug Conjugates: Methods in Molecular Biology, vol. 1045, pp. 71-100, Laurent Ducry (Ed.), Springer Science & Business Medica, LLC, 2013.
Например, наблюдалось, что ADC осуществляют уничтожение антиген-отрицательных клеток-"свидетелей", присутствующих поблизости от антиген-положительных опухолевых клеток. Механизм уничтожения клеток-"свидетелей" посредством ADC указывает на то, что в этом могут играть роль продукты метаболизма, образующиеся в ходе внутриклеточного процессинга ADC. Нейтральные цитотоксические метаболиты, образующиеся в ходе метаболизма ADC в антиген-положительных клетках, по-видимому, играют роль в уничтожении клеток-"свидетелей", тогда как заряженные метаболиты могут быть лишены возможности диффундировать через мембрану в среду и, следовательно, не способны оказывать влияния на уничтожение клеток-"свидетелей". В определенных вариантах осуществления линкер для ADC выбран с целью ослабления эффекта уничтожения клеток-"свидетелей", обусловленного клеточными метаболитами ADC. В определенных вариантах осуществления линкер для ADC выбран с целью увеличения эффекта уничтожения клеток-"свидетелей".
Свойства линкера для ADC могут также влиять на агрегацию ADC в условиях применения и/или хранения. Как правило, ADC, о которых сообщалось в литературе, содержат не более 3-4 молекул лекарственного средства на молекулу антитела (см., например, Chari, 2008, Acc Chem Res 41:98-107). Попытки достижения более высоких соотношений лекарственное средство/антитело ("DAR") часто не имели успеха, в частности из-за агрегации ADC, если как лекарственное средство, так и линкер для ADC были гидрофобными (King et al., 2002, J Med Chem 45:4336-4343; Hollander et al., 2008, Bioconjugate Chem 19:358-361; Burke et al., 2009 Bioconjugate Chem 20:1242-1250). Во многих случаях значения DAR выше 3-4 могут являться благоприятными в качестве средств, обеспечивающих увеличение активности. В случаях, если цитотоксическое и/или цитостатическое средство является гидрофобным по природе, может потребоваться выбрать линкеры для ADC, которые являются относительно гидрофильными, в качестве средств, обеспечивающих снижение агрегации ADC, особенно в случаях, когда требуются значения DAR, составляющие более 3-4. Таким образом, в определенных вариантах осуществления линкер для ADC содержит в своем составе химические фрагменты, которые обеспечивают снижение агрегации ADC во время хранения и/или применения. Линкер для ADC может содержать в своем составе полярные или гидрофильные группы, такие как заряженные группы или группы, которые становятся заряженными при физиологическом значении pH, для снижения агрегации ADC. Например, линкер для ADC может содержать в своем составе заряженные группы, такие как соли, или группы, которые депротонируются, например, карбоксилаты, или протонируются, например, амины, при физиологическом значении pH.
Иллюстративные поливалентные линкеры для ADC, о которых сообщалось, что они обеспечивают достижение значений DAR, достигающих 20, которые можно применять для связывания многочисленных цитотоксических и/или цитостатических средств с BCMA-связывающей молекулой, описаны в WO 2009/073445; WO 2010/068795; WO 2010/138719; WO 2011/120053; WO 2011/171020; WO 2013/096901; WO 2014/008375; WO 2014/093379; WO 2014/093394; WO 2014/093640.
В конкретных вариантах осуществления агрегация ADC во время хранения или применения составляет менее чем приблизительно 10%, как определено посредством эксклюзионной хроматографии (SEC). В конкретных вариантах осуществления агрегация ADC во время хранения или применения составляет менее 10%, например, менее чем приблизительно 5%, менее чем приблизительно 4%, менее чем приблизительно 3%, менее чем приблизительно 2%, менее чем приблизительно 1%, менее чем приблизительно 0,5%, менее чем приблизительно 0,1% или даже ниже, как определено посредством эксклюзионной хроматографии (SEC).
7.9.3. Способы получения ADC
ADC можно синтезировать с применением химических веществ, которые являются широко известными. Выбор химических веществ будет зависеть, среди прочего, от отличительных характеристик цитотоксического(цитотоксических) и/или цитостатического(цитостатических) средства(средств), линкера для ADC и групп, применяемых для присоединения линкера для ADC к BCMA-связывающей молекуле. ADC в соответствии с формулой (I) обычно можно получать в соответствии со следующей схемой:
D-L-Rx+Ab-Ry→[D-L-XY]n-Ab (I),
где D, L, Ab, XY и n являются такими, как определено ранее, и Rx и Ry представляют комплементарные группы, способные к образованию ковалентных связей друг с другом, как обсуждается выше.
Отличительные характеристики групп Rx и Ry будут зависеть от химического вещества, применяемого для связывания синтона D-L-Rx с BCMA-связывающей молекулой. Применяемое химическое вещество обычно не должно изменять функциональные характеристики BCMA-связывающей молекулы, например, ее способность к связыванию своей мишени. В некоторых случаях свойства связывания конъюгированного антитела будут очень похожими на свойства связывания неконъюгированной BCMA-связывающей молекулы. Разнообразные химические вещества и методики для конъюгации молекул с биологическими молекулами и, в частности, с иммуноглобулинами, компоненты которых, как правило, являются структурными элементами BCMA-связывающей молекулы по настоящему изобретению, являются широко известными. См., например, Amon et al., "Monoclonal Antibodies For Immunotargeting Of Drugs In Cancer Therapy", в Monoclonal Antibodies And Cancer Therapy, Reisfeld et al. Eds., Alan R. Liss, Inc., 1985; Hellstrom et al., "Antibodies For Drug Delivery", в Controlled Drug Delivery, Robinson et al. Eds., Marcel Dekker, Inc., 2nd Ed. 1987; Thorpe, "Antibody Carriers Of Cytotoxic Agents In Cancer Therapy: A Review", в Monoclonal Antibodies '84: Biological And Clinical Applications, Pinchera et al., Eds., 1985; "Analysis, Results, and Future Prospective of the Therapeutic Use of Radiolabeled Antibody In Cancer Therapy", в Monoclonal Antibodies For Cancer Detection And Therapy, Baldwin et al., Eds., Academic Press, 1985; Thorpe et al., 1982, Immunol. Rev. 62:119-58; PCT-публикацию WO 89/12624. Любое из этих химических веществ можно применять для связывания синтонов с BCMA-связывающей молекулой.
Известен ряд функциональных групп Rx и химических веществ, применимых для связывания синтонов с доступными остатками лизина, и они включают, в качестве примера и без ограничения, NHS-сложные эфиры и изотиоцианаты.
Известен ряд функциональных групп Rx и химических веществ, применимых для связывания синтонов с доступными свободными сульфгидрильными группами остатков цистеина, и они включают, в качестве примера и без ограничения, галогенацетильные группы и малеимидные группы.
Однако химические вещества для конъюгации не ограничены доступными группами боковых цепей. Боковые цепи, такие как аминогруппы, можно превращать в другие применимые группы, такие как гидроксильные группы, посредством связывания подходящей небольшой молекулы с аминогруппой. Эту стратегию можно применять для увеличения количества доступных сайтов связывания в антителе посредством конъюгации полифункциональных небольших молекул с боковыми цепями доступных аминокислотных остатков BCMA-связывающей молекулы. Функциональные группы Rx, подходящие для ковалентного связывания синтонов с этими "превращенными" функциональными группами, затем включаются в синтоны.
BCMA-связывающую молекулу можно также сконструировать таким образом, чтобы она содержала аминокислотные остатки для конъюгации. Подход к конструированию BBM таким образом, чтобы они содержали аминокислотные остатки, которые не кодируются генетически, применимые для конъюгации лекарственных средств в качестве составной части ADC, описан в Axup et al., 2012, Proc Natl Acad Sci USA. 109(40):16101-16106, равно как и химические вещества и функциональные группы, применимые для связывания синтонов с некодируемыми аминокислотами.
Как правило, синтоны связаны с боковыми цепями аминокислотных остатков BCMA-связывающей молекулы, в том числе, например, с первичной аминогруппой доступных остатков лизина или сульфгидрильной группой доступных остатков цистеина. Свободные сульфгидрильные группы можно получать посредством восстановления межцепочечных дисульфидных связей.
В случае со связями, где Ry представляет собой сульфгидрильную группу (например, если Rx представляет собой малеимид), BCMA-связывающую молекулу обычно вначале полностью или частично восстанавливают для разрушения межцепочечных дисульфидных мостиков между остатками цистеина.
Остатки цистеина, которые не принимают участия в образовании дисульфидных мостиков, можно встроить в BCMA-связывающую молекулу посредством модификации одного или нескольких кодонов. Восстановление этих неспаренных остатков цистеина обеспечивает получение сульфгидрильной группы, подходящей для конъюгации. В некоторых вариантах осуществления BCMA-связывающая молекула сконструирована с введением одного или нескольких остатков цистеина в качестве сайтов для конъюгации с фрагментом, представляющим собой лекарственное средство (см. Junutula, et al, 2008, Nat Biotechnol, 26:925-932).
Сайты для замены на цистеин могут быть выбраны в константном участке для получения стабильных и однородных конъюгатов. BCMA-связывающая молекула может содержать, например, одну, две или больше замен на цистеин, и эти замены могут применяться в комбинации с другими способами модификации и конъюгации, описанными в данном документе. Известны способы обеспечения вставки цистеина в конкретные местоположения антитела, см., например, Lyons et al., 1990, Protein Eng., 3:703-708, WO 2011/005481, WO2014/124316, WO 2015/138615. В некоторых вариантах осуществления BCMA-связывающая молекула содержит замену одной или нескольких аминокислот на цистеин в константном участке в положении, выбранном из положений 117, 119, 121, 124, 139, 152, 153, 155, 157, 164, 169, 171, 174, 189, 205, 207, 246, 258, 269, 274, 286, 288, 290, 292, 293, 320, 322, 326, 333, 334, 335, 337, 344, 355, 360, 375, 382, 390, 392, 398, 400 и 422 тяжелой цепи, где нумерация положений соответствует системе EU. В некоторых вариантах осуществления BCMA-связывающая молекула содержит замену одной или нескольких аминокислот на цистеин в константном участке в положении, выбранном из положений 107, 108, 109, 114, 129, 142, 143, 145, 152, 154, 156, 159, 161, 165, 168, 169, 170, 182, 183, 197, 199, и 203 легкой цепи, где нумерация положений соответствует системе EU, и где легкая цепь представляет собой человеческую легкую каппа-цепь. В определенных вариантах осуществления BCMA-связывающая молекула содержит комбинацию из замен двух или более аминокислот на цистеин в константном участке, где комбинации включают замены в положении 375 тяжелой цепи, положении 152 тяжелой цепи, положении 360 тяжелой цепи или положении 107 легкой цепи, и где положения пронумерованы согласно системе EU. В определенных вариантах осуществления BCMA-связывающая молекула содержит замену одной аминокислоты на цистеин в константном участке, где замена находится в положении 375 тяжелой цепи, положении 152 тяжелой цепи, положении 360 тяжелой цепи, положении 107 легкой цепи, положении 165 легкой цепи или положении 159 легкой цепи, и где положения пронумерованы согласно системе EU, и где легкая цепь представляет собой каппа-цепь.
В конкретных вариантах осуществления BCMA-связывающая молекула содержит комбинацию замен двух аминокислот на цистеин в константных участках, где BCMA-связывающая молекула содержит остатки цистеина в положениях 152 и 375 тяжелой цепи, где положения пронумерованы согласно системе EU.
В других конкретных вариантах осуществления BCMA-связывающая молекула содержит замену одной аминокислоты на цистеин в положении 360 тяжелой цепи, где положения пронумерованы согласно системе EU.
В других конкретных вариантах осуществления BCMA-связывающая молекула содержит замену одной аминокислоты на цистеин в положении 107 легкой цепи, где положения пронумерованы согласно системе EU, и где легкая цепь представляет собой каппа-цепь.
Другие положения для включения встроенных остатков цистеина могут включать в качестве примера и без ограничения положения S112C, S113C, A114C, S115C, A176C, 5180C, S252C, V286C, V292C, S357C, A359C, S398C, S428C (нумерация по Kabat) в тяжелой цепи человеческого IgG1 и положения V110C, S114C, S121C, S127C, S168C, V205C (нумерация по Kabat) в легкой каппа-цепи человеческого Ig (см., например, патент США № 7521541, патент США № 7855275 и патент США № 8455622).
BCMA-связывающие молекулы, применимые в ADC, раскрытых в данном документе, дополнительно или в качестве альтернативы могут быть модифицированы с введением одной или нескольких других реакционноспособных аминокислот (отличных от цистеина), включая Pcl, пирролизин, пептидные метки (такие как метки S6, A1 и ybbR) и неприродные аминокислоты, вместо по меньшей мере одной аминокислоты из нативной последовательности с получением таким образом реакционноспособного сайта в BCMA-связывающей молекуле для конъюгации с фрагментом, представляющим собой лекарственное средство. Например, BCMA-связывающие молекулы могут быть модифицированы таким образом, чтобы они содержали в своем составе Pcl или пирролизин (W. Ou et al., 2011, PNAS, 108(26):10437-10442; WO2014124258) или неприродные аминокислоты (Axup, et al., 2012, PNAS, 109:16101-16106; для обзора см. C.C. Liu and P.G. Schultz, 2010, Annu Rev Biochem 79:413-444; Kim, et al., 2013, Curr Opin Chem Biol. 17:412-419) в качестве сайтов для конъюгации с лекарственным средством. Аналогичным образом в BCMA-связывающую молекулу могут быть введены пептидные метки для способов ферментативной конъюгации (см. Strop et al. 2013, Chem Biol. 20(2):161-7; Rabuka, 2010, Curr Opin Chem Biol. 14(6):790-6; Rabuka, et al., 2012, Nat Protoc. 7(6):1052-67). Еще одним примером является применение 4'-фосфопантетеинилтрансфераз (PPTазы) для конъюгации аналогов кофермента A (WO2013184514). Такие модифицированные или сконструированные MBM могут быть конъюгированы с полезными нагрузками или комбинациями линкер-полезная нагрузка в соответствии с известными способами.
Как будет понятно специалистам в данной области техники, количество средств (например, цитотоксических и/или цитостатических средств), связанных с BCMA-связывающей молекулой, может варьироваться, так что совокупность ADC может быть гетерогенной по природе, где некоторые BCMA-связывающие молекулы содержат одно связанное средство, некоторые два, некоторые три и т. д. (и некоторые ни одного). Степень гетерогенности будет зависеть, среди прочего, от химических веществ, применяемых для связывания цитотоксических и/или цитостатических средств. Например, если BCMA-связывающие молекулы восстанавливают с получением сульфгидрильных групп для присоединения, то часто получают гетерогенные смеси BCMA-связывающих молекул, содержащие ноль, 2, 4, 6 или 8 связанных средств на молекулу. Кроме того, посредством ограничения молярного соотношения для присоединяемого соединения часто получают BCMA-связывающие молекулы, содержащие ноль, 1, 2, 3, 4, 5, 6, 7 или 8 связанных средств на молекулу. Таким образом будет понятно, что в зависимости от контекста установленные соотношения лекарственного средства и BCMA-связывающей молекулы (DTR) могут представлять собой средние значения для совокупности BCMA-связывающих молекул. Например, "DTR4" может относиться к препарату на основе ADC, который не был подвергнут очистке для выделения конкретных пиков DTR и может содержать гетерогенную смесь молекул ADC, содержащую различные количества присоединенных цитостатических и/или цитотоксических средств на BCMA-связывающую молекулу (например, 0, 2, 4, 6, 8 средств на BCMA-связывающую молекулу), но характеризующуюся средним соотношением лекарственного средства и BCMA-связывающей молекулы, составляющим 4. Подобным образом, в некоторых вариантах осуществления "DTR2" относится к гетерогенному препарату на основе ADC, в котором среднее соотношение лекарственного средства и BCMA-связывающей молекулы составляет 2.
Если необходимы обогащенные препараты, то BCMA-связывающие молекулы, содержащие определенные количества связанных цитотоксических и/или цитостатических средств, можно получать посредством очистки гетерогенных смесей, например, посредством колоночной хроматографии, например, хроматографии гидрофобных взаимодействий.
Чистоту можно оценивать посредством различных способов. В качестве конкретного примера, препарат на основе ADC можно анализировать посредством HPLC или другой методики хроматографии, а чистоту оценивать посредством анализа площадей под кривыми полученных в результате пиков.
7.10. BCMA-связывающие молекулы, конъюгированные с выявляемыми средствами
BCMA-связывающие молекулы по настоящему изобретению могут быть конъюгированы с диагностическим или выявляемым средством. Такие молекулы могут быть применимыми для контроля или прогнозирования проявления, развития, прогрессирования и/или тяжести заболевания или нарушения в рамках процедуры клинического тестирования, такой как определение эффективности конкретной терапии. Такая диагностика и выявление могут осуществляться посредством связывания BCMA-связывающих молекул с выявляемыми веществами, в том числе без ограничения с различными ферментами, такими как без ограничения пероксидаза хрена, щелочная фосфатаза, бета-галактозидаза или ацетилхолинэстераза; простетическими группами, такими как без ограничения стрептавидин/биотин и авидин/биотин; флуоресцентными материалами, такими как без ограничения умбеллиферон, флуоресцеин, изотиоцианат флуоресцеина, родамин, дихлортриазиниламинфлуоресцеин, дансилхлорид или фикоэритрин; люминесцентными материалами, такими как без ограничения люминол; биолюминесцентными материалами, такими как без ограничения люцифераза, люциферин и экворин; радиоактивными материалами, такими как без ограничения йод (131I, 125I, 123I и 121I), углерод (14C), сера (35S), тритий (3H), индий (115In, 113In, 112In и 111In), технеций (99Tc), таллий (201Ti), галлий (68Ga, 67Ga), палладий (103Pd), молибден (99Mo), ксенон (133Xe), фтор (18F), 153Sm, 177Lu, 159Gd, 149Pm, 140La, 175Yb, 166Ho, 90Y, 47Sc, 186Re, 188Re, 142Pr, 105Rh, 97Ru, 68Ge, 57Co, 65Zn, 85Sr, 32P, 153Gd, 169Yb, 51Cr, 54Mn, 75Se, 113Sn и 117олово; и позитрон-излучающими металлами с применением различных способов позитронной эмиссионной томографии, и нерадиоактивными ионами парамагнитных металлов.
7.11. BCMA-связывающие молекулы, прикрепленные к твердым подложкам
BCMA-связывающие молекулы также могут быть прикреплены к твердым подложкам, которые являются особенно применимыми для иммунологических анализов или очистки антигена-мишени(антигенов-мишеней). Такие твердые подложки включают без ограничения стекло, целлюлозу, полиакриламид, нейлон, полистирол, поливинилхлорид или полипропилен.
7.12. Фармацевтические композиции
BCMA-связывающие молекулы по настоящему изобретению (а также их конъюгаты; ссылки на BCMA-связывающие молекулы в настоящем изобретении также относятся к конъюгатам, содержащим BCMA-связывающие молекулы, таким как ADC, если контекст не предусматривает иное) можно составлять в виде фармацевтических композиций, содержащих BCMA-связывающие молекулы, например, содержащих одно или несколько фармацевтически приемлемых вспомогательных веществ или носителей. Для получения фармацевтических или стерильных композиций, содержащих BCMA-связывающие молекулы по настоящему изобретению, препарат на основе BCMA-связывающей молекулы можно комбинировать с одним или несколькими фармацевтически приемлемыми вспомогательными веществами или носителями.
Например, составы на основе BCMA-связывающих молекул можно получать посредством смешивания BCMA-связывающих молекул с физиологически приемлемыми носителями, наполнителями или стабилизаторами в форме, например, лиофилизированных порошков, взвесей, водных растворов, лосьонов или суспензий (см., например, Hardman et al., 2001, Goodman and Gilman's The Pharmacological Basis of Therapeutics, McGraw-Hill, New York, N.Y.; Gennaro, 2000, Remington: The Science and Practice of Pharmacy, Lippincott, Williams, and Wilkins, New York, N.Y.; Avis, et al. (eds.), 1993, Pharmaceutical Dosage Forms: General Medications, Marcel Dekker, NY; Lieberman, et al. (eds.), 1990, Pharmaceutical Dosage Forms: Tablets, Marcel Dekker, NY; Lieberman, et al. (eds.), 1990, Pharmaceutical Dosage Forms: Disperse Systems, Marcel Dekker, NY; Weiner and Kotkoskie, 2000, Excipient Toxicity and Safety, Marcel Dekker, Inc., New York, N.Y.).
Выбор схемы введения BCMA-связывающей молекулы зависит от нескольких факторов, в том числе скорости метаболизма BCMA-связывающей молекулы в сыворотке крови или ткани, уровня тяжести симптомов, иммуногенности BCMA-связывающей молекулы и доступности клеток-мишеней. В определенных вариантах осуществления схема введения предусматривает максимальное количество BCMA-связывающей молекулы, доставляемой субъекту в соответствии с приемлемым уровнем побочных эффектов. Соответственно, количество доставляемой BCMA-связывающей молекулы частично зависит от конкретной BCMA-связывающей молекулы и тяжести состояния, подлежащего лечению. Доступно руководство по выбору подходящих доз антител и небольших молекул (см., например, Wawrzynczak, 1996, Antibody Therapy, Bios Scientific Pub. Ltd, Oxfordshire, UK; Kresina (ed.), 1991, Monoclonal Antibodies, Cytokines and Arthritis, Marcel Dekker, New York, N.Y.; Bach (ed.), 1993, Monoclonal Antibodies and Peptide Therapy in Autoimmune Diseases, Marcel Dekker, New York, N.Y.; Baert et al., 2003, New Engl. J. Med. 348:601-608; Milgrom et al., 1999, New Engl. J. Med. 341:1966-1973; Slamon et al., 2001, New Engl. J. Med. 344:783-792; Beniaminovitz et al., 2000, New Engl. J. Med. 342:613-619; Ghosh et al., 2003, New Engl. J. Med. 348:24-32; Lipsky et al., 2000, New Engl. J. Med. 343:1594-1602).
Определение подходящей дозы выполняет лечащий врач, например, с использованием параметров или факторов, которые, как известно или предполагается из уровня техники, влияют на лечение или согласно прогнозам влияют на лечение. Введение доз обычно начинают с количества, несколько меньшего, чем оптимальная доза, и после этого его увеличивают с небольшими приращениями до тех пор, пока не достигается требуемый или оптимальный эффект по сравнению с любыми отрицательными побочными эффектами. Важные диагностические показатели включают, например, показатели симптомов воспаления или уровня вырабатываемых воспалительных цитокинов.
Фактические уровни доз BCMA-связывающих молекул в фармацевтических композициях по настоящему изобретению можно изменять таким образом, чтобы получить количество BCMA-связывающей молекулы, которое является эффективным для достижения требуемого терапевтического ответа для конкретного субъекта, композиции и способа введения, не являясь токсичным для субъекта. Выбранный уровень дозы будет зависеть от разнообразных фармакокинетических факторов, в том числе активности конкретной BCMA-связывающей молекулы, пути введения, времени введения, скорости экскреции конкретной используемой BCMA-связывающей молекулы, продолжительности лечения, других средств (например, активных средств, таких как терапевтические лекарственные средства или соединения и/или инертные материалы, применяемые в качестве носителей) в комбинации с конкретной используемой BCMA-связывающей молекулой, возраста, пола, веса, состояния, общего состояния здоровья и анамнеза субъекта, подлежащего лечению, и подобных факторов, известных в области медицины.
Композиции, содержащие BCMA-связывающие молекулы, можно предоставлять посредством непрерывной инфузии или посредством введения доз с интервалами, составляющими, например, один день, одну неделю или 1-7 раз в неделю. Дозы можно предоставлять внутривенно, подкожно, местно, перорально, назально, ректально, внутримышечно, интрацеребрально или посредством ингаляции. Конкретный протокол введения доз предусматривает максимальную дозу или частоту введения доз, при которых удается избежать значительных нежелательных побочных эффектов.
Эффективное количество для конкретного субъекта может варьироваться в зависимости от таких факторов, как состояние, подлежащее лечению, общее состояние здоровья субъекта, путь и доза введения согласно способу и тяжесть побочных эффектов (см., например, Maynard, et al. (1996) A Handbook of SOPs for Good Clinical Practice, Interpharm Press, Boca Raton, Fla.; Dent (2001) Good Laboratory and Good Clinical Practice, Urch Publ., London, UK).
Путь введения может представлять собой введение посредством, например, местного или накожного применения, инъекции или инфузии путем внутривенного, интраперитонеального, интрацеребрального, внутримышечного, внутриглазного, внутриартериального, интрацереброспинального, внутриочагового введения или посредством систем с замедленным высвобождением или имплантата (см., например, Sidman et al., 1983, Biopolymers 22:547-556; Langer et al., 1981, J. Biomed. Mater. Res. 15:167-277; Langer, 1982, Chem. Tech. 12:98-105; Epstein et al., 1985, Proc. Natl. Acad. Sci. USA 82:3688-3692; Hwang et al., 1980, Proc. Natl. Acad. Sci. USA 77:4030-4034; патенты США №№ 6350466 и 6316024). При необходимости композиция также может содержать солюбилизирующее средство и анестетик местного действия, такой как лидокаин, для облегчения боли в месте инъекции. Кроме того, внутрилегочное введение также можно использовать, например, путем применения ингалятора или небулайзера и состава с аэрозолирующим средством. См., например, патенты США №№ 6019968, 5985320, 5985309, 5934272, 5874064, 5855913, 5290540 и 4880078; а также PCT-публикации №№ WO 92/19244, WO 97/32572, WO 97/44013, WO 98/31346 и WO 99/66903.
Композицию по настоящему изобретению также можно вводить посредством одного или нескольких путей введения с применением одного или нескольких из множества известных способов. Как будет понятно специалисту в данной области техники, путь и/или способ введения будут варьироваться в зависимости от требуемых результатов. Выбранные пути введения BCMA-связывающих молекул включают внутривенный, внутримышечный, внутрикожный, интраперитонеальный, подкожный, спинальный или другие обычные пути введения, например, посредством инъекции или инфузии. Системное введение может представлять собой способы введения, отличные от энтерального и местного введения, обычно посредством инъекции, и включает без ограничения внутривенную, внутримышечную, внутриартериальную, интратекальную, интракапсулярную, внутриглазничную, внутрисердечную, внутрикожную, интраперитонеальную, транстрахеальную, подкожную, субкутикулярную, внутрисуставную, подкапсульную, субарахноидальную, интраспинальную, эпидуральную и интрастернальную инъекцию и инфузию. В качестве альтернативы, композицию по настоящему изобретению можно вводить посредством пути, отличного от системного, такого как местный, эпидермальный или мукозальный путь введения, например, интраназально, перорально, вагинально, ректально, сублингвально или местно. В одном варианте осуществления BCMA-связывающую молекулу вводят посредством инфузии. В другом варианте осуществления BCMA-связывающую молекулу вводят подкожно.
Если BCMA-связывающие молекулы вводят в системе с контролируемым высвобождением или замедленным высвобождением, то можно применять насос для достижения контролируемого или замедленного высвобождения (см. Langer, выше; Sefton, 1987, CRC Crit. Ref Biomed. Eng. 14:20; Buchwald et al., 1980, Surgery 88:507; Saudek et al., 1989, N. Engl. J. Med. 321:574). Для достижения контролируемого или замедленного высвобождения средств терапии по настоящему изобретению можно применять полимерные материалы (см., например, Medical Applications of Controlled Release, Langer and Wise (eds.), CRC Pres., Boca Raton, Fla. (1974); Controlled Drug Bioavailability, Drug Product Design and Performance, Smolen and Ball (eds.), Wiley, New York (1984); Ranger and Peppas, 1983, J., Macromol. Sci. Rev. Macromol. Chem. 23:61; см. также Levy et al., 1985, Science 228:190; During et al., 1989, Ann. Neurol. 25:351; Howard et al., 1989, J. Neurosurg. 71:105); патент США № 5679377; патент США № 5916597; патент США № 5912015; патент США № 5989463; патент США № 5128326; PCT-публикацию № WO 99/15154 и PCT-публикацию № WO 99/20253. Примеры полимеров, применяемых в составах с замедленным высвобождением, включают без ограничения поли(2-гидроксиэтилметакрилат), поли(метилметакрилат), поли(акриловую кислоту), сополимер этилена и винилацетата, поли(метакриловую кислоту), полигликолиды (PLG), полиангидриды, поли(N-винилпирролидон), поли(виниловый спирт), полиакриламид, поли(этиленгликоль), полилактиды (PLA), сополимеры лактида и гликолидов (PLGA) и сложные полиортоэфиры. В одном варианте осуществления полимер, применяемый в составе с замедленным высвобождением, является инертным, не содержащим выщелачиваемые примеси, стабильным при хранении, стерильным и биодеградируемым. Систему с контролируемым или замедленным высвобождением можно поместить вблизи профилактической или терапевтической мишени, благодаря чему будет требоваться только часть системной дозы (см., например, Goodson, в Medical Applications of Controlled Release, выше, vol. 2, pp. 115-138 (1984)).
Системы с контролируемым высвобождением обсуждаются в обзоре Langer (1990, Science 249:1527-1533). Любую методику, известную специалисту в данной области техники, можно применять для получения составов с замедленным высвобождением, содержащих одну или несколько BCMA-связывающих молекул по настоящему изобретению. См., например, патент США № 4526938, PCT-публикацию WO 91/05548, PCT-публикацию WO 96/20698, Ning et al., 1996, Radiotherapy & Oncology 39:179-189, Song et al., 1995, PDA Journal of Pharmaceutical Science & Technology 50:372-397, Cleek et al., 1997, Pro. Int'l. Symp. Control. Rel. Bioact. Mater. 24:853-854, и Lam et al., 1997, Proc. Int'l. Symp. Control Rel. Bioact. Mater. 24:759-760.
Если BCMA-связывающие молекулы вводят местно, то они могут быть составлены в форме мази, крема, трансдермального пластыря, лосьона, геля, шампуня, спрея, аэрозоля, раствора, эмульсии или другой формы, хорошо известной специалисту в данной области техники. См., например, Remington's Pharmaceutical Sciences and Introduction to Pharmaceutical Dosage Forms, 19th ed., Mack Pub. Co., Easton, Pa. (1995). В случае с нераспыляемыми лекарственными формами для местного применения обычно используют формы от вязких до полутвердых или твердых, содержащие носитель или один или несколько наполнителей, совместимые с местным применением и, в некоторых случаях, характеризующиеся большей динамической вязкостью, чем у воды. Подходящие составы включают без ограничения растворы, суспензии, эмульсии, кремы, мази, порошки, линименты, бальзамы и т. п., которые при необходимости стерилизуют или смешивают со вспомогательными средствами (например, консервантами, стабилизаторами, смачивающими средствами, буферами или солями) для влияния на различные свойства, такие как, например, осмотическое давление. Другие подходящие лекарственные формы для местного применения включают распыляемые аэрозольные препараты, где активный ингредиент, в некоторых случаях в комбинации с твердым или жидким инертным носителем, упакован в смеси с летучим веществом под давлением (например, газообразным пропеллентом, таким как фреон) или в бутылке-пульверизаторе. При необходимости в фармацевтические композиции и лекарственные формы также можно добавлять увлажняющие или влагоудерживающие средства. Примеры таких дополнительных ингредиентов являются хорошо известными.
Если композиции, содержащие BCMA-связывающие молекулы, вводят интраназально, то BCMA-связывающие молекулы могут быть составлены в форме аэрозоля, спрея, тумана или в форме капель. В частности, в целях удобства профилактические или терапевтические средства для применения согласно настоящему изобретению могут доставляться в лекарственной форме аэрозольного спрея из пакетов под давлением или небулайзера с применением подходящего пропеллента (например, дихлордифторметана, трихлорфторметана, дихлортетрафторэтана, диоксида углерода или другого подходящего газа). В случае с аэрозолем под давлением единица дозирования может определяться посредством обеспечения клапана для доставки отмеренного количества. Капсулы и картриджи (например, состоящие из желатина) для применения в ингаляторе или инсуффляторе можно составлять содержащими порошковую смесь BCMA-связывающей молекулы и подходящей порошковой основы, такой как лактоза или крахмал.
BCMA-связывающие молекулы по настоящему изобретению можно вводить в схемах комбинированной терапии, описанных в разделе 7.14 ниже.
В определенных вариантах осуществления BCMA-связывающие молекулы могут быть составлены для обеспечения надлежащего распределения in vivo. Например, гематоэнцефалический барьер (BBB) не пропускает множество высокогидрофильных соединений. Для обеспечения пересечения BBB терапевтическими соединениями по настоящему изобретению (при необходимости) их можно составлять, например, в липосомах. В отношении способов получения липосом см., например, патенты США №№ 4522811; 5374548 и 5399331. Липосомы могут содержать один или несколько фрагментов, которые селективно транспортируются в специфические клетки или органы, с улучшением тем самым нацеленной доставки лекарственного средства (см., например, Ranade, 1989, J. Clin. Pharmacol. 29:685). Иллюстративные нацеливающиеся фрагменты включают фолат или биотин (см., например, патент США № 5416016, выданный Low et al.); маннозиды (Umezawa et al., 1988, Biochem. Biophys. Res. Commun. 153:1038); антитела (Bloeman et al., 1995, FEBS Lett. 357:140; Owais et al., 1995, Antimicrob. Agents Chemother. 39:180); рецептор поверхностно-активного белка A (Briscoe et al., 1995, Am. J. Physiol. 1233:134); p120 (Schreier et al., 1994, J. Biol. Chem. 269:9090); см. также Keinanen and Laukkanen, 1994, FEBS Lett. 346:123; Killion and Fidler, 1994, Immunomethods 4:273.
При применении в комбинированной терапии, например, как описано в разделе 7.14 ниже, BCMA-связывающая молекула и одно или несколько дополнительных средств можно вводить субъекту в одной и той же фармацевтической композиции. В качестве альтернативы, BCMA-связывающую молекулу и дополнительное(дополнительные) средство(средства) для видов комбинированной терапии можно одновременно вводить субъекту в отдельных фармацевтических композициях.
Терапевтические способы, описанные в данном документе, могут дополнительно включать проведение "сопутствующего диагностического" теста, посредством которого образец от субъекта, который представляет собой кандидата для терапии с помощью BCMA-связывающей молекулы, тестируют в отношении экспрессии BCMA. Сопутствующий диагностический тест можно выполнять до начала терапии с помощью BCMA-связывающей молекулы и/или в ходе осуществления схемы терапии с помощью BCMA-связывающей молекулы для отслеживания сохраняющейся пригодности субъекта для терапии с помощью BCMA-связывающей молекулы. Средство, применяемое в сопутствующей диагностике, может представлять собой саму BCMA-связывающую молекулу или другое диагностическое средство, например, меченое моноспецифическое антитело к BCMA или зонд на основе нуклеиновых кислот для выявления РНК BCMA. Образец, который можно тестировать в ходе сопутствующего диагностического анализа, может представлять собой любой образец, в котором могут присутствовать клетки, на которые нацеливается BCMA-связывающая молекула, например, биоптат опухоли (например, солидной опухоли), лимфа, кал, моча, кровь или любая другая биологическая жидкость, которая может содержать циркулирующие опухолевые клетки.
7.13. Терапевтические показания
ВСМА-связывающие молекулы по настоящему изобретению можно использовать для лечения любого заболевания, ассоциированного с экспрессией ВСМА. Например, ВСМА-связывающую молекулу можно использовать для лечения субъекта, который прошел лечение от заболевания, ассоциированного с повышенной экспрессией ВСМА, где у субъекта, который прошел лечение при повышенных уровнях BCMA, проявляется заболевание, ассоциированное с повышенными уровнями BCMA.
В одном аспекте в настоящем изобретении предусмотрен способ ингибирования роста опухолевой клетки, экспрессирующей ВСМА, включающий приведение опухолевой клетки в контакт с ВСМА-связывающей молекулой таким образом, чтобы рост опухолевой клетки подавлялся.
В одном аспекте в настоящем изобретении предусмотрен способ лечения и/или предупреждения заболевания, которое возникает у индивидуумов с ослабленным иммунитетом, включающий введение ВСМА-связывающей молекулы. В частности, в настоящем документе раскрыт способ лечения заболеваний, нарушений и состояний, ассоциированных с экспрессией BCMA, включающий введение BCMA-связывающей молекулы.
В определенных аспектах в настоящем документе раскрыт способ лечения пациентов с риском развития заболеваний, нарушений и состояний, ассоциированных с экспрессией BCMA, включающий введение BCMA-связывающей молекулы.
Таким образом, в настоящем изобретении предусмотрены способы лечения или предупреждения заболеваний, нарушений и состояний, ассоциированных с экспрессией BCMA, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества BCMA-связывающей молекулы.
В настоящем изобретении также предусмотрены способы предупреждения, лечения и/или контроля заболевания, ассоциированного с клетками, экспрессирующими BCMA (например, клетками гематологического рака или атипичного рака, экспрессирующими BCMA), при этом способы включают введение нуждающемуся в этом субъекту BCMA-связывающей молекулы. В одном аспекте субъектом является человек. Неограничивающие примеры нарушений, ассоциированных с клетками, экспрессирующими ВСМА, включают вирусные или грибковые инфекции и нарушения, связанные с иммунитетом слизистых оболочек.
7.13.1. Рак и связанные с раком заболевания и нарушения
В одном аспекте в настоящем изобретении предусмотрен способ лечения рака у субъекта. Способ включает введение субъекту BCMA-связывающей молекулы, благодаря чему обеспечивается лечение рака у субъекта. Примером рака, который поддается лечению с помощью средства, нацеливающегося на BCMA, является рак, ассоциированный с экспрессией BCMA.
В одном аспекте в настоящем изобретении предусмотрены способы лечения рака, где часть опухоли является отрицательной в отношении BCMA, и часть опухоли является положительной в отношении BCMA.
В одном аспекте в настоящем изобретении предусмотрены способы лечения рака, где BCMA экспрессируется как на нормальных клетках, так и на раковых клетках, но на нормальных клетках BCMA экспрессируется на более низких уровнях, с использованием BCMA-связывающей молекулы по настоящему изобретению. В одном варианте осуществления способ дополнительно включает проведение отбора BCMA-связывающей молекулы, которая связывается с такой аффинностью, которая позволяет BCMA-связывающей молекуле связывать и уничтожать раковые клетки, экспрессирующие ВСМА, но при этом уничтожать менее 30%, 25%, 20%, 15%, 10%, 5% или меньше нормальных клеток, экспрессирующих ВСМА, например, как определено с помощью анализа, описанного в данном документе. Например, можно применять анализ уничтожения, такой как проточная цитометрия на основе CTL с Cr51. В одном варианте осуществления BCMA-связывающая молекула содержит антигенсвязывающий домен, который характеризуется аффинностью связывания с KD в отношении BCMA, составляющей от 10-4 М до 10-8 М, например, от 10-5 М до 10-7 М, например, 10-6 М или 10-7 М.
В одном аспекте в настоящем документе раскрыт способ лечения пролиферативного заболевания, такого как рак или злокачественное новообразование, или предракового состояния, такого как миелодисплазия, миелодиспластический синдром или предлейкоз, включающий введение ВСМА-связывающей молекулы. В одном аспекте рак представляет собой гематологический рак. Состояния, связанные с гематологическими видами рака, представляют собой типы рака, такие как лейкоз и злокачественные лимфопролиферативные состояния, при которых поражается кровь, костный мозг и лимфатическая система. В одном аспекте гематологический рак представляет собой лейкоз. Примером заболевания или нарушения, ассоциированного с BCMA, является множественная миелома (также известная как MM) (см. Claudio et al., Blood. 2002, 100(6):2175-86; и Novak et al., Blood. 2004, 103(2):689-94). Множественная миелома, также известная как плазмоклеточная миелома или болезнь Калера, представляет собой рак, характеризующийся накоплением аномальных или злокачественных плазматических B-клеток в костном мозге. Часто раковые клетки внедряются в смежную кость, разрушая скелетные структуры, что вызывает болевые ощущения в костях и переломы. Большинство случаев миеломы также характеризуются продуцированием парапротеина (также известного как M-белки или миеломные белки), который представляет собой аномальный иммуноглобулин, продуцируемый в избытке вследствие клональной пролиферации злокачественных плазматических клеток. Уровни парапротеина в сыворотке крови, составляющие более 30 г/л, являются диагностическим критерием множественной миеломы в соответствии с диагностическими критериями Международной группы по изучению множественной миеломы (IMWG) (см.See Kyle et al. (2009), Leukemia. 23:3-9). Другие симптомы или признаки множественной миеломы включают ухудшение функции почек или почечную недостаточность, очаги поражения костей, анемию, гиперкальциемию и неврологические симптомы.
Другие нарушения пролиферации плазматических клеток, которые можно лечить с помощью композиций и способов, описанных в данном документе, включают без ограничения бессимптомную миелому (тлеющую множественную миелому или вялотекущую миелому), моноклональную гаммапатию неясного генеза (MGUS), макроглобулинемию Вальденстрема, виды плазмоцитомы (например, плазмоклеточную дискразию, солитарную миелому, солитарную плазмоцитому, экстрамедуллярную плазмоцитому и множественную плазмоцитому), системный амилоидоз в форме амилоидоза легких цепей и POEMS-синдром (также известный как синдром Кроу-Фукаса, болезнь Такатсуки и PEP-синдром).
Другим примером заболевания или нарушения, ассоциированного с BCMA, является лимфома Ходжкина и неходжкинская лимфома (см. Chiu et al., Blood. 2007, 109(2):729-39; He et al., J Immunol. 2004, 172(5):3268-79).
Лимфома Ходжкина (HL), также известная как болезнь Ходжкина, представляет собой рак лимфатической системы, который происходит из белых кровяных клеток или лимфоцитов. Аномальные клетки, которые образуют лимфому, называются клетками Рида-Штернберга. При лимфоме Ходжкина происходит распространение рака из одной группы лимфатических узлов в другую. Лимфому Ходжкина можно подразделить на четыре патологических подтипа на основании морфологических характеристик клеток Рида-Штернберга и клеточного состава вокруг клеток Рида-Штернберга (что определяют посредством биопсии лимфатических узлов): нодулярная склерозирующая HL, смешанно-клеточный подтип, богатая лимфоцитами или с лимфоидным преобладанием, с лимфоидным истощением. Иногда лимфома Ходжкина также может представлять собой нодулярную лимфому Ходжкина с лимфоидным преобладанием или может быть неуточненной. Симптомы и признаки лимфомы Ходжкина включают безболезненное увеличение лимфатических узлов в области шеи, подмышечных впадин или паха, лихорадку, ночную потливость, потерю веса, утомляемость, кожный зуд или боль в животе.
Неходжкинская лимфома (NHL) представляет собой группу разнообразных видов рака крови, которые включают любую разновидность лимфомы, отличную от лимфомы Ходжкина. Подтипы неходжкинской лимфомы классифицируют в основном по морфологическим характеристикам клеток, хромосомным аберрациям и поверхностным маркерам. Подтипы NHL (или NHL-ассоциированные виды рака) включают В-клеточные лимфомы, такие как без ограничения лимфома Беркитта, хронический лимфоцитарный В-клеточный лейкоз (B-CLL), пролимфоцитарный B-клеточный лейкоз (B-PLL), хронический лимфоцитарный лейкоз (CLL), диффузная крупноклеточная В-клеточная лимфома (DLBCL) (например, внутрисосудистая крупноклеточная B-клеточная лимфома и первичная медиастинальная B-клеточная лимфома), фолликулярная лимфома (например, лимфома из клеток центра фолликула, фолликулярная мелкоклеточная лимфома с расщепленными ядрами), волосатоклеточный лейкоз, B-клеточная лимфома высокой степени злокачественности (подобная лимфоме Беркитта), лимфоплазмоцитарная лимфома (макроглобулинемия Вальденстрема), мантийноклеточная лимфома, виды B-клеточной лимфомы из клеток маргинальной зоны (например, внеузловая B-клеточная лимфома из клеток маргинальной зоны или лимфома из лимфоидной ткани слизистых оболочек (MALT), узловая В-клеточная лимфома из клеток маргинальной зоны и В-клеточная лимфома из клеток маргинальной зоны селезенки), плазмоцитома/миелома, B-лимфобластный лейкоз/лимфома из клеток-предшественников (PB-LBL/L), первичная лимфома центральной нервной системы (CNS), первичная внутриглазная лимфома, мелкоклеточная лимфоцитарная лимфома (SLL); и виды T-клеточной лимфомы, такие как без ограничения анапластическая крупноклеточная лимфома (ALCL), T-клеточная лимфома/лейкоз взрослых (например, "тлеющая", хроническая, острая и лимфоматозная), лимфангиома, ангиоиммунобластная Т-клеточная лимфома, виды T-клеточной лимфомы кожи (например, фунгоидный микоз, синдром Сезари и т. д.), внеузловая лимфома из T-клеток/естественных киллеров (назальный тип), Т-клеточная лимфома кишечника энтеропатического типа, лейкоз из больших гранулярных лимфоцитов, T-лимфобластная лимфома/лейкоз из клеток-предшественников (T-LBL/L), T-клеточный хронический лимфоцитарный лейкоз/пролимфоцитарный лейкоз (T-CLL/PLL) и неуточненная периферическая T-клеточная лимфома. Симптомы и признаки лимфомы Ходжкина включают безболезненное увеличение лимфатических узлов в области шеи, подмышечных впадин или паха, лихорадку, ночную потливость, потерю веса, утомляемость, кожный зуд, боль в животе, кашель или боль в груди.
Также было установлено, что экспрессия BCMA ассоциирована с макроглобулинемией Вальденстрема (WM), также известной как лимфоплазмоцитарная лимфома (LPL). (см. Elsawa et al., Blood. 2006, 107(7):2882-8). Ранее считалось, что макроглобулинемия Вальденстрема является родственной по отношению к множественной миеломе, но совсем недавно ее классифицировали как подтип неходжкинской лимфомы. WM характеризуется неконтролируемой пролиферацией В-клеточных лимфоцитов, что приводит к анемии и продуцированию избыточных количеств парапротеина или иммуноглобулина М (IgM), который сгущает кровь и приводит к синдрому повышенной вязкости крови. Другие симптомы или признаки WM включают лихорадку, ночную потливость, утомляемость, анемию, потерю веса, лимфаденопатию или спленомегалию, нечеткость зрения, головокружение, носовые кровотечения, кровоточивость десен, нетипичные кровоподтеки, нарушение функции почек или почечную недостаточность, амилоидоз или периферическую нейропатию.
Другим примером заболевания или нарушения, ассоциированного с экспрессией BCMA, является рак головного мозга. В частности, экспрессия ВСМА была ассоциирована с астроцитомой или глиобластомой (см. Deshayes et al, Oncogene. 2004, 23(17):3005-12, Pelekanou et al., PLoS One. 2013, 8(12):e83250). Астроцитомы представляют собой опухоли, которые возникают из астроцитов, представляющих собой тип глиальных клеток в головном мозге. Глиобластома (также известная как мультиформная глиобластома или GBM) является наиболее злокачественной формой астроцитомы и считается наиболее поздней стадией рака головного мозга (стадией IV). Существуют два варианта глиобластомы: гигантоклеточная глиобластома и глиосаркома. Другие виды астроцитомы включают ювенильную пилоцитарную астроцитому (JPA), фибриллярную астроцитому, плеоморфную ксантоастроцитому (PXA), дисэмбриопластическую нейроэпителиальную опухоль (DNET) и анапластическую астроцитому (AA).
Симптомы или признаки, ассоциированные с глиобластомой или астроцитомой, включают повышенное давление в головном мозге, головные боли, эпилептические припадки, потерю памяти, изменения в поведении, нарушение движения или потерю чувствительности на одной стороне тела, речевую дисфункцию, когнитивные нарушения, нарушения зрения, тошноту, рвоту и слабость в руках или ногах.
Хирургическое удаление опухоли (или резекция) является стандартным лечением для удаления как можно большей части глиомы без повреждения или с минимальным повреждением окружающей нормальной ткани головного мозга. Лучевая терапия и/или химиотерапия часто используются после хирургического вмешательства для подавления и замедления рецидивирующего заболевания, обусловленного любыми оставшимися раковыми клетками или сопутствующими очагами. Лучевая терапия включает лучевую терапию всего головного мозга (традиционную дистанционную лучевую терапию), целенаправленную трехмерную конформную лучевую терапию и применение целенаправленно воздействующих радионуклидов. Химиотерапевтические средства, обычно используемые для лечения глиобластомы, включают темозоломид, гефитиниб или эрлотиниб и цисплатин. Ингибиторы ангиогенеза, такие как бевацизумаб (Avastin®), также обычно используют в комбинации с химиотерапией и/или лучевой терапией.
Поддерживающее лечение также часто используют для облегчения неврологических симптомов и улучшения неврологической функции и используют в комбинации с любым из средств терапии рака, описанных в данном документе. Основные поддерживающие средства включают противосудорожные средства и кортикостероиды. Таким образом, композиции и способы по настоящему изобретению можно применять в комбинации с любыми видами стандартного или поддерживающего лечения с целью лечения глиобластомы или астроцитомы.
В настоящем изобретении предусмотрены композиции и способы для лечения рака. В одном аспекте рак представляет собой гематологический рак, включая без ограничения лейкоз или лимфому. В одном аспекте в настоящем документе раскрыты способы лечения видов рака и злокачественных новообразований, включая без ограничения, например, острые лейкозы, включая без ограничения, например, B-клеточный острый лимфоидный лейкоз ("BALL"), T-клеточный острый лимфоидный лейкоз ("TALL"), острый лимфоидный лейкоз (ALL); один или более видов хронического лейкоза, включая без ограничения, например, хронический миелоидный лейкоз (CML), хронический лимфоидный лейкоз (CLL); дополнительные гематологические виды рака или гематологические состояния, включая без ограничения, например, B-клеточный пролимфоцитарный лейкоз, бластное плазмоцитоидное дендритное клеточное новообразование, лимфому Беркитта, диффузную крупноклеточную B-клеточную лимфому, фолликулярную лимфому, волосатоклеточный лейкоз, мелкоклеточную или крупноклеточную фолликулярную лимфому, злокачественные лимфопролиферативные состояния, MALT-лимфому, мантийноклеточную лимфому, лимфому из клеток маргинальной зоны, множественную миелому, миелодисплазию и миелодиспластический синдром, неходжкинскую лимфому, плазмобластную лимфому, плазмоцитоидное дендритное клеточное новообразование, макроглобулинемию Вальденстрема и "предлейкоз", которые представляют собой совокупность различных гематологических состояний, объединенных неэффективным образованием (или дисплазией) миелоидных клеток крови и т. п. Другие заболевания, ассоциированные с экспрессией ВСМА, включают без ограничения, например, атипичные и/или неклассические виды рака, злокачественные новообразования, предраковые состояния или пролиферативные заболевания, характеризующиеся экспрессией ВСМА.
В некоторых вариантах осуществления BCMA-связывающую молекулу можно применять для лечения заболевания, включающего без ограничения нарушение пролиферации плазматических клеток, например, бессимптомную миелому (тлеющую множественную миелому или вялотекущую миелому), моноклональную гаммапатию неясного генеза (MGUS), макроглобулинемию Вальденстрема, виды плазмоцитомы (например, плазмоклеточную дискразию, солитарную миелому, солитарную плазмоцитому, экстрамедуллярную плазмоцитому и множественную плазмоцитому), системный амилоидоз в форме амилоидоза легких цепей и POEMS-синдром (также известный как синдром Кроу-Фукаса, болезнь Такатсуки и PEP-синдром).
В некоторых вариантах осуществления BCMA-связывающую молекулу можно применять для лечения заболевания, включающего без ограничения рак, например, рак, описанный в данном документе, например, рак предстательной железы (например, резистентный к кастрации или резистентный к терапии рак предстательной железы или метастатический рак предстательной железы), рак поджелудочной железы или рак легкого.
В настоящем изобретении также предусмотрены способы подавления пролиферации или уменьшения популяции клеток, экспрессирующих BCMA, при этом способы включают приведение популяции клеток, содержащей клетку, экспрессирующую BMCA, в контакт с BCMA-связывающей молекулой. В определенном аспекте в настоящем изобретении предусмотрены способы подавления пролиферации или уменьшения популяции раковых клеток, экспрессирующих BCMA, при этом способы включают приведение популяции раковых клеток, экспрессирующих BCMA, в контакт с BCMA-связывающей молекулой. В одном аспекте в настоящем изобретении предусмотрены способы подавления пролиферации или уменьшения популяции раковых клеток, экспрессирующих BCMA, при этом способы включают приведение популяции раковых клеток, экспрессирующих BMCA, в контакт с BCMA-связывающей молекулой. В определенных аспектах способы снижают количество, число, численность или процентное содержание клеток и/или раковых клеток на по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 65%, по меньшей мере 75%, по меньшей мере 85%, по меньшей мере 95% или по меньшей мере 99% у субъекта с миелоидным лейкозом или другим видом рака, ассоциированным с клетками, экспрессирующими BCMA, или в соответствующей животной модели, по сравнению с отрицательным контролем. В одном аспекте субъектом является человек.
В настоящем изобретении предусмотрены способы предупреждения рецидива рака, ассоциированного с клетками, экспрессирующими BCMA, при этом способы включают введение нуждающемуся в этом субъекту BCMA-связывающей молекулы.
7.13.2. Заболевания и нарушения, не связанные с раком
Заболевания и нарушения, не связанные с раком, но ассоциированные с экспрессией ВСМА, также можно лечить с помощью композиций и способов, раскрытых в данном документе. Примеры заболеваний и нарушений, не связанных с раком, но ассоциированных с экспрессией BCMA, включают без ограничения вирусные инфекции, например, вызванные HIV; грибковые инфекции, например, вызванные C. neoformans; и аутоиммунные заболевания.
Аутоиммунные нарушения, которые можно лечить с помощью BCMA-связывающих молекул по настоящему изобретению, включают системную красную волчанку (SLE), синдром Шегрена, склеродермию, ревматоидный артрит (RA), ювенильный идиопатический артрит, реакцию "трансплантат против хозяина", дерматомиозит, сахарный диабет I типа, тиреоидит Хашимото, болезнь Грейвса, болезнь Аддисона, целиакию, нарушения, связанные с иммунитетом слизистых оболочек, заболевания, связанные с раздраженным кишечником (например, болезнь Крона, язвенный колит), злокачественную анемию, обыкновенную пузырчатку, витилиго, аутоиммунную гемолитическую анемию, идиопатическую тромбоцитопеническую пурпуру, гигантоклеточный артериит, тяжелую миастению, рассеянный склероз (MS) (например, рецидивирующе-ремиттирующий MS (RRMS)), гломерулонефрит, синдром Гудпасчера, буллезный пемфигоид, язвенный колит, синдром Гийена-Барре, хроническую воспалительную демиелинизирующую полинейропатию, антифосфолипидный синдром, нарколепсию, саркоидоз и гранулематоз Вегенера.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения системной красной волчанки (SLE).
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения синдрома Шегрена.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения склеродермии.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения ревматоидного артрита (RA).
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения ювенильного идиопатического артрита.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения реакции "трансплантат против хозяина".
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения дерматомиозита.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения сахарного диабета I типа.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения тиреоидита Хашимото.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения болезни Грейвса.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения болезни Аддисона.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения целиакии.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения болезни Крона.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения злокачественной анемии.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения обыкновенной пузырчатки.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения витилиго.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения аутоиммунной гемолитической анемии.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения идиопатической тромбоцитопенической пурпуры.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения гигантоклеточного артериита.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения тяжелой миастении.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения рассеянного склероза (MS). В некоторых вариантах осуществления MS представляет собой рецидивирующе-ремиттирующий MS (RRMS).
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения гломерулонефрита.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения синдрома Гудпасчера.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения буллезного пемфигоида.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения язвенного колита.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения синдрома Гийена-Барре.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения хронической воспалительной демиелинизирующей полинейропатии.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения антифосфолипидного синдрома.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения нарколепсии.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения саркоидоза.
В некоторых вариантах осуществления BCMA-связывающие молекулы применяют для лечения гранулематоза Вегенера.
7.14. Комбинированная терапия
BCMA-связывающую молекулу по настоящему изобретению можно применять в комбинации с другими известными средствами и видами терапии. Например, BCMA-связывающие молекулы можно применять в схемах лечения в комбинации с хирургическим вмешательством, химиотерапией, антителами, облучением, пептидными вакцинами, стероидами, цитотоксинами, ингибиторами протеасом, иммуномодулирующими лекарственными средствами (например, IMiD), миметиками BH3, средствами цитокиновой терапии, трансплантацией стволовых клеток или любой их комбинацией.
Для удобства средство, которое применяют в комбинации с BCMA-связывающей молекулой, в данном документе называется "дополнительным" средством.
Как используется в данном документе, вводимый "в комбинации" означает, что два (или более) различных средства для лечения доставляют субъекту в период, когда субъект страдает нарушением, например, два или более средства для лечения доставляют после того, как у субъекта было диагностировано нарушение, и до того, как нарушение было излечено или устранено или лечение было прекращено по другим причинам. В некоторых вариантах осуществления доставка одного средства для лечения все еще осуществляется, когда начинается доставка второго, так что в отношении введения имеет место перекрывание. Это иногда упоминается в данном документе как "одновременная" или "параллельная" доставка. Термин "одновременно" не ограничивается введением средств терапии (например, BCMA-связывающей молекулы и дополнительного средства) точно в одно и то же время, а скорее означает, что фармацевтическую композицию, содержащую BCMA-связывающую молекулу, вводят субъекту последовательно и в течение временного интервала таким образом, чтобы BCMA-связывающие молекулы могли действовать вместе с дополнительным(дополнительными) средством(средствами) терапии с обеспечением большей пользы, чем если бы их вводили иным способом. Например, каждое средство терапии можно вводить субъекту в одно и то же время или последовательно в любом порядке в разные моменты времени; однако, если их не вводят в одно и то же время, их следует вводить достаточно близко друг к другу по времени, чтобы обеспечить требуемый терапевтический эффект.
BCMA-связывающую молекулу и одно или несколько дополнительных средств можно вводить одновременно в одной и той же или отдельных композициях или последовательно. В случае последовательного введения BCMA-связывающую молекулу можно вводить первой, а дополнительное средство можно вводить вторым, или порядок введения может быть обратным.
BCMA-связывающую молекулу и дополнительное(дополнительные) средство(средства) можно вводить субъекту в любой подходящей форме и любым подходящим путем. В некоторых вариантах осуществления пути введения являются одинаковыми. В других вариантах осуществления пути введения являются разными.
В других вариантах осуществления доставка одного средства для лечения завершается до начала доставки другого средства для лечения.
В некоторых вариантах осуществления в любом случае лечение является более эффективным благодаря комбинированному введению. Например, второе средство для лечения является более эффективным, например, эквивалентный эффект наблюдается при меньшем количестве второго средства для лечения, или второе средство для лечения обеспечивает снижение интенсивности симптомов в большей степени, чем наблюдалось бы при введении второго средства для лечения в отсутствие первого средства для лечения, или аналогичная ситуация наблюдается с первым средством для лечения. В некоторых вариантах осуществления доставка является такой, при которой снижение интенсивности симптома или другого параметра, связанного с нарушением, является более значительным, чем наблюдалось бы при доставке одного средства для лечения в отсутствие другого. Эффект двух средств для лечения может быть частично аддитивным, полностью аддитивным или превышающим аддитивный. Доставка может быть такой, что эффект от первого доставленного средства для лечения все еще поддается выявлению при доставке второго.
BCMA-связывающую молекулу и/или дополнительные средства можно вводить в течение периодов активного проявления нарушения или в течение периода ремиссии или менее активного проявления заболевания. BCMA-связывающую молекулу можно вводить до лечения с помощью дополнительного(дополнительных) средства(средств), одновременно с лечением с помощью дополнительного(дополнительных) средства(средств), после лечения с помощью дополнительного(дополнительных) средства(средств) или во время ремиссии нарушения.
При введении в комбинации BCMA-связывающая молекула и/или дополнительное(дополнительные) средство(средства) можно вводить в количестве или дозе, которые являются более высокими, более низкими или такими же по сравнению с количеством или дозой каждого средства, применяемого отдельно, например, в качестве монотерапии.
Дополнительное(дополнительные) средство(средства) в видах комбинированной терапии по настоящему изобретению можно вводить субъекту одновременно. Термин "одновременно" не ограничивается введением средств терапии (например, профилактических или терапевтических средств) точно в одно и то же время, а скорее означает, что фармацевтическую композицию, содержащую BCMA-связывающую молекулу, вводят субъекту последовательно и в течение временного интервала таким образом, чтобы молекулы по настоящему изобретению могли действовать вместе с дополнительным(дополнительными) средством(средствами) терапии с обеспечением большей пользы, чем если бы их вводили иным способом. Например, каждое средство терапии можно вводить субъекту в одно и то же время или последовательно в любом порядке в разные моменты времени; однако, если их не вводят в одно и то же время, их следует вводить достаточно близко друг к другу по времени, чтобы обеспечить требуемый терапевтический или профилактический эффект. Каждое средство терапии можно вводить субъекту отдельно в любой подходящей форме и любым подходящим путем.
BCMA-связывающую молекулу и дополнительное(дополнительные) средство(средства) можно вводить субъекту одинаковыми или разными путями введения.
BCMA-связывающие молекулы и дополнительное(дополнительные) средство(средства) можно вводить циклически. Циклическая терапия предусматривает введение первого средства терапии (например, первого профилактического или терапевтического средства) в течение некоторого периода времени, а затем введение второго средства терапии (например, второго профилактического или терапевтического средства) в течение некоторого периода времени, необязательно с последующим введением третьего средства терапии (например, профилактического или терапевтического средства) в течение некоторого периода времени и т. д. и повторение этого последовательного введения, т. е. цикла, с целью снижения темпов развития устойчивости к одному из средств терапии, для недопущения или снижения побочных эффектов одного из средств терапии и/или для улучшения эффективности средств терапии.
В определенных случаях одно или несколько дополнительных средств представляют собой другие противораковые средства, противоаллергические средства, противотошнотные средства (или противорвотные средства), обезболивающие средства, цитопротекторные средства и их комбинации.
В одном варианте осуществления BCMA-связывающую молекулу можно применять в комбинации с противораковым средством (например, с химиотерапевтическим средством). Иллюстративные химиотерапевтические средства включают антрациклин (например, доксорубицин (например, липосомальный доксорубицин)), алкалоид барвинка (например, винбластин, винкристин, виндезин, винорелбин), алкилирующее средство (например, циклофосфамид, декарбазин, мелфалан, ифосфамид, темозоломид), антитело к клеткам иммунной системы (например, алемтузумаб, гемтузумаб, ритуксимаб, тозитумомаб, обинутузумаб, офатумумаб, даратумумаб, элотузумаб), антиметаболит (в том числе, например, антагонисты фолиевой кислоты, аналоги пиримидина, аналоги пурина и ингибиторы аденозиндезаминазы (например, флударабин)), ингибитор mTOR, агонист белка, родственного глюкокортикоид-индуцируемым TNFR (GITR), ингибитор протеасом (например, аклациномицин A, глиотоксин или бортезомиб), иммуномодулятор, такой как талидомид или производное талидомида (например, леналидомид).
Основные химиотерапевтические средства, рассматриваемые для применения в видах комбинированной терапии, включают анастрозол (Arimidex®), бикалутамид (Casodex®), сульфат блеомицина (Blenoxane®), бусульфан (Myleran®), бусульфан для инъекций (Busulfex®), капецитабин (Xeloda®), N4-пентоксикарбонил-5-дезокси-5-фторцитидин, карбоплатин (Paraplatin®), кармустин (BiCNU®), хлорамбуцил (Leukeran®), цисплатин (Platinol®), кладрибин (Leustatin®), циклофосфамид (Cytoxan® или Neosar®), цитарабин, цитозинарабинозид (Cytosar-U®), липосомальный цитарабин для инъекций (DepoCyt®), дакарбазин (DTIC-Dome®), дактиномицин (актиномицин D, Cosmegan), гидрохлорид даунорубицина (Cerubidine®), липосомальный цитрат даунорубицина для инъекций (DaunoXome®), дексаметазон, доцетаксел (Taxotere®), гидрохлорид доксорубицина (Adriamycin®, Rubex®), этопозид (Vepesid®), фосфат флударабина (Fludara®), 5-фторурацил (Adrucil®, Efudex®), флутамид (Eulexin®), тезацитибин, гемцитабин (дифтордезоксицитидин), гидроксимочевину (Hydrea®), идарубицин (Idamycin®), ифосфамид (IFEX®), иринотекан (Camptosar®), L-аспарагиназу (ELSPAR®), лейковорин кальция, мелфалан (Alkeran®), 6-меркаптопурин (Purinethol®), метотрексат (Folex®), митоксантрон (Novantrone®), милотарг, паклитаксел (Taxol®), феникс (иттрий-90/MX-DTPA), пентостатин, полифепрозан 20 с кармустином для имплантации (Gliadel®), цитрат тамоксифена (Nolvadex®), тенипозид (Vumon®), 6-тиогуанин, тиотепу, тирапазамин (Tirazone®), гидрохлорид топотекана для инъекций (Hycamptin®), винбластин (Velban®), винкристин (Oncovin®) и винорелбин (Navelbine®).
Противораковые средства, представляющие особый интерес для комбинаций с BCMA-связывающими молекулами по настоящему изобретению, включают антрациклины; алкилирующие средства; антиметаболиты; лекарственные средства, которые ингибируют кальций-зависимую фосфатазу кальциневрин или киназу p70S6 (FK506) или ингибируют киназу p70S6; ингибиторы mTOR; иммуномодуляторы; антрациклины; алкалоиды барвинка; ингибиторы протеасом; агонисты GITR (например, GWN323); ингибиторы протеинтирозинфосфатаз; ингибитор киназы CDK4; ингибитор BTK; ингибитор киназы MKN; ингибитор киназы DGK; онколитический вирус; миметик BH3 и средства цитокиновой терапии.
Иллюстративные алкилирующие средства включают без ограничения азотистые иприты, производные этиленимина, алкилсульфонаты, нитрозомочевины и триазены: урациловый иприт (Aminouracil Mustard®, Chlorethaminacil®, Demethyldopan®, Desmethyldopan®, Haemanthamine®, Nordopan®, Uracil nitrogen mustard®, Uracillost®, Uracilmostaza®, Uramustin®, Uramustine®), хлорметин (Mustargen®), циклофосфамид (Cytoxan®, Neosar®, Clafen®, Endoxan®, Procytox®, RevimmuneTM), ифосфамид (Mitoxana®), мелфалан (Alkeran®), хлорамбуцил (Leukeran®), пипоброман (Amedel®, Vercyte®), триэтиленмеламин (Hemel®, Hexalen®, Hexastat®), триэтилентиофосфорамин, темозоломид (Temodar®), тиотепу (Thioplex®), бусульфан (Busilvex®, Myleran®), кармустин (BiCNU®), ломустин (CeeNU®), стрептозоцин (Zanosar®) и дакарбазин (DTIC-Dome®). Дополнительные иллюстративные алкилирующие средства включают без ограничения оксалиплатин (Eloxatin®); темозоломид (Temodar® и Temodal®); дактиномицин (также известный как актиномицин-D, Cosmegen®); мелфалан (также известный как L-PAM, L-сарколизин и фенилаланиновый иприт, Alkeran®); алтретамин (также известный как гексаметилмеламин (HMM), Hexalen®); кармустин (BiCNU®); бендамустин (Treanda®); бусульфан (Busulfex® и Myleran®); карбоплатин (Paraplatin®); ломустин (также известный как CCNU, CeeNU®); цисплатин (также известный как CDDP, Platinol® и Platinol®-AQ); хлорамбуцил (Leukeran®); циклофосфамид (Cytoxan® и Neosar®); дакарбазин (также известный как DTIC, DIC и имидазолкарбоксамид, DTIC-Dome®); алтретамин (также известный как гексаметилмеламин (HMM), Hexalen®); ифосфамид (Ifex®); преднумустин; прокарбазин (Matulane®); мехлорэтамин (также известный как азотистый иприт, мустин и гидрохлорид мехлорэтамина, Mustargen®); стрептозоцин (Zanosar®); тиотепу (также известную как тиофосфамид, TESPA и TSPA, Thioplex®); циклофосфамид (Endoxan®, Cytoxan®, Neosar®, Procytox®, Revimmune®) и бендамустин-HCl (Treanda®).
Иллюстративные ингибиторы mTOR включают, например, темсиролимус; ридафоролимус (ранее известный как деферолимус, (1R,2R,4S)-4-[(2R)-2-[(1R,9S,12S,15R,16E,18R,19R,21R, 23S,24E,26E,28Z,30S,32S,35R)-1,18-дигидрокси-19,30-диметокси-15,17,21,23,29,35-гексаметил-2,3,10,14,20-пентаоксо-11,36-диокса-4-азатрицикло[30.3.1.04,9]гексатриаконта-16,24,26,28-тетраен-12-ил]пропил]-2-метоциклогексилдиметилфосфинат, также известный как AP23573 и MK8669 и описанный в PCT-публикации № WO 03/064383); эверолимус (Afinitor® или RAD001); рапамицин (AY22989, Sirolimus®); симапимод (CAS 164301-51-3); эмсиролимус, (5-{2,4-бис[(3S)-3-метилморфолин-4-ил]пиридо[2,3-d]пиримидин-7-ил}-2-метоксифенил)метанол (AZD8055); 2-амино-8-[транс-4-(2-гидроксиэтокси)циклогексил]-6-(6-метокси-3-пиридинил)-4-метилпиридо[2,3-d]пиримидин-7(8H)-он (PF04691502, CAS 1013101-36-4), а также N2-[1,4-диоксо-4-[[4-(4-оксо-8-фенил-4H-1-бензoпиран-2-ил)морфолиний-4-ил]метокси]бутил]-L-аргинилглицил-L-α-аспартил-L-серин (SEQ ID NO:514) в форме внутренней соли (SF1126, CAS 936487-67-1) и XL765.
Иллюстративные иммуномодуляторы включают, например, афутузумаб (доступный от Roche®); пегфилграстим (Neulasta®); леналидомид (CC-5013, Revlimid®); IMID (такие как талидомид (Thalomid®), леналидомид, помалидомид и апремиласт), актимид (CC4047) и IRX-2 (смесь цитокинов человека, содержащую интерлейкин-1, интерлейкин-2 и интерферон γ, CAS 951209-71-5, доступную от IRX Therapeutics).
Иллюстративные антрациклины включают, например, доксорубицин (Adriamycin® и Rubex®); блеомицин (Lenoxane®); даунорубицин (гидрохлорид даунорубицина, дауномицин и гидрохлорид рубидомицина, Cerubidine®); липосомальный даунорубицин (липосомальный цитрат даунорубицина, DaunoXome®); митоксантрон (DHAD, Novantrone®); эпирубицин (Ellence™); идарубицин (Idamycin®, Idamycin PFS®); митомицин C (Mutamycin®); гелданамицин; гербимицин; равидомицин и дезацетилравидомицин.
Иллюстративные алкалоиды барвинка включают, например, тартрат винорелбина (Navelbine®), винкристин (Oncovin®) и виндезин (Eldisine®); винбластин (также известный как сульфат винбластина, винкалейкобластин и VLB, Alkaban-AQ® и Velban®) и винорелбин (Navelbine®).
Иллюстративные ингибиторы протеасом включают бортезомиб (Velcade®); карфилзомиб (PX-171-007, (S)-4-метил-N-((S)-1-(((S)-4-метил-1-((R)-2-метилоксиран-2-ил)-1-оксопентан-2-ил)амино)-1-оксо-3-фенилпропан-2-ил)-2-((S)-2-(2-морфолиноацетамидо)-4-фенилбутанамидо)пентанамид); маризомиб (NPI-0052); цитрат иксазомиба (MLN-9708); деланзомиб (CEP-18770) и O-метил-N-[(2-метил-5-тиазолил)карбонил]-L-серил-O-метил-N-[(1S)-2-[(2R)-2-метил-2-оксиранил]-2-оксо-1-(фенилметил)этил]-L-серинамид (ONX-0912).
Иллюстративные миметики BH3 включают венетоклакс, ABT-737 (4-{4-[(4'-хлор-2-бифенилил)метил]-1-пиперазинил}-N-[(4-{[(2R)-4-(диметиламино)-1-(фенилсульфанил)-2-бутанил]амино}-3-нитрофенил)сульфонил]бензамид и навитоклакс (ранее ABT-263).
Иллюстративные средства цитокиновой терапии включают интерлейкин 2 (IL-2) и интерферон альфа (IFN-альфа).
В определенных аспектах в качестве дополнительного(дополнительных) средства(средств) вводят "коктейли" различных химиотерапевтических средств.
В одном аспекте в настоящем изобретении предусмотрен способ лечения субъектов, у которых имеется заболевание, ассоциированное с экспрессией BCMA, включающий введение субъекту эффективного количества: (i) BCMA-связывающей молекулы и (ii) ингибитора гамма-секретазы (GSI).
В одном аспекте в настоящем изобретении предусмотрен способ лечения субъектов, которые прошли лечение от заболевания, ассоциированного с экспрессией BCMA, включающий введение субъекту эффективного количества: (i) BCMA-связывающей молекулы и (ii) GSI.
В одном варианте осуществления BCMA-связывающую молекулу и GSI вводят одновременно или последовательно. В одном варианте осуществления BCMA-связывающую молекулу вводят до введения GSI. В одном варианте осуществления GSI вводят до введения BCMA-связывающей молекулы. В одном варианте осуществления BCMA-связывающую молекулу и GSI вводят одновременно.
В одном варианте осуществления GSI вводят до введения ВСМА-связывающей молекулы (например, GSI вводят за 1, 2, 3, 4 или 5 дней до введения ВСМА-связывающей молекулы), где необязательно после введения GSI и до введения ВСМА-связывающей молекулы у субъекта наблюдается повышение уровней экспрессии ВСМА на клеточной поверхности и/или снижение уровней растворимого ВСМА.
В некоторых вариантах осуществления GSI представляет собой небольшую молекулу, которая снижает экспрессию и/или функцию гамма-секретазы, например, описанный в данном документе низкомолекулярный GSI. В одном варианте осуществления GSI выбран из LY-450139, PF-5212362, BMS-708163, MK-0752, ELN-318463, BMS-299897, LY-411575, DAPT, AL-101 (также известный как BMS-906024), AL-102 (также известный как BMS-986115), PF-3084014, RO4929097 и LY3039478. В одном варианте осуществления GSI выбран из PF-5212362, ELN-318463, BMS-906024 и LY3039478. Иллюстративные GSI раскрыты в Takebe et al., Pharmacol Ther. 2014 Feb;141(2):140-9; и Ran et al., EMBO Mol Med. 2017 Jul;9(7):950-966. В некоторых вариантах осуществления GSI представляет собой AL-101. В некоторых вариантах осуществления GSI представляет собой AL-102.
В некоторых вариантах осуществления MK-0752 вводят в комбинации с доцетакселом. В некоторых вариантах осуществления MK-0752 вводят в комбинации с гемцитабином. В некоторых вариантах осуществления BMS-906024 вводят в комбинации с химиотерапией.
В некоторых вариантах осуществления GSI может представлять собой соединение формулы (I) или его фармацевтически приемлемую соль;
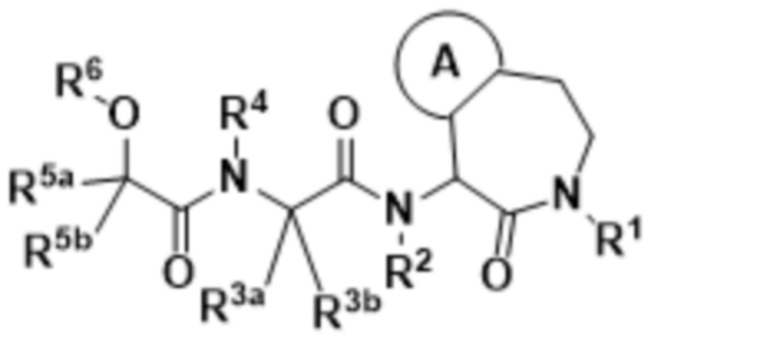 (I)
(I)
где кольцо A представляет собой арил или гетероарил; каждый из R1, R2 и R4 независимо представляет собой водород, C1-C6алкил, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил, где каждый C1-C6алкил, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил замещен в 0-6 независимых случаях галогеном, -ORA, -SRA, -C(O)ORA, -C(O)N(RA)(RB), -N(RA)(RB) или -C(NRC)N(RA)(RB); каждый R3a, R3b, R5a и R5b независимо представляет собой водород, галоген, -OH, C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил, где каждый C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил замещен в 0-6 независимых случаях галогеном, -OH, -ORA, -SRA, -C(O)ORA, -C(O)N(RA)(RB), -N(RA)(RB) или -C(NRC)N(RA)(RB); R6 представляет собой водород, C1-C6алкил, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил, где каждый C1-C6алкил, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил замещен в 0-6 независимых случаях галогеном, -OH или C1-C6 алкокси; и каждый RA, RB и RC независимо представляет собой водород, C1-C6алкил, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил, где каждый C1-C6алкил, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил замещен в 0-6 независимых случаях галогеном, -OH или C1-C6алкокси.
В некоторых вариантах осуществления кольцо A представляет собой арил (например, фенил). В некоторых вариантах осуществления R1 представляет собой -CH3. В некоторых вариантах осуществления каждый из R2 и R4 независимо представляет собой водород. В некоторых вариантах осуществления R3a представляет собой -CH3, а R3b представляет собой водород. В некоторых вариантах осуществления R5a представляет собой водород, а R5b представляет собой -CH(CH3)2. В некоторых вариантах осуществления R6 представляет собой водород.
В дополнительном варианте осуществления GSI представляет собой соединение, описанное в патенте США № 7468365. В одном варианте осуществления GSI представляет собой LY-450139, т. е. семагацестат, (S)-2-гидрокси-3-метил-N-((S)-1-(((S)-3-метил-2-оксо-2,3,4,5-тетрагидро-1H-бензо[d]азепин-1-ил)амино)-1-оксопропан-2-ил)бутанамид или его фармацевтически приемлемую соль. В одном варианте осуществления GSI представляет собой
или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления GSI представляет собой соединение формулы (II) или его фармацевтически приемлемую соль;
 (II)
(II)
где кольцо B представляет собой арил или гетероарил; L представляет собой связь, C1-C6алкилен, -S(O)2-, -C(O)-, -N(RE)(O)C- или -OC(O)-; каждый R7 независимо представляет собой галоген, -OH, C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил, где каждый C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил независимо замещен в 0-6 случаях галогеном, -ORD, -SRD, -C(O)ORD, -C(O)N(RD)(RE), -N(RD)(RE) или -C(NRF)N(RD)(RE); R8 представляет собой водород, C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил, где каждый C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил замещен в 0-6 независимых случаях галогеном, -ORD, -SRD, -C(O)ORD, -C(O)N(RD)(RE), -N(RD)(RE) или -C(NRF)N(RD)(RE); каждый из R9 и R10 независимо представляет собой водород, галоген, -OH, C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил, где каждый C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, арил, гетероарил, аралкил или гетероаралкил замещен в 0-6 независимых случаях галогеном, -ORD, -SRD, -C(O)ORD, -C(O)N(RD)(RE), -N(RD)(RE) или -C(NRI)N(RG)(RH); каждый RD, RE и RF независимо представляет собой водород, C1-C6алкил, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил, где каждый C1-C6алкил, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил замещен в 0-6 независимых случаях галогеном, -OH или C1-C6алкокси; и n равняется 0, 1, 2, 3, 4 или 5.
В некоторых вариантах осуществления кольцо B представляет собой гетероарил (например, тиофуранил). В некоторых вариантах осуществления L представляет собой -S(O)2. В некоторых вариантах осуществления R7 представляет собой хлор, и n равняется 1. В некоторых вариантах осуществления R8 представляет собой -CH2OH. В некоторых вариантах осуществления каждый из R9 и R10 независимо представляет собой -CF3.
В дополнительном варианте осуществления GSI представляет собой соединение, описанное в патенте США № 7687666. В одном варианте осуществления GSI представляет собой PF-5212362, т. е. бегацестат, GSI-953 или (R)-5-хлор-N-(4,4,4-трифтор-1-гидрокси-3-(трифторметил)бутан-2-ил)тиофен-2-сульфонамид или его фармацевтически приемлемую соль. В одном варианте осуществления GSI представляет собой
или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления GSI представляет собой соединение формулы (III) или его фармацевтически приемлемую соль:
 (III)
(III)
где каждое из колец C и D независимо представляет собой арил или гетероарил;
каждый из R11, R12 и R14 независимо представляет собой водород, C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил, где каждый C1-C6алкил, C1-C6алкокси, -S(O)RG-, -S(O)2RG-, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил замещен в 0-6 независимых случаях галогеном, -ORG, -SRG, -C(O)ORG, -C(O)N(RG)(RH), -N(RG)(RH) или -C(NRI)N(RG)(RH); каждый из R13a и R13b представляет собой водород, галоген, -OH, C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил, где каждый C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил замещен в 0-6 независимых случаях галогеном, -ORG, -SRG, -C(O)ORG, -C(O)N(RG)(RH), -N(RG)(RH) или -C(NRI)N(RG)(RH); каждый R15 и R16 независимо представляет собой галоген, -OH, C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил, где каждый C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил замещен в 0-6 независимых случаях галогеном, -ORG, -SRG, -C(O)ORG, -C(O)N(RG)(RH), -N(RG)(RH) или -C(NRI)N(RG)(RH); каждый RG, RH и RI независимо представляет собой водород, C1-C6алкил, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил, где каждый C1-C6алкил, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил замещен в 0-6 независимых случаях галогеном, -OH или C1-C6алкокси; и каждый из m, n и p независимо равняется 0, 1, 2, 3, 4 или 5.
В некоторых вариантах осуществления кольцо C представляет собой арил (например, фенил). В некоторых вариантах осуществления кольцо D представляет собой гетероарил (например, 1,2,4-оксадиазол). В некоторых вариантах осуществления R15 представляет собой фтор, и n равняется 1. В некоторых вариантах осуществления p равняется 0. В некоторых вариантах осуществления m равняется 1. В некоторых вариантах осуществления R14 представляет собой -S(O)2RG, и RG представляет собой хлорфенил. В некоторых вариантах осуществления R13a представляет собой -CH2CH2CF3, а R13b представляет собой водород. В некоторых вариантах осуществления каждый R11 и R12 независимо представляет собой водород.
В дополнительном варианте осуществления GSI представляет собой соединение, описанное в патенте США № 8084477. В одном варианте осуществления GSI представляет собой BMS-708163, т. е. авагацестат, или (R)-2-((4-хлор-N-(2-фтор-4-(1,2,4-оксадиазол-3-ил)бензил)фенил)сульфонамидо)-5,5,5-трифторпентанамид или его фармацевтически приемлемую соль. В одном варианте осуществления GSI представляет собой
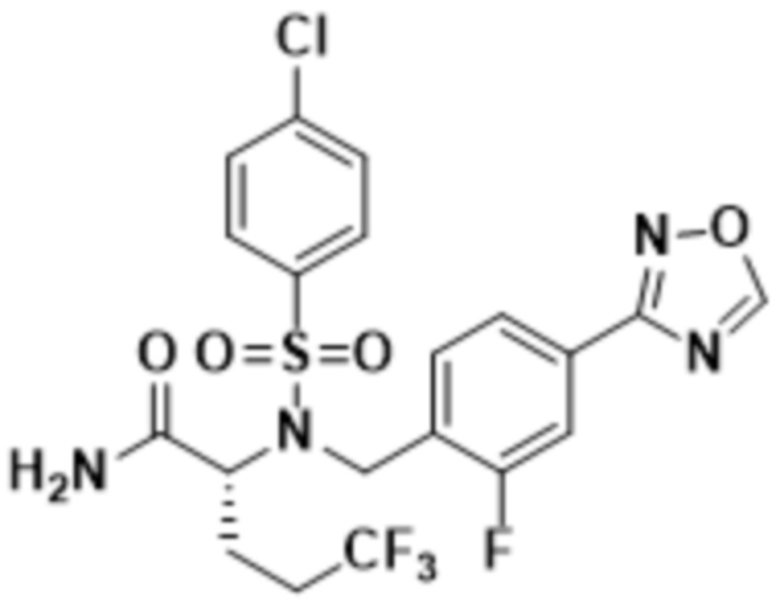
или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления ингибитор гамма-секретазы представляет собой соединение формулы (IV) или его фармацевтически приемлемую соль:
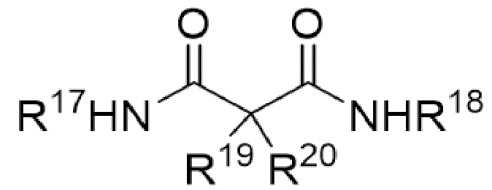 (IV),
(IV),
где R17 выбран из
a. 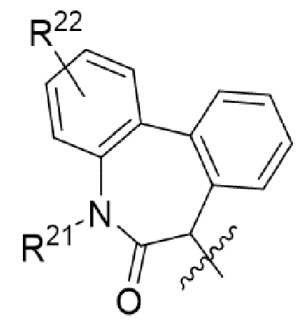 ,
,
b. 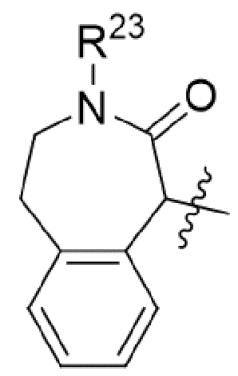 ,
,
c. 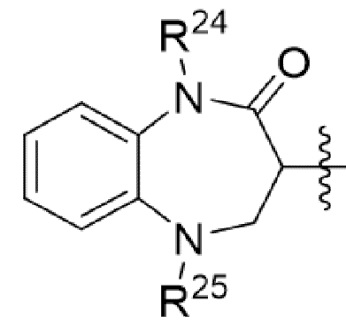 и
и
d. 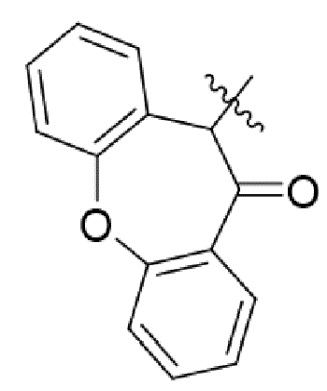 ,
,
R18 представляет собой низший алкил, низший алкинил, -(CH2)n-O-низший алкил, -(CH2)n-S-низший алкил, -(CH2)n-CN, -(CR'R")n-CF3, -(CR'R")n-CHF2, -(CR'R")n-CH2F, -(CH2)n, -C(O)O-низший алкил, -(CH2)n-галоген или представляет собой -(CH2)n-циклоалкил, необязательно замещенный одним или несколькими заместителями, выбранными из группы, состоящей из фенила, галогена и CF3; каждый из R', R" независимо представляет собой водород, низший алкил, низший алкокси, галоген или гидрокси; каждый из R19, R20 независимо представляет собой водород, низший алкил, низший алкокси, фенил или галоген; R21 представляет собой водород, низший алкил, -(CH2)n-CF3 или -(CH2)n-циклоалкил; R22 представляет собой водород или галоген; R23 представляет собой водород или низший алкил; R24 представляет собой водород, низший алкил, низший алкинил, -(CH2)n-CF3, -(CH2)n-циклоалкил или -(CH2)n-фенил, необязательно замещенный галогеном; R25 представляет собой водород, низший алкил, -C(O)H, -C(O)-низший алкил, -C(O)-CF3, -C(O)-CH2F, -C(O)-CHF2, -C(O)-циклоалкил, -C(O)-(CH2)n-O-низший алкил, -C(O)O-(CH2)n-циклоалкил, -C(O)-фенил, необязательно замещенный одним или несколькими заместителями, выбранными из группы, состоящей из галогена и -C(O)O-низшего алкила, или представляет собой -S(O)2-низший алкил, -S(O)2-CF3, -(CH2)n-циклоалкил, или представляет собой -(CH2)n-фенил, необязательно замещенный галогеном; n равняется 0, 1, 2, 3 или 4.
В некоторых вариантах осуществления R17 представляет собой 5,7-дигидро-6H-дибензо[b, d]азепин-6-онил. В некоторых вариантах осуществления каждый R19 и R20 независимо представляет собой -CH3. В некоторых вариантах осуществления R18 представляет собой CH2CF2CF3.
В некоторых вариантах осуществления GSI представляет собой соединение, описанное в патенте США № 7160875. В одном варианте осуществления GSI представляет собой RO4929097, т. е. (S)-2,2-диметил-N1-(6-оксо-6,7-дигидро-5H-дибензо[b, d]азепин-7-ил)-N3-(2,2,3,3,3-пентафторпропил)малонамид или его фармацевтически приемлемую соль. В одном варианте осуществления GSI представляет собой
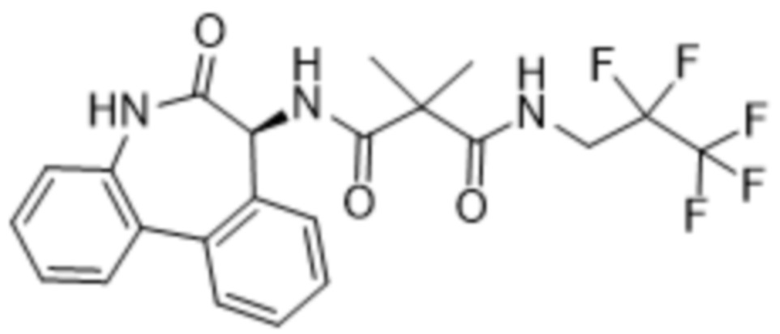
или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления GSI представляет собой
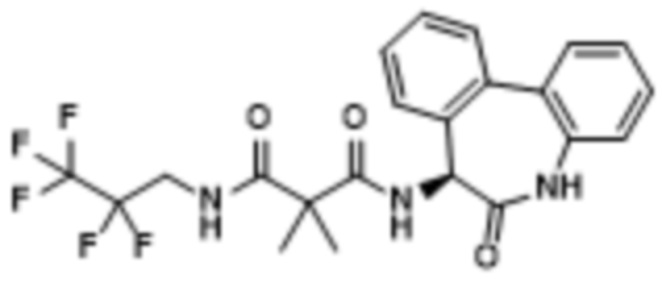
или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления GSI представляет собой соединение формулы (V) или его фармацевтически приемлемую соль:
 (V),
(V),
где
q равняется 0 или 1; Z представляет собой галоген, -CN, -NO2, -N3, -CF3, -OR2a, -N(R2a)2, -CO2R2a, -OCOR2a, -COR2a, -CON(R2a)2, -OCON(R2a)2, -CONR2a(OR2a), -CON(R2a)N(R2a)2, -CONHC(=NOH)R2a, гетероциклил, фенил или гетероарил, при этом гетероциклил, фенил или гетероарил несут 0-3 заместителя, выбранных из галогена, -CN, -NO2, -CF3, -OR2a, -N(R2a)2, -CO2R2a, -COR2a, -CON(R2a)2 и C1-4алкила; R27 представляет собой H, C1-4алкил или OH; R26 представляет собой H или C1-4алкил; при условии, что если m равняется 1, то как R26, так и R27 не представляют собой C1-4алкил; Ar1 представляет собой C6-10арил или гетероарил, любой из которых несет 0-3 заместителя, независимо выбранных из галогена, -CN, -NO2, -CF3, -OH, -OCF3, C1-4алкокси или C1-4алкила, который необязательно несет заместитель, выбранный из галогена, CN, NO2, CF3, OH и C1-4алкокси; Ar2 представляет C6-10арил или гетероарил, любой из которых несет 0-3 заместителя, независимо выбранных из галогена, -CN, -NO2, -CF3, -OH, -OCF3, C1-4алкокси или C1-4алкила, который необязательно несет заместитель, выбранный из галогена, -CN, -NO2, -CF3, -OH и C1-4алкокси; R2a представляет собой H, C1-6алкил, C3-6циклоалкил, C3-6циклоалкил, C1-6алкил, C2-6алкенил, любой из которых необязательно несет заместитель, выбранный из галогена, -CN, -NO2, -CF3, -OR2b, -CO2R2b, -N(R2b)2, -CON(R2b)2, Ar и COAr; или R2a представляет собой Ar; или две группы R2a вместе с атомом азота, к которому они совместно присоединены, могут составлять N-гетероциклильную группу, несущую 0-4 заместителя, независимо выбранных из =O, =S, галогена, C1-4алкила, -CN, -NO2, -CF3, -OH, C1-4алкокси, C1-4алкоксикарбонила, CO2H, амино, C1-4алкиламино, ди(C1-4алкил)амино, карбамоила, Ar и COAr; R2b представляет собой H, C1-6алкил, C3-6циклоалкил, C3-6циклоалкил-C1-6алкил, C2-6алкенил, любой из которых необязательно несет заместитель, выбранный из галогена, -CN, -NO2, -CF3, -OH, C1-4алкокси, C1-4алкоксикарбонила, -CO2H, амино, C1-4алкиламино, ди(C1-4алкил)амино, карбамоила, Ar и COAr; или R2b представляет собой Ar; или две группы R2b вместе с атомом азота, к которому они совместно присоединены, могут составлять N-гетероциклильную группу, несущую 0-4 заместителя, независимо выбранных из =O, =S, галогена, C1-4алкила, -CN, -NO2, CF3, -OH, C1-4алкокси, C1-4алкоксикарбонила, -CO2H, амино, C1-4алкиламино, ди(C1-4алкил)амино, карбамоила, Ar и COAr; Ar представляет собой фенил или гетероарил, несущий 0-3 заместителя, выбранных из галогена, C1-4алкила, -CN, -NO2, -CF3, -OH, C1-4алкокси, C1-4алкоксикарбонила, амино, C1-4алкиламино, ди(C1-4алкил)амино, карбамоила, C1-4алкилкарбамоила и ди(C1-4алкил)карбамоила.
В некоторых вариантах осуществления q равняется 1. В некоторых вариантах осуществления Z представляет собой CO2H. В некоторых вариантах осуществления каждый из R27 и R26 независимо представляет собой водород. В некоторых вариантах осуществления Ar1 представляет собой хлорфенил. В некоторых вариантах осуществления Ar2 представляет собой дифторфенил.
В некоторых вариантах осуществления GSI представляет собой соединение, описанное в патенте США № 6984663. В одном варианте осуществления GSI представляет собой MK-0752, т. е. 3-((1S,4R)-4-((4-хлорфенил)сульфонил)-4-(2,5-дифторфенил)циклогексил)пропановую кислоту или ее фармацевтически приемлемую соль. В некоторых вариантах осуществления GSI представляет собой
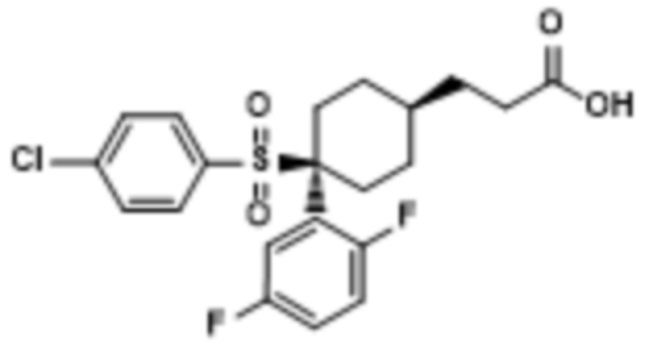
или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления GSI представляет собой соединение формулы (VI) или его фармацевтически приемлемую соль:
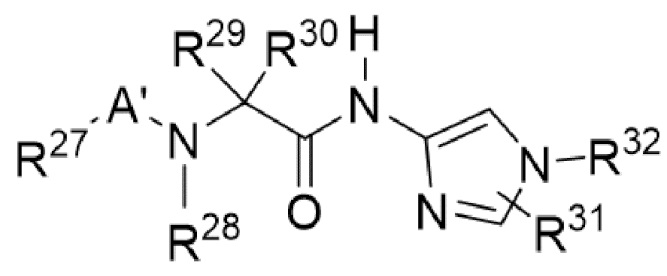 (VI)
(VI)
где A' отсутствует или выбран из
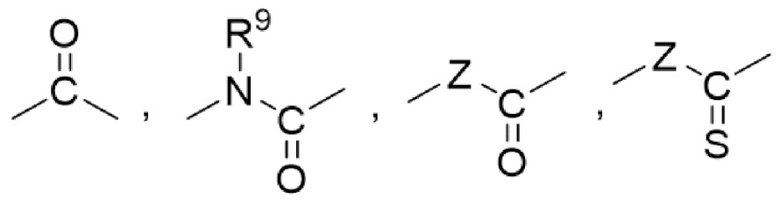 ,
,
а также -S(O)2-;
Z выбран из -CH2, -CH(OH), -CH(C1-C6алкила), -CH(C1-C6алкокси), -CH(NR33R34), -CH(CH2(OH)), -CH(CH(C1-C4алкил)(OH)) и -CH(C(C1-C4 алкил)(C1-C4алкил)(OH)), например, -CH(C(CH3)(CH3)(OH)) или -CH(C(CH3)(CH2CH3)(OH)); R27 выбран из C1-C20алкила, C2-C20алкенила, C2-C20алкинила, C1-C20алкокси, C2-C20алкенокси, C1-C20гидроксиалкила, C3-C8циклоалкила, бензо(C3-C8циклоалкила), бензо(C3-C8гетероциклоалкила), C4-C8циклоалкенила, (C5-C11)би- или трициклоалкила, бензо(C5-C11)би- или трициклоалкила, C7-C11трициклоалкенила, (3-8-членного) гетероциклоалкила, C6-C14арила и (5-14-членного) гетероарила, где каждый атом водорода в алкиле, алкениле, алкиниле, алкокси и алкенокси необязательно независимо заменен на галоген, и где циклоалкил, бензо(C3-C8циклоалкил), циклоалкенил, (3-8-членный) гетероциклоалкил, C6-C14арил и (5-14-членный) гетероарил необязательно независимо замещен заместителями в количестве от одного до четырех, независимо выбранными из C1-C10алкила, необязательно замещенного атомами галогена в количестве от одного до трех, C1-C10алкокси, необязательно замещенного атомами галогена в количестве от одного до трех, C1-C10гидроксиалкила, галогена, например, фтора, -OH, -CN, -NR33R34, -C(=O)NR33R34, -C(=O)R35, C3-C8циклоалкила и (3-8-членного) гетероциклоалкила; R28 выбран из водорода, C1-C6алкила, C2-C6алкенила, C3-C8циклоалкила и C5-C8циклоалкенила, где R28 необязательно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из C1-C4алкила, необязательно замещенного атомами галогена в количестве от одного до трех, C1-C4алкокси, необязательно замещенного атомами галогена в количестве от одного до трех, галогена и -OH; или R27 и R28 вместе с группой A', если она присутствует, и атомом азота, к которому присоединен R28, или R27 и R28 вместе с атомом азота, к которому присоединены R27 и R28, если A' отсутствует, необязательно могут образовывать четырех-восьмичленное кольцо; R29 выбран из водорода, C1-C6алкила, C2-C6алкенила, C2-C6алкинила, C3-C6циклоалкила, C5-C6циклоалкенила и (3-8-членного) гетероциклоалкила, где каждый из алкила, алкенила, алкинила, циклоалкила, циклоалкенила и гетероциклоалкила необязательно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из C1-C4 алкокси, галогена, -OH-S(C1-C4)алкила и (3-8-членного)гетероциклоалкила; R30 представляет собой водород, C1-C6алкил или галоген; или R29 и R30 вместе с атомом углерода, к которому они присоединены, необязательно могут образовывать фрагмент, выбранный из циклопропила, циклобутила, циклопентила, циклогексила, морфолино, пиперидино, пирролидино, тетрагидрофуранила и пергидро-2H-пирана, где фрагмент, образованный R29 и R30, необязательно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из C1-C6алкила, необязательно замещенного атомами галогена в количестве от одного до трех, C1-C6алкокси, необязательно замещенного атомами галогена в количестве от одного до трех, галогена, -OH, -CN и аллила; R31 выбран из водорода, C1-C6алкила, C2-C6алкилена, C1-C6алкокси, галогена, -CN, C3-C12циклоалкила, C4-C12циклоалкенила и C6-C10арила, (5-10-членного) гетероарила, где каждый из алкила, алкилена и алкокси в R31 необязательно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из галогена и -CN, и каждый из циклоалкила, циклоалкенила и арила и гетероарила в R31 необязательно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из C1-C4алкила, необязательно замещенного атомами галогена в количестве от одного до трех, C1-C4алкокси, необязательно замещенного атомами галогена в количестве от одного до трех, галогена и -CN; R32 выбран из водорода, C1-C20алкила, C1-C20алкокси, C1-C20гидроксиалкила, C3-C12циклоалкила, C4-C12циклоалкенила, (C5-C20)би- или трициклоалкила, (C7-C20)би- или трициклоалкенила, (3-12-членного) гетероциклоалкила, (7-20-членного)гетероби- или гетеротрициклоалкила, C6-C14арила и (5-15-членного) гетероарила, где R32 необязательно независимо замещен заместителями в количестве от одного до четырех, независимо выбранными из C1-C20алкила, необязательно замещенного атомами галогена в количестве от одного до трех, C1-C20алкокси, -OH, -CN, -NO2, -NR33R34, -C(=O)NR33R34, -C(=O)R35, -C(=O)OR35, -S(O)nNR33R34, -S(O)nR35, C3-C12циклоалкила, (4-12-членного) гетероциклоалкила, необязательно замещенного группами OH или галогена в количестве от одной до трех, (4-12-членного)гетероциклоалкокси, C6-C14арила, (5-15-членного)гетероарила, C6-C12арилокси и (5-12 членного)гетероарилокси; или R33 и R34 вместе с атомами углерода и азота, к которым они соответственно присоединены, необязательно могут образовывать (5-8-членное) гетероциклоалкильное кольцо, (5-8-членное) гетероциклоалкенильное кольцо или (6-10-членное) гетероарильное кольцо, где каждое из гетероциклоалкильного, гетероциклоалкенильного и гетероарильного кольца необязательно независимо замещено заместителями в количестве от одного до трех, независимо выбранными из галогена, C1-C6алкила, необязательно замещенного атомами галогена в количестве от одного до трех, C1-C6алкокси, необязательно замещенного атомами галогена в количестве от одного до трех, C1-C6гидроксиалкила, -OH, -(CH2)ноль-10NR33R34, -(CH2)ноль-10C(=O)NR33R34, -S(O)2NR33R34 и C3-C12циклоалкила; каждый из R33 и R34 независимо выбран из водорода, C1-C10алкила, где каждый атом водорода в C1-C10алкиле необязательно независимо заменен на атом галогена, например, на атом фтора, C2-C10алкенила, C2-C10алкинила, C1-C6алкокси, где каждый атом водорода в C1-C6алкокси необязательно независимо заменен на атом галогена, C2-C6алкенокси, C2-C6алкинокси, -C(=O)R11, -S(O)nR11, C3-C8циклоалкила, C4-C8циклоалкенила, (C5-C11)би- или трициклоалкила, (C7-C11)би- или трициклоалкенила, (3-8-членного) гетероциклоалкила, C6-C14арила и (5-14-членного) гетероарила, где каждый из алкила и алкокси необязательно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из галогена и -OH, и где каждый из циклоалкила, циклоалкенила, би- или трициклоалкила, би- или трициклоалкенила, гетероциклоалкила, арила и гетероарила необязательно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из галогена, -OH, C1-C6алкила, необязательно независимо замещенного атомами галогена в количестве от одного до шести, C2-C6алкенила, C2-C6алкинила, C1-C6алкокси, C2-C6алкенокси, C2-C6алкинокси и C1-C6гидроксиалкила; или NR33R34 может образовывать (4-7-членный) гетероциклоалкил, где гетероциклоалкил необязательно содержит один или два дополнительных гетероатома, независимо выбранных из N, O и S, и где гетероциклоалкил необязательно содержит двойные связи в количестве от одной до трех, и где гетероциклоалкил необязательно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из C1-C6алкила, необязательно замещенного атомами галогена в количестве от одного до шести, C2-C6алкенила, C2-C6алкинила, C1-C6алкокси, C2-C6алкенокси, C2-C6алкинокси, C1-C6гидроксиалкила, C2-C6гидроксиалкенила, C2-C6гидроксиалкинила, галогена, -OH, -CN, -NO2, -C(=O)R35, -C(=O)OR35, -S(O)nR35 и -S(O)nNR33R34; R35 выбран из водорода, C1-C8алкила, C3-C8циклоалкила, C4-C8циклоалкенила, (C5-C11)би- или трициклоалкила, -(C7-C11)би- или трициклоалкенила, (3-8-членного) гетероциклоалкила, C6-C10арила и (5-14 членного) гетероарила, где алкил в R35 необязательно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из -OH, -CN и C3-C8циклоалкила, и где каждый атом водорода в алкиле необязательно независимо заменен на атом галогена, например, на атом фтора, и где каждый из циклоалкила, циклоалкенила, гетероциклоалкила, арила и гетероарила в R35 необязательно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из галогена, C1-C8алкила, необязательно замещенного атомами галогена в количестве от одного до трех, -OH, -CN и C3-C8циклоалкила; n в каждом случае представляет собой целое число, независимо выбранное из нуля, 1, 2 и 3; и фармацевтически приемлемые соли таких соединений.
В некоторых вариантах осуществления GSI представляет собой соединение, описанное в патенте США № 7795447. В одном варианте осуществления GSI представляет собой PF-3084014, т. е. нирогацестат или (S)-2-(((S)-6,8-дифтор-1,2,3,4-тетрагидронафталин-2-ил)амино)-N-(1-(2-метил-1-(неопентиламино)пропан-2-ил)-1H-имидазол-4-ил)пентанамид или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления GSI представляет собой
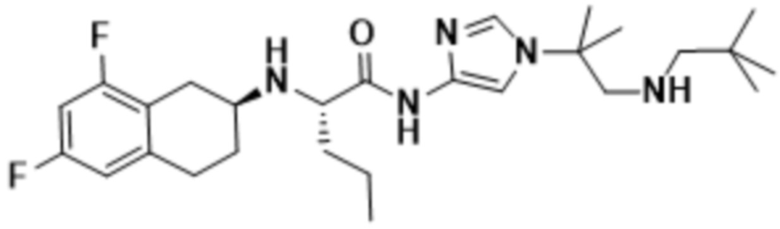
или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления GSI представляет собой соединение формулы (VII):
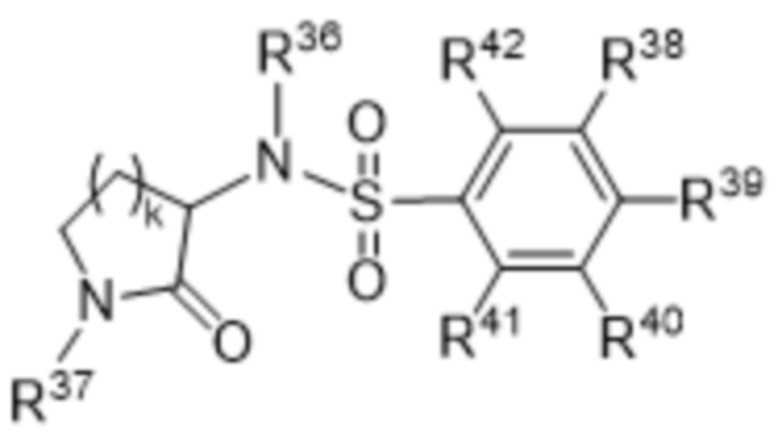 (VII)
(VII)
или его фармацевтически приемлемую соль, где k равняется 1, 2 или 3; R36 представляет собой арил C1-C8алкил, арил C2-C6алкенил или арилалкинил, где арильная группа замещена в 0-5 случаях C1-C6алкилом, C1-C6алкокси, галогеном, галогеналкилом, галогеналкокси, гетероарилом, гетероарил(C1-C6)алкокси, арилалкокси, арилокси, C1-C6 алкоксикарбонилом, -OCH2CH2O-, -OCH2O-, -C(O)NR43R44, -NHR′, -NR′R″, -N(R16)C(O)R17, гетероциклоалкилом, фенилом, арилом C1-C6алканоилом, фенилалкокси, фенилокси, CN, -SO2-арилом, -S(O)nR25, -(C1-C4 алкил)-S(O)xR25, -(C1-C4алкил)-SO2-арилом, OH, C1-C6тиоалкокси, C2-C6алкенилом, -OSO2-арилом или CO2H, где каждый гетероарил независимо замещен в 0-3 случаях C1-C6алкилом, гетероарил замещен в 0-2 случаях галогеном, алкилом, алкокси, галогеналкилом, галогеналкокси, алкоксиалкилом или CN, C1-C6алкокси, C1-C4алкокси, C1-C4алкилом, C3-C6циклоалкилом, галогеном, или фенил замещен в 0-5 случаях галогеном, OH, C1-C6алкилом, C1-C4алкокси, CF3, OCF3, CN или C1-C6тиоалкокси,
где каждый гетероциклоалкил и арил независимо замещены в 0-2 случаях галогеном, алкилом, алкокси, галогеналкилом, галогеналкокси, алкоксиалкилом или CN, C1-C6алкилом, C1-C6алкокси, C1-C4алкокси, C1-C4алкилом, C3-C6циклоалкилом, галогеном, или фенил замещен в 0-5 случаях галогеном, OH, C1-C6алкилом, C1-C4алкокси, CF3, OCF3, CN или C1-C6тиоалкокси; R16 представляет собой водород или C1-C6алкил; R17 представляет собой C1-C6алкил, арил, гетероарил, C1-C6алкокси, OH, арилокси, гетероарилокси, арил(C1-C6)алкокси, -NR18R19, циклоалкил или арилалкил, где циклические части каждого независимо замещены в 0-5 случаях алкилом, алкокси, галогеном, галогеналкилом, галогеналкокси, CN, NH2, NH(алкил), N(алкил)(алкил), CO2H или C1-C6алкоксикарбонилом; R18 и R19 независимо представляют собой водород, C1-C6алкил, арил, гетероарил, гетероциклоалкил или арил(C1-C6)алкил, где циклические части каждого замещены в 0-3 случаях алкилом, алкокси, галогеном, гидроксилом, CF3 или OCF3; каждый R' независимо представляет собой водород, C1-C6алкил, арил, арил(C1-C4)алкил, C1-C6алканоил, C3-C8циклоалкил, арил(C1-C6)алканоил, гетероциклоалкил, гетероарил(C1-C4)алкил, -SO2-алкил, -SO2-арил, -SO2-гетероарил, гетероциклоалкил(C1-C6)алканоил или гетероарил(C1-C6)алканоил, где алкильная часть алкильной и алканоильной групп необязательно замещена галогеном или C1-C6алкокси, а арильная и гетероарильная группы необязательно замещены алкилом, алкокси, галогеном, галогеналкилом, галогеналкокси; каждый R'' независимо представляет собой водород или C1-C6алкил, где алкильная группа необязательно замещена галогеном;
R36 представляет собой C3-C7циклоалкил(C1-C6алкил), где циклическая часть замещена в 0-5 случаях галогеном, C1-C6алкилом, OH, алкоксикарбонилом или C1-C6алкокси; или R36 представляет собой C1-C14алкил, C2-C16алкенил или C2-C8алкинил, каждый из которых замещен в 0-5 случаях OH, галогеном, C1-C6алкокси, арилом, арилалкокси, арилокси, гетероарилом, гетероциклоалкилом, арил(C1-C6)алкилом, -CO2(C1-C6алкил), -NR'R'', C1-C6тиоалкокси, -NHS(O)xR25, -N(C1-C6алкил)-S(O)nR25, -S(O)xR25, -C(O)NR43R44, -N(R16)C(O)NR16R17 или -N(R16)C(O)R17; где указанные выше арильные группы замещены в 0-3 случаях ОН, C1-C6алкокси, C1-C6алкилом или галогеном; R43 и R44 независимо представляют собой водород, C1-C6алкил, арил, арилалкил, гетероарил, гетероарилалкил, гетероциклоалкил, гетероциклоалкилалкил, арилалканоил, алкенил, циклоалкил, алкинил, циклоалкенил, пиридил, имидазолил, тиазолил, оксазолил или индолил, где каждый алкил в 0-3 случаях замещен NH2, NH(C1-C6алкил), N(C1-C6алкил) (C1-C6алкил), OH, C1-C6тиоалкокси, гетероциклоалкилом, арилом, гетероарилом, CN, галогеном или алкокси, необязательно замещенным ОН или фенилом, где арильная, гетероарильная и гетероциклоалкильная группы замещены в 0-3 случаях C1-C4алкилом, C1-C4алкокси, CF3, OCF3, OH, галогеном, тиоалкокси, фенилом или гетероарилом; или R43, R44 и азот, к которому они присоединены, образуют гетероциклоалкильное кольцо, содержащее от 3 до 7 членов кольца, где циклические части R43 и R44 или гетероциклическое кольцо, образованное из R43, R44 и азота, к которому они присоединены, замещены в 0-3 случаях алкилом, алкокси, галогеном, OH, тиоалкокси, NH2, NH(C1-C6алкил), N(C1-C6 алкил)(C1-C6алкил), CF3, OCF3, фенилом, необязательно замещенным галогеном, -(C1-C4алкил)-N(H или C1-C4алкил)фенилом, C1-C4гидроксиалкилом, арилалкокси, арилалкилом, арилалканоилом, C(O)NH2, C(O)NH(C1-C6алкил), C(O)N(C1-C6алкил)(C1-C6алкил), гетероциклоалкилалкилом, C1-C6алкоксикарбонилом, C2-C6алканоилом, гетероарилом или -SO2(C1-C6алкил); х равняется 0, 1 или 2; R25 представляет собой 1-C6алкил, OH, NR26R27; R26 и R27 независимо представляют собой водород, C1-C6алкил, фенил(C1-C4алкил), арил или гетероарил; или R26, R27 и азот, к которому они присоединены, образуют гетероциклоалкильное кольцо;
R36 представляет собой гетероарил(C1-C6)алкил, где циклическая часть замещена в 0-5 случаях галогеном, C1-C6алкилом, C1-C6алкокси, C1-C4галогеналкилом, C1-C4галогеналкокси, арилом, арилалкилом, арилокси, гетероарилом, -SO2-арилом, -S(O)xR25, (C1-C4алкил)-S(O)xR25, CN, C1-C6тиоалкокси, C1-C6алкоксикарбонилом, -NR'R'', -C(O)NR'R'', гетероциклоалкилом, где вышеуказанные арильные группы замещены в 0-4 случаях галогеном, C1-C6алкилом, C1-C6алкокси, C1-C4галогеналкилом, C1-C4галогеналкокси или CN; где указанные выше гетероарильные и гетероциклоалкильные группы замещены в 0-3 случаях галогеном, CF3, (C1-C4)алкилом, C1-C6тиоалкокси, OH, C1-C4гидроксиалкилом или C1-C4алкокси; или
R36 представляет собой гетероциклоалкил(C1-C6алкил), где циклическая часть замещена в 0-3 случаях галогеном, C1-C6алкилом, C1-C6алкокси, C1-C4галогеналкилом, C1-C4галогеналкокси, арилом, арилалкилом, арилокси, гетероарилом, -SO2-арилом, -S(O)xR25, (C1-C4алкил)-S(O)xR25, CN, C1-C6тиоалкокси, C1-C6алкоксикарбонилом, -NR'R'', -C(O)NR'R'', гетероциклоалкилом;
R37 представляет собой водород, C1-C6алкил или фенил(C1-C4)алкил; R38 представляет собой водород, галоген, C1-C6алкил, C1-C6алкокси, C1-C6галогеналкил, CN; R39 представляет собой водород, галоген, C1-C6алкил, необязательно замещенный -CO2-(C1-C6алкил), C1-C6алкокси, C1-C6галогеналкилом, C1-C6галогеналкокси, CN, арилокси, изоцианато, -SO2(C1-C6алкил), -NHR', -NR'R'', C1-C6алканоилом, гетероарилом, арилом; или
R38 и R39 и атомы углерода, к которым они присоединены, образуют гетероциклоалкильное кольцо, которое замещено в 0-3 случаях C1-C4алкилом, C1-C4алкокси, галогеном или C1-C4алканоилом, где алканоильная группа замещена 0-3 атомами галогена; R40 представляет собой водород, -SO2NR'R'', галоген; или R39 и R40 и атомы углерода, к которым они присоединены, образуют бензокольцо; или R39 и R40 и атомы углерода, к которым они присоединены, образуют 1-окса-2,3-диазациклопентильное кольцо;
R40 и R41 независимо представляют собой водород или F; или R40, R41 и атомы углерода, к которым они присоединены, образуют 1,2,5-оксадиазолильное кольцо; или R40, R41 и атомы углерода, к которым они присоединены, образуют нафтильное кольцо.
В некоторых вариантах осуществления R36 представляет собой бромбензил. В некоторых вариантах осуществления R37 представляет собой водород. В некоторых вариантах осуществления k равняется 2. В некоторых вариантах осуществления каждый из R38, R40, R41 и R42 независимо представляет собой водород. В некоторых вариантах осуществления R39 представляет собой хлор.
В некоторых вариантах осуществления GSI представляет собой соединение, описанное в патенте США № 7939657. В одном варианте осуществления GSI представляет собой ELN-318463, т. е. HY-50882 или (R)-N-(4-бромбензил)-4-хлор-N-(2-оксоазепан-3-ил)бензолсульфонамид, или его фармацевтически приемлемую соль. В некоторых вариантах осуществления GSI представляет собой
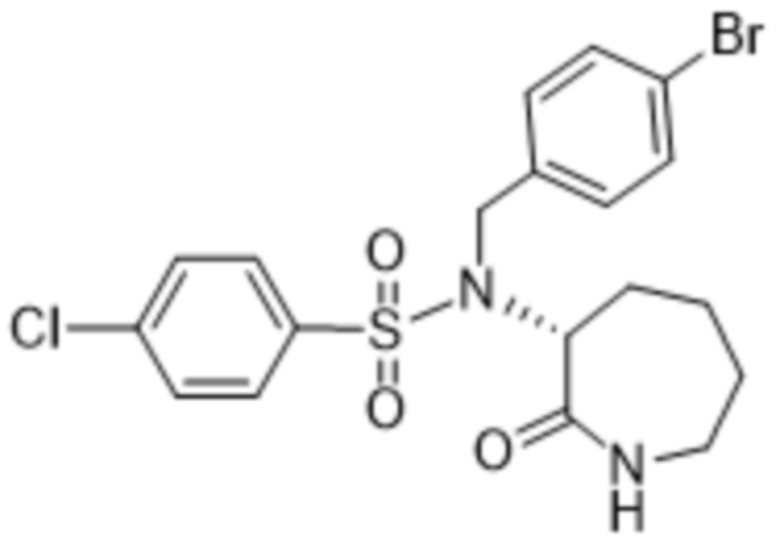
или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления GSI представляет собой соединение формулы (VIII):
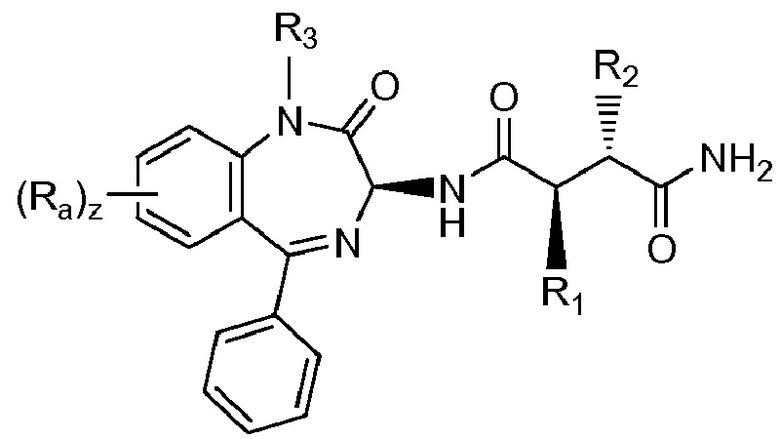 (VIII)
(VIII)
или его фармацевтически приемлемую соль, где R1 представляет собой -CH2CF3 или -CH2CH2CF3; R2 представляет собой -CH2CF3, -CH2CH2CF3 или -CH2CH2CH2CF3; R3 представляет собой водород или -CH3; каждый Ra независимо представляет собой F, CI, -CN, -OCH3 и/или -NHCH2CH2OCH3; и z равняется 0, 1 или 2.
В некоторых вариантах осуществления R1 представляет собой -CH2CH2CF3CH2CH2CF3. В некоторых вариантах осуществления R2 представляет собой -CH2CH2CF3. В некоторых вариантах осуществления R3 представляет собой -CH3. В некоторых вариантах осуществления z равняется 0.
В некоторых вариантах осуществления GSI представляет собой соединение, описанное в патенте США № 8629136. В одном варианте осуществления GSI представляет собой BMS-906024, т. е. (2R,3S)-N-[(3S)-1-метил-2-оксо-5-фенил-2,3-дигидро-1H-1,4-бензодиазепин-3-ил]-2,3-бис(3,3,3-трифторпропил)сукцинамид или его фармацевтически приемлемую соль. В одном варианте осуществления GSI представляет собой
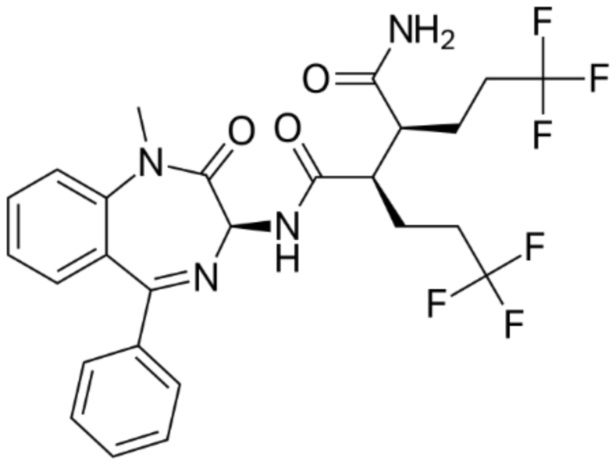
или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления GSI представляет собой соединение, описанное в патенте США № 8629136. В одном варианте осуществления GSI представляет собой LY3039478, т. е. кренигацестат или 4,4,4-трифтор-N-((R)-1-(((S)-5-(2-гидроксиэтил)-6-оксо-6,7-дигидро-5H-бензо[d]пиридо[2,3-b]азепин-7-ил)амино)-1-оксопропан-2-ил)бутанамид или его фармацевтически приемлемую соль. В некоторых вариантах осуществления GSI представляет собой:
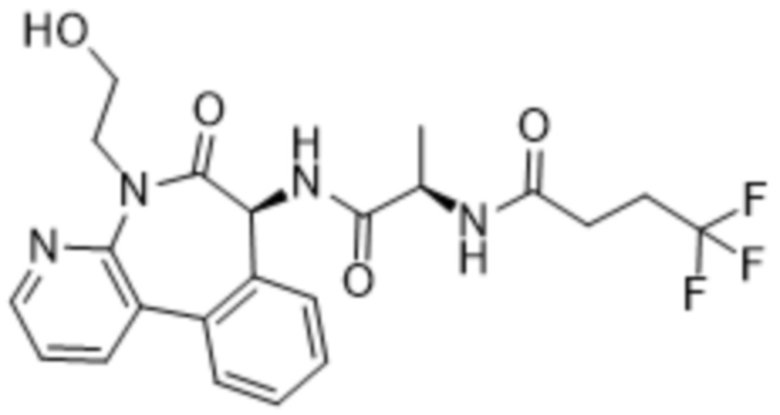
или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления GSI представляет собой BMS-299897, т. е. 2-[(1R)-1-[[(4-хлорфенил)сульфонил](2,5-дифторфенил)амино]этил-5-фторбензолбутановую кислоту или ее фармацевтически приемлемую соль. В некоторых вариантах осуществления GSI представляет собой
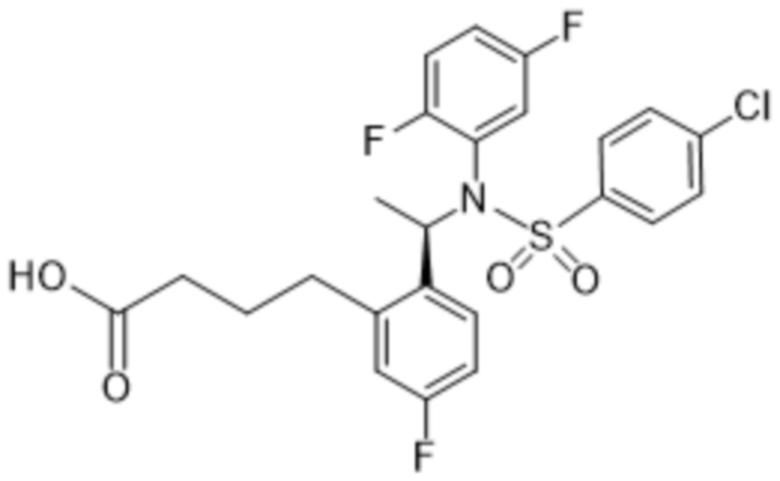
или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления GSI представляет собой LY-411575, т. е. LSN-411575, (S)-2-((S)-2-(3,5-дифторфенил)-2-гидроксиацетамидо)-N-((S)-5-метил-6-оксо-6,7-дигидро-5H-дибензо[b, d]азепин-7-ил)пропанамид или его фармацевтически приемлемую соль. В некоторых вариантах осуществления GSI представляет собой
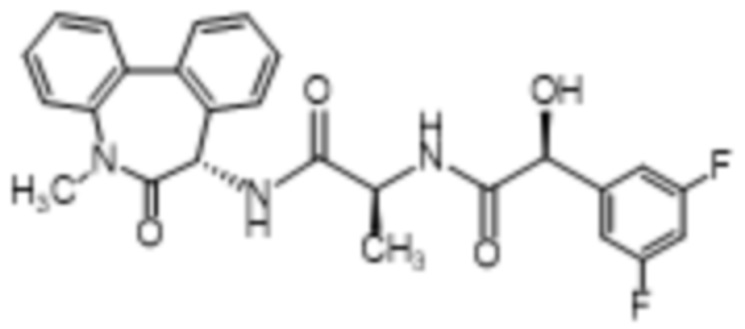
или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления GSI представляет собой DAPT, т. е. N-[(3,5-дифторфенил)ацетил]-L-аланил-2-фенил]глицин-1,1-диметилэтиловый эфир или его фармацевтически приемлемую соль. В некоторых вариантах осуществления GSI представляет собой

или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления GSI представляет собой соединение следующих формул:
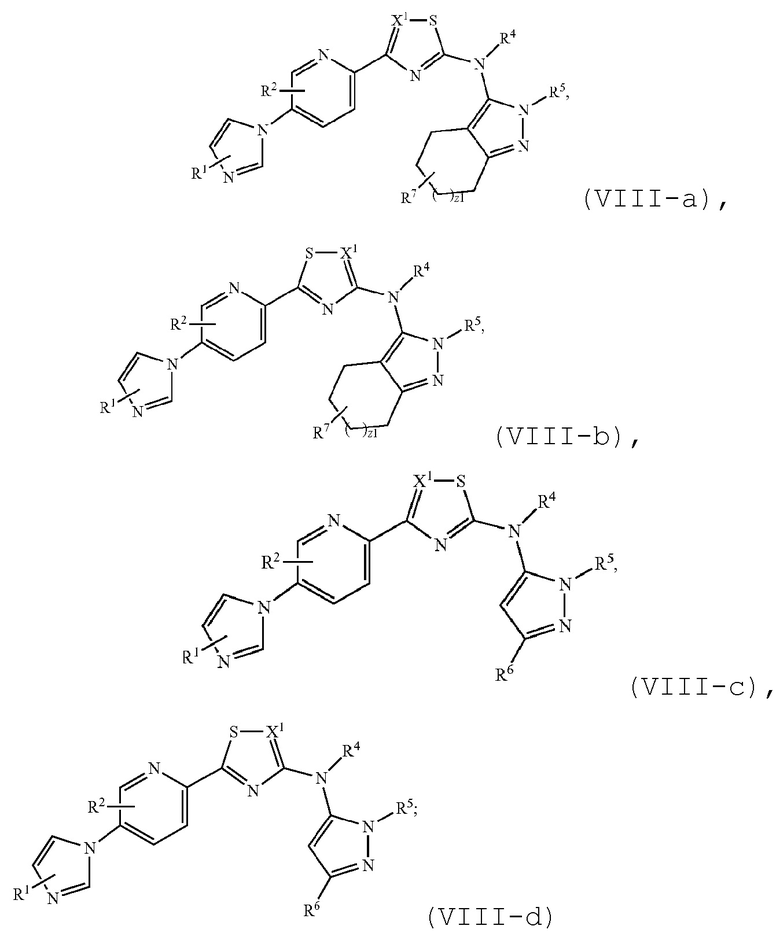
где z1 равняется 0, 1 или 2; X1 представляет собой C(R3) или N; R1 представляет собой водород, галоген, -N3, -CF3, -CCl3, -CBr3, -CI3, -CN, -CHO, -OR1A, -NR1AR1B, -COOR1A, -C(O)NR1AR1B, -NO2, -SR1A, -S(O)n1OR1A, -S(O)n1NR1AR1B, -NHNR1AR1B, -ONR1AR1B, -NHC(O)NHNR1AR1B, замещенный или незамещенный алкил, замещенный или незамещенный гетероалкил, замещенный или незамещенный циклоалкил, замещенный или незамещенный гетероциклоалкил, замещенный или незамещенный арил или замещенный или незамещенный гетероарил; R2 представляет собой водород, галоген, -N3, -CF3, -CCl3, -CBr3, -CI3, -CN, -CHO, -OR2A, -NR2AR2B, -COOR2A, -C(O)NR2AR2B, -NO2, -SR2A, -S(O)n2R2A, -S(O)n2OR2A, -S(O)n2NR2AR2B, -NHNR2AR2B, -ONR2AR2B, -NHC(O)NHNR2AR2B, замещенный или незамещенный алкил, замещенный или незамещенный гетероалкил, замещенный или незамещенный циклоалкил, замещенный или незамещенный гетероциклоалкил, замещенный или незамещенный арил или замещенный или незамещенный гетероарил; R3 представляет собой водород, галоген, -N3, -CF3, -CCl3, -CBr3, -CI3, -CN, -CHO, -OR3A, -NR3AR3B, -COOR3A, -C(O)NR3AR3B, -NO2, -SR3A, -S(O)n3R3A, -S(O)n3OR3A, -S(O)n3ONR3AR3B, -NHNR3AR3B, -ONR3AR3B, -NHC(O)NHNR3AR3B, замещенный или незамещенный алкил, замещенный или незамещенный гетероалкил, замещенный или незамещенный циклоалкил, замещенный или незамещенный гетероциклоалкил, замещенный или незамещенный арил или замещенный или незамещенный гетероарил; R4 представляет собой водород, галоген, -N3, -CF3, -CCl3, -CBr3, -CI3, -CN, -CHO, -OR4A, -NR4AR4B, -COOR4A, -C(O)NR4AR4B, -NO2, -SR4A, -S(O)n4R4A, -S(O)n4OR4A, -S(O)n4NR4AR4B, -NHNR4AR4B, -ONR4AR4B, -NHC(O)NHNR4AR4B, замещенный или незамещенный алкил, замещенный или незамещенный гетероалкил, замещенный или замещенный циклоалкил, замещенный или незамещенный гетероциклоалкил, замещенный или незамещенный арил или замещенный или незамещенный гетероарил; R5 представляет собой водород, галоген, -N3, -CF3, -CCl3, -CBr3, -CI3, -CN, -CHO, -OR5A, -NR5AR5B, -COOR5A, -C(O)NR5AR5B, -NO2, -SR5A, -S(O)n5R5A, -S(O)n5OR5A, -S(O)n5NR5AR5B, -NHNR5AR5B, -ONR5AR5B, -NHC(O)NHNR5AR5B, замещенный или незамещенный алкил, замещенный или незамещенный гетероалкил, замещенный или незамещенный циклоалкил, замещенный или незамещенный гетероциклоалкил, замещенный или незамещенный арил или замещенный или незамещенный гетероарил, где R4 и R5 необязательно соединены вместе с образованием замещенного или незамещенного гетероциклоалкила или замещенного или незамещенного гетероарила; R6 представляет собой -CF3, замещенный или незамещенный циклопропил или замещенный или незамещенный циклобутил; R7 независимо представляет собой водород, галоген, -N3, -CF3, -CCl3, -CBr3, -CI3, -CN, -CHO, -OR7A, -NR7AR7B, -COOR7A, -C(O)NR7AR7B, -NO2, -SR7A, -S(O)n7R7A, -S(O)n7OR7A, -S(O)n7NR7AR7B, -NHNR7AR7B, -ONR7AR7B, -NHC(O)NHNR7AR7B, замещенный или незамещенный алкил, замещенный или незамещенный гетероалкил, замещенный или незамещенный циклоалкил, замещенный или незамещенный гетероциклоалкил, замещенный или незамещенный арил или замещенный или незамещенный гетероарил; R1A, R1B, R2A, R2B, R3A, R3B, R4A, R4B, R5A, R5B, R7A и R7B независимо представляют собой водород, замещенный или незамещенный алкил, замещенный или незамещенный гетероалкил, замещенный или незамещенный циклоалкил, замещенный или незамещенный гетероциклоалкил, замещенный или незамещенный арил или замещенный или незамещенный гетероарил; и n1, n2, n3, n4, n5 и n7 независимо равняются 1 или 2.
В некоторых вариантах осуществления GSI формул (VIII-a), (VIII-b), (VIII-c) или (VIII-d) описан в международной публикации патента № WO 2014/165263 (например, в вариантах осуществления P1-P12). В некоторых вариантах осуществления GSI формул (VIII-a), (VIII-b), (VIII-c) или (VIII-d) выбран из:
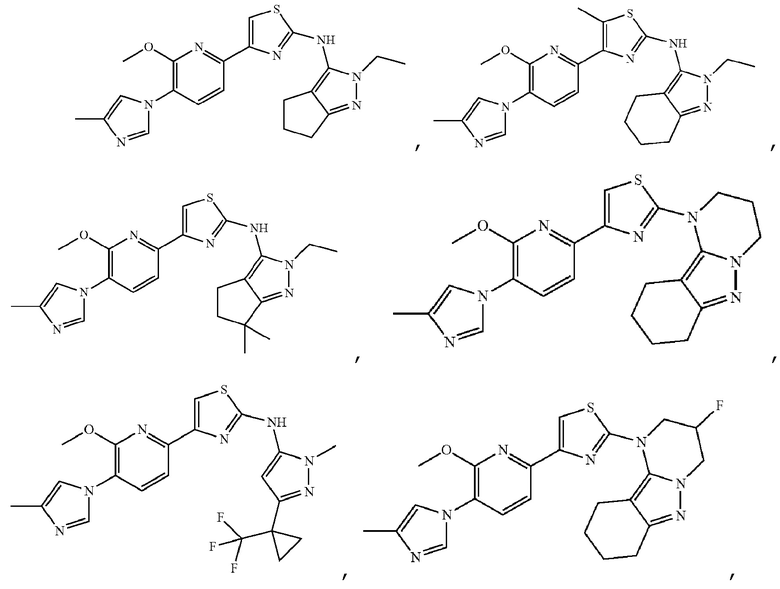
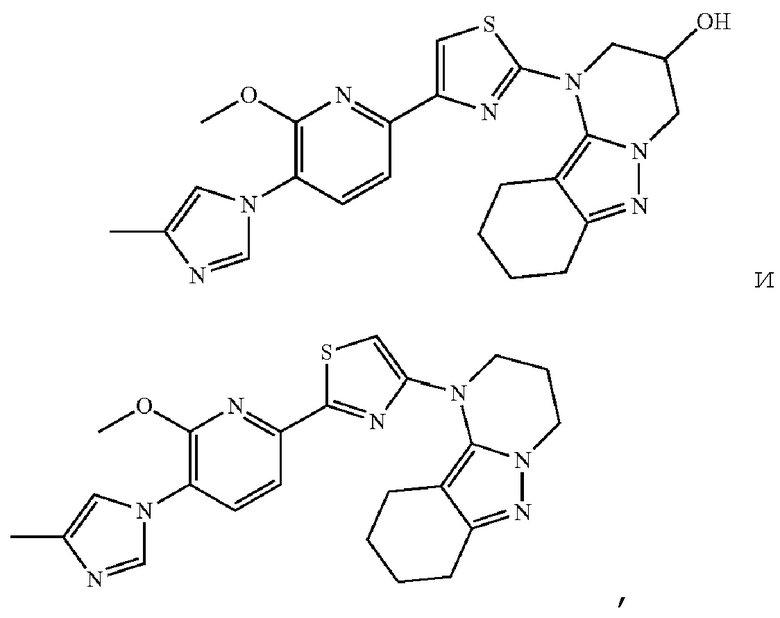
или их фармацевтически приемлемой соли.
В некоторых вариантах осуществления GSI представляет собой соединение формулы (IX):
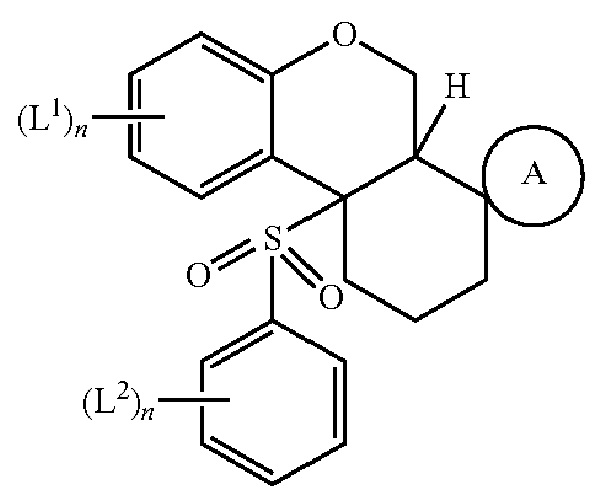 (XIV)
(XIV)
или его фармацевтически приемлемую соль, где A представляет собой 4-7-членное спироциклическое кольцо, содержащее по меньшей мере один гетероатом, выбранный из группы, состоящей из N, O, S, S(O)2, P(O)R1 и N-S(O)2-R1, где спироциклическое кольцо необязательно замещено заместителями в количестве от 1 до 3, выбранными из группы, состоящей из C1-3алкила и =O; R1 представляет собой C1-6алкил, необязательно замещенный галогеном; каждый L1 независимо выбран из группы, состоящей из 1) C1-3алкила, необязательно замещенного галогеном, и 2) галогена; каждый L2 независимо выбран из группы, состоящей из 1) C1-3алкила, необязательно замещенного галогеном, и 2) галогена; и
n равняется 0-3.
В некоторых вариантах осуществления GSI представляет собой соединение, описанное в публикации патента США № US-2015-307533 (например, в таблице на страницах 13-16). В некоторых вариантах осуществления GSI формулы (IX) выбран из:
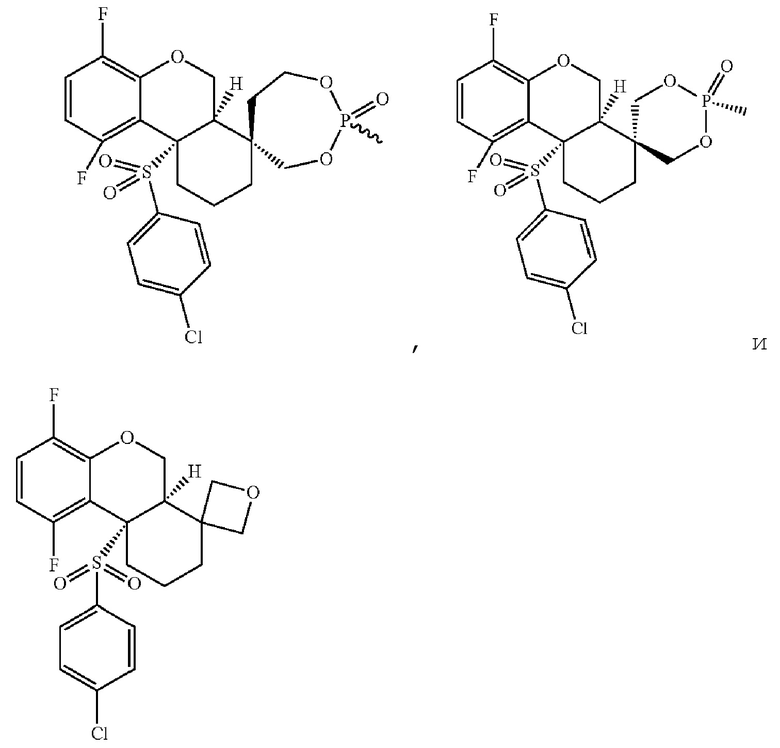
или их фармацевтически приемлемой соли.
В некоторых вариантах осуществления GSI представляет собой соединение формулы (X):
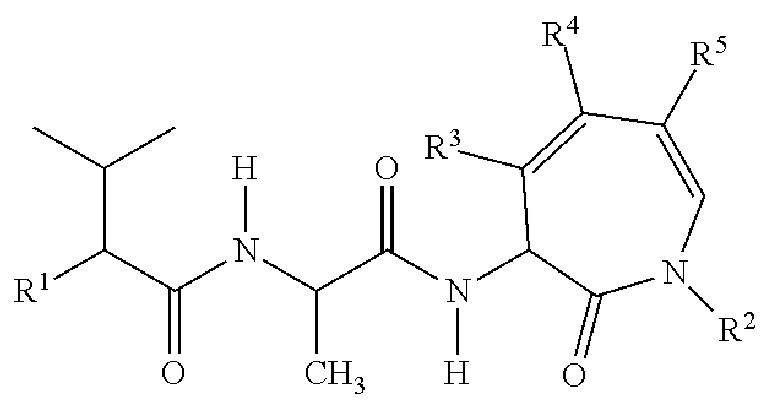 (X),
(X),
или его фармацевтически приемлемую соль, где R1 представляет собой гидрокси или фтор; R2 представляет собой C1-C4алкил; R3 представляет собой водород или фенил; R4 представляет собой водород, фенил или C1-C4алкил; R5 представляет собой водород или фенил; при условии, что один из R3, R4 и R5 не представляет собой водород, а два других представляют собой водород.
В некоторых вариантах осуществления GSI представляет собой соединение из патента США № 8188069. В одном варианте осуществления GSI представляет собой
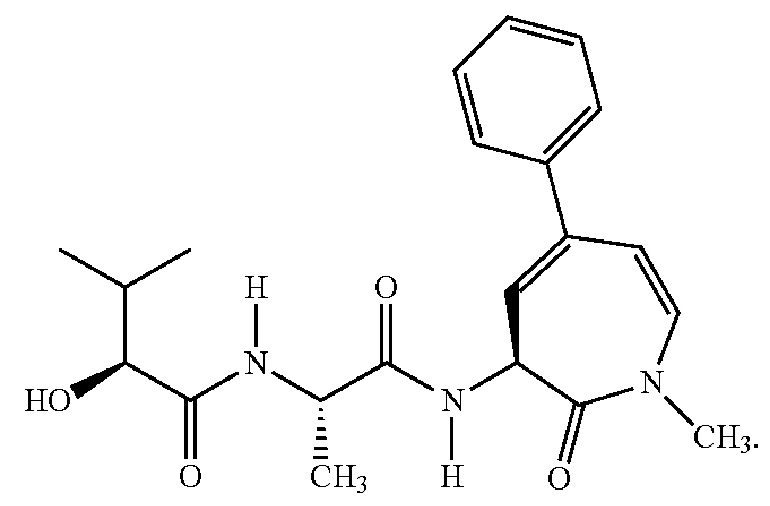 или его фармацевтически приемлемую соль.
или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления GSI представляет собой соединение формулы (XI):
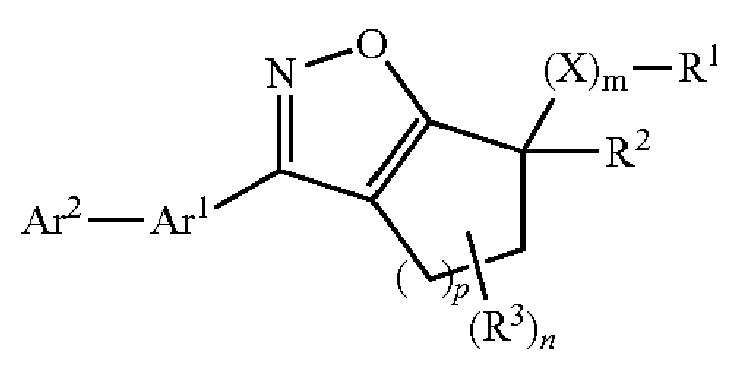 (XI)
(XI)
или его фармацевтически приемлемую соль, где: R1 представляет собой 1) водород, 2) (C1-C6)алкил, необязательно замещенный 1-5 галогенами или фенилом, где фенил необязательно замещен 1-3 галогенами, 3) фенил, необязательно замещенный 1-3 (C1-C6)алкилами или 1-5 галогенами, или 4) (C4-C6)циклоалкил, необязательно замещенный 1-3 (C1-C6)алкилами или 1-5 галогенами; R2 представляет собой 1) водород, 2) (C1-C6)алкил, необязательно замещенный 1-5 галогенами или фенилом, где фенил необязательно замещен 1-3 галогенами, или 3) фенил, необязательно замещенный 1-3 галогенами; R3 представляет собой (C1-C6)алкил, -OH или галоген;
X представляет собой -NR4-, -O-, -S- или -SO2-; R4 представляет собой водород или (C1-C3)алкил;
p равняется 1-3; m равняется 0 или 1; n равняется 0-3; и Ar2-Ar1 выбран из группы, состоящей из:


или их фармацевтически приемлемой соли.
В некоторых вариантах осуществления GSI представляет собой соединение, описанное в патенте США № 9096582 (например, в таблице на страницах 13-17). В некоторых вариантах осуществления GSI выбран из:

или их фармацевтически приемлемой соли.
В некоторых вариантах осуществления GSI представляет собой соединение формулы (XII):
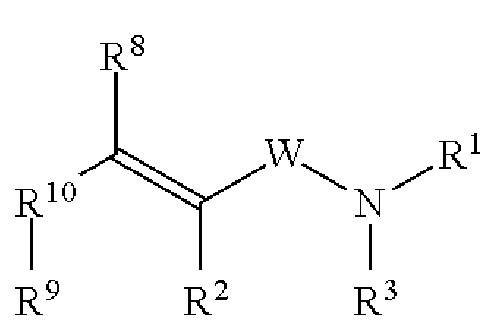 (XII)
(XII)
или его фармацевтически приемлемую соль, где или его фармацевтически приемлемые соли, где: R1, R2, R3, R8, R9, R10 и W выбраны независимо; W выбран из группы, состоящей из; -S(O)- и -S(O)2-; R1 выбран из группы, состоящей из Н, алкил-, алкенил-, алкинил-, арил-, арилалкил, алкиларил-, циклоалкил-, циклоалкенил, циклоалкилалкил-, конденсированного бензоциклоалкила (т. е. бензоконденсированного циклоалкила), конденсированного бензогетероциклоалкила (т. е. бензоконденсированного гетероциклоалкила), конденсированного гетероарилциклоалкила (т. е. гетероарилконденсированного циклоалкила), конденсированного гетероарилгетероциклоалкила (т. е. гетероарилконденсированного гетероциклоалкила), гетероарил-, гетероарилалкил-, гетероциклил-, гетероцикленила -и гетероциклиалкил-; где каждая из групп алкил-, алкенил- и алкинил-, арил-, арилалкил-, алкиларил-, циклоалкил-, циклоалкенил-, циклоалкилалкил-, конденсированного бензоциклоалкила, конденсированного бензогетероциклоалкила, конденсированного гетероарилциклоалкила, конденсированного гетероарилгетероциклоалкила, гетероарил-, гетероарилалкил-, гетероциклил-, гетероцикленил- и гетероциклилкил-R1 необязательно замещена 1-5 независимо выбранными группами R21; каждый из R2 и R3 независимо выбран из группы, состоящей из H, алкил-, алкенил-, алкинил-, арил-, арилалкил-, алкиларил-, циклоалкил-, циклоалкенил-, циклоалкилалкил-, гетероарил-, гетероарилалкил-, гетероциклил-, гетероцикленил- и гетероциклилалкил-; где каждая из групп алкил-, алкенил- и алкинил-, арил-, арилалкил-, алкиларил-, циклоалкил-, циклоалкенил-, циклоалкилалкил-, циклоалкенил-, гетероарил-, гетероарилалкил-, гетероциклил-, гетероцикленил- и гетероциклилалкил-R1 необязательно замещена 1-5 независимо выбранными группами R21; или R2 и R3, взятые вместе, с атомами, с которыми они связаны, образуют кольцо, выбранное из группы, состоящей из: (а) 5-6-членного гетероциклоалкильного кольца, причем гетероциклоалкильное кольцо необязательно содержит, в дополнение к W и в дополнение к N, смежному с W, по меньшей мере еще один гетероатом, независимо выбранный из группы, состоящей из: -O-, -S(O)-, -S(O)2 и -C(O)-, и (b) 5-6-членного гетероциклоалкенильного кольца, причем гетероциклоалкенильное кольцо необязательно содержит, в дополнение к W и в дополнение к N, смежному с W, по меньшей мере еще один гетероатом, независимо выбранный из группы, состоящей из: -O-, -S(O)-, -S(O)2 и -C(O)-; где кольцо необязательно замещено 1-5 независимо выбранными группами R21; или R2 и R3, взятые вместе с атомами, с которыми они связаны, и R1 и R3, взятые вместе с атомами, с которыми они связаны, образуют фрагмент, представляющий собой конденсированное кольцо:
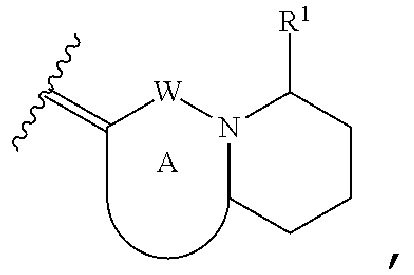
где кольцо A выбрано из группы, состоящей из:
(а) 5-6-членного гетероциклоалкильного кольца, причем гетероциклоалкильное кольцо необязательно содержит, в дополнение к W и в дополнение к N, смежному с W, по меньшей мере еще один гетероатом, независимо выбранный из группы, состоящей из: -O-, -NR14-, -S(O)-, -S(O)2 и -C(O)-, и (b) 5-6-членного гетероциклоалкенильного кольца, причем гетероциклоалкенильное кольцо необязательно содержит, в дополнение к W и в дополнение к N, смежному с W, по меньшей мере еще один гетероатом, независимо выбранный из группы, состоящей из: -O-, -NR14-, -S(O)-, -S(O)2 и -C(O)-, и где фрагмент, представляющий собой конденсированное кольцо, необязательно замещен 1-5 независимо выбранными группами R21; или R1 и R3, взятые вместе с атомами, с которыми они связаны, образуют конденсированное бензогетероциклоалкильное кольцо, и где конденсированное кольцо необязательно замещено 1-5 независимо выбранными группами R21, R8 выбран из группы, состоящей из H, алкил-, алкенил-, алкинил-, арил-, арилалкил-, алкиларил-, циклоалкил-, циклоалкенил-, циклоалкилалкил-, гетероарил-, гетероарилалкил-, гетероциклил-, гетероцикленил- и гетероциклилалкил-; где каждый из R8алкил-, алкенил- и алкинил-, арил-, арилалкил-, алкиларил-, циклоалкил-, циклоалкенил-, циклоалкилалкил-, гетероарил-, гетероарилалкил-, гетероциклил-, гетероцикленил- и гетероциклилалкил- замещен 1-3 независимо выбранными группами R21; R9 выбран из группы, состоящей из: алкил-, алкенил-, алкинил-, арил-, арилалкил-, алкиларил-, циклоалкил-, циклоалкенил, циклоалкилалкил, гетероарил-, гетероарилалкил-, гетероциклил-, гетероцикленил- и гетероциклилалкил-, где каждый из R9алкил-, алкенил- и алкинил-, арил-, арилалкил-, алкиларил-, циклоалкил-, циклоалкенил-, циклоалкилалкил-, гетероарил-, гетероарилалкил-, гетероциклил-, гетероцикленил-, гетероциклилалкил- и гетероциклилалкил- необязательно замещен 1-3 независимо выбранными группами R21;
R10 выбран из группы, состоящей из связи, алкил-, алкенил-, алкинил-, арил-, арилалкил-, алкиларил-, циклоалкил-, циклоалкенил, циклоалкилалкил, гетероарил-, гетероарилалкил-, гетероциклил-, гетероцикленил, гетероциклиалкил-, гетероциклиалкенил-,
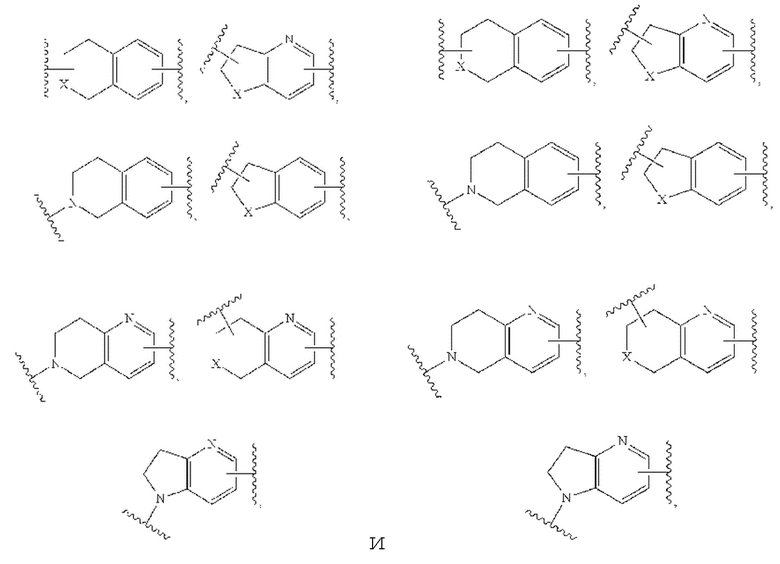
где X выбран из группы, состоящей из: O, -N(R14)- или -S-; и
где каждый из фрагментов, представляющих собой R10, необязательно замещен 1-3 независимо выбранными группами R21; R14 выбран из группы, состоящей из H, алкила, алкенила, алкинила, циклоалкила, циклоалкилалкила, циклоалкенила, гетероциклила, гетероцикленила, гетероциклилалкила, гетероциклилалкенила, арила, арилалкила, гетероарила, гетероарилалкила, -ON, -C(O)R15, -C(O)OR15, -C(O)N(R15)(R16), -S(O)N(R15)(R16), -S(O)2N(R15)(R16), -C(═NOR15)R16 и -P(O)(OR15)(OR16); R15, R16 и R17 независимо выбраны из группы, состоящей из H, алкила, алкенила, алкинила, циклоалкила, циклоалкилалкила, гетероциклила, гетероциклилалкила, арила, арилалкила, гетероарила, гетероарилалкила, арилциклоалкила, арилгетероциклила, (R18)n-алкила, (R18)n-циклоалкила, (R18)n-циклоалкилалкила, (R18)n-гетероциклила, (R18)n-гетероциклилалкила, (R18)n-арила, (R18)n-арилалкила, (R18)n-гетероарила и (R18)n-гетероарилалкила; каждый R18 независимо выбран из группы, состоящей из алкила, алкенила, алкинила, арила, арилалкила, арилалкенила, арилалкинила, -NO2, галогена, гетероарила, HO-алкиоксиалкила, -CF3, -CN, алкил-CN, -C(O)R19, -C(O)OH, -C(O)OR19, -C(O)NHR20, -C(O)NH2, -C(O)NH2-C(O)N(алкил)2, -C(O)N(алкил)(арил), -C(O)N(алкил)(гетероарил), -SR19, -S(O)2R20, -S(O)NH2, -S(O)NH(алкил), -S(O)N(алкил)(алкил), -S(O)NH(арил), -S(O)2NH2, -S(O)2NHR19, -S(O)2NH(гетероциклил), -S(O)2N(алкил)2, -S(O)2N(алкил)(арил), -OCF3, -OH, -OR20, -O-гетероциклила, -O-циклоалкилалкила, -O-гетероциклилалкила, -NH2, -NHR20, -N(алкил)2, -N(арилалкил)2, -N(арилалкил)-(гетероарилалкил), -NHC(O)R20, -NHC(O)NH2, -NHC(O)NH(алкил), -NHC(O)N(алкил)(алкил), -N(алкил)C(O)NH(алкил), -N(алкил)C(O)N(алкил)(алкил), -NHS(O)2R20, -NHS(O)2NH(алкил), -NHS(O)2N(алкил)(алкил), -N(алкил)S(O)2NH(алкил) и -N(алкил)S(O)2N(алкил)(алкил); или два фрагмента, представляющих собой R18, на смежных атомах углерода могут быть связаны вместе с образованием
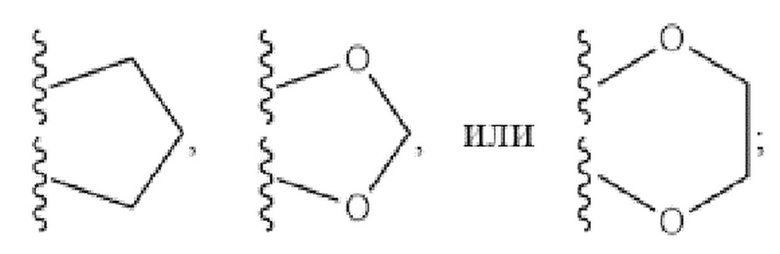
R19 выбран из группы, состоящей из: алкила, циклоалкила, арила, арилалкила и гетероарилалкила; R20 выбран из группы, состоящей из: алкила, циклоалкила, арила, замещенного галогеном арила, арилалкила, гетероарила и гетероарилалкила; каждый R21 независимо выбран из группы, состоящей из: алкила, алкенила, алкинила, циклоалкила, циклоалкилалкила, циклоалкенила, гетероциклоалкила, гетероциклоалкилалкила, арила, арилалкила, гетероарила, гетероарилалкила, галогена, -ON, -OR15, -C(O)R15, -C(O)OR15, -C(O)N(R15)(R16), -SR15, -S(O)N(R16)(R16), -CH(R15)(R16), -S(O)2N(R16)(R16), -C(═NOR16)R16, -P(O)(OR15)(OR16), -N(R15)(R16), -алкил-N(R15)(R16), -N(R15)C(O)R16, -CH2-N(R15)C(O)R16, -CH2-N(R15)C(O)N(R16)(R17), -OH2-R15; -CH2N(R15)(R16), -N(R15)S(O)R16, -N(R15)S(O)2R16, -CH2-N(R15)S(O)2R16, -N(R15)S(O)2N(R16)(R17), -N(R15)S(O)N(R16)(R17), -N(R15)C(O)N(R16)(R17), -CH2-N(R15)C(O)N(R16)(R17), -N(R15)C(O)OR16, -CH2-N(R15)C(O)OR16, -S(O)R15, ═NOR15, -N3, -NO2 и -S(O)2R15; где каждая из групп R21алкила, алкенила, алкинила, циклоалкила, циклоалкилалкила, циклоалкенила, гетероциклоалкила, гетероциклоалкилалкила, арила, арилалкила, гетероарила и гетероарилалкила необязательно замещена 1-5 независимо выбранными группами R22; и каждая группа R22 независимо выбрана из группы, состоящей из алкила, циклоалкила, циклоалкенила, гетероциклоалкила, арила, гетероарила, галогена, -CF3, -CN, -OR15, -C(O)R15, -C(O)OR15, -алкил-C(O)OR15, C(O)N(R15)(R16), -SR15, -S(O)N(R15)(R16), -S(O)2N(R15)(R16), -C(═NOR15)R16, -P(O)(OR15)(OR16), -N(R15)(R16), -алкил-N(R15)(R16), -N(R15)C(O)R16, -CH2-N(R15)C(O)R16, -N(R15)S(O)R16, -N(R15)S(O)2R16, -CH2-N(R15)S(O)2R16, -N(R15)S(O)2N(R16)(R17), -N(R15)S(O)N(R16)(R17), -N(R15)C(O)N(R16)(R17), -CH2-N(R15)C(O)N(R16)(R17); -N(R15)C(O)OR16, -CH2-N(R15)C(O)OR16, -N3, ═NOR15, -NO2, -S(O)R15 и -S(O)2R15.
В некоторых вариантах осуществления GSI представляет собой соединение, описанное в публикации патента США № US-2011-0257163 (например, в абзацах). В некоторых вариантах осуществления GSI формулы (XII) представляет собой фармацевтически приемлемый сложный эфир. В некоторых вариантах осуществления GSI формулы (XII) выбран из:
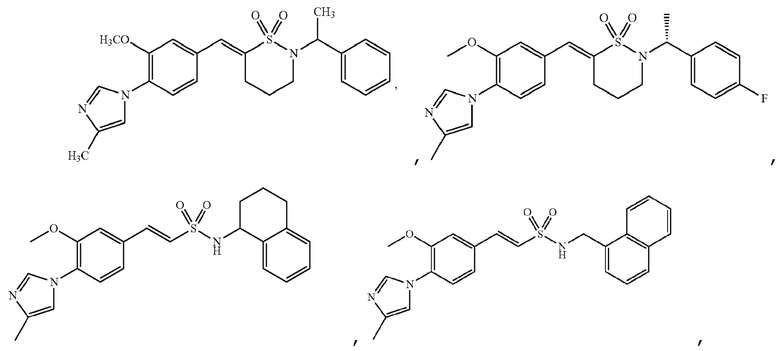
и их фармацевтически приемлемых солей.
В некоторых вариантах осуществления GSI представляет собой соединение формулы (XIII):
 (XIII)
(XIII)
или его фармацевтически приемлемую соль, где кольцо A представляет собой арил, циклоалкил, гетероарил или гетероциклоалкил, где каждое кольцо необязательно замещено в замещаемом положении галогеном, C1-C6алкилом, C2-C6алкенилом, C2-C6алкинилом, C1-C6алкокси, галогеналкилом, галогеналкокси, гидроксилом, гидроксиалкилом, CN, фенокси, -S(O)0-2-(C1-C6алкил), -NR10R11, C1-C6алканоилом, C0-C3алкил-CO2R', гетероарилом, гетероциклоалкилом, арилом, аралкилом или -SO2NR10R11; R1 и R2 объединены с образованием кольцевой системы [3.3.1] или [3.2.1], где 0 или 1 атом углерода в кольцевой системе необязательно заменен группой -O-, -S(O)x- или -NR15-; и где кольцевая система [3.3.1] или [3.2.1] необязательно замещена 1, 2, 3 или 4 группами, которые независимо представляют собой оксо, галоген, C1-C6алкил, -O(C1-C2алкил)O-, -S(C1-C2алкил)S-, C2-C6алкенил, C1-C6галогеналкил, C2-C6алкинил, гидрокси, гидроксиалкил, C1-C6алкокси, галогеналкокси, -C(O)OR13, -(C1-C4 алкил)-C(O)OR16, -CONR10R11, -OC(O)NR10R11, -NR'C(O)OR'' -NR'S(O)2R'', -OS(O)2R', -NR'COR'', CN, ═N-NR12 или ═N-O-R13; где х равняется 0, 1 или 2; R10 и R11 в каждом случае независимо представляют собой водород или C1-C6алкил, где алкил необязательно замещен арилом, где арил необязательно замещен 1-5 группами, которые независимо представляют собой галоген, гидроксил, алкил, алкокси, галогеналкил, галогеналкокси, CN или NO2; или
R10 и R11 вместе могут образовывать 3-8-членное кольцо, необязательно содержащее дополнительный гетероатом, такой как N, O или S; R12 представляет собой водород, C1-C6алкил или -SO2-арил, где арил необязательно замещен 1-5 группами, которые независимо представляют собой галоген, гидроксил, алкил, алкокси, галогеналкил, галогеналкокси, CN или NO2; R13 представляет собой водород или C1-C6алкил, необязательно замещенный арилом, гидроксилом или галогеном, где арил необязательно замещен 1-5 группами, которые независимо представляют собой галоген, гидроксил, алкил, алкокси, галогеналкил, галогеналкокси, CN или NO2;
R15 представляет собой водород, арил, гетероарил, -SO2R', -C(O)R', -C(O)OR', или C1-C6алкил, необязательно замещенный арилом, гидроксилом или галогеном, где арильные группы необязательно замещены 1-5 группами, которые независимо представляют собой галоген, гидроксил, алкил, алкокси, галогеналкил, галогеналкокси, CN или NO2; и R' и R'' независимо представляют собой водород, C1-C6алкил, галогеналкил, C2-C6алкенил или фенил, необязательно замещенный 1-5 группами, которые независимо представляют собой галоген, C1-C6алкил, -C(O)OR', C1-C6алкокси, галогеналкил, галогеналкокси, гидроксил, CN, фенокси, -SO2-(C1-C6алкил), -NR10R11, C1-C6алканоил, пиридил, фенил, NO2 или -SO2NR10R11.
В некоторых вариантах осуществления GSI формулы (XIII) описан в публикации патента США № US-2011-178199 (например, в абзацах и таблицах 1-4). В некоторых вариантах осуществления GSI формулы (XIII) включает мостиковый н-бициклический сульфонамид или его фармацевтически приемлемую соль. В некоторых вариантах осуществления GSI формулы (XIII) выбран из:
и их фармацевтически приемлемых солей.
В некоторых вариантах осуществления GSI представляет собой соединение формулы (XIV):
 (XIV)
(XIV)
или его фармацевтически приемлемую соль, где R выбран из группы, состоящей из: (1) -пиридинила, (2) -пиразолинила, (3) -1,2,4-оксадиазолила, (4) -(C1-C2)алкилпиридинила, (5) -(C1-C2)алкил-пиразолинила, и (6) -(C1-C2)алкил-1,2,4-оксадиазолила, где пиридинил, пиразолинил и -1,2,4-оксадиазолил не замещены или замещены одной группой L1; R1 независимо выбран из группы, состоящей из галогена, (C1-C6)алкила, -CN, -CF3, -O-(C1-C6)алкила, -O-(галоген(C1-C6)алкил), -C(O)-O-(C1-C6)-OH-замещенного (C1-C4)алкила, галоген(C1-C6)алкила, -(C1-C4)алкокси-OH, -(C1-C4)алкокси(C1-C4)алкокси и -S(O)2(C1-C6)алкила; n равняется 0, 1, 2 или 3; Ar выбран из группы, состоящей из фенила, необязательно замещенного 1 или 2 группами L2, и пиридила, необязательно замещенного 1 или 2 группами L2;
L1 независимо выбран из группы, состоящей из -OCH3, -NH2, ═O и (С1-С5алкила; и L2 независимо выбран из группы, состоящей из галогена, (С1-С6)алкила, -CN, -CF3, -O-(C1-C6)алкила, -O-(галоген(C1-C6)алкила), -C(O)-O-(C1-C6)алкила, -OH-замещенного (C1-C6)алкила, галоген(C1-C6)алкила, -OH-замещенного (C1-C4)алокси, -(C1-C4)алокси(C1-C4)алокси и -S(O)2(C1-C6)алкила.
В некоторых вариантах осуществления GSI представляет собой соединение, описанное в патенте США № 9226927 (например, соединение 4, 8a, 8b, 11, 14, 25a, 25b, 25c, 25d, 25e, 25f, 25g, 25h, 27a или 27b). В некоторых вариантах осуществления GSI формулы (XIV) включает мостиковый н-бициклический сульфонамид или его фармацевтически приемлемую соль. В некоторых вариантах осуществления GSI формулы (XIV) выбран из:

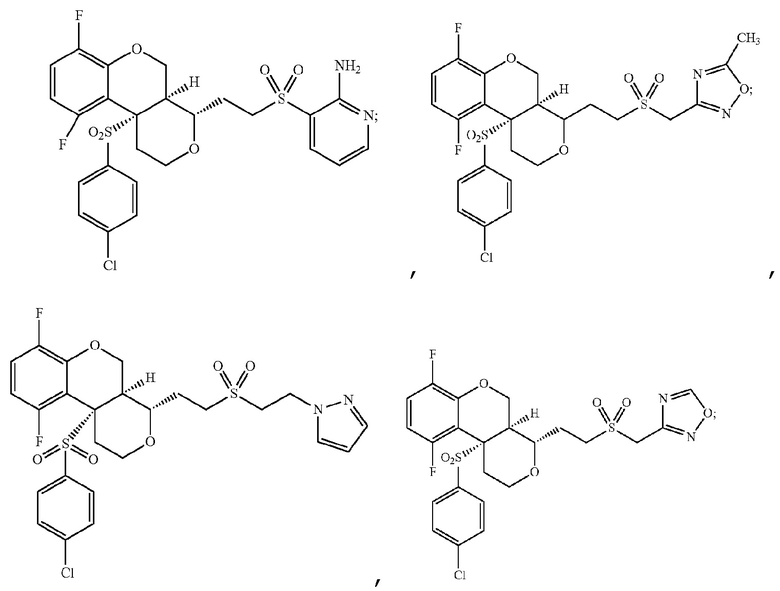
и их фармацевтически приемлемых солей.
В некоторых вариантах осуществления GSI представляет собой молекулу антитела, которая снижает экспрессию и/или функцию гамма-секретазы. В некоторых вариантах осуществления GSI представляет собой молекулу антитела, нацеливающуюся на субъединицу гамма-секретазы. В некоторых вариантах осуществления GSI выбран из молекулы антитела к пресенилину, молекулы антитела к никастрину, молекулы антитела к APH-1 или молекулы антитела к PEN-2.
Иллюстративные молекулы антител, которые нацеливаются на субъединицу гамма-секретазы (например, пресенилин, никастрин, APH-1 или PEN-2), описаны в US 8394376, US 8637274 и US 5942400.
В одном аспекте в настоящем изобретении предусмотрен способ лечения субъектов, которые имеют В-клеточное состояние или нарушение, включающий введение субъекту эффективного количества: (i) BCMA-связывающей молекулы и (ii) модулятора гамма-секретазы (например, GSI). Иллюстративные В-клеточные состояния или нарушения, которые можно лечить с помощью комбинации ВСМА-связывающей молекулы и модулятора гамма-секретазы, включают множественную миелому, макроглобулинемию Вальденстрема, хроническую лимфоцитарную лейкемию, В-клеточную неходжкинскую лимфому, плазмоцитому, лимфому Ходжкина, фолликулярную лимфому, мелкоклеточные лимфомы с нерасщепленными ядрами, эндемическую лимфому Беркитта, спорадическую лимфому Беркитта, лимфому маргинальной зоны, внеузловую лимфому из лимфоидной ткани слизистых оболочек, узловую моноцитоидную B-клеточную лимфому, лимфому селезенки, мантийноклеточную лимфому, крупноклеточную лимфому, диффузную смешанно-клеточную лимфому, иммунобластную лимфому, первичную медиастинальную B-клеточная лимфому, легочную B-клеточную ангиоцентрическую лимфому, малую лимфоцитарную лимфому, пролиферацию B-клеток с неопределенным потенциалом злокачественности, лимфоматоидный гранулематоз, посттрансплантационное лимфопролиферативное нарушение, иммунорегуляторное нарушение, ревматоидный артрит, тяжелую миастению, идиопатическую тромбоцитопеническую пурпуру, антифосфолипидный синдром, болезнь Шагаса, болезнь Грейвса, гранулематоз Вегенера, узелковый полиартериит, синдром Шегрена, обыкновенную пузырчатку, склеродермию, рассеянный склероз, антифосфолипидный синдром, ANCA-ассоциированный васкулит, болезнь Гудпасчера, болезнь Кавасаки, аутоиммунную гемолитическую анемию, быстропрогрессирующий гломерулонефрит, болезнь тяжелых цепей, первичный или ассоциированный с иммуноцитами амилоидоз и моноклональную гаммапатию неустановленной этиологии.
В некоторых вариантах осуществления модулятор гамма-секретазы представляет собой модулятор гамма-секретазы, описанный в WO 2017/019496. В некоторых вариантах осуществления модулятор гамма-секретазы представляет собой ингибитор I γ-секретазы (GSI I) Z-Leu-Leu-норлейцин; ингибитор II γ-секретазы (GSI II); ингибитор III γ-секретазы (GSI III) N-бензилоксикарбонил-Leu-лейцинал, N-(2-нафтоил)-Val-фенилаланинал; ингибитор IV γ-секретазы (GSI IV); ингибитор V γ-секретазы (GSI V) N-бензилоксикарбонил-Leu-фенилаланинал; ингибитор VI γ-секретазы (GSI VI) 1-(S)-эндо-N-(1,3,3)-триметилбицикло[2.2.1]гепт-2-ил)-4-фторфенилсульфонамид; ингибитор VII γ-секретазы (GSI VII) ментилоксикарбонил-LL-CHO; ингибитор IX γ-секретазы (GSI IX) (DAPT) трет-бутиловый сложный эфир N-[N-(3,5-дифторфенацетил-L-аланил)]-S-фенилглицина; ингибитор X γ-секретазы (GSI X) трет-бутиловый сложный эфир {1S-бензил-4R-[1-(1S-карбамоил-2-фенэтилкарбамоил)-1S-3-метилбутилкарбамоил]-2R-гидрокси-5-фенилпентил}карбаминовой кислоты; ингибитор XI γ-секретазы (GSI XI) 7-амино-4-хлор-3-метоксиизокумарин; ингибитор XII γ-секретазы (GSI XII) Z-Ile-Leu-CHO; ингибитор XIII γ-секретазы (GSI XIII) Z-Tyr-Ile-Leu-CHO; ингибитор XIV γ-секретазы (GSI XIV) Z-Cys(t-Bu)-Ile-Leu-CHO; ингибитор XVI γ-секретазы (GSI XVI) метиловый сложный эфир N-[N-3,5-дифторфенацетил]-L-аланил-S-фенилглицина; ингибитор XVII γ-секретазы (GSI XVII); ингибитор XIX γ-секретазы (GSI XIX) бензо[e][1,4]диазепин-3-ил)-бутирамид; ингибитор XX γ-секретазы (GSI XX) (S, S)-2-[2-(3,5-дифторфенил)ацетиламино]-N-(5-метил-6-оксо-6,7-дигидро-5H-дибензо[b, d]азепин-7-ил)пропионамид; ингибитор XXI γ-секретазы (GSI XXI) (S, S)-2-[2-(3,5-дифторфенил)-ацетиламино]-N-(1-метил-2-оксо-5-фенил-2-,3-дигидро-1H-бензо[e][1,4]диазепин-3-ил)-пропионамид; ингибитор I гамма-40-секретазы N-транс-3,5-диметоксициннамоил-Ile-лейцинал; ингибитор II гамма-40-секретазы N-трет-бутилоксикарбонил-Gly-Val-валинал; изовалерил-V-V-Sta-A-Sta-OCH3; MK-0752 (Merck); MRK-003 (Merck); семагацестат/LY450139 (Eli Lilly); RO4929097; PF-03084014; BMS-708163; MPC-7869 (модификатор γ-секретазы), YO-01027 (дибензазепин); LY411575 (Eli Lilly and Co.); L-685458 (Sigma-Aldrich); BMS-289948 (гидрохлорид 4-хлор-N-(2,5-дифторфенил)-N-((1R)-{4-фтор-2-[3-(1H-имидазол-1-ил)пропил]фенил}этил)бензолсульфонамида) или BMS-299897 (4-[2-((1R)-1-{[(4-хлорфенил)сульфонил]-2,5-дифторанилино}этил)-5-фторфенилбутановая кислота) (Bristol Myers Squibb).
В некоторых вариантах осуществления ВСМА-связывающая молекула может использоваться в комбинации с представителем соединений класса талидомидов. Представители соединений класса талидомидов включают без ограничения леналидомид (CC-5013), помалидомид (CC-4047 или актимид), талидомид и их соли и производные. В некоторых вариантах осуществления BCMA-связывающая молекула используется в комбинации со смесью из одного, двух, трех или более представителей соединений класса талидомидов. Аналоги талидомида и иммуномодулирующие свойства аналогов талидомида описаны в Bodera and Stankiewicz, Recent Pat Endocr Metab Immune Drug Discov. 2011 Sep; 5(3):192-6. Структурный комплекс аналогов талидомида и убиквитина E3 описан в Gandhi et al., Br J Haematol. 2014 Mar; 164(6):811-21. Модулирование убиквитинлигазы E3 под действием аналогов талидомида описано в Fischer et al., Nature. 2014 Aug 7; 512(7512):49-53.
В некоторых вариантах осуществления представитель соединений класса талидомидов включает соединение формулы (I):
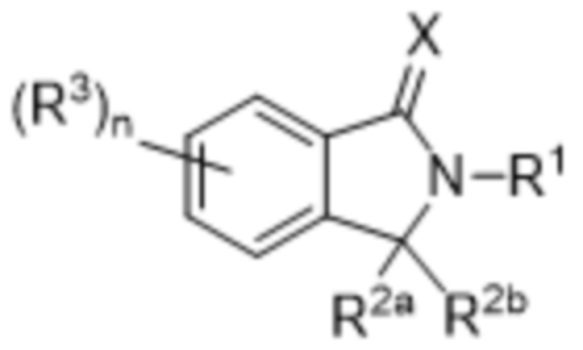 (I)
(I)
или его фармацевтически приемлемую соль, сложный эфир, гидрат, сольват или таутомер, где:
X представляет собой O или S;
R1 представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, карбоциклил, гетероциклил, арил или гетероарил, каждый из которых необязательно замещен одним или несколькими R4;
каждый из R2a и R2b независимо представляет собой водород или C1-C6алкил; или R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют карбонильную группу или тиокарбонильную группу;
каждый из R3 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD) или -N(RC)S(O)xRE, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен одним или несколькими R6;
каждый R4 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, оксо, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD), -N(RC)S(O)xRE, карбоциклил, гетероциклил, арил или гетероарил, где каждый алкил, алкенил, алкинил, гетероалкил, карбоциклил, гетероциклил, арил и гетероарил независимо и необязательно замещен одним или несколькими R7;
каждый из RA, RB, RC, RD и RE независимо представляет собой водород или C1-C6алкил;
каждый R6 независимо представляет собой C1-C6алкил, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, арил или гетероарил, где каждый арил и гетероарил независимо и необязательно замещен одним или несколькими R8;
каждый R7 независимо представляет собой галоген, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
каждый R8 независимо представляет собой C1-C6алкил, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
n равняется 0, 1, 2, 3 или 4; и
x равняется 0, 1 или 2.
В некоторых вариантах осуществления X представляет собой O.
В некоторых вариантах осуществления R1 представляет собой гетероциклил. В некоторых вариантах осуществления R1 представляет собой 6-членный гетероциклил или 5-членный гетероциклил. В некоторых вариантах осуществления R1 представляет собой азотсодержащий гетероциклил. В некоторых вариантах осуществления R1 представляет собой пиперидинил (например, пиперидин-2,6-дионил).
В некоторых вариантах осуществления каждый из R2a и R2b независимо представляет собой водород. В некоторых вариантах осуществления R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют карбонильную группу.
В некоторых вариантах осуществления R3 представляет собой C1-C6гетероалкил, -N(RC)(RD) или -N(RC)C(O)RA. В некоторых вариантах осуществления R3 представляет собой C1-C6гетероалкил (например, CH2NHC(O)CH2-фенил-трет-бутил), -N(RC)(RD) (например, NH2) или -N(RC)C(O)RA (например, NHC(O)CH3).
В одном варианте осуществления X представляет собой O. В одном варианте осуществления R1 представляет собой гетероциклил (например, пиперидин-2,6-дионил). В одном варианте осуществления каждый из R2a и R2b независимо представляет собой водород. В одном варианте осуществления n равняется 1. В одном варианте осуществления R3 представляет собой -N(RC)(RD) (например, -NH2). В одном варианте осуществления соединение включает в себя леналидомид, например, 3-(4-амино-1-оксоизоиндолин-2-ил)пиперидин-2,6-дион, или его фармацевтически приемлемую соль. В одном варианте осуществления соединение представляет собой леналидомид, например, следующей формулы:
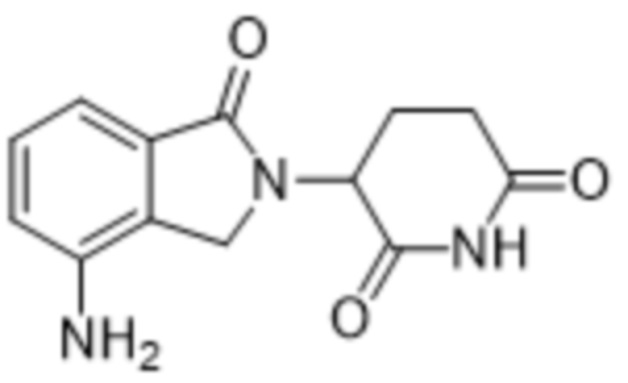 .
.
В одном варианте осуществления X представляет собой O. В одном варианте осуществления R1 представляет собой гетероциклил (например, пиперидинил-2,6-дионил). В некоторых вариантах осуществления R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют карбонильную группу. В одном варианте осуществления n равняется 1. В одном варианте осуществления R3 представляет собой -N(RC)(RD) (например, -NH2). В одном варианте осуществления соединение включает в себя помалидомид, например, 4-амино-2-(2,6-диоксопиперидин-3-ил)изоиндолин-1,3-дион, или его фармацевтически приемлемую соль. В одном варианте осуществления соединение представляет собой помалидомид, например, следующей формулы:
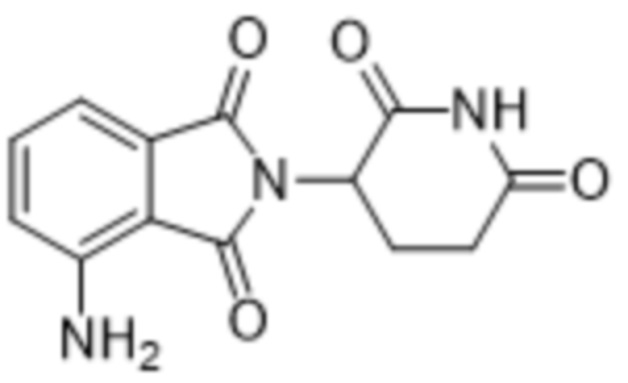 .
.
В одном варианте осуществления X представляет собой O. В одном варианте осуществления R1 представляет собой гетероциклил (например, пиперидинил-2,6-дионил). В одном варианте осуществления R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют карбонильную группу. В одном варианте осуществления n равняется 0. В одном варианте осуществления соединение включает в себя талидомид, например, 2-(2,6-диоксопиперидин-3-ил)изоиндолин-1,3-дион, или его фармацевтически приемлемую соль. В одном варианте осуществления продукт представляет собой талидомид, например, следующей формулы:
 .
.
В одном варианте осуществления X представляет собой O. В одном варианте осуществления R1 представляет собой гетероциклил (например, пиперидин-2,6-дионил). В одном варианте осуществления каждый из R2a и R2b независимо представляет собой водород. В одном варианте осуществления n равняется 1. В одном варианте осуществления R3 представляет собой C1-C6гетероалкил (например, CH2NHC(O)CH2-фенил-трет-бутил). В одном варианте осуществления соединение включает в себя 2-(4-(трет-бутил)фенил)-N-((2-(2,6-диоксопиперидин-3-ил)-1-оксоизоиндолин-5-ил)метил)ацетамид или его фармацевтически приемлемую соль. В одном варианте осуществления соединение имеет структуру, показанную следующей формулой:
 .
.
В некоторых вариантах осуществления соединение представляет собой соединение формулы (I-a):
 (I-a)
(I-a)
или его фармацевтически приемлемую соль, сложный эфир, гидрат или таутомер, где:
кольцо A представляет собой карбоциклил, гетероциклил, арил или гетероарил, каждый из которых независимо и необязательно замещен одним или несколькими R4;
M отсутствует или представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил или C1-C6гетероалкил, где каждый алкил, алкенил, алкинил и гетероалкил необязательно замещен одним или несколькими R4;
каждый из R2a и R2b независимо представляет собой водород или C1-C6алкил; или R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют карбонильную группу или тиокарбонильную группу;
R3a представляет собой водород, C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD) или -N(RC)S(O)xRE, где каждый алкил, алкенил, алкинил и гетероалкил необязательно замещен одним или несколькими R6;
каждый из R3 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD) или -N(RC)S(O)xRE, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен одним или несколькими R6;
каждый R4 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, оксо, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD), -N(RC)S(O)xRE, карбоциклил, гетероциклил, арил или гетероарил, где каждый алкил, алкенил, алкинил, гетероалкил, карбоциклил, гетероциклил, арил и гетероарил независимо и необязательно замещен одним или несколькими R7;
каждый из RA, RB, RC, RD и RE независимо представляет собой водород или C1-C6алкил;
каждый R6 независимо представляет собой C1-C6алкил, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, арил или гетероарил, где каждый арил и гетероарил независимо и необязательно замещен одним или несколькими R8;
каждый R7 независимо представляет собой галоген, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
каждый R8 независимо представляет собой C1-C6алкил, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
n равняется 0, 1, 2 или 3;
o равняется 0, 1, 2, 3, 4 или 5; и
x равняется 0, 1 или 2.
В некоторых вариантах осуществления X представляет собой O.
В некоторых вариантах осуществления M отсутствует.
В некоторых вариантах осуществления кольцо A представляет собой гетероциклил. В некоторых вариантах осуществления кольцо A представляет собой гетероциклил, например, 6-членный гетероциклил или 5-членный гетероциклил. В некоторых вариантах осуществления кольцо A представляет собой азотсодержащий гетероциклил. В некоторых вариантах осуществления кольцо A представляет собой пиперидинил (например, пиперидин-2,6-дионил).
В некоторых вариантах осуществления M отсутствует, и кольцо A представляет собой гетероциклил (например, пиперидинил, например, пиперидин-2,6-дионил).
В некоторых вариантах осуществления каждый из R2a и R2b независимо представляет собой водород. В некоторых вариантах осуществления R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют карбонильную группу.
В некоторых вариантах осуществления R3a представляет собой водород, -N(RC)(RD) или -N(RC)C(O)RA. В некоторых вариантах осуществления R3a представляет собой водород. В некоторых вариантах осуществления R3a представляет собой -N(RC)(RD) (например, -NH2). В некоторых вариантах осуществления R3a представляет собой -N(RC)C(O)RA (например, NHC(O)CH3).
В некоторых вариантах осуществления R3 представляет собой C1-C6гетероалкил (например, CH2NHC(O)CH2-фенил-трет-бутил). В некоторых вариантах осуществления n равняется 0 или 1. В некоторых вариантах осуществления n равняется 0. В некоторых вариантах осуществления n равняется 1.
Соединение может содержать один или несколько хиральных центров или существовать в виде одного или нескольких стереоизомеров. В некоторых вариантах осуществления соединение содержит один хиральный центр и представляет собой смесь стереоизомеров, например, R-стереоизомера и S-стереоизомера. В некоторых вариантах осуществления смесь содержит R-стереоизомеры и S стереоизомеры в определенном соотношении, например, R-стереоизомеры и S-стереоизомеры в соотношении, составляющем приблизительно 1:1 (т. е. представляет собой рацемическую смесь). В некоторых вариантах осуществления смесь содержит R-стереоизомеры и S-стереоизомеры в соотношении, составляющем приблизительно 51:49, приблизительно 52:48, приблизительно 53:47, приблизительно 54:46, приблизительно 55:45, приблизительно 60:40, приблизительно 65:35, приблизительно 70:30, приблизительно 75:25, приблизительно 80:20, приблизительно 85:15, приблизительно 90:10, приблизительно 95:5 или приблизительно 99:1. В некоторых вариантах осуществления смесь содержит S-стереоизомеры и R-стереоизомеры в соотношении, составляющем приблизительно 51:49, приблизительно 52: 48, приблизительно 53:47, приблизительно 54:46, приблизительно 55:45, приблизительно 60:40, приблизительно 65:35, приблизительно 70:30, приблизительно 75:25, приблизительно 80:20, приблизительно 85:15, приблизительно 90:10, приблизительно 95:5 или приблизительно 99:1. В некоторых вариантах осуществления соединение представляет собой один стереоизомер формулы (I) или формулы (I-a), например, один R-стереоизомер или один S-стереоизомер.
В некоторых вариантах осуществления BCMA-связывающую молекулу вводят в комбинации с ингибитором киназы. В одном варианте осуществления ингибитор киназы представляет собой ингибитор PI3-киназы, например, CLR457, BGT226 или BYL719. В одном варианте осуществления ингибитор киназы представляет собой ингибитор CDK4, например, ингибитор CDK4, описанный в данном документе, например, ингибитор CDK4/6, такой как, например, гидрохлорид 6-ацетил-8-циклопентил-5-метил-2-(5-пиперазин-1-илпиридин-2-иламино)-8H-пиридо[2,3-d]пиримидин-7-она (также называемый палбоциклибом или PD0332991). В одном варианте осуществления ингибитор киназы является ингибитором BTK, например, ингибитором BTK, описанным в данном документе, таким как, например, ибрутиниб. В одном варианте осуществления ингибитор киназы представляет собой ингибитор mTOR, например, ингибитор mTOR, описанный в данном документе, такой как, например, рапамицин, аналог рапамицина, OSI-027. Ингибитор mTOR может представлять собой, например, ингибитор mTORC1 и/или ингибитор mTORC2, например, ингибитор mTORC1 и/или ингибитор mTORC2, описанный в данном документе. В одном варианте осуществления ингибитор киназы представляет собой ингибитор MNK, например ингибитор MNK, описанный в данном документе, такой как, например, 4-амино-5-(4-фторанилино)-пиразолo[3,4-d]пиримидин. Ингибитор MNK может представлять собой, например, ингибитор MNK1a, MNK1b, MNK2a и/или MNK2b. В одном варианте осуществления ингибитор киназы представляет собой двойной ингибитор PI3K/mTOR, описанный в данном документе, такой как, например, PF-04695102. В одном варианте осуществления ингибитор киназы представляет собой ингибитор DGK, например, ингибитор DGK, описанный в данном документе, такой как, например, DGKinh1 (D5919) или DGKinh2 (D5794).
В одном варианте осуществления ингибитор киназы представляет собой ингибитор BTK, выбранный из ибрутиниба (PCI-32765); GDC-0834; RN-486; CGI-560; CGI-1764; HM-71224; CC-292; ONO-4059; CNX-774 и LFM-A13. В одном варианте осуществления ингибитор BTK не снижает или не ингибирует киназную активность интерлейкин-2-индуцируемой киназы (ITK) и выбран из GDC-0834; RN-486; CGI-560; CGI-1764; HM-71224; CC-292; ONO-4059; CNX-774 и LFM-A13.
В одном варианте осуществления ингибитор киназы представляет собой ингибитор BTK, например, ибрутиниб (PCI-32765). В некоторых вариантах осуществления BCMA-связывающую молекулу вводят субъекту в комбинации с ингибитором BTK (например, ибрутинибом). В ряде вариантов осуществления ВСМА-связывающую молекулу вводят субъекту в комбинации с ибрутинибом (также называемым PCI-32765) (например, субъекту, имеющему CLL, мантийноклеточную лимфому (MCL) или малую лимфоцитарную лимфому (SLL)). Например, субъект может иметь делецию в коротком плече хромосомы 17 (del(17p), например в лейкозной клетке). В других примерах у субъекта не имеется del(17p). В некоторых вариантах осуществления субъект имеет рецидивирующую CLL или SLL, например субъекту ранее вводили средство противораковой терапии (например, ранее вводили одно, два, три или четыре предшествующих средства противораковой терапии). В некоторых вариантах осуществления субъект имеет рефрактерную CLL или SLL. В других вариантах осуществления субъект имеет фолликулярную лимфому, например рецидивирующую или рефрактерную фолликулярную лимфому. В некоторых вариантах осуществления ибрутиниб вводят при дозировке приблизительно 300-600 мг/день (например, приблизительно 300-350, 350-400, 400-450, 450-500, 500-550 или 550-600 мг/день, например, приблизительно 420 мг/день или приблизительно 560 мг/день), например, перорально. В некоторых вариантах осуществления ибрутиниб вводят в дозе, составляющей приблизительно 250 мг, 300 мг, 350 мг, 400 мг, 420 мг, 440 мг, 460 мг, 480 мг, 500 мг, 520 мг, 540 мг, 560 мг, 580 мг, 600 мг (например, 250 мг, 420 мг или 560 мг) ежедневно в течение некоторого периода времени, например, ежедневно в течение 21-дневного цикла или ежедневно в течение 28-дневного цикла. В одном варианте осуществления ибрутиниб вводят в течение 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 или больше циклов. В некоторых вариантах осуществления ибрутиниб вводят в комбинации с ритуксимабом. См., например, Burger et al. (2013) Ibrutinib In Combination With Rituximab (iR) Is Well Tolerated and Induces a High Rate Of Durable Remissions In Patients With High-Risk Chronic Lymphocytic Leukemia (CLL): New, Updated Results Of a Phase II Trial In 40 Patients, Abstract 675, представленную на 55-м ежегодном собрании и выставке ASH, Новый Орлеан, Луизиана, США, 7-10 декабря. Не ограничиваясь какой-либо теорией, полагают, что при добавлении ибрутиниба усиливается пролиферативный ответ T-клеток и может происходить сдвиг фенотипа T-клеток от T-хелперов 2 типа (Th2) к T-хелперам 1 типа (Th1). Th1 и Th2 представляют собой фенотипы хелперных T-клеток, при этом Th1 и Th2 регулируют различные пути иммунных ответов. Фенотип Th1 ассоциирован с провоспалительными ответами, например, для уничтожения клеток, таких как внутриклеточные патогены/вирусы или раковые клетки, или поддерживающимися длительное время аутоиммунными ответами. Фенотип Th2 ассоциирован с накоплением эозинофилов и противовоспалительными ответами.
В определенных вариантах осуществления ВСМА-связывающую молекулу вводят в комбинации с ингибитором рецептора эпидермального фактора роста (EGFR).
В некоторых вариантах осуществления ингибитор EGFR представляет собой (R, E)-N-(7-хлор-1-(1-(4-(диметиламино)бут-2-еноил)азепан-3-ил)-1H-бензо[d]имидазол-2-ил)-2-метилизоникотинамид (соединение A40) или соединение, раскрытое в публикации согласно РСТ № WO 2013/184757.
В некоторых вариантах осуществления ингибитор EGFR, например, (R, E)-N-(7-хлор-1-(1-(4-(диметиламино)бут-2-еноил)азепан-3-ил)-1H-бензо[d]имидазол-2-ил)-2-метилизоникотинамид (соединение A40) или соединение, раскрытое в публикации согласно РСТ № WO 2013/184757, вводят в дозе 150-250 мг, например, в день. В некоторых вариантах осуществления ингибитор EGFR, например, (R, E)-N-(7-хлор-1-(1-(4-(диметиламино)бут-2-еноил)азепан-3-ил)-1H-бензо[d]имидазол-2-ил)-2-метилизоникотинамид (соединение A40) или соединение, раскрытое в публикации согласно РСТ № WO 2013/184757, вводят в дозе приблизительно 150, 200 или 250 мг, или приблизительно 150-200 или 200-250 мг.
В некоторых вариантах осуществления ингибитор EGFR, например (R, E)-N-(7-хлор-1-(1-(4-(диметиламино)бут-2-еноил)азепан-3-ил)-1H-бензо[d]имидазол-2-ил)-2-метилизоникотинамид (соединение A40) или соединение, раскрытое в публикации согласно РСТ № WO 2013/184757, является ковалентным необратимым ингибитором тирозинкиназы. В определенных вариантах осуществления ингибитор EGFR, например, (R, E)-N-(7-хлор-1-(1-(4-(диметиламино)бут-2-еноил)азепан-3-ил)-1H-бензо[d]имидазол-2-ил)-2-метилизоникотинамид (соединение A40) или соединение, раскрытое в публикации согласно РСТ № WO 2013/184757, ингибирует EGFR с активирующими мутациями (L858R, ex19del). В других вариантах осуществления ингибитор EGFR, представляющий собой (R, E)-N-(7-хлор-1-(1-(4-(диметиламино)бут-2-еноил)азепан-3-ил)-1H-бензо[d]имидазол-2-ил)-2-метилизоникотинамид (соединение A40) или соединение, раскрытое в публикации согласно РСТ № WO 2013/184757, не ингибирует или по сути не ингибирует EGFR дикого типа (wt). Соединение A40 продемонстрировало эффективность у пациентов с NSCLC с мутантным EGFR. В некоторых вариантах осуществления ингибитор EGFR, представляющий собой (R, E)-N-(7-хлор-1-(1-(4-(диметиламино)бут-2-еноил)азепан-3-ил)-1H-бензо[d]имидазол-2-ил)-2-метилизоникотинамид (соединение A40) или соединение, раскрытое в публикации согласно РСТ № WO 2013/184757, также ингибирует одну или несколько киназ семейства Tec. Киназы семейства Tec включают, например, ITK, BMX, TEC, RLK и BTK и играют центральную роль в распространении сигналов от T-клеточных рецепторов и рецепторов хемокинов (Schwartzberg et al. (2005) Nat. Rev. Immunol. p. 284-95). Например, соединение A40 может ингибировать ITK с IC50 при биохимическом взаимодействии, составляющей 1,3 нМ. ITK является критически важным ферментом для выживания Th2-клеток, и ее ингибирование приводит к смещению равновесия между Th2- и Th1-клетками.
В некоторых вариантах осуществления ингибитор EGFR выбран из одного или нескольких из эрлотиниба, гефитиниба, цетуксимаба, панитумумаба, нецитумумаба, PF-00299804, нимотузумаба или RO5083945.
В некоторых вариантах осуществления BCMA-связывающую молекулу вводят в комбинации с антагонистом аденозинового рецептора A2A (A2AR). Иллюстративные антагонисты A2AR включают, например, PBF509 (Palobiofarma/Novartis), CPI444/V81444 (Corvus/Genentech), AZD4635/HTL-1071 (AstraZeneca/Heptares), випаденант (Redox/Juno), GBV-2034 (Globav) (Globavir) AB928 (Arcus Biosciences), теофиллин, истрадефиллин (Kyowa Hakko Kogyo), тозаденант/SYN-115 (Acorda), KW-6356 (Kyowa Hakko Kogyo), ST-4206 (Leadiant Biosciences), преладенант/SCH 420814 (Merck/Schering) и NIR178 (Novartis).
В определенных вариантах осуществления антагонист A2AR представляет собой PBF509. PBF509 и другие антагонисты A2AR раскрыты в US 8796284 и WO 2017/025918. В определенных вариантах осуществления антагонист A2AR представляет собой 5-бром-2,6-ди-(1H-пиразол-1-ил)пиримидин-4-амин. В определенных вариантах осуществления антагонист A2AR имеет следующую структуру:
В определенных вариантах осуществления антагонист A2AR представляет собой CPI444/V81444. CPI-444 и другие антагонисты A2AR раскрыты в WO 2009/156737. В определенных вариантах осуществления антагонист A2AR представляет собой (S)-7-(5-метилфуран-2-ил)-3-((6-(((тетрагидрофуран-3-ил)окси)метил)пиридин-2-ил)метил)-3H[1,2,3]триазоло[4,5-d]пиримидин-5-амин. В определенных вариантах осуществления антагонист A2AR представляет собой (R)-7-(5-метилфуран-2-ил)-3-((6-(((тетрагидрофуран-3-ил)окси)метил)пиридин-2-ил)метил)-3H[1,2,3]триазоло[4,5-d]пиримидин-5-амин или его рацемат. В определенных вариантах осуществления антагонист A2AR представляет собой 7-(5-метилфуран-2-ил)-3-((6-(((тетрагидрофуран-3-ил)окси)метил)пиридин-2-ил)метил)-3H[1,2,3]триазоло[4,5-d]пиримидин-5-амин. В определенных вариантах антагонист A2AR имеет следующую структуру:
В определенных вариантах осуществления антагонист A2AR представляет собой AZD4635/HTL-1071. Антагонисты A2AR раскрыты в WO 2011/095625. В определенных вариантах осуществления антагонист A2AR представляет собой 6-(2-хлор-6-метилпиридин-4-ил)-5-(4-фторфенил)-1,2,4-триазин-3-амин. В определенных вариантах осуществления антагонист A2AR имеет следующую структуру:
В определенных вариантах осуществления антагонист A2AR представляет собой ST-4206 (Leadiant Biosciences). В определенных вариантах осуществления антагонист A2AR представляет собой антагонист A2AR, описанный в US 9133197. В определенных вариантах осуществления антагонист A2AR имеет следующую структуру:
В определенных вариантах осуществления антагонист A2AR представляет собой антагонист A2AR, описанный в US8114845, US9029393, US20170015758 или US20160129108.
В определенных вариантах осуществления антагонист A2AR представляет собой истрадефиллин (регистрационный номер CAS: 155270-99-8). Истрадефиллин также известен как KW-6002 или 8-[(E)-2-(3,4-диметоксифенил)винил]-1,3-диэтил-7-метил-3,7-дигидро-1H-пурин-2,6-дион. Истрадефиллин раскрыт, например, в LeWitt et al. (2008) Annals of Neurology 63 (3): 295-302).
В определенных вариантах осуществления антагонист A2aR представляет собой тозаденант (Biotie). Тозаденант также известен как SYN115 или 4-гидрокси-N-(4-метокси-7-морфолин-4-ил-1,3-бензотиазол-2-ил)-4-метилпиперидин-1-карбоксамид. Тозаденант блокирует действие эндогенного аденозина в отношении рецепторов А2а, что приводит к усилению действия дофамина в отношении рецептора D2 и ингибированию действия глутамата на рецептор mGluR5. В некоторых вариантах осуществления антагонист A2aR представляет собой преладенант (регистрационный номер CAS: 377727-87-2). Преладенант также известен как SCH 420814 или 2-(2-фуранил)-7-[2-[4-[4-(2-метоксиэтокси)фенил]-1-пиперазинил]этил]7H-пиразоло[4,3-е][1,2,4]триазоло[1,5-с]пиримидин-5-амин. Преладенант был разработан как лекарственное средство, действующее как эффективный и избирательный антагонист аденозинового рецептора А2А.
В определенных вариантах осуществления антагонист A2aR представляет собой випаденан. Випаденан также известен как BIIB014, V2006 или 3-[(4-амино-3-метилфенил)метил]-7-(фуран-2-ил)триазоло[4,5-d]пиримидин-5-амин.
Другие иллюстративные антагонисты A2aR включают, например, ATL-444, MSX-3, SCH-58261, SCH-412348, SCH-442416, VER-6623, VER-6947, VER-7835, CGS-15943 или ZM-241385.
В некоторых вариантах осуществления антагонист A2aR представляет собой антагонист пути с участием A2aR (например, ингибитор CD-73, например антитело к CD73), представляет собой MEDI9447. MEDI9447 представляет собой моноклональное антитело, специфичное к CD73. Нацеливание на внеклеточное продуцирование аденозина посредством CD73 может снижать иммуносупрессивное действие аденозина. Сообщалось, что MEDI9447 обладает рядом параметров активности, например ингибированием активности эктонуклеотидазы CD73, ослаблением АМР-опосредованной супрессии лимфоцитов и подавлением роста сингенной опухоли. MEDI9447 может управлять изменениями как в миелоидных, так и лимфоидных инфильтрирующих популяциях лейкоцитов в микроокружении опухоли. Эти изменения включают, например, увеличение показателей эффекторных клеток CD8 и активированных макрофагов и уменьшение пропорций клеток-супрессоров миелоидного происхождения (MDSC) и регуляторных Т-лимфоцитов.
В некоторых вариантах осуществления ВСМА-связывающую молекулу вводят в комбинации со средством терапии на основе клеток, экспрессирующих CAR, таким как средство терапии на основе клеток, экспрессирующих CAR для CD19.
В одном варианте осуществления антигенсвязывающий домен CAR для CD19 характеризуется такой же или аналогичной специфичностью связывания, которой характеризуется scFv-фрагмент FMC63, описанный в Nicholson et al. Mol. Immun. 34 (16-17): 1157-1165 (1997). В одном варианте осуществления антигенсвязывающий домен CAR для CD19 включает в себя scFv-фрагмент, описанный в Nicholson et al. Mol.Immun. 34 (16-17): 1157-1165 (1997).
В некоторых вариантах осуществления CAR для CD19 содержит антигенсвязывающий домен (например, гуманизированный антигенсвязывающий домен) согласно таблице 3 из WO2014/153270. В WO2014/153270 также описаны способы выполнения анализа связывания и эффективности различных конструкций CAR.
В одном аспекте исходная последовательность мышиного scFv представляет собой конструкцию CAR19, представленную в публикации согласно PCT WO2012/079000. В одном варианте осуществления CD19-связывающий домен представляет собой scFv, описанный в WO2012/079000.
В одном варианте осуществления молекула CAR содержит последовательность слитого полипептида, представленную под SEQ ID NO:12 в публикации согласно РСТ WO2012/079000, которая предусматривает scFv-фрагмент мышиного происхождения, который специфически связывается с CD19 человека.
В одном варианте осуществления CAR для CD19 содержит аминокислотную последовательность, представленную под SEQ ID NO:12 в публикации согласно РСТ WO2012/079000.
В одном варианте осуществления CAR для CD19 имеет обозначение TISAGENLECLEUCEL-T согласно USAN. В вариантах осуществления CTL019 получают путем генной модификации T-клеток, опосредованной стабильной вставкой путем трансдукции с помощью самоинактивирующегося лентивирусного (LV) вектора, дефектного по репликации, содержащего трансген CTL019 под контролем промотора EF-1 альфа. CTL019 может представлять собой смесь положительных и отрицательных по трансгену Т-клеток, которые доставляются субъекту из расчета процентного количества положительных по трансгену Т-клеток.
В других вариантах осуществления CAR для CD19 содержит антигенсвязывающий домен (например, гуманизированный антигенсвязывающий домен) согласно таблице 3 из WO2014/153270.
Гуманизация антитела мыши к CD19 необходима в клинической ситуации, когда специфические для мышей остатки могут индуцировать ответ с образованием антител человека к антигену мыши (HAMA) у пациентов, которые получают лечение с помощью CART19, т. е. лечение с помощью T-клеток, трансдуцированных конструкцией CAR19. Получение, определение характеристик и эффективность гуманизированных последовательностей CAR для CD19 описаны в международной заявке WO2014/153270, включая примеры 1-5 (стр. 115-159).
В некоторых вариантах осуществления конструкции CAR для CD19 описаны в публикации согласно РСТ WO 2012/079000.
Конструкции CAR для CD19, содержащие гуманизированные scFv-домены антител к CD19, описаны в публикации согласно PCT WO 2014/153270.
В соответствии с настоящим изобретением можно применять любой известный CAR для CD19, например, антигенсвязывающий домен для CD19 из любого известного из уровня техники CAR для CD19. Например, CAR для CD19, LG-740, описан в патенте США № 8399645; патенте США № 7446190; Xu et al., Leuk Lymphoma. 2013 54(2):255-260(2012); Cruz et al., Blood 122(17):2965-2973 (2013); Brentjens et al., Blood, 118(18):4817-4828 (2011); Kochenderfer et al., Blood 116(20):4099-102 (2010); Kochenderfer et al., Blood 122 (25):4129-39(2013); и 16th Annu Meet Am Soc Gen Cell Ther (ASGCT) (May 15-18, Salt Lake City) 2013, Abst 10.
Иллюстративные CAR для CD19 включают CAR для CD19, описанные в данном документе, или CAR для CD19, описанные в Xu et al. Blood 123.24(2014):3750-9; Kochenderfer et al. Blood 122.25(2013):4129-39, Cruz et al. Blood 122.17(2013):2965-73, NCT00586391, NCT01087294, NCT02456350, NCT00840853, NCT02659943, NCT02650999, NCT02640209, NCT01747486, NCT02546739, NCT02656147, NCT02772198, NCT00709033, NCT02081937, NCT00924326, NCT02735083, NCT02794246, NCT02746952, NCT01593696, NCT02134262, NCT01853631, NCT02443831, NCT02277522, NCT02348216, NCT02614066, NCT02030834, NCT02624258, NCT02625480, NCT02030847, NCT02644655, NCT02349698, NCT02813837, NCT02050347, NCT01683279, NCT02529813, NCT02537977, NCT02799550, NCT02672501, NCT02819583, NCT02028455, NCT01840566, NCT01318317, NCT01864889, NCT02706405, NCT01475058, NCT01430390, NCT02146924, NCT02051257, NCT02431988, NCT01815749, NCT02153580, NCT01865617, NCT02208362, NCT02685670, NCT02535364, NCT02631044, NCT02728882, NCT02735291, NCT01860937, NCT02822326, NCT02737085, NCT02465983, NCT02132624, NCT02782351, NCT01493453, NCT02652910, NCT02247609, NCT01029366, NCT01626495, NCT02721407, NCT01044069, NCT00422383, NCT01680991, NCT02794961 или NCT02456207.
В некоторых вариантах осуществления BCMA-связывающую молекулу вводят в комбинации с ингибитором CD20.
В одном варианте осуществления ингибитор CD20 представляет собой антитело к CD20 или его фрагмент. В одном варианте осуществления антитело представляет собой моноспецифическое антитело, а в другом варианте осуществления антитело представляет собой биспецифическое антитело. В одном варианте осуществления ингибитор CD20 представляет собой химерное моноклональное антитело мыши/человека, например, ритуксимаб. В варианте осуществления ингибитор CD20 представляет собой моноклональное антитело человека, такое как офатумумаб. В варианте осуществления ингибитор CD20 представляет собой гуманизированное антитело, такое как окрелизумаб, велтузумаб, обинутузумаб, окаратузумаб или PRO131921 (Genentech). В варианте осуществления ингибитор CD20 представляет собой слитый белок, содержащий часть антитела к CD20, такого как TRU-015 (Trubion Pharmaceuticals).
В некоторых вариантах осуществления BCMA-связывающую молекулу вводят в комбинации со средством терапии на основе клеток, экспрессирующих CAR для CD22 (например, клетками, экспрессирующими CAR, который связывается с CD22 человека).
В некоторых вариантах осуществления BCMA-связывающую молекулу вводят в комбинации с ингибитором CD22. В некоторых вариантах осуществления ингибитор CD22 представляет собой малую молекулу или молекулу антитела к CD22. В некоторых вариантах осуществления антитело представляет собой моноспецифическое антитело, необязательно конъюгированное со вторым средством, таким как химиотерапевтическое средство. Например, в одном варианте осуществления антитело к CD22 представляет собой конъюгат моноклонального антитела к CD22 и MMAE (например, DCDT2980S). В одном варианте осуществления антитело представляет собой scFv антитела к CD22, например, scFv антитела RFB4. scFv может быть слитым с полным экзотоксином A Pseudomonas или с его фрагментом (например, BL22). В одном варианте осуществления антитело является гуманизированным моноклональным антителом к CD22 (например, представляет собой эпратузумаб). В одном варианте осуществления антитело или его фрагмент содержит Fv-часть антитела к CD22, которая необязательно ковалентно слита с полным экзотоксином A Pseudomonas или его фрагментом (например, фрагментом размером 38 кДа) (например, представляет собой моксетумомаб пасудотокс). В одном варианте осуществления антитело к CD22 представляет собой биспецифическое антитело к CD19/CD22, необязательно конъюгированное с токсином. Например, в одном варианте осуществления антитело к CD22 содержит биспецифическую часть антитела к CD19/CD22 (например, два scFv-лиганда, распознающих CD19 и CD22 человека), необязательно связанную с полным дифтерийным токсином (DT) или его частью, например, первыми 389 аминокислотами дифтерийного токсина (DT) DT 390, например, представляет собой лиганд-управляемый токсин, такой как DT2219ARL. В другом варианте осуществления биспецифическая часть (например, из антитела к CD19/к CD22) связана с токсином, таким как дегликозилированная цепь рицина А (например, комботокс).
В некоторых вариантах осуществления ингибитор CD22 представляет собой молекулу полиспецифического антитела, например, молекулу биспецифического антитела, например, молекулу биспецифического антитела, которая связывается с CD20 и CD3. Иллюстративные молекулы биспецифических антител, которые связываются с CD20 и CD3, раскрыты в WO2016086189 и WO2016182751. В некоторых вариантах осуществления молекула биспецифического антитела, которая связывается с CD20 и CD3, представляет собой XENP13676, раскрытый на фигуре 74 и под SEQ ID NO: 323, 324 и 325 в WO2016086189.
В некоторых вариантах осуществления средство терапии на основе клеток, экспрессирующих CAR для CD22, содержит антигенсвязывающий домен в соответствии с WO2016/164731.
В некоторых вариантах осуществления ВСМА-связывающую молекулу вводят в комбинации с ингибитором FCRL2 или FCRL5. В некоторых вариантах осуществления ингибитор FCRL2 или FCRL5 представляет собой молекулу антитела к FCRL2, например, молекулу биспецифического антитела, например, биспецифическое антитело, которое связывается с FCRL2 и CD3. В некоторых вариантах осуществления ингибитор FCRL2 или FCRL5 представляет собой молекулу антитела к FCRL5, например, молекулу биспецифического антитела, например, биспецифическое антитело, которое связывается с FCRL5 и CD3. В некоторых вариантах осуществления ингибитор FCRL2 или FCRL5 представляет собой средство терапии на основе клеток, экспрессирующих CAR для FCRL2. В некоторых вариантах осуществления ингибитор FCRL2 или FCRL5 представляет собой средство терапии на основе клеток, экспрессирующих CAR для FCRL5.
Иллюстративные молекулы антитела к FCRL5 раскрыты в US20150098900, US20160368985, WO2017096120 (например, антитела ET200-001, ET200-002, ET200-003, ET200-006, ET200-007, ET200-008, ET200-009, ET200-010, ET200-011, ET200-012, ET200-013, ET200-014, ET200-015, ET200-016, ET200-017, ET200-018, ET200-019, ET200-020, ET200-021, ET200-022, ET200-023, ET200-024, ET200-025, ET200-026, ET200-027, ET200-028, ET200-029, ET200-030, ET200-031, ET200-032, ET200-033, ET200-034, ET200-035, ET200-037, ET200-038, ET200-039, ET200-040, ET200-041, ET200-042, ET200-043, ET200-044, ET200-045, ET200-069, ET200-078, ET200-079, ET200-081, ET200-097, ET200-098, ET200-099, ET200-100, ET200-101, ET200-102, ET200-103, ET200-104, ET200-105, ET200-106, ET200-107, ET200-108, ET200-109, ET200-110, ET200-111, ET200-112, ET200-113, ET200-114, ET200-115, ET200-116, ET200-117, ET200-118, ET200-119, ET200-120, ET200-121, ET200-122, ET200-123, ET200-125, ET200-005 и ET200-124, раскрытые в WO2017096120).
Иллюстративные молекулы CAR для FCRL5 раскрыты в WO2016090337.
В некоторых вариантах осуществления ВСМА-связывающую молекулу, вводят в комбинации с комплексом IL15/IL-15Ra. В некоторых вариантах осуществления комплекс IL-15/IL-15Ra выбран из NIZ985 (Novartis), ATL-803 (Altor) или CYP0150 (Cytune).
В некоторых вариантах осуществления комплекс IL-15/IL-15Ra содержит IL-15 человека в комплексе с растворимой формой IL-15Ra человека. Комплекс может содержать IL-15, ковалентно или нековалентно связанный с растворимой формой IL-15Ra. В конкретном варианте осуществления IL-15 человека нековалентно связан с растворимой формой IL-15Ra. В конкретном варианте осуществления IL-15 человека композиции содержит аминокислотную последовательность, описанную в WO 2014/066527, а растворимая форма IL-15Ra человека содержит аминокислотную последовательность, описанную в WO 2014/066527. Молекулы, описанные в данном документе, можно получать с помощью векторов, клеток-хозяев и способов, описанных в WO 2007/084342.
В некоторых вариантах осуществления комплекс IL-15/IL-15Ra представляет собой ALT-803, слитый белок на основе IL-15/IL-15Ra и Fc (растворимый комплекс IL-15N72D:IL-15RaSu/Fc). ALT-803 раскрыт в WO 2008/143794.
В некоторых вариантах осуществления комплекс IL-15/IL-15Ra содержит IL-15, слитый с доменом Sushi IL-15Ra (CYP0150, Cytune). Домен Sushi IL-15Ra относится к домену, который начинается с первого цистеинового остатка после сигнального пептида IL-15Ra и заканчивается четвертым цистеиновым остатком после сигнального пептида. Комплекс IL-15, слитого с доменом Sushi IL-15Ra, раскрыт в WO 2007/04606 и WO 2012/175222.
В некоторых вариантах осуществления BCMA-связывающую молекулу вводят в комбинации с ингибитором PD-1. В некоторых вариантах осуществления ингибитор PD-1 выбран из PDR001 (Novartis), ниволумаба (Bristol-Myers Squibb), пембролизумаба (Merck & Co), пидилизумаба (CureTech), MEDI0680 (Medimmune), REGN2810 (Regeneron), TSR-042 (Tesaro), PF-06801591 (Pfizer), BGB-A317 (Beigene), BGB-108 (Beigene), INCSHR1210 (Incyte) или AMP-224 (Amplimmune). В одном варианте осуществления ингибитор PD-1 представляет собой молекулу антитела к PD-1. В одном варианте осуществления ингибитор PD-1 представляет собой молекулу антитела к PD-1, описанную в US 2015/0210769.
В одном варианте осуществления молекула антитела к PD-1 представляет собой ниволумаб (Bristol-Myers Squibb), также известный как MDX-1106, MDX-1106-04, ONO-4538, BMS-936558 или OPDIVO®. Ниволумаб (клон 5C4) и другие антитела к PD-1 раскрыты в US 8008449 и WO 2006/121168. В одном варианте осуществления молекула антитела к PD-1 содержит одну или несколько из последовательностей CDR (или в совокупности все из последовательностей CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи ниволумаба.
В одном варианте осуществления молекула антитела к PD-1 представляет собой пембролизумаб (Merck & Co), также известный как ламбролизумаб, MK-3475, MK03475, SCH-900475 или KEYTRUDA®. Пембролизумаб и другие антитела к PD-1 раскрыты в Hamid, O. et al. (2013) New England Journal of Medicine 369 (2): 134-44, US 8354509 и WO 2009/114335. В одном варианте осуществления молекула антитела к PD-1 содержит одну или несколько из последовательностей CDR (или в совокупности все из последовательностей CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи пембролизумаба.
В одном варианте осуществления молекула антитела к PD-1 представляет собой пидилизумаб (CureTech), также известный как CT-011. Пидилизумаб и другие антитела к PD-1 раскрыты в Rosenblatt, J. et al. (2011) J Immunotherapy 34(5): 409-18, US 7695715, US 7332582 и US 8686119. В одном варианте осуществления молекула антитела к PD-1 содержит одну или несколько из последовательностей CDR (или в совокупности все из последовательностей CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи пидилизумаба.
В одном варианте осуществления молекула антитела к PD-1 представляет собой MEDI0680 (Medimmune), также известное как AMP-514. MEDI0680 и другие антитела к PD-1 раскрыты в US 9205148 и WO 2012/145493. В одном варианте осуществления молекула антитела к PD-1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи MEDI0680.
В одном варианте осуществления молекула антитела к PD-1 представляет собой REGN2810 (Regeneron). В одном варианте осуществления молекула антитела к PD-1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи REGN2810.
В одном варианте осуществления молекула антитела к PD-1 представляет собой PF-06801591 (Pfizer). В одном варианте осуществления молекула антитела к PD-1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи PF-06801591.
В одном варианте осуществления молекула антитела к PD-1 представляет собой BGB-A317 или BGB-108 (Beigene). В одном варианте осуществления молекула антитела к PD-1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи BGB-A317 или BGB-108.
В одном варианте осуществления молекула антитела к PD-1 представляет собой INCSHR1210 (Incyte), также известное как INCSHR01210 или SHR-1210. В одном варианте осуществления молекула антитела к PD-1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи INCSHR1210.
В одном варианте осуществления молекула антитела к PD-1 представляет собой TSR-042 (Tesaro), также известное как ANB011. В одном варианте осуществления молекула антитела к PD-1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи TSR-042.
Дополнительные известные антитела к PD-1 включают антитела, описанные, например, в WO 2015/112800, WO 2016/092419, WO 2015/085847, WO 2014/179664, WO 2014/194302, WO 2014/209804, WO 2015/200119, US 8735553, US 7488802, US 8927697, US 8993731 и US 9102727.
В одном варианте осуществления антитело к PD-1 представляет собой антитело, которое конкурирует за связывание и/или связывается с тем же эпитопом в PD-1, что и одно из антител к PD-1, описанных в данном документе.
В одном варианте осуществления ингибитор PD-1 представляет собой пептид, который ингибирует сигнальный путь PD-1, например, как описано в US 8907053. В одном варианте осуществления ингибитор PD-1 представляет собой иммуноадгезин (например, иммуноадгезин, который содержит внеклеточную или PD-1-связывающую часть PD-L1 или PD-L2, слитую с константным участком (например, Fc-участком последовательности иммуноглобулина)). В одном варианте осуществления ингибитор PD-1 представляет собой AMP-224 (B7-DCIg (Amplimmune), например, раскрытый в WO 2010/027827 и WO 2011/066342).
В некоторых вариантах осуществления BCMA-связывающую молекулу вводят в комбинации с ингибитором PD-L1. В некоторых вариантах осуществления ингибитор PD-L1 выбран из FAZ053 (Novartis), атезолизумаба (Genentech/Roche), авелумаба (Merck Serono и Pfizer), дурвалумаба (MedImmune/AstraZeneca) или BMS-936559 (Bristol-Myers Squibb).
В одном варианте осуществления ингибитор PD-L1 представляет собой молекулу антитела к PD-L1. В одном варианте осуществления ингибитор PD-L1 представляет собой молекулу антитела к PD-L1, раскрытую в US 2016/0108123.
В одном варианте осуществления молекула антитела к PD-L1 представляет собой атезолизумаб (Genentech/Roche), также известный как MPDL3280A, RG7446, RO5541267, YW243.55.S70 или TECENTRIQ™. Атезолизумаб и другие антитела к PD-L1 раскрыты в US 8217149. В одном варианте осуществления молекула антитела к PD-L1 содержит одну или несколько из последовательностей CDR (или в совокупности все из последовательностей CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи атезолизумаба.
В одном варианте осуществления молекула антитела к PD-L1 представляет собой авелумаб (Merck Serono и Pfizer), также известный как MSB0010718C. Авелумаб и другие антитела к PD-L1 раскрыты в WO 2013/079174. В одном варианте осуществления молекула антитела к PD-L1 содержит одну или несколько из последовательностей CDR (или в совокупности все из последовательностей CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи авелумаба.
В одном варианте осуществления молекула антитела к PD-L1 представляет собой дурвалумаб (MedImmune/AstraZeneca), также известный как MEDI4736. Дурвалумаб и другие антитела к PD-L1 раскрыты в US 8779108. В одном варианте осуществления молекула антитела к PD-L1 содержит одну или несколько из последовательностей CDR (или в совокупности все из последовательностей CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи дурвалумаба.
В одном варианте осуществления молекула антитела к PD-L1 представляет собой BMS-936559 (Bristol-Myers Squibb), также известное как MDX-1105 или 12A4. BMS-936559 и другие антитела к PD-L1 раскрыты в US 7 943 743 и WO 2015/081158. В одном варианте осуществления молекула антитела к PD-L1 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи BMS-936559.
Дополнительные известные антитела к PD-L1 включают антитела, описанные, например, в WO 2015/181342, WO 2014/100079, WO 2016/000619, WO 2014/022758, WO 2014/055897, WO 2015/061668, WO 2013/079174, WO 2012/145493, WO 2015/112805, WO 2015/109124, WO 2015/195163, US 8168179, US 8552154, US 8460927 и US 9175082.
В некоторых вариантах осуществления BCMA-связывающую молекулу вводят в комбинации с ингибитором LAG-3. В некоторых вариантах осуществления ингибитор LAG-3 выбран из LAG525 (Novartis), BMS-986016 (Bristol-Myers Squibb) или TSR-033 (Tesaro).
В одном варианте осуществления ингибитор LAG-3 представляет собой молекулу антитела к LAG-3. В одном варианте осуществления ингибитор LAG-3 представляет собой молекулу антитела к LAG-3, раскрытую в US 2015/0259420.
В одном варианте осуществления молекула антитела к LAG-3 представляет собой BMS-986016 (Bristol-Myers Squibb), также известное как BMS986016. BMS-986016 и другие антитела к LAG-3 раскрыты в WO 2015/116539 и US 9505839. В одном варианте осуществления молекула антитела к LAG-3 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи BMS-986016.
В одном варианте осуществления молекула антитела к LAG-3 представляет собой TSR-033 (Tesaro). В одном варианте осуществления молекула антитела к LAG-3 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи TSR-033.
В одном варианте осуществления молекула антитела к LAG-3 представляет собой IMP731 или GSK2831781 (GSK и Prima BioMed). IMP731 и другие антитела к LAG-3 раскрыты в WO 2008/132601 и US 9244059. В одном варианте осуществления молекула антитела к LAG-3 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи IMP731. В одном варианте осуществления молекула антитела к LAG-3 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи GSK2831781.
Дополнительные известные антитела к LAG-3 включают антитела, описанные, например, в WO 2008/132601, WO 2010/019570, WO 2014/140180, WO 2015/116539, WO 2015/200119, WO 2016/028672, US 9244059, US 9505839.
В одном варианте осуществления ингибитор LAG-3 представляет собой растворимый белок LAG-3, например, IMP321 (Prima BioMed), например, раскрытый в WO 2009/044273.
В некоторых вариантах осуществления BCMA-связывающую молекулу вводят в комбинации с ингибитором TIM-3. В некоторых вариантах осуществления ингибитор TIM-3 представляет собой MGB453 (Novartis) или TSR-022 (Tesaro).
В одном варианте осуществления ингибитор TIM-3 представляет собой молекулу антитела к TIM-3. В одном варианте осуществления ингибитор TIM-3 представляет собой молекулу антитела к TIM-3, раскрытую в US 2015/0218274.
В одном варианте осуществления молекула антитела к TIM-3 представляет собой TSR-022 (AnaptysBio/Tesaro). В одном варианте осуществления молекула антитела к TIM-3 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи TSR-022. В одном варианте осуществления молекула антитела к TIM-3 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи APE5137 или APE5121. APE5137, APE5121 и другие антитела к TIM-3 раскрыты в WO 2016/161270.
В одном варианте осуществления молекула антитела к TIM-3 представляет собой клон антитела F38-2E2. В одном варианте осуществления молекула антитела к TIM-3 содержит одну или несколько последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи F38-2E2.
Дополнительные известные антитела к TIM-3 включают антитела, описанные, например, в WO 2016/111947, WO 2016/071448, WO 2016/144803, US 8552156, US 8841418 и US 9163087.
В одном варианте осуществления антитело к TIM-3 представляет собой антитело, которое конкурирует за связывание и/или связывается с тем же эпитопом в TIM-3, что и одно из антител к TIM-3, описанных в данном документе.
В некоторых вариантах осуществления BCMA-связывающую молекулу вводят в комбинации с ингибитором трансформирующего фактора роста бета (TGF-β). В некоторых вариантах осуществления ингибитор TGF-β представляет собой фрезолимумаб (регистрационный номер CAS: 948564-73-6). Фрезолимумаб также известен как GC1008. Фрезолимумаб представляет собой моноклональное антитело человека, которое связывается с изоформами 1, 2 и 3 TGF-бета и ингибирует их. Фрезолимумаб раскрыт, например, в WO 2006/086469, US 8383780 и US 8591901.
В некоторых вариантах осуществления ингибитор TGF-β представляет собой XOMA 089. XOMA 089 также известен как XPA.42.089. XOMA 089 представляет собой полностью человеческое моноклональное антитело, которое связывает и нейтрализует лиганды TGF-бета 1 и 2, и раскрыто в публикации согласно РСТ № WO 2012/167143.
В некоторых вариантах осуществления ВСМА-связывающую молекулу вводят в комбинации с молекулой антитела к CD73. В одном варианте осуществления молекула антитела к CD73 представляет собой полную молекулу антитела или ее антигенсвязывающий фрагмент. В определенных вариантах осуществления молекула антитела к CD73 связывается с белком CD73 и снижает активность CD73, например, CD73 человека, например, ингибирует ее или оказывает на нее антагонистическое действие.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO2016/075099. В одном варианте осуществления молекула антитела к CD73 представляет собой MEDI 9447, например, раскрытый в WO2016/075099. Альтернативные названия MEDI 9447 включают клон 10.3 или 73combo3. MEDI 9447 представляет собой антитело IgG1, которое ингибирует активность CD73, например, оказывает на нее антагонистическое действие. MEDI 9447 и другие молекулы антител к CD73 также раскрыты в WO2016/075176 и US2016/0129108.
В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из MEDI 9477.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO2016/081748. В одном варианте осуществления молекула антитела к CD73 представляет собой 11F11, например, раскрытый в WO2016/081748. 11F11 представляет собой антитело IgG2, которое ингибирует активность CD73, например, оказывает на нее антагонистическое действие. Антитела, полученные из 11F11, например CD73.4 и CD73.10; клоны 11F11, например 11F11-1 и 11F11-2; и другие молекулы антитела к CD73 раскрыты в WO2016/081748 и US 9605080.
В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из 11F11-1 или 11F11-2.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое, например, в US 9605080.
В одном варианте осуществления молекула антитела к CD73 представляет собой CD73.4, например, раскрытый в US 9605080. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из CD73.4.
В одном варианте осуществления молекула антитела к CD73 представляет собой CD73.10, например, раскрытый в US 9605080. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из CD73.10.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO2009/0203538. В одном варианте осуществления молекула антитела к CD73 представляет собой 067-213, например, раскрытый в WO2009/0203538.
В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из 067-213.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в US 9090697. В одном варианте осуществления молекула антитела к CD73 представляет собой TY/23, например, раскрытый в US 9090697. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из TY/23.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO2016/055609. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в WO2016/055609.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO2016/146818. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в WO2016/146818.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO2004/079013. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в WO2004/079013.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO2012/125850. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в WO2012/125850.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO2015/004400. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в WO2015/004400.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO2007/146968. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в WO2007146968.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в US2007/0042392. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в US2007/0042392.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в US2009/0138977. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в US2009/0138977.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в Flocke et al., Eur J Cell Biol. 1992 Jun;58(1):62-70. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в Flocke et al., Eur J Cell Biol. 1992 Jun;58(1):62-70.
В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в Stagg et al., PNAS. 2010 Jan 107(4): 1547-1552. В некоторых вариантах осуществления молекула антитела к CD73 представляет собой TY/23 или TY11.8, раскрытую в Stagg et al. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого у Stagg et al.
В некоторых вариантах осуществления BCMA-связывающую молекулу вводят в комбинации с ингибитором интерлейкина-17 (IL-17).
В некоторых вариантах осуществления ингибитор IL-17 представляет собой секукинумаб (регистрационный номер CAS: 875356-43-7 (тяжелая цепь) и 875356-44-8 (легкая цепь)). Секукинумаб также известен как AIN457 и COSENTYX®. Секукинумаб представляет собой рекомбинантное моноклональное антитело IgG1/κ человека, которое специфически связывается с IL-17A. Оно экспрессируется в рекомбинантной линии клеток яичника китайского хомячка (CHO). Секукинумаб описан, например, в WO 2006/013107, US 7807155, US 8119131, US 8617552 и EP 1776142.
В некоторых вариантах осуществления ингибитор IL-17 представляет собой CJM112. CJM112 также известен как XAB4. CJM112 представляет собой полностью человеческое моноклональное антитело (например, изотипа IgG1/κ), которое нацеливается на IL-17A. CJM112 раскрыт, например, в WO 2014/122613.
CJM112 может связываться с IL-17A человека, макака-крабоеда, мыши и крысы и нейтрализовать биологическую активность этих цитокинов in vitro и in vivo. IL-17A, представитель семейства IL-17, является главным провоспалительным цитокином, который, как было показано, играет важные роли при множестве иммуноопосредованных состояний, таких как псориаз и виды рака (Witowski et al. (2004) Cell Mol. Life Sci. p. 567-79; Miossec and Kolls (2012) Nat. Rev. Drug Discov. p. 763-76).
В некоторых вариантах осуществления ингибитор IL-17 представляет собой иксекизумаб (регистрационный номер CAS: 1143503-69-8). Иксекизумаб также известен как LY2439821. Иксекизумаб представляет собой гуманизированное моноклональное антитело IgG4, которое нацеливается на IL-17A. Иксекизумаб описан, например, в WO 2007/070750, US 7838638 и US 8110191.
В некоторых вариантах осуществления ингибитор IL-17 представляет собой бродалумаб (регистрационный номер CAS: 1174395-19-7). Бродалумаб также известен как AMG 827 или AM-14. Бродалумаб связывается с рецептором A интерлейкина-17 (IL-17RA) и предотвращает активацию рецептора, опосредованную IL-17. Бродалумаб раскрыт, например, в WO 2008/054603, US 7767206, US 7786284, US 7833527, US 7939070, US 8435518, US 8545842, US 8790648 и US 9073999.
В некоторых вариантах осуществления ВСМА-связывающую молекулу вводят в комбинации с ингибитором интерлейкина-1-бета (IL-1β).
В некоторых вариантах осуществления ингибитор IL-1β представляет собой канакинумаб. Канакинумаб также известен как ACZ885 или ILARIS®. Канакинумаб представляет собой человеческое моноклональное антитело IgG1/κ, которое нейтрализует биоактивность IL-1β человека. Канакинумаб раскрыт, например, в WO 2002/16436, US 7446175 и EP 1313769.
В некоторых вариантах осуществления BCMA-связывающую молекулу вводят в комбинации с ингибитором CD32B. В некоторых вариантах осуществления ингибитор CD32B представляет собой молекулу антитела к CD32B. Иллюстративные молекулы антитела к CD32B раскрыты в US 8187593, US 8778339, US 8802089, US 20060073142, US 20170198040 и US 20130251706.
В определенных вариантах осуществления ВСМА-связывающую молекулу вводят в комбинации с одним из соединений, перечисленных в таблице А.
Торговое наименование
US 2007/142401
WO 2005/039549
TASIGNA®
HCl • H2O
US 7169791 
US 2010/0105667
EXJADE®
FEMARA®
GLEEVEC®
Мезилат
Дигидрохлоридная соль
US 7767675
US 8420645 H3PO4
H3PO4
WO 2002/022577
EP 1870399
ZYKADIA™ 
KISQALI®
US 8685980 
WO2008/106692
US 8735551
Линкер: SMCC (см. абзац [00117])
Полезная нагрузка: DM1 (см. абзац [00111])
См. также п. 29 формулы изобретения 
US 2012/252785
SIGNIFOR®
US 8519129 
AMDRAY™ 
сукцинат
или его холиновая соль
US 7989497
WO2011/121418
US 8796284

US 7378423
US 7994185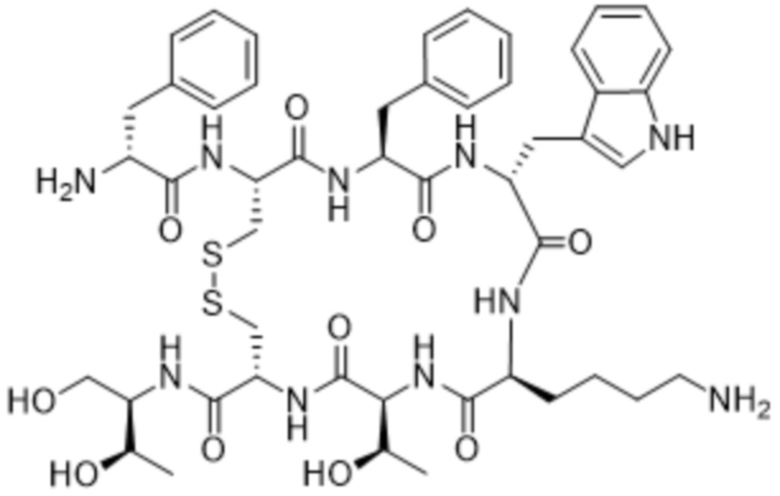
EP 0029579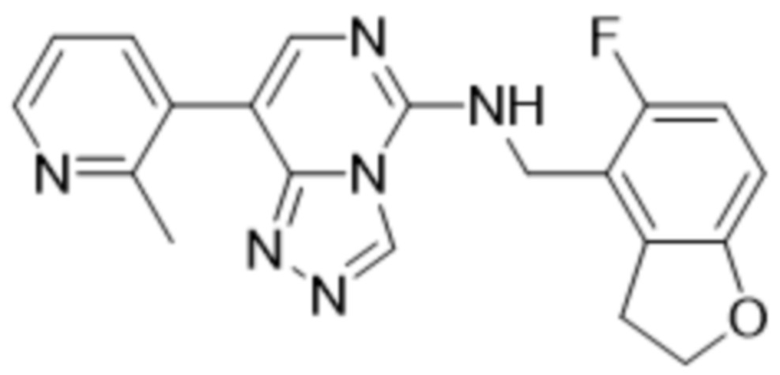
US 9580437
EP 3237418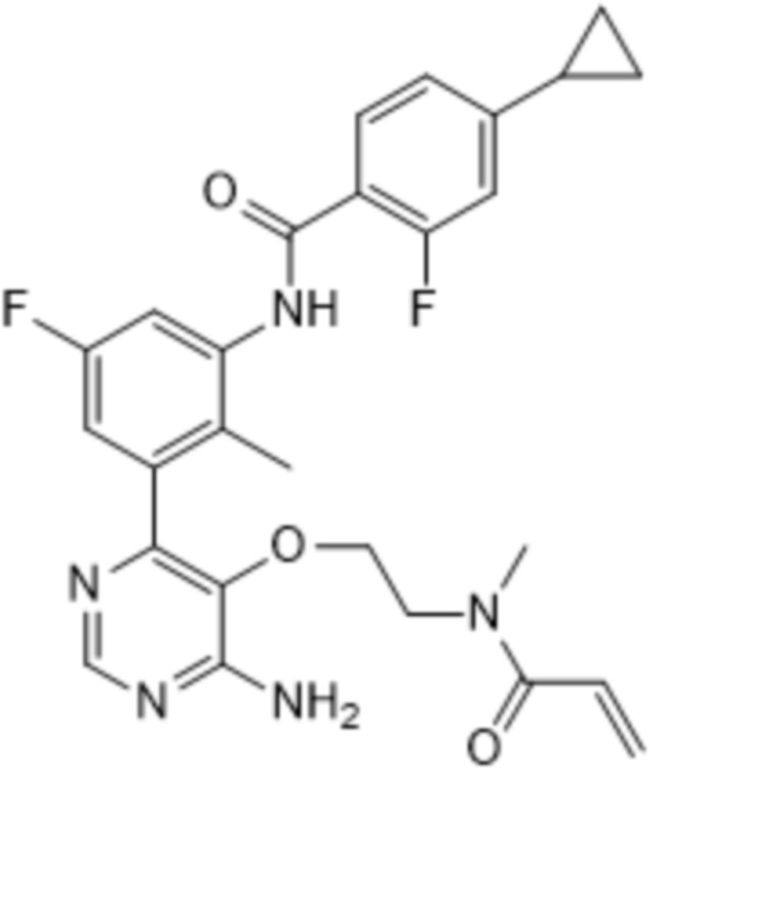
WO/2015/079417
В некоторых вариантах осуществления ВСМА-связывающую молекулу вводят в комбинации с одним или несколькими из средств терапии CAR-T-клеткамик, NIZ985, агонистов GITR, таких как GWN323, PTK787, MBG453, mAb12425, CLR457, BGT226, BYL719, AMN107, ABL001, IDH305/LQS305, LJM716, MCS110, WNT974/LGK974, BLZ945, NIR178, QBM076, MBG453, CGS-20267, LHS534, LKG960, LDM099/SHP099, TNO155, LCL161, MAP855/LQN716, RAD001, LEJ511, LDK378, LOU064, LSZ102, LEQ506, RAF265/CHIR265, канакинумаб, гевокизумаб, анакинра, рилонацепт, CGS-20267, PSC833, GGP-57148B, CGM097, HDM201, LBH589, PKC412, LHC165, MAK683, INC280, INC424, LJE704, LAG525 и NIS793.
В некоторых вариантах осуществления BCMA-связывающую молекулу вводят в комбинации со стандартным лечением.
Стандартное лечение множественной миеломы и ассоциированных заболеваний включает химиотерапию, трансплантацию стволовых клеток (аутологичную или аллогенную), лучевую терапию и другие средства лекарственной терапии. Лекарственные средства, часто используемые для лечения миеломы, включают алкилирующие средства (например, бендамустин, циклофосфамид и мелфалан), ингибиторы протеасом (например, бортезомиб), кортикостероиды (например, дексаметазон и преднизон) и иммуномодуляторы (например, талидомид и леналидомид или Revlimid®) или их любую комбинацию. Лекарственные средства из группы бисфосфонатов также часто вводят в комбинации со стандартными средствами лечения MM для предупреждения потери костной ткани. Пациенты старше 65-70 лет в редких случаях являются кандидатами для трансплантации стволовых клеток. В некоторых случаях возможными вариантами лечения для пациентов младше 60 лет с субоптимальным ответом на первую трансплантацию являются двойные трансплантации аутологичных стволовых клеток. Композиции и способы по настоящему изобретению можно вводить в комбинации с любым из назначаемых в настоящее время средств лечения множественной миеломы.
Лимфому Ходжкина обычно лечат с помощью лучевой терапии, химиотерапии или трансплантации гемопоэтических стволовых клеток. Наиболее распространенным средством терапии неходжкинской лимфомы является режим R-CHOP, который состоит из четырех различных химиотерапевтических препаратов (циклофосфамид, доксорубицин, винкристин и преднизолон) и ритуксимаба (Rituxan®). Другие средства терапии, обычно применяемые для лечения NHL, включают другие химиотерапевтические средства, лучевую терапию, трансплантацию стволовых клеток (аутологичную или аллогенная трансплантация костного мозга) или биологическую терапию, такую как иммунотерапия. Другие примеры биологических терапевтических средств включают без ограничения ритуксимаб (Rituxan®), тозитумомаб (Bexxar®), эпратузумаб (LymphoCide®) и алемтузумаб (MabCampath®). Композиции и способы по настоящему изобретению можно вводить в комбинации с любым из назначаемых в настоящее время средств лечения лимфомы Ходжкина или неходжкинской лимфомы.
Стандартное лечение WM заключается в химиотерапии, в частности ритуксимабом (Rituxan®). Другие химиотерапевтические лекарственные средства, такие как хлорамбуцил (Leukeran®), циклофосфамид (Neosar®), флударабин (Fludara®), кладрибин (Leustatin®), винкристин и/или талидомид, можно применять в комбинации. Кортикостероиды, такие как преднизон, также можно вводить в комбинации с химиотерапией. Плазмаферез или замещение плазмы обычно применяют в ходе всего лечения пациента для облегчения некоторых симптомов посредством удаления парапротеина из крови. В некоторых случаях трансплантация стволовых клеток является вариантом лечения для некоторых пациентов.
ВСМА-связывающие молекулы, которые являются биспецифическими по отношению к ВСМА и CD3, можно вводить в комбинации со средством, которое снижает или ослабляет побочный эффект, ассоциированный с введением ВСМА-связывающей молекулы, биспецифической в отношении ВСМА и CD3. Побочные эффекты, ассоциированные с введением биспецифической BCMA-связывающей молекулы могут включать без ограничения синдром высвобождения цитокинов ("CRS") и гематологический лимфогистиоцитоз (HLH), также называемый синдромом активации макрофагов (MAS). Симптомы CRS могут включать высокую температуру, тошноту, преходящую гипотензию, гипоксию и т. п. CRS может включать клинические системные признаки и симптомы, такие как лихорадка, усталость, анорексия, виды миалгии, виды артралгии, тошнота, рвота и головная боль. CRS может включать клинические признаки и симптомы со стороны кожи, такие как сыпь. CRS может включать клинические признаки и симптомы со стороны желудочно-кишечного тракта такие как тошнота, рвота и диарея. CRS может включать клинические признаки и симптомы со стороны дыхательной системы, такие как тахипноэ и гипоксемия. CRS может включать клинические признаки и симптомы со стороны сердечно-сосудистой системы, такие как тахикардия, "расширенное" пульсовое давление, гипотензия, повышенный сердечный выброс (ранний) и потенциально сниженный сердечный выброс (поздний). CRS может включать признаки и симптомы клинического свертывания крови, такие как повышенное содержание d-димера, гипофибриногенемия с кровотечением и без такового. CRS может включать клинические признаки и симптомы со стороны почек, такие как азотемия. CRS может включать клинические признаки и симптомы со стороны печени, такие как трансаминит и гипербилирубинемия. CRS может включать клинические признаки и симптомы со стороны нервной системы, такие как головная боль, изменения психического состояния, спутанность, делирий, затруднения с подбором слов или явная афазия, галлюцинации, тремор, дисметрия, нарушение походки и судороги.
Соответственно, способы, описанные в данном документе, могут предусматривать введение описанной в данном документе BCMA-связывающей молекулы, которая является биспецифической в отношении BCMA и CD3, субъекту и дополнительное введение одного или нескольких средств для контроля повышенных уровней растворимого фактора, образующегося в результате лечения с помощью BCMA-связывающей молекулы, которая является биспецифической в отношении BCMA и CD3. В одном варианте осуществления повышенный растворимый фактор у субъекта представляет собой одно или несколько из IFN-ɣ, TNFα, IL-2 и IL-6. В одном варианте осуществления повышенный фактор у субъекта представляет собой одно или несколько из IL-1, GM-CSF, IL-10, IL-8, IL-5 и фракталкина. Следовательно, средство, вводимое для лечения этого побочного эффекта, может представлять собой средство, которое нейтрализует один или несколько из этих растворимых факторов. В одном варианте осуществления средство, которое нейтрализует одну или несколько из этих растворимых форм, представляет собой антитело или его антигенсвязывающий фрагмент. Примеры таких средств включают без ограничения стероид (например, кортикостероид), ингибитор TNFα, ингибитор IL-1R и ингибитор IL-6. Примером ингибитора TNFα является молекула антитела к TNFα, такая как инфликсимаб, адалимумаб, цертолизумаб пегол и голимумаб. Другим примером ингибитора TNFα является слитый белок, такой как этанерцепт. Низкомолекулярный ингибитор TNFα включает без ограничения производные ксантина (например, пентоксифиллин) и бупропион. Примером ингибитора IL-6 является молекула антитела к IL-6, такая как тоцилизумаб (toc), сарилумаб, элсилимомаб, CNTO 328, ALD518/BMS-945429, CNTO 136, CPSI-2364, CDP6038, VX30, ARGX-109, FE301 и FM101. В одном варианте осуществления молекула антитела к IL-6 представляет собой тоцилизумаб. Примером ингибитора на основе IL-1R является анакинра.
В некоторых вариантах осуществления субъекту вводят кортикостероид, такой как, например, метилпреднизолон, гидрокортизон, среди прочего. В некоторых вариантах осуществления субъекту вводят кортикостероид, например метилпреднизолон, гидрокортизон, в комбинации с бенадрилом и тайленолом перед введением ВСМА-связывающей молекулы, которая является биспецифической в отношении ВСМА и CD3, для снижения риска CRS.
В некоторых вариантах осуществления субъекту вводят сосудосуживающее средство, такое как, например, норэпинефрин, дофамин, фенилэфрин, эпинефрин, вазопрессин или любую их комбинацию.
В одном варианте осуществления субъекту могут вводить жаропонижающее средство. В одном варианте осуществления субъекту могут вводить аналгезирующее средство.
Известно, однако, что в некоторых случаях виды терапии на основе антитела, включая биспецифические антитела, могут вызывать массивное высвобождение цитокина, ведущее к CRS, даже при совместном введении или лечении средствами, которые могут контролировать CRS. В некоторых случаях CRS может быть настолько серьезным, что является опасным для жизни и/или приводит к смерти. См., Shimabukuro-Vornhagen, A. et al., 2018, J. Immunother Cancer. 6:56. Следовательно, существует необходимость в разработке видов терапии на основе антитела, которые вызывают меньшее высвобождение цитокина, но в то же время сохраняют и/или улучшают свою эффективность.
8. ПРИМЕРЫ
8.1. Пример 1: Выделение антител к BCMA с использованием фагового дисплея
8.1.1. Краткий обзор
BCMA представляет собой рецептор клеточной поверхности, экспрессируемый на плазматических клетках, а также на других B-клеточных злокачественных новообразованиях, особенно на клетках множественной миеломы. Для эффективной фармацевтической разработки крайне необходимо иметь антитело, которое характеризуется перекрестной реактивностью как с человеческими антигенами, так и с соответствующим антигеном у модельных видов приматов, отличных от человека, таких как макак-крабоед, с целью исследований доклинической фармакокинетики и токсикологии.
8.1.2. Материалы и способы
8.1.2.1. Пэннинг
Чтобы найти антитела, которые характеризовались перекрестной реактивностью как с ВСМА человека, так и с ВСМА макака-крабоеда, проводили пэннинг библиотеки наивных фагов, содержащей фрагменты антител человека, в отношении рекомбинантных антигенов ВСМА человека и макака-крабоеда с помощью стандартных процедур. Вкратце, меченные посредством Fc белки ВСМА человека (№ по кат. BC7-H5254) и ВСМА макака-крабоеда (№ по кат. BCA-C5253) приобрели у ACRO Biosystems (Ньюарк, Делавэр, США) и биотинилировали в лаборатории.
В первом цикле пэннинга пул наивных фагов ресуспендировали и трижды истощали биотинилированным Fc человека (№ по кат. 009-060-008, Jackson ImmunoResearch, Вест-Гроув, Пенсильвания, США), захваченным на Dynabeads со стрептавидином (№ по кат. M-280, Thermo Fisher Scientific, Уолтем, Массачусетс, США). Затем пул фагов разделяли на две части и проводили пэннинг в отношении 40 мкг биотинилированного BCMA-Fc либо человека, либо макака-крабоеда, захваченного на Dynabeads в присутствии 5-кратного избытка небиотинилированного Fc человека (№ по кат. 009-000-008, Jackson ImmunoResearch, Вест-Гроув, Пенсильвания, США). Захваченные фаги инкубировали в течение 60 минут, промывали 10 раз промывочным буфером (PBS+2% молока+1% BSA+0,05% Tween 20) и элюировали с гранул с помощью обработки посредством 200 мкл буфера для элюирования (Pierce IgG Elution Buffer, № по кат. 21004, Thermo Fisher Scientific, Уолтем, Массачусетс, США). Затем элюированные фаги нейтрализовали с помощью обработки посредством 20 мкл буфера для нейтрализации (1M Tris pH 9, № по кат. T1090, Teknova, Холлистер, Калифорния, США). Стадии элюирования и нейтрализации повторяли один раз, элюаты объединяли и использовали для заражения 10 мл клеток ER2738 (№ по кат. 60522, Lucigen, Миддлтон, Висконсин, США), культивированных в среде 2YT (№ по кат. Y0167, Teknova, Холлистер, Калифорния, США). Отдельные культуры поддерживали для фаговых пулов, подвергаемых скринингу в отношении BCMA человека или макака-крабоеда. Инфицированные клетки ER2738 инкубировали при 37°C в течение 30 минут, затем добавляли к 25 мл буфера 2YT, содержащего 100 мкг/мл карбенциллина (№ по кат. C2112, Teknova, Холлистер, Калифорния, США). Затем в среду добавляли избыток хелперного фага M13K07 (№ по кат. N0315S, New England Biolabs, Ипсуич, Массачусетс, США) и полученную культуру выращивали в течение ночи при 37°C. Супернатант культуры собирали посредством центрифугирования, декантировали, и амплифицированный фаг извлекали из супернатанта путем осаждения с помощью PEG/NaCl (PEG 6000/2,5M NaCl, № по кат. P4168, Teknova, Холлистер, Калифорния, США), центрифугирования и ресуспендирования в PBS.
Во втором цикле пэннинга приблизительно 1×1013 фагов из каждого из выходных пулов первого цикла подвергали пэннингу в отношении альтернативных антигенов (фаги, подверженные пэннингу в отношении BCMA человека в первом цикле, использовали для пэннинга в отношении BCMA макака-крабоеда во втором цикле и наоборот), с использованием более низкой концентрации захваченного антигена (15 мкг биотинилированного BCMA-Fc либо человека, либо макака-крабоеда, захваченного на Dynabeads). Оставшийся протокол соответствовал протоколу первого цикла пэннинга, включая стадию истощения Fc.
В третьем цикле пэннинга выходящий фаг из обоих пулов пэннинга объединяли и подвергали пэннингу в отношении 1 мкг человеческого BCMA-His-APP-Avi (таблица 12), захваченного на Sera-Mag SpeedBead Neutravidin (№ по кат. 7815-2104-011150, Thermo Fisher Scientific, Уолтем, Массачусетс, США). Оставшийся протокол соответствовал тому, который использовался в первом и втором циклах пэннинга, включая стадии истощения Fc, а также дополнительную стадию истощения с немечеными гранулами Sera-Mag SpeedBead Neutravidin.
В четвертом цикле пэннинга выходной фаг из третьего цикла подвергали пэннингу в отношении 1 мкг BCMA-Fc макака-крабоеда (№ по кат. 90103-C02H-50, Sino Biological, Пекин, Китай), захваченного на Dynabeads с белком A (№ по кат. 10001D, Thermo Fisher Scientific, Уолтем, Массачусетс, США). Оставшийся протокол соответствовал тому, который применялся в первом, втором и третьем циклах пэннинга, включая стадии истощения Fc, а также дополнительную стадию истощения с немечеными Dynabeads с белком A.
8.1.2.2. Обогащение последовательности и скрининг на основе фагового ELISA
Приблизительно 400 одиночных фаговых колоний отбирали из выходного пула четвертого цикла пэннинга и секвенировали с использованием обратного праймера M13. Пять лучших обогащенных клонов и несколько синглетных клонов (PI-26, PI-28, PI-61, PIII-78, PIII-79, PIV-24, PI-45, PII-45, PII-55) выбирали для амплифицирования и восстановления в качестве фага для фагового ELISA. Синглетные клоны выбирали на основе обогащенных дублетов (наивысшая степень обогащения) после третьего цикла пэннинга, а синглеты после четвертого цикла пэннинга.
Каждый из трех 96-луночных планшетов NUNC с прозрачным плоским дном, покрытых стрептавидином (№ по кат. 436014, Thermo Fisher Scientific, Уолтем, Массачусетс, США), покрывали биотинилированным в лаборатории человеческим ВСМА, меченным посредством Fc (№ по кат. BC7-H5254, ACRO Biosystems, Ньюарк, Делавэр, США), человеческим BCMA-His-APP-Avi и биотинилированным Fc человеческого IgG1 (№ по кат. 009-060-008, Jackson Immunoresearch, Вест-Гроув, Пенсильвания, США) в концентрации 1 мкг/мл в dPBS. 96-луночный планшет NUNC Maxisorp с прозрачным плоским дном (№ по кат. 442404, Thermo Fisher Scientific, Уолтем, Массачусетс, США) покрывали с помощью ВСМА макака-крабоеда, меченного посредством Fc (№ по кат. BCA-C5253, ACRO Biosystems, Ньюарк, Делавэр, США) в дозе 1 мкг/мл в dPBS. Планшеты инкубировали в течение ночи при 2-8°C.
Покрытые антигеном планшеты промывали в устройстве для промывания планшетов BioTek (EL406, BioTek, Винуски, Вермонт, США) с помощью PBS, Tween20 и блокировали с помощью 300 мкл/лунка блокирующего буфера (dPBS, 5% BSA, 0,05% полисорбат 20, 0,01% d-биотин) в течение 2 часов. Планшеты снова промывали, добавляли 100 мкл/лунка титрованных фаговых образцов и инкубировали в течение 2 часов при комнатной температуре. Планшеты промывали после инкубации фагового образца и добавляли 50 мкл/лунка разведенного 1:5000 HRP-конъюгированного детекторного антитела к M13 (№ по кат. 27-9421-01, GE, Пискатауэй, Нью-Джерси, США) инкубировали в течение 30 минут при комнатной температуре. Планшеты промывали и проявляли ELISA путем внесения 100 мкл/лунка 1-компонентного субстрата пероксидазы (№ по кат. 50-77-04, SeraCare, Милфорд, Массачусетс, США) и гашения реакции с помощью 50 мкл/лунка 1 н. HCl. Оптическую плотность при 450 нм считывали на планшет-ридере EnVision (2105-0010, Perkin Elmer, Уолтем, Массачусетс, США).
8.1.3. Результаты
Данные ELISA для каждого титрования моноклонального фага показаны на фиг. 2. Все пять обогащенных клонов продемонстрировали надежное связывание с BCMA человека в форматах, меченных либо посредством Fc, либо His-APP-Avi. Клоны PI-26 и PI-61 продемонстрировали сравнимые уровни связывания между меченным посредством Fc BCMA макака-крабоеда и меченным посредством Fc BCMA человека. Клоны PI-28 и PIII-79 продемонстрировали связывание с меченным посредством Fc BCMA макака-крабоеда и BCMA человека, но сигнал связывания с BCMA макака-крабоеда снижался до BCMA человека, что указывает на более низкую аффинность связывания. Клон PIII-78 продемонстрировал остаточные уровни связывания с меченным посредством Fc BCMA макака-крабоеда, а также с Fc-меткой отдельно, что свидетельствует о степени неспецифического связывания и минимальной перекрестной реактивности с макаком-крабоедом. Все четыре синглетных клона продемонстрировали сильное связывание с меченным посредством Fc BCMA человека, но более слабое связывание с меченным посредством Fc BCMA макака-крабоеда с точки зрения аффинности для клонов PII-55 и PII-45 и амплитуды сигнала для клонов PI-45 и PIV-24. Неспецифическое связывание с Fc было минимальным для всех четырех клонов. Из-за их сопоставимого связывания с BCMA человека и макака-крабоеда только клон PIII-78 исключили из этого скрининга, а оставшиеся восемь клонов, PI-26, PI-61, PI-28, PIII-79, PI-45, PII-45 , PII-55, PIV-24, идентифицировали как потенциальные ведущие кандидаты и их преобразовали в биспецифические антитела.
8.2. Пример 2. Созревание аффинности PI-61 с использованием дрожжевого дисплея
8.2.1. Краткий обзор
Как подробно описано в примере 1, антитело PI-61 характеризовалось более низкой аффинностью к ВСМА макака-крабоеда (KD ~240 нМ) по сравнению с ВСМА человека (KD ~34 нМ), как определено с помощью поверхностного плазмонного резонанса. Для фармацевтических разработок было бы желательно иметь эквивалентные аффинности как к антигенам человека, так и к антигенам макака-крабоеда, а также более высокую общую аффинность связывания. Для повышения аффинности синтезировали три библиотеки вариантов с мутациями в 4 CDR-участках, отображаемых на поверхности дрожжей, и проводили скрининг для выделения вариантов PI-61 с более высокими аффинностями связывания с ВСМА человека и макака-крабоеда.
8.2.2. Конструирование и скрининг библиотеки 1: Варианты CDR H2/CDR L2
Участки CDR H2 и CDR L2 PI-61 (показанные в таблице 13) выбирали для мутагенеза, поскольку они содержали участки, отличные от зародышевой линии человека, и предполагаемый сайт изомеризации аспарагиновой кислоты (DG), что было бы нежелательно для фармацевтических разработок. Библиотеки ДНК конструировали с мутациями в положениях 57-64 (SYDGSN, (SEQ ID NO:141)) (нумерация по IMGT) CDR H2 и положениях 56-57 (DV) и 68-69 (PS) CDR L2.
Первой созданной библиотекой была CDR L2. Синтетическую ДНК, соответствующую scFv PI-61, модифицированному библиотекой L2, объединили с векторной ДНК из вектора экспрессии дрожжей pYUNBC4 и электропорировали в дрожжевой штамм, сверхэкспрессирующий белок Aga1 под контролем промотора Gal1, для обеспечения гомологичной рекомбинации и сборки конечной библиотеки.
Для первого цикла скрининга дрожжевую библиотеку L2 выращивали при 20°C в течение 3 дней в 400 мл бульона SD-ura (Clontech, Маунтин-Вью, Калифорния, США), затем осаждали центрифугированием в течение 5 минут при 5000 x g. Супернатант удаляли и дрожжевой осадок ресуспендировали в 400 мл бульона SD-ura с 1% рафинозы и 2% галактозы (Clontech, Маунтин-Вью, Калифорния, США) и выращивали при 20°C в течение 22 часов для индукции экспрессии. Культуру осаждали, супернатант удаляли, осадок один раз промывали с помощью PBSM (PBS (Invitrogen) с 1% BSA (бычий сывороточный альбумин) и 2 мМ EDTA), затем ресуспендировали в 15 мл PBSM. Библиотеку L2 подвергали термообработке при 37°C в течение 10 мин, охлаждали до 4°C, затем истощали стрептавидином и магнитными гранулами для связывания биотина (Miltenyi) в течение 15 мин, гранулы удаляли с помощью колонки MACS LS (Miltenyi) и промывали. Затем дрожжевую библиотеку ресуспендировали в 35 мл PBSM, содержащего 10 нМ биотинилированного ВСМА человека (последовательность показана в таблице 12), и инкубировали в течение 1 часа при комнатной температуре. Дрожжи осаждали, дважды промывали с помощью PBSM и ресуспендировали в 10 мл PBSM со 100 мкл магнитных гранул со стрептавидином, инкубировали в течение 5 минут при 4°C, осаждали, ресуспендировали в 15 мл PBSM и отделяли на колонке MACS LS. Захваченные клетки промывали с помощью PBSM, элюировали и добавляли к 10 мл бульона SD-ura с 2% глюкозой и выращивали при 30°C со встряхиванием в течение ночи.
Выход библиотеки L2 из первого цикла отбора использовали в качестве матрицы для конструирования библиотеки H2. Синтетическую ДНК с увеличенным разнообразием CDR H2 в VH-домене объединяли с векторной ДНК из библиотеки L2 и электропорировали в дрожжи. Эта полученная библиотека, сочетающая разнообразие CDR L2 и CDR H2, в дальнейшем будет называться библиотекой L2/H2.
Для второго цикла скрининга библиотеку L2/H2 культивировали и индуцировали экспрессию, как описано для первого цикла скрининга, и аналогичным образом истощали в отношении стрептавидина и магнитных гранул для связывания биотина. Библиотеку L2/H2 подвергали термообработке при 34°C в течение 10 минут, охлаждали до 4°C, ресуспендировали в PBSM и инкубировали с 25 нМ биотинилированного ВСМА человека в течение 1 ч. при комнатной температуре. Дрожжи осаждали, дважды промывали с помощью PBSM и ресуспендировали в 10 мл PBSM с 200 мкл магнитных гранул со стрептавидином, инкубировали в течение 5 мин. при 4°C, осаждали, ресуспендировали в 15 мл PBSM и отделяли на колонке MACS LS. Захваченные клетки промывали с помощью PBSM, элюировали и добавляли к 50 мл бульона SD-ura с 1% рафинозы, 2% галактозы и инкубировали в течение 24 часов при 23°C.
Для третьего цикла скрининга полученные дрожжи из второго цикла осаждали, промывали и ресуспендировали в PBSM и инкубировали с 1 нМ BCMA макака-крабоеда-APP-Avi (таблица 13) в течение 1 часа при комнатной температуре. Дрожжи осаждали, дважды промывали с помощью PBSM и ресуспендировали в 5 мл PBSM с 50 мкл магнитных гранул со стрептавидином, инкубировали в течение 5 мин. при 4°C, осаждали, ресуспендировали в 15 мл PBSM и отделяли на колонке MACS LS. Захваченные клетки промывали с помощью PBSM, элюировали и добавляли к 200 мл бульона SD-ura с 2% глюкозой и выращивали в течение 3 дней при 18°C.
Для четвертого цикла скрининга полученные дрожжи из третьего цикла осаждали, промывали и ресуспендировали в 200 мл бульона SD-ura с 1% раффинозы, 2% галактозы и инкубировали в течение 22 часов при 20°C для индукции экспрессии. Из полученной культуры отбирали два образца по 2,5 мл, осаждали, ресуспендировали в PBSM и каждый инкубировали с 250 пМ биотинилированного ВСМА человека. Первый образец инкубировали с ВСМА человека в течение 45 минут при комнатной температуре, осаждали, дважды промывали с помощью PBSF и затем ресуспендировали в 1 мл PBSF (PBS с 0,1% BSA). Второй образец инкубировали с ВСМА человека в течение 45 минут при комнатной температуре. Оба образца осаждали, дважды промывали с помощью PBSF и ресуспендировали в 200 мкл PBSF+разведение 1:30 кроличьего антитела к cMyc-FITC (Abcam) + разведение 1:100 нейтравидин-dylight 633 (Invitrogen). Образцы инкубировали при 4°C в течение 30 мин., осаждали, дважды промывали с помощью PBSF, ресуспендировали в 3 мл PBSF, фильтровали через фильтры 40 мкм, затем сортировали с использованием проточной цитометрии на клеточном сортере FACS Aria (Becton Dickinson Biosciences, Сан-Хосе, Калифорния, США). Приблизительно 5×105 дрожжей выделяли и ресуспендировали в 4 мл бульона SD-ura с 2% глюкозы и выращивали в течение ночи при 30°C.
Для пятого цикла скрининга ночную культуру, полученную из выхода четвертого цикла, разбавляли до 20 мл в бульоне SD-ura. 10 мл отбирали, осаждали, ресуспендировали в 20 мл бульона SD-ura с 1% рафинозы, 2% галактозы и инкубировали в течение 22 часов при 20°C для индукции экспрессии. На следующий день полученную библиотеку подвергали термообработке при 40°C в течение 10 мин.т, охлаждали до 4°C, ресуспендировали в PBSM, разделяли на два образца и инкубировали со 100 пМ биотинилированного BCMA макака-крабоеда по протоколу, аналогичному четвертому циклу скрининга, как указано выше. Однако куриные антитела к cMyc-FITC (Abcam) и стрептавидин-dylight 633 (Invitrogen) использовали для мечения дрожжей перед сортировкой клеток. Опять же, дрожжи, демонстрирующие высокую интенсивность окрашивания, гейтировали и сортировали. Приблизительно 1,5×105 дрожжей выделяли и ресуспендировали в 4 мл бульона SD-ura с 2% глюкозы и выращивали в течение ночи при 30°C.
Для шестого цикла скрининга ночную культуру, полученную из выхода пятого цикла, использовали для инокуляции 100 мл бульона SD-ura с 2% глюкозой и выращивали в течение 6 часов при 30°C. Затем культуру осаждали, ресуспендировали в 50 мл бульона SD-ura с 1% рафинозы, 2% галактозы и инкубировали в течение 20 часов при 20°C для индукции экспрессии. Затем культуру осаждали, дважды промывали с помощью PBSM, ресуспендировали в 10 мл PBSM с 2,5 нМ биотинилированного ВСМА человека и перемешивали в течение 2 мин, осаждали, дважды промывали с помощью PBSM, затем ресуспендировали в 1 мл PBSM со 100 нМ немеченого BCMA человека и инкубировали в течение 2 часов. Затем образцы осаждали, ресуспендировали в 100 мкл PBSF+разведение 1:30 козьих антител к cMyc-FITC (Abcam) + разведение 1:100 нейтравидин-dylight 633 (Invitrogen) и инкубировали в течение 25 минут. Затем образцы осаждали, дважды промывали с помощью PBSF, ресуспендировали в 1 мл PBSF и сортировали на клеточном сортере FACS Aria. Приблизительно 1,6×105 дрожжей выделяли и ресуспендировали в 3 мл бульона SD-ura с 2% глюкозы и выращивали в течение ночи при 30°C.
Полученный пул разбавляли в SD-URA с 2% глюкозы и высевали на чашки с агаром с глюкозой CM-URA (Teknova) для получения колоний на достаточном удалении друг от друга. Чашки с агаром выращивали при 30°C в течение трех дней, затем 384 колонии собирали в 4×96-луночные планшеты с глубокими лунками, содержащие 500 мкл/лунка SD-URA, 1% рафинозы, 2% галактозы. Эти планшеты инкубировали при 20°C со встряхиванием в течение 2 дней для индукции экспрессии.
Каждый планшет с образцами использовали для создания трех тестовых планшетов для анализа методом проточной цитометрии. Приблизительно 100000 дрожжевых клеток из каждой лунки с образцом переносили в соответствующую лунку на каждом из трех 96-луночных тестовых планшетов, которые содержат 20 нМ, 900 пМ биотинилированного ВСМА макака-крабоеда или не содержат его. Мечение было по сути таким же, как указано выше для сортировки, за исключением использования 1:200 стрептавидин-dylight 633 (Invitrogen) и нейтравидин-dylight 633 (Invitrogen) в PBSF в качестве вторичного реагента и исключая любые антитела к cMyc. Тестовые планшеты анализировали на проточном цитометре Cytoflex (Beckman Coulter, Брея, Калифорния, США).
94 лучших совпадения, ранжированных по соотношению медианной флуоресценции выше фона при 900 пМ ВСМА к средней флуоресценции выше фона при 20 нМ, переносили с исходной чашки с агаром на чашки со свежим агаром с глюкозой CM-URA (Teknova) и выращивали при 30°C в течение 2 дней. Часть scFv из 94 совпадений амплифицировали с помощью ПЦР колоний, очищали с использованием HT ExoSap-IT (Thermo Fisher Scientific, Уолтем, Массачусетс, США) и отправляли в Genewiz (Саут-Плейнфилд, Нью-Джерси, США) для секвенирования по Сенгеру.
Девять лучших клонов, которые не содержали каких-либо нежелательных мутаций (дополнительных цистеинов, предполагаемых сайтов посттрансляционной модификации и т. д.) (последовательности показаны в таблице 13), отобрали для преобразования из scFv в CD3-биспецифический формат. Эти клоны должны характеризоваться самой высокой аффинностью связывания с ВСМА, что должно приводить к более эффективным молекулам при форматировании в качестве биспецифических антител. На фиг. 3 показано титрование растворимого ВСМА на поверхности отдельных клонов дрожжей. Значения MFI для каждого клона показаны в таблице 14.
CDR H1
CDR H2
CDR H3
CDR L1
CDR L2
CDR L3
Сводные данные значений MFI из анализа методом проточной цитометрии одиночного клона
На фиг. 4 подчеркнуты различия CDRH2 между исходным PI-61 и отобранными клонами. Представляет интерес положение 59 (нумерация по IMGT), которое в виде аспартата в исходной последовательности образует часть потенциального сайта изомеризации аспартата. В идентифицированных последовательностях оно было подвержено мутации с заменой в основном на аргинин или треонин.
На фиг. 5 показаны дополнительные мутации в CDRL2 идентифицированных клонов по сравнению с исходным PI-61. В положении 56 (нумерация по IMGT) в некоторых последовательностях произошла мутация с заменой аспартата на глутамат. Большинство последовательностей имеют мутацию с заменой пролина на лейцин в положении 61. Кроме того, в положении 62 произошла мутация с заменой серина либо на аргинин, либо на триптофан в большинстве идентифицированных последовательностей.
Условия скрининга для всех шести циклов приведены в таблице 15.
Скрининг дрожжевых библиотек CDR L2 и CDR L2/H2
8.2.3. Конструирование и скрининг библиотеки 2: Варианты CDR H3.1
N-концевую половину CDR H3 из PI-61 выбирали для мутагенеза, поскольку она содержала участки, отличные от зародышевой линии человека, и участки CDR H3 обычно важны для контактов с антигеном. Библиотеку ДНК (далее именуемую H3.1) конструировали с мутациями в положениях 107-112.2 (SGYALHD (SEQ ID NO:530)) (нумерация по IMGT) CDR-H3. Выходные данные из библиотеки 1 использовали в качестве входных данных для создания этой библиотеки, чтобы гарантировать, что все идентифицированные последовательности имеют мутации для удаления потенциального сайта изомеризации аспартата, который присутствовал в исходном CDRH2 PI-61.
ДНК scFv из выхода H2/L2 амплифицировали, модифицировали библиотекой H3.1, объединяли с векторной ДНК из вектора экспрессии дрожжей pYUNBC4 и электропорировали в дрожжи для обеспечения гомологичной рекомбинации и сборки конечной библиотеки.
Скрининг библиотеки 2 проводили практически так же, как скрининг библиотеки 1 (см. выше). Процедура сортировки и вторичные реагенты были по сути одинаковыми, за исключением количества циклов и порядка чередования антигенов между циклами. Используемые концентрации антигена, время ассоциации и время диссоциации также различались и перечислены в таблице 16.
Скрининг дрожжевой библиотеки CDR H3.1
8.2.4. Конструирование и скрининг библиотеки 3: Варианты CDR H3.2
С-концевую половину CDR H3 из PI-61 также выбирали для мутагенеза, поскольку она содержала участки, отличные от зародышевой линии человека, и участки CDR H3 обычно важны для контактов с антигеном. Библиотеку ДНК (далее именуемую H3.2) конструировали с мутациями в положениях 112.1-117 (DYYGLDV (SEQ ID NO:531)) (нумерация по IMGT) CDR H3. Выходные данные библиотеки 1 использовали в качестве входных данных для создания этой библиотеки, чтобы гарантировать, что все идентифицированные последовательности имеют мутации для удаления потенциального сайта изомеризации аспартата, который присутствовал в исходном CDRH2 PI-61.
ДНК scFv из выхода H2/L2 амплифицировали, модифицировали библиотекой H3.2, объединяли с векторной ДНК из вектора экспрессии дрожжей pYUNBC4 и электропорировали в дрожжи для обеспечения гомологичной рекомбинации и сборки конечной библиотеки.
Скрининг библиотеки 3 проводили практически так же, как скрининг библиотеки 1 (см. выше). Процедура сортировки и вторичные реагенты были по сути одинаковыми, за исключением количества циклов и порядка чередования антигенов между циклами. Используемые концентрации антигена, время ассоциации и время диссоциации также различались и перечислены в таблице 17.
Скрининг дрожжевой библиотеки CDR H3.1
8.3. Пример 3. Скрининг библиотек с созревшей аффинностью с использованием анализов активации
8.3.1. Краткий обзор
Пулы антител к ВСМА с созревшей аффинностью идентифицировали в примере 2, но эти антитела отображались на поверхности дрожжей в виде scFv. Одним из терапевтических применений этих последовательностей антител может быть использование биспецифических антител для перенаправления цитотоксичности Т-клеток в отношении опухолевых клеток, экспрессирующих ВСМА. Чтобы оценить применимость этих последовательностей антител в качестве биспецифических антител, последовательности вариабельного домена клонировали в формат гетеродимерного биспецифического антитела (фиг. 6), экспрессировали в клетках HEK 293 и протестировали в отношении способности связывать BCMA на опухолевых клетках и способности активировать Т-клетки в зависимости от мишени с помощью анализа репортерного гена люциферазы Jurkat NFAT luciferase (JNL).
8.3.2. Котрансфекция и экспрессия CD3
Пулы библиотек H3.1 и H3.2 из примера 2 преобразовывали в формат Fab и субклонировали в бицистронный вектор IgG с гетеродимерным Fc (фиг. 6). При котрансфекции с аналогичным вектором, содержащим scFv к CD3, слитый с гетеродимерным Fc, экспрессия этих клонов дает гетеродимерные биспецифические антитела с Fab к ВСМА на первой тяжелой цепи и scFv к CD3 на второй тяжелой цепи (фиг. 6). Смесь двух векторов в соотношении 1:1 при общей концентрации ДНК 1 мкг/мл смешивали с 3 мкг/мл PEI (40K линейный, Polysciences, Уоррингтон, Пенсильвания, США), добавляли к клеткам Expi293 (Invitrogen) и выращивали в течение пяти дней при 37°C/8% углекислого газа со встряхиванием для получения биспецифических антител. После экспрессии клетки осаждали центрифугированием, а затем кондиционированную среду осветляли фильтрацией с помощью фильтра с размером пор 0,45 мкм. Эту осветленную кондиционированную среду использовали непосредственно в анализах активации JNL.
8.3.3. Анализы активации JNL
Используемые клетки-мишени представляли собой сконструированную клеточную линию 300-19 (Университет Тафтса, Бостон, Массачусетс, США), сверхэкспрессирующую конструкцию ВСМА макака-крабоеда. Их предварительно смешивали с репортерными клетками JNL в RPMI (Invitrogen) + 10% фетальной бычьей сыворотки (VWR Seradigm, Рэднор, Пенсильвания, США) + 2 мМ L-глутамина и добавляли в каждую лунку 384-луночных белых планшетов для культур ткани. Для каждого 96-луночного планшета с образцами устанавливали один 384-луночный тестовый планшет. Кондиционированную среду, содержащую тестируемые антитела, разводили в RPMI, и каждый образец добавляли в четыре лунки в соответствующем содержащем клетки тестовом планшете в конечных разведениях 1:10, 1:100, 1:1000 и 1:10000. Тестовые планшеты инкубировали в течение пяти часов при 37°C/5% углекислого газа, чтобы произошла управляемая NFAT экспрессия люциферазы. Тестовые планшеты уравновешивали до комнатной температуры, а затем в каждую лунку добавляли One-Glo (Promega, Мадисон, Висконсин, США) в разведении 1:1. Планшеты инкубировали в течение 10 минут при комнатной температуре, затем считывали на планшет-ридере Envision (Perkin Elmer) с использованием фильтра Luminescence 700. Использовали средние концентрации антител и данные подгоняли с использованием GraphPad Prism и уравнения Y=Bottom + (Top-Bottom)/(1+10^((LogEC50-X))) для получения приблизительных значений EC50 для каждого образца. 94 лучших клона, оцененных по приблизительным значениям EC50, секвенировали, и после отбрасывания нежелательных последовательностей CDR (цистеины, предполагаемые сайты модификации и т. д.) 72 клона отбирали для повторного тестирования. Второй анализ был аналогичен первому, за исключением того, что каждый клон тестировали отдельно с использованием клеточных линий, сверхэкспрессирующих ВСМА как человека, так и макака-крабоеда. Кроме того, для каждого образца антитела использовали восьмиэтапную серию трехкратных разведений с максимальной приблизительной концентрацией 4000 пМ и минимальной концентрацией 1,83 пМ. Эти данные снова подгоняли с использованием того же уравнения, и для масштабирования и дополнительного тестирования отбирали лучшие клоны, которые продемонстрировали высокую эффективность активации как с BCMA человека, так и с BCMA макака-крабоеда (таблица 18). Нуклеотидные и аминокислотные последовательности VH и VL для клонов показаны в таблице 19.
Эффективность выбранных совпадений в анализах активации JNL в отношении клеточных линий, экспрессирующих BCMA человека и макака-крабоеда
Эти идентифицированные клоны, которые имеют значение ЕС50 500 пМ или ниже в анализе активации JNL в отношении ВСМА как человека, так и макака-крабоеда, представляют заметное улучшение по сравнению с первоначально идентифицированным клоном PI-61. Этот исходный клон характеризовался приблизительными аффинностями 34 нМ к ВСМА человека и 240 нМ к ВСМА макака-крабоеда.
На фиг. 7 показаны участки CDR H2 идентифицированного и исходного клонов. Особо следует отметить, что сайт вероятной изомеризации аспартат-глицин с в положениях 59 и 62 (нумерация по IMGT) CDRH2 заменен несколькими парами аминокислот, чаще всего аспартат-аспартат. Кроме того, положение 63 подвергли мутации с заменой серина на аланин в большинстве зрелых совпадений.
На фиг. 8 показаны участки CDR L2 идентифицированного и исходного клонов. Все идентифицированные клоны проявляют мутацию с заменой аспартата на глутамат в положении 56 и мутацию с заменой пролина на лейцин в положении 61. Кроме того, в большинстве клонов присутствовала мутация с заменой серина на аргинин в положении 62.
На фиг. 9 показаны участки CDR H3 идентифицированного и исходного клонов. Несколько мутаций обогащены в улучшенных клонах, в том числе замена аланина на глутамат в положении 110, замена аспартата на глутамин в положении 111c и мутация тирозин-глицин-лейцин на лизин-пролин-валин в положениях 113-115.
8.4. Пример 4: Выделение антител к BCMA с использованием фагового дисплея
8.4.1. Получение исходного клона R1F2
Пэннинг проводили путем покрытия гранул со стрептавидином биотинилированными белками ВСМА (ВСМА человека и BCMA макака-крабоеда (Ag)). Гранулы, покрытые антигенами, промывали фосфатно-солевым буфером (PBS) с 0,05% Tween 20 (PBST) и блокировали 2% бычьим сывороточным альбумином (BSA). Фаговые библиотеки блокировали с помощью 2% BSA и предварительно адсорбировали на пустых гранулах со стрептавидином для удаления фагов, которые связываются со стрептавидином. Блокированные и предварительно адсорбированные фаговые библиотеки добавляли к гранулам, покрытым Ag, и инкубировали в течение 1 часа при комнатной температуре с перемешиванием. Неспецифически связанные фаги промывали посредством нескольких стадий промывки. Специфически связанные фаги элюировали с гранул со стрептавидином посредством добавления глицина с pH 2. Элюат переносили в культуру E. coli TG1 для фагового заражения. После инкубации при 37°C в течение 45 минут культуры центрифугировали; осадки бактерий ресуспендировали в свежей среде и высевали на чашки с агаром с ампициллином и инкубировали при 37°C в течение ночи. Колонии из каждого пула соскребали с планшетов и использовали для получения глицериновых растворов или непосредственно использовали для восстановления фага, поликлональной амплификации фага и для осаждения фага.
Новые фаговые частицы, представляющие Fab-фрагменты на своей поверхности, получали для каждого цикла отбора. Для каждого фагового препарата 12 мл 2x среды YT/ампициллин/глюкоза инокулировали бактериями из соответствующей библиотеки (как описано в предыдущем абзаце) или ее глицериновым раствором, в результате чего значение OD600 составляло 0,1-0,2. Культуры встряхивали в течение 60-90 минут при 120 об/мин при 37°C до достижения OD600 0,45-0,55. Затем к бактериальной культуре добавляли хелперный фаг при множественности заражения 20 с последующей инкубацией в течение 30 минут при 37°C без встряхивания, а затем в течение 30 минут при 37°C со встряхиванием при 160 об/мин. Бактерии центрифугировали и супернатант, содержащий хелперный фаг, отбрасывали. Инфицированные фагом бактерии ресуспендировали в 20 мл 2x среды YT/Amp/Kan/IPTG и инкубировали в течение ночи при 25°C со встряхиванием при 120 об/мин. На следующий день бактерии из ночной культуры осаждали и собирали супернатант, содержащий Fab-презентирующий фаг. Осаждение фага проводили посредством добавления 1/5 общего объема предварительно охлажденного PEG/NaCl к фагосодержащему супернатанту. Образец инкубировали в течение не менее 30 минут на льду, пока облака осаждающегося фага не становились видимыми. Осажденные фаги центрифугировали и ресуспендировали в PBS. Очищенные фаги использовали для последующего цикла пэннинга.
Пулы пэннинга из последнего цилка субклонировали в бактериальный вектор экспрессии, и полученную культуру высевали на чашки с агаром для отбора одиночной колонии. Одиночные клоны отбирали из планшетов с агаром в лунки 2 микротитрационных планшетов (в двух повторностях), мастер-планшета и дочернего планшета. Лунки мастер-планшета предварительно заполняли средой 2xYT, содержащей ампициллин и низкую концентрацию глюкозы. После разрастания в эти планшеты добавляли глицерин и хранили при -80°C. Дочерние планшеты предварительно заполняли индукционной средой (2xYT, содержащая ампициллин, и IPTG). Планшеты инкубировали при 30°C и встряхивали в течение ночи для экспрессии Fab. На следующий день экспрессионные культуры лизировали добавлением лизоцимного буфера.
Иммуноферментный анализ (ELISA) использовали для тестирования связывания Fab (в неочищенных бактериальных лизатах) с рекомбинантными полноразмерными Ag BCMA. Биотинилированные антигены захватывали посредством покрытых нейтравидином планшетов. Планшеты промывали с помощью PBST и блокировали с помощью 2% BSA. Бактериальные лизаты (содержащие Fab) добавляли в планшеты после инкубации и промывания для удаления неспецифического связывания, связанные Fab обнаруживали с помощью антитела к Fab-HRP (пероксидаза хрена). После инкубации и нескольких промывок добавляли субстрат, и проявление цвета останавливали добавлением 0,5 н. HCl. Сигнал (поглощение) измеряли при 450 нм.
Аффинность Fab к его антигену можно повышать с помощью подхода итеративной оптимизации CDR, вводя предварительно созданные библиотеки кассет созревания CDR, в то время как каркасные участки остаются незатронутыми. Клонирование библиотек созревания выполняли в векторе, кодирующем исходные Fab-фрагменты. Для клона R1F2 создавали три библиотеки; 2 библиотеки для CDR3 легкой цепи (CDR-L3), представляющие 2 разные длины CDR-L3, и одну библиотеку для CDR-H2 тяжелой цепи. Соответствующий CDR удаляли из исходного клона фрагментом рестрикции и заменяли нерелевантной последовательностью для уменьшения фона исходного клона. На второй стадии нерелевантную последовательность удаляли и заменяли спектром фрагментов ДНК, содержащих требуемые различные CDR, путем реакции лигирования. Смесь для лигирования электропорировали в бактериальные клетки (TG1F`) для амплификации библиотеки.
Пэннинг созревших библиотек проводили, как описано выше, с повышенной жесткостью на стадиях промывания. Скрининг проводили с помощью ELISA, как описано выше, с использованием низких концентраций антигена, чтобы отличить профиль улучшенных клонов от исходного профиля (фиг. 10). Отобранные клоны повторно помещали в компрессионные планшеты и секвенировали для определения уникальности и для последующих анализов.
8.4.2. Характеристика зрелых человеческих антител к ВСМА
Для определения аффинности уникальных клонов к белкам BCMA использовали биослойную интерферометрию (BLI). Наконечники со стрептавидином (ForteBio) покрывали биотинилированным антигеном, Fab-содержащие бактериальные лизаты разбавляли в связывающем буфере, и покрытые антигеном наконечники погружали в лизаты для измерения связывания/ассоциации (скорость ассоциации). После этого наконечники погружали в буфер для контроля диссоциации (скорость диссоциации). Расчеты кажущейся KD выполняли с использованием запатентованного аналитического программного обеспечения Fortebio. Идентифицировали много клонов с улучшенными аффинностями по сравнению с исходным R1F2 (фиг. 11 и фиг. 12; таблица 20) и впоследствии их субклонировали в биспецифический формат для анализов получения и функционирования.
EDFATYYCQQSYSSPLTFGQGTKVEIK
8.5. Пример 5: Получение и характеристика биспецифических связывающих молекул к BCMA и к CD3
Антитела PALF01 и PALF11 (пример 4) и H2/L2-20 (пример 2) преобразовали в биспецифический формат, связывающий BCMA и CD3, и полученные биспецифические антитела назвали AB1, AB2 и AB3 соответственно.
8.5.1. Материалы и способы
8.5.1.1. Приведение к зародышевой линии кандидата H2/L2-20 для получения AB3
Все последовательности клона кандидата для последующей характеристики выравнивали с ближайшими к ним зародышевыми линиями человека, чтобы убедиться, что каркасные участки были максимально близки к естественным каркасным участкам, представленным в спектре антител человека. Клоны из примера 4 были на 100% идентичны последовательностям зародышевой линии человека вне CDR и, таким образом, их получали без дополнительных изменений их первичной аминокислотной последовательности. Клон H2/L2-20 имел мутации вне CDR как в вариабельном участке легкой цепи, так и в вариабельном участке тяжелой цепи, и их подвергали мутации до остатков ближайшей зародышевой линии человека для получения конечной последовательности AB3 в рамках синтеза гена конечных конструкций.
8.5.1.2. Получение биспецифических антител IgG1 к ВСМА и CD3 в формате "выступы во впадины"
Синтез генов проводила компания ATUM (Ньюарк, Калифорния, США). Синтезировали тяжелые цепи антител к BCMA в виде продуктов слияния вариабельных доменов с константными доменами hIgG1, содержащими мутации типа "впадин" для облегчения гетеродимеризации, а также молчащую мутацию N297A. Плазмиды легкой цепи синтезировали, как описано выше. Плечи антитела к CD3 получали в виде одноцепочечного вариабельного фрагмента, слитого с константными доменами hIgG1, содержащими мутации типа "выступов" для облегчения гетеродимеризации, а также молчащую мутацию N297A. Биспецифические антитела совместно транзиентно экспрессировались в клетках HEK293. Вкратце, трансфекцию выполняли с использованием PEI Max в качестве реагента для трансфекции. Для осуществления трансфекций в небольших масштабах (< 5 л) клетки выращивали во встряхиваемых колбах на орбитальном шейкере (115 об./мин) в увлажненном инкубаторе (85%) при 5% CO2. Плазмиды для легких и тяжелых цепей антитела к BCMA, объединяли с плазмидами антитела к CD3, в соотношении 2:2:3 и с PEI при конечном соотношении 1 ДНК: 3 PEI. Использовали 1 мг/л культуры плазмиды для трансфекции при 0,5 миллиона клеток/мл сывороточной среды. После 5 дней экспрессии антитело собирали путем осветления среды посредством центрифугирования и фильтрации. Очистку проводили либо с помощью пакетной аффинной хроматографии с антителом к CH1 (CaptureSelect IgG-CH1 Affinity Matrix, Thermo-Fisher Scientific, Уолтем, Массачусетс, США), либо с помощью пакетной аффинной хроматографии с белком A (MabSelect®SuRe, GE Healthcare Life Sciences, Уппсала, Швеция). Смолу добавляли в соотношении 1 мл на каждые 100 мл супернатанта и давали возможность связываться в течение периода до 4 часов. В одноразовые колонки загружали супернатант, которому давали возможность стекать под действием силы тяжести, и промывали с помощью 20 CV PBS. Антитело элюировали с помощью 20 CV 20 мМ цитрата, 125 мМ NaCl, 50 мМ сахарозы, pH 3,2. Элюированный белок IgG доводили до pH 5,5 с помощью 1 M цитрата натрия. Если антитело содержало агрегаты, то выполняли препаративную эксклюзионную хроматографию с использованием колонки Hi Load 16/60 с Superdex 200 препаративной чистоты (GE Healthcare Life Sciences, Уппсала, Швеция) в качестве стадии заключительной доочистки.
8.5.1.3. Получение би- и тривалентных связывающих молекул к BCMA и к CD3
Получали бивалентные связывающие молекулы в формате, показанном на фиг. 1C, и тривалентные связывающие молекулы в формате, показанном на фиг. 1H.
Синтез генов выполняли, как описано выше. Синтезировали тяжелые цепи антител к BCMA в виде продуктов слияния вариабельных доменов с константными доменами hIgG1, содержащими мутации L368D/K370S для облегчения гетеродимеризации, а также молчащие мутации E233P/L234V/L235A/G236del/S267K. Плазмиды легкой цепи синтезировали, как описано выше. Плечо антитела к CD3 для бивалентной BBM получали в виде одноцепочечного вариабельного фрагмента, слитого с константными доменами hIgG1, содержащими мутации S364K/E357Q для облегчения гетеродимеризации, а также молчащие мутации E233P/L234V/L235A/G236del/S267K. Плечо антитела к CD3 для тривалентных BBM получали в виде Fab тяжелой цепи антитела к BCMA, слитого с одноцепочечным вариабельным фрагментом CD3, слитого с константными доменами hIgG1, содержащими мутации S364K/E357Q для облегчения гетеродимеризации, а также молчащие мутации E233P/L234V/L235A/G236del/S267K. BBM совместно транзиентно экспрессировались в клетках HEK293. Вкратце, трансфекцию выполняли с использованием PEI Max в качестве реагента для трансфекции. Для осуществления трансфекций в небольших масштабах (< 5 л) клетки выращивали во встряхиваемых колбах на орбитальном шейкере (115 об./мин) в увлажненном инкубаторе (85%) при 5% CO2. Плазмиды для легких и тяжелых цепей антитела к BCMA, объединяли с плазмидами антитела к CD3, и с PEI при конечном соотношении 1 ДНК: 3 PEI. Использовали 1 мг/л культуры плазмиды для трансфекции при 0,5 миллиона клеток/мл сывороточной среды. После 5 дней экспрессии BBM собирали путем механического очищения среды посредством центрифугирования и фильтрации. Очистку проводили либо с помощью пакетной аффинной хроматографии с антителом к CH1 (CaptureSelect IgG-CH1 Affinity Matrix, Thermo-Fisher Scientific, Уолтем, Массачусетс, США), либо с помощью пакетной аффинной хроматографии с белком A (MabSelect®SuRe, GE Healthcare Life Sciences, Уппсала, Швеция). Смолу добавляли в соотношении 1 мл на каждые 100 мл супернатанта и давали возможность связываться в течение периода до 4 часов. В одноразовые колонки загружали супернатант, которому давали возможность стекать под действием силы тяжести, и промывали с помощью 20 CV PBS. BBM элюировали с помощью 20 CV 20 мМ цитрата, 125 мМ NaCl, 50 мМ сахарозы, pH 3,2. Элюированный белок IgG доводили до pH 5,5 с помощью 1 M цитрата натрия. Если BBM содержало агрегаты, то выполняли препаративную эксклюзионную хроматографию с использованием колонки Hi Load 16/60 с Superdex 200 препаративной чистоты (GE Healthcare Life Sciences, Уппсала, Швеция) в качестве стадии заключительной доочистки. Образцы, содержащие гомодимеры, очищали с помощью препаративной катионообменной хроматографии.
8.5.1.4. Последовательности BBM BCMA x CD3
Последовательности аминокислот и ДНК для конструкций, полученных в примере 5, показаны в таблице 21.
Бивалентное AB1
(формат 1×1 hBCMA Fab/hCD3 scFv)
Тривалентное AB1
(формат 2×1 hBCMA Fab/hCD3 scfv)
(PALF01)
Бивалентное AB2 к BCMA-CD3
(формат 1×1 BCMA Fab/hCD3 scFv)
(PALF11)
Тривалентное AB2 к BCMA-CD3
(формат 2×1 BCMA Fab/hCD3 scFv)
(PALF11)
Бивалентное AB3 к BCMA-CD3
(формат 1×1 hBCMA Fab/hCD3 scFv)
Тривалентное AB3
(формат 2×1 hBCMA Fab/hCD3 scFv)
(B61-11)
8.5.1.5. Определение аффинности посредством равновесного титрования в растворе
Равновесное титрование в растворе (SET) выполняли для получения кажущихся KD для биспецифических BCMA-связывающих молекул. В этом формате рекомбинантный ВСМА человека и рекомбинантный ВСМА макака-крабоеда наносили на планшеты MSD при низкой концентрации, так что концентрации комплекса в идеале были ниже KD. Биспецифические молекулы фиксировали и тестировали при нескольких концентрациях (1 нМ, 0,1 нМ, 0,01 нМ), и каждую концентрацию предварительно инкубировали с титрованным ВСМА в растворе. Этому комплексу давали возможность предварительно инкубироваться в течение ночи. Затем эту смесь добавляли в планшет для непродолжительной инкубации для захвата свободных биспецифических молекул. Чем больше свободных биспецифических молекул обнаруживается, тем слабее взаимодействие и, следовательно, слабее аффинность. Вкратце, антиген наносили на стандартные планшеты MSD для связывания (Meso-Scale Discovery, 384-луночный: MSD, № по кат. L21XA, 96-луночный: MSD, № по кат. L15XA) при концентрации 0,2-0,3 мкг/мл в 25 мкл PBS и инкубировали в течение ночи при 4°C.
Биспецифические антитела разводили до фиксированной концентрации (например, 10 пМ) в инкубационном буфере (PBS с 2% BSA (Sigma, № по кат. A4503) и 1% Tween20 и 1% Triton-X (Sigma, № по кат. 234729)) и добавляли в серийное разведение антигена в инкубационном буфере. Образцам позволяли достичь равновесия путем инкубации при комнатной температуре в течение ночи.
Планшеты промывали 3x промывочным буфером (PBS с 0,05% Tween20) и блокировали посредством 100 мкл инкубационного буфера при комнатной температуре в течение 2 ч. Затем планшеты промывали 3x промывочным буфером. Образцы, содержащие биспецифические антитела (фиксированная концентрация) и антиген (титрование), добавляли в планшет (25 мкл) и инкубировали при комнатной температуре в течение 15 мин. Затем планшеты промывали 3 раза промывочным буфером. Затем добавляли 25 мкл детекторного антитела (антитела человека (козьего) Sulfo-TAG, 1:1000 в инкубационном буфере, MSD, № по кат. R32AJ-1) и инкубировали при комнатной температуре в течение 30 мин. Затем планшеты промывали 3x промывочным буфером и добавляли 50 мкл 1х MSD буфера для считывания T (с поверхностно-активным веществом, MSD, № по кат. R92TC-1). Затем планшеты считывали на MSD Spector Imager 6000.
Данные анализировали с использованием программного обеспечения GraphPad Prism v4, при этом фон (среднее значение лунок, не содержащих Fab) вычитали из каждого значения. Значения оси X (концентрация антигена в растворе) преобразовали в log10x.
Значения KD (KD) подгоняли на основе следующей модели:
Y=(Top-((Top/(2×Fab))×((((10^x)+Fab)+KD)-((((((10^x)+Fab)+KD)×(((10^x)+Fab)+KD)) -((4×(10^x))×Fab))^0,5))))
Top=сигнал при концентрации антигена=0
x=концентрация BCMA в растворе
Fab=концентрация используемого моновалентного аналита (Fab)
8.5.2. Результаты
Кажущиеся аффинности для каждого из протестированных ВСМА-связывающих плеч показаны в таблице 22.
Аффинность связывания BCMA биспецифических антител к BCMA
8.6. Пример 6: Противоопухолевая активность бивалентных и тривалентных AB1 и AB2 к BCMA-CD3 в адаптации адоптивного переноса ортотопической модели опухоли множественной миеломы KMS11-Luc у мышей NSG
8.6.1. Материалы и способы
Противоопухолевую активность би- и тривалентных AB1 и AB2 к BCMA-CD3 тестировали в отношении адаптации адоптивного переноса ортотопической модели опухоли множественной миеломы KMS11-Luc у мышей NSG.
В день 0 клетки KMS11-Luc собирали и суспендировали в сбалансированном солевом растворе Хенкса (HBSS) при концентрации 10×106 клеток/мл. Самкам мышей NOD.Cg-Prkdcscid Il2rgtm1Wjl/SzJ (мыши NSG) в возрасте ~6 недель (Jackson Laboratories, Мэн, США) инъецировали 1×106 клеток KMS11-Luc (в объеме 100 мкл) внутривенно (в/в) в латеральную хвостовую вену.
Через семь дней после инокуляции опухоли каждая мышь получала адоптивный перенос (AdT) 10X106 мононуклеарных клеток периферической крови (PBMC) (в объеме 100 мкл) посредством в/в инъекции в латеральную хвостовую вену. РВМС предварительно выделяли из лейкопака человека, замораживали и хранили в среде Cryostor10 в паровой фазе в резервуаре с жидким азотом до использования. Непосредственно перед AdT РВМС размораживали и суспендировали при концентрации 100X106 клеток/мл в сбалансированном солевом растворе Хенкса (HBSS).
Когда опухолевая нагрузка (TB) достигала в среднем ~1,0×107 фотонов/сек (p/s), что измерялось с помощью биолюминесценции, мышь (n=5/группа) обрабатывали однократным в/в введением бивалентного AB1 к BCMA-CD3, тривалентного AB1 к BCMA-CD3, бивалентного AB2 к BCMA-CD3 или тривалентного AB2 к BCMA-CD3 при уровнях доз 0,03 мг/кг, 0,3 мг/кг или 3,0 мг/кг. Противоопухолевую активность каждого антитела сравнивали с необработанной контрольной группой, которая получала опухолевый имплантат и AdT, но не получала обработку (опухоль+AdT). Группу только с опухолью включали для измерения аллогенного ответа, наблюдаемого у необработанного контроля. Все обработки вводили в дозе 10 мл/кг в зависимости от массы тела каждой мыши. Противоопухолевую активность определяли по процентному изменению опухолевой нагрузки по сравнению с изменением необработанного контроля (%ΔT/ΔC) или по % регрессии.
Опухолевую нагрузку и массы тела регистрировали дважды в неделю. Опухолевую нагрузку измеряли по интенсивности сигнала биолюминесценции в p/s с использованием системы визуализации биолюминесценции (IVIS200, Perkin Elmer). Противоопухолевую активность определяли по процентному изменению опухолевой нагрузки по сравнению с контролем (%ΔT/ΔC) с использованием формулы: 100 X ΔTB обработка, время/ΔTB контрольная группа, время, если ΔTB≥ 0; или по проценту регрессии: (-1 X (100 X (TB конечная - TB исходная/TB исходная), если ΔTB< 0, TB исходная представляет собой опухолевую нагрузку в день начала обработки (значения %ΔT/ΔC <42% считались указывающими на противоопухолевую активность). Процент изменения массы тела определяли по формуле: 100 X ((BW время - BW исходная)/BW исходная). Статистический анализ с использованием однофакторного ANOVA с критерием множественного сравнения Даннета проводили с использованием программного обеспечения Graphpad Prism, версии 7.03.
На 36 день после имплантации KMS11-Luc всех животных из необработанной контрольной группы подвергли умерщвлению из-за опухолевой нагрузки.
8.6.2. Результаты
8.6.2.1. Противоопухолевая активность бивалентного и тривалентного AB1 к BCMA-CD3
Обработка антителом с помощью бивалентного AB1 к BCMA-CD3 в дозах 0,3 мг/кг и 3,0 мг/кг приводила к значительным регрессиям опухоли на 57,8% и 85,3% соответственно. Обработка антителом с помощью бивалентного AB1 к BCMA-CD3 в дозе 0,03 мг/кг не показала значительной противоопухолевой активности (значение ΔT/ΔC 67,4%). Обработка антителом с помощью тривалентного AB1 к BCMA-CD3 приводила к значительному противоопухолевому ответу при дозах 0,3 мг/кг (ΔT/ΔC 2,4%) и 3,0 мг/кг (регрессия 73,6%). Обработка антителом с помощью тривалентного AB1 к BCMA-CD3 в дозе 0,03 мг/кг не была активной в данной модели (таблица 23, фиг. 13).
Эффективность in vivo бивалентного или тривалентного AB1 к BCMA-CD3, оцененная в адаптации адоптивного переноса PBMC человека ортотопической модели опухоли KMS11-Luc у мышей на 36 день после имплантации
(мг/кг)
ΔC
(%)
(%)
(геометрическое среднее)
День 36
(среднее ± SEM)
День 36
Потеря массы тела, связанная с применением антитела при использовании бивалентного или тривалентного AB1 к BCMA-CD3, отсутствовала. Изменение массы тела, наблюдаемое при обработке бивалентным и тривалентным AB1 к BCMA-CD3, скорее всего было связано с началом реакции "трансплантат против хозяина" (GvHD). Потеря массы тела является параметром конечной точки как для бремени болезни, так и для начала GvHD. Через 35-42 дней после инъекции PBMC (28-35 дней после имплантации опухоли) у животных начинали наблюдать потерю массы тела, связанную с GvHD. Животные с высокой опухолевой нагрузкой также демонстрировали потерю массы тела, связанную с бременем болезни. В ходе исследования массы тела увеличивались по сравнению с исходным измерением, проведенным в день имплантации опухоли (таблица 23, фиг. 14). Однако в конце исследования наблюдаемая потеря массы тела относительно максимального прироста свидетельствует о потере массы тела, вызванной GvHD и бременем болезни. Это исследование имело минимальный аллогенный ответ (фиг. 13).
8.6.2.2. Противоопухолевая активность бивалентного и тривалентного AB2 к BCMA-CD3
Обработка антителом с помощью бивалентного AB2 к BCMA-CD3 приводила к значительной противоопухолевой активности. Бивалентное AB2 к BCMA-CD3 в дозе 0,03 мг/кг приводило к значению %ΔT/ΔC 0,9%, а дозы 0,3 мг/кг и 3,0 мг/кг приводили к 90,7% и 91,7% регрессии соответственно. Обработка тривалентным AB2 к BCMA-CD3 приводила к значительным противоопухолевым ответам со значениями %ΔT/ΔC 2,4% и 5,7% для уровней доз 0,03 мг/кг и 0,3 мг/кг соответственно. Тривалентное AB2 к BCMA-CD3 в дозе 3,0 мг/кг приводило к 96,8% регрессии (таблица 24, фиг. 13).
Эффективность in vivo бивалентного или тривалентного AB2 к BCMA-CD3, оцененная в адаптации адоптивного переноса PBMC человека ортотопической модели опухоли KMS11-Luc у мышей на 36 день после имплантации
(мг/кг)
ΔC
(%)
(%)
(геометрическое среднее)
День 36
(среднее ± SEM)
День 36
Потеря массы тела, связанная с применением антитела при использовании бивалентного или тривалентного AB2 к BCMA-CD3, отсутствовала. К концу исследования для этой конструкции не наблюдали потери массы тела из-за начала GvHD (таблица 24, фиг. 14). Это исследование имело минимальный аллогенный ответ (фиг. 13).
8.7. Пример 7: Противоопухолевая активность бивалентных и тривалентных AB1, AB2 и AB3 к BCMA-CD3 в адаптации адоптивного переноса ортотопической модели опухоли множественной миеломы KMS11-Luc у мышей NSG
8.7.1. Материалы и способы
Материалы и способы, использованные в примере 7, соответствуют тем, которые использовали в примере 6, за исключением того, что на 38 день после имплантации KMS11-Luc всех животных из необработанной контрольной группы подвергали умерщвлению из-за опухолевой нагрузки, а оставшихся животных подвергали умерщвлению на 40 день.
8.7.2. Результаты
8.7.2.1. Противоопухолевая активность бивалентного и тривалентного AB1 к BCMA-CD3
Обработки антителом с помощью бивалентного AB1 к BCMA-CD3 приводили к значительной противоопухолевой активности. Бивалентное AB1 к BCMA-CD3 в дозе 0,03 мг/кг приводило к %ΔT/ΔC 24,7%. Бивалентное AB1 к BCMA-CD3 в дозах 0,3 мг/кг и 3,0 мг/кг приводило к регрессии на 50,7% и 22,7% соответственно. Обработка тривалентным AB1 к BCMA-CD3 приводила к значительным противоопухолевым ответам при дозах 0,03 мг/кг (ΔT/ΔC 2,6%), 0,3 мг/кг (регрессия 64,2%) и 3,0 мг/кг (регрессия 89,5%) (таблица 25, фиг. 15).
Эффективность in vivo бивалентного или тривалентного AB1 к BCMA-CD3, оцененная в адаптации адоптивного переноса PBMC человека ортотопической модели опухоли KMS11-Luc у мышей на 38 день после имплантации
(мг/кг)
ΔC
(%)
(%)
(геометрическое среднее)
День 38
(среднее ± SEM)
День 38
День 38
Потеря массы тела, связанная с применением антитела при использовании бивалентного или тривалентного AB1 к BCMA-CD3, отсутствовала. Изменение массы тела, наблюдаемое при обработке бивалентным и тривалентным AB1 к BCMA-CD3, скорее всего связано с началом GvHD. Потеря массы тела является параметром конечной точки как для бремени болезни, так и для начала GvHD. Через 35-42 дней после инъекции PBMC (28-35 дней после имплантации опухоли) у животных начинали наблюдать потерю массы тела, связанную с GvHD. Животные с высокой опухолевой нагрузкой также демонстрировали потерю массы тела, связанную с бременем болезни. В ходе исследования массы тела увеличивались по сравнению с исходным измерением, проведенным в день имплантации опухоли (таблица 25, фиг. 16). Однако в конце исследования наблюдаемая потеря массы тела относительно максимального прироста свидетельствовала о потере массы тела, вызванной GvHD и бременем болезни (таблица 25, фиг. 16).
8.7.2.2. Противоопухолевая активность бивалентного и тривалентного AB2 к BCMA-CD3
Обработки бивалентным антителом AB2 к BCMA-CD3 в дозах 0,3 мг/кг и 3,0 мг/кг приводили к значительной противоопухолевой активности, достигая значений %ΔT/ΔC 33,3% и 0,4% при дозах 0,03 мг/кг и 0,3 мг/кг соответственно. Бивалентное AB2 BCMA-CD3 в дозе 3,0 мг/кг приводило к 96% регрессии. Тривалентное AB2 к BCMA-CD3 приводило к значительному противоопухолевому ответу при всех видах обработки, достигая значений регрессии 66,1% для дозы 0,03 мг/кг, 80,8% для дозы 0,3 мг/кг и 69,3% для дозы 3,0 мг/кг (таблица 26, фиг. 15).
Эффективность in vivo бивалентного или тривалентного AB2 к BCMA-CD3, оцененная в адаптации адоптивного переноса PBMC человека ортотопической модели опухоли KMS11-Luc у мышей на 38 день после имплантации
(мг/кг)
ΔC
(%)
(%)
(геометрическое среднее)
День 38
(среднее ± SEM)
День 38
День 38
Потеря массы тела, связанная с применением антитела при использовании бивалентного или тривалентного AB2 к BCMA-CD3, отсутствовала. Изменение массы тела, наблюдаемое при обработке бивалентным и тривалентным AB2 к BCMA-CD3, скорее всего связано с началом GvHD. Потеря массы тела является параметром конечной точки как для бремени болезни, так и для начала GvHD. Через 35-42 дней после инъекции PBMC (28-35 дней после имплантации опухоли) у животных начинали наблюдать потерю массы тела, связанную с GvHD. Животные с высокой опухолевой нагрузкой также демонстрировали потерю массы тела, связанную с бременем болезни. В ходе исследования масса тела увеличивалась по сравнению с исходным измерением, проведенным в день имплантации опухоли (таблица 26, фиг. 16). Однако в конце исследования наблюдаемая потеря массы тела относительно максимального прироста свидетельствует о потере массы тела, вызванной GvHD и бременем болезни (таблица 26, фиг. 16).
8.7.2.3. Противоопухолевая активность бивалентного и тривалентного AB3 к BCMA-CD3
Бивалентное AB3 к BCMA-CD3 приводило к значительной противоопухолевой активности с % регрессии 87,6%, 91,3% и 85,2% при дозах 0,03 мг/кг, 0,3 мг/кг и 3,0 мг/кг соответственно. Обработки тривалентным AB3 к BCMA-CD3 приводили к значительным противоопухолевым ответам. Тривалентное AB3 к BCMA-CD3 в дозе 0,03 мг/кг приводило к значению %ΔT/ΔC 29,0%, а дозы 0,3 мг/кг и 3,0 мг/кг приводили к 85,4% и 90,4% регрессии соответственно. (таблица 27, фиг. 15).
Эффективность in vivo бивалентного или тривалентного AB3 к BCMA-CD3, оцененная в адаптации адоптивного переноса PBMC человека ортотопической модели опухоли KMS11-Luc у мышей на 38 день после имплантации
(мг/кг)
ΔC
(%)
(%)
(геометрическое среднее)
День 38
(среднее ± SEM)
День 38
День 38
Потеря массы тела, связанная с применением антитела при использовании бивалентного или тривалентного AB3 к BCMA-CD3, отсутствовала. Изменение массы тела, наблюдаемое при обработке бивалентным и тривалентным AB3 к BCMA-CD3, скорее всего связано с началом GvHD. Потеря массы тела является параметром конечной точки как для бремени болезни, так и для начала GvHD. Через 35-42 дней после инъекции PBMC (28-35 дней после имплантации опухоли) у животных начинали наблюдать потерю массы тела, связанную с GvHD. Животные с высокой опухолевой нагрузкой также демонстрировали потерю массы тела, связанную с бременем болезни. В ходе исследования массы тела увеличивались по сравнению с исходным измерением, проведенным в день имплантации опухоли (таблица 27, фиг. 16). Однако в конце исследования наблюдаемая потеря массы тела относительно максимального прироста свидетельствует о потере массы тела, вызванной GvHD и бременем болезни (таблица 27, фиг. 16).
8.8. Пример 8: Лизис BCMA+ клетки MM Т-клетками in vitro, опосредованный биспецифическим антителом к BCMAxCD3
8.8.1. Краткий обзор
Эффективность биспецифических антител AB1, AB2 и AB3 к ВСМА x CD3 в бивалентном и тривалентном формате в отношении опосредования лизиса линии клеток множественной миеломы (ММ) Т-клетками человека измеряли в анализах перенаправленной Т-клеточной цитотоксичности (RTCC). В качестве клеток-мишеней использовали пять линий клеток MM (NCI-H929, MM1S, MOLP8, U266B1, MC116) и BCMA-отрицательную контрольную клеточную линию (NALM6).
8.8.2. Материалы и способы
BCMA+ линии MM (NCI-H929, MM1S, MOLP8, U266B1, MC116), а также контрольную клеточную линию BCMA- (NALM6) трансдуцировали с использованием лентивирусных частиц (GenTarget Inc, № по кат. LVP435) для конститутивной экспрессии люциферазы. Экспрессию BCMA на клеточной поверхности определяли с помощью проточной цитометрии с использованием меченых посредством BV421 антител к BCMA (клон 19F2, Biolegend 357520, данные получали на BD LSRFortessa и проанализировали с использованием FlowJo, v10).
Т-клетки человека выделяли из периферической крови здоровых доноров-людей. Вначале мононуклеарные клетки периферической крови (PBMC) выделяли путем фракционирования из донорской крови с использованием градиента плотности Ficoll-Paque PLUS (GE Healthcare № 17-1440-02). Затем Т-клетки выделяли из PBMC путем отрицательного отбора согласно протоколу, рекомендованному производителем (Miltenyi № 130-096-535). В некоторых исследованиях свежевыделенные Т-клетки использовали в качестве эффекторных клеток непосредственно в анализах RTCC при соотношении эффекторные клетки:клетки-мишени (E:T) 3:1 или 6:1. В других исследованиях выделенные Т-клетки далее размножали с использованием Dynabeads с антителами к CD3/CD28 для активации T-клеток человека (Gibco № 11132D) в течение девяти дней, затем очищали от гранул магнитным способом и хранили в виде жизнеспособных замороженных аликвот в жидком азоте. Размножившиеся Т-клетки использовали в качестве эффекторных Т-клеток в анализах RTCC, в которых их размораживали из замороженных аликвот, подсчитывали и незамедлительно использовали при соотношении клеток эффектор:мишень (Е:Т), составляющем 3:1.
Для анализов RTCC с использованием свежих Т-клеток клетки-мишени высевали из расчета 25000 клеток/лунка вместе с 75000 или 150000 клеток/лунка эффекторных клеток (свежевыделенных Т-клеток) в 96-луночные планшеты Costar (Corning 3904) в Т-клеточной среде (TCM). Для анализов RTCC с использованием размноженных Т-клеток клетки-мишени высевали из расчета 7500 клеток/лунка вместе с 22500 клеток/лунка эффекторных клеток (размножившихся Т-клеток) в 384-луночные планшеты (Costar 3765) в TCM. В основе TCM лежит RPMI/1640 с добавлением 10% FBS, 2 мМ L-глутамина, 0,1 мМ заменимых аминокислот, 1 мМ пирувата натрия, 10 мМ HEPES, 0,055 мМ 2-меркаптоэтанола (Gibco 22400089, 16140, 25030-081, 11140-050, 11360-070, 15630-080, 21985-023 соответственно). Биспецифические антитела отдельно разводили в серийных разведениях и добавляли в лунки. Аналитическую смесь инкубировали при 37°C/5% CO2 в течение 48 часов (свежие T-клетки) или в течение 20 часов (размножившиеся T-клетки) с последующими измерениями активности люциферазы для определения жизнеспособности клеток-мишеней (Bright-Glo, Promega, № по кат. E2650) в соответствии с протоколами производителя. Клетки-мишени отдельно без Т-клеток или антител служили в качестве контроля для 100% активности люциферазы (100% жизнеспособности). Данные анализировали с помощью Spotfire, где значения EC50 рассчитывали с использованием подбора кривой логистической регрессии.
8.8.3. Результаты
NCI-H929 экспрессируют высокие уровни BCMA, MM1S, MOLP8 и U266B1 характеризуются средним уровнем экспрессии BCMA, тогда как MC116 показали низкий уровень BCMA на клеточной поверхности (фиг. 17). Контрольная клеточная линия NALM6 не показала детектируемой экспрессии BCMA. Все протестированные бивалентные и тривалентные антитела были селективными в отношении ВСМА+ клеток множественной миеломы (ММ) и опосредовали эффективную активность RTCC за счет размножившихся Т-клеток (фиг. 18). Среди всех бивалентных антител активность RTCC коррелирует с аффинностью к BCMA. Для BCMA-связывающего средства со средней аффинностью AB2 к BCMA-CD3, тривалентное AB2 продемонстрировало более высокую активность, чем бивалентное AB2, на BCMAmed и BCMAlow клетках MM, но не на BCMAhigh клетках MM. Для BCMA-связывающих средств с высокой или низкой аффинностью AB3 и AB1 к BCMA-CD3, тривалентный формат не демонстрировал явного преимущества по сравнению с бивалентным форматом на большинстве тестируемых клеточных линий. Аналогичным образом, когда в качестве эффекторных клеток использовали свежевыделенные Т-клетки, антитела к BCMA-CD3 опосредовали RTCC на линиях BCMA+ клеток MM (фиг. 19A и фиг. 19B), что указывает на то, что предварительная активация Т-клеток in vitro не требуется.
8.9. Пример 9: Биспецифические антитела к BCMAxCD3 индуцировали активацию Т-клетки в присутствии BCMA+ клеток MM
8.9.1. Краткий обзор
Некоторые пациенты с ММ имеют низкое количество Т-лимфоцитов и высокую опухолевую нагрузку, и было показано, что клетки ММ экспрессируют молекулы контрольных точек, которые подавляют цитотоксичность Т-клетки. Следовательно, активация и пролиферация Т-клетки являются необходимыми результатами введения биспецифического Ab. Степень активации Т-клетки определяли путем измерения секреции цитокина и пролиферации Т-клетки, опосредованной биспецифическими антителами AB1, AB2 и AB3, в присутствии клеток-мишеней.
8.9.2. Материалы и способы
8.9.2.1. Секреция цитокина
Цитокины измеряли в супернатанте из анализов RTCC с использованием свежих Т-клеток через 48 ч. 96-луночные планшеты центрифугировали при 500xg в течение 5 минут, супернатанты собирали и выполняли количественное определение цитокина с использованием набора V-Plex Pro-inflammatory Panel I (human) (MesoScale Discovery, № по кат. K15049D-4) согласно протоколу производителя.
8.9.2.2. Пролиферация T-клетки
Клетки-мишени MM1S и MC116 облучали в день проведения анализа и высевали при плотности 60000 клеток на лунку в 96-луночные планшеты Costar (Corning, № по кат. 3904) в Т-клеточной среде (TCM). Т-клетки были свежевыделены из крови здорового донора, как описано в примере 8. Выделенные Т-клетки метили с помощью 2,5 мкМ Cell Trace Violet в соответствии с протоколом производителя, а затем культивировали совместно с клетками-мишенями при соотношении Е:Т 1:1. К клеткам добавляли серии разведений антител к BCMA-CD3 в диапазоне от 0,005 пМ до 10 000 пМ и планшеты инкубировали в инкубаторе при 5% CO2 и 37°C в течение 96 ч. После этого клетки собирали, обрабатывали с помощью Human TruStain FcX (Fc Block) [Biolegend, № по кат. 422302] следуя инструкциям производителя, а затем окрашивали с помощью Fixable Viability Dye eFlour 780 (ThermoFisher Scientific, № по кат. 65-0865-14) путем инкубации при 4°C в течение 30 мин. Затем клетки промывали и окрашивали с помощью mAb к CD3 человека, конъюгированных с PerCP-Cy5. (Biolegend, № по кат. 317336), путем инкубации при 4°C в течение 30 мин. Затем образцы проганяли на BD LSR Fortessa и анализировали с помощью FlowJo для определения % пролиферированных CD3+ Т-клеток на основе окрашивания CD3 и разбавления красителя Cell Trace Violet.
8.9.3. Результаты
Все бивалентные и тривалентные антитела к BCMA-CD3 способны индуцировать секрецию цитокина IFNγ и TNFα Т-клетками после совместного культивирования с BCMA+ клетками MM1S или MC116 (фиг. 20A-B). Уровень секретируемых цитокинов коррелировал с аффинностью биспецифических антител. Следует отметить, что тривалентные антитела индуцировали более низкую секрецию TNFα, чем соответствующие бивалентные антитела. Ненацеленное антитело к RSV-CD3 использовали в качестве отрицательного контроля, и обнаружили минимальную секрецию цитокина, за исключением самой высокой протестированной концентрации. Данные показали, что только специфическое по отношению к мишени взаимодействие и активация Т-клеток, опосредованная антителами к BCMA-CD3, индуцируют стойкую секрецию цитокинов.
Все шесть антител к ВСМА-CD3 способствовали пролиферации Т-клетки дозозависимым образом в присутствии линий ВСМА+ клеток ММ (фиг. 21). Антитело к RSV-CD3, представляющее собой отрицательный контроль, стимулировало пролиферацию Т-клетки только при высоких концентрациях (> 1 мкМ), указывая на то, что требуется одновременное задействование ВСМА- и CD3-связывающих плеч для эффективной индукции пролиферации Т-клетки, что согласуется с активностью RTCC и секрецией цитокина. Для бивалентного формата эффективность пролиферации Т-клеток коррелировала с аффинностью антитела. Кроме того, степень пролиферации может зависеть от плотности BCMA на клеточной поверхности, поскольку BCMAlow клетки MC116 индуцировали менее эффективную пролиферацию Т-клетки, чем BCMAmed клетки MM1S.
8.10. Пример 10: Временная динамика ответа линии клеток множественной миеломы KMS11 в отношении обработки ингибиторами гамма-секретазы
8.10.1. Краткий обзор
Обработка клеток MM с помощью GSI ингибирует выделение BCMA как циркулирующего растворимого фактора, что приводит к накоплению BCMA на поверхности клетки. Для определения кинетики активности GSI клетки KMS11 обрабатывали с помощью GSI. Образцы собирали в течение 42 ч.в для измерения sBCMA (выделенного BCMA) и mBCMA (мембранного BCMA). Исследования проводили для того, чтобы определить, насколько быстро клетки реагируют на обработку с помощью GSI, и чтобы определить, как долго эффект обработки с помощью GSI сохраняется после предварительной обработки и удаления препарата.
8.10.2. Материалы и способы
8.10.2.1. Обработка клеток KMS11 с помощью GSI
[01000] Клетки KMS11 культивировали в 6-луночном планшете из расчета 4×106 клеток/лунка в 4 мл RPMI1640 с добавлением 20% FBS (Gibco, № по кат. 11875-085, Seradigm, № по кат. 1500-500) на лунку. Исходные растворы GSI получали в DMSO при 10 мМ и добавляли к клеткам при конечных концентрациях 2 нМ для LY411575 (Sigma, № по кат. SML0506) или 200 нМ для PF03084014 (Selleckchem, № по кат. S8018) соответственно. Клетки инкубировали при 37°C/5% CO2 и образцы собирали в следующие моменты времени: 0, 1, 2, 4, 6, 8, 12, 18, 24, 30 и 42 ч. Собранные образцы оценивали в отношении экспрессии BCMA с помощью ELISA и проточной цитометрии, как показано ниже.
Исследование предварительной обработки проводили как указано выше, за исключением того, что клетки KMS11 обрабатывали в течение ночи (22 ч.) только с помощью LY411575. Клетки дважды промывали 3 объемами питательной среды и повторно засевали со свежей питательной средой без GSI до исходного объема 4 мл. Клетки инкубировали при 37°C/5% CO2 и образцы собирали в следующие моменты времени: 0, 1, 2, 4, 6, 8, 12, 18, 24, 30 и 42 ч. 0 часов представляет собой начальную точку после ночной обработки и промывки.
8.10.2.2. Анализ экспрессии BCMA на мембране in vitro с помощью проточной цитометрии
Для каждого собранного образца клетки осаждали посредством центрифугирования. Супернатанты переносили на свежий планшет и замораживали при -20°C для последующего анализа с помощью ELISA. Клеточные осадки ресуспендировали в 50 мкл буфера MACS, содержащего BSA (Miltenyi, № по кат. 130-091-222, 130-091-376), и окрашивали с помощью антитела к BCMA-PE (Biolegend, № по кат. 357504, разведение 3:50) в течение 30 минут при 4°С. Клетки промывали, фиксировали в течение 20 минут в 10% нейтральном забуференном формалине (VWR, № по кат. 16004-126) и хранили при 4°C до тех пор, пока не были собраны образцы со всех временных точек. Образцы со всех временных точек анализировали вместе с помощью проточной цитометрии на приборе BD LSR Fortessa. Для анализа использовали программное обеспечение FlowJo v10. Соотношение средней интенсивности флуоресценции (MFI) PE (BCMA) для лунок, обработанных с помощью GSI, было разделено на MFI для необработанных лунок KMS11. Эти соотношения были нанесены на график в Tibco Spotfire или Graphpad Prism в зависимости от концентрации GSI.
Если была указана плотность рецепторов ВСМА, антителосвязывающую способность (ABC) в отношении ВСМА клеток KMS11 определяли с использованием гранул Quantum Simply Cellular (Bangs Laboratories, № по кат. 815) в соответствии с протоколом, предоставленным поставщиком. ABC представляет собой расчетное количество рецепторов на клетку.
8.10.2.3. Измерение уровней выделенного BCMA с помощью ELISA
Уровни sBCMA в супернатантах, собранных и замороженных в различные временные точки, определяли с помощью ELISA в соответствии с протоколом, предоставленным поставщиком (R&D Systems, № по кат. DY193). Вкратце, в набор был включен рекомбинантный человеческий белок BCMA-Fc, который использовали для построения стандартной кривой. Собранные образцы анализировали, и концентрации sBCMA экстраполировали из стандартной кривой. Количественные значения, определенные с помощью набора, разделяли на 5,5 для корректировки разницы в молекулярной массе между слитым белком BCMA-Fc, используемым в наборе в качестве стандартной кривой (32554,6 Да), и массой внеклеточного домена ВСМА с эндогенным выделением (5899,3 Да). Результаты были нанесены на график в Tibco Spotfire или Graphpad Prism в зависимости от концентрации GSI.
8.10.3. Результаты
Концентрации sBCMA в клетках KMS11 не показывали увеличения с течением времени при обработке с помощью LY411575 или PF03084014 (фиг. 22A, черные линии), тогда как наблюдалось устойчивое увеличение sBCMA с течением времени в необработанных клетках (фиг. 22A, серая линия). Уровни mBCMA увеличивались с течением времени для клеток KMS11, обработанных с помощью LY411575 или PF03084014 (фиг. 22B, черные линии), но оставались постоянными для необработанных клеток KMS11.
Результаты показали, что GSI действуют быстро, с увеличением мембранного BCMA, наблюдаемым всего за 1 час, и с почти максимальным эффектом через 6 часов. GSI продолжали ингибировать выделение BCMA и повышать уровни мембранного BCMA в течение более 30 часов в культуре клеток.
Концентрации sBCMA в клетках KMS11 после предварительной обработки с помощью GSI и удаления (промывки) оставались низкими с очень медленным увеличением с течением времени, тогда как в необработанных клетках накопление sBCMA происходило гораздо быстрее (фиг. 23A). Уровни mBCMA в необработанных клетках оставались постоянными с течением времени (фиг. 23B). Напротив, плотность mBCMA на обработанных с помощью GSI клетках KMS11 достигала максимального уровня через 4 ч. и сохранялась на уровне, приблизительно в 12 раз превышающем уровень в необработанных клетках, до временной точки 30 ч. перед тем, как снизиться (фиг. 23B).
Данные показали, что при обработке в течение ночи эффект GSI на sBCMA и mBCMA может сохраняться до 30 часов после удаления препарата (промывки).
8.11. Пример 11: Активность бивалентного AB3 в комбинации с GSI
8.11.1. Краткий обзор
Проводили анализ перенаправленной Т-клеточной цитотоксичности (RTCC) для изучения увеличения активности бивалентного AB3 при введении в комбинации с GSI. Анализ проводили с различными комбинациями диапазонов дозы бивалентного AB3 и трех различных GSI в матрице 8×8.
8.11.2. Материалы и способы
8.11.2.1. Выделение и размножение Т-клетки здорового человека
Т-клетки человека выделяли из периферической крови здоровых доноров-людей. Вначале мононуклеарные клетки периферической крови (PBMC) выделяли путем фракционирования из донорской крови с использованием градиента плотности Ficoll-Paque PLUS (GE Healthcare № 17-1440-02). Затем Т-клетки выделяли из PBMC путем отрицательного отбора согласно протоколу, рекомендованному производителем (Miltenyi № 130-096-535). Выделенные Т-клетки далее размножали с использованием Dynabeads с антителами к CD3/CD28 для активации T-клеток человека (Gibco № 11132D) в течение девяти дней, затем очищали от гранул магнитным способом и хранили в виде жизнеспособных замороженных аликвот в жидком азоте. Размножившиеся Т-клетки использовали в качестве эффекторных Т-клеток в анализах RTCC, в которых их размораживали из замороженных аликвот, подсчитывали и незамедлительно использовали при соотношении клеток эффектор:мишень (Е:Т), составляющем 3:1.
8.11.2.2. Анализ RTCC
Клетки-мишени ММ линии KMS11 трансдуцировали для постоянной экспрессии люциферазы, которую использовали для измерения жизнеспособности/выживаемости клеток. Клетки KMS11 осаждали и ресуспендировали в свежей среде непосредственно перед посевом для удаления любого базального уровня выделенного BCMA, который мог присутствовать. 2500 клеток-мишеней KMS11-luc в 25 мкл TCM добавляли в лунки 384-луночных планшетов. 50 нл серийно разведенных бивалентных растворов AB3 и GSI (LY411575, PR03084014 и BMS0708163) акустически распределяли в соответствующие лунки аналитических планшетов. 7500 размноженных Т-клеток, как описано выше, добавляли в соответствующие лунки аналитического планшета в 20 мкл TCM. Аналитическую смесь инкубировали при 37°C/5% CO2 в течение 20 часов с последующими измерениями активности люциферазы для определения жизнеспособности клеток-мишеней (Bright-Glo, Promega, № по кат. E2650) в соответствии с протоколами производителя. Клетки-мишени отдельно (KMS11) без Т-клеток или антител служили в качестве контроля и представляли 100% активность люциферазы (100% жизнеспособность). Данные наносили на график и анализировали с помощью Spotfire, где значения EC50 рассчитывали с использованием подбора сигмоидальной 4-параметрической кривой нелинейной регрессии.
8.11.3. Результаты
Бивалентное AB3 показало дозозависимый эффект на гибель клетки KMS11 в анализе RTCC. Когда концентрации GSI увеличивались в присутствии бивалентного AB3, кривые ответа сдвигались влево, и это происходило при комбинации каждого из трех GSI: LY411575 (фиг. 24A), PF03084014 (фиг. 24B) и BMS0708163 (фиг. 24C).
LY411575 при 7,8 пМ или ниже не оказывал влияния на активность бивалентного AB3, проявлял небольшой эффект при 31,2 пМ и значительное увеличение активности бивалентного AB3 при концентрациях 125 пМ или выше. Аналогично PF03084014 проявлял умеренное увеличение при 3 нМ и значительное увеличение при 12 нМ или выше. Для BMS-708163 умеренное увеличение наблюдали при 8 нМ, а значительное увеличение наблюдали при 31 нМ или выше. Максимальное увеличение эффективности бивалентного AB3 с помощью комбинации с GSI составляет от 10 до 15 раз (значения EC50 на фиг. 3C). Эти результаты продемонстрировали, что эффективность бивалентного AB3 в отношении RTCC была синергетически увеличена при введении в комбинации с GSI.
8.12. Пример 12: Диапазон эффективных доз GSI для ингибирования выделения BCMA, ингибирования передачи сигналов Notch и синергизма с бивалентным AB3
8.12.1. Краткий обзор
Использовали одинаковые концентрации GSI в различных анализах для наложения и сравнения диапазонов эффективных доз GSI. Влияние GSI на sBCMA и mBCMA клеток KMS11 измеряли повторно, чтобы сопоставить с теми же концентрациями, которые использовали в комбинации с бивалентным AB3. Чтобы определить диапазон эффективных доз GSI для ингибирования NOTCH, клетки HPB-ALL обрабатывали с помощью GSI и оценивали мРНК транскриптов-мишеней NOTCH. Влияние GSI на значения EC50 RTCC бивалентного AB3 (фиг. 24) наносили на график в зависимости от концентрации GSI для наложения и сравнения диапазонов эффективных доз.
8.12.2. Материалы и способы
8.12.2.1. Обработка клеток KMS11 с помощью GSI
Клетки KMS11 культивировали в 96-луночном планшете по 50000 клеток на лунку в конечном объеме 100 мкл, который включал 12-этапную серию 5-кратных разведений GSI в RPMI1640 с добавлением 20% FBS (Gibco, № по кат. 11875-085, Seradigm, № по кат. 1500-500). Начальная концентрация LY411575 (Sigma, № по кат. SML0506) до разведения составляла 1 мкМ. Начальные концентрации PF03084014 (Selleckchem, № по кат. S8018) и BMS-708163 (Selleckchem, № по кат. S1262) до разведения составляли 10 мкМ. Клетки инкубировали в течение 20 часов при 37°C/5% CO2. Клетки осаждали, супернатант собирали для определения уровней выделенного BCMA с помощью ELISA и клеточные осадки окрашивали для оценки уровней экспрессии BCMA на мембране методом проточной цитометрии в соответствии со способами, описанными в примере 10. Результаты наносили на график в Tibco Spotfire.
8.12.2.2. Анализ ингибирования передачи сигналов NOTCH
Линию клеток Т-клеточной лейкемии HBP-ALL (DSMZ, № по кат. ACC483) культивировали и обрабатывали с помощью GSI таким же образом, как описано выше для клеток KMS11. Клетки инкубировали в течение 29 часов при 37°C/5% CO2, осаждали и лизировали буфером RLT (Qiagen). РНК очищали с использованием RNeasy mini (Qiagen, № по кат. 74106) в соответствии с протоколом, предоставленным поставщиком. Полученную РНК использовали для синтеза кДНК в соответствии с протоколом, предоставленным поставщиком (ABI, № по кат. 4322171). Уровни транскриптов нижестоящих генов-мишеней Notch HES1 и DTX1 (ABI, № по кат. Hs_0017878.m1, Hs_01114113.m1), каждый из которых мультиплексирован с эндогенным контролем, представляющим собой циклофилин А человека (ABI, № по кат. 4326316RE), для нормализации матрицы, оценивали с помощью qPCR на приборе ABI7900 с использованием универсального мастер-микса для ПЦР TaqMan (ABI, № по кат. 4304437) и в соответствии с протоколом, предоставленным поставщиком. Полученные значения порогового цикла (СТ) использовали для определения относительной экспрессии каждого гена по сравнению с необработанным контролем. Для каждой лунки CT эндогенного контроля вычитали из CT гена-мишени (дельта CT, ΔCT). Затем дельта CT необработанной контрольной лунки вычитали из дельта CT обработанной лунки (дельта дельта CT, ΔΔCT). Для корректировки логарифмической амплификации ПЦР удвоение продукта с каждым циклом, относительный уровень экспрессии выражали как 2-ΔΔCT. Необработанные лунки характеризуются относительной экспрессией 1; снижение экспрессии после обработки будет характеризоваться относительным уровнем экспрессии ниже 1. Относительные уровни экспрессии наносили на график в Tibco Spotfire.
8.12.2.3. Значения EC50 RTCC
Данные для комбинаций бивалентного AB3 и GSI из примера 11 (фиг. 24) наносили на график и анализировали с помощью Spotfire, где значения EC50 рассчитывали с использованием подбора сигмоидальной 4-параметрической кривой нелинейной регрессии.
8.12.3. Результаты
Кривые доза-ответ GSI для sBCMA и mBCMA (клетки KMS11), передачи сигналов Notch (клетки HBP-ALL) и активности RTCC бивалентного AB3 (клетки KMS11) в тех же диапазонах доз выравнивали. Обработка с помощью GSI ингибировала sBCMA и усиливала экспрессию mBCMA на клетках KMS11 дозозависимым образом (фиг. 25A). Минимальная концентрация GSI для усиления активности RTCC бивалентного AB3 была немного выше, чем та, которая требуется для уменьшения выделения BCMA. Как и ожидалось, наибольший синергизм с бивалентным AB3 был достигнут при тех же концентрациях, при которых наблюдался максимальный эффект в отношении sBCMA и mBCMA (фиг. 25A; фиг. 25C). В пределах того же диапазона эффективных доз (обозначенного пунктирными линиями) наблюдали ингибирование передачи сигналов Notch в зависимости от концентрации (фиг. 25B).
8.13. Пример 13: Ответ in vivo на обработку с помощью GSI в модели ксенотрансплантата KMS11
8.13.1. Краткий обзор
Не ограничиваясь какой-либо теорией, полагают, что GSI, вводимый в комбинации с BCMA-связывающей молекулой (например, BBM), повысит эффективность BCMA-связывающей молекулы при лечении заболеваний и нарушений, связанных с экспрессией BCMA, за счет уменьшения количества растворимого BCMA и увеличения количества связанного с мембраной BCMA, доступного для связывания с BCMA-связывающей молекулой. Проводили исследования для оценки влияния GSI на sBCMA и mBCMA in vivo на модели ксенотрансплантата KMS11.
8.13.2. Материалы и способы
8.13.2.1. Обработка с помощью GSI in vivo
В день 0 клетки KMS11-Luc собирали и суспендировали в сбалансированном солевом растворе Хенкса (HBSS) и 50% растворе матригеля при концентрации 25×106 клеток/мл. Самкам мышей NOD.Cg-Prkdcscid Il2rgtm1Wjl/SzJ (мыши NSG) в возрасте ~6 недель (Jackson Laboratories, Мэн, США) подкожно (SQ) имплантировали 200 мкл клеточной суспензии для доставки 5×106 клеток KMS11-Luc подкожно в правый бок. Через семь дней после инокуляции опухоли каждая мышь получала адоптивный перенос (AdT) 10X106 мононуклеарных клеток периферической крови (PBMC) в 100 мкл посредством в/в инъекции в латеральную хвостовую вену. РВМС предварительно выделяли из лейкопака человека, замораживали и хранили в среде Cryostor10 в паровой фазе в резервуаре с жидким азотом до использования. Непосредственно перед AdT РВМС размораживали и суспендировали при концентрации 100X106 клеток/мл в сбалансированном солевом растворе Хенкса (HBSS). Когда опухолевая нагрузка (TB) достигала в среднем ~400 мм3 (день 15), животных рандомизировали и они получали либо среду-носитель в дозе 150 мг/кг, либо PF03084014 в дозе 10 мл/кг BID в течение 5 дней. Через 1, 7, 24 и 48 часов после последней дозы когорты животных (n=3) подвергали умерщвлению, и опухоли и сыворотку извлекали для оценки уровней мембранного BCMA (PD опухоли) и выделенного/растворимого BCMA (сыворотка).
Опухолевую нагрузку и массы тела регистрировали дважды в неделю. Опухолевую нагрузку измеряли штангенциркулем и регистрировали в WinWedge. Массы тела фиксировали и регистрировали в WinWedge.
8.13.2.2. Оценка мембранного BCMA методом проточной цитометрии
Для получения суспензий отдельных клеток из вырезанных опухолей ткани измельчали ножницами с последующей механической гомогенизацией в буфере для диссоциации, содержащем RPMI (Gibco, Life Technologies) с коллагеназой высокой степени чистоты LiberaseTM (Roche) и рекомбиназой ДНКазой I (Roche), с использованием GentleMAX (Miltenyi). После 5-минутной инкубации при 37°C на водяной бане или бане с гранулами гомогенаты гасили с помощью 10% FBS и фильтровали на сите с диаметром пор 70 мкМ (352350, Falcon). Концентрацию суспензий отдельных клеток измеряли на Vi-Cell (Beckman Coulter), и клетки осаждали центрифугированием в течение 5 минут при 1200 об/мин. Супернатанты отбрасывали, а клеточные осадки ресуспендировали в 400 мкл RPMI (Gibco, Life Technologies). Опухолевые клетки высевали в объеме 100 мкл/лунка при плотности клеток от 500000 до 2 миллионов на лунку.
Для окрашивания клеточной поверхности краситель live/dead для определения жизнеспособности добавляли к образцам на чашках в DPBS и инкубировали в течение 30 минут. После окрашивания с помощью live/dead клетки инкубировали с насыщенными концентрациями мышиного Fc block (BD Biosciences) в течение 30 минут с последующей 30-минутной инкубацией с антителами, конъюгированными с флуорохромом, и панель проточной цитометрии приведена в таблице 28.
Во время процедур блокирования и окрашивания клетки выдерживали на льду и защищали их от света. После окрашивания поверхности клетки фиксировали в 4% PFA и ресуспендировали в 200 мкл 2% FBS+PBS. По завершении исследования все образцы анализировали методом проточной цитометрии. Сбор данных выполняли на проточном цитометре LSR-II (BD biosciences). Рабочие характеристики машины калибровали ежедневно с помощью программы Cytometer Setup в DIVA (BD Biosciences).
Анализ выполняли с использованием программного обеспечения FLOWJO v10.0.7 от Treestar. Для каждого анализа представляющую интерес популяцию гейтировали для идентификации живых лейкоцитов с использованием комбинации морфологических параметров (все клетки: SSC-A по сравнению с FSC-A, отдельные клетки: SSC-H по сравнению с SSC-W) и исключение мертвых клеток с использованием eFluor780 (BD Biosciences). Мечение, специфическое в отношении CD45 мыши, использовали для исключения клеток крови мыши, мечение, специфическое в отношении HLA человека, использовали для выделения и идентификации клеток человека, а затем использовали меченное антитело, специфическое в отношении ВСМА человека, для определения мембранных уровней ВСМА на опухолевых клетках. Экспрессия BCMA на обработанных образцах по сравнению с необработанными в каждый момент времени была зарегистрирована как средняя интенсивность флуоресценции (MFI).
8.13.2.3. Измерение уровней выделенного BCMA с помощью ELISA
Уровни выделенного BCMA в сыворотке измеряли с помощью ELISA, как описано в примере 10.
8.13.3. Результаты
Уровни мембранного ВСМА, измеренные как средняя интенсивность флуоресценции (MFI), показаны на фиг. 26. Уровни выделенного BCMA, представленные как средние данные с помощью SEM, показаны на фиг. 27. Наблюдали 10-кратное повышение mBCMA после обработки с помощью PFZ03084014 по сравнению с обработкой средой-носителем в качестве контроля. Это повышение удерживалось в момент времени 7 часов. К временной точке ≥24 часов после последней дозы уровни mBCMA упали до уровней, аналогичных тем, которые наблюдались для обработки средой-носителем в качестве контроля. Уровни sBCMA снижались в течение 24 часов после последней дозы PFZ03084014. Между 24 и 48 часами после последней дозы уровни sBCMA впоследствии увеличивались, возвращаясь к уровням, сравнимым с уровнями, наблюдаемыми у животных, которых обрабатывали среду-носитель. Результаты данного исследования in vivo свидетельствуют в пользу использования GSI в комбинации с BCMA-связывающими молекулами для лечения заболеваний и нарушений, связанных с экспрессией BCMA, поскольку было обнаружено, что обработка с помощью GSI увеличивает уровни mBCMA и снижает уровни sBCMA.
8.14. Пример 14: Бивалентное AB3 по сравнению с другими BCMA-CD3-биспецифическими молекулами
h2B4_C29 представляет собой биспецифическое антитело к ВСМА-CD3, разрабатываемое для лечения множественной миеломы (см. WO2016/0166629). Предварительные данные в отношении бивалентного AB3 и h2B4_C29 из исследований совместного культивирования KMS11 и PBMC/T-клеток указывают на то, что бивалентное AB3 опосредует более низкие уровни индукции цитокина, чем h2B4_C29 (фиг. 28), что позволяет предположить, что пациенты, которые подвергались лечению с помощью AB3, могут иметь пониженный риск синдрома высвобождения цитокина по сравнению с пациентами, которые подвергались лечению с помощью h2B4_C29. Предварительные данные также указывают на то, что Т-клетки, активированные посредством h2B4_C29 в присутствии клеток KMS11, опосредуют большее подавление TCR, чем Т-клетки, активированные посредством бивалентного AB3 (данные не показаны), что позволяет предположить, что бивалентное AB3 может проявлять более устойчивую противораковую активность, чем h2B4_C29.
В модели ксенотрансплантата KMS11 некоторые предварительные данные позволяют предположить, что бивалентное AB3 и h2B4_C29 обладают большей противоопухолевой активностью по сравнению с BCMA-CD3-биспецифическими молекулами от EngMab и Janssen (данные не показаны).
9. КОНКРЕТНЫЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ, ЦИТИРОВАНИЕ ЛИТЕРАТУРНЫХ ИСТОЧНИКОВ
Хотя были проиллюстрированы и описаны различные конкретные варианты осуществления, следует понимать, что различные изменения могут быть осуществлены без отступления от сущности и объема настоящего изобретения. Настоящее изобретение проиллюстрировано с помощью пронумерованных вариантов осуществления, изложенных ниже.
1. ВСМА-связывающая молекула, которая специфически связывается с ВСМА человека и содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 1A-1, таблице 1B-1, таблице 1C-1, таблице 1D-1, таблице 1E-1, таблице 1F-1, таблице 1G-1, таблице 1H-1, таблице 1I-1, таблице 1J-1, таблице 1K-1(a), таблице 1K-1(b), таблице 1L-1, таблице 1M-1, таблице 1N-1(a) или таблице 1N-1(b), и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 1A-2, таблице 1B-2, таблице 1C-2, таблице 1D-2, таблице 1E-2, таблице 1F-2, таблице 1G-2, таблице 1H-2, таблице 1I-2, таблице 1J-2, таблице 1K-2, таблице 1K-2, таблице 1L-2, таблице 1M-2, таблице 1N-2 или таблице 1N-2 соответственно.
2. ВСМА-связывающая молекула, которая специфически связывается с ВСМА человека и содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 1A-1, таблице 1B-1, таблице 1C-1, таблице 1D-1, таблице 1E-1, таблице 1F-1, таблице 1G-1, таблице 1H-1, таблице 1I-1, таблице 1J-1, таблице 1K-1(a), таблице 1L-1, таблице 1M-1 или таблице 1N-1(a), и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 1A-2, таблице 1B-2, таблице 1C-2, таблице 1D-2, таблице 1E-2, таблице 1F-2, таблице 1G-2, таблице 1H-2, таблице 1I-2, таблице 1J-2, таблице 1K-2, таблице 1L-2, таблице 1M-2 или таблице 1N-2 соответственно.
3. ВСМА-связывающая молекула по варианту осуществления 1 или варианту осуществления 2, которая содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 1A-1, и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 1A-2.
4. ВСМА-связывающая молекула по варианту осуществления 1 или варианту осуществления 2, которая содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 1B-1, и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 1B-2.
5. ВСМА-связывающая молекула по варианту осуществления 1 или варианту осуществления 2, которая содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 1C-1, и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 1C-2.
6. ВСМА-связывающая молекула по варианту осуществления 1 или варианту осуществления 2, которая содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 1D-1, и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 1D-2.
7. ВСМА-связывающая молекула по варианту осуществления 1 или варианту осуществления 2, которая содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 1E-1, и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 1E-2.
8. ВСМА-связывающая молекула по варианту осуществления 1 или варианту осуществления 2, которая содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 1F-1, и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 1F-2.
9. ВСМА-связывающая молекула по варианту осуществления 1 или варианту осуществления 2, которая содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 1G-1, и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 1G-2.
10. ВСМА-связывающая молекула по варианту осуществления 1 или варианту осуществления 2, которая содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 1H-1, и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 1H-2.
11. ВСМА-связывающая молекула по варианту осуществления 1 или варианту осуществления 2, которая содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 1I-1, и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 1I-2.
12. ВСМА-связывающая молекула по варианту осуществления 1 или варианту осуществления 2, которая содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 1J-1, и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 1J-2.
13. ВСМА-связывающая молекула по варианту осуществления 1 или варианту осуществления 2, которая содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 1K-1(a), и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 1K-2.
14. ВСМА-связывающая молекула по варианту осуществления 1, которая содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 1K-1(b), и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 1K-2.
15. ВСМА-связывающая молекула по варианту осуществления 1 или варианту осуществления 2, которая содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 1L-1, и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 1L-2.
16. ВСМА-связывающая молекула по варианту осуществления 1 или варианту осуществления 2, которая содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 1M-1, и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 1M-2.
17. ВСМА-связывающая молекула по варианту осуществления 1 или варианту осуществления 2, которая содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 1N-1(a), и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 1N-2.
18. ВСМА-связывающая молекула по варианту осуществления 1, которая содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 1N-1(b), и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 1N-2.
19. ВСМА-связывающая молекула по варианту осуществления 3, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C1.
20. ВСМА-связывающая молекула по варианту осуществления 3, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C2.
21. ВСМА-связывающая молекула по варианту осуществления 3, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C3.
22. ВСМА-связывающая молекула по варианту осуществления 3, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C4.
23. ВСМА-связывающая молекула по варианту осуществления 3, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C5.
24. ВСМА-связывающая молекула по варианту осуществления 3, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C6.
25. ВСМА-связывающая молекула по варианту осуществления 3, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C7.
26. ВСМА-связывающая молекула по варианту осуществления 3, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C8.
27. ВСМА-связывающая молекула по варианту осуществления 3, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C9.
28. ВСМА-связывающая молекула по варианту осуществления 3, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C10.
29. ВСМА-связывающая молекула по варианту осуществления 3, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C11.
30. ВСМА-связывающая молекула по варианту осуществления 3, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C12.
31. ВСМА-связывающая молекула по варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C13.
32. ВСМА-связывающая молекула по варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C14.
33. ВСМА-связывающая молекула по варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C15.
34. ВСМА-связывающая молекула по варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C16.
35. ВСМА-связывающая молекула по варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C17.
36. ВСМА-связывающая молекула по варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C18.
37. ВСМА-связывающая молекула по варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C19.
38. ВСМА-связывающая молекула по варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C20.
39. ВСМА-связывающая молекула по варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C21.
40. ВСМА-связывающая молекула по варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C22.
41. ВСМА-связывающая молекула по варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C23.
42. ВСМА-связывающая молекула по варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C24.
43. ВСМА-связывающая молекула по варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C25.
44. ВСМА-связывающая молекула по варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C26.
45. ВСМА-связывающая молекула по варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C27.
46. ВСМА-связывающая молекула по варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C28.
47. ВСМА-связывающая молекула по любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из AB1.
48. ВСМА-связывающая молекула по любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из AB2.
49. ВСМА-связывающая молекула по любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из R1F2.
50. ВСМА-связывающая молекула по любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF03.
51. ВСМА-связывающая молекула по любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF04.
52. ВСМА-связывающая молекула по любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF05.
53. ВСМА-связывающая молекула по любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF06.
54. ВСМА-связывающая молекула по любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF07.
55. ВСМА-связывающая молекула по любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF08.
56. ВСМА-связывающая молекула по любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF09.
57. ВСМА-связывающая молекула по любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF12.
58. ВСМА-связывающая молекула по любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF13.
59. ВСМА-связывающая молекула по любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF14.
60. ВСМА-связывающая молекула по любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF15.
61. ВСМА-связывающая молекула по любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF16.
62. ВСМА-связывающая молекула по любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF17.
63. ВСМА-связывающая молекула по любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF18.
64. ВСМА-связывающая молекула по любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF19.
65. ВСМА-связывающая молекула по любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF20.
66. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из AB3.
67. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PI-61.
68. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H2/L2-22.
69. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H2/L2-88.
70. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H2/L2-36.
71. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H2/L2-34.
72. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H2/L2-68.
73. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H2/L2-18.
74. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H2/L2-47.
75. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H2/L2-20.
76. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H2/L2-80.
77. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H2/L2-83.
78. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-1.
79. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-2.
80. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-3.
81. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-4.
82. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-5.
83. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-6.
84. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-7.
85. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-8.
86. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-9.
87. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-10.
88. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-11.
89. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-12.
90. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-13.
91. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-14.
92. ВСМА-связывающая молекула по любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-15.
93. ВСМА-связывающая молекула по варианту осуществления 1 или варианту осуществления 2, которая содержит последовательность вариабельного участка легкой цепи, представленную в таблице 1O-1, и соответствующую последовательность вариабельного участка тяжелой цепи, представленную в таблице 1O-2.
94. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из AB1.
95. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из AB2.
96. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из AB3.
97. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из R1F2.
98. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF03.
99. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF04.
100. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF05.
101. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF06.
102. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF07.
103. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF08.
104. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF09.
105. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF12.
106. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF13.
107. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF14.
108. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF15.
109. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF16.
110. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF17.
111. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF18.
112. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF19.
113. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF20.
114. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PI-61.
115. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H2/L2-88.
116. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H2/L2-36.
117. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H2/L2-34.
118. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H2/L2-68.
119. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H2/L2-18.
120. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H2/L2-47.
121. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H2/L2-20.
122. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H2/L2-80.
123. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H2/L2-83.
124. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-1.
125. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-2.
126. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-3.
127. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-4.
128. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-5.
129. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-6.
130. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-7.
131. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-8.
132. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-9.
133. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-10.
134. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-11.
135. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-12.
136. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-13.
137. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-14.
138. ВСМА-связывающая молекула по варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-15.
139. ВСМА-связывающая молекула по любому из вариантов осуществления 1-138, которая содержит антитело, фрагмент антитела, scFv, dsFv, Fv, Fab, scFab, (Fab')2 или однодоменное антитело (SDAB).
140. ВСМА-связывающая молекула по варианту осуществления 139, которая содержит антитело или фрагмент антитела.
141. ВСМА-связывающая молекула по варианту осуществления 139, которая содержит scFv.
142. ВСМА-связывающая молекула по варианту осуществления 141, где scFv содержит последовательность, представленную в таблице 1P.
143. ВСМА-связывающая молекула по любому из вариантов осуществления 1-142, которая представляет собой полиспецифическую связывающую молекулу.
144. ВСМА-связывающая молекула по варианту осуществления 143, которая представляет собой биспецифическую связывающую молекулу (BBM).
145. BCMA-связывающая молекула по варианту осуществления 144, где BBM содержит:
(a) антигенсвязывающий домен 1 (ABD1), который специфически связывается с BCMA; и
(b) антигенсвязывающий домен 2 (ABD2), который специфически связывается с компонентом комплекса T-клеточного рецептора (TCR) человека.
146. ВСМА-связывающая молекула по варианту осуществления 145, где ABD1 способен связывать ВСМА в то же время, когда ABD2 связан с компонентом комплекса TCR человека.
147. BCMA-связывающая молекула по варианту осуществления 145 или варианту осуществления 146, где ABD1 представляет собой антитело, фрагмент антитела, scFv, dsFv, Fv, Fab, scFab, (Fab')2, однодоменное антитело (SDAB), VH- или VL-домен или VHH-домен антитела верблюдовых.
148. BCMA-связывающая молекула по варианту осуществления 147, где ABD1 представляет собой scFv.
149. BCMA-связывающая молекула по варианту осуществления 147, где ABD1 представляет собой Fab.
150. BCMA-связывающая молекула по варианту осуществления 147, где Fab представляет собой гетеродимер Fab.
151. BCMA-связывающая молекула по варианту осуществления 147, где ABD1 представляет собой антитело к BCMA или его антигенсвязывающий домен.
152. BCMA-связывающая молекула по любому из вариантов осуществления 145-151, где ABD2 представляет собой антитело, фрагмент антитела, scFv, dsFv, Fv, Fab, scFab, (Fab')2, однодоменное антитело (SDAB), VH- или VL-домен или VHH-домен верблюдовых.
153. BCMA-связывающая молекула по варианту осуществления 152, где ABD2 представляет собой scFv.
154. BCMA-связывающая молекула по варианту осуществления 152, где ABD2 представляет собой Fab.
155. BCMA-связывающая молекула по варианту осуществления 154, где Fab представляет собой гетеродимер Fab.
156. BCMA-связывающая молекула по любому из вариантов осуществления 145-155, где компонент комплекса TCR представляет собой CD3.
157. BCMA-связывающая молекула по варианту осуществления 156, где ABD2 представляет собой антитело к CD3 или его антигенсвязывающий домен.
158. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности CDR из любого из от CD3-1 до CD3-127.
159. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-1.
160. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-2.
161. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-3.
162. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-4.
163. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-5.
164. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-6.
165. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-7.
166. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-8.
167. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-9.
168. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-10.
169. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-11.
170. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-12.
171. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-13.
172. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-14.
173. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-15.
174. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-16.
175. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-17.
176. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-18.
177. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-19.
178. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-20.
179. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-21.
180. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-22.
181. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-23.
182. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-24.
183. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-25.
184. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-26.
185. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-27.
186. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-28.
187. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-29.
188. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-30.
189. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-31.
190. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-32.
191. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-33.
192. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-34.
193. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-35.
194. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-36.
195. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-37.
196. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-38.
197. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-39.
198. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-40.
199. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-41.
200. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-42.
201. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-43.
202. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-44.
203. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-45.
204. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-46.
205. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-47.
206. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-48.
207. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-49.
208. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-50.
209. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-51.
210. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-52.
211. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-53.
212. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-54.
213. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-55.
214. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-56.
215. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-57.
216. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-58.
217. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-59.
218. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-60.
219. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-61.
220. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-62.
221. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-63.
222. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-64.
223. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-65.
224. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-66.
225. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-67.
226. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-68.
227. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-69.
228. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-70.
229. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-71.
230. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-72.
231. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-73.
232. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-74.
233. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-75.
234. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-76.
235. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-77.
236. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-78.
237. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-79.
238. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-80.
239. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-81.
240. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-82.
241. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-83.
242. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-84.
243. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-85.
244. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-86.
245. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-87.
246. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-88.
247. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-89.
248. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-90.
249. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-91.
250. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-92.
251. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-93.
252. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-94.
253. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-95.
254. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-96.
255. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-97.
256. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-98.
257. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-99.
258. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-100.
259. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-101.
260. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-102.
261. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-103.
262. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-104.
263. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-105.
264. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-106.
265. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-107.
266. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-108.
267. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-109.
268. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-110.
269. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-111.
270. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-112.
271. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-113.
272. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-114.
273. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-115.
274. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-116.
275. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-117.
276. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-118.
277. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-119.
278. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-120.
279. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-121.
280. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-122.
281. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-123.
282. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-124.
283. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-125.
284. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-126.
285. ВСМА-связывающая молекула по варианту осуществления 158, где ABD2 содержит последовательности CDR из CD3-127.
286. ВСМА-связывающая молекула по любому из вариантов осуществления 159-285, где CDR определены согласно нумерации по Kabat, как представлено в таблице 3B.
287. ВСМА-связывающая молекула по любому из вариантов осуществления 159-178, где CDR определены согласно нумерации по Chothia, как представлено в таблице 3C.
288. ВСМА-связывающая молекула по любому из вариантов осуществления 159-178, где CDR определены согласно комбинации схем нумерации по Kabat и по Chothia, как представлено в таблице 3D.
289. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-1, как представлено в таблице 3A.
290. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-2, как представлено в таблице 3A.
291. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-3, как представлено в таблице 3A.
292. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-4, как представлено в таблице 3A.
293. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-5, как представлено в таблице 3A.
294. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-6, как представлено в таблице 3A.
295. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-7, как представлено в таблице 3A.
296. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-8, как представлено в таблице 3A.
297. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-9, как представлено в таблице 3A.
298. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-10, как представлено в таблице 3A.
299. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-11, как представлено в таблице 3A.
300. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-12, как представлено в таблице 3A.
301. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-13, как представлено в таблице 3A.
302. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-14, как представлено в таблице 3A.
303. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-15, как представлено в таблице 3A.
304. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-16, как представлено в таблице 3A.
305. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-17, как представлено в таблице 3A.
306. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-18, как представлено в таблице 3A.
307. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-19, как представлено в таблице 3A.
308. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-20, как представлено в таблице 3A.
309. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-21, как представлено в таблице 3A.
310. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-22, как представлено в таблице 3A.
311. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-23, как представлено в таблице 3A.
312. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-24, как представлено в таблице 3A.
313. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-25, как представлено в таблице 3A.
314. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-26, как представлено в таблице 3A.
315. ВСМА-связывающая молекула по варианту осуществления 157, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-27, как представлено в таблице 3A.
316. ВСМА-связывающая молекула по любому из вариантов осуществления 145-155, где компонент комплекса TCR представляет собой TCRα, TCRβ или димер TCRα/β.
317. BCMA-связывающая молекула по варианту осуществления 316, где ABD2 представляет собой антитело или его антигенсвязывающий домен.
318. ВСМА-связывающая молекула по варианту осуществления 317, где ABD2 содержит последовательности CDR из BMA031.
319. ВСМА-связывающая молекула по варианту осуществления 318, где последовательности CDR определены согласно нумерации по Kabat.
320. ВСМА-связывающая молекула по варианту осуществления 318, где последовательности CDR определены согласно нумерации по Chothia.
321. ВСМА-связывающая молекула по варианту осуществления 318, где последовательности CDR определены согласно комбинации схем нумерации по Kabat и по Chothia.
322. ВСМА-связывающая молекула по варианту осуществления 318, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из BMA031.
323. ВСМА-связывающая молекула по любому из вариантов осуществления 145-155, где компонент комплекса TCR представляет собой TCR-γ, TCR-δ или димер TCR-γ/δ.
324. BCMA-связывающая молекула по варианту осуществления 323, где ABD2 представляет собой антитело или его антигенсвязывающий домен.
325. ВСМА-связывающая молекула по варианту осуществления 324, где ABD2 содержит последовательности CDR из δTCS1.
326. ВСМА-связывающая молекула по варианту осуществления 325, где последовательности CDR определены согласно нумерации по Kabat.
327. ВСМА-связывающая молекула по варианту осуществления 325, где последовательности CDR определены согласно нумерации по Chothia.
328. ВСМА-связывающая молекула по варианту осуществления 325, где последовательности CDR определены согласно комбинации схем нумерации по Kabat и по Chothia.
329. ВСМА-связывающая молекула по варианту осуществления 325, где ABD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из δTCS1.
330. ВСМА-связывающая молекула по любому из вариантов осуществления 145-151, где ABD2 представляет собой ABD на основе, отличной от каркасной структуры иммуноглобулина.
331. ВСМА-связывающая молекула по варианту осуществления 330, где ABD2 представляет собой домен Куница, аднексин, аффитело, дарпин, авимер, антикалин, липокалин, центирин, версатело, ноттин, аднектин, пронектин, аффитин/нанофитин, аффилин, атример/тетранектин, бициклический пептид, цистиновый узел, каркасную структуру Fn3, O-тело, Tn3, аффимер, BD, адгирон, дуокалин, альфатело, белок с повторами Armadillo, репетело или финомер.
332. ВСМА-связывающая молекула по любому из вариантов осуществления 145-331, которая содержит первый вариант Fc-участка и второй вариант Fc-участка, которые вместе образуют гетеродимер Fc.
333. ВСМА-связывающая молекула по варианту осуществления 332, где первый и второй варианты Fc-участков содержат аминокислотные замены S364K/E357Q : L368D/K370S.
334. ВСМА-связывающая молекула по варианту осуществления 332, где первый и второй варианты Fc-участков содержат аминокислотные замены L368D/K370S : S364.
335. ВСМА-связывающая молекула по варианту осуществления 332, где первый и второй варианты Fc-участков содержат аминокислотные замены L368E/K370S : S364K.
336. ВСМА-связывающая молекула по варианту осуществления 332, где первый и второй варианты Fc-участков содержат аминокислотные замены T411T/E360E/Q362E : D401K.
337. ВСМА-связывающая молекула по варианту осуществления 332, где первый и второй варианты Fc-участков содержат аминокислотные замены L368D 370S : S364/E357L.
338. ВСМА-связывающая молекула по варианту осуществления 332, где первый и второй варианты Fc-участков содержат аминокислотные замены 370S : S364K/E357Q.
339. ВСМА-связывающая молекула по варианту осуществления 332, где первый и второй варианты Fc-участков содержат аминокислотные замены из любого из стерических вариантов, перечисленных на фигуре 4 из WO 2014/110601 (воспроизведены в таблице 6).
340. ВСМА-связывающая молекула по варианту осуществления 332, где первый и второй варианты Fc-участков содержат аминокислотные замены из любого из вариантов, перечисленных на фигуре 5 из WO 2014/110601 (воспроизведены в таблице 6).
341. ВСМА-связывающая молекула по варианту осуществления 332, где первый и второй варианты Fc-участков содержат аминокислотные замены из любого из вариантов, перечисленных на фигуре 6 из WO 2014/110601 (воспроизведены в таблице 6).
342. ВСМА-связывающая молекула по любому из вариантов осуществления 332-341, где первый вариант Fc-участка функционально связан с ABD1, а второй вариант Fc-участка функционально связан с ABD2.
343. ВСМА-связывающая молекула по любому из вариантов осуществления 332-341, где первый вариант Fc-участка функционально связан с ABD2, а второй вариант Fc-участка функционально связан с ABD1.
344. ВСМА-связывающая молекула по любому из вариантов осуществления 332-343, где по меньшей мере один из Fc-участков содержит модификацию, обеспечивающую получение варианта с устранением связывания с Fcγ-рецепторами.
345. ВСМА-связывающая молекула по варианту осуществления 342, где модификации, обеспечивающие получение варианта с устранением связывания с Fcγ-рецепторами, выбраны из таблицы 5.
346. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает G236R.
347. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает S239G.
348. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает S239K.
349. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает S239Q.
350. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает S239R.
351. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает V266D.
352. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает S267K.
353. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает S267R.
354. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает H268K.
355. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает E269R.
356. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает 299R.
357. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает 299K
358. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает K322A
359. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает A327G
360. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает A327L
361. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает A327N
362. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает A327Q
363. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает L328E
364. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает L328R
365. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает P329A
366. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает P329H
367. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает P329K
368. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает A330L
369. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает A330S/P331S
370. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает I332K
371. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает I332R
372. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает V266D/A327Q
373. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает V266D/P329K
374. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает G236R/L328R
375. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с удалением, включает E233P/L234V/L235A/G236del/S239K.
376. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает E233P/L234V/L235A/G236del/S267K.
377. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает E233P/L234V/L235A/G236del/S239K/A327G.
378. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает E233P/L234V/L235A/G236del/S267K/A327G.
379. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает E233P/L234V/L235A/G236del.
380. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает S239K/S267K.
381. ВСМА-связывающая молекула по варианту осуществления 345, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает 267K/P329K.
382. ВСМА-связывающая молекула по любому из вариантов осуществления 344-381, где Fc-участок, содержащий модификацию, обеспечивающую получение варианта с устранением связывания с Fcγ-рецепторами, функционально связан с ABD1.
383. ВСМА-связывающая молекула по любому из вариантов осуществления 344-381, где Fc-участок, содержащий модификацию, обеспечивающую получение варианта с устранением связывания с Fcγ-рецепторами, функционально связан с ABD2.
384. ВСМА-связывающая молекула по любому из вариантов осуществления 344-381, где оба Fc-участка содержат модификацию, обеспечивающую получение варианта с устранением связывания с Fcγ-рецепторами.
385. ВСМА-связывающая молекула по любому из вариантов осуществления 332-384, где по меньшей мере один из Fc-участков дополнительно содержит замены, обеспечивающие получение pI-варианта.
386. ВСМА-связывающая молекула по варианту осуществления 342, где замены, обеспечивающие получение pI-варианта, выбраны из таблицы 8.
387. ВСМА-связывающая молекула по варианту осуществления 386, где замены, обеспечивающие получение pI-варианта, включают замены, присутствующие в pI_ISO(-).
388. ВСМА-связывающая молекула по варианту осуществления 386, где замены, обеспечивающие получение pI-варианта, включают замены, присутствующие в pl_(-)_изостерический_A.
389. ВСМА-связывающая молекула по варианту осуществления 386, где замены, обеспечивающие получение pI-варианта, включают замены, присутствующие в pl_(-)_изостерический_B.
390. ВСМА-связывающая молекула по варианту осуществления 386, где замены, обеспечивающие получение pI-варианта, включают замены, присутствующие в Pl_ISO(+RR).
391. ВСМА-связывающая молекула по варианту осуществления 386, где замены, обеспечивающие получение pI-варианта, включают замены, присутствующие в pI_ISO(+).
392. ВСМА-связывающая молекула по варианту осуществления 386, где замены, обеспечивающие получение pI-варианта, включают замены, присутствующие в pl_(+)_изостерический_A.
393. ВСМА-связывающая молекула по варианту осуществления 386, где замены, обеспечивающие получение pI-варианта, включают замены, присутствующие в pl_(+)_изостерический_B.
394. ВСМА-связывающая молекула по варианту осуществления 386, где замены, обеспечивающие получение pI-варианта, включают замены, присутствующие в pl_(+)_изостерический_E269Q/E272Q.
395. ВСМА-связывающая молекула по варианту осуществления 386, где замены, обеспечивающие получение pI-варианта, включают замены, присутствующие в pl_(+)_изостерический_E269Q/E283Q.
396. ВСМА-связывающая молекула по варианту осуществления 386, где замены, обеспечивающие получение pI-варианта, включают замены, присутствующие в pl_(+)_изостерический_E2720/E283Q.
397. ВСМА-связывающая молекула по варианту осуществления 386, где замены, обеспечивающие получение pI-варианта, включают замены, присутствующие в pl_(+)_изостерический_E269Q.
398. ВСМА-связывающая молекула по любому из вариантов осуществления 385-397, где Fc-участок, функционально связанный с AB1, содержит замены, обеспечивающие получение pI-варианта.
399. ВСМА-связывающая молекула по любому из вариантов осуществления 385-398, где Fc-участок, функционально связанный с AB1, содержит замены, обеспечивающие получение pI-варианта.
400. ВСМА-связывающая молекула по любому из вариантов осуществления 332-399, где первый и/или второй Fc-участок дополнительно содержит одну или несколько аминокислотных замен, выбранных из 434A, 434S, 428L, 308F, 259I, 428L/434S, 259I/308F, 436I/428L, 4361 или V/434S, 436V/428L, 252Y, 252Y/254T/256E, 259I/308F/428L, 236A, 239D, 239E, 332E, 332D, 239D/332E, 267D, 267E, 328F, 267E/328F, 236A/332E, 239D/332E/330Y, 239D, 332E/330L, 236R, 328R, 236R/328R, 236N/267E, 243L, 298A и 299T.
401. ВСМА-связывающая молекула по любому из вариантов осуществления 332-399, где первый и/или второй Fc-участки, дополнительно содержащие одну или несколько аминокислотных замен, содержат аминокислотную замену 434A, 434S или 434V.
402. ВСМА-связывающая молекула по варианту осуществления 401, где первый и/или второй Fc-участки, дополнительно содержащие одну или несколько аминокислотных замен, содержат аминокислотную замену 428L.
403. ВСМА-связывающая молекула по любому из вариантов осуществления 401-402, где первый и/или второй Fc-участки, дополнительно содержащие одну или несколько аминокислотных замен, содержат аминокислотную замену 308F.
404. ВСМА-связывающая молекула по любому из вариантов осуществления 401-403, где первый и/или второй Fc-участки, дополнительно содержащие одну или несколько аминокислотных замен, содержат аминокислотную замену 259I.
405. ВСМА-связывающая молекула по любому из вариантов осуществления 401-404, где первый и/или второй Fc-участки, дополнительно содержащие одну или несколько аминокислотных замен, содержат аминокислотную замену 436I.
406. ВСМА-связывающая молекула по любому из вариантов осуществления 401-405, где первый и/или второй Fc-участки, дополнительно содержащие одну или несколько аминокислотных замен, содержат аминокислотную замену 252Y.
407. ВСМА-связывающая молекула по любому из вариантов осуществления 401-406, где первый и/или второй Fc-участки, дополнительно содержащие одну или несколько аминокислотных замен, содержат аминокислотную замену 254T.
408. ВСМА-связывающая молекула по любому из вариантов осуществления 401-407, где первый и/или второй Fc-участки, дополнительно содержащие одну или несколько аминокислотных замен, содержат аминокислотную замену 256E.
409. ВСМА-связывающая молекула по любому из вариантов осуществления 401-408, где первый и/или второй Fc-участки, дополнительно содержащие одну или несколько аминокислотных замен, содержат аминокислотную замену 239D или 239E.
410. ВСМА-связывающая молекула по любому из вариантов осуществления 401-409, где первый и/или второй Fc-участки, дополнительно содержащие одну или несколько аминокислотных замен, содержат аминокислотную замену 332E или 332D.
411. ВСМА-связывающая молекула по любому из вариантов осуществления 401-410, где первый и/или второй Fc-участки, дополнительно содержащие одну или несколько аминокислотных замен, содержат аминокислотную замену 267D или 267E.
412. ВСМА-связывающая молекула по любому из вариантов осуществления 401-411, где первый и/или второй Fc-участки, дополнительно содержащие одну или несколько аминокислотных замен, содержат аминокислотную замену 330L.
413. ВСМА-связывающая молекула по любому из вариантов осуществления 401-412, где первый и/или второй Fc-участки, дополнительно содержащие одну или несколько аминокислотных замен, содержат аминокислотную замену 236R или 236N.
414. ВСМА-связывающая молекула по любому из вариантов осуществления 401-413, где первый и/или второй Fc-участки, дополнительно содержащие одну или несколько аминокислотных замен, содержат аминокислотную замену 328R.
415. ВСМА-связывающая молекула по любому из вариантов осуществления 401-414, где первый и/или второй Fc-участки, дополнительно содержащие одну или несколько аминокислотных замен, содержат аминокислотную замену 243L.
416. ВСМА-связывающая молекула по любому из вариантов осуществления 401-415, где первый и/или второй Fc-участки, дополнительно содержащие одну или несколько аминокислотных замен, содержат аминокислотную замену 298A.
417. ВСМА-связывающая молекула по любому из вариантов осуществления 401-416, где первый и/или второй Fc-участки, дополнительно содержащие одну или несколько аминокислотных замен, содержат аминокислотную замену 299T.
418. BCMA-связывающая молекула по варианту осуществления 332, где:
(a) первый и второй варианты Fc-участков содержат аминокислотные замены S364K/E357Q : L368D/K370S;
(b) первый и/или второй варианты Fc-участков содержат модификации, обеспечивающие получение варианта с устранением связывания с Fcγ-рецепторами, E233P/L234V/L235A/G236del/S267K, и
(c) первый и/или второй варианты Fc-участков содержат замены, обеспечивающие получение pI-варианта, N208D/Q295E/N384D/Q418E/N421D (pl_(-)_изостерический_A).
419. ВСМА-связывающая молекула по варианту осуществления 418, где первый вариант Fc-участка функционально связан с ABD1, а второй вариант Fc-участка функционально связан с ABD2.
420. ВСМА-связывающая молекула по варианту осуществления 418, где первый вариант Fc-участка функционально связан с ABD2, а второй вариант Fc-участка функционально связан с ABD1.
421. ВСМА-связывающая молекула по любому из вариантов осуществления 418-420, где первый вариант Fc-участка содержит модификации, обеспечивающие получение варианта с устранением связывания с Fcγ-рецепторами, E233P/L234V/L235A/G236del/S267K.
422. ВСМА-связывающая молекула по любому из вариантов осуществления 418-421, где второй вариант Fc-участка содержит модификации, обеспечивающие получение варианта с устранением связывания с Fcγ-рецепторами, E233P/L234V/L235A/G236del/S267K.
423. ВСМА-связывающая молекула по любому из вариантов осуществления 418-422, где первый вариант Fc-участка содержит замены, обеспечивающие получение pI-варианта, N208D/Q295E/N384D/Q418E/N421D (pl_(-)_изостерический_A).
424. ВСМА-связывающая молекула по любому из вариантов осуществления 418-423, где второй вариант Fc-участка содержит замены, обеспечивающие получение pI-варианта, N208D/Q295E/N384D/Q418E/N421D (pl_(-)_изостерический_A).
425. ВСМА-связывающая молекула по любому из вариантов осуществления 145-331, которая содержит Fc-домен.
426. ВСМА-связывающая молекула по варианту осуществления 425, где Fc-домен представляет собой гетеродимер Fc.
427. ВСМА-связывающая молекула по варианту осуществления 426, где гетеродимер Fc содержит по меньшей мере одну из модификаций Fc, представленных в таблице 6.
428. ВСМА-связывающая молекула по варианту осуществления 426, где гетеродимер Fc содержит модификации типа "выступ в углубление" ("KIH").
429. ВСМА-связывающая молекула по варианту осуществления 428, где модификации KIH являются любыми из модификаций KIH, описанных в разделе 7.4.1.5.1 или в таблице 6.
430. ВСМА-связывающая молекула по варианту осуществления 428, где модификации KIH являются любыми из альтернативных модификаций KIH, описанных в разделе 7.4.1.5.2 или в таблице 6.
431. ВСМА-связывающая молекула по любому из вариантов осуществления 426-430, которая содержит модификации с образованием полярных мостиков.
432. ВСМА-связывающая молекула по варианту осуществления 431, где модификации с образованием полярных мостиков являются любыми из модификаций с образованием полярных мостиков, описанных в разделе 7.4.1.5.7 или в таблице 6.
433. ВСМА-связывающая молекула по любому из вариантов осуществления 426-432, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 1 - Fc 150.
434. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 1 - Fc 5.
435. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 6 - Fc 10.
436. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 11 - Fc 15.
437. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 16 - Fc 20.
438. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 21 - Fc 25.
439. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 26 - Fc 30.
440. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 31 - Fc 35.
441. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 36 - Fc 40.
442. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 41 - Fc 45.
443. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 46 - Fc 50.
444. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 51 - Fc 55.
445. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 56 - Fc 60.
446. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 61 - Fc 65.
447. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 66 - Fc 70.
448. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 71 - Fc 75.
449. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 76 - Fc 80.
450. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 81 - Fc 85.
451. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 86 - Fc 90.
452. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 91 - Fc 95.
453. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 96 - Fc 100.
454. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 101 - Fc 105.
455. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 106 - Fc 110.
456. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 111 - Fc 115.
457. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 116 - Fc 120.
458. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 121 - Fc 125.
459. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 126 - Fc 130.
460. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 131 - Fc 135.
461. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 136 - Fc 140.
462. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 141 - Fc 145.
463. ВСМА-связывающая молекула по варианту осуществления 433, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 146 - Fc 150.
464. ВСМА-связывающая молекула по любому из вариантов осуществления 425-463, где Fc-домен характеризуется измененной эффекторной функцией.
465. ВСМА-связывающая молекула по варианту осуществления 464, где Fc-домен характеризуется измененным связыванием с одним или несколькими Fc-рецепторами.
466. ВСМА-связывающая молекула по варианту осуществления 465, где один или несколько Fc-рецепторов включают FcRN.
467. ВСМА-связывающая молекула по варианту осуществления 465 или варианту осуществления 466, где один или несколько Fc-рецепторов включают лейкоцитарные рецепторы.
468. ВСМА-связывающая молекула по любому из вариантов осуществления 425-467, где Fc характеризуется модифицированной архитектурой дисульфидных связей.
469. ВСМА-связывающая молекула по любому из вариантов осуществления 425-468, где Fc характеризуется измененными паттернами гликозилирования.
470. ВСМА-связывающая молекула по любому из вариантов осуществления 425-469, где Fc содержит шарнирный участок.
471. ВСМА-связывающая молекула по варианту осуществления 470, где шарнирный участок включает любой из шарнирных участков, описанных в разделе 7.4.2.
472. ВСМА-связывающая молекула по варианту осуществления 471, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H1.
473. ВСМА-связывающая молекула по варианту осуществления 471, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H2.
474. ВСМА-связывающая молекула по варианту осуществления 471, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H3.
475. ВСМА-связывающая молекула по варианту осуществления 471, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H4.
476. ВСМА-связывающая молекула по варианту осуществления 471, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H5.
477. ВСМА-связывающая молекула по варианту осуществления 471, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H6.
478. ВСМА-связывающая молекула по варианту осуществления 471, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H7.
479. ВСМА-связывающая молекула по варианту осуществления 471, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H8.
480. ВСМА-связывающая молекула по варианту осуществления 471, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H9.
481. ВСМА-связывающая молекула по варианту осуществления 471, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H10.
482. ВСМА-связывающая молекула по варианту осуществления 471, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H11.
483. ВСМА-связывающая молекула по варианту осуществления 471, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H12.
484. ВСМА-связывающая молекула по варианту осуществления 471, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H13.
485. ВСМА-связывающая молекула по варианту осуществления 471, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H14.
486. ВСМА-связывающая молекула по варианту осуществления 471, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H15.
487. ВСМА-связывающая молекула по варианту осуществления 471, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H16.
488. ВСМА-связывающая молекула по варианту осуществления 471, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H17.
489. ВСМА-связывающая молекула по варианту осуществления 471, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H18.
490. ВСМА-связывающая молекула по варианту осуществления 471, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H19.
491. ВСМА-связывающая молекула по варианту осуществления 471, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H20.
492. ВСМА-связывающая молекула по варианту осуществления 471, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H21.
493. ВСМА-связывающая молекула по любому из вариантов осуществления 1-492, которая содержит по меньшей мере один scFv-домен.
494. ВСМА-связывающая молекула по варианту осуществления 493, где по меньшей мере один scFv содержит линкер, соединяющий VH- и VL-домены.
495. ВСМА-связывающая молекула по варианту осуществления 494, где длина линкера составляет 5-25 аминокислот.
496. ВСМА-связывающая молекула по варианту осуществления 495, где длина линкера составляет 12-20 аминокислот.
497. ВСМА-связывающая молекула по любому из вариантов осуществления 494-496, где линкер представляет собой заряженный линкер и/или гибкий линкер.
498. ВСМА-связывающая молекула по любому из вариантов осуществления 494-497, где линкер выбран из любого из линкеров L1-L54.
499. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L1.
500. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L2.
501. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L3.
502. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L4.
503. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L5.
504. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L6.
505. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L7.
506. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L8.
507. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L9.
508. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L10.
509. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L11.
510. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L12.
511. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L13.
512. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L14.
513. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L15.
514. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L16.
515. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L17.
516. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L18.
517. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L19.
518. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L20.
519. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L21.
520. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L22.
521. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L23.
522. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L24.
523. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L25.
524. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L26.
525. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L27.
526. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L28.
527. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L29.
528. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L30.
529. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L31.
530. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L32.
531. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L33.
532. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L34.
533. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L35.
534. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L36.
535. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L37.
536. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L38.
537. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L39.
538. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L40.
539. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L41.
540. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L42.
541. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L43.
542. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L44.
543. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L45.
544. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L46.
545. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L47.
546. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L48.
547. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L49.
548. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L50.
549. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L51.
550. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L52.
551. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L53.
552. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L54.
553. ВСМА-связывающая молекула по любому из вариантов осуществления 1-552, которая содержит по меньшей мере один Fab-домен.
554. ВСМА-связывающая молекула по варианту осуществления 553, где по меньшей мере один Fab-домен содержит любые из модификаций, обеспечивающих гетеродимеризацию Fab, представленных в таблице 2.
555. ВСМА-связывающая молекула по варианту осуществления 554, где по меньшей мере один Fab-домен содержит модификации, обеспечивающие гетеродимеризацию Fab, обозначенные как F1.
556. ВСМА-связывающая молекула по варианту осуществления 554, где по меньшей мере один Fab-домен содержит модификации, обеспечивающие гетеродимеризацию Fab, обозначенные как F2.
557. ВСМА-связывающая молекула по варианту осуществления 554, где по меньшей мере один Fab-домен содержит модификации, обеспечивающие гетеродимеризацию Fab, обозначенные как F3.
558. ВСМА-связывающая молекула по варианту осуществления 554, где по меньшей мере один Fab-домен содержит модификации, обеспечивающие гетеродимеризацию Fab, обозначенные как F4.
559. ВСМА-связывающая молекула по варианту осуществления 554, где по меньшей мере один Fab-домен содержит модификации, обеспечивающие гетеродимеризацию Fab, обозначенные как F5.
560. ВСМА-связывающая молекула по варианту осуществления 554, где по меньшей мере один Fab-домен содержит модификации, обеспечивающие гетеродимеризацию Fab, обозначенные как F6.
561. ВСМА-связывающая молекула по варианту осуществления 554, где по меньшей мере один Fab-домен содержит модификации, обеспечивающие гетеродимеризацию Fab, обозначенные как F7.
562. ВСМА-связывающая молекула по любому из вариантов осуществления 145-561, которая представляет собой биспецифическую связывающую молекулу, которая содержит по меньшей мере два ABD, ABD и цепь ABD, или две цепи ABD, соединенные друг с другом посредством линкера.
563. ВСМА-связывающая молекула по варианту осуществления 562, где длина линкера составляет 5-25 аминокислот.
564. ВСМА-связывающая молекула по варианту осуществления 563, где длина линкера составляет 12-20 аминокислот.
565. ВСМА-связывающая молекула по любому из вариантов осуществления 562-564, где линкер представляет собой заряженный линкер и/или гибкий линкер.
566. ВСМА-связывающая молекула по любому из вариантов осуществления 562-565, где линкер выбран из любого из линкеров L1-L54.
567. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L1.
568. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L2.
569. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L3.
570. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L4.
571. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L5.
572. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L6.
573. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L7.
574. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L8.
575. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L9.
576. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L10.
577. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L11.
578. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L12.
579. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L13.
580. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L14.
581. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L15.
582. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L16.
583. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L17.
584. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L18.
585. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L19.
586. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L20.
587. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L21.
588. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L22.
589. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L23.
590. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L24.
591. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L25.
592. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L26.
593. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L27.
594. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L28.
595. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L29.
596. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L30.
597. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L31.
598. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L32.
599. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L33.
600. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L34.
601. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L35.
602. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L36.
603. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L37.
604. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L38.
605. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L39.
606. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L40.
607. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L41.
608. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L42.
609. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L43.
610. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L44.
611. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L45.
612. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L46.
613. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L47.
614. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L48.
615. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L49.
616. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L50.
617. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L51.
618. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L52.
619. ВСМА-связывающая молекула по варианту осуществления 498, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L53.
620. ВСМА-связывающая молекула по варианту осуществления 566, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L54.
621. ВСМА-связывающая молекула по любому из вариантов осуществления 145-620, которая представляет собой бивалентную BCMA-связывающую молекулу.
622. ВСМА-связывающая молекула по варианту осуществления 621, где бивалентная ВСМА-связывающая молекула имеет любую из конфигураций, изображенных на фиг. 1B-1F.
623. ВСМА-связывающая молекула по варианту осуществления 622, где бивалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1B.
624. ВСМА-связывающая молекула по варианту осуществления 622, где бивалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1C.
625. ВСМА-связывающая молекула по варианту осуществления 622, где бивалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1D.
626. ВСМА-связывающая молекула по варианту осуществления 622, где бивалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1E.
627. ВСМА-связывающая молекула по варианту осуществления 622, где бивалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1F.
628. ВСМА-связывающая молекула по любому из вариантов осуществления 622-627, в которой ABD имеют конфигурацию, обозначенную как B1.
629. ВСМА-связывающая молекула по любому из вариантов осуществления 622-627, в которой ABD имеют конфигурацию, обозначенную как B2.
630. ВСМА-связывающая молекула по любому из вариантов осуществления 145-620, которая представляет собой тривалентную BCMA-связывающую молекулу.
631. ВСМА-связывающая молекула по варианту осуществления 630, где тривалентная ВСМА-связывающая молекула имеет любую из конфигураций, изображенных на фиг. 1G-1Z.
632. ВСМА-связывающая молекула по варианту осуществления 631, где тривалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1G.
633. ВСМА-связывающая молекула по варианту осуществления 631, где тривалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1H.
634. ВСМА-связывающая молекула по варианту осуществления 631, где тривалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1I.
635. ВСМА-связывающая молекула по варианту осуществления 631, где тривалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1J.
636. ВСМА-связывающая молекула по варианту осуществления 631, где тривалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1K.
637. ВСМА-связывающая молекула по варианту осуществления 631, где тривалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1L.
638. ВСМА-связывающая молекула по варианту осуществления 631, где тривалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1M.
639. ВСМА-связывающая молекула по варианту осуществления 631, где тривалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1N.
640. ВСМА-связывающая молекула по варианту осуществления 631, где тривалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1O.
641. ВСМА-связывающая молекула по варианту осуществления 631, где тривалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1P.
642. ВСМА-связывающая молекула по варианту осуществления 631, где тривалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1Q.
643. ВСМА-связывающая молекула по варианту осуществления 631, где тривалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1R.
644. ВСМА-связывающая молекула по варианту осуществления 631, где тривалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1S.
645. ВСМА-связывающая молекула по варианту осуществления 631, где тривалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1T.
646. ВСМА-связывающая молекула по варианту осуществления 631, где тривалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1U.
647. ВСМА-связывающая молекула по варианту осуществления 631, где тривалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1V.
648. ВСМА-связывающая молекула по варианту осуществления 631, где тривалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1W.
649. ВСМА-связывающая молекула по варианту осуществления 631, где тривалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1X.
650. ВСМА-связывающая молекула по варианту осуществления 631, где тривалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1Y.
651. ВСМА-связывающая молекула по варианту осуществления 631, где тривалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1Z.
652. ВСМА-связывающая молекула по любому из вариантов осуществления 631-651, в которой ABD имеют конфигурацию, обозначенную как T1.
653. ВСМА-связывающая молекула по любому из вариантов осуществления 631-651, в которой ABD имеют конфигурацию, обозначенную как T2.
654. ВСМА-связывающая молекула по любому из вариантов осуществления 631-651, в которой ABD имеют конфигурацию, обозначенную как T3.
655. ВСМА-связывающая молекула по любому из вариантов осуществления 631-651, в которой ABD имеют конфигурацию, обозначенную как T4.
656. ВСМА-связывающая молекула по любому из вариантов осуществления 631-651, в которой ABD имеют конфигурацию, обозначенную как T5.
657. ВСМА-связывающая молекула по любому из вариантов осуществления 631-651, в которой ABD имеют конфигурацию, обозначенную как T6.
658. ВСМА-связывающая молекула по любому из вариантов осуществления 145-620, которая представляет собой тетравалентную BCMA-связывающую молекулу.
659. ВСМА-связывающая молекула по варианту осуществления 658, где тетравалентная ВСМА-связывающая молекула имеет любую из конфигураций, изображенных на фиг. 1AA-1AG.
660. ВСМА-связывающая молекула по варианту осуществления 659, где тетравалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1AA.
661. ВСМА-связывающая молекула по варианту осуществления 659, где тетравалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1AB.
662. ВСМА-связывающая молекула по варианту осуществления 659, где тетравалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1AC.
663. ВСМА-связывающая молекула по варианту осуществления 659, где тетравалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1AD.
664. ВСМА-связывающая молекула по варианту осуществления 659, где тетравалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1AE.
665. ВСМА-связывающая молекула по варианту осуществления 659, где тетравалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1AF.
666. ВСМА-связывающая молекула по варианту осуществления 659, где тетравалентная ВСМА-связывающая молекула имеет конфигурацию, изображенную на фиг. 1AG.
667. ВСМА-связывающая молекула по любому из вариантов осуществления 659-666, в которой ABD имеют любую из конфигураций, обозначенных как Tv 1 - Tv 24.
668. ВСМА-связывающая молекула по варианту осуществления 667, в которой ABD имеют конфигурацию, обозначенную как Tv 1.
669. ВСМА-связывающая молекула по варианту осуществления 667, в которой ABD имеют конфигурацию, обозначенную как Tv 2.
670. ВСМА-связывающая молекула по варианту осуществления 667, в которой ABD имеют конфигурацию, обозначенную как Tv 3.
671. ВСМА-связывающая молекула по варианту осуществления 667, в которой ABD имеют конфигурацию, обозначенную как Tv 4.
672. ВСМА-связывающая молекула по варианту осуществления 667, в которой ABD имеют конфигурацию, обозначенную как Tv 5.
673. ВСМА-связывающая молекула по варианту осуществления 667, в которой ABD имеют конфигурацию, обозначенную как Tv 6.
674. ВСМА-связывающая молекула по варианту осуществления 667, в которой ABD имеют конфигурацию, обозначенную как Tv 7.
675. ВСМА-связывающая молекула по варианту осуществления 667, в которой ABD имеют конфигурацию, обозначенную как Tv 8.
676. ВСМА-связывающая молекула по варианту осуществления 667, в которой ABD имеют конфигурацию, обозначенную как Tv 9.
677. ВСМА-связывающая молекула по варианту осуществления 667, в которой ABD имеют конфигурацию, обозначенную как Tv 10.
678. ВСМА-связывающая молекула по варианту осуществления 667, в которой ABD имеют конфигурацию, обозначенную как Tv 11.
679. ВСМА-связывающая молекула по варианту осуществления 667, в которой ABD имеют конфигурацию, обозначенную как Tv 12.
680. ВСМА-связывающая молекула по варианту осуществления 667, в которой ABD имеют конфигурацию, обозначенную как Tv 13.
681. ВСМА-связывающая молекула по варианту осуществления 667, в которой ABD имеют конфигурацию, обозначенную как Tv 14.
682. ВСМА-связывающая молекула по любому из вариантов осуществления 1-681, которая обладает межвидовой перекрестной реактивностью.
683. ВСМА-связывающая молекула по варианту осуществления 682, где ВСМА-связывающая молекула дополнительно специфически связывается с BCMA у одного или нескольких видов млекопитающих, отличных от человека.
684. ВСМА-связывающая молекула по варианту осуществления 683, где один или несколько видов млекопитающих, отличных от человека, включают один или несколько видов приматов, отличных от человека.
685. ВСМА-связывающая молекула по варианту осуществления 684, где один или несколько видов приматов, отличных от человека, включают Macaca fascicularis.
686. ВСМА-связывающая молекула по варианту осуществления 684 или варианту осуществления 685, где один или несколько видов приматов, отличных от человека, включают Macaca mulatta.
687. ВСМА-связывающая молекула по любому из вариантов осуществления 684-686, где один или несколько видов приматов, отличных от человека, включают Macaca nemestrina.
688. ВСМА-связывающая молекула по любому из вариантов осуществления 682-687, где один или несколько видов млекопитающих, отличных от человека, включают Mus musculus.
689. ВСМА-связывающая молекула по любому из вариантов осуществления 1-681, где ВСМА-связывающая молекула не обладает межвидовой перекрестной реактивностью.
690. ВСМА-связывающая молекула по любому из вариантов осуществления 145-681, которая представляет собой BBM, и где ABD1 и/или ABD2 обладают межвидовой перекрестной реактивностью.
691. ВСМА-связывающая молекула по варианту осуществления 690, где ABD1 дополнительно специфически связывается с BCMA у одного или нескольких видов млекопитающих, отличных от человека.
692. ВСМА-связывающая молекула по варианту осуществления 690 или варианту осуществления 691, где ABD2 дополнительно специфически связывается с компонентом комплекса TCR у одного или нескольких видов млекопитающих, отличных от человека.
693. ВСМА-связывающая молекула по любому из вариантов осуществления 690-692, где один или несколько видов млекопитающих, отличных от человека, включают один или несколько видов приматов, отличных от человека.
694. ВСМА-связывающая молекула по варианту осуществления 693, где один или несколько видов приматов, отличных от человека, включают Macaca fascicularis.
695. ВСМА-связывающая молекула по варианту осуществления 693 или варианту осуществления 694, где один или несколько видов приматов, отличных от человека, включают Macaca mulatta.
696. ВСМА-связывающая молекула по любому из вариантов осуществления 693-695, где один или несколько видов приматов, отличных от человека, включают Macaca nemestrina.
697. ВСМА-связывающая молекула по любому из вариантов осуществления 692-696, где один или несколько видов млекопитающих, отличных от человека, включают Mus musculus.
698. ВСМА-связывающая молекула по любому из вариантов осуществления 145-681, которая представляет собой BBM, и где ABD1 и ABD2 не обладают межвидовой перекрестной реактивностью.
699. ВСМА-связывающая молекула, содержащая:
(a) первый полипептид, содержащий:
(i) константный домен первой тяжелой цепи, содержащий первый Fc-участок;
(ii) scFv, содержащий вариабельный домен легкой цепи scFv, линкер для scFv и вариабельный домен тяжелой цепи scFv; где scFv ковалентно соединен с N-концом первого Fc-участка посредством шарнирного участка;
(b) второй полипептид, содержащий:
(i) вариабельный домен тяжелой цепи;
(ii) константный домен второй тяжелой цепи, содержащий второй Fc-участок; и
(c) третий полипептид, содержащий константный домен легкой цепи и вариабельный домен легкой цепи;
где
A. первый и второй Fc-участки образуют Fc-домен;
B. первый и второй Fc-участки содержат набор аминокислотных замен, предусматривающий S364K/E357Q : L368D/370S, например, где первый Fc-участок содержит замены S364K/E357Q, а второй Fc-участок содержит замены L368D/370S;
C. первый и/или второй Fc-участки содержат аминокислотные модификации E223P, L234V, L235A, G236del, S267K, например, где первый и второй Fc-участки содержат аминокислотные модификации E223P, L234V, L235A, G236del, S267K;
D. первый и/или второй Fc-участки содержат аминокислотные замены N208D, Q295E, N384D, Q418E и N421D, например, где второй Fc-участок, но не первый Fc-участок, содержит аминокислотные замены N208D, Q295E, N384D, Q418E и N421D;
E. вариабельный домен тяжелой цепи второго полипептида и вариабельный домен легкой цепи третьего полипептида содержат последовательности CDR из AB1, как представлено в таблице 1C-1 и таблице 1C-2, таблице 1D-1 и таблице 1D-2, таблице 1E-1 и таблице 1E-2, таблице 1F-1 и таблице 1F-2, таблице 1G-1 и таблице 1G-2 или таблице 1H-1 и таблице 1H-2; и
F. scFv связывает CD3 человека.
700. ВСМА-связывающая молекула по варианту осуществления 699, где вариабельный домен легкой цепи третьего полипептида и домен тяжелой цепи второго полипептида содержат последовательности вариабельного домена легкой цепи и вариабельного домена тяжелой цепи из AB1, как представлено в таблице 1O-1 и таблице 1O-2.
701. ВСМА-связывающая молекула, содержащая:
(a) первый полипептид, содержащий:
(i) константный домен первой тяжелой цепи, содержащий первый Fc-участок;
(ii) scFv, содержащий вариабельный домен легкой цепи scFv, линкер для scFv и вариабельный домен тяжелой цепи scFv; где scFv ковалентно соединен с N-концом первого Fc-участка посредством шарнирного участка;
(b) второй полипептид, включающий вторую тяжелую цепь, содержащую:
(i) вариабельный домен тяжелой цепи;
(ii) константный домен второй тяжелой цепи, содержащий второй Fc-участок; и
(c) третий полипептид, содержащий константный домен легкой цепи и вариабельный домен легкой цепи;
где
A. первый и второй Fc-участки образуют Fc-домен;
B. первый и второй Fc-участки содержат набор аминокислотных замен, предусматривающий S364K/E357Q : L368D/370S, например, где первый Fc-участок содержит замены S364K/E357Q, а второй Fc-участок содержит замены L368D/370S;
C. первый и/или второй Fc-участки содержат аминокислотные модификации E223P, L234V, L235A, G236del, S267K, например, где первый и второй Fc-участки содержат аминокислотные модификации E223P, L234V, L235A, G236del, S267K;
D. первый и/или второй Fc-участки содержат аминокислотные замены N208D, Q295E, N384D, Q418E и N421D, например, где второй Fc-участок, но не первый Fc-участок, содержит аминокислотные замены N208D, Q295E, N384D, Q418E и N421D;
E. вариабельный домен тяжелой цепи второго полипептида и вариабельный домен легкой цепи третьего полипептида содержат последовательности CDR из AB2, как представлено в таблице 1C-1 и таблице 1C-2, таблице 1D-1 и таблице 1D-2, таблице 1E-1 и таблице 1E-2, таблице 1F-1 и таблице 1F-2, таблице 1G-1 и таблице 1G-2 или таблице 1H-1 и таблице 1H-2; и
F. scFv связывает CD3 человека.
702. ВСМА-связывающая молекула по варианту осуществления 701, где вариабельный домен легкой цепи третьего полипептида и домен тяжелой цепи второго полипептида содержат последовательности вариабельного домена легкой цепи и вариабельного домена тяжелой цепи из AB2, как представлено в таблице 1O-1 и таблице 1O-2.
703. ВСМА-связывающая молекула, содержащая:
(a) первый полипептид, содержащий:
(i) константный домен первой тяжелой цепи, содержащий первый Fc-участок;
(ii) scFv, содержащий вариабельный домен легкой цепи scFv, линкер для scFv и вариабельный домен тяжелой цепи scFv; где scFv ковалентно соединен с N-концом первого Fc-участка посредством шарнирного участка;
(b) второй полипептид, включающий вторую тяжелую цепь, содержащую:
(i) вариабельный домен тяжелой цепи;
(ii) константный домен второй тяжелой цепи, содержащий второй Fc-участок; и
(c) третий полипептид, содержащий константный домен легкой цепи и вариабельный домен легкой цепи;
где
A. первый и второй Fc-участки образуют Fc-домен;
B. первый и второй Fc-участки содержат набор аминокислотных замен, предусматривающий S364K/E357Q : L368D/370S, например, где первый Fc-участок содержит замены S364K/E357Q, а второй Fc-участок содержит замены L368D/370S;
C. первый и/или второй Fc-участки содержат аминокислотные модификации E223P, L234V, L235A, G236del, S267K, например, где первый и второй Fc-участки содержат аминокислотные модификации E223P, L234V, L235A, G236del, S267K;
D. первый и/или второй Fc-участки содержат аминокислотные замены N208D, Q295E, N384D, Q418E и N421D, например, где второй Fc-участок, но не первый Fc-участок, содержит аминокислотные замены N208D, Q295E, N384D, Q418E и N421D;
E. вариабельный домен тяжелой цепи второго полипептида и вариабельный домен легкой цепи третьего полипептида содержат последовательности CDR из AB3, как представлено в таблице 1I-1 и таблице 1I-2, таблице 1J-1 и таблице 1J-2, таблице 1K-1(a) и таблице 1K-2, таблице 1K-1(b) и таблице 1K-2, таблице 1L-1 и таблице 1L-2, таблице 1M-1 и таблице 1M-2 или таблице 1N-1 и таблице 1N-2; и
F. scFv связывает CD3 человека.
704. ВСМА-связывающая молекула по варианту осуществления 703, где вариабельный домен легкой цепи третьего полипептида и домен тяжелой цепи второго полипептида содержат последовательности вариабельного домена легкой цепи и вариабельного домена тяжелой цепи из AB3, как представлено в таблице 1O-1 и таблице 1O-2.
705. ВСМА-связывающая молекула по любому из вариантов осуществления 699-704, где вариабельный домен легкой цепи scFv и вариабельный домен тяжелой цепи scFv содержат вариабельный домен легкой цепи и вариабельный домен тяжелой цепи из CD3-23, как представлено в таблице 3A.
706. ВСМА-связывающая молекула по любому из вариантов осуществления 699-705, где аминокислотная последовательность линкера для scFv выбрана из аминокислотных последовательностей, представленных в таблице 10.
707. ВСМА-связывающая молекула по варианту осуществления 706, где линкер scFv содержит аминокислотную последовательность линкера, обозначенного как L36.
708. ВСМА-связывающая молекула, содержащая:
(a) первый полипептид, содержащий:
(i) константный домен первой тяжелой цепи, содержащий первый Fc-участок;
(ii) scFv, содержащий аминокислотную последовательность scFv, обозначенного как CD3-23 в таблице 3A; где scFv ковалентно соединен с N-концом первого Fc-участка посредством шарнирного участка;
(b) второй полипептид, содержащий:
(i) вариабельный домен тяжелой цепи;
(ii) константный домен второй тяжелой цепи, содержащий второй Fc-участок; и
(c) третий полипептид, содержащий константный домен легкой цепи и вариабельный домен легкой цепи;
где
A. первый и второй Fc-участки образуют Fc-домен;
B. первый и второй Fc-участки содержат набор аминокислотных замен, предусматривающий S364K/E357Q : L368D/370S, например, где первый Fc-участок содержит замены S364K/E357Q, а второй Fc-участок содержит замены L368D/370S;
C. первый и/или второй Fc-участки содержат аминокислотные модификации E223P, L234V, L235A, G236del, S267K, например, где первый и второй Fc-участки содержат аминокислотные модификации E223P, L234V, L235A, G236del, S267K;
D. первый и/или второй Fc-участки содержат аминокислотные замены N208D, Q295E, N384D, Q418E и N421D, например, где второй Fc-участок, но не первый Fc-участок, содержит аминокислотные замены N208D, Q295E, N384D, Q418E и N421D;
E. вариабельный домен легкой цепи и вариабельный домен тяжелой цепи содержат последовательности вариабельного домена легкой цепи и вариабельного домена тяжелой цепи из AB1, как представлено в таблице 1O-1 и таблице 1O-2.
709. ВСМА-связывающая молекула, содержащая:
(a) первый полипептид, содержащий:
(i) константный домен первой тяжелой цепи, содержащий первый Fc-участок;
(ii) scFv, содержащий аминокислотную последовательность scFv, обозначенного как CD3-23 в таблице 3A; где scFv ковалентно соединен с N-концом первого Fc-участка посредством шарнирного участка;
(b) второй полипептид, содержащий:
(i) вариабельный домен тяжелой цепи;
(ii) константный домен второй тяжелой цепи, содержащий второй Fc-участок; и
(c) третий полипептид, содержащий константный домен легкой цепи и вариабельный домен легкой цепи;
где
A. первый и второй Fc-участки образуют Fc-домен;
B. первый и второй Fc-участки содержат набор аминокислотных замен, предусматривающий S364K/E357Q : L368D/370S, например, где первый Fc-участок содержит замены S364K/E357Q, а второй Fc-участок содержит замены L368D/370S;
C. первый и/или второй Fc-участки содержат аминокислотные модификации E223P, L234V, L235A, G236del, S267K, например, где первый и второй Fc-участки содержат аминокислотные модификации E223P, L234V, L235A, G236del, S267K;
D. первый и/или второй Fc-участки содержат аминокислотные замены N208D, Q295E, N384D, Q418E и N421D, например, где второй Fc-участок, но не первый Fc-участок, содержит аминокислотные замены N208D, Q295E, N384D, Q418E и N421D;
E. вариабельный домен легкой цепи и вариабельный домен тяжелой цепи содержат последовательности вариабельного домена легкой цепи и вариабельного домена тяжелой цепи из AB2, как представлено в таблице 1O-1 и таблице 1O-2.
710. ВСМА-связывающая молекула, содержащая:
(a) первый полипептид, содержащий:
(i) константный домен первой тяжелой цепи, содержащий первый Fc-участок;
(ii) scFv, содержащий аминокислотную последовательность scFv, обозначенного как CD3-23 в таблице 3A; где scFv ковалентно соединен с N-концом первого Fc-участка посредством шарнирного участка;
(b) второй полипептид, содержащий:
(i) вариабельный домен тяжелой цепи;
(ii) константный домен второй тяжелой цепи, содержащий второй Fc-участок; и
(c) третий полипептид, содержащий константный домен легкой цепи и вариабельный домен легкой цепи;
где
A. первый и второй Fc-участки образуют Fc-домен;
B. первый и второй Fc-участки содержат набор аминокислотных замен, предусматривающий S364K/E357Q : L368D/370S, например, где первый Fc-участок содержит замены S364K/E357Q, а второй Fc-участок содержит замены L368D/370S;
C. первый и/или второй Fc-участки содержат аминокислотные модификации E223P, L234V, L235A, G236del, S267K, например, где первый и второй Fc-участки содержат аминокислотные модификации E223P, L234V, L235A, G236del, S267K;
D. первый и/или второй Fc-участки содержат аминокислотные замены N208D, Q295E, N384D, Q418E и N421D, например, где второй Fc-участок, но не первый Fc-участок, содержит аминокислотные замены N208D, Q295E, N384D, Q418E и N421D;
E. вариабельный домен легкой цепи и вариабельный домен тяжелой цепи содержат последовательности вариабельного домена легкой цепи и вариабельного домена тяжелой цепи из AB3, как представлено в таблице 1O-1 и таблице 1O-2.
711. ВСМА-связывающая молекула, содержащая полипептиды, содержащие аминокислотные последовательности из бивалентного AB1, или состоящая из них, как представлено в таблице 11A.
712. ВСМА-связывающая молекула, содержащая полипептиды, содержащие аминокислотные последовательности из тривалентного AB1, или состоящая из них, как представлено в таблице 11B.
713. ВСМА-связывающая молекула, содержащая полипептиды, содержащие аминокислотные последовательности из бивалентного AB2, или состоящая из них, как представлено в таблице 11C.
714. ВСМА-связывающая молекула, содержащая полипептиды, содержащие аминокислотные последовательности из тривалентного AB2, или состоящая из них, как представлено в таблице 11D.
715. ВСМА-связывающая молекула, содержащая полипептиды, содержащие аминокислотные последовательности из бивалентного AB3, или состоящая из них, как представлено в таблице 11E.
716. ВСМА-связывающая молекула, содержащая полипептиды, содержащие аминокислотные последовательности из тривалентного AB3, или состоящая из них, как представлено в таблице 11F.
717. ВСМА-связывающая молекула по любому из вариантов осуществления 1-716 для применения в качестве лекарственного препарата.
718. ВСМА-связывающая молекула по любому из вариантов осуществления 1-716 для применения для лечения заболевания или нарушения, связанного с экспрессией ВСМА.
719. ВСМА-связывающая молекула по варианту осуществления 718, где заболевание или нарушение включает рак.
720. ВСМА-связывающая молекула по варианту осуществления 719, где рак включает В-клеточное злокачественное новообразование.
721. ВСМА-связывающая молекула по варианту осуществления 720, где В-клеточное злокачественное новообразование представляет собой лимфому Ходжкина, неходжкинскую лимфому или множественную миелому.
722. ВСМА-связывающая молекула по варианту осуществления 719, где рак представляет собой лимфому Ходжкина.
723. ВСМА-связывающая молекула по варианту осуществления 722, где лимфома Ходжкина представляет собой лимфому Ходжкина с нодулярным склерозом.
724. ВСМА-связывающая молекула по варианту осуществления 722, где лимфома Ходжкина представляет собой лимфому Ходжкина смешанноклеточного подтипа.
725. ВСМА-связывающая молекула по варианту осуществления 722, где лимфома Ходжкина представляет собой богатую лимфоцитами лимфому Ходжкина или лимфому Ходжкина с лимфоидным преобладанием.
726. ВСМА-связывающая молекула по варианту осуществления 722, где лимфома Ходжкина представляет собой лимфому Ходжкина с лимфоидным истощением.
727. ВСМА-связывающая молекула по варианту осуществления 719, где рак представляет собой неходжкинскую лимфому.
728. ВСМА-связывающая молекула по варианту осуществления 727, где неходжкинская лимфома представляет собой В-клеточную лимфому или Т-клеточную лимфому.
729. ВСМА-связывающая молекула по варианту осуществления 727, где неходжкинская лимфома представляет собой В-клеточную лимфому.
730. ВСМА-связывающая молекула по варианту осуществления 727, где неходжкинская лимфома представляет собой диффузную крупноклеточную В-клеточную лимфому (DLBCL), фолликулярную лимфому, хронический лимфоцитарный лейкоз (CLL)/мелкоклеточную лимфоцитарную лимфому (SLL), мантийноклеточную лимфому (MCL), лимфому из клеток маргинальной зоны, лимфому Беркитта, лимфоплазмоцитарную лимфому (макроглобулинемию Вальденстрема), волосатоклеточный лейкоз, первичную лимфому центральной нервной системы (CNS), первичную медиастинальную крупноклеточную В-клеточную лимфому, медиастинальную лимфому серой зоны (MGZL), B-клеточную лимфому из клеток маргинальной зоны селезенки, внеузловую B-клеточную лимфому из клеток маргинальной зоны MALT, узловую B-клеточную лимфому из клеток маргинальной зоны или первичную эффузионную лимфому.
731. ВСМА-связывающая молекула по варианту осуществления 730, где неходжкинская лимфома представляет собой диффузную крупноклеточную В-клеточную лимфому (DLBCL).
732. ВСМА-связывающая молекула по варианту осуществления 730, где неходжкинская лимфома представляет собой фолликулярную лимфому.
733. ВСМА-связывающая молекула по варианту осуществления 730, где неходжкинская лимфома представляет собой хронический лимфоцитарный лейкоз (CLL)/мелкоклеточную лимфоцитарную лимфому (SLL).
734. ВСМА-связывающая молекула по варианту осуществления 730, где неходжкинская лимфома представляет собой мантийноклеточную лимфому (MCL).
735. ВСМА-связывающая молекула по варианту осуществления 730, где неходжкинская лимфома представляет собой лимфому из клеток маргинальной зоны.
736. ВСМА-связывающая молекула по варианту осуществления 730, где неходжкинская лимфома представляет собой лимфому Беркитта.
737. ВСМА-связывающая молекула по варианту осуществления 730, где неходжкинская лимфома представляет собой лимфоплазмоцитарную лимфому (макроглобулинемию Вальденстрема).
738. ВСМА-связывающая молекула по варианту осуществления 730, где неходжкинская лимфома представляет собой волосатоклеточный лейкоз.
739. ВСМА-связывающая молекула по варианту осуществления 730, где неходжкинская лимфома представляет собой первичную лимфому центральной нервной системы (CNS).
740. ВСМА-связывающая молекула по варианту осуществления 730, где неходжкинская лимфома представляет собой первичную медиастинальную крупноклеточную В-клеточную лимфому.
741. ВСМА-связывающая молекула по варианту осуществления 730, где неходжкинская лимфома представляет собой медиастинальную лимфому серой зоны (MGZL).
742. ВСМА-связывающая молекула по варианту осуществления 730, где неходжкинская лимфома представляет собой B-клеточную лимфому из клеток маргинальной зоны селезенки.
743. ВСМА-связывающая молекула по варианту осуществления 730, где неходжкинская лимфома представляет собой внеузловую B-клеточную лимфому из клеток маргинальной зоны MALT.
744. ВСМА-связывающая молекула по варианту осуществления 730, где неходжкинская лимфома представляет собой узловую B-клеточную лимфому из клеток маргинальной зоны.
745. ВСМА-связывающая молекула по варианту осуществления 730, где неходжкинская лимфома представляет собой первичную эффузионную лимфому.
746. ВСМА-связывающая молекула по варианту осуществления 727, где неходжкинская лимфома представляет собой T-клеточную лимфому.
747. ВСМА-связывающая молекула по варианту осуществления 746, где неходжкинская лимфома представляет собой анапластическую крупноклеточную лимфому (ALCL), Т-клеточную лимфому/лейкоз взрослых, ангиоцентрическую лимфому, ангиоиммунобластную Т-клеточную лимфому, Т-клеточную лимфому кожи, внеузловую лимфому из естественных киллеров/T-клеток, Т-клеточную лимфому кишечника энтеропатического типа, T-лимфобластную лимфому/лейкоз из клеток-предшественников (T-LBL/L) или неуточненную периферическую Т-клеточную лимфому.
748. ВСМА-связывающая молекула по варианту осуществления 747, где неходжкинская лимфома представляет собой анапластическую крупноклеточную лимфому (ALCL).
749. ВСМА-связывающая молекула по варианту осуществления 747, где неходжкинская лимфома представляет собой Т-клеточную лимфому/лейкоз взрослых.
750. ВСМА-связывающая молекула по варианту осуществления 747, где неходжкинская лимфома представляет собой ангиоцентрическую лимфому.
751. ВСМА-связывающая молекула по варианту осуществления 747, где неходжкинская лимфома представляет собой ангиоиммунобластную Т-клеточную лимфому.
752. ВСМА-связывающая молекула по варианту осуществления 747, где неходжкинская лимфома представляет собой Т-клеточную лимфому кожи.
753. ВСМА-связывающая молекула по варианту осуществления 747, где неходжкинская лимфома представляет собой внеузловую лимфому из естественных киллеров/T-клеток.
754. ВСМА-связывающая молекула по варианту осуществления 747, где неходжкинская лимфома представляет собой Т-клеточную лимфому кишечника энтеропатического типа.
755. ВСМА-связывающая молекула по варианту осуществления 747, где неходжкинская лимфома представляет собой T-лимфобластную лимфому/лейкоз из клеток-предшественников (T-LBL/L).
756. ВСМА-связывающая молекула по варианту осуществления 747, где неходжкинская лимфома представляет собой неуточненную периферическую Т-клеточную лимфому.
757. ВСМА-связывающая молекула по варианту осуществления 719, где рак представляет собой множественную миелому.
758. ВСМА-связывающая молекула по варианту осуществления 719, где рак представляет собой новообразование из плазмоцитарных дендритных клеток.
759. ВСМА-связывающая молекула по варианту осуществления 719, где рак включает лейкоз.
760. BCMA-связывающая молекула по варианту осуществления 759, где лейкоз представляет собой В-клеточный острый лимфоидный лейкоз ("BALL"), T-клеточный острый лимфоидный лейкоз ("TALL"), острый лимфоидный лейкоз (ALL), хронический миелогенный лейкоз (CML), хронический лимфоцитарный лейкоз (CLL), B-клеточный хронический лимфоцитарный лейкоз (B-CLL), B-клеточный пролимфоцитарный лейкоз (B-PLL), волосатоклеточный лейкоз, плазмоцитому/миелому, B-лимфобластный лейкоз/лимфому из клеток-предшественников (PB-LBL/L), лейкоз из больших гранулярных лимфоцитов, Т-лимфобластную лимфому/лейкоз из клеток-предшественников (T-LBL/L), Т-клеточный хронический лимфоцитарный лейкоз/пролимфоцитарный лейкоз (T-CLL/PLL).
761. ВСМА-связывающая молекула по варианту осуществления 760, где лейкоз представляет собой В-клеточный острый лимфоидный лейкоз ("BALL").
762. ВСМА-связывающая молекула по варианту осуществления 760, где лейкоз представляет собой T-клеточный острый лимфоидный лейкоз ("TALL").
763. ВСМА-связывающая молекула по варианту осуществления 760, где лейкоз представляет собой острый лимфоидный лейкоз (ALL).
764. ВСМА-связывающая молекула по варианту осуществления 760, где лейкоз представляет собой хронический миелогенный лейкоз (CML).
765. ВСМА-связывающая молекула по варианту осуществления 760, где лейкоз представляет собой хронический лимфоцитарный лейкоз (CLL).
766. ВСМА-связывающая молекула по варианту осуществления 760, где лейкоз представляет собой B-клеточный хронический лимфоцитарный лейкоз (B-CLL).
767. ВСМА-связывающая молекула по варианту осуществления 760, где лейкоз представляет собой B-клеточный пролимфоцитарный лейкоз (B-PLL).
768. ВСМА-связывающая молекула по варианту осуществления 760, где лейкоз представляет собой волосатоклеточный лейкоз.
769. ВСМА-связывающая молекула по варианту осуществления 760, где лейкоз представляет собой плазмоцитому/миелому.
770. ВСМА-связывающая молекула по варианту осуществления 760, где лейкоз представляет собой B-лимфобластный лейкоз/лимфому из клеток-предшественников (PB-LBL/L).
771. ВСМА-связывающая молекула по варианту осуществления 760, где лейкоз представляет собой лейкоз из больших гранулярных лимфоцитов.
772. ВСМА-связывающая молекула по варианту осуществления 760, где лейкоз представляет собой T-лимфобластную лимфому/лейкоз из клеток-предшественников.
773. ВСМА-связывающая молекула по варианту осуществления 760, где лейкоз представляет собой Т-клеточный хронический лимфоцитарный лейкоз/пролимфоцитарный лейкоз (T-CLL/PLL).
774. ВСМА-связывающая молекула по варианту осуществления 719, где рак представляет собой рак головного мозга.
775. ВСМА-связывающая молекула по варианту осуществления 774, где рак головного мозга представляет собой астроцитому или глиобластому.
776. ВСМА-связывающая молекула по варианту осуществления 775, рак головного мозга представляет собой астроцитому.
777. ВСМА-связывающая молекула по варианту осуществления 775, где рак головного мозга представляет собой глиобластому.
778. ВСМА-связывающая молекула по варианту осуществления 719, где рак представляет собой рак предстательной железы.
779. ВСМА-связывающая молекула по варианту осуществления 778, где рак предстательной железы представляет собой резистентный к кастрации рак предстательной железы.
780. ВСМА-связывающая молекула по варианту осуществления 778, где рак предстательной железы представляет собой резистентный к терапии рак предстательной железы.
781. ВСМА-связывающая молекула по варианту осуществления 778, где рак предстательной железы представляет собой метастатический рак предстательной железы.
782. ВСМА-связывающая молекула по варианту осуществления 719, где рак представляет собой рак поджелудочной железы.
783. ВСМА-связывающая молекула по варианту осуществления 719, где рак представляет собой рак легкого.
784. ВСМА-связывающая молекула по варианту осуществления 718, где заболевание или нарушение включает новообразование из плазматических клеток.
785. ВСМА-связывающая молекула по варианту осуществления 784, где новообразование из плазматических клеток включает тлеющую множественную миелому (SMM) или моноклональную гаммапатию неясного генеза (MGUS)
786. ВСМА-связывающая молекула по варианту осуществления 785, где новообразование из плазматических клеток включает тлеющую множественную миелому (SMM).
787. ВСМА-связывающая молекула по варианту осуществления 785, где новообразование из плазматических клеток включает моноклональную гаммапатию неясного генеза (MGUS).
788. ВСМА-связывающая молекула по варианту осуществления 718, где заболевание или нарушение включает плазмоцитому.
789. ВСМА-связывающая молекула по варианту осуществления 788, где плазмоцитома представляет собой плазмоклеточную дискразию, солитарную миелому, солитарную плазмоцитому, экстрамедуллярную плазмоцитому и множественную плазмоцитому.
790. ВСМА-связывающая молекула по варианту осуществления 788, где плазмоцитома представляет собой плазмоклеточную дискразию.
791. ВСМА-связывающая молекула по варианту осуществления 788, где плазмоцитома представляет собой солитарную миелому.
792. ВСМА-связывающая молекула по варианту осуществления 788, где плазмоцитома представляет собой солитарную плазмоцитому.
793. ВСМА-связывающая молекула по варианту осуществления 788, где плазмоцитома представляет собой экстрамедуллярную плазмоцитому.
794. ВСМА-связывающая молекула по варианту осуществления 788, где плазмоцитома представляет собой множественную плазмоцитому.
795. ВСМА-связывающая молекула по варианту осуществления 718, где заболевание или нарушение включает системный амилоидоз в форме амилоидоза легких цепей.
796. ВСМА-связывающая молекула по варианту осуществления 718, где заболевание или нарушение включает POEMS-синдром.
797. ВСМА-связывающая молекула по варианту осуществления 718, где заболевание или нарушение представляет собой инфекцию.
798. ВСМА-связывающая молекула по варианту осуществления 797, где инфекция представляет собой вирусную инфекцию.
799. ВСМА-связывающая молекула по варианту осуществления 798, где вирусная инфекция представляет собой HIV-инфекцию.
800. ВСМА-связывающая молекула по варианту осуществления 797, где инфекция представляет собой грибковую инфекцию.
801. ВСМА-связывающая молекула по варианту осуществления 800, где грибковая инфекция представляет собой инфекцию, вызванную C. neoformans.
802. ВСМА-связывающая молекула по варианту осуществления 718, где заболевание или нарушение представляет собой аутоиммунное нарушение.
803. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой системную красную волчанку (SLE), синдром Шегрена, склеродермию, ревматоидный артрит (RA), ювенильный идиопатический артрит, реакцию "трансплантат против хозяина", дерматомиозит, сахарный диабет I типа, тиреоидит Хашимото, болезнь Грейвса, болезнь Аддисона, целиакию, болезнь Крона, злокачественную анемию, обыкновенную пузырчатку, витилиго, аутоиммунную гемолитическую анемию, идиопатическую тромбоцитопеническую пурпуру, гигантоклеточный артериит, тяжелую миастению, рассеянный склероз (MS) (например, рецидивирующе-ремиттирующий MS (RRMS)), гломерулонефрит, синдром Гудпасчера, буллезный пемфигоид, язвенный колит, синдром Гийена-Барре, хроническую воспалительную демиелинизирующую полинейропатию, антифосфолипидный синдром, нарколепсию, саркоидоз или гранулематоз Вегенера.
804. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой системную красную волчанку (SLE).
805. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой синдром Шегрена.
806. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой склеродермию.
807. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой ревматоидный артрит (RA).
808. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой ювенильный идиопатический артрит.
809. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой реакцию "трансплантат против хозяина".
810. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой дерматомиозит.
811. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой сахарный диабет I типа.
812. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой тиреоидит Хашимото.
813. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой болезнь Грейвса.
814. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой болезнь Аддисона.
815. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой целиакию.
816. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой болезнь Крона.
817. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой злокачественную анемию.
818. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой обыкновенную пузырчатку.
819. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой витилиго.
820. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой аутоиммунную гемолитическую анемию.
821. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой идиопатическую тромбоцитопеническую пурпуру.
822. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой гигантоклеточный артериит.
823. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой тяжелую миастению.
824. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой рассеянный склероз (MS).
825. ВСМА-связывающая молекула по варианту осуществления 802, где MS представляет собой рецидивирующе-ремиттирующий MS (RRMS).
826. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой гломерулонефрит.
827. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой синдром Гудпасчера.
828. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой буллезный пемфигоид.
829. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой язвенный колит.
830. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой синдром Гийена-Барре.
831. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой хроническую воспалительную демиелинизирующую полинейропатию.
832. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой антифосфолипидный синдром.
833. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой нарколепсию.
834. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой саркоидоз.
835. ВСМА-связывающая молекула по варианту осуществления 802, где аутоиммунное нарушение представляет собой гранулематоз Вегенера.
836. Конъюгат, содержащий ВСМА-связывающую молекулу по любому из вариантов осуществления 1-716 и фрагмент, который увеличивает период полужизни ВСМА-связывающей молекулы in vivo.
837. Конъюгат по варианту осуществления 836, где фрагмент представляет собой любой из фрагментов, описанных в разделе 7.8.
838. Конъюгат по варианту осуществления 836 или варианту осуществления 837, где фрагмент включает полиэтиленгликоль, полипептид, углевод, жирную кислоту или любую их комбинацию.
839. Конъюгат по варианту осуществления 838, где фрагмент включает полиэтиленгликоль.
840. Конъюгат по варианту осуществления 838, где фрагмент включает полипептид.
841. Конъюгат по варианту осуществления 840, где полипептид включает альбумин, необязательно сывороточный альбумин человека.
842. Конъюгат по варианту осуществления 838, где фрагмент включает углевод.
843. Конъюгат по варианту осуществления 842, где углевод включает полисиаловую кислоту.
844. Конъюгат по варианту осуществления 842, где углевод включает производное гидроксиэтилкрахмала (HES).
845. Конъюгат по варианту осуществления 838, где фрагмент включает жирную кислоту.
846. Конъюгат, содержащий ВСМА-связывающую молекулу по любому из вариантов осуществления 1-716, или конъюгат по любому из вариантов осуществления 836-845 и диагностическое или выявляемое средство.
847. Конъюгат по варианту осуществления 846, где диагностическое или выявляемое средство представляет собой любое из средств, описанных в разделе 7.10.
848. Конъюгат по варианту осуществления 846 или варианту осуществления 847, где диагностическое или выявляемое средство включает фермент.
849. Конъюгат по варианту осуществления 846 или варианту осуществления 847, где диагностическое или выявляемое средство включает флуоресцентный краситель.
850. Конъюгат по варианту осуществления 846 или варианту осуществления 847, где диагностическое или выявляемое средство включает радионуклид.
851. Конъюгат, содержащий ВСМА-связывающую молекулу по любому из вариантов осуществления 1-716 или конъюгат по любому из вариантов осуществления 836-850 и средство, необязательно терапевтическое средство, диагностическое средство, маскирующий фрагмент, расщепляемый фрагмент или любую их комбинацию.
852. Конъюгат по варианту осуществления 851, где средство представляет собой цитотоксическое или цитостатическое средство.
853. Конъюгат по варианту осуществления 852, где средство представляет собой любое из средств, описанных в разделе 7.9.
854. Конъюгат по варианту осуществления 852 или 853, где средство представляет собой любое из средств, описанных в разделе 7.9.1.
855. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с радионуклидом.
856. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с алкилирующим средством.
857. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с ингибитором топоизомеразы, который необязательно представляет собой ингибитор топоизомеразы I или ингибитор топоизомеразы II.
858. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована со средством, повреждающим ДНК.
859. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с ДНК-интеркалирующим средством, необязательно средством, связывающимся с бороздкой, таким как средство, связывающееся с малой бороздкой.
860. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с антиметаболитом РНК/ДНК.
861. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с ингибитором киназы.
862. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с ингибитором синтеза белка.
863. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с ингибитором гистондеацетилазы (HDAC).
864. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с митохондриальным ингибитором, который необязательно представляет собой ингибитор реакции переноса фосфорильной группы в митохондриях.
865. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с антимитотическим средством.
866. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с майтанзиноидом.
867. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с ингибитором кинезина.
868. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с ингибитором кинезин-подобного белка KIF11.
869. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с ингибитором V-АТФазы (Н+-АТФазы вакуолярного типа).
870. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с проапоптотическим средством.
871. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с ингибитором Bcl2 (белка B-клеточной лимфомы 2).
872. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с ингибитором MCL1 (белка 1 миелоидноклеточного лейкоза).
873. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с ингибитором HSP90 (белка теплового шока 90).
874. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с ингибитором IAP (ингибитором апоптоза).
875. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с ингибитором mTOR (механистической мишени рапамицина).
876. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована со стабилизатором микротрубочек.
877. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с дестабилизатором микротрубочек.
878. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с ауристатином.
879. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с доластатином.
880. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с MetAP (метионинаминопептидазой).
881. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с ингибитором CRM1 (белка поддержания структуры хромосом 1).
882. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с ингибитором DPPIV (дипептидилпептидазы IV).
883. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с ингибитором протеасомы.
884. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с ингибитором синтеза белка.
885. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с ингибитором CDK2 (циклин-зависимой киназы 2).
886. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с ингибитором CDK9 (циклин-зависимой киназы 9).
887. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с ингибитором РНК-полимеразы.
888. Конъюгат по любому из вариантов осуществления 851-854, где BCMA-связывающая молекула конъюгирована с ингибитором DHFR (дигидрофолатредуктазы).
889. Конъюгат по любому из вариантов осуществления 851-888, где средство присоединено к BCMA-связывающей молекуле с помощью линкера, который необязательно представляет собой расщепляемый линкер или нерасщепляемый линкер, например, линкер, описанный в разделе 7.9.2.
890. Конъюгат, содержащий ВСМА-связывающую молекулу по любому из вариантов осуществления 1-716 или конъюгат по любому из вариантов осуществления 836-889 и твердую подложку.
891. Конъюгат по варианту осуществления 890, где твердая подложка включает стекло, целлюлозу, полиакриламид, нейлон, полистирол, поливинилхлорид, полипропилен или любую их комбинацию.
892. Фармацевтическая композиция, содержащая ВСМА-связывающую молекулу по любому из вариантов осуществления 1-716 или конъюгат по любому из вариантов осуществления 836-889 и фармацевтически приемлемое вспомогательное вещество.
893. Способ лечения субъекта, у которого имеется заболевание или нарушение, связанное с экспрессией BCMA, включающий введение субъекту эффективного количества BCMA-связывающей молекулы по любому из вариантов осуществления 1-716, конъюгата по любому из вариантов осуществления 836-889 или фармацевтической композиции по варианту осуществления 892.
894. Способ по варианту осуществления 893, где заболевание или нарушение включает рак.
895. Способ по варианту осуществления 894, где рак включает В-клеточное злокачественное новообразование.
896. Способ по варианту осуществления 895, где В-клеточное злокачественное новообразование представляет собой лимфому Ходжкина, неходжкинскую лимфому или множественную миелому.
897. Способ по варианту осуществления 894, где рак представляет собой лимфому Ходжкина.
898. Способ по варианту осуществления 897, где лимфома Ходжкина представляет собой лимфому Ходжкина с нодулярным склерозом.
899. Способ по варианту осуществления 897, где лимфома Ходжкина представляет собой лимфому Ходжкина смешанноклеточного подтипа.
900. Способ по варианту осуществления 897, где лимфома Ходжкина представляет собой богатую лимфоцитами лимфому Ходжкина или лимфому Ходжкина с лимфоидным преобладанием.
901. Способ по варианту осуществления 897, где лимфома Ходжкина представляет собой лимфому Ходжкина с лимфоидным истощением.
902. Способ по варианту осуществления 894, где рак представляет собой неходжкинскую лимфому.
903. Способ по варианту осуществления 902, где неходжкинская лимфома представляет собой В-клеточную лимфому или Т-клеточную лимфому.
904. Способ по варианту осуществления 903, где неходжкинская лимфома представляет собой B-клеточную лимфому.
905. Способ по варианту осуществления 904, где неходжкинская лимфома представляет собой диффузную крупноклеточную В-клеточную лимфому (DLBCL), фолликулярную лимфому, хронический лимфоцитарный лейкоз (CLL)/мелкоклеточную лимфоцитарную лимфому (SLL), мантийноклеточную лимфому (MCL), лимфому из клеток маргинальной зоны, лимфому Беркитта, лимфоплазмоцитарную лимфому (макроглобулинемию Вальденстрема), волосатоклеточный лейкоз, первичную лимфому центральной нервной системы (CNS), первичную медиастинальную крупноклеточную В-клеточную лимфому, медиастинальную лимфому серой зоны (MGZL), B-клеточную лимфому из клеток маргинальной зоны селезенки, внеузловую B-клеточную лимфому из клеток маргинальной зоны MALT, узловую B-клеточную лимфому из клеток маргинальной зоны или первичную эффузионную лимфому.
906. Способ по варианту осуществления 905, где неходжкинская лимфома представляет собой диффузную крупноклеточную В-клеточную лимфому (DLBCL).
907. Способ по варианту осуществления 905, где неходжкинская лимфома представляет собой фолликулярную лимфому.
908. Способ по варианту осуществления 905, где неходжкинская лимфома представляет собой хронический лимфоцитарный лейкоз (CLL)/мелкоклеточную лимфоцитарную лимфому (SLL).
909. Способ по варианту осуществления 905, где неходжкинская лимфома представляет собой мантийноклеточную лимфому (MCL).
910. Способ по варианту осуществления 905, где неходжкинская лимфома представляет собой лимфому из клеток маргинальной зоны.
911. Способ по варианту осуществления 905, где неходжкинская лимфома представляет собой лимфому Беркитта.
912. Способ по варианту осуществления 905, где неходжкинская лимфома представляет собой лимфоплазмоцитарную лимфому (макроглобулинемию Вальденстрема).
913. Способ по варианту осуществления 905, где неходжкинская лимфома представляет собой волосатоклеточный лейкоз.
914. Способ по варианту осуществления 905, где неходжкинская лимфома представляет собой первичную лимфому центральной нервной системы (CNS).
915. Способ по варианту осуществления 905, где неходжкинская лимфома представляет собой первичную медиастинальную крупноклеточную В-клеточную лимфому.
916. Способ по варианту осуществления 905, где неходжкинская лимфома представляет собой медиастинальную лимфому серой зоны (MGZL).
917. Способ по варианту осуществления 905, где неходжкинская лимфома представляет собой B-клеточную лимфому из клеток маргинальной зоны селезенки.
918. Способ по варианту осуществления 905, где неходжкинская лимфома представляет собой внеузловую B-клеточную лимфому из клеток маргинальной зоны MALT.
919. Способ по варианту осуществления 905, где неходжкинская лимфома представляет собой узловую B-клеточную лимфому из клеток маргинальной зоны.
920. Способ по варианту осуществления 905, где неходжкинская лимфома представляет собой первичную эффузионную лимфому.
921. Способ по варианту осуществления 903, где неходжкинская лимфома представляет собой T-клеточную лимфому.
922. Способ по варианту осуществления 921, где неходжкинская лимфома представляет собой анапластическую крупноклеточную лимфому (ALCL), Т-клеточную лимфому/лейкоз взрослых, ангиоцентрическую лимфому, ангиоиммунобластную Т-клеточную лимфому, Т-клеточную лимфому кожи, внеузловую лимфому из естественных киллеров/T-клеток, Т-клеточную лимфому кишечника энтеропатического типа, T-лимфобластную лимфому/лейкоз из клеток-предшественников (T-LBL/L) или неуточненную периферическую Т-клеточную лимфому.
923. Способ по варианту осуществления 922, где неходжкинская лимфома представляет собой анапластическую крупноклеточную лимфому (ALCL).
924. Способ по варианту осуществления 922, где неходжкинская лимфома представляет собой Т-клеточную лимфому/лейкоз взрослых.
925. Способ по варианту осуществления 922, где неходжкинская лимфома представляет собой ангиоцентрическую лимфому.
926. Способ по варианту осуществления 922, где неходжкинская лимфома представляет собой ангиоиммунобластную Т-клеточную лимфому.
927. Способ по варианту осуществления 922, где неходжкинская лимфома представляет собой Т-клеточную лимфому кожи.
928. Способ по варианту осуществления 922, где неходжкинская лимфома представляет собой внеузловую лимфому из естественных киллеров/T-клеток.
929. Способ по варианту осуществления 922, где неходжкинская лимфома представляет собой Т-клеточную лимфому кишечника энтеропатического типа.
930. Способ по варианту осуществления 922, где неходжкинская лимфома представляет собой T-лимфобластную лимфому/лейкоз из клеток-предшественников (T-LBL/L).
931. Способ по варианту осуществления 922, где неходжкинская лимфома представляет собой неуточненную периферическую Т-клеточную лимфому.
932. Способ по варианту осуществления 894, где рак представляет собой множественную миелому.
933. Способ по варианту осуществления 894, где рак представляет собой новообразование из плазмоцитарных дендритных клеток.
934. Способ по варианту осуществления 894, где рак включает лейкоз.
935. Способ по варианту осуществления 934, где лейкоз представляет собой В-клеточный острый лимфоидный лейкоз ("BALL"), T-клеточный острый лимфоидный лейкоз ("TALL"), острый лимфоидный лейкоз (ALL), хронический миелогенный лейкоз (CML), хронический лимфоцитарный лейкоз (CLL), B-клеточный хронический лимфоцитарный лейкоз (B-CLL), B-клеточный пролимфоцитарный лейкоз (B-PLL), волосатоклеточный лейкоз, плазмоцитому/миелому, B-лимфобластный лейкоз/лимфому из клеток-предшественников (PB-LBL/L), лейкоз из больших гранулярных лимфоцитов, Т-лимфобластную лимфому/лейкоз из клеток-предшественников (T-LBL/L), Т-клеточный хронический лимфоцитарный лейкоз/пролимфоцитарный лейкоз (T-CLL/PLL).
936. Способ по варианту осуществления 934, где лейкоз представляет собой В-клеточный острый лимфоидный лейкоз ("BALL").
937. Способ по варианту осуществления 934, где лейкоз представляет собой T-клеточный острый лимфоидный лейкоз ("TALL").
938. Способ по варианту осуществления 934, где лейкоз представляет собой острый лимфоидный лейкоз (ALL).
939. Способ по варианту осуществления 934, где лейкоз представляет собой хронический миелогенный лейкоз (CML).
940. Способ по варианту осуществления 934, где лейкоз представляет собой хронический лимфоцитарный лейкоз (CLL).
941. Способ по варианту осуществления 934, где лейкоз представляет собой B-клеточный хронический лимфоцитарный лейкоз (B-CLL).
942. Способ по варианту осуществления 934, где лейкоз представляет собой B-клеточный пролимфоцитарный лейкоз (B-PLL).
943. Способ по варианту осуществления 934, где лейкоз представляет собой волосатоклеточный лейкоз.
944. Способ по варианту осуществления 934, где лейкоз представляет собой плазмоцитому/миелому.
945. Способ по варианту осуществления 934, где лейкоз представляет собой B-лимфобластный лейкоз/лимфому из клеток-предшественников (PB-LBL/L).
946. Способ по варианту осуществления 934, где лейкоз представляет собой лейкоз из больших гранулярных лимфоцитов.
947. Способ по варианту осуществления 934, где лейкоз представляет собой T-лимфобластную лимфому/лейкоз из клеток-предшественников (T-LBL/L).
948. Способ по варианту осуществления 934, где лейкоз представляет собой Т-клеточный хронический лимфоцитарный лейкоз/пролимфоцитарный лейкоз (T-CLL/PLL).
949. Способ по варианту осуществления 894, где рак представляет собой рак головного мозга.
950. Способ по варианту осуществления 949, где рак головного мозга представляет собой астроцитому или глиобластому.
951. Способ по варианту осуществления 950, где рак головного мозга представляет собой астроцитому.
952. Способ по варианту осуществления 950, где рак головного мозга представляет собой глиобластому.
953. Способ по варианту осуществления 894, где рак представляет собой рак предстательной железы.
954. Способ по варианту осуществления 953, где рак предстательной железы представляет собой резистентный к кастрации рак предстательной железы.
955. Способ по варианту осуществления 953, где рак предстательной железы представляет собой резистентный к терапии рак предстательной железы.
956. Способ по варианту осуществления 953, где рак предстательной железы представляет собой метастатический рак предстательной железы.
957. Способ по варианту осуществления 894, где рак представляет собой рак поджелудочной железы.
958. Способ по варианту осуществления 894, где рак представляет собой рак легкого.
959. Способ по варианту осуществления 893, где заболевание или нарушение включает новообразование из плазматических клеток.
960. Способ по варианту осуществления 959, где новообразование из плазматических клеток включает тлеющую множественную миелому (SMM) или моноклональную гаммапатию неясного генеза (MGUS)
961. Способ по варианту осуществления 960, где новообразование из плазматических клеток включает тлеющую множественную миелому (SMM).
962. Способ по варианту осуществления 960, где новообразование из плазматических клеток включает моноклональную гаммапатию неясного генеза (MGUS).
963. Способ по варианту осуществления 893, где заболевание или нарушение включает плазмоцитому.
964. Способ по варианту осуществления 963, где плазмоцитома представляет собой плазмоклеточную дискразию, солитарную миелому, солитарную плазмоцитому, экстрамедуллярную плазмоцитому и множественную плазмоцитому.
965. Способ по варианту осуществления 963, где плазмоцитома представляет собой плазмоклеточную дискразию.
966. Способ по варианту осуществления 963, где плазмоцитома представляет собой солитарную миелому.
967. Способ по варианту осуществления 963, где плазмоцитома представляет собой солитарную плазмоцитому.
968. Способ по варианту осуществления 963, где плазмоцитома представляет собой экстрамедуллярную плазмоцитому.
969. Способ по варианту осуществления 963, где плазмоцитома представляет собой множественную плазмоцитому.
970. Способ по варианту осуществления 893, где заболевание или нарушение включает системный амилоидоз в форме амилоидоза легких цепей.
971. Способ по варианту осуществления 893, где заболевание или нарушение включает POEMS-синдром.
972. Способ по любому из вариантов осуществления 893-971, дополнительно включающий введение по меньшей мере одного дополнительного средства субъекту.
973. Способ по варианту осуществления 972, где дополнительное средство представляет собой химиотерапевтическое средство.
974. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой антрациклин.
975. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой алкалоид барвинка.
976. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой алкилирующее средство.
977. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой антитело ко клеткам иммунной системы.
978. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой антиметаболит.
979. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой ингибитор аденозиндезаминазы.
980. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой ингибитор mTOR.
981. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой агонист глюкокортикоид-индуцируемого TNFR-родственного белка (GITR).
982. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой ингибитор протеасомы.
983. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой миметик BH3.
984. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой цитокин.
985. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство предотвращает или замедляет отщепление BCMA от раковой клетки.
986. Способ по варианту осуществления 985, где дополнительное средство включает ингибитор ADAM10 и/или ингибитор ADAM 17.
987. Способ по варианту осуществления 985, где дополнительное средство включает ингибитор фосфолипазы.
988. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой ингибитор гамма-секретазы (GSI).
989. Способ по варианту осуществления 988, где GSI представляет собой BMS-986115.
990. Способ по варианту осуществления 988, где GSI представляет собой BMS-906024.
991. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство является иммуномодулирующим.
992. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой производное талидомида.
993. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой ингибитор EGFR.
994. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой антагонист рецептора аденозина А2А.
995. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой ингибитор CD20.
996. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой ингибитор CD22.
997. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой ингибитор FCRL2.
998. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой ингибитор FCRL5.
999. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой комплекс IL-15/IL15-Ra.
1000. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой ингибитор PD-1.
1001. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой ингибитор PD-L1.
1002. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой ингибитор LAG-3.
1003. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой ингибитор TIM-3.
1004. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой ингибитор TGF-β.
1005. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой ингибитор CD73.
1006. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой ингибитор IL-17.
1007. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой ингибитор CD32B.
1008. Способ по варианту осуществления 972 или варианту осуществления 973, где дополнительное средство представляет собой средство, выбранное из средств, перечисленных в таблице A.
1009. Способ по варианту осуществления 972, где дополнительное средство представляет собой средство, которое снижает или ослабляет побочный эффект, связанный с введением ВСМА-связывающей молекулы, которая является биспецифической по отношению к ВСМА и CD3.
1010. Способ по варианту осуществления 1009, где дополнительное средство включает
стероид (например, кортикостероид), ингибитор TNFα (например, молекулу антитела к TNFα, такую как инфликсимаб, адалимумаб, цертолизумаб пегол или голимумаб, слитый белок, такой как этанерцепт, низкомолекулярный ингибитор TNFα, такой как производное ксантина (например, пентоксифиллин) или бупропион), ингибитор IL-6 (например, молекулу антитела к IL-6, такую как тоцилизумаб (toc), сарилумаб, элсилимомаб, CNTO 328, ALD518/BMS-945429, CNTO 136, CPSI-2364, CDP6038, VX30, ARGX-109, FE301 или FM101), ингибитор на основе IL-1R, такой как анакинра, кортикостероид (например, метилпреднизолон или гидрокортизон) в комбинации с бенадрилом и тайленолом, вазопрессор (например, норэпинефрин, дофамин, фенилэфрин, эпинефрин, вазопрессин или любую их комбинацию), жаропонижающее средство или анальгезирующее средство.
1011. Способ по любому из вариантов осуществления 972-1010, где дополнительное средство не представляет собой антитело.
1012. Способ по варианту осуществления 893, где заболевание или нарушение представляет собой инфекцию.
1013. Способ по варианту осуществления 1012, где инфекция представляет собой вирусную инфекцию.
1014. Способ по варианту осуществления 1013, где вирусная инфекция представляет собой HIV-инфекцию.
1015. Способ по варианту осуществления 1012, где инфекция представляет собой грибковую инфекцию.
1016. Способ по варианту осуществления 1015, где грибковая инфекция представляет собой инфекцию, вызванную C. neoformans.
1017. Способ по варианту осуществления 893, где заболевание или нарушение представляет собой аутоиммунное нарушение.
1018. Способ по варианту осуществления 1017, где аутоиммунное нарушение представляет собой системную красную волчанку (SLE), синдром Шегрена, склеродермию, ревматоидный артрит (RA), ювенильный идиопатический артрит, реакцию "трансплантат против хозяина", дерматомиозит, сахарный диабет I типа, тиреоидит Хашимото, болезнь Грейвса, болезнь Аддисона, целиакию, болезнь Крона, злокачественную анемию, обыкновенную пузырчатку, витилиго, аутоиммунную гемолитическую анемию, идиопатическую тромбоцитопеническую пурпуру, гигантоклеточный артериит, тяжелую миастению, рассеянный склероз (MS) (например, рецидивирующе-ремиттирующий MS (RRMS)), гломерулонефрит, синдром Гудпасчера, буллезный пемфигоид, язвенный колит, синдром Гийена-Барре, хроническую воспалительную демиелинизирующую полинейропатию, антифосфолипидный синдром, нарколепсию, саркоидоз или гранулематоз Вегенера.
1019. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой системную красную волчанку (SLE).
1020. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой синдром Шегрена.
1021. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой склеродермию.
1022. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой ревматоидный артрит (RA).
1023. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой ювенильный идиопатический артрит.
1024. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой реакцию "трансплантат против хозяина".
1025. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой дерматомиозит.
1026. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой сахарный диабет I типа.
1027. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой тиреоидит Хашимото.
1028. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой болезнь Грейвса.
1029. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой болезнь Аддисона.
1030. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой целиакию.
1031. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой болезнь Крона.
1032. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой злокачественную анемию.
1033. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой обыкновенную пузырчатку.
1034. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой витилиго.
1035. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой аутоиммунную гемолитическую анемию.
1036. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой идиопатическую тромбоцитопеническую пурпуру.
1037. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой гигантоклеточный артериит.
1038. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой тяжелую миастению.
1039. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой рассеянный склероз (MS).
1040. Способ по варианту осуществления 1039, где MS представляет собой рецидивирующе-ремиттирующий MS (RRMS).
1041. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой гломерулонефрит.
1042. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой синдром Гудпасчера.
1043. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой буллезный пемфигоид.
1044. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой язвенный колит.
1045. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой синдром Гийена-Барре.
1046. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой хроническую воспалительную демиелинизирующую полинейропатию.
1047. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой антифосфолипидный синдром.
1048. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой нарколепсию.
1049. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой саркоидоз.
1050. Способ по варианту осуществления 1018, где аутоиммунное нарушение представляет собой гранулематоз Вегенера.
1051. Нуклеиновая кислота или совокупность нуклеиновых кислот, кодирующие BCMA-связывающую молекулу по любому из вариантов осуществления 1-716.
1052. Нуклеиновая кислота или совокупность нуклеиновых кислот по варианту осуществления 1051, которые представляют собой ДНК.
1053. Нуклеиновая кислота или совокупность нуклеиновых кислот по варианту осуществления 1051, которые представляют собой мРНК.
1054. Клетка, сконструированная для экспрессии BCMA-связывающей молекулы по любому из вариантов осуществления 1-716.
1055. Клетка, трансфицированная одним или несколькими векторами экспрессии, содержащими одну или несколько последовательностей нуклеиновой кислоты, кодирующих BCMA-связывающую молекулу по любому из вариантов осуществления 1-716 или конъюгат по любому из вариантов осуществления 717-889 под контролем одного или нескольких промоторов.
1056. Клетка по варианту осуществления 1054 или варианту осуществления 1055, где экспрессия BCMA-связывающей молекулы находится под контролем индуцибельного промотора.
1057. Клетка по любому из вариантов осуществления 1054-1056, где BCMA-связывающая молекула продуцируется в секретируемой форме.
1058. Способ получения BCMA-связывающей молекулы, включающий:
(a) культивирование клетки по любому из вариантов осуществления 1054-1057 в условиях, при которых экспрессируется BCMA-связывающая молекула; и
(b) извлечение BCMA-связывающей молекулы из культуры клеток.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> NOVARTIS AG
<120> МОЛЕКУЛЫ, СВЯЗЫВАЮЩИЕ BCMA, И ПУТИ ИХ ПРИМЕНЕНИЯ
<130> NOV-003WO
<140>
<141>
<150> 62/684,046
<151> 2018-06-12
<150> 62/679,611
<151> 2018-06-01
<160> 603
<170> PatentIn версия 3.5
<210> 1
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 1
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 2
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 2
Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn
1 5 10
<210> 3
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 3
Ser Gln Ser Ile Ser Ser Tyr
1 5
<210> 4
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 4
Gln Ser Ile Ser Ser Tyr
1 5
<210> 5
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 5
Ala Ala Ser Ser Leu Gln Ser
1 5
<210> 6
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 6
Ala Ala Ser
1
<210> 7
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="T"
<220>
<221> Сайт
<222> (1)..(9)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 7
Gln Gln Ser Tyr Ser Ser Pro Leu Thr
1 5
<210> 8
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="G" или "D" или "Y" или "A"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="T" или "A"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="L"
<220>
<221> Сайт
<222> (1)..(9)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 8
Gln Gln Ser Tyr Ser Ser Pro Pro Thr
1 5
<210> 9
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="T"
<220>
<221> Сайт
<222> (1)..(6)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 9
Ser Tyr Ser Ser Pro Leu
1 5
<210> 10
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="G" или "D" или "Y" или "A"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="T" или "A"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="L"
<220>
<221> Сайт
<222> (1)..(6)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 10
Ser Tyr Ser Ser Pro Pro
1 5
<210> 11
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 11
Ser Tyr Ala Met Ser
1 5
<210> 12
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 12
Gly Phe Thr Phe Ser Ser Tyr
1 5
<210> 13
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 13
Gly Phe Thr Phe Ser Ser Tyr Ala
1 5
<210> 14
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 14
Gly Phe Thr Phe Ser Ser Tyr Ala Met Ser
1 5 10
<210> 15
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="E"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="R"
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> /замена="A"
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /замена="A"
<220>
<221> Сайт
<222> (1)..(17)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 15
Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 16
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="E" или "A"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="A" или "H" или "E"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="D" или "E" или "H" или "R" или "A"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="R" или "V" или "T" или "Y"
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> /замена="A" или "E" или "H" или "R"
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /замена="A" или "S"
<220>
<221> Сайт
<222> (1)..(17)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 16
Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 17
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /замена="E"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="R"
<220>
<221> Сайт
<222> (1)..(6)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 17
Ser Gly Ser Gly Gly Ser
1 5
<210> 18
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /замена="E" или "A"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="A" или "H" или "E"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="D" или "E" или "H" или "R" или "A"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="R" или "V" или "T" или "Y"
<220>
<221> Сайт
<222> (1)..(6)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 18
Ser Gly Ser Gly Gly Ser
1 5
<210> 19
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="E"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="R"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="A"
<220>
<221> Сайт
<222> (1)..(8)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 19
Ile Ser Gly Ser Gly Gly Ser Thr
1 5
<210> 20
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="E" или "A"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="A" или "H" или "E"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="D" или "E" или "H" или "R" или "A"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="R" или "V" или "T" или "Y"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="A" или "E" или "H" или "R"
<220>
<221> Сайт
<222> (1)..(8)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 20
Ile Ser Gly Ser Gly Gly Ser Thr
1 5
<210> 21
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="E" или "A"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="A" или "H" или "E"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="D" или "E" или "H" или "R" или "A"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="R" или "V" или "T" или "Y"
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> /замена="A" или "E" или "H" или "R"
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /замена="A" или "S"
<220>
<221> Сайт
<222> (1)..(17)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 21
Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 22
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="E"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="R"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="A"
<220>
<221> Сайт
<222> (1)..(8)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 22
Ile Ser Gly Ser Gly Gly Ser Thr
1 5
<210> 23
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="E" или "A"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="A" или "H" или "E"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="D" или "E" или "H" или "R" или "A"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="R" или "V" или "T" или "Y"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="A" или "E" или "H" или "R"
<220>
<221> Сайт
<222> (1)..(8)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 23
Ile Ser Gly Ser Gly Gly Ser Thr
1 5
<210> 24
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 24
Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr
1 5 10
<210> 25
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 25
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr
1 5 10
<210> 26
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 26
Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr Asn Tyr Val Ser
1 5 10
<210> 27
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 27
Thr Ser Ser Asp Val Gly Gly Tyr Asn Tyr
1 5 10
<210> 28
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 28
Ser Ser Asp Val Gly Gly Tyr Asn Tyr
1 5
<210> 29
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="P"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="S"
<220>
<221> Сайт
<222> (1)..(7)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 29
Asp Val Ser Asn Arg Leu Arg
1 5
<210> 30
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена="E"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="P" или "A"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="S" или "G" или "W"
<220>
<221> Сайт
<222> (1)..(7)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 30
Asp Val Ser Asn Arg Leu Arg
1 5
<210> 31
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 31
Asp Val Ser
1
<210> 32
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена="E"
<220>
<221> Сайт
<222> (1)..(3)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 32
Asp Val Ser
1
<210> 33
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="P"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="S"
<220>
<221> Сайт
<222> (1)..(10)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 33
Asp Val Ser Asn Arg Leu Arg Gly Val Ser
1 5 10
<210> 34
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена="E"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="P" или "A"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="S" или "G" или "W"
<220>
<221> Сайт
<222> (1)..(10)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 34
Asp Val Ser Asn Arg Leu Arg Gly Val Ser
1 5 10
<210> 35
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="P"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="S"
<220>
<221> Сайт
<222> (1)..(10)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 35
Asp Val Ser Asn Arg Leu Arg Gly Val Ser
1 5 10
<210> 36
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена="E"
<220>
<221> Сайт
<222> (1)..(3)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 36
Asp Val Ser
1
<210> 37
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="T"
<220>
<221> Сайт
<222> (1)..(11)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 37
Ser Ser Tyr Thr Ser Ser Ser Ala Leu Tyr Val
1 5 10
<210> 38
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="T"
<220>
<221> Сайт
<222> (1)..(8)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 38
Tyr Thr Ser Ser Ser Ala Leu Tyr
1 5
<210> 39
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 39
Ser Tyr Gly Met His
1 5
<210> 40
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="F"
<220>
<221> Сайт
<222> (1)..(7)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 40
Gly Phe Thr Val Ser Ser Tyr
1 5
<210> 41
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="F"
<220>
<221> Сайт
<222> (1)..(8)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 41
Gly Phe Thr Val Ser Ser Tyr Gly
1 5
<210> 42
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="F"
<220>
<221> Сайт
<222> (1)..(10)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 42
Gly Phe Thr Val Ser Ser Tyr Gly Met His
1 5 10
<210> 43
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="D"
<220>
<221> Сайт
<222> (1)..(17)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 43
Val Ile Ser Tyr Thr Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 44
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="K" или "T" или "R" или "D" или "N" или "S"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="D" или "E"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="T" или "F" или "A" или "L"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="N" или "K"
<220>
<221> Сайт
<222> (1)..(17)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 44
Val Ile Ser Tyr His Gly Ser His Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 45
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="D"
<220>
<221> Сайт
<222> (1)..(6)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 45
Ser Tyr Thr Gly Ser Asn
1 5
<210> 46
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="K" или "T" или "R" или "D" или "N" или "S"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="D" или "E"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="T" или "F" или "A" или "L"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="N" или "K"
<220>
<221> Сайт
<222> (1)..(8)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 46
Ser Tyr His Gly Ser His Lys Gly
1 5
<210> 47
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="D"
<220>
<221> Сайт
<222> (1)..(8)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 47
Ile Ser Tyr Thr Gly Ser Asn Lys
1 5
<210> 48
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="K" или "T" или "R" или "D" или "N" или "S"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="D" или "E"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="T" или "F" или "A" или "L"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="N" или "K"
<220>
<221> Сайт
<222> (1)..(8)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 48
Ile Ser Tyr His Gly Ser His Lys
1 5
<210> 49
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 49
Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
1 5 10
<210> 50
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="N" или "E"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="F" или "V" или "Y"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Q" или "R" или "D"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="E" или "G" или "Q"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="Q" или "F"
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> /замена="Q"
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /замена="K" или "D"
<220>
<221> ВАРИАНТ
<222> (11)..(11)
<223> /замена="P"
<220>
<221> ВАРИАНТ
<222> (12)..(12)
<223> /замена="Q" или "V" или "T"
<220>
<221> Сайт
<222> (1)..(14)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 50
Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
1 5 10
<210> 51
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 51
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
1 5 10 15
<210> 52
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="N" или "E"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="F" или "V" или "Y"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="Q" или "R" или "D"
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> /замена="E" или "G" или "Q"
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /замена="Q" или "F"
<220>
<221> ВАРИАНТ
<222> (11)..(11)
<223> /замена="Q"
<220>
<221> ВАРИАНТ
<222> (12)..(12)
<223> /замена="K" или "D"
<220>
<221> ВАРИАНТ
<222> (13)..(13)
<223> /замена="P"
<220>
<221> ВАРИАНТ
<222> (14)..(14)
<223> /замена="Q" или "V" или "T"
<220>
<221> Сайт
<222> (1)..(16)
<223> /примечание="Остатки вариантов, приведенные в
последовательности, не имеют предпочтения по отношению к тем, которые
указаны в аннотациях для положений вариантов"
<400> 52
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
1 5 10 15
<210> 53
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 53
Gln Gln Ser Tyr Ser Ser Pro Leu Thr
1 5
<210> 54
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 54
Gln Gln Ser Tyr Ser Thr Pro Leu Thr
1 5
<210> 55
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 55
Gln Gln Ser Tyr Gly Ser Pro Pro Thr
1 5
<210> 56
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 56
Gln Gln Ser Tyr Asp Ser Pro Leu Thr
1 5
<210> 57
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 57
Gln Gln Ser Tyr Tyr Ser Pro Leu Thr
1 5
<210> 58
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 58
Gln Gln Ser Tyr Tyr Ala Pro Leu Thr
1 5
<210> 59
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 59
Gln Gln Ser Tyr Ala Ser Pro Leu Thr
1 5
<210> 60
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 60
Gln Gln Ser Tyr Gly Ser Pro Leu Thr
1 5
<210> 61
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 61
Gln Gln Ser Tyr Asp Ala Pro Leu Thr
1 5
<210> 62
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 62
Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 63
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 63
Ala Ile Ser Glu Ser Gly Gly Arg Ala Ala Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 64
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 64
Ala Ile Ser Gly Ser Gly Gly Arg Ala Ala Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 65
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 65
Ala Ile Ser Glu Ser Gly Asp Val Glu Ala Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 66
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 66
Ala Ile Ser Glu Ala Gly Glu Thr Thr Ser Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 67
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 67
Ala Ile Ser Glu His Gly His Tyr Thr Ser Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 68
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 68
Ala Ile Ser Gly Ser Gly His Thr Ala Ala Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 69
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 69
Ala Ile Ser Gly Ser Gly Arg Thr His Ala Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 70
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 70
Ala Ile Ser Ala Glu Gly Gly Val Arg Ala Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 71
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 71
Ala Ile Ser Gly Ser Gly Gly Thr Thr Ala Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 72
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 72
Ala Ile Ser Gly Ser Gly Ala Thr Thr Ala Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 73
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 73
Ser Tyr Ser Ser Pro Leu
1 5
<210> 74
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 74
Ser Tyr Ser Thr Pro Leu
1 5
<210> 75
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 75
Ser Tyr Gly Ser Pro Pro
1 5
<210> 76
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 76
Ser Tyr Asp Ser Pro Leu
1 5
<210> 77
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 77
Ser Tyr Tyr Ser Pro Leu
1 5
<210> 78
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 78
Ser Tyr Tyr Ala Pro Leu
1 5
<210> 79
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 79
Ser Tyr Ala Ser Pro Leu
1 5
<210> 80
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 80
Ser Tyr Gly Ser Pro Leu
1 5
<210> 81
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 81
Ser Tyr Asp Ala Pro Leu
1 5
<210> 82
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 82
Ser Gly Ser Gly Gly Ser
1 5
<210> 83
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 83
Ser Glu Ser Gly Gly Arg
1 5
<210> 84
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 84
Ser Gly Ser Gly Gly Arg
1 5
<210> 85
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 85
Ser Glu Ser Gly Asp Val
1 5
<210> 86
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 86
Ser Glu His Gly His Tyr
1 5
<210> 87
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 87
Ser Gly Ser Gly His Thr
1 5
<210> 88
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 88
Ser Gly Ser Gly Arg Thr
1 5
<210> 89
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 89
Ser Ala Glu Gly Gly Val
1 5
<210> 90
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 90
Ser Gly Ser Gly Gly Thr
1 5
<210> 91
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 91
Ser Gly Ser Gly Ala Thr
1 5
<210> 92
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 92
Ile Ser Gly Ser Gly Gly Ser Thr
1 5
<210> 93
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 93
Ile Ser Glu Ser Gly Gly Arg Ala
1 5
<210> 94
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 94
Ile Ser Gly Ser Gly Gly Arg Ala
1 5
<210> 95
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 95
Ile Ser Glu Ser Gly Asp Val Glu
1 5
<210> 96
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 96
Ile Ser Glu His Gly His Tyr Thr
1 5
<210> 97
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 97
Ile Ser Gly Ser Gly His Thr Ala
1 5
<210> 98
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 98
Ile Ser Gly Ser Gly Arg Thr His
1 5
<210> 99
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 99
Ile Ser Ala Glu Gly Gly Val Arg
1 5
<210> 100
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 100
Ile Ser Gly Ser Gly Gly Thr Thr
1 5
<210> 101
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 101
Ile Ser Gly Ser Gly Ala Thr Thr
1 5
<210> 102
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 102
Asp Val Ser Asn Arg Leu Arg
1 5
<210> 103
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 103
Asp Val Ser Asn Arg Pro Ser
1 5
<210> 104
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 104
Glu Val Ser Asn Arg Leu Ser
1 5
<210> 105
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 105
Glu Val Ser Asn Arg Leu Arg
1 5
<210> 106
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 106
Asp Val Ser Asn Arg Pro Trp
1 5
<210> 107
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 107
Asp Val Ser Asn Arg Leu Ser
1 5
<210> 108
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 108
Asp Val Ser Asn Arg Ala Trp
1 5
<210> 109
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 109
Glu Val Ser Asn Arg Leu Gly
1 5
<210> 110
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 110
Ser Ser Tyr Thr Ser Ser Ser Ala Leu Tyr Val
1 5 10
<210> 111
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 111
Ser Ser Tyr Thr Ser Ser Ser Thr Leu Tyr Val
1 5 10
<210> 112
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 112
Val Ile Ser Tyr Thr Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 113
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 113
Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 114
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 114
Val Ile Ser Tyr His Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 115
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 115
Val Ile Ser Tyr Lys Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 116
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 116
Val Ile Ser Tyr Thr Gly Thr Lys Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 117
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 117
Val Ile Ser Tyr Arg Gly Phe Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 118
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 118
Val Ile Ser Tyr Lys Gly Ser His Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 119
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 119
Val Ile Ser Tyr Asp Asp Ala His Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 120
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 120
Val Ile Ser Tyr Asn Asp Leu Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 121
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 121
Val Ile Ser Tyr Ser Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 122
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 122
Val Ile Ser Tyr Thr Gly Ala Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 123
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 123
Val Ile Ser Tyr Asn Asp Ala Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 124
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 124
Val Ile Ser Tyr Asp Glu Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 125
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 125
Val Ile Ser Tyr Asp Asp Ala Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 126
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 126
Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Gln Asp Val
1 5 10
<210> 127
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 127
Ser Gly Tyr Ala Leu His Asp Gln Tyr Lys Pro Val Asp Val
1 5 10
<210> 128
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 128
Ser Gly Tyr Ala Leu His Asp Phe Gln Asp Pro Thr Asp Val
1 5 10
<210> 129
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 129
Ser Gly Tyr Asn Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
1 5 10
<210> 130
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 130
Ser Gly Tyr Glu Phe His Glu Asp Tyr Tyr Gly Leu Asp Val
1 5 10
<210> 131
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 131
Ser Gly Tyr Glu Phe Gln Gly Asp Tyr Tyr Gly Leu Asp Val
1 5 10
<210> 132
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 132
Ser Gly Tyr Glu Leu Arg Asp Asp Tyr Tyr Gly Leu Asp Val
1 5 10
<210> 133
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 133
Ser Gly Tyr Glu Val Asp Gln Asp Tyr Tyr Gly Leu Asp Val
1 5 10
<210> 134
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 134
Ser Gly Tyr Ala Tyr Asp Gly Asp Tyr Tyr Gly Leu Asp Val
1 5 10
<210> 135
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 135
Glu Val Ser
1
<210> 136
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 136
Tyr Thr Ser Ser Ser Ala Leu Tyr
1 5
<210> 137
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 137
Tyr Thr Ser Ser Ser Thr Leu Tyr
1 5
<210> 138
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 138
Gly Phe Thr Val Ser Ser Tyr
1 5
<210> 139
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 139
Gly Phe Thr Leu Ser Ser Tyr
1 5
<210> 140
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 140
Ser Tyr Thr Gly Ser Asn
1 5
<210> 141
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 141
Ser Tyr Asp Gly Ser Asn
1 5
<210> 142
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 142
Ser Tyr His Gly Ser Asn
1 5
<210> 143
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 143
Ser Tyr Lys Gly Ser Asn
1 5
<210> 144
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 144
Ser Tyr Thr Gly Thr Lys
1 5
<210> 145
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 145
Ser Tyr Arg Gly Phe Asn
1 5
<210> 146
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 146
Ser Tyr Lys Gly Ser His
1 5
<210> 147
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 147
Ser Tyr Asp Asp Ala His
1 5
<210> 148
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 148
Ser Tyr Asn Asp Leu Asn
1 5
<210> 149
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 149
Ser Tyr Ser Gly Ser Asn
1 5
<210> 150
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 150
Ser Tyr Thr Gly Ala Asn
1 5
<210> 151
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 151
Ser Tyr Asn Asp Ala Asn
1 5
<210> 152
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 152
Ser Tyr Asp Glu Ser Asn
1 5
<210> 153
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 153
Ser Tyr Asp Asp Ala Asn
1 5
<210> 154
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 154
Asp Val Ser Asn Arg Leu Arg Gly Val Ser
1 5 10
<210> 155
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 155
Asp Val Ser Asn Arg Pro Ser Gly Val Ser
1 5 10
<210> 156
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 156
Glu Val Ser Asn Arg Leu Ser Gly Val Ser
1 5 10
<210> 157
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 157
Glu Val Ser Asn Arg Leu Arg Gly Val Ser
1 5 10
<210> 158
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 158
Asp Val Ser Asn Arg Pro Trp Gly Val Ser
1 5 10
<210> 159
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 159
Asp Val Ser Asn Arg Leu Ser Gly Val Ser
1 5 10
<210> 160
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 160
Asp Val Ser Asn Arg Ala Trp Gly Val Ser
1 5 10
<210> 161
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 161
Glu Val Ser Asn Arg Leu Gly Gly Val Ser
1 5 10
<210> 162
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 162
Gly Phe Thr Val Ser Ser Tyr Gly
1 5
<210> 163
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 163
Gly Phe Thr Phe Ser Ser Tyr Gly
1 5
<210> 164
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 164
Gly Phe Thr Leu Ser Ser Tyr Gly
1 5
<210> 165
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 165
Ile Ser Tyr Thr Gly Ser Asn Lys
1 5
<210> 166
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 166
Ile Ser Tyr Asp Gly Ser Asn Lys
1 5
<210> 167
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 167
Ile Ser Tyr His Gly Ser Asn Lys
1 5
<210> 168
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 168
Ile Ser Tyr Lys Gly Ser Asn Lys
1 5
<210> 169
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 169
Ile Ser Tyr Thr Gly Thr Lys Lys
1 5
<210> 170
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 170
Ile Ser Tyr Arg Gly Phe Asn Lys
1 5
<210> 171
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 171
Ile Ser Tyr Lys Gly Ser His Lys
1 5
<210> 172
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 172
Ile Ser Tyr Asp Asp Ala His Lys
1 5
<210> 173
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 173
Ile Ser Tyr Asn Asp Leu Asn Lys
1 5
<210> 174
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 174
Ile Ser Tyr Ser Gly Ser Asn Lys
1 5
<210> 175
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 175
Ile Ser Tyr Thr Gly Ala Asn Lys
1 5
<210> 176
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 176
Ile Ser Tyr Asn Asp Ala Asn Lys
1 5
<210> 177
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 177
Ile Ser Tyr Asp Glu Ser Asn Lys
1 5
<210> 178
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 178
Ile Ser Tyr Asp Asp Ala Asn Lys
1 5
<210> 179
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 179
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Gln Asp Val
1 5 10 15
<210> 180
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 180
Gly Gly Ser Gly Tyr Ala Leu His Asp Gln Tyr Lys Pro Val Asp Val
1 5 10 15
<210> 181
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 181
Gly Gly Ser Gly Tyr Ala Leu His Asp Phe Gln Asp Pro Thr Asp Val
1 5 10 15
<210> 182
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 182
Gly Gly Ser Gly Tyr Asn Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
1 5 10 15
<210> 183
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 183
Gly Gly Ser Gly Tyr Glu Phe His Glu Asp Tyr Tyr Gly Leu Asp Val
1 5 10 15
<210> 184
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 184
Gly Gly Ser Gly Tyr Glu Phe Gln Gly Asp Tyr Tyr Gly Leu Asp Val
1 5 10 15
<210> 185
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 185
Gly Gly Ser Gly Tyr Glu Leu Arg Asp Asp Tyr Tyr Gly Leu Asp Val
1 5 10 15
<210> 186
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 186
Gly Gly Ser Gly Tyr Glu Val Asp Gln Asp Tyr Tyr Gly Leu Asp Val
1 5 10 15
<210> 187
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 187
Gly Gly Ser Gly Tyr Ala Tyr Asp Gly Asp Tyr Tyr Gly Leu Asp Val
1 5 10 15
<210> 188
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 188
Gly Phe Thr Val Ser Ser Tyr Gly Met His
1 5 10
<210> 189
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 189
Gly Phe Thr Phe Ser Ser Tyr Gly Met His
1 5 10
<210> 190
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 190
Gly Phe Thr Leu Ser Ser Tyr Gly Met His
1 5 10
<210> 191
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 191
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 192
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 192
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 193
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 193
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Gly Ser Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 194
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 194
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Asp Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 195
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 195
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Tyr Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 196
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 196
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Tyr Ala Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 197
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 197
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ala Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 198
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 198
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Gly Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 199
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 199
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Asp Ala Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 200
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 200
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Leu Arg Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Ala Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 201
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 201
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Thr Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 202
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 202
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Glu Val Ser Asn Arg Leu Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Thr Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 203
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 203
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Glu Val Ser Asn Arg Leu Arg Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Ala Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 204
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 204
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Glu Val Ser Asn Arg Leu Arg Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Thr Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 205
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 205
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Pro Trp Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Ala Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Met
100 105 110
<210> 206
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 206
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Leu Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Thr Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 207
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 207
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Pro Trp Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Thr Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 208
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 208
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Leu Arg Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Ala Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 209
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 209
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Ala Trp Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Ala Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 210
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 210
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Glu Val Ser Asn Arg Leu Arg Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Tyr Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Thr Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 211
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 211
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Glu Val Ser Asn Arg Leu Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Ala Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 212
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 212
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Glu Val Ser Asn Arg Leu Gly Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Ala Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 213
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 213
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 214
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 214
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Glu Ser Gly Gly Arg Ala Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 215
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 215
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Arg Ala Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 216
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 216
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Glu Ser Gly Asp Val Glu Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 217
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 217
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Glu Ala Gly Glu Thr Thr Ser Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 218
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 218
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Glu His Gly His Tyr Thr Ser Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 219
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 219
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly His Thr Ala Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 220
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 220
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Arg Thr His Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 221
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 221
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Ala Glu Gly Gly Val Arg Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 222
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 222
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Thr Thr Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 223
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 223
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Ala Thr Thr Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 224
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 224
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 225
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 225
Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 226
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 226
Gln Ala Gln Leu Gln Ser Ser Glu Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr His Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ser
115 120
<210> 227
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 227
Gln Val Gln Leu Gln Ser Ser Glu Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Lys Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 228
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 228
Gln Ala Gln Leu Gln Ser Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Lys Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 229
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 229
Gln Val Gln Leu Gln Asp Ser Glu Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Thr Lys Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 230
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 230
Gln Ala Gln Leu Gln Ser Ser Glu Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Arg Gly Phe Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Gln Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 231
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 231
Gln Ala Gln Leu Gln Gly Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Lys Gly Ser His Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 232
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 232
Gln Ala Gln Leu Gln Ser Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 233
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 233
Gln Val Gln Leu Gln Ser Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 234
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 234
Gln Ala Gln Leu Gln Gly Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Lys Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 235
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 235
Gln Val Gln Leu Gln Gly Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Asp Ala His Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Gln Tyr Lys Pro Val Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 236
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 236
Gln Ala Gln Leu Gln Glu Ser Glu Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asn Asp Leu Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Phe Gln Asp Pro Thr Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 237
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 237
Gln Val Gln Leu Gln Ser Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Ser Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Gln Tyr Lys Pro Val Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 238
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 238
Gln Val Gln Leu Gln Gly Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Ala Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Asn Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 239
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 239
Gln Ala Gln Leu Gln Arg Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Asp Ala His Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Gln Tyr Lys Pro Val Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 240
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 240
Gln Val Gln Leu Gln Ser Ser Glu Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Glu Phe His Glu Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 241
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 241
Gln Ala Gln Leu Gln Gly Ser Glu Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Asp Ala His Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Gln Tyr Lys Pro Val Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 242
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 242
Gln Val Gln Leu Gln Ser Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asn Asp Leu Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Glu Phe Gln Gly Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 243
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 243
Gln Val Gln Leu Gln Ser Ser Glu Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asn Asp Ala Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Glu Leu Arg Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 244
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 244
Gln Ala Gln Leu Gln Ser Ser Glu Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Glu Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Glu Val Asp Gln Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 245
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 245
Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Asp Ala His Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Gln Tyr Lys Pro Val Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 246
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 246
Gln Val Gln Leu Gln Gly Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Asp Ala Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Ser Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Tyr Asp Gly Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 247
<211> 255
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 247
Gln Val Gln Leu Gln Ser Ser Glu Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Lys Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
145 150 155 160
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
165 170 175
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
180 185 190
Met Ile Tyr Glu Val Ser Asn Arg Leu Arg Gly Val Ser Asn Arg Phe
195 200 205
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
210 215 220
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
225 230 235 240
Ser Ala Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
245 250 255
<210> 248
<211> 255
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 248
Gln Ala Gln Leu Gln Ser Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Lys Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
145 150 155 160
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
165 170 175
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
180 185 190
Met Ile Tyr Glu Val Ser Asn Arg Leu Arg Gly Val Ser Asn Arg Phe
195 200 205
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
210 215 220
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
225 230 235 240
Ser Thr Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
245 250 255
<210> 249
<211> 255
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 249
Gln Val Gln Leu Gln Asp Ser Glu Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Thr Lys Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
145 150 155 160
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
165 170 175
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
180 185 190
Met Ile Tyr Asp Val Ser Asn Arg Pro Trp Gly Val Ser Asn Arg Phe
195 200 205
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
210 215 220
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
225 230 235 240
Ser Ala Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Met
245 250 255
<210> 250
<211> 255
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 250
Gln Ala Gln Leu Gln Ser Ser Glu Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Arg Gly Phe Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Gln Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
145 150 155 160
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
165 170 175
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
180 185 190
Met Ile Tyr Asp Val Ser Asn Arg Leu Ser Gly Val Ser Asn Arg Phe
195 200 205
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
210 215 220
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
225 230 235 240
Ser Thr Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
245 250 255
<210> 251
<211> 255
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 251
Gln Ala Gln Leu Gln Gly Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Lys Gly Ser His Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
145 150 155 160
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
165 170 175
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
180 185 190
Met Ile Tyr Asp Val Ser Asn Arg Pro Trp Gly Val Ser Asn Arg Phe
195 200 205
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
210 215 220
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
225 230 235 240
Ser Thr Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
245 250 255
<210> 252
<211> 255
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 252
Gln Val Gln Leu Gln Ser Ser Glu Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Lys Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
145 150 155 160
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
165 170 175
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
180 185 190
Met Ile Tyr Asp Val Ser Asn Arg Pro Trp Gly Val Ser Asn Arg Phe
195 200 205
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
210 215 220
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
225 230 235 240
Ser Thr Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
245 250 255
<210> 253
<211> 255
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 253
Gln Ala Gln Leu Gln Ser Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
145 150 155 160
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
165 170 175
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
180 185 190
Met Ile Tyr Asp Val Ser Asn Arg Leu Arg Gly Val Ser Asn Arg Phe
195 200 205
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
210 215 220
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
225 230 235 240
Ser Ala Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
245 250 255
<210> 254
<211> 255
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 254
Gln Val Gln Leu Gln Ser Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
145 150 155 160
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
165 170 175
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
180 185 190
Met Ile Tyr Asp Val Ser Asn Arg Ala Trp Gly Val Ser Asn Arg Phe
195 200 205
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
210 215 220
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
225 230 235 240
Ser Ala Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
245 250 255
<210> 255
<211> 255
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 255
Gln Ala Gln Leu Gln Gly Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Lys Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
145 150 155 160
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
165 170 175
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
180 185 190
Met Ile Tyr Glu Val Ser Asn Arg Leu Arg Gly Val Ser Asn Arg Phe
195 200 205
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
210 215 220
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
225 230 235 240
Ser Thr Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
245 250 255
<210> 256
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 256
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Arg Tyr
20 25 30
Thr Met His Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Thr Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Tyr Asp Asp His Tyr Cys Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Leu Thr Val Ser Ser
115
<210> 257
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 257
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ala His Phe Arg Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Gly Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Phe Thr
85 90 95
Phe Gly Ser Gly Thr Lys Leu Glu Ile Asn
100 105
<210> 258
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 258
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Lys Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Asp Arg Phe Thr Ile Ser Arg Asp Asp Ser Gln Ser Ile
65 70 75 80
Leu Tyr Leu Gln Met Asn Asn Leu Lys Thr Glu Asp Thr Ala Met Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala
115 120 125
<210> 259
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 259
Gln Ala Val Val Thr Gln Glu Ser Ala Leu Thr Thr Ser Pro Gly Glu
1 5 10 15
Thr Val Thr Leu Thr Cys Arg Ser Ser Thr Gly Ala Val Thr Thr Ser
20 25 30
Asn Tyr Ala Asn Trp Val Gln Glu Lys Pro Asp His Leu Phe Thr Gly
35 40 45
Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Val Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Ile Gly Asp Lys Ala Ala Leu Thr Ile Thr Gly Ala
65 70 75 80
Gln Thr Glu Asp Glu Ala Ile Tyr Phe Cys Ala Leu Trp Tyr Ser Asn
85 90 95
Leu Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 260
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 260
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Thr Met His Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Ser Ser Gly Tyr Thr Lys Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Trp Gln Asp Tyr Asp Val Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Leu Thr Val Ser Ser
115
<210> 261
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 261
Gln Ile Val Leu Ser Gln Ser Pro Ala Ile Leu Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Pro Trp Ile Tyr
35 40 45
Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Arg Val Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Pro Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Thr Lys
100 105
<210> 262
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 262
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Val Ala Ser Gly Val Pro Tyr Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ser Gly Thr Lys Leu Glu Ile Asn
100 105
<210> 263
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 263
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Arg Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn Tyr Asn Gln Lys Val
50 55 60
Lys Asp Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Ala Phe
65 70 75 80
Leu Gln Met Asp Ser Leu Arg Pro Glu Asp Thr Gly Val Tyr Phe Cys
85 90 95
Ala Arg Tyr Tyr Asp Asp His Tyr Cys Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Pro Val Thr Val Ser Ser
115
<210> 264
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 264
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Thr Pro Gly Lys Ala Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Tyr Thr Phe Thr Ile Ser Ser Leu Gln Pro Glu
65 70 75 80
Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Phe Thr
85 90 95
Phe Gly Gln Gly Thr Lys Leu Gln Ile Thr
100 105
<210> 265
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 265
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Lys Phe Ser Gly Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Lys Lys Tyr Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Met Gly Tyr Trp His Phe Asp Leu Trp Gly Arg Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 266
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 266
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 267
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 267
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Asp Arg Phe Ile Ser Arg Asp Asp Ser Lys Asn Ser Leu
65 70 75 80
Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala
100 105 110
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 268
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 268
Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly
1 5 10 15
Thr Val Thr Leu Thr Cys Arg Ser Ser Thr Gly Ala Val Thr Thr Ser
20 25 30
Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg Gly
35 40 45
Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Trp Thr Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Ile Gly Ala Gln Ala
65 70 75 80
Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn Leu Trp
85 90 95
Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 269
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 269
Asp Ile Lys Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Arg Tyr
20 25 30
Thr Met His Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Thr Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Tyr Asp Asp His Tyr Cys Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Leu Thr Val Ser Ser
115
<210> 270
<211> 105
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 270
Asp Ile Gln Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Val Ala Ser Gly Val Pro Tyr Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Ile Ser Ser Met Glu Ala Glu Asp
65 70 75 80
Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr Phe
85 90 95
Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 271
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 271
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Asp Arg Phe Ile Ser Arg Asp Asp Ser Lys Asn Ser Leu
65 70 75 80
Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala
100 105 110
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 272
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 272
Glu Val Lys Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Lys Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Asp Arg Phe Thr Ile Ser Arg Asp Asp Ser Gln Ser Ile
65 70 75 80
Leu Tyr Leu Gln Met Asn Asn Leu Lys Thr Glu Asp Thr Ala Met Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala
115 120 125
<210> 273
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 273
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Ala Tyr Leu Gln Met Asn Asn Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Trp
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 274
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 274
Gln Thr Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly
1 5 10 15
Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Ser Gly
20 25 30
Asn Tyr Pro Asn Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg Gly
35 40 45
Leu Ile Gly Gly Thr Lys Phe Leu Ala Pro Gly Thr Pro Gln Arg Phe
50 55 60
Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly Val
65 70 75 80
Gln Pro Glu Asp Glu Ala Glu Tyr Tyr Cys Val Leu Trp Tyr Ser Asn
85 90 95
Arg Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 275
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 275
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Lys Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Asp Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Ala Tyr Leu Gln Met Asn Asn Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Ile Ser Tyr Trp
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 276
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 276
Gln Thr Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly
1 5 10 15
Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Ser Gly
20 25 30
Asn Tyr Pro Asn Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg Gly
35 40 45
Leu Ile Gly Gly Thr Lys Phe Leu Ala Pro Gly Thr Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly Val
65 70 75 80
Gln Pro Glu Asp Glu Ala Glu Tyr Tyr Cys Val Leu Trp Tyr Ser Asn
85 90 95
Arg Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 277
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 277
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Arg Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Met Thr Thr Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Tyr Asp Asp His Tyr Cys Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 278
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 278
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ala His Phe Arg Gly Ser
50 55 60
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu
65 70 75 80
Asp Phe Ala Val Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Phe Thr
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 279
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 279
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Asp Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Ala Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 280
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 280
Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly
1 5 10 15
Thr Val Thr Leu Thr Cys Arg Ser Ser Thr Gly Ala Val Thr Thr Ser
20 25 30
Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg Gly
35 40 45
Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Thr Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly Val
65 70 75 80
Gln Pro Glu Asp Glu Ala Glu Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn
85 90 95
Leu Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 281
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 281
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Asp Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 282
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 282
Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly
1 5 10 15
Thr Val Thr Leu Thr Cys Arg Ser Ser Thr Gly Ala Val Thr Thr Ser
20 25 30
Asn Tyr Ala Asn Trp Val Gln Glu Lys Pro Gly Gln Ala Pro Arg Gly
35 40 45
Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Trp Thr Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Ile Thr Gly Ala
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn
85 90 95
Leu Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 283
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 283
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 284
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 284
Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly
1 5 10 15
Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr Ser
20 25 30
Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg Gly
35 40 45
Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Val Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly Ala
65 70 75 80
Gln Pro Glu Asp Glu Ala Glu Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn
85 90 95
Leu Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 285
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 285
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 286
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 286
Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly
1 5 10 15
Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr Ser
20 25 30
Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Lys Ser Pro Arg Gly
35 40 45
Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Val Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Ile Ser Gly Ala
65 70 75 80
Gln Pro Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn
85 90 95
His Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 287
<211> 101
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 287
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Thr Pro Gly Lys Ala Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Tyr Thr Phe Thr Ile Ser Ser Leu Gln Pro Glu
65 70 75 80
Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Phe Thr
85 90 95
Phe Gly Gln Gly Thr
100
<210> 288
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 288
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Arg Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn Tyr Asn Gln Lys Val
50 55 60
Lys Asp Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Ala Phe
65 70 75 80
Leu Gln Met Asp Ser Leu Arg Pro Glu Asp Thr Gly Val Tyr Phe Cys
85 90 95
Ala Arg Tyr Tyr Asp Asp His Tyr Ser Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Pro Val Thr Val Ser Ser
115
<210> 289
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 289
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Met Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Thr Met Asn Trp Val Lys Gln Ser His Gly Lys Asn Leu Glu Trp Met
35 40 45
Gly Leu Ile Asn Pro Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Leu Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Gly Tyr Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Leu Thr Val Phe Ser
115 120
<210> 290
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 290
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Arg Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Arg Leu His Ser Gly Val Pro Ser Lys Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Trp
85 90 95
Thr Phe Ala Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 291
<211> 257
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 291
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ala Val Val
130 135 140
Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly Thr Val Thr Leu
145 150 155 160
Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr Ala Asn
165 170 175
Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg Gly Leu Ile Gly Gly
180 185 190
Thr Asn Lys Arg Ala Pro Gly Val Pro Ala Arg Phe Ser Gly Ser Leu
195 200 205
Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly Ala Gln Pro Glu Asp
210 215 220
Glu Ala Glu Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn Leu Trp Val Phe
225 230 235 240
Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Ser His His His His His
245 250 255
His
<210> 292
<211> 254
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 292
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Lys Pro
115 120 125
Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly
130 135 140
Ser Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly
145 150 155 160
Gly Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr
165 170 175
Ser Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Lys Ser Pro Arg
180 185 190
Gly Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Val Pro Ala Arg
195 200 205
Phe Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Ile Ser Gly
210 215 220
Ala Gln Pro Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Leu Trp Tyr Ser
225 230 235 240
Asn His Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
245 250
<210> 293
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 293
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Ala Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 294
<211> 254
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 294
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Ala Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Lys Pro
115 120 125
Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly
130 135 140
Ser Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly
145 150 155 160
Gly Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr
165 170 175
Ser Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Lys Ser Pro Arg
180 185 190
Gly Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Val Pro Ala Arg
195 200 205
Phe Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Ile Ser Gly
210 215 220
Ala Gln Pro Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Leu Trp Tyr Ser
225 230 235 240
Asn His Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
245 250
<210> 295
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 295
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Glu Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 296
<211> 254
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 296
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Glu Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Lys Pro
115 120 125
Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly
130 135 140
Ser Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly
145 150 155 160
Gly Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr
165 170 175
Ser Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Lys Ser Pro Arg
180 185 190
Gly Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Val Pro Ala Arg
195 200 205
Phe Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Ile Ser Gly
210 215 220
Ala Gln Pro Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Leu Trp Tyr Ser
225 230 235 240
Asn His Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
245 250
<210> 297
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 297
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Pro Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 298
<211> 254
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 298
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Pro Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Lys Pro
115 120 125
Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly
130 135 140
Ser Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly
145 150 155 160
Gly Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr
165 170 175
Ser Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Lys Ser Pro Arg
180 185 190
Gly Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Val Pro Ala Arg
195 200 205
Phe Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Ile Ser Gly
210 215 220
Ala Gln Pro Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Leu Trp Tyr Ser
225 230 235 240
Asn His Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
245 250
<210> 299
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 299
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe
100 105 110
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 300
<211> 254
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 300
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe
100 105 110
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Lys Pro
115 120 125
Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly
130 135 140
Ser Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly
145 150 155 160
Gly Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr
165 170 175
Ser Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Lys Ser Pro Arg
180 185 190
Gly Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Val Pro Ala Arg
195 200 205
Phe Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Ile Ser Gly
210 215 220
Ala Gln Pro Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Leu Trp Tyr Ser
225 230 235 240
Asn His Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
245 250
<210> 301
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 301
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 302
<211> 254
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 302
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Lys Pro
115 120 125
Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly
130 135 140
Ser Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly
145 150 155 160
Gly Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr
165 170 175
Ser Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Lys Ser Pro Arg
180 185 190
Gly Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Val Pro Ala Arg
195 200 205
Phe Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Ile Ser Gly
210 215 220
Ala Gln Pro Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Leu Trp Tyr Ser
225 230 235 240
Asn His Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
245 250
<210> 303
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 303
Arg Tyr Thr Met His
1 5
<210> 304
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 304
Ser Ala Ser Ser Ser Val Ser Tyr Met Asn
1 5 10
<210> 305
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 305
Thr Tyr Ala Met Asn
1 5
<210> 306
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 306
Arg Ser Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr Ala Asn
1 5 10
<210> 307
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 307
Ser Tyr Thr Met His
1 5
<210> 308
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 308
Arg Ala Ser Ser Ser Val Ser Tyr Met His
1 5 10
<210> 309
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 309
Arg Ala Ser Ser Ser Val Ser Tyr Met Asn
1 5 10
<210> 310
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 310
Gly Tyr Gly Met His
1 5
<210> 311
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 311
Arg Ala Ser Gln Ser Val Ser Ser Tyr Leu Ala
1 5 10
<210> 312
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 312
Ser Tyr Ala Met Asn
1 5
<210> 313
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 313
Gly Ser Ser Thr Gly Ala Val Thr Ser Gly Asn Tyr Pro Asn
1 5 10
<210> 314
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 314
Lys Tyr Ala Met Asn
1 5
<210> 315
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 315
Gly Ser Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr Ala Asn
1 5 10
<210> 316
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 316
Gly Tyr Thr Met Asn
1 5
<210> 317
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 317
Arg Ala Ser Gln Asp Ile Arg Asn Tyr Leu Asn
1 5 10
<210> 318
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 318
Thr Tyr Ala Met Ser
1 5
<210> 319
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 319
Thr Tyr Ala Met His
1 5
<210> 320
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 320
Gly Ser Ser Thr Gly Ala Val Thr Ser Ser Asn Tyr Ala Asn
1 5 10
<210> 321
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 321
Gly Ser Ser Thr Gly Ala Val Thr Ser Gly His Tyr Ala Asn
1 5 10
<210> 322
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 322
Lys Ser Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr Ala Asn
1 5 10
<210> 323
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 323
Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn Tyr Asn Gln Lys Phe Lys
1 5 10 15
Asp
<210> 324
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 324
Asp Thr Ser Lys Leu Ala Ser
1 5
<210> 325
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 325
Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser
1 5 10 15
Val Lys Asp
<210> 326
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 326
Gly Thr Asn Lys Arg Ala Pro
1 5
<210> 327
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 327
Tyr Ile Asn Pro Ser Ser Gly Tyr Thr Lys Tyr Asn Gln Lys Phe Lys
1 5 10 15
Asp
<210> 328
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 328
Ala Thr Ser Asn Leu Ala Ser
1 5
<210> 329
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 329
Asp Thr Ser Lys Val Ala Ser
1 5
<210> 330
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 330
Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn Tyr Asn Gln Lys Val Lys
1 5 10 15
Asp
<210> 331
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 331
Val Ile Trp Tyr Asp Gly Ser Lys Lys Tyr Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 332
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 332
Asp Ala Ser Asn Arg Ala Thr
1 5
<210> 333
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 333
Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
1 5 10 15
<210> 334
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 334
Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser
1 5 10 15
Val Lys Gly
<210> 335
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 335
Gly Thr Lys Phe Leu Ala Pro
1 5
<210> 336
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 336
Leu Ile Asn Pro Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys Phe Lys
1 5 10 15
Asp
<210> 337
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 337
Tyr Thr Ser Arg Leu His
1 5
<210> 338
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 338
Arg Ile Arg Ser Lys Ala Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser
1 5 10 15
Val Lys Gly
<210> 339
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 339
Arg Ile Arg Ser Lys Ala Asn Asn Tyr Tyr Ala Thr Tyr Tyr Ala Asp
1 5 10 15
Ser Val Lys Gly
20
<210> 340
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 340
Arg Ile Arg Ser Lys Ala Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser
1 5 10 15
Val Lys Gly
<210> 341
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 341
Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Ala Tyr Ala Asp Ser
1 5 10 15
Val Lys Gly
<210> 342
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 342
Asp Thr Asn Lys Arg Ala Pro
1 5
<210> 343
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 343
Gly Thr Asn Asn Arg Ala Pro
1 5
<210> 344
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 344
Gly Thr Asn Lys Arg Ala Ser
1 5
<210> 345
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 345
Gly Thr Ser Asn Lys His Ser
1 5
<210> 346
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 346
Arg Ile Arg Ser Asn Gly Gly Tyr Ser Thr Tyr Tyr Ala Asp Ser Val
1 5 10 15
Lys Gly
<210> 347
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 347
Tyr Tyr Asp Asp His Tyr Cys Leu Asp Tyr
1 5 10
<210> 348
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 348
Gln Gln Trp Ser Ser Asn Pro Phe Thr
1 5
<210> 349
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 349
His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala Tyr
1 5 10
<210> 350
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 350
Ala Leu Trp Tyr Ser Asn Leu Trp Val
1 5
<210> 351
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 351
Trp Gln Asp Tyr Asp Val Tyr Phe Asp Tyr
1 5 10
<210> 352
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 352
Gln Gln Trp Ser Ser Asn Pro Pro Thr
1 5
<210> 353
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 353
Gln Gln Trp Ser Ser Asn Pro Leu Thr
1 5
<210> 354
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 354
Gln Met Gly Tyr Trp His Phe Asp Leu
1 5
<210> 355
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 355
Gln Gln Arg Ser Asn Trp Pro Pro Leu Thr
1 5 10
<210> 356
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 356
Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala Tyr
1 5 10 15
<210> 357
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 357
His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Trp Ala Tyr
1 5 10
<210> 358
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 358
Val Leu Trp Tyr Ser Asn Arg Trp Val
1 5
<210> 359
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 359
His Gly Asn Phe Gly Asn Ser Tyr Ile Ser Tyr Trp Ala Tyr
1 5 10
<210> 360
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 360
His Gly Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe Ala Tyr
1 5 10
<210> 361
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 361
Ala Leu Trp Tyr Ser Asn His Trp Val
1 5
<210> 362
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 362
Tyr Tyr Asp Asp His Tyr Ser Leu Asp Tyr
1 5 10
<210> 363
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 363
Ser Gly Tyr Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val
1 5 10
<210> 364
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 364
Gln Gln Gly Asn Thr Leu Pro Trp Thr
1 5
<210> 365
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 365
His Gly Asn Phe Gly Asp Glu Tyr Val Ser Trp Phe Ala Tyr
1 5 10
<210> 366
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 366
His Gly Asn Phe Gly Asp Pro Tyr Val Ser Trp Phe Ala Tyr
1 5 10
<210> 367
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 367
His Gly Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe Asp Tyr
1 5 10
<210> 368
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 368
His Gly Asn Phe Gly Gln Ser Tyr Val Ser Trp Phe Ala Tyr
1 5 10
<210> 369
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 369
His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Asp Tyr
1 5 10
<210> 370
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 370
Leu Leu Trp Tyr Ser Asn Leu Trp Val
1 5
<210> 371
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 371
Gly Tyr Thr Phe Thr Arg Tyr
1 5
<210> 372
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 372
Ser Ser Ser Val Ser Tyr
1 5
<210> 373
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 373
Gly Phe Thr Phe Asn Thr Tyr
1 5
<210> 374
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 374
Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr
1 5 10
<210> 375
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 375
Gly Tyr Thr Phe Thr Ser Tyr
1 5
<210> 376
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 376
Gly Phe Lys Phe Ser Gly Tyr
1 5
<210> 377
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 377
Ser Gln Ser Val Ser Ser Tyr
1 5
<210> 378
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 378
Gly Phe Thr Phe Ser Thr Tyr
1 5
<210> 379
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 379
Gly Phe Thr Phe Asn Ser Tyr
1 5
<210> 380
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 380
Ser Thr Gly Ala Val Thr Ser Gly Asn Tyr
1 5 10
<210> 381
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 381
Gly Phe Thr Phe Asn Lys Tyr
1 5
<210> 382
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 382
Gly Tyr Ser Phe Thr Gly Tyr
1 5
<210> 383
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 383
Ser Gln Asp Ile Arg Asn Tyr
1 5
<210> 384
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 384
Asn Pro Ser Arg Gly Tyr
1 5
<210> 385
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 385
Asp Thr Ser
1
<210> 386
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 386
Arg Ser Lys Tyr Asn Asn Tyr Ala
1 5
<210> 387
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 387
Gly Thr Asn
1
<210> 388
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 388
Asn Pro Ser Ser Gly Tyr
1 5
<210> 389
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 389
Ala Thr Ser
1
<210> 390
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 390
Trp Tyr Asp Gly Ser Lys
1 5
<210> 391
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 391
Asp Ala Ser
1
<210> 392
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 392
Arg Ser Lys Tyr Asn Asn Tyr Ala Thr
1 5
<210> 393
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 393
Gly Thr Lys
1
<210> 394
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 394
Asn Pro Tyr Lys Gly Val
1 5
<210> 395
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 395
Tyr Thr Ser
1
<210> 396
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 396
Trp Ser Ser Asn Pro Phe
1 5
<210> 397
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 397
Trp Tyr Ser Asn Leu Trp
1 5
<210> 398
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 398
Trp Ser Ser Asn Pro Pro
1 5
<210> 399
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 399
Trp Ser Ser Asn Pro Leu
1 5
<210> 400
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 400
Arg Ser Asn Trp Pro Pro Leu
1 5
<210> 401
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 401
His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala
1 5 10
<210> 402
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 402
Trp Tyr Ser Asn Arg Trp
1 5
<210> 403
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 403
Trp Tyr Ser Asn His Trp
1 5
<210> 404
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 404
Gly Asn Thr Leu Pro Trp
1 5
<210> 405
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 405
Gly Tyr Thr Phe Thr Arg Tyr Thr Met His
1 5 10
<210> 406
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 406
Gly Phe Thr Phe Asn Thr Tyr Ala Met Asn
1 5 10
<210> 407
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 407
Gly Tyr Thr Phe Thr Ser Tyr Thr Met His
1 5 10
<210> 408
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 408
Gly Phe Lys Phe Ser Gly Tyr Gly Met His
1 5 10
<210> 409
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 409
Gly Phe Thr Phe Ser Thr Tyr Ala Met Asn
1 5 10
<210> 410
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 410
Gly Phe Thr Phe Asn Ser Tyr Ala Met Asn
1 5 10
<210> 411
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 411
Gly Phe Thr Phe Asn Lys Tyr Ala Met Asn
1 5 10
<210> 412
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 412
Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn
1 5 10
<210> 413
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 413
Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser
1 5 10 15
Val Lys
<210> 414
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 414
Tyr Thr Ser Arg Leu His Ser
1 5
<210> 415
<211> 152
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 415
Met Gln Ile Phe Val Lys Thr Leu Thr Gly Lys Thr Ile Thr Leu Glu
1 5 10 15
Val Glu Pro Ser Asp Thr Ile Glu Asn Val Lys Ala Lys Ile Gln Asp
20 25 30
Lys Glu Gly Ile Pro Pro Asp Gln Gln Trp Leu Trp Phe Ala Gly Lys
35 40 45
Gln Leu Glu Asp Gly Arg Thr Leu Ser Asp Tyr Asn Ile Gln Lys Glu
50 55 60
Ser Thr Leu Lys Leu Trp Leu Val Asp Lys Ala Ala Met Gln Ile Phe
65 70 75 80
Val Tyr Thr Arg Thr Gly Lys Thr Ile Thr Leu Glu Val Glu Pro Ser
85 90 95
Asp Thr Ile Glu Asn Val Lys Ala Lys Ile Gln Asp Lys Glu Gly Ile
100 105 110
Pro Pro Asp Gln Gln Arg Leu Ile Trp Ala Gly Lys Gln Leu Glu Asp
115 120 125
Gly Arg Thr Leu Ser Asp Tyr Asn Ile Ala Leu Glu Ser Gly Leu His
130 135 140
Leu Val Leu Arg Leu Arg Ala Ala
145 150
<210> 416
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 416
Lys Ala Ser Gly Tyr Lys Phe Thr Ser Tyr Val Met His
1 5 10
<210> 417
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 417
Tyr Ile Asn Pro Tyr Asn Asp Val Thr Lys Tyr Asn Glu Lys Phe Lys
1 5 10 15
<210> 418
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 418
Gly Ser Tyr Tyr Asp Tyr Asp Gly Phe Val Tyr
1 5 10
<210> 419
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 419
Ser Ala Thr Ser Ser Val Ser Tyr Met His
1 5 10
<210> 420
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 420
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Ser Tyr
20 25 30
Val Met His Trp Val Lys Gln Lys Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Tyr Asn Asp Val Thr Lys Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val His Tyr Cys
85 90 95
Ala Arg Gly Ser Tyr Tyr Asp Tyr Asp Gly Phe Val Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala
115 120
<210> 421
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 421
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Thr Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 422
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 422
Cys Pro Pro Cys
1
<210> 423
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 423
Ser Pro Pro Ser
1
<210> 424
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 424
Val Pro Ser Thr Pro Pro Thr Pro Ser Pro Ser Thr Pro Pro Thr Pro
1 5 10 15
Ser Pro Ser
<210> 425
<211> 6
<212> БЕЛОК
<213> Homo sapiens
<400> 425
Val Pro Pro Pro Pro Pro
1 5
<210> 426
<211> 58
<212> БЕЛОК
<213> Homo sapiens
<400> 426
Glu Ser Pro Lys Ala Gln Ala Ser Ser Val Pro Thr Ala Gln Pro Gln
1 5 10 15
Ala Glu Gly Ser Leu Ala Lys Ala Thr Thr Ala Pro Ala Thr Thr Arg
20 25 30
Asn Thr Gly Arg Gly Gly Glu Glu Lys Lys Lys Glu Lys Glu Lys Glu
35 40 45
Glu Gln Glu Glu Arg Glu Thr Lys Thr Pro
50 55
<210> 427
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 427
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
1 5 10 15
<210> 428
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 428
Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro
1 5 10
<210> 429
<211> 62
<212> БЕЛОК
<213> Homo sapiens
<400> 429
Glu Leu Lys Thr Pro Leu Gly Asp Thr Thr His Thr Cys Pro Arg Cys
1 5 10 15
Pro Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro
20 25 30
Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro Glu
35 40 45
Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro
50 55 60
<210> 430
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 430
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Ser Cys Pro
1 5 10
<210> 431
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 431
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro
1 5 10
<210> 432
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 432
Cys Pro Ser Cys
1
<210> 433
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 433
Cys Pro Arg Cys
1
<210> 434
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 434
Ser Pro Pro Cys
1
<210> 435
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 435
Cys Pro Pro Ser
1
<210> 436
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 436
Asp Lys Thr His Thr Cys Ala Ala
1 5
<210> 437
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 437
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10
<210> 438
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 438
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Thr Cys Pro Pro Cys
1 5 10 15
Pro Ala
<210> 439
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 439
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Thr Cys Pro Pro Cys
1 5 10 15
Pro Ala Thr Cys Pro Pro Cys Pro Ala
20 25
<210> 440
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 440
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Gly Lys Pro Thr Leu
1 5 10 15
Tyr Asn Ser Leu Val Met Ser Asp Thr Ala Gly Thr Cys Tyr
20 25 30
<210> 441
<211> 31
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 441
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Gly Lys Pro Thr His
1 5 10 15
Val Asn Val Ser Val Val Met Ala Glu Val Asp Gly Thr Cys Tyr
20 25 30
<210> 442
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 442
Asp Lys Thr His Thr Cys Cys Val Glu Cys Pro Pro Cys Pro Ala
1 5 10 15
<210> 443
<211> 26
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 443
Asp Lys Thr His Thr Cys Pro Arg Cys Pro Glu Pro Lys Ser Cys Asp
1 5 10 15
Thr Pro Pro Pro Cys Pro Arg Cys Pro Ala
20 25
<210> 444
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 444
Asp Lys Thr His Thr Cys Pro Ser Cys Pro Ala
1 5 10
<210> 445
<211> 50
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<220>
<221> Сайт
<222> (1)..(50)
<223> /примечание="Эта последовательность может охватывать 1-10
повторяющихся звеньев 'Gly Gly Gly Gly Ser'"
<220>
<221> источник
<223> /примечание="См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления"
<400> 445
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
20 25 30
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
35 40 45
Gly Ser
50
<210> 446
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 446
Ala Asp Ala Ala Pro
1 5
<210> 447
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 447
Ala Asp Ala Ala Pro Thr Val Ser Ile Phe Pro
1 5 10
<210> 448
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 448
Ala Asp Ala Ala Pro Thr Val Ser Ile Phe Pro Pro
1 5 10
<210> 449
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 449
Ala Lys Thr Thr Ala Pro
1 5
<210> 450
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 450
Ala Lys Thr Thr Ala Pro Ser Val Tyr Pro Leu Ala Pro
1 5 10
<210> 451
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 451
Ala Lys Thr Thr Pro Lys Leu Glu Glu Gly Glu Phe Ser Glu Ala Arg
1 5 10 15
Val
<210> 452
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 452
Ala Lys Thr Thr Pro Lys Leu Gly Gly
1 5
<210> 453
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 453
Ala Lys Thr Thr Pro Pro
1 5
<210> 454
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 454
Ala Lys Thr Thr Pro Pro Ser Val Thr Pro Leu Ala Pro
1 5 10
<210> 455
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 455
Ala Ser Thr Lys Gly Pro
1 5
<210> 456
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 456
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
1 5 10
<210> 457
<211> 26
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 457
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ala Ser Thr
1 5 10 15
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
20 25
<210> 458
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 458
Glu Gly Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr
1 5 10
<210> 459
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 459
Gly Glu Gly Glu Ser Gly Glu Gly Glu Ser Gly Glu Gly Glu Ser
1 5 10 15
<210> 460
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 460
Gly Glu Gly Glu Ser Gly Glu Gly Glu Ser Gly Glu Gly Glu Ser Gly
1 5 10 15
Glu Gly Glu Ser
20
<210> 461
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 461
Gly Glu Gly Gly Ser Gly Glu Gly Gly Ser Gly Glu Gly Gly Ser
1 5 10 15
<210> 462
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 462
Gly Glu Asn Lys Val Glu Tyr Ala Pro Ala Leu Met Ala Leu Ser
1 5 10 15
<210> 463
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 463
Gly Gly Glu Gly Ser Gly Gly Glu Gly Ser Gly Gly Glu Gly Ser
1 5 10 15
<210> 464
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 464
Gly Gly Gly Glu Ser Gly Gly Glu Gly Ser Gly Glu Gly Gly Ser
1 5 10 15
<210> 465
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 465
Gly Gly Gly Glu Ser Gly Gly Gly Glu Ser Gly Gly Gly Glu Ser
1 5 10 15
<210> 466
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 466
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10
<210> 467
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 467
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser
20
<210> 468
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 468
Gly Gly Gly Lys Ser Gly Gly Gly Lys Ser Gly Gly Gly Lys Ser
1 5 10 15
<210> 469
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 469
Gly Gly Gly Lys Ser Gly Gly Lys Gly Ser Gly Lys Gly Gly Ser
1 5 10 15
<210> 470
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 470
Gly Gly Lys Gly Ser Gly Gly Lys Gly Ser Gly Gly Lys Gly Ser
1 5 10 15
<210> 471
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 471
Gly Gly Ser Gly Gly
1 5
<210> 472
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 472
Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5
<210> 473
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 473
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10
<210> 474
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 474
Gly His Glu Ala Ala Ala Val Met Gln Val Gln Tyr Pro Ala Ser
1 5 10 15
<210> 475
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 475
Gly Lys Gly Gly Ser Gly Lys Gly Gly Ser Gly Lys Gly Gly Ser
1 5 10 15
<210> 476
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 476
Gly Lys Gly Lys Ser Gly Lys Gly Lys Ser Gly Lys Gly Lys Ser
1 5 10 15
<210> 477
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 477
Gly Lys Gly Lys Ser Gly Lys Gly Lys Ser Gly Lys Gly Lys Ser Gly
1 5 10 15
Lys Gly Lys Ser
20
<210> 478
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 478
Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser
1 5 10 15
<210> 479
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 479
Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly
1 5 10 15
Lys Pro Gly Ser
20
<210> 480
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 480
Gly Pro Ala Lys Glu Leu Thr Pro Leu Lys Glu Ala Lys Val Ser
1 5 10 15
<210> 481
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 481
Gly Ser Ala Gly Ser Ala Ala Gly Ser Gly Glu Phe
1 5 10
<210> 482
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 482
Ile Arg Pro Arg Ala Ile Gly Gly Ser Lys Pro Arg Val Ala
1 5 10
<210> 483
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 483
Lys Glu Ser Gly Ser Val Ser Ser Glu Gln Leu Ala Gln Phe Arg Ser
1 5 10 15
Leu Asp
<210> 484
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 484
Lys Thr Thr Pro Lys Leu Glu Glu Gly Glu Phe Ser Glu Ala Arg
1 5 10 15
<210> 485
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 485
Gln Pro Lys Ala Ala Pro
1 5
<210> 486
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 486
Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro
1 5 10
<210> 487
<211> 27
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 487
Arg Ala Asp Ala Ala Ala Ala Gly Gly Gly Gly Ser Gly Gly Gly Gly
1 5 10 15
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
20 25
<210> 488
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 488
Arg Ala Asp Ala Ala Ala Ala Gly Gly Pro Gly Ser
1 5 10
<210> 489
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 489
Arg Ala Asp Ala Ala Pro
1 5
<210> 490
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 490
Arg Ala Asp Ala Ala Pro Thr Val Ser
1 5
<210> 491
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 491
Ser Ala Lys Thr Thr Pro
1 5
<210> 492
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 492
Ser Ala Lys Thr Thr Pro Lys Leu Glu Glu Gly Glu Phe Ser Glu Ala
1 5 10 15
Arg Val
<210> 493
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 493
Ser Ala Lys Thr Thr Pro Lys Leu Gly Gly
1 5 10
<210> 494
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 494
Ser Thr Ala Gly Asp Thr His Leu Gly Gly Glu Asp Phe Asp
1 5 10
<210> 495
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 495
Thr Val Ala Ala Pro
1 5
<210> 496
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 496
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro
1 5 10
<210> 497
<211> 24
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 497
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Thr Val Ala Ala
1 5 10 15
Pro Ser Val Phe Ile Phe Pro Pro
20
<210> 498
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 498
Gly Ser Thr Ser Gly Ser Gly Lys Pro Gly Ser Gly Glu Gly Ser Thr
1 5 10 15
Lys Gly
<210> 499
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 499
Pro Arg Gly Ala Ser Lys Ser Gly Ser Ala Ser Gln Thr Gly Ser Ala
1 5 10 15
Pro Gly Ser
<210> 500
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 500
Gly Thr Ala Ala Ala Gly Ala Gly Ala Ala Gly Gly Ala Ala Ala Gly
1 5 10 15
Ala Ala Gly
<210> 501
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 501
Gly Thr Ser Gly Ser Ser Gly Ser Gly Ser Gly Gly Ser Gly Ser Gly
1 5 10 15
Gly Gly Gly
<210> 502
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 502
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asp Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 503
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 503
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 504
<211> 485
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 504
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Ala Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Lys Pro
115 120 125
Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly
130 135 140
Ser Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly
145 150 155 160
Gly Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr
165 170 175
Ser Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Lys Ser Pro Arg
180 185 190
Gly Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Val Pro Ala Arg
195 200 205
Phe Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Ile Ser Gly
210 215 220
Ala Gln Pro Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Leu Trp Tyr Ser
225 230 235 240
Asn His Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Glu Pro
245 250 255
Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro
260 265 270
Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
275 280 285
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
290 295 300
Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
305 310 315 320
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
325 330 335
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
340 345 350
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
355 360 365
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
370 375 380
Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn Gln
385 390 395 400
Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
405 410 415
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
420 425 430
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
435 440 445
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
450 455 460
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
465 470 475 480
Leu Ser Pro Gly Lys
485
<210> 505
<211> 723
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 505
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu
225 230 235 240
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
245 250 255
Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr Ala Met Asn Trp Val Arg
260 265 270
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Gly Arg Ile Arg Ser Lys
275 280 285
Ala Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe
290 295 300
Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn
305 310 315 320
Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Val Arg His Gly
325 330 335
Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe Ala Tyr Trp Gly Gln Gly
340 345 350
Thr Leu Val Thr Val Ser Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly
355 360 365
Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gln Ala Val Val Thr
370 375 380
Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly Thr Val Thr Leu Thr
385 390 395 400
Cys Gly Ser Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr Ala Asn Trp
405 410 415
Val Gln Gln Lys Pro Gly Lys Ser Pro Arg Gly Leu Ile Gly Gly Thr
420 425 430
Asn Lys Arg Ala Pro Gly Val Pro Ala Arg Phe Ser Gly Ser Leu Leu
435 440 445
Gly Gly Lys Ala Ala Leu Thr Ile Ser Gly Ala Gln Pro Glu Asp Glu
450 455 460
Ala Asp Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn His Trp Val Phe Gly
465 470 475 480
Gly Gly Thr Lys Leu Thr Val Leu Gly Gly Gly Gly Ser Gly Gly Gly
485 490 495
Gly Ser Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
500 505 510
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
515 520 525
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
530 535 540
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
545 550 555 560
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
565 570 575
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
580 585 590
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
595 600 605
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
610 615 620
Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn Gln Val Lys
625 630 635 640
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
645 650 655
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
660 665 670
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
675 680 685
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
690 695 700
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
705 710 715 720
Pro Gly Lys
<210> 506
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 506
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Glu Ser Gly Gly Arg Ala Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asp Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 507
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 507
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 508
<211> 723
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 508
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Glu Ser Gly Gly Arg Ala Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu Val Glu
225 230 235 240
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
245 250 255
Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr Ala Met Asn Trp Val Arg
260 265 270
Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Gly Arg Ile Arg Ser Lys
275 280 285
Ala Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe
290 295 300
Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln Met Asn
305 310 315 320
Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Val Arg His Gly
325 330 335
Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe Ala Tyr Trp Gly Gln Gly
340 345 350
Thr Leu Val Thr Val Ser Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly
355 360 365
Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gln Ala Val Val Thr
370 375 380
Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly Thr Val Thr Leu Thr
385 390 395 400
Cys Gly Ser Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr Ala Asn Trp
405 410 415
Val Gln Gln Lys Pro Gly Lys Ser Pro Arg Gly Leu Ile Gly Gly Thr
420 425 430
Asn Lys Arg Ala Pro Gly Val Pro Ala Arg Phe Ser Gly Ser Leu Leu
435 440 445
Gly Gly Lys Ala Ala Leu Thr Ile Ser Gly Ala Gln Pro Glu Asp Glu
450 455 460
Ala Asp Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn His Trp Val Phe Gly
465 470 475 480
Gly Gly Thr Lys Leu Thr Val Leu Gly Gly Gly Gly Ser Gly Gly Gly
485 490 495
Gly Ser Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
500 505 510
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
515 520 525
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
530 535 540
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
545 550 555 560
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
565 570 575
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
580 585 590
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
595 600 605
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
610 615 620
Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn Gln Val Lys
625 630 635 640
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
645 650 655
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
660 665 670
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
675 680 685
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
690 695 700
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
705 710 715 720
Pro Gly Lys
<210> 509
<211> 452
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 509
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
195 200 205
Asn His Lys Pro Ser Asp Thr Lys Val Asp Lys Lys Val Glu Pro Lys
210 215 220
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val
225 230 235 240
Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys
260 265 270
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
275 280 285
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr
290 295 300
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
305 310 315 320
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
325 330 335
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
340 345 350
Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val
355 360 365
Ser Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val
370 375 380
Glu Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
385 390 395 400
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
405 410 415
Val Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val
420 425 430
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
435 440 445
Ser Pro Gly Lys
450
<210> 510
<211> 217
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 510
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Leu Arg Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Ala Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu Gly
100 105 110
Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu
115 120 125
Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe
130 135 140
Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro Val
145 150 155 160
Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn Lys
165 170 175
Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser
180 185 190
His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu
195 200 205
Lys Thr Val Ala Pro Thr Glu Cys Ser
210 215
<210> 511
<211> 725
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 511
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
195 200 205
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
210 215 220
Ser Cys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu
225 230 235 240
Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu
245 250 255
Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr Ala Met Asn Trp
260 265 270
Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Gly Arg Ile Arg
275 280 285
Ser Lys Ala Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Gly
290 295 300
Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Gln
305 310 315 320
Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Val Arg
325 330 335
His Gly Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe Ala Tyr Trp Gly
340 345 350
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Lys Pro Gly Ser Gly Lys
355 360 365
Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gln Ala Val
370 375 380
Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly Thr Val Thr
385 390 395 400
Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr Ala
405 410 415
Asn Trp Val Gln Gln Lys Pro Gly Lys Ser Pro Arg Gly Leu Ile Gly
420 425 430
Gly Thr Asn Lys Arg Ala Pro Gly Val Pro Ala Arg Phe Ser Gly Ser
435 440 445
Leu Leu Gly Gly Lys Ala Ala Leu Thr Ile Ser Gly Ala Gln Pro Glu
450 455 460
Asp Glu Ala Asp Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn His Trp Val
465 470 475 480
Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Gly Gly Gly Ser Gly
485 490 495
Gly Gly Gly Ser Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro
500 505 510
Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
515 520 525
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
530 535 540
Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
545 550 555 560
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
565 570 575
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
580 585 590
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
595 600 605
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
610 615 620
Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn Gln
625 630 635 640
Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
645 650 655
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
660 665 670
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
675 680 685
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
690 695 700
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
705 710 715 720
Leu Ser Pro Gly Lys
725
<210> 512
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 512
Gly Phe Leu Gly
1
<210> 513
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 513
Ala Leu Ala Leu
1
<210> 514
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 514
Arg Gly Asp Ser
1
<210> 515
<211> 249
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 515
atgttgcaaa tggctgggca atgtagtcag aatgagtact tcgattctct tctccatgct
60
tgtatcccct gccagctgag gtgttcaagc aatactccgc cccttacctg tcaacgatat
120
tgtaatgcct ccgtgaccaa ttccgtgaag ggaaccaatg ctggatccca tcaccatcac
180
catcacgaat ttagacatga tagcggcctg aacgacattt tcgaggctca aaagatcgag
240
tggcacgag
249
<210> 516
<211> 369
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 516
caggtgcagc tgcaggagtc ggggggaggc gtggtccagc ctgggaggtc cctgagactc
60
tcctgtgcag cctctggatt caccttcagt agctatggca tgcactgggt ccgccaggct
120
ccaggcaagg ggctggagtg ggtggcagtt atatcatatg atggaagtaa taaatactat
180
gcagactccg tgaagggccg attcaccatc tccagagaca attccaagaa cacgctgtat
240
ctgcaaatga acagcctgag agccgaggac acggccgtat attactgtgg ggggagtggt
300
tacgcccttc acgatgacta ctacggcttg gacgtctggg gccaaggcac cctggtcacc
360
gtctcctca
369
<210> 517
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 517
cagtctgccc tgactcagcc tgcctccgtg tctgggtctc ctggacagtc gatcaccatc
60
tcctgcactg gaaccagcag tgacgttggt ggttataact atgtctcctg gtaccaacag
120
cacccaggca aagcccccaa actcatgatt tatgatgtca gtaatcggcc ctcaggggtt
180
tctaatcgct tctctggctc caagtctggc aacacggcct ccctgaccat ctctgggctc
240
caggctgagg acgaggctga ttattactgc agctcatata caagcagcag caccctttat
300
gtcttcggaa gtgggaccaa ggtcaccgtc cta
333
<210> 518
<211> 83
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 518
Met Leu Gln Met Ala Gly Gln Cys Ser Gln Asn Glu Tyr Phe Asp Ser
1 5 10 15
Leu Leu His Ala Cys Ile Pro Cys Gln Leu Arg Cys Ser Ser Asn Thr
20 25 30
Pro Pro Leu Thr Cys Gln Arg Tyr Cys Asn Ala Ser Val Thr Asn Ser
35 40 45
Val Lys Gly Thr Asn Ala Gly Ser His His His His His His Glu Phe
50 55 60
Arg His Asp Ser Gly Leu Asn Asp Ile Phe Glu Ala Gln Lys Ile Glu
65 70 75 80
Trp His Glu
<210> 519
<211> 246
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 519
atgctccaga tggcacggca atgtagtcag aacgagtatt ttgatagcct gctccacgat
60
tgcaagccct gtcagctgcg gtgtagctcc actccgccat tgacgtgtca gcggtactgc
120
aacgcaagta tgacaaactc agtcaagggc atgaacgcag gatcccatca ccatcaccat
180
cacgaattta gacatgatag cggcctgaac gacattttcg aggctcaaaa gatcgagtgg
240
cacgag
246
<210> 520
<211> 765
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 520
caagtgcagc tccagagttc cgaaggcgga gtggtgcagc ctggaaggag cctgcgcctg
60
tcatgcgcag cgtccgggtt caccttctca tcctacggca tgcactgggt cagacaggcc
120
ccgggaaaag gattggaatg ggtggccgtg atttcataca agggttccaa caagtactac
180
gccgattccg tgaagggacg gtttaccatc tcgcgggaca actcgaagaa caccctgtac
240
ctccaaatga acagcctgcg cgccgaagat actgccgtgt actactgcgg cggttccggt
300
tacgcgctcc acgacgacta ttacgggctg gacgtctggg gacagggcac cctggtcact
360
gtgtcctcgt caggtggtgg tggttctggt ggtggcggct caggcggcgg cggctcaggt
420
ggtggaggat cccagtccgc tctgacccaa ccggcttccg tgagcggaag ccccggacag
480
tccattacta tcagctgtac cggcacctcc tccgacgtcg gtggatacaa ctacgtgtcc
540
tggtatcagc agcatcctgg aaaggctcca aagctcatga tctacgaggt gtcgaacaga
600
ctgaggggtg tgtccaatcg cttttcgggc tccaagttcg gaaacacggc ctcactgact
660
atctcgggac tgcaggccga agatgaagcc gactactact gctcctccta cacctcgtcc
720
tccgctctgt acgtgttcgg gtccggcacc aaagtcactg tgctg
765
<210> 521
<211> 765
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 521
caagcgcagc tccagagttc cggaggcgga gtggtgcagc ctggaaggag cctgcgcctg
60
tcatgcgcag cgtccgggtt caccttctca tcctacggca tgcactgggt cagacaggcc
120
ccgggaaaag gattggaatg ggtggccgtg atttcctaca aggggtccaa caagtactac
180
gccgattccg tgaagggacg gtttaccatc tcgcgggaca actcgaagaa caccctgtac
240
ctccaaatga acagcctgcg cgccgaagat actgccgtgt actactgcgg cggttccggt
300
tacgcgctcc acgacgacta ttacgggctg gacgtctggg gacagggcac cctggtcact
360
gtgtcctcgt caggtggtgg tggttctggt ggtggcggct caggcggcgg cggctcaggt
420
ggtggaggat cccagtccgc tctgacccaa ccggcttccg tgagcggaag ccccggacag
480
tccattacta tcagctgtac cggcacctcc tccgacgtcg gtggatacaa ctacgtgtcc
540
tggtatcagc agcatcctgg aaaggctcca aagctcatga tctacgaagt gtcgaacaga
600
ctgagaggtg tgtccaatcg cttttcgggc tccaagttcg gaaacacggc ctcactgact
660
atctcgggac tgcaggccga agatgaagcc gactactact gctcctccta cacctcgtcc
720
tccactctgt acgtgttcgg gtccggcacc aaagtcactg tgctg
765
<210> 522
<211> 765
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 522
caagtgcagc tccaggattc cgaaggcgga gtggtgcagc ctggaaggag cctgcgcctg
60
tcatgcgcag cgtccgggtt caccttctca tcctacggca tgcactgggt cagacaggcc
120
ccgggaaaag gattggaatg ggtggccgtg atttcctaca ctggtaccaa aaagtactac
180
gccgattccg tgaagggacg gtttaccatc tcgcgggaca actcgaagaa caccctgtac
240
ctccaaatga acagcctgcg cgccgaagat actgccgtgt actactgcgg cggttccggt
300
tacgcgctcc acgacgacta ttacgggctg gacgtctggg gacagggcac cctggtcact
360
gtgtcctcgt caggtggtgg tggttctggt ggtggcggct caggcggcgg cggctcaggt
420
ggtggaggat cccagtccgc tctgacccaa ccggcttccg tgagcggaag ccccggacag
480
tccattacta tcagctgtac cggcacctcc tccgacgtcg gtggatacaa ctacgtgtcc
540
tggtatcagc agcatcctgg aaaggctcca aagctcatga tctacgacgt gtcgaacaga
600
ccgtggggtg tgtccaatcg cttttcgggc tccaagttcg gaaacacggc ctcactgact
660
atctcgggac tgcaggccga agatgaagcc gactactact gctcctccta cacctcgtcc
720
tccgctctgt acgtgttcgg gtccggcacc aaagtcactg tgatg
765
<210> 523
<211> 765
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 523
caagcgcagc tccagagttc cgaaggcgga gtggtgcagc ctggaaggag cctgcgcctg
60
tcatgcgcag cgtccgggtt caccttctca tcctacggca tgcactgggt cagacaggcc
120
ccgggaaaag gattggaatg ggtggccgtg atttcctacc ggggttttaa caagtactac
180
gccgattccg tgaagggacg gtttaccatc tcgcgggaca actcgaagaa caccctgtac
240
ctccaaatga acagcctgcg cgccgaagat actgccgtgt actactgcgg cggttccggt
300
tacgcgctcc acgacgacta ttacgggcag gacgtctggg gacagggcac cctggtcact
360
gtgtcctcgt caggtggtgg tggttctggt ggtggcggct caggcggcgg cggctcaggt
420
ggtggaggat cccagtccgc tctgacccaa ccggcttccg tgagcggaag ccccggacag
480
tccattacta tcagctgtac cggcacctcc tccgacgtcg gtggatacaa ctacgtgtcc
540
tggtatcagc agcatcctgg aaaggctcca aagctcatga tctacgacgt gtcgaacaga
600
ctgagcggtg tgtccaatcg cttttcgggc tccaagttcg gaaacacggc ctcactgact
660
atctcgggac tgcaggccga agatgaagcc gactactact gctcctccta cacatcgtcc
720
tccactctgt acgtgttcgg gtccggcacc aaagtcactg tgctg
765
<210> 524
<211> 765
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 524
caagcgcagc tccaggggtc cggaggcgga gtggtgcagc ctggaaggag cctgcgcctg
60
tcatgcgcag cgtccgggtt caccttctca tcctacggca tgcactgggt cagacaggcc
120
ccgggaaaag gattggaatg ggtggccgtg atttcctaca aggggtccca caagtactac
180
gccgattccg tgaagggacg gtttaccatc tcgcgggaca actcgaagaa caccctgtac
240
ctccaaatga acagcctgcg cgccgaagat actgccgtgt actactgcgg cggttccggt
300
tacgcgctcc acgacgacta ttacgggctg gacgtctggg gacagggcac cctggtcact
360
gtgtcctcgt caggtggtgg tggttctggt ggtggcggct caggcggcgg cggctcaggt
420
ggtggaggat cccagtccgc tctgacccaa ccggcttccg tgagcggaag ccccggacag
480
tccattacta tcagctgtac cggcacctcc tccgacgtcg gtggatacaa ctacgtgtcc
540
tggtatcagc agcatcctgg aaaggctcca aagctcatga tctacgacgt gtcgaacaga
600
ccgtggggtg tgtccaatcg cttttcgggc tccaagttcg gaaacacggc ctcactgact
660
atctcgggac tgcaggccga agatgaagcc gactactact gctcctccta cacctcgtcc
720
tccactctgt acgtgttcgg gtccggcacc aaagtcactg tgctg
765
<210> 525
<211> 765
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 525
caagtgcagc tccagagttc cgaaggcgga gtggtgcagc ctggaaggag cctgcgcctg
60
tcatgcgcag cgtccgggtt caccttctca tcctacggca tgcactgggt cagacaggcc
120
ccgggaaaag gattggaatg ggtggccgtg atttcctaca aggggtcgaa caagtactac
180
gccgattccg tgaagggacg gtttaccatc tcgcgggaca actcgaagaa caccctgtac
240
ctccaaatga acagcctgcg cgccgaagat actgccgtgt actactgcgg cggttccggt
300
tacgcgctcc acgacgacta ttacgggctg gacgtctggg gacagggcac cctggtcact
360
gtgtcctcgt caggtggtgg tggttctggt ggtggcggct caggcggcgg cggctcaggt
420
ggtggaggat cccagtccgc tctgacccaa ccggcttccg tgagcggaag ccccggacag
480
tccattacta tcagctgtac cggcacctcc tccgacgtcg gtggatacaa ctacgtgtcc
540
tggtatcagc agcatcctgg aaaggctcca aagctcatga tctacgacgt gtcgaacaga
600
ccgtggggtg tgtccaatcg cttttcgggc tccaagttcg gaaacacggc ctcactgact
660
atctcgggac tgcaggccga agatgaagcc gactactact gctcctccta cacctcgtcc
720
tccactctgt acgtgttcgg gtccggcacc aaagtcactg tgctg
765
<210> 526
<211> 765
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 526
caagcgcagc tccagagttc cggaggtgga gtggtgcagc ctggaaggag cctgcgcctg
60
tcatgcgcag cgtccgggtt caccgtctca tcctacggca tgcactgggt cagacaggcc
120
ccgggaaaag gattggaatg ggtggccgtg atttcctaca ctgggtccaa caagtactac
180
gccgattccg tgaagggacg gtttaccatc tcgcgggaca actcgaagaa caccctgtac
240
ctccaaatga acagcctgcg cgccgaagat actgccgtgt actactgcgg cggttccggt
300
tacgcgctcc acgacgacta ttacgggctg gacgtctggg gacagggcac cctggtcact
360
gtgtcctcgt caggtggtgg tggttctggt ggtggcggct caggcggcgg cggctcaggt
420
ggtggaggat cccagtccgc tctgacccaa ccggcttccg tgagcggaag ccccggacag
480
tccattacta tcagctgtac cggcacctcc tccgacgtcg gtggatacaa ctacgtgtcc
540
tggtatcagc agcatcctgg aaaggctcca aagctcatga tctacgacgt gtcgaacaga
600
ctgaggggtg tgtccaatcg cttttcgggc tccaagttcg gaaacacggc ctcactgact
660
atctcgggat tgcaggccga agatgaagcc gactactact gctcctccta cacctcgtca
720
tccgctctgt acgtgttcgg gtccggcacc aaagtcactg tgctg
765
<210> 527
<211> 765
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 527
caagtgcagc tccagagttc cggaggcgga gtggtgcagc ctggaaggag cctgcgcctg
60
tcatgcgcag cgtccgggtt caccttctca tcctacggca tgcactgggt cagacaggcc
120
ccgggaaaag gattggaatg ggtggccgtg atttcataca ctggttctaa caagtactac
180
gccgattccg tgaagggacg gtttaccatc tcgcgggaca actcgaagaa caccctgtac
240
ctccaaatga acagcctgcg cgccgaagat actgccgtgt actactgcgg cggttccggt
300
tacgcgctcc acgacgacta ttacgggctg gacgtctggg gacagggcac cctggtcact
360
gtgtcctcgt caggtggtgg tggttctggt ggtggcggct caggcggcgg cggctcaggt
420
ggtggaggat cccagtccgc tctgacccaa ccggcttccg tgagcggaag ccccggacag
480
tccattacta tcagctgtac cggcacctcc tccgacgtcg gtggatacaa ctacgtgtcc
540
tggtatcagc agcatcctgg aaaggctcca aagctcatga tctacgacgt gtcgaacaga
600
gcgtggggtg tgtccaatcg cttttcgggc tccaagttcg gaaacacggc ctcactgact
660
atctcgggac tgcaggccga agatgaagcc gactactact gctcctccta cacctcgtcc
720
tccgctctgt acgtgttcgg gtccggtacc aaagtcactg tgctg
765
<210> 528
<211> 765
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 528
caagcgcagc tccaggggtc cggaggcgga gtggtgcagc ctggaaggag cctgcgcctg
60
tcatgcgcag cgtccgggtt caccttctca tcctacggca tgcactgggt cagacaggcc
120
ccgggaaaag gattggaatg ggtggccgtg atttcctata agggttccaa caagtactac
180
gccgattccg tgaagggacg gtttaccatc tcgcgggaca actcgaagaa caccctgtac
240
ctccaaatga acagcctgcg cgccgaagat actgccgtgt actactgcgg cggttccggt
300
tacgcgctcc acgacgacta ttacgggctg gacgtctggg gacagggcac cctggtcact
360
gtgtcctcgt caggtggtgg tggttctggt ggtggcggct caggcggcgg cggctcaggt
420
ggtggaggat cccagtccgc tctgacccaa ccggcttccg tgagcggaag ccccggacag
480
tccattacta tcagctgtac cggcacctcc tccgacgtcg gtggatacaa ctacgtgtcc
540
tggtatcagc agcatcctgg aaaggctcca aagctcatga tctacgaagt gtcgaacaga
600
ttgagaggtg tgtccaatcg cttttcgggc tccaagttcg gaaacacggc ctcactgact
660
atctcgggac tgcaggccga agatgaagcc gactactact gctcctccta cacctcgtcc
720
tccactctgt acgtgttcgg gtccggcacc aaagtcactg tgctg
765
<210> 529
<211> 82
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 529
Met Leu Gln Met Ala Arg Gln Cys Ser Gln Asn Glu Tyr Phe Asp Ser
1 5 10 15
Leu Leu His Asp Cys Lys Pro Cys Gln Leu Arg Cys Ser Ser Thr Pro
20 25 30
Pro Leu Thr Cys Gln Arg Tyr Cys Asn Ala Ser Met Thr Asn Ser Val
35 40 45
Lys Gly Met Asn Ala Gly Ser His His His His His His Glu Phe Arg
50 55 60
His Asp Ser Gly Leu Asn Asp Ile Phe Glu Ala Gln Lys Ile Glu Trp
65 70 75 80
His Glu
<210> 530
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 530
Ser Gly Tyr Ala Leu His Asp
1 5
<210> 531
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 531
Asp Tyr Tyr Gly Leu Asp Val
1 5
<210> 532
<211> 369
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 532
caagtgcagc tccaggggtc cggaggtgga gtggtgcagc ctggaaggag cctgcgcctg
60
tcatgcgcag cgtccgggtt caccttctca tcctacggca tgcactgggt cagacaggcc
120
ccgggaaaag gattggaatg ggtggccgtg atttcctacg atgatgccca caagtactac
180
gccgattccg tgaagggacg gtttaccatc tcgcgggaca actcgaagaa caccctgtac
240
ctccaaatga acagcctgcg cgccgaagat actgccgtgt actactgcgg cggttccggt
300
tacgcgctcc acgaccagta taagccagtc gatgtctggg gacagggcac cctggtcact
360
gtgtcctcg
369
<210> 533
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 533
cagtccgctc tgacccaacc ggcttccgtg agcggaagcc ccggacagtc cattactatc
60
agctgtaccg gcacctcctc cgacgtcggt ggatacaact acgtgtcctg gtatcagcag
120
catcctggaa aggctccaaa gctcatgatc tacgaagtgt cgaacagact aagcggtgtg
180
tccaatcgct tttcgggctc caagttcgga aacacggcct cactgactat ctcgggactg
240
caggccgaag atgaagccga ctactactgc tcctcctaca cctcgtcctc cgctctgtac
300
gtgttcgggt ccggcaccaa agtcactgtg ctg
333
<210> 534
<211> 369
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 534
caagcgcagc tccaggagtc cgaaggcgga gtggtgcagc ctggagggag cctgcgcctg
60
tcatgcgcag cgtccgggtt caccttctca tcctacggca tgcactgggt cagacaggcc
120
ccgggaaaag gattggaatg ggtggccgtg atttcctaca atgatttgaa caagtactac
180
gccgattccg tgaagggacg gtttaccatc tcgcgggaca actcgaagaa caccctgtac
240
ctccaaatga acagcctgcg cgccgaagat actgccgtgt actactgcgg cggttccggt
300
tacgcgctcc acgacttcca ggatccaaca gatgtctggg gacagggcac cctggtcact
360
gtgtcctcg
369
<210> 535
<211> 369
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 535
caagtgcagc tccagagttc cggaggtgga gtggtgcagc ctggaaggag cctgcgcctg
60
tcatgcgcag cgtccgggtt caccgtctca tcctacggca tgcactgggt cagacaggcc
120
ccgggaaaag gattggaatg ggtggccgtg atttcctaca gtgggtccaa caagtactac
180
gccgattccg tgaagggacg gtttaccatc tcgcgggaca actcgaagaa caccctgtac
240
ctccaaatga acagcctgcg cgccgaagat actgccgtgt actactgcgg cggttccggt
300
tacgcgctcc acgaccagta taagccagtc gatgtctggg gacagggcac cctggtcact
360
gtgtcctcg
369
<210> 536
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 536
cagtccgctc tgacccaacc ggcttccgtg agcggaagcc ccggacagtc cattactatc
60
agctgtaccg gcacctcctc cgacgtcggt ggatacaact acgtgtcctg gtatcagcag
120
catcctggaa aggctccaaa gctcatgatc tacgaggtgt cgaacagact gagcggtgtg
180
tccaatcgct tttcgggctc caagttcgga aacacggcct cactgactat ctcgggactg
240
caggccgaag atgaagccga ctactactgc tcctcctaca cctcgtcctc cgctctgtac
300
gtgttcgggt ccggcaccaa agtcactgtg ctg
333
<210> 537
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 537
cagtccgctc tgacccaacc ggcttccgtg agcggaagcc ccggacagtc cattactatc
60
agctgtaccg gcacctcctc cgacgtcggt ggatacaact acgtgtcctg gtatcagcag
120
catcctggaa aggctccaaa gctcatgatc tacgaagtgt cgaacagact gagaggtgtg
180
tccaatcgct tttcgggctc caagttcgga aacacggcat cactgactat ctcgggactg
240
caggccgaag atgaagccta ctactactgc tcctcctaca cctcgtcctc cactctgtac
300
gtgttcgggt ccggcaccaa agtcactgtg ctg
333
<210> 538
<211> 369
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 538
caagtgcagc tccagggttc cggaggcgga gtggtgcagc ctggaaggag cctgcgcctg
60
tcatgcgcag cgtccgggtt caccttctca tcctacggca tgcactgggt cagacaggcc
120
ccgggaaaag gattggaatg ggtggccgtg atttcctaca ctggggccaa caagtactac
180
gccgattccg tgaagggacg gtttaccatc tcgcgggaca actcgaagaa caccctgtac
240
ctccaaatga acagcctgcg cgccgaagat actgccgtgt actactgcgg cggttctggt
300
tataacttgc acgatgacta ttacgggctg gacgtctggg gacagggcac cctggtcact
360
gtgtcctcg
369
<210> 539
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 539
cagtccgctc tgacccaacc ggcttccgtg agcggaagcc ccggacagtc cattactatc
60
agctgtaccg gcacctcctc cgacgtcggt ggatacaact acgtgtcctg gtatcagcag
120
catcctggaa aggctccaaa gctcatgatc tacgaggtgt cgaacagact gaggggtgtg
180
tccaatcgct tttcgggctc caagttcgga aacacggcct cactgactat ctcgggactg
240
caggccgaag atgaagccga ctactactgc tcctcctaca cctcgtcctc cactctgtac
300
gtgttcgggt ccggcaccaa agtcactgtg ctg
333
<210> 540
<211> 369
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 540
caagcgcagc tccagaggtc cggaggtgga gtggtgcagc ctggaaggag cctgcgcctg
60
tcatgcgcag cgtccgggtt caccttctca tcctacggca tgcactgggt cagacaggcc
120
ccgggaaaag gattggaatg ggtggccgtg atttcctacg atgatgccca caagtactac
180
gccgattccg tgaagggacg gtttaccatc tcgcgggaca actcgaagaa caccctgtac
240
ctccaaatga acagcctgcg cgccgaagat actgccgtgt actactgcgg cggttccggt
300
tacgcgctcc acgaccagta taagccagtc gatgtctggg gacagggcac cctggtcact
360
gtgtcctcg
369
<210> 541
<211> 369
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 541
caagtgcagc tccagagttc cgaaggtgga gtggtgcagc ctggaaggag cctgcgcctg
60
tcatgcgcag cgtccgggtt caccttatca tcctacggca tgcactgggt cagacaggcc
120
ccgggaaaag gattggaatg ggtggccgtg atttcctaca ctgggtccaa taagtactac
180
gccgattccg tgaagggacg gtttaccatc tcgcgggaca actcgaagaa caccctgtac
240
ctccaaatga acagcctgcg cgccgaagat actgccgtgt actactgcgg cggttctggt
300
tatgaattcc acgaagacta ttacgggctg gacgtctggg gacagggcac cctggtcact
360
gtgtcctcg
369
<210> 542
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 542
cagtccgctc tgacccaacc ggcttccgtg agcggaagcc ccggacagtc cattactatc
60
agctgtaccg gcacctcctc cgacgtcggt ggatacaact acgtgtcctg gtatcagcag
120
catcctggaa aggctccaaa gctcatgatc tacgaagtgt cgaacagact gaggggtgtg
180
tccaatcgct tttcgggctc caagttcgga aacacggcct cactgactat ctctggactg
240
caggccgaag atgaagccga ctactactgc tcctcctaca ccacgtcctc cactctgtac
300
gtgttcgggt ccggcaccaa agtcactgtg ctg
333
<210> 543
<211> 369
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 543
caagcgcagc tccaggggtc cgaaggtgga gtggtgcagc ctggaaggag cctgcgcctg
60
tcatgcgcag cgtccgggtt caccttctca tcctacggca tgcactgggt cagacaggcc
120
ccgggaaaag gattggaatg ggtggccgtg atttcctacg atgatgccca caagtactac
180
gccgattccg tgaagggacg gtttaccatc tcgcgggaca actcgaagaa caccctgtac
240
ctccaaatga acagcctgcg cgccgaagat actgccgtgt actactgcgg cggttccggt
300
tacgcgctcc acgaccagta taagccagtc gatgtctggg gacagggcac cctggtcact
360
gtgtcctcg
369
<210> 544
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 544
cagtccgctc tgacccaacc ggcttccgtg agcggaagcc ccggacagtc cattactatc
60
agctgtaccg gcacctcctc cgacgtcggt ggatacaact acgtgtcctg gtatcagcag
120
catcctggaa aggctccaaa gctcatgatc tacgaggtgt cgaacagact gagcggtgtg
180
tccaatcgct tttcgggctc caagttcgga aacacggcct cactgactat ctcgggactg
240
caggccgaag atgaagccga ctactactgc tcctcctaca cctcgtcctc cactctgtac
300
gtgttcgggt ccggcaccaa agtcactgtg ctg
333
<210> 545
<211> 369
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 545
caagtgcagc tccagagttc cggaggtgga gtggtgcagc ctggaaggag cctgcgcctg
60
tcatgcgcag cgtccgggtt caccttctca tcctacggca tgcactgggt cagacaggcc
120
ccgggaaaag gattggaatg ggtggccgtg atttcctaca atgatttgaa caagtactac
180
gccgattccg tgaagggacg gtttaccatc tcgcgggaca actcgaagaa caccctgtac
240
ctccaaatga acagcctgcg cgccgaagat actgccgtgt actactgcgg cggttctggt
300
tatgaattcc agggtgacta ttacgggctg gacgtctggg gacagggcac cctggtcact
360
gtgtcctcg
369
<210> 546
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 546
cagtccgctc tgacccaacc ggcttccgtg agcggaagcc ccggacagtc cattactatc
60
agctgtaccg gcacctcctc cgacgtcggt ggatacaact acgtgtcctg gtatcagcag
120
catcctggaa aggctccaaa gctcatgatc tacgaagtgt cgaacagact gaggggtgtg
180
tccaatcgct tttcgggctc caagttcgga aacacggcct cactgactat ctcgggactg
240
caggccgaag atgaagccga ctactactgc tcctcctaca cctcgtcctc cactctgtac
300
gtgttcgggt ccggcaccaa agtcactgtg ctg
333
<210> 547
<211> 369
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 547
caagtgcagc tccagagttc cgaaggtgga gtggtgcagc ctggaaggag cctgcgcctg
60
tcatgcgcag cgtccgggtt caccttctca tcctacggca tgcactgggt cagacaggcc
120
ccgggaaaag gattggaatg ggtggccgtg atttcctaca atgatgccaa caagtactac
180
gccgattccg tgaagggacg gtttaccatc tcgcgggaca actcgaagaa caccctgtac
240
ctccaaatga acagcctgcg cgccgaagat actgccgtgt actactgcgg cggttctggt
300
tatgaattga gagatgacta ttacgggctg gacgtctggg gacagggcac cctggtcact
360
gtgtcctcg
369
<210> 548
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 548
cagtccgctc tgacccaacc ggcttccgtg agcggaagcc ccggacagtc cattactatc
60
agctgtaccg gcacctcctc cgacgtcggt ggatacaact acgtgtcctg gtatcagcag
120
catcctggaa aggctccaaa gctcatgatc tacgaggtgt cgaacagact gagaggtgtg
180
tccaatcgct tttcgggctc caagttcgga aacacggcct cactgactat ctcgggactg
240
caggccgaag atgaagccga ctactactgc tcctcctaca cctcgtcctc cactctgtac
300
gtgttcgggt ccggcaccaa agtcactgtg ctg
333
<210> 549
<211> 369
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 549
caagcgcagc tccagagttc cgaaggcgga gtggtgcagc ctggaaggag cctgcgtctg
60
tcatgcgcag cgtccgggtt caccttctca tcctacggca tgcactgggt cagacaggcc
120
ccgggaaaag gattggaatg ggtggccgtg atttcctacg atgagtccaa caagtactac
180
gccgattccg tgaagggacg gtttaccatc tcgcgggaca actcgaagaa caccctgtac
240
ctccaaatga acagcctgcg cgccgaagat actgccgtgt actactgcgg cggttctggt
300
tatgaagtcg atcaggacta ttacgggctg gacgtctggg gacagggcac cctggtcact
360
gtgtcctcg
369
<210> 550
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 550
cagtccgctc tgacccaacc ggcttccgtg agcggaagcc ccggacagtc cattactatc
60
agctgtaccg gcacctcctc cgacgtcggt ggatacaact acgtgtcctg gtatcagcag
120
catcctggaa aggctccaaa gctcatgatc tacgaggtgt cgaacagact gcgcggtgtg
180
tccaatcgct tttcgggctc caagttcgga aacacggcct cactgactat ctcgggactg
240
caggccgaag atgaagccga ctactactgc tcctcctaca cctcgtcctc cacactgtac
300
gtgttcgggt ccggcaccaa agtcactgtg ctg
333
<210> 551
<211> 369
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 551
caagtgcagc tccaggagtc cggaggtgga gtggtgcagc ctggaaggag cctgcgcctg
60
tcatgcgcag cgtccgggtt caccttctca tcctacggca tgcactgggt cagacaggcc
120
ccgggaaaag gattggaatg ggtggccgtg atttcctacg atgatgccca caagtactac
180
gccgattccg tgaagggacg gtttaccatc tcgcgggaca actcgaagaa caccctgtac
240
ctccaaatga acagcctgcg cgccgaagat actgccgtgt actactgcgg cggttccggt
300
tacgcgctcc acgaccagta taagccagtc gatgtctggg gacagggcac cctggtcact
360
gtgtcctcg
369
<210> 552
<211> 369
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 552
caagtgcagc tccagggttc cggaggtgga gtggtgcagc ctggaaggag cctgcgcctg
60
tcatgcgcag cgtccgggtt caccgtctca tcctacggca tgcactgggt cagacaggcc
120
ccgggaaaag gattggaatg ggtggccgtg atttcatacg atgatgccaa caagtactac
180
gccgattccg tgaagggacg gtttaccatc tcgcgggaca gctcgaagaa caccctgtac
240
ctccaaatga acagcctgcg cgccgaagat actgccgtgt actactgcgg cggttctggt
300
tatgcttatg atggtgacta ttacgggctg gacgtctggg gacagggcac cctggtcact
360
gtgtcctcg
369
<210> 553
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 553
cagtccgctc tgacccaacc ggcttccgtg agcggaagcc ccggacagtc cattactatc
60
agctgtaccg gcacctcctc cgacgtcggt ggatacaact acgtgtcctg gtatcagcag
120
catcctggaa aggctccaaa gctcatgatc tacgaggtgt cgaacagact gcgcggtgtg
180
tccaatcgct tttcgggctc caagttcgga aacacggcct cactgactat ctcgggactg
240
caggccgaag atgaagccga ctactactgc tcctcctaca cctcgtcctc cgctctgtac
300
gtgttcgggt ccggcaccaa agtcactgtg ctg
333
<210> 554
<211> 363
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 554
gaggtgcagc tgctggagag cgggggtgga ctggtgcagc cgggaggttc cctccggttg
60
tcatgtgccg catccggctt tactttctct tcctacgcca tgtcgtgggt cagacaggcc
120
ccgggaaagg gacttgagtg ggtgtcggcc atctccggtt ccgggggatc cacctactac
180
gcggactccg tgaagggccg cttcactatt tcacgggaca acagcaagaa caccctgtac
240
ctccaaatga actcgctgcg cgccgaagat accgccgtct actactgcgc gcggagggaa
300
tggtggtacg acgattggta tctggactac tggggccagg gcactctcgt gaccgtgtcc
360
agc
363
<210> 555
<211> 224
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 555
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asp Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
<210> 556
<211> 672
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 556
gaggtgcagc tgctggagag cgggggtgga ctggtgcagc cgggaggttc cctccggttg
60
tcatgtgccg catccggctt tactttctct tcctacgcca tgtcgtgggt cagacaggcc
120
ccgggaaagg gacttgagtg ggtgtcggcc atctccggtt ccgggggatc cacctactac
180
gcggactccg tgaagggccg cttcactatt tcacgggaca acagcaagaa caccctgtac
240
ctccaaatga actcgctgcg cgccgaagat accgccgtct actactgcgc gcggagggaa
300
tggtggtacg acgattggta tctggactac tggggccagg gcactctcgt gaccgtgtcc
360
agcgctagca ccaagggccc gtcagtgttt cctctggccc caagctccaa gtccacctcc
420
ggtggtacag ccgcgttggg atgcttggtc aaggactact ttccggaacc cgtgaccgtg
480
tcctggaact ccggcgccct gactagcgga gtgcacacct tccccgctgt gctgcagtct
540
agcgggctgt attccctctc gtccgtggtc accgtgccgt cctcatccct gggaacccag
600
acctacattt gcaacgtgaa ccacaagccg tcagacacca aggtggacaa gaaggtggag
660
ccgaagtcct gc
672
<210> 557
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 557
gacattcaga tgactcagtc cccgtcctcc ttgtccgcct ccgtgggaga cagagtcacc
60
atcacttgcc gggcatcgca gagcatctct tcatacctga actggtatca gcagaagccc
120
ggaaaggccc ctaagctgct gatctacgcg gccagcagcc ttcagtccgg cgtgccatca
180
aggttcagcg gatcgggttc gggcaccgat tttactctga ccattagctc cctgcaaccc
240
gaggacttcg ctacctacta ctgtcagcag tcctactcct ccccgctgac cttcggacaa
300
gggaccaaag tcgaaatcaa g
321
<210> 558
<211> 642
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 558
gacattcaga tgactcagtc cccgtcctcc ttgtccgcct ccgtgggaga cagagtcacc
60
atcacttgcc gggcatcgca gagcatctct tcatacctga actggtatca gcagaagccc
120
ggaaaggccc ctaagctgct gatctacgcg gccagcagcc ttcagtccgg cgtgccatca
180
aggttcagcg gatcgggttc gggcaccgat tttactctga ccattagctc cctgcaaccc
240
gaggacttcg ctacctacta ctgtcagcag tcctactcct ccccgctgac cttcggacaa
300
gggaccaaag tcgaaatcaa gcgtacggtg gccgctccca gcgtgttcat cttccccccc
360
agcgacgagc agctgaagag cggcaccgcc agcgtggtgt gcctgctgaa caacttctac
420
ccccgggagg ccaaggtgca gtggaaggtg gacaacgccc tgcagagcgg caacagccag
480
gagagcgtca ccgagcagga cagcaaggac tccacctaca gcctgagcag caccctgacc
540
ctgagcaagg ccgactacga gaagcataag gtgtacgcct gcgaggtgac ccaccagggc
600
ctgtccagcc ccgtgaccaa gagcttcaac aggggcgagt gc
642
<210> 559
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 559
Arg Ser Lys Ala Asn Asn Tyr Ala
1 5
<210> 560
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 560
Gly Phe Thr Phe Ser Thr Tyr Ala
1 5
<210> 561
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 561
Ile Arg Ser Lys Ala Asn Asn Tyr Ala Thr
1 5 10
<210> 562
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 562
Val Arg His Gly Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe Ala Tyr
1 5 10 15
<210> 563
<211> 375
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 563
gaagtgcagc ttgtggagtc cgggggagga ttggtccaac ccggtggctc gctgaggctg
60
agttgcgccg cttcggggtt taccttcagc acctacgcta tgaactgggt cagacaggcg
120
cctggaaagg gtttggagtg ggtcggacgc atccggtcca aggccaacaa ctacgcgact
180
tactatgccg actccgtcaa gggacggttc accatctccc gggacgacag caagaacacc
240
ctgtacctcc aaatgaactc ccttcgggcc gaagataccg ccgtgtacta ctgcgtgaga
300
cacggcaact tcggcgactc ctacgtgtcc tggtttgcct actggggcca gggtactctc
360
gtgaccgtgt catca
375
<210> 564
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 564
Thr Gly Ala Val Thr Thr Ser Asn Tyr
1 5
<210> 565
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 565
Gly Thr Asn Lys Arg Ala Pro Gly Val Pro
1 5 10
<210> 566
<211> 327
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 566
caggctgtgg tcacccagga accctccctg actgtgtccc cgggaggaac cgtgacactg
60
acttgtggca gctccaccgg agccgtgacc acctccaact acgccaactg ggtgcagcaa
120
aagccaggaa agtcccctag ggggctgatc ggtggcacga acaagcgggc acctggagtg
180
cctgcccgat tctcgggtag cctgctgggg ggaaaagccg ccctgaccat ttcgggcgct
240
cagccagagg acgaagccga ctattactgc gcactctggt actccaacca ctgggtgttc
300
ggtggaggca ccaagctgac cgtgctg
327
<210> 567
<211> 762
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 567
gaagtgcagc ttgtggagtc cgggggagga ttggtccaac ccggtggctc gctgaggctg
60
agttgcgccg cttcggggtt taccttcagc acctacgcta tgaactgggt cagacaggcg
120
cctggaaagg gtttggagtg ggtcggacgc atccggtcca aggccaacaa ctacgcgact
180
tactatgccg actccgtcaa gggacggttc accatctccc gggacgacag caagaacacc
240
ctgtacctcc aaatgaactc ccttcgggcc gaagataccg ccgtgtacta ctgcgtgaga
300
cacggcaact tcggcgactc ctacgtgtcc tggtttgcct actggggcca gggtactctc
360
gtgaccgtgt catcaggaaa gccaggctcg gggaagcctg gctccggaaa gcctgggagc
420
ggaaagccgg gatcgcaggc tgtggtcacc caggaaccct ccctgactgt gtccccggga
480
ggaaccgtga cactgacttg tggcagctcc accggagccg tgaccacctc caactacgcc
540
aactgggtgc agcaaaagcc aggaaagtcc cctagggggc tgatcggtgg cacgaacaag
600
cgggcacctg gagtgcctgc ccgattctcg ggtagcctgc tggggggaaa agccgccctg
660
accatttcgg gcgctcagcc agaggacgaa gccgactatt actgcgcact ctggtactcc
720
aaccactggg tgttcggtgg aggcaccaag ctgaccgtgc tg
762
<210> 568
<211> 1350
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 568
gaggtgcagc tgctggagag cgggggtgga ctggtgcagc cgggaggttc cctccggttg
60
tcatgtgccg catccggctt tactttctct tcctacgcca tgtcgtgggt cagacaggcc
120
ccgggaaagg gacttgagtg ggtgtcggcc atctccggtt ccgggggatc cacctactac
180
gcggactccg tgaagggccg cttcactatt tcacgggaca acagcaagaa caccctgtac
240
ctccaaatga actcgctgcg cgccgaagat accgccgtct actactgcgc gcggagggaa
300
tggtggtacg acgattggta tctggactac tggggccagg gcactctcgt gaccgtgtcc
360
agcgctagca ccaagggccc gtcagtgttt cctctggccc caagctccaa gtccacctcc
420
ggtggtacag ccgcgttggg atgcttggtc aaggactact ttccggaacc cgtgaccgtg
480
tcctggaact ccggcgccct gactagcgga gtgcacacct tccccgctgt gctgcagtct
540
agcgggctgt attccctctc gtccgtggtc accgtgccgt cctcatccct gggaacccag
600
acctacattt gcaacgtgaa ccacaagccg tcagacacca aggtggacaa gaaggtggag
660
ccgaagtcct gcgacaagac ccatacttgt cctccttgcc ccgctccacc tgtggcggga
720
ccttccgtgt tccttttccc gccgaagccg aaggacactc tgatgatctc gcggactccc
780
gaagtcactt gcgtggtggt ggacgtcaaa cacgaagatc ccgaggtcaa gttcaattgg
840
tacgtggacg gggtggaagt ccacaacgcc aagactaagc cgcgcgagga agagtacaat
900
tccacttacc gggtcgtgtc ggtgctgact gtgctgcatc aggactggct gaacggaaag
960
gagtacaagt gcaaagtgtc gaacaaggcc ctgcctgcac caatcgaaaa gaccattagc
1020
aaagccaagg gccagccgag agaaccccaa gtctacactc tgccaccatc ccgcgaagaa
1080
atgaccaaga accaagtgtc gctgacgtgc gacgtgtcgg gattctaccc gtccgatatt
1140
gccgtggaat gggagagcga cggccaaccc gagaacaact acaagactac cccccccgtc
1200
ttggattccg atggttcctt cttcctgtac tccaagctga ccgtggataa gtcccgatgg
1260
gagcagggcg atgtgttctc gtgctccgtg atgcatgaag ccctgcacaa ccactatacc
1320
cagaagtcac tgtcgctgag ccctgggaag
1350
<210> 569
<211> 1455
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 569
gaagtgcagc ttgtggagtc cgggggagga ttggtccaac ccggtggctc gctgaggctg
60
agttgcgccg cttcggggtt taccttcagc acctacgcta tgaactgggt cagacaggcg
120
cctggaaagg gtttggagtg ggtcggacgc atccggtcca aggccaacaa ctacgcgact
180
tactatgccg actccgtcaa gggacggttc accatctccc gggacgacag caagaacacc
240
ctgtacctcc aaatgaactc ccttcgggcc gaagataccg ccgtgtacta ctgcgtgaga
300
cacggcaact tcggcgactc ctacgtgtcc tggtttgcct actggggcca gggtactctc
360
gtgaccgtgt catcaggaaa gccaggctcg gggaagcctg gctccggaaa gcctgggagc
420
ggaaagccgg gatcgcaggc tgtggtcacc caggaaccct ccctgactgt gtccccggga
480
ggaaccgtga cactgacttg tggcagctcc accggagccg tgaccacctc caactacgcc
540
aactgggtgc agcaaaagcc aggaaagtcc cctagggggc tgatcggtgg cacgaacaag
600
cgggcacctg gagtgcctgc ccgattctcg ggtagcctgc tggggggaaa agccgccctg
660
accatttcgg gcgctcagcc agaggacgaa gccgactatt actgcgcact ctggtactcc
720
aaccactggg tgttcggtgg aggcaccaag ctgaccgtgc tggagccaaa gtcaagcgac
780
aaaactcaca cttgccctcc ttgtccggct cctcctgtgg ctggtccctc cgtgttcctc
840
ttcccgccga agccgaagga caccctcatg atttcccgga cgcccgaagt cacttgtgtg
900
gtggtcgatg tgaagcatga ggaccccgaa gtgaagttca attggtacgt ggatggcgtg
960
gaggtccaca acgccaagac caagccgcgc gaagaacagt acaacagcac ctaccgcgtc
1020
gtgagcgtgc tcaccgtgct ccaccaagat tggctgaacg gaaaggagta caagtgcaaa
1080
gtgtccaaca aggcccttcc tgcacctatt gaaaagacta ttagcaaggc caagggacag
1140
ccccgcgaac ctcaagtgta cactctgccg ccgtccagag agcagatgac caaaaaccag
1200
gtcaagctca cttgtctcgt gaagggcttc tacccgtccg atatcgcggt cgaatgggag
1260
tcaaacggcc agcccgagaa caactacaag actaccccac cggtgcttga ctccgacggt
1320
tcgttctttc tgtactccaa gctgaccgtg gacaagtccc ggtggcagca agggaatgtg
1380
ttcagctgct ccgtgatgca cgaagccctg cataaccact acacccagaa gtcgctcagc
1440
ctgtcccctg gaaaa
1455
<210> 570
<211> 363
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 570
gaagtgcaac ttttggaaag cggaggcgga ttggtgcaac ctggcggctc actgagactg
60
agctgcgccg cctccggatt cactttctcc tcctacgcca tgtcctgggt ccgacaggcg
120
cccgggaagg gcctcgaatg ggtgtcggcc atttccggat ctggtggaag cacctactac
180
gctgatagcg tgaagggtcg cttcaccatt tcgcgcgaca attcgaagaa caccctgtat
240
ctgcaaatga atagcttgag agccgaagat accgccgtgt actactgcgc acggcgggag
300
tggtggtacg acgattggta cctggactac tgggggcagg ggacactcgt gaccgtgtcg
360
agc
363
<210> 571
<211> 672
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 571
gaagtgcaac ttttggaaag cggaggcgga ttggtgcaac ctggcggctc actgagactg
60
agctgcgccg cctccggatt cactttctcc tcctacgcca tgtcctgggt ccgacaggcg
120
cccgggaagg gcctcgaatg ggtgtcggcc atttccggat ctggtggaag cacctactac
180
gctgatagcg tgaagggtcg cttcaccatt tcgcgcgaca attcgaagaa caccctgtat
240
ctgcaaatga atagcttgag agccgaagat accgccgtgt actactgcgc acggcgggag
300
tggtggtacg acgattggta cctggactac tgggggcagg ggacactcgt gaccgtgtcg
360
agcgcttcca ccaagggacc gagcgtgttc ccgctggcgc cgagcagcaa atcgacttct
420
gggggaaccg cagccctggg ttgcctggtc aaggactact tcccggaacc agtcactgtg
480
tcctggaaca gcggtgccct cacctcgggc gtgcacacct tcccggccgt gctgcagtct
540
agcggactct actcgctctc ctccgtggtc accgtgccct cctcatcact gggaacccag
600
acatacattt gcaacgtgaa ccacaagccc tcggacacta aggtggacaa aaaagtggaa
660
ccaaagtcct gc
672
<210> 572
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 572
gacattcaga tgacccagtc cccgagctcc ctgtcggctt ccgtgggcga cagagtgacg
60
attacttgcc gcgcgtccca aagcatctcc tcctacctga actggtacca gcagaagccg
120
ggaaaggccc caaagctgtt gatctacgcc gcctcatcgc tccaatctgg agtgccttcc
180
cggttttcgg ggtcgggcag cgggactgat ttcaccctga ccatcagcag cctgcagcct
240
gaagatttcg ccacctacta ctgccagcag tcctattcct cacccctgac tttcggacaa
300
ggcaccaagg tcgagatcaa g
321
<210> 573
<211> 642
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 573
gacattcaga tgacccagtc cccgagctcc ctgtcggctt ccgtgggcga cagagtgacg
60
attacttgcc gcgcgtccca aagcatctcc tcctacctga actggtacca gcagaagccg
120
ggaaaggccc caaagctgtt gatctacgcc gcctcatcgc tccaatctgg agtgccttcc
180
cggttttcgg ggtcgggcag cgggactgat ttcaccctga ccatcagcag cctgcagcct
240
gaagatttcg ccacctacta ctgccagcag tcctattcct cacccctgac tttcggacaa
300
ggcaccaagg tcgagatcaa gcgtacggtg gctgcaccat ctgtcttcat cttcccgcca
360
tctgatgagc agttgaaatc tggaactgcc tctgttgtgt gcctgctgaa taacttctat
420
cccagagagg ccaaagtaca gtggaaggtg gataacgccc tccaatcggg taactcccag
480
gagagtgtca cagagcagga cagcaaggac agcacctaca gcctcagcag caccctgacg
540
ctgagcaaag cagactacga gaaacacaaa gtctacgcct gcgaagtcac ccatcagggc
600
ctgagctcgc ccgtcacaaa gagcttcaac aggggagagt gt
642
<210> 574
<211> 375
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 574
gaggtgcagc tcgtcgaatc cggtggaggg ctggtgcaac cggggggctc gcttaggctt
60
agctgcgctg cgtcagggtt caccttctca acttacgcga tgaattgggt cagacaggca
120
cccggaaagg gactggaatg ggtcggaaga atcagatcga aggccaacaa ctacgccact
180
tactacgccg actccgtgaa gggaaggttc actatctcgc gggacgactc caagaacact
240
ctgtatctcc aaatgaactc actccgggcc gaggatactg cggtgtacta ttgcgtgcgg
300
catggaaact tcggggacag ctacgtcagc tggttcgcct actggggcca aggcactctc
360
gtcaccgtgt catcc
375
<210> 575
<211> 327
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 575
caggccgtcg tgacccagga accgagcctg accgtgtccc ccggcggtac cgtgaccttg
60
acttgcggtt cctccactgg agccgtgact acctcgaact acgccaactg ggtgcagcag
120
aagccgggaa agtcgcctcg cggactgatc ggtggaacta acaaacgcgc cccgggcgtg
180
ccagccagat tcagcggtag cctgctcggc ggaaaggccg cgctgaccat ctccggggcc
240
cagcccgagg atgaggccga ctattactgc gctctgtggt actccaacca ctgggtgttt
300
ggcgggggca ctaagctgac tgtgctg
327
<210> 576
<211> 762
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 576
gaggtgcagc tcgtcgaatc cggtggaggg ctggtgcaac cggggggctc gcttaggctt
60
agctgcgctg cgtcagggtt caccttctca acttacgcga tgaattgggt cagacaggca
120
cccggaaagg gactggaatg ggtcggaaga atcagatcga aggccaacaa ctacgccact
180
tactacgccg actccgtgaa gggaaggttc actatctcgc gggacgactc caagaacact
240
ctgtatctcc aaatgaactc actccgggcc gaggatactg cggtgtacta ttgcgtgcgg
300
catggaaact tcggggacag ctacgtcagc tggttcgcct actggggcca aggcactctc
360
gtcaccgtgt catccgggaa gccgggttcc ggaaagcctg gatcgggcaa accgggatcg
420
ggaaaacccg gaagccaggc cgtcgtgacc caggaaccga gcctgaccgt gtcccccggc
480
ggtaccgtga ccttgacttg cggttcctcc actggagccg tgactacctc gaactacgcc
540
aactgggtgc agcagaagcc gggaaagtcg cctcgcggac tgatcggtgg aactaacaaa
600
cgcgccccgg gcgtgccagc cagattcagc ggtagcctgc tcggcggaaa ggccgcgctg
660
accatctccg gggcccagcc cgaggatgag gccgactatt actgcgctct gtggtactcc
720
aaccactggg tgtttggcgg gggcactaag ctgactgtgc tg
762
<210> 577
<211> 1350
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 577
gaagtgcaac ttttggaaag cggaggcgga ttggtgcaac ctggcggctc actgagactg
60
agctgcgccg cctccggatt cactttctcc tcctacgcca tgtcctgggt ccgacaggcg
120
cccgggaagg gcctcgaatg ggtgtcggcc atttccggat ctggtggaag cacctactac
180
gctgatagcg tgaagggtcg cttcaccatt tcgcgcgaca attcgaagaa caccctgtat
240
ctgcaaatga atagcttgag agccgaagat accgccgtgt actactgcgc acggcgggag
300
tggtggtacg acgattggta cctggactac tgggggcagg ggacactcgt gaccgtgtcg
360
agcgcttcca ccaagggacc gagcgtgttc ccgctggcgc cgagcagcaa atcgacttct
420
gggggaaccg cagccctggg ttgcctggtc aaggactact tcccggaacc agtcactgtg
480
tcctggaaca gcggtgccct cacctcgggc gtgcacacct tcccggccgt gctgcagtct
540
agcggactct actcgctctc ctccgtggtc accgtgccct cctcatcact gggaacccag
600
acatacattt gcaacgtgaa ccacaagccc tcggacacta aggtggacaa aaaagtggaa
660
ccaaagtcct gcgacaagac ccacacttgt ccgccctgcc ctgcccctcc cgtggcgggc
720
ccgtcagtgt ttctgtttcc gccaaagcct aaggataccc tcatgatcag ccgcactcct
780
gaagtgacct gtgtcgtggt ggacgtgaaa cacgaggacc cggaggtcaa gtttaattgg
840
tacgtggatg gggtggaggt gcacaacgcc aaaactaagc cccgggaaga agagtacaat
900
tccacctacc gcgtcgtgtc agtgttgacg gtcctgcacc aagactggct gaacggaaag
960
gagtacaagt gcaaggtgtc caacaaggca ctgcccgccc ccatcgaaaa gaccatttca
1020
aaagctaagg gccagccgcg ggaaccacag gtctacaccc tgcctccctc ccgggaagag
1080
atgaccaaga accaagtctc cctcacgtgt gacgtgtccg gcttctaccc ttcggacatt
1140
gctgtggaat gggagtccga cgggcagccc gaaaacaact acaagaccac tccccctgtg
1200
ctggactccg acggctcatt ctttctgtac tccaagctca ccgtcgataa gtcgagatgg
1260
gagcagggag atgtgttctc ctgctccgtg atgcacgagg ccctgcataa ccattacact
1320
cagaagtccc tctccctgtc ccctgggaag
1350
<210> 578
<211> 2169
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 578
gaagtgcaac ttttggaaag cggaggcgga ttggtgcaac ctggcggctc actgagactg
60
agctgcgccg cctccggatt cactttctcc tcctacgcca tgtcctgggt ccgacaggcg
120
cccgggaagg gcctcgaatg ggtgtcggcc atttccggat ctggtggaag cacctactac
180
gctgatagcg tgaagggtcg cttcaccatt tcgcgcgaca attcgaagaa caccctgtat
240
ctgcaaatga atagcttgag agccgaagat accgccgtgt actactgcgc acggcgggag
300
tggtggtacg acgattggta cctggactac tgggggcagg ggacactcgt gaccgtgtcg
360
agcgcttcca ccaagggacc gagcgtgttc ccgctggcgc cgagcagcaa atcgacttct
420
gggggaaccg cagccctggg ttgcctggtc aaggactact tcccggaacc agtcactgtg
480
tcctggaaca gcggtgccct cacctcgggc gtgcacacct tcccggccgt gctgcagtct
540
agcggactct actcgctctc ctccgtggtc accgtgccct cctcatcact gggaacccag
600
acatacattt gcaacgtgaa ccacaagccg tccaacacca aggtcgacaa gaaagtggag
660
cctaagtcct gtggtggcgg aggctccggc ggaggaggat cggaggtgca gctcgtcgaa
720
tccggtggag ggctggtgca accggggggc tcgcttaggc ttagctgcgc tgcgtcaggg
780
ttcaccttct caacttacgc gatgaattgg gtcagacagg cacccggaaa gggactggaa
840
tgggtcggaa gaatcagatc gaaggccaac aactacgcca cttactacgc cgactccgtg
900
aagggaaggt tcactatctc gcgggacgac tccaagaaca ctctgtatct ccaaatgaac
960
tcactccggg ccgaggatac tgcggtgtac tattgcgtgc ggcatggaaa cttcggggac
1020
agctacgtca gctggttcgc ctactggggc caaggcactc tcgtcaccgt gtcatccggg
1080
aagccgggtt ccggaaagcc tggatcgggc aaaccgggat cgggaaaacc cggaagccag
1140
gccgtcgtga cccaggaacc gagcctgacc gtgtcccccg gcggtaccgt gaccttgact
1200
tgcggttcct ccactggagc cgtgactacc tcgaactacg ccaactgggt gcagcagaag
1260
ccgggaaagt cgcctcgcgg actgatcggt ggaactaaca aacgcgcccc gggcgtgcca
1320
gccagattca gcggtagcct gctcggcgga aaggccgcgc tgaccatctc cggggcccag
1380
cccgaggatg aggccgacta ttactgcgct ctgtggtact ccaaccactg ggtgtttggc
1440
gggggcacta agctgactgt gctgggcggc ggcggctccg gggggggggg ctccaagacc
1500
cacacttgtc cgccctgccc tgcccctccc gtggcgggcc cgtcagtgtt tctgtttccg
1560
ccaaagccta aggataccct catgatcagc cgcactcctg aagtgacctg tgtcgtggtg
1620
gacgtgaaac acgaggaccc ggaggtcaag tttaattggt acgtggatgg ggtggaggtg
1680
cacaacgcca aaactaagcc ccgggaagaa cagtacaatt ccacctaccg cgtcgtgtca
1740
gtgttgacgg tcctgcacca agactggctg aacggaaagg agtacaagtg caaggtgtcc
1800
aacaaggcac tgcccgcccc catcgaaaag accatttcaa aagctaaggg ccagccgcgg
1860
gaaccacagg tctacaccct gcctccctcc cgggaacaga tgaccaagaa ccaagtcaag
1920
ctcacgtgtc tcgtgaaggg cttctaccct tcggacattg ctgtggaatg ggagtccaac
1980
gggcagcccg aaaacaacta caagaccact ccccctgtgc tggactccga cggctcattc
2040
tttctgtact ccaagctcac cgtcgataag tcgagatggc agcagggaaa cgtgttctcc
2100
tgctccgtga tgcacgaggc cctgcataac cattacactc agaagtccct ctccctgtcc
2160
cctgggaag
2169
<210> 579
<211> 363
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 579
gaagtgcagc tgctggagag cggcggaggt ctggtgcagc caggcggatc cttgcgcctc
60
agttgtgccg cgtccggatt cactttctcg tcttacgcca tgtcctgggt cagacaggcc
120
cctgggaagg gtctggagtg ggtgtccgcg atcagcgagt caggagggag agccgcctac
180
gccgactccg tgaagggccg ctttaccatt tcgcgggaca actccaagaa caccctgtac
240
cttcaaatga acagcctgcg ggcagaggac accgccgtct actactgcgc ccggagggaa
300
tggtggtacg atgattggta tctggactac tggggccagg gaactctcgt gaccgtgtcc
360
tcg
363
<210> 580
<211> 224
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 580
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Glu Ser Gly Gly Arg Ala Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asp Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
<210> 581
<211> 672
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 581
gaagtgcagc tgctggagag cggcggaggt ctggtgcagc caggcggatc cttgcgcctc
60
agttgtgccg cgtccggatt cactttctcg tcttacgcca tgtcctgggt cagacaggcc
120
cctgggaagg gtctggagtg ggtgtccgcg atcagcgagt caggagggag agccgcctac
180
gccgactccg tgaagggccg ctttaccatt tcgcgggaca actccaagaa caccctgtac
240
cttcaaatga acagcctgcg ggcagaggac accgccgtct actactgcgc ccggagggaa
300
tggtggtacg atgattggta tctggactac tggggccagg gaactctcgt gaccgtgtcc
360
tcggctagca ccaagggccc gtcagtgttt cctctggccc caagctccaa gtccacctcc
420
ggtggtacag ccgcgttggg atgcttggtc aaggactact ttccggaacc cgtgaccgtg
480
tcctggaact ccggcgccct gactagcgga gtgcacacct tccccgctgt gctgcagtct
540
agcgggctgt attccctctc gtccgtggtc accgtgccgt cctcatccct gggaacccag
600
acctacattt gcaacgtgaa ccacaagccg tcagacacca aggtggacaa gaaggtggag
660
ccgaagtcct gc
672
<210> 582
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 582
gacattcaga tgacccagtc cccgtcctcg ctgagcgcat cagtcggcga tcgcgtgact
60
attacttgtc gggcgtccca gtcgatctcc tcgtacttga actggtatca gcagaagccc
120
ggaaaagccc cgaagttact gatctacgct gcctcatccc tccaatctgg ggtgccttcg
180
cggttctccg gttccggaag cggaaccgac ttcaccctga ccatcagcag cctgcagcca
240
gaggactttg ccacctacta ctgccagcag tcctactcca cacccctcac tttcggacaa
300
ggcaccaagg tcgaaatcaa g
321
<210> 583
<211> 642
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 583
gacattcaga tgacccagtc cccgtcctcg ctgagcgcat cagtcggcga tcgcgtgact
60
attacttgtc gggcgtccca gtcgatctcc tcgtacttga actggtatca gcagaagccc
120
ggaaaagccc cgaagttact gatctacgct gcctcatccc tccaatctgg ggtgccttcg
180
cggttctccg gttccggaag cggaaccgac ttcaccctga ccatcagcag cctgcagcca
240
gaggactttg ccacctacta ctgccagcag tcctactcca cacccctcac tttcggacaa
300
ggcaccaagg tcgaaatcaa gcgtacggtg gccgctccca gcgtgttcat cttccccccc
360
agcgacgagc agctgaagag cggcaccgcc agcgtggtgt gcctgctgaa caacttctac
420
ccccgggagg ccaaggtgca gtggaaggtg gacaacgccc tgcagagcgg caacagccag
480
gagagcgtca ccgagcagga cagcaaggac tccacctaca gcctgagcag caccctgacc
540
ctgagcaagg ccgactacga gaagcataag gtgtacgcct gcgaggtgac ccaccagggc
600
ctgtccagcc ccgtgaccaa gagcttcaac aggggcgagt gc
642
<210> 584
<211> 1350
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 584
gaagtgcagc tgctggagag cggcggaggt ctggtgcagc caggcggatc cttgcgcctc
60
agttgtgccg cgtccggatt cactttctcg tcttacgcca tgtcctgggt cagacaggcc
120
cctgggaagg gtctggagtg ggtgtccgcg atcagcgagt caggagggag agccgcctac
180
gccgactccg tgaagggccg ctttaccatt tcgcgggaca actccaagaa caccctgtac
240
cttcaaatga acagcctgcg ggcagaggac accgccgtct actactgcgc ccggagggaa
300
tggtggtacg atgattggta tctggactac tggggccagg gaactctcgt gaccgtgtcc
360
tcggctagca ccaagggccc gtcagtgttt cctctggccc caagctccaa gtccacctcc
420
ggtggtacag ccgcgttggg atgcttggtc aaggactact ttccggaacc cgtgaccgtg
480
tcctggaact ccggcgccct gactagcgga gtgcacacct tccccgctgt gctgcagtct
540
agcgggctgt attccctctc gtccgtggtc accgtgccgt cctcatccct gggaacccag
600
acctacattt gcaacgtgaa ccacaagccg tcagacacca aggtggacaa gaaggtggag
660
ccgaagtcct gcgacaagac ccatacttgt cctccttgcc ccgctccacc tgtggcggga
720
ccttccgtgt tccttttccc gccgaagccg aaggacactc tgatgatctc gcggactccc
780
gaagtcactt gcgtggtggt ggacgtcaaa cacgaagatc ccgaggtcaa gttcaattgg
840
tacgtggacg gggtggaagt ccacaacgcc aagactaagc cgcgcgagga agagtacaat
900
tccacttacc gggtcgtgtc ggtgctgact gtgctgcatc aggactggct gaacggaaag
960
gagtacaagt gcaaagtgtc gaacaaggcc ctgcctgcac caatcgaaaa gaccattagc
1020
aaagccaagg gccagccgag agaaccccaa gtctacactc tgccaccatc ccgcgaagaa
1080
atgaccaaga accaagtgtc gctgacgtgc gacgtgtcgg gattctaccc gtccgatatt
1140
gccgtggaat gggagagcga cggccaaccc gagaacaact acaagactac cccccccgtc
1200
ttggattccg atggttcctt cttcctgtac tccaagctga ccgtggataa gtcccgatgg
1260
gagcagggcg atgtgttctc gtgctccgtg atgcatgaag ccctgcacaa ccactatacc
1320
cagaagtcac tgtcgctgag ccctgggaag
1350
<210> 585
<211> 672
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 585
gaagtgcagc tgctggagag cggcggaggt ctggtgcagc caggcggatc cttgcgcctc
60
agttgtgccg cgtccggatt cactttctcg tcttacgcca tgtcctgggt cagacaggcc
120
cctgggaagg gtctggagtg ggtgtccgcg atcagcgagt caggagggag agccgcctac
180
gccgactccg tgaagggccg ctttaccatt tcgcgggaca actccaagaa caccctgtac
240
cttcaaatga acagcctgcg ggcagaggac accgccgtct actactgcgc ccggagggaa
300
tggtggtacg atgattggta tctggactac tggggccagg gaactctcgt gaccgtgtcc
360
tcggctagca ccaagggtcc gtcagtgttt cctctggccc caagctccaa gtccacctcc
420
ggtggtacag ccgcgttggg atgcttggtc aaggactact ttccggaacc cgtgaccgtg
480
tcctggaact ccggcgccct gactagcgga gtgcacacct tccccgctgt gctgcagtct
540
agcgggctgt attccctctc gtccgtggtc accgtgccgt cctcatccct gggaacccag
600
acctacattt gcaacgtgaa ccacaagccg tcagacacca aggtggacaa gaaggtggag
660
ccgaagtcct gc
672
<210> 586
<211> 375
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 586
gaagtccaac tggtcgagtc aggcggcgga cttgtccagc ccggaggtag cctgcgcctc
60
tcctgtgctg cctccggttt taccttctcg acctatgcca tgaactgggt gcgccaagca
120
cctgggaagg gactcgaatg ggtcggcagg attcggtcca aggccaacaa ctacgctacc
180
tactacgccg actcggtcaa ggggcggttc actatttccc gcgacgactc caagaacact
240
ctgtatcttc agatgaatag cttgagagcc gaggataccg ccgtgtacta ttgcgtgcgc
300
cacgggaact tcggcgattc ctacgtgtcc tggttcgctt actggggaca gggcaccctg
360
gtcaccgtgt caagc
375
<210> 587
<211> 326
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 587
aggcggtggt gacccaagaa ccctccctga ccgtgtcacc gggaggcacc gtgaccctga
60
cttgcgggag ctccactggc gcagtgacta catccaacta cgccaactgg gtgcagcaga
120
agcctggaaa gtccccgaga ggactcattg gaggaaccaa caagagagcc cctggtgtcc
180
ctgcccgctt tagcggttcg ctgttgggag gaaaggccgc tctgactatt tccggcgctc
240
agccagagga cgaggctgac tactactgcg cattgtggta ctccaatcac tgggtgttcg
300
gagggggcac taagctgacc gtgctg
326
<210> 588
<211> 762
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 588
gaagtccaac tggtcgagtc aggcggcgga cttgtccagc ccggaggtag cctgcgcctc
60
tcctgtgctg cctccggttt taccttctcg acctatgcca tgaactgggt gcgccaagca
120
cctgggaagg gactcgaatg ggtcggcagg attcggtcca aggccaacaa ctacgctacc
180
tactacgccg actcggtcaa ggggcggttc actatttccc gcgacgactc caagaacact
240
ctgtatcttc agatgaatag cttgagagcc gaggataccg ccgtgtacta ttgcgtgcgc
300
cacgggaact tcggcgattc ctacgtgtcc tggttcgctt actggggaca gggcaccctg
360
gtcaccgtgt caagcggaaa gcccgggtcc ggaaaacccg ggtcgggaaa gccggggagc
420
ggaaagcccg gttcacaggc ggtggtgacc caagaaccct ccctgaccgt gtcaccggga
480
ggcaccgtga ccctgacttg cgggagctcc actggcgcag tgactacatc caactacgcc
540
aactgggtgc agcagaagcc tggaaagtcc ccgagaggac tcattggagg aaccaacaag
600
agagcccctg gtgtccctgc ccgctttagc ggttcgctgt tgggaggaaa ggccgctctg
660
actatttccg gcgctcagcc agaggacgag gctgactact actgcgcatt gtggtactcc
720
aatcactggg tgttcggagg gggcactaag ctgaccgtgc tg
762
<210> 589
<211> 1350
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 589
gaagtgcagc tgctggagag cggcggaggt ctggtgcagc caggcggatc cttgcgcctc
60
agttgtgccg cgtccggatt cactttctcg tcttacgcca tgtcctgggt cagacaggcc
120
cctgggaagg gtctggagtg ggtgtccgcg atcagcgagt caggagggag agccgcctac
180
gccgactccg tgaagggccg ctttaccatt tcgcgggaca actccaagaa caccctgtac
240
cttcaaatga acagcctgcg ggcagaggac accgccgtct actactgcgc ccggagggaa
300
tggtggtacg atgattggta tctggactac tggggccagg gaactctcgt gaccgtgtcc
360
tcggctagca ccaagggtcc gtcagtgttt cctctggccc caagctccaa gtccacctcc
420
ggtggtacag ccgcgttggg atgcttggtc aaggactact ttccggaacc cgtgaccgtg
480
tcctggaact ccggcgccct gactagcgga gtgcacacct tccccgctgt gctgcagtct
540
agcgggctgt attccctctc gtccgtggtc accgtgccgt cctcatccct gggaacccag
600
acctacattt gcaacgtgaa ccacaagccg tcagacacca aggtggacaa gaaggtggag
660
ccgaagtcct gcgacaagac ccatacttgt cctccttgcc ccgctccacc tgtggcggga
720
ccttccgtgt tccttttccc gccgaagccg aaggacactc tgatgatctc gcggactccc
780
gaagtcactt gcgtggtggt ggacgtcaaa cacgaagatc ccgaggtcaa gttcaattgg
840
tacgtggacg gggtggaagt ccacaacgcc aagactaagc cgcgcgagga agagtacaat
900
tccacttacc gggtcgtgtc ggtgctgact gtgctgcatc aggactggct gaacggaaag
960
gagtacaagt gcaaagtgtc gaacaaggcc ctgcctgcac caatcgaaaa gaccattagc
1020
aaagccaagg gccagccgag agaaccccaa gtctacactc tgccaccatc ccgcgaagaa
1080
atgaccaaga accaagtgtc gctgacgtgc gacgtgtcgg gattctaccc gtccgatatt
1140
gccgtggaat gggagagcga cggccaaccc gagaacaact acaagactac cccccccgtc
1200
ttggattccg atggttcctt cttcctgtac tccaagctga ccgtggataa gtcccgatgg
1260
gagcagggcg atgtgttctc gtgctccgtg atgcatgaag ccctgcacaa ccactatacc
1320
cagaagtcac tgtcgctgag ccctgggaag
1350
<210> 590
<211> 2169
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 590
gaagtgcagc tgctggagag cggcggaggt ctggtgcagc caggcggatc cttgcgcctc
60
agttgtgccg cgtccggatt cactttctcg tcttacgcca tgtcctgggt cagacaggcc
120
cctgggaagg gtctggagtg ggtgtccgcg atcagcgagt caggagggag agccgcctac
180
gccgactccg tgaagggccg ctttaccatt tcgcgggaca actccaagaa caccctgtac
240
cttcaaatga acagcctgcg ggcagaggac accgccgtct actactgcgc ccggagggaa
300
tggtggtacg atgattggta tctggactac tggggccagg gaactctcgt gaccgtgtcc
360
tcggctagca ccaagggccc ttcggtgttc cccctcgccc cttcatcaaa gtccacttca
420
ggaggaaccg ccgccttggg ttgcctcgtg aaggattact tccccgaacc agtgaccgtg
480
tcctggaact ccggagccct gaccagcgga gtgcacactt tccctgcggt gttgcagagc
540
tccggcctct acagcctgag cagcgtggtg accgtgccga gctcctccct gggcactcag
600
acctacatct gcaacgtcaa ccacaagccc tcgaatacca aggtcgacaa gaaggtggag
660
ccgaagtcct gtggcggagg aggatcggga gggggtggat cggaagtcca actggtcgag
720
tcaggcggcg gacttgtcca gcccggaggt agcctgcgcc tctcctgtgc tgcctccggt
780
tttaccttct cgacctatgc catgaactgg gtgcgccaag cacctgggaa gggactcgaa
840
tgggtcggca ggattcggtc caaggccaac aactacgcta cctactacgc cgactcggtc
900
aaggggcggt tcactatttc ccgcgacgac tccaagaaca ctctgtatct tcagatgaat
960
agcttgagag ccgaggatac cgccgtgtac tattgcgtgc gccacgggaa cttcggcgat
1020
tcctacgtgt cctggttcgc ttactgggga cagggcaccc tggtcaccgt gtcaagcgga
1080
aagcccgggt ccggaaaacc cgggtcggga aagccgggga gcggaaagcc cggttcacag
1140
gcggtggtga cccaagaacc ctccctgacc gtgtcaccgg gaggcaccgt gaccctgact
1200
tgcgggagct ccactggcgc agtgactaca tccaactacg ccaactgggt gcagcagaag
1260
cctggaaagt ccccgagagg actcattgga ggaaccaaca agagagcccc tggtgtccct
1320
gcccgcttta gcggttcgct gttgggagga aaggccgctc tgactatttc cggcgctcag
1380
ccagaggacg aggctgacta ctactgcgca ttgtggtact ccaatcactg ggtgttcgga
1440
gggggcacta agctgaccgt gctgggtggt ggcggatctg gtggtggcgg ctcgaaaacc
1500
cacacctgtc caccttgtcc ggcgcctcct gtcgctggac cctccgtgtt cctcttccct
1560
cccaagccga aggatacgct gatgatcagc cggacccccg aagtgacttg tgtggtggtg
1620
gatgtgaagc acgaagatcc cgaagtcaag ttcaactggt acgtggacgg agtggaggtc
1680
cacaatgcca agaccaagcc gcgggaagaa cagtacaact cgacctaccg ggtggtcagc
1740
gtgctgactg tgctccacca agactggctg aacgggaagg agtacaagtg caaagtgtcg
1800
aacaaggccc ttcctgcacc tatcgaaaag accatctcca aggcgaaagg acagccgaga
1860
gagccccagg tctacactct gccgccatcc agagagcaaa tgaccaagaa ccaagtcaag
1920
ctgacctgtc ttgtcaaggg tttctacccg tccgatatcg cggtcgaatg ggagtcaaac
1980
ggccagcccg agaacaacta caagactacc ccaccggtgc ttgactccga cggttcgttc
2040
tttctgtact ccaagctgac cgtggacaag tcccggtggc agcaagggaa tgtgttcagc
2100
tgctccgtga tgcacgaagc cctgcataac cactacaccc agaagtcgct cagcctgtcc
2160
cctggaaaa
2169
<210> 591
<211> 369
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 591
caagtgcagc tcgtggagtc tggaggggga gtcgtgcagc ctggacgctc cctgagactg
60
tcctgtgcgg cttcgggatt cactgtgtcc agctacggca tgcattgggt ccgccaagca
120
ccgggaaaag gcctggagtg ggtggccgtg atctcctaca ccggctcaaa caagtactac
180
gccgacagcg tgaagggccg gttcaccatt tcaagggaca actccaagaa taccctgtat
240
ctgcaaatga actcgctgcg ggcagaggac accgccgtgt actactgcgg tggctccggt
300
tacgccctgc acgatgacta ctacgggctc gatgtctggg gacaggggac gctcgtgact
360
gtgtcctcg
369
<210> 592
<211> 226
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 592
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
195 200 205
Asn His Lys Pro Ser Asp Thr Lys Val Asp Lys Lys Val Glu Pro Lys
210 215 220
Ser Cys
225
<210> 593
<211> 678
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 593
caagtgcagc tcgtggagtc tggaggggga gtcgtgcagc ctggacgctc cctgagactg
60
tcctgtgcgg cttcgggatt cactgtgtcc agctacggca tgcattgggt ccgccaagca
120
ccgggaaaag gcctggagtg ggtggccgtg atctcctaca ccggctcaaa caagtactac
180
gccgacagcg tgaagggccg gttcaccatt tcaagggaca actccaagaa taccctgtat
240
ctgcaaatga actcgctgcg ggcagaggac accgccgtgt actactgcgg tggctccggt
300
tacgccctgc acgatgacta ctacgggctc gatgtctggg gacaggggac gctcgtgact
360
gtgtcctcgg ctagcaccaa gggcccgtca gtgtttcctc tggccccaag ctccaagtcc
420
acctccggtg gtacagccgc gttgggatgc ttggtcaagg actactttcc ggaacccgtg
480
accgtgtcct ggaactccgg cgccctgact agcggagtgc acaccttccc cgctgtgctg
540
cagtctagcg ggctgtattc cctctcgtcc gtggtcaccg tgccgtcctc atccctggga
600
acccagacct acatttgcaa cgtgaaccac aagccgtcag acaccaaggt ggacaagaag
660
gtggagccga agtcctgc
678
<210> 594
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 594
cagtcggcgc tgactcagcc cgcatccgtg agcggttcac cgggacagag catcaccatt
60
tcctgcaccg gaacctcaag cgacgtgggc ggctacaact acgtgtcctg gtatcagcag
120
cacccgggaa aggccccaaa gctcatgatc tacgacgtgt ccaatagact gcggggagtg
180
tccaaccggt tctcgggaag caaatccggc aacactgctt ccctgaccat cagcggactc
240
caggccgaag atgaggccga ctactactgc tcatcctaca cgtcctcttc ggcgctttac
300
gtgttcgggt cggggaccaa ggtcaccgtc ctg
333
<210> 595
<211> 651
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 595
cagtcggcgc tgactcagcc cgcatccgtg agcggttcac cgggacagag catcaccatt
60
tcctgcaccg gaacctcaag cgacgtgggc ggctacaact acgtgtcctg gtatcagcag
120
cacccgggaa aggccccaaa gctcatgatc tacgacgtgt ccaatagact gcggggagtg
180
tccaaccggt tctcgggaag caaatccggc aacactgctt ccctgaccat cagcggactc
240
caggccgaag atgaggccga ctactactgc tcatcctaca cgtcctcttc ggcgctttac
300
gtgttcgggt cggggaccaa ggtcaccgtc ctgggccaac ctaaggcggc gccctcagtg
360
accctgttcc ctccgtcgtc tgaagaactc caggccaaca aggccaccct cgtgtgcctg
420
atttcggact tctacccggg agccgtcact gtggcctgga aggccgacag cagcccagtg
480
aaggccggcg tggaaactac caccccgtcc aagcagtcca acaataagta cgcagccagc
540
tcctacctgt ccctgacccc cgaacaatgg aagtcacaca gatcctactc ctgtcaagtc
600
acccacgagg gcagcactgt cgaaaagacc gtggcaccga ctgagtgctc g
651
<210> 596
<211> 1356
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 596
caagtgcagc tcgtggagtc tggaggggga gtcgtgcagc ctggacgctc cctgagactg
60
tcctgtgcgg cttcgggatt cactgtgtcc agctacggca tgcattgggt ccgccaagca
120
ccgggaaaag gcctggagtg ggtggccgtg atctcctaca ccggctcaaa caagtactac
180
gccgacagcg tgaagggccg gttcaccatt tcaagggaca actccaagaa taccctgtat
240
ctgcaaatga actcgctgcg ggcagaggac accgccgtgt actactgcgg tggctccggt
300
tacgccctgc acgatgacta ctacgggctc gatgtctggg gacaggggac gctcgtgact
360
gtgtcctcgg ctagcaccaa gggcccgtca gtgtttcctc tggccccaag ctccaagtcc
420
acctccggtg gtacagccgc gttgggatgc ttggtcaagg actactttcc ggaacccgtg
480
accgtgtcct ggaactccgg cgccctgact agcggagtgc acaccttccc cgctgtgctg
540
cagtctagcg ggctgtattc cctctcgtcc gtggtcaccg tgccgtcctc atccctggga
600
acccagacct acatttgcaa cgtgaaccac aagccgtcag acaccaaggt ggacaagaag
660
gtggagccga agtcctgcga caagacccat acttgtcctc cttgccccgc tccacctgtg
720
gcgggacctt ccgtgttcct tttcccgccg aagccgaagg acactctgat gatctcgcgg
780
actcccgaag tcacttgcgt ggtggtggac gtcaaacacg aagatcccga ggtcaagttc
840
aattggtacg tggacggggt ggaagtccac aacgccaaga ctaagccgcg cgaggaagag
900
tacaattcca cttaccgggt cgtgtcggtg ctgactgtgc tgcatcagga ctggctgaac
960
ggaaaggagt acaagtgcaa agtgtcgaac aaggccctgc ctgcaccaat cgaaaagacc
1020
attagcaaag ccaagggcca gccgagagaa ccccaagtct acactctgcc accatcccgc
1080
gaagaaatga ccaagaacca agtgtcgctg acgtgcgacg tgtcgggatt ctacccgtcc
1140
gatattgccg tggaatggga gagcgacggc caacccgaga acaactacaa gactaccccc
1200
cccgtcttgg attccgatgg ttccttcttc ctgtactcca agctgaccgt ggataagtcc
1260
cgatgggagc agggcgatgt gttctcgtgc tccgtgatgc atgaagccct gcacaaccac
1320
tatacccaga agtcactgtc gctgagccct gggaag
1356
<210> 597
<211> 369
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 597
caagtgcagc ttgtggagtc gggaggggga gtggtgcagc ctggtcgctc actgaggctg
60
agctgtgctg cctccggctt taccgtgtcc tcctacggaa tgcattgggt cagacaggca
120
ccgggaaaag gcctggaatg ggtggccgtc atcagctaca ccggctccaa caagtactac
180
gccgactcag tgaaggggcg gttcactatt agccgcgata actcgaagaa taccctgtat
240
ctgcaaatga actctttgcg ggccgaagat accgccgtgt actactgcgg aggctccggt
300
tacgcgctcc acgacgacta ctacggactg gacgtgtggg gacaggggac tctcgtgacc
360
gtgtcgtcc
369
<210> 598
<211> 678
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 598
caagtgcagc ttgtggagtc gggaggggga gtggtgcagc ctggtcgctc actgaggctg
60
agctgtgctg cctccggctt taccgtgtcc tcctacggaa tgcattgggt cagacaggca
120
ccgggaaaag gcctggaatg ggtggccgtc atcagctaca ccggctccaa caagtactac
180
gccgactcag tgaaggggcg gttcactatt agccgcgata actcgaagaa taccctgtat
240
ctgcaaatga actctttgcg ggccgaagat accgccgtgt actactgcgg aggctccggt
300
tacgcgctcc acgacgacta ctacggactg gacgtgtggg gacaggggac tctcgtgacc
360
gtgtcgtccg ctagcaccaa gggaccgagc gtgttcccgc tggcgccgag cagcaaatcg
420
acttctgggg gaaccgcagc cctgggttgc ctggtcaagg actacttccc ggaaccagtc
480
actgtgtcct ggaacagcgg tgccctcacc tcgggcgtgc acaccttccc ggccgtgctg
540
cagtctagcg gactctactc gctctcctcc gtggtcaccg tgccctcctc atcactggga
600
acccagacat acatttgcaa cgtgaaccac aagccctcgg acactaaggt ggacaaaaaa
660
gtggaaccaa agtcctgc
678
<210> 599
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 599
caatccgccc tgactcagcc ggccagcgtg tcaggttccc cgggccaaag cattaccatc
60
tcctgcactg ggacctcctc cgatgtcggg ggctacaact acgtgtcgtg gtatcagcag
120
caccctggaa aggcgcccaa gctgatgatc tacgacgtgt ccaaccggct gaggggagtc
180
agcaaccgct tcagcggctc caagtccgga aacaccgcat cactcacaat cagcggtctg
240
caggctgagg atgaagcgga ctactactgt tcctcctaca cctcctcctc ggcgctttac
300
gtctttgggt cgggaaccaa agtcactgtg ctg
333
<210> 600
<211> 651
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 600
caatccgccc tgactcagcc ggccagcgtg tcaggttccc cgggccaaag cattaccatc
60
tcctgcactg ggacctcctc cgatgtcggg ggctacaact acgtgtcgtg gtatcagcag
120
caccctggaa aggcgcccaa gctgatgatc tacgacgtgt ccaaccggct gaggggagtc
180
agcaaccgct tcagcggctc caagtccgga aacaccgcat cactcacaat cagcggtctg
240
caggctgagg atgaagcgga ctactactgt tcctcctaca cctcctcctc ggcgctttac
300
gtctttgggt cgggaaccaa agtcactgtg ctgggacagc cgaaggcagc cccatccgtg
360
accctgttcc ccccgtcatc cgaggaactg caggctaaca aggccaccct cgtgtgcctg
420
attagcgact tctaccctgg agccgtgacc gtggcctgga aggccgactc cagcccagtg
480
aaggccggag tggagactac caccccgagc aaacagtcga acaataagta cgccgcgtca
540
tcgtacctgt ccctcacgcc cgaacagtgg aagtcccata gatcgtactc ctgccaagtg
600
acccacgagg gcagcactgt ggaaaagact gtggccccta ccgagtgctc t
651
<210> 601
<211> 1356
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 601
caagtgcagc ttgtggagtc gggaggggga gtggtgcagc ctggtcgctc actgaggctg
60
agctgtgctg cctccggctt taccgtgtcc tcctacggaa tgcattgggt cagacaggca
120
ccgggaaaag gcctggaatg ggtggccgtc atcagctaca ccggctccaa caagtactac
180
gccgactcag tgaaggggcg gttcactatt agccgcgata actcgaagaa taccctgtat
240
ctgcaaatga actctttgcg ggccgaagat accgccgtgt actactgcgg aggctccggt
300
tacgcgctcc acgacgacta ctacggactg gacgtgtggg gacaggggac tctcgtgacc
360
gtgtcgtccg ctagcaccaa gggaccgagc gtgttcccgc tggcgccgag cagcaaatcg
420
acttctgggg gaaccgcagc cctgggttgc ctggtcaagg actacttccc ggaaccagtc
480
actgtgtcct ggaacagcgg tgccctcacc tcgggcgtgc acaccttccc ggccgtgctg
540
cagtctagcg gactctactc gctctcctcc gtggtcaccg tgccctcctc atcactggga
600
acccagacat acatttgcaa cgtgaaccac aagccctcgg acactaaggt ggacaaaaaa
660
gtggaaccaa agtcctgcga caagacccac acttgtccgc cctgccctgc ccctcccgtg
720
gcgggcccgt cagtgtttct gtttccgcca aagcctaagg ataccctcat gatcagccgc
780
actcctgaag tgacctgtgt cgtggtggac gtgaaacacg aggacccgga ggtcaagttt
840
aattggtacg tggatggggt ggaggtgcac aacgccaaaa ctaagccccg ggaagaagag
900
tacaattcca cctaccgcgt cgtgtcagtg ttgacggtcc tgcaccaaga ctggctgaac
960
ggaaaggagt acaagtgcaa ggtgtccaac aaggcactgc ccgcccccat cgaaaagacc
1020
atttcaaaag ctaagggcca gccgcgggaa ccacaggtct acaccctgcc tccctcccgg
1080
gaagagatga ccaagaacca agtctccctc acgtgtgacg tgtccggctt ctacccttcg
1140
gacattgctg tggaatggga gtccgacggg cagcccgaaa acaactacaa gaccactccc
1200
cctgtgctgg actccgacgg ctcattcttt ctgtactcca agctcaccgt cgataagtcg
1260
agatgggagc agggagatgt gttctcctgc tccgtgatgc acgaggccct gcataaccat
1320
tacactcaga agtccctctc cctgtcccct gggaag
1356
<210> 602
<211> 2175
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полинуклеотид"
<400> 602
caagtgcagc ttgtggagtc gggaggggga gtggtgcagc ctggtcgctc actgaggctg
60
agctgtgctg cctccggctt taccgtgtcc tcctacggaa tgcattgggt cagacaggca
120
ccgggaaaag gcctggaatg ggtggccgtc atcagctaca ccggctccaa caagtactac
180
gccgactcag tgaaggggcg gttcactatt agccgcgata actcgaagaa taccctgtat
240
ctgcaaatga actctttgcg ggccgaagat accgccgtgt actactgcgg aggctccggt
300
tacgcgctcc acgacgacta ctacggactg gacgtgtggg gacaggggac tctcgtgacc
360
gtgtcgtccg ctagcaccaa gggaccgagc gtgttcccgc tggcgccgag cagcaaatcg
420
acttctgggg gaaccgcagc cctgggttgc ctggtcaagg actacttccc ggaaccagtc
480
actgtgtcct ggaacagcgg tgccctcacc tcgggcgtgc acaccttccc ggccgtgctg
540
cagtctagcg gactctactc gctctcctcc gtggtcaccg tgccctcctc atcactggga
600
acccagacat acatttgcaa cgtgaaccac aagccgtcca acaccaaggt cgacaagaaa
660
gtggagccta agtcctgtgg tggcggaggc tccggcggag gaggatcgga ggtgcagctc
720
gtcgaatccg gtggagggct ggtgcaaccg gggggctcgc ttaggcttag ctgcgctgcg
780
tcagggttca ccttctcaac ttacgcgatg aattgggtca gacaggcacc cggaaaggga
840
ctggaatggg tcggaagaat cagatcgaag gccaacaact acgccactta ctacgccgac
900
tccgtgaagg gaaggttcac tatctcgcgg gacgactcca agaacactct gtatctccaa
960
atgaactcac tccgggccga ggatactgcg gtgtactatt gcgtgcggca tggaaacttc
1020
ggggacagct acgtcagctg gttcgcctac tggggccaag gcactctcgt caccgtgtca
1080
tccgggaagc cgggttccgg aaagcctgga tcgggcaaac cgggatcggg aaaacccgga
1140
agccaggccg tcgtgaccca ggaaccgagc ctgaccgtgt cccccggcgg taccgtgacc
1200
ttgacttgcg gttcctccac tggagccgtg actacctcga actacgccaa ctgggtgcag
1260
cagaagccgg gaaagtcgcc tcgcggactg atcggtggaa ctaacaaacg cgccccgggc
1320
gtgccagcca gattcagcgg tagcctgctc ggcggaaagg ccgcgctgac catctccggg
1380
gcccagcccg aggatgaggc cgactattac tgcgctctgt ggtactccaa ccactgggtg
1440
tttggcgggg gcactaagct gactgtgctg ggcggcggcg gctccggggg ggggggctcc
1500
aagacccaca cttgtccgcc ctgccctgcc cctcccgtgg cgggcccgtc agtgtttctg
1560
tttccgccaa agcctaagga taccctcatg atcagccgca ctcctgaagt gacctgtgtc
1620
gtggtggacg tgaaacacga ggacccggag gtcaagttta attggtacgt ggatggggtg
1680
gaggtgcaca acgccaaaac taagccccgg gaagaacagt acaattccac ctaccgcgtc
1740
gtgtcagtgt tgacggtcct gcaccaagac tggctgaacg gaaaggagta caagtgcaag
1800
gtgtccaaca aggcactgcc cgcccccatc gaaaagacca tttcaaaagc taagggccag
1860
ccgcgggaac cacaggtcta caccctgcct ccctcccggg aacagatgac caagaaccaa
1920
gtcaagctca cgtgtctcgt gaagggcttc tacccttcgg acattgctgt ggaatgggag
1980
tccaacgggc agcccgaaaa caactacaag accactcccc ctgtgctgga ctccgacggc
2040
tcattctttc tgtactccaa gctcaccgtc gataagtcga gatggcagca gggaaacgtg
2100
ttctcctgct ccgtgatgca cgaggccctg cataaccatt acactcagaa gtccctctcc
2160
ctgtcccctg ggaag
2175
<210> 603
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетическая 6xHis метка"
<400> 603
His His His His His His
1 5
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ТРИСПЕЦИФИЧЕСКИЕ МОЛЕКУЛЫ, СВЯЗЫВАЮЩИЕ BCMA, И ПУТИ ИХ ПРИМЕНЕНИЯ | 2020 |
|
RU2829901C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ ДЛЯ BCMA И ПУТИ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2785658C2 |
| АНТИ-BCMA АНТИТЕЛА, СОДЕРЖАЩИЕ ТОЛЬКО ТЯЖЁЛУЮ ЦЕПЬ | 2017 |
|
RU2781301C2 |
| МОЛЕКУЛЫ, СВЯЗЫВАЮЩИЕ ADAM9, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2783619C2 |
| НАЦЕЛЕННЫЕ НА ОПУХОЛЬ АГОНИСТИЧЕСКИЕ CD28-АНТИГЕНСВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2019 |
|
RU2837821C1 |
| НАЦЕЛЕННЫЕ НА ОПУХОЛЬ АГОНИСТИЧЕСКИЕ CD28-АНТИГЕНСВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2019 |
|
RU2808030C2 |
| РЕАГЕНТЫ ДЛЯ РАЗМНОЖЕНИЯ КЛЕТОК, ЭКСПРЕССИРУЮЩИХ РЕКОМБИНАНТНЫЕ РЕЦЕПТОРЫ | 2018 |
|
RU2783956C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ КЛЕТОК, ЭКСПРЕССИРУЮЩИХ ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР | 2019 |
|
RU2822196C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ И ПУТИ ИХ ПРИМЕНЕНИЯ | 2020 |
|
RU2841244C2 |
| АНТИТЕЛА, СВЯЗЫВАЮЩИЕ CD3 | 2017 |
|
RU2807216C2 |

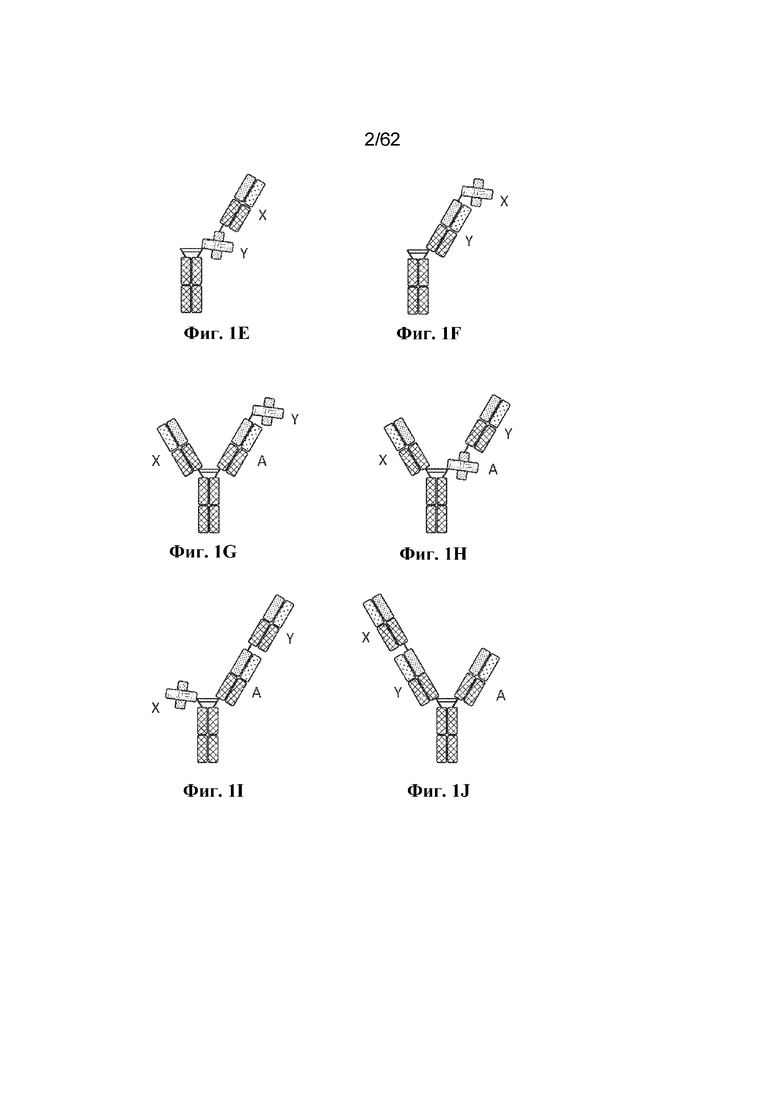
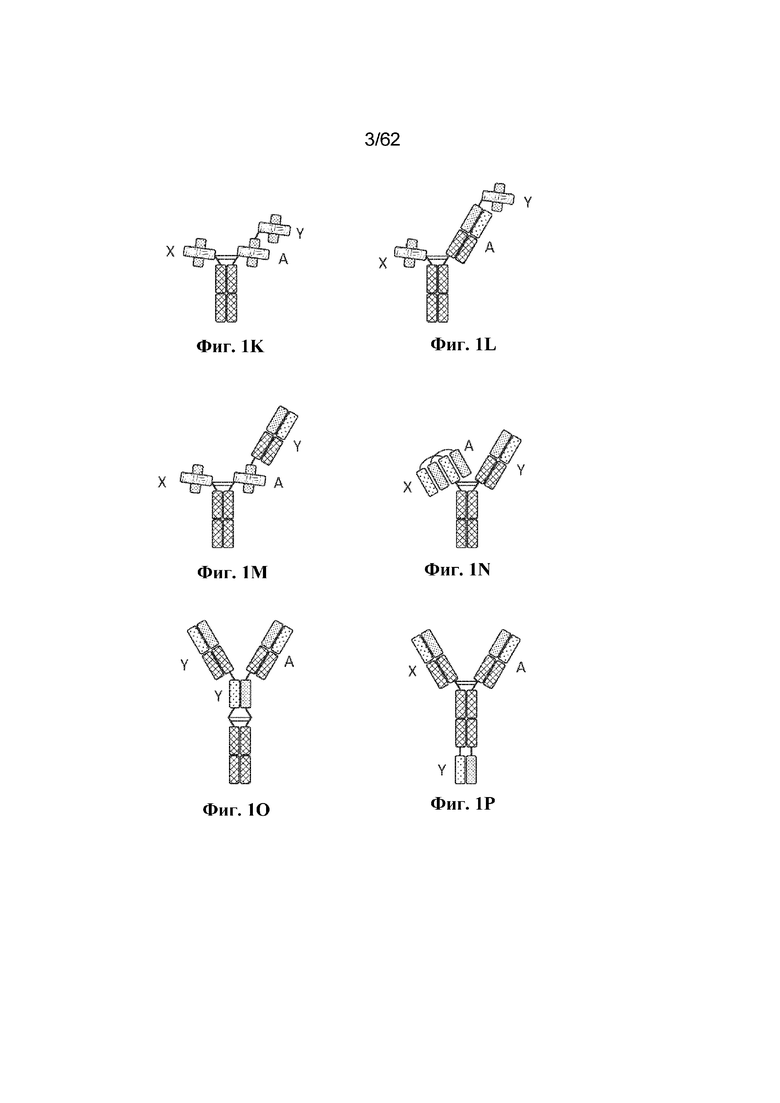
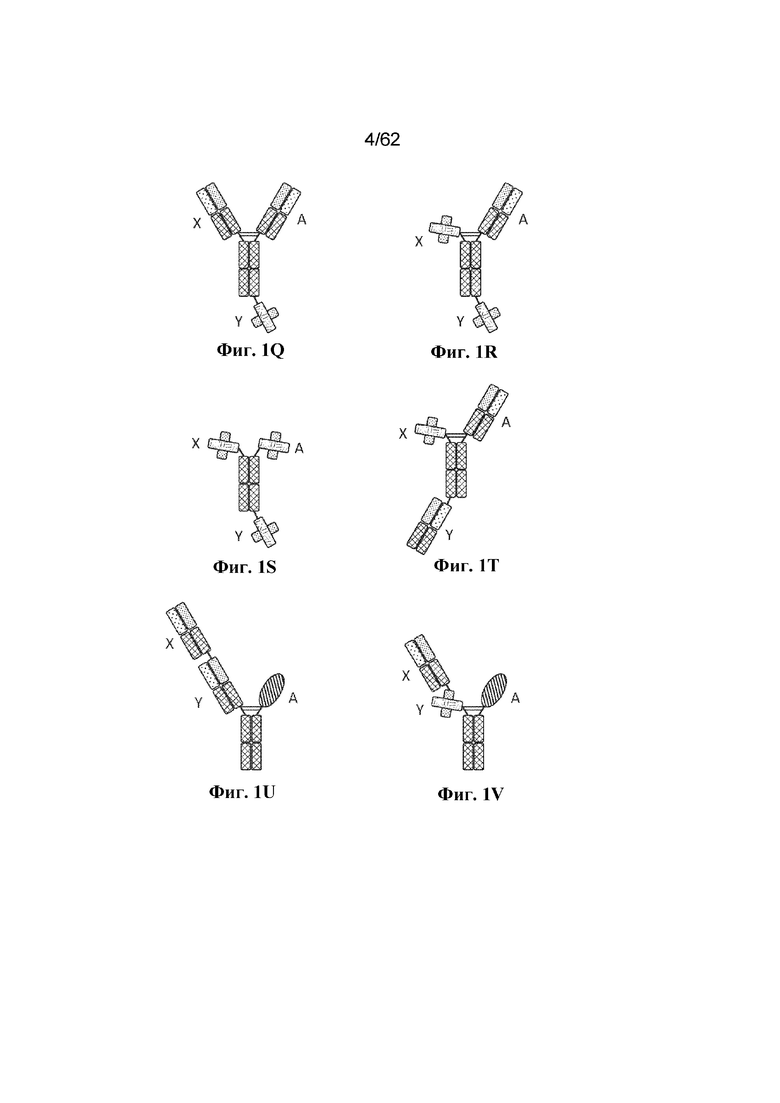
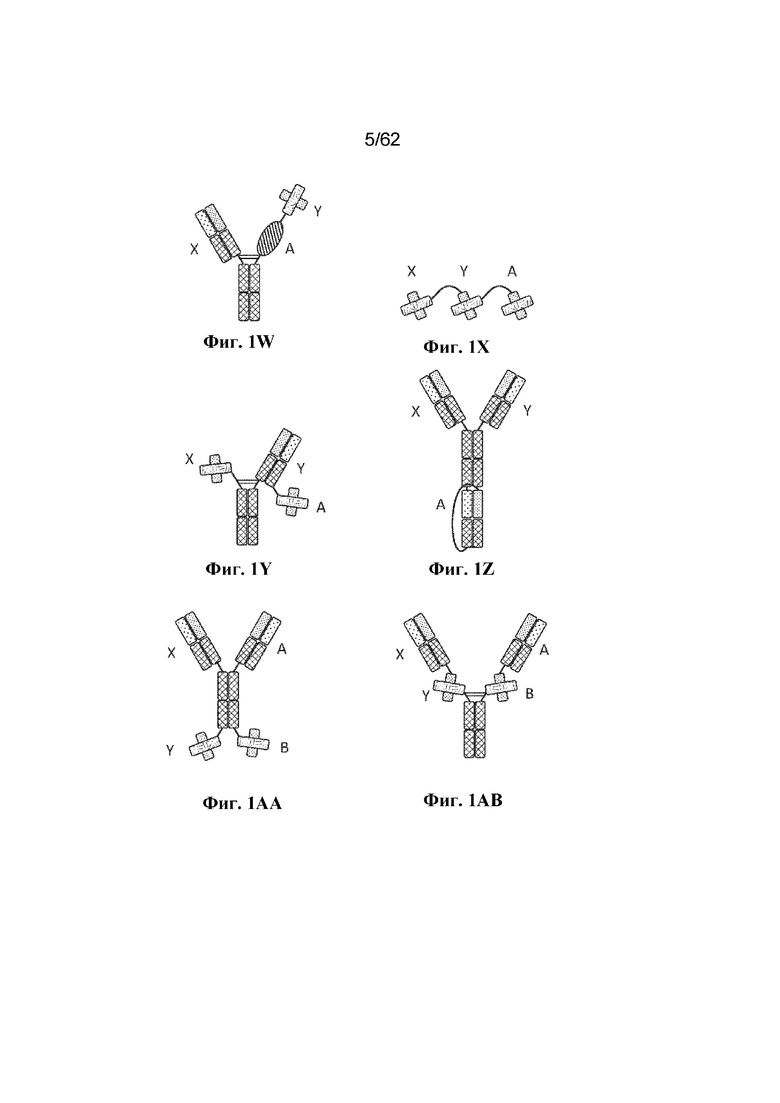
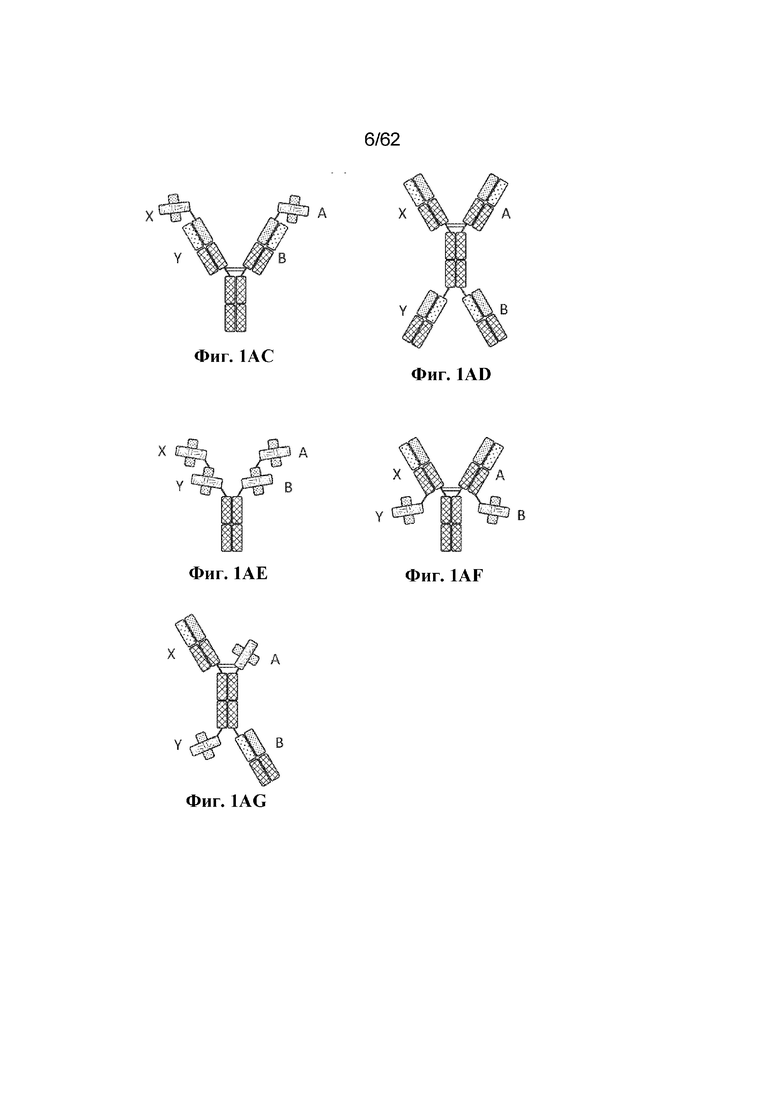


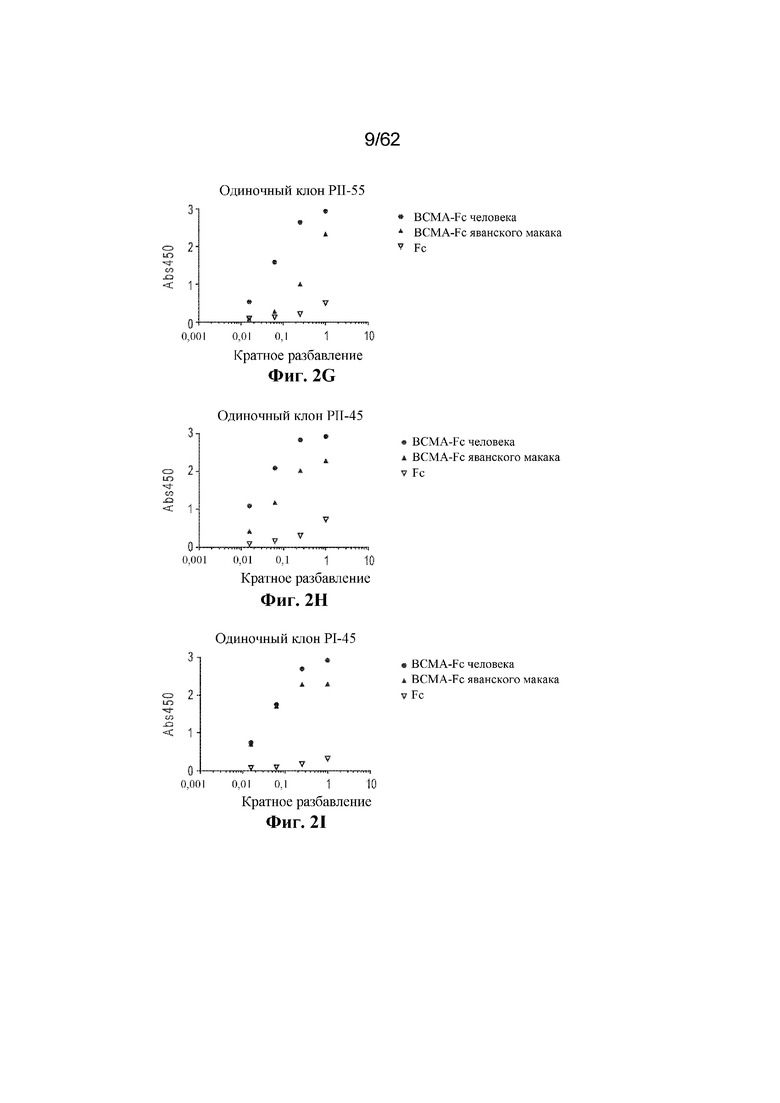
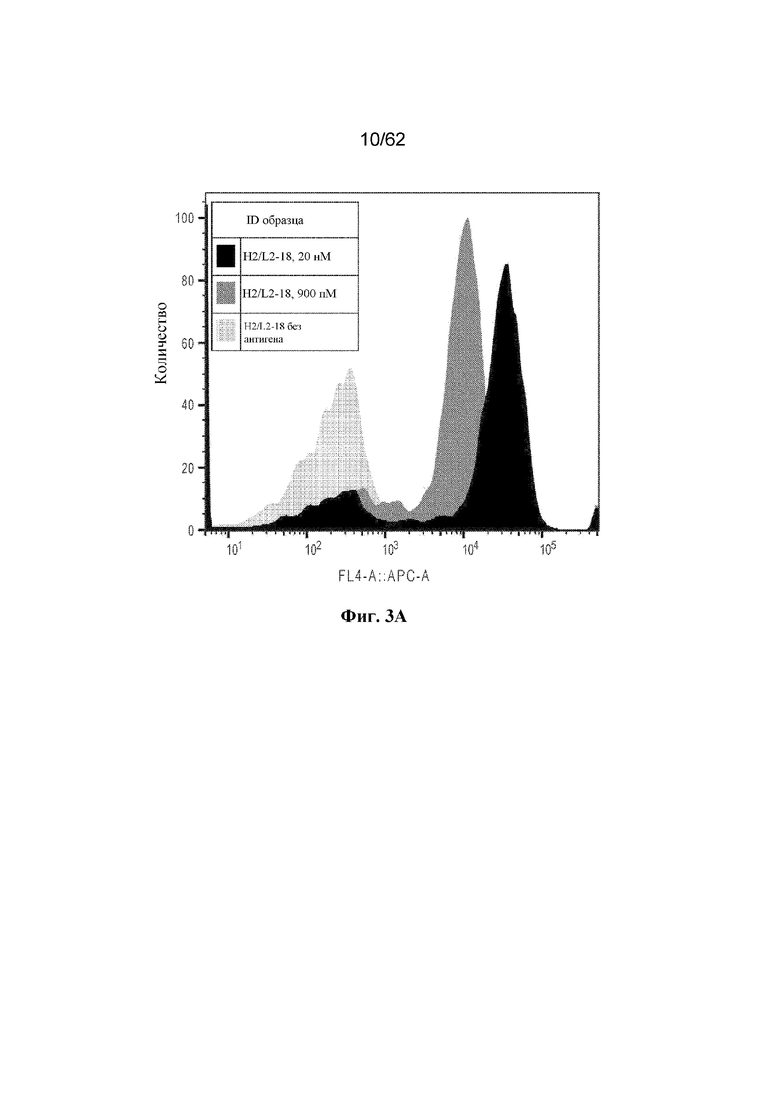
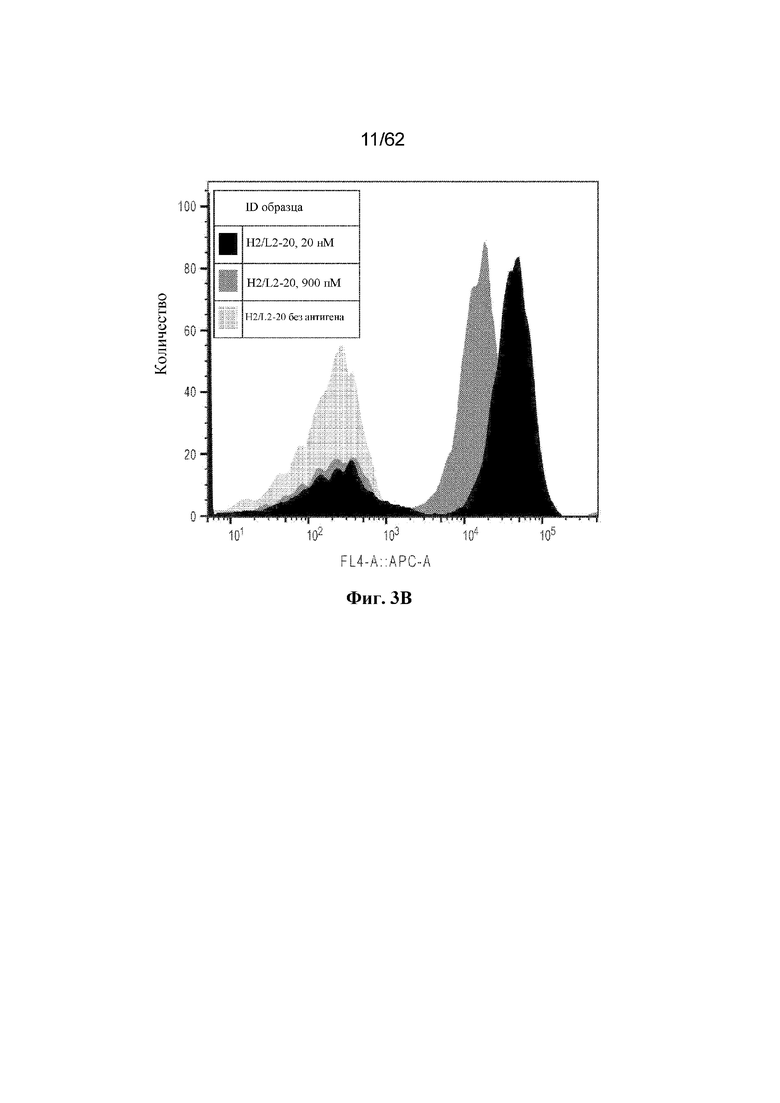
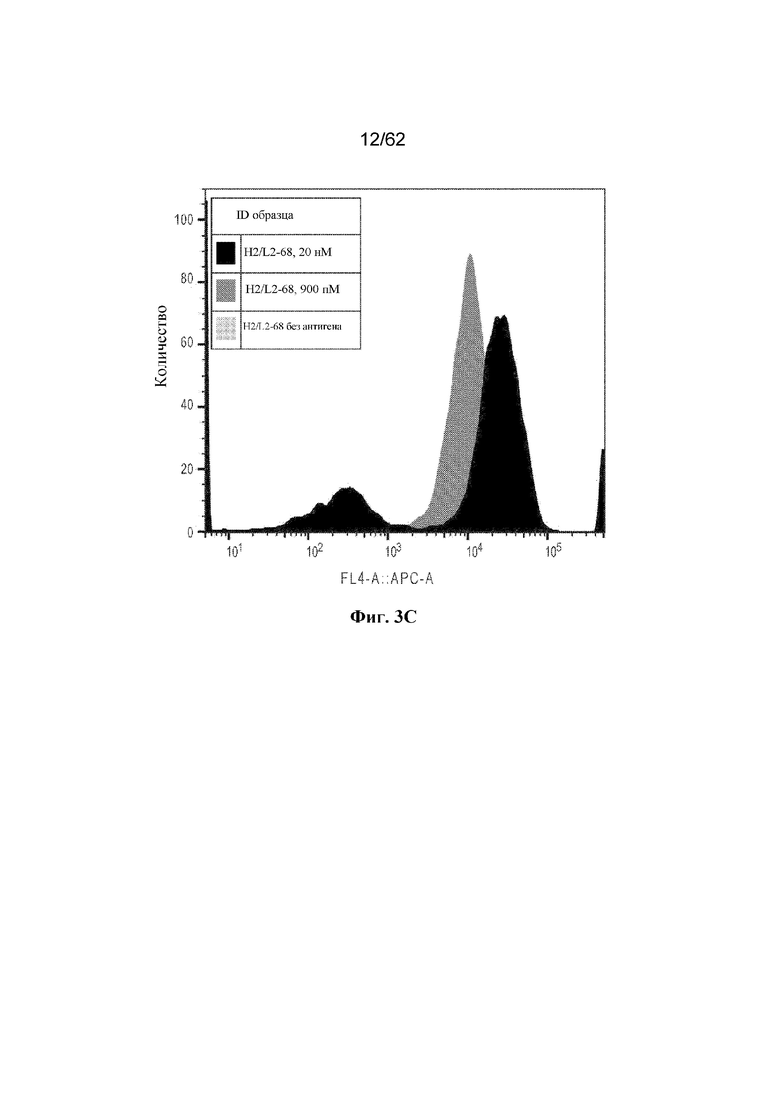
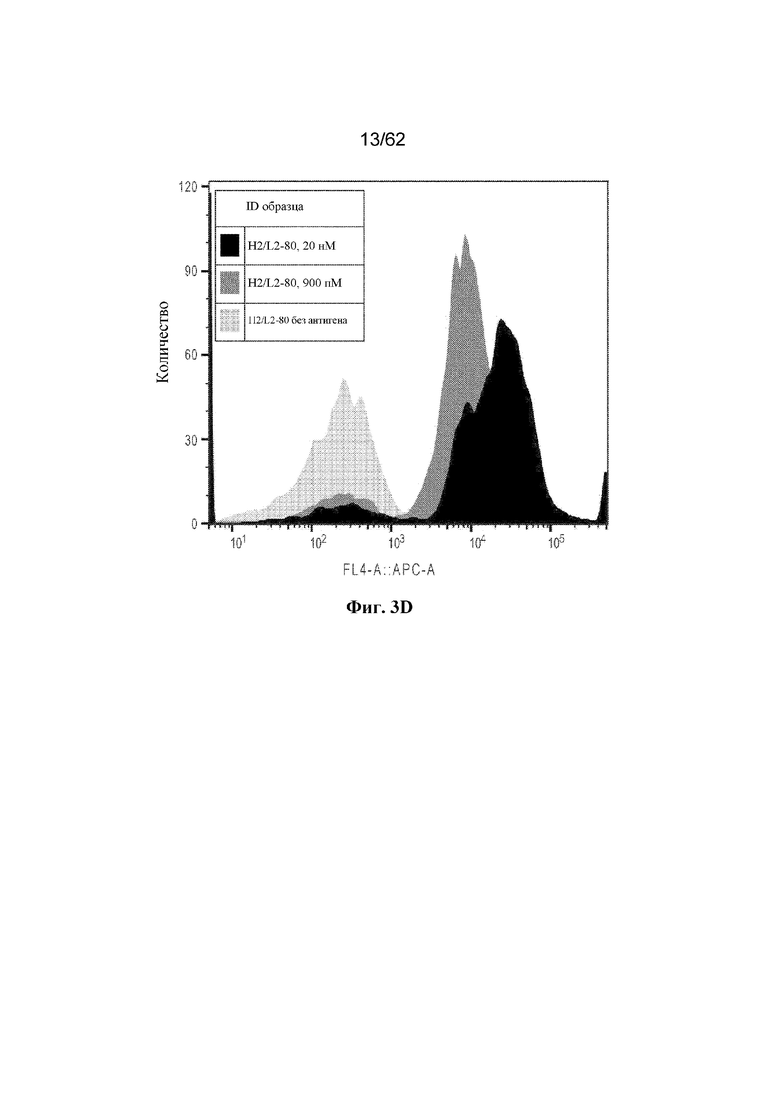
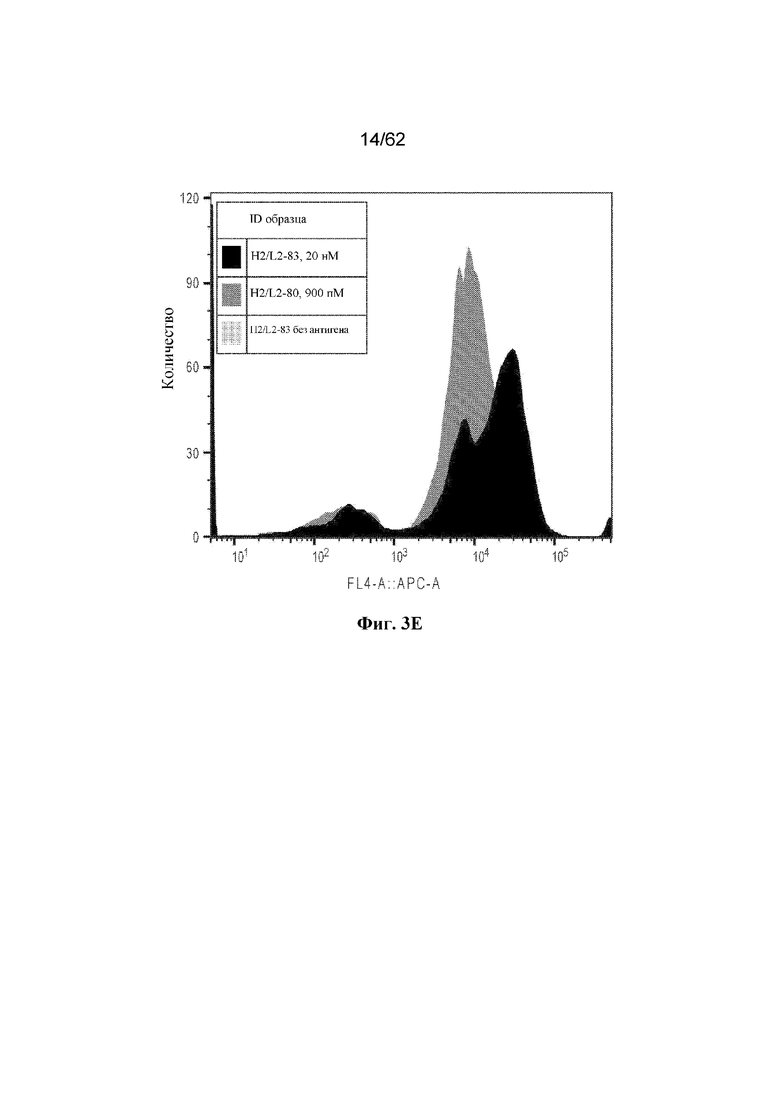

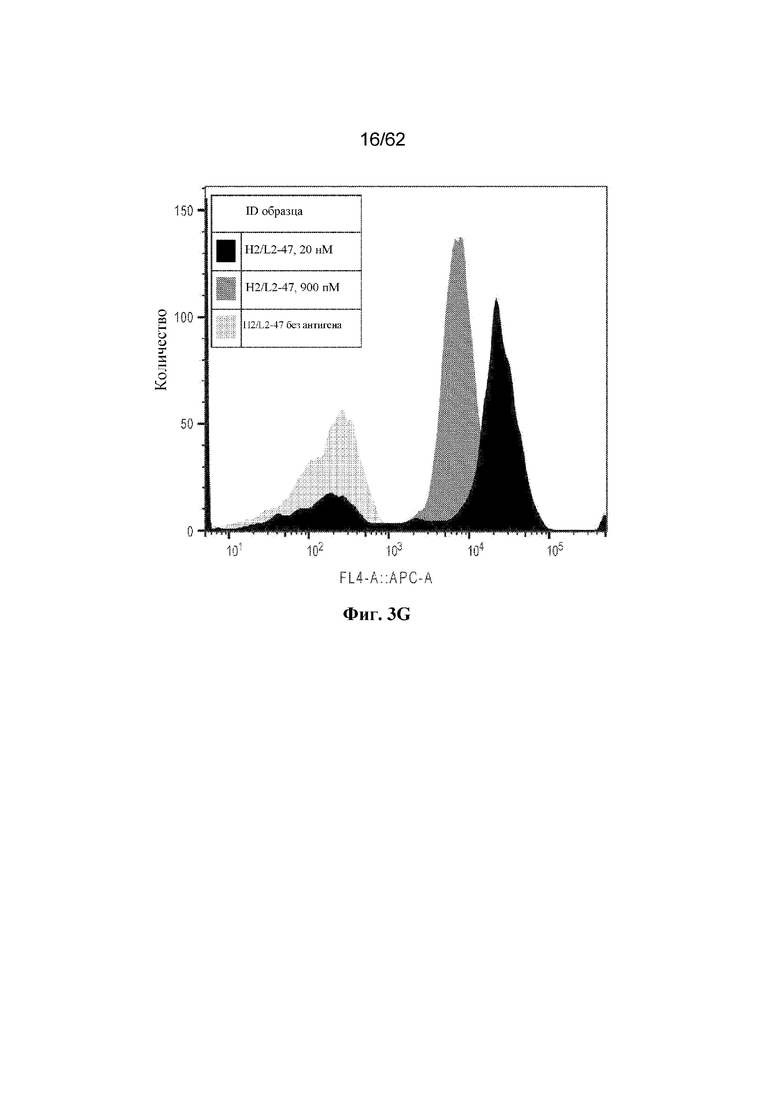
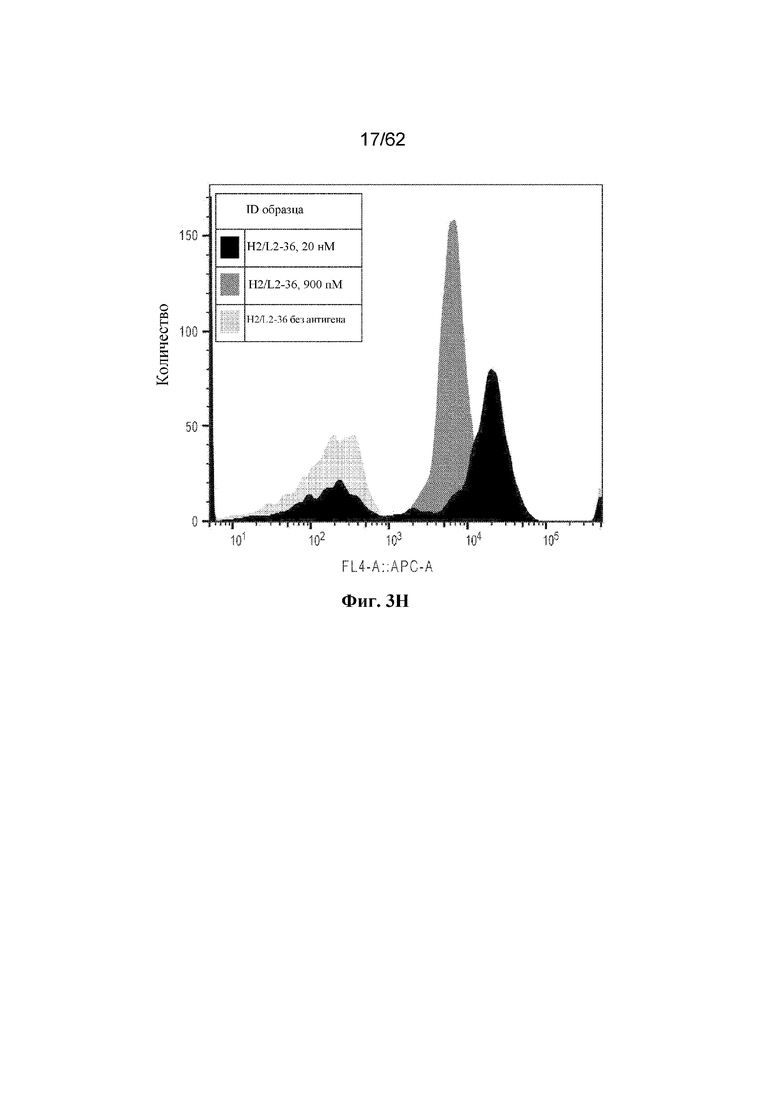
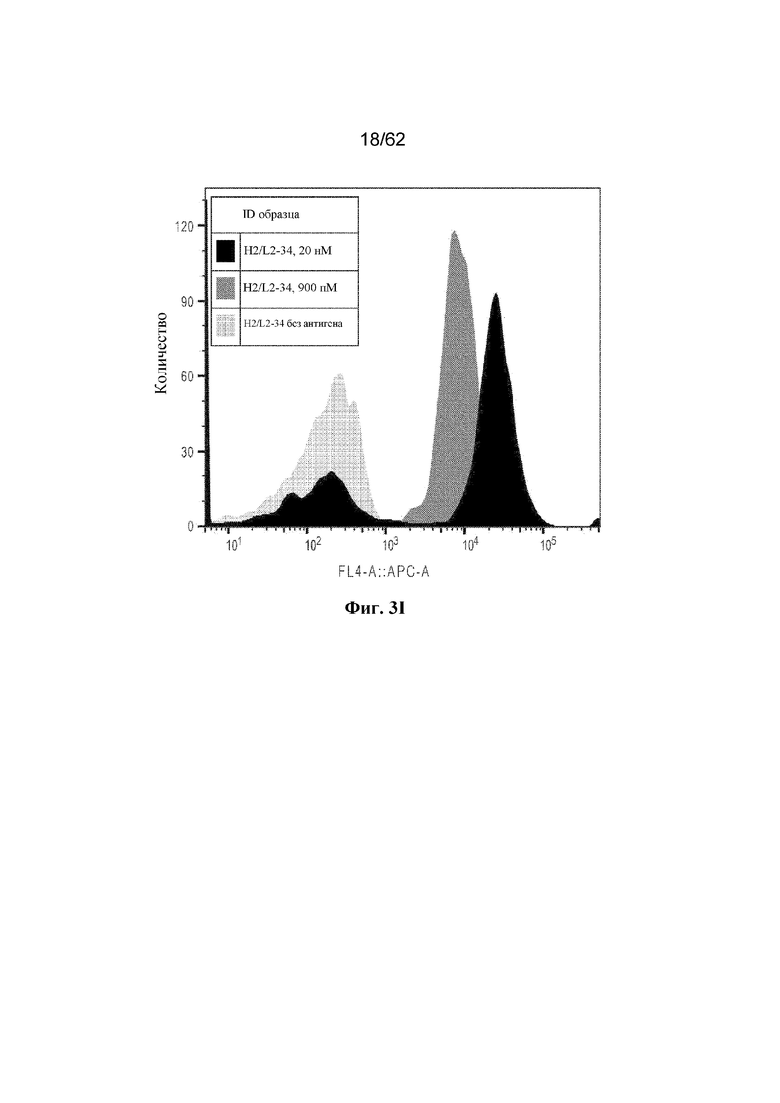

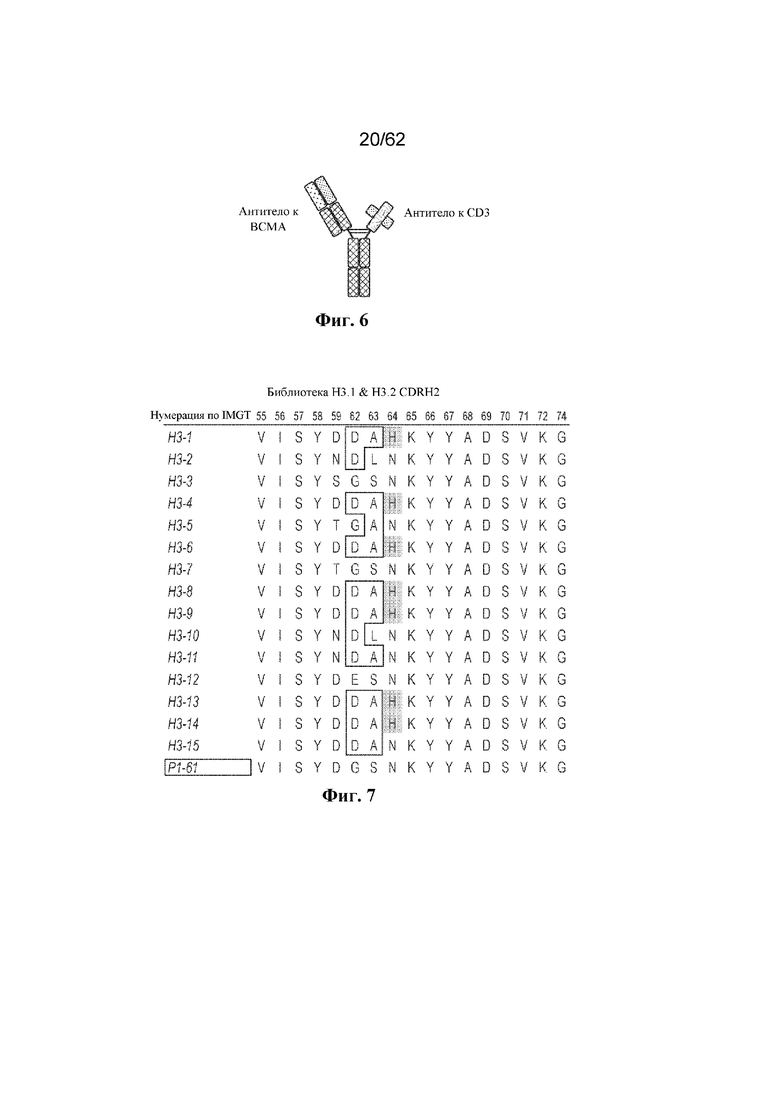



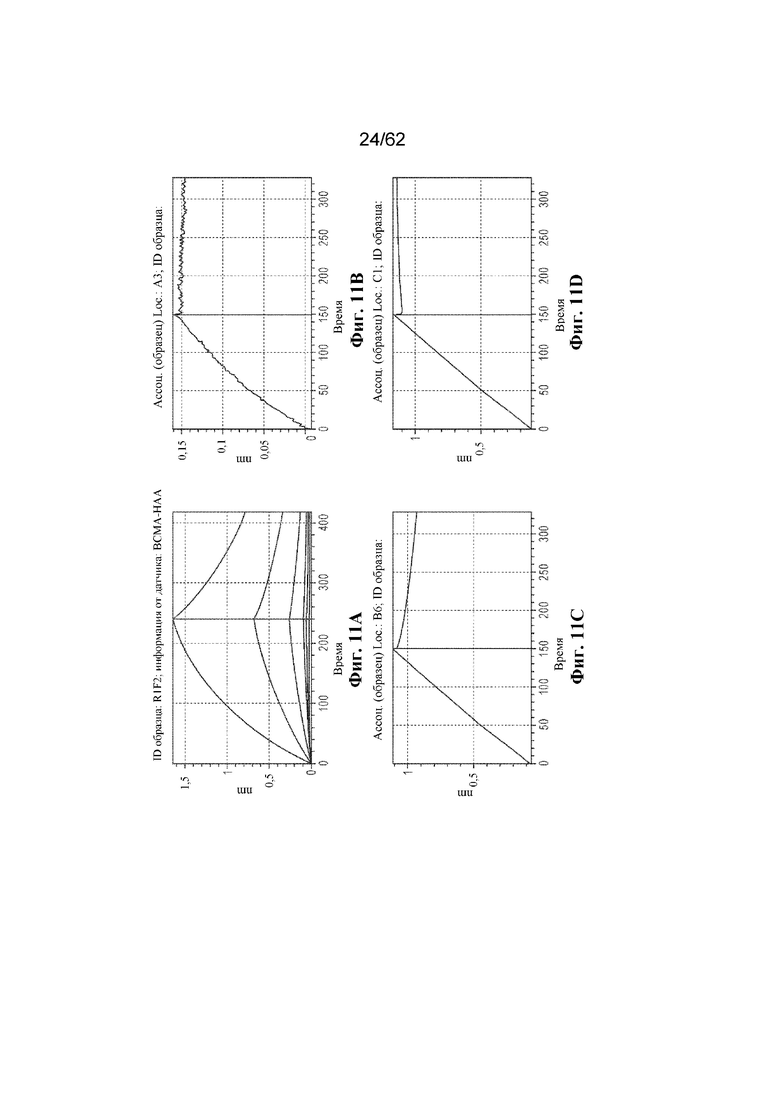

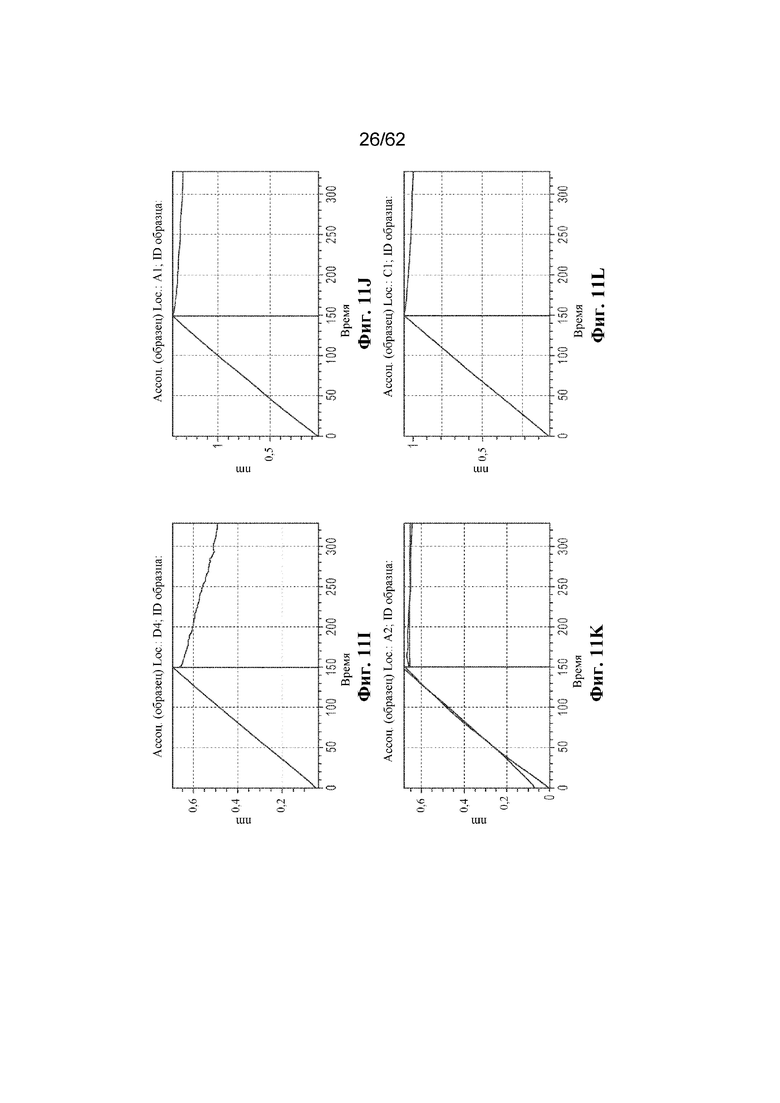
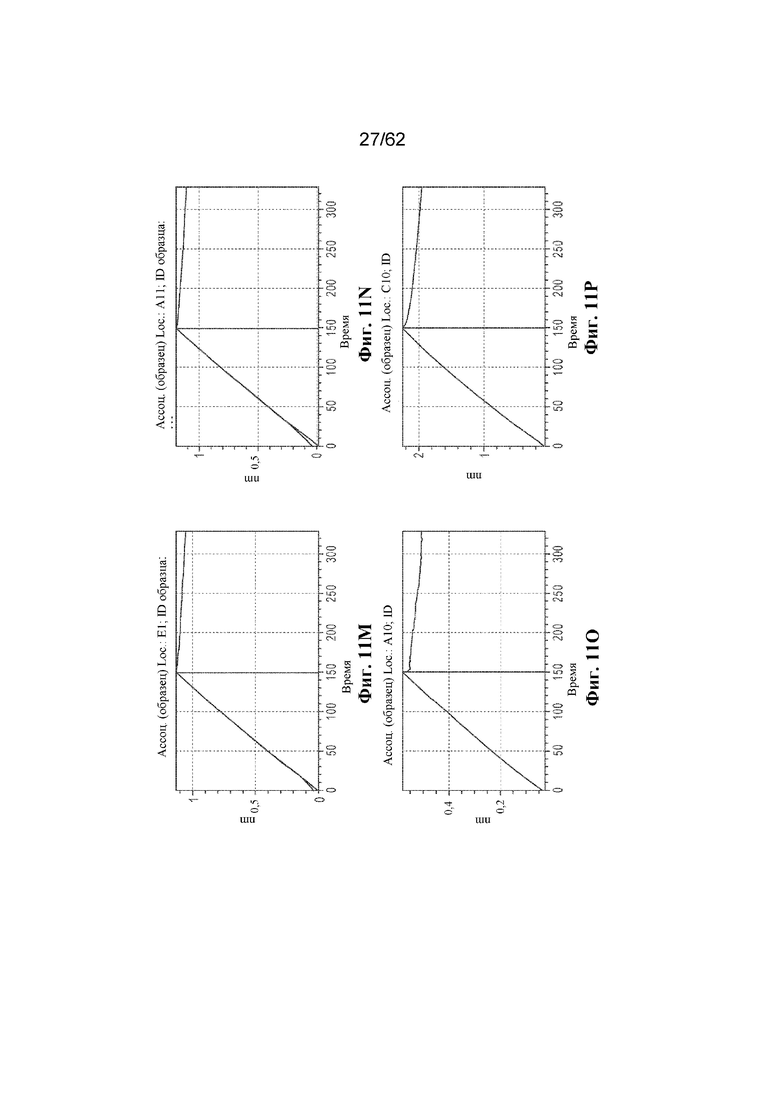
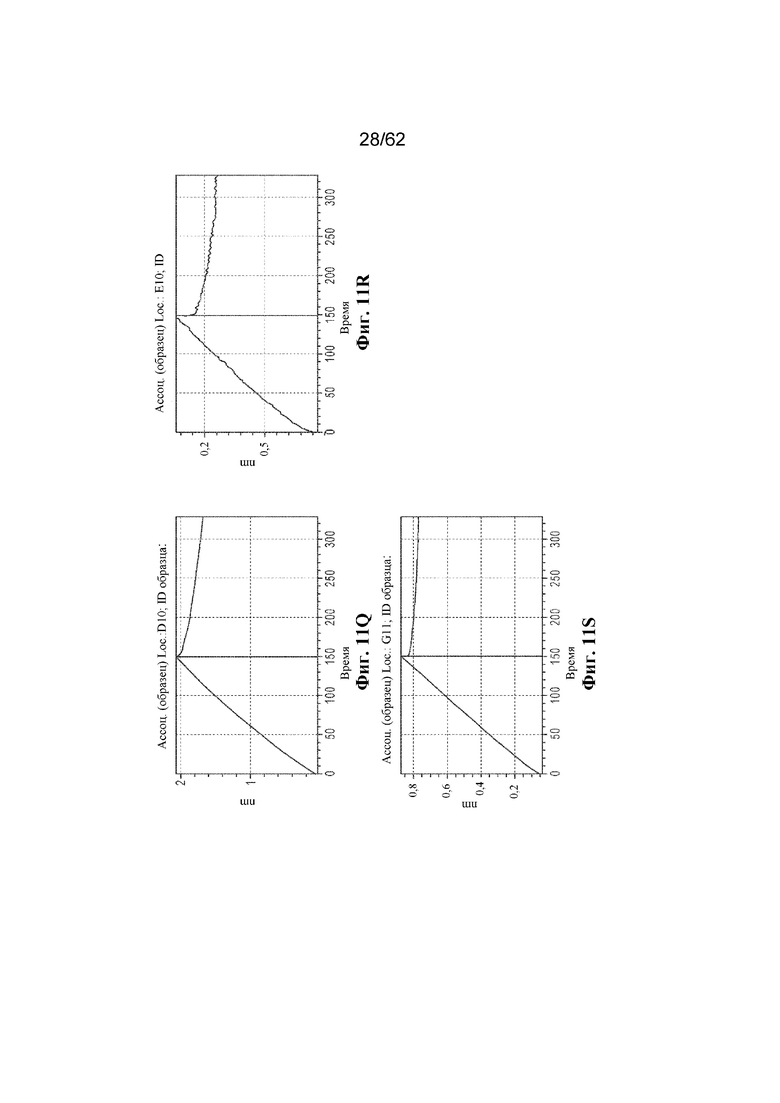
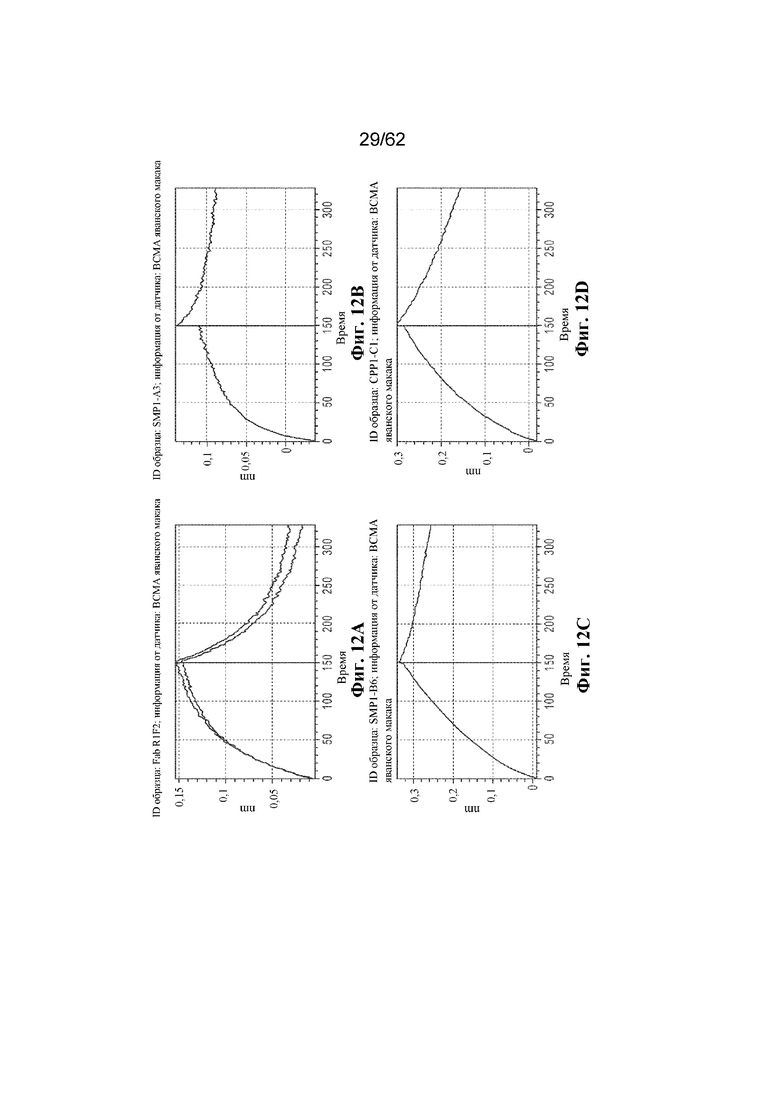

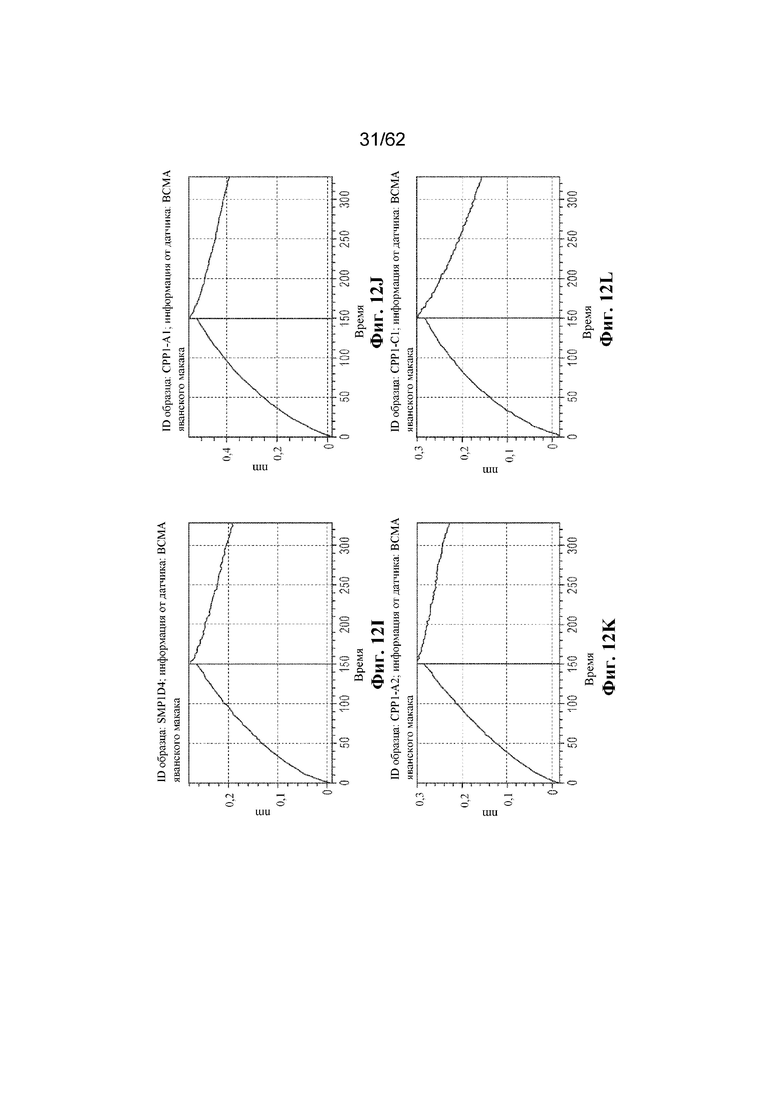

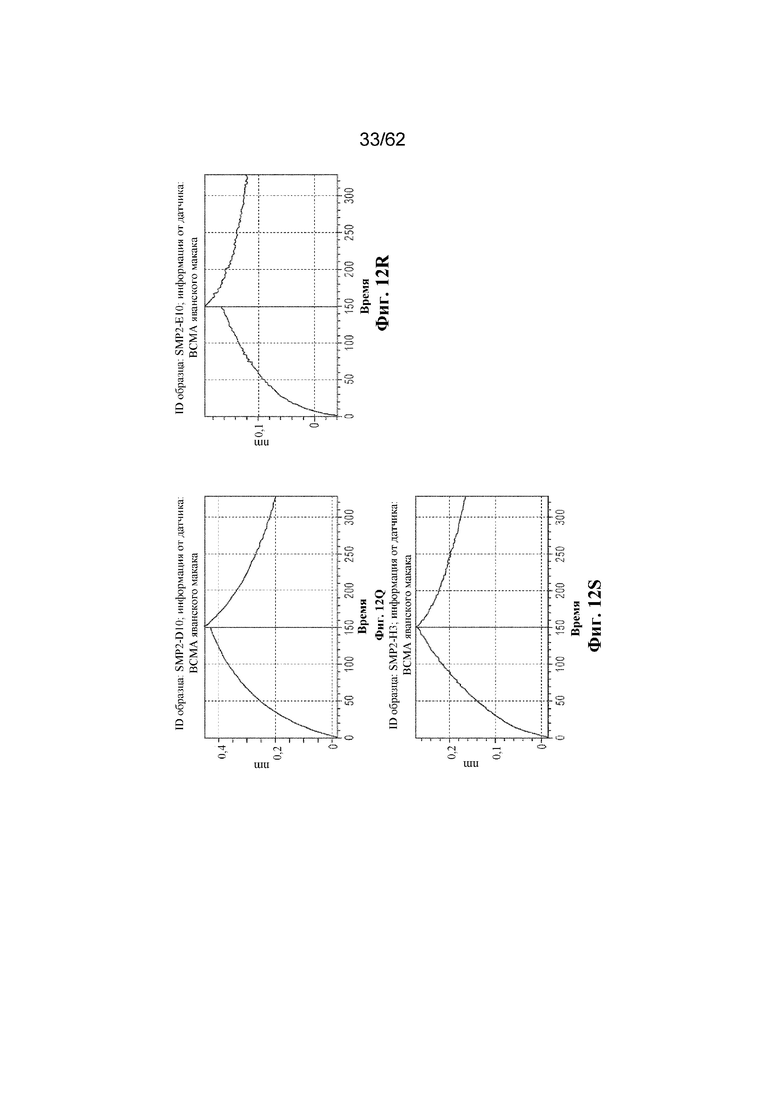
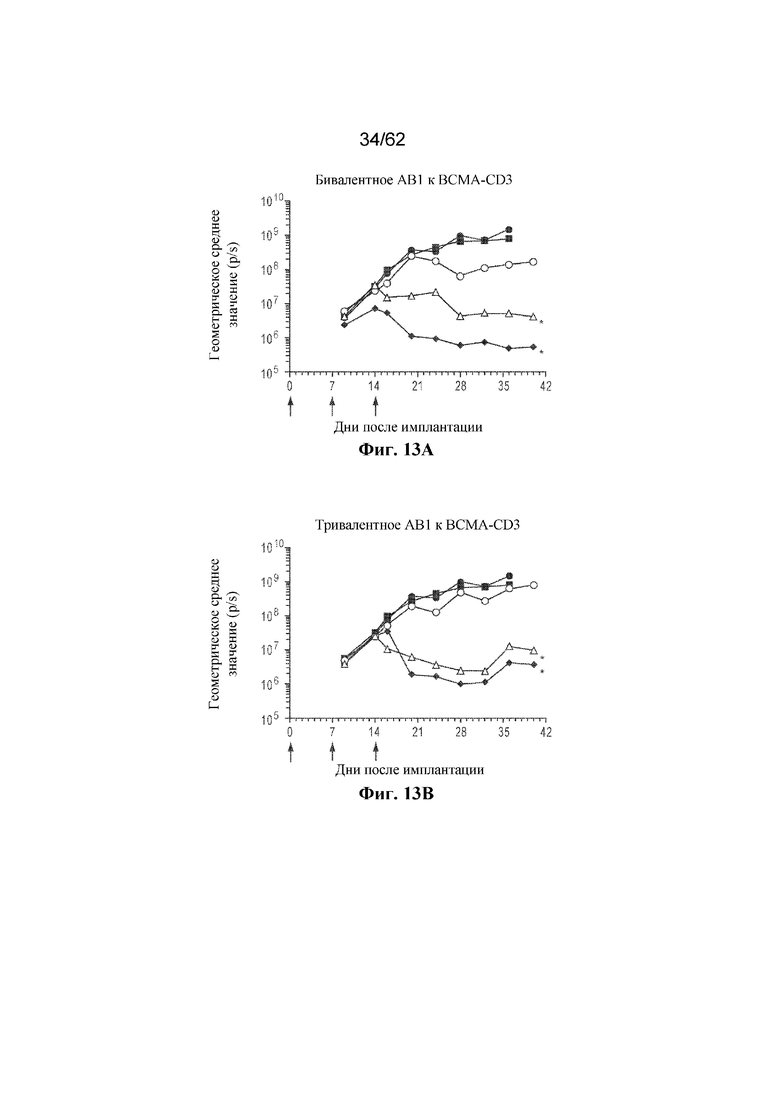
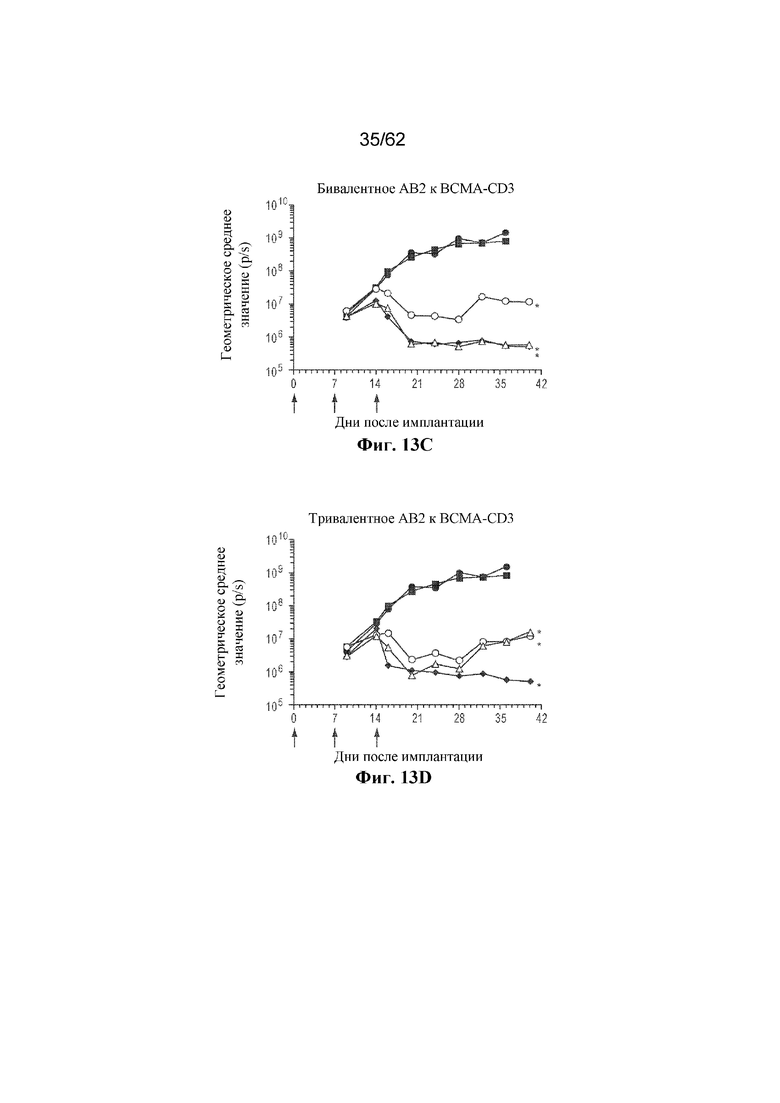
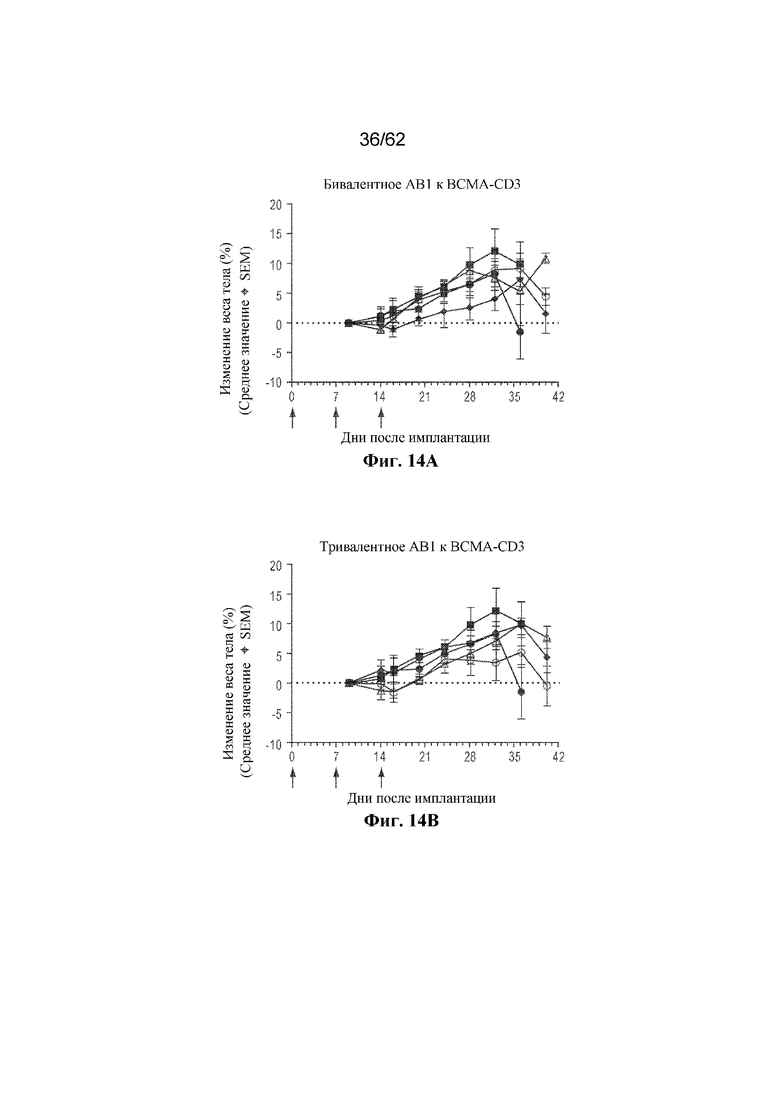
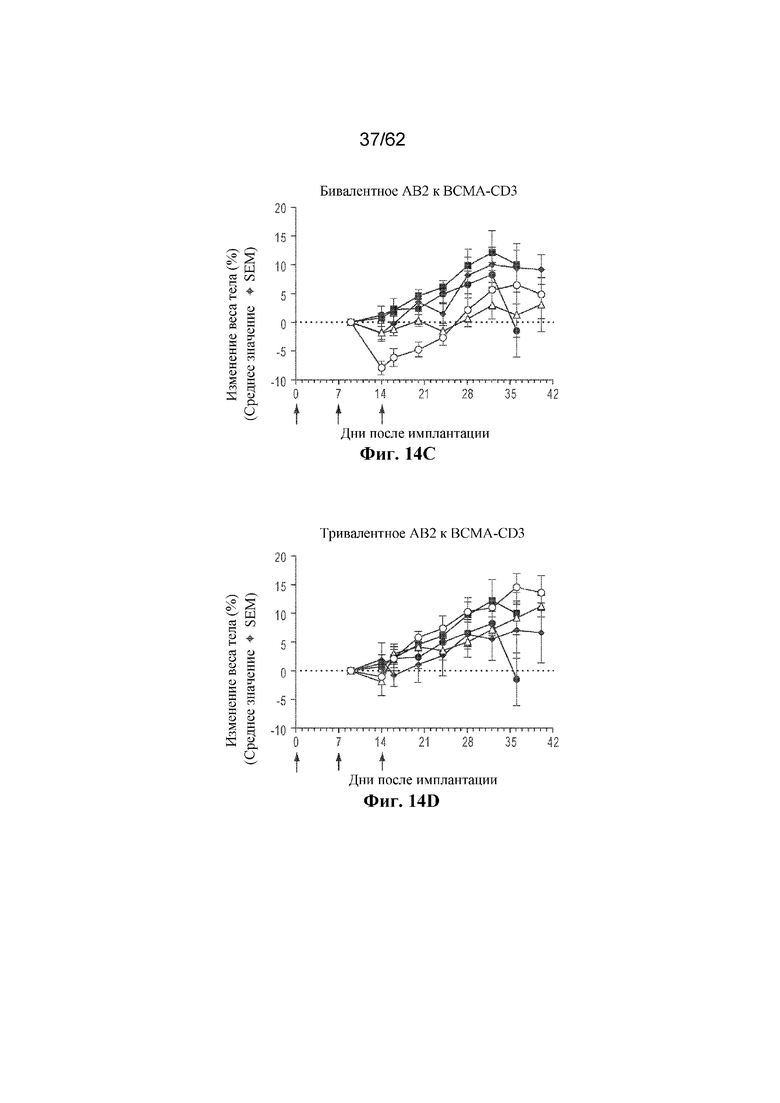
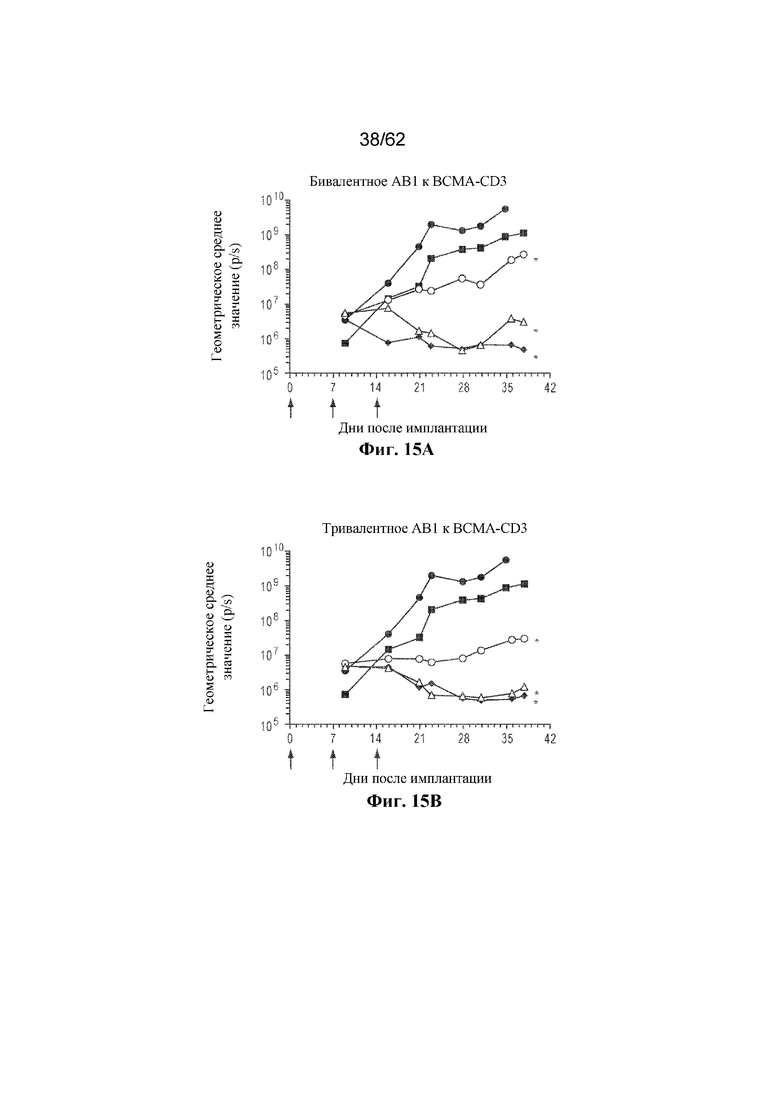
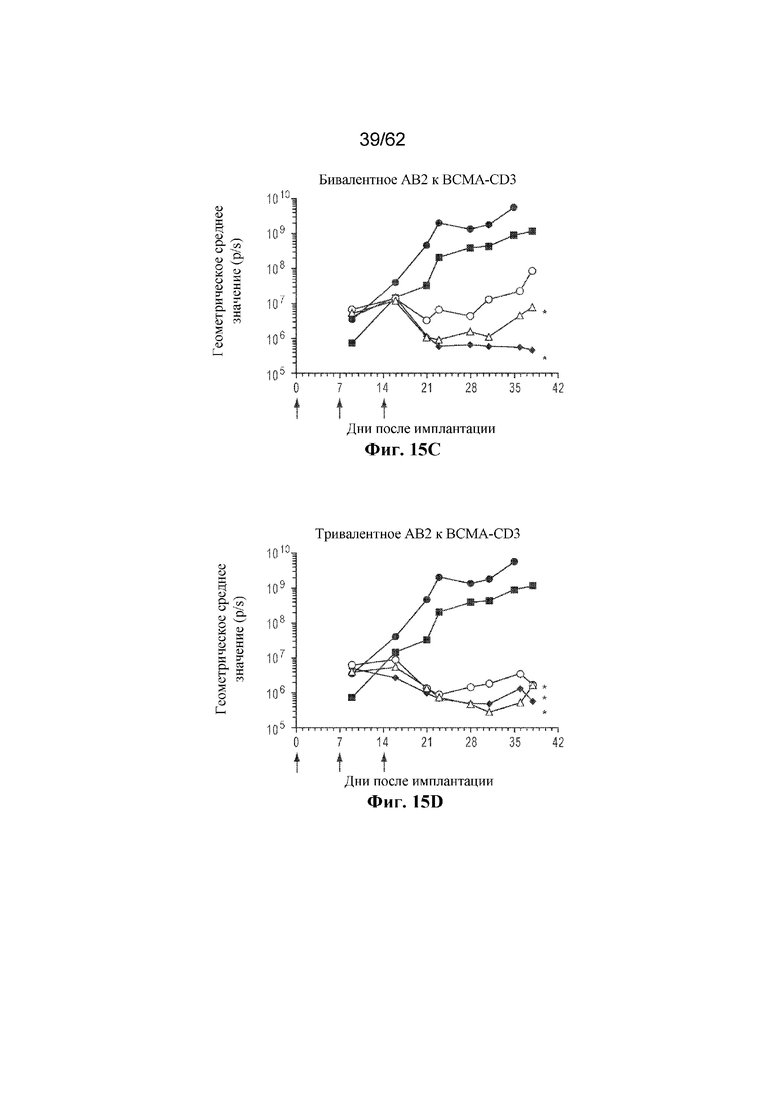


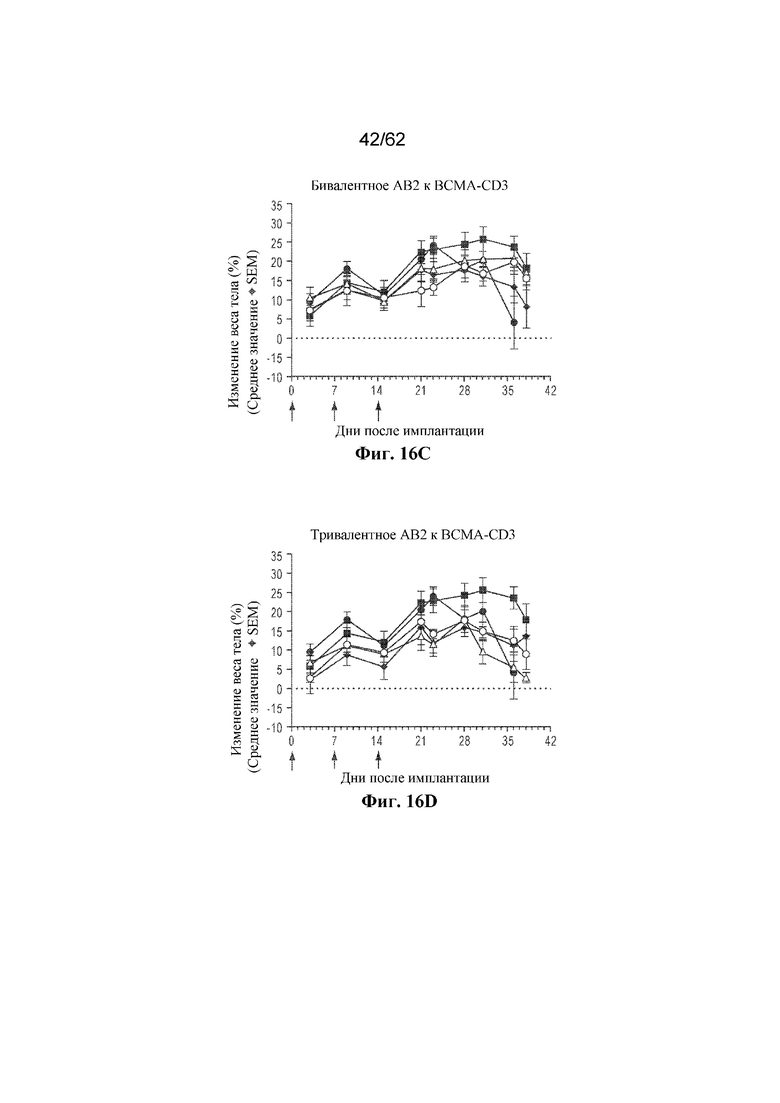
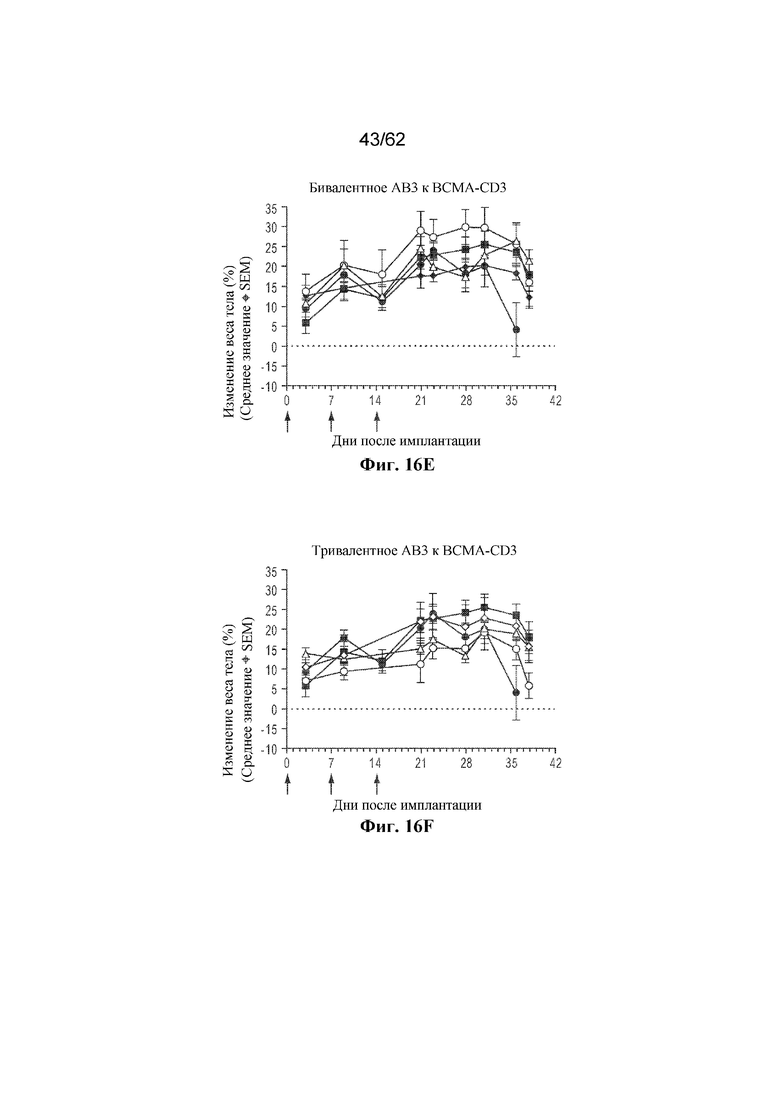
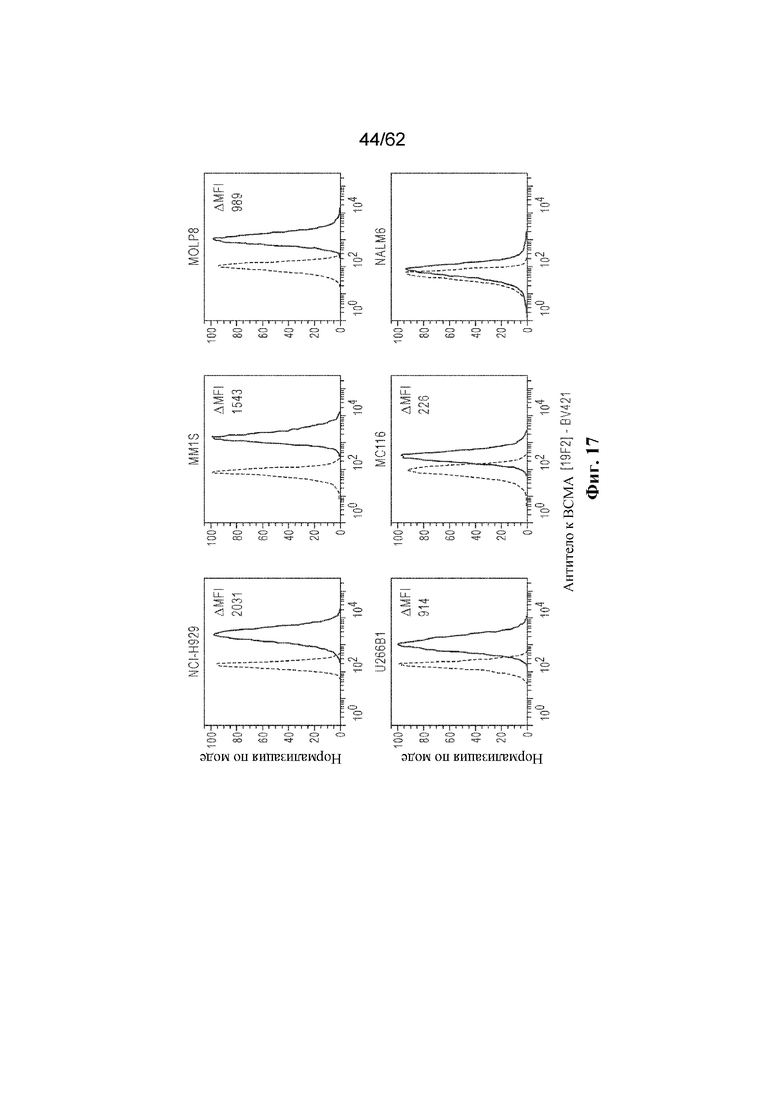
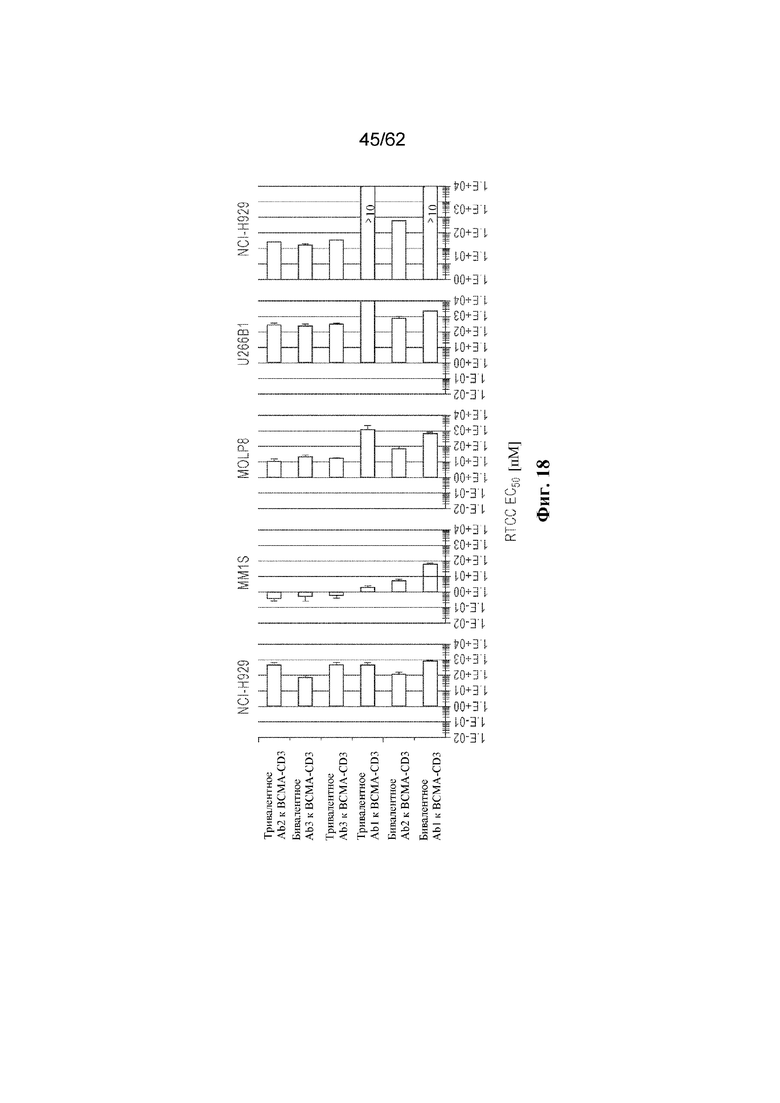
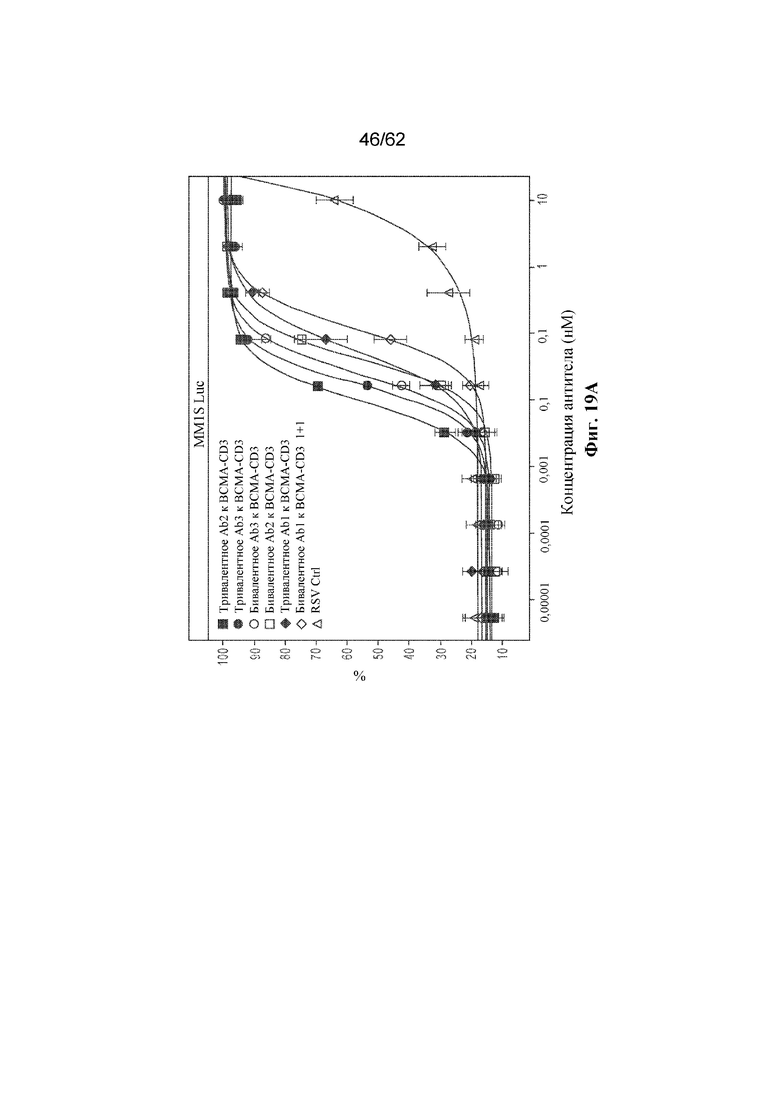



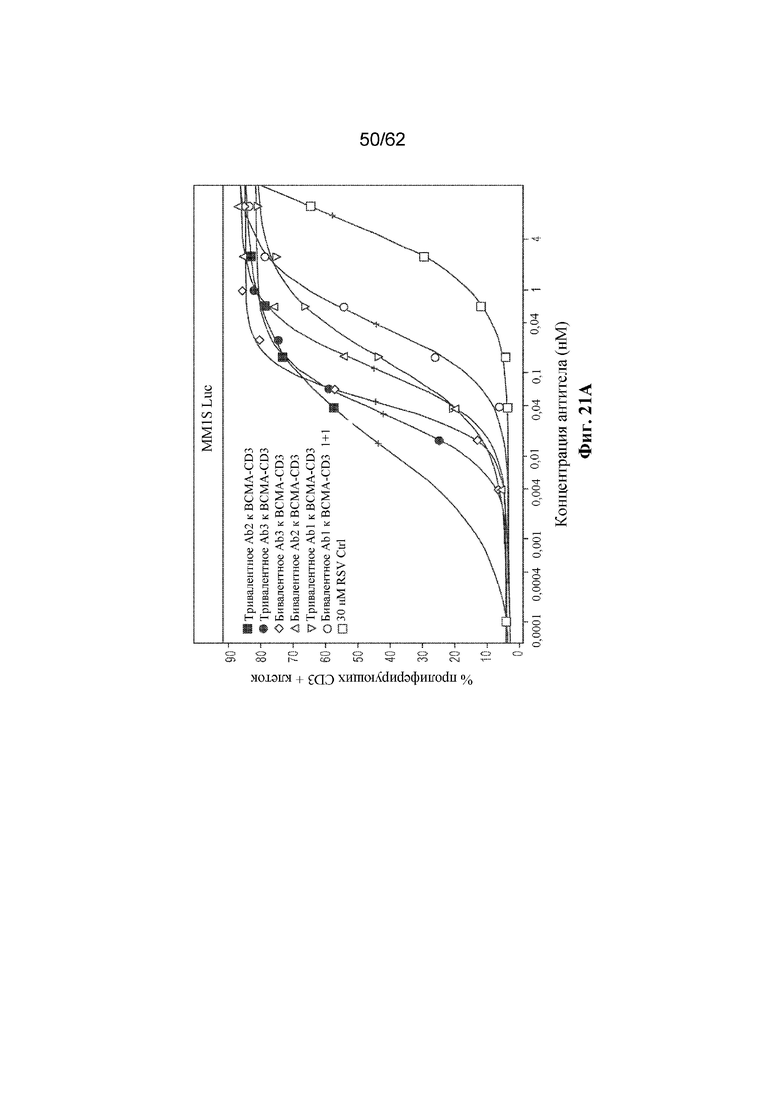

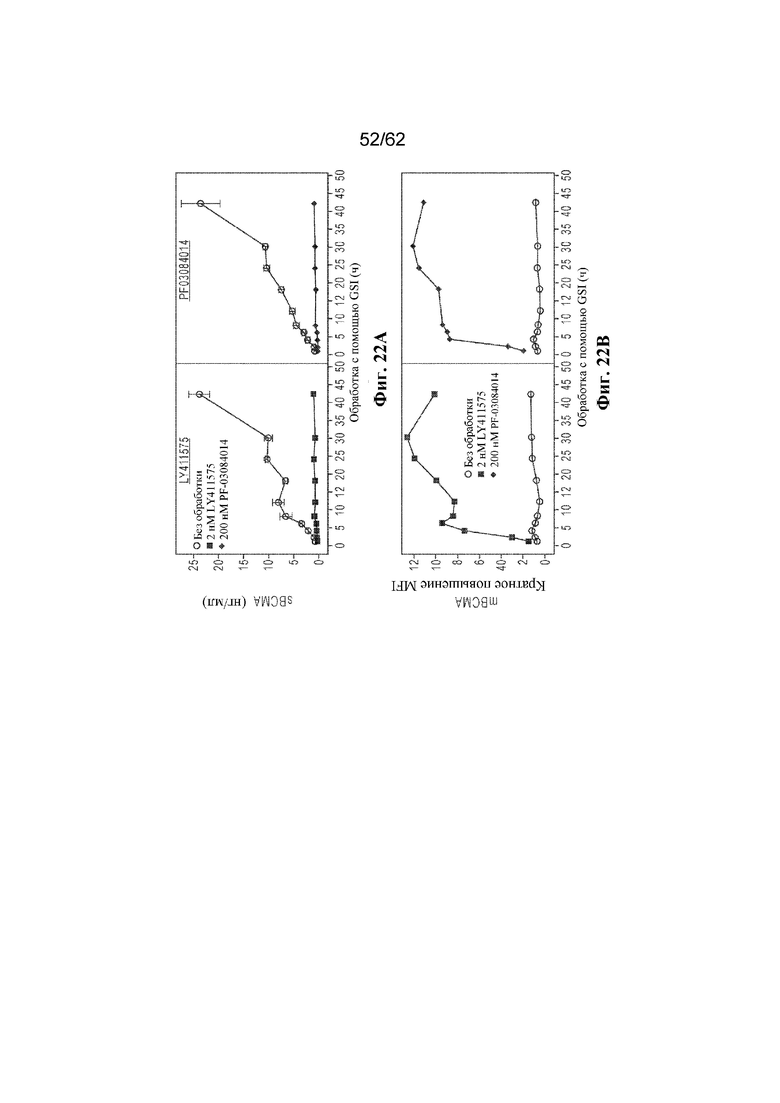
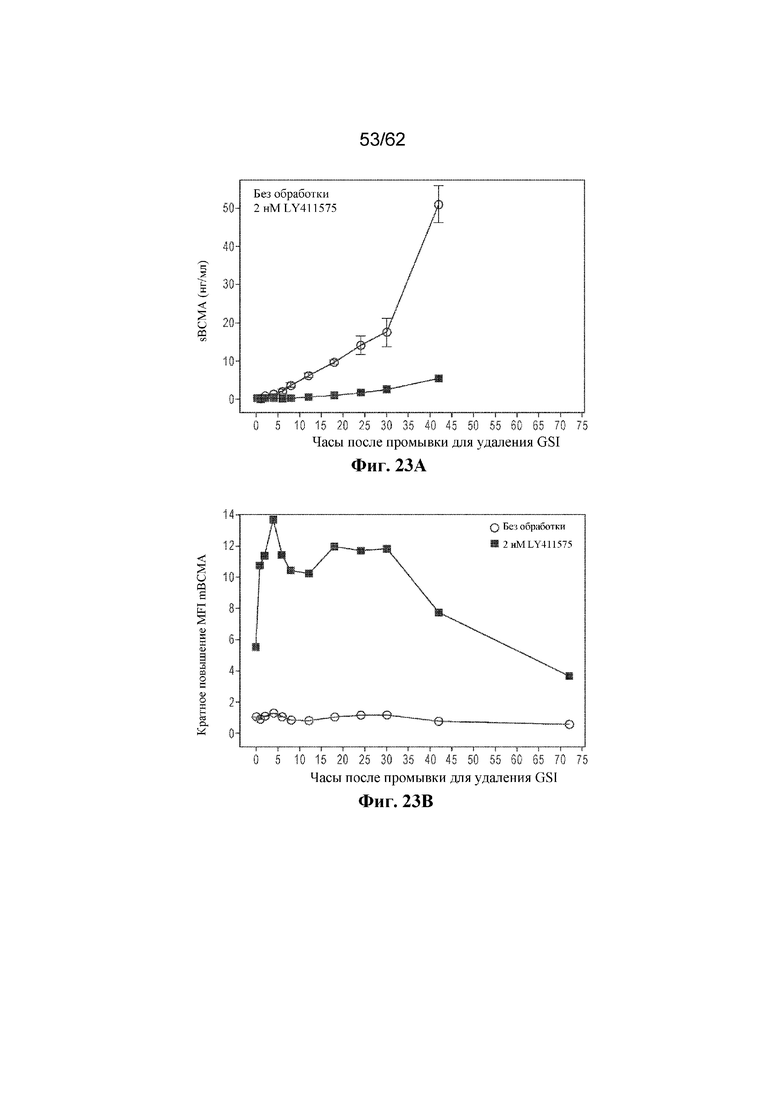
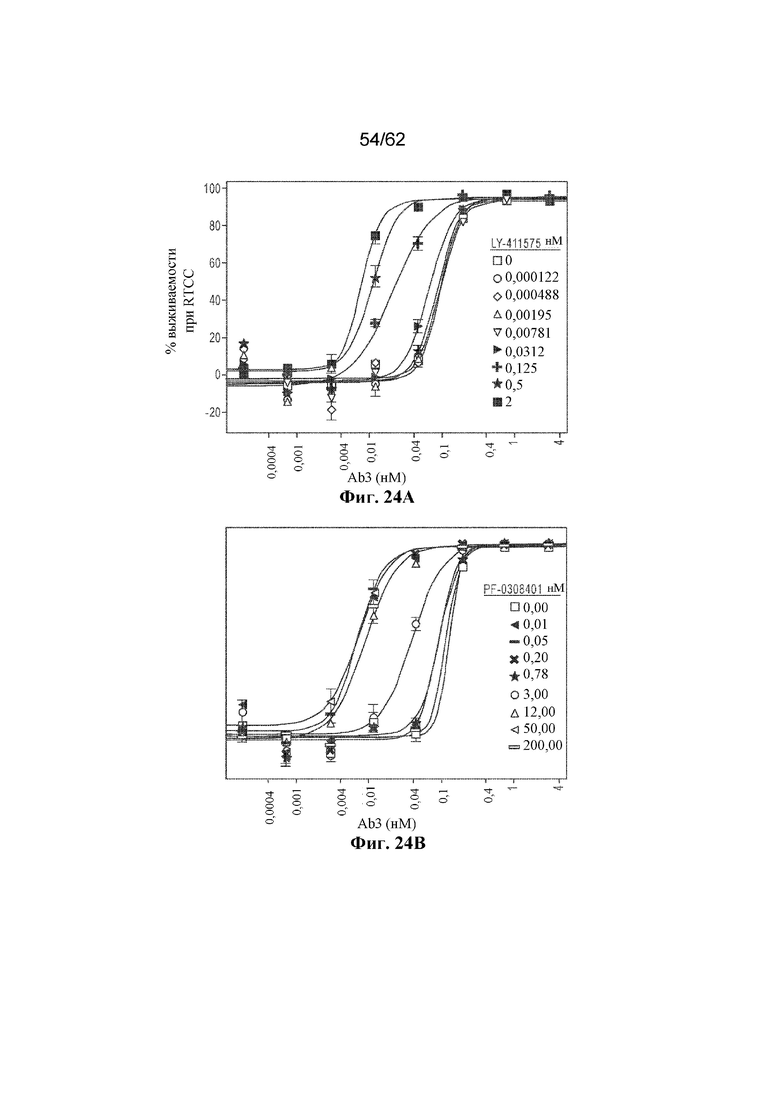
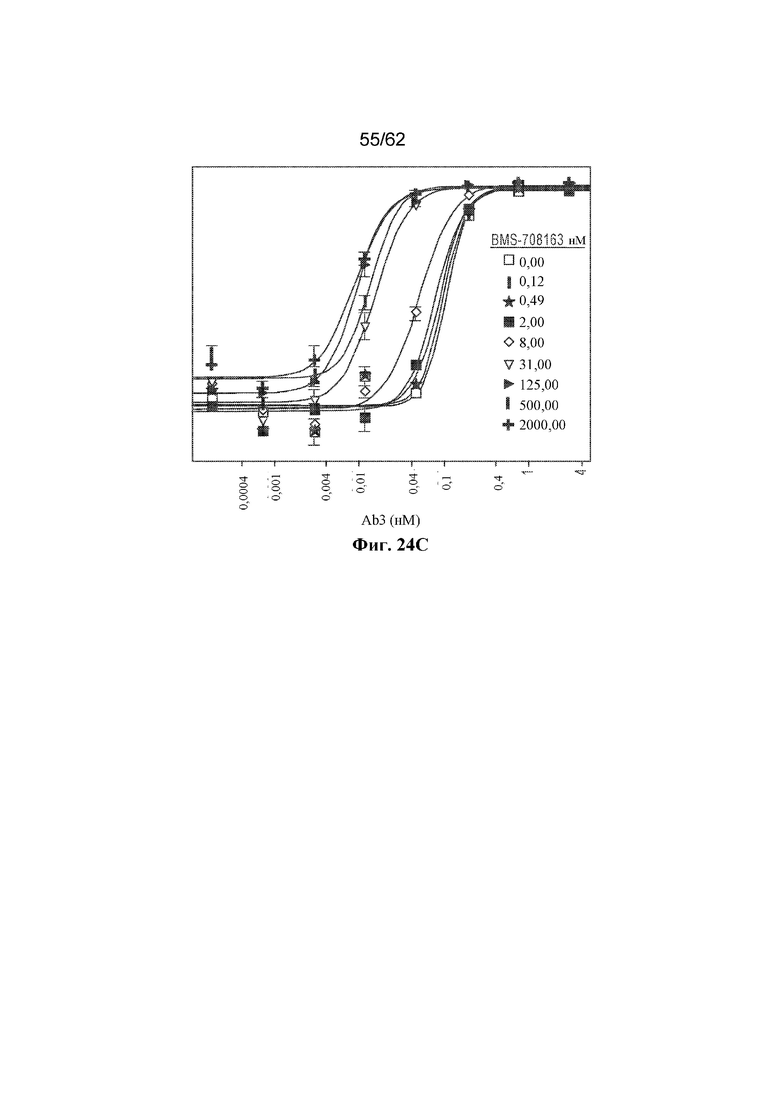

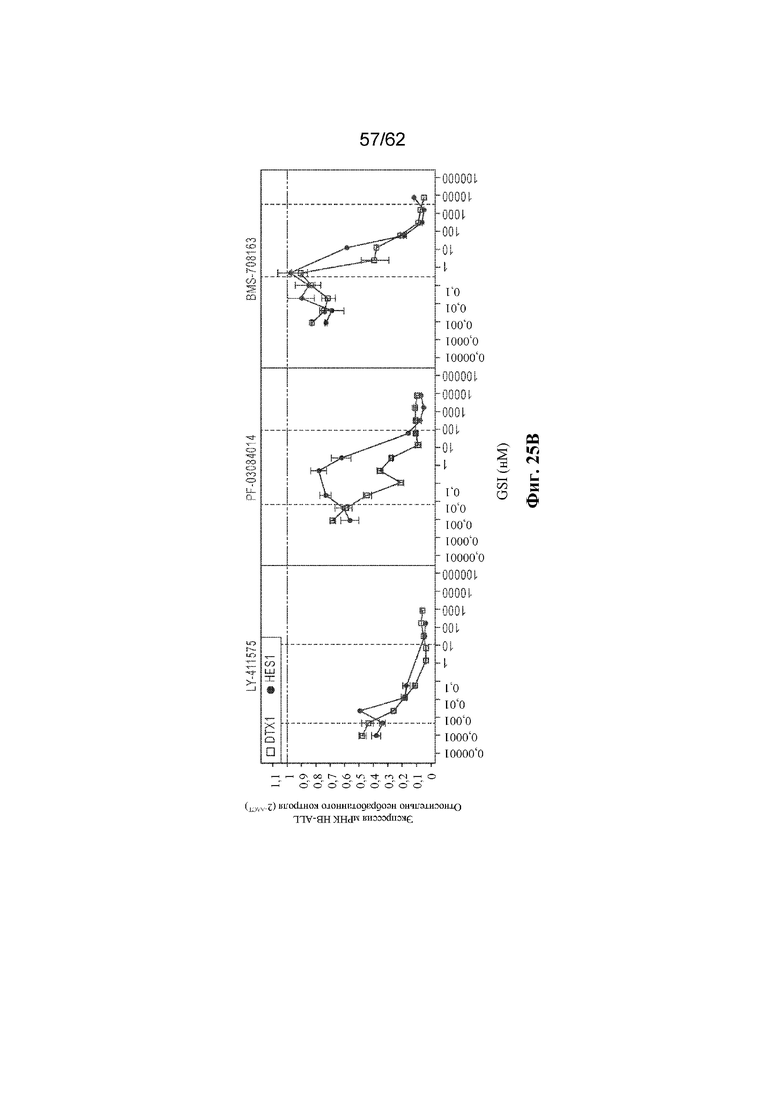
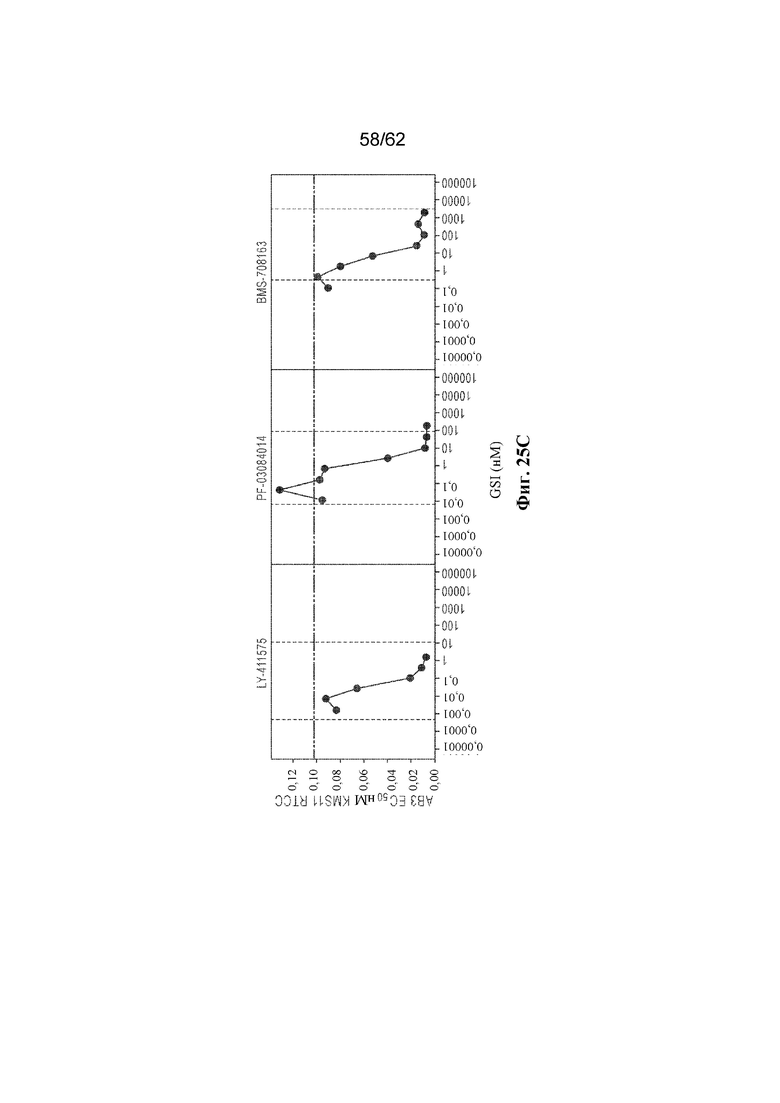


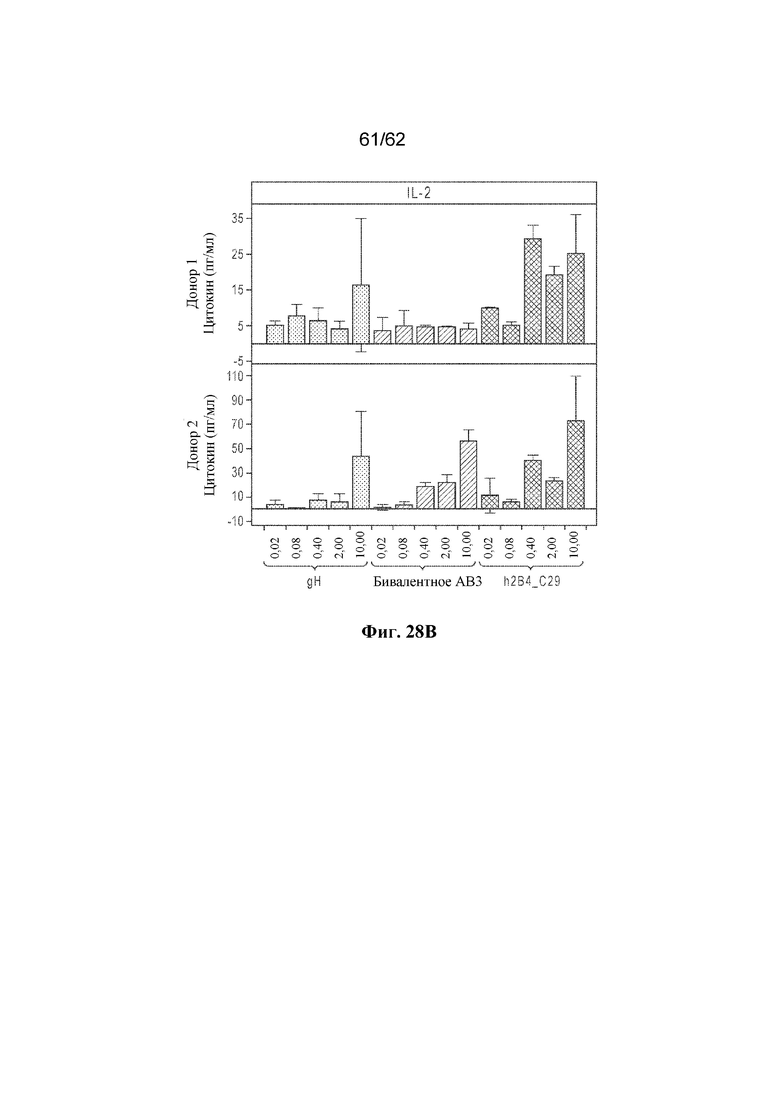
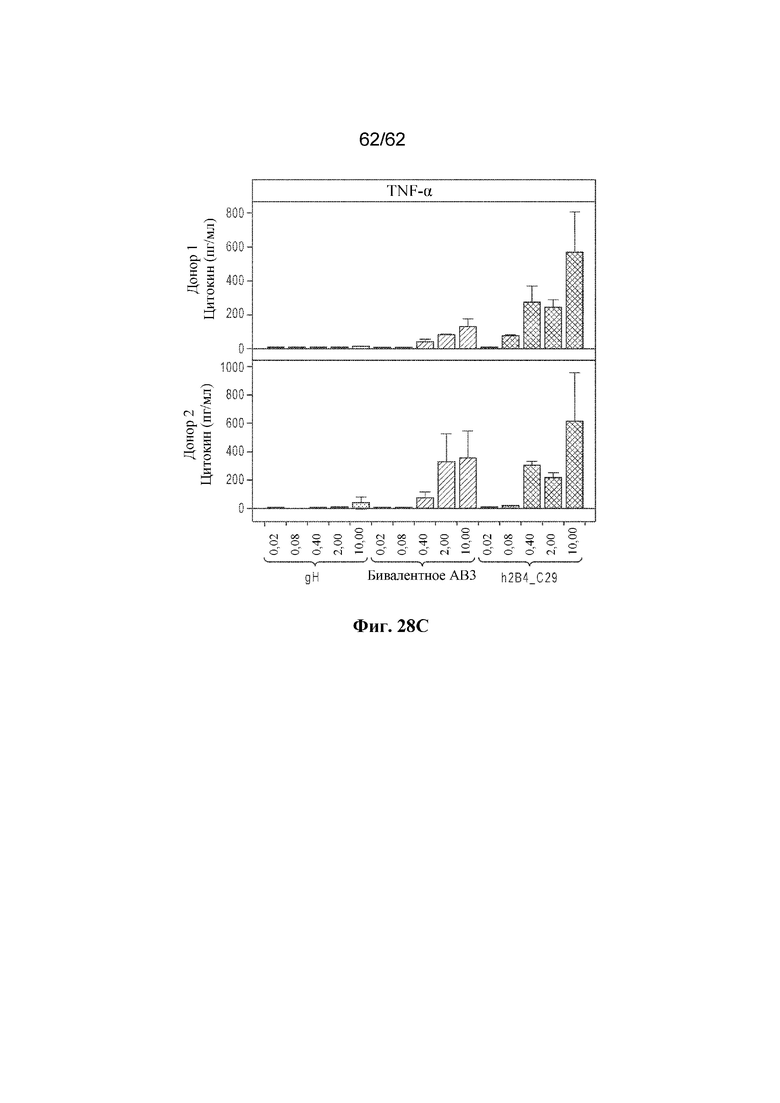
Изобретение относится к области биотехнологии. Описана группа изобретений, включающая связывающую антиген созревания В-клеток (ВСМА) молекулу, которая специфически связывается с ВСМА человека, конъюгат для лечения субъекта с заболеванием или нарушением, ассоциированными с экспрессией BCMA, фармацевтическую композицию для лечения субъекта с заболеванием или нарушением, ассоциированными с экспрессией BCMA, способ лечения субъекта с заболеванием или нарушением, ассоциированными с экспрессией BCMA, применение BCMA-связывающей молекулы, конъюгата или фармацевтической композиции в производстве лекарственного средства для лечения заболевания или нарушения, связанного с экспрессией BCMA, применение BCMA-связывающей молекулы, конъюгата или фармацевтической композиции для лечения заболевания или нарушения, связанного с экспрессией BCMA, нуклеиновую кислоту, кодирующую BCMA-связывающую молекулу, клетку, сконструированную для экспрессии BCMA-связывающей молекулы, клетку для получения BCMA-связывающей молекулы, и способ получения BCMA-связывающей молекулы. Изобретение расширяет арсенал средств, специфически связывающихся с антигеном созревания В-клеток (ВСМА). 10 н. и 40 з.п. ф-лы, 139 ил., 75 табл., 14 пр.
1. Связывающая антиген созревания В-клеток (BCMA) молекула, которая специфически связывается с ВСМА человека и содержит:
(a) в соответствии с определением Kabat последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в SEQ ID NO: 26, 102 и 110 соответственно, и последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в SEQ ID NO: 39, 112 и 49 соответственно;
(b) в соответствии с определением Chothia последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в SEQ ID NO: 27, 31 и 136 соответственно, и последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в SEQ ID NO: 138, 140 и 49 соответственно; или
(c) в соответствии с определением IMGT последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в SEQ ID NO: 28, 154 и 110 соответственно, и последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в SEQ ID NO: 162, 165 и 51 соответственно.
2. ВСМА-связывающая молекула по п. 1, которая содержит последовательность вариабельного участка легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 200, и последовательность вариабельного участка тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 224.
3. ВСМА-связывающая молекула по п. 1 или 2, которая содержит антитело, фрагмент антитела, scFv, dsFv, Fv, Fab, scFab или (Fab')2.
4. ВСМА-связывающая молекула по п. 3, которая содержит антитело или фрагмент антитела.
5. ВСМА-связывающая молекула по п. 3, которая содержит scFv.
6. ВСМА-связывающая молекула по любому из пп. 1-5, которая представляет собой полиспецифическую связывающую молекулу.
7. ВСМА-связывающая молекула по п. 6, которая представляет собой биспецифическую связывающую молекулу (BBM).
8. BCMA-связывающая молекула по п. 7, где BBM содержит:
(a) антигенсвязывающий домен 1 (ABD1), который специфически связывается с BCMA; и
(b) антигенсвязывающий домен 2 (ABD2), который специфически связывается с компонентом комплекса T-клеточного рецептора (TCR) человека.
9. ВСМА-связывающая молекула по п. 8, где ABD1 способен связывать ВСМА в то же время, когда ABD2 связан с компонентом комплекса TCR человека.
10. BCMA-связывающая молекула по п. 8 или 9, где ABD1 представляет собой антитело, фрагмент антитела, scFv, dsFv, Fv, Fab, scFab или (Fab')2.
11. BCMA-связывающая молекула по п. 10, где ABD1 представляет собой scFv.
12. BCMA-связывающая молекула по п. 10, где ABD1 представляет собой Fab.
13. BCMA-связывающая молекула по п. 10, где ABD1 представляет собой антитело к BCMA или его антигенсвязывающий домен.
14. BCMA-связывающая молекула по любому из пп. 8-13, где ABD2 представляет собой антитело, фрагмент антитела, scFv, dsFv, Fv, Fab, scFab, (Fab')2, однодоменное антитело (SDAB), VH- или VL-домен или VHH-домен верблюдовых.
15. BCMA-связывающая молекула по п. 14, где ABD2 представляет собой scFv.
16. BCMA-связывающая молекула по п. 14, где ABD2 представляет собой Fab.
17. BCMA-связывающая молекула по любому из пп. 8-16, где компонент комплекса TCR представляет собой CD3.
18. BCMA-связывающая молекула по п. 17, где ABD2 представляет собой антитело к CD3 или его антигенсвязывающий домен.
19. ВСМА-связывающая молекула по п. 18, где ABD2 содержит последовательности CDR из любого из от CD3-1 до CD3-127.
20. ВСМА-связывающая молекула по любому из пп. 7-19, которая является бивалентной.
21. ВСМА-связывающая молекула по любому из пп. 7-19, которая является тривалентной.
22. ВСМА-связывающая молекула по любому из пп. 7-19, которая является тетравалентной.
23. ВСМА-связывающая молекула по п. 1, содержащая:
(a) первый полипептид, содержащий:
(i) константный домен первой тяжелой цепи, содержащий первый Fc-участок;
(ii) scFv, содержащий аминокислотную последовательность SEQ ID NO: 294; где scFv ковалентно соединен с N-концом первого Fc-участка посредством шарнирного участка;
(b) второй полипептид, содержащий:
(i) вариабельный домен тяжелой цепи;
(ii) константный домен второй тяжелой цепи, содержащий второй Fc-участок; и
(c) третий полипептид, содержащий константный домен легкой цепи и вариабельный домен легкой цепи;
где
A) первый и второй Fc-участки образуют Fc-домен;
B) первый и второй Fc-участки содержат набор аминокислотных замен, содержащий S364K/E357Q и L368D/K370S;
C) первый и/или второй Fc-участки содержат аминокислотные модификации E223P, L234V, L235A, G236del и S267K;
D) первый и/или второй Fc-участки содержат аминокислотные замены N208D, Q295E, N384D, Q418E и N421D; и
E) вариабельный домен легкой цепи и вариабельный домен тяжелой цепи содержат последовательности вариабельного домена легкой цепи и вариабельного домена тяжелой цепи SEQ ID NO: 200 и SEQ ID NO: 224 соответственно.
24. ВСМА-связывающая молекула по п. 1, содержащая:
(a) первый полипептид, аминокислотная последовательность которого содержит аминокислотную последовательность под SEQ ID NO: 509;
(b) второй полипептид, аминокислотная последовательность которого содержит аминокислотную последовательность под SEQ ID NO: 510; и
(c) третий полипептид, аминокислотная последовательность которого содержит аминокислотную последовательность под SEQ ID NO: 504.
25. Конъюгат для лечения субъекта с заболеванием или нарушением, ассоциированным с экспрессией BCMA, содержащий ВСМА-связывающую молекулу по любому из пп. 1-24 и лекарственное средство.
26. Фармацевтическая композиция для лечения субъекта с заболеванием или нарушением, ассоциированным с экспрессией BCMA, содержащая ВСМА-связывающую молекулу по любому из пп. 1-24 или конъюгат по п. 25 и фармацевтически приемлемое вспомогательное вещество.
27. Способ лечения субъекта с заболеванием или нарушением, ассоциированным с экспрессией BCMA, включающий введение субъекту эффективного количества BCMA-связывающей молекулы по любому из пп. 1-24, конъюгата по п. 25 или фармацевтической композиции по п. 26.
28. Способ по п. 27, где заболевание или нарушение включает новообразование из плазматических клеток.
29. Способ по п. 27, где заболевание или нарушение включает В-клеточное злокачественное новообразование, которое характеризуется экспрессией BCMA на клеточной поверхности.
30. Способ по п. 27, где заболевание или нарушение представляет собой множественную миелому.
31. Способ по любому из пп. 27-30, дополнительно включающий введение по меньшей мере одного дополнительного средства субъекту.
32. Способ по п. 31, где указанное по меньшей мере одно дополнительное средство содержит ингибитор гамма-секретазы (GSI).
33. Способ по п. 27, где заболевание или нарушение включает аутоиммунное нарушение.
34. Применение BCMA-связывающей молекулы по любому из пп. 1-24, конъюгата по п. 25 или фармацевтической композиции по п. 26 в производстве лекарственного средства для лечения заболевания или нарушения, связанного с экспрессией BCMA.
35. Применение по п.34, где заболевание или нарушение включает неоплазму плазматических клеток.
36. Применение по п.34, где заболевание или нарушение включает В-клеточное злокачественное новообразование, которое характеризуется экспрессией BCMA на клеточной поверхности.
37. Применение по п.34, где заболевание или нарушение представляет собой множественную миелому.
38. Применение по любому из пп. 34-37, где лекарственное средство предназначено для введения в комбинации по меньшей мере с одним дополнительным средством.
39. Применение по п. 38, где указанное по меньшей мере одно дополнительное средство содержит ингибитор гамма-секретазы (GSI).
40. Применение по п. 34, где заболевание или расстройство включает аутоиммунное расстройство.
41. Применение BCMA-связывающей молекулы по любому из пп.1-24, конъюгата по п.25 или фармацевтической композиции по п.26 для лечения заболевания или нарушения, связанного с экспрессией BCMA.
42. Применение по п.41, где заболевание или нарушение включает неоплазму плазматических клеток.
43. Применение по п.41, где заболевание или нарушение включает В-клеточное злокачественное новообразование, которое характеризуется экспрессией BCMA на клеточной поверхности.
44. Применение по п.41, где заболевание или нарушение представляет собой множественную миелому.
45. Применение по любому из пп.41-44, где BCMA-связывающую молекулу, конъюгат или фармацевтическую композицию вводят в комбинации по меньшей мере с одним дополнительным средством.
46. Применение по п.41, где заболевание или нарушение включает аутоиммунное расстройство.
47. Нуклеиновая кислота, кодирующая BCMA-связывающую молекулу по любому из пп. 1-24.
48. Клетка, сконструированная для экспрессии BCMA-связывающей молекулы по любому из пп. 1-24, содержащая нуклеиновую кислоту или совокупность нуклеиновых кислот, кодирующие указанную BCMA-связывающую молекулу.
49. Клетка для получения BCMA-связывающей молекулы, представляющая собой клетку, трансфицированную одним или несколькими векторами экспрессии, содержащими одну или несколько последовательностей нуклеиновой кислоты, кодирующих BCMA-связывающую молекулу по любому из пп. 1-24 или конъюгат по п. 25 под контролем одного или нескольких промоторов.
50. Способ получения BCMA-связывающей молекулы, включающий:
(a) культивирование клетки по п. 48 или 49 в условиях, при которых экспрессируется BCMA-связывающая молекула; и
(b) извлечение BCMA-связывающей молекулы из культуры клеток.
| ПРИБОР ДЛЯ МАССАЖА ТЕЛА АТМОСФЕРНЫМ ВОЗДУХОМ | 1926 |
|
SU4635A1 |
| Устройство для проволочной радиофикации домов | 1929 |
|
SU28162A1 |
| WO 2017031104 A1, 23.02.2017 | |||
| WO 2014089335 A2, 12.06.2014 | |||
| WO 2014122144 A1, 14.08.2014. | |||
Авторы
Даты
2024-01-29—Публикация
2019-05-30—Подача