1. ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Настоящая заявка испрашивает преимущество приоритета по предварительным заявкам на патент США № 62/850889, поданной 21 мая 2019 г., и № 62/854667, поданной 30 мая 2019 г., содержание обеих из которых включено в данный документ во всей своей полноте посредством ссылки.
2. ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[0002] Настоящая заявка содержит перечень последовательностей, который был подан в электронном виде в формате ASCII и тем самым включен посредством ссылки во всей своей полноте. Указанная копия в формате ASCII, созданная 13 мая 2020 г., имеет название NOV-005WO_SL.txt, и ее размер составляет 595602 байта.
3. ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0003] Настоящее изобретение в целом относится к полиспецифическим связывающим молекулам, которые взаимодействуют с BCMA, CD3 или другим компонентом комплекса TCR на T-клетках, а также с CD2 либо опухолеассоциированным антигеном ("TAA") человека, и их применению для лечения заболеваний и нарушений, ассоциированных с экспрессией BCMA.
4. ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
[0004] BCMA является представителем семейства рецепторов фактора некроза опухоли (TNFR), который экспрессируется на клетках B-клеточной линии дифференцировки. Экспрессия BCMA является наиболее высокой на терминально дифференцированных B-клетках, которые приобретают судьбу долгоживущих плазматических клеток, в том числе на плазматических клетках, плазмобластах и в субпопуляции активированных B-клеток и B-клеток памяти. BCMA участвует в опосредовании выживания плазматических клеток для поддержания длительного гуморального иммунитета. Было показано, что экспрессия BCMA связана с рядом форм рака, аутоиммунных нарушений и инфекционных заболеваний. Формы рака с увеличенной экспрессией BCMA включают некоторые формы гематологического рака, такие как множественная миелома, лимфома Ходжкина и неходжкинская лимфома, различные формы лейкоза и глиобластому.
[0005] Перенаправленный нацеленный T-клеточный лизис (RTCC) представляет собой перспективный механизм для лечения первой линии и состояний, трудно поддающихся лечению. Антитела и фрагменты антител с их исключительной селективностью были успешно сконструированы в разнообразных форматах для обеспечения двойной специфичности, необходимой для перекрестного связывания T-клеток с одним рецептором на клетке-мишени.
[0006] Существует необходимость в улучшенных подходах на основе RTCC, нацеливающихся на BCMA.
5. КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0007] Настоящее изобретение расширяет принципы перенаправленного нацеленного T-клеточного лизиса (RTCC), предусматривая полиспецифические связывающие молекулы ("MBM"), которые взаимодействуют с BCMA, CD3 или другим компонентом T-клеточного рецепторного комплекса (TCR) на T-клетках, а также с CD2 либо опухолеассоциированным антигеном человека ("TAA"). Не ограничиваясь какой-либо теорией, авторы настоящего изобретения считают, что комбинация взаимодействия с CD2 и комплексом TCR в одной полиспецифической молекуле может стимулировать как первичный сигнальный путь, который способствует лизису опухолевых клеток, опосредованному T-клетками (например, посредством кластеризации TCR), так и второй костимулирующий сигнальный путь для индукции пролиферации T-клеток и потенциального преодоления анергии. Кроме того, не ограничиваясь какой-либо теорией, полагают, что взаимодействия с TAA в дополнение к BCMA и компоненту комплекса TCR будут приводить к улучшению клинических результатов терапии рака на основе RTCC, например, В-клеточных злокачественных новообразований, благодаря нацеливанию на большее количество злокачественных В-клеток, чем с применением биспецифических привлекающих активаторов, которые нацелены только на BCMA и компонент комплекса TCR.
[0008] В одном аспекте в настоящем изобретении предусмотрены MBM (например, триспецифические связывающие молекулы ("TBM")), которые связываются с (1) BCMA человека, (2) CD3 или другим компонентом комплекса TCR и (3) CD2.
[0009] В другом аспекте в настоящем изобретении предусмотрены MBM (например, триспецифические связывающие молекулы ("TBM")), которые связываются с (1) BCMA человека, (2) CD3 или другим компонентом комплекса TCR и (3) TAA.
[0010] MBM (например, TBM) содержат по меньшей мере три антигенсвязывающих модуля ("ABM"), которые могут связывать (i) BCMA (ABM1), (ii) компонент комплекса TCR (ABM2) и (iii) CD2 либо TAA (ABM3). В некоторых вариантах осуществления каждый антигенсвязывающий модуль способен к связыванию своей соответствующей мишени одновременно со связыванием каждого из других антигенсвязывающих модулей со своей соответствующей мишенью. В основе ABM1 лежат иммуноглобулины, тогда как в основе ABM2 и ABM3 могут лежать иммуноглобулины или молекулы, отличные от иммуноглобулинов. Следовательно, MBM (например, TBM) могут содержать ABM на основе иммуноглобулинов или любую комбинацию ABM на основе иммуноглобулинов и на основе молекул, отличных от иммуноглобулинов. ABM на основе иммуноглобулинов, которые можно применять в MBM (например, TBM), описаны в разделе 7.2.1 и конкретных вариантах осуществления 1-142, 145-741, 782-793, 798-803 и 833-856 ниже. ABM на основе молекул, отличных от иммуноглобулинов, которые можно применять в MBM (например, TBM), описаны в разделе 7.2.2 и конкретных вариантах осуществления 143-144, 743-782 и 795-797 ниже. Дополнительные признаки иллюстративных ABM, которые связываются с BCMA человека, описаны в разделе 7.5 и конкретных вариантах осуществления 1-142 ниже. Дополнительные признаки иллюстративных ABM, которые связываются с компонентом комплекса TCR, описаны в разделе 7.6 и конкретных вариантах осуществления 151-741 ниже. Дополнительные признаки иллюстративных ABM, которые связываются с CD2, описаны в разделе 7.7 и конкретных вариантах осуществления 742-793 ниже. Дополнительные признаки иллюстративных ABM, которые связываются с TAA, описаны в разделе 7.8 и конкретных вариантах осуществления 794-856 ниже.
[0011] ABM из MBM (например, TBM) (или их части) могут быть соединены друг с другом, например, посредством коротких пептидных линкеров или посредством Fc-домена. Способы и компоненты для соединения ABM с образованием MBM описаны в разделе 7.3 и конкретных вариантах осуществления 857-1159 ниже.
[0012] MBM (например, TBM) имеют по меньшей мере три ABM (например, TBM является по меньшей мере тривалентной), но также могут иметь более трех ABM. Например, MBM (например, TBM) может иметь четыре ABM (т. е. быть тетравалентной), пять ABM (т. е. быть пентавалентной) или шесть ABM (т. е. быть гексавалентной) при условии, что MBM имеет по меньшей мере один ABM, который способен связывать BCMA, по меньшей мере один ABM, который способен связывать компонент комплекса TCR, и по меньшей мере один ABM, который способен связывать CD2 либо TAA. Иллюстративные тривалентные, тетравалентные, пентавалентные и гексавалентные конфигурации TBM показаны на фиг. 1 и описаны в разделе 7.4 и конкретных вариантах осуществления 1160-1263 ниже.
[0013] В настоящем изобретении дополнительно предусмотрены нуклеиновые кислоты, кодирующие МBM (в виде одной нуклеиновой кислоты либо в виде совокупности нуклеиновых кислот), и рекомбинантные клетки-хозяева и линии клеток, сконструированные для экспрессии нуклеиновых кислот и МBM по настоящему изобретению. Иллюстративные нуклеиновые кислоты, клетки-хозяева и линии клеток описаны в разделе 7.9 и конкретных вариантах осуществления 1653-1660 ниже.
[0014] В настоящем изобретении дополнительно предусмотрены конъюгаты лекарственных средств, содержащие МBM по настоящему изобретению. Такие конъюгаты для удобства называются в данном документе "конъюгатами антител и лекарственных средств" или "ADC", несмотря на то, что некоторые ABM могут представлять собой неиммуноглобулиновые домены. Примеры ADC описаны в разделе 7.10 и конкретных вариантах осуществления 1396-1435 ниже.
[0015] Также предусмотрены фармацевтические композиции, содержащие MBM и ADC. Примеры фармацевтических композиций описаны в разделе 7.11 и конкретном варианте осуществления 1494 ниже.
[0016] В данном документе дополнительно предусмотрены способы применения MBM, ADC и фармацевтических композиций по настоящему изобретению, например, для лечения пролиферативных состояний (например, форм рака), при которых экспрессируется BCMA, для лечения аутоиммунных нарушений и для лечения других заболеваний и состояний, ассоциированных с экспрессией BCMA. Иллюстративные способы описаны в разделе 7.12 и конкретных вариантах осуществления 1495-1575 ниже.
[0017] В настоящем изобретении дополнительно предусмотрены способы применения МBM, ADC и фармацевтических композиций в комбинации с другими средствами и видами терапии. Иллюстративные средства, виды терапии и способы комбинированной терапии описаны в разделе 7.13 и конкретных вариантах осуществления 1576-1652 ниже.
6. КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[0018] Фиг. 1A-1V: иллюстративные конфигурации TBM. На фиг. 1A проиллюстрированы компоненты иллюстративных конфигураций TBM, проиллюстрированных на фиг. 1B-1V. Не все участки, соединяющие различные домены каждой цепи, проиллюстрированы (например, линкер, соединяющий VH- и VL-домены scFv, шарнирный участок, соединяющий CH2- и CH3-домены Fc, и т. д. пропущены). На фиг. 1B-1P проиллюстрированы тривалентные TBM; на фиг. 1Q-1S проиллюстрированы тетравалентные TBM; на фиг. 1T проиллюстрирована пентавалентная TBM, и на фиг. 1U-1V проиллюстрированы гексавалентные TBM.
[0019] Фиг. 2A-2B: схемы триспецифических конструкций из примера 2.
[0020] Фиг. 3A-3F: результаты анализа RTCC из примера 2. ФИГ. 3A: соотношение E:T 5:1; фиг. 3B: соотношение E:T 3:1; фиг. 3C: соотношение E:T 1:1; фиг. 3D: соотношение E:T 1:3; фиг. 3E: соотношение E:T 1:5; фиг. 3F: условные обозначения к фигурам.
[0021] Фиг. 4A-C: измерения уровней цитокинов для IFN-γ (фиг. 4A), IL-2 (фиг. 4B) и TNF-α (фиг. 4C) в анализе высвобождения цитокинов из примера 2 при соотношении E:T, составляющем 1:5. Слева направо на каждой фигуре показаны данные для триспецифической AB3_TCR-CD58, триспецифической AB3_CD58-TCR, BSP, OAA, биспецифической AB3_TCR-HEL.
[0022] Фиг. 5: схематическое изображение CD58.
7. ПОДРОБНОЕ ОПИСАНИЕ
7.1. Определения
[0023] Предполагается, что используемые в данном документе следующие термины имеют приведенные ниже значения.
[0024] Цепь ABM. Отдельные ABM могут существовать в виде одной (например, в случае с scFv) полипептидной цепи или образовываться посредством ассоциации более чем одной полипептидной цепи (например, в случае с Fab). Используемый в данном документе термин "цепь ABM" относится ко всему ABM или его части, которые существуют в виде одной полипептидной цепи. Использование термина "цепь ABM" предполагается только для удобства и описательных целей и не означает конкретную конфигурацию или способ получения.
[0025] ADCC. Используемый в данном документе термин "ADCC" или "антителозависимая клеточноопосредованная цитотоксичность" означает клеточноопосредованную реакцию, где неспецифические цитотоксические клетки, которые экспрессируют FcγR, распознают связанное антитело на клетке-мишени и затем вызывают лизис клетки-мишени. ADCC коррелирует со связыванием с FcγRIIIa; увеличение связывания с FcγRIIIa приводит к увеличению активности ADCC.
[0026] ADCP. Используемый в данном документе термин "ADCP" или антителозависимый клеточноопосредованный фагоцитоз означает клеточноопосредованную реакцию, где неспецифические фагоцитарные клетки, которые экспрессируют FcγR, распознают связанное антитело на клетке-мишени и затем вызывают фагоцитоз клетки-мишени.
[0027] Дополнительное средство. Для удобства средство, которое применяют в комбинации с MBM, в данном документе называется "дополнительным" средством.
[0028] Антитело. Используемый в данном документе термин "антитело" относится к полипептиду (или к набору полипептидов) из семейства иммуноглобулинов, который способен к связыванию антигена нековалентно, обратимо и специфично. Например, встречающееся в природе "антитело" типа IgG представляет собой тетрамер, содержащий по меньшей мере две тяжелые (H) цепи и две легкие (L) цепи, соединенные между собой посредством дисульфидных связей. Каждая тяжелая цепь состоит из вариабельного участка тяжелой цепи (сокращенно обозначенного в данном документе как VH) и константного участка тяжелой цепи. Константный участок тяжелой цепи состоит из трех доменов - CH1, CH2 и CH3. Каждая легкая цепь состоит из вариабельного участка легкой цепи (сокращенно обозначенного в данном документе как VL) и константного участка легкой цепи. Константный участок легкой цепи состоит из одного домена (сокращенно обозначенного в данном документе как CL). VH- и VL-участки могут быть дополнительно подразделены на участки гипервариабельности, называемые участками, определяющими комплементарность (CDR), которые чередуются с участками, являющимися более консервативными, называемыми каркасными участками (FR). Каждый VH и VL состоит из трех CDR и четырех FR, расположенных от амино-конца к карбокси-концу в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. Вариабельные участки тяжелой и легкой цепей содержат связывающий домен, который взаимодействует с антигеном. Константные участки антител способны опосредовать связывание иммуноглобулина с тканями или факторами хозяина, в том числе с различными клетками иммунной системы (например, эффекторными клетками) и первым компонентом (Clq) классического пути активации системы комплемента. Термин "антитело" включает без ограничения моноклональные антитела, человеческие антитела, гуманизированные антитела, камелизированные антитела, химерные антитела, биспецифические или полиспецифические антитела и антиидиотипические (анти-Id) антитела (в том числе, например, анти-Id антитела к антителам по настоящему изобретению). Антитела могут относиться к любому изотипу/классу (например, IgG, IgE, IgM, IgD, IgA и IgY) или подклассу (например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2).
[0029] Как легкая, так и тяжелая цепи подразделяются на участки структурной и функциональной гомологии. Термины "константный" и "вариабельный" используются в функциональном смысле. В связи с этим следует понимать, что вариабельные домены из частей как легкой (VL), так и тяжелой (VH) цепей определяют распознавание антигена и специфичность. Напротив, константные домены легкой цепи (CL) и тяжелой цепи (CH1, CH2 или CH3) придают важные биологические свойства, такие как секреция, трансплацентарный переход, связывание с Fc-рецепторами, связывание комплемента и т. п. Принято, что нумерация доменов константных участков возрастает по мере их удаления от антигенсвязывающего центра или аминоконца антитела. N-конец представляет собой вариабельный участок, а на C-конце находится константный участок; CH3- и CL-домены фактически содержат карбокси-конец тяжелой и легкой цепей соответственно.
[0030] Фрагмент антитела. Используемый в данном документе термин "фрагмент антитела" из антитела относится к одной или более частям антитела. В некоторых вариантах осуществления эти части представляют собой часть контактного(контактных) домена(доменов) антитела. В некоторых других вариантах осуществления эта(эти) часть(части) представляет(представляют) собой антигенсвязывающие фрагменты, которые сохраняют способность к связыванию антигена нековалентно, обратимо и специфично и иногда называются в данном документе "антигенсвязывающим фрагментом", "его антигенсвязывающим фрагментом", "антигенсвязывающей частью" и т. п. Примеры связывающих фрагментов включают без ограничения одноцепочечные Fv (scFv), Fab-фрагмент, одновалентный фрагмент, состоящий из VL-, VH-, CL- и CH1-доменов; F(ab)2-фрагмент - бивалентный фрагмент, содержащий два Fab-фрагмента, соединенных дисульфидным мостиком в шарнирном участке; Fd-фрагмент, состоящий из VH- и CH1-доменов; Fv-фрагмент, состоящий из VL- и VH-доменов одного плеча антитела; dAb-фрагмент (Ward et al., (1989) Nature 341:544-546), который состоит из VH-домена; и выделенный участок, определяющий комплементарность (CDR). Таким образом, термин "фрагмент антитела" охватывает как протеолитические фрагменты антител (например, Fab- и F(ab)2-фрагменты), так и сконструированные белки, содержащие одну или более частей антитела (например, scFv).
[0031] Фрагменты антител также могут быть включены в состав однодоменных антител, максиантител, миниантител, интрател, диател, триател, тетрател, v-NAR и бис-scFv (см., например, Hollinger and Hudson, 2005, Nature Biotechnology 23: 1126-1136). Фрагменты антител могут быть привиты на каркасные структуры на основе полипептидов, таких как фибронектин III типа (Fn3) (см. патент США № 6703199, в котором описаны монотела на основе полипептида фибронектина).
[0032] Фрагменты антител могут быть включены в состав одноцепочечных молекул, содержащих пару тандемных Fv-сегментов (например, VH-CH1-VH-CH1), которые вместе с комплементарными полипептидами легкой цепи (например, VL-VC-VL-VC) образуют пару антигенсвязывающих участков (Zapata et al., 1995, Protein Eng. 8:1057-1062; и патент США № 5641870).
[0033] Система нумерации антител. В настоящем описании ссылки на пронумерованные аминокислотные остатки в доменах антител приводятся на основе системы нумерации EU, если не указано иное (например, в таблицах 11C-1-11C-2). Эта система была первоначально разработана Edelman et al., 1969, Proc. Nat'l Acad. Sci. USA 63:78-85, и описана подробно в Kabat et al., 1991, в Sequences of Proteins of Immunological Interest, US Department of Health and Human Services, NIH, USA.
[0034] Антигенсвязывающий модуль. Используемый в данном документе термин "антигенсвязывающий модуль" или "ABM" относится к части МBM, которая обладает способностью связываться с антигеном нековалентно, обратимо и специфично. В основе ABM может лежать иммуноглобулин или молекула, отличная от иммуноглобулина. Используемые в данном документе термины "ABM1" и "ABM для BCMA" (и т. п.) относятся к ABM, который специфично связывается с BCMA, термины "ABM2" и "ABM для TCR" (и т. п.) относятся к ABM, который специфично связывается с компонентом комплекса TCR, термин "ABM3" относится к ABM, который специфично связывается с CD2 или с TAA (в зависимости от контекста), термин "ABM для CD2" (и т. п.) относятся к ABM, который специфично связывается с CD2, и термин "ABM для TAA" (и т. п.) относится к ABM, который специфично связывается с TAA. Термины ABM1, ABM2 и ABM3 используются исключительно для удобства и не предполагаются как обозначающие какую-либо конкретную конфигурацию МBM. В некоторых вариантах осуществления ABM2 связывается с CD3 (и называется в данном документе "ABM для CD3" или т. п.). Соответственно, раскрытия, относящиеся к одному ABM2 и множеству ABM2, также применимы к ABM для CD3.
[0035] Антигенсвязывающий домен. Термин "антигенсвязывающий домен" (ABD) относится к части молекулы, которая обладает способностью связываться с антигеном нековалентно, обратимо и специфично. Иллюстративные антигенсвязывающие домены включают в себя антигенсвязывающие фрагменты и части каркасных структур как на основе иммуноглобулинов, так и на основе молекул, отличных от иммуноглобулинов, которые сохраняют способность к связыванию антигена нековалентно, обратимо и специфично. Используемый в данном документе термин "антигенсвязывающий домен" охватывает фрагменты антител, которые сохраняют способность к связыванию антигена нековалентно, обратимо и специфично.
[0036] Антигенсвязывающий фрагмент. Термин "антигенсвязывающий фрагмент" антитела относится к части антитела, которая сохраняет способность связываться с антигеном нековалентно, обратимо и специфично.
[0037] Ассоциированный. Термин "ассоциированный" применительно к МBM относится к функциональной связи между двумя или более полипептидными цепями. В частности, термин "ассоциированный" означает, что два или более полипептида ассоциированы друг с другом, например, нековалентно посредством молекулярных взаимодействий или ковалентно посредством одного или более дисульфидных мостиков или химических сшивок, так что они образуют функциональную MBM (например, TBM), в которой ABM1, ABM2 и ABM3 могут связывать свои соответствующие мишени. Примеры ассоциаций, которые могут присутствовать в МBM, включают (без ограничения) ассоциации между Fc-участками в Fc-домене (гомодимерном или гетеродимерном, который описан в разделе 7.3.1.5), ассоциации между VH- и VL-участками в Fab или Fv и ассоциации между CH1 и CL в Fab.
[0038] B-клетка. Используемый в данном документе термин "В-клетка" относится к клетке В-клеточной линии дифференцировки, которая принадлежит к типу белых кровяных телец и подтипу лимфоцитов. Примеры В-клеток включают плазмобласты, плазматические клетки, лимфоплазмоцитоидные клетки, В-клетки памяти, фолликулярные В-клетки, В-клетки маргинальной зоны, B-1-клетки, B-2-клетки и регуляторные В-клетки.
[0039] В-клеточное злокачественное новообразование. Как используется в данном документе, В-клеточное злокачественное новообразование относится к неконтролируемой пролиферации В-клеток. Примеры В-клеточного злокачественного новообразования включают неходжкинские лимфомы (NHL), формы лимфомы Ходжкина, лейкоз и миелому. Например, В-клеточное злокачественное новообразование может представлять собой без ограничения множественную миелому, хронический лимфоцитарный лейкоз (CLL)/мелкоклеточную лимфоцитарную лимфому (SLL), фолликулярную лимфому, мантийноклеточную лимфому (MCL), диффузную крупноклеточную В-клеточную лимфому (DLBCL), формы лимфомы из клеток маргинальной зоны, лимфому Беркитта, лимфоплазмоцитарную лимфому (макроглобулинемию Вальденстрема), волосатоклеточный лейкоз, первичную лимфому центральной нервной системы (CNS), первичную медиастинальную крупноклеточную В-клеточную лимфому, медиастинальную лимфому "серой зоны" (MGZL), B-клеточную лимфому из клеток маргинальной зоны селезенки, внеузловую B-клеточную лимфому из клеток маргинальной зоны MALT, узловую B-клеточную лимфому из клеток маргинальной зоны и первичную эффузионную лимфому, а также новообразования из плазмоцитоидных дендритных клеток.
[0040] BCMA. Используемый в данном документе термин "ВСМА" относится к антигену созревания В-клеток. BCMA (также известный как TNFRSF17, BCM или CD269) является представителем семейства рецепторов фактора некроза опухоли (TNFR) и преимущественно экспрессируется на терминально дифференцированных B-клетках, например, B-клетках памяти и плазматических клетках. Его лиганды включают фактор активации В-клеток (BAFF) и лиганд, индуцирующий пролиферацию (APRIL). Белок BCMA кодируется геном TNFRSF17. Иллюстративные последовательности BCMA доступны в базе данных Uniprot под номером доступа Q02223.
[0041] Связывающие последовательности. Что касается таблиц 11, 12, 13, 14 или 17 (включая их подразделы), термин "связывающие последовательности" означает ABM, имеющий полный набор CDR, пару VH-VL или scFv, представленные в этой таблице.
[0042] Бивалентный. Используемый в данном документе термин "бивалентный" применительно к антигенсвязывающей молекуле относится к антигенсвязывающей молекуле, которая имеет два антигенсвязывающих домена. Домены могут быть одинаковыми или разными. Соответственно, бивалентная антигенсвязывающая молекула может быть моноспецифической или биспецифической.
[0043] Рак. Термин "рак" относится к заболеванию, которое характеризуется неконтролируемым (и часто быстрым) ростом аберрантных клеток. Раковые клетки могут распространяться локально или через кровоток и лимфатическую систему в другие части организма. Примеры различных форм рака описаны в данном документе и включают без ограничения лейкоз, множественную миелому, бессимптомную миелому, лимфому Ходжкина и неходжкинскую лимфому, например, любые BCMA-положительные формы рака любого из вышеуказанных видов. Термин "раковая В-клетка" относится к В-клетке, которая подвергается или подверглась неконтролируемой пролиферации.
[0044] CD3. Термин "CD3" или "кластер дифференцировки 3" относится к корецептору Т-клеточного рецептора, представляющему собой кластер дифференцировки 3. CD3 содействует активации как цитотоксических Т-клеток (например, CD8+ необученных Т-клеток), так и Т-хелперных клеток (например, CD4+ необученных Т-клеток) и состоит из четырех отдельных цепей: одной цепи CD3γ (например, под номерами доступа в Genbank NM_000073 и MP_000064 (человек)), одной цепи CD3δ (например, под номерами доступа в Genbank NM_000732, NM_001040651, NP_00732 и NP_001035741 (человек)) и двух цепей CD3ε (например, под номерами доступа в Genbank NM_000733 и NP_00724 (человек)). Цепи CD3 представляют собой белки клеточной поверхности с высокой степенью родства из суперсемейства иммуноглобулинов, содержащие единственный внеклеточный иммуноглобулиновый домен. Молекула CD3 ассоциирует с Т-клеточным рецептором (TCR) и ζ-цепью с образованием Т-клеточного рецепторного комплекса (TCR), функция которого заключается в генерации сигналов активации в Т-лимфоцитах.
[0045] Если специально не указано иное, упоминание CD3 в настоящей заявке может относиться к корецептору CD3, корецепторному комплексу CD3 или любой полипептидной цепи корецепторного комплекса CD3.
[0046] Химерное антитело. Термин "химерное антитело" (или его антигенсвязывающий фрагмент) представляет собой молекулу антитела (или ее антигенсвязывающий фрагмент), в которой (a) константный участок или его часть изменены, заменены или обменены таким образом, что антигенсвязывающий центр (вариабельный участок) связан с константным участком, соответствующим другим или измененным классу, эффекторной функции и/или виду, или с совершенно другой молекулой, которая придает новые свойства химерному антителу, например, ферментом, токсином, гормоном, фактором роста, лекарственным средством и т. д.; или (b) вариабельный участок или его часть изменены, заменены или обменены на вариабельный участок, обладающий другой или измененной специфичностью к антигену. Например, мышиное антитело можно модифицировать посредством замены его константного участка на константный участок из человеческого иммуноглобулина. Вследствие замены на человеческий константный участок химерное антитело может сохранять свою специфичность в распознавании антигена и при этом обладать сниженной антигенностью у человека по сравнению с исходным мышиным антителом.
[0047] В комбинации. Как используется в данном документе, вводимый "в комбинации" означает, что два (или более) различных средства для лечения доставляются субъекту в течение периода, когда субъект страдает нарушением, например, два или более средства для лечения доставляются после того, как у субъекта было диагностировано нарушение, и до того, как нарушение было излечено или устранено или лечение было прекращено по другим причинам.
[0048] Участок, определяющий комплементарность. Используемые в данном документе термины "участок, определяющий комплементарность" или "CDR" относятся к последовательностям аминокислот в пределах вариабельных участков антитела, которые придают специфичность к антигену и аффинность связывания. Например, как правило, имеются три CDR в каждом вариабельном участке тяжелой цепи (например, CDR-H1, CDR-H2 и CDR-H3) и три CDR в каждом вариабельном участке легкой цепи (CDR-L1, CDR-L2 и CDR-L3). Точные границы аминокислотной последовательности данного CDR можно определять с применением любой из множества широко известных схем, включая схемы, описанные Kabat et al., 1991, "Sequences of Proteins of Immunological Interest", 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD (схема нумерации по "Kabat"), Al-Lazikani et al., 1997, JMB 273:927-948 (схема нумерации по "Chothia"), и нумерацию ImMunoGenTics (IMGT) (Lefranc, 1999, The Immunologist 7:132-136 (1999); Lefranc et al., 2003, Dev. Comp. Immunol. 27:55-77 (схема нумерации по "IMGT"). Например, в случае с классическими форматами, согласно Kabat аминокислотные остатки CDR в вариабельном домене тяжелой цепи (VH) пронумерованы 31-35 (CDR-H1), 50-65 (CDR-H2) и 95-102 (CDR-H3); и аминокислотные остатки CDR в вариабельном домене легкой цепи (VL) пронумерованы 24-34 (CDR-L1), 50-56 (CDR-L2) и 89-97 (CDR-L3). Согласно Chothia аминокислоты CDR в VH пронумерованы 26-32 (CDR-H1), 52-56 (CDR-H2) и 95-102 (CDR-H3); и аминокислотные остатки в VL пронумерованы 26-32 (CDR-L1), 50-52 (CDR-L2) и 91-96 (CDR-L3). В комбинации определений CDR как по Kabat, так и по Chothia CDR состоят из аминокислотных остатков 26-35 (CDR-H1), 50-65 (CDR-H2) и 95-102 (CDR-H3) в VH человека и аминокислотных остатков 24-34 (CDR-L1), 50-56 (CDR-L2) и 89-97 (CDR-L3) в VL человека. Согласно IMGT аминокислотные остатки CDR в VH пронумерованы примерно 26-35 (CDR-H1), 51-57 (CDR-H2) и 93-102 (CDR-H3), и аминокислотные остатки CDR в VL пронумерованы примерно 27-32 (CDR-L1), 50-52 (CDR-L2) и 89-97 (CDR-L3) (нумерация в соответствии с "Kabat"). Согласно IMGT CDR-участки антитела можно определять с применением программы IMGT/DomainGapAlign.
[0049] Одновременно. Термин "одновременно" не ограничивается введением средств терапии (например, профилактических или терапевтических средств) точно в одно и то же время, а скорее означает, что фармацевтическую композицию, содержащую MBM или ADC, вводят субъекту последовательно и в течение временного интервала таким образом, чтобы молекулы могли действовать вместе с дополнительным(дополнительными) средством(средствами) терапии с обеспечением большей пользы, чем если бы их вводили иным способом.
[0050] Консервативные модификации последовательностей. Термин "консервативные модификации последовательностей" относится к аминокислотным модификациям, которые не оказывают значительного влияния на характеристики связывания МBM или ее компонента (например, ABM или Fc-участка) или не изменяют их. Такие консервативные модификации включают аминокислотные замены, добавления и делеции. Модификации можно вводить в MBM с помощью стандартных методик, таких как сайт-направленный мутагенез и ПЦР-опосредованный мутагенез. Консервативные аминокислотные замены представляют собой замены, при которых аминокислотный остаток заменяют на аминокислотный остаток, имеющий сходную боковую цепь. Семейства аминокислотных остатков, имеющих сходные боковые цепи, были определены в уровне техники. Эти семейства включают аминокислоты с основными боковыми цепями (например, лизин, аргинин, гистидин), кислыми боковыми цепями (например, аспарагиновую кислоту, глутаминовую кислоту), незаряженными полярными боковыми цепями (например, глицин, аспарагин, глутамин, серин, треонин, тирозин, цистеин, триптофан), неполярными боковыми цепями (например, аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин), бета-разветвленными боковыми цепями (например, треонин, валин, изолейцин) и ароматическими боковыми цепями (например, тирозин, фенилаланин, триптофан, гистидин). Таким образом, один или более аминокислотных остатков в MBM можно заменить другими аминокислотными остатками из того же семейства боковой цепи, и измененную MBM можно тестировать в отношении, например, связывания с молекулами-мишенями и/или эффективной гетеродимеризации и/или эффекторной функции.
[0051] Диатело. Используемый в данном документе термин "диатело" относится к небольшим фрагментам антител с двумя антигенсвязывающими центрами, как правило, образованным посредством спаривания цепей scFv. Каждый scFv содержит вариабельный домен тяжелой цепи (VH), соединенный с вариабельным доменом легкой цепи (VL) в той же полипептидной цепи (VH-VL, где VH расположен с N-концевой либо с C-концевой стороны от VL). В отличие от типичного scFv, в котором VH и VL разделены линкером, который обеспечивает для VH и VL в одной и той же полипептидной цепи возможность спаривания и образования антигенсвязывающего домена, диатела, как правило, содержат линкер, который является слишком коротким для обеспечения возможности спаривания между VH- и VL-доменами в одной и той же цепи, что вынуждает VH- и VL-домены спариваться с комплементарными доменами другой цепи и образовывать два антигенсвязывающих центра. Диатела описаны более подробно, например, в EP 404097; WO 93/11161 и Hollinger et al., 1993, Proc. Natl. Acad. Sci. USA 90:6444-6448.
[0052] dsFv. Термин "dsFv" относится к Fv-фрагментам, стабилизированным посредством дисульфидных связей. VH и VL в dsFv соединены междоменной дисульфидной связью. Для получения таких молекул по одной аминокислоте в каждом из каркасных участков VH и VL подвергают мутации по типу замены на цистеин, который в свою очередь образует стабильную межцепочечную дисульфидную связь. Как правило, положение 44 в VH и положение 100 в VL подвергают мутации по типу замены на остатки цистеина. См. Brinkmann, 2010, Antibody Engineering 181-189, DOI:10.1007/978-3-642-01147-4_14. Термин dsFv охватывает как то, что известно как dsFv (молекула, в которой VH и VL соединены межцепочечной дисульфидной связью, но не линкерным пептидом), так и то, что известно как scdsFv (молекула, в которой VH и VL соединены линкером, а также межцепочечной дисульфидной связью).
[0053] Эффекторная функция. Термин "эффекторная функция" относится к активности молекулы антитела, которая опосредована связыванием посредством домена антитела, отличного от антигенсвязывающего домена, и обычно опосредована связыванием эффекторных молекул. Эффекторная функция включает комплемент-опосредованную эффекторную функцию, которая опосредована, например, связыванием компонента C1 системы комплемента с антителом. Активация комплемента важна для опсонизации и лизиса клеточных патогенов. Активация комплемента также стимулирует воспалительный ответ и может также участвовать в аутоиммунной гиперчувствительности. Эффекторная функция также включает эффекторную функцию, опосредованную Fc-рецептором (FcR), которая может запускаться при связывании константного домена антитела с Fc-рецептором (FcR). При связывании антитела с Fc-рецепторами на клеточных поверхностях запускается ряд важных и разнообразных биологических реакций, в том числе поглощение и разрушение частиц, покрытых антителами, выведение иммунных комплексов, лизис клеток-мишеней, покрытых антителами, клетками-киллерами (называемый антителозависимой клеточноопосредованной цитотоксичностью или ADCC), высвобождение медиаторов воспаления, перенос через плаценту и контроль продуцирования иммуноглобулинов. Эффекторная функция антитела может быть изменена посредством изменения, например, усиления или снижения, аффинности антитела к эффектoрной молекуле, такой как Fc-рецептор или компонент системы комплемента. Аффинность связывания обычно будет варьироваться посредством модификации сайта связывания эффектoрной молекулы, и в данном случае целесообразно определить местоположение сайта, представляющего интерес, и модифицировать по меньшей мере часть данного сайта подходящим образом. Также предусматривается, что для изменения в сайте связывания эффекторной молекулы на антителе не является необходимым значительное изменение общей аффинности связывания, но можно изменять геометрические параметры взаимодействия, делая эффекторный механизм неэффективным, как при непродуктивном связывании. Дополнительно предусматривается, что эффекторную функцию также можно изменять посредством модификации сайта, не участвующего непосредственно в связывании эффекторной молекулы, но иным образом участвующего в выполнении эффекторной функции.
[0054] Эпитоп. Эпитоп или антигенная детерминанта представляет собой часть антигена, распознаваемую антителом или другим антигенсвязывающим фрагментом, описанным в данном документе. Эпитоп может быть линейным или конформационным.
[0055] Fab. Используемый в данном документе термин "Fab" или "Fab-участок" означает участок полипептида, который содержит VH-, CH1-, VL- и CL-домены иммуноглобулина. Эти термины могут относиться к данному участку в отдельности или к данному участку в качестве составной части антигенсвязывающей молекулы по настоящему изобретению.
[0056] Fab-домены образуются посредством ассоциации CH1-домена, присоединенного к VH-домену, с CL-доменом, присоединенным к VL-домену. VH-домен спаривается с VL-доменом с образованием Fv-участка, и CH1-домен спаривается с CL-доменом для дополнительной стабилизации связывающего модуля. Дисульфидная связь между двумя константными доменами может дополнительно стабилизировать Fab-домен.
[0057] Fab-участки можно получать посредством протеолитического расщепления молекул иммуноглобулинов (например, с применением ферментов, таких как папаин) или посредством рекомбинантной экспрессии. В нативных молекулах иммуноглобулинов Fab образуются посредством ассоциации двух разных полипептидных цепей (например, VH-CH1 в одной цепи ассоциирует с VL-CL в другой цепи). Как правило, Fab-участки экспрессируются рекомбинантно, как правило, в двух полипептидных цепях, хотя в данном документе также рассматриваются одноцепочечные Fab.
[0058] Fc-домен. Термин "Fc-домен" относится к паре ассоциированных Fc-участков. Два Fc-участка димеризуются с образованием Fc-домена. Два Fc-участка в Fc-домене могут быть одинаковыми (такой Fc-домен упоминается в данном документе как "гомодимер Fc") или могут отличаться друг от друга (такой Fc-домен упоминается в данном документе как "гетеродимер Fc").
[0059] Fc-участок. Используемый в данном документе термин "Fc-участок" или "Fc-цепь" означает полипептид, содержащий CH2-CH3-домены молекулы IgG, в некоторых случаях включая шарнирный участок. В системе нумерации EU в случае с IgG1 человека CH2-CH3-домен состоит из аминокислот 231-447, а шарнирный участок состоит из аминокислот 216-230. Таким образом, определение "Fc-участок" включает как аминокислоты 231-447 (CH2-CH3), так и аминокислоты 216-447 (шарнирный участок-CH2-CH3), или их фрагменты. "Fc-фрагмент" в данном контексте может содержать меньше аминокислот с одного или обоих из N- и C-концов, но все еще сохраняет способность к образованию димера с другим Fc-участком, что можно определить с использованием стандартных способов, как правило, на основании размера (например, хроматографии в неденатурирующих условиях, эксклюзионной хроматографии). Fc-участки IgG человека особенно применимы в настоящем изобретении и могут представлять собой Fc-участок из IgG1, IgG2 или IgG4 человека.
[0060] Fv. Термин "Fv" относится к минимальному фрагменту антитела, получаемому из иммуноглобулина, который содержит полный сайт распознавания и связывания мишени. Этот участок состоит из димера одного вариабельного домена тяжелой цепи и одного вариабельного домена легкой цепи в тесной нековалентной ассоциации (димера VH-VL). Именно в этой конфигурации три CDR каждого вариабельного домена взаимодействуют для определения сайта связывания мишени на поверхности димера VH-VL. Зачастую шесть CDR придают антителу специфичность связывания мишени. Однако, в некоторых случаях даже один вариабельный домен (или половина Fv, содержащая только три CDR, специфичных в отношении мишени) может обладать способностью распознавать и связывать мишень. Ссылка на димер VH-VL в данном документе не предполагается как обозначающая какую-либо конкретную конфигурацию. В качестве примера и без ограничения, VH и VL способны объединяться друг с другом в любой конфигурации, описанной в данном документе, с образованием полуантитела, или каждый из них может присутствовать в отдельном полуантителе, и они способны объединяться друг с другом с образованием антигенсвязывающего домена при ассоциации отдельных полуантител, например, с образованием TBM по настоящему изобретению. В случае присутствия в одной полипептидной цепи (например, scFv) VH может быть расположен с N-концевой или C-концевой стороны от VL.
[0061] Полуантитело. Термин "полуантитело" относится к молекуле, которая содержит по меньшей мере один ABM или цепь ABM и может ассоциировать с другой молекулой, содержащей ABM или цепь ABM, посредством, например, дисульфидного мостика или молекулярных взаимодействий (например, взаимодействий типа "выступ во впадину" между гетеродимерами Fc). Полуантитело может состоять из одной полипептидной цепи или более чем одной полипептидной цепи (например, двух полипептидных цепей Fab). В одном варианте осуществления полуантитело содержит Fc-участок.
[0062] Примером полуантитела является молекула, содержащая тяжелую и легкую цепь антитела (например, антитела IgG). Другим примером полуантитела является молекула, содержащая первый полипептид, содержащий VL-домен и CL-домен, и второй полипептид, содержащий VH-домен, CH1-домен, шарнирный домен, CH2-домен и CH3-домен, где VL- и VH-домены образуют ABM. Еще одним примером полуантитела является полипептид, содержащий scFv-домен, CH2-домен и CH3-домен.
[0063] Полуантитело может содержать более одного ABM, например, полуантитело, содержащее (в направлении от N-конца к C-концу) scFv-домен, CH2-домен, CH3-домен и другой scFv-домен.
[0064] Полуантитела могут также содержать цепь ABM, которая при ассоциации с другой цепью ABM в другом полуантителе образует полный ABM.
[0065] Таким образом, MBM (например, TBM) может содержать одно, чаще два или даже более двух полуантител, и полуантитело может содержать один или более ABM или цепей ABM.
[0066] В некоторых MBM первое полуантитело будет ассоциировать, например, гетеродимеризоваться, со вторым полуантителом. В других MBM первое полуантитело будет ковалентно связано со вторым полуантителом, например, посредством дисульфидных мостиков или химического сшивания. В еще нескольких других МBM первое полуантитело будет ассоциировать со вторым полуантителом посредством как ковалентных присоединений, так и нековалентных взаимодействий, например, дисульфидных мостиков и взаимодействий типа "выступ во впадину".
[0067] Термин "полуантитело" предполагается только для описательных целей и не означает конкретную конфигурацию или способ получения. Описания полуантитела как "первого" полуантитела, "второго" полуантитела, "левого" полуантитела, "правого" полуантитела или т. п. приведены исключительно для удобства и описательных целей.
[0068] Гексавалентный. Используемый в данном документе термин "гексавалентный" применительно к антигенсвязывающей молекуле (например, TBM) относится к антигенсвязывающей молекуле, которая имеет шесть антигенсвязывающих доменов. Гексавалентные TBM по настоящему изобретению, как правило, имеют три пары антигенсвязывающих доменов, каждый из которых связывается с одним и тем же антигеном, хотя различные конфигурации (например, три антигенсвязывающих домена, которые связываются с BCMA, два антигенсвязывающих домена, которые связываются с компонентом комплекса TCR, и один антигенсвязывающий домен, который связывается с CD2 или TAA, или три антигенсвязывающих домена, которые связываются с BCMA, два антигенсвязывающих домена, которые связываются с CD2 или TAA, и один антигенсвязывающий домен, который связывается с компонентом комплекса TCR) находятся в пределах объема настоящего изобретения. Примеры гексавалентных TBM схематически показаны на фиг. 1U-1V.
[0069] Впадина. Применительно к взаимодействию типа "выступ во впадину" "впадина" относится к по меньшей мере одной боковой цепи аминокислоты, которая углублена относительно области контакта первой Fc-цепи и, следовательно, может располагаться в компенсирующем "выступе" в соседней области контакта второй Fc-цепи, чтобы стабилизировать гетеродимер Fc и, таким образом, способствовать, например, образованию гетеродимера Fc вместо образования гомодимера Fc.
[0070] Клетка-хозяин или рекомбинантная клетка-хозяин. Термины "клетка-хозяин" или "рекомбинантная клетка-хозяин" относятся к клетке, которая была генетически сконструирована, например, посредством введения гетерологичной нуклеиновой кислоты. Следует понимать, что такие термины предполагаются как обозначающие не только конкретную рассматриваемую клетку, но и потомство такой клетки. Поскольку определенные модификации могут происходить в последующих поколениях вследствие мутации либо влияний окружающей среды, такое потомство может в действительности не являться идентичным родительской клетке, но, тем не менее, оно все же включено в объем термина "клетка-хозяин", используемого в данном документе. Клетка-хозяин может нести гетерологичную нуклеиновую кислоту транзиентно, например, во внехромосомном гетерологичном векторе экспрессии, или стабильно, например, посредством интеграции гетерологичной нуклеиновой кислоты в геном клетки-хозяина. Для целей экспрессии МBM по настоящему изобретению клетка-хозяин может относиться к линии клеток, происходящей от млекопитающих или обладающей характеристиками, сходными с характеристиками клеток млекопитающих, такой как клетки почки обезьяны (COS, например, COS-1, COS-7), HEK293, клетки почки новорожденного хомячка (BHK, например, BHK21), клетки яичника китайского хомячка (CHO), NSO, PerC6, BSC-1, клетки гепатоцеллюлярной карциномы человека (например, Hep G2), SP2/0, HeLa, клетки почки быка Мадин-Дарби (MDBK), клетки миеломы и лимфомы или их производные и/или сконструированные варианты. Сконструированные варианты включают, например, производные с модифицированным профилем гликанов и/или производные, модифицированные по сайтам сайт-специфической интеграции.
[0071] Человеческое антитело. Используемый в данном документе термин "человеческое антитело" включает антитела, имеющие вариабельные участки, в которых как каркасные, так и CDR-участки получены из последовательностей, происходящих от человека. Кроме того, если антитело содержит константный участок, то константный участок также получен из таких человеческих последовательностей, например, человеческих последовательностей зародышевого типа, или мутантных вариантов человеческих последовательностей зародышевого типа, или антитела, содержащего консенсусные последовательности каркасных участков, полученные посредством анализа человеческих последовательностей каркасных участков, например, как описано в Knappik et al., 2000, J Mol Biol 296, 57-86. Структуры и местоположения вариабельных доменов иммуноглобулинов, например, CDR, можно определять с применением широко известных схем нумерации, например, схемы нумерации по Kabat, схемы нумерации по Chothia или комбинации схем по Kabat и по Chothia (см., например, Lazikani et al., 1997, J. Mol. Bio. 273:927-948; Kabat et al., 1991, Sequences of Proteins of Immunological Interest, 5th edit., NIH Publication no. 91-3242 U.S. Department of Health and Human Services; Chothia et al., 1987, J. Mol. Biol. 196:901-917; Chothia et al., 1989, Nature 342:877-883).
[0072] Человеческие антитела могут содержать аминокислотные остатки, которые не кодируются человеческими последовательностями (например, мутации, введенные посредством случайного или сайт-специфического мутагенеза in vitro или посредством соматической мутации in vivo, или консервативную замену, которая способствует стабильности или изготовлению). Однако используемый в данном документе термин "человеческое антитело" не предполагается как включающий антитела, в которых последовательности CDR, полученные из антитела зародышевого типа другого вида млекопитающих, такого как мышь, были привиты на человеческие последовательности каркасных участков.
[0073] Гуманизированный. Термин "гуманизированные" формы антител, отличных от человеческих (например, мышиных), относится к химерным антителам, которые содержат минимальную последовательность, полученную из иммуноглобулина, отличного от человеческого. В большинстве случаев гуманизированные антитела представляют собой человеческие иммуноглобулины (реципиентное антитело), в которых остатки из гипервариабельного участка, полученного от реципиента, заменены остатками из гипервариабельного участка, полученного из вида, отличного от человека (донорного антитела), такого как мышь, крыса, кролик или примат, отличный от человека, обладающего необходимой специфичностью, аффинностью и способностью. В некоторых случаях остатки каркасного участка (FR) человеческого иммуноглобулина заменены соответствующими остатками, отличными от человеческих. Кроме того, гуманизированные антитела могут содержать остатки, которые не обнаруживаются в реципиентном антителе или в донорном антителе. Эти модификации осуществляют для дополнительного улучшения характеристик антитела. Как правило, гуманизированное антитело будет содержать по существу все из по меньшей мере одного, и, как правило, двух, вариабельных доменов, в которых все или по существу все гипервариабельные петли соответствуют гипервариабельным петлям иммуноглобулина, отличного от человеческого, и все или по существу все FR представляют собой FR из последовательности lo человеческого иммуноглобулина. Гуманизированное антитело будет также необязательно содержать по меньшей мере часть константного участка иммуноглобулина (Fc), как правило, человеческого иммуноглобулина. Подробнее см. Jones et al., 1986, Nature 321:522-525; Riechmann et al., 1988, Nature 332:323-329 и Presta, 1992, Curr. Op. Struct. Biol. 2:593-596. См. также следующие обзорные статьи и литературные источники, цитируемые в них: Vaswani and Hamilton, 1998, Ann. Allergy, Asthma & Immunol. 1:105-115; Harris, 1995, Biochem. Soc. Transactions 23:1035-1038; Hurle and Gross, 1994, Curr. Op. Biotech. 5:428-433.
[0074] Выступ. Применительно к взаимодействию типа "выступ во впадину" "выступ" относится к по меньшей мере одной боковой цепи аминокислоты, которая выступает над областью контакта первой Fc-цепи и, следовательно, может располагаться в компенсирующей "впадине" в области контакта второй Fc-цепи, чтобы стабилизировать гетеродимер Fc и, таким образом, способствовать, например, образованию гетеродимера Fc вместо образования гомодимера Fc.
[0075] Выступы и впадины (или "выступы во впадины"). Один механизм гетеродимеризации Fc обычно упоминается в уровне техники как "выступы и впадины", или "выступ во впадину", или "выступы во впадины". Эти термины относятся к аминокислотным мутациям, которые создают стерические влияния, способствующие образованию гетеродимеров Fc вместо гомодимеров Fc, как описано, например, в Ridgway et al., 1996, Protein Engineering 9(7):617; Atwell et al., 1997, J. Mol. Biol. 270:26; и патенте США № 8216805. Мутации типа "выступ во впадину" можно использовать в комбинации с другими стратегиями для улучшения гетеродимеризации, например, как описано в разделе 7.3.1.6.
[0076] Моноклональное антитело. Используемый в данном документе термин "моноклональное антитело" относится к полипептидам, в том числе антителам, фрагментам антител, молекулам (включая TBM) и т. д., которые получены из одного и того же генетического источника.
[0077] Одновалентный. Используемый в данном документе термин "моновалентный" применительно к антигенсвязывающей молекуле относится к антигенсвязывающей молекуле, которая имеет один антигенсвязывающий домен.
[0078] Полиспецифические связывающие молекулы. Термин "полиспецифические связывающие молекулы" или "MBM" относится к молекулам, которые специфично связываются с по меньшей мере двумя антигенами и содержат два или более антигенсвязывающих домена. Каждый из антигенсвязывающих доменов может независимо представлять собой фрагмент антитела (например, scFv, Fab, нанотело), лиганд или связывающее средство, полученное не из антитела (например, фибронектин, финомер, дарпин).
[0079] Мутация или модификация. Применительно к первичной аминокислотной последовательности полипептида термины "модификация" и "мутация" относятся к аминокислотной замене, вставке и/или делеции в полипептидной последовательности относительно эталонного полипептида. Кроме того, термин "модификация" дополнительно охватывает изменение аминокислотного остатка, например, посредством химической конъюгации (например, с лекарственным средством или полиэтиленгликолевым фрагментом) или посттрансляционной модификации (например, гликозилирования).
[0080] Нуклеиновая кислота. Термин "нуклеиновая кислота" используется в данном документе взаимозаменяемо с термином "полинуклеотид" и относится к дезоксирибонуклеотидам или рибонуклеотидам и их полимерам в однонитевой либо двухнитевой форме. Термин охватывает нуклеиновые кислоты, содержащие известные аналоги нуклеотидов или модифицированные остатки или связи в остове, которые являются синтетическими, встречающимися в природе и не встречающимися в природе, которые обладают свойствами связывания, сходными со свойствами эталонной нуклеиновой кислоты, и которые метаболизируются подобно эталонным нуклеотидам. Примеры таких аналогов включают без ограничения фосфотиоаты, фосфорамидаты, метилфосфонаты, хиральные метилфосфонаты, 2-O-метилрибонуклеотиды и пептидные нуклеиновые кислоты (PNA).
[0081] Если не указано иное, конкретная последовательность нуклеиновой кислоты также в неявной форме охватывает ее варианты с консервативными модификациями (например, с заменами вырожденными кодонами) и комплементарные последовательности, а также последовательность, указанную явным образом. В частности, как подробно описано ниже, замены вырожденными кодонами можно осуществлять путем получения последовательностей, в которых третье положение одного или более выбранных (или всех) кодонов заменено на любой из канонических нуклеозидов и/или остатков дезоксиинозина (Batzer et al., (1991) Nucleic Acid Res. 19:5081; Ohtsuka et al., (1985) J. Biol. Chem. 260:2605-2608 и Rossolini et al., (1994) Mol. Cell. Probes 8:91-98).
[0082] Функционально связанный. Термин "функционально связанный" относится к функциональной связи между двумя или более пептидными или полипептидными доменами или сегментами нуклеиновой кислоты (например, ДНК). Применительно к слитому белку или другому полипептиду термин "функционально связанный" означает, что два или более аминокислотных сегмента связаны таким образом, что образуют функциональный полипептид. Например, применительно к MBM по настоящему изобретению отдельные ABM (или цепи ABM) могут быть связаны посредством последовательностей пептидных линкеров. Применительно к нуклеиновой кислоте, кодирующей слитый белок, такой как полипептидная цепь MBM по настоящему изобретению, "функционально связанный" означает, что две нуклеиновые кислоты соединены таким образом, что аминокислотные последовательности, кодируемые двумя нуклеиновыми кислотами, остаются в одной рамке считывания. Применительно к регуляции транскрипции термин относится к функциональной связи последовательности, регулирующей транскрипцию, с транскрибируемой последовательностью. Например, промоторная или энхансерная последовательность функционально связана с кодирующей последовательностью, если она стимулирует или модулирует транскрипцию кодирующей последовательности в подходящей клетке-хозяине или другой системе экспрессии.
[0083] Пентавалентный. Используемый в данном документе термин "пентавалентный" применительно к антигенсвязывающей молекуле (например, TBM) относится к антигенсвязывающей молекуле, которая имеет пять антигенсвязывающих доменов. Пентавалентные TBM по настоящему изобретению обычно имеют (a) две пары антигенсвязывающих доменов, каждый из которых связывается с одним и тем же антигеном, и один антигенсвязывающий домен, который связывается с третьим антигеном, либо (b) три антигенсвязывающих домена, которые связываются с одним и тем же антигеном, и два антигенсвязывающих домена, каждый из которых связывается с отдельным антигеном. Пример пентавалентной TBM схематически показан на фиг. 1T.
[0084] Полипептид и белок. Термины "полипептид" и "белок" используются в данном документе взаимозаменяемо для обозначения полимера из аминокислотных остатков. Данные термины охватывают полимеры из аминокислот, в которых один или более аминокислотных остатков представляют собой искусственный химический миметик соответствующей встречающейся в природе аминокислоты, а также полимеры из встречающихся в природе аминокислот и полимер из не встречающихся в природе аминокислот. Кроме того, данные термины охватывают полимеры из аминокислот, которые дериватизированы, например, посредством синтетической дериватизации одной или более боковых цепей или концов, подвергнуты гликозилированию, пегилированию, циклической перестановке, циклизации, связыванию с другими молекулами посредством линкеров, слиянию с белками или доменами белков и добавлению пептидных меток или маркеров.
[0085] Распознавать. Используемый в данном документе термин "распознавать" относится к ABM, который находит свой эпитоп и взаимодействует (например, связывается) с ним.
[0086] Идентичность последовательностей. Идентичность последовательностей между двумя сходными последовательностями (например, вариабельных доменов антитела) можно измерить с помощью таких алгоритмов, как алгоритм в Smith, T.F. & Waterman, M.S. (1981) "Comparison Of Biosequences", Adv. Appl. Math. 2:482 [алгоритм поиска локальной гомологии]; Needleman, S.B. & Wunsch, CD. (1970) "A General Method Applicable To The Search For Similarities In The Amino Acid Sequence Of Two Proteins", J. Mol. Biol.48:443 [алгоритм выравнивания участков гомологии], Pearson, W.R. & Lipman, D.J. (1988) "Improved Tools For Biological Sequence Comparison", Proc. Natl. Acad. Sci. (U.S.A.) 85:2444 [способ поиска сходства]; или Altschul, S.F. et al, (1990) "Basic Local Alignment Search Tool," J. Mol. Biol. 215:403-10, алгоритм "BLAST", см. blast.ncbi.nlm.nih.gov/Blast.cgi. При использовании любого из вышеупомянутых алгоритмов используются параметры по умолчанию (для длины окна, штрафа за гэп и т. д.). В одном варианте осуществления идентичность последовательностей определяется с использованием алгоритма BLAST с использованием параметров по умолчанию.
Идентичность необязательно определяется по участку, длина которого составляет по меньшей мере приблизительно 50 нуклеотидов (или, в случае с пептидом или полипептидом, по меньшей мере приблизительно 10 аминокислот), или в некоторых случаях по участку, длина которого составляет от 100 до 500 или 1000 или больше нуклеотидов (или 20, 50, 200 или больше аминокислот). В некоторых вариантах осуществления идентичность определяется по определенному домену, например, VH или VL антитела. Если не указано иное, идентичность последовательностей между двумя последовательностями определяется по всей длине более короткой из двух последовательностей.
[0087] Одноцепочечный Fab или scFab. Термины "одноцепочечный Fab" и "scFab" означают полипептид, содержащий вариабельный домен тяжелой цепи антитела (VH), константный домен 1 антитела (CH1), вариабельный домен легкой цепи антитела (VL), константный домен легкой цепи антитела (CL) и линкер, так что VH и VL ассоциированы друг с другом, и CH1 и CL ассоциированы друг с другом. В некоторых вариантах осуществления домены антитела и линкер расположены в одном из следующих порядков в направлении от N-конца к C-концу: a) VH-CH1-линкер-VL-CL, b) VL-CL-линкер-VH-CH1, c) VH-CL-линкер-VL-CH1 или d) VL-CH1-линкер-VH-CL. Линкер может представлять собой полипептид из по меньшей мере 30 аминокислот, например, от 32 до 50 аминокислот. Одноцепочечные Fab стабилизированы посредством природной дисульфидной связи между CL-доменом и CH1-доменом.
[0088] Одноцепочечный Fv или scFv. Используемый в данном документе термин "одноцепочечный Fv" или "scFv" относится к фрагментам антител, которые содержат VH- и VL-домены антитела, где эти домены присутствуют в одной полипептидной цепи. Полипептид Fv может дополнительно содержать полипептидный линкер между VH- и VL-доменами, который позволяет scFv образовывать необходимую структуру для связывания антигена. Для обзора scFv см. Plückthun, The Pharmacology of Monoclonal Antibodies, vol. 113, Rosenburg and Moore eds., (1994) Springer-Verlag, New York, pp. 269-315.
[0089] Специфично (или селективно) связывается. Термин "специфично (или селективно) связывается" с антигеном или эпитопом относится к реакции связывания, которая определяет наличие когнатного антигена или эпитопа в неоднородной совокупности белков и других биологических материалов. Реакция связывания может быть опосредована, хотя это и не является необходимым, антителом или фрагментом антитела, но может также быть опосредована, например, любым типом ABM, описанным в разделе 7.2, таким как лиганд, дарпин и т. д. ABM, как правило, также характеризуется константой скорости диссоциации (KD) (koff/kon), составляющей менее 5×10-2 M, менее 10-2 M, менее 5×10-3 M, менее 10-3 M, менее 5×10-4 M, менее 10-4 M, менее 5×10-5 M, менее 10-5 M, менее 5×10-6 M, менее 10-6 M, менее 5×10-7 M, менее 10-7 M, менее 5×10-8 M, менее 10-8 M, менее 5×10-9 M или менее 10-9 M, и связывается с антигеном-мишенью с аффинностью, которая по меньшей мере в два раза превышает его аффинность связывания с неспецифичным антигеном (например, HSA). Термин "специфично связывает" не исключает межвидовую перекрестную реактивность. Например, антигенсвязывающий модуль (например, антигенсвязывающий фрагмент антитела), который "специфично связывается" с антигеном из одного вида, также способен "специфично связываться" с этим антигеном из одного или более других видов. Таким образом, такая межвидовая перекрестная реактивность сама по себе не изменяет классификацию антигенсвязывающего модуля как "специфичного" связывающего средства. В определенных вариантах осуществления антигенсвязывающий модуль (например, ABM1, ABM2 и/или ABM3), который специфично связывается с антигеном человека, обладает межвидовой перекрестной реактивностью с одним или более видами млекопитающих, отличных от человека, например, видами приматов (в том числе без ограничения одним или более из Macaca fascicularis, Macaca mulatta и Macaca nemestrina) или видами грызунов, например, Mus musculus. В других вариантах осуществления антигенсвязывающий модуль (например, ABM1, ABM2 и/или ABM3) не обладает межвидовой перекрестной реактивностью.
[0090] Субъект. Термин "субъект" включает человека и животных, отличных от человека. Животные, отличные от человека, включают всех позвоночных, например, млекопитающих и животных, отличных от млекопитающих, такие как приматы, отличные от человека, овца, собака, корова, куры, амфибии и рептилии. За исключением случаев, когда это отмечено, термины "пациент" или "субъект" используются в данном документе взаимозаменяемо.
[0091] Тандем VH-доменов. Используемый в данном документе термин "тандем VH-доменов (или VH)" относится к цепочке VH-доменов, состоящей из множества идентичных VH-доменов антитела. У каждого из VH-доменов, за исключением последнего на конце тандема, C-конец соединен с N-концом другого VH-домена с помощью или без помощи линкера. Тандем имеет по меньшей мере 2 VH-домена, и в конкретных вариантах осуществления MBM имеет 3, 4, 5, 6, 7, 8, 9 или 10 VH-доменов. Тандем VH можно получать посредством соединения нуклеиновых кислот, кодирующих каждый VH-домен, в необходимом порядке с применением рекомбинантных способов с помощью или без помощи линкера (например, описанных в разделе 7.3.3), что позволяет получать их в виде одной полипептидной цепи. N-конец первого VH-домена в тандеме определяется как N-конец тандема, тогда как C-конец последнего VH-домена в тандеме определяется как C-конец тандема.
[0092] Тандем VL-доменов. Используемый в данном документе термин "тандем VL-доменов (или VL)" относится к цепочке VL-доменов, состоящей из множества идентичных VL-доменов антитела. У каждого из VL-доменов, за исключением последнего на конце тандема, C-конец соединен с N-концом другого VL с помощью или без помощи линкера. Тандем имеет по меньшей мере 2 VL-домена, и в определенных вариантах осуществления MBM имеет 3, 4, 5, 6, 7, 8, 9 или 10 VL-доменов. Тандем VL можно получать посредством соединения нуклеиновых кислот, кодирующих каждый VL-домен, в необходимом порядке с применением рекомбинантных способов с помощью или без помощи линкера (например, описанных в разделе 7.3.3), что позволяет получать их в виде одной полипептидной цепи. N-конец первого VL-домена в тандеме определяется как N-конец тандема, тогда как C-конец последнего VL-домена в тандеме определяется как C-конец тандема.
[0093] Антиген-мишень. Используемый в данном документе термин "антиген-мишень" означает молекулу, которая нековалентно, обратимо и специфично связывается антигенсвязывающим доменом.
[0094] Тетравалентный. Используемый в данном документе термин "тетравалентный" применительно к антигенсвязывающей молекуле (например, TBM) относится к антигенсвязывающей молекуле, которая имеет четыре антигенсвязывающих домена. Тетравалентные TBM по настоящему изобретению обычно имеют два антигенсвязывающих домена, которые связываются с одним и тем же антигеном (например, BCMA), и два антигенсвязывающих домена, каждый из которых связывается с отдельным антигеном (например, компонентом комплекса TCR и CD2 либо TAA). Примеры тетравалентных TBM схематически показаны на фиг. 1Q-1S.
[0095] Терапевтически эффективное количество. "Терапевтически эффективное количество" относится к количеству, эффективному в дозах и в течение периодов времени, необходимых для достижения желаемого терапевтического результата.
[0096] Лечить, лечение, осуществление лечения. Используемые в данном документе термины "лечить", "лечение" и "осуществление лечения" относятся к уменьшению или ослаблению прогрессирования, тяжести и/или длительности заболевания или нарушения (например, пролиферативного нарушения) или ослаблению одного или более симптомов (например, одного или более различимых симптомов) нарушения в результате введения одной или более MBM (например, TBM) по настоящему изобретению. В некоторых вариантах осуществления термины "лечить", "лечение" и "осуществление лечения" относятся к ослаблению по меньшей мере одного поддающегося измерению физического параметра нарушения, такого как рост опухоли, необязательно различимого для пациента. В других вариантах осуществления термины "лечить", "лечение" и "проведение лечения" относятся к подавлению прогрессирования нарушения физическим путем, например, посредством стабилизации различимого симптома, физиологическим путем, например, посредством стабилизации физического параметра, либо ими обоими. В некоторых вариантах осуществления термины "лечить", "лечение" и "осуществление лечения" могут относиться к снижению или стабилизации размера опухоли или количества раковых клеток.
[0097] Триспецифические связывающие молекулы. Термин "триспецифические связывающие молекулы" или "TBM" относится к молекулам, которые специфично связываются с тремя антигенами и содержат три или более антигенсвязывающих домена. TBM по настоящему изобретению содержат по меньшей мере один антигенсвязывающий домен, специфичный в отношении BCMA, по меньшей мере один антигенсвязывающий домен, специфичный в отношении компонента комплекса TCR, и по меньшей мере один антигенсвязывающий домен, специфичный в отношении CD2 или TAA. Каждый из антигенсвязывающих доменов может независимо представлять собой фрагмент антитела (например, scFv, Fab, нанотело), лиганд или связывающее средство, полученное не из антитела (например, фибронектин, финомер, дарпин). Иллюстративные TBM проиллюстрированы на фиг. 1. TBM могут содержать одну, две, три, четыре или еще больше полипептидных цепей. Например, TBM, проиллюстрированная на фиг. 1M, содержит одну полипептидную цепь, содержащую три scFv, соединенных линкерами для ABM в одну полипептидную цепь. TBM, проиллюстрированная на фиг. 1K, содержит две полипептидные цепи, содержащие три scFv, соединенных, помимо прочего, Fc-доменом. TBM, проиллюстрированная на фиг. 1J, содержит три полипептидные цепи, образующие scFv, лиганд и Fab, соединенные, помимо прочего, Fc-доменом. TBM, проиллюстрированная на фиг. 1C, содержит четыре полипептидные цепи, образующие три Fab, соединенных, помимо прочего, Fc-доменом. TBM, проиллюстрированная на фиг. 1U, содержит 6 полипептидных цепей, образующих четыре Fab и два scFv, соединенных, помимо прочего, Fc-доменом.
[0098] Тривалентный. Используемый в данном документе термин "тривалентный" применительно к антигенсвязывающей молекуле (например, TBM) относится к антигенсвязывающей молекуле, которая имеет три антигенсвязывающих домена. TBM по настоящему изобретению являются триспецифическими и специфично связываются с BCMA, компонентом комплекса TCR и CD2 или TAA. Соответственно, тривалентные TBM содержат три антигенсвязывающих домена, каждый из которых связывается с отличным от других антигеном. Примеры тривалентных TBM схематически показаны на фиг. 1B-1V.
[0099] Опухоль. Термин "опухоль" используется в данном документе взаимозаменяемо с термином "рак", например, оба термина охватывают солидные опухоли и опухоли жидких тканей, например, диффузные или циркулирующие. Используемый в данном документе термин "рак" или "опухоль" включает предзлокачественные, а также злокачественные формы рака и опухоли.
[0100] Опухолеассоциированный антиген. Термин "опухолеассоциированный антиген" или "TAA" относится к молекуле (как правило, белку, углеводу, липиду или некоторой их комбинации), которая экспрессируется на поверхности раковой клетки полностью либо в виде фрагмента (например, в виде комплекса молекула MHC/пептид) и которая является применимой для предпочтительного нацеливания фармакологического средства на раковую клетку. В некоторых вариантах осуществления TAA представляет собой маркер, который экспрессируется как нормальными клетками, так и раковыми клетками, например, маркер линии дифференцировки, например, CD19 на B-клетках. В некоторых вариантах осуществления TAA представляет собой молекулу клеточной поверхности, которая сверхэкспрессируется в раковой клетке по сравнению с нормальной клеткой, например, характеризуется 1-кратной сверхэкспрессией, 2-кратной сверхэкспрессией, 3-кратной сверхэкспрессией или большей сверхэкспрессией по сравнению с нормальной клеткой. В некоторых вариантах осуществления TAA представляет собой молекулу клеточной поверхности, которая ненадлежащим образом синтезируется в раковой клетке, например, молекулу, которая содержит делеции, добавления или мутации по сравнению с молекулой, которая экспрессируется на поверхности нормальной клетки. В некоторых вариантах осуществления TAA будет экспрессироваться исключительно на клеточной поверхности раковой клетки, полностью или в виде фрагмента (например, в виде комплекса молекула MHC/пептид), и не будет синтезироваться или экспрессироваться на поверхности нормальной клетки. Соответственно, термин "TAA" охватывает антигены, которые являются специфичными для раковых клеток, иногда упоминаемые как опухолеспецифические антигены ("TSA"). Хотя BCMA имеет признаки опухолеассоциированного антигена, термины "опухолеассоциированный антиген" и "ТАА" используются на протяжении настоящего раскрытия для обозначения молекул, отличных от BCMA.
[0101] Вариабельный участок. Используемый в данном документе термин "вариабельный участок" или "вариабельный домен" означает участок иммуноглобулина, который содержит один или более доменов Ig, по существу кодируемых любым из генов Vκ, Vλ и/или VH, которые составляют генетические локусы каппа, лямбда и тяжелой цепи иммуноглобулина соответственно, и содержит CDR, которые придают специфичность к антигену. "Вариабельный домен тяжелой цепи" способен спариваться с "вариабельным доменом легкой цепи" с образованием антигенсвязывающего домена ("ABD") или антигенсвязывающего модуля ("ABM"). Кроме того, каждый вариабельный домен содержит три гипервариабельных участка ("участка, определяющих комплементарность", "CDR") (CDR-H1, CDR-H2, CDR-H3 в случае с вариабельным доменом тяжелой цепи и CDR-L1, CDR-L2, CDR-L3 в случае с вариабельным доменом легкой цепи) и четыре каркасных (FR) участка, расположенных от аминоконца к карбоксиконцу в следующем порядке: FR1-CDR1-FR2-CDR2-FR3-CDR3-FR4.
[0102] Вектор. Термин "вектор" предназначен для обозначения молекулы полинуклеотида, способной транспортировать другой полинуклеотид, с которым она была связана. Одним типом вектора является "плазмида", которая относится к кольцевой двухнитевой петле ДНК, в которую посредством лигирования могут быть встроены дополнительные сегменты ДНК. Другим типом вектора является вирусный вектор, где дополнительные сегменты ДНК могут быть встроены в вирусный геном посредством лигирования. Определенные векторы способны к автономной репликации в клетке-хозяине, в которую их вводят (например, бактериальные векторы, содержащие бактериальную точку начала репликации, и эписомные векторы для млекопитающих). Другие векторы (например, неэписомные векторы для млекопитающих) могут быть интегрированы в геном клетки-хозяина после введения в клетку-хозяина и благодаря этому реплицируются вместе с геномом хозяина. Более того, определенные векторы способны регулировать экспрессию генов, с которыми они функционально связаны. Такие векторы называются в данном документе "рекомбинантными векторами экспрессии" (или просто "векторами экспрессии"). В целом, векторы экспрессии, применимые в методиках рекомбинантной ДНК, часто представлены в форме плазмид. В настоящем описании "плазмида" и "вектор" могут использоваться взаимозаменяемо, поскольку плазмида является наиболее широко используемой формой вектора. Тем не менее, предполагается, что настоящее изобретение включает такие другие формы векторов экспрессии, как вирусные векторы (например, на основе ретровирусов, аденовирусов и аденоассоциированных вирусов, дефектных по репликации), которые выполняют эквивалентные функции.
[0103] VH. Термин "VH" относится к вариабельному участку тяжелой цепи иммуноглобулина антитела, в том числе тяжелой цепи Fv, scFv, dsFv или Fab.
[0104] VL. Термин "VL" относится к вариабельному участку легкой цепи иммуноглобулина, в том числе легкой цепи Fv, scFv, dsFv или Fab.
[0105] VH-VL или пара VH-VL. Что касается пары VH-VL, независимо от того, находятся ли они на одной и той же полипептидной цепи или на разных полипептидных цепях, термины "VH-VL" и "пара VH-VL" используются для удобства и не предполагаются как обозначающие какую-либо конкретную ориентацию, если контекст не предусматривает иное. Таким образом, scFv, содержащий "VH-VL" или "пару VH-VL", может содержать VH- и VL-домены в любой ориентации, например, VH, расположенный с N-концевой стороны от VL, или VL, расположенный с N-концевой стороны от VH.
7.2. Антигенсвязывающие модули
[0106] Как правило, один или более ABM из МBM содержат антигенсвязывающие домены на основе иммуноглобулинов, например, последовательности фрагментов или производных антител. Эти фрагменты и производные антител, как правило, включают в себя CDR антитела и могут включать в себя фрагменты большего размера и их производные, например, Fab, scFab, Fv и scFv.
[0107] ABM на основе иммуноглобулинов могут содержать модификации каркасных участков в VH и/или VL, например, для улучшения свойств MBM, содержащей ABM. Например, модификации каркасных участков могут быть произведены для уменьшения иммуногенности MBM. Один подход к произведению таких модификаций каркасных участков заключается в том, что один или более остатков каркасных участков АВМ "подвергают обратной мутации" с получением соответствующей последовательности зародышевого типа. Такие остатки могут быть идентифицированы посредством сравнения последовательностей каркасных участков с последовательностями зародышевого типа, из которых получен АВМ. Чтобы последовательности каркасного участка "соответствовали" требуемой конфигурации зародышевого типа, остатки могут быть "подвергнуты обратной мутации" с получением соответствующей последовательности зародышевого типа, например, посредством сайт-направленного мутагенеза. Предполагается, что МВМ, имеющие такие "подвергнутые обратной мутации" АВМ, также охватываются настоящим изобретением.
[0108] Другой тип модификации каркасного участка предусматривает мутацию одного или более остатков в пределах каркасного участка или даже в пределах одного или более CDR-участков с целью удаления T-клеточных эпитопов со снижением тем самым потенциальной иммуногенности МВМ. Данный подход также называется "деиммунизацией" и более подробно описан в публикации заявки на патент США № 20030153043 авторства Carr et al.
[0109] ABM также можно модифицировать таким образом, чтобы они характеризовались измененным гликозилированием, что может быть применимо, например, для увеличения аффинности MBM к одному или более ее антигенам. Такие углеводные модификации можно осуществлять, например, посредством изменения одного или более сайтов гликозилирования в пределах последовательности АВМ. Например, можно произвести одну или более аминокислотных замен, которые приводят к устранению одного или более сайтов гликозилирования в каркасной части вариабельного участка, устраняя таким образом гликозилирование в этом сайте. Такое агликозилирование может приводить к увеличению аффинности МВМ к антигену. Такой подход описан, например, в патентах США №№ 5714350 и 6350861 авторства Co et al.
7.2.1. Модули на основе иммуноглобулинов
7.2.1.1. Fab
[0110] В определенных аспектах ABM представляет собой Fab-домен. Fab-домены можно получать посредством протеолитического расщепления молекул иммуноглобулинов с применением ферментов, таких как папаин, или посредством рекомбинантной экспрессии. Fab-домены, как правило, содержат CH1-домен, присоединенный к VH-домену, который образует пару с CL-доменом, присоединенным к VL-домену.
[0111] В иммуноглобулине дикого типа VH-домен спарен с VL-доменом с образованием Fv-участка, и CH1-домен спарен с CL-доменом для дополнительной стабилизации связывающего модуля. Дисульфидная связь между двумя константными доменами может дополнительно стабилизировать Fab-домен.
[0112] Для MBM (например, TBM) по настоящему изобретению является преимущественным применение стратегий гетеродимеризации Fab для обеспечения надлежащей ассоциации Fab-доменов, входящих в состав одного и того же ABM, и минимизации аберрантного спаривания Fab-доменов, входящих в состав разных ABM. Например, можно применять стратегии гетеродимеризации Fab, показанные в таблице 1 ниже.
Стратегии гетеродимеризации Fab
[0113] Соответственно, в определенных вариантах осуществления надлежащей ассоциации между двумя полипептидами Fab способствует обмен VL- и VH-доменов Fab друг на друга или обмен CH1- и CL-доменов друг на друга, например, как описано в WO 2009/080251.
[0114] Надлежащему спариванию Fab также может способствовать введение одной или более аминокислотных модификаций в CH1-домен и одной или более аминокислотных модификаций в CL-домен Fab и/или одной или более аминокислотных модификаций в VH-домен и одной или более аминокислотных модификаций в VL-домен. Аминокислоты, которые подвергают модификации, как правило, являются частью области контакта VH:VL и CH1:CL таким образом, что компоненты Fab предпочтительно спариваются друг с другом, а не с компонентами других Fab.
[0115] В одном варианте осуществления одна или более аминокислотных модификаций ограничены консервативными остатками каркасных участков в вариабельных (VH, VL) и константных (CH1, CL) доменах, которые указаны согласно нумерации остатков по Kabat. В Almagro, 2008, Frontiers In Bioscience 13:1619-1633 приводится определение остатков каркасных участков на основании схем нумерации по Kabat, Chothia и IMGT.
[0116] В одном варианте осуществления модификации, введенные в VH- и CH1-домены и/или VL- и CL-домены, являются комплементарными друг другу. Комплементарности в области контакта тяжелой и легкой цепей можно достигать с использованием стерических и гидрофобных контактов, электростатических взаимодействий/взаимодействий зарядов или любой комбинации разнообразных взаимодействий. Комплементарность между поверхностями белков широко описана в литературе в терминах соответствия "ключ-замок", взаимодействий типа "выступ во впадину", выпячивания и полости, донора и акцептора и т. д., при этом во всех из них подразумевается природа структурного и химического соответствия между двумя взаимодействующими поверхностями.
[0117] В одном варианте осуществления посредством одной или более введенных модификаций вводят новую водородную связь в области контакта компонентов Fab. В одном варианте осуществления посредством одной или более введенных модификаций вводят новый солевой мостик в области контакта компонентов Fab. Иллюстративные замены описаны в WO 2014/150973 и WO 2014/082179.
[0118] В некоторых вариантах осуществления Fab-домен содержит замену 192E в CH1-домене и замены 114A и 137K в CL-домене, посредством которых вводят солевой мостик между CH1- и CL-доменами (см. Golay et al., 2016, J Immunol 196:3199-211).
[0119] В некоторых вариантах осуществления Fab-домен содержит замены 143Q и 188V в CH1-домене и замены 113T и 176V в CL-домене, которые способствуют обмену гидрофобных и полярных участков контакта между CH1- и CL-доменами (см. Golay et al., 2016, J Immunol 196:3199-211).
[0120] В некоторых вариантах осуществления Fab-домен может содержать модификации в некоторых или во всех из VH-, CH1-, VL-, CL-доменов для введения ортогональных областей контакта в Fab, которые способствуют надлежащей сборке Fab-доменов (Lewis et al., 2014 Nature Biotechnology 32:191-198). В одном варианте осуществления модификации 39K, 62E вводят в VH-домен, модификации H172A, F174G вводят в CH1-домен, модификации 1R, 38D, (36F) вводят в VL-домен, и модификации L135Y, S176W вводят в CL-домен. В другом варианте осуществления модификацию 39Y вводят в VH-домен, и модификацию 38R вводят в VL-домен.
[0121] Fab-домены также можно модифицировать, замещая нативную дисульфидную связь CH1:CL сконструированной дисульфидной связью, за счет чего обеспечивается увеличение эффективности спаривания компонентов Fab. Например, сконструированную дисульфидную связь можно вводить посредством введения 126C в CH1-домен и 121C в CL-домен (см. Mazor et al., 2015, MAbs 7:377-89).
[0122] Fab-домены также можно модифицировать посредством замены CH1-домена и CL-домена на альтернативные домены, которые способствуют надлежащей сборке. Например, в Wu et al., 2015, MAbs 7:364-76 описана замена CH1-домена на константный домен T-клеточного рецептора α и замена CL-домена на β-домен T-клеточного рецептора, а также спаривание этих замененных доменов с помощью дополнительного взаимодействия типа "заряд-заряд" между VL- и VH-доменами посредством введения модификации 38D в VL-домен и модификации 39K в VH-домен.
[0123] ABM может содержать одноцепочечный Fab-фрагмент, который представляет собой полипептид, состоящий из вариабельного домена тяжелой цепи (VH) антитела, константного домена 1 (CH1) антитела, вариабельного домена легкой цепи (VL) антитела, константного домена легкой цепи (CL) антитела и линкера. В некоторых вариантах осуществления домены антитела и линкер расположены в одном из следующих порядков в направлении от N-конца к C-концу: a) VH-CH1-линкер-VL-CL, b) VL-CL-линкер-VH-CH1, c) VH-CL-линкер-VL-CH1 или d) VL-CH1-линкер-VH-CL. Линкер может представлять собой полипептид из по меньшей мере 30 аминокислот, например, от 32 до 50 аминокислот. Одноцепочечные Fab-домены стабилизированы посредством природной дисульфидной связи между CL-доменом и CH1-доменом.
[0124] В одном варианте осуществления домены антитела и линкер в одноцепочечном Fab-фрагменте расположены в одном из следующих порядков в направлении от N-конца к C-концу: a) VH-CH1-линкер-VL-CL или b) VL-CL-линкер-VH-CH1. В некоторых случаях используют VL-CL-линкер-VH-CH1.
[0125] В другом варианте осуществления домены антитела и линкер в одноцепочечном Fab-фрагменте расположены в одном из следующих порядков в направлении от N-конца к C-концу: a) VH-CL-линкер-VL-CH1 или b) VL-CH1-линкер-VH-CL.
[0126] В одноцепочечном Fab-фрагменте в дополнение к природной дисульфидной связи между CL-доменом и CH1-доменом вариабельный домен тяжелой цепи (VH) антитела и вариабельный домен легкой цепи (VL) антитела также необязательно стабилизированы дисульфидными связями посредством введения дисульфидной связи между следующими положениями: i) положением 44 вариабельного домена тяжелой цепи и положением 100 вариабельного домена легкой цепи, ii) положением 105 вариабельного домена тяжелой цепи и положением 43 вариабельного домена легкой цепи или iii) положением 101 вариабельного домена тяжелой цепи и положением 100 вариабельного домена легкой цепи (нумерация в соответствии с EU-индексом по Kabat).
[0127] Такую дополнительную стабилизацию одноцепочечных Fab-фрагментов дисульфидными связями осуществляют посредством введения дисульфидной связи между вариабельными доменами VH и VL одноцепочечных Fab-фрагментов. Методики введения неприродных дисульфидных мостиков для стабилизации одноцепочечного Fv описаны, например, в WO 94/029350, Rajagopal et al., 1997, Prot. Engin. 10:1453-59; Kobayashi et al., 1998, Nuclear Medicine & Biology, 25:387-393; и Schmidt, et al., 1999, Oncogene 18:1711-1721. В одном варианте осуществления необязательная дисульфидная связь между вариабельными доменами одноцепочечных Fab-фрагментов находится между положением 44 вариабельного домена тяжелой цепи и положением 100 вариабельного домена легкой цепи. В одном варианте осуществления необязательная дисульфидная связь между вариабельными доменами одноцепочечных Fab-фрагментов находится между положением 105 вариабельного домена тяжелой цепи и положением 43 вариабельного домена легкой цепи (нумерация в соответствии с EU-индексом по Kabat).
7.2.1.2. scFv
[0128] Фрагменты антител, представляющие собой одноцепочечные Fv или "scFv", содержат VH- и VL-домены антитела в одной полипептидной цепи, способны экспрессироваться в виде одноцепочечного полипептида и сохраняют специфичность интактного антитела, из которого они получены. Обычно полипептид scFv дополнительно содержит полипептидный линкер между VH- и VL-доменами, который позволяет scFv образовывать необходимую структуру для связывания мишени. Примерами линкеров, подходящих для соединения VH- и VL-цепей scFv, являются линкеры для ABM, идентифицированные в разделе 7.3.3, например, любой из линкеров, обозначенных от L1 до L54.
[0129] Если не указано иное, то scFv, как используется в данном документе, может содержать вариабельные VL- и VH-участки в любом порядке, например, по отношению к N-концу и С-концу полипептида scFv может содержать VL-линкер-VH или может содержать VH-линкер-VL.
[0130] Для образования нуклеиновой кислоты, кодирующей scFv, фрагменты ДНК, кодирующие VH и VL, функционально связывают с другим фрагментом, кодирующим линкер, например, кодирующим любой из линкеров для ABM, описанных в разделе 7.3.3 (как, например, имеющий аминокислотную последовательность (Gly4˜Ser)3 (SEQ ID NO: 1)), таким образом, чтобы последовательности VH и VL могли экспрессироваться в виде непрерывного одноцепочечного белка с VL- и VH-участками, соединенными посредством гибкого линкера (см., например, Bird et al., 1988, Science 242:423-426; Huston et al., 1988, Proc. Natl. Acad. Sci. USA 85:5879-5883; McCafferty et al., 1990, Nature 348:552-554).
7.2.1.3. Другие модули на основе иммуноглобулинов
[0131] МBM также могут содержать ABM, имеющие формат иммуноглобулина, который отличается от Fab или scFv, например, Fv, dsFv, (Fab’)2, однодоменное антитело (SDAB), VH- или VL-домен или VHH-домен верблюдовых (также называемый нанотелом).
[0132] ABM может представлять собой однодоменное антитело, состоящее из одного VH- или VL-домена, который проявляет достаточную аффинность к мишени. В некоторых вариантах осуществления однодоменное антитело представляет собой VHH-домен верблюдовых (см., например, Riechmann, 1999, Journal of Immunological Methods 231:25-38; WO 94/04678).
7.2.2. Модули на основе молекул, отличных от иммуноглобулинов
[0133] В определенных вариантах осуществления один или более ABM получены из каркасных белков, отличных от антител (в том числе без ограничения сконструированных белков с анкириновыми повторами (дарпинов), авимеров (что сокращенно обозначает авидные мультимеры), антикалинов/липокалинов, центиринов, доменов Куница, аднексинов, аффилинов, аффитинов (также известных как нонфитины), ноттинов, пронектинов, версател, дуокалинов и финомеров), лигандов, рецепторов, цитокинов или хемокинов.
[0134] Неиммуноглобулиновые каркасные структуры, которые можно применять в МBM, включают каркасные структуры, которые перечислены в таблицах 3 и 4 из Mintz and Crea, 2013, Bioprocess International 11(2):40-48; на фигуре 1, в таблице 1 и на фигуре I в Vazquez-Lombardi et al., 2015, Drug Discovery Today 20(10):1271-83; в таблице 1 и врезке 2 в Skrlec et al., 2015, Trends in Biotechnology 33(7):408-18. Содержание таблиц 3 и 4 из Mintz and Crea, 2013, Bioprocess International 11(2):40-48; фигуры 1, таблицы 1 и фигуры I из Vazquez-Lombardi et al., 2015, Drug Discovery Today 20(10):1271-83; таблицы 1 и врезки 2 из Skrlec et al., 2015, Trends in Biotechnology 33(7):408-18 (совместно называемое "раскрытия каркасных структур") включено в данный документ. В конкретном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении аднексинов. В другом варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении авимеров. В другом варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении аффител. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении антикалинов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении дарпинов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении доменов Куница. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении ноттинов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении пронектинов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении нанофитинов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении аффилинов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении аднектинов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении ABD. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении адгиронов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении аффимеров. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении альфател. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении белков с повторами Armadillo. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении атримеров/тетранектинов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении O-тел/OB-складок. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении центиринов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении репетел. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении антикалинов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении атримеров. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении бициклических пептидов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении цистиновых узлов. В еще одном варианте осуществления раскрытия каркасных структур включены посредством ссылки на то, что в них раскрыто в отношении каркасных структур Fn3 (включая аднектины, центирины, пронектины и Tn3).
[0135] В одном варианте осуществления ABM может представлять собой сконструированный белок с анкириновым повтором ("дарпин"). Дарпины представляют собой белки-миметики антител, которые, как правило, проявляют высокоспецифичное и высокоаффинное связывание белков-мишеней. Как правило, они являются генетически сконструированными и полученными из природных белков-анкиринов и состоят из по меньшей мере трех, обычно четырех или пяти повторяющихся мотивов этих белков. Их молекулярная масса составляет приблизительно 14 или 18 кДа (килодальтонов) для дарпинов, содержащих четыре или пять повторов соответственно. Примеры дарпинов можно найти, например, в патенте США № 7417130. Полиспецифические связывающие молекулы, содержащие связывающие модули на основе дарпинов и связывающие модули на основе иммуноглобулинов, раскрыты, например, в публикации заявки на патент США № 2015/0030596 A1.
[0136] В другом варианте осуществления ABM может представлять собой аффитело. Аффитело широко известно и относится к аффинным белкам на основе белкового домена из 58 аминокислотных остатков, полученного из одного из IgG-связывающих доменов стафилококкового белка A.
[0137] В другом варианте осуществления ABM может представлять собой антикалин. Антикалины широко известны и относятся к другой технологии с использованием миметиков антител, где специфичность связывания определяется липокалинами. Антикалины также могут существовать в формате белков с двойным нацеливанием, называемых дуокалинами.
[0138] В другом варианте осуществления ABM может представлять собой версатело. Версатела широко известны и относятся к другой технологии с использованием миметиков антител. Они представляют собой небольшие белки размером 3-5 кДа с > 15% содержанием остатков цистеина, которые образуют каркасную структуру с высокой плотностью дисульфидных связей, заменяющую гидрофобное ядро типичных белков.
[0139] Другие неиммуноглобулиновые ABM включают в себя олигомеры "A"-доменов (также известные как авимеры) (см., например, публикации заявок на патент США №№ 2005/0164301, 2005/0048512 и 2004/017576), белковые каркасные структуры на основе Fn3 (см., например, публикацию заявки на патент США 2003/0170753), полипептиды VASP, птичий панкреатический полипептид (aPP), тетранектин (на основе CTLD3), аффилин (на основе γB-кристаллина/убиквитина), ноттины, SH3-домены, PDZ-домены, тендамистат, неокарциностатин, домены белка A, липокалины, трансферрин или домены Куница. В одном аспекте ABM, применимые в конструкции МBM, содержат каркасные структуры на основе фибронектина, как проиллюстрировано на примерах в WO 2011/130324.
7.3. Соединительные элементы
[0140] Предполагается, что MBM в некоторых случаях могут содержать пары ABM или цепей ABM (например, компонент VH-CH1 или VL-CL из Fab), непосредственно соединенные друг с другом, например, в виде слитого белка без линкера. Например, MBM содержат соединительные фрагменты, связывающие отдельные ABM или цепи ABM. Применение соединительных фрагментов может улучшать связывание мишени, например, посредством увеличения гибкости ABM в МBM и, таким образом, снижения стерического несоответствия. ABM могут быть соединены друг с другом посредством, например, Fc-доменов (при этом каждый Fc-домен представляет собой пару ассоциированных Fc-участков) и/или линкеров для ABM. При применении Fc-доменов будет, как правило, требоваться применение шарнирных участков в качестве соединительных элементов для ABM или цепей ABM для оптимального связывания антигена. Таким образом, термин "соединительный элемент" охватывает без ограничения Fc-участки, Fc-домены, шарнирные участки и линкеры для ABM.
[0141] Соединительные элементы могут быть выбраны или модифицированы, например, для увеличения или уменьшения биологического периода полужизни MBM по настоящему изобретению. Например, для уменьшения биологического периода полужизни одна или более аминокислотных мутаций могут быть введены в участок области контакта доменов CH2-CH3 фрагмента Fc-шарнирный участок таким образом, чтобы MBM, содержащая фрагмент, характеризовалась ухудшенным связыванием со стафилококковым белком A (SpA) по сравнению со связыванием нативного домена Fc-шарнирный участок с SpA. Данный подход более подробно описан в патенте США № 6165745 авторства Ward et al. В качестве альтернативы MBM может быть модифицирована для увеличения ее биологического периода полужизни. Например, можно вводить одну или более из следующих мутаций: T252L, T254S, T256F, как описано в патенте США № 6277375, выданном Ward. В качестве альтернативы, для увеличения биологического периода полужизни MBM можно изменять в пределах CH1- или CL-участка таким образом, чтобы она содержала эпитоп связывания рецептора реутилизации, взятый из двух петель CH2-домена Fc-участка IgG, как описано в патентах США №№ 5869046 и 6121022 авторства Presta et al.
[0142] Примеры Fc-доменов (образованных посредством спаривания двух Fc-участков), шарнирных участков и линкеров для ABM описаны в разделах 7.3.1, 7.3.2 и 7.3.3 соответственно.
7.3.1. Fc-домены
[0143] MBM (например, TBM) могут содержать Fc-домен, полученный из любого подходящего вида. В одном варианте осуществления Fc-домен получен из человеческого Fc-домена.
[0144] Fc-домен может быть получен из антитела любого подходящего класса, в том числе IgA (включая подклассы IgA1 и IgA2), IgD, IgE, IgG (включая подклассы IgG1, IgG2, IgG3 и IgG4) и IgM. В одном варианте осуществления Fc-домен получен из IgG1, IgG2, IgG3 или IgG4. В одном варианте осуществления Fc-домен получен из IgG1. В одном варианте осуществления Fc-домен получен из IgG4.
[0145] Fc-домен содержит две полипептидные цепи, каждая из которых называется Fc-участком тяжелой цепи. Два Fc-участка тяжелой цепи димеризуются с образованием Fc-домена. Два Fc-участка в Fc-домене могут быть одинаковыми или отличающимися друг от друга. В нативном антителе Fc-участки, как правило, являются идентичными, но для цели получения полиспецифических связывающих молекул, например, TBM по настоящему изобретению, Fc-участки могут быть преимущественно отличающимися для обеспечения возможности гетеродимеризации, которая описана в разделе 7.3.1.5 ниже.
[0146] Как правило, каждый Fc-участок тяжелой цепи содержит два или три константных домена тяжелой цепи или состоит из них.
[0147] В нативных антителах Fc-участок тяжелой цепи IgA, IgD и IgG состоит из двух константных доменов тяжелой цепи (CH2 и CH3), и Fc-участок тяжелой цепи IgE и IgM состоит из трех константных доменов тяжелой цепи (CH2, CH3 и CH4). Они димеризуются с образованием Fc-домена.
[0148] В настоящем изобретении Fc-участок тяжелой цепи может содержать константные домены тяжелой цепи из одного или более различных классов антител, например, одного, двух или трех различных классов.
[0149] В одном варианте осуществления Fc-участок тяжелой цепи содержит CH2- и CH3-домены, полученные из IgG1. Иллюстративная последовательность Fc-участка тяжелой цепи, полученная из IgG1 человека, представлена под SEQ ID NO: 872:
DKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSP (SEQ ID NO: 872).
[0150] В некоторых вариантах осуществления MBM по настоящему изобретению содержит Fc-участок, аминокислотная последовательность которого содержит аминокислотную последовательность под SEQ ID NO: 872, модифицированную с помощью одной или более замен, описанных в разделе 7.3.1 и его подразделах.
[0151] В одном варианте осуществления Fc-участок тяжелой цепи содержит CH2- и CH3-домены, полученные из IgG2.
[0152] В одном варианте осуществления Fc-участок тяжелой цепи содержит CH2- и CH3-домены, полученные из IgG3.
[0153] В одном варианте осуществления Fc-участок тяжелой цепи содержит CH2- и CH3-домены, полученные из IgG4.
[0154] В одном варианте осуществления Fc-участок тяжелой цепи содержит CH4-домен из IgM. CH4-домен IgM, как правило, расположен на C-конце CH3-домена.
[0155] В одном варианте осуществления Fc-участок тяжелой цепи содержит CH2- и CH3-домены, полученные из IgG, и CH4-домен, полученный из IgM.
[0156] Следует понимать, что константные домены тяжелой цепи для применения при получении Fc-участка тяжелой цепи для MBM по настоящему изобретению могут включать в себя варианты встречающихся в природе константных доменов, описанных выше. Такие варианты могут содержать одно или более аминокислотных видоизменений по сравнению с константными доменами дикого типа. В одном примере Fc-участок тяжелой цепи по настоящему изобретению содержит по меньшей мере один константный домен, который отличается по последовательности от константного домена дикого типа. Следует понимать, что варианты константных доменов могут быть более длинными или более короткими, чем константный домен дикого типа. Например, варианты константных доменов являются на по меньшей мере 60% идентичными константному домену дикого типа или сходными с ним. В другом примере варианты константных доменов являются на по меньшей мере 70% идентичными или сходными. В другом примере варианты константных доменов являются на по меньшей мере 75% идентичными или сходными. В другом примере варианты константных доменов являются на по меньшей мере 80% идентичными или сходными. В другом примере варианты константных доменов являются на по меньшей мере 85% идентичными или сходными. В другом примере варианты константных доменов являются на по меньшей мере 90% идентичными или сходными. В другом примере варианты константных доменов являются на по меньшей мере 95% идентичными или сходными. В другом примере варианты константных доменов являются на по меньшей мере 99% идентичными или сходными. Иллюстративные варианты Fc описаны в разделах 7.3.1.1-7.3.1.5 ниже.
[0157] IgM и IgA встречаются в природе у людей в виде ковалентных мультимеров общего звена антитела H2L2. IgM встречается в виде пентамера, если он содержит в своем составе J-цепь, или в виде гексамера, если он лишен J-цепи. IgA встречается в виде мономерных и димерных форм. Тяжелые цепи IgM и IgA имеют 18-аминокислотное удлинение C-концевого константного домена, известное как хвостовая часть. Хвостовая часть содержит остаток цистеина, который образует дисульфидную связь между тяжелыми цепями в полимере и, как полагают, играет важную роль при полимеризации. Хвостовая часть также содержит сайт гликозилирования. В определенных вариантах осуществления МBM по настоящему изобретению не содержат хвостовую часть.
[0158] Fc-домены, которые включены в состав MBM (например, TBM) по настоящему изобретению, могут содержать одну или более модификаций, которые изменяют одно или более функциональных свойств белков, таких как период полужизни в сыворотке крови, фиксация комплемента, связывание с Fc-рецепторами и/или антигензависимая клеточная цитотоксичность. Кроме того, MBM может быть химически модифицирована (например, к MBM могут быть присоединены один или более химических фрагментов) или быть модифицирована с изменением ее гликозилирования, опять-таки для изменения одного или более функциональных свойств MBM.
[0159] Эффекторная функция молекулы антитела включает в себя комплемент-опосредованную эффекторную функцию, которая опосредована, например, связыванием компонента C1 системы комплемента с антителом. Активация комплемента важна для опсонизации и прямого лизиса патогенов. Кроме того, она стимулирует воспалительный ответ посредством привлечения фагоцитов к месту активации комплемента и их активации. Эффекторная функция включает в себя эффекторную функцию, опосредованную Fc-рецептором (FcR), которая может запускаться при связывании константных доменов антитела с Fc-рецептором (FcR). При опосредованном комплексом антиген-антитело перекрестном связывании Fc-рецепторов на поверхностях эффекторных клеток запускается ряд важных и разнообразных биологических реакций, в том числе поглощение и разрушение частиц, покрытых антителами, выведение иммунных комплексов, лизис клеток-мишеней, покрытых антителами, клетками-киллерами (называемый антителозависимой клеточноопосредованной цитотоксичностью или ADCC), высвобождение медиаторов воспаления, перенос через плаценту и контроль продуцирования иммуноглобулинов.
[0160] Fc-участки могут быть изменены посредством замены по меньшей мере одного аминокислотного остатка на другой аминокислотный остаток для изменения эффекторных функций. Например, одну или более аминокислот можно заменить на другой аминокислотный остаток таким образом, чтобы Fc-участок характеризовался измененной аффинностью к эффекторному лиганду. Эффекторный лиганд, аффинность к которому изменяют, может представлять собой, например, Fc-рецептор или компонент C1 системы комплемента. Данный подход описан, например, в патентах США №№ 5624821 и 5648260, оба авторства Winter et al. Модифицированные Fc-участки также способны приводить к изменению связывания C1q и/или снижению или устранению комплемент-зависимой цитотоксичности (CDC). Данный подход описан, например, в патенте США № 6194551 авторства Idusogie et al. Модифицированные Fc-участки также способны приводить к изменению способности Fc-участка к фиксации комплемента. Данный подход описан, например, в PCT-публикации WO 94/29351 авторства Bodmer et al. Аллотипические аминокислотные остатки включают в себя без ограничения константный участок тяжелой цепи подклассов IgG1, IgG2 и IgG3, а также константный участок легкой цепи изотипа каппа, как описано в Jefferis et al., 2009, MAbs, 1:332-338.
[0161] Fc-участки также могут быть модифицированы для "подавления" эффекторной функции, например, для снижения или устранения способности MBM опосредовать антителозависимую клеточную цитотоксичность (ADCC) и/или антителозависимый клеточный фагоцитоз (ADCP). Это может быть достигнуто, например, путем введения мутации в Fc-участок. Такие мутации были описаны в уровне техники: LALA и N297A (Strohl, 2009, Curr. Opin. Biotechnol. 20(6):685-691); а также D265A (Baudino et al., 2008, J. Immunol. 181: 6664-69; Strohl, выше). Примеры антител IgG1 с подавленной активностью Fc включают так называемый мутантный вариант LALA, содержащий мутации L234A и L235A в аминокислотной последовательности Fc IgG1. Другой пример антитела IgG1 с подавленной активностью содержит мутацию D265A. Другой пример антитела IgG1 с подавленной активностью включает так называемый мутантный вариант DAPA, содержащий мутации D265A и P329A в аминокислотной последовательности Fc IgG1. Другое антитело IgG1 с подавленной активностью содержит мутацию N297A, которая приводит к образованию агликозилированных/негликозилированных антител.
[0162] Fc-участки могут быть модифицированы для увеличения способности MBM, содержащей Fc-участок, опосредовать антителозависимую клеточную цитотоксичность (ADCC) и/или антителозависимый клеточный фагоцитоз (ADCP), например, посредством модификации одного или более аминокислотных остатков с увеличением аффинности MBM к активирующему Fcγ-рецептору или уменьшением аффинности MBM к ингибирующему Fcγ-рецептору. Активирующие Fcγ-рецепторы человека включают в себя FcγRIa, FcγRIIa, FcγRIIIa и FcγRIIIb, а ингибирующий Fcγ-рецептор человека включает в себя FcγRIIb. Данный подход описан, например, в PCT-публикации WO 00/42072 авторства Presta. Кроме того, сайты связывания на IgG1 человека для FcγRI, FcγRII, FcγRIII и FcRn были картированы, и были описаны варианты с улучшенным связыванием (см. Shields et al., J. Biol. Chem. 276:6591-6604, 2001). Была описана оптимизация Fc-опосредованных эффекторных функций моноклональных антител, как, например, увеличение функции ADCC/ADCP (см. Strohl, 2009, Current Opinion in Biotechnology 20:685-691). Мутации, которые способны усиливать функцию ADCC/ADCP, включают в себя одну или более мутаций, выбранных из G236A, S239D, F243L, P247I, D280H, K290S, R292P, S298A, S298D, S298V, Y300L, V305I, A330L, I332E, E333A, K334A, A339D, A339Q, A339T и P396L (все положения согласно нумерации EU).
[0163] Fc-участки также могут быть модифицированы для увеличения способности MBM опосредовать ADCC и/или ADCP, например, посредством модификации одной или более аминокислот с увеличением аффинности MBM к активирующему рецептору, который, как правило, не будет распознаваться исходной MBM, такого как FcαRI. Данный подход описан, например, в Borrok et al., 2015, mAbs. 7(4):743-751.
[0164] Соответственно, в определенных аспектах MBM по настоящему изобретению могут содержать Fc-домены с измененной эффекторной функцией, такой как, без ограничения, связывание с Fc-рецепторами, такими как FcRn или лейкоцитарные рецепторы (например, как описано выше или в разделе 7.3.1.1), связывание с комплементом (например, как описано выше или в разделе 7.3.1.2), модифицированной архитектурой дисульфидных связей (например, как описано выше или в разделе 7.3.1.3) или измененными паттернами гликозилирования (например, как описано выше или в разделе 7.3.1.4). Fc-домены также можно изменять таким образом, чтобы они содержали модификации, которые улучшают технологичность получения асимметричных МBM, например, посредством обеспечения возможности гетеродимеризации, которая заключается в предпочтительном спаривании неидентичных Fc-участков по сравнению с идентичными Fc-участками. Гетеродимеризация позволяет получать МBM, в которых различные ABM соединены друг с другом посредством Fc-домена, содержащего Fc-участки, которые отличаются по последовательности. Примеры стратегий гетеродимеризации проиллюстрированы в разделе 7.3.1.5 (и в его подразделах).
[0165] Следует понимать, что любые модификации, описанные в разделах 7.3.1.1-7.3.1.5, можно использовать в комбинации любым подходящим образом для достижения необходимых функциональных свойств и/или использовать в комбинации с другими модификациями для изменения свойств МBM. В некоторых вариантах осуществления MBM содержит Fc-домен IgG1, имеющий мутацию в 1, 2, 3, 4, 5, 6 или более чем 6 из положений 233, 234, 235, 236, 237, 239, 265, 266, 267, 268, 269, 297, 299, 322, 327, 328, 329, 330, 331 и 332 (нумерация согласно EU). Например, MBM может содержать последовательность IgG1 под SEQ ID NO: 872 с мутацией в 1, 2, 3, 4, 5, 6 или более чем 6 из положений 233, 234, 235, 236, 237, 239, 265, 266, 267, 268, 269, 297, 299, 322, 327, 328, 329, 330, 331 и 332.
7.3.1.1. Fc-домены с измененным связыванием FcR
[0166] Fc-домены MBM (например, TBM) способны демонстрировать измененное связывание с одним или более Fc-рецепторами (FcR) по сравнению с соответствующим нативным иммуноглобулином. Связывание с любым конкретным Fc-рецептором может быть увеличенным или уменьшенным. В одном варианте осуществления Fc-домен содержит одну или более модификаций, которые изменяют его профиль связывания с Fc-рецепторами.
[0167] Клетки человека могут экспрессировать ряд мембраносвязанных FcR, выбранных из FcαR, FcεR, FcγR, FcRn и гликановых рецепторов. Некоторые клетки также способны к экспрессии растворимого FcR (эктодомена) (Fridman et al., 1993, J Leukocyte Biology 54: 504-512). FcγR могут дополнительно подразделяться по аффинности связывания IgG (высокая/низкая) и биологическому эффекту (активирующие/ингибирующие). Общепризнанно, что FcγRI человека представляет собой единственный рецептор с "высокой аффинностью", тогда как все остальные считаются рецепторами с аффинностью от средней до низкой. FcγRIIb представляет собой единственный рецептор с "ингибирующими" функциональными свойствами благодаря своему внутриклеточному ITIM-мотиву, тогда как все остальные считаются "активирующими" рецепторами благодаря ITAM-мотивам или спариванию с общей γ-цепью FcγR. FcγRIIIb также уникален тем, что, хотя он и является активирующим, он ассоциирует с клеткой посредством GPI-якоря. В целом, у людей экспрессируются шесть "стандартных" FcγR: FcγRI, FcγRIIa, FcγRIIb, FcγRIIc, FcγRIIIa и FcγRIIIb. В дополнение к этим последовательностям существует большое количество последовательностей или аллотипических вариантов, распространенных в этих семействах. Было обнаружено, что некоторые из них имеют важное функциональное значение и поэтому иногда считаются самостоятельными подтипами рецепторов. Примеры включают FcγRIIaH134R, FcγRIIbI190T, FcγRIIIaF158V, FcγRIIIbNA1, FcγRIIIbNA2 и FcγRIIISH. Было показано, что каждая последовательность рецептора имеет различные значения аффинности для 4 подклассов IgG: IgG1, IgG2, IgG3 и IgG4 (Bruhns, 1993, Blood 113:3716-3725). Другие виды имеют несколько иные количества и функциональные свойства FcγR, при этом мышиная система является на сегодняшний день наиболее хорошо изученной и содержит 4 FcγR: FcγRI, FcγRIIb, FcγRIII, FcγRIV (Bruhns, 2012, Blood 119:5640-5649). FcγRI человека на клетках обычно считается "занятым" мономерным IgG при нормальных условиях в сыворотке крови ввиду его аффинности к IgG1/IgG3/IgG4 (приблизительно 10-8 M) и концентрации этих IgG в сыворотке крови (приблизительно 10 мг/мл). Следовательно, клетки, несущие FcγRI на своей поверхности, считаются способными к "скринингу" их антигенного окружения или "отбору образцов" из него опосредованно с помощью связанного полиспецифического IgG. Другие рецепторы, имеющие более низкие значения аффинности к подклассам IgG (в диапазоне от приблизительно 10-5 до 10-7 M), обычно считаются "незанятыми". Следовательно, низкоаффинные рецепторы по своей природе чувствительны к выявлению иммунных комплексов, образованных при участии антител, и активации ими. Увеличенная плотность Fc в иммунных комплексах антител приводит к увеличению функциональной аффинности авидности связывания с низкоаффинным FcγR. Это было продемонстрировано in vitro с применением ряда способов (Shields et al., 2001, J Biol Chem 276(9):6591-6604; Lux et al., 2013, J Immunol 190:4315-4323). Это также считается одним из основных механизмов действия при применении антител к RhD для лечения ITP у людей (Crow, 2008, Transfusion Medicine Reviews 22:103-116).
[0168] Множество типов клеток экспрессируют множество типов FcγR, и поэтому связывание IgG или иммунного комплекса антител с клетками, несущими FcγR, может иметь множественные и сложные результаты в зависимости от биологического контекста. Говоря наиболее просто, клетки могут получать активирующий, ингибирующий либо смешанный сигнал. Это может приводить к таким событиям, как фагоцитоз (например, в случае с макрофагами и нейтрофилами), процессирование антигена (например, в случае с дендритными клетками), снижение продуцирования IgG (например, в случае с B-клетками) или дегрануляция (например, в случае с нейтрофилами, тучными клетками). Существуют данные, подтверждающие, что ингибирующий сигнал от FcγRIIb может преобладать над активирующими сигналами (Proulx, 2010, Clinical Immunology 135:422-429).
[0169] Существует ряд полезных замен в Fc, которые можно осуществлять для изменения связывания с одним или более FcγR-рецепторами. Могут быть полезны замены, которые приводят к увеличению связывания, а также к уменьшению связывания. Например, известно, что увеличение связывания с FcγRIIIa обычно приводит к увеличению ADCC (антителозависимой клеточноопосредованной цитотоксичности - клеточноопосредованной реакции, где неспецифические цитотоксические клетки, которые экспрессируют FcγR, распознают связанное антитело на клетке-мишени и впоследствии вызывают лизис клетки-мишени). Аналогичным образом, в некоторых обстоятельствах также может быть полезным уменьшение связывания с FcγRIIb (ингибирующим рецептором). Аминокислотные замены, которые находят применение в настоящем изобретении, включают замены, перечисленные в US 2006/0024298 (в частности на фиг. 41), US 2006/0121032, US 2006/0235208, US 2007/0148170 и US 2019/0100587. Конкретные варианты, которые находят применение, включают без ограничения 236A, 239D, 239E, 332E, 332D, 239D/332E, 267D, 267E, 328F, 267E/328F, 236A/332E, 239D/332E/330Y, 239D, 332E/330L, 243A, 243L, 264A, 264V, 299T, 265A/297A/329A, 265N/297D/329G и 265E/297Q/329S.
[0170] FcRn играет решающую роль при поддержании длительного периода полужизни IgG в сыворотке крови взрослых и детей. Рецептор связывает IgG в подкисленных везикулах (pH < 6,5), защищая молекулу IgG от разрушения и затем высвобождая ее в кровь при более высоком pH, составляющем 7,4.
[0171] FcRn отличается от лейкоцитарных Fc-рецепторов и вместе с этим имеет структурное сходство с молекулами MHC I класса. Он представляет собой гетеродимер, состоящий из цепи β2-микроглобулина, нековалентно присоединенной к мембраносвязанной цепи, которая содержит три внеклеточных домена. Один из этих доменов, содержащий углеводную цепь, вместе с β2-микроглобулином взаимодействует с сайтом между CH2- и CH3-доменами Fc. Взаимодействие включает образование солевых мостиков с остатками гистидина в IgG, которые являются положительно заряженными при pH < 6,5. При более высоком pH остатки His теряют свои положительные заряды, взаимодействие FcRn-IgG ослабляется, и IgG диссоциирует.
[0172] В одном варианте осуществления MBM содержит Fc-домен, который связывается с FcRn человека.
[0173] В одном варианте осуществления Fc-домен имеет Fc-участки (например, один или два), содержащие остаток гистидина в положении 310 и в некоторых случаях также в положении 435. Эти остатки гистидина важны для связывания FcRn человека. В одном варианте осуществления остатки гистидина в положениях 310 и 435 представляют собой нативные остатки, т. е. положения 310 и 435 не являются модифицированными. В качестве альтернативы один или оба из этих остатков гистидина могут присутствовать в результате модификации.
[0174] MBM могут содержать один или более Fc-участков, которые изменяют связывание Fc с FcRn. Изменение связывания может представлять собой увеличение связывания или уменьшение связывания.
[0175] В одном варианте осуществления МBM содержит Fc-домен, в котором по меньшей мере один Fc-участок (и необязательно оба таковых) содержит одну или более таких модификаций, при которых он связывается с FcRn с большей аффинностью и авидностью, чем соответствующий нативный иммуноглобулин.
[0176] Замены Fc, которые приводят к увеличению связывания с FcRn-рецептором и увеличению периода полужизни в сыворотке крови, описаны в US 2009/0163699, в том числе без ограничения 434S, 434A, 428L, 308F, 259I, 428L/434S, 259I/308F, 436I/428L, 436I или V/434S, 436V/428L и 259I/308F/428L.
[0177] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка треонина в положении 250 на остаток глутамина (T250Q).
[0178] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка метионина в положении 252 на остаток тирозина (M252Y).
[0179] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка серина в положении 254 на остаток треонина (S254T).
[0180] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка треонина в положении 256 на остаток глутаминовой кислоты (T256E).
[0181] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка треонина в положении 307 на остаток аланина (T307A).
[0182] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка треонина в положении 307 на остаток пролина (T307P).
[0183] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка валина в положении 308 на остаток цистеина (V308C).
[0184] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка валина в положении 308 на остаток фенилаланина (V308F).
[0185] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка валина в положении 308 на остаток пролина (V308P).
[0186] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка глутамина в положении 311 на остаток аланина (Q311A).
[0187] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка глутамина в положении 311 на остаток аргинина (Q311R).
[0188] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка метионина в положении 428 на остаток лейцина (M428L).
[0189] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка гистидина в положении 433 на остаток лизина (H433K).
[0190] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка аспарагина в положении 434 на остаток фенилаланина (N434F).
[0191] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка аспарагина в положении 434 на остаток тирозина (N434Y).
[0192] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка метионина в положении 252 на остаток тирозина, остатка серина в положении 254 на остаток треонина и остатка треонина в положении 256 на остаток глутаминовой кислоты (M252Y/S254T/T256E).
[0193] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка валина в положении 308 на остаток пролина и остатка аспарагина в положении 434 на остаток тирозина (V308P/N434Y).
[0194] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка метионина в положении 252 на остаток тирозина, остатка серина в положении 254 на остаток треонина, остатка треонина в положении 256 на остаток глутаминовой кислоты, остатка гистидина в положении 433 на остаток лизина и остатка аспарагина в положении 434 на остаток фенилаланина (M252Y/S254T/T256E/H433K/N434F).
[0195] Следует понимать, что любые перечисленные выше модификации можно использовать в комбинации для изменения связывания FcRn.
[0196] В одном варианте осуществления МBM содержит Fc-домен, в котором один или оба Fc-участка содержат одну или более таких модификаций, при которых Fc-домен связывается с FcRn с более низкой аффинностью и авидностью, чем соответствующий нативный иммуноглобулин.
[0197] В одном варианте осуществления Fc-участок содержит любой аминокислотный остаток, отличный от гистидина, в положении 310 и/или положении 435.
[0198] MBM может содержать Fc-домен, в котором один или оба Fc-участка содержат одну или более модификаций, которые приводят к увеличению его связывания с FcγRIIb. FcγRIIb является единственным ингибирующим рецептором у людей и единственным Fc-рецептором, обнаруживаемым на B-клетках.
[0199] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка пролина в положении 238 на остаток аспарагиновой кислоты (P238D).
[0200] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка глутаминовой кислоты в положении 258 на остаток аланина (E258A).
[0201] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка серина в положении 267 на остаток аланина (S267A).
[0202] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка серина в положении 267 на остаток глутаминовой кислоты (S267E).
[0203] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка лейцина в положении 328 на остаток фенилаланина (L328F).
[0204] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка глутаминовой кислоты в положении 258 на остаток аланина и остатка серина в положении 267 на остаток аланина (E258A/S267A).
[0205] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка серина в положении 267 на остаток глутаминовой кислоты и остатка лейцина в положении 328 на остаток фенилаланина (S267E/L328F).
[0206] Следует понимать, что любые перечисленные выше модификации можно использовать в комбинации для увеличения связывания FcγRIIb.
[0207] В одном варианте осуществления предусмотрены МBM, содержащие Fc-домены, которые проявляют уменьшенное связывание с FcγR.
[0208] В одном варианте осуществления МBM содержит Fc-домен, в котором один или оба Fc-участка содержат одну или более модификаций, которые уменьшают связывание Fc с FcγR.
[0209] Fc-домен может быть получен из IgG1.
[0210] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка лейцина в положении 234 на остаток аланина (L234A).
[0211] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка лейцина в положении 235 на остаток аланина (L235A).
[0212] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка глицина в положении 236 на остаток аргинина (G236R).
[0213] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка аспарагина в положении 297 на остаток аланина (N297A) или остаток глутамина (N297Q).
[0214] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка серина в положении 298 на остаток аланина (S298A).
[0215] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка лейцина в положении 328 на остаток аргинина (L328R).
[0216] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка лейцина в положении 234 на остаток аланина и остатка лейцина в положении 235 на остаток аланина (L234A/L235A).
[0217] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка фенилаланина в положении 234 на остаток аланина и остатка лейцина в положении 235 на остаток аланина (F234A/L235A).
[0218] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка глицина в положении 236 на остаток аргинина и остатка лейцина в положении 328 на остаток аргинина (G236R/L328R).
[0219] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка аспартата в положении 265 на остаток аланина, остатка аспарагина в положении 297 на остаток аланина и остатка пролина в положении 329 на остаток аланина (D265A/N297A/P329A).
[0220] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка аспартата в положении 265 на остаток аспарагина, остатка аспарагина в положении 297 на остаток аспартата и остатка пролина в положении 329 на остаток глицина (D265N/N297D/P329G).
[0221] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка аспартата в положении 265 на остаток глутамата, остатка аспарагина в положении 297 на остаток глутамина и остатка пролина в положении 329 на остаток серина (D265E/N297Q/P329S).
[0222] Следует понимать, что любые перечисленные выше модификации можно использовать в комбинации для уменьшения связывания FcγR.
[0223] В одном варианте осуществления MBM содержит Fc-домен, в котором один или оба Fc-участка содержат одну или более модификаций, которые уменьшают связывание Fc с FcγRIIIa без влияния на связывание Fc с FcγRII.
[0224] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка серина в положении 239 на остаток аланина (S239A).
[0225] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка глутаминовой кислоты в положении 269 на остаток аланина (E269A).
[0226] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка глутаминовой кислоты в положении 293 на остаток аланина (E293A).
[0227] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка тирозина в положении 296 на остаток фенилаланина (Y296F).
[0228] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка валина в положении 303 на остаток аланина (V303A).
[0229] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка аланина в положении 327 на остаток глицина (A327G).
[0230] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка лизина в положении 338 на остаток аланина (K338A).
[0231] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка аспарагиновой кислоты в положении 376 на остаток аланина (D376A).
[0232] Следует понимать, что любые перечисленные выше модификации можно использовать в комбинации для уменьшения связывания FcγRIIIa.
[0233] Варианты Fc-участков с уменьшенным связыванием с FcR могут называться "вариантами с устранением связывания с FcγR", "вариантами с подавлением связывания с FcγR" или вариантами "Fc с нокаутом (FcKO или KO)". Для некоторых путей терапевтического применения желательно снизить или устранить нормальное связывание Fc-домена с одним или более или всеми из Fcγ-рецепторов (например, FcγR1, FcγRIIa, FcγRIIb, FcγRIIIa), чтобы избежать дополнительных механизмов действия. То есть, например, во многих вариантах осуществления, особенно при применении MBM, которые моновалентно связывают CD3, обычно желательно устранять связывание FcγRIIIa для элиминации или значительного снижения активности ADCC. В некоторых вариантах осуществления по меньшей мере один из Fc-участков MBM, описанных в данном документе, содержит один или более вариантов с устранением связывания с Fcγ-рецепторами. В некоторых вариантах осуществления оба Fc-участка содержат один или более вариантов с устранением связывания с Fcγ-рецепторами. Эти варианты с устранением связывания с Fcγ-рецепторами показаны в таблице 2, и каждый из них может быть независимо и необязательно включен или исключен, причем в некоторых аспектах используют варианты с устранением связывания с Fcγ-рецепторами, выбранные из группы, состоящей из G236R/L328R, E233P/L234V/L235A/G236del/S239K, E233P/L234V/L235A/G236del/S267K, E233P/L234V/L235A/G236del/S239K/A327G, E233P/L234V/L235A/G236del/S267K/A327G, E233P/L234V/L235A/G236del, D265A/N297A/P329A, D265N/N297D/P329G и D265E/N297Q/P329S ("del" означает делецию, например, G236del относится к делеции глицина в положении 236). Следует отметить, что в вариантах с устранением связывания с Fcγ-рецепторами, упоминаемых в данном документе, устранено связывание FcγR, но, как правило, не связывание FcRn.
Варианты с устранением связывания с Fcγ-рецепторами
[0234] В некоторых вариантах осуществления MBM по настоящему изобретению содержат первый Fc-участок и второй Fc-участок. В некоторых вариантах осуществления первый Fc-участок и/или второй Fc-участок могут содержать следующие мутации: E233P, L234V, L235A, G236del и S267K.
[0235] Fc-домен IgG1 человека характеризуется наиболее высокой степенью связывания с Fcγ-рецепторами и, таким образом, можно использовать варианты с устранением связывания с Fcγ-рецепторами, когда константный домен (или Fc-домен) в остове гетеродимерного антитела представляет собой IgG1.
[0236] В качестве альтернативы или в дополнение к вариантам с устранением связывания с Fcγ-рецепторами в окружении IgG1, мутации в положении гликозилирования 297, например, замена остатка аспарагина в положении 297 на остаток аланина (N297A) или остаток глутамина (N297Q), способны, например, в значительной степени устранять связывание с FcγRIIIa. IgG2 и IgG4 человека характеризуются естественным сниженным связыванием с Fcγ-рецепторами, и, таким образом, эти остовы можно использовать с вариантами с устранением связывания с Fcγ-рецепторами или без них.
7.3.1.2. Fc-домены с измененным связыванием с комплементом
[0237] MBM (например, TBM) могут содержать Fc-домен, в котором один или оба Fc-участка содержат одну или более модификаций, которые изменяют связывание Fc с комплементом. Изменение связывания комплемента может представлять собой увеличение связывания или уменьшение связывания.
[0238] В одном варианте осуществления Fc-участок содержит одну или более модификаций, которые приводят к уменьшению его связывания с C1q. Инициация классического пути активации системы комплемента начинается со связывания гексамерного белка C1q с CH2-доменом IgG и IgM, связанных с антигеном.
[0239] В одном варианте осуществления МBM содержит Fc-домен, в котором один или оба Fc-участка содержат одну или более модификаций для уменьшения связывания Fc с C1q.
[0240] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка лейцина в положении 234 на остаток аланина (L234A).
[0241] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка лейцина в положении 235 на остаток аланина (L235A).
[0242] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка лейцина в положении 235 на остаток глутаминовой кислоты (L235E).
[0243] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка глицина в положении 237 на остаток аланина (G237A).
[0244] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка лизина в положении 322 на остаток аланина (K322A).
[0245] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка пролина в положении 331 на остаток аланина (P331A).
[0246] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка пролина в положении 331 на остаток серина (P331S).
[0247] В одном варианте осуществления MBM содержит Fc-домен, полученный из IgG4. IgG4 по своей природе характеризуется более низким профилем активации комплемента, чем IgG1, но также более слабым связыванием FcγR. Таким образом, в одном варианте осуществления МBM содержит Fc-домен IgG4 и также содержит одну или более модификаций, которые увеличивают связывание FcγR.
[0248] Следует понимать, что любые перечисленные выше модификации можно использовать в комбинации для снижения связывания C1q.
7.3.1.3. Fc-домены с измененной архитектурой дисульфидных связей
[0249] MBM (например, TBM) может содержать Fc-домен, содержащий одну или более модификаций с образованием и/или удалением остатка цистеина. Остатки цистеина играют важную роль в самопроизвольной сборке полиспецифических связывающих молекул на основе Fc посредством образования дисульфидных мостиков между отдельными парами полипептидных мономеров. Таким образом, посредством изменения количества и/или положения остатков цистеина возможно модифицировать структуру МBM для получения белка с улучшенными терапевтическими свойствами.
[0250] МBM может содержать Fc-домен, в котором один или оба Fc-участка, например, оба Fc-участка, содержат остаток цистеина в положении 309. В одном варианте осуществления остаток цистеина в положении 309 образован посредством модификации, например, в случае с Fc-доменом, полученным из IgG1, остаток лейцина в положении 309 заменен на остаток цистеина (L309C), в случае с Fc-доменом, полученным из IgG2, остаток валина в положении 309 заменен на остаток цистеина (V309C).
[0251] В одном варианте осуществления Fc-участок модифицирован посредством замены остатка валина в положении 308 на остаток цистеина (V308C).
[0252] В одном варианте осуществления две дисульфидные связи в шарнирном участке удалены посредством осуществления мутации последовательности CPPC центрального шарнирного участка (SEQ ID NO: 2) по типу замены на SPPS (SEQ ID NO: 3).
7.3.1.4. Fc-домены с измененным гликозилированием
[0253] В определенных аспектах предусмотрены MBM (например, TBM) с улучшенной технологичностью получения, которые содержат меньше сайтов гликозилирования, чем соответствующий иммуноглобулин. Эти белки характеризуются менее сложными паттернами посттрансляционного гликозилирования, и, таким образом, их изготовление является более простым и менее дорогостоящим.
[0254] В одном варианте осуществления сайт гликозилирования в CH2-домене удален посредством замены остатка аспарагина в положении 297 на остаток аланина (N297A) или остаток глутамина (N297Q). В дополнение к улучшенной технологичности получения эти агликозилированные мутантные варианты также характеризуются сниженным связыванием FcγR, как описано в данном документе выше.
[0255] В некоторых вариантах осуществления может быть получена МВМ, которая характеризуется измененным типом гликозилирования, такая как гипофукозилированное антитело, имеющее сниженное количество фукозильных остатков, или антитело, имеющее увеличенное содержание структур с остатком GlcNac в точке ветвления. Было продемонстрировано, что такие измененные паттерны гликозилирования увеличивают способность антител к ADCC. Такие углеводные модификации можно осуществлять, например, посредством экспрессии МВМ в клетке-хозяине с измененным аппаратом гликозилирования. Клетки с измененным аппаратом гликозилирования были описаны в уровне техники, и их можно применять в качестве клеток-хозяев, в которых экспрессируются MBM, за счет чего обеспечивается получение MBM с измененным гликозилированием. Например, в EP 1176195 авторства Hang et al. описывается линия клеток с функциональным нарушением гена FUT8, который кодирует фукозилтрансферазу, благодаря чему антитела, которые экспрессируются в такой линии клеток, демонстрируют гипофукозилирование. В PCT-публикации WO 03/035835 авторства Presta описывается вариант линии клеток CHO - клетки Lecl3 со сниженной способностью к присоединению фукозы к Asn(297)-связанным углеводам, что также приводит к гипофукозилированию антител, которые экспрессируются в такой клетке-хозяине (см. также Shields et al., 2002, J. Biol. Chem. 277:26733-26740). В PCT-публикации WO 99/54342 авторства Umana et al. описываются линии клеток, сконструированные так, что они экспрессируют гликозилтрансферазы, модифицирующие гликопротеины (например, бета-(1,4)-N-ацетилглюкозаминилтрансферазы III (GnTIII)), благодаря чему антитела, которые экспрессируются в сконструированных линиях клеток, демонстрируют повышенное содержание структур с остатком GlcNac в точках ветвления, что приводит к увеличению активности ADCC у антител (см. также Umana et al., Nat. Biotech. 17:176-180, 1999).
7.3.1.5. Гетеродимеризация Fc
[0256] Множество форматов полиспецифических молекул подразумевают димеризацию между двумя Fc-участками, которые, в отличие от нативного иммуноглобулина, функционально связаны с неидентичными антигенсвязывающими доменами (или их частями, например, VH или VH-CH1 в Fab). Ненадлежащая гетеродимеризация двух Fc-участков с образованием Fc-домена всегда была препятствием для увеличения выхода необходимых полиспецифических молекул и представляет трудности для очистки. Разнообразные подходы, доступные из уровня техники, можно применять для усиления димеризации Fc-участков, которые могут присутствовать в MBM (например, TBM) по настоящему изобретению, например, как раскрыто в EP 1870459A1; патенте США № 5582996; патенте США № 5731168; патенте США № 5910573; патенте США № 5932448; патенте США № 6833441; патенте США № 7183076; публикации заявки на патент США № 2006204493A1 и PCT-публикации № WO2009/089004A1.
[0257] В настоящем изобретении предусмотрены MBM (например, TBM), содержащие гетеродимеры Fc, т. е. Fc-домены, содержащие гетерологичные неидентичные Fc-участки. Стратегии гетеродимеризации применяют для усиления димеризации Fc-участков, функционально связанных с разными ABM (или их частями, например, VH или VH-CH1 в Fab), и снижения димеризации Fc-участков, функционально связанных с одним и тем же ABM или его частью. Как правило, каждый Fc-участок в гетеродимере Fc содержит CH3-домен антитела. CH3-домены получают из константного участка антитела любого изотипа, класса или подкласса, а в некоторых случаях класса IgG (IgG1, IgG2, IgG3 и IgG4), как описано в предыдущем разделе.
[0258] Как правило, МBM содержат другие фрагменты антител в дополнение к CH3-доменам, такие как CH1-домены, CH2-домены, шарнирный домен, VH-домен(домены), VL-домен(домены), CDR и/или антигенсвязывающие фрагменты, описанные в данном документе. В некоторых вариантах осуществления два гетерополипептида представляют собой две тяжелые цепи, образующие биспецифические или полиспецифические молекулы. Гетеродимеризация двух различных тяжелых цепей в CH3-доменах приводит к образованию необходимых антитела или антителоподобной молекулы, тогда как гомодимеризация идентичных тяжелых цепей приводит к снижению выхода необходимых антитела или молекулы. В иллюстративном варианте осуществления две или более гетерополипептидные цепи содержат две цепи, содержащие CH3-домены и образующие молекулы в любом из форматов полиспецифических молекул, описанных в настоящем изобретении выше. В одном варианте осуществления две гетерополипептидные цепи, содержащие CH3-домены, содержат модификации, которые способствуют гетеродимерной ассоциации полипептидов по сравнению с немодифицированными цепями. Различные примеры стратегий модификации приведены ниже в таблице 3 и разделах 7.3.1.5.1-7.3.1.5.7.
Стратегии гетеродимеризации Fc
[0259] Иллюстративные пары гетерологичных неидентичных последовательностей Fc, которые могут спариваться с образованием гетеродимера Fc и которые могут быть включены в MBM по настоящему изобретению, включают (i) SEQ ID NO: 869 и SEQ ID NO: 870, а также (ii) SEQ ID NO: 869 и SEQ ID NO: 871.
[0260] DKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVCTLPPSREEMTKNQVSLSCAVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLVSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK (SEQ ID NO: 869)
[0261] DKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPCREEMTKNQVSLWCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK (SEQ ID NO: 870)
[0262] DKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPCREEMTKNQVSLWCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNRYTQKSLSLSPGK (SEQ ID NO: 871)
Fc-участок, имеющий аминокислотную последовательность под одним из SEQ ID NO: 869-871, может быть модифицирован с включением одной или более замен, описанных в разделе 7.3.1 (включая его подразделы), например, для включения замены(замен), соответствующей(соответствующих) варианту с устранением связывания с Fcγ-рецепторами, представленному в таблице 3. В некоторых вариантах осуществления MBM содержит Fc-участок, имеющий аминокислотную последовательность под одним из SEQ ID NO: 869-871 с мутацией в 1, 2, 3, 4, 5, 6 или более чем 6 из положений 233, 234, 235, 236, 237, 239, 265, 266, 267, 268, 269, 297, 299, 322, 327, 328, 329, 330, 331 и 332 (нумерация согласно EU), например, с мутацией(мутациями), описанной(описанными) в разделе 7.3.1 (включая его подразделы). Например, MBM может содержать Fc-участок, имеющий аминокислотную последовательность под SEQ ID NO: 869 с мутацией в 1, 2, 3, 4, 5, 6 или более чем 6 из положений 233, 234, 235, 236, 237, 239, 265, 266, 267, 268, 269, 297, 299, 322, 327, 328, 329, 330, 331 и 332, и/или Fc-участок, имеющий аминокислотную последовательность под SEQ ID NO: 870 с мутацией в 1, 2, 3, 4, 5, 6 или более чем 6 из положений 233, 234, 235, 236, 237, 239, 265, 266, 267, 268, 269, 297, 299, 322, 327, 328, 329, 330, 331 и 332, и/или Fc-участок, имеющий аминокислотную последовательность под SEQ ID NO: 871 с мутацией в 1, 2, 3, 4, 5, 6 или более чем 6 из положений 233, 234, 235, 236, 237, 239, 265, 266, 267, 268, 269, 297, 299, 322, 327, 328, 329, 330, 331 и 332.
7.3.1.5.1. Стерические варианты
[0263] MBM (например, TBM) могут содержать одну или более, например, множество, модификаций в одном или более константных доменах Fc-домена, например, в CH3-доменах. В одном примере MBM (например, TBM) содержит два полипептида, каждый из которых содержит константный домен тяжелой цепи антитела, например, CH2- или CH3-домен. В одном примере два константных домена тяжелой цепи, например, CH2- или CH3-домены MBM (например, TBM), содержат одну или более модификаций, которые обеспечивают возможность гетеродимерной ассоциации между двумя цепями. В одном аспекте одна или более модификаций расположены в CH2-доменах двух тяжелых цепей. В одном аспекте одна или более модификаций расположены в CH3-доменах по меньшей мере двух полипептидов МBM.
[0264] Один механизм гетеродимеризации Fc обычно упоминается в уровне техники как "выступы и впадины", или "выступ во впадину", или "выступы во впадины". Эти термины относятся к аминокислотным мутациям, которые создают стерические влияния, способствующие образованию гетеродимеров Fc вместо гомодимеров Fc, как описано, например, в Ridgway et al., 1996, Protein Engineering 9(7):617; Atwell et al., 1997, J. Mol. Biol. 270:26; патенте США № 8216805. Мутации типа "выступ во впадину" можно использовать в комбинации с другими стратегиями для улучшения гетеродимеризации.
[0265] В одном аспекте одна или более модификаций в первом полипептиде MBM, содержащем константный домен тяжелой цепи, могут образовывать "выступ", и одна или более модификаций во втором полипептиде MBM образуют "впадину", так что гетеродимеризация полипептида MBM, содержащего константный домен тяжелой цепи, приводит к тому, что "выступ" вступает в контакт (например, взаимодействует, например, CH2-домен первого полипептида взаимодействует с CH2-доменом второго полипептида, или CH3-домен первого полипептида взаимодействует с CH3-доменом второго полипептида) с "впадиной". "Выступ" выступает над областью контакта первого полипептида MBM, содержащего константный домен тяжелой цепи, и поэтому способен располагаться в компенсирующей "впадине" в области контакта со вторым полипептидом MBM, содержащим константный домен тяжелой цепи, чтобы таким образом стабилизировать гетеромультимер и, таким образом, способствовать, например, образованию гетеромультимера вместо образования гомомультимера. Выступ может существовать в исходной области контакта или может быть введен синтетически (например, посредством изменения нуклеиновой кислоты, кодирующей область контакта). Вводимыми остатками для образования выступа обычно являются встречающиеся в природе аминокислотные остатки, и они могут быть выбраны из аргинина (R), фенилаланина (F), тирозина (Y) и триптофана (W). В некоторых случаях выбирают триптофан и тирозин. В одном варианте осуществления исходный остаток для образования выпячивания имеет небольшой объем боковой цепи, такой как у аланина, аспарагина, аспарагиновой кислоты, глицина, серина, треонина или валина.
[0266] "Впадина" содержит по меньшей мере одну боковую цепь аминокислоты, которая углублена в область контакта второго полипептида MBM, содержащего константный домен тяжелой цепи и, следовательно, создает условия для размещения соответствующего "выступа" на прилегающей области контакта первого полипептида MBM, содержащего константный домен тяжелой цепи. Впадина может существовать в исходной области контакта или может быть введена синтетически (например, посредством изменения нуклеиновой кислоты, кодирующей область контакта). Вводимыми остатками для образования впадины обычно являются встречающиеся в природе аминокислотные остатки, и они в некоторых вариантах осуществления выбраны из аланина (A), серина (S), треонина (T) и валина (V). В одном варианте осуществления аминокислотный остаток представляет собой серин, аланин или треонин. В другом варианте осуществления исходный остаток для образования впадины имеет большой объем боковой цепи, такой как у тирозина, аргинина, фенилаланина или триптофана.
[0267] В одном варианте осуществления первый CH3-домен модифицирован по остатку 366, 405 или 407 с образованием "выступа" либо "впадины" (как описано выше), и второй CH3-домен, который гетеродимеризуется с первым CH3-доменом, модифицирован по остатку 407, если в первом CH3-домене модифицирован остаток 366, остатку 394, если в первом CH3-домене модифицирован остаток 405, или остатку 366, если в первом CH3-домене модифицирован остаток 407, с образованием "впадины" или "выступа", комплементарных "выступу" или "впадине" первого CH3-домена.
[0268] В другом варианте осуществления первый CH3-домен модифицирован по остатку 366, и второй CH3-домен, который гетеродимеризуется с первым CH3-доменом, модифицирован по остаткам 366, 368 и/или 407 с образованием "впадины" или "выступа", комплементарных "выступу" или "впадине" первого CH3-домена. В одном варианте осуществления в ходе модификации в первом CH3-домене вводится остаток тирозина (Y) в положении 366. В одном варианте осуществления модификация в первом CH3 представляет собой T366Y. В одном варианте осуществления в ходе модификации в первом CH3-домене вводится остаток триптофана (W) в положении 366. В одном варианте осуществления модификация в первом CH3 представляет собой T366W. В некоторых вариантах осуществления модификация во втором CH3-домене, который гетеродимеризуется с первым CH3-доменом, модифицированным в положении 366 (например, имеющим тирозин (Y) или триптофан (W), введенный в положение 366, например, содержащим модификацию T366Y или T366W), включает в себя модификацию в положении 366, модификацию в положении 368 и модификацию в положении 407. В некоторых вариантах осуществления в ходе модификации в положении 366 вводится остаток серина (S), в ходе модификации в положении 368 вводится аланин (A), и в ходе модификации в положении 407 вводится валин (V). В некоторых вариантах осуществления модификации включают в себя T366S, L368A и Y407V. В одном варианте осуществления первый CH3-домен полиспецифической молекулы содержит модификацию T366Y, а второй CH3-домен, который гетеродимеризуется с первым CH3-доменом, содержит модификации T366S, L368A и Y407V, или наоборот. В одном варианте осуществления первый CH3-домен полиспецифической молекулы содержит модификацию T366W, а второй CH3-домен, который гетеродимеризуется с первым CH3-доменом, содержит модификации T366S, L368A и Y407V, или наоборот.
[0269] Дополнительные стерические или "асимметричные" (например, типа "выступ во впадину") модификации описаны в PCT-публикации № WO2014/145806 (например, на фигуре 3, фигуре 4 и фигуре 12 в WO2014/145806), PCT-публикации № WO2014/110601 и PCT-публикациях №№ WO 2016/086186, WO 2016/086189, WO 2016/086196 и WO 2016/182751. Пример KIH-варианта содержит первый константный домен цепи, содержащий модификации L368D и K370S, спаренный со вторым константным доменом цепи, содержащим модификации S364K и E357Q.
[0270] Дополнительные пары модификаций типа "выступ во впадину", подходящие для применения в любой из MBM по настоящему изобретению, дополнительно описаны, например, в WO1996/027011 и Merchant et al., 1998, Nat. Biotechnol., 16:677-681.
[0271] В дополнительных вариантах осуществления CH3-домены могут быть дополнительно модифицированы с введением пары остатков цистеина. Не ограничиваясь какой-либо теорией, полагают, что введение пары остатков цистеина, способных к образованию дисульфидной связи, обеспечивает стабильность гетеродимеризованных MBM (например, TBM), содержащих спаренные CH3-домены. В некоторых вариантах осуществления первый CH3-домен содержит цистеин в положении 354, а второй CH3-домен, который гетеродимеризуется с первым CH3-доменом, содержит цистеин в положении 349. В некоторых вариантах осуществления первый CH3-домен содержит цистеин в положении 354 (например, содержит модификацию S354C) и тирозин (Y) в положении 366 (например, содержит модификацию T366Y), а второй CH3-домен, который гетеродимеризуется с первым CH3-доменом, содержит цистеин в положении 349 (например, содержит модификацию Y349C), серин в положении 366 (например, содержит модификацию T366S), аланин в положении 368 (например, содержит модификацию L368A) и валин в положении 407 (например, содержит модификацию Y407V). В некоторых вариантах осуществления первый CH3-домен содержит цистеин в положении 354 (например, содержит модификацию S354C) и триптофан (W) в положении 366 (например, содержит модификацию T366W), а второй CH3-домен, который гетеродимеризуется с первым CH3-доменом, содержит цистеин в положении 349 (например, содержит модификацию Y349C), серин в положении 366 (например, содержит модификацию T366S), аланин в положении 368 (например, содержит модификацию L368A) и валин в положении 407 (например, содержит модификацию Y407V).
[0272] Дополнительный механизм, который находит применение при получении гетеродимеров, иногда называют "направленным электростатическим взаимодействием", как описано в Gunasekaran et al., 2010, J. Biol. Chem. 285(25):19637. Это иногда упоминается в данном документе как "пары зарядов". В данном варианте осуществления используют электростатические силы для обеспечения асимметрии образования в сторону гетеродимеризации. Они могут также оказывать эффект в отношении pI и, следовательно, в отношении очистки, и поэтому в некоторых случаях также могут рассматриваться pI-варианты. Однако поскольку их создавали для усиления гетеродимеризации и не использовали в качестве инструментов для очистки, их классифицируют как "стерические варианты". Они включают без ограничения D221E/P228E/L368E в паре с D221R/P228R/K409R и C220E/P228E/368E в паре с C220R/E224R/P228R/K409R.
[0273] Представлены дополнительные варианты, которые можно использовать в комбинации с другими вариантами, необязательно и независимо в любом количестве, такие как pI-варианты, описанные в данном документе, или другие стерические варианты, которые показаны на фигуре 37 в US 2012/0149876.
[0274] В некоторых вариантах осуществления стерические варианты, описанные в данном документе, могут быть необязательно и независимо включены в любой pI-вариант (или другие варианты, такие как варианты Fc, варианты FcRn) в одном или обоих Fc-участках и могут быть независимо и необязательно включены или исключены из MBM по настоящему изобретению.
[0275] Список подходящих асимметричных вариантов представлен в таблице 4, где показаны некоторые пары, особенно практически ценные во многих вариантах осуществления. Особенно применимыми во многих вариантах осуществления являются пары наборов, в том числе без ограничения S364K/E357Q : L368D/K370S; L368D/K370S : S364K; L368E/K370S : S364K; T411T/E360E/Q362E : D401K; L368D/K370S : S364K/E357L и K370S : S364K/E357Q. С точки зрения номенклатуры пара "S364K/E357Q : L368D/K370S" означает, что один из Fc-участков имеет двойной набор вариантов S364K/E357Q, а другой имеет двойной набор вариантов L368D/K370S.
Иллюстративные асимметричные варианты
[0276] В некоторых вариантах осуществления MBM содержит первый Fc-участок и второй Fc-участок. В некоторых вариантах осуществления первый Fc-участок содержит следующие мутации: L368D и K370S, а второй Fc-участок содержит следующие мутации: S364K и E357Q. В некоторых вариантах осуществления первый Fc-участок содержит следующие мутации: S364K и E357Q, а второй Fc-участок содержит следующие мутации: L368D и K370S.
7.3.1.5.2. Альтернативные выступы и впадины: гетеродимеризация IgG
[0277] Гетеродимеризацию полипептидных цепей MBM (например, TBM), содержащих спаренные CH3-домены, можно увеличить посредством введения одной или более модификаций в CH3-домен, который получен из антитела класса IgG1. В одном варианте осуществления модификации включают в себя модификацию K409R в одном CH3-домене в паре с модификацией F405L во втором CH3-домене. Дополнительные модификации также или в качестве альтернативы можно осуществлять в положениях 366, 368, 370, 399, 405, 407 и 409. В некоторых случаях гетеродимеризацию полипептидов, содержащих такие модификации, осуществляют в восстанавливающих условиях, например, в 10-100 мМ 2-MEA (например, в 25, 50 или 100 мМ 2-MEA), в течение 1-10, например, 1,5-5, например, 5 часов при 25-37°С, например, 25°С или 37°С.
[0278] Аминокислотные замены, описанные в данном документе, можно вводить в CH3-домены с применением методик, которые широко известны (см., например, McPherson, ed., 1991, Directed Mutagenesis: a Practical Approach; Adelman et al., 1983, DNA, 2:183).
[0279] Стратегия гетеродимеризации IgG дополнительно описана, например, в WO2008/119353, WO2011/131746 и WO2013/060867.
[0280] В любом из вариантов осуществления, описанных в данном разделе, CH3-домены могут быть дополнительно модифицированы с введением пары остатков цистеина, как описано в разделе 7.3.1.3.
7.3.1.5.3. pI-варианты (варианты с измененной изоэлектрической точкой)
[0281] В целом, как будет понятно специалисту в данной области, существуют две общие категории pI-вариантов: те, которые увеличивают pI белка (щелочные изменения), и те, которые уменьшают pI белка (кислые изменения). Как описано в данном документе, можно осуществлять все комбинации этих вариантов: один Fc-участок может представлять собой Fc-участок дикого типа или представлять собой вариант, который не демонстрирует pI, значительно отличающуюся от дикого типа, а другой может быть более щелочным либо более кислым. В качестве альтернативы изменяют каждый Fc-участок - один на более щелочной, а другой на более кислый.
[0282] Иллюстративные комбинации pI-вариантов показаны в таблице 5. Как описано в данном документе и показано в таблице 5, эти изменения показаны относительно IgG1, но все изотипы можно изменить таким образом, а также гибриды изотипов. В случае, когда константный домен тяжелой цепи получен из IgG2-4, можно также использовать R133E и R133Q.
Иллюстративные комбинации pI-вариантов
[0283] В одном варианте осуществления комбинация pI-вариантов содержит один Fc-участок (отрицательная Fab-сторона), содержащий варианты 208D/295E/384D/418E/421D (N208D/Q295E/N384D/Q418E/N421D, если рассматривать относительно IgG1 человека), и второй Fc-участок (положительная scFv-сторона), содержащий положительно заряженный линкер для scFv, например, L36 (описанный в разделе 7.3.3). Однако, как будет понятно специалисту в данной области, первый Fc-участок содержит CH1-домен, в том числе положение 208. Соответственно, в конструкциях, которые не содержат CH1-домен (например, для MBM, в которых не используется CH1-домен в качестве одного из доменов, например, в формате, изображенном на фиг. 1K), набор отрицательных pI-вариантов Fc может включать варианты 295E/384D/418E/421D (Q295E/N384D/Q418E/N421D, если рассматривать относительно IgG1 человека).
[0284] В некоторых вариантах осуществления первый Fc-участок содержит набор замен из таблицы 5, а второй Fc-участок соединен с заряженным линкером (например, выбранным из линкеров, описанных в разделе 7.3.3).
[0285] В некоторых вариантах осуществления MBM содержит первый Fc-участок и второй Fc-участок. В некоторых вариантах осуществления первый Fc-участок содержит следующие мутации: N208D, Q295E, N384D, Q418E и N421D. В некоторых вариантах осуществления второй Fc-участок содержит следующие мутации: N208D, Q295E, N384D, Q418E и N421D.
7.3.1.5.4. Изотипические варианты
[0286] Кроме того, многие варианты осуществления настоящего изобретения основываются на "импорте" pI-аминокислот в определенных положениях из одного изотипа IgG в другой, за счет чего обеспечивается снижение или устранение возможности введения нежелательной иммуногенности в варианты. Некоторые из них показаны на фигуре 21 в публикации заявки на патент США № 2014/0370013. То есть IgG1 является распространенным изотипом для терапевтических антител по множеству причин, включая высокую эффекторную функцию. Однако константный участок тяжелой цепи IgG1 характеризуется более высокой pI, чем у IgG2 (8,10 по сравнению с 7,31). Посредством введения остатков IgG2 в определенные положения в остов IgG1 pI полученного Fc-участка понижается (или увеличивается), и дополнительно проявляется более длительный период полужизни в сыворотке крови. Например, IgG1 содержит глицин (pI 5,97) в положении 137, а IgG2 содержит глутаминовую кислоту (pI 3,22); импорт глутаминовой кислоты будет влиять на pI получаемого белка. Как описано ниже, обычно требуется ряд аминокислотных замен, чтобы оказывать значительное влияние на pI варианта антитела. Однако следует отметить, как обсуждается ниже, что даже изменения в молекулах IgG2 позволяют увеличить период полужизни в сыворотке крови.
[0287] В других вариантах осуществления осуществляют неизотипические аминокислотные замены для снижения общего зарядового состояния получаемого белка (например, посредством замены аминокислоты с более высокой pI на аминокислоту с более низкой pI) либо для обеспечения приспособлений структуры в целях стабильности, как дополнительно описано ниже.
[0288] Кроме того, посредством pI-конструирования константных доменов как тяжелой, так и легкой цепей MBM, содержащей два полуантитела, можно увидеть значительные изменения в каждом полуантителе. Наличие pI двух полуантител, отличающихся на по меньшей мере 0,5, может позволить провести разделение с помощью ионообменной хроматографии или изоэлектрического фокусирования или других способов, чувствительных к изоэлектрической точке.
7.3.1.5.5. Расчет pI
[0289] Значение pI полуантитела, содержащего Fc-участок и ABD или цепь ABD, может зависеть от pI варианта константного домена тяжелой цепи и pI полного полуантитела, включая вариант константного домена тяжелой цепи и ABD или цепь ABD. Таким образом, в некоторых вариантах осуществления изменение pI рассчитывают по варианту константного домена тяжелой цепи, используя диаграмму на фигуре 19 из публикации заявки на патент США № 2014/0370013. Как обсуждается в данном документе, выбор полуантитела для конструирования обычно определяется собственной pI полуантител. В качестве альтернативы можно сравнить pI каждого полуантитела.
7.3.1.5.6. pI-варианты, которые также придают лучшее связывание FcRn in vivo
[0290] В случае, когда pI-вариант уменьшает pI Fc-участка, он может обладать дополнительным преимуществом в виде улучшения удержания в сыворотке крови in vivo.
[0291] Считается, что pI-варианты Fc-участков обеспечивают более длительные периоды полужизни антигенсвязывающих молекул in vivo, поскольку связывание с FcRn при pH 6 в эндосоме приводит к секвестрации Fc (Ghetie and Ward, 1997 Immunol Today. 18(12): 592-598). Затем Fc возвращается из эндосомального компартмента на поверхность клетки. После того, как компартмент открывается во внеклеточное пространство, более высокий pH ~ 7,4 индуцирует высвобождение Fc обратно в кровь. Dall' Acqua и соавт. показали, что у мышей мутантные варианты Fc с увеличенным связыванием FcRn при pH 6 и pH 7,4 фактически имели сниженные концентрации в сыворотке крови и такой же период полужизни, как у Fc дикого типа (Dall' Acqua et al, 2002, J. Immunol. 169:5171-5180). Считается, что увеличенная аффинность Fc к FcRn при рН 7,4 препятствует высвобождению Fc обратно в кровь. Следовательно, мутации Fc, которые увеличивают период полужизни Fc in vivo, в идеальном случае увеличивают связывание FcRn при более низком рН, в то же время обеспечивая возможность высвобождения Fc при более высоком рН. Аминокислота гистидин изменяет свое зарядовое состояние в диапазоне рН 6,0-7,4. Поэтому неудивительно обнаруживать остатки His в важных положениях в комплексе Fc/FcRn.
[0292] Было высказано предположение, что антитела с вариабельными участками, которые характеризуются более низкими значениями изоэлектрических точек, также могут иметь более длительные периоды полужизни в сыворотке крови (Igawa et al., 2010, PEDS. 23(5): 385-392). Однако механизм этого явления все еще слабо понятен. Более того, вариабельные участки различаются от антитела к антителу. Варианты константных участков со сниженным значением pI и увеличенным периодом полужизни обеспечили бы более модульный подход к улучшению фармакокинетических свойств MBM, описанных в данном документе.
7.3.1.5.7. Полярный мостик
[0293] Гетеродимеризацию полипептидных цепей MBM (например, TBM), содержащих Fc-домен, можно увеличивать посредством введения модификаций на основании рациональной идеи "образования полярного мостика", что необходимо для того, чтобы остатки в области связывающего контакта двух полипептидных цепей взаимодействовали с остатками, имеющими сходные (или дополняющие) физические свойства, в гетеродимерной конфигурации и в то же время с остатками, имеющими другие физические свойства, в гомодимерной конфигурации. В частности, эти модификации сконструированы таким образом, чтобы при образовании гетеродимера полярные остатки взаимодействовали с полярными остатками, а гидрофобные остатки при этом взаимодействовали с гидрофобными остатками. В отличие от этого, при образовании гомодимера остатки модифицируют таким образом, чтобы полярные остатки взаимодействовали с гидрофобными остатками. Благоприятные взаимодействия в гетеродимерной конфигурации и неблагоприятные взаимодействия в гомодимерной конфигурации совместно повышают вероятность того, что Fc-участки будут образовывать гетеродимеры вместо образования гомодимеров.
[0294] В иллюстративном варианте осуществления вышеуказанные модификации вводят в одно или более положений с остатками 364, 368, 399, 405, 409 и 411 CH3-домена.
[0295] В некоторых вариантах осуществления одну или более модификаций, выбранных из группы, состоящей из S364L, T366V, L368Q, N399K, F405S, K409F и R411K, вводят в один из двух CH3-доменов. Одну или более модификаций, выбранных из группы, состоящей из Y407F, K409Q и T411N, можно вводить во второй CH3-домен.
[0296] В другом варианте осуществления одну или более модификаций, выбранных из группы, состоящей из S364L, T366V, L368Q, D399K, F405S, K409F и T411K, вводят в один CH3-домен, тогда как одну или более модификаций, выбранных из группы, состоящей из Y407F, K409Q и T411D, вводят во второй CH3-домен.
[0297] В одном иллюстративном варианте осуществления исходный остаток треонина в положении 366 одного CH3-домена заменен на валин, тогда как исходный остаток тирозина в положении 407 другого CH3-домена заменен на фенилаланин.
[0298] В другом иллюстративном варианте осуществления исходный остаток серина в положении 364 одного CH3-домена заменен на лейцин, тогда как исходный остаток лейцина в положении 368 того же CH3-домена заменен на глутамин.
[0299] В еще одном иллюстративном варианте осуществления исходный остаток фенилаланина в положении 405 одного CH3-домена заменен на серин, а исходный остаток лизина в положении 409 этого CH3-домена заменен на фенилаланин, тогда как исходный остаток лизина в положении 409 другого CH3-домена заменен на глутамин.
[0300] В еще одном иллюстративном варианте осуществления исходный остаток аспарагиновой кислоты в положении 399 одного CH3-домена заменен на лизин, а исходный остаток треонина в положении 411 того же CH3-домена заменен на лизин, тогда как исходный остаток треонина в положении 411 другого CH3-домена заменен на аспарагиновую кислоту.
[0301] Аминокислотные замены, описанные в данном документе, можно вводить в CH3-домены с применением методик, которые широко известны (см., например, McPherson, ed., 1991, Directed Mutagenesis: a Practical Approach; Adelman et al., 1983, DNA, 2:183). Стратегия полярного мостика описывается, например, в WO2006/106905, WO2009/089004 и K. Gunasekaran, et al. (2010) JBC, 285:19637-19646.
[0302] Дополнительные модификации типа полярных мостиков описаны, например, в PCT-публикации № WO2014/145806 (например, на фигуре 6 в WO2014/145806), PCT-публикации № WO2014/110601 и PCT-публикациях №№ WO 2016/086186, WO 2016/086189, WO 2016/086196 и WO 2016/182751. Пример варианта с полярным мостиком содержит константный домен цепи, содержащий модификации N208D, Q295E, N384D, Q418E и N421D.
[0303] В любом из вариантов осуществления, описанных в данном документе, CH3-домены могут быть дополнительно модифицированы с введением пары остатков цистеина, как описано в разделе 7.3.1.3.
[0304] Дополнительные стратегии для усиления гетеродимеризации описаны, например, в WO2016/105450, WO2016/086186, WO2016/086189, WO2016/086196, WO2016/141378, WO2014/145806 и WO2014/110601. Любую из стратегий можно использовать в МBM, описанной в данном документе.
7.3.1.6. Комбинация вариантов гетеродимеризации и других вариантов Fc
[0305] Как будет понятно специалисту в данной области, все перечисленные варианты гетеродимеризации (включая асимметричные и/или pI-варианты) можно необязательно и независимо использовать в комбинации любым способом, при условии, что Fc-участки Fc-домена сохраняют свою способность к димеризации. Кроме того, все эти варианты можно использовать в комбинации в любом из форматов гетеродимеризации.
[0306] В случае с pI-вариантами при том, что варианты осуществления, находящие конкретное применение, показаны в таблице 5, можно создавать другие комбинации, следуя основному правилу изменения разницы pI между двумя Fc-участками в гетеродимере Fc для облегчения очистки.
[0307] Кроме того, любые из вариантов гетеродимеризации - асимметричных и pI - также независимо и необязательно используют в комбинации с вариантами Fc с устранением связывания с Fcγ-рецепторами, вариантами Fc, вариантами FcRn, как в общем описано в данном документе.
[0308] В некоторых вариантах осуществления конкретная комбинация асимметричных и pI-вариантов, которая находит применение в настоящем изобретении, представляет собой T366S/L368A/Y407V : T366W (необязательно включая мостиковую дисульфидную связь, T366S/L368A/Y407V/Y349C : T366W/S354C), при этом один Fc-участок содержит Q295E/N384D/Q418E/N481D, а другой содержит положительно заряженный линкер для scFv (если формат включает scFv-домен). Как будет понятно специалисту в данной области, варианты типа "выступы во впадины" не изменяют pI и, таким образом, могут использоваться в любом из Fc-участков в гетеродимере Fc.
[0309] В некоторых вариантах осуществления первый и второй Fc-участки, которые находят применение в настоящем изобретении, содержат аминокислотные замены S364K/E357Q : L368D/K370S, где первый и/или второй Fc-участки содержат замены 233P/L234V/L235A/G236del/S267K, обеспечивающие получение варианта с устранением связывания с Fcγ-рецепторами, и первый и/или второй Fc-участки содержат замены N208D/Q295E/N384D/Q418E/N421D, обеспечивающие получение pI-варианта (pl_(-)_изостерический_A).
7.3.2. Шарнирные участки
[0310] MBM (например, TBM) могут также содержать шарнирные участки, например, соединяющие антигенсвязывающий модуль с Fc-участком. Шарнирный участок может представлять собой нативный или модифицированный шарнирный участок. Шарнирные участки, как правило, находятся на N-концах Fc-участков.
[0311] Нативный шарнирный участок представляет собой шарнирный участок, который обычно будет находиться между Fab- и Fc-доменами встречающегося в природе антитела. Модифицированный шарнирный участок представляет собой любой шарнирный участок, который отличается по длине и/или составу от нативного шарнирного участка. Такие шарнирные участки могут включать в себя шарнирные участки из других видов, такие как шарнирные участки человека, мыши, крысы, кролика, акулы, свиньи, хомяка, верблюда, ламы или козы. Другие модифицированные шарнирные участки могут содержать полный шарнирный участок, полученный из антитела класса или подкласса, отличающегося от класса или подкласса Fc-участка тяжелой цепи. В качестве альтернативы модифицированный шарнирный участок может содержать часть природного шарнирного участка или повторяющееся звено, в котором каждое звено в повторе получено из природного шарнирного участка. В качестве дополнительной альтернативы природный шарнирный участок можно изменять посредством превращения одного или более остатков цистеина или других остатков в нейтральные остатки, такие как серин или аланин, или посредством превращения подходящим образом размещенных остатков в остатки цистеина. С помощью этого количество остатков цистеина в шарнирном участке может быть увеличено или уменьшено. Данный подход дополнительно описывается в патенте США № 5677425 авторства Bodmer et al. Изменение количества остатков цистеина в шарнирном участке может, например, облегчать сборку легких и тяжелых цепей или приводить к увеличению или уменьшению стабильности МВМ. Другие модифицированные шарнирные участки могут быть полностью синтетическими и могут быть сконструированы таким образом, чтобы они обладали необходимыми свойствами, такими как длина, содержание остатков цистеина в составе и гибкость.
[0312] Ряд модифицированных шарнирных участков был описан, например, в патентах США №№ 5677425, WO9915549, WO2005003170, WO2005003169, WO2005003170, WO9825971 и WO2005003171.
[0313] Примеры подходящих последовательностей шарнирных участков показаны в таблице 6.
Последовательности шарнирных участков
[0314] В одном варианте осуществления Fc-участок тяжелой цепи имеет интактный шарнирный участок на своем N-конце.
[0315] В одном варианте осуществления Fc-участок тяжелой цепи и шарнирный участок получены из IgG4, и шарнирный участок содержит модифицированную последовательность CPPC (SEQ ID NO: 2). Центральный шарнирный участок IgG4 человека содержит последовательность CPSC (SEQ ID NO: 12) в отличие от IgG1, который содержит последовательность CPPC (SEQ ID NO: 2). Остаток серина, присутствующий в последовательности IgG4, приводит к увеличению гибкости данного участка, и, следовательно, определенная доля молекул образует дисульфидные связи в пределах одной и той же белковой цепи (внутрицепочечную дисульфидную связь), а не образует мостик с другой тяжелой цепью в молекуле IgG с образованием межцепочечной дисульфидной связи (Angel et al., 1993, Mol Immunol 30(1):105-108). Изменение остатка серина на пролин с получением той же последовательности центрального участка, что и у IgG1, обеспечивает возможность завершения образования межцепочечных дисульфидных связей в шарнирном участке IgG4, за счет чего обеспечивается снижение неоднородности очищенного продукта. Этот измененный изотип называется IgG4P.
7.3.3. Линкеры для ABM
[0316] В определенных аспектах в настоящем изобретении предусмотрены MBM (например, TBM), содержащие по меньшей мере три ABM, где два или более компонента ABM (например, VH и VL scFv), два или более ABM или ABM и домен, отличный от ABM (например, димеризационный домен, такой как Fc-участок), соединены друг с другом посредством пептидного линкера. Такие линкеры называются в данном документе "линкерами для ABM", в отличие от линкеров для ADC, применяемых для присоединения лекарственных средств к MBM, как описано, например, в разделе 7.10.2.
[0317] Длина пептидного линкера может находиться в диапазоне от 2 аминокислот до 60 или более аминокислот, и в определенных аспектах длина пептидного линкера находится в диапазоне от 3 аминокислот до 50 аминокислот, от 4 до 30 аминокислот, от 5 до 25 аминокислот, от 10 до 25 аминокислот или от 12 до 20 аминокислот. В конкретных вариантах осуществления длина пептидного линкера составляет 2 аминокислоты, 3 аминокислоты, 4 аминокислоты, 5 аминокислот, 6 аминокислот, 7 аминокислот, 8 аминокислот, 9 аминокислот, 10 аминокислот, 11 аминокислот, 12 аминокислот, 13 аминокислот, 14 аминокислот, 15 аминокислот, 16 аминокислот, 17 аминокислот, 18 аминокислот, 19 аминокислот, 20 аминокислот, 21 аминокислоту, 22 аминокислоты, 23 аминокислоты, 24 аминокислоты, 25 аминокислот, 26 аминокислот, 27 аминокислот, 28 аминокислот, 29 аминокислот, 30 аминокислот, 31 аминокислоту, 32 аминокислоты, 33 аминокислоты, 34 аминокислоты, 35 аминокислот, 36 аминокислот, 37 аминокислот, 38 аминокислот, 39 аминокислот, 40 аминокислот, 41 аминокислоту, 42 аминокислоты, 43 аминокислоты, 44 аминокислоты, 45 аминокислот, 46 аминокислот, 47 аминокислот, 48 аминокислот, 49 аминокислот или 50 аминокислот.
[0318] Можно применять заряженные и/или гибкие линкеры.
[0319] Примеры гибких линкеров для ABM, которые можно применять в MBM, включают линкеры, раскрытые в Chen et al., 2013, Adv Drug Deliv Rev. 65(10):1357-1369, и Klein et al., 2014, Protein Engineering, Design & Selection 27(10):325-330. Особенно применимым гибким линкером является (GGGGS)n (также называемый (G4S)n) (SEQ ID NO: 25). В некоторых вариантах осуществления n равняется любому числу между 1 и 10, т. е. 1, 2, 3, 4, 5, 6, 7, 8, 9 и 10, или находится в любом диапазоне, ограниченном любыми двумя из вышеуказанных чисел, например, от 1 до 5, от 2 до 5, от 3 до 6, от 2 до 4, от 1 до 4 и т. д. и т. п.
[0320] Другие примеры линкеров для ABM, подходящих для применения в МBM по настоящему изобретению, показаны в таблице 7 ниже.
Последовательности линкеров для ABM
[0321] В различных аспектах в настоящем изобретении предусмотрена MBM (например, TBM), которая содержит один или более линкеров для ABM. Длина каждого из линкеров для ABM может находиться в диапазоне от 2 аминокислот до 60 аминокислот, например, длина составляет от 4 до 30 аминокислот, от 5 до 25 аминокислот, от 10 до 25 аминокислот или от 12 до 20 аминокислот, при этом линкер необязательно выбран из таблицы 7 выше. В конкретных вариантах осуществления МBM содержит два, три, четыре, пять или шесть линкеров для ABM. Линкеры для ABM могут находиться в одной, двух, трех, четырех или даже более полипептидных цепях МBM.
7.4. Иллюстративные триспецифические связывающие молекулы
[0322] Иллюстративные конфигурации TBM показаны на фиг. 1. На фиг. 1A показаны компоненты конфигураций TBM, показанных на фиг. 1B-1V. Каждый из scFv, Fab, ABM на основе молекулы, отличной от иммуноглобулина, и Fc может иметь характеристики, описанные для этих компонентов в разделах 7.2 и 7.3. Компоненты конфигураций TBM, показанных на фиг. 1, могут быть ассоциированы друг с другом посредством любого из средств, описанных в разделах 7.2 и 7.3 (например, с помощью прямых связей, линкеров для ABM, дисульфидных связей, Fc-доменов, модифицированных для взаимодействий типа "выступ во впадину", и т. д.). Ориентации и ассоциации различных компонентов, показанных на фиг. 1, являются исключительно иллюстративными; как будет понятно специалисту в данной области, другие ориентации и ассоциации могут быть подходящими (например, которые описаны в разделах 7.2 и 7.3).
[0323] TBM не ограничены конфигурациями, показанными на фиг. 1. Другие конфигурации, которые можно применять, известны специалистам в данной области. См., например, WO 2014/145806; WO 2017/124002; Liu et al., 2017, Front Immunol. 8:38; Brinkmann & Kontermann, 2017, mAbs 9:2, 182-212; US 2016/0355600; Klein et al., 2016, MAbs 8(6):1010-20; и US 2017/0145116.
7.4.1. Иллюстративные тривалентные TBM
[0324] TBM по настоящему изобретению могут быть тривалентными, т. е. они имеют три антигенсвязывающих домена, один из которых связывает BCMA, один из которых связывает компонент комплекса TCR, и один из которых связывает CD2 либо TAA.
[0325] Иллюстративные тривалентные конфигурации TBM показаны на фиг. 1B-1P.
[0326] Как изображено на фиг. 1B-1K и 1N-1P, TBM может содержать два полуантитела, одно из которых содержит два ABM, а другое содержит один ABM, и эти две половины спарены посредством Fc-домена.
[0327] В варианте осуществления на фиг. 1B первое (или левое) полуантитело содержит scFv и Fc-участок, а второе (или правое) полуантитело содержит Fab, scFv и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
[0328] В варианте осуществления на фиг. 1C первое (или левое) полуантитело содержит два Fab и Fc-участок, а второе (или правое) полуантитело содержит Fab и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
[0329] В варианте осуществления на фиг. 1D первое (или левое) полуантитело содержит Fab, scFv и Fc-участок, а второе (или правое) полуантитело содержит Fab и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
[0330] В варианте осуществления на фиг. 1E первое (или левое) полуантитело содержит scFv и Fc-участок, а второе (или правое) полуантитело содержит два Fab и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
[0331] В варианте осуществления на фиг. 1F первое (или левое) полуантитело содержит scFv, Fc-участок и Fab, а второе (или правое) полуантитело содержит Fab и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
[0332] В варианте осуществления на фиг. 1G первое (или левое) полуантитело содержит scFv и Fc-участок, а второе (или правое) полуантитело содержит Fab, Fc-участок и scFv. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
[0333] В варианте осуществления на фиг. 1H первое (или левое) полуантитело содержит два Fab и Fc-участок, а второе (или правое) полуантитело содержит ABM на основе молекулы, отличной от иммуноглобулина, и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
[0334] В варианте осуществления на фиг. 1I первое (или левое) полуантитело содержит Fab, scFv и Fc-участок, а второе (или правое) полуантитело содержит ABM на основе молекулы, отличной от иммуноглобулина, и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
[0335] В варианте осуществления на фиг. 1J первое (или левое) полуантитело содержит Fab и Fc-участок, а второе (или правое) полуантитело содержит scFv, ABM на основе молекулы, отличной от иммуноглобулина, и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
[0336] В варианте осуществления на фиг. 1K первое (или левое) полуантитело содержит scFv и Fc-участок, а второе (или правое) полуантитело содержит scFv, Fc-участок и второй scFv. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
[0337] В варианте осуществления на фиг. 1N первое (или левое) полуантитело содержит Fab, Fc-участок и scFv, а второе (или правое) полуантитело содержит Fab и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
[0338] В варианте осуществления на фиг. 1O первое (или левое) полуантитело содержит Fab, Fc-участок и scFab, а второе (или правое) полуантитело содержит Fab и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
[0339] В варианте осуществления на фиг. 1P первое (или левое) полуантитело содержит Fab, ABM на основе молекулы, отличной от иммуноглобулина, и Fc-участок, а второе (или правое) полуантитело содержит scFv и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
[0340] В качестве альтернативы, как изображено на фиг. 1L, тривалентная TBM может содержать два полуантитела, при этом каждое из них содержит один полный ABM и часть другого ABM (одно содержит VH, а другое содержит VL). Два полуантитела спарены посредством Fc-домена, благодаря чему VH и VL ассоциируют с образованием полного антигенсвязывающего Fv-домена.
[0341] TBM может быть одноцепочечной, как показано на фиг. 1M. TBM на фиг. 1M содержит три scFv-домена, соединенных посредством линкеров.
[0342] В каждой из конфигураций, показанных на фиг. 1B-1P, каждый из доменов, обозначенных как X, Y и Z, представляет собой ABM1, ABM2 или ABM3, хоть и не обязательно в таком порядке. Другими словами, X может представлять собой ABM1, ABM2 или ABM3, Y может представлять собой ABM1, ABM2 или ABM3, а Z может представлять собой ABM1, ABM2 или ABM3, при условии, что TBM содержит один ABM1, один ABM2 и один ABM3.
[0343] Соответственно, в настоящем изобретении предусмотрена тривалентная TBM, которая показана на любой из фиг. 1B-1P, где X представляет собой ABM1, Y представляет собой ABM3, и Z представляет собой ABM2 (эта конфигурация ABM обозначена как "T1" для удобства).
[0344] В настоящем изобретении также предусмотрена тривалентная TBM, которая показана на любой из фиг. 1B-1P, где X представляет собой ABM1, Y представляет собой ABM2, и Z представляет собой ABM3 (эта конфигурация ABM обозначена как "T2" для удобства).
[0345] В настоящем изобретении дополнительно предусмотрена тривалентная TBM, которая показана на любой из фиг. 1B-1P, где X представляет собой ABM3, Y представляет собой ABM1, и Z представляет собой ABM2 (эта конфигурация ABM обозначена как "T3" для удобства).
[0346] В настоящем изобретении еще дополнительно предусмотрена тривалентная TBM, которая показана на любой из фиг. 1B-1P, где X представляет собой ABM3, Y представляет собой ABM2, и Z представляет собой ABM1 (эта конфигурация ABM обозначена как "T4" для удобства).
[0347] В настоящем изобретении еще дополнительно предусмотрена тривалентная TBM, которая показана на любой из фиг. 1B-1P, где X представляет собой ABM2, Y представляет собой ABM1, и Z представляет собой ABM3 (эта конфигурация ABM обозначена как "T5" для удобства).
[0348] В настоящем изобретении еще дополнительно предусмотрена тривалентная TBM, которая показана на любой из фиг. 1B-1P, где X представляет собой ABM2, Y представляет собой ABM3, и Z представляет собой ABM1 (эта конфигурация ABM обозначена как "T6" для удобства).
7.4.2. Иллюстративные тетравалентные TBM
[0349] TBM по настоящему изобретению могут быть тетравалентными, т. е. они имеют четыре антигенсвязывающих домена, один или два из которых связывают BCMA, один или два из которых связывают компонент комплекса TCR, и один или два из которых связывают CD2 или TAA.
[0350] Иллюстративные тетравалентные конфигурации TBM показаны на фиг. 1Q-1S.
[0351] Как изображено на фиг. 1Q-1S, тетравалентная TBM может содержать два полуантитела, при этом каждое из них содержит два полных ABM, и эти две половины спарены посредством Fc-домена.
[0352] В варианте осуществления на фиг. 1Q первое (или левое) полуантитело содержит Fab, Fc-участок и второй Fab, а второе (или правое) полуантитело содержит Fab, Fc-участок и второй Fab. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
[0353] В варианте осуществления на фиг. 1R первое (или левое) полуантитело содержит Fab, Fc-участок и scFv, а второе (или правое) полуантитело содержит Fab, Fc-участок и scFv. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
[0354] В варианте осуществления на фиг. 1S первое (или левое) полуантитело содержит Fab, Fc-участок и scFv, а второе (или правое) полуантитело содержит scFv, Fc-участок и Fab. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
[0355] В конфигурации, показанной на фиг. 1Q-1S, каждый из X, Y, Z и A представляет собой ABM1, ABM2 или ABM3, хоть и не обязательно в таком порядке, при условии, что TBM содержит по меньшей мере один ABM1, по меньшей мере один ABM2 и по меньшей мере один ABM3. Таким образом, тетравалентные ABM будут содержать два ABM для одного из BCMA, компонента комплекса TCR и CD2 или TAA. В некоторых случаях тетравалентная TBM имеет два ABM для BCMA.
[0356] Соответственно, в настоящем изобретении предусмотрены тетравалентные TBM, которые показаны на любой из фиг. 1Q-1S, где X, Y, Z и A представляют собой ABM, направленные на BCMA, компонент комплекса TCR и CD2 или TAA, которые показаны в таблице 8.
Варианты сочетания ABM в тетравалентных TBM
7.4.3. Иллюстративные пентавалентные TBM
[0357] TBM по настоящему изобретению могут быть пентавалентными, т. е. они имеют пять антигенсвязывающих доменов, один, два или три из которых связывают BCMA, один, два или три из которых связывают компонент комплекса TCR, и один, два или три из которых связывают CD2 или TAA.
[0358] Иллюстративная пентавалентная конфигурация TBM показана на фиг. 1T.
[0359] Как изображено на фиг. 1T, пентавалентная TBM может содержать два полуантитела, одно из которых содержит два полных ABM, а другое из которых содержит один полный ABM, и эти две половины спарены посредством Fc-домена.
[0360] В варианте осуществления на фиг. 1T первое (или левое) полуантитело содержит Fab, scFv и Fc-участок, а второе (или правое) полуантитело содержит Fab, Fc-участок и scFv. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
[0361] В конфигурации, показанной на фиг. 1T, каждый из X, Y, Z, A и B представляет собой ABM1, ABM2 или ABM3, хоть и не обязательно в таком порядке, при условии, что TBM содержит по меньшей мере один ABM1, один ABM2 и один ABM3. Таким образом, пентавалентные TBM могут содержать два ABM для двух из BCMA, компонента комплекса TCR и CD2 или TAA или три ABM для одного из BCMA, компонента комплекса TCR и CD2 или TAA. В некоторых случаях пентавалентная TBM имеет два или три ABM для BCMA. В некоторых вариантах осуществления пентавалентная TBM имеет три ABM1, один ABM2 и один ABM3.
[0362] Соответственно, в настоящем изобретении предусмотрена пентавалентная TBM, которая показана на фиг. 1T, где X, Y, Z, A и B представляют собой ABM, направленные на BCMA, компонент комплекса TCR и CD2 или TAA, которые показаны в таблице 9.
Варианты сочетания ABM в пентавалентных TBM
7.4.4. Иллюстративные гексавалентные TBM
[0363] TBM по настоящему изобретению могут быть гексавалентными, т. е. они имеют шесть антигенсвязывающих доменов, один, два, три или четыре из которых связывают BCMA, один, два, три или четыре из которых связывают компонент комплекса TCR, и один, два, три или четыре из которых связывают CD2 или TAA.
[0364] Иллюстративные гексавалентные конфигурации TBM показаны на фиг. 1U-1V.
[0365] Как изображено на фиг. 1U-1V, пентавалентная TBM может содержать два полуантитела, одно из которых содержит два полных ABM, а другое из которых содержит один полный ABM, и эти две половины спарены посредством Fc-домена.
[0366] В варианте осуществления на фиг. 1U первое (или левое) полуантитело содержит Fab, второй Fab, Fc-участок и scFv, а второе (или правое) полуантитело содержит Fab, второй Fab, Fc-участок и scFv. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
[0367] В варианте осуществления на фиг. 1V первое (или левое) полуантитело содержит первый Fv, второй Fv, третий Fv и Fc-участок, а второе (или правое) полуантитело содержит первый Fv, второй Fv, третий Fv и Fc-участок. Первое и второе полуантитела ассоциированы посредством Fc-участков, образующих Fc-домен.
[0368] В конфигурации, показанной на фиг. 1U-1V, каждый из X, Y, Z, A, B и C представляет собой ABM1, ABM2 или ABM3, хоть и не обязательно в таком порядке, при условии, что TBM содержит по меньшей мере один ABM1, один ABM2 и один ABM3. Таким образом, гексавалентные TBM могут содержать (i) два ABM для каждого из BCMA, компонента комплекса TCR и CD2 или TAA, (ii) три ABM для одного из BCMA, компонента комплекса TCR и CD2 или TAA (iii) или четыре ABM для одного из BCMA, компонента комплекса TCR и CD2 или TAA. Например, гексавалентный ABM может содержать три ABM для BCMA, два ABM для CD2 или TAA и один ABM для компонента комплекса TCR. В качестве другого примера гексавалентный ABM может содержать три ABM для BCMA, два ABM для компонента комплекса TCR и один ABM для CD2 или TAA. В некоторых случаях гексавалентная TBM имеет два, три или четыре ABM для BCMA. В некоторых вариантах осуществления гексавалентная TBM имеет три ABM для BCMA. В других вариантах осуществления гексавалентная TBM имеет четыре ABM для BCMA.
[0369] Соответственно, в настоящем изобретении предусмотрены гексавалентные TBM, которые показаны на любой из фиг. 1U-1V, где X, Y, Z, A, B и C представляют собой ABM, направленные на BCMA, компонент комплекса TCR и CD2 или TAA, которые показаны в таблице 10.
Варианты сочетания ABM в гексавалентных TBM
7.5. ABM для BCMA
[0370] MBM (например, TBM) содержат ABM (ABM1), который специфично связывается с BCMA человека. BCMA является представителем семейства рецепторов фактора некроза опухоли (TNFR), который экспрессируется на клетках B-клеточной линии дифференцировки. Экспрессия BCMA является наиболее высокой на терминально дифференцированных B-клетках, которые приобретают судьбу долгоживущих плазматических клеток, в том числе на плазматических клетках, плазмобластах и в субпопуляции активированных B-клеток и B-клеток памяти. BCMA участвует в опосредовании выживания плазматических клеток для поддержания длительного гуморального иммунитета. Недавно было показано, что экспрессия BCMA связана с рядом форм рака, аутоиммунных нарушений и инфекционных заболеваний. Формы рака с увеличенной экспрессией BCMA включают некоторые формы гематологического рака, такие как множественная миелома, лимфома Ходжкина и неходжкинская лимфома, различные формы лейкоза и глиобластому.
[0371] ABM1 может включать в себя, например, антитело к BCMA или его антигенсвязывающий домен. Антитело к BCMA или его антигенсвязывающий домен могут содержать, например, последовательности CDR, VH, VL или scFv, представленные в таблицах с 11A-1 по 11P (в совокупности называемых "таблицей 11").
Консенсусные последовательности CDR легкой цепи семейства AB1/AB2
(консенсусная последовательность AB1/AB2 - по Kabat)
(x=s или t)
(консенсусная последовательность семейства AB1/AB2 - по Kabat)
(X1=S, G, D, Y, или A; x2=s, t, или A; X3=P или L)
(консенсусная последовательность AB1/AB2 - по Chothia)
(X=S или T)
(консенсусная последовательность семейства AB1/AB2 - по Chothia)
(X1=S, G, D, Y, или A; x2=s, t, или A; X3=P или L)
(консенсусная последовательность AB1/AB2 - по IMGT)
(X=S или T)
(консенсусная последовательность семейства AB1/AB2 - по IMGT)
(X1=S, G, D, Y, или A; x2=s, t, или A; X3=P или L)
(консенсусная последовательность AB1/AB2 - по Kabat+Chothia)
(X=S ИЛИ T)
(консенсусная последовательность семейства AB1/AB2 - по Kabat+Chothia)
(X1=S, G, D, Y ИЛИ A; X2=S, T ИЛИ A; X3=P ИЛИ L)
(консенсусная последовательность AB1/AB2 - по Kabat+IMGT)
(X=S ИЛИ T)
(консенсусная последовательность семейства AB1/AB2 - по Kabat+IMGT)
(X1=S, G, D, Y ИЛИ A; X2=S, T ИЛИ A; X3=P ИЛИ L)
(консенсусная последовательность AB1/AB2 - по Chothia+IMGT)
(X=S ИЛИ T)
(консенсусная последовательность семейства AB1/AB2 - по Chothia+IMGT)
(X1=S, G, D, Y ИЛИ A; X2=S, T ИЛИ A; X3=P ИЛИ L)
Консенсусные последовательности CDR тяжелой цепи семейства AB1/AB2
(консенсусная последовательность AB1/AB2 - по Kabat)
(X1=G или E; X2=S или R; X3=T или A; X4=Y или A)
(консенсусная последовательность семейства AB1/AB2 - по Kabat)
(X1=G, E, или A; X2=S, A, H, или E; X3=G, D, E, H, R, или A; X4=S, R, V, T, Y; X5=
T, A, E, H, или R; X6=Y, A, или S)
(консенсусная последовательность AB1/AB2 - по Chothia)
(X1=G или E; X2=S или R)
(консенсусная последовательность семейства AB1/AB2 - по Chothia)
(X1=G, E, или A; X2=S, A, H, или E; X3=G, D, E, H, R, или A; X4=S, R, V, T, Y)
(консенсусная последовательность AB1/AB2 - по IMGT)
(X1=G или E; X2=S или R; X3=T или A)
(консенсусная последовательность семейства AB1/AB2 - по IMGT)
(X1=G, E, или A; X2=S, A, H, или E; X3=G, D, E, H, R, или A; X4=S, R, V, T, Y; X5=
T, A, E, H, или R)
(консенсусная последовательность AB1/AB2 - по Kabat+Chothia)
(X1=G или E; X2=S или R; X3=T или A; X4=Y или A)
(консенсусная последовательность семейства AB1/AB2 - по Kabat+Chothia)
(X1=G, E, или A; X2=S, A, H, или E; X3=G, D, E, H, R, или A; X4=S, R, V, T, Y; X5=
T, A, E, H, или R; X6=Y, A, или S)
(консенсусная последовательность AB1/AB2 - по Kabat+IMGT)
(X1=G или E; X2=S или R; X3=T или A; X4=Y или A)
(консенсусная последовательность семейства AB1/AB2 - по Kabat+IMGT)
(X1=G, E, или A; X2=S, A, H, или E; X3=G, D, E, H, R, или A; X4=S, R, V, T, Y; X5=
T, A, E, H, или R; X6=Y, A, или S)
(консенсусная последовательность AB1/AB2 - по Chothia+IMGT)
(X1=G или E, X2=S или R; X3=T или A)
(консенсусная последовательность семейства AB1/AB2 - по Chothia+IMGT)
(X1=G, E, или A; X2=S, A, H, или E; X3=G, D, E, H, R, или A; X4=S, R, V, T, Y; X5=
T, A, E, H, или R)
Консенсусные последовательности CDR легкой цепи семейства AB3
(консенсусная последовательность AB3/PI-61 - по Kabat)
(X1=l или p; x2=r или s)
(X=A или T)
(консенсусная последовательность семейства AB3 - по Kabat)
(X1=D или E; X2=L, P, или A; X3=R, S, G, или W)
(X=A или T)
(консенсусная последовательность AB3/PI-61 - по Chothia)
(X=A или T)
(консенсусная последовательность семейства AB3 - по Chothia)
(X=D или E)
(X=A или T)
(консенсусная последовательность AB3/PI-61 - по IMGT, с удлиненным CDR-L2)
(X1=L или P; X2=R или S)
(X=A или T)
(консенсусная последовательность семейства AB3 - по IMGT, с удлиненным CDR-L2)
(X1=D или E; X2=L, P, или A; X3=R, S, G, или W)
(X=A или T)
(консенсусная последовательность AB3/PI-61 - по Kabat+Chothia)
(X1=L или P; X2=R или S)
(X=A или T)
(консенсусная последовательность семейства AB3 - по Kabat+Chothia)
(X1=D или E; X2=L, P, или A; X3=R, S, G, или W)
(X=A или T)
(консенсусная последовательность AB3/PI-61 - по Kabat+IMGT)
(X1=L или P; X2=R или S)
(X=A или T)
(консенсусная последовательность семейства AB3 - по Kabat+IMGT)
(X1=D или E; X2=L, P, или A; X3=R, S, G, или W)
(X=A или T)
(консенсусная последовательность AB3/PI-61 - по Chothia+IMGT, с удлиненным CDR-L2)
(X1=L или P; X2=R или S)
(X=A или T)
(консенсусная последовательность семейства AB3 - по Chothia+IMGT, с удлиненным CDR-L2)
(X1=D или E; X2=L, P, или A; X3=R, S, G, или W)
(X=A или T)
(консенсусная последовательность AB3/PI-61 - по IMGT)
(X=A или T)
(консенсусная последовательность семейства AB3 - по IMGT)
(X1=D или E)
(X=A или T)
(консенсусная последовательность AB3/PI-61 - по Chothia+IMGT)
(X=A или T)
(консенсусная последовательность семейства AB3 - по Chothia+IMGT)
(X1=D или E)
(X=A или T)
Консенсусные последовательности CDR тяжелой цепи семейства AB3
(консенсусная последовательность AB3/PI-61 - по Kabat)
(X=T или D)
(консенсусная последовательность семейства AB3 - по Kabat)
(X1=H, K, T, R, D, N, S; X2=G, D, или E; X3=S, T, F, A, L; X4=H, N или K)
(X1=A, N, E; X2=L, F, V, или Y; X3=H, Q, R, или D; X4=D, E, G, или Q; X5=D, Q, или F; X6=Y или Q; X7=Y, K, или D; X8=G или P; X9=L, Q, V, или T)
(консенсусная последовательность AB3/PI-61 - по Chothia)
(X=T или D)
(консенсусная последовательность семейства AB3 - по Chothia)
(X1=H, K, T, R, D, N, S; X2=G, D, или E; X3=S, T, F, A, L; X4=H, N или K)
(X1=A, N, E; X2=L, F, V, или Y; X3=H, Q, R, или D; X4=D, E, G, или Q; X5=D, Q, или F; X6=Y или Q; X7=Y, K, или D; X8=G или P; X9=L, Q, V, или T)
(консенсусная последовательность AB3/PI-61 - по IMGT)
(консенсусная последовательность семейства AB3 - по IMGT)
(X1=H, K, T, R, D, N, S; X2=G, D, или E; X3=S, T, F, A, L; X4=H, N или K)
(X1=A, N, E; X2=L, F, V, или Y; X3=H, Q, R, или D; X4=D, E, G, или Q; X5=D, Q, или F; X6=Y или Q; X7=Y, K, или D; X8=G или P; X9=L, Q, V, или T)
(консенсусная последовательность AB3/PI-61 - по Kabat+Chothia)
(X=T или D)
(консенсусная последовательность семейства AB3 - по Kabat+Chothia)
(X1=H, K, T, R, D, N, S; X2=G, D, или E; X3=S, T, F, A, L; X4=H, N или K)
(X1=A, N, E; X2=L, F, V, или Y; X3=H, Q, R, или D; X4=D, E, G, или Q; X5=D, Q, или F; X6=Y или Q; X7=Y, K, или D; X8=G или P; X9=L, Q, V, или T)
(консенсусная последовательность AB3/PI-61 - по Kabat+IMGT)
(X=T или D)
(консенсусная последовательность семейства AB3 - по Kabat+IMGT)
(X1=H, K, T, R, D, N, S; X2=G, D, или E; X3=S, T, F, A, L; X4=H, N или K)
(X1=A, N, E; X2=L, F, V, или Y; X3=H, Q, R, или D; X4=D, E, G, или Q; X5=D, Q, или F; X6=Y или Q; X7=Y, K, или D; X8=G или P; X9=L, Q, V, или T)
(консенсусная последовательность AB3/PI-61 - по Chothia+IMGT)
(X=T или D)
(консенсусная последовательность семейства AB3 - по Chothia+IMGT)
(X1=H, K, T, R, D, N, S; X2=G, D, или E; X3=S, T, F, A, L; X4=H, N или K)
(X1=A, N, E; X2=L, F, V, или Y; X3=H, Q, R, или D; X4=D, E, G, или Q; X5=D, Q, или F; X6=Y или Q; X7=Y, K, или D; X8=G или P; X9=L, Q, V, или T)
(консенсусная последовательность AB3/PI-61 - по IMGT)
(консенсусная последовательность семейства AB3 - по IMGT)
(X1=H, K, T, R, D, N, S; X2=G, D, или E; X3=S, T, F, A, L; X4=H, N или K)
(X1=A, N, E; X2=L, F, V, или Y; X3=H, Q, R, или D; X4=D, E, G, или Q; X5=D, Q, или F; X6=Y или Q; X7=Y, K, или D; X8=G или P; X9=L, Q, V, или T)
(консенсусная последовательность AB3/PI-61 - по Chothia+IMGT)
(X=T или D)
(консенсусная последовательность семейства AB3 - по Chothia+IMGT)
(X1=H, K, T, R, D, N, S; X2=G, D, или E; X3=S, T, F, A, L; X4=H, N или K)
(X1=A, N, E; X2=L, F, V, или Y; X3=H, Q, R, или D; X4=D, E, G, или Q; X5=D, Q, или F; X6=Y или Q; X7=Y, K, или D; X8=G или P; X9=L, Q, V, или T)
Средства, связывающие BCMA, из семейства AB1/AB2 - последовательности CDR легкой цепи в соответствии со схемой нумерации по Kabat
Средства, связывающие BCMA, из семейства AB1/AB2 - последовательности CDR тяжелой цепи в соответствии со схемой нумерации по Kabat
Средства, связывающие BCMA, из семейства AB1/AB2 - последовательности CDR легкой цепи в соответствии со схемой нумерации по Chothia
Средства, связывающие BCMA, из семейства AB1/AB2 - последовательности CDR тяжелой цепи в соответствии со схемой нумерации по Chothia
Средства, связывающие BCMA, из семейства AB1/AB2 - последовательности CDR легкой цепи в соответствии со схемой нумерации по IMGT
Средства, связывающие BCMA, из семейства AB1/AB2 - последовательности CDR тяжелой цепи в соответствии со схемой нумерации по IMGT
Средства, связывающие BCMA, из семейства AB1/AB2 - последовательности CDR легкой цепи в соответствии с комбинацией схем нумерации по Kabat и по Chothia
Средства, связывающие BCMA, из семейства AB1/AB2 - последовательности CDR тяжелой цепи в соответствии с комбинацией схем нумерации по Kabat и по Chothia
Средства, связывающие BCMA, из семейства AB1/AB2 - последовательности CDR легкой цепи в соответствии с комбинацией схем нумерации по Kabat и по IMGT
Средства, связывающие BCMA, из семейства AB1/AB2 - последовательности CDR тяжелой цепи в соответствии с комбинацией схем нумерации по Kabat и по IMGT
Средства, связывающие BCMA, из семейства AB1/AB2 - последовательности CDR легкой цепи в соответствии с комбинацией схем нумерации по Chothia и по IMGT
Средства, связывающие BCMA, из семейства AB1/AB2 - последовательности CDR тяжелой цепи в соответствии с комбинацией схем нумерации по Chothia и по IMGT
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR легкой цепи в соответствии со схемой нумерации по Kabat
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR тяжелой цепи в соответствии со схемой нумерации по Kabat
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR легкой цепи в соответствии со схемой нумерации по Chothia
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR тяжелой цепи в соответствии со схемой нумерации по Chothia
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR-L1 и CDR-L3 в соответствии со схемой нумерации по IMGT и удлиненные последовательности CDR-L2
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR легкой цепи в соответствии со схемой нумерации по IMGT
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR тяжелой цепи в соответствии со схемой нумерации по IMGT
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR легкой цепи в соответствии с комбинацией схем нумерации по Kabat и по Chothia
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR тяжелой цепи в соответствии с комбинацией схем нумерации по Kabat и по Chothia
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR легкой цепи в соответствии с комбинацией схем нумерации по Kabat и по IMGT
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR тяжелой цепи в соответствии с комбинацией схем нумерации по Kabat и по IMGT
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR-L1 и CDR-L3 в соответствии с комбинацией схем нумерации по Chothia и по IMGT и удлиненные последовательности CDR-L2
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR легкой цепи в соответствии с комбинацией схем нумерации по Chothia и по IMGT
Средства, связывающие BCMA, из семейства AB3 - последовательности CDR тяжелой цепи в соответствии с комбинацией схем нумерации по Chothia и по IMGT
Средства, связывающие BCMA - последовательности вариабельных участков легкой цепи
Средства, связывающие BCMA - последовательности вариабельных участков тяжелой цепи
Средства, связывающие BCMA - последовательности scFv
[0372] В таблицах с 11A-1 по 11B-2 перечислены консенсусные последовательности CDR, полученные из последовательностей CDR иллюстративных BCMA-связывающих молекул. Консенсусные последовательности CDR включают последовательности на основе последовательностей CDR по Kabat иллюстративных BCMA-связывающих молекул, последовательностей CDR по Chothia иллюстративных BCMA-связывающих молекул, последовательностей CDR по IMGT иллюстративных BCMA-связывающих молекул, последовательностей CDR в соответствии с комбинацией по Kabat и по Chothia иллюстративных BCMA-связывающих молекул, последовательностей CDR в соответствии с комбинацией по Kabat и по IMGT иллюстративных BCMA-связывающих молекул и последовательностей CDR в соответствии с комбинацией по Chothia и по IMGT иллюстративных BCMA-связывающих молекул. Конкретные последовательности CDR иллюстративных ВСМА-связывающих молекул перечислены в таблицах с 11C1 по 11N-2. Иллюстративные последовательности VL и VH перечислены в таблицах 11O-1 и 11O-2 соответственно. Иллюстративные последовательности scFv перечислены в таблице 11P.
[0373] В некоторых вариантах осуществления ABM1 содержит CDR легкой цепи, имеющий аминокислотную последовательность любой из консенсусных последовательностей CDR, перечисленных в таблице 11A-1 или таблице 11B-1. В конкретных вариантах осуществления в настоящем изобретении предусмотрены MBM, содержащие ABM1, который содержит один, два, три или более CDR легкой цепи (или в качестве альтернативы состоит из них), выбранных из CDR легкой цепи, описанных в таблице 11A-1 или таблице 11B-1.
[0374] В некоторых вариантах осуществления ABM1 содержит CDR тяжелой цепи, имеющий аминокислотную последовательность любого из CDR тяжелой цепи, перечисленных в таблице 11A-2 или таблице 11B-2. В конкретных вариантах осуществления в настоящем изобретении предусмотрены MBM, содержащие ABM1, который содержит один, два, три или более CDR тяжелой цепи (или в качестве альтернативы состоит из них), выбранных из CDR тяжелой цепи, описанных в таблице 11A-2 или таблице 11B-2.
[0375] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C1, представленные в таблицах 11A-1 и 11A-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C2, представленные в таблицах 11A-1 и 11A-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C3, представленные в таблицах 11A-1 и 11A-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C4, представленные в таблицах 11A-1 и 11A-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C5, представленные в таблицах 11A-1 и 11A-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C6, представленные в таблицах 11A-1 и 11A-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C7, представленные в таблицах 11A-1 и 11A-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C8, представленные в таблицах 11A-1 и 11A-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C9, представленные в таблицах 11A-1 и 11A-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C10, представленные в таблицах 11A-1 и 11A-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C11, представленные в таблицах 11A-1 и 11A-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C12, представленные в таблицах 11A-1 и 11A-2.
[0376] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C13, представленные в таблицах 11B-1 и 11B-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C14, представленные в таблицах 11B-1 и 11B-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C15, представленные в таблицах 11B-1 и 11B-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C16, представленные в таблицах 11B-1 и 11B-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C17, представленные в таблицах 11B-1 и 11B-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C18, представленные в таблицах 11B-1 и 11B-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C19, представленные в таблицах 11B-1 и 11B-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C20, представленные в таблицах 11B-1 и 11B-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C21, представленные в таблицах 11B-1 и 11B-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C22, представленные в таблицах 11B-1 и 11B-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C23, представленные в таблицах 11B-1 и 11B-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C24, представленные в таблицах 11B-1 и 11B-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C25, представленные в таблицах 11B-1 и 11B-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C26, представленные в таблицах 11B-1 и 11B-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C27, представленные в таблицах 11B-1 и 11B-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из C28, представленные в таблицах 11B-1 и 11B-2.
[0377] В некоторых вариантах осуществления ABM1 содержит CDR легкой цепи, имеющий аминокислотную последовательность любого из CDR, перечисленных в таблице 11C-1, таблице 11D-1, таблице 11E-1, таблице 11F-1, таблице 11G-1, таблице 11H-1, таблице 11I-1, таблице 11J-1, таблице 11K-1(a), таблице 11K-1(b), таблице 11L-1, таблице 11M-1, таблице 11N-1(a) или таблице 11N-1(b). В конкретных вариантах осуществления ABM1 содержит CDR легкой цепи, содержащие один, два, три или более CDR легкой цепи (или в качестве альтернативы состоящие из них), выбранных из CDR легкой цепи, описанных в таблице 11C-1, таблице 11D-1, таблице 11E-1, таблице 11F-1, таблице 11G-1, таблице 11H-1, таблице 11I-1, таблице 11J-1, таблице 11K-1(a), таблице 11K-1(b), таблице 11L-1, таблице 11M-1, таблице 11N-1(a) и таблице 11N-1(b).
[0378] В некоторых вариантах осуществления ABM1 содержит CDR тяжелой цепи, имеющий аминокислотную последовательность любого из CDR тяжелой цепи, перечисленных в таблице 11C-2, таблице 11D-2, таблице 11E-2, таблице 11F-2, таблице 11G-2, таблице 11H-2, таблице 11I-2, таблице 11J-2, таблице 11K-2, таблице 11L-2, таблице 11M-2 или таблице 11N-2. В конкретных вариантах осуществления в настоящем изобретении ABM1 содержит CDR тяжелой цепи, содержащие один, два, три или более CDR тяжелой цепи (или в качестве альтернативы состоящие из них), выбранных из CDR тяжелой цепи, описанных в таблице 11C-2, таблице 11D-2, таблице 11E-2, таблице 11F-2, таблице 11G-2, таблице 11H-2, таблице 11I-2, таблице 11J-2, таблице 11K-2, таблице 11L-2, таблице 11M-2 и таблице 11N-2.
[0379] В некоторых вариантах осуществления ABM1 содержит VL-домен, имеющий аминокислотную последовательность любого VL-домена, описанного в таблице 11O-1. В других вариантах осуществления ABM1 может содержать аминокислоты, которые были подвергнуты мутации, но при этом они характеризуются по меньшей мере 80-, 85-, 90-, 95-, 96-, 97-, 98- или 99-процентной идентичностью VL-домена с VL-доменами, показанными в последовательностях, описанных в таблице 11O-1.
[0380] В некоторых вариантах осуществления ABM1 содержит VH-домен, имеющий аминокислотную последовательность любого VH-домена, описанного в таблице 11O-2. В других вариантах осуществления ABM1 может содержать аминокислоты, которые были подвергнуты мутации, но при этом они характеризуются по меньшей мере 80-, 85-, 90-, 95-, 96-, 97-, 98- или 99-процентной идентичностью VH-домена с VH-доменами, показанными в последовательностях, описанных в таблице 11O-2.
[0381] В других вариантах осуществления ABM1 содержит аминокислоты, которые были подвергнуты мутации, но при этом они характеризуются по меньшей мере 80-, 85-, 90-, 95-, 96-, 97-, 98- или 99-процентной идентичностью CDR-участков с последовательностями CDR, описанными в таблице 11. В некоторых вариантах осуществления такие ABM содержат мутантные аминокислотные последовательности, в которых не более 1, 2, 3, 4 или 5 аминокислот были подвергнуты мутации в CDR-участках по сравнению с последовательностями CDR, описанными в таблице 11.
[0382] Другие ABM содержат VH- и/или VL-домены, содержащие аминокислотные последовательности, характеризующиеся по меньшей мере 80-, 85-, 90-, 95-, 96-, 97-, 98- или 99-процентной идентичностью с последовательностями VH и/или VL, описанными в таблице 11. В некоторых вариантах осуществления ABM1 содержит VH- и/или VL-домены, где не более 1, 2, 3, 4 или 5 аминокислот были подвергнуты мутации по сравнению с VH- и/или VL-доменами, показанными в последовательностях, описанных в таблице 11, при этом они сохраняют по существу такую же терапевтическую активность.
[0383] Последовательности VH и VL (аминокислотные последовательности и нуклеотидные последовательности, кодирующие аминокислотные последовательности) могут быть подвергнуты "смешиванию и подбору" для создания других BCMA-связывающих ABM. Такие подвергнутые "смешиванию и подбору" BCMA-связывающие ABM можно тестировать с применением известных анализов связывания (например, разновидностей ELISA). Когда цепи подвергают смешиванию и подбору, последовательность VH из конкретной пары VH/VL следует заменить на структурно сходную последовательность VH. Последовательность VL из конкретной пары VH/VL следует заменить на структурно сходную последовательность VL.
[0384] Соответственно, в одном варианте осуществления в настоящем изобретении предусмотрены MBM, имеющие ABM1, содержащий вариабельный участок тяжелой цепи (VH), содержащий аминокислотную последовательность, выбранную из любой из последовательностей VH, описанных в таблице 11-O2; и вариабельный участок легкой цепи (VL), содержащий аминокислотную последовательность, описанную в таблице 11-O1.
[0385] В другом варианте осуществления в настоящем изобретении предусмотрены MBM, имеющие ABM1, содержащий CDR-H1, описанный в таблице 11, CDR-H2, описанный в таблице 11, CDR-H3, описанный в таблице 11, CDR-L1, описанный в таблице 11, CDR-L2, описанный в таблице 11, и CDR-L3, описанный в таблице 11.
[0386] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB1, представленные в таблицах 11C-1 и 11C-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB1, представленные в таблицах 11D-1 и 11D-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB1, представленные в таблицах 11E-1 и 11E-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB1, представленные в таблицах 11F-1 и 11F-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB1, представленные в таблицах 11G-1 и 11G-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB1, представленные в таблицах 11H-1 и 11H-2.
[0387] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB2, представленные в таблицах 11C-1 и 11C-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB2, представленные в таблицах 11D-1 и 11D-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB2, представленные в таблицах 11E-1 и 11E-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB2, представленные в таблицах 11F-1 и 11F-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB2, представленные в таблицах 11G-1 и 11G-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB2, представленные в таблицах 11H-1 и 11H-2.
[0388] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из R1F2, представленные в таблицах 11C-1 и 11C-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из R1F2, представленные в таблицах 11D-1 и 11D-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из R1F2, представленные в таблицах 11E-1 и 11E-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из R1F2, представленные в таблицах 11F-1 и 11F-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из R1F2, представленные в таблицах 11G-1 и 11G-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из R1F2, представленные в таблицах 11H-1 и 11H-2.
[0389] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF03, представленные в таблицах 11C-1 и 11C-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF03, представленные в таблицах 11D-1 и 11D-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF03, представленные в таблицах 11E-1 и 11E-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF03, представленные в таблицах 11F-1 и 11F-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF03, представленные в таблицах 11G-1 и 11G-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF03, представленные в таблицах 11H-1 и 11H-2.
[0390] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF04, представленные в таблицах 11C-1 и 11C-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF04, представленные в таблицах 11D-1 и 11D-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF04, представленные в таблицах 11E-1 и 11E-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF04, представленные в таблицах 11F-1 и 11F-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF04, представленные в таблицах 11G-1 и 11G-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF04, представленные в таблицах 11H-1 и 11H-2.
[0391] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF05, представленные в таблицах 11C-1 и 11C-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF05, представленные в таблицах 11D-1 и 11D-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF05, представленные в таблицах 11E-1 и 11E-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF05, представленные в таблицах 11F-1 и 11F-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF05, представленные в таблицах 11G-1 и 11G-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF05, представленные в таблицах 11H-1 и 11H-2.
[0392] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF06, представленные в таблицах 11C-1 и 11C-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF06, представленные в таблицах 11D-1 и 11D-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF06, представленные в таблицах 11E-1 и 11E-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF06, представленные в таблицах 11F-1 и 11F-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF06, представленные в таблицах 11G-1 и 11G-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF06, представленные в таблицах 11H-1 и 11H-2.
[0393] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF07, представленные в таблицах 11C-1 и 11C-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF07, представленные в таблицах 11D-1 и 11D-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF07, представленные в таблицах 11E-1 и 11E-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF07, представленные в таблицах 11F-1 и 11F-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF07, представленные в таблицах 11G-1 и 11G-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF07, представленные в таблицах 11H-1 и 11H-2.
[0394] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF08, представленные в таблицах 11C-1 и 11C-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF08, представленные в таблицах 11D-1 и 11D-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF08, представленные в таблицах 11E-1 и 11E-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF08, представленные в таблицах 11F-1 и 11F-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF08, представленные в таблицах 11G-1 и 11G-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF08, представленные в таблицах 11H-1 и 11H-2.
[0395] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF09, представленные в таблицах 11C-1 и 11C-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF09, представленные в таблицах 11D-1 и 11D-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF09, представленные в таблицах 11E-1 и 11E-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF09, представленные в таблицах 11F-1 и 11F-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF09, представленные в таблицах 11G-1 и 11G-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF09, представленные в таблицах 11H-1 и 11H-2.
[0396] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF12, представленные в таблицах 11C-1 и 11C-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF12, представленные в таблицах 11D-1 и 11D-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF12, представленные в таблицах 11E-1 и 11E-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF12, представленные в таблицах 11F-1 и 11F-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF12, представленные в таблицах 11G-1 и 11G-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF12, представленные в таблицах 11H-1 и 11H-2.
[0397] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF13, представленные в таблицах 11C-1 и 11C-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF13, представленные в таблицах 11D-1 и 11D-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF13, представленные в таблицах 11E-1 и 11E-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF13, представленные в таблицах 11F-1 и 11F-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF13, представленные в таблицах 11G-1 и 11G-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF13, представленные в таблицах 11H-1 и 11H-2.
[0398] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF14, представленные в таблицах 11C-1 и 11C-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF14, представленные в таблицах 11D-1 и 11D-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF14, представленные в таблицах 11E-1 и 11E-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF14, представленные в таблицах 11F-1 и 11F-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF14, представленные в таблицах 11G-1 и 11G-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF14, представленные в таблицах 11H-1 и 11H-2.
[0399] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF15, представленные в таблицах 11C-1 и 11C-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF15, представленные в таблицах 11D-1 и 11D-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF15, представленные в таблицах 11E-1 и 11E-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF15, представленные в таблицах 11F-1 и 11F-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF15, представленные в таблицах 11G-1 и 11G-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF15, представленные в таблицах 11H-1 и 11H-2.
[0400] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF16, представленные в таблицах 11C-1 и 11C-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF16, представленные в таблицах 11D-1 и 11D-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF16, представленные в таблицах 11E-1 и 11E-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF16, представленные в таблицах 11F-1 и 11F-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF16, представленные в таблицах 11G-1 и 11G-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF16, представленные в таблицах 11H-1 и 11H-2.
[0401] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF17, представленные в таблицах 11C-1 и 11C-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF17, представленные в таблицах 11D-1 и 11D-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF17, представленные в таблицах 11E-1 и 11E-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF17, представленные в таблицах 11F-1 и 11F-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF17, представленные в таблицах 11G-1 и 11G-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF17, представленные в таблицах 11H-1 и 11H-2.
[0402] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF18, представленные в таблицах 11C-1 и 11C-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF18, представленные в таблицах 11D-1 и 11D-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF18, представленные в таблицах 11E-1 и 11E-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF18, представленные в таблицах 11F-1 и 11F-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF18, представленные в таблицах 11G-1 и 11G-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF18, представленные в таблицах 11H-1 и 11H-2.
[0403] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF19, представленные в таблицах 11C-1 и 11C-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF19, представленные в таблицах 11D-1 и 11D-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF19, представленные в таблицах 11E-1 и 11E-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF19, представленные в таблицах 11F-1 и 11F-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF19, представленные в таблицах 11G-1 и 11G-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF19, представленные в таблицах 11H-1 и 11H-2.
[0404] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF20, представленные в таблицах 11C-1 и 11C-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF20, представленные в таблицах 11D-1 и 11D-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF20, представленные в таблицах 11E-1 и 11E-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF20, представленные в таблицах 11F-1 и 11F-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF20, представленные в таблицах 11G-1 и 11G-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PALF20, представленные в таблицах 11H-1 и 11H-2.
[0405] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB3, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB3, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB3, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB3, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB3, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из AB3, представленные в таблицах 11N-1 и 11N-2.
[0406] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PI-61, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PI-61, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PI-61, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PI-61, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PI-61, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из PI-61, представленные в таблицах 11N-1 и 11N-2.
[0407] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-22, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-22, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-22, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-22, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-22, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-22, представленные в таблицах 11N-1 и 11N-2.
[0408] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-88, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-88, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-88, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-88, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-88, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-88, представленные в таблицах 11N-1 и 11N-2.
[0409] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-36, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-36, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-36, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-36, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-36, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-36, представленные в таблицах 11N-1 и 11N-2.
[0410] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-34, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-34, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-34, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-34, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-34, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-34, представленные в таблицах 11N-1 и 11N-2.
[0411] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-68, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-68, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-68, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-68, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-68, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-68, представленные в таблицах 11N-1 и 11N-2.
[0412] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-18, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-18, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-18, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-18, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-18, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-18, представленные в таблицах 11N-1 и 11N-2.
[0413] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-47, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-47, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-47, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-47, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-47, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-47, представленные в таблицах 11N-1 и 11N-2.
[0414] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-20, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-20, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-20, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-20, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-20, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-20, представленные в таблицах 11N-1 и 11N-2.
[0415] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-80, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-80, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-80, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-80, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-80, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-80, представленные в таблицах 11N-1 и 11N-2.
[0416] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-83, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-83, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-83, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-83, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-83, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H2/L2-83, представленные в таблицах 11N-1 и 11N-2.
[0417] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-1, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-1, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-1, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-1, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-1, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-1, представленные в таблицах 11N-1 и 11N-2.
[0418] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-2, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-2, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-2, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-2, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-2, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-2, представленные в таблицах 11N-1 и 11N-2.
[0419] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-3, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-3, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-3, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-3, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-3, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-3, представленные в таблицах 11N-1 и 11N-2.
[0420] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-4, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-4, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-4, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-4, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-4, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-4, представленные в таблицах 11N-1 и 11N-2.
[0421] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-5, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-5, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-5, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-5, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-5, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-5, представленные в таблицах 11N-1 и 11N-2.
[0422] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-6, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-6, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-6, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-6, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-6, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-6, представленные в таблицах 11N-1 и 11N-2.
[0423] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-7, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-7, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-7, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-7, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-7, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-7, представленные в таблицах 11N-1 и 11N-2.
[0424] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-8, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-8, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-8, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-8, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-8, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-8, представленные в таблицах 11N-1 и 11N-2.
[0425] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-9, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-9, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-9, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-9, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-9, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-9, представленные в таблицах 11N-1 и 11N-2.
[0426] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-10, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-10, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-10, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-10, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-10, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-10, представленные в таблицах 11N-1 и 11N-2.
[0427] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-11, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-11, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-11, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-11, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-11, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-11, представленные в таблицах 11N-1 и 11N-2.
[0428] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-12, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-12, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-12, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-12, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-12, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-12, представленные в таблицах 11N-1 и 11N-2.
[0429] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-13, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-13, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-13, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-13, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-13, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-13, представленные в таблицах 11N-1 и 11N-2.
[0430] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-14, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-14, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-14, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-14, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-14, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-14, представленные в таблицах 11N-1 и 11N-2.
[0431] В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-15, представленные в таблицах 11I-1 и 11I-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-15, представленные в таблицах 11J-1 и 11J-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-15, представленные в таблицах 11K-1 и 11K-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-15, представленные в таблицах 11L-1 и 11L-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-15, представленные в таблицах 11M-1 и 11M-2. В некоторых вариантах осуществления ABM1 содержит последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 из H3-15, представленные в таблицах 11N-1 и 11N-2.
[0432] В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи AB1, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи AB2, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи R1F2, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF03, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF04, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF05, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF06, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF07, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF08, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF09, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF12, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF13, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF14, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF15, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF16, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF17, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF18, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF19, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PALF20, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи AB3, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи PI-61, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-1, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-2, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-3, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-4, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-5, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-6, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-7, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-8, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-9, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-10, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-11, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-12, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-13, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-14, представленные в таблице 11O-1 и таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность вариабельного участка легкой цепи и/или последовательность вариабельного участка тяжелой цепи H3-15, представленные в таблице 11O-1 и таблице 11O-2.
[0433] В некоторых вариантах осуществления ABM1 содержит последовательность scFv из H2/L2-88, представленную в таблице 11P. В некоторых вариантах осуществления ABM1 содержит последовательность scFv из H2/L2-36, представленную в таблице 11P. В некоторых вариантах осуществления ABM1 содержит последовательность scFv из H2/L2-34, представленную в таблице 11P. В некоторых вариантах осуществления ABM1 содержит последовательность scFv из H2/L2-68, представленную в таблице 11P. В некоторых вариантах осуществления ABM1 содержит последовательность scFv из H2/L2-18, представленную в таблице 11P. В некоторых вариантах осуществления ABM1 содержит последовательность scFv из H2/L2-47, представленную в таблице 11P. В некоторых вариантах осуществления ABM1 содержит последовательность scFv из H2/L2-20, представленную в таблице 11P. В некоторых вариантах осуществления ABM1 содержит последовательность scFv из H2/L2-80, представленную в таблице 11P. В некоторых вариантах осуществления ABM1 содержит последовательность scFv из H2/L2-83, представленную в таблице 11P.
[0434] С учетом того, что ABM1 связывает ВСМА, и что специфичность связывания антигена обеспечивается в первую очередь участками CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3, последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 могут быть подвергнуты "смешиванию и подбору". Такие подвергнутые "смешиванию и подбору" BCMA-связывающие ABM можно тестировать с применением известных анализов связывания (например, разновидностей ELISA). Когда последовательности CDR VH подвергают смешиванию и подбору, последовательность CDR-H1, CDR-H2 и/или CDR-H3 из конкретной последовательности VH следует заменить на структурно сходную(сходные) последовательность(последовательности) CDR. Аналогичным образом, когда последовательности CDR VL подвергают смешиванию и подбору, последовательность CDR-L1, CDR-L2 и/или CDR-L3 из конкретной последовательности VL следует заменить на структурно сходную(сходные) последовательность(последовательности) CDR. Рядовому специалисту в данной области будет совершенно очевидно, что новые последовательности VH и VL можно создавать путем замены одной или более последовательностей CDR-участков VH и/или VL структурно сходными последовательностями из последовательностей CDR, показанных в данном документе.
[0435] В некоторых вариантах осуществления ABM1 содержит последовательность VL, выбранную из последовательностей VL, представленных в таблице 11O-1, и последовательность VH, выбранную из последовательностей VH, представленных в таблице 11O-2. В некоторых вариантах осуществления ABM1 содержит последовательность CDR-H1, выбранную из последовательностей CDR-H1, представленных в таблице 11A-2, таблице 11B-2, таблице 11C-2, таблице 11D-2, таблице 11E-2, таблице 11F-2, таблице 11G-2, таблице 11H-2, таблице 11I-2, таблице 11J-2, таблице 11K-2, таблице 11L-2, таблице 11M-2 и таблице 11N-2; последовательность CDR-H2, выбранную из последовательностей CDR-H2, представленных в таблице 11A-2, таблице 11B-2, таблице 11C-2, таблице 11D-2, таблице 11E-2, таблице 11F-2, таблице 11G-2, таблице 11H-2, таблице 11I-2, таблице 11J-2, таблице 11K-2, таблице 11L-2, таблице 11M-2 и таблице 11N-2; последовательность CDR-H3, выбранную из последовательностей CDR-H3, представленных в таблице 11A-2, таблице 11B-2, таблице 11C-2, таблице 11D-2, таблице 11E-2, таблице 11F-2, таблице 11G-2, таблице 11H-2, таблице 11I-2, таблице 11J-2, таблице 11K-2, таблице 11L-2, таблице 11M-2 и таблице 11N-2; последовательность CDR-L1, выбранную из последовательностей CDR-L1, представленных в таблице 11A-1, таблице 11B-1, таблице 11C-1, таблице 11D-1, таблице 11E-1, таблице 11F-1, таблице 11G-1, таблице 11H-1, таблице 11I-1, таблице 11J-1, таблице 11K-1(a), таблице 11K-1(b), таблице 11L-1, таблице 11M-1, таблице 11N-1(a) и таблице 11N-1(b); последовательность CDR-L2, выбранную из последовательностей CDR-L2, представленных в таблице 11A-1, таблице 11B-1, таблице 11C-1, таблице 11D-1, таблице 11E-1, таблице 11F-1, таблице 11G-1, таблице 11H-1, таблице 11I-1, таблице 11J-1, таблице 11K-1(a), таблице 11K-1(b), таблице 11L-1, таблице 11M-1, таблице 11N-1(a) и таблице 11N-1(b); и последовательность CDR-L3, выбранную из последовательностей CDR-L3, представленных в таблице 11A-1, таблице 11B-1, таблице 11C-1, таблице 11D-1, таблице 11E-1, таблице 11F-1, таблице 11G-1, таблице 11H-1, таблице 11I-1, таблице 11J-1, таблице 11K-1(a), таблице 11K-1(b), таблице 11L-1, таблице 11M-1, таблице 11N-1(a) и таблице 11N-1(b).
[0436] Дополнительные ABM для BCMA можно получать с помощью методик перетасовки генов, перетасовки мотивов, перетасовки экзонов и/или перетасовки кодонов (в совокупности называемых "перетасовкой ДНК"). Перетасовку ДНК можно использовать для изменения форм активности молекул по настоящему изобретению или их фрагментов (например, молекул или их фрагментов с более высокими значениями аффинности и более низкими значениями скорости диссоциации). См. в целом патенты США №№ 5605793, 5811238, 5830721, 5834252 и 5837458; Patten et al., (1997) Curr. Opinion Biotechnol. 8:724-33; Harayama, (1998) Trends Biotechnol. 16(2):76-82; Hansson et al., (1999) J. Mol. Biol. 287:265-76; и Lorenzo and Blasco, (1998) Biotechniques 24(2):308-313. ABM для BCMA, описанные в данном документе, можно изменять посредством воздействия на них случайного мутагенеза с помощью ПЦР с внесением ошибок, случайной вставки нуклеотидов или других способов до проведения рекомбинации.
7.6. ABM для TCR
[0437] MBM (например, TBM) содержат ABM, который специфично связывается с компонентом комплекса TCR. TCR представляет собой стабилизированный дисульфидными связями заякоренный в мембране гетеродимерный белок, обычно состоящий из высоковариабельных альфа- (α-) и бета- (β-) цепей, которые экспрессируются в виде части комплекса с молекулами инвариантных цепей CD3. T-клетки, экспрессирующие этот рецептор, называются α:β- (или αβ-) T-клетками, хотя меньшая часть T-клеток, называемая γδ-T-клетками, экспрессирует альтернативный рецептор, образованный вариабельными гамма- (γ-) и дельта- (δ-) цепями.
[0438] В одном варианте осуществления MBM содержат ABM, который специфично связывается с CD3.
7.6.1. ABM для CD3
[0439] MBM (например, TBM) могут содержать ABM, который специфично связывается с CD3. Термин "CD3" относится к корецептору (или корецепторному комплексу, или полипептидной цепи корецепторного комплекса) T-клеточного рецептора, представляющему собой кластер дифференцировки 3. Аминокислотные последовательности полипептидных цепей CD3 человека приведены в NCBI под номерами доступа P04234, P07766 и P09693. Белки CD3 также могут включать в себя варианты. Белки CD3 также могут включать в себя фрагменты. Белки CD3 также содержат посттрансляционные модификации аминокислотных последовательностей CD3. Посттрансляционные модификации включают без ограничения N- и O-связанное гликозилирование.
[0440] В некоторых вариантах осуществления MBM (например, TBM) может содержать ABM, который представляет собой антитело к CD3 (например, как описано в US 2016/0355600, WO 2014/110601 и WO 2014/145806) или его антигенсвязывающий домен. Иллюстративные последовательности VH, VL и scFv для CD3, которые можно применять в MBM (например, TBM), приведены в таблице 12A.
Средства, связывающие CD3 - последовательности вариабельных доменов
[0441] Последовательности CDR для ряда средств, связывающих CD3, которые определены согласно схеме нумерации по Kabat (Kabat et al, 1991, Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, Md.), схеме нумерации по Chothia (Al-Lazikani et al., 1997, J. Mol. Biol 273:927-948) и комбинации схем нумерации по Kabat и по Chothia, приведены в таблицах 12B-12D соответственно.
Средства, связывающие CD3 - последовательности CDR в соответствии со схемой нумерации по Kabat
Средства, связывающие CD3 - последовательности CDR в соответствии со схемой нумерации по Chothia
Средства, связывающие CD3 - последовательности CDR в соответствии с комбинацией схем нумерации по Kabat и по Chothia
[0442] В некоторых вариантах осуществления MBM (например, TBM) может содержать ABM для CD3, который содержит CDR любого из от CD3-1 до CD3-130, которые определены согласно нумерации по Kabat (например, как представлено в таблице 12B). В других вариантах осуществления MBM (например, TBM) может содержать ABM для CD3, который содержит CDR любого из от CD3-1 до CD3-130, которые определены согласно нумерации по Chothia (например, как представлено в таблице 12C). В еще нескольких других вариантах осуществления MBM (например, TBM) может содержать ABM для CD3, который содержит CDR любого из от CD3-1 до CD3-130, которые определены согласно комбинации схем нумерации по Kabat и по Chothia (например, как представлено в таблице 12D).
[0443] В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-1. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-2. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-3. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-4. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-5. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-6. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-7. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-8. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-9. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-10. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-11. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-12. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-13. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-14. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-15. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-16. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-17. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-18. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-19. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-20. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-21. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-22. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-23. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-24. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-25. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-26. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-27. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-28. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-29. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-30. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-31. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-32. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-33. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-34. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-35. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-36. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-37. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-38. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-39. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-40. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-41. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-42. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-43. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-44. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-45. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-46. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-47. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-48. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-49. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-50. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-51. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-52. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-53. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-54. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-55. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-56. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-57. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-58. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-59. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-60. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-61. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-62. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-63. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-64. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-65. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-66. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-67. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-68. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-69. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-70. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-71. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-72. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-73. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-74. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-75. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-76. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-77. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-78. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-79. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-80. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-81. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-82. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-83. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-84. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-85. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-86. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-87. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-88. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-89. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-90. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-91. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-92. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-93. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-94. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-95. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-96. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-97. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-98. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-99. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-100. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-101. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-102. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-103. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-104. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-105. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-106. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-107. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-108. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-109. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-110. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-111. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-112. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-113. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-114. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-115. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-116. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-117. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-118. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-119. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-120. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-121. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-122. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-123. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-124. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-125. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-126. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-127. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-128. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-129. В некоторых вариантах осуществления ABM для CD3 содержит последовательности CDR из CD3-130.
[0444] MBM (например, TBM) может содержать последовательности полных вариабельных участков тяжелых и легких цепей из любого из от CD3-1 до CD3-130. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-1. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-1. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-2. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-3. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-4. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-5. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-6. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-7. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-8. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-9. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-10. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-11. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-12. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-13. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-14. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-15. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-16. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-17. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-18. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-19. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-20. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-21. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-22. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-23. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-24. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-25. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-26. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-27. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-28. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-129. В некоторых вариантах осуществления МBM содержит ABM для CD3, который содержит последовательности VH и VL из CD3-130.
[0445] В дополнение к наборам CDR, описанным в таблицах 12B-12D (т. е. набору из шести CDR для каждого из от CD3-1 до CD3-130), в настоящем изобретении предусмотрены варианты наборов CDR. В одном варианте осуществления набор из 6 CDR может содержать 1, 2, 3, 4 или 5 аминокислотных изменений по сравнению с набором CDR, описанным в таблицах 12B-12D, при условии, что ABM для CD3 все еще способен связываться с антигеном-мишенью, как измерено с помощью по меньшей мере одного из анализа Biacore, анализа поверхностного плазмонного резонанса (SPR) и/или анализа BLI (биослойная интерферометрия, например, анализ Octet).
[0446] В дополнение к вариабельным доменам тяжелой цепи и вариабельным доменам легкой цепи, раскрытым в таблице 12A, которые образуют ABM для CD3, в настоящем изобретении предусмотрены варианты VH- и VL-доменов. В одном варианте осуществления каждый вариант VH- и VL-доменов может содержать от 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 аминокислотных изменений по сравнению с VH- и VL-доменом, представленными в таблице 12A, при условии, что ABM все еще способен связываться с антигеном-мишенью, как измерено с помощью по меньшей мере одного из анализа Biacore, анализа поверхностного плазмонного резонанса (SPR) и/или анализа BLI (биослойная интерферометрия, например, анализ Octet). В другом варианте осуществления варианты VH и VL на по меньшей мере 90, 95, 97, 98 или 99% идентичны соответствующим VH или VL, раскрытым в таблице 12A, при условии, что ABM все еще способен связываться с антигеном-мишенью, как измерено с помощью по меньшей мере одного из анализа Biacore, анализа поверхностного плазмонного резонанса (SPR) и/или анализа BLI (биослойная интерферометрия, например, анализ Octet).
[0447] В некоторых вариантах осуществления MBM может содержать ABM, который представляет собой CD3-связывающую молекулу, как описано в WO 2020/052692, или ее антигенсвязывающий домен. В таблицах с AA по AJ-2 (в совокупности называемых "таблицей A") перечислены последовательности CD3-связывающих молекул, которые могут быть включены в CD3-связывающие ABM.
Консенсусные последовательности CDR тяжелых цепей и легких цепей консенсусной группы № C1
Консенсусные последовательности CDR тяжелых цепей и легких цепей консенсусной группы № C2
Консенсусные последовательности CDR тяжелых цепей и легких цепей консенсусной группы № C3
Средства, связывающие CD3 - последовательности CDR тяжелой цепи в соответствии со схемой нумерации по Kabat
Средства, связывающие CD3 - последовательности CDR легкой цепи в соответствии со схемой нумерации по Kabat
Средства, связывающие CD3 - последовательности CDR тяжелой цепи в соответствии со схемой нумерации по Chothia
Средства, связывающие CD3 - последовательности CDR легкой цепи в соответствии со схемой нумерации по Chothia
Средства, связывающие CD3 - последовательности CDR тяжелой цепи в соответствии со схемой нумерации по IMGT
Средства, связывающие CD3 - последовательности CDR легкой цепи в соответствии со схемой нумерации по IMGT
Средства, связывающие CD3 - последовательности CDR тяжелой цепи в соответствии с комбинацией схем нумерации по Kabat и по Chothia
Средства, связывающие CD3 - последовательности CDR легкой цепи в соответствии с комбинацией схем нумерации по Kabat и по Chothia
Средства, связывающие CD3 - последовательности CDR тяжелой цепи в соответствии с комбинацией схем нумерации по Kabat и по IMGT
Средства, связывающие CD3 - последовательности CDR легкой цепи в соответствии с комбинацией схем нумерации по Kabat и по IMGT
Средства, связывающие CD3 - последовательности CDR тяжелой цепи в соответствии с комбинацией схем нумерации по Chothia и по IMGT
Средства, связывающие CD3 - последовательности CDR легкой цепи в соответствии с комбинацией схем нумерации по Chothia и по IMGT
Средства, связывающие CD3 - последовательности вариабельных участков тяжелой цепи
Средства, связывающие CD3 - последовательности вариабельных участков легкой цепи
[0448] В основе последовательностей CDR группы C1 в таблице AA лежат последовательности CDR по Kabat, последовательности CDR по Chothia, последовательности CDR по IMGT и их комбинации из CD3-связывающих молекул NOV292, NOV589, NOV567 и CD3-связывающих молекул, которые содержат "sp11a" в названии связывающего средства. В основе последовательностей CDR группы C2 в таблице AB лежат последовательности CDR по Kabat, последовательности CDR по Chothia, последовательности CDR по IMGT и их комбинации из CD3-связывающих молекул NOV453, NOV229, NOV580, NOV221 и CD3-связывающих молекул, которые содержат "sp9a" в названии связывающего средства. В основе последовательностей CDR группы C3 в таблице AC лежат последовательности CDR по Kabat, последовательности CDR по Chothia, последовательности CDR по IMGT и их комбинации из CD3-связывающих молекул NOV123, sp10b, NOV110 и NOV832.
[0449] Конкретные последовательности CDR CD3-связывающих молекул, описанных в примерах WO 2020/052692, перечислены в таблицах с AB-1 по AH-2. Последовательности VH и VL, описанные в WO 2020/052692, перечислены в таблице AJ-1 и таблице AJ-2 соответственно.
[0450] В некоторых вариантах осуществления ABM для CD3 может содержать CDR тяжелой цепи, имеющий аминокислотную последовательность любой из консенсусных последовательностей CDR, перечисленных в таблице AA, таблице AB или таблице AC. В конкретных вариантах осуществления ABM для CD3 может содержать один, два, три или более CDR тяжелой цепи (или в качестве альтернативы состоять из них), выбранных из CDR тяжелой цепи, описанных в таблице AA, таблице AB или таблице AC.
[0451] В некоторых вариантах осуществления ABM для CD3 может содержать CDR легкой цепи, имеющий аминокислотную последовательность любой из консенсусных последовательностей CDR, перечисленных в таблице AA, таблице AB или таблице AC. В конкретных вариантах осуществления ABM для CD3 может содержать один, два, три или более CDR легкой цепи (или в качестве альтернативы состоять из них), выбранных из CDR легкой цепи, описанных в таблице AA, таблице AB или таблице AC.
[0452] В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H1, последовательность CDR-H2, последовательность CDR-H3, последовательность CDR-L1, последовательность CDR-L2 и последовательность CDR-L3, представленные в таблице AA.
[0453] В некоторых вариантах осуществления аминокислота, обозначенная как X1 в таблице AA, представляет собой T. В некоторых вариантах осуществления аминокислота, обозначенная как X1 в таблице AA, представляет собой A. В некоторых вариантах осуществления аминокислота, обозначенная как X2 в таблице AA, представляет собой S. В некоторых вариантах осуществления аминокислота, обозначенная как X2 в таблице AA, представляет собой R. В некоторых вариантах осуществления аминокислота, обозначенная как X3 в таблице AA, представляет собой N. В некоторых вариантах осуществления аминокислота, обозначенная как X3 в таблице AA, представляет собой Y. В некоторых вариантах осуществления аминокислота, обозначенная как X3 в таблице AA, представляет собой Q. В некоторых вариантах осуществления аминокислота, обозначенная как X4 в таблице AA, представляет собой H. В некоторых вариантах осуществления аминокислота, обозначенная как X4 в таблице AA, представляет собой S. В некоторых вариантах осуществления аминокислота, обозначенная как X5 в таблице AA, представляет собой M. В некоторых вариантах осуществления аминокислота, обозначенная как X5 в таблице AA, представляет собой L. В некоторых вариантах осуществления аминокислота, обозначенная как X6 в таблице AA, представляет собой K. В некоторых вариантах осуществления аминокислота, обозначенная как X6 в таблице AA, представляет собой R. В некоторых вариантах осуществления аминокислота, обозначенная как X7 в таблице AA, представляет собой S. В некоторых вариантах осуществления аминокислота, обозначенная как X7 в таблице AA, представляет собой K. В некоторых вариантах осуществления аминокислота, обозначенная как X55 в таблице AA, представляет собой F. В некоторых вариантах осуществления аминокислота, обозначенная как X55 в таблице AA, представляет собой Y. В некоторых вариантах осуществления аминокислота, обозначенная как X55 в таблице AA, представляет собой S. В некоторых вариантах осуществления аминокислота, обозначенная как X8 в таблице AA, представляет собой W. В некоторых вариантах осуществления аминокислота, обозначенная как X8 в таблице AA, представляет собой Y. В некоторых вариантах осуществления аминокислота, обозначенная как X8 в таблице AA, представляет собой S. В некоторых вариантах осуществления аминокислота, обозначенная как X8 в таблице AA, представляет собой T. В некоторых вариантах осуществления аминокислота, обозначенная как X9 в таблице AA, представляет собой W. В некоторых вариантах осуществления аминокислота, обозначенная как X9 в таблице AA, представляет собой Y. В некоторых вариантах осуществления аминокислота, обозначенная как X9 в таблице AA, представляет собой S. В некоторых вариантах осуществления аминокислота, обозначенная как X9 в таблице AA, представляет собой T. В некоторых вариантах осуществления аминокислота, обозначенная как X10 в таблице AA, представляет собой H. В некоторых вариантах осуществления аминокислота, обозначенная как X10 в таблице AA, представляет собой Y. В некоторых вариантах осуществления аминокислота, обозначенная как X11 в таблице AA, представляет собой S. В некоторых вариантах осуществления аминокислота, обозначенная как X11 в таблице AA, представляет собой G. В некоторых вариантах осуществления аминокислота, обозначенная как X12 в таблице AA, представляет собой I. В некоторых вариантах осуществления аминокислота, обозначенная как X12 в таблице AA, представляет собой L. В некоторых вариантах осуществления аминокислота, обозначенная как X13 в таблице AA, представляет собой V. В некоторых вариантах осуществления аминокислота, обозначенная как X13 в таблице AA, представляет собой G. В некоторых вариантах осуществления аминокислота, обозначенная как X14 в таблице AA, представляет собой R. В некоторых вариантах осуществления аминокислота, обозначенная как X14 в таблице AA, представляет собой N. В некоторых вариантах осуществления аминокислота, обозначенная как X15 в таблице AA, представляет собой D. В некоторых вариантах осуществления аминокислота, обозначенная как X15 в таблице AA, представляет собой E. В некоторых вариантах осуществления аминокислота, обозначенная как X15 в таблице AA, представляет собой L. В некоторых вариантах осуществления аминокислота, обозначенная как X16 в таблице AA, представляет собой G. В некоторых вариантах осуществления аминокислота, обозначенная как X16 в таблице AA, представляет собой N. В некоторых вариантах осуществления аминокислота, обозначенная как X16 в таблице AA, представляет собой E. В некоторых вариантах осуществления аминокислота, обозначенная как X17 в таблице AA, представляет собой R. В некоторых вариантах осуществления аминокислота, обозначенная как X17 в таблице AA, представляет собой S. В некоторых вариантах осуществления аминокислота, обозначенная как X18 в таблице AA, представляет собой V. В некоторых вариантах осуществления аминокислота, обозначенная как X18 в таблице AA, представляет собой T. В некоторых вариантах осуществления аминокислота, обозначенная как X19 в таблице AA, представляет собой N. В некоторых вариантах осуществления аминокислота, обозначенная как X19 в таблице AA, представляет собой T. В некоторых вариантах осуществления аминокислота, обозначенная как X20 в таблице AA, представляет собой R. В некоторых вариантах осуществления аминокислота, обозначенная как X20 в таблице AA, представляет собой L. В некоторых вариантах осуществления аминокислота, обозначенная как X21 в таблице AA, представляет собой F. В некоторых вариантах осуществления аминокислота, обозначенная как X21 в таблице AA, представляет собой E. В некоторых вариантах осуществления аминокислота, обозначенная как X22 в таблице AA, представляет собой S. В некоторых вариантах осуществления аминокислота, обозначенная как X22 в таблице AA, представляет собой Y. В некоторых вариантах осуществления аминокислота, обозначенная как X23 в таблице AA, представляет собой S. В некоторых вариантах осуществления аминокислота, обозначенная как X23 в таблице AA, представляет собой Y. В некоторых вариантах осуществления аминокислота, обозначенная как X24 в таблице AA, представляет собой S. В некоторых вариантах осуществления аминокислота, обозначенная как X24 в таблице AA, представляет собой A. В некоторых вариантах осуществления аминокислота, обозначенная как X25 в таблице AA, представляет собой H. В некоторых вариантах осуществления аминокислота, обозначенная как X25 в таблице AA, представляет собой T. В некоторых вариантах осуществления аминокислота, обозначенная как X26 в таблице AA, представляет собой F. В некоторых вариантах осуществления аминокислота, обозначенная как X26 в таблице AA, представляет собой Y. В некоторых вариантах осуществления аминокислота, обозначенная как X27 в таблице AA, представляет собой W. В некоторых вариантах осуществления аминокислота, обозначенная как X27 в таблице AA, представляет собой Y.
[0454] В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H1 из C1-1. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H1 из C1-2. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H1 из C1-3. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H1 из C1-4.
[0455] В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H2 из C1-5. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H2 из C1-6. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H2 из C1-7.
[0456] В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H3 из C1-8. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H3 из C1-9. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H3 из C1-10. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H3 из C1-11.
[0457] В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L1 из C1-12. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L1 из C1-13. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L1 из C1-14. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L1 из C1-15. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L1 из C1-16. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L1 из C1-17.
[0458] В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L2 из C1-18. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L2 из C1-19.
[0459] В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L3 из C1-20. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L3 из C1-21. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L3 из C1-22. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L3 из C1-23.
[0460] В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H1, последовательность CDR-H2, последовательность CDR-H3, последовательность CDR-L1, последовательность CDR-L2 и последовательность CDR-L3, представленные в таблице AB.
[0461] В некоторых вариантах осуществления аминокислота, обозначенная как X28 в таблице AB, представляет собой V. В некоторых вариантах осуществления аминокислота, обозначенная как X28 в таблице AB, представляет собой I. В некоторых вариантах осуществления аминокислота, обозначенная как X29 в таблице AB, представляет собой F. В некоторых вариантах осуществления аминокислота, обозначенная как X29 в таблице AB, представляет собой Y. В некоторых вариантах осуществления аминокислота, обозначенная как X30 в таблице AB, представляет собой N. В некоторых вариантах осуществления аминокислота, обозначенная как X30 в таблице AB, представляет собой S. В некоторых вариантах осуществления аминокислота, обозначенная как X31 в таблице AB, представляет собой A. В некоторых вариантах осуществления аминокислота, обозначенная как X31 в таблице AB, представляет собой S. В некоторых вариантах осуществления аминокислота, обозначенная как X32 в таблице AB, представляет собой T. В некоторых вариантах осуществления аминокислота, обозначенная как X32 в таблице AB, представляет собой K. В некоторых вариантах осуществления аминокислота, обозначенная как X33 в таблице AB, представляет собой T. В некоторых вариантах осуществления аминокислота, обозначенная как X33 в таблице AB, представляет собой A. В некоторых вариантах осуществления аминокислота, обозначенная как X34 в таблице AB, представляет собой S. В некоторых вариантах осуществления аминокислота, обозначенная как X34 в таблице AB, представляет собой R. В некоторых вариантах осуществления аминокислота, обозначенная как X35 в таблице AB, представляет собой N. В некоторых вариантах осуществления аминокислота, обозначенная как X35 в таблице AB, представляет собой G. В некоторых вариантах осуществления аминокислота, обозначенная как X36 в таблице AB, представляет собой S. В некоторых вариантах осуществления аминокислота, обозначенная как X36 в таблице AB, представляет собой A. В некоторых вариантах осуществления аминокислота, обозначенная как X37 в таблице AB, представляет собой A. В некоторых вариантах осуществления аминокислота, обозначенная как X37 в таблице AB, представляет собой T. В некоторых вариантах осуществления аминокислота, обозначенная как X37 в таблице AB, представляет собой S. В некоторых вариантах осуществления аминокислота, обозначенная как X38 в таблице AB, представляет собой N. В некоторых вариантах осуществления аминокислота, обозначенная как X38 в таблице AB, представляет собой D. В некоторых вариантах осуществления аминокислота, обозначенная как X39 в таблице AB, представляет собой N. В некоторых вариантах осуществления аминокислота, обозначенная как X39 в таблице AB, представляет собой K. В некоторых вариантах осуществления аминокислота, обозначенная как X40 в таблице AB, представляет собой D. В некоторых вариантах осуществления аминокислота, обозначенная как X40 в таблице AB, представляет собой N. В некоторых вариантах осуществления аминокислота, обозначенная как X41 в таблице AB, представляет собой H. В некоторых вариантах осуществления аминокислота, обозначенная как X41 в таблице AB, представляет собой N. В некоторых вариантах осуществления аминокислота, обозначенная как X42 в таблице AB, представляет собой Q. В некоторых вариантах осуществления аминокислота, обозначенная как X42 в таблице AB, представляет собой E. В некоторых вариантах осуществления аминокислота, обозначенная как X43 в таблице AB, представляет собой R. В некоторых вариантах осуществления аминокислота, обозначенная как X43 в таблице AB, представляет собой S. В некоторых вариантах осуществления аминокислота, обозначенная как X43 в таблице AB, представляет собой G.
[0462] В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H1 из C2-1. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H1 из C2-2. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H1 из C2-3. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H1 из C2-4.
[0463] В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H2 из C2-5. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H2 из C2-6. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H2 из C2-7.
[0464] В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H3 из C2-8. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H3 из C2-9.
[0465] В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L1 из C2-10. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L1 из C2-11. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L1 из C2-12.
[0466] В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L2 из C2-13. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L2 из C2-14. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L2 из C2-15.
[0467] В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L3 из C2-16. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L3 из C2-17.
[0468] В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H1, последовательность CDR-H2, последовательность CDR-H3, последовательность CDR-L1, последовательность CDR-L2 и последовательность CDR-L3, представленные в таблице AC.
[0469] В некоторых вариантах осуществления аминокислота, обозначенная как X44 в таблице AC, представляет собой G. В некоторых вариантах осуществления аминокислота, обозначенная как X44 в таблице AC, представляет собой A. В некоторых вариантах осуществления аминокислота, обозначенная как X45 в таблице AC, представляет собой H. В некоторых вариантах осуществления аминокислота, обозначенная как X45 в таблице AC, представляет собой N. В некоторых вариантах осуществления аминокислота, обозначенная как X46 в таблице AC, представляет собой D. В некоторых вариантах осуществления аминокислота, обозначенная как X46 в таблице AC, представляет собой G. В некоторых вариантах осуществления аминокислота, обозначенная как X47 в таблице AC, представляет собой A. В некоторых вариантах осуществления аминокислота, обозначенная как X47 в таблице AC, представляет собой G. В некоторых вариантах осуществления аминокислота, обозначенная как X48 в таблице AC, представляет собой N. В некоторых вариантах осуществления аминокислота, обозначенная как X48 в таблице AC, представляет собой K. В некоторых вариантах осуществления аминокислота, обозначенная как X49 в таблице AC, представляет собой V. В некоторых вариантах осуществления аминокислота, обозначенная как X49 в таблице AC, представляет собой A. В некоторых вариантах осуществления аминокислота, обозначенная как X50 в таблице AC, представляет собой N. В некоторых вариантах осуществления аминокислота, обозначенная как X50 в таблице AC, представляет собой V. В некоторых вариантах осуществления аминокислота, обозначенная как X51 в таблице AC, представляет собой A. В некоторых вариантах осуществления аминокислота, обозначенная как X51 в таблице AC, представляет собой V. В некоторых вариантах осуществления аминокислота, обозначенная как X52 в таблице AC, представляет собой Y. В некоторых вариантах осуществления аминокислота, обозначенная как X52 в таблице AC, представляет собой F. В некоторых вариантах осуществления аминокислота, обозначенная как X53 в таблице AC, представляет собой I. В некоторых вариантах осуществления аминокислота, обозначенная как X53 в таблице AC, представляет собой V. В некоторых вариантах осуществления аминокислота, обозначенная как X54 в таблице AC, представляет собой I. В некоторых вариантах осуществления аминокислота, обозначенная как X54 в таблице AC, представляет собой H.
[0470] В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H1 из C3-1. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H1 из C3-2. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H1 из C3-3. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H1 из C3-4.
[0471] В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H2 из C3-5. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H2 из C3-6. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H2 из C3-7.
[0472] В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H3 из C3-8. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-H3 из C3-9.
[0473] В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L1 из C3-10. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L1 из C3-11. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L1 из C3-12.
[0474] В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L2 из C3-13. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L2 из C3-14.
[0475] В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L3 из C3-15. В некоторых вариантах осуществления ABM для CD3 может содержать последовательность CDR-L3 из C3-16.
[0476] В некоторых вариантах осуществления ABM для CD3 может содержать последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице AD-1, и соответствующие последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице AD-2.
[0477] В некоторых вариантах осуществления ABM для CD3 может содержать последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице AE-1, и соответствующие последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице AE-2.
[0478] В некоторых вариантах осуществления ABM для CD3 может содержать последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице AF-1, и соответствующие последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице AF-2.
[0479] В некоторых вариантах осуществления ABM для CD3 может содержать последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице AG-1, и соответствующие последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице AG-2.
[0480] В некоторых вариантах осуществления ABM для CD3 может содержать последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице AH-1, и соответствующие последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице AH-2.
[0481] В некоторых вариантах осуществления ABM для CD3 может содержать последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице AI-1, и соответствующие последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице AI-2.
[0482] В некоторых вариантах осуществления ABM для CD3 может содержать CDR тяжелой цепи, имеющий аминокислотную последовательность любого из CDR, перечисленных в таблице AB-1, таблице AC-1, таблице AD-1, таблице AE-1, таблице AF-1, таблице AG-1, таблице AH-1 или таблице AI-1. В конкретных вариантах осуществления ABM для CD3 может содержать один, два, три или более CDR тяжелой цепи (или в качестве альтернативы состоять из них), выбранных из CDR тяжелой цепи, описанных в таблице AB-1, таблице AC-1, таблице AD-1, таблице AE-1, таблице AF-1, таблице AG-1, таблице AH-1 и таблице AI-1.
[0483] В некоторых вариантах осуществления ABM для CD3 может содержать CDR легкой цепи, имеющий аминокислотную последовательность любого из CDR, перечисленных в таблице AB-2, таблице AC-2, таблице AD-2, таблице AE-2, таблице AF-2, таблице AG-2, таблице AH-2 или таблице AI-2. В конкретных вариантах осуществления ABM для CD3 может содержать один, два, три или более CDR легкой цепи (или в качестве альтернативы состоять из них), выбранных из CDR легкой цепи, описанных в таблице AB-2, таблице AC-2, таблице AD-2, таблице AE-2, таблице AF-2, таблице AG-2, таблице AH-2 и таблице AI-2.
[0484] Другие ABM для CD3 содержат аминокислоты, которые были подвергнуты мутации, но при этом они характеризуются по меньшей мере 80-, 85-, 90-, 95-, 96-, 97-, 98- или 99-процентной идентичностью CDR-участков с последовательностями CDR, описанными в таблице A. В некоторых вариантах осуществления такие ABM для CD3 содержат мутантные аминокислотные последовательности, в которых не более 1, 2, 3, 4 или 5 аминокислот были подвергнуты мутации в CDR-участках по сравнению с последовательностями CDR, описанными в таблице A.
[0485] В некоторых вариантах осуществления ABM для CD3 может содержать VH- и/или VL-домен, имеющий аминокислотную последовательность любого VH- и/или VL-домена, описанного в таблице A. Другие ABM для CD3 содержат VH- и/или VL-домены, содержащие аминокислотные последовательности, характеризующиеся по меньшей мере 80-, 85-, 90-, 95-, 96-, 97-, 98- или 99-процентной идентичностью с последовательностями VH и/или VL, описанными в таблице A. В некоторых вариантах осуществления ABM для CD3 содержат VH- и/или VL-домены, в которых не более 1, 2, 3, 4 или 5 аминокислот были подвергнуты мутации по сравнению с VH- и/или VL-доменами, показанными в последовательностях, описанных в таблице A, при этом они сохраняют по существу такую же терапевтическую активность.
[0486] Последовательности VH и VL (аминокислотные последовательности и нуклеотидные последовательности, кодирующие аминокислотные последовательности) могут быть подвергнуты "смешиванию и подбору" для создания других ABM для CD3. Такие подвергнутые "смешиванию и подбору" ABM для CD3 можно тестировать с применением анализов связывания, известных из уровня техники (например, анализов методом FACS). Когда цепи подвергают смешиванию и подбору, последовательность VH из конкретной пары VH/VL следует заменить на структурно сходную последовательность VH. Последовательность VL из конкретной пары VH/VL следует заменить на структурно сходную последовательность VL.
[0487] Соответственно, в одном варианте осуществления ABM для CD3 содержит вариабельный участок тяжелой цепи (VH), содержащий аминокислотную последовательность, выбранную из любой из последовательностей VH, описанных в таблице A-J1; и вариабельный участок легкой цепи (VL), содержащий аминокислотную последовательность, описанную в таблице A-J2.
[0488] В некоторых вариантах осуществления в основе антигенсвязывающего домена, который специфично связывается с CD3 человека, лежит молекула, отличная от иммуноглобулина, и вместо этого он получен из каркасного белка, отличного от антитела, например, из одного из каркасных белков, отличных от антител, описанных в разделе 7.2.2. В одном варианте осуществления антигенсвязывающий домен, который специфично связывается с CD3 человека, включает в себя аффилин-144160, который описан в WO 2017/013136. Аффилин-144160 имеет следующую аминокислотную последовательность:
MQIFVKTLTGKTITLEVEPSDTIENVKAKIQDKEGIPPDQQWLWFAGKQLEDGRTLSDYNIQKESTLKLWLVDKAAMQIFVYTRTGKTITLEVEPSDTIENVKAKIQDKEGIPPDQQRLIWAGKQLEDGRTLSDYNIALESGLHLVLRLRAA (SEQ ID NO: 498)
7.6.2. ABM для TCRα/β
[0489] MBM (например, TBM) могут содержать ABM, который специфично связывается с α-цепью TCR, β-цепью TCR или димером TCR-αβ. Известны иллюстративные антитела к TCRα/β (см., например, US 2012/0034221; Borst et al., 1990, Hum Immunol. 29(3):175-88 (в которых описано антитело BMA031)). Последовательности VH, VL и CDR по Kabat из антитела BMA031 приведены в таблице 13.
Последовательности BMA031
[0490] В одном варианте осуществления ABM2 может содержать последовательности CDR антитела BMA031. В других вариантах осуществления ABM2 может содержать последовательности VH и VL антитела BMA031.
7.6.3. ABM для TCRγ/δ
[0491] MBM (например, TBM) могут содержать ABM, который специфично связывается с γ-цепью TCR, δ-цепью TCR или димером TCR-γδ. Известны иллюстративные антитела к TCR-γ/δ (см., например, патент США № 5980892 (в котором описано δTCS1, полученное с помощью гибридомы, депонированной в ATCC под номером доступа HB 9578)).
7.7. ABM для CD2
7.7.1. ABM для CD2 на основе иммуноглобулинов
[0492] MBM (например, TBM) может содержать ABM, который представляет собой антитело к CD2 или его антигенсвязывающий домен. Известны иллюстративные антитела к CD2 (см., например, US 6849258, CN102827281A, US 2003/0139579 A1 и US 5795572). В таблице 14 приведены иллюстративные последовательности CDR, VH и VL, которые можно включать в антитела к CD2 или их антигенсвязывающие фрагменты для применения в MBM по настоящему изобретению.
Средства, связывающие CD2, на основе иммуноглобулинов
[0493] В некоторых вариантах осуществления ABM для CD2 содержит последовательности CDR из CD2-1 (SEQ ID NO: 505-510). В некоторых вариантах осуществления ABM для CD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD2-1 (SEQ ID NO: 511-512). В некоторых вариантах осуществления ABM для CD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из hu1CD2-1 (SEQ ID NO: 513-514). В некоторых вариантах осуществления ABM для CD2 содержит последовательности вариабельных участков тяжелой и легкой цепей из hu2CD2-1 (SEQ ID NO: 511 и 514 соответственно).
[0494] В других вариантах осуществления ABM для CD2 может содержать последовательности CDR антитела 9D1, полученного с помощью гибридомы, депонированной в Главном микробиологическом центре Китайского комитета по коллекциям культур 16 мая 2012 года под номером доступа CGMCC 6132, и которое описано в CN102827281A. В других вариантах осуществления ABM для CD2 может содержать последовательности CDR антитела LO-CD2b, полученного с помощью гибридомы, депонированной в Американской коллекции типовых культур 22 июня 1999 года под номером доступа PTA-802, и которое описано в US 2003/0139579 A1. В еще нескольких других вариантах осуществления ABM для CD2 может содержать последовательности CDR из SFv-Ig для CD2, полученного посредством экспрессии конструкции, клонированной в рекомбинантной E. coli, депонированной в ATCC 9 апреля 1993 года под номером доступа 69277, и который описан в US 5795572.
[0495] В других вариантах осуществления ABM для CD2 может содержать последовательности VH и VL антитела 9D1. В других вариантах осуществления ABM для CD2 может содержать последовательности VH и VL антитела LO-CD2b. В еще нескольких вариантах осуществления ABM для CD2 может содержать последовательности VH и VL SFv-Ig для CD2, полученного посредством экспрессии конструкции, клонированной в рекомбинантной E. coli, имеющей номер доступа в ATCC 69277.
7.7.2. ABM для CD2 на основе CD58
[0496] В определенных аспектах в настоящем изобретении предусмотрена MBM, содержащая ABM для CD2, который представляет собой лиганд. ABM для CD2 специфично связывается с CD2 человека, природным лигандом которого является CD58, также известный как LFA-3. Белки CD58/LFA-3 представляют собой гликопротеины, которые экспрессируются на поверхности различных типов клеток (Dustin et al., 1991, Annu. Rev. Immunol. 9:27) и играют роли в опосредовании взаимодействий T-клеток с APC как антигензависимым, так и антигеннезависимым образом (Wallner et al., 1987, J. Exp. Med. 166:923). Соответственно, в определенных аспектах ABM для CD2 представляет собой фрагмент CD58. Как используется в данном документе, фрагмент CD58 содержит аминокислотную последовательность, характеризующуюся по меньшей мере 70% идентичностью последовательности с CD2-связывающей частью CD58, например, по меньшей мере 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичностью с CD2-связывающей частью CD58. Последовательность CD58 человека имеет идентификатор Uniprot P19256 (www.uniprot.org/uniprot/P19256). Было установлено, что фрагменты CD58, содержащие аминокислотные остатки 30-123 полноразмерного CD58 (т. е. последовательность, обозначенную как CD58-6 в таблице 15 ниже), являются достаточными для связывания с CD2. Wang et al., 1999, Cell 97:791-803. Соответственно, в определенных аспектах фрагмент CD58 содержит аминокислотную последовательность, характеризующуюся по меньшей мере 70% идентичностью последовательности с аминокислотами 30-123 из CD58, например, по меньшей мере 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичностью с аминокислотной последовательностью, обозначенной как CD58-6.
[0497] Взаимодействия между CD58 и CD2 были картированы с помощью рентгеноструктурной кристаллографии и молекулярного моделирования. Замена остатков E25, K29, K30, K32, D33, K34, E37, D84 и K87 (где нумерация относится к зрелому полипептиду) приводит к снижению связывания с CD2. Ikemizu et al., 1999, Proc. Natl. Acad. Sci. USA 96:4289-94. Соответственно, в некоторых вариантах осуществления фрагмент CD58 сохраняет остатки дикого типа в положениях E25, K29, K30, K32, D33, K34, E37, D84 и K87.
[0498] В отличие от этого, следующие замены (где нумерация относится к полноразмерному полипептиду) не оказывали влияния на связывание с CD2: F29S; V37K; V49Q; V86K; T113S и L121G. Соответственно, фрагмент CD58 может содержать одну, две, три, четыре, пять или все шесть из вышеуказанных замен.
[0499] В некоторых вариантах осуществления фрагмент CD58 сконструирован так, что он содержит замены в виде пары остатков цистеина, которые при рекомбинантной экспрессии образуют дисульфидный мостик. Иллюстративные пары аминокислот, которые могут быть заменены остатками цистеина для образования дисульфидного мостика при экспрессии (где нумерация относится к полноразмерному полипептиду), представляют собой: (а) замену V45C и замену M105C; (b) замену V54C и замену G88C; (c) замену V45C и замену M114C и (d) замену W56C и замену L90C.
[0500] Иллюстративные фрагменты CD58 приведены в таблице 15 ниже.
Последовательности CD58
B=F или S
J= V или K
O=V или Q
U=V или K
X= T или S
Z= L или G
Ig-V-подобный домен
Ig-V-подобный домен
J= V или K
O=V или Q
Ig-V-подобный домен
Ig-V-подобный домен
Ig-V-подобный домен
Ig-V-подобный домен
7.7.3. ABM для CD2 на основе CD48
[0501] В определенных аспектах в настоящем изобретении предусмотрена MBM, содержащая ABM для CD2, который представляет собой фрагмент CD48. Как используется в данном документе, фрагмент CD48 содержит аминокислотную последовательность, характеризующуюся по меньшей мере 70% идентичностью последовательности с CD2-связывающей частью CD48, например, по меньшей мере 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичностью с CD2-связывающей частью CD48. Последовательность CD48 человека имеет идентификатор Uniprot P09326 (www.uniprot.org/uniprot/P09326) и содержит сигнальный пептид (аминокислоты 1-26) и GPI-якорь (аминокислоты 221-243). В определенных аспектах фрагмент CD48 содержит аминокислотную последовательность, характеризующуюся по меньшей мере 70% идентичностью последовательности (например, по меньшей мере 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичностью) с аминокислотной последовательностью, состоящей из аминокислот 27-220 из последовательности с идентификатором Uniprot P09326. CD48 человека имеет Ig-подобный домен 1 C2-типа (аминокислоты 29-127 из последовательности с идентификатором Uniprot P09326) и Ig-подобный домен 2 C2-типа (аминокислоты 132-212 из последовательности с идентификатором Uniprot P09326). Соответственно, в некоторых вариантах осуществления фрагмент CD48 содержит аминокислотную последовательность, характеризующуюся по меньшей мере 70% идентичностью последовательности (например, по меньшей мере 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичностью) с аминокислотной последовательностью, состоящей из аминокислот 29-212 из последовательности с идентификатором Uniprot P09326, с доменом 1 C2-типа (аминокислоты 29-127 из последовательности с идентификатором Uniprot P09326) и/или с Ig-подобным доменом 2 C2-типа (аминокислоты 132-212 из последовательности с идентификатором Uniprot P09326). Фрагмент CD48 в некоторых вариантах осуществления может содержать один или более природных вариантов, родственных последовательности с идентификатором Uniprot P09326. Например, фрагмент CD48 может содержать замену E102Q. В качестве другого примера фрагмент CD48 может содержать аминокислотную последовательность, соответствующую изоформе CD-48 или ее CD2-связывающей части, например, изоформе, имеющей идентификатор Uniprot P09326-2, или ее CD2-связывающей части.
7.8. ABM для опухолеассоциированных антигенов
[0502] MBM (например, TBM) могут содержать ABM, который специфично связывается с опухолеассоциированным антигеном (TAA). В некоторых вариантах осуществления TAA представляет собой TAA человека. Антиген может присутствовать или не присутствовать на нормальных клетках. В определенных вариантах осуществления TAA предпочтительно экспрессируется или характеризуется повышенным уровнем экспрессии на поверхности опухолевых клеток по сравнению с нормальными клетками. В других вариантах осуществления TAA представляет собой маркер линии дифференцировки.
[0503] В определенных вариантах осуществления TAA экспрессируется или характеризуется повышенным уровнем экспрессии на раковых В-клетках по сравнению с нормальными B-клетками. В других вариантах осуществления TAA представляет собой маркер В-клеточной линии дифференцировки.
[0504] Предполагается, что на любой тип В-клеточного злокачественного новообразования могут нацеливаться МBM по настоящему изобретению. Иллюстративные типы В-клеточных злокачественных новообразований, на которые может происходить нацеливание, включают формы лимфомы Ходжкина, неходжкинские лимфомы (NHL) и множественную миелому. Примеры NHL включают диффузную крупноклеточную В-клеточную лимфому (DLBCL), фолликулярную лимфому, хронический лимфоцитарный лейкоз (CLL)/мелкоклеточную лимфоцитарную лимфому (SLL), мантийноклеточную лимфому (MCL), формы лимфомы из клеток маргинальной зоны, лимфому Беркитта, лимфоплазмоцитарную лимфому (макроглобулинемию Вальденстрема), волосатоклеточный лейкоз, первичную лимфому центральной нервной системы (CNS), первичную медиастинальную крупноклеточную В-клеточную лимфому, медиастинальную лимфому "серой зоны" (MGZL), B-клеточную лимфому из клеток маргинальной зоны селезенки, внеузловую B-клеточную лимфому из клеток маргинальной зоны MALT, узловую B-клеточную лимфому из клеток маргинальной зоны и первичную эффузионную лимфому.
[0505] Примеры TAA, на которые могут нацеливаться MBM (например, TBM), включают CD19, CD20, CD22, CD123, CD33, CLL1, CD138 (также известный как синдекан 1, SDC1), CS1, CD38, CD133, FLT3, CD52, TNFRSF13C (представителя 13С суперсемейства рецепторов TNF, также называемого в данной области техники BAFFR - рецептором фактора активации В-клеток), TNFRSF13B (представителя 13В суперсемейства рецепторов TNF, также называемого в данной области техники TACI - трансмембранным активатором и партнером CAML), CXCR4 (хемокиновый рецептор 4 с мотивом С-Х-С), PD-L1 (лиганд 1 белка запрограммированной клеточной гибели), LY9 (лимфоцитарный антиген 9, также называемый CD229 в данной области техники), CD200, FCGR2B (фрагмент Fc-рецептора IIb IgG, также называемый CD32b в данной области техники), CD21, CD23, CD24, CD40L, CD72, CD79a и CD79b. В некоторых вариантах осуществления TAA представляет собой CD19. В некоторых вариантах осуществления TAA представляет собой CD20. В некоторых вариантах осуществления TAA представляет собой CD22. В некоторых вариантах осуществления TAA представляет собой CD123. В некоторых вариантах осуществления TAA представляет собой CD33. В некоторых вариантах осуществления TAA представляет собой CLL1. В некоторых вариантах осуществления TAA представляет собой CD138. В некоторых вариантах осуществления TAA представляет собой CS1. В некоторых вариантах осуществления TAA представляет собой CD38. В некоторых вариантах осуществления TAA представляет собой CD133. В некоторых вариантах осуществления TAA представляет собой FLT3. В некоторых вариантах осуществления TAA представляет собой CD52. В некоторых вариантах осуществления TAA представляет собой TNFRSF13C. В некоторых вариантах осуществления TAA представляет собой TNFRSF13B. В некоторых вариантах осуществления TAA представляет собой CXCR4. В некоторых вариантах осуществления TAA представляет собой PD-L1. В некоторых вариантах осуществления TAA представляет собой LY9. В некоторых вариантах осуществления TAA представляет собой CD200. В некоторых вариантах осуществления TAA представляет собой CD21. В некоторых вариантах осуществления TAA представляет собой CD23. В некоторых вариантах осуществления TAA представляет собой CD24. В некоторых вариантах осуществления TAA представляет собой CD40L. В некоторых вариантах осуществления TAA представляет собой CD72. В некоторых вариантах осуществления TAA представляет собой CD79a. В некоторых вариантах осуществления TAA представляет собой CD79b.
[0506] TАА-связывающий ABM может включать в себя, например, антитело к TAA или его антигенсвязывающий фрагмент. Антитело к TAA или антигенсвязывающий фрагмент могут содержать, например, последовательности CDR антитела, представленного в таблице 16. В некоторых вариантах осуществления антитело к TAA или его антигенсвязывающий домен имеют последовательности вариабельных участков тяжелой и легкой цепей антитела, представленного в таблице 16.
Иллюстративные антитела к опухолеассоциированным антигенам
[0507] В определенных вариантах осуществления TAA выбран из CD19 и CD20. В некоторых вариантах осуществления TAA представляет собой CD19. CD19 представляет собой B-клеточный маркер человека и обнаруживается на зрелых B-клетках, но не на плазматических клетках. CD19 экспрессируется во время раннего развития пре-B-клеток и остается до дифференцировки в плазматические клетки. CD19 экспрессируется как на нормальных B-клетках, так и на раковых B-клетках, аномальный рост которых может привести к развитию B-клеточных лимфом. Например, CD19 экспрессируется на раковых опухолях из клеток B-клеточной линии дифференцировки, включающих без ограничения неходжкинскую лимфому (B-NHL), хронический лимфоцитарный лейкоз и острый лимфобластный лейкоз.
[0508] В определенных аспектах MBM (например, TBM) содержит ABM3, который специфично связывается с CD19. Иллюстративные последовательности CDR и вариабельных доменов, которые могут быть включены в состав ABM, который специфично связывается с CD19, представлены в таблице 17 ниже.
Средства, связывающие CD19
[0509] В определенных аспектах ABM3 содержит CDR тяжелой цепи, имеющие аминокислотные последовательности CD19-H1, CD19-H2A и CD19-H3, представленные в таблице 17, и CDR легкой цепи, имеющие аминокислотные последовательности CD19-L1, CD19-L2 и CD19-L3, представленные в таблице 17. В одном варианте осуществления ABM3 содержит вариабельный участок тяжелой цепи, имеющий аминокислотные последовательности VHA, представленные в таблице 17, и вариабельный участок легкой цепи, имеющий аминокислотные последовательности VLA, представленные в таблице 17.
[0510] В других аспектах ABM3 содержит CDR тяжелой цепи, имеющие аминокислотные последовательности CD19-H1, CD19-H2B и CD19-H3, представленные в таблице 17, и CDR легкой цепи, имеющие аминокислотные последовательности CD19-L1, CD19-L2 и CD19-L3, представленные в таблице 17. В одном варианте осуществления ABM3 содержит вариабельный участок тяжелой цепи, имеющий аминокислотные последовательности VHB, представленные в таблице 17, и вариабельный участок легкой цепи, имеющий аминокислотные последовательности VLB, представленные в таблице 17.
[0511] В дополнительных аспектах ABM3 содержит CDR тяжелой цепи, имеющие аминокислотные последовательности CD19-H1, CD19-H2C и CD19-H3, представленные в таблице 17, и CDR легкой цепи, имеющие аминокислотные последовательности CD19-L1, CD19-L2 и CD19-L3, представленные в таблице 17. В одном варианте осуществления ABM3 содержит вариабельный участок тяжелой цепи, имеющий аминокислотные последовательности VHC, представленные в таблице 17, и вариабельный участок легкой цепи, имеющий аминокислотные последовательности VLB, представленные в таблице 17.
[0512] В дополнительных аспектах ABM3 содержит CDR тяжелой цепи, имеющие аминокислотные последовательности CD19-H1, CD19-H2D и CD19-H3, представленные в таблице 17, и CDR легкой цепи, имеющие аминокислотные последовательности CD19-L1, CD19-L2 и CD19-L3, представленные в таблице 17. В одном варианте осуществления ABM3 содержит вариабельный участок тяжелой цепи, имеющий аминокислотные последовательности VHD, представленные в таблице 17, и вариабельный участок легкой цепи, имеющий аминокислотные последовательности VLB, представленные в таблице 17.
[0513] В еще нескольких дополнительных аспектах ABM3 представлен в форме scFv. Иллюстративные scFv антител к CD19 содержат аминокислотную последовательность любого из от CD19-scFv1 до CD19-scFv12, представленных в таблице 17.
7.9. Нуклеиновые кислоты и клетки-хозяева
[0514] В другом аспекте в настоящем изобретении предусмотрены нуклеиновые кислоты (т. е. полинуклеотиды), кодирующие MBM (например, TBM) по настоящему изобретению. В некоторых вариантах осуществления МBM кодируются одной нуклеиновой кислотой. В других вариантах осуществления МBM кодируются совокупностью (например, двумя, тремя, четырьмя или больше) нуклеиновых кислот.
[0515] Одна нуклеиновая кислота может кодировать MBM, которая содержит одну полипептидную цепь, MBM, которая содержит две или более полипептидные цепи, или часть MBM, которая содержит более двух полипептидных цепей (например, одна нуклеиновая кислота может кодировать две полипептидные цепи TBM, содержащей три, четыре или больше полипептидных цепей, или три полипептидные цепи TBM, содержащей четыре или больше полипептидных цепей). Для индивидуального контроля экспрессии открытые рамки считывания, кодирующие две или более полипептидные цепи, могут находиться под контролем отдельных элементов, регулирующих транскрипцию (например, промоторов и/или энхансеров). Открытые рамки считывания, кодирующие два или более полипептида, могут также находиться под контролем одних и тех же элементов, регулирующих транскрипцию, и могут быть отделены последовательностями внутреннего участка посадки рибосомы (IRES), что обеспечивает возможность трансляции с образованием отдельных полипептидов.
[0516] В некоторых вариантах осуществления MBM, содержащая две или более полипептидные цепи, кодируется двумя или более нуклеиновыми кислотами. Количество нуклеиновых кислот, кодирующих МBM, может равняться количеству полипептидных цепей в MBM (например, если более чем одна полипептидная цепь кодируется одной нуклеиновой кислотой) или быть меньшим, чем это количество.
[0517] Нуклеиновые кислоты могут представлять собой ДНК или РНК (например, мРНК).
[0518] В другом аспекте в настоящем изобретении предусмотрены клетки-хозяева и векторы, содержащие нуклеиновые кислоты по настоящему изобретению. Нуклеиновые кислоты могут присутствовать в одном векторе или отдельных векторах, присутствующих в одной и той же клетке-хозяине или отдельных клетках-хозяевах, как более подробно описано в данном документе ниже.
7.9.1. Векторы
[0519] В настоящем изобретении предусмотрены векторы, содержащие нуклеотидные последовательности, кодирующие MBM (например, TBM) или компонент МBM, описанные в данном документе. В одном варианте осуществления векторы содержат нуклеотиды, кодирующие ABM на основе иммуноглобулина, описанный в данном документе. В одном варианте осуществления векторы содержат нуклеотиды, кодирующие Fc-домен, описанный в данном документе. В одном варианте осуществления векторы содержат нуклеотиды, кодирующие рекомбинантный ABM на основе молекулы, отличной от иммуноглобулина, описанный в данном документе. Вектор может кодировать один или более ABM, один или более Fc-доменов, один или более ABM на основе молекул, отличных от иммуноглобулинов, или любую их комбинацию (например, если несколько компонентов или субкомпонентов кодируются в виде одной полипептидной цепи). В одном варианте осуществления векторы содержат нуклеотидные последовательности, описанные в данном документе. Векторы включают без ограничения вирус, плазмиду, космиду, фаг лямбда или искусственную хромосому дрожжей (YAC).
[0520] Можно использовать многочисленные векторные системы. Например, в одном классе векторов используются ДНК-элементы, которые получены из вирусов животных, таких как, например, вирус папилломы крупного рогатого скота, вирус полиомы, аденовирус, вирус осповакцины, бакуловирус, ретровирусы (вирус саркомы Рауса, MMTV или MOMLV) или вирус SV40. В другом классе векторов используются РНК-элементы, полученные из РНК-содержащих вирусов, таких как вирус леса Семлики, вирус восточного энцефалита лошадей и флавивирусы.
[0521] Кроме того, клетки, которые стабильно интегрировали ДНК в свои хромосомы, могут быть отобраны посредством введения одного или более маркеров, которые обеспечивают возможность отбора трансфицированных клеток-хозяев. Маркер может обеспечивать, например, прототрофность для ауксотрофного хозяина, устойчивость к биоцидам (например, антибиотикам) или устойчивость к тяжелым металлам, таким как медь и т. п. Селектируемый маркерный ген может быть непосредственно связан с последовательностями ДНК, которые должны экспрессироваться, либо введен в ту же самую клетку путем котрансформации. Дополнительные элементы также могут быть необходимы для оптимального синтеза мРНК. Эти элементы могут включать в себя сигналы сплайсинга, а также промоторы транскрипции, энхансеры и сигналы терминации.
[0522] После того, как вектор экспрессии или последовательность ДНК, содержащие конструкции, были подготовлены для экспрессии, векторами экспрессии можно трансфицировать соответствующую клетку-хозяина или векторы экспрессии можно вводить в соответствующую клетку-хозяина. Для достижения этого можно использовать различные методики, такие как, например, слияние протопластов, осаждение фосфатом кальция, электропорация, ретровирусная трансдукция, вирусная трансфекция, генная пушка, трансфекция с использованием липидов или другие традиционные методики. Способы и условия культивирования полученных в результате трансфицированных клеток и извлечения экспрессированных полипептидов известны специалистам в данной области и могут быть изменены или оптимизированы в зависимости от конкретных используемых вектора экспрессии и клетки-хозяина, представляющей собой клетку млекопитающего, исходя из настоящего описания.
7.9.2. Клетки
[0523] В настоящем изобретении также предусмотрены клетки-хозяева, содержащие нуклеиновую кислоту по настоящему изобретению.
[0524] В одном варианте осуществления клетки-хозяева являются генетически сконструированными так, что они содержат одну или более нуклеиновых кислот, описанных в данном документе.
[0525] В одном варианте осуществления клетки-хозяева являются генетически сконструированными с применением кассеты экспрессии. Фраза "кассета экспрессии" относится к нуклеотидным последовательностям, которые способны влиять на экспрессию гена у хозяев, совместимых с такими последовательностями. Такие кассеты могут содержать промотор, открытую рамку считывания с интронами или без них и сигнал терминации. Также можно применять дополнительные факторы, необходимые или полезные при осуществлении экспрессии, такие как, например, индуцируемый промотор.
[0526] В настоящем изобретении также предусмотрены клетки-хозяева, содержащие векторы, описанные в данном документе.
[0527] Клетка может представлять собой без ограничения эукариотическую клетку, бактериальную клетку, клетку насекомого или клетку человека. Подходящие эукариотические клетки включают без ограничения клетки Vero, клетки HeLa, клетки COS, клетки CHO, клетки HEK293, клетки BHK и клетки MDCKII. Подходящие клетки насекомых включают без ограничения клетки Sf9.
7.10. Конъюгаты антител и лекарственных средств
[0528] MBM (например, TBM) могут быть конъюгированы, например, посредством линкера, с фрагментом, представляющим собой лекарственное средство. Такие конъюгаты называются в данном документе конъюгатами антител и лекарственных средств (или "ADC") для удобства, несмотря на то, что в основе одного или более (или всех) из ABM могут лежать неиммуноглобулиновые каркасные структуры.
[0529] В определенных аспектах фрагмент, представляющий собой лекарственное средство, проявляет цитотоксическую или цитостатическую активность. В одном варианте осуществления фрагмент, представляющий собой лекарственное средство, выбран из майтанзиноида, ингибитора кинезиноподобного белка KIF11, ингибитора V-ATPазы (Н+-ATPазы вакуолярного типа), проапоптотического средства, ингибитора Bcl2 (белка 2 B-клеточной лимфомы), ингибитора MCL1 (белка 1 миелоидноклеточного лейкоза), ингибитора HSP90 (белка теплового шока 90), ингибитора IAP (ингибитора апоптоза), ингибитора mTOR (механистической мишени рапамицина), стабилизатора микротрубочек, дестабилизатора микротрубочек, ауристатина, доластатина, MetAP (метионинаминопептидазы), ингибитора CRM1 (белка 1 поддержания структуры хромосом), ингибитора DPPIV (дипептидилпептидазы IV), ингибитора протеасом, ингибитора реакции переноса фосфорильной группы в митохондриях, ингибитора синтеза белка, ингибитора киназы, ингибитора CDK2 (циклинзависимой киназы 2), ингибитора CDK9 (циклинзависимой киназы 9), ингибитора кинезина, ингибитора HDAC (деацетилаз гистонов), средства, повреждающего ДНК, средства, алкилирующего ДНК, ДНК-интеркалятора, средства, связывающегося с малой бороздкой ДНК, ингибитора РНК-полимеразы, ингибитора топоизомеразы или ингибитора DHFR (дигидрофолатредуктазы).
[0530] В одном варианте осуществления линкер выбран из расщепляемого линкера, нерасщепляемого линкера, гидрофильного линкера, предварительно заряженного линкера или линкера на основе дикарбоновой кислоты.
[0531] В некоторых вариантах осуществления ADC представляют собой соединения в соответствии со структурной формулой (I):
[D-L-XY]n-Ab
или их соли, где каждый "D" представляет независимо от других цитотоксическое и/или цитостатическое средство ("лекарственное средство"); каждый "L" представляет независимо от других линкер; "Ab" представляет МBM, описанную в данном документе; каждый "XY" представляет связь, образованную между функциональной группой Rx в линкере и "комплементарной" функциональной группой Ry в антителе, и n представляет количество связанных лекарственных средств или соотношение лекарственное средство/антитело (DAR) в ADC.
[0532] Некоторые варианты осуществления различных антител (Ab), которые могут содержаться в ADC, включают различные варианты осуществления MBM, описанные выше.
[0533] В некоторых вариантах осуществления ADC и/или солей структурной формулы (I) все D являются одинаковыми и/или все L являются одинаковыми.
[0534] Некоторые варианты осуществления цитотоксических и/или цитостатических средств (D) и линкеров (L), которые могут содержаться в ADC по настоящему изобретению, а также количества цитотоксических и/или цитостатических средств, связанных с ADC, более подробно описаны ниже.
7.10.1. Цитотоксические и/или цитостатические средства
[0535] Цитотоксические и/или цитостатические средства могут представлять собой любые средства, которые, как известно, подавляют рост и/или репликацию клеток, и в частности раковых и/или опухолевых клеток, и/или уничтожают их. В литературе известны многочисленные средства, обладающие цитотоксическими и/или цитостатическими свойствами. Неограничивающие примеры классов цитотоксических и/или цитостатических средств включают в качестве примера и без ограничения радионуклиды, алкилирующие средства, ингибиторы топоизомеразы I, ингибиторы топоизомеразы II, ДНК-интеркалирующие средства (например, средства, связывающиеся с бороздками, такие как средства, связывающиеся с малой бороздкой), антиметаболиты РНК/ДНК, модуляторы клеточного цикла, ингибиторы киназ, ингибиторы синтеза белка, ингибиторы деацетилаз гистонов, ингибиторы митохондрий и антимитотические средства.
[0536] Ниже приведены конкретные неограничивающие примеры средств в пределах некоторых из этих различных классов.
[0537] Алкилирующие средства: асалей ((L-лейцин, N-[N-ацетил-4-[бис-(2-хлорэтил)амино]-D/L-фенилaланил]-, этиловый сложный эфир; NSC 167780; регистрационный № CAS 3577897)); AZQ ((1,4-циклогексадиен-1,4-дикарбаминовая кислота, 2,5-бис(1-азиридинил)-3,6-диоксо-, диэтиловый сложный эфир; NSC 182986; регистрационный № CAS 57998682)); BCNU ((N, N'-бис(2-хлорэтил)-N-нитрозомочевина; NSC 409962; регистрационный № CAS 154938)); бусульфан (1,4-бутандиолдиметансульфонат; NSC 750; регистрационный № CAS 55981); (карбоксифталато)платина (NSC 27164; регистрационный № CAS 65296813); CBDCA ((цис-(1,1-циклобутандикарбоксилато)диаминоплатина(II)); NSC 241240; регистрационный № CAS 41575944)); CCNU ((N-(2-хлорэтил)-N'-циклогексил-N-нитрозомочевина; NSC 79037; регистрационный № CAS 13010474)); CHIP (ипроплатин; NSC 256927); хлорамбуцил (NSC 3088; регистрационный № CAS 305033); хлорозотоцин ((2-[[[(2-хлорэтил)нитрозамино]карбонил]амино]-2-дезокси-D-глюкопиранoза; NSC 178248; регистрационный № CAS 54749905)); цис-платина (цисплатин; NSC 119875; регистрационный № CAS 15663271); кломезон (NSC 338947; регистрационный № CAS 88343720); цианоморфолинодоксорубицин (NCS 357704; регистрационный № CAS 88254073); циклодизон (NSC 348948; регистрационный № CAS 99591738); диангидрогалактит (5,6-диэпоксидульцит; NSC 132313; регистрационный № CAS 23261203); фтордопан (5-[(2-хлорэтил)(2-фторэтил)амино]-6-метилурацил; NSC 73754; регистрационный № CAS 834913); гепсульфам (NSC 329680; регистрационный № CAS 96892578); гикантон (NSC 142982; регистрационный № CAS 23255938); мелфалан (NSC 8806; регистрационный № CAS 3223072); метил-CCNU (1-(2-хлорэтил)-3-(транс-4-метилциклогексан)-1-нитрозомочевина; NSC 95441; 13909096); митомицин C (NSC 26980; регистрационный № CAS 50077); митозоламид (NSC 353451; регистрационный № CAS 85622953); азотистый иприт (гидрохлорид бис(2-хлорэтил)метиламина; NSC 762; регистрационный № CAS 55867); PCNU ((1-(2-хлорэтил)-3-(2,6-диоксо-3-пиперидил)-1-нитрозомочевина; NSC 95466; регистрационный № CAS 13909029)); пиперазиновый алкилятор (дигидрохлорид (1-(2-хлорэтил)-4-(3-хлорпропил)пиперазина; NSC 344007)); пиперазиндион (NSC 135758; регистрационный № CAS 41109802); пипоброман ((N, N-бис(3-бромпропионил)пиперазин; NSC 25154; регистрационный № CAS 54911)); порфиромицин (N-метилмитомицин C; NSC 56410; регистрационный № CAS 801525); спирогидантоиновый иприт (NSC 172112; регистрационный № CAS 56605164); тероксирон (триглицидилизоцианурат; NSC 296934; регистрационный № CAS 2451629); тетраплатин (NSC 363812; регистрационный № CAS 62816982); тиотепа (N, N',N''-три-1,2-этандиилтиофосфорамид; NSC 6396; регистрационный № CAS 52244); триэтиленмеламин (NSC 9706; регистрационный № CAS 51183); урациловый иприт (десметилдопан; NSC 34462; регистрационный № CAS 66751); Yoshi-864 (гидрохлорид бис(3-мезилоксипропил)амина; NSC 102627; регистрационный № CAS 3458228).
[0538] Ингибиторы топоизомеразы I: камптотецин (NSC 94600; регистрационный № CAS 7689-03-4); различные производные и аналоги камптотецина (например, NSC 100880, NSC 603071, NSC 107124, NSC 643833, NSC 629971, NSC 295500, NSC 249910, NSC 606985, NSC 74028, NSC 176323, NSC 295501, NSC 606172, NSC 606173, NSC 610458, NSC 618939, NSC 610457, NSC 610459, NSC 606499, NSC 610456, NSC 364830 и NSC 606497); морфолиноизоксорубицин (NSC 354646; регистрационный № CAS 89196043); SN-38 (NSC 673596; регистрационный № CAS 86639-52-3).
[0539] Ингибиторы топоизомеразы II: доксорубицин (NSC 123127; регистрационный № CAS 25316409); амонафид (бензизохинолиндион; NSC 308847; регистрационный № CAS 69408817); м-AMSA ((4'-(9-акридиниламино)-3'-метоксиметансульфонанилид; NSC 249992; регистрационный № CAS 51264143)); производное антрапиразола (NSC 355644); этопозид (VP-16; NSC 141540; регистрационный № CAS 33419420); пиразолоакридин (пиразолo[3,4,5-kl]акридин-2(6H)пропанамин, 9-метокси-N, N-диметил-5-нитро-, монометансульфонат; NSC 366140; регистрационный № CAS 99009219); гидрохлорид бисантрена (NSC 337766; регистрационный № CAS 71439684); даунорубицин (NSC 821151; регистрационный № CAS 23541506); дезоксидоксорубицин (NSC 267469; регистрационный № CAS 63950061); митоксантрон (NSC 301739; регистрационный № CAS 70476823); меногарил (NSC 269148; регистрационный № CAS 71628961); N, N-дибензилдауномицин (NSC 268242; регистрационный № CAS 70878512); оксантразол (NSC 349174; регистрационный № CAS 105118125); рубидазон (NSC 164011; регистрационный № CAS 36508711); тенипозид (VM-26; NSC 122819; регистрационный № CAS 29767202).
[0540] ДНК-интеркалирующие средства: антрамицин (регистрационный № CAS 4803274); чикамицин A (регистрационный № CAS 89675376); томаймицин (регистрационный № CAS 35050556); DC-81 (регистрационный № CAS 81307246); сибиромицин (регистрационный № CAS 12684332); производное пирролобензодиазепина (регистрационный № CAS 945490095); SGD-1882 ((S)-2-(4-аминофенил)-7-метокси-8-(3-4-(S)-7-метокси-2-(4-метоксифенил)-5-оксо-5,11a-дигидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-8-ил)окси)пропокси)-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-5-(11aH)-он); SG2000 (SJG-136; (11aS,11a'S)-8,8'-(пропан-1,3-диилбис(окси)бис(7-метокси-2-метилен-2,3-дигидро-1H-бензо[e]пирроло[1,2-a][1,4]диазепин-5(11aH)-он); NSC 694501; регистрационный № CAS 232931576).
[0541] Антиметаболиты РНК/ДНК: L-аланозин (NSC 153353; регистрационный № CAS 59163416); 5-азацитидин (NSC 102816; регистрационный № CAS 320672); 5-фторурацил (NSC 19893; регистрационный № CAS 51218); ацивицин (NSC 163501; регистрационный № CAS 42228922); производное аминоптерина N-[2-хлор-5-[[(2,4-диамино-5-метил-6-хиназолинил)метил]амино]бензоил]-L-аспарагиновая кислота (NSC 132483); производное аминоптерина N-[4-[[(2,4-диамино-5-этил-6-хиназолинил)метил]амино]бензоил]-L-аспарагиновая кислота (NSC 184692); производное аминоптерина моногидрат N-[2-хлор-4-[[(2,4-диамино-6-птеридинил)метил]амино]бензоил]-L-аспарагиновой кислоты (NSC 134033); антифолат ((Nα-(4-амино-4-дезоксиптероил)-N7-гемифталоил-L-орнитин; NSC 623017)); растворимый антифолат Бейкера (NSC 139105; регистрационный № CAS 41191042); дихлораллиллаусон (2-(3,3-дихлораллил)-3-гидрокси-1,4-нафтохинон; NSC 126771; регистрационный № CAS 36417160); бреквинар (NSC 368390; регистрационный № CAS 96201886); фторафур (пролекарство; 5-фтор-1-(тетрагидро-2-фурил)урацил; NSC 148958; регистрационный № CAS 37076689); 5,6-дигидро-5-азацитидин (NSC 264880; регистрационный № CAS 62402317); метотрексат (NSC 740; регистрационный № CAS 59052); производное метотрексата (N-[[4-[[(2,4-диамино-6-птеридинил)метил]метиламино]-1-нафталинил]карбонил]-L-глутаминовая кислота; NSC 174121); PALA (N-(фосфоноацетил)-L-аспартат; NSC 224131; регистрационный № CAS 603425565); пиразофурин (NSC 143095; регистрационный № CAS 30868305); триметрексат (NSC 352122; регистрационный № CAS 82952645).
[0542] Антиметаболиты ДНК: 3-HP (NSC 95678; регистрационный № CAS 3814797); 2'-дезокси-5-фторуридин (NSC 27640; регистрационный № CAS 50919); 5-HP (NSC 107392; регистрационный № CAS 19494894); α-TGDR (α-2'-дезокси-6-тиогуанозин; NSC 71851; регистрационный № CAS 2133815); глицинат афидиколина (NSC 303812; регистрационный № CAS 92802822); Ara-C (цитозинарабинозид; NSC 63878; регистрационный № CAS 69749); 5-аза-2'-дезоксицитидин (NSC 127716; регистрационный № CAS 2353335); β-TGDR (β-2'-дезокси-6-тиогуанозин; NSC 71261; регистрационный № CAS 789617); циклоцитидин (NSC 145668; регистрационный № CAS 10212256); гуаназол (NSC 1895; регистрационный № CAS 1455772); гидроксимочевина (NSC 32065; регистрационный № CAS 127071); инозингликодиальдегид (NSC 118994; регистрационный № CAS 23590990); макбецин II (NSC 330500; регистрационный № CAS 73341738); пиразолоимидазол (NSC 51143; регистрационный № CAS 6714290); тиогуанин (NSC 752; регистрационный № CAS 154427); тиопурин (NSC 755; регистрационный № CAS 50442).
[0543] Модуляторы клеточного цикла: силибинин (регистрационный № CAS 22888-70-6); галлат эпигаллокатехина (EGCG; регистрационный № CAS 989515); производные процианидина (например, процианидин A1 [регистрационный № CAS 103883030], процианидин B1 [регистрационный № CAS 20315257], процианидин B4 [регистрационный № CAS 29106512], арекатанин B1 [регистрационный № CAS 79763283]); изофлавоны (например, генистеин [4',5,7-тригидроксиизофлавон; регистрационный № CAS 446720], дайдзеин [4',7-дигидроксиизофлавон, регистрационный № CAS 486668]; индол-3-карбинол (регистрационный № CAS 700061); кверцетин (NSC 9219; регистрационный № CAS 117395); эстрамустин (NSC 89201; регистрационный № CAS 2998574); нокодазол (регистрационный № CAS 31430189); подофиллотоксин (регистрационный № CAS 518285); тартрат винорелбина (NSC 608210; регистрационный № CAS 125317397); криптофицин (NSC 667642; регистрационный № CAS 124689652).
[0544] Ингибиторы киназ: афатиниб (регистрационный № CAS 850140726); акситиниб (регистрационный № CAS 319460850); ARRY-438162 (биниметиниб) (регистрационный № CAS 606143899); босутиниб (регистрационный № CAS 380843754); кабозантиниб (регистрационный № CAS 1140909483); церитиниб (регистрационный № CAS 1032900256); кризотиниб (регистрационный № CAS 877399525); дабрафениб (регистрационный № CAS 1195765457); дазатиниб (NSC 732517; регистрационный № CAS 302962498); эрлотиниб (NSC 718781; регистрационный № CAS 183319699); эверолимус (NSC 733504; регистрационный № CAS 159351696); фостаматиниб (NSC 745942; регистрационный № CAS 901119355); гефитиниб (NSC 715055; регистрационный № CAS 184475352); ибрутиниб (регистрационный № CAS 936563961); иматиниб (NSC 716051; регистрационный № CAS 220127571); лапатиниб (регистрационный № CAS 388082788); ленватиниб (регистрационный № CAS 857890392); мубритиниб (CAS 366017096); нилотиниб (регистрационный № CAS 923288953); нинтеданиб (регистрационный № CAS 656247175); палбоциклиб (регистрационный № CAS 571190302); пазопаниб (NSC 737754; регистрационный № CAS 635702646); пегаптаниб (регистрационный № CAS 222716861); понатиниб (регистрационный № CAS 1114544318); рапамицин (NSC 226080; регистрационный № CAS 53123889); регорафениб (регистрационный № CAS 755037037); AP 23573 (ридафоролимус) (регистрационный № CAS 572924540); INCB018424 (руксолитиниб) (регистрационный № CAS 1092939177); ARRY-142886 (селуметиниб) (NSC 741078; регистрационный № CAS 606143-52-6); сиролимус (NSC 226080; регистрационный № CAS 53123889); сорафениб (NSC 724772; регистрационный № CAS 475207591); сунитиниб (NSC 736511; регистрационный № CAS 341031547); тофацитиниб (регистрационный № CAS 477600752); темсиролимус (NSC 683864; регистрационный № CAS 163635043); траметиниб (регистрационный № CAS 871700173); вандетаниб (регистрационный № CAS 443913733); вемурафениб (регистрационный № CAS 918504651); SU6656 (регистрационный № CAS 330161870); CEP-701 (лесауртиниб) (регистрационный № CAS 111358884); XL019 (регистрационный № CAS 945755566); PD-325901 (регистрационный № CAS 391210109); PD-98059 (регистрационный № CAS 167869218); конкурирующие c ATP ингибиторы TORC1/TORC2, включая PI-103 (регистрационный № CAS 371935749), PP242 (регистрационный № CAS 1092351671), PP30 (регистрационный № CAS 1092788094), торин 1 (регистрационный № CAS 1222998368), LY294002 (регистрационный № CAS 154447366), XL-147 (регистрационный № CAS 934526893), CAL-120 (регистрационный № CAS 870281348), ETP-45658 (регистрационный № CAS 1198357797), PX 866 (регистрационный № CAS 502632668), GDC-0941 (регистрационный № CAS 957054307), BGT226 (регистрационный № CAS 1245537681), BEZ235 (регистрационный № CAS 915019657), XL-765 (регистрационный № CAS 934493762).
[0545] Ингибиторы синтеза белка: акрифлавин (регистрационный № CAS 65589700); амикацин (NSC 177001; регистрационный № CAS 39831555); арбекацин (регистрационный № CAS 51025855); астромицин (регистрационный № CAS 55779061); азитромицин (NSC 643732; регистрационный № CAS 83905015); беканамицин (регистрационный № CAS 4696768); хлортетрациклин (NSC 13252; регистрационный № CAS 64722); кларитромицин (NSC 643733; регистрационный № CAS 81103119); клиндамицин (регистрационный № CAS 18323449); кломоциклин (регистрационный № CAS 1181540); циклогексимид (регистрационный № CAS 66819); дактиномицин (NSC 3053; регистрационный № CAS 50760); далфопристин (регистрационный № CAS 112362502); демеклоциклин (регистрационный № CAS 127333); дибекацин (регистрационный № CAS 34493986); дигидрострептомицин (регистрационный № CAS 128461); диритромицин (регистрационный № CAS 62013041); доксициклин (регистрационный № CAS 17086281); эметин (NSC 33669; регистрационный № CAS 483181); эритромицин (NSC 55929; регистрационный № CAS 114078); флуритромицин (регистрационный № CAS 83664208); фрамицетин (неомицин B; регистрационный № CAS 119040); гентамицин (NSC 82261; регистрационный № CAS 1403663); глицилциклины, такие как тигециклин (регистрационный № CAS 220620097); гигромицин B (регистрационный № CAS 31282049); изепамицин (регистрационный № CAS 67814760); джозамицин (NSC 122223; регистрационный № CAS 16846245); канамицин (регистрационный № CAS 8063078); кетолиды, такие как телитромицин (регистрационный № CAS 191114484), цетромицин (регистрационный № CAS 205110481) и солитромицин (регистрационный № CAS 760981837); линкомицин (регистрационный № CAS 154212); лимециклин (регистрационный № CAS 992212); меклоциклин (NSC 78502; регистрационный № CAS 2013583); метациклин (рондомицин; NSC 356463; регистрационный № CAS 914001); мидекамицин (регистрационный № CAS 35457808); миноциклин (NSC 141993; регистрационный № CAS 10118908); миокамицин (регистрационный № CAS 55881077); неомицин (регистрационный № CAS 119040); нетилмицин (регистрационный № CAS 56391561); олеандомицин (регистрационный № CAS 3922905); оксазолидиноны, такие как эперезолид (регистрационный № CAS 165800044), линезолид (регистрационный № CAS 165800033), посизолид (регистрационный № CAS 252260029), радезолид (регистрационный № CAS 869884786), ранбезолид (регистрационный № CAS 392659380), сутезолид (регистрационный № CAS 168828588), тедизолид (регистрационный № CAS 856867555); окситетрациклин (NSC 9169; регистрационный № CAS 2058460); паромомицин (регистрационный № CAS 7542372); пенимепициклин (регистрационный № CAS 4599604); ингибиторы пептидилтрансферазы, например, хлорамфеникол (NSC 3069; регистрационный № CAS 56757) и его производные, такие как азидамфеникол (регистрационный № CAS 13838089), флорфеникол (регистрационный № CAS 73231342) и тиамфеникол (регистрационный № CAS 15318453), а также плевромутилины, такие как ретапамулин (регистрационный № CAS 224452668), тиамулин (регистрационный № CAS 55297955), вальнемулин (регистрационный № CAS 101312929); пирлимицин (регистрационный № CAS 79548735); пуромицин (NSC 3055; регистрационный № CAS 53792); хинупристин (регистрационный № CAS 120138503); рибостамицин (регистрационный № CAS 53797356); рокитaмицин (регистрационный № CAS 74014510); ролитетрациклин (регистрационный № CAS 751973); рокситромицин (регистрационный № CAS 80214831); сизомицин (регистрационный № CAS 32385118); спектиномицин (регистрационный № CAS 1695778); спирамицин (регистрационный № CAS 8025818); стрептограмины, такие как пристинамицин (регистрационный № CAS 270076603), хинупристин/далфопристин (регистрационный № CAS 126602899) и виргиниамицин (регистрационный № CAS 11006761); стрептомицин (регистрационный № CAS 57921); тетрациклин (NSC 108579; регистрационный № CAS 60548); тобрамицин (регистрационный № CAS 32986564); тролеандомицин (регистрационный № CAS 2751099); тилозин (регистрационный № CAS 1401690); вердамицин (регистрационный № CAS 49863481).
[0546] Ингибиторы деацетилаз гистонов: абексиностат (регистрационный № CAS 783355602); белиностат (NSC 726630; регистрационный № CAS 414864009); чидамид (регистрационный № CAS 743420022); энтиностат (регистрационный № CAS 209783802); гивиностат (регистрационный № CAS 732302997); моцетиностат (регистрационный № CAS 726169739); панобиностат (регистрационный № CAS 404950807); квизиностат (регистрационный № CAS 875320299); резминостат (регистрационный № CAS 864814880); ромидепсин (регистрационный № CAS 128517077); сульфорафан (регистрационный № CAS 4478937); тиоуреидобутиронитрил (Kevetrin™; регистрационный № CAS 6659890); вальпроевая кислота (NSC 93819; регистрационный № CAS 99661); вориностат (NSC 701852; регистрационный № CAS 149647789); ACY-1215 (роцилиностат; регистрационный № CAS 1316214524); CUDC-101 (регистрационный № CAS 1012054599); CHR-2845 (тефиностат; регистрационный № CAS 914382608); CHR-3996 (регистрационный № CAS 1235859138); 4SC-202 (регистрационный № CAS 910462430); CG200745 (регистрационный № CAS 936221339); SB939 (прациностат; регистрационный № CAS 929016966).
[0547] Ингибиторы митохондрий: панкратистатин (NSC 349156; регистрационный № CAS 96281311); родамин-123 (регистрационный № CAS 63669709); эдельфозин (NSC 324368; регистрационный № CAS 70641519); сукцинат d-альфа-токоферола (NSC 173849; регистрационный № CAS 4345033); соединение 11β (регистрационный № CAS 865070377); аспирин (NSC 406186; регистрационный № CAS 50782); эллиптицин (регистрационный № CAS 519233); берберин (регистрационный № CAS 633658); церуленин (регистрационный № CAS 17397896); GX015-070 (Obatoclax®; 2-(2-((3,5-диметил-1H-пиррол-2-ил)метилен)-3-метокси-2H-пиррол-5-ил)-1H-индол; NSC 729280; регистрационный № CAS 803712676); целастрол (триптерин; регистрационный № CAS 34157830); метформин (NSC 91485; регистрационный № CAS 1115704); бриллиантовый зеленый (NSC 5011; регистрационный № CAS 633034); ME-344 (регистрационный № CAS 1374524556).
[0548] Антимитотические средства: аллоколхицин (NSC 406042); ауристатины, такие как MMAE (монометилауристатин E; регистрационный № CAS 474645-27-7) и MMAF (монометилауристатин F; регистрационный № CAS 745017-94-1); галихондрин B (NSC 609395); колхицин (NSC 757; регистрационный № CAS 64868); производное колхицина (N-бензоилдеацетилбензамид; NSC 33410; регистрационный № CAS 63989753); доластатин 10 (NSC 376128; регистрационный № CAS 110417-88-4); майтанзин (NSC 153858; регистрационный № CAS 35846-53-8); розоксин (NSC 332598; регистрационный № CAS 90996546); таксол (NSC 125973; регистрационный № CAS 33069624); производное таксола (2'-N-[3-(диметиламино)пропил]глутарамат таксола; NSC 608832); тиоколхицин (3-деметилтиоколхицин; NSC 361792); тритилцистеин (NSC 49842; регистрационный № CAS 2799077); сульфат винбластина (NSC 49842; регистрационный № CAS 143679); сульфат винкристина (NSC 67574; регистрационный № CAS 2068782).
[0549] Любое из этих средств, которые содержат или которые могут быть модифицированы таким образом, чтобы они содержали сайт прикрепления к МBM, может быть включено в ADC, раскрытые в данном документе.
[0550] В некоторых вариантах осуществления цитотоксическое и/или цитостатическое средство представляет собой антимитотическое средство.
[0551] В некоторых вариантах осуществления цитотоксическое и/или цитостатическое средство представляет собой ауристатин, например, монометилауристатин E ("MMAE") или монометилауристатин F ("MMAF").
7.10.2. Линкеры для ADC
[0552] В ADC по настоящему изобретению цитотоксические и/или цитостатические средства связаны с МBM посредством линкеров для ADC. Линкер для ADC, связывающий цитотоксическое и/или цитостатическое средство с MBM в ADC, может быть коротким, длинным, гидрофобным, гидрофильным, гибким или жестким или может состоять из сегментов, каждый из которых независимо обладает одним или более из вышеуказанных свойств, так что линкер может содержать сегменты, обладающие различными свойствами. Линкеры могут быть поливалентными, так что они ковалентно связывают более одного средства с одним сайтом в MBM, или моновалентными, так что они ковалентно связывают одно средство с одним сайтом в MBM.
[0553] Как будет понятно специалисту в данной области, линкеры для ADC связывают цитотоксические и/или цитостатические средства с MBM посредством образования ковалентной связи с цитотоксическим и/или цитостатическим средством в одном местоположении и ковалентной связи с MBM в другом. Ковалентные связи образуются посредством реакции между функциональными группами в линкере для ADC и функциональными группами в средствах и МBM. Используемое в данном документе выражение "линкер для ADC" предполагается как включающее (i) неконъюгированные формы линкера для ADC, которые содержат функциональную группу, способную ковалентно связывать линкер для ADC с цитотоксическим и/или цитостатическим средством, и функциональную группу, способную ковалентно связывать линкер для ADC с МBM; (ii) частично конъюгированные формы линкера для ADC, которые содержат функциональную группу, способную ковалентно связывать линкер для ADC с МBM, и которые при этом являются ковалентно связанными с цитотоксическим и/или цитостатическим средством, или наоборот; и (iii) полностью конъюгированные формы линкера для ADC, которые являются ковалентно связанными как с цитотоксическим и/или цитостатическим средством, так и с МBM. В некоторых вариантах осуществления линкеров для ADC и ADC по настоящему изобретению, а также синтонов, применяемых для конъюгации линкеров, связанных со средствами, с MBM, фрагменты, содержащие функциональные группы в линкере для ADC, и ковалентные связи, образованные между линкером для ADC и MBM, конкретно проиллюстрированы в виде Rx и XY соответственно.
[0554] Линкеры для ADC могут являться, хотя и не обязательно должны являться, химически стабильными в условиях вне клетки и могут быть разработаны таким образом, чтобы они расщеплялись, разлагались и/или иным образом специфично разрушались внутри клетки. В качестве альтернативы можно применять линкеры для ADC, которые не разработаны таким образом, чтобы они специфично расщеплялись или разрушались внутри клетки. Выбор стабильного или нестабильного линкера для ADC может зависеть от токсичности цитотоксического и/или цитостатического средства. В случае со средствами, которые являются токсичными для нормальных клеток, можно применять стабильные линкеры. Можно использовать средства, которые являются селективными или нацеливающимися и характеризуются низкой токсичностью в отношении нормальных клеток, при этом химическая стабильность линкера для ADC во внеклеточной среде является менее важной. Известно большое разнообразие линкеров для ADC, применимых для связывания лекарственных средств с MBM в качестве составной части ADC. Любой из этих линкеров для ADC, а также другие линкеры для ADC можно применять для связывания цитотоксических и/или цитостатических средств с MBM в ADC по настоящему изобретению.
[0555] Иллюстративные поливалентные линкеры для ADC, которые можно применять для связывания множества цитотоксических и/или цитостатических средств с одной молекулой MBM, описаны, например, в WO 2009/073445; WO 2010/068795; WO 2010/138719; WO 2011/120053; WO 2011/171020; WO 2013/096901; WO 2014/008375; WO 2014/093379; WO 2014/093394; WO 2014/093640. Например, технология линкеров Fleximer, разработанная Mersana и соавт., обладает потенциалом обеспечения получения ADC с высоким DAR и хорошими физико-химическими свойствами. Как показано ниже, технология от Mersana основана на включении молекул лекарственного средства в солюбилизирующий полиацетальный каркас с помощью последовательности сложноэфирных связей. Данная методика обеспечивает получение ADC с высокой нагрузкой (с DAR до 20) при сохранении в то же время хороших физико-химических свойств.
[0556] Дополнительные примеры линкеров дендритного типа можно найти в US 2006/116422; US 2005/271615; de Groot et al., 2003, Angew. Chem. Int. Ed. 42:4490-4494; Amir et al., 2003, Angew. Chem. Int. Ed. 42:4494-4499; Shamis et al., 2004, J. Am. Chem. Soc. 126:1726-1731; Sun et al., 2002, Bioorganic & Medicinal Chemistry Letters 12:2213-2215; Sun et al., 2003, Bioorganic & Medicinal Chemistry 11:1761-1768; King et al., 2002, Tetrahedron Letters 43:1987-1990.
[0557] Иллюстративные моновалентные линкеры для ADC, которые можно применять, описаны, например, в Nolting, 2013, Antibody-Drug Conjugates, Methods in Molecular Biology 1045:71-100; Kitson et al., 2013, CROs-MOs--Chemica-ggi--Chemistry Today 31(4):30-38; Ducry et al., 2010, Bioconjugate Chem. 21:5-13; Zhao et al., 2011, J. Med. Chem. 54:3606-3623; патенте США № 7223837; патенте США № 8568728; патенте США № 8535678 и WO2004010957.
[0558] В качестве примера и без ограничения, некоторые расщепляемые и нерасщепляемые линкеры для ADC, которые могут быть включены в ADC, описаны ниже.
7.10.2.1. Расщепляемые линкеры для ADC
[0559] В определенных вариантах осуществления выбранный линкер для ADC является расщепляемым in vivo. Расщепляемые линкеры для ADC могут содержать химически или ферментативно нестабильные или разрушаемые связи. В случае с расщепляемыми линкерами для ADC высвобождение лекарственного средства обычно зависит от процессов внутри клетки, таких как восстановление в цитоплазме, воздействие кислых условий в лизосоме или расщепление посредством специфичных протеаз или других ферментов в клетке. Расщепляемые линкеры для ADC обычно содержат в своем составе одну или более химических связей, которые являются химически либо ферментативно расщепляемыми, тогда как остальная часть линкера для ADC является нерасщепляемой. В определенных вариантах осуществления линкер для ADC содержит химически неустойчивую группу, такую как гидразоновые и/или дисульфидные группы. В линкерах, содержащих химически неустойчивые группы, используются различия в свойствах между плазмой крови и некоторыми цитоплазматическими компартментами. Внутриклеточные условия, содействующие высвобождению лекарственного средства гидразонсодержащими линкерами для ADC, представляют собой кислую среду эндосом и лизосом, тогда как дисульфидсодержащие линкеры для ADC восстанавливаются в цитозоле, который содержит высокие концентрации тиолов, например, глутатиона. В определенных вариантах осуществления стабильность линкера для ADC, содержащего химически неустойчивую группу, в плазме крови можно увеличить посредством введения стерического несоответствия с использованием заместителей вблизи химически неустойчивой группы.
[0560] Кислотонеустойчивые группы, такие как гидразоновые, остаются интактными в ходе системного кровообращения в среде крови с нейтральным pH (pH 7,3-7,5) и подвергаются гидролизу и высвобождают лекарственное средство после интернализации ADC в слабокислые эндосомальные (pH 5,0-6,5) и лизосомальные (pH 4,5-5,0) компартменты клетки. Было показано, что данный pH-зависимый механизм высвобождения связан с неспецифическим высвобождением лекарственного средства. Для увеличения стабильности гидразоновой группы линкера для ADC линкер для ADC можно изменять посредством химической модификации, например, замещения, что обеспечивает возможность перестраивания для достижения более эффективного высвобождения в лизосоме со сведенными к минимуму потерями в кровотоке.
[0561] Гидразонсодержащие линкеры для ADC могут содержать дополнительные сайты расщепления, такие как дополнительные кислотонеустойчивые сайты расщепления и/или ферментативно неустойчивые сайты расщепления. ADC, содержащие иллюстративные гидразонсодержащие линкеры для ADC, включают в себя следующие структуры:
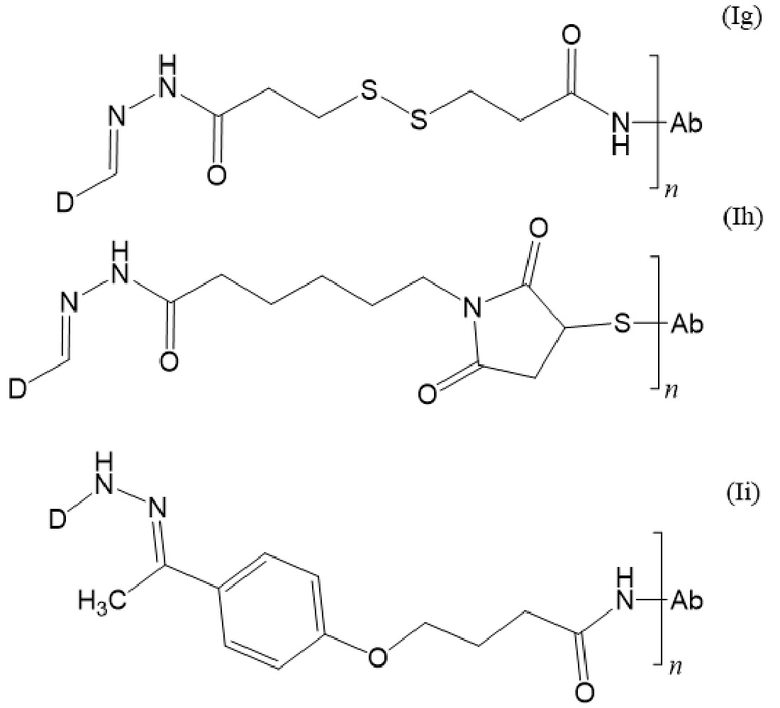
где D и Ab представляют цитотоксическое и/или цитостатическое средство (лекарственное средство) и Ab соответственно, и n представляет количество линкеров для ADC с лекарственным средством, связанных с МBM. В определенных линкерах для ADC, таких как линкер (Ig), линкер для ADC содержит две расщепляемые группы - дисульфидный и гидразоновый фрагменты. В случае с такими линкерами для ADC для эффективного высвобождения немодифицированного лекарственного средства в свободной форме требуется кислое значение pH или восстановление дисульфида и кислое значение pH. Было показано, что такие линкеры, как (Ih) и (Ii), являются эффективными с одним гидразоновым сайтом расщепления.
[0562] Дополнительные линкеры для ADC, которые остаются интактными в ходе системного кровообращения и подвергаются гидролизу и высвобождают лекарственное средство, когда ADC интернализируется в кислые клеточные компартменты, содержат карбонаты. Такие линкеры для ADC могут быть применимыми в случаях, когда цитотоксическое и/или цитостатическое средство может быть ковалентно присоединено посредством атома кислорода.
[0563] Другие кислотонеустойчивые группы, которые могут быть включены в линкеры для ADC, включают в себя цис-аконитилсодержащие линкеры для ADC. Химические свойства цис-аконитила обусловлены карбоновой кислотой, смежной с амидной связью, что обеспечивает ускорение гидролиза амидов в кислых условиях.
[0564] Расщепляемые линкеры для ADC могут также содержать дисульфидную группу. Дисульфиды являются термодинамически стабильными при физиологическом значении pH и разработаны таким образом, чтобы они высвобождали лекарственное средство при интернализации внутрь клеток, где цитозоль обеспечивает в значительной степени более восстановительную среду по сравнению с внеклеточной средой. Для разрыва дисульфидных связей обычно требуется присутствие цитоплазматического тиольного кофактора, такого как (восстановленный) глутатион (GSH), так что дисульфидсодержащие линкеры для ADC являются довольно стабильными в кровотоке, селективно высвобождая лекарственное средство в цитозоле. Внутриклеточный ферментный белок дисульфидизомераза или подобные ферменты, способные расщеплять дисульфидные связи, могут также способствовать предпочтительному расщеплению дисульфидных связей внутри клеток. Сообщалось, что GSH присутствует в клетках в диапазоне концентраций 0,5-10 мМ по сравнению со в значительной степени более низкой концентрацией GSH или цистеина, наиболее широко распространенного низкомолекулярного тиола, в кровотоке при примерно 5 опухолевых клетках, при этом нарушенный ток крови приводит к состоянию гипоксии, в результате чего повышается активность восстановительных ферментов и, следовательно, еще больше возрастают концентрации глутатиона. В определенных вариантах осуществления стабильность дисульфидсодержащего линкера для ADC in vivo можно повысить посредством химической модификации линкера для ADC, например, посредством применения стерического несоответствия рядом с дисульфидной связью.
[0565] ADC, содержащие иллюстративные дисульфидсодержащие линкеры для ADC, включают в себя следующие структуры:
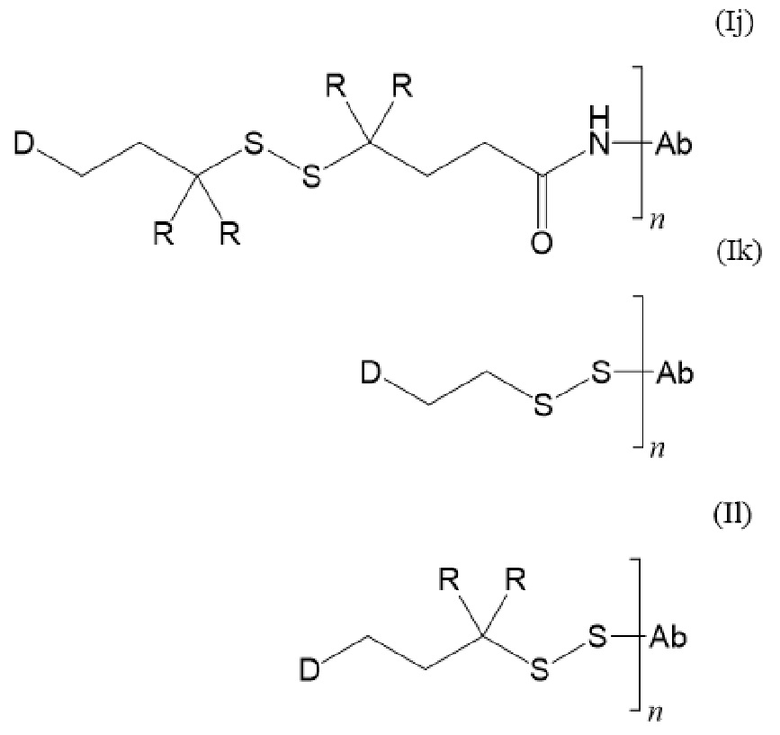
где D и Ab представляют лекарственное средство и МBM соответственно, при этом n представляет количество линкеров для ADC с лекарственным средством, связанных с МBM, и R в каждом случае независимо выбран, например, из водорода или алкила. В определенных вариантах осуществления увеличение стерического несоответствия рядом с дисульфидной связью приводит к увеличению стабильности линкера для ADC. Структуры, такие как (Ij) и (Il), демонстрируют увеличенную стабильность in vivo, если одна или более групп R выбраны из низшего алкила, такого как метил.
[0566] Другой тип расщепляемого линкера для ADC, который можно применять, представляет собой линкер для ADC, который специфично расщепляется ферментом. Такие линкеры для ADC, как правило, представляют собой линкеры на основе пептидов или содержат пептидные участки, которые выступают в качестве субстратов для ферментов. Линкеры для ADC на основе пептидов оказываются более стабильными в плазме крови и внеклеточной среде, чем химически неустойчивые линкеры для ADC. Пептидные связи обычно характеризуются хорошей стабильностью в сыворотке крови, поскольку лизосомальные протеолитические ферменты обладают очень низкой активностью в крови вследствие наличия эндогенных ингибиторов и неблагоприятно высокого значения pH крови по сравнению с лизосомами. Высвобождение лекарственного средства из МBM происходит специфично благодаря действию лизосомальных протеаз, например, катепсина и плазмина. Эти протеазы могут присутствовать на повышенных уровнях в определенных опухолевых клетках.
[0567] В иллюстративных вариантах осуществления расщепляемый пептид выбран из тетрапептидов, таких как Gly-Phe-Leu-Gly (SEQ ID NO: 553), Ala-Leu-Ala-Leu (SEQ ID NO: 554), или дипептидов, таких как Val-Cit, Val-Ala, Met-(D)Lys, Asn-(D)Lys, Val-(D)Asp, Phe-Lys, Ile-Val, Asp-Val, His-Val, нор-Val-(D)Asp, Ala-(D)Asp 5, Met-Lys, Asn-Lys, Ile-Pro, Me3Lys-Pro, фенил-Gly-(D)Lys, Met-(D)Lys, Asn-(D)Lys, Pro-(D)Lys, Met-(D)Lys, Asn-(D)Lys, AM Met-(D)Lys, Asn-(D)Lys, AW Met-(D)Lys и Asn-(D)Lys. В определенных вариантах осуществления дипептиды могут быть выбраны вместо более длинных полипептидов вследствие гидрофобности более длинных пептидов.
[0568] Были описаны разнообразные расщепляемые линкеры для ADC на основе дипептидов, применимые для связывания лекарственных средств, таких как доксорубицин, митомицин, камптотецин, пирролобензодиазепин, таллизомицин и ауристатин/представители семейства ауристатинов, с MBM (см. Dubowchik et al., 1998, J. Org. Chem. 67:1866-1872; Dubowchik et al., 1998, Bioorg. Med. Chem. Lett. 8(21):3341-3346; Walker et al., 2002, Bioorg. Med. Chem. Lett. 12:217-219; Walker et al., 2004, Bioorg. Med. Chem. Lett. 14:4323-4327; Sutherland et al., 2013, Blood 122: 1455-1463; и Francisco et al., 2003, Blood 102:1458-1465). Все эти дипептидные линкеры для ADC или модифицированные варианты этих дипептидных линкеров для ADC можно применять в ADC по настоящему изобретению. Другие дипептидные линкеры для ADC, которые можно применять, включают в себя линкеры, которые можно найти в ADC, таких как брентуксимаб-ведотин SGN-35 от Seattle Genetics (Adcetris™), SGN-75 от Seattle Genetics (антитело к CD-70, Val-Cit-монометилауристатин F (MMAF)), SGN-CD33A от Seattle Genetics (антитело к CD-33, Val-Ala-(SGD-1882)), глембатумумаб от Celldex Therapeutics (CDX-011) (антитело к NMB, Val-Cit-монометилауристатин E (MMAE)) и PSMA-ADC от Cytogen (PSMA-ADC-1301) (антитело к PSMA, Val-Cit-MMAE).
[0569] Ферментативно расщепляемые линкеры для ADC могут содержать саморазлагающийся спейсер для пространственного отделения лекарственного средства от сайта ферментативного расщепления. Прямое присоединение лекарственного средства к пептидному линкеру для ADC может в результате приводить к протеолитическому высвобождению аддукта лекарственного средства с аминокислотой, в результате чего, таким образом, ухудшается его активность. Применение саморазлагающегося спейсера обеспечивает возможность элиминирования полностью активного химически немодифицированного лекарственного средства при гидролизе амидных связей.
[0570] Один саморазлагающийся спейсер представляет собой бифункциональную группу пара-аминобензилового спирта, которая связана с пептидом посредством аминогруппы, образуя амидную связь, при этом аминосодержащие лекарственные средства могут быть присоединены посредством карбаматных функциональных групп к бензильной гидроксильной группе линкера для ADC (PABC). Полученные в результате пролекарства активируются при расщеплении, опосредованном протеазой, что приводит к реакции 1,6-элиминирования с высвобождением немодифицированного лекарственного средства, диоксида углерода и остатков линкерной группы для ADC. На следующей схеме изображены фрагментация п-амидобензилового эфира и высвобождение лекарственного средства:
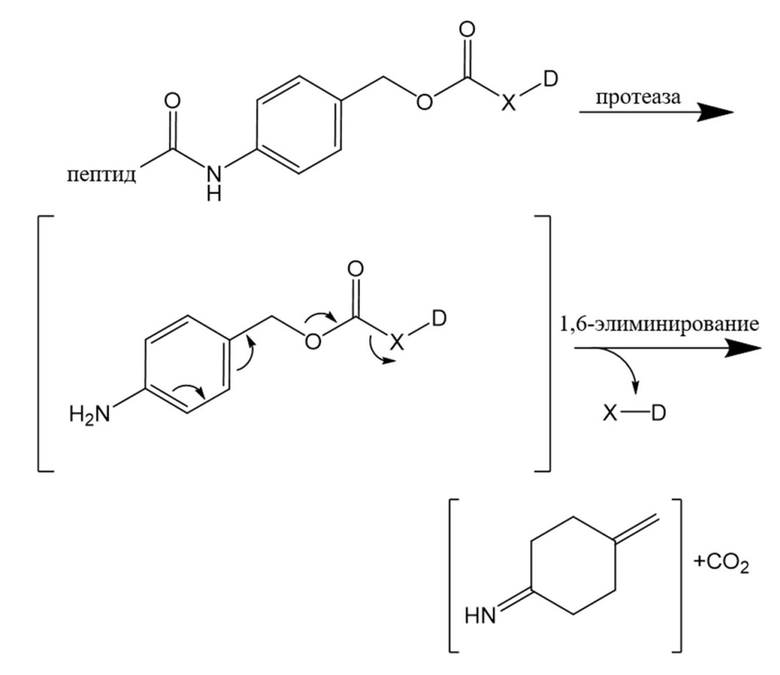
где X-D представляет немодифицированное лекарственное средство.
[0571] Гетероциклические варианты данной саморазлагающейся группы также были описаны. См., например, патент США № 7989434.
[0572] В некоторых вариантах осуществления ферментативно расщепляемый линкер для ADC представляет собой линкер для ADC на основе β-глюкуроновой кислоты. Легкое высвобождение лекарственного средства можно реализовать посредством расщепления гликозидной связи β-глюкуронида с помощью лизосомального фермента β-глюкуронидазы. Данный фермент в большом количестве присутствует внутри лизосом и сверхэкспрессируется в некоторых типах опухолей, хотя активность фермента вне клеток является низкой. Для предотвращения склонности ADC подвергаться агрегации из-за гидрофильной природы β-глюкуронидов можно применять линкеры для ADC на основе β-глюкуроновой кислоты. В некоторых вариантах осуществления линкеры для ADC на основе β-глюкуроновой кислоты можно применять в качестве линкеров для ADC в ADC, связанных с гидрофобными лекарственными средствами. На следующей схеме изображены высвобождение лекарственного средства от линкера для ADC на основе β-глюкуроновой кислоты и ADC, содержащий данный линкер:
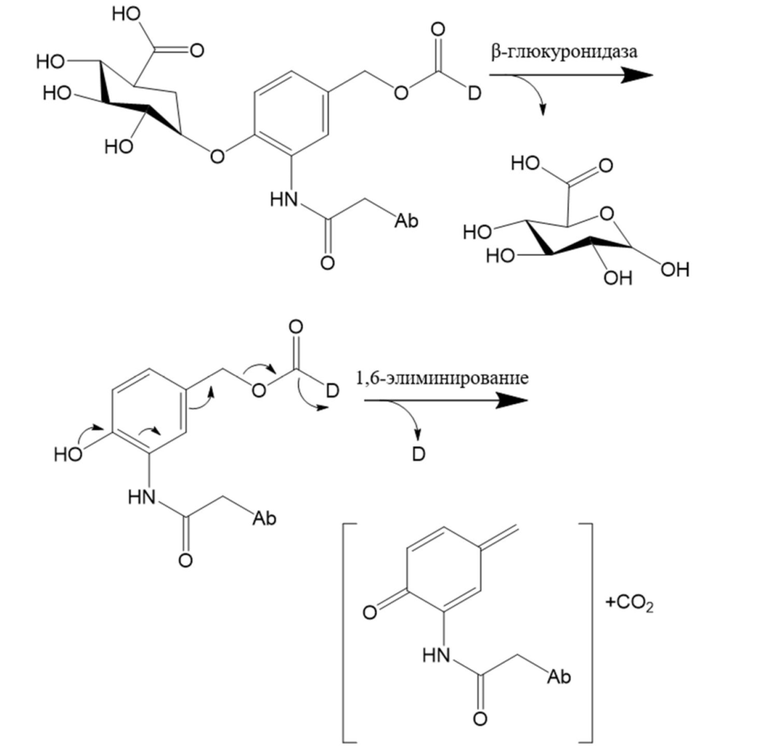
[0573] Были описаны разнообразные расщепляемые линкеры для ADC на основе β-глюкуроновой кислоты, применимые для связывания лекарственных средств, таких как аналоги ауристатинов, камптотецина и доксорубицина, средства на основе CBI, связывающиеся с малой бороздкой, и псимберин, с MBM (см. Nolting, Chapter 5 "Linker Technology in Antibody-Drug Conjugates", в Antibody-Drug Conjugates: Methods in Molecular Biology, vol. 1045, pp. 71-100, Laurent Ducry (Ed.), Springer Science & Business Medica, LLC, 2013; Jeffrey et al., 2006, Bioconjug. Chem. 17:831-840; Jeffrey et al., 2007, Bioorg. Med. Chem. Lett. 17:2278-2280; и Jiang et al., 2005, J. Am. Chem. Soc. 127:11254-11255). Все эти линкеры для ADC на основе β-глюкуроновой кислоты можно применять в ADC по настоящему изобретению.
[0574] Кроме того, цитотоксические и/или цитостатические средства, содержащие фенольную группу, могут быть ковалентно связаны с линкером для ADC посредством фенольного атома кислорода. Использование одного такого линкера для ADC, описанного в WO 2007/089149, основывается на методике, в которой диаминоэтан "SpaceLink" применяют совместно с традиционными саморазлагающимися группами на основе "PABO" для доставки фенолов. Расщепление линкера для ADC схематически изображено ниже, где D представляет собой цитотоксическое и/или цитостатическое средство, содержащее фенольную гидроксильную группу.
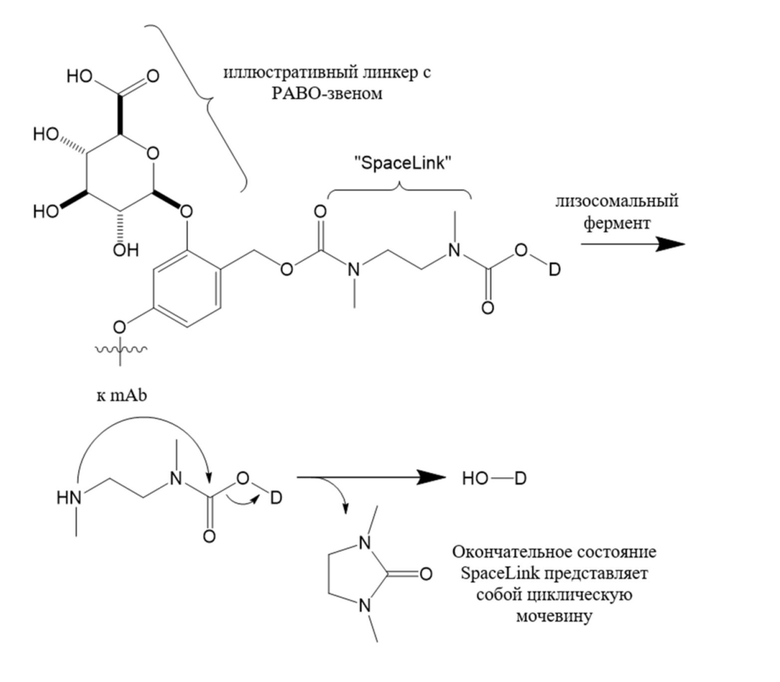
[0575] Расщепляемые линкеры для ADC могут содержать нерасщепляемые части или сегменты, и/или расщепляемые сегменты или части могут быть включены в линкер для ADC, в ином случае являющийся нерасщепляемым, чтобы сделать его расщепляемым. Исключительно в качестве примера, полиэтиленгликоль (PEG) и родственные полимеры могут содержать расщепляемые группы в полимерном остове. Например, линкер для ADC на основе полиэтиленгликоля или полимера может содержать одну или более расщепляемых групп, таких как дисульфид, гидразон или дипептид.
[0576] Другие разрушаемые связи, которые могут быть включены в линкеры для ADC, включают в себя сложноэфирные связи, образующиеся посредством реакции PEG, функционализированного группами карбоновых кислот, или PEG, функционализированного активированными группами карбоновых кислот, со спиртовыми группами в биологически активном средстве, где такие сложноэфирные группы обычно гидролизуются при физиологических условиях с высвобождением биологически активного средства. Гидролитически разрушаемые связи включают в себя без ограничения карбонатные связи; иминные связи, образующиеся в результате реакции амина и альдегида; фосфатные сложноэфирные связи, образующиеся посредством осуществления реакции спирта с фосфатной группой; ацетальные связи, которые представляют собой продукт реакции альдегида и спирта; ортоэфирные связи, которые представляют собой продукт реакции формиата и спирта; и олигонуклеотидные связи, образуемые фосфорамидитной группой, в том числе без ограничения на конце полимера, и 5'-гидроксильной группой олигонуклеотида.
[0577] В определенных вариантах осуществления линкер для ADC содержит ферментативно расщепляемый пептидный фрагмент, например, линкер для ADC, предусматривающий структурную формулу (IVa) или (IVb):
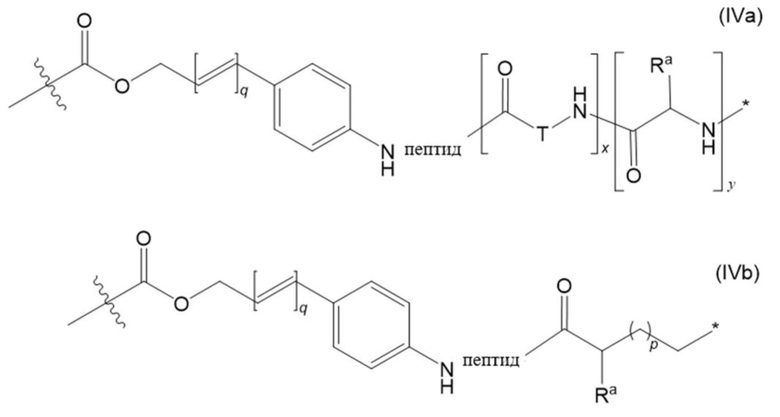
или его соль, где пептид представляет пептид (который проиллюстрирован в направлении C→N и в котором не показаны карбокси- и амино-"концы"), расщепляемый лизосомальным ферментом; T представляет полимер, содержащий одно или более этиленгликолевых звеньев или алкиленовую цепь или их комбинации; Ra выбран из водорода, алкила, сульфоната и метилсульфоната; p представляет целое число, находящееся в диапазоне от 0 до 5; q равняется 0 или 1; x равняется 0 или 1; y равняется 0 или 1; 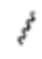 представляет точку присоединения линкера для ADC к цитотоксическому и/или цитостатическому средству; и * представляет точку присоединения к остальной части линкера для ADC.
представляет точку присоединения линкера для ADC к цитотоксическому и/или цитостатическому средству; и * представляет точку присоединения к остальной части линкера для ADC.
[0578] В определенных вариантах осуществления пептид выбран из трипептида или дипептида. В конкретных вариантах осуществления дипептид выбран из Val-Cit; Cit-Val; Ala-Ala; Ala-Cit; Cit-Ala; Asn-Cit; Cit-Asn; Cit-Cit; Val-Glu; Glu-Val; Ser-Cit; Cit-Ser; Lys-Cit; Cit-Lys; Asp-Cit; Cit-Asp; Ala-Val; Val-Ala; Phe-Lys; Val-Lys; Ala-Lys; Phe-Cit; Leu-Cit; Ile-Cit; Phe-Arg и Trp-Cit. В определенных вариантах осуществления дипептид выбран из Cit-Val и Ala-Val.
[0579] Конкретные иллюстративные варианты осуществления линкеров для ADC в соответствии со структурной формулой (IVа), которые могут быть включены в ADC, включают линкеры для ADC, проиллюстрированные ниже (как проиллюстрировано, линкеры для ADC содержат группу, подходящую для ковалентного связывания линкера для ADC с MBM):
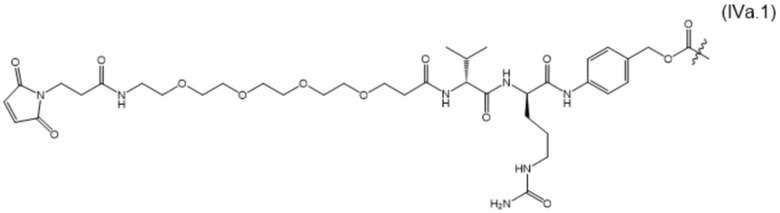
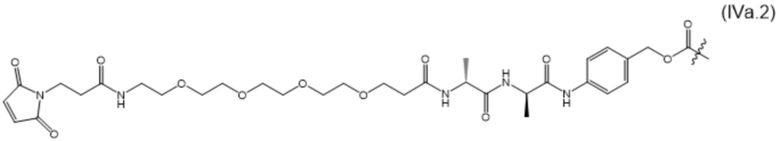
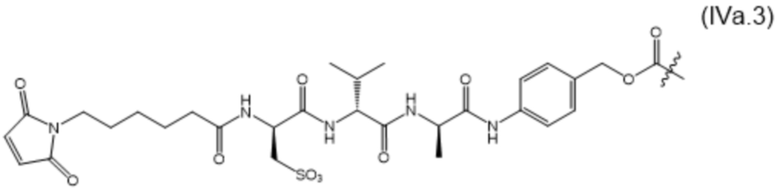
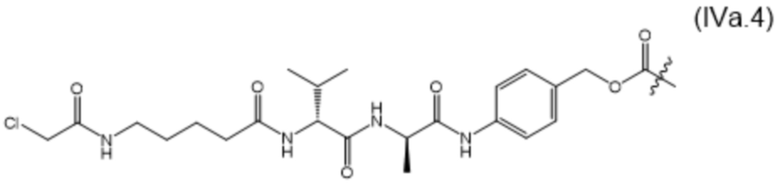
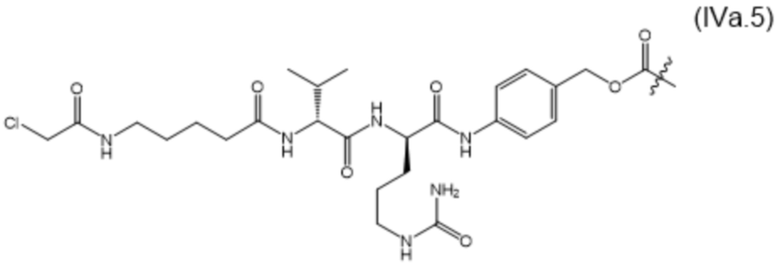
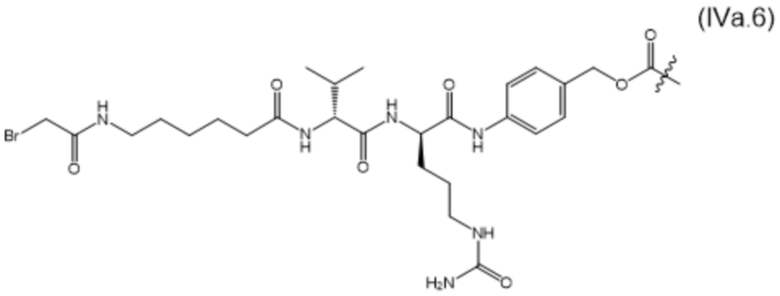
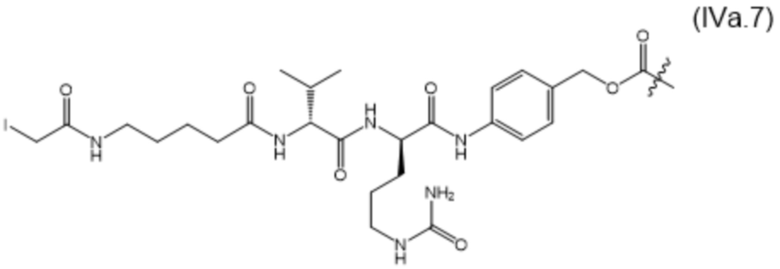
[0580] Конкретные иллюстративные варианты осуществления линкеров для ADC в соответствии со структурной формулой (IVb), которые могут быть включены в ADC, включают линкеры для ADC, проиллюстрированные ниже (как проиллюстрировано, линкеры для ADC содержат группу, подходящую для ковалентного связывания линкера для ADC с MBM):
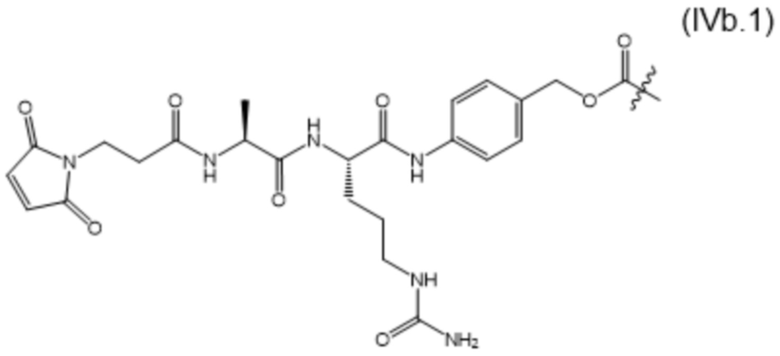
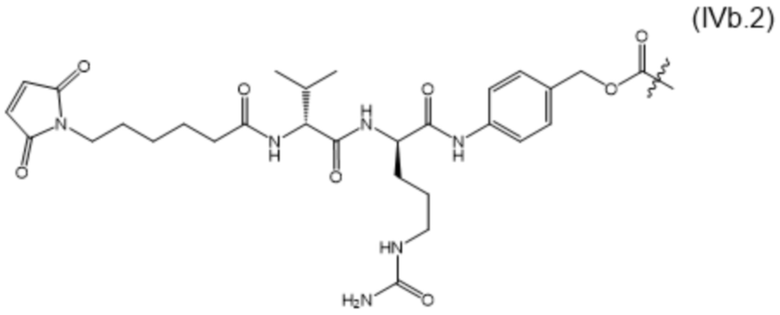
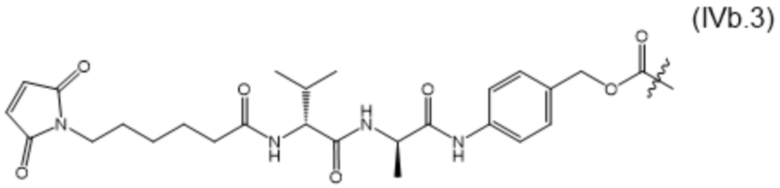
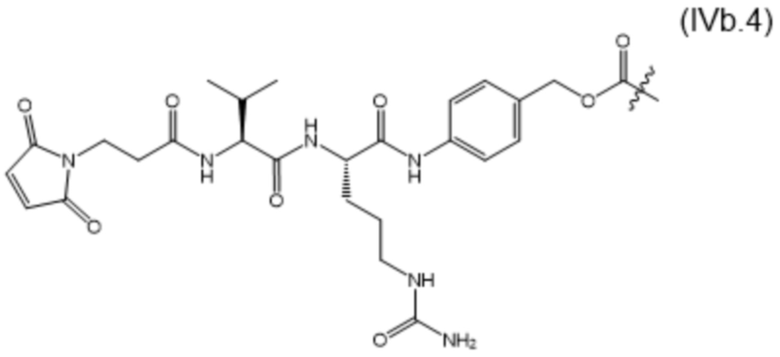
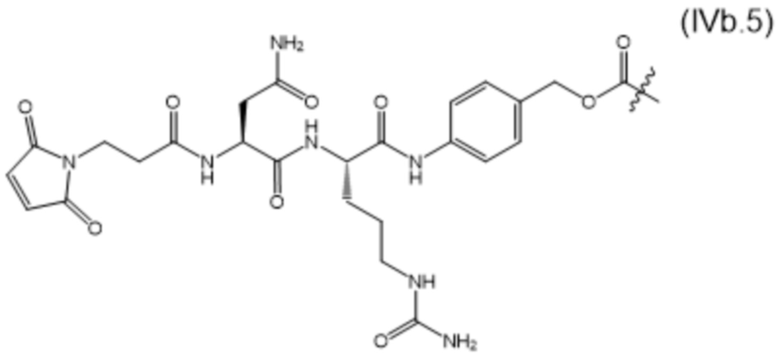
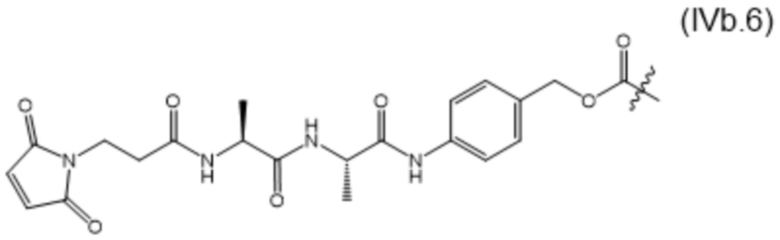
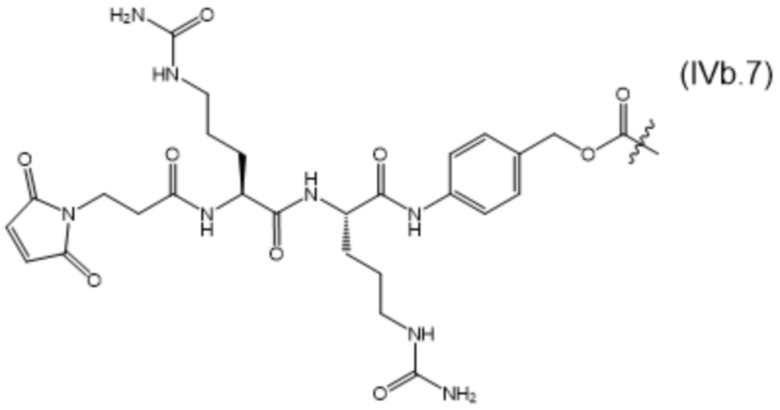
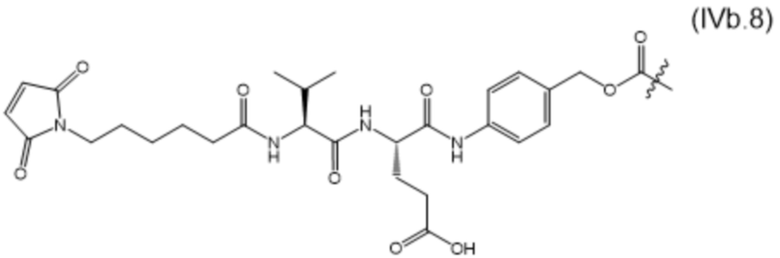
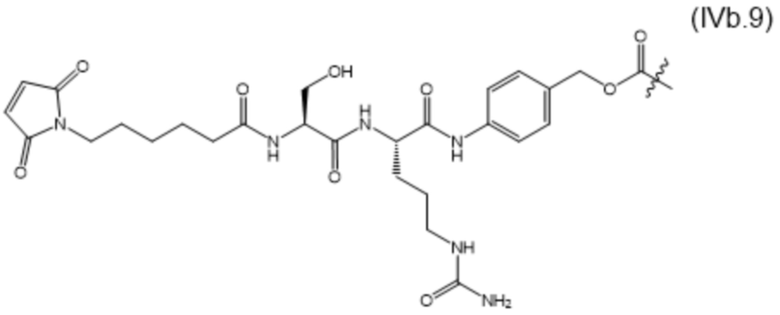
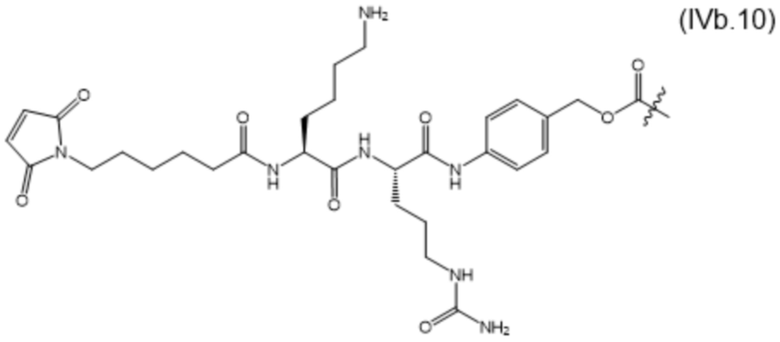
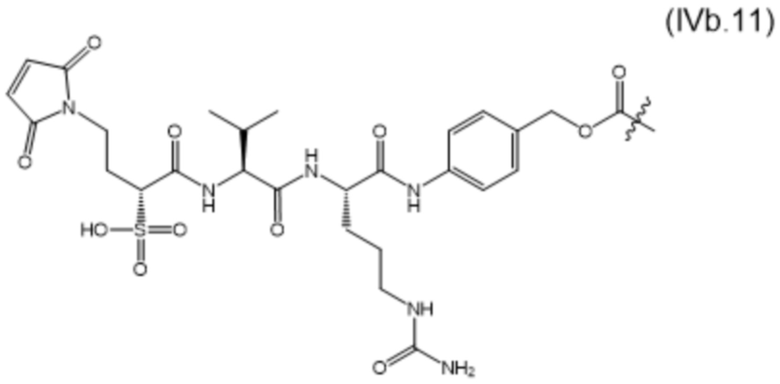
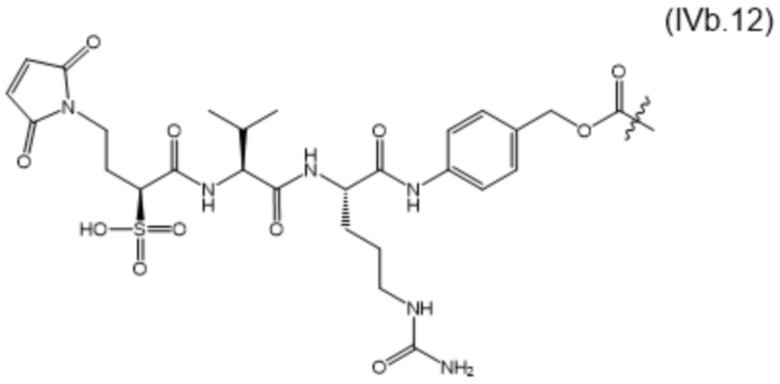
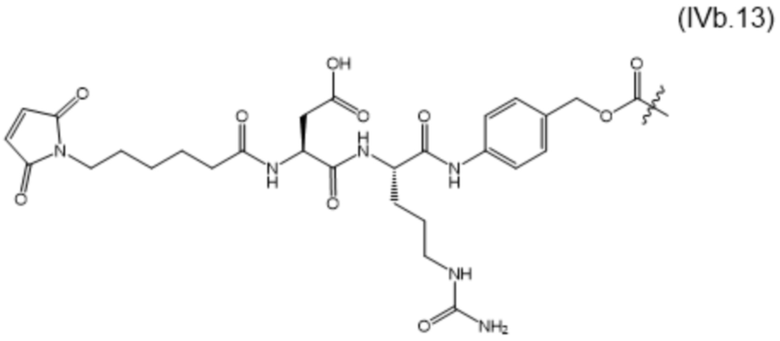
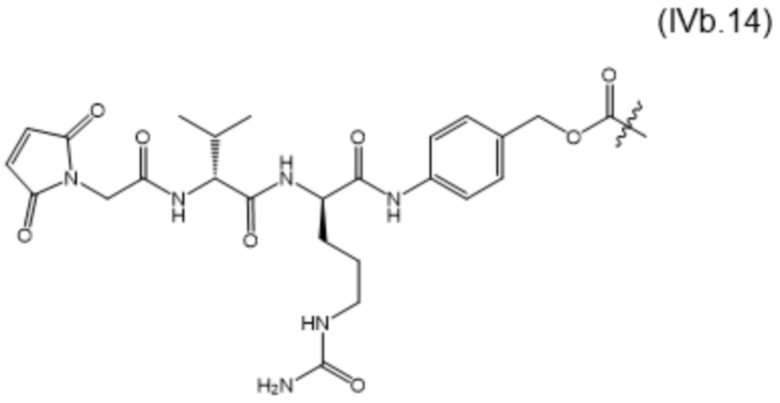
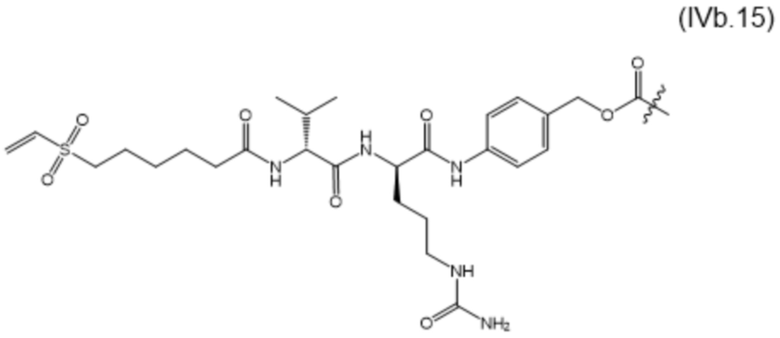
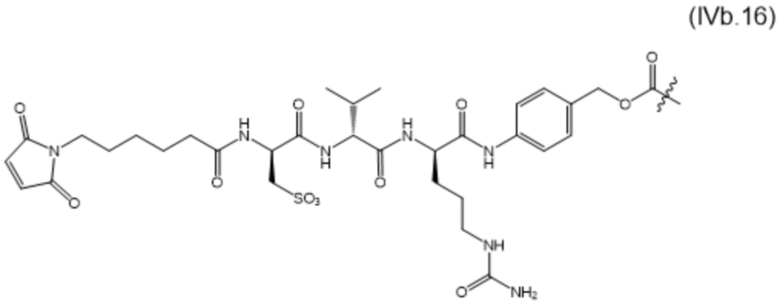
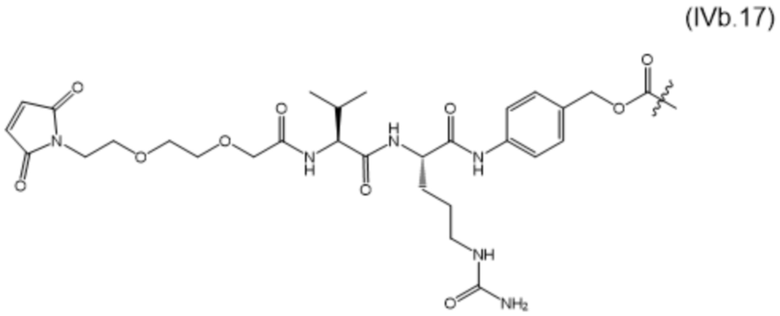
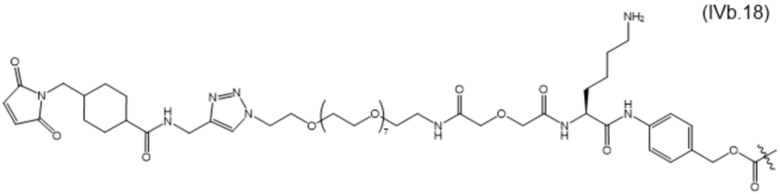
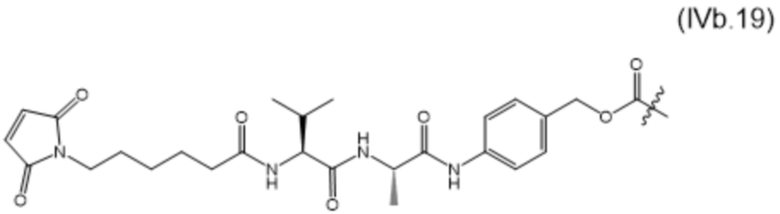
[0581] В определенных вариантах осуществления линкер для ADC содержит ферментативно расщепляемый пептидный фрагмент, например, линкер для ADC, предусматривающий структурную формулу (IVc) или (IVd):
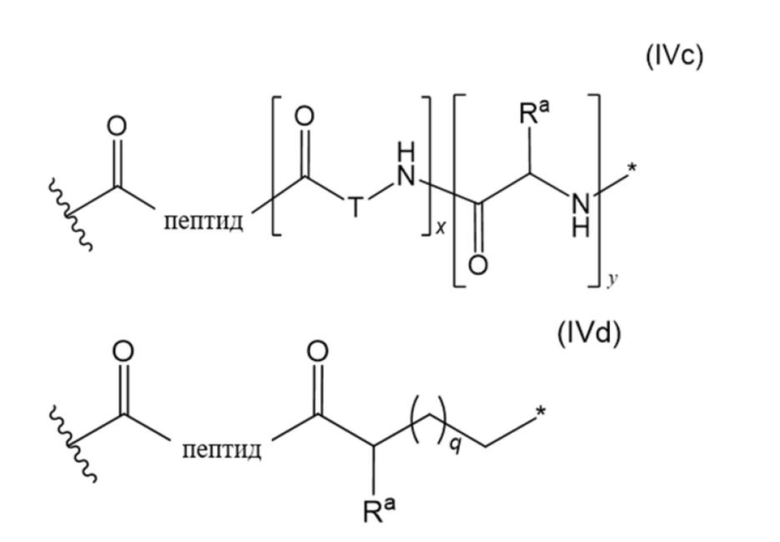
или его соль, где пептид представляет пептид (который проиллюстрирован в направлении C→N и в котором не показаны карбокси- и амино-"концы"), расщепляемый лизосомальным ферментом; T представляет полимер, содержащий одно или более этиленгликолевых звеньев или алкиленовую цепь или их комбинации; Ra выбран из водорода, алкила, сульфоната и метилсульфоната; p представляет целое число, находящееся в диапазоне от 0 до 5; q равняется 0 или 1; x равняется 0 или 1; y равняется 0 или 1;  x
x  представляет точку присоединения линкера для ADC к цитотоксическому и/или цитостатическому средству; и * представляет точку присоединения к остальной части линкера для ADC.
представляет точку присоединения линкера для ADC к цитотоксическому и/или цитостатическому средству; и * представляет точку присоединения к остальной части линкера для ADC.
[0582] Конкретные иллюстративные варианты осуществления линкеров для ADC в соответствии со структурной формулой (IVc), которые могут быть включены в ADC, включают линкеры для ADC, проиллюстрированные ниже (как проиллюстрировано, линкеры для ADC содержат группу, подходящую для ковалентного связывания линкера для ADC с MBM):
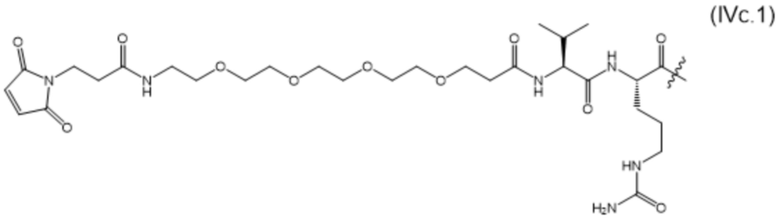
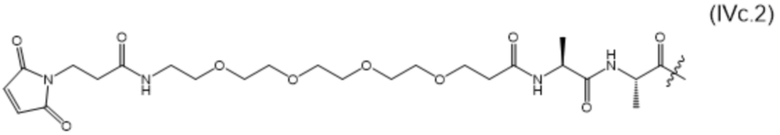
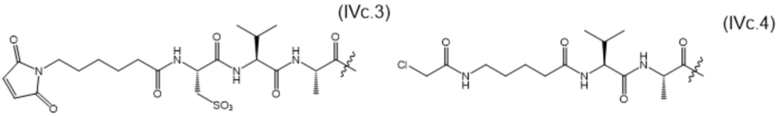
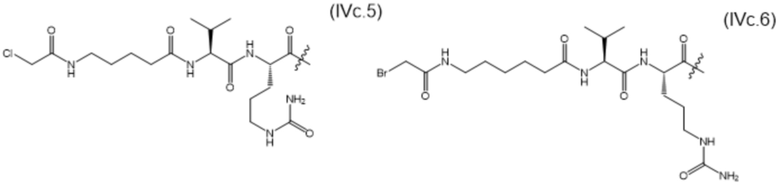
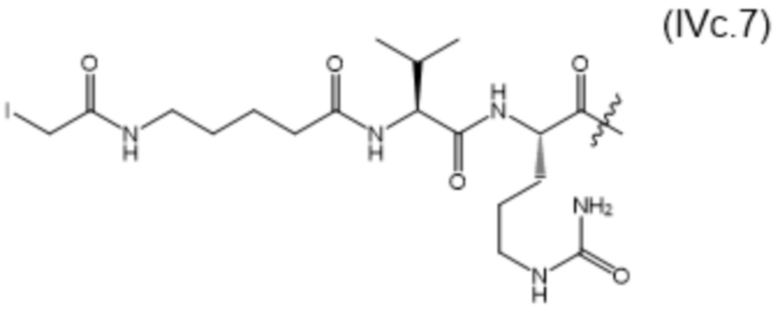
[0583] Конкретные иллюстративные варианты осуществления линкеров для ADC в соответствии со структурной формулой (IVd), которые могут быть включены в ADC, включают линкеры для ADC, проиллюстрированные ниже (как проиллюстрировано, линкеры для ADC содержат группу, подходящую для ковалентного связывания линкера для ADC с MBM):
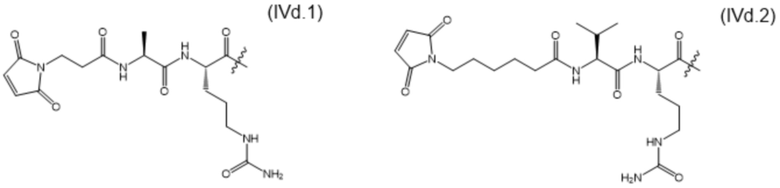
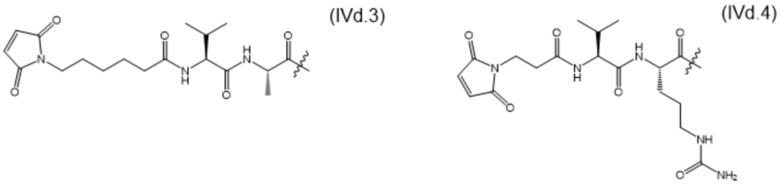
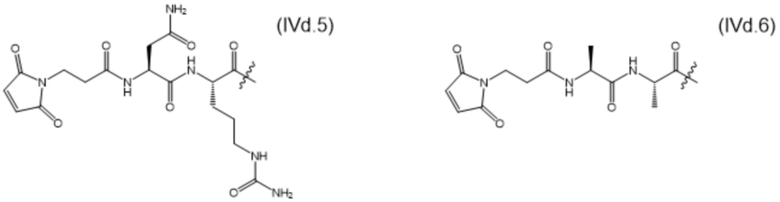
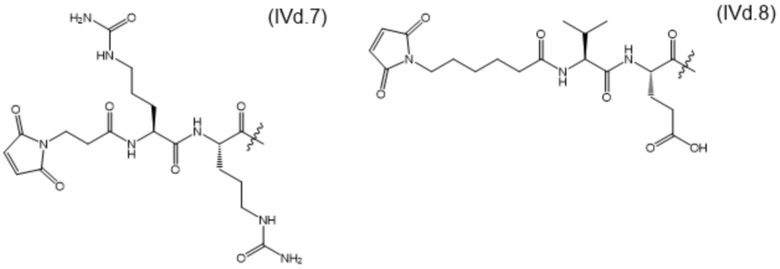
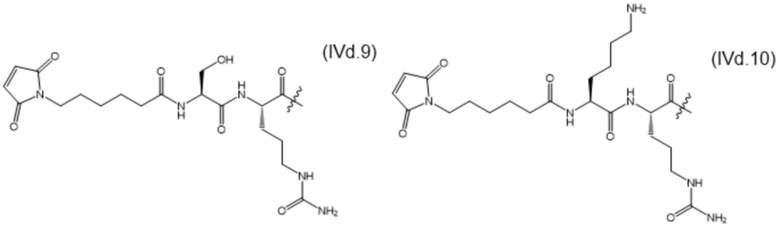
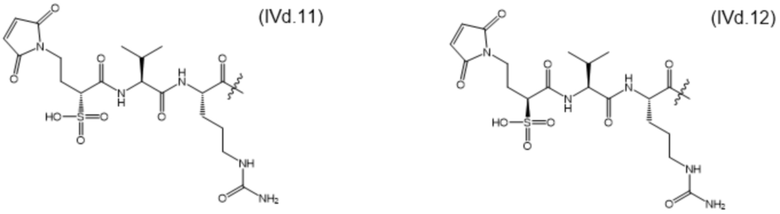
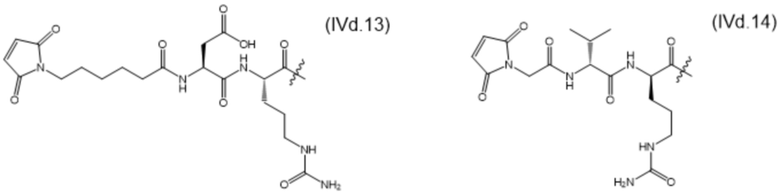
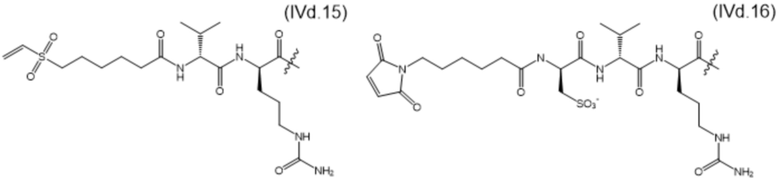
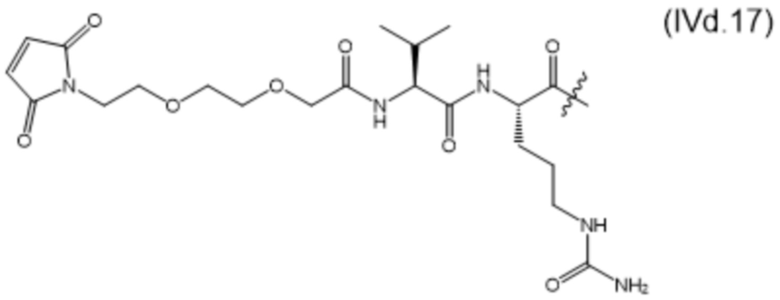
[0584] В определенных вариантах осуществления линкер для ADC, предусматривающий структурную формулу (IVa), (IVb), (IVc) или (IVd), дополнительно содержит карбонатный фрагмент, расщепляемый посредством воздействия кислой среды. В конкретных вариантах осуществления линкер для ADC присоединен к цитотоксическому и/или цитостатическому средству посредством атома кислорода.
7.10.2.2. Нерасщепляемые линкеры
[0585] Хотя расщепляемые линкеры для ADC могут обеспечивать определенные преимущества, линкеры для ADC, содержащие ADC, не обязательно должны быть расщепляемыми. В случае с нерасщепляемыми линкерами для ADC высвобождение лекарственного средства не зависит от различий в свойствах между плазмой крови и некоторыми цитоплазматическими компартментами. Высказано предположение, что высвобождение лекарственного средства происходит после интернализации ADC посредством антиген-опосредованного эндоцитоза и доставки в лизосомальный компартмент, где MBM разрушается до уровня аминокислот посредством внутриклеточного протеолитического разрушения. Данный способ обеспечивает высвобождение производного лекарственного средства, которое образовано лекарственным средством, линкером для ADC и аминокислотным остатком, к которому был ковалентно присоединен линкер для ADC. Аминокислотные метаболиты лекарственных средств из конъюгатов с нерасщепляемыми линкерами для ADC являются более гидрофильными и обычно характеризуются меньшей способностью к проникновению через мембраны, что приводит к менее интенсивным эффектам "свидетеля" и менее интенсивным проявлениям неспецифической токсичности по сравнению с конъюгатами с расщепляемым линкером для ADC. В целом, ADC с нерасщепляемыми линкерами для ADC характеризуются большей стабильностью в кровотоке, чем ADC с расщепляемыми линкерами для ADC. Нерасщепляемые линкеры для ADC могут представлять собой алкиленовые цепи или могут быть полимерными по природе, такими как, например, полимеры на основе полиалкиленгликоля, амидные полимеры, или могут содержать сегменты алкиленовых цепей, полиалкиленгликолей и/или амидных полимеров.
[0586] Были описаны разнообразные нерасщепляемые линкеры для ADC, применяемые для связывания лекарственных средств с МBM. См. Jeffrey et al., 2006, Bioconjug. Chem. 17; 831-840; Jeffrey et al., 2007, Bioorg. Med. Chem. Lett. 17:2278-2280; и Jiang et al., 2005, J. Am. Chem. Soc. 127:11254-11255. Все эти линкеры для ADC могут быть включены в ADC по настоящему изобретению.
[0587] В определенных вариантах осуществления линкер для ADC является нерасщепляемым in vivo, например, линкер для ADC в соответствии со структурной формулой (VIa), (VIb), (VIc) или (VId) (как проиллюстрировано, линкеры для ADC содержат группу, подходящую для ковалентного связывания линкера для ADC с MBM):
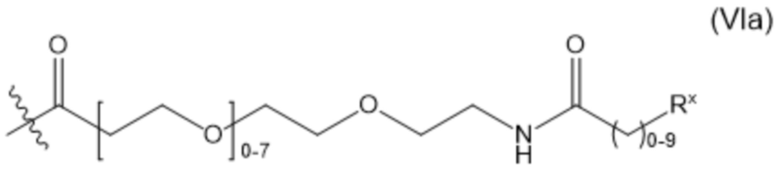
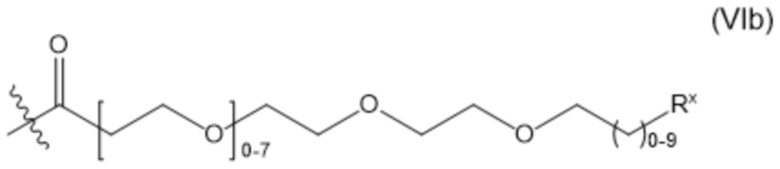

или его соли, где: Ra выбран из водорода, алкила, сульфоната и метилсульфоната; Rx представляет собой фрагмент, содержащий функциональную группу, способную ковалентно связывать линкер для ADC с MBM; и  представляет точку присоединения линкера для ADC к цитотоксическому и/или цитостатическому средству.
представляет точку присоединения линкера для ADC к цитотоксическому и/или цитостатическому средству.
[0588] Конкретные иллюстративные варианты осуществления линкеров для ADC в соответствии со структурной формулой (VIa)-(VId), которые могут быть включены в ADC, включают линкеры для ADC, проиллюстрированные ниже (как проиллюстрировано, линкеры для ADC содержат группу, подходящую для ковалентного связывания линкера для ADC с MBM, и 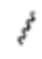 представляет точку присоединения к цитотоксическому и/или цитостатическому средству):
представляет точку присоединения к цитотоксическому и/или цитостатическому средству):

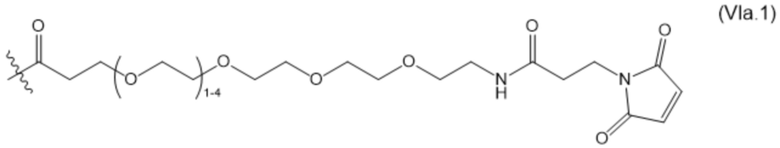
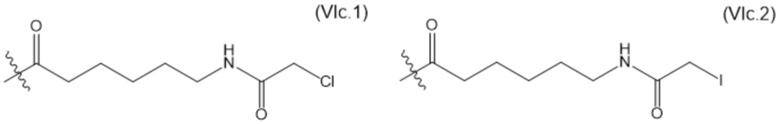
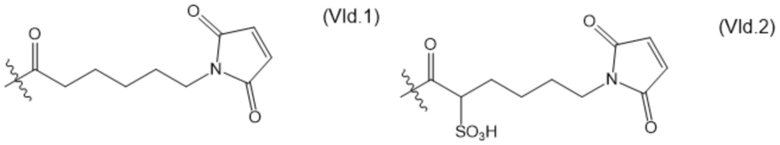
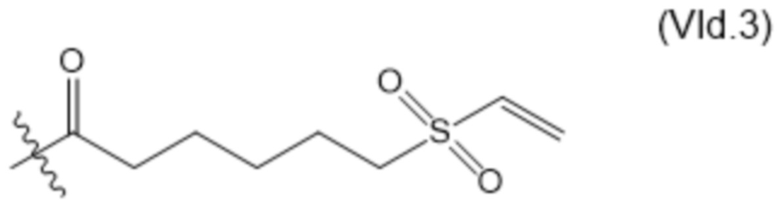
7.10.2.3. Группы, применяемые для присоединения линкеров к МBM
[0589] Для присоединения синтонов линкер для ADC-лекарственное средство к MBM (например, TBM) с получением ADC можно применять разнообразные группы. Группы для присоединения могут являться электрофильными по своей природе и включают в себя малеимидные группы, активированные дисульфидные группы, активные сложноэфирные группы, такие как NHS-сложноэфирные группы и HOBt-сложноэфирные группы, галогенформиатные группы, галогенангидридные группы, алкил- и бензилгалогенидные группы, такие как галогенацетамидные группы. Как обсуждается ниже, существуют также перспективные технологии, связанные с "самостабилизирующимися" малеимидами и "мостикообразующими дисульфидами", которые можно применять в соответствии с настоящим изобретением. Выбор конкретной применяемой группы будет частично зависеть от сайта присоединения к MBM.
[0590] Один пример "самостабилизирующейся" малеимидной группы, которая самопроизвольно гидролизуется в условиях конъюгации с MBM с получением молекул ADC с улучшенной стабильностью, изображен на схеме ниже. См. US20130309256 A1; также Lyon et al., Nature Biotech, опубликованный в режиме онлайн, doi:10.1038/nbt.2968.
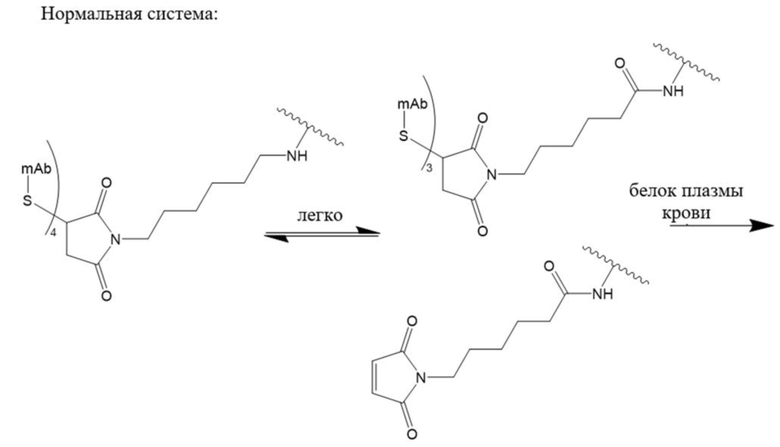
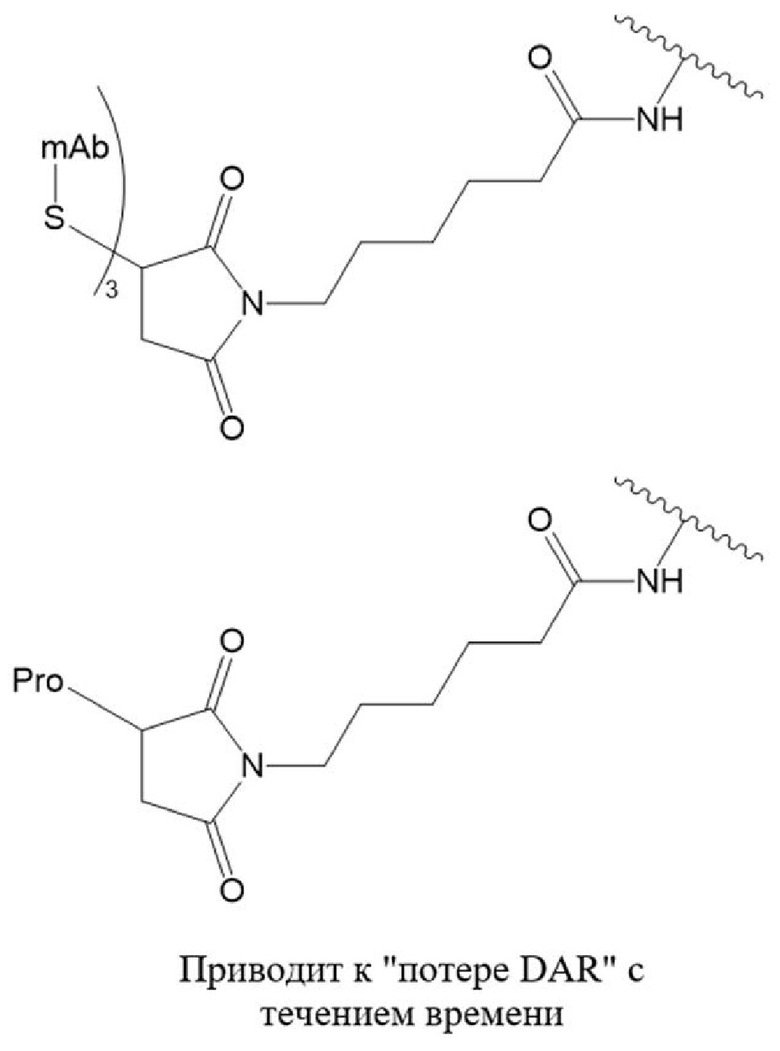
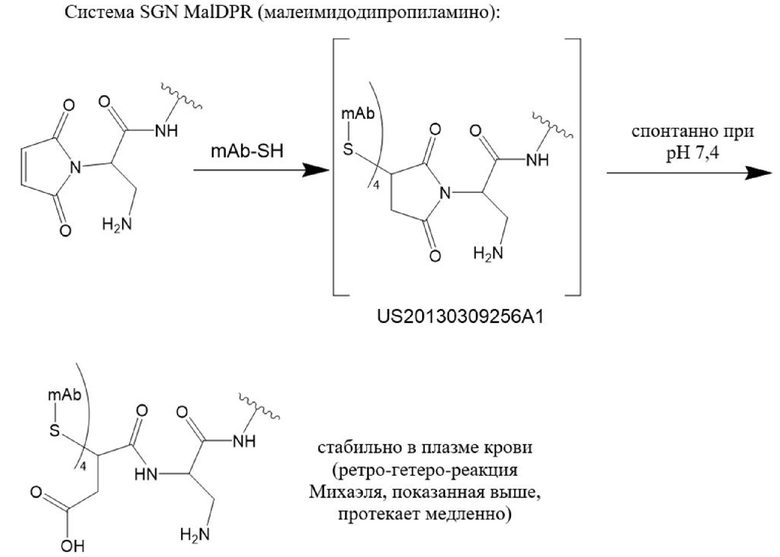
[0591] PolyTherics раскрыли способ образования мостика между парой сульфгидрильных групп, полученных в результате восстановления нативной дисульфидной связи в шарнирном участке. См. Badescu et al., 2014, Bioconjugate Chem. 25:1124-1136. Реакция изображена на схеме ниже. Преимущество данной методики состоит в возможности синтезировать обогащенные ADC с DAR4 посредством полного восстановления молекул IgG (с получением 4 пар сульфгидрильных групп) с последующей реакцией с 4 эквивалентами алкилирующего средства. ADC, содержащие "мостиковые дисульфиды", обладают увеличенной стабильностью.
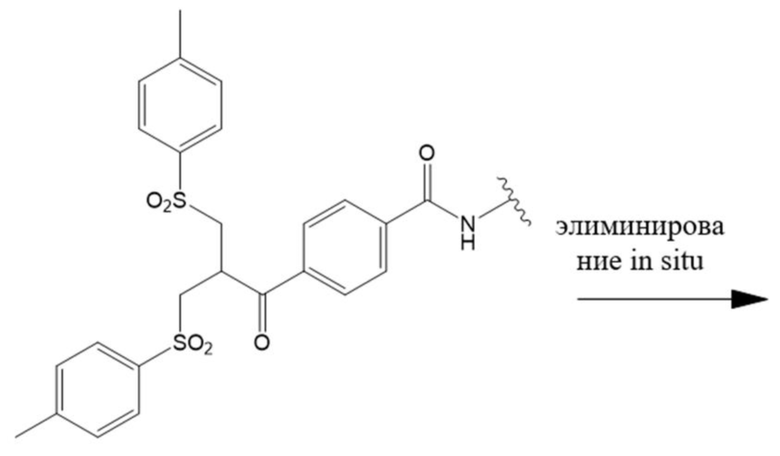
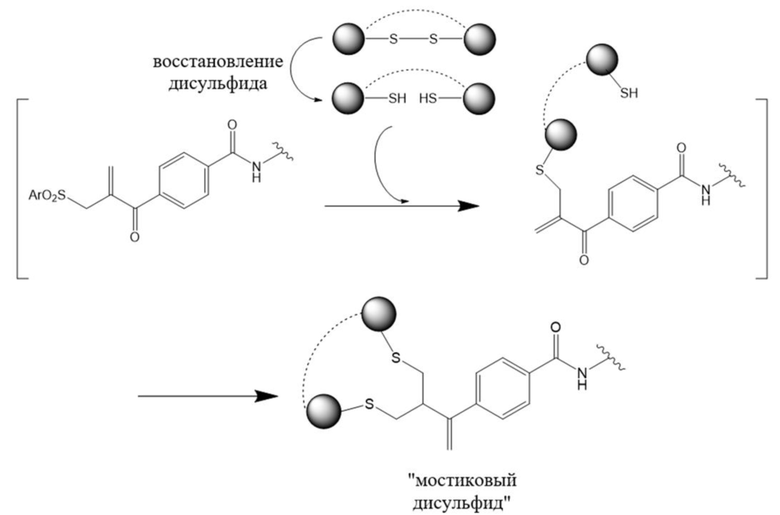
[0592] Аналогичным образом, как изображено ниже, было разработано малеимидное производное (1, ниже), которое способно к образованию мостика между парой сульфгидрильных групп. См. WO2013/085925.
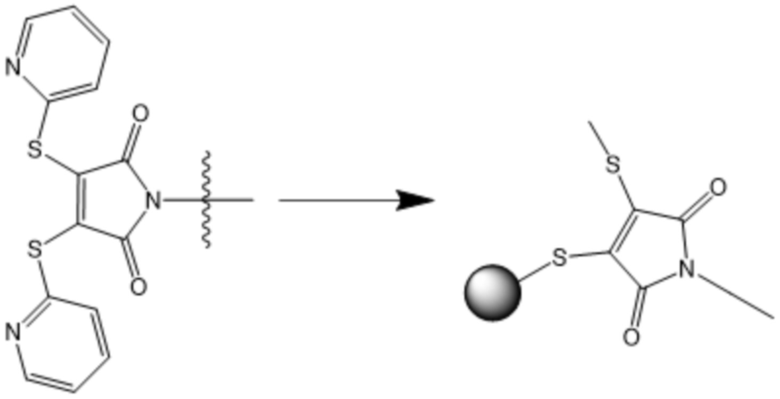
7.10.2.4. Критерии выбора линкеров для ADC
[0593] Как известно специалистам в данной области, на выбор линкера для ADC для конкретного ADC могут влиять разнообразные факторы, в том числе без ограничения сайт присоединения к MBM (например, Lys, Cys или другие аминокислотные остатки), структурные ограничения фармакофора лекарственного средства и липофильность лекарственного средства. Конкретный линкер для ADC, выбранный для ADC, должен стремиться сбалансировать эти различные факторы для конкретной комбинации MBM/лекарственное средство. Для обзора факторов, которые влияют на выбор линкеров для ADC в ADC, см. Nolting, Chapter 5 "Linker Technology in Antibody-Drug Conjugates", в Antibody-Drug Conjugates: Methods in Molecular Biology, vol. 1045, pp. 71-100, Laurent Ducry (Ed.), Springer Science & Business Medica, LLC, 2013.
[0594] Например, наблюдалось, что ADC осуществляют уничтожение антиген-отрицательных клеток-"свидетелей", присутствующих поблизости от антиген-положительных опухолевых клеток. Механизм уничтожения клеток-"свидетелей" посредством ADC указывает на то, что в этом могут играть роль продукты метаболизма, образующиеся во время внутриклеточного процессинга ADC. Нейтральные цитотоксические метаболиты, образующиеся в ходе метаболизма ADC в антиген-положительных клетках, по-видимому, играют роль в уничтожении клеток-"свидетелей", тогда как заряженные метаболиты могут быть лишены возможности диффундировать через мембрану в среду и, следовательно, не способны оказывать влияние на уничтожение клеток-"свидетелей". В определенных вариантах осуществления линкер для ADC выбран с целью ослабления эффекта уничтожения клеток-"свидетелей", обусловленного клеточными метаболитами ADC. В определенных вариантах осуществления линкер для ADC выбран с целью увеличения эффекта уничтожения клеток-"свидетелей".
[0595] Свойства линкера для ADC могут также влиять на агрегацию ADC в условиях применения и/или хранения. Как правило, ADC, о которых сообщалось в литературе, содержат не более 3-4 молекул лекарственного средства на молекулу антитела (см., например, Chari, 2008, Acc Chem Res 41:98-107). Попытки достижения более высоких соотношений лекарственное средство/антитело ("DAR") часто не имели успеха, в частности из-за агрегации ADC, если как лекарственное средство, так и линкер для ADC были гидрофобными (King et al., 2002, J Med Chem 45:4336-4343; Hollander et al., 2008, Bioconjugate Chem 19:358-361; Burke et al., 2009 Bioconjugate Chem 20:1242-1250). Во многих случаях значения DAR выше 3-4 могут являться благоприятными в качестве средств, обеспечивающих увеличение активности. В случаях, если цитотоксическое и/или цитостатическое средство является гидрофобным по природе, может потребоваться выбрать линкеры для ADC, которые являются относительно гидрофильными, в качестве средств, обеспечивающих снижение агрегации ADC, особенно в случаях, когда требуются значения DAR, составляющие более 3-4. Таким образом, в определенных вариантах осуществления линкер для ADC содержит в своем составе химические фрагменты, которые обеспечивают снижение агрегации ADC во время хранения и/или применения. Линкер для ADC может содержать в своем составе полярные или гидрофильные группы, такие как заряженные группы или группы, которые становятся заряженными при физиологическом значении pH, для снижения агрегации ADC. Например, линкер для ADC может содержать в своем составе заряженные группы, такие как соли, или группы, которые депротонируются, например, карбоксилатные группы, или протонируются, например, аминные группы, при физиологическом значении pH.
[0596] Иллюстративные поливалентные линкеры для ADC, о которых сообщалось, что они обеспечивают достижение значений DAR, достигающих 20, которые можно применять для связывания многочисленных цитотоксических и/или цитостатических средств с MBM, описаны в WO 2009/073445; WO 2010/068795; WO 2010/138719; WO 2011/120053; WO 2011/171020; WO 2013/096901; WO 2014/008375; WO 2014/093379; WO 2014/093394; WO 2014/093640.
[0597] В конкретных вариантах осуществления агрегация ADC во время хранения или применения составляет менее чем приблизительно 10%, как определено посредством эксклюзионной хроматографии (SEC). В конкретных вариантах осуществления агрегация ADC во время хранения или применения составляет менее 10%, например, менее чем приблизительно 5%, менее чем приблизительно 4%, менее чем приблизительно 3%, менее чем приблизительно 2%, менее чем приблизительно 1%, менее чем приблизительно 0,5%, менее чем приблизительно 0,1% или даже ниже, как определено посредством эксклюзионной хроматографии (SEC).
7.10.3. Способы получения ADC
[0598] ADC можно синтезировать с применением химических веществ, которые являются широко известными. Выбор химических веществ будет зависеть, среди прочего, от отличительных характеристик цитотоксического(цитотоксических) и/или цитостатического(цитостатических) средства(средств), линкера для ADC и групп, применяемых для присоединения линкера для ADC к МBM. ADC в соответствии с формулой (I) обычно можно получать в соответствии со следующей схемой:
D-L-Rx+Ab-Ry→[D-L-XY]n-Ab (I),
[0599] где D, L, Ab, XY и n являются такими, как определено ранее, и Rx и Ry представляют комплементарные группы, способные к образованию ковалентных связей друг с другом, как обсуждается выше.
[0600] Отличительные характеристики групп Rx и Ry будут зависеть от химического вещества, применяемого для связывания синтона D-L-Rx с MBM. Применяемое химическое вещество обычно не должно изменять функциональные характеристики МBM, например, ее способность связывать свою мишень. В некоторых случаях свойства связывания конъюгированного антитела будут очень похожими на свойства связывания неконъюгированной MBM. Разнообразные химические вещества и методики для конъюгации молекул с биологическими молекулами и, в частности, с иммуноглобулинами, компоненты которых, как правило, являются структурными элементами МBM по настоящему изобретению, являются широко известными. См., например, Amon et al., "Monoclonal Antibodies For Immunotargeting Of Drugs In Cancer Therapy", в Monoclonal Antibodies And Cancer Therapy, Reisfeld et al. Eds., Alan R. Liss, Inc., 1985; Hellstrom et al., "Antibodies For Drug Delivery", в Controlled Drug Delivery, Robinson et al. Eds., Marcel Dekker, Inc., 2nd Ed. 1987; Thorpe, "Antibody Carriers Of Cytotoxic Agents In Cancer Therapy: A Review", в Monoclonal Antibodies '84: Biological And Clinical Applications, Pinchera et al., Eds., 1985; "Analysis, Results, and Future Prospective of the Therapeutic Use of Radiolabeled Antibody In Cancer Therapy", в Monoclonal Antibodies For Cancer Detection And Therapy, Baldwin et al., Eds., Academic Press, 1985; Thorpe et al., 1982, Immunol. Rev. 62:119-58; PCT-публикацию WO 89/12624. Любое из этих химических веществ можно применять для связывания синтонов с MBM.
[0601] Известен ряд функциональных групп Rx и химических веществ, применимых для связывания синтонов с доступными остатками лизина, и они включают, в качестве примера и без ограничения, NHS-сложные эфиры и изотиоцианаты.
[0602] Известен ряд функциональных групп Rx и химических веществ, применимых для связывания синтонов с доступными свободными сульфгидрильными группами остатков цистеина, и они включают, в качестве примера и без ограничения, галогенацетильные группы и малеимидные группы.
[0603] Однако химические вещества для конъюгации не ограничены доступными группами боковых цепей. Боковые цепи, такие как аминогруппы, можно превращать в другие применимые группы, такие как гидроксильные группы, посредством связывания подходящей малой молекулы с аминогруппой. Данную стратегию можно применять для увеличения количества доступных сайтов связывания в антителе посредством конъюгации малых молекул с несколькими функциональными группами с боковыми цепями доступных аминокислотных остатков МBM. Функциональные группы Rx, подходящие для ковалентного связывания синтонов с этими "превращенными" функциональными группами, затем включаются в синтоны.
[0604] МBM можно также сконструировать таким образом, чтобы она содержала аминокислотные остатки для конъюгации. Подход к конструированию MBM таким образом, чтобы они содержали аминокислотные остатки, которые не кодируются генетически, применимые для конъюгации лекарственных средств в качестве составной части ADC, описан в Axup et al., 2012, Proc Natl Acad Sci USA. 109(40):16101-16106, равно как и химические вещества и функциональные группы, применимые для связывания синтонов с некодируемыми аминокислотами.
[0605] Как правило, синтоны связаны с боковыми цепями аминокислотных остатков MBM, в том числе, например, с первичной аминогруппой доступных остатков лизина или сульфгидрильной группой доступных остатков цистеина. Свободные сульфгидрильные группы можно получать посредством восстановления межцепочечных дисульфидных связей.
[0606] В случае со связями, где Ry представляет собой сульфгидрильную группу (например, если Rx представляет собой малеимид), MBM обычно вначале полностью или частично восстанавливают для разрушения межцепочечных дисульфидных мостиков между остатками цистеина.
[0607] Остатки цистеина, которые не принимают участия в образовании дисульфидных мостиков, можно встроить в МBM посредством модификации одного или более кодонов. Восстановление этих неспаренных остатков цистеина обеспечивает получение сульфгидрильной группы, подходящей для конъюгации. В некоторых вариантах осуществления MBM сконструирована с введением одного или более остатков цистеина в качестве сайтов для конъюгации с фрагментом, представляющим собой лекарственное средство (см. Junutula, et al, 2008, Nat Biotechnol, 26:925-932).
[0608] Сайты для замены на цистеин могут быть выбраны в константном участке для получения стабильных и однородных конъюгатов. MBM может содержать, например, две или больше замен на цистеин, и эти замены могут применяться в комбинации с другими способами модификации и конъюгации, описанными в данном документе. Известны способы обеспечения вставки цистеина в конкретные местоположения антитела, см., например, Lyons et al., 1990, Protein Eng., 3:703-708, WO 2011/005481, WO2014/124316, WO 2015/138615. В определенных вариантах осуществления MBM содержит замену одной или более аминокислот на цистеин в константном участке в положениях, выбранных из 117, 119, 121, 124, 139, 152, 153, 155, 157, 164, 169, 171, 174, 189, 205, 207, 246, 258, 269, 274, 286, 288, 290, 292, 293, 320, 322, 326, 333, 334, 335, 337, 344, 355, 360, 375, 382, 390, 392, 398, 400 и 422 тяжелой цепи, где положения пронумерованы согласно системе EU. В некоторых вариантах осуществления MBM содержит замену одной или более аминокислот на цистеин в константном участке в положениях, выбранных из 107, 108, 109, 114, 129, 142, 143, 145, 152, 154, 156, 159, 161, 165, 168, 169, 170, 182, 183, 197, 199 и 203 легкой цепи, где положения пронумерованы согласно системе EU, и где легкая цепь представляет собой легкую каппа-цепь человека. В определенных вариантах осуществления MBM содержит комбинацию из замен двух или более аминокислот на цистеин в константном участке, где комбинации включают замены в положении 375 тяжелой цепи, положении 152 тяжелой цепи, положении 360 тяжелой цепи или положении 107 легкой цепи, и где положения пронумерованы согласно системе EU. В определенных вариантах осуществления MBM содержит замену одной аминокислоты на цистеин в константном участке, где замена находится в положении 375 тяжелой цепи, положении 152 тяжелой цепи, положении 360 тяжелой цепи, положении 107 легкой цепи, положении 165 легкой цепи или положении 159 легкой цепи, и где положения пронумерованы согласно системе EU, и где легкая цепь представляет собой каппа-цепь.
[0609] В конкретных вариантах осуществления MBM содержит комбинацию замен двух аминокислот на цистеин в константных участках, где MBM содержит остатки цистеина в положениях 152 и 375 тяжелой цепи, где положения пронумерованы согласно системе EU.
[0610] В других конкретных вариантах осуществления MBM содержит замену одной аминокислоты на цистеин в положении 360 тяжелой цепи, где положения пронумерованы согласно системе EU.
[0611] В других конкретных вариантах осуществления MBM содержит замену одной аминокислоты на цистеин в положении 107 легкой цепи, где положения пронумерованы согласно системе EU, и где легкая цепь представляет собой каппа-цепь.
[0612] Другие положения для включения встроенных цистеиновых остатков могут включать в качестве примера и без ограничения положения S112C, S113C, A114C, S115C, A176C, 5180C, S252C, V286C, V292C, S357C, A359C, S398C, S428C (нумерация по Kabat) в тяжелой цепи IgG1 человека и положения V110C, S114C, S121C, S127C, S168C, V205C (нумерация по Kabat) в легкой каппа-цепи Ig человека (см., например, патент США № 7521541, патент США № 7855275 и патент США № 8455622).
[0613] MBM, применимые в ADC, раскрытых в данном документе, дополнительно или в качестве альтернативы могут быть модифицированы с введением одной или более других реакционноспособных аминокислот (отличных от цистеина), включая Pcl, пирролизин, пептидные метки (такие как метки S6, A1 и ybbR) и неприродные аминокислоты, вместо по меньшей мере одной аминокислоты из нативной последовательности с получением таким образом реакционноспособного сайта в MBM для конъюгации с фрагментом, представляющим собой лекарственное средство. Например, MBM могут быть модифицированы таким образом, чтобы они содержали в своем составе Pcl или пирролизин (W. Ou et al., 2011, PNAS, 108(26):10437-10442; WO2014124258) или неприродные аминокислоты (Axup, et al., 2012, PNAS, 109:16101-16106; для обзора см. C.C. Liu and P.G. Schultz, 2010, Annu Rev Biochem 79:413-444; Kim, et al., 2013, Curr Opin Chem Biol. 17:412-419) в качестве сайтов для конъюгации с лекарственным средством. Аналогичным образом, в МВМ могут быть введены пептидные метки для способов ферментативной конъюгации (см. Strop et al. 2013, Chem Biol. 20(2):161-7; Rabuka, 2010, Curr Opin Chem Biol. 14(6):790-6; Rabuka, et al., 2012, Nat Protoc. 7(6):1052-67). Еще одним примером является применение 4'-фосфопантетеинилтрансфераз (PPTазы) для конъюгации аналогов кофермента A (WO2013184514). Такие модифицированные или сконструированные MBM могут быть конъюгированы с полезными нагрузками или комбинациями линкер-полезная нагрузка в соответствии с известными способами.
[0614] Как будет понятно специалистам в данной области, количество средств (например, цитотоксических и/или цитостатических средств), связанных с молекулой МBM, может варьироваться, так что совокупность ADC может быть неоднородной по своей природе, где некоторые МBM содержат одно связанное средство, некоторые два, некоторые три и т. д. (и некоторые ни одного). Степень неоднородности будет зависеть, среди прочего, от химических веществ, применяемых для связывания средств. Например, если МBM восстанавливают с получением сульфгидрильных групп для присоединения, то часто получают неоднородные смеси МBM, содержащие ноль, 2, 4, 6 или 8 связанных средств на молекулу. Кроме того, посредством ограничения молярного соотношения для присоединяемого соединения часто получают МBM, содержащие ноль, 1, 2, 3, 4, 5, 6, 7 или 8 связанных средств на молекулу. Таким образом, будет понятно, что в зависимости от контекста установленные соотношения лекарственного средства и MBM (DTR) могут представлять собой средние значения для совокупности MBM. Например, "DTR4" может относиться к препарату на основе ADC, который не был подвергнут очистке для выделения конкретных пиков DTR и может содержать неоднородную смесь молекул ADC, содержащую различные количества присоединенных цитостатических и/или цитотоксических средств на МBM (например, 0, 2, 4, 6, 8 средств на МBM), но характеризующуюся средним соотношением лекарственное средство/МBM, составляющим 4. Аналогичным образом, в некоторых вариантах осуществления "DTR2" относится к неоднородному препарату на основе ADC, в котором среднее соотношение лекарственное средство/MBM составляет 2.
[0615] Если необходимы обогащенные препараты, то МBM, содержащие определенные количества связанных средств (например, цитотоксических и/или цитостатических средств), можно получать посредством очистки неоднородных смесей, например, посредством колоночной хроматографии, например, хроматографии гидрофобных взаимодействий.
[0616] Чистоту можно оценивать посредством различных известных способов. В качестве примера, препарат на основе ADC можно анализировать посредством HPLC или другой методики хроматографии, а чистоту оценивать посредством анализа площадей под кривыми полученных в результате пиков.
7.11. Фармацевтические композиции
[0617] МBM (например, TBM) (а также их конъюгаты; ссылки на МBM в настоящем изобретении также относятся к конъюгатам, содержащим МBM, таким как ADC, если контекст не предусматривает иное) можно составлять в виде фармацевтических композиций, содержащих МBM, например, содержащих один или более фармацевтически приемлемых наполнителей или носителей. Для получения фармацевтических или стерильных композиций, содержащих МBM по настоящему изобретению, препарат на основе МBM можно объединять с одним или более фармацевтически приемлемыми наполнителями или носителями.
[0618] Например, составы на основе MBM можно получать посредством смешивания MBM с физиологически приемлемыми носителями, наполнителями или стабилизаторами в форме, например, лиофилизированных порошков, взвесей, водных растворов, лосьонов или суспензий (см., например, Hardman et al., 2001, Goodman and Gilman's The Pharmacological Basis of Therapeutics, McGraw-Hill, New York, N.Y.; Gennaro, 2000, Remington: The Science and Practice of Pharmacy, Lippincott, Williams, and Wilkins, New York, N.Y.; Avis, et al. (eds.), 1993, Pharmaceutical Dosage Forms: General Medications, Marcel Dekker, NY; Lieberman, et al. (eds.), 1990, Pharmaceutical Dosage Forms: Tablets, Marcel Dekker, NY; Lieberman, et al. (eds.), 1990, Pharmaceutical Dosage Forms: Disperse Systems, Marcel Dekker, NY; Weiner and Kotkoskie, 2000, Excipient Toxicity and Safety, Marcel Dekker, Inc., New York, N.Y.).
[0619] Выбор режима введения МBM зависит от нескольких факторов, в том числе скорости метаболизма МBM в сыворотке крови или ткани, уровня тяжести симптомов, иммуногенности МBM и доступности клеток-мишеней. В определенных вариантах осуществления режим введения предусматривает максимальное количество МBM, доставляемой субъекту в соответствии с приемлемым уровнем побочных эффектов. Соответственно, количество доставляемой МBM частично зависит от конкретной МBM и тяжести состояния, лечение которого осуществляют. Доступно руководство по выбору подходящих доз антител и малых молекул (см., например, Wawrzynczak, 1996, Antibody Therapy, Bios Scientific Pub. Ltd, Oxfordshire, UK; Kresina (ed.), 1991, Monoclonal Antibodies, Cytokines and Arthritis, Marcel Dekker, New York, N.Y.; Bach (ed.), 1993, Monoclonal Antibodies and Peptide Therapy in Autoimmune Diseases, Marcel Dekker, New York, N.Y.; Baert et al., 2003, New Engl. J. Med. 348:601-608; Milgrom et al., 1999, New Engl. J. Med. 341:1966-1973; Slamon et al., 2001, New Engl. J. Med. 344:783-792; Beniaminovitz et al., 2000, New Engl. J. Med. 342:613-619; Ghosh et al., 2003, New Engl. J. Med. 348:24-32; Lipsky et al., 2000, New Engl. J. Med. 343:1594-1602).
[0620] Определение подходящей дозы выполняет лечащий врач, например, с использованием параметров или факторов, которые, как известно или предполагается из уровня техники, влияют на лечение или согласно прогнозам влияют на лечение. Введение доз обычно начинают с количества, несколько меньшего, чем оптимальная доза, и после этого его увеличивают с небольшими приращениями до тех пор, пока не достигается требуемый или оптимальный эффект по сравнению с любыми отрицательными побочными эффектами. Важные диагностические показатели включают, например, показатели симптомов воспаления или уровня продуцируемых воспалительных цитокинов.
[0621] Фактические уровни доз MBM в фармацевтических композициях по настоящему изобретению можно изменять таким образом, чтобы получить количество MBM, которое является эффективным для достижения требуемого терапевтического ответа для конкретного субъекта, композиции и способа введения, не являясь токсичным для субъекта. Выбранный уровень дозы будет зависеть от разнообразных фармакокинетических факторов, в том числе активности конкретной МBM, пути введения, времени введения, скорости экскреции конкретной используемой МBM, продолжительности лечения, других средств (например, активных средств, таких как терапевтические лекарственные средства или соединения и/или инертные материалы, применяемые в качестве носителей) в комбинации с конкретной используемой МBM, возраста, пола, веса, состояния, общего состояния здоровья и анамнеза субъекта, получающего лечение, и подобных факторов, известных в области медицины.
[0622] Композиции, содержащие МBM, можно предоставлять посредством непрерывной инфузии или посредством введения доз с интервалами, составляющими, например, один день, одну неделю, или 1-7 раз в неделю. Дозы можно предоставлять внутривенно, подкожно, местно, перорально, назально, ректально, внутримышечно, интрацеребрально или посредством ингаляции. Иллюстративный протокол введения доз предусматривает максимальную дозу или частоту введения доз, при которых удается избежать значительных нежелательных побочных эффектов.
[0623] Эффективное количество для конкретного субъекта может варьироваться в зависимости от таких факторов, как состояние, лечение которого осуществляют, общее состояние здоровья субъекта, путь и доза введения согласно способу и тяжесть побочных эффектов (см., например, Maynard, et al. (1996) A Handbook of SOPs for Good Clinical Practice, Interpharm Press, Boca Raton, Fla.; Dent (2001) Good Laboratory and Good Clinical Practice, Urch Publ., London, UK).
[0624] Путь введения может представлять собой введение посредством, например, местного или накожного применения, инъекции или инфузии путем внутривенного, внутрибрюшинного, интрацеребрального, внутримышечного, внутриглазного, внутриартериального, интрацереброспинального, внутриочагового введения или посредством систем с замедленным высвобождением или имплантата (см., например, Sidman et al., 1983, Biopolymers 22:547-556; Langer et al., 1981, J. Biomed. Mater. Res. 15:167-277; Langer, 1982, Chem. Tech. 12:98-105; Epstein et al., 1985, Proc. Natl. Acad. Sci. USA 82:3688-3692; Hwang et al., 1980, Proc. Natl. Acad. Sci. USA 77:4030-4034; патенты США №№ 6350466 и 6316024). При необходимости композиция также может содержать солюбилизирующее средство и анестетик местного действия, такой как лидокаин, для облегчения боли в месте инъекции. Кроме того, внутрилегочное введение также можно использовать, например, путем применения ингалятора или небулайзера и состава с аэрозолирующим средством. См., например, патенты США №№ 6019968, 5985320, 5985309, 5934272, 5874064, 5855913, 5290540 и 4880078; а также PCT-публикации №№ WO 92/19244, WO 97/32572, WO 97/44013, WO 98/31346 и WO 99/66903.
[0625] Композицию по настоящему изобретению также можно вводить посредством одного или более путей введения с применением одного или более из множества известных способов. Как будет понятно специалисту в данной области, путь и/или способ введения будут варьироваться в зависимости от требуемых результатов. Выбранные пути введения для МBM включают внутривенный, внутримышечный, внутрикожный, внутрибрюшинный, подкожный, спинальный или другие системные пути введения, например, посредством инъекции или инфузии. Системное введение может представлять собой способы введения, отличные от энтерального и местного введения, обычно посредством инъекции, и включает без ограничения внутривенную, внутримышечную, внутриартериальную, интратекальную, интракапсулярную, внутриглазничную, внутрисердечную, внутрикожную, внутрибрюшинную, транстрахеальную, подкожную, субкутикулярную, внутрисуставную, подкапсульную, субарахноидальную, интраспинальную, эпидуральную и интрастернальную инъекцию и инфузию. В качестве альтернативы, композицию по настоящему изобретению можно вводить посредством пути, отличного от системного, такого как местный, эпидермальный или мукозальный путь введения, например, интраназально, перорально, вагинально, ректально, сублингвально или местно. В одном варианте осуществления МBM вводят посредством инфузии. В другом варианте осуществления MBM вводят подкожно.
[0626] Если MBM вводят в системе с контролируемым высвобождением или замедленным высвобождением, то можно применять насос для достижения контролируемого или замедленного высвобождения (см. Langer, выше; Sefton, 1987, CRC Crit. Ref Biomed. Eng. 14:20; Buchwald et al., 1980, Surgery 88:507; Saudek et al., 1989, N. Engl. J. Med. 321:574). Для достижения контролируемого или замедленного высвобождения средств терапии по настоящему изобретению можно применять полимерные материалы (см., например, Medical Applications of Controlled Release, Langer and Wise (eds.), CRC Pres., Boca Raton, Fla. (1974); Controlled Drug Bioavailability, Drug Product Design and Performance, Smolen and Ball (eds.), Wiley, New York (1984); Ranger and Peppas, 1983, J., Macromol. Sci. Rev. Macromol. Chem. 23:61; см. также Levy et al., 1985, Science 228:190; During et al., 1989, Ann. Neurol. 25:351; Howard et al., 1989, J. Neurosurg. 71:105); патент США № 5679377; патент США № 5916597; патент США № 5912015; патент США № 5989463; патент США № 5128326; PCT-публикацию № WO 99/15154 и PCT-публикацию № WO 99/20253. Примеры полимеров, применяемых в составах с замедленным высвобождением, включают без ограничения поли(2-гидроксиэтилметакрилат), поли(метилметакрилат), поли(акриловую кислоту), сополимер этилена и винилацетата, поли(метакриловую кислоту), полигликолиды (PLG), полиангидриды, поли(N-винилпирролидон), поли(виниловый спирт), полиакриламид, поли(этиленгликоль), полилактиды (PLA), сополимеры лактида и гликолида (PLGA) и сложные полиортоэфиры. В одном варианте осуществления полимер, применяемый в составе с замедленным высвобождением, является инертным, не содержащим выщелачиваемые примеси, стабильным при хранении, стерильным и биоразлагаемым. Систему с контролируемым или замедленным высвобождением можно поместить вблизи профилактической или терапевтической мишени, благодаря чему будет требоваться только часть системной дозы (см., например, Goodson, в Medical Applications of Controlled Release, выше, vol. 2, pp. 115-138 (1984)).
[0627] Системы с контролируемым высвобождением обсуждаются в обзоре Langer (1990, Science 249:1527-1533). Любую методику, известную специалисту в данной области, можно применять для получения составов с замедленным высвобождением, содержащих одну или более МBM по настоящему изобретению. См., например, патент США № 4526938, PCT-публикацию WO 91/05548, PCT-публикацию WO 96/20698, Ning et al., 1996, Radiotherapy & Oncology 39:179-189, Song et al., 1995, PDA Journal of Pharmaceutical Science & Technology 50:372-397, Cleek et al., 1997, Pro. Int'l. Symp. Control. Rel. Bioact. Mater. 24:853-854, и Lam et al., 1997, Proc. Int'l. Symp. Control Rel. Bioact. Mater. 24:759-760.
[0628] Если MBM вводят местно, то они могут быть составлены в форме мази, крема, трансдермального пластыря, лосьона, геля, шампуня, спрея, аэрозоля, раствора, эмульсии или другой формы, хорошо известной специалисту в данной области. См., например, Remington's Pharmaceutical Sciences and Introduction to Pharmaceutical Dosage Forms, 19th ed., Mack Pub. Co., Easton, Pa. (1995). В случае с нераспыляемыми лекарственными формами для местного применения обычно используют формы от вязких до полутвердых или твердых, содержащие носитель или один или более наполнителей, совместимые с местным применением и в некоторых случаях характеризующиеся большей динамической вязкостью, чем у воды. Подходящие составы включают без ограничения растворы, суспензии, эмульсии, кремы, мази, порошки, линименты, бальзамы и т. п., которые при необходимости стерилизуют или смешивают со вспомогательными средствами (например, консервантами, стабилизаторами, смачивающими средствами, буферами или солями) для влияния на различные свойства, такие как, например, осмотическое давление. Другие подходящие лекарственные формы для местного применения включают распыляемые аэрозольные препараты, где активный ингредиент, в некоторых случаях в комбинации с твердым или жидким инертным носителем, упакован в смеси с летучим веществом под давлением (например, газообразным пропеллентом, таким как фреон) или в бутылке-пульверизаторе. При необходимости в фармацевтические композиции и лекарственные формы также можно добавлять увлажняющие или влагоудерживающие средства. Примеры таких дополнительных ингредиентов являются хорошо известными.
[0629] Если композиции, содержащие МBM, вводят интраназально, то МBM могут быть составлены в форме аэрозоля, спрея, тумана или в форме капель. В частности, в целях удобства профилактические или терапевтические средства для применения согласно настоящему изобретению могут доставляться в лекарственной форме аэрозольного спрея из пакетов под давлением или небулайзера с применением подходящего пропеллента (например, дихлордифторметана, трихлорфторметана, дихлортетрафторэтана, диоксида углерода или другого подходящего газа). В случае с аэрозолем под давлением единица дозирования может определяться посредством обеспечения клапана для доставки отмеренного количества. Капсулы и картриджи (например, состоящие из желатина) для применения в ингаляторе или инсуффляторе можно составлять содержащими порошковую смесь соединения и подходящей порошковой основы, такой как лактоза или крахмал.
[0630] MBM (например, TBM) можно вводить в режимах комбинированной терапии, описанных в разделе 7.13 ниже.
[0631] В определенных вариантах осуществления MBM могут быть составлены для обеспечения надлежащего распределения in vivo. Например, гематоэнцефалический барьер (BBB) не пропускает множество высокогидрофильных соединений. Для обеспечения пересечения BBB терапевтическими соединениями по настоящему изобретению (при необходимости) их можно составлять, например, в липосомах. В отношении способов получения липосом см., например, патенты США №№ 4522811; 5374548 и 5399331. Липосомы могут содержать один или более фрагментов, которые селективно транспортируются в конкретные клетки или органы, благодаря чему улучшается целенаправленная доставка лекарственных средств (см., например, Ranade, 1989, J. Clin. Pharmacol. 29:685). Иллюстративные нацеливающиеся фрагменты включают фолат или биотин (см., например, патент США № 5416016, выданный Low et al.); маннозиды (Umezawa et al., 1988, Biochem. Biophys. Res. Commun. 153:1038); антитела (Bloeman et al., 1995, FEBS Lett. 357:140; Owais et al., 1995, Antimicrob. Agents Chemother. 39:180); рецептор поверхностно-активного белка A (Briscoe et al., 1995, Am. J. Physiol. 1233:134); p120 (Schreier et al., 1994, J. Biol. Chem. 269:9090); см. также Keinanen and Laukkanen, 1994, FEBS Lett. 346:123; Killion and Fidler, 1994, Immunomethods 4:273.
[0632] При применении в комбинированной терапии, например, как описано в разделе 7.13 ниже, MBM и одно или более дополнительных средств можно вводить субъекту в одной и той же фармацевтической композиции. В качестве альтернативы, МBM и дополнительное(дополнительные) средство(средства) для видов комбинированной терапии можно одновременно вводить субъекту в отдельных фармацевтических композициях.
[0633] Терапевтические способы, описанные в данном документе, могут дополнительно включать проведение "сопутствующего диагностического" теста, посредством которого образец от субъекта, который является кандидатом на терапию с помощью MBM, тестируют в отношении экспрессии BCMA и/или TAA, на которые нацеливается MBM. Сопутствующий диагностический тест можно проводить до начала терапии с помощью MBM и/или в ходе осуществления режима терапии с помощью MBM для мониторинга сохраняющейся пригодности субъекта для терапии с помощью MBM. Средство, применяемое в сопутствующей диагностике, может представлять собой MBM саму по себе или другое диагностическое средство, например, меченое моноспецифическое антитело к BCMA или TAA, распознаваемым MBM, или зонд на основе нуклеиновой кислоты для выявления РНК TAA. Образец, который можно тестировать в ходе сопутствующего диагностического анализа, может представлять собой любой образец, в котором могут присутствовать клетки, на которые нацеливается MBM, например, биоптат опухоли (например, солидной опухоли), лимфу, кал, мочу, кровь или любую другую биологическую жидкость, которая может содержать циркулирующие опухолевые клетки.
7.12. Терапевтические показания
[0634] MBM можно применять для лечения любого заболевания, ассоциированного с экспрессией BCMA. Например, MBM можно применять для лечения субъекта, который подвергся лечению заболевания, ассоциированного с повышенной экспрессией BCMA, где у субъекта, который подвергся лечению при повышенных уровнях BCMA, проявляется заболевание, ассоциированное с повышенными уровнями BCMA.
[0635] В одном аспекте в настоящем изобретении предусмотрен способ подавления роста опухолевой клетки, экспрессирующей BCMA, включающий приведение опухолевой клетки в контакт с MBM таким образом, чтобы рост опухолевой клетки подавлялся.
[0636] В одном аспекте в настоящем изобретении предусмотрен способ лечения и/или предупреждения заболевания, которое возникает у индивидуумов с ослабленным иммунитетом, включающий введение MBM по настоящему изобретению. В частности, в данном документе раскрыт способ лечения заболеваний, нарушений и состояний, ассоциированных с экспрессией BCMA, включающий введение MBM по настоящему изобретению.
[0637] В определенных аспектах в данном документе раскрыт способ лечения пациентов с риском развития заболеваний, нарушений и состояний, ассоциированных с экспрессией BCMA, включающий введение MBM по настоящему изобретению.
[0638] Таким образом, в настоящем изобретении предусмотрены способы лечения или предупреждения заболеваний, нарушений и состояний, ассоциированных с экспрессией BCMA, включающие введение субъекту, нуждающемуся в этом, терапевтически эффективного количества MBM по настоящему изобретению.
[0639] В настоящем изобретении также предусмотрены способы предупреждения, лечения и/или контроля заболевания, ассоциированного с клетками, экспрессирующими BCMA (например, клетками гематологического рака или атипичного рака, экспрессирующими BCMA), при этом способы включают введение субъекту, нуждающемуся в этом, MBM. В одном аспекте субъектом является человек. Неограничивающие примеры нарушений, ассоциированных с клетками, экспрессирующими ВСМА, включают вирусные или грибковые инфекции и нарушения, связанные с иммунитетом слизистых оболочек.
7.12.1. Рак и заболевания и нарушения, связанные с раком
[0640] В одном аспекте в настоящем изобретении предусмотрен способ лечения рака у субъекта. Способ включает введение субъекту MBM, благодаря чему обеспечивается лечение рака у субъекта. Примером рака, который поддается лечению с помощью MBM, является рак, ассоциированный с экспрессией BCMA.
[0641] В одном аспекте в настоящем изобретении предусмотрены способы лечения рака, где часть опухоли является отрицательной в отношении BCMA, и часть опухоли является положительной в отношении BCMA.
[0642] В одном аспекте в настоящем изобретении предусмотрены способы лечения рака, где BCMA экспрессируется как на нормальных клетках, так и на раковых клетках, но на нормальных клетках экспрессируется на более низких уровнях, с использованием MBM по настоящему изобретению. В одном варианте осуществления способ дополнительно включает проведение отбора MBM, которая связывается с такой аффинностью, которая позволяет MBM связывать и уничтожать раковые клетки, экспрессирующие BCMA, но при этом уничтожать менее 30%, 25%, 20%, 15%, 10%, 5% или меньше нормальных клеток, экспрессирующих BCMA, например, как определено с помощью анализа, описанного в данном документе. Например, можно применять анализ уничтожения, такой как проточная цитометрия с использованием CTL с Cr51. В одном варианте осуществления MBM имеет ABM1, который характеризуется аффинностью связывания с KD в отношении BCMA, составляющей от 10-4 М до 10-8 М, например, от 10-5 М до 10-7 М, например, 10-6 М или 10-7 М.
[0643] В одном аспекте в данном документе раскрыт способ лечения пролиферативного заболевания, такого как рак или злокачественное новообразование, или предракового состояния, такого как миелодисплазия, миелодиспластический синдром или предлейкоз, включающий введение MBM. В одном аспекте рак представляет собой гематологический рак. Состояния, связанные с гематологическими формами рака, представляют собой типы рака, такие как лейкоз и злокачественные лимфопролиферативные состояния, при которых поражается кровь, костный мозг и лимфатическая система. В одном аспекте гематологический рак представляет собой лейкоз. Примером заболевания или нарушения, ассоциированного с BCMA, является множественная миелома (также известная как MM) (см. Claudio et al., Blood. 2002, 100(6):2175-86; и Novak et al., Blood. 2004, 103(2):689-94). Множественная миелома, также известная как плазмоклеточная миелома или болезнь Калера, представляет собой рак, характеризующийся накоплением аномальных или злокачественных плазматических B-клеток в костном мозге. Часто раковые клетки внедряются в смежную кость, разрушая скелетные структуры, что приводит к боли в костях и переломам. Большинство случаев миеломы также характеризуются продуцированием парапротеина (также известного как M-белки или миеломные белки), который представляет собой аномальный иммуноглобулин, продуцируемый в избытке вследствие клональной пролиферации злокачественных плазматических клеток. Уровни парапротеина в сыворотке крови, составляющие более 30 г/л, являются диагностическим критерием множественной миеломы в соответствии с диагностическими критериями Международной группы по изучению множественной миеломы (IMWG) (см. Kyle et al. (2009), Leukemia. 23:3-9). Другие симптомы или признаки множественной миеломы включают снижение функции почек или почечную недостаточность, очаги поражения костей, анемию, гиперкальциемию и неврологические симптомы.
[0644] Другие нарушения пролиферации плазматических клеток, которые можно лечить с помощью композиций и способов, описанных в данном документе, включают без ограничения бессимптомную миелому ("тлеющую" множественную миелому или вялотекущую миелому), моноклональную гаммапатию неустановленной этиологии (MGUS), макроглобулинемию Вальденстрема, формы плазмоцитомы (например, плазмоклеточную дискразию, солитарную миелому, солитарную плазмоцитому, экстрамедуллярную плазмоцитому и множественную плазмоцитому), системный амилоидоз в форме амилоидоза легких цепей и POEMS-синдром (также известный как синдром Кроу-Фукаса, болезнь Такатсуки и PEP-синдром).
[0645] Другим примером заболевания или нарушения, ассоциированного с BCMA, является лимфома Ходжкина и неходжкинская лимфома (см. Chiu et al., Blood. 2007, 109(2):729-39; He et al., J Immunol. 2004, 172(5):3268-79).
[0646] Лимфома Ходжкина (HL), также известная как болезнь Ходжкина, представляет собой рак лимфатической системы, который происходит из белых кровяных телец, или лимфоцитов. Аномальные клетки, которые образуют лимфому, называются клетками Рида-Штернберга. При лимфоме Ходжкина происходит распространение рака из одной группы лимфатических узлов в другую. Лимфому Ходжкина можно подразделить на четыре патологических подтипа на основании морфологических характеристик клеток Рида-Штернберга и клеточного состава вокруг клеток Рида-Штернберга (что определяют посредством биопсии лимфатических узлов): HL с нодулярным склерозом, смешанно-клеточный подтип, богатая лимфоцитами или с лимфоидным преобладанием, с лимфоидным истощением. Иногда лимфома Ходжкина также может представлять собой нодулярную лимфому Ходжкина с лимфоидным преобладанием или может быть неуточненной. Симптомы и признаки лимфомы Ходжкина включают безболезненное увеличение лимфатических узлов в области шеи, подмышечных впадин или паха, лихорадку, ночную потливость, потерю веса, утомляемость, кожный зуд или боль в животе.
[0647] Неходжкинская лимфома (NHL) представляет собой группу разнообразных форм рака крови, которые включают любую разновидность лимфомы, отличную от лимфомы Ходжкина. Подтипы неходжкинской лимфомы классифицируют в основном по морфологическим характеристикам клеток, хромосомным аберрациям и поверхностным маркерам. Подтипы NHL (или NHL-ассоциированные формы рака) включают В-клеточные лимфомы, такие как, без ограничения, лимфома Беркитта, хронический лимфоцитарный В-клеточный лейкоз (B-CLL), пролимфоцитарный B-клеточный лейкоз (B-PLL), хронический лимфоцитарный лейкоз (CLL), диффузная крупноклеточная В-клеточная лимфома (DLBCL) (например, внутрисосудистая крупноклеточная B-клеточная лимфома и первичная медиастинальная B-клеточная лимфома), фолликулярная лимфома (например, лимфома из клеток центра фолликула, фолликулярная мелкоклеточная лимфома с расщепленными ядрами), волосатоклеточный лейкоз, B-клеточная лимфома высокой степени злокачественности (подобная лимфоме Беркитта), лимфоплазмоцитарная лимфома (макроглобулинемия Вальденстрема), мантийноклеточная лимфома, формы B-клеточной лимфомы из клеток маргинальной зоны (например, внеузловая B-клеточная лимфома из клеток маргинальной зоны или лимфома из лимфоидной ткани слизистых оболочек (MALT), узловая В-клеточная лимфома из клеток маргинальной зоны и В-клеточная лимфома из клеток маргинальной зоны селезенки), плазмоцитома/миелома, B-лимфобластный лейкоз/лимфома из клеток-предшественников (PB-LBL/L), первичная лимфома центральной нервной системы (CNS), первичная внутриглазная лимфома, мелкоклеточная лимфоцитарная лимфома (SLL); и T-клеточные лимфомы, такие как, без ограничения, анапластическая крупноклеточная лимфома (ALCL), T-клеточная лимфома/лейкоз взрослых (например, "тлеющая", хроническая, острая и лимфоматозная), лимфангиома, ангиоиммунобластная Т-клеточная лимфома, формы T-клеточной лимфомы кожи (например, фунгоидный микоз, синдром Сезари и т. д.), внеузловая лимфома из естественных киллеров/T-клеток (назального типа), Т-клеточная лимфома кишечника энтеропатического типа, лейкоз из больших гранулярных лимфоцитов, T-лимфобластная лимфома/лейкоз из клеток-предшественников (T-LBL/L), T-клеточный хронический лимфоцитарный лейкоз/пролимфоцитарный лейкоз (T-CLL/PLL) и неуточненная периферическая T-клеточная лимфома. Симптомы и признаки лимфомы Ходжкина включают безболезненное увеличение лимфатических узлов в области шеи, подмышечных впадин или паха, лихорадку, ночную потливость, потерю веса, утомляемость, кожный зуд, боль в животе, кашель или боль в груди.
[0648] Также было установлено, что экспрессия BCMA ассоциирована с макроглобулинемией Вальденстрема (WM), также известной как лимфоплазмоцитарная лимфома (LPL) (см. Elsawa et al., Blood. 2006, 107(7):2882-8). Ранее считалось, что макроглобулинемия Вальденстрема является родственной по отношению к множественной миеломе, но совсем недавно ее классифицировали как подтип неходжкинской лимфомы. WM характеризуется неконтролируемой пролиферацией В-клеточных лимфоцитов, что приводит к анемии и продуцированию избыточных количеств парапротеина или иммуноглобулина М (IgM), который сгущает кровь и приводит к синдрому повышенной вязкости крови. Другие симптомы или признаки WM включают лихорадку, ночную потливость, утомляемость, анемию, потерю веса, лимфаденопатию или спленомегалию, нечеткость зрения, головокружение, носовые кровотечения, кровоточивость десен, нетипичные кровоподтеки, нарушение функции почек или почечную недостаточность, амилоидоз или периферическую нейропатию.
[0649] Другим примером заболевания или нарушения, ассоциированного с экспрессией BCMA, является рак головного мозга. В частности, было установлено, что экспрессия BCMA ассоциирована с астроцитомой или глиобластомой (см. Deshayes et al, Oncogene. 2004, 23(17):3005-12, Pelekanou et al., PLoS One. 2013, 8(12):e83250). Астроцитомы представляют собой опухоли, которые возникают из астроцитов, представляющих собой тип глиальных клеток в головном мозге. Глиобластома (также известная как мультиформная глиобластома или GBM) является наиболее злокачественной формой астроцитомы и считается наиболее поздней стадией рака головного мозга (стадией IV). Существуют два варианта глиобластомы: гигантоклеточная глиобластома и глиосаркома. Другие формы астроцитомы включают ювенильную пилоцитарную астроцитому (JPA), фибриллярную астроцитому, плеоморфную ксантоастроцитому (PXA), дисэмбриопластическую нейроэпителиальную опухоль (DNET) и анапластическую астроцитому (AA).
[0650] Симптомы или признаки, ассоциированные с глиобластомой или астроцитомой, включают повышенное давление в головном мозге, головные боли, эпилептические припадки, потерю памяти, изменения в поведении, нарушение движения или потерю чувствительности на одной стороне тела, речевую дисфункцию, когнитивные нарушения, нарушения зрения, тошноту, рвоту и слабость в руках или ногах.
[0651] Хирургическое удаление опухоли (или резекция) является стандартным лечением для удаления как можно большей части глиомы без повреждения или с минимальным повреждением окружающей нормальной ткани головного мозга. Лучевая терапия и/или химиотерапия часто применяются после хирургического вмешательства для подавления и замедления рецидивирующего заболевания, обусловленного любыми оставшимися раковыми клетками или сопутствующими очагами поражения. Лучевая терапия включает лучевую терапию всего головного мозга (традиционную дистанционную лучевую терапию), целенаправленную трехмерную конформную лучевую терапию и применение целенаправленно воздействующих радионуклидов. Химиотерапевтические средства, обычно применяемые для лечения глиобластомы, включают темозоломид, гефитиниб или эрлотиниб и цисплатин. Ингибиторы ангиогенеза, такие как бевацизумаб (Avastin®), также обычно применяются в комбинации с химиотерапией и/или лучевой терапией.
[0652] Поддерживающее лечение также часто применяют для облегчения неврологических симптомов и улучшения неврологической функции и используют в комбинации с любым из средств терапии рака, описанных в данном документе. Основные поддерживающие средства включают противосудорожные средства и кортикостероиды. Таким образом, композиции и способы по настоящему изобретению можно применять в комбинации с любыми видами стандартного или поддерживающего лечения с целью лечения глиобластомы или астроцитомы.
[0653] В настоящем изобретении предусмотрены композиции и способы для лечения рака. В одном аспекте рак представляет собой гематологический рак, включающий без ограничения лейкоз или лимфому. В одном аспекте в данном документе раскрыты способы лечения форм рака и злокачественных новообразований, в том числе без ограничения, например, форм острого лейкоза, включая без ограничения, например, B-клеточный острый лимфоидный лейкоз ("BALL"), T-клеточный острый лимфоидный лейкоз ("TALL"), острый лимфоидный лейкоз (ALL); одной или более форм хронического лейкоза, включая без ограничения, например, хронический миелогенный лейкоз (CML), хронический лимфоцитарный лейкоз (CLL); дополнительных форм гематологического рака или гематологических состояний, включая без ограничения, например, B-клеточный пролимфоцитарный лейкоз, новообразование из бластных плазмоцитоидных дендритных клеток, лимфому Беркитта, диффузную крупноклеточную B-клеточную лимфому, фолликулярную лимфому, волосатоклеточный лейкоз, мелкоклеточную или крупноклеточную фолликулярную лимфому, злокачественные лимфопролиферативные состояния, MALT-лимфому, мантийноклеточную лимфому, лимфому из клеток маргинальной зоны, множественную миелому, миелодисплазию и миелодиспластический синдром, неходжкинскую лимфому, плазмобластную лимфому, новообразование из плазмоцитоидных дендритных клеток, макроглобулинемию Вальденстрема и "предлейкоз", который представляет собой разнообразную группу гематологических состояний, объединенных неэффективным образованием (или дисплазией) миелоидных клеток крови, и т. п. Другие заболевания, ассоциированные с экспрессией ВСМА, включают без ограничения, например, атипичные и/или неклассические формы рака, злокачественные новообразования, предраковые состояния или пролиферативные заболевания, характеризующиеся экспрессией ВСМА.
[0654] В некоторых вариантах осуществления MBM можно применять для лечения заболевания, включающего без ограничения нарушение пролиферации плазматических клеток, например, бессимптомную миелому ("тлеющую" множественную миелому или вялотекущую миелому), моноклональную гаммапатию неустановленной этиологии (MGUS), макроглобулинемию Вальденстрема, формы плазмоцитомы (например, плазмоклеточную дискразию, солитарную миелому, солитарную плазмоцитому, экстрамедуллярную плазмоцитому и множественную плазмоцитому), системный амилоидоз в форме амилоидоза легких цепей и POEMS-синдром (также известный как синдром Кроу-Фукаса, болезнь Такатсуки и PEP-синдром).
[0655] В некоторых вариантах осуществления MBM можно применять для лечения заболевания, включающего без ограничения рак, например, рак, описанный в данном документе, например, рак предстательной железы (например, кастрационно-резистентный или терапевтически резистентный рак предстательной железы или метастатический рак предстательной железы), рак поджелудочной железы или рак легкого.
[0656] В настоящем изобретении также предусмотрены способы подавления пролиферации или уменьшения популяции клеток, экспрессирующих BCMA, при этом способы включают приведение популяции клеток, содержащей клетку, экспрессирующую BCMA, в контакт с MBM по настоящему изобретению. В одном аспекте в настоящем изобретении предусмотрены способы подавления пролиферации или уменьшения популяции раковых клеток, экспрессирующих BCMA, при этом способы включают приведение популяции раковых клеток, экспрессирующих BCMA, в контакт с MBM. В одном аспекте в настоящем изобретении предусмотрены способы подавления пролиферации или уменьшения популяции раковых клеток, экспрессирующих BCMA, при этом способы включают приведение популяции раковых клеток, экспрессирующих BCMA, в контакт с MBM. В определенных аспектах способы обеспечивают снижение количества, числа, численности или процентного содержания клеток и/или раковых клеток на по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 65%, по меньшей мере 75%, по меньшей мере 85%, по меньшей мере 95% или по меньшей мере 99% у субъекта с миелоидным лейкозом или другой формой рака, ассоциированной с клетками, экспрессирующими BCMA, или в соответствующей животной модели, по сравнению с отрицательным контролем. В одном аспекте субъектом является человек.
[0657] В настоящем изобретении предусмотрены способы предупреждения рецидива рака, ассоциированного с клетками, экспрессирующими BCMA, при этом способы включают введение субъекту, нуждающемуся в этом, MBM.
7.12.2. Заболевания и нарушения, не связанные с раком
[0658] Заболевания и нарушения, не связанные с раком, но ассоциированные с экспрессией BCMA, также можно лечить с помощью композиций и способов, раскрытых в данном документе. Примеры заболеваний и нарушений, не связанных с раком, но ассоциированных с экспрессией BCMA, включают без ограничения вирусные инфекции, например, вызванные HIV; грибковые инфекции, например, вызванные C. neoformans; и аутоиммунные заболевания.
[0659] Аутоиммунные нарушения, которые можно лечить с помощью MBM по настоящему изобретению, включают системную красную волчанку (SLE), синдром Шегрена, склеродермию, ревматоидный артрит (RA), ювенильный идиопатический артрит, реакцию "трансплантат против хозяина", дерматомиозит, сахарный диабет I типа, тиреоидит Хашимото, болезнь Грейвса, болезнь Аддисона, целиакию, нарушения, связанные с иммунитетом слизистых оболочек, заболевания раздраженного кишечника (например, болезнь Крона, неспецифический язвенный колит), пернициозную анемию, обыкновенную пузырчатку, витилиго, аутоиммунную гемолитическую анемию, идиопатическую тромбоцитопеническую пурпуру, гигантоклеточный артериит, тяжелую миастению, рассеянный склероз (MS) (например, рецидивирующе-ремиттирующий MS (RRMS)), гломерулонефрит, синдром Гудпасчера, буллезный пемфигоид, язвенный колит, синдром Гийена-Барре, хроническую воспалительную демиелинизирующую полинейропатию, антифосфолипидный синдром, нарколепсию, саркоидоз и гранулематоз Вегенера.
[0660] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения системной красной волчанки (SLE).
[0661] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения синдрома Шегрена.
[0662] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения склеродермии.
[0663] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения ревматоидного артрита (RA).
[0664] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения ювенильного идиопатического артрита.
[0665] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения реакции "трансплантат против хозяина".
[0666] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения дерматомиозита.
[0667] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения сахарного диабета I типа.
[0668] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения тиреоидита Хашимото.
[0669] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения болезни Грейвса.
[0670] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения болезни Аддисона.
[0671] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения целиакии.
[0672] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения болезни Крона.
[0673] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения пернициозной анемии.
[0674] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения обыкновенной пузырчатки.
[0675] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения витилиго.
[0676] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения аутоиммунной гемолитической анемии.
[0677] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения идиопатической тромбоцитопенической пурпуры.
[0678] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения гигантоклеточного артериита.
[0679] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения тяжелой миастении.
[0680] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения рассеянного склероза (MS). В некоторых вариантах осуществления MS представляет собой рецидивирующе-ремиттирующий MS (RRMS).
[0681] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения гломерулонефрита.
[0682] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения синдрома Гудпасчера.
[0683] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения буллезного пемфигоида.
[0684] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения язвенного колита.
[0685] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения синдрома Гийена-Барре.
[0686] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения хронической воспалительной демиелинизирующей полинейропатии.
[0687] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения антифосфолипидного синдрома.
[0688] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения нарколепсии.
[0689] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения саркоидоза.
[0690] В некоторых вариантах осуществления MBM по настоящему изобретению применяют для лечения гранулематоза Вегенера.
7.13. Комбинированная терапия
[0691] MBM (например, TBM) по настоящему изобретению можно применять в комбинации с другими известными средствами и видами терапии. Например, MBM можно применять в режимах лечения в комбинации с хирургическим вмешательством, химиотерапией, антителами, облучением, пептидными вакцинами, стероидами, цитотоксинами, ингибиторами протеасом, иммуномодулирующими лекарственными средствами (например, IMiD), миметиками BH3, средствами цитокиновой терапии, трансплантацией стволовых клеток или любой их комбинацией. Не ограничиваясь какой-либо теорией, полагают, что одним из преимуществ MBM по настоящему изобретению является то, что они могут позволить избежать необходимости введения отдельных антител субъекту, страдающему раком (например, В-клеточным злокачественным новообразованием). Соответственно, в определенных вариантах осуществления одно или более дополнительных средств не включают в себя антитело (например, ритуксимаб).
[0692] Для удобства средство, которое применяют в комбинации с MBM, в данном документе называется "дополнительным" средством.
[0693] Как используется в данном документе, вводимый "в комбинации" означает, что два (или более) различных средства для лечения доставляются субъекту в течение периода, когда субъект страдает нарушением, например, два или более средства для лечения доставляются после того, как у субъекта было диагностировано нарушение, и до того, как нарушение было излечено или устранено или лечение было прекращено по другим причинам. В некоторых вариантах осуществления доставка одного средства для лечения все еще осуществляется, когда начинается доставка второго, так что в отношении введения имеет место перекрывание. Это иногда упоминается в данном документе как "одновременная" или "параллельная" доставка. Например, каждое средство терапии можно вводить субъекту в одно и то же время или последовательно в любом порядке в разные моменты времени; однако, если их не вводят в одно и то же время, их следует вводить достаточно близко друг к другу по времени, чтобы обеспечить требуемый терапевтический эффект.
[0694] MBM и одно или более дополнительных средств можно вводить одновременно в одной и той же или отдельных композициях или последовательно. В случае последовательного введения МBM можно вводить первой, а дополнительное средство можно вводить вторым, или порядок введения может быть обратным.
[0695] MBM и дополнительное(дополнительные) средство(средства) можно вводить субъекту в любой подходящей форме и любым подходящим путем. В некоторых вариантах осуществления пути введения являются одинаковыми. В других вариантах осуществления пути введения являются разными.
[0696] В других вариантах осуществления доставка одного средства для лечения завершается до начала доставки другого средства для лечения.
[0697] В некоторых вариантах осуществления в любом случае лечение является более эффективным благодаря комбинированному введению. Например, второе средство для лечения является более эффективным, например, эквивалентный эффект наблюдается при меньшем количестве второго средства для лечения, или второе средство для лечения обеспечивает снижение интенсивности симптомов в большей степени, чем наблюдалось бы при введении второго средства для лечения в отсутствие первого средства для лечения, или аналогичная ситуация наблюдается с первым средством для лечения. В некоторых вариантах осуществления доставка является такой, при которой снижение интенсивности симптома или другого параметра, связанного с нарушением, является более значительным, чем наблюдалось бы при доставке одного средства для лечения в отсутствие другого. Эффект двух средств для лечения может быть частично аддитивным, полностью аддитивным или превышающим аддитивный. Доставка может быть такой, что эффект от первого доставленного средства для лечения все еще поддается выявлению при доставке второго.
[0698] MBM и/или дополнительные средства можно вводить в течение периодов активного проявления нарушения или в течение периода ремиссии или менее активного проявления заболевания. МBM можно вводить до лечения с помощью дополнительного(дополнительных) средства(средств), одновременно с лечением с помощью дополнительного(дополнительных) средства(средств), после лечения с помощью дополнительного(дополнительных) средства(средств) или во время ремиссии нарушения.
[0699] При введении в комбинации MBM и/или дополнительное(дополнительные) средство(средства) можно вводить в количестве или дозе, которые являются более высокими, более низкими или такими же по сравнению с количеством или дозой каждого средства, применяемого отдельно, например, в режиме монотерапии.
[0700] Дополнительное(дополнительные) средство(средства) в видах комбинированной терапии по настоящему изобретению можно вводить субъекту одновременно. Каждое средство терапии можно вводить субъекту вместе с другими или отдельно в любой подходящей форме и любым подходящим путем.
[0701] MBM и дополнительное(дополнительные) средство(средства) можно вводить субъекту одинаковыми или разными путями введения.
[0702] MBM и дополнительное(дополнительные) средство(средства) можно вводить циклически. Циклическая терапия предусматривает введение первого средства терапии (например, первого профилактического или терапевтического средства) в течение некоторого периода времени, а затем введение второго средства терапии (например, второго профилактического или терапевтического средства) в течение некоторого периода времени, необязательно с последующим введением третьего средства терапии (например, профилактического или терапевтического средства) в течение некоторого периода времени и т. д. и повторение этого последовательного введения, т. е. цикла, с целью снижения темпов развития устойчивости к одному из средств терапии, для недопущения или снижения побочных эффектов одного из средств терапии и/или для улучшения эффективности средств терапии.
[0703] В определенных случаях одно или более дополнительных средств представляют собой другие противораковые средства, противоаллергические средства, противотошнотные средства (или противорвотные средства), обезболивающие средства, цитопротекторные средства и их комбинации.
[0704] В одном варианте осуществления MBM вводят в комбинации с противораковым средством (например, с химиотерапевтическим средством). Иллюстративные химиотерапевтические средства включают антрациклин (например, доксорубицин (например, липосомальный доксорубицин)), алкалоид барвинка (например, винбластин, винкристин, виндезин, винорелбин), алкилирующее средство (например, циклофосфамид, декарбазин, мелфалан, ифосфамид, темозоломид), антитело к иммунным клеткам (например, алемтузумаб, гемтузумаб, ритуксимаб, тозитумомаб, обинутузумаб, офатумумаб, даратумумаб, элотузумаб), антиметаболит (в том числе, например, антагонисты фолиевой кислоты, аналоги пиримидина, аналоги пурина и ингибиторы аденозиндезаминазы (например, флударабин)), ингибитор mTOR, агонист глюкокортикоид-индуцируемого белка, родственного TNFR (GITR), ингибитор протеасом (например, аклациномицин A, глиотоксин или бортезомиб), иммуномодулятор, такой как талидомид или производное талидомида (например, леналидомид).
[0705] Основные химиотерапевтические средства, рассматриваемые для применения в видах комбинированной терапии, включают анастрозол (Arimidex®), бикалутамид (Casodex®), сульфат блеомицина (Blenoxane®), бусульфан (Myleran®), бусульфан для инъекций (Busulfex®), капецитабин (Xeloda®), N4-пентоксикарбонил-5-дезокси-5-фторцитидин, карбоплатин (Paraplatin®), кармустин (BiCNU®), хлорамбуцил (Leukeran®), цисплатин (Platinol®), кладрибин (Leustatin®), циклофосфамид (Cytoxan® или Neosar®), цитарабин, цитозинарабинозид (Cytosar-U®), липосомальный цитарабин для инъекций (DepoCyt®), дакарбазин (DTIC-Dome®), дактиномицин (актиномицин D, Cosmegan), гидрохлорид даунорубицина (Cerubidine®), липосомальный цитрат даунорубицина для инъекций (DaunoXome®), дексаметазон, доцетаксел (Taxotere®), гидрохлорид доксорубицина (Adriamycin®, Rubex®), этопозид (Vepesid®), фосфат флударабина (Fludara®), 5-фторурацил (Adrucil®, Efudex®), флутамид (Eulexin®), тезацитибин, гемцитабин (дифтордезоксицитидин), гидроксимочевину (Hydrea®), идарубицин (Idamycin®), ифосфамид (IFEX®), иринотекан (Camptosar®), L-аспарагиназу (ELSPAR®), лейковорин кальция, мелфалан (Alkeran®), 6-меркаптопурин (Purinethol®), метотрексат (Folex®), митоксантрон (Novantrone®), милотарг, паклитаксел (Taxol®), феникс (иттрий-90/MX-DTPA), пентостатин, полифепрозан 20 с кармустином для имплантации (Gliadel®), цитрат тамоксифена (Nolvadex®), тенипозид (Vumon®), 6-тиогуанин, тиотепу, тирапазамин (Tirazone®), гидрохлорид топотекана для инъекций (Hycamptin®), винбластин (Velban®), винкристин (Oncovin®) и винорелбин (Navelbine®).
[0706] Противораковые средства, представляющие особый интерес для комбинаций с MBM по настоящему изобретению, включают антрациклины; алкилирующие средства; антиметаболиты; лекарственные средства, которые ингибируют кальций-зависимую фосфатазу кальциневрин или киназу p70S6 (FK506) или ингибируют киназу p70S6; ингибиторы mTOR; иммуномодуляторы; алкалоиды барвинка; ингибиторы протеасом; агонисты GITR (например, GWN323); ингибиторы протеинтирозинфосфатаз; ингибитор киназы CDK4; ингибитор BTK; ингибитор киназы MKN; ингибитор киназы DGK; онколитический вирус; миметик BH3 и средства цитокиновой терапии.
[0707] MBM можно вводить в комбинации с одним или более противораковыми средствами, которые предупреждают или замедляют слущивание антигена, на который нацеливается один или более ABM в MBM, за счет чего обеспечивается снижение количества растворимого антигена и/или увеличение количества антигена, связанного с клеточной поверхностью. Например, MBM можно вводить в комбинации с ингибитором ADAM10/17 (например, INCB7839), например, для блокирования слущивания антигена, высвобождаемого из раковой клетки под действием ADAM10/17, или в комбинации с ингибитором фосфолипазы, например, для блокирования слущивания антигена, высвобождаемого из раковой клетки под действием фосфолипазы. Также особый интерес для комбинаций с MBM по настоящему изобретению представляют модуляторы гамма-секретазы, такие как ингибиторы гамма-секретазы (GSI).
[0708] Иллюстративные алкилирующие средства включают без ограничения азотистые иприты, производные этиленимина, алкилсульфонаты, нитрозомочевины и триазены: урациловый иприт (Aminouracil Mustard®, Chlorethaminacil®, Demethyldopan®, Desmethyldopan®, Haemanthamine®, Nordopan®, Uracil nitrogen mustard®, Uracillost®, Uracilmostaza®, Uramustin®, Uramustine®), хлорметин (Mustargen®), циклофосфамид (Cytoxan®, Neosar®, Clafen®, Endoxan®, Procytox®, RevimmuneTM), ифосфамид (Mitoxana®), мелфалан (Alkeran®), хлорамбуцил (Leukeran®), пипоброман (Amedel®, Vercyte®), триэтиленмеламин (Hemel®, Hexalen®, Hexastat®), триэтилентиофосфорамин, темозоломид (Temodar®), тиотепу (Thioplex®), бусульфан (Busilvex®, Myleran®), кармустин (BiCNU®), ломустин (CeeNU®), стрептозоцин (Zanosar®) и дакарбазин (DTIC-Dome®). Дополнительные иллюстративные алкилирующие средства включают без ограничения оксалиплатин (Eloxatin®); темозоломид (Temodar® и Temodal®); дактиномицин (также известный как актиномицин-D, Cosmegen®); мелфалан (также известный как L-PAM, L-сарколизин и фенилаланиновый иприт, Alkeran®); алтретамин (также известный как гексаметилмеламин (HMM), Hexalen®); кармустин (BiCNU®); бендамустин (Treanda®); бусульфан (Busulfex® и Myleran®); карбоплатин (Paraplatin®); ломустин (также известный как CCNU, CeeNU®); цисплатин (также известный как CDDP, Platinol® и Platinol®-AQ); хлорамбуцил (Leukeran®); циклофосфамид (Cytoxan® и Neosar®); дакарбазин (также известный как DTIC, DIC и имидазолкарбоксамид, DTIC-Dome®); алтретамин (также известный как гексаметилмеламин (HMM), Hexalen®); ифосфамид (Ifex®); преднумустин; прокарбазин (Matulane®); мехлорэтамин (также известный как азотистый иприт, мустин и гидрохлорид мехлорэтамина, Mustargen®); стрептозоцин (Zanosar®); тиотепу (также известную как тиофосфамид, TESPA и TSPA, Thioplex®); циклофосфамид (Endoxan®, Cytoxan®, Neosar®, Procytox®, Revimmune®) и бендамустин-HCl (Treanda®).
[0709] Иллюстративные ингибиторы mTOR включают, например, темсиролимус; ридафоролимус (ранее известный как деферолимус, (1R,2R,4S)-4-[(2R)-2-[(1R,9S,12S,15R,16E,18R,19R,21R, 23S,24E,26E,28Z,30S,32S,35R)-1,18-дигидрокси-19,30-диметокси-15,17,21,23,29,35-гексаметил-2,3,10,14,20-пентаоксо-11,36-диокса-4-азатрицикло[30.3.1.04,9]гексатриаконта-16,24,26,28-тетраен-12-ил]пропил]-2-метоциклогексилдиметилфосфинат, также известный как AP23573 и MK8669 и описанный в PCT-публикации № WO 03/064383); эверолимус (Afinitor® или RAD001); рапамицин (AY22989, Sirolimus®); симапимод (CAS 164301-51-3); эмсиролимус, (5-{2,4-бис[(3S)-3-метилморфолин-4-ил]пиридо[2,3-d]пиримидин-7-ил}-2-метоксифенил)метанол (AZD8055); 2-амино-8-[транс-4-(2-гидроксиэтокси)циклогексил]-6-(6-метокси-3-пиридинил)-4-метилпиридо[2,3-d]пиримидин-7(8H)-он (PF04691502, CAS 1013101-36-4), а также N2-[1,4-диоксо-4-[[4-(4-оксо-8-фенил-4H-1-бензoпиран-2-ил)морфолиний-4-ил]метокси]бутил]-L-аргинилглицил-L-α-аспартил-L-серин- (SEQ ID NO: 555) в форме внутренней соли (SF1126, CAS 936487-67-1) и XL765.
[0710] Иллюстративные иммуномодуляторы включают, например, афутузумаб (доступный от Roche®); пегфилграстим (Neulasta®); леналидомид (CC-5013, Revlimid®); IMID (такие как талидомид (Thalomid®), леналидомид, помалидомид и апремиласт), актимид (CC4047) и IRX-2 (смесь человеческих цитокинов, содержащую интерлейкин-1, интерлейкин-2 и интерферон γ, CAS 951209-71-5, доступную от IRX Therapeutics).
[0711] Иллюстративные антрациклины включают, например, доксорубицин (Adriamycin® и Rubex®); блеомицин (Lenoxane®); даунорубицин (гидрохлорид даунорубицина, дауномицин и гидрохлорид рубидомицина, Cerubidine®); липосомальный даунорубицин (липосомальный цитрат даунорубицина, DaunoXome®); митоксантрон (DHAD, Novantrone®); эпирубицин (Ellence™); идарубицин (Idamycin®, Idamycin PFS®); митомицин C (Mutamycin®); гелданамицин; гербимицин; равидомицин и дезацетилравидомицин.
[0712] Иллюстративные алкалоиды барвинка включают, например, тартрат винорелбина (Navelbine®), винкристин (Oncovin®) и виндезин (Eldisine®); винбластин (также известный как сульфат винбластина, винкалейкобластин и VLB, Alkaban-AQ® и Velban®) и винорелбин (Navelbine®).
[0713] Иллюстративные ингибиторы протеасом включают бортезомиб (Velcade®); карфилзомиб (PX-171-007, (S)-4-метил-N-((S)-1-(((S)-4-метил-1-((R)-2-метилоксиран-2-ил)-1-оксопентан-2-ил)амино)-1-оксо-3-фенилпропан-2-ил)-2-((S)-2-(2-морфолиноацетамидо)-4-фенилбутанамидо)пентанамид); маризомиб (NPI-0052); цитрат иксазомиба (MLN-9708); деланзомиб (CEP-18770) и O-метил-N-[(2-метил-5-тиазолил)карбонил]-L-серил-O-метил-N-[(1S)-2-[(2R)-2-метил-2-оксиранил]-2-оксо-1-(фенилметил)этил]-L-серинамид (ONX-0912).
[0714] Иллюстративные миметики BH3 включают венетоклакс, ABT-737 (4-{4-[(4'-хлор-2-бифенилил)метил]-1-пиперазинил}-N-[(4-{[(2R)-4-(диметиламино)-1-(фенилсульфанил)-2-бутанил]амино}-3-нитрофенил)сульфонил]бензамид и навитоклакс (ранее ABT-263).
[0715] Иллюстративные средства цитокиновой терапии включают интерлейкин 2 (IL-2) и интерферон альфа (IFN-альфа).
[0716] В определенных аспектах в качестве дополнительного(дополнительных) средства(средств) вводят "коктейли" различных химиотерапевтических средств.
[0717] В одном аспекте в настоящем изобретении предусмотрен способ лечения субъектов, у которых имеется заболевание, ассоциированное с экспрессией BCMA, включающий введение субъекту эффективного количества: (i) MBM по настоящему изобретению и (ii) ингибитора гамма-секретазы (GSI).
[0718] В одном аспекте в настоящем изобретении предусмотрен способ лечения субъектов, которые подверглись лечению заболевания, ассоциированного с экспрессией BCMA, включающий введение субъекту эффективного количества: (i) MBM по настоящему изобретению и (ii) GSI.
[0719] В одном варианте осуществления MBM и GSI вводят одновременно или последовательно. В одном варианте осуществления MBM вводят до введения GSI. В одном варианте осуществления GSI вводят до введения MBM. В одном варианте осуществления MBM и GSI вводят одновременно.
[0720] В одном варианте осуществления GSI вводят до введения MBM (например, GSI вводят за 1, 2, 3, 4 или 5 дней до введения MBM), где необязательно после введения GSI и до введения MBM у субъекта наблюдается увеличение уровней экспрессии ВСМА на клеточной поверхности и/или уменьшение уровней растворимого ВСМА.
[0721] В некоторых вариантах осуществления GSI представляет собой малую молекулу, которая снижает экспрессию и/или функцию гамма-секретазы, например, низкомолекулярный GSI, раскрытый в данном документе. В одном варианте осуществления GSI выбран из LY-450139, PF-5212362, BMS-708163, MK-0752, ELN-318463, BMS-299897, LY-411575, DAPT, BMS-906024, PF-3084014, RO4929097 и LY3039478. В одном варианте осуществления GSI выбран из PF-5212362, ELN-318463, BMS-906024 и LY3039478. Иллюстративные GSI раскрыты в Takebe et al., Pharmacol Ther. 2014 Feb;141(2):140-9; и Ran et al., EMBO Mol Med. 2017 Jul;9(7):950-966.
[0722] В некоторых вариантах осуществления MK-0752 вводят в комбинации с доцетакселом. В некоторых вариантах осуществления MK-0752 вводят в комбинации с гемцитабином. В некоторых вариантах осуществления BMS-906024 вводят в комбинации с химиотерапией.
[0723] В некоторых вариантах осуществления GSI может представлять собой соединение формулы (I) или его фармацевтически приемлемую соль:
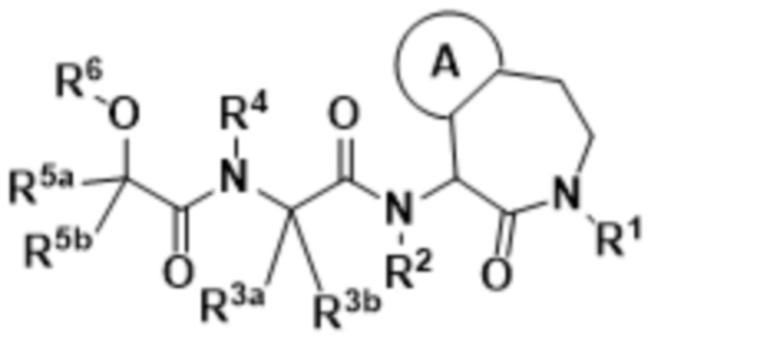 (I),
(I),
где кольцо A представляет собой арил или гетероарил; каждый из R1, R2 и R4 независимо представляет собой водород, C1-C6алкил, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил, где каждый C1-C6алкил, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил замещен в 0-6 независимых случаях галогеном, -ORA, -SRA, -C(O)ORA, -C(O)N(RA)(RB), -N(RA)(RB) или -C(NRC)N(RA)(RB); каждый R3a, R3b, R5a и R5b независимо представляет собой водород, галоген, -OH, C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил, где каждый C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил замещен в 0-6 независимых случаях галогеном, -OH, -ORA, -SRA, -C(O)ORA, -C(O)N(RA)(RB), -N(RA)(RB) или -C(NRC)N(RA)(RB); R6 представляет собой водород, C1-C6алкил, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил, где каждый C1-C6алкил, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил замещен в 0-6 независимых случаях галогеном, -OH или C1-C6 алкокси; и каждый RA, RB и RC независимо представляет собой водород, C1-C6алкил, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил, где каждый C1-C6алкил, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил замещен в 0-6 независимых случаях галогеном, -OH или C1-C6алкокси.
[0724] В некоторых вариантах осуществления кольцо A представляет собой арил (например, фенил). В некоторых вариантах осуществления R1 представляет собой -CH3. В некоторых вариантах осуществления каждый из R2 и R4 независимо представляет собой водород. В некоторых вариантах осуществления R3a представляет собой -CH3, а R3b представляет собой водород. В некоторых вариантах осуществления R5a представляет собой водород, а R5b представляет собой -CH(CH3)2. В некоторых вариантах осуществления R6 представляет собой водород.
[0725] В дополнительном варианте осуществления GSI представляет собой соединение, описанное в патенте США № 7468365. В одном варианте осуществления GSI представляет собой LY-450139, т. е. семагацестат, (S)-2-гидрокси-3-метил-N-((S)-1-(((S)-3-метил-2-оксо-2,3,4,5-тетрагидро-1H-бензо[d]азепин-1-ил)амино)-1-оксопропан-2-ил)бутанамид, или его фармацевтически приемлемую соль. В одном варианте осуществления GSI представляет собой
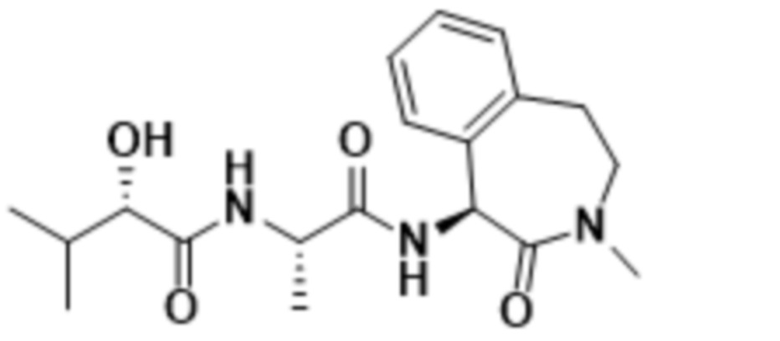
или его фармацевтически приемлемую соль.
[0726] В некоторых вариантах осуществления GSI представляет собой соединение формулы (II) или его фармацевтически приемлемую соль:
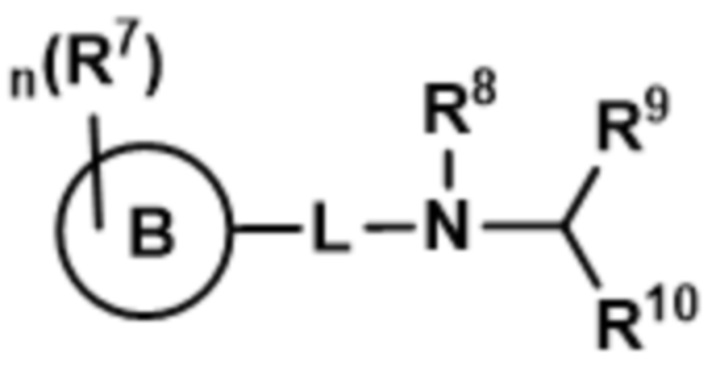 (II),
(II),
где кольцо B представляет собой арил или гетероарил; L представляет собой связь, C1-C6алкилен, -S(O)2-, -C(O)-, -N(RE)(O)C- или -OC(O)-; каждый R7 независимо представляет собой галоген, -OH, C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил, где каждый C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил независимо замещен в 0-6 случаях галогеном, -ORD, -SRD, -C(O)ORD, -C(O)N(RD)(RE), -N(RD)(RE) или -C(NRF)N(RD)(RE); R8 представляет собой водород, C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил, где каждый C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил замещен в 0-6 независимых случаях галогеном, -ORD, -SRD, -C(O)ORD, -C(O)N(RD)(RE), -N(RD)(RE) или -C(NRF)N(RD)(RE); каждый из R9 и R10 независимо представляет собой водород, галоген, -OH, C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил, где каждый C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, арил, гетероарил, аралкил или гетероаралкил замещен в 0-6 независимых случаях галогеном, -ORD, -SRD, -C(O)ORD, -C(O)N(RD)(RE), -N(RD)(RE) или -C(NRI)N(RG)(RH); каждый RD, RE и RF независимо представляет собой водород, C1-C6алкил, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил, где каждый C1-C6алкил, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил замещен в 0-6 независимых случаях галогеном, -OH или C1-C6алкокси; и n равняется 0, 1, 2, 3, 4 или 5.
[0727] В некоторых вариантах осуществления кольцо B представляет собой гетероарил (например, тиофуранил). В некоторых вариантах осуществления L представляет собой -S(O)2. В некоторых вариантах осуществления R7 представляет собой хлор, и n равняется 1. В некоторых вариантах осуществления R8 представляет собой -CH2OH. В некоторых вариантах осуществления каждый из R9 и R10 независимо представляет собой -CF3.
[0728] В дополнительном варианте осуществления GSI представляет собой соединение, описанное в патенте США № 7687666. В одном варианте осуществления GSI представляет собой PF-5212362, т. е. бегацестат, GSI-953 или (R)-5-хлор-N-(4,4,4-трифтор-1-гидрокси-3-(трифторметил)бутан-2-ил)тиофен-2-сульфонамид, или его фармацевтически приемлемую соль. В одном варианте осуществления GSI представляет собой
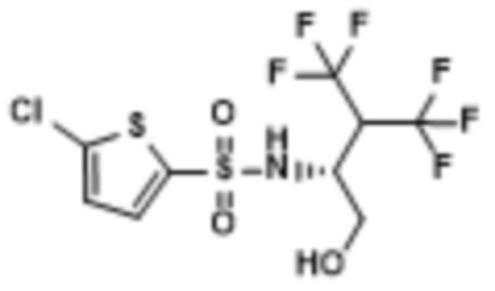
или его фармацевтически приемлемую соль.
[0729] В некоторых вариантах осуществления GSI представляет собой соединение формулы (III) или его фармацевтически приемлемую соль:
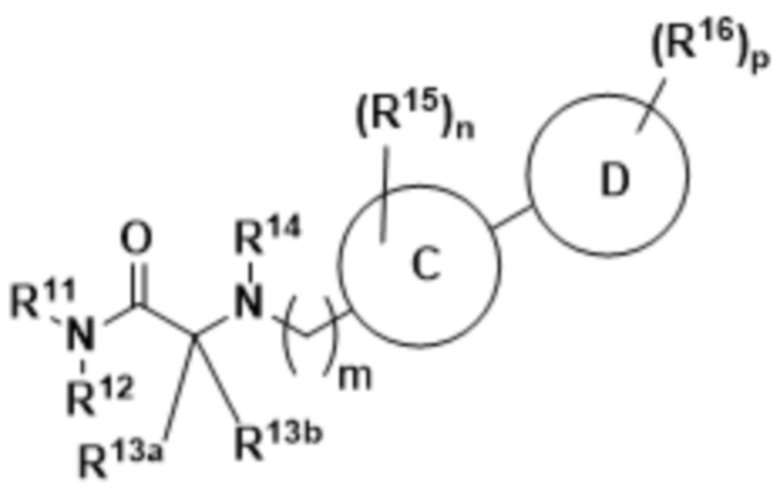 (III),
(III),
где каждое из колец C и D независимо представляет собой арил или гетероарил;
каждый из R11, R12 и R14 независимо представляет собой водород, C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил, где каждый C1-C6алкил, C1-C6алкокси, -S(O)RG-, -S(O)2RG-, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил замещен в 0-6 независимых случаях галогеном, -ORG, -SRG, -C(O)ORG, -C(O)N(RG)(RH), -N(RG)(RH) или -C(NRI)N(RG)(RH); каждый из R13a и R13b представляет собой водород, галоген, -OH, C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил, где каждый C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил замещен в 0-6 независимых случаях галогеном, -ORG, -SRG, -C(O)ORG, -C(O)N(RG)(RH), -N(RG)(RH) или -C(NRI)N(RG)(RH); каждый R15 и R16 независимо представляет собой галоген, -OH, C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил, где каждый C1-C6алкил, C1-C6алкокси, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил замещен в 0-6 независимых случаях галогеном, -ORG, -SRG, -C(O)ORG, -C(O)N(RG)(RH), -N(RG)(RH) или -C(NRI)N(RG)(RH); каждый RG, RH и RI независимо представляет собой водород, C1-C6алкил, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил, где каждый C1-C6алкил, циклоалкил, гетероциклил, циклоалкилалкил, гетероциклилалкил, арил, гетероарил, аралкил или гетероаралкил замещен в 0-6 независимых случаях галогеном, -OH или C1-C6алкокси; и каждый из m, n и p независимо равняется 0, 1, 2, 3, 4 или 5.
[0730] В некоторых вариантах осуществления кольцо C представляет собой арил (например, фенил). В некоторых вариантах осуществления кольцо D представляет собой гетероарил (например, 1,2,4-оксадиазол). В некоторых вариантах осуществления R15 представляет собой фтор, и n равняется 1. В некоторых вариантах осуществления p равняется 0. В некоторых вариантах осуществления m равняется 1. В некоторых вариантах осуществления R14 представляет собой -S(O)2RG, и RG представляет собой хлорфенил. В некоторых вариантах осуществления R13a представляет собой -CH2CH2CF3, а R13b представляет собой водород. В некоторых вариантах осуществления каждый R11 и R12 независимо представляет собой водород.
[0731] В дополнительном варианте осуществления GSI представляет собой соединение, описанное в патенте США № 8084477. В одном варианте осуществления GSI представляет собой BMS-708163, т. е. авагацестат или (R)-2-((4-хлор-N-(2-фтор-4-(1,2,4-оксадиазол-3-ил)бензил)фенил)сульфонамидо)-5,5,5-трифторпентанамид, или его фармацевтически приемлемую соль. В одном варианте осуществления GSI представляет собой
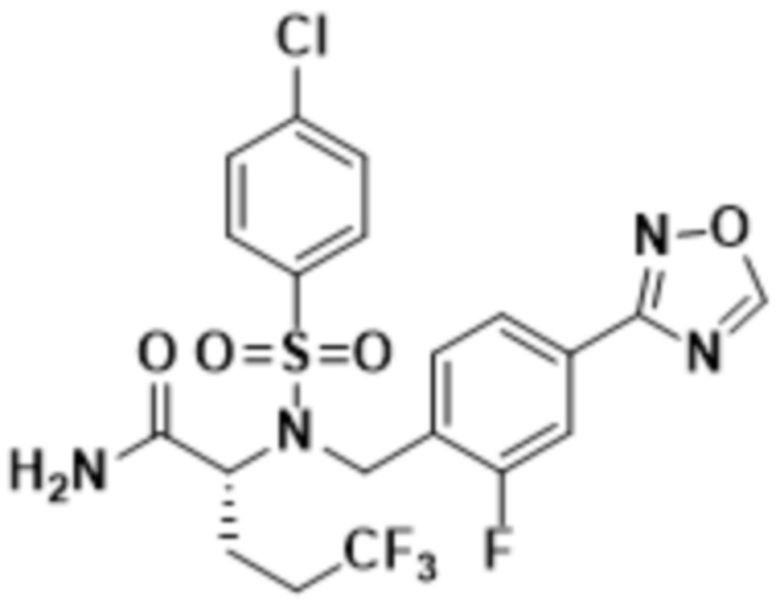
или его фармацевтически приемлемую соль.
[0732] В некоторых вариантах осуществления GSI представляет собой соединение формулы (IV) или его фармацевтически приемлемую соль:
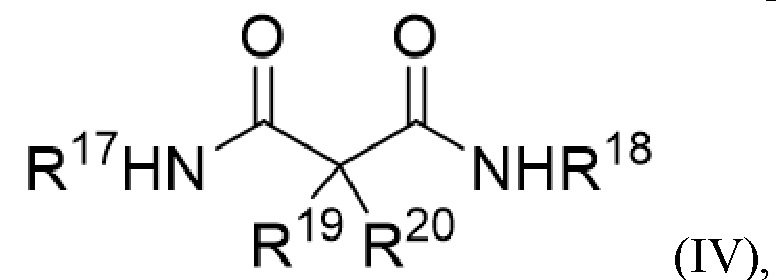 (IV),
(IV),
где R17 выбран из
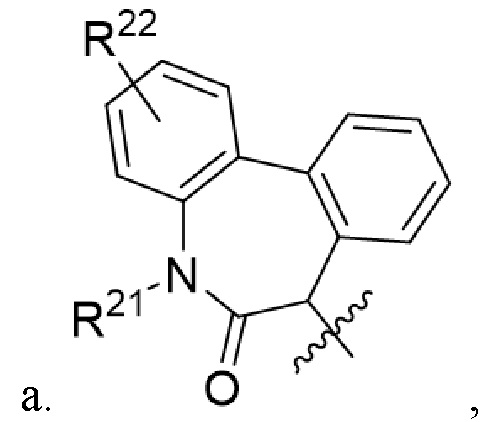
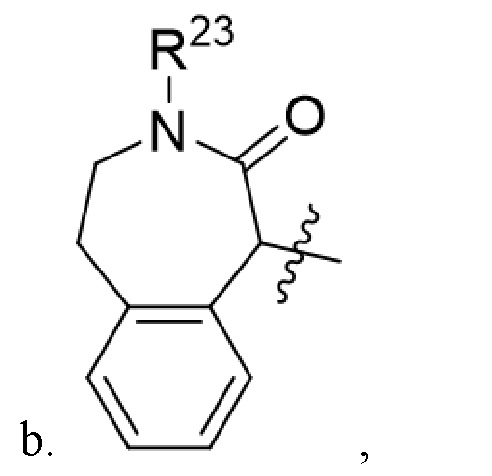
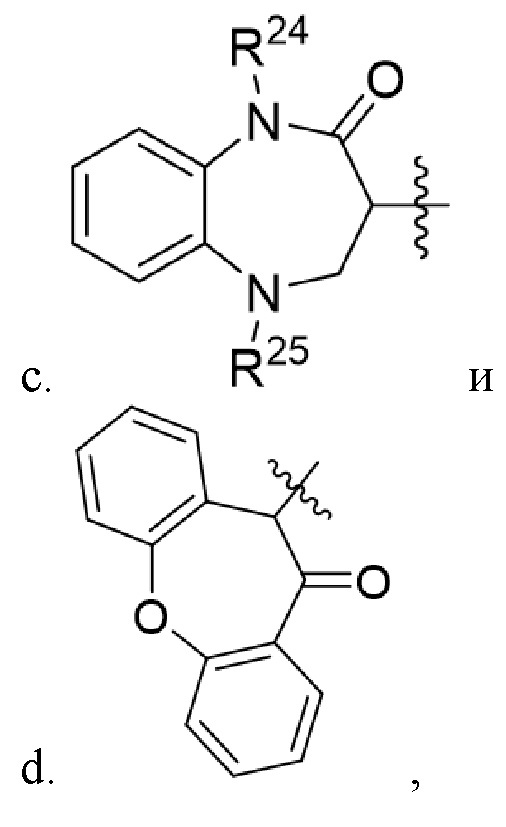
R18 представляет собой низший алкил, низший алкинил, -(CH2)n-O-низший алкил, -(CH2)n-S-низший алкил, -(CH2)n-CN, -(CR'R’’)n-CF3, -(CR'R’’)n-CHF2, -(CR'R’’)n-CH2F, -(CH2)n, -C(O)O-низший алкил, -(CH2)n-галоген или представляет собой -(CH2)n-циклоалкил, необязательно замещенный одним или более заместителями, выбранными из группы, состоящей из фенила, галогена и CF3; каждый из R', R’’ независимо представляет собой водород, низший алкил, низший алкокси, галоген или гидрокси; каждый из R19, R20 независимо представляет собой водород, низший алкил, низший алкокси, фенил или галоген; R21 представляет собой водород, низший алкил, -(CH2)n-CF3 или -(CH2)n-циклоалкил; R22 представляет собой водород или галоген; R23 представляет собой водород или низший алкил; R24 представляет собой водород, низший алкил, низший алкинил, -(CH2)n-CF3, -(CH2)n-циклоалкил или -(CH2)n-фенил, необязательно замещенный галогеном; R25 представляет собой водород, низший алкил, -C(O)H, -C(O)-низший алкил, -C(O)-CF3, -C(O)-CH2F, -C(O)-CHF2, -C(O)-циклоалкил, -C(O)-(CH2)n-O-низший алкил, -C(O)O-(CH2)n-циклоалкил, -C(O)-фенил, необязательно замещенный одним или более заместителями, выбранными из группы, состоящей из галогена и -C(O)O-низшего алкила, или представляет собой -S(O)2-низший алкил, -S(O)2-CF3, -(CH2)n-циклоалкил, или представляет собой -(CH2)n-фенил, необязательно замещенный галогеном; n равняется 0, 1, 2, 3 или 4.
[0733] В некоторых вариантах осуществления R17 представляет собой 5,7-дигидро-6H-дибензо[b, d]азепин-6-онил. В некоторых вариантах осуществления каждый R19 и R20 независимо представляет собой -CH3. В некоторых вариантах осуществления R18 представляет собой CH2CF2CF3.
[0734] В некоторых вариантах осуществления GSI представляет собой соединение, описанное в патенте США № 7160875. В одном варианте осуществления GSI представляет собой RO4929097, т. е. (S)-2,2-диметил-N1-(6-оксо-6,7-дигидро-5H-дибензо[b, d]азепин-7-ил)-N3-(2,2,3,3,3-пентафторпропил)малонамид, или его фармацевтически приемлемую соль. В одном варианте осуществления GSI представляет собой
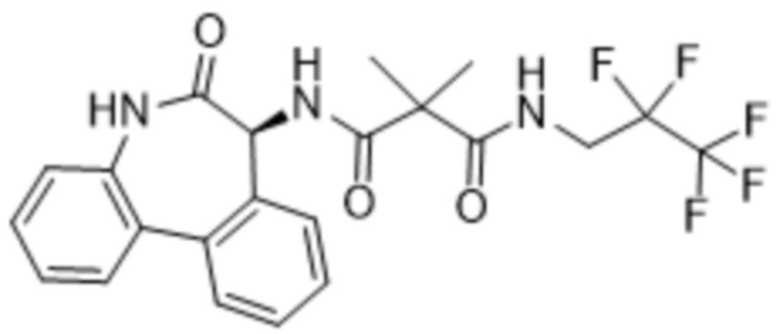
или его фармацевтически приемлемую соль.
[0735] В некоторых вариантах осуществления GSI представляет собой
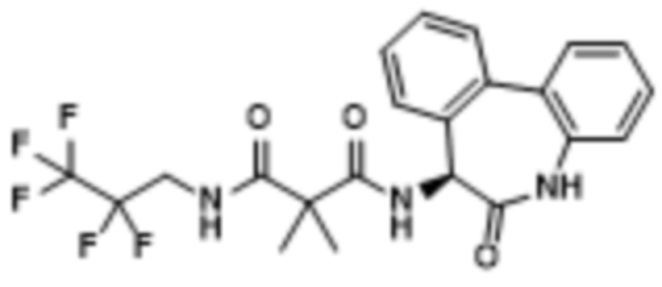
или его фармацевтически приемлемую соль.
[0736] В некоторых вариантах осуществления GSI представляет собой соединение формулы (V) или его фармацевтически приемлемую соль:
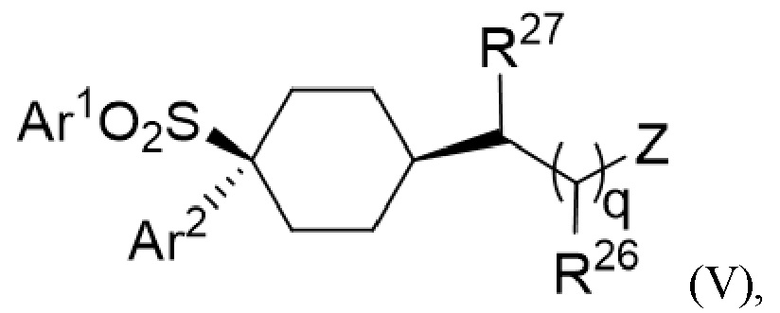
где
q равняется 0 или 1; Z представляет собой галоген, -CN, -NO2, -N3, -CF3, -OR2a, -N(R2a)2, -CO2R2a, -OCOR2a, -COR2a, -CON(R2a)2, -OCON(R2a)2, -CONR2a(OR2a), -CON(R2a)N(R2a)2, -CONHC(=NOH)R2a, гетероциклил, фенил или гетероарил, при этом гетероциклил, фенил или гетероарил несут 0-3 заместителя, выбранных из галогена, -CN, -NO2, -CF3, -OR2a, -N(R2a)2, -CO2R2a, -COR2a, -CON(R2a)2 и C1-4алкила; R27 представляет собой H, C1-4алкил или OH; R26 представляет собой H или C1-4алкил; при условии, что если m равняется 1, то как R26, так и R27 не представляют собой C1-4алкил; Ar1 представляет собой C6-10арил или гетероарил, любой из которых несет 0-3 заместителя, независимо выбранных из галогена, -CN, -NO2, -CF3, -OH, -OCF3, C1-4алкокси или C1-4алкила, который необязательно несет заместитель, выбранный из галогена, CN, NO2, CF3, OH и C1-4алкокси; Ar2 представляет собой C6-10арил или гетероарил, любой из которых несет 0-3 заместителя, независимо выбранных из галогена, -CN, -NO2, -CF3, -OH, -OCF3, C1-4алкокси или C1-4алкила, который необязательно несет заместитель, выбранный из галогена, -CN, -NO2, -CF3, -OH и C1-4алкокси; R2a представляет собой H, C1-6алкил, C3-6циклоалкил, C3-6циклоалкил, C1-6алкил, C2-6алкенил, любой из которых необязательно несет заместитель, выбранный из галогена, -CN, -NO2, -CF3, -OR2b, -CO2R2b, -N(R2b)2, -CON(R2b)2, Ar и COAr; или R2a представляет собой Ar; или две группы R2a вместе с атомом азота, к которому они совместно присоединены, могут составлять N-гетероциклильную группу, несущую 0-4 заместителя, независимо выбранных из =O, =S, галогена, C1-4алкила, -CN, -NO2, -CF3, -OH, C1-4алкокси, C1-4алкоксикарбонила, CO2H, амино, C1-4алкиламино, ди(C1-4алкил)амино, карбамоила, Ar и COAr; R2b представляет собой H, C1-6алкил, C3-6циклоалкил, C3-6циклоалкил-C1-6алкил, C2-6алкенил, любой из которых необязательно несет заместитель, выбранный из галогена, -CN, -NO2, -CF3, -OH, C1-4алкокси, C1-4алкоксикарбонила, -CO2H, амино, C1-4алкиламино, ди(C1-4алкил)амино, карбамоила, Ar и COAr; или R2b представляет собой Ar; или две группы R2b вместе с атомом азота, к которому они совместно присоединены, могут составлять N-гетероциклильную группу, несущую 0-4 заместителя, независимо выбранных из =O, =S, галогена, C1-4алкила, -CN, -NO2, CF3, -OH, C1-4алкокси, C1-4алкоксикарбонила, -CO2H, амино, C1-4алкиламино, ди(C1-4алкил)амино, карбамоила, Ar и COAr; Ar представляет собой фенил или гетероарил, несущий 0-3 заместителя, выбранных из галогена, C1-4алкила, -CN, -NO2, -CF3, -OH, C1-4алкокси, C1-4алкоксикарбонила, амино, C1-4алкиламино, ди(C1-4алкил)амино, карбамоила, C1-4алкилкарбамоила и ди(C1-4алкил)карбамоила.
[0737] В некоторых вариантах осуществления q равняется 1. В некоторых вариантах осуществления Z представляет собой CO2H. В некоторых вариантах осуществления каждый из R27 и R26 независимо представляет собой водород. В некоторых вариантах осуществления Ar1 представляет собой хлорфенил. В некоторых вариантах осуществления Ar2 представляет собой дифторфенил.
[0738] В некоторых вариантах осуществления GSI представляет собой соединение, описанное в патенте США № 6984663. В одном варианте осуществления GSI представляет собой MK-0752, т. е. 3-((1S,4R)-4-((4-хлорфенил)сульфонил)-4-(2,5-дифторфенил)циклогексил)пропановую кислоту, или ее фармацевтически приемлемую соль. В некоторых вариантах осуществления GSI представляет собой
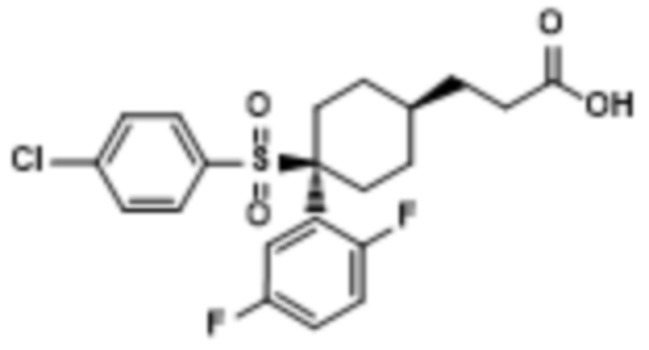
или его фармацевтически приемлемую соль.
[0739] В некоторых вариантах осуществления GSI представляет собой соединение формулы (VI) или его фармацевтически приемлемую соль:
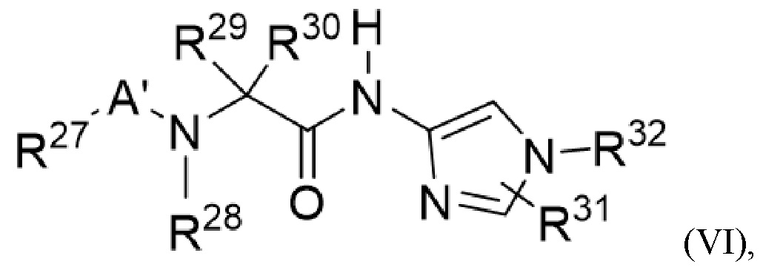
где A’ отсутствует или выбран из
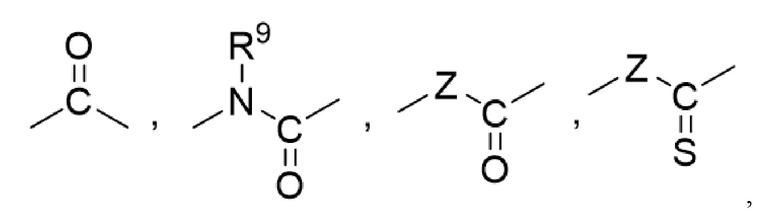 ,
,
а также -S(O)2-;
Z выбран из -CH2, -CH(OH), -CH(C1-C6алкил), -CH(C1-C6алкокси), -CH(NR33R34), -CH(CH2(OH)), -CH(CH(C1-C4алкил)(OH)) и -CH(C(C1-C4алкил)(C1-C4алкил)(OH)), например, -CH(C(CH3)(CH3)(OH)) или -CH(C(CH3)(CH2CH3)(OH)); R27 выбран из C1-C20алкила, C2-C20алкенила, C2-C20алкинила, C1-C20алкокси, C2-C20алкенокси, C1-C20гидроксиалкила, C3-C8циклоалкила, бензо(C3-C8циклоалкил), бензо(C3-C8гетероциклоалкил), C4-C8циклоалкенила, (C5-C11)би- или трициклоалкила, бензо(C5-C11)би- или трициклоалкила, C7-C11трициклоалкенила, (3-8-членного) гетероциклоалкила, C6-C14арила и (5-14-членного) гетероарила, где каждый атом водорода алкила, алкенила, алкинила, алкокси и алкенокси необязательно независимо заменен на галоген, и где циклоалкил, бензо(C3-C8циклоалкил), циклоалкенил, (3-8-членный) гетероциклоалкил, C6-C14арил и (5-14-членный) гетероарил необязательно независимо замещены заместителями в количестве от одного до четырех, независимо выбранными из C1-C10алкила, необязательно замещенного атомами галогена в количестве от одного до трех, C1-C10алкокси, необязательно замещенного атомами галогена в количестве от одного до трех, C1-C10гидроксиалкила, галогена, например, фтора, -OH, -CN, - NR33R34, -C(=O)NR33R34, -C(=O)R35, C3-C8циклоалкила и (3-8-членного) гетероциклоалкила; R28 выбран из водорода, C1-C6алкила, C2-C6алкенила, C3-C8циклоалкила и C5-C8циклоалкенила, где R28 необязательно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из C1-C4алкила, необязательно замещенного атомами галогена в количестве от одного до трех, C1-C4алкокси, необязательно замещенного атомами галогена в количестве от одного до трех, галогена и -OH; или R27 и R28 вместе с группой A’, если она присутствует, и атомом азота, к которому присоединен R28, или R27 и R28 вместе с атомом азота, к которому присоединены R27 и R28, если A’ отсутствует, необязательно могут образовывать кольцо от четырех- до восьмичленного; R29 выбран из водорода, C1-C6алкила, C2-C6алкенила, C2-C6алкинила, C3-C6циклоалкила, C5-C6циклоалкенила и (3-8-членного) гетероциклоалкила, где каждый из алкила, алкенила, алкинила, циклоалкила, циклоалкенила и гетероциклоалкила необязательно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из C1-C4алкокси, галогена, -OH-S(C1-C4)алкила и (3-8-членного) гетероциклоалкила; R30 представляет собой водород, C1-C6алкил или галоген; или R29 и R30 вместе с атомом углерода, к которому они присоединены, необязательно могут образовывать фрагмент, выбранный из циклопропила, циклобутила, циклопентила, циклогексила, морфолинo, пиперидино, пирролидино, тетрагидрофуранила и пергидро-2H-пирана, где фрагмент, образованный R29 и R30, необязательно замещен заместителями в количестве от одного до трех, независимо выбранными из C1-C6алкила, необязательно замещенного атомами галогена в количестве от одного до трех, C1-C6алкокси, необязательно замещенного атомами галогена в количестве от одного до трех, галогена, -OH, -CN и аллила; R31 выбран из водорода, C1-C6алкила, C2-C6алкилена, C1-C6алкокси, галогена, -CN, C3-C12циклоалкила, C4-C12циклоалкенила и C6-C10арила, (5-10-членного) гетероарила, где каждый из алкила, алкилена и алкокси в R31 необязательно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из галогена и -CN, и где каждый из циклоалкила, циклоалкенила и арила, а также гетероарила в R31 необязательно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из C1-C4алкила, необязательно замещенного атомами галогена в количестве от одного до трех, C1-C4алкокси, необязательно замещенного атомами галогена в количестве от одного до трех, галогена и -CN; R32 выбран из водорода, C1-C20алкила, C1-C20алкокси, C1-C20гидроксиалкила, C3-C12циклоалкила, C4-C12циклоалкенила, (C5-C20)би- или трициклоалкила, (C7-C20)би- или трициклоалкенила, (3-12-членного) гетероциклоалкила, (7-20-членного) гетероби- или гетеротрициклоалкила, C6-C14арила и (5-15-членного) гетероарила, где R32 необязательно независимо замещен заместителями в количестве от одного до четырех, независимо выбранными из C1-C20алкила, необязательно замещенного атомами галогена в количестве от одного до трех, C1-C20алкокси, -OH, -CN, -NO2, -NR33R34, -C(=O)NR33R34, -C(=O)R35, -C(=O)OR35, -S(O)nNR33R34, -S(O)nR35, C3-C12циклоалкила, (4-12-членного) гетероциклоалкила, необязательно замещенного группами OH или галогена в количестве от одной до трех, (4-12-членного) гетероциклоалкокси, C6-C14арила, (5-15-членного) гетероарила, C6-C12арилокси и (5-12-членного) гетероарилокси; или R33 и R34 вместе с атомами углерода и азота, к которым они соответственно присоединены, необязательно могут образовывать (5-8-членное) гетероциклоалкильное кольцо, (5-8-членное) гетероциклоалкенильное кольцо или (6-10-членное) гетероарильное кольцо, где каждое из гетероциклоалкильного, гетероциклоалкенильного и гетероарильного колец необязательно независимо замещено заместителями в количестве от одного до трех, независимо выбранными из галогена, C1-C6алкила, необязательно замещенного атомами галогена в количестве от одного до трех, C1-C6алкокси, необязательно замещенного атомами галогена в количестве от одного до трех, C1-C6гидроксиалкила, -OH, -(CH2)ноль-10NR33R34, -(CH2)ноль-10C(=O)NR33R34, -S(O)2NR33R34 и C3-C12циклоалкила; каждый из R33 и R34 независимо выбран из водорода, C1-C10алкила, где каждый атом водорода C1-C10алкила необязательно независимо заменен на атом галогена, например, атом фтора, C2-C10алкенила, C2-C10алкинила, C1-C6алкокси, где каждый атом водорода C1-C6алкокси необязательно независимо заменен на атом галогена, C2-C6алкенокси, C2-C6алкинокси, -C(=O)R11, -S(O)nR11, C3-C8циклоалкила, C4-C8циклоалкенила, (C5-C11)би- или трициклоалкила, (C7-C11)би- или трициклоалкенила, (3-8-членного) гетероциклоалкила, C6-C14арила и (5-14-членного) гетероарила, где каждый из алкила и алкокси необязательно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из галогена и -OH, и где каждый из циклоалкила, циклоалкенила, би- или трициклоалкила, би- или трициклоалкенила, гетероциклоалкила, арила и гетероарила необязательно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из галогена, -OH, C1-C6алкила, необязательно независимо замещенного атомами галогена в количестве от одного до шести, C2-C6алкенила, C2-C6алкинила, C1-C6алкокси, C2-C6алкенокси, C2-C6алкинокси и C1-C6гидроксиалкила; или NR33R34 может образовывать (4-7-членный) гетероциклоалкил, где гетероциклоалкил необязательно содержит от одного до двух дополнительных гетероатомов, независимо выбранных из N, O и S, и где гетероциклоалкил необязательно содержит от одной до трех двойных связей, и где гетероциклоалкил необязательно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из C1-C6алкила, необязательно замещенного атомами галогена в количестве от одного до шести, C2-C6алкенила, C2-C6алкинила, C1-C6алкокси, C2-C6алкенокси, C2-C6алкинокси, C1-C6гидроксиалкила, C2-C6гидроксиалкенила, C2-C6гидроксиалкинила, галогена, -OH, -CN, -NO2, -C(=O)R35, -C(=O)OR35, -S(O)nR35 и -S(O)nNR33R34; R35 выбран из водорода, C1-C8алкила, C3-C8циклоалкила, C4-C8циклоалкенила, (C5-C11)би- или трициклоалкила, -(C7-C11)би- или трициклоалкенила, (3-8-членного) гетероциклоалкила, C6-C10арила и (5-14-членного) гетероарила, где алкил в R35 необязательно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из -OH, -CN и C3-C8циклоалкила, и где каждый атом водорода алкила необязательно независимо заменен на атом галогена, например, атом фтора, и где каждый из циклоалкила, циклоалкенила, гетероциклоалкила, арила и гетероарила в R35 необязательно независимо замещен заместителями в количестве от одного до трех, независимо выбранными из галогена, C1-C8алкила, необязательно замещенного атомами галогена в количестве от одного до трех, -OH, -CN и C3-C8циклоалкила; n в каждом случае представляет собой целое число, независимо выбранное из нуля, 1, 2 и 3; и фармацевтически приемлемые соли таких соединений.
[0740] В некоторых вариантах осуществления GSI представляет собой соединение, описанное в патенте США № 7795447. В одном варианте осуществления GSI представляет собой PF-3084014, т. е. нирогацестат или (S)-2-(((S)-6,8-дифтор-1,2,3,4-тетрагидронафталин-2-ил)амино)-N-(1-(2-метил-1-(неопентиламино)пропан-2-ил)-1H-имидазол-4-ил)пентанамид, или его фармацевтически приемлемую соль.
[0741] В некоторых вариантах осуществления GSI представляет собой
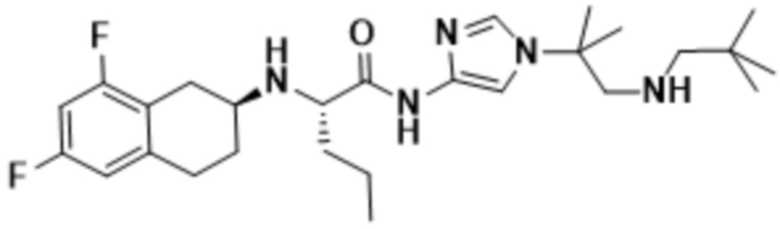
или его фармацевтически приемлемую соль.
[0742] В некоторых вариантах осуществления соединение представляет собой соединение формулы (VII):
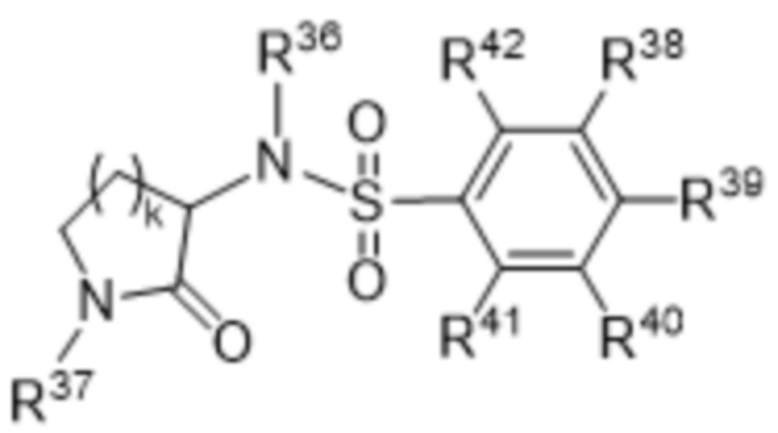 (VII),
(VII),
или его фармацевтически приемлемую соль, где k равняется 1, 2 или 3; R36 представляет собой арил-C1-C8алкил, арил-C2-C6алкенил или арилалкинил, где арильная группа замещена в 0-5 случаях C1-C6алкилом, C1-C6алкокси, галогеном, галогеналкилом, галогеналкокси, гетероарилом, гетероарил(C1-C6)алкокси, арилалкокси, арилокси, C1-C6алкоксикарбонилом, -OCH2CH2O-, -OCH2O-, -C(O)NR43R44, -NHR′, -NR′R″, -N(R16)C(O)R17, гетероциклоалкилом, фенилом, арил-C1-C6алканоилом, фенилалкокси, фенилокси, CN, -SO2-арилом, -S(O)nR25, -(C1-C4алкил)-S(O)xR25, -(C1-C4алкил)-SO2-арилом, OH, C1-C6тиоалкокси, C2-C6алкенилом, -OSO2-арилом или CO2H, где каждый гетероарил независимо замещен в 0-3 случаях C1-C6алкилом, гетероарилом, замещенным в 0-2 случаях галогеном, алкилом, алкокси, галогеналкилом, галогеналкокси, алкоксиалкилом или CN, C1-C6алкокси, C1-C4алкокси, C1-C4алкилом, C3-C6циклоалкилом, галогеном или фенилом, замещенным в 0-5 случаях галогеном, OH, C1-C6алкилом, C1-C4алкокси, CF3, OCF3, CN или C1-C6тиоалкокси,
где каждый гетероциклоалкил и арил независимо замещены в 0-2 случаях галогеном, алкилом, алкокси, галогеналкилом, галогеналкокси, алкоксиалкилом или CN, C1-C6алкилом, C1-C6алкокси, C1-C4алкокси, C1-C4алкилом, C3-C6циклоалкилом, галогеном, или фенил замещен в 0-5 случаях галогеном, OH, C1-C6алкилом, C1-C4алкокси, CF3, OCF3, CN или C1-C6тиоалкокси; R16 представляет собой водород или C1-C6алкил; R17 представляет собой C1-C6алкил, арил, гетероарил, C1-C6алкокси, OH, арилокси, гетероарилокси, арил(C1-C6)алкокси, -NR18R19, циклоалкил или арилалкил, где циклические части каждого из них независимо замещены в 0-5 случаях алкилом, алкокси, галогеном, галогеналкилом, галогеналкокси, CN, NH2, NH(алкил), N(алкил)(алкил), CO2H или C1-C6алкоксикарбонилом; R18 и R19 независимо представляют собой водород, C1-C6алкил, арил, гетероарил, гетероциклоалкил или арил(C1-C6)алкил, где циклические части каждого из них замещены в 0-3 случаях алкилом, алкокси, галогеном, гидроксилом, CF3 или OCF3; каждый R' независимо представляет собой водород, C1-C6алкил, арил, арил(C1-C4)алкил, C1-C6алканоил, C3-C8циклоалкил, арил(C1-C6)алканоил, гетероциклоалкил, гетероарил(C1-C4)алкил, -SO2-алкил, -SO2-арил, -SO2-гетероарил, гетероциклоалкил(C1-C6)алканоил или гетероарил(C1-C6)алканоил, где алкильная часть алкильной и алканоильной групп необязательно замещена галогеном или C1-C6алкокси, а арильная и гетероарильная группы необязательно замещены алкилом, алкокси, галогеном, галогеналкилом, галогеналкокси; каждый R'' независимо представляет собой водород или C1-C6алкил, где алкильная группа необязательно замещена галогеном;
R36 представляет собой C3-C7циклоалкил(C1-C6алкил), где циклическая часть замещена в 0-5 случаях галогеном, C1-C6алкилом, OH, алкоксикарбонилом или C1-C6алкокси; или R36 представляет собой C1-C14алкил, C2-C16алкенил или C2-C8алкинил, каждый из которых замещен в 0-5 случаях OH, галогеном, C1-C6алкокси, арилом, арилалкокси, арилокси, гетероарилом, гетероциклоалкилом, арил(C1-C6)алкилом, -CO2(C1-C6алкил), -NR'R'', C1-C6тиоалкокси, -NHS(O)xR25, -N(C1-C6алкил)-S(O)nR25, -S(O)xR25, -C(O)NR43R44, -N(R16)C(O)NR16R17 или -N(R16)C(O)R17; где указанные выше арильные группы замещены в 0-3 случаях ОН, C1-C6алкокси, C1-C6алкилом или галогеном; R43 и R44 независимо представляют собой водород, C1-C6алкил, арил, арилалкил, гетероарил, гетероарилалкил, гетероциклоалкил, гетероциклоалкилалкил, арилалканоил, алкенил, циклоалкил, алкинил, циклоалкенил, пиридил, имидазолил, тиазолил, оксазолил или индолил, где каждый алкил замещен в 0-3 случаях NH2, NH(C1-C6алкил), N(C1-C6алкил)(C1-C6алкил), OH, C1-C6тиоалкокси, гетероциклоалкилом, арилом, гетероарилом, CN, галогеном или алкокси, необязательно замещенным ОН или фенилом, где арильная, гетероарильная и гетероциклоалкильная группы замещены в 0-3 случаях C1-C4алкилом, C1-C4алкокси, CF3, OCF3, OH, галогеном, тиоалкокси, фенилом или гетероарилом; или R43, R44 и атом азота, к которому они присоединены, образуют гетероциклоалкильное кольцо, содержащее от 3 до 7 членов кольца, где циклические части R43 и R44 или гетероциклическое кольцо, образованное из R43, R44 и атома азота, к которому они присоединены, замещены в 0-3 случаях алкилом, алкокси, галогеном, OH, тиоалкокси, NH2, NH(C1-C6алкил), N(C1-C6алкил)(C1-C6алкил), CF3, OCF3, фенилом, необязательно замещенным галогеном, -(C1-C4алкил)-N(H или C1-C4алкил)фенилом, C1-C4гидроксиалкилом, арилалкокси, арилалкилом, арилалканоилом, C(O)NH2, C(O)NH(C1-C6алкил), C(O)N(C1-C6алкил)(C1-C6алкил), гетероциклоалкилалкилом, C1-C6алкоксикарбонилом, C2-C6алканоилом, гетероарилом или -SO2(C1-C6алкил); х равняется 0, 1 или 2; R25 представляет собой C1-C6алкил, OH, NR26R27; R26 и R27 независимо представляют собой водород, C1-C6алкил, фенил(C1-C4алкил), арил или гетероарил; или R26, R27 и атом азота, к которому они присоединены, образуют гетероциклоалкильное кольцо;
R36 представляет собой гетероарил(C1-C6)алкил, где циклическая часть замещена в 0-5 случаях галогеном, C1-C6алкилом, C1-C6алкокси, C1-C4галогеналкилом, C1-C4галогеналкокси, арилом, арилалкилом, арилокси, гетероарилом, -SO2-арилом, -S(O)xR25, (C1-C4алкил)-S(O)xR25, CN, C1-C6тиоалкокси, C1-C6алкоксикарбонилом, -NR'R'', -C(O)NR'R'', гетероциклоалкилом, где вышеуказанные арильные группы замещены в 0-4 случаях галогеном, C1-C6алкилом, C1-C6алкокси, C1-C4галогеналкилом, C1-C4галогеналкокси или CN; где указанные выше гетероарильные и гетероциклоалкильные группы замещены в 0-3 случаях галогеном, CF3, (C1-C4)алкилом, C1-C6тиоалкокси, OH, C1-C4гидроксиалкилом или C1-C4алкокси; или
R36 представляет собой гетероциклоалкил(C1-C6алкил), где циклическая часть замещена в 0-3 случаях галогеном, C1-C6алкилом, C1-C6алкокси, C1-C4галогеналкилом, C1-C4галогеналкокси, арилом, арилалкилом, арилокси, гетероарилом, -SO2-арилом, -S(O)xR25, (C1-C4алкил)-S(O)xR25, CN, C1-C6тиоалкокси, C1-C6алкоксикарбонилом, -NR'R'', -C(O)NR'R'', гетероциклоалкилом;
R37 представляет собой водород, C1-C6алкил или фенил(C1-C4)алкил; R38 представляет собой водород, галоген, C1-C6алкил, C1-C6алкокси, C1-C6галогеналкил, CN; R39 представляет собой водород, галоген, C1-C6алкил, необязательно замещенный с помощью -CO2-(C1-C6алкил), C1-C6алкокси, C1-C6галогеналкил, C1-C6галогеналкокси, CN, арилокси, изоцианато, -SO2(C1-C6алкил), -NHR', -NR'R'', C1-C6алканоил, гетероарил, арил; или
R38 и R39 и атомы углерода, к которым они присоединены, образуют гетероциклоалкильное кольцо, которое замещено в 0-3 случаях C1-C4алкилом, C1-C4алкокси, галогеном или C1-C4алканоилом, где алканоильная группа замещена 0-3 атомами галогена; R40 представляет собой водород, -SO2NR'R'', галоген; или R39 и R40 и атомы углерода, к которым они присоединены, образуют бензокольцо; или R39 и R40 и атомы углерода, к которым они присоединены, образуют 1-окса-2,3-диазациклопентильное кольцо;
R40 и R41 независимо представляют собой водород или F; или R40, R41 и атомы углерода, к которым они присоединены, образуют 1,2,5-оксадиазолильное кольцо; или R40, R41 и атомы углерода, к которым они присоединены, образуют нафтильное кольцо.
[0743] В некоторых вариантах осуществления R36 представляет собой 4-бромбензил. В некоторых вариантах осуществления R37 представляет собой водород. В некоторых вариантах осуществления k равняется 2. В некоторых вариантах осуществления каждый из R38, R40, R41 и R42 независимо представляет собой водород. В некоторых вариантах осуществления R39 представляет собой хлор.
[0744] В некоторых вариантах осуществления GSI представляет собой соединение, описанное в патенте США № 7939657. В одном варианте осуществления GSI представляет собой ELN-318463, т. е. HY-50882 или (R)-N-(4-бромбензил)-4-хлор-N-(2-оксоазепан-3-ил)бензолсульфонамид, или его фармацевтически приемлемую соль. В некоторых вариантах осуществления GSI представляет собой
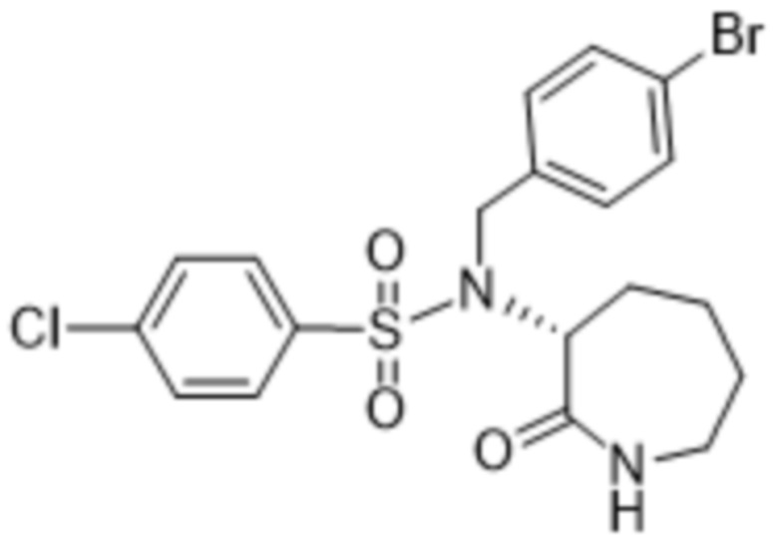
или его фармацевтически приемлемую соль.
[0745] В некоторых вариантах осуществления GSI представляет собой соединение формулы (VIII):
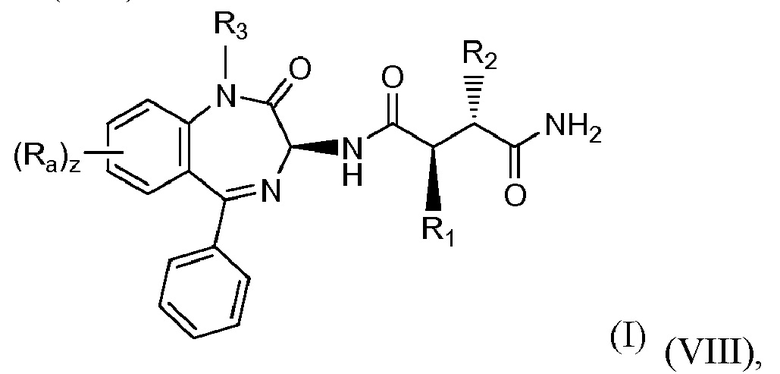
или его фармацевтически приемлемую соль, где R1 представляет собой -CH2CF3 или -CH2CH2CF3; R2 представляет собой -CH2CF3, -CH2CH2CF3 или -CH2CH2CH2CF3; R3 представляет собой водород или -CH3; каждый Ra независимо представляет собой F, CI, -CN, -OCH3 и/или -NHCH2CH2OCH3; и z равняется 0, 1 или 2.
[0746] В некоторых вариантах осуществления R1 представляет собой -CH2CH2CF3CH2CH2CF3. В некоторых вариантах осуществления R2 представляет собой -CH2CH2CF3. В некоторых вариантах осуществления R3 представляет собой -CH3. В некоторых вариантах осуществления z равняется 0.
[0747] В некоторых вариантах осуществления GSI представляет собой соединение, описанное в патенте США № 8629136. В одном варианте осуществления GSI представляет собой BMS-906024, т. е. (2R,3S)-N-[(3S)-1-метил-2-оксо-5-фенил-2,3-дигидро-1H-1,4-бензодиазепин-3-ил]-2,3-бис(3,3,3-трифторпропил)сукцинамид, или его фармацевтически приемлемую соль. В одном варианте осуществления GSI представляет собой
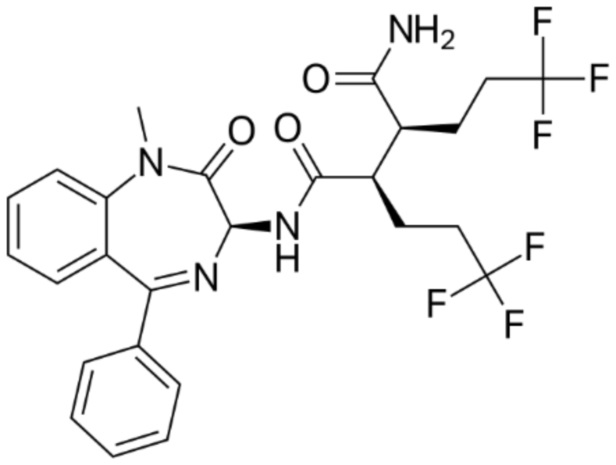
или его фармацевтически приемлемую соль.
[0748] В некоторых вариантах осуществления GSI представляет собой соединение, описанное в патенте США № 8629136. В одном варианте осуществления GSI представляет собой LY3039478, т. е. кренигацестат или 4,4,4-трифтор-N-((R)-1-(((S)-5-(2-гидроксиэтил)-6-оксо-6,7-дигидро-5H-бензо[d]пиридо[2,3-b]азепин-7-ил)амино)-1-оксопропан-2-ил)бутанамид, или его фармацевтически приемлемую соль. В некоторых вариантах осуществления GSI представляет собой
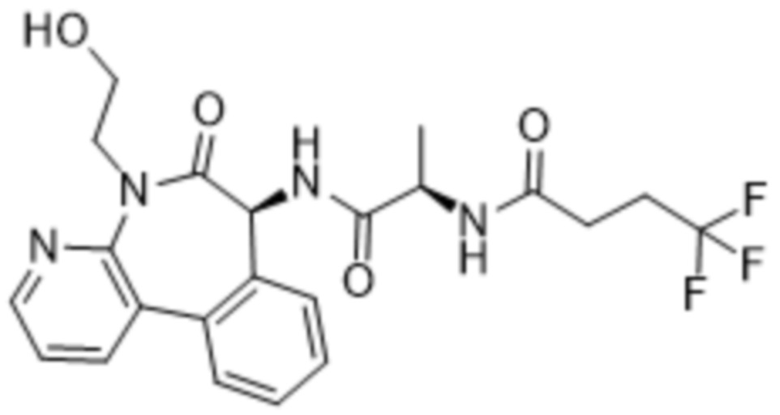
или его фармацевтически приемлемую соль.
[0749] В некоторых вариантах осуществления GSI представляет собой BMS-299897, т. е. 2-[(1R)-1-[[(4-хлорфенил)сульфонил](2,5-дифторфенил)амино]этил-5-фторбензолбутановую кислоту, или ее фармацевтически приемлемую соль. В некоторых вариантах осуществления GSI представляет собой
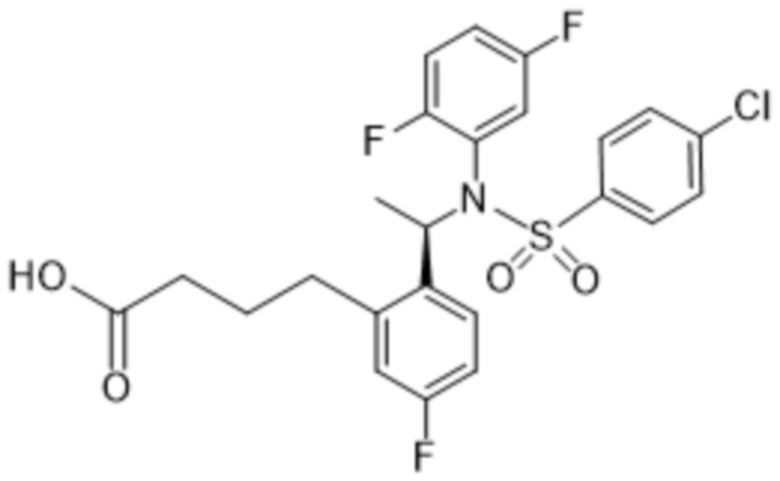
или его фармацевтически приемлемую соль.
[0750] В некоторых вариантах осуществления GSI представляет собой LY-411575, т. е. LSN-411575, (S)-2-((S)-2-(3,5-дифторфенил)-2-гидроксиацетамидо)-N-((S)-5-метил-6-оксо-6,7-дигидро-5H-дибензо[b, d]азепин-7-ил)пропанамид, или его фармацевтически приемлемую соль. В некоторых вариантах осуществления GSI представляет собой
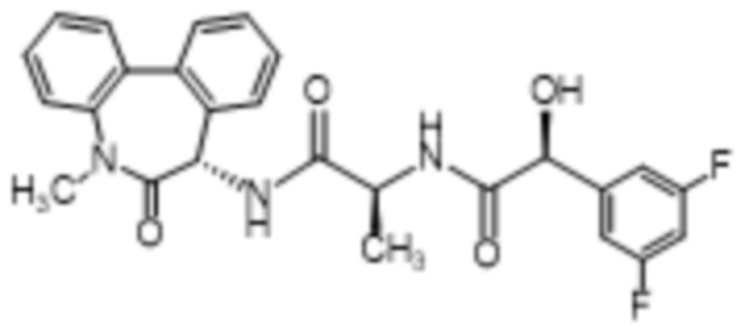
или его фармацевтически приемлемую соль.
[0751] В некоторых вариантах осуществления GSI представляет собой DAPT, т. е. N-[[(3,5-дифторфенил)ацетил]-L-аланил-2-фенил]глицин-1,1-диметилэтиловый сложный эфир, или его фармацевтически приемлемую соль. В некоторых вариантах осуществления GSI представляет собой
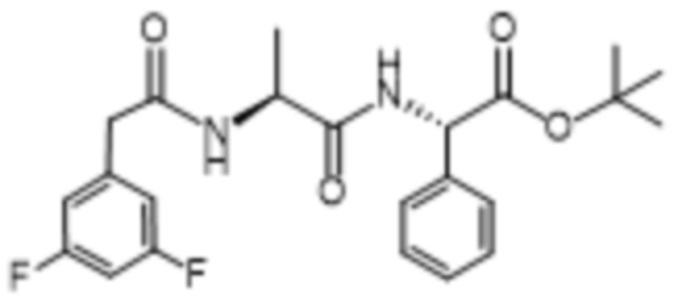
или его фармацевтически приемлемую соль.
[0752] В некоторых вариантах осуществления GSI представляет собой соединение следующих формул:
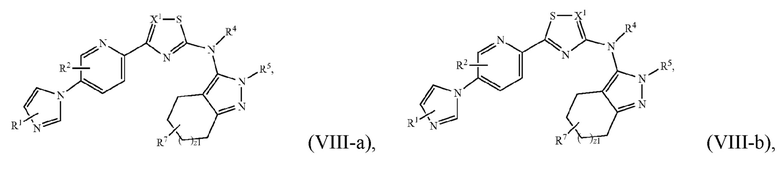
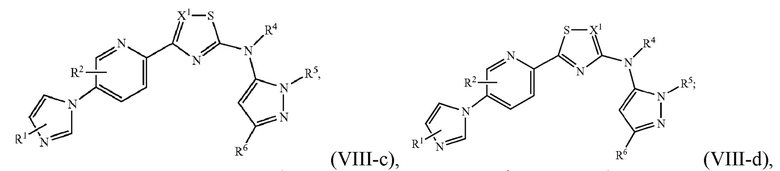
где z1 равняется 0, 1 или 2; X1 представляет собой C(R3) или N; R1 представляет собой водород, галоген, -N3, -CF3, -CCl3, -CBr3, -CI3, -CN, -CHO, -OR1A, -NR1AR1B, -COOR1A, -C(O)NR1AR1B, -NO2, -SR1A, -S(O)n1OR1A, -S(O)n1NR1AR1B, -NHNR1AR1B, -ONR1AR1B, -NHC(O)NHNR1AR1B, замещенный или незамещенный алкил, замещенный или незамещенный гетероалкил, замещенный или незамещенный циклоалкил, замещенный или незамещенный гетероциклоалкил, замещенный или незамещенный арил или замещенный или незамещенный гетероарил; R2 представляет собой водород, галоген, -N3, -CF3, -CCl3, -CBr3, -CI3, -CN, -CHO, -OR2A, -NR2AR2B, -COOR2A, -C(O)NR2AR2B, -NO2, -SR2A, -S(O)n2R2A, -S(O)n2OR2A, -S(O)n2NR2AR2B, -NHNR2AR2B, -ONR2AR2B, -NHC(O)NHNR2AR2B, замещенный или незамещенный алкил, замещенный или незамещенный гетероалкил, замещенный или незамещенный циклоалкил, замещенный или незамещенный гетероциклоалкил, замещенный или незамещенный арил или замещенный или незамещенный гетероарил; R3 представляет собой водород, галоген, -N3, -CF3, -CCl3, -CBr3, -CI3, -CN, -CHO, -OR3A, -NR3AR3B, -COOR3A, -C(O)NR3AR3B, -NO2, -SR3A, -S(O)n3R3A, -S(O)n3OR3A, -S(O)n3ONR3AR3B, -NHNR3AR3B, -ONR3AR3B, -NHC(O)NHNR3AR3B, замещенный или незамещенный алкил, замещенный или незамещенный гетероалкил, замещенный или незамещенный циклоалкил, замещенный или незамещенный гетероциклоалкил, замещенный или незамещенный арил или замещенный или незамещенный гетероарил; R4 представляет собой водород, галоген, -N3, -CF3, -CCl3, -CBr3, -CI3, -CN, -CHO, -OR4A, -NR4AR4B, -COOR4A, -C(O)NR4AR4B, -NO2, -SR4A, -S(O)n4R4A, -S(O)n4OR4A, -S(O)n4NR4AR4B, -NHNR4AR4B, -ONR4AR4B, -NHC(O)NHNR4AR4B, замещенный или незамещенный алкил, замещенный или незамещенный гетероалкил, замещенный или замещенный циклоалкил, замещенный или незамещенный гетероциклоалкил, замещенный или незамещенный арил или замещенный или незамещенный гетероарил; R5 представляет собой водород, галоген, -N3, -CF3, -CCl3, -CBr3, -CI3, -CN, -CHO, -OR5A, -NR5AR5B, -COOR5A, -C(O)NR5AR5B, -NO2, -SR5A, -S(O)n5R5A, -S(O)n5OR5A, -S(O)n5NR5AR5B, -NHNR5AR5B, -ONR5AR5B, -NHC(O)NHNR5AR5B, замещенный или незамещенный алкил, замещенный или незамещенный гетероалкил, замещенный или незамещенный циклоалкил, замещенный или незамещенный гетероциклоалкил, замещенный или незамещенный арил или замещенный или незамещенный гетероарил, где R4 и R5 необязательно соединены вместе с образованием замещенного или незамещенного гетероциклоалкила или замещенного или незамещенного гетероарила; R6 представляет собой -CF3, замещенный или незамещенный циклопропил или замещенный или незамещенный циклобутил; R7 независимо представляет собой водород, галоген, -N3, -CF3, -CCl3, -CBr3, -CI3, -CN, -CHO, -OR7A, -NR7AR7B, -COOR7A, -C(O)NR7AR7B, -NO2, -SR7A, -S(O)n7R7A, -S(O)n7OR7A, -S(O)n7NR7AR7B, -NHNR7AR7B, -ONR7AR7B, -NHC(O)NHNR7AR7B, замещенный или незамещенный алкил, замещенный или незамещенный гетероалкил, замещенный или незамещенный циклоалкил, замещенный или незамещенный гетероциклоалкил, замещенный или незамещенный арил или замещенный или незамещенный гетероарил; R1A, R1B, R2A, R2B, R3A, R3B, R4A, R4B, R5A, R5B, R7A и R7B независимо представляют собой водород, замещенный или незамещенный алкил, замещенный или незамещенный гетероалкил, замещенный или незамещенный циклоалкил, замещенный или незамещенный гетероциклоалкил, замещенный или незамещенный арил или замещенный или незамещенный гетероарил; и n1, n2, n3, n4, n5 и n7 независимо равняются 1 или 2.
[0753] В некоторых вариантах осуществления GSI формул (VIII-a), (VIII-b), (VIII-c) или (VIII-d) описан в публикации международной заявки на патент № WO 2014/165263 (например, в вариантах осуществления P1-P12). В некоторых вариантах осуществления GSI формул (VIII-a), (VIII-b), (VIII-c) или (VIII-d) выбран из
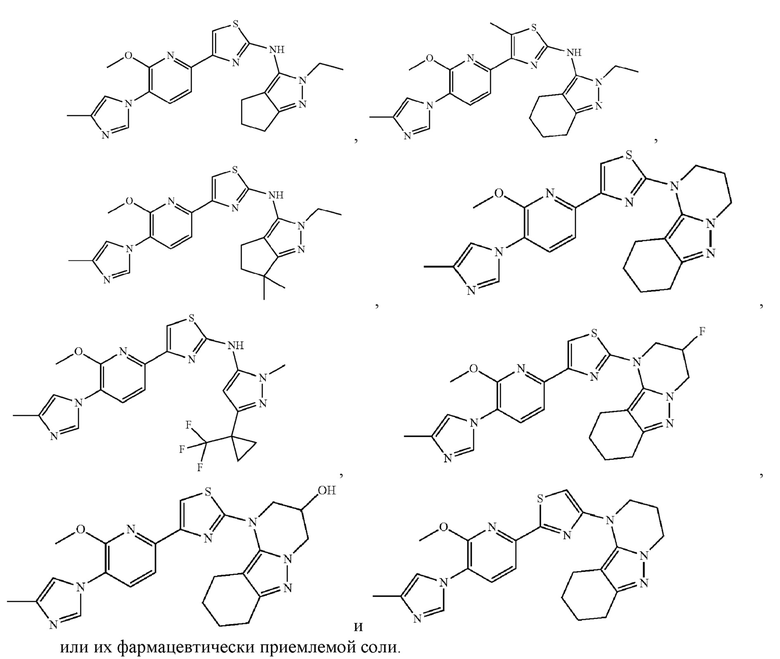
[0754] В некоторых вариантах осуществления GSI представляет собой соединение формулы (IX):
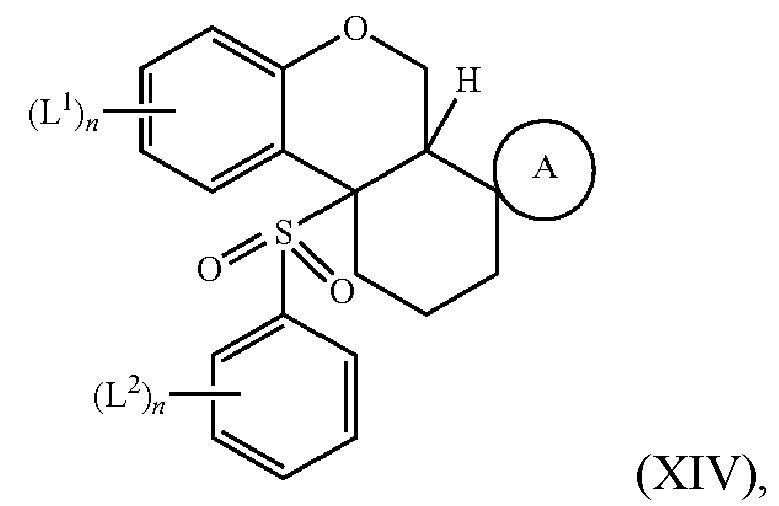
или его фармацевтически приемлемую соль, где A представляет собой 4-7-членное спироциклическое кольцо, содержащее по меньшей мере один гетероатом, выбранный из группы, состоящей из N, O, S, S(O)2, P(O)R1 и N-S(O)2-R1, где спироциклическое кольцо необязательно замещено заместителями в количестве от 1 до 3, выбранными из группы, состоящей из C1-3алкила и =O; R1 представляет собой C1-6алкил, необязательно замещенный галогеном; каждый L1 независимо выбран из группы, состоящей из 1) C1-3алкила, необязательно замещенного галогеном, и 2) галогена; каждый L2 независимо выбран из группы, состоящей из 1) C1-3алкила, необязательно замещенного галогеном, и 2) галогена; и
n равняется 0-3.
[0755] В некоторых вариантах осуществления GSI представляет собой соединение, описанное в публикации заявки на патент США № US-2015-307533 (например, в таблице на страницах 13-16). В некоторых вариантах осуществления GSI выбран из
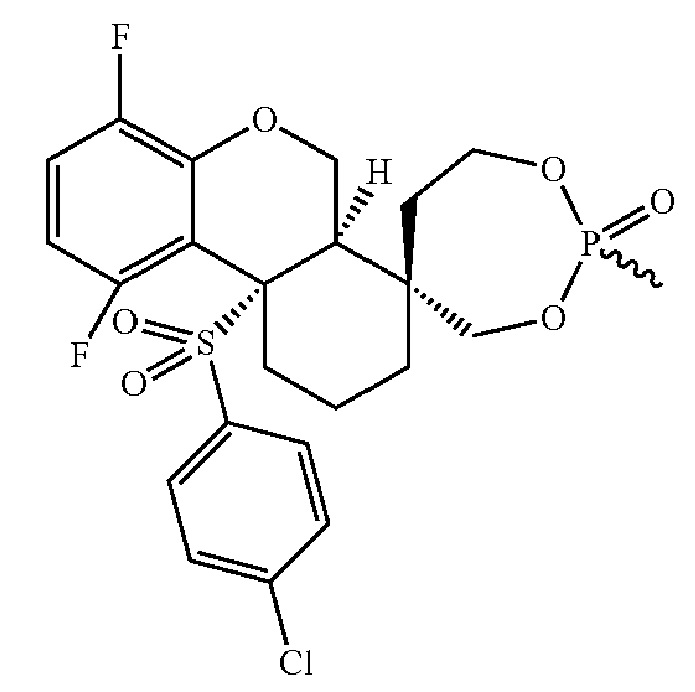 ,
, 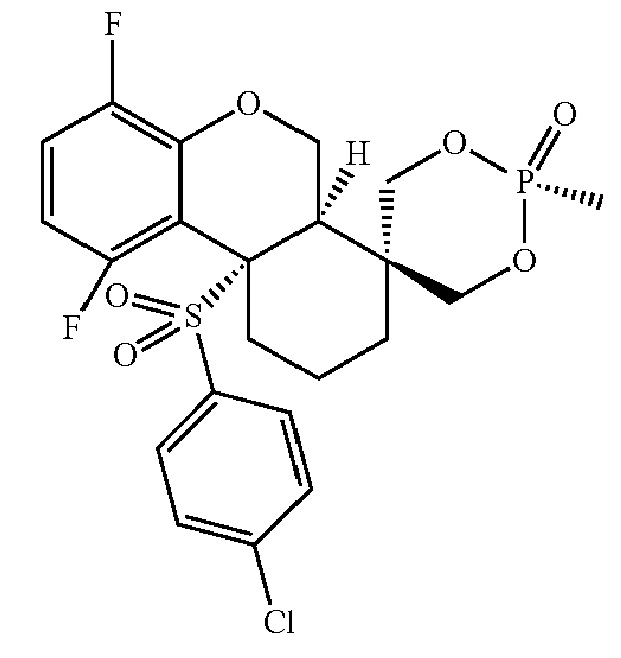 и
и 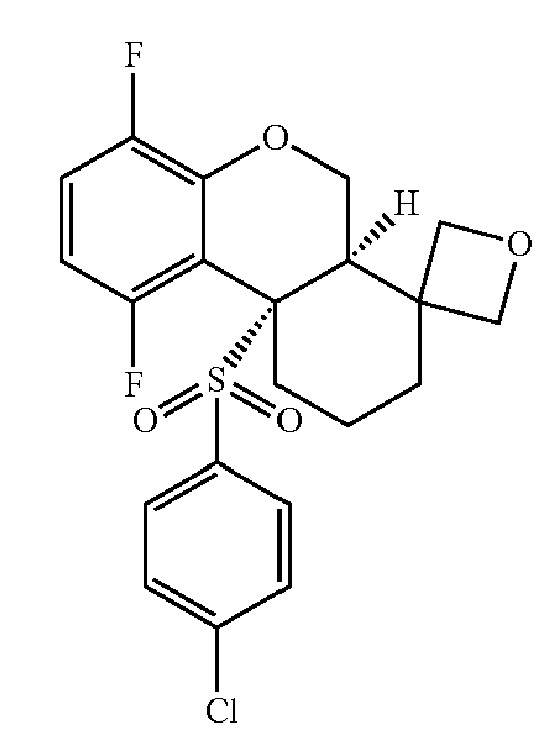 или их фармацевтически приемлемой соли.
или их фармацевтически приемлемой соли.
[0756] В некоторых вариантах осуществления GSI представляет собой соединение формулы (X):
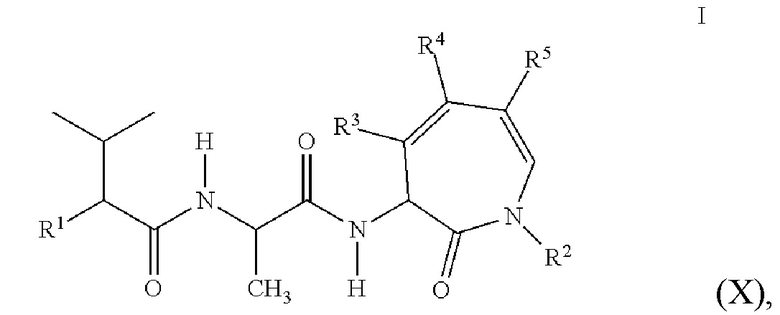
или его фармацевтически приемлемую соль, где R1 представляет собой гидрокси или фтор; R2 представляет собой C1-C4алкил; R3 представляет собой водород или фенил; R4 представляет собой водород, фенил или C1-C4алкил; R5 представляет собой водород или фенил; при условии, что один из R3, R4 и R5 отличается от водорода, а два других представляют собой водород.
[0757] В некоторых вариантах осуществления GSI представляет собой соединение, описанное в патенте США № 8188069. В одном варианте осуществления GSI представляет собой
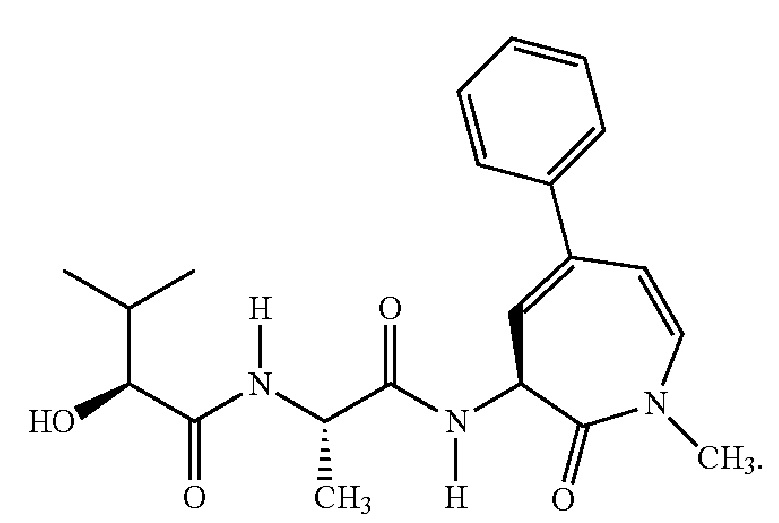 или его фармацевтически приемлемую соль.
или его фармацевтически приемлемую соль.
[0758] В некоторых вариантах осуществления GSI представляет собой соединение формулы (XI):
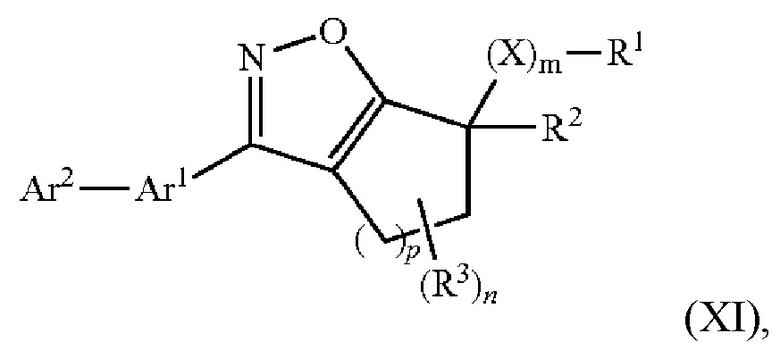
или его фармацевтически приемлемую соль, где: R1 представляет собой 1) водород, 2) (C1-C6)алкил, необязательно замещенный 1-5 атомами галогена или фенилом, где фенил необязательно замещен 1-3 атомами галогена, 3) фенил, необязательно замещенный 1-3 (C1-C6)алкилами или 1-5 атомами галогена, или 4) (C4-C6)циклоалкил, необязательно замещенный 1-3 (C1-C6)алкилами или 1-5 атомами галогена; R2 представляет собой 1) водород, 2) (C1-C6)алкил, необязательно замещенный 1-5 атомами галогена или фенилом, где фенил необязательно замещен 1-3 атомами галогена, или 3) фенил, необязательно замещенный 1-3 атомами галогена; R3 представляет собой (C1-C6)алкил, -OH или галоген;
X представляет собой -NR4-, -O-, -S- или -SO2-; R4 представляет собой водород или (C1-C3)алкил;
p равняется 1-3; m равняется 0 или 1; n равняется 0-3; и Ar2-Ar1 выбран из группы, состоящей из
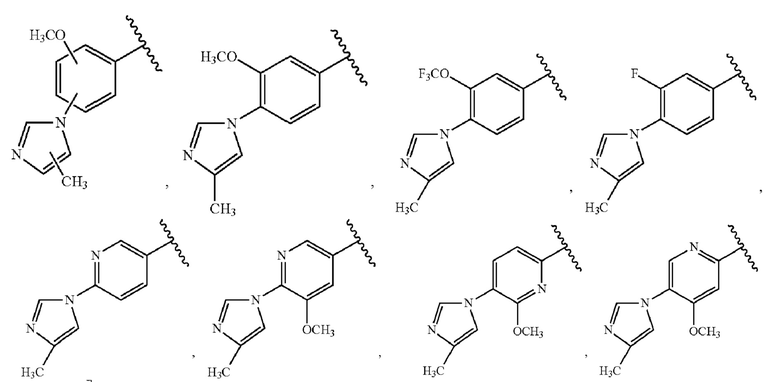
и 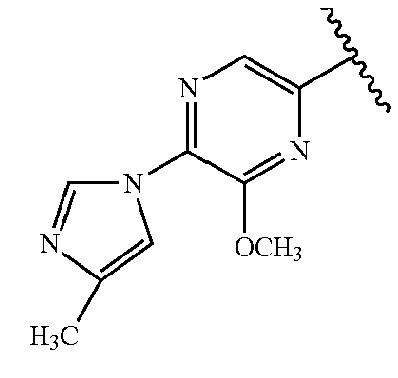 или их фармацевтически приемлемой соли.
или их фармацевтически приемлемой соли.
[0759] В некоторых вариантах осуществления GSI представляет собой соединение, описанное в патенте США № 9096582 (например, в таблице на страницах 13-17). В некоторых вариантах осуществления GSI представляет собой
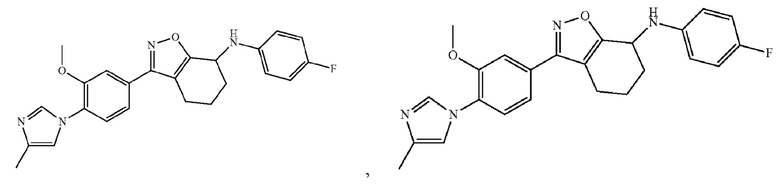
или их фармацевтически приемлемую соль.
[0760] В некоторых вариантах осуществления GSI представляет собой соединение формулы (XII):
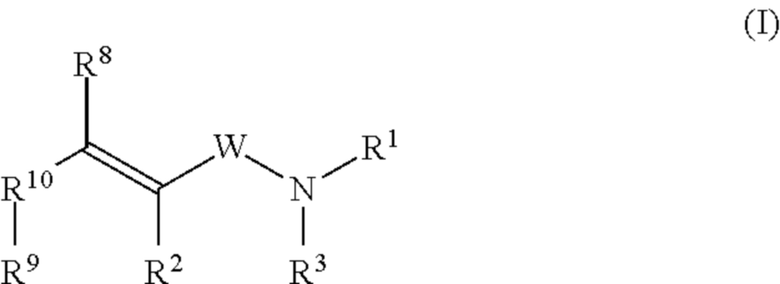 (XII),
(XII),
или его фармацевтически приемлемую соль или его фармацевтически приемлемые соли, где: R1, R2, R3, R8, R9, R10 и W выбраны независимо; W выбран из группы, состоящей из -S(O)- и -S(O)2-; R1 выбран из группы, состоящей из Н, алкила, алкенила, алкинила, арила, арилалкила, алкиларила, циклоалкила, циклоалкенила, циклоалкилалкила, конденсированного бензоциклоалкила (т. е. бензоконденсированного циклоалкила), конденсированного бензогетероциклоалкила (т. е. бензоконденсированного гетероциклоалкила), конденсированного гетероарилциклоалкила (т. е. гетероарилконденсированного циклоалкила), конденсированного гетероарилгетероциклоалкила (т. е. гетероарилконденсированного гетероциклоалкила), гетероарила, гетероарилалкила, гетероциклила, гетероцикленила и гетероциклилалкила; где каждая из алкильной, алкенильной и алкинильной, арильной, арилалкильной, алкиларильной, циклоалкильной, циклоалкенильной, циклоалкилалкильной, конденсированной бензоциклоалкильной, конденсированной бензогетероциклоалкильной, конденсированной гетероарилциклоалкильной, конденсированной гетероарилгетероциклоалкильной, гетероарильной, гетероарилалкильной, гетероциклильной, гетероцикленильной и гетероциклилалкильной групп R1 необязательно замещена 1-5 независимо выбранными группами R21; каждый из R2 и R3 независимо выбран из группы, состоящей из H, алкила, алкенила, алкинила, арила, арилалкила, алкиларила, циклоалкила, циклоалкенила, циклоалкилалкила, гетероарила, гетероарилалкила, гетероциклила, гетероцикленила и гетероциклилалкила; где каждая из алкильной, алкенильной и алкинильной, арильной, арилалкильной, алкиларильной, циклоалкильной, циклоалкенильной, циклоалкилалкильной, циклоалкенильной, гетероарильной, гетероарилалкильной, гетероциклильной, гетероцикленильной и гетероциклилалкильной групп R1 необязательно замещена 1-5 независимо выбранными группами R21; или R2 и R3, взятые вместе наряду с атомами, с которыми они связаны, образуют кольцо, выбранное из группы, состоящей из (а) 5-6-членного гетероциклоалкильного кольца, при этом гетероциклоалкильное кольцо необязательно содержит, в дополнение к W и в дополнение к N, смежному с W, по меньшей мере один другой гетероатом, независимо выбранный из группы, состоящей из -O-, -S(O)-, -S(O)2 и -C(O)-, и (b) 5-6-членного гетероциклоалкенильного кольца, при этом гетероциклоалкенильное кольцо необязательно содержит, в дополнение к W и в дополнение к N, смежному с W, по меньшей мере один другой гетероатом, независимо выбранный из группы, состоящей из -O-, -S(O)-, -S(O)2 и -C(O)-; где кольцо необязательно замещено 1-5 независимо выбранными группами R21; или R2 и R3, взятые вместе наряду с атомами, с которыми они связаны, и R1 и R3, взятые вместе наряду с атомами, с которыми они связаны, образуют конденсированный кольцевой фрагмент:
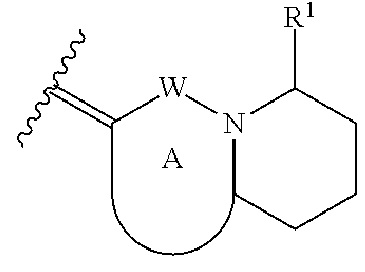 , где кольцо A представляет собой кольцо, выбранное из группы, состоящей из:
, где кольцо A представляет собой кольцо, выбранное из группы, состоящей из:
(а) 5-6-членного гетероциклоалкильного кольца, при этом гетероциклоалкильное кольцо необязательно содержит, в дополнение к W и в дополнение к N, смежному с W, по меньшей мере один другой гетероатом, независимо выбранный из группы, состоящей из -O-, -NR14-, -S(O)-, -S(O)2 и -C(O)-, и (b) 5-6-членного гетероциклоалкенильного кольца, при этом гетероциклоалкенильное кольцо необязательно содержит, в дополнение к W и в дополнение к N, смежному с W, по меньшей мере один другой гетероатом, независимо выбранный из группы, состоящей из -O-, -NR14-, -S(O)-, -S(O)2 и -C(O)-, и где конденсированный кольцевой фрагмент необязательно замещен 1-5 независимо выбранными группами R21; или R1 и R3, взятые вместе с атомами, с которыми они связаны, образуют конденсированное бензогетероциклоалкильное кольцо, и где конденсированное кольцо необязательно замещено 1-5 независимо выбранными группами R21, R8 выбран из группы, состоящей из H, алкила, алкенила, алкинила, арила, арилалкила, алкиларила, циклоалкила, циклоалкенила, циклоалкилалкила, гетероарила, гетероарилалкила, гетероциклила, гетероцикленила и гетероциклилалкила; где каждый из алкила, алкенила и алкинила, арила, арилалкила, алкиларила, циклоалкила, циклоалкенила, циклоалкилалкила, гетероарила, гетероарилалкила, гетероциклила, гетероцикленила и гетероциклилалкила R8замещен 1-3 независимо выбранными группами R21; R9 выбран из группы, состоящей из алкила, алкенила, алкинила, арила, арилалкила, алкиларила, циклоалкила, циклоалкенила, циклоалкилалкила, гетероарила, гетероарилалкила, гетероциклила, гетероцикленила и гетероциклилалкила, где каждый из алкила, алкенила и алкинила, арила, арилалкила, алкиларила, циклоалкила, циклоалкенила, циклоалкилалкила, гетероарила, гетероарилалкила, гетероциклила, гетероцикленила, гетероциклилалкила и гетероциклилалкила R9 необязательно замещен 1-3 независимо выбранными группами R21;
R10 выбран из группы, состоящей из связи, алкила, алкенила, алкинила, арила, арилалкила, алкиларила, циклоалкила, циклоалкенила, циклоалкилалкила, гетероарила, гетероарилалкила, гетероциклила, гетероцикленила, гетероциклилалкила, гетероциклилалкенила,
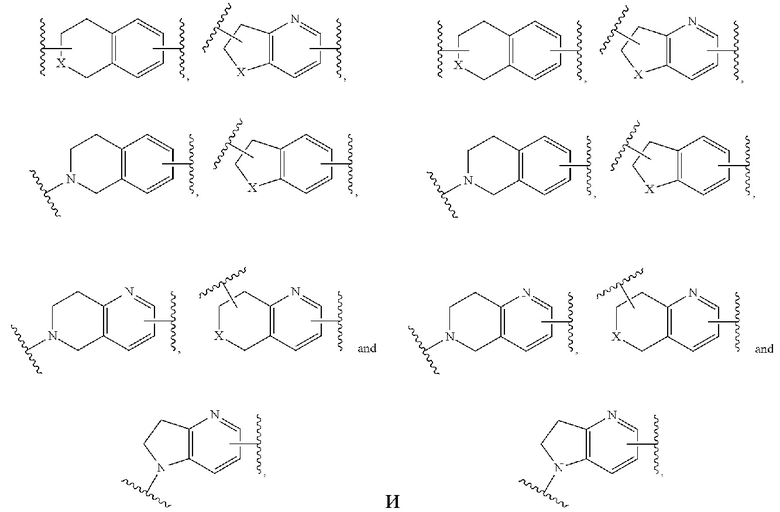
где X выбран из группы, состоящей из O, -N(R14)- или -S-; и
где каждый из фрагментов R10 необязательно замещен 1-3 независимо выбранными группами R21; R14 выбран из группы, состоящей из H, алкила, алкенила, алкинила, циклоалкила, циклоалкилалкила, циклоалкенила, гетероциклила, гетероцикленила, гетероциклилалкила, гетероциклилалкенила, арила, арилалкила, гетероарила, гетероарилалкила, -ON, -C(O)R15, -C(O)OR15, -C(O)N(R15)(R16), -S(O)N(R15)(R16), -S(O)2N(R15)(R16), -C(═NOR15)R16 и -P(O)(OR15)(OR16); R15, R16 и R17 независимо выбраны из группы, состоящей из H, алкила, алкенила, алкинила, циклоалкила, циклоалкилалкила, гетероциклила, гетероциклилалкила, арила, арилалкила, гетероарила, гетероарилалкила, арилциклоалкила, арилгетероциклила, (R18)n-алкила, (R18)n-циклоалкила, (R18)n-циклоалкилалкила, (R18)n-гетероциклила, (R18)n-гетероциклилалкила, (R18)n-арила, (R18)n-арилалкила, (R18)n-гетероарила и (R18)n-гетероарилалкила; каждый R18 независимо выбран из группы, состоящей из алкила, алкенила, алкинила, арила, арилалкила, арилалкенила, арилалкинила, -NO2, галогена, гетероарила, HO-алкилоксиалкила, -CF3, -CN, алкил-CN, -C(O)R19, -C(O)OH, -C(O)OR19, -C(O)NHR20, -C(O)NH2, -C(O)NH2-C(O)N(алкил)2, -C(O)N(алкил)(арил), -C(O)N(алкил)(гетероарил), -SR19, -S(O)2R20, -S(O)NH2, -S(O)NH(алкил), -S(O)N(алкил)(алкил), -S(O)NH(арил), -S(O)2NH2, -S(O)2NHR19, -S(O)2NH(гетероциклил), -S(O)2N(алкил)2, -S(O)2N(алкил)(арил), -OCF3, -OH, -OR20, -O-гетероциклила, -O-циклоалкилалкила, -O-гетероциклилалкила, -NH2, -NHR20, -N(алкил)2, -N(арилалкил)2, -N(арилалкил)-(гетероарилалкил), -NHC(O)R20, -NHC(O)NH2, -NHC(O)NH(алкил), -NHC(O)N(алкил)(алкил), -N(алкил)C(O)NH(алкил), -N(алкил)C(O)N(алкил)(алкил), -NHS(O)2R20, -NHS(O)2NH(алкил), -NHS(O)2N(алкил)(алкил), -N(алкил)S(O)2NH(алкил) и -N(алкил)S(O)2N(алкил)(алкил); или два фрагмента R18 при смежных атомах углерода могут быть связаны друг с другом с образованием 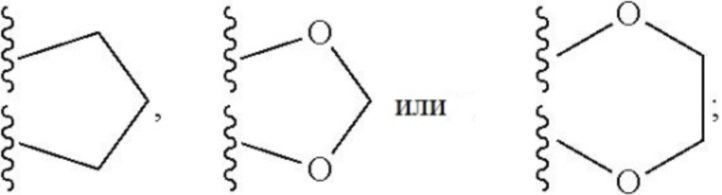 ; R19 выбран из группы, состоящей из алкила, циклоалкила, арила, арилалкила и гетероарилалкила; R20 выбран из группы, состоящей из алкила, циклоалкила, арила, галогензамещенного арила, арилалкила, гетероарила и гетероарилалкила; каждый R21 независимо выбран из группы, состоящей из алкила, алкенила, алкинила, циклоалкила, циклоалкилалкила, циклоалкенила, гетероциклоалкила, гетероциклоалкилалкила, арила, арилалкила, гетероарила, гетероарилалкила, галогена, -ON, -OR15, -C(O)R15, -C(O)OR15, -C(O)N(R15)(R16), -SR15, -S(O)N(R16)(R16), -CH(R15)(R16), -S(O)2N(R16)(R16), -C(═NOR16)R16, -P(O)(OR15)(OR16), -N(R15)(R16), -алкил-N(R15)(R16), -N(R15)C(O)R16, -CH2-N(R15)C(O)R16, -CH2-N(R15)C(O)N(R16)(R17), -OH2-R15; -CH2N(R15)(R16), -N(R15)S(O)R16, -N(R15)S(O)2R16, -CH2-N(R15)S(O)2R16, -N(R15)S(O)2N(R16)(R17), -N(R15)S(O)N(R16)(R17), -N(R15)C(O)N(R16)(R17), -CH2-N(R15)C(O)N(R16)(R17), -N(R15)C(O)OR16, -CH2-N(R15)C(O)OR16, -S(O)R15, ═NOR15, -N3, -NO2 и -S(O)2R15; где каждая из алкильной, алкенильной, алкинильной, циклоалкильной, циклоалкилалкильной, циклоалкенильной, гетероциклоалкильной, гетероциклоалкилалкильной, арильной, арилалкильной, гетероарильной и гетероарилалкильной групп R21 необязательно замещена 1-5 независимо выбранными группами R22; и каждая группа R22 независимо выбрана из группы, состоящей из алкила, циклоалкила, циклоалкенила, гетероциклоалкила, арила, гетероарила, галогена, -CF3, -CN, -OR15, -C(O)R15, -C(O)OR15, -алкил-C(O)OR15, C(O)N(R15)(R16), -SR15, -S(O)N(R15)(R16), -S(O)2N(R15)(R16), -C(═NOR15)R16, -P(O)(OR15)(OR16), -N(R15)(R16), -алкил-N(R15)(R16), -N(R15)C(O)R16, -CH2-N(R15)C(O)R16, -N(R15)S(O)R16, -N(R15)S(O)2R16, -CH2-N(R15)S(O)2R16, -N(R15)S(O)2N(R16)(R17), -N(R15)S(O)N(R16)(R17), -N(R15)C(O)N(R16)(R17), -CH2-N(R15)C(O)N(R16)(R17); -N(R15)C(O)OR16, -CH2-N(R15)C(O)OR16, -N3, ═NOR15, -NO2, -S(O)R15 и -S(O)2R15.
; R19 выбран из группы, состоящей из алкила, циклоалкила, арила, арилалкила и гетероарилалкила; R20 выбран из группы, состоящей из алкила, циклоалкила, арила, галогензамещенного арила, арилалкила, гетероарила и гетероарилалкила; каждый R21 независимо выбран из группы, состоящей из алкила, алкенила, алкинила, циклоалкила, циклоалкилалкила, циклоалкенила, гетероциклоалкила, гетероциклоалкилалкила, арила, арилалкила, гетероарила, гетероарилалкила, галогена, -ON, -OR15, -C(O)R15, -C(O)OR15, -C(O)N(R15)(R16), -SR15, -S(O)N(R16)(R16), -CH(R15)(R16), -S(O)2N(R16)(R16), -C(═NOR16)R16, -P(O)(OR15)(OR16), -N(R15)(R16), -алкил-N(R15)(R16), -N(R15)C(O)R16, -CH2-N(R15)C(O)R16, -CH2-N(R15)C(O)N(R16)(R17), -OH2-R15; -CH2N(R15)(R16), -N(R15)S(O)R16, -N(R15)S(O)2R16, -CH2-N(R15)S(O)2R16, -N(R15)S(O)2N(R16)(R17), -N(R15)S(O)N(R16)(R17), -N(R15)C(O)N(R16)(R17), -CH2-N(R15)C(O)N(R16)(R17), -N(R15)C(O)OR16, -CH2-N(R15)C(O)OR16, -S(O)R15, ═NOR15, -N3, -NO2 и -S(O)2R15; где каждая из алкильной, алкенильной, алкинильной, циклоалкильной, циклоалкилалкильной, циклоалкенильной, гетероциклоалкильной, гетероциклоалкилалкильной, арильной, арилалкильной, гетероарильной и гетероарилалкильной групп R21 необязательно замещена 1-5 независимо выбранными группами R22; и каждая группа R22 независимо выбрана из группы, состоящей из алкила, циклоалкила, циклоалкенила, гетероциклоалкила, арила, гетероарила, галогена, -CF3, -CN, -OR15, -C(O)R15, -C(O)OR15, -алкил-C(O)OR15, C(O)N(R15)(R16), -SR15, -S(O)N(R15)(R16), -S(O)2N(R15)(R16), -C(═NOR15)R16, -P(O)(OR15)(OR16), -N(R15)(R16), -алкил-N(R15)(R16), -N(R15)C(O)R16, -CH2-N(R15)C(O)R16, -N(R15)S(O)R16, -N(R15)S(O)2R16, -CH2-N(R15)S(O)2R16, -N(R15)S(O)2N(R16)(R17), -N(R15)S(O)N(R16)(R17), -N(R15)C(O)N(R16)(R17), -CH2-N(R15)C(O)N(R16)(R17); -N(R15)C(O)OR16, -CH2-N(R15)C(O)OR16, -N3, ═NOR15, -NO2, -S(O)R15 и -S(O)2R15.
[0761] В некоторых вариантах осуществления GSI представляет собой соединение, описанное в публикации заявки на патент США № US-2011-0257163 (например, в абзацах с [0506] по [0553]). В некоторых вариантах осуществления соединение формулы (XII) представляет собой фармацевтически приемлемый сложный эфир. В некоторых вариантах осуществления соединение формулы (XII) выбрано из
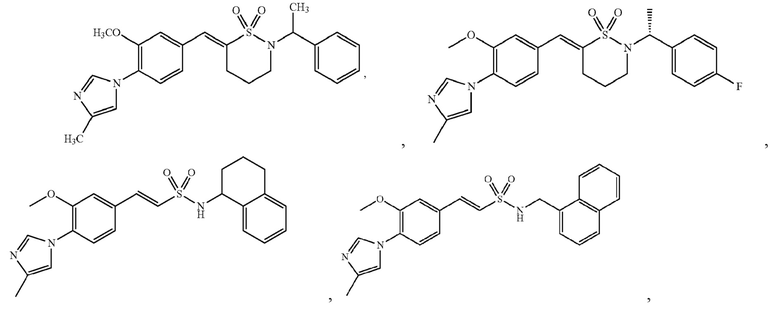
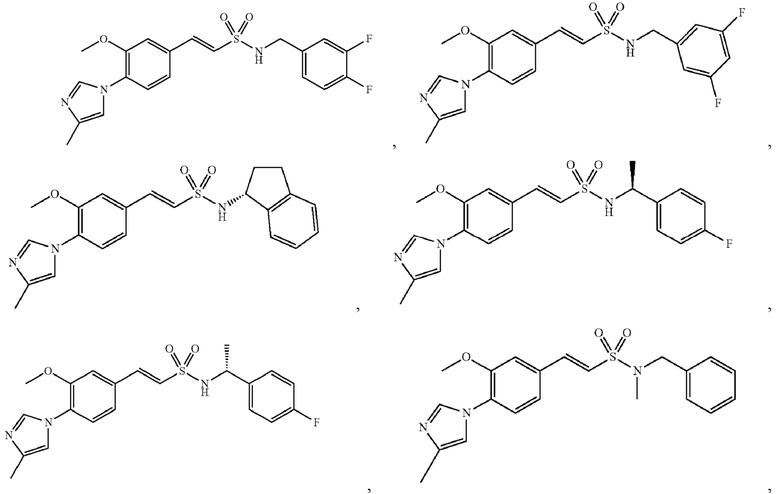
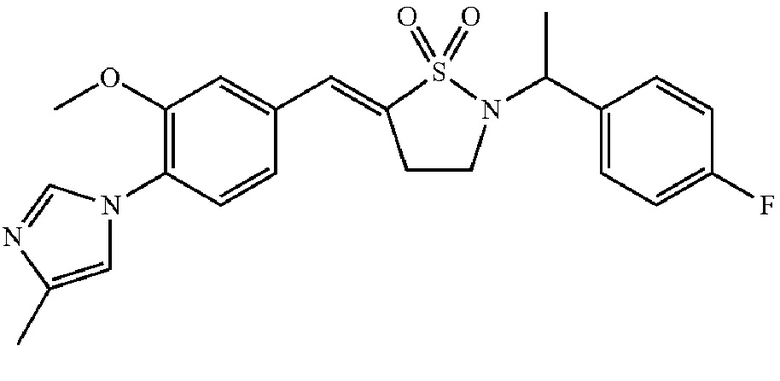 и их фармацевтически приемлемых солей.
и их фармацевтически приемлемых солей.
[0762] В некоторых вариантах осуществления GSI представляет собой соединение формулы (XIII):
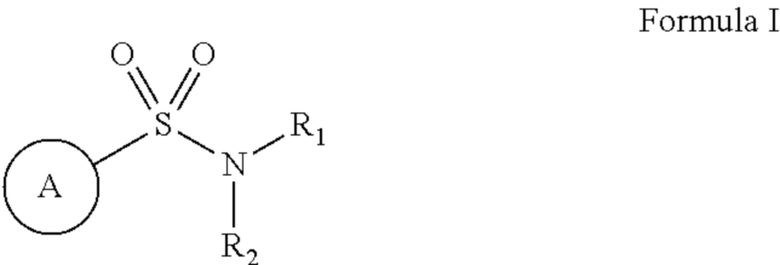 (XIII),
(XIII),
или его фармацевтически приемлемую соль, где кольцо A представляет собой арил, циклоалкил, гетероарил или гетероциклоалкил, где каждое кольцо необязательно замещено в замещаемом положении галогеном, C1-C6алкилом, C2-C6алкенилом, C2-C6алкинилом, C1-C6алкокси, галогеналкилом, галогеналкокси, гидроксилом, гидроксиалкилом, CN, фенокси, -S(O)0-2-(C1-C6алкил), -NR10R11, C1-C6алканоилом, C0-C3алкил-CO2R', гетероарилом, гетероциклоалкилом, арилом, аралкилом или -SO2NR10R11; R1 и R2 совместно образуют кольцевую систему [3.3.1] или [3.2.1], где 0 или 1 атом углерода в кольцевой системе необязательно заменен на группу -O-, -S(O)x- или -NR15-; и где кольцевая система [3.3.1] или [3.2.1] необязательно замещена 1, 2, 3 или 4 группами, которые независимо представляют собой оксо, галоген, C1-C6алкил, -O(C1-C2алкил)O-, -S(C1-C2алкил)S-, C2-C6алкенил, C1-C6галогеналкил, C2-C6алкинил, гидрокси, гидроксиалкил, C1-C6алкокси, галогеналкокси, -C(O)OR13, -(C1-C4алкил)-C(O)OR16, -CONR10R11, -OC(O)NR10R11, -NR'C(O)OR'', -NR'S(O)2R'', -OS(O)2R', -NR'COR'', CN, ═N-NR12 или ═N-O-R13; где х равняется 0, 1 или 2; R10 и R11 в каждом случае независимо представляют собой водород или C1-C6алкил, где алкил необязательно замещен арилом, где арил необязательно замещен 1-5 группами, которые независимо представляют собой галоген, гидроксил, алкил, алкокси, галогеналкил, галогеналкокси, CN или NO2; или
R10 и R11 вместе могут образовывать 3-8-членное кольцо, необязательно содержащее дополнительный гетероатом, такой как N, O или S; R12 представляет собой водород, C1-C6алкил или -SO2-арил, где арил необязательно замещен 1-5 группами, которые независимо представляют собой галоген, гидроксил, алкил, алкокси, галогеналкил, галогеналкокси, CN или NO2; R13 представляет собой водород или C1-C6алкил, необязательно замещенный арилом, гидроксилом или галогеном, где арил необязательно замещен 1-5 группами, которые независимо представляют собой галоген, гидроксил, алкил, алкокси, галогеналкил, галогеналкокси, CN или NO2;
R15 представляет собой водород, арил, гетероарил, -SO2R', -C(O)R', -C(O)OR' или C1-C6алкил, необязательно замещенный арилом, гидроксилом или галогеном, где арильные группы необязательно замещены 1-5 группами, которые независимо представляют собой галоген, гидроксил, алкил, алкокси, галогеналкил, галогеналкокси, CN или NO2; и R' и R'' независимо представляют собой водород, C1-C6алкил, галогеналкил, C2-C6алкенил или фенил, необязательно замещенный 1-5 группами, которые независимо представляют собой галоген, C1-C6алкил, -C(O)OR', C1-C6алкокси, галогеналкил, галогеналкокси, гидроксил, CN, фенокси, -SO2-(C1-C6алкил), -NR10R11, C1-C6алканоил, пиридил, фенил, NO2 или -SO2NR10R11.
[0763] В некоторых вариантах осуществления GSI представляет собой соединение, описанное в публикации заявки на патент США № US-2011-178199 (например, в абзацах с [0798] по [0799] и таблицах 1-4). В некоторых вариантах осуществления соединение формулы (XIII) включает в себя N-мостиковый бициклический сульфонамид или его фармацевтически приемлемую соль. В некоторых вариантах осуществления GSI выбран из
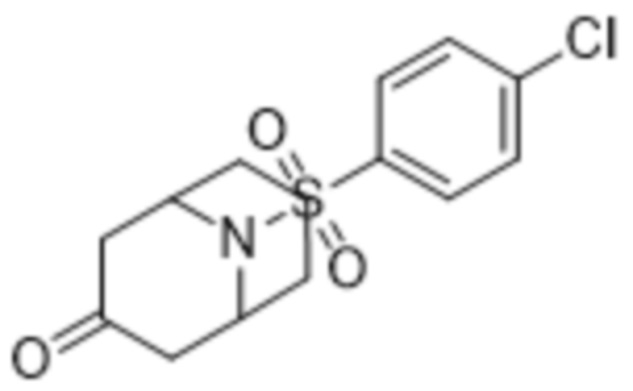 ,
, 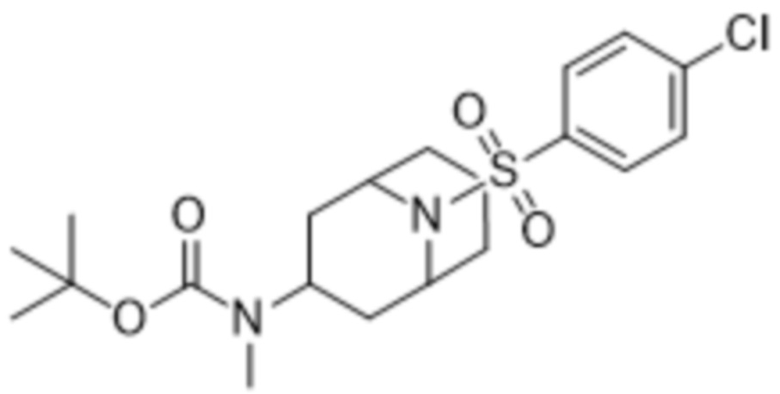 ,
, 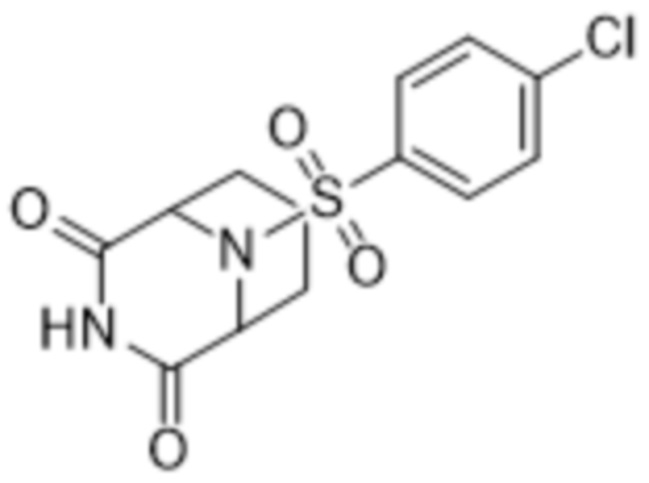 ,
, 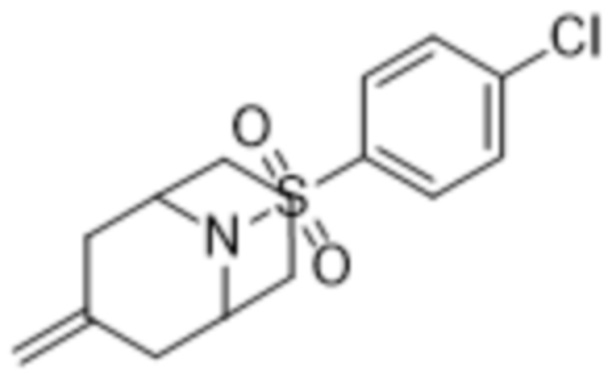 и их фармацевтически приемлемых солей.
и их фармацевтически приемлемых солей.
[0764] В некоторых вариантах осуществления GSI представляет собой соединение формулы (XIV):
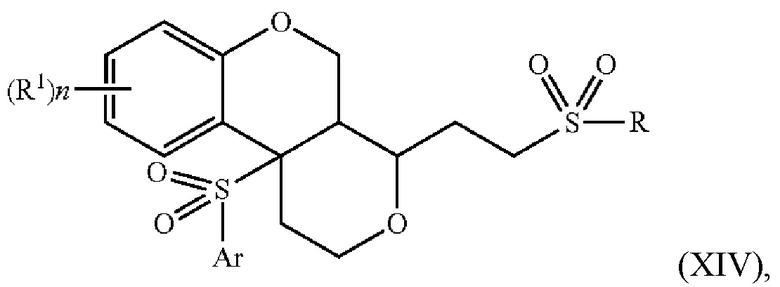
или его фармацевтически приемлемую соль, где R выбран из группы, состоящей из (1) -пиридинила, (2) -пиразолинила, (3) -1,2,4-оксадиазолила, (4) -(C1-C2)алкилпиридинила, (5) -(C1-C2)алкилпиразолинила и (6) -(C1-C2)алкил-1,2,4-оксадиазолила, где пиридинил, пиразолинил и -1,2,4-оксадиазолил являются незамещенными или замещены одной группой L1; R1 независимо выбран из группы, состоящей из галогена, (C1-C6)алкила, -CN, -CF3, -O-(C1-C6)алкила, -O-(галоген(C1-C6)алкил), -C(O)-O-(C1-C6)-OH-замещенного (C1-C4)алкила, галоген(C1-C6)алкила, -(C1-C4)алкокси-OH, -(C1-C4)алкокси(C1-C4)алкокси и -S(O)2(C1-C6)алкила; n равняется 0, 1, 2 или 3; Ar выбран из группы, состоящей из фенила, необязательно замещенного 1 или 2 группами L2, и пиридила, необязательно замещенного 1 или 2 группами L2;
L1 независимо выбран из группы, состоящей из -OCH3, -NH2, ═O и (С1-С5)алкила; и L2 независимо выбран из группы, состоящей из галогена, (С1-С6)алкила, -CN, -CF3, -O-(C1-C6)алкила, -O-(галоген(C1-C6)алкила), -C(O)-O-(C1-C6)алкила, -OH-замещенного (C1-C6)алкила, галоген(C1-C6)алкила, -OH-замещенного (C1-C4)алкокси, -(C1-C4)алкокси(C1-C4)алкокси и -S(O)2(C1-C6)алкила.
[0765] В некоторых вариантах осуществления GSI представляет собой соединение, описанное в патенте США № 9226927 (например, соединение 4, 8a, 8b, 11, 14, 25a, 25b, 25c, 25d, 25e, 25f, 25g, 25h, 27a или 27b). В некоторых вариантах осуществления соединение формулы (XIV) включает в себя N-мостиковый бициклический сульфонамид или его фармацевтически приемлемую соль. В некоторых вариантах осуществления GSI выбран из
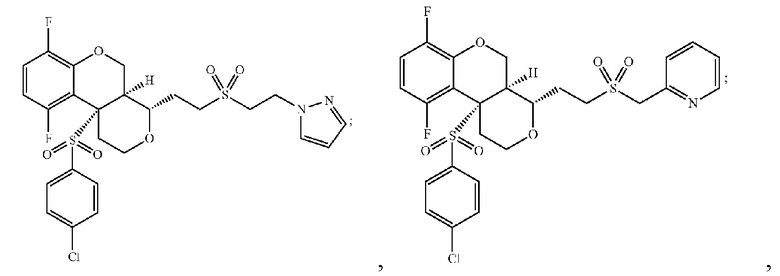
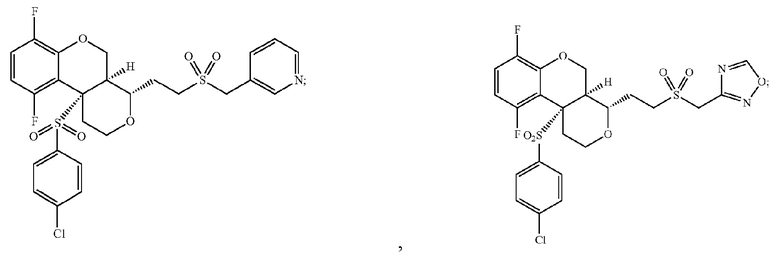 ,
, 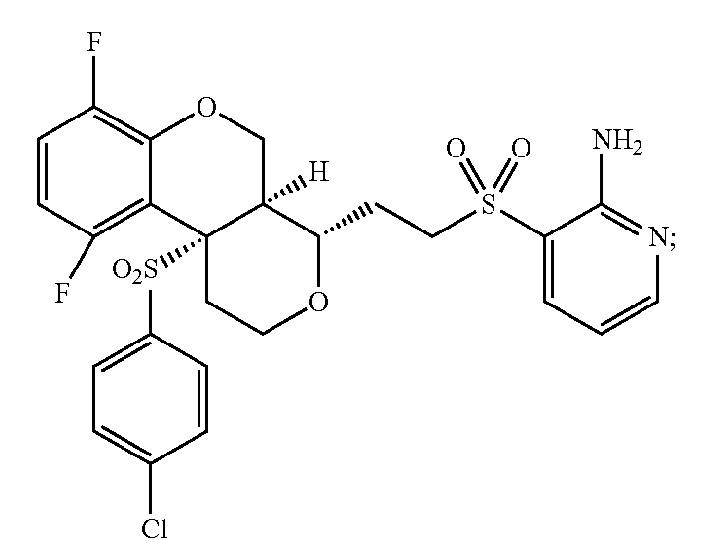 ,
, 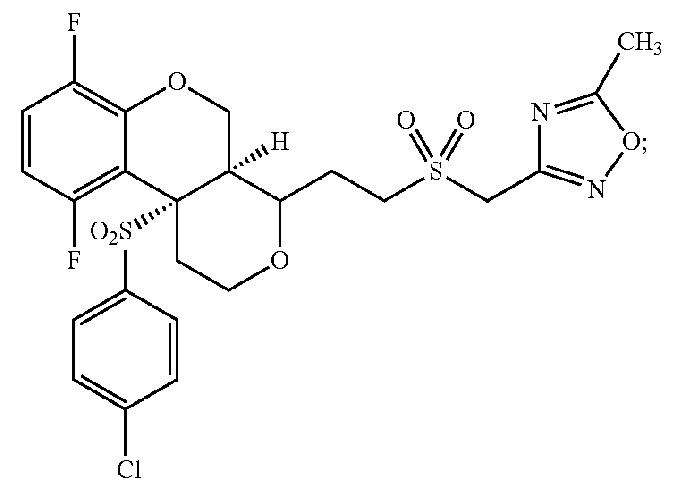 ,
, 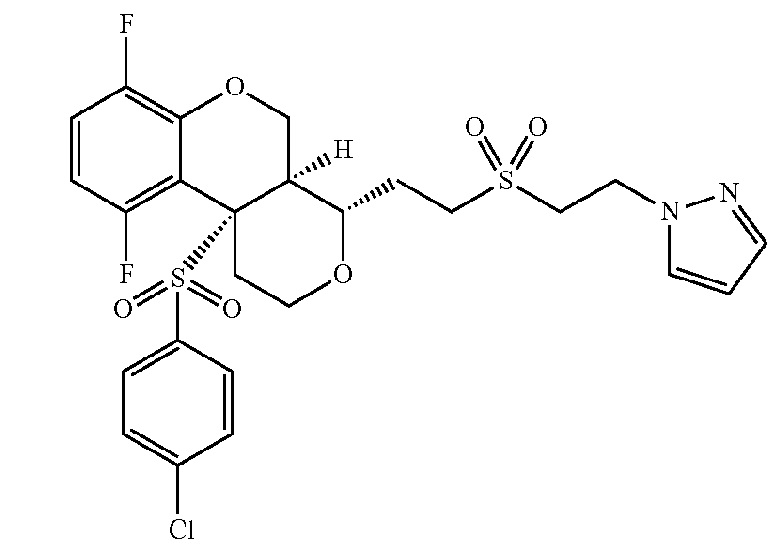 ,
, 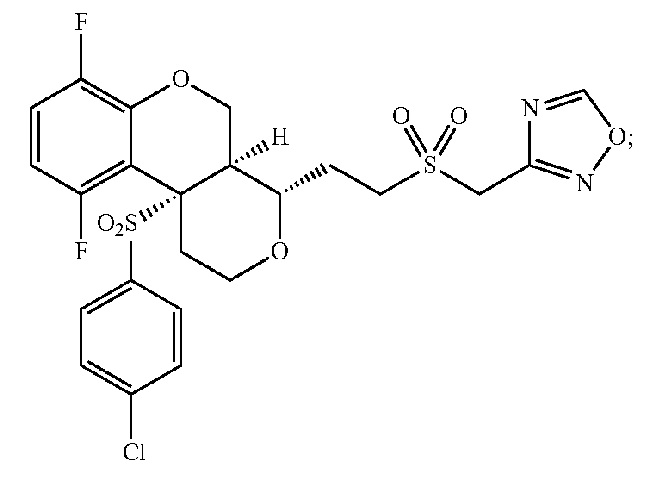
и их фармацевтически приемлемых солей.
[0766] В некоторых вариантах осуществления GSI представляет собой молекулу антитела, которая снижает экспрессию и/или функцию гамма-секретазы. В некоторых вариантах осуществления GSI представляет собой молекулу антитела, нацеливающуюся на субъединицу гамма-секретазы. В некоторых вариантах осуществления GSI выбран из молекулы антитела к пресенилину, молекулы антитела к никастрину, молекулы антитела к APH-1 или молекулы антитела к PEN-2.
[0767] Иллюстративные молекулы антител, которые нацеливаются на субъединицу гамма-секретазы (например, пресенилин, никастрин, APH-1 или PEN-2), описаны в US 8394376, US 8637274 и US 5942400.
[0768] В одном аспекте в настоящем изобретении предусмотрен способ лечения субъектов, у которых имеется состояние или нарушение, затрагивающее В-клетки, включающий введение субъекту эффективного количества (i) MBM и (ii) модулятора гамма-секретазы (например, GSI). Иллюстративные состояния или нарушения, затрагивающие В-клетки, которые можно лечить с помощью комбинации MBM-связывающей молекулы и модулятора гамма-секретазы, включают множественную миелому, макроглобулинемию Вальденстрема, хроническую лимфоцитарную лейкемию, В-клеточную неходжкинскую лимфому, плазмоцитому, лимфому Ходжкина, формы фолликулярной лимфомы, формы мелкоклеточной лимфомы с нерасщепленными ядрами, эндемическую лимфому Беркитта, спорадическую лимфому Беркитта, лимфому из клеток маргинальной зоны, внеузловую лимфому из лимфоидной ткани слизистых оболочек, узловую моноцитоидную B-клеточную лимфому, лимфому селезенки, мантийноклеточную лимфому, крупноклеточную лимфому, диффузную смешанноклеточную лимфому, иммунобластную лимфому, первичную медиастинальную B-клеточную лимфому, легочную B-клеточную лимфангиому, мелкоклеточную лимфоцитарную лимфому, явления пролиферации B-клеток с неопределенным потенциалом злокачественности, лимфогранулематоз, посттрансплантационное лимфопролиферативное нарушение, иммунорегуляторное нарушение, ревматоидный артрит, тяжелую миастению, идиопатическую тромбоцитопеническую пурпуру, антифосфолипидный синдром, болезнь Шагаса, болезнь Грейвса, гранулематоз Вегенера, узелковый полиартериит, синдром Шегрена, обыкновенную пузырчатку, склеродермию, рассеянный склероз, антифосфолипидный синдром, ANCA-ассоциированный васкулит, болезнь Гудпасчера, болезнь Кавасаки, аутоиммунную гемолитическую анемию, быстропрогрессирующий гломерулонефрит, болезнь тяжелых цепей, первичный амилоидоз или амилоидоз, ассоциированный с иммуноцитами, и моноклональную гаммапатию неустановленной этиологии.
[0769] В некоторых вариантах осуществления модулятор гамма-секретазы представляет собой модулятор гамма-секретазы, описанный в WO 2017/019496. В некоторых вариантах осуществления модулятор гамма-секретазы представляет собой ингибитор I γ-секретазы (GSI I) Z-Leu-Leu-норлейцин; ингибитор II γ-секретазы (GSI II); ингибитор III γ-секретазы (GSI III) N-бензилоксикарбонил-Leu-лейциналь, N-(2-нафтоил)-Val-фенилаланиналь; ингибитор IV γ-секретазы (GSI IV); ингибитор V γ-секретазы (GSI V) N-бензилоксикарбонил-Leu-фенилаланиналь; ингибитор VI γ-секретазы (GSI VI) 1-((S)-эндо-N-(1,3,3)-триметилбицикло[2.2.1]гепт-2-ил)-4-фторфенилсульфонамид; ингибитор VII γ-секретазы (GSI VII) ментилоксикарбонил-LL-CHO; ингибитор IX γ-секретазы (GSI IX) (DAPT) трет-бутиловый сложный эфир N-[N-(3,5-дифторфенацетил-L-аланил)]-S-фенилглицина; ингибитор X γ-секретазы (GSI X) трет-бутиловый сложный эфир {1S-бензил-4R-[1-(1S-карбамоил-2-фенэтилкарбамоил)-1S-3-метилбутилкарбамоил]-2R-гидрокси-5-фенилпентил}карбаминовой кислоты; ингибитор XI γ-секретазы (GSI XI) 7-амино-4-хлор-3-метоксиизокумарин; ингибитор XII γ-секретазы (GSI XII) Z-Ile-Leu-CHO; ингибитор XIII γ-секретазы (GSI XIII) Z-Tyr-Ile-Leu-CHO; ингибитор XIV γ-секретазы (GSI XIV) Z-Cys(t-Bu)-Ile-Leu-CHO; ингибитор XVI γ-секретазы (GSI XVI) метиловый сложный эфир N-[N-3,5-дифторфенацетил]-L-аланил-S-фенилглицина; ингибитор XVII γ-секретазы (GSI XVII); ингибитор XIX γ-секретазы (GSI XIX) бензо[e][1,4]диазепин-3-ил)-бутирамид; ингибитор XX γ-секретазы (GSI XX) (S, S)-2-[2-(3,5-дифторфенил)ацетиламино]-N-(5-метил-6-оксо-6,7-дигидро-5H-дибензо[b, d]азепин-7-ил)пропионамид; ингибитор XXI γ-секретазы (GSI XXI) (S, S)-2-[2-(3,5-дифторфенил)-ацетиламино]-N-(1-метил-2-оксо-5-фенил-2,3-дигидро-1H-бензо[e][1,4]диазепин-3-ил)-пропионамид; ингибитор I гамма-40-секретазы N-транс-3,5-диметоксициннамоил-Ile-лейциналь; ингибитор II гамма-40-секретазы N-трет-бутилоксикарбонил-Gly-Val-валиналь; изовалерил-V-V-Sta-A-Sta-OCH3; MK-0752 (Merck); MRK-003 (Merck); семагацестат/LY450139 (Eli Lilly); RO4929097; PF-03084014; BMS-708163; MPC-7869 (модификатор γ-секретазы), YO-01027 (дибензазепин); LY411575 (Eli Lilly and Co.); L-685458 (Sigma-Aldrich); BMS-289948 (гидрохлорид 4-хлор-N-(2,5-дифторфенил)-N-((1R)-{4-фтор-2-[3-(1H-имидазол-1-ил)пропил]фенил}этил)бензолсульфонамида) или BMS-299897 (4-[2-((1R)-1-{[(4-хлорфенил)сульфонил]-2,5-дифторанилино}этил)-5-фторфенилбутановую кислоту) (Bristol Myers Squibb).
[0770] В некоторых вариантах осуществления MBM можно применять в комбинации с представителем соединений класса талидомидов. Представители соединений класса талидомидов включают без ограничения леналидомид (CC-5013), помалидомид (CC-4047 или актимид), талидомид и их соли и производные. В некоторых вариантах осуществления соединение может представлять собой смесь из одного, двух, трех или более представителей соединений класса талидомидов. Аналоги талидомида и иммуномодулирующие свойства аналогов талидомида описаны в Bodera and Stankiewicz, Recent Pat Endocr Metab Immune Drug Discov. 2011 Sep; 5(3):192-6. Структурный комплекс аналогов талидомида и убиквитина E3 описан в Gandhi et al., Br J Haematol. 2014 Mar; 164(6):811-21. Модулирование убиквитинлигазы E3 под действием аналогов талидомида описано в Fischer et al., Nature. 2014 Aug 7; 512(7512):49-53.
[0771] В некоторых вариантах осуществления представитель соединений класса талидомидов включает соединение формулы (I):
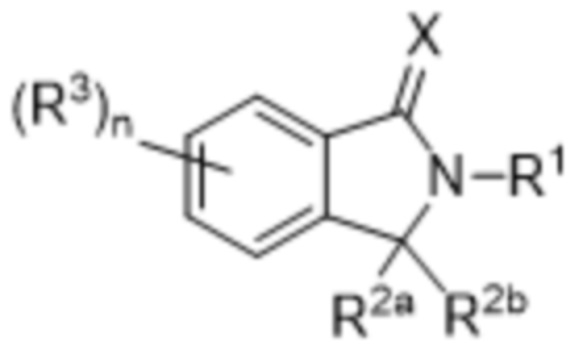 (I),
(I),
или его фармацевтически приемлемую соль, сложный эфир, гидрат, сольват или таутомер, где:
X представляет собой O или S;
R1 представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, карбоциклил, гетероциклил, арил или гетероарил, каждый из которых необязательно замещен одним или более R4;
каждый из R2a и R2b независимо представляет собой водород или C1-C6алкил; или R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют карбонильную группу или тиокарбонильную группу;
каждый из R3 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD) или -N(RC)S(O)xRE, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен одним или более R6;
каждый R4 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, оксо, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD), -N(RC)S(O)xRE, карбоциклил, гетероциклил, арил или гетероарил, где каждый алкил, алкенил, алкинил, гетероалкил, карбоциклил, гетероциклил, арил и гетероарил независимо и необязательно замещен одним или более R7;
каждый из RA, RB, RC, RD и RE независимо представляет собой водород или C1-C6алкил;
каждый R6 независимо представляет собой C1-C6алкил, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, арил или гетероарил, где каждый арил и гетероарил независимо и необязательно замещен одним или более R8;
каждый R7 независимо представляет собой галоген, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
каждый R8 независимо представляет собой C1-C6алкил, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
n равняется 0, 1, 2, 3 или 4; и
x равняется 0, 1 или 2.
[0772] В некоторых вариантах осуществления X представляет собой O.
[0773] В некоторых вариантах осуществления R1 представляет собой гетероциклил. В некоторых вариантах осуществления R1 представляет собой 6-членный гетероциклил или 5-членный гетероциклил. В некоторых вариантах осуществления R1 представляет собой азотсодержащий гетероциклил. В некоторых вариантах осуществления R1 представляет собой пиперидинил (например, пиперидин-2,6-дионил).
[0774] В некоторых вариантах осуществления каждый из R2a и R2b независимо представляет собой водород. В некоторых вариантах осуществления R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют карбонильную группу.
[0775] В некоторых вариантах осуществления R3 представляет собой C1-C6гетероалкил, -N(RC)(RD) или -N(RC)C(O)RA. В некоторых вариантах осуществления R3 представляет собой C1-C6гетероалкил (например, CH2NHC(O)CH2-фенил-трет-бутил), -N(RC)(RD) (например, NH2) или -N(RC)C(O)RA (например, NHC(O)CH3).
[0776] В одном варианте осуществления X представляет собой O. В одном варианте осуществления R1 представляет собой гетероциклил (например, пиперидин-2,6-дионил). В одном варианте осуществления каждый из R2a и R2b независимо представляет собой водород. В одном варианте осуществления n равняется 1. В одном варианте осуществления R3 представляет собой -N(RC)(RD) (например, -NH2). В одном варианте осуществления соединение включает в себя леналидомид, например, 3-(4-амино-1-оксоизоиндолин-2-ил)пиперидин-2,6-дион, или его фармацевтически приемлемую соль. В одном варианте осуществления соединение представляет собой леналидомид, например, следующей формулы:
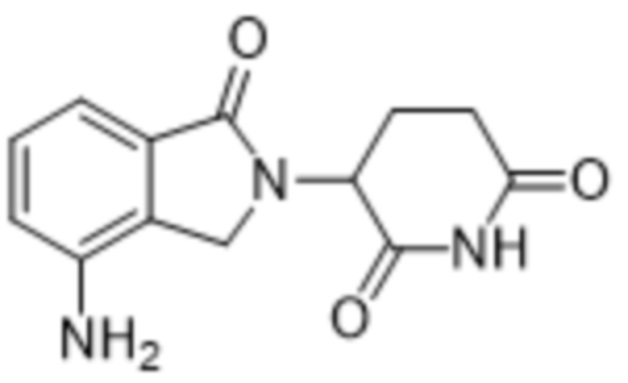 .
.
[0777] В одном варианте осуществления X представляет собой O. В одном варианте осуществления R1 представляет собой гетероциклил (например, пиперидинил-2,6-дионил). В некоторых вариантах осуществления R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют карбонильную группу. В одном варианте осуществления n равняется 1. В одном варианте осуществления R3 представляет собой -N(RC)(RD) (например, -NH2). В одном варианте осуществления соединение включает в себя помалидомид, например, 4-амино-2-(2,6-диоксопиперидин-3-ил)изоиндолин-1,3-дион, или его фармацевтически приемлемую соль. В одном варианте осуществления соединение представляет собой помалидомид, например, следующей формулы:
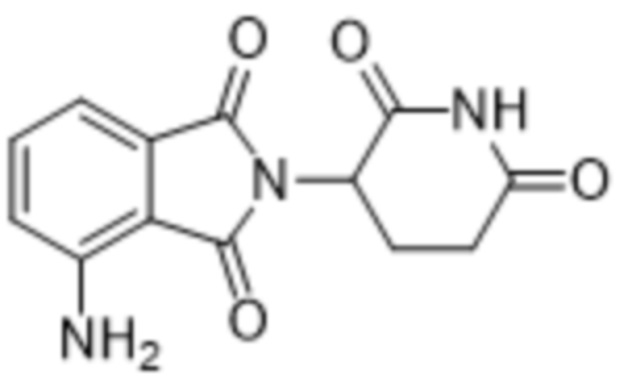 .
.
[0778] В одном варианте осуществления X представляет собой O. В одном варианте осуществления R1 представляет собой гетероциклил (например, пиперидинил-2,6-дионил). В одном варианте осуществления R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют карбонильную группу. В одном варианте осуществления n равняется 0. В одном варианте осуществления соединение включает в себя талидомид, например, 2-(2,6-диоксопиперидин-3-ил)изоиндолин-1,3-дион, или его фармацевтически приемлемую соль. В одном варианте осуществления продукт представляет собой талидомид, например, следующей формулы:
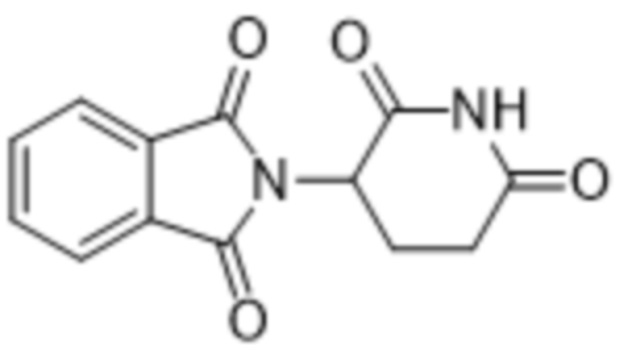 .
.
[0779] В одном варианте осуществления X представляет собой O. В одном варианте осуществления R1 представляет собой гетероциклил (например, пиперидин-2,6-дионил). В одном варианте осуществления каждый из R2a и R2b независимо представляет собой водород. В одном варианте осуществления n равняется 1. В одном варианте осуществления R3 представляет собой C1-C6гетероалкил (например, CH2NHC(O)CH2-фенил-трет-бутил). В одном варианте осуществления соединение включает в себя 2-(4-(трет-бутил)фенил)-N-((2-(2,6-диоксопиперидин-3-ил)-1-оксоизоиндолин-5-ил)метил)ацетамид или его фармацевтически приемлемую соль. В одном варианте осуществления соединение имеет структуру, показанную следующей формулой:
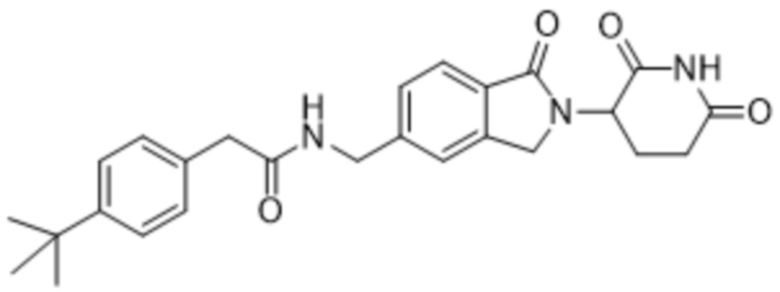 .
.
[0780] В некоторых вариантах осуществления соединение представляет собой соединение формулы (I-a):
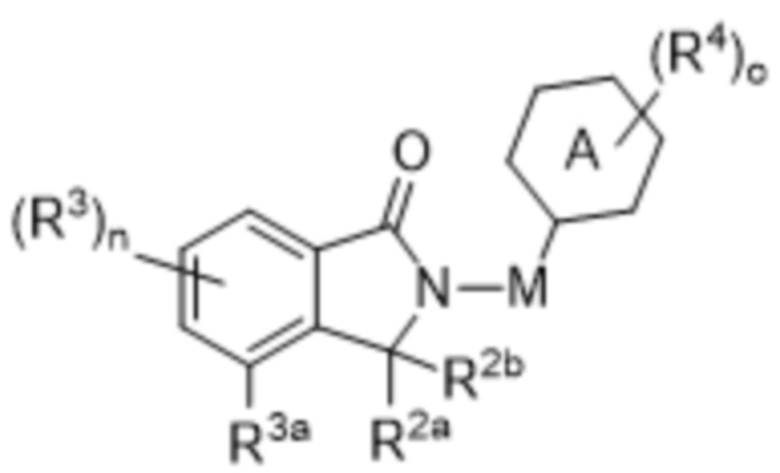 (I-a),
(I-a),
или его фармацевтически приемлемую соль, сложный эфир, гидрат или таутомер, где:
кольцо A представляет собой карбоциклил, гетероциклил, арил или гетероарил, каждый из которых независимо и необязательно замещен одним или более R4;
M отсутствует или представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил или C1-C6гетероалкил, где каждый алкил, алкенил, алкинил и гетероалкил необязательно замещен одним или более R4;
каждый из R2a и R2b независимо представляет собой водород или C1-C6алкил; или R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют карбонильную группу или тиокарбонильную группу;
R3a представляет собой водород, C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD) или -N(RC)S(O)xRE, где каждый алкил, алкенил, алкинил и гетероалкил необязательно замещен одним или более R6;
каждый из R3 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD) или -N(RC)S(O)xRE, где каждый алкил, алкенил, алкинил и гетероалкил независимо и необязательно замещен одним или более R6;
каждый R4 независимо представляет собой C1-C6алкил, C2-C6алкенил, C2-C6алкинил, C1-C6гетероалкил, галоген, циано, оксо, -C(O)RA, -C(O)ORB, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, -S(O)xRE, -S(O)xN(RC)(RD), -N(RC)S(O)xRE, карбоциклил, гетероциклил, арил или гетероарил, где каждый алкил, алкенил, алкинил, гетероалкил, карбоциклил, гетероциклил, арил и гетероарил независимо и необязательно замещен одним или более R7;
каждый из RA, RB, RC, RD и RE независимо представляет собой водород или C1-C6алкил;
каждый R6 независимо представляет собой C1-C6алкил, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD), -N(RC)C(O)RA, арил или гетероарил, где каждый арил и гетероарил независимо и необязательно замещен одним или более R8;
каждый R7 независимо представляет собой галоген, оксо, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
каждый R8 независимо представляет собой C1-C6алкил, циано, -ORB, -N(RC)(RD), -C(O)N(RC)(RD) или -N(RC)C(O)RA;
n равняется 0, 1, 2 или 3;
o равняется 0, 1, 2, 3, 4 или 5; и
x равняется 0, 1 или 2.
[0781] В некоторых вариантах осуществления X представляет собой O.
[0782] В некоторых вариантах осуществления M отсутствует.
[0783] В некоторых вариантах осуществления кольцо A представляет собой гетероциклил. В некоторых вариантах осуществления кольцо A представляет собой гетероциклил, например, 6-членный гетероциклил или 5-членный гетероциклил. В некоторых вариантах осуществления кольцо A представляет собой азотсодержащий гетероциклил. В некоторых вариантах осуществления кольцо A представляет собой пиперидинил (например, пиперидин-2,6-дионил).
[0784] В некоторых вариантах осуществления M отсутствует, и кольцо A представляет собой гетероциклил (например, пиперидинил, например, пиперидин-2,6-дионил).
[0785] В некоторых вариантах осуществления каждый из R2a и R2b независимо представляет собой водород. В некоторых вариантах осуществления R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют карбонильную группу.
[0786] В некоторых вариантах осуществления R3a представляет собой водород, -N(RC)(RD) или -N(RC)C(O)RA. В некоторых вариантах осуществления R3a представляет собой водород. В некоторых вариантах осуществления R3a представляет собой -N(RC)(RD) (например, -NH2). В некоторых вариантах осуществления R3a представляет собой -N(RC)C(O)RA (например, NHC(O)CH3).
[0787] В некоторых вариантах осуществления R3 представляет собой C1-C6гетероалкил (например, CH2NHC(O)CH2-фенил-трет-бутил). В некоторых вариантах осуществления n равняется 0 или 1. В некоторых вариантах осуществления n равняется 0. В некоторых вариантах осуществления n равняется 1.
[0788] Соединение может содержать один или более хиральных центров или существовать в виде одного или более стереоизомеров. В некоторых вариантах осуществления соединение содержит один хиральный центр и представляет собой смесь стереоизомеров, например, R-стереоизомера и S-стереоизомера. В некоторых вариантах осуществления смесь содержит R-стереоизомеры и S-стереоизомеры в определенном соотношении, например, R-стереоизомеры и S-стереоизомеры в соотношении, составляющем приблизительно 1:1 (т. е. представляет собой рацемическую смесь). В некоторых вариантах осуществления смесь содержит R-стереоизомеры и S-стереоизомеры в соотношении, составляющем приблизительно 51:49, приблизительно 52:48, приблизительно 53:47, приблизительно 54:46, приблизительно 55:45, приблизительно 60:40, приблизительно 65:35, приблизительно 70:30, приблизительно 75:25, приблизительно 80:20, приблизительно 85:15, приблизительно 90:10, приблизительно 95:5 или приблизительно 99:1. В некоторых вариантах осуществления смесь содержит S-стереоизомеры и R-стереоизомеры в соотношении, составляющем приблизительно 51:49, приблизительно 52:48, приблизительно 53:47, приблизительно 54:46, приблизительно 55:45, приблизительно 60:40, приблизительно 65:35, приблизительно 70:30, приблизительно 75:25, приблизительно 80:20, приблизительно 85:15, приблизительно 90:10, приблизительно 95:5 или приблизительно 99:1. В некоторых вариантах осуществления соединение представляет собой один стереоизомер формулы (I) или формулы (I-a), например, один R-стереоизомер или один S-стереоизомер.
[0789] В некоторых вариантах осуществления MBM вводят в комбинации с ингибитором киназы. В одном варианте осуществления ингибитор киназы представляет собой ингибитор PI3-киназы, например, CLR457, BGT226 или BYL719. В одном варианте осуществления ингибитор киназы представляет собой ингибитор CDK4, например, ингибитор CDK4, описанный в данном документе, например, ингибитор CDK4/6, такой как, например, гидрохлорид 6-ацетил-8-циклопентил-5-метил-2-(5-пиперазин-1-илпиридин-2-иламино)-8H-пиридо[2,3-d]пиримидин-7-она (также называемый палбоциклибом или PD0332991). В одном варианте осуществления ингибитор киназы представляет собой ингибитор BTK, например, ингибитор BTK, описанный в данном документе, такой как, например, ибрутиниб. В одном варианте осуществления ингибитор киназы представляет собой ингибитор mTOR, например, ингибитор mTOR, описанный в данном документе, такой как, например, рапамицин, аналог рапамицина, OSI-027. Ингибитор mTOR может представлять собой, например, ингибитор mTORC1 и/или ингибитор mTORC2, например, ингибитор mTORC1 и/или ингибитор mTORC2, описанный в данном документе. В одном варианте осуществления ингибитор киназы представляет собой ингибитор MNK, например, ингибитор MNK, описанный в данном документе, такой как, например, 4-амино-5-(4-фторанилино)-пиразолo[3,4-d]пиримидин. Ингибитор MNK может представлять собой, например, ингибитор MNK1a, MNK1b, MNK2a и/или MNK2b. В одном варианте осуществления ингибитор киназы представляет собой двойной ингибитор PI3K/mTOR, описанный в данном документе, такой как, например, PF-04695102. В одном варианте осуществления ингибитор киназы представляет собой ингибитор DGK, например, ингибитор DGK, описанный в данном документе, такой как, например, DGKinh1 (D5919) или DGKinh2 (D5794).
[0790] В одном варианте осуществления ингибитор киназы представляет собой ингибитор BTK, выбранный из ибрутиниба (PCI-32765); GDC-0834; RN-486; CGI-560; CGI-1764; HM-71224; CC-292; ONO-4059; CNX-774 и LFM-A13. В одном варианте осуществления ингибитор BTK не снижает и не подавляет киназную активность интерлейкин-2-индуцируемой киназы (ITK) и выбран из GDC-0834; RN-486; CGI-560; CGI-1764; HM-71224; CC-292; ONO-4059; CNX-774 и LFM-A13.
[0791] В одном варианте осуществления ингибитор киназы представляет собой ингибитор BTK, например, ибрутиниб (PCI-32765). В некоторых вариантах осуществления MBM вводят субъекту в комбинации с ибрутинибом (также называемым PCI-32765) (например, субъекту с CLL, MCL или SLL). Например, у субъекта может иметься делеция в коротком плече хромосомы 17 (del(17p), например, в лейкозной клетке). В других примерах у субъекта не имеется del(17p). В некоторых вариантах осуществления у субъекта имеется рецидивирующая CLL или SLL, например, субъекту ранее вводили средство противораковой терапии (например, ранее вводили одно, два, три или четыре предшествующих средства противораковой терапии). В некоторых вариантах осуществления у субъекта имеется рефрактерная CLL или SLL. В других вариантах осуществления у субъекта имеется фолликулярная лимфома, например, рецидивирующая или рефрактерная фолликулярная лимфома. В некоторых вариантах осуществления ибрутиниб вводят в дозе, составляющей приблизительно 300-600 мг/день (например, приблизительно 300-350, 350-400, 400-450, 450-500, 500-550 или 550-600 мг/день, например, приблизительно 420 мг/день или приблизительно 560 мг/день), например, перорально. В некоторых вариантах осуществления ибрутиниб вводят в дозе, составляющей приблизительно 250 мг, 300 мг, 350 мг, 400 мг, 420 мг, 440 мг, 460 мг, 480 мг, 500 мг, 520 мг, 540 мг, 560 мг, 580 мг, 600 мг (например, 250 мг, 420 мг или 560 мг), ежедневно в течение некоторого периода времени, например, ежедневно в течение 21-дневного цикла или ежедневно в течение 28-дневного цикла. В одном варианте осуществления ибрутиниб вводят в течение 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 или больше циклов. В некоторых вариантах осуществления ибрутиниб вводят в комбинации с ритуксимабом. См., например, Burger et al. (2013) Ibrutinib In Combination With Rituximab (iR) Is Well Tolerated and Induces a High Rate Of Durable Remissions In Patients With High-Risk Chronic Lymphocytic Leukemia (CLL): New, Updated Results Of a Phase II Trial In 40 Patients, Abstract 675, представленную на 55-м ежегодном собрании и выставке ASH, Новый Орлеан, Луизиана, 7-10 декабря. Не ограничиваясь какой-либо теорией, полагают, что при добавлении ибрутиниба усиливается пролиферативный ответ T-клеток и может происходить сдвиг фенотипа T-клеток от T-хелперов 2 типа (Th2) к T-хелперам 1 типа (Th1). Th1 и Th2 представляют собой фенотипы хелперных T-клеток, при этом Th1 и Th2 регулируют различные пути иммунных ответов. Фенотип Th1 ассоциирован с провоспалительными ответами, например, для уничтожения клеток, таких как внутриклеточные патогены/вирусы или раковые клетки, или поддерживающимися в течение длительного времени аутоиммунными ответами. Фенотип Th2 ассоциирован с накоплением эозинофилов и противовоспалительными ответами.
[0792] В определенных вариантах осуществления MBM вводят в комбинации с ингибитором рецептора эпидермального фактора роста (EGFR).
[0793] В некоторых вариантах осуществления ингибитор EGFR представляет собой (R, E)-N-(7-хлор-1-(1-(4-(диметиламино)бут-2-еноил)азепан-3-ил)-1H-бензо[d]имидазол-2-ил)-2-метилизоникотинамид (соединение A40) или соединение, раскрытое в РСТ-публикации № WO 2013/184757.
[0794] В некоторых вариантах осуществления ингибитор EGFR, например, (R, E)-N-(7-хлор-1-(1-(4-(диметиламино)бут-2-еноил)азепан-3-ил)-1H-бензо[d]имидазол-2-ил)-2-метилизоникотинамид (соединение A40) или соединение, раскрытое в РСТ-публикации № WO 2013/184757, вводят в дозе 150-250 мг, например, в день. В некоторых вариантах осуществления ингибитор EGFR, например, (R, E)-N-(7-хлор-1-(1-(4-(диметиламино)бут-2-еноил)азепан-3-ил)-1H-бензо[d]имидазол-2-ил)-2-метилизоникотинамид (соединение A40) или соединение, раскрытое в РСТ-публикации № WO 2013/184757, вводят в дозе, составляющей приблизительно 150, 200 или 250 мг или приблизительно 150-200 или 200-250 мг.
[0795] В некоторых вариантах осуществления ингибитор EGFR, представляющий собой (R, E)-N-(7-хлор-1-(1-(4-(диметиламино)бут-2-еноил)азепан-3-ил)-1H-бензо[d]имидазол-2-ил)-2-метилизоникотинамид (соединение A40) или соединение, раскрытое в РСТ-публикации № WO 2013/184757, является ковалентным необратимым ингибитором тирозинкиназы. В определенных вариантах осуществления ингибитор EGFR, представляющий собой (R, E)-N-(7-хлор-1-(1-(4-(диметиламино)бут-2-еноил)азепан-3-ил)-1H-бензо[d]имидазол-2-ил)-2-метилизоникотинамид (соединение A40) или соединение, раскрытое в РСТ-публикации № WO 2013/184757, ингибирует EGFR с активирующими мутациями (L858R, ex19del). В других вариантах осуществления ингибитор EGFR, представляющий собой (R, E)-N-(7-хлор-1-(1-(4-(диметиламино)бут-2-еноил)азепан-3-ил)-1H-бензо[d]имидазол-2-ил)-2-метилизоникотинамид (соединение A40) или соединение, раскрытое в РСТ-публикации № WO 2013/184757, не ингибирует или по существу не ингибирует EGFR дикого типа (wt). Соединение A40 продемонстрировало эффективность у пациентов с NSCLC с мутантным EGFR. В некоторых вариантах осуществления ингибитор EGFR, представляющий собой (R, E)-N-(7-хлор-1-(1-(4-(диметиламино)бут-2-еноил)азепан-3-ил)-1H-бензо[d]имидазол-2-ил)-2-метилизоникотинамид (соединение A40) или соединение, раскрытое в РСТ-публикации № WO 2013/184757, также ингибирует одну или более киназ из семейства киназ Tec. Киназы семейства Tec включают, например, ITK, BMX, TEC, RLK и BTK и играют центральную роль в распространении сигналов от T-клеточных рецепторов и рецепторов хемокинов (Schwartzberg et al. (2005) Nat. Rev. Immunol. p. 284-95). Например, соединение A40 может ингибировать ITK с IC50 при биохимическом взаимодействии, составляющей 1,3 нМ. ITK является критически важным ферментом для выживания Th2-клеток, и ее ингибирование приводит к смещению равновесия между Th2- и Th1-клетками.
[0796] В некоторых вариантах осуществления ингибитор EGFR выбран из одного или более из эрлотиниба, гефитиниба, цетуксимаба, панитумумаба, нецитумумаба, PF-00299804, нимотузумаба или RO5083945.
[0797] В некоторых вариантах осуществления MBM вводят в комбинации с антагонистом аденозинового рецептора A2A (A2AR). Иллюстративные антагонисты A2AR включают, например, PBF509 (Palobiofarma/Novartis), CPI444/V81444 (Corvus/Genentech), AZD4635/HTL-1071 (AstraZeneca/Heptares), випаденант (Redox/Juno), GBV-2034 (Globavir), AB928 (Arcus Biosciences), теофиллин, истрадефиллин (Kyowa Hakko Kogyo), тозаденант/SYN-115 (Acorda), KW-6356 (Kyowa Hakko Kogyo), ST-4206 (Leadiant Biosciences), преладенант/SCH 420814 (Merck/Schering) и NIR178 (Novartis).
[0798] В определенных вариантах осуществления антагонист A2AR представляет собой PBF509. PBF509 и другие антагонисты A2AR раскрыты в US 8796284 и WO 2017/025918. В определенных вариантах осуществления антагонист A2AR представляет собой 5-бром-2,6-ди-(1H-пиразол-1-ил)пиримидин-4-амин. В определенных вариантах осуществления антагонист A2AR имеет следующую структуру:
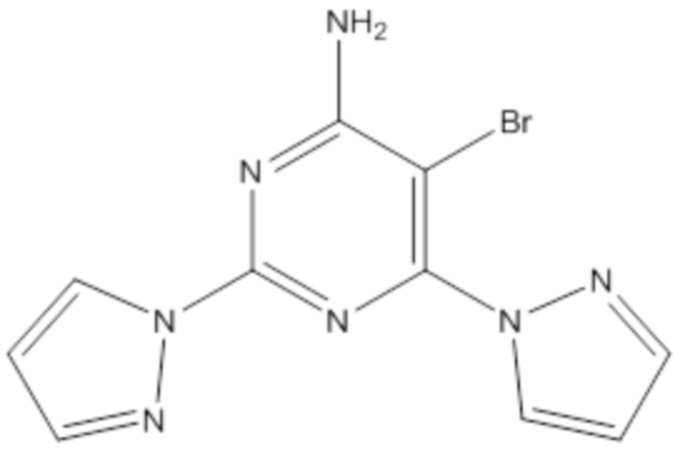
[0799] В определенных вариантах осуществления антагонист A2AR представляет собой CPI444/V81444. CPI-444 и другие антагонисты A2AR раскрыты в WO 2009/156737. В определенных вариантах осуществления антагонист A2AR представляет собой (S)-7-(5-метилфуран-2-ил)-3-((6-(((тетрагидрофуран-3-ил)окси)метил)пиридин-2-ил)метил)-3H[1,2,3]триазоло[4,5-d]пиримидин-5-амин. В определенных вариантах осуществления антагонист A2AR представляет собой (R)-7-(5-метилфуран-2-ил)-3-((6-(((тетрагидрофуран-3-ил)окси)метил)пиридин-2-ил)метил)-3H[1,2,3]триазоло[4,5-d]пиримидин-5-амин или его рацемат. В определенных вариантах осуществления антагонист A2AR представляет собой 7-(5-метилфуран-2-ил)-3-((6-(((тетрагидрофуран-3-ил)окси)метил)пиридин-2-ил)метил)-3H[1,2,3]триазоло[4,5-d]пиримидин-5-амин. В определенных вариантах осуществления антагонист A2AR имеет следующую структуру:
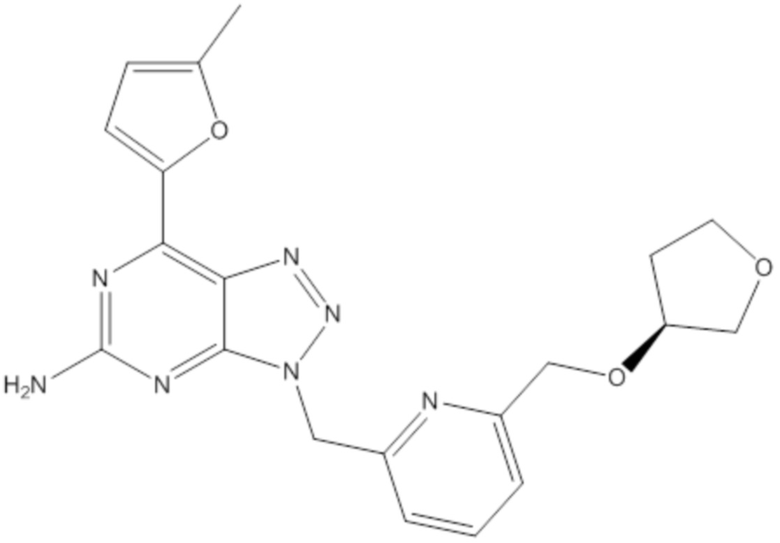
[0800] В определенных вариантах осуществления антагонист A2AR представляет собой AZD4635/HTL-1071. Антагонисты A2AR раскрыты в WO 2011/095625. В определенных вариантах осуществления антагонист A2AR представляет собой 6-(2-хлор-6-метилпиридин-4-ил)-5-(4-фторфенил)-1,2,4-триазин-3-амин. В определенных вариантах осуществления антагонист A2AR имеет следующую структуру:
[0801] В определенных вариантах осуществления антагонист A2AR представляет собой ST-4206 (Leadiant Biosciences). В определенных вариантах осуществления антагонист A2AR представляет собой антагонист A2AR, описанный в US 9133197. В определенных вариантах осуществления антагонист A2AR имеет следующую структуру:
[0802] В определенных вариантах осуществления антагонист A2AR представляет собой антагонист A2AR, описанный в US8114845, US9029393, US20170015758 или US20160129108.
[0803] В определенных вариантах осуществления антагонист A2AR представляет собой истрадефиллин (регистрационный номер CAS: 155270-99-8). Истрадефиллин также известен как KW-6002 или 8-[(E)-2-(3,4-диметоксифенил)винил]-1,3-диэтил-7-метил-3,7-дигидро-1H-пурин-2,6-дион. Истрадефиллин раскрыт, например, в LeWitt et al. (2008) Annals of Neurology 63 (3): 295-302).
[0804] В определенных вариантах осуществления антагонист A2aR представляет собой тозаденант (Biotie). Тозаденант также известен как SYN115 или 4-гидрокси-N-(4-метокси-7-морфолин-4-ил-1,3-бензотиазол-2-ил)-4-метилпиперидин-1-карбоксамид. Тозаденант блокирует эффект эндогенного аденозина в отношении рецепторов А2а, что приводит к усилению эффекта дофамина в отношении рецептора D2 и подавлению эффекта глутамата в отношении рецептора mGluR5. В некоторых вариантах осуществления антагонист A2aR представляет собой преладенант (регистрационный номер CAS: 377727-87-2). Преладенант также известен как SCH 420814 или 2-(2-фуранил)-7-[2-[4-[4-(2-метоксиэтокси)фенил]-1-пиперазинил]этил]7H-пиразоло[4,3-е][1,2,4]триазоло[1,5-с]пиримидин-5-амин. Преладенант был разработан как лекарственное средство, действующее как эффективный и селективный антагонист аденозинового рецептора А2А.
[0805] В определенных вариантах осуществления антагонист A2aR представляет собой випаденант. Випаденант также известен как BIIB014, V2006 или 3-[(4-амино-3-метилфенил)метил]-7-(фуран-2-ил)триазоло[4,5-d]пиримидин-5-амин.
[0806] Другие иллюстративные антагонисты A2aR включают, например, ATL-444, MSX-3, SCH-58261, SCH-412348, SCH-442416, VER-6623, VER-6947, VER-7835, CGS-15943 или ZM-241385.
[0807] В некоторых вариантах осуществления антагонист A2aR представляет собой антагонист сигнального пути A2aR (например, ингибитор CD-73, например, антитело к CD73), который представляет собой MEDI9447. MEDI9447 представляет собой моноклональное антитело, специфичное к CD73. Целенаправленное воздействие на внеклеточное продуцирование аденозина посредством CD73 может ослаблять иммуносупрессивные эффекты аденозина. Сообщалось, что MEDI9447 характеризуется рядом форм активности, например, подавлением активности эктонуклеотидазы CD73, ослаблением АМР-опосредованной супрессии лимфоцитов и подавлением роста сингенных опухолей. MEDI9447 может управлять изменениями как в миелоидных, так и лимфоидных популяциях инфильтрирующих лейкоцитов в микроокружении опухоли. Эти изменения включают, например, увеличение количества CD8 эффекторных клеток и активированных макрофагов, а также снижение доли супрессорных клеток миелоидного происхождения (MDSC) и регуляторных Т-лимфоцитов.
[0808] В некоторых вариантах осуществления MBM вводят в комбинации со средством терапии на основе клеток, экспрессирующих CAR, таким как средство терапии на основе клеток, экспрессирующих CAR для CD19.
[0809] В одном варианте осуществления антигенсвязывающий домен CAR для CD19 характеризуется такой же или сходной специфичностью связывания по сравнению с scFv-фрагментом FMC63, описанным в Nicholson et al. Mol. Immun. 34 (16-17): 1157-1165 (1997). В одном варианте осуществления антигенсвязывающий домен CAR для CD19 включает в себя scFv-фрагмент, описанный в Nicholson et al. Mol. Immun. 34 (16-17): 1157-1165 (1997).
[0810] В некоторых вариантах осуществления CAR для CD19 содержит антигенсвязывающий домен (например, гуманизированный антигенсвязывающий домен) согласно таблице 3 из WO2014/153270. В WO2014/153270 также описаны способы выполнения анализа связывания и эффективности различных конструкций CAR.
[0811] В одном аспекте исходная последовательность мышиного scFv представляет собой конструкцию CAR19, представленную в PCT-публикации WO2012/079000. В одном варианте осуществления CD19-связывающий домен представляет собой scFv, описанный в WO2012/079000.
[0812] В одном варианте осуществления молекула CAR содержит последовательность слитого полипептида, представленную под SEQ ID NO: 12 в PCT-публикации WO2012/079000, в которой представлен scFv-фрагмент мышиного происхождения, который специфично связывается с CD19 человека.
[0813] В одном варианте осуществления CAR для CD19 содержит аминокислотную последовательность, представленную под SEQ ID NO: 12 в PCT-публикации WO2012/079000.
[0814] В одном варианте осуществления CAR для CD19 имеет обозначение согласно USAN тисагенлеклейсел-T. В ряде вариантов осуществления CTL019 получают посредством генной модификации T-клеток, опосредованной стабильной вставкой путем трансдукции с помощью самоинактивирующегося лентивирусного (LV) вектора, дефектного по репликации, содержащего трансген CTL019 под контролем промотора гена EF-1-альфа. CTL019 может представлять собой смесь положительных и отрицательных по трансгену Т-клеток, которые доставляются субъекту из расчета процентного количества Т-клеток, положительных по трансгену.
[0815] В других вариантах осуществления CAR для CD19 содержит антигенсвязывающий домен (например, гуманизированный антигенсвязывающий домен) согласно таблице 3 из WO2014/153270.
[0816] Гуманизация антитела мыши к CD19 необходима в клинической ситуации, когда специфические для мышей остатки могут индуцировать ответ с образованием антител человека к антигену мыши (HAMA) у пациентов, которые получают лечение с помощью CART19, т. е. лечение с помощью T-клеток, трансдуцированных конструкцией CAR19. Получение, определение характеристик и эффективность гуманизированных последовательностей CAR для CD19 описаны в международной заявке WO2014/153270, включая примеры 1-5 (стр. 115-159).
[0817] В некоторых вариантах осуществления конструкции CAR для CD19 описаны в РСТ-публикации WO 2012/079000.
[0818] Конструкции CAR для CD19, содержащие гуманизированные scFv-домены антител к CD19, описаны в публикации согласно PCT WO 2014/153270.
[0819] В соответствии с настоящим изобретением можно применять любой известный CAR для CD19, например, антигенсвязывающий домен для CD19 из любого известного из уровня техники CAR для CD19. Например, CAR для CD19 LG-740 описан в патенте США № 8399645; патенте США № 7446190; Xu et al., Leuk Lymphoma. 2013 54(2):255-260(2012); Cruz et al., Blood 122(17):2965-2973 (2013); Brentjens et al., Blood, 118(18):4817-4828 (2011); Kochenderfer et al., Blood 116(20):4099-102 (2010); Kochenderfer et al., Blood 122 (25):4129-39 (2013); и 16th Annu Meet Am Soc Gen Cell Ther (ASGCT) (May 15-18, Salt Lake City) 2013, Abst 10.
[0820] Иллюстративные CAR для CD19 включают CAR для CD19, описанные в данном документе, или CAR для CD19, описанный в Xu et al. Blood 123.24(2014):3750-9; Kochenderfer et al. Blood 122.25(2013):4129-39, Cruz et al. Blood 122.17(2013):2965-73, NCT00586391, NCT01087294, NCT02456350, NCT00840853, NCT02659943, NCT02650999, NCT02640209, NCT01747486, NCT02546739, NCT02656147, NCT02772198, NCT00709033, NCT02081937, NCT00924326, NCT02735083, NCT02794246, NCT02746952, NCT01593696, NCT02134262, NCT01853631, NCT02443831, NCT02277522, NCT02348216, NCT02614066, NCT02030834, NCT02624258, NCT02625480, NCT02030847, NCT02644655, NCT02349698, NCT02813837, NCT02050347, NCT01683279, NCT02529813, NCT02537977, NCT02799550, NCT02672501, NCT02819583, NCT02028455, NCT01840566, NCT01318317, NCT01864889, NCT02706405, NCT01475058, NCT01430390, NCT02146924, NCT02051257, NCT02431988, NCT01815749, NCT02153580, NCT01865617, NCT02208362, NCT02685670, NCT02535364, NCT02631044, NCT02728882, NCT02735291, NCT01860937, NCT02822326, NCT02737085, NCT02465983, NCT02132624, NCT02782351, NCT01493453, NCT02652910, NCT02247609, NCT01029366, NCT01626495, NCT02721407, NCT01044069, NCT00422383, NCT01680991, NCT02794961 или NCT02456207.
[0821] В некоторых вариантах осуществления MBM вводят в комбинации с ингибитором CD20.
[0822] В одном варианте осуществления ингибитор CD20 представляет собой антитело к CD20 или его фрагмент. В одном варианте осуществления антитело представляет собой моноспецифическое антитело, а в другом варианте осуществления антитело представляет собой биспецифическое антитело. В одном варианте осуществления ингибитор CD20 представляет собой химерное мышиное/человеческое моноклональное антитело, например, ритуксимаб. В одном варианте осуществления ингибитор CD20 представляет собой человеческое моноклональное антитело, такое как офатумумаб. В одном варианте осуществления ингибитор CD20 представляет собой гуманизированное антитело, такое как окрелизумаб, велтузумаб, обинутузумаб, окаратузумаб или PRO131921 (Genentech). В одном варианте осуществления ингибитор CD20 представляет собой слитый белок, содержащий часть антитела к CD20, такой как TRU-015 (Trubion Pharmaceuticals).
[0823] В некоторых вариантах осуществления MBM вводят в комбинации со средством терапии на основе клеток, экспрессирующих CAR для CD22 (например, клетками, экспрессирующими CAR, который связывается с CD22 человека).
[0824] В некоторых вариантах осуществления MBM вводят в комбинации с ингибитором CD22. В некоторых вариантах осуществления ингибитор CD22 представляет собой малую молекулу или молекулу антитела к CD22. В некоторых вариантах осуществления антитело представляет собой моноспецифическое антитело, необязательно конъюгированное со вторым средством, таким как химиотерапевтическое средство. Например, в одном варианте осуществления антитело представляет собой конъюгат моноклонального антитела к CD22 и MMAE (например, DCDT2980S). В одном варианте осуществления антитело представляет собой scFv антитела к CD22, например, scFv антитела RFB4. Этот scFv может быть слит с полным экзотоксином A Pseudomonas или с его фрагментом (например, BL22). В одном варианте осуществления антитело является гуманизированным моноклональным антителом к CD22 (например, представляет собой эпратузумаб). В одном варианте осуществления антитело или его фрагмент содержит Fv-часть антитела к CD22, которая необязательно ковалентно слита с полным экзотоксином A Pseudomonas или его фрагментом (например, фрагментом размером 38 кДа) (например, представляет собой моксетумомаб пасудотокс). В одном варианте осуществления антитело к CD22 представляет собой биспецифическое антитело к CD19/CD22, необязательно конъюгированное с токсином. Например, в одном варианте осуществления антитело к CD22 содержит биспецифическую часть антитела к CD19/CD22 (например, два scFv-лиганда, распознающих CD19 и CD22 человека), необязательно связанную с полным дифтерийным токсином (DT) или его частью, например, первыми 389 аминокислотами дифтерийного токсина (DT) DT 390, например, представляет собой лиганд-управляемый токсин, такой как DT2219ARL. В другом варианте осуществления биспецифическая часть (например, из антитела к CD19/CD22) связана с токсином, таким как дегликозилированная А-цепь рицина (например, комботокс).
[0825] В некоторых вариантах осуществления ингибитор CD22 представляет собой молекулу полиспецифического антитела, например, молекулу биспецифического антитела, например, молекулу биспецифического антитела, которая связывается с CD20 и CD3. Иллюстративные молекулы биспецифических антител, которые связываются с CD20 и CD3, раскрыты в WO2016086189 и WO2016182751. В некоторых вариантах осуществления молекула биспецифического антитела, которая связывается с CD20 и CD3, представляет собой XENP13676, раскрытый на фигуре 74 и под SEQ ID NO: 323, 324 и 325 в WO2016086189.
[0826] В некоторых вариантах осуществления средство терапии на основе клеток, экспрессирующих CAR для CD22, содержит антигенсвязывающий домен в соответствии с WO2016/164731.
[0827] В некоторых вариантах осуществления MBM вводят в комбинации с ингибитором FCRL2 или FCRL5. В некоторых вариантах осуществления ингибитор FCRL2 или FCRL5 представляет собой молекулу антитела к FCRL2, например, молекулу биспецифического антитела, например, биспецифическое антитело, которое связывается с FCRL2 и CD3. В некоторых вариантах осуществления ингибитор FCRL2 или FCRL5 представляет собой молекулу антитела к FCRL5, например, молекулу биспецифического антитела, например, биспецифическое антитело, которое связывается с FCRL5 и CD3. В некоторых вариантах осуществления ингибитор FCRL2 или FCRL5 представляет собой средство терапии на основе клеток, экспрессирующих CAR для FCRL2. В некоторых вариантах осуществления ингибитор FCRL2 или FCRL5 представляет собой средство терапии на основе клеток, экспрессирующих CAR для FCRL5.
[0828] Иллюстративные молекулы антител к FCRL5 раскрыты в US20150098900, US20160368985, WO2017096120 (например, антитела ET200-001, ET200-002, ET200-003, ET200-006, ET200-007, ET200-008, ET200-009, ET200-010, ET200-011, ET200-012, ET200-013, ET200-014, ET200-015, ET200-016, ET200-017, ET200-018, ET200-019, ET200-020, ET200-021, ET200-022, ET200-023, ET200-024, ET200-025, ET200-026, ET200-027, ET200-028, ET200-029, ET200-030, ET200-031, ET200-032, ET200-033, ET200-034, ET200-035, ET200-037, ET200-038, ET200-039, ET200-040, ET200-041, ET200-042, ET200-043, ET200-044, ET200-045, ET200-069, ET200-078, ET200-079, ET200-081, ET200-097, ET200-098, ET200-099, ET200-100, ET200-101, ET200-102, ET200-103, ET200-104, ET200-105, ET200-106, ET200-107, ET200-108, ET200-109, ET200-110, ET200-111, ET200-112, ET200-113, ET200-114, ET200-115, ET200-116, ET200-117, ET200-118, ET200-119, ET200-120, ET200-121, ET200-122, ET200-123, ET200-125, ET200-005 и ET200-124, раскрытые в WO2017096120).
[0829] Иллюстративные молекулы CAR для FCRL5 раскрыты в WO2016090337.
[0830] В некоторых вариантах осуществления MBM вводят в комбинации с комплексом IL15/IL-15Ra. В некоторых вариантах осуществления комплекс IL-15/IL-15Ra выбран из NIZ985 (Novartis), ATL-803 (Altor) или CYP0150 (Cytune).
[0831] В некоторых вариантах осуществления комплекс IL-15/IL-15Ra содержит IL-15 человека в комплексе с растворимой формой IL-15Ra человека. Комплекс может содержать IL-15, ковалентно или нековалентно связанный с растворимой формой IL-15Ra. В конкретном варианте осуществления IL-15 человека нековалентно связан с растворимой формой IL-15Ra. В конкретном варианте осуществления IL-15 человека в композиции содержит аминокислотную последовательность, описанную в WO 2014/066527, а растворимая форма IL-15Ra человека содержит аминокислотную последовательность, описанную в WO 2014/066527. Молекулы, описанные в данном документе, можно получать с помощью векторов, клеток-хозяев и способов, описанных в WO 2007/084342.
[0832] В некоторых вариантах осуществления комплекс IL-15/IL-15Ra представляет собой ALT-803 - слитый белок на основе IL-15/IL-15Ra и Fc (растворимый комплекс IL-15N72D:IL-15RaSu/Fc). ALT-803 раскрыт в WO 2008/143794.
[0833] В некоторых вариантах осуществления комплекс IL-15/IL-15Ra содержит IL-15, слитый с доменом Sushi IL-15Ra (CYP0150, Cytune). Домен Sushi IL-15Ra относится к домену, который начинается с первого остатка цистеина после сигнального пептида IL-15Ra и заканчивается четвертым остатком цистеина после сигнального пептида. Комплекс IL-15, слитого с доменом Sushi IL-15Ra, раскрыт в WO 2007/04606 и WO 2012/175222.
[0834] В некоторых вариантах осуществления MBM вводят в комбинации с ингибитором PD-1. В некоторых вариантах осуществления ингибитор PD-1 выбран из PDR001 (Novartis), ниволумаба (Bristol-Myers Squibb), пембролизумаба (Merck & Co), пидилизумаба (CureTech), MEDI0680 (Medimmune), REGN2810 (Regeneron), TSR-042 (Tesaro), PF-06801591 (Pfizer), BGB-A317 (Beigene), BGB-108 (Beigene), INCSHR1210 (Incyte) или AMP-224 (Amplimmune). В одном варианте осуществления ингибитор PD-1 представляет собой молекулу антитела к PD-1. В одном варианте осуществления ингибитор PD-1 представляет собой молекулу антитела к PD-1, описанную в US 2015/0210769.
[0835] В одном варианте осуществления молекула антитела к PD-1 представляет собой ниволумаб (Bristol-Myers Squibb), также известный как MDX-1106, MDX-1106-04, ONO-4538, BMS-936558 или OPDIVO®. Ниволумаб (клон 5C4) и другие антитела к PD-1 раскрыты в US 8008449 и WO 2006/121168. В одном варианте осуществления молекула антитела к PD-1 содержит одну или более из последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи ниволумаба.
[0836] В одном варианте осуществления молекула антитела к PD-1 представляет собой пембролизумаб (Merck & Co), также известный как ламбролизумаб, MK-3475, MK03475, SCH-900475 или KEYTRUDA®. Пембролизумаб и другие антитела к PD-1 раскрыты в Hamid, O. et al. (2013) New England Journal of Medicine 369 (2): 134-44, US 8354509 и WO 2009/114335. В одном варианте осуществления молекула антитела к PD-1 содержит одну или более из последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи пембролизумаба.
[0837] В одном варианте осуществления молекула антитела к PD-1 представляет собой пидилизумаб (CureTech), также известный как CT-011. Пидилизумаб и другие антитела к PD-1 раскрыты в Rosenblatt, J. et al. (2011) J Immunotherapy 34(5): 409-18, US 7695715, US 7332582 и US 8686119. В одном варианте осуществления молекула антитела к PD-1 содержит одну или более из последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи пидилизумаба.
[0838] В одном варианте осуществления молекула антитела к PD-1 представляет собой MEDI0680 (Medimmune), также известный как AMP-514. MEDI0680 и другие антитела к PD-1 раскрыты в US 9205148 и WO 2012/145493. В одном варианте осуществления молекула антитела к PD-1 содержит одну или более последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи MEDI0680.
[0839] В одном варианте осуществления молекула антитела к PD-1 представляет собой REGN2810 (Regeneron). В одном варианте осуществления молекула антитела к PD-1 содержит одну или более последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи REGN2810.
[0840] В одном варианте осуществления молекула антитела к PD-1 представляет собой PF-06801591 (Pfizer). В одном варианте осуществления молекула антитела к PD-1 содержит одну или более последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи PF-06801591.
[0841] В одном варианте осуществления молекула антитела к PD-1 представляет собой BGB-A317 или BGB-108 (Beigene). В одном варианте осуществления молекула антитела к PD-1 содержит одну или более последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи BGB-A317 или BGB-108.
[0842] В одном варианте осуществления молекула антитела к PD-1 представляет собой INCSHR1210 (Incyte), также известный как INCSHR01210 или SHR-1210. В одном варианте осуществления молекула антитела к PD-1 содержит одну или более последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи INCSHR1210.
[0843] В одном варианте осуществления молекула антитела к PD-1 представляет собой TSR-042 (Tesaro), также известный как ANB011. В одном варианте осуществления молекула антитела к PD-1 содержит одну или более последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи TSR-042.
[0844] Дополнительные известные антитела к PD-1 включают антитела, описанные, например, в WO 2015/112800, WO 2016/092419, WO 2015/085847, WO 2014/179664, WO 2014/194302, WO 2014/209804, WO 2015/200119, US 8735553, US 7488802, US 8927697, US 8993731 и US 9102727.
[0845] В одном варианте осуществления антитело к PD-1 представляет собой антитело, которое конкурирует за связывание и/или связывается с тем же эпитопом в PD-1, что и одно из антител к PD-1, описанных в данном документе.
[0846] В одном варианте осуществления ингибитор PD-1 представляет собой пептид, который ингибирует сигнальный путь PD-1, например, как описано в US 8907053. В одном варианте осуществления ингибитор PD-1 представляет собой иммуноадгезин (например, иммуноадгезин, который содержит внеклеточную или PD-1-связывающую часть PD-L1 или PD-L2, слитую с константным участком (например, Fc-участком последовательности иммуноглобулина)). В одном варианте осуществления ингибитор PD-1 представляет собой AMP-224 (B7-DCIg (Amplimmune), например, раскрытый в WO 2010/027827 и WO 2011/066342).
[0847] В некоторых вариантах осуществления MBM вводят в комбинации с ингибитором PD-L1. В некоторых вариантах осуществления ингибитор PD-L1 выбран из FAZ053 (Novartis), атезолизумаба (Genentech/Roche), авелумаба (Merck Serono и Pfizer), дурвалумаба (MedImmune/AstraZeneca) или BMS-936559 (Bristol-Myers Squibb).
[0848] В одном варианте осуществления ингибитор PD-L1 представляет собой молекулу антитела к PD-L1. В одном варианте осуществления ингибитор PD-L1 представляет собой молекулу антитела к PD-L1, раскрытую в US 2016/0108123.
[0849] В одном варианте осуществления молекула антитела к PD-L1 представляет собой атезолизумаб (Genentech/Roche), также известный как MPDL3280A, RG7446, RO5541267, YW243.55.S70 или TECENTRIQ™. Атезолизумаб и другие антитела к PD-L1 раскрыты в US 8217149. В одном варианте осуществления молекула антитела к PD-L1 содержит одну или более из последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи атезолизумаба.
[0850] В одном варианте осуществления молекула антитела к PD-L1 представляет собой авелумаб (Merck Serono и Pfizer), также известный как MSB0010718C. Авелумаб и другие антитела к PD-L1 раскрыты в WO 2013/079174. В одном варианте осуществления молекула антитела к PD-L1 содержит одну или более из последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи авелумаба.
[0851] В одном варианте осуществления молекула антитела к PD-L1 представляет собой дурвалумаб (MedImmune/AstraZeneca), также известный как MEDI4736. Дурвалумаб и другие антитела к PD-L1 раскрыты в US 8779108. В одном варианте осуществления молекула антитела к PD-L1 содержит одну или более из последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи дурвалумаба.
[0852] В одном варианте осуществления молекула антитела к PD-L1 представляет собой BMS-936559 (Bristol-Myers Squibb), также известный как MDX-1105 или 12A4. BMS-936559 и другие антитела к PD-L1 раскрыты в US 7943743 и WO 2015/081158. В одном варианте осуществления молекула антитела к PD-L1 содержит одну или более последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи BMS-936559.
[0853] Дополнительные известные антитела к PD-L1 включают антитела, описанные, например, в WO 2015/181342, WO 2014/100079, WO 2016/000619, WO 2014/022758, WO 2014/055897, WO 2015/061668, WO 2013/079174, WO 2012/145493, WO 2015/112805, WO 2015/109124, WO 2015/195163, US 8168179, US 8552154, US 8460927 и US 9175082.
[0854] В некоторых вариантах осуществления MBM вводят в комбинации с ингибитором LAG-3. В некоторых вариантах осуществления ингибитор LAG-3 выбран из LAG525 (Novartis), BMS-986016 (Bristol-Myers Squibb) или TSR-033 (Tesaro).
[0855] В одном варианте осуществления ингибитор LAG-3 представляет собой молекулу антитела к LAG-3. В одном варианте осуществления ингибитор LAG-3 представляет собой молекулу антитела к LAG-3, раскрытую в US 2015/0259420.
[0856] В одном варианте осуществления молекула антитела к LAG-3 представляет собой BMS-986016 (Bristol-Myers Squibb), также известный как BMS986016. BMS-986016 и другие антитела к LAG-3 раскрыты в WO 2015/116539 и US 9505839. В одном варианте осуществления молекула антитела к LAG-3 содержит одну или более последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи BMS-986016.
[0857] В одном варианте осуществления молекула антитела к LAG-3 представляет собой TSR-033 (Tesaro). В одном варианте осуществления молекула антитела к LAG-3 содержит одну или более последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи TSR-033.
[0858] В одном варианте осуществления молекула антитела к LAG-3 представляет собой IMP731 или GSK2831781 (GSK и Prima BioMed). IMP731 и другие антитела к LAG-3 раскрыты в WO 2008/132601 и US 9244059. В одном варианте осуществления молекула антитела к LAG-3 содержит одну или более последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи IMP731. В одном варианте осуществления молекула антитела к LAG-3 содержит одну или более последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи GSK2831781.
[0859] Дополнительные известные антитела к LAG-3 включают антитела, описанные, например, в WO 2008/132601, WO 2010/019570, WO 2014/140180, WO 2015/116539, WO 2015/200119, WO 2016/028672, US 9244059, US 9505839.
[0860] В одном варианте осуществления ингибитор LAG-3 представляет собой растворимый белок LAG-3, например, IMP321 (Prima BioMed), например, раскрытый в WO 2009/044273.
[0861] В некоторых вариантах осуществления MBM вводят в комбинации с ингибитором TIM-3. В некоторых вариантах осуществления ингибитор TIM-3 представляет собой MBG453 (Novartis) или TSR-022 (Tesaro).
[0862] В одном варианте осуществления ингибитор TIM-3 представляет собой молекулу антитела к TIM-3. В одном варианте осуществления ингибитор TIM-3 представляет собой молекулу антитела к TIM-3, раскрытую в US 2015/0218274.
[0863] В одном варианте осуществления молекула антитела к TIM-3 представляет собой TSR-022 (AnaptysBio/Tesaro). В одном варианте осуществления молекула антитела к TIM-3 содержит одну или более последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи TSR-022. В одном варианте осуществления молекула антитела к TIM-3 содержит одну или более последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи APE5137 или APE5121. APE5137, APE5121 и другие антитела к TIM-3 раскрыты в WO 2016/161270.
[0864] В одном варианте осуществления молекула антитела к TIM-3 представляет собой клон антитела F38-2E2. В одном варианте осуществления молекула антитела к TIM-3 содержит одну или более последовательностей CDR (или в совокупности все последовательности CDR), последовательность вариабельного участка тяжелой цепи или легкой цепи или последовательность тяжелой цепи или легкой цепи F38-2E2.
[0865] Дополнительные известные антитела к TIM-3 включают антитела, описанные, например, в WO 2016/111947, WO 2016/071448, WO 2016/144803, US 8552156, US 8841418 и US 9163087.
[0866] В одном варианте осуществления антитело к TIM-3 представляет собой антитело, которое конкурирует за связывание и/или связывается с тем же эпитопом в TIM-3, что и одно из антител к TIM-3, описанных в данном документе.
[0867] В некоторых вариантах осуществления MBM вводят в комбинации с ингибитором трансформирующего фактора роста бета (TGF-β). В некоторых вариантах осуществления ингибитор TGF-β представляет собой фрезолимумаб (регистрационный номер CAS: 948564-73-6). Фрезолимумаб также известен как GC1008. Фрезолимумаб представляет собой человеческое моноклональное антитело, которое связывается с изоформами 1, 2 и 3 TGF-бета и ингибирует их. Фрезолимумаб раскрыт, например, в WO 2006/086469, US 8383780 и US 8591901.
[0868] В некоторых вариантах осуществления ингибитор TGF-β представляет собой XOMA 089. XOMA 089 также известен как XPA.42.089. XOMA 089 представляет собой полностью человеческое моноклональное антитело, которое связывает и нейтрализует лиганды TGF-бета 1 и 2 и раскрыто в РСТ-публикации № WO 2012/167143.
[0869] В некоторых вариантах осуществления MBM вводят в комбинации с молекулой антитела к CD73. В одном варианте осуществления молекула антитела к CD73 представляет собой полную молекулу антитела или ее антигенсвязывающий фрагмент. В определенных вариантах осуществления молекула антитела к CD73 связывается с белком CD73 и снижает активность CD73, например, CD73 человека, например, подавляет ее или оказывает на нее антагонистическое действие.
[0870] В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO2016/075099. В одном варианте осуществления молекула антитела к CD73 представляет собой MEDI 9447, например, раскрытый в WO2016/075099. Альтернативные названия MEDI 9447 включают клон 10.3 или 73combo3. MEDI 9447 представляет собой антитело IgG1, которое подавляет активность CD73, например, оказывает на нее антагонистическое действие. MEDI 9447 и другие молекулы антител к CD73 также раскрыты в WO2016/075176 и US2016/0129108.
[0871] В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из MEDI 9477.
[0872] В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO2016/081748. В одном варианте осуществления молекула антитела к CD73 представляет собой 11F11, например, раскрытый в WO2016/081748. 11F11 представляет собой антитело IgG2, которое подавляет активность CD73, например, оказывает на нее антагонистическое действие. Антитела, полученные из 11F11, например, CD73.4 и CD73.10; клоны 11F11, например, 11F11-1 и 11F11-2; и другие молекулы антител к CD73 раскрыты в WO2016/081748 и US 9605080.
[0873] В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из 11F11-1 или 11F11-2.
[0874] В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое, например, в US 9605080.
[0875] В одном варианте осуществления молекула антитела к CD73 представляет собой CD73.4, например, раскрытый в US 9605080. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из CD73.4.
[0876] В одном варианте осуществления молекула антитела к CD73 представляет собой CD73.10, например, раскрытый в US 9605080. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из CD73.10.
[0877] В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO2009/0203538. В одном варианте осуществления молекула антитела к CD73 представляет собой 067-213, например, раскрытый в WO2009/0203538.
[0878] В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из 067-213.
[0879] В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в US 9090697. В одном варианте осуществления молекула антитела к CD73 представляет собой TY/23, например, раскрытый в US 9090697. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из TY/23.
[0880] В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO2016/055609. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в WO2016/055609.
[0881] В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO2016/146818. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в WO2016/146818.
[0882] В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO2004/079013. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в WO2004/079013.
[0883] В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO2012/125850. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в WO2012/125850.
[0884] В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO2015/004400. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в WO2015/004400.
[0885] В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в WO2007/146968. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в WO2007146968.
[0886] В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в US2007/0042392. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в US2007/0042392.
[0887] В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в US2009/0138977. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в US2009/0138977.
[0888] В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в Flocke et al., Eur J Cell Biol. 1992 Jun;58(1):62-70. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого в Flocke et al., Eur J Cell Biol. 1992 Jun;58(1):62-70.
[0889] В одном варианте осуществления молекула антитела к CD73 представляет собой антитело к CD73, раскрытое в Stagg et al., PNAS. 2010 Jan 107(4): 1547-1552. В некоторых вариантах осуществления молекула антитела к CD73 представляет собой TY/23 или TY11.8, раскрытый в Stagg et al. В одном варианте осуществления молекула антитела к CD73 содержит вариабельный домен тяжелой цепи, вариабельный домен легкой цепи или их оба из антитела к CD73, раскрытого у Stagg и соавт.
[0890] В некоторых вариантах осуществления MBM вводят в комбинации с ингибитором интерлейкина-17 (IL-17).
[0891] В некоторых вариантах осуществления ингибитор IL-17 представляет собой секукинумаб (регистрационный номер CAS: 875356-43-7 (тяжелая цепь) и 875356-44-8 (легкая цепь)). Секукинумаб также известен как AIN457 и COSENTYX®. Секукинумаб представляет собой рекомбинантное человеческое моноклональное антитело IgG1/κ, которое специфично связывается с IL-17A. Оно экспрессируется в рекомбинантной линии клеток яичника китайского хомячка (CHO). Секукинумаб описан, например, в WO 2006/013107, US 7807155, US 8119131, US 8617552 и EP 1776142.
[0892] В некоторых вариантах осуществления ингибитор IL-17 представляет собой CJM112. CJM112 также известен как XAB4. CJM112 представляет собой полностью человеческое моноклональное антитело (например, изотипа IgG1/κ), которое нацеливается на IL-17A. CJM112 раскрыт, например, в WO 2014/122613.
[0893] CJM112 может связываться с IL-17A человека, макака-крабоеда, мыши и крысы и нейтрализовать биологическую активность этих цитокинов in vitro и in vivo. IL-17A, представитель семейства IL-17, является главным провоспалительным цитокином, который, как было показано, играет важные роли при множестве иммуноопосредованных состояний, таких как псориаз и формы рака (Witowski et al. (2004) Cell Mol. Life Sci. p. 567-79; Miossec and Kolls (2012) Nat. Rev. Drug Discov. p. 763-76).
[0894] В некоторых вариантах осуществления ингибитор IL-17 представляет собой иксекизумаб (регистрационный номер CAS: 1143503-69-8). Иксекизумаб также известен как LY2439821. Иксекизумаб представляет собой гуманизированное моноклональное антитело IgG4, которое нацеливается на IL-17A. Иксекизумаб описан, например, в WO 2007/070750, US 7838638 и US 8110191.
[0895] В некоторых вариантах осуществления ингибитор IL-17 представляет собой бродалумаб (регистрационный номер CAS: 1174395-19-7). Бродалумаб также известен как AMG 827 или AM-14. Бродалумаб связывается с рецептором A интерлейкина-17 (IL-17RA) и предотвращает активацию рецептора, опосредованную IL-17. Бродалумаб раскрыт, например, в WO 2008/054603, US 7767206, US 7786284, US 7833527, US 7939070, US 8435518, US 8545842, US 8790648 и US 9073999.
[0896] В некоторых вариантах осуществления MBM вводят в комбинации с ингибитором интерлейкина-1-бета (IL-1β).
[0897] В некоторых вариантах осуществления ингибитор IL-1β представляет собой канакинумаб. Канакинумаб также известен как ACZ885 или ILARIS®. Канакинумаб представляет собой человеческое моноклональное антитело IgG1/κ, которое нейтрализует биологическую активность IL-1β человека. Канакинумаб раскрыт, например, в WO 2002/16436, US 7446175 и EP 1313769.
[0898] В некоторых вариантах осуществления MBM вводят в комбинации с ингибитором CD32B. В некоторых вариантах осуществления ингибитор CD32B представляет собой молекулу антитела к CD32B. Иллюстративные молекулы антитела к CD32B раскрыты в US 8187593, US 8778339, US 8802089, US 20060073142, US 20170198040 и US 20130251706.
[0899] В определенных вариантах осуществления MBM вводят в комбинации с одним из соединений, перечисленных в таблице 18.
Торговое наименование
US 2007/142401
WO 2005/039549
TASIGNA®
HCl • H2O
US 7169791 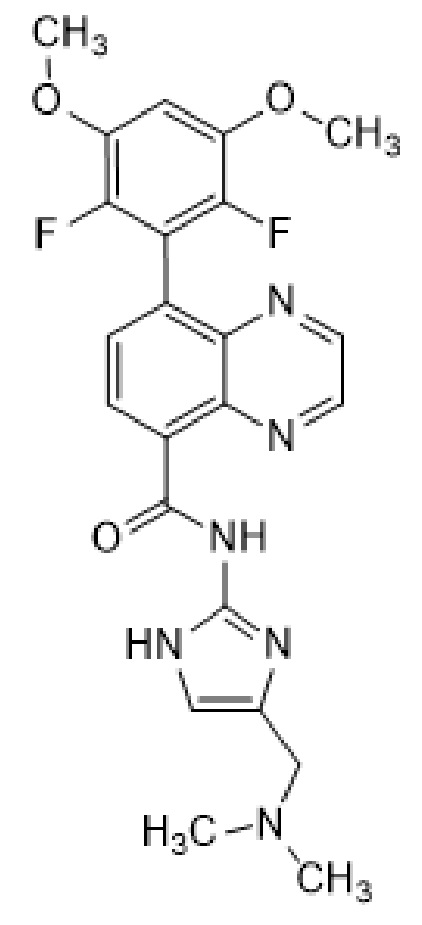
US 2010/0105667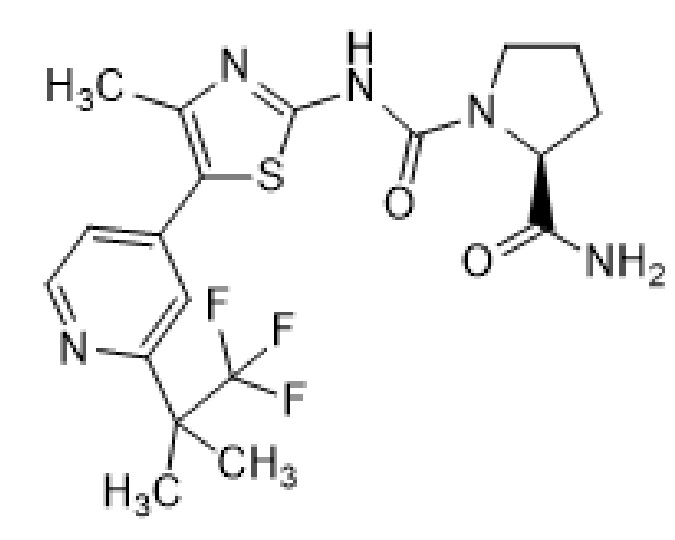
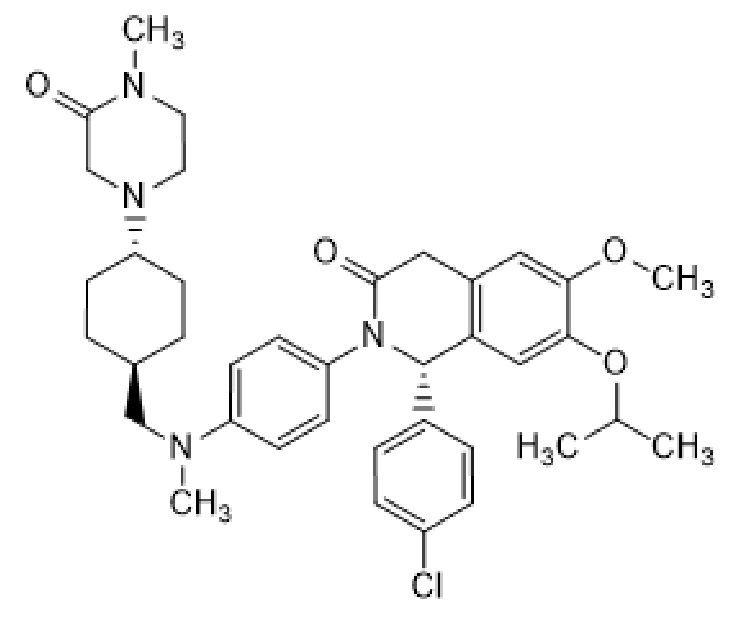
EXJADE®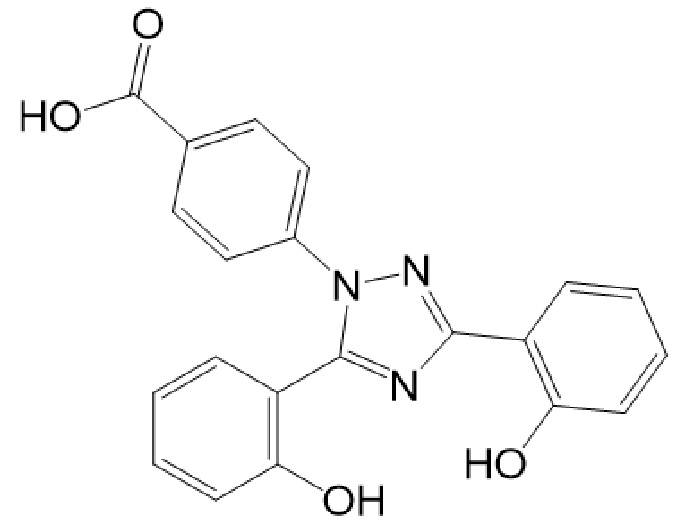
FEMARA®
GLEEVEC®
Мезилат
Дигидрохлоридная соль
US 7767675
US 8420645 H3PO4
H3PO4
WO 2002/022577
EP 1870399
ZYKADIA™ 
KISQALI®
US 8685980 
WO2008/106692
US 8735551
Линкер: SMCC (см. абзац [00117])
Полезная нагрузка: DM1 (см. абзац [00111])
См. также п. 29 формулы изобретения 
US 2012/252785
SIGNIFOR®
US 8519129 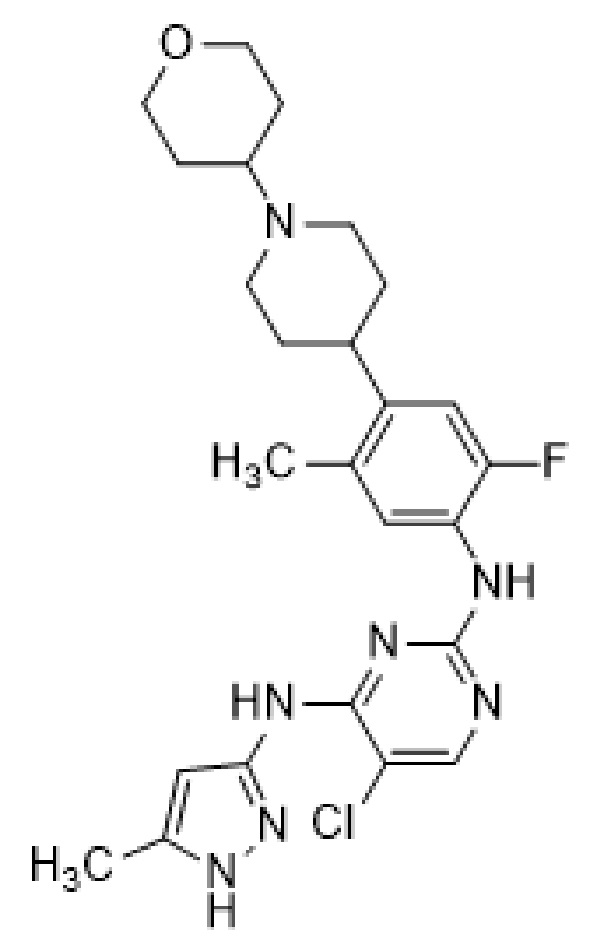
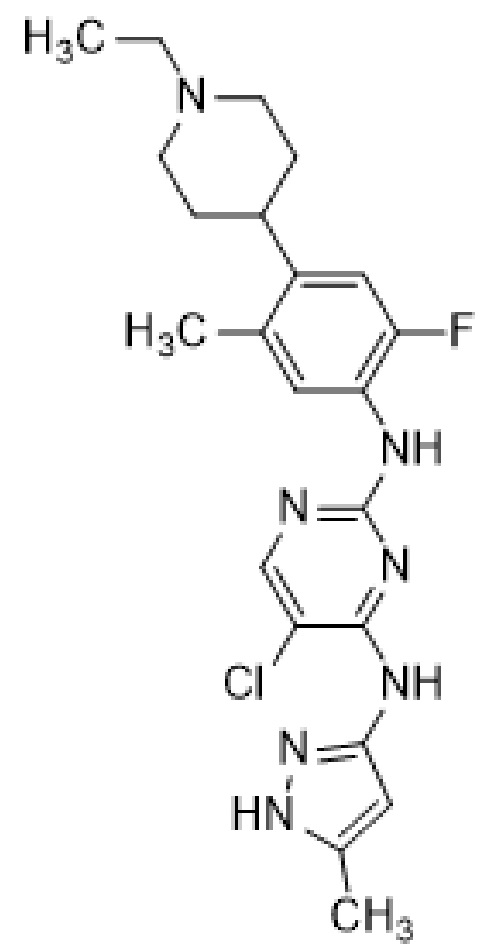
AMDRAY™ 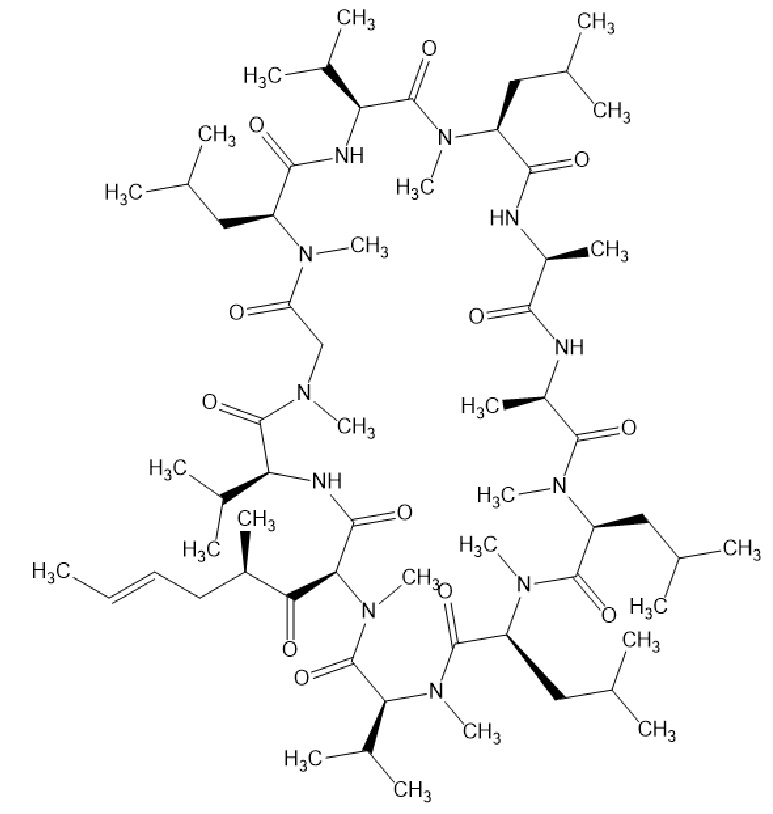
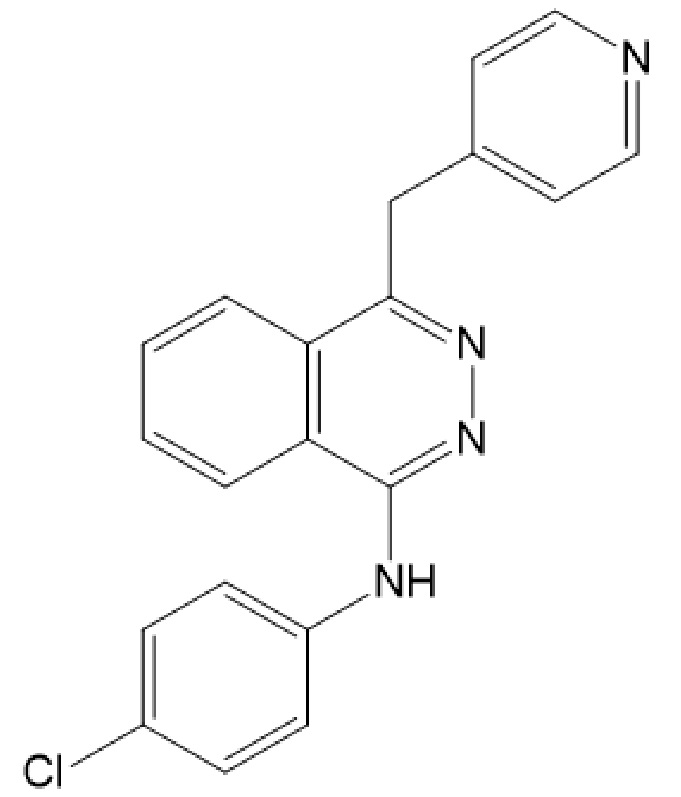
сукцинат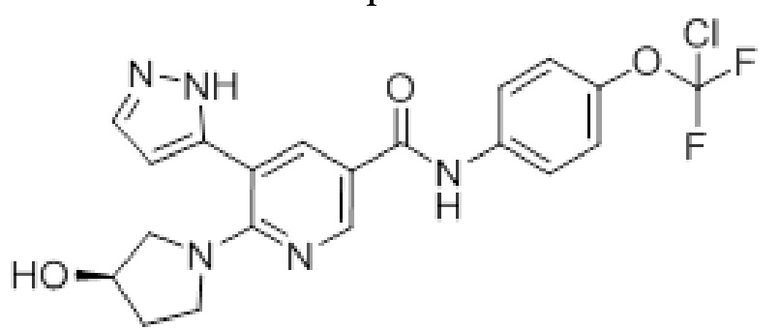
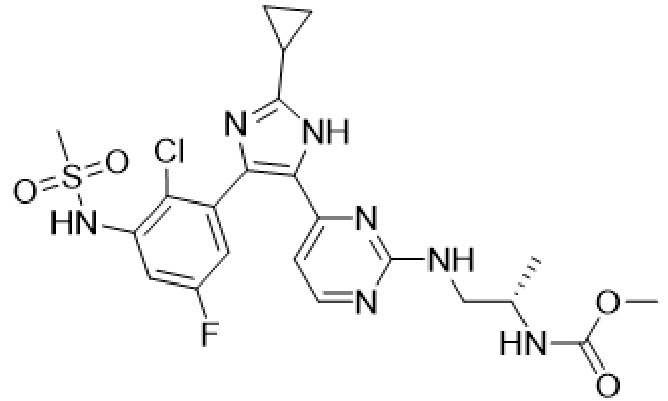
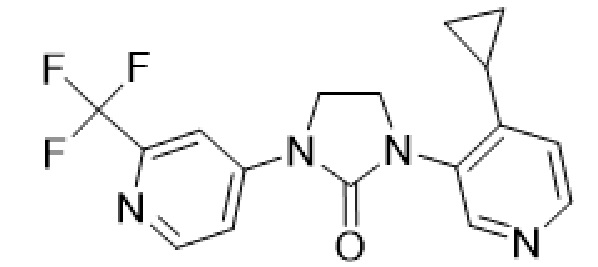
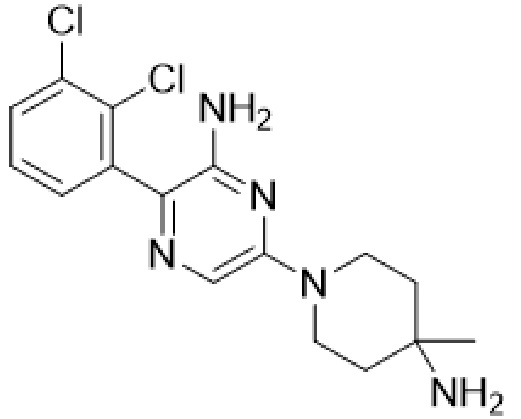
или его холиновая соль
US 7989497
WO2011/121418
US 8796284
US 7378423
US 7994185
EP 0029579
US 9580437
EP 3237418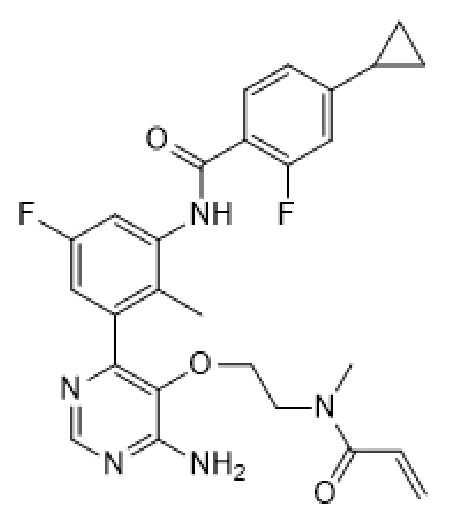
WO/2015/079417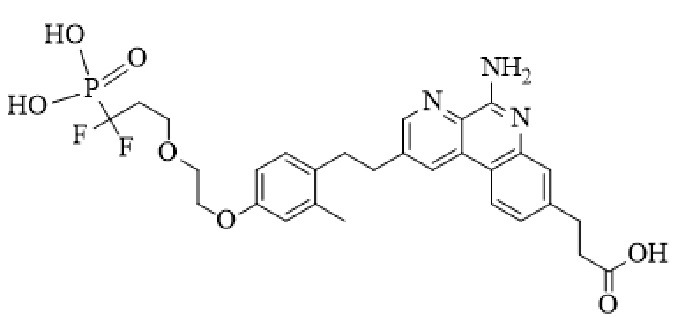
[0900] В некоторых вариантах осуществления MBM вводят в комбинации с одним или более из средства CAR-T-клеточной терапии, NIZ985, агониста GITR, такого как GWN323, PTK787, MBG453, mAb12425, CLR457, BGT226, BYL719, AMN107, ABL001, IDH305/LQS305, LJM716, MCS110, WNT974/LGK974, BLZ945, NIR178, QBM076, MBG453, CGS-20267, LHS534, LKG960, LDM099/SHP099, TNO155, LCL161, MAP855/LQN716, RAD001, LEJ511, LDK378, LOU064, LSZ102, LEQ506, RAF265/CHIR265, канакинумаба, гевокизумаба, анакинры, рилонацепта, CGS-20267, PSC833, GGP-57148B, CGM097, HDM201, LBH589, PKC412, LHC165, MAK683, INC280, INC424, LJE704, LAG525 и NIS793.
[0901] В некоторых вариантах осуществления MBM вводят в комбинации со стандартным лечением.
[0902] Стандартное лечение множественной миеломы и ассоциированных заболеваний включает химиотерапию, трансплантацию стволовых клеток (аутологичную или аллогенную), лучевую терапию и другие виды лекарственной терапии. Лекарственные средства, часто применяемые для лечения миеломы, включают алкилирующие средства (например, бендамустин, циклофосфамид и мелфалан), ингибиторы протеасом (например, бортезомиб), кортикостероиды (например, дексаметазон и преднизон) и иммуномодуляторы (например, талидомид и леналидомид или Revlimid®) или любую их комбинацию. Лекарственные средства из группы бисфосфонатов также часто вводят в комбинации со стандартными средствами лечения MM для предупреждения потери костной ткани. Пациенты старше 65-70 лет являются маловероятными кандидатами на трансплантацию стволовых клеток. В некоторых случаях возможными вариантами лечения для пациентов младше 60 лет с субоптимальным ответом на первую трансплантацию являются двойные трансплантации аутологичных стволовых клеток. Композиции и способы по настоящему изобретению можно применять в комбинации с любым из назначаемых в настоящее время средств лечения множественной миеломы.
[0903] Лимфому Ходжкина обычно лечат с помощью лучевой терапии, химиотерапии или трансплантации гемопоэтических стволовых клеток. Наиболее распространенным средством терапии неходжкинской лимфомы является режим R-CHOP, который состоит из четырех различных химиотерапевтических препаратов (циклофосфамид, доксорубицин, винкристин и преднизолон) и ритуксимаба (Rituxan®). Другие средства терапии, обычно применяемые для лечения NHL, включают другие химиотерапевтические средства, лучевую терапию, трансплантацию стволовых клеток (аутологичную или аллогенную трансплантацию костного мозга) или биологическую терапию, такую как иммунотерапия. Другие примеры биологических терапевтических средств включают без ограничения ритуксимаб (Rituxan®), тозитумомаб (Bexxar®), эпратузумаб (LymphoCide®) и алемтузумаб (MabCampath®). Композиции и способы по настоящему изобретению можно применять в комбинации с любым из назначаемых в настоящее время средств лечения лимфомы Ходжкина или неходжкинской лимфомы.
[0904] Стандартное лечение WM заключается в химиотерапии, в частности ритуксимабом (Rituxan®). Другие химиотерапевтические лекарственные средства, такие как хлорамбуцил (Leukeran®), циклофосфамид (Neosar®), флударабин (Fludara®), кладрибин (Leustatin®), винкристин и/или талидомид, можно применять в комбинации. Кортикостероиды, такие как преднизон, также можно вводить в комбинации с химиотерапией. Плазмаферез или замещение плазмы обычно применяют в ходе всего лечения пациента для облегчения некоторых симптомов посредством удаления парапротеина из крови. В некоторых случаях трансплантация стволовых клеток является вариантом лечения для некоторых пациентов.
[0905] MBM, имеющие ABM2, который связывается с CD3, можно вводить в комбинации со средством, которое снижает или ослабляет побочный эффект, ассоциированный с введением MBM, которая связывается с CD3. Побочные эффекты, ассоциированные с введением средств, связывающих CD3, могут включать без ограничения синдром высвобождения цитокинов ("CRS") и гемофагоцитарный лимфогистиоцитоз (HLH), также называемый синдромом активации макрофагов (MAS). Симптомы CRS могут включать высокую температуру, тошноту, преходящую гипотензию, гипоксию и т. п. CRS может включать клинические системные признаки и симптомы, такие как лихорадка, утомляемость, анорексия, виды миалгии, виды артралгии, тошнота, рвота и головная боль. CRS может включать клинические признаки и симптомы со стороны кожи, такие как сыпь. CRS может включать клинические признаки и симптомы со стороны желудочно-кишечного тракта, такие как тошнота, рвота и диарея. CRS может включать клинические признаки и симптомы со стороны дыхательной системы, такие как тахипноэ и гипоксемия. CRS может включать клинические признаки и симптомы со стороны сердечно-сосудистой системы, такие как тахикардия, "расширенное" пульсовое давление, гипотензия, повышенный сердечный выброс (ранний) и потенциально сниженный сердечный выброс (поздний). CRS может включать признаки и симптомы клинического свертывания крови, такие как повышенное содержание d-димера, гипофибриногенемия с кровотечением и без кровотечения. CRS может включать клинические признаки и симптомы со стороны почек, такие как азотемия. CRS может включать клинические признаки и симптомы со стороны печени, такие как трансаминит и гипербилирубинемия. CRS может включать клинические признаки и симптомы со стороны нервной системы, такие как головная боль, изменения психического состояния, спутанность, делирий, затруднения с подбором слов или явная афазия, галлюцинации, тремор, дисметрия, нарушение походки и судороги.
[0906] Соответственно, способы, описанные в данном документе, могут включать введение MBM, имеющей ABM2, который связывается с CD3, субъекту и дополнительное введение одного или более средств для контроля повышенных уровней растворимого фактора, появляющихся в результате лечения с помощью MBM. В одном варианте осуществления растворимый фактор, уровень которого повышен у субъекта, представляет собой одно или более из IFN-γ, TNFα, IL-2 и IL-6. В одном варианте осуществления фактор, уровень которого повышен у субъекта, представляет собой одно или более из IL-1, GM-CSF, IL-10, IL-8, IL-5 и фракталкина. Следовательно, средство, вводимое для лечения этого побочного эффекта, может представлять собой средство, которое нейтрализует один или более из этих растворимых факторов. В одном варианте осуществления средство, которое нейтрализует одну или более из этих растворимых форм, представляет собой антитело или его антигенсвязывающий фрагмент. Примеры таких средств включают без ограничения стероид (например, кортикостероид), ингибитор TNFα, ингибитор IL-1R и ингибитор IL-6. Примером ингибитора TNFα является молекула антитела к TNFα, такая как инфликсимаб, адалимумаб, цертолизумаб пегол и голимумаб. Другим примером ингибитора TNFα является слитый белок, такой как этанерцепт. Низкомолекулярный ингибитор TNFα включает без ограничения производные ксантина (например, пентоксифиллин) и бупропион. Примером ингибитора IL-6 является молекула антитела к IL-6, такая как тоцилизумаб (toc), сарилумаб, элсилимомаб, CNTO 328, ALD518/BMS-945429, CNTO 136, CPSI-2364, CDP6038, VX30, ARGX-109, FE301 и FM101. В одном варианте осуществления молекула антитела к IL-6 представляет собой тоцилизумаб. Примером ингибитора IL-1R является анакинра.
[0907] В некоторых вариантах осуществления субъекту вводят кортикостероид, такой как, например, среди прочего, метилпреднизолон, гидрокортизон. В некоторых вариантах осуществления субъекту вводят кортикостероид, например, метилпреднизолон, гидрокортизон, в комбинации с бенадрилом и тайленолом перед введением MBM, которая связывается с CD3, для уменьшения риска CRS.
[0908] В некоторых вариантах осуществления субъекту вводят сосудосуживающее средство, такое как, например, норэпинефрин, дофамин, фенилэфрин, эпинефрин, вазопрессин или любую их комбинацию.
[0909] В одном варианте осуществления субъекту могут вводить жаропонижающее средство. В одном варианте осуществления субъекту могут вводить аналгезирующее средство.
8. ПРИМЕРЫ
8.1. Пример 1. Получение и определение характеристик антител к BCMA
[0910] Антитела к BCMA, которые обладают перекрестной реактивностью с BCMA как человека, так и макака-крабоеда, идентифицировали с применением фагового дисплея. Созревание аффинности выбранного антитела, обозначенного как R1F2 в таблице 11, проводили для получения антител, обладающих увеличенной аффинностью к BCMA. Получали несколько дополнительных антител к BCMA, полученных из исходного антитела R1F2. Эти антитела обозначены как связывающие средства из "семейства AB1/AB2" в таблице 11. Другое антитело, идентифицированное в отдельности с применением фагового дисплея, обозначенное как PI-61 в таблице 11, также подвергали созреванию аффинности для получения клонов, обладающих увеличенной аффинностью к BCMA. Получали несколько дополнительных антител к BCMA, полученных из исходного антитела PI-61. Эти антитела обозначены как связывающие средства из "семейства AB3" в таблице 11.
[0911] Получали биспецифические антитела к BCMA x CD3, имеющие последовательности VH и VL из AB1, AB2 и AB3. Было обнаружено, что биспецифические антитела являются активными в анализах RTCC in vitro с BCMA+ линиями клеток множественной миеломы, и было обнаружено, что они обладают противоопухолевой активностью в ортотопической модели опухоли при множественной миеломе из клеток KMS11-Luc у мышей NSG.
8.2. Пример 2. Получение и определение характеристик TBM, связывающих BCMA, компонент комплекса TCR и CD2
[0912] Получали TBM, имеющие ABM для BCMA, содержащий последовательности VH и VL из AB3, ABM для TCR и ABM для CD2, в формате "выступ во впадину" (KIH), и определяли их характеристики. TBM из этого примера схематически показаны на фиг. 2A-2B. Каждая TBM в этом примере содержит первое полуантитело (схематически показанное как левая половина каждой конструкции, показанной на фиг. 2A-2B) и второе полуантитело (схематически показанное как правая половина каждой конструкции, показанной на фиг. 2A-2B). Не ограничиваясь какой-либо теорией, полагают, что комбинация взаимодействия с CD2 и комплексом TCR в TBM способна стимулировать как первичный сигнальный путь, который способствует лизису опухолевых клеток, опосредованному T-клетками (посредством кластеризации TCR, например), так и второй костимулирующий сигнальный путь для индукции пролиферации T-клеток и потенциального преодоления анергии.
8.2.1. Материалы и способы
8.2.1.1. Плазмиды, кодирующие TBM
[0913] Синтезировали плазмиды, кодирующие белки, для двух TBM, нацеливающихся на BCMA, компонент комплекса TCR и CD2.
[0914] Для первой TBM (схематически показанной на фиг. 2A) плазмиду, кодирующую кодон-оптимизированную тяжелую цепь антитела к BCMA, синтезировали в виде продукта слияния, содержащего (в направлении от N-конца к C-концу) (i) VH-домен AB3, слитый с константным CH1-доменом hIgG1, (ii) линкер, (iii) scFv для TCR, соответствующий BMA031, (iv) второй линкер и (v) Fc-участок hIgG1, содержащий мутации T366S, L368A и Y407V для получения "впадины" для облегчения гетеродимеризации TBM, а также мутации, обеспечивающие сайленсинг. Плазмиду, кодирующую легкую цепь, синтезировали в виде продукта слияния, содержащего (в направлении от N-конца к C-концу) VL-домен AB3 и последовательность константного участка лямбда-цепи человека. Плазмиду, кодирующую второе полуантитело, синтезировали в виде продукта слияния, содержащего (в направлении от N-конца к C-концу) (i) IgV-домен из CD58 (CD58-6), (ii) линкер и (iii) константный домен hIgG1, содержащий мутацию T366W для получения "выступа" для облегчения гетеродимеризации TBM, а также мутации, обеспечивающие сайленсинг.
[0915] Для второй TBM (схематически показанной на фиг. 2B) плазмиду, кодирующую кодон-оптимизированную тяжелую цепь антитела к BCMA, синтезировали в виде продукта слияния, содержащего (в направлении от N-конца к C-концу) (i) VH-домен AB3, слитый с константным CH1-доменом hIgG1, (ii) линкер, (iii) IgV-домен CD58 (CD58-6), (iv) второй линкер и (v) Fc-участок hIgG1, содержащий мутации T366S, L368A и Y407V для получения "впадины" для облегчения гетеродимеризации TBM, а также мутации, обеспечивающие сайленсинг. Плазмиду, кодирующую легкую цепь, синтезировали в виде продукта слияния, содержащего (в направлении от N-конца к C-концу) VL-домен AB3 и последовательность константного участка лямбда-цепи человека. Плазмиду, кодирующую второе полуантитело, синтезировали в виде продукта слияния, содержащего (в направлении от N-конца к C-концу) (i) scFv для TCR, соответствующий BMA031, (ii) линкер и (iii) константный домен hIgG1, содержащий мутацию T366W для получения "выступа" для облегчения гетеродимеризации TBM, а также мутации, обеспечивающие сайленсинг.
[0916] Также получали антитела с контрольной архитектурой для обеспечения возможности оценки влияния геометрических параметров ABM для BCMA и CD3 на функциональную активность. Получали конструкцию, соответствующую AB3_TCR-CD58, в которой ABM для CD2 был заменен на Vhh для лизоцима куриных яиц (AB3_TCR-HEL). Также получали одноплечевое антитело (OAA), соответствующее AB3_TCR-CD58, но не имеющее ABM для CD2, и соответствующее биспецифическое антитело, имеющее ABM для BCMA и ABM для CD3 в отдельных полуантителах (BSP).
[0917] Аминокислотные последовательности для компонентов TBM показаны в таблице 19-A (без последовательностей Fc) и в таблице 19-B (с последовательностями Fc).
Аминокислотные последовательности TBM
(последовательность Fc не показана)
(последовательность Fc не показана)
(последовательность Fc не показана)
(последовательность Fc не показана)
(последовательность Fc не показана)
(последовательность Fc не показана)
Аминокислотные последовательности TBM
(включая последовательность Fc)
(включая последовательность Fc)
(включая последовательность Fc)
(включая последовательность Fc)
(включая последовательность Fc)
(включая последовательность Fc)
8.2.1.2. Экспрессия и очистка
[0918] Обеспечивали транзиентную экспрессию TBM путем котрансфекции соответствующими цепями клеток HEK293. Вкратце, трансфекцию клеток плазмидами, кодирующими тяжелые и легкие цепи, проводили с использованием PEI в качестве реагента для трансфекции при конечном соотношении ДНК:PEI, составляющем 1:3. Для трансфекции культур, содержащих 2,0 миллиона клеток/мл сывороточной среды, использовали 1 мг плазмиды на литр культуры. После 5 дней экспрессии TBM собирали путем осветления среды посредством центрифугирования и фильтрации. Очистку выполняли с помощью аффинного связывания антител к CH1 в периодическом режиме (аффинная матрица для CH1 IgG CaptureSelect, Thermo-Fisher Scientific, Уолтем, Массачусетс, США) или связывания с белком A (сефароза rProteinA, для быстрого потока, GE Healthcare, Уппсала, Швеция) в периодическом режиме с использованием 1 мл смолы/100 мл надосадочной жидкости. Белку позволяли связываться на протяжении минимум 2 часов при осторожном перемешивании, и надосадочную жидкость загружали в колонку для гравитационной фильтрации. Смолу промывали с помощью 20-50 CV PBS. TBM элюировали с помощью 20 CV 50 мМ цитрата, 90 мМ NaCl при pH 3,2, 50 мМ сахарозы. Элюированные фракции TBM доводили до pH 5,5 с помощью 1 M цитрата натрия, 50 мM сахарозы. Выполняли препаративную эксклюзионную хроматографию с использованием колонки Hi Load 16/60 с Superdex 200 препаративной чистоты (GE Healthcare Life Sciences, Уппсала, Швеция) в качестве стадии заключительной доочистки, если присутствовали агрегаты. Чтобы подтвердить, что отличительные характеристики экспрессируемых белков TBM соответствуют прогнозируемым массам для первичных аминокислотных последовательностей, белки анализировали с помощью высокоэффективной жидкостной хроматографии в сочетании с масс-спектрометрией.
[0919] Аналогичным образом экспрессировали и очищали биспецифические конструкции.
8.2.1.3. Анализ RTCC
[0920] Триспецифические и биспецифические конструкции оценивали в отношении их потенциала индукции апоптоза, опосредованного T-клетками, в опухолевых клетках-мишенях. Вкратце, клетки-мишени KMS11, экспрессирующие huBCMA, конструировали так, чтобы они сверхэкспрессировали люциферазу светлячка. Клетки собирали и ресуспендировали в среде RPMI (Invitrogen, № 11875-093) с 10% FBS. В 384-луночный планшет с плоским дном высевали 2500 клеток-мишеней на лунку. Общую популяцию эффекторных T-клеток человека выделяли посредством отрицательного отбора (Stemcell Technologies, № 17951) из криоконсервированных PBMC, которые были отделены от лейкоцитарной массы (HemaCare, № PB001F-1) посредством центрифугирования в градиенте плотности фиколла. Затем очищенные Т-клетки добавляли в планшет до получения конечного соотношения Е:Т, составляющего 5:1, 3:1, 1:1, 1:3 или 1:5. Совместно культивируемые клетки инкубировали со всеми конструкциями и контролями в серии разведений. Для нормализации использовали среднее максимальное значение люминесценции, относящееся к клеткам-мишеням, совместно культивируемым с эффекторными клетками, но без какой-либо тестируемой конструкции. После инкубирования в течение 48 часов при 37°C с 5% CO2 в планшет добавляли субстрат люциферазы OneGlo (Promega, № E6120). Люминесценцию измеряли на планшет-ридере Envision после инкубирования в течение 10 минут. Процент специфического лизиса рассчитывали с помощью следующего уравнения:
специфический лизис (%)=(1 - (люминесценция образца/средняя максимальная люминесценция)) * 100
8.2.1.4. Анализ высвобождения цитокинов
[0921] Триспецифические конструкции анализировали в отношении их способности индуцировать секрецию цитокинов de novo, опосредованную Т-клетками, в присутствии опухолевых клеток-мишеней. Вкратце, клетки-мишени KMS11, экспрессирующие huBCMA, конструировали так, чтобы они сверхэкспрессировали люциферазу светлячка. Клетки собирали и ресуспендировали в среде RPMI (Invitrogen, № 11875-093) с 10% FBS. В 96-луночный планшет с плоским дном высевали 10000 клеток-мишеней на лунку. Общую популяцию эффекторных T-клеток человека выделяли посредством отрицательного отбора (StemCell Technologies, № 17951) из криоконсервированных PBMC, которые были отделены от лейкоцитарной массы (HemaCare, № PB001F-1) посредством центрифугирования в градиенте плотности фиколла. Затем очищенные Т-клетки добавляли в планшет до получения конечного соотношения Е:Т, составляющего 5:1, 1:1 либо 1:5. Совместно культивируемые клетки инкубировали со всеми конструкциями и контролями в серии разведений. После инкубирования в течение 24 часов при 37°C с 5% CO2 образцы надосадочной жидкости собирали посредством центрифугирования при 300 x g в течение 5 мин для последующего анализа. Мультиплексный ELISA проводили в соответствии с инструкциями производителя с применением панели 1 для анализа провоспалительных цитокинов из набора V-PLEX (MesoScale Discovery, № K15049D).
8.2.2. Результаты
[0922] Данные о RTCC показаны на фиг. 3A-E, и уровни цитокинов показаны на фиг. 4A-C. Каждая из конструкций была активной в анализе RTCC.
8.3. Пример 3. Получение и определение характеристик TBM, связывающих BCMA, CD3 и CD2
[0923] Получали TBM, нацеливающиеся на BCMA, CD3 и CD2, в формате "выступ во впадину" (KIH), и определяли их характеристики в соответствии с материалами и способами, описанными в примере 2, за исключением того, что ABM для TCR в конструкциях из примера 2 заменяли на последовательности средств, связывающих CD3, как показано в таблице 20-A (без последовательностей Fc) и таблице 20-B (с последовательностями Fc).
Аминокислотные последовательности TBM
(последовательность Fc не показана)
(последовательность Fc не показана)
(последовательность Fc не показана)
(последовательность Fc не показана)
(последовательность Fc не показана)
(последовательность Fc не показана)
Аминокислотные последовательности TBM
(включая последовательность Fc)
(включая последовательность Fc)
(включая последовательность Fc)
(включая последовательность Fc)
(включая последовательность Fc)
(включая последовательность Fc)
[0924] Анализы RTCC и высвобождения цитокинов проводили согласно примеру 2. Триспецифические конструкции являются активными в анализе RTCC.
8.4. Пример 4. Конструирование CD58 для улучшения стабильности
8.4.1. Предпосылки
[0925] CD58 человека содержит сигнальный пептид из 29 аминокислот и два Ig-подобных домена. Ближайший к N-концу Ig-подобный домен, называемый доменом 1, относится к V-типу и сходен с вариабельным участком антитела, а второй домен, называемый доменом 2, относится к C-типу и сходен с константными участками антитела. Схематический обзор структуры доменов CD58 показан на фиг. 5.
[0926] Как проиллюстрировано в примере 2, домен 1 CD58, который взаимодействует с CD2, можно использовать вместо связывающего фрагмента антитела к CD2 в полиспецифических связывающих молекулах. Однако CD58 демонстрирует более низкую стабильность, чем иммуноглобулины.
[0927] Чтобы улучшить стабильность домена 1 CD58 человека, белок конструировали так, чтобы он содержал пару остатков цистеина, которые при экспрессии образуют дисульфидный мостик для стабилизации молекулы.
[0928] Конструировали замены остатками цистеина четырех разных пар аминокислот: (1) V45 и M105, (2) V45 и M114, (3) V54 и G88 и (4) W56 и L90.
8.4.2. Материалы и способы
8.4.2.1. Рекомбинантная экспрессия
[0929] Для оценки связывания и биофизических характеристик варианты CD58 с дисульфидными связями получали путем транзиентной экспрессии и очищали из клеток HEK293 вместе с внеклеточным доменом CD2. Все плазмиды подвергали оптимизации кодонов для экспрессии у млекопитающих. Конструкции CD2 человека и макака-крабоеда получали с C-концевой меткой Avi-Tag и N-концевой меткой 8xHis (SEQ ID NO: 564), за которыми следует последовательность EVNLYFQS (SEQ ID NO: 565) для отщепления His-метки после очистки. Конструкции CD2 подвергали сайт-селективному биотинилированию в ходе экспрессии посредством котрансфекции плазмиды, кодирующей фермент BirA. CD58 экспрессировался с C-концевой меткой 8xHis (SEQ ID NO: 564). Транзиентную экспрессию и очистку в клетках HEK293F проводили по стандартной методике. Последовательности показаны в таблице 21.
[0930] Для экспрессии трансфекцию проводили с использованием PEI в качестве реагента для трансфекции. Для осуществления трансфекций в небольших масштабах (< 5 л) клетки выращивали во встряхиваемых колбах на орбитальном шейкере (100 об./мин) в увлажненном инкубаторе (85%) при 8% CO2. Трансфекцию проводили при соотношении 1 ДНК: 3 PEI. Использовали 1 мг/л культуры плазмид для трансфекции при 2,0 миллиона клеток/мл в среде Expi293. После 5 дней экспрессии культуру центрифугировали и фильтровали. Очистку проводили путем связывания с никель-NTA в периодическом режиме с использованием 1 мл смолы/100 мл надосадочной жидкости. Белку позволяли связываться на протяжении минимум 2 часов при осторожном перемешивании, и смесь загружали в колонку для гравитационной фильтрации. Смолу промывали с помощью 30 CV PBS. Белки элюировали имидазолом. Элюированный белок концентрировали и подвергали заключительной очистке посредством препаративной эксклюзионной хроматографии (колонка Hi Load 16/60 с Superdex 75 препаративной чистоты, GE Healthcare Life Sciences, Упсала, Швеция). Чтобы подтвердить, что отличительные характеристики экспрессируемых белков соответствуют прогнозируемым массам для первичных аминокислотных последовательностей, белки анализировали с помощью высокоэффективной жидкостной хроматографии в сочетании с масс-спектрометрией.
8.4.2.2. Стабильность
[0931] Варианты, стабилизированные дисульфидными связями, оценивали в отношении улучшенной термической стабильности с помощью как дифференциальной сканирующей калориметрии (DSC), так и дифференциальной сканирующей флуориметрии (DSF) с использованием стандартных методик. Для DSF 1-3 мкг каждой конструкции добавляли к 1x Sypro оранжевого (Thermo-Fisher) в общем объеме 25 мкл в 96-луночном планшете для ПЦР. Используя систему для RT-PCR Bio-Rad CFX96, оснащенную термоциклером C1000, температуру увеличивали с 25°C до 95°C со скоростью 0,5°C/мин, и отслеживали флуоресценцию. Для определения Tm использовали программное обеспечение, поставляемое производителем.
[0932] Для DSC все образцы подвергали диализу в солевом растворе с HEPES-буфером (HBS) и разбавляли до конечной концентрации 0,5 мг/мл. Tm и T начала определяли с использованием системы для DSC MicroCal VP-Capillary (Malvern) путем увеличения температуры с 25°C до 100°C со скоростью 1°C/мин с периодом фильтрации 2 секунды и настройкой среднего усиления.
8.4.2.3. Аффинность связывания
[0933] Чтобы убедиться в том, что аффинность связывания остается ненарушенной при добавлении изменения в виде стабилизирующей дисульфидной связи, проводили изотермическую калориметрию (ITC) получаемых рекомбинантных белков CD58 для определения их кажущейся KD и стехиометрических характеристик связывания (n) с рекомбинантным CD2 человека.
[0934] Вкратце, рекомбинантный CD2 человека и рекомбинантные варианты CD58 человека подвергали диализу в солевом растворе с HEPES-буфером (HBS). CD2 разбавляли до конечной концентрации 100 мкМ, варианты CD58 разбавляли до 10 мкМ. CD2 постепенно прибавляли к 10 мкМ вариантов CD58 путем нескольких введений, и определяли δH (ккал/моль) с использованием калориметра для изотермического титрования MicroCal VP-ITC (Malvern). Постепенное прибавление CD2 к HBS использовали в качестве эталона, и KD и n определяли из полученных данных.
8.4.3. Результаты
[0935] Результаты измерений как DSF, так и DSC для конструкций показаны в таблице 22 ниже.
[0936] Результаты исследований аффинности показаны в таблице 23 ниже. Добавление стабилизирующих дисульфидных связей не оказало пагубного влияния на аффинность или стехиометрические характеристики связывания.
9. КОНКРЕТНЫЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ, ЦИТИРОВАНИЕ ЛИТЕРАТУРНЫХ ИСТОЧНИКОВ
[0937] Хотя были проиллюстрированы и описаны различные конкретные варианты осуществления, следует понимать, что различные изменения могут быть осуществлены без отступления от сущности и объема настоящего изобретения. Настоящее изобретение проиллюстрировано на примерах с помощью пронумерованных вариантов осуществления, изложенных ниже.
1. Полиспецифическая связывающая молекула (MBM), содержащая:
(a) антигенсвязывающий модуль 1 (ABM1), который специфично связывается с ВСМА человека и содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 11A-1, таблице 11B-1, таблице 11C-1, таблице 11D-1, таблице 11E-1, таблице 11F-1, таблице 11G-1, таблице 11H-1, таблице 11I-1, таблице 11J-1, таблице 11K-1(a), таблице 11K-1(b), таблице 11L-1, таблице 11M-1, таблице 11N-1(a) или таблице 11N-1(b), и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 11A-2, таблице 11B-2, таблице 11C-2, таблице 11D-2, таблице 11E-2, таблице 11F-2, таблице 11G-2, таблице 11H-2, таблице 11I-2, таблице 11J-2, таблице 11K-2, таблице 11K-2, таблице 11L-2, таблице 11M-2, таблице 11N-2 или таблице 11N-2 соответственно;
(b) антигенсвязывающий модуль 2 (ABM2), который специфично связывается с компонентом T-клеточного рецепторного комплекса (TCR) человека; и
(c) антигенсвязывающий модуль 3 (ABM3), который специфично связывается с CD2 человека или опухолеассоциированным антигеном (TAA) человека.
2. MBM согласно варианту осуществления 1, где ABM1 содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 11A-1, таблице 11B-1, таблице 11C-1, таблице 11D-1, таблице 11E-1, таблице 11F-1, таблице 11G-1, таблице 11H-1, таблице 11I-1, таблице 11J-1, таблице 11K-1(a), таблице 11L-1, таблице 11M-1 или таблице 11N-1(a), и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 11A-2, таблице 11B-2, таблице 11C-2, таблице 11D-2, таблице 11E-2, таблице 11F-2, таблице 11G-2, таблице 11H-2, таблице 11I-2, таблице 11J-2, таблице 11K-2, таблице 11L-2, таблице 11M-2 или таблице 11N-2 соответственно.
3. MBM согласно варианту осуществления 1 или варианту осуществления 2, где ABM1 содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 11A-1, и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 11A-2.
4. MBM согласно варианту осуществления 1 или варианту осуществления 2, где ABM1 содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 11B-1, и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 11B-2.
5. MBM согласно варианту осуществления 1 или варианту осуществления 2, где ABM1 содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 11C-1, и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 11C-2.
6. MBM согласно варианту осуществления 1 или варианту осуществления 2, где ABM1 содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 11D-1, и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 11D-2.
7. MBM согласно варианту осуществления 1 или варианту осуществления 2, где ABM1 содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 11E-1, и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 11E-2.
8. MBM согласно варианту осуществления 1 или варианту осуществления 2, где ABM1 содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 11F-1, и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 11F-2.
9. MBM согласно варианту осуществления 1 или варианту осуществления 2, где ABM1 содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 11G-1, и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 11G-2.
10. MBM согласно варианту осуществления 1 или варианту осуществления 2, где ABM1 содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 11H-1, и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 11H-2.
11. MBM согласно варианту осуществления 1 или варианту осуществления 2, где ABM1 содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 11I-1, и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 11I-2.
12. MBM согласно варианту осуществления 1 или варианту осуществления 2, где ABM1 содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 11J-1, и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 11J-2.
13. MBM согласно варианту осуществления 1 или варианту осуществления 2, где ABM1 содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 11K-1(a), и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 11K-2.
14. MBM согласно варианту осуществления 1, где ABM1 содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 11K-1(b), и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 11K-2.
15. MBM согласно варианту осуществления 1 или варианту осуществления 2, где ABM1 содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 11L-1, и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 11L-2.
16. MBM согласно варианту осуществления 1 или варианту осуществления 2, где ABM1 содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 11M-1, и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 11M-2.
17. MBM согласно варианту осуществления 1 или варианту осуществления 2, где ABM1 содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 11N-1(a), и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 11N-2.
18. MBM согласно варианту осуществления 1, где ABM1 содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице 11N-1(b), и соответствующие последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице 11N-2.
19. MBM согласно варианту осуществления 3, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C1.
20. MBM согласно варианту осуществления 3, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C2.
21. MBM согласно варианту осуществления 3, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C3.
22. MBM согласно варианту осуществления 3, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C4.
23. MBM согласно варианту осуществления 3, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C5.
24. MBM согласно варианту осуществления 3, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C6.
25. MBM согласно варианту осуществления 3, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C7.
26. MBM согласно варианту осуществления 3, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C8.
27. MBM согласно варианту осуществления 3, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C9.
28. MBM согласно варианту осуществления 3, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C10.
29. MBM согласно варианту осуществления 3, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C11.
30. MBM согласно варианту осуществления 3, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C12.
31. MBM согласно варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C13.
32. MBM согласно варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C14.
33. MBM согласно варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C15.
34. MBM согласно варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C16.
35. MBM согласно варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C17.
36. MBM согласно варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C18.
37. MBM согласно варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C19.
38. MBM согласно варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C20.
39. MBM согласно варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C21.
40. MBM согласно варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C22.
41. MBM согласно варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C23.
42. MBM согласно варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C24.
43. MBM согласно варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C25.
44. MBM согласно варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C26.
45. MBM согласно варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C27.
46. MBM согласно варианту осуществления 4, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из C28.
47. MBM согласно любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из AB1.
48. MBM согласно любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из AB2.
49. MBM согласно любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из R1F2.
50. MBM согласно любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF03.
51. MBM согласно любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF04.
52. MBM согласно любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF05.
53. MBM согласно любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF06.
54. MBM согласно любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF07.
55. MBM согласно любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF08.
56. MBM согласно любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF09.
57. MBM согласно любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF12.
58. MBM согласно любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF13.
59. MBM согласно любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF14.
60. MBM согласно любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF15.
61. MBM согласно любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF16.
62. MBM согласно любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF17.
63. MBM согласно любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF18.
64. MBM согласно любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF19.
65. MBM согласно любому из вариантов осуществления 5-10, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PALF20.
66. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из AB3.
67. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из PI-61.
68. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H2/L2-22.
69. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H2/L2-88.
70. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H2/L2-36.
71. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H2/L2-34.
72. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H2/L2-68.
73. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H2/L2-18.
74. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H2/L2-47.
75. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H2/L2-20.
76. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H2/L2-80.
77. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H2/L2-83.
78. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-1.
79. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-2.
80. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-3.
81. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-4.
82. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-5.
83. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-6.
84. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-7.
85. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-8.
86. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-9.
87. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-10.
88. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-11.
89. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-12.
90. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-13.
91. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-14.
92. MBM согласно любому из вариантов осуществления 11-18, где последовательности CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3 представляют собой последовательности из H3-15.
93. MBM согласно варианту осуществления 1 или варианту осуществления 2, где ABM1 содержит последовательность вариабельного участка легкой цепи, представленную в таблице 11O-1, и соответствующую последовательность вариабельного участка тяжелой цепи, представленную в таблице 11O-2.
94. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из AB1.
95. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из AB2.
96. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из AB3.
97. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из R1F2.
98. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF03.
99. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF04.
100. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF05.
101. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF06.
102. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF07.
103. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF08.
104. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF09.
105. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF12.
106. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF13.
107. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF14.
108. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF15.
109. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF16.
110. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF17.
111. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF18.
112. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF19.
113. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PALF20.
114. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из PI-61.
115. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H2/L2-88.
116. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H2/L2-36.
117. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H2/L2-34.
118. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H2/L2-68.
119. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H2/L2-18.
120. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H2/L2-47.
121. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H2/L2-20.
122. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H2/L2-80.
123. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H2/L2-83.
124. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-1.
125. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-2.
126. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-3.
127. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-4.
128. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-5.
129. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-6.
130. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-7.
131. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-8.
132. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-9.
133. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-10.
134. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-11.
135. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-12.
136. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-13.
137. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-14.
138. MBM согласно варианту осуществления 93, где последовательность вариабельного участка легкой цепи и соответствующая последовательность вариабельного участка тяжелой цепи представляют собой последовательности из H3-15.
139. MBM согласно любому из вариантов осуществления 1-138, где ABM1 представляет собой антитело, фрагмент антитела, scFv, dsFv, Fv, Fab, scFab, (Fab’)2 или однодоменное антитело (SDAB).
140. МBM согласно варианту осуществления 139, где ABM1 содержит антитело или его антигенсвязывающий домен.
141. МBM согласно варианту осуществления 139, где ABM1 содержит scFv.
142. MBM согласно варианту осуществления 141, где scFv ABM1 содержит последовательность, представленную в таблице 11P.
143. MBM согласно любому из вариантов осуществления 1-142, где ABM2 представляет собой ABM на основе неиммуноглобулиновой каркасной структуры.
144. MBM согласно варианту осуществления 143, где ABM2 представляет собой домен Куница, аднексин, аффитело, дарпин, авимер, антикалин, липокалин, центирин, версатело, ноттин, аднектин, пронектин, аффитин/нанофитин, аффилин, атример/тетранектин, бициклический пептид, цистиновый узел, каркасную структуру Fn3, O-тело, Tn3, аффимер, BD, адгирон, дуокалин, альфатело, белок с повторами Armadillo, репетело или финомер.
145. MBM согласно любому из вариантов осуществления 1-142, где ABM2 представляет собой ABM на основе иммуноглобулиновой каркасной структуры.
146. MBM согласно варианту осуществления 145, где ABM2 представляет собой антитело, фрагмент антитела, scFv, dsFv, Fv, Fab, scFab, (Fab’)2, однодоменное антитело (SDAB), VH- или VL-домен или VHH-домен верблюдовых.
147. МBM согласно варианту осуществления 146, где ABM2 представляет собой антитело или его антигенсвязывающий домен.
148. МBM согласно варианту осуществления 146, где ABM2 представляет собой scFv.
149. МBM согласно варианту осуществления 146, где ABM2 представляет собой Fab.
150. МBM согласно варианту осуществления 149, где ABM2 представляет собой гетеродимер Fab.
151. MBM согласно любому из вариантов осуществления 1-150, где компонент комплекса TCR представляет собой CD3.
152. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-1.
153. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-2.
154. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-3.
155. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-4.
156. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-5.
157. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-6.
158. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-7.
159. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-8.
160. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-9.
161. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-10.
162. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-11.
163. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-12.
164. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-13.
165. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-14.
166. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-15.
167. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-16.
168. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-17.
169. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-18.
170. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-19.
171. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-20.
172. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-21.
173. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-22.
174. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-23.
175. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-24.
176. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-25.
177. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-26.
178. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-27.
179. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-28.
180. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-29.
181. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-30.
182. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-31.
183. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-32.
184. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-33.
185. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-34.
186. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-35.
187. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-36.
188. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-37.
189. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-38.
190. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-39.
191. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-40.
192. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-41.
193. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-42.
194. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-43.
195. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-44.
196. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-45.
197. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-46.
198. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-47.
199. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-48.
200. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-49.
201. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-50.
202. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-51.
203. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-52.
204. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-53.
205. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-54.
206. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-55.
207. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-56.
208. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-57.
209. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-58.
210. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-59.
211. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-60.
212. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-61.
213. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-62.
214. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-63.
215. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-64.
216. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-65.
217. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-66.
218. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-67.
219. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-68.
220. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-69.
221. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-70.
222. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-71.
223. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-72.
224. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-73.
225. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-74.
226. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-75.
227. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-76.
228. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-77.
229. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-78.
230. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-79.
231. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-80.
232. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-81.
233. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-82.
234. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-83.
235. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-84.
236. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-85.
237. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-86.
238. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-87.
239. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-88.
240. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-89.
241. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-90.
242. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-91.
243. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-92.
244. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-93.
245. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-94.
246. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-95.
247. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-96.
248. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-97.
249. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-98.
250. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-99.
251. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-100.
252. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-101.
253. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-102.
254. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-103.
255. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-104.
256. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-105.
257. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-106.
258. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-107.
259. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-108.
260. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-109.
261. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-110.
262. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-111.
263. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-112.
264. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-113.
265. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-114.
266. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-115.
267. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-116.
268. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-117.
269. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-118.
270. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-119.
271. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-120.
272. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-121.
273. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-122.
274. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-123.
275. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-124.
276. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-125.
277. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-126.
278. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-127.
279. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-128.
280. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-129.
281. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR из CD3-130.
282. MBM согласно любому из вариантов осуществления 152-281, где CDR определены согласно нумерации по Kabat, как представлено в таблице 12B.
283. MBM согласно любому из вариантов осуществления 152-281, где CDR определены согласно нумерации по Chothia, как представлено в таблице 12C.
284. MBM согласно любому из вариантов осуществления 152-281, где CDR определены согласно комбинации нумераций по Kabat и по Chothia, как представлено в таблице 12D.
285. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-1, представленные в таблице 12A.
286. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-2, представленные в таблице 12A.
287. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-3, представленные в таблице 12A.
288. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-4, представленные в таблице 12A.
289. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-5, представленные в таблице 12A.
290. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-6, представленные в таблице 12A.
291. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-7, представленные в таблице 12A.
292. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-8, представленные в таблице 12A.
293. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-9, представленные в таблице 12A.
294. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-10, представленные в таблице 12A.
295. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-11, представленные в таблице 12A.
296. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-12, представленные в таблице 12A.
297. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-13, представленные в таблице 12A.
298. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-14, представленные в таблице 12A.
299. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-15, представленные в таблице 12A.
300. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-16, представленные в таблице 12A.
301. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-17, представленные в таблице 12A.
302. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-18, представленные в таблице 12A.
303. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-19, представленные в таблице 12A.
304. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-20, представленные в таблице 12A.
305. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-21, представленные в таблице 12A.
306. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-22, представленные в таблице 12A.
307. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-23, представленные в таблице 12A.
308. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-24, представленные в таблице 12A.
309. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-25, представленные в таблице 12A.
310. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-26, представленные в таблице 12A.
311. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-27, представленные в таблице 12A.
312. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-28, представленные в таблице 12A.
313. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-129, представленные в таблице 12A.
314. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD3-130, представленные в таблице 12A.
315. MBM согласно варианту осуществления 151, где ABM2 содержит аминокислотную последовательность scFv, обозначенного как CD3-12 в таблице 12A.
316. MBM согласно варианту осуществления 151, где ABM2 содержит аминокислотную последовательность scFv, обозначенного как CD3-21 в таблице 12A.
317. MBM согласно варианту осуществления 151, где ABM2 содержит аминокислотную последовательность scFv, обозначенного как CD3-22 в таблице 12A.
318. MBM согласно варианту осуществления 151, где ABM2 содержит аминокислотную последовательность scFv, обозначенного как CD3-23 в таблице 12A.
319. MBM согласно варианту осуществления 151, где ABM2 содержит аминокислотную последовательность scFv, обозначенного как CD3-24 в таблице 12A.
320. MBM согласно варианту осуществления 151, где ABM2 содержит аминокислотную последовательность scFv, обозначенного как CD3-25 в таблице 12A.
321. MBM согласно варианту осуществления 151, где ABM2 содержит аминокислотную последовательность scFv, обозначенного как CD3-26 в таблице 12A.
322. MBM согласно варианту осуществления 151, где ABM2 содержит аминокислотную последовательность scFv, обозначенного как CD3-27 в таблице 12A.
323. MBM согласно варианту осуществления 151, где ABM2 содержит аминокислотную последовательность scFv, обозначенного как CD3-28 в таблице 12A.
324. MBM согласно варианту осуществления 151, где ABM2 содержит аминокислотную последовательность scFv, обозначенного как CD3-129 в таблице 12A.
325. MBM согласно варианту осуществления 151, где ABM2 содержит аминокислотную последовательность scFv, обозначенного как CD3-130 в таблице 12A.
326. MBM согласно варианту осуществления 151, где ABM2 содержит последовательность CDR-H1, последовательность CDR-H2, последовательность CDR-H3, последовательность CDR-L1, последовательность CDR-L2 и последовательность CDR-L3, представленные в таблице AA, таблице AB или таблице AC.
327. MBM согласно варианту осуществления 326, где ABM2 содержит последовательность CDR-H1, последовательность CDR-H2, последовательность CDR-H3, последовательность CDR-L1, последовательность CDR-L2 и последовательность CDR-L3, представленные в таблице AA.
328. MBM согласно варианту осуществления 327, где аминокислота, обозначенная как X1 в таблице AA, представляет собой T.
329. MBM согласно варианту осуществления 327, где аминокислота, обозначенная как X1 в таблице AA, представляет собой A.
330. MBM согласно любому из вариантов осуществления 327-329, где аминокислота, обозначенная как X2 в таблице AA, представляет собой S.
331. MBM согласно любому из вариантов осуществления 327-329, где аминокислота, обозначенная как X2 в таблице AA, представляет собой R.
332. MBM согласно любому из вариантов осуществления 327-331, где аминокислота, обозначенная как X3 в таблице AA, представляет собой N.
333. MBM согласно любому из вариантов осуществления 327-331, где аминокислота, обозначенная как X3 в таблице AA, представляет собой Y.
334. MBM согласно любому из вариантов осуществления 327-331, где аминокислота, обозначенная как X3 в таблице AA, представляет собой Q.
335. MBM согласно любому из вариантов осуществления 327-334, где аминокислота, обозначенная как X4 в таблице AA, представляет собой H.
336. MBM согласно любому из вариантов осуществления 327-334, где аминокислота, обозначенная как X4 в таблице AA, представляет собой S.
337. MBM согласно любому из вариантов осуществления 327-336, где аминокислота, обозначенная как X5 в таблице AA, представляет собой M.
338. MBM согласно любому из вариантов осуществления 327-336, где аминокислота, обозначенная как X5 в таблице AA, представляет собой L.
339. MBM согласно любому из вариантов осуществления 327-338, где аминокислота, обозначенная как X6 в таблице AA, представляет собой K.
340. MBM согласно любому из вариантов осуществления 327-338, где аминокислота, обозначенная как X6 в таблице AA, представляет собой R.
341. MBM согласно любому из вариантов осуществления 327-340, где аминокислота, обозначенная как X7 в таблице AA, представляет собой S.
342. MBM согласно любому из вариантов осуществления 327-340, где аминокислота, обозначенная как X7 в таблице AA, представляет собой K.
343. MBM согласно любому из вариантов осуществления 327-342, где аминокислота, обозначенная как X55 в таблице AA, представляет собой F.
344. MBM согласно любому из вариантов осуществления 327-342, где аминокислота, обозначенная как X55 в таблице AA, представляет собой Y.
345. MBM согласно любому из вариантов осуществления 327-342, где аминокислота, обозначенная как X55 в таблице AA, представляет собой S.
346. MBM согласно любому из вариантов осуществления 327-345, где аминокислота, обозначенная как X8 в таблице AA, представляет собой W.
347. MBM согласно любому из вариантов осуществления 327-345, где аминокислота, обозначенная как X8 в таблице AA, представляет собой Y.
348. MBM согласно любому из вариантов осуществления 327-345, где аминокислота, обозначенная как X8 в таблице AA, представляет собой S.
349. MBM согласно любому из вариантов осуществления 327-345, где аминокислота, обозначенная как X8 в таблице AA, представляет собой T.
350. MBM согласно любому из вариантов осуществления 327-349, где аминокислота, обозначенная как X9 в таблице AA, представляет собой W.
351. MBM согласно любому из вариантов осуществления 327-349, где аминокислота, обозначенная как X9 в таблице AA, представляет собой Y.
352. MBM согласно любому из вариантов осуществления 327-349, где аминокислота, обозначенная как X9 в таблице AA, представляет собой S.
353. MBM согласно любому из вариантов осуществления 327-349, где аминокислота, обозначенная как X9 в таблице AA, представляет собой T.
354. MBM согласно любому из вариантов осуществления 327-353, где аминокислота, обозначенная как X10 в таблице AA, представляет собой H.
355. MBM согласно любому из вариантов осуществления 327-353, где аминокислота, обозначенная как X10 в таблице AA, представляет собой Y.
356. MBM согласно любому из вариантов осуществления 327-355, где аминокислота, обозначенная как X11 в таблице AA, представляет собой S.
357. MBM согласно любому из вариантов осуществления 327-355, где аминокислота, обозначенная как X11 в таблице AA, представляет собой G.
358. MBM согласно любому из вариантов осуществления 327-357, где аминокислота, обозначенная как X12 в таблице AA, представляет собой I.
359. MBM согласно любому из вариантов осуществления 327-357, где аминокислота, обозначенная как X12 в таблице AA, представляет собой L.
360. MBM согласно любому из вариантов осуществления 327-359, где аминокислота, обозначенная как X13 в таблице AA, представляет собой V.
361. MBM согласно любому из вариантов осуществления 327-359, где аминокислота, обозначенная как X13 в таблице AA, представляет собой G.
362. MBM согласно любому из вариантов осуществления 327-361, где аминокислота, обозначенная как X14 в таблице AA, представляет собой R.
363. MBM согласно любому из вариантов осуществления 327-361, где аминокислота, обозначенная как X14 в таблице AA, представляет собой N.
364. MBM согласно любому из вариантов осуществления 327-363, где аминокислота, обозначенная как X15 в таблице AA, представляет собой D.
365. MBM согласно любому из вариантов осуществления 327-363, где аминокислота, обозначенная как X15 в таблице AA, представляет собой E.
366. MBM согласно любому из вариантов осуществления 327-363, где аминокислота, обозначенная как X15 в таблице AA, представляет собой L.
367. MBM согласно любому из вариантов осуществления 327-366, где аминокислота, обозначенная как X16 в таблице AA, представляет собой G.
368. MBM согласно любому из вариантов осуществления 327-366, где аминокислота, обозначенная как X16 в таблице AA, представляет собой N.
369. MBM согласно любому из вариантов осуществления 327-366, где аминокислота, обозначенная как X16 в таблице AA, представляет собой E.
370. MBM согласно любому из вариантов осуществления 327-369, где аминокислота, обозначенная как X17 в таблице AA, представляет собой R.
371. MBM согласно любому из вариантов осуществления 327-369, где аминокислота, обозначенная как X17 в таблице AA, представляет собой S.
372. MBM согласно любому из вариантов осуществления 327-371, где аминокислота, обозначенная как X18 в таблице AA, представляет собой V.
373. MBM согласно любому из вариантов осуществления 327-371, где аминокислота, обозначенная как X18 в таблице AA, представляет собой T.
374. MBM согласно любому из вариантов осуществления 327-373, где аминокислота, обозначенная как X19 в таблице AA, представляет собой N.
375. MBM согласно любому из вариантов осуществления 327-373, где аминокислота, обозначенная как X19 в таблице AA, представляет собой T.
376. MBM согласно любому из вариантов осуществления 327-375, где аминокислота, обозначенная как X20 в таблице AA, представляет собой R.
377. MBM согласно любому из вариантов осуществления 327-375, где аминокислота, обозначенная как X20 в таблице AA, представляет собой L.
378. MBM согласно любому из вариантов осуществления 327-377, где аминокислота, обозначенная как X21 в таблице AA, представляет собой F.
379. MBM согласно любому из вариантов осуществления 327-377, где аминокислота, обозначенная как X21 в таблице AA, представляет собой E.
380. MBM согласно любому из вариантов осуществления 327-379, где аминокислота, обозначенная как X22 в таблице AA, представляет собой S.
381. MBM согласно любому из вариантов осуществления 327-379, где аминокислота, обозначенная как X22 в таблице AA, представляет собой Y.
382. MBM согласно любому из вариантов осуществления 327-381, где аминокислота, обозначенная как X23 в таблице AA, представляет собой S.
383. MBM согласно любому из вариантов осуществления 327-381, где аминокислота, обозначенная как X23 в таблице AA, представляет собой Y.
384. MBM согласно любому из вариантов осуществления 327-383, где аминокислота, обозначенная как X24 в таблице AA, представляет собой S.
385. MBM согласно любому из вариантов осуществления 327-383, где аминокислота, обозначенная как X24 в таблице AA, представляет собой A.
386. MBM согласно любому из вариантов осуществления 327-385, где аминокислота, обозначенная как X25 в таблице AA, представляет собой H.
387. MBM согласно любому из вариантов осуществления 327-385, где аминокислота, обозначенная как X25 в таблице AA, представляет собой T.
388. MBM согласно любому из вариантов осуществления 327-387, где аминокислота, обозначенная как X26 в таблице AA, представляет собой F.
389. MBM согласно любому из вариантов осуществления 327-387, где аминокислота, обозначенная как X26 в таблице AA, представляет собой Y.
390. MBM согласно любому из вариантов осуществления 327-389, где аминокислота, обозначенная как X27 в таблице AA, представляет собой W.
391. MBM согласно любому из вариантов осуществления 327-389, где аминокислота, обозначенная как X27 в таблице AA, представляет собой Y.
392. MBM согласно любому из вариантов осуществления 327-391, где ABM2 содержит последовательность CDR-H1 из C1-1.
393. MBM согласно любому из вариантов осуществления 327-391, где ABM2 содержит последовательность CDR-H1 из C1-2.
394. MBM согласно любому из вариантов осуществления 327-391, где ABM2 содержит последовательность CDR-H1 из C1-3.
395. MBM согласно любому из вариантов осуществления 327-391, где ABM2 содержит последовательность CDR-H1 из C1-4.
396. MBM согласно любому из вариантов осуществления 327-395, где ABM2 содержит последовательность CDR-H2 из C1-5.
397. MBM согласно любому из вариантов осуществления 327-395, где ABM2 содержит последовательность CDR-H2 из C1-6.
398. MBM согласно любому из вариантов осуществления 327-395, где ABM2 содержит последовательность CDR-H2 из C1-7.
399. MBM согласно любому из вариантов осуществления 327-398, где ABM2 содержит последовательность CDR-H3 из C1-8.
400. MBM согласно любому из вариантов осуществления 327-398, где ABM2 содержит последовательность CDR-H3 из C1-9.
401. MBM согласно любому из вариантов осуществления 327-398, где ABM2 содержит последовательность CDR-H3 из C1-10.
402. MBM согласно любому из вариантов осуществления 327-398, где ABM2 содержит последовательность CDR-H3 из C1-11.
403. MBM согласно любому из вариантов осуществления 327-402, где ABM2 содержит последовательность CDR-L1 из C1-12.
404. MBM согласно любому из вариантов осуществления 327-402, где ABM2 содержит последовательность CDR-L1 из C1-13.
405. MBM согласно любому из вариантов осуществления 327-402, где ABM2 содержит последовательность CDR-L1 из C1-14.
406. MBM согласно любому из вариантов осуществления 327-402, где ABM2 содержит последовательность CDR-L1 из C1-15.
407. MBM согласно любому из вариантов осуществления 327-402, где ABM2 содержит последовательность CDR-L1 из C1-16.
408. MBM согласно любому из вариантов осуществления 327-402, где ABM2 содержит последовательность CDR-L1 из C1-17.
409. MBM согласно любому из вариантов осуществления 327-408, где ABM2 содержит последовательность CDR-L2 из C1-18.
410. MBM согласно любому из вариантов осуществления 327-408, где ABM2 содержит последовательность CDR-L2 из C1-19.
411. MBM согласно любому из вариантов осуществления 327-410, где ABM2 содержит последовательность CDR-L3 из C1-20.
412. MBM согласно любому из вариантов осуществления 327-410, где ABM2 содержит последовательность CDR-L3 из C1-21.
413. MBM согласно любому из вариантов осуществления 327-410, где ABM2 содержит последовательность CDR-L3 из C1-22.
414. MBM согласно любому из вариантов осуществления 327-410, где ABM2 содержит последовательность CDR-L3 из C1-23.
415. MBM согласно варианту осуществления 326, где ABM2 содержит последовательность CDR-H1, последовательность CDR-H2, последовательность CDR-H3, последовательность CDR-L1, последовательность CDR-L2 и последовательность CDR-L3, представленные в таблице AB.
416. MBM согласно варианту осуществления 415, где аминокислота, обозначенная как X28 в таблице AB, представляет собой V.
417. MBM согласно варианту осуществления 415, где аминокислота, обозначенная как X28 в таблице AB, представляет собой I.
418. MBM согласно любому из вариантов осуществления 415-417, где аминокислота, обозначенная как X29 в таблице AB, представляет собой F.
419. MBM согласно любому из вариантов осуществления 415-417, где аминокислота, обозначенная как X29 в таблице AB, представляет собой Y.
420. MBM согласно любому из вариантов осуществления 415-419, где аминокислота, обозначенная как X30 в таблице AB, представляет собой N.
421. MBM согласно любому из вариантов осуществления 415-419, где аминокислота, обозначенная как X30 в таблице AB, представляет собой S.
422. MBM согласно любому из вариантов осуществления 415-421, где аминокислота, обозначенная как X31 в таблице AB, представляет собой A.
423. MBM согласно любому из вариантов осуществления 415-421, где аминокислота, обозначенная как X31 в таблице AB, представляет собой S.
424. MBM согласно любому из вариантов осуществления 415-423, где аминокислота, обозначенная как X32 в таблице AB, представляет собой T.
425. MBM согласно любому из вариантов осуществления 415-423, где аминокислота, обозначенная как X32 в таблице AB, представляет собой K.
426. MBM согласно любому из вариантов осуществления 415-425, где аминокислота, обозначенная как X33 в таблице AB, представляет собой T.
427. MBM согласно любому из вариантов осуществления 415-425, где аминокислота, обозначенная как X33 в таблице AB, представляет собой A.
428. MBM согласно любому из вариантов осуществления 415-427, где аминокислота, обозначенная как X34 в таблице AB, представляет собой S.
429. MBM согласно любому из вариантов осуществления 415-427, где аминокислота, обозначенная как X34 в таблице AB, представляет собой R.
430. MBM согласно любому из вариантов осуществления 415-429, где аминокислота, обозначенная как X35 в таблице AB, представляет собой N.
431. MBM согласно любому из вариантов осуществления 415-429, где аминокислота, обозначенная как X35 в таблице AB, представляет собой G.
432. MBM согласно любому из вариантов осуществления 415-431, где аминокислота, обозначенная как X36 в таблице AB, представляет собой S.
433. MBM согласно любому из вариантов осуществления 415-431, где аминокислота, обозначенная как X36 в таблице AB, представляет собой A.
434. MBM согласно любому из вариантов осуществления 415-433, где аминокислота, обозначенная как X37 в таблице AB, представляет собой A.
435. MBM согласно любому из вариантов осуществления 415-433, где аминокислота, обозначенная как X37 в таблице AB, представляет собой T.
436. MBM согласно любому из вариантов осуществления 415-433, где аминокислота, обозначенная как X37 в таблице AB, представляет собой S.
437. MBM согласно любому из вариантов осуществления 415-436, где аминокислота, обозначенная как X38 в таблице AB, представляет собой N.
438. MBM согласно любому из вариантов осуществления 415-436, где аминокислота, обозначенная как X38 в таблице AB, представляет собой D.
439. MBM согласно любому из вариантов осуществления 415-438, где аминокислота, обозначенная как X39 в таблице AB, представляет собой N.
440. MBM согласно любому из вариантов осуществления 415-438, где аминокислота, обозначенная как X39 в таблице AB, представляет собой K.
441. MBM согласно любому из вариантов осуществления 415-440, где аминокислота, обозначенная как X40 в таблице AB, представляет собой D.
442. MBM согласно любому из вариантов осуществления 415-440, где аминокислота, обозначенная как X40 в таблице AB, представляет собой N.
443. MBM согласно любому из вариантов осуществления 415-442, где аминокислота, обозначенная как X41 в таблице AB, представляет собой H.
444. MBM согласно любому из вариантов осуществления 415-442, где аминокислота, обозначенная как X41 в таблице AB, представляет собой N.
445. MBM согласно любому из вариантов осуществления 415-444, где аминокислота, обозначенная как X42 в таблице AB, представляет собой Q.
446. MBM согласно любому из вариантов осуществления 415-444, где аминокислота, обозначенная как X42 в таблице AB, представляет собой E.
447. MBM согласно любому из вариантов осуществления 415-446, где аминокислота, обозначенная как X43 в таблице AB, представляет собой R.
448. MBM согласно любому из вариантов осуществления 415-446, где аминокислота, обозначенная как X43 в таблице AB, представляет собой S.
449. MBM согласно любому из вариантов осуществления 415-446, где аминокислота, обозначенная как X43 в таблице AB, представляет собой G.
450. MBM согласно любому из вариантов осуществления 415-449, где ABM2 содержит последовательность CDR-H1 из C2-1.
451. MBM согласно любому из вариантов осуществления 415-449, где ABM2 содержит последовательность CDR-H1 из C2-2.
452. MBM согласно любому из вариантов осуществления 415-449, где ABM2 содержит последовательность CDR-H1 из C2-3.
453. MBM согласно любому из вариантов осуществления 415-449, где ABM2 содержит последовательность CDR-H1 из C2-4.
454. MBM согласно любому из вариантов осуществления 415-453, где ABM2 содержит последовательность CDR-H2 из C2-5.
455. MBM согласно любому из вариантов осуществления 415-453, где ABM2 содержит последовательность CDR-H2 из C2-6.
456. MBM согласно любому из вариантов осуществления 415-453, где ABM2 содержит последовательность CDR-H2 из C2-7.
457. MBM согласно любому из вариантов осуществления 415-456, где ABM2 содержит последовательность CDR-H3 из C2-8.
458. MBM согласно любому из вариантов осуществления 415-456, где ABM2 содержит последовательность CDR-H3 из C2-9.
459. MBM согласно любому из вариантов осуществления 415-458, где ABM2 содержит последовательность CDR-L1 из C2-10.
460. MBM согласно любому из вариантов осуществления 415-458, где ABM2 содержит последовательность CDR-L1 из C2-11.
461. MBM согласно любому из вариантов осуществления 415-458, где ABM2 содержит последовательность CDR-L1 из C2-12.
462. MBM согласно любому из вариантов осуществления 415-461, где ABM2 содержит последовательность CDR-L2 из C2-13.
463. MBM согласно любому из вариантов осуществления 415-461, где ABM2 содержит последовательность CDR-L2 из C2-14.
464. MBM согласно любому из вариантов осуществления 415-461, где ABM2 содержит последовательность CDR-L2 из C2-15.
465. MBM согласно любому из вариантов осуществления 415-464, где ABM2 содержит последовательность CDR-L3 из C2-16.
466. MBM согласно любому из вариантов осуществления 415-464, где ABM2 содержит последовательность CDR-L3 из C2-17.
467. MBM согласно варианту осуществления 326, где ABM2 содержит последовательность CDR-H1, последовательность CDR-H2, последовательность CDR-H3, последовательность CDR-L1, последовательность CDR-L2 и последовательность CDR-L3, представленные в таблице AC.
468. MBM согласно варианту осуществления 467, где аминокислота, обозначенная как X44 в таблице AC, представляет собой G.
469. MBM согласно варианту осуществления 467, где аминокислота, обозначенная как X44 в таблице AC, представляет собой A.
470. MBM согласно любому из вариантов осуществления 467-469, где аминокислота, обозначенная как X45 в таблице AC, представляет собой H.
471. MBM согласно любому из вариантов осуществления 467-469, где аминокислота, обозначенная как X45 в таблице AC, представляет собой N.
472. MBM согласно любому из вариантов осуществления 467-471, где аминокислота, обозначенная как X46 в таблице AC, представляет собой D.
473. MBM согласно любому из вариантов осуществления 467-471, где аминокислота, обозначенная как X46 в таблице AC, представляет собой G.
474. MBM согласно любому из вариантов осуществления 467-473, где аминокислота, обозначенная как X47 в таблице AC, представляет собой A.
475. MBM согласно любому из вариантов осуществления 467-473, где аминокислота, обозначенная как X47 в таблице AC, представляет собой G.
476. MBM согласно любому из вариантов осуществления 467-475, где аминокислота, обозначенная как X48 в таблице AC, представляет собой N.
477. MBM согласно любому из вариантов осуществления 467-475, где аминокислота, обозначенная как X48 в таблице AC, представляет собой K.
478. MBM согласно любому из вариантов осуществления 467-477, где аминокислота, обозначенная как X49 в таблице AC, представляет собой V.
479. MBM согласно любому из вариантов осуществления 467-477, где аминокислота, обозначенная как X49 в таблице AC, представляет собой A.
480. MBM согласно любому из вариантов осуществления 467-479, где аминокислота, обозначенная как X50 в таблице AC, представляет собой N.
481. MBM согласно любому из вариантов осуществления 467-479, где аминокислота, обозначенная как X50 в таблице AC, представляет собой V.
482. MBM согласно любому из вариантов осуществления 467-481, где аминокислота, обозначенная как X51 в таблице AC, представляет собой A.
483. MBM согласно любому из вариантов осуществления 467-481, где аминокислота, обозначенная как X51 в таблице AC, представляет собой V.
484. MBM согласно любому из вариантов осуществления 467-483, где аминокислота, обозначенная как X52 в таблице AC, представляет собой Y.
485. MBM согласно любому из вариантов осуществления 467-483, где аминокислота, обозначенная как X52 в таблице AC, представляет собой F.
486. MBM согласно любому из вариантов осуществления 467-485, где аминокислота, обозначенная как X53 в таблице AC, представляет собой I.
487. MBM согласно любому из вариантов осуществления 467-485, где аминокислота, обозначенная как X53 в таблице AC, представляет собой V.
488. MBM согласно любому из вариантов осуществления 467-487, где аминокислота, обозначенная как X54 в таблице AC, представляет собой I.
489. MBM согласно любому из вариантов осуществления 467-487, где аминокислота, обозначенная как X54 в таблице AC, представляет собой H.
490. MBM согласно любому из вариантов осуществления 467-489, где ABM2 содержит последовательность CDR-H1 из C3-1.
491. MBM согласно любому из вариантов осуществления 467-489, где ABM2 содержит последовательность CDR-H1 из C3-2.
492. MBM согласно любому из вариантов осуществления 467-489, где ABM2 содержит последовательность CDR-H1 из C3-3.
493. MBM согласно любому из вариантов осуществления 467-489, где ABM2 содержит последовательность CDR-H1 из C3-4.
494. MBM согласно любому из вариантов осуществления 467-493, где ABM2 содержит последовательность CDR-H2 из C3-5.
495. MBM согласно любому из вариантов осуществления 467-493, где ABM2 содержит последовательность CDR-H2 из C3-6.
496. MBM согласно любому из вариантов осуществления 467-493, где ABM2 содержит последовательность CDR-H2 из C3-7.
497. MBM согласно любому из вариантов осуществления 467-496, где ABM2 содержит последовательность CDR-H3 из C3-8.
498. MBM согласно любому из вариантов осуществления 467-496, где ABM2 содержит последовательность CDR-H3 из C3-9.
499. MBM согласно любому из вариантов осуществления 467-498, где ABM2 содержит последовательность CDR-L1 из C3-10.
500. MBM согласно любому из вариантов осуществления 467-498, где ABM2 содержит последовательность CDR-L1 из C3-11.
501. MBM согласно любому из вариантов осуществления 467-498, где ABM2 содержит последовательность CDR-L1 из C3-12.
502. MBM согласно любому из вариантов осуществления 467-501, где ABM2 содержит последовательность CDR-L2 из C3-13.
503. MBM согласно любому из вариантов осуществления 467-501, где ABM2 содержит последовательность CDR-L2 из C3-14.
504. MBM согласно любому из вариантов осуществления 467-503, где ABM2 содержит последовательность CDR-L3 из C3-15.
505. MBM согласно любому из вариантов осуществления 467-503, где ABM2 содержит последовательность CDR-L3 из C3-16.
506. MBM согласно варианту осуществления 151, где ABM2 содержит последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице AD-1, таблице AE-1, таблице AF-1, таблице AG-1, таблице AH-1 или таблице AI-1, и соответствующие последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице AD-2, таблице AE-2, таблице AF-2, таблице AG-2, таблице AH-2 или таблице AI-2 соответственно.
507. MBM согласно варианту осуществления 506, где ABM2 содержит последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице AD-1, и соответствующие последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице AD-2.
508. MBM согласно варианту осуществления 506, где ABM2 содержит последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице AE-1, и соответствующие последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице AE-2.
509. MBM согласно варианту осуществления 506, где ABM2 содержит последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице AF-1, и соответствующие последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице AF-2.
510. MBM согласно варианту осуществления 506, где ABM2 содержит последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице AG-1, и соответствующие последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице AG-2.
511. MBM согласно варианту осуществления 506, где ABM2 содержит последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице AH-1, и соответствующие последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице AH-2.
512. MBM согласно варианту осуществления 506, где ABM2 содержит последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в таблице AI-1, и соответствующие последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в таблице AI-2.
513. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из NOV292.
514. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из NOV123.
515. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из Sp10b.
516. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из NOV453.
517. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из NOV229.
518. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из NOV110.
519. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из NOV832.
520. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из NOV589.
521. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из NOV580.
522. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из NOV567.
523. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из NOV221.
524. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_bkm1.
525. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11a_bkm2.
526. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_hz0.
527. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_HZ1.
528. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_sansPTM_hz1.
529. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_sansPTM_rat.
530. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_YY.
531. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VHVL_SS.
532. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VHVL_WS.
533. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_SW.
534. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VHVL_TT.
535. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VHVL_TW.
536. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VHVL_WT.
537. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VH3_VLK_3.
538. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VH1_VK2.
539. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VH3_VLK1.
540. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VH5_VK2.
541. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp9aFW1_VL_VH_S56G.
542. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP9AFW4_VL_VH_S56G.
543. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp9aFW1_VL_VH.
544. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp9aFW4_VLVH.
545. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp9arabtor_VHVL.
546. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp9arabtor_VLVH.
547. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_YY_SANSPTM.
548. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_YY_SANSPTM_Y.
549. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_YY_SANSPTM_S.
550. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_YY_Y.
551. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_YY_s.
552. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_SS_SANSPTM.
553. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_SS_SANSPTM_Y.
554. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_SS_SANSPTM_S.
555. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_SS_Y.
556. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_SS_S.
557. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_SS_SANSPTM.
558. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_WS_SANSPTM_Y.
559. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_WS_SANSPTM_S.
560. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_WS_Y.
561. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_WS_S.
562. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_WS_SANSPTM.
563. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_SW_SANSPTM_Y.
564. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_SW_SANSPTM_S.
565. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_SW_Y.
566. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_SW_S.
567. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_SW_SANSPTM.
568. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_TW_SANSPTM_Y.
569. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_TW_SANSPTM_S.
570. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_TW_Y.
571. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_TW_S.
572. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_TW_SANSPTM.
573. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_TT_SANSPTM_Y.
574. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_TT_SANSPTM_S.
575. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_TT_Y.
576. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_TT_S.
577. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VHVL_TT_SANSPTM.
578. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11AVH3_VLK_3_Y.
579. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11AVH3_VLK_3_S.
580. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11AVH3_VLK_3_Y_PTM.
581. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11AVH3_VLK_3_S_PTM.
582. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11AVH3_VLK_3_Y_SW.
583. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11AVH3_VLK_3_S_SW.
584. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11AVH3_VLK_3_Y_PTM_SW.
585. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11AVH3_VLK_3_S_SWPTM.
586. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11AVH3_VLK_SWPTM.
587. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11AVH3_VLK_3_SW.
588. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VH1_VK2_Y.
589. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VH1_VK2_S.
590. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VH1_VK2_Y_PTM.
591. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VH1_VK2_S_PTM.
592. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VH1_VK2_Y_SW.
593. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VH1_VK2_S_SW.
594. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VH1_VK2_Y_PTM.
595. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VH1_VK2_S_PTM_SW.
596. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VH1_VK2_SW.
597. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_sp11a_VH1_VK2_SW_PTM.
598. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VH3_VLK1_Y.
599. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VH3_VLK1_S.
600. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VH3_VLK1_Y_PTM.
601. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VH3_VLK1_S_PTM.
602. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VH3_VLK1_Y_SW.
603. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VH3_VLK1_S_SW.
604. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VH3_VLK1_Y_PTM.
605. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VH3_VLK1_S_PTM_SW.
606. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VH3_VLK1PTM_SW.
607. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VH3_VLK1_SW.
608. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VH5_VK2_Y.
609. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VH5_VK2_S.
610. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VH5_VK2_Y_PTM.
611. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VH5_VK2_S_PTM.
612. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VH5_VK2_Y_SW.
613. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VH5_VK2_S_SW.
614. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VH5_VK2_Y_PTM_SW.
615. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VH5_VK2_S_PTM_SW.
616. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VH5_VK2_PTM_SW.
617. MBM согласно любому из вариантов осуществления 507-512, где ABM2 содержит последовательности CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3 из CD3_SP11A_VH5_VK2_SW.
618. MBM согласно варианту осуществления 506, где ABM2 содержит последовательность вариабельного участка тяжелой цепи, представленную в таблице AJ-1, и соответствующую последовательность вариабельного участка легкой цепи, представленную в таблице AJ-2.
619. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из NOV292.
620. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из NOV123.
621. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из Sp10b.
622. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из NOV453.
623. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из NOV229.
624. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из NOV110.
625. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из NOV832.
626. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из NOV589.
627. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из NOV580.
628. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из NOV567.
629. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из NOV221.
630. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_bkm1.
631. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11a_bkm2.
632. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_hz0.
633. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_HZ1.
634. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_sansPTM_hz1.
635. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_sansPTM_rat.
636. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_YY.
637. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VHVL_SS.
638. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VHVL_WS.
639. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_SW.
640. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VHVL_TT.
641. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VHVL_TW.
642. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VHVL_WT.
643. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VH3_VLK_3.
644. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VH1_VK2.
645. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VH3_VLK1.
646. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VH5_VK2.
647. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp9aFW1_VL_VH_S56G.
648. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP9AFW4_VL_VH_S56G.
649. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp9aFW1_VL_VH.
650. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp9aFW4_VLVH.
651. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp9arabtor_VHVL.
652. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp9arabtor_VLVH.
653. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_YY_SANSPTM.
654. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_YY_SANSPTM_Y.
655. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_YY_SANSPTM_S.
656. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_YY_Y.
657. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_YY_s.
658. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_SS_SANSPTM.
659. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_SS_SANSPTM_Y.
660. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_SS_SANSPTM_S.
661. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_SS_Y.
662. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_SS_S.
663. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_SS_SANSPTM.
664. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_WS_SANSPTM_Y.
665. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_WS_SANSPTM_S.
666. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_WS_Y.
667. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_WS_S.
668. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_WS_SANSPTM.
669. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_SW_SANSPTM_Y.
670. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_SW_SANSPTM_S.
671. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_SW_Y.
672. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_SW_S.
673. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_SW_SANSPTM.
674. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_TW_SANSPTM_Y.
675. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_TW_SANSPTM_S.
676. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_TW_Y.
677. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_TW_S.
678. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_TW_SANSPTM.
679. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_TT_SANSPTM_Y.
680. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_TT_SANSPTM_S.
681. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_TT_Y.
682. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_TT_S.
683. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VHVL_TT_SANSPTM.
684. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11AVH3_VLK_3_Y.
685. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11AVH3_VLK_3_S.
686. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11AVH3_VLK_3_Y_PTM.
687. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11AVH3_VLK_3_S_PTM.
688. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11AVH3_VLK_3_Y_SW.
689. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11AVH3_VLK_3_S_SW.
690. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11AVH3_VLK_3_Y_PTM_SW.
691. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11AVH3_VLK_3_S_SWPTM.
692. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11AVH3_VLK_SWPTM.
693. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11AVH3_VLK_3_SW.
694. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VH1_VK2_Y.
695. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VH1_VK2_S.
696. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VH1_VK2_Y_PTM.
697. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VH1_VK2_S_PTM.
698. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VH1_VK2_Y_SW.
699. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VH1_VK2_S_SW.
700. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VH1_VK2_Y_PTM.
701. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VH1_VK2_S_PTM_SW.
702. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VH1_VK2_SW.
703. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_sp11a_VH1_VK2_SW_PTM.
704. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VH3_VLK1_Y.
705. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VH3_VLK1_S.
706. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VH3_VLK1_Y_PTM.
707. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VH3_VLK1_S_PTM.
708. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VH3_VLK1_Y_SW.
709. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VH3_VLK1_S_SW.
710. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VH3_VLK1_Y_PTM.
711. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VH3_VLK1_S_PTM_SW.
712. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VH3_VLK1PTM_SW.
713. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VH3_VLK1_SW.
714. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VH5_VK2_Y.
715. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VH5_VK2_S.
716. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VH5_VK2_Y_PTM.
717. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VH5_VK2_S_PTM.
718. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VH5_VK2_Y_SW.
719. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VH5_VK2_S_SW.
720. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VH5_VK2_Y_PTM_SW.
721. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VH5_VK2_S_PTM_SW.
722. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VH5_VK2_PTM_SW.
723. MBM согласно варианту осуществления 618, где ABM2 содержит последовательность вариабельного участка тяжелой цепи и последовательность вариабельного участка легкой цепи из CD3_SP11A_VH5_VK2_SW.
724. MBM согласно любому из вариантов осуществления 1-150, где компонент комплекса TCR представляет собой TCR-α, TCR-β или димер TCR-α/β.
725. MBM согласно варианту осуществления 724, где компонент комплекса TCR представляет собой TCR-α.
726. MBM согласно варианту осуществления 724, где компонент комплекса TCR представляет собой TCR-β.
727. MBM согласно варианту осуществления 724, где компонент комплекса TCR представляет собой димер TCR-α/β.
728. MBM согласно варианту осуществления 724, где ABM2 содержит последовательности CDR из BMA031.
729. МBM согласно варианту осуществления 728, где последовательности CDR определены согласно нумерации по Kabat.
730. МBM согласно варианту осуществления 728, где последовательности CDR определены согласно нумерации по Chothia.
731. МBM согласно варианту осуществления 728, где последовательности CDR определены согласно комбинации нумераций по Kabat и по Chothia.
732. МBM согласно варианту осуществления 728, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из BMA031.
733. MBM согласно любому из вариантов осуществления 1-150, где компонент комплекса TCR представляет собой TCR-γ, TCR-δ или димер TCR-γ/δ.
734. MBM согласно варианту осуществления 733, где компонент комплекса TCR представляет собой TCR-γ.
735. MBM согласно варианту осуществления 733, где компонент комплекса TCR представляет собой TCR-δ.
736. MBM согласно варианту осуществления 733, где компонент комплекса TCR представляет собой димер TCR-γ/δ.
737. MBM согласно варианту осуществления 733, где ABM2 содержит последовательности CDR из δTCS1.
738. МBM согласно варианту осуществления 737, где последовательности CDR определены согласно нумерации по Kabat.
739. МBM согласно варианту осуществления 737, где последовательности CDR определены согласно нумерации по Chothia.
740. МBM согласно варианту осуществления 737, где последовательности CDR определены согласно комбинации нумераций по Kabat и по Chothia.
741. МBM согласно варианту осуществления 737, где ABM2 содержит последовательности вариабельных участков тяжелой и легкой цепей из δTCS1.
742. MBM согласно любому из вариантов осуществления 1-741, где ABM3 специфично связывается с CD2 человека.
743. MBM согласно варианту осуществления 742, где ABM3 представляет собой ABM на основе неиммуноглобулиновой каркасной структуры.
744. MBM согласно варианту осуществления 743, где ABM3 представляет собой домен Куница, аднексин, аффитело, дарпин, авимер, антикалин, липокалин, центирин, версатело, ноттин, аднектин, пронектин, аффитин/нанофитин, аффилин, атример/тетранектин, бициклический пептид, цистиновый узел, каркасную структуру Fn3, O-тело, Tn3, аффимер, BD, адгирон, дуокалин, альфатело, белок с повторами Armadillo, репетело или финомер.
745. MBM согласно варианту осуществления 743, где ABM3 содержит рецепторсвязывающий домен лиганда CD2.
746. MBM согласно варианту осуществления 745, где лиганд CD2 представляет собой CD58.
747. MBM согласно варианту осуществления 745, где лиганд CD2 представляет собой CD48.
748. MBM согласно варианту осуществления 745, где ABM3 представляет собой фрагмент CD58.
749. MBM согласно варианту осуществления 748, где фрагмент CD58 содержит аминокислотную последовательность CD58-1, представленную в таблице 15.
750. MBM согласно варианту осуществления 748, где фрагмент CD58 содержит аминокислотную последовательность CD58-2, представленную в таблице 15.
751. MBM согласно варианту осуществления 748, где фрагмент CD58 содержит аминокислотную последовательность CD58-3, представленную в таблице 15.
752. MBM согласно варианту осуществления 748, где фрагмент CD58 содержит аминокислотную последовательность CD58-4, представленную в таблице 15.
753. MBM согласно варианту осуществления 748, где фрагмент CD58 содержит аминокислотную последовательность CD58-5, представленную в таблице 15.
754. MBM согласно варианту осуществления 753, где аминокислота, обозначенная как B, представляет собой фенилаланин.
755. MBM согласно варианту осуществления 753, где аминокислота, обозначенная как B, представляет собой серин.
756. MBM согласно любому из вариантов осуществления 753-755, где аминокислота, обозначенная как J, представляет собой валин.
757. MBM согласно любому из вариантов осуществления 753-755, где аминокислота, обозначенная как J, представляет собой лизин.
758. MBM согласно любому из вариантов осуществления 753-757, где аминокислота, обозначенная как O, представляет собой валин.
759. MBM согласно любому из вариантов осуществления 753-757, где аминокислота, обозначенная как O, представляет собой глутамин.
760. MBM согласно любому из вариантов осуществления 753-759, где аминокислота, обозначенная как U, представляет собой валин.
761. MBM согласно любому из вариантов осуществления 753-759, где аминокислота, обозначенная как U, представляет собой лизин.
762. MBM согласно любому из вариантов осуществления 753-761, где аминокислота, обозначенная как X, представляет собой треонин.
763. MBM согласно любому из вариантов осуществления 753-761, где аминокислота, обозначенная как X, представляет собой серин.
764. MBM согласно любому из вариантов осуществления 753-763, где аминокислота, обозначенная как Z, представляет собой лейцин.
765. MBM согласно любому из вариантов осуществления 753-763, где аминокислота, обозначенная как Z, представляет собой глицин.
766. MBM согласно варианту осуществления 748, где фрагмент CD58 содержит аминокислотную последовательность CD58-6, представленную в таблице 15.
767. MBM согласно варианту осуществления 748, где фрагмент CD58 содержит аминокислотную последовательность CD58-7, представленную в таблице 15.
768. MBM согласно варианту осуществления 767, где аминокислота, обозначенная как J, представляет собой валин.
769. MBM согласно варианту осуществления 767, где аминокислота, обозначенная как J, представляет собой лизин.
770. MBM согласно любому из вариантов осуществления 767-769, где аминокислота, обозначенная как O, представляет собой валин.
771. MBM согласно любому из вариантов осуществления 767-769, где аминокислота, обозначенная как O, представляет собой глутамин.
772. MBM согласно варианту осуществления 748, где фрагмент CD58 содержит аминокислотную последовательность CD58-8, представленную в таблице 15.
773. MBM согласно варианту осуществления 748, где фрагмент CD58 содержит аминокислотную последовательность CD58-9, представленную в таблице 15.
774. MBM согласно варианту осуществления 748, где фрагмент CD58 содержит аминокислотную последовательность CD58-10, представленную в таблице 15.
775. MBM согласно варианту осуществления 748, где фрагмент CD58 содержит аминокислотную последовательность CD58-11, представленную в таблице 15.
776. MBM согласно варианту осуществления 745, где ABM3 представляет собой фрагмент CD48.
777. MBM согласно варианту осуществления 776, где фрагмент CD48 характеризуется по меньшей мере 70% идентичностью последовательности с аминокислотами 27-220 из аминокислотной последовательности с идентификатором UniProt P09326.
778. MBM согласно варианту осуществления 776, где фрагмент CD48 характеризуется по меньшей мере 80% идентичностью последовательности с аминокислотами 27-220 из аминокислотной последовательности с идентификатором UniProt P09326.
779. MBM согласно варианту осуществления 776, где фрагмент CD48 характеризуется по меньшей мере 90% идентичностью последовательности с аминокислотами 27-220 из аминокислотной последовательности с идентификатором UniProt P09326.
780. MBM согласно варианту осуществления 776, где фрагмент CD48 характеризуется по меньшей мере 95% идентичностью последовательности с аминокислотами 27-220 из аминокислотной последовательности с идентификатором UniProt P09326.
781. MBM согласно варианту осуществления 776, где фрагмент CD48 характеризуется по меньшей мере 99% идентичностью последовательности с аминокислотами 27-220 из аминокислотной последовательности с идентификатором UniProt P09326.
782. MBM согласно варианту осуществления 742, где ABM3 представляет собой ABM на основе иммуноглобулиновой каркасной структуры.
783. MBM согласно варианту осуществления 782, где ABM3 представляет собой антитело, фрагмент антитела, scFv, dsFv, Fv, Fab, scFab, (Fab’)2, однодоменное антитело (SDAB), VH- или VL-домен или VHH-домен верблюдовых.
784. МBM согласно варианту осуществления 783, где ABM3 представляет собой антитело или его антигенсвязывающий домен.
785. МBM согласно варианту осуществления 783, где ABM3 представляет собой scFv.
786. МBM согласно варианту осуществления 783, где ABM3 представляет собой Fab.
787. МBM согласно варианту осуществления 786, где ABM3 представляет собой гетеродимер Fab.
788. MBM согласно любому из вариантов осуществления 782-787, где ABM3 содержит последовательности CDR из CD2-1.
789. МBM согласно варианту осуществления 788, где ABM3 содержит последовательности вариабельных участков тяжелой и легкой цепей из CD2-1.
790. МBM согласно варианту осуществления 788, где ABM3 содержит вариабельные последовательности тяжелой и легкой цепей из hu1CD2-1.
791. МBM согласно варианту осуществления 788, где ABM3 содержит вариабельные последовательности тяжелой и легкой цепей из hu2CD2-1.
792. МBM согласно варианту осуществления 788, где ABM3 содержит последовательности CDR из Medi 507.
793. МBM согласно варианту осуществления 792, где ABM3 содержит вариабельные последовательности тяжелой и легкой цепей из Medi 507.
794. MBM согласно любому из вариантов осуществления 1-741, где ABM3 специфично связывается с TAA человека.
795. MBM согласно варианту осуществления 794, где ABM3 представляет собой ABM на основе неиммуноглобулиновой каркасной структуры.
796. MBM согласно варианту осуществления 795, где в случае, если TAA представляет собой рецептор, ABM3 содержит рецепторсвязывающий домен лиганда рецептора, и в случае, если TAA представляет собой лиганд, ABM3 содержит лигандсвязывающий домен рецептора лиганда.
797. MBM согласно варианту осуществления 795, где ABM1 представляет собой домен Куница, аднексин, аффитело, дарпин, авимер, антикалин, липокалин, центирин, версатело, ноттин, аднектин, пронектин, аффитин/нанофитин, аффилин, атример/тетранектин, бициклический пептид, цистиновый узел, каркасную структуру Fn3, O-тело, Tn3, аффимер, BD, адгирон, дуокалин, альфатело, белок с повторами Armadillo, репетело или финомер.
798. MBM согласно варианту осуществления 794, где ABM3 представляет собой ABM на основе иммуноглобулиновой каркасной структуры.
799. MBM согласно варианту осуществления 798, где ABM3 представляет собой антитело, фрагмент антитела, scFv, dsFv, Fv, Fab, scFab, (Fab’)2, однодоменное антитело (SDAB), VH- или VL-домен или VHH-домен верблюдовых.
800. МBM согласно варианту осуществления 799, где ABM3 представляет собой антитело или его антигенсвязывающий домен.
801. МBM согласно варианту осуществления 799, где ABM3 представляет собой scFv.
802. МBM согласно варианту осуществления 799, где ABM3 представляет собой Fab.
803. МBM согласно варианту осуществления 802, где ABM3 представляет собой гетеродимер Fab.
804. MBM согласно вариантам осуществления 794-803, где TAA представляет собой TAA, экспрессирующийся на раковых В-клетках, которые представляют собой плазматические клетки В-клеточного происхождения.
805. MBM согласно вариантам осуществления 794-803, где TAA представляет собой TAA, экспрессирующийся на раковых В-клетках, которые не являются плазматическими клетками.
806. MBM согласно любому из вариантов осуществления 794-805, где TAA выбран из CD19, CD20, CD22, CD123, CD33, CLL1, CD138, CS1, CD38, CD133, FLT3, CD52, TNFRSF13C, TNFRSF13B, CXCR4, PD-L1, LY9, CD200, FCGR2B, CD21, CD23, CD24, CD40L, CD72, CD79a и CD79b.
807. MBM согласно варианту осуществления 806, где TAA представляет собой CD19.
808. MBM согласно варианту осуществления 806, где TAA представляет собой CD20.
809. MBM согласно варианту осуществления 806, где TAA представляет собой CD22.
810. MBM согласно варианту осуществления 806, где TAA представляет собой CD123.
811. MBM согласно варианту осуществления 806, где TAA представляет собой CD33.
812. MBM согласно варианту осуществления 806, где TAA представляет собой CLL1.
813. MBM согласно варианту осуществления 806, где TAA представляет собой CD138.
814. MBM согласно варианту осуществления 806, где TAA представляет собой CS1.
815. MBM согласно варианту осуществления 806, где TAA представляет собой CD38.
816. MBM согласно варианту осуществления 806, где TAA представляет собой CD133.
817. MBM согласно варианту осуществления 806, где TAA представляет собой FLT3.
818. MBM согласно варианту осуществления 806, где TAA представляет собой CD52.
819. MBM согласно варианту осуществления 806, где TAA представляет собой TNFRSF13C.
820. MBM согласно варианту осуществления 806, где TAA представляет собой TNFRSF13B.
821. MBM согласно варианту осуществления 806, где TAA представляет собой CXCR4.
822. MBM согласно варианту осуществления 806, где TAA представляет собой PD-L1.
823. MBM согласно варианту осуществления 806, где TAA представляет собой LY9.
824. MBM согласно варианту осуществления 806, где TAA представляет собой CD200.
825. MBM согласно варианту осуществления 806, где TAA представляет собой FCGR2B.
826. MBM согласно варианту осуществления 806, где TAA представляет собой CD21.
827. MBM согласно варианту осуществления 806, где TAA представляет собой CD23.
828. MBM согласно варианту осуществления 806, где TAA представляет собой CD24.
829. MBM согласно варианту осуществления 806, где TAA представляет собой CD40L.
830. MBM согласно варианту осуществления 806, где TAA представляет собой CD72.
831. MBM согласно варианту осуществления 806, где TAA представляет собой CD79a.
832. MBM согласно варианту осуществления 806, где TAA представляет собой CD79b.
833. MBM согласно варианту осуществления 807, где ABM3 содержит:
(a) CDR-H1, содержащий аминокислотную последовательность CDR, обозначенного как CD19-H1;
(b) CDR-H2, содержащий аминокислотную последовательность любого из CDR, обозначенных как CD19-H2A, HD19-H2B, CD19-H2C и CD19-H2D;
(c) CDR-H3, содержащий аминокислотную последовательность CDR, обозначенного как CD19-H3;
(d) CDR-L1, содержащий аминокислотную последовательность CDR, обозначенного как CD19-L1;
(e) CDR-L2, содержащий аминокислотную последовательность CDR, обозначенного как CD19-L2; и
(f) CDR-L3, содержащий аминокислотную последовательность CDR, обозначенного как CD19-L23.
834. MBM согласно варианту осуществления 833, где ABM3 содержит:
(a) VH, содержащий аминокислотную последовательность любого из VH, обозначенных как CD19-VHA, CD19-VHB, CD19-VHC и CD19-VHD; и
(b) VL, содержащий аминокислотную последовательность любого из VL, обозначенных как CD19-VLA и CD19-VLB.
835. MBM согласно варианту осуществления 807, где ABM3 содержит CDR тяжелой цепи, имеющие аминокислотные последовательности CD19-H1, CD19-H2A и CD19-H3, представленные в таблице 17, и CDR легкой цепи, имеющие аминокислотные последовательности CD19-L1, CD19-L2 и CD19-L3, представленные в таблице 17.
836. MBM согласно варианту осуществления 807, где ABM3 содержит вариабельный участок тяжелой цепи, имеющий аминокислотные последовательности VHA, представленные в таблице 17, и вариабельный участок легкой цепи, имеющий аминокислотные последовательности VLA, представленные в таблице 17.
837. MBM согласно варианту осуществления 807, где ABM3 содержит CDR тяжелой цепи, имеющие аминокислотные последовательности CD19-H1, CD19-H2B и CD19-H3, представленные в таблице 17, и CDR легкой цепи, имеющие аминокислотные последовательности CD19-L1, CD19-L2 и CD19-L3, представленные в таблице 17.
838. MBM согласно варианту осуществления 807, где ABM3 содержит вариабельный участок тяжелой цепи, имеющий аминокислотные последовательности VHB, представленные в таблице 17, и вариабельный участок легкой цепи, имеющий аминокислотные последовательности VLB, представленные в таблице 17.
839. MBM согласно варианту осуществления 807, где ABM3 содержит CDR тяжелой цепи, имеющие аминокислотные последовательности CD19-H1, CD19-H2C и CD19-H3, представленные в таблице 17, и CDR легкой цепи, имеющие аминокислотные последовательности CD19-L1, CD19-L2 и CD19-L3, представленные в таблице 17.
840. MBM согласно варианту осуществления 807, где ABM3 содержит вариабельный участок тяжелой цепи, имеющий аминокислотные последовательности VHC, представленные в таблице 17, и вариабельный участок легкой цепи, имеющий аминокислотные последовательности VLB, представленные в таблице 2.
841. MBM согласно варианту осуществления 807, где ABM3 содержит CDR тяжелой цепи, имеющие аминокислотные последовательности CD19-H1, CD19-H2D и CD19-H3, представленные в таблице 17, и CDR легкой цепи, имеющие аминокислотные последовательности CD19-L1, CD19-L2 и CD19-L3, представленные в таблице 17.
842. MBM согласно варианту осуществления 807, где ABM3 содержит вариабельный участок тяжелой цепи, имеющий аминокислотные последовательности VHD, представленные в таблице 17, и вариабельный участок легкой цепи, имеющий аминокислотные последовательности VLB, представленные в таблице 17.
843. MBM согласно варианту осуществления 807, где ABM3 содержит scFv, содержащий аминокислотную последовательность CD19-scFv1, представленную в таблице 17.
844. MBM согласно варианту осуществления 807, где ABM3 содержит scFv, содержащий аминокислотную последовательность CD19-scFv2, представленную в таблице 17.
845. MBM согласно варианту осуществления 807, где ABM3 содержит scFv, содержащий аминокислотную последовательность CD19-scFv3, представленную в таблице 17.
846. MBM согласно варианту осуществления 807, где ABM3 содержит scFv, содержащий аминокислотную последовательность CD19-scFv4, представленную в таблице 17.
847. MBM согласно варианту осуществления 807, где ABM3 содержит scFv, содержащий аминокислотную последовательность CD19-scFv5, представленную в таблице 17.
848. MBM согласно варианту осуществления 807, где ABM3 содержит scFv, содержащий аминокислотную последовательность CD19-scFv6, представленную в таблице 17.
849. MBM согласно варианту осуществления 807, где ABM3 содержит scFv, содержащий аминокислотную последовательность CD19-scFv7, представленную в таблице 17.
850. MBM согласно варианту осуществления 807, где ABM3 содержит scFv, содержащий аминокислотную последовательность CD19-scFv8, представленную в таблице 17.
851. MBM согласно варианту осуществления 807, где ABM3 содержит scFv, содержащий аминокислотную последовательность CD19-scFv9, представленную в таблице 17.
852. MBM согласно варианту осуществления 807, где ABM3 содержит scFv, содержащий аминокислотную последовательность CD19-scFv10, представленную в таблице 17.
853. MBM согласно варианту осуществления 807, где ABM3 содержит scFv, содержащий аминокислотную последовательность CD19-scFv11, представленную в таблице 17.
854. MBM согласно варианту осуществления 807, где ABM3 содержит scFv, содержащий аминокислотную последовательность CD19-scFv12, представленную в таблице 17.
855. MBM согласно любому из вариантов осуществления 798-803, где ABM3 содержит связывающую последовательность, описанную в таблице 16.
856. МBM согласно варианту осуществления 855, где ABM3 содержит последовательности CDR или вариабельных участков антител, представленные в таблице 16.
857. MBM согласно любому из вариантов осуществления 1-856, которая содержит первый вариант Fc-участка и второй вариант Fc-участка, которые вместе образуют гетеродимер Fc.
858. MBM согласно варианту осуществления 857, где первый и второй варианты Fc-участков содержат аминокислотные замены S364K/E357Q : L368D/K370S.
859. MBM согласно варианту осуществления 857, где первый и второй варианты Fc-участков содержат аминокислотные замены L368D/K370S : S364K.
860. MBM согласно варианту осуществления 857, где первый и второй варианты Fc-участков содержат аминокислотные замены L368E/K370S : S364K.
861. MBM согласно варианту осуществления 857, где первый и второй варианты Fc-участков содержат аминокислотные замены T411T/E360E/Q362E : D401K.
862. MBM согласно варианту осуществления 857, где первый и второй варианты Fc-участков содержат аминокислотные замены L368D 370S : S364/E357L.
863. MBM согласно варианту осуществления 857, где первый и второй варианты Fc-участков содержат аминокислотные замены 370S : S364K/E357Q.
864. MBM согласно варианту осуществления 857, где первый и второй варианты Fc-участков содержат аминокислотные замены из любого из стерических вариантов, перечисленных на фигуре 4 из WO 2014/110601 (которые воспроизведены в таблице 3).
865. MBM согласно варианту осуществления 857, где первый и второй варианты Fc-участков содержат аминокислотные замены из любого из вариантов, перечисленных на фигуре 5 из WO 2014/110601 (которые воспроизведены в таблице 3).
866. MBM согласно варианту осуществления 857, где первый и второй варианты Fc-участков содержат аминокислотные замены из любого из вариантов, перечисленных на фигуре 6 из WO 2014/110601 (которые воспроизведены в таблице 3).
867. MBM согласно любому из вариантов осуществления 857-866, где по меньшей мере один из Fc-участков содержит модификацию, обеспечивающую получение варианта с устранением связывания с Fcγ-рецепторами.
868. MBM согласно варианту осуществления 867, где модификации, обеспечивающие получение варианта с устранением связывания с Fcγ-рецепторами, выбраны из таблицы 2.
869. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя G236R.
870. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя S239G.
871. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя S239K.
872. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя S239Q.
873. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя S239R.
874. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя V266D.
875. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя S267K.
876. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя S267R.
877. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя H268K.
878. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя E269R.
879. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя 299R.
880. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя 299K.
881. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя K322A.
882. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя A327G.
883. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя A327L.
884. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя A327N.
885. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя A327Q.
886. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя L328E.
887. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя L328R.
888. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя P329A.
889. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя P329H.
890. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя P329K.
891. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя A330L.
892. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя A330S/P331S.
893. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя I332K.
894. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя I332R.
895. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя V266D/A327Q.
896. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя V266D/P329K.
897. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя G236R/L328R.
898. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя E233P/L234V/L235A/G236del/S239K.
899. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя E233P/L234V/L235A/G236del/S267K.
900. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя E233P/L234V/L235A/G236del/S239K/A327G.
901. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя E233P/L234V/L235A/G236del/S267K/A327G.
902. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя E233P/L234V/L235A/G236del.
903. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя S239K/S267K.
904. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя 267K/P329K.
905. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя D265A/N297A/P329A.
906. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя D265N/N297D/P329G.
907. MBM согласно варианту осуществления 868, где модификация, обеспечивающая получение варианта с устранением связывания с Fcγ-рецепторами, включает в себя D265E/N297Q/P329S.
908. MBM согласно любому из вариантов осуществления 867-907, где Fc-участок, содержащий модификацию, обеспечивающую получение варианта с устранением связывания с Fcγ-рецепторами, функционально связан с ABM1.
909. MBM согласно любому из вариантов осуществления 867-907, где Fc-участок, содержащий модификацию, обеспечивающую получение варианта с устранением связывания с Fcγ-рецепторами, функционально связан с ABM2.
910. MBM согласно любому из вариантов осуществления 867-907, где Fc-участок, содержащий модификацию, обеспечивающую получение варианта с устранением связывания с Fcγ-рецепторами, функционально связан с ABM3.
911. MBM согласно любому из вариантов осуществления 867-907, где оба варианта Fc-участка содержат модификацию, обеспечивающую получение варианта с устранением связывания с Fcγ-рецепторами.
912. MBM согласно любому из вариантов осуществления 857-911, где по меньшей мере один из Fc-участков дополнительно содержит замены, обеспечивающие получение pI-варианта.
913. MBM согласно варианту осуществления 912, где замены, обеспечивающие получение pI-варианта, выбраны из таблицы 3.
914. МBM согласно варианту осуществления 913, где замены, обеспечивающие получение pI-варианта, включают в себя замены, присутствующие в pI_ISO(-).
915. МBM согласно варианту осуществления 913, где замены, обеспечивающие получение pI-варианта, включают в себя замены, присутствующие в pI_(-)_изостерический_A.
916. МBM согласно варианту осуществления 913, где замены, обеспечивающие получение pI-варианта, включают в себя замены, присутствующие в pI_(-)_изостерический_B.
917. МBM согласно варианту осуществления 913, где замены, обеспечивающие получение pI-варианта, включают в себя замены, присутствующие в PI_ISO(+RR).
918. МBM согласно варианту осуществления 913, где замены, обеспечивающие получение pI-варианта, включают в себя замены, присутствующие в pI_ISO(+).
919. МBM согласно варианту осуществления 913, где замены, обеспечивающие получение pI-варианта, включают в себя замены, присутствующие в pI_(+)_изостерический_A.
920. МBM согласно варианту осуществления 913, где замены, обеспечивающие получение pI-варианта, включают в себя замены, присутствующие в pI_(+)_изостерический_B.
921. МBM согласно варианту осуществления 913, где замены, обеспечивающие получение pI-варианта, включают в себя замены, присутствующие в pI_(+)_изостерический_E269Q/E272Q.
922. МBM согласно варианту осуществления 913, где замены, обеспечивающие получение pI-варианта, включают в себя замены, присутствующие в pI_(+)_изостерический_E269Q/E283Q.
923. МBM согласно варианту осуществления 913, где замены, обеспечивающие получение pI-варианта, включают в себя замены, присутствующие в pI_(+)_изостерический_E2720/E283Q.
924. МBM согласно варианту осуществления 913, где замены, обеспечивающие получение pI-варианта, включают в себя замены, присутствующие в pI_(+)_изостерический_E269Q.
925. MBM согласно любому из вариантов осуществления 857-924, где первый и/или второй Fc-участки дополнительно содержат одну или более аминокислотных замен, выбранных из 434A, 434S, 428L, 308F, 259I, 428L/434S, 259I/308F, 436I/428L, 4361 или V/434S, 436V/428L, 252Y, 252Y/254T/256E, 259I/308F/428L, 236A, 239D, 239E, 332E, 332D, 239D/332E, 267D, 267E, 328F, 267E/328F, 236A/332E, 239D/332E/330Y, 239D, 332E/330L, 236R, 328R, 236R/328R, 236N/267E, 243L, 298A и 299T.
926. MBM согласно любому из вариантов осуществления 857-924, где первый и/или второй Fc-участки дополнительно содержат аминокислотную замену 434A, 434S или 434V.
927. MBM согласно варианту осуществления 926, где первый и/или второй Fc-участки дополнительно содержат аминокислотную замену 428L.
928. MBM согласно любому из вариантов осуществления 926-927, где первый и/или второй Fc-участки дополнительно содержат аминокислотную замену 308F.
929. MBM согласно любому из вариантов осуществления 926-928, где первый и/или второй Fc-участки дополнительно содержат аминокислотную замену 259I.
930. MBM согласно любому из вариантов осуществления 926-929, где первый и/или второй Fc-участки дополнительно содержат аминокислотную замену 436I.
931. MBM согласно любому из вариантов осуществления 926-930, где первый и/или второй Fc-участки дополнительно содержат аминокислотную замену 252Y.
932. MBM согласно любому из вариантов осуществления 926-931, где первый и/или второй Fc-участки дополнительно содержат аминокислотную замену 254T.
933. MBM согласно любому из вариантов осуществления 926-932, где первый и/или второй Fc-участки дополнительно содержат аминокислотную замену 256E.
934. MBM согласно любому из вариантов осуществления 926-933, где первый и/или второй Fc-участки дополнительно содержат аминокислотную замену 239D или 239E.
935. MBM согласно любому из вариантов осуществления 926-934, где первый и/или второй Fc-участки дополнительно содержат аминокислотную замену 332E или 332D.
936. MBM согласно любому из вариантов осуществления 926-935, где первый и/или второй Fc-участки дополнительно содержат аминокислотную замену 267D или 267E.
937. MBM согласно любому из вариантов осуществления 926-936, где первый и/или второй Fc-участки дополнительно содержат аминокислотную замену 330L.
938. MBM согласно любому из вариантов осуществления 926-937, где первый и/или второй Fc-участки дополнительно содержат аминокислотную замену 236R или 236N.
939. MBM согласно любому из вариантов осуществления 926-938, где первый и/или второй Fc-участки дополнительно содержат аминокислотную замену 328R.
940. MBM согласно любому из вариантов осуществления 926-939, где первый и/или второй Fc-участки дополнительно содержат аминокислотную замену 243L.
941. MBM согласно любому из вариантов осуществления 926-940, где первый и/или второй Fc-участки дополнительно содержат аминокислотную замену 298A.
942. MBM согласно любому из вариантов осуществления 926-941, где первый и/или второй Fc-участки дополнительно содержат аминокислотную замену 299T.
943. MBM согласно варианту осуществления 857, где:
(a) первый и второй варианты Fc-участков содержат аминокислотные замены S364K/E357Q : L368D/K370S;
(b) первый и/или второй варианты Fc-участков содержат модификации E233P/L234V/L235A/G236del/S267K, обеспечивающие получение варианта с устранением связывания с Fcγ-рецепторами, и
(c) первый и/или второй варианты Fc-участков содержат замены N208D/Q295E/N384D/Q418E/N421D, обеспечивающие получение pI-варианта (pl_(-)_изостерический_A).
944. MBM согласно варианту осуществления 943, где первый вариант Fc-участка содержит модификации E233P/L234V/L235A/G236del/S267K, обеспечивающие получение варианта с устранением связывания с Fcγ-рецепторами.
945. MBM согласно любому из вариантов осуществления 943-944, где второй вариант Fc-участка содержит модификации E233P/L234V/L235A/G236del/S267K, обеспечивающие получение варианта с устранением связывания с Fcγ-рецепторами.
946. MBM согласно любому из вариантов осуществления 943-945, где первый вариант Fc-участка содержит замены N208D/Q295E/N384D/Q418E/N421D, обеспечивающие получение pI-варианта (pl_(-)_изостерический_A).
947. MBM согласно любому из вариантов осуществления 943-946, где второй вариант Fc-участка содержит замены N208D/Q295E/N384D/Q418E/N421D, обеспечивающие получение pI-варианта (pl_(-)_изостерический_A).
948. MBM согласно любому из вариантов осуществления 857-947, где первый или второй варианты Fc-участка содержат аминокислотную последовательность, которая на по меньшей мере 90% идентична SEQ ID NO: 869.
949. MBM согласно любому из вариантов осуществления 857-947, где первый или второй варианты Fc-участка содержат аминокислотную последовательность, которая на по меньшей мере 95% идентична SEQ ID NO: 869.
950. MBM согласно любому из вариантов осуществления 857-947, где первый или второй варианты Fc-участка содержат аминокислотную последовательность под SEQ ID NO: 869, модифицированную с помощью замен, перечисленных в любом из вариантов осуществления 858-947.
951. MBM согласно любому из вариантов осуществления 857-947, где первый или второй варианты Fc-участка содержат аминокислотную последовательность под SEQ ID NO: 869 с заменой в 1, 2, 3, 4, 5 или 6 из положений 233, 234, 235, 236, 237, 239, 265, 266, 267, 268, 269, 297, 299, 322, 327, 328, 329, 330, 331 и 332, где одна или более замен необязательно представляют собой замены, перечисленные в любом из вариантов осуществления 858-947.
952. MBM согласно любому из вариантов осуществления 857-951, где первый или второй варианты Fc-участка содержат аминокислотную последовательность, которая на по меньшей мере 90% идентична SEQ ID NO: 870.
953. MBM согласно любому из вариантов осуществления 857-951, где первый или второй варианты Fc-участка содержат аминокислотную последовательность, которая на по меньшей мере 95% идентична SEQ ID NO: 870.
954. MBM согласно любому из вариантов осуществления 857-951, где первый или второй варианты Fc-участка содержат аминокислотную последовательность под SEQ ID NO: 870, модифицированную с помощью замен, перечисленных в любом из вариантов осуществления 858-947.
955. MBM согласно любому из вариантов осуществления 857-951, где первый или второй варианты Fc-участка содержат аминокислотную последовательность под SEQ ID NO: 870 с заменой в 1, 2, 3, 4, 5 или 6 из положений 233, 234, 235, 236, 237, 239, 265, 266, 267, 268, 269, 297, 299, 322, 327, 328, 329, 330, 331 и 332, где одна или более замен необязательно представляют собой замены, перечисленные в любом из вариантов осуществления 858-947.
956. MBM согласно любому из вариантов осуществления 857-951, где первый или второй варианты Fc-участка содержат аминокислотную последовательность, которая на по меньшей мере 90% идентична SEQ ID NO: 871.
957. MBM согласно любому из вариантов осуществления 857-951, где первый или второй варианты Fc-участка содержат аминокислотную последовательность, которая на по меньшей мере 95% идентична SEQ ID NO: 871.
958. MBM согласно любому из вариантов осуществления 857-951, где первый или второй варианты Fc-участка содержат аминокислотную последовательность под SEQ ID NO: 871, модифицированную с помощью замен, перечисленных в любом из вариантов осуществления 858-947.
959. MBM согласно любому из вариантов осуществления 857-951, где первый или второй варианты Fc-участка содержат аминокислотную последовательность под SEQ ID NO: 871 с заменой в 1, 2, 3, 4, 5 или 6 из положений 233, 234, 235, 236, 237, 239, 265, 266, 267, 268, 269, 297, 299, 322, 327, 328, 329, 330, 331 и 332, где одна или более замен необязательно представляют собой замены, перечисленные в любом из вариантов осуществления 858-947.
960. MBM согласно любому из вариантов осуществления 857-959, где первый или второй варианты Fc-участка содержат аминокислотную последовательность, которая на по меньшей мере 90% идентична SEQ ID NO: 872.
961. MBM согласно любому из вариантов осуществления 857-959, где первый или второй варианты Fc-участка содержат аминокислотную последовательность, которая на по меньшей мере 95% идентична SEQ ID NO: 872.
962. MBM согласно любому из вариантов осуществления 857-959, где первый или второй варианты Fc-участка содержат аминокислотную последовательность под SEQ ID NO: 872, модифицированную с помощью замен, перечисленных в любом из вариантов осуществления 858-947.
963. MBM согласно любому из вариантов осуществления 857-959, где первый или второй варианты Fc-участка содержат аминокислотную последовательность под SEQ ID NO: 872 с заменой в 1, 2, 3, 4, 5 или 6 из положений 233, 234, 235, 236, 237, 239, 265, 266, 267, 268, 269, 297, 299, 322, 327, 328, 329, 330, 331 и 332, где одна или более замен необязательно представляют собой замены, перечисленные в любом из вариантов осуществления 858-947.
964. МBM согласно любому из вариантов осуществления 1-856, которая содержит Fc-домен.
965. МBM согласно варианту осуществления 964, где Fc-домен представляет собой гетеродимер Fc.
966. MBM согласно варианту осуществления 965, где гетеродимер Fc содержит любую из модификаций Fc, представленных в таблице 3.
967. МBM согласно варианту осуществления 965, где гетеродимер Fc содержит модификации типа "выступ во впадину" ("KIH").
968. МBM согласно варианту осуществления 967, где KIH-модификации являются любыми из KIH-модификаций, описанных в разделе 7.3.1.5.1 или в таблице 3.
969. МBM согласно варианту осуществления 967, где KIH-модификации являются любыми из альтернативных KIH-модификаций, описанных в разделе 7.3.1.5.2 или в таблице 3.
970. МBM согласно любому из вариантов осуществления 965-969, которая содержит модификации типа полярных мостиков.
971. МBM согласно варианту осуществления 970, где модификации типа полярных мостиков являются любыми из модификаций типа полярных мостиков, описанных в разделе 7.3.1.5.7 или в таблице 3.
972. МBM согласно любому из вариантов осуществления 965-971, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 1 - Fc 150.
973. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 1 - Fc 5.
974. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 6 - Fc 10.
975. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 11 - Fc 15.
976. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 16 - Fc 20.
977. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 21 - Fc 25.
978. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 26 - Fc 30.
979. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 31 - Fc 35.
980. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 36 - Fc 40.
981. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 41 - Fc 45.
982. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 46 - Fc 50.
983. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 51 - Fc 55.
984. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 56 - Fc 60.
985. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 61 - Fc 65.
986. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 66 - Fc 70.
987. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 71 - Fc 75.
988. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 76 - Fc 80.
989. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 81 - Fc 85.
990. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 86 - Fc 90.
991. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 91 - Fc 95.
992. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 96 - Fc 100.
993. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 101 - Fc 105.
994. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 106 - Fc 110.
995. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 111 - Fc 115.
996. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 116 - Fc 120.
997. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 121 - Fc 125.
998. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 126 - Fc 130.
999. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 131 - Fc 135.
1000. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 136 - Fc 140.
1001. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 141 - Fc 145.
1002. МBM согласно варианту осуществления 972, которая содержит по меньшей мере одну из модификаций Fc, обозначенных как Fc 146 - Fc 150.
1003. MBM согласно любому из вариантов осуществления 964-1002, где Fc-домен характеризуется измененной эффекторной функцией.
1004. МBM согласно варианту осуществления 1003, где Fc-домен характеризуется измененным связыванием с одним или более Fc-рецепторами.
1005. МBM согласно варианту осуществления 1004, где один или более Fc-рецепторов включают в себя FcRN.
1006. МBM согласно варианту осуществления 1004 или варианту осуществления 1005, где один или более Fc-рецепторов включают в себя лейкоцитарные рецепторы.
1007. MBM согласно любому из вариантов осуществления 964-1006, где Fc характеризуется модифицированной архитектурой дисульфидных связей.
1008. МBM согласно любому из вариантов осуществления 964-1007, где Fc характеризуется измененными паттернами гликозилирования.
1009. МBM согласно любому из вариантов осуществления 964-1008, где Fc содержит шарнирный участок.
1010. МBM согласно варианту осуществления 1009, где шарнирный участок включает в себя любой из шарнирных участков, описанных в разделе 7.3.2.
1011. МBM согласно варианту осуществления 1010, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H1.
1012. МBM согласно варианту осуществления 1010, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H2.
1013. МBM согласно варианту осуществления 1010, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H3.
1014. МBM согласно варианту осуществления 1010, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H4.
1015. МBM согласно варианту осуществления 1010, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H5.
1016. МBM согласно варианту осуществления 1010, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H6.
1017. МBM согласно варианту осуществления 1010, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H7.
1018. МBM согласно варианту осуществления 1010, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H8.
1019. МBM согласно варианту осуществления 1010, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H9.
1020. МBM согласно варианту осуществления 1010, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H10.
1021. МBM согласно варианту осуществления 1010, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H11.
1022. МBM согласно варианту осуществления 1010, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H12.
1023. МBM согласно варианту осуществления 1010, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H13.
1024. МBM согласно варианту осуществления 1010, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H14.
1025. МBM согласно варианту осуществления 1010, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H15.
1026. МBM согласно варианту осуществления 1010, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H16.
1027. МBM согласно варианту осуществления 1010, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H17.
1028. МBM согласно варианту осуществления 1010, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H18.
1029. МBM согласно варианту осуществления 1010, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H19.
1030. МBM согласно варианту осуществления 1010, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H20.
1031. МBM согласно варианту осуществления 1010, где шарнирный участок содержит аминокислотную последовательность шарнирного участка, обозначенного как H21.
1032. МBM согласно любому из вариантов осуществления 1-1031, которая содержит по меньшей мере один scFv-домен.
1033. МBM согласно варианту осуществления 1032, где по меньшей мере один scFv содержит линкер, соединяющий VH- и VL-домены.
1034. МBM согласно варианту осуществления 1033, где длина линкера составляет 5-25 аминокислот.
1035. МBM согласно варианту осуществления 1034, где длина линкера составляет 12-20 аминокислот.
1036. МBM согласно любому из вариантов осуществления 1033-1035, где линкер представляет собой заряженный линкер и/или гибкий линкер.
1037. МBM согласно любому из вариантов осуществления 1033-1036, где линкер выбран из любого из линкеров L1 - L54.
1038. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L1.
1039. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L2.
1040. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L3.
1041. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L4.
1042. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L5.
1043. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L6.
1044. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L7.
1045. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L8.
1046. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L9.
1047. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L10.
1048. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L11.
1049. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L12.
1050. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L13.
1051. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L14.
1052. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L15.
1053. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L16.
1054. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L17.
1055. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L18.
1056. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L19.
1057. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L20.
1058. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L21.
1059. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L22.
1060. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L23.
1061. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L24.
1062. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L25.
1063. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L26.
1064. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L27.
1065. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L28.
1066. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L29.
1067. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L30.
1068. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L31.
1069. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L32.
1070. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L33.
1071. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L34.
1072. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L35.
1073. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L36.
1074. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L37.
1075. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L38.
1076. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L39.
1077. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L40.
1078. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L41.
1079. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L42.
1080. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L43.
1081. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L44.
1082. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L45.
1083. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L46.
1084. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L47.
1085. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L48.
1086. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L49.
1087. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L50.
1088. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L51.
1089. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L52.
1090. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L53.
1091. МBM согласно варианту осуществления 1037, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L54.
1092. МBM согласно любому из вариантов осуществления 1-1091, которая содержит по меньшей мере один Fab-домен.
1093. МBM согласно варианту осуществления 1092, где по меньшей мере один Fab-домен содержит любые из модификаций, обеспечивающих гетеродимеризацию Fab, представленных в таблице 1.
1094. МBM согласно варианту осуществления 1093, где по меньшей мере один Fab-домен содержит модификации, обеспечивающие гетеродимеризацию Fab, обозначенные как F1.
1095. МBM согласно варианту осуществления 1093, где по меньшей мере один Fab-домен содержит модификации, обеспечивающие гетеродимеризацию Fab, обозначенные как F2.
1096. МBM согласно варианту осуществления 1093, где по меньшей мере один Fab-домен содержит модификации, обеспечивающие гетеродимеризацию Fab, обозначенные как F3.
1097. МBM согласно варианту осуществления 1093, где по меньшей мере один Fab-домен содержит модификации, обеспечивающие гетеродимеризацию Fab, обозначенные как F4.
1098. МBM согласно варианту осуществления 1093, где по меньшей мере один Fab-домен содержит модификации, обеспечивающие гетеродимеризацию Fab, обозначенные как F5.
1099. МBM согласно варианту осуществления 1093, где по меньшей мере один Fab-домен содержит модификации, обеспечивающие гетеродимеризацию Fab, обозначенные как F6.
1100. МBM согласно варианту осуществления 1093, где по меньшей мере один Fab-домен содержит модификации, обеспечивающие гетеродимеризацию Fab, обозначенные как F7.
1101. MBM согласно любому из вариантов осуществления 1-1100, которая содержит по меньшей мере два ABM, ABM и цепь ABM или две цепи ABM, соединенные друг с другом посредством линкера.
1102. МBM согласно варианту осуществления 1101, где длина линкера составляет 5-25 аминокислот.
1103. МBM согласно варианту осуществления 1102, где длина линкера составляет 12-20 аминокислот.
1104. МBM согласно любому из вариантов осуществления 1101-1103, где линкер представляет собой заряженный линкер и/или гибкий линкер.
1105. МBM согласно любому из вариантов осуществления 1101-1104, где линкер выбран из любого из линкеров L1 - L54.
1106. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L1.
1107. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L2.
1108. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L3.
1109. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L4.
1110. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L5.
1111. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L6.
1112. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L7.
1113. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L8.
1114. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L9.
1115. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L10.
1116. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L11.
1117. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L12.
1118. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L13.
1119. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L14.
1120. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L15.
1121. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L16.
1122. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L17.
1123. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L18.
1124. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L19.
1125. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L20.
1126. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L21.
1127. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L22.
1128. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L23.
1129. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L24.
1130. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L25.
1131. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L26.
1132. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L27.
1133. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L28.
1134. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L29.
1135. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L30.
1136. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L31.
1137. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L32.
1138. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L33.
1139. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L34.
1140. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L35.
1141. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L36.
1142. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L37.
1143. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L38.
1144. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L39.
1145. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L40.
1146. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L41.
1147. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L42.
1148. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L43.
1149. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L44.
1150. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L45.
1151. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L46.
1152. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L47.
1153. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L48.
1154. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L49.
1155. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L50.
1156. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L51.
1157. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L52.
1158. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L53.
1159. МBM согласно варианту осуществления 1105, где линкерный участок содержит аминокислотную последовательность линкера, обозначенного как L54.
1160. МBM согласно любому из вариантов осуществления 1-1159, которая представляет собой тривалентную МBM.
1161. МBM согласно варианту осуществления 1160, где тривалентная МBM имеет любую из конфигураций, изображенных на фиг. 1B-1P.
1162. МBM согласно варианту осуществления 1161, где тривалентная МBM имеет конфигурацию, изображенную на фиг. 1B.
1163. МBM согласно варианту осуществления 1161, где тривалентная МBM имеет конфигурацию, изображенную на фиг. 1C.
1164. МBM согласно варианту осуществления 1161, где тривалентная МBM имеет конфигурацию, изображенную на фиг. 1D.
1165. МBM согласно варианту осуществления 1161, где тривалентная МBM имеет конфигурацию, изображенную на фиг. 1E.
1166. МBM согласно варианту осуществления 1161, где тривалентная МBM имеет конфигурацию, изображенную на фиг. 1F.
1167. МBM согласно варианту осуществления 1161, где тривалентная МBM имеет конфигурацию, изображенную на фиг. 1G.
1168. МBM согласно варианту осуществления 1161, где тривалентная МBM имеет конфигурацию, изображенную на фиг. 1H.
1169. МBM согласно варианту осуществления 1161, где тривалентная МBM имеет конфигурацию, изображенную на фиг. 1I.
1170. МBM согласно варианту осуществления 1161, где тривалентная МBM имеет конфигурацию, изображенную на фиг. 1J.
1171. МBM согласно варианту осуществления 1161, где тривалентная МBM имеет конфигурацию, изображенную на фиг. 1K.
1172. МBM согласно варианту осуществления 1161, где тривалентная МBM имеет конфигурацию, изображенную на фиг. 1L.
1173. МBM согласно варианту осуществления 1161, где тривалентная МBM имеет конфигурацию, изображенную на фиг. 1M.
1174. МBM согласно варианту осуществления 1161, где тривалентная МBM имеет конфигурацию, изображенную на фиг. 1N.
1175. МBM согласно варианту осуществления 1161, где тривалентная МBM имеет конфигурацию, изображенную на фиг. 1O.
1176. МBM согласно варианту осуществления 1161, где тривалентная МBM имеет конфигурацию, изображенную на фиг. 1P.
1177. МBM согласно любому из вариантов осуществления 1161-1176, в которой ABM имеют конфигурацию, обозначенную как T1.
1178. МBM согласно любому из вариантов осуществления 1161-1176, в которой ABM имеют конфигурацию, обозначенную как T2.
1179. МBM согласно любому из вариантов осуществления 1161-1176, в которой ABM имеют конфигурацию, обозначенную как T3.
1180. МBM согласно любому из вариантов осуществления 1161-1176, в которой ABM имеют конфигурацию, обозначенную как T4.
1181. МBM согласно любому из вариантов осуществления 1161-1176, в которой ABM имеют конфигурацию, обозначенную как T5.
1182. МBM согласно любому из вариантов осуществления 1161-1176, в которой ABM имеют конфигурацию, обозначенную как T6.
1183. МBM согласно любому из вариантов осуществления 1-1159, которая представляет собой тетравалентную МBM.
1184. МBM согласно варианту осуществления 1183, где тетравалентная МBM имеет любую из конфигураций, изображенных на фиг. 1Q-1S.
1185. МBM согласно варианту осуществления 1184, где тетравалентная МBM имеет конфигурацию, изображенную на фиг. 1Q.
1186. МBM согласно варианту осуществления 1184, где тетравалентная МBM имеет конфигурацию, изображенную на фиг. 1R.
1187. МBM согласно варианту осуществления 1184, где тетравалентная МBM имеет конфигурацию, изображенную на фиг. 1S.
1188. МBM согласно любому из вариантов осуществления 1184-1187, в которой ABM имеют любую из конфигураций, обозначенных как Tv 1 - Tv 24.
1189. МBM согласно варианту осуществления 1188, в которой ABM имеют конфигурацию, обозначенную как Tv 1.
1190. МBM согласно варианту осуществления 1188, в которой ABM имеют конфигурацию, обозначенную как Tv 2.
1191. МBM согласно варианту осуществления 1188, в которой ABM имеют конфигурацию, обозначенную как Tv 3.
1192. МBM согласно варианту осуществления 1188, в которой ABM имеют конфигурацию, обозначенную как Tv 4.
1193. МBM согласно варианту осуществления 1188, в которой ABM имеют конфигурацию, обозначенную как Tv 5.
1194. МBM согласно варианту осуществления 1188, в которой ABM имеют конфигурацию, обозначенную как Tv 6.
1195. МBM согласно варианту осуществления 1188, в которой ABM имеют конфигурацию, обозначенную как Tv 7.
1196. МBM согласно варианту осуществления 1188, в которой ABM имеют конфигурацию, обозначенную как Tv 8.
1197. МBM согласно варианту осуществления 1188, в которой ABM имеют конфигурацию, обозначенную как Tv 9.
1198. МBM согласно варианту осуществления 1188, в которой ABM имеют конфигурацию, обозначенную как Tv 10.
1199. МBM согласно варианту осуществления 1188, в которой ABM имеют конфигурацию, обозначенную как Tv 11.
1200. МBM согласно варианту осуществления 1188, в которой ABM имеют конфигурацию, обозначенную как Tv 12.
1201. МBM согласно варианту осуществления 1188, в которой ABM имеют конфигурацию, обозначенную как Tv 13.
1202. МBM согласно варианту осуществления 1188, в которой ABM имеют конфигурацию, обозначенную как Tv 14.
1203. МBM согласно варианту осуществления 1188, в которой ABM имеют конфигурацию, обозначенную как Tv 15.
1204. МBM согласно варианту осуществления 1188, в которой ABM имеют конфигурацию, обозначенную как Tv 16.
1205. МBM согласно варианту осуществления 1188, в которой ABM имеют конфигурацию, обозначенную как Tv 17.
1206. МBM согласно варианту осуществления 1188, в которой ABM имеют конфигурацию, обозначенную как Tv 18.
1207. МBM согласно варианту осуществления 1188, в которой ABM имеют конфигурацию, обозначенную как Tv 19.
1208. МBM согласно варианту осуществления 1188, в которой ABM имеют конфигурацию, обозначенную как Tv 20.
1209. МBM согласно варианту осуществления 1188, в которой ABM имеют конфигурацию, обозначенную как Tv 21.
1210. МBM согласно варианту осуществления 1188, в которой ABM имеют конфигурацию, обозначенную как Tv 22.
1211. МBM согласно варианту осуществления 1188, в которой ABM имеют конфигурацию, обозначенную как Tv 23.
1212. МBM согласно варианту осуществления 1188, в которой ABM имеют конфигурацию, обозначенную как Tv 24.
1213. МBM согласно любому из вариантов осуществления 1-1159, которая представляет собой пентавалентную МBM.
1214. МBM согласно варианту осуществления 1213, где пентавалентная МBM имеет конфигурацию, изображенную на фиг. 1T.
1215. МBM согласно варианту осуществления 1214, в которой ABM имеют любую из конфигураций, обозначенных как Pv 1 - Pv 80.
1216. МBM согласно варианту осуществления 1215, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Pv 1 - Pv 10.
1217. МBM согласно варианту осуществления 1215, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Pv 11 - Pv 20.
1218. МBM согласно варианту осуществления 1215, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Pv 21 - Pv 30.
1219. МBM согласно варианту осуществления 1215, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Pv 31 - Pv 40.
1220. МBM согласно варианту осуществления 1215, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Pv 41 - Pv 50.
1221. МBM согласно варианту осуществления 1215, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Pv 51 - Pv 60.
1222. МBM согласно варианту осуществления 1215, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Pv 61 - Pv 70.
1223. МBM согласно варианту осуществления 1215, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Pv 71 - Pv 80.
1224. МBM согласно варианту осуществления 1215, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Pv 81 - Pv 90.
1225. МBM согласно варианту осуществления 1215, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Pv 91 - Pv 100.
1226. МBM согласно любому из вариантов осуществления 1-1159, которая представляет собой гексавалентную МBM.
1227. МBM согласно варианту осуществления 1226, где гексавалентная МBM имеет конфигурацию, изображенную на фиг. 1U или фиг. 1V.
1228. МBM согласно варианту осуществления 1227, где гексавалентная МBM имеет конфигурацию, изображенную на фиг. 1U.
1229. МBM согласно варианту осуществления 1227, где гексавалентная МBM имеет конфигурацию, изображенную на фиг. 1V.
1230. МBM согласно любому из вариантов осуществления 1227-1229, в которой ABM имеют любую из конфигураций, обозначенных как Hv 1 - Hv 330.
1231. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 1 - Hv 10.
1232. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 11 - Hv 20.
1233. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 21 - Hv 30.
1234. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 31 - Hv 40.
1235. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 41 - Hv 50.
1236. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 51 - Hv 60.
1237. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 61 - Hv 70.
1238. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 71 - Hv 80.
1239. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 81 - Hv 90.
1240. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 91 - Hv 100.
1241. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 101 - Hv 110.
1242. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 111 - Hv 120.
1243. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 121 - Hv 130.
1244. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 131 - Hv 140.
1245. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 141 - Hv 150.
1246. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 151 - Hv 160.
1247. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 161 - Hv 70.
1248. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 171 - Hv 80.
1249. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 181 - Hv 90.
1250. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 191 - Hv 200.
1251. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 201 - Hv 210.
1252. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 211 - Hv 220.
1253. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 221 - Hv 230.
1254. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 231 - Hv 240.
1255. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 241 - Hv 250.
1256. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 251 - Hv 260.
1257. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 261 - Hv 270.
1258. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 271 - Hv 280.
1259. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 281 - Hv 290.
1260. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 291 - Hv 300.
1261. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 301 - Hv 310.
1262. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 311 - Hv 320.
1263. МBM согласно варианту осуществления 1230, в которой ABM имеют конфигурацию, выбранную из любой из конфигураций, обозначенных как Hv 321 - Hv 330.
1264. MBM согласно любому из вариантов осуществления 1-1263, где каждый антигенсвязывающий модуль способен к связыванию своей соответствующей мишени одновременно со связыванием каждого из других антигенсвязывающих модулей со своей соответствующей мишенью.
1265. МBM согласно любому из вариантов осуществления 1-1264, где любой один, любые два или все три из ABM1, ABM2 и ABM3 обладают межвидовой перекрестной реактивностью.
1266. МBM согласно варианту осуществления 1265, где ABM1 дополнительно специфично связывается с BCMA у одного или более видов млекопитающих, отличных от человека.
1267. MBM согласно варианту осуществления 1265 или варианту осуществления 1266, где ABM2 дополнительно специфично связывается с компонентом комплекса TCR у одного или более видов млекопитающих, отличных от человека.
1268. MBM согласно любому из вариантов осуществления 1264-1267, где ABM3 дополнительно специфично связывается с CD2 или TAA у одного или более видов млекопитающих, отличных от человека.
1269. МBM согласно любому из вариантов осуществления 1265-1268, где один или более видов млекопитающих, отличных от человека, включают в себя один или более видов приматов, отличных от человека.
1270. MBM согласно варианту осуществления 1269, где один или более видов приматов, отличных от человека, включают в себя Macaca fascicularis.
1271. MBM согласно варианту осуществления 1269, где один или более видов приматов, отличных от человека, включают в себя Macaca mulatta.
1272. MBM согласно варианту осуществления 1269, где один или более видов приматов, отличных от человека, включают в себя Macaca nemestrina.
1273. MBM согласно любому из вариантов осуществления 1265-1272, где один или более видов млекопитающих, отличных от человека, включают в себя Mus musculus.
1274. МBM согласно любому из вариантов осуществления 1-1273, где любой один, любые два или все три из ABM1, ABM2 и ABM3 не обладают межвидовой перекрестной реактивностью.
1275. МBM согласно любому из вариантов осуществления 1-1274, которая была получена рекомбинантным путем, необязательно в клетке-хозяине, являющейся клеткой млекопитающего, которая необязательно выбрана из клеток Vero, клеток HeLa, клеток COS, клеток CHO, клеток HEK293, клеток BHK и клеток MDCKII.
1276. MBM согласно любому из вариантов осуществления 1-1275, где MBM представляет собой триспецифическую связывающую молекулу (TBM).
1277. MBM согласно любому из вариантов осуществления 1-1276 для применения в качестве лекарственного препарата.
1278. MBM согласно любому из вариантов осуществления 1-1276 для применения в лечении заболевания или нарушения, ассоциированного с экспрессией ВСМА.
1279. MBM согласно варианту осуществления 1278, где заболевание или нарушение включает в себя рак.
1280. MBM согласно варианту осуществления 1279, где рак включает в себя В-клеточное злокачественное новообразование.
1281. MBM согласно варианту осуществления 1280, где В-клеточное злокачественное новообразование выбрано из лимфомы Ходжкина, неходжкинской лимфомы и множественной миеломы.
1282. MBM согласно варианту осуществления 1279, где рак представляет собой лимфому Ходжкина.
1283. MBM согласно варианту осуществления 1282, где лимфома Ходжкина представляет собой лимфому Ходжкина с нодулярным склерозом.
1284. MBM согласно варианту осуществления 1282, где лимфома Ходжкина представляет собой лимфому Ходжкина смешанно-клеточного подтипа.
1285. MBM согласно варианту осуществления 1282, где лимфома Ходжкина представляет собой лимфому Ходжкина, богатую лимфоцитами или с лимфоидным преобладанием.
1286. MBM согласно варианту осуществления 1282, где лимфома Ходжкина представляет собой лимфому Ходжкина с лимфоидным истощением.
1287. MBM согласно варианту осуществления 1279, где рак представляет собой неходжкинскую лимфому.
1288. MBM согласно варианту осуществления 1287, где неходжкинская лимфома представляет собой В-клеточную лимфому или Т-клеточную лимфому.
1289. MBM согласно варианту осуществления 1287, где неходжкинская лимфома представляет собой В-клеточную лимфому.
1290. MBM согласно варианту осуществления 1287, где неходжкинская лимфома представляет собой диффузную крупноклеточную В-клеточную лимфому (DLBCL), фолликулярную лимфому, хронический лимфоцитарный лейкоз (CLL)/мелкоклеточную лимфоцитарную лимфому (SLL), мантийноклеточную лимфому (MCL), лимфому из клеток маргинальной зоны, лимфому Беркитта, лимфоплазмоцитарную лимфому (макроглобулинемию Вальденстрема), волосатоклеточный лейкоз, первичную лимфому центральной нервной системы (CNS), первичную медиастинальную крупноклеточную В-клеточную лимфому, медиастинальную лимфому "серой зоны" (MGZL), B-клеточную лимфому из клеток маргинальной зоны селезенки, внеузловую B-клеточную лимфому из клеток маргинальной зоны MALT, узловую B-клеточную лимфому из клеток маргинальной зоны или первичную эффузионную лимфому.
1291. MBM согласно варианту осуществления 1290, где неходжкинская лимфома представляет собой диффузную крупноклеточную В-клеточную лимфому (DLBCL).
1292. MBM согласно варианту осуществления 1290, где неходжкинская лимфома представляет собой фолликулярную лимфому.
1293. MBM согласно варианту осуществления 1290, где неходжкинская лимфома представляет собой хронический лимфоцитарный лейкоз (CLL)/мелкоклеточную лимфоцитарную лимфому (SLL).
1294. MBM согласно варианту осуществления 1290, где неходжкинская лимфома представляет собой мантийноклеточную лимфому (MCL).
1295. MBM согласно варианту осуществления 1290, где неходжкинская лимфома представляет собой лимфому из клеток маргинальной зоны.
1296. MBM согласно варианту осуществления 1290, где неходжкинская лимфома представляет собой лимфому Беркитта.
1297. MBM согласно варианту осуществления 1290, где неходжкинская лимфома представляет собой лимфоплазмоцитарную лимфому (макроглобулинемию Вальденстрема).
1298. MBM согласно варианту осуществления 1290, где неходжкинская лимфома представляет собой волосатоклеточный лейкоз.
1299. MBM согласно варианту осуществления 1290, где неходжкинская лимфома представляет собой первичную лимфому центральной нервной системы (CNS).
1300. MBM согласно варианту осуществления 1290, где неходжкинская лимфома представляет собой первичную медиастинальную крупноклеточную В-клеточную лимфому.
1301. MBM согласно варианту осуществления 1290, где неходжкинская лимфома представляет собой медиастинальную лимфому "серой зоны" (MGZL).
1302. MBM согласно варианту осуществления 1290, где неходжкинская лимфома представляет собой B-клеточную лимфому из клеток маргинальной зоны селезенки.
1303. MBM согласно варианту осуществления 1290, где неходжкинская лимфома представляет собой внеузловую B-клеточную лимфому из клеток маргинальной зоны MALT.
1304. MBM согласно варианту осуществления 1290, где неходжкинская лимфома представляет собой узловую B-клеточную лимфому из клеток маргинальной зоны.
1305. MBM согласно варианту осуществления 1290, где неходжкинская лимфома представляет собой первичную эффузионную лимфому.
1306. MBM согласно варианту осуществления 1287, где неходжкинская лимфома представляет собой T-клеточную лимфому.
1307. MBM согласно варианту осуществления 1306, где неходжкинская лимфома представляет собой анапластическую крупноклеточную лимфому (ALCL), Т-клеточную лимфому/лейкоз взрослых, лимфангиому, ангиоиммунобластную Т-клеточную лимфому, Т-клеточную лимфому кожи, внеузловую лимфому из естественных киллеров/T-клеток, Т-клеточную лимфому кишечника энтеропатического типа, T-лимфобластную лимфому/лейкоз из клеток-предшественников (T-LBL/L) или неуточненную периферическую Т-клеточную лимфому.
1308. MBM согласно варианту осуществления 1307, где неходжкинская лимфома представляет собой анапластическую крупноклеточную лимфому (ALCL).
1309. MBM согласно варианту осуществления 1307, где неходжкинская лимфома представляет собой Т-клеточную лимфому/лейкоз взрослых.
1310. MBM согласно варианту осуществления 1307, где неходжкинская лимфома представляет собой лимфангиому.
1311. MBM согласно варианту осуществления 1307, где неходжкинская лимфома представляет собой ангиоиммунобластную Т-клеточную лимфому.
1312. MBM согласно варианту осуществления 1307, где неходжкинская лимфома представляет собой Т-клеточную лимфому кожи.
1313. MBM согласно варианту осуществления 1307, где неходжкинская лимфома представляет собой внеузловую лимфому из естественных киллеров/T-клеток.
1314. MBM согласно варианту осуществления 1307, где неходжкинская лимфома представляет собой Т-клеточную лимфому кишечника энтеропатического типа.
1315. MBM согласно варианту осуществления 1307, где неходжкинская лимфома представляет собой T-лимфобластную лимфому/лейкоз из клеток-предшественников (T-LBL/L).
1316. MBM согласно варианту осуществления 1307, где неходжкинская лимфома представляет собой неуточненную периферическую Т-клеточную лимфому.
1317. MBM согласно варианту осуществления 1279, где рак представляет собой множественную миелому.
1318. MBM согласно варианту осуществления 1279, где рак представляет собой новообразование из плазмоцитоидных дендритных клеток.
1319. MBM согласно варианту осуществления 1279, где рак включает в себя лейкоз.
1320. MBM согласно варианту осуществления 1319, где лейкоз представляет собой В-клеточный острый лимфоидный лейкоз ("BALL"), T-клеточный острый лимфоидный лейкоз ("TALL"), острый лимфоидный лейкоз (ALL), хронический миелогенный лейкоз (CML), хронический лимфоцитарный лейкоз (CLL), B-клеточный хронический лимфоцитарный лейкоз (B-CLL), B-клеточный пролимфоцитарный лейкоз (B-PLL), волосатоклеточный лейкоз, плазмоцитому/миелому, B-лимфобластный лейкоз/лимфому из клеток-предшественников (PB-LBL/L), лейкоз из больших гранулярных лимфоцитов, Т-лимфобластную лимфому/лейкоз из клеток-предшественников (T-LBL/L), Т-клеточный хронический лимфоцитарный лейкоз/пролимфоцитарный лейкоз (T-CLL/PLL).
1321. MBM согласно варианту осуществления 1320, где лейкоз представляет собой В-клеточный острый лимфоидный лейкоз ("BALL").
1322. MBM согласно варианту осуществления 1320, где лейкоз представляет собой T-клеточный острый лимфоидный лейкоз ("TALL").
1323. MBM согласно варианту осуществления 1320, где лейкоз представляет собой острый лимфоидный лейкоз (ALL).
1324. MBM согласно варианту осуществления 1320, где лейкоз представляет собой хронический миелогенный лейкоз (CML).
1325. MBM согласно варианту осуществления 1320, где лейкоз представляет собой хронический лимфоцитарный лейкоз (CLL).
1326. MBM согласно варианту осуществления 1320, где лейкоз представляет собой B-клеточный хронический лимфоцитарный лейкоз (B-CLL).
1327. MBM согласно варианту осуществления 1320, где лейкоз представляет собой B-клеточный пролимфоцитарный лейкоз (B-PLL).
1328. MBM согласно варианту осуществления 1320, где лейкоз представляет собой волосатоклеточный лейкоз.
1329. MBM согласно варианту осуществления 1320, где лейкоз представляет собой плазмоцитому/миелому.
1330. MBM согласно варианту осуществления 1320, где лейкоз представляет собой B-лимфобластный лейкоз/лимфому из клеток-предшественников (PB-LBL/L).
1331. MBM согласно варианту осуществления 1320, где лейкоз представляет собой лейкоз из больших гранулярных лимфоцитов.
1332. MBM согласно варианту осуществления 1320, где лейкоз представляет собой T-лимфобластную лимфому/лейкоз из клеток-предшественников (T-LBL/L).
1333. MBM согласно варианту осуществления 1320, где лейкоз представляет собой Т-клеточный хронический лимфоцитарный лейкоз/пролимфоцитарный лейкоз (T-CLL/PLL).
1334. MBM согласно варианту осуществления 1279, где рак представляет собой рак головного мозга.
1335. MBM согласно варианту осуществления 1334, где рак головного мозга представляет собой астроцитому или глиобластому.
1336. MBM согласно варианту осуществления 1335, где рак головного мозга представляет собой астроцитому.
1337. MBM согласно варианту осуществления 1335, где рак головного мозга представляет собой глиобластому.
1338. MBM согласно варианту осуществления 1279, где рак представляет собой рак предстательной железы.
1339. MBM согласно варианту осуществления 1338, где рак предстательной железы представляет собой кастрационно-резистентный рак предстательной железы.
1340. MBM согласно варианту осуществления 1338, где рак предстательной железы представляет собой терапевтически резистентный рак предстательной железы.
1341. MBM согласно варианту осуществления 1338, где рак предстательной железы представляет собой метастатический рак предстательной железы.
1342. MBM согласно варианту осуществления 1279, где рак представляет собой рак поджелудочной железы.
1343. MBM согласно варианту осуществления 1279, где рак представляет собой рак легкого.
1344. MBM согласно варианту осуществления 1278, где заболевание или нарушение включает в себя новообразование из плазматических клеток.
1345. MBM согласно варианту осуществления 1344, где новообразование из плазматических клеток включает в себя "тлеющую" множественную миелому (SMM) или моноклональную гаммапатию неустановленной этиологии (MGUS).
1346. MBM согласно варианту осуществления 1345, где новообразование из плазматических клеток включает в себя "тлеющую" множественную миелому (SMM).
1347. MBM согласно варианту осуществления 1345, где новообразование из плазматических клеток включает в себя моноклональную гаммапатию неустановленной этиологии (MGUS).
1348. MBM согласно варианту осуществления 1278, где заболевание или нарушение включает в себя плазмоцитому.
1349. MBM согласно варианту осуществления 1348, где плазмоцитома представляет собой плазмоклеточную дискразию, солитарную миелому, солитарную плазмоцитому, экстрамедуллярную плазмоцитому или множественную плазмоцитому.
1350. MBM согласно варианту осуществления 1348, где плазмоцитома представляет собой плазмоклеточную дискразию.
1351. MBM согласно варианту осуществления 1348, где плазмоцитома представляет собой солитарную миелому.
1352. MBM согласно варианту осуществления 1348, где плазмоцитома представляет собой солитарную плазмоцитому.
1353. MBM согласно варианту осуществления 1348, где плазмоцитома представляет собой экстрамедуллярную плазмоцитому.
1354. MBM согласно варианту осуществления 1348, где плазмоцитома представляет собой множественную плазмоцитому.
1355. MBM согласно варианту осуществления 1278, где заболевание или нарушение включает в себя системный амилоидоз в форме амилоидоза легких цепей.
1356. MBM согласно варианту осуществления 1278, где заболевание или нарушение включает в себя POEMS-синдром.
1357. MBM согласно варианту осуществления 1278, где заболевание или нарушение представляет собой инфекцию.
1358. MBM согласно варианту осуществления 1357, где инфекция представляет собой вирусную инфекцию.
1359. MBM согласно варианту осуществления 1358, где вирусная инфекция представляет собой HIV-инфекцию.
1360. MBM согласно варианту осуществления 1357, где инфекция представляет собой грибковую инфекцию.
1361. MBM согласно варианту осуществления 1360, где грибковая инфекция представляет собой инфекцию, вызванную C. neoformans.
1362. MBM согласно варианту осуществления 1278, где заболевание или нарушение представляет собой аутоиммунное нарушение.
1363. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение выбрано из системной красной волчанки (SLE), синдрома Шегрена, склеродермии, ревматоидного артрита (RA), ювенильного идиопатического артрита, реакции "трансплантат против хозяина", дерматомиозита, сахарного диабета I типа, тиреоидита Хашимото, болезни Грейвса, болезни Аддисона, целиакии, болезни Крона, пернициозной анемии, обыкновенной пузырчатки, витилиго, аутоиммунной гемолитической анемии, идиопатической тромбоцитопенической пурпуры, гигантоклеточного артериита, тяжелой миастении, рассеянного склероза (MS) (например, рецидивирующе-ремиттирующего MS (RRMS)), гломерулонефрита, синдрома Гудпасчера, буллезного пемфигоида, язвенного колита, синдрома Гийена-Барре, хронической воспалительной демиелинизирующей полинейропатии, антифосфолипидного синдрома, нарколепсии, саркоидоза и гранулематоза Вегенера.
1364. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой системную красную волчанку (SLE).
1365. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой синдром Шегрена.
1366. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой склеродермию.
1367. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой ревматоидный артрит (RA).
1368. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой ювенильный идиопатический артрит.
1369. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой реакцию "трансплантат против хозяина".
1370. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой дерматомиозит.
1371. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой сахарный диабет I типа.
1372. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой тиреоидит Хашимото.
1373. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой болезнь Грейвса.
1374. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой болезнь Аддисона.
1375. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой целиакию.
1376. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой болезнь Крона.
1377. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой пернициозную анемию.
1378. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой обыкновенную пузырчатку.
1379. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой витилиго.
1380. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой аутоиммунную гемолитическую анемию.
1381. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой идиопатическую тромбоцитопеническую пурпуру.
1382. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой гигантоклеточный артериит.
1383. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой тяжелую миастению.
1384. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой рассеянный склероз (MS).
1385. MBM согласно варианту осуществления 1362, где MS представляет собой рецидивирующе-ремиттирующий MS (RRMS).
1386. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой гломерулонефрит.
1387. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой синдром Гудпасчера.
1388. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой буллезный пемфигоид.
1389. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой язвенный колит.
1390. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой синдром Гийена-Барре.
1391. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой хроническую воспалительную демиелинизирующую полинейропатию.
1392. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой антифосфолипидный синдром.
1393. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой нарколепсию.
1394. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой саркоидоз.
1395. MBM согласно варианту осуществления 1362, где аутоиммунное нарушение представляет собой гранулематоз Вегенера.
1396. Конъюгат, содержащий МBM согласно любому из вариантов осуществления 1-1276 и средство, необязательно терапевтическое средство, диагностическое средство, маскирующий фрагмент, расщепляемый фрагмент или любую их комбинацию.
1397. Конъюгат согласно варианту осуществления 1396, где средство представляет собой цитотоксическое или цитостатическое средство.
1398. Конъюгат согласно варианту осуществления 1397, где средство представляет собой любое из средств, описанных в разделе 7.10.
1399. Конъюгат согласно вариантам осуществления 1397 или 1398, где средство представляет собой любое из средств, описанных в разделе 7.10.1.
1400. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с радионуклидом.
1401. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с алкилирующим средством.
1402. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с ингибитором топоизомеразы, который необязательно представляет собой ингибитор топоизомеразы I или ингибитор топоизомеразы II.
1403. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована со средством, повреждающим ДНК.
1404. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с ДНК-интеркалирующим средством, необязательно средством, связывающимся с бороздкой, таким как средство, связывающееся с малой бороздкой.
1405. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с антиметаболитом РНК/ДНК.
1406. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с ингибитором киназы.
1407. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с ингибитором синтеза белка.
1408. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с ингибитором деацетилазы гистонов (HDAC).
1409. Конъюгат согласно любому из вариантов осуществления 1396-1399, где MBM конъюгирована с ингибитором митохондрий, который необязательно представляет собой ингибитор реакции переноса фосфорильной группы в митохондриях.
1410. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с антимитотическим средством.
1411. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с майтанзиноидом.
1412. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с ингибитором кинезина.
1413. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с ингибитором кинезиноподобного белка KIF11.
1414. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с ингибитором V-ATPазы (Н+-ATPазы вакуолярного типа).
1415. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с проапоптотическим средством.
1416. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с ингибитором Bcl2 (белка 2 B-клеточной лимфомы).
1417. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с ингибитором MCL1 (белка 1 миелоидноклеточного лейкоза).
1418. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с ингибитором HSP90 (белка теплового шока 90).
1419. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с ингибитором IAP (ингибитора апоптоза).
1420. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с ингибитором mTOR (механистической мишени рапамицина).
1421. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована со стабилизатором микротрубочек.
1422. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с дестабилизатором микротрубочек.
1423. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с ауристатином.
1424. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с доластатином.
1425. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с MetAP (метионинаминопептидазой).
1426. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с ингибитором CRM1 (белка 1 поддержания структуры хромосом).
1427. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с ингибитором DPPIV (дипептидилпептидазы IV).
1428. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с ингибитором протеасом.
1429. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с ингибитором синтеза белка.
1430. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с ингибитором CDK2 (циклинзависимой киназы 2).
1431. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с ингибитором CDK9 (циклинзависимой киназы 9).
1432. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с ингибитором РНК-полимеразы.
1433. Конъюгат согласно любому из вариантов осуществления 1396-1399, где МBM конъюгирована с ингибитором DHFR (дигидрофолатредуктазы).
1434. Конъюгат согласно любому из вариантов осуществления 1396-1433, где средство присоединено к МBM с помощью линкера, который необязательно представляет собой расщепляемый линкер или нерасщепляемый линкер, например, линкер, описанный в разделе 7.10.2.
1435. Конъюгат согласно любому из вариантов осуществления 1396-1434, где цитотоксическое или цитостатическое средство конъюгировано с МBM посредством линкера, описанного в разделе 7.10.2.
1436. Препарат на основе MBM, содержащий совокупность молекул MBM в соответствии с любым из вариантов осуществления 1-1395 или совокупность молекул конъюгатов в соответствии с любым из вариантов осуществления 1396-1435, где совокупность необязательно содержит по меньшей мере 100, по меньшей мере 1000, по меньшей мере 10000 или по меньшей мере 100000 молекул MBM или молекул конъюгатов.
1437. Препарат согласно варианту осуществления 1436, где по меньшей мере 50% молекул MBM в препарате имеют одинаковую первичную аминокислотную последовательность.
1438. Препарат согласно варианту осуществления 1436, где по меньшей мере 60% молекул MBM в препарате имеют одинаковую первичную аминокислотную последовательность.
1439. Препарат согласно варианту осуществления 1436, где по меньшей мере 70% молекул MBM в препарате имеют одинаковую первичную аминокислотную последовательность.
1440. Препарат согласно варианту осуществления 1436, где по меньшей мере 80% молекул MBM в препарате имеют одинаковую первичную аминокислотную последовательность.
1441. Препарат согласно варианту осуществления 1436, где по меньшей мере 90% молекул MBM в препарате имеют одинаковую первичную аминокислотную последовательность.
1442. Препарат согласно варианту осуществления 1436, где по меньшей мере 95% молекул MBM в препарате имеют одинаковую первичную аминокислотную последовательность.
1443. Препарат согласно варианту осуществления 1436, где по меньшей мере 97% молекул MBM в препарате имеют одинаковую первичную аминокислотную последовательность.
1444. Препарат согласно варианту осуществления 1436, где по меньшей мере 98% молекул MBM в препарате имеют одинаковую первичную аминокислотную последовательность.
1445. Препарат согласно варианту осуществления 1436, где по меньшей мере 99% молекул MBM в препарате имеют одинаковую первичную аминокислотную последовательность.
1446. Препарат согласно варианту осуществления 1436, где от 50% до 95% молекул MBM в препарате имеют одинаковую первичную аминокислотную последовательность.
1447. Препарат согласно варианту осуществления 1436, где от 50% до 80% молекул MBM в препарате имеют одинаковую первичную аминокислотную последовательность.
1448. Препарат согласно варианту осуществления 1436, где от 50% до 70% молекул MBM в препарате имеют одинаковую первичную аминокислотную последовательность.
1449. Препарат согласно варианту осуществления 1436, где от 60% до 95% молекул MBM в препарате имеют одинаковую первичную аминокислотную последовательность.
1450. Препарат согласно варианту осуществления 1436, где от 60% до 80% молекул MBM в препарате имеют одинаковую первичную аминокислотную последовательность.
1451. Препарат согласно варианту осуществления 1436, где от 60% до 70% молекул MBM в препарате имеют одинаковую первичную аминокислотную последовательность.
1452. Препарат согласно варианту осуществления 1436, где от 70% до 95% молекул MBM в препарате имеют одинаковую первичную аминокислотную последовательность.
1453. Препарат согласно варианту осуществления 1436, где от 70% до 80% молекул MBM в препарате имеют одинаковую первичную аминокислотную последовательность.
1454. Препарат согласно варианту осуществления 1436, где от 80% до 95% молекул MBM в препарате имеют одинаковую первичную аминокислотную последовательность.
1455. Препарат согласно варианту осуществления 1436, где от 95% до 99% молекул MBM в препарате имеют одинаковую первичную аминокислотную последовательность.
1456. Препарат согласно любому из вариантов осуществления 1436-1455, где по меньшей мере 50% молекул MBM в препарате имеют одинаковые межцепочечные поперечные связи.
1457. Препарат согласно любому из вариантов осуществления 1436-1455, где по меньшей мере 60% молекул MBM в препарате имеют одинаковые межцепочечные поперечные связи.
1458. Препарат согласно любому из вариантов осуществления 1436-1455, где по меньшей мере 70% молекул MBM в препарате имеют одинаковые межцепочечные поперечные связи.
1459. Препарат согласно любому из вариантов осуществления 1436-1455, где по меньшей мере 80% молекул MBM в препарате имеют одинаковые межцепочечные поперечные связи.
1460. Препарат согласно любому из вариантов осуществления 1436-1455, где по меньшей мере 90% молекул MBM в препарате имеют одинаковые межцепочечные поперечные связи.
1461. Препарат согласно любому из вариантов осуществления 1436-1455, где по меньшей мере 95% молекул MBM в препарате имеют одинаковые межцепочечные поперечные связи.
1462. Препарат согласно любому из вариантов осуществления 1436-1455, где по меньшей мере 97% молекул MBM в препарате имеют одинаковые межцепочечные поперечные связи.
1463. Препарат согласно любому из вариантов осуществления 1436-1455, где по меньшей мере 98% молекул MBM в препарате имеют одинаковые межцепочечные поперечные связи.
1464. Препарат согласно любому из вариантов осуществления 1436-1455, где по меньшей мере 99% молекул MBM в препарате имеют одинаковые межцепочечные поперечные связи.
1465. Препарат согласно любому из вариантов осуществления 1436-1455, где от 50% до 95% молекул MBM в препарате имеют одинаковые межцепочечные поперечные связи.
1466. Препарат согласно любому из вариантов осуществления 1436-1455, где от 50% до 80% молекул MBM в препарате имеют одинаковые межцепочечные поперечные связи.
1467. Препарат согласно любому из вариантов осуществления 1436-1455, где от 50% до 70% молекул MBM в препарате имеют одинаковые межцепочечные поперечные связи.
1468. Препарат согласно любому из вариантов осуществления 1436-1455, где от 60% до 95% молекул MBM в препарате имеют одинаковые межцепочечные поперечные связи.
1469. Препарат согласно любому из вариантов осуществления 1436-1455, где от 60% до 80% молекул MBM в препарате имеют одинаковые межцепочечные поперечные связи.
1470. Препарат согласно любому из вариантов осуществления 1436-1455, где от 60% до 70% молекул MBM в препарате имеют одинаковые межцепочечные поперечные связи.
1471. Препарат согласно любому из вариантов осуществления 1436-1455, где от 70% до 95% молекул MBM в препарате имеют одинаковые межцепочечные поперечные связи.
1472. Препарат согласно любому из вариантов осуществления 1436-1455, где от 70% до 80% молекул MBM в препарате имеют одинаковые межцепочечные поперечные связи.
1473. Препарат согласно любому из вариантов осуществления 1436-1455, где от 80% до 95% молекул MBM в препарате имеют одинаковые межцепочечные поперечные связи.
1474. Препарат согласно любому из вариантов осуществления 1436-1455, где от 95% до 99% молекул MBM в препарате имеют одинаковые межцепочечные поперечные связи.
1475. Препарат согласно любому из вариантов осуществления 1436-1474, где по меньшей мере 50% молекул MBM в препарате имеют одинаковое соотношение ABM1:ABM2:ABM3.
1476. Препарат согласно любому из вариантов осуществления 1436-1474, где по меньшей мере 60% молекул MBM в препарате имеют одинаковое соотношение ABM1:ABM2:ABM3.
1477. Препарат согласно любому из вариантов осуществления 1436-1474, где по меньшей мере 70% молекул MBM в препарате имеют одинаковое соотношение ABM1:ABM2:ABM3.
1478. Препарат согласно любому из вариантов осуществления 1436-1474, где по меньшей мере 80% молекул MBM в препарате имеют одинаковое соотношение ABM1:ABM2:ABM3.
1479. Препарат согласно любому из вариантов осуществления 1436-1474, где по меньшей мере 90% молекул MBM в препарате имеют одинаковое соотношение ABM1:ABM2:ABM3.
1480. Препарат согласно любому из вариантов осуществления 1436-1474, где по меньшей мере 95% молекул MBM в препарате имеют одинаковое соотношение ABM1:ABM2:ABM3.
1481. Препарат согласно любому из вариантов осуществления 1436-1474, где по меньшей мере 97% молекул MBM в препарате имеют одинаковое соотношение ABM1:ABM2:ABM3.
1482. Препарат согласно любому из вариантов осуществления 1436-1474, где по меньшей мере 98% молекул MBM в препарате имеют одинаковое соотношение ABM1:ABM2:ABM3.
1483. Препарат согласно любому из вариантов осуществления 1436-1474, где по меньшей мере 99% молекул MBM в препарате имеют одинаковое соотношение ABM1:ABM2:ABM3.
1484. Препарат согласно любому из вариантов осуществления 1436-1474, где от 50% до 95% молекул MBM в препарате имеют одинаковое соотношение ABM1:ABM2:ABM3.
1485. Препарат согласно любому из вариантов осуществления 1436-1474, где от 50% до 80% молекул MBM в препарате имеют одинаковое соотношение ABM1:ABM2:ABM3.
1486. Препарат согласно любому из вариантов осуществления 1436-1474, где от 50% до 70% молекул MBM в препарате имеют одинаковое соотношение ABM1:ABM2:ABM3.
1487. Препарат согласно любому из вариантов осуществления 1436-1474, где от 60% до 95% молекул MBM в препарате имеют одинаковое соотношение ABM1:ABM2:ABM3.
1488. Препарат согласно любому из вариантов осуществления 1436-1474, где от 60% до 80% молекул MBM в препарате имеют одинаковое соотношение ABM1:ABM2:ABM3.
1489. Препарат согласно любому из вариантов осуществления 1436-1474, где от 60% до 70% молекул MBM в препарате имеют одинаковое соотношение ABM1:ABM2:ABM3.
1490. Препарат согласно любому из вариантов осуществления 1436-1474, где от 70% до 95% молекул MBM в препарате имеют одинаковое соотношение ABM1:ABM2:ABM3.
1491. Препарат согласно любому из вариантов осуществления 1436-1474, где от 70% до 80% молекул MBM в препарате имеют одинаковое соотношение ABM1:ABM2:ABM3.
1492. Препарат согласно любому из вариантов осуществления 1436-1474, где от 80% до 95% молекул MBM в препарате имеют одинаковое соотношение ABM1:ABM2:ABM3.
1493. Препарат согласно любому из вариантов осуществления 1436-1474, где от 95% до 99% молекул MBM в препарате имеют одинаковое соотношение ABM1:ABM2:ABM3.
1494. Фармацевтическая композиция, содержащая MBM согласно любому из вариантов осуществления 1-1276, конъюгат согласно любому из вариантов осуществления 1396-1435 или препарат согласно любому из вариантов осуществления 1436-1493 и вспомогательное вещество.
1495. Способ лечения субъекта, у которого имеется заболевание или нарушение, ассоциированное с экспрессией BCMA, включающий введение субъекту эффективного количества MBM согласно любому из вариантов осуществления 1-1395, конъюгата согласно любому из вариантов осуществления 1396-1435, препарата согласно любому из вариантов осуществления 1436-1493 или фармацевтической композиции согласно варианту осуществления 1494.
1496. Способ согласно варианту осуществления 1495, где заболевание или нарушение включает в себя рак.
1497. Способ согласно варианту осуществления 1496, где рак включает в себя В-клеточное злокачественное новообразование.
1498. Способ согласно варианту осуществления 1497, где в случае, когда MBM представляет собой MBM, которая специфично связывается с TAA, В-клеточное злокачественное новообразование содержит раковые B-клетки, экспрессирующие как BCMA, так TAA.
1499. Способ согласно варианту осуществления 1497, где в случае, когда MBM представляет собой MBM, которая специфично связывается с TAA, В-клеточное злокачественное новообразование содержит раковые B-клетки, экспрессирующие BCMA, но не TAA, и раковые B-клетки, экспрессирующие TAA, но не BCMA.
1500. Способ согласно любому из вариантов осуществления 1497-1499, где В-клеточное злокачественное новообразование выбрано из лимфомы Ходжкина, неходжкинской лимфомы и множественной миеломы.
1501. Способ согласно варианту осуществления 1496, где рак представляет собой лимфому Ходжкина.
1502. Способ согласно варианту осуществления 1501, где лимфома Ходжкина представляет собой лимфому Ходжкина с нодулярным склерозом.
1503. Способ согласно варианту осуществления 1501, где лимфома Ходжкина представляет собой лимфому Ходжкина смешанно-клеточного подтипа.
1504. Способ согласно варианту осуществления 1501, где лимфома Ходжкина представляет собой лимфому Ходжкина, богатую лимфоцитами или с лимфоидным преобладанием.
1505. Способ согласно варианту осуществления 1501, где лимфома Ходжкина представляет собой лимфому Ходжкина с лимфоидным истощением.
1506. Способ согласно варианту осуществления 1496, где рак представляет собой неходжкинскую лимфому.
1507. Способ согласно варианту осуществления 1506, где неходжкинская лимфома представляет собой В-клеточную лимфому или Т-клеточную лимфому.
1508. Способ согласно варианту осуществления 1507, где неходжкинская лимфома представляет собой B-клеточную лимфому.
1509. Способ согласно варианту осуществления 1508, где неходжкинская лимфома представляет собой диффузную крупноклеточную В-клеточную лимфому (DLBCL), фолликулярную лимфому, хронический лимфоцитарный лейкоз (CLL)/мелкоклеточную лимфоцитарную лимфому (SLL), мантийноклеточную лимфому (MCL), лимфому из клеток маргинальной зоны, лимфому Беркитта, лимфоплазмоцитарную лимфому (макроглобулинемию Вальденстрема), волосатоклеточный лейкоз, первичную лимфому центральной нервной системы (CNS), первичную медиастинальную крупноклеточную В-клеточную лимфому, медиастинальную лимфому "серой зоны" (MGZL), B-клеточную лимфому из клеток маргинальной зоны селезенки, внеузловую B-клеточную лимфому из клеток маргинальной зоны MALT, узловую B-клеточную лимфому из клеток маргинальной зоны или первичную эффузионную лимфому.
1510. Способ согласно варианту осуществления 1509, где неходжкинская лимфома представляет собой диффузную крупноклеточную В-клеточную лимфому (DLBCL).
1511. Способ согласно варианту осуществления 1509, где неходжкинская лимфома представляет собой фолликулярную лимфому.
1512. Способ согласно варианту осуществления 1509, где неходжкинская лимфома представляет собой хронический лимфоцитарный лейкоз (CLL)/мелкоклеточную лимфоцитарную лимфому (SLL).
1513. Способ согласно варианту осуществления 1509, где неходжкинская лимфома представляет собой мантийноклеточную лимфому (MCL).
1514. Способ согласно варианту осуществления 1509, где неходжкинская лимфома представляет собой лимфому из клеток маргинальной зоны.
1515. Способ согласно варианту осуществления 1509, где неходжкинская лимфома представляет собой лимфому Беркитта.
1516. Способ согласно варианту осуществления 1509, где неходжкинская лимфома представляет собой лимфоплазмоцитарную лимфому (макроглобулинемию Вальденстрема).
1517. Способ согласно варианту осуществления 1509, где неходжкинская лимфома представляет собой волосатоклеточный лейкоз.
1518. Способ согласно варианту осуществления 1509, где неходжкинская лимфома представляет собой первичную лимфому центральной нервной системы (CNS).
1519. Способ согласно варианту осуществления 1509, где неходжкинская лимфома представляет собой первичную медиастинальную крупноклеточную В-клеточную лимфому.
1520. Способ согласно варианту осуществления 1509, где неходжкинская лимфома представляет собой медиастинальную лимфому "серой зоны" (MGZL).
1521. Способ согласно варианту осуществления 1509, где неходжкинская лимфома представляет собой B-клеточную лимфому из клеток маргинальной зоны селезенки.
1522. Способ согласно варианту осуществления 1509, где неходжкинская лимфома представляет собой внеузловую B-клеточную лимфому из клеток маргинальной зоны MALT.
1523. Способ согласно варианту осуществления 1509, где неходжкинская лимфома представляет собой узловую B-клеточную лимфому из клеток маргинальной зоны.
1524. Способ согласно варианту осуществления 1509, где неходжкинская лимфома представляет собой первичную эффузионную лимфому.
1525. Способ согласно варианту осуществления 1507, где неходжкинская лимфома представляет собой T-клеточную лимфому.
1526. Способ согласно варианту осуществления 1525, где неходжкинская лимфома представляет собой анапластическую крупноклеточную лимфому (ALCL), Т-клеточную лимфому/лейкоз взрослых, лимфангиому, ангиоиммунобластную Т-клеточную лимфому, Т-клеточную лимфому кожи, внеузловую лимфому из естественных киллеров/T-клеток, Т-клеточную лимфому кишечника энтеропатического типа, T-лимфобластную лимфому/лейкоз из клеток-предшественников (T-LBL/L) или неуточненную периферическую Т-клеточную лимфому.
1527. Способ согласно варианту осуществления 1526, где неходжкинская лимфома представляет собой анапластическую крупноклеточную лимфому (ALCL).
1528. Способ согласно варианту осуществления 1526, где неходжкинская лимфома представляет собой Т-клеточную лимфому/лейкоз взрослых.
1529. Способ согласно варианту осуществления 1526, где неходжкинская лимфома представляет собой лимфангиому.
1530. Способ согласно варианту осуществления 1526, где неходжкинская лимфома представляет собой ангиоиммунобластную Т-клеточную лимфому.
1531. Способ согласно варианту осуществления 1526, где неходжкинская лимфома представляет собой Т-клеточную лимфому кожи.
1532. Способ согласно варианту осуществления 1526, где неходжкинская лимфома представляет собой внеузловую лимфому из естественных киллеров/T-клеток.
1533. Способ согласно варианту осуществления 1526, где неходжкинская лимфома представляет собой Т-клеточную лимфому кишечника энтеропатического типа.
1534. Способ согласно варианту осуществления 1526, где неходжкинская лимфома представляет собой T-лимфобластную лимфому/лейкоз из клеток-предшественников (T-LBL/L).
1535. Способ согласно варианту осуществления 1526, где неходжкинская лимфома представляет собой неуточненную периферическую Т-клеточную лимфому.
1536. Способ согласно варианту осуществления 1496, где рак представляет собой множественную миелому.
1537. Способ согласно варианту осуществления 1496, где рак представляет собой новообразование из плазмоцитоидных дендритных клеток.
1538. Способ согласно варианту осуществления 1496, где рак включает в себя лейкоз.
1539. Способ согласно варианту осуществления 1538, где лейкоз представляет собой В-клеточный острый лимфоидный лейкоз ("BALL"), T-клеточный острый лимфоидный лейкоз ("TALL"), острый лимфоидный лейкоз (ALL), хронический миелогенный лейкоз (CML), хронический лимфоцитарный лейкоз (CLL), B-клеточный хронический лимфоцитарный лейкоз (B-CLL), B-клеточный пролимфоцитарный лейкоз (B-PLL), волосатоклеточный лейкоз, плазмоцитому/миелому, B-лимфобластный лейкоз/лимфому из клеток-предшественников (PB-LBL/L), лейкоз из больших гранулярных лимфоцитов, Т-лимфобластную лимфому/лейкоз из клеток-предшественников (T-LBL/L), Т-клеточный хронический лимфоцитарный лейкоз/пролимфоцитарный лейкоз (T-CLL/PLL).
1540. Способ согласно варианту осуществления 1538, где лейкоз представляет собой В-клеточный острый лимфоидный лейкоз ("BALL").
1541. Способ согласно варианту осуществления 1538, где лейкоз представляет собой T-клеточный острый лимфоидный лейкоз ("TALL").
1542. Способ согласно варианту осуществления 1538, где лейкоз представляет собой острый лимфоидный лейкоз (ALL).
1543. Способ согласно варианту осуществления 1538, где лейкоз представляет собой хронический миелогенный лейкоз (CML).
1544. Способ согласно варианту осуществления 1538, где лейкоз представляет собой хронический лимфоцитарный лейкоз (CLL).
1545. Способ согласно варианту осуществления 1538, где лейкоз представляет собой B-клеточный хронический лимфоцитарный лейкоз (B-CLL).
1546. Способ согласно варианту осуществления 1538, где лейкоз представляет собой B-клеточный пролимфоцитарный лейкоз (B-PLL).
1547. Способ согласно варианту осуществления 1538, где лейкоз представляет собой волосатоклеточный лейкоз.
1548. Способ согласно варианту осуществления 1538, где лейкоз представляет собой плазмоцитому/миелому.
1549. Способ согласно варианту осуществления 1538, где лейкоз представляет собой B-лимфобластный лейкоз/лимфому из клеток-предшественников (PB-LBL/L).
1550. Способ согласно варианту осуществления 1538, где лейкоз представляет собой лейкоз из больших гранулярных лимфоцитов.
1551. Способ согласно варианту осуществления 1538, где лейкоз представляет собой T-лимфобластную лимфому/лейкоз из клеток-предшественников (T-LBL/L).
1552. Способ согласно варианту осуществления 1538, где лейкоз представляет собой Т-клеточный хронический лимфоцитарный лейкоз/пролимфоцитарный лейкоз (T-CLL/PLL).
1553. Способ согласно варианту осуществления 1496, где рак представляет собой рак головного мозга.
1554. Способ согласно варианту осуществления 1553, где рак головного мозга представляет собой астроцитому или глиобластому.
1555. Способ согласно варианту осуществления 1554, где рак головного мозга представляет собой астроцитому.
1556. Способ согласно варианту осуществления 1554, где рак головного мозга представляет собой глиобластому.
1557. Способ согласно варианту осуществления 1496, где рак представляет собой рак предстательной железы.
1558. Способ согласно варианту осуществления 1557, где рак предстательной железы представляет собой кастрационно-резистентный рак предстательной железы.
1559. Способ согласно варианту осуществления 1557, где рак предстательной железы представляет собой терапевтически резистентный рак предстательной железы.
1560. Способ согласно варианту осуществления 1557, где рак предстательной железы представляет собой метастатический рак предстательной железы.
1561. Способ согласно варианту осуществления 1496, где рак представляет собой рак поджелудочной железы.
1562. Способ согласно варианту осуществления 1496, где рак представляет собой рак легкого.
1563. Способ согласно варианту осуществления 1496, где заболевание или нарушение включает в себя новообразование из плазматических клеток.
1564. Способ согласно варианту осуществления 1563, где новообразование из плазматических клеток включает в себя "тлеющую" множественную миелому (SMM) или моноклональную гаммапатию неустановленной этиологии (MGUS).
1565. Способ согласно варианту осуществления 1564, где новообразование из плазматических клеток включает в себя "тлеющую" множественную миелому (SMM).
1566. Способ согласно варианту осуществления 1564, где новообразование из плазматических клеток включает в себя моноклональную гаммапатию неустановленной этиологии (MGUS).
1567. Способ согласно варианту осуществления 1495, где заболевание или нарушение включает в себя плазмоцитому.
1568. Способ согласно варианту осуществления 1567, где плазмоцитома представляет собой плазмоклеточную дискразию, солитарную миелому, солитарную плазмоцитому, экстрамедуллярную плазмоцитому или множественную плазмоцитому.
1569. Способ согласно варианту осуществления 1567, где плазмоцитома представляет собой плазмоклеточную дискразию.
1570. Способ согласно варианту осуществления 1567, где плазмоцитома представляет собой солитарную миелому.
1571. Способ согласно варианту осуществления 1567, где плазмоцитома представляет собой солитарную плазмоцитому.
1572. Способ согласно варианту осуществления 1567, где плазмоцитома представляет собой экстрамедуллярную плазмоцитому.
1573. Способ согласно варианту осуществления 1567, где плазмоцитома представляет собой множественную плазмоцитому.
1574. Способ согласно варианту осуществления 1495, где заболевание или нарушение включает в себя системный амилоидоз в форме амилоидоза легких цепей.
1575. Способ согласно варианту осуществления 1495, где заболевание или нарушение включает в себя POEMS-синдром.
1576. Способ согласно любому из вариантов осуществления 1495-1537, дополнительно включающий введение субъекту по меньшей мере одного дополнительного средства.
1577. Способ согласно варианту осуществления 1576, где дополнительное средство представляет собой химиотерапевтическое средство.
1578. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой антрациклин.
1579. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой алкалоид барвинка.
1580. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой алкилирующее средство.
1581. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой антитело к иммунным клеткам.
1582. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой антиметаболит.
1583. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой ингибитор аденозиндезаминазы.
1584. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой ингибитор mTOR.
1585. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой агонист глюкокортикоид-индуцируемого белка, родственного TNFR (GITR).
1586. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой ингибитор протеасом.
1587. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой миметик BH3.
1588. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой цитокин.
1589. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство предупреждает или замедляет слущивание BCMA с раковой клетки и/или, в случае, когда MBM специфично связывается с TAA, TAA с раковой клетки.
1590. Способ согласно варианту осуществления 1589, где дополнительное средство включает в себя ингибитор ADAM10 и/или ингибитор ADAM17.
1591. Способ согласно варианту осуществления 1589, где дополнительное средство включает в себя ингибитор фосфолипазы.
1592. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой ингибитор гамма-секретазы.
1593. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство является иммуномодулирующим.
1594. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой производное талидомида.
1595. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой ингибитор EGFR.
1596. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой антагонист аденозинового рецептора А2А.
1597. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой ингибитор CD20.
1598. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой ингибитор CD22.
1599. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой ингибитор FCRL2.
1600. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой ингибитор FCRL5.
1601. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой комплекс IL-15/IL15-Ra.
1602. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой ингибитор PD-1.
1603. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой ингибитор PD-L1.
1604. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой ингибитор LAG-3.
1605. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой ингибитор TIM-3.
1606. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой ингибитор TGF-β.
1607. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой ингибитор CD73.
1608. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой ингибитор IL-17.
1609. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой ингибитор CD32B.
1610. Способ согласно варианту осуществления 1576 или варианту осуществления 1577, где дополнительное средство представляет собой средство, выбранное из средств, перечисленных в таблице 18.
1611. Способ согласно варианту осуществления 1576, где дополнительное средство представляет собой средство, которое снижает или ослабляет побочный эффект, ассоциированный с введением MBM, которая связывает CD3.
1612. Способ согласно варианту осуществления 1611, где дополнительное средство включает в себя стероид (например, кортикостероид), ингибитор TNFα (например, молекулу антитела к TNFα, такую как инфликсимаб, адалимумаб, цертолизумаб пегол или голимумаб, слитый белок, такой как этанерцепт, низкомолекулярный ингибитор TNFα, такой как производное ксантина (например, пентоксифиллин) или бупропион), ингибитор IL-6 (например, молекулу антитела к IL-6, такую как тоцилизумаб (toc), сарилумаб, элсилимомаб, CNTO 328, ALD518/BMS-945429, CNTO 136, CPSI-2364, CDP6038, VX30, ARGX-109, FE301 или FM101), ингибитор IL-1R, такой как анакинра, кортикостероид (например, метилпреднизолон или гидрокортизон) в комбинации с бенадрилом и тайленолом, сосудосуживающее средство (например, норэпинефрин, дофамин, фенилэфрин, эпинефрин, вазопрессин или любую их комбинацию), жаропонижающее средство или аналгезирующее средство.
1613. Способ согласно любому из вариантов осуществления 1576-1612, где дополнительное средство не представляет собой антитело.
1614. Способ согласно варианту осуществления 1495, где заболевание или нарушение представляет собой инфекцию.
1615. Способ согласно варианту осуществления 1614, где инфекция представляет собой вирусную инфекцию.
1616. Способ согласно варианту осуществления 1615, где вирусная инфекция представляет собой HIV-инфекцию.
1617. Способ согласно варианту осуществления 1614, где инфекция представляет собой грибковую инфекцию.
1618. Способ согласно варианту осуществления 1617, где грибковая инфекция представляет собой инфекцию, вызванную C. neoformans.
1619. Способ согласно варианту осуществления 1495, где заболевание или нарушение представляет собой аутоиммунное нарушение.
1620. Способ согласно варианту осуществления 1619, где аутоиммунное нарушение выбрано из системной красной волчанки (SLE), синдрома Шегрена, склеродермии, ревматоидного артрита (RA), ювенильного идиопатического артрита, реакции "трансплантат против хозяина", дерматомиозита, сахарного диабета I типа, тиреоидита Хашимото, болезни Грейвса, болезни Аддисона, целиакии, болезни Крона, пернициозной анемии, обыкновенной пузырчатки, витилиго, аутоиммунной гемолитической анемии, идиопатической тромбоцитопенической пурпуры, гигантоклеточного артериита, тяжелой миастении, рассеянного склероза (MS) (например, рецидивирующе-ремиттирующего MS (RRMS)), гломерулонефрита, синдрома Гудпасчера, буллезного пемфигоида, язвенного колита, синдрома Гийена-Барре, хронической воспалительной демиелинизирующей полинейропатии, антифосфолипидного синдрома, нарколепсии, саркоидоза и гранулематоза Вегенера.
1621. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой системную красную волчанку (SLE).
1622. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой синдром Шегрена.
1623. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой склеродермию.
1624. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой ревматоидный артрит (RA).
1625. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой ювенильный идиопатический артрит.
1626. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой реакцию "трансплантат против хозяина".
1627. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой дерматомиозит.
1628. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой сахарный диабет I типа.
1629. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой тиреоидит Хашимото.
1630. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой болезнь Грейвса.
1631. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой болезнь Аддисона.
1632. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой целиакию.
1633. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой болезнь Крона.
1634. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой пернициозную анемию.
1635. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой обыкновенную пузырчатку.
1636. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой витилиго.
1637. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой аутоиммунную гемолитическую анемию.
1638. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой идиопатическую тромбоцитопеническую пурпуру.
1639. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой гигантоклеточный артериит.
1640. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой тяжелую миастению.
1641. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой рассеянный склероз (MS).
1642. Способ согласно варианту осуществления 1641, где MS представляет собой рецидивирующе-ремиттирующий MS (RRMS).
1643. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой гломерулонефрит.
1644. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой синдром Гудпасчера.
1645. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой буллезный пемфигоид.
1646. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой язвенный колит.
1647. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой синдром Гийена-Барре.
1648. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой хроническую воспалительную демиелинизирующую полинейропатию.
1649. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой антифосфолипидный синдром.
1650. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой нарколепсию.
1651. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой саркоидоз.
1652. Способ согласно варианту осуществления 1620, где аутоиммунное нарушение представляет собой гранулематоз Вегенера.
1653. Нуклеиновая кислота или совокупность нуклеиновых кислот, кодирующие МBM согласно любому из вариантов осуществления 1-1395.
1654. Нуклеиновая кислота или совокупность нуклеиновых кислот согласно варианту осуществления 1653, которая представляет собой ДНК (которые представляют собой ДНК).
1655. Нуклеиновая кислота или совокупность нуклеиновых кислот согласно варианту осуществления 1654, которые представлены в форме одного или более векторов, необязательно векторов экспрессии.
1656. Нуклеиновая кислота или совокупность нуклеиновых кислот согласно варианту осуществления 1653, которая представляет собой мРНК (которые представляют собой мРНК).
1657. Клетка, сконструированная для экспрессии МBM согласно любому из вариантов осуществления 1-1395.
1658. Клетка, трансфицированная одним или более векторами экспрессии, содержащими одну или более последовательностей нуклеиновой кислоты, кодирующих МBM согласно любому из вариантов осуществления 1-1395, под контролем одного или более промоторов.
1659. Клетка согласно варианту осуществления 1657 или варианту осуществления 1658, где экспрессия МBM находится под контролем одного или более индуцируемых промоторов.
1660. Клетка согласно любому из вариантов осуществления 1657-1659, где МBM продуцируется в секретируемой форме.
1661. Способ получения MBM, включающий:
(a) культивирование клетки согласно любому из вариантов осуществления 1657-1660 в условиях, в которых экспрессируется MBM; и
(b) извлечение МBM из культуры клеток.
10. ВКЛЮЧЕНИЕ ПОСРЕДСТВОМ ССЫЛКИ
[0938] Все публикации, патенты, заявки на патенты и другие документы, цитируемые в настоящей заявке, тем самым включены в данный документ посредством ссылки во всей своей полноте для всех целей в той же степени, как если бы каждая отдельная публикация, патент, заявка на патент или другой документ были отдельно указаны как включенные посредством ссылки для всех целей. В случае наличия любых несоответствий между идеями одного или более литературных источников, включенных в данный документ, и настоящего изобретения предполагается, что следует руководствоваться идеями настоящего описания.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> NOVARTIS AG
<120> ТРИСПЕЦИФИЧЕСКИЕ МОЛЕКУЛЫ, СВЯЗЫВАЮЩИЕ BCMA, И ПУТИ ИХ ПРИМЕНЕНИЯ
<130> NOV-005WO
<140>
<141>
<150> 62/854,667
<151> 2019-05-30
<150> 62/850,889
<151> 2019-05-21
<160> 872
<170> PatentIn версия 3.5
<210> 1
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 1
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 2
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 2
Cys Pro Pro Cys
1
<210> 3
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 3
Ser Pro Pro Ser
1
<210> 4
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 4
Val Pro Ser Thr Pro Pro Thr Pro Ser Pro Ser Thr Pro Pro Thr Pro
1 5 10 15
Ser Pro Ser
<210> 5
<211> 6
<212> БЕЛОК
<213> Homo sapiens
<400> 5
Val Pro Pro Pro Pro Pro
1 5
<210> 6
<211> 58
<212> БЕЛОК
<213> Homo sapiens
<400> 6
Glu Ser Pro Lys Ala Gln Ala Ser Ser Val Pro Thr Ala Gln Pro Gln
1 5 10 15
Ala Glu Gly Ser Leu Ala Lys Ala Thr Thr Ala Pro Ala Thr Thr Arg
20 25 30
Asn Thr Gly Arg Gly Gly Glu Glu Lys Lys Lys Glu Lys Glu Lys Glu
35 40 45
Glu Gln Glu Glu Arg Glu Thr Lys Thr Pro
50 55
<210> 7
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 7
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
1 5 10 15
<210> 8
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 8
Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro
1 5 10
<210> 9
<211> 62
<212> БЕЛОК
<213> Homo sapiens
<400> 9
Glu Leu Lys Thr Pro Leu Gly Asp Thr Thr His Thr Cys Pro Arg Cys
1 5 10 15
Pro Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro
20 25 30
Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro Glu
35 40 45
Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro
50 55 60
<210> 10
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 10
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Ser Cys Pro
1 5 10
<210> 11
<211> 12
<212> БЕЛОК
<213> Homo sapiens
<400> 11
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro
1 5 10
<210> 12
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 12
Cys Pro Ser Cys
1
<210> 13
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 13
Cys Pro Arg Cys
1
<210> 14
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 14
Ser Pro Pro Cys
1
<210> 15
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 15
Cys Pro Pro Ser
1
<210> 16
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 16
Asp Lys Thr His Thr Cys Ala Ala
1 5
<210> 17
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 17
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10
<210> 18
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 18
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Thr Cys Pro Pro Cys
1 5 10 15
Pro Ala
<210> 19
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 19
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Thr Cys Pro Pro Cys
1 5 10 15
Pro Ala Thr Cys Pro Pro Cys Pro Ala
20 25
<210> 20
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 20
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Gly Lys Pro Thr Leu
1 5 10 15
Tyr Asn Ser Leu Val Met Ser Asp Thr Ala Gly Thr Cys Tyr
20 25 30
<210> 21
<211> 31
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 21
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Gly Lys Pro Thr His
1 5 10 15
Val Asn Val Ser Val Val Met Ala Glu Val Asp Gly Thr Cys Tyr
20 25 30
<210> 22
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 22
Asp Lys Thr His Thr Cys Cys Val Glu Cys Pro Pro Cys Pro Ala
1 5 10 15
<210> 23
<211> 26
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 23
Asp Lys Thr His Thr Cys Pro Arg Cys Pro Glu Pro Lys Ser Cys Asp
1 5 10 15
Thr Pro Pro Pro Cys Pro Arg Cys Pro Ala
20 25
<210> 24
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 24
Asp Lys Thr His Thr Cys Pro Ser Cys Pro Ala
1 5 10
<210> 25
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<220>
<221> источник
<223> /примечание="См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления"
<400> 25
Gly Gly Gly Gly Ser
1 5
<210> 26
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 26
Ala Asp Ala Ala Pro
1 5
<210> 27
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 27
Ala Asp Ala Ala Pro Thr Val Ser Ile Phe Pro
1 5 10
<210> 28
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 28
Ala Asp Ala Ala Pro Thr Val Ser Ile Phe Pro Pro
1 5 10
<210> 29
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 29
Ala Lys Thr Thr Ala Pro
1 5
<210> 30
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 30
Ala Lys Thr Thr Ala Pro Ser Val Tyr Pro Leu Ala Pro
1 5 10
<210> 31
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 31
Ala Lys Thr Thr Pro Lys Leu Glu Glu Gly Glu Phe Ser Glu Ala Arg
1 5 10 15
Val
<210> 32
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 32
Ala Lys Thr Thr Pro Lys Leu Gly Gly
1 5
<210> 33
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 33
Ala Lys Thr Thr Pro Pro
1 5
<210> 34
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 34
Ala Lys Thr Thr Pro Pro Ser Val Thr Pro Leu Ala Pro
1 5 10
<210> 35
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 35
Ala Ser Thr Lys Gly Pro
1 5
<210> 36
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 36
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
1 5 10
<210> 37
<211> 26
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 37
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ala Ser Thr
1 5 10 15
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
20 25
<210> 38
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 38
Glu Gly Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr
1 5 10
<210> 39
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 39
Gly Glu Gly Glu Ser Gly Glu Gly Glu Ser Gly Glu Gly Glu Ser
1 5 10 15
<210> 40
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 40
Gly Glu Gly Glu Ser Gly Glu Gly Glu Ser Gly Glu Gly Glu Ser Gly
1 5 10 15
Glu Gly Glu Ser
20
<210> 41
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 41
Gly Glu Gly Gly Ser Gly Glu Gly Gly Ser Gly Glu Gly Gly Ser
1 5 10 15
<210> 42
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 42
Gly Glu Asn Lys Val Glu Tyr Ala Pro Ala Leu Met Ala Leu Ser
1 5 10 15
<210> 43
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 43
Gly Gly Glu Gly Ser Gly Gly Glu Gly Ser Gly Gly Glu Gly Ser
1 5 10 15
<210> 44
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 44
Gly Gly Gly Glu Ser Gly Gly Glu Gly Ser Gly Glu Gly Gly Ser
1 5 10 15
<210> 45
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 45
Gly Gly Gly Glu Ser Gly Gly Gly Glu Ser Gly Gly Gly Glu Ser
1 5 10 15
<210> 46
<211> 50
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<220>
<221> Сайт
<222> (1)..(50)
<223> /примечание="Эта последовательность может охватывать
1-10 повторяющихся звеньев "Gly Gly Gly Gly Ser"
<400> 46
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
20 25 30
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
35 40 45
Gly Ser
50
<210> 47
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 47
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10
<210> 48
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 48
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser
20
<210> 49
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 49
Gly Gly Gly Lys Ser Gly Gly Gly Lys Ser Gly Gly Gly Lys Ser
1 5 10 15
<210> 50
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 50
Gly Gly Gly Lys Ser Gly Gly Lys Gly Ser Gly Lys Gly Gly Ser
1 5 10 15
<210> 51
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 51
Gly Gly Lys Gly Ser Gly Gly Lys Gly Ser Gly Gly Lys Gly Ser
1 5 10 15
<210> 52
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 52
Gly Gly Ser Gly Gly
1 5
<210> 53
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 53
Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5
<210> 54
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 54
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10
<210> 55
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 55
Gly His Glu Ala Ala Ala Val Met Gln Val Gln Tyr Pro Ala Ser
1 5 10 15
<210> 56
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 56
Gly Lys Gly Gly Ser Gly Lys Gly Gly Ser Gly Lys Gly Gly Ser
1 5 10 15
<210> 57
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 57
Gly Lys Gly Lys Ser Gly Lys Gly Lys Ser Gly Lys Gly Lys Ser
1 5 10 15
<210> 58
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 58
Gly Lys Gly Lys Ser Gly Lys Gly Lys Ser Gly Lys Gly Lys Ser Gly
1 5 10 15
Lys Gly Lys Ser
20
<210> 59
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 59
Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser
1 5 10 15
<210> 60
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 60
Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly
1 5 10 15
Lys Pro Gly Ser
20
<210> 61
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 61
Gly Pro Ala Lys Glu Leu Thr Pro Leu Lys Glu Ala Lys Val Ser
1 5 10 15
<210> 62
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 62
Gly Ser Ala Gly Ser Ala Ala Gly Ser Gly Glu Phe
1 5 10
<210> 63
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 63
Ile Arg Pro Arg Ala Ile Gly Gly Ser Lys Pro Arg Val Ala
1 5 10
<210> 64
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 64
Lys Glu Ser Gly Ser Val Ser Ser Glu Gln Leu Ala Gln Phe Arg Ser
1 5 10 15
Leu Asp
<210> 65
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 65
Lys Thr Thr Pro Lys Leu Glu Glu Gly Glu Phe Ser Glu Ala Arg
1 5 10 15
<210> 66
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 66
Gln Pro Lys Ala Ala Pro
1 5
<210> 67
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 67
Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro
1 5 10
<210> 68
<211> 27
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 68
Arg Ala Asp Ala Ala Ala Ala Gly Gly Gly Gly Ser Gly Gly Gly Gly
1 5 10 15
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
20 25
<210> 69
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 69
Arg Ala Asp Ala Ala Ala Ala Gly Gly Pro Gly Ser
1 5 10
<210> 70
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 70
Arg Ala Asp Ala Ala Pro
1 5
<210> 71
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 71
Arg Ala Asp Ala Ala Pro Thr Val Ser
1 5
<210> 72
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 72
Ser Ala Lys Thr Thr Pro
1 5
<210> 73
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 73
Ser Ala Lys Thr Thr Pro Lys Leu Glu Glu Gly Glu Phe Ser Glu Ala
1 5 10 15
Arg Val
<210> 74
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 74
Ser Ala Lys Thr Thr Pro Lys Leu Gly Gly
1 5 10
<210> 75
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 75
Ser Thr Ala Gly Asp Thr His Leu Gly Gly Glu Asp Phe Asp
1 5 10
<210> 76
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 76
Thr Val Ala Ala Pro
1 5
<210> 77
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 77
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro
1 5 10
<210> 78
<211> 24
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 78
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Thr Val Ala Ala
1 5 10 15
Pro Ser Val Phe Ile Phe Pro Pro
20
<210> 79
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 79
Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn
1 5 10
<210> 80
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 80
Ser Gln Ser Ile Ser Ser Tyr
1 5
<210> 81
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 81
Gln Ser Ile Ser Ser Tyr
1 5
<210> 82
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 82
Ala Ala Ser Ser Leu Gln Ser
1 5
<210> 83
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 83
Ala Ala Ser
1
<210> 84
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Thr"
<220>
<221> Сайт
<222> (1)..(9)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 84
Gln Gln Ser Tyr Ser Ser Pro Leu Thr
1 5
<210> 85
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Gly", или "Asp", или "Tyr", или "Ala"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Thr" или "Ala"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="Leu"
<220>
<221> Сайт
<222> (1)..(9)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 85
Gln Gln Ser Tyr Ser Ser Pro Pro Thr
1 5
<210> 86
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Thr"
<220>
<221> Сайт
<222> (1)..(6)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 86
Ser Tyr Ser Ser Pro Leu
1 5
<210> 87
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Gly", или "Asp", или "Tyr", или "Ala"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Thr" или "Ala"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Leu"
<220>
<221> Сайт
<222> (1)..(6)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 87
Ser Tyr Ser Ser Pro Pro
1 5
<210> 88
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 88
Ser Tyr Ala Met Ser
1 5
<210> 89
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 89
Gly Phe Thr Phe Ser Ser Tyr
1 5
<210> 90
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 90
Gly Phe Thr Phe Ser Ser Tyr Ala
1 5
<210> 91
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 91
Gly Phe Thr Phe Ser Ser Tyr Ala Met Ser
1 5 10
<210> 92
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Glu"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="Arg"
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> /замена="Ala"
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /замена="Ala"
<220>
<221> Сайт
<222> (1)..(17)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 92
Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 93
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замещение="Glu" или "Ala"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Ala", или "His", или "Glu"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Asp", или "Glu", или "His", или "Arg", или "Ala"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="Arg", или "Val", или "Thr", или "Tyr"
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> /замена="Ala", или "Glu", или "His", или "Arg"
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /замена="Ala" или "Ser"
<220>
<221> Сайт
<222> (1)..(17)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 93
Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 94
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /замена="Glu"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Arg"
<220>
<221> Сайт
<222> (1)..(6)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 94
Ser Gly Ser Gly Gly Ser
1 5
<210> 95
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /замещение="Glu" или "Ala"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Ala", или "His", или "Glu"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Asp", или "Glu", или "His", или "Arg", или "Ala"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Arg", или "Val", или "Thr", или "Tyr"
<220>
<221> Сайт
<222> (1)..(6)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 95
Ser Gly Ser Gly Gly Ser
1 5
<210> 96
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Glu"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Arg"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="Ala"
<220>
<221> Сайт
<222> (1)..(8)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 96
Ile Ser Gly Ser Gly Gly Ser Thr
1 5
<210> 97
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замещение="Glu" или "Ala"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Ala", или "His", или "Glu"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Asp", или "Glu", или "His", или "Arg", или "Ala"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Arg", или "Val", или "Thr", или "Tyr"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="Ala", или "Glu", или "His", или "Arg"
<220>
<221> Сайт
<222> (1)..(8)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 97
Ile Ser Gly Ser Gly Gly Ser Thr
1 5
<210> 98
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 98
Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr
1 5 10
<210> 99
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 99
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr
1 5 10
<210> 100
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 100
Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr Asn Tyr Val Ser
1 5 10
<210> 101
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 101
Thr Ser Ser Asp Val Gly Gly Tyr Asn Tyr
1 5 10
<210> 102
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 102
Ser Ser Asp Val Gly Gly Tyr Asn Tyr
1 5
<210> 103
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Pro"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Ser"
<220>
<221> Сайт
<222> (1)..(7)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 103
Asp Val Ser Asn Arg Leu Arg
1 5
<210> 104
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена="Glu"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Pro" или "Ala"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Ser", или "Gly", или "Trp"
<220>
<221> Сайт
<222> (1)..(7)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 104
Asp Val Ser Asn Arg Leu Arg
1 5
<210> 105
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 105
Asp Val Ser
1
<210> 106
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена="Glu"
<220>
<221> Сайт
<222> (1)..(3)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 106
Asp Val Ser
1
<210> 107
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Pro"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Ser"
<220>
<221> Сайт
<222> (1)..(10)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 107
Asp Val Ser Asn Arg Leu Arg Gly Val Ser
1 5 10
<210> 108
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена="Glu"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Pro" или "Ala"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Ser", или "Gly", или "Trp"
<220>
<221> Сайт
<222> (1)..(10)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 108
Asp Val Ser Asn Arg Leu Arg Gly Val Ser
1 5 10
<210> 109
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена="Glu"
<220>
<221> Сайт
<222> (1)..(3)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 109
Asp Val Ser
1
<210> 110
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="Thr"
<220>
<221> Сайт
<222> (1)..(11)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 110
Ser Ser Tyr Thr Ser Ser Ser Ala Leu Tyr Val
1 5 10
<210> 111
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Thr"
<220>
<221> Сайт
<222> (1)..(8)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 111
Tyr Thr Ser Ser Ser Ala Leu Tyr
1 5
<210> 112
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 112
Ser Tyr Gly Met His
1 5
<210> 113
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Phe"
<220>
<221> Сайт
<222> (1)..(7)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 113
Gly Phe Thr Val Ser Ser Tyr
1 5
<210> 114
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Phe"
<220>
<221> Сайт
<222> (1)..(8)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 114
Gly Phe Thr Val Ser Ser Tyr Gly
1 5
<210> 115
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Phe"
<220>
<221> Сайт
<222> (1)..(10)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 115
Gly Phe Thr Val Ser Ser Tyr Gly Met His
1 5 10
<210> 116
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Asp"
<220>
<221> Сайт
<222> (1)..(17)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 116
Val Ile Ser Tyr Thr Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 117
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Lys", или "Thr", или "Arg", или "Asp", или "Asn", или "Ser"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Asp" или "Glu"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Thr", или "Phe", или "Ala", или "Leu"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="Asn" или "Lys"
<220>
<221> Сайт
<222> (1)..(17)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 117
Val Ile Ser Tyr His Gly Ser His Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 118
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Asp"
<220>
<221> Сайт
<222> (1)..(6)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 118
Ser Tyr Thr Gly Ser Asn
1 5
<210> 119
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Lys", или "Thr", или "Arg", или "Asp", или "Asn", или "Ser"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Asp" или "Glu"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Thr", или "Phe", или "Ala", или "Leu"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Asn" или "Lys"
<220>
<221> Сайт
<222> (1)..(8)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 119
Ser Tyr His Gly Ser His Lys Gly
1 5
<210> 120
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Asp"
<220>
<221> Сайт
<222> (1)..(8)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 120
Ile Ser Tyr Thr Gly Ser Asn Lys
1 5
<210> 121
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Lys", или "Thr", или "Arg", или "Asp", или "Asn", или "Ser"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Asp" или "Glu"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Thr", или "Phe", или "Ala", или "Leu"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Asn" или "Lys"
<220>
<221> Сайт
<222> (1)..(8)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 121
Ile Ser Tyr His Gly Ser His Lys
1 5
<210> 122
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 122
Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
1 5 10
<210> 123
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Asn" или "Glu"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Phe", или "Val", или "Tyr"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Gln", или "Arg", или "Asp"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Glu", или "Gly", или "Gln"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="Gln" или "Phe"
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> /замена="Gln"
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /замена="Lys" или "Asp"
<220>
<221> ВАРИАНТ
<222> (11)..(11)
<223> /замена="Pro"
<220>
<221> ВАРИАНТ
<222> (12)..(12)
<223> /замена="Gln", или "Val", или "Thr"
<220>
<221> Сайт
<222> (1)..(14)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 123
Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
1 5 10
<210> 124
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 124
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
1 5 10 15
<210> 125
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Asn" или "Glu"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Phe", или "Val", или "Tyr"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="Gln", или "Arg", или "Asp"
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> /замена="Glu", или "Gly", или "Gln"
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /замена="Gln" или "Phe"
<220>
<221> ВАРИАНТ
<222> (11)..(11)
<223> /замена="Gln"
<220>
<221> ВАРИАНТ
<222> (12)..(12)
<223> /замена="Lys" или "Asp"
<220>
<221> ВАРИАНТ
<222> (13)..(13)
<223> /замена="Pro"
<220>
<221> ВАРИАНТ
<222> (14)..(14)
<223> /замена="Gln", или "Val", или "Thr"
<220>
<221> Сайт
<222> (1)..(16)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 125
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
1 5 10 15
<210> 126
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 126
Gln Gln Ser Tyr Ser Ser Pro Leu Thr
1 5
<210> 127
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 127
Gln Gln Ser Tyr Ser Thr Pro Leu Thr
1 5
<210> 128
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 128
Gln Gln Ser Tyr Gly Ser Pro Pro Thr
1 5
<210> 129
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 129
Gln Gln Ser Tyr Asp Ser Pro Leu Thr
1 5
<210> 130
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 130
Gln Gln Ser Tyr Tyr Ser Pro Leu Thr
1 5
<210> 131
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 131
Gln Gln Ser Tyr Tyr Ala Pro Leu Thr
1 5
<210> 132
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 132
Gln Gln Ser Tyr Ala Ser Pro Leu Thr
1 5
<210> 133
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 133
Gln Gln Ser Tyr Gly Ser Pro Leu Thr
1 5
<210> 134
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 134
Gln Gln Ser Tyr Asp Ala Pro Leu Thr
1 5
<210> 135
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 135
Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 136
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 136
Ala Ile Ser Glu Ser Gly Gly Arg Ala Ala Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 137
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 137
Ala Ile Ser Gly Ser Gly Gly Arg Ala Ala Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 138
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 138
Ala Ile Ser Glu Ser Gly Asp Val Glu Ala Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 139
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 139
Ala Ile Ser Glu Ala Gly Glu Thr Thr Ser Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 140
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 140
Ala Ile Ser Glu His Gly His Tyr Thr Ser Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 141
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 141
Ala Ile Ser Gly Ser Gly His Thr Ala Ala Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 142
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 142
Ala Ile Ser Gly Ser Gly Arg Thr His Ala Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 143
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 143
Ala Ile Ser Ala Glu Gly Gly Val Arg Ala Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 144
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 144
Ala Ile Ser Gly Ser Gly Gly Thr Thr Ala Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 145
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 145
Ala Ile Ser Gly Ser Gly Ala Thr Thr Ala Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 146
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 146
Ser Tyr Ser Ser Pro Leu
1 5
<210> 147
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 147
Ser Tyr Ser Thr Pro Leu
1 5
<210> 148
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 148
Ser Tyr Gly Ser Pro Pro
1 5
<210> 149
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 149
Ser Tyr Asp Ser Pro Leu
1 5
<210> 150
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 150
Ser Tyr Tyr Ser Pro Leu
1 5
<210> 151
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 151
Ser Tyr Tyr Ala Pro Leu
1 5
<210> 152
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 152
Ser Tyr Ala Ser Pro Leu
1 5
<210> 153
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 153
Ser Tyr Gly Ser Pro Leu
1 5
<210> 154
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 154
Ser Tyr Asp Ala Pro Leu
1 5
<210> 155
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 155
Ser Gly Ser Gly Gly Ser
1 5
<210> 156
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 156
Ser Glu Ser Gly Gly Arg
1 5
<210> 157
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 157
Ser Gly Ser Gly Gly Arg
1 5
<210> 158
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 158
Ser Glu Ser Gly Asp Val
1 5
<210> 159
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 159
Ser Glu His Gly His Tyr
1 5
<210> 160
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 160
Ser Gly Ser Gly His Thr
1 5
<210> 161
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 161
Ser Gly Ser Gly Arg Thr
1 5
<210> 162
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 162
Ser Ala Glu Gly Gly Val
1 5
<210> 163
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 163
Ser Gly Ser Gly Gly Thr
1 5
<210> 164
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 164
Ser Gly Ser Gly Ala Thr
1 5
<210> 165
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 165
Ile Ser Gly Ser Gly Gly Ser Thr
1 5
<210> 166
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 166
Ile Ser Glu Ser Gly Gly Arg Ala
1 5
<210> 167
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 167
Ile Ser Gly Ser Gly Gly Arg Ala
1 5
<210> 168
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 168
Ile Ser Glu Ser Gly Asp Val Glu
1 5
<210> 169
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 169
Ile Ser Glu His Gly His Tyr Thr
1 5
<210> 170
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 170
Ile Ser Gly Ser Gly His Thr Ala
1 5
<210> 171
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 171
Ile Ser Gly Ser Gly Arg Thr His
1 5
<210> 172
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 172
Ile Ser Ala Glu Gly Gly Val Arg
1 5
<210> 173
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 173
Ile Ser Gly Ser Gly Gly Thr Thr
1 5
<210> 174
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 174
Ile Ser Gly Ser Gly Ala Thr Thr
1 5
<210> 175
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 175
Asp Val Ser Asn Arg Leu Arg
1 5
<210> 176
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 176
Asp Val Ser Asn Arg Pro Ser
1 5
<210> 177
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 177
Glu Val Ser Asn Arg Leu Ser
1 5
<210> 178
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 178
Glu Val Ser Asn Arg Leu Arg
1 5
<210> 179
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 179
Asp Val Ser Asn Arg Pro Trp
1 5
<210> 180
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 180
Asp Val Ser Asn Arg Leu Ser
1 5
<210> 181
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 181
Asp Val Ser Asn Arg Ala Trp
1 5
<210> 182
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 182
Glu Val Ser Asn Arg Leu Gly
1 5
<210> 183
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 183
Ser Ser Tyr Thr Ser Ser Ser Ala Leu Tyr Val
1 5 10
<210> 184
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 184
Ser Ser Tyr Thr Ser Ser Ser Thr Leu Tyr Val
1 5 10
<210> 185
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 185
Val Ile Ser Tyr Thr Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 186
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 186
Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 187
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 187
Val Ile Ser Tyr His Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 188
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 188
Val Ile Ser Tyr Lys Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 189
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 189
Val Ile Ser Tyr Thr Gly Thr Lys Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 190
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 190
Val Ile Ser Tyr Arg Gly Phe Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 191
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 191
Val Ile Ser Tyr Lys Gly Ser His Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 192
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 192
Val Ile Ser Tyr Asp Asp Ala His Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 193
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 193
Val Ile Ser Tyr Asn Asp Leu Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 194
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 194
Val Ile Ser Tyr Ser Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 195
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 195
Val Ile Ser Tyr Thr Gly Ala Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 196
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 196
Val Ile Ser Tyr Asn Asp Ala Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 197
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 197
Val Ile Ser Tyr Asp Glu Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 198
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 198
Val Ile Ser Tyr Asp Asp Ala Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 199
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 199
Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Gln Asp Val
1 5 10
<210> 200
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 200
Ser Gly Tyr Ala Leu His Asp Gln Tyr Lys Pro Val Asp Val
1 5 10
<210> 201
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 201
Ser Gly Tyr Ala Leu His Asp Phe Gln Asp Pro Thr Asp Val
1 5 10
<210> 202
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 202
Ser Gly Tyr Asn Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
1 5 10
<210> 203
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 203
Ser Gly Tyr Glu Phe His Glu Asp Tyr Tyr Gly Leu Asp Val
1 5 10
<210> 204
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 204
Ser Gly Tyr Glu Phe Gln Gly Asp Tyr Tyr Gly Leu Asp Val
1 5 10
<210> 205
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 205
Ser Gly Tyr Glu Leu Arg Asp Asp Tyr Tyr Gly Leu Asp Val
1 5 10
<210> 206
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 206
Ser Gly Tyr Glu Val Asp Gln Asp Tyr Tyr Gly Leu Asp Val
1 5 10
<210> 207
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 207
Ser Gly Tyr Ala Tyr Asp Gly Asp Tyr Tyr Gly Leu Asp Val
1 5 10
<210> 208
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 208
Glu Val Ser
1
<210> 209
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 209
Tyr Thr Ser Ser Ser Ala Leu Tyr
1 5
<210> 210
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 210
Tyr Thr Ser Ser Ser Thr Leu Tyr
1 5
<210> 211
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 211
Gly Phe Thr Val Ser Ser Tyr
1 5
<210> 212
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 212
Gly Phe Thr Leu Ser Ser Tyr
1 5
<210> 213
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 213
Ser Tyr Thr Gly Ser Asn
1 5
<210> 214
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 214
Ser Tyr Asp Gly Ser Asn
1 5
<210> 215
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 215
Ser Tyr His Gly Ser Asn
1 5
<210> 216
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 216
Ser Tyr Lys Gly Ser Asn
1 5
<210> 217
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 217
Ser Tyr Thr Gly Thr Lys
1 5
<210> 218
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 218
Ser Tyr Arg Gly Phe Asn
1 5
<210> 219
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 219
Ser Tyr Lys Gly Ser His
1 5
<210> 220
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 220
Ser Tyr Asp Asp Ala His
1 5
<210> 221
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 221
Ser Tyr Asn Asp Leu Asn
1 5
<210> 222
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 222
Ser Tyr Ser Gly Ser Asn
1 5
<210> 223
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 223
Ser Tyr Thr Gly Ala Asn
1 5
<210> 224
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 224
Ser Tyr Asn Asp Ala Asn
1 5
<210> 225
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 225
Ser Tyr Asp Glu Ser Asn
1 5
<210> 226
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 226
Ser Tyr Asp Asp Ala Asn
1 5
<210> 227
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 227
Asp Val Ser Asn Arg Leu Arg Gly Val Ser
1 5 10
<210> 228
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 228
Asp Val Ser Asn Arg Pro Ser Gly Val Ser
1 5 10
<210> 229
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 229
Glu Val Ser Asn Arg Leu Ser Gly Val Ser
1 5 10
<210> 230
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 230
Glu Val Ser Asn Arg Leu Arg Gly Val Ser
1 5 10
<210> 231
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 231
Asp Val Ser Asn Arg Pro Trp Gly Val Ser
1 5 10
<210> 232
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 232
Asp Val Ser Asn Arg Leu Ser Gly Val Ser
1 5 10
<210> 233
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 233
Asp Val Ser Asn Arg Ala Trp Gly Val Ser
1 5 10
<210> 234
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 234
Glu Val Ser Asn Arg Leu Gly Gly Val Ser
1 5 10
<210> 235
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 235
Gly Phe Thr Val Ser Ser Tyr Gly
1 5
<210> 236
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 236
Gly Phe Thr Phe Ser Ser Tyr Gly
1 5
<210> 237
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 237
Gly Phe Thr Leu Ser Ser Tyr Gly
1 5
<210> 238
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 238
Ile Ser Tyr Thr Gly Ser Asn Lys
1 5
<210> 239
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 239
Ile Ser Tyr Asp Gly Ser Asn Lys
1 5
<210> 240
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 240
Ile Ser Tyr His Gly Ser Asn Lys
1 5
<210> 241
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 241
Ile Ser Tyr Lys Gly Ser Asn Lys
1 5
<210> 242
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 242
Ile Ser Tyr Thr Gly Thr Lys Lys
1 5
<210> 243
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 243
Ile Ser Tyr Arg Gly Phe Asn Lys
1 5
<210> 244
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 244
Ile Ser Tyr Lys Gly Ser His Lys
1 5
<210> 245
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 245
Ile Ser Tyr Asp Asp Ala His Lys
1 5
<210> 246
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 246
Ile Ser Tyr Asn Asp Leu Asn Lys
1 5
<210> 247
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 247
Ile Ser Tyr Ser Gly Ser Asn Lys
1 5
<210> 248
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 248
Ile Ser Tyr Thr Gly Ala Asn Lys
1 5
<210> 249
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 249
Ile Ser Tyr Asn Asp Ala Asn Lys
1 5
<210> 250
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 250
Ile Ser Tyr Asp Glu Ser Asn Lys
1 5
<210> 251
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 251
Ile Ser Tyr Asp Asp Ala Asn Lys
1 5
<210> 252
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 252
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Gln Asp Val
1 5 10 15
<210> 253
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 253
Gly Gly Ser Gly Tyr Ala Leu His Asp Gln Tyr Lys Pro Val Asp Val
1 5 10 15
<210> 254
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 254
Gly Gly Ser Gly Tyr Ala Leu His Asp Phe Gln Asp Pro Thr Asp Val
1 5 10 15
<210> 255
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 255
Gly Gly Ser Gly Tyr Asn Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
1 5 10 15
<210> 256
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 256
Gly Gly Ser Gly Tyr Glu Phe His Glu Asp Tyr Tyr Gly Leu Asp Val
1 5 10 15
<210> 257
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 257
Gly Gly Ser Gly Tyr Glu Phe Gln Gly Asp Tyr Tyr Gly Leu Asp Val
1 5 10 15
<210> 258
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 258
Gly Gly Ser Gly Tyr Glu Leu Arg Asp Asp Tyr Tyr Gly Leu Asp Val
1 5 10 15
<210> 259
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 259
Gly Gly Ser Gly Tyr Glu Val Asp Gln Asp Tyr Tyr Gly Leu Asp Val
1 5 10 15
<210> 260
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 260
Gly Gly Ser Gly Tyr Ala Tyr Asp Gly Asp Tyr Tyr Gly Leu Asp Val
1 5 10 15
<210> 261
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 261
Gly Phe Thr Val Ser Ser Tyr Gly Met His
1 5 10
<210> 262
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 262
Gly Phe Thr Phe Ser Ser Tyr Gly Met His
1 5 10
<210> 263
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 263
Gly Phe Thr Leu Ser Ser Tyr Gly Met His
1 5 10
<210> 264
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 264
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 265
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 265
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 266
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 266
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Gly Ser Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 267
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 267
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Asp Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 268
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 268
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Tyr Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 269
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 269
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Tyr Ala Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 270
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 270
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ala Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 271
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 271
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Gly Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 272
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 272
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Asp Ala Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 273
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 273
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Leu Arg Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Ala Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 274
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 274
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Pro Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Thr Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 275
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 275
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Glu Val Ser Asn Arg Leu Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Thr Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 276
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 276
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Glu Val Ser Asn Arg Leu Arg Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Ala Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 277
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 277
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Glu Val Ser Asn Arg Leu Arg Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Thr Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 278
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 278
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Pro Trp Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Ala Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Met
100 105 110
<210> 279
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 279
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Leu Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Thr Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 280
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 280
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Pro Trp Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Thr Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 281
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 281
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Leu Arg Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Ala Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 282
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 282
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Ala Trp Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Ala Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 283
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 283
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Glu Val Ser Asn Arg Leu Arg Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Tyr Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Thr Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 284
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 284
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Glu Val Ser Asn Arg Leu Ser Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Ala Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 285
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 285
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Glu Val Ser Asn Arg Leu Gly Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Ala Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
100 105 110
<210> 286
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 286
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 287
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 287
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Glu Ser Gly Gly Arg Ala Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 288
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 288
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Arg Ala Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 289
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 289
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Glu Ser Gly Asp Val Glu Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 290
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 290
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Glu Ala Gly Glu Thr Thr Ser Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 291
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 291
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Glu His Gly His Tyr Thr Ser Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 292
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 292
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly His Thr Ala Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 293
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 293
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Arg Thr His Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 294
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 294
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Ala Glu Gly Gly Val Arg Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 295
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 295
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Thr Thr Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 296
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 296
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Ala Thr Thr Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Glu Trp Trp Tyr Asp Asp Trp Tyr Leu Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 297
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 297
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 298
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 298
Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 299
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 299
Gln Ala Gln Leu Gln Ser Ser Glu Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr His Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ser
115 120
<210> 300
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 300
Gln Val Gln Leu Gln Ser Ser Glu Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Lys Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 301
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 301
Gln Ala Gln Leu Gln Ser Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Lys Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 302
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 302
Gln Val Gln Leu Gln Asp Ser Glu Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Thr Lys Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 303
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 303
Gln Ala Gln Leu Gln Ser Ser Glu Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Arg Gly Phe Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Gln Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 304
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 304
Gln Ala Gln Leu Gln Gly Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Lys Gly Ser His Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 305
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 305
Gln Ala Gln Leu Gln Ser Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 306
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 306
Gln Val Gln Leu Gln Ser Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 307
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 307
Gln Ala Gln Leu Gln Gly Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Lys Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 308
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 308
Gln Val Gln Leu Gln Gly Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Asp Ala His Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Gln Tyr Lys Pro Val Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 309
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 309
Gln Ala Gln Leu Gln Glu Ser Glu Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asn Asp Leu Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Phe Gln Asp Pro Thr Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 310
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 310
Gln Val Gln Leu Gln Ser Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Ser Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Gln Tyr Lys Pro Val Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 311
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 311
Gln Val Gln Leu Gln Gly Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Ala Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Asn Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 312
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 312
Gln Ala Gln Leu Gln Arg Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Asp Ala His Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Gln Tyr Lys Pro Val Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 313
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 313
Gln Val Gln Leu Gln Ser Ser Glu Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Glu Phe His Glu Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 314
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 314
Gln Ala Gln Leu Gln Gly Ser Glu Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Asp Ala His Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Gln Tyr Lys Pro Val Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 315
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 315
Gln Val Gln Leu Gln Ser Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asn Asp Leu Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Glu Phe Gln Gly Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 316
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 316
Gln Val Gln Leu Gln Ser Ser Glu Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asn Asp Ala Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Glu Leu Arg Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 317
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 317
Gln Ala Gln Leu Gln Ser Ser Glu Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Glu Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Glu Val Asp Gln Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 318
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 318
Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Asp Ala His Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Gln Tyr Lys Pro Val Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 319
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 319
Gln Val Gln Leu Gln Gly Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Asp Ala Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Ser Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Tyr Asp Gly Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 320
<211> 255
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 320
Gln Val Gln Leu Gln Ser Ser Glu Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Lys Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
145 150 155 160
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
165 170 175
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
180 185 190
Met Ile Tyr Glu Val Ser Asn Arg Leu Arg Gly Val Ser Asn Arg Phe
195 200 205
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
210 215 220
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
225 230 235 240
Ser Ala Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
245 250 255
<210> 321
<211> 255
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 321
Gln Ala Gln Leu Gln Ser Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Lys Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
145 150 155 160
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
165 170 175
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
180 185 190
Met Ile Tyr Glu Val Ser Asn Arg Leu Arg Gly Val Ser Asn Arg Phe
195 200 205
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
210 215 220
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
225 230 235 240
Ser Thr Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
245 250 255
<210> 322
<211> 255
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 322
Gln Val Gln Leu Gln Asp Ser Glu Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Thr Lys Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
145 150 155 160
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
165 170 175
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
180 185 190
Met Ile Tyr Asp Val Ser Asn Arg Pro Trp Gly Val Ser Asn Arg Phe
195 200 205
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
210 215 220
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
225 230 235 240
Ser Ala Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Met
245 250 255
<210> 323
<211> 255
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 323
Gln Ala Gln Leu Gln Ser Ser Glu Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Arg Gly Phe Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Gln Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
145 150 155 160
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
165 170 175
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
180 185 190
Met Ile Tyr Asp Val Ser Asn Arg Leu Ser Gly Val Ser Asn Arg Phe
195 200 205
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
210 215 220
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
225 230 235 240
Ser Thr Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
245 250 255
<210> 324
<211> 255
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 324
Gln Ala Gln Leu Gln Gly Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Lys Gly Ser His Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
145 150 155 160
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
165 170 175
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
180 185 190
Met Ile Tyr Asp Val Ser Asn Arg Pro Trp Gly Val Ser Asn Arg Phe
195 200 205
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
210 215 220
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
225 230 235 240
Ser Thr Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
245 250 255
<210> 325
<211> 255
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 325
Gln Val Gln Leu Gln Ser Ser Glu Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Lys Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
145 150 155 160
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
165 170 175
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
180 185 190
Met Ile Tyr Asp Val Ser Asn Arg Pro Trp Gly Val Ser Asn Arg Phe
195 200 205
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
210 215 220
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
225 230 235 240
Ser Thr Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
245 250 255
<210> 326
<211> 255
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 326
Gln Ala Gln Leu Gln Ser Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
145 150 155 160
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
165 170 175
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
180 185 190
Met Ile Tyr Asp Val Ser Asn Arg Leu Arg Gly Val Ser Asn Arg Phe
195 200 205
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
210 215 220
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
225 230 235 240
Ser Ala Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
245 250 255
<210> 327
<211> 255
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 327
Gln Val Gln Leu Gln Ser Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
145 150 155 160
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
165 170 175
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
180 185 190
Met Ile Tyr Asp Val Ser Asn Arg Ala Trp Gly Val Ser Asn Arg Phe
195 200 205
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
210 215 220
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
225 230 235 240
Ser Ala Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
245 250 255
<210> 328
<211> 255
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 328
Gln Ala Gln Leu Gln Gly Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Lys Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
145 150 155 160
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
165 170 175
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
180 185 190
Met Ile Tyr Glu Val Ser Asn Arg Leu Arg Gly Val Ser Asn Arg Phe
195 200 205
Ser Gly Ser Lys Phe Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
210 215 220
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
225 230 235 240
Ser Thr Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu
245 250 255
<210> 329
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 329
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Arg Tyr
20 25 30
Thr Met His Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Thr Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Tyr Asp Asp His Tyr Cys Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Leu Thr Val Ser Ser
115
<210> 330
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 330
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ala His Phe Arg Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Gly Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Phe Thr
85 90 95
Phe Gly Ser Gly Thr Lys Leu Glu Ile Asn
100 105
<210> 331
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 331
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Lys Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Asp Arg Phe Thr Ile Ser Arg Asp Asp Ser Gln Ser Ile
65 70 75 80
Leu Tyr Leu Gln Met Asn Asn Leu Lys Thr Glu Asp Thr Ala Met Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala
115 120 125
<210> 332
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 332
Gln Ala Val Val Thr Gln Glu Ser Ala Leu Thr Thr Ser Pro Gly Glu
1 5 10 15
Thr Val Thr Leu Thr Cys Arg Ser Ser Thr Gly Ala Val Thr Thr Ser
20 25 30
Asn Tyr Ala Asn Trp Val Gln Glu Lys Pro Asp His Leu Phe Thr Gly
35 40 45
Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Val Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Ile Gly Asp Lys Ala Ala Leu Thr Ile Thr Gly Ala
65 70 75 80
Gln Thr Glu Asp Glu Ala Ile Tyr Phe Cys Ala Leu Trp Tyr Ser Asn
85 90 95
Leu Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 333
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 333
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Thr Met His Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Ser Ser Gly Tyr Thr Lys Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Trp Gln Asp Tyr Asp Val Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Leu Thr Val Ser Ser
115
<210> 334
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 334
Gln Ile Val Leu Ser Gln Ser Pro Ala Ile Leu Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Pro Trp Ile Tyr
35 40 45
Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Arg Val Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Pro Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Thr Lys
100 105
<210> 335
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 335
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Val Ala Ser Gly Val Pro Tyr Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ser Gly Thr Lys Leu Glu Ile Asn
100 105
<210> 336
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 336
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Arg Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn Tyr Asn Gln Lys Val
50 55 60
Lys Asp Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Ala Phe
65 70 75 80
Leu Gln Met Asp Ser Leu Arg Pro Glu Asp Thr Gly Val Tyr Phe Cys
85 90 95
Ala Arg Tyr Tyr Asp Asp His Tyr Cys Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Pro Val Thr Val Ser Ser
115
<210> 337
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 337
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Thr Pro Gly Lys Ala Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Tyr Thr Phe Thr Ile Ser Ser Leu Gln Pro Glu
65 70 75 80
Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Phe Thr
85 90 95
Phe Gly Gln Gly Thr Lys Leu Gln Ile Thr
100 105
<210> 338
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 338
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Lys Phe Ser Gly Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Lys Lys Tyr Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Met Gly Tyr Trp His Phe Asp Leu Trp Gly Arg Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 339
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 339
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Pro
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 340
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 340
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Asp Arg Phe Ile Ser Arg Asp Asp Ser Lys Asn Ser Leu
65 70 75 80
Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala
100 105 110
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 341
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 341
Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly
1 5 10 15
Thr Val Thr Leu Thr Cys Arg Ser Ser Thr Gly Ala Val Thr Thr Ser
20 25 30
Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg Gly
35 40 45
Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Trp Thr Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Ile Gly Ala Gln Ala
65 70 75 80
Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn Leu Trp
85 90 95
Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 342
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 342
Asp Ile Lys Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Arg Tyr
20 25 30
Thr Met His Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Thr Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Tyr Asp Asp His Tyr Cys Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Leu Thr Val Ser Ser
115
<210> 343
<211> 105
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 343
Asp Ile Gln Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Val Ala Ser Gly Val Pro Tyr Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Ile Ser Ser Met Glu Ala Glu Asp
65 70 75 80
Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr Phe
85 90 95
Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 344
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 344
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Asp Arg Phe Ile Ser Arg Asp Asp Ser Lys Asn Ser Leu
65 70 75 80
Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala
100 105 110
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 345
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 345
Glu Val Lys Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Lys Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Asp Arg Phe Thr Ile Ser Arg Asp Asp Ser Gln Ser Ile
65 70 75 80
Leu Tyr Leu Gln Met Asn Asn Leu Lys Thr Glu Asp Thr Ala Met Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala
115 120 125
<210> 346
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 346
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Ala Tyr Leu Gln Met Asn Asn Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Trp
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 347
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 347
Gln Thr Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly
1 5 10 15
Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Ser Gly
20 25 30
Asn Tyr Pro Asn Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg Gly
35 40 45
Leu Ile Gly Gly Thr Lys Phe Leu Ala Pro Gly Thr Pro Gln Arg Phe
50 55 60
Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly Val
65 70 75 80
Gln Pro Glu Asp Glu Ala Glu Tyr Tyr Cys Val Leu Trp Tyr Ser Asn
85 90 95
Arg Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 348
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 348
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Lys Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Asp Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Ala Tyr Leu Gln Met Asn Asn Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Ile Ser Tyr Trp
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 349
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 349
Gln Thr Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly
1 5 10 15
Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Ser Gly
20 25 30
Asn Tyr Pro Asn Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg Gly
35 40 45
Leu Ile Gly Gly Thr Lys Phe Leu Ala Pro Gly Thr Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly Val
65 70 75 80
Gln Pro Glu Asp Glu Ala Glu Tyr Tyr Cys Val Leu Trp Tyr Ser Asn
85 90 95
Arg Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 350
<211> 254
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 350
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Lys Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Asp Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Ala Tyr Leu Gln Met Asn Asn Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Ile Ser Tyr Trp
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gln Thr Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly
145 150 155 160
Gly Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Ser
165 170 175
Gly Asn Tyr Pro Asn Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg
180 185 190
Gly Leu Ile Gly Gly Thr Lys Phe Leu Ala Pro Gly Thr Pro Ala Arg
195 200 205
Phe Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly
210 215 220
Val Gln Pro Glu Asp Glu Ala Glu Tyr Tyr Cys Val Leu Trp Tyr Ser
225 230 235 240
Asn Arg Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
245 250
<210> 351
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 351
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Arg Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Arg Val Thr Met Thr Thr Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Tyr Asp Asp His Tyr Cys Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 352
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 352
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ala His Phe Arg Gly Ser
50 55 60
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu
65 70 75 80
Asp Phe Ala Val Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Phe Thr
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 353
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 353
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Asp Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Ala Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 354
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 354
Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly
1 5 10 15
Thr Val Thr Leu Thr Cys Arg Ser Ser Thr Gly Ala Val Thr Thr Ser
20 25 30
Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg Gly
35 40 45
Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Thr Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly Val
65 70 75 80
Gln Pro Glu Asp Glu Ala Glu Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn
85 90 95
Leu Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 355
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 355
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Asp Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 356
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 356
Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly
1 5 10 15
Thr Val Thr Leu Thr Cys Arg Ser Ser Thr Gly Ala Val Thr Thr Ser
20 25 30
Asn Tyr Ala Asn Trp Val Gln Glu Lys Pro Gly Gln Ala Pro Arg Gly
35 40 45
Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Trp Thr Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Ile Thr Gly Ala
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn
85 90 95
Leu Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 357
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 357
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 358
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 358
Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly
1 5 10 15
Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr Ser
20 25 30
Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg Gly
35 40 45
Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Val Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly Ala
65 70 75 80
Gln Pro Glu Asp Glu Ala Glu Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn
85 90 95
Leu Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 359
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 359
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 360
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 360
Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly
1 5 10 15
Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr Ser
20 25 30
Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Lys Ser Pro Arg Gly
35 40 45
Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Val Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Ile Ser Gly Ala
65 70 75 80
Gln Pro Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn
85 90 95
His Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 361
<211> 101
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 361
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
Asn Trp Tyr Gln Gln Thr Pro Gly Lys Ala Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Tyr Thr Phe Thr Ile Ser Ser Leu Gln Pro Glu
65 70 75 80
Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Phe Thr
85 90 95
Phe Gly Gln Gly Thr
100
<210> 362
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 362
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Arg Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn Tyr Asn Gln Lys Val
50 55 60
Lys Asp Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Ala Phe
65 70 75 80
Leu Gln Met Asp Ser Leu Arg Pro Glu Asp Thr Gly Val Tyr Phe Cys
85 90 95
Ala Arg Tyr Tyr Asp Asp His Tyr Ser Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Pro Val Thr Val Ser Ser
115
<210> 363
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 363
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Met Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Thr Met Asn Trp Val Lys Gln Ser His Gly Lys Asn Leu Glu Trp Met
35 40 45
Gly Leu Ile Asn Pro Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Leu Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Gly Tyr Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Leu Thr Val Phe Ser
115 120
<210> 364
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 364
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Arg Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Arg Leu His Ser Gly Val Pro Ser Lys Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Trp
85 90 95
Thr Phe Ala Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 365
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 365
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Ser Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Asp Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 366
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 366
Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly
1 5 10 15
Thr Val Thr Leu Thr Cys Arg Ser Ser Thr Gly Ala Val Thr Thr Ser
20 25 30
Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg Gly
35 40 45
Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Trp Thr Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Leu Gly Asp Lys Ala Ala Leu Thr Leu Ser Gly Ala
65 70 75 80
Gln Pro Glu Asp Glu Ala Glu Tyr Phe Cys Ala Leu Trp Tyr Ser Asn
85 90 95
Leu Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 367
<211> 254
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 367
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Ser Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Asp Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly
145 150 155 160
Gly Thr Val Thr Leu Thr Cys Arg Ser Ser Thr Gly Ala Val Thr Thr
165 170 175
Ser Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg
180 185 190
Gly Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Trp Thr Pro Ala Arg
195 200 205
Phe Ser Gly Ser Leu Leu Gly Asp Lys Ala Ala Leu Thr Leu Ser Gly
210 215 220
Ala Gln Pro Glu Asp Glu Ala Glu Tyr Phe Cys Ala Leu Trp Tyr Ser
225 230 235 240
Asn Leu Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
245 250
<210> 368
<211> 254
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 368
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Lys Pro
115 120 125
Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly
130 135 140
Ser Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly
145 150 155 160
Gly Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr
165 170 175
Ser Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Lys Ser Pro Arg
180 185 190
Gly Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Val Pro Ala Arg
195 200 205
Phe Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Ile Ser Gly
210 215 220
Ala Gln Pro Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Leu Trp Tyr Ser
225 230 235 240
Asn His Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
245 250
<210> 369
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 369
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Ala Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 370
<211> 254
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 370
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Ala Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Lys Pro
115 120 125
Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly
130 135 140
Ser Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly
145 150 155 160
Gly Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr
165 170 175
Ser Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Lys Ser Pro Arg
180 185 190
Gly Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Val Pro Ala Arg
195 200 205
Phe Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Ile Ser Gly
210 215 220
Ala Gln Pro Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Leu Trp Tyr Ser
225 230 235 240
Asn His Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
245 250
<210> 371
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 371
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Glu Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 372
<211> 254
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 372
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Glu Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Lys Pro
115 120 125
Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly
130 135 140
Ser Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly
145 150 155 160
Gly Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr
165 170 175
Ser Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Lys Ser Pro Arg
180 185 190
Gly Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Val Pro Ala Arg
195 200 205
Phe Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Ile Ser Gly
210 215 220
Ala Gln Pro Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Leu Trp Tyr Ser
225 230 235 240
Asn His Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
245 250
<210> 373
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 373
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Pro Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 374
<211> 254
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 374
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Pro Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Lys Pro
115 120 125
Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly
130 135 140
Ser Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly
145 150 155 160
Gly Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr
165 170 175
Ser Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Lys Ser Pro Arg
180 185 190
Gly Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Val Pro Ala Arg
195 200 205
Phe Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Ile Ser Gly
210 215 220
Ala Gln Pro Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Leu Trp Tyr Ser
225 230 235 240
Asn His Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
245 250
<210> 375
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 375
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe
100 105 110
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 376
<211> 254
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 376
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe
100 105 110
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Lys Pro
115 120 125
Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly
130 135 140
Ser Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly
145 150 155 160
Gly Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr
165 170 175
Ser Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Lys Ser Pro Arg
180 185 190
Gly Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Val Pro Ala Arg
195 200 205
Phe Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Ile Ser Gly
210 215 220
Ala Gln Pro Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Leu Trp Tyr Ser
225 230 235 240
Asn His Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
245 250
<210> 377
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 377
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 378
<211> 254
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 378
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Lys Pro
115 120 125
Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly
130 135 140
Ser Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly
145 150 155 160
Gly Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr
165 170 175
Ser Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Lys Ser Pro Arg
180 185 190
Gly Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Gly Val Pro Ala Arg
195 200 205
Phe Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Ile Ser Gly
210 215 220
Ala Gln Pro Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Leu Trp Tyr Ser
225 230 235 240
Asn His Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
245 250
<210> 379
<211> 257
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 379
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ala Val Val
130 135 140
Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly Thr Val Thr Leu
145 150 155 160
Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr Ala Asn
165 170 175
Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg Gly Leu Ile Gly Gly
180 185 190
Thr Asn Lys Arg Ala Pro Gly Val Pro Ala Arg Phe Ser Gly Ser Leu
195 200 205
Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly Ala Gln Pro Glu Asp
210 215 220
Glu Ala Glu Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn Leu Trp Val Phe
225 230 235 240
Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Ser His His His His His
245 250 255
His
<210> 380
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 380
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Ser Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Asp Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Ala Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe
100 105 110
Ala His Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 381
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 381
Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly
1 5 10 15
Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Ser Ser
20 25 30
Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg Gly
35 40 45
Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Trp Thr Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly Ala
65 70 75 80
Gln Pro Glu Asp Glu Ala Glu Tyr Tyr Cys Ala Leu Trp Tyr Ser Asn
85 90 95
Leu Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 382
<211> 254
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 382
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Ser Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Asp Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Ala Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe
100 105 110
Ala His Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly
145 150 155 160
Gly Thr Val Thr Leu Thr Cys Gly Ser Ser Thr Gly Ala Val Thr Ser
165 170 175
Ser Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg
180 185 190
Gly Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Trp Thr Pro Ala Arg
195 200 205
Phe Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly
210 215 220
Ala Gln Pro Glu Asp Glu Ala Glu Tyr Tyr Cys Ala Leu Trp Tyr Ser
225 230 235 240
Asn Leu Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
245 250
<210> 383
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 383
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Ser Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Asp Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Thr
65 70 75 80
Ala Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 384
<211> 254
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 384
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Ser Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Asp Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Thr
65 70 75 80
Ala Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly
145 150 155 160
Gly Thr Val Thr Leu Thr Cys Arg Ser Ser Thr Gly Ala Val Thr Thr
165 170 175
Ser Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg
180 185 190
Gly Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Trp Thr Pro Ala Arg
195 200 205
Phe Ser Gly Ser Leu Leu Gly Asp Lys Ala Ala Leu Thr Leu Ser Gly
210 215 220
Ala Gln Pro Glu Asp Glu Ala Glu Tyr Phe Cys Ala Leu Trp Tyr Ser
225 230 235 240
Asn Leu Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
245 250
<210> 385
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 385
Arg Tyr Thr Met His
1 5
<210> 386
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 386
Ser Ala Ser Ser Ser Val Ser Tyr Met Asn
1 5 10
<210> 387
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 387
Thr Tyr Ala Met Asn
1 5
<210> 388
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 388
Arg Ser Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr Ala Asn
1 5 10
<210> 389
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 389
Ser Tyr Thr Met His
1 5
<210> 390
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 390
Arg Ala Ser Ser Ser Val Ser Tyr Met His
1 5 10
<210> 391
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 391
Arg Ala Ser Ser Ser Val Ser Tyr Met Asn
1 5 10
<210> 392
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 392
Gly Tyr Gly Met His
1 5
<210> 393
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 393
Arg Ala Ser Gln Ser Val Ser Ser Tyr Leu Ala
1 5 10
<210> 394
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 394
Ser Tyr Ala Met Asn
1 5
<210> 395
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 395
Gly Ser Ser Thr Gly Ala Val Thr Ser Gly Asn Tyr Pro Asn
1 5 10
<210> 396
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 396
Lys Tyr Ala Met Asn
1 5
<210> 397
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 397
Gly Ser Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr Ala Asn
1 5 10
<210> 398
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 398
Gly Tyr Thr Met Asn
1 5
<210> 399
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 399
Arg Ala Ser Gln Asp Ile Arg Asn Tyr Leu Asn
1 5 10
<210> 400
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 400
Thr Tyr Ala Met Ser
1 5
<210> 401
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 401
Thr Tyr Ala Met His
1 5
<210> 402
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 402
Gly Ser Ser Thr Gly Ala Val Thr Ser Ser Asn Tyr Ala Asn
1 5 10
<210> 403
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 403
Gly Ser Ser Thr Gly Ala Val Thr Ser Gly His Tyr Ala Asn
1 5 10
<210> 404
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 404
Lys Ser Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr Ala Asn
1 5 10
<210> 405
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 405
Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn Tyr Asn Gln Lys Phe Lys
1 5 10 15
Asp
<210> 406
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 406
Asp Thr Ser Lys Leu Ala Ser
1 5
<210> 407
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 407
Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser
1 5 10 15
Val Lys Asp
<210> 408
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 408
Gly Thr Asn Lys Arg Ala Pro
1 5
<210> 409
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 409
Tyr Ile Asn Pro Ser Ser Gly Tyr Thr Lys Tyr Asn Gln Lys Phe Lys
1 5 10 15
Asp
<210> 410
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 410
Ala Thr Ser Asn Leu Ala Ser
1 5
<210> 411
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 411
Asp Thr Ser Lys Val Ala Ser
1 5
<210> 412
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 412
Tyr Ile Asn Pro Ser Arg Gly Tyr Thr Asn Tyr Asn Gln Lys Val Lys
1 5 10 15
Asp
<210> 413
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 413
Val Ile Trp Tyr Asp Gly Ser Lys Lys Tyr Tyr Val Asp Ser Val Lys
1 5 10 15
Gly
<210> 414
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 414
Asp Ala Ser Asn Arg Ala Thr
1 5
<210> 415
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 415
Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
1 5 10 15
<210> 416
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 416
Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser
1 5 10 15
Val Lys Gly
<210> 417
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 417
Gly Thr Lys Phe Leu Ala Pro
1 5
<210> 418
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 418
Leu Ile Asn Pro Tyr Lys Gly Val Ser Thr Tyr Asn Gln Lys Phe Lys
1 5 10 15
Asp
<210> 419
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 419
Tyr Thr Ser Arg Leu His
1 5
<210> 420
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 420
Arg Ile Arg Ser Lys Ala Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser
1 5 10 15
Val Lys Gly
<210> 421
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 421
Arg Ile Arg Ser Lys Ala Asn Asn Tyr Tyr Ala Thr Tyr Tyr Ala Asp
1 5 10 15
Ser Val Lys Gly
20
<210> 422
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 422
Arg Ile Arg Ser Lys Ala Asn Ser Tyr Ala Thr Tyr Tyr Ala Asp Ser
1 5 10 15
Val Lys Gly
<210> 423
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 423
Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Ala Tyr Ala Asp Ser
1 5 10 15
Val Lys Gly
<210> 424
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 424
Asp Thr Asn Lys Arg Ala Pro
1 5
<210> 425
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 425
Gly Thr Asn Asn Arg Ala Pro
1 5
<210> 426
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 426
Gly Thr Asn Lys Arg Ala Ser
1 5
<210> 427
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 427
Gly Thr Ser Asn Lys His Ser
1 5
<210> 428
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 428
Arg Ile Arg Ser Asn Gly Gly Tyr Ser Thr Tyr Tyr Ala Asp Ser Val
1 5 10 15
Lys Gly
<210> 429
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 429
Tyr Tyr Asp Asp His Tyr Cys Leu Asp Tyr
1 5 10
<210> 430
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 430
Gln Gln Trp Ser Ser Asn Pro Phe Thr
1 5
<210> 431
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 431
His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala Tyr
1 5 10
<210> 432
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 432
Ala Leu Trp Tyr Ser Asn Leu Trp Val
1 5
<210> 433
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 433
Trp Gln Asp Tyr Asp Val Tyr Phe Asp Tyr
1 5 10
<210> 434
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 434
Gln Gln Trp Ser Ser Asn Pro Pro Thr
1 5
<210> 435
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 435
Gln Gln Trp Ser Ser Asn Pro Leu Thr
1 5
<210> 436
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 436
Gln Met Gly Tyr Trp His Phe Asp Leu
1 5
<210> 437
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 437
Gln Gln Arg Ser Asn Trp Pro Pro Leu Thr
1 5 10
<210> 438
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 438
Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala Tyr
1 5 10 15
<210> 439
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 439
His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Trp Ala Tyr
1 5 10
<210> 440
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 440
Val Leu Trp Tyr Ser Asn Arg Trp Val
1 5
<210> 441
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 441
His Gly Asn Phe Gly Asn Ser Tyr Ile Ser Tyr Trp Ala Tyr
1 5 10
<210> 442
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 442
His Gly Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe Ala Tyr
1 5 10
<210> 443
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 443
Ala Leu Trp Tyr Ser Asn His Trp Val
1 5
<210> 444
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 444
Tyr Tyr Asp Asp His Tyr Ser Leu Asp Tyr
1 5 10
<210> 445
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 445
Ser Gly Tyr Tyr Gly Asp Ser Asp Trp Tyr Phe Asp Val
1 5 10
<210> 446
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 446
Gln Gln Gly Asn Thr Leu Pro Trp Thr
1 5
<210> 447
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 447
His Gly Asn Phe Gly Asp Glu Tyr Val Ser Trp Phe Ala Tyr
1 5 10
<210> 448
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 448
His Gly Asn Phe Gly Asp Pro Tyr Val Ser Trp Phe Ala Tyr
1 5 10
<210> 449
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 449
His Gly Asn Phe Gly Asp Ser Tyr Val Ser Trp Phe Asp Tyr
1 5 10
<210> 450
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 450
His Gly Asn Phe Gly Gln Ser Tyr Val Ser Trp Phe Ala Tyr
1 5 10
<210> 451
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 451
His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Asp Tyr
1 5 10
<210> 452
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 452
Leu Leu Trp Tyr Ser Asn Leu Trp Val
1 5
<210> 453
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 453
His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala His
1 5 10
<210> 454
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 454
Gly Tyr Thr Phe Thr Arg Tyr
1 5
<210> 455
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 455
Ser Ser Ser Val Ser Tyr
1 5
<210> 456
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 456
Gly Phe Thr Phe Asn Thr Tyr
1 5
<210> 457
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 457
Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr
1 5 10
<210> 458
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 458
Gly Tyr Thr Phe Thr Ser Tyr
1 5
<210> 459
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 459
Gly Phe Lys Phe Ser Gly Tyr
1 5
<210> 460
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 460
Ser Gln Ser Val Ser Ser Tyr
1 5
<210> 461
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 461
Gly Phe Thr Phe Ser Thr Tyr
1 5
<210> 462
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 462
Gly Phe Thr Phe Asn Ser Tyr
1 5
<210> 463
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 463
Ser Thr Gly Ala Val Thr Ser Gly Asn Tyr
1 5 10
<210> 464
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 464
Gly Phe Thr Phe Asn Lys Tyr
1 5
<210> 465
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 465
Gly Tyr Ser Phe Thr Gly Tyr
1 5
<210> 466
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 466
Ser Gln Asp Ile Arg Asn Tyr
1 5
<210> 467
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 467
Asn Pro Ser Arg Gly Tyr
1 5
<210> 468
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 468
Asp Thr Ser
1
<210> 469
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 469
Arg Ser Lys Tyr Asn Asn Tyr Ala
1 5
<210> 470
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 470
Gly Thr Asn
1
<210> 471
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 471
Asn Pro Ser Ser Gly Tyr
1 5
<210> 472
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 472
Ala Thr Ser
1
<210> 473
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 473
Trp Tyr Asp Gly Ser Lys
1 5
<210> 474
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 474
Asp Ala Ser
1
<210> 475
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 475
Arg Ser Lys Tyr Asn Asn Tyr Ala Thr
1 5
<210> 476
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 476
Gly Thr Lys
1
<210> 477
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 477
Asn Pro Tyr Lys Gly Val
1 5
<210> 478
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 478
Tyr Thr Ser
1
<210> 479
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 479
Trp Ser Ser Asn Pro Phe
1 5
<210> 480
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 480
Trp Tyr Ser Asn Leu Trp
1 5
<210> 481
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 481
Trp Ser Ser Asn Pro Pro
1 5
<210> 482
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 482
Trp Ser Ser Asn Pro Leu
1 5
<210> 483
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 483
Arg Ser Asn Trp Pro Pro Leu
1 5
<210> 484
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 484
His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala
1 5 10
<210> 485
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 485
Trp Tyr Ser Asn Arg Trp
1 5
<210> 486
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 486
Trp Tyr Ser Asn His Trp
1 5
<210> 487
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 487
Gly Asn Thr Leu Pro Trp
1 5
<210> 488
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 488
Gly Tyr Thr Phe Thr Arg Tyr Thr Met His
1 5 10
<210> 489
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 489
Gly Phe Thr Phe Asn Thr Tyr Ala Met Asn
1 5 10
<210> 490
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 490
Gly Tyr Thr Phe Thr Ser Tyr Thr Met His
1 5 10
<210> 491
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 491
Gly Phe Lys Phe Ser Gly Tyr Gly Met His
1 5 10
<210> 492
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 492
Gly Phe Thr Phe Ser Thr Tyr Ala Met Asn
1 5 10
<210> 493
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 493
Gly Phe Thr Phe Asn Ser Tyr Ala Met Asn
1 5 10
<210> 494
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 494
Gly Phe Thr Phe Asn Lys Tyr Ala Met Asn
1 5 10
<210> 495
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 495
Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn
1 5 10
<210> 496
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 496
Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser
1 5 10 15
Val Lys
<210> 497
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 497
Tyr Thr Ser Arg Leu His Ser
1 5
<210> 498
<211> 152
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 498
Met Gln Ile Phe Val Lys Thr Leu Thr Gly Lys Thr Ile Thr Leu Glu
1 5 10 15
Val Glu Pro Ser Asp Thr Ile Glu Asn Val Lys Ala Lys Ile Gln Asp
20 25 30
Lys Glu Gly Ile Pro Pro Asp Gln Gln Trp Leu Trp Phe Ala Gly Lys
35 40 45
Gln Leu Glu Asp Gly Arg Thr Leu Ser Asp Tyr Asn Ile Gln Lys Glu
50 55 60
Ser Thr Leu Lys Leu Trp Leu Val Asp Lys Ala Ala Met Gln Ile Phe
65 70 75 80
Val Tyr Thr Arg Thr Gly Lys Thr Ile Thr Leu Glu Val Glu Pro Ser
85 90 95
Asp Thr Ile Glu Asn Val Lys Ala Lys Ile Gln Asp Lys Glu Gly Ile
100 105 110
Pro Pro Asp Gln Gln Arg Leu Ile Trp Ala Gly Lys Gln Leu Glu Asp
115 120 125
Gly Arg Thr Leu Ser Asp Tyr Asn Ile Ala Leu Glu Ser Gly Leu His
130 135 140
Leu Val Leu Arg Leu Arg Ala Ala
145 150
<210> 499
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 499
Lys Ala Ser Gly Tyr Lys Phe Thr Ser Tyr Val Met His
1 5 10
<210> 500
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 500
Tyr Ile Asn Pro Tyr Asn Asp Val Thr Lys Tyr Asn Glu Lys Phe Lys
1 5 10 15
<210> 501
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 501
Gly Ser Tyr Tyr Asp Tyr Asp Gly Phe Val Tyr
1 5 10
<210> 502
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 502
Ser Ala Thr Ser Ser Val Ser Tyr Met His
1 5 10
<210> 503
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 503
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Ser Tyr
20 25 30
Val Met His Trp Val Lys Gln Lys Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Tyr Asn Asp Val Thr Lys Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val His Tyr Cys
85 90 95
Ala Arg Gly Ser Tyr Tyr Asp Tyr Asp Gly Phe Val Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala
115 120
<210> 504
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 504
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Thr Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 505
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 505
Glu Tyr Tyr Met Tyr
1 5
<210> 506
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 506
Arg Ile Asp Pro Glu Asp Gly Ser Ile Asp Tyr Val Glu Lys Phe Lys
1 5 10 15
Lys
<210> 507
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 507
Gly Lys Phe Asn Tyr Arg Phe Ala Tyr
1 5
<210> 508
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 508
Arg Ser Ser Gln Ser Leu Leu His Ser Ser Gly Asn Thr Tyr Leu Asn
1 5 10 15
<210> 509
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 509
Leu Val Ser Lys Leu Glu Ser
1 5
<210> 510
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 510
Gln Phe Thr His Tyr Pro Tyr Thr
1 5
<210> 511
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 511
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Gln Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Glu Tyr
20 25 30
Tyr Met Tyr Trp Val Lys Gln Arg Pro Lys Gln Gly Leu Glu Leu Val
35 40 45
Gly Arg Ile Asp Pro Glu Asp Gly Ser Ile Asp Tyr Val Glu Lys Phe
50 55 60
Lys Lys Lys Ala Thr Leu Thr Ala Asp Thr Ser Ser Asn Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Thr Tyr Phe Cys
85 90 95
Ala Arg Gly Lys Phe Asn Tyr Arg Phe Ala Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 512
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 512
Asp Val Val Leu Thr Gln Thr Pro Pro Thr Leu Leu Ala Thr Ile Gly
1 5 10 15
Gln Ser Val Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Ser Gly Asn Thr Tyr Leu Asn Trp Leu Leu Gln Arg Thr Gly Gln Ser
35 40 45
Pro Gln Pro Leu Ile Tyr Leu Val Ser Lys Leu Glu Ser Gly Val Pro
50 55 60
Asn Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Gly Val Glu Ala Glu Asp Leu Gly Val Tyr Tyr Cys Met Gln Phe
85 90 95
Thr His Tyr Pro Tyr Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105 110
<210> 513
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 513
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Glu Tyr
20 25 30
Tyr Met Tyr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Leu Met
35 40 45
Gly Arg Ile Asp Pro Glu Asp Gly Ser Ile Asp Tyr Val Glu Lys Phe
50 55 60
Lys Lys Lys Val Thr Leu Thr Ala Asp Thr Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Lys Phe Asn Tyr Arg Phe Ala Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 514
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 514
Asp Val Val Met Thr Gln Ser Pro Pro Ser Leu Leu Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Ser Gly Asn Thr Tyr Leu Asn Trp Leu Leu Gln Arg Pro Gly Gln Ser
35 40 45
Pro Gln Pro Leu Ile Tyr Leu Val Ser Lys Leu Glu Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Gly Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Phe
85 90 95
Thr His Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 515
<211> 250
<212> БЕЛОК
<213> Homo sapiens
<400> 515
Met Val Ala Gly Ser Asp Ala Gly Arg Ala Leu Gly Val Leu Ser Val
1 5 10 15
Val Cys Leu Leu His Cys Phe Gly Phe Ile Ser Cys Phe Ser Gln Gln
20 25 30
Ile Tyr Gly Val Val Tyr Gly Asn Val Thr Phe His Val Pro Ser Asn
35 40 45
Val Pro Leu Lys Glu Val Leu Trp Lys Lys Gln Lys Asp Lys Val Ala
50 55 60
Glu Leu Glu Asn Ser Glu Phe Arg Ala Phe Ser Ser Phe Lys Asn Arg
65 70 75 80
Val Tyr Leu Asp Thr Val Ser Gly Ser Leu Thr Ile Tyr Asn Leu Thr
85 90 95
Ser Ser Asp Glu Asp Glu Tyr Glu Met Glu Ser Pro Asn Ile Thr Asp
100 105 110
Thr Met Lys Phe Phe Leu Tyr Val Leu Glu Ser Leu Pro Ser Pro Thr
115 120 125
Leu Thr Cys Ala Leu Thr Asn Gly Ser Ile Glu Val Gln Cys Met Ile
130 135 140
Pro Glu His Tyr Asn Ser His Arg Gly Leu Ile Met Tyr Ser Trp Asp
145 150 155 160
Cys Pro Met Glu Gln Cys Lys Arg Asn Ser Thr Ser Ile Tyr Phe Lys
165 170 175
Met Glu Asn Asp Leu Pro Gln Lys Ile Gln Cys Thr Leu Ser Asn Pro
180 185 190
Leu Phe Asn Thr Thr Ser Ser Ile Ile Leu Thr Thr Cys Ile Pro Ser
195 200 205
Ser Gly His Ser Arg His Arg Tyr Ala Leu Ile Pro Ile Pro Leu Ala
210 215 220
Val Ile Thr Thr Cys Ile Val Leu Tyr Met Asn Gly Ile Leu Lys Cys
225 230 235 240
Asp Arg Lys Pro Asp Arg Thr Asn Ser Asn
245 250
<210> 516
<211> 237
<212> БЕЛОК
<213> Homo sapiens
<400> 516
Met Val Ala Gly Ser Asp Ala Gly Arg Ala Leu Gly Val Leu Ser Val
1 5 10 15
Val Cys Leu Leu His Cys Phe Gly Phe Ile Ser Cys Phe Ser Gln Gln
20 25 30
Ile Tyr Gly Val Val Tyr Gly Asn Val Thr Phe His Val Pro Ser Asn
35 40 45
Val Pro Leu Lys Glu Val Leu Trp Lys Lys Gln Lys Asp Lys Val Ala
50 55 60
Glu Leu Glu Asn Ser Glu Phe Arg Ala Phe Ser Ser Phe Lys Asn Arg
65 70 75 80
Val Tyr Leu Asp Thr Val Ser Gly Ser Leu Thr Ile Tyr Asn Leu Thr
85 90 95
Ser Ser Asp Glu Asp Glu Tyr Glu Met Glu Ser Pro Asn Ile Thr Asp
100 105 110
Thr Met Lys Phe Phe Leu Tyr Val Leu Glu Ser Leu Pro Ser Pro Thr
115 120 125
Leu Thr Cys Ala Leu Thr Asn Gly Ser Ile Glu Val Gln Cys Met Ile
130 135 140
Pro Glu His Tyr Asn Ser His Arg Gly Leu Ile Met Tyr Ser Trp Asp
145 150 155 160
Cys Pro Met Glu Gln Cys Lys Arg Asn Ser Thr Ser Ile Tyr Phe Lys
165 170 175
Met Glu Asn Asp Leu Pro Gln Lys Ile Gln Cys Thr Leu Ser Asn Pro
180 185 190
Leu Phe Asn Thr Thr Ser Ser Ile Ile Leu Thr Thr Cys Ile Pro Ser
195 200 205
Ser Gly His Ser Arg His Arg Tyr Ala Leu Ile Pro Ile Pro Leu Ala
210 215 220
Val Ile Thr Thr Cys Ile Val Leu Tyr Met Asn Val Leu
225 230 235
<210> 517
<211> 248
<212> БЕЛОК
<213> Homo sapiens
<400> 517
Met Val Ala Gly Ser Asp Ala Gly Arg Ala Leu Gly Val Leu Ser Val
1 5 10 15
Val Cys Leu Leu His Cys Phe Gly Phe Ile Ser Cys Phe Ser Gln Gln
20 25 30
Ile Tyr Gly Val Val Tyr Gly Asn Val Thr Phe His Val Pro Ser Asn
35 40 45
Val Pro Leu Lys Glu Val Leu Trp Lys Lys Gln Lys Asp Lys Val Ala
50 55 60
Glu Leu Glu Asn Ser Glu Phe Arg Ala Phe Ser Ser Phe Lys Asn Arg
65 70 75 80
Val Tyr Leu Asp Thr Val Ser Gly Ser Leu Thr Ile Tyr Asn Leu Thr
85 90 95
Ser Ser Asp Glu Asp Glu Tyr Glu Met Glu Ser Pro Asn Ile Thr Asp
100 105 110
Thr Met Lys Phe Phe Leu Tyr Val Leu Glu Ser Leu Pro Ser Pro Thr
115 120 125
Leu Thr Cys Ala Leu Thr Asn Gly Ser Ile Glu Val Gln Cys Met Ile
130 135 140
Pro Glu His Tyr Asn Ser His Arg Gly Leu Ile Met Tyr Ser Trp Asp
145 150 155 160
Cys Pro Met Glu Gln Cys Lys Arg Asn Ser Thr Ser Ile Tyr Phe Lys
165 170 175
Met Glu Asn Asp Leu Pro Gln Lys Ile Gln Cys Thr Leu Ser Asn Pro
180 185 190
Leu Phe Asn Thr Thr Ser Ser Ile Ile Leu Thr Thr Cys Ile Pro Ser
195 200 205
Ser Gly His Ser Arg His Arg Tyr Ala Leu Ile Pro Ile Pro Leu Ala
210 215 220
Val Ile Thr Thr Cys Ile Val Leu Tyr Met Asn Gly Ile Leu Lys Cys
225 230 235 240
Asp Arg Lys Pro Asp Arg Thr Lys
245
<210> 518
<211> 187
<212> БЕЛОК
<213> Homo sapiens
<400> 518
Phe Ser Gln Gln Ile Tyr Gly Val Val Tyr Gly Asn Val Thr Phe His
1 5 10 15
Val Pro Ser Asn Val Pro Leu Lys Glu Val Leu Trp Lys Lys Gln Lys
20 25 30
Asp Lys Val Ala Glu Leu Glu Asn Ser Glu Phe Arg Ala Phe Ser Ser
35 40 45
Phe Lys Asn Arg Val Tyr Leu Asp Thr Val Ser Gly Ser Leu Thr Ile
50 55 60
Tyr Asn Leu Thr Ser Ser Asp Glu Asp Glu Tyr Glu Met Glu Ser Pro
65 70 75 80
Asn Ile Thr Asp Thr Met Lys Phe Phe Leu Tyr Val Leu Glu Ser Leu
85 90 95
Pro Ser Pro Thr Leu Thr Cys Ala Leu Thr Asn Gly Ser Ile Glu Val
100 105 110
Gln Cys Met Ile Pro Glu His Tyr Asn Ser His Arg Gly Leu Ile Met
115 120 125
Tyr Ser Trp Asp Cys Pro Met Glu Gln Cys Lys Arg Asn Ser Thr Ser
130 135 140
Ile Tyr Phe Lys Met Glu Asn Asp Leu Pro Gln Lys Ile Gln Cys Thr
145 150 155 160
Leu Ser Asn Pro Leu Phe Asn Thr Thr Ser Ser Ile Ile Leu Thr Thr
165 170 175
Cys Ile Pro Ser Ser Gly His Ser Arg His Arg
180 185
<210> 519
<211> 187
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена="Ser"
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> /замена="Lys"
<220>
<221> ВАРИАНТ
<222> (21)..(21)
<223> /замена="Gln"
<220>
<221> ВАРИАНТ
<222> (58)..(58)
<223> /замена="Lys"
<220>
<221> ВАРИАНТ
<222> (85)..(85)
<223> /замена="Ser"
<220>
<221> ВАРИАНТ
<222> (93)..(93)
<223> /замена="Gly"
<220>
<221> Сайт
<222> (1)..(187)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 519
Phe Ser Gln Gln Ile Tyr Gly Val Val Tyr Gly Asn Val Thr Phe His
1 5 10 15
Val Pro Ser Asn Val Pro Leu Lys Glu Val Leu Trp Lys Lys Gln Lys
20 25 30
Asp Lys Val Ala Glu Leu Glu Asn Ser Glu Phe Arg Ala Phe Ser Ser
35 40 45
Phe Lys Asn Arg Val Tyr Leu Asp Thr Val Ser Gly Ser Leu Thr Ile
50 55 60
Tyr Asn Leu Thr Ser Ser Asp Glu Asp Glu Tyr Glu Met Glu Ser Pro
65 70 75 80
Asn Ile Thr Asp Thr Met Lys Phe Phe Leu Tyr Val Leu Glu Ser Leu
85 90 95
Pro Ser Pro Thr Leu Thr Cys Ala Leu Thr Asn Gly Ser Ile Glu Val
100 105 110
Gln Cys Met Ile Pro Glu His Tyr Asn Ser His Arg Gly Leu Ile Met
115 120 125
Tyr Ser Trp Asp Cys Pro Met Glu Gln Cys Lys Arg Asn Ser Thr Ser
130 135 140
Ile Tyr Phe Lys Met Glu Asn Asp Leu Pro Gln Lys Ile Gln Cys Thr
145 150 155 160
Leu Ser Asn Pro Leu Phe Asn Thr Thr Ser Ser Ile Ile Leu Thr Thr
165 170 175
Cys Ile Pro Ser Ser Gly His Ser Arg His Arg
180 185
<210> 520
<211> 94
<212> БЕЛОК
<213> Homo sapiens
<400> 520
Ser Gln Gln Ile Tyr Gly Val Val Tyr Gly Asn Val Thr Phe His Val
1 5 10 15
Pro Ser Asn Val Pro Leu Lys Glu Val Leu Trp Lys Lys Gln Lys Asp
20 25 30
Lys Val Ala Glu Leu Glu Asn Ser Glu Phe Arg Ala Phe Ser Ser Phe
35 40 45
Lys Asn Arg Val Tyr Leu Asp Thr Val Ser Gly Ser Leu Thr Ile Tyr
50 55 60
Asn Leu Thr Ser Ser Asp Glu Asp Glu Tyr Glu Met Glu Ser Pro Asn
65 70 75 80
Ile Thr Asp Thr Met Lys Phe Phe Leu Tyr Val Leu Glu Ser
85 90
<210> 521
<211> 94
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="Lys"
<220>
<221> ВАРИАНТ
<222> (20)..(20)
<223> /замена="Gln"
<220>
<221> Сайт
<222> (1)..(94)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 521
Ser Gln Gln Ile Tyr Gly Val Val Tyr Gly Asn Val Thr Phe His Val
1 5 10 15
Pro Ser Asn Val Pro Leu Lys Glu Val Leu Trp Lys Lys Gln Lys Asp
20 25 30
Lys Val Ala Glu Leu Glu Asn Ser Glu Phe Arg Ala Phe Ser Ser Phe
35 40 45
Lys Asn Arg Val Tyr Leu Asp Thr Val Ser Gly Ser Leu Thr Ile Tyr
50 55 60
Asn Leu Thr Ser Ser Asp Glu Asp Glu Tyr Glu Met Glu Ser Pro Asn
65 70 75 80
Ile Thr Asp Thr Met Lys Phe Phe Leu Tyr Val Leu Glu Ser
85 90
<210> 522
<211> 94
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 522
Ser Gln Gln Ile Tyr Gly Val Val Tyr Gly Asn Val Thr Phe His Cys
1 5 10 15
Pro Ser Asn Val Pro Leu Lys Glu Val Leu Trp Lys Lys Gln Lys Asp
20 25 30
Lys Val Ala Glu Leu Glu Asn Ser Glu Phe Arg Ala Phe Ser Ser Phe
35 40 45
Lys Asn Arg Val Tyr Leu Asp Thr Val Ser Gly Ser Leu Thr Ile Tyr
50 55 60
Asn Leu Thr Ser Ser Asp Glu Asp Glu Tyr Glu Cys Glu Ser Pro Asn
65 70 75 80
Ile Thr Asp Thr Met Lys Phe Phe Leu Tyr Val Leu Glu Ser
85 90
<210> 523
<211> 94
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 523
Ser Gln Gln Ile Tyr Gly Val Val Tyr Gly Asn Val Thr Phe His Val
1 5 10 15
Pro Ser Asn Val Pro Leu Lys Glu Cys Leu Trp Lys Lys Gln Lys Asp
20 25 30
Lys Val Ala Glu Leu Glu Asn Ser Glu Phe Arg Ala Phe Ser Ser Phe
35 40 45
Lys Asn Arg Val Tyr Leu Asp Thr Val Ser Cys Ser Leu Thr Ile Tyr
50 55 60
Asn Leu Thr Ser Ser Asp Glu Asp Glu Tyr Glu Met Glu Ser Pro Asn
65 70 75 80
Ile Thr Asp Thr Met Lys Phe Phe Leu Tyr Val Leu Glu Ser
85 90
<210> 524
<211> 94
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 524
Ser Gln Gln Ile Tyr Gly Val Val Tyr Gly Asn Val Thr Phe His Cys
1 5 10 15
Pro Ser Asn Val Pro Leu Lys Glu Val Leu Trp Lys Lys Gln Lys Asp
20 25 30
Lys Val Ala Glu Leu Glu Asn Ser Glu Phe Arg Ala Phe Ser Ser Phe
35 40 45
Lys Asn Arg Val Tyr Leu Asp Thr Val Ser Gly Ser Leu Thr Ile Tyr
50 55 60
Asn Leu Thr Ser Ser Asp Glu Asp Glu Tyr Glu Met Glu Ser Pro Asn
65 70 75 80
Ile Thr Asp Thr Cys Lys Phe Phe Leu Tyr Val Leu Glu Ser
85 90
<210> 525
<211> 94
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 525
Ser Gln Gln Ile Tyr Gly Val Val Tyr Gly Asn Val Thr Phe His Val
1 5 10 15
Pro Ser Asn Val Pro Leu Lys Glu Val Leu Cys Lys Lys Gln Lys Asp
20 25 30
Lys Val Ala Glu Leu Glu Asn Ser Glu Phe Arg Ala Phe Ser Ser Phe
35 40 45
Lys Asn Arg Val Tyr Leu Asp Thr Val Ser Gly Ser Cys Thr Ile Tyr
50 55 60
Asn Leu Thr Ser Ser Asp Glu Asp Glu Tyr Glu Met Glu Ser Pro Asn
65 70 75 80
Ile Thr Asp Thr Met Lys Phe Phe Leu Tyr Val Leu Glu Ser
85 90
<210> 526
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 526
Asp Tyr Gly Val Ser
1 5
<210> 527
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 527
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser
1 5 10 15
<210> 528
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 528
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser
1 5 10 15
<210> 529
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 529
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser
1 5 10 15
<210> 530
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 530
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ser Leu Lys Ser
1 5 10 15
<210> 531
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 531
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr
1 5 10
<210> 532
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 532
Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn
1 5 10
<210> 533
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 533
His Thr Ser Arg Leu His Ser
1 5
<210> 534
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 534
Gln Gln Gly Asn Thr Leu Pro Tyr Thr
1 5
<210> 535
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 535
Glu Val Lys Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys
50 55 60
Ser Arg Leu Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 536
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 536
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 537
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 537
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 538
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 538
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 539
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 539
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr
100 105
<210> 540
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 540
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 541
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 541
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
115 120 125
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
130 135 140
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
145 150 155 160
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser
165 170 175
Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser
180 185 190
Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr
195 200 205
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
210 215 220
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
225 230 235 240
Ser Ser
<210> 542
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 542
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
115 120 125
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
130 135 140
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
145 150 155 160
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser
165 170 175
Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser Arg Val Thr Ile Ser
180 185 190
Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr
195 200 205
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
210 215 220
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
225 230 235 240
Ser Ser
<210> 543
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 543
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met Thr Gln Ser Pro Ala
130 135 140
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
145 150 155 160
Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly
180 185 190
Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu
195 200 205
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln
210 215 220
Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu
225 230 235 240
Ile Lys
<210> 544
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 544
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met Thr Gln Ser Pro Ala
130 135 140
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
145 150 155 160
Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly
180 185 190
Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu
195 200 205
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln
210 215 220
Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu
225 230 235 240
Ile Lys
<210> 545
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 545
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
115 120 125
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
130 135 140
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
145 150 155 160
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
165 170 175
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser
180 185 190
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
195 200 205
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
210 215 220
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser
245
<210> 546
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 546
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
115 120 125
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
130 135 140
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
145 150 155 160
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
165 170 175
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser
180 185 190
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
195 200 205
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
210 215 220
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser
245
<210> 547
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 547
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met
130 135 140
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
145 150 155 160
Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr
165 170 175
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser
180 185 190
Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
210 215 220
Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln
225 230 235 240
Gly Thr Lys Leu Glu Ile Lys
245
<210> 548
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 548
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met
130 135 140
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
145 150 155 160
Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr
165 170 175
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser
180 185 190
Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
210 215 220
Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln
225 230 235 240
Gly Thr Lys Leu Glu Ile Lys
245
<210> 549
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 549
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
115 120 125
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
130 135 140
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
145 150 155 160
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
165 170 175
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ser Leu Lys Ser
180 185 190
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
195 200 205
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
210 215 220
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser
245
<210> 550
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 550
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met
130 135 140
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
145 150 155 160
Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr
165 170 175
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser
180 185 190
Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
210 215 220
Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln
225 230 235 240
Gly Thr Lys Leu Glu Ile Lys
245
<210> 551
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 551
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
115 120 125
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
130 135 140
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
145 150 155 160
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser
165 170 175
Glu Thr Thr Tyr Tyr Asn Ser Ser Leu Lys Ser Arg Val Thr Ile Ser
180 185 190
Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr
195 200 205
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
210 215 220
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
225 230 235 240
Ser Ser
<210> 552
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 552
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met Thr Gln Ser Pro Ala
130 135 140
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
145 150 155 160
Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly
180 185 190
Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu
195 200 205
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln
210 215 220
Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu
225 230 235 240
Ile Lys
<210> 553
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 553
Gly Phe Leu Gly
1
<210> 554
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 554
Ala Leu Ala Leu
1
<210> 555
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 555
Arg Gly Asp Ser
1
<210> 556
<211> 487
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 556
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
195 200 205
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys
210 215 220
Ser Cys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu
225 230 235 240
Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala Ser Val Lys Met
245 250 255
Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Ser Tyr Val Met His Trp
260 265 270
Val Lys Gln Lys Pro Gly Gln Gly Leu Glu Trp Ile Gly Tyr Ile Asn
275 280 285
Pro Tyr Asn Asp Val Thr Lys Tyr Asn Glu Lys Phe Lys Gly Lys Ala
290 295 300
Thr Leu Thr Ser Asp Lys Ser Ser Ser Thr Ala Tyr Met Glu Leu Ser
305 310 315 320
Ser Leu Thr Ser Glu Asp Ser Ala Val His Tyr Cys Ala Arg Gly Ser
325 330 335
Tyr Tyr Asp Tyr Asp Gly Phe Val Tyr Trp Gly Gln Gly Thr Leu Val
340 345 350
Thr Val Ser Ala Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
355 360 365
Gly Gly Ser Gly Gly Gly Gly Ser Gln Ile Val Leu Thr Gln Ser Pro
370 375 380
Ala Ile Met Ser Ala Ser Pro Gly Glu Lys Val Thr Met Thr Cys Ser
385 390 395 400
Ala Thr Ser Ser Val Ser Tyr Met His Trp Tyr Gln Gln Lys Ser Gly
405 410 415
Thr Ser Pro Lys Arg Trp Ile Tyr Asp Thr Ser Lys Leu Ala Ser Gly
420 425 430
Val Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Ser Tyr Ser Leu
435 440 445
Thr Ile Ser Ser Met Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln
450 455 460
Gln Trp Ser Ser Asn Pro Leu Thr Phe Gly Ala Gly Thr Lys Leu Glu
465 470 475 480
Leu Lys Gly Gly Gly Gly Ser
485
<210> 557
<211> 217
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 557
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Gly Ser Pro Gly Gln
1 5 10 15
Ser Ile Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
20 25 30
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
35 40 45
Met Ile Tyr Asp Val Ser Asn Arg Leu Arg Gly Val Ser Asn Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Tyr Thr Ser Ser
85 90 95
Ser Ala Leu Tyr Val Phe Gly Ser Gly Thr Lys Val Thr Val Leu Gly
100 105 110
Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu
115 120 125
Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe
130 135 140
Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro Val
145 150 155 160
Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn Lys
165 170 175
Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser
180 185 190
His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu
195 200 205
Lys Thr Val Ala Pro Thr Glu Cys Ser
210 215
<210> 558
<211> 99
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 558
Ser Gln Gln Ile Tyr Gly Val Val Tyr Gly Asn Val Thr Phe His Val
1 5 10 15
Pro Ser Asn Val Pro Leu Lys Glu Val Leu Trp Lys Lys Gln Lys Asp
20 25 30
Lys Val Ala Glu Leu Glu Asn Ser Glu Phe Arg Ala Phe Ser Ser Phe
35 40 45
Lys Asn Arg Val Tyr Leu Asp Thr Val Ser Gly Ser Leu Thr Ile Tyr
50 55 60
Asn Leu Thr Ser Ser Asp Glu Asp Glu Tyr Glu Met Glu Ser Pro Asn
65 70 75 80
Ile Thr Asp Thr Met Lys Phe Phe Leu Tyr Val Leu Glu Ser Gly Gly
85 90 95
Gly Gly Ser
<210> 559
<211> 335
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 559
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
195 200 205
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys
210 215 220
Ser Cys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Gln Gln Ile
225 230 235 240
Tyr Gly Val Val Tyr Gly Asn Val Thr Phe His Val Pro Ser Asn Val
245 250 255
Pro Leu Lys Glu Val Leu Trp Lys Lys Gln Lys Asp Lys Val Ala Glu
260 265 270
Leu Glu Asn Ser Glu Phe Arg Ala Phe Ser Ser Phe Lys Asn Arg Val
275 280 285
Tyr Leu Asp Thr Val Ser Gly Ser Leu Thr Ile Tyr Asn Leu Thr Ser
290 295 300
Ser Asp Glu Asp Glu Tyr Glu Met Glu Ser Pro Asn Ile Thr Asp Thr
305 310 315 320
Met Lys Phe Phe Leu Tyr Val Leu Glu Ser Gly Gly Gly Gly Ser
325 330 335
<210> 560
<211> 251
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 560
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Ser Tyr
20 25 30
Val Met His Trp Val Lys Gln Lys Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Tyr Asn Asp Val Thr Lys Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val His Tyr Cys
85 90 95
Ala Arg Gly Ser Tyr Tyr Asp Tyr Asp Gly Phe Val Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ile Val Leu
130 135 140
Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly Glu Lys Val Thr
145 150 155 160
Met Thr Cys Ser Ala Thr Ser Ser Val Ser Tyr Met His Trp Tyr Gln
165 170 175
Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr Asp Thr Ser Lys
180 185 190
Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu Asp Ala Ala Thr
210 215 220
Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr Phe Gly Ala Gly
225 230 235 240
Thr Lys Leu Glu Leu Lys Gly Gly Gly Gly Ser
245 250
<210> 561
<211> 138
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 561
Asp Val Gln Leu Gln Ala Ser Gly Gly Gly Ser Val Gln Ala Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Ile Gly Pro Tyr
20 25 30
Cys Met Gly Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Gly Val
35 40 45
Ala Ala Ile Asn Met Gly Gly Gly Ile Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Gln Asp Asn Ala Lys Asn Thr Val Tyr
65 70 75 80
Leu Leu Met Asn Ser Leu Glu Pro Glu Asp Thr Ala Ile Tyr Tyr Cys
85 90 95
Ala Ala Asp Ser Thr Ile Tyr Ala Ser Tyr Tyr Glu Cys Gly His Gly
100 105 110
Leu Ser Thr Gly Gly Tyr Gly Tyr Asp Ser Trp Gly Gln Gly Thr Gln
115 120 125
Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135
<210> 562
<211> 495
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 562
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
195 200 205
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys
210 215 220
Ser Cys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu
225 230 235 240
Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Lys Leu
245 250 255
Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Thr Tyr Ala Met Asn Trp
260 265 270
Val Arg Gln Ala Ser Gly Lys Gly Leu Glu Trp Val Gly Arg Ile Arg
275 280 285
Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Asp
290 295 300
Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Thr Leu Tyr Leu Gln
305 310 315 320
Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr Tyr Cys Val Arg
325 330 335
His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala Tyr Trp Gly
340 345 350
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
355 360 365
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ala Val
370 375 380
Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly Thr Val Thr
385 390 395 400
Leu Thr Cys Arg Ser Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr Ala
405 410 415
Asn Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg Gly Leu Ile Gly
420 425 430
Gly Thr Asn Lys Arg Ala Pro Trp Thr Pro Ala Arg Phe Ser Gly Ser
435 440 445
Leu Leu Gly Asp Lys Ala Ala Leu Thr Leu Ser Gly Ala Gln Pro Glu
450 455 460
Asp Glu Ala Glu Tyr Phe Cys Ala Leu Trp Tyr Ser Asn Leu Trp Val
465 470 475 480
Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Gly Gly Gly Ser
485 490 495
<210> 563
<211> 259
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 563
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Ser Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Asp Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly
145 150 155 160
Gly Thr Val Thr Leu Thr Cys Arg Ser Ser Thr Gly Ala Val Thr Thr
165 170 175
Ser Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg
180 185 190
Gly Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Trp Thr Pro Ala Arg
195 200 205
Phe Ser Gly Ser Leu Leu Gly Asp Lys Ala Ala Leu Thr Leu Ser Gly
210 215 220
Ala Gln Pro Glu Asp Glu Ala Glu Tyr Phe Cys Ala Leu Trp Tyr Ser
225 230 235 240
Asn Leu Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Gly
245 250 255
Gly Gly Ser
<210> 564
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетическая 8xHis метка"
<400> 564
His His His His His His His His
1 5
<210> 565
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 565
Glu Val Asn Leu Tyr Phe Gln Ser
1 5
<210> 566
<211> 206
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 566
Ser Lys Glu Ile Thr Asn Ala Leu Glu Thr Trp Gly Ala Leu Gly Gln
1 5 10 15
Asp Ile Asn Leu Asp Ile Pro Ser Phe Gln Met Ser Asp Asp Ile Asp
20 25 30
Asp Ile Lys Trp Glu Lys Thr Ser Asp Lys Lys Lys Ile Ala Gln Phe
35 40 45
Arg Lys Glu Lys Glu Thr Phe Lys Glu Lys Asp Thr Tyr Lys Leu Phe
50 55 60
Lys Asn Gly Thr Leu Lys Ile Lys His Leu Lys Thr Asp Asp Gln Asp
65 70 75 80
Ile Tyr Lys Val Ser Ile Tyr Asp Thr Lys Gly Lys Asn Val Leu Glu
85 90 95
Lys Ile Phe Asp Leu Lys Ile Gln Glu Arg Val Ser Lys Pro Lys Ile
100 105 110
Ser Trp Thr Cys Ile Asn Thr Thr Leu Thr Cys Glu Val Met Asn Gly
115 120 125
Thr Asp Pro Glu Leu Asn Leu Tyr Gln Asp Gly Lys His Leu Lys Leu
130 135 140
Ser Gln Arg Val Ile Thr His Lys Trp Thr Thr Ser Leu Ser Ala Lys
145 150 155 160
Phe Lys Cys Thr Ala Gly Asn Lys Val Ser Lys Glu Ser Ser Val Glu
165 170 175
Pro Val Ser Cys Pro Glu Lys Gly Leu Asp Gly Gly Gly Gly Ser Gly
180 185 190
Leu Asn Asp Ile Phe Glu Ala Gln Lys Ile Glu Trp His Glu
195 200 205
<210> 567
<211> 206
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 567
Ser Lys Glu Ile Arg Asn Ala Leu Glu Thr Trp Gly Ala Leu Gly Gln
1 5 10 15
Asp Ile Asp Leu Asp Ile Pro Ser Phe Gln Met Ser Asp Asp Ile Asp
20 25 30
Asp Ile Arg Trp Glu Lys Thr Ser Asp Lys Lys Lys Ile Ala Gln Phe
35 40 45
Arg Lys Glu Lys Glu Thr Phe Glu Glu Lys Asp Ala Tyr Lys Leu Phe
50 55 60
Lys Asn Gly Thr Leu Lys Ile Lys His Leu Lys Ile His Asp Gln Asp
65 70 75 80
Ser Tyr Lys Val Ser Ile Tyr Asp Thr Lys Gly Lys Asn Val Leu Glu
85 90 95
Lys Thr Phe Asp Leu Lys Ile Gln Glu Arg Val Ser Glu Pro Lys Ile
100 105 110
Ser Trp Thr Cys Ile Asn Thr Thr Leu Thr Cys Glu Val Met Asn Gly
115 120 125
Thr Asp Pro Glu Leu Asn Leu Tyr Gln Asp Gly Lys His Val Lys Leu
130 135 140
Ser Gln Arg Val Ile Thr His Lys Trp Thr Thr Ser Leu Ser Ala Lys
145 150 155 160
Phe Lys Cys Thr Ala Gly Asn Lys Val Ser Lys Glu Ser Arg Met Glu
165 170 175
Thr Val Ser Cys Pro Glu Lys Gly Leu Asp Gly Gly Gly Gly Ser Gly
180 185 190
Leu Asn Asp Ile Phe Glu Ala Gln Lys Ile Glu Trp His Glu
195 200 205
<210> 568
<211> 199
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 568
Ser Gln Gln Ile Tyr Gly Val Val Tyr Gly Asn Val Thr Phe His Val
1 5 10 15
Pro Ser Asn Val Pro Leu Lys Glu Val Leu Trp Lys Lys Gln Lys Asp
20 25 30
Lys Val Ala Glu Leu Glu Asn Ser Glu Phe Arg Ala Phe Ser Ser Phe
35 40 45
Lys Asn Arg Val Tyr Leu Asp Thr Val Ser Gly Ser Leu Thr Ile Tyr
50 55 60
Asn Leu Thr Ser Ser Asp Glu Asp Glu Tyr Glu Met Glu Ser Pro Asn
65 70 75 80
Ile Thr Asp Thr Met Lys Phe Phe Leu Tyr Val Leu Glu Ser Leu Pro
85 90 95
Ser Pro Thr Leu Thr Cys Ala Leu Thr Asn Gly Ser Ile Glu Val Gln
100 105 110
Cys Met Ile Pro Glu His Tyr Asn Ser His Arg Gly Leu Ile Met Tyr
115 120 125
Ser Trp Asp Cys Pro Met Glu Gln Cys Lys Arg Asn Ser Thr Ser Ile
130 135 140
Tyr Phe Lys Met Glu Asn Asp Leu Pro Gln Lys Ile Gln Cys Thr Leu
145 150 155 160
Ser Asn Pro Leu Phe Asn Thr Thr Ser Ser Ile Ile Leu Thr Thr Cys
165 170 175
Ile Pro Ser Ser Gly His Ser Arg His Arg Gly Gly Gly Gly Ser His
180 185 190
His His His His His His His
195
<210> 569
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 569
Ser Gln Gln Ile Tyr Gly Val Val Tyr Gly Asn Val Thr Phe His Val
1 5 10 15
Pro Ser Asn Val Pro Leu Lys Glu Val Leu Trp Lys Lys Gln Lys Asp
20 25 30
Lys Val Ala Glu Leu Glu Asn Ser Glu Phe Arg Ala Phe Ser Ser Phe
35 40 45
Lys Asn Arg Val Tyr Leu Asp Thr Val Ser Gly Ser Leu Thr Ile Tyr
50 55 60
Asn Leu Thr Ser Ser Asp Glu Asp Glu Tyr Glu Met Glu Ser Pro Asn
65 70 75 80
Ile Thr Asp Thr Met Lys Phe Phe Leu Tyr Val Leu Glu Ser Gly Gly
85 90 95
Gly Gly Ser His His His His His His His His
100 105
<210> 570
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 570
Ser Gln Gln Ile Tyr Gly Val Val Tyr Gly Asn Val Thr Phe His Cys
1 5 10 15
Pro Ser Asn Val Pro Leu Lys Glu Val Leu Trp Lys Lys Gln Lys Asp
20 25 30
Lys Val Ala Glu Leu Glu Asn Ser Glu Phe Arg Ala Phe Ser Ser Phe
35 40 45
Lys Asn Arg Val Tyr Leu Asp Thr Val Ser Gly Ser Leu Thr Ile Tyr
50 55 60
Asn Leu Thr Ser Ser Asp Glu Asp Glu Tyr Glu Cys Glu Ser Pro Asn
65 70 75 80
Ile Thr Asp Thr Met Lys Phe Phe Leu Tyr Val Leu Glu Ser Gly Gly
85 90 95
Gly Gly Ser His His His His His His His His
100 105
<210> 571
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 571
Ser Gln Gln Ile Tyr Gly Val Val Tyr Gly Asn Val Thr Phe His Val
1 5 10 15
Pro Ser Asn Val Pro Leu Lys Glu Cys Leu Trp Lys Lys Gln Lys Asp
20 25 30
Lys Val Ala Glu Leu Glu Asn Ser Glu Phe Arg Ala Phe Ser Ser Phe
35 40 45
Lys Asn Arg Val Tyr Leu Asp Thr Val Ser Cys Ser Leu Thr Ile Tyr
50 55 60
Asn Leu Thr Ser Ser Asp Glu Asp Glu Tyr Glu Met Glu Ser Pro Asn
65 70 75 80
Ile Thr Asp Thr Met Lys Phe Phe Leu Tyr Val Leu Glu Ser Gly Gly
85 90 95
Gly Gly Ser His His His His His His His His
100 105
<210> 572
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 572
Ser Gln Gln Ile Tyr Gly Val Val Tyr Gly Asn Val Thr Phe His Cys
1 5 10 15
Pro Ser Asn Val Pro Leu Lys Glu Val Leu Trp Lys Lys Gln Lys Asp
20 25 30
Lys Val Ala Glu Leu Glu Asn Ser Glu Phe Arg Ala Phe Ser Ser Phe
35 40 45
Lys Asn Arg Val Tyr Leu Asp Thr Val Ser Gly Ser Leu Thr Ile Tyr
50 55 60
Asn Leu Thr Ser Ser Asp Glu Asp Glu Tyr Glu Met Glu Ser Pro Asn
65 70 75 80
Ile Thr Asp Thr Cys Lys Phe Phe Leu Tyr Val Leu Glu Ser Gly Gly
85 90 95
Gly Gly Ser His His His His His His His His
100 105
<210> 573
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Ala"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Arg"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Tyr" или "Gln"
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /замена="Ser"
<220>
<221> Сайт
<222> (1)..(10)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 573
Gly Phe Thr Phe Ser Lys Asn Gly Met His
1 5 10
<210> 574
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Ala"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Arg"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Tyr" или "Gln"
<220>
<221> Сайт
<222> (1)..(8)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 574
Gly Phe Thr Phe Ser Lys Asn Gly
1 5
<210> 575
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /замена="Tyr" или "Gln"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Ser"
<220>
<221> Сайт
<222> (1)..(5)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 575
Lys Asn Gly Met His
1 5
<210> 576
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Ala"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Arg"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Tyr" или "Gln"
<220>
<221> Сайт
<222> (1)..(7)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 576
Gly Phe Thr Phe Ser Lys Asn
1 5
<210> 577
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена="Leu"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="Arg"
<220>
<221> Сайт
<222> (1)..(17)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 577
Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val Lys
1 5 10 15
Gly
<210> 578
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Arg"
<220>
<221> Сайт
<222> (1)..(6)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 578
Tyr Tyr Asp Ser Ser Lys
1 5
<210> 579
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Arg"
<220>
<221> Сайт
<222> (1)..(8)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 579
Ile Tyr Tyr Asp Ser Ser Lys Met
1 5
<210> 580
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена="Tyr" или "Ser"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /замена="Tyr", или "Ser", или "Thr"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Tyr", или "Ser", или "Thr"
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> /замена="Tyr"
<220>
<221> Сайт
<222> (1)..(9)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 580
Phe Trp Trp Asp Leu Asp Phe Asp His
1 5
<210> 581
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /замена="Lys"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Tyr" или "Ser"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Tyr", или "Ser", или "Thr"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Tyr", или "Ser", или "Thr"
<220>
<221> ВАРИАНТ
<222> (11)..(11)
<223> /замена="Tyr"
<220>
<221> Сайт
<222> (1)..(11)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 581
Ala Ser Phe Trp Trp Asp Leu Asp Phe Asp His
1 5 10
<210> 582
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 582
Ala Ala Leu Asn Ser Glu Tyr Asp
1 5
<210> 583
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 583
Leu Asn Ser Glu Tyr Asp
1 5
<210> 584
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /замена="Gly"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Leu"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Gly"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="Asn"
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /замена="Glu" или "Leu"
<220>
<221> ВАРИАНТ
<222> (11)..(11)
<223> /замена="Asn" или "Glu"
<220>
<221> Сайт
<222> (1)..(16)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 584
Arg Ser Ser Gln Ser Ile Val Arg Ser Asp Gly Thr Thr Tyr Phe Asn
1 5 10 15
<210> 585
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Leu"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Gly"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Asn"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Glu" или "Leu"
<220>
<221> Сайт
<222> (1)..(10)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 585
Gln Ser Ile Val Arg Ser Asp Thr Thr Tyr
1 5 10
<210> 586
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Leu"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Gly"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Asn"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="Glu" или "Leu"
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> /замена="Asn" или "Glu"
<220>
<221> Сайт
<222> (1)..(12)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 586
Ser Gln Ser Ile Val Arg Ser Asp Gly Thr Thr Tyr
1 5 10
<210> 587
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /замена="Gly"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Leu"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Gly"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="Asn"
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /замена="Glu" или "Leu"
<220>
<221> ВАРИАНТ
<222> (11)..(11)
<223> /замена="Asn" или "Glu"
<220>
<221> Сайт
<222> (1)..(11)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 587
Arg Ser Ser Gln Ser Ile Val Arg Ser Asp Gly
1 5 10
<210> 588
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Leu"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Gly"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Asn"
<220>
<221> Сайт
<222> (1)..(7)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 588
Ser Gln Ser Ile Val Arg Ser
1 5
<210> 589
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Leu"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Gly"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Asn"
<220>
<221> Сайт
<222> (1)..(6)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 589
Gln Ser Ile Val Arg Ser
1 5
<210> 590
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена="Ser"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /замена="Thr"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Thr"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Leu"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Glu"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Tyr"
<220>
<221> Сайт
<222> (1)..(7)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 590
Arg Val Ser Asn Arg Phe Ser
1 5
<210> 591
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена="Ser"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /замена="Thr"
<220>
<221> Сайт
<222> (1)..(3)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 591
Arg Val Ser
1
<210> 592
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Tyr"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Ala"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Thr"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Tyr"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="Tyr"
<220>
<221> Сайт
<222> (1)..(9)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 592
Leu Gln Ser Ser His Phe Pro Trp Thr
1 5
<210> 593
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена="Tyr"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /замена="Ala"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Thr"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Tyr"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Tyr"
<220>
<221> Сайт
<222> (1)..(6)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 593
Ser Ser His Phe Pro Trp
1 5
<210> 594
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Tyr"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Ala"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Thr"
<220>
<221> Сайт
<222> (1)..(5)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 594
Leu Gln Ser Ser His
1 5
<210> 595
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Tyr"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Ala"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Thr"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Tyr"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="Tyr"
<220>
<221> Сайт
<222> (1)..(8)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 595
Leu Gln Ser Ser His Phe Pro Trp
1 5
<210> 596
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> /замена="Ile"
<220>
<221> Сайт
<222> (1)..(10)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 596
Gly Phe Ser Leu Thr Thr Tyr Asn Val His
1 5 10
<210> 597
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 597
Gly Phe Ser Leu Thr Thr Tyr Asn
1 5
<210> 598
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Ile"
<220>
<221> Сайт
<222> (1)..(5)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 598
Thr Tyr Asn Val His
1 5
<210> 599
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 599
Gly Phe Ser Leu Thr Thr Tyr
1 5
<210> 600
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /замена="Tyr"
<220>
<221> ВАРИАНТ
<222> (11)..(11)
<223> /замена="Ser"
<220>
<221> ВАРИАНТ
<222> (12)..(12)
<223> /замена="Ser"
<220>
<221> ВАРИАНТ
<222> (15)..(15)
<223> /замена="Lys"
<220>
<221> Сайт
<222> (1)..(16)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 600
Arg Met Arg Tyr Ser Gly Asp Thr Ser Phe Asn Ala Ala Leu Thr Ser
1 5 10 15
<210> 601
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 601
Arg Tyr Ser Gly Asp
1 5
<210> 602
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 602
Met Arg Tyr Ser Gly Asp Thr
1 5
<210> 603
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Gly"
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> /замена="Ala"
<220>
<221> Сайт
<222> (1)..(15)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 603
Asp Pro Met Tyr Ile Pro Asn Tyr Ser Tyr Gly Val Met Asn Ala
1 5 10 15
<210> 604
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена="Ala"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /замена="Arg"
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> /замена="Gly"
<220>
<221> ВАРИАНТ
<222> (11)..(11)
<223> /замена="Ala"
<220>
<221> Сайт
<222> (1)..(17)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 604
Thr Ser Asp Pro Met Tyr Ile Pro Asn Tyr Ser Tyr Gly Val Met Asn
1 5 10 15
Ala
<210> 605
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /замена="Thr" или "Ser"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Asp"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="Lys"
<220>
<221> Сайт
<222> (1)..(11)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 605
Lys Ala Ser Gln Asn Ile Asn Asn Tyr Leu Asn
1 5 10
<210> 606
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Asp"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Lys"
<220>
<221> Сайт
<222> (1)..(7)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 606
Ser Gln Asn Ile Asn Asn Tyr
1 5
<210> 607
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Asp"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Lys"
<220>
<221> Сайт
<222> (1)..(6)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 607
Gln Asn Ile Asn Asn Tyr
1 5
<210> 608
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Asn"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Asn"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Glu"
<220>
<221> Сайт
<222> (1)..(10)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 608
Asn Thr Asp His Leu Gln Ala Gly Val Pro
1 5 10
<210> 609
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Asn"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Asn"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Glu"
<220>
<221> Сайт
<222> (1)..(7)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 609
Asn Thr Asp His Leu Gln Ala
1 5
<210> 610
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Asn"
<220>
<221> Сайт
<222> (1)..(3)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 610
Asn Thr Asp
1
<210> 611
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Ser" или "Gly"
<220>
<221> Сайт
<222> (1)..(8)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 611
Leu Gln His Arg Ser Arg Tyr Thr
1 5
<210> 612
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Ser" или "Gly"
<220>
<221> Сайт
<222> (1)..(5)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 612
His Arg Ser Arg Tyr
1 5
<210> 613
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 613
Gly Tyr Thr Phe Thr Ser Tyr Tyr Ile Tyr
1 5 10
<210> 614
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 614
Gly Tyr Thr Phe Thr Ser Tyr Tyr
1 5
<210> 615
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 615
Ser Tyr Tyr Ile Tyr
1 5
<210> 616
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Ala"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Asn"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Gly"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="Gly"
<220>
<221> ВАРИАНТ
<222> (14)..(14)
<223> /замена="Lys"
<220>
<221> Сайт
<222> (1)..(17)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 616
Tyr Ile Tyr Pro Gly His Asp Ala Ile Tyr Tyr Ser Glu Asn Phe Lys
1 5 10 15
Gly
<210> 617
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> /замена="Ala"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Asn"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Gly"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Gly"
<220>
<221> Сайт
<222> (1)..(6)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 617
Tyr Pro Gly His Asp Ala
1 5
<210> 618
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Ala"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Asn"
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> /замена="Gly"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Gly"
<220>
<221> Сайт
<222> (1)..(8)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 618
Ile Tyr Pro Gly His Asp Ala Ile
1 5
<210> 619
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена="Ala"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Val"
<220>
<221> ВАРИАНТ
<222> (11)..(11)
<223> /замена="Val"
<220>
<221> ВАРИАНТ
<222> (12)..(12)
<223> /замена="Phe"
<220>
<221> Сайт
<222> (1)..(12)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 619
Val Arg Pro Asn Thr Met Met Ala Pro Leu Ala Tyr
1 5 10
<210> 620
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> /замена="Val"
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> /замена="Val"
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /замена="Phe"
<220>
<221> Сайт
<222> (1)..(10)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 620
Pro Asn Thr Met Met Ala Pro Leu Ala Tyr
1 5 10
<210> 621
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="Val"
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> /замена="His"
<220>
<221> Сайт
<222> (1)..(16)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 621
Arg Ser Ser Gln Ser Leu Ile Tyr Ser Ile Gly Asn Thr Tyr Leu His
1 5 10 15
<210> 622
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> /замена="Val"
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> /замена="His"
<220>
<221> Сайт
<222> (1)..(12)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 622
Ser Gln Ser Leu Ile Tyr Ser Ile Gly Asn Thr Tyr
1 5 10
<210> 623
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> /замена="Val"
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> /замена="His"
<220>
<221> Сайт
<222> (1)..(11)
<223> /примечание="Остатки вариантов, приведенные в последовательности,
не имеют предпочтения по отношению к тем, которые указаны в аннотациях
для положений вариантов»
<400> 623
Gln Ser Leu Ile Tyr Ser Ile Gly Asn Thr Tyr
1 5 10
<210> 624
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 624
Arg Val Ser Asn Arg Phe Ser
1 5
<210> 625
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 625
Arg Val Ser
1
<210> 626
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 626
Phe Gln Ser Thr His Leu Pro Tyr Thr
1 5
<210> 627
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 627
Ser Thr His Leu Pro Tyr
1 5
<210> 628
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 628
Lys Asn Gly Met His
1 5
<210> 629
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 629
Thr Tyr Asn Val His
1 5
<210> 630
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 630
Thr Tyr Asn Ile His
1 5
<210> 631
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 631
Lys Tyr Gly Met Ser
1 5
<210> 632
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 632
Lys Gln Gly Met His
1 5
<210> 633
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 633
Lys Asn Gln Met His
1 5
<210> 634
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 634
Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val Lys
1 5 10 15
Gly
<210> 635
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 635
Tyr Ile Tyr Pro Gly His Asp Ala Ile Tyr Tyr Ser Glu Asn Phe Lys
1 5 10 15
Gly
<210> 636
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 636
Arg Met Arg Tyr Ser Gly Asp Thr Ser Phe Asn Ala Ala Leu Thr Ser
1 5 10 15
<210> 637
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 637
Tyr Ile Tyr Pro Ala Asn Gly Gly Ile Tyr Tyr Ser Glu Lys Phe Lys
1 5 10 15
Gly
<210> 638
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 638
Met Ile Tyr Tyr Asp Ser Ser Arg Met Tyr Tyr Ala Asp Thr Val Lys
1 5 10 15
Gly
<210> 639
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 639
Arg Met Arg Tyr Ser Gly Asp Thr Ser Tyr Ser Ser Ala Leu Lys Ser
1 5 10 15
<210> 640
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 640
Leu Ile Tyr Tyr Asp Ser Ser Lys Met Asn Tyr Ala Asp Thr Val Lys
1 5 10 15
Gly
<210> 641
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 641
Phe Trp Trp Asp Leu Asp Phe Asp His
1 5
<210> 642
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 642
Pro Asn Thr Met Met Ala Pro Leu Ala Tyr
1 5 10
<210> 643
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 643
Asp Pro Met Tyr Ile Pro Asn Tyr Ser Tyr Gly Val Met Asn Ala
1 5 10 15
<210> 644
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 644
Pro Val Thr Met Met Ala Pro Leu Val Phe
1 5 10
<210> 645
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 645
Phe Trp Trp Asp Leu Asp Phe Asp Tyr
1 5
<210> 646
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 646
Asp Pro Met Tyr Ile Pro Gly Tyr Ser Tyr Gly Val Met Asn Ala
1 5 10 15
<210> 647
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 647
Phe Tyr Tyr Asp Leu Asp Phe Asp His
1 5
<210> 648
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 648
Phe Ser Ser Asp Leu Asp Phe Asp His
1 5
<210> 649
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 649
Phe Trp Ser Asp Leu Asp Phe Asp His
1 5
<210> 650
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 650
Phe Ser Trp Asp Leu Asp Phe Asp His
1 5
<210> 651
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 651
Phe Thr Thr Asp Leu Asp Phe Asp His
1 5
<210> 652
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 652
Phe Thr Trp Asp Leu Asp Phe Asp His
1 5
<210> 653
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 653
Phe Trp Thr Asp Leu Asp Phe Asp His
1 5
<210> 654
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 654
Asp Pro Met Tyr Ile Pro Asn Tyr Ala Tyr Gly Val Met Asn Ala
1 5 10 15
<210> 655
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 655
Tyr Tyr Tyr Asp Leu Asp Phe Asp His
1 5
<210> 656
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 656
Ser Tyr Tyr Asp Leu Asp Phe Asp His
1 5
<210> 657
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 657
Tyr Ser Ser Asp Leu Asp Phe Asp His
1 5
<210> 658
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 658
Ser Ser Ser Asp Leu Asp Phe Asp His
1 5
<210> 659
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 659
Tyr Trp Ser Asp Leu Asp Phe Asp His
1 5
<210> 660
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 660
Ser Trp Ser Asp Leu Asp Phe Asp His
1 5
<210> 661
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 661
Tyr Ser Trp Asp Leu Asp Phe Asp His
1 5
<210> 662
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 662
Ser Ser Trp Asp Leu Asp Phe Asp His
1 5
<210> 663
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 663
Tyr Thr Trp Asp Leu Asp Phe Asp His
1 5
<210> 664
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 664
Ser Thr Trp Asp Leu Asp Phe Asp His
1 5
<210> 665
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 665
Tyr Thr Thr Asp Leu Asp Phe Asp His
1 5
<210> 666
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 666
Ser Thr Thr Asp Leu Asp Phe Asp His
1 5
<210> 667
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 667
Tyr Trp Trp Asp Leu Asp Phe Asp His
1 5
<210> 668
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 668
Ser Trp Trp Asp Leu Asp Phe Asp His
1 5
<210> 669
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 669
Arg Ser Ser Gln Ser Leu Val Arg Ser Asp Gly Thr Thr Tyr Phe Asn
1 5 10 15
<210> 670
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 670
Arg Ser Ser Gln Ser Leu Ile Tyr Ser Ile Gly Asn Thr Tyr Leu His
1 5 10 15
<210> 671
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 671
Lys Ala Ser Gln Asn Ile Asn Asn Tyr Leu Asn
1 5 10
<210> 672
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 672
Arg Ser Ser Gln Ser Leu Val Tyr Ser His Gly Asn Thr Tyr Leu His
1 5 10 15
<210> 673
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 673
Lys Thr Ser Gln Asn Ile Asp Lys Tyr Leu Asn
1 5 10
<210> 674
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 674
Arg Gly Ser Gln Ser Ile Gly Asn Ser Leu Asn
1 5 10
<210> 675
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 675
Lys Ser Ser Gln Asn Ile Asp Lys Tyr Leu Asn
1 5 10
<210> 676
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 676
Arg Ser Ser Gln Ser Leu Val Arg Ser Glu Gly Thr Thr Tyr Phe Asn
1 5 10 15
<210> 677
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 677
Asn Thr Asp His Leu Gln Ala
1 5
<210> 678
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 678
Asn Thr Asn Asn Leu Glu Ala
1 5
<210> 679
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 679
Ser Thr Ser Thr Leu Glu Tyr
1 5
<210> 680
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 680
Leu Gln Ser Ser His Phe Pro Trp Thr
1 5
<210> 681
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 681
Leu Gln His Arg Ser Arg Tyr Thr
1 5
<210> 682
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 682
Leu Gln His Arg Ser Ser Tyr Thr
1 5
<210> 683
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 683
Leu Gln Tyr Ala Thr Tyr Pro Tyr Thr
1 5
<210> 684
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 684
Leu Gln His Arg Ser Gly Tyr Thr
1 5
<210> 685
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 685
Leu Gln Ser Ser His
1 5
<210> 686
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 686
Gly Phe Thr Phe Ser Lys Asn
1 5
<210> 687
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 687
Gly Phe Ala Phe Arg Lys Tyr
1 5
<210> 688
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 688
Gly Phe Thr Phe Ser Lys Gln
1 5
<210> 689
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 689
Tyr Tyr Asp Ser Ser Lys
1 5
<210> 690
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 690
Tyr Pro Gly His Asp Ala
1 5
<210> 691
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 691
Tyr Pro Ala Asn Gly Gly
1 5
<210> 692
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 692
Tyr Tyr Asp Ser Ser Arg
1 5
<210> 693
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 693
Ser Gln Ser Leu Val Arg Ser Asp Gly Thr Thr Tyr
1 5 10
<210> 694
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 694
Ser Gln Ser Leu Ile Tyr Ser Ile Gly Asn Thr Tyr
1 5 10
<210> 695
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 695
Ser Gln Asn Ile Asn Asn Tyr
1 5
<210> 696
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 696
Ser Gln Ser Leu Val Tyr Ser His Gly Asn Thr Tyr
1 5 10
<210> 697
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 697
Ser Gln Asn Ile Asp Lys Tyr
1 5
<210> 698
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 698
Ser Gln Ser Ile Gly Asn Ser
1 5
<210> 699
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 699
Ser Gln Ser Leu Val Arg Ser Glu Gly Thr Thr Tyr
1 5 10
<210> 700
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 700
Asn Thr Asp
1
<210> 701
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 701
Asn Thr Asn
1
<210> 702
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 702
Ser Thr Ser
1
<210> 703
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 703
Ser Ser His Phe Pro Trp
1 5
<210> 704
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 704
His Arg Ser Arg Tyr
1 5
<210> 705
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 705
His Arg Ser Ser Tyr
1 5
<210> 706
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 706
Tyr Ala Thr Tyr Pro Tyr
1 5
<210> 707
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 707
His Arg Ser Gly Tyr
1 5
<210> 708
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 708
Gly Phe Thr Phe Ser Lys Asn Gly
1 5
<210> 709
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 709
Gly Phe Ala Phe Arg Lys Tyr Gly
1 5
<210> 710
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 710
Gly Phe Thr Phe Ser Lys Gln Gly
1 5
<210> 711
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 711
Ile Tyr Tyr Asp Ser Ser Lys Met
1 5
<210> 712
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 712
Ile Tyr Pro Gly His Asp Ala Ile
1 5
<210> 713
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 713
Ile Tyr Pro Ala Asn Gly Gly Ile
1 5
<210> 714
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 714
Ile Tyr Tyr Asp Ser Ser Arg Met
1 5
<210> 715
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 715
Ala Ser Phe Trp Trp Asp Leu Asp Phe Asp His
1 5 10
<210> 716
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 716
Val Arg Pro Asn Thr Met Met Ala Pro Leu Ala Tyr
1 5 10
<210> 717
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 717
Thr Ser Asp Pro Met Tyr Ile Pro Asn Tyr Ser Tyr Gly Val Met Asn
1 5 10 15
Ala
<210> 718
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 718
Ala Arg Asp Pro Met Tyr Ile Pro Asn Tyr Ser Tyr Gly Val Met Asn
1 5 10 15
Ala
<210> 719
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 719
Ala Arg Pro Val Thr Met Met Ala Pro Leu Val Phe
1 5 10
<210> 720
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 720
Ala Ser Phe Trp Trp Asp Leu Asp Phe Asp Tyr
1 5 10
<210> 721
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 721
Thr Arg Asp Pro Met Tyr Ile Pro Gly Tyr Ser Tyr Gly Val Met Asn
1 5 10 15
Ala
<210> 722
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 722
Ala Lys Phe Trp Trp Asp Leu Asp Phe Asp His
1 5 10
<210> 723
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 723
Ala Ser Phe Tyr Tyr Asp Leu Asp Phe Asp His
1 5 10
<210> 724
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 724
Ala Ser Phe Ser Ser Asp Leu Asp Phe Asp His
1 5 10
<210> 725
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 725
Ala Ser Phe Trp Ser Asp Leu Asp Phe Asp His
1 5 10
<210> 726
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 726
Ala Ser Phe Ser Trp Asp Leu Asp Phe Asp His
1 5 10
<210> 727
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 727
Ala Ser Phe Thr Thr Asp Leu Asp Phe Asp His
1 5 10
<210> 728
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 728
Ala Ser Phe Thr Trp Asp Leu Asp Phe Asp His
1 5 10
<210> 729
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 729
Ala Ser Phe Trp Thr Asp Leu Asp Phe Asp His
1 5 10
<210> 730
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 730
Ala Ser Asp Pro Met Tyr Ile Pro Asn Tyr Ala Tyr Gly Val Met Asn
1 5 10 15
Ala
<210> 731
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 731
Ala Ser Tyr Tyr Tyr Asp Leu Asp Phe Asp His
1 5 10
<210> 732
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 732
Ala Ser Ser Tyr Tyr Asp Leu Asp Phe Asp His
1 5 10
<210> 733
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 733
Ala Ser Tyr Ser Ser Asp Leu Asp Phe Asp His
1 5 10
<210> 734
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 734
Ala Ser Ser Ser Ser Asp Leu Asp Phe Asp His
1 5 10
<210> 735
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 735
Ala Ser Tyr Trp Ser Asp Leu Asp Phe Asp His
1 5 10
<210> 736
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 736
Ala Ser Ser Trp Ser Asp Leu Asp Phe Asp His
1 5 10
<210> 737
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 737
Ala Ser Tyr Ser Trp Asp Leu Asp Phe Asp His
1 5 10
<210> 738
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 738
Ala Ser Ser Ser Trp Asp Leu Asp Phe Asp His
1 5 10
<210> 739
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 739
Ala Ser Tyr Thr Trp Asp Leu Asp Phe Asp His
1 5 10
<210> 740
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 740
Ala Ser Ser Thr Trp Asp Leu Asp Phe Asp His
1 5 10
<210> 741
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 741
Ala Ser Tyr Thr Thr Asp Leu Asp Phe Asp His
1 5 10
<210> 742
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 742
Ala Ser Ser Thr Thr Asp Leu Asp Phe Asp His
1 5 10
<210> 743
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 743
Ala Ser Tyr Trp Trp Asp Leu Asp Phe Asp His
1 5 10
<210> 744
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 744
Ala Ser Ser Trp Trp Asp Leu Asp Phe Asp His
1 5 10
<210> 745
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 745
Gln Ser Leu Val Arg Ser Asp Gly Thr Thr Tyr
1 5 10
<210> 746
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 746
Gln Ser Leu Ile Tyr Ser Ile Gly Asn Thr Tyr
1 5 10
<210> 747
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 747
Gln Asn Ile Asn Asn Tyr
1 5
<210> 748
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 748
Gln Ser Leu Val Tyr Ser His Gly Asn Thr Tyr
1 5 10
<210> 749
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 749
Gln Asn Ile Asp Lys Tyr
1 5
<210> 750
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 750
Gln Ser Ile Gly Asn Ser
1 5
<210> 751
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 751
Gln Ser Leu Val Arg Ser Glu Gly Thr Thr Tyr
1 5 10
<210> 752
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 752
Gln Ser Leu Val Arg Ser Asp Glu Thr Thr Tyr
1 5 10
<210> 753
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 753
Asn Thr Asp His Leu Gln Ala Gly Val Pro
1 5 10
<210> 754
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 754
Asn Thr Asn Asn Leu Glu Ala Gly Val Pro
1 5 10
<210> 755
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 755
Ser Thr Ser Thr Leu Glu Tyr Gly Val Pro
1 5 10
<210> 756
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 756
Gly Phe Thr Phe Ser Lys Asn Gly Met His
1 5 10
<210> 757
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 757
Gly Phe Ser Leu Thr Thr Tyr Asn Val His
1 5 10
<210> 758
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 758
Gly Phe Ser Leu Thr Thr Tyr Asn Ile His
1 5 10
<210> 759
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 759
Gly Phe Ala Phe Arg Lys Tyr Gly Met Ser
1 5 10
<210> 760
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 760
Gly Phe Thr Phe Ser Lys Gln Gly Met His
1 5 10
<210> 761
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический пептид"
<400> 761
Leu Gln Ser Ser His Phe Pro Trp
1 5
<210> 762
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 762
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Phe Trp Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 763
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 763
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile Tyr Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Tyr Ile Tyr Pro Gly His Asp Ala Ile Tyr Tyr Ser Glu Asn Phe
50 55 60
Lys Gly Arg Val Thr Ile Thr Ala Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Arg Pro Asn Thr Met Met Ala Pro Leu Ala Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 764
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 764
Gln Val Gln Leu His Gln Ser Gly Ala Glu Leu Ala Lys Pro Gly Thr
1 5 10 15
Ser Val Asn Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile Tyr Trp Ile Lys Arg Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Tyr Pro Gly His Asp Ala Ile Tyr Tyr Ser Glu Asn Phe
50 55 60
Lys Gly Lys Ala Thr Phe Thr Ala Asp Thr Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Leu Leu Gly Ser Leu Thr Pro Glu Asp Ser Ala Tyr Tyr Phe Cys
85 90 95
Val Arg Pro Asn Thr Met Met Ala Pro Leu Ala Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 765
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 765
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Thr Tyr
20 25 30
Asn Val His Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Arg Met Arg Tyr Ser Gly Asp Thr Ser Phe Asn Ala Ala Leu Thr
50 55 60
Ser Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Thr
85 90 95
Ser Asp Pro Met Tyr Ile Pro Asn Tyr Ser Tyr Gly Val Met Asn Ala
100 105 110
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 766
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 766
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Thr Tyr
20 25 30
Asn Val His Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Arg Met Arg Tyr Ser Gly Asp Thr Ser Phe Asn Ala Ala Leu Thr
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Asp Pro Met Tyr Ile Pro Asn Tyr Ser Tyr Gly Val Met Asn Ala
100 105 110
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 767
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 767
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile Tyr Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Tyr Ile Tyr Pro Ala Asn Gly Gly Ile Tyr Tyr Ser Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Ile Thr Ala Asp Thr Ser Ala Gly Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Pro Val Thr Met Met Ala Pro Leu Val Phe Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 768
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 768
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Ile Tyr Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Tyr Ile Tyr Pro Ala Asn Gly Gly Ile Tyr Tyr Ser Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Pro Val Thr Met Met Ala Pro Leu Val Phe Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 769
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 769
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Arg Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Phe Trp Trp Asp Leu Asp Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 770
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 770
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Thr Tyr
20 25 30
Asn Ile His Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Arg Met Arg Tyr Ser Gly Asp Thr Ser Tyr Ser Ser Ala Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Thr
85 90 95
Arg Asp Pro Met Tyr Ile Pro Gly Tyr Ser Tyr Gly Val Met Asn Ala
100 105 110
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 771
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 771
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ala Phe Arg Lys Tyr
20 25 30
Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Leu Ile Tyr Tyr Asp Ser Ser Lys Met Asn Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ala Leu Asn Ser Glu Tyr Asp Trp Gly Gln Gly Thr Met Val Thr
100 105 110
Val Ser Ser
115
<210> 772
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 772
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Phe Trp Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 773
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 773
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Phe Trp Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 774
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 774
Glu Val Lys Leu Val Glu Ser Gly Gly Asp Leu Val Gln Pro Gly Asp
1 5 10 15
Ser Leu Thr Leu Ser Cys Val Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Ile Arg Gln Ala Pro Lys Lys Gly Leu Glu Trp Ile
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Glu Met Asn Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Ser Phe Trp Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Val
100 105 110
Met Val Thr Val Ser Ser
115
<210> 775
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 775
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Phe Tyr Tyr Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 776
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 776
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Phe Ser Ser Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 777
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 777
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Phe Trp Ser Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 778
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 778
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Phe Ser Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 779
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 779
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Phe Thr Thr Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 780
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 780
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Phe Thr Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 781
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 781
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Phe Trp Thr Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 782
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 782
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Asn Thr Leu Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Phe Trp Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 783
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 783
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Gln Val Thr Ile Ser Arg Asp Asn Ser Ile Asn Thr Leu Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Ser Phe Trp Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 784
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 784
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Leu Thr Thr Tyr
20 25 30
Asn Val His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Met Arg Tyr Ser Gly Asp Thr Ser Phe Asn Ala Ala Leu Thr
50 55 60
Ser Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Ser Asp Pro Met Tyr Ile Pro Asn Tyr Ala Tyr Gly Val Met Asn Ala
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 785
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 785
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Arg Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Leu Thr Thr Tyr
20 25 30
Asn Val His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Met Arg Tyr Ser Gly Asp Thr Ser Phe Asn Ala Ala Leu Thr
50 55 60
Ser Arg Phe Thr Ile Ser Arg Asp Thr Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Gly Val Tyr Tyr Cys Ala
85 90 95
Ser Asp Pro Met Tyr Ile Pro Asn Tyr Ala Tyr Gly Val Met Asn Ala
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 786
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 786
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Arg Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Leu Thr Thr Tyr
20 25 30
Asn Val His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Arg Met Arg Tyr Ser Gly Asp Thr Ser Phe Asn Ala Ala Leu Thr
50 55 60
Ser Arg Phe Thr Ile Ser Arg Asp Thr Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Gly Val Tyr Tyr Cys Ala
85 90 95
Ser Asp Pro Met Tyr Ile Pro Asn Tyr Ala Tyr Gly Val Met Asn Ala
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 787
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 787
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
1 5 10 15
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Leu Thr Thr Tyr Asn
20 25 30
Val His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser
35 40 45
Arg Met Arg Tyr Ser Gly Asp Thr Ser Phe Asn Ala Ala Leu Thr Ser
50 55 60
Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr Leu Gln
65 70 75 80
Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Ser
85 90 95
Asp Pro Met Tyr Ile Pro Asn Tyr Ala Tyr Gly Val Met Asn Ala Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 788
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 788
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Ser Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Thr Ala Ser Gly Phe Ser Leu Thr Thr Tyr
20 25 30
Asn Val His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Met Arg Tyr Ser Gly Asp Thr Ser Phe Asn Ala Ala Leu Thr
50 55 60
Ser Arg Phe Thr Ile Ser Arg Asp Thr Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Ser Asp Pro Met Tyr Ile Pro Asn Tyr Ala Tyr Gly Val Met Asn Ala
100 105 110
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 789
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 789
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Phe Tyr Tyr Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 790
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 790
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Tyr Tyr Tyr Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 791
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 791
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Ser Tyr Tyr Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 792
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 792
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Tyr Tyr Tyr Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 793
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 793
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Ser Tyr Tyr Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 794
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 794
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Phe Ser Ser Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 795
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 795
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Tyr Ser Ser Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 796
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 796
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Ser Ser Ser Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 797
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 797
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Tyr Ser Ser Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 798
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 798
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Ser Ser Ser Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 799
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 799
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Tyr Trp Ser Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 800
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 800
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Ser Trp Ser Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 801
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 801
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Tyr Trp Ser Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 802
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 802
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Ser Trp Ser Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 803
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 803
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Phe Trp Ser Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 804
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 804
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Tyr Ser Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 805
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 805
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Ser Ser Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 806
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 806
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Tyr Ser Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 807
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 807
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Ser Ser Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 808
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 808
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Phe Ser Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 809
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 809
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Tyr Thr Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 810
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 810
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Ser Thr Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 811
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 811
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Tyr Thr Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 812
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 812
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Ser Thr Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 813
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 813
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Phe Thr Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 814
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 814
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Tyr Thr Thr Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 815
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 815
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Ser Thr Thr Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 816
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 816
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Tyr Thr Thr Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 817
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 817
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Ser Thr Thr Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 818
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 818
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Phe Thr Thr Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 819
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 819
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Tyr Trp Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 820
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 820
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Ser Trp Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 821
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 821
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Asn Thr Leu Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Tyr Trp Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 822
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 822
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Asn Thr Leu Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Ser Trp Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 823
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 823
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Asn Thr Leu Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Tyr Trp Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 824
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 824
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Asn Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Asn Thr Leu Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Ser Trp Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 825
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 825
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Asn Thr Leu Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Tyr Ser Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 826
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 826
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Asn Thr Leu Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Ser Ser Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 827
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 827
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Asn Thr Leu Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Tyr Ser Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 828
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 828
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Asn Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Asn Thr Leu Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Ser Ser Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 829
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 829
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Asn Thr Leu Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Phe Ser Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 830
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 830
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Asn Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Asn Thr Leu Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Phe Ser Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 831
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 831
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Tyr Trp Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 832
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 832
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Ser Trp Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 833
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 833
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Gln Val Thr Ile Ser Arg Asp Asn Ser Ile Asn Thr Leu Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Ser Tyr Trp Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 834
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 834
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Gln Val Thr Ile Ser Arg Asp Asn Ser Ile Asn Thr Leu Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Ser Ser Trp Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 835
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 835
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Gln Val Thr Ile Ser Arg Asp Asn Ser Ile Asn Thr Leu Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Ser Tyr Trp Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 836
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 836
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Gln Val Thr Ile Ser Arg Asp Asn Ser Ile Asn Thr Leu Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Ser Ser Trp Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 837
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 837
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Gln Val Thr Ile Ser Arg Asp Asn Ser Ile Asn Thr Leu Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Ser Tyr Ser Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 838
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 838
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Gln Val Thr Ile Ser Arg Asp Asn Ser Ile Asn Thr Leu Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Ser Ser Ser Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 839
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 839
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Gln Val Thr Ile Ser Arg Asp Asn Ser Ile Asn Thr Leu Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Ser Tyr Ser Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 840
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 840
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Gln Val Thr Ile Ser Arg Asp Asn Ser Ile Asn Thr Leu Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Ser Ser Ser Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 841
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 841
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Phe Thr Phe Ser Lys Asn
20 25 30
Gly Met His Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Gln Val Thr Ile Ser Arg Asp Asn Ser Ile Asn Thr Leu Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Ser Phe Ser Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 842
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 842
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Phe Thr Phe Ser Lys Gln
20 25 30
Gly Met His Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Tyr Tyr Asp Ser Ser Lys Met Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Gln Val Thr Ile Ser Arg Asp Asn Ser Ile Asn Thr Leu Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Ser Phe Ser Trp Asp Leu Asp Phe Asp His Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 843
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 843
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Ser Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val Arg Ser
20 25 30
Asp Gly Thr Thr Tyr Phe Asn Trp Tyr Gln Gln Arg Pro Gly Gln Pro
35 40 45
Pro Arg Leu Leu Ile Tyr Arg Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ala Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Leu Gln Ser
85 90 95
Ser His Phe Pro Trp Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 844
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 844
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Ile Tyr Ser
20 25 30
Ile Gly Asn Thr Tyr Leu His Trp Tyr Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Leu Leu Ile Tyr Arg Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Phe Gln Ser
85 90 95
Thr His Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 845
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 845
Val Val Val Leu Thr Gln Thr Pro Val Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Gly Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Ile Tyr Ser
20 25 30
Ile Gly Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Arg Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Pro Glu Asp Leu Gly Asp Tyr Tyr Cys Phe Gln Ser
85 90 95
Thr His Leu Pro Tyr Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105 110
<210> 846
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 846
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Ile Asn Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asn Thr Asp His Leu Gln Ala Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Phe Cys Leu Gln His Arg Ser Arg Tyr Thr
85 90 95
Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 847
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 847
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Ile Asn Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asn Thr Asp His Leu Gln Ala Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln His Arg Ser Arg Tyr Thr
85 90 95
Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 848
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 848
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val Tyr Ser
20 25 30
His Gly Asn Thr Tyr Leu His Trp Tyr Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Leu Leu Ile Tyr Arg Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Phe Gln Ser
85 90 95
Thr His Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 849
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 849
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val Tyr Ser
20 25 30
His Gly Asn Thr Tyr Leu His Trp Phe Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Arg Leu Ile Tyr Arg Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Phe Gln Ser
85 90 95
Thr His Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 850
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 850
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Thr Ser Gln Asn Ile Asp Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asn Thr Asn Asn Leu Glu Ala Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Leu Gln His Arg Ser Ser Tyr Thr
85 90 95
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 851
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 851
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Gly Ser Gln Ser Ile Gly Asn Ser
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Arg Leu Ile
35 40 45
Tyr Ser Thr Ser Thr Leu Glu Tyr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Tyr Ala Thr Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 852
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 852
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ser Ser Gln Asn Ile Asp Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asn Thr Asn Asn Leu Glu Ala Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Leu Gln His Arg Ser Gly Tyr Thr
85 90 95
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 853
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 853
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Ser Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val Arg Ser
20 25 30
Asp Gly Thr Thr Tyr Phe Asn Trp Leu Gln Gln Arg Pro Gly Gln Pro
35 40 45
Pro Arg Leu Leu Ile Tyr Arg Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ala Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Leu Gln Ser
85 90 95
Ser His Phe Pro Trp Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 854
<211> 98
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 854
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Ser Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val Arg Ser
20 25 30
Asp Gly Thr Thr Tyr Phe Asn Trp Tyr Gln Gln Arg Pro Gly Gln Pro
35 40 45
Pro Arg Leu Leu Ile Tyr Arg Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ala Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Leu Gln Ser
85 90 95
Ser His
<210> 855
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 855
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Ser Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val Arg Ser
20 25 30
Glu Gly Thr Thr Tyr Phe Asn Trp Tyr Gln Gln Arg Pro Gly Gln Pro
35 40 45
Pro Arg Leu Leu Ile Tyr Arg Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ala Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Leu Gln Ser
85 90 95
Ser His Phe Pro Trp Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 856
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 856
Asp Ile Leu Val Thr Gln Thr Pro Val Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Gly His Val Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val Arg Ser
20 25 30
Glu Gly Thr Thr Tyr Phe Asn Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Arg Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Pro Glu Asp Leu Gly Val Tyr Tyr Cys Leu Gln Ser
85 90 95
Ser His Phe Pro Trp Thr Phe Gly Gly Gly Thr Lys Leu Glu Leu Lys
100 105 110
<210> 857
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 857
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ser Ser Gln Ser Leu Val Arg Ser
20 25 30
Glu Gly Thr Thr Tyr Phe Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Arg Val Ser Asn Arg Phe Ser Gly Ile Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Arg Leu Glu Pro Glu Asp Leu Ala Val Tyr Tyr Cys Leu Gln Ser
85 90 95
Ser His Phe Pro Trp Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 858
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 858
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ser Ser Gln Ser Leu Val Arg Ser
20 25 30
Glu Gly Thr Thr Tyr Phe Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
35 40 45
Pro Lys Leu Leu Ile Tyr Arg Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Ser
85 90 95
Ser His Phe Pro Trp Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 859
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 859
Glu Ile Val Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Ile Ile Thr Cys Lys Ala Ser Gln Asn Ile Asn Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asn Thr Asp His Leu Gln Ala Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Ala Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Asp Asp Phe Ala Thr Tyr Tyr Cys Leu Gln His Arg Ser Arg Tyr Thr
85 90 95
Phe Gly Gln Gly Thr Lys Leu Thr Val Leu
100 105
<210> 860
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 860
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ser Ser Gln Ser Leu Val Arg Ser
20 25 30
Asp Gly Thr Thr Tyr Phe Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Arg Val Ser Asn Arg Phe Ser Gly Ile Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Arg Leu Glu Pro Glu Asp Leu Ala Val Tyr Tyr Cys Leu Gln Ser
85 90 95
Ser His Phe Pro Trp Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 861
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 861
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ser Ser Gln Ser Leu Val Arg Ser
20 25 30
Asp Gly Thr Thr Tyr Phe Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
35 40 45
Pro Lys Leu Leu Ile Tyr Arg Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Ser
85 90 95
Ser His Phe Pro Trp Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 862
<211> 714
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 862
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
195 200 205
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys
210 215 220
Ser Cys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu
225 230 235 240
Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala Ser Val Lys Met
245 250 255
Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Ser Tyr Val Met His Trp
260 265 270
Val Lys Gln Lys Pro Gly Gln Gly Leu Glu Trp Ile Gly Tyr Ile Asn
275 280 285
Pro Tyr Asn Asp Val Thr Lys Tyr Asn Glu Lys Phe Lys Gly Lys Ala
290 295 300
Thr Leu Thr Ser Asp Lys Ser Ser Ser Thr Ala Tyr Met Glu Leu Ser
305 310 315 320
Ser Leu Thr Ser Glu Asp Ser Ala Val His Tyr Cys Ala Arg Gly Ser
325 330 335
Tyr Tyr Asp Tyr Asp Gly Phe Val Tyr Trp Gly Gln Gly Thr Leu Val
340 345 350
Thr Val Ser Ala Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
355 360 365
Gly Gly Ser Gly Gly Gly Gly Ser Gln Ile Val Leu Thr Gln Ser Pro
370 375 380
Ala Ile Met Ser Ala Ser Pro Gly Glu Lys Val Thr Met Thr Cys Ser
385 390 395 400
Ala Thr Ser Ser Val Ser Tyr Met His Trp Tyr Gln Gln Lys Ser Gly
405 410 415
Thr Ser Pro Lys Arg Trp Ile Tyr Asp Thr Ser Lys Leu Ala Ser Gly
420 425 430
Val Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Ser Tyr Ser Leu
435 440 445
Thr Ile Ser Ser Met Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln
450 455 460
Gln Trp Ser Ser Asn Pro Leu Thr Phe Gly Ala Gly Thr Lys Leu Glu
465 470 475 480
Leu Lys Gly Gly Gly Gly Ser Asp Lys Thr His Thr Cys Pro Pro Cys
485 490 495
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
500 505 510
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
515 520 525
Val Val Val Ala Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
530 535 540
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
545 550 555 560
Glu Gln Tyr Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
565 570 575
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
580 585 590
Lys Ala Leu Ala Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
595 600 605
Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Arg Glu Glu
610 615 620
Met Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr
625 630 635 640
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
645 650 655
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
660 665 670
Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
675 680 685
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
690 695 700
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
705 710
<210> 863
<211> 326
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 863
Ser Gln Gln Ile Tyr Gly Val Val Tyr Gly Asn Val Thr Phe His Val
1 5 10 15
Pro Ser Asn Val Pro Leu Lys Glu Val Leu Trp Lys Lys Gln Lys Asp
20 25 30
Lys Val Ala Glu Leu Glu Asn Ser Glu Phe Arg Ala Phe Ser Ser Phe
35 40 45
Lys Asn Arg Val Tyr Leu Asp Thr Val Ser Gly Ser Leu Thr Ile Tyr
50 55 60
Asn Leu Thr Ser Ser Asp Glu Asp Glu Tyr Glu Met Glu Ser Pro Asn
65 70 75 80
Ile Thr Asp Thr Met Lys Phe Phe Leu Tyr Val Leu Glu Ser Gly Gly
85 90 95
Gly Gly Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
100 105 110
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
115 120 125
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Ala
130 135 140
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
145 150 155 160
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala
165 170 175
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
180 185 190
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Ala
195 200 205
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
210 215 220
Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Glu Glu Met Thr Lys Asn
225 230 235 240
Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
245 250 255
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
260 265 270
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
275 280 285
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
290 295 300
Ser Val Met His Glu Ala Leu His Asn Arg Tyr Thr Gln Lys Ser Leu
305 310 315 320
Ser Leu Ser Pro Gly Lys
325
<210> 864
<211> 562
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 864
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
195 200 205
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys
210 215 220
Ser Cys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Gln Gln Ile
225 230 235 240
Tyr Gly Val Val Tyr Gly Asn Val Thr Phe His Val Pro Ser Asn Val
245 250 255
Pro Leu Lys Glu Val Leu Trp Lys Lys Gln Lys Asp Lys Val Ala Glu
260 265 270
Leu Glu Asn Ser Glu Phe Arg Ala Phe Ser Ser Phe Lys Asn Arg Val
275 280 285
Tyr Leu Asp Thr Val Ser Gly Ser Leu Thr Ile Tyr Asn Leu Thr Ser
290 295 300
Ser Asp Glu Asp Glu Tyr Glu Met Glu Ser Pro Asn Ile Thr Asp Thr
305 310 315 320
Met Lys Phe Phe Leu Tyr Val Leu Glu Ser Gly Gly Gly Gly Ser Asp
325 330 335
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
340 345 350
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
355 360 365
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Ala Val Ser His Glu
370 375 380
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
385 390 395 400
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg
405 410 415
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
420 425 430
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Ala Ala Pro Ile Glu
435 440 445
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys
450 455 460
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
465 470 475 480
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
485 490 495
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
500 505 510
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
515 520 525
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
530 535 540
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
545 550 555 560
Gly Lys
<210> 865
<211> 478
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 865
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Ser Tyr
20 25 30
Val Met His Trp Val Lys Gln Lys Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Tyr Asn Asp Val Thr Lys Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val His Tyr Cys
85 90 95
Ala Arg Gly Ser Tyr Tyr Asp Tyr Asp Gly Phe Val Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ile Val Leu
130 135 140
Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly Glu Lys Val Thr
145 150 155 160
Met Thr Cys Ser Ala Thr Ser Ser Val Ser Tyr Met His Trp Tyr Gln
165 170 175
Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr Asp Thr Ser Lys
180 185 190
Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu Asp Ala Ala Thr
210 215 220
Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr Phe Gly Ala Gly
225 230 235 240
Thr Lys Leu Glu Leu Lys Gly Gly Gly Gly Ser Asp Lys Thr His Thr
245 250 255
Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe
260 265 270
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
275 280 285
Glu Val Thr Cys Val Val Val Ala Val Ser His Glu Asp Pro Glu Val
290 295 300
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
305 310 315 320
Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg Val Val Ser Val
325 330 335
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
340 345 350
Lys Val Ser Asn Lys Ala Leu Ala Ala Pro Ile Glu Lys Thr Ile Ser
355 360 365
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
370 375 380
Cys Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val
385 390 395 400
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
405 410 415
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
420 425 430
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
435 440 445
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
450 455 460
Asn Arg Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
465 470 475
<210> 866
<211> 365
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 866
Asp Val Gln Leu Gln Ala Ser Gly Gly Gly Ser Val Gln Ala Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr Ile Gly Pro Tyr
20 25 30
Cys Met Gly Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Gly Val
35 40 45
Ala Ala Ile Asn Met Gly Gly Gly Ile Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Gln Asp Asn Ala Lys Asn Thr Val Tyr
65 70 75 80
Leu Leu Met Asn Ser Leu Glu Pro Glu Asp Thr Ala Ile Tyr Tyr Cys
85 90 95
Ala Ala Asp Ser Thr Ile Tyr Ala Ser Tyr Tyr Glu Cys Gly His Gly
100 105 110
Leu Ser Thr Gly Gly Tyr Gly Tyr Asp Ser Trp Gly Gln Gly Thr Gln
115 120 125
Val Thr Val Ser Ser Gly Gly Gly Gly Ser Asp Lys Thr His Thr Cys
130 135 140
Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu
145 150 155 160
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
165 170 175
Val Thr Cys Val Val Val Ala Val Ser His Glu Asp Pro Glu Val Lys
180 185 190
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
195 200 205
Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg Val Val Ser Val Leu
210 215 220
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
225 230 235 240
Val Ser Asn Lys Ala Leu Ala Ala Pro Ile Glu Lys Thr Ile Ser Lys
245 250 255
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Cys
260 265 270
Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys
275 280 285
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
290 295 300
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
305 310 315 320
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
325 330 335
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
340 345 350
Arg Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
355 360 365
<210> 867
<211> 722
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 867
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Val Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Thr Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Gly Gly Ser Gly Tyr Ala Leu His Asp Asp Tyr Tyr Gly Leu Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
195 200 205
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys
210 215 220
Ser Cys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Gln Leu
225 230 235 240
Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Lys Leu
245 250 255
Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Thr Tyr Ala Met Asn Trp
260 265 270
Val Arg Gln Ala Ser Gly Lys Gly Leu Glu Trp Val Gly Arg Ile Arg
275 280 285
Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys Asp
290 295 300
Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Thr Leu Tyr Leu Gln
305 310 315 320
Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr Tyr Cys Val Arg
325 330 335
His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala Tyr Trp Gly
340 345 350
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
355 360 365
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ala Val
370 375 380
Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly Thr Val Thr
385 390 395 400
Leu Thr Cys Arg Ser Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr Ala
405 410 415
Asn Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg Gly Leu Ile Gly
420 425 430
Gly Thr Asn Lys Arg Ala Pro Trp Thr Pro Ala Arg Phe Ser Gly Ser
435 440 445
Leu Leu Gly Asp Lys Ala Ala Leu Thr Leu Ser Gly Ala Gln Pro Glu
450 455 460
Asp Glu Ala Glu Tyr Phe Cys Ala Leu Trp Tyr Ser Asn Leu Trp Val
465 470 475 480
Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Gly Gly Gly Ser Asp
485 490 495
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
500 505 510
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
515 520 525
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Ala Val Ser His Glu
530 535 540
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
545 550 555 560
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg
565 570 575
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
580 585 590
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Ala Ala Pro Ile Glu
595 600 605
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Cys
610 615 620
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
625 630 635 640
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
645 650 655
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
660 665 670
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
675 680 685
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
690 695 700
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
705 710 715 720
Gly Lys
<210> 868
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 868
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Ser Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Asp Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gln Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly
145 150 155 160
Gly Thr Val Thr Leu Thr Cys Arg Ser Ser Thr Gly Ala Val Thr Thr
165 170 175
Ser Asn Tyr Ala Asn Trp Val Gln Gln Lys Pro Gly Gln Ala Pro Arg
180 185 190
Gly Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Trp Thr Pro Ala Arg
195 200 205
Phe Ser Gly Ser Leu Leu Gly Asp Lys Ala Ala Leu Thr Leu Ser Gly
210 215 220
Ala Gln Pro Glu Asp Glu Ala Glu Tyr Phe Cys Ala Leu Trp Tyr Ser
225 230 235 240
Asn Leu Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Gly
245 250 255
Gly Gly Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
260 265 270
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
275 280 285
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Ala
290 295 300
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
305 310 315 320
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala
325 330 335
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
340 345 350
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Ala
355 360 365
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
370 375 380
Pro Gln Val Tyr Thr Leu Pro Pro Cys Arg Glu Glu Met Thr Lys Asn
385 390 395 400
Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
405 410 415
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
420 425 430
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
435 440 445
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
450 455 460
Ser Val Met His Glu Ala Leu His Asn Arg Tyr Thr Gln Lys Ser Leu
465 470 475 480
Ser Leu Ser Pro Gly Lys
485
<210> 869
<211> 227
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 869
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
1 5 10 15
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
20 25 30
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
35 40 45
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
50 55 60
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
65 70 75 80
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
85 90 95
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
100 105 110
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
115 120 125
Cys Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
130 135 140
Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
145 150 155 160
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
165 170 175
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val
180 185 190
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
195 200 205
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
210 215 220
Pro Gly Lys
225
<210> 870
<211> 227
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 870
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
1 5 10 15
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
20 25 30
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
35 40 45
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
50 55 60
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
65 70 75 80
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
85 90 95
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
100 105 110
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
115 120 125
Tyr Thr Leu Pro Pro Cys Arg Glu Glu Met Thr Lys Asn Gln Val Ser
130 135 140
Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
145 150 155 160
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
165 170 175
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
180 185 190
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
195 200 205
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
210 215 220
Pro Gly Lys
225
<210> 871
<211> 227
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 871
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
1 5 10 15
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
20 25 30
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
35 40 45
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
50 55 60
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
65 70 75 80
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
85 90 95
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
100 105 110
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
115 120 125
Tyr Thr Leu Pro Pro Cys Arg Glu Glu Met Thr Lys Asn Gln Val Ser
130 135 140
Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
145 150 155 160
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
165 170 175
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
180 185 190
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
195 200 205
His Glu Ala Leu His Asn Arg Tyr Thr Gln Lys Ser Leu Ser Leu Ser
210 215 220
Pro Gly Lys
225
<210> 872
<211> 225
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание=«Описание искусственной последовательности:
синтетический полипептид"
<400> 872
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
1 5 10 15
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
20 25 30
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
35 40 45
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
50 55 60
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
65 70 75 80
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
85 90 95
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
100 105 110
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
115 120 125
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
130 135 140
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
145 150 155 160
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
165 170 175
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
180 185 190
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
195 200 205
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
210 215 220
Pro
225
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| МОЛЕКУЛЫ, СВЯЗЫВАЮЩИЕ BCMA, И ПУТИ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2812322C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ ДЛЯ BCMA И ПУТИ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2785658C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ И ПУТИ ИХ ПРИМЕНЕНИЯ | 2020 |
|
RU2841244C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ КЛЕТОК, ЭКСПРЕССИРУЮЩИХ ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР | 2019 |
|
RU2822196C2 |
| СОЧЕТАНИЕ КЛЕТОЧНОЙ ТЕРАПИИ И ИММУНОМОДУЛЯТОРНОГО СОЕДИНЕНИЯ | 2018 |
|
RU2777911C2 |
| HPV-СПЕЦИФИЧЕСКИЕ СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2018 |
|
RU2804664C2 |
| ЛЕЧЕНИЕ ЗЛОКАЧЕСТВЕННОГО НОВООБРАЗОВАНИЯ С ИСПОЛЬЗОВАНИЕМ ГУМАНИЗИРОВАННОГО ХИМЕРНОГО АНТИГЕННОГО РЕЦЕПТОРА ПРОТИВ ВСМА | 2015 |
|
RU2751660C2 |
| ХИМЕРНЫЕ КОНСТРУКЦИИ АНТИТЕЛО/Т-КЛЕТОЧНЫЙ РЕЦЕПТОР И ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2767209C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ ДЛЯ ЛЕЧЕНИЯ РАКА | 2017 |
|
RU2826270C2 |
| РЕАГЕНТЫ ДЛЯ РАЗМНОЖЕНИЯ КЛЕТОК, ЭКСПРЕССИРУЮЩИХ РЕКОМБИНАНТНЫЕ РЕЦЕПТОРЫ | 2018 |
|
RU2783956C2 |
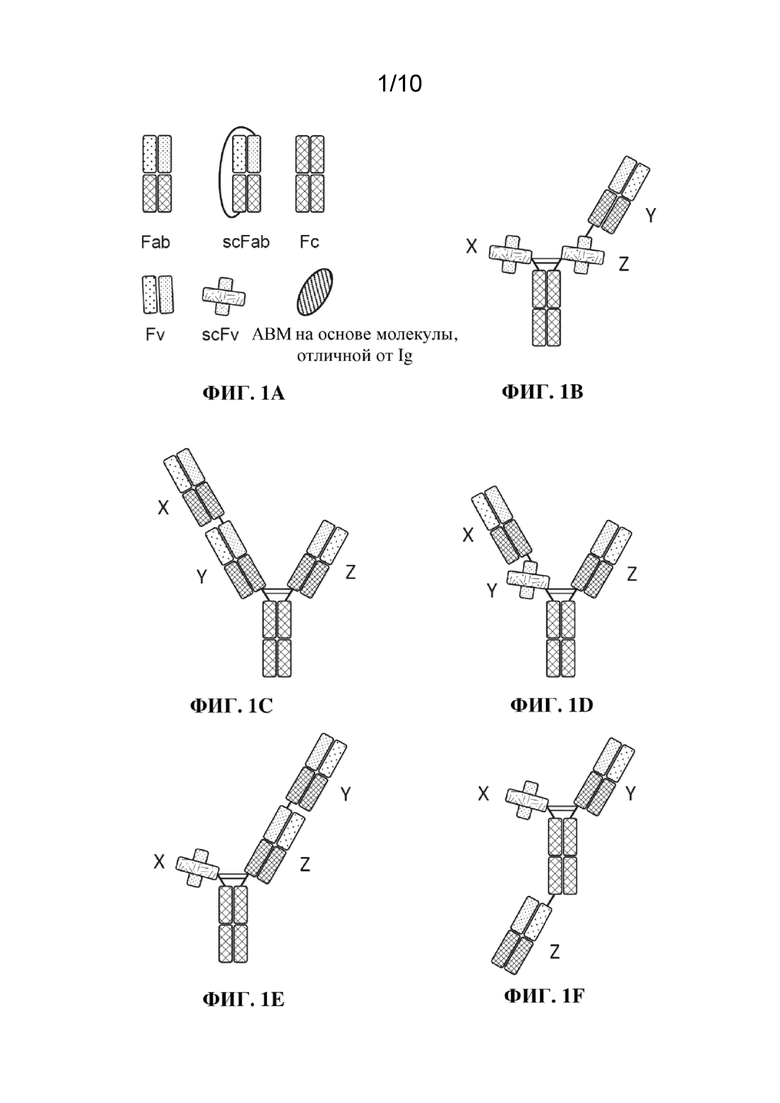
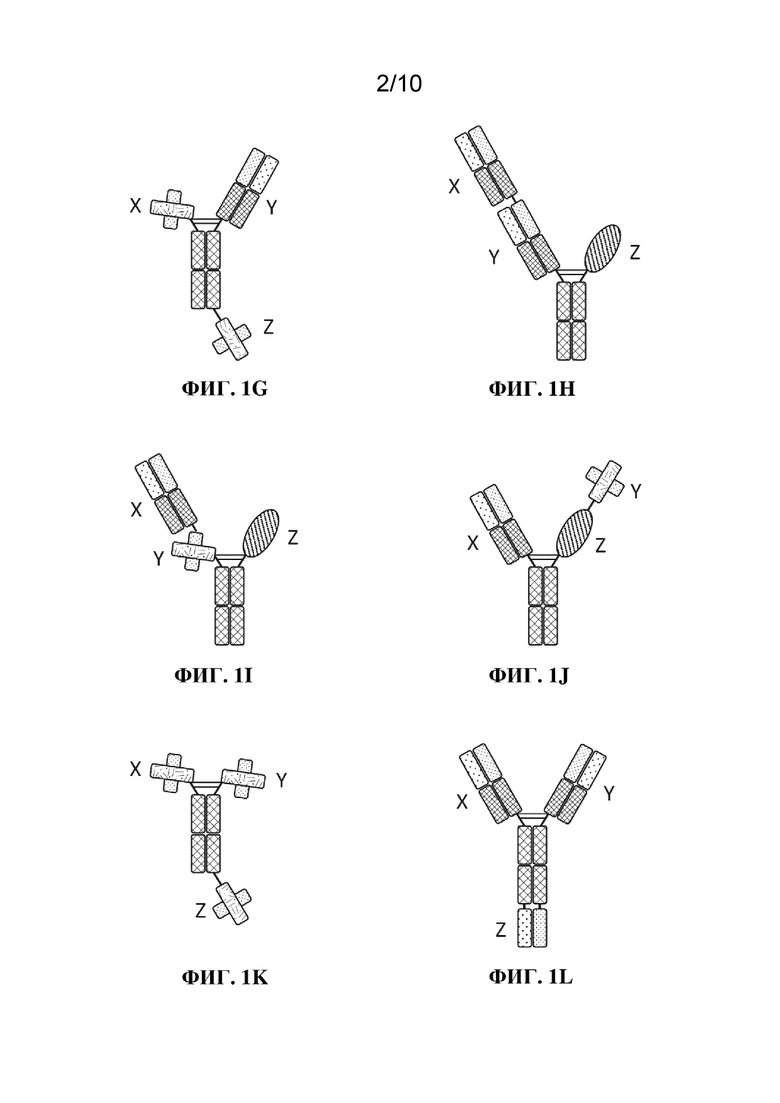
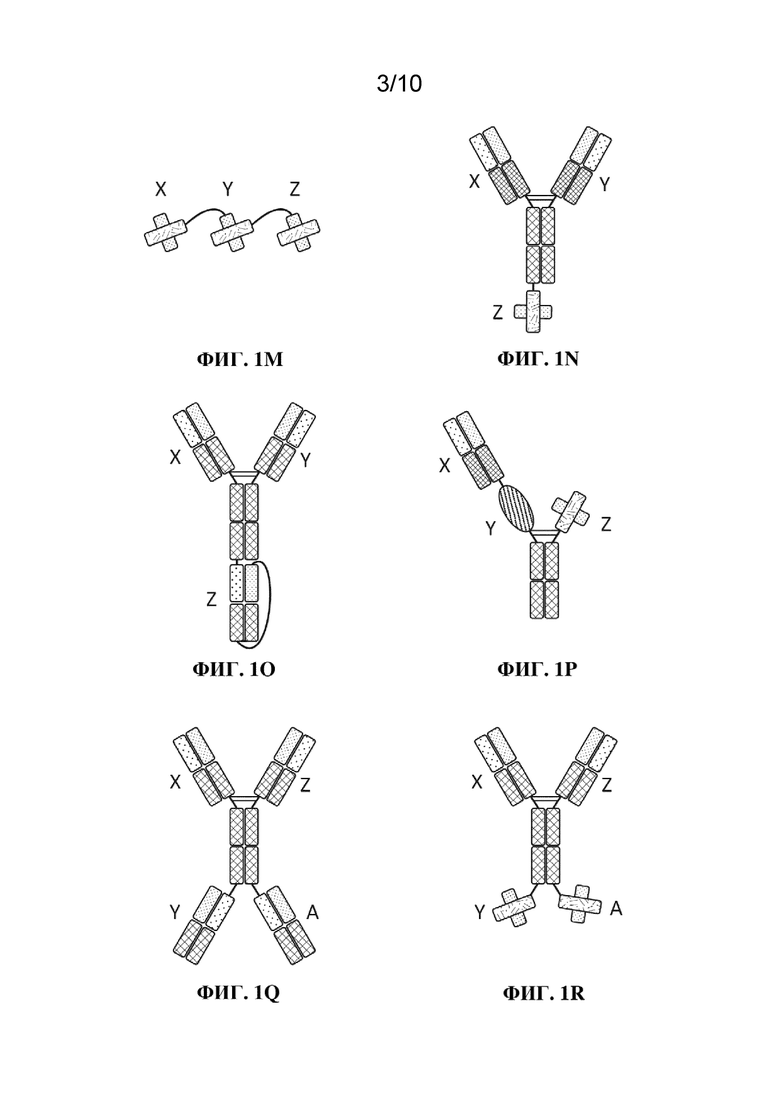
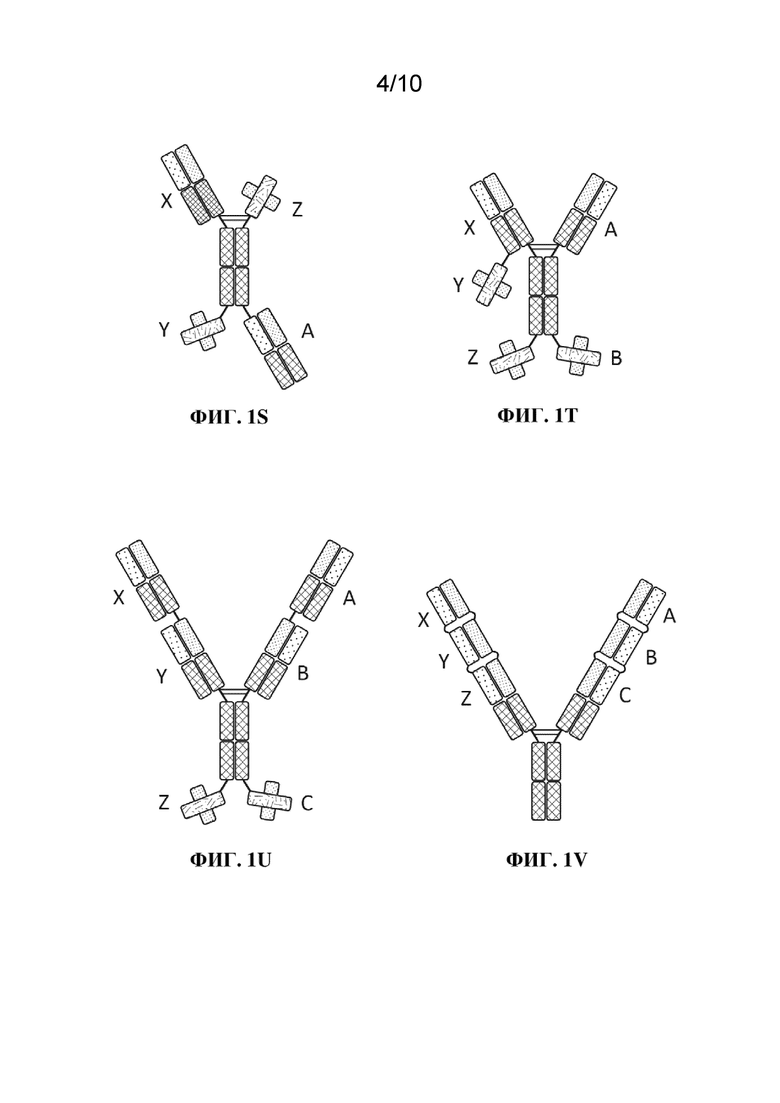
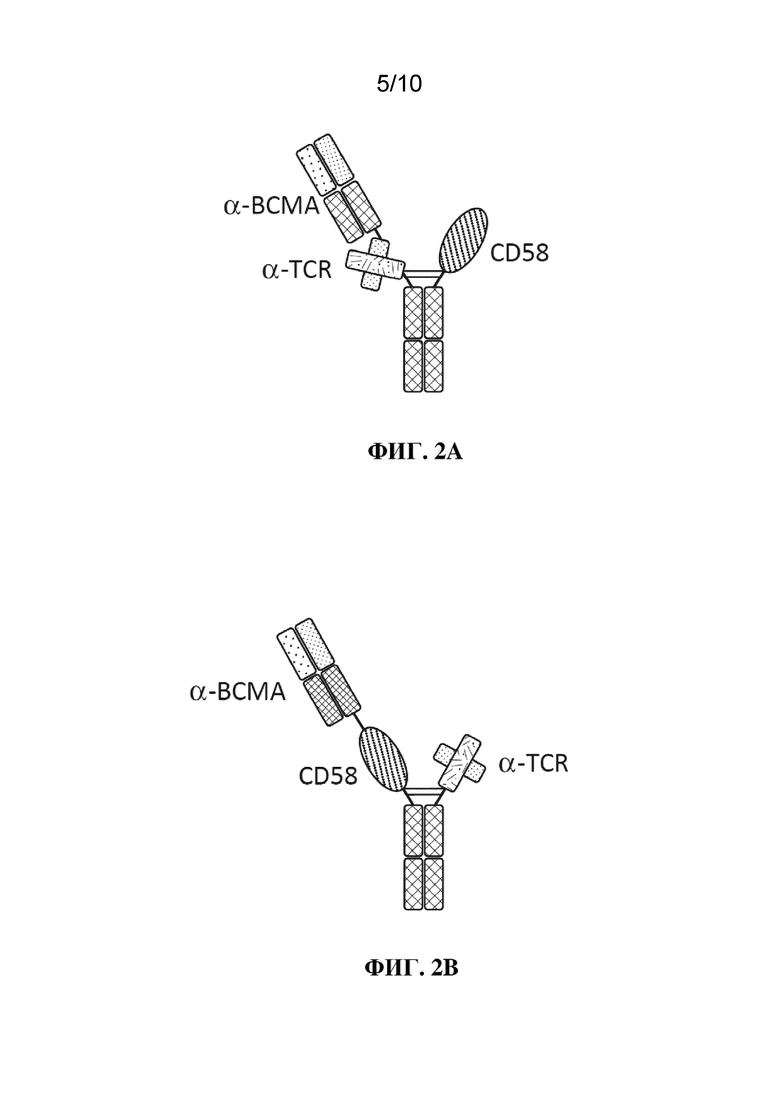
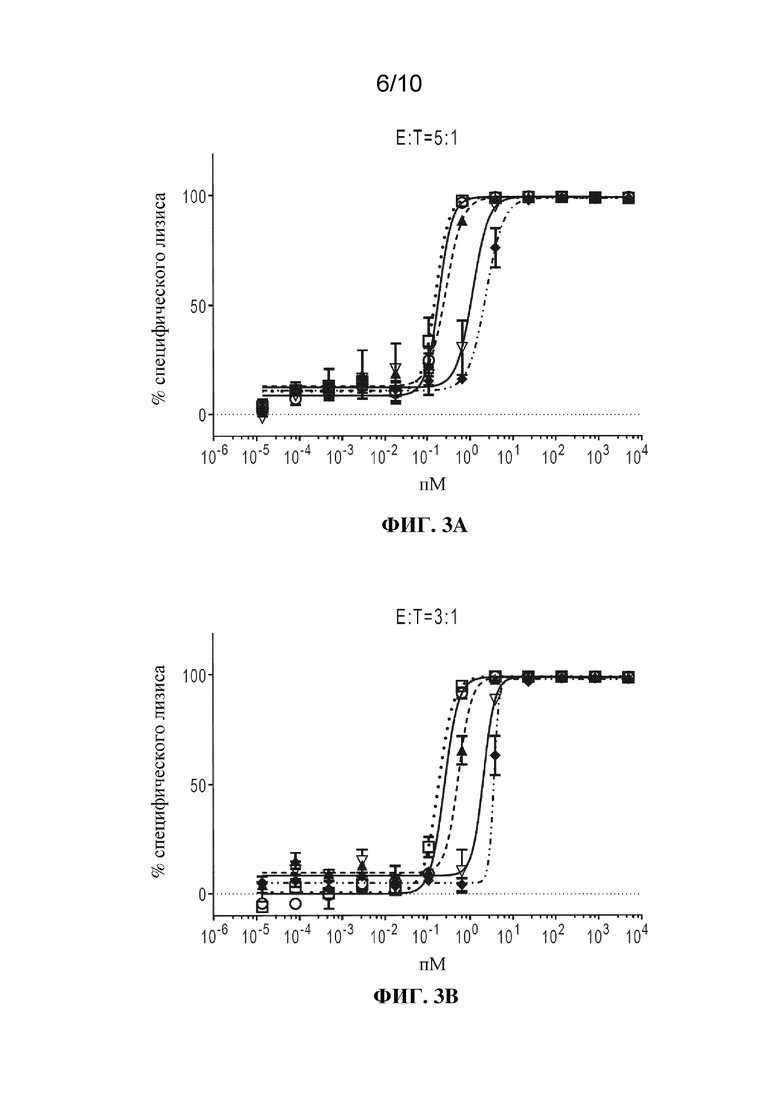
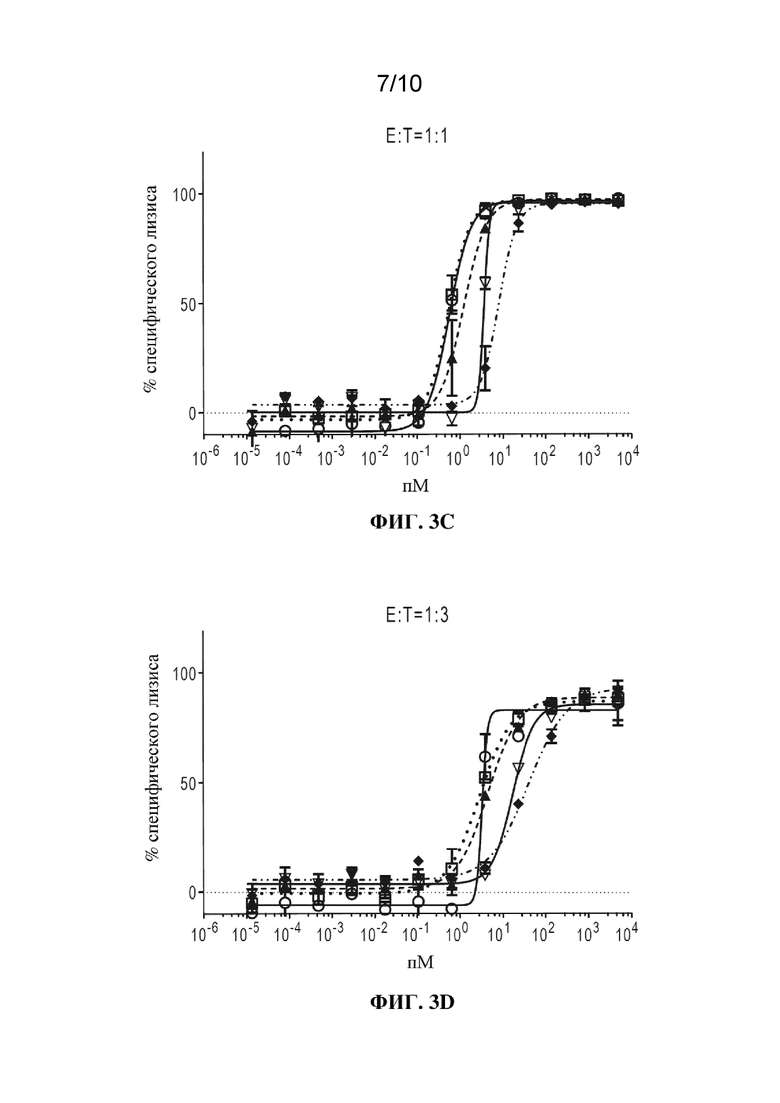
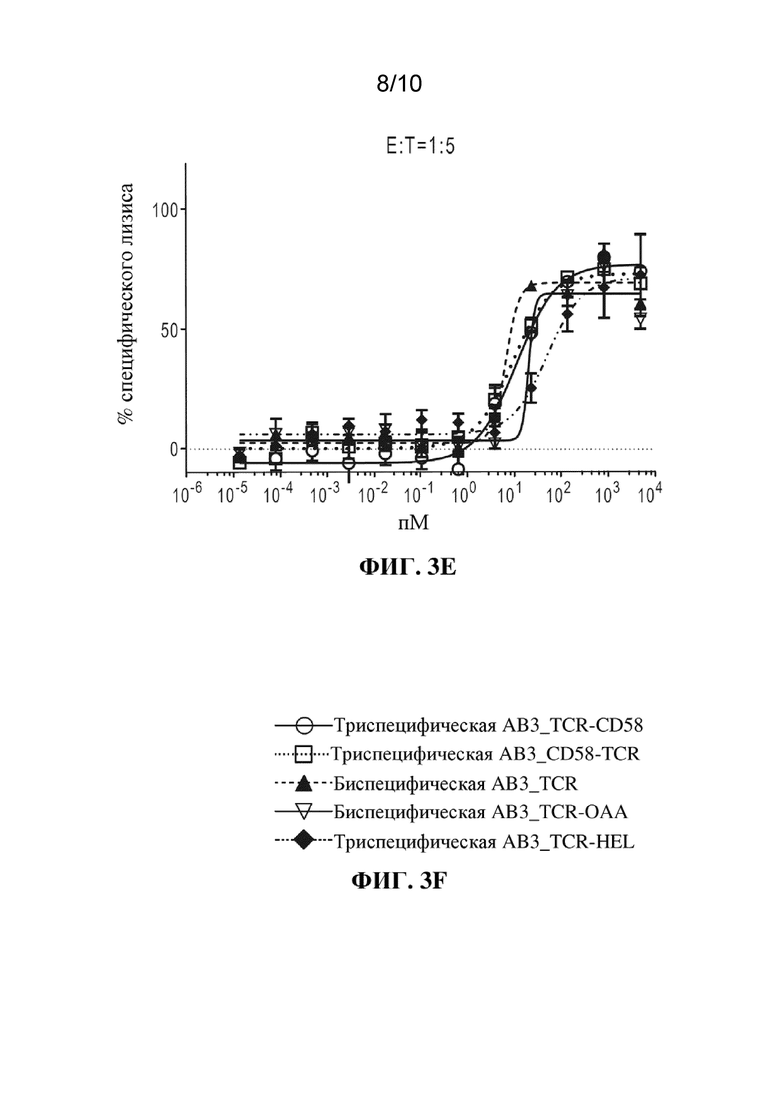
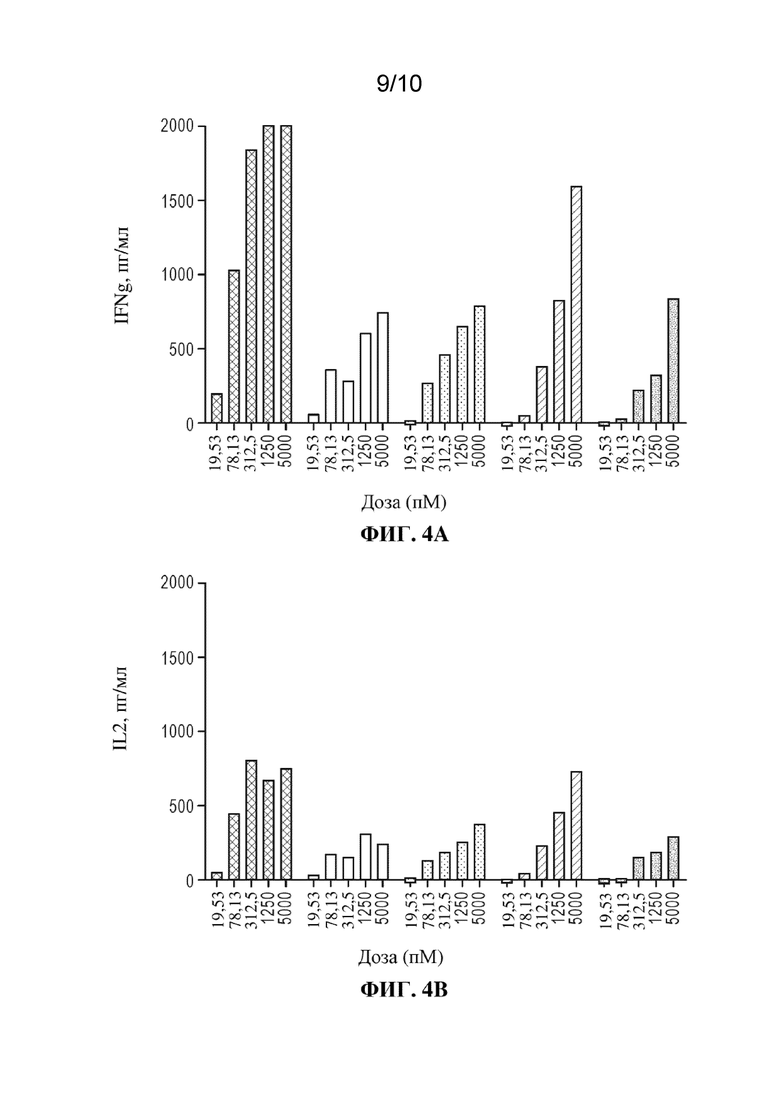
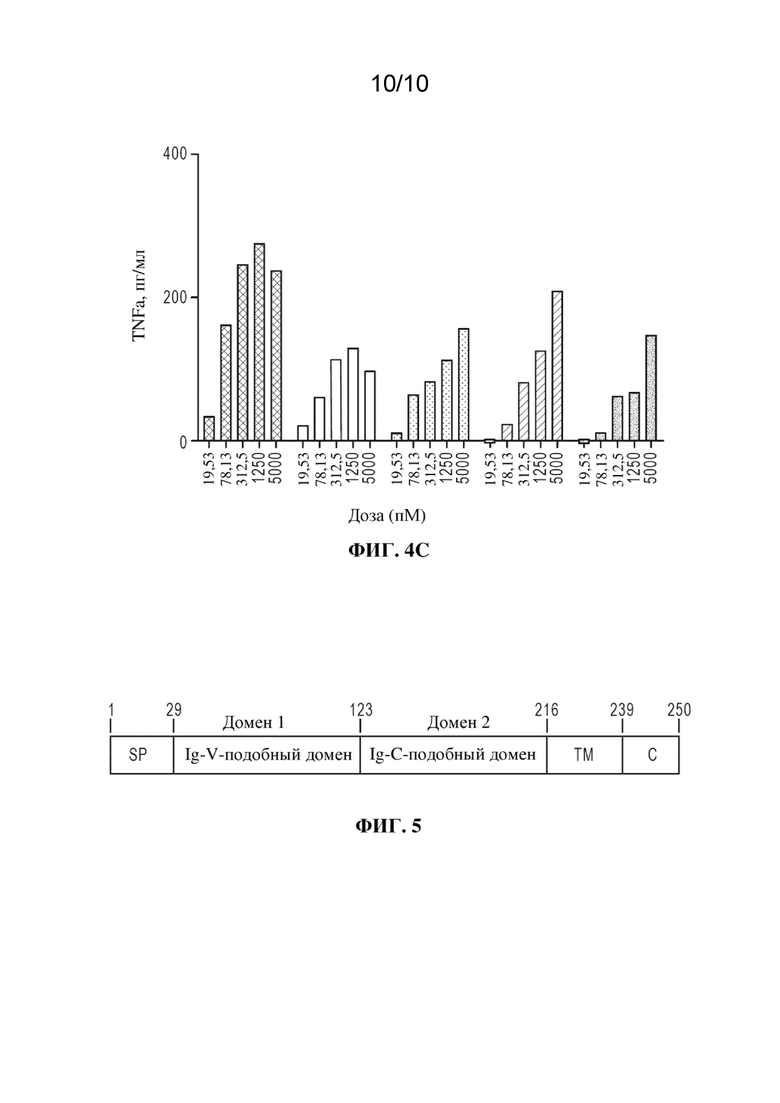
Группа изобретений относится к области биотехнологии. Предложены триспецифические связывающие молекулы (TBM), которые специфично связываются с BCMA, компонентом T-клеточного рецепторного комплекса человека и CD2 либо опухолеассоциированным антигеном. Антигенсвязывающий модуль, который специфично связывается с ВСМА человека, содержит в соответствии с определением Kabat последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в SEQ ID NO: 100, 175 и 183, соответственно, и последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в SEQ ID NO: 112, 185 и 122 соответственно. Дополнительно предложены конъюгаты, содержащие TBM, и фармацевтические композиции, содержащие TBM и конъюгаты, способы применения TBM для лечения заболеваний и нарушений, ассоциированных с экспрессией BCMA, рекомбинантная клетка-хозяин, сконструированная для экспрессии TBM, и способ получения TBM посредством культивирования клетки-хозяина. Изобретения применимы в терапии рака, например, В-клеточных злокачественных новообразований, благодаря нацеливанию на большее количество злокачественных В-клеток, чем с применением биспецифических активаторов, которые нацелены только на BCMA и компонент комплекса TCR. 8 н. и 23 з.п. ф-лы, 5 ил., 23 табл., 4 пр.
1. Триспецифическая связывающая молекула (TBM), содержащая:
(a) антигенсвязывающий модуль 1 (ABM1), который специфично связывается с ВСМА человека и содержит:
(i) в соответствии с определением Kabat, последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в SEQ ID NO: 100, 175 и 183, соответственно, и последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в SEQ ID NO: 112, 185 и 122 соответственно;
(ii) в соответствии с определением Chothia, последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в SEQ ID NO: 101, 105 и 209, соответственно, и последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в SEQ ID NO: 211, 213 и 122 соответственно; или
(iii) в соответствии с определением IMGT, последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в SEQ ID NO: 102, 105 и 183, соответственно, и последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в SEQ ID NO: 235, 238 и 124 соответственно;
(iv) в соответствии с объединенными определениями Kabat и Chothia, последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в SEQ ID NO: 100, 175 и 183, соответственно, и последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в SEQ ID NO: 261, 185 и 122 соответственно;
(v) в соответствии с объединенными определениями Kabat и IMGT, последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в SEQ ID NO: 100, 175 и 183, соответственно, и последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в SEQ ID NO: 261, 185 и 124 соответственно; или
(vi) в соответствии с объединенными определениями Chothia и IMGT, последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в SEQ ID NO: 101, 105 и 183, соответственно, и последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в SEQ ID NO: 235, 238 и 124 соответственно;
(b) антигенсвязывающий модуль 2 (ABM2), который специфично связывается с компонентом T-клеточного рецепторного комплекса (TCR) человека; и
(c) антигенсвязывающий модуль 3 (ABM3), который специфично связывается с CD2 человека или опухолеассоциированным антигеном (TAA) человека.
2. TBM по п. 1, где ABM1 содержит последовательности CDR-L1, CDR-L2 и CDR-L3, представленные в SEQ ID NO: 100, 175 и 183, соответственно, и последовательности CDR-H1, CDR-H2 и CDR-H3, представленные в SEQ ID NO: 112, 185 и 122 соответственно.
3. TBM по п. 1, где ABM1 содержит последовательность вариабельного участка легкой цепи, представленную в SEQ ID NO: 273, и соответствующую последовательность вариабельного участка тяжелой цепи, представленную в SEQ ID NO: 297.
4. TBM по любому из пп. 1-3, где ABM1 представляет собой антитело, фрагмент антитела, scFv, dsFv, Fv, Fab, scFab или (Fab’)2.
5. TBM по п.5, где ABM1 содержит антитело или его антигенсвязывающий домен.
6. TBM по п.5, где ABM1 содержит scFv.
7. TBM по любому из пп. 1-6, где компонент комплекса TCR представляет собой CD3.
8. TBM по любому из пп. 1-7, где компонент комплекса TCR представляет собой TCR-α, TCR-β, димер TCR-α/β, TCR-γ, TCR-δ или димер TCR-γ/δ.
9. TBM по любому из пп. 1-8, где ABM3 специфично связывается с CD2 человека.
10. TBM по п. 9, где ABM3 содержит рецепторсвязывающий домен лиганда CD2.
11. TBM по п. 10, где ABM3 представляет собой фрагмент CD58.
12. TBM по любому из пп. 1-11, где ABM3 специфично связывается с TAA человека.
13. TBM по п. 12, где TAA представляет собой TAA, экспрессирующийся на раковых В-клетках, которые представляют собой плазматические клетки В-клеточного происхождения.
14. TBM по п. 12 или 13, где TAA представляет собой TAA, экспрессирующийся на раковых В-клетках, которые не являются плазматическими клетками.
15. TBM по любому из пп. 12-14, где TAA выбран из группы, состоящей из CD19, CD20, CD22, CD123, CD33, CLL1, CD138, CS1, CD38, CD133, FLT3, CD52, TNFRSF13C, TNFRSF13B, CXCR4, PD-L1, LY9, CD200, FCGR2B, CD21, CD23, CD24, CD40L, CD72, CD79a и CD79b.
16. TBM по любому из пп. 1-15, которая содержит Fc-домен.
17. TBM по п. 16, где Fc-домен представляет собой гетеродимер Fc.
18. TBM по любому из пп. 1-17, которая представляет собой тривалентную, тетравалентную, пентавалентную или гексавалентную TBM.
19. TBM по любому из пп. 1-18, где каждый антигенсвязывающий модуль способен к связыванию своей соответствующей мишени одновременно со связыванием каждого из других антигенсвязывающих модулей со своей соответствующей мишенью.
20. Конъюгат для лечения заболевания или нарушения, ассоциированных с экспрессией BCMA, содержащий TBM по любому из пп. 1-19 и цитотоксическое или цитостатическое средство.
21. Фармацевтическая композиция для лечения заболевания или нарушения, ассоциированных с экспрессией BCMA, содержащая TBM по любому из пп. 1-19 или конъюгат по п. 20 и вспомогательное вещество.
22. Способ лечения субъекта, у которого имеется заболевание или нарушение, ассоциированное с экспрессией BCMA, включающий введение субъекту эффективного количества TBM по любому из пп. 1-19, конъюгата по п. 20 или фармацевтической композиции по п. 21.
23. Способ по п. 22, где заболевание или нарушение включает в себя рак, например, В-клеточное злокачественное новообразование.
24. Способ по п. 23, где В-клеточное злокачественное новообразование выбрано из группы, состоящей из лимфомы Ходжкина, неходжкинской лимфомы и множественной миеломы.
25. Способ по п. 22, где заболевание или нарушение представляют собой аутоиммунное нарушение.
26. Способ по любому из пп. 22-25, дополнительно включающий введение субъекту по меньшей мере одного дополнительного средства.
27. Способ по п. 26, где указанное по меньшей мере одно дополнительное средство содержит ингибитор гамма-секретазы (GSI).
28. Нуклеиновая кислота, кодирующая TBM по любому из пп. 1-19.
29. Совокупность нуклеиновых кислот, кодирующая TBM по любому из пп. 1-19.
30. Клетка для экспрессии TBM по любому из пп. 1-19, трансфицированная одним или более векторами экспрессии, содержащими одну или несколько последовательностей нуклеиновой кислоты, кодирующих TBM по любому из пп. 1-19, под контролем одного или нескольких промоторов.
31. Способ получения TBM, включающий:
(a) культивирование клетки по п.30 в условиях, в которых экспрессируется TBM; и
(b) извлечение TBM из культуры клеток.
| WO 2013072406 A1, 23.05.2013 | |||
| WO 2013072415 A1, 23.05.2013 | |||
| WO 2017165464 A1, 28.09.2017 | |||
| WO 2018201047 A1, 01.11.2018 | |||
| WO 2018201051 A1, 01.11.2018 | |||
| Law C | |||
| L | |||
| et al | |||
| Искусственный двухслойный мельничный жернов | 1921 |
|
SU217A1 |
Авторы
Даты
2024-11-08—Публикация
2020-05-19—Подача