Предпосылки настоящего изобретения
Область техники, к которой относится настоящее изобретение
[0001] Настоящее изобретение относится к применению анестезирующей композиции для устранения боли. Настоящее изобретение относится к способу устранения боли.
Предшествующий уровень техники настоящего изобретения
[0002] Местные анестетики имеют широкое применение для хирургической анестезии и послеоперационной анальгезии из-за их способности обратимо ингибировать потенциалзависимые натриевые каналы и блокировать потенциалы действия в нервных волокнах. Однако при высоких уровнях в плазме такой тип анестетика также взаимодействует с другими ионными каналами, вызывая острую нервную и сердечную токсичность, а также аллергические реакции. Так называемая системная токсичность местных анестетиков (LAST) всегда является потенциальным осложнением всех местных анестетиков и любого пути введения и может быть фатальной.
[0003] Ропивакаин был представлен в 1996 году как местный анестетик амидного типа в виде чистого S (‒) изомера и одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) в 2000 году под торговым названием Naropin®. Он обладает значительно меньшей липофильностью и способностью блокировать моторную функцию и имеет больший запас по безопасности за счет сниженной кардиотоксичности по сравнению с бупивакаином (Marcaine®). Naropin® можно вводить различными инъекционными путями, в том числе спинномозговой анестезией, эпидуральной анестезией, местной блокадой и местной инфильтрацией. Несмотря на наличие многих преимуществ перед другими местными анестетиками, продолжительность обезболивания после однократного введения 0,5% Naropin® (инъекция 200 мг ропивакаина гидрохлорида) посредством инфильтрации в ране составляла всего приблизительно 6-8 часов. Этого недостаточно для охвата значительного периода восстановления после хирургической операции и особенно критичного 3-суточного периода после операции.
[0004] Местные анестетики характеризуются ограниченной продолжительностью действия и риском LAST. Также в качестве послеоперационной схемы купирования боли широко применяют NSAID и инфильтрацию местными анестетиками (например, ропивакаина гидрохлоридом). Однако в отношении применения NSAID существуют некоторые потенциальные проблемы безопасности, а продолжительность послеоперационного обезболивания местными анестетиками обычно ограничивается приблизительно 8 часами. Медицинской целью является облегчение острой послеоперационной боли без применения опиоидов в течение критичного 2-4-суточного периода после операции. Таким образом, существует неудовлетворенная медицинская потребность в создании длительного, неопиоидного, более безопасного и более эффективного способа лечения послеоперационной боли посредством периоперационного введения однократной дозы лекарственного средства.
[0005] При использовании длительных блокад местными анестетиками либо путем непрерывной инфузии, либо путем многократного струйного введения существует высокий риск достижения токсической концентрации в плазме или локального повреждения нервной системы. Факты, подтверждающие нейротоксичность местных анестетиков, были обнаружены в результате анализа стойкости парестезии после инъекции местного анестетизирующего лекарственного средства. Тяжесть парестезии связана с продолжительностью измененных ощущений, хотя в большинстве случаев пораженные нервы будут самопроизвольно восстанавливаться за некоторый период времени, а в некоторых случаях такой нежелательный эффект может продлеваться и сохраняться в течение нескольких месяцев или даже может сделать нерв неспособным к полному восстановлению.
[0006] Следовательно, для создания полезного и эффективного способа устранения боли с требуемым пролонгированным анальгетическим действием существуют неудовлетворенные потребности в улучшенном применении ропивакаина или других анестетиков амидного типа при устранении боли. Композиции и способы по настоящему изобретению удовлетворяют эти и другие потребности.
Краткое раскрытие настоящего изобретения
[0007] Настоящее изобретение относится к способам лечения конкретными диапазонами доз и схемами приема анестетика амидного типа по настоящему изобретению, которые приводят к такому пролонгированному эффекту устранения боли. В частности, настоящее изобретение относится к фармакологически активным средствам, композициям, способам и/или схемам приема, которые обладают определенным преимуществами по сравнению со средствами, композициями, способами и/или схемами приема, которые применяют в настоящее время и/или которые известны из уровня техники, в том числе возможностью менее частого приема дозы или введения более низких доз с получением эквивалентных эффектов в устранении боли или анестезирующих эффектов и, таким образом, уменьшения количеств нежелательных эффектов анестетика амидного типа у нуждающемся в том субъекта. Такие преимущества станут понятны из дальнейшего приведенного ниже описания.
[0008] Настоящее изобретение относится к анестезирующей композиции с замедленным высвобождением или способу ее получения с помощью лиофилизации (например, одностадийной лиофилизации) для получения липидной лепешки, содержащей анестетик амидного типа и по меньшей мере один липид, причем мольное соотношение анестетика амидного типа по меньшей мере к одному липиду в липидном комплексе составляет по меньшей мере 0,5:1, а затем гидратации липидной лепешки фармацевтически приемлемым буферным раствором с получением анестезирующей композиции с замедленным высвобождением. Такая анестезирующая композиция с замедленным высвобождением обеспечивает быстрое начало анестезии и увеличенную продолжительность местной анестезии с минимальной токсичностью.
[0009] Согласно одному аспекту, анестезирующая композиция представляет собой фармацевтическую композицию для применения при лечении послеоперационной боли у нуждающегося в том субъекта. Фармацевтическая композиция в соответствии с настоящим изобретением содержит липидный комплекс анестетика амидного типа и по меньшей мере одного липида, причем мольное соотношение анестетика амидного типа по меньшей мере к одному липиду в липидном комплексе составляет по меньшей мере 0,5:1, а общее количество анестетика амидного типа в фармацевтической композиции по меньшей мере в 1,5-5 раз превышает стандартную терапевтическую дозу анестетика амидного типа. Общее количество анестетика амидного типа в фармацевтической композиции может варьировать в диапазоне от приблизительно 3 мг до приблизительно 1000 мг, от приблизительно 100 мг до приблизительно 800 мг, от приблизительно 200 мг до приблизительно 600 мг, от приблизительно 300 мг до приблизительно 600 мг, от приблизительно 300 мг до приблизительно 500 мг и необязательно составляет приблизительно 380 мг, приблизительно 475 мг, приблизительно 570 мг; или в диапазоне от приблизительно 3 мг до приблизительно 300 мг, от приблизительно 10 мг до приблизительно 250 мг и необязательно составляет приблизительно 50 мг, приблизительно 152 мг, приблизительно 190 мг или приблизительно 228 мг. В соответствии с некоторыми вариантами осуществления, анестетик амидного типа в фармацевтической композиции присутствует в количестве, которое по меньшей мере приблизительно в 1,5, 1,6, 1,7, 1,8, 1,9, 2,0, 2,1, 2,2, 2,3, 2,4, 2,5, 2,6, 2,7, 2,8, 2,9, 3,0, 3,1, 3,2, 3,3, 3,4, 3,5, 3,6, 3,7, 3,8, 3,9, 4,0, 4,1, 4,2, 4,3, 4,4, 4,5, 4,6, 4,7, 4,8, 4,9 до 5 раз превышает стандартную терапевтическую дозу анестетика амидного типа. К другим анестетикам амидного типа, которые можно применять, относятся лидокаин, бупивакаин, мепивакаин, левобупивакаин, их основания или их комбинации. В соответствии с некоторыми вариантами осуществления, анестетик амидного типа представляет собой бупивакаин, ропивакаин или их основание.
[0010] В соответствии с настоящим изобретением, липидный комплекс содержит анестетик амидного типа и один или несколько липидов. В соответствии с некоторыми вариантами осуществления, липиды включают по меньшей мере один нейтральный насыщенный фосфолипид. По меньшей мере один нейтральный насыщенный фосфолипид содержит насыщенные жирные кислоты с длинной углеродной цепью с количеством атомов углерода не более 18. В соответствии с некоторыми вариантами осуществления, липидный комплекс получен в заранее определенных условиях для доклинического применения, например, при температуре окружающей среды, а насыщенные жирные кислоты с длинными углеродными цепями имеют количество атомов углерода, равное 14, 16 и/или 18.
[0011] В соответствии с некоторыми вариантами осуществления, липидный комплекс анестезирующей композиции получают путем гидратации лиофилизированной липидной лепешки фармацевтически приемлемым буферным раствором с pH выше 5,5. Теоретически незаряженный ропивакаин составляет 0,8% от доступного ропивакаина при pH 6,0, исходя из расчета его pKa (pKa ропивакаина составляет 8,1). В соответствии с некоторыми вариантами осуществления, липидную лепешку по настоящему изобретению получают путем растворения аполярного ропивакаина, фосфолипида и холестерина в системе растворителей, например, в одном трет-бутаноле или в совместном растворителе трет-бутанол/вода, с последующим удалением системы растворителей с помощью методики лиофилизации.
[0012] В соответствии с определенными вариантами осуществления, мольное соотношение анестетика амидного типа к фосфолипиду (мольлекарственного средства:мольфосфолипида) в липидном комплексе составляет по меньшей мере 0,5:1. Настоящая фармацевтическая композиция может обеспечивать достаточное количество анестетика амидного типа нуждающемуся в том субъекту для того, чтобы продлить продолжительность анестезии после местного введения in vivo. Кроме того, заранее определенное количество анестетика амидного типа в его свободной форме, не захватываемое липидным комплексом, может обеспечить быстрое начало анестезии с минимальным воздействием максимальной концентрации в плазме (Cmax).
[0013] Согласно другому аспекту, настоящее изобретение также относится к способам лечения послеоперационной боли у нуждающегося в анестезии субъекта. Способ может предусматривать введение фармацевтической композиции по настоящему изобретению посредством блокады нерва, посредством местной анестезии или посредством инфильтрационной анестезии.
[0014] В соответствии с конкретными вариантами осуществления, послеоперационная боль вызвана хирургическим вмешательством, таким как без ограничения хирургическая операция по пластике грыжи, хирургическая операция по бурсэктомии, хирургическая операция на мочеполовой системе, ортопедическая хирургическая операция, акушерская хирургическая операция, лапароскопическая хирургическая операция, абдоминопластика, хирургическая операция на молочных железах и процедура трансплантации почки (KTX).
[0015] Согласно еще одному аспекту, настоящее изобретение относится к способам лечения послеоперационной боли. Способ может предусматривать введение дозы фармацевтической композиции по настоящему изобретению за период, составляющий от приблизительно получаса (30 минут) до приблизительно трех часов, необязательно от получаса (30 минут) до приблизительно двух часов и необязательно от получаса до приблизительно одного часа, до хирургической операции или после начала хирургической операции (во время хирургической операции) и, в частности, до завершения хирургической операции, причем уменьшение боли составляет по меньшей мере приблизительно 2 в соответствии с оценкой по числовой шкале оценки боли (NPRS) в течение периода после хирургической операции, причем период составляет по меньшей мере 48 часов, необязательно по меньшей мере 72 часа, по меньшей мере 96 часов или по меньшей мере 168 часов. NPRS может иметь шкалу от 0 до 10, где 0 означает отсутствие боли, а 10 означает наихудшую боль, которую только можно представить. В соответствии с некоторыми вариантами осуществления, при введении композиции по настоящему изобретению посредством блокады нерва или местной анестезии композицию можно вводить за период, составляющий от приблизительно получаса до приблизительно одного часа, до операции. В соответствии с другими неограничивающими вариантами осуществления, при введении композиции по настоящему изобретению посредством местной инфильтрации, которая подходит для хирургической операции по пластике грыжи и хирургической операции по бурсэктомии, композицию можно вводить во время хирургической операции, обычно на последних стадиях хирургической операции перед окончательным закрытием разреза.
[0016] Другие цели, преимущества и новые признаки настоящего изобретения станут более очевидными из последующего подробного описания при рассмотрении в сочетании с прилагаемыми чертежами.
Краткое описание чертежей
[0017] На фиг. 1 проиллюстрирована схема клинического испытания анестезирующей композиции по настоящему изобретению для лечения послеоперационной боли после хирургической операции по пластике грыжи;
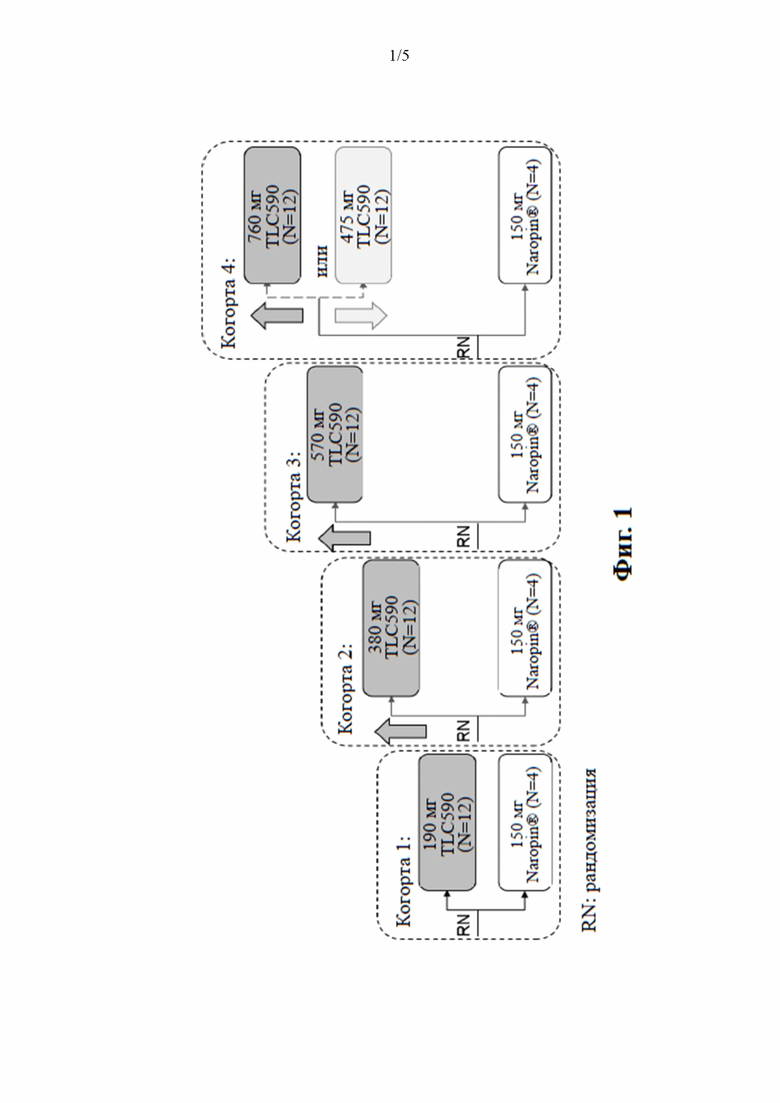
[0018] на фиг. 1A проиллюстрирована диаграмма сравнения максимальной концентрации ропивакаина в плазме крови после лечения послеоперационной боли анестезирующей композицией по настоящему изобретению с различными указанными вводимыми количествами;
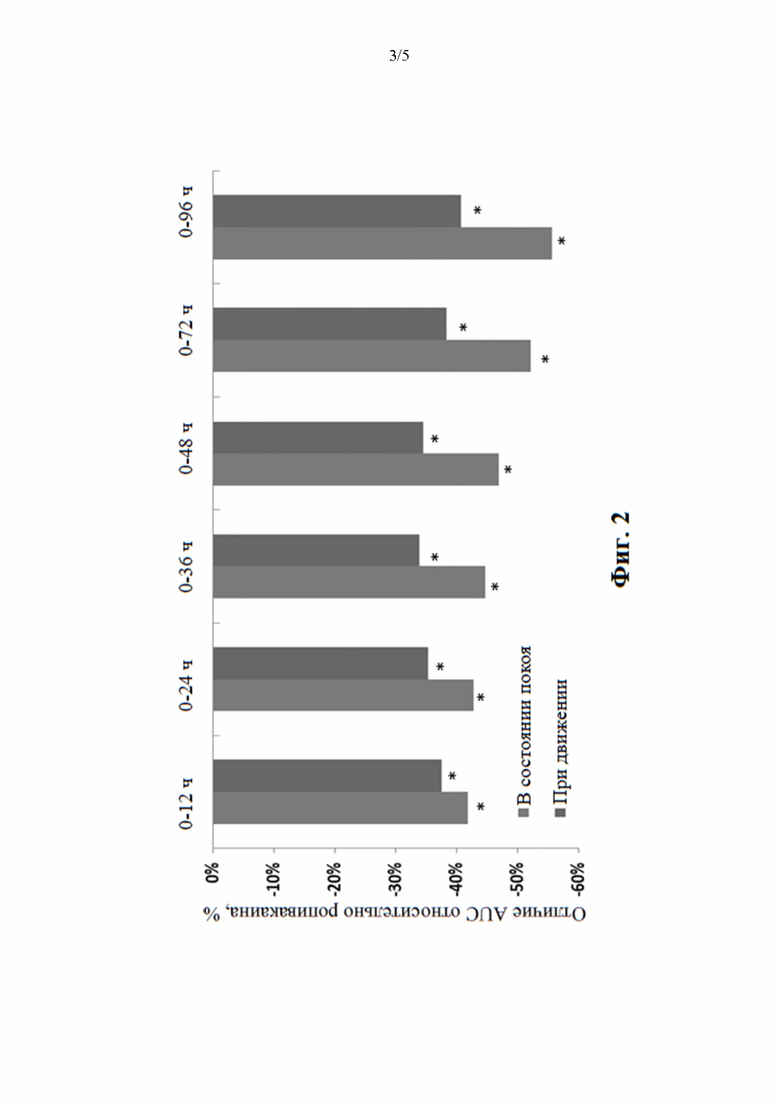
[0019] на фиг. 2 проиллюстрированы результаты клинического испытания анестезирующей композиции по настоящему изобретению, где AUC = площадь под кривой зависимости боли от времени; LS = метод наименьших квадратов; NPRS = числовая шкала оценки боли; LS означает модель дисперсионного анализа, включающая AUC для NPRS в качестве ответа и группу лечения в качестве фиксированного основного эффекта; NPRS скорректирована с учетом применения экстренных лекарственных препаратов с использованием взвешенного переноса вперед наихудших результатов наблюдения (wWOCF); *p<0,05 по сравнению с ропивакаином;
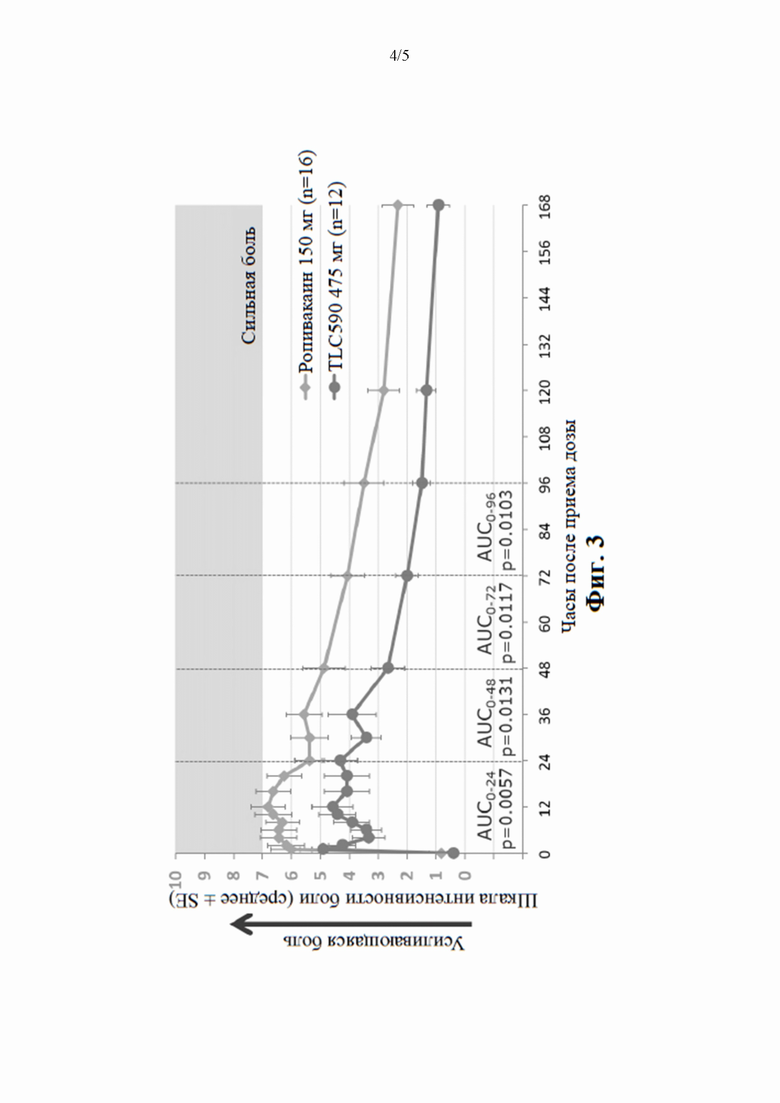
[0020] на фиг. 3 проиллюстрировано полученное методом LS среднее (SE) боли при движении для анестезирующей композиции по настоящему изобретению при дозе 475 мг по сравнению с ропивакаином, где LOCF (перенос вперед последнего наблюдения) относится к отсутствующим данным; а wWOCF (взвешенный перенос вперед наихудших результатов наблюдения) — для экстренного лекарственного препарата; и
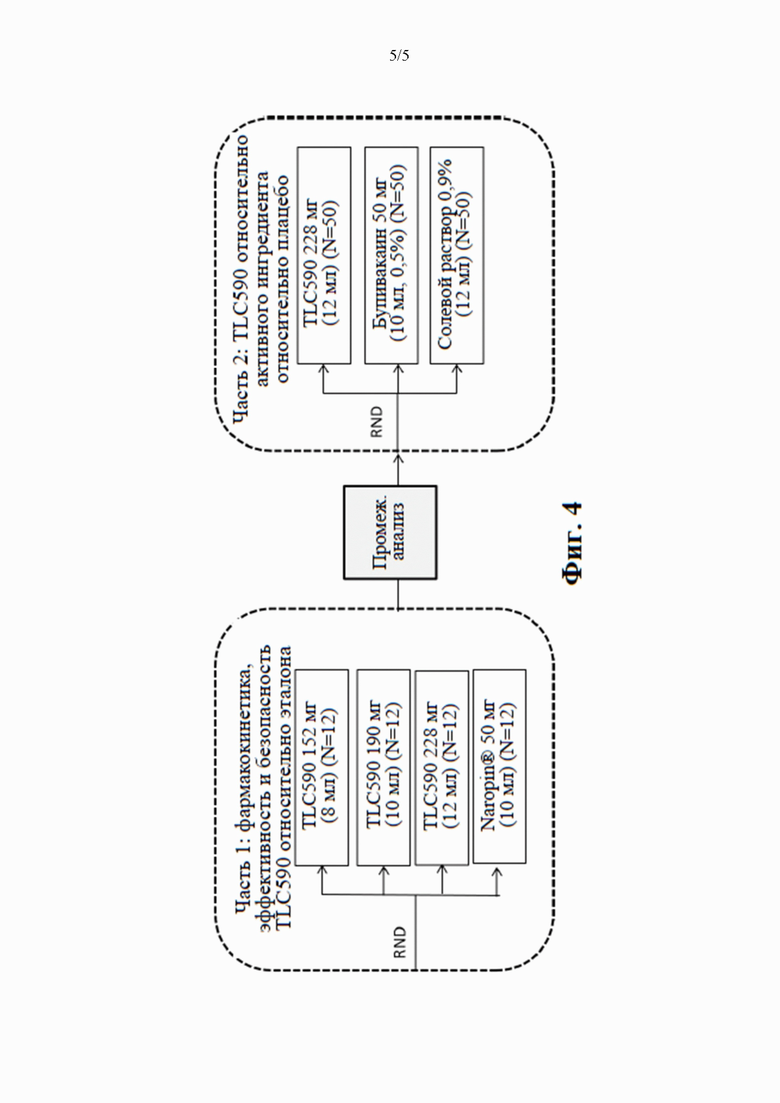
[0021] на фиг. 4 проиллюстрирована схема клинического испытания анестезирующей композиции по настоящему изобретению для лечения послеоперационной боли после хирургической операции по бурсэктомии.
Подробное раскрытие настоящего изобретения
[0022] При использовании выше и во всем настоящем раскрытии представленные далее термины, если не указано иное, следует понимать как имеющие описываемые далее значения.
[0023] Применяемые в настоящем документе формы единственного числа включают отсылку к формам во множественном числе, если контекст явно не указывает на иное.
[0024] Все числа в настоящем документе можно понимать как модифицированные словом «приблизительно», которое, если речь идет об измеряемой величине, такой как количество, временная продолжительность и др., понимают как охватывающее отклонения на ±10%, предпочтительно ±5%, предпочтительно ±1% и еще более предпочтительно ±0,1% от указанного значения, поскольку такие отклонения подходят для получения требуемого количества анестетика амидного типа, если не указано иное.
[0025] Применяемые в настоящем документе термины «осуществлять лечение», «подвергать лечению» или «лечение» включают превентивные (например, профилактические), паллиативные и лечебные способы, применения или результаты. Термины «средство лечения» или «средства лечения» также могут относиться к композициям или лекарственным препаратам. В настоящей заявке под «лечением» подразумевают способ уменьшения или отсрочки появления одного или нескольких симптомов или признаков боли, облегчения боли по результатам обнаружения с помощью известных в настоящей области техники методик, или сокращения применения обезболивающих препаратов. Для оценки боли и ее симптомов доступны признанные в настоящей области техники способы. К ним относятся без ограничения 6-балльная описательная шкала оценки боли, 11-балльная шкала NPRS, визуальная аналоговая шкала, висконсинский краткий опросник оценки боли, краткий опросник оценки боли, опросник оценки боли МакГилла и краткая форма опросника оценки боли МакГилла, а также другие способы оценки, в том числе общая оценка пациентом (PGA) способа устранения боли. Для субъекта-человека для определения уровня боли можно применять самооценку, например, с использованием градуированной шкалы от (0) отсутствия боли до (10) максимальной боли. Необязательно, для выявления уменьшения боли после введения фармацевтической композиции по настоящему изобретению на субъекте можно применять функциональную магнитно-резонансную томографию (fMRI). Например, раскрываемый способ считают лечением, если имеет место уменьшение по меньшей мере на 1% у одного или нескольких симптомов боли у субъекта по сравнению с субъектом до лечения или одним или несколькими контрольными субъектами. Так, уменьшение может составлять 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% или любую промежуточную величину уменьшения между данными значениями. Лечение субъекта можно также оценить по сокращению применения обезболивающих препаратов, таких как опиоиды или другие анальгетики, и/или уменьшению побочных эффектов, связанных с такими анальгетиками, таких как желудочно-кишечные симптомы, связанные с применением опиоидов. Для оценки боли и восстановления, а также побочных эффектов, которые могут быть связаны с применением опиоидов, можно использовать дополнительные опросники по оценке эффективности, такие как индекс послеоперационного восстановления. В частности, послеоперационная боль может быть острой болью и/или хронической болью. Острая боль может иметь место непосредственно сразу или в течение до 7 суток (например, приблизительно 1 сутки, 2 суток, 3 суток, 4 суток, 5 суток, 6 суток или 7 суток) после хирургической операции.
[0026] Термин «субъект» может относиться к позвоночному животному, страдающему болью или имеющему риск развития боли или болезней, приводящих к боли, или к позвоночному животному, которое, как считается, нуждается в лечении или купировании боли. К субъектам относятся все теплокровные животные, такие как млекопитающие, в том числе примат и, более предпочтительно, человек. Субъектами также являются отличные от человека приматы. Термин «субъект» включает домашних животных, таких как кошки, собаки и т. д., домашний скот (например, крупный рогатый скот, лошадей, свиней, овец, коз и т. д.) и лабораторных животных (например, мышь, кролика, крысу, песчанку, морскую свинку и т. д.). Таким образом, в настоящем документе предусмотрены ветеринарные применения и медицинские составы.
[0027] «Эффективность ассоциации» (AE) представляет собой количество лекарственного средства, заключенного в липидном комплексе, и рассчитывается как соотношение количества лекарственного средства в отделенном липидном комплексе к общему количеству лекарственного средства в исходной композиции до разделения. Отделенные липидные комплексы можно получить любым известным из уровня техники способом. В соответствии с некоторыми вариантами осуществления, отделенные липидные комплексы получают способами центрифугирования, например, традиционным центрифугированием, центрифугированием в градиенте плотности, дифференциальным центрифугированием, или способами фильтрации, например, диафильтрацией, гель-фильтрацией и мембранной фильтрацией.
[0028] Термин «стандартная терапевтическая доза» может относиться к количеству указанного терапевтического средства для получения требуемого эффекта или результата, в частности, к категории, подобной настоящему изобретению, что проиллюстрировано путем уравновешивания лекарственного средства с плохо поддающимися перфузии тканями, такими как мягкая ткань, мышца и жировая и тому подобное; и твердая ткань, костная и тому подобное. Рядовой специалист в настоящей области техники сможет определить стандартные терапевтические дозы. Подходящая стандартная терапевтическая доза для каждого показания может обозначать отсылки к соответствующим анестетикам, в том числе без ограничения к Фармакопее США (USP) и одобренным лекарственным продуктам, перечисленным в библиотеке Drugs@FDA, спонсируемой Управлением по санитарному надзору за качеством пищевых продуктов и лекарственных препаратов США. Терапевтическую дозу можно ввести в операционное поле с помощью инфильтрации или инъекции. Например, стандартная терапевтическая доза раствора ропивакаина HCl (Naropin®) для инъекции с целью купирования боли после хирургической операции по пластике грыжи путем местной инфильтрации составляет менее 300 мг, в частности от 2 мг до 200 мг. В соответствии с одним вариантом осуществления, стандартная терапевтическая доза раствора свободного ропивакаина для инъекции или инфильтрации с целью лечения боли после хирургической операции по бурсэктомии составляет 50 мг. В соответствии с другим вариантом осуществления, стандартная терапевтическая доза для инъекции бупивакаина гидрохлорида USP (от Hospira) составляет до 225 мг с эпинефрином 1:200000 и 175 мг без эпинефрина. Стандартные терапевтические дозы можно определить, исходя из типа хирургической операции, и их сможет определить любой специалист в настоящей области техники.
Анестетики амидного типа
[0029] Термин «анестетики амидного типа» относится к одной или нескольким группам веществ, вызывающих потерю чувствительности в ограниченной области субъекта, вызванную подавлением возбуждения в нервных окончаниях или ингибированием процесса проводимости в периферических нервах. Типичная структура анестетика амидного типа содержит липофильную часть и гидрофильную часть, которые соединяются связью —NHCO—. К подходящим анестетикам амидного типа относятся без ограничения лидокаин, бупивакаин, левобупивакаин, ропивакаин, мепивакаин, пиррокаин, артикаин и прилокаин и их свободные основания. В соответствии с определенными вариантами осуществления, анестетик амидного типа представляет собой ропивакаиновое основание.
Липидный комплекс и липиды
[0030] Липидный комплекс в соответствии с настоящим изобретением содержит один или несколько липидов и анестетик амидного типа. В соответствии с одним вариантом осуществления, липидный комплекс можно производить и хранить в течение длительного времени, что продлевает срок годности композиции. Липидный комплекс можно получить непосредственно перед клиническим применением путем гидратации липидной лепешки, содержащей один или несколько липидов и анестетик амидного типа.
[0031] Описанная выше липидная лепешка может содержать один или несколько фосфолипидов и анестетик амидного типа при отсутствии стеринов. Альтернативно, липидная лепешка может содержать анестетик амидного типа и один или несколько фосфолипидов с содержанием не более 50% одного или нескольких стеринов, например, холестерина, по отношению к количеству общих липидов. В соответствии с определенными
вариантами осуществления мольная концентрация холестерина в пересчете на общие липиды составляет от приблизительно 0% до 50% и, необязательно, от приблизительно 33% до 40%. В соответствии с некоторыми вариантами осуществления, мольное соотношение фосфолипида(-ов) и холестерина составляет от 1:1 до 3:1.
[0032] Липидную лепешку можно получить путем 1) растворения одного или нескольких липидов и анестетиков амидного типа в системе растворителей с получением жидкой структуры, содержащей один или несколько растворителей, с получением гомогенного раствора и 2) удаления растворителя(-ей) до отверждения состава с липидами и анестетиком(-ами) амидного типа. Удаление растворителя можно осуществить с помощью известных методик, таких как сублимационная сушка (лиофилизация). Примеры систем растворителей, подходящих для сублимационной сушки, включают без ограничения системы совместных растворителей трет-бутанол и трет-бутанол/вода с другими неводными растворителями, такими как ацетон, ацетонитрил, этанол, н-пропанол, изопропанол, н-бутанол, метанол, дихлорметан, диметилсульфоксид и четыреххлористый углерод, или без них.
[0033] В соответствии с некоторыми вариантами осуществления, липиды в липидном комплексе включают один или несколько фосфолипидов и холестерин, а мольное соотношение анестетика амидного типа к фосфолипидам в липидном комплексе составляет по меньшей мере 0,5:1 и, необязательно, от 0,5:1 до 2:1, такое как приблизительно 0,5:1, приблизительно 0,8:1, приблизительно 1:1, приблизительно 1,2:1, приблизительно 1,5:1, приблизительно 1,8:1 или приблизительно 2:1.
[0034] Один или несколько липидов выбраны из группы, состоящей из липидов с диалифатической цепью, таких как фосфолипиды, диглицериды, диалифатические гликолипиды; одиночных липидов, таких как сфингомиелин и гликосфинголипид; стеринов, таких как холестерин и его производные; и их комбинаций. Примеры фосфолипидов в соответствии с настоящим изобретением включают без ограничения 1,2-дилауроил-sn-глицеро-3-фосфохолин (DLPC), 1,2-димиристоил-sn-глицеро-3-фосфохолин (DMPC), 1,2-дипальмитоил-sn-глицеро-3-фосфохолин (DPPC), 1-пальмитоил-2-стеароил-sn-глицеро-3-фосфохолин (PSPC), 1-пальмитоил-2-олеоил-sn-глицеро-3-фосфатидилхолин (POPC), 1,2-дистеароил-sn-глицеро-3-фосфохолин (DSPC), 1,2-диолеоил-sn-глицеро-3-фосфохолин (DOPC), гидрогенезированный соевый фосфатидилхолин (HSPC), 1,2-димиристоил-sn-глицеро-3-фосфо-(1’-рац-глицерин) (натриевую соль) (DMPG), 1,2-дипальмитоил-sn-глицеро-3-фосфо-(1’-рац-глицерин) (натриевую соль) (DPPG), 1-пальмитоил-2-стеароил-sn-глицеро-3-фосфо-(1’-рац-глицерин) (натриевую соль) (PSPG), 1,2-дистеароил-sn-глицеро-3-фосфо-(1’-рац-глицерин) (натриевую соль) (DSPG), 1,2-диолеоил-sn-глицеро-3-фосфо-(1’-рац-глицерин) (DOPG), 1,2-димиристоил-sn-глицеро-3-фосфо-L-серин (натриевую соль) (DMPS), 1,2-дипальмитоил-sn-глицеро-3-фосфо-L-серин (натриевую соль) (DPPS), 1,2-дистеароил-sn-глицеро-3-фосфо-L-серин (натриевую соль) (DSPS), 1,2-диолеоил-sn-глицеро-3-фосфо-L-серин (DOPS), 1,2-димиристоил-sn-глицеро-3-фосфат (натриевую соль) (DMPA), 1,2-дипальмитоил-sn-глицеро-3-фосфат (натриевую соль) (DPPA), 1,2-дистеароил-sn-глицеро-3-фосфат (натриевую соль) (DSPA), 1,2-диолеоил-sn-глицеро-3-фосфат (натриевую соль) (DOPA), 1,2-дипальмитоил-sn-глицеро-3-фосфоэтаноламин (DPPE), 1-пальмитоил-2-олеоил-sn-глицеро-3-фосфоэтаноламин (POPE), 1,2-дистеароил-sn-глицеро-3-фосфоэтаноламин (DSPE), 1,2-диолеоил-sn-глицеро-3-фосфоэтаноламин (DOPE), 1,2-дипальмитоил-sn-глицеро-3-фосфо-(1’-миоинозитол) (аммониевую соль) (DPPI), 1,2-дистеароил-sn-глицеро-3-фосфоинозитол (аммониевую соль) (DSPI), 1,2-диолеоил-sn-глицеро-3-фосфо-(1’-миоинозитол) (аммониевую соль) (DOPI), кардиолипин, L-α-фосфатидилхолин (EPC) и L-α-фосфатидилэтаноламин (EPE).
[0035] Примеры фосфолипидов включают без ограничения димиристоилфосфатидилхолин (DMPC), 1,2-дилауроил-sn-глицеро-3-фосфохолин (DLPC), дипальмитоилфосфатидилхолин (DPPC), диолелдиофосфатидилглицерин (DOPG), 1,2-диолеоил-sn-глицеро-3-фосфатидилхолин (DOPC), 1,2-диолеоил-sn-глицеро-3-фосфатидилсерин (DOPS), диолеоилфосфатидную кислоту (DOPA), яичный фосфатидилхолин (яичный PC), фосфатидилэтаноламин (яичный PE), 1-пальмитоил-2-олеоил-sn-глицеро-3-фосфатидилэтаноламин (POPE), кардиолипин и 1,2-димиристоил-sn-глицеро-3-фосфат (натриевую соль) (DMPA).
[0036] Подходящими фосфолипидами в соответствии с настоящим изобретением являются насыщенные фосфолипиды, производные двух насыщенных жирных кислот с длинной углеродной цепью, причем каждая жирная кислота имеет длинную углеродную цепь по меньшей мере из 12 атомов углерода, альтернативно, по меньшей мере из 14 атомов углерода; и не более чем из 20 атомов углерода, альтернативно, из 18 атомов углерода или из 16 атомов углерода. В соответствии с некоторыми вариантами осуществления, подходящие насыщенные фосфолипиды согласно настоящему изобретению выбраны из группы, состоящей из DLPC, DMPC, DPPC и их комбинаций.
[0037] В соответствии с некоторыми вариантами осуществления, липидный комплекс содержит липосомы и анестетик амидного типа. Липосома содержит один или несколько липидов, включая подходящие фосфолипиды согласно настоящему изобретению, положительно или отрицательно заряженный фосфолипид и определенное количество ненасыщенного фосфолипида, причем определенное количество составляет менее 10% мольных процентов от общего количества фосфолипидов, например, приблизительно 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1%.
Анестезирующая композиция
[0038] Термины «анестезирующая композиция» и «фармацевтическая композиция для применения при лечении боли» применяют как взаимозаменяемые. В соответствии с определенными вариантами осуществления, анестезирующая композиция содержит липидный комплекс и незахваченное местное анестезирующее средство. В соответствии с некоторыми вариантами осуществления, липидный комплекс включает многослойные везикулы и местное анестезирующее средство, заключенное в многослойных везикулах. Термин «заключать» или «заключение» относится к двухслойной мембране из многослойных везикул, инкапсулирующих, включающих целевое лекарственное вещество или связанных с целевым лекарственным веществом.
[0039] Распределение по размеру частиц липидного комплекса согласно настоящему изобретению можно определить с помощью различных известных из уровня техники способов. В соответствии с некоторыми вариантами осуществления, средний размер частиц липидного комплекса анестезирующей композиции составляет не менее 1 мкм; и, необязательно, составляет более 5 мкм, например, в диапазоне от 5 мкм до 50 мкм или от 10 мкм до 25 мкм. В качестве альтернативы, объемный медианный диаметр частиц (D50) липидного комплекса анестезирующей композиции составляет не менее 1 мкм; и, необязательно, составляет не менее 5 мкм, например, в диапазоне от 5 мкм до 50 мкм, от 5 мкм до 40 мкм, от 5 мкм до 30 мкм, от 5 мкм до 20 мкм или от 5 мкм до 15 мкм. В соответствии с некоторыми вариантами осуществления, медианный диаметр частиц (D50) относится к диаметру частиц, при котором совокупный процент липидного комплекса, состоящего из агломерированных частиц, составляет 50% в совокупном распределении размера частиц, при этом данный диаметр составляет 5 мкм или более или 7 мкм или более. В соответствии с некоторыми вариантами осуществления, медианный диаметр частиц (D50) относится к диаметру частиц, при котором совокупный процент липидного комплекса, состоящего из агломерированных частиц, составляет 50% в совокупном распределении размера частиц, при этом данный диаметр составляет 25 мкм или меньше, 20 мкм или меньше или 15 мкм или меньше; и, необязательно, от 5 мкм до 25 мкм, от 5 мкм до 20 мкм или от 5 мкм до 15 мкм.
[0040] В соответствии с некоторыми вариантами осуществления, диаметр частиц при совокупном проценте 90% в совокупном распределении размеров частиц (D90) липидного комплекса анестезирующей композиции составляет не менее 10 мкм, например, в диапазоне от 10 мкм до 300 мкм, от 20 мкм до 300 мкм, от 20 мкм до 200 мкм или от 20 мкм до 100 мкм. Кроме того, нижнее предельное значение D90 составляет, например, без ограничения 25 мкм или более или 30 мкм или более. Кроме того, для повышения эффективности ассоциации на однократную дозу нет особых ограничений для формы агломерированной частицы в липидном комплексе.
[0041] В соответствии с некоторыми вариантами осуществления, фармацевтическая композиция для применения при лечении боли содержит многослойные везикулы, порцию анестетика амидного типа, заключенную в многослойные везикулы, а также порцию анестетика амидного типа в его свободной форме, которую также называют анестетиком амидного типа в свободной форме (незахваченный). Распределение частиц многослойных везикул по размеру вместе с захваченным анестетиком амидного типа в липидном комплексе согласно настоящему изобретению можно определить с помощью различных известных из уровня техники способов. В соответствии с некоторыми вариантами осуществления, размер частиц многослойных везикул вместе с захваченным анестетиком амидного типа в анестезирующей композиции согласно настоящему изобретению составляет не менее 1 мкм; и, необязательно, составляет более 5 мкм, например, в диапазоне от 5 мкм до 200 мкм, от 10 мкм до 100 мкм или от 10 мкм до 50 мкм. Альтернативно, медианный диаметр (D50) липидного комплекса в анестезирующей композиции согласно настоящему изобретению составляет не менее 1 мкм; и, необязательно, составляет более 5 мкм, например, в диапазоне от 5 мкм до 100 мкм или от 10 мкм до 50 мкм.
[0042] В соответствии с некоторыми вариантами осуществления, липидный комплекс получают путем гидратации липидной лепешки, содержащей анестетик амидного типа, фармацевтически приемлемым буферным раствором с pH выше 5,5. Полученная таким образом анестезирующая композиция может обеспечивать замедленное высвобождение анестетика амидного типа, готового к применению или с последующим разведением водным буферным раствором или другим подходящим разбавителем перед введением. В соответствии с некоторыми вариантами осуществления, водный буферный раствор имеет диапазон pH от 5,5 до 8,0 и, необязательно, от 6,0 до 7,5 или от 6,5 до 7,0.
[0043] К подходящим водным буферным растворам согласно настоящему изобретению относятся без ограничения растворы цитрата, ацетата, малата, пиперазина, сукцината, 2-(N-морфолино)этансульфоновой кислоты (MES), гистидина, бис-триса, фосфата, этаноламина, N-(2-ацетамидо)иминодиуксусной кислоты (ADA), карбоната, N-(2-ацетамидо)-2-аминоэтансульфоновой кислоты (ACES), 1,4-пиперазиндиэтансульфоновой кислоты (PIPES), 3-морфолино-2-гидроксипропансульфоновой кислоты (MOPSO), имидазола, N,N-бис(2-гидроксиэтил)-2-аминоэтансульфоновой кислоты (BES), 4-(2-гидроксиэтил)пиперазин-1-этансульфоновой кислоты (HEPES), триэтаноламина, лизина, триса и глицилглицина. Количество незахваченного анестетика амидного типа в композиции можно корректировать на основе коэффициента распределения анестетика путем подбора подходящего значения pH для водного буферного раствора на основе клинических показаний и общей дозы инъекции.
[0044] В соответствии с некоторыми вариантами осуществления, водный буферный раствор содержит гистидин в концентрации, варьирующей в диапазоне от 1 мМ до 200 мМ, от 10 мМ до 150 мМ, от 20 мМ до 140 мМ, от 30 мМ до 130 мМ или от 40 мМ до 120 мМ.
[0045] В соответствии с некоторыми вариантами осуществления, водный буферный раствор содержит фосфат в концентрации, варьирующей в диапазоне от 1 мМ до 200 мМ, от 10 мМ до 180 мМ, от 10 мМ до 170 мМ, от 10 мМ до 160 мМ, от 10 до 150 мМ, от 10 мМ до 100 мМ, от 10 мМ до 75 мМ, от 15 мМ до 75 мМ, от 15 мМ до 50 мМ или от 20 мМ до 50 мМ.
[0046] Количество анестетика амидного типа в свободной форме характеризуется зависимостью от эффективности ассоциации (AE) липидного комплекса анестезирующей композиции, которую определяют с помощью способа центрифугирования. Математически количество анестетика амидного типа в свободной форме имеет следующее выражение:
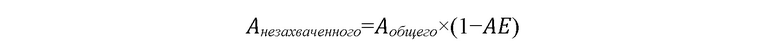
где Анезахваченного это количество незахваченного анестетика амидного типа; Аобщего представляет собой общее количество анестетика амидного типа в анестезирующей композиции; и AE получают путем деления количества анестетика амидного типа в липидном комплексе на общее количество анестетика амидного типа в анестезирующей композиции. AE в соответствии с настоящим изобретением составляет по меньшей мере 60% и, необязательно, от 60% до 99%, от 70% до 95% и от 80% до 90%.
[0047] В соответствии с определенными вариантами осуществления, мольное соотношение анестетика амидного типа к липиду(-ам) (мольлекарственного средства:мольлипида, D:PL) в липидном комплексе составляет по меньшей мере 0,5:1, в том числе без ограничения 0,7:1, 0,9:1, 1,2:1, 1,4:1 или 2:1. В соответствии с определенными вариантами осуществления, медианный диаметр (D50) совокупности частиц в липидном комплексе составляет не менее 1 мкм, например, не менее 5 мкм; и необязательно, в диапазоне от 5 мкм до 200 мкм, от 5 мкм до 190 мкм, от 5 мкм до 180 мкм, от 5 мкм до 170 мкм, от 5 мкм до 160 мкм, от 5 мкм до 150 мкм, от 5 мкм до 140 мкм, от 5 мкм до 130 мкм, от 5 мкм до 120 мкм, от 5 мкм до 110 мкм, от 5 мкм до 100 мкм, от 10 мкм до 100 мкм, от 12 мкм до 100 мкм, от 14 мкм до 100 мкм, от 16 мкм до 100 мкм, от 18 мкм до 100 мкм или от 20 мкм до 100 мкм.
[0048] Для достижения клинического терапевтического эффекта концентрация анестетика амидного типа в анестезирующей композиции может превышать 2 мг/мл. Подходящие концентрации анестетика амидного типа включают без ограничения по меньшей мере 10 мг/мл, в диапазоне от 2 мг/мл до 30 мг/мл, от 10 мг/мл до 30 мг/мл, от 10,5 мг/мл до 30 мг/мл, от 11 мг/мл до 30 мг/мл, от 11,5 мг/мл до 30 мг/мл, от 12 мг/мл до 30 мг/мл, от 12,5 мг/мл до 30 мг/мл, от 10 мг/мл до 25 мг/мл, от 10,5 мг/мл до 25 мг/мл, от 11 мг/мл до 30 мг/мл, от 11,5 мг/мл до 25 мг/мл, от 12 мг/мл до 25 мг/мл, от 12,5 мг/мл до 25 мг/мл, от 15 мг/мл до 25 мг/мл и, в частности, до 19 мг/мл. Ограниченное количество незахваченного анестетика амидного типа в анестезирующей композиции по настоящему изобретению может обеспечивать преимущество достижения более высокой максимальной переносимой дозы (в зависимости от концентрации анестетика в плазме, которая вызывает токсичность для центральной нервной системы и сердечно-сосудистой системы) и может быть использовано для обеспечения быстрого начала действия.
[0049] Для клинического применения анестетик амидного типа в свободной форме, в соответствии с определенными вариантами осуществления настоящего изобретения, может быть в диапазоне от приблизительно 1% до приблизительно 50%, от приблизительно 5% до приблизительно 40% или от приблизительно 10% до приблизительно 30%. Остальной анестетик амидного типа в липидном комплексе играет роль депо для постепенного высвобождения анестетика амидного типа в местную среду таким образом, чтобы поддерживать терапевтически эффективную дозу в локальном участке. В соответствии с некоторыми вариантами осуществления, период полувыведения ропивакаина, полученного при однократном подкожном введении анестезирующей композиции в соответствии с настоящим изобретением, продлевается по меньшей мере в 10 раз по сравнению с периодом полувыведения ропивакаина вне состава. Продолжительность анестезирующего действия после введения анестезирующей композиции по настоящему изобретению значительно превышает продолжительность полувыведения ропивакаина вне состава.
[0050] Фармацевтические композиции в соответствии с настоящим изобретением характеризуются профилем значительно пролонгированного высвобождения терапевтического средства и обеспечивают немедленное и длительное уменьшение боли от 2 до 4 по шкале от 0 до 10 в соответствии с оценкой по числовой шкале оценки боли (NPRS) в течение периода после хирургической операции после введения клинически релевантной дозы местного анестетика. Например, фармацевтическая композиция по настоящему изобретению продлевает период полувыведения локально вводимой липосомальной анестезирующей композиции. Настоящая композиция может обеспечивать проявление более низкой средней боли в соответствии с оценкой по NPRS во всех моментах времени и значительно уменьшить общую боль после хирургической операции через временные интервалы в 24 часа, 48 часов, 72 часа, 4 суток или 1 неделю у людей по сравнению с болью при введении свободного анестетика или коммерческого анестетика.
[0051] Липидный комплекс в соответствии с настоящим изобретением можно вводить периневрально, в операционное поле или в послеоперационную рану. Термины «послеоперационная боль» и «боль после оперативного вмешательства» применяют взаимозаменяемо, и они обозначают боль, обусловленную различными хирургическими операциями. В соответствии с некоторыми вариантами осуществления, послеоперационная боль обусловлена хирургической операцией по пластике грыжи, хирургической операцией на мочеполовой системе, хирургической операцией по удалению геморроидального узла, хирургической операцией органов брюшной полости, хирургической операцией на органах грудной полости, ортопедической хирургической операцией, включая без ограничения бурсэктомию, вертебропластику, акромиопластику, кифопластику, полную замену колена или бедра, акушерской хирургической операцией, хирургической операцией на молочной железе, стоматологической хирургической операцией, абдоминопластикой, хирургической операцией на молочной железе, процедурой трансплантации почки (KTX) или любым типом лапароскопической хирургической операции.
[0052] Фармацевтическую композицию в соответствии с настоящим изобретением можно вводить путем инъекции, инстилляции или вносить с помощью стандартных шприцев и игл. Инъекцию фармацевтической композиции в соответствии с настоящим изобретением можно производить подкожным, внутрикожным или внутримышечным путем.
[0053] В соответствии с другим вариантом осуществления, фармацевтическую композицию согласно настоящему изобретению вводят в виде блокады нервов в качестве профилактического лечения болезненного состояния, например, введение перед хирургической операцией для лечения послеоперационной боли, у нуждающегося в том субъекта. В соответствии с некоторыми вариантами осуществления, фармацевтическую композицию согласно настоящему изобретению вводят в виде блокады нервов, такой как блокада квадратной мышцы поясницы (QLB).
[0054] Блокада периферического нерва предусматривает введение средства рядом с периферическим нервом или в него для уменьшения боли или для обеспечения онемения.
[0055] В соответствии с другим вариантом осуществления, фармацевтическую композицию согласно настоящему изобретению вводят в операционное поле в виде местной анестезии, такой как блокада Майо множественных нервов стопы для бурсэктомии, блокада поперечной мышцы живота (TAPB) для открытой лапаротомии или кесарева сечения и методика участок-специфической местной анестезии для полной замены тазобедренного или коленного сустава.
[0056] Настоящее изобретение далее будет описано на основании представленных далее конкретных неограничивающих примеров.
Примеры
[0057] Представленные ниже примеры иллюстрируют получение и свойства определенных вариантов осуществления настоящего изобретения.
Пример 1
Получение анестезирующих композиций
[0058] 1,2-димиристоил-sn-глицеро-3-фосфохолин приобретали у NOF Corporation (Токио, Япония) или Lipoid GmbH (Людвигсхафен, Германия). Холестерин приобретали у Sigma-Aldrich (Дармштадт, Германия) или Dishman Pharmaceuticals and Chemicals (Гуджарат, Индия), а ропивакаин приобретали у Apollo Scientific (Чешир, Великобритания) или Dishman Pharmaceuticals and Chemicals. Все остальные химические вещества приобретали у Sigma-Aldrich.
[0059] Для получения липидной лепешки ропивакаин объединяли с указанным липидным комплексом при соотношении лекарственного средства к фосфолипидам (D:PL), равном 1,458 мкмоль/мкмоль, т. е. фосфохолин:холестерин:ропивакаин = 2:1:2,9. Липиды и ропивакаин смешивали, а затем растворяли в трет-бутаноле или системе совместных растворителей трет-бутанол/вода (1/1, об./об.) с получением жидкой структуры. Жидкую структуру замораживали, а затем лиофилизировали в течение ночи с получением липидной лепешки анестетика амидного типа.
[0060] Для получения липидных структур для контрольной среды взвешивали фосфолипиды:холестерин в мольном соотношении 2:1, а затем растворяли в трет-бутаноле. Полученный образец замораживали, а затем лиофилизировали в течение ночи с получением липидной лепешки контрольной среды.
[0061] Липидные лепешки анестетика или контрольной среды гидратировали буферным раствором с pH от 6,5 до 6,8 при температуре не ниже температуры окружающей среды (AT) (25°C) с получением анестезирующей композиции и композиции с контрольной средой соответственно с последующим изучением характеристик эффективности ассоциации и распределения частиц по размеру.
Изучение характеристик анестезирующих композиций
[0062] Эффективность ассоциации (AE) каждого из описанных выше препаратов определяли следующим образом. Аликвоту в двести микролитров каждого образца анестезирующей композиции центрифугировали в течение 5 минут при 3000 × g при 4°C с получением липидного комплекса. После декантации супернатанта липидный комплекс ресуспендировали до конечного объема 200 мкл. Для каждого лекарственного вещества (например, ропивакаина) устанавливали эталонный стандарт абсорбции на основе растворов тестируемого лекарственного вещества с известной концентрацией. Количества лекарственного средства как в исходной анестезирующей композиции, так и в липидном комплексе измеряли с помощью спектрофотометра в ультрафиолетовом/видимом (УФ/видимом диапазонах) спектрах. AE представляет собой соотношение количества лекарственного средства в липидном комплексе к количеству лекарственного вещества в исходной анестезирующей композиции. D:PL у липидного комплекса рассчитывали путем умножения D:PL лиофилизированной липидной лепешки на AE и обозначали как «полученное D:PL».
[0063] Размер частиц каждой анестезирующей композиции измеряли с помощью лазерного дифракционного анализатора (LA-950V2, Horiba). Исследовали медианный диаметр (D50) липидного комплекса, полученного при гидратации лиофилизированной липидной лепешки фармацевтически приемлемым буферным раствором (например, 50 мМ гистидиновым буфером с pH 6,5).
[0064] Было определено, что липидный комплекс в анестезирующей композиции имеет конечное соотношение лекарственного средства к фосфолипидам, равное приблизительно 1,32. Медианный диаметр (D50) совокупности частиц липидной смеси в анестезирующей композиции составлял приблизительно от 5 мкм до 10 мкм.
Пример 2
Лечение боли у взрослых субъектов после хирургической операции по пластике паховой грыжи
[0065] Было проведено рандомизированное, двойное слепое, с использованием активного препарата в качестве контроля исследование с увеличением дозы I/II фазы для оценки безопасности, фармакокинетики и эффективности однократного послеоперационного применения анестезирующей композиции по настоящему изобретению (обозначенной как TLC590) по сравнению с препаратом Naropin® путем однократного инфильтративного местного введения взрослым субъектам после хирургической операции по пластике паховой грыжи.
[0066] В исследовании принимало участие примерно 64 оцениваемых субъектов, которые соответствовали всем критериям включения, в 4 когортах. Повышение дозы при однократном послеоперационном введении TLC590 производили с использованием последовательных уровней доз в сравнении с препаратом Naropin®. Повышение дозы определялось путем обзора связанных с лечением нежелательных явлений (TEAE) и всех серьезных AE (SAE) комитетом по контролю за безопасностью (SMC).
[0067] Ниже перечислены критерии включения:
1. способен и желает предоставить письменное информированное согласие;
2. мужчина или женщина в возрасте от 18 до 65 лет включительно;
3. для него/нее запланировано проведение первичной односторонней пластики паховой грыжи по Лихтенштейну с использованием сетки, и он/она может переносить режим анестезии;
4. имеет 1-й или 2-й статус по классификации физического статуса ASA;
5. субъекты женского пола допускались лишь в том случае, если они не были беременны, не лактировали, не планировали забеременеть во время исследования, обязались использовать приемлемую форму контрацепции; или субъекты мужского пола должны были быть бесплодными или использовать надежный способ контрацепции на протяжении всего исследования по меньшей мере через 1 неделю после введения слепого исследуемого лекарственного препарата; и
6. имели индекс массы тела ≤35 кг/м2.
[0068] Субъектов в каждую когорту включали в соотношении 3:1. Каждая когорта включала субъектов, получавших дозу TLC590 или активного лекарственного препарата в качестве контроля (150 мг препарата Naropin®; [0,5%, 5 мг/мл]) в соответствии с графиком рандомизации и схемой повышения дозы (фиг. 1).
[0069] Для сохранения объективности исследуемое лекарственное средство контролировалось и вводилось независимой командой, проинформированной о проходимом субъектом курсе лечения, в которую входили специалисты по инъекциям, фармацевты и партнеры по клиническим исследованиям. Субъекты, исследователи и весь остальной персонал центра, который напрямую взаимодействовал с субъектами, оценивали безопасность и эффективность и собирали данные по субъектам, оставались непроинформированными о проходимом субъектом курсе лечения и не должны были сообщать или обсуждать какую-либо информацию об исследовании с командой, проинформированной о проходимом субъектом курсе лечения.
[0070] Группы и вмешательства имели представленную ниже схему:
Группы
[0071] Экспериментальная: группа TLC590:
TLC590 (композиция с ропивакаином) представляла собой липосомный состав с замедленным высвобождением ропивакаина, белую водную суспензию с концентрацией ропивакаина примерно 19 мг/мл.
[0072] Активный лекарственный препарат в качестве контроля: Naropin®:
инъекция препарата Naropin® содержала ропивакаин HCl. Концентрация: 150 мг/30 мл (5 мг/мл). Размер: 30 мл содержимого в 30-мл флаконе с однократной дозой.
Вмешательства
[0073] Лекарственное средство: TLC590 (композиция с ропивакаином).
Липидную лепешку TLC590 ресуспендировали раствором для ресуспендирования TLC590 с получением анестезирующей композиции TLC590.
[0074] Лекарственное средство: Naropin®
Местная инфильтрация препаратом Naropin® для осуществления анестезии во время хирургической операции и аналгезии при послеоперационном купировании боли. 150 мг препарата Naropin® [0,5%, 5 мг/мл] × 30 мл
Другое название: Naropin®, 0,5% инъекционный раствор.
[0075] Ниже перечислены первичные конечные точки исследования: безопасность и переносимость: (i) количество SAE и связанных с лечением тяжелых AE (для определения MTD) [временные рамки: скрининг до 30 дней после внутрибрюшинного введения] и;
[0076] Ниже перечислены вторичные конечные точки исследования.
1. Интенсивность боли в состоянии покоя и при движении, оцениваемая с помощью 11-балльной шкалы NPRS в диапазоне от оценки 0 (отсутствие боли) до 10 (наихудшая из возможных болей).
2. Общая оценка пациентом (PGA) способа устранения боли (плохой, удовлетворительный, хороший или отличный).
3. AUC для NPRS в состоянии покоя и при движении.
4. Суммарная доля субъектов без болей (определяемых как NPRS в состоянии покоя, равная 0 или 1) в запланированные моменты времени.
5. Доля субъектов без болей (определяемых как NPRS в состоянии покоя, равная 0 или 1) в запланированные моменты времени.
6. Суммарная доля субъектов, которые не использовали экстренное обезболивающее средство в течение 12, 24, 36, 48, 72 и 96 часов.
7. Время до первого послеоперационного использования экстренных обезболивающих средств.
8. Общее послеоперационное употребление каждого типа экстренных обезболивающих средств в течение 12, 24, 36, 48, 72 и 96 часов.
9. Среднесуточное употребление экстренных обезболивающих средств с разбивкой по типам в течение 24, 48, 72 и 96 часов.
10. Интегрированная оценка анальгетиков с использованием оценки NPRS и употребления экстренных обезболивающих средств.
11. Суммарная доля субъектов, которые не использовали послеоперационную противорвотную терапию в течение 12, 24, 36, 48, 72 и 96 часов.
12. Частота всех нежелательных явлений по степени тяжести и степени родства.
13. Причинно-следственная связь между фармакокинетическими параметрами и оценками по NPRS.
[0077] Изменения с момента описанного выше скрининга анализировали статистическими методами. Терапия посредством TLC590 путем однократного инфильтративного местного введения дозой 190 мг, 380 мг, 475 мг и 570 мг приводила к положительному клиническому ответу в соответствии с любой одной или несколькими указанными выше конечными точками.
Результаты
[0078] В общей сложности было рандомизировано 64 субъекта в четыре когорты. В ходе исследования не наблюдали никаких серьезных неблагоприятных явлений или явлений системной токсичности местных анестетиков (LAST). Во всех 4 группах, принимавших дозу TLC590, наблюдали схожую безопасность и переносимость, как и в случае 150 мг ропивакаина. Даже при дозе 570 мг средняя максимальная концентрация TLC590 в виде несвязанного ропивакаина в плазме была ниже, чем в группе ропивакаина. Средние концентрации в плазме в случае доз TLC590 оставались на плато в течение около 24 часов и снижались с наблюдаемым t½ значимо дольше, чем в группе ропивакаина, с Cmax ниже одной пятой от таковой для 300 мг 7,5 мг/мл раствора ропивакаина в случае инфильтрации (2,7 мг/мл) (Regional Anesthesia and Pain Medicine 23(2): 189-196, 1998) (фиг. 1A). Все 4 дозы TLC590 снижали послеоперационную боль по сравнению с группой ропивакаина по результатам измерения средней площади под кривыми (AUC) боли по NPRS методом наименьших квадратов (LS). В случае 475 мг TLC590 имели место стойкие, статистически значимые и клинически значимые снижения интенсивности боли при движении и в состоянии покоя с течением времени (фиг. 2) по сравнению с ропивакаином (все p<0,05; наивысшее p-значение 0,0131); состояние сниженной боли в сравнении с ропивакаином сохранялось в течение 168 часов (фиг. 3). Медианное время до первого экстренного обезболивающего средства было в 3,2 раза дольше в случае группы 475 мг TLC590, чем в случае группы ропивакаина (42 часа в сравнении с 13 часами). Большинство (58,3%) пациентов, обрабатываемых посредством TLC590 (475 мг), не использовали никаких экстренных опиоидных обезболивающих средств на протяжении всего хода исследования. Среди тех, кто принимал экстренные опиоидные обезболивающие средства, медианное время до первого послеоперационного употребления опиоидов было приблизительно в 4 раза большим, чем в группе ропивакаина (13,0 часа в сравнении с 3,3 часа). Среднее общее употребление опиоидов через 96 часов после хирургической операции было на 54% меньше, чем в группе ропивакаина.
Заключение
[0079] У TLC590 наблюдали такую же безопасность и переносимость, как и у ропивакаина, без LAST-событий, и она обеспечивала немедленное и длительное уменьшение боли по сравнению с теми, кто принимал ропивакаин, уменьшая или устраняя потребность в опиоидах. У субъектов, получавших 475 мг TLC590, наблюдали более высокую эффективность по сравнению с клинически значимой дозой одобренного лекарственного средства ропивакаин с более низкой средней болью во всех моментах времени и значимым уменьшением общей боли через временные интервалы в течение 4 суток после хирургической операции.
Пример
Лечение боли у взрослых субъектов после хирургической операции по бурсэктомии
[0080] Было проведено рандомизированное, двойное слепое, с использованием активного препарата и плацебо в качестве контроля исследование II фазы для оценки безопасности, фармакокинетики и эффективности однократного послеоперационного применения TLC590 по сравнению с препаратом Naropin® или бупивакаином и плацебо посредством однократного инфильтративного местного введения взрослым субъектам после хирургической операции по бурсэктомии.
[0081] В данном исследовании принимали участие примерно 223 подходящих субъекта. Исследование было разделено на две части:
Часть 1: слепая фармакокинетика TLC590 и препарата Naropin®, примерно 48 субъектов рандомизировали в соотношении 1:1:1:1 для обработки с помощью 152 мг (8 мл) TLC590, 190 мг (10 мл) TLC590, 228 мг (12 мл) TLC590 или препаратом Naropin® (50 мг; 10 мл). График рандомизации был назначен централизованной интерактивной системой с доступом через Интернет (IWRS). В части 1 испытания проводили неслепой промежуточный анализ для оценки безопасности, эффективности и фармакокинетики 3 доз TLC590 и препарата Naropin®.
Часть 2: эффективность и безопасность TLC590 по сравнению с бупивакаином и плацебо, в части 2 исследования участвовало примерно 150 субъектов, которые соответствовали всем критериям включения, с соотношением рандомизации 1:1:1 для обработки с помощью 228 мг TLC590, бупивакаином и плацебо. График рандомизации был назначен централизованной IWRS. Схема исследования представлена на фиг. 4.
[0082] Изменения с момента описанного выше скрининга анализировали статистическими методами. Терапия посредством TLC590 путем однократного инфильтративного местного введения дозой 152 мг, 190 мг и 228 мг приводила к положительному клиническому ответу в соответствии с любой одной или несколькими указанными выше конечными точками.
Группа изобретений относится к области медицины, а именно к фармацевтическим композиция для лечения послеоперационной боли и к способам лечения послеоперационной боли. Фармацевтическая композиция для лечения послеоперационной боли содержит липидный комплекс, причем липидный комплекс содержит анестетик амидного типа и по меньшей мере один фосфолипид, причем мольное соотношение анестетика амидного типа по меньшей мере и одного фосфолипида в липидном комплексе составляет от 0,5:1 до 2:1, причем общее количество анестетика амидного типа в фармацевтической композиции составляет в диапазоне от 300 мг до 600 мг. Фармацевтическая композиция для лечения боли у нуждающегося в анестезии субъекта посредством блокады нерва, посредством местной анестезии или посредством инфильтрационной анестезии, при этом фармацевтическая композиция содержит: липидный комплекс, содержащий анестетик амидного типа и нейтральный насыщенный фосфолипид, причем нейтральный насыщенный фосфолипид содержит насыщенные жирные кислоты, при этом каждая насыщенная жирная кислота независимо содержит углеродную цепь с количеством атомов углерода менее 18; причем мольное соотношение анестетика амидного типа и нейтрального насыщенного фосфолипида в липидном комплексе составляет от 0,5:1 до 2:1; причем медианный диаметр липидного комплекса составляет в диапазоне от 5 мкм до 200 мкм и причем общее количество анестетика амидного типа в фармацевтической композиции составляет в диапазоне от 300 мг до 600 мг. Способ лечения послеоперационной боли у нуждающегося в анестезии субъекта предусматривает введение фармацевтической композиции посредством блокады нерва, посредством местной анестезии или посредством инфильтрационной анестезии. Способ лечения послеоперационной боли предусматривает введение фармацевтической композиции за период, составляющий от получаса до трех часов, до хирургической операции или во время хирургической операции, причем уменьшение боли составляет по меньшей мере 2 в соответствии с оценкой NPRS по шкале от 0 до 10 в течение периода по меньшей мере 48 часов после хирургической операции. Вышеописанная группа изобретений позволяет реализовать улучшенный способ лечения послеоперационной боли с менее частым дозированием или более низкими дозами для получения эквивалентного эффекта обезболивания или анестезирующего действия и, таким образом, уменьшения нежелательных эффектов анестетика амидного типа. 4 н. и 16 з.п. ф-лы, 4 ил., 3 пр.
1. Фармацевтическая композиция для лечения послеоперационной боли, которая содержит липидный комплекс, причем липидный комплекс содержит анестетик амидного типа и по меньшей мере один фосфолипид, причем мольное соотношение анестетика амидного типа и по меньшей мере одного фосфолипида в липидном комплексе составляет от 0,5:1 до 2:1, причем общее количество анестетика амидного типа в фармацевтической композиции составляет в диапазоне от 300 мг до 600 мг.
2. Фармацевтическая композиция по п. 1, причем послеоперационная боль обусловлена хирургической операцией по пластике грыжи.
3. Фармацевтическая композиция по п. 1, причем фармацевтическая композиция содержит от 15 мг/мл до 25 мг/мл анестетика амидного типа.
4. Фармацевтическая композиция по п. 1, причем по меньшей мере один фосфолипид включает нейтральный насыщенный фосфолипид.
5. Фармацевтическая композиция по п. 4, причем нейтральный насыщенный фосфолипид содержит одну или несколько насыщенных жирных кислот, при этом каждая насыщенная жирная кислота независимо содержит углеродную цепь с количеством атомов углерода не более 18.
6. Фармацевтическая композиция по п. 4, причем нейтральный насыщенный фосфолипид выбран из группы, состоящей из димиристоилфосфатидилхолина (DMPC), 1,2-дилауроил-sn-глицеро-3-фосфохолина (DLPC), дипальмитоилфосфатидилхолина (DPPC) и их комбинаций.
7. Фармацевтическая композиция по п. 1, причем липидный комплекс дополнительно содержит стерин.
8. Фармацевтическая композиция по п. 7, причем стерин представляет собой холестерин.
9. Фармацевтическая композиция по любому из пп. 1-8, причем анестетик амидного типа выбран из группы, состоящей из лидокаина, бупивакаина, левобупивакаина, ропивакаина, мепивакаина, пиррокаина, артикаина, прилокаина и их комбинаций.
10. Фармацевтическая композиция по любому из пп. 1-8, причем медианный диаметр липидного комплекса составляет в диапазоне от 5 мкм до 200 мкм.
11. Фармацевтическая композиция для лечения боли у нуждающегося в анестезии субъекта посредством блокады нерва, посредством местной анестезии или посредством инфильтрационной анестезии, при этом фармацевтическая композиция содержит:
липидный комплекс, содержащий анестетик амидного типа и нейтральный насыщенный фосфолипид,
причем нейтральный насыщенный фосфолипид содержит насыщенные жирные кислоты, при этом каждая насыщенная жирная кислота независимо содержит углеродную цепь с количеством атомов углерода менее 18; причем мольное соотношение анестетика амидного типа и нейтрального насыщенного фосфолипида в липидном комплексе составляет от 0,5:1 до 2:1; причем медианный диаметр липидного комплекса составляет в диапазоне от 5 мкм до 200 мкм;
и причем общее количество анестетика амидного типа в фармацевтической композиции составляет в диапазоне от 300 мг до 600 мг.
12. Фармацевтическая композиция по п. 11, причем общее количество анестетика амидного типа составляет 475 мг.
13. Фармацевтическая композиция по п. 12, причем фармацевтическая композиция содержит от 10 мг/мл до 30 мг/мл анестетика амидного типа.
14. Способ лечения послеоперационной боли у нуждающегося в анестезии субъекта, при этом способ предусматривает:
введение фармацевтической композиции по п. 1 посредством блокады нерва, посредством местной анестезии или посредством инфильтрационной анестезии.
15. Способ по п. 14, причем послеоперационная боль обусловлена хирургической операцией по пластике грыжи.
16. Способ лечения послеоперационной боли, предусматривающий:
введение фармацевтической композиции по п. 1 за период, составляющий от получаса до трех часов, до хирургической операции или во время хирургической операции, причем уменьшение боли составляет по меньшей мере 2 в соответствии с оценкой NPRS по шкале от 0 до 10 в течение периода по меньшей мере 48 часов после хирургической операции.
17. Способ по п. 16, причем период составляет по меньшей мере 72 часа.
18. Способ по п. 16, причем период составляет по меньшей мере 96 часов.
19. Способ по п. 16, причем период составляет по меньшей мере 168 часов.
20. Способ по п. 16, причем хирургическая операция представляет собой хирургическую операцию по пластике грыжи.
| US 2015250724 A1, 10.09.2015, | |||
| CN 108379269 A, 10.08.2018 | |||
| EXPAREL (bupivacaine liposome injectable suspension), апрель, 2018 | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| WO 2016070826 A1, 12.05.2016 | |||
| СПОСОБ АВТОМАТИЧЕСКОГО НАХОЖДЕНИЯ ЦЕНТРА СЧИТЫВАНИЯ ДАКТИЛОСКОПИЧЕСКИХ ОТПЕЧАТКОВ | 0 |
|
SU290296A1 |
| ЖАРНИКОВ А.В., ПЛЕХАНОВ А.Н., Сравнительная характеристика | |||
Авторы
Даты
2024-02-05—Публикация
2020-02-26—Подача