Область изобретения
Изобретение относится к химии и медицине, а именно к новым биологически активным органическим солям N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметоксибензил)амино]этил}-1,2-этан-диамина общей формулы:
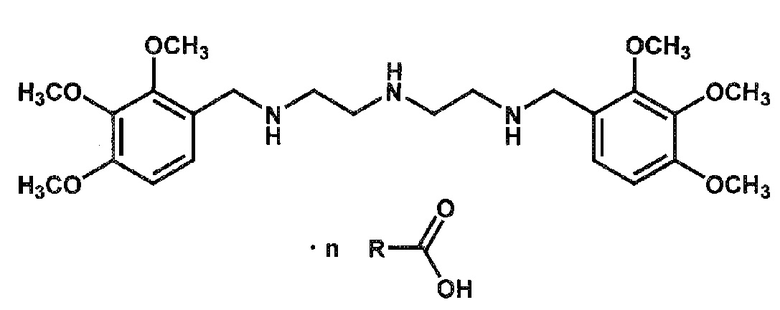
где n=1/3-3;
R=углеродсодержащий органический радикал.
Новые соединения обладают антиаритмической и антиишемической активностью.
Актуальной задачей является расширение арсенала средств, демонстрирующих антиаритмические и антиишемические свойства, при этом являющихся малотоксичными веществами, без местно-раздражающего действия и нежелательных органолептических свойств.
С целью решения такой задачи в качестве прототипа предлагаемого технического решения было выбрано соединение тригидрохлорид N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметокси-бензил)амино]этил}-1,2-этан-диамина [Патент РФ №2624438].
Соединение АЛМ-802 (тригидрохлорид N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметокси-бензил)амино]этил}-1,2-этан-диамина) было сконструировано в рамках развития концепции обобщенной фармакофорной модели кардиопротекторных средств, имеющих в своем составе две ароматические группы, связанные линейным линкером [Патент РФ №2624438.; Г.В. Мокров, A.M. Лихошерстов, В.В. Барчуков, В.Н. Столярук, И.Б. Цорин, М.Б. Вититнова, С.А. Крыжановский, Т.А. Гудашева, С.Б. Середенин. Синтез и кардиотропная активность линейных метоксифенилтриазаалканов. Химико-фармацевтический журнал. 2019, том 53, №6, стр. 16-23].
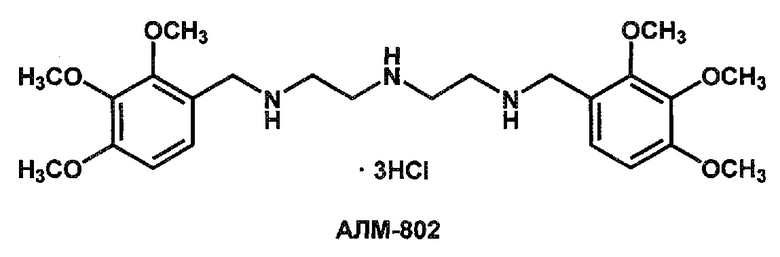
Соединение АЛМ-802 в дозе 2 мг/кг (3,5 мкмоль/кг) при внутривенном введении в физрастворе препятствовало развитию аритмий у крыс на моделях аконитиновой, хлоридкальциевой и реперфузионной аритмий, увеличивало порог электрической фибрилляции желудочков сердца крыс с 2 до 10 мА. Соединение АЛМ-802 в дозе 2 мг/кг при внутривенном введении в физрастворе в условиях модели субэндокардиальной ишемии у крыс препятствовало депрессии сегмента ST на электрокардиограмме животных по сравнению с контрольной группой, демонстрируя выраженный антиишемический эффект [Г.В. Мокров, A.M. Лихошерстов, В.В. Барчуков, В.Н. Столярук, И.Б. Цорин, М.Б. Вититнова, С.А. Крыжановский, Т.А. Гудашева, С.Б. Середенин. Синтез и кардиотропная активность линейных метоксифенилтриазаалканов. Химико-фармацевтический журнал. 2019, том 53, №6, стр. 16-23].
В отличие от эталонных препаратов триметазидина (30 мг/кг, в/в) и ранолазина (10 мг/кг, в/в), которые были эффективны только у интактных крыс, соединение АЛМ-802 (2 мг/кг, в/в) проявляло выраженное противоишемическое действие и у животных с эндотелиальной дисфункцией [В.В. Барчуков, И.Б. Цорин, A.M. Лихошерстов, М.Б. Вититнова, Г.В. Мокров, Т.А. Гудашева, С.А. Крыжановский. Противоишемическая активность триамина АЛМ-802 в условиях эндотелиальной дисфункции. Бюллетень экспериментальной биологии и медицины. 2019. N 4. - С. 443-446].
В модельных экспериментах, воспроизводящих постинфарктную хроническую сердечную недостаточность, которая формируется у крыс с передним трансмуральным инфарктом миокарда через 90 сут после его воспроизведения, показано, что соединение АЛМ-802 проявляет кардиопротективную активность: уменьшает размеры левого желудочка сердца и увеличивает его инотропную функцию (р=0.038). Действие соединения реализуется в случае систематического применения в течение 28 сут (начиная с 91-х суток от момента воспроизведения инфаркта миокарда) [В.В. Барчуков, И.Б. Цорин, М.Б. Вититнова, А.О. Ефимова, А.М. Лихошерстов, Г.В. Мокров, С.А. Крыжановский. Выбор тактики экспериментальной терапии хронической сердечной недостаточности соединением АЛМ-802. Бюллетень экспериментальной биологии и медицины. 2020 г., Т. 170, №12, стр. 752-758.].
При изучении механизма действия соединения АЛМ-802 был подтвержден его мультитаргетный характер. АЛМ-802 блокирует потенциал-зависимые натриевые каналы (IC50=94±4 μM) и потенциал-зависимые калиевые каналы (IC50=67±3 μM). АЛМ-802 полностью блокирует положительный инотропный ответ кофеина, агониста RyR, что позволяет предположить, что ALM-802 обладает свойствами антагониста RyR. Методом ПЦР в реальном времени показано, что у опытных крыс соединение АЛМ-802 (ежедневно внутрибрюшинно в дозе 2 мг/кг в течение 28 сут, с 91-х суток от момента воспроизведения инфаркта миокарда) восстанавливает в миокарде экспрессию генов β1- и β2-адренорецепторов (р=0.00001 и р=0.01 соответственно), а также рианодиновых рецепторов 2-го типа (р=0.008), сниженную у контрольных животных [Л.М. Кожевникова, В.В. Барчуков, Н.П. Семенова, М.Б. Вититнова, С.А. Крыжановский. Изучение молекулярных механизмов, лежащих в основе кардиопротективного действия соединения АЛМ-802. Бюллетень экспериментальной биологии и медицины. 2020 г., Т. 170, №9, стр. 301-305].
Соединение АЛМ-802 характеризуется умеренной токсичностью (LD50=119 мг/кг, мыши, внутрибрюшинно) [Г.В. Мокров, A.M. Лихошерстов, В.В. Барчуков, В.Н. Столярук, И.Б. Цорин, М.Б. Вититнова, С.А. Крыжановский, Т.А. Гудашева, С.Б. Середенин. Синтез и кардиотропная активность линейных метоксифенилтриазаалканов. Химико-фармацевтический журнал. 2019, том 53, №6, стр. 16-23].
Так как АЛМ-802 является тригидрохлоридом слабого основания - молекулы с тремя вторичными атомами азота - рН водного раствора этого соединения имеет очень низкие значения (менее 4), что ограничивает спектр возможных путей доставки в организм этого соединения, например, в виде сублингвальной лекарственной формы, ввиду наличия у него потенциального местно раздражающего действия. Также АЛМ-802 проявляет и нежелательными органолептические свойства, в частности, обладает резко горьким вкусом.
Одним из возможных путей решения данной задачи является использование слабых органических кислот для образования солей основания АЛМ-802.
Известно, что разные соли одного и того же активного действующего вещества могут обладать различной активностью, вплоть до ее отсутствия. Так, в работе Толстиковой с соавторами, в которой анализировалась антиаритмическая активность различных неорганических и органических солей алкалоида лаппаконитина, было установлено, что лишь гидробромид этого соединения обладал антиаритмическими свойствами, в то время как гидрохлорид и сукцинат лаппаконитина активностью не обладали [Толстикова, Т.Г., Брызгалов, А.О., Сорокина, И.В., Долгих, М.П., Шульц, Э.Э., Осадчий, С.А., Толстиков, Г.А. Солеобразование с бромистоводородной кислотой как фактор, определяющий аритмическое действие производных лаппаконитина. Докл. АН. - 2007. - Т. 415. - №6. - С. 837-838].
Неочевидность представляемых результатов заключается в том, что полученные органические соли основания АЛМ-802 проявляют целевую активность, что показано в примерах, иллюстрирующих изобретение.
Сущность изобретения
Целью нашей работы было получение органических солей N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметоксибензил)амино]этил}-1,2-этан-диамина с кардиопротекторной, антиаритмической и антиишемической активностью.
Мы нашли, что эта цель может быть достигнута при помощи соединений общей формулы:
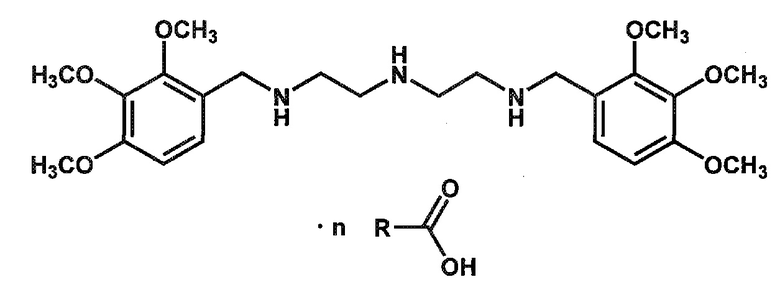
где n=0,5-3,0;
R=углеродсодержащий органический радикал.
Примерами осуществления изобретения могут служить следующие соединения:
1. Сукцинат N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметоксибензил)амино]этил}-1,2-этан-диамина;
2. Цитрат N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметоксибензил)амино]этил}-1,2-этан-диамина.
Эти соединения не описаны в литературе, их получение и физико-химические характеристики не известны из уровня техники.
Техническим результатом изобретения является расширение арсенала лекарственных средств для лечения заболеваний и состояний сердечнососудистой системы, требующих применения средств обладающих кардиопротекторной, антиаритмической и антиишмемической активностями.
Синтез органических солей N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметоксибензил)амино]этил}-1,2-этан-диамина
Синтез органических солей N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметоксибензил)амино]этил}-1,2-этан-диамина осуществляется по следующей схеме:
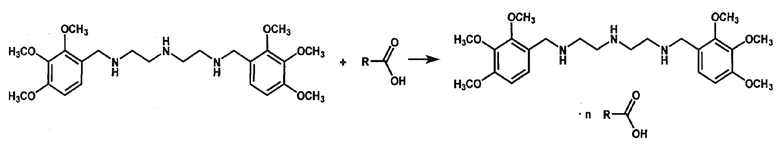
К раствору N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметоксибензил)амино]этил}-1,2-этан-диамина в спирте, в качестве которого может быть использован этанол или другой спирт, при кипячении прибавляют раствор избытка органической кислоты в спирте, в качестве которого может быть использован этанол или другой спирт. Полученную смесь оставляют охлаждаться до выпадения осадка. Выпавший осадок отфильтровывают и перекристаллизовывают из спирта, в качестве которого может быть использован этанол или другой спирт.
Пример 1. Сукцинат N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметоксибензил)амино]этил}-1,2-этан-диамина (АЛМ-802-S).
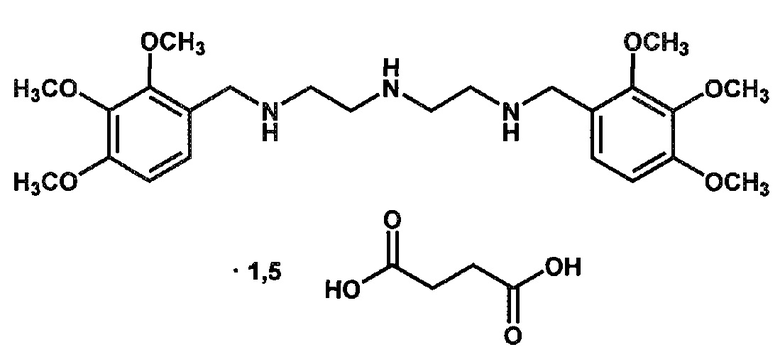
К раствору 4,64 г (10 ммоль) N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметоксибензил)амино]этил}-1,2-этан-диамина в 20 мл 96%-ного этанола при кипячении прибавляют раствор 2,36 г (20 ммоль) янтарной кислоты в 20 мл 96%-ного этанола. Полученную смесь оставляют охлаждаться до комнатной температуры, после чего оставляют на сутки при -15°С. Выпавший осадок отфильтровывают, перекристаллизовывают из минимального количества 96%-ного этанола, получая 4,0 г продукта в виде белого порошка (выход 62%).
Спектр ЯМР lH (DMSO, δ, м.д., J/Гц): 2.30 (с, 6Н, 1,5*2СН2-СОО-), 2.73-2.75 (м, 4Н, CH2-N) 2.85-2.87 (м, 4 Н, CH2-N); 3.69 (4Н, с, CH2-Ar), 3.74, 3.78, 3.89 (три с, по 6 Н, 6 ОМе); 6.76 и 7.04 (оба д, по 2 Н, 4 ArH, J3=8.6), 8.45 (уш. с, 3Н, -NH2+-).
Элементный анализ на брутто-формулу C24H37N3O6*1,5(СН2СООН)2: Вычислено, %: С, 56.24; Н, 7.24; N, 6.56; Найдено: С, 56.35; Н, 7.11; N, 6.59.
Т.пл. 139-141°С.
Пример 2. Цитрат N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметоксибензил)амино]этил}-1,2-этан-диамина (АЛМ-802-С).
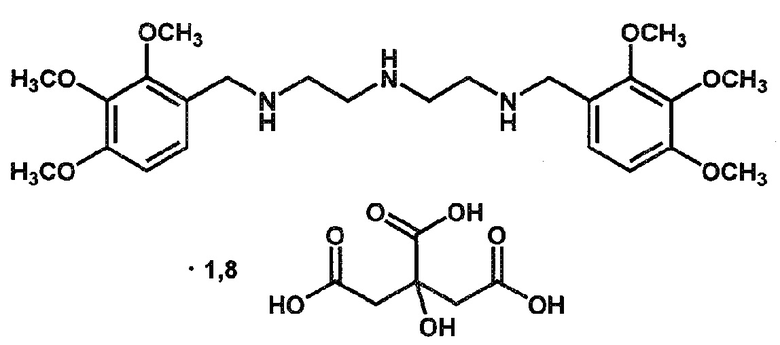
К раствору 4,64 г (10 ммоль) N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметоксибензил)амино]этил}-1,2-этан-диамина в 20 мл 96%-ного этанола при кипячении прибавляют раствор 2,88 г (15 ммоль) лимонной кислоты в 20 мл 96%-ного этанола. Полученную смесь оставляют охлаждаться до комнатной температуры, после чего оставляют на сутки при -15°С. Выпавший осадок отфильтровывают, перекристаллизовывают из минимального количества 96%-ного этанола, получая 6,45 г продукта в виде белого порошка (выход 79%).
Спектр ЯМР 1H (DMSO, δ, м.д., J/Гц): 2.47-2.59 (м, 7,2Н, 1,8*2СН2-СОО-), 2.87 (с, 8Н, CH2-N); 3.76, 3.80, 3.84 (три с, по 6 Н, 6 ОМе); 3.92 (4Н, с, СН2-Ar); 6.82 и 7.12 (оба д, по 2 Н, 4 ArH, J3=8.6), 9.08 (уш.с, 9.38Н, -NH2+-).
Элементный анализ на брутто-формулу C24H37N3O6*1,8(C6H8O7): Вычислено, %: С, 51.64; Н, 6.40; N, 5.19; Найдено: С, 51.60; Н, 6.21; N, 5.33.
Т.пл. 154-156°С.
Пример 3. Определение значений рН солей N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметоксибензил)амино]этил}-1,2-этан-диамина
Значение показателя рН солей N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметоксибензил)амино]этил}-1,2-этан-диамина определяли в дистиллированной воде (значение рН=5,0). Для определения рН приготавливали растворы солей N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметоксибензил)амино]этил}-1,2-этан-диамина с концентрацией 0,08 моль/л в 1 мл воды. Значения рН определяли с использованием интервальной индикаторной бумаги «Рифан» с интервалами определения «от 1,8 до 3,6», «от 4,0 до 5,4» и «от 1 до 11». Результаты определения значений рН водных растворов соединений АЛМ-802, АЛМ-802-S и АЛМ-802-С представлены в таблице 1.
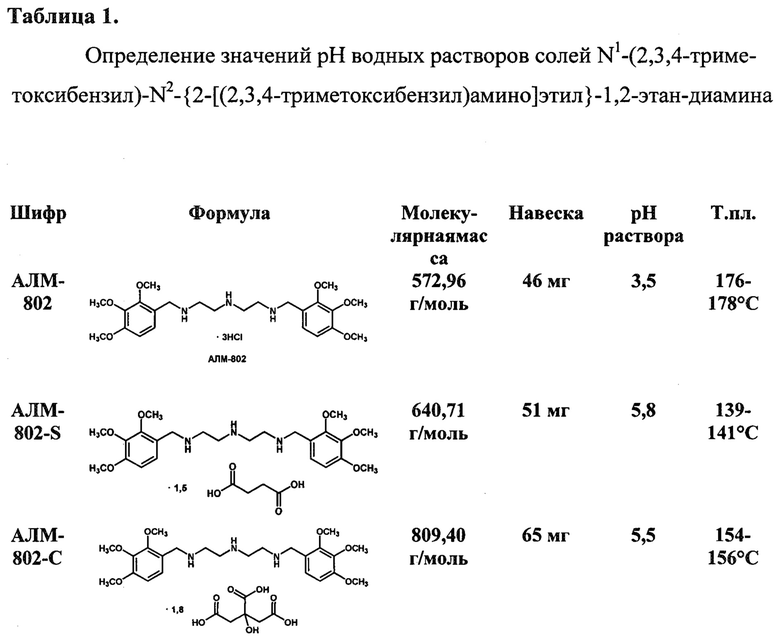
Согласно результатам определения рН водных растворов солей N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметоксибензил)амино]этил}-1,2-этандиамина значение рН 0,08 М раствора тригидрохлорида АЛМ-802 составило 3,5, в то время как для солей органических кислот - сукцината АЛМ-802-S и цитрата АЛМ-802-С - рН 0,08 М растворов составили 5,8 и 5,5, соответственно. Таким образом подтверждено преимущество полученных органических солей N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметоксибензил)-амино]этил}-1,2-этан-диамина, заключающееся в существенно более высоких значениях рН их водных растворов.
Пример 4. Фармакологическое изучение заявляемых соединений
Животные.
Животные содержались в стандартных условиях вивария ФГБНУ «НИИ фармакологи имени В.В. Закусова» при контролируемом освещении (12 ч - свет/12 ч - темнота) и постоянной температуре (+21 - +23°С) со свободным доступом к воде и брикетированному корму в течение 10 суток до начала тестирования. Условия содержания животных соответствовали ГОСТ 33215-2014 «Руководство по содержанию и уходу за лабораторными животными. Правила оборудования помещений и организации процедур» (Переиздание) и ГОСТ 33216-2014 «Руководство по содержанию и уходу за лабораторными животными. Правила содержания и ухода за лабораторными грызунами и кроликами» (Переиздание). Все работы с лабораторными животными были выполнены в соответствии с общепринятыми нормами обращения с животными, на основе стандартных операционных процедур, принятых в НИИ фармакологии имении В.В. Закусова, международными правилами (European Communities Council Directive of November 24, 1986 (86/609/EEC), а также в соответствии с «Правилами работы с животными», утвержденными биоэтической комиссией ФГБНУ «НИИ фармакологии имени В.В. Закусова».
Определение острой токсичности (LD50) заявляемых соединений.
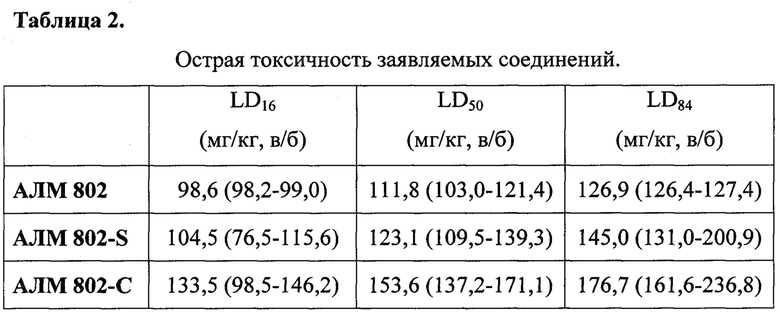
Острую токсичность заявляемых соединений изучали в опытах на беспородных альбиносах мышах - самцах массой тела 23-28 г. Животные были рандомизированы. Острую токсичность каждого соединения определяли в пяти различных дозах, количество животных в каждой группе - 6. Растворы вводили внутрибрюшинно, в качестве растворителя использовали 0,9% раствор натрия хлорида. Летальность животных в группах оценивали через 24 часа после введения заявляемых соединений. По методу Литчфилда-Вилкоксона рассчитывали LD16, LD50 и LD84 с их доверительными 95% интервалами.
Как следует из полученных данных, обе заявляемых соли относятся к соединениям IV класса токсичности, то есть являются малотоксичными веществами (табл. 2).
Изучение антиаритмической активности заявляемых соединений на модели аконитиновой аритмии.
Эксперимент проводили на беспородных альбиносах крысах - самцах массой тела 197-223 г. Вещества исследовали в дозах эквимолярных таковым соединения АЛМ-802 (3,5 мкмоль/кг). Животные были рандомизированы на 3 группы: 1-я (n=10) - контроль получала эквивалентный объем 0,9% раствор натрия хлорида для инфузий; 2-я (n=6) получала соединение АЛМ-802-S в дозе 2,15 мг/кг (концентрация раствора 2,15 мг/мл); 3-я (n=6) получала соединение АЛМ-802-С в дозе 2,75 мг/кг (концентрация раствора 2,75 мг/мл). В качестве растворителя использовали 0,9% раствор натрия хлорида для инфузий.
Наркотизированных животных (уретан, 250 мг/кг, в/б) фиксировали на спине. Через трахеальную канюлю проводили искусственную вентиляцию легких (вентилятор для грызунов фирмы «Ugo Basile») атмосферным воздухом с частотой 95 дыхательных движений в минуту объемом 2,5 мл. Мониторинг и запись ЭКГ вели в стандартных отведениях (компьютерный электрокардиограф «Поли-Спектр 8/В», Россия).
Далее подбирали минимальную дозу аконитина таким образом, чтобы во всех пробах контрольной группы в течение пяти минут от начала введения развивалась политопная экстрасистолия. В настоящем эксперименте величина подобранной дозы составила 30 мкг/кг. В опытных группах исследуемые вещества, а в контрольной группе 0,9% раствор натрия хлорида, вводили за две минуты до введения аконитина. Растворы вводили в бедренную вену болюсом. Регистрировали ЭКГ фонового состояния, далее в течение двух минут после введения исследуемых веществ и в течение 20 минут от начала введения аконитина. Критерием антиаритмического эффекта считали отсутствие политопной экстрасистолии в течение 10 минут после начала введения аконитина.
В каждой группе подсчитывали количество крыс с нарушениями ритма сердца. Статистическую обработку данных проводили с помощью метода точной вероятности Фишера с учетом множественности сравнений. Различия считали значимыми при р≤0,05.
Как следует из полученных данных, оба заявляемых соединения, как и соединение АЛМ-802, предотвращают политопные аритмии, вызываемые аконитином, на протяжении минимум 20 минут после введения минимально эффективной дозы аконитина (табл. 3).

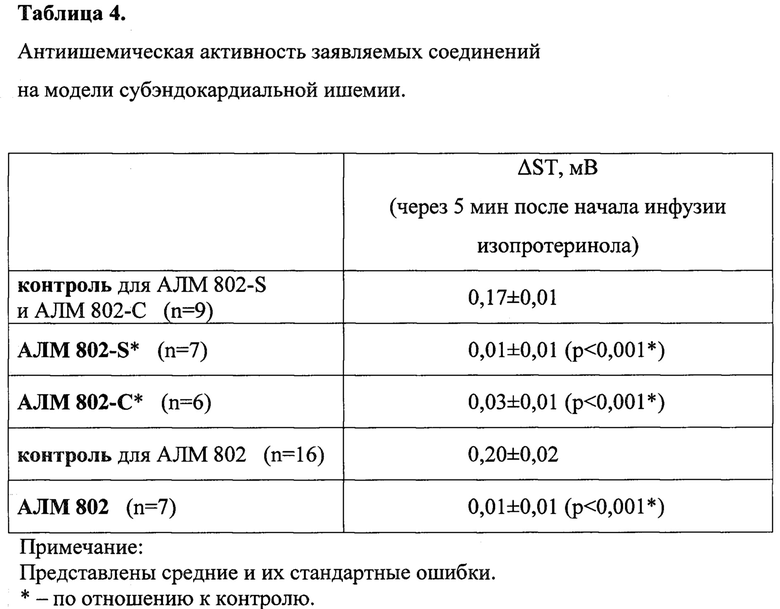
Изучение антиишемической активности заявляемых соединений на модели субэндокардиальной ишемии, вызываемой изопротеринолом.
Эксперимент проводили на беспородных альбиносах крысах - самцах массой тела 213-274 г. Исследуемые вещества вводили в дозах эквимолярных таковым соединения АЛМ-802. Животные были рандомизированы на 3 группы: 1-я (n=9) - контроль получала эквивалентный объем 0,9% раствор натрия хлорида для инфузий; 2-я (n=7) получала соединение АЛМ-802-S в дозе 2,15 мг/кг (концентрация раствора 2,15 мг/мл); 3-я (n=6) получала соединение АЛМ-802 С в дозе 2,75 мг/кг (концентрация раствора 2,75 мг/мл). В качестве растворителя использовали 0,9% раствор натрия хлорида для инфузий.
Наркотизированных животных (уретан, 250 мг/кг, в/б) фиксировали на спине. Мониторинг и запись ЭКГ вели в стандартных отведениях (компьютерный электрокардиограф «Поли-Спектр 8/В», Россия). В опытных группах исследуемые вещества, а в контрольной группе 0,9% раствор натрия хлорида, вводили в бедренную вену болюсно за 2 минуты до начала инфузий изопротеринола.
Острую субэндокардиальную ишемию миокарда вызывали по методу, описанному S. Yamamoto с соавторами [Effect of SMP-300, a new Na+/H+exchange inhibitor, on myocardial ischemia and experimental angina models in rats. // S. Yamamoto, K. Matsui, M. Sasabe, at all // Jpn J. Pharmacol. 84, 196-205 (2002)]. Для этого раствор неселективного агониста β-адренорецепторов изопротеренола вводили в бедренную вену посредством инфузомата (Линеомат, Россия) в дозе 20 мкг/кг/мин. Об интенсивности ишемического повреждения судили по депрессии сегмента ST на ЭКГ во II стандартном отведении через 5 минут от момента начала инфузии изопротеренола.
Статистический анализ проводили с помощью однофакторного дисперсионного анализа с дальнейшей обработкой методом множественных сравнений по Даннету.
Как следует из полученных данных, оба заявляемых соединения, как и соединение АЛМ-802, предотвращают депрессию сегмента ST, что свидетельствует о предотвращении субэндокардиальной ишемии, вызываемой изопротеринолом (табл. 4).
Заключение
Таким образом, установлено, что органические соли N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметоксибензил)амино]этил}-1,2-этан-диамина, такие как сукцинат и цитрат, полностью сохраняют антиаритмические и антиишемические свойства тригидрохлорида N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметоксибензил)амино]этил}-1,2-этан-диамина в эквимолярных дозах. Кроме того, новые соединения относятся к VI классу токсичности, то есть являются малотоксичными веществами.
Значения LD50 для органических солей N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметоксибензил)амино]этил}-1,2-этандиамина в пересчете на основание соответствуют таковому для его тригидрохлорида. При этом рН растворов органических солей N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметоксибензил)амино]этил}-1,2-этандиамина значительно выше чем для тригидрохлорида, что обуславливает отсутствие у полученных солей местнораздражающего действия и нежелательных органолептических свойств, ведущее к расширению спектра их использования в различных лекарственных формах, включая диспергируемые во рту и сублингвальные.
| название | год | авторы | номер документа |
|---|---|---|---|
| N-бензил-N-(2-((2,3,4-триметоксибензил)амино)этан-1,2-диамины, обладающие кардиотропной активностью | 2023 |
|
RU2834294C1 |
| 2,2'-окси- и 2,2'-тио-бис(N-(2,3,4-триметоксибензил)этан-1-амины), обладающие кардиотропной активностью | 2023 |
|
RU2813348C1 |
| ВЕЩЕСТВО, ВОССТАНАВЛИВАЮЩЕЕ ФИЗИЧЕСКУЮ РАБОТОСПОСОБНОСТЬ ПОСЛЕ ОСТРОГО УТОМЛЕНИЯ | 2021 |
|
RU2784542C2 |
| Бис(метоксибензиламиноалкил)амины, обладающие кардиотропной активностью | 2014 |
|
RU2624438C2 |
| Кардиотропное средство с анксиолитическими и анальгетическими свойствами | 2020 |
|
RU2773018C2 |
| БИС(АЛКОКСИБЕНЗИЛ)АЛКАНДИАМИНЫ, ОБЛАДАЮЩИЕ КАРДИОТРОПНОЙ АКТИВНОСТЬЮ | 2021 |
|
RU2791576C2 |
| 1-(Метоксибензил)-4-[2-((метоксибензил)амино)этил]пиперазины, обладающие антиаритмической активностью | 2018 |
|
RU2751878C2 |
| СПОСОБ ПОЛУЧЕНИЯ ДИГИДРОХЛОРИДА 1-(2,3,4-ТРИМЕТОКСИБЕНЗИЛ)ПИПЕРАЗИНА | 2002 |
|
RU2234501C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИГИДРОХЛОРИДА 1-(2,3,4-ТРИМЕТОКСИБЕНЗИЛ)ПИПЕРАЗИНА | 2007 |
|
RU2340606C1 |
| Замещенные 1,2,5-триметил- и 2,2,6,6-тетраметил-4-аминопиперидины, обладающие антиишемическим действием | 2015 |
|
RU2686317C2 |
Изобретение относится к способу получения органических солей N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметоксибензил)амино]этил}-1,2-этан-диамина общей формулы
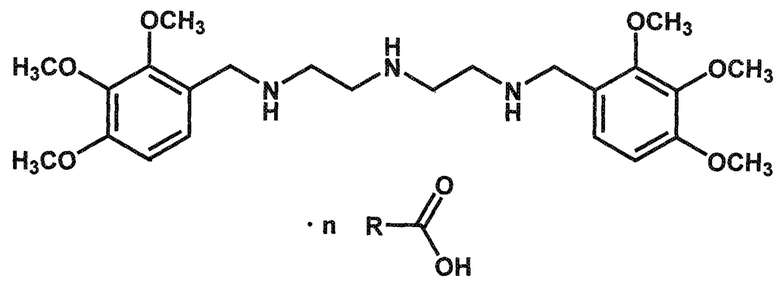
где n=1,5-2; R-С(O)ОН=лимонная или янтарная кислота, который заключается в том, что основание N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметоксибензил)амино]этил}-1,2-этандиамина вводят во взаимодействие с избытком органической кислоты, такой как янтарная или лимонная кислота, в растворах спиртов, таких как этанол или изопропанол при нагревании с последующей фильтрацией выпадающего осадка целевой соли. Технический результат – разработан способ получения новых солей N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметоксибензил)амино]этил}-1,2-этан-диамина, а именно сукцината и цитрата, которые являются малотоксичными и могут найти применение в медицине в качестве средств, обладающих кардиотропной активностью. 4 табл., 4 пр.
Способ получения органических солей N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметоксибензил)амино]этил}-1,2-этан-диамина общей формулы
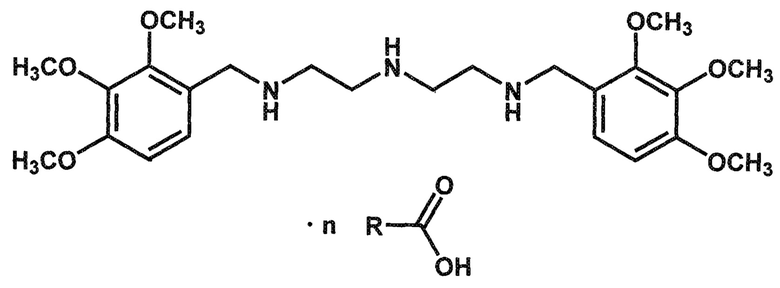
где n=1,5-2;
R-С(O)ОН=лимонная или янтарная кислота,
заключающийся в том, что основание N1-(2,3,4-триметоксибензил)-N2-{2-[(2,3,4-триметоксибензил)амино]этил}-1,2-этандиамина вводят во взаимодействие с избытком органической кислоты, такой как янтарная или лимонная кислота, в растворах спиртов, таких как этанол или изопропанол при нагревании с последующей фильтрацией выпадающего осадка целевой соли.
| Бис(метоксибензиламиноалкил)амины, обладающие кардиотропной активностью | 2014 |
|
RU2624438C2 |
| Бис(метоксибензиламиноалкил)амины, обладающие кардиотропной активностью | 2014 |
|
RU2624438C2 |
| Кардиотропное средство с анксиолитическими и анальгетическими свойствами | 2020 |
|
RU2773018C2 |
| 1-(Метоксибензил)-4-[2-((метоксибензил)амино)этил]пиперазины, обладающие антиаритмической активностью | 2018 |
|
RU2751878C2 |
| Способ получения производных @ -(3,3-дифенилпропил)-пропилендиамина или их солей | 1973 |
|
SU1014468A3 |
| US 5929112 A1, 27.07.1999. | |||
Авторы
Даты
2024-02-12—Публикация
2022-08-09—Подача