Изобретение относится к области синтеза лекарственных веществ и конкретно к получению дигидрохлорида 1-(2,3,4-триметоксибензил)пиперазина (I), являющегося субстанцией лекарственного препарата триметазидина.

Известен способ получения соединения (I), по которому 2,3,4-триметоксибензальдегид (II) и избыток пиперазина растворяют в спиртовом растворителе либо метил-трет-бутиловом эфире и гидрируют водородом в присутствии палладия на угле при 45-75°С, а полученное основание (I) переводят в дигидрохлорид действием соляной кислоты (патент США №5142053, кл. С 07 D 295/73, 1992 г.). Поскольку использование метил-трет-бутилового эфира для данного процесса в производстве практически исключено из-за свойств этого растворителя, в качестве прототипа принят пример со спиртовой средой.
78,4 г 2,3,4-триметоксибензальдегида (II), 137,6 г безводного пиперазина, 400 мл этанола и 4 г 5% Pd/C вносят в реактор, продувают азотом и водородом, а затем как можно скорее нагревают до 70°С, создавая при достижении 45°С давление водорода ~10 бар, и прекращают гидрирование через 70 мин. Реакционную смесь при 20°С фильтруют, фильтрат упаривают досуха, остаток вносят в 200 мл охлажденного до (-5) - (-10)°С толуола и фильтруют. К фильтрату прибавляют 200 мл воды, доводят до рН 6 прибавлением концентрированной соляной кислоты, органический слой отделяют, а водный экстрагируют дважды 120 мл толуола. К водному слою прибавляют 42 г едкого натра, экстрагируют трижды 120 мл толуола, объединенный экстракт упаривают досуха и получают основание (I) с выходом 92% и содержанием основного вещества 96,8% (по ВЭЖХ).
Нами в результате проведенного исследования установлено, что альдегид (II) и пиперазин вступают в поликонденсацию с образованием олигомеров (VI) (см. схему превращений):
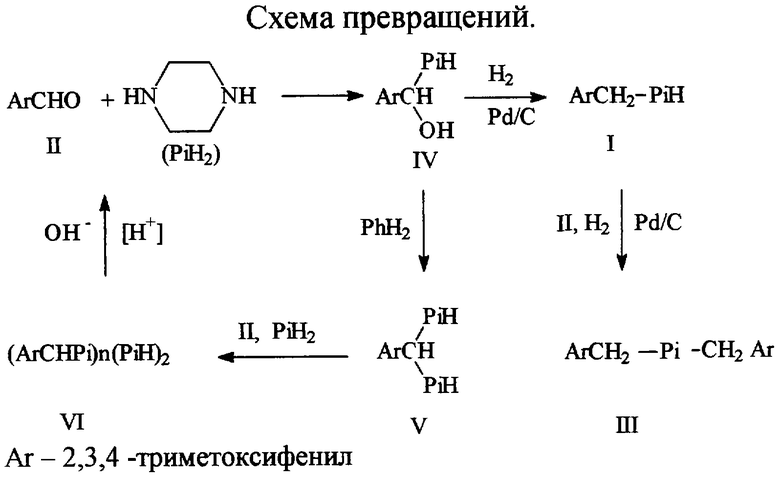
Реакция идет уже на холоду, сильно ускоряясь при нагревании, и исключить ее в условиях указанного патента не удается. Помимо вывода альдегида (II) из целевого направления процесса, образование олигомеров вызывает большие осложнения, т.к. они обладают вязкими, клейкими свойствами и осаждаются на поверхности катализатора и аппаратуры. Последнее, в частности, приводит к заклиниванию ротора мешалки автоклава с индукционным приводом и в принципе противопоказано для производства. По прототипу, вероятно, для того, чтобы уменьшить образование олигомеров, раствор обоих реагентов нагревают как можно быстрее до 70°С и начинают гидрирование при 45°С. Однако в производстве вообще нельзя быстро нагреть, используя традиционные методы обогрева, из-за тепловой инерционности больших объемов действующих масс. А при моделировании производственных условий реакционная смесь превращается в гелеобразную массу.
Недостатком известного способа является то, что его абсолютно невозможно использовать в производственных условиях из-за протекания рассмотренной выше побочной реакции.
Задачей настоящего изобретения является создание способа, который может быть освоен в промышленном масштабе. Это достигается тем, что 2,3,4-триметоксибензальдегид (II) вводится в реакцию постепенно при температуре 80-85°С.
Раствор альдегида (II) постепенно прибавляется к раствору пиперазина, содержащему Pd/C, нагретому до 80-85°С при рабочем давлении водорода (5-10 ата). В качестве растворителя нами использован изопропанол. Повышение температуры увеличивает скорость гидрирования, благодаря чему первичный продукт взаимодействия - аминоспирт (IV) быстро превращается в целевой продукт (I), что уменьшает вероятность образования гем-диамина (V) и дальнейшей поликонденсации. Реакция завершается во время прибавления водорода (30 мин), на что указывает прекращение падения давления водорода. Одновременно постепенное прибавление альдегида уменьшает и степень протекания другой нежелательной реакции, приводящей к образованию 1,4-ди(2,3,4-триметоксибензил)пиперазина (III), т.к. создается громадный избыток пиперазина в каждой точке процесса по времени.
В приведенных условиях не наблюдается осложнений, связанных с образованием олигомеров. Более того, их образование можно вообще исключить. Установлено, что олигомеры (VI) быстро гидролизуются при кислотном катализе. Вода всегда имеется в реакционной смеси, т.к. выделяется по реакции и в определенных количествах вносится с реагентами. В условиях процесса гидролизу должен подвергаться гем-диамин (V) в момент образования, что исключает последующую поликонденсацию. Однако гидролизоваться может и аминоспирт (IV). Поэтому количество и сила кислоты должны быть оптимальными. Так, при введении в реакционную смесь уксусной кислоты в количестве 1-2% к весу альдегида (II) наблюдается повышение выхода конечного продукта (до 5%), что указывает на более полное участие альдегида в основной реакции.
На основную реакцию оказывают влияние и свойства реакционной среды. В неполярных средах она протекает с гораздо меньшей скоростью, что в свете вышеизложенного нежелательно. Однако добавление части, например, толуола практически не влияет на ход процесса. Это важно, т.к. позволяет использовать толуольный раствор альдегида (II), получающийся на предыдущей стадии синтеза субстанции триметазидина и не содержащий других примесей, кроме исходного 1,2,3-триметоксибензола (благодаря очистке). Введение толуола в реакционную смесь также хорошо сочетается с последующей заменой им изопропанола. Примесь инертного в реакции 1,2,3-триметоксибензола остается в толуоле при переводе продукта в водный слой.
Изобретение иллюстрируется следующими примерами конкретного выполнения.
Пример 1
В автоклав вносят 100 мл изопропанола, 34,4 г пиперазина и 2 г 5% палладия на угле, продувают азотом и водородом, создают давление водорода 5 ата, нагревают до 80-85°С и постепенно в течение 30 мин прибавляют раствор 38,2 г 2,3,4-триметоксибензальдегида, через 15 мин охлаждают, сбрасывают давление и отделяют катализатор. Отгоняют изопропанол, остаток растворяют в 150 мл толуола, охлаждают до -5°С и отфильтровывают пиперазин. К фильтрату при перемешивании добавляют 100 мл воды и соляную кислоту, доводя до рН 7,9-8, к водному слою добавляют 22 г едкого натра и экстрагируют дважды 60 мл толуола. Из экстракта отгоняют толуол, добавляют 100 мл изопропанола и постепенно прибавляют раствор 30 г 35% соляной кислоты в 150 мл изопропанола, отгоняют 150 мл смеси изопропанол - вода, охлаждают до 0-5°С, перемешивают 1 ч, отфильтровывают кристаллический осадок, промывают изопропанолом, сушат и получают 54,9 г дигидрохлорида 1-(2,3,4-три-метоксибензил)пиперазина, выход 81%, содержание 99,9-100% (по ВЭЖХ).
Пример 2
Проводят аналогично примеру 1, но в присутствии 0,5 г уксусной кислоты. Получают дигидрохлорид 1-(2,3,4-триметоксибензил)пиперазина с выходом 85%.
Пример 3
К комплексу, полученному смешением 120 г диметилформамида и 220 г хлорокиси фосфора, прибавляют 160 г 2,3,4-триметоксибензальдегида, нагревают 9 ч при 80°С, охлаждают, выливают на 1,5 кг смеси лед - вода, перемешивают 4-5 ч и экстрагируют 400 г толуола. Экстракт промывают дважды 150 мл 10%-ного раствора едкого натра и дважды 150 мл насыщенного водного раствора хлористого натрия, отгоняют 200 г толуола, а также немного воды, и определяют содержание 2,3,4-триметоксибензальдегида методом ГЖХ. Часть полученного раствора (80-85 г), содержащую 38,2 г 2,3,4-триметоксибензальдегида, постепенно в течение 30 мин прибавляют к 34,4 г пиперазина и 2 г 5% Pd/C в 200 мл изопропанола при 80-85°С и давлении водорода 5 ата. Далее проводят аналогично примеру 1 и получают дигидрохлорид 1-(2,3,4-триметоксибензил)пиперазина с выходом 80%, содержание 99,9-100% (по ВЭЖХ).
Заявляемый способ получения дигидрохлорида 1-(2,3,4-триметокси-бензил)пиперазина может быть освоен в промышленном масштабе.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ДИГИДРОХЛОРИДА 1-(2,3,4-ТРИМЕТОКСИБЕНЗИЛ)ПИПЕРАЗИНА | 2007 |
|
RU2340606C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3,4-ТРИМЕТОКСИБЕНЗАЛЬДЕГИДА | 2002 |
|
RU2236397C1 |
| БИС(АЛКОКСИБЕНЗИЛ)АЛКАНДИАМИНЫ, ОБЛАДАЮЩИЕ КАРДИОТРОПНОЙ АКТИВНОСТЬЮ | 2021 |
|
RU2791576C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3,4-ТРИМЕТОКСИБЕНЗАЛЬДЕГИДА | 2003 |
|
RU2234492C1 |
| Бис(метоксибензиламиноалкил)амины, обладающие кардиотропной активностью | 2014 |
|
RU2624438C2 |
| 2,2'-окси- и 2,2'-тио-бис(N-(2,3,4-триметоксибензил)этан-1-амины), обладающие кардиотропной активностью | 2023 |
|
RU2813348C1 |
| 1-(Метоксибензил)-4-[2-((метоксибензил)амино)этил]пиперазины, обладающие антиаритмической активностью | 2018 |
|
RU2751878C2 |
| Способ получения 9(3-амино-1-пропенил) -9,10-дигидро-9,10-этаноантраценов | 1973 |
|
SU502602A3 |
| N-бензил-N-(2-((2,3,4-триметоксибензил)амино)этан-1,2-диамины, обладающие кардиотропной активностью | 2023 |
|
RU2834294C1 |
| Способ получения сульфонильных соединений | 1972 |
|
SU559646A3 |
Изобретение относится к области синтеза лекарственных веществ, конкретно, к получению дигидрохлорида 1-(2,3,4-триметоксибензил)пиперазина (I), являющегося субстанцией лекарственного препарата триметазидина. Соединение (I) получают взаимодействием 2,3,4-триметоксибензальдегида с пиперазином путем каталитического гидрирования водородом на катализаторе палладий на угле при температуре 80-85°С, причем 2,3,4-триметоксибензальдегид вводят в реакцию постепенно. Также возможно проведение реакции в присутствии каталитических количеств уксусной кислоты. Настоящий способ может быть освоен в промышленном масштабе.
| ПРОИЗВОДНЫЕ 1-[(3-ХЛОРКАРБАЗОЛИЛ-9)-3-(2-ОКСИПРОПИЛ)]-ПИПЕРАЗИНА, ПРОЯВЛЯЮЩИЕ АНКСИОЛИТИЧЕСКУЮ АКТИВНОСТЬ | 1989 |
|
SU1584341A1 |
| US 5142053 A, 25.08.1992 | |||
| КОМПОЗИЦИЯ ДЛЯ УКРЕПЛЕНИЯ ГРУНТОВ | 2011 |
|
RU2493316C2 |
Авторы
Даты
2004-08-20—Публикация
2002-12-25—Подача