Настоящее изобретение относится к области гальванотехники, а именно к способам нанесения защитных покрытий на титан и его сплавы.
Титан обладает отличной коррозионной стойкостью в самых суровых условиях и промышленных решениях. Высокая коррозионная стойкость титана обеспечивается за счет образования на поверхности сплошного оксидного покрытия, хорошо сцепляющегося с основным металлом. Но в растворах сильных кислот при температуре окружающей среды и температуре кипения развивается интенсивная коррозия титана (происходит разрушение защитного оксидного покрытия), что приводит к переходу металла из пассивного состояния в активное и к увеличению скорости коррозии. Примерами таких сред являются серная, соляная и фосфорная кислоты, кислые растворы концентрированных галогенидов.
Актуальным является необходимость повышения коррозионной стойкости титана и титановых сплавов в указанных выше растворах сильных кислот, содержащих галогенид-ионы, при различной температуре.
В настоящее время перспективным подходом является повышение анодного торможения коррозионного процесса за счет легирования титана, которое облегчает переход сплава в пассивное состояние или повышает устойчивость этого состояния. Существуют две принципиально различные возможности такого повышения пассивируемости: легирование, непосредственно повышающее пассивируемость (анодную поляризуемость), и легирование, облегчающее протекание катодного процесса. В последнем случае происходит смещение электродного потенциала коррозии сплава в пассивную область, и пассивация наступает при неизменной анодной характеристике основы сплава.
Одним из вариантов является нанесение (формирование) толстого оксидного слояна титане.
Из существующего уровня техники известен способ обработки титана и его сплавов с целью повышения его коррозионной стойкости (патент RU2756672, МПК C25D 11/26, опубл. 04.10.2021).Способ включает микродуговое оксидирование в растворе КОН при напряжении формовки 500-550 В, анодно-катодном режиме с частотой 50 Гц, при равенстве анодного и катодного токов и плотности тока 45 А/дм2, при этом микродуговое оксидирование проводят в электролите, содержащем 3 г/л КОН и 1-5 г/л семиводного сульфата никеля NiSO4⋅7Н2О, при продолжительности микродугового оксидирования не менее 10 минут.
Недостатками данного технического решения являются сложность аппаратурного оформления и высокая энергоемкость процесса.
Кроме того, возможно создание на поверхности титана и титановых сплавов нитридных пленок.
Известен способ формирования покрытия на поверхности титана и его сплавов, включающий электролитическое получение тонкого слоя нитрида титана на поверхности титана, в котором формирование покрытия осуществляют методом анодной поляризации при постоянном токе в электролитах на основе полярных органических растворителей с добавлением воды в присутствии 0,1-0,5 мас. % электропроводящих добавок с барботированием азотсодержащим газом, при этом электролиз проводят при комнатной температуре электролита (RU2496924, МПК C25D9/06, C25D11/26, опуб. 27.10.2013).
Известен способ модификации поверхности изделий из титановых сплавов, включающий электроискровое легирование поверхностного слоя, при этом электроискровое легирование проводят нитридообразующими элементами или сплавами на их основе, затем осуществляют термическое оксидирование в окислительной воздушной среде при температуре 600-800°С в течение 2-16 ч или диффузионное азотирование, которое проводят в каталитически приготовленных газовых аммиачных средах при температуре 500-680°С и времени выдержки 15-40 ч (патент RU2346080, МПК C23C26/00, С23С8/02, опуб. 10.02.2009).
Недостатком известных способов является сложность аппаратурного оформления, высокие затраты энергии при получении защитных покрытий на титане и его сплавах.
Из научной литературы известно, что модифицирование пассивирующихся сплавов добавками катодно-активного электроположительного металла (Pd, R, Ru) оказывает сильное влияние на повышение пассивируемости и коррозионной стойкости даже при малом содержании катодного компонента в сплаве (доли процента). Такой эффект катодных добавок объясняется электрохимическим механизмом действия добавок и накоплением электроположительного легирующего элемента в начальный период активной коррозии на поверхности сплава. Это позволяет повысить коррозионную стойкость [Томашов Н.Д., Чернова Г.П., Федосеева Т.А. Катодное легирование поверхности титана, хрома и нержавеющих сталей - новый метод повышения их пассивируемости и коррозионной стойкости. Сборник научных трудов «Защита металлов от коррозии в химической промышленности». - М.: НИИТЭХИМ, 1979. - 119 с.].
Из уровня техники известен способ нанесения палладия на титан, который включает электролитическое осаждение палладия, проводимое при плотности тока 10 мА/см2 в аминохлоридном электролите, содержащем 25 г/л хлорида палладия (15 г/л палладия в пересчете на металл), аммиак до рН 9, аммоний хлористый 10 г/л; протальбиновую кислоту 0,2 г/л, в течение 10 мин (Томашов Н.Д. Титан и коррозионно-стойкие сплавы на его основе. - М.: Металлургия, 1985. - 80 с. С. 66-67). Данный способ выбран в качестве прототипа.
Недостатками прототипа являются высокий расход палладия при формировании сплошного слоя покрытия, существенные энергозатраты при его осуществлении.
Технической проблемой, на решение которой направлено заявляемое изобретение, является снижение материальных и энергозатрат при сохранении или улучшении защитных свойств палладиевого покрытия на титане и его сплавах.
Данная проблема решается способом обработки титана и его сплавов, включающим электрохимическое осаждение палладия на поверхность титана или его сплава в электролите, содержащем ионы палладия и хлора, в котором процесс ведут при переменном токе частотой 0,01-0,1 Гц при плотности тока 1-10 мкА/см2 в электролите, содержащем хлорид натрия в количестве 58,5±0,5 г/л и хлорид палладия в количестве 1±0,1 г/л, в течение 60 мин.
Техническим результатом является снижение расхода палладия уменьшается в 150 раз, а электроэнергии - минимум в 180 раз, по показателю коррозионного расхода образцы с полученным покрытием не уступают образцам, полученным по прототипу.
Сущность способа заключается в следующем.
Для обеспечения противокоррозионной защиты нет необходимости нанесения сплошного покрытия, достаточно нанести локальное покрытие.
В прототипе электроосаждение палладиевого покрытия осуществляют при постоянном токе, при этом на поверхности образца формируется сплошное покрытие. В предлагаемом способе покрытие осаждается в условиях воздействия переменного тока, что позволяет нанести на обрабатываемую поверхность титана или титанового сплава локальное палладиевое покрытие, которое формируется за счет вытравливания «слабых» мест поверхности в анодный период и осаждения частиц палладия в катодный период [И.Л. Розенфельд Коррозия и защита металлов (локальные коррозионные процессы). - Москва: Металлургия, 1970. - 448 с]. Поляризуя исследуемый металл слабым переменным током низкой частоты (в присутствии раствора, содержащего Cl- анионы и ионы благородного металла (например, Pd2+) возможно достигнуть осаждения островковых нанопокрытий данного металла в местах, подвергшихся локальному травлению и зонах концентрирования поверхностных дефектов.
В заявляемом способе предлагается использовать поляризацию переменными слабыми токами плотностью 1-10 мкА/см2 и частотой 0,01-0,1 Гц в электролите, содержащем ионы палладия и хлора. Данные условия выбраны исходя из фактов протекания локальных процессов на поверхности пассивирующегося металла - титана или его сплавов - в хлоридсодержащих средах, приводящих к появлению локальных субмикронных очагов растворения.
В случае низких частот (ниже 0,01 Гц) процесс осаждения существенно замедлится, а при частоте выше 0,1 Гц осаждение палладия не происходит, т.к. данная частота не способствует синхронизации процесса растворения/осаждения с внешним переменным током.
Концентрация хлорида палладия 1±0,1 г/л в электролите обеспечивает получение локального палладиевого покрытия с коррозионной стойкостью, не уступающей прототипу. Выбор концентрации хлориданатрия 58,5±0,5 г/л обусловлен тем, что данная концентрация хлорид-ионов оптимальна для протекания локальных процессов активации, пассивации поверхности и формирования локального осадка благородного металла.
Оптимальное время осаждения локального палладиевого покрытия составляет 60 мин. Увеличение времени нецелесообразно, т.к. увеличивается расход палладия и электроэнергии, а коррозионная стойкость практически не изменяется, а уменьшение времени поляризации приводит к ухудшению коррозионной стойкости.
Примеры конкретного осуществления способа
Хлорид натрия выбран в качестве источника хлорид ионов, а хлорид палладия в качестве источника ионов палладия.
Образцы титанового сплава ВТ1-0 предварительно обезжиривали этанолом и промывали водой. Затем помещали в электрохимическую ячейку с электролитом, содержащим хлорид натрия 58,5 г/л и хлорид палладия 1 г/л, и подключали к потенциостату в качестве рабочего электрода, туда же опускали платиновый электрод в качестве вспомогательного электрода и хлоридсеребряный электрод сравнения. К потенциостату подключали генератор электрических сигналов для наложения внешней частотной составляющей. После этого выдерживали образец в растворе 15 минут и проводили поляризацию в гальваностатическом режиме при плотности тока в диапазоне 1-10 мкА/см2 и частотной составляющей, равной 0,01-0,1 Гц, в течение 1 часа.
Пример 1. Электролит заливают в электрохимическую ячейку. Затем в него помещают обезжиренный образец титанового сплава и подключают его к клемме потенциостата «Work», помещают в ячейку хлоридсеребряный электрод сравнения и подключают к клемме «Ref», вспомогательный платиновый электрод подсоединяют к клемме «Counter». К потенциостату подключают внешний генератор сигналов и устанавливают значение 0,01 Гц. В программе потенциостата устанавливают значение тока, равное 1 мкА/см2 и запускают процесс. Процесс осаждения проводят в течение 60 мин. После завершения процесса пластину с покрытием промывают водой и высушивают на воздухе.
Примеры 2-9 аналогичны примеру 1, режимные условия процесса сведены в таблицу.
Пример 10 аналогичен примеру 1, но концентрацию хлорида палладия уменьшили в 10 раз для того, чтобы показать, что при снижении хлорида палладия коррозионный расход увеличивается до 0,46 г/м2⋅час.
Пример 11 аналогичен примеру 1, но концентрацию хлорида натрия уменьшили в 10 раз для того, чтобы показать, что при снижении хлорида натрия коррозионный расход увеличивается по сравнению с прототипом до 0,30 г/м2⋅час.
Пример 12 по способу-прототипу.
Покрытие осаждают из электролита состава: 25 г/л хлорида палладия; аммиак до рН 9; аммоний хлористый 10 г/л; протальбиновая кислота 0,2 г/л; плотность тока 10 мА/см2; время осаждения 10 мин.
После осаждения образец промывают и высушивают на воздухе.
Полученные образцы исследовали методами растровой электронной микроскопии (РЭМ) и Оже-электронной спектроскопии (ОЭС) в соответствии с методикой ASTM Е 827 08 для исследования морфологии поверхности.
На фиг. 1-2 приведены РЭМ-изображения поверхности образца во вторичных (SEI), композиционный контраст (СОМРО), приборное увеличение *10000.
Затем проводили коррозионные испытания и рассчитывали затраты электроэнергии и расход палладия следующим образом.
После нанесения покрытий образцы выдерживают в 10% (100 г/л) HCl в течение 30 мин. Фиксируют массу до испытания и после, измеряют площадь рабочей поверхности образца и рассчитывают коррозионный расход по формуле:

где КР М коррозионный расход, г/м2⋅час; m0 - начальная масса образца, г; m1 - масса образца после коррозионного процесса после удалении продуктов коррозии, г; S0 - поверхность образца, м2; τ - время коррозии, час.
Исходя из среднего значения задаваемого тока, напряжения, продолжительности электрохимического осаждения, рассчитывают затраты электроэнергии на 1 дм2 поверхности металла:
Е=Р⋅τ=I⋅U⋅cosϕ⋅τ,
где Е - расход электроэнергии за единицу времени, Вт⋅ч/дм2; Р - активная мощность в цепи переменного тока, Вт; I - среднее значение задаваемого тока, A; U - напряжение питания прибора, B; cosϕ - коэффициент мощности переменного тока, безразмерная величина, cosϕ=0,92; τ - продолжительность электрохимического осаждения, ч,
а также расход палладия по закону Фарадея:
m=k⋅I⋅τ,
где k - электрохимический эквивалент, г/А⋅ч; I - среднее значение задаваемого тока, А; τ - продолжительность электрохимического осаждения, ч.
Результаты приведены в таблице в сравнении с прототипом.
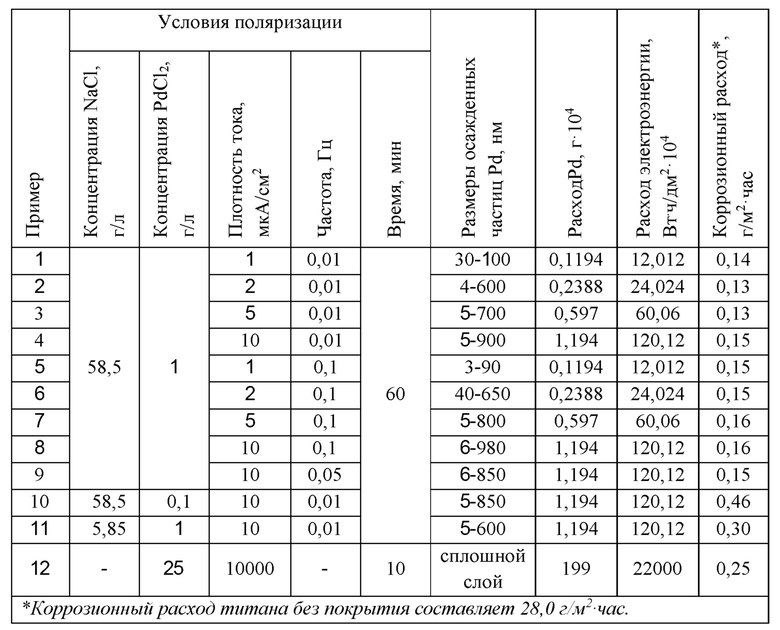
Изображения поверхности обработанных предлагаемым способом титановых образцов (фиг. 1-2) свидетельствуют об образовании на поверхности обрабатываемого металла локального палладиевого покрытия. Размеры частиц Pd лежат в пределах от 40-50 нм до 500-600 нм.
Как видно из таблицы обработанные предлагаемым способом образцы (примеры 1-9) по сравнению с прототипом (пример 14) более коррозионноустойчивые (коррозионный расход в 1,5 раза меньше, чем у прототипа), при этом расход палладия уменьшается минимум в 150 раз, а электроэнергии - минимум в 180 раз.
Как видно из таблицы уменьшение хлорида палладия (пример 10) и хлорида натрия (пример 11) в 10 раз приводит к увеличению коррозионного расхода по сравнению с прототипом (пример 12).
Таким образом, заявляемое изобретение позволяет модифицировать поверхность титана или титанового сплава путем локального электроосаждения палладия, придавая антикоррозионные свойства, не худшие по сравнению с прототипом при существенно меньших расходах палладия и электроэнергии.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ электрохимического легирования | 1989 |
|
SU1723204A1 |
| Способ обработки титана и его сплавов с целью повышения его коррозионной стойкости и электролит для микродугового оксидирования титана и его сплавов с целью повышения коррозионной стойкости | 2021 |
|
RU2756672C1 |
| Электролит для осаждения покрытий из сплава палладий-индий | 1980 |
|
SU931812A1 |
| Способ получения защитных антикоррозионных покрытий на сплавах алюминия со сварными швами | 2019 |
|
RU2703087C1 |
| Способ получения коррозионностойкого электрохимического покрытия цинк-никель-кобальт | 2019 |
|
RU2720269C1 |
| СПОСОБ ПОЛУЧЕНИЯ СУПЕРГИДРОФОБНЫХ ЗАЩИТНЫХ ПОКРЫТИЙ НА ТИТАНЕ И ЕГО СПЛАВАХ | 2010 |
|
RU2441945C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАЩИТНЫХ СУПЕРГИДРОФОБНЫХ ПОКРЫТИЙ НА СТАЛИ | 2012 |
|
RU2486295C1 |
| СПОСОБ ФОРМИРОВАНИЯ КОРРОЗИОННО-СТОЙКОГО ПОКРЫТИЯ НА ИЗДЕЛИЯХ ИЗ ТИТАНОВЫХ СПЛАВОВ | 2010 |
|
RU2451771C2 |
| СПОСОБ НАНЕСЕНИЯ ОКИСНО-МЕТАЛЛИЧЕСКИХ ПОКРЫТИЙ НА ПОВЕРХНОСТЬ НЕЛЕГИРОВАННОЙ СТАЛИ | 2014 |
|
RU2588962C2 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИКОРРОЗИОННЫХ ПОКРЫТИЙ НА СТАЛИ | 2009 |
|
RU2392360C1 |

Изобретение относится к области гальванотехники, а именно к способам нанесения защитных покрытий на титан и его сплавы. Способ включает электрохимическое осаждение палладия на поверхность титана или его сплава в электролите, содержащем 58,5±0,5 г/л хлорида натрия и 1±0,1 г/л хлорида палладия, при переменном токе частотой 0,01-0,1 Гц при плотности тока 1-10 мкА/см2 в течение 60 мин. Техническим результатом является снижение расхода палладия и энергозатрат при обеспечении коррозионной стойкости не хуже, чем у прототипа. 2 ил., 1 табл., 12 пр.
Способ обработки титана и его сплавов, включающий электрохимическое осаждение палладия на поверхность титана или его сплава в электролите, содержащем ионы палладия и хлора, отличающийся тем, что процесс ведут при переменном токе частотой 0,01-0,1 Гц при плотности тока 1-10 мкА/см2 в электролите, содержащем 58,5±0,5 г/л хлорида натрия и 1±0,1 г/л хлорида палладия, в течение 60 мин.
| SU 224243 A1, 28.11.1968 | |||
| Томашов Н.Д | |||
| Титан и коррозионно-стойкие сплавы на его основе | |||
| М., Металлургия, 1985 | |||
| СПОСОБ МОДИФИЦИРОВАНИЯ ПОВЕРХНОСТИ ТИТАНА И ЕГО СПЛАВОВ | 2012 |
|
RU2496924C1 |
| US 3920526 A1, 18.11.1975. | |||
Авторы
Даты
2024-02-12—Публикация
2023-10-24—Подача