Изобретение относится к медицине, а именно к лечению тромботических микроангиопатий. Тромботическая тромбоцитопеническая пурпура (ТТП) – заболевание, проявляющееся неиммунной тромбоцитопенией, микроангиопатической гемолитической анемией и нарушением функций органов и систем вследствие тромбоза мелких артерий. Причиной ТТП является дефицит металлопротеиназы ADAMTS13, расщепляющей высокомолекулярный фактор фон Виллебранда. Диагноз ТТП подтверждается при выявлении в плазме крови активности ADAMTS13 < 10% [1].
При приобретенной ТТП происходит выработка аутоантител, ингибирующих активность ADAMTS13. ТТП – угрожающее жизни состояние. Среди пациентов с ТТП в переводе в отделение реанимации нуждались 40%, в инфузии катехоламинов – 34%, проведении искусственной вентиляции легких – 30% пациентов, внутрибольничная смертность достигала 32% [2].
При лечении ТТП различают следующие понятия. Клинический ответ - нормализация концентрации тромбоцитов выше нижней границы (> 150 х109/л) и активность лактатдегидрогеназы (ЛДГ) не превышает 1,5 нормы после прекращения терапевтических плазмообменов (ТПО). Клиническая ремиссия - клинический ответ, сохраняющийся после прекращения ТПО более 30 дней. Частичная ADAMTS13-ремиссия - состояние, когда у пациента плазменная активность ADAMTS13 ≥ 20%, но ниже нижней границы нормы для данного метода определения активности. Полная ADAMTS13-ремиссия - состояние, когда у пациента плазменная активность ADAMTS13 выше нижней границы нормальных значений для данного метода определения активности.
Известен способ лечения ТТП с применением терапевтического плазмообмена (ТПО), который позволяет удалять ингибитор ADAMTS13, восполнять дефицит ADAMTS13, элиминировать мультимеры фактора фон Виллебранда [3]. В контролируемом рандомизированном исследовании клинический ответ был лучше у тех, кому проводили ТПО по сравнению с теми, кому выполняли трансфузии свежезамороженной плазмы (СЗП): в группе ТПО ответ получен у 47% пациентов, в группе СЗП – у 25% (р =0,025), умерли 3,9% пациентов, леченных ТПО, и 15,7%, леченных СЗП. Через 6 мес. от начала лечения в группе ТПО было 78 % ответивших на терапию, в группе СЗП 49 % (р = 0,002 [4]. Недостатком этого метода является неполное достижение ремиссии у всех пациентов, сохраняющийся риск развития рецидива заболевания при прекращении ТПО.
Известен способ лечения ТТП с применением глюкокортикостероидов (ГКС), основанный на способности ГКС подавлять продукцию антител к ADAMTS13 [5]. Назначение ГКС увеличивает выживаемость больных ТТП [6,7] Для начального лечения используют дозу 1 мг/кг массы тела пациента в пересчете на преднизолон, при тяжелом течении применяют большие дозы ГКС. Рекомендуют сочетать с ТПО [8]. Недостатками этого метода является невысокая частота достижения ремиссии, возможные летальные исходы, высокая частота рецидивов. При назначении ГКС в сочетании с ТПО у 23-43% больных не была достигнута ремиссия на 9 сутки лечения, а на 23 сутки ремиссия не была достигнута у 3-13% пациентов, смертельные исходы были у 3-13% пациентов [9], частота рецидивов составила 38% [10].
Известен способ лечения ТТП с применением ритуксимаба, который элиминирует В-лимфоциты, уменьшая тем самым продукцию ингибитора ADAMTS13 [11]. Ритуксимаб не является препаратом для лечения острой фазы заболевания, его эффект наступает отсрочено, он используется для достижения и сохранения ремиссии, предотвращения рецидивов заболевания [8,11–14]. Средний интервал до повышения количества тромбоцитов после первой инфузии ритуксимаба составляет 12 дней [15]. Недостатком этого метода является то, что ритуксимаб не может применяться для лечения острой атаки ТТП. Другим недостатком является то, что поскольку ритуксимаб применяется часто у больных ТТП, которым одновременно проводится ТПО, то после каждой процедуры ТПО концентрации ритуксимаба в сыворотке уменьшается на 65% [16] и, следовательно, необходимо либо увеличивать дозу ритуксимаба, либо кратность его введения (каждые 3-4 дня) [16,17].
Известен способ лечения ТТП с применением каплацизумаба. Каплацизумаб - гуманизированный, двухвалентный фрагмент иммуноглобулина с вариабельным доменом, ингибирующий взаимодействие тромбоцитов с фактором фон Виллебранда, уменьшающий тем самым адгезию тромбоцитов и препятствующий микрососудистому тромбозу [10]. Недостатком этого метода является то, что эффект достигается только при введении препарата, он не влияет на активность ADAMTS13, а при прекращении лечения возникает рецидив заболевания [10].
Ближайшим прототипом лечения ТТП является способ сочетанного применения каплацизумаба, иммуносупрессии и ТПО – «триплет-терапия» [18]. Этот способ лечения подразумевает назначение каплацизумаба сразу же после установки диагноза ТТП в дозе 10 мг внутривенно перед ТПО, затем после ТПО и в дальнейшем ежедневно в дозе 10 мг подкожно. ТПО проводят до увеличения количества тромбоцитов крови ≥150 х 109/л, сохраняющееся в течение не менее двух дней. Лечение каплацизумабом по 10 мг подкожно ежедневно продолжают в течение 30 дней после прекращения проведения ТПО (всего 35 дней). Ритуксимаб в дозе 375 мг/м2 вводят в 1-ый, 4-ый, 8-ой и 15-ый дни лечения [18]. Преимуществами этого метода по сравнению с другими методами лечения является в 1,8 раз более быстрое достижение нормализации количества тромбоцитов крови, меньшая потребность в проведении сеансов ТПО, меньшая частота обострения ТТП, меньшая длительность госпитализации [18].
Недостатками является то, что после каждой процедуры ТПО медиана уменьшения концентрации ритуксимаба в сыворотке составляет 65% [16] и, следовательно, необходимо увеличивать дозу ритуксимаба либо кратность его введения. При введении неполных доз ритуксимаба риск развития рецидивов увеличивается более чем в 2 раза [13].
Еще одним недостатком является тот факт, что прекращение лечения не ориентировано на достижение ремиссии, определяемой по плазменной активности ADAMTS13 [19]. Хотя, согласно данной схеме терапии, у большинства пациентов с ТТП к окончанию лечения достигается ремиссия, всегда остаются пациенты, у которых сохраняется низкая активность ADAMTS13, этим можно объяснить рецидивы, возникшие у получавших каплацизумаб при последующем наблюдении [10].
Еще одним ограничением прототипа является высокая стоимость лечения. Каплацизумаб является дорогостоящим препаратом. Согласно опубликованным данным, стоимость 10 мг составляет 7700 долларов США, следовательно на курс лечения (35 введений) требуется препарат на сумму 270 000 долларов США [20].
Технической задачей, на решение которой направлено предлагаемое изобретение, является разработка альтернативного способа лечения пациентов с приобретенной формой ТТП, имеющего уменьшенную стоимость лечения, а также повышение эффективности способа лечения пациентов с приобретенной формой ТТП.
Поставленная задача решается способом, заключающимся в том, что пациенту после установления диагноза ТТП в первый же день начинают лечение каплацизумабом, ТПО и ГКС. Каплацизумаб в первый день вводят однократно 10 мг внутривенно, а затем подкожно после ТПО, далее каплацизумаб вводят подкожно по 10 мг ежедневно. При проведении ТПО обменивают в первые 3 дня по 1,5 объема циркулирующей плазмы (ОЦП), затем – по 1 ОЦП. ТПО выполняют до получения клинического ответа, т.е. до тех пор, в течение 2 дней не будет количество тромбоцитов крови (> 150 х109/л) и сывороточная концентрация ЛДГ не будет превышать референсные значения более чем в 1,5 раза, исчезнут признаки гемолиза и органного поражения. При резистентных, тяжелых случаях (например, при тяжелых неврологических расстройствах, кардиоваскулярных нарушениях) ТПО выполняется дважды в сутки. ГКС вводят в дозе в дозе 1 мг/кг в пересчете на преднизолон с момента установки диагноза ТТП и до достижения полной ремиссии (и клинической ремиссии, и ремиссии по активности ADAMTS13), после чего доза преднизолона постепенно уменьшается под контролем количества тромбоцитов крови и активности ADAMTS13 вплоть до полной его отмены. Лечение ритуксимабом откладывают до увеличения количества тромбоцитов крови ≥ 150 x 109/л, после чего прекращают ТПО и начинают введение ритуксимаба в дозе 375 мг/м2 раз в неделю в течение 4 недель. При этом еженедельно измеряют активность ADAMTS13, количество тромбоцитов в крови. При достижении активности ADAMTS13 более 20 % , т.е. частичной ремиссии ТТП по активности ADAMTS13, введение каплацизумаба прекращают), поскольку такая активность ADAMTS13 достаточна для осуществления его патофизиологической роли – расщепления мультимеров фактора фон Виллебранда. Далее продолжают лечение только ритуксимабом и ГКС (рис. 1). Еженедельно продолжают оценивать активность ADAMTS13. После достижения полной ремиссии ТТП (активность ADAMTS13 > 50%) начинают постепенно уменьшать дозу ГКС вплоть до полной отмены, продолжая контролировать активность ADAMTS13 в плазме. Если после первого курса ритуксимаба активность ADAMTS13 сохраниться менее 20%, вне зависимости от количества тромбоцитов крови повторяют 4-недельный курс терапии ритуксимабом.
Проведение лечения по предложенной схеме позволяет, во-первых, избежать элиминации ритуксимаба при проведении ТПО, и пациенты получают препарат в полной дозе, следовательно, уменьшаются расход препарата и риск развития рецидивов. Во-вторых, проведение лечения под контролем активности ADAMTS13 позволяет прекратить лечения в большинстве случаев значительно раньше, чем по предлагаемой в прототипе схеме лечения, при этом подобная тактика не влияет на эффективность лечения, поскольку при повышении активности ADAMTS13 более 20% активности фермента достаточно для расщепления мультимеров фактора фон Виллебранда, и нет необходимости в введении каплацизумаба.
Сущность изобретения пояснена примерами реализации, предложенного способа лечения в ФГБУ «НМИЦ гематологии» Минздрава России, которые иллюстрируют, но не ограничивают запрашиваемый объем правовой охраны.
Общие данные результатов лечения группы пациентов с ТТП по предложенному способу.
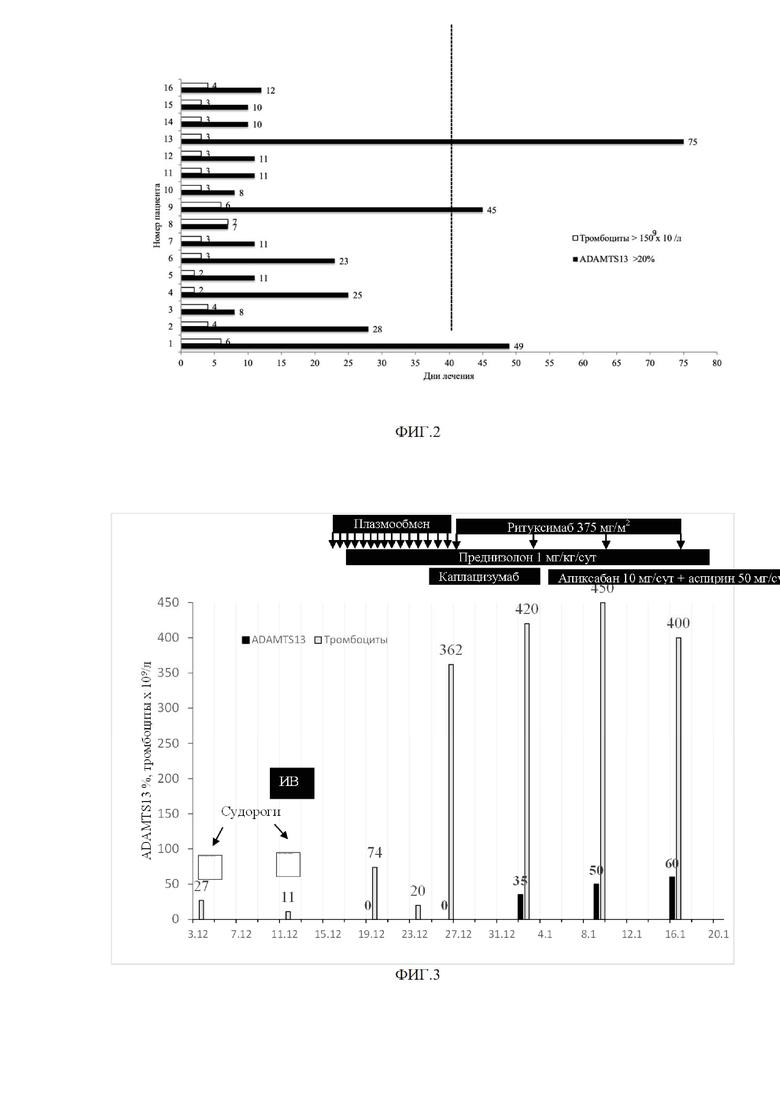
По программе раннего доступа, одобренной Министерством здравоохранения Российской Федерации, в ФГБУ «НМИЦ гематологии» Минздрава России с февраля 2021 г. по декабрь 2022 г. 16 пациентов с приобретенной ТТП получили лечение по предложенному способу. Как видно из фигуры 1, количество тромбоцитов ≥150 х 109/л было достигнуто у пациентов в сроки от 2 до 7 дней (медиана 3 дня), а повышение активности ADAMTS13 ≥20%, а, следовательно, и прекращение введения каплацизумаба, было минимально на 7 день, максимально у 1 пациентки – на 75 день (медиана 11 дней) лечения. Как видно из фигуры 2, лишь у 3 из 16 пациентов длительность лечения каплацизумабом превысила 35 дней, у большинства она была значимо меньше. Суммарно все 16 пациентов получали каплацизумаб 344 дня, медиана длительности лечения пациента составила 11 дней, у всех пациентов достигнута ремиссия ТТП. Если бы эти 16 пациентов получали лечение согласно прототипу 35 дней, то общая длительность лечения составила бы в 1,6 раз больше, т.е. 560 дней. В соответствии с опубликованной стоимостью каплацизумаба, стоимость лечения каплацизумабом составила 2 млн 648 800 долларов США против 4 312 000 долларов США, если бы лечили согласно прототипу. Таким образом, при лечении по предложенному способу удалось уменьшить стоимость лечения каплацизумабом на 1 млн 663200 долларов США, сохраняя при этом эффективность лечения. Более того, если бы, согласно прототипу, ограничились бы суммарным лечением 35 дней, то у 3 пациентов, у которых не была достигнута ремиссия по ADAMTS13, возник бы рецидив. Поэтому, согласно предложенному методу, хотя медиана лечения каплацизумабом составила 11 дней, у этих 3 пациентов лечение каплацизумабом было продолжено до достижения ремиссии по ADAMTS13 вне зависимости от количества тромбоцитов крови, что позволило избежать осложнений ТТП.
Пример 1. Клиническое наблюдение успешного кратковременного назначения каплацизумаба и быстрого достижения ремиссии у пациентки с ТТП.
Пациентка М-н, 32 лет, с начала декабря 2022 г. стала отмечать общее недомогание, повышение температуры тела до 38,0С, принимала азитромицин. 03.12.22 впервые развился судорожный приступ, в связи с чем госпитализирована больницу по месту жительства в г. Краснодаре. В гемограмме обнаружены: анемия (гемоглобин 66 г/л), тромбоцитопения (27 х 109/л). Была выполнена трансфузия эритроцитной массы. При компьютерной томографии головного мозга очаговые и/или объемные поражения головного мозга не выявлены. При электроэнцефалографии обнаружена умеренно выраженная церебральная дисфункция на фоне дезорганизованной и неустойчивой корковой ритмики без четкой латерализации, без эпилептиформной активности. Спустя неделю у нее развились повторный судорожный приступ, сопор, в связи с чем была переведена на искусственную вентиляцию легких, которую проводили в течение 2 суток. При магнитно-резонансной томографии (МРТ) очаговая патология не обнаружена. В анализах крови сохранялись анемия (гемоглобин 73 г/л), тромбоцитопения (11 х 109/л), обнаружены шистоциты 1,2%, гипербилирубинемия (билирубин общий 41 мкмоль/л, прямая фракция 13 мкмоль/л), концентрация ЛДГ в сыворотке 1200 ед/л. Заподозрена ТТП. В связи с подозрением на ТТП начата терапия преднизолоном в дозе 1 мг/кг, ежедневно - процедуры плазмообмена. Судорожный синдром был купирован, сознание у пациентки восстановилось до ясного, прекращена искусственная вентиляция легких. 19.12.2022 был подтвержден диагноз ТТП: активность ADAMTS13 составила 0%, ингибитор ADAMTS13 3,5 единиц Бетезда. 22.12.2022 пациентка была переведена в ФГБУ «НМИЦ гематологии» Минздрава России.
При поступлении в ФГБУ «НМИЦ гематологии» Минздрава России пациентка была неадекватна, плаксива, неадекватна, возбуждена. На коже – конечностей и туловища множественные гематомы, петехии. При МРТ патологии не выявлено. При ЭЭГ выявлены выраженные нарушения электрической активности диффузного характера, преобладавшие справа, зональные различия были сглажены с двух сторон, регистрировалась множественная пароксизмальная билатеральная активность с максимальной амплитудой в лобно-центральных отведениях с акцентом справа с тенденцией к генерализации, в связи с чем был назначен леветирацетам. В лабораторных данных: гемоглобин 77 г/л, тромбоцитопения 22 х 109/л, лейкоциты 12,4 х 109/л, шистоциты 12,6%, ретикулоциты 13,45% (341,6 х 109/л), прямая проба Кумбса отрицательная, общий белок 54,3 г/л, калий 3,2 ммоль/л, креатинин 44,5 мкмоль/л, мочевина 7,09 ммоль/л, билирубин 76,2 мкмоль/л, прямая фракция 15,8 мкмоль/л, непрямой 60,4 мкмоль/л, аспартатаминотрансфераза 61,7 ед/л, ЛДГ 1375 ед/л.
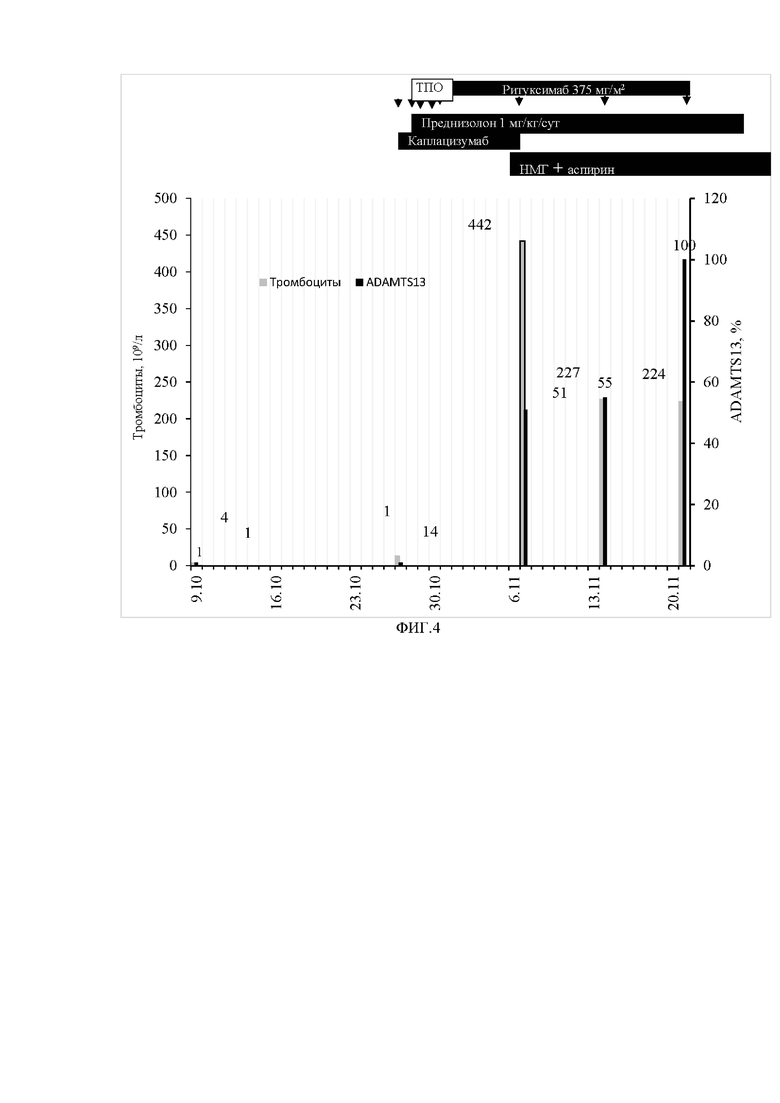
На 4-ые сутки лечения количество тромбоцитов крови составило 310 х 109/л. Плазмообмены были прекращены, начато введение ритуксимаба в дозе 375 мг/м2 раз в неделю. В результате лечения исчезла неадекватность поведения, судорожные припадки не возобновлялись, на 12 день лечения каплацизумабом, т.е. спустя неделю после первого введения ритуксимаба, при контрольном исследовании активность ADAMTS13 составила 35%, лечение каплацизумабом было прекращено, продолжена терапия преднизолоном и ритуксимабом (схема лечения приведена на фигуре 3), к терапии был добавлен апиксабан 10 мг/сут, аспирин 50 мг/сут. Спустя еще 7 дней переведена на амбулаторное лечение. После четвертого введения ритуксимабом выписана домой с рекомендацией постепенной отмены преднизолона. При выписке в анализах крови: тромбоциты 460 х 109/л, активность ADAMTS13 55%, гемоглобин 110 г/л, концентрация ЛДГ в сыворотке 210 ед/л.
Пример 2. Клиническое наблюдение успешного кратковременного назначения каплацизумаба и быстрого достижения ремиссии у пациентки с ТТП
Пациентка Кр-ва, 43 лет, в начале октября 2022 г. отметила обильных характер менструаций и появление гематом на теле, кровоточивость десен. С 09.10.2022 г. у больной внезапно появились выраженная слабость при обычной физической нагрузке, асимметрия лица, головные боли, несколько эпизодов пресинкопальных состояний, пожелтение кожи и склер, потемнение мочи. В анализе крови 13.10.22 г. впервые была выявлены тромбоцитопения 4 х 109/л, анемия 67 г/л. Была госпитализирована по месту жительства, где при обследовании: гемоглобин 47 г/л, ретикулоциты 7,3%, тромбоциты 28 х109/л, общий билирубин 43 мкмоль/л, ЛДГ 1600 ед/л При эзофагогастроскопии исключено желудочно-кишечное кровотечение. Проводили трансфузии эритроцитной взвеси, концентратов тромбоцитов. Учитывая сочетание гемолиза, тромбоцитопении с неврологической симптоматикой, заподозрена ТТП. Была исследована активность ADAMTS13 в плазме, которая составила 1%, ингибитор ADAMTS13 - 1 единица Бетезда, и 27.10.2022 пациентка была переведена в ФГБУ «НМИЦ гематологии» Минздрава России.
При поступлении имелись множественные экхимозы в области руки и ног различной степени давности, кровоизлияния в склеру левого глаза. В лабораторных данных: гемоглобин 73 г/л, ретикулоциты 13%, шистоциты 13%, лейкоциты 4х109/л, тромбоциты 14х109/л, свободный гемоглобин плазмы 0,2 г/л, креатинин 71 мкмоль/л, мочевина 3,7 ммоль/л, общий билирубин 21 мкмоль/л, общий белок 66 г/л, альбумин 41 г/л, ЛДГ 768 ед/л. При МРТ головного мозга выявлены единичные очаговые измененного сигнала размерами до 2 мм в лобных долях головного мозга, очаги микроангиопатии.
Было начато лечение каплацизумабом, преднизолоном в дозе 1 мг/кг/сут, ежедневно - процедуры плазмообмена. На 4-ые сутки лечения количество тромбоцитов крови составило 213 х 109/л, гемоглобин 75 г/л, проведение плазмообменов было прекращено (суммарно проведено 4 сеанса, удалено 8000 мл плазмы), и 31.10.2022 начато введение ритуксимаба в дозе 375 мг/м2 раз в неделю. Спустя неделю 07.11.2022 активность ADAMTS13 в плазме составила 51%, концентрация ЛДГ сыворотки снизилась до 266 ед/л, количество тромбоцитов крови повысилось до 442 х 109/л. Каплацизумаб был отменен (всего было 10 введений препарата). Назначен эноксапарин 40 мг/сут и аспирин 50 мг/сут. Продолжена терапия преднизолоном и ритуксимабом. После 4-го введения ритуксимаба активность ADAMTS13 в плазме составила 100%, количество тромбоцитов крови – 224 х 109/л, гемоглобин 130 г/л (схема лечения приведена на фигуре 4). Пациентка была выписана домой в удовлетворительном состоянии с рекомендацией постепенного уменьшения суточной дозы преднизолона вплоть до полной отмены. Сохраняется ремиссия заболевания.
Пример 3. Клиническое наблюдение длительного назначения каплацизумаба и достижения ремиссии после 2 курсов лечения ритуксимабом.
Пациентка Куд-ва, 38 лет, считает себя больной с августа 2022 года, когда стала отмечать эпизоды головокружения, нарушение речи, онемение верхних конечностей, губ, нарушение зрения, обильные менструации, спонтанные синяки на поверхности тела. Была выполнена МРТ головного мозга, при которой патологические очаги не выявлены. Повторно нарушение речи, слабость в нижних и верхних конечностях возникли 12.08.22 г. был заподозрена транзиторная ишемическая атака, выявлены анемия (гемоглобин 63 г/л), тромбоцитопения 24 х109/л, в связи с чем выполняли заместительные гемотрансфузии. Проводили терапию преднизолоном (60-90-30 мг/сут), однако эффекта получено не было. Учитывая признаки внутрисосудистого гемолиза, анемии, тромбоцитопении, была заподозрена ТТП. 24.08.22 г. активность ADAMTS-13 составила 0,8%, ингибитор — 2 единицы Бетезда, таким образом подтвержден диагноз ТТП. Проводили пульс терапию метилпреднизолоном 500 мг в течение 3 дней (24, 25, 26 августа 2022 г), плазмообмен в объеме 3000 мл, что привело к регрессии неврологической симптоматики, однако сохранялись признаки внутрисосудистого гемолиза, анемии, тромбоцитопении, в связи с чем для дальнейшего лечения переведена в ФГБУ «НМИЦ гематологии» Минздрава России.
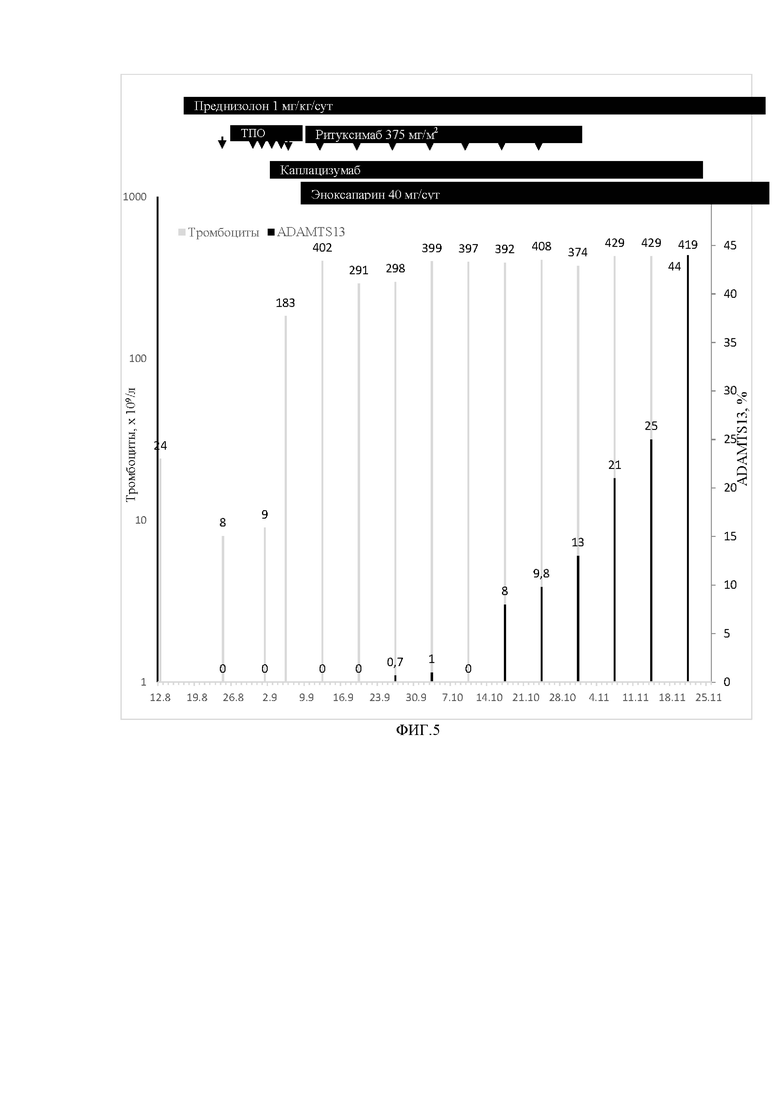
При поступлении состояние пациентки было тяжелым. Очаговых и общемозговых неврологических симптомов не было. Геморрагический синдром был представлен гематомами различной степени давности в местах венепункций на верхних конечностях, на коленях, задней поверхности обоих бедер. В лабораторных данных: анемия (гемоглобин 94 г/л), тромбоцитопения (9 х 109/л), лейкоцитоз (18 х 109/л). При МРТ в белом веществе перивентрикулярных отделов головного мозга, в области задних рогов выявлены очаги измененного сигнала размерами до 11 х 5 мм (ишемический инсульт). Была начата терапия каплацизумабом, продолжено лечение преднизолоном в дозе 1 мг/кг/сут., процедуры плазмообмена. После 5 процедур плазмообмена 05.10.2022 количество тромбоцитов крови составило 183 х 109/л. Плазмообмены были прекращены, к терапии добавлен эноксапарин 40 мг/сут, начато введение ритуксимаба по 375 мг/м2 раз в неделю. Однако, хотя после курса терапии ритуксимабом (4 введения) количество тромбоцитов крови было нормальным (298 х 109/л), активность ADAMTS13 в плазме оставалась 0,7% (схема лечения приведена на фигуре 5), в связи с чем терапия каплацизумабом была продолжена, и было решено выполнить повторный курс терапии ритуксимабом. Лишь после 8-го введения ритуксимаба активность ADAMTS13 повысилась до 9,8%. Несмотря на тромбоцитоз до 408 х 109/л, учитывая низкую активность ADAMTS13, терапия каплацизумабом была продолжена. Каплацизумаб был отменен лишь 15 ноября, когда активность ADAMTS13 повысилась до 25%. Суммарно пациентка получала каплацизумаб в течение 75 дней (рис. 5). В настоящее время период наблюдения за больной составил 6 месяцев, преднизолон постепенно отменен, сохраняется ремиссия заболевания, активность ADAMTS13 составляет 53%.
Таким образом, предложенный способ позволил, ориентируясь на активность ADAMTS13 в плазме крови, достичь ремиссии заболевания на фоне лечения каплацизумабом, длительность которого у данной пациентки более чем в 2 раза превысила рекомендуемую в прототипе.
Сущность предлагаемого изобретения пояснена на графических материалах:
Фигура 1- Предлагаемый метод лечения ТТП.
Фигура 2 - Продолжительность лечения до нормализации количества тромбоцитов крови (≥150 x 109/л) и повышения концентрации в плазме крови ADAMTS13 >20%, после чего прекращалось введение каплацизумаба, у 16 пациентов с ТТП. Нормализация количества тромбоцитов крови происходила в течение от 2 до 7 дней (медиана 3 дня), повышение активности ADAMTS13 >20% происходило в течение от 7 до 75 дней (медиана 11 дней). Пунктирной линией обозначена рекомендуемая в прототипе длительность терапии каплацизумабом.
Фигура 3 - Схема лечения больной М-н. Лечение было начато плазмообменами и преднизолоном. После добавления к терапии каплацизумаба отмечено быстрое восстановление количества тромбоцитов, что позволило прекратить лечение плазмобменами и начать введение ритуксимаба. Спустя неделю после первого введения ритуксимаба отмечено увеличение плазменной активности ADAMTS13 до 35%, что позволило прекратить введение каплацизумаба и продолжить лечение преднизолоном и ритуксимабом.
Фигура 4 - Схема лечения пациентки Кр-вой. НМГ – низкомолекулярный гепарин (эноксапарин), ТПО – терапевтический плазмообмен. После 4 процедур ТПО, назначения каплацизумаба и преднизолона количество тромбоцитов повысилось до 442 х 109/л, ТПО был прекращен, назначен ритуксимаб. Спустя неделю – активность ADAMTS13 составила 51%, каплацизумаб был отменен, продолжено лечение ритуксимабом и преднизолоном, к терапии добавлены антикоагулянты и дезагреганты.
Фигура 5- Схема лечения пациентки Куд-вой. ТПО – терапевтический плазмообмен. После 5 процедур ТПО, назначения каплацизумаба и преднизолона количество тромбоцитов повысилось до 183 х 109/л, ТПО был прекращен, назначен ритуксимаб. Потребовалось проведения 2 курсов терапии ритуксимабом (8 введений) и длительного, в течение 75 дней, лечения каплацизумабом для достижения ремиссии у пациентки.
Список литературы.
1. Scully M., Cataland S., Coppo P., et al. Consensus on the standardization of terminology in thrombotic thrombocytopenic purpura and related thrombotic microangiopathies. J Thromb Haemost. 2017;15(2):312–22. DOI:10.1111/jth.13571.
2. Yamada Y., Ohbe H., Yasunaga H., et al. Clinical Practice Pattern of Acquired Thrombotic Thrombocytopenic Purpura in Japan: A nationwide Inpatient Database Analysis. Blood. 2019;134(Suppl 1):2374. DOI:10.1182/blood-2019-125170.
3. Nguyen T.C., Han Y.Y. Plasma exchange therapy for thrombotic microangiopathies. Organogenesis. 2011;7(1):28–31. DOI:10.4161/org.7.1.14027.
4. Rock G., Shumak K.H.H., Buskard N.A.A., et al. Comparison of Plasma Exchange with Plasma Infusion in the Treatment of Thrombotic Thrombocytopenic Purpura. N Engl J Med. 1991;115(Suppl. 3):81. DOI:10.1056/NEJM199108083250604.
5. Sayani F.A., Abrams C.S. How I treat refractory thrombotic thrombocytopenic purpura. Blood. 2015;125(25):3860–7. DOI:10.1182/blood-2014-11-551580.
6. Bell W.R., Ness P.M., Kickler T.S., et al. Improved survival in thrombotic thrombocytopenic purpura–hemolytic uremic syndrome: Clinical experience in 108 patients. N Engl J Med. 1991;325(6):398–403. DOI:10.1056/NEJM199108083250605.
7. Toyoshige M., Zaitsu Y., Okafuji K., et al. Successful treatment of thrombotic thrombocytopenic purpura with high‐dose corticosteroid. Am J Hematol. 1992;41(1):69. DOI:10.1002/ajh.2830410119.
8. Scully M., Hunt B.J., Benjamin S., et al. Guidelines on the diagnosis and management of thrombotic thrombocytopenic purpura and other thrombotic microangiopathies. Br J Haematol. 2012;158(3):323–35. DOI:10.1111/j.1365-2141.2012.09167.x.
9. Balduini C.L., Gugliotta L., Luppi M., et al. High versus standard dose methylprednisolone in the acute phase of idiopathic thrombotic thrombocytopenic purpura: A randomized study. Ann Hematol. 2010;89(6):591–6. DOI:10.1007/s00277-009-0877-5.
10. Scully M., Cataland S.R., Peyvandi F., et al. Caplacizumab Treatment for Acquired Thrombotic Thrombocytopenic Purpura. New Engl J Med. 2019;380(4):335–46. DOI:10.1056/nejmoa1806311.
11. George J.N., Woodson R.D., Kiss J.E., et al. Rituximab Therapy for Thrombotic Thrombocytopenic Purpura: A Proposed Study of the Transfusion Medicine/Hemostasis Clinical Trials Network With a Systematic Review of Rituximab Therapy for Immune-Mediated Disorders. J Clin Apher. 2006;21:49–56. DOI:10.1002/jca.20091.
12. Sadler J.E.E. Pathophysiology of Thrombotic Thrombocytopenic Purpura. Blood. 2017;130(10):1181–8. DOI:10.1182/blood-2017-04-636431.
13. Westwood J.P., Thomas M., Alwan F., et al. Rituximab prophylaxis to prevent thrombotic thrombocytopenic purpura relapse: Outcome and evaluation of dosing regimens. Blood Adv. 2017;1(15):1159–66. DOI:10.1182/bloodadvances.2017008268.
14. Chen H., Fu A., Wang J., et al. Rituximab as first-line treatment for acquired thrombotic thrombocytopenic purpura. J Int Med Res. 2017;45(3):1253–60. DOI:10.1177/0300060517695646.
15. Scully M., McDonald V., Cavenagh J., et al. A phase 2 study of the safety and efficacy of rituximab with plasma exchange in acute acquired thrombotic thrombocytopenic purpura. Blood. 2011;118(7):1746–53. DOI:10.1182/blood-2011-03-341131.
16. McDonald V., Manns K., Mackie I.J., et al. Rituximab pharmacokinetics during the management of acute idiopathic thrombotic thrombocytopenic purpura. J Thromb Haemost. 2010;8(6):1201–8. DOI:10.1111/j.1538-7836.2010.03818.x.
17. Azoulay E., Bauer P.R., Mariotte E., et al. Expert statement on the ICU management of patients with thrombotic thrombocytopenic purpura. Intensive Care Med. 2019;45(11):1518–39. DOI:10.1007/s00134-019-05736-5.
18. Coppo P., Bubenheim M., Azoulay E., et al. A regimen with caplacizumab, immunosuppression, and plasma exchange prevents unfavorable outcomes in immune-mediated TTP. Blood. 2021;137(6):733–42. DOI:10.1182/blood.2020008021.
19. Cuker A., Cataland S.R., Coppo P., et al. Redefining Outcomes in Immune TTP: an International Working Group Consensus Report. Blood. 2021;137(14):1855–61. DOI:10.1182/blood.2020009150.
20. Mazepa M.A., Masias C., Chaturvedi S. How targeted therapy disrupts the treatment paradigm for acquired TTP: the risks, benefits, and unknowns. Blood. 2019;134(5):415–20. DOI:10.1182/blood.2019000954.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ ЛЕЧЕНИЯ ТТП ИММУНОГЛОБУЛИНОВЫМИ ОДИНОЧНЫМИ ВАРИАБЕЛЬНЫМИ ДОМЕНАМИ И ИХ ПРИМЕНЕНИЕ | 2015 |
|
RU2704444C2 |
| СПОСОБЫ ЛЕЧЕНИЯ ТТП ИММУНОГЛОБУЛИНОВЫМИ ОДИНОЧНЫМИ ВАРИАБЕЛЬНЫМИ ДОМЕНАМИ И ИХ ПРИМЕНЕНИЕ | 2015 |
|
RU2807602C2 |
| СПОСОБЫ ЛЕЧЕНИЯ ПЕРВОНАЧАЛЬНОГО ЭПИЗОДА TTP С ПОМОЩЬЮ ОДИНОЧНЫХ ВАРИАБЕЛЬНЫХ ДОМЕНОВ ИММУНОГЛОБУЛИНОВ | 2019 |
|
RU2794143C2 |
| Способ лабораторной диагностики тяжести COVID-19 по определению соотношения активности фактора Виллебранда и ADAMTS-13 | 2022 |
|
RU2774143C1 |
| Способ лечения иммунной тромбоцитопении | 2018 |
|
RU2703458C1 |
| СПОСОБ ЛЕЧЕНИЯ СИСТЕМНОЙ КРАСНОЙ ВОЛЧАНКИ ЧЕЛОВЕКА | 2024 |
|
RU2829414C1 |
| СПОСОБ ПРОФИЛАКТИКИ РАЗВИТИЯ ТРОМБОЦИТОПЕНИИ У БОЛЬНЫХ ХГС В СОЧЕТАНИИ С ИНФЕКЦИЕЙ Helicobacter pylori, ПОЛУЧАЮЩИХ КПВТ | 2013 |
|
RU2536285C1 |
| Способ прогнозирования течения первичной медиастинальной В-крупноклеточной лимфомы | 2021 |
|
RU2772187C1 |
| Способ лечения больных первичной диффузной В-клеточной крупноклеточной лимфомой ЦНС | 2024 |
|
RU2831407C1 |
| Способ оценки эффективности терапии лимфомы Ходжкина у мальчиков пубертатного возраста | 2024 |
|
RU2840699C1 |

Изобретение относится к медицине, а именно к гематологии, и может быть использовано для течения приобретенной тромботической тромбоцитопенической пурпуры. Лечение основано на проведении процедур плазмообмена (ТПО), применении глюкокортикостероидов, ритуксимаба и каплацизумаба. При этом терапию ритуксимабом начинают после увеличения количества тромбоцитов крови ≥150×109/л и прекращения проведения процедур плазмообмена. Длительность терапии каплацизумабом определяют достижением активности ADAMTS13 в плазме крови ≥20%. Способ позволяет снизить риск рецидивов заболевания за счет исключения возможности элиминации ритуксимаба при проведении ТПО, а также сократить длительность проводимой терапии за счет определения активности ADAMTS13 в плазме крови. 6 з.п. ф-лы, 5 ил., 3 пр.
1. Способ лечения приобретенной тромботической тромбоцитопенической пурпуры, включающий проведение процедуры плазмообмена, введение глюкокортикостероида, ритуксимаба и каплацизумаба, отличающийся тем, что ритуксимаб применяют только после увеличения количества тромбоцитов крови ≥150×109/л и прекращения проведения процедур плазмообмена, а длительность терапии каплацизумабом определяется достижением активности ADAMTS13 в плазме крови ≥ 20%.
2. Способ по п.1, отличающийся тем, что проводят терапию каплацизумабом в первый день 10 мг перед первым плазмообменом внутривенно и 10 мг подкожно после окончания первой процедуры плазмообмена, а затем ежедневно по 10 мг подкожно.
3. Способ по п. 2, отличающийся тем, что терапию каплацизумабом продолжают до достижения активности ADAMTS13 в плазме крови ≥20%.
4. Способ по п.1, отличающийся тем, что проводят терапию ритуксимабом по 375 мг/м2 раз в неделю, всего 4 введения.
5. Способ по п.1, отличающийся тем, что терапию ежедневными плазмообменами начинают при подтверждении диагноза тромботической тромбоцитопенической пурпуры.
6. Способ по п.5, отличающийся тем, что при проведении плазмообмена за процедуру пациенту обменивают по 1,5 объема циркулирующей плазмы в первые 3 дня, затем по 1 объему циркулирующей плазмы.
7. Способ по п. 1, отличающийся тем, что проводят терапию глюкокортикостероидными гормонами в дозе 1 мг/кг в пересчете на преднизолон со дня установки диагноза ТТП до достижения полной ремиссии ТТП.
| ГАЛСТЯН Г.М | |||
| и др | |||
| Тромботическая тромбоцитопеническая пурпура у беременных: родоразрешать нельзя прерывать | |||
| Где поставить запятую? Гематология и трансфузиология | |||
| Способ получения продуктов конденсации фенолов с формальдегидом | 1924 |
|
SU2022A1 |
| Устройство для усиления микрофонного тока с применением самоиндукции | 1920 |
|
SU42A1 |
| RU 2020129228 A, 09.03.2022 | |||
| RU 2019131713 A, 11.11.2019 | |||
| ГАЛСТЯН Г.М | |||
| и др | |||
| Лечение преобретенной тромботической тромбоцитопенической пурпуры | |||
| Терапевтический | |||
Авторы
Даты
2024-02-12—Публикация
2023-03-09—Подача