Изобретение относится к химической промышленности, а именно к получению соединения, которое может быть использовано в качестве кислотно-основного индикатора, характеризующегося высоким контрастом цветового перехода для визуального определения рН или использования в качестве оптического сенсора, а также узким интервалом рН перехода 6,9-6,7.
Кислотно-основные индикаторы – это, как правило, синтетические органические красители, являющиеся слабыми кислотами или основаниями, меняющие видимую окраску в зависимости от рН раствора. Кислотно-основные индикаторы с визуальной оценкой изменения рН востребованы в аналитической химии, биологии, медицине, микробиологии. Их несомненным преимуществом является быстрота, наглядность исследования и дешевизна анализа. К настоящему времени известно большое количество индикаторов, однако подавляющее большинство из них эффективно работают в сильно основных или кислых средах, в то время как чувствительных индикаторов рН в области 4,0-6,0 сравнительно мало. Наиболее известные и распространенные кислотно-основные индикаторы, работающие интересующей рН области – метиловый красный с областью перехода рН =4.2-6.2 и бромкрезоловый зеленый с областью перехода рН 3,8-5,4. [Ю. Ю. Лурье Справочник по аналитической химии / Ю. Ю. Лурье – М.: Книга по Требованию, 2012. – 440 с.]. Основной недостаток указанных традиционно применяемых индикаторов плохая растворимость в водных средах, вызывающая необходимость использования органических сорастворителей (N,N-диметилформамида или этанола). Кроме того, традиционно применяемые кислотно-основные индикаторы имеют широкий интервал перехода и небольшую контрастность цветового перехода в точке эквивалентности от красного до желто-оранжевого в случае метилового красного и от красного до сине-фиолетового в случае бромкрезолового зеленого.
Известны соединения [Патент 2176654 C1 Российская Федерация, МПК C09B 11/08 (2000.01), G01N 31/22 (2000.01) 3,3'-Замещенные трифенилметановые красители в качестве кислотно-основных индикаторов / Осипов А.К. (RU), Новопольцев В. М. (RU); заявитель Мордовский государственный университет им. Н.П. Огарева, патентообладатель Мордовский государственный университет им. Н.П. Огарева; заявл. 04.04.2000; опубл. 10.12.2001 г., Бюл. №34], относящиеся к замещенным трифенилметановым красителям, которые могут быть использованы в титриметрическом анализе в качестве кислотно - основных индикаторов при изменении окраски с желтой на красную в интервале рН от 5,9-7,9 и 6,8-7,5 при использовании в качестве индикатора 3,3'-бис-{(2-карбокси-3,3-диметил-7-оксо-4-тиа-1-азабицикло [3,2,0] гептил)-6-аминометил} -фенолсульфофталеина и 3,3'-бис-(2-карбоксифениламинометил)-5,5-дихлорфенолсульфофталеин, соответственно.
Известно также в качестве кислотно-основного индикатора, работающего в интервале значений рН 4,0-6,0 [Патент 2742270 C1 Российская Федерация, МПК C09B 33/06 (2006.01), C07C 309/46 (2006.01). СПК C07C 309/46 (2020.08), C09B 33/06 (2020.08), G01N 21/77 (2020.08). Индикаторный дисазокраситель стильбенового ряда для работающих в интервале значений pН 4,0-6,0 оптических pН-сенсоров и способ его получения [Текст] /Кудрявцева Татьяна Николаевна (RU), Ефанов Сергей Анатольевич (RU), Грехнева Елена Владимировна (RU), Атрепьева Лариса Васильевна (RU), Кометиани Илона Бучуевна (RU); заявитель Федеральное государственное бюджетное образовательное учреждение высшего образования "Курский государственный университет" (RU), патентообладатель Федеральное государственное бюджетное образовательное учреждение высшего образования "Курский государственный университет" (RU); заявл. 20.06.2020; опубл. 04.02.2021 г., Бюл. №4] соединение – дисазокраситель стильбенового ряда. Характерной особенностью которого является способность окрашивать целлюлозные, полиамидные, шерстяные, шелковые текстильные материалы, способных к изменению окраски при иммобилизации на текстильном носителе в зависимости от рН. Краситель имеет цветовой переход сине-фиолетовый – розовый.
Существенным недостатком перечисленных изобретений является низкая растворимость индикаторов, требующая наличие органического сорастворителя, что является особенно нежелательным при использовании индикатора в биомедицинских и биологических целях. Другим существенным недостатком является низкий коэффициент экстинкции рН-чувствительных красителей, что приводит к требованию сравнительно высоких концентраций красителя в анализируемых средах для обеспечения визуального определения рН перехода. Кроме того, представленные рН индикаторы характеризуются широким интервалом рН перехода, что дает большую погрешность в определении точки эквивалентности.
За прототип принят тетрасульфозамещенный тетрафенилпорфирин [Pat. 8983565 B2 United States, Int. Cl. https://patents.google.com/?q=pH-sensitive+dyes&q=A61B5%2f14532, А61B 5/14532. Optical determination of pH and glucose [Text] / David R. Markle, Berwyn, PA (US); Jeff T. Suri, Rancho Santa Margarita, CA (US); Ritchie A. Wessling, Watsonville, CA (US); Matthew A. Romey, Aliso Viejo, CA (US); Medtronic Minimed, Inc., Northridge, CA (US). Appl. № 13/951,125; Filed Jul. 25, 2013; Pub. Date Feb. 27, 2014. - 33 p.: pic.], хорошо растворимый в водных средах и имеющий большой коэффициент экстинкции. Основным недостатком прототипа являются рН переход в области 2,6-4,8 и широкий интервал рН перехода [Шейнин В.Б., Шабунин С.А., Бобрицкая Е.В., Койфман О.И. (2011). Протонирование 5, 10, 15, 20-тетракис(4-сульфонатофенил)порфина в воде. Макрогетероциклы 2011, 4 , 80-84.].
Задачей изобретения является получение нового химического соединения для применения в качестве кислотно-основного индикатора с рН переходом в области 4 - 5, с высокой контрастностью цветового перехода, наряду с уменьшением области перехода.
Поставленная задача решена новым химическим соединением формулы:
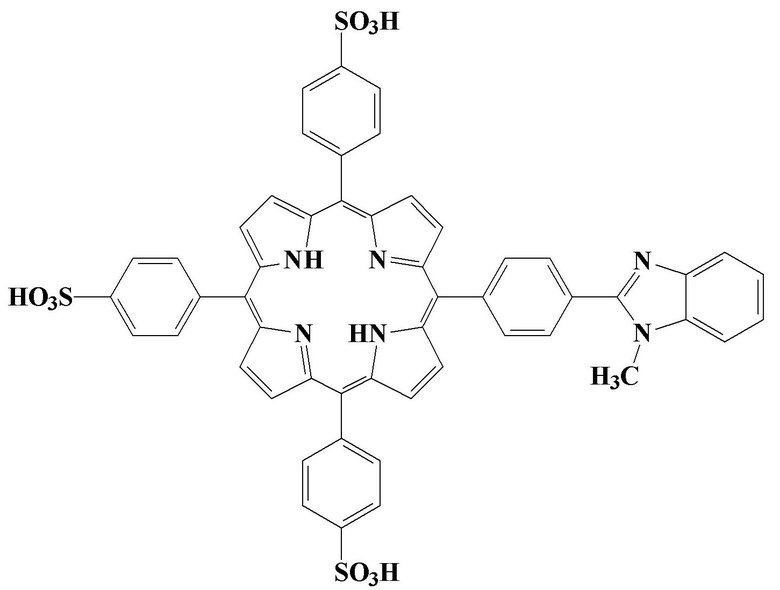
Поставленная задача решена также применением данного нового химического соединения в качестве кислотного индикатора для оптического и визуального определения рН.
Поставленная задача решена за счет того, что получено новое порфириновое соединение, содержащее три сульфо-группы и остаток бензимидазола, структура которого подтверждена физико-химическими методами анализа. Выбор порфирина обусловлен следующими причинами: три сульфо-группы обеспечивают растворимость соединения в водных и физиологических средах, а также способность соединения участвовать в кислотно-основных равновесиях за счет протонирования или депротонирования сульфо-групп порфирина, гетерильный заместитель с остатком бензимидазола обеспечивает гидрофобно-гидрофильный баланс, что важно при использовании индикатора в медицинских и биологических целях. Кроме того, три сульфо-группы и гетерильный заместитель, выступают как электроноакцепторные заместители, обладающие отрицательным индукционным эффектом, что приводит к изменению протоакцепторной способности пирролеиновых атомов азота реакционного центра порфирина. Таким образом, новое порфириновое соединение способно участвовать в нескольких кислотно-основных равновесиях, что сопровождается изменением контрастным и резким изменением цвета раствора от коричнево-красного (RAL 3011) в щелочной и слабощелочной среде до зеленого (RAL 6038) в слабокислой и кислой среде. рН переход визуально детектируется при использовании порфиринового соединения в концентрации (1-4)⋅10-4 моль/л в диапазоне рН =4,02-5,65. При использовании спектрофотометра, т.е. при оптической регистрации спектра возможно использование индикатора в концентрации (1-4)⋅10-6 моль/л с фиксацией перехода в диапазоне рН=4,02 -5,13.
Предлагаемое соединение является двухцветным кислотно-основным индикатором, более чувствительным к изменению рН среды в области рН 4-5, работает в более узком диапазоне рН, по сравнению с прототипом, следовательно, является более точным индикатором. Полученное соединение хорошо растворимо в водных и физиологических средах, для визуализации перехода достаточно низкой концентрации соединения 10-4 моль/л.
Для получения этого соединения используют следующие вещества:
- пара-ксилол нефтяной ТУ 38.101255-87;
- бензальдегид - коммерческий продукт TCI EUROPE N.V.;
- трифторуксусная кислота ту 6-09-3877-80;
- пиррол - ТУ 6-09-07-242-84;
- ацетат цинка – ГОСТ 5852-78;
- оксид алюминия - ТУ 6-09-426-75;
- хлороформ - ТУ 263-44493179-01 с изм. №1, 2;
- метанол - ГОСТ 2222-95;
- трифенилфосфин - коммерческий продукт TCI EUROPE N.V.;
- поташ (карбонат калия) - ГОСТ 4221-76;
- ацетат меди – ГОСТ 5852-79;
- ацетат палладия – ТУ 2625-024-00205067-2003;
- бензоксазол - коммерческий продукт TCI EUROPE N.V.;
- N-метилбензимидазол - коммерческий продукт TCI EUROPE N.V.;
- бензотиазол - коммерческий продукт TCI EUROPE N.V.;
- хлористый метилен - ТУ 2631-44493179-98 с изм. №1, 2, 3;
- гексан - ТУ 6-09-06-4521-77;
- бензол - ГОСТ 5955-75 с изм. №1, 2;
-толуол ТУ 2414-006-72021999-2009
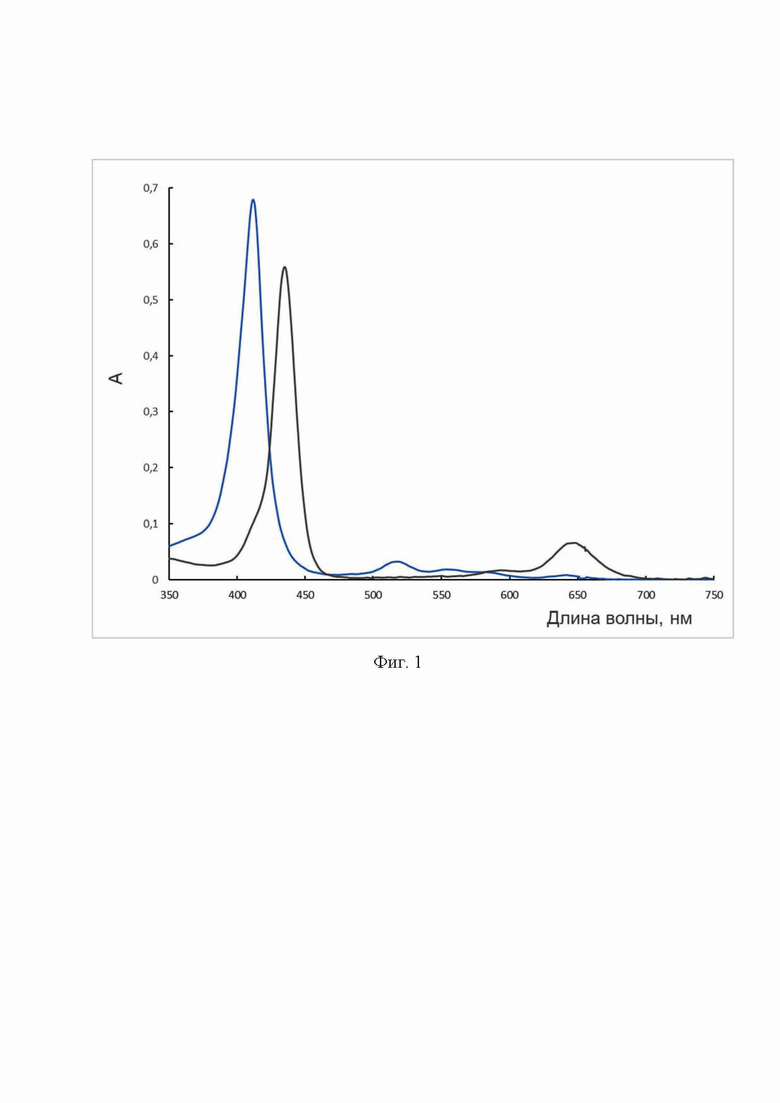
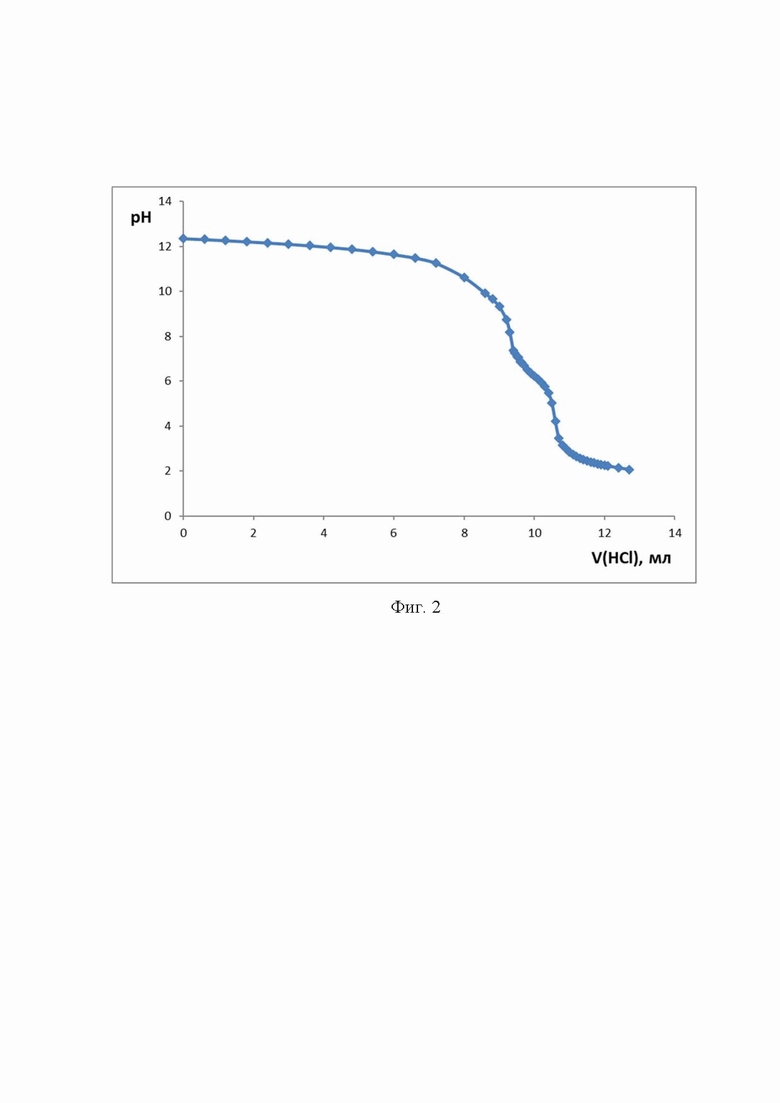
Изобретение поясняется чертежами, где на фиг. 1 показан результат изменения электронных спектров поглощения 5-[4′-(N-метил-1′′,3′′-бензимидазол-2′′-ил)-фенил]-10,15,20-трис(4′-сульфофенил)порфина в водной среде при титровании соляной кислотой. Исходный электронный спектр поглощения порфиринового соединения является классическим и содержит полосу Соре (412 нм) и четыре полосы поглощения в дальневолновой части спектра (517, 555, 586, 643нм), что соответствует симметрии порфиринового соединения D2h. Протонирование реакционного центра при переходе от слабощелочной, нейтральной в кислую среду приводит к батохромному смещению полосы Соре до 435 нм. Исчезновению поглощения в области 517, 555, 586 нм и появлению двух относительно интенсивных полос поглощения при 591 и 644 нм. Данные спектральные изменения говорят о росте симметрии порфиринового соединения до D4h по причине протонирования реакционного центра порфирина. На фиг. 2 представлена потенциометрическая кривая титрования раствора порфиринового соединения в концентрации 4⋅10-5 моль/л в растворе КОН при добавлении HCl. Потенциометрическая кривая имеет два характерных перехода, первый типичен для титрования сильного основания сильной кислотой в интервале рН=6,3-9,3; второй - соответствует процессу протонирования порфиринового соединения в интервале рН=3,14-5,74. На фиг.3. представлены фотографии потенциометрической ячейки с анализируемым раствором на фоне индикатора – порфиринового соединения с концентрацией 4⋅10-5 моль/л.
На фиг.4 приведены фотографии растворов с рН=5,65 и 4,02, при внесении порфиринового соединения в концентрации (1,5⋅10-4 моль/л).
Заявленное соединение получают следующим образом:
Вначале получают 5-(4′-бромфенил)-10,15,20-трифенилпорфин следующим образом:
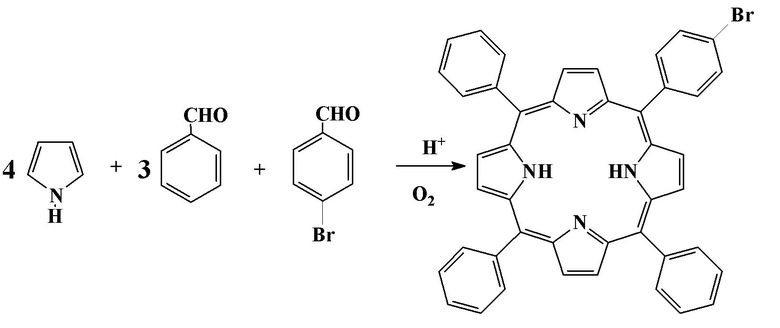
К кипящему раствору 2 мл трифторуксусной кислоты в 250 мл пара-ксилола при пропускании тока азота прибавляют из капельной воронки за 20 мин раствор 5 мл (72 ммоль) пиррола, 3,3 г (18 ммоль) 4-бромбензальдегида и 5,5 мл (54 ммоль) бензальдегида в 50 мл пара-ксилола. Смесь кипятят 40 мин в токе азота и затем 1 час в токе воздуха. Раствор охлаждают и нейтрализуют 20 мл 25%-ного раствора аммиака. Ксилол отгоняют с водяным паром, остаток в колбе отфильтровывают, высушивают при комнатной температуре, растворяют в 200 мл хлороформа и хроматографируют на колонке с Al2O3 (II ст. активности по Брокману), элюируя смесью хлороформом-гексан (1:1). Cобирают первую темно-красную зону 5-(4’-бромфенил)-10,15,20-трифенилпорфина содержащую в качестве примеси попутно образующийся тетрафенилпорфин. Элюат упаривают до 5 мл, монобромпорфирин осаждают 50 мл метанола, и высушивают при комнатной температуре до постоянного веса.
Выход 1,14 г (23%). Rf 0,67 (силуфол, хлорофом). ЭСП (хлороформ), λmax, нм (lgε): 648 (3.63), 590 (3,77), 551 (3,91), 515 (4,26), 491(5,64). Масс-спектр (MALDI-TOF), m/z: рассчитано: 693,63 С44H29BrN4: Найдено: 694,42 [M+H]+.
Далее получают 5-(4′-бромфенил)-10,15,20-трифенилпорфинат цинка.
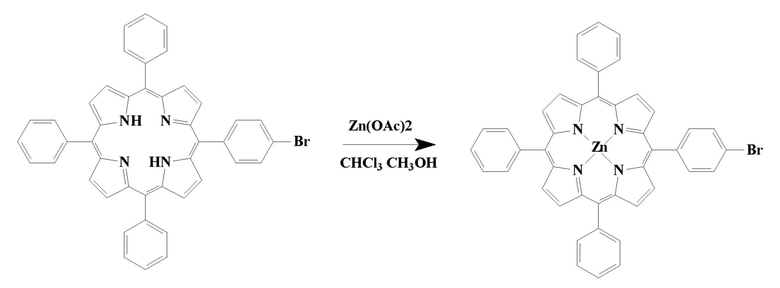
Растворяют 3 г (4,3 ммоль) 5-(4′-бромфенил)-10,15,20-трифенилпорфирина и 4,7 г (0,021 моль) безводного ацетата цинка в смеси 200 мл метанола и 100 мл хлороформа. Смесь кипятят 1,5 ч, контролируя протекание реакции с помощью ЭСП. Смесь охлаждают, отгоняют избыток растворителя, остаток хроматографируют на колонке с Al2O3 (III ст. активности по Брокману), элюируя хлорофором. Растворитель отгоняют, остаток промывают водой, отфильтровывают и высушивают при комнатной температуре до постоянной массы.
Выход 3,3 г. (98%). 1H ЯМР δ, м.д.: 9,02-8,99m (2H, H8,12), 8,97-8,96m (2H, H2,18), 8,27-8,24m (4H, H3,7,13,17), 8,14-8,12m (1H, H4-HPh), 7,78–7,73m (10H; 8H, H2,6-HPh; 2H, H4-HPh), 7,59–7,51m (8H, H3,5-HPh) (CDCl3). ЭСП: λmax, нм (lgε): 595(3,70), 551(4,14), 424(5,51) (CHCl3). MALDI-TOF MS: m/z Рассчитано: C44H27BrN4Zn, 757,0156; Найдено: 757,5608.
Затем получают 5-[4′-(N-метил-1′′,3′′-бензимидазол-2′′-ил)фенил]-10,15,20-трифенилпорфинат цинка:
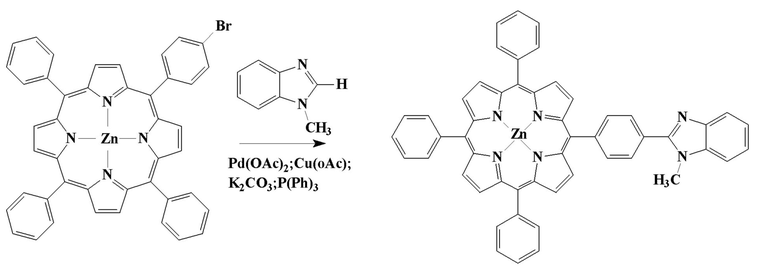
В колбе на 100 мл, снабженной магнитной мешалкой и обратным холодильником, кипятят при перемешивании в течении 52 ч смесь 1 г (0,132 ммоль)5-(4′-бромфенил)-10,15,20-трифенилпорфината цинка, 0,0592 г (0,264 ммоль) Pd(OAc)2, 0,0575 г (0,264 ммоль) Cu(OAc)2·H2O 0,34 г (0,132 ммоль) трифенилфосфина, 0,364 г (1,342 ммоль) карбоната калия, и 0,349 г (0,264 ммлоль) 1-метилбензимидазола в 45 мл толуола. Далее смесь охлаждают до комнатной температуры и добавляют 50 мл хлористого метилена и фильтруют. Осадок промывают 10 мл хлористого метилена, объединенные органические фракции упаривают в вакууме. Остаток растворяют в 30 мл хлористого метилена и хроматографируют на колонке с селикагелем, элюируя первоначально смесью гексан- хлористый метилен (1:1) (сходит зона примесей тетрафенилпорфина), затем хлористым метиленом, собирая темно-красную зону моногетерилпорфирина. Растворитель упаривают досуха.
Выход 0,18 г (89%). Rf 0,55 (силуфол, хлорофом).
1H ЯМР δ, м.д.: 8,99-8,98m (2H, H8,12), 8,97-8,96m (2H, H2,18), 8,26-8,24m (4H, H3,7,13,17), 8,14-8,12m (1H, H4-HPh), 7,79–7,73m (10H; 8H, H2,6-HPh; 2H, H4-HPh), 7,58–7,51m (8H, H3,5-HPh), 7,42-7,39m (4H, от N-метилбензимидазола), 3,88 s (3H N-Me) (CDCl3). ЭСП: λmax, нм (lgε): 595(3,70), 552(4,13), 424(5,50) (CHCl3). MALDI-TOF MS: m/z Рассчитано: C52H34N6Zn, 808,26; Найдено: 808,62.
Получение заявляемого соединения - 5-[4′-(N-метил-1′′,3′′-бензимидазол-2′′-ил)фенил]-10,15,20-трис(4′-сульфофенил)порфина:
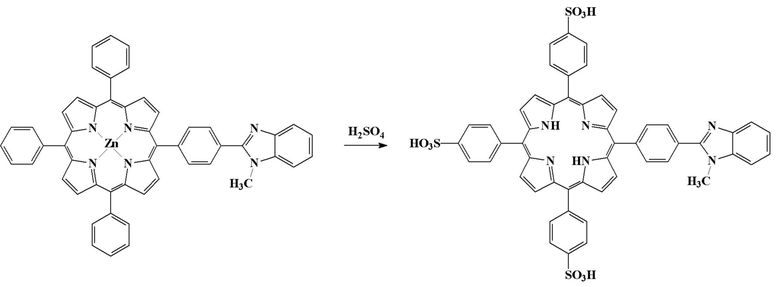
В колбе на 50 мл, снабженной воздушным холодильником, нагревают при перемешивании до 70 °С 100 мг 5-[4′-(N-метил-1′′,3′′-бензимидазол-2′′-ил)фенил]-10,15,20-трифенилпорфинат цинка, добавляют 10 мл серной кислоты (98%). Смесь перемешивают при 70 °С в течении 48 часов, затем охлаждают до комнатной температуры и перемешивают еще 72 часа. Затем выливают на лёд. Тёмно-зелёную суспензию фильтруют, промывают холодной водой до отсутствия помутнения раствора хлорида бария, затем ацетоном. Сульфированный порфирин высушивают при комнатной температуре до постоянной массы.
Выход 0,112 г (92%). Rf = 0,52 (EtOH - 25%-ный раствор аммиака (20:1). 1H ЯМР δ, м.д.: 8,92-8,89m (4H, H3,7,13,17), 8,67-8,66m (2H, H8,12), 8,44-8,43m (2H, H2,18), 8,22–8,21m (8H, H2,6-HPh), 8,07–8,06m (8H, H3,5-HPh), 8,01-7,94m (4H, от N-метилбензимидазола), 4,40 s (3H N-Me); -0,82 bs (2H, NH) (DMSO-d6). ЭСП: λmax, нм (lgε): 639(3,57), 581(3,75), 556(3,83), 517(4,06), 414(5,43) (H2O). MALDI-TOF MS: m/z Рассчитано: C52H36N6O9S3, 987,07; Найдено: 987,12.
Примеры применения заявляемого соединения
Готовят концентрированный раствор 5-[4′-(N-метил-1′′,3′′-бензимидазол-2′′-ил)фенил]-10,15,20-трис(4′-сульфофенил)порфина в воде, для этого навеску соединения массой 0,00088 г растворяют в 2 мл дистиллированной воды. Полученный раствор индикатора с концентраций 4,5⋅10-4 моль/л хранят в герметичной таре в свето-защищенном месте. Полученный раствор индикатора добавляют в количестве в 1,5 мкл на каждые 1 мл анализируемого раствора.
Пример 1. Раствор порфиринового соединения используют в аналитической химии, например, при титровании сильной кислоты сильным основанием. Титруют раствор HCl с рН 2 раствором KOH. Значения рН определяют потенциометрически. Измерения ЭДС цепи проводят с помощью прибора «Мультитест» ИПЛ-311. В потенциометрическую ячейку помещают анализируемый раствор в количестве 25 мл, вносят 37,5 мкл раствора индикатора с концентраций 4,5⋅10-4 моль/л и осуществляют титрование внесением в ячейку заданного объема раствора щелочи. рН переход оценивают визуально (фиг.3).
Пример 2.
Раствор порфиринового соединения используют в аналитической химии, для контроля рН буферных растворов при их приготовлении и хранении. Готовят два реперных буферных раствора с рН ≥ 5 и рН ≤ 4. В нашем случае для получения реперного раствора с рН=7,4 растворяют 1 таблетку фосфатного буфера (Am-E404, VVR international LLC (США) в 100 мл деионизированной воды. В 1 мл полученного буферного раствора вносят 1,5 мкл раствора индикатора с концентраций 4,5⋅10-4 моль/л. Фиксируют цвет полученного раствора, в нашем случае получен коричнево-красный (RAL 3011), аналогичный, представленному на фиг.4а
Для получения второго реперного раствора с рН=4, фосфатный буферный раствор с рН =7,4 подкисляют соляной кислотой, до рН=4. Вносят 1,5 мкл раствора индикатора с концентраций 4,5⋅10-4 моль/л. Фиксируют цвет полученного раствора, в нашем случае цвет - зеленый (RAL 6038), аналогичный, представленному на фиг.4 б.
Для визуального определения рН анализируемого раствора, в 1 мл вносят 1,5 мкл раствора индикатора с концентраций 4,5⋅10-4 моль/л, фиксируют цвет полученного раствора и сравнивают его с цветом реперных растворов. Тем самым определяют кислотность среды анализируемого раствора.
Пример 3. Для оптического определения рН анализируемого раствора. Пробу анализируемого раствора 2 мл вносят в спектрофотометрическую кювету, добавляют 3 мкл индикаторного раствора. С использованием любого спектрофотометра, спектрофлуориметра, спектрометра фиксируют спектр анализируемого раствора. Если максимум оптической плотности приходится на 412 нм или регистрируется поглощение в области 517 нм, то рН раствора >5,13. В том случае, если регистрируется максимум оптической плотности на 435 нм или регистрируется поглощение в области 644 нм, то рН раствора <4,02.
| название | год | авторы | номер документа |
|---|---|---|---|
| 5-[4′-(1′′,3′′-БЕНЗОТИАЗОЛ-2′′-ИЛ)ФЕНИЛ]-10,15,20-ТРИС(4′-СУЛЬФОФЕНИЛ)ПОРФИН В КАЧЕСТВЕ ЦВЕТОВОГО ИНДИКАТОРА ДЛЯ ВИЗУАЛЬНОГО ОБНАРУЖЕНИЯ ХЛОРОВОДОРОДА | 2022 |
|
RU2806627C1 |
| 5-[4'-(1'',3''-БЕНЗОКСАЗОЛ-2''-ИЛ)ФЕНИЛ]-10,15,20-ТРИС(4'-СУЛЬФОФЕНИЛ)ПОРФИН В КАЧЕСТВЕ ФЛУОРЕСЦЕНТНОГО СЕНСОРА ДЛЯ ОБНАРУЖЕНИЯ И КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ АЛЬБУМИНА | 2022 |
|
RU2807912C1 |
| 5-[4'-(1",3",7"-ТРИМЕТИКСАНТ-2"-ИЛ)ФЕНИЛ] 10,15,20-ТРИС-(N-МЕТИЛПИРИДИНИЙ-3'-ИЛ)ПОРФИРИН ТРИИОДИД, ПРОЯВЛЯЮЩИЙ СВОЙСТВА рН-ИНДИКАТОРА СИЛЬНОКИСЛЫХ СРЕД | 2023 |
|
RU2818821C1 |
| 5-[4'-(1"-МЕТИЛИНДОЛ-2"-ИЛ)ФЕНИЛ]-10,15,20-ТРИС(N-МЕТИЛПИРИДИН-3'-ИЛ)ПОРФИРИН ТРИИОДИД, ПРОЯВЛЯЮЩИЙ СВОЙСТВО ОСАЖДЕНИЯ НУКЛЕИНОВЫХ КИСЛОТ ИЗ РАСТВОРОВ | 2024 |
|
RU2835079C1 |
| 5-[4-(1,3-БЕНЗОТИАЗОЛ-2-ИЛ)ФЕНИЛ]-10,15,20-ТРИС(1-МЕТИЛПИРИДИНИЙ-3-ИЛ)ПОРФИРИН ТРИИОДИД, ПРОЯВЛЯЮЩИЙ СВОЙСТВО СВЯЗЫВАНИЯ СПАЙКОВОГО БЕЛКА ВИРУСА SARS-CoV-2 | 2021 |
|
RU2773397C1 |
| 5,15-БИС(4'-БИС-L-ТИРОЗИНИЛАМИДОФЕНИЛ)-10,20-БИС(N-МЕТИЛПИРИДИНИЙ-3'-ИЛ)ПОРФИН ДИИОДИД, ПРОЯВЛЯЮЩИЙ СВОЙСТВО СВЯЗЫВАНИЯ S-БЕЛКА ВИРУСА SARS-CoV-2 | 2022 |
|
RU2784940C1 |
| ТЕТРА-4-{ 4-[1-МЕТИЛ-1-(4-СУЛЬФОФЕНИЛ)ЭТИЛ]ФЕНОКСИ} -ТЕТРА-5-НИТРОФТАЛОЦИАНИН КОБАЛЬТА | 2016 |
|
RU2622290C1 |
| ТЕТРА-4-[4-(1-МЕТИЛ-1-ФЕНИЛЭТИЛ)ФЕНОКСИ]ТЕТРА-5-НИТРОФТАЛОЦИАНИНЫ КОБАЛЬТА И НИКЕЛЯ | 2016 |
|
RU2620270C1 |
| 4-[4-(1-МЕТИЛ-1-ФЕНИЛЭТИЛ)ФЕНОКСИ]-5-НИТРОФТАЛОНИТРИЛ | 2016 |
|
RU2620381C1 |
| ЭЛЕКТРОЛИТ СЕРЕБРЕНИЯ | 2019 |
|
RU2702511C1 |


Группа изобретений относится к химической промышленности, а именно к 5-[4'-(N-метил-1'',3''-бензимидазол-2''-ил)фенил]-10,15,20-трис(4'-сульфофенил)порфину и применению его в качестве кислотного индикатора для оптического и визуального определения рН. Технический результат - создание красителя, характеризующегося высоким контрастом цветового перехода для визуального и оптического определения рН, а также узким интервалом рН перехода. 2 н.п. ф-лы, 4 ил., 3 пр.
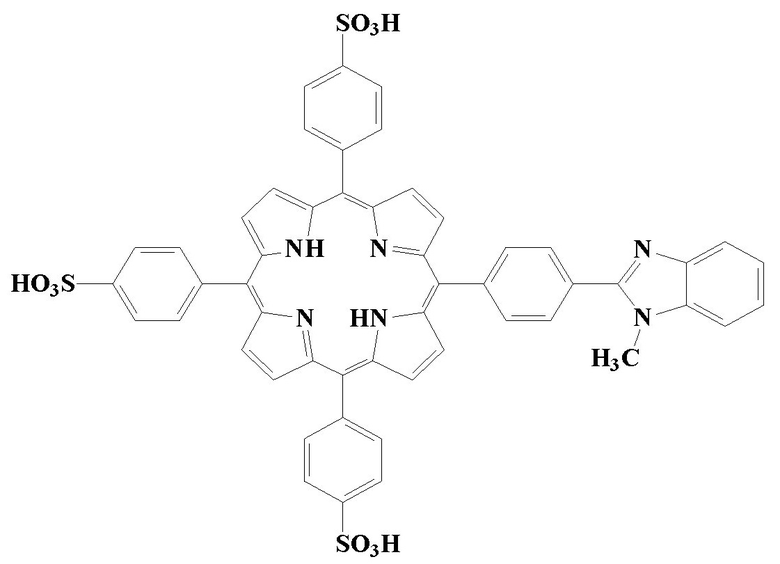
1. 5-[4′-(N-метил-1′′,3′′-бензимидазол-2′′-ил)фенил]-10,15,20-трис(4′-сульфофенил)порфин формулы:
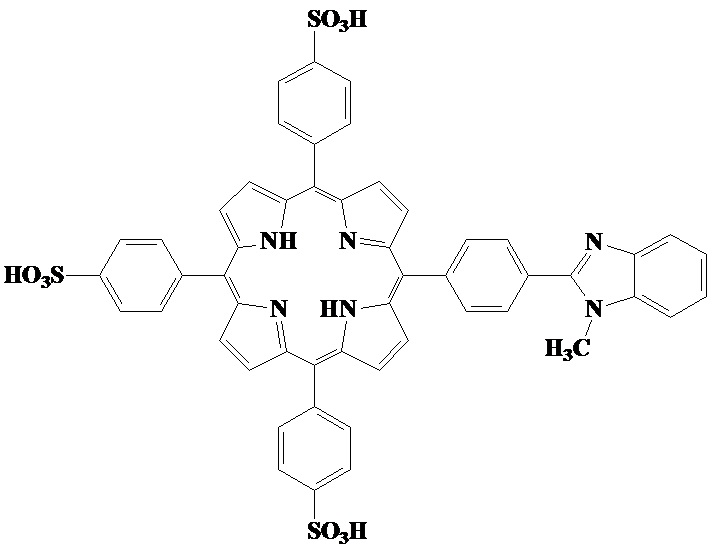
2. Применение 5-[4′-(N-метил-1′′,3′′-бензимидазол-2′′-ил)фенил]-10,15,20-трис(4′-сульфофенил)порфина в качестве кислотного индикатора для оптического и визуального определения рH.
| US 8983565 B2, 17.03.2015 | |||
| Eugenia Fagadar-Cosma et al | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Arabian journal of chemistry, 2019, vol.12, issue 7, p | |||
| Дорога сельфактора для крестовой мотки | 1924 |
|
SU1587A1 |
| С | |||
| А | |||
| Сырбу и др | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
Авторы
Даты
2024-02-14—Публикация
2022-12-15—Подача