ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] По настоящей заявке испрашивается приоритет по временной заявке США №62/712608, поданной 31 июля 2018 года, включенной в настоящее описание в качестве ссылки в полном объеме.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0002] Настоящее изобретение относится к моноклональным антителам, специфически связывающимся с MICA/B и, таким образом, модулирующим иммунный ответ против пораженных клеток.
[0003] В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам или их антигенсвязывающим фрагментам, содержащим легкую цепь, содержащую аминокислотную последовательность, по меньшей мере на 80% идентичную в отношении аминокислотной последовательности, приведенной как SEQ ID NO: 21, SEQ ID NO: 23 или SEQ ID NO: 24. В некоторых вариантах осуществления моноклональные антитела или их антигенсвязывающие фрагменты дополнительно содержат тяжелую цепь, содержащую аминокислотную последовательность, по меньшей мере на 80% идентичную в отношении аминокислотной последовательности, приведенной как SEQ ID NO: 22, SEQ ID NO: 25 или SEQ ID NO: 26.
[0004] В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам или их антигенсвязывающим фрагментам, содержащим вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19. В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам или их антигенсвязывающим фрагментам, содержащим вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 90% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19. В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам или их антигенсвязывающим фрагментам, содержащим вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 95% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19. В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам или их антигенсвязывающим фрагментам, содержащим вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19. В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам или их антигенсвязывающим фрагментам, содержащим вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 90% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 95% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 7, и вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 8. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 15, и вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 16. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 19, и вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 20. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит легкую цепь, содержащую аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 21, SEQ ID NO: 23 или SEQ ID NO: 24. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит тяжелую цепь, содержащую аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 22, SEQ ID NO: 25 или SEQ ID NO: 26. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент специфически связывается с белком MICA, белком MICB или обоими белками MICA и MICB. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент связывается с доменом альфа-3 белка MICA, белка MICB или обоих белков MICA и MICB. В некоторых случаях белок MICA является мембраносвязанным белком MICA, растворимым белком MICA или и тем, и другим. В некоторых случаях белок MICB является мембраносвязанным белком MICB, растворимым белком MICB или и тем, и другим. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент выбрано из целого иммуноглобулина, scFv, Fab, F(ab’)2 или соединенного дисульфидной связью Fv. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент является IgG или IgM. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент является гуманизированным или химерным.
[0005] В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам или их антигенсвязывающим фрагментам, содержащим вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам или их антигенсвязывающим фрагментам, содержащим вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 90% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам или их антигенсвязывающим фрагментам, содержащим вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 95% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам или их антигенсвязывающим фрагментам, содержащим вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам или их антигенсвязывающим фрагментам, содержащим вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере 90% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 95% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 8, и вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 7. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 16, и вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 15. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 20, и вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 19. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит тяжелую цепь, содержащую аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 22, SEQ ID NO: 25 или SEQ ID NO: 26. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит легкую цепь, содержащую аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 21, SEQ ID NO: 23 или SEQ ID NO: 24. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент специфически связывается с белком MICA, белком MICB или обоими белками MICA и MICB. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент связывается с доменом альфа-3 белка MICA, белка MICB или обоих белков MICA MICB. В некоторых случаях белок MICA является мембраносвязанным белком MICA, растворимым белком MICA или и тем, и другим. В некоторых случаях белок MICB является мембраносвязанным белком MICB, растворимым белком MICB или и тем, и другим. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент выбрано из целого иммуноглобулина, scFv, Fab, F(ab’)2 или соединенного дисульфидной связью Fv. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент является IgG или IgM. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент является гуманизированным или химерным.
[0006] В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам или их антигенсвязывающим фрагментам, содержащим определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17, где моноклональное антитело не содержит по меньшей мере одну CDR, выбранную из группы, содержащей: SASQGISNYLN, TSLLHSG, QQYSKFPRT, GYTFTNYGMN, INTYTGEPTYADDFKG и NYGNYLFDY. В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам или их антигенсвязывающим фрагментам, содержащим определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 90% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17, где моноклональное антитело не содержит по меньшей мере одну CDR, выбранную из группы, содержащей: SASQGISNYLN, TSLLHSG, QQYSKFPRT, GYTFTNYGMN, INTYTGEPTYADDFKG и NYGNYLFDY. В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам или их антигенсвязывающим фрагментам, содержащим определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 95% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17, где моноклональное антитело не содержит по меньшей мере одну CDR, выбранную из группы, содержащей: SASQGISNYLN, TSLLHSG, QQYSKFPRT, GYTFTNYGMN, INTYTGEPTYADDFKG и NYGNYLFDY. В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам или их антигенсвязывающим фрагментам, содержащим определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 99% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17, где моноклональное антитело не содержит по меньшей мере одну CDR, выбранную из группы, содержащей: SASQGISNYLN, TSLLHSG, QQYSKFPRT, GYTFTNYGMN, INTYTGEPTYADDFKG и NYGNYLFDY. В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам или их антигенсвязывающим фрагментам, содержащим определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, на 100% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17, где моноклональное антитело не содержит по меньшей мере одну CDR, выбранную из группы, содержащей: SASQGISNYLN, TSLLHSG, QQYSKFPRT, GYTFTNYGMN, INTYTGEPTYADDFKG и NYGNYLFDY. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 90% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 95% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 99% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, на 100% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит определяющую комплементарность область 1 (CDR1) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 1, SEQ ID NO: 9 или SEQ ID NO: 17, определяющую комплементарность область 2 (CDR2) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 2 или SEQ ID NO: 10, определяющую комплементарность область 3 (CDR3) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 3 или SEQ ID NO: 11, определяющую комплементарность область 1 (CDR1) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 4 или SEQ ID NO: 12, определяющую комплементарность область 2 (CDR2) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 5, SEQ ID NO: 13 или SEQ ID NO: 18, и определяющую комплементарность область 3 (CDR3) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 6 или SEQ ID NO: 14. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 1, определяющей комплементарность области 2 (CDR2) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 2, и определяющей комплементарность области 3 (CDR3) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 3. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 9, определяющей комплементарность области 2 (CDR2) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 10, и определяющей комплементарность области 3 (CDR3) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 11. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 17, определяющей комплементарность области 2 (CDR2) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 2, и определяющей комплементарность области 3 (CDR3) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 3. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 4, определяющей комплементарность области 2 (CDR2) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 5, и определяющей комплементарность области 3 (CDR3) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 6. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 12, определяющей комплементарность области 2 (CDR2) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 13, и определяющей комплементарность области 3 (CDR3) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 14. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 4, определяющей комплементарность области 2 (CDR2) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 18, и определяющей комплементарность области 3 (CDR3) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 6. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7 или SEQ ID NO: 15; и вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8 или SEQ ID NO: 16. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8 или SEQ ID NO: 16; и вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7 или SEQ ID NO: 15. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 7, и вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 8. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 15, и вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 16. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 19, и вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 20. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит легкую цепь, содержащую аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 21, SEQ ID NO: 23 или SEQ ID NO: 24. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит тяжелую цепь, содержащую аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 22, SEQ ID NO: 25 или SEQ ID NO: 26. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент специфически связывается с белком MICA, белком MICB или обоими белками MICA и MICB. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент связывается с доменом альфа-3 белка MICA, белка MICB или обоих белков MICA и MICB. В некоторых случаях белок MICA является мембраносвязанным белком MICA, растворимым белком MICA или и тем, и другим. В некоторых случаях белок MICB является мембраносвязанным белком MICB, растворимым белком MICB или и тем, и другим. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент выбрано из целого иммуноглобулина, scFv, Fab, F(ab’)2 или соединенного дисульфидной связью Fv. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент является IgG или IgM. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент является гуманизированным или химерным.
[0007] В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам или их антигенсвязывающим фрагментам, содержащим определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18, где моноклональное антитело не содержит по меньшей мере одну CDR, выбранную из группы, содержащей: SASQGISNYLN, TSLLHSG, QQYSKFPRT, GYTFTNYGMN, INTYTGEPTYADDFKG и NYGNYLFDY. В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам или их антигенсвязывающим фрагментам, содержащим определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 90% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18, где моноклональное антитело не содержит по меньшей мере одну CDR, выбранную из группы, содержащей: SASQGISNYLN, TSLLHSG, QQYSKFPRT, GYTFTNYGMN, INTYTGEPTYADDFKG и NYGNYLFDY. В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам или их антигенсвязывающим фрагментам, содержащим определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 95% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18, где моноклональное антитело не содержит по меньшей мере одну CDR, выбранную из группы, содержащей: SASQGISNYLN, TSLLHSG, QQYSKFPRT, GYTFTNYGMN, INTYTGEPTYADDFKG и NYGNYLFDY. В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам или их антигенсвязывающим фрагментам, содержащим определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 99% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18, где моноклональное антитело не содержит по меньшей мере одну CDR, выбранную из группы, содержащей: SASQGISNYLN, TSLLHSG, QQYSKFPRT, GYTFTNYGMN, INTYTGEPTYADDFKG и NYGNYLFDY. В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам или их антигенсвязывающим фрагментам, содержащим определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, на 100% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18, где моноклональное антитело не содержит по меньшей мере одну CDR, выбранную из группы, содержащей: SASQGISNYLN, TSLLHSG, QQYSKFPRT, GYTFTNYGMN, INTYTGEPTYADDFKG и NYGNYLFDY. В некоторых случаях моноклональное антитело или антигенсвязывающий фрагмент содержит определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17. В некоторых случаях моноклональное антитело или антигенсвязывающий фрагмент содержит определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 90% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17. В некоторых случаях моноклональное антитело или антигенсвязывающий фрагмент содержит определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 95% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17. В некоторых случаях моноклональное антитело или антигенсвязывающий фрагмент содержит определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 99% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17. В некоторых случаях моноклональное антитело или антигенсвязывающий фрагмент содержит определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, на 100% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит определяющую комплементарность область 1 (CDR1) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 4 или SEQ ID NO: 12, определяющую комплементарность область 2 (CDR2) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 5, SEQ ID NO: 13 или SEQ ID NO: 18, определяющую комплементарность область 3 (CDR3) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 6 или SEQ ID NO: 14, определяющую комплементарность область 1 (CDR1) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 1, SEQ ID NO: 9 или SEQ ID NO: 17, определяющую комплементарность область 2 (CDR2) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 2 или SEQ ID NO: 10, и определяющую комплементарность область 3 (CDR3) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 3 или SEQ ID NO: 11. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 4, определяющей комплементарность области 2 (CDR2) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 5, и определяющей комплементарность области 3 (CDR3) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 6. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 12, определяющей комплементарность области 2 (CDR2) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 13, и определяющей комплементарность области 3 (CDR3) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 14. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 4, определяющей комплементарность области 2 (CDR2) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 18, и определяющей комплементарность области 3 (CDR3) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 6. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 1, определяющей комплементарность области 2 (CDR2) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 2, и определяющей комплементарность области 3 (CDR3) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 3. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 9, определяющей комплементарность области 2 (CDR2) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 10, и определяющей комплементарность области 3 (CDR3) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 11. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 17, определяющей комплементарность области 2 (CDR2) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 2, и определяющей комплементарность области 3 (CDR3) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 3. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20; и вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7 или SEQ ID NO: 15; и вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8 или SEQ ID NO: 16. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, и вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 16; и вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 15. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 20; и вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 19. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит тяжелую цепь, содержащую аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 22, SEQ ID NO: 25 или SEQ ID NO: 26. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит легкую цепь, содержащую аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 21, SEQ ID NO: 23 или SEQ ID NO: 24. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент специфически связывается с белком MICA, белком MICB или обоими белками MICA и MICB. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент связывается с доменом альфа-3 белка MICA, белка MICB или обоих белков MICA и MICB. В некоторых случаях белок MICA является мембраносвязанным белком MICA, растворимым белком MICA или и тем, и другим. В некоторых случаях белок MICB является мембраносвязанным белком MICB, растворимым белком MICB или и тем, и другим. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент выбрано из целого иммуноглобулина, scFv, Fab, F(ab’)2 или соединенного дисульфидной связью Fv. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент является IgG или IgM. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент является гуманизированным или химерным.
[0008] В некоторых вариантах осуществления настоящее изобретение относится к фармацевтическим композициям, содержащим: моноклональное антитело или его антигенсвязывающий фрагмент по настоящему изобретению и фармацевтически приемлемый носитель или эксципиент.
[0009] В некоторых вариантах осуществления настоящее изобретение относится к способам лечения злокачественного новообразования у больного, включающим введение индивидууму эффективного количества моноклонального антитела или его антигенсвязывающего фрагмента, содержащего определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17, где моноклональное антитело не содержит по меньшей мере одну CDR, выбранную из группы, содержащей: SASQGISNYLN, TSLLHSG, QQYSKFPRT, GYTFTNYGMN, INTYTGEPTYADDFKG и NYGNYLFDY. В некоторых вариантах осуществления настоящее изобретение относится к способам лечения злокачественного новообразования у больного, включающим введение индивидууму эффективного количества моноклонального антитела или его антигенсвязывающего фрагмента, содержащего определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18, где моноклональное антитело не содержит по меньшей мере одну CDR, выбранную из группы, содержащей: SASQGISNYLN, TSLLHSG, QQYSKFPRT, GYTFTNYGMN, INTYTGEPTYADDFKG и NYGNYLFDY. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит (a) определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17; и (b) определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит (a) определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 90% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17; и (b) определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 90% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит (a) определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 95% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17; и (b) определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 95% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит (a) определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 99% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17; и (b) определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 99% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит (a) определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, на 100% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17; и (b) определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, на 100% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит определяющую комплементарность область 1 (CDR1) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 1, SEQ ID NO: 9 или SEQ ID NO: 17, определяющую комплементарность область 2 (CDR2) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 2 или SEQ ID NO: 10, определяющую комплементарность область 3 (CDR3) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 3 или SEQ ID NO: 11, определяющую комплементарность область 1 (CDR1) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 4 или SEQ ID NO: 12, определяющую комплементарность область 2 (CDR2) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 5, SEQ ID NO: 13 или SEQ ID NO: 18, и определяющую комплементарность область 3 (CDR3) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 6 или SEQ ID NO: 14. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 1, определяющей комплементарность области 2 (CDR2) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 2, и определяющей комплементарность области 3 (CDR3) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 3. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 9, определяющей комплементарность области 2 (CDR2) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 10, и определяющей комплементарность области 3 (CDR3) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 11. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 1, определяющей комплементарность области 2 (CDR2) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 2, и определяющей комплементарность области 3 (CDR3) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 3. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 4, определяющей комплементарность области 2 (CDR2) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 5, и определяющей комплементарность области 3 (CDR3) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 6. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 12, определяющей комплементарность области 2 (CDR2) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 13, и определяющей комплементарность области 3 (CDR3) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 14. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 4, определяющей комплементарность области 2 (CDR2) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 18, и определяющей комплементарность области 3 (CDR3) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 6. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19; и вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 7, и вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 8. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 15, и вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 16. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 19, и вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 20. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит легкую цепь, содержащую аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 21, SEQ ID NO: 23 или SEQ ID NO: 24. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит тяжелую цепь, содержащую аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 22, SEQ ID NO: 25 или SEQ ID NO: 26. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент специфически связывается с белком MICA, белком MICB или обоими белками MICA и MICB. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент связывается с доменом альфа-3 белка MICA, белка MICB или обоих белков MICA и MICB. В некоторых случаях белок MICA является мембраносвязанным белком MICA, растворимым белком MICA или и тем, и другим. В некоторых случаях белок MICB является мембраносвязанным белком MICB, растворимым белком MICB или и тем, и другим. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент выбрано из целого иммуноглобулина, scFv, Fab, F(ab’)2 или соединенного дисульфидной связью Fv. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент является IgG или IgM. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент является гуманизированным или химерным. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент снижает уровень растворимого белка MICA, растворимого бека MICB, или и того, и другого. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент снижает шеддинг растворимого белка MICA, растворимого белка MICB или и того, и другого. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент ингибирует шеддинг растворимого белка MICA, растворимого белка MICB или и того, и другого. В некоторых случаях злокачественное новообразование является печеночноклеточной карциномой.
[0010] В некоторых вариантах осуществления настоящее изобретение относится к способам лечения печеночноклеточной карциномы у больного, включающим введение индивидууму эффективного количества моноклонального антитела или его антигенсвязывающего фрагмента, содержащего определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17, где моноклональное антитело не содержит по меньшей мере одну CDR, выбранную из группы, содержащей: SASQGISNYLN, TSLLHSG, QQYSKFPRT, GYTFTNYGMN, INTYTGEPTYADDFKG и NYGNYLFDY. В некоторых вариантах осуществления настоящее изобретение относится к способам лечения печеночноклеточной карциномы у больного, включающим введение индивидууму эффективного количества моноклонального антитела или его антигенсвязывающего фрагмента, содержащего определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18, где моноклональное антитело не содержит по меньшей мере одну CDR, выбранную из группы, содержащей: SASQGISNYLN, TSLLHSG, QQYSKFPRT, GYTFTNYGMN, INTYTGEPTYADDFKG и NYGNYLFDY. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит (a) определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17; и (b) определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит (a) определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 90% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17; и (b) определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 90% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит (a) определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 95% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17; и (b) определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 95% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит (a) определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 99% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17; и (b) определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 99% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит (a) определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, на 100% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17; и (b) определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, на 100% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит определяющую комплементарность область 1 (CDR1) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 1, SEQ ID NO: 9 или SEQ ID NO: 17, определяющую комплементарность область 2 (CDR2) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 2 или SEQ ID NO: 10, определяющую комплементарность область 3 (CDR3) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 3 или SEQ ID NO: 11, определяющую комплементарность область 1 (CDR1) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 4 или SEQ ID NO: 12, определяющую комплементарность область 2 (CDR2) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 5, SEQ ID NO: 13 или SEQ ID NO: 18, и определяющую комплементарность область 3 (CDR3) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 6 или SEQ ID NO: 14. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 1, определяющей комплементарность области 2 (CDR2) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 2, и определяющей комплементарность области 3 (CDR3) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 3. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 9, определяющей комплементарность области 2 (CDR2) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 10, и определяющей комплементарность области 3 (CDR3) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 11. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 1, определяющей комплементарность области 2 (CDR2) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 2, и определяющей комплементарность области 3 (CDR3) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 3. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 4, определяющей комплементарность области 2 (CDR2) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 5, и определяющей комплементарность области 3 (CDR3) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 6. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 12, определяющей комплементарность области 2 (CDR2) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 13, и определяющей комплементарность области 3 (CDR3) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 14. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 4, определяющей комплементарность области 2 (CDR2) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 18, и определяющей комплементарность области 3 (CDR3) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 6. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19; и вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 7, и вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 8. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 15, и вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 16. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 19, и вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 20. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит легкую цепь, содержащую аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 21, SEQ ID NO: 23 или SEQ ID NO: 24. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит тяжелую цепь, содержащую аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 22, SEQ ID NO: 25 или SEQ ID NO: 26. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент специфически связывается с белком MICA, белком MICB или обоими белками MICA и MICB. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент связывается с доменом альфа-3 белка MICA, белка MICB или обоих белков MICA и MICB. В некоторых случаях белок MICA является мембраносвязанным белком MICA, растворимым белком MICA или и тем, и другим. В некоторых случаях белок MICB является мембраносвязанным белком MICB, растворимым белком MICB или и тем, и другим. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент выбрано из целого иммуноглобулина, scFv, Fab, F(ab’)2 или соединенного дисульфидной связью Fv. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент является IgG или IgM. В некоторых случаях моноклональное антитело или его фрагмент является гуманизированным или химерным. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент снижает уровень растворимого белка MICA, растворимого белка MICB или и того, и другого. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент снижает шеддинг растворимого белка MICA, растворимого белка MICB или и того, и другого. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент ингибирует шеддинг растворимого белка MICA, растворимого белка MICB или и того, и другого.
[0011] В некоторых вариантах осуществления настоящее изобретение относится к способам снижения уровня растворимого белка MICA, растворимого белка MICB или и того, и другого у больного, включающим введение индивидууму эффективного количества моноклонального антитела или его антигенсвязывающего фрагмента, содержащего определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17, где моноклональное антитело не содержит по меньшей мере одну CDR, выбранную из группы, содержащей: SASQGISNYLN, TSLLHSG, QQYSKFPRT, GYTFTNYGMN, INTYTGEPTYADDFKG и NYGNYLFDY. В некоторых вариантах осуществления настоящее изобретение относится к способам снижения уровня растворимого белка MICA, растворимого белка MICB или и того, и другого у больного, включающим введение индивидууму эффективного количества моноклонального антитела или его антигенсвязывающего фрагмента, содержащего определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18, где моноклональное антитело не содержит по меньшей мере одну CDR, выбранную из группы, содержащей: SASQGISNYLN, TSLLHSG, QQYSKFPRT, GYTFTNYGMN, INTYTGEPTYADDFKG и NYGNYLFDY. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит (a) определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17; и (b) определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит (a) определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 90% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17; и (b) определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 90% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит (a) определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 95% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17; и (b) определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 95% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит (a) определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 99% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17; и (b) определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 99% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит (a) определяющую комплементарность область (CDR) легкой цепи, имеющую аминокислотную последовательность, на 100% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17; и (b) определяющую комплементарность область (CDR) тяжелой цепи, имеющую аминокислотную последовательность, на 100% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит определяющую комплементарность область 1 (CDR1) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 1, SEQ ID NO: 9 или SEQ ID NO: 17, определяющую комплементарность область 2 (CDR2) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 2 или SEQ ID NO: 10, определяющую комплементарность область 3 (CDR3) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 3 или SEQ ID NO: 11, определяющую комплементарность область 1 (CDR1) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 4 или SEQ ID NO: 12, определяющую комплементарность область 2 (CDR2) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 5, SEQ ID NO: 13 или SEQ ID NO: 18, и определяющую комплементарность область 3 (CDR3) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на 80% идентичную одной из SEQ ID NO: 6 или SEQ ID NO: 14. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 1, определяющей комплементарность области 2 (CDR2) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 2, и определяющей комплементарность области 3 (CDR3) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 3. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 9, определяющей комплементарность области 2 (CDR2) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 10, и определяющей комплементарность области 3 (CDR3) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 11. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 17, определяющей комплементарность области 2 (CDR2) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 2, и определяющей комплементарность области 3 (CDR3) легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 3. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 4, определяющей комплементарность области 2 (CDR2) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 5, и определяющей комплементарность области 3 (CDR3) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 6. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 12, определяющей комплементарность области 2 (CDR2) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 13, и определяющей комплементарность области 3 (CDR3) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 14. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит по меньшей мере одну из определяющей комплементарность области 1 (CDR1) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 4, определяющей комплементарность области 2 (CDR2) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 18, и определяющей комплементарность области 3 (CDR3) тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 6. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15, SEQ ID NO: 19. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19; и вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 7, и вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 8. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 15, и вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 16. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 19, и вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, по меньшей мере на 80% идентичную SEQ ID NO: 20. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит легкую цепь, содержащую аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 21, SEQ ID NO: 23 или SEQ ID NO: 24. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент содержит тяжелую цепь, содержащую аминокислотную последовательность, по меньшей мере на 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 22, SEQ ID NO: 25 или SEQ ID NO: 26. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент специфически связывается с белком MICA, белком MICB или обоими белками MICA и MICB. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент связывается с доменом альфа-3 белка MICA, белка MICB или обоих белков MICA и MICB. В некоторых случаях белок MICA является мембраносвязанным белком MICA, растворимым белком MICA или и тем, и другим. В некоторых случаях белок MICB является мембраносвязанным белком MICB, растворимым белком MICB или и тем, и другим. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент выбрано из целого иммуноглобулина, scFv, Fab, F(ab’)2 или соединенного дисульфидной связью Fv. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент является IgG или IgM. В некоторых случаях моноклональное антитело или его фрагмент является гуманизированным или химерным. В некоторых случаях моноклональное антитело или его антигенсвязывающий фрагмент снижает или ингибирует шеддинг растворимого белка MICA, растворимого белка MICB или и того, и другого, таким образом, снижая уровень растворимого белка MICA, растворимого белка MICB или и того, и другого у индивидуума. В некоторых случаях индивидуум имеет злокачественное новообразование, отличающееся повышенными уровнями растворимого белка MICA, растворимого белка MICB или и того, и другого. В некоторых случаях злокачественное новообразование является печеночноклеточной карциномой.
[0012] В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам или их антигенсвязывающим фрагментам по настоящему изобретению для применения в лечении злокачественного новообразования у больного. В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам или их антигенсвязывающим фрагментам по настоящему изобретению для применения в получении лекарственного средства для лечения злокачественного новообразования у больного. В некоторых случаях злокачественное новообразование является печеночноклеточной карциномой.
[0013] В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам или их антигенсвязывающим фрагментам, связывающимся с MICA/B конкурентно с антителом, содержащим вариабельный домен легкой цепи (VL), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 27. В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам или их антигенсвязывающим фрагментам, связывающимся с MICA/B конкурентно с антителом, содержащим вариабельный домен тяжелой цепи (VH), имеющим аминокислотную последовательность, по меньшей мере на приблизительно 80% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 28.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0014] Признаки и преимущества настоящего изобретения будут понятны со ссылкой на следующее подробное описание, в котором приведены иллюстративные варианты осуществления, в которых использованы принципы настоящего изобретения, и сопутствующие чертежи, на которых:
[0015] На фиг.1A-фиг.1B приведен пример связывания антител 3F9.E4 (фиг.1A) и 16F10.C12 (фиг.1B) с аллелями MICA/B по результатам ELISA.
[0016] На фиг.2 приведен пример связывания 3F9.E4 с MICA на поверхности клетки, оцениваемого посредством окрашивания клеток TRAMP C2, трансфицированных с использованием MICA*08, по сравнению с родительскими клетками TC2.
[0017] На фиг.3 приведен пример ингибирования антителами 3F9.E4 и 16F10.C12 шеддинга MICA с клеток PLC/PRF/5.
[0018] На фиг.4A-фиг.4B приведен пример повышения антителами 3F9.E4 (фиг.4A) и 16F10.C12 (фиг.4B) опосредованной клетками NK-92 цитотоксичности клеток PLC/PRF/5.
[0019] На фиг.5 приведен пример противоопухолевой активности антитела 3F9 в отношении трансфектантов B16/MICA относительно изотипического контроля (IC).
[0020] На фиг.6A-фиг.6C приведен пример более высокой процентной доли NKG2D-положительных NK-клеток (фиг.6A), CD8+T-клеток (фиг.6B) и гамма-дельта-T-клеток (фиг.6C), наблюдаемых в опухолевых инфильтратах (TIL) в обработанных антителом 3F9 опухолях по сравнению с изотипическим контролем.
[0021] На фиг.7A-фиг.7B приведен пример того, что введение антитела 3F9 в B16/MICA MICA-трансгенным животным снижает уровни растворимого MICA (фиг.7A) и MICA на поверхности клеток в опухолях (фиг.7B).
[0022] На фиг.8A-фиг.8C приведен пример конкурентного анализа связывания для иллюстрирования того, что все антитела связываются со "структурным" эпитопом, и антитело 3F9.E4 конкурентно связывается с антителом PDI-1 (фиг.8B), и антитело 16F10 связывается с немного иным эпитопом, чем PDI-1 и 3F9, но находящимся в непосредственной близости (фиг.8C).
ПОДРОБНОЕ ОПИСАНИЕ
[0023] В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам, специфически связывающимся с MICA/B. В некоторых вариантах осуществления антитела против MICA/B по настоящему изобретению связываются с белками MICA/B или их фрагментами и модулируют иммунный ответ у индивидуума, таким образом, делая возможным лечение злокачественного новообразования (например, печеночноклеточной карциномы).
[0024] Родственные главному комплексу гистосовместимости класса I цепи A и B (MICA/B) являются двумя стресс-индуцируемыми лигандами для рецептора NKG2D естественных киллеров (NK-клеток) и играют важную роль в опосредовании цитотоксичности NK-клеток и T-клеток. Растворимый MICA/B, подвергаемый шеддингу пораженными клетками (например, злокачественными клетки), десенсибилизирует NK-клетки и T-клетки посредством связывания рецептора NKG2D, таким образом, супрессируя иммунный ответ.Таким образом, модуляцию MICA/B можно использовать в модулировании иммунного ответа у индивидуума, например, у индивидуума, страдающего злокачественным новообразованием. Антитела, связывающиеся с MICA/B и модулирующие его активность, являются желательными для разработки новых терапевтических средств для лечения злокачественного новообразования.
Терминология
[0025] В рамках изобретения термин "MICA/B" относится к белку MICA, белку MICB или обоим белкам MICA и MICB, включая их варианты, изоформы и видовые гомологи MICA/B человека.
[0026] В рамках изобретения термин "антитело" относится к гликопротеину, демонстрирующему специфичность связывания с конкретным антигеном. Антитело зачастую содержит вариабельный домен и константный домен в каждой из тяжелой цепи и легкой цепи. Таким образом, большинство антител содержит вариабельный домен тяжелой цепи (VH) и вариабельный домен легкой цепи (VL), вместе образующие часть антитела, связывающегося с антигеном. В каждом вариабельном домене есть три определяющие комплементарность области (CDR), образующие петли в вариабельном домене тяжелой цепи (VH) и вариабельном домене легкой цепи (VL), контактирующие с поверхностью антигена. Антитела по настоящему изобретению также включают "антигенсвязывающую часть" или фрагменты антитела, способные связываться с антигеном.
[0027] В рамках изобретения "химерные" антитела являются антителами, содержащими часть тяжелой и/или легкой цепи, идентичную или гомологичную соответствующим последовательностям в антителах, полученных из конкретного биологического вида или принадлежащих к конкретному классу или подклассу антитела, в то время как остальные части цепей идентичны или гомологичны соответствующим последовательностям в антителах, полученных из другого биологического вида или принадлежащих к другому классу или подклассу антител, а также фрагментами таких антител, при условии, что они проявляют желательную биологическая активность (см., например, Morrison et al., Proc. Natl. Acad. Sci. USA 81:6851-6855 (1984)). В настоящем описании термин "гуманизированные антитела" относится к химерным антителам, содержащим последовательности человека, которыми замещают последовательности антитела.
[0028] Термины "реципиент", "индивидуум", "организм-хозяин" и "пациент" используют в настоящем описании взаимозаменяемо, и в некоторых случаях они относятся к индивидууму-млекопитающему, в отношении которых желательными являются диагностика, лечение или терапия, в частности, людям. Термин "млекопитающее" в целях лечения относится к любому животному, классифицируемому как млекопитающее, включая людей, домашних и сельскохозяйственных животных и лабораторных, содержащихся в зоопарках, спортивных животных или животных-питомцев, таких как собаки, лошади, кошки, коровы, овцы, козы, свиньи, мыши, крысы, кролики, морские свинки, обезьяны и т.д. В некоторых вариантах осуществления млекопитающее является человеком.
[0029] В рамках изобретения термин "лечение" и т.п.в некоторых случаях относится к введению средства или осуществлению способа с целью достижения эффекта. Эффект может являться профилактическим в терминах полной или частичной профилактики заболевания или его симптома и/или терапевтическим в терминах осуществления частичного или полного излечения заболевания и/или симптомов заболевания. В рамках изобретения термин "лечение" может включать лечение заболевания или нарушения (например, злокачественного новообразования) у млекопитающего, в частности, человека, и включает: (a) профилактику возникновения заболевания или симптома заболевания у индивидуума, который может быть предрасположен к заболеванию, но у которого его еще не диагностировали (например, включая заболевания, которые могут быть ассоциированы с первичным заболеванием или вызваны им); (b) ингибирование заболевания, т.е. прекращение его развития; и (c) облегчение заболевания, т.е. вызывание регрессирования заболевания. Термин "лечение" может относиться к любым показателям успеха лечения, или улучшения, или профилактики злокачественного новообразования, включая любой объективный или субъективный параметр, такой как уменьшение выраженности симптома; ремиссию; уменьшение симптомов или преобразование заболевания в более переносимое для пациента; замедление дегенерации или ухудшения заболевания; или преобразование конечной точки дегенерации в менее инвалидизирующее. Лечение или улучшение симптомов основано на один или более объективных или субъективных параметров; включая результаты осмотра лечащим врачом. Таким образом, термин "лечение" включает введение соединений или средств по настоящему изобретению для профилактики или замедления, улучшения, или прекращения, или ингибирования развития симптомов или состояний, ассоциированных с заболеваниями (например, злокачественным новообразование). Термин "терапевтический эффект" относится к снижению, устранению или профилактике заболевания, симптомов заболевания или побочных эффектов заболевания у индивидуума.
[0030] В некоторых случаях термин "терапевтически эффективное количество" означает количество, которое при введении индивидууму для лечения заболевания является достаточным для осуществления лечения этого заболевания.
[0031] В рамках изобретения термины в единственном числе включают ссылку на множественное число, если контекст четко не указывает на иное. Таким образом, например, ссылка на "антитело" включает множество антител, и в некоторых вариантах осуществления ссылка на "антитело" включает многочисленные антитела, и т.д.
[0032] В рамках изобретения все числовые значения или числовые диапазоны включают целые числа, в пределах таких диапазонов или включая их, и доли значений или целых чисел, в пределах диапазонов или включаяих, если контекст четко не указывает на иное. Таким образом, например, ссылка на диапазон 90-100% включает 91%, 92%, 93%, 94%, 95%, 95%, 97% и т.д., а также 91,1%, 91,2%, 91,3%, 91,4%, 91,5% и т.д., 92,1%, 92,2%, 92,3%, 92,4%, 92,5% и т.д. В другом примере ссылка на диапазон 1-5000 раз включает 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 раз и т.д., а также 1,1, 1,2, 1,3, 1,4, 1,5 раз и т.д., 2,1, 2,2, 2,3, 2,4, 2,5 раз, и т.д.
[0033] В рамках изобретения термин "приблизительно" в отношении числа относится к диапазону, включающему число и диапазон от значения на 10% ниже этого числа до значения на 10% выше этого числа. Термин "приблизительно" в отношении диапазона относится к значению на 10% ниже нижнего предела диапазона до значения на 10% выше верхнего предела диапазона.
[0034] Термин "процент (%) идентичности" относится к степени, с которой две последовательности (нуклеотидные или аминокислотные) имеют один и тот же остаток в одном и том же положении при выравнивании. Например, фраза "аминокислотная последовательность является на X% идентичной SEQ ID NO: Y" относится к % идентичности аминокислотной последовательности в отношении SEQ ID NO: Y, и ее выражают как X% остатков в аминокислотной последовательности, являющихся идентичными остаткам последовательности, описанной как SEQ ID NO: Y. Как правило, для таких вычислений используют компьютерные программы. Примеры программ, с помощью которых сравнивают и выравнивают пары последовательностей, включают ALIGN (Myers and Miller, 1988), FASTA (Pearson and Lipman, 1988; Pearson, 1990) и gapped BLAST (Altschul et al., 1997), BLASTP, BLASTN или GCG (Devereux et al., 1984).
MICA/B
[0035] В некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам, специфически связывающимся с MICA/B. Кроме того, в некоторых вариантах осуществления настоящее изобретение относится к моноклональным антителам, конкурентно связывающимся с MICA/B.
[0036] Родственные главному комплексу гистосовместимости (MHC) класса I цепи A и B (MICA/B) являются гликозилированными, полиморфными и заякоренными в мембране неклассическими белками MHC класса I. MICA/B родственны MHC класса I и имеют схожую доменную структуру, содержащую три внеклеточных Ig-подобных домена (альфа-1, альфа-2 и альфа-3), трансмембранный домен и C-концевой цитоплазматический хвост.Однако MICA/B не связываются с β2-микроглобулином, в них отсутствует участок связывания CD8, и они не презентируют какие-либо антигены. MICA/B являются лигандами лектин-подобного активирующего рецептора C-типа естественных киллеров группы 2D (NKG2D) на иммунных эффекторных клетках, включая NK-клетки, NKT-клетки и αβ- и γδ-CD8+T-клетки. Взаимодействие MICA/B и NKG2D играет роль в иммунном надзоре за опухолями и иммунном ответе.
[0037] Белки MICA/B в норме экспрессируются на низких уровнях в нормальных клетках, но индуцируются до более высоких уровней в подвергнутых стрессу или трансформированных клетках (например, злокачественных клетках). Взаимодействие NKG2D-несущих иммунных эффекторных клеток с подвергнутыми стрессу или пораженными клетками, экспрессирующими лиганды MICA/B на поверхности клетки, приводит к клеточному иммунному ответу против подвергнутых стрессу/пораженных клеток, достигающему высшей степени в гибели экспрессирующих MICA/B клеток. В злокачественных клетках укороченные белки MICA/B (белки, в которых отсутствуют трансмембранный домен и цитоплазматический хвост, но сохраняются три внеклеточных домена, включающих домены альфа- 1, -2 и -3) часто подвергаются шеддингу в кровь под действием протеаз, что приводит к отрицательной модуляции (интернализации рецептора) его предполагаемого рецептора NKG2D на эффекторных иммунных клетках. В некоторых случаях гликопротеины MICA/B продуцируются внутриклеточно, при этом им обычно не суждено стать мембраносвязанными на поверхности клетки, вместо этого они встраиваются в экзосомы и высвобождаются вне клетки, где происходит взаимодействие с рецепторами NKG2D на иммунных клетках. Эти укороченные или растворимые лиганды MICA/B, подвергающиеся шеддингу с поверхности злокачественных клеток, функционируют подобно молекулам-ловушкам, что приводит к отрицательной модуляции рецептора NKG2D на иммунных эффекторных клетках, таких как NK-клетки, NKT-клетки и различные CD8+T-клетки. В некоторых случаях образование растворимого MICA/B приводит к необычным ситуациям, в которых эффекторы врожденной иммунной системы, естественной ролью которых является поиск и разрушение трансформированных клеток, "отключаются" иммуносупрессорными действиями этих молекул лигандов-ловушек, таким образом, позволяя злокачественным клеткам прятаться от иммунной системы и неконтролируемо расти.
Печеночноклеточная карцинома (HCC)
[0038] В некоторых вариантах осуществления антитела против MICA/B, представленные в настоящем описании, связываются с белками MICA/B или их фрагментами и модулируют иммунный ответ у индивидуума, таким образом, делая возможным лечение злокачественного новообразования (например, печеночноклеточной карциномы).
[0039] Печеночноклеточная карцинома (HCC) является первичным злокачественным новообразованием печени и возникает, главным образом, у индивидуумов с основным хроническим заболеванием печени и циррозом. Опухоли прогрессируют с локальной экспансией, внутрипеченочным распространением и отдаленными метастазами. Гепатит B и гепатит C вызывают предрасположенность индивидуумов к развитию хронического заболевания печени и последующему развитию HCC. Ожирение, диабет и злоупотребление алкоголем представляют собой некоторые другие причины, вызывающие предрасположенность индивидуумов к последующему развитию HCC.
Антитела против MICA/B
[0040] Настоящее изобретение относится к антителам, специфически связывающимся с белками MICA/B. В некоторых вариантах осуществления антитела против MICA/B содержат по меньшей мере одну тяжелую цепь, и антитела против MICA/B содержат по меньшей мере одну легкую цепь. В некоторых вариантах осуществления антитела против MICA/B содержат по меньшей мере одну тяжелую цепь, содержащую вариабельный домен тяжелой цепи (VH), и по меньшей мере одну легкую цепь, содержащую вариабельный домен легкой цепи (VL). Каждый VH и VL содержит три определяющие комплементарность области (CDR). Аминокислотные последовательности VH и VL и CDR определяют специфичность связывания антигена и силу связывания антигена антителом. Аминокислотные последовательности тяжелых и легких цепей, VH и VL и CDR приведены в таблице 1.
[0041] В некоторых вариантах осуществления антитела специфически связываются с белком MICA. В некоторых вариантах осуществления антитела специфически связываются с белком MICB. В некоторых вариантах осуществления антитела специфически связываются с обоими белками MICA и MICB. В некоторых вариантах осуществления антитела связываются с доменом альфа-3 белка MICA. В некоторых вариантах осуществления антитела связываются с доменом альфа-3 белка MICB. В некоторых вариантах осуществления антитела связываются с доменом альфа-3 обоих белков MICA и MICB. В некоторых вариантах осуществления антитела связываются с белком MICA, являющимся мембраносвязанным белком MICA. В некоторых вариантах осуществления антитела связываются с белком MICA, являющимся растворимым белком MICA. В некоторых вариантах осуществления антитела связываются с белком MICA, являющимся и мембраносвязанным белком MICA, и растворимым белком MICA. В некоторых вариантах осуществления антитела связываются с белком MICB, являющимся мембраносвязанным белком MICB. В некоторых вариантах осуществления антитела связываются с белком MICB, являющимся растворимым белком MICB. В некоторых вариантах осуществления антитела связываются с белком MICB, являющимся и мембраносвязанным белком MICB, и растворимым белком MICB.
[0042] В некоторых вариантах осуществления антитела, специфически связывающийся с MICA/B, являются моноклональными антителами. В некоторых вариантах осуществления антитело является антигенсвязывающим фрагментом. В некоторых вариантах осуществления антитело выбрано из целого иммуноглобулина, scFv, Fab, F(ab’)2 или соединенного дисульфидной связью Fv. В некоторых вариантах осуществления антитело является IgG или IgM. В некоторых вариантах осуществления антитело является гуманизированным. В некоторых вариантах осуществления антитело является химерным.
Тяжелая и легкая цепь антитела против MICA/B
[0043] Настоящее изобретение относится к антителам, специфически связывающимся с MICA/B, имеющим легкую цепь. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат легкую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 21, SEQ ID NO: 23 или SEQ ID NO: 24. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 21, SEQ ID NO: 23 или SEQ ID NO: 24. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 21, SEQ ID NO: 23 или SEQ ID NO: 24.
[0044] Настоящее изобретение дополнительно относится к антителам, специфически связывающимся с MICA/B, имеющим тяжелую цепь. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат тяжелую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 22, SEQ ID NO: 25 или SEQ ID NO: 26. В некоторых вариантах осуществления тяжелая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 22, SEQ ID NO: 25 или SEQ ID NO: 26. В некоторых вариантах осуществления тяжелая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 22, SEQ ID NO: 25 или SEQ ID NO: 26.
[0045] Настоящее изобретение также относится к антителам, связывающимся с MICA/B, содержащим легкую цепь и тяжелую цепь. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат легкую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 21, SEQ ID NO: 23 или SEQ ID NO: 24, и тяжелую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 22, SEQ ID NO: 25 или SEQ ID NO: 26. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 21, SEQ ID NO: 23 или SEQ ID NO: 24, и тяжелая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 22, SEQ ID NO: 25 или SEQ ID NO: 26. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 21, SEQ ID NO: 23 или SEQ ID NO: 24, и тяжелая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 22, SEQ ID NO: 25 или SEQ ID NO: 26.
[0046] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат легкую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 21, и тяжелую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 22. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 21, и тяжелая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 22. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 21, и тяжелая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 22.
[0047] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат легкую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 23, и тяжелую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 25. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 23, и тяжелая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 25. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 23, и тяжелая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 25.
[0048] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат легкую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 23, и тяжелую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 26. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 23, и тяжелая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 26. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 23, и тяжелая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 26.
[0049] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат легкую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 24, и тяжелую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 25. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 24, и тяжелая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 25. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 24, и тяжелая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 25.
[0050] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат легкую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 24, и тяжелую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 26. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 24, и тяжелая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 26. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 24, и тяжелая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 26.
Вариабельный домен антитела против MICA/B
[0051] Настоящее изобретение относится к антителам, специфически связывающимся с MICA/B, имеющим легкую цепь, содержащую вариабельный домен легкой цепи (VL). В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат вариабельный домен легкой цепи (VL), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19.
[0052] Настоящее изобретение дополнительно относится к антителам, специфически связывающимся с MICA/B, имеющим тяжелую цепь, содержащую вариабельный домен тяжелой цепи (VH). В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат вариабельный домен тяжелой цепи (VH), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых вариантах осуществления VH имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых вариантах осуществления VH имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20.
[0053] Настоящее изобретение также относится к антителам, связывающимся с MICA/B, содержащим вариабельный домен легкой цепи (VL) и вариабельный домен тяжелой цепи (VH). В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат вариабельный домен легкой цепи (VL), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19, и вариабельный домен тяжелой цепи (VH), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19, и VH имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19, и VH имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20.
[0054] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат вариабельный домен легкой цепи (VL), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, и вариабельный домен тяжелой цепи (VH), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, и VH имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, и VH имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8.
[0055] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат вариабельный домен легкой цепи (VL), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 15, и вариабельный домен тяжелой цепи (VH), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 16. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 15, и VH имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 16. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 15, и VH имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 16.
[0056] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат вариабельный домен легкой цепи (VL), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 19, и вариабельный домен тяжелой цепи (VH), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 20. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 19, и VH имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 20. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 19, и VH имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 20.
Определяющие комплементарность области антитела против MICA/B
[0057] Настоящее изобретение относится к антителам, специфически связывающимся с MICA/B, имеющим легкую цепь, содержащую определяющую комплементарность область (CDR) легкой цепи. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат последовательность CDR легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат последовательность CDR легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат последовательность CDR легкой цепи, имеющую аминокислотную последовательность, на 100% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17.
[0058] Настоящее изобретение дополнительно относится к антителам, специфически связывающимся с MICA/B, имеющим тяжелую цепь, содержащую определяющая комплементарность область (CDR) тяжелой цепи. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат последовательность CDR тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат последовательность CDR тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат последовательность CDR тяжелой цепи, имеющую аминокислотную последовательность, на 100% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18.
[0059] Настоящее изобретение также относится к антителам, связывающимся с MICA/B, содержащим определяющую комплементарность область (CDR) легкой цепи и определяющую комплементарность область (CDR) тяжелой цепи. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат последовательность CDR легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17, и последовательность CDR тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат последовательность CDR легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17, и последовательность CDR тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат последовательность CDR легкой цепи, имеющую аминокислотную последовательность, на 100% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17, и последовательность CDR тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 100% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18.
[0060] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат определяющую комплементарность область 1 (CDR1) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную одной из SEQ ID NO: 1, SEQ ID NO: 9 или SEQ ID NO: 17, определяющую комплементарность область 2 (CDR2) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную одной из SEQ ID NO: 2 или SEQ ID NO: 10, определяющую комплементарность область 3 (CDR3) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную одной из SEQ ID NO: 3 или SEQ ID NO: 11, определяющую комплементарность область 1 (CDR1) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную одной из SEQ ID NO: 4 или SEQ ID NO: 12, определяющую комплементарность область 2 (CDR2) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную одной из SEQ ID NO: 5, SEQ ID NO: 13 или SEQ ID NO: 18, и определяющую комплементарность область 3 (CDR3) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную одной из SEQ ID NO: 6 или SEQ ID NO: 14. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат определяющую комплементарность область 1 (CDR1) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную одной из SEQ ID NO: 1, SEQ ID NO: 9 или SEQ ID NO: 17, определяющую комплементарность область 2 (CDR2) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную одной из SEQ ID NO: 2 или SEQ ID NO: 10, определяющую комплементарность область 3 (CDR3) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную одной из SEQ ID NO: 3 или SEQ ID NO: 11, определяющую комплементарность область 1 (CDR1) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную одной из SEQ ID NO: 4 или SEQ ID NO: 12, определяющую комплементарность область 2 (CDR2) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную одной из SEQ ID NO: 5, SEQ ID NO: 13 или SEQ ID NO: 18, и определяющую комплементарность область 3 (CDR3) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную одной из SEQ ID NO: 6 или SEQ ID NO: 14. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат определяющую комплементарность область 1 (CDR1) легкой цепи, имеющую аминокислотную последовательность, на 100% идентичную одной из SEQ ID NO: 1, SEQ ID NO: 9 или SEQ ID NO: 17, определяющую комплементарность область 2 (CDR2) легкой цепи, имеющую аминокислотную последовательность, на 100% идентичную одной из SEQ ID NO: 2 или SEQ ID NO: 10, определяющую комплементарность область 3 (CDR3) легкой цепи, имеющую аминокислотную последовательность, на 100% идентичную одной из SEQ ID NO: 3 или SEQ ID NO: 11, определяющую комплементарность область 1 (CDR1) тяжелой цепи, имеющую аминокислотную последовательность, на 100% идентичную одной из SEQ ID NO: 4 или SEQ ID NO: 12, определяющую комплементарность область 2 (CDR2) тяжелой цепи, имеющую аминокислотную последовательность, на 100% идентичную одной из SEQ ID NO: 5, SEQ ID NO: 13 или SEQ ID NO: 18, и определяющую комплементарность область 3 (CDR3) тяжелой цепи, имеющую аминокислотную последовательность, на 100% идентичную одной из SEQ ID NO: 6 или SEQ ID NO: 14.
[0061] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 1, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 2, и CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 3. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 1, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 2, и CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 3. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 1, CDR2 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 2, и CDR3 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 3.
[0062] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 9, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 10, и CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 11. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 9, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 10, и CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 11. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 9, CDR2 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 10, и CDR3 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 11.
[0063] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 17, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 2, и CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 3. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 17, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 2, и CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 3. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 17, CDR2 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 2, и CDR3 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 3.
[0064] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 5, CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 6. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 5, CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 6. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 5, CDR3 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 6.
[0065] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 12, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 13, CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 14. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 12, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 13, CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 14. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 12, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 13, CDR3 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 14.
[0066] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 18, CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 6. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 18, CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 6. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 18, CDR3 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 6.
[0067] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 1, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 2, CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 3, CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 5, и CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 6. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 1, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 2, CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 3, CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 5, и CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 6. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 1, CDR2 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 2, CDR3 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 3, CDR1 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 5, и CDR3 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 6.
[0068] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 9, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 10, CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 11, CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 12, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 13, и CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 14. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 9, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 10, CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 11, CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 12, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 13, и CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 14. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 9, CDR2 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 10, CDR3 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 11, CDR1 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 12, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 13, и CDR3 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 14.
[0069] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 17, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 2, CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 3, CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 18, и CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 6. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 17, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 2, CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 3, CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 18, и CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 6. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 17, CDR2 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 2, CDR3 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 3, CDR1 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 18, и CDR3 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 6.
[0070] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, не содержат по меньшей мере одну CDR, выбранную из группы, содержащей: SASQGISNYLN, TSLLHSG, QQYSKFPRT, GYTFTNYGMN, INTYTGEPTYADDFKG и NYGNYLFDY.
Конкурентное связывание
[0071] В некоторых вариантах осуществления настоящее изобретение относится к антителам, связывающимся с MICA/B конкурентно с антителом, содержащим вариабельный домен легкой цепи (VL), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 27. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 27. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 27.
[0072] В некоторых вариантах осуществления настоящее изобретение относится к антителам, связывающимся с MICA/B конкурентно с антителом, содержащим вариабельный домен тяжелой цепи (VH), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 28. В некоторых вариантах осуществления VH имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 28. В некоторых вариантах осуществления VH имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 28.
[0073] В некоторых вариантах осуществления настоящее изобретение относится к антителам, связывающимся с MICA/B конкурентно с антителом, содержащим вариабельный домен легкой цепи (VL), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 27, и вариабельный домен тяжелой цепи (VH), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 28. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 27, и VH имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 28. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 27, и VH имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 28.
Способы лечения и применение
[0074] Настоящее изобретение относится к способам лечения злокачественного новообразования (например, печеночноклеточной карциномы) у больного, включающим введение антитела против MICA/B, представленного в настоящем описании.
[0075] Настоящее изобретение дополнительно относится к способам снижения уровня растворимых белков MICA/B у больного, включающим введение антитела против MICA/B, представленного в настоящем описании.
[0076] Настоящее изобретение также относится к способам уменьшения или ингибирования иммуносупрессорного окружения посредством предотвращения или блокирования взаимодействия между растворимым MICA/B и рецепторами NKG2D у больного, включающим введение антитела против MICA/B, представленного в настоящем описании.
[0077] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат последовательность CDR легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат последовательность CDR легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат последовательность CDR легкой цепи, имеющую аминокислотную последовательность, на 100% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17.
[0078] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат последовательность CDR тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат последовательность CDR тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат последовательность CDR тяжелой цепи, имеющую аминокислотную последовательность, на 100% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18.
[0079] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат последовательность CDR легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17, и последовательность CDR тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат последовательность CDR легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17, и последовательность CDR тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат последовательность CDR легкой цепи, имеющую аминокислотную последовательность, на 100% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 1-3, 9-11 и 17, и последовательность CDR тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 100% идентичную по меньшей мере одной из аминокислотных последовательностей, приведенных как SEQ ID NO: 4-6, 12-14 и 18.
[0080] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат определяющую комплементарность область 1 (CDR1) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную одной из SEQ ID NO: 1, SEQ ID NO: 9 или SEQ ID NO: 17, определяющую комплементарность область 2 (CDR2) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную одной из SEQ ID NO: 2 или SEQ ID NO: 10, определяющую комплементарность область 3 (CDR3) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную одной из SEQ ID NO: 3 или SEQ ID NO: 11, определяющую комплементарность область 1 (CDR1) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную одной из SEQ ID NO: 4 или SEQ ID NO: 12, определяющую комплементарность область 2 (CDR2) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную одной из SEQ ID NO: 5, SEQ ID NO: 13 или SEQ ID NO: 18, и определяющую комплементарность область 3 (CDR3) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную одной из SEQ ID NO: 6 или SEQ ID NO: 14. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат определяющую комплементарность область 1 (CDR1) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную одной из SEQ ID NO: 1, SEQ ID NO: 9 или SEQ ID NO: 17, определяющую комплементарность область 2 (CDR2) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную одной из SEQ ID NO: 2 или SEQ ID NO: 10, определяющую комплементарность область 3 (CDR3) легкой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную одной из SEQ ID NO: 3 или SEQ ID NO: 11, определяющую комплементарность область 1 (CDR1) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную одной из SEQ ID NO: 4 или SEQ ID NO: 12, определяющую комплементарность область 2 (CDR2) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную одной из SEQ ID NO: 5, SEQ ID NO: 13 или SEQ ID NO: 18, и определяющую комплементарность область 3 (CDR3) тяжелой цепи, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную одной из SEQ ID NO: 6 или SEQ ID NO: 14. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат определяющую комплементарность область 1 (CDR1) легкой цепи, имеющую аминокислотную последовательность, на 100% идентичную одной из SEQ ID NO: 1, SEQ ID NO: 9 или SEQ ID NO: 17, определяющую комплементарность область 2 (CDR2) легкой цепи, имеющую аминокислотную последовательность, на 100% идентичную одной из SEQ ID NO: 2 или SEQ ID NO: 10, определяющую комплементарность область 3 (CDR3) легкой цепи, имеющую аминокислотную последовательность, на 100% идентичную одной из SEQ ID NO: 3 или SEQ ID NO: 11, определяющую комплементарность область 1 (CDR1) тяжелой цепи, имеющую аминокислотную последовательность, на 100% идентичную одной из SEQ ID NO: 4 или SEQ ID NO: 12, определяющую комплементарность область 2 (CDR2) тяжелой цепи, имеющую аминокислотную последовательность, на 100% идентичную одной из SEQ ID NO: 5, SEQ ID NO: 13 или SEQ ID NO: 18, и определяющую комплементарность область 3 (CDR3) тяжелой цепи, имеющую аминокислотную последовательность, на 100% идентичную одной из SEQ ID NO: 6 или SEQ ID NO: 14.
[0081] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 1, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 2, и CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 3. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 1, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 2, и CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 3. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 1, CDR2 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 2, и CDR3 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 3.
[0082] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 9, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 10, и CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 11. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 9, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 10, и CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 11. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 9, CDR2 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 10, и CDR3 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 11.
[0083] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 17, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 2, и CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 3. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 17, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 2, и CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 3. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 17, CDR2 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 2, и CDR3 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 3.
[0084] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 5, CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 6. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 5, CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 6. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 5, CDR3 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 6.
[0085] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 12, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 13, CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 14. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 12, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 13, CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 14. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 12, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 13, CDR3 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 14.
[0086] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 18, CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 6. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 18, CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 6. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 18, CDR3 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 6.
[0087] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 1, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 2, CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 3, CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 5, и CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 6. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 1, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 2, CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 3, CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 5, и CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 6. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 1, CDR2 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 2, CDR3 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 3, CDR1 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 5, и CDR3 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 6.
[0088] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 9, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 10, CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 11, CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 12, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 13, и CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 14. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 9, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 10, CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 11, CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 12, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 13, и CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 14. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 9, CDR2 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 10, CDR3 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 11, CDR1 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 12, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 13, и CDR3 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 14.
[0089] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 17, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 2, CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 3, CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 18, и CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 6. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 17, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 2, CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 3, CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 18, и CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 6. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 17, CDR2 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 2, CDR3 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 3, CDR1 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 18, и CDR3 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 6.
[0090] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, не содержат по меньшей мере одну CDR, выбранную из группы, содержащей: SASQGISNYLN, TSLLHSG, QQYSKFPRT, GYTFTNYGMN, INTYTGEPTYADDFKG и NYGNYLFDY.
[0091] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат вариабельный домен легкой цепи (VL), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19.
[0092] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат вариабельный домен тяжелой цепи (VH), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых вариантах осуществления VH имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых вариантах осуществления VH имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20.
[0093] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат вариабельный домен легкой цепи (VL), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19, и вариабельный домен тяжелой цепи (VH), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19, и VH имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, SEQ ID NO: 15 или SEQ ID NO: 19, и VH имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8, SEQ ID NO: 16 или SEQ ID NO: 20.
[0094] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат вариабельный домен легкой цепи (VL), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, и вариабельный домен тяжелой цепи (VH), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, и VH имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 7, и VH имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 8.
[0095] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат вариабельный домен легкой цепи (VL), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 15, и вариабельный домен тяжелой цепи (VH), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 16. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 15, и VH имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 16. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 15, и VH имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 16.
[0096] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат вариабельный домен легкой цепи (VL), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 19, и вариабельный домен тяжелой цепи (VH), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 20. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 19, и VH имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 20. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 19, и VH имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 20.
[0097]
[0098] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат легкую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 21, SEQ ID NO: 23 или SEQ ID NO: 24. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 21, SEQ ID NO: 23 или SEQ ID NO: 24. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 21, SEQ ID NO: 23 или SEQ ID NO: 24.
[0099] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат тяжелую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 22, SEQ ID NO: 25 или SEQ ID NO: 26. В некоторых вариантах осуществления тяжелая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 22, SEQ ID NO: 25 или SEQ ID NO: 26. В некоторых вариантах осуществления тяжелая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 22, SEQ ID NO: 25 или SEQ ID NO: 26.
[00100] Настоящее изобретение также относится к антителам, связывающимся с MICA/B, содержащим легкую цепь и тяжелую цепь. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат легкую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 21, SEQ ID NO: 23 или SEQ ID NO: 24, и тяжелую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 22, SEQ ID NO: 25 или SEQ ID NO: 26. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 21, SEQ ID NO: 23 или SEQ ID NO: 24, и тяжелая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 22, SEQ ID NO: 25 или SEQ ID NO: 26. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 21, SEQ ID NO: 23 или SEQ ID NO: 24, и тяжелая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 22, SEQ ID NO: 25 или SEQ ID NO: 26.
[00101] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат легкую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 21, и тяжелую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 22. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 21, и тяжелая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 22. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 21, и тяжелая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 22.
[00102] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат легкую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 23, и тяжелую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 25. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 23, и тяжелая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 25. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 23, и тяжелая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 25.
[00103] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат легкую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 23, и тяжелую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 26. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 23, и тяжелая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 26. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 23, и тяжелая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 26.
[00104] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат легкую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 24, и тяжелую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 25. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 24, и тяжелая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 25. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 24, и тяжелая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 25.
[00105] В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, содержат легкую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 24, и тяжелую цепь, имеющую аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 26. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 24, и тяжелая цепь имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 26. В некоторых вариантах осуществления легкая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 24, и тяжелая цепь имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 26.
[00106] В некоторых вариантах осуществления антитела связываются с MICA/B конкурентно с антителом, содержащим вариабельный домен легкой цепи (VL), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 27. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 27. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 27.
[00107] В некоторых вариантах осуществления антитела связываются с MICA/B конкурентно с антителом, содержащим вариабельный домен тяжелой цепи (VH), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 28. В некоторых вариантах осуществления VH имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 28. В некоторых вариантах осуществления VH имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 28.
[00108] В некоторых вариантах осуществления антитела связываются с MICA/B конкурентно с антителом, содержащим вариабельный домен легкой цепи (VL), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 27, и вариабельный домен тяжелой цепи (VH), имеющий аминокислотную последовательность, по меньшей мере на приблизительно 70% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 28. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 27, и VH имеет аминокислотную последовательность, по меньшей мере на приблизительно 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 28. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 27, и VH имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности, приведенной как SEQ ID NO: 28.
[00109] В некоторых вариантах осуществления антитела специфически связываются с белком MICA. В некоторых вариантах осуществления антитела специфически связываются с белком MICB. В некоторых вариантах осуществления антитела специфически связываются с обоими белками MICA и MICB. В некоторых вариантах осуществления антитела связываются с доменом альфа-3 белка MICA. В некоторых вариантах осуществления антитела связываются с доменом альфа-3 белка MICB. В некоторых вариантах осуществления антитела связываются с доменом альфа-3 обоих белков MICA и MICB. В некоторых вариантах осуществления антитела связываются с белком MICA, являющимся мембраносвязанным белком MICA. В некоторых вариантах осуществления антитела связываются с белком MICA, являющимся растворимым белком MICA. В некоторых вариантах осуществления антитела связываются с белком MICA, являющимся и мембраносвязанным белком MICA, и растворимым белком MICA. В некоторых вариантах осуществления антитела связываются с белком MICB, являющимся мембраносвязанным белком MICB. В некоторых вариантах осуществления антитела связываются с белком MICB, являющимся растворимым белком MICB. В некоторых вариантах осуществления антитела связываются с белком MICB, являющимся и мембраносвязанным белком MICB, и растворимым белком MICB.
[00110] В некоторых вариантах осуществления антитела, специфически связывающийся с MICA/B, являются моноклональными антителами. В некоторых вариантах осуществления антитело является антигенсвязывающим фрагментом. В некоторых вариантах осуществления антитело выбрано из целого иммуноглобулина, scFv, Fab, F(ab’)2 или соединенного дисульфидной связью Fv. В некоторых вариантах осуществления антитело является IgG или IgM. В некоторых вариантах осуществления антитело является гуманизированным. В некоторых вариантах осуществления антитело является химерным.
[00111] В некоторых вариантах осуществления антитела, представленные в настоящем описании, снижают уровень растворимого белка MICA. В некоторых вариантах осуществления антитела, представленные в настоящем описании, снижают уровень растворимого белка MICB. В некоторых вариантах осуществления антитела, представленные в настоящем описании, снижают уровень и растворимого белка MICA, и растворимого белка MICB. В некоторых вариантах осуществления антитела, представленные в настоящем описании, снижают шеддинг растворимого белка MICA. В некоторых вариантах осуществления антитела, представленные в настоящем описании, снижают шеддинг растворимого белка MICB. В некоторых вариантах осуществления антитела, представленные в настоящем описании, снижают шеддинг и растворимого белка MICA, и растворимого белка MICB. В некоторых вариантах осуществления антитела, представленные в настоящем описании, ингибируют шеддинг растворимого белка MICA. В некоторых вариантах осуществления антитела, представленные в настоящем описании, ингибируют шеддинг растворимого белка MICB. В некоторых вариантах осуществления антитела, представленные в настоящем описании, ингибируют шеддинг и растворимого белка MICA, и растворимого белка MICB.
[00112] Для использования в способах, представленных в настоящем описании, предусмотрен любой подходящий путь введения. В некоторых вариантах осуществления антитело вводят посредством внутривенного введения. В некоторых вариантах осуществления антитело вводят посредством подкожного введения. В некоторых вариантах осуществления антитело вводят локально. В некоторых вариантах осуществления антитело вводят системно (например, внутривенно, внутримышечно, подкожно, внутрикожно, перорально, интраназально, сублингвально). В некоторых вариантах осуществления антитело составляют в виде мази, лосьона или эмульсии. В некоторых вариантах осуществления антитело составляют в виде раствора. В некоторых вариантах осуществления антитело составляют для местного, перорального, буккального или назального введения.
[00113] В некоторых вариантах осуществления индивидуума подвергают мониторингу перед введением антитела. Идентифицируют симптомы и оценивают их тяжесть. Антитело, представленное в настоящем описании, вводят в отдельности или в комбинации с дополнительным лечением, однократно или многократно в течение периода времени, как представлено в настоящем описании или известно специалисту в этой области. В некоторых вариантах осуществления индивидуума подвергают мониторингу таким образом, что определяют эффективность схемы лечения. В некоторых вариантах осуществления схему лечения модифицируют с учетом исходов предварительного лечения, таким образом, что лечебную дозу, или частоту, или дозу и частоту изменяют так, чтобы достигать желаемого уровня ответа у индивидуума с учетом облегчения симптомов, снижения побочных эффектов или комбинации облегчения симптомов и снижения побочных эффектов.
[00114] Терапевтически эффективные количества или дозы предназначены для включения доз от приблизительно 0,01 мг/кг до приблизительно 20 мг/кг, например, приблизительно 0,01 мг/кг, приблизительно 0,02 мг/кг, приблизительно 0,03 мг/кг, приблизительно 0,04 мг/кг, приблизительно 0,05 мг/кг, приблизительно 0,06 мг/кг, приблизительно 0,07 мг/кг, приблизительно 0,08 мг/кг, приблизительно 0,09 мг/кг, приблизительно 0,1 мг/кг, приблизительно 0,2 мг/кг, приблизительно 0,3 мг/кг, приблизительно 0,4 мг/кг, приблизительно 0,5 мг/кг, приблизительно 0,6 мг/кг, приблизительно 0,7 мг/кг, приблизительно 0,8 мг/кг, приблизительно 0,9 мг/кг, приблизительно 1,0 мг/кг, приблизительно 1,1 мг/кг, приблизительно 1,2 мг/кг, приблизительно 1,3 мг/кг, приблизительно 1,4 мг/кг, приблизительно 1,5 мг/кг, приблизительно 1,6 мг/кг, приблизительно 1,7 мг/кг, приблизительно 1,8 мг/кг, приблизительно 1,9 мг/кг, приблизительно 2 мг/кг, приблизительно 2,1 мг/кг, приблизительно 2,2 мг/кг, приблизительно 2,3 мг/кг, приблизительно 2,4 мг/кг, приблизительно 2,5 мг/кг, приблизительно 2,6 мг/кг, приблизительно 2,7 мг/кг, приблизительно 2,8 мг/кг, приблизительно 2,9 мг/кг, приблизительно 3 мг/кг, приблизительно 3,1 мг/кг, приблизительно 3,2 мг/кг, приблизительно 3,3 мг/кг, приблизительно 3,4 мг/кг, приблизительно 3,5 мг/кг, приблизительно 3,6 мг/кг, приблизительно 3,7 мг/кг, приблизительно 3,8 мг/кг, приблизительно 3,9 мг/кг, приблизительно 4 мг/кг, приблизительно 4,1 мг/кг, приблизительно 4,2 мг/кг, приблизительно 4,3 мг/кг, приблизительно 4,4 мг/кг, приблизительно 4,5 мг/кг, приблизительно 4,6 мг/кг, приблизительно 4,7 мг/кг, приблизительно 4,8 мг/кг, приблизительно 4,9 мг/кг, приблизительно 5 мг/кг, приблизительно 5,1 мг/кг, приблизительно 5,2 мг/кг, приблизительно 5,3 мг/кг, приблизительно 5,4 мг/кг, приблизительно 5,5 мг/кг, приблизительно 5,6 мг/кг, приблизительно 5,7 мг/кг, приблизительно 5,8 мг/кг, приблизительно 5,9 мг/кг, приблизительно 6 мг/кг, приблизительно 6,1 мг/кг, приблизительно 6,2 мг/кг, приблизительно 6,3 мг/кг, приблизительно 6,4 мг/кг, приблизительно 6,5 мг/кг, приблизительно 6,6 мг/кг, приблизительно 6,7 мг/кг, приблизительно 6,8 мг/кг, приблизительно 6,9 мг/кг, приблизительно 7 мг/кг, приблизительно 7,1 мг/кг, приблизительно 7,2 мг/кг, приблизительно 7,3 мг/кг, приблизительно 7,4 мг/кг, приблизительно 7,5 мг/кг, приблизительно 7,6 мг/кг, приблизительно 7,7 мг/кг, приблизительно 7,8 мг/кг, приблизительно 7,9 мг/кг, приблизительно 8 мг/кг, приблизительно 8,1 мг/кг, приблизительно 8,2 мг/кг, приблизительно 8,3 мг/кг, приблизительно 8,4 мг/кг, приблизительно 8,5 мг/кг, приблизительно 8,6 мг/кг, приблизительно 8,7 мг/кг, приблизительно 8,8 мг/кг, приблизительно 8,9 мг/кг, приблизительно 9 мг/кг, приблизительно 9,1 мг/кг, приблизительно 9,2 мг/кг, приблизительно 9,3 мг/кг, приблизительно 9,4 мг/кг, приблизительно 9,5 мг/кг, приблизительно 9,6 мг/кг, приблизительно 9,7 мг/кг, приблизительно 9,8 мг/кг, приблизительно 9,9 мг/кг, приблизительно 10 мг/кг, приблизительно 10,1 мг/кг, приблизительно 10,2 мг/кг, приблизительно 10,3 мг/кг, приблизительно 10,4 мг/кг, приблизительно 10,5 мг/кг, приблизительно 10,6 мг/кг, приблизительно 10,7 мг/кг, приблизительно 10,8 мг/кг, приблизительно 10,9 мг/кг, приблизительно 11 мг/кг, приблизительно 11,1 мг/кг, приблизительно 11,2 мг/кг, приблизительно 11,3 мг/кг, приблизительно 11,4 мг/кг, приблизительно 11,5 мг/кг, приблизительно 11,6 мг/кг, приблизительно 11,7 мг/кг, приблизительно 11,8 мг/кг, приблизительно 11,9 мг/кг, приблизительно 12 мг/кг, приблизительно 12,1 мг/кг, приблизительно 12,2 мг/кг, приблизительно 12,3 мг/кг, приблизительно 12,4 мг/кг, приблизительно 12,5 мг/кг, приблизительно 12,6 мг/кг, приблизительно 12,7 мг/кг, приблизительно 12,8 мг/кг, приблизительно 12,9 мг/кг, приблизительно 13 мг/кг, приблизительно 13,1 мг/кг, приблизительно 13,2 мг/кг, приблизительно 13,3 мг/кг, приблизительно 13,4 мг/кг, приблизительно 13,5 мг/кг, приблизительно 13,6 мг/кг, приблизительно 13,7 мг/кг, приблизительно 13,8 мг/кг, приблизительно 13,9 мг/кг, приблизительно 14 мг/кг, приблизительно 14,1 мг/кг, приблизительно 14,2 мг/кг, приблизительно 14,3 мг/кг, приблизительно 14,4 мг/кг, приблизительно 14,5 мг/кг, приблизительно 14,6 мг/кг, приблизительно 14,7 мг/кг, приблизительно 14,8 мг/кг, приблизительно 14,9 мг/кг, приблизительно 15 мг/кг, приблизительно 15,1 мг/кг, приблизительно 15,2 мг/кг, приблизительно 15,3 мг/кг, приблизительно 15,4 мг/кг, приблизительно 15,5 мг/кг, приблизительно 15,6 мг/кг, приблизительно 15,7 мг/кг, приблизительно 15,8 мг/кг, приблизительно 15,9 мг/кг, приблизительно 16 мг/кг, приблизительно 16,1 мг/кг, приблизительно 16,2 мг/кг, приблизительно 16,3 мг/кг, приблизительно 16,4 мг/кг, приблизительно 16,5 мг/кг, приблизительно 16,6 мг/кг, приблизительно 16,7 мг/кг, приблизительно 16,8 мг/кг, приблизительно 16,9 мг/кг, приблизительно 17 мг/кг, приблизительно 17,1 мг/кг, приблизительно 17,2 мг/кг, приблизительно 17,3 мг/кг, приблизительно 17,4 мг/кг, приблизительно 17,5 мг/кг, приблизительно 17,6 мг/кг, приблизительно 17,7 мг/кг, приблизительно 17,8 мг/кг, приблизительно 17,9 мг/кг, приблизительно 18 мг/кг, приблизительно 18,1 мг/кг, приблизительно 18,2 мг/кг, приблизительно 18,3 мг/кг, приблизительно 18,4 мг/кг, приблизительно 18,5 мг/кг, приблизительно 18,6 мг/кг, приблизительно 18,7 мг/кг, приблизительно 18,8 мг/кг, приблизительно 18,9 мг/кг, приблизительно 19 мг/кг, приблизительно 19,1 мг/кг, приблизительно 19,2 мг/кг, приблизительно 19,3 мг/кг, приблизительно 19,4 мг/кг, приблизительно 19,5 мг/кг, приблизительно 19,6 мг/кг, приблизительно 19,7 мг/кг, приблизительно 19,8 мг/кг, приблизительно 19,9 мг/кг, приблизительно или 20 мг/кг.В некоторых случаях терапевтически эффективные количества или дозы предназначены для включения доз от приблизительно 0,1 мг/кг до приблизительно 2,0 мг/кг.
[00115] Способы лечения по настоящему изобретению включают одно или более введений антител против MICA/B в дозах, представленных в настоящем описании. В некоторых вариантах осуществления способы включают одно введение антител против MICA/B. В некоторых вариантах осуществления способы включают два введения антител против MICA/B. В некоторых вариантах осуществления способы включают три введения антител против MICA/B. В некоторых вариантах осуществления способы включают четыре введения антител против MICA/B. В некоторых вариантах осуществления способы включают пять введений антител против MICA/B. В некоторых вариантах осуществления способы включают шесть введений антител против MICA/B. В некоторых вариантах осуществления одно или более введений антител против MICA/B осуществляют ежедневно. В некоторых вариантах осуществления одно или более введений антител против MICA/B осуществляют еженедельно. В некоторых вариантах осуществления одно или более введений антител против MICA/B осуществляют раз в две недели. В некоторых вариантах осуществления одно или более введений антител против MICA/B осуществляют ежемесячно. В некоторых вариантах осуществления одно или более введений антител против MICA/B осуществляют каждые три месяца. В некоторых вариантах осуществления одно или более введений антител против MICA/B осуществляют каждые шесть месяцев. В некоторых вариантах осуществления одно или более введений антител против MICA/B осуществляют ежегодно.
[00116] В некоторых вариантах осуществления способы лечения, представленные в настоящем описании, представляет собой монотерапию. В некоторых вариантах осуществления способы лечения, представленные в настоящем описании, представляют собой комбинированное лечение. В некоторых вариантах осуществления комбинированное лечение включает введения антител против MICA/B в комбинации с другим терапевтическим средством. В некоторых вариантах осуществления терапевтическое средство включает химиотерапевтическое средство. В некоторых вариантах осуществления химиотерапевтическое средство включают, в качестве неограничивающих примеров, цитотоксические средства, антиметаболиты (например, антагонисты фолиевой кислоты, аналоги пурина, аналоги пиримидина и т.д.), ингибиторы топоизомераз (например, производные камптотецина, антрацендион, антрациклины, эпиподофиллотоксины, хинолиновые алкалоиды и т.д.), средства против микротрубочек (например, таксаны, алкалоиды барвинка), ингибиторы белкового синтеза (например, цефалотаксин, производные камптотецина, хинолиновые алкалоиды), алкилирующие средства (например, алкилсульфонаты, этиленимины, азотистые иприты, нитрозомочевину, производные платины, триазены и т.д.), алкалоиды, терпеноиды, ингибиторы киназ и ингибиторы иммунных контрольных точек. В некоторых вариантах осуществления антитела против MICA/B, представленные в настоящем описании, вводят в комбинации с терапевтическим средством, индуцирующим иммунный ответ.В некоторых вариантах осуществления антитела против MICA/B, представленные в настоящем описании, вводят в комбинации с терапевтическим средством, ингибирующим отрицательную регуляцию иммунного ответа. В некоторых вариантах осуществления индуцирование иммунного ответа включает активацию или положительную регуляцию активности NK-клеток. В некоторых вариантах осуществления индуцирование иммунного ответа включает активацию или положительную регуляцию активности T-клеток. В некоторых вариантах осуществления мишень ингибитора иммунных контрольных точек включает PD-1. В некоторых вариантах осуществления мишень ингибитора иммунных контрольных точек включает PD-L1. В некоторых вариантах осуществления ингибитор иммунных контрольных точек включает пембролизумаб, ниволумаб, цемиплимаб, AMP-224, AMP-514, PDR001, атезолизумаб, авелумаб, дурвалумаб, BMS-936559 и CK-301.
Фармацевтические композиции
[00117] Настоящее изобретение также относится к фармацевтическим композициям, содержащим антитела против MICA/B, представленные в настоящем описании, и фармацевтически приемлемый носитель или эксципиент.
[00118] В некоторых вариантах осуществления эксципиенты для использования с композициями, представленными в настоящем описании, включают малеиновую кислоту, винную кислоту, молочную кислоту, лимонную кислоту, уксусную кислоту, бикарбонат натрия, фосфат натрия, гистидин, глицин, хлорид натрия, хлорид калия, хлорид кальция, хлорид цинка, воду, декстрозу, N-метилпирролидон, диметилсульфоксид, N, N-диметилацетамид, этанол, пропиленгликоль, полиэтиленгликоль, моноэтиловый простой эфир диэтиленгликоля и поверхностно-активное вещество полиоксиэтилен-сорбитан моноолеат.
[00119] В некоторых вариантах осуществления композиции дополнительно содержат дополнительное терапевтическое средство. В некоторых вариантах осуществления терапевтическое средство является химиотерапевтическим средством. Химиотерапевтические средства могут включать, помимо прочего, цитотоксические средства, антиметаболиты (например, антагонисты фолиевой кислоты, аналоги пурина, аналоги пиримидин и т.д.), ингибиторы топоизомераз (например, производные камптотецина, антрацендион, антрациклины, эпиподофиллотоксины, хинолиновые алкалоиды и т.д.), средства против микротрубочек (например, таксаны, алкалоиды барвинка), ингибиторы белкового синтеза (например, цефалотаксин, производные камптотецина, хинолиновые алкалоиды), алкилирующие средства (например, алкилсульфонаты, этиленимины, азотистые иприты, нитрозомочевину, производные платины, триазены и т.д.), алкалоиды, терпеноиды и ингибиторы киназ.
[00120] В некоторых вариантах осуществления антитело и терапевтическое средство находятся в одном и том же составе. В некоторых вариантах осуществления антитело и терапевтическое средство находятся в разных составах. В некоторых вариантах осуществления антитело, представленное в настоящем описании, используют до введения другого терапевтического средства. В некоторых вариантах осуществления антитело, представленное в настоящем описании, используют одновременно с введением другого терапевтического средства. В некоторых вариантах осуществления антитело, представленное в настоящем описании, используют после введения другого терапевтического средства.
[00121] В некоторых вариантах осуществления фармацевтические составы делают совместимыми с конкретным локальным, регионарным или системным введением или путем доставки. Таким образом, фармацевтические составы включают носители, дилюенты или эксципиенты, подходящие для введения конкретными путями. Конкретными неограничивающими примерами путей введения композиций по настоящему изобретению являются парентеральное, например, внутривенное, внутриартериальное, внутрикожное, внутримышечное, подкожное, внутриплевральное, трансдермальное (топическое), чрезслизистое, внутричерепное, интраспинальное, внутриглазное, ректальное, пероральное (алиментарное), слизистое введение, и любой другой состав, подходящий для способа лечения или способа введения.
[00122] В некоторых вариантах осуществления растворы или суспензии, используемые для парентерального использования, включают: стерильный дилюент, такой как вода для инъекций, физиологический раствор, жирные масла, полиэтиленгликоли, глицерин, пропиленгликоль или другие синтетические растворители; антибактериальные средства, такие как бензиловый спирт или метилпарабены; антиоксиданты, такие как аскорбиновая кислота или бисульфат натрия; хелатирующие средства, такие как этилендиаминтетрауксусная кислота; буферы, такие как ацетаты, цитраты или фосфаты; и средства для регуляции тоничности, такие как хлорид натрия или декстроза. В некоторых вариантах осуществления pH корректируют посредством кислот или оснований, таких как соляная кислота или гидроксид натрия.
[00123] Фармацевтические составы для инъекций включают стерильные водные растворы (где вещество является водорастворимым) или дисперсии и стерильные порошки для экстемпорального получения стерильных инъецируемых растворов или дисперсий. В случае внутривенного введения подходящие носители включают физиологический раствор, бактериостатическую воду, Cremophor EL™ (BASF, Parsippany, N.J.) или фосфатно-солевой буфер (PBS). В некоторых вариантах осуществления носитель является растворителем или дисперсионной средой, содержащей, например, воду, этанол, полиол (например, глицерин, пропиленгликоль и жидкий полиэтиленгликоль и т.п.), или их подходящие смеси. В некоторых вариантах осуществления текучесть поддерживают, например, с использованием покрытия, такого как лецитин, посредством поддержания необходимого размера частиц в случае дисперсии и с использованием поверхностно-активных веществ. Антибактериальные и противогрибковые средства включают, например, парабены, хлорбутанол, фенол, аскорбиновую кислоту и тиомерсал. В некоторых вариантах осуществления в композицию включают изотонические средства, например, сахара; полиспирты, такие как маннит или сорбит; или хлорид натрия. В некоторых случаях также включают средство, замедляющее абсорбцию, например, в некоторых вариантах осуществления моностеарат алюминия или желатин пролонгируют абсорбцию инъецируемых композиций.
[00124] В некоторых вариантах осуществления стерильные инъецируемые составы получают посредством включения активной композиции в необходимом количестве в подходящем растворителе с одним или комбинации указанных выше ингредиентов. Как правило, дисперсии получают посредством включения активной композиции в стерильный носитель, содержащий основную дисперсионную среду и любой другой ингредиент.В случае стерильных порошков для получения стерильных инъецируемых растворов, способы получения включают, например, вакуумную сушку и лиофилизацию, посредством которых получают порошок активного ингредиента и любой дополнительный желаемый ингредиент из полученного ранее раствора.
[00125] В случае чрезслизистого или трансдермального введения в составе используют пенетранты, подходящие для барьера, подлежащего проникновению. Такие пенетранты известны в этой области и включают, например, в случае чрезслизистого введения, детергенты, соли желчных кислот и производные фусидовой кислоты. В некоторых вариантах осуществления чрезслизистое введение осуществляют с использованием назальных спреев, ингаляционных устройств (например, аспираторов) или суппозиториев. В случае трансдермального введения активные соединения составляют в мазях, гелях, кремах или пластырях.
[00126] В некоторых вариантах осуществления фармацевтические составы получают с использованием носителей, защищающих от быстрого выведения из организма, таких как состав с контролируемым высвобождением или материал с отложенным высвобождением, такой как глицерилмоностеарат или глицерилстеарат.В некоторых вариантах осуществления составы также вводят с использованием промышленных изделий, таких как имплантаты и микроинкапсулированные системы доставки, для достижения локальной, регионарной или системной доставки или контролируемого или замедленного высвобождения.
ПРИМЕРЫ
[00127] Следующие примеры приведены для иллюстрирования различных вариантов осуществления изобретения, а не для ограничения настоящего изобретения каким-либо образом. Настоящие примеры, вместе со способами по настоящему изобретению, в настоящее время являются типичными для предпочтительных вариантов осуществления, являются примерами и не предназначены для ограничения объема изобретения. Изменения в настоящем изобретении и другое применение, включенное в сущность изобретения, определяемую объемом формулы изобретения, будут очевидны специалистам в этой области.
Пример 1. Измерение кинетики связывания антител
[00128] Кинетику аффинности определяли с помощью анализатора ForteBio Octet Red96. В кратком изложении, mAb против MICA/B (30 мкг/мл) фиксировали на биосенсорах Dip и Read(с захватом посредством антитела против Fc IgG мыши (AMC) (ForteBio) при комнатной температуре в буфере для анализа PBS+0,1% BSA+0,02% Tween-20 (pH 7,2). Сенсоры промывали в буфере для анализа, а затем инкубировали с очищенными белками 6xHis-MICA*08 или 6xHis-MICA*04 (100 нМ) в серии 2-двухкратных разведений в течение 5 минут в буфере для анализа для определения кинетики ассоциации антитела с белком-антигеном. Затем сенсоры инкубировали в буфере для анализа в течение 10 минут для определения кинетики диссоциации. Получаемые параметры кинетики вычисляли с использованием пакета программ ForteBio 8.0 с помощью модели 1:1. Результаты этих анализов приведены в таблице 2.
Пример 2. Связывание антитела с аллелями MICA/B
[00129] Рекомбинантные белки MICA*01, MICA*02, MICA*04, MICA*08, MICA*09 и MICB разводили до 1 мкг/мл в 50 мМ буфере карбоната натрия, pH 9,6, и наносили в виде покрытия на 96-луночные микропланшеты с высокой степенью связывания (Corning, кат.№9018), 100 нг в 100 мкл на лунку. На следующее утро покрытые планшеты для ELISA трижды промывали TBS-Tween-20, pH 7,4, а затем блокировали в блокирующем буфере SuperBlock T20 (Pierce, кат.№37536). После блокирования планшеты для ELISA однократно промывали TBS-T и инкубировали с серийно разведенным антителом против MICA (0-1 мкг/мл) в течение приблизительно двух часов при комнатной температуре. После инкубации планшеты для ELISA трижды промывали TBS-T, а затем инкубировали с конъюгатом антитела козы против IgG мыши (H+L)-HRP (ThermoFisher Scientific, кат.№626520) в течение 45 минут при комнатной температуре при встряхивании (~400 об./мин). После инкубации планшеты для ELISA трижды промывали TBS-T и инкубировали с субстратом Super Sensitive Liquid Substrate TMB (Sigma, кат.№T4444), 100 мкл на лунку, до тех пор, пока окраска не проявится в достаточной степени. Реакцию останавливали с помощью 1 Н серной кислоты, 100 мкл на лунку. Значения оптической плотности (OD) измеряли при 450 нм с помощью спектрофотометра для чтения микропланшетов. Результаты этого анализа приведены на фиг.1A-фиг.1B.
Пример 3. Связывание антитела с MICA на поверхности клетки
[00130] Клетки аденокарциномы предстательной железы мыши TRAMP-C2 (TC2) (ATCC, Manassas, VA) использовали для получения стабильной линии клеток, экспрессирующих аллель MICA*08 (TC2-MICA-08). Связывание антитела против MICA с TC2-MICA-08 анализировали посредством проточной цитометрии. В кратком изложении, клетки сначала окрашивали красителем для ближней ИК-области LIVE/DEAD (Thermo) в течение 30 мин при 4°C, а затем однократно промывали посредством центрифугирования с буфером для FACS (1 мМ ЭДТА, 25 мМ HEPES, 2% FBS в 1-кратном PBS). Приблизительно 2-3×105 клеток TC2-MICA-08 инкубировали с 100 мкл буфера для FACS, содержащего 500 нг антитела против MICA, при 4°C в течение 30 мин с последующей инкубацией с 100 мкл 2 мкг/мл PE-конъюгированного вторичного антитела козы против IgG мыши (Biolegend, San Diego, CA) при 4°C в течение 30 мин. Затем клетки однократно промывали и клеточный осадок промывали буфером для FACS для анализа FACS с гейтированием по живым клеткам. Наблюдали значимо более высокий сигнал флуоресценции PE в случае клеток TC2-MICA-08 по сравнению с родительскими клетками TC2, что свидетельствует о связывании mAb против MICA с экспрессирующимся на поверхности MICA. Результат этого анализа приведен на фиг.2.
Пример 4. Антитело ингибирует шеддинг MICA с клеток PLC/PRF/5
[00131] 4×104 клеток PLC/PRF/5 (печеночноклеточной карциномы) (ATCC, Manassas, VA) высевали в 96-луночный планшет и инкубировали при 37°C в течение ночи. Затем клетки обрабатывали 100 мкл полной среды (MEM+10% FBS, Thermo, Grand Island, NY), содержащей антитело против MICA, связывающегося с доменом α3 MICA, и антитела отрицательного контроля, соответственно, и инкубировали при 37°C в течение еще одного дня. Супернатанты клеток, содержащие подвергнутый шеддингу MICA, использовали для определения уровня растворимого MICA посредством ELISA. В кратком изложении, 96-луночный планшет покрывали 100 мкл 2 мкг/мл антитела против MICA/B человека (клон BAMO1, MBL, Japan) в течение ночи при 4°C. Планшет блокировали, а затем инкубировали с супернатантами клеток и стандартами MICA в течение 2 часов. После инкубации планшеты промывали, а затем инкубировали в течение 1 часа с 1 мкг/мл запатентованного mAb против MICA/MICB человека, клона 10E9, конъюгированного с биотином. Затем в лунки добавляли 100 мкл HRP-конъюгированного стрептавидина (HRP-SA) (R&D Systems, Minneapolis, MN) и инкубировали в течение 30 мин. Образцы проявляли с помощью TMB в течение 4 мин, реакцию останавливали с помощью 1 Н серной кислоты и определяли по поглощению при 450 нм. Уровень растворимого MICA интерполировали из стандартной кривой. Результат этого анализа приведен на фиг.3.
Пример 5. Антитело повышает опосредованную клетками NK-92 цитотоксичность в отношении клеток PLC/PRF/5
[00132] Клетки PLC/PRF/5 (мишень) суспендировали в RPMI-1640 с 10% FBS и высевали в 96-луночные плоскодонные планшеты (Costar) в количестве 6000 клеток/лунку. Затем клетки инкубировали с антителом против MICA (10 мкг/мл), связывающимся с доменом α3 MICA, в течение 24 часов до того, как их подвергали мечению кальцеином AM (1 мкМ) в течение 3 часов при 37°C, 5% CO2. Лунки промывали, а затем добавляли в них клетки NK-92 (эффекторы), суспендированные в RPMI-1640 с 10% FBS, в различных соотношениях эффектора и мишени (E:T), как указано, и сокультивировали с клетками-мишенями в течение 4 часов. В конце культивирования супернатант удаляли, заменяли PBS и измеряли сигнал кальцеина AM с использованием многоканального спектрофотометра для чтения планшетов VICTOR (Perkin Elmer). В качестве контроля использовали совпадающий по изотипу нереактивный иммуноглобулин (R&D). Результат этого анализа приведен на фиг.4A-фиг.4B.
Пример 6. Эффективность 3F9.E4 в терапии опухолей in vivo (выживаемость) и экспрессия NKG2S инфильтрирующими опухоль лимфоцитами у несущих опухоли мышей
[00133] MICA-трансгенным мышам (MICAgen) инокулировали 104 клеток B16F10-MICA*01 (трансфектантов B16) и после дня 11, когда опухоли достигали желаемого порога размера, мышам вводили 3F9.E4 или изотипический контроль (стрелками указаны дни инъекций) (логарифмический ранговый критерий). Результаты приведены на фиг.5.
[00134] Мышей умерщвляли при достижении высокой опухолевой нагрузки и анализировали инфильтрирующие опухоль лимфоциты на экспрессию NKG2D (SFI) NK-клетками, CD8+αβ-T-клетками и γδ-T-клетками. Степень экспрессии NKG2D (SFI) NKG2D-экспрессирующими клетками приведены на фиг.6A-фиг.6C. Каждый символ соответствует анализу отдельной мыши (односторонний ANOVA+критерий множественного сравнения Тьюки).
Пример 7. Экспрессия MICA опухолями трансфектантов B16 ex vivo и детекция растворимого MICA в сыворотках несущих опухоли мышей
[00135] MICA-трансгенным мышам (MICAgen) инокулировали 104 клеток B16F10-MICA*01 (трансфектантов B16) и после дня 11, когда опухоли достигали желаемого порога размера, мышам вводили 3F9.E4, или BAMO3, или изотипический контроль. Мышей умерщвляли при достижении высокой опухолевой нагрузки и выделенные отдельные опухолевые клетки анализировали на экспрессию MICA с использованием окрашивания mAb AMO1 (односторонний ANOVA+критерий множественного сравнения Тьюки). AMO1 связывается с a1a2-доменом MICA (≠ BAMO3 и 3F9). Каждый символ соответствует анализу отдельной мыши. Результаты приведены на фиг.7B. Сыворотки также анализировали на sMICA с использованием ELISA сэндвич-типа с помощью AMO1/BAMO1. Каждый символ соответствует анализу отдельной мыши (непарный t-критерий). Результаты приведены на фиг.7A.
Пример 8. Эпитопный биннинг
[00136] Белок MICA *04-His (30 мкг/мл) иммобилизовали на конце биосенсора Ni-NTA (FortrBio, кат.№18-5101) для устройства для интерферометрии биослоя (Octet Red, ForteBio) в течение 300 сек. Исходный сигнал снова измеряли в течение 60 сек до погружения концов биосенсоров в лунки, содержащие 1 мМ или 0,5 мМ первичного антитела, в течение 300 сек. После этого биосенсоры погружали в лунки, содержащие 100 нМ или 50 нМ второго mAb, в течение 300 сек. Процент связывания вторых mAb в присутствии первого mAb определяли посредством сравнения максимального сигнала второго mAb после добавления первого mAb с максимальным сигналом второго mAb в отдельности. mAb считали неконкурирующими, если максимальное связывание второго mAb составляло ≥66% связывания без конкуренции. Уровень от 33% до 66% от связывания без конкуренции считали промежуточной конкуренцией, и ≤33% считали конкуренцией. Результаты этого анализа приведены на фиг.8A-фиг.8C.
[00137] Хотя в настоящем описании представлены предпочтительные варианты осуществления настоящего изобретения, специалистам в этой области будет очевидно, что такие варианты осуществления приведены исключительно в качестве примера. Специалистам в этой области будут очевидны многочисленные варианты, изменения и замены без отклонения от сущности изобретения. Следует понимать, что можно использовать различные альтернативы вариантам осуществления, представленным в настоящем описании. Следует понимать, что в следующей формуле изобретения определен объем изобретения, и что, таким образом, будут охвачены способы и структуры в объеме формулы изобретения и их эквиваленты.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110>КАЛЛИНЕН МАЙКА КОРП.
<120>АНТИТЕЛА ПРОТИВ MICA/B, БЛОКИРУЮЩИЕ ШЕДДИНГ MICA/B, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ
<130>53620-702.601
<140>PCT/US2019/044234
<141>2019-07-30
<150>62/712,608
<151>2018-07-31
<160>34
<170>PatentIn version 3.5
<210>1
<211>16
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический пептид
<400>1
Arg Ser Ser Lys Ser Leu Leu His Ser Asn Gly Asn Thr Tyr Leu Tyr
1 5 10 15
<210>2
<211>7
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический пептид
<400>2
Arg Met Ser Asn Leu Ala Ser
1 5
<210>3
<211>9
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический пептид
<400>3
Met Gln His Leu Glu Tyr Pro Phe Thr
1 5
<210>4
<211>10
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический пептид
<400>4
Gly Phe Thr Phe Ser Asn Tyr Ala Met Ser
1 5 10
<210>5
<211>17
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический пептид
<400>5
Tyr Ile Ser Pro Gly Gly Asp Tyr Ile Tyr Tyr Ala Asp Thr Val Lys
1 5 10 15
Gly
<210>6
<211>12
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический пептид
<400>6
Asp Arg Arg His Tyr Gly Ser Tyr Ala Met Asp Tyr
1 5 10
<210>7
<211>112
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический полипептид
<400>7
Asp Ile Val Met Thr Gln Ala Ala Pro Ser Val Pro Val Thr Pro Gly
1 5 10 15
Glu Ser Val Ser Ile Ser Cys Arg Ser Ser Lys Ser Leu Leu His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu Tyr Trp Phe Leu Gln Arg Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Arg Met Ser Asn Leu Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Ala Phe Thr Leu Arg Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln His
85 90 95
Leu Glu Tyr Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210>8
<211>121
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический полипептид
<400>8
Glu Val Gln Leu Gln Glu Ser Gly Glu Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Thr Pro Glu Lys Arg Leu Glu Trp Val
35 40 45
Ala Tyr Ile Ser Pro Gly Gly Asp Tyr Ile Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Arg Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Lys Ser Glu Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Thr Thr Asp Arg Arg His Tyr Gly Ser Tyr Ala Met Asp Tyr Trp Gly
100 105 110
Gln Gly Ile Ser Val Thr Val Ser Ser
115 120
<210>9
<211>12
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический пептид
<400>9
Thr Ala Ser Ser Ser Val Ser Ser Asn Tyr Leu His
1 5 10
<210>10
<211>7
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический пептид
<400>10
Thr Thr Ser Asn Leu Ala Ser
1 5
<210>11
<211>9
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический пептид
<400>11
His Gln Phe His Arg Ser Pro Phe Thr
1 5
<210>12
<211>10
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический пептид
<400>12
Gly Phe Ser Leu Thr Ala Phe Gly Val Asn
1 5 10
<210>13
<211>16
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический пептид
<400>13
Met Ile Trp Gly Asp Gly Asn Thr Asp Tyr Asn Ser Thr Leu Arg Ser
1 5 10 15
<210>14
<211>12
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический пептид
<400>14
Glu Thr Tyr Tyr Gly Asn Tyr Ala Gly Leu Gly Tyr
1 5 10
<210>15
<211>108
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический полипептид
<400>15
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Ile Gly
1 5 10 15
Glu Arg Val Thr Met Thr Cys Thr Ala Ser Ser Ser Val Ser Ser Asn
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Arg Ser Ser Pro Lys Leu Trp
35 40 45
Ile Tyr Thr Thr Ser Asn Leu Ala Ser Gly Val Pro Thr Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu
65 70 75 80
Ala Glu Asp Ala Ala Thr Tyr Tyr Cys His Gln Phe His Arg Ser Pro
85 90 95
Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210>16
<211>120
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический полипептид
<400>16
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ala Phe
20 25 30
Gly Val Asn Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Met Ile Trp Gly Asp Gly Asn Thr Asp Tyr Asn Ser Thr Leu Arg
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Leu Asn Ser Leu Gln Thr Asp Asp Thr Ala Arg Tyr Phe Cys Ala
85 90 95
Arg Glu Thr Tyr Tyr Gly Asn Tyr Ala Gly Leu Gly Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala
115 120
<210>17
<211>16
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический пептид
<400>17
Arg Ser Ser Lys Ser Leu Leu His Ser Asn Leu Asn Thr Tyr Leu Tyr
1 5 10 15
<210>18
<211>17
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический пептид
<400>18
Tyr Ile Ser Pro Gly Gly Asp Tyr Ile Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210>19
<211>113
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический полипептид
<400>19
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Lys Ser Leu Leu His Ser
20 25 30
Asn Leu Asn Thr Tyr Leu Tyr Trp Phe Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ile Leu Ile Tyr Arg Met Ser Asn Leu Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Ala Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln His
85 90 95
Leu Glu Tyr Pro Phe Thr Phe Gly Pro Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg
<210>20
<211>98
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический полипептид
<400>20
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Ala Met Ser Trp Ile Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Pro Gly Gly Asp Tyr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Thr
<210>21
<211>219
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический полипептид
<400>21
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Lys Ser Leu Leu His Ser
20 25 30
Asn Leu Asn Thr Tyr Leu Tyr Trp Phe Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Ile Leu Ile Tyr Arg Met Ser Asn Leu Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Ala Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln His
85 90 95
Leu Glu Tyr Pro Phe Thr Phe Gly Pro Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210>22
<211>450
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический полипептид
<400>22
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Ala Met Ser Trp Ile Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Pro Gly Gly Asp Tyr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Thr Asp Arg Arg His Tyr Gly Ser Tyr Ala Met Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly
450
<210>23
<211>234
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический полипептид
<400>23
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser
20 25 30
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Ser Ala Ser Gln Gly
35 40 45
Ile Ser Asn Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
50 55 60
Lys Leu Leu Ile Gln Tyr Thr Ser Leu Leu His Ser Gly Val Pro Ser
65 70 75 80
Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Tyr Thr Leu Thr Ile Ser
85 90 95
Ser Leu Gln Pro Asp Asp Phe Ala Thr Tyr Phe Cys Gln Gln Tyr Ser
100 105 110
Lys Phe Pro Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg
115 120 125
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
130 135 140
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
145 150 155 160
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
165 170 175
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
180 185 190
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
195 200 205
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
210 215 220
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
225 230
<210>24
<211>234
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический полипептид
<400>24
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
20 25 30
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Ser Ala Ser Gln Gly
35 40 45
Ile Ser Asn Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
50 55 60
Lys Leu Leu Ile Gln Tyr Thr Ser Leu Leu His Ser Gly Val Pro Ser
65 70 75 80
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser
85 90 95
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Phe Cys Gln Gln Tyr Ser
100 105 110
Lys Phe Pro Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg
115 120 125
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
130 135 140
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
145 150 155 160
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
165 170 175
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
180 185 190
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
195 200 205
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
210 215 220
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
225 230
<210>25
<211>471
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический полипептид
<400>25
Met Asp Pro Lys Gly Ser Leu Ser Trp Arg Ile Leu Leu Phe Leu Ser
1 5 10 15
Leu Ala Phe Glu Leu Ser Tyr Gly Gln Ile Gln Leu Val Gln Ser Gly
20 25 30
Ser Glu Leu Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala
35 40 45
Phe Gly Tyr Thr Phe Thr Asn Tyr Gly Met Asn Trp Val Lys Gln Ala
50 55 60
Pro Gly Gln Gly Leu Lys Trp Met Gly Trp Ile Asn Thr Tyr Thr Gly
65 70 75 80
Glu Pro Thr Tyr Ala Gln Gly Phe Thr Gly Arg Phe Val Phe Ser Leu
85 90 95
Glu Thr Ser Val Ser Thr Ala Tyr Leu Gln Ile Ser Ser Leu Lys Ala
100 105 110
Glu Asp Thr Ala Val Tyr Phe Cys Ala Arg Asn Tyr Gly Asn Tyr Leu
115 120 125
Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser
130 135 140
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
145 150 155 160
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
165 170 175
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
180 185 190
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
195 200 205
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
210 215 220
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val
225 230 235 240
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
245 250 255
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
260 265 270
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
275 280 285
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
290 295 300
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
305 310 315 320
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
325 330 335
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
340 345 350
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
355 360 365
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr
370 375 380
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
385 390 395 400
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
405 410 415
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
420 425 430
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
435 440 445
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
450 455 460
Ser Leu Ser Leu Ser Pro Gly
465 470
<210>26
<211>471
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический полипептид
<400>26
Met Asp Pro Lys Gly Ser Leu Ser Trp Arg Ile Leu Leu Phe Leu Ser
1 5 10 15
Leu Ala Phe Glu Leu Ser Tyr Gly Gln Ile Gln Leu Val Gln Ser Gly
20 25 30
Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala
35 40 45
Phe Gly Tyr Thr Phe Thr Asn Tyr Gly Met Asn Trp Val Lys Gln Ala
50 55 60
Pro Gly Gln Gly Leu Lys Trp Met Gly Trp Ile Asn Thr Tyr Thr Gly
65 70 75 80
Glu Pro Thr Tyr Ala Asp Asp Phe Lys Gly Arg Val Thr Phe Thr Leu
85 90 95
Glu Thr Ser Ile Ser Thr Ala Tyr Met Glu Leu Ser Arg Leu Arg Ser
100 105 110
Asp Asp Thr Ala Val Tyr Phe Cys Ala Arg Asn Tyr Gly Asn Tyr Leu
115 120 125
Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser
130 135 140
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
145 150 155 160
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
165 170 175
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
180 185 190
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
195 200 205
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
210 215 220
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val
225 230 235 240
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
245 250 255
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
260 265 270
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
275 280 285
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
290 295 300
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
305 310 315 320
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
325 330 335
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
340 345 350
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
355 360 365
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr
370 375 380
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
385 390 395 400
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
405 410 415
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
420 425 430
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
435 440 445
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
450 455 460
Ser Leu Ser Leu Ser Pro Gly
465 470
<210>27
<211>108
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический полипептид
<400>27
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Ser Ala Ser Gln Gly Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Leu Lys Leu Leu Ile
35 40 45
Gln Tyr Thr Ser Leu Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Tyr Ser Leu Thr Ile Ser Asn Leu Glu Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Tyr Ser Lys Phe Pro Arg
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105
<210>28
<211>118
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический полипептид
<400>28
Gln Ile Gln Leu Val Gln Ser Gly Pro Glu Leu Lys Lys Ser Gly Glu
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Ala Phe Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Lys Gln Ala Pro Gly Lys Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Tyr Thr Gly Glu Pro Thr Tyr Ala Asp Asp Phe
50 55 60
Lys Gly Arg Phe Ala Phe Ser Leu Glu Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Asn His Leu Lys Asn Glu Asp Thr Ala Thr Tyr Phe Cys
85 90 95
Ala Arg Asn Tyr Gly Asn Tyr Leu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Leu Thr Val Ser Ser
115
<210>29
<211>11
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический пептид
<400>29
Ser Ala Ser Gln Gly Ile Ser Asn Tyr Leu Asn
1 5 10
<210>30
<211>7
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический пептид
<400>30
Thr Ser Leu Leu His Ser Gly
1 5
<210>31
<211>9
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический пептид
<400>31
Gln Gln Tyr Ser Lys Phe Pro Arg Thr
1 5
<210>32
<211>10
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический пептид
<400>32
Gly Tyr Thr Phe Thr Asn Tyr Gly Met Asn
1 5 10
<210>33
<211>16
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический пептид
<400>33
Ile Asn Thr Tyr Thr Gly Glu Pro Thr Tyr Ala Asp Asp Phe Lys Gly
1 5 10 15
<210>34
<211>9
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Описание искусственной последовательности: Синтетический пептид
<400>34
Asn Tyr Gly Asn Tyr Leu Phe Asp Tyr
1 5
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛА К MICA/B И СПОСОБЫ ПРИМЕНЕНИЯ | 2019 |
|
RU2821021C2 |
| АНТИТЕЛА К TIGIT И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2827445C2 |
| АНТИТЕЛА В7-Н4 И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2809243C2 |
| АНТИТЕЛА ПРОТИВ NGF И СВЯЗАННЫЕ С НИМИ СПОСОБЫ | 2019 |
|
RU2838175C2 |
| НЕЙТРАЛИЗУЮЩИЕ АНТИТЕЛА К ВИРУСУ ГРИППА B И ПУТИ ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2739952C2 |
| БЕЛКИ, СВЯЗЫВАЮЩИЕ CD33, NKG2D И CD16 | 2018 |
|
RU2820603C2 |
| ВАКЦИНАЦИЯ С ИСПОЛЬЗОВАНИЕМ АЛЬФА3 ДОМЕНА MICA/B ДЛЯ ЛЕЧЕНИЯ РАКА | 2016 |
|
RU2747296C2 |
| НЕЙТРАЛИЗУЮЩИЕ АНТИТЕЛА К ВИРУСУ ГРИППА B И ПУТИ ИХ ПРИМЕНЕНИЯ | 2020 |
|
RU2784915C2 |
| СПОСОБЫ ОБНАРУЖЕНИЯ ФОЛАТНОГО РЕЦЕПТОРА 1 В ОБРАЗЦЕ ПАЦИЕНТА | 2018 |
|
RU2759410C2 |
| АНТИТЕЛО К ЦИТОМЕГАЛОВИРУСУ ЧЕЛОВЕКА И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2817217C1 |
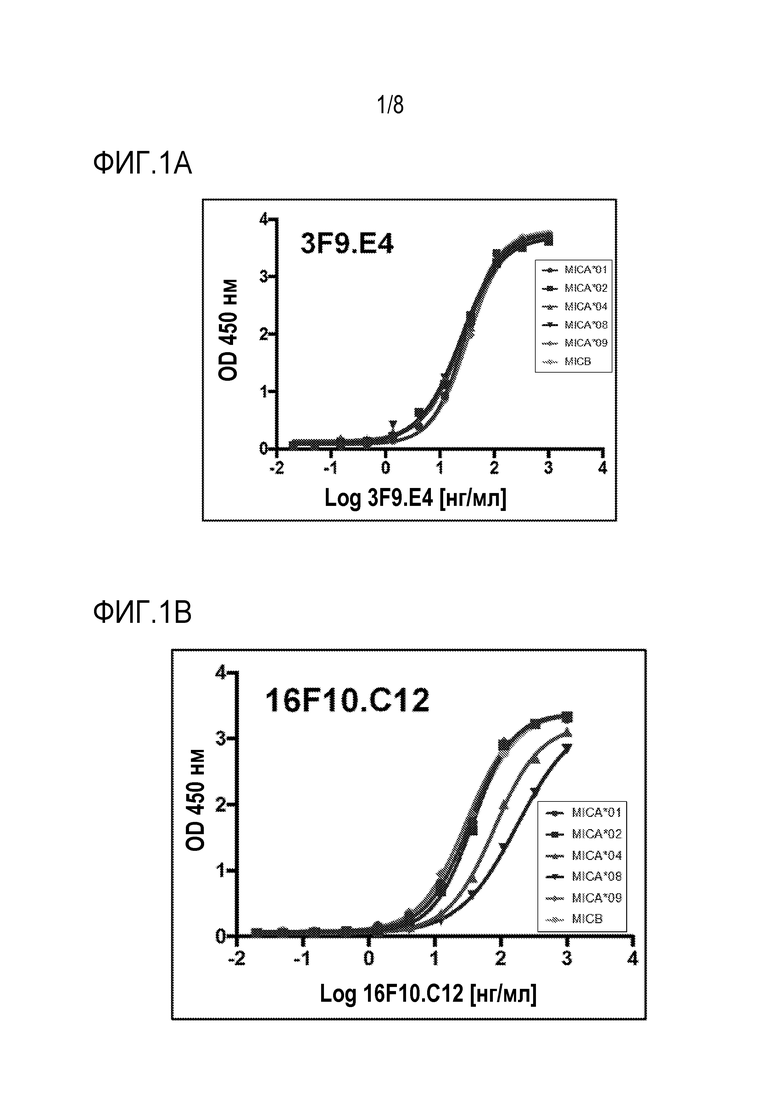
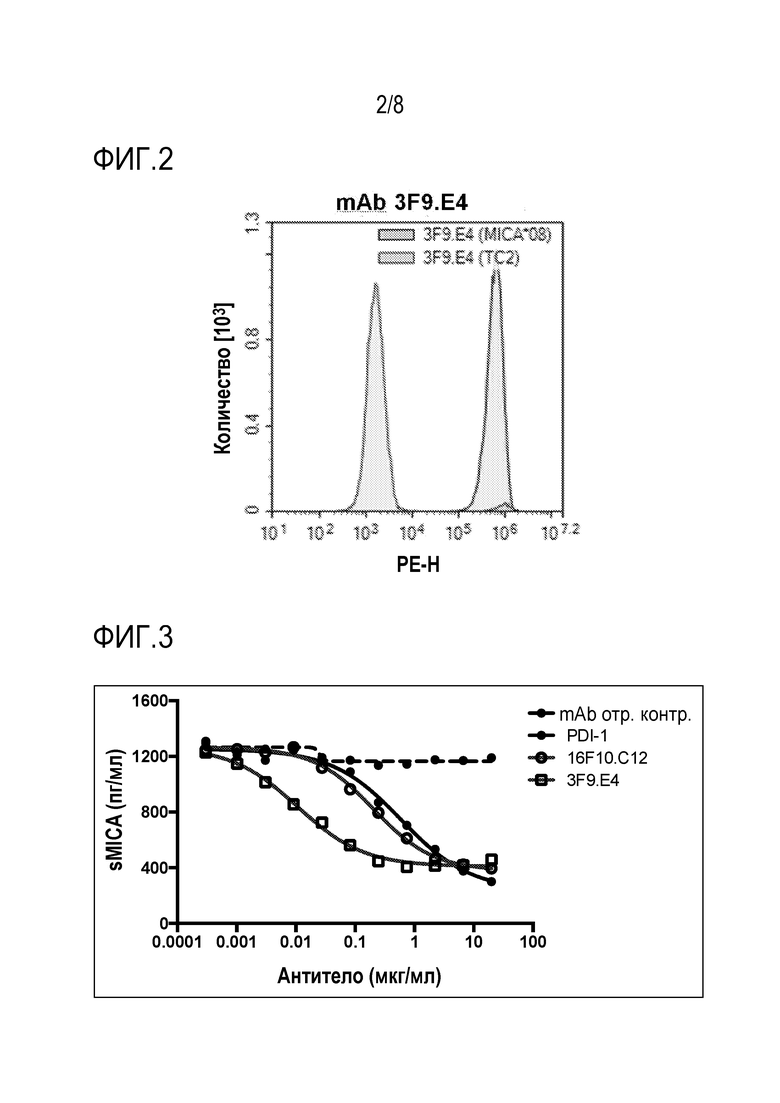
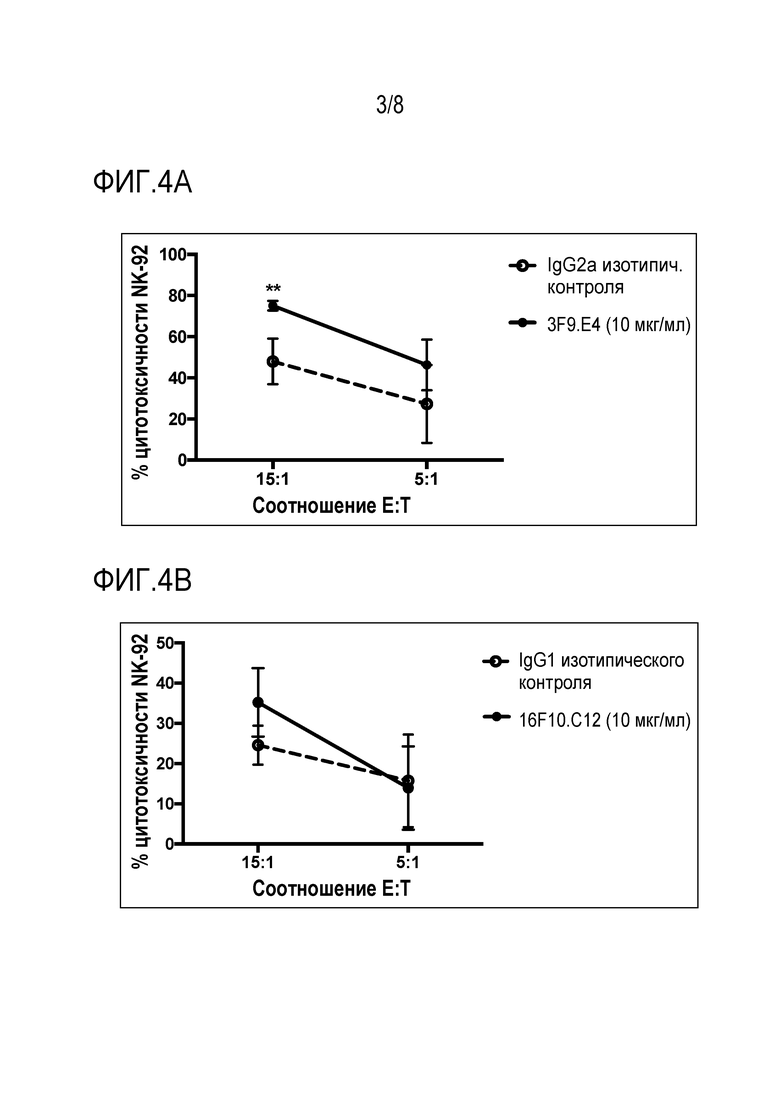
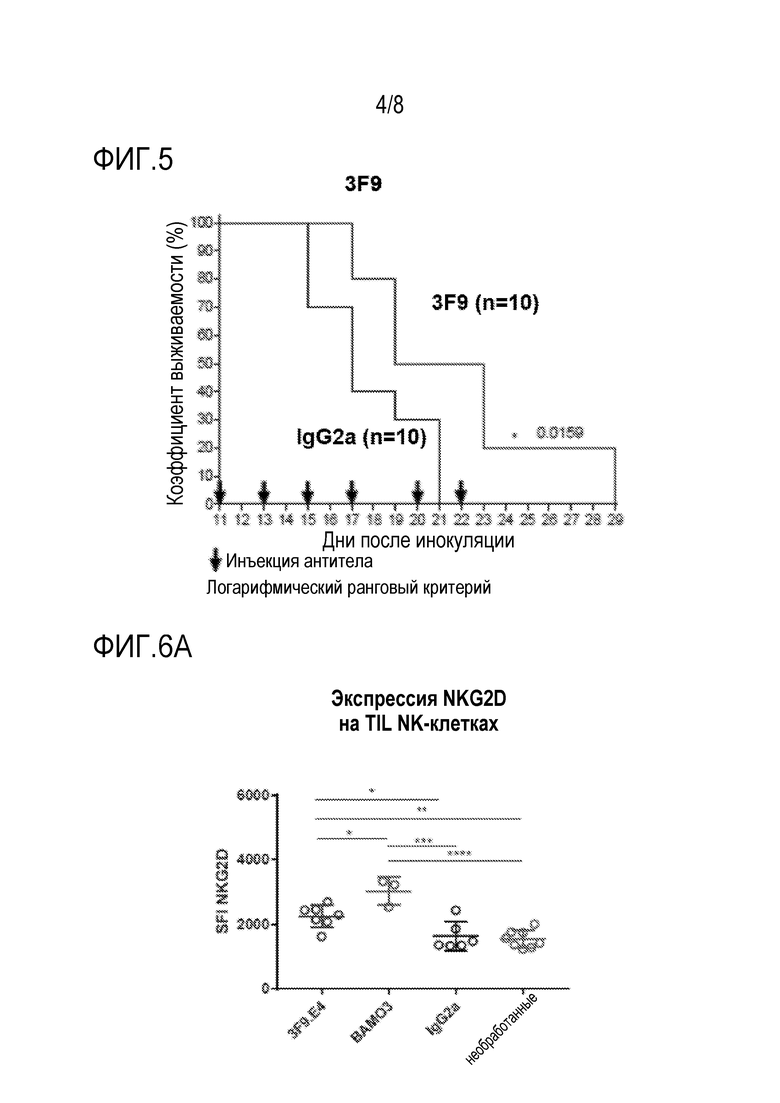
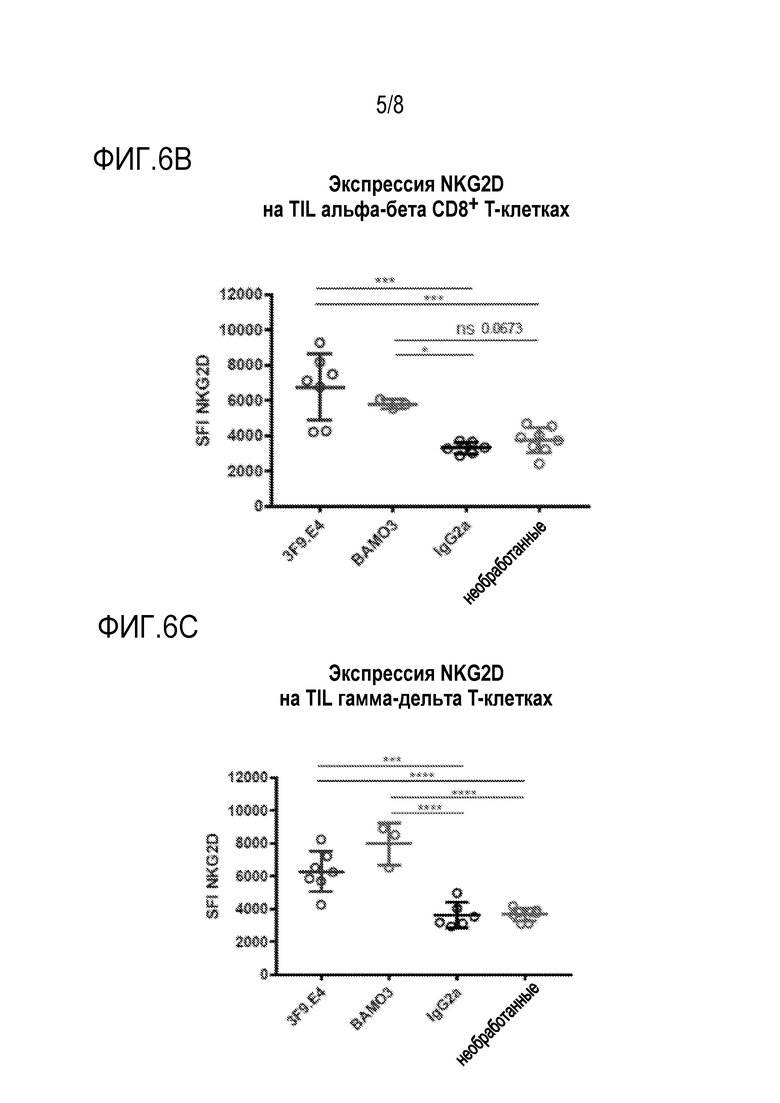
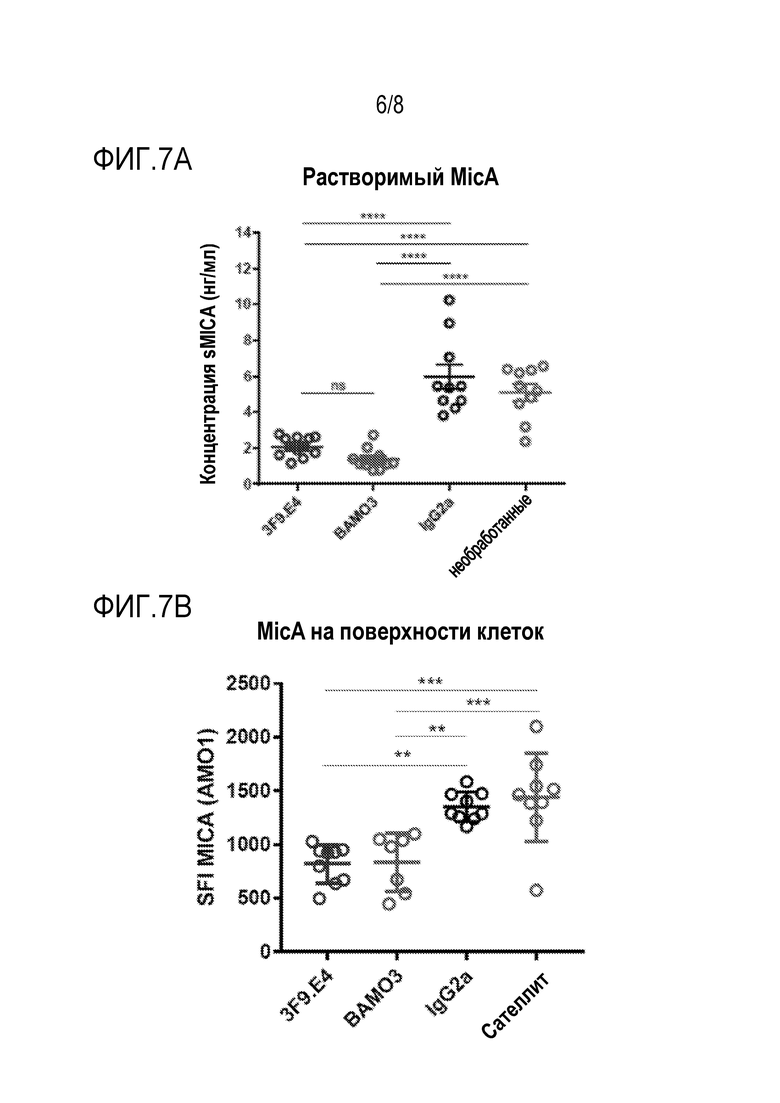

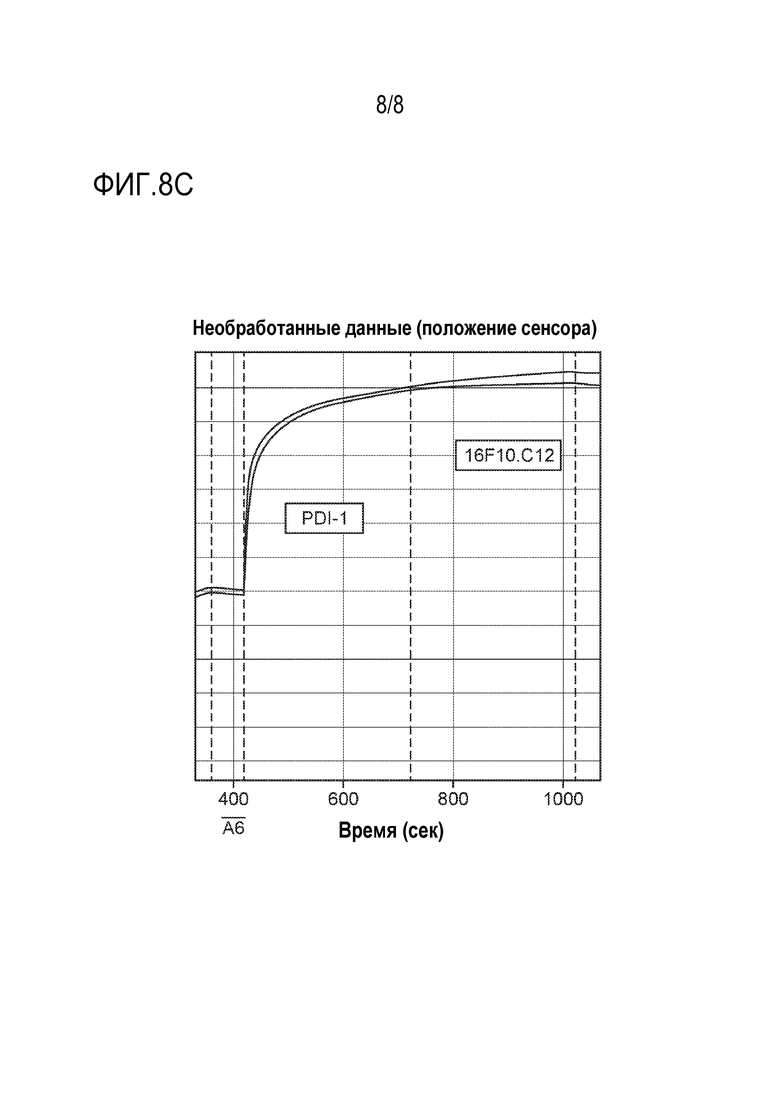
Изобретение относится к области биохимии, в частности к антителу против MICA/MICB или его антигенсвязывающему фрагменту. Также раскрыта фармацевтическая композиция, содержащая указанное антитело. Изобретение позволяет эффективно лечить опухоли, связанные с MICA. 3 н. и 13 з.п. ф-лы, 8 ил., 2 табл., 8 пр.
1. Моноклональное антитело против MICA, или его антигенсвязывающий фрагмент, содержащее
A) определяющую комплементарность область (CDR) легкой цепи с аминокислотной последовательностью SEQ ID NO:17, 2 и 3, определяющую комплементарность область (CDR) тяжелой цепи с аминокислотной последовательностью SEQ ID NO:4, 18 и 6, или
В) определяющую комплементарность область (CDR) легкой цепи с аминокислотной последовательностью SEQ ID NO:9, 10 и 11, определяющую комплементарность область (CDR) тяжелой цепи с аминокислотной последовательностью SEQ ID NO:12, 13 и 14, или
С) определяющую комплементарность область (CDR) легкой цепи с аминокислотной последовательностью SEQ ID NO:1, 2 и 3, определяющую комплементарность область (CDR) тяжелой цепи с аминокислотной последовательностью SEQ ID NO:4, 5 и 6,
где моноклональное антитело не содержит по меньшей мере одну CDR, выбранную из группы, содержащей: SASQGISNYLN, TSLLHSG, QQYSKFPRT, GYTFTNYGMN, INTYTGEPTYADDFKG и NYGNYLFDY.
2. Моноклональное антитело по п.1, где моноклональное антитело, или его антигенсвязывающий фрагмент, содержит
определяющую комплементарность область 1 (CDR1) легкой цепи с аминокислотной последовательностью, которая идентична одной из SEQ ID NO:1, SEQ ID NO:9 или SEQ ID NO:17,
определяющую комплементарность область 2 (CDR2) легкой цепи с аминокислотной последовательностью, которая идентична одной из SEQ ID NO:2 или SEQ ID NO:10,
определяющую комплементарность область 3 (CDR3) легкой цепи с аминокислотной последовательностью, которая идентична одной из SEQ ID NO:3 или SEQ ID NO:11,
определяющую комплементарность область 1 (CDR1) тяжелой цепи с аминокислотной последовательностью, которая идентична одной из SEQ ID NO:4 или SEQ ID NO:12,
определяющую комплементарность область 2 (CDR2) тяжелой цепи с аминокислотной последовательностью, которая идентична одной из SEQ ID NO:5, SEQ ID NO:13 или SEQ ID NO:18, и
определяющую комплементарность область 3 (CDR3) тяжелой цепи с аминокислотной последовательностью, которая идентична одной из SEQ ID NO:6 или SEQ ID NO:14.
3. Моноклональное антитело по п.1, где моноклональное антитело, или его антигенсвязывающий фрагмент, содержит по меньшей мере одну из
определяющей комплементарность области 1 (CDR1) легкой цепи с аминокислотной последовательностью, которая идентична SEQ ID NO:1,
определяющей комплементарность области 2 (CDR2) легкой цепи с аминокислотной последовательностью, которая идентична SEQ ID NO:2, и
определяющей комплементарность области 3 (CDR3) легкой цепи с аминокислотной последовательностью, которая идентична SEQ ID NO:3, или
где моноклональное антитело, или его антигенсвязывающий фрагмент, содержит по меньшей мере одну из
определяющей комплементарность области 1 (CDR1) легкой цепи с аминокислотной последовательностью, которая идентична SEQ ID NO:9,
определяющей комплементарность области 2 (CDR2) легкой цепи с аминокислотной последовательностью, которая идентична SEQ ID NO:10, и
определяющей комплементарность области 3 (CDR3) легкой цепи с аминокислотной последовательностью, которая идентична SEQ ID NO:11, или
где моноклональное антитело, или его антигенсвязывающий фрагмент, содержит по меньшей мере одну из
определяющей комплементарность области 1 (CDR1) легкой цепи с аминокислотной последовательностью, которая идентична SEQ ID NO:17,
определяющей комплементарность области 2 (CDR2) легкой цепи с аминокислотной последовательностью, которая идентична SEQ ID NO:2, и
определяющей комплементарность области 3 (CDR3) легкой цепи с аминокислотной последовательностью, которая идентична SEQ ID NO:3, или
где моноклональное антитело, или его антигенсвязывающий фрагмент содержит по меньшей мере одну из
определяющей комплементарность области 1 (CDR1) тяжелой цепи с аминокислотной последовательностью, которая идентична SEQ ID NO:4,
определяющей комплементарность области 2 (CDR2) тяжелой цепи с аминокислотной последовательностью, которая идентична SEQ ID NO:5, и
определяющей комплементарность области 3 (CDR3) тяжелой цепи с аминокислотной последовательностью, которая идентична SEQ ID NO:6, или
где моноклональное антитело, или его антигенсвязывающий фрагмент содержит по меньшей мере одну из
определяющей комплементарность области 1 (CDR1) тяжелой цепи с аминокислотной последовательностью, которая идентична SEQ ID NO:12,
определяющей комплементарность области 2 (CDR2) тяжелой цепи с аминокислотной последовательностью, которая идентична SEQ ID NO:13, и
определяющей комплементарность области 3 (CDR3) тяжелой цепи с аминокислотной последовательностью, которая идентична SEQ ID NO:14, или
где моноклональное антитело, или его антигенсвязывающий фрагмент содержит по меньшей мере одну из
определяющей комплементарность области 1 (CDR1) тяжелой цепи с аминокислотной последовательностью, которая идентична SEQ ID NO:4,
определяющей комплементарность области 2 (CDR2) тяжелой цепи с аминокислотной последовательностью, которая идентична SEQ ID NO:18, и
определяющей комплементарность области 3 (CDR3) тяжелой цепи с аминокислотной последовательностью, которая идентична SEQ ID NO:6.
4. Моноклональное антитело по любому из пп.1-3, где моноклональное антитело, или его антигенсвязывающий фрагмент, содержит
вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO:7, SEQ ID NO:15 или SEQ ID NO:19.
5. Моноклональное антитело по любому из пп.1-4, где моноклональное антитело, или его антигенсвязывающий фрагмент, содержит
вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO:8, SEQ ID NO:16 или SEQ ID NO:20.
6. Моноклональное антитело по п. 4 или 5, где моноклональное антитело, или его антигенсвязывающий фрагмент, содержит
вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, идентичную SEQ ID NO:7, и
вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, идентичную SEQ ID NO:8, или
где моноклональное антитело, или его антигенсвязывающий фрагмент, содержит
вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, идентичную SEQ ID NO:15, и
вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, идентичную SEQ ID NO:16, или
где моноклональное антитело, или его антигенсвязывающий фрагмент содержит
вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, идентичную SEQ ID NO:19, и
вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, идентичную SEQ ID NO:20.
7. Моноклональное антитело по любому из предшествующих пунктов, где моноклональное антитело, или его антигенсвязывающий фрагмент, содержит
легкую цепь, содержащую аминокислотную последовательность, идентичную аминокислотной последовательности SEQ ID NO:21, SEQ ID NO:23 или SEQ ID NO:24.
8. Моноклональное антитело по любому из предшествующих пунктов, где моноклональное антитело, или его антигенсвязывающий фрагмент, содержит
тяжелую цепь, содержащую аминокислотную последовательность, идентичную аминокислотной последовательности SEQ ID NO:22, SEQ ID NO:25 или SEQ ID NO:26.
9. Моноклональное антитело или его антигенсвязывающий фрагмент, содержащее
A) определяющую комплементарность область (CDR) легкой цепи с аминокислотной последовательностью SEQ ID NO:17, 2 и 3, определяющую комплементарность область (CDR) тяжелой цепи с аминокислотной последовательностью SEQ ID NO:4, 18 и 6, или
В) определяющую комплементарность область (CDR) легкой цепи с аминокислотной последовательностью SEQ ID NO:9, 10 и 11, определяющую комплементарность область (CDR) тяжелой цепи с аминокислотной последовательностью SEQ ID NO:12, 13 и 14, или
С) определяющую комплементарность область (CDR) легкой цепи с аминокислотной последовательностью SEQ ID NO:1, 2 и 3, определяющую комплементарность область (CDR) тяжелой цепи с аминокислотной последовательностью SEQ ID NO:4, 5 и 6,
где моноклональное антитело не содержит по меньшей мере одну CDR, выбранную из группы, содержащей: SASQGISNYLN, TSLLHSG, QQYSKFPRT, GYTFTNYGMN, INTYTGEPTYADDFKG и NYGNYLFDY, и
где моноклональное антитело, или его антигенсвязывающий фрагмент, специфически связывается с белком MICA, белком MICB или обоими белками MICA и MICB.
10. Моноклональное антитело по п.9, где белок MICA является мембраносвязанным белком MICA, растворимым белком MICA или и тем, и другим, или
где белок MICB является мембраносвязанным белком MICB, растворимым белком MICB или и тем, и другим.
11. Моноклональное антитело по любому из предшествующих пунктов, где моноклональное антитело, или его антигенсвязывающий фрагмент, выбрано из полноразмерного иммуноглобулина, scFv, Fab, F(ab’)2 или соединенного дисульфидной связью Fv, или
где моноклональное антитело, или его антигенсвязывающий фрагмент, является IgG или IgM, или
где моноклональное антитело, или его антигенсвязывающий фрагмент, является гуманизированным или химерным.
12. Фармацевтическая композиция для лечения опухолей, связанных с MICA, содержащая:
моноклональное антитело, или его антигенсвязывающий фрагмент, по любому из предшествующих пунктов и
фармацевтически приемлемый носитель или эксципиент.
13. Моноклональное антитело против MICA, или его антигенсвязывающий фрагмент, по любому из пп.1-11, или фармацевтическая композиция по п.12 для применения в лечении злокачественного новообразования.
14. Моноклональное антитело против MICA, или его антигенсвязывающий фрагмент, по любому из пп.1-11, или фармацевтическая композиция по п.12, для применения в лечении гепатоцеллюлярной карциномы.
15. Моноклональное антитело против MICA, или его антигенсвязывающий фрагмент, по любому из пп.1-8, 11 для применения в способе уменьшения уровня растворимого белка MICA у индивида.
16. Моноклональное антитело против MICA, или его антигенсвязывающий фрагмент, по любому из пп.9-11 для применения в способе уменьшения уровня растворимого белка MICA у индивида растворимого белка MICB, или того, и другого, у индивида.
| US 9725515 B2, 08.08.2017 | |||
| WO 2014140904 A2, 18.09.2014 | |||
| RU 2014131317 A, 27.03.2016. |
Авторы
Даты
2024-03-11—Публикация
2019-07-30—Подача