Перекрестная ссылка
Настоящая заявка испрашивает преимущество предварительной заявки США № 62/621892, поданной 25 января 2018 года, которая включена в настоящую заявку посредством ссылки.
Сущность изобретения
В настоящей заявке раскрыты моноклональные антитела, которые специфически связываются с MICA/B и, таким образом, модулируют иммунный ответ против больных клеток.
В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:7. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 90% идентична аминокислотной последовательности SEQ ID NO:7. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности SEQ ID NO:7. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 99% идентична аминокислотной последовательности SEQ ID NO:7. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:7. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:7, где моноклональное антитело или его антиген-связывающий фрагмент содержит легкую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:9, или где моноклональное антитело или его антиген-связывающий фрагмент содержит тяжелую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:10. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 90% идентична аминокислотной последовательности SEQ ID NO:7, где моноклональное антитело или его антиген-связывающий фрагмент содержит легкую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:9, или где моноклональное антитело или его антиген-связывающий фрагмент содержит тяжелую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:10. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности SEQ ID NO:7, где моноклональное антитело или его антиген-связывающий фрагмент содержит легкую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:9, или где моноклональное антитело или его антиген-связывающий фрагмент содержит тяжелую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:10. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 99% идентична аминокислотной последовательности SEQ ID NO:7, где моноклональное антитело или его антиген-связывающий фрагмент содержит легкую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:9, или где моноклональное антитело или его антиген-связывающий фрагмент содержит тяжелую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:10. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:7, где моноклональное антитело или его антиген-связывающий фрагмент содержит легкую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:9, или где моноклональное антитело или его антиген-связывающий фрагмент содержит тяжелую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:10. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 90% идентична аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 99% идентична аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления легкая цепь включает аминокислотную последовательность, где по меньшей мере от 1 до 10 аминокислот аминокислотной последовательности SEQ ID NO:9, модифицированы. В некоторых вариантах осуществления тяжелая цепь включает аминокислотную последовательность, где по меньшей мере от 1 до 10 аминокислот аминокислотной последовательности SEQ ID NO:10, модифицированы. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент специфически связывается с белком MICA, белком MICB или обоими белками MICA и MICB. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент связывается с альфа-3 доменом белка MICA, белка MICB или обоих белков MICA и MICB. В некоторых вариантах осуществления белок MICA является мембраносвязанным белком MICA, растворимым белком MICA или и тем и другим. В некоторых вариантах осуществления белок MICB является мембраносвязанным белком MICB, растворимым белком MICB или и тем и другим. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент выбирают из целого иммуноглобулина, scFv, Fab, F(ab’)2 или дисульфид-связанного Fv. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент представляет собой IgG или IgM. В некоторых вариантах осуществления моноклональное антитело или его фрагмент является гуманизированным или химерным.
В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:8. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 90% идентична аминокислотной последовательности SEQ ID NO:8. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности SEQ ID NO:8. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 99% идентична аминокислотной последовательности SEQ ID NO:8. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:8. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:8, где моноклональное антитело или его антиген-связывающий фрагмент содержит тяжелую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:10, или где моноклональное антитело или его антиген-связывающий фрагмент содержит легкую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:9. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 90% идентична аминокислотной последовательности SEQ ID NO:8, где моноклональное антитело или его антиген-связывающий фрагмент содержит тяжелую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:10, или где моноклональное антитело или его антиген-связывающий фрагмент содержит легкую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:9. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности SEQ ID NO:8, где моноклональное антитело или его антиген-связывающий фрагмент содержит тяжелую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:10, или где моноклональное антитело или его антиген-связывающий фрагмент содержит легкую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:9. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 99% идентична аминокислотной последовательности SEQ ID NO:8, где моноклональное антитело или его антиген-связывающий фрагмент содержит тяжелую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:10, или где моноклональное антитело или его антиген-связывающий фрагмент содержит легкую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:9. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:8, где моноклональное антитело или его антиген-связывающий фрагмент содержит тяжелую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:10, или где моноклональное антитело или его антиген-связывающий фрагмент содержит легкую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:9. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:7. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 90% идентична аминокислотной последовательности SEQ ID NO:7. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности SEQ ID NO:7. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 99% идентична аминокислотной последовательности SEQ ID NO:7. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:7. В некоторых вариантах осуществления тяжелая цепь включает аминокислотную последовательность, где по меньшей мере от 1 до 10 аминокислот аминокислотной последовательности SEQ ID NO:10, модифицированы. В некоторых вариантах осуществления легкая цепь включает аминокислотную последовательность, где по меньшей мере от 1 до 10 аминокислот аминокислотной последовательности SEQ ID NO:9, модифицированы. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент специфически связывается с белком MICA, белком MICB или обоими белками MICA и MICB. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент связывается с альфа-3 доменом белка MICA, белка MICB или обоих белков MICA и MICB. В некоторых вариантах осуществления белок MICA является мембраносвязанным белком MICA, растворимым белком MICA или и тем и другим. В некоторых вариантах осуществления белок MICB является мембраносвязанным белком MICB, растворимым белком MICB или и тем и другим. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент выбирают из целого иммуноглобулина, scFv, Fab, F(ab’)2 или дисульфид-связанного Fv. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент представляет собой IgG или IgM. В некоторых вариантах осуществления моноклональное антитело или его фрагмент является гуманизированным или химерным.
В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:1, последовательности определяющей комплементарность области 2 (CDR2) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:2, и последовательности определяющей комплементарность области 3 (CDR3) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:3. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) легкой цепи, по меньшей мере на 90% идентичной SEQ ID NO:1, последовательности определяющей комплементарность области 2 (CDR2) легкой цепи, по меньшей мере на 90% идентичной SEQ ID NO:2, и последовательности определяющей комплементарность области 3 (CDR3) легкой цепи, по меньшей мере на 90% идентичной SEQ ID NO:3. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) легкой цепи, по меньшей мере на 95% идентичной SEQ ID NO:1, последовательности определяющей комплементарность области 2 (CDR2) легкой цепи, по меньшей мере на 95% идентичной SEQ ID NO:2, и последовательности определяющей комплементарность области 3 (CDR3) легкой цепи, по меньшей мере на 95% идентичной SEQ ID NO:3. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) легкой цепи, по меньшей мере на 99% идентичной SEQ ID NO:1, последовательности определяющей комплементарность области 2 (CDR2) легкой цепи, по меньшей мере на 99% идентичной SEQ ID NO:2, и последовательности определяющей комплементарность области 3 (CDR3) легкой цепи, по меньшей мере на 99% идентичной SEQ ID NO:3. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) легкой цепи, по меньшей мере на 100% идентичной SEQ ID NO:1, последовательности определяющей комплементарность области 2 (CDR2) легкой цепи, по меньшей мере на 100% идентичной SEQ ID NO:2, и последовательности определяющей комплементарность области 3 (CDR3) легкой цепи, по меньшей мере на 100% идентичной SEQ ID NO:3. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:1, последовательности определяющей комплементарность области 2 (CDR2) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:2, и последовательности определяющей комплементарность области 3 (CDR3) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:3, где моноклональное антитело или его антиген-связывающий фрагмент содержит легкую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:9, или где моноклональное антитело или его антиген-связывающий фрагмент содержит тяжелую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:10. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) легкой цепи, по меньшей мере на 90% идентичной SEQ ID NO:1, последовательности определяющей комплементарность области 2 (CDR2) легкой цепи, по меньшей мере на 90% идентичной SEQ ID NO:2, и последовательности определяющей комплементарность области 3 (CDR3) легкой цепи, по меньшей мере на 90% идентичной SEQ ID NO:3, где моноклональное антитело или его антиген-связывающий фрагмент содержит легкую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:9, или где моноклональное антитело или его антиген-связывающий фрагмент содержит тяжелую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:10. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) легкой цепи, по меньшей мере на 95% идентичной SEQ ID NO:1, последовательности определяющей комплементарность области 2 (CDR2) легкой цепи, по меньшей мере на 95% идентичной SEQ ID NO:2, и последовательности определяющей комплементарность области 3 (CDR3) легкой цепи, по меньшей мере на 95% идентичной SEQ ID NO:3, где моноклональное антитело или его антиген-связывающий фрагмент содержит легкую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:9, или где моноклональное антитело или его антиген-связывающий фрагмент содержит тяжелую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:10. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) легкой цепи, по меньшей мере на 99% идентичной SEQ ID NO:1, последовательности определяющей комплементарность области 2 (CDR2) легкой цепи, по меньшей мере на 99% идентичной SEQ ID NO:2, и последовательности определяющей комплементарность области 3 (CDR3) легкой цепи, по меньшей мере на 99% идентичной SEQ ID NO:3, где моноклональное антитело или его антиген-связывающий фрагмент содержит легкую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:9, или где моноклональное антитело или его антиген-связывающий фрагмент содержит тяжелую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:10. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) легкой цепи, по меньшей мере на 100% идентичной SEQ ID NO:1, последовательности определяющей комплементарность области 2 (CDR2) легкой цепи, по меньшей мере на 100% идентичной SEQ ID NO:2, и последовательности определяющей комплементарность области 3 (CDR3) легкой цепи, по меньшей мере на 100% идентичной SEQ ID NO:3, где моноклональное антитело или его антиген-связывающий фрагмент содержит легкую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:9, или где моноклональное антитело или его антиген-связывающий фрагмент содержит тяжелую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:10. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:4, последовательности определяющей комплементарность области 2 (CDR2) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:5, и последовательности определяющей комплементарность области 3 (CDR3) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:6. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) тяжелой цепи, по меньшей мере на 90% идентичной SEQ ID NO:4, последовательности определяющей комплементарность области 2 (CDR2) тяжелой цепи, по меньшей мере на 90% идентичной SEQ ID NO:5, и последовательности определяющей комплементарность области 3 (CDR3) тяжелой цепи, по меньшей мере на 90% идентичной SEQ ID NO:6. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) тяжелой цепи, по меньшей мере на 95% идентичной SEQ ID NO:4, последовательности определяющей комплементарность области 2 (CDR2) тяжелой цепи, по меньшей мере на 95% идентичной SEQ ID NO:5, и последовательности определяющей комплементарность области 3 (CDR3) тяжелой цепи, по меньшей мере на 95% идентичной SEQ ID NO:6. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) тяжелой цепи, по меньшей мере на 99% идентичной SEQ ID NO:4, последовательности определяющей комплементарность области 2 (CDR2) тяжелой цепи, по меньшей мере на 99% идентичной SEQ ID NO:5, и последовательности определяющей комплементарность области 3 (CDR3) тяжелой цепи, по меньшей мере на 99% идентичной SEQ ID NO:6. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) тяжелой цепи, на 100% идентичной SEQ ID NO:4, последовательности определяющей комплементарность области 2 (CDR2) тяжелой цепи, на 100% идентичной SEQ ID NO:5, и последовательности определяющей комплементарность области 3 (CDR3) тяжелой цепи, на 100% идентичной SEQ ID NO:6. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:7. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:7. В некоторых вариантах осуществления легкая цепь включает аминокислотную последовательность, где по меньшей мере от 1 до 10 аминокислот аминокислотной последовательности SEQ ID NO:9, модифицированы. В некоторых вариантах осуществления тяжелая цепь включает аминокислотную последовательность, где по меньшей мере от 1 до 10 аминокислот аминокислотной последовательности SEQ ID NO:10, модифицированы. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент специфически связывается с белком MICA, белком MICB или обоими белками MICA и MICB. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент связывается с альфа-3 доменом белка MICA, белка MICB или обоих белков MICA и MICB. В некоторых вариантах осуществления белок MICA является мембраносвязанным белком MICA, растворимым белком MICA или и тем и другим. В некоторых вариантах осуществления белок MICB является мембраносвязанным белком MICB, растворимым белком MICB или и тем и другим. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент выбирают из целого иммуноглобулина, scFv, Fab, F(ab’)2 или дисульфид-связанного Fv. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент представляет собой IgG или IgM. В некоторых вариантах осуществления моноклональное антитело или его фрагмент является гуманизированным или химерным.
В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:4, последовательности определяющей комплементарность области 2 (CDR2) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:5, и последовательности определяющей комплементарность области 3 (CDR3) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:6. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) тяжелой цепи, по меньшей мере на 90% идентичной SEQ ID NO:4, последовательности определяющей комплементарность области 2 (CDR2) тяжелой цепи, по меньшей мере на 90% идентичной SEQ ID NO:5, и последовательности определяющей комплементарность области 3 (CDR3) тяжелой цепи, по меньшей мере на 90% идентичной SEQ ID NO:6. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) тяжелой цепи, по меньшей мере на 95% идентичной SEQ ID NO:4, последовательности определяющей комплементарность области 2 (CDR2) тяжелой цепи, по меньшей мере на 95% идентичной SEQ ID NO:5, и последовательности определяющей комплементарность области 3 (CDR3) тяжелой цепи, по меньшей мере на 95% идентичной SEQ ID NO:6. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) тяжелой цепи, по меньшей мере на 99% идентичной SEQ ID NO:4, последовательности определяющей комплементарность области 2 (CDR2) тяжелой цепи, по меньшей мере на 99% идентичной SEQ ID NO:5, и последовательности определяющей комплементарность области 3 (CDR3) тяжелой цепи, по меньшей мере на 99% идентичной SEQ ID NO:6. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) тяжелой цепи, на 100% идентичной SEQ ID NO:4, последовательности определяющей комплементарность области 2 (CDR2) тяжелой цепи, на 100% идентичной SEQ ID NO:5, и последовательности определяющей комплементарность области 3 (CDR3) тяжелой цепи, на 100% идентичной SEQ ID NO:6. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:4, последовательности определяющей комплементарность области 2 (CDR2) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:5, и последовательности определяющей комплементарность области 3 (CDR3) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:6, где моноклональное антитело или его антиген-связывающий фрагмент содержит тяжелую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:10, или где моноклональное антитело или его антиген-связывающий фрагмент содержит легкую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:9. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) тяжелой цепи, по меньшей мере на 90% идентичной SEQ ID NO:4, последовательности определяющей комплементарность области 2 (CDR2) тяжелой цепи, по меньшей мере на 90% идентичной SEQ ID NO:5, и последовательности определяющей комплементарность области 3 (CDR3) тяжелой цепи, по меньшей мере на 90% идентичной SEQ ID NO:6, где моноклональное антитело или его антиген-связывающий фрагмент содержит тяжелую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:10, или где моноклональное антитело или его антиген-связывающий фрагмент содержит легкую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:9. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) тяжелой цепи, по меньшей мере на 95% идентичной SEQ ID NO:4, последовательности определяющей комплементарность области 2 (CDR2) тяжелой цепи, по меньшей мере на 95% идентичной SEQ ID NO:5, и последовательности определяющей комплементарность области 3 (CDR3) тяжелой цепи, по меньшей мере на 95% идентичной SEQ ID NO:6, где моноклональное антитело или его антиген-связывающий фрагмент содержит тяжелую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:10, или где моноклональное антитело или его антиген-связывающий фрагмент содержит легкую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:9. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) тяжелой цепи, по меньшей мере на 99% идентичной SEQ ID NO:4, последовательности определяющей комплементарность области 2 (CDR2) тяжелой цепи, по меньшей мере на 99% идентичной SEQ ID NO:5, и последовательности определяющей комплементарность области 3 (CDR3) тяжелой цепи, по меньшей мере на 99% идентичной SEQ ID NO:6, где моноклональное антитело или его антиген-связывающий фрагмент содержит тяжелую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:10, или где моноклональное антитело или его антиген-связывающий фрагмент содержит легкую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:9. В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты, включающие по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) тяжелой цепи, на 100% идентичной SEQ ID NO:4, последовательности определяющей комплементарность области 2 (CDR2) тяжелой цепи, на 100% идентичной SEQ ID NO:5, и последовательности определяющей комплементарность области 3 (CDR3) тяжелой цепи, на 100% идентичной SEQ ID NO:6, где моноклональное антитело или его антиген-связывающий фрагмент содержит тяжелую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:10, или где моноклональное антитело или его антиген-связывающий фрагмент содержит легкую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:9. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:1, последовательности определяющей комплементарность области 2 (CDR2) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:2, и последовательности определяющей комплементарность области 3 (CDR3) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:3. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) легкой цепи, по меньшей мере на 90% идентичной SEQ ID NO:1, последовательности определяющей комплементарность области 2 (CDR2) легкой цепи, по меньшей мере на 90% идентичной SEQ ID NO:2, и последовательности определяющей комплементарность области 3 (CDR3) легкой цепи, по меньшей мере на 90% идентичной SEQ ID NO:3. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) легкой цепи, по меньшей мере на 95% идентичной SEQ ID NO:1, последовательности определяющей комплементарность области 2 (CDR2) легкой цепи, по меньшей мере на 95% идентичной SEQ ID NO:2, и последовательности определяющей комплементарность области 3 (CDR3) легкой цепи, по меньшей мере на 95% идентичной SEQ ID NO:3. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) легкой цепи, по меньшей мере на 99% идентичной SEQ ID NO:1, последовательности определяющей комплементарность области 2 (CDR2) легкой цепи, по меньшей мере на 99% идентичной SEQ ID NO:2, и последовательности определяющей комплементарность области 3 (CDR3) легкой цепи, по меньшей мере на 99% идентичной SEQ ID NO:3. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) легкой цепи, на 100% идентичной SEQ ID NO:1, последовательности определяющей комплементарность области 2 (CDR2) легкой цепи, на 100% идентичной SEQ ID NO:2, и последовательности определяющей комплементарность области 3 (CDR3) легкой цепи, на 100% идентичной SEQ ID NO:3. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:7. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:7. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления тяжелая цепь включает аминокислотную последовательность, где по меньшей мере от 1 до 10 аминокислот аминокислотной последовательности SEQ ID NO:10, модифицированы. В некоторых вариантах осуществления легкая цепь включает аминокислотную последовательность, где по меньшей мере от 1 до 10 аминокислот аминокислотной последовательности SEQ ID NO:9, модифицированы. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент специфически связывается с белком MICA, белком MICB или обоими белками MICA и MICB. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент связывается с альфа-3 доменом белка MICA, белка MICB или обоих белков MICA и MICB. В некоторых вариантах осуществления белок MICA является мембраносвязанным белком MICA, растворимым белком MICA или и тем и другим. В некоторых вариантах осуществления белок MICB является мембраносвязанным белком MICB, растворимым белком MICB или и тем и другим. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент выбирают из целого иммуноглобулина, scFv, Fab, F(ab’)2 или дисульфид-связанного Fv. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент представляет собой IgG или IgM. В некоторых вариантах осуществления моноклональное антитело или его фрагмент является гуманизированным или химерным.
В настоящей заявке раскрыты, в некоторых вариантах осуществления, фармацевтические композиции, включающие: моноклональное антитело или его антиген-связывающий фрагмент в соответствии с любым из раскрытий, представленных в настоящей заявке; и фармацевтически приемлемый носитель или эксципиент.
В настоящей заявке раскрыты, в некоторых вариантах осуществления, способы лечения рака у больного, включающие введение индивиду эффективного количества моноклонального антитела или его антиген-связывающего фрагмента, включающего по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:1, последовательности определяющей комплементарность области 2 (CDR2) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:2, и последовательности определяющей комплементарность области 3 (CDR3) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:3. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:4, последовательности определяющей комплементарность области 2 (CDR2) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:5, и последовательности определяющей комплементарность области 3 (CDR3) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:6. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:7. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:7. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент специфически связывается с белком MICA, белком MICB или обоими белками MICA и MICB. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент связывается с альфа-3 доменом белка MICA, белка MICB или обоих белков MICA и MICB. В некоторых вариантах осуществления белок MICA является мембраносвязанным белком MICA, растворимым белком MICA или и тем и другим. В некоторых вариантах осуществления белок MICB является мембраносвязанным белком MICB, растворимым белком MICB или и тем и другим. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент выбирают из целого иммуноглобулина, scFv, Fab, F(ab’)2 или дисульфид-связанного Fv. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент представляет собой IgG или IgM. В некоторых вариантах осуществления моноклональное антитело или его фрагмент является гуманизированным или химерным. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент снижает уровень растворимого белка MICA, растворимого белка MICB или обоих. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент уменьшает шеддинг растворимого белка MICA, растворимого белка MICB или обоих. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент ингибирует шеддинг растворимого белка MICA, растворимого белка MICB или обоих. В некоторых вариантах осуществления рак представляет собой гепатоцеллюлярную карциному.
В настоящей заявке раскрыты, в некоторых вариантах осуществления, способы лечения рака у больного, включающие введение индивиду эффективного количества моноклонального антитела или его антиген-связывающего фрагмента, включающего по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:4, последовательности определяющей комплементарность области 2 (CDR2) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:5, и последовательности определяющей комплементарность области 3 (CDR3) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:6. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:1, последовательности определяющей комплементарность области 2 (CDR2) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:2, и последовательности определяющей комплементарность области 3 (CDR3) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:3. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:7. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:7. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент специфически связывается с белком MICA, белком MICB или обоими белками MICA и MICB. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент связывается с альфа-3 доменом белка MICA, белка MICB или обоих белков MICA и MICB. В некоторых вариантах осуществления белок MICA является мембраносвязанным белком MICA, растворимым белком MICA или и тем и другим. В некоторых вариантах осуществления белок MICB является мембраносвязанным белком MICB, растворимым белком MICB или и тем и другим. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент выбирают из целого иммуноглобулина, scFv, Fab, F(ab’)2 или дисульфид-связанного Fv. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент представляет собой IgG или IgM. В некоторых вариантах осуществления моноклональное антитело или его фрагмент является гуманизированным или химерным. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент снижает уровень растворимого белка MICA, растворимого белка MICB или обоих. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент уменьшает шеддинг растворимого белка MICA, растворимого белка MICB или обоих. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент ингибирует шеддинг растворимого белка MICA, растворимого белка MICB или обоих. В некоторых вариантах осуществления рак представляет собой гепатоцеллюлярную карциному.
В настоящей заявке раскрыты, в некоторых вариантах осуществления, способы лечения гепатоцеллюлярной карциномы у больного, включающие введение индивиду эффективного количества моноклонального антитела или его антиген-связывающего фрагмента, включающего по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:1, последовательности определяющей комплементарность области 2 (CDR2) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:2, и последовательности определяющей комплементарность области 3 (CDR3) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:3. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:4, последовательности определяющей комплементарность области 2 (CDR2) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:5, и последовательности определяющей комплементарность области 3 (CDR3) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:6. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:7. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:7. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент специфически связывается с белком MICA, белком MICB или обоими белками MICA и MICB. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент связывается с альфа-3 доменом белка MICA, белка MICB или обоих белков MICA и MICB. В некоторых вариантах осуществления белок MICA является мембраносвязанным белком MICA, растворимым белком MICA или и тем и другим. В некоторых вариантах осуществления белок MICB является мембраносвязанным белком MICB, растворимым белком MICB или и тем и другим. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент выбирают из целого иммуноглобулина, scFv, Fab, F(ab’)2 или дисульфид-связанного Fv. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент представляет собой IgG или IgM. В некоторых вариантах осуществления моноклональное антитело или его фрагмент является гуманизированным или химерным. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент снижает уровень растворимого белка MICA, растворимого белка MICB или обоих. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент уменьшает шеддинг растворимого белка MICA, растворимого белка MICB или обоих. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент ингибирует шеддинг растворимого белка MICA, растворимого белка MICB или обоих.
В настоящей заявке раскрыты, в некоторых вариантах осуществления, способы лечения гепатоцеллюлярной карциномы у больного, включающие введение индивиду эффективного количества моноклонального антитела или его антиген-связывающего фрагмента, включающего по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:4, последовательности определяющей комплементарность области 2 (CDR2) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:5, и последовательности определяющей комплементарность области 3 (CDR3) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:6. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:1, последовательности определяющей комплементарность области 2 (CDR2) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:2, и последовательности определяющей комплементарность области 3 (CDR3) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:3. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:7. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:7. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент специфически связывается с белком MICA, белком MICB или обоими белками MICA и MICB. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент связывается с альфа-3 доменом белка MICA, белка MICB или обоих белков MICA и MICB. В некоторых вариантах осуществления белок MICA является мембраносвязанным белком MICA, растворимым белком MICA или и тем и другим. В некоторых вариантах осуществления белок MICB является мембраносвязанным белком MICB, растворимым белком MICB или и тем и другим. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент выбирают из целого иммуноглобулина, scFv, Fab, F(ab’)2 или дисульфид-связанного Fv. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент представляет собой IgG или IgM. В некоторых вариантах осуществления моноклональное антитело или его фрагмент является гуманизированным или химерным. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент снижает уровень растворимого белка MICA, растворимого белка MICB или обоих. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент уменьшает шеддинг растворимого белка MICA, растворимого белка MICB или обоих. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент ингибирует шеддинг растворимого белка MICA, растворимого белка MICB или обоих.
В настоящей заявке раскрыты, в некоторых вариантах осуществления, способы снижения уровня растворимого белка MICA, растворимого белка MICB или обоих у больного, включающие введение индивиду эффективного количества моноклонального антитела или его антиген-связывающего фрагмента, включающего по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:1, последовательности определяющей комплементарность области 2 (CDR2) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:2, и последовательности определяющей комплементарность области 3 (CDR3) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:3. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:4, последовательности определяющей комплементарность области 2 (CDR2) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:5, и последовательности определяющей комплементарность области 3 (CDR3) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:6. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:7. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:7. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент специфически связывается с белком MICA, белком MICB или обоими белками MICA и MICB. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент связывается с альфа-3 доменом белка MICA, белка MICB или обоих белков MICA и MICB. В некоторых вариантах осуществления белок MICA представляет собой растворимый белок MICA. В некоторых вариантах осуществления белок MICB представляет собой растворимый белок MICB. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент выбирают из целого иммуноглобулина, scFv, Fab, F(ab’)2 или дисульфид-связанного Fv. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент представляет собой IgG или IgM. В некоторых вариантах осуществления моноклональное антитело или его фрагмент является гуманизированным или химерным. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент уменьшает или ингибирует шеддинг растворимого белка MICA, растворимого белка MICB или обоих, снижая, таким образом, уровень растворимого белка MICA, растворимого белка MICB или обоих у индивида. В некоторых вариантах осуществления индивид имеет рак, характеризующийся повышенными уровнями растворимого белка MICA, растворимого белка MICB или обоих. В некоторых вариантах осуществления рак представляет собой гепатоцеллюлярную карциному.
В настоящей заявке раскрыты, в некоторых вариантах осуществления, способы снижения уровня растворимого белка MICA, растворимого белка MICB или обоих у больного, включающие введение индивиду эффективного количества моноклонального антитела или его антиген-связывающего фрагмента, включающего по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:4, последовательности определяющей комплементарность области 2 (CDR2) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:5, и последовательности определяющей комплементарность области 3 (CDR3) тяжелой цепи, по меньшей мере на 80% идентичной SEQ ID NO:6. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит по меньшей мере одну из последовательности определяющей комплементарность области 1 (CDR1) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:1, последовательности определяющей комплементарность области 2 (CDR2) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:2, и последовательности определяющей комплементарность области 3 (CDR3) легкой цепи, по меньшей мере на 80% идентичной SEQ ID NO:3. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:7. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен легкой цепи (VL), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:7. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит вариабельный домен тяжелой цепи (VH), содержащий аминокислотную последовательность, которая по меньшей мере на 80% идентична аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент специфически связывается с белком MICA, белком MICB или обоими белками MICA и MICB. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент связывается с альфа-3 доменом белка MICA, белка MICB или обоих белков MICA и MICB. В некоторых вариантах осуществления белок MICA представляет собой растворимый белок MICA. В некоторых вариантах осуществления белок MICB представляет собой растворимый белок MICB. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент выбирают из целого иммуноглобулина, scFv, Fab, F(ab’)2 или дисульфид-связанного Fv. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент представляет собой IgG или IgM. В некоторых вариантах осуществления моноклональное антитело или его фрагмент является гуманизированным или химерным. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент уменьшает или ингибирует шеддинг растворимого белка MICA, растворимого белка MICB или обоих, снижая, таким образом, уровень растворимого белка MICA, растворимого белка MICB или обоих у индивида. В некоторых вариантах осуществления индивид имеет рак, характеризующийся повышенными уровнями растворимого белка MICA, растворимого белка MICB или обоих. В некоторых вариантах осуществления рак представляет собой гепатоцеллюлярную карциному.
В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты в соответствии с любым из раскрытий, представленных в настоящей заявке, для применения в лечении рака у больного. Также, в настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела или их антиген-связывающие фрагменты в соответствии с любым из раскрытий, представленных в настоящей заявке, для применения в получении лекарственного средства для лечения рака у больного. В некоторых вариантах осуществления рак представляет собой гепатоцеллюлярную карциному.
Краткое описание чертежей
Характеристики и преимущества настоящего изобретения будут понятны посредством ссылки на следующее подробное описание, которое представляет иллюстративные варианты осуществления, в которых используются принципы изобретения, и на прилагаемые чертежи, которые:
Фиг. 1 иллюстрирует кинетические измерения антитела PDI-1 к MICA антигенам (MICA*01 и MICA*08) методом интерферометрии BioLayer.
Фиг. 2 иллюстрирует связывание антитела PDI-1 с аллелями MICA/B, определенное методом ELISA.
Фиг. 3 иллюстрирует связывание антитела PDI-1 с клеточно-поверхностным MICA, определенное методом клеточного окрашивания TRAMP C2 клеток, трансфицированных MICA*04.
Фиг. 4 иллюстрирует ингибирование антителом PDI-1 шеддинга MICA из PLC/PRF/5 клеток.
Фиг. 5 иллюстрирует, что PDI-1 усиливает NK-92 клеточно- опосредованную цитотоксичность PLC/PRF/5 клеток.
Фиг. 6 иллюстрирует измерение уровней растворимого MICA в сыворотке в модели кспенотрансплантата рака печени человека с использованием PDI-1 антитела.
Подробное описание изобретения
В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела, которые специфически связываются с MICA/B. В некоторых вариантах осуществления антитела к MICA/B связываются с белками MICA/B или их фрагментами и модулируют иммунный ответ у индивида, обеспечивая таким образом лечение рака (например, гепатоцеллюлярной карциномы).
Родственные главному комплексу гистосовместимости класса I цепь A и B (MICA/B) представляют собой два стресс-индуцируемых лиганда для рецептора NKG2D природных киллерных клеток (NK) и играют важную роль в опосредовании цитотоксичности NK и T-клеток. Растворимый MICA/B, выделяемый больными клетками (например, раковыми клетками), снижает чувствительность NK- и T-клеток за счет связывания рецептора NKG2D, тем самым подавляя иммунный ответ. Соответственно, модуляция MICA/B полезна для модуляции иммунного ответа у индивида, например, у индивида, страдающего раком. Антитела, связывающиеся с MICA/B и модулирующие его активность, желательны для разработки новых терапевтических средств для лечения рака.
Некоторая терминология
В контексте настоящей заявки “MICA/B” относится к белку MICA, белку MICB или обоим MICA и MICB белкам, включая их варианты, изоформы и видовые гомологи человеческого MICA/B.
В контексте настоящей заявки “антитело” относится к гликопротеину, который демонстрирует специфичность связывания с конкретным антигеном. Антитело часто включает вариабельный домен и константный домен в каждой из тяжелой цепи и легкой цепи. Соответственно, большинство антител имеют вариабельный домен тяжелой цепи (VH) и вариабельный домен легкой цепи (VL), которые вместе образуют часть антитела, которая связывается с антигеном. В каждом вариабельном домене присутствуют три определяющие комплементарность области (CDR), которые образуют петли в вариабельном домене тяжелой цепи (VH) и вариабельном домене легкой цепи (VL), которые контактируют с поверхностью антигена. Антитела в настоящей заявке также включают “антиген-связывающую часть” или фрагменты антитела, которые способны к связыванию с антигеном.
В контексте настоящей заявки “химерные” антитела представляют собой антитела, имеющие часть тяжелой и/или легкой цепи, идентичную или гомологичную соответствующим последовательностям в антителах, происходящих от определенного вида или принадлежащих к конкретному классу или подклассу антител, тогда как остальная цепь(цепи) идентична или гомологична соответствующим последовательностям в антителах, происходящих от другого вида или принадлежащих к другому классу или подклассу антител, а также фрагменты таких антител, если они проявляют желаемую биологическую активность (см., например, Morrison et al., Proc. Natl. Acad. Sci. USA 81:6851-6855 (1984)). “Гуманизированные антитела” в настоящей заявке относятся к химерным антителам, имеющим заменены человеческими последовательностями в последовательности антитела.
Термины “реципиент”, “индивидуум”, “индивид”, “хозяин” и “пациент” используются взаимозаменяемо и в некоторых случаях относятся к любому индивиду-млекопитающему, которому необходима диагностика, лечение или терапия, в частности к человеку. “Млекопитающее”, в целях лечения, относится к любому животному, классифицированному как млекопитающее, включая людей, домашних и сельскохозяйственных животных, а также лабораторных, зоопарковых, спортивных или домашних животных, таких как собаки, лошади, кошки, коровы, овцы, козы, свиньи, мыши, крысы, кролики, морские свинки, обезьяны и т.д. В некоторых вариантах осуществления млекопитающее является человеком.
В контексте настоящей заявки термины “лечение”, “осуществление лечения” и т.п. в некоторых случаях относятся к введению средства или осуществлению процедуры с целью получения эффекта. Эффект может быть профилактическим, с точки зрения полного или частичного предотвращения заболевания или его симптома, и/или может быть терапевтическим, с точки зрения частичного или полного излечения от заболевания и/или симптомов заболевания. “Лечение” в контексте настоящей заявки может включать лечение заболевания или расстройства (например, рака) у млекопитающего, особенно у человека, и включает: (а) предотвращение возникновения заболевания или симптома заболевания у индивида, который может быть предрасположен к заболеванию, но оно еще не диагностировано у него (например, включая заболевания, которые могут быть связаны с первичным заболеванием или вызваны им; (b) подавление заболевания, т.е. остановка его развития; и (c) облегчение заболевание, т.е. вызывая регресс заболевания. Лечение может относиться к любым признакам успеха в лечении, облегчении или профилактике рака, включая любой объективный или субъективный параметр, такой как ослабление; ремиссия; уменьшение симптомов или воздействие на болезненное состояние, делая его терпимым для пациента; замедление скорости дегенерации или ухудшения; или облегчение тяжести конечной точки дегенерации. Лечение или облегчение симптомов основано на одном или нескольких объективных или субъективных параметрах; включая результаты осмотра врачом. Соответственно, термин “лечение” включает введение соединений или средств по настоящему изобретению для предотвращения или задержки, облегчения или остановки или ингибирования развития симптомов или состояний, связанных с заболеваниями (например, раком). Термин “терапевтический эффект” относится к уменьшению, устранению или предотвращению заболевания, симптомов заболевания или побочных эффектов заболевания у индивида.
“Терапевтически эффективное количество” в некоторых случаях означает количество, которое при введении индивиду для лечения заболевания является достаточным для эффективного лечения этого заболевания.
В контексте настоящей заявки формы единственного числа, определяемые артиклями “a”, “and” и “the”, включают множественное число, если контекст явно не указывает иное. Таким образом, например, ссылка на “антитело” включает более одного антитела, а ссылка на “антитело” в некоторых вариантах осуществления включает множество антител и т.д.
В контексте настоящей заявки все числовые значения или числовые диапазоны включают целые числа в пределах таких диапазонов или охватывающие такие диапазоны, и части значений или целых чисел в пределах диапазонов или охватывающих диапазоны, если контекст явно не указывает иное. Таким образом, например, ссылка на диапазон 90-100% включает 91%, 92%, 93%, 94%, 95%, 95%, 97% и т.д., а также 91,1%, 91,2%, 91,3%, 91,4%, 91,5% и т.д., 92,1%, 92,2%, 92,3%, 92,4%, 92,5% и т.д. и т.п. В другом примере, ссылка на диапазон 1-5000 кратности включает 1-, 2-, 3-, 4-, 5-, 6-, 7-, 8-, 9-, 10-, 11-, 12-, 13-, 14-, 15-, 16-, 17-, 18-, 19-, 20-кратные значения и т.д., а также 1,1-, 1,2-, 1,3-, 1,4-, 1,5- кратные значения и т.д., 2,1-, 2,2-, 2,3-, 2,4-, 2,5- кратные значения и т.д. и т.п.
“Около” определенного значения, в контексте настоящей заявки, относится к диапазону, включающему это значение и охватывающему от 10% ниже этого значения до 10% выше этого значения. “Около” определенного диапазона относится к 10% ниже нижнего предела диапазона до 10% выше верхнего предела диапазона.
MICA/B
В настоящей заявке раскрыты, в некоторых вариантах осуществления, моноклональные антитела, которые специфически связываются с MICA/B.
Родственные цепи главного комплекса гистосовместимости (MHC) класса I, белок гена A и белок гена B (MICA/B) представляют собой гликозилированные полиморфные и заякоренные на мембране неклассические белки MHC класса I. MICA/B родственны MHC класса I и имеют подобную доменную структуру, включающую три внеклеточных Ig-подобных домена (альфа-1, альфа-2 и альфа-3), трансмембранный домен и C-концевой цитоплазматический хвост. Однако MICA/B не ассоциируется с β2-микроглобулином, не содержит сайт связывания CD8 и не презентирует никакие антигены. MICA/B являются лигандами лектиноподобного активирующего рецептора C-типа природных киллеров группы 2D (NKG2D) на иммунных эффекторных клетках, включая NK, NKT и как αβ, так и γδ М CD8+ Т-клетки. Взаимодействие MICA/B и NKG2D играет роль в надзоре за опухолью и иммунном ответе.
Белки MICA/B обычно экспрессируются на низких уровнях в нормальных клетках, но индуцируются до более высоких уровней в подверженных стрессу или трансформированных клетках (например, раковых клетках). Взаимодействие NKG2D-несущих иммунных эффекторных клеток с подверженными стрессу или заболевшими клетками, экспрессирующими MICA/B лиганды на клеточной поверхности, создает клеточный иммунный ответ против подверженной стрессу/больной клетки, который завершается гибелью экспрессирующих MICA/B клеток. В раковых клетках усеченные белки MICA/B (белки, которые лишены трансмембранного домена и цитоплазматического хвоста, но сохраняют три внеклеточных домена, включающих альфа-1, -2 и -3 домены) часто выделяются в кровь под действием протеаз и приводят к даун-модуляции (интернализации рецептора) их предполагаемого рецептора, NKG2D, на эффекторных иммунных клетках. В некоторых вариантах осуществления гликопротеины MICA/B продуцируются внутриклеточно, которые обычно не предназначены для того, чтобы быть мембраносвязанными на клеточной поверхности, а вместо этого включаются в экзосомы и высвобождаются из клетки наружу, где происходит взаимодействие с рецепторами NKG2D на иммунных клетках. Эти усеченные или растворимые лиганды MICA/B, отщепляемые с поверхности раковых клеток, действуют как молекулы-ловушки и приводят к даун-модуляции NKG2D рецептора на иммунных эффекторных клетках, таких как NK, NKT и различные CD8+ Т-клетки. В некоторых вариантах осуществления образование растворимого MICA/B приводит к необычной ситуации, когда эффекторы врожденной защитной системы, естественная роль которых заключается в поиске и разрушении трансформированных клеток, блокируются иммуносупрессивными действиями этих лигандных молекул-ловушек, тем самым позволяя раковым клеткам прятаться от иммунной системы и бесконтрольно расти.
Гепатоцеллюлярная карцинома (HCC)
В некоторых вариантах осуществления антитела к MICA/B, раскрытые в настоящей заявке, связываются с MICA/B белками или их фрагментами и модулируют иммунный ответ у индивида, осуществляя таким образом лечение рака (например, гепатоцеллюлярной карциномы).
Гепатоцеллюлярная карцинома (HCC) представляет собой первичное злокачественное новообразование печени, которое встречается преимущественно у лиц с хроническим заболеванием печени и циррозом. Опухоли прогрессируют с локальным распространением, внутрипеченочным распространением и отдаленными метастазами. Гепатит B и гепатит C предрасполагают к развитию хронического заболевания печени и последующему развитию HCC. Некоторыми другими причинами, предрасполагающими к последующему развитию HCC у индивидов, являются ожирение, диабет и злоупотребление алкоголем.
Антитела к MICA/B
В настоящей заявке представлены антитела, которые специфически связываются с MICA/B белками. В некоторых вариантах осуществления, антитела к MICA/B включают по меньшей мере одну тяжелую цепь, включающую вариабельный домен тяжелой цепи (VH), и по меньшей мере одну легкую цепь, включающую вариабельный домен легкой цепи (VL). Каждый VH и VL включает три определяющие комплементарность области (CDR). Аминокислотные последовательности VH и VL и CDRs определяют специфичность связывания с антигеном и антиген-связывающую силу антитела. Аминокислотные последовательности VH и VL и CDRs представлены в Таблице 1.
Последовательности анти-MICA/B моноклонального антитела (PDI-1)
В некоторых вариантах осуществления антитела специфически связываются с MICA белком. В некоторых вариантах осуществления антитела специфически связываются с MICB белком. В некоторых вариантах осуществления антитела специфически связываются с обоими белками MICA и MICB. В некоторых вариантах осуществления антитела связываются с альфа-3 доменом белка MICA. В некоторых вариантах осуществления антитела связываются с альфа-3 доменом белка MICB. В некоторых вариантах осуществления антитела связываются с альфа-3 доменом обоих белков MICA и MICB. В некоторых вариантах осуществления антитела связываются с белком MICA, который представляет собой мембраносвязанный белок MICA. В некоторых вариантах осуществления антитела связываются с белком MICA, который представляет собой растворимый белок MICA. В некоторых вариантах осуществления антитела связываются с белком MICA, который является как мембраносвязанным белком MICA, так и растворимым белком MICA. В некоторых вариантах осуществления антитела связываются с белком MICB, который представляет собой мембраносвязанный белок MICB. В некоторых вариантах осуществления антитела связываются с белком MICB, который представляет собой растворимый белок MICB. В некоторых вариантах осуществления антитела связываются с белком MICB, который является как мембраносвязанным белком MICB, так и растворимым белком MICB.
В некоторых вариантах осуществления антитела, которые специфически связываются с MICA/B, являются моноклональными антителами. В некоторых вариантах осуществления антитело представляет собой антиген-связывающий фрагмент. В некоторых вариантах осуществления антитело выбирают из целого иммуноглобулина, scFv, Fab, F(ab’)2 или дисульфид-связанного Fv. В некоторых вариантах осуществления антитело представляет собой IgG или an IgM. В некоторых вариантах осуществления антитело является гуманизированным. В некоторых вариантах осуществления антитело является химерным.
Вариабельный домен антитела к MICA/B
В настоящей заявке раскрыты антитела, которые специфически связываются с MICA/B, имеющие легкую цепь, включающую вариабельный домен легкой цепи (VL). В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, включают вариабельный домен легкой цепи (VL), имеющий аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:7. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:7. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:7.
Также в настоящей заявке раскрыты антитела, которые специфически связываются с MICA/B, имеющие тяжелую цепь, включающую вариабельный домен тяжелой цепи (VH). В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, включают вариабельный домен тяжелой цепи (VH), имеющий аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления VH имеет аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления VH имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:8.
Также в настоящей заявке раскрыты антитела, связывающиеся с MICA/B, включающие вариабельный домен легкой цепи (VL) и вариабельный домен тяжелой цепи (VH). В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, включают вариабельный домен легкой цепи (VL), имеющий аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:7, и вариабельный домен тяжелой цепи (VH), имеющий аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:7, и VH имеет аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:7, и VH имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит легкую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:9. В некоторых вариантах осуществления легкая цепь включает аминокислотную последовательность, где по меньшей мере от 1 до 10 аминокислот аминокислотной последовательности SEQ ID NO:9, модифицированы. В некоторых вариантах осуществления легкая цепь включает аминокислотную последовательность, где по меньшей мере 1 аминокислота аминокислотной последовательности SEQ ID NO:9, модифицирована. В некоторых вариантах осуществления легкая цепь включает аминокислотную последовательность, где по меньшей мере 2 аминокислоты аминокислотной последовательности SEQ ID NO:9, модифицированы. В некоторых вариантах осуществления легкая цепь включает аминокислотную последовательность, где по меньшей мере 3 аминокислоты аминокислотной последовательности SEQ ID NO:9, модифицированы. В некоторых вариантах осуществления легкая цепь включает аминокислотную последовательность, где по меньшей мере 4 аминокислоты аминокислотной последовательности SEQ ID NO:9, модифицированы. В некоторых вариантах осуществления легкая цепь включает аминокислотную последовательность, где по меньшей мере 5 аминокислот аминокислотной последовательности SEQ ID NO:9, модифицированы. В некоторых вариантах осуществления легкая цепь включает аминокислотную последовательность, где по меньшей мере 6 аминокислот аминокислотной последовательности SEQ ID NO:9, модифицированы. В некоторых вариантах осуществления легкая цепь включает аминокислотную последовательность, где по меньшей мере 7 аминокислот аминокислотной последовательности SEQ ID NO:9, модифицированы. В некоторых вариантах осуществления легкая цепь включает аминокислотную последовательность, где по меньшей мере 8 аминокислот аминокислотной последовательности SEQ ID NO:9, модифицированы. В некоторых вариантах осуществления легкая цепь включает аминокислотную последовательность, где по меньшей мере 9 аминокислот аминокислотной последовательности SEQ ID NO:9, модифицированы. В некоторых вариантах осуществления легкая цепь включает аминокислотную последовательность, где по меньшей мере 10 аминокислот аминокислотной последовательности SEQ ID NO:9, модифицированы. В некоторых вариантах осуществления моноклональное антитело или его антиген-связывающий фрагмент содержит тяжелую цепь, которая не имеет аминокислотную последовательность SEQ ID NO:10. В некоторых вариантах осуществления тяжелая цепь включает аминокислотную последовательность, где по меньшей мере от 1 до 10 аминокислот аминокислотной последовательности SEQ ID NO:10, модифицированы. В некоторых вариантах осуществления тяжелая цепь включает аминокислотную последовательность, где по меньшей мере 1 аминокислота аминокислотной последовательности SEQ ID NO:10, модифицирована. В некоторых вариантах осуществления тяжелая цепь включает аминокислотную последовательность, где по меньшей мере 2 аминокислоты аминокислотной последовательности SEQ ID NO:10, модифицированы. В некоторых вариантах осуществления тяжелая цепь включает аминокислотную последовательность, где по меньшей мере 3 аминокислоты аминокислотной последовательности SEQ ID NO:10, модифицированы. В некоторых вариантах осуществления тяжелая цепь включает аминокислотную последовательность, где по меньшей мере 4 аминокислоты аминокислотной последовательности SEQ ID NO:10, модифицированы. В некоторых вариантах осуществления тяжелая цепь включает аминокислотную последовательность, где по меньшей мере 5 аминокислот аминокислотной последовательности SEQ ID NO:10, модифицированы. В некоторых вариантах осуществления тяжелая цепь включает аминокислотную последовательность, где по меньшей мере 6 аминокислот аминокислотной последовательности SEQ ID NO:10, модифицированы. В некоторых вариантах осуществления тяжелая цепь включает аминокислотную последовательность, где по меньшей мере 7 аминокислот аминокислотной последовательности SEQ ID NO:10, модифицированы. В некоторых вариантах осуществления тяжелая цепь включает аминокислотную последовательность, где по меньшей мере 8 аминокислот аминокислотной последовательности SEQ ID NO:10, модифицированы. В некоторых вариантах осуществления тяжелая цепь включает аминокислотную последовательность, где по меньшей мере 9 аминокислот аминокислотной последовательности SEQ ID NO:10, модифицированы. В некоторых вариантах осуществления тяжелая цепь включает аминокислотную последовательность, где по меньшей мере 10 аминокислот аминокислотной последовательности SEQ ID NO:10, модифицированы.
Определяющие комплементарность области антитела к MICA/B
В настоящей заявке раскрыты антитела, которые специфически связываются с MICA/B, имеющие легкую цепь, включающую определяющую комплементарность область легкой цепи (CDR). В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, включают по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:1, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:2, и CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:3. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, включают по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:1, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:2, и CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:3. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, включают по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:1, CDR2 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:2, и CDR3 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:3.
Также в настоящей заявке раскрыты антитела, которые специфически связываются с MICA/B, имеющие тяжелую цепь, включающую определяющую комплементарность область (CDR) тяжелой цепи. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, включают по меньшей мере одну из CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:5, CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:6. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, включают по меньшей мере одну из CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:5, CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:6. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, включают по меньшей мере одну из CDR1 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:5, CDR3 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:6.
Также в настоящей заявке раскрыты антитела, связывающиеся с MICA/B, включающие определяющую комплементарность область (CDR) легкой цепи и определяющую комплементарность область (CDR)тяжелой цепи. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, включают по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:1, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:2, CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:3, CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:5, и CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:6. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, включают по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:1, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:2, CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:3, CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:5, и CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:6. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, включают по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:1, CDR2 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:2, CDR3 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:3, CDR1 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:5, и CDR3 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:6.
Способы лечения и применения
В настоящей заявке представлены способы лечения рака (например, гепатоцеллюлярной карциномы) у больного, включающие введение антитела к MICA/B, раскрытого в настоящей заявке.
Также в настоящей заявке представлены способы снижения уровня растворимых MICA/B белков у больного, включающие введение антитела к MICA/B, раскрытого в настоящей заявке.
В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, включают по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:1, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:2, и CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:3. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, включают по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:1, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:2, и CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:3. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, включают по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:1, CDR2 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:2, и CDR3 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:3.
Также в настоящей заявке раскрыты антитела, которые специфически связываются с MICA/B, имеющие тяжелую цепь, включающую определяющую комплементарность область тяжелой цепи (CDR). В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, включают по меньшей мере одну из CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:5, CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:6. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, включают по меньшей мере одну из CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:5, CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:6. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, включают по меньшей мере одну из CDR1 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:5, CDR3 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:6.
Также в настоящей заявке раскрыты антитела, связывающиеся с MICA/B, включающие определяющую комплементарность область (CDR) легкой цепи и определяющую комплементарность область (CDR) тяжелой цепи. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, включают по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:1, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:2, CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:3, CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:5, и CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:6. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, включают по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:1, CDR2 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:2, CDR3 легкой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:3, CDR1 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:5, и CDR3 тяжелой цепи, имеющей аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:6. В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, включают по меньшей мере одну из CDR1 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:1, CDR2 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:2, CDR3 легкой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:3, CDR1 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:4, CDR2 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:5, и CDR3 тяжелой цепи, имеющей аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:6.
В настоящей заявке раскрыты антитела, которые специфически связываются с MICA/B, имеющие легкую цепь, включающую вариабельный домен легкой цепи (VL). В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, включают вариабельный домен легкой цепи (VL), имеющий аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:7. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:7. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:7.
Также в настоящей заявке раскрыты антитела, которые специфически связываются с MICA/B, имеющие тяжелую цепь, включающую вариабельный домен тяжелой цепи (VH). В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, включают вариабельный домен тяжелой цепи (VH), имеющий аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления VH имеет аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления VH имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:8.
Также в настоящей заявке раскрыты антитела, связывающиеся с MICA/B, включающие вариабельный домен легкой цепи (VL) и вариабельный домен тяжелой цепи (VH). В некоторых вариантах осуществления антитела, связывающиеся с MICA/B, включают вариабельный домен легкой цепи (VL), имеющий аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:7, и вариабельный домен тяжелой цепи (VH), имеющий аминокислотную последовательность, по меньшей мере на около 70% идентичную аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:7, и VH имеет аминокислотную последовательность, по меньшей мере на около 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичную аминокислотной последовательности SEQ ID NO:8. В некоторых вариантах осуществления VL имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:7, и VH имеет аминокислотную последовательность, на 100% идентичную аминокислотной последовательности SEQ ID NO:8.
В некоторых вариантах осуществления антитела специфически связываются с белком MICA. В некоторых вариантах осуществления антитела специфически связываются с белком MICB. В некоторых вариантах осуществления антитела специфически связываются с обоими белками MICA и MICB. В некоторых вариантах осуществления антитела связываются с альфа-3 доменом белка MICA. В некоторых вариантах осуществления антитела связываются с альфа-3 доменом белка MICB. В некоторых вариантах осуществления антитела связываются с альфа-3 доменом обоих белков MICA и MICB. В некоторых вариантах осуществления антитела связываются с белком MICA, который представляет собой мембраносвязанный белок MICA. В некоторых вариантах осуществления антитела связываются с белком MICA, который представляет собой растворимый белок MICA. В некоторых вариантах осуществления антитела связываются с белком MICA, который является как мембраносвязанным белком MICA, так и растворимым белком MICA. В некоторых вариантах осуществления антитела связываются с белком MICB, который представляет собой мембраносвязанный белок MICB. В некоторых вариантах осуществления антитела связываются с белком MICB, который представляет собой растворимый белок MICB. В некоторых вариантах осуществления антитела связываются с белком MICB, который является как мембраносвязанным MICB белком, так и растворимым MICB белком.
В некоторых вариантах осуществления антитела, которые специфически связываются с MICA/B, являются моноклональными антителами. В некоторых вариантах осуществления антитело представляет собой антиген-связывающий фрагмент. В некоторых вариантах осуществления антитело выбирают из целого иммуноглобулина, scFv, Fab, F(ab’)2 или дисульфид-связанного Fv. В некоторых вариантах осуществления антитело представляет собой IgG или IgM. В некоторых вариантах осуществления антитело является гуманизированным. В некоторых вариантах осуществления антитело является химерным.
В некоторых вариантах осуществления антитела, раскрытые в настоящей заявке, снижают уровень растворимого белка MICA. В некоторых вариантах осуществления антитела, раскрытые в настоящей заявке, снижают уровень растворимого белка MICB. В некоторых вариантах осуществления антитела, раскрытые в настоящей заявке, снижают уровень как растворимого белка MICA, так и растворимого белка MICB. В некоторых вариантах осуществления антитела, раскрытые в настоящей заявке, уменьшают шеддинг растворимого белка MICA. В некоторых вариантах осуществления антитела, раскрытые в настоящей заявке, уменьшают шеддинг растворимого белка MICB. В некоторых вариантах осуществления антитела, раскрытые в настоящей заявке, уменьшают шеддинг как растворимого белка MICA, так и растворимого белка MICB. В некоторых вариантах осуществления антитела, раскрытые в настоящей заявке, ингибируют шеддинг растворимого белка MICA. В некоторых вариантах осуществления антитела, раскрытые в настоящей заявке, ингибируют шеддинг растворимого MICB белка. В некоторых вариантах осуществления антитела, раскрытые в настоящей заявке, ингибируют шеддинг как растворимого MICA белка, так и растворимого белка MICB. В некоторых вариантах осуществления антитела, раскрытые в настоящей заявке, уменьшают или ингибируют шеддинг растворимого белка MICA, растворимого белка MICB или обоих, снижая, таким образом, уровень растворимого белка MICA, растворимого белка MICB или обоих.
Любой подходящий путь введения предусматривается для использования с раскрытыми в настоящей заявке способами. В некоторых вариантах осуществления антитело вводят внутривенно. В некоторых вариантах осуществления антитело вводят подкожно. В некоторых вариантах осуществления антитело вводят местно. В некоторых вариантах осуществления антитело вводят системно (например, внутривенно, внутримышечно, подкожно, внутрикожно, перорально, интраназально, сублингвально). В некоторых вариантах осуществления антитело сформулировано в виде мази, лосьона или эмульсии. В некоторых вариантах осуществления антитело сформулировано в виде раствора. В некоторых вариантах осуществления антитело сформулировано для местного, перорального, буккального или назального введения.
В некоторых вариантах осуществления до введения антитела осуществляют мониторинг индивида. Выявляются симптомы и оценивается их тяжесть. Антитело, описанное в настоящей заявке, вводят отдельно или в комбинации с дополнительными лечениями, однократно или многократно с течением времени, как обсуждается в настоящей заявке или известно специалистам в данной области. В некоторых вариантах осуществления индивид находится под наблюдением, чтобы определить эффективность схемы лечения. В некоторых вариантах осуществления схему лечения модифицируют в ответ на предварительные результаты лечения таким образом, чтобы терапевтическую дозу или частоту введения, или и дозу и частоту, изменить так, чтобы достичь желаемого уровня ответа индивида, что касается облегчения симптомов, уменьшения побочных эффектов или сочетания облегчения симптомов и уменьшения побочных эффектов.
Предусматриваются терапевтически эффективные количества или дозировки, включающие дозировки от около 0,01 мг/кг до около 20 мг/кг, например около 0,01 мг/кг, около 0,02 мг/кг, около 0,03 мг/кг, около 0,04 мг/кг, около 0,05 мг/кг, около 0,06 мг/кг, около 0,07 мг/кг, около 0,08 мг/кг, около 0,09 мг/кг, около 0,1 мг/кг, около 0,2 мг/кг, около 0,3 мг/кг, около 0,4 мг/кг, около 0,5 мг/кг, около 0,6 мг/кг, около 0,7 мг/кг, около 0,8 мг/кг, около 0,9 мг/кг, около 1,0 мг/кг, около 1,1 мг/кг, около 1,2 мг/кг, около 1,3 мг/кг, около 1,4 мг/кг, около 1,5 мг/кг, около 1,6 мг/кг, около 1,7 мг/кг, около 1,8 мг/кг, около 1,9 мг/кг, около 2 мг/кг, около 2,1 мг/кг, около 2,2 мг/кг, около 2,3 мг/кг, около 2,4 мг/кг, около 2,5 мг/кг, около 2,6 мг/кг, около 2,7 мг/кг, около 2,8 мг/кг, около 2,9 мг/кг, около 3 мг/кг, около 3,1 мг/кг, около 3,2 мг/кг, около 3,3 мг/кг, около 3,4 мг/кг, около 3,5 мг/кг, около 3,6 мг/кг, около 3,7 мг/кг, около 3,8 мг/кг, около 3,9 мг/кг, около 4 мг/кг, около 4,1 мг/кг, около 4,2 мг/кг, около 4,3 мг/кг, около 4,4 мг/кг, около 4,5 мг/кг, около 4,6 мг/кг, около 4,7 мг/кг, около 4,8 мг/кг, около 4,9 мг/кг, около 5 мг/кг, около 5,1 мг/кг, около 5,2 мг/кг, около 5,3 мг/кг, около 5,4 мг/кг, около 5,5 мг/кг, около 5,6 мг/кг, около 5,7 мг/кг, около 5,8 мг/кг, около 5,9 мг/кг, около 6 мг/кг, около 6,1 мг/кг, около 6,2 мг/кг, около 6,3 мг/кг, около 6,4 мг/кг, около 6,5 мг/кг, около 6,6 мг/кг, около 6,7 мг/кг, около 6,8 мг/кг, около 6,9 мг/кг, около 7 мг/кг, около 7,1 мг/кг, около 7,2 мг/кг, около 7,3 мг/кг, около 7,4 мг/кг, около 7,5 мг/кг, около 7,6 мг/кг, около 7,7 мг/кг, около 7,8 мг/кг, около 7,9 мг/кг, около 8 мг/кг, около 8,1 мг/кг, около 8,2 мг/кг, около 8,3 мг/кг, около 8,4 мг/кг, около 8,5 мг/кг, около 8,6 мг/кг, около 8,7 мг/кг, около 8,8 мг/кг, около 8,9 мг/кг, около 9 мг/кг, около 9,1 мг/кг, около 9,2 мг/кг, около 9,3 мг/кг, около 9,4 мг/кг, около 9,5 мг/кг, около 9,6 мг/кг, около 9,7 мг/кг, около 9,8 мг/кг, около 9,9 мг/кг, около 10 мг/кг, около 10,1 мг/кг, около 10,2 мг/кг, около 10,3 мг/кг, около 10,4 мг/кг, около 10,5 мг/кг, около 10,6 мг/кг, около 10,7 мг/кг, около 10,8 мг/кг, около 10,9 мг/кг, около 11 мг/кг, около 11,1 мг/кг, около 11,2 мг/кг, около 11,3 мг/кг, около 11,4 мг/кг, около 11,5 мг/кг, около 11,6 мг/кг, около 11,7 мг/кг, около 11,8 мг/кг, около 11,9 мг/кг, около 12 мг/кг, около 12,1 мг/кг, около 12,2 мг/кг, около 12,3 мг/кг, около 12,4 мг/кг, около 12,5 мг/кг, около 12,6 мг/кг, около 12,7 мг/кг, около 12,8 мг/кг, около 12,9 мг/кг, около 13 мг/кг, около 13,1 мг/кг, около 13,2 мг/кг, около 13,3 мг/кг, около 13,4 мг/кг, около 13,5 мг/кг, около 13,6 мг/кг, около 13,7 мг/кг, около 13,8 мг/кг, около 13,9 мг/кг, около 14 мг/кг, около 14,1 мг/кг, около 14,2 мг/кг, около 14,3 мг/кг, около 14,4 мг/кг, около 14,5 мг/кг, около 14,6 мг/кг, около 14,7 мг/кг, около 14,8 мг/кг, около 14,9 мг/кг, около 15 мг/кг, около 15,1 мг/кг, около 15,2 мг/кг, около 15,3 мг/кг, около 15,4 мг/кг, около 15,5 мг/кг, около 15,6 мг/кг, около 15,7 мг/кг, около 15,8 мг/кг, около 15,9 мг/кг, около 16 мг/кг, около 16,1 мг/кг, около 16,2 мг/кг, около 16,3 мг/кг, около 16,4 мг/кг, около 16,5 мг/кг, около 16,6 мг/кг, около 16,7 мг/кг, около 16,8 мг/кг, около 16,9 мг/кг, около 17 мг/кг, около 17,1 мг/кг, около 17,2 мг/кг, около 17,3 мг/кг, около 17,4 мг/кг, около 17,5 мг/кг, около 17,6 мг/кг, около 17,7 мг/кг, около 17,8 мг/кг, около 17,9 мг/кг, около 18 мг/кг, около 18,1 мг/кг, около 18,2 мг/кг, около 18,3 мг/кг, около 18,4 мг/кг, около 18,5 мг/кг, около 18,6 мг/кг, около 18,7 мг/кг, около 18,8 мг/кг, около 18,9 мг/кг, около 19 мг/кг, около 19,1 мг/кг, около 19,2 мг/кг, около 19,3 мг/кг, около 19,4 мг/кг, около 19,5 мг/кг, около 19,6 мг/кг, около 19,7 мг/кг, около 19,8 мг/кг, около 19,9 мг/кг, около или 20 мг/кг. В некоторых случаях предусматриваются терапевтически эффективные количества или дозировки, включающие дозировки от около 0,1 мг/кг до около 2,0 мг/кг.
Способы лечения, описанные в настоящей заявке, включают одно или несколько введений антител к MICA/B в дозах, раскрытых в настоящей заявке. В некоторых вариантах осуществления способы включают одно введение антител к MICA/B. В некоторых вариантах осуществления способы включают два введения антител к MICA/B. В некоторых вариантах осуществления способы включают три введения антител к MICA/B. В некоторых вариантах осуществления способы включают четыре введения антител к MICA/B. в некоторых вариантах осуществления способы включают пять введений антител к MICA/B. В некоторых вариантах осуществления способы включают шесть введений антител к MICA/B. В некоторых вариантах осуществления одно или несколько введений антител к MICA/B осуществляют ежедневно. В некоторых вариантах осуществления одно или несколько введений антител к MICA/B осуществляют еженедельно. В некоторых вариантах осуществления одно или несколько введений антител к MICA/B осуществляют раз в две недели. В некоторых вариантах осуществления одно или несколько введений антител к MICA/B осуществляют раз в месяц. В некоторых вариантах осуществления одно или несколько введений антител к MICA/B осуществляют рав в три месяца. В некоторых вариантах осуществления одно или несколько введений антител к MICA/B осуществляют раз в шесть месяцев. В некоторых вариантах осуществления одно или несколько введений антител к MICA/B осуществляют раз в год.
Фармацевтические композиции
Также в настоящей заявке раскрыты фармацевтические композиции, включающие антитела к MICA/B, раскрытые в настоящей заявке, и фармацевтически приемлемый носитель или эксципиент.
В некоторых вариантах осуществления эксципиенты для использования с композициями, раскрытыми в настоящей заявке, включают малеиновую кислоту, винную кислоту, молочную кислоту, лимонную кислоту, уксусную кислоту, бикарбонат натрия, фосфат натрия, гистидин, глицин, хлорид натрия, хлорид калия, хлорид кальция, хлорид цинка, воду, декстрозу, N-метилпирролидон, диметилсульфоксид, N, N-диметилацетамид, этанол, пропиленгликоль, полиэтиленгликоль, моноэтиловый эфир диэтиленгликоля и поверхностно-активное вещество полиоксиэтилен-сорбитанмоноолеат.
В некоторых вариантах осуществления композиции также включают дополнительное терапевтическое средство. В некоторых вариантах осуществления терапевтическое средство представляет собой химиотерапевтическое средство. Химиотерапевтические средства могут включать, среди прочего, цитотоксические средства, антиметаболиты (например, антагонисты фолиевой кислоты, пуриновые аналоги, пиримидиновые аналоги и т.д.), ингибиторы топоизомеразы (например, производные камптотецина, антрацендион, антрациклины, эпиподофиллотоксины, хинолиновые алкалоиды и т.д.), средства против микротрубочек (например, таксаны, алкалоиды барвинка), ингибиторы синтеза белка (например, цефалотаксин, производные камптотецина, хинолиновые алкалоиды), алкилирующие средства (например, алкилсульфонаты, этиленимины, азотистый иприт, нитрозомочевины, производные платины, триазены и т.д.), алкалоиды, терпеноиды и ингибиторы киназ.
В некоторых вариантах осуществления антитело и терапевтическое средство находятся в одной композиции. В некоторых вариантах осуществления антитело и терапевтическое средство находятся в разных композициях. В некоторых вариантах осуществления антитело, описанное в настоящей заявке, используют до введения другого терапевтического средства. В некоторых вариантах осуществления антитело, описанное в настоящей заявке, используют одновременно с введением другого терапевтического средства. В некоторых вариантах осуществления антитело, описанное в настоящей заявке, используют после введения другого терапевтического средства.
Фармацевтические композиции в некоторых вариантах осуществления получают таким образом, чтобы они были совместимы с конкретным местным, регионарным или системным путем введения или доставки. Таким образом, фармацевтические композиции включают носители, разбавители или эксципиенты, подходящие для введения определенными путями. Конкретными неограничивающими примерами путей введения композиций в настоящей заявке являются парентеральный, например, внутривенный, интраартериальный, внутрикожный, внутримышечный, подкожный, интраплевральный, трансдермальный (местный), через слизистую оболочку, интракраниальный, интраспинальный, внутриглазной, ректальный, пероральный (алиментарный), мукозальный пути введения, и любая другая композиция, подходящая для способа лечения или протокола введения.
В некоторых вариантах осуществления растворы или суспензии, используемые для парентерального применения, включают: стерильный разбавитель, такой как вода для инъекций, физиологический раствор, жирные масла, полиэтиленгликоли, глицерин, пропиленгликоль или другие синтетические растворители; антибактериальные агенты, такие как бензиловый спирт или метилпарабены; антиоксиданты, такие как аскорбиновая кислота или бисульфат натрия; хелатирующие агенты, такие как этилендиаминтетрауксусная кислота; буферы, такие как ацетаты, цитраты или фосфаты; и агенты для регулирования тоничности, такие как хлорид натрия или декстроза. В некоторых вариантах осуществления pH регулируют при помощи кислот или оснований, таких как хлористоводородная кислота или гидроксид натрия.
Фармацевтические композиции для инъекций включают стерильные водные растворы (если они водорастворимы) или дисперсии и стерильные порошки для получения экстемпоральных стерильных растворов или дисперсий для инъекций. Для внутривенного введения подходящие носители включают физиологический раствор, бактериостатическую воду, Cremophor EL™ (BASF, Parsippany, N.J.) или фосфатно-солевой буферный раствор (PBS). В некоторых вариантах осуществления носитель представляет собой растворитель или дисперсионную среду, содержащую, например, воду, этанол, полиол (например, глицерин, пропиленгликоль и жидкий полиэтиленгликоль и т.п.) или их подходящие смеси. В некоторых вариантах осуществления текучесть поддерживают, например, за счет использования покрытия, такого как лецитин, путем поддержания требуемого размера частиц в случае дисперсии и за счет использования поверхностно-активных веществ. Антибактериальные и противогрибковые средства включают, например, парабены, хлорбутанол, фенол, аскорбиновую кислоту и тимеросал. В некоторых вариантах осуществления в композицию включают изотонические агенты, например сахара; многоатомные спирты, такие как маннит или сорбит; или хлорид натрия. В некоторых случаях также включают агент, который замедляет абсорбцию, в некоторых вариантах осуществления, например, моностеарат алюминия или желатин замедляет абсорбцию инъекционных композиций.
В некоторых вариантах осуществления стерильные композиции для инъекций получают путем включения композиции активного вещества в необходимом количестве в соответствующий растворитель с одним или комбинацией вышеуказанных ингредиентов. Обычно дисперсии получают путем включения композиции активного вещества в стерильный носитель, содержащий основную дисперсионную среду и любой другой ингредиент. В случае стерильных порошков для получения стерильных растворов для инъекций способы получения включают, например, вакуумную сушку и сублимационную сушку, которая дает порошок активного ингредиента плюс любой дополнительный желаемый ингредиент из содержащего их предварительно приготовленного раствора.
Для чрескожного или трансдермального введения в композиции используются пенетранты, подходящие для барьера, через который должна проникать композиция. Такие пенетранты известны в данной области и включают, например для трансмукозального введения, детергенты, соли желчных кислот и производные фузидовой кислоты. В некоторых вариантах осуществления изобретения трансмукозальное введение осуществляют с использованием назальных спреев, ингаляционных устройств (например, аспираторов) или суппозиториев. Для трансдермального введения активные соединения формулируют в виде мазей, бальзамов, гелей, кремов или пластырей.
В некоторых вариантах осуществления фармацевтические композиции получают с носителями, которые защищают от быстрого выведения из организма, такими как композиции для контролируемого высвобождения или замедляющее высвобождение вещество, такое как глицерилмоностеарат или глицерилстеарат. Доставку композиций, в некоторых вариантах осуществления, также осуществляют с использованием промышленных изделий, таких как имплантаты и микрокапсулированные системы доставки, для достижения местной, регионарной или системной доставки или контролируемого или длительного высвобождения.
ПРИМЕРЫ
Следующие примеры представлены с целью иллюстрации различных вариантов осуществления изобретения и не предназначены для ограничения настоящего изобретения каким-либо образом. Представленные примеры, наряду со способами, описанными в настоящей заявке, на данный момент представляют предпочтительные варианты осуществления, являются иллюстративными и не предназначены для ограничения объема изобретения. Изменения в них и другие применения, которые охватываются сущностью изобретения, как определено объемом формулы изобретения, будут очевидны специалистам в данной области.
Пример 1: Получение и скрининг моноклональных антител к MICA/B
Антитела получают с использованием традиционных методов, известных из уровня техники, например, Kohler and Milstein, 1975, Nature 256(5517):495-7; Coligan et al., supra, sections 2.5.1-2.6.7; Current Protocols in Immunology, John Wiley & Sons, Inc. (1992); и Antibodies: A Laboratory Manual, Harlow and Lane, eds., Cold Spring Harbor Press, New York (1988); Monoclonal Antibodies: Methods and Protocols in Methods Mol Biol., Vol. 378, Albitar M., ed., Humana Press (2007), которые включены в настоящую заявку посредством ссылки. Моноклональные антитела генерируются у мышей, которым вводят иммуноген, с последующим выделением B-клеток, которые продуцируют антитела. Затем осуществляют иммортализацию B-клеток путем их слияния с другим стабильным клеточным типом того же вида B-клеток для создания гибридомы. Клоны гибридом скринируют с использованием ELISA на их способность к связыванию с антигеном (MICA/B). Отдельная B-клетка образует одно специфическое антитело (т.е. является клонально моноспецифической), которое определяют по его первичной аминокислотной последовательности и лежащей в основе последовательности гена. Моноклональные антитела, демонстрирующие специфическое связывание с MICA/B, выделяют и очищают от культуры с гибридомами с использованием традиционного способа, такого как аффинная хроматография с Белком-A Сефарозой, эксклюзионная хроматография и ионообменная хроматография (см., например, Coligan, et al., supra, sections 2.7.1-2.7.12 and sections 2.9.1-2.9.3; Barnes, et al., Purification of Immunoglobulin G (IgG), in Methods Mol. Biol., Vol. 10, pages 79-104, Humana Press (1992)).
Пример 2: Измерение кинетики связывания PDI-1 антитела
Кинетику аффинности определяли на анализаторе ForteBio Octet Red96. Вкратце, PDI-1 (30мкг/мл) захватывали на Dip and Read Anti-mouse IgG Fc Capture (AMC) биосенсорах (ForteBio) при комнатной температуре в аналитическом буфере PBS+0,1% BSA+0,02% Tween-20 (pH 7,2). Сенсоры промывали в аналитическом буфере и затем инкубировали с очищенными 6×His-MICA*08 и 6×His-MICA*01 белками (100нМ), соответственно, в 2-кратном серийном разведении в течение 5 минут в аналитическом буфере для определения кинетики ассоциации антитела с белковым антигеном. Сенсоры затем инкубировали в аналитическом буфере в течение 10 минут для определения кинетики диссоциации. Кинетические параметры рассчитывали при помощи системы анализа ForteBio 8.0 с использованием 1:1 модели. Результаты этих анализов показаны на Фиг. 1.
Пример 3: PDI-1 антитело, связывающееся с аллелями MICA/B
Рекомбинантные MICA*01, MICA*02, MICA*04, MICA*08, MICA*09 и MICB белки разводили до 1 мкг/мл в буферном растворе 50 мМ карбоната натрия, pH 9,6 и наносили на 96-луночный микропланшет с высокой степенью связывания (Corning #9018), 100 нг в 100 мкл на лунку. На следующее утро покрытые ELISA планшеты промывали три раза TBS-Tween-20, pH 7,4, и затем блокировали в блокирующем буфере SuperBlock T20 (Pierce #37536). После блокирования ELISA планшеты промывали один раз TBS-T и инкубировали с серийно разведенным PDI-1 антителом (0-1 мкг/мл) приблизительно в течение двух часов при комнатной температуре. После инкубации ELISA планшеты промывали три раза TBS-T и затем инкубировали с конъюгатом Козлиное анти-Мышиное IgG (H+L)-HRP (ThermoFisher Scientific #626520) в течение 45 минут при комнатной температуре при встряхивании (400 об/мин). После инкубации ELISA планшеты промывали три раза TBS-T и инкубировали со сверхчувствительным жидким субстратом TMB (Sigma #T4444), 100 мкл на лунку, до достаточного проявления цвета. Реакцию останавливали 1N раствором серной кислоты, 100 мкл на лунку. Значения оптической плотности (OD) измеряли при 450 нм с использованием микропланшет-ридера. Результат этого анализа показан на Фиг. 2.
Пример 4: PDI-1 Антитело, связывающееся с клеточноповерхностным MICA
Мышиные клетки аденокарциномы предстательной железы TRAMP-C2 (TC2) (ATCC, Manassas, VA) использовали для генерирования стабильной клеточной линии, экспрессирующей аллель MICA*04 (TC2-MICA-04). Связывание PDI-1 с TC2-MICA-04 анализировали методом проточной цитометрии. Вкратце, клетки сначала окрашивали при помощи LIVE/DEAD Near IR Stain (Thermo) в течение 30 минут при 4°C и затем промывали один раз путем центрифугирования с FACS буфером (1мМ EDTA, 25мМ HEPES, 2% FBS в 1X PBS). Около 2-3×105 TC2-MICA-04 клеток инкубировали с 100мкл FACS буфера, содержащего 500нг PDI-1 антитела, при 4°C в течение 30 минут, с последующей инкубацией с 100мкл 2мкг/мл PE конъюгированного козлиного-анти-мышиного IgG (Biolegend, San Diego, CA) вторичного Ab при 4°C в течение 30 мин. Клетки затем промывали один раз и клеточный осадок ресуспендировали с FACS буфером для FACS анализа, гейтированного на живых клетках. Значительно более высокий сигнал PE флуоресценции, наблюдаемый с TC2-MICA-04 клетками, по сравнению с исходными TC2 клетками указывал на связывание PDI-1 с экспрессируемым на поверхности MICA. Результат для этого анализа показан на Фиг. 3.
Пример 5: PDI-1 антитело ингибирует шеддинг MICA из PLC/PRF/5 клеток
4×104 PLC/PRF/5 клеток (гепатоцеллюлярной карциномы) (ATCC, Manassas, VA) высевали в 96-луночный планшет и инкубировали при 37°C в течение ночи. Клетки затем обрабатывали 100мкл полной среды (MEM+10% FBS, Thermo, Grand Island, NY), содержащей PDI-1 и отрицательные контрольные антитела, соответственно, и инкубировали при 37°C еще в течение одного дня. Клеточные супернатанты, содержащие отщепленный MICA, использовали для определения уровня растворимого MICA методом ELISA. Вкратце, 96-луночный планшет покрывали 100мкл 2мкг/мл иммобилизованного Ab против человеческого MICA/MICB, клон 6D4 (Biolegend, San Diego, CA), в течение ночи при 4oC. Планшет блокировали и затем инкубировали с клеточными супернатантами и MICA стандартами в течение 2 часов. После инкубации планшеты промывали, с последующей 1-часовой инкубацией с 100мкл 500 нг/мл детекторного Ab (mAb против человеческого MICA, клон 159227, R&D Systems, Minneapolis, MN), конъюгированного с биотином. Затем 100мкл HRP-конъюгированного стрептавидина (HRP-SA) (R&D Systems, Minneapolis, MN) добавляли в лунки и инкубировали в течение 30 мин. Образцы проявляли с использованием TMB в течение 4 мин, реакцию останавливали 1N раствором серной кислоты и осуществляли детекцию с поглощением при 450 нм. Уровень растворимого MICA интерполировали из стандартной кривой. Результат для этого анализа показан на Фиг. 4.
Пример 6: PDI-1 антитело усиливает NK-92 клеточно-опосредованную цитотоксичность в отношении PLC/PRF/5 клеток
PLC/PRF/5 (Target) клетки суспендировали в RPMI-1640 с 10% FBS и высевали в 96-луночный плоскодонный планшет (Costar) при 6000 клеток/лунка. Клетки затем инкубировали с PDI-1 антителом (10мкг/мл) в течение 24 часов, затем метили кальцеином AM (1 мкМ) в течение 3 часов при 37°C, 5% CO2. Лунки промывали и NK-92 клетки (Эффектор) суспендировали в RPMI-1640 с 10% FBS, затем добавляли в лунки при различных указанных отношениях Эффектор-к-Мишени (E:T) и совместно культивировали с клетками-мишенями в течение 4 часов. По завершении культивирования супернатант удаляли, заменяли на PBS и измеряли сигнал кальцеина AM с использованием многоканального планшет-ридера VICTOR (Perkin Elmer). Изотипически сходное нереактивное иммуноглобулиновое (R&D) антитело использовали в качестве контроля. Результат для этого анализа показан на Фиг. 5.
Пример 7: Анализ растворимого MICA с использованием сэндвич-варианта ELISA
96-луночный планшет с высокой степенью связывания (Costar #9018) покрывали в течение ночи при 4°C 200 нг/лунка анти-MICA иммобилизованным антителом в буферном растворе карбоната натрия (50 мМ pH 9,6) в объеме 100 мкл, затем блокировали при помощи SuperBlock T20 (Pierce #37536) и промывали буфером TBS-T. Затем образцы сыворотки из модели кспенотрансплантата рака печени человека, разбавленные 1:3 в SuperBlock T20, или рекомбинантный MICA*08 стандарт добавляли в планшет и инкубировали в течение 2 часов при комнатной температуре. После 2 часов инкубации планшет промывали три раза TBS-T и затем инкубировали с биотинилированным PDI-1 детекторным антителом, разбавленным до 1 мкг/мл в SuperBlock T20. После 1-часовой инкубации планшет промывали три раза TBS-T и затем инкубировали в течение 45 минут с конъюгатом Стрептавидин-HRP (Invitrogen #SNN2004), разбавленным 1/5000 в SuperBlock T20, 100 мкл на лунку. После 45 минут инкубации планшет промывали три раза TBS-T. Затем добавляли сверхчувствительный жидкий субстрат TMB для ELISA (Sigma T4444), 100 мкл на лунку, и происходила реакция проявления цвета. Реакцию останавливали путем добавления 100 мкл на лунку 1N H2SO4. Выход измеряли по O.D., определяемой при 450 нм. Результат этого анализа показан на Фиг. 6.
Хотя были показаны и описаны предпочтительные варианты осуществления настоящего изобретения, для специалистов в данной области техники будет очевидно, что такие варианты осуществления представлены только в качестве примера. Многочисленные варианты, изменения и замены теперь будут очевидны специалистам в данной области техники без отступления от изобретения. Должно быть понятно, что можно использовать различные альтернативы вариантам осуществления, описанным в настоящей заявке. Предполагается, что нижеследующая формула изобретения определяет объем изобретения и что охватываются способы и структуры в пределах объема этой формулы изобретения и их эквиваленты.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> КАЛЛИНЕН МАЙКА КОРП.
<120> АНТИТЕЛА К MICA/B И СПОСОБЫ ПРИМЕНЕНИЯ
<130> 53620-701.601
<140> PCT/US2019/015025
<141> 2019-01-24
<150> 62/621,892
<151> 2018-01-25
<160> 11
<170> PatentIn version 3.5
<210> 1
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 1
Ser Ala Ser Gln Gly Ile Ser Asn Tyr Leu Asn
1 5 10
<210> 2
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 2
Thr Ser Leu Leu His Ser Gly
1 5
<210> 3
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 3
Gln Gln Tyr Ser Lys Phe Pro Arg Thr
1 5
<210> 4
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 4
Gly Tyr Thr Phe Thr Asn Tyr Gly Met Asn
1 5 10
<210> 5
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 5
Ile Asn Thr Tyr Thr Gly Glu Pro Thr Tyr Ala Asp Asp Phe Lys Gly
1 5 10 15
<210> 6
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 6
Asn Tyr Gly Asn Tyr Leu Phe Asp Tyr
1 5
<210> 7
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 7
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Ser Ala Ser Gln Gly Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Leu Lys Leu Leu Ile
35 40 45
Gln Tyr Thr Ser Leu Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Tyr Ser Leu Thr Ile Ser Asn Leu Glu Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Tyr Ser Lys Phe Pro Arg
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105
<210> 8
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 8
Gln Ile Gln Leu Val Gln Ser Gly Pro Glu Leu Lys Lys Ser Gly Glu
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Ala Phe Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Lys Gln Ala Pro Gly Lys Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Tyr Thr Gly Glu Pro Thr Tyr Ala Asp Asp Phe
50 55 60
Lys Gly Arg Phe Ala Phe Ser Leu Glu Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Asn His Leu Lys Asn Glu Asp Thr Ala Thr Tyr Phe Cys
85 90 95
Ala Arg Asn Tyr Gly Asn Tyr Leu Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Leu Thr Val Ser Ser
115
<210> 9
<211> 234
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 9
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser
20 25 30
Ala Ser Leu Gly Asp Arg Val Thr Ile Ser Cys Ser Ala Ser Gln Gly
35 40 45
Ile Ser Asn Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Leu
50 55 60
Lys Leu Leu Ile Gln Tyr Thr Ser Leu Leu His Ser Gly Val Pro Ser
65 70 75 80
Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Tyr Ser Leu Thr Ile Ser
85 90 95
Asn Leu Glu Pro Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Tyr Ser
100 105 110
Lys Phe Pro Arg Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
115 120 125
Ala Asp Ala Ala Pro Thr Val Ser Ile Phe Pro Pro Ser Ser Glu Gln
130 135 140
Leu Thr Ser Gly Gly Ala Ser Val Val Cys Phe Leu Asn Asn Phe Tyr
145 150 155 160
Pro Lys Asp Ile Asn Val Lys Trp Lys Ile Asp Gly Ser Glu Arg Gln
165 170 175
Asn Gly Val Leu Asn Ser Trp Thr Asp Gln Asp Ser Lys Asp Ser Thr
180 185 190
Tyr Ser Met Ser Ser Thr Leu Thr Leu Thr Lys Asp Glu Tyr Glu Arg
195 200 205
His Asn Ser Tyr Thr Cys Glu Ala Thr His Lys Thr Ser Thr Ser Pro
210 215 220
Ile Val Lys Ser Phe Asn Arg Asn Glu Cys
225 230
<210> 10
<211> 467
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 10
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Gln Ile Gln Leu Val Gln Ser Gly Pro Glu Leu Lys
20 25 30
Lys Ser Gly Glu Thr Val Lys Ile Ser Cys Lys Ala Phe Gly Tyr Thr
35 40 45
Phe Thr Asn Tyr Gly Met Asn Trp Val Lys Gln Ala Pro Gly Lys Gly
50 55 60
Leu Lys Trp Met Gly Trp Ile Asn Thr Tyr Thr Gly Glu Pro Thr Tyr
65 70 75 80
Ala Asp Asp Phe Lys Gly Arg Phe Ala Phe Ser Leu Glu Thr Ser Ala
85 90 95
Ser Thr Ala Tyr Leu Gln Ile Asn His Leu Lys Asn Glu Asp Thr Ala
100 105 110
Thr Tyr Phe Cys Ala Arg Asn Tyr Gly Asn Tyr Leu Phe Asp Tyr Trp
115 120 125
Gly Gln Gly Thr Thr Leu Thr Val Ser Ser Ala Lys Thr Thr Ala Pro
130 135 140
Ser Val Tyr Pro Leu Ala Pro Val Cys Gly Asp Thr Thr Gly Ser Ser
145 150 155 160
Val Thr Leu Gly Cys Leu Val Lys Gly Tyr Phe Pro Glu Pro Val Thr
165 170 175
Leu Thr Trp Asn Ser Gly Ser Leu Ser Ser Gly Val His Thr Phe Pro
180 185 190
Ala Val Leu Gln Ser Asp Leu Tyr Thr Leu Ser Ser Ser Val Thr Val
195 200 205
Thr Ser Ser Thr Trp Pro Ser Gln Ser Ile Thr Cys Asn Val Ala His
210 215 220
Pro Ala Ser Ser Thr Lys Val Asp Lys Lys Ile Glu Pro Arg Gly Pro
225 230 235 240
Thr Ile Lys Pro Cys Pro Pro Cys Lys Cys Pro Ala Pro Asn Leu Leu
245 250 255
Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Ile Lys Asp Val Leu
260 265 270
Met Ile Ser Leu Ser Pro Ile Val Thr Cys Val Val Val Asp Val Ser
275 280 285
Glu Asp Asp Pro Asp Val Gln Ile Ser Trp Phe Val Asn Asn Val Glu
290 295 300
Val His Thr Ala Gln Thr Gln Thr His Arg Glu Asp Tyr Asn Ser Thr
305 310 315 320
Leu Arg Val Val Ser Ala Leu Pro Ile Gln His Gln Asp Trp Met Ser
325 330 335
Gly Lys Glu Phe Lys Cys Lys Val Asn Asn Lys Asp Leu Pro Ala Pro
340 345 350
Ile Glu Arg Thr Ile Ser Lys Pro Lys Gly Ser Val Arg Ala Pro Gln
355 360 365
Val Tyr Val Leu Pro Pro Pro Glu Glu Glu Met Thr Lys Lys Gln Val
370 375 380
Thr Leu Thr Cys Met Val Thr Asp Phe Met Pro Glu Asp Ile Tyr Val
385 390 395 400
Glu Trp Thr Asn Asn Gly Lys Thr Glu Leu Asn Tyr Lys Asn Thr Glu
405 410 415
Pro Val Leu Asp Ser Asp Gly Ser Tyr Phe Met Tyr Ser Lys Leu Arg
420 425 430
Val Glu Lys Lys Asn Trp Val Glu Arg Asn Ser Tyr Ser Cys Ser Val
435 440 445
Val His Glu Gly Leu His Asn His His Thr Thr Lys Ser Phe Ser Arg
450 455 460
Thr Pro Gly
465
<210> 11
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетическая
6xHis метка
<400> 11
His His His His His His
1 5
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛА ПРОТИВ MICA/B, БЛОКИРУЮЩИЕ ШЕДДИНГ MICA/B, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2815101C2 |
| АНТИТЕЛО MICA С СОЗРЕВАНИЕМ АФФИННОСТИ И ЕГО ПРИМЕНЕНИЕ | 2024 |
|
RU2838565C1 |
| СВЯЗЫВАЮЩИЕ MICA АГЕНТЫ | 2013 |
|
RU2656183C2 |
| АНТИТЕЛА К ЧЕЛОВЕЧЕСКОМУ NKG2D И ИХ ПРИМЕНЕНИЯ | 2008 |
|
RU2563343C2 |
| ЧЕЛОВЕЧЕСКИЕ АНТИТЕЛА К ТОКСИНАМ CLOSTRIDIUM DIFFICILE | 2013 |
|
RU2628305C2 |
| Моноклональное антитело, которое специфически связывается с GITR | 2019 |
|
RU2734432C1 |
| Белок, связанный с гликопротеином человека, композиция, фармацевтическая композиция, вектор экспрессии | 2016 |
|
RU2773819C2 |
| Анти-LAG-3 антитела | 2016 |
|
RU2760582C2 |
| БЕЛКИ, СВЯЗЫВАЮЩИЕ ВСМА, NKG2D И CD16 | 2018 |
|
RU2805254C2 |
| АНТИТЕЛА, НАПРАВЛЕННЫЕ К БЕЛКУ ЗАПРОГРАММИРОВАННОЙ ГИБЕЛИ КЛЕТКИ-1 (PD-1) | 2014 |
|
RU2723050C2 |
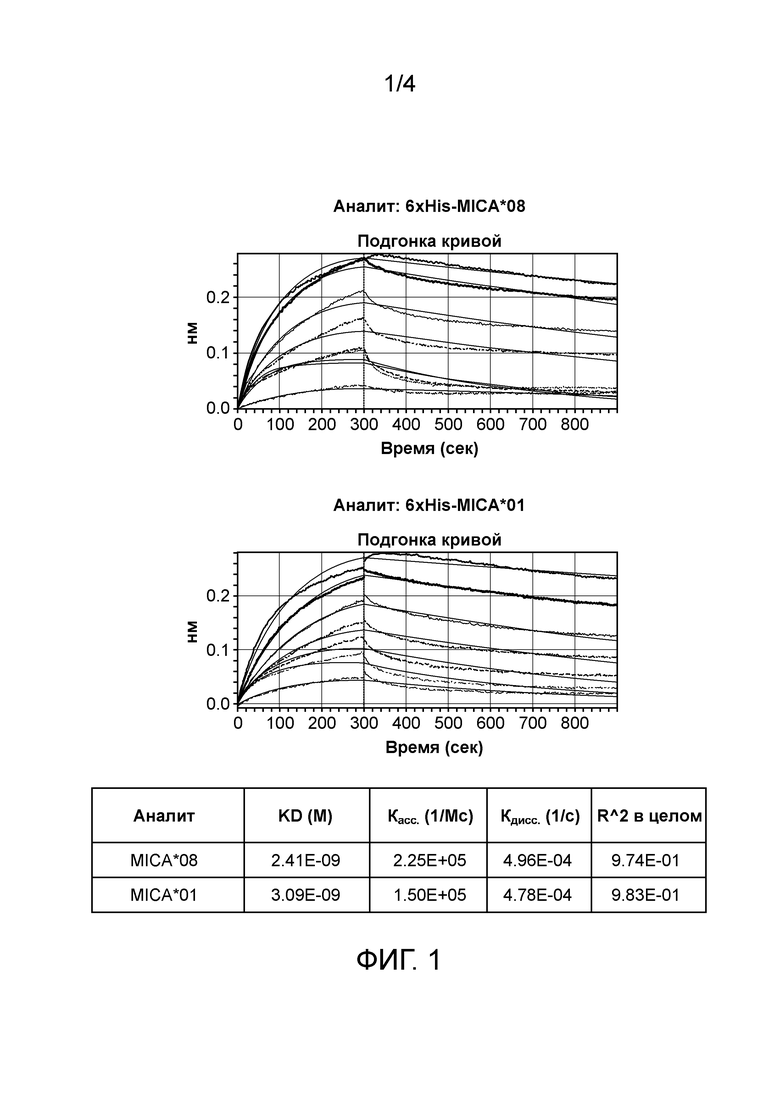
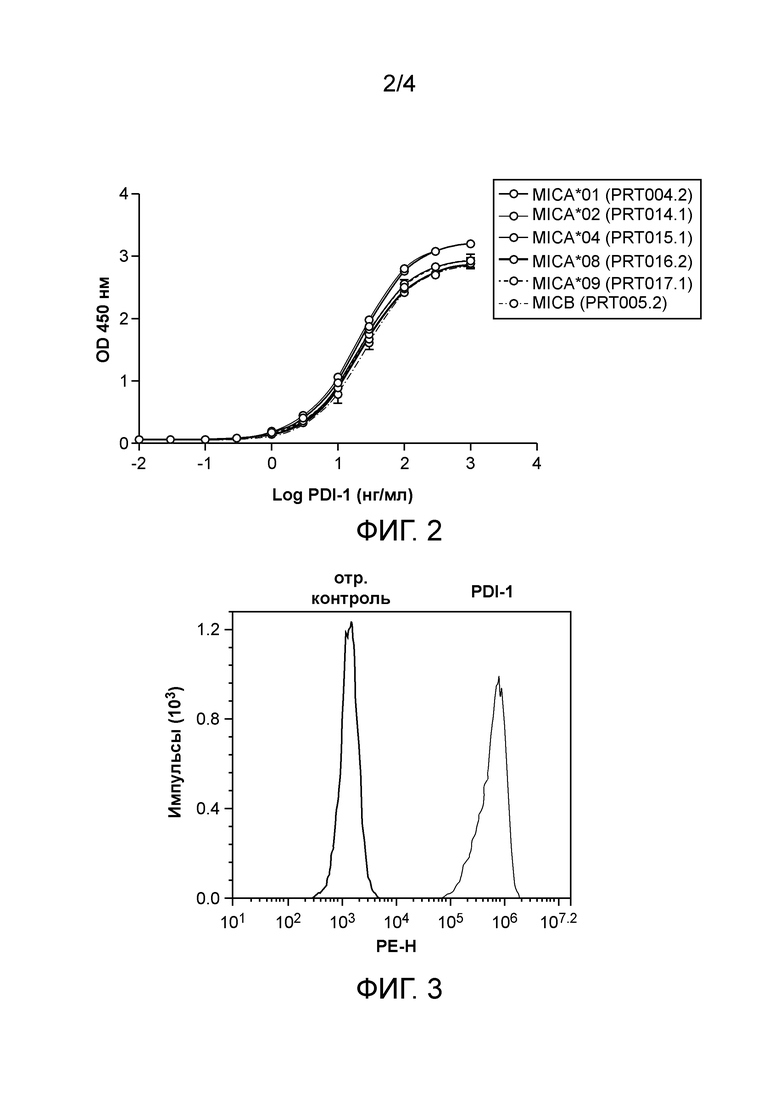
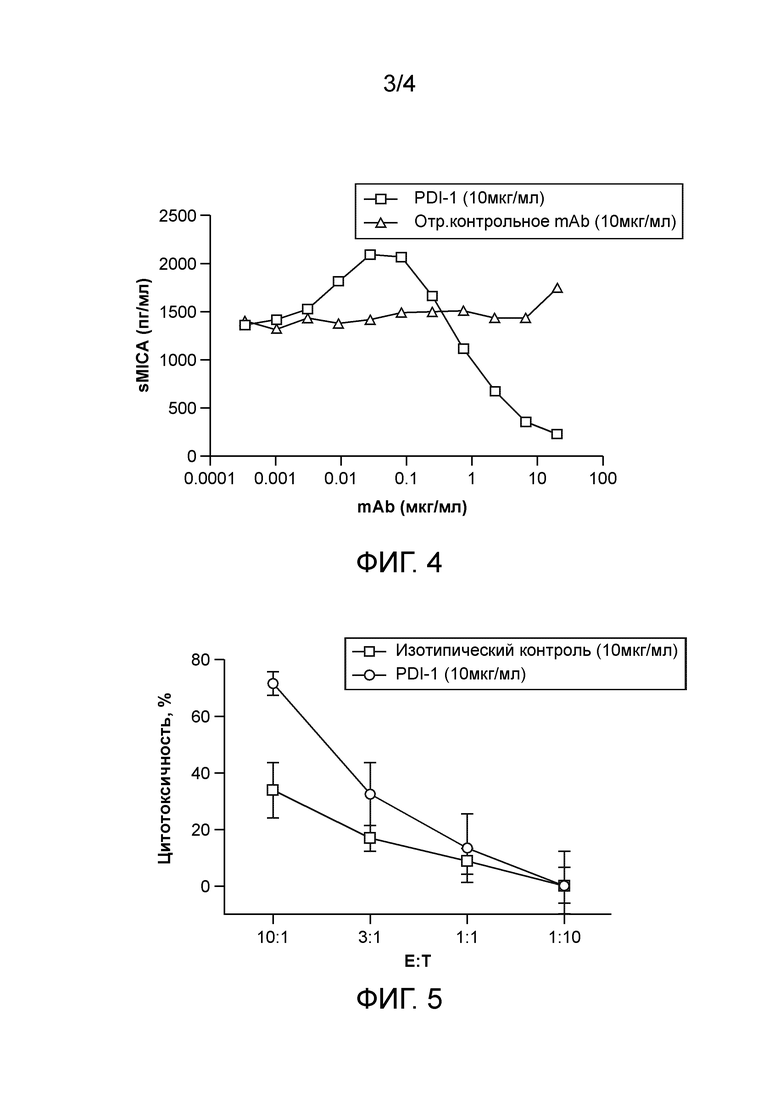
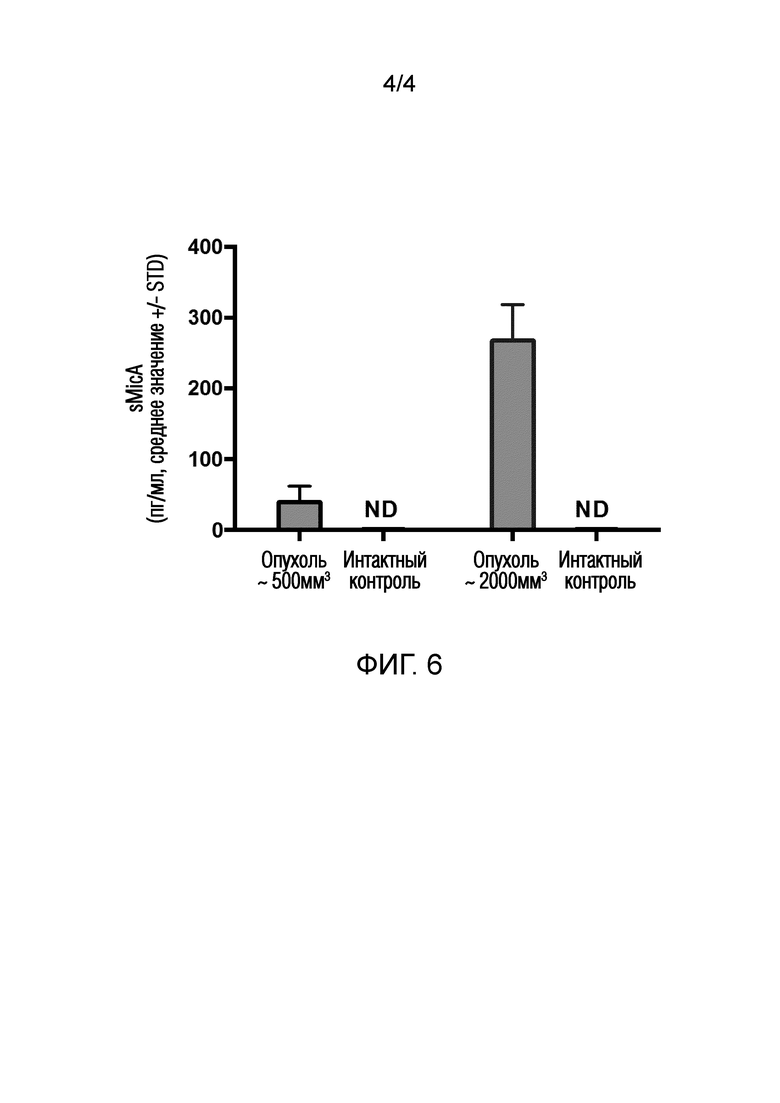
Изобретение относится к области биохимии, в частности к моноклональному антителу или его антигенсвязывающему фрагменту, которые связываются с MICA/B. Также раскрыта фармацевтическая композиция, содержащая указанное антитело. Раскрыто применение указанного антитела в способе лечения рака, связанного с экспрессией MICA/B. Изобретение позволяет эффективно лечить рак, который связан с экспрессией MICA/B. 3 н. и 5 з.п. ф-лы, 7 пр., 1 табл., 6 ил.
1. Моноклональное антитело или его антигенсвязывающий фрагмент, которые связываются с MICA/B, содержащие
последовательность определяющей комплементарность области 1 легкой цепи (CDR1), содержащую аминокислотную последовательность SEQ ID NO: 1, последовательность определяющей комплементарность области 2 легкой цепи (CDR2), содержащую аминокислотную последовательность SEQ ID NO: 2, и последовательность определяющей комплементарность области 3 легкой цепи (CDR3), содержащую аминокислотную последовательность SEQ ID NO: 3,
где моноклональное антитело или его антигенсвязывающий фрагмент содержит легкую цепь, которая не имеет аминокислотной последовательности SEQ ID NO: 9; или
где моноклональное антитело или его антигенсвязывающий фрагмент содержит тяжелую цепь, которая не имеет аминокислотной последовательности SEQ ID NO: 10, и
при этом моноклональное антитело или его антигенсвязывающий фрагмент содержит последовательность определяющей комплементарность области 1, тяжелой цепи (CDR1), содержащую аминокислотную последовательность SEQ ID NO: 4, последовательность определяющей комплементарность области 2 тяжелой цепи (CDR2), содержащую аминокислотную последовательность SEQ ID NO: 5, и последовательность определяющей комплементарность области 3 тяжелой цепи (CDR3), содержащую аминокислотную последовательность SEQ ID NO: 6.
2. Моноклональное антитело или его антигенсвязывающий фрагмент по п.1, где VL содержит аминокислотную последовательность SEQ ID NO:7.
3. Моноклональное антитело или его антигенсвязывающий фрагмент по п.1 или 2, где VH содержит аминокислотную последовательность SEQ ID NO:8.
4. Моноклональное антитело по любому из пп.1-3, где:
моноклональное антитело или его антигенсвязывающий фрагмент специфически связываются с белком MICA, белком MICB или как с белком MICA, так и с белком MICB;
моноклональное антитело или его антигенсвязывающий фрагмент связываются с альфа-3 доменом белка MICA, белка MICB или как белка MICA, так и белка MICB;
моноклональное антитело или его антигенсвязывающий фрагмент выбраны из полноразмерного иммуноглобулина, scFv, Fab, F(ab’)2 или Fv, связанного дисульфидной связью;
моноклональное антитело или его антигенсвязывающий фрагмент представляет собой IgG или IgM; и/или
моноклональное антитело или его фрагмент являются гуманизированными или химерными;
где:
белок MICA представляет собой мембраносвязанный белок MICA, растворимый белок MICA или оба варианта; или
белок MICB представляет собой мембраносвязанный белок MICB, растворимый белок MICB или оба варианта.
5. Фармацевтическая композиция для лечения заболевания или расстройства, связанного с экспрессией MICA/B, содержащая моноклональное антитело или его антигенсвязывающий фрагмент по любому из пп.1-4 и фармацевтически приемлемый носитель или эксципиент.
6. Применение моноклонального антитела или его антигенсвязывающего фрагмента по п. 1 или 4 в способе лечения рака, связанного с экспрессией MICA/B, у индивида, нуждающегося в этом.
7. Применение по п.6, где:
(а) (i) больной страдает раком с повышенным уровнем растворимого белка MICA, растворимого белка MICB или обоих этих белков;
(ii) моноклональное антитело или его антигенсвязывающий фрагмент снижает уровень растворимого белка MICA, растворимого белка MICB или обоих этих белков; или
(iii) моноклональное антитело или его антигенсвязывающий фрагмент ингибирует шеддинг растворимого белка MICA, растворимого белка MICB или обоих этих белков; и/или
(b) рак представляет собой гепатоцеллюлярную карциному.
8. Моноклональное антитело или его антигенсвязывающий фрагмент по любому из пп.1-4 для применения в лечении рака, связанного с экспрессией MICA/B, у больного, необязательно, где рак представляет собой гепатоцеллюлярную карциному.
| WO 2017221072 A2, 28.12.2017 | |||
| WO 2017096374 A1, 08.06.2017 | |||
| US 8414885 B2, 09.04.2013 | |||
| ПРИМЕНЕНИЕ ИНГИБИТОРОВ NKG2D ДЛЯ ЛЕЧЕНИЯ СЕРДЕЧНО-СОСУДИСТЫХ И МЕТАБОЛИЧЕСКИХ ЗАБОЛЕВАНИЙ, ТАКИХ КАК ДИАБЕТ 2 ТИПА | 2010 |
|
RU2566264C2 |
Авторы
Даты
2024-06-17—Публикация
2019-01-24—Подача