Область техники
[0001]
Настоящее изобретение относится к антителу, которое связывается с EphA4, нуклеиновой кислоте, которая кодирует это антитело, вектору, который содержит нуклеиновую кислоту, клетке, содержащей вектор, способу получения антитела и к фармацевтической композиции, содержащей это антитело.
Уровень техники
[0002]
EphA4 является представителем семейства рецепторных тирозинкиназ. Эфрины типа A и типа B известны как лиганды для EphA4, и при связывании EphA4 с эфрином, который является его лигандом, подается сигнал деадгезии. До сих пор предполагалось участие EphA4 в патологии болезни Альцгеймера (далее также называемой "AD") (непатентные литературные источники 1-4) и сообщалось, что ингибирование связывания между EphA4 и эфрином спасает от опосредованной амилоидным β (Aβ)(1-42) олигомером дисфункции передачи нервных импульсов (патентный литературный источник 1). Считается, что при AD гибель нервных клеток происходит с участием агрегатов (нейрофибриллярных клубков), образованных чрезмерно фосфорилированным тау-белком (непатентный литературный источник 5), а также сообщалось, что супрессия фосфорилирования тау-белка супрессирует нейродегенерацию в форме исчезновения синапсов (непатентный литературный источник 6 и непатентный литературный источник 7), а также снижает нарушения памяти или когнитивную дисфункцию (непатентный литературный источник 8-11). Имеются публикации, в которых высказано предположение, что причиной фосфорилирования тау-белка является активация CDK5 (непатентный литературный источник 12 и непатентный литературный источник 13). Генетически модифицированная мышь, экспрессирующая мутацию P301L, которая была обнаружена при наследственной лобно-височной деменции (мышь rTg4510), является мышиной моделью AD и так же, как при AD, у мыши обнаружено гиперфосфорилирование тау-белка и аномальное накопление тау-белка в нейронах. У мыши rTg4510 образуются нейрофибриллярные клубки, что является патологическим признаком AD, и это вызывает когнитивную дисфункцию из-за атрофии головного мозга и утраты нейронов (непатентный литературный источник 14 и непатентный литературный источник 5).
[0003]
EphA4 обильно экспрессируется в гиппокампе или коре головного мозга и расщепляется в зависимости от нервной активности матриксной металлопротеиназой (MMP), ADAM (дезинтегрин и металлопротеиназа) и γ-селектазой. Известно, что такая реакция расщепления EphA4 стабилизирует спинной мозг, который является ключевой структурой в функционировании нервной системы (непатентный литературный источник 15). Сообщалось, что при AD снижается плотность спинного мозга (непатентный литературный источник 16), и поскольку при AD на стадиях V и VI NFT также подтверждено уменьшение количества расщепленных фрагментов EphA4, считается, что в патологии AD задействована реакция расщепления EphA4 (непатентный литературный источник 17).
[0004]
И хотя в качестве существующих средств, ингибирующих EphA4, известны пептид KYL и соединение 1 и т.д. (патентный литературный источник 2, непатентный литературный источник 18 и непатентный литературный литература 19), до сих пор не было публикаций об антителах, обладающих активностью, которая усиливает расщепление EphA4.
Перечень цитируемой литературы
[0005]
[Патентный литературный источник 1] WO2016/019280A1.
[Патентный литературный источник 2] WO2012/156351A1.
[0006]
[Непатентный литературный источник 1] Vargas LM et al., PLoS One. 2014 Mar 21; 9 (3).
[Непатентный литературный источник 2] Fu AK et al., Proc Natl Acad Sci U S A. 2014 Jul 8; 111 (27): 9959-64.
[Непатентный литературный источник 3] Rosenberger AF et al., Acta Neuropathol Commun. 2014 Jul 16; 2: 79.
[Непатентный литературный источник 4] Huang TY et al., J Exp Med. 2017 Dec 4; 214 (12): 3669-3685.
[Непатентный литературный источник 5] Santa Cruz et al., Science. 2005 Jul 15; 309 (5733): 476-81.
[Непатентный литературный источник 6] Seo J et al., J Neurosci. 2017 Oct 11; 37 (41): 9917-9924.
[Непатентный литературный источник 7] Patrick GN et al., Nature. 1999 Dec 9; 402 (6762): 615-22.
[Непатентный литературный источник 8] Onishi T et al., J Neurochem. 2011 Dec; 119 (6): 1330-40.
[Непатентный литературный источник 9] Belfiore R et al., Aging Cell. 2019 Feb; 18 (1): e12873.
[Непатентный литературный источник 10] Webster SJ et al., Front Genet. 2014 Apr 23; 5: 88.
[Непатентный литературный источник 11] Grayson B et al., Behav Brain Res. 2015 May 15; 285: 176-93.
[Непатентный литературный источник 12] Cancino GI et al., Neurobiol Aging. 2011 Jul; 32 (7): 1249-61.
[Непатентный литературный источник 13] Vargas LM et al., Biochim Biophys Acta Mol Basis Dis. 2018 Apr; 1864: 1148-1159.
[Непатентный литературный источник 14] Ramsden M et al., J Neurosci. 2005 Nov 16; 25 (46): 10637-47.
[Непатентный литературный источник 15] Inoue E et al., J Cell Biol. 2009 May 4; 185 (3): 551-64.
[Непатентный литературный источник 16] Boros et al., Ann Neurol. 2017 Oct; 82 (4): 602-614.
[Непатентный литературный источник 17] Matsui C et al., Brain Pathol. 2012 Nov; 22 (6): 776-87. doi: 10.1111/j.1750-3639.
[Непатентный литературный источник 18] Goldshmit et al., PLoS one. 2011; 6 (9): e24636.
[Непатентный литературный источник 19] Van Hoecke et al., Nature Medicine. 2012 Sep; 18 (9): 1418-22,2012.
Краткое описание изобретения
Задачи, решаемые с помощью настоящего изобретения
[0007]
Целью настоящего изобретения является получение антитела к EphA4, которое может связываться с EphA4 и усиливать расщепление EphA4, а также создание фармацевтической композиции, содержащей антитело в качестве активного ингредиента.
Средства для решения задач
[0008]
В результате широкого исследования с целью поиска решения вышеуказанных проблем авторы настоящего изобретения получили моноклональное антитело мыши к EphA4, которое может связываться с EphA4 и усиливать расщепление EphA4, и получили гуманизированное антитело к антителу, получив таким образом окончательное антитело, представляющее интерес.
[0009]
Настоящее изобретение охватывает следующие отличительные признаки.
(1) Антитело к EphA4, где
антитело к EphA4 содержит тяжелую и легкую цепи, а также содержит:
(a) CDR1 тяжелой цепи, состоящую из аминокислотной последовательности, показанной под SEQ ID NO: 44;
(b) CDR2 тяжелой цепи, состоящую из аминокислотной последовательности, показанной под SEQ ID NO: 27;
(c) CDR3 тяжелой цепи, состоящую из аминокислотной последовательности, показанной под SEQ ID NO: 28;
(d) CDR1 легкой цепи, состоящую из аминокислотной последовательности, показанной под SEQ ID NO: 29;
(e) CDR2 легкой цепи, состоящую из аминокислотной последовательности, показанной под SEQ ID NO: 30; и
(f) CDR3 легкой цепи, состоящую из аминокислотной последовательности, показанной под SEQ ID NO: 31.
[0010]
(2) Антитело к EphA4 в соответствии с пунктом (1), где антитело к EphA4 является гуманизированным.
[0011]
(3) Антитело к EphA4 в соответствии с пунктами (1) или (2), где антитело к EphA4 специфически связывается с EphA4 и усиливает расщепление EphA4.
[0012]
(4) Антитело к EphA4 в соответствии с любым из пунктов (1) - (3), где антитело к EphA4 специфически связывается с EphA4 и ингибирует связывание между EphA4 и эфрином.
[0013]
(5) Антитело к EphA4 в соответствии с любым из пунктов (1) - (4), где
вариабельная область тяжелой цепи состоит из аминокислотной последовательности, показанной под SEQ ID NO: 45, и
вариабельная область легкой цепи состоит из аминокислотной последовательности, показанной под SEQ ID NO: 46.
[0014]
(6) Антитело к EphA4 в соответствии с любым из пунктов (1) - (5), где
константная область тяжелой цепи и константная область легкой цепи содержат аминокислотные последовательности, полученные из человеческого антитела.
[0015]
(7) Антитело к EphA4 в соответствии с пунктом (6), где
константная область тяжелой цепи представляет собой константную область человеческого IgG.
[0016]
(8) Антитело к EphA4 в соответствии с пунктом (7), где
константная область человеческого IgG представляет собой константную область человеческого IgG2.
[0017]
(9) Антитело к EphA4 в соответствии с пунктом (8), где
константная область человеческого IgG2 содержит аминокислотную последовательность, показанную под SEQ ID NO: 47.
[0018]
(10) Антитело к EphA4 в соответствии с любым из пунктов (6) - (9), где
константная область легкой цепи представляет собой константную область человеческого Igκ.
[0019]
(11) Антитело к EphA4 в соответствии с пунктом (10), где
константная область человеческого Igκ содержит аминокислотную последовательность, показанную под SEQ ID NO: 48.
[0020]
(12) Антитело к EphA4, где
антитело к EphA4 содержит тяжелую и легкую цепи,
тяжелая цепь содержит аминокислотную последовательность, показанную под SEQ ID NO: 59, и
легкая цепь содержит аминокислотную последовательность, показанную под SEQ ID NO: 60.
[0021]
(13) Антитело к EphA4 в соответствии с пунктом (12), где
С-концевой лизин тяжелой цепи удален.
[0022]
(14) Антитело к EphA4, где
антитело к EphA4 содержит тяжелую и легкую цепи,
тяжелая цепь содержит аминокислотную последовательность, показанную под SEQ ID NO: 59,
легкая цепь содержит аминокислотную последовательность, показанную под SEQ ID NO: 60, и
С-концевой лизин тяжелой цепи удален.
[0023]
(15) Выделенная нуклеиновая кислота, кодирующая антитело к EphA4 в соответствии с любым из пунктов (1) - (14).
[0024]
(16) Вектор, содержащий нуклеиновую кислоту в соответствии с пунктом (15).
[0025]
(17) Клетка-хозяин, содержащая вектор в соответствии с пунктом (16).
[0026]
(18) Способ получения антитела к EphA4, предусматривающий стадию культивирования клетки-хозяина в соответствии с пунктом (17).
[0027]
(19) Фармацевтическая композиция, содержащая антитело к EphA4 в соответствии с любым из пунктов (1) - (14).
[0028]
(20) Фармацевтическая композиция в соответствии с пунктом (19), где фармацевтическая композиция содержит по меньшей мере один фармацевтически приемлемый носитель.
[0029]
(21) Фармацевтическая композиция в соответствии с пунктами (19) или (20) для лечения болезни Альцгеймера.
[0030]
(22) Антитело к EphA4 в соответствии с любым из пунктов (1) - (14) для применения в лечении болезни Альцгеймера.
[0031]
(23) Способ лечения болезни Альцгеймера, предусматривающий введение пациенту, нуждающемуся в этом, терапевтически эффективного количества антитела к EphA4 в соответствии с любым из пунктов (1) - (14).
[0032]
(24) Применение антитела к EphA4 в соответствии с любым из пунктов (1) - (14) для изготовления фармацевтической композиции для лечения болезни Альцгеймера.
[0033]
(25) Фармацевтическая композиция в соответствии с пунктами (19) или (20) для лечения таупатии.
[0034]
(26) Антитело к EphA4 в соответствии с любым из пунктов (1) - (14) для применения в лечении таупатии.
[0035]
(27) Способ лечения таупатии, предусматривающий введение пациенту, нуждающемуся в этом, терапевтически эффективного количества антитела к EphA4 в соответствии с любым из пунктов (1) - (14).
[0036]
(28) Применение антитела к EphA4 в соответствии с любым из пунктов (1) - (14) для изготовления фармацевтической композиции для лечения таупатии.
[0037]
(29) Фармацевтическая композиция, антитело к EphA4, способ лечения или применение в соответствии с любым из пунктов (25) - (28), где таупатия представляет собой болезнь Альцгеймера или лобно-височную долевую дегенерацию с патологией тау-белка.
[0038]
(30) Фармацевтическая композиция, антитело к EphA4, способ лечения или применение в соответствии с (29), где таупатия представляет собой болезнь Альцгеймера.
[0039]
(31) Фармацевтическая композиция, антитело к EphA4, способ лечения или применение в соответствии с пунктом (29), где таупатия представляет собой лобно-височную долевую дегенерацию с патологией тау-белка.
[0040]
(32) Фармацевтическая композиция, антитело к EphA4, способ лечения или применение в соответствии с пунктом (31), где лобно-височная долевая дегенерация с патологией тау-белка представляет собой прогрессирующий надъядерный паралич, кортикобазальную дегенерацию, деменцию с аргирофильными зернами, старческую деменцию по типу нейрофибриллярного клубка или болезнь Пика.
[0041]
(33) Фармацевтическая композиция, антитело к EphA4, способ лечения или применение в соответствии с пунктом (32), где лобно-височная долевая дегенерация с патологией тау-белка представляет собой прогрессирующий надъядерный паралич.
[0042]
(34) Фармацевтическая композиция, антитело к EphA4, способ лечения или применение в соответствии с пунктом (32), где лобно-височная долевая дегенерация с патологией тау-белка представляет собой кортикобазальную дегенерацию.
[0043]
(35) Фармацевтическая композиция, антитело к EphA4, способ лечения или применение в соответствии с пунктом (32), где лобно-височная долевая дегенерация с патологией тау-белка представляет собой деменцию с аргирофильными зернами.
[0044]
(36) Фармацевтическая композиция, антитело к EphA4, способ лечения или применение в соответствии с пунктом (32), где лобно-височная долевая дегенерация с патологией тау-белка представляет собой старческую деменцию по типу нейрофибриллярного клубка.
[0045]
(37) Фармацевтическая композиция, антитело к EphA4, способ лечения или применение в соответствии с пунктом (32), где лобно-височная долевая дегенерация с патологией тау-белка представляет собой болезнь Пика.
Эффекты изобретения
[0046]
Настоящее изобретение относится к антителу к EphA4, которое может связываться с EphA4 и усиливать расщепление EphA4, нуклеиновой кислоте, которая кодирует антитело, вектору, который содержит нуклеиновую кислоту, клетке, содержащей вектор, способу получения антитела и к фармацевтической композиции, содержащей антитело в качестве активного ингредиента.
Краткое описание графических материалов
[0047]
На фигуре 1 показана аффинность связывания моноклонального антитела к EphA4 (антитела A) с EphA4 мыши и человека.
На фигуре 2 показана активность в отношении усиления расщепления EphA4 моноклональным антителом к EphA4 (антитело A) с использованием нейронов гиппокампа.
На фигуре 3 показана ингибирующая активность моноклонального антитела к EphA4 (антитело А) по отношению к мышиному лиганд-связывающему EphA4 мыши.
На фигуре 4 показана ингибирующая активность моноклонального антитела к EphA4 (антитело А) по отношению к человеческому лиганд-связывающему EphA4 человека.
На фигуре 5 показана селективность моноклонального антитела к EphA4 (антитела А) по отношению к каждому рецептору Eph человека.
На фигуре 6 показана селективность моноклонального антитела к EphA4 (антитела А) по отношению к каждому рецептору Eph мыши.
На фигуре 7 показана реактивность моноклонального антитела к EphA4 (антитела A) по отношению к EphA4 мыши, крысы, обезьяны и человека.
На фигуре 8 показана реактивность моноклонального антитела к EphA4 (антитело A) по отношению к внеклеточной области EphA4 человека (ECD), лиганд-связывающему домену (LBD), домену 1 фибронектина III типа (FN1) и домену 2 фибронектина III типа (FN2).
На фигуре 9 показан эффект моноклонального антитела к EphA4 (антитела А) в отношении увеличения количества шипов у нейрона гиппокампа.
На фигуре 10 показан эффект в отношении супрессии фосфорилирования тау-белка для моноклонального антитела к EphA4 in vivo.
На фигуре 11A по горизонтальной оси показаны аминокислоты лиганд-связывающего домена EphA4 (EphA4-LBD), а по вертикальной оси показана структурная область антитела A-Fab. Черными фрагментами показаны точки пересечения комбинаций, в которых присутствует взаимодействие.
На фигуре 11B показана структура поверхности лиганд-связывающего домена EphA4 (EphA4-LBD). На фигуре 11B названия аминокислот и номера остатков, содержащихся в связывающей области, показаны в соответствующих положениях, а CDR H-цепи и L-цепи связывающего антитела A-Fab показаны в виде ленточной модели.
На фигуре 12 показана аффинность гуманизированного моноклонального антитела к EphA4 (антитела B) к EphA4 человека.
На фигуре 13 для гуманизированного моноклонального антитела к EphA4 (антитела B) показана активность по отношению к усилению расщепления EphA4 в нейроне гиппокампа.
На фигуре 14 для гуманизированного моноклонального антитела к EphA4 (антитела B) показана ингибирующая активность по отношению к человеческому лиганд-связывающему домену EphA4 человека.
На фигуре 15 для гуманизированного моноклонального антитела к EphA4 (антитела B) показана ингибирующая активность по отношению к мышиному лиганд-связывающему EphA4 мыши.
На фигуре 16 показана селективность гуманизированного моноклонального антитела к EphA4 (антитела B) по отношению к рецептору Eph человека.
На фигуре 17 показана селективность гуманизированного моноклонального антитела к EphA4 (антитела B) по отношению к рецептору Eph мыши.
На фигуре 18 показана реактивность гуманизированного моноклонального антитела к EphA4 (антитела В) по отношению к EphA4 мыши, крысы, обезьяны и человека.
На фигуре 19 показана реактивность гуманизированного моноклонального антитела к EphA4 (антитело В) по отношению к внеклеточной области EphA4 человека (ECD), лиганд-связывающему домену (LBD), домену 1 фибронектина III типа (FN1) и домену 2 фибронектина III типа (FN2).
На фигуре 20 показан эффект гуманизированного моноклонального антитела к EphA4 (антитела А) в отношении увеличения количества шипов у нейрона гиппокампа.
На фигуре 21 для гуманизированного моноклонального антитела к EphA4 (антитела B) показана активность в отношении усиления расщепления EphA4 человека в нейроне гиппокампа.
На фигуре 22 показан эффект гуманизированного моноклонального антитела к EphA4 (антитела А) посредством MMP и ADAM в отношении увеличения количества шипов у нейрона гиппокампа.
На фигуре 23 показан эффект супрессии фосфорилирования тау-белка в отношении гуманизированного моноклонального антитела к EphA4 (антитела В) in vivo.
Описание вариантов осуществления
[0048]
Области, указанные или кодируемые с помощью SEQ ID NO: используются в данном документе следующим образом.
[0049]
Настоящее изобретение относится к антителу к EphA4, которое связывается с EphA4.
Антитело к EphA4 в соответствии с настоящим изобретением представляет собой антитело, которое может распознавать и связываться с EphA4, и, как описано ниже, антитело может представлять собой интактное антитело или может представлять собой синтетическое антитело (такое как рекомбинантное антитело, химерное антитело, гуманизированное антитело и т д.), при условии, что оно обладает аффинностью связывания с EphA4. Под EphA4 в данном документе можно понимать EphA4, полученный из человека, мыши, крысы и обезьяны. EphA4, полученный из человека, мыши, крысы и обезьяны, можно получить из общедоступной базы данных, в которой зарегистрирована информация о последовательностях, такой как Genbank, предоставленной Национальным центром биотехнологической информации США, или информацию о последовательности гена EphA4 можно получить с помощью конструирования праймеров на основе информации о нуклеотидной последовательности EphA4 близкородственного вида животного, а затем клонирования из РНК, выделенной из требуемого вида животного. Например, информация о нуклеотидных последовательностях EphA4 человека, мыши, крысы и обезьяны зарегистрирована в базе данных под номерами доступа Genbank NM_004438.5, NM_007936.3, NM_001162411.1 и NM_001260870.1 соответственно.
[0050]
В одном аспекте антитело к EphA4 представляет собой антитело, которое специфически связывается с EphA4. Термин "специфически связывающийся" представляет собой термин, хорошо известный специалистам в соответствующей области техники, а также хорошо известны способы определения специфического связывания между антителом или его антигенсвязывающим фрагментом и антигеном или эпитопом. В одном варианте осуществления "специфическое связывание" понимают как то, что антитело к EphA4 может связываться с EphA4 посредством иммунологической реакции с более высокой аффинностью связывания и активностью связывания, быстрее и/или на более длительный период времени по сравнению со связыванием с другими молекулами-мишенями. Это не означает, что антитело, которое специфически связывается с EphA4, не связывается с другими молекулами-мишенями. В другом варианте осуществления "специфическое связывание" может демонстрироваться антителом, имеющим KD относительно EphA4, составляющее по меньшей мере приблизительно 10-7 М, или по меньшей мере приблизительно 10-8 М, или по меньшей мере приблизительно 10-9 М, или меньше. Более того, в другом дополнительном варианте осуществления "специфическое связывание" понимают как связывание с EphA4 посредством иммунологической реакции, но практически без связывания с молекулами другого семейства рецептора Eph.
[0051]
В одном аспекте антитело к EphA4 представляет собой антитело, которое связывается с внеклеточной областью EphA4. В одном варианте осуществления антитело к EphA4 представляет собой антитело, которое связывается с лиганд-связывающим доменом (LBD) во внеклеточных областях EphA4.
[0052]
В одном варианте осуществления антитело к EphA4 может специфически связываться с EphA4 и усиливать расщепление EphA4. В конкретном варианте осуществления антитело к EphA4 может специфически связываться с EphA4 и усиливать расщепление внеклеточного домена EphA4 с помощью матриксной металлопротеиназы (ММР) или ADAM (дизинтегрина и металлопротеиназы).
[0053]
В одном варианте осуществления антитело к EphA4 может специфически связываться с EphA4 и ингибировать связывание между EphA4 и эфрином, который является его лигандом.
[0054]
В другом варианте осуществления антитело к EphA4 может специфически связываться с EphA4 и увеличивать количество шипов у нейрона гиппокампа или стабилизировать шипы у нейрона гиппокампа.
[0055]
В одном варианте осуществления настоящее изобретение охватывает антитело к EphA4, которое может специфически связываться с по меньшей мере одним из EphA4 человека, EphA4 мыши, EphA4 крысы и EphA4 обезьяны и ингибировать связывание с их лигандом. В другом варианте осуществления настоящее изобретение охватывает антитело к EphA4, которое может специфически связываться с двумя или более из EphA4 человека, EphA4 мыши, EphA4 крысы и EphA4 обезьяны и ингибировать связывание с их лигандом. В дополнительном варианте осуществления настоящее изобретение охватывает антитело к EphA4, которое может специфически связываться со всеми из EphA4 человека, EphA4 мыши, EphA4 крысы и EphA4 обезьяны и ингибировать связывание с их лигандом.
[0056]
Для способа измерения антигенсвязывающего свойства (такого как аффинность связывания и межвидовая реактивность) антитела к EphA4 можно применять способы, хорошо известные специалистам в соответствующей области техники. Например, аффинность связывания можно измерить с использованием без ограничения биосенсора Biacore™, биосенсора KinExA, сцинтилляционного анализа сближения, ELISA, иммуноанализа ORIGEN (IGEN), проточной цитометрии, гашения флуоресценции, флуоресценции метастаз, дрожжевого дисплея и/или иммуноокрашивания. Нейтрализующую активность антитела к EphA4 в отношении связывания между EphA4 и его лигандом можно измерить с использованием без ограничения биосенсора Biacore™, ELISA и/или проточной цитометрии.
[0057]
Антитело к EphA4 в соответствии с настоящим изобретением может представлять собой моноклональное антитело, при условии, что оно связывается с EphA4.
[0058]
Антитело к EphA4 в соответствии с настоящим изобретением может относиться к любому классу, такому как IgG, IgA или IgM (или их подклассам), и не ограничивается конкретным классом. Иммуноглобулины разделяют на различные классы в зависимости от аминокислотной последовательности константной области тяжелой цепи (может называться H-цепью) антитела. Существует пять основных классов иммуноглобулинов: IgA, IgD, IgE, IgG и IgM, некоторые из которых могут быть дополнительно разделены на подклассы (изотипы), например: IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2. Константные области тяжелой цепи, соответствующие различным классам иммуноглобулинов, называются α, δ, ε, γ и μ соответственно. Более того, легкая цепь (может называться L-цепью) антитела подразделяется на следующие типы: цепь λ и цепь κ. Антитело к EphA4 в соответствии с настоящим изобретением может представлять собой антитело IgG, например, может представлять собой антитело IgG1 или антитело IgG2 и т.п. Более того, антитело к EphA4 в соответствии с настоящим изобретением в некоторых случаях может быть в форме мономера, димера или мультимера.
[0059]
Вариабельная область антитела в соответствии с настоящим изобретением может означать вариабельную область легкой цепи антитела и/или вариабельную область тяжелой цепи антитела, и константная область антитела может означать константную область легкой цепи антитела и/или константную область тяжелой цепи антитела. Каждая из вариабельных областей тяжелой и легкой цепей состоит из четырех каркасных областей (FR), соединенных тремя CDR, также известными как области, определяющие комплементарность. CDR в каждой цепи удерживаются поблизости с помощью FR и вместе с CDR в другой цепи участвуют в образовании антигенсвязывающего участка в антителе. Технологии определения CDR предусматривают без ограничения, например, (1) подход, основанный на межвидовой вариабельности последовательностей (например, Kabat et al., Sequences of Proteins of Immunological Interest, 5th ed., 1991, National Institutes of Health, Bethesda MD); и (2) подход, основанный на исследовании кристаллической структуры комплексов антиген-антитело (Al-lazikani et al., 1997 J. Molec. Biol. 273: 927-948). Эти и другие подходы могут использоваться в комбинации.
[0060]
Моноклональное антитело в данном документе может означать антитело, полученное из популяции фактически однородных антител. Другими словами, отдельные антитела, содержащиеся в популяции, идентичны, за исключением естественных мутантов, которые возможно могут присутствовать в небольших количествах. Моноклональные антитела нацелены на отдельные антигенные участки и являются высокоспецифическими. Кроме того, в отличие от типичного поликлонального антитела, которое нацелено на разные антигены или разные эпитопы, каждое моноклональное антитело нацелено на один эпитоп антигена. Определение "моноклональное" указывает на свойство антитела, полученного из популяции фактически однородных антител, и оно не должно истолковываться как ограниченное необходимостью получения антител с помощью конкретного способа.
[0061]
Антитело к EphA4 в соответствии с настоящим изобретением может представлять собой мышиное антитело, химерное антитело или гуманизированное антитело. Химерное антитело представляет собой, например, антитело, в котором вариабельная область антитела, отличного от человеческого (как например, мыши или крысы), слита с константной областью человеческого антитела, и может относиться, например, к антителу, в котором вариабельная область получена из антитела, отличного от человеческого, и константная область получена из человеческого антитела. Гуманизированное антитело представляет собой, например, антитело, в котором область, определяющая комплементарность (CDR (также может называться гипервариабельной областью)), антитела, отличного от человеческого, введена в человеческое антитело, и, например, может относиться к антителу, в котором CDR получена из антитела, отличного от человеческого, и остальные области антитела получены из человеческого антитела. Следует отметить, что граница между химерным антителом и гуманизированным антителом не обязательно должна быть четкой, и антитело может находиться в состоянии, которое может называться химерным антителом или гуманизированным антителом. Более того, в химерном антителе или гуманизированном антителе область антитела, полученная из человеческого антитела (FR, константная область), не обязательно должна полностью состоять из аминокислот, полученных из человеческого антитела, а может содержать одну или несколько аминокислот, полученных из антитела, отличного от человеческого, при условии, что его можно обычно использовать в субъекте-человеке. Один вариант осуществления гуманизированного антитела представляет собой антитело, в котором CDR получена из антитела грызуна, а остальные области антитела получены из человеческого антитела. Конкретный вариант осуществления гуманизированного антитела представляет собой антитело, в котором CDR получены из мышиного антитела, а остальные области антитела получены из человеческого антитела. В таких вариантах осуществления CDR может содержать одну или несколько аминокислот, полученных из антитела, отличного от антитела грызуна, или одну или несколько аминокислот, полученных из антитела, отличного от мышиного, и области антитела, отличные от CDR, могут содержать одну или несколько аминокислот, полученных из антитела, отличного от человеческого. В данном документе "несколько" означает без ограничения 2-20 или 2-15, как например, 14, 13, 12, 11, 10, 9, 8, 7, 6, 5, 4, 3 или 2, или в пределах 10%, в пределах 9%, в пределах 8%, в пределах 7%, в пределах 6%, в пределах 5%, в пределах 4%, в пределах 3%, в пределах 2% или в пределах 1% от количества аминокислот в аминокислотной последовательности. Гуманизацию можно осуществлять с применением способа трансплантации CDR (Kontermann and Dubel, Antibody Engineering, Springer Lab Manual (2001) и Tsurushita et al., Methods 36: 69-83 (2005)) и дополнительно также можно осуществлять с помощью замены последовательности CDR на соответствующую последовательность в человеческом антителе с применением способов, хорошо известных в соответствующей области техники (см., например, Jones et al., Nature 321: 522-525 (1986); Riechmann et al., Nature 332: 323-327 (1988) и Verhoeyen et al., Science 239: 1534-1536 (1988)).
[0062]
Для снижения антигенности при получении гуманизированного антитела может быть важным выбрать использование человеческих вариабельных областей как в легких, так и в тяжелых цепях. В соответствии со способом "наилучшего соответствия" последовательность вариабельной области антитела грызуна подвергают скринингу в отношении всей библиотеки известных человеческих последовательностей FR. После этого человеческую последовательность, которая наиболее близка к последовательности грызуна, принимают за человеческую FR гуманизированного антитела. См., например, Sims et al., J. Immunol. 151: 2296-2308 (1993) и Chothia et al., J. Mol. Biol. 196: 901-917 (1987). В другом способе используют конкретную каркасную область, полученную из последовательности, общей для всех человеческих антител в конкретной подгруппе легкой или тяжелой цепей. Одну и ту же каркасную область можно использовать для нескольких различных гуманизированных антител. См., например Carter et al., Proc. Natl. Acad. Set USA 89: 4285-4289 (1992) и Presta et al., J. Immunol. 151: 2623-2632 (1993).
[0063]
Кроме того, в целом желательно, чтобы гуманизированное антитело сохраняло высокую аффинность связывания с антигеном и другие предпочтительные биологические свойства. С этой целью в соответствии с одним способом гуманизированные антитела получают с помощью стадии анализа исходной последовательности и различных концептуальных гуманизированных продуктов с использованием трехмерных моделей исходной и гуманизированной последовательностей. Как правило, доступны трехмерные модели иммуноглобулина, и они известны специалистам в данной области. Доступны компьютерные программы, которые иллюстрируют и представляют многообещающие трехмерные конформации выбранных последовательностей иммуноглобулинов-кандидатов. Исследование таких представлений даст возможность проанализировать возможные роли остатков в функциях последовательностей иммуноглобулинов-кандидатов, т. е. проанализировать остатки, которые влияют на способность иммуноглобулинов-кандидатов связываться со своими антигенами. С помощью такого способа остатки FR можно отобрать из последовательностей реципиента и импортированных последовательностей и использовать в комбинации для достижения требуемых свойств антитела, таких как повышение аффинности связывания с одним или несколькими антигенами-мишенями (такими как EphA4 или его фрагмент).
[0064]
Совершенно очевидно, что антителом к EphA4 в соответствии с настоящим изобретением также охватывается антитело с соответствующим изменением (таким как модификация антитела или частичная замена, добавление и/или делеция в аминокислотной последовательности антитела) в проиллюстрированном выше химерном или гуманизированном антителе с сохранением при этом функции антитела (или с добавлением или улучшением функции антитела). Более конкретно, в объем настоящего изобретения также входит антитело, имеющее изменение в аминокислотной последовательности константной области с целью модификации эффекторной функции антитела. Например, в объем настоящего изобретения также включено антитело, содержащее валин (Val) в положении 234 (нумерация Eu) человеческого антитела IgG2, замещенный на аланин (Ala), и содержащее глицин (Gly) в положении 237, замещенный на аланин (Ala), с целью уменьшения активности по типу антителозависимой клеточноопосредованной цитотоксичности (ADCC) и/или активности по типу антителозависимого клеточного фагоцитоза (ADCP) и т.д. Кроме того, в объемом настоящего изобретения также включено биспецифическое антитело, которое имеет антигенсвязывающий участок с последовательностью CDR антитела к EphA4 в соответствии с настоящим изобретением, вместе с антигенсвязывающим участком, который связывается с другим антигеном (Kontermann (2012), mAbs 4, 182-97).
[0065]
При необходимости, антитело к EphA4 в соответствии с настоящим изобретением может быть модифицировано. Модификация антитела к EphA4 может представлять собой модификацию, которая изменяет (а) трехмерную структуру аминокислотной последовательности в подлежащей модификации области, как например, конформация листа или спирали и т д.; (b) заряд или гидрофобное состояние молекулы в целевом участке или (c) эффект модификации в отношении поддержания объема боковой цепи, или может представлять собой модификацию, при которой эти изменения не являются четко выраженными.
[0066]
Модификацию антитела к EphA4 в соответствии с настоящим изобретением можно осуществить, например, с помощью замены, делеции, добавления и т.п. составных аминокислотных остатков.
[0067]
Аминокислота в данном документе используется в ее наиболее широком смысле и включает не только природные аминокислоты, такие как серин (Ser), аспарагин (Asn), валин (Val), лейцин (Leu), изолейцин (Ile), аланин (Ala), тирозин (Tyr), глицин (Gly), лизин (Lys), аргинин (Arg), гистидин (His), аспарагиновая кислота (Asp), глутаминовая кислота (Glu), глутамин (Gln), треонин (Thr), цистеин (Cys), метионин (Met), фенилаланин (Phe), триптофан (Trp) и пролин (Pro), но также и неприродные аминокислоты, такие как варианты и производные аминокислот. Специалистам в данной области, естественно, будет понятно с учетом данного широкого определения, что примеры аминокислот согласно настоящему описанию включают, например, L-аминокислоты; D-аминокислоты; химически модифицированные аминокислоты, такие как варианты аминокислот и производные аминокислот; аминокислоты, которые не будут белковыми компонентами в организме, такие как норлейцин, β-аланин и орнитин; и химически синтезированные соединения, обладающие аминокислотными свойствами, хорошо известными специалистам в данной области, и т.п. Примеры не встречающейся в природе аминокислоты могут включать, например, α-метиламинокислоты (такие как α-метилаланин), D-аминокислоты (такие как D-аспарагиновая кислота и D-глутаминовая кислота), гистидиноподобные аминокислоты (такие как 2-аминогистидин, β-гидроксигистидин, гомогистидин, α-фторметилгистидин и α-метилгистидин), аминокислоты с избытком метиленовых групп в боковой цепи ("гомо"-аминокислоты) и аминокислоты, в которых карбоксилатная функциональная группа в боковой цепи аминокислоты замещена сульфонатной группой (такие как цистеиновая кислота).
[0068]
Остатки встречающихся в природе аминокислот могут быть разделены на следующие группы на основании общих свойств боковой цепи:
(1) гидрофобные: Met, Ala, Val, Leu, Ile;
(2) нейтральные гидрофильные: Asn, Gln, Cys, Ser, Thr;
(3) кислые: Asp, Glu;
(4) основные: His, Lys, Arg;
(5) остатки, которые влияют на ориентацию цепи: Gly, Pro; и
(6) ароматические: Trp, Tyr, Phe.
[0069]
Неконсервативную замену аминокислотной последовательности, составляющей антитело, можно осуществить с помощью замены аминокислоты, принадлежащей одной из этих групп, на аминокислоту, принадлежащую другой группе. Более консервативную замену можно осуществить с помощью замены аминокислоты, принадлежащей к одной из этих групп, на другую аминокислоту в той же группе. Аналогично можно соответствующим образом осуществить делецию или замену в аминокислотной последовательности.
[0070]
Модификация аминокислот, придающих форму антителу, может представлять собой, например, гликозилирование углеводом или посттрансляционные модификации, такие как ацетилирование или фосфорилирование. Антитело может быть гликозилировано в консервативном положении в своей константной области. Гликозилирование антитела, как правило, является либо N-связанным, либо O-связанным. N-связанное означает связывание углеводной части с боковой цепью аспарагинового остатка. Трипептидные последовательности аспарагин-X-серин, аспарагин-X-треонин и аспарагин-X-цистеин (где X представляет собой любую аминокислоту, отличную от пролина) являются последовательностями распознавания для ферментативного добавления углеводной части к боковой цепи аспарагина. В случае если одна из этих трипептидных последовательностей присутствует в антителе, то присутствует потенциальный участок гликозилирования. O-связанное гликозилирование может представлять собой связывание N-ацетилгалактозамина, галактозы или ксилозы с гидроксиаминокислотой (такой как серин или треонин), и в некоторых случаях может представлять собой связывание с 5-гидроксипролином или 5-гидроксилизином. Специалисты в данной области в соответствии с требуемой целью смогут соответствующим образом подобрать условия гликозилирования (такие как тип клетки-хозяина или клеточной среды и pH и т.д., если гликозилирование производят с помощью биологических средств).
[0071]
Антитело к EphA4 в соответствии с настоящим изобретением может быть дополнительно модифицировано с помощью других способов модификации, отдельно или в комбинации, на основе общих технических сведений, хорошо известных специалистам в данной области.
[0072]
Антитело к EphA4 в соответствии с настоящим изобретением можно получить с помощью способа, хорошо известного специалистам в данной области. Например, антитело можно получить с помощью встраивания нуклеиновой кислоты, кодирующей антитело к EphA4 в соответствии с настоящим изобретением, в вектор экспрессии, введения вектора экспрессии в клетку-хозяина и культивирования клетки-хозяина. Соответственно, настоящее изобретение охватывает нуклеиновую кислоту, кодирующую антитело к EphA4, вектор, который содержит нуклеиновую кислоту, клетку-хозяина, содержащую вектор, и способ получения антитела к EphA4, предусматривающий стадию культивирования клетки-хозяина.
[0073]
Нуклеиновая кислота, кодирующая антитело к EphA4 в соответствии с настоящим изобретением, может содержать ДНК, кодирующую сигнальную последовательность, или может содержать ДНК, кодирующую сигнальную последовательность на 5'-конце ДНК, кодирующей вариабельную область тяжелой цепи, и ДНК, кодирующей вариабельную область легкой цепи. Сигнальная последовательность представляет собой аминокислотные остатки, присутствующие на N-конце белка, которые необходимы для секреторного белка или интегрального мембранного белка для прохождения через липидный бислой после синтеза на рибосоме, и в настоящем изобретения не имеет особых ограничений при условии, что она является последовательностью, которая обладает данной функцией. К сигнальным последовательностям, которые могут содержаться в антителе к EphA4 в соответствии с настоящим изобретением, относятся сигнальные последовательности, полученные от человека, мыши, крысы, кролика, осла, козы, лошади, птицы, собаки, кошки, дрожжей и т.д. В частности, в настоящем изобретении пептид, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 12 или 16, может быть включен в качестве сигнальной последовательности, относящейся к тяжелой цепи, и пептид, содержащий аминокислотную последовательность, представленную под SEQ ID NO: 14 или 18, может быть включен в качестве сигнальной последовательности, относящейся к легкой цепи. Более того, при условии, что она функционально эквивалентна, сигнальная последовательность может характеризоваться заменой, добавлением и/или делецией одной или нескольких (как например, 2, 3, 4 или 5) аминокислот в аминокислотной последовательности, представленной под SEQ ID NO: 12 или 16, и аминокислотной последовательности, представленной под SEQ ID NO: 14 или 18.
[0074]
Антитело к EphA4 в соответствии с настоящим изобретением могут быть выделены или очищены в соответствии со способом, хорошо известным специалистам в данной области.
[0075]
В данном документе "выделенный" или "очищенный" означает искусственно выделенный или очищенный из естественного состояния. Если молекула или композиция встречаются в природе, то они являются "выделенными" или "очищенными", в случае если ее изменили или удалили из исходной среды, или как первое, так и второе. Примеры способа выделения или очистки включают без ограничения способы посредством электрофореза, молекулярной биологии, иммунологии или хроматографии и т.д., в частности, ионообменную хроматографию, гидрофобную хроматографию, обращенно-фазовую HPLC-хроматографию, изоэлектрическое фокусирование или щелочной способ экстракции и т.п.
[0076]
В одном варианте осуществления антитело к EphA4 содержит следующие CDR:
(a) CDR1 тяжелой цепи, состоящую из аминокислотной последовательности, показанной под SEQ ID NO: 44;
(b) CDR2 тяжелой цепи, состоящую из аминокислотной последовательности, показанной под SEQ ID NO: 27;
(c) CDR3 тяжелой цепи, состоящую из аминокислотной последовательности, показанной под SEQ ID NO: 28;
(d) CDR1 легкой цепи, состоящую из аминокислотной последовательности, показанной под SEQ ID NO: 29;
(e) CDR2 легкой цепи, состоящую из аминокислотной последовательности, показанной под SEQ ID NO: 30; и
(f) CDR3 легкой цепи, состоящую из аминокислотной последовательности, показанной под SEQ ID NO: 31.
[0077]
В одном варианте осуществления антитело к EphA4 представляет собой гуманизированное антитело или химерное антитело, а в конкретном варианте осуществления - гуманизированное антитело.
[0078]
В другом варианте осуществления антитело к EphA4 содержит тяжелую и легкую цепи, при этом вариабельная область тяжелой цепи содержит аминокислотную последовательность, показанную под SEQ ID NO: 45, и вариабельная область легкой цепи содержит аминокислотную последовательность, показанную под SEQ ID NO: 46. Следует обратить внимание на то обстоятельство, что в варианте осуществления вариабельная область тяжелой цепи и/или вариабельная область легкой цепи могут содержать аминокислотную последовательность, в которой одна или несколько аминокислот заменены, добавлены и/или удалены в аминокислотной последовательности, показанной под SEQ ID NO: 45, и/или аминокислотной последовательности, показанной под SEQ ID NO: 46. В данном документе "несколько" не имеет ограничений при условии, что сохраняется аффинность связывания с EphA4 и усиливается расщепление EphA4, и обозначает 2-15 или 2-10, как например, 9, 8, 7, 6, 5, 4, 3 или 2, или в пределах 10%, как например, в пределах 9%, в пределах 8%, в пределах 7%, в пределах 6%, в пределах 5%, в пределах 4%, в пределах 3%, в пределах 2% или в пределах 1% от количества аминокислот в аминокислотной последовательности.
[0079]
В одном варианте осуществления тяжелая цепь антитела к EphA4 содержит константную область человеческого IgG2.
[0080]
В конкретном варианте осуществления константная область человеческого IgG2 содержит аминокислотную последовательность под SEQ ID NO: 47.
[0081]
В одном варианте осуществления легкая цепь антитела к EphA4 содержит константную область человеческого Igκ.
[0082]
В конкретном варианте осуществления константная область цепи κ человеческого Ig содержит аминокислотную последовательность под SEQ ID NO: 48.
[0083]
В одном варианте осуществления антитело к EphA4 содержит тяжелую цепь, содержащую аминокислотную последовательность, показанную под SEQ ID NO: 59, и легкую цепь, содержащую аминокислотную последовательность, показанную под SEQ ID NO: 60.
[0084]
В другом варианте осуществления, например, по таким причинам, как уменьшение однородности антител, продуцируемых антителопродуцирующими клетками (публикация патентной заявки США № 2010/0297697 или Liu H et al., MAbs. 2014 Sep-Oct; 6 (5): 1145-1154), у антитела к EphA4 удален лизин, расположенный на С-конце (карбокси-конце) тяжелой цепи. В настоящем изобретении антитело к EphA4 с удаленным С-концевым лизином тяжелой цепи, также включает антитело к EphA4 с удаленным С-концевым лизином тяжелой цепи, удаленный посредством генетической модификации, или антитело к EphA4 с удаленным С-концевым лизином тяжелой цепи, посттрансляционно отщепляемый карбоксипептидазой и т.д., и т.п. Более того, в настоящем изобретении антитело к EphA4 с удаленным С-концевым лизином тяжелой цепи, включает не только антитело к EphA4 с удаленным С-концевым лизином в обеих тяжелых цепях, но также и антитело к EphA4 с удаленным С-концевым лизином только в одной тяжелой цепи.
[0085]
В одном аспекте настоящее изобретение относится к выделенной нуклеиновой кислоте, кодирующей антитело к EphA4. Выделенная нуклеиновая кислота, кодирующая антитело к EphA4, относится к одной или нескольким молекулам нуклеиновой кислоты, кодирующим тяжелую цепь и/или легкую цепь антитела к EphA4. В одном варианте осуществления нуклеиновая кислота в соответствии с настоящим изобретением кодирует тяжелую цепь антитела к EphA4. В другом варианте осуществления нуклеиновая кислота в соответствии с настоящим изобретением кодирует легкую цепь антитела к EphA4. В другом дополнительном варианте осуществления нуклеиновая кислота в соответствии с настоящим изобретением кодирует тяжелую и легкую цепи антитела к EphA4. Нуклеиновая кислота в соответствии с настоящим изобретением также включает первую молекулу нуклеиновой кислоты, кодирующую тяжелую цепь антитела к EphA4, и вторую молекулу нуклеиновой кислоты, кодирующую легкую цепь антитела к EphA4.
[0086]
В другом аспекте настоящее изобретение относится к вектору, содержащему выделенную нуклеиновую кислоту, кодирующую антитело к EphA4. Вектор в соответствии с настоящим изобретением относится к одному или нескольким векторам, содержащим выделенную нуклеиновую кислоту, кодирующую антитело к EphA4. В одном варианте осуществления вектор в соответствии с настоящим изобретением представляет собой вектор, содержащий нуклеиновую кислоту, кодирующую тяжелую цепь антитела к EphA4, и нуклеиновую кислоту, кодирующую легкую цепь антитела к EphA4. В другом варианте осуществления вектор в соответствии с настоящим изобретением представляет собой вектор, содержащий нуклеиновую кислоту, кодирующую тяжелую и легкую цепи антитела к EphA4. В другом дополнительном варианте осуществления вектор в соответствии с настоящим изобретением содержит первый вектор, содержащий нуклеиновую кислоту, кодирующую тяжелую цепь антитела к EphA4, и второй вектор, содержащий нуклеиновую кислоту, кодирующую легкую цепь антитела к EphA4. Вектор в соответствии с настоящим изобретением может представлять собой без ограничения плазмиду, космиду, вирус, фаг и т.п. Например, в вектор в соответствии с настоящим изобретением также включены такие как вирусный вектор, вектор на основе ретровируса, лентивируса, аденовируса, аденоассоциированного вируса или вектор на основе вируса простого герпеса и т.п.
[0087]
В еще одном аспекте в настоящее изобретение также включены клетка-хозяин, содержащая вектор в соответствии с настоящим изобретением, и способ получения антитела к EphA4, предусматривающий стадию культивирования клетки-хозяина. Клетка-хозяин в соответствии с настоящим изобретением может представлять собой без ограничения клетки E. coli, клетки COS обезьяны, клетки яичника китайского хомячка (CHO), клетки NS0 и т.п. В одном варианте осуществления способ получения антитела к EphA4 предусматривает стадию культивирования клетки-хозяина и стадию выделения антитела к EphA4, секретируемого из клетки-хозяина (или культуральной среды клетки-хозяина).
[0088]
В одном аспекте настоящее изобретение относится к фармацевтической композиции, содержащей антитело к EphA4. Фармацевтическая композиция в соответствии с настоящим изобретением может быть изготовлена в соответствии с известными способами, такими как способы, описанные в Фармакопее Японии (JP), Фармакопее Соединенных штатов Америки(USP) или Европейской Фармакопее (EP) и т.п.
[0089]
Антитело к EphA4 в соответствии с настоящим изобретением может быть применимым для лечения болезни Альцгеймера. Другими словами, в других аспектах настоящее изобретение охватывает способ лечения болезни Альцгеймера, предусматривающий стадию введения терапевтически эффективного количества антитела к EphA4 субъекту, имеющему болезнь Альцгеймера. Более того, в других аспектах настоящее изобретение охватывает применение антитела к EphA4 для изготовления терапевтического лекарственного средства от болезни Альцгеймера. В других аспектах настоящее изобретение охватывает антитело к EphA4 для применения в лечении болезни Альцгеймера.
[0090]
Антитело к EphA4 в соответствии с настоящим изобретением может быть применимо для лечения таупатии. Другими словами, в других аспектах настоящее изобретение охватывает способ лечения таупатии, предусматривающий стадию введения терапевтически эффективного количества антитела к EphA4 субъекту, страдающему таупатией. Более того, в других аспектах настоящее изобретение охватывает применение антитела к EphA4 для изготовления терапевтического лекарственного средства от таупатии. В других аспектах настоящее изобретение охватывает антитело к EphA4 для применения в лечении таупатии. Таупатия по настоящему изобретению включает болезнь Альцгеймера или лобно-височную долевую дегенерацию с патологией тау-белка (FTLD-tau). Более того, к лобно-височной долевой дегенерации с патологией тау-белка относятся прогрессирующий надъядерный паралич (PSP), кортикобазальная дегенерация (CBD), деменция с аргирофильными зернами (AGD), старческая деменция по типу нейрофибриллярного клубка (SD-NFT), болезнь Пика (PiD) и др.
[0091]
Антитело к EphA4 в соответствии с настоящим изобретением можно использовать отдельно в терапевтическом способе или в комбинации с другими средствами или композициями. Например, антитело к EphA4 в соответствии с настоящим изобретением можно вводить в то же время или в разные моменты времени, что и другое средство. Такая комбинированная терапия предусматривает комбинированное введение (два или более средства включены в один и тот же или отдельный состав) и раздельное введение (такое как одновременное или последовательное). При раздельном введении двух или более средств введение антитела к EphA4 в соответствии с настоящим изобретением можно осуществлять до или после сопутствующего терапевтического способа.
[0092]
Предмет для введения фармацевтической композиции в соответствии с настоящим изобретением не ограничен и может использоваться, например, в отношении человека или отличного от человека млекопитающего (такого как обезьяна, мышь, крыса, кролик, корова, лошадь и коза).
[0093]
Способ введения фармацевтической композиции в соответствии с настоящим изобретением субъекту (как, например, путь введения, дозировка, количество введений в день и график введения) не ограничен и может быть соответствующим образом определен специалистами в данной области (такими как, врач) в зависимости от состояния здоровья субъекта, степени заболевания, типа средств, применяемых в комбинации, и т.п.
[0094]
Специалисты в данной области должны понимать, что до тех пор, пока это технически не противоречит, настоящее изобретение может быть реализовано в соответствующей комбинации с любым одним или несколькими из всех возможных аспектов, описанных в данном документе. Кроме того, специалисты в данной области должны понимать, что до тех пор, пока это технически не противоречит, предпочтительно, чтобы настоящее изобретение осуществлялось в соответствующей комбинации всех возможных предпочтительных или преимущественных аспектов, описанных в данном документе.
[0095]
Все раскрытия литературных источников, цитируемых в данном документе, следует рассматривать как четко процитированные в данном документе посредством ссылки, и специалисты в данной области смогут понять соответствующее содержание раскрытия в этих литературных источниках посредством упоминания их в качестве части настоящего описания в соответствии с контекстом данного документа без отступления от сути и объема настоящего изобретения.
[0096]
Литературные источники, цитируемые в данном документе, представлены исключительно с целью раскрытия состояния соответствующей технологии, предшествующего дате подачи настоящей заявки, и это не должно истолковываться как признание авторами настоящего изобретения того, что настоящее изобретение не имеет права считаться предшествующим указанным раскрытиям как более раннее изобретение или по любой другой причине. Все описание всех этих литературных источников основано на информации, доступной авторам настоящей заявки, и никоим образом не является признанием того, что содержание этих описаний является точным.
[0097]
Термины, используемые в данном документе, используются для описания конкретных вариантов осуществления и не предусмотрены для ограничения настоящего изобретения.
[0098]
Термин "содержать", используемый в данном документе, если содержание явно не означает, что подразумевается иное, означает наличие описываемых объектов (таких как компоненты, стадии, элементы или числа) и не исключает наличие других объектов (таких как компоненты, стадии, элементы и числа). Термин "состоять из" охватывает аспекты, описываемые терминами "состоять из" и/или "фактически состоять из".
[0099]
Используемый в данном документе термин "нейтрализующая активность" означает активность ингибирования связывания между EphA4 и его лигандом и/или активность ингибирования передачи сигнала, или реакции молекулярной экспрессии, или изменения функциональных свойств клеток, которые индуцируются EphA4 вследствие связывания с его лигандом в организме человека.
[0100]
Если не указано иное, то все термины, используемые в данном документе (в том числе технические и научные термины), имеют те же значения, которые широко известны специалистам в области технологии, к которой относится настоящее изобретение. Используемые в данном документе термины, если явно не указано иное, следует понимать, как имеющие значения, соответствующие значениям в данном документе и в соответствующих областях техники, и их не следует считать, как имеющие упрощенные или чрезмерно формальные значения.
[0101]
Такие термины, как первый и второй, используются для обозначения различных элементов, и следует понимать, что эти элементы не должны ограничиваться только этими терминами. Эти термины используются исключительно с целью установления различия между одним элементом и другим, и, например, можно описывать первый элемент как второй элемент и аналогичным образом описывать второй элемент как первый элемент без отступления от объема настоящего изобретения.
[0102]
Числовые значения, используемые в данном документе для указания содержания компонента или диапазона числовых значений и т.п., если явно не указано, следует понимать как модифицированные термином "приблизительно". Например, если явно не указано иное, то "4°C" следует понимать как "приблизительно 4°C", и очевидно, что специалисты в данной области смогут рационально понять его объем в соответствии с техническим здравым смыслом и значением представленных в данном документе частей текста.
[0103]
Следует понимать, что если четко не указано, что контекст подразумевает иное, то при использовании в данном документе в описании и формуле изобретения каждый аспект, представленный в форме единственного числа, также может иметь форму множественного числа, если это не является технически противоречивым, и наоборот.
[0104]
Далее настоящее изобретение будет подробно описано со ссылкой на примеры. Однако настоящее изобретение может быть осуществлено с помощью различных аспектов, и оно не должно истолковываться как ограниченное примерами, описанными в данном документе. Специалисты в соответствующей области смогут осуществить настоящее изобретение с различными модификациями, добавлениями, делециями, заменами и т.п. без изменения сути или объема настоящего изобретения.
Примеры
[0105]
Сравнительный пример 1. Получение моноклонального антитела к EphA4
(A) Получение моноклонального антитела мыши к EphA4
Для получения моноклонального антитела, связывающегося с EphA4 мыши (№ доступа в Genbank NP_031962.2, SEQ ID NO: 1), белок, содержащий секреторную щелочную фосфатазу (SEAP) и гистидиновую метку, слитый с внеклеточной областью EphA4 мыши (положения 20-547) (SEQ ID NO: 2) (в дальнейшем называемый "белок внеклеточной области-EphA4-SEAP-His мыши", SEQ ID NO: 3) получали с помощью следующих стадий.
[0106]
Сначала последовательности ДНК, кодирующие сигнальную последовательность (SEQ ID NO: 4) и внеклеточную область (SEQ ID NO: 2) EphA4 мыши, амплифицировали с помощью RT-PCR с общей РНК, полученной из головного мозга мыши, и клонировали в сайт Sal I/Not I вектора pENTR1A (Invitrogen/LifeTechnologies), имеющего последовательность ДНК, кодирующую SEAP и гистидиновую метку. Затем последовательность ДНК, кодирующую сигнальную последовательность и внеклеточную область EphA4 мыши, SEAP и гистидиновую метку, переносили в вектор pcDNA 3.1_rfcB с помощью LR-реакции с использованием системы Gateway (Invitrogen/LifeTechnologies) с конструированием вектора экспрессии pcDNA 3.1-внеклеточная область-EphA4-SEAP-His мыши. Сконструированный вектор экспрессии pcDNA 3.1-внеклеточной области-EphA4-SEAP-His мыши трансфицировали в клетки HEK293 EBNA (Invitrogen/LifeTechnologies) с помощью TransIT-LT1 (TAKARA). Через 6 дней инкубирования (5% CO2, 37°C) выделяли надосадочную жидкость культуры. Из выделенной надосадочной жидкости культуры белка внеклеточной области-EphA4-SEAP-His мыши (SEQ ID NO: 3) очищали с помощью колонки Protino (MACHEREY-NAGEL).
[0107]
Двадцать микрограмм белка внеклеточной области-EphA4-SEAP-His мыши смешивали с таким же количеством адъюванта TiterMax Gold (TiterMax, США) или адъюванта GERBU (GERBU Biotechnik GmbH) и подкожно вводили в подушечку стопы мышей Balb/c. Затем аналогичным образом вводили белок внеклеточной области-EphA4-SEAP-His мыши в дни 3, 7 и 10. В данном случае адъювант TiterMax Gold (TiterMax, США) использовали только в день 10, и адъювант GERBU (GERBU Biotechnik GmbH) использовали в дни 3, 7 и 10. Мышей умерщвляли в день 13 и выделяли периферические лимфатические узлы с получением клеток лимфатических узлов. Полученные клетки лимфатических узлов и клетки миеломы P3U1 (предоставленные Киотским университетом) сливали в соотношении 5:1 в присутствии GenomeONE-CF (Ishihara Sangyo Kaisha, Ltd.). Слитые клетки культивировали в 96-луночном пластиковом планшете. Через 7 дней инкубирования (5% CO2, 37°C) выделяли надосадочную жидкость культуры.
[0108]
При использовании полученной надосадочной жидкости культуры отбирали лунки, обладающие реактивностью по отношению к EphA4 мыши, крысы и человека.
[0109]
Реактивность по отношению к EphA4 мыши, крысы и человека оценивали с помощью ELISA с использованием белков, имеющих Fc-область человеческого IgG1 и гистидиновую метку, слитых с внеклеточной областью EphA4 мыши, внеклеточной областью (положения 20-547) EphA4 крысы (GenBank, № NP_001155883.1) или внеклеточной областью (положения 20-547) (SEQ ID NO: 6) EphA4 человека (№ доступа в Genbank NP_004429.1, SEQ ID NO: 5) (далее в данном документе обозначаемых как "белок внеклеточной области-EphA4-Fc-His мыши", "белок внеклеточной области-EphA4-Fc-His крысы" или "белок внеклеточной области-EphA4-Fc-His человека" соответственно).
[0110]
Белки внеклеточной области-EphA4-Fc-His мыши, крысы или человека получали с помощью следующих стадий. Первоначально конструировали векторы экспрессии внеклеточной области-EphA4-Fc-His pcDNA 3.1 мыши, крысы или человека. Сначала последовательности ДНК, кодирующие сигнальную последовательность и внеклеточную область EphA4 мыши, крысы или человека, амплифицировали с помощью RT-PCR с общей РНК, полученной из мозга мыши, крысы или человека, и клонировали в сайт Sal I/Not I вектора pENTR1A (Invitrogen/LifeTechnologies), содержащего последовательность ДНК, кодирующую Fc и гистидиновую метку. Затем последовательности ДНК, кодирующую сигнальную последовательность и внеклеточную область EphA4 мыши, крысы или человека, Fc и гистидиновую метку, переносили в вектор pcDNA 3.1_rfcB с помощью LR-реакции с использованием системы Gateway (Invitrogen/LifeTechnologies) с конструированием векторов экспрессии pcDNA 3.1-внеклеточной области-EphA4-Fc-His мыши, крысы или человека. Такие сконструированные векторы экспрессии трансфицировали в клетки HEK293 EBNA (Invitrogen/LifeTechnologies) с использованием TransIT-LT1 (TAKARA). Через 6 дней инкубирования (5% CO2, 37°C) выделяли надосадочную жидкость культуры.
[0111]
ELISA с использованием белков внеклеточной области-EphA4-Fc-His мыши, крысы или человека выполняли согласно приведенным ниже стадиям. Антителом к человеческому IgG (Jackson ImmunoResearch Laboratories) покрывали лунки 96-луночного планшета (Nunc). После инкубации при 4°C в течение ночи лунки блокировали при комнатной температуре в течение одного часа с помощью 1 x Block ACE (Dainippon Seiyaku). После трехкратного промывания с помощью 0,02% Tween 20/PBS (Nacalai Tesque) в каждую лунку добавляли надосадочную жидкость культуры, содержащую белок внеклеточной области-EphA4-Fc-His мыши, крысы или человека (конечная концентрация 1 нМ) и инкубировали ее при комнатной температуре в течение одного часа. После трехкратного промывания надосадочную жидкость культуры слитых клеток добавляли в каждую лунку. После инкубирования при комнатной температуре в течение одного часа и трехкратного промывания добавляли меченое пероксидазой хрена антитело к мышиному IgG (Jackson ImmunoResearch Laboratories) и эту смесь инкубировали при комнатной температуре в течение одного часа. После трехкратного промывания в каждую лунку добавляли раствор ™BZ (3,3',5,5'-тетраметилбензидин, Sigma) и инкубировали при комнатной температуре в течение 5-20 минут. В каждую лунку добавляли равное количество стоп-раствора (2 н. H2SO4, Wako Pure Chemical) и считывали поглощение при 450 нм с помощью считывающего устройства для микропланшетов (PerkinElmer).
[0112]
Клонировали из лунок гибридомы, собранные на указанных выше стадиях, с помощью способа с ограничением разбавления и в конечном итоге получали гибридомные клоны, экспрессирующие антитела мыши к EphA4, обладающее активностью связывания к EphA4 мыши, крысы или человека.
[0113]
Полученные гибридомные клоны культивировали и моноклональное антитело мыши к EphA4 очищали из надосадочной жидкости культуры с помощью белка A (GE Healthcare).
[0114]
(B) Оценка активности в отношении усиления расщепления EphA4
Подготовку нейронов гиппокампа крысы выполняли согласно приведенным ниже стадиям. У крысы в день 18 беременности (Charles River Laboratories, Япония) извлекали зародышей и разрезали у них голову для извлечения головного мозга. Под стереомикроскопом иссекали область гиппокампа, помещали ее в дигестирующий раствор (137 мМ NaCl (Wako Pure Chemical), 5 мМ KCl (Wako Pure Chemical), 7 мМ Na2HPO4 (Wako Pure Chemical), 25 мМ Hepes (DOJINDO), 0,5 мг/мл ДНКазы (Sigma) и 0,25% трипсина (Life technologies)) и встряхивали при температуре 37°C в течение 10 минут. Раствор удаляли и добавляли 20% фетальную бычью сыворотку/буфер Хенкса (Sigma). После удаления раствора и двукратного промывания в буфере Хенкса ткань гиппокампа пипетировали в буфере Хенкса с получением клеточной суспензии. Клетки высевали в 96-луночный планшет (Falcon), покрытый культуральной жидкостью, содержащей поли-L-лизин (нейробазальная среда (Life technologies), 1 х добавка B-27 (Life technologies) и 0,5 мМ L-глутамина (Life technologies)).
[0115]
Оценку активности в отношении усиления расщепления EphA4 с использованием нейронов гиппокампа проводили согласно приведенным ниже стадиям. Нейроны гиппокампа крысы, посеянные в 96-луночный планшет (Falcon), обрабатывали моноклональным антителом к EphA4 (67 нМ) и лекарственным средством, ингибирующим γ-селектазу, представляющим собой соединение E (50 нМ, Enzo Life Sciences). Через шестнадцать часов его промывали с помощью PBS (Wako Pure Chemical), добавляли буфер для образцов с SDS (буфер для образцов Laemmli (Bio-Rad) и 5% 2-меркаптоэтанол (Bio-Rad)) для извлечения клеток и кипятили в течение 5 минут. С этим образцом осуществляли SDS-PAGE, осуществляли вестерн-блоттинг с моноклональным антителом к EphA4 (Abnova), количественно определяли концентрацию в бэнде и рассчитывали значение C-концевого фрагмента EphA4/полноразмерного EphA4.
[0116]
Получали моноклональное антитело мыши к EphA4, обладающее активностью, которая усиливает расщепление EphA4 (антитело A). Изотип антитела A определяли с помощью набора для изотипирования моноклональных антител (Serotec), и при этом он представлял собой IgG1 для тяжелой цепи и κ для легкой цепи.
[0117]
(C) Анализ последовательности антитела A
Последовательность ДНК, кодирующая сигнальную последовательность и вариабельную область тяжелой и легкой цепей антитела А, амплифицировали с помощью способа 5'-RACE (быстрой амплификации 5'-концов кДНК). Общую РНК получали из гибридомы с помощью набора RNeasy (QIAGEN) и обрабатывали ДНКазой (QIAGEN, набор ДНКаз, не содержащих РНКаз). Двухцепочечную кДНК получали из общей РНК с помощью набора для синтеза кДНК (TAKARA). 5'-адаптор, полученный путем гибридизации ДНК-олигонуклеотида ad29S (ACATCACTCCGT) (SEQ ID NO: 7) и ДНК-олигонуклеотида ad29AS (ACGGAGTGATGTCCGTCGACGTATCTCTGCGTTGATACTTCAGCGTAGCT) (SEQ ID NO: 8), добавляли к кДНК. Полученную кДНК амплифицировали с прямым 5'-праймером (праймером 5'-PCR4, AGCTACGCTGAAGTATCAACGCAGAG) (SEQ ID NO: 9), а обратный 3'-праймер (GCCAGTGGATAGACTGATGG (SEQ ID NO: 10) использовали для амплификации гена тяжелой цепи мышиного IgG и GATGGATACAGTTGGTGCAGC (SEQ ID NO: 11) использовали для амплификации легкой цепи κ мышиного Ig). Амплифицированную кДНК встраивали в вектор pCR2.1 (Invitrogen/LifeTechnologies). Последовательность гена антитела А анализировали с помощью ABI 3130XL. Что касается аминокислотных последовательностей, кодируемых последовательностью гена антитела А, идентифицированной с помощью настоящего анализа, то сигнальная последовательность тяжелой цепи представляла собой последовательность, показанную под SEQ ID NO: 12, вариабельная область тяжелой цепи представляла собой последовательность, показанную под SEQ ID NO: 13, сигнальная последовательность легкой цепи представляла собой последовательность, показанную под SEQ ID NO: 14, и вариабельная область легкой цепи представляла собой последовательность, показанную под SEQ ID NO: 15. Что касается нуклеотидных последовательностей, кодирующих последовательность гена антитела А, то сигнальная последовательность тяжелой цепи представляла собой последовательность, показанную под SEQ ID NO: 16, вариабельная область тяжелой цепи представляла собой последовательность, показанную под SEQ ID NO: 17, сигнальная последовательность легкой цепи представляла собой последовательность, показанную под SEQ ID NO: 18, и вариабельная область легкой цепи представляла собой последовательность, показанную под SEQ ID NO: 19.
[0118]
Полноразмерные последовательности тяжелой и легкой цепей антитела A получали с помощью следующих стадий. Общую РНК получали из гибридомы с помощью набора RNeasy (QIAGEN) и обрабатывали ДНКазой (QIAGEN, набор ДНКаз, не содержащих РНКаз). Продукты обратной транскрипции получали из общей РНК с помощью набора для ПЦР РНК (TAKARA). Используя продукты обратной транскрипции, полученные с матриц, последовательность гена, кодирующую тяжелую и легкую цепи антитела А, амплифицировали с помощью ПЦР с 5'-прямым праймером(GCGAAGCTTGCCGCCACCATGGCTGTCCTGGTGCTGCTCC (праймер ID 7455) (SEQ ID NO: 20), который использовали для амплификации тяжелой цепи, и GCGAAGCTTGCCGCCACCATGGACATGAGGGTTCCTGCTCACG (праймер ID 7453) (SEQ ID NO: 21), который использовали для амплификации легкой цепи) и 3'-обратным праймером (GCGGAATTCATCATTTACCAGGAGAGTGGGAGAGGC (праймер ID 7257) (SEQ ID NO: 22), который использовали для амплификации тяжелой цепи, и CGCGAATTCACTAACACTCATTCCTGTTGAAGCTCTTGAC (праймер ID 7249) (SEQ ID NO: 23), который использовали для амплификации легкой цепи), и соответственно клонировали в векторы pEE6.4 и pEE12.4 (Lonza). Последовательность гена анализировали с помощью ABI3130XL. Что касается аминокислотных последовательностей, кодируемых последовательностью гена антитела А, идентифицированной с помощью настоящего анализа, константная область тяжелой цепи представляла собой последовательность, показанную под SEQ ID NO: 24, и константная область легкой цепи представляла собой последовательность, представленную под SEQ ID NO: 25.
[0119]
CDR антитела А определяли следующим способом. Аминокислотная последовательность антитела A была пронумерована в соответствии с системой нумерации Kabat с помощью программного обеспечения Abysis (UCL). На основании этой нумерации было принято решение в соответствии с определением Kabat для идентификации CDR. Аминокислотные последовательности CDR антитела A показаны в таблице 1.
[0120]
Сравнительный пример 2. Аффинность связывания моноклонального антитела к EphA4 по отношению к EphA4 мыши и человека
Аффинность связывания антитела A по отношению к EphA4 мыши и человека определяли с помощью поверхностного плазмонного резонанса (способ SPR) с использованием Biacore T200 (GE Healthcare). Сначала антитело к His (GE Healthcare, 28-9950-56) фиксировали на сенсорном чипе CM5. Фиксацию осуществляли способом аминового связывания с использованием N-гидроксисукцинимида (NHS) и гидрохлорида N-этил-N'-(3-диметиламинопропил)карбодиимида (EDC), а для блокирования использовали этаноламин (сенсорный чип и все реагенты для фиксации были приобретены у GE Healthcare). Его разбавляли до 3,5 мкг/мл буфером для фиксации (10 мМ ацетат натрия, pH 4,5) и фиксировали на сенсорном чипе в соответствии с протоколом, прилагаемым к Biacore T200. Белок внеклеточной области-EphA4-SEAP-His10 мыши или человека разбавляли рабочим буфером HBS-EP (GE Healthcare, BR-1001-88) и раствор вносили в проточную кювету в течение 120 секунд для захвата (захватываемое количество составляло приблизительно 10 RU). Затем антитело А, серийно разбавленное до диапазона 100, 50, 25, 12,5, 6,3, 3,2, 1,6 и 0 нМ с помощью HBS-EP, добавляли в сенсорный чип в течение 120 секунд и последовательно отслеживали кривую реакции связывания с момента добавления (фаза связывания, 120 секунд) и до момента после завершения добавления (фаза диссоциации, 600 секунд). После завершения каждого отслеживания добавляли 4 M MgCl2 (60 секунд, Wako Pure Chemical) для регенерации сенсорного чипа. На полученной кривой реакции связывания проводили аппроксимирующий анализ с использованием модели связывания 1:1 с помощью программного обеспечения для оценки BIA, прилагаемого к системе, и рассчитывали аффинность связывания (KD=kd/ka) по отношению к EphA4 мыши и человека.
[0121]
Аффинность связывания антитела A по отношению к EphA4 мыши и человека (значение KD) составляло 1,32 × 10-9 M и 1,19 × 10-9 M соответственно (фигура 1). Другие параметры связывания по отношению к EphA4 мыши и человека были почти в такой же степени. Следовательно, было выдвинуто предположение, что антитело А имело ту же степень аффинности связывания с EphA4 мыши и человека.
[0122]
Сравнительный пример 3. Активность в отношении усиления расщепления EphA4 у моноклонального антитела к EphA4 в нейронах гиппокампа
В случае антитела А оценку активности в отношении усиления расщепления EphA4 с использованием нейронов гиппокампа проводили согласно приведенным ниже стадиям. Нейроны гиппокампа крысы, посеянные в 96-луночный планшет (Falcon), обрабатывали антителом А (2,0, 6,7 и 20 нМ) и лекарственным средством, ингибирующим γ-селектазу, представляющим собой соединение E (50 нМ, Enzo Life Sciences). Через двадцать четыре часа его промывали с помощью PBS (Wako Pure Chemical), добавляли буфер для образцов с SDS (буфер для образцов Laemmli (Bio-Rad) и 5% 2-меркаптоэтанол (Bio-Rad)) для извлечения клеток и кипятили в течение 5 минут. С этим образцом осуществляли SDS-PAGE, осуществляли вестерн-блоттинг с моноклональным антителом к EphA4 (Abnova), количественно определяли концентрацию в бэнде и рассчитывали значение C-концевого фрагмента EphA4/полноразмерного EphA4.
[0123]
Антитело A зависимым от концентрации образом усиливало реакцию расщепления EphA4 в нейронах гиппокампа (фигура 2).
[0124]
Сравнительный пример 4. Ингибирующая активность моноклонального антитела к EphA4 по отношению к мышиному лиганд-связывающему EphA4 мыши
Для антитела A оценку ингибирующей активности связывания между EphA4 мыши и мышиным лигандом выполняли согласно приведенным ниже стадиям. Антителом к щелочной фосфатазе (Thermo SCIENTIFIC) покрывали лунки 96-луночного планшета (Nunc). После инкубации при 4°C в течение ночи лунки блокировали при комнатной температуре в течение одного часа с помощью 1% Block ACE (DS Pharma Biomedical). После трехкратного промывания с помощью 0,02% Tween 20/PBS (Thermo SCIENTIFIC) в лунки добавляли белок внеклеточной области-SEAP-His EphA4 мыши (конечная концентрация 10 нМ) и инкубировали указанное при комнатной температуре в течение одного часа. После трехкратного промывания в каждую лунку добавляли лиганд и антитело A (0, 0,003, 0,01, 0,03, 0,1, 0,3, 1, 3, 10, 30, 100, 300, 1000 и 3000 нM). Следует отметить, что в качестве лигандов использовали биотинилированную химеру Ephrin A1-Fc мыши (R&D Systems, конечная концентрация 6 нМ) и биотинилированную химеру Ephrin B2-Fc мыши (R&D Systems, конечная концентрация 2,5 нМ). После инкубирования при комнатной температуре в течение одного часа и трехкратного промывания добавляли меченый пероксидазой хрена стрептавидин (GE Healthcare) и эту смесь инкубировали при комнатной температуре в течение одного часа. После трехкратного промывания в лунки добавляли раствор ™BZ (3,3',5,5'-тетраметилбензидин, Sigma) и инкубировали при комнатной температуре в течение 2 минут. В лунки добавляли равное количество стоп-раствора (1 н. H2SO4, Wako Pure Chemical) и считывали поглощение при 450 нм с помощью считывающего устройства для микропланшетов (PerkinElmer).
[0125]
Антитело A зависимым от концентрации образом подавляло связывание между EphA4 мыши и мышиным лигандом, а значения IC50 в отношении связывания Ephrin A1 и Ephrin B2 мыши составляли приблизительно 5,9 нМ и 3,1 нМ соответственно (фигура 3). Соответственно, было показано, что антитело A сильно ингибировало связывание между EphA4 мыши и мышиным лигандом.
[0126]
Сравнительный пример 5. Ингибирующая активность моноклонального антитела к EphA4 по отношению к человеческому лиганд-связывающему EphA4
Для антитела A оценку ингибирующей активности связывания между EphA4 человека и человеческим лигандом выполняли согласно приведенным ниже стадиям. Антителом к щелочной фосфатазе (Thermo SCIENTIFIC) покрывали лунки 96-луночного планшета (Nunc). После инкубации при 4°C в течение ночи лунки блокировали при комнатной температуре в течение одного часа с помощью 1% Block ACE (DS Pharma Biomedical). После трехкратного промывания с помощью 0,05% Tween 20/PBS (Thermo SCIENTIFIC) в лунки добавляли белок внеклеточной области-SEAP-His EphA4 человека (конечная концентрация 10 нМ) и инкубировали ее при комнатной температуре в течение одного часа. После трехкратного промывания в каждую лунку добавляли лиганд и серийно разбавленное антитело A (0, 0,003, 0,01, 0,03, 0,1, 0,3, 1, 3, 10, 30, 100, 300, 1000 и 3000 нM). Следует отметить, что в качестве лигандов использовали биотинилированную химеру Ephrin A5-Fc человека (R&D Systems, конечная концентрация 0,7 нМ) и биотинилированную химеру Ephrin B3-Fc человека (R&D Systems, конечная концентрация 2,3 нМ). После инкубирования при комнатной температуре в течение одного часа и трехкратного промывания добавляли меченый пероксидазой хрена стрептавидин (GE Healthcare) и эту смесь инкубировали при комнатной температуре в течение одного часа. После трехкратного промывания в лунки добавляли раствор ™BZ (3,3',5,5'-тетраметилбензидин, Sigma) и инкубировали при комнатной температуре в течение 2-5 минут. В лунки добавляли равное количество стоп-раствора (1 н. H2SO4, Wako Pure Chemical) и считывали поглощение при 450 нм с помощью считывающего устройства для микропланшетов (Molecular Devices или PerkinElmer).
[0127]
Антитело A зависимым от концентрации образом подавляло связывание между EphA4 человека и человеческим лигандом, а значения IC50 в отношении связывания Ephrin A5 и Ephrin B3 человека составляли соответственно приблизительно 2,8 нМ и 1,4 нМ (фигура 4). Соответственно, было показано, что антитело A сильно ингибировало связывание между EphA4 человека и человеческим лигандом.
[0128]
Сравнительный пример 6. Избирательность моноклонального антитела к EphA4 по отношению к рецептору Eph человека
Согласно способу получения белка внеклеточной области-SEAP-His EphA4 мыши, описанному в сравнительном примере 1, последовательности ДНК, кодирующие сигнальную последовательность и внеклеточную область каждого рецептора Eph человека (EphA1, EphA2, EphA3, EphA4, EphA5, EphA6, EphA7, EphA8, EphA10, EphB1, EphB2, EphB3, EphB4 и EphB6), амплифицировали с помощью RT-PCR с общей РНК, полученной из ткани, и клонировали в вектор pENTR1A (Invitrogen/LifeTechnologies), имеющий последовательность ДНК, кодирующую SEAP и гистидиновую метку. Затем последовательности ДНК, кодирующие сигнальную последовательность и внеклеточную область каждого рецептора Eph человека, SEAP и гистидиновой метки, переносили в вектор pcDNA 3.1_rfcB с помощью LR-реакции с использованием Gateway System (Invitrogen/Life Technologies) с конструированием векторов (называемых "вектором экспрессии белка внеклеточной области-SEAP-His рецептора Eph"), экспрессирующих белок, имеющий SEAP и His-метку, слитый с внеклеточной областью каждого рецептора Eph человека (называемый "белок внеклеточной области-SEAP-His рецептора Eph").
[0129]
Затем каждый вектор экспрессии белка внеклеточной области-SEAP-His рецептора Eph человека вводили в клетки Expi293F (Gibco/ThermoFisher) с системой экспрессии Expi293 (Gibco/ThermoFisher). Через 5 дней культивирования (5% CO2, 37°C, 120 об/мин) собирали надосадочную жидкость культуры и центрифугировали при комнатной температуре на 1500 об/мин в течение 5 минут. Центрифугированную надосадочную жидкость фильтровали через фильтр с размером пор 0,45 мкм (Millipore).
[0130]
В случае антитела А оценку активности связывания рецептора Eph человека проводили согласно приведенным ниже стадиям.
Лунки 96-луночного планшета (Nunc) покрывали антителом кролика к 6-His (Bethyl Laboratories). После инкубации при 4°C в течение ночи лунки блокировали при комнатной температуре в течение одного часа с помощью 1% Block ACE (DS Pharma Biomedical). После трехкратного промывания с помощью 0,05% Tween 20/PBS (Thermo SCIENTIFIC) каждый белок внеклеточной области-SEAP-His рецептора Eph человека (в конечной концентрации 1 нМ) высевали в каждую лунку и инкубировали при комнатной температуре в течение одного часа. После трехкратного промывания в лунки добавляли раствор человеческого IgG (100 мкг/мл, Mitsubishi Pharma Corporation) и антитела A (10 мкг/мл) и инкубировали при комнатной температуре в течение одного часа. К указанному добавляли меченое пероксидазой хрена антитело осла к мышиному IgG (Jackson ImmunoResearch Laboratories) и инкубировали при комнатной температуре в течение одного часа. После трехкратного промывания в лунки добавляли раствор ™BZ (3,3',5,5'-тетраметилбензидина, Sigma), а после подтверждении умеренного окрашивания в лунки добавляли равное количество стоп-раствора (1 н. H2SO4, Wako Pure Chemical) и оптическую плотность при 450 нм считывали с помощью считывающего устройства для микропланшетов (PerkinElmer).
[0131]
Среди семейства рецепторов Eph человека антитело A обладало специфической активностью связывания только в отношении EphA4 человека (фигура 5).
[0132]
Сравнительный пример 7. Селективность моноклонального антитела к EphA4 по отношению к рецептору Eph мыши
Согласно способу получения белка внеклеточной области-Fc-His EphA4 в соответствии со сравнительным примером 1 последовательности ДНК, кодирующие сигнальную последовательность и внеклеточную область каждого рецептора Eph мыши (EphA1, EphA3, EphA4, EphA5, EphA6, EphA7, EphA8, EphA10, EphB1, EphB2, EphB3, EphB4 и EphB6), амплифицировали с помощью RT-PCR с общей РНК, полученной из ткани, и клонировали в вектор pENTR1A (Invitrogen/LifeTechnologies), имеющий последовательность ДНК, кодирующую Fc-область человеческого IgG1 и гистидиновую метку. Затем последовательности ДНК, кодирующие сигнальную последовательность и внеклеточную область каждого рецептора Eph мыши, Fc и гистидиновую метку (EphA1, EphA3, EphA4, EphA5, EphA6, EphA7, EphA8, EphA10, EphB1, EphB2, EphB3, EphB6 и EphB4), переносили в вектор pcDNA 3.1_rfcB с помощью LR-реакции с использованием Gateway System (Invitrogen/LifeTechnologies) для построения вектора экспрессии внеклеточной области каждого рецептора Eph белка Fc-His мыши. При построении вектора экспрессии белка внеклеточной области EphA2-Fc-His мыши последовательности ДНК, кодирующие сигнальную последовательность и внеклеточную область EphA2 мыши, амплифицировали с помощью RT-PCR с общей РНК, полученной из ткани, и клонировали в вектор pcDNA 3.1., имеющий последовательность ДНК, кодирующую Fc и гистидиновую метку, для построения вектора экспрессии белка внеклеточной области-Fc-His EphA2 мыши.
[0133]
Затем каждый вектор экспрессии белка внеклеточной области Fc-His рецептора Eph мыши вводили в клетки Expi293F (Gibco/ThermoFisher) с системой экспрессии Expi293 (Gibco/ThermoFisher). Через 5 дней культивирования (5% CO2, 37°C, 120 об/мин) собирали надосадочную жидкость культуры и центрифугировали при комнатной температуре на 1500 об/мин в течение 5 минут. Центрифугированную надосадочную жидкость фильтровали через фильтр с размером пор 0,45 мкм (Millipore).
[0134]
В случае антитела А оценку активности связывания рецептора Eph мыши проводили согласно приведенным ниже стадиям.
Лунки 96-луночного планшета (Nunc) покрывали антителом кролика к 6-His (Bethyl Laboratories). После инкубации при 4°C в течение ночи лунки блокировали при комнатной температуре в течение одного часа с помощью 1% Block ACE (DS Pharma Biomedical). После трехкратного промывания с помощью 0,05% Tween 20/PBS (Thermo SCIENTIFIC) каждый белок внеклеточной области-Fc-His рецептора Eph мыши (в конечной концентрации 1 нМ) высевали в каждую лунку и инкубировали при комнатной температуре в течение одного часа. После трехкратного промывания в лунки добавляли раствор человеческого IgG (100 мкг/мл,Sigma) и антитела A (10 мкг/мл) и инкубировали при комнатной температуре в течение одного часа. К указанному добавляли меченое пероксидазой хрена антитело осла к мышиному IgG (Jackson ImmunoResearch Laboratories) и инкубировали при комнатной температуре в течение одного часа. После трехкратного промывания в лунки добавляли раствор ™BZ (3,3',5,5'-тетраметилбензидина, Sigma), а после подтверждении умеренного окрашивания в лунки добавляли равное количество стоп-раствора (1 н. H2SO4, Wako Pure Chemical) и оптическую плотность при 450 нм считывали с помощью считывающего устройства для микропланшетов (PerkinElmer).
[0135]
Среди семейства рецепторов Eph мыши антитело A обладало специфической активностью связывания только по отношению к EphA4 мыши (фигура 6).
[0136]
Сравнительный пример 8. Реактивность моноклонального антитела к EphA4 по отношению к EphA4 мыши, крысы, обезьяны и человека
Получение белков внеклеточных областей-Fc-His EphA4 мыши, крысы, обезьяны и человека осуществляли согласно приведенным ниже стадиям. Сначала, согласно способу получения белка внеклеточной области-Fc-His EphA4 в соответствии со сравнительным примером 1, строили вектор экспрессии белка внеклеточной области-Fc-His EphA4 обезьяны. Аминокислотная последовательность EphA4 обезьяны, используемая в конструкции вектора, показана под SEQ ID NO: 32, а его внеклеточная область показана под SEQ ID NO: 33. Различные белки внеклеточной области-Fc-His EphA4 получали с использованием вектора экспрессии белка внеклеточной области-Fc-His EphA4 обезьяны, а также векторов экспрессии белков внеклеточной области-Fc-His EphA4 мыши, крысы и человека, которые описаны в сравнительном примере 1.
[0137]
В случае антитела A оценку активности связывания с различными внеклеточными областями EphA4 выполняли согласно приведенным ниже стадиям.
Лунки 96-луночного планшета (Nunc) покрывали антителом осла к человеческому IgG (Jackson ImmunoResearch Laboratories). После инкубации при 4°C в течение ночи лунки блокировали при комнатной температуре в течение одного часа с помощью 1% Block ACE (DS Pharma Biomedical). После трехкратного промывания с помощью 0,05% Tween 20/PBS (Thermo SCIENTIFIC) белки внеклеточной области-Fc-His EphA4 мыши, крысы, обезьяны и человека (конечная концентрация 1 нМ) высевали в лунки и инкубировали при комнатной температуре в течение одного часа. После трехкратного промывания в лунки добавляли раствор человеческого IgG (100 мкг/мл, Mitsubishi Pharma Corporation) и антитела A (0, 0,00013, 0,00064, 0,0032, 0,016, 0,08, 0,4, 2 и 10 мкг/мл) и инкубировали при комнатной температуре в течение одного часа. К указанному добавляли меченое пероксидазой хрена антитело осла к мышиному IgG (Jackson ImmunoResearch Laboratories) и инкубировали при комнатной температуре в течение одного часа. После трехкратного промывания в лунки добавляли раствор ™BZ (3,3',5,5'-тетраметилбензидина, Sigma), а после подтверждении умеренного окрашивания в лунки добавляли равное количество стоп-раствора (1 н. H2SO4, Wako Pure Chemical) и оптическую плотность при 450 нм считывали с помощью считывающего устройства для микропланшетов (PerkinElmer).
[0138]
Антитело A характеризовалось эквивалентной активностью связывания по отношению ко всем из EphA4 мыши, крысы, обезьяны и человека (фигура 7).
[0139]
Сравнительный пример 9. Реактивность моноклонального антитела к EphA4 по отношению к внеклеточной области, лиганд-связывающему домену, домену 1 фибронектина III типа, домену 2 фибронектина III типа EphA4 человека
Получение белков, содержащих внеклеточную область (ECD), лиганд-связывающий домен (LBD), домен 1 фибронектина III типа (FN1) или домен 2 фибронектина III типа (FN2) EphA4 человека, слитые с мальтоза-связывающим белком (MBP) и гистидиновой меткой (в дальнейшем называемые в данном документе "белок внеклеточной области-MBP-His EphA4 человека", "белок лиганд-связывающего домена-MBP-His EphA4 человека", "белок домена 1-MBP-His фибронектина III типа EphA4 человека" и "белок домена 2-MBP-His фибронектина III типа EphA4 человека"), осуществляли согласно приведенным ниже стадиям. Сначала конструировали векторы экспрессии pcDNA 3.4 для внеклеточной области, лиганд-связывающего домена, домена 1 фибронектина III типа или домена 2-MBP-His фибронектина III типа EphA4 человека. Во-первых, сигнальную последовательность EphA4 человека (SEQ ID NO: 34) или сигнальную последовательность препротрипсина (SEQ ID NO: 35) и последовательности ДНК, кодирующие каждый домен EphA4 человека, амплифицировали с помощью ПЦР и клонировали в вектор pcDNA 3.4, имеющий последовательность ДНК, кодирующую MBP и гистидиновую метку (Invitrogen/LifeTechnologies), для построения векторов экспрессии белка внеклеточной области-MBP-His EphA4 человека, белка лиганд-связывающего домена-MBP-His EphA4 человека, белка домена 1-MBP-His фибронектина III типа EphA4 человека и белка домена 2-MBP-His фибронектина III типа EphA4 человека. Аминокислотная последовательность EphA4 человека, используемая при построении вектора, показана под SEQ ID NO: 5, его внеклеточная область показана под SEQ ID NO: 36, лиганд-связывающий домен показан под SEQ ID NO: 37, домен 1 фибронектина III типа показан под SEQ ID NO: 38 и домен 2 фибронектина III типа показан под SEQ ID NO: 39. Вышеуказанные векторы экспрессии трансфицировали в клетки Expi293F (Thermo SCIENTIFIC) с помощью системы экспрессии Expi293 (Thermo SCIENTIFIC). Через четыре дня собирали надосадочную жидкость культуры и пропускали ее через 0,45 мкм фильтр (Millipore). Грубую очистку осуществляли с помощью амилозной смолы (NEB), а буфер заменяли на PBS (Wako Pure Chemical) с колонкой для обессоливания Zeba Spin Desalting (Thermo SCIENTIFIC). Фракцию мономеров подвергали дифференциальной очистке с помощью Superdex 200 10/300 (GE Healthcare).
[0140]
В случае антитела A оценку активности связывания с различными доменами в EphA4 человека выполняли согласно приведенным ниже стадиям.
Лунки 96-луночного планшета (Nunc) покрывали антителом кролика к 6-His (Bethyl Laboratories). После инкубации при 4°C в течение ночи лунки блокировали при комнатной температуре в течение одного часа с помощью 1% Block ACE (DS Pharma Biomedical). После двукратного промывания с помощью 0,02% Tween 20/PBS (Nacalai Tesque) белок внеклеточной области-MBP-His EphA4 человека, белок лиганд-связывающего домена EphA4 человека-MBP-His, белок домена 1-MBP-His фибронектина III типа EphA4 человека и белок домена 2-MBP-His фибронектина III типа EphA4 человека (конечная концентрация 10 нМ) высевали в лунки и инкубировали при комнатной температуре в течение одного часа. После трехкратного промывания в лунки добавляли антитело А (конечная концентрация 10 нМ) и инкубировали при комнатной температуре в течение одного часа. К указанному добавляли меченое пероксидазой хрена антитело козы к фрагменту Fcγ антитела к мышиному IgG (Jackson ImmunoResearch Laboratories) и инкубировали при комнатной температуре в течение одного часа. После пятикратного промывания в лунки добавляли раствор ™B (KPL) и после подтверждения умеренного количества окрашивания в лунки добавляли равное количество стоп-раствора (2 н. H2SO4, Wako Pure Chemical). Поглощение при 450 нм и 650 нм считывали с помощью считывающего устройства для микропланшетов (PerkinElmer).
[0141]
Антитело А обладало связывающей активностью по отношению к внеклеточной области (ECD) и лиганд-связывающему домену (LBD) EphA4 человека (фигура 8). Реакция по отношению к домену 1 фибронектина III типа (FN1) и домену 2 фибронектина III типа (FN2) отсутствовала. Соответственно, было обнаружено, что антитело А специфически связывалось с лиганд-связывающим доменом внеклеточной области EphA4 человека.
[0142]
Сравнительный пример 10. Эффект моноклонального антитела к EphA4 в отношении увеличения количества шипов у нейрона гиппокампа
Получение нейронов гиппокампа крысы проводили так, как описано в приведенном выше сравнительном примере 1 (B). В нейроны гиппокампа крысы с использованием нуклеофектора (Lonza) вводили ген EGFP, смешивали с нейронами гиппокампа крысы без введения гена и высевали в 24-луночный планшет (Falcon) с покровным стеклом (Matsunami Glass Industries), покрытым поли-L-лизином.
[0143]
Подсчет шипов с использованием нейронов гиппокампа производили согласно приведенным ниже стадиям. Нейроны гиппокампа крысы, которым был введен EGFP в день 13 культивирования, высеянные в 24-луночный планшет (Falcon) с покровным стеклом (Matsunami Glass Industries), покрытым поли-L-лизином, обрабатывали контрольным антителом (мышиным IgG1; BioLegend) или антителом A (6,7 и 20 нМ) в течение 24 часов. Затем покровное стекло переносили в раствор 2% PFA (Wako Pure Chemical)/4% сахароза (Wako Pure Chemical)/PBS и оставляли на 20 минут для фиксации клеток. После удаления фиксирующего раствора и трехкратного промывания клеток с помощью PBS добавляли 0,25% Triton X-100 (Wako Pure Chemical)/PBS и осуществляли пермеабилизацию клеток в течение 15 минут. Раствор удаляли, покровное стекло переносили в 2% BSA (Sigma)/0,25% Triton X-100/Opti-MEM (GIBCO) и подвергали блокированию в течение одного часа, после чего в течение 1,5 часа оставляли с антителом к GFP (Nacalai Tesque) для осуществления реакции. После удаления раствора первичного антитела и трехкратного промывания с помощью PBS оставляли в течение одного часа со вторичным антителом для осуществления реакции. После удаления раствора вторичных антител и трехкратного промывания с помощью PBS для фиксации добавляли препятствующий выгоранию флуоресценции реагент Prolong Gold (Molecular probes) и осуществляли наблюдение с помощью LSM800 (ZEISS). Описанный выше эксперимент осуществляли трижды и в ходе каждого эксперимента с двух покровных стекол извлекали нейроны, подсчитывали шипы на каждом дендрите с помощью программного обеспечения для анализа изображений Imaris® (Bitplane) и для каждого нейрона рассчитывали количество шипов на 10 мкм.
[0144]
Антитело А увеличивало количество шипов у нейрона гиппокампа (фигура 9). Из указанного результата видно, что антитело А обладало активностью по отношению к стабилизации шипов у нейронов гиппокампа.
[0145]
Сравнительный пример 11. Эффект моноклонального антитела к EphA4 в отношении подавления фосфорилирования тау-белка in vivo
Оценку эффекта в отношении подавления фосфорилирования тау-белка in vivo с использованием трансгенной по тау-белку мыши (rTg4510) проводили согласно приведенным ниже стадиям. Трансгенным по тау-белку мышам (rTg4510) в возрасте от 20 до 26 недель дважды в неделю вводили подкожно антитело А или контрольное антитело, полученные традиционными способами путем иммунизации мышей динитрофенолом (антитело мыши к динитрофенолу), каждый раз в дозе 100 мг/кг (10 мл/кг). Через 3,5 дня после последнего введения осуществляли анестезию 2% изофлураном (Intervet) и смесью трех типов анестетиков (4,0 мг/кг дормикума (Astellas Pharma), 0,3 мг/кг домитора (Nippon Zenyaku Kogyo) и 5,0 мг/кг веторфала (Meiji Seika Pharma)), под анестезией осуществляли перфузию с помощью PBS (Wako Pure Chemical), содержащего 3 единицы/мл гепарина (Ajinomoto) и 1% коктейль ингибиторов фосфатазы (Nacalai Tesque), и иссекали полушарие головного мозга. Собранное полушарие головного мозга фиксировали при 4°C со встряхиванием в течение ночи в 2% параформальдегиде (TAAB)/0,1 М фосфатном буфере (Wako Pure Chemical). Среду для полушария головного мозга заменяли средой 20% сахароза (Wako Pure Chemical)/0,1 M фосфатного буфера (Wako Pure Chemical), а впоследствии средой 25% сахарозы/0,1 M фосфатного буфера (Wako Pure Chemical), а затем помещали в Tissue-Tek O.C.T. (Sakura Finetek Japan)/25% сахарозы и замораживали жидким азотом. Осуществляли срезы толщиной 7 мкм с помощью криостата CM1860 (Leica), наклеивали на предметное стекло (Muto Pure Chemicals), высушивали с помощью холодного воздуха, а затем помещали в герметичный пакет и хранили при -80°C. Предметное стекло, используемое для иммуноокрашивания, размораживали, высушивали с помощью холодного воздуха, а затем промывали с помощью PBS (Wako Pure Chemical), погружали в 1% BSA (Sigma)/10% нормальную ослиную сыворотку (Jackson ImmunoResearch Laboratories)/0,5% Triton X-100 (Wako Pure Chemical)/PBS и подвергали блокированию в течение одного часа, после чего оставляли на ночь с антителом AT8 к фосфорилированному тау-белку (Fujirebio Europe NV) для осуществления реакции при обычных температурах. После трехкратного промывания с помощью PBS оставляли в течение одного часа со вторичным антителом для осуществления реакции. После трехкратного промывания с помощью PBS на срез помещали препятствующий выгоранию флуоресценции реагент Prolong Gold (молекулярные зонды), и фиксировали препарат, и проводили наблюдение с помощью LSM700 (ZEISS). Площадь с положительным сигналом от AT8 в stratum radiatum СА1 гиппокампа измеряли с помощью программного обеспечения для анализа изображений ImageJ и рассчитывали долю площади с AT8-положительным сигналом относительно общей площади.
[0146]
Антитело А уменьшало сигнал фосфорилированного тау-белка в области СА1 гиппокампа (фигура 10). Из указанного результата видно, что антитело А обладало активностью в отношении подавления прогрессирования патологии у трансгенных по тау-белку мышей (rTg4510).
[0147]
Сравнительный пример 12. Картирование эпитопа лиганд-связывающего домена EphA4 (EphA4-LBD) с помощью рентгеновского анализа кристаллической структуры
Получение антитела A-Fab осуществляли согласно приведенным ниже стадиям. Растворяли 101,1 мг антитела А в 0,1 М натрий-фосфатном буфере (pH 7,0), содержащем 30 мМ L-цистеина и 2 мМ EDTA в концентрации 15 мг/мл. К этому раствору антител добавляли папаин (Sigma) в количестве 1/200 от антитела и осуществляли ферментативное расщепление при 37°С в течение 18 часов. Раствор для ферментативного расщепления антитела А подвергали диализу относительно PBS и удаляли осадок центрифугированием (полученный осадок повторно растворяли в PBS и смешивали с полученной после центрифугирования надосадочной жидкостью). Затем с целью удаления примесей, отличных от антитела A-Fab, осуществляли следующие стадии.
1) Очистка на колонке с белком А
Этот раствор для ферментативного расщепления наносили на 2 мл колонки ProSep vA High Capacity (Millipore), уравновешенной с помощью PBS, и выделяли промежуточную фракцию и фракцию промывания с помощью PBS.
2) Аффинная очистка с использованием антитела к Fcγ человеческого IgG
Аффинную колонку с антителом к Fcγ человеческого IgG (Jackson ImmunoResearch Laboratories), ковалентно связанным с NHS-активированной сефарозой 4FF (GE Healthcare), получали в соответствии с руководством для этой сефарозы. Раствор, выделенный на описанной выше стадии 1), загружали в эту аффинную колонку и выделяли промежуточный раствор и раствор ее промывания с помощью PBS.
3) Очистка гель-фильтрацией
Промежуточную фракцию, полученную на вышеупомянутой стадии 2), концентрировали с помощью ультрафильтрационной мембраны. Суперозу 12 (GE Healthcare) уравновешивали с помощью PBS, наносили концентрированный образец и подвергали разделению и очистке. Часть отделенной и очищенной фракции анализировали с помощью SDS-PAGE и фракцию, содержащую антитело A-Fab с высокой степенью чистоты, выделяли и объединяли в пул. Очищенный таким образом образец считали антителом A-Fab.
[0148]
С целью получения комплекса антитела A-Fab и антигена EphA4-LBD получали EphA4-LBD (Qin H. et al., J. Biol. Chem., 283: 29473-29484 (2008)). Смешивали EphA4-LBD в количестве 0,68 мкмоль (200 мкМ, 3,4 мл) и антитело A-Fab в количестве 0,45 мкмоль (300 мкМ, 1,5 мл) так, чтобы EphA4-LBD имел приблизительно 1,5-кратное молярное соотношение относительно антитела A-Fab. После этого смешанный раствор наносили на HILOAD 26/60 Superdex 75 prep grade (GE Healthcare) и элюировали буферным раствором для хроматографии (25 мM Tris/HCl (pH 7,5), 100 мM NaCl). Фракцию, содержащую комплекс, анализировали с помощью SDS PAGE, фракции, имеющие высокую степень чистоты, собирали и концентрировали до приблизительно 40,8 мг/мл и полученный продукт использовали для кристаллизации.
[0149]
Кристаллизацию комплекса осуществляли с помощью способа диффузии паров в сидячей капле с использованием автокристаллизационного устройства Hydra II Plus One System (Matrix Technologies Corp., Ltd.). В качестве пластины использовали MRC-2 (Molecular Dimensions). Композиция резервуарного раствора представляла собой 100 мМ HEPES (pH 7,5), 10% полиэтиленгликоля 8000 и 8% этиленгликоля, и этот резервуарный раствор и раствор вышеупомянутого комплекса смешивали таким образом, чтобы объемное соотношение составляло 1:1, для того, чтобы вызвать кристаллизацию капель. Образовавшуюся кристаллизационную пластину оставляли отстаиваться при 20°C.
[0150]
После кристаллизации в вышеуказанных условиях получали кристаллы, характеризующиеся пространственной группой P212121, постоянными решетки a=71,0 Å, b=84,5 Å и c=116,1 Å. На полученные кристаллы подавали рентгеновское излучение (1,0 Å) с получением дифракционных данных 1,79 Å. Дифракционные данные обрабатывали с помощью HKL2000 (HKL Research Inc.), а фазовое определение осуществляли с помощью способа молекулярного замещения. Для способа молекулярного замещения использовали программу PHASER (версия 2.5.0, McCoy A. J. et al., J. Appl. Cryst. 40: 658-674 (2007)), входящую в состав пакета программного обеспечения CCP4 (Collaborative computational project number 4, [CCP4] version 6.5.0, Acta Cryst. D 67: 235-242 (2011)). В качестве поисковой модели способа молекулярного замещения использовали кристаллическую структуру EphA4-LBD (PDBID: 3CKH) и кристаллическую структуру Fab-области IgG (PDBID: 2VXT (L-цепь) и 1FGN (H-цепь)). Молекулярную модель строили с помощью программы COOT (Emsley P. et al., Acta Cryst. D 60: 2126-2132n (2004)) так, чтобы она соответствовала электронной плотности, полученной из определенной фазы, а уточнение структуры осуществляли с помощью программы REFMAC (Murshudov G.N., Acta Cryst. D 53: 240-255 (1997)).
Кристаллическую структуру комплекса с разрешением 2,0 Å получали с помощью расчета структуры (R=0,212, Rfree=0,258).
[0151]
Кристаллическую структуру полученного комплекса антитела A-Fab/EphA4-LBD анализировали с помощью инструмента для выявления взаимодействия, оснащенного вычислительной химической системой MOE 2018.0101 (Chemical Computing Group Inc.), и идентифицировали аминокислотные остатки на EphA4-LBD, которые находились в непосредственном контакте с антителом A-Fab (фигура 11A). Идентифицированными аминокислотными остатками были Glu51, Gly52, Ile59, Gln71, Cys73, Asn74, Val75, Met76, Glu77, Thr104, Arg106, Leu111, Pro112, Met115, Arg162, Met164, Cys191, Ala193 и Val195. На фигуре 11B показана структура поверхности EphA4-LBD, созданная с помощью Maestro (версия 11.0, Schrodinger, LLC). В результате авторами настоящего изобретения был сделан вывод, что область, в которой присутствуют эти аминокислотные остатки, представляет собой область связывания антитела A-Fab в EphA4-LBD.
[0152]
Пример 1. Получение гуманизированного антитела из антитела A
Получение гуманизированного антитела к EphA4
Конструировали вариабельную область гуманизированного антитела. На основании высокой степени гомологии в отношении каркасной области (FR) антитела A среди FR человеческого антитела IGHV3-33*03 (SEQ ID NO: 42) и JH6 (SEQ ID NO: 43) для тяжелой цепи и IGKV1-17*01 (SEQ ID NO: 40) и JK4 (SEQ ID NO: 41) для легкой цепи были отобраны в качестве FR для гуманизированного антитела. Затем с использованием прогностической модели трехмерной структуры антитела мыши A прогнозировали аминокислоты в FR, которые взаимодействуют с аминокислотами CDR, трансплантировали их вместе с CDR антитела A, имеющего мутацию Y32F в CDR1 тяжелой цепи (SEQ ID NO: 44, 27, 28 и 29-31), и конструировали HK2-42 (SEQ ID NO: 45) в качестве вариабельной области тяжелой цепи гуманизированного антитела, и конструировали L1-8 (SEQ ID NO: 46) в качестве вариабельной области легкой цепи гуманизированного антитела. Аминокислотные последовательности трансплантированных CDR показаны в таблице 2, а последовательности нуклеиновых кислот показаны в таблице 3.
[0153]
Константную область человеческого IgG2 (SEQ ID NO: 47) использовали в качестве константной области тяжелой цепи. Цепь κ человеческого Ig (SEQ ID NO: 48) использовали в качестве константной области легкой цепи. Вектор экспрессии (pcDNA 3.4), содержащий генную последовательность, кодирующую аминокислотную последовательность гуманизированного антитела, трансфицировали в клетки Expi293F (Gibco/ThermoFisher) с помощью системы экспрессии Expi293 (Gibco/ThermoFisher). В качестве генной последовательности, кодирующей аминокислотную последовательность гуманизированного антитела, последовательность нуклеиновой кислоты, показанную под SEQ ID NO: 55, использовали как вариабельную область тяжелой цепи, последовательность нуклеиновой кислоты, показанную под SEQ ID NO: 56, использовали как вариабельную область легкой цепи, последовательность нуклеиновой кислоты, показанную под SEQ ID NO: 57, использовали как константную область тяжелой цепи, и последовательность нуклеиновой кислоты, показанную под SEQ ID NO: 58, использовали как константную область легкой цепи соответственно. Аминокислотная последовательность полной длины тяжелой цепи (не включая сигнальную последовательность) гуманизированного антитела представляла собой аминокислотную последовательность, показанную под SEQ ID NO: 59, аминокислотная последовательность полной длины легкой цепи (не включая сигнальную последовательность) представляла собой аминокислотную последовательность, показанную под SEQ ID NO: 60. Последовательность нуклеиновой кислоты, кодирующая полную длину тяжелой цепи гуманизированного антитела, представляла собой последовательность нуклеиновой кислоты, показанную под SEQ ID NO: 61, и последовательность нуклеиновой кислоты, кодирующая полную длину легкой цепи, представляла собой последовательность нуклеиновой кислоты, показанную под SEQ ID NO: 62. Собирали надосадочную жидкость, и гуманизированную версию антитела А (антитело В) очищали с помощью MabSelectSuRe (GE Healthcare).
[0154]
[0155]
Пример 2. Аффинность гуманизированного моноклонального антитела к EphA4 по отношению к EphA4 человека
Аффинность связывания антитела В, полученного в примере 1, по отношению к EphA4 человека определяли с помощью поверхностного плазмонного резонанса (способ SPR) с использованием Biacore T200 (GE Healthcare). Сначала антитело к His (GE Healthcare, 28-9950-56) фиксировали на сенсорном чипе CM5. Фиксацию осуществляли способом аминового связывания с использованием N-гидроксисукцинимида (NHS) и гидрохлорида N-этил-N'-(3-диметиламинопропил)карбодиимида (EDC), а для блокирования использовали этаноламин (сенсорный чип и все реагенты для фиксации были приобретены у GE Healthcare). Его разбавляли до 3,5 мкг/мл буфером для фиксации (10 мМ ацетат натрия, pH 4,5) и фиксировали на сенсорном чипе в соответствии с протоколом, прилагаемым к Biacore T200. Белок внеклеточной области-SEAP-His10 EphA4 человека разбавляли рабочим буфером HBS-EP (GE Healthcare, BR-1001-88) и раствор вносили в проточную кювету в течение 120 секунд для захвата (захватываемое количество составляло приблизительно 10 RU). Затем антитело В, серийно разбавленное до диапазона 100, 50, 25, 12,5, 6,3, 3,2, 1,6 и 0 нМ с помощью HBS-EP, вносили в сенсорный чип в течение 120 секунд и последовательно отслеживали кривую реакции связывания во время добавления (фаза связывания, 120 секунд) и после завершения добавления (фаза диссоциации, 600 секунд). После завершения каждого отслеживания добавляли 4 M MgCl2 (60 секунд, Wako Pure Chemical) для регенерации сенсорного чипа. На полученной кривой реакции связывания проводили аппроксимирующий анализ с использованием модели связывания 1:1 с помощью программного обеспечения для оценки BIA, прилагаемого к системе, и рассчитывали аффинность (KD=kd/ka) по отношению к EphA4 человека.
[0156]
Аффинность связывания антитела B по отношению к EphA4 человека (значение KD) составляла 1,34×10-9 M (фигура 12). Было показано, что антитело B проявляет почти такую же аффинность, как и антитело A, которое представляло собой антитело до гуманизации.
[0157]
Пример 3. Активность в отношении усиления расщепления EphA4 у гуманизированного моноклонального антитела к EphA4 в нейронах гиппокампа
В случае антитела В, полученного в примере 1, оценку активности в отношении усиления расщепления EphA4 с использованием нейронов гиппокампа проводили согласно приведенным ниже стадиям.
Нейроны гиппокампа крысы, посеянные в 96-луночный планшет (Falcon), обрабатывали антителом B (2,0, 6,7 и 20 нМ) и лекарственным средством, ингибирующим γ-селектазу, представляющим собой соединение E (50 нМ, Enzo Life Sciences). Через двадцать четыре часа его промывали с помощью PBS (Wako Pure Chemical), добавляли буфер для образцов с SDS (буфер для образцов Laemmli (Bio-Rad) и 5% 2-меркаптоэтанол (Bio-Rad)) для извлечения клеток и кипятили в течение 5 минут. С этим образцом осуществляли SDS-PAGE, осуществляли вестерн-блоттинг с моноклональным антителом к EphA4 (Abnova), количественно определяли концентрацию в бэнде и рассчитывали значение C-концевого фрагмента EphA4/полноразмерного EphA4.
[0158]
Антитело B зависимым от концентрации образом усиливало реакцию расщепления EphA4 в нейронах гиппокампа (фигура 13).
[0159]
Пример 4. Ингибирующая активность гуманизированного моноклонального антитела к EphA4 по отношению к человеческому лиганд-связывающему EphA4
Для антитела В, полученного в примере 1, оценку ингибирующей активности связывания между EphA4 человека и человеческим лигандом выполняли согласно приведенным ниже стадиям. Антителом к щелочной фосфатазе (Thermo SCIENTIFIC) покрывали лунки 96-луночного планшета (Nunc). После инкубации при 4°C в течение ночи лунки блокировали при комнатной температуре в течение одного часа с помощью 1% Block ACE (DS Pharma Biomedical). После трехкратного промывания посредством 0,05% Tween 20/PBS (Thermo SCIENTIFIC) белок внеклеточной области-SEAP-His EphA4 человека (в конечной концентрации 10 нМ) высевали в лунки и инкубировали при комнатной температуре в течение одного часа. После трехкратного промывания в каждую лунку добавляли лиганд и серийно разбавленное антитело В (0, 0,003, 0,01, 0,03, 0,1, 0,3, 1, 3, 10, 30, 100, 300, 1000 и 3000 нM). Следует отметить, что в качестве лигандов использовали биотинилированную химеру Ephrin A5-Fc человека (R&D Systems, конечная концентрация 0,7 нМ) и биотинилированную химеру Ephrin B3-Fc человека (R&D Systems, конечная концентрация 2,3 нМ). После инкубирования при комнатной температуре в течение одного часа и трехкратного промывания добавляли меченный пероксидазой хрена стрептавидин (GE Healthcare) и эту смесь инкубировали при комнатной температуре в течение одного часа. После трехкратного промывания в лунки добавляли раствор ™BZ (3,3',5,5'-тетраметилбензидин, Sigma) и инкубировали при комнатной температуре в течение 2-5 минут. В лунки добавляли равное количество стоп-раствора (1 н. H2SO4, Wako Pure Chemical) и считывали поглощение при 450 нм с помощью считывающего устройства для микропланшетов (Molecular Devices или PerkinElmer).
[0160]
Антитело В зависимым от концентрации образом подавляло связывание между EphA4 человека и человеческим лигандом, а значения IC50 в отношении связывания человеческого Ephrin A5 и Ephrin B3 составляли приблизительно 4,9 нМ и 1,6 нМ соответственно. Соответственно, было обнаружено, что антитело B сильно ингибировало связывание между EphA4 человека и человеческим лигандом и проявляло почти такую же ингибирующую активность, как антитело A, которое представляло собой антитело до гуманизации (фигура 14).
[0161]
Пример 5. Ингибирующая активность гуманизированного моноклонального антитела к EphA4 по отношению к мышиному лиганд-связывающему EphA4 мыши
Для антитела В, полученного в примере 1, оценку ингибирующей активности связывания между EphA4 мыши и мышиным лигандом выполняли согласно приведенным ниже стадиям. Антителом к щелочной фосфатазе (Thermo SCIENTIFIC) покрывали лунки 96-луночного планшета (Nunc). После инкубации при 4°C в течение ночи лунки блокировали при комнатной температуре в течение одного часа с помощью 1% Block ACE (DS Pharma Biomedical). После трехкратного промывания с помощью 0,02% Tween 20/PBS (Thermo SCIENTIFIC) в лунки добавляли белок внеклеточной области-SEAP-His EphA4 мыши (конечная концентрация 10 нМ) и инкубировали указанное при комнатной температуре в течение одного часа. После трехкратного промывания в каждую лунку добавляли лиганд и серийно разбавленное антитело В (0, 0,003, 0,01, 0,03, 0,1, 0,3, 1, 3, 10, 30, 100, 300, 1000 и 3000 нM). Следует отметить, что в качестве лигандов использовали биотинилированную химеру Ephrin A1-Fc мыши (R&D Systems, конечная концентрация 6 нМ) и биотинилированную химеру Ephrin B2-Fc мыши (R&D Systems, конечная концентрация 2,5 нМ). После инкубирования при комнатной температуре в течение одного часа и трехкратного промывания добавляли меченный пероксидазой хрена стрептавидин (GE Healthcare) и эту смесь инкубировали при комнатной температуре в течение одного часа. После трехкратного промывания в лунки добавляли раствор ™BZ (3,3',5,5'-тетраметилбензидин, Sigma) и инкубировали при комнатной температуре в течение 2 минут. В лунки добавляли равное количество стоп-раствора (1 н. H2SO4, Wako Pure Chemical) и считывали поглощение при 450 нм с помощью считывающего устройства для микропланшетов (Molecular Devices или PerkinElmer).
[0162]
Антитело В зависимым от концентрации образом подавляло связывание между EphA4 мыши и мышиным лигандом, а значения IC50 в отношении связывания Ephrin A1 и Ephrin B2 мыши составляли приблизительно 8,7 нМ и 4,2 нМ соответственно. Соответственно, было обнаружено, что антитело B сильно ингибировало связывание между EphA4 мыши и мышиным лигандом и проявляло почти такую же ингибирующую активность, как и антитело A, которое представляло собой антитело до гуманизации (фигура 15).
[0163]
Пример 6. Селективность гуманизированного моноклонального антитела к EphA4 по отношению к рецептору Eph человека
Аналогично способу получения белка внеклеточной области-SEAP-His EphA4 мыши, описанному в сравнительном примере 1, последовательности ДНК, кодирующие сигнальную последовательность и внеклеточную область каждого рецептора Eph человека (EphA1, EphA2, EphA3, EphA4, EphA5, EphA6, EphA7, EphA8, EphA10, EphB1, EphB2, EphB3, EphB4 и EphB6), амплифицировали с помощью RT-PCR с общей РНК, полученной из ткани, и клонировали в вектор pENTR1A (Invitrogen/LifeTechnologies), имеющий последовательность ДНК, кодирующую белок SEAP и гистидиновую метку. Затем последовательности ДНК, кодирующие сигнальную последовательность и внеклеточную область каждого рецептора Eph человека, белка SEAP и гистидиновой метки, переносили в вектор pcDNA 3.1_rfcB с помощью LR-реакции с использованием Gateway System (Invitrogen/Life Technologies) с конструированием векторов (называемых "вектором экспрессии белка внеклеточной области-SEAP-His рецептора Eph"), экспрессирующих белок, содержащий белок SEAP и His-метку, слитый с внеклеточной областью каждого рецептора Eph человека (называемый "белок внеклеточной области-SEAP-His рецептора Eph").
[0164]
Затем каждый из векторов экспрессии белка внеклеточной области-SEAP-His рецептора Eph человека вводили в клетки Expi293F (Gibco/ThermoFisher) с помощью системы экспрессии Expi293 (Gibco/ThermoFisher). Через пять дней после инкубации (5% CO2, 37°C) собирали надосадочную жидкость культуры и центрифугировали при комнатной температуре при 1500 об/мин в течение 5 минут. Центрифугированную надосадочную жидкость фильтровали через фильтр с размером пор 0,45 мкм (Millipore).
[0165]
В случае антитела В, полученного в примере 1, оценку активности связывания рецептора Eph человека проводили согласно приведенным ниже стадиям.
Лунки 96-луночного планшета (Nunc) покрывали антителом кролика к 6-His (Bethyl Laboratories). После инкубации при 4°C в течение ночи лунки блокировали при комнатной температуре в течение одного часа с помощью 1% Block ACE (DS Pharma Biomedical). После трехкратного промывания посредством 0,05% Tween 20/PBS (Thermo SCIENTIFIC) каждый из белков внеклеточной области-SEAP-His рецептора Eph человека (конечная концентрация 1 нМ) высевали в каждую лунку и инкубировали при комнатной температуре в течение одного часа. После трехкратного промывания в лунки добавляли раствор человеческого IgG (100 мкг/мл, Mitsubishi Pharma Corporation) и антитела В (10 мкг/мл) и инкубировали при комнатной температуре в течение одного часа. К указанному добавляли меченое пероксидазой хрена антитело осла к человеческому IgG (Jackson ImmunoResearch Laboratories) и инкубировали при комнатной температуре в течение одного часа. После трехкратного промывания в лунки добавляли раствор ™BZ (3,3',5,5'-тетраметилбензидина, Sigma), а после подтверждения умеренного окрашивания в лунки добавляли равное количество стоп-раствора (1 н. H2SO4, Wako Pure Chemical) и оптическую плотность при 450 нм считывали с помощью считывающего устройства для микропланшетов (PerkinElmer).
[0166]
Было обнаружено, что антитело В, подобно антителу А, которое представляло собой антитело до гуманизации, специфически связывалось с EphA4 человека из семейства рецепторов Eph человека (фигура 16).
[0167]
Пример 7. Селективность гуманизированного моноклонального антитела к EphA4 по отношению к рецептору Eph мыши
Согласно способу получения белка внеклеточной области-Fc-His EphA4 в соответствии со сравнительным примером 1 последовательности ДНК, кодирующие сигнальную последовательность и внеклеточную область каждого рецептора Eph мыши (EphA1, EphA3, EphA4, EphA5, EphA6, EphA7, EphA8, EphA10, EphB1, EphB2, EphB3, EphB4 и EphB6), амплифицировали с помощью RT-PCR с общей РНК, полученной из ткани, и клонировали в вектор pENTR1A (Invitrogen/LifeTechnologies), имеющий последовательность ДНК, кодирующую Fc-область человеческого IgG1 и гистидиновую метку. Затем последовательности ДНК, кодирующие сигнальную последовательность и внеклеточную область каждого рецептора Eph(EphA1, EphA3, EphA4, EphA5, EphA6, EphA7, EphA8, EphA10, EphB1, EphB2, EphB3, EphB4 и EphB6) мыши, Fc и гистидиновую метку, переносили в вектор pcDNA 3.1_rfcB с помощью LR реакции с использованием Gateway System (Invitrogen/Life Technologies) для построения вектора экспрессии белка внеклеточной области-Fc-His каждого рецептора Eph мыши. При построении вектора экспрессии белка внеклеточной области-Fc-His EphA2 мыши последовательности ДНК, кодирующие сигнальную последовательность и внеклеточную область EphA2 мыши, амплифицировали с помощью RT-PCR с общей РНК, полученной из ткани, и клонировали в вектор pcDNA 3.1., имеющий последовательность ДНК, кодирующую Fc и гистидиновую метку, для построения вектора экспрессии белка внеклеточной области-Fc-His EphA2 мыши.
[0168]
Затем каждый из векторов экспрессии белка внеклеточной области-Fc-His рецептора Eph мыши вводили в клетки Expi293F (Gibco/ThermoFisher) с помощью системы экспрессии Expi293 (Gibco/ThermoFisher). Через 5 дней культивирования (5% CO2, 37°C, 120 об/мин) собирали надосадочную жидкость культуры и центрифугировали при комнатной температуре на 1500 об/мин в течение 5 минут. Центрифугированную надосадочную жидкость фильтровали через фильтр с размером пор 0,45 мкм (Millipore).
[0169]
В случае антитела В оценку активности связывания рецептора Eph мыши проводили согласно приведенным ниже стадиям.
Лунки 96-луночного планшета (Nunc) покрывали антителом кролика к 6-His (Bethyl Laboratories). После инкубации при 4°C в течение ночи лунки блокировали при комнатной температуре в течение одного часа с помощью 1% Block ACE (DS Pharma Biomedical). После трехкратного промывания с помощью 0,05% Tween 20/PBS (Thermo SCIENTIFIC) каждый из белков внеклеточной области-Fc-His рецептора Eph мыши (конечная концентрация 1 нМ) высевали в каждую лунку и инкубировали при комнатной температуре в течение одного часа. После трехкратного промывания в лунки добавляли раствор человеческого IgG (100 мкг/мл, Sigma) и антитела В (10 мкг/мл) и инкубировали при комнатной температуре в течение одного часа. Добавляли меченное пероксидазой хрена антитело козы к человеческой легкой цепи каппа (IBL) и инкубировали при комнатной температуре в течение одного часа. После трехкратного промывания в лунки добавляли раствор ™BZ (3,3',5,5'-тетраметилбензидина, Sigma), а после подтверждении умеренного окрашивания в лунки добавляли равное количество стоп-раствора (1 н. H2SO4, Wako Pure Chemical) и оптическую плотность при 450 нм считывали с помощью считывающего устройства для микропланшетов (PerkinElmer).
[0170]
Среди семейства рецепторов Eph мыши антитело В обладало специфической активностью связывания только по отношению к EphA4 мыши (фигура 17).
[0171]
Пример 8. Реактивность гуманизированного моноклонального антитела к EphA4 по отношению к EphA4 мыши, крысы, обезьяны и человека
[0172]
В случае антитела В оценку активности связывания с различным EphA4 выполняли согласно приведенным ниже стадиям.
Антителом к щелочной фосфатазе (Thermo SCIENTIFIC) покрывали лунки 96-луночного планшета (Nunc). После инкубации при 4°C в течение ночи лунки блокировали при комнатной температуре в течение одного часа с помощью 1% Block ACE (DS Pharma Biomedical). После трехкратного промывания с помощью 0,05% Tween 20/PBS (Thermo SCIENTIFIC) белки внеклеточной области-SEAP-His EphA4 мыши, крысы, обезьяны и человека (конечная концентрация 1 нМ) высевали в лунки и инкубировали при комнатной температуре в течение одного часа. После трехкратного промывания в лунки добавляли раствор человеческого IgG (100 мкг/мл, Mitsubishi Pharma Corporation) и антитела В (0, 0,00013, 0,00064, 0,0032, 0,016, 0,08, 0,4, 2 и 10 мкг/мл) и инкубировали при комнатной температуре в течение одного часа. К указанному добавляли меченое пероксидазой хрена антитело осла к человеческому IgG (Jackson ImmunoResearch Laboratories) и инкубировали при комнатной температуре в течение одного часа. После трехкратного промывания в лунки добавляли раствор ™BZ (3,3',5,5'-тетраметилбензидина, Sigma), а после подтверждения умеренного окрашивания в лунки добавляли равное количество стоп-раствора (1 н. H2SO4, Wako Pure Chemical) и оптическую плотность при 450 нм считывали с помощью считывающего устройства для микропланшетов (PerkinElmer).
[0173]
Антитело В характеризовалось эквивалентной активностью связывания по отношению ко всем из EphA4 мыши, крысы, обезьяны и человека (фигура 18).
[0174]
Пример 9. Реактивность гуманизированного моноклонального антитела к EphA4 по отношению к внеклеточной области, лиганд-связывающему домену, домену 1 фибронектина III типа, домену 2 фибронектина III типа EphA4 человека
В случае антитела В, полученного в примере 1, оценку активности связывания с различными доменами в EphA4 человека выполняли согласно приведенным ниже стадиям.
Лунки 96-луночного планшета (Nunc) покрывали антителом кролика к 6-His (Bethyl Laboratories). После инкубации при 4°C в течение ночи лунки блокировали при комнатной температуре в течение одного часа с помощью 1% Block ACE (DS Pharma Biomedical). После двукратного промывания с помощью 0,02% Tween 20/PBS (Nacalai Tesque) белок внеклеточной области-MBP-His EphA4 человека, белок лиганд-связывающего домена EphA4 человека-MBP-His, белок домена 1-MBP-His фибронектина III типа EphA4 человека и белок домена 2-MBP-His фибронектина III типа EphA4 человека (конечная концентрация 10 нМ) высевали в лунки и инкубировали при комнатной температуре в течение одного часа. После трехкратного промывания в лунки добавляли антитело В (конечная концентрация 10 нМ) и инкубировали при комнатной температуре в течение одного часа. Добавляли меченое пероксидазой хрена антитело кролика к фрагменту Fcγ антитела к человеческому IgG (Jackson ImmunoResearch Laboratories) и инкубировали при комнатной температуре в течение одного часа. После пятикратного промывания в лунки добавляли раствор ™B (KPL) и после подтверждения умеренного количества окрашивания в лунки добавляли равное количество стоп-раствора (2 н. H2SO4, Wako Pure Chemical). Поглощение при 450 нм и 650 нм считывали с помощью считывающего устройства для микропланшетов (PerkinElmer).
[0175]
Антитело В обладало связывающей активностью по отношению к внеклеточной области (ECD) и лиганд-связывающему домену (LBD) EphA4 человека (фигура 19). Реакция по отношению к домену 1 фибронектина III типа (FN1) и домену 2 фибронектина III типа (FN2) отсутствовала. Соответственно, было обнаружено, что антитело B специфически связывалось с лиганд-связывающим доменом внеклеточной области EphA4 человека.
[0176]
Пример 10. Эффект гуманизированного моноклонального антитела к EphA4 в отношении увеличения количества шипов у нейрона гиппокампа
Получение нейронов гиппокампа крысы проводили так, как описано в сравнительном примере 1 (B). В нейроны гиппокампа крысы с использованием нуклеофектора (Lonza) вводили ген EGFP и высевали в 24-луночный планшет (Falcon) с покровным стеклом (Matsunami Glass Industries), покрытым поли-L-лизином.
[0177]
Подсчет шипов с использованием нейронов гиппокампа производили согласно приведенным ниже стадиям. Нейроны гиппокампа крысы, которым был введен EGFP в день 13 культивирования, высеянные в 24-луночный планшет (Falcon) с покровным стеклом (Matsunami Glass Industries), покрытым поли-L-лизином, обрабатывали контрольным антителом (человеческим IgG2; Sigma) или антителом B (6,7 и 20 нМ) в течение 24 часов. Затем покровное стекло переносили в раствор 2% PFA (Wako Pure Chemical)/4% сахароза (Wako Pure Chemical)/PBS и оставляли на 20 минут для фиксации клеток. После удаления фиксирующего раствора и трехкратного промывания клеток с помощью PBS добавляли 0,25% Triton X-100 (Wako Pure Chemical)/PBS и осуществляли пермеабилизацию клеток в течение 15 минут. Раствор удаляли, покровное стекло переносили в 2% BSA (Sigma)/0,25% Triton X-100/OPTI-MEM (GIBCO) и подвергали блокированию в течение одного часа, после чего в течение 1,5 часа оставляли с антителом к GFP (Nacalai Tesque) для осуществления реакции. После удаления раствора первичного антитела и трехкратного промывания с помощью PBS оставляли в течение одного часа со вторичным антителом для осуществления реакции. После удаления раствора вторичных антител и трехкратного промывания с помощью PBS для фиксации добавляли препятствующий выгоранию флуоресценции реагент Prolong Gold (Molecular probes) и осуществляли наблюдение с помощью LSM800 (ZEISS). Описанный выше эксперимент осуществляли трижды и в ходе каждого эксперимента с двух покровных стекол извлекали нейроны, подсчитывали шипы на каждом дендрите с помощью программного обеспечения для анализа изображений Imaris® (Bitplane) и для каждого нейрона рассчитывали количество шипов на 10 мкм.
[0178]
Антитело В увеличивало количество шипов у нейрона гиппокампа (фигура 20). Из указанного результата видно, что антитело B обладало активностью по отношению к стабилизации шипов у нейронов гиппокампа.
[0179]
Пример 11. Активность в отношении усиления расщепления EphA4 человека у гуманизированного моноклонального антитела к EphA4
В случае антитела B, полученного в примере 1, оценку активности в отношении усиления расщепления связывания EphA4 человека проводили согласно приведенным ниже стадиям.
Получение нейронов гиппокампа крысы проводили так, как описано в сравнительном примере 1 (B). В нейроны гиппокампа крысы с использованием нуклеофектора (Lonza) вводили вектор экспрессии белка EphA4-HA человека и высевали в 96-луночный планшет (Falcon), покрытый поли-L-лизином. Посеянные нейроны крысиного гиппокампа обрабатывали антителом B (6,7, 20 и 67 нМ) и лекарственным средством, ингибирующим γ-селектазу, представляющим собой соединение E (50 нМ, Enzo Life Sciences). Через приблизительно двадцать четыре часа его промывали с помощью PBS (Wako Pure Chemical), добавляли буфер для образцов с SDS (буфер для образцов Laemmli (Bio-Rad) и 5% 2-меркаптоэтанол (Bio-Rad)) для извлечения клеток и кипятили в течение 5 минут. С этим образцом осуществляли SDS-PAGE, осуществляли вестерн-блоттинг с моноклональным антителом крысы к HA (Roche), количественно определяли концентрацию в бэнде и рассчитывали значение C-концевого фрагмента EphA4/полноразмерного EphA4.
[0180]
Антитело B усиливало реакцию расщепления EphA4 человека в нейронах гиппокампа (фигура 21).
[0181]
Пример 12. Вовлеченность MMP и ADAM относительно эффекта гуманизированного моноклонального антитела к EphA4 в отношении увеличения количества шипов у нейрона гиппокампа
Получение нейронов гиппокампа крысы проводили так, как описано в сравнительном примере 1 (B). В часть нейронов гиппокампа крысы с использованием нуклеофектора (Lonza) вводили ген EGFP и высевали в 24-луночный планшет (Falcon) с покровным стеклом (Matsunami Glass Industries), покрытым поли-L-лизином.
[0182]
Подсчет шипов с использованием нейронов гиппокампа производили согласно приведенным ниже стадиям. Нейроны гиппокампа крысы, которым был введен EGFP в день 13 культивирования, высеянные в 24-луночный планшет (Falcon) с покровным стеклом (Matsunami Glass Industries), покрытым поли-L-лизином, обрабатывали контрольным антителом (человеческим IgG2; Sigma) или антителом В (20 нМ), а также DMSO (Sigma) или ингибитором MMP и ADAM GM6001 (2,5 мкМ, MedChemExpress) в течение 24 часов. Затем покровное стекло переносили в раствор 2% PFA (Wako Pure Chemical)/4% сахароза (Wako Pure Chemical)/PBS и оставляли на 20 минут для фиксации клеток. После удаления фиксирующего раствора и трехкратного промывания клеток с помощью PBS добавляли 0,25% Triton X-100 (Wako Pure Chemical)/PBS и осуществляли пермеабилизацию клеток в течение 15 минут. Удаляли 0,25% Triton X-100/PBS, покровное стекло переносили в 2% BSA (Sigma)/0,25% Triton X-100/OPTI-MEM (GIBCO) и подвергали блокированию в течение одного часа, после чего в течение 1,5 часа оставляли с антителом к GFP (Nacalai Tesque) для осуществления реакции. После удаления раствора первичного антитела и трехкратного промывания с помощью PBS оставляли в течение одного часа со вторичным антителом для осуществления реакции. После удаления раствора вторичных антител и трехкратного промывания с помощью PBS для фиксации добавляли препятствующий выгоранию флуоресценции реагент Prolong Gold (Molecular probes) и осуществляли наблюдение с помощью LSM800 (ZEISS). Описанный выше эксперимент осуществляли трижды и в ходе каждого эксперимента с двух покровных стекол извлекали нейроны, подсчитывали шипы на каждом дендрите с помощью программного обеспечения для анализа изображений Imaris® (Bitplane) и для каждого нейрона рассчитывали количество шипов на 10 мкм.
[0183]
Увеличение количества шипов в нейроне гиппокампа под действием антитела B ингибировали посредством одновременной обработки с помощью GM6001 (фигура 22). Из указанного результата видно, что антитело B обладало активностью по отношению к стабилизации шипов посредством MMP и ADAM в нейронах гиппокампа.
[0184]
Пример 13. Эффект гуманизированного моноклонального антитела к EphA4 в отношении подавления фосфорилирования тау-белка in vivo
Оценку эффекта в отношении подавления фосфорилирования тау-белка in vivo с использованием трансгенной по тау-белку мыши (rTg4510) проводили согласно приведенным ниже стадиям. Трансгенным по тау-белку мышам (rTg4510) в возрасте от 20 до 26 недель подкожно вводили два раза в неделю антитело В в дозе 100 мг/кг (10 мл/кг). Контрольной группе вводили подкожно PBS (Wako Pure Chemical) в дозе 10 мл/кг. Через 3,5 дня после последнего введения мышей анестезировали с помощью ингаляции анестетика в виде 2-2,5% изофлурана (Intervet) и смеси трех типов анестетиков (4,0 мг/кг дормикума (Astellas Pharma), 0,3 мг/кг домитора (Nippon Zenyaku Kogyo) и 5,0 мг/кг веторфала (Meiji Seika Pharma)), под анестезией осуществляли перфузию с помощью PBS (Wako Pure Chemical), содержащего 3 единицы/мл гепарина (Ajinomoto) и 1% коктейль ингибиторов фосфатазы (Nacalai Tesque), и иссекали полушарие головного мозга мышей. Собранное полушарие головного мозга фиксировали при 4°C со встряхиванием в течение ночи с погружением в 2% параформальдегид (TAAB)/0,1 М фосфатный буфер (Wako Pure Chemical). Среду для полушария головного мозга заменяли средой 10% сахароза (Wako Pure Chemical)/0,1 M фосфатного буфера (Wako Pure Chemical), а впоследствии средой 20% сахарозы/0,1 M фосфатного буфера (Wako Pure Chemical), а затем помещали в соединение Tissue-Tek O.C.T. (Sakura Finetek Japan)/20% сахарозы и замораживали с использованием алюминиевого блока, охлажденного жидким азотом. Срезы полушария головного мозга толщиной 7 мкм получали с помощью криостата CM1860 (Leica). Срезы наклеивали на покрытое силаном предметное стекло (Muto Pure Chemicals), высушивали с помощью холодного воздуха, а затем помещали в герметичный мешок и хранили при -80°C. Предметное стекло, используемое для иммуноокрашивания, убирали из 80°С, высушивали с помощью холодного воздуха, а затем промывали с помощью PBS (Wako Pure Chemical), погружали в 1% BSA (Sigma)/10% нормальную ослиную сыворотку (Jackson ImmunoResearch Laboratories)/0,5% Triton X-100 (Wako Pure Chemical)/PBS и подвергали блокированию в течение одного часа, после чего оставляли на ночь с антителом AT8 к фосфорилированному тау-белку (Fujirebio Europe NV) для осуществления реакции при обычных температурах. После трехкратного промывания с помощью PBS оставляли в течение одного часа со вторичным антителом для осуществления реакции. После трехкратного промывания с помощью PBS на срез помещали препятствующий выгоранию флуоресценции реагент Prolong Gold (молекулярные зонды), и фиксировали препарат, и проводили наблюдение с помощью LSM700 (ZEISS). Площадь с положительным сигналом от AT8 в stratum radiatum СА1 гиппокампа измеряли с помощью программного обеспечения для анализа изображений Metamorph и рассчитывали долю площади с AT8-положительным сигналом относительно общей площади.
[0185]
Антитело B уменьшало сигнал фосфорилированного тау-белка в области СА1 гиппокампа (фигура 23). Из указанного результата видно, что антитело В обладало активностью в отношении подавления прогрессирования патологии у трансгенных по тау-белку мышей (rTg4510).
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ЭЙСАЙ Ар ЭНД Ди МЕНЕДЖМЕНТ КО., ЛТД.
<120> Область техники
<130> ESAP1901F
<150> JP2019-122982
<151> 2019-07-01
<160> 62
<170> PatentIn версия 3.5
<210> 1
<211> 986
<212> БЕЛОК
<213> Mus musculus
<400> 1
Met Ala Gly Ile Phe Tyr Phe Ile Leu Phe Ser Phe Leu Phe Gly Ile
1 5 10 15
Cys Asp Ala Val Thr Gly Ser Arg Val Tyr Pro Ala Asn Glu Val Thr
20 25 30
Leu Leu Asp Ser Arg Ser Val Gln Gly Glu Leu Gly Trp Ile Ala Ser
35 40 45
Pro Leu Glu Gly Gly Trp Glu Glu Val Ser Ile Met Asp Glu Lys Asn
50 55 60
Thr Pro Ile Arg Thr Tyr Gln Val Cys Asn Val Met Glu Ala Ser Gln
65 70 75 80
Asn Asn Trp Leu Arg Thr Asp Trp Ile Thr Arg Glu Gly Ala Gln Arg
85 90 95
Val Tyr Ile Glu Ile Lys Phe Thr Leu Arg Asp Cys Asn Ser Leu Pro
100 105 110
Gly Val Met Gly Thr Cys Lys Glu Thr Phe Asn Leu Tyr Tyr Tyr Glu
115 120 125
Ser Asp Asn Asp Lys Glu Arg Phe Ile Arg Glu Ser Gln Phe Gly Lys
130 135 140
Ile Asp Thr Ile Ala Ala Asp Glu Ser Phe Thr Gln Val Asp Ile Gly
145 150 155 160
Asp Arg Ile Met Lys Leu Asn Thr Glu Ile Arg Asp Val Gly Pro Leu
165 170 175
Ser Lys Lys Gly Phe Tyr Leu Ala Phe Gln Asp Val Gly Ala Cys Ile
180 185 190
Ala Leu Val Ser Val Arg Val Phe Tyr Lys Lys Cys Pro Leu Thr Val
195 200 205
Arg Asn Leu Ala Gln Phe Pro Asp Thr Ile Thr Gly Ala Asp Thr Ser
210 215 220
Ser Leu Val Glu Val Arg Gly Ser Cys Val Asn Asn Ser Glu Glu Lys
225 230 235 240
Asp Val Pro Lys Met Tyr Cys Gly Ala Asp Gly Glu Trp Leu Val Pro
245 250 255
Ile Gly Asn Cys Leu Cys Asn Ala Gly His Glu Glu Gln Asn Gly Glu
260 265 270
Cys Gln Ala Cys Lys Ile Gly Tyr Tyr Lys Ala Leu Ser Thr Asp Ala
275 280 285
Ser Cys Ala Lys Cys Pro Pro His Ser Tyr Ser Val Trp Glu Gly Ala
290 295 300
Thr Ser Cys Thr Cys Asp Arg Gly Phe Phe Arg Ala Asp Asn Asp Ala
305 310 315 320
Ala Ser Met Pro Cys Thr Arg Pro Pro Ser Ala Pro Leu Asn Leu Ile
325 330 335
Ser Asn Val Asn Glu Thr Ser Val Asn Leu Glu Trp Ser Ser Pro Gln
340 345 350
Asn Thr Gly Gly Arg Gln Asp Ile Ser Tyr Asn Val Val Cys Lys Lys
355 360 365
Cys Gly Ala Gly Asp Pro Ser Lys Cys Arg Pro Cys Gly Ser Gly Val
370 375 380
His Tyr Thr Pro Gln Gln Asn Gly Leu Lys Thr Thr Arg Val Ser Ile
385 390 395 400
Thr Asp Leu Leu Ala His Thr Asn Tyr Thr Phe Glu Ile Trp Ala Val
405 410 415
Asn Gly Val Ser Lys Tyr Asn Pro Ser Pro Asp Gln Ser Val Ser Val
420 425 430
Thr Val Thr Thr Asn Gln Ala Ala Pro Ser Ser Ile Ala Leu Val Gln
435 440 445
Ala Lys Glu Val Thr Arg Tyr Ser Val Ala Leu Ala Trp Leu Glu Pro
450 455 460
Asp Arg Pro Asn Gly Val Ile Leu Glu Tyr Glu Val Lys Tyr Tyr Glu
465 470 475 480
Lys Asp Gln Asn Glu Arg Ser Tyr Arg Ile Val Arg Thr Ala Ala Arg
485 490 495
Asn Thr Asp Ile Lys Gly Leu Asn Pro Leu Thr Ser Tyr Val Phe His
500 505 510
Val Arg Ala Arg Thr Ala Ala Gly Tyr Gly Asp Phe Ser Glu Pro Leu
515 520 525
Glu Val Thr Thr Asn Thr Val Pro Ser Arg Ile Ile Gly Asp Gly Ala
530 535 540
Asn Ser Thr Val Leu Leu Val Ser Val Ser Gly Ser Val Val Leu Val
545 550 555 560
Val Ile Leu Ile Ala Ala Phe Val Ile Ser Arg Arg Arg Ser Lys Tyr
565 570 575
Ser Lys Ala Lys Gln Glu Ala Asp Glu Glu Lys His Leu Asn Gln Gly
580 585 590
Val Arg Thr Tyr Val Asp Pro Phe Thr Tyr Glu Asp Pro Asn Gln Ala
595 600 605
Val Arg Glu Phe Ala Lys Glu Ile Asp Ala Ser Cys Ile Lys Ile Glu
610 615 620
Lys Val Ile Gly Val Gly Glu Phe Gly Glu Val Cys Ser Gly Arg Leu
625 630 635 640
Lys Val Pro Gly Lys Arg Glu Ile Cys Val Ala Ile Lys Thr Leu Lys
645 650 655
Ala Gly Tyr Thr Asp Lys Gln Arg Arg Asp Phe Leu Ser Glu Ala Ser
660 665 670
Ile Met Gly Gln Phe Asp His Pro Asn Ile Ile His Leu Glu Gly Val
675 680 685
Val Thr Lys Cys Lys Pro Val Met Ile Ile Thr Glu Tyr Met Glu Asn
690 695 700
Gly Ser Leu Asp Ala Phe Leu Arg Lys Asn Asp Gly Arg Phe Thr Val
705 710 715 720
Ile Gln Leu Val Gly Met Leu Arg Gly Ile Gly Ser Gly Met Lys Tyr
725 730 735
Leu Ser Asp Met Ser Tyr Val His Arg Asp Leu Ala Ala Arg Asn Ile
740 745 750
Leu Val Asn Ser Asn Leu Val Cys Lys Val Ser Asp Phe Gly Met Ser
755 760 765
Arg Val Leu Glu Asp Asp Pro Glu Ala Ala Tyr Thr Thr Arg Gly Gly
770 775 780
Lys Ile Pro Ile Arg Trp Thr Ala Pro Glu Ala Ile Ala Tyr Arg Lys
785 790 795 800
Phe Thr Ser Ala Ser Asp Val Trp Ser Tyr Gly Ile Val Met Trp Glu
805 810 815
Val Met Ser Tyr Gly Glu Arg Pro Tyr Trp Asp Met Ser Asn Gln Asp
820 825 830
Val Ile Lys Ala Ile Glu Glu Gly Tyr Arg Leu Pro Pro Pro Met Asp
835 840 845
Cys Pro Ile Ala Leu His Gln Leu Met Leu Asp Cys Trp Gln Lys Glu
850 855 860
Arg Ser Asp Arg Pro Lys Phe Gly Gln Ile Val Asn Met Leu Asp Lys
865 870 875 880
Leu Ile Arg Asn Pro Asn Ser Leu Lys Arg Thr Gly Ser Glu Ser Ser
885 890 895
Arg Pro Asn Thr Ala Leu Leu Asp Pro Ser Ser Pro Glu Phe Ser Ala
900 905 910
Val Val Ser Val Gly Asp Trp Leu Gln Ala Ile Lys Met Asp Arg Tyr
915 920 925
Lys Asp Asn Phe Thr Ala Ala Gly Tyr Thr Thr Leu Glu Ala Val Val
930 935 940
His Met Ser Gln Asp Asp Leu Ala Arg Ile Gly Ile Thr Ala Ile Thr
945 950 955 960
His Gln Asn Lys Ile Leu Ser Ser Val Gln Ala Met Arg Thr Gln Met
965 970 975
Gln Gln Met His Gly Arg Met Val Pro Val
980 985
<210> 2
<211> 528
<212> БЕЛОК
<213> Mus musculus
<400> 2
Val Thr Gly Ser Arg Val Tyr Pro Ala Asn Glu Val Thr Leu Leu Asp
1 5 10 15
Ser Arg Ser Val Gln Gly Glu Leu Gly Trp Ile Ala Ser Pro Leu Glu
20 25 30
Gly Gly Trp Glu Glu Val Ser Ile Met Asp Glu Lys Asn Thr Pro Ile
35 40 45
Arg Thr Tyr Gln Val Cys Asn Val Met Glu Ala Ser Gln Asn Asn Trp
50 55 60
Leu Arg Thr Asp Trp Ile Thr Arg Glu Gly Ala Gln Arg Val Tyr Ile
65 70 75 80
Glu Ile Lys Phe Thr Leu Arg Asp Cys Asn Ser Leu Pro Gly Val Met
85 90 95
Gly Thr Cys Lys Glu Thr Phe Asn Leu Tyr Tyr Tyr Glu Ser Asp Asn
100 105 110
Asp Lys Glu Arg Phe Ile Arg Glu Ser Gln Phe Gly Lys Ile Asp Thr
115 120 125
Ile Ala Ala Asp Glu Ser Phe Thr Gln Val Asp Ile Gly Asp Arg Ile
130 135 140
Met Lys Leu Asn Thr Glu Ile Arg Asp Val Gly Pro Leu Ser Lys Lys
145 150 155 160
Gly Phe Tyr Leu Ala Phe Gln Asp Val Gly Ala Cys Ile Ala Leu Val
165 170 175
Ser Val Arg Val Phe Tyr Lys Lys Cys Pro Leu Thr Val Arg Asn Leu
180 185 190
Ala Gln Phe Pro Asp Thr Ile Thr Gly Ala Asp Thr Ser Ser Leu Val
195 200 205
Glu Val Arg Gly Ser Cys Val Asn Asn Ser Glu Glu Lys Asp Val Pro
210 215 220
Lys Met Tyr Cys Gly Ala Asp Gly Glu Trp Leu Val Pro Ile Gly Asn
225 230 235 240
Cys Leu Cys Asn Ala Gly His Glu Glu Gln Asn Gly Glu Cys Gln Ala
245 250 255
Cys Lys Ile Gly Tyr Tyr Lys Ala Leu Ser Thr Asp Ala Ser Cys Ala
260 265 270
Lys Cys Pro Pro His Ser Tyr Ser Val Trp Glu Gly Ala Thr Ser Cys
275 280 285
Thr Cys Asp Arg Gly Phe Phe Arg Ala Asp Asn Asp Ala Ala Ser Met
290 295 300
Pro Cys Thr Arg Pro Pro Ser Ala Pro Leu Asn Leu Ile Ser Asn Val
305 310 315 320
Asn Glu Thr Ser Val Asn Leu Glu Trp Ser Ser Pro Gln Asn Thr Gly
325 330 335
Gly Arg Gln Asp Ile Ser Tyr Asn Val Val Cys Lys Lys Cys Gly Ala
340 345 350
Gly Asp Pro Ser Lys Cys Arg Pro Cys Gly Ser Gly Val His Tyr Thr
355 360 365
Pro Gln Gln Asn Gly Leu Lys Thr Thr Arg Val Ser Ile Thr Asp Leu
370 375 380
Leu Ala His Thr Asn Tyr Thr Phe Glu Ile Trp Ala Val Asn Gly Val
385 390 395 400
Ser Lys Tyr Asn Pro Ser Pro Asp Gln Ser Val Ser Val Thr Val Thr
405 410 415
Thr Asn Gln Ala Ala Pro Ser Ser Ile Ala Leu Val Gln Ala Lys Glu
420 425 430
Val Thr Arg Tyr Ser Val Ala Leu Ala Trp Leu Glu Pro Asp Arg Pro
435 440 445
Asn Gly Val Ile Leu Glu Tyr Glu Val Lys Tyr Tyr Glu Lys Asp Gln
450 455 460
Asn Glu Arg Ser Tyr Arg Ile Val Arg Thr Ala Ala Arg Asn Thr Asp
465 470 475 480
Ile Lys Gly Leu Asn Pro Leu Thr Ser Tyr Val Phe His Val Arg Ala
485 490 495
Arg Thr Ala Ala Gly Tyr Gly Asp Phe Ser Glu Pro Leu Glu Val Thr
500 505 510
Thr Asn Thr Val Pro Ser Arg Ile Ile Gly Asp Gly Ala Asn Ser Thr
515 520 525
<210> 3
<211> 1030
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 3
Val Thr Gly Ser Arg Val Tyr Pro Ala Asn Glu Val Thr Leu Leu Asp
1 5 10 15
Ser Arg Ser Val Gln Gly Glu Leu Gly Trp Ile Ala Ser Pro Leu Glu
20 25 30
Gly Gly Trp Glu Glu Val Ser Ile Met Asp Glu Lys Asn Thr Pro Ile
35 40 45
Arg Thr Tyr Gln Val Cys Asn Val Met Glu Ala Ser Gln Asn Asn Trp
50 55 60
Leu Arg Thr Asp Trp Ile Thr Arg Glu Gly Ala Gln Arg Val Tyr Ile
65 70 75 80
Glu Ile Lys Phe Thr Leu Arg Asp Cys Asn Ser Leu Pro Gly Val Met
85 90 95
Gly Thr Cys Lys Glu Thr Phe Asn Leu Tyr Tyr Tyr Glu Ser Asp Asn
100 105 110
Asp Lys Glu Arg Phe Ile Arg Glu Ser Gln Phe Gly Lys Ile Asp Thr
115 120 125
Ile Ala Ala Asp Glu Ser Phe Thr Gln Val Asp Ile Gly Asp Arg Ile
130 135 140
Met Lys Leu Asn Thr Glu Ile Arg Asp Val Gly Pro Leu Ser Lys Lys
145 150 155 160
Gly Phe Tyr Leu Ala Phe Gln Asp Val Gly Ala Cys Ile Ala Leu Val
165 170 175
Ser Val Arg Val Phe Tyr Lys Lys Cys Pro Leu Thr Val Arg Asn Leu
180 185 190
Ala Gln Phe Pro Asp Thr Ile Thr Gly Ala Asp Thr Ser Ser Leu Val
195 200 205
Glu Val Arg Gly Ser Cys Val Asn Asn Ser Glu Glu Lys Asp Val Pro
210 215 220
Lys Met Tyr Cys Gly Ala Asp Gly Glu Trp Leu Val Pro Ile Gly Asn
225 230 235 240
Cys Leu Cys Asn Ala Gly His Glu Glu Gln Asn Gly Glu Cys Gln Ala
245 250 255
Cys Lys Ile Gly Tyr Tyr Lys Ala Leu Ser Thr Asp Ala Ser Cys Ala
260 265 270
Lys Cys Pro Pro His Ser Tyr Ser Val Trp Glu Gly Ala Thr Ser Cys
275 280 285
Thr Cys Asp Arg Gly Phe Phe Arg Ala Asp Asn Asp Ala Ala Ser Met
290 295 300
Pro Cys Thr Arg Pro Pro Ser Ala Pro Leu Asn Leu Ile Ser Asn Val
305 310 315 320
Asn Glu Thr Ser Val Asn Leu Glu Trp Ser Ser Pro Gln Asn Thr Gly
325 330 335
Gly Arg Gln Asp Ile Ser Tyr Asn Val Val Cys Lys Lys Cys Gly Ala
340 345 350
Gly Asp Pro Ser Lys Cys Arg Pro Cys Gly Ser Gly Val His Tyr Thr
355 360 365
Pro Gln Gln Asn Gly Leu Lys Thr Thr Arg Val Ser Ile Thr Asp Leu
370 375 380
Leu Ala His Thr Asn Tyr Thr Phe Glu Ile Trp Ala Val Asn Gly Val
385 390 395 400
Ser Lys Tyr Asn Pro Ser Pro Asp Gln Ser Val Ser Val Thr Val Thr
405 410 415
Thr Asn Gln Ala Ala Pro Ser Ser Ile Ala Leu Val Gln Ala Lys Glu
420 425 430
Val Thr Arg Tyr Ser Val Ala Leu Ala Trp Leu Glu Pro Asp Arg Pro
435 440 445
Asn Gly Val Ile Leu Glu Tyr Glu Val Lys Tyr Tyr Glu Lys Asp Gln
450 455 460
Asn Glu Arg Ser Tyr Arg Ile Val Arg Thr Ala Ala Arg Asn Thr Asp
465 470 475 480
Ile Lys Gly Leu Asn Pro Leu Thr Ser Tyr Val Phe His Val Arg Ala
485 490 495
Arg Thr Ala Ala Gly Tyr Gly Asp Phe Ser Glu Pro Leu Glu Val Thr
500 505 510
Thr Asn Thr Val Pro Ser Arg Ile Ile Gly Asp Gly Ala Asn Ser Thr
515 520 525
Ala Ala Ala Ile Ile Pro Val Glu Glu Glu Asn Pro Asp Phe Trp Asn
530 535 540
Arg Glu Ala Ala Glu Ala Leu Gly Ala Ala Lys Lys Leu Gln Pro Ala
545 550 555 560
Gln Thr Ala Ala Lys Asn Leu Ile Ile Phe Leu Gly Asp Gly Met Gly
565 570 575
Val Ser Thr Val Thr Ala Ala Arg Ile Leu Lys Gly Gln Lys Lys Asp
580 585 590
Lys Leu Gly Pro Glu Ile Pro Leu Ala Met Asp Arg Phe Pro Tyr Val
595 600 605
Ala Leu Ser Lys Thr Tyr Asn Val Asp Lys His Val Pro Asp Ser Gly
610 615 620
Ala Thr Ala Thr Ala Tyr Leu Cys Gly Val Lys Gly Asn Phe Gln Thr
625 630 635 640
Ile Gly Leu Ser Ala Ala Ala Arg Phe Asn Gln Cys Asn Thr Thr Arg
645 650 655
Gly Asn Glu Val Ile Ser Val Met Asn Arg Ala Lys Lys Ala Gly Lys
660 665 670
Ser Val Gly Val Val Thr Thr Thr Arg Val Gln His Ala Ser Pro Ala
675 680 685
Gly Thr Tyr Ala His Thr Val Asn Arg Asn Trp Tyr Ser Asp Ala Asp
690 695 700
Val Pro Ala Ser Ala Arg Gln Glu Gly Cys Gln Asp Ile Ala Thr Gln
705 710 715 720
Leu Ile Ser Asn Met Asp Ile Asp Val Ile Leu Gly Gly Gly Arg Lys
725 730 735
Tyr Met Phe Arg Met Gly Thr Pro Asp Pro Glu Tyr Pro Asp Asp Tyr
740 745 750
Ser Gln Gly Gly Thr Arg Leu Asp Gly Lys Asn Leu Val Gln Glu Trp
755 760 765
Leu Ala Lys Arg Gln Gly Ala Arg Tyr Val Trp Asn Arg Thr Glu Leu
770 775 780
Met Gln Ala Ser Leu Asp Pro Ser Val Thr His Leu Met Gly Leu Phe
785 790 795 800
Glu Pro Gly Asp Met Lys Tyr Glu Ile His Arg Asp Ser Thr Leu Asp
805 810 815
Pro Ser Leu Met Glu Met Thr Glu Ala Ala Leu Arg Leu Leu Ser Arg
820 825 830
Asn Pro Arg Gly Phe Phe Leu Phe Val Glu Gly Gly Arg Ile Asp His
835 840 845
Gly His His Glu Ser Arg Ala Tyr Arg Ala Leu Thr Glu Thr Ile Met
850 855 860
Phe Asp Asp Ala Ile Glu Arg Ala Gly Gln Leu Thr Ser Glu Glu Asp
865 870 875 880
Thr Leu Ser Leu Val Thr Ala Asp His Ser His Val Phe Ser Phe Gly
885 890 895
Gly Tyr Pro Leu Arg Gly Ser Ser Ile Phe Gly Leu Ala Pro Gly Lys
900 905 910
Ala Arg Asp Arg Lys Ala Tyr Thr Val Leu Leu Tyr Gly Asn Gly Pro
915 920 925
Gly Tyr Val Leu Lys Asp Gly Ala Arg Pro Asp Val Thr Glu Ser Glu
930 935 940
Ser Gly Ser Pro Glu Tyr Arg Gln Gln Ser Ala Val Pro Leu Asp Glu
945 950 955 960
Glu Thr His Ala Gly Glu Asp Val Ala Val Phe Ala Arg Gly Pro Gln
965 970 975
Ala His Leu Val His Gly Val Gln Glu Gln Thr Phe Ile Ala His Val
980 985 990
Met Ala Phe Ala Ala Cys Leu Glu Pro Tyr Thr Ala Cys Asp Leu Ala
995 1000 1005
Pro Pro Ala Gly Thr Thr Asp Ala Ala His Pro Gly His His His
1010 1015 1020
His His His His His His His
1025 1030
<210> 4
<211> 19
<212> БЕЛОК
<213> Mus musculus
<400> 4
Met Ala Gly Ile Phe Tyr Phe Ile Leu Phe Ser Phe Leu Phe Gly Ile
1 5 10 15
Cys Asp Ala
<210> 5
<211> 986
<212> БЕЛОК
<213> Homo sapiens
<400> 5
Met Ala Gly Ile Phe Tyr Phe Ala Leu Phe Ser Cys Leu Phe Gly Ile
1 5 10 15
Cys Asp Ala Val Thr Gly Ser Arg Val Tyr Pro Ala Asn Glu Val Thr
20 25 30
Leu Leu Asp Ser Arg Ser Val Gln Gly Glu Leu Gly Trp Ile Ala Ser
35 40 45
Pro Leu Glu Gly Gly Trp Glu Glu Val Ser Ile Met Asp Glu Lys Asn
50 55 60
Thr Pro Ile Arg Thr Tyr Gln Val Cys Asn Val Met Glu Pro Ser Gln
65 70 75 80
Asn Asn Trp Leu Arg Thr Asp Trp Ile Thr Arg Glu Gly Ala Gln Arg
85 90 95
Val Tyr Ile Glu Ile Lys Phe Thr Leu Arg Asp Cys Asn Ser Leu Pro
100 105 110
Gly Val Met Gly Thr Cys Lys Glu Thr Phe Asn Leu Tyr Tyr Tyr Glu
115 120 125
Ser Asp Asn Asp Lys Glu Arg Phe Ile Arg Glu Asn Gln Phe Val Lys
130 135 140
Ile Asp Thr Ile Ala Ala Asp Glu Ser Phe Thr Gln Val Asp Ile Gly
145 150 155 160
Asp Arg Ile Met Lys Leu Asn Thr Glu Ile Arg Asp Val Gly Pro Leu
165 170 175
Ser Lys Lys Gly Phe Tyr Leu Ala Phe Gln Asp Val Gly Ala Cys Ile
180 185 190
Ala Leu Val Ser Val Arg Val Phe Tyr Lys Lys Cys Pro Leu Thr Val
195 200 205
Arg Asn Leu Ala Gln Phe Pro Asp Thr Ile Thr Gly Ala Asp Thr Ser
210 215 220
Ser Leu Val Glu Val Arg Gly Ser Cys Val Asn Asn Ser Glu Glu Lys
225 230 235 240
Asp Val Pro Lys Met Tyr Cys Gly Ala Asp Gly Glu Trp Leu Val Pro
245 250 255
Ile Gly Asn Cys Leu Cys Asn Ala Gly His Glu Glu Arg Ser Gly Glu
260 265 270
Cys Gln Ala Cys Lys Ile Gly Tyr Tyr Lys Ala Leu Ser Thr Asp Ala
275 280 285
Thr Cys Ala Lys Cys Pro Pro His Ser Tyr Ser Val Trp Glu Gly Ala
290 295 300
Thr Ser Cys Thr Cys Asp Arg Gly Phe Phe Arg Ala Asp Asn Asp Ala
305 310 315 320
Ala Ser Met Pro Cys Thr Arg Pro Pro Ser Ala Pro Leu Asn Leu Ile
325 330 335
Ser Asn Val Asn Glu Thr Ser Val Asn Leu Glu Trp Ser Ser Pro Gln
340 345 350
Asn Thr Gly Gly Arg Gln Asp Ile Ser Tyr Asn Val Val Cys Lys Lys
355 360 365
Cys Gly Ala Gly Asp Pro Ser Lys Cys Arg Pro Cys Gly Ser Gly Val
370 375 380
His Tyr Thr Pro Gln Gln Asn Gly Leu Lys Thr Thr Lys Val Ser Ile
385 390 395 400
Thr Asp Leu Leu Ala His Thr Asn Tyr Thr Phe Glu Ile Trp Ala Val
405 410 415
Asn Gly Val Ser Lys Tyr Asn Pro Asn Pro Asp Gln Ser Val Ser Val
420 425 430
Thr Val Thr Thr Asn Gln Ala Ala Pro Ser Ser Ile Ala Leu Val Gln
435 440 445
Ala Lys Glu Val Thr Arg Tyr Ser Val Ala Leu Ala Trp Leu Glu Pro
450 455 460
Asp Arg Pro Asn Gly Val Ile Leu Glu Tyr Glu Val Lys Tyr Tyr Glu
465 470 475 480
Lys Asp Gln Asn Glu Arg Ser Tyr Arg Ile Val Arg Thr Ala Ala Arg
485 490 495
Asn Thr Asp Ile Lys Gly Leu Asn Pro Leu Thr Ser Tyr Val Phe His
500 505 510
Val Arg Ala Arg Thr Ala Ala Gly Tyr Gly Asp Phe Ser Glu Pro Leu
515 520 525
Glu Val Thr Thr Asn Thr Val Pro Ser Arg Ile Ile Gly Asp Gly Ala
530 535 540
Asn Ser Thr Val Leu Leu Val Ser Val Ser Gly Ser Val Val Leu Val
545 550 555 560
Val Ile Leu Ile Ala Ala Phe Val Ile Ser Arg Arg Arg Ser Lys Tyr
565 570 575
Ser Lys Ala Lys Gln Glu Ala Asp Glu Glu Lys His Leu Asn Gln Gly
580 585 590
Val Arg Thr Tyr Val Asp Pro Phe Thr Tyr Glu Asp Pro Asn Gln Ala
595 600 605
Val Arg Glu Phe Ala Lys Glu Ile Asp Ala Ser Cys Ile Lys Ile Glu
610 615 620
Lys Val Ile Gly Val Gly Glu Phe Gly Glu Val Cys Ser Gly Arg Leu
625 630 635 640
Lys Val Pro Gly Lys Arg Glu Ile Cys Val Ala Ile Lys Thr Leu Lys
645 650 655
Ala Gly Tyr Thr Asp Lys Gln Arg Arg Asp Phe Leu Ser Glu Ala Ser
660 665 670
Ile Met Gly Gln Phe Asp His Pro Asn Ile Ile His Leu Glu Gly Val
675 680 685
Val Thr Lys Cys Lys Pro Val Met Ile Ile Thr Glu Tyr Met Glu Asn
690 695 700
Gly Ser Leu Asp Ala Phe Leu Arg Lys Asn Asp Gly Arg Phe Thr Val
705 710 715 720
Ile Gln Leu Val Gly Met Leu Arg Gly Ile Gly Ser Gly Met Lys Tyr
725 730 735
Leu Ser Asp Met Ser Tyr Val His Arg Asp Leu Ala Ala Arg Asn Ile
740 745 750
Leu Val Asn Ser Asn Leu Val Cys Lys Val Ser Asp Phe Gly Met Ser
755 760 765
Arg Val Leu Glu Asp Asp Pro Glu Ala Ala Tyr Thr Thr Arg Gly Gly
770 775 780
Lys Ile Pro Ile Arg Trp Thr Ala Pro Glu Ala Ile Ala Tyr Arg Lys
785 790 795 800
Phe Thr Ser Ala Ser Asp Val Trp Ser Tyr Gly Ile Val Met Trp Glu
805 810 815
Val Met Ser Tyr Gly Glu Arg Pro Tyr Trp Asp Met Ser Asn Gln Asp
820 825 830
Val Ile Lys Ala Ile Glu Glu Gly Tyr Arg Leu Pro Pro Pro Met Asp
835 840 845
Cys Pro Ile Ala Leu His Gln Leu Met Leu Asp Cys Trp Gln Lys Glu
850 855 860
Arg Ser Asp Arg Pro Lys Phe Gly Gln Ile Val Asn Met Leu Asp Lys
865 870 875 880
Leu Ile Arg Asn Pro Asn Ser Leu Lys Arg Thr Gly Thr Glu Ser Ser
885 890 895
Arg Pro Asn Thr Ala Leu Leu Asp Pro Ser Ser Pro Glu Phe Ser Ala
900 905 910
Val Val Ser Val Gly Asp Trp Leu Gln Ala Ile Lys Met Asp Arg Tyr
915 920 925
Lys Asp Asn Phe Thr Ala Ala Gly Tyr Thr Thr Leu Glu Ala Val Val
930 935 940
His Val Asn Gln Glu Asp Leu Ala Arg Ile Gly Ile Thr Ala Ile Thr
945 950 955 960
His Gln Asn Lys Ile Leu Ser Ser Val Gln Ala Met Arg Thr Gln Met
965 970 975
Gln Gln Met His Gly Arg Met Val Pro Val
980 985
<210> 6
<211> 528
<212> БЕЛОК
<213> Homo sapiens
<400> 6
Val Thr Gly Ser Arg Val Tyr Pro Ala Asn Glu Val Thr Leu Leu Asp
1 5 10 15
Ser Arg Ser Val Gln Gly Glu Leu Gly Trp Ile Ala Ser Pro Leu Glu
20 25 30
Gly Gly Trp Glu Glu Val Ser Ile Met Asp Glu Lys Asn Thr Pro Ile
35 40 45
Arg Thr Tyr Gln Val Cys Asn Val Met Glu Pro Ser Gln Asn Asn Trp
50 55 60
Leu Arg Thr Asp Trp Ile Thr Arg Glu Gly Ala Gln Arg Val Tyr Ile
65 70 75 80
Glu Ile Lys Phe Thr Leu Arg Asp Cys Asn Ser Leu Pro Gly Val Met
85 90 95
Gly Thr Cys Lys Glu Thr Phe Asn Leu Tyr Tyr Tyr Glu Ser Asp Asn
100 105 110
Asp Lys Glu Arg Phe Ile Arg Glu Asn Gln Phe Val Lys Ile Asp Thr
115 120 125
Ile Ala Ala Asp Glu Ser Phe Thr Gln Val Asp Ile Gly Asp Arg Ile
130 135 140
Met Lys Leu Asn Thr Glu Ile Arg Asp Val Gly Pro Leu Ser Lys Lys
145 150 155 160
Gly Phe Tyr Leu Ala Phe Gln Asp Val Gly Ala Cys Ile Ala Leu Val
165 170 175
Ser Val Arg Val Phe Tyr Lys Lys Cys Pro Leu Thr Val Arg Asn Leu
180 185 190
Ala Gln Phe Pro Asp Thr Ile Thr Gly Ala Asp Thr Ser Ser Leu Val
195 200 205
Glu Val Arg Gly Ser Cys Val Asn Asn Ser Glu Glu Lys Asp Val Pro
210 215 220
Lys Met Tyr Cys Gly Ala Asp Gly Glu Trp Leu Val Pro Ile Gly Asn
225 230 235 240
Cys Leu Cys Asn Ala Gly His Glu Glu Arg Ser Gly Glu Cys Gln Ala
245 250 255
Cys Lys Ile Gly Tyr Tyr Lys Ala Leu Ser Thr Asp Ala Thr Cys Ala
260 265 270
Lys Cys Pro Pro His Ser Tyr Ser Val Trp Glu Gly Ala Thr Ser Cys
275 280 285
Thr Cys Asp Arg Gly Phe Phe Arg Ala Asp Asn Asp Ala Ala Ser Met
290 295 300
Pro Cys Thr Arg Pro Pro Ser Ala Pro Leu Asn Leu Ile Ser Asn Val
305 310 315 320
Asn Glu Thr Ser Val Asn Leu Glu Trp Ser Ser Pro Gln Asn Thr Gly
325 330 335
Gly Arg Gln Asp Ile Ser Tyr Asn Val Val Cys Lys Lys Cys Gly Ala
340 345 350
Gly Asp Pro Ser Lys Cys Arg Pro Cys Gly Ser Gly Val His Tyr Thr
355 360 365
Pro Gln Gln Asn Gly Leu Lys Thr Thr Lys Val Ser Ile Thr Asp Leu
370 375 380
Leu Ala His Thr Asn Tyr Thr Phe Glu Ile Trp Ala Val Asn Gly Val
385 390 395 400
Ser Lys Tyr Asn Pro Asn Pro Asp Gln Ser Val Ser Val Thr Val Thr
405 410 415
Thr Asn Gln Ala Ala Pro Ser Ser Ile Ala Leu Val Gln Ala Lys Glu
420 425 430
Val Thr Arg Tyr Ser Val Ala Leu Ala Trp Leu Glu Pro Asp Arg Pro
435 440 445
Asn Gly Val Ile Leu Glu Tyr Glu Val Lys Tyr Tyr Glu Lys Asp Gln
450 455 460
Asn Glu Arg Ser Tyr Arg Ile Val Arg Thr Ala Ala Arg Asn Thr Asp
465 470 475 480
Ile Lys Gly Leu Asn Pro Leu Thr Ser Tyr Val Phe His Val Arg Ala
485 490 495
Arg Thr Ala Ala Gly Tyr Gly Asp Phe Ser Glu Pro Leu Glu Val Thr
500 505 510
Thr Asn Thr Val Pro Ser Arg Ile Ile Gly Asp Gly Ala Asn Ser Thr
515 520 525
<210> 7
<211> 12
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ad29S
<400> 7
acatcactcc gt 12
<210> 8
<211> 50
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ad29AS
<400> 8
acggagtgat gtccgtcgac gtatctctgc gttgatactt cagcgtagct 50
<210> 9
<211> 26
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический праймер
<400> 9
agctacgctg aagtatcaac gcagag 26
<210> 10
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический праймер
<400> 10
gccagtggat agactgatgg 20
<210> 11
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический праймер
<400> 11
gatggataca gttggtgcag c 21
<210> 12
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 12
Met Ala Val Leu Val Leu Leu Leu Cys Leu Val Thr Phe Pro Ser Cys
1 5 10 15
Val Leu Ser
<210> 13
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 13
Gln Val Gln Leu Lys Gln Ser Gly Pro Ser Leu Val Gln Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Arg Tyr
20 25 30
Gly Val His Trp Val Arg Gln Ser Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Arg Gly Gly Ser Thr Asp Tyr Asn Ala Ala Phe Met
50 55 60
Ser Arg Leu Ser Ile Thr Lys Asp Asn Ser Lys Ser Gln Val Phe Phe
65 70 75 80
Lys Met Asn Ser Leu Gln Ala Asp Asp Thr Ala Ile Tyr Tyr Cys Ala
85 90 95
Lys Glu Ser Leu Phe Gly Val Tyr Tyr Asp Tyr Gly Tyr Tyr Ser Met
100 105 110
Asp Tyr Trp Gly Gln Gly Thr Ser Val Thr Val Ser Ser
115 120 125
<210> 14
<211> 22
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 14
Met Asp Met Arg Val Pro Ala His Val Phe Gly Phe Leu Leu Leu Trp
1 5 10 15
Phe Pro Gly Thr Arg Cys
20
<210> 15
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 15
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Ser Leu Thr Cys Arg Ala Ser Gln Glu Ile Ser Gly Tyr
20 25 30
Leu Ser Trp Leu Gln Gln Lys Pro Asp Gly Thr Ile Lys Arg Leu Ile
35 40 45
Tyr Ala Ala Ser Thr Leu Asp Ser Gly Val Pro Lys Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Ser Asp Tyr Ser Leu Thr Ile Ser Ser Leu Glu Ser
65 70 75 80
Glu Asp Phe Ala Asp Tyr Tyr Cys Leu Gln Tyr Ala Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 16
<211> 57
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 16
atggctgtcc tggtgctgct cctctgcctg gtgacattcc caagctgtgt cctgtcc 57
<210> 17
<211> 375
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 17
caggtgcagc tgaagcagtc aggacctagc ctagtgcagc cctcacagag cctgtccata 60
acctgcacag tctctggttt ctcattaact aggtatggtg tacactgggt tcgccagtct 120
ccaggaaagg gtctggagtg gctgggagtg atttggagag gtggaagcac agactacaat 180
gcagctttca tgtccagact gagcatcacc aaggacaact ccaagagcca agttttcttt 240
aaaatgaaca gtctgcaagc tgatgacact gccatatact actgtgccaa agaaagccta 300
tttggggtct actatgatta cgggtactat tctatggact actggggtca aggaacctca 360
gtcaccgtct cctca 375
<210> 18
<211> 66
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 18
atggacatga gggttcctgc tcacgttttt ggcttcttgt tgctctggtt tccaggtacc 60
agatgt 66
<210> 19
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 19
gacatccaaa tgacccagtc tccatcctcc ttatctgcct ctctgggaga aagagtcagt 60
ctcacttgtc gggcaagtca ggaaattagt ggttacttaa gctggcttca gcagaaacca 120
gatggaacta ttaaacgcct gatctacgcc gcatccactt tagattctgg tgtcccaaaa 180
aggttcagtg gcagtaggtc tgggtcagat tattctctca ccatcagcag ccttgagtct 240
gaagattttg cagactatta ctgtctacaa tatgctagtt atccgctcac gttcggtgct 300
gggaccaagc tggagctgaa a 321
<210> 20
<211> 40
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический праймер
<400> 20
gcgaagcttg ccgccaccat ggctgtcctg gtgctgctcc 40
<210> 21
<211> 43
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический праймер
<400> 21
gcgaagcttg ccgccaccat ggacatgagg gttcctgctc acg 43
<210> 22
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический праймер
<400> 22
gcggaattca tcatttacca ggagagtggg agaggc 36
<210> 23
<211> 40
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический праймер
<400> 23
cgcgaattca ctaacactca ttcctgttga agctcttgac 40
<210> 24
<211> 324
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 24
Ala Lys Thr Thr Pro Pro Ser Val Tyr Pro Leu Ala Pro Gly Ser Ala
1 5 10 15
Ala Gln Thr Asn Ser Met Val Thr Leu Gly Cys Leu Val Lys Gly Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Thr Trp Asn Ser Gly Ser Leu Ser Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Asp Leu Tyr Thr Leu
50 55 60
Ser Ser Ser Val Thr Val Pro Ser Ser Thr Trp Pro Ser Glu Thr Val
65 70 75 80
Thr Cys Asn Val Ala His Pro Ala Ser Ser Thr Lys Val Asp Lys Lys
85 90 95
Ile Val Pro Arg Asp Cys Gly Cys Lys Pro Cys Ile Cys Thr Val Pro
100 105 110
Glu Val Ser Ser Val Phe Ile Phe Pro Pro Lys Pro Lys Asp Val Leu
115 120 125
Thr Ile Thr Leu Thr Pro Lys Val Thr Cys Val Val Val Asp Ile Ser
130 135 140
Lys Asp Asp Pro Glu Val Gln Phe Ser Trp Phe Val Asp Asp Val Glu
145 150 155 160
Val His Thr Ala Gln Thr Gln Pro Arg Glu Glu Gln Phe Asn Ser Thr
165 170 175
Phe Arg Ser Val Ser Glu Leu Pro Ile Met His Gln Asp Trp Leu Asn
180 185 190
Gly Lys Glu Phe Lys Cys Arg Val Asn Ser Ala Ala Phe Pro Ala Pro
195 200 205
Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Arg Pro Lys Ala Pro Gln
210 215 220
Val Tyr Thr Ile Pro Pro Pro Lys Glu Gln Met Ala Lys Asp Lys Val
225 230 235 240
Ser Leu Thr Cys Met Ile Thr Asp Phe Phe Pro Glu Asp Ile Thr Val
245 250 255
Glu Trp Gln Trp Asn Gly Gln Pro Ala Glu Asn Tyr Lys Asn Thr Gln
260 265 270
Pro Ile Met Asp Thr Asp Gly Ser Tyr Phe Val Tyr Ser Lys Leu Asn
275 280 285
Val Gln Lys Ser Asn Trp Glu Ala Gly Asn Thr Phe Thr Cys Ser Val
290 295 300
Leu His Glu Gly Leu His Asn His His Thr Glu Lys Ser Leu Ser His
305 310 315 320
Ser Pro Gly Lys
<210> 25
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 25
Arg Ala Asp Ala Ala Pro Thr Val Ser Ile Phe Pro Pro Ser Ser Glu
1 5 10 15
Gln Leu Thr Ser Gly Gly Ala Ser Val Val Cys Phe Leu Asn Asn Phe
20 25 30
Tyr Pro Lys Asp Ile Asn Val Lys Trp Lys Ile Asp Gly Ser Glu Arg
35 40 45
Gln Asn Gly Val Leu Asn Ser Trp Thr Asp Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Met Ser Ser Thr Leu Thr Leu Thr Lys Asp Glu Tyr Glu
65 70 75 80
Arg His Asn Ser Tyr Thr Cys Glu Ala Thr His Lys Thr Ser Thr Ser
85 90 95
Pro Ile Val Lys Ser Phe Asn Arg Asn Glu Cys
100 105
<210> 26
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический пептид
<400> 26
Arg Tyr Gly Val His
1 5
<210> 27
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический пептид
<400> 27
Val Ile Trp Arg Gly Gly Ser Thr Asp Tyr Asn Ala Ala Phe Met Ser
1 5 10 15
<210> 28
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический пептид
<400> 28
Glu Ser Leu Phe Gly Val Tyr Tyr Asp Tyr Gly Tyr Tyr Ser Met Asp
1 5 10 15
Tyr
<210> 29
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический пептид
<400> 29
Arg Ala Ser Gln Glu Ile Ser Gly Tyr Leu Ser
1 5 10
<210> 30
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический пептид
<400> 30
Ala Ala Ser Thr Leu Asp Ser
1 5
<210> 31
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический пептид
<400> 31
Leu Gln Tyr Ala Ser Tyr Pro Leu Thr
1 5
<210> 32
<211> 986
<212> БЕЛОК
<213> Macaca mulatta
<400> 32
Met Ala Gly Ile Phe Tyr Phe Ala Leu Phe Ser Cys Leu Phe Gly Ile
1 5 10 15
Cys Asp Ala Val Thr Gly Ser Arg Val Tyr Pro Ala Asn Glu Val Thr
20 25 30
Leu Leu Asp Ser Arg Ser Val Gln Gly Glu Leu Gly Trp Ile Ala Ser
35 40 45
Pro Leu Glu Gly Gly Trp Glu Glu Val Ser Ile Met Asp Glu Lys Asn
50 55 60
Thr Pro Ile Arg Thr Tyr Gln Val Cys Asn Val Met Glu Pro Ser Gln
65 70 75 80
Asn Asn Trp Leu Arg Thr Asp Trp Ile Thr Arg Glu Gly Ala Gln Arg
85 90 95
Val Tyr Ile Glu Ile Lys Phe Thr Leu Arg Asp Cys Asn Ser Leu Pro
100 105 110
Gly Val Met Gly Thr Cys Lys Glu Thr Phe Asn Leu Tyr Tyr Tyr Glu
115 120 125
Ser Asp Asn Asp Lys Glu Arg Phe Ile Arg Glu Asn Gln Phe Val Lys
130 135 140
Ile Asp Thr Ile Ala Ala Asp Glu Ser Phe Thr Gln Val Asp Ile Gly
145 150 155 160
Asp Arg Ile Met Lys Leu Asn Thr Glu Ile Arg Asp Val Gly Pro Leu
165 170 175
Ser Lys Lys Gly Phe Tyr Leu Ala Phe Gln Asp Val Gly Ala Cys Ile
180 185 190
Ala Leu Val Ser Val Arg Val Phe Tyr Lys Lys Cys Pro Leu Thr Val
195 200 205
Arg Asn Leu Ala Gln Phe Pro Asp Thr Ile Thr Gly Ala Asp Thr Ser
210 215 220
Ser Leu Val Glu Val Arg Gly Ser Cys Val Asn Asn Ser Glu Glu Lys
225 230 235 240
Asp Val Pro Lys Met Tyr Cys Gly Ala Asp Gly Glu Trp Leu Val Pro
245 250 255
Ile Gly Asn Cys Leu Cys Asn Ala Gly His Glu Glu Arg Ser Gly Glu
260 265 270
Cys Gln Ala Cys Lys Ile Gly Tyr Tyr Lys Ala Leu Ser Thr Asp Ala
275 280 285
Thr Cys Ala Lys Cys Pro Pro His Ser Tyr Ser Val Trp Glu Gly Ala
290 295 300
Thr Ser Cys Thr Cys Asp Arg Gly Phe Phe Arg Ala Asp Asn Asp Ala
305 310 315 320
Ala Ser Met Pro Cys Thr Arg Pro Pro Ser Ala Pro Leu Asn Leu Ile
325 330 335
Ser Asn Val Asn Glu Thr Ser Val Asn Leu Glu Trp Ser Ser Pro Gln
340 345 350
Asn Thr Gly Gly Arg Gln Asp Ile Ser Tyr Asn Val Val Cys Lys Lys
355 360 365
Cys Gly Ala Gly Asp Pro Ser Lys Cys Arg Pro Cys Gly Ser Gly Val
370 375 380
His Tyr Thr Pro Gln Gln Asn Gly Leu Lys Thr Thr Lys Val Ser Ile
385 390 395 400
Thr Asp Leu Leu Ala His Thr Asn Tyr Thr Phe Glu Ile Trp Ala Val
405 410 415
Asn Gly Val Ser Lys Tyr Asn Pro Ser Pro Asp Gln Ser Val Ser Val
420 425 430
Thr Val Thr Thr Asn Gln Ala Ala Pro Ser Ser Ile Ala Leu Val Gln
435 440 445
Ala Lys Glu Val Thr Arg Tyr Ser Val Ala Leu Ala Trp Leu Glu Pro
450 455 460
Asp Arg Pro Asn Gly Val Ile Leu Glu Tyr Glu Val Lys Tyr Tyr Glu
465 470 475 480
Lys Asp Gln Asn Glu Arg Ser Tyr Arg Ile Val Arg Thr Ala Ala Arg
485 490 495
Asn Thr Asp Ile Lys Gly Leu Asn Pro Leu Thr Ser Tyr Val Phe His
500 505 510
Val Arg Ala Arg Thr Ala Ala Gly Tyr Gly Asp Phe Ser Glu Pro Leu
515 520 525
Glu Val Thr Thr Asn Thr Val Pro Ser Arg Ile Ile Gly Asp Gly Ala
530 535 540
Asn Ser Thr Val Leu Leu Val Ser Val Ser Gly Ser Val Val Leu Val
545 550 555 560
Val Ile Leu Ile Ala Ala Phe Val Ile Ser Arg Arg Arg Ser Lys Tyr
565 570 575
Ser Lys Ala Lys Gln Glu Ala Asp Glu Glu Lys His Leu Asn Gln Gly
580 585 590
Val Arg Thr Tyr Val Asp Pro Phe Thr Tyr Glu Asp Pro Asn Gln Ala
595 600 605
Val Arg Glu Phe Ala Lys Glu Ile Asp Ala Ser Cys Ile Lys Ile Glu
610 615 620
Lys Val Ile Gly Val Gly Glu Phe Gly Glu Val Cys Ser Gly Arg Leu
625 630 635 640
Lys Val Pro Gly Lys Arg Glu Ile Cys Val Ala Ile Lys Thr Leu Lys
645 650 655
Ala Gly Tyr Thr Asp Lys Gln Arg Arg Asp Phe Leu Ser Glu Ala Ser
660 665 670
Ile Met Gly Gln Phe Asp His Pro Asn Ile Ile His Leu Glu Gly Val
675 680 685
Val Thr Lys Cys Lys Pro Val Met Ile Ile Thr Glu Tyr Met Glu Asn
690 695 700
Gly Ser Leu Asp Ala Phe Leu Arg Lys Asn Asp Gly Arg Phe Thr Val
705 710 715 720
Ile Gln Leu Val Gly Met Leu Arg Gly Ile Gly Ser Gly Met Lys Tyr
725 730 735
Leu Ser Asp Met Ser Tyr Val His Arg Asp Leu Ala Ala Arg Asn Ile
740 745 750
Leu Val Asn Ser Asn Leu Val Cys Lys Val Ser Asp Phe Gly Met Ser
755 760 765
Arg Val Leu Glu Asp Asp Pro Glu Ala Ala Tyr Thr Thr Arg Gly Gly
770 775 780
Lys Ile Pro Ile Arg Trp Thr Ala Pro Glu Ala Ile Ala Tyr Arg Lys
785 790 795 800
Phe Thr Ser Ala Ser Asp Val Trp Ser Tyr Gly Ile Val Met Trp Glu
805 810 815
Val Met Ser Tyr Gly Glu Arg Pro Tyr Trp Asp Met Ser Asn Gln Asp
820 825 830
Val Ile Lys Ala Ile Glu Glu Gly Tyr Arg Leu Pro Pro Pro Met Asp
835 840 845
Cys Pro Ile Ala Leu His Gln Leu Met Leu Asp Cys Trp Gln Lys Glu
850 855 860
Arg Ser Asp Arg Pro Lys Phe Gly Gln Ile Val Asn Met Leu Asp Lys
865 870 875 880
Leu Ile Arg Asn Pro Asn Ser Leu Lys Arg Thr Gly Thr Glu Ser Ser
885 890 895
Arg Pro Asn Thr Ala Leu Leu Asp Pro Ser Ser Pro Glu Phe Ser Ala
900 905 910
Val Val Ser Val Gly Asp Trp Leu Gln Ala Ile Lys Met Asp Arg Tyr
915 920 925
Lys Asp Asn Phe Thr Ala Ala Gly Tyr Thr Thr Leu Glu Ala Val Val
930 935 940
His Val Asn Gln Glu Asp Leu Ala Arg Ile Gly Ile Thr Ala Ile Thr
945 950 955 960
His Gln Asn Lys Ile Leu Ser Ser Val Gln Ala Met Arg Thr Gln Met
965 970 975
Gln Gln Met His Gly Arg Met Val Pro Val
980 985
<210> 33
<211> 528
<212> БЕЛОК
<213> Macaca mulatta
<400> 33
Val Thr Gly Ser Arg Val Tyr Pro Ala Asn Glu Val Thr Leu Leu Asp
1 5 10 15
Ser Arg Ser Val Gln Gly Glu Leu Gly Trp Ile Ala Ser Pro Leu Glu
20 25 30
Gly Gly Trp Glu Glu Val Ser Ile Met Asp Glu Lys Asn Thr Pro Ile
35 40 45
Arg Thr Tyr Gln Val Cys Asn Val Met Glu Pro Ser Gln Asn Asn Trp
50 55 60
Leu Arg Thr Asp Trp Ile Thr Arg Glu Gly Ala Gln Arg Val Tyr Ile
65 70 75 80
Glu Ile Lys Phe Thr Leu Arg Asp Cys Asn Ser Leu Pro Gly Val Met
85 90 95
Gly Thr Cys Lys Glu Thr Phe Asn Leu Tyr Tyr Tyr Glu Ser Asp Asn
100 105 110
Asp Lys Glu Arg Phe Ile Arg Glu Asn Gln Phe Val Lys Ile Asp Thr
115 120 125
Ile Ala Ala Asp Glu Ser Phe Thr Gln Val Asp Ile Gly Asp Arg Ile
130 135 140
Met Lys Leu Asn Thr Glu Ile Arg Asp Val Gly Pro Leu Ser Lys Lys
145 150 155 160
Gly Phe Tyr Leu Ala Phe Gln Asp Val Gly Ala Cys Ile Ala Leu Val
165 170 175
Ser Val Arg Val Phe Tyr Lys Lys Cys Pro Leu Thr Val Arg Asn Leu
180 185 190
Ala Gln Phe Pro Asp Thr Ile Thr Gly Ala Asp Thr Ser Ser Leu Val
195 200 205
Glu Val Arg Gly Ser Cys Val Asn Asn Ser Glu Glu Lys Asp Val Pro
210 215 220
Lys Met Tyr Cys Gly Ala Asp Gly Glu Trp Leu Val Pro Ile Gly Asn
225 230 235 240
Cys Leu Cys Asn Ala Gly His Glu Glu Arg Ser Gly Glu Cys Gln Ala
245 250 255
Cys Lys Ile Gly Tyr Tyr Lys Ala Leu Ser Thr Asp Ala Thr Cys Ala
260 265 270
Lys Cys Pro Pro His Ser Tyr Ser Val Trp Glu Gly Ala Thr Ser Cys
275 280 285
Thr Cys Asp Arg Gly Phe Phe Arg Ala Asp Asn Asp Ala Ala Ser Met
290 295 300
Pro Cys Thr Arg Pro Pro Ser Ala Pro Leu Asn Leu Ile Ser Asn Val
305 310 315 320
Asn Glu Thr Ser Val Asn Leu Glu Trp Ser Ser Pro Gln Asn Thr Gly
325 330 335
Gly Arg Gln Asp Ile Ser Tyr Asn Val Val Cys Lys Lys Cys Gly Ala
340 345 350
Gly Asp Pro Ser Lys Cys Arg Pro Cys Gly Ser Gly Val His Tyr Thr
355 360 365
Pro Gln Gln Asn Gly Leu Lys Thr Thr Lys Val Ser Ile Thr Asp Leu
370 375 380
Leu Ala His Thr Asn Tyr Thr Phe Glu Ile Trp Ala Val Asn Gly Val
385 390 395 400
Ser Lys Tyr Asn Pro Ser Pro Asp Gln Ser Val Ser Val Thr Val Thr
405 410 415
Thr Asn Gln Ala Ala Pro Ser Ser Ile Ala Leu Val Gln Ala Lys Glu
420 425 430
Val Thr Arg Tyr Ser Val Ala Leu Ala Trp Leu Glu Pro Asp Arg Pro
435 440 445
Asn Gly Val Ile Leu Glu Tyr Glu Val Lys Tyr Tyr Glu Lys Asp Gln
450 455 460
Asn Glu Arg Ser Tyr Arg Ile Val Arg Thr Ala Ala Arg Asn Thr Asp
465 470 475 480
Ile Lys Gly Leu Asn Pro Leu Thr Ser Tyr Val Phe His Val Arg Ala
485 490 495
Arg Thr Ala Ala Gly Tyr Gly Asp Phe Ser Glu Pro Leu Glu Val Thr
500 505 510
Thr Asn Thr Val Pro Ser Arg Ile Ile Gly Asp Gly Ala Asn Ser Thr
515 520 525
<210> 34
<211> 19
<212> БЕЛОК
<213> Homo sapiens
<400> 34
Met Ala Gly Ile Phe Tyr Phe Ala Leu Phe Ser Cys Leu Phe Gly Ile
1 5 10 15
Cys Asp Ala
<210> 35
<211> 15
<212> БЕЛОК
<213> Homo sapiens
<400> 35
Met Ser Ala Leu Leu Ile Leu Ala Leu Val Gly Ala Ala Val Ala
1 5 10 15
<210> 36
<211> 547
<212> БЕЛОК
<213> Homo sapiens
<400> 36
Met Ala Gly Ile Phe Tyr Phe Ala Leu Phe Ser Cys Leu Phe Gly Ile
1 5 10 15
Cys Asp Ala Val Thr Gly Ser Arg Val Tyr Pro Ala Asn Glu Val Thr
20 25 30
Leu Leu Asp Ser Arg Ser Val Gln Gly Glu Leu Gly Trp Ile Ala Ser
35 40 45
Pro Leu Glu Gly Gly Trp Glu Glu Val Ser Ile Met Asp Glu Lys Asn
50 55 60
Thr Pro Ile Arg Thr Tyr Gln Val Cys Asn Val Met Glu Pro Ser Gln
65 70 75 80
Asn Asn Trp Leu Arg Thr Asp Trp Ile Thr Arg Glu Gly Ala Gln Arg
85 90 95
Val Tyr Ile Glu Ile Lys Phe Thr Leu Arg Asp Cys Asn Ser Leu Pro
100 105 110
Gly Val Met Gly Thr Cys Lys Glu Thr Phe Asn Leu Tyr Tyr Tyr Glu
115 120 125
Ser Asp Asn Asp Lys Glu Arg Phe Ile Arg Glu Asn Gln Phe Val Lys
130 135 140
Ile Asp Thr Ile Ala Ala Asp Glu Ser Phe Thr Gln Val Asp Ile Gly
145 150 155 160
Asp Arg Ile Met Lys Leu Asn Thr Glu Ile Arg Asp Val Gly Pro Leu
165 170 175
Ser Lys Lys Gly Phe Tyr Leu Ala Phe Gln Asp Val Gly Ala Cys Ile
180 185 190
Ala Leu Val Ser Val Arg Val Phe Tyr Lys Lys Cys Pro Leu Thr Val
195 200 205
Arg Asn Leu Ala Gln Phe Pro Asp Thr Ile Thr Gly Ala Asp Thr Ser
210 215 220
Ser Leu Val Glu Val Arg Gly Ser Cys Val Asn Asn Ser Glu Glu Lys
225 230 235 240
Asp Val Pro Lys Met Tyr Cys Gly Ala Asp Gly Glu Trp Leu Val Pro
245 250 255
Ile Gly Asn Cys Leu Cys Asn Ala Gly His Glu Glu Arg Ser Gly Glu
260 265 270
Cys Gln Ala Cys Lys Ile Gly Tyr Tyr Lys Ala Leu Ser Thr Asp Ala
275 280 285
Thr Cys Ala Lys Cys Pro Pro His Ser Tyr Ser Val Trp Glu Gly Ala
290 295 300
Thr Ser Cys Thr Cys Asp Arg Gly Phe Phe Arg Ala Asp Asn Asp Ala
305 310 315 320
Ala Ser Met Pro Cys Thr Arg Pro Pro Ser Ala Pro Leu Asn Leu Ile
325 330 335
Ser Asn Val Asn Glu Thr Ser Val Asn Leu Glu Trp Ser Ser Pro Gln
340 345 350
Asn Thr Gly Gly Arg Gln Asp Ile Ser Tyr Asn Val Val Cys Lys Lys
355 360 365
Cys Gly Ala Gly Asp Pro Ser Lys Cys Arg Pro Cys Gly Ser Gly Val
370 375 380
His Tyr Thr Pro Gln Gln Asn Gly Leu Lys Thr Thr Lys Val Ser Ile
385 390 395 400
Thr Asp Leu Leu Ala His Thr Asn Tyr Thr Phe Glu Ile Trp Ala Val
405 410 415
Asn Gly Val Ser Lys Tyr Asn Pro Asn Pro Asp Gln Ser Val Ser Val
420 425 430
Thr Val Thr Thr Asn Gln Ala Ala Pro Ser Ser Ile Ala Leu Val Gln
435 440 445
Ala Lys Glu Val Thr Arg Tyr Ser Val Ala Leu Ala Trp Leu Glu Pro
450 455 460
Asp Arg Pro Asn Gly Val Ile Leu Glu Tyr Glu Val Lys Tyr Tyr Glu
465 470 475 480
Lys Asp Gln Asn Glu Arg Ser Tyr Arg Ile Val Arg Thr Ala Ala Arg
485 490 495
Asn Thr Asp Ile Lys Gly Leu Asn Pro Leu Thr Ser Tyr Val Phe His
500 505 510
Val Arg Ala Arg Thr Ala Ala Gly Tyr Gly Asp Phe Ser Glu Pro Leu
515 520 525
Glu Val Thr Thr Asn Thr Val Pro Ser Arg Ile Ile Gly Asp Gly Ala
530 535 540
Asn Ser Thr
545
<210> 37
<211> 328
<212> БЕЛОК
<213> Homo sapiens
<400> 37
Met Ala Gly Ile Phe Tyr Phe Ala Leu Phe Ser Cys Leu Phe Gly Ile
1 5 10 15
Cys Asp Ala Val Thr Gly Ser Arg Val Tyr Pro Ala Asn Glu Val Thr
20 25 30
Leu Leu Asp Ser Arg Ser Val Gln Gly Glu Leu Gly Trp Ile Ala Ser
35 40 45
Pro Leu Glu Gly Gly Trp Glu Glu Val Ser Ile Met Asp Glu Lys Asn
50 55 60
Thr Pro Ile Arg Thr Tyr Gln Val Cys Asn Val Met Glu Pro Ser Gln
65 70 75 80
Asn Asn Trp Leu Arg Thr Asp Trp Ile Thr Arg Glu Gly Ala Gln Arg
85 90 95
Val Tyr Ile Glu Ile Lys Phe Thr Leu Arg Asp Cys Asn Ser Leu Pro
100 105 110
Gly Val Met Gly Thr Cys Lys Glu Thr Phe Asn Leu Tyr Tyr Tyr Glu
115 120 125
Ser Asp Asn Asp Lys Glu Arg Phe Ile Arg Glu Asn Gln Phe Val Lys
130 135 140
Ile Asp Thr Ile Ala Ala Asp Glu Ser Phe Thr Gln Val Asp Ile Gly
145 150 155 160
Asp Arg Ile Met Lys Leu Asn Thr Glu Ile Arg Asp Val Gly Pro Leu
165 170 175
Ser Lys Lys Gly Phe Tyr Leu Ala Phe Gln Asp Val Gly Ala Cys Ile
180 185 190
Ala Leu Val Ser Val Arg Val Phe Tyr Lys Lys Cys Pro Leu Thr Val
195 200 205
Arg Asn Leu Ala Gln Phe Pro Asp Thr Ile Thr Gly Ala Asp Thr Ser
210 215 220
Ser Leu Val Glu Val Arg Gly Ser Cys Val Asn Asn Ser Glu Glu Lys
225 230 235 240
Asp Val Pro Lys Met Tyr Cys Gly Ala Asp Gly Glu Trp Leu Val Pro
245 250 255
Ile Gly Asn Cys Leu Cys Asn Ala Gly His Glu Glu Arg Ser Gly Glu
260 265 270
Cys Gln Ala Cys Lys Ile Gly Tyr Tyr Lys Ala Leu Ser Thr Asp Ala
275 280 285
Thr Cys Ala Lys Cys Pro Pro His Ser Tyr Ser Val Trp Glu Gly Ala
290 295 300
Thr Ser Cys Thr Cys Asp Arg Gly Phe Phe Arg Ala Asp Asn Asp Ala
305 310 315 320
Ala Ser Met Pro Cys Thr Arg Pro
325
<210> 38
<211> 236
<212> БЕЛОК
<213> Homo sapiens
<400> 38
Pro Leu Thr Val Arg Asn Leu Ala Gln Phe Pro Asp Thr Ile Thr Gly
1 5 10 15
Ala Asp Thr Ser Ser Leu Val Glu Val Arg Gly Ser Cys Val Asn Asn
20 25 30
Ser Glu Glu Lys Asp Val Pro Lys Met Tyr Cys Gly Ala Asp Gly Glu
35 40 45
Trp Leu Val Pro Ile Gly Asn Cys Leu Cys Asn Ala Gly His Glu Glu
50 55 60
Arg Ser Gly Glu Cys Gln Ala Cys Lys Ile Gly Tyr Tyr Lys Ala Leu
65 70 75 80
Ser Thr Asp Ala Thr Cys Ala Lys Cys Pro Pro His Ser Tyr Ser Val
85 90 95
Trp Glu Gly Ala Thr Ser Cys Thr Cys Asp Arg Gly Phe Phe Arg Ala
100 105 110
Asp Asn Asp Ala Ala Ser Met Pro Cys Thr Arg Pro Pro Ser Ala Pro
115 120 125
Leu Asn Leu Ile Ser Asn Val Asn Glu Thr Ser Val Asn Leu Glu Trp
130 135 140
Ser Ser Pro Gln Asn Thr Gly Gly Arg Gln Asp Ile Ser Tyr Asn Val
145 150 155 160
Val Cys Lys Lys Cys Gly Ala Gly Asp Pro Ser Lys Cys Arg Pro Cys
165 170 175
Gly Ser Gly Val His Tyr Thr Pro Gln Gln Asn Gly Leu Lys Thr Thr
180 185 190
Lys Val Ser Ile Thr Asp Leu Leu Ala His Thr Asn Tyr Thr Phe Glu
195 200 205
Ile Trp Ala Val Asn Gly Val Ser Lys Tyr Asn Pro Asn Pro Asp Gln
210 215 220
Ser Val Ser Val Thr Val Thr Thr Asn Gln Ala Ala
225 230 235
<210> 39
<211> 112
<212> БЕЛОК
<213> Homo sapiens
<400> 39
Thr Asn Gln Ala Ala Pro Ser Ser Ile Ala Leu Val Gln Ala Lys Glu
1 5 10 15
Val Thr Arg Tyr Ser Val Ala Leu Ala Trp Leu Glu Pro Asp Arg Pro
20 25 30
Asn Gly Val Ile Leu Glu Tyr Glu Val Lys Tyr Tyr Glu Lys Asp Gln
35 40 45
Asn Glu Arg Ser Tyr Arg Ile Val Arg Thr Ala Ala Arg Asn Thr Asp
50 55 60
Ile Lys Gly Leu Asn Pro Leu Thr Ser Tyr Val Phe His Val Arg Ala
65 70 75 80
Arg Thr Ala Ala Gly Tyr Gly Asp Phe Ser Glu Pro Leu Glu Val Thr
85 90 95
Thr Asn Thr Val Pro Ser Arg Ile Ile Gly Asp Gly Ala Asn Ser Thr
100 105 110
<210> 40
<211> 96
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 40
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp
20 25 30
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Arg Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln His Asn Ser Tyr Pro Pro
85 90 95
<210> 41
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 41
Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
1 5 10
<210> 42
<211> 98
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 42
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys
<210> 43
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 43
Tyr Tyr Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr
1 5 10 15
Val Ser
<210> 44
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 44
Arg Phe Gly Val His
1 5
<210> 45
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 45
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ser Leu Thr Arg Phe
20 25 30
Gly Val His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Arg Gly Gly Ser Thr Asp Tyr Asn Ala Ala Phe Met
50 55 60
Ser Arg Leu Thr Ile Ser Lys Asp Asn Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys Glu Ser Leu Phe Gly Val Tyr Tyr Asp Tyr Gly Tyr Tyr Ser Met
100 105 110
Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 46
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 46
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Glu Ile Ser Gly Tyr
20 25 30
Leu Ser Trp Leu Gln Gln Lys Pro Gly Lys Ala Pro Lys Arg Leu Ile
35 40 45
Tyr Ala Ala Ser Thr Leu Asp Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Glu Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Tyr Ala Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 47
<211> 326
<212> БЕЛОК
<213> Homo sapiens
<400> 47
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Asn Phe Gly Thr Gln Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Thr Val Glu Arg Lys Ser Cys Val Glu Cys Pro Pro Cys Pro Ala Pro
100 105 110
Pro Ala Ala Ala Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
115 120 125
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
130 135 140
Val Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly
145 150 155 160
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn
165 170 175
Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Val His Gln Asp Trp
180 185 190
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro
195 200 205
Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu
210 215 220
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn
225 230 235 240
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
245 250 255
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
260 265 270
Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
275 280 285
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
290 295 300
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
305 310 315 320
Ser Leu Ser Pro Gly Lys
325
<210> 48
<211> 107
<212> БЕЛОК
<213> Homo sapiens
<400> 48
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 49
<211> 15
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 49
agatttggag tgcat 15
<210> 50
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 50
gtgatctgga ggggaggatc caccgactac aacgctgctt ttatgagc 48
<210> 51
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 51
gagagcctgt tcggcgtgta ctatgactac ggctactatt ctatggatta t 51
<210> 52
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 52
cgcgcctccc aggagatctc tggctacctg tcc 33
<210> 53
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 53
gctgcctcca ccctggactc t 21
<210> 54
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 54
ctgcagtacg cttcctatcc actgacc 27
<210> 55
<211> 375
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 55
caggtgcagc tggtggagag cggaggagga gtggtgcagc ctggcaggtc cctgaggctg 60
agctgtgccg tgtccggctt cagcctgaca agatttggag tgcattgggt gcgccaggct 120
ccaggcaagg gactggagtg ggtggccgtg atctggaggg gaggatccac cgactacaac 180
gctgctttta tgagccggct gacaatctct aaggataact ccaagaatac cgtgtatctg 240
cagatgaact ccctgagggc tgaggacacc gccgtgtact attgcgccaa ggagagcctg 300
ttcggcgtgt actatgacta cggctactat tctatggatt attggggcca gggcaccaca 360
gtgacagtgt cctcc 375
<210> 56
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 56
gatatccaga tgacacagtc cccttccagc ctgtctgcct ccgtgggcga cagagtgacc 60
atcacatgtc gcgcctccca ggagatctct ggctacctgt cctggctgca gcagaagcca 120
ggcaaggctc ccaagcgcct gatctatgct gcctccaccc tggactctgg agtgccttcc 180
aggttcagcg gctctcggtc cggcacagag tacaccctga caatctcttc cctgcagcct 240
gaggatttcg ccacctacta ttgcctgcag tacgcttcct atccactgac ctttggcggc 300
ggcacaaagg tggagatcaa g 321
<210> 57
<211> 978
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 57
gcctccacca agggaccatc cgtgttccca ctggccccat cttcccggag cacatctgag 60
tccaccgccg ctctgggctg tctggtgaag gattacttcc ctgagccagt gacagtgtct 120
tggaactccg gcgctctgac atccggcgtg cacacctttc ctgccgtgct gcagagctct 180
ggcctgtaca gcctgtccag cgtggtgacc gtgccctctt ccaatttcgg cacccagaca 240
tatacctgca acgtggacca taagccttcc aatacaaagg tggataagac cgtggagaga 300
aagagctgcg tggagtgtcc accttgccca gctccaccag ccgctgcccc tagcgtgttc 360
ctgtttcctc caaagccaaa ggacacactg atgatctctc gcacacccga ggtgacctgc 420
gtggtggtgg acgtgtccca cgaggatcca gaggtgcagt ttaactggta cgtggatggc 480
gtggaggtgc ataatgctaa gaccaagccc agggaggagc agttcaactc cacatttcgg 540
gtggtgagcg tgctgaccgt ggtgcaccag gactggctga acggcaagga gtataagtgt 600
aaggtgagca ataagggcct gcccgcccct atcgagaaga caatctctaa gaccaagggc 660
cagcctagag agccacaggt gtacaccctg cccccttctc gcgaggagat gacaaagaac 720
caggtgtccc tgacctgcct ggtgaagggc ttctatccta gcgacatcgc tgtggagtgg 780
gagtctaatg gccagccaga gaacaattac aagaccacac cacccatgct ggacagcgat 840
ggctctttct ttctgtattc taagctgaca gtggataagt ccaggtggca gcagggcaac 900
gtgtttagct gctctgtgat gcatgaggcc ctgcacaatc attacaccca gaagtccctg 960
agcctgtctc caggcaag 978
<210> 58
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 58
aggacagtgg ccgctccatc cgtgttcatc tttcccccta gcgacgagca gctgaagagc 60
ggcaccgcct ctgtggtgtg cctgctgaac aatttctacc ccagggaggc caaggtgcag 120
tggaaggtgg ataacgctct gcagagcggc aattctcagg agtccgtgac cgagcaggac 180
agcaaggatt ctacatattc cctgagctct accctgacac tgagcaaggc cgattacgag 240
aagcacaagg tgtatgcttg cgaggtgacc catcagggcc tgtccagccc agtgacaaag 300
tcttttaaca ggggcgagtg t 321
<210> 59
<211> 451
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 59
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ser Leu Thr Arg Phe
20 25 30
Gly Val His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Arg Gly Gly Ser Thr Asp Tyr Asn Ala Ala Phe Met
50 55 60
Ser Arg Leu Thr Ile Ser Lys Asp Asn Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys Glu Ser Leu Phe Gly Val Tyr Tyr Asp Tyr Gly Tyr Tyr Ser Met
100 105 110
Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Arg Ser Thr Ser
130 135 140
Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Asn Phe Gly Thr Gln Thr Tyr Thr Cys
195 200 205
Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Thr Val Glu
210 215 220
Arg Lys Ser Cys Val Glu Cys Pro Pro Cys Pro Ala Pro Pro Ala Ala
225 230 235 240
Ala Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Phe
290 295 300
Arg Val Val Ser Val Leu Thr Val Val His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Met Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 60
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический полипептид
<400> 60
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Glu Ile Ser Gly Tyr
20 25 30
Leu Ser Trp Leu Gln Gln Lys Pro Gly Lys Ala Pro Lys Arg Leu Ile
35 40 45
Tyr Ala Ala Ser Thr Leu Asp Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Arg Ser Gly Thr Glu Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Tyr Ala Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 61
<211> 1353
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 61
caggtgcagc tggtggagag cggaggagga gtggtgcagc ctggcaggtc cctgaggctg 60
agctgtgccg tgtccggctt cagcctgaca agatttggag tgcattgggt gcgccaggct 120
ccaggcaagg gactggagtg ggtggccgtg atctggaggg gaggatccac cgactacaac 180
gctgctttta tgagccggct gacaatctct aaggataact ccaagaatac cgtgtatctg 240
cagatgaact ccctgagggc tgaggacacc gccgtgtact attgcgccaa ggagagcctg 300
ttcggcgtgt actatgacta cggctactat tctatggatt attggggcca gggcaccaca 360
gtgacagtgt cctccgcctc caccaaggga ccatccgtgt tcccactggc cccatcttcc 420
cggagcacat ctgagtccac cgccgctctg ggctgtctgg tgaaggatta cttccctgag 480
ccagtgacag tgtcttggaa ctccggcgct ctgacatccg gcgtgcacac ctttcctgcc 540
gtgctgcaga gctctggcct gtacagcctg tccagcgtgg tgaccgtgcc ctcttccaat 600
ttcggcaccc agacatatac ctgcaacgtg gaccataagc cttccaatac aaaggtggat 660
aagaccgtgg agagaaagag ctgcgtggag tgtccacctt gcccagctcc accagccgct 720
gcccctagcg tgttcctgtt tcctccaaag ccaaaggaca cactgatgat ctctcgcaca 780
cccgaggtga cctgcgtggt ggtggacgtg tcccacgagg atccagaggt gcagtttaac 840
tggtacgtgg atggcgtgga ggtgcataat gctaagacca agcccaggga ggagcagttc 900
aactccacat ttcgggtggt gagcgtgctg accgtggtgc accaggactg gctgaacggc 960
aaggagtata agtgtaaggt gagcaataag ggcctgcccg cccctatcga gaagacaatc 1020
tctaagacca agggccagcc tagagagcca caggtgtaca ccctgccccc ttctcgcgag 1080
gagatgacaa agaaccaggt gtccctgacc tgcctggtga agggcttcta tcctagcgac 1140
atcgctgtgg agtgggagtc taatggccag ccagagaaca attacaagac cacaccaccc 1200
atgctggaca gcgatggctc tttctttctg tattctaagc tgacagtgga taagtccagg 1260
tggcagcagg gcaacgtgtt tagctgctct gtgatgcatg aggccctgca caatcattac 1320
acccagaagt ccctgagcct gtctccaggc aag 1353
<210> 62
<211> 642
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 62
gatatccaga tgacacagtc cccttccagc ctgtctgcct ccgtgggcga cagagtgacc 60
atcacatgtc gcgcctccca ggagatctct ggctacctgt cctggctgca gcagaagcca 120
ggcaaggctc ccaagcgcct gatctatgct gcctccaccc tggactctgg agtgccttcc 180
aggttcagcg gctctcggtc cggcacagag tacaccctga caatctcttc cctgcagcct 240
gaggatttcg ccacctacta ttgcctgcag tacgcttcct atccactgac ctttggcggc 300
ggcacaaagg tggagatcaa gaggacagtg gccgctccat ccgtgttcat ctttccccct 360
agcgacgagc agctgaagag cggcaccgcc tctgtggtgt gcctgctgaa caatttctac 420
cccagggagg ccaaggtgca gtggaaggtg gataacgctc tgcagagcgg caattctcag 480
gagtccgtga ccgagcagga cagcaaggat tctacatatt ccctgagctc taccctgaca 540
ctgagcaagg ccgattacga gaagcacaag gtgtatgctt gcgaggtgac ccatcagggc 600
ctgtccagcc cagtgacaaa gtcttttaac aggggcgagt gt 642
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛО К EPHA4 | 2016 |
|
RU2719158C2 |
| ВЫДЕЛЕННОЕ АНТИТЕЛО (ВАРИАНТЫ), СПОСОБ ПОЛУЧЕНИЯ АНТИТЕЛА, ВЫДЕЛЕННАЯ НУКЛЕИНОВАЯ КИСЛОТА, ЭКСПРЕССИОННАЯ КАССЕТА (ВАРИАНТЫ), ПЛАЗМИДА (ВАРИАНТЫ), КЛЕТКА-ХОЗЯИН, ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ, НАБОР, СПОСОБ ЛЕЧЕНИЯ БОЛЬНОГО, ПОДВЕРЖЕННОГО РИСКУ ИЛИ СТРАДАЮЩЕГО ОТ ИНФЕКЦИИ E.COLI, И СПОСОБ ДИАГНОСТИКИ ОПРЕДЕЛЕНИЯ ИНФЕКЦИЙ E.COLI | 2014 |
|
RU2724530C2 |
| АНТИТЕЛА К РЕЦЕПТОРУ IL4 ДЛЯ ПРИМЕНЕНИЯ В ВЕТЕРИНАРИИ | 2019 |
|
RU2837141C2 |
| БИСПЕЦИФИЧЕСКОЕ АНТИТЕЛО ПРОТИВ ВИРУСА БЕШЕНСТВА И ЕГО ПРИМЕНЕНИЕ | 2019 |
|
RU2764740C1 |
| ИНДУЦИРУЮЩИЙ ЦИТОТОКСИЧНОСТЬ ТЕРАПЕВТИЧЕСКИЙ АГЕНТ | 2015 |
|
RU2743464C2 |
| АНТИ-IL31 АНТИТЕЛА ДЛЯ ПРИМЕНЕНИЯ В ВЕТЕРИНАРИИ | 2020 |
|
RU2835543C1 |
| Биспецифическое антитело анти-HER2/анти-4-1BB и его применение | 2020 |
|
RU2831838C2 |
| АНТИТЕЛО ПРОТИВ LILRB1 И ЕГО ПРИМЕНЕНИЯ | 2021 |
|
RU2813373C1 |
| КОНСТРУКЦИИ СЛИТОГО БЕЛКА ДЛЯ ЗАБОЛЕВАНИЯ, СВЯЗАННОГО С КОМПЛЕМЕНТОМ | 2019 |
|
RU2824402C2 |
| НАЦЕЛЕННЫЕ НА ОПУХОЛЬ АГОНИСТИЧЕСКИЕ CD28-АНТИГЕНСВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2019 |
|
RU2837821C1 |
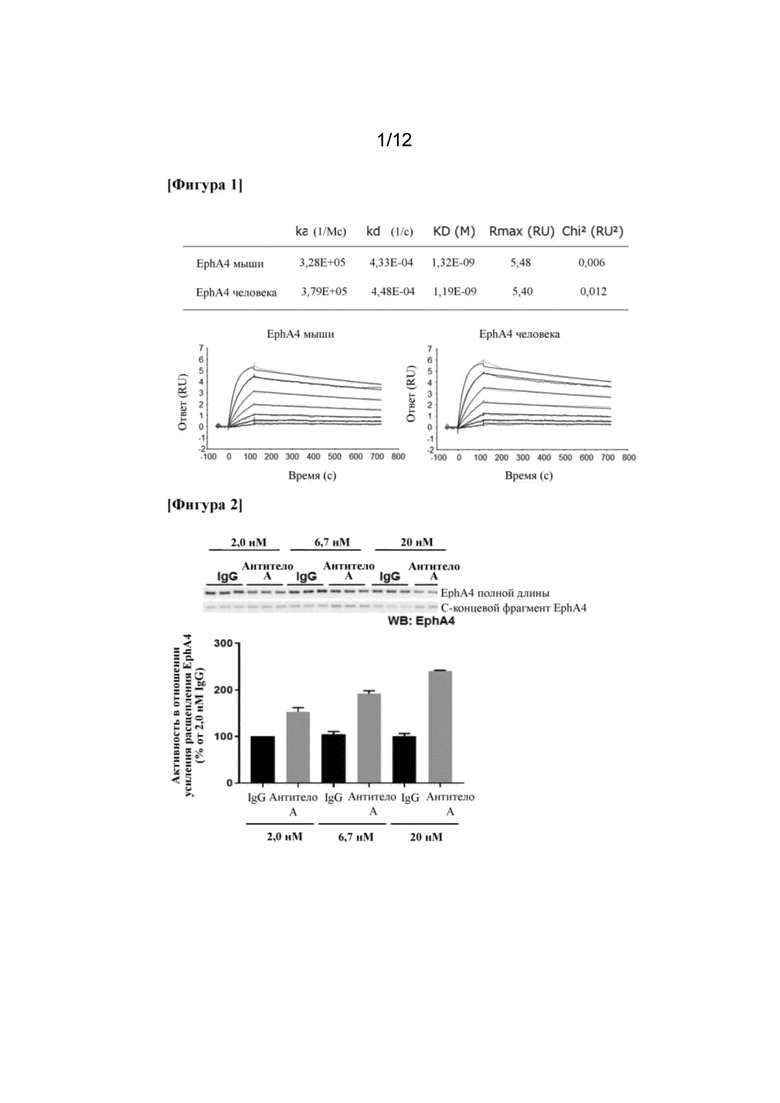
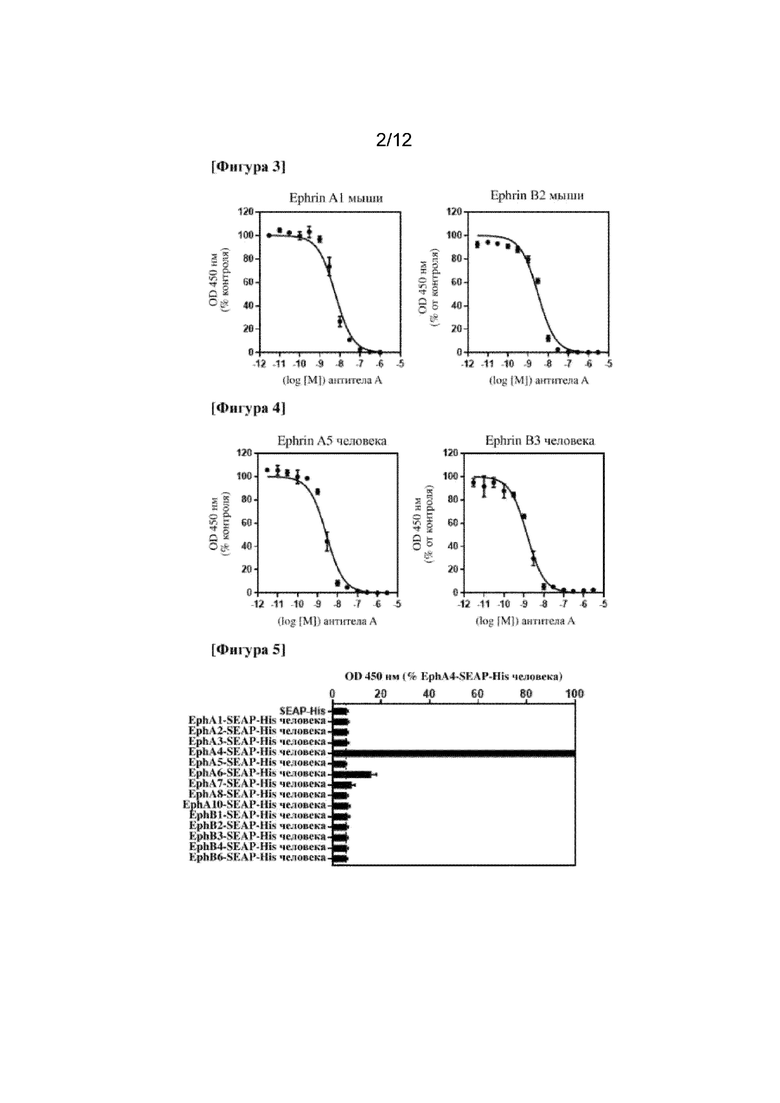
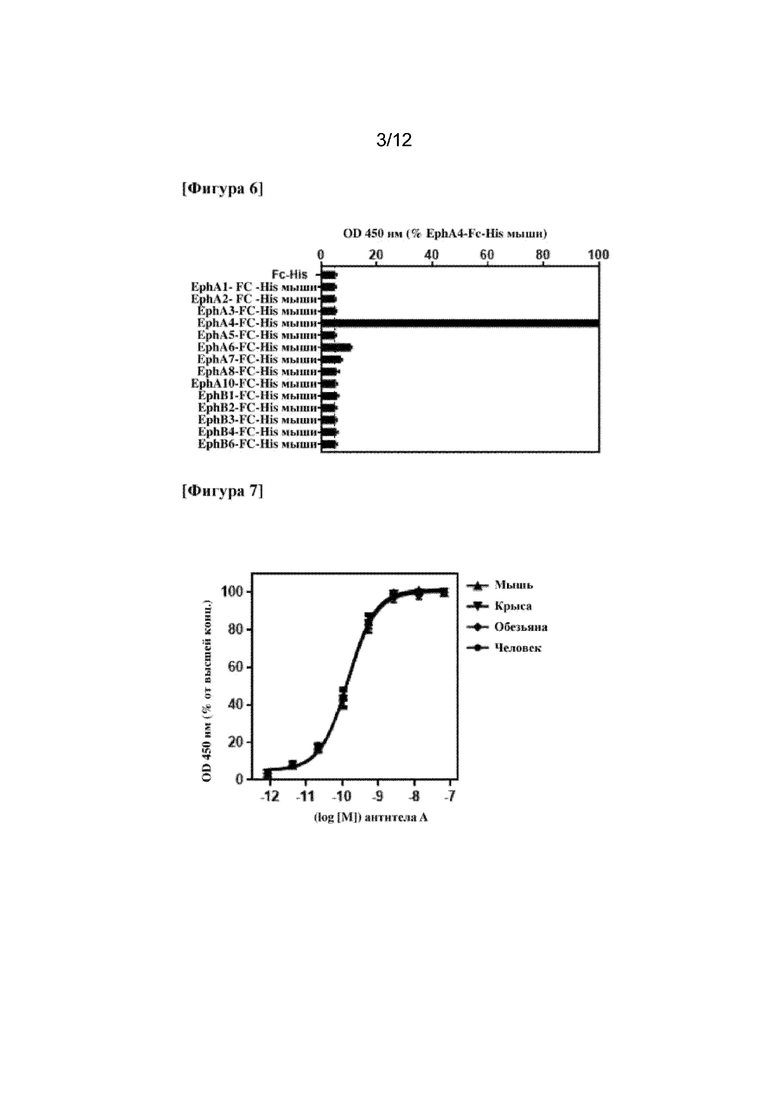
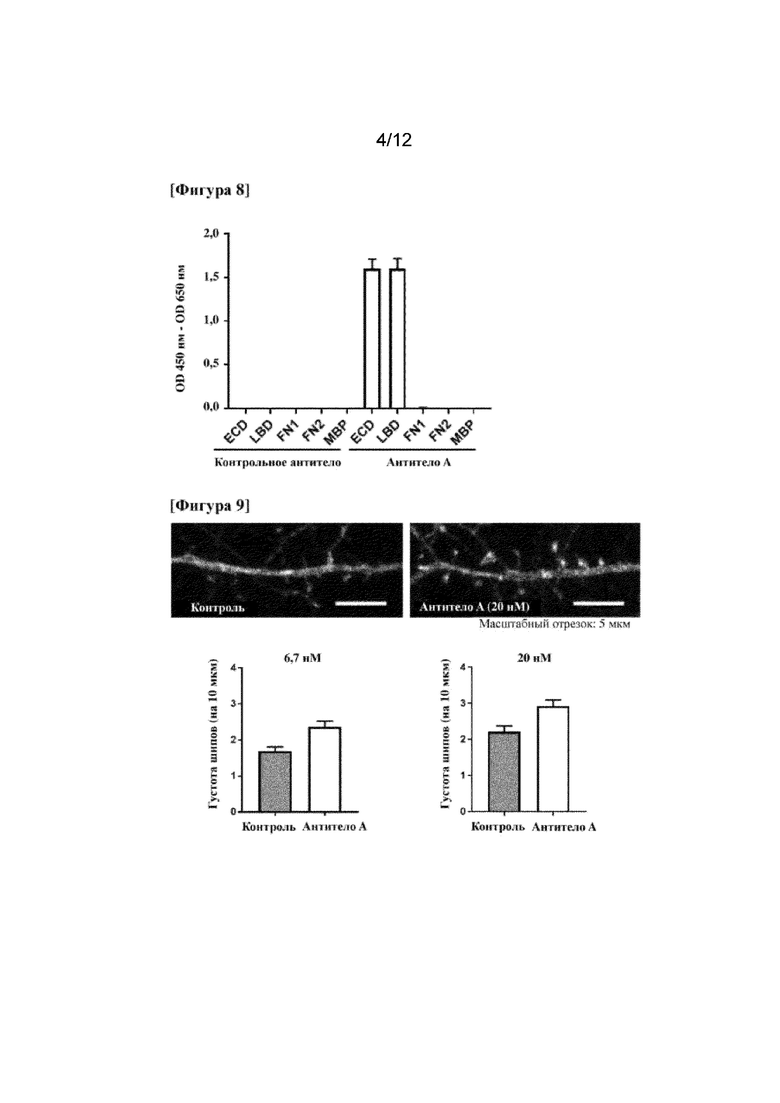
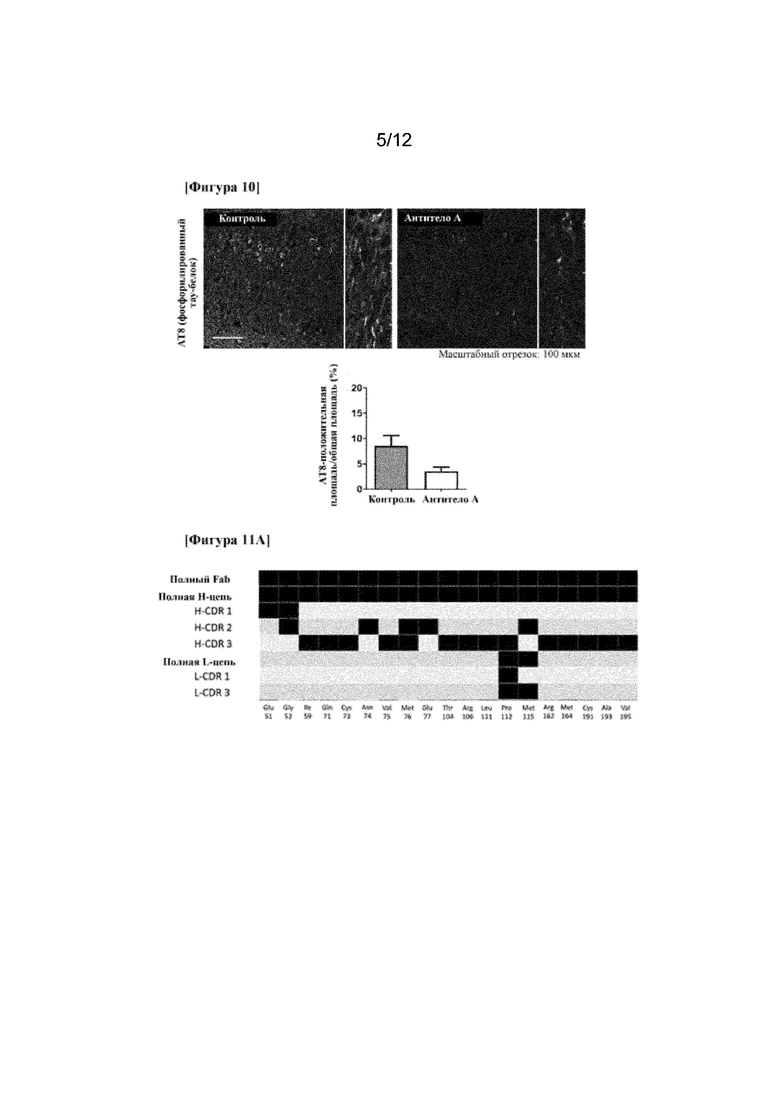
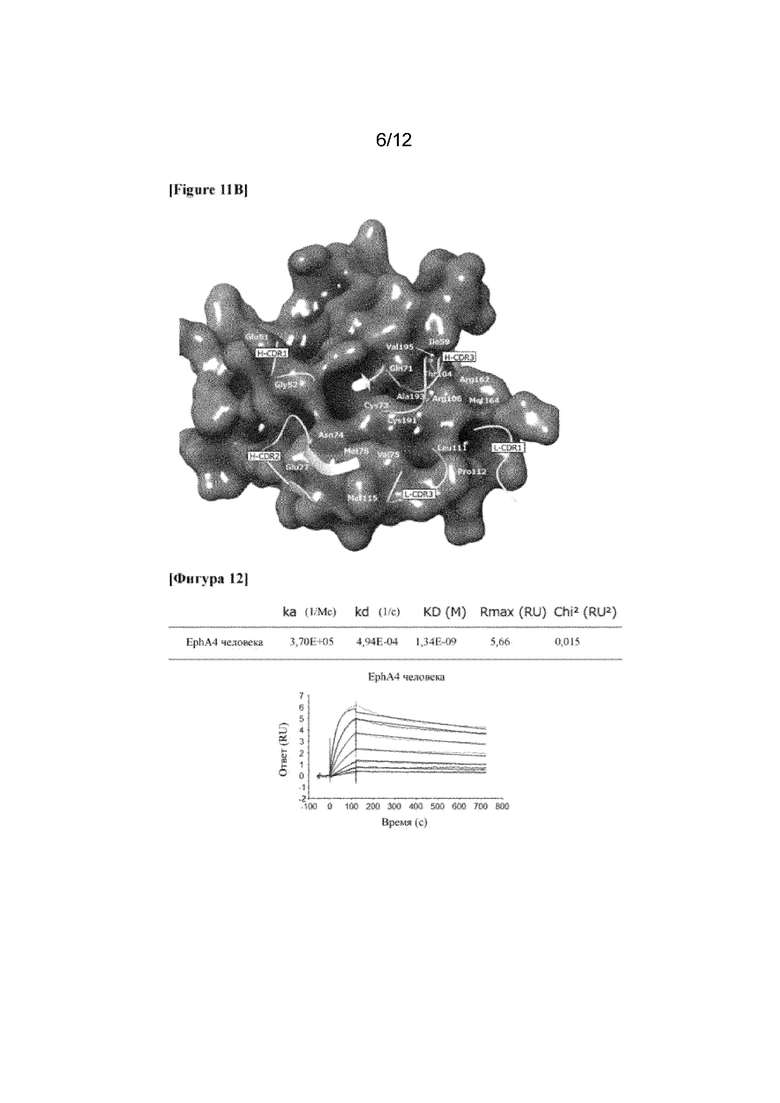
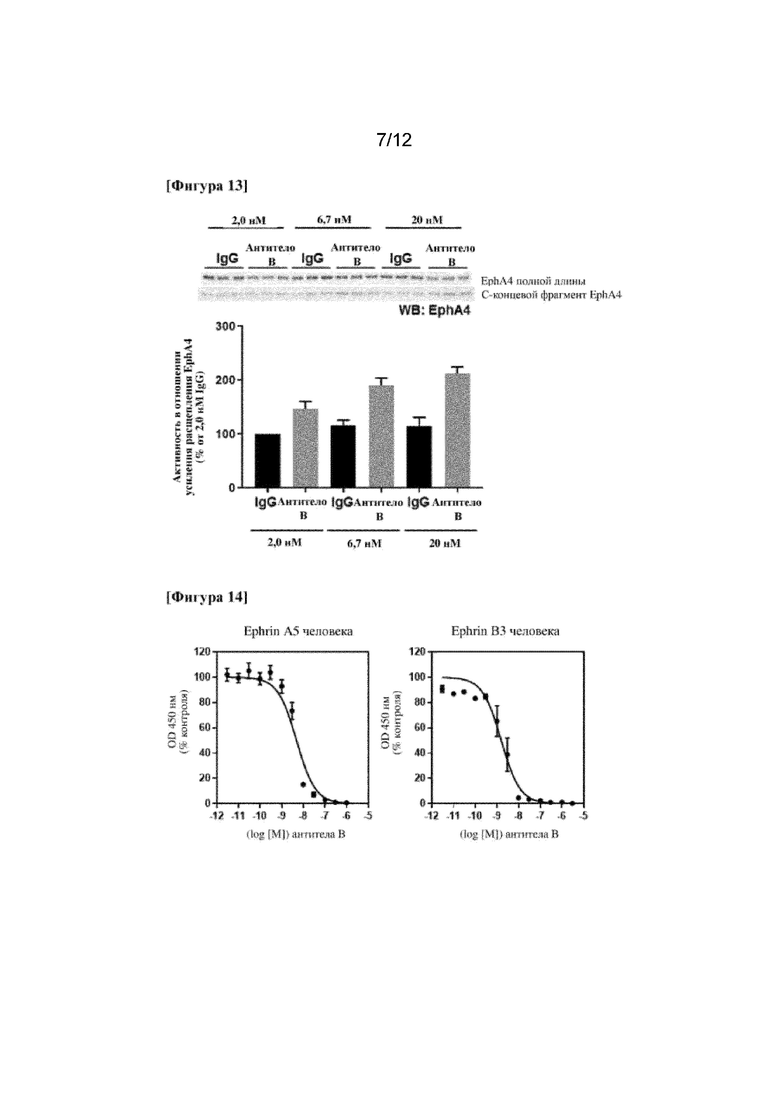
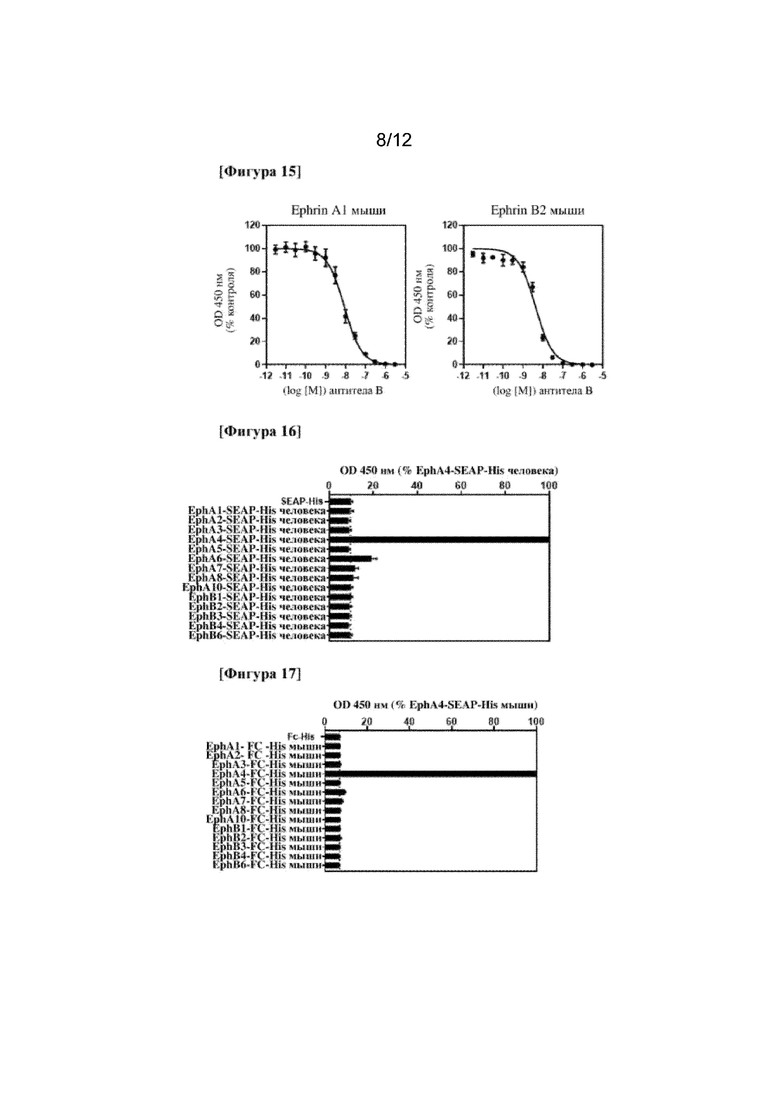
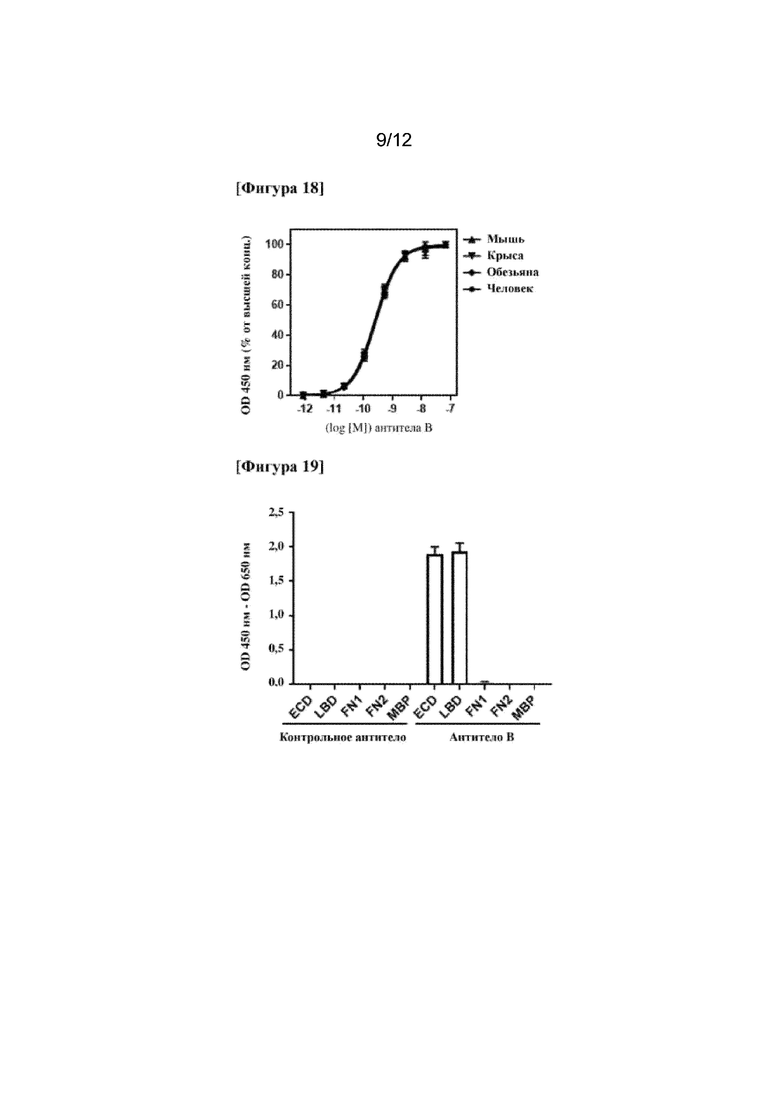
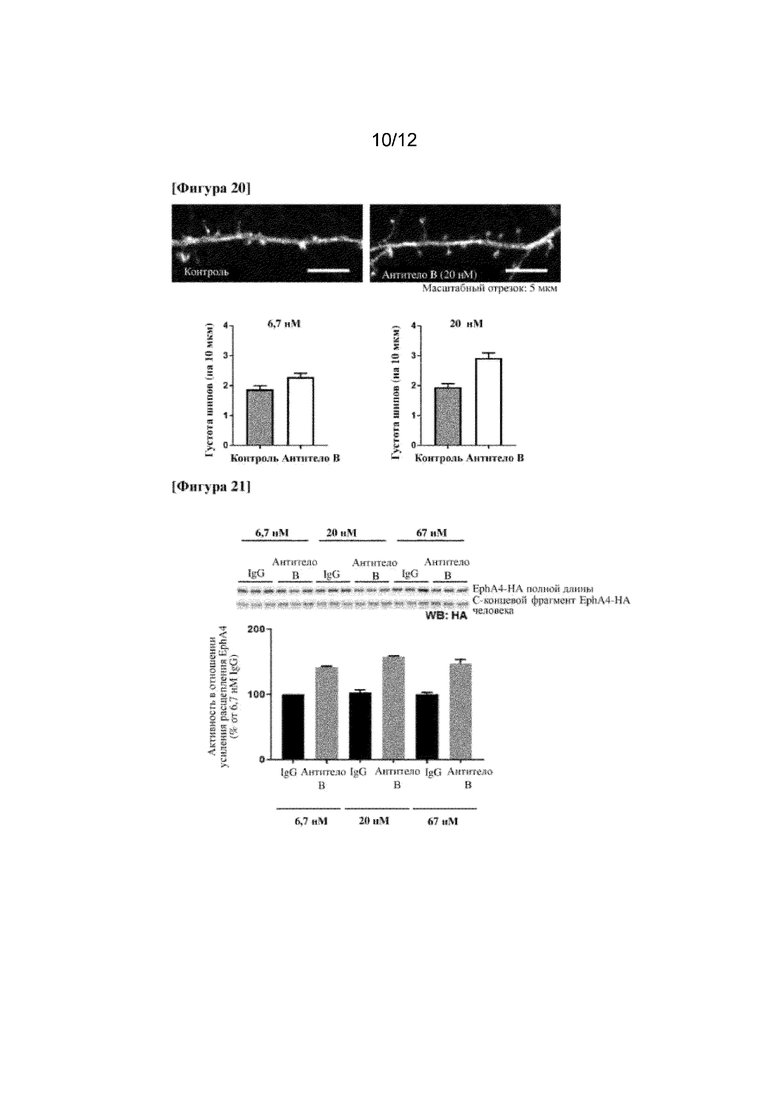
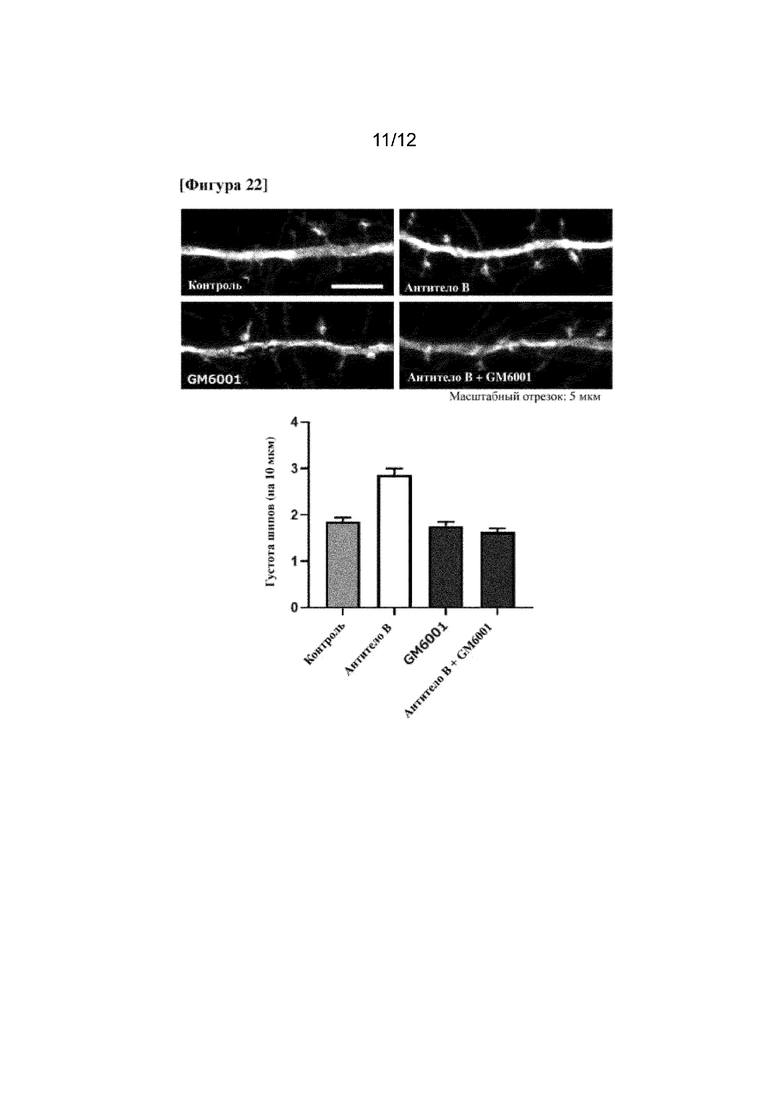
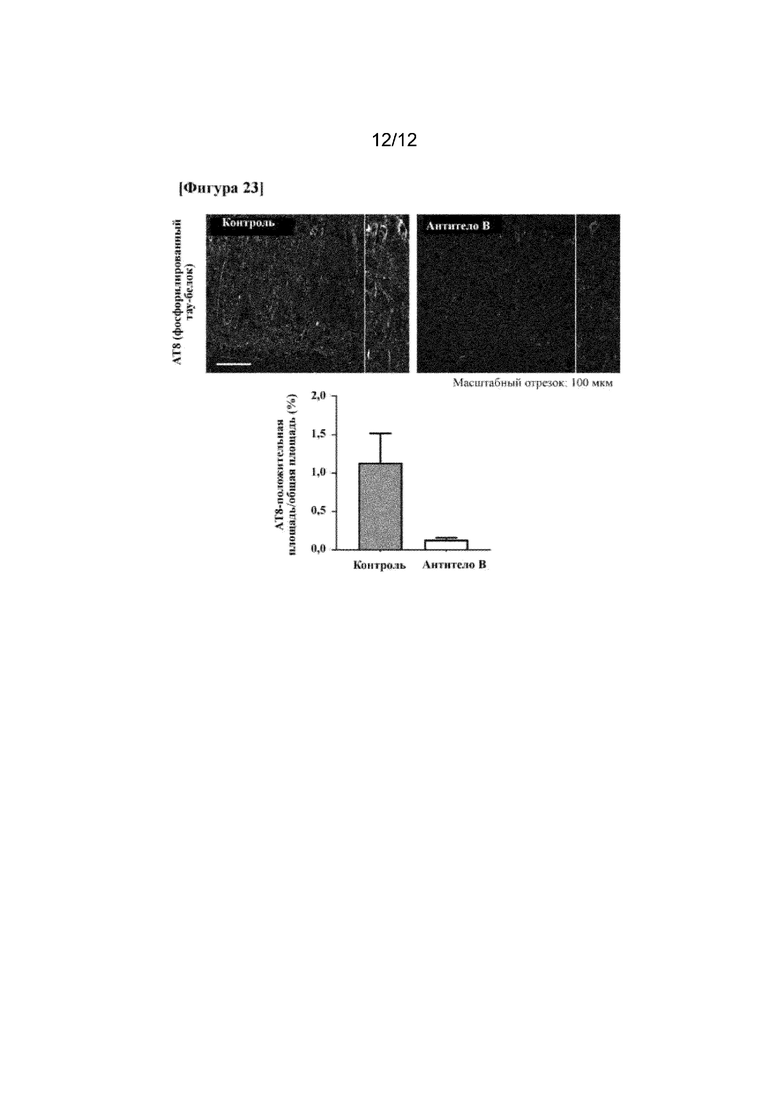
Изобретение относится к области биотехнологии, а именно к анти-EphA4 антителу, способу его получения, а также к содержащей его композиции. Также раскрыты выделенная нуклеиновая кислота, кодирующая вышеуказанное антитело, а также вектор и клетка-хозяин, ее содержащие. Изобретение эффективно для подавления фосфорилирования тау-белка. 7 н. и 11 з.п. ф-лы, 23 ил., 3 табл., 13 пр.
1. Анти-EphA4 антитело, где
анти-EphA4 антитело содержит:
(a) CDR1 тяжелой цепи, состоящую из аминокислотной последовательности SEQ ID NO: 44;
(b) CDR2 тяжелой цепи, состоящую из аминокислотной последовательности SEQ ID NO: 27;
(c) CDR3 тяжелой цепи, состоящую из аминокислотной последовательности SEQ ID NO: 28;
(d) CDR1 легкой цепи, состоящую из аминокислотной последовательности SEQ ID NO: 29;
(e) CDR2 легкой цепи, состоящую из аминокислотной последовательности SEQ ID NO: 30; и
(f) CDR3 легкой цепи, состоящую из аминокислотной последовательности SEQ ID NO: 31.
2. Анти-EphA4 антитело по п.1, где aнти-EphA4 антитело является гуманизированным.
3. Анти-EphA4 антитело по п.1 или 2, где aнти-EphA4 антитело специфически связывается с EphA4 и усиливает расщепление EphA4.
4. Анти-EphA4 антитело по любому из пп.1-3, где aнти-EphA4 антитело специфически связывается с EphA4 и ингибирует связывание между EphA4 и эфрином.
5. Анти-EphA4 антитело по любому из пп.1-4, где
вариабельная область тяжелой цепи состоит из аминокислотной последовательности SEQ ID NO: 45, и
вариабельная область легкой цепи состоит из аминокислотной последовательности SEQ ID NO: 46.
6. Анти-EphA4 антитело по любому из пп.1-5, где
константная область тяжелой цепи и константная область легкой цепи содержат аминокислотные последовательности, полученные из человеческого антитела.
7. Анти-EphA4 антитело по п.6, где
константная область тяжелой цепи представляет собой константную область IgG человека.
8. Анти-EphA4 антитело по п.7, где
константная область IgG человека представляет собой константную область IgG2 человека.
9. Анти-EphA4 антитело по п.8, где
константная область IgG2 человека содержит аминокислотную последовательность SEQ ID NO: 47.
10. Анти-EphA4 антитело по любому из пп.6-9, где
константная область легкой цепи представляет собой константную область Igκ человека.
11. Анти-EphA4 антитело по п.10, где
константная область Igκ человека содержит аминокислотную последовательность SEQ ID NO: 48.
12. Анти-EphA4 антитело, где
анти-EphA4 антитело содержит
тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 59, и
легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 60.
13. Анти-EphA4 по п.12, где
С-концевой лизин тяжелой цепи удален.
14. Выделенная нуклеиновая кислота, кодирующая анти-EphA4 антитело по любому из пп.1-13.
15. Вектор экспрессии, содержащий нуклеиновую кислоту по п.14.
16. Клетка-хозяин для получения анти-EphA4 антитела по любому из пп.1-13, содержащая вектор по п.15.
17. Способ получения анти-EphA4 антитела, включающий стадию культивирования клетки-хозяина по п.16.
18. Фармацевтическая композиция для подавления фосфорилирования тау-белка, где композиция содержит анти-EphA4 антитело по любому из пп.1-13.
| US 2017218075 A1, 03.08.2017 | |||
| WO 2017043466 A1, 16.03.2017 | |||
| LIES SCHOONAERT et al., Identification and characterization of Nanobodies targeting the EphA4 receptor, J | |||
| Biol | |||
| Chem., 2017, 292(27), pp | |||
| Прибор для построения контуров при аэрофотосъемках | 1928 |
|
SU11452A1 |
| SERGE GAUTHIER et al., Efficacy and safety of tau-aggregation inhibitor therapy in patients with mild or moderate Alzheimer’s disease: a | |||
Авторы
Даты
2024-03-28—Публикация
2020-06-29—Подача