Область техники: изобретение относится к области биоинформатики и клинической онкологии, диагностики злокачественных новообразований (ЗНО) и оценки потенциальной эффективности иммунотерапии.
Описание уровня техники
Консервативная противоопухолевая иммунотерапия ингибиторами контрольных точек иммунного ответа (ИКТ), в частности, ингибиторами рецептора программируемой клеточной гибели (PD-1) или его лиганда PD-L1, является крайне полезной терапевтической опцией при лечении многих ЗНО различной этиологии и локализации (меланома, рак легких, рак головы и шеи, лимфома Ходжкина, уротелиальный рак, рак пищевода, рак желудка, колоректальный рак, рак шейки матки, рак почки, рак эндометрия, тройной негативный рак молочной железы, рак печени) [Darvishi М, et al. (2023), Pathol Res Pract, 241, 154241]. Иммунотерапию применяют как в монорежиме, так и в комбинации с иными терапевтическими опциями (химиотерапия или лучевая терапия) [Zhang Z., et al. (2022), Sig Transduct Target Ther, 7, 258].
Прогнозирование эффективности иммунотерапии до ее начала или при необходимости - в процессе прохождения курсов лечения критично по нескольким параметрам: достижение максимальной выживаемости пациентов и повышение качества их жизни, экономия дорогостоящих препаратов и снижение избыточной токсичности при использовании комбинированных терапевтических схем. Для большинства анти-PD-L1/анти-PD-1 препаратов предиктивным маркером является уровень экспрессии PD-L1 в опухоли. Однако ввиду наличия нескольких различных клинически валидированных диагностических платформ для оценки статуса PD-L1 в разных типах ЗНО для отдельных анти-PD-L1/анти-PD-1 препаратов, данный вариант теста не может выступать в роли универсального анализа. В российской клинической практике для стратификации пациентов для назначения иммунотерапии также не используются мультипараметрические тест-системы, применение которых позволило бы одновременно оценивать наличие нескольких возможных биомаркеров эффективности и резистентности к анти-PD-L1/анти-PD-1 терапии.
В реальной клинической практике нередко регистрируют невысокую частоту ответа на монотерапию ИКТ (в общей популяции пациентов), что может быть обусловлено различиями индивидуальных профилей иммуногенных опухолевых антигенов у пациентов и реализацией различных молекулярных механизмов резистентности - первичной или вторичной, приобретенной в результате проведения курсов иммунотерапии [Bai R, et al., Mechanisms of cancer resistance to immunotherapy. Front Oncol, 2020, 10, 1290]. В последних случаях некоторые из вариантов резистентности могут быть преодолены переходом к схемам иммунотерапии в сочетании с другими препаратами.
В настоящее время в качестве предиктивных маркеров для назначения анти-PD-L1/анти-PD-1 препаратов (здесь и далее упоминаются в значении маркеров, ассоциированных с потенциальной эффективностью проводимой терапии) Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) были одобрены три показателя: экспрессия PD-L1, мутационная нагрузка опухоли и микросателлитная нестабильность (MSI) [Sankar K., et al. (2022), 10(1), 1-13]. На доклинической стадии исследуют широкий профиль кандидатных предиктивных биомаркеров с использованием методик анализа экспрессии панелей генов, мультиплексного иммуногистохимического анализа (ИГХ), иммунофлуоресценции, оценки количества инфильтрирующих опухоль лимфоцитов (TILs) и репертуара рецепторов Т-клеток (TCR), биомаркеров периферической крови и комплексной оценки иммунной системы [Sankar K., et al. (2022), 10(1), 1-13].
Наиболее распространенными способами определения предиктивных маркеров является геномное и транскриптомное профилирование опухоли для выявления генетических вариантов целевых генов и количественных изменений уровней их транскриптов в клетках, соответственно, с помощью доступных коммерческих платформ (например, NanoString nCounter). Образец РНК смешивается с биотинилированным зондом и репортерным зондом, помеченным флуоресцентной меткой, уникальной для таргетного гена. Зонды и целевые транскрипты гибридизуют в течение 12-16 ч при 65°С. Тройные комплексы, специфичные для транскрипта, иммобилизуют в картридже со стрептавидином. В частности, было показано, что сигнатура экспрессии генов, ассоциированная с сигнальным каскадом интерферона гамма, может выступать в качестве биомаркера ответа на терапию пембролизумабом у пациентов с плоскоклеточной карциномой головы и шеи [Ayers М., et al. (2017), 127(8), 2930-2940]. Второй способ основан на исследовании методом высокопроизводительного секвенирования (NGS) не только РНК, но и опухолевой ДНК (полноэкзомное, полногеномное или таргетное секвенирование), с использованием платформ «Illumina» или «PacBio». Так, было установлено, что уровень экспрессии PD-L1 более 5% не обладает предиктивным потенциалом для назначения ниволумаба вместо химиотерапии, однако ассоциирован с меньшим количеством нежелательных эффектов при применении ниволумаба после курса химиотерапии [Carbone D. P., et al., (2017), 376(25), 2415-2426]. Третий способ основан на хорошо воспроизводимых подходах количественной полимеразной цепной реакции (ПЦР). Например, при наследственном опухолевом синдроме - синдроме Линча, MSI выявляют путем проведения мультиплексной ПЦР ДНК опухолевых клеток и расположенных рядом нормальных клеток слизистой оболочки кишечника. Наличие либо отсутствие микросателлитных повторов определяется при сопоставлении длины амплифицированных ПЦР-фрагментов. В зависимости от наличия или отсутствия микросателлитной нестабильности, а также от того, сколько именно локусов нестабильны, прогноз эффективности иммунотерапии может отличаться [Baretti М., et al., (2018), 189, 45-62].
ИГХ-исследование, выполняемое с использованием различных техник флуорохромной микроскопии и микродиссекции тканей, широко применяется для исследования протеомного профиля опухолевого материала, заключенного в парафиновые блоки, или свежезамороженного материала. Сущность ИГХ-анализа заключается либо в выявлении конкретного белка, ассоциированного с прогрессированием заболевания или эффективностью терапии, либо в исследовании изменений соотношений ряда белков, либо регистрации увеличения/уменьшения количества некоторого белка в опухолевых клетках. Например, посредством ИГХ-исследования была выявлена связь между повышенной экспрессией PD-L1 и наилучшими клиническими ответами у пациентов с немелклеточным раком легкого, получивших терапию пембролизумабом [Roach С, et al., (2016), Appl. Immunohistochem. Mol. Morphol., 24(6), 392]. С другой стороны, также удалось установить, что высокий уровень экспрессии PD-1/PD-L1 и/или IDO-1/HLA-DR в опухолевой ткани коррелирует с высокой чувствительностью метастатической меланомы к пембролизумабу или ниволумабу [Johnson D. В., et al. (2018). Clin Cancer Res, 24(21), 5250-5260]. Данный подход технически проще генетического профилирования, однако обладает меньшей точностью и меньшей предсказательной силой (особенно когда биомаркером служит некоторый диапазон значений концентрации белка).
Перспективным выглядит подход с применением генетической панели, при использовании которой возможно будет проанализировать в опухолевой ДНК наличие терапевтически значимых маркеров и биомаркеров в нескольких генах сразу. Важно, что геномная ДНК по сравнению с РНК и белковыми фракциями - более стабильный аналит для выявления биомаркеров. Для генетических исследований используют секвенирование целевых регионов по Сэнгеру либо аллель-специфическую ПЦР, либо варианты NGS-исследований. В настоящее время существуют патенты, в которых описаны панели, включающие участки небольшого числа генов. Большинство панелей при этом адаптированы под конкретный тип злокачественного новообразования (например, рак легкого). Из мирового уровня техники известны несколько тест-систем на основе NGS-анализа, которые используют для исследования опухолевой ДНК на предмет выявления кандидатных генетических биомаркеров, в том числе с предиктивной значимостью.
Таким образом, среди аналогов можно выделить следующие.
Панель для оценки наличия микросателлитной нестабильности (https://fg-onko.ru/msi/) от F-Genetics предназначена для выявления 13 микросателлитных локусов (ВАТ-25, ВАТ-26, ВАТ-40, САТ-25, NR-21, NR-22, NR-24, NR-27, ABI-16, ABI-17, ABI-19, ABI-20A, ABI-20B) и 2 высокополиморфных пентануклеотидных локусов. Так, высокий уровень микросателлитной нестабильности (MSI-H) в опухоли является предиктивным маркером, определяющим чувствительность к терапии ИКТ (пембролизумаб, ниволумаб).
РФ, RU2747746 С2, 13.05.2021. «Тест-классификатор клинического ответа на лечение сорафенибом индивидуальных пациентов с раком почки». Предложен способ определения клинической эффективности применения сорафениба для лечения почечноклеточной карциномы, основанный на определении экспрессии целевых генов в образце ткани с нормированием относительно экспрессии ряда генов. Определение уровня экспрессии целевых генов проводят методом секвенирования тотальной РНК, методом исследования на микрочипах, либо методом обратной транскрипции и ПЦР. Данный аналог от изобретения отличает то, что эффективность терапии онкологического заболевания определяется по профилю генной экспрессии.
Кроме того, препарат (сорафениб) относится к ингибиторам протеинкиназ и не входит в схемы противоопухолевой терапии с применением ИКТ.
РФ, RU2741703 С1, 28.01.2021. «Платформа анализа генетической информации ОпсоЬох». Предложен способ оценки клинической эффективности таргетных лекарственных средств для лечения пациента с пролиферативным или онкологическим заболеванием, в котором получают данные по меньшей мере одного типа из образца, при этом тип данных выбирается из следующего списка: (i) данные по экспрессии тотальной мРНК, (ii) полногеномные данные по экспрессии белков, (iii) полногеномные данные по сайтам связывания транскрипционных факторов, (iv) полногеномные данные по мутациям в геномной ДНК, (v) полногеномные данные по экспрессии микроРНК. Предложен способ лечения пациента с пролиферативным или онкологическим заболеванием и система для оценки клинической эффективности таргетных лекарственных средств, выбранных из группы таргетных лекарственных средств, для пациента с пролиферативным или онкологическим заболеванием. Предложенный способ оценки клинической эффективности таргетной терапии онкологических заболеваний совпадает с подходом по использованию генной панели для оценки эффективности терапии ИКТ с точки зрения концепции оценки эффективности терапии и используемого материала. Однако в патенте не указан конкретный тип и схемы терапии, также нет совпадения генов панели.
Панель научно-клинического центра Memorial Sloan Kettering (США) - MSK-IMPACT, одобренная для клинического применения FDA (https://www.accessdata.fda.gov/cdrh_docs/reviews/DEN170058.pdf) как панель для расширенного генетического профилирования, включает в себя 505 генов и предназначена для выявления в опухолевой ДНК как предиктивных генетических маркеров для назначения препаратов (в том числе ИКТ), так и терапевтически значимых биомаркеров для анализа процессов прогрессирования опухолей, и в том числе для разработки таргетных препаратов. Для интерпретации геномных данных существует портал OncoKB® (https://www.oncokb.org/), включающий сведения о клинических и биологических эффектах более 4000 геномных изменений. Существуют принципиальные различия настоящего технического решения по шести генам, включенных в мультигенную панель (пересечение составляет 28 из 34 генов), а также по отсутствию в панели MSK-IMPACT аналогичного покрытия по межгенным регионам локуса 9р24.1 (согласно опубликованным данным о таргетных генах панели).
Диагностический тест FoundationOne®CDx (Roche, США), одобренный FDA для клинического применения (https://www.accessdata.fda.gov/cdrh_docs/pdf17/P170019a.pdf), основан на NGS-исследовании ДНК для выявления ряда мутационных событий и изменения числа копий генов в 324 генах, а также оценки наличия MSI и мутационной нагрузки опухоли с целью стратификации пациентов, которые могут получить пользу от лечения таргетными препаратами и ИКТ в соответствии с утвержденными инструкциями по медицинскому применению лекарственных препаратов. Данный тест одобрен для клинического применения как исследование для выявления предиктивных маркеров чувствительности к ИКТ - конкретно для назначения пембролизумаба, при этом тест отдельно не валидирован для оценки предиктивных биомаркеров резистентности к ИКТ (https://assets.ctfassets.net/w98cd481qyp0/YqqKHaqQmFeqc5ueQk48w/d12f19680205941ea3fee417f08e9524/F1CDx_Technical_Specifications.pdf). Существуют принципиальные различия настоящего технического решения по девяти генам, включенным в мультигенную панель (пересечение составляет 25 из 34 генов), а также по отсутствию в панели FoundationOne®CDx аналогичного покрытия по межгенным регионам локуса 9р24.1 (согласно опубликованным данным о таргетных генах панели).
Панель Illumina TruSight Oncology 500 - TSO500 (Illumina, США), включает полноразмерные кодирующие последовательности 523 генов. Разные варианты панели TSO500 позволяют выполнить NGS опухолевой ДНК и РНК, а также исследование свободно циркулирующей ДНК из плазмы крови для выявления коротких генетических вариантов, инделов, изменений копийности генов, фьюженов (https://www.illumina.com/products/by-brand/trusight-oncology/tso-500-portfolio.html). Существуют принципиальные различия настоящего технического решения по семи генам, включенным в мультигенную панель (пересечение составляет 27 из 34 генов), а также по отсутствию в панели TSO500 аналогичного покрытия по межгенным регионам локуса 9р24.1 (согласно опубликованным данным о таргетных генах панели). Кроме того, исследование с применением TSO500 пока не получило одобрения регуляторов для потокового применения в зарубежной клинической практике, в том числе для выявления предиктивных маркеров ИКТ [Wei В, et al. (2022). J Mol Diagn, 24(6), 600-608] и, в целом, панель TSO500 используется для решения широкого спектра научных и диагностических задач. Панель TSO500, как и другие широкие таргетные панели (в том числе вышеупомянутые FoundationOne®CDx, MSK-IMPACT) менее пригодна для рутинного лабораторного анализа в связи с большим спектром генов (сотни генов) и более трудоемкой интерпретацией массива выходных данных о генетических вариантах с целью определения их потенциальной клинической значимости.
В качестве еще одного актуального аналога уместно рассматривать два продукта компании АО "Ферст Генетике": набор реагентов «ОнкоФокус» и NGS-панель Онкопрофиль, которые нужны для таргетного исследования.
РЗН 2022/16970, 20.04.2022. Набор реагентов "ОнкоФокус" (https://fg-onko.ru/onkofokus/) для NGS-анализа генов, ассоциированных с возникновением опухолей человека, на системе "F-Genetics" по ТУ 21.20.23-003-03569019-2019. АО "Ферст Генетике" (класс потенциального риска 2б, Вид мед изделия с соответствующей номенклатурой 339880). Анализ заключается в определении характерных мутаций (хотспотов) в 35 генах, оценки копийности генов и хромосомных перестроек в 19 и 23 генах, соответственно. Основные показания для генотипирования при помощи данного продукта - выбор противоопухолевой терапии и коррекции терапии в случае рецидива ЗНО.
Панель «Онкопрофиль» (https://fg-onko.ru/onkoprofil/) составлена для определения хотспотов в 87 генах, нарушений числа копий 43 генов, интер и интра-хромосомных перестроек 51 гена, и секвенирования полной последовательности 48 генов. Показания для проведения исследования: молекулярное профилирование опухоли, выбор терапии, выявление неблагоприятного прогноза, коррекция терапии в случае рецидива, диагностика наследственного онкологического синдрома. Панель «Онкопрофиль» позволяет также выявить ряд генетических детерминант наследственных опухолевых синдромов. Главное отличие настоящего технического решения заключается в существенной разнице спектра генов, включенных в панель и пригодных для таргетного молекулярно-генетического анализа, а именно отличие по 13 уникальным генам (IFNG, IDO1, IFNGR1, HAVCR2, LAG3, CD274, CD8A, STAT1, В2М, VHL, PBRM1, POLD1, PDCD1LG2) от обоих продуктов «Онкопрофиль» и «ОнкоФокус».
Наиболее близких аналогов настоящего изобретения выявлено не было.
Достигаемым при использовании предлагаемого изобретения техническим результатом является создание таргетной панели для исследования целевых геномных регионов с целью идентификации терапевтических маркеров и биомаркеров - предикторов потенциальной эффективности и/или резистентности к иммунотерапии ингибиторами ИКТ (анти-PD-1 препараты, например, пембролизумаб или ниволумаб; анти-PD-L1 препараты, например, дурвалумаб или атезолизумаб или авелумаб), который осуществляется через создание таргетной панели, включающей целевые геномные регионы, посредством дизайна специфических для них праймеров, которые используют для анализа ДНК, выделенной из образцов опухолей пациентов с ЗНО, методом высокопроизводительного секвенирования.
Технический результат достигается тем, что в предлагаемом способе выполняют-создание таргетной панели для исследования целевых геномных регионов для идентификации терапевтических маркеров и биомаркеров - предикторов потенциальной эффективности и/или резистентности к иммунотерапии ингибиторами ИКТ (анти-PD-1 препараты, например, пембролизумаб или ниволумаб; анти-PD-L1 препараты, например, дурвалумаб или атезолизумаб или авелумаб, и иные анти-PD-1/анти-PD-L1 препараты), который осуществляется через формирование списка целевых геномных регионов (включающих кодирующие последовательности 34 генов (JAK3, JAK2, MDM2, CD274, PBRM1, В2М, ERBB2, IFNGR1, CD8A, JAK1, МЕТ, В API, POLE, POLD1. EGFR, LAG3, BRAF, HAVCR2, MLH1, KRAS, IFNG, ALK, PIK3CA, IDO1, AXL, TP53, ST ATI, SMAD4, ROS1, ARID 1 A, PTEN, PDCD1LG2, STK11, VHL), a также участки локуса 9p24.1 (гены JAK2, PD-L1 и PD-L2, и межгенные регионы)) и дизайн набора праймеров, специфических для целевых геномных регионов, которые будут использовать для анализа ДНК, выделенной из образцов опухолей пациентов с ЗНО, методом высокопроизводительного секвенирования. Исследование с использованием набора праймеров таргетной панели включает стадии лабораторного выделения ДНК из образца опухолевого материала (резекционного или биопсийного материала опухолевой ткани пациента, у которого диагностировано ЗНО (рак почки, рак шейки матки, рак легкого, рак желудка, меланома или другие типы ЗНО) до начала или в процессе иммунотерапии ингибиторами ИКТ), измерения концентрации выделенной ДНК, подготовку ДНК-библиотек с использованием опухолевой ДНК в качестве матрицы для амлификации целевых геномных регионов при ПЦР с праймерами, высокопроизводительного секвенирования ДНК-библиотек, последующей биоинформатической обработки результатов секвенирования, интерпретации биологической и клинической значимости генетических вариантов, детектированных по результатам таргетного секвенирования.
Предлагаемый способ позволяет получить таргетную панель для выполнения генетических исследований образцов ЗНО при выборе противоопухолевой терапии или оценки ее эффективности посредством секвенирования целевых геномных регионов в опухолевой ДНК для идентификации терапевтических маркеров и биомаркеров потенциальной эффективности и/или резистентности к иммунотерапии ингибиторами ИКТ.
Осуществление изобретения
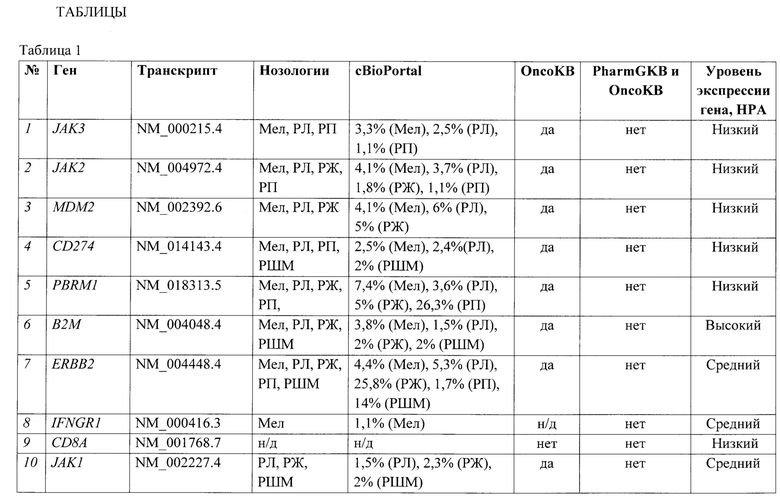
Список из 167 кандидатных генов, в которых, по данным литературы и анализу публичных баз геномных и транскриптомных данных, были обнаружены повреждающие генетические варианты или отмечено изменение экспрессии, ассоциированных с ответом на терапию ИКТ или резистентностью к ней, далее был проанализирован на предмет частот встречаемости мутаций в разных типах ЗНО. По результатам анализа были выбраны 34 гена и участки локуса 9р24.1 (таблица 1), целевые геномные регионы которых были включены в состав таргетной панели.
В таблице 1 также приведены результаты анализа частот встречаемости генетических нарушений в тканях меланомы (Мел), рака легкого (РЛ), рака почки (РП), рака желудка (РЖ), рака шейки матки (РШМ) по данным онлайн-ресурса cBioPortal (https://www.cbioportal.org/) - когорта MSK-IMPACT Clinical Sequencing Cohort (MSK, Nat. Med. 2017, 10945 случаев), известной аннотации онкогенных и вероятно патогенных генетических изменений по данным онлайн-ресурса OncoKB (https://www.oncokb.org/), а также информация о наличии клинической аннотации генетических вариантов, относящихся к целевым геномным регионам таргетной панели, для оценки потенциальной эффективности иммунотерапии анти-PD-1/анти-PD-L1 препаратов (по данным OncoKB и PharmGKB (https://www.pharmgkb.org/)). Медианные значения экспрессии генов в опухолевой ткани был извлечены из базы данных онлайн-ресурса The Human Proteome Atlas (НРА, https://www.proteinatlas.org/) с выделением условных диапазонов уровней экспрессии генов: от 0,1 до 10 FPKM -низкий уровень экспрессии, от 10 до 100 FPKM - средний уровень экспрессии, свыше 100 FPKM - высокий уровень экспрессии.
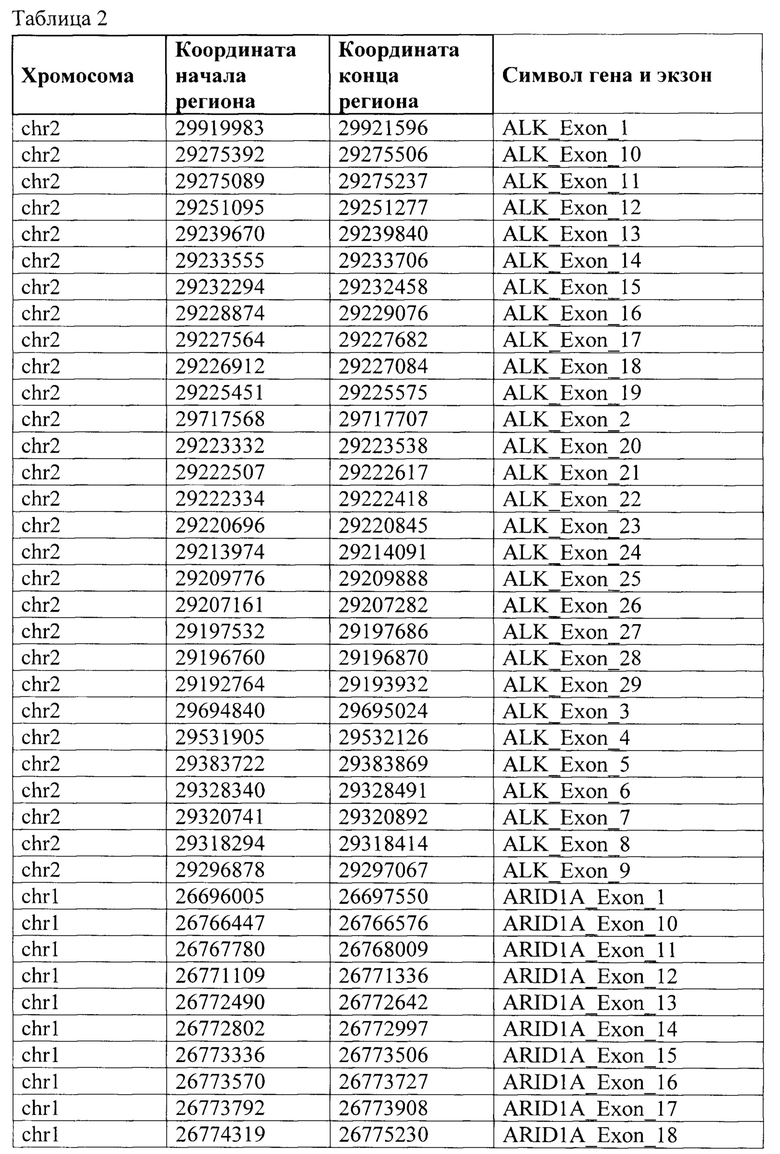
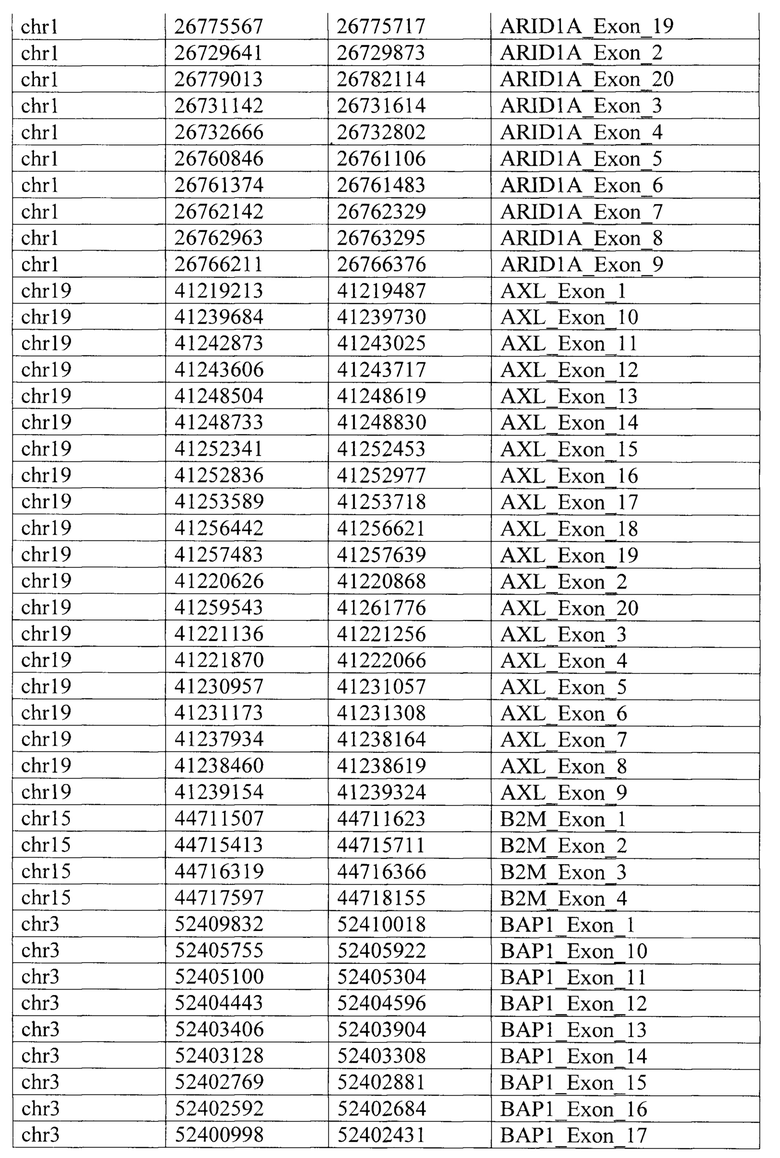
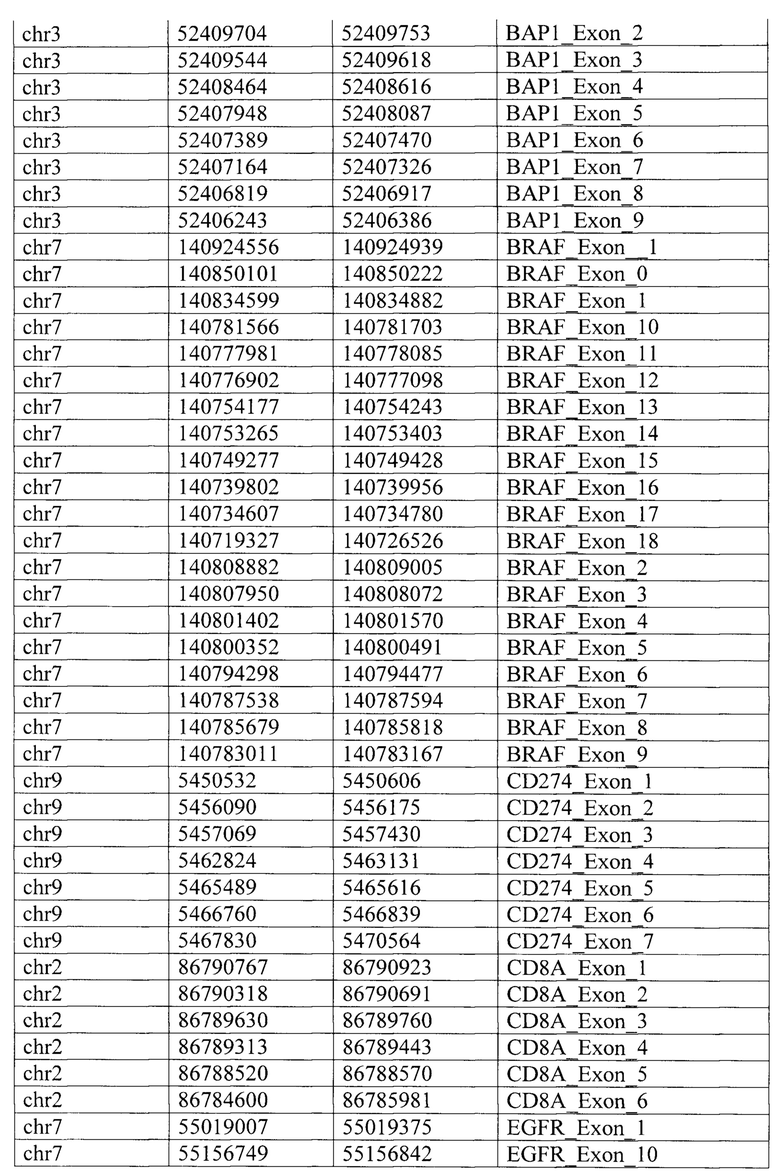
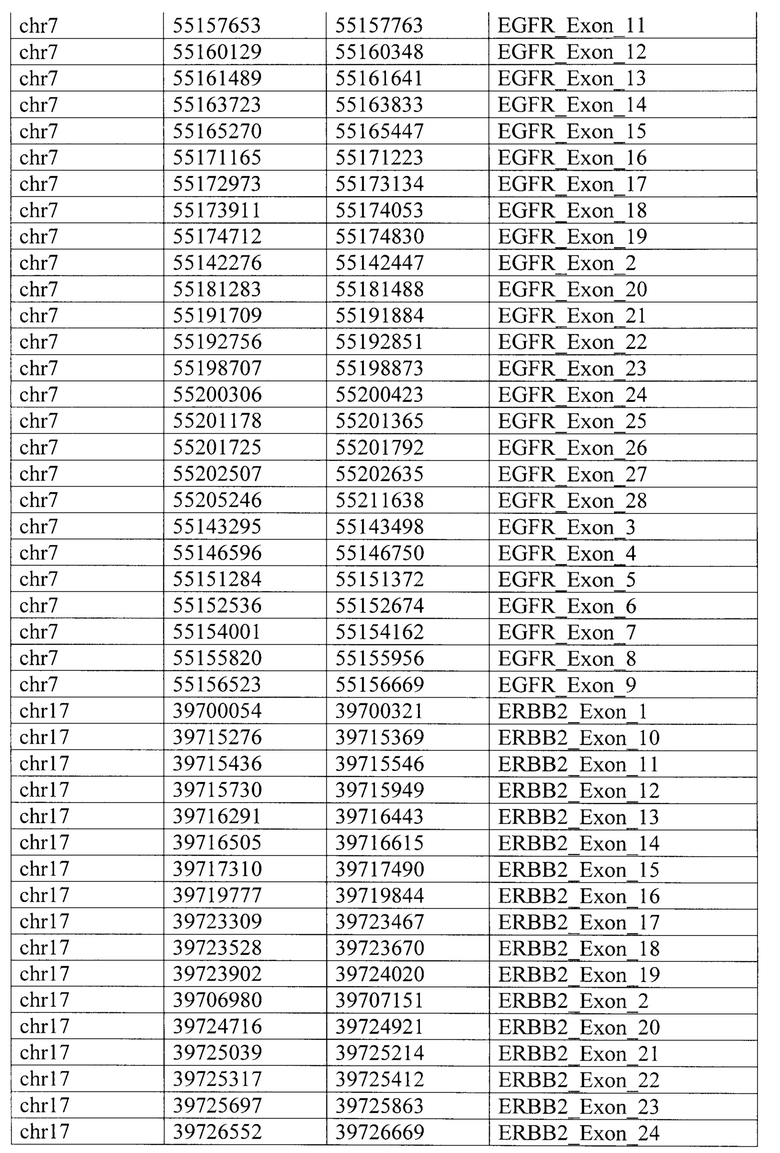
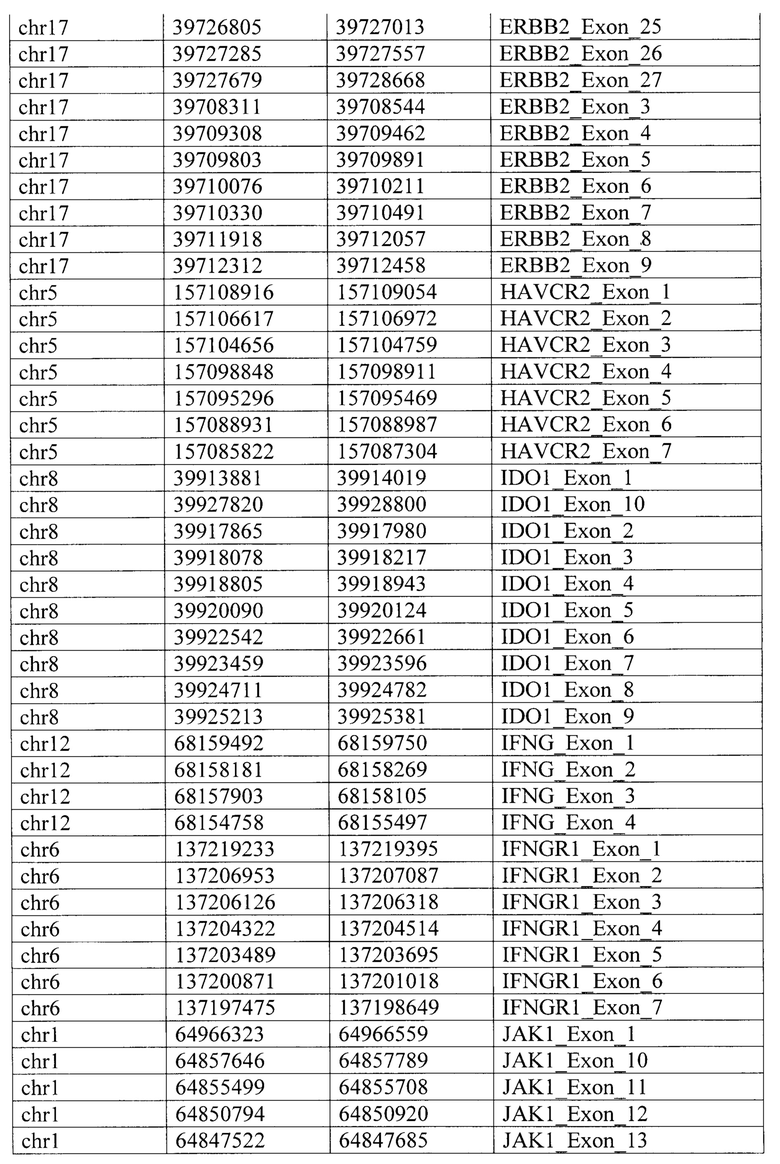
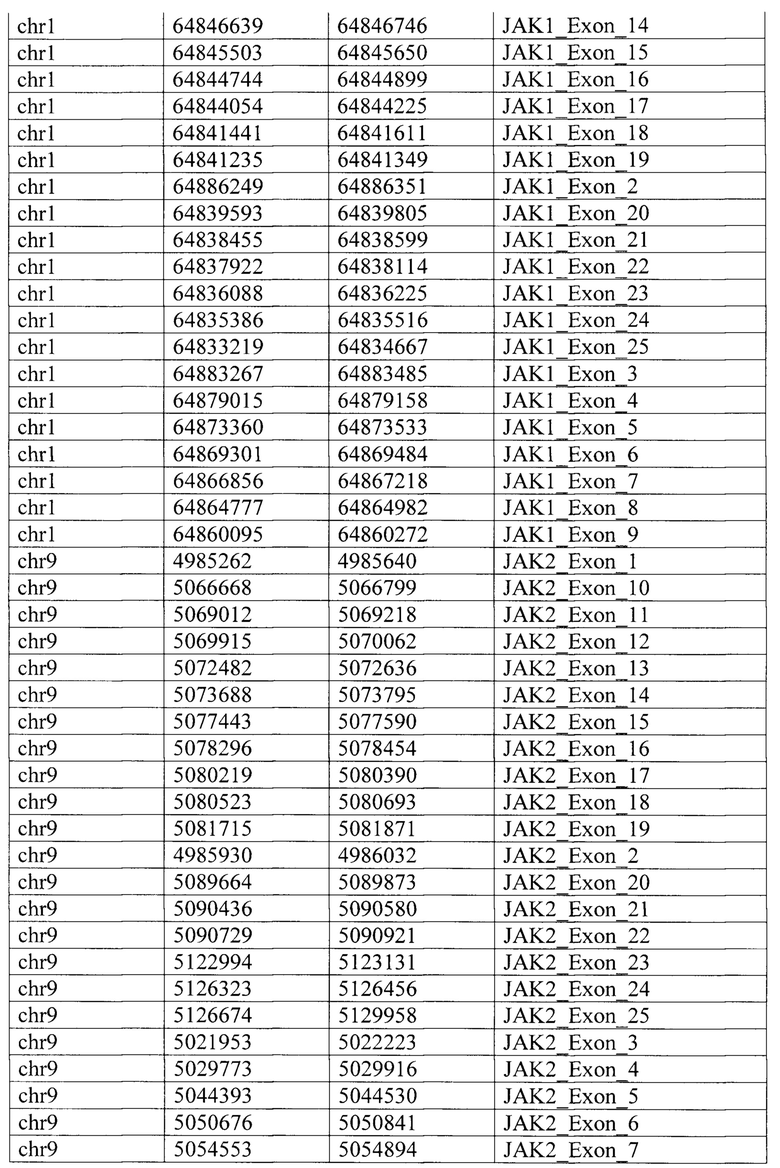
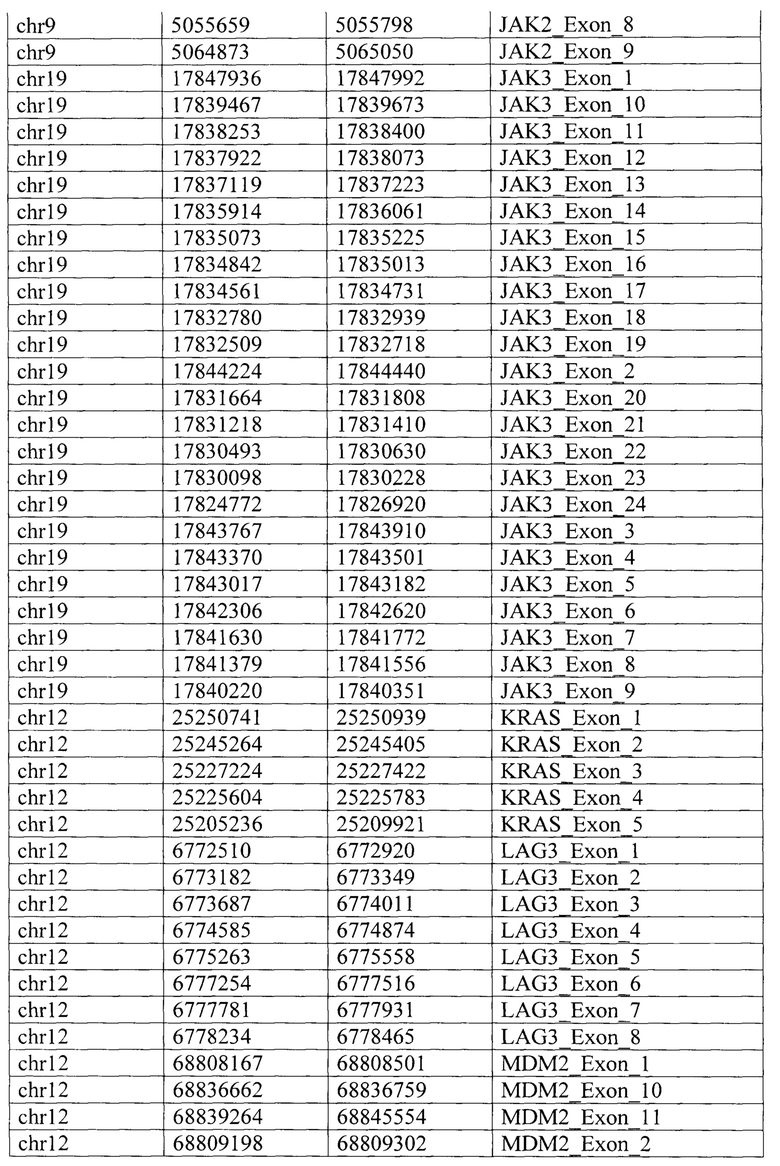
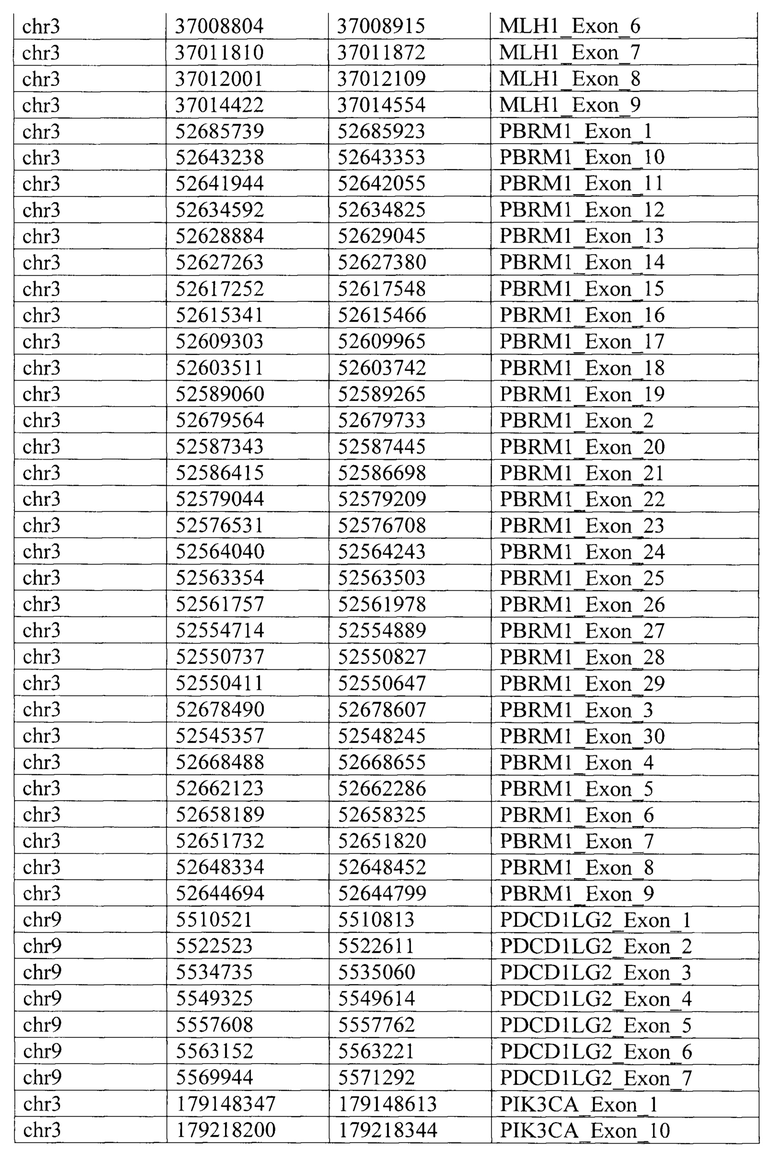
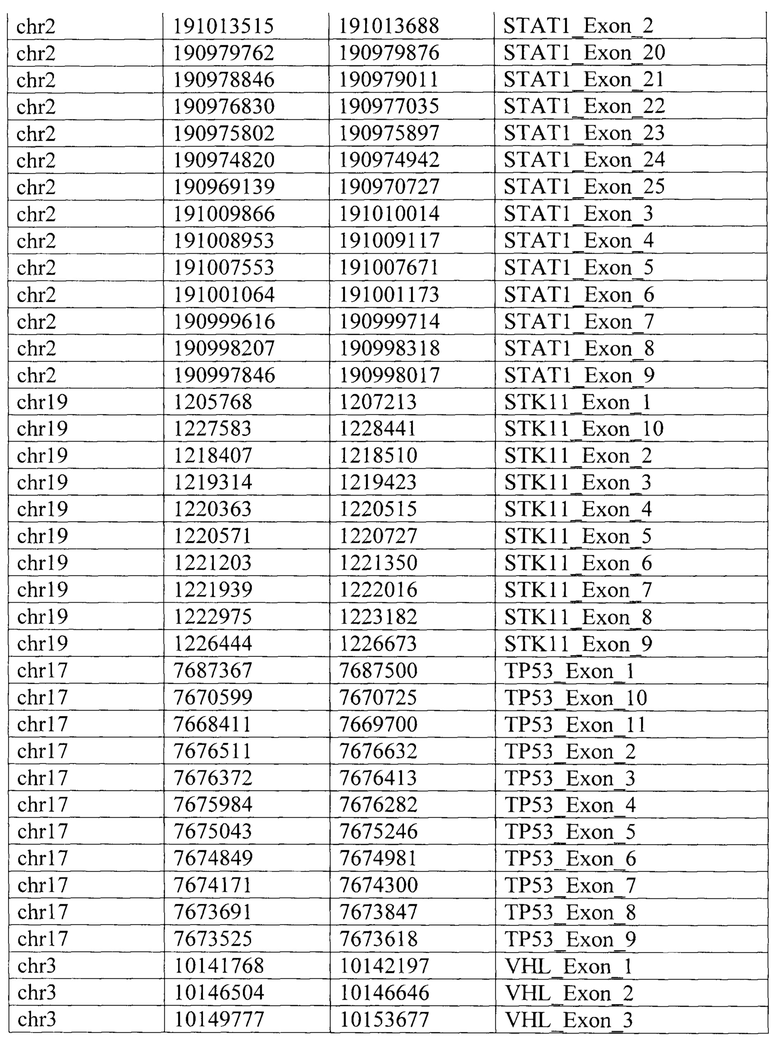
Таргетная панель состоит из целевых геномных регионов 34 генов (JAK3, JAK2, MDM2, CD274, PBRM1, В2М, ERBB2, IFNGR1, CD8A, JAK1, MET, ВАР1, POLE, POLD1. EGFR, LAG3, BRAF, HAVCR2, MLH1, KRAS, IFNG, ALK, PIK3CA, IDO1, AXL, TP53, STATI, SMAD4, ROS1, ARID1A, PTEN, PDCD1LG2, STK11, VHL), определяемых специфическими координатами регионов (таблица 2) и дополнительных целевых геномных регионов (обозначены как «регионы 1/2/3/4») локуса 9р24.1, содержащего гены JAK2, PD-L1 и PD-L2, связанные с осуществлением противоопухолевого иммунного ответа и межгенные регионы 9р24.1, координаты которых приведены по версии генома человека hg38 в таблице 3.
Для каждого целевого геномного региона панели, включающего кодирующие экзоны генов или последовательности прилежащих к ним 10 пар нуклеотидов или некоторые межгенные регионы, праймеры были сконструированы в программе MFEprimer (версия 3.1) с учетом следующих параметров:
1) диапазон возможных длин ампликонов 100-200 п.н. (предпочтительный диапазон 130-180 п.н.), для всех целевых регионов ампликоны должны перекрываться;
2) диапазон возможных длин праймеров: 22-25 п.н.;
3) Tm для обоих праймеров (прямой/forward и обратный/reverse) в каждой паре набора не должны отличаться более чем на 2°С; диапазон различий между Tm всех праймеров в целом наборе не более 4°С,
4) возможный диапазон температур отжига (Та) праймеров - плюс 60-70°С, Та для обоих праймеров в каждой паре набора не должны отличаться более чем на 2°С, диапазон различий между Та всех праймеров в целом наборе не более 4°С;
5) GC-состав всего праймера не менее 40% и не более 60%;
6) допустимая длина гомополимеров в праймере: не более 5 нуклеотидов на всю последовательность праймера;
7) первые 6 нуклеотидов с 3'-конца праймера не должны быть комплементарны самому праймеру или другим праймерам в наборе.
Получившиеся праймеры были проверены на специфичность (т.е. наличие в наборе праймеров, специфических для конкретных целевых регионов, а значит, не картирующихся на другие последовательности в рамках генома). Для этого полученный набор праймеров был проанализирован на неспецифическое картирование праймеров, которое может привести к гибридизации с нецелевыми участками генома (версия hg38) и получению ампликонов вне целевых последовательностей панели, и проверен на возможность гибридизации праймеров с другими праймерами набора. Для этого была использована программа blastn (версия 2.9.0) с параметрами:
1) -word_size 11
2) -qcov_hsp_perc (при проверке значение этого параметра не выставляли)
3) -penalty -3
4) -reward 2
5) -gapopen 5
6) -gapextend 2
7) -evalue 0.01
Для оценки возможности димеризации между праймерами панели выполняли проверку на картирование праймеров на последовательности других праймеров, входящих в набор. Это было выполнено аналогично проверке на неспецифическое картирование, только вместо последовательности генома hg38 в качестве базы данных для blastn (версия 2.9.0) использовали сами последовательности праймеров, составляющие набор. Таким образом, при данной проверке все праймеры, которые картировались более одного раза в наборе, были отмечены как праймеры с высокой вероятностью образования димеров и были отбракованы по этому критерию.
После отбраковывания неспецифических праймеров (на основании выявления множественного картирования праймеров или наличия е-value>0,01) были проверены координаты картирования праймеров, прошедших критерии отбора, на пересечение с координатами полиморфизмов и хотспотов. Проверка праймеров на картирование на данные генетические варианты была выполнена с использованием программы MFEprimer (версия 3.2.6) с использованием файлов в формате bed с известными генетическими вариантами из базы dbSNP (https://www.ncbi.nlm.nih.gov/snp/) и с координатами хотспотов, характерных для целевых генов панели. В случае попадания полиморфизмов и хотспотов в координаты картирования праймеров, данные праймеры были исключены из набора и для данного ампликона были скорректированы координаты таким образом, чтобы новые праймеры не попадали непосредственно на регионы с полиморфизмами и хотспотами.
Также при помощи программы blastn (версия 2.9.0) проведена проверка отсутствия картирования праймеров, на так называемые (т.н.) сложные регионы генома: тандемные повторы, гомополимерные области, и во избежание образования неспецифических продуктов, - проверка отсутствия картирования праймеров на псевдогены для целевых генов панели.
Праймеры, в координаты которых попадают хотспоты, праймеры, картирующиеся в рамках т.н. сложных регионов генома, были заменены на другие праймеры путем нового дизайна с учетом следующих параметров:
1) диапазон возможных длин ампликонов 60-220 п.н., для всех целевых регионов ампликоны должны перекрываться,
2) диапазон возможных длин праймеров: 22-30 п.н.,
3) Tm для обоих праймеров в каждой паре набора не должны отличаться более чем на 2°С; диапазон различий между Tm всех праймеров в целом наборе не более 4°С,
4) возможный диапазон Та праймеров 60-70°С, Та для обоих праймеров в каждой паре набора не должны отличаться более чем на 2°С, диапазон различий между Та всех праймеров в целом наборе не более 4°С,
5) GC-состав всего праймера не менее 30%и не более 70%
6) допустимая длина гомополимеров в праймере: не более 5 нуклеотидов на всю последовательность праймера,
7) первые 6 нуклеотидов с 3'-конца праймера не должны быть комплементарны самому праймеру или другим праймерам в наборе.
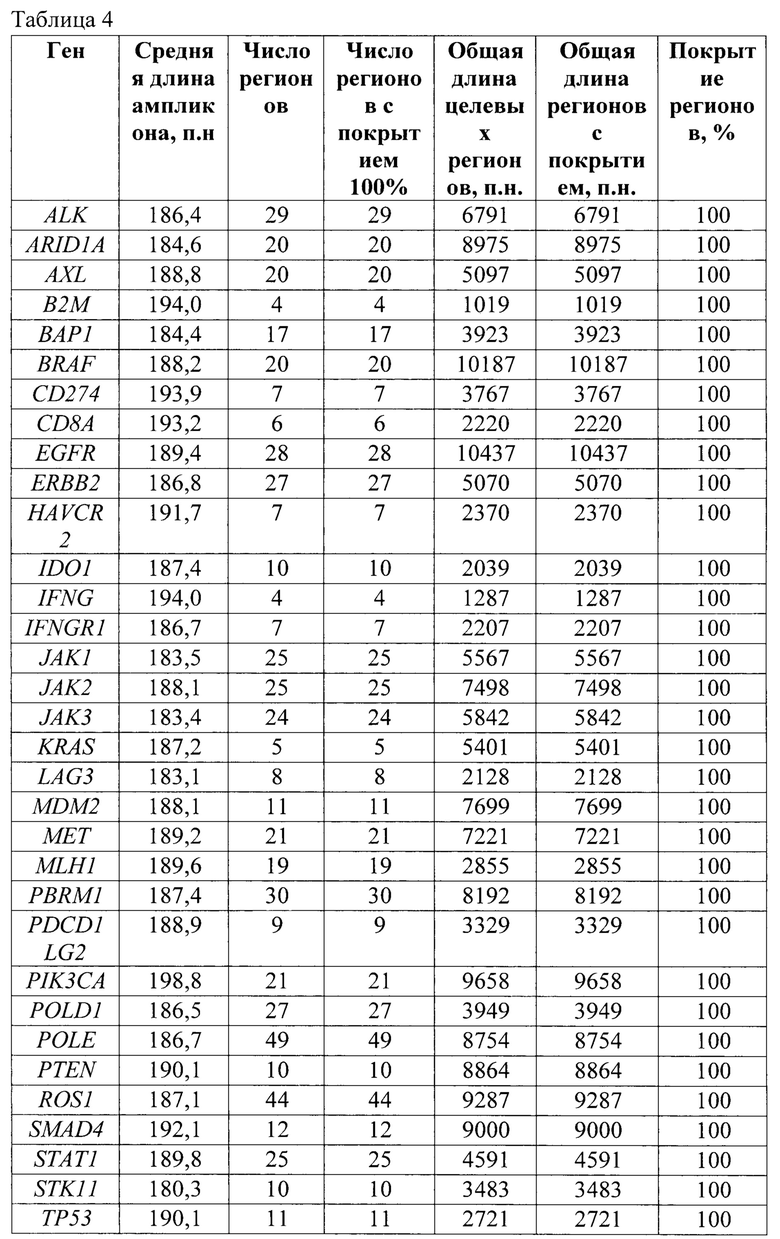
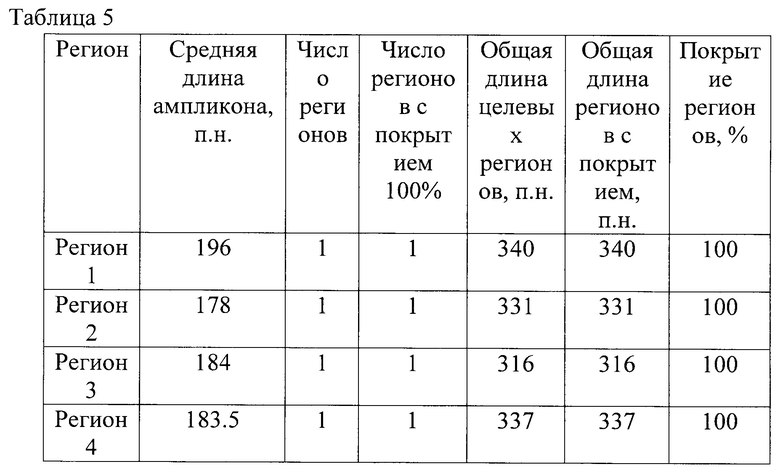
Для всего набора праймеров была выполнена валидация in silico для теоретической оценки результатов ПЦР с разработанными праймерами и проверки возможного покрытия ампликонами всех целевых геномных регионов, входящих в состав таргетной панели. Для валидации панели in silico были использованы программы MFEprimer (версия 3.2.6) и blastn (версия 2.9.0). Результаты in silico валидации праймеров, специфичных для целевых геномных регионов 34 генов приведены в таблице 4. В таблице 5 приведены результаты in silico валидации праймеров для дополнительных геномных регионов в локусе 9р24.1.
В результате в составе набора праймеров остались только праймеры, специфические для целевых геномных регионов, с характеристиками, описанными ранее.








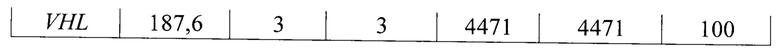
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ малоинвазивной диагностики рака легкого по фрагментированной свободно циркулирующей ДНК на основе методов машинного обучения | 2023 |
|
RU2820322C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ТИПА РАКА ЖЕЛУДКА МЕТОДОМ ИММУНОГИСТОХИМИЧЕСКОГО ТЕСТИРОВАНИЯ | 2023 |
|
RU2813670C1 |
| Способ повышения эффективности ингибиторов иммунных контрольных точек при помощи терапевтической композиции на основе производных индола и пробиотика | 2023 |
|
RU2826495C1 |
| Способ прогноза эффективности терапии меланомы | 2021 |
|
RU2766739C1 |
| СПОСОБ ПОЛУЧЕНИЯ КУЛЬТУРЫ ЛИМФОЦИТОВ, ОБОГАЩЕННЫХ ОПУХОЛЬ-СПЕЦИФИЧНЫМИ КЛОНАМИ Т-ЛИМФОЦИТОВ, И КЛЕТОЧНЫЕ КУЛЬТУРЫ, ПОЛУЧЕННЫЕ С ИСПОЛЬЗОВАНИЕМ УКАЗАННОГО СПОСОБА | 2022 |
|
RU2808595C1 |
| Набор высокоспецифичных олигонуклеотидных праймеров для детекции генетических вариантов методом высокопроизводительного секвенирования ДНК | 2024 |
|
RU2833429C1 |
| Генотерапевтический препарат FCU1-BsFm/PP для лечения солидных опухолей | 2023 |
|
RU2824977C1 |
| ИНСЕРЦИЯ ТАРГЕТНОГО ГЕНА ДЛЯ УЛУЧШЕННОЙ КЛЕТОЧНОЙ ИММУНОТЕРАПИИ | 2017 |
|
RU2824204C2 |
| VEGF ПОЛИМОРФИЗМ И АНТИ-АНГИОГЕНЕЗНАЯ ТЕРАПИЯ | 2008 |
|
RU2482491C2 |
| СПОСОБЫ ВЫЯВЛЕНИЯ И МОНИТОРИНГА РАКА ПУТЕМ ПЕРСОНАЛИЗИРОВАННОГО ВЫЯВЛЕНИЯ ЦИРКУЛИРУЮЩЕЙ ОПУХОЛЕВОЙ ДНК | 2019 |
|
RU2811503C2 |
Изобретение относится к биотехнологии. Описан способ создания таргетной панели для исследования целевых геномных регионов для выявления предиктивных генетических биомаркеров потенциальной эффективности и/или резистентности к ингибиторам иммунных контрольных точек (ИКТ). Способ включает генетический анализ резекционного или биопсийного материала опухолевой ткани пациента с диагностированным злокачественным новообразованием (ЗНО) до начала курса или в ходе иммунотерапии на основе ингибиторов ИКТ - анти-PD-l или анти-PD-L1 препаратов, а именно: лабораторное выделение ДНК из образца опухолевого материала, измерение концентрации выделенной ДНК, подготовку ДНК-библиотек с использованием опухолевой ДНК в качестве матрицы для амлификации целевых геномных регионов при ПЦР со специфическими для них праймерами, секвенирование ДНК-библиотек, последующую биоинформатическую обработку результатов секвенирования, интерпретацию биологической и клинической значимости генетических вариантов, детектированных по результатам таргетного секвенирования, идентификацию предиктивных генетических биомаркеров потенциальной эффективности и/или резистентности к иммунотерапии ингибиторами ИКТ на основе целевых геномных регионов, включающих кодирующие последовательности 34 генов: JAK3, JAK2, MDM2, CD274, PBRM1, В2М, ERBB2, IFNGR1, CD8A, JAK1, MET, ВАР1, POLE, POLD1, EGFR, LAG3, BRAF, HAVCR2, MLH1, KRAS, IFNG, ALK, PIK3CA, IDO1, AXL, TP53, STATI, SMAD4, ROS1, ARID1A, PTEN, PDCD1LG2, STK11, VHL), а также участки локуса 9p24.1: гены JAK2, PD-L1, и PD-L2 и межгенные регионы. Изобретение может быть использовано при выборе противоопухолевой терапии или определении ее возможной эффективности. 11 з.п. ф-лы, 5 табл.
1. Способ создания таргетной панели для исследования целевых геномных регионов для выявления предиктивных генетических биомаркеров потенциальной эффективности и/или резистентности к ингибиторам иммунных контрольных точек (ИКТ), который включает генетический анализ резекционного или биопсийного материала опухолевой ткани пациента с диагностированным злокачественным новообразованием (ЗНО) до начала курса или в ходе иммунотерапии на основе ингибиторов ИКТ - анти-PD-l или анти-PD-L1 препаратов, а именно: лабораторное выделение ДНК из образца опухолевого материала, измерение концентрации выделенной ДНК, подготовку ДНК-библиотек с использованием опухолевой ДНК в качестве матрицы для амлификации целевых геномных регионов при ПЦР со специфическими для них праймерами, секвенирование ДНК-библиотек, последующую биоинформатическую обработку результатов секвенирования, интерпретацию биологической и клинической значимости генетических вариантов, детектированных по результатам таргетного секвенирования, идентификацию предиктивных генетических биомаркеров потенциальной эффективности и/или резистентности к иммунотерапии ингибиторами ИКТ на основе целевых геномных регионов, включающих кодирующие последовательности 34 генов: JAK3, JAK2, MDM2, CD274, PBRM1, В2М, ERBB2, IFNGR1, CD8A, JAK1, MET, ВАР1, POLE, POLD1, EGFR, LAG3, BRAF, HAVCR2, MLH1, KRAS, IFNG, ALK, PIK3CA, IDO1, AXL, TP53, STATI, SMAD4, ROS1, ARID1A, PTEN, PDCD1LG2, STK11, VHL, а также участки локуса 9p24.1: гены JAK2, PD-L1, и PD-L2 и межгенные регионы.
2. Способ по п. 1, в котором ЗНО локализовано в почке, шейке матки, легком, желудке, кожных покровах и кожном эпидермисе, и в других тканях, либо пациенту был поставлен диагноз рак почки или рак шейки матки или рак легкого или рак желудка или меланома.
3. Способ по п. 1, в котором анти-PD-1 препараты представляют собой: пембролизумаб или ниволумаб, а анти-PD-L1 препараты представляют собой: дурвалумаб или атезолизумаб или авелумаб.
4. Способ по п. 1, в котором процедура таргетного секвенирования ДНК-библиотек выполняется с использованием одной из известных NGS-платформ.
5. Способ по п. 1, в котором для выполнения таргетного секвенирования используют набор праймеров, специфических для целевых геномных регионов, составляющих таргетную панель.
6. Способ по пп. 1-5, где таргетная панель состоит из целевых геномных регионов 34 генов: JAK3, JAK2, MDM2, CD274, PBRM1, В2М, ERBB2, IFNGR1, CD8A, JAK1, MET, ВАР1, POLE, POLD1, EGFR, LAG3, BRAF, HAVCR2, MLH1, KRAS, IFNG, ALK, PIK3CA, IDO1, AXL, ТР53, STATI, SMAD4, ROS1, ARID1A, PTEN, PDCD1LG2, STK11, VHL), координаты которых определены в таблице 2, а также участки локуса 9р24.1: гены JAK2, PD-L1 и PD-L2 и межгенные регионы, координаты которых определены в таблице 3.
7. Способ по пп. 1-6, где таргетная панель включает дополнительные целевые геномные регионы - высокополиморфные локусы для оценки принадлежности образцов ДНК конкретным пациентам, биологические идентификаторы.
8. Способ по пп. 1-7, где результатом секвенирования ДНК с использованием таргетной панели на одной из известных NGS-платформ является массив данных либо о последовательностях целевых геномных регионов, не отличающихся от референсного генома, либо о последовательностях целевых геномных регионов, содержащих генетические варианты.
9. Способ по пп. 1-8, где генетические варианты, выявленные в целевых геномных регионах, могут включать:
а) точковые замены нуклеотидов в последовательностях целевых геномных регионов;
б) короткие делеции нуклеотидов в последовательностях целевых геномных регионов до 30 пар нуклеотидов;
в) короткие вставки нуклеотидов в последовательностях целевых геномных регионов до 30 пар нуклеотидов;
г) амплификации участков целевых геномных регионов;
д) делеции участков целевых геномных регионов.
10. Способ по пп. 1-9, где генетические варианты, выявленные в целевых геномных регионах, известны из уровня техники как повреждающие, изменяющие функции гена или транскрипта, или белкового продукта, и/или ассоциированы либо с клинической эффективностью ИКТ, либо с резистентностью к ИКТ.
11. Способ по пп. 1-10, где генетические варианты, выявленные в целевых геномных регионах, можно рассматривать в качестве кандидатных предиктивных биомаркеров эффективности ИКТ и/или резистентности ингибиторов ИКТ для случаев диагностированного рака почки или рака шейки матки, или рака легкого, или рака желудка, или меланомы, или других типов ЗНО.
12. Способ по пп. 1-11, где генетические варианты, выявленные в целевых геномных регионах, известны из уровня техники как предиктивные биомаркеры противоопухолевых препаратов для случаев диагностированного рака почки или рака шейки матки, или рака легкого, или рака желудка, или меланомы, или других типов ЗНО.
| А | |||
| Б | |||
| ЧУХЛОВИН Клиническая значимость молекулярно-биологической диагностики, Ученые записки СПбГМУ ИМ | |||
| АКАД | |||
| И | |||
| П | |||
| ПАВЛОВА, 2010, ТОМ XVII, номер 01, стр.62-68 | |||
| Способ получения библиотеки генов для диагностики патологий печени | 2020 |
|
RU2743858C1 |
| WO 2016174085 A1, 03.11.2016. | |||
Авторы
Даты
2024-05-02—Публикация
2023-07-10—Подача