Изобретение относится к медицине, а именно к онкологии, и может быть использовано для дооперационной диагностики медуллярного рака щитовидной железы.
Медуллярная рак щитовидной железы (МРЩЖ) это нейроэндокринная карцинома, возникающая из С-клеток щитовидной железы. Дооперационная диагностика этого заболевания основана на проведении тонкоигольной аспирационная биопсии узлов щитовидной железы (ТАБ), определении специфичных мутации гена RET и определении уровня кальцитонина крови. Первые два метода являются информативными примерно в половине случаев, а кальцитонин имеет так называемую «серую зону» (при значении от 10 до 100 пг/мл) и как следствие низкую предсказательную ценность положительного результата. Сложность и неоднозначность первичной диагностики МРЩЖ отражена в клинических рекомендациях Американской тиреоидной ассоциации (АТА), в которых с одной стороны осуждается целесообразность определения уровня кальцитонина у всех пациентов с узлами щитовидной железы, что экономически нецелесообразно, а с другой стороны, динамическое наблюдение при неопределенных заключениях результатов ТАБ увеличивает сроки до выполнения оперативного лечения, тем самым ухудшая его прогноз (1). Все это диктует необходимость поиска новых маркеров, которые способны повысить точность дооперационной диагностики МРЩЖ.
В последнее время особое внимание уделяется роли микроРНК в развитии МРЩЖ. Это класс малых некодирующих РНК, которые регулируют посттранскрипционную экспрессию генов. Использование различных микроРНК в качестве диагностических маркеров дифференцированных форм рака щитовидной железы в настоящее время уже успешно реализовано в различных генетических панелях, таких как ThyGenX/ThyraMIR, Rosetta Reveal (2), mir-THYpe (3) ТироидИНФО (4).
Известен способ дооперационной диагностики МРЩЖ, основанный на анализе 108 генов из смыва пунктата узла щитовидной железы Afirma Genomic Sequencing Classifier (GSC). Этот способ позволили со 100% чувствительностью и специфичностью определить МРЩЖ у 21 из 211 пациентов с цитологическим заключением Bethesda III-VI (5).
Также известен способ диагностики МРЩЖ в комплексе молекулярно-генетического теста ThyraMIR, основанный на анализе экспрессии 10 различных микроРНК. Данный тест основан на вычитании критического порогового значения одной микроРНК из критических пороговых значений других микроРНК. Тест также позволили со 100% чувствительностью и специфичностью определить МРЩЖ у 11 из 314 пациентов с цитологическим заключением Bethesda III-IV, основываясь в основном на показателях микроРНК-375 (6).
Известен способ дооперационной дифференциальной диагностики узловых образований щитовидной железы человека (7), включающий взятие образца ткани узлового образования щитовидной железы, выделение суммарного пула РНК из образца, измерение уровня экспрессии диагностируемых микроРНК методом ОТ-ПЦР в реальном времени, анализ уровня экспрессии гена HMGA2, митохондриальной ДНК, а также определение мутации V600E в гене BRAF с последующим сравнительным анализом изменения уровня экспрессии диагностируемых биомаркеров в норме и при узловых образованиях щитовидной железы и составлением заключения о наличии и характере узлового образования, характеризующийся тем, что измеряют уровень экспрессии трех микроРНК, а именно микроРНК-146b, -221, -375, дополнительно измеряют уровень экспрессии гена GCM2, характеризующего клетки паращитовидной железы, а заключение о наличии и характере узлового образования составляют на основании дерева принятия решений, построенного на основе средних значений уровней экспрессии измеряемых биомаркеров в разных типах узловых образований щитовидной железы, согласно которому анализируемый образец относят к одному, выбранному из следующей группы: узловое образование паращитовидной железы, доброкачественное узловое образование щитовидной железы, злокачественное узловое образование щитовидной железы, включающее папиллярный рак, медуллярный рак, гюртлеклеточный рак, фолликулярные опухоли с маркерами злокачественности, при этом, в частном случае, если в образце опухолевой ткани значение биомаркера HMGA2 выше или равно 0,015, miR-221 выше или равно 0,07, miR-375 выше или равно 3,5, уровень митохондриальной ДНК менее 5500 и отсутствует мутация V600E в гене BRAF, то делают заключение о вероятности наличия у пациента фолликулярной опухоли с маркерами злокачественности.
Недостатками способа являются длительность и высокая трудоемкость, связанная с необходимостью измерения уровня экспрессии гена HMGA2, митохондриальной ДНК, а также определение мутации V600E в гене BRAF с последующим сравнительным анализом изменения уровня экспрессии диагностируемых биомаркеров в норме и при узловых образованиях щитовидной железы, кроме этого, дополнительно измеряют уровень экспрессии гена GCM2, характеризующего клетки паращитовидной железы. Для диагностики МРЩЖ используют показания уровня экспрессии только одной микроРНК-375 (выше или равно 3,5), что недостаточно для точной дооперационной диагностики МРЩЖ.
Наиболее близким к заявляемому способу - прототипом, является способ дооперационной дифференциальной диагностики новообразований щитовидной железы, включающий молекулярно-генетическое исследование, при котором предварительно высушенный цитологический препарат смывают с цитологических стекол лизирующим буфером, далее производят выделение ДНК и микроРНК с помощью наборов для выделения, а затем производят детекцию и количественную оценку диагностически значимых микроРНК, основанную на методе полимеразной цепной реакции (ПЦР). При условии показателей HMGA2 более 0,09, микроРНК-221 более 0,0105 и микроРНК-375 более -12,1213, определяют фолликулярную опухоль с признаками злокачественности. При условии показателей микроРНК-146b более 0,1721, определяют папиллярный рак. При показателях микроРНК-375 более 5,2514, определяют медуллярный рак. Показатель соотношения митохондриальной ДНК/ядерной ДНК более 5716,3013 определяет В-клеточный рак. Наличие мутации V600 в гене BRAF определяет папиллярный рак и является риском наличия высокой биологической агрессивности данного папиллярного рака и распространенного процесса (8).
Недостатками известного способа являются длительность и трудоемкость способа, связанная с необходимостью измерения большого количества биомаркеров, а также недостаточная точность анализа, поскольку для диагностики МРЩЖ используют показания уровня экспрессии только одной микроРНК-375 (более 5,2514), что недостаточно для точной дооперационной диагностики МРЩЖ.
Задачей изобретения является создание точного и более простого и быстрого способа дооперационной диагностики МРЩЖ щитовидной железы с целью как можно более раннего начала лечения данной группы пациентов.
Технический результат: упрощение и ускорение дооперационной диагностики МРЩЖ при сохранении высокой точности анализа.
Предлагаемый молекулярно-генетический способ заключается в следующем.
Цитологический окрашенный препарат, полученный путем тонкоигольной аспирационной пункционной биопсии из опухоли щитовидной железы, смывают с цитологических стекол 200 мкл лизирующего буфера, далее из него производят выделение ДНК и микроРНК с помощью наборов для выделения, затем производят детекцию и количественную оценку микроРНК-375 и микроРНК-323, основанную на методе ОТ-ПЦР (полимеразной цепной реакции). Используют стандартную концентрацию праймеров 0,5 мкМ, концентрация флуоресцентно меченого зонда - 0,25 мкМ. Реакцию обратной транскрипции проводят в течение 15 мин. при 16°С, 15 мин. при 42°С, затем обратную транскриптазу инактивируют 2 мин. при 95°С и отбирают 3 мкл полученной смеси для ПЦР в реальном времени. Протокол ПЦР: предварительный прогрев при 95°С - 2 мин, 50 циклов: денатурация при 94°С - 10 сек, отжиг праймеров и элонгация: 60°С - 20 сек. Рассчитывают значение соотношения 1/[(уровень экспрессии микроРНК-375) × (уровень экспрессии микроРНК-323)] и при полученном значении соотношения, равном или менее 110, диагностируют МРЩЖ.
Предлагаемый способ отличается простотой и меньшей трудоемкостью в сравнении с прототипом, вследствие подбора минимально значимого количества диагностируемых микроРНК (микроРНК-375 и микро РНК-323), что позволяет упростить и ускорить проведение диагностики (на проведение анализа необходимо 3,5 часа, вместо 8 часов по прототипу), а также полностью исключить ложноположительные заключения.
Для доказательства достижения решаемой задачи, анализу подвергнуты цитологические образцы 30 пациентов с МРЩЖ. Контрольные группы составили доброкачественное образование (ДО) - 23 случаев, фолликулярная аденома (ФА) - 25, Гюртлеклеточная аденома (ГКА) - 30, фолликулярный рак (ФР) - 30, Гюртлеклеточная рак (ГКР) - 24, папиллярный рак (ПР) - 37. Были оценены уровни экспрессии микроРНК-375, микроРНК-323, а также рассчитаны значения соотношения 1/[(уровень экспрессии микроРНК-375) × (уровень экспрессии микроРНК-323)].
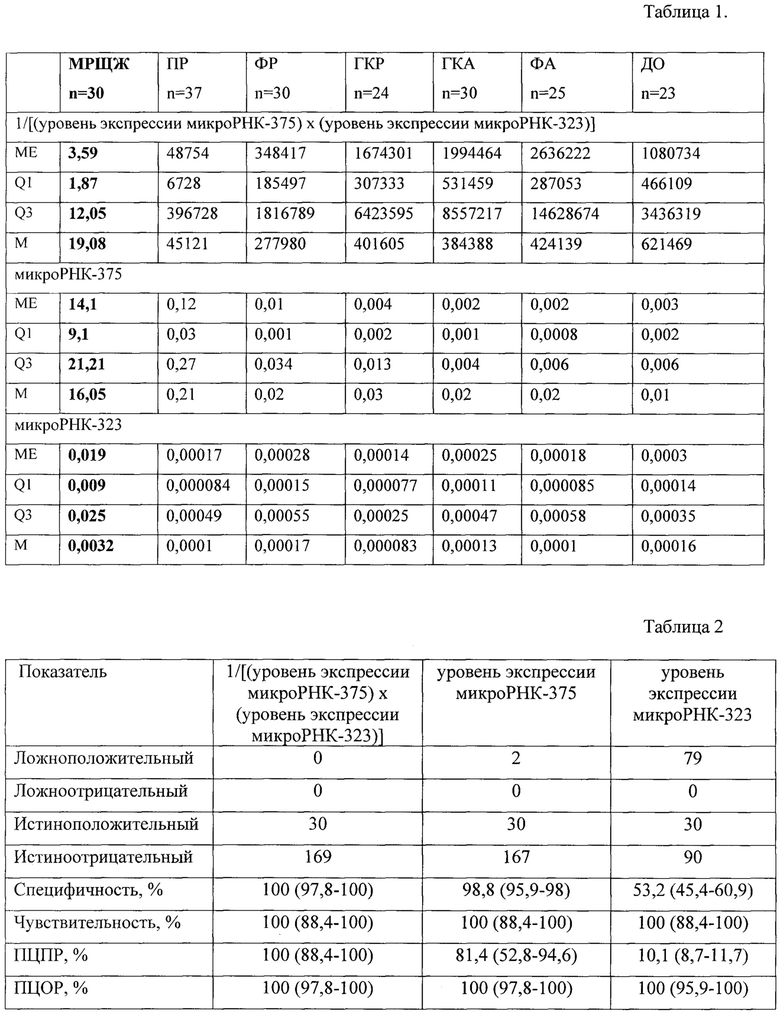
В таблице 1 представлены уровни экспрессии микроРНК-375, микроРНК-323, значения соотношения 1/[(уровень экспрессии микроРНК-375) × (уровень экспрессии микроРНК-323)] в различных типах опухолей, где ME - медиана, Q1, Q3 - 1 и 3 квартили, М - среднее. При МРЩЖ уровень микроРНК-375, микроРНК-323 и значения соотношения 1/[(уровень экспрессии микроРНК-375) × (уровень экспрессии микроРНК-323)] статистически значимо отличались от всех типов опухолей (р менее 0,0001).
Наименьшее значение уровня экспрессии микроРНК-375 при МРЩЖ составило 2,1, наименьшее значение уровня экспрессии микроРНК-323 составило 0,0002, наибольшее значение соотношения 1/[(уровень экспрессии микроРНК-375) × (уровень экспрессии микроРНК-323)] при МРЩЖ составило 110. Пороговое значение для диагностики МРЩЖ с помощью микроРНК-375 принято 2,1 и выше, для микроРНК-323 - 0,0002 и выше, соответственно для соотношения 1/[(уровень экспрессии микроРНК-375) × (уровень экспрессии микроРНК-323)] - 110 и ниже.
В таблице 2 представлены диагностические характеристики микроРНК-375, микроРНК-323 и соотношения 1/[(уровень экспрессии микроРНК-375) × (уровень экспрессии микроРНК-323)] для выявления МРЩЖ (включая 95% доверительный интервал), где ПЦПР -предсказательная ценность положительного результата, ПЦОР - предсказательная ценность отрицательного результата.
Из таблицы 2 видно, что способ диагностики МРЩЖ, основанный на измерении уровня экспрессии микроРНК-375 и уровня экспрессии микроРНК-323 (колонки 3, 4) не позволяет обеспечить 100% точность диагностики, и только использование для анализа значений соотношения 1/[(уровень экспрессии микроРНК-375) × (уровень экспрессии микроРНК-323)] позволяет повысить точность диагностики и обладает 100% чувствительностью, 100% специфичностью, 100% ПЦПР и 100% ПЦОР.
Ниже приведены конкретные примеры, иллюстрирующие эффективность заявленного способа дооперационной диагностики МРЩЖ. Пример 1.
У пациентки А., 39 лет, выявлен узел в щитовидной железе 1,0 см. Ей была выполнена тонкоигольная пункционная биопсия щитовидной железы под УЗИ контролем, по результатам цитологического исследования получено доброкачественное заключение (Bethesda II). Однако уровень базального кальцитонина был выше референтного значения - 15 (норма до 10 пг/мл). Для исключения МРЩЖ пациентке была выполнена операция тиреоидэктомия. Гистологическое заключение - зоб. Ретроспективно был проведен молекулярно-генетический анализ первичного цитологического материала с окрашенного стекла этой пациентки заявляемым способом.
Цитологический окрашенный препарат с цитологических стекол смывали 200 мкл лизирующего буфера в пробирку объемом 1,5 мл, далее произвели выделение ДНК и микроРНК с помощью набора «РеалБест экстракция 100» (АО «Вектор-Бест», Новосибирск) в соответствии с инструкцией производителя. Затем провели детекцию и количественную оценку микроРНК-375 и микроРНК-323, основанную на методе ОТ-ПЦР в реальном времени на амплификаторе CFX96 (Bio-Rad Laboratories, США).
Использовали стандартную концентрацию праймеров 0,5 мкМ, концентрация флуоресцентно меченого зонда - 0,25 мкМ. Реакцию обратной транскрипции провели в течение 15 мин. при 16°С, 15 мин. при 42°С, затем обратную транскриптазу инактивировали 2 мин. при 95°С и отбирали 3 мкл полученной смеси для ПЦР в реальном времени. Протокол ПЦР: предварительный прогрев при 95°С - 2 мин, 50 циклов: денатурация при 94°С - 10 сек, отжиг праймеров и элонгация: 60°С - 20 сек. Анализ полученных данных проводили 2(-ΔCt) методом (9). Уровень экспрессии микроРНК-375 составил 0,00208, а уровень экспрессии микроРНК-323 составил 0,040037. Значение показателя 1/[(уровень экспрессии микроРНК-375) × (уровень экспрессии микроРНК-323)]=1/(0,00208 × 0,040037) составило 12008, на основании чего было сделано заключение об отсутствии у пациентки МРЩЖ.
Пример 2.
Пациентка В. 25 лет, выявлен узел щитовидной железы. Выполнена тонкоигольная пункционная биопсия щитовидной железы под УЗИ контролем, по результатам цитологического исследования фолликулярная опухоль (Bethesda II, риск злокачественности менее 5%). Уровень кальцитонина 35 пг/мл. В соответствии с клиническими рекомендациями, цитологическое заключение Bethesda II не является показанием к оперативному лечению. Однако, повышенный уровень кальцитонина, стал основанием для проведения диагностической операции. Ретроспективно был проведен молекулярно-генетический анализ первичного цитологического материала с окрашенного стекла этой пациентки заявляемым способом, аналогично примеру 1. Уровень экспрессии микроРНК-375 составил 2,80106, а уровень экспрессии микроРНК-323 составил 0,00327. Значение показателя 1/[(уровень экспрессии микроРНК-375) × (уровень экспрессии микроРНК-323)]=1/(2,80106 × 0,00327) составило 109, на основании чего было сделано заключение о наличии у пациентки МРЩЖ.
Предлагаемый способ обеспечивает сокращение количества необоснованных хирургических вмешательств, которые могут привести к значительному снижению качества жизни за счет наличия специфических послеоперационных осложнений.
Источники информации
1. Wells SA Jr et al. American Thyroid Association Guidelines Task Force on Medullary Thyroid Carcinoma. Revised American Thyroid Association guidelines for the management of medullary thyroid carcinoma. Thyroid. 2015 Jun; 25(6):567-610. doi: 10.1089/thy.2014.0335. PMID: 25810047; PMCID: PMC4490627.
2. Vargas-Salas, S.,  , J.R., Urra, S.,
, J.R., Urra, S.,  , J.M., Mena, N., Uslar, Т., Lagos, M.,
, J.M., Mena, N., Uslar, Т., Lagos, M.,  , M., &
, M., &  , H.E. (2018). Genetic testing for indeterminate thyroid cytology: review and meta-analysis. Endocrine-related cancer, 25(3), R163-R177. https://doi.org/10.1530/ERC-17-0405.
, H.E. (2018). Genetic testing for indeterminate thyroid cytology: review and meta-analysis. Endocrine-related cancer, 25(3), R163-R177. https://doi.org/10.1530/ERC-17-0405.
3. Santos, M., Buzolin, A.L., Gama, R.R., Silva, E., Dufloth, R.M., Figueiredo, D., & Carvalho, A.L. (2018). Molecular Classification of Thyroid Nodules with Indeterminate Cytology: Development and Validation of a Highly Sensitive and Specific New miRNA-Based Classifier Test Using Fine-Needle Aspiration Smear Slides. Thyroid: official journal of the American Thyroid Association, 28(12), 1618-1626. https://doi.org/10.1089/thy.2018.0254.
4. Titov S, Demenkov PS, Lukyanov SA, et al. Preoperative detection of malignancy in fine-needle aspiration cytology (FNAC) smears with indeterminate cytology (Bethesda III, IV) by a combined molecular classifier [published online ahead of print, 2020 Mar 25.
5. Randolph GW, Sosa JA, Hao Y, et al. Preoperative Identification of Medullary Thyroid Carcinoma (MTC): Clinical Validation of the Afirma MTC RNA-Sequencing Classifier. Thyroid. 2022 Sep; 32(9): 1069-1076. doi: 10.1089/thy.2022.0189. Epub 2022 Aug 8. PMID: 35793115; PMCID: PMC9526471.
6. Ciarletto AM, Narick C, Malchoff CD, et al. Analytical and clinical validation of pairwise microRNA expression analysis to identify medullary thyroid cancer in thyroid fine-needle aspiration samples. Cancer Cytopathol. 2021; 129(3):239-249. doi: 10.1002/cncy.22365.
7. Патент RU 2757347 C1, опубл. 13.10.2021, Бюл. 29.
8. Патент RU 2705110 C1, опубл. 06.11.2019, Бюл. 31.
9. Livak KJ, Schmittgen TD. Analysis of relative gene expression data using realtime quantitative PCR and the 2(-Delta Delta C(T)) Method. Methods. 2001 Dec; 25(4):402
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ дифференциальной диагностики узловых образований щитовидной железы человека | 2021 |
|
RU2757347C1 |
| Способ дифференциальной диагностики новообразований щитовидной железы | 2019 |
|
RU2705110C1 |
| Способ оценки риска наличия рака щитовидной железы у пациентов с синдромом узлового зоба | 2023 |
|
RU2814933C1 |
| Способ комплексной дооперационной дифференциальной диагностики доброкачественных и злокачественных узловых образований щитовидной железы | 2022 |
|
RU2805941C1 |
| Способ дооперационной дифференциальной диагностики доброкачественных и злокачественных узловых образований щитовидной железы | 2021 |
|
RU2783304C1 |
| Способ дооперационной дифференциальной диагностики анапластического рака щитовидной железы | 2021 |
|
RU2759128C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ НОВООБРАЗОВАНИЙ ЩИТОВИДНОЙ ЖЕЛЕЗЫ ЧЕЛОВЕКА | 2014 |
|
RU2569154C1 |
| СПОСОБ ДИАГНОСТИКИ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ ЩИТОВИДНОЙ ЖЕЛЕЗЫ | 2023 |
|
RU2820815C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ДОБРОКАЧЕСТВЕННЫХ И ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ ЩИТОВИДНОЙ ЖЕЛЕЗЫ ЧЕЛОВЕКА | 2014 |
|
RU2548773C1 |
| Способ выбора тактики лечения узловых образований щитовидной железы | 2023 |
|
RU2823767C1 |
Изобретение относится к медицине, а именно к онкологии, и может быть использовано для дооперационной диагностики медуллярного рака щитовидной железы (МРЩЖ). Из образцов опухоли щитовидной железы, полученных путем тонкоигольной аспирационной пункционной биопсии, выделяют микроРНК. Определяют уровни экспрессии микроРНК-375 и микроРНК-323. Рассчитывают значение показателя 1/[(уровень экспрессии микроРНК-375) × (уровень экспрессии микроРНК-323)]. При значении данного показателя, равном или менее 110, диагностируют МРЩЖ. Способ обеспечивает упрощение и ускорение дооперационной диагностики МРЩЖ при сохранении высокой точности анализа за счет использования минимального набора значимых микроРНК. 2 табл., 2 пр.
Способ дооперационной диагностики медуллярного рака щитовидной железы, включающий выделение микроРНК из цитологических препаратов, полученных путем тонкоигольной аспирационной пункционной биопсии из опухоли щитовидной железы, определение уровня экспрессии микроРНК, основанное на методе полимеразной цепной реакции с обратной транскрипцией в реальном времени, отличающийся тем, что определяют уровни экспрессии микроРНК-375 и микроРНК-323, далее рассчитывают значение показателя 1/[(уровень экспрессии микроРНК-375) × (уровень экспрессии микроРНК-323)] и при значении данного показателя, равном или менее 110, диагностируют у пациента медуллярный рак щитовидной железы.
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ НОВООБРАЗОВАНИЙ ЩИТОВИДНОЙ ЖЕЛЕЗЫ ЧЕЛОВЕКА | 2014 |
|
RU2569154C1 |
| Многоканальная измерительная система для измерения геометрического профиля трубопровода | 2021 |
|
RU2772550C1 |
| СЕРДЮКОВА О.С | |||
| и др | |||
| МикроРНК - перспективные молекулярные маркеры обнаружения рака в узлах щитовидной железы | |||
| Клиническая и экспериментальная тиреоидология | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| GALUPPINI F | |||
| et al | |||
| MicroRNAs in Medullary Thyroid Carcinoma: A State of the Art Review of the Regulatory | |||
Авторы
Даты
2024-05-21—Публикация
2023-11-22—Подача