Изобретение относится к области аналитической химии и может быть использовано для количественного экстракционно-колориметрического определения общего содержания кальция в цельном и сухом молоке, молочных детских смесях с применением смартфона. Кальций является макроэлементом, который участвует во многих процессах жизнедеятельности человека, и находится в молоке в легкоусвояемой и сбалансированной с фосфором форме, а его длительный дефицит в рационе приводит ко множеству негативных последствий для здоровья человека. Содержание кальция в молоке относится к важным его показателям с физиологической точки зрения питания человека, а также учитывается при производстве ферментированных молочных продуктов (сыры, творог и т.п.), поэтому необходимо контролировать содержание кальция в молоке и молочных продуктах.
Известен способ определения растворенного кальция (ионов кальция) в цельном молоке [1], включающий следующие стадии анализа: отбор пробы и термостатирование при 20-25°С, отделение сыворотки молока при помощи добавления избытка хлорида натрия в течение 10-15 мин, фильтрование смеси через бумажный фильтр и определение в фильтрате растворенного кальция комплексонометрическим методом путем титрования пробы раствором трилона Б. Также известен способ ионометрического определения ионов кальция, натрия, аммония, хлорид-ионов в молоке и кислотности молока [2] с использованием экспресс-анализатора, состоящего из комбинированного электрода, в котором объединены ионоселективный и вспомогательный электроды, и высокоомного преобразователя, снабженного встроенным программируемым контроллером. Общим недостатком данных способов является возможность определения только одной формы кальция (растворенной).
Для определения кальция в продуктах питания, в частности в молочных продуктах, часто используются методы атомной спектрометрии. Например, известен способ определения кальция в молоке и молочных продуктах методом атомно-абсорбционной спектрометрии с пламенной атомизацией [3]. Данный способ позволяет проводить определение общего содержания кальция в образцах, так как в схему анализа включена стадия озоления, во время которой в течение 6 ч при 550°С кальций высвобождается из соединений с белками и прочими компонентами матрицы молока и молочных продуктов. При растворении золы пробы в концентрированных соляной или азотной кислотах все формы кальция, присутствовавшие в пробе, переходят в форму ионов кальция. Полученный раствор после разбавления анализируют с помощью спектрометра. Таким образом, предложенный способ является энерго- и времязатратным в связи с необходимостью озоления пробы, а также включает большое количество стадий с применением токсичных реагентов. Кроме того, муфельная печь, используемая для озоления, и атомно-абсорбционный спектрометр являются исключительно лабораторным немобильным оборудованием.
Наиболее близким к заявленному изобретению и выбранным в качестве прототипа является способ экстракционно-фотометрического определения кальция в различных пробах, в частности, в сухом молоке с применением смартфона [4]. На первом этапе проводят мокрое разложение в присутствии азотной кислоты и пероксида водорода и разбавление минерализата дистиллированной водой в мерной колбе. На втором этапе полученный раствор пробы смешивают с раствором фотометрического реагента (бис-(2-гидроксианил)-глиоксаля), этанолом и боратным буферным раствором для образования аналитической формы. Затем добавляют раствор поверхностно-активного вещества (тетрадецилдиметилбензиламмония хлорида) и экстрагент (смесь трихлорметана и дихлорметана). В присутствии поверхностно-активного вещества происходит жидкостно-жидкостная микроэкстракция аналитической формы в фазу экстрагента. После центрифугирования получают изображение нижней окрашенной фазы экстрагента в колориметрическом боксе с помощью смартфона и рассчитывают общее содержание кальция в молоке на основании интенсивности окраски по значениям цветовых координат. Недостатком способа является применение опасных концентрированных сильных кислот и окислителей (азотной кислоты, пероксида водорода), а также токсичных хлорорганических растворителей (трихлорметана и дихлорметана). Кроме того, проведение мокрого разложения требует наличия дополнительного оборудования, высоких затрат электроэнергии, представляет опасность для оператора. Также, представленный способ содержит стадию разбавления минерализата до 100 раз, что может приводить к увеличению погрешности получаемого результата.
Техническим результатом предложенного изобретения по сравнению с прототипом является более простой (не требует мокрого разложения), энергоэффективный (не предполагает нагревания), экологически безопасный (позволяет исключить применение концентрированных кислот, окислителей и токсичных хлорорганических растворителей), экспрессный (отсутствует необходимость охлаждения пробы после мокрого разложения, более короткое время центрифугирования) и универсальный (процедура аналогична для проб цельного и сухого молока, молочных детских смесей) способ подготовки проб цельного и сухого молока, молочных детских смесей и их последующего анализа экстракционно-фотометрическим методом с применением смартфона.
Техническая задача заявленного изобретения состоит в увеличении производительности анализа, проведении пробоподготовки цельного и сухого молока, молочных детских смесей без мокрого разложения и сопутствующих минеральных кислот и окислителей, применении более безопасного экстрагента и доступного, мобильного оборудования (смартфона) для фотометрического определения кальция в образцах.
Заявленный технический результат достигается за счет перевода различных форм кальция, находящихся в пробе, в растворенную ионизированную форму в присутствии трихлоруксусной кислоты без нагревания с последующим образованием окрашенной аналитической формы аналита, ее концентрированием методом жидкостно-жидкостной микроэкстракции, получением изображения экстракта с применением смартфона и его обработкой с целью количественного определения кальция в пробе на основании значений координат цвета в системе RGB, связанных с интенсивностью окраски экстракта. Пробы цельного молока не требуют восстановления. Пробы сухого молока и молочных детских смесей восстанавливают путем добавления деионизированной воды к навеске твердофазного объекта, перемешивания смеси стеклянной палочкой и выдерживания в течение 15 мин для набухания белков. Сначала к пробе цельного молока или восстановленного сухого молока или восстановленной молочной детской смеси добавляют 20% водный раствор трихлоруксусной кислоты и перемешивают гетерогенную смесь в течение 30-35 мин, после чего центрифугируют в течение 5 мин при 4500-5500 об/мин, разбавляют прозрачную надосадочную жидкость в 10 раз деионизированной водой и путем добавления концентрированного раствора гидроксида калия доводят рН полученного раствора до значения 6,00±0,05. Затем проводят получение окрашенной аналитической формы в полимерной пробирке при добавлении раствора хромогенного реагента (1-(2-пиридилазо)-2-нафтола) и первичного амина (н-октиламина), после чего вводят водный раствор хлорида калия. Протекает жидкостно-жидкостная микроэкстракция окрашенного производного (хелатного комплексного соединения) в фазу н-октиламина, разделение фаз осуществляют центрифугированием в течение 3 мин при 4500-5500 об/мин. Пробирку с разделенными жидкими фазами (водной фазой и фазой н-октиламина) переносят в лабораторный колориметрический бокс и вставляют в держатель. Включают ручной светодиодный фонарь, обеспечивающий равномерное освещение образца внутри бокса, и плотно закрывают бокс. Затем получают изображение пробирки с помощью камеры смартфона, присоединяя ее к прямоугольному отверстию в стенке бокса, без активации вспышки и рассчитывают значение аналитического сигнала на основании значений цветовых координат, соответствующих области окрашенной фазы н-октиламина, с помощью приложения. Количественное определение кальция в пробе проводят с использованием метода абсолютной градуировки. Предложенный способ обеспечивает степень извлечения кальция 97%. Предел обнаружения составляет 40 мг/дм3, диапазон определяемых концентраций 120-5000 мг/дм3 (естественное содержание кальция в цельном молоке, восстановленных сухом молоке и молочных детских смесях варьируется в диапазоне 500-2000 мг/дм3 [5]).
Отличительными признаками заявляемого способа от наиболее близкого аналога, взятого за прототип, являются:
- применение раствора трихлоруксусной кислоты для перевода кальция в ионизированную растворенную форму и осаждения белков вместо энергозатратного мокрого разложения образца в присутствии агрессивных реагентов (концентрированной минеральной кислоты и окислителя);
- использование для жидкостно-жидкостной микроэкстракции более экологически безопасного и гораздо менее летучего экстрагента (н-октиламина вместо смеси трихлорметана и дихлорметана), а также доступного и нетоксичного вспомогательного вещества (хлорида калия вместо поверхностно-активного вещества тетрадецилдиметилбензиламмония хлорида);
- отсутствие необходимости поддерживать значение рН раствора пробы с помощью буферного раствора, так как экстрагент является первичным амином (основанием) и создает необходимые условия для образования аналитической формы;
- широкий диапазон определяемых концентраций, позволяющий анализировать пробы с высоким содержанием кальция (молоко, сухое молоко, молочные детские смеси) с меньшим разбавлением.
Заявленные отличительные признаки позволяют проводить количественное определение кальция в цельном и сухом молоке и детских смесях портативно, без использования больших объемов токсичных реагентов и временных затрат, не уступая при этом в точности анализа.
Заявленный способ был апробирован в лабораторных условиях СПбГУ, результаты апробации представлены в виде конкретных примеров реализации. Исследования проведены с использованием оборудования ресурсного центра «Методы анализа состава вещества» Научного парка СПбГУ и инструментального обеспечения кафедры аналитической химии СПбГУ.
Пример 1.
Пробоотбор
Образец цельного молока №1 был приобретен в местном супермаркете (г. Санкт-Петербург). Сохранность продукта обеспечивали соблюдением условий, указанных производителем на упаковке.
Пробоподготовка
На первом этапе 4 см3 пробы цельного молока помещали в стеклянную пробирку вместимостью 10 см3. Затем добавляли 6 см3 20% водного раствора трихлоруксусной кислоты и перемешивали гетерогенную смесь на перемешивающем устройстве в течение 30 мин для полного осаждения белков. После центрифугирования в течение 5 мин при 5000 об/мин полученную прозрачную надосадочную жидкость разбавляли в 10 раз деионизированной водой. рН разбавленного образца доводили с помощью 5 моль/дм3 раствора гидроксида калия до 6,00±0,05, контролируя его при помощи рН-метра. На втором этапе проводили процедуру получения окрашенной формы аналита и ее микроэкстракции в фазу н-октиламина. Для этого 1,5 см3 разбавленной и нейтрализованной надосадочной жидкости, полученной на первом этапе, переносили в пробирку Эппендорфа вместимостью 4 см3. Затем к пробе добавляли 0,15 см3 н-октиламина, 0,6 см3 50 мкмоль/дм3 раствора хромогенного реагента (1-(2-пиридилазо)-2-нафтола) и 0,9 см3 1,3 моль/дм3 водного раствора хлорида калия. До и после добавления раствора хлорида калия образец осторожно встряхивали вручную в течение 20 с. Разделение фаз осуществляли центрифугированием в течение 3 мин при 5000 об/мин. Холостой образец (деионизированную воду) также проводили через все стадии пробоподготовки.
Анализ
Пробирку с разделенными жидкими фазами (водной фазой и фазой н-октиламина) переносили в лабораторный колориметрический бокс и вставляли в держатель образца. Включали ручной светодиодный фонарь, обеспечивающий равномерное освещение образца, и плотно закрывали бокс.Затем получали изображение пробирки с помощью задней камеры смартфона, присоединяя ее к прямоугольному отверстию в стенке бокса, без активации вспышки.
Цифровые изображения сохранялись в формате JPEG и затем обрабатывались с помощью бесплатного и простого в использовании приложения для смартфонов (мобильное устройство: iPhone 8 (Apple Inc., USA); приложение Colorimeter, версия 13.2). На основании участка изображения, относящегося к центральной части окрашенной фазы н-октиламина, получали значения цветовых координат по модели RGB. Среднее значение для каждой координаты по модели RGB для выбранной интересующей области указывалось непосредственно на экране смартфона приложением без дополнительных вычислительных преобразований. Значение аналитического сигнала (А), коррелирующее с интенсивностью окраски фазы н-октиламина и концентрацией кальция в образце, рассчитывали по следующей формуле:
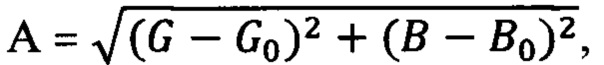
где G и В представляют средние значения цветовых координат для зеленого и синего каналов по модели RGB для анализируемого образца соответственно, a G0 и В0 обозначают значения для зеленого и синего каналов по модели RGB для холостого образца.
Количественное определение кальция в пробе проводили с использованием метода абсолютной градуировки. Результаты анализа представлены в таблице 1. Содержание кальция в пробе цельного молока составило 949 мг/дм3. Правильность результатов подтверждали путем анализа с помощью независимого способа (атомно-эмиссионная спектрометрия с индуктивно-связанной плазмой (АЭС-ИСП) с предварительным мокрым микроволновым разложением) [6]. Из полученных результатов (таблица 1) видно, что расхождение между концентрациями, установленными с помощью разработанного и независимого способов, незначимо (составляет 8%).

Пример 2.
Пробоотбор
Образец сухого молока №2 был приобретен в местном супермаркете (г.Санкт-Петербург). Сохранность продукта обеспечивали соблюдением условий, указанных производителем на упаковке. Сухое молоко массой (1,5000±0,0010) г восстанавливали перед анализом путем добавления дистиллированной воды (40°С) до достижения конечной массы (12,00±0,02) г. Восстановленный образец гомогенизировали путем тщательного перемешивания стеклянной палочкой и оставляли на 15 мин для набухания белков.
Пробоподготовка
На первом этапе 4 см3 пробы восстановленного сухого молока помещали в стеклянную пробирку вместимостью 10 см3. Затем добавляли 6 см3 20% водного раствора трихлоруксусной кислоты и перемешивали гетерогенную смесь на перемешивающем устройстве в течение 30 мин для полного осаждения белков. После центрифугирования в течение 5 мин при 5000 об/мин полученную прозрачную надосадочную жидкость разбавляли в 10 раз деионизированной водой. рН разбавленного образца доводили с помощью 5 моль/дм3 раствора гидроксида калия до 6,00±0,05, контролируя его при помощи рН-метра. На втором этапе проводили процедуру получения окрашенной формы аналита и ее микроэкстракции в фазу н-октиламина. Для этого 1,5 см3 разбавленной и нейтрализованной надосадочной жидкости, полученной на первом этапе, переносили в пробирку Эппендорфа вместимостью 4 см3. Затем к пробе добавляли 0,15 см3 н-октиламина, 0,6 см3 50 мкмоль/дм3 раствора хромогенного реагента (1-(2-пиридилазо)-2-нафтола) и 0,9 см3 1,3 моль/дм3 водного раствора хлорида калия. До и после добавления раствора хлорида калия образец осторожно встряхивали вручную в течение 20 с. Разделение фаз осуществляли центрифугированием в течение 3 мин при 5000 об/мин. Холостой образец (деионизированную воду) также проводили через все стадии пробоподготовки.
Анализ
Пробирку с разделенными жидкими фазами (водной фазой и фазой н-октиламина) переносили в лабораторный колориметрический бокс и вставляли в держатель образца. Включали ручной светодиодный фонарь, обеспечивающий равномерное освещение образца, и плотно закрывали бокс. Затем получали изображение пробирки с помощью задней камеры смартфона, присоединяя ее к прямоугольному отверстию в стенке бокса, без активации вспышки.
Цифровые изображения сохранялись в формате JPEG и затем обрабатывались с помощью бесплатного и простого в использовании приложения для смартфонов (мобильное устройство: iPhone 8 (Apple Inc., USA); приложение Colorimeter, версия 13.2). На основании участка изображения, относящегося к центральной части окрашенной фазы н-октиламина, получали значения цветовых координат по модели RGB. Среднее значение для каждой координаты по модели RGB для выбранной интересующей области указывалось непосредственно на экране смартфона приложением без дополнительных вычислительных преобразований. Значение аналитического сигнала (А), коррелирующее с интенсивностью окраски фазы н-октиламина и концентрацией кальция в образце, рассчитывали по следующей формуле:
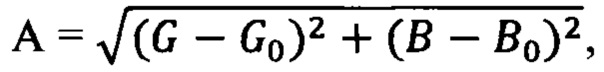
где G и В представляют средние значения для зеленого и синего каналов по модели RGB для анализируемого образца соответственно, a G0 и В0 обозначают значения для зеленого и синего каналов по модели RGB для холостого образца.
Количественное определение кальция в пробе проводили с использованием метода абсолютной градуировки. Результаты анализа представлены в таблице 2. Содержание кальция в пробе восстановленного сухого молока составило 1074 мг/дм3. Правильность результатов подтверждали путем анализа с помощью независимого способа (атомно-эмиссионная спектрометрия с индуктивно-связанной плазмой (АЭС-ИСП) с предварительным мокрым микроволновым разложением) [6]. Из полученных результатов (таблица 2) видно, что расхождение между концентрациями, установленными с помощью разработанного и независимого способов, незначимо (составляет 11%).

Пример 3.
Пробоотбор
Образец сухой детской молочной смеси №3 был приобретен в местном супермаркете (г. Санкт-Петербург). Сохранность продукта обеспечивали соблюдением условий, указанных производителем на упаковке. Сухую детскую молочную смесь массой (1,5000±0,0010) г восстанавливали перед анализом путем добавления дистиллированной воды (40°С) до достижения конечной массы (12,00±0,02) г. Восстановленный образец гомогенизировали путем тщательного перемешивания стеклянной палочкой и оставляли на 15 мин для набухания белков.
Пробоподготовка
На первом этапе 4 см3 пробы восстановленной сухой детской молочной смеси помещали в стеклянную пробирку вместимостью 10 см3. Затем добавляли 6 см3 20% водного раствора трихлоруксусной кислоты и перемешивали гетерогенную смесь на перемешивающем устройстве в течение 30 мин для полного осаждения белков. После центрифугирования в течение 5 мин при 5000 об/мин полученную прозрачную надосадочную жидкость разбавляли в 10 раз деионизированной водой. рН разбавленного образца доводили с помощью 5 моль/дм3 раствора гидроксида калия до 6,00±0,05, контролируя его при помощи рН-метра. На втором этапе проводили процедуру получения окрашенной формы аналита и ее микроэкстракции в фазу н-октиламина. Для этого 1,5 см3 разбавленной и нейтрализованной надосадочной жидкости, полученной на первом этапе, переносили в пробирку Эппендорфа вместимостью 4 см3. Затем к пробе добавляли 0,15 см3 н-октиламина, 0,6 см3 50 мкмоль/дм3 раствора хромогенного реагента (1-(2-пиридилазо)-2-нафтола) и 0,9 см3 1,3 моль/дм3 водного раствора хлорида калия. До и после добавления раствора хлорида калия образец осторожно встряхивали вручную в течение 20 с. Разделение фаз осуществляли центрифугированием в течение 3 мин при 5000 об/мин. Холостой образец (деионизированную воду) также проводили через все стадии пробоподготовки.
Анализ
Пробирку с разделенными жидкими фазами (водной фазой и фазой н-октиламина) переносили в лабораторный колориметрический бокс и вставляли в держатель образца. Включали ручной светодиодный фонарь, обеспечивающий равномерное освещение образца, и плотно закрывали бокс.Затем получали изображение пробирки с помощью задней камеры смартфона, присоединяя ее к прямоугольному отверстию в стенке бокса, без активации вспышки.
Цифровые изображения сохранялись в формате JPEG и затем обрабатывались с помощью бесплатного и простого в использовании приложения для смартфонов (мобильное устройство: iPhone 8 (Apple Inc., USA); приложение Colorimeter, версия 13.2). На основании участка изображения, относящегося к центральной части окрашенной фазы н-октиламина, получали значения цветовых координат по модели RGB. Среднее значение для каждой координаты по модели RGB для выбранной интересующей области указывалось непосредственно на экране смартфона приложением без дополнительных вычислительных преобразований. Значение аналитического сигнала (А), коррелирующее с интенсивностью окраски фазы н-октиламина и концентрацией кальция в образце, рассчитывали по следующей формуле:

где G и В представляют средние значения для зеленого и синего каналов по модели RGB для анализируемого образца соответственно, a G0 и В0 обозначают значения для зеленого и синего каналов по модели RGB для холостого образца.
Количественное определение кальция в пробе проводили с использованием метода абсолютной градуировки. Результаты анализа представлены в таблице 3. Содержание кальция в пробе восстановленной сухой детской молочной смеси составило 512 мг/дм3. Правильность результатов подтверждали путем анализа с помощью независимого способа (атомно-эмиссионная спектрометрия с индуктивно-связанной плазмой (АЭС-ИСП) с предварительным мокрым микроволновым разложением) [6]. Из полученных результатов (таблица 3) видно, что расхождение между концентрациями, установленными с помощью разработанного и независимого способов, незначимо (составляет 4%).

Как показывают результаты проведенного анализа на примерах конкретной реализации, заявленное изобретение подтверждает достижение указанного технического результата и наглядно демонстрирует возможность эффективного извлечения кальция из проб сухого и цельного молока, детских молочных смесей за счет осаждения белков, перевода аналита в окрашенную форму и микроэкстракции полученного комплекса в фазу н-октиламина. Продемонстрирована возможность количественного определения кальция в пробах сухого и цельного молока, детских молочных смесей с помощью колориметрического анализа с применением смартфона в качестве детектирующего устройства. Предложенный способ позволяет уменьшить объемы использующихся растворителей и сократить время анализа, а также увеличивает доступность анализа, так как не предполагает использования дорогостоящего лабораторного оборудования.
Список использованных источников информации
1. SU 1557520 "Способ определения растворимого кальция в цельном молоке".
2. RU 6629 "Ионометрический экспресс-анализатор для контроля пищевых продуктов".
3. Sowmya R., Indumathi K.Р., Arora S., Sharma V., Singh A.K. (2015). Detection of calcium-based neutralizers in milk and milk products by AAS. Journal of Food Science and Technology, 52(2), 1188-1193.
4. CN 109100309 В "Method for determining trace calcium ions by dispersion liquid microextraction-android mobile phone colorimetry" (прототип).
5. Masotti F., Cattaneo S., Stuknyte M., Pica V., De Noni I. (2020). Analytical advances in the determination of calcium in bovine milk, dairy products and milk-based infant formulas. Trends in Food Science & Technology, 103, 348-360.
6. ISO 15151: 2018 Milk, milk products, infant formula and adult nutritionals - Determination of minerals and trace elements - Inductively coupled plasma atomic emission spectrometry (ICP-AES) method.
Изобретение относится к области аналитической химии, а именно для проведения контроля качества молока и детских смесей. Способ количественного экстракционно-колориметрического определения кальция в цельном и сухом молоке, молочных детских смесях включает осаждение белков, переведение кальция в раствор в форме ионов, образование окрашенного комплекса между хромогенным реагентом и ионами кальция, микроэкстракцию полученного комплекса в фазу первичного амина и установление интенсивности ее окраски с применением смартфона. Осаждение белков пробы цельного молока, сухого молока, молочной детской смеси и высвобождение кальция осуществляют путем добавления водного раствора трихлоруксусной кислоты, перемешивания, а также центрифугирования до разделения фаз. Полученную прозрачную надосадочную жидкость разбавляют так, чтобы концентрация трихлоруксусной кислоты в образце составляла не более 2%, и доводят кислотность образца с помощью сильного основания до нейтральной реакции среды. Затем проводят процедуру получения окрашенной формы аналита и ее экстракции в фазу первичного амина при смешении нейтрализованной надосадочной жидкости с первичным амином, раствором хромогенного реагента и раствором электролита. Осуществляют центрифугирование до разделения фаз. Емкость с разделенными жидкими фазами, в качестве которых выступают водная фаза и фаза первичного амина, переносят в камеру, предназначенную для получения изображений и защищенную от внешнего света, включают источник освещения, и плотно закрывают камеру, затем получают изображение емкости с помощью смартфона, присоединяя его к отверстию в боксе. На основании участка изображения, относящегося к окрашенной фазе первичного амина, получают значения цветовых координат, после чего вычисляют значение аналитического сигнала А, коррелирующее с интенсивностью окраски фазы первичного амина, по формуле:  где G и В - значения цветовых координат для зеленого и синего каналов для анализируемого образца соответственно, a G0 и В0 - те же характеристики для холостого образца, и рассчитывают концентрацию кальция в цельном молоке, сухом молоке, молочной детской смеси С согласно формуле, полученной методом абсолютной градуировки:
где G и В - значения цветовых координат для зеленого и синего каналов для анализируемого образца соответственно, a G0 и В0 - те же характеристики для холостого образца, и рассчитывают концентрацию кальция в цельном молоке, сухом молоке, молочной детской смеси С согласно формуле, полученной методом абсолютной градуировки:  где р, k и t - числовые коэффициенты. Техническим результатом является упрощение пробоподготовки, повышение экспрессности, доступности и точность анализа. 2 з.п. ф-лы, 3 табл.
где р, k и t - числовые коэффициенты. Техническим результатом является упрощение пробоподготовки, повышение экспрессности, доступности и точность анализа. 2 з.п. ф-лы, 3 табл.
1. Способ количественного экстракционно-колориметрического определения кальция в цельном и сухом молоке, молочных детских смесях, включающий осаждение белков, переведение кальция в раствор в форме ионов, образование окрашенного комплекса между хромогенным реагентом и ионами кальция, микроэкстракцию полученного комплекса в фазу первичного амина и установление интенсивности ее окраски с применением смартфона, отличающийся тем, что осаждение белков пробы цельного молока, сухого молока, молочной детской смеси и высвобождение кальция осуществляют путем добавления водного раствора трихлоруксусной кислоты, перемешивания, а также центрифугирования до разделения фаз, после чего полученную прозрачную надосадочную жидкость разбавляют так, чтобы концентрация трихлоруксусной кислоты в образце составляла не более 2%, и доводят кислотность образца с помощью сильного основания до нейтральной реакции среды, затем проводят процедуру получения окрашенной формы аналита и ее экстракции в фазу первичного амина при смешении нейтрализованной надосадочной жидкости с первичным амином, раствором хромогенного реагента и раствором электролита, после чего осуществляют центрифугирование до разделения фаз, емкость с разделенными жидкими фазами, в качестве которых выступают водная фаза и фаза первичного амина, переносят в камеру, предназначенную для получения изображений и защищенную от внешнего света, включают источник освещения, и плотно закрывают камеру, затем получают изображение емкости с помощью смартфона, присоединяя его к отверстию в боксе, и на основании участка изображения, относящегося к окрашенной фазе первичного амина, получают значения цветовых координат, после чего вычисляют значение аналитического сигнала А, коррелирующее с интенсивностью окраски фазы первичного амина, по формуле:
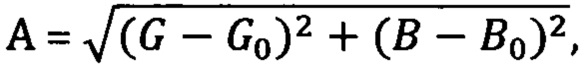
где G и В - значения цветовых координат для зеленого и синего каналов для анализируемого образца соответственно, a G0 и В0 - те же характеристики для холостого образца, и рассчитывают концентрацию кальция в цельном молоке, сухом молоке, молочной детской смеси С согласно формуле, полученной методом абсолютной градуировки:
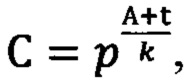
где р, k и t - числовые коэффициенты.
2. Способ по п. 1, отличающийся тем, что вместо раствора электролита используют сухой электролит.
3. Способ по п. 1, отличающийся тем, что в качестве первичного амина используют н-октиламин, в качестве хромогенного реагента - 1-(2-пиридилазо)-2-нафтол, а в качестве раствора электролита - раствор хлорида калия.
| CN 109100309 A (UNIV NORTHWEST NORMAL), 28.12.2018 | |||
| SOWMYA R., INDUMATHI K.Р., ARORA S., SHARMA V., SINGH A.K | |||
| "DETECTION OF CALCIUM-BASED NEUTRALIZERS IN MILK AND MILK PRODUCTS BY AAS", JOURNAL OF FOOD SCIENCE AND TECHNOLOGY, V | |||
| Устройство для устранения мешающего действия зажигательной электрической системы двигателей внутреннего сгорания на радиоприем | 1922 |
|
SU52A1 |
| Механизм для быстрого, прерывчатого вращения ведомого вала | 1924 |
|
SU1188A1 |
| КЛАДКА ИЗ КЛИНКЕРНОГО КИРПИЧА С ЖЕЛЕЗНОЙ АРМАТУРОЙ ДЛЯ СТЕН, ДВЕРЕЙ ИЛИ ОБМУРОВКИ ДЕНЕЖНЫХ КАСС И Т. П. | 1926 |
|
SU6629A1 |
| Способ определения растворимого кальция в цельном молоке | 1987 |
|
SU1557520A1 |
Авторы
Даты
2024-05-30—Публикация
2023-12-22—Подача