ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Настоящей заявке испрашивается приоритет по предварительной заявке США № 62/717771, поданной 10 августа 2018 года, содержание которой включено в настоящее описание в качестве ссылки в полном объеме.
УТВЕРЖДЕНИЕ, КАСАЮЩЕЕСЯ ФЕДЕРАЛЬНО СПОНСИРУЕМОГО ИССЛЕДОВАНИЯ И РАЗРАБОТКИ
[0002] Настоящее изобретение было осуществлено при выполнении Соглашения о совместном проведении исследований с National Institutes of Health, an Agency of the U.S. Department of Health and Human Services, и при поддержке правительством под номером проекта ZIA HG200318 14, National Institutes of Health, National Human Genome Research Institute. Правительство США обладает определенными правами на изобретение.
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[0003] Настоящая заявка содержит список последовательностей, предоставленный в электронной форме в формате ASCII и включенный в настоящее описание в качестве ссылки в полном объеме. Указанная копия ASCII, созданная 30 октября 2018 года, названа 2012538_0062_SL.txt и имеет размер 78203 байт.
УРОВЕНЬ ТЕХНИКИ
[0004] Существует подгруппа заболеваний человека, которые могут быть отслежены по изменениям ДНК, которые являются либо наследственными, либо приобретенными на раннем этапе эмбрионального развития. Особый интерес для разработчиков способов генной терапии представляют заболевания, вызываемые мутацией в одном гене, известные как моногенные. Полагают, что существует более 6000 моногенных заболеваний. Как правило, любое конкретное генетическое заболевание, вызываемое наследуемыми мутациями, является относительно редким, однако в совокупности потери от генетически-обусловленных заболеваний высоки. Хорошо известные генетические заболевания включают кистозный фиброз, мышечную дистрофию Дюшенна, болезнь Гентингтона и серповидноклеточную анемию. Другие классы генетических заболеваний включают метаболические нарушения, такие как органические ацидемии, и лизосомальные болезни накопления, где гены с нарушением функций приводят к дефектам в метаболических процессах и накоплению токсических побочных продуктов, которые могут приводить к серьезной заболеваемости и смертности как за короткий, так и за длительный срок.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0005] Моногенные заболевания представляют особый интерес для биомедицинских изобретателей вследствие кажущейся простоты их патологии заболевания. Однако широкое большинство этих заболеваний и нарушений остаются по существу неизлечимыми. Таким образом, в данной области остается давно испытываемая потребность в способе лечения таких заболеваний.
[0006] В некоторых вариантах осуществления настоящее изобретение относится к способам встраивания трансгена в геном по меньшей мере популяции клеток в ткани индивидуума, причем указанные способы включают стадию введения индивидууму, у которого клетки в ткани не экспрессируют функциональный белок, кодируемый продуктом гена, композиции, которая доставляет трансген, кодирующий функциональный белок, где композиция включает: полинуклеотидную кассету, содержащую первую последовательность нуклеиновой кислоты и вторую последовательность нуклеиновой кислоты, где первая последовательность нуклеиновой кислоты кодирует трансген и вторая последовательность нуклеиновой кислоты находится с 5’- или 3’-стороны от первой последовательности нуклеиновой кислоты и способствует продуцированию двух независимых продуктов генов при встраивании в заданный участок встраивания в геноме клетки, третью последовательность нуклеиновой кислоты, находящуюся с 5’-стороны от полинуклеотида и содержащую последовательность, которая по существу гомологична геномной последовательности с 5’-стороны от участка встраивания, являющегося мишенью, в геноме клетки, и четвертую последовательность нуклеиновой кислоты, находящуюся с 3’-стороны от полинуклеотида и содержащую последовательность, которая по существу гомологична геномной последовательности с 3’-стороны от участка встраивания, являющегося мишенью, в геноме клетки, где после введения композиции трансген встраивается в геном популяции клеток.
[0007] В некоторых вариантах осуществления настоящее изобретение относится к способам повышения уровня экспрессии трансгена в ткани в течение периода времени, причем указанные способы включают стадию введения индивидууму, нуждающемуся в этом, композиции, которая доставляет трансген, который встраивается в геном по меньшей мере популяции клеток в ткани индивидуума, где композиция включает: полинуклеотид, содержащий первую последовательность нуклеиновой кислоты и вторую последовательность нуклеиновой кислоты, где первая последовательность нуклеиновой кислоты кодирует трансген; и вторая последовательность нуклеиновой кислоты находится с 5’- или 3’-стороны от первой последовательности нуклеиновой кислоты и способствует продуцированию двух независимых продуктов генов при встраивании в участок встраивания, являющийся мишенью, в геноме клетки, третью последовательность нуклеиновой кислоты, находящуюся с 5’-стороны от полинуклеотида и содержащую последовательность, которая по существу гомологична геномной последовательности, находящейся с 5’-стороны от участка встраивания, являющегося мишенью, в геноме клетки, и четвертую последовательность нуклеиновой кислоты, находящуюся с 3’-стороны от полинуклеотида и содержащую последовательность, которая по существу гомологична геномной последовательности, находящейся с 3’-стороны от участка встраивания, являющегося мишенью, в геноме клетки, где после введения композиции трансген встраивается в геном популяции клеток и уровень экспрессии трансгена в ткани возрастает на протяжении некоторого периода времени. В некоторых вариантах осуществления, увеличенный уровень экспрессии включает увеличенный процент клеток в ткани, экспрессирующих трансген.
[0008] В некоторых вариантах осуществления настоящее изобретение относится к способам, включающим стадию введения индивидууму дозы композиции, которая доставляет в клетки ткани индивидуума трансген, кодирующий представляющий интерес продукт, который не экспрессируется функционально клетками до введения, где трансген (i) кодирует представляющий интерес продукт; (ii) встраивается в участок встраивания, являющийся мишенью, в геноме множества клеток; (iii) функционально экспрессирует представляющий интерес продукт после встраивания; и (iv) обеспечивает селективное преимущество множеству клеток относительно других клеток в ткани, так что с течением времени ткань достигает уровня функциональной экспрессии представляющего интерес продукта, который, как определено, является более высоким, чем уровень, достигаемый посредством в остальном сравнимого введения, где клетки, в которые встроен трансген, функционально экспрессируют представляющий интерес продукт до введения, где композиция содержит: полинуклеотид, содержащий первую последовательность нуклеиновой кислоты и вторую последовательность нуклеиновой кислоты, где первая последовательность нуклеиновой кислоты кодирует трансген; и вторая последовательность нуклеиновой кислоты находится с 5’- или 3’-стороны от первой последовательности нуклеиновой кислоты и способствует продуцированию двух независимых продуктов генов, когда трансген встраивается в участок встраивания, являющийся мишенью, третью последовательность нуклеиновой кислоты, находящуюся с 5’-стороны от полинуклеотида и содержащую последовательность, которая по существу гомологична геномной последовательность с 5’-стороны от участка встраивания, являющегося мишенью, и четвертую последовательность нуклеиновой кислоты, находящуюся с 3’-стороны от полинуклеотида и содержащую последовательность, которая по существу гомологичная геномной последовательности с 3’-стороны от участка встраивания, являющегося мишенью. В некоторых вариантах осуществления селективное преимущество включает увеличенный процент клеток в ткани, экспрессирующей трансген.
[0009] В некоторых вариантах осуществления композиция содержит рекомбинантный вирусный вектор. В некоторых вариантах осуществления рекомбинантный вирусный вектор представляет собой рекомбинантный вектор на основе AAV. В некоторых вариантах осуществления рекомбинантный вирусный вектор представляет собой или содержит капсидный белок, содержащий или аминокислотную последовательность, обладающую по меньшей мере 95% идентичностью последовательности с аминокислотной последовательностью LK03, AAV8, AAV-DJ; AAV-LK03 или AAVNP59. В некоторых вариантах осуществления композиция дополнительно содержит последовательности ITR AAV2.
[0010] В соответствии с различными вариантами осуществления любой из различных трансгенов можно экспрессироввать в соответствии со способами и композициями, описанными в настоящем описании. Например, в некоторых вариантах осуществления трансген представляет собой или содержит трансген MUT. В некоторых вариантах осуществления трансген MUT представляет собой MUT wt человека; кодон-оптимизированный MUT; синтетический MUT; вариант MUT; мутант MUT или фрагмент MUT.
[0011] В некоторых вариантах осуществления настоящее изобретение относится к рекомбинантным вирусным векторам для встраивания трансгена в участок встраивания, являющийся мишенью, в геноме клетки, включающим: полинуклеотидную кассету, содержащую первую последовательность нуклеиновой кислоты и вторую последовательность нуклеиновой кислоты, где первая последовательность нуклеиновой кислоты содержит трансген MUT; и вторая последовательность нуклеиновой кислоты находится с 5’- или 3’-стороны от первой последовательности нуклеиновой кислоты и способствует продуцированию двух независимых продуктов генов при встраивании в участок встраивания, являющийся мишенью, в геноме клетки, третью последовательность нуклеиновой кислоты, находящуюся с 5’-стороны от полинуклеотидной кассеты вектора и содержащую последовательность, которая по существу гомологична геномной последовательности с 5’-стороны от участка встраивания, являющегося мишенью, в геноме клетки, и четвертую последовательность нуклеиновой кислоты, находящуюся с 3’-стороны от полинуклеотидной кассеты вектора и содержащую последовательность, которая по существу гомологична геномной последовательности с 3’-стороны от участка встраивания, являющегося мишенью, в геноме клетки, где вирусный вектор содержит капсид LK03 AAV.
[0012] Как описано в настоящем описании, настоящее изобретение охватывает несколько преимущественных общепризнанных способов встраивания одного или нескольких трансгенов в геном клетки. Например, в некоторых вариантах осуществления встраивание не включает нуклеазную активность.
[0013] В то время как может быть осуществлено нацеливание на любую пригодную для применения ткань, в некоторых вариантах осуществления тканью является печень.
[0014] Как описано в настоящем описании, предусматриваемые способы и композиции включают полинуклеотидные кассеты по меньшей мере с четырьмя последовательностями нуклеиновых кислот. В некоторых вариантах осуществления вторая последовательность нуклеиновой кислоты содержит: a) пептид 2A, b) участок внутренней посадки рибосомы (IRES), c) N-концевой участок сплайсинга интеина и C-концевой участок сплайсинга интеина, или d) донор сплайсинга и акцептор сплайсинга. В некоторых вариантах осуществления третья и четвертая последовательности нуклеиновых кислот представляют собой плечи гомологии, которые встраивают трансген и вторую последовательность нуклеиновой кислоты в эндогенный локус альбумина, содержащий эндогенный промотор альбумина и эндогенный ген альбумина. В некоторых вариантах осуществления плечи гомологии направляют встраивание полинуклеотидной кассеты непосредственно с 3'-стороны от инициирующего кодона эндогенного гена альбумина или непосредственно с 5'-стороны от стоп-кодона эндогенного гена альбумина.
[0015] В соответствии с различными аспектами третья и/или четвертая нуклеиновые кислоты могут иметь значительную длину (например, длину по меньшей мере 800 нуклеотидов). В некоторых вариантах осуществления третья нуклеиновая кислота имеет 800-1200 нуклеотидов. В некоторых вариантах осуществления четвертая нуклеиновая кислота имеет 800-1200 нуклеотидов.
[0016] В некоторых вариантах осуществления полинуклеотидная кассета не содержит промоторную последовательность. В некоторых вариантах осуществления при встраивании полинуклеотидной кассеты в участок встраивания, являющийся мишенью, в геноме клетки-хозяина трансген экспрессируется под контролем эндогенного промотора в участке встраивания, являющемся мишенью. В некоторых вариантах осуществления участок встраивания, являющийся мишенью, представляет собой локус альбумина, содержащий эндогенный промотор альбумина и эндогенный ген альбумина. В некоторых вариантах осуществления при встраивании полинуклеотидной кассеты в участок встраивания, являющийся мишенью, в геноме клетки-хозяина, трансген экспрессируется под контролем эндогенного промотора альбумина без нарушения экспрессии эндогенного гена альбумина.
[0017] Как используют в настоящей заявке, термины "приблизительно" и "примерно" используются в качестве эквивалентов. Любое цитирование публикаций, патентов или патентных заявок в настоящем описании включено в качестве ссылок в полном объеме. Подразумевается, что любые числа, используемые в настоящей заявке с приблизительно/примерно или без них, охватывают любые нормальные отклонения, понятные среднему специалисту в соответствующей области.
[0018] Другие признаки, задачи и преимущества настоящего изобретения станут очевидными из подробного описания, приведенного ниже. Однако следует понимать, что подробное описание, хотя и указывает на варианты осуществления настоящего изобретения, приводится только в качестве иллюстрации, а не ограничения. Различные изменения и модификации в объеме изобретения станут понятными специалистам в данной области из подробного описания.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0019] На фиг. 1 представлены каскады репарации ДНК: направляемая гомологией репарация (HDR) и репарация посредством негомологичного соединения концов (NHEJ).
[0020] На фиг. 2 представлена схема конструкции GENERIDE™ до встраивания (AAV) и после HR-опосредуемого встраивания в геном в являющемся мишенью локусе альбумина, или ALB. Экспрессия с локуса-мишени приводит к продуцированию альбумина и трансгена в качестве отдельных белков на эквивалентных уровнях, который кодируется геном ALB.
[0021] На фиг. 3 представлены гены, в наибольшей степени экспрессирующиеся в печени, ранжированные от наивысшего (ALB) до номера 2000. Каждый круг соответствует индивидуальному гену. Большинство генов в печени экспрессируются в качестве малой доли от уровней альбумина. TPM=количество транскриптов на миллион.
[0022] На фиг. 4 показано, что печень является органом, где экспрессируется практически весь альбумин организма. Специфические для печени конструкции GENERIDE™, нацеленные на локус ALB, преимущественно будут экспрессироваться в печени.
[0023] На фиг. 5 показано, что уровни экспрессии альбумина в 100x выше экспрессии других определенных генов печени, ассоциированных с моногенными заболеваниями (PAH: фенилкетонурия, F9: гемофилия B, MUT: MMA, UGT1A1: синдром Криглера-Найяра).
[0024] На фиг. 6 проиллюстрировано, как мутации в MUT приводят к нарушению метаболического пути для разветвленных аминокислот, в частности, метионина, треонина, валина и изолейцина.
[0025] На фиг. 7A - фиг. 7B проиллюстрирована структура конструкции LB-001 GENERIDE™. Фиг. 7A) Конструкция GENERIDE™ для LB-001 внутри капсида LK03 AAV. Фиг. 7B) Нуклеиновая кислота, которую можно использовать с капсидом AAV-LK03 для экспрессии последовательности Mut человека (SEQ ID NO: 15).
[0026] На фиг. 8 показано, что мыши Mut-/- демонстрируют увеличенную выживаемость (верхняя панель) и увеличение массы (нижняя панель) после введения новорожденным конструкции GENERIDE™ LB-001 мыши. Планки погрешностей указывают на стандартную ошибку среднего значения, или SEM. В этом исследовании контрольные мыши для сравнения один к одному не были включены; данные для контрольных мышей получены из испытаний, проведенных другими исследователями.
[0027] На фиг. 9 представлено, что мыши MCK-Mut, которым вводили конструкцию GENERIDE™ LB-001 мыши, демонстрируют значительное улучшение роста через один месяц после введения новорожденным. * Указывает на значение p<0,05.
[0028] На фиг. 10 показано, что мыши MCK, которым вводили конструкцию GENERIDE™ LB-001 мыши, демонстрируют значительное снижение двух циркулирующих связанных с заболеванием метаболитов через один месяц после введения новорожденным. На верхней панели представлено снижение концентраций метилмалоновой кислоты в плазме. На нижней панели представлено снижение концентраций метилцитрата в плазме. Не все мыши без введения были включены для сравнения один к одному. Данные мышей без введения включали исторических контрольных мышей. * Указывает на значение p<0,05.
[0029] На фиг. 11 показано, что введение GENERIDE™ может приводить к селективному преимуществу для модифицированных клеток печени. Верхняя панель: Анализ RNAscope срезов печени от мышей, которым вводили конструкцию GENERIDE™ LB-001 мыши. Мышам, генетически модифицированным без (слева) и с (справа) функционирующей копией Mut в печени, проводили введение неонатально. Через более чем один год уровень клеток, экспрессирующих мРНК Mut, специфическую для конструкции GENERIDE™ (закрашенные темным области), был увеличен у мышей, лишенных естественного функционирования копии Mut в печени, что указывает на полезное селективное преимущество конструкции GENERIDE™ LB-001. Нижняя панель: количественное определение для срезов RNAscope, проведенное независимым патологом.
[0030] На фиг. 12 представлен процент клеток печени, содержащих встроенную копию специфического гена Mut GENERIDE™ более чем через один год после однократного введения новорожденным конструкции MUT GENERIDE™ у мышей. Количественное определение ДНК с геном Mut, встроенной в локус альбумина, посредством LR-qPCR. Планки погрешности указывают на SEM. LR-qPCR=количественная ПЦР длинных фрагментов.
[0031] На фиг. 13 продемонстрировано увеличение количества клеток с интегрированной конструкцией GENERIDE™, наблюдаемое с течением времени. Мышам с дефицитом Mut в печени вводили конструкцию GENERIDE™ неонатально. Анализ ДНК в отношении встраивания в локус альбумина проводили посредством LR-qPCR через 1 месяц и более чем через один год после введения дозы. Планки погрешности указывают на SEM.
[0032] На фиг. 14 представлены уровни метилмалоновой кислоты в плазме у мышей Mut-/-; Mck-Mut (гипоморфная модель MMA), которым не проводили и проводили введение. Мыши, которым проводили введение, имели значительно сниженные уровни метилмалоновой кислоты в плазме по сравнению с мышами, которым не проводили введение, через 1, 2 и 12-15 месяцев после лечения (непарный t-критерий; p>0,041). Уровни метилмалоновой кислоты в плазме снижались с течением времени у животных Mut-/-; Mck-Mut, которым проводили введение.
[0033] На фиг. 15A - фиг. 15B представлены вирусные геномы и встраивание трансгенов в гепатоциты после доставки. Фиг. 15A) Количество вирусных геномов (MUT) относительно геномов хозяев (Gapdh), обнаруженное посредством цифровой капельной ПЦР в печение через 1 месяц (n=3); 2 месяца (n=3); и 12-15 месяцев (n=5) после инъекции. После доставки гена новорожденным, описанной ранее, происходит быстрое снижение количества вирусных геномов. (Вирусные геномы через 1 месяц против 2 или 12-15 месяцев; односторонний ANOVA; p>0,001). Фиг. 15B) Процент гепатоцитов с встраиванием трансгена в альбумин. Процент встраивания, определенный посредством кПЦР, значительно возрастал между 1-2 месяцами (n=6) и 12-15 месяцами (n=5) у мышей, которым вводили MMA (непарный t-критерий; p>0,043). Однако через 12-15 месяцев животные дикого типа, которым проводили введение, имеют меньше встраиваний, чем мыши с MMA, которым проводили введение.
[0034] На фиг. 16 представлена экспрессия белка MUT в печени у мышей, которым проводили введение. Общую экспрессию MUT в печени у мышей AAV-Alb-2A-MUT, которым проводили введение, определяли посредством вестерн-блоттинга. Белок MUT у мышей, которым проводили введение, выражен в качестве процента относительно контрольных однопометных животных дикого типа, и его нормализовывали к бета-актину мыши. Количество белка MUT у мышей, которым проводили введение, возрастает с течением времени при сравнении результатов через 1-2 месяца (n=6) и 12-15 месяцев (n=5) после введения (непарный t-критерий; p>0,015).
[0035] На фиг. 17 представлен RNAscope для мышей, которым вводили AAV-Alb-2A-MUT, для детекции клеток, положительных по мРНК MUT. Происходило увеличения количества MUT-положительных клеток у мышей через 12-15 месяцев после введения по сравнению с 2 месяцами после введения. Напротив, мыши дикого типа, которым вводили AAV-Alb-2A-MUT, через 12-15 месяцев после введения (n=5) имеют меньше MUT-положительных клеток, чем их однопометные животные с MMA через 12-15 месяцев после введения (n=5) (p>0,03).
[0035] На фиг. 17 представлен RNAscope для мышей, которым вводили AAV-Alb-2A-MUT, для детекции клеток, положительных по мРНК MUT. Происходило увеличение количества MUT-положительных клеток у мышей через 12-15 месяцев после введения по сравнению с 2 месяцами после введения. Напротив, мыши дикого типа, которым вводили AAV-Alb-2A-MUT, через 12-15 месяцев после введения (n=5) имеют меньше MUT-положительных клеток, чем их однопометные животные с MMA через 12-15 месяцев после введения (n=5) (p>0,03).
[0036] На фиг. 18A - фиг. 18B. представлено процентное встраивание гДНК, определенное посредством анализа LR-qPCR после в/в введения перечисленных доз заместительного LB001 мыши через лицевую вену на 1 сутки после рождения. Образцы печени получали в указанные моменты времени. Фиг. 18A) Представлены данные для мышей Mut-/-; Mck+. Фиг. 18B) Представленные данные для гетерозиготных мышей Mut+/-.
[0037] На фиг. 19 представлена слитая мРНК из первичных гепатоцитов человека. Экзоны 12 и 15 находятся за пределами плеч гомологии. На фиг. представлены SEQ ID NO: 17-19, соответственно, в указанном порядке.
[0038] На фиг. 20 представлена первичная культуральная сэндвич-система гепатоцитов человека.
[0039] На фиг. 21A - фиг. 21B проиллюстрирован анализ встраивания ДНК. Фиг. 21A) В качестве положительного контроля в анализе встраивания ДНК использовали стабильную клеточную линию HepG2-2A-PuroR. Фмг. 21B) кПЦР длинных фрагментов (LR) использовали для определения уровня сайт-специфического встраивания.
[0040] На фиг. 22 представлена относительная экспрессия MUT и ALB в первичных гепатоцитах человека (PHH).
[0041] На фиг. 23A - фиг. 23B представлены три донора первичных гепатоцитов (PHH) с одинаковым гаплотипом 1, которые были выбраны для анализа GENERIDE™ LB-001. Фиг. 23A) Скрининг гаплотипов от 22 доноров PHH. Фиг. 23B) Информация о гаплотипах.
[0042] На фиг. 24 представлена оптимизация условий трансдукции первичных гепатоцитов человека (PHH) с использованием AAV-LK03-LSP-GFP. Эффективность трансдукции представлена в PHH от трех выбранных доноров.
[0043] На фиг. 25 представлен результат вестерн-блоттинга для экспрессии ALB-2a и MUT после введения GENERIDE™ LB001 в первичные гепатоциты человека (PHH).
[0044] На фиг. 26 представлена увеличенная выживаемость в модели на мышах синдрома Криглера-Найяра после введения новорожденным конструкции GENERIDE™, доставляющей UGT1A1 (Porro et al. EMBO Mol Med 2017). Все животные, которым не проводили введение (n=6) погибли в пределах 20 суток после рождения без непрерывной терапии синим светом. Терапию синим светом, лечение, которое способствует выведению и сокращению токсичных уровней билирубина, применяли от рождения до 8 суток. Без непрерывной терапии синим светом животные, которым вводили конструкцию GENERIDE™ (n=5), выживали в течение одного года.
[0045] На фиг. 27 представлены терапевтические и стабильные уровни фактора IX человека с конструкцией GENERIDE™ LB-101 мыши (Barzel et al. Nature 2015). Стабильные и терапевтические уровни продуцирования фактора IX в печени после введения новорожденным сохранялось в течение 20 недель после введения, даже когда PH проводили в возрасте 8 недель (терапевтические уровни фактора IX между 5% и 20% от нормального уровня фактора IX, показанные пунктирными линиями и затененной областью). Планки погрешности указывают на стандартное отклонение.
[0046] На фиг. 28 представлено смягчение геморрагического диатеза у мышей с гемофилией B при использовании вектора GENERIDE™, кодирующего гиперактивный hFIX. Измерение эффективности коагуляции посредством активированного частичного тромбопластинового времени (aPTT) через 2 недели после инъекций в хвостовую вену варианта AAV-DJ-hFIX (V-hFIX) по сравнению с AAV-DJ-WThFIX, носителем и относительно дикого типа (WT), самцам мышей с гемофилией B (FIX-KO) в возрасте 9 недель в указанных дозах. Треугольных обозначает различие между AAV-DJ-V-hFIX и WT-hFIX в одной и той же дозе. Планки погрешности соответствуют стандартному отклонению. * p<0,01, ** p<0,001.
[0047] На фиг. 29 представлено облегчение геморрагического диатеза у новорожденных мышей с гемофилией B с использованием вектора GENERIDE™, кодирующего запатентованный гиперактивный hFIX. Измерение эффективности коагуляции по активированному частичному тромбопластиновому времени (aPTT) через 4 недели (левая панель) и 12 недель (правая панель) после внутрибрюшинных (IP) инъекций AAV-V-hFIX по сравнению с носителем и относительно эталона WT. Для лечения новорожденных мышей с гемофилией B авторы изобретения проводили внутрибрюшинные (в/б) инъекции самцам мышей с нокаутом F9tm1Dws в возрасте 2 суток с 1,5e14, 1,5e13, 1,5e12 и 5e11 векторных геномов (вг) на килограмм (кг) вектора AAV-DJ GENERIDE™, кодирующего вариант hFIX. Авторы изобретения продемонстрировали смягчение заболевание уже в дозах 1,5e12 вг/кг. Функциональная свертываемость, определяемая по активированному частичному тромбопластиновому времени (aPTT) у самцов мышей с KO, которым проводили введение, восстанавливалась до уровней, сходных с уровнями у мышей дикого типа (WT). Планки погрешности соответствуют стандартному отклонению. * p<0,01, ** p<0,001.
[0048] На фиг. 30A - фиг. 30C показано, что GENERIDE™ остается эффективным в случае несоответствующих плеч гомологии. Представлены два основных гаплотипа в локусе альбумина человека. Гаплотипы отличаются 5 SNP в последовательности, соответствующей 5’-плечу гомологии. Фиг. 30A) Сегмент локуса альбумина человека, охватывающий стоп-кодон, представлен в качестве горизонтального тонкого прямоугольника. Короткие продольные линии соответствуют относительному положению нуклеотидных полиморфизмов между двумя наиболее распространенными гаплотипами в человеческой популяции, гаплотип 1 и гаплотип 2. 95% аллелей альбумина в человеческой популяции равномерно распределены, в соответствующем сегменте, между этими двумя гаплотипами, отличающимися только 6 нуклеотидами. Конкретные нуклеотиды в полиморфных положениях в гаплотипах 1 и 2 представлены выше и ниже линии, соответственно. Фиг. 30B) Представлены два вектора на основе AAV GENERIDE™, нацеливающих запатентованный вариант FIX человека (V-hFIX) в локус альбумина человека. Плечи гомологии в верхнем векторе "плечи дикого типа (WTA)" идентичны геномным последовательностям, охватывающим стоп-кодон альбумина, у мышей B6. Плечи гомологии в нижнем векторе "несоответствующие плечи (MA)" отличаются от плеч WT так, чтобы имитировать различие между гаплотипами человека: гаплотипом 1 и гаплотипом 2. Короткие продольные линии соответствуют положению нуклеотидных полиморфизмов между двумя векторами. Конкретные нуклеотиды в полиморфных положениях в двух векторах представлены выше каждой линии. Фиг. 30C) Уровень hFIX в плазме, измеренный посредством ELISA после инъекций в хвостовую вену мышей B6 в возрасте 9 недель 5e13 вг/кг либо экспериментальной конструкции AAV V-hFIX-WTA (n=5), либо не совпадающего по гаплотипу AAV V-hFIX-MA из трех независимых партий (n=5/группа). Планки погрешности соответствуют стандартному отклонению.
[0049] На фиг. 31A - фиг. 31B представлены модели MMA на мышах. Фиг. 31A) модель на мышах Mut-/- с нокаутом экзона 3 Mut. Эти мыши погибают новорожденными. Ранее описана в Chandler et al. BMC Med Genet. 2007. Фиг. 31B) Модель на мышах Mut-/-Mck+. Эта модель на мышах имеет специфическую для мышц экспрессию Mut и мыши являются жизнеспособными.
[0050] На фиг. 32 представлена схема эксперимента для анализа моделей MMA на мышах после введения конструкций GENERIDE™.
ПОДРОБНОЕ ОПИСАНИЕ
Генная терапия
[0051] Генная терапия изменяет профиль экспрессии генов в клетках пациента посредством генного переноса, способа доставки терапевтического гена, называемого трансгеном. Разработчики лекарственных средств используют модифицированные вирусы в качестве векторов для транспортировки трансгенов в ядро клетки для изменения или усиления способностей клеток. Разработчики достигли больших успехов в отношении введения в клетки тканей, таких как печень, сетчатка глаза и кроветворные клетки костного мозга, с использованием различных векторов. Эти подходы в некоторых случали привели к одобренным способам терапии и, в других случаях, показали в значительной степени перспективные результаты в клинических испытаниях.
[0052] Существует множество подходов генной терапии. В традиционной генной терапии на основе AAV трансген вводят в ядро клетки-хозяина, но не предполагается его встраивание в хромосомную ДНК. Трансген экспрессируется с не встроенного генетического элемента, называемого эписомой, который находится в ядре. Во втором типе генной терапии используется вирус другого типа, такой как лентивирус, который встраивается вместе с трансгеном в хромосомную ДНК, но в произвольные участки.
[0053] Эписомальная экспрессия гена должна запускаться экзогенным промотором, вызывая продуцирование белка, который корректирует или смягчает болезненное состояние.
Ограничения генной терапии
[0054] Эффекты разведения по мере деления клеток и роста тканей. В случае генной терапии на основе эписомальной экспрессии, когда клетки делятся в процессе роста или регенерации тканей, польза терапии, как правило, снижается, поскольку трансгены не предназначены для встраивания в хромосому хозяина, и, таким образом, не реплицируются в ходе деления клеток. Таким образом, в каждом новом поколении клеток далее снижается доля клеток, экспрессирующих трансген в ткани-мишени, вызывая снижение или устранение терапевтической пользы с течением времени.
[0055] Неспособность контролировать участок встраивания. В то время как использование некоторых способов генной терапии с помощью опосредуемого вирусом встраивания имеет потенциал к обеспечению долговременной пользы, поскольку ген встраивается в хромосому хозяина, невозможно контролировать, когда ген встраивается, что несет в себе риск нарушения важного гена или встраивания или встраивания в область, в которой могут возникнуть нежелательные эффекты, такие как образование опухоли. По этой причине эти подходы генной терапии с встраиванием в основном ограничены подходами ex vivo, где клетки обрабатывают вне организма, а затем вводят обратно.
[0056] Использование экзогенных промоторов повышает риск образования опухоли. Общим признаком обоих подходов генной терапии является то, что трансген вводят в клетки вместе с экзогенным промотором. Промоторы необходимы для инициации транскрипции и амплификации ДНК в матричную РНК, или мРНК, которая в конечном итоге транслируется в белок. Экспрессия высоких уровней терапевтических белков с трансгена, используемого в генной терапии, требует сильных сконструированных промоторов. В то время как эти промоторы необходимы для экспрессии белка, предшествующие исследования, проведенные другими исследователями в моделях на животных, показали, что неспецифическое встраивание векторов для генной терапии может приводить к значительному усилению развития опухолей. Сила промоторов играет ключевую роль в повышении развития этих опухолей. Таким образом, попытки запустить высокие уровни экспрессии с сильных промоторов могут иметь долговременные неблагоприятные последствия.
Редактирование генов
[0057] Редактирование генов представляет собой делецию, изменение или усиление аберрантных генов путем внесения разрывов в ДНК клеток с использованием экзогенно доставляемых механизмов редактирования генов. Большинство современных подходов к редактированию генов ограничены в отношении их эффективности вследствие высокой частоты нежелательных модификаций в мишени и вне мишени и низкой эффективности коррекции генов, что отчасти является результатом попытки клетки быстро репарировать внесенный разрыв ДНК. Современное редактирование генов сфокусировано на выключении гена с нарушением функции или коррекции или пропускании индивидуальной вредоносной мутации в гене. Вследствие количества возможных мутаций, ни один из этих подходов не может быть направлен на всю совокупность мутаций при конкретном генетическом заболевании, на которую направлено встраивание полного корректирующего гена.
[0058] В отличие от подхода генной терапии, редактирование генов позволяет репарированной генетической области переходить в новые поколения клеток посредством нормального деления клеток. Более того, желаемый белок может экспрессироваться с использованием собственного регуляторого аппарата клеток. Традиционный подход редактирования генов основан на нуклеазах, и в нем используются нуклеазы, происходящие из бактерий, для разрезания ДНК в конкретном участке для обеспечения делеции, внесения изменения и вставки корректирующей последовательности ДНК организма.
[0059] После разрезания нуклеазами ДНК традиционные способы редактирования генов модифицируют ДНК с использованием двух путей: направляемая гомологией репарация, или HDR, и негомологичное соединение концов, или NHEJ. HDR вовлекает высоко точное включение правильных последовательностей ДНК, комплементарных участку повреждения ДНК. HDR имеет ключевые преимущества, состоящие в том, что она может репарировать ДНК с высокой точностью и препятствует внесению нежелательных мутаций в участок коррекции. NHEJ является менее селективным, более склонным к ошибкам процессом, который быстро соединяет концы разорванной ДНК, что приводит к высокой частоте инсерций или делеций в участке разрыва.
Редактирование генов на основе нуклеаз
[0060] В редактировании генов на основе нуклеаз используются нуклеазы - ферменты, расщепляющие ДНК, которые сконструированы или изначально идентифицированы в бактериях. Редактирование генов на основе нуклеаз представляет собой двухстадийный процесс. Сначала экзогенная нуклеаза, которая способна разрезать одну или обе цепи в двухцепочечной ДНК, направляется в желаемый участок посредством синтетической гидовой РНК и вносит специфический разрез. После внесения нуклеазой желаемого разреза или разрезов активируется аппарат репарации ДНК и завершает процесс редактирования либо через NHEJ, либо, менее часто, через HDR.
[0061] NHEJ может происходить в отсутствии ДНК-матрицы для копирования клеткой в процессе репарации разрыва ДНК. Это является основным каскадом или каскадом по умолчанию, который клетка использует для репарации двухцепочечных разрывов. Механизм NHEJ можно использовать для внесения небольших инсерций или делеций, известных как инсерции-делеции, вызывающих нокаут функции гена. NHEJ вносит инсерции и делеции в ДНК вследствие его способа репарации, а также может приводить к внесению нежелательных мутаций вне мишени, включая хромосомные аберрации.
[0062] Опосредуемая нуклеазой HDR происходит с совместной доставкой нуклеазы, гидовой РНК и ДНК-матрицы, сходной с разрезаемой ДНК. Следовательно, клетка может использовать эту матрицу для конструирования репарирующей ДНК, что приводит к замене дефектных генетических последовательностей правильными. Авторы изобретения полагают, что механизм HDR является предпочтительным путем репарации при использовании подхода на основе нуклеаз для вставки корректирующей последовательности вследствие ее высокой точности. Однако в основном репарация генома после разрезания нуклеазой продолжается с использованием механизма NHEJ. Более частый каскад репарации NHEJ обладает потенциалом к возникновению нежелательных мутаций в участке разрезания, таким образом, ограничивая диапазон заболеваний, на который в настоящее время могут быть нацелены любые подходы к редактированию генов на основе нуклеазы.
[0063] Пути направляемой гомологией репарации ДНК и негомологичного соединения концов, используемые для редактирования генома, проиллюстрированы на фиг. 1.
[0064] В традиционном редактировании генов используется один из трех подходов на основе нуклеаз: подобные активатору транскрипции эффекторные нуклеазы, или TALEN; ассоциированный с короткими палиндромными повторами, регулярно расположенные кластерами, белок 9, или CRISPR/Cas9; и нуклеазы с цинковыми пальцами, или ZFN. В то время как эти подходы уже обеспечили значительные достижения в исследованиях и разработке продуктов, авторы полагают, что они имеют присущие им ограничения.
Ограничения редактирования генов на основе нуклеаз
[0065] Подходы к редактированию генов на основе нуклеаз ограничиваются использованием бактериальных нуклеазных ферментов для расщепления ДНК и их зависимости от экзогенных промоторов для экспрессии трансгена. Эти ограничения включают следующие:
[0066] Нуклеазы вызывают мутации в мишени и вне мишени. Общепринятые технологии редактирования генов могут приводить к генной токсичности, включая хромосомные изменения, на основе процесса склонной к ошибкам NHEJ и потенциальной активности нуклеазы вне мишени.
[0067] Доставка редактирующих гены компонентов в клетки является сложной. Редактирование генов требует доставки множества компонентов в одну и ту же клетку за один раз. Это технически трудно и в настоящее время требует использования множества векторов.
[0068] Бактериально доставляемые нуклеазы являются иммуногенными. Поскольку нуклеазы, используемые в общепринятых подходах к редактированию генов по большей части имеют бактериальное происхождение, они обладают более высоким потенциалом к иммуногенности, который в свою очередь ограничивает их применимость.
[0069] Вследствие этих ограничений редактирование генов ограничивается в основном применениями ex vivo в клетках, таких как кроветворные клетки.
Технологическая платформа GENERIDE™
[0070] GENERIDE™ представляет собой технологию редактирования генома, в которой используется гомологичная рекомбинация, или HR, - встречающийся в природе процесс репарации ДНК, который сохраняет точность генома. С использованием HR, GENERIDE™ позволяет встраивание терапевтических генов, известных как трансгены, в конкретные заданные геномные положения без использования экзогенных нуклеаз, которые представляют собой ферменты, сконструированные для разрезания ДНК. Направляемое GENERIDE™ встраивание трансгена предполагает использование эндогенных промоторов в этих заданных положениях для обеспечения высоких уровней тканеспецифической экспрессии генов без проблем, ассоциированных с использованием экзогенных промоторов.
[0071] Технология GENERIDE™ предназначена для точного встраивания корректирующих генов в геном пациента для обеспечения стабильного терапевтического эффекта. Поскольку технология GENERIDE™ предполагает наличие этого длительного терапевтического эффекта, ее можно использовать для нацеливания на редкие нарушения печени у пациентов-детей, где важно обеспечить лечение рано в жизни пациента до возникновения необратимой патологии. Иллюстративный продукт, являющийся кандидатом, LB-001, описан в настоящем описании для лечения метилмалоновой ацидемии, или MMA, угрожающего жизни заболевания, которое проявляется при рождении.
[0072] Платформенная технология GENERIDE™ имеет потенциал к преодолению некоторых из ключевых ограничений как традиционных подходов к генной терапии, так и общепринятых подходов к редактированию генов, способом, который имеет хорошие возможности в отношении лечения генетических заболеваний, в частности, у пациентов-детей. В GENERIDE™ используется вектор на основе AAV для доставки гена в ядро клетки. Затем в нем используется HR для стабильного встраивания корректирующего гена в геном реципиента в области, где он регулируется эндогенным промотором, обеспечивая потенциал к длительному продуцированию белка, даже по мере роста и изменения организма с течением времени, что не является осуществимым в случае общепринятой генной терапии на основе AAV.
[0073] GENERIDE™ обеспечивает несколько ключевых преимуществ над технологиями генной терапии и редактирования генов, которые основаны на экзогенных промоторах и нуклеазах. Посредством использования встречающегося в природе процесса HR, GENERIDE™ не сталкивается с теми же проблемами, которая ассоциированы с подходами редактирования генов на основе модифицированных бактериальных нуклеазных ферментов. Использование этих ферментов ассоциировано со значительно увеличенным риском нежелательных и потенциально опасных модификаций в ДНК клетки-хозяина, которые могут приводить к увеличенному риску образования опухоли. Более того, в противоположность общепринятой генной терапии, GENERIDE™ предназначен для обеспечения точного, сайт-специфического и длительного встраивания корректирующего гена в хромосому клетки-хозяина. В доклинических исследованиях на животных с конструкциями GENERIDE™ наблюдается встраивание корректирующего гена в конкретное положение в геноме. Это дает возможность обеспечения более долговременного подхода, чем технологии генной терапии без встраивания в геном и с утратой их эффекта по мере деления клеток. Эта польза обеспечивает GENERIDE™ хорошие возможности для лечения генетических заболеваний, в частности, у педиатрических пациентов.
[0074] Модульный подход, описанный в настоящем описании, можно использовать, чтобы позволить GENERIDE™ обеспечивать надежную тканеспецифическую экспрессию генов, которая будет воспроизводимой для различных терапевтических средств, доставляемых в одну и ту же ткань. Путем подстановки другого трансгена в конструкцию GENERIDE™, этот трансген можно доставлять для нового терапевтического показания, одновременно по существу сохраняя все другие компоненты конструкции. Этот подход позволит задействовать общие способы производства и аналитику для различных продуктов-кандидатов GENERIDE™ и может укоротить процесс разработки других программ лечения.
[0075] Предшествующая работа по недеструктивному нацеливанию на гены описана в WO 2013/158309, включенной в настоящее описание в качестве ссылки. Предшествующая работа по редактированию генома без нуклеаз описана в WO 2015/143177, включенной в настоящее описание в качестве ссылки.
Редактирование генома с использованием GENERIDE™: механизм и характерные особенности
[0076] Редактирование генома посредством платформы GENERIDE™ отличается от редактирования генов, поскольку в нем используется HR для доставки корректирующего гена в одну конкретную область в геноме. GENERIDE™ встраивает корректирующий ген точным образом, что ведет к сайт-специфическому встраиванию в геном. Подход редактирования генома GENERIDE™ не требует использования экзогенных нуклеаз или промоторов; вместо этого, в нем используется существующий аппарат для встраивания и инициации транскрипции терапевтических трансгенов.
[0077] На фиг. 2 показано, как конструкция GENERIDE™ встраивает трансген в конкретной точке рядом с геном альбумина с использованием HR.
[0078] Технология GENERIDE™ состоит из трех фундаментальных компонентов, каждый из которых обеспечивает потенциальную пользу подхода GENERIDE™:
[0079] Плечи гомологии, состоящие из сотен нуклеотидов. Фланкирующие последовательности, известные как плечи гомологии, обеспечивают сайт-специфическое встраивание конструкции и ограничивают ее встраивание вне мишени. Каждое плечо имеет длину сотни нуклеотидов в противоположность гидовым последовательностям, используемым в CRISPR/Cas9, которые имеют только несколько десятков пар оснований в длину, и эта увеличенная длина может обеспечить увеличенную точность и сайт-специфическое встраивание. Плечи гомологии GENERIDE™ направляют встраивание трансгена непосредственно за геном с высокой экспрессией, что, как было показано в моделях на животных, приводит к высоким уровням экспрессии без необходимости во внесении экзогенного промотора.
[0080] Трансген. Корректирующие гены, известные как трансгены, выбирают для встраивания в геном клетки-хозяина. Эти трансгены являются функциональными версиями ассоциированных с заболеванием генов, встречающихся в клетках пациентов. Совокупный размер трансгенов и плеч гомологии можно оптимизировать для повышения вероятности того, что эти трансгены имеют подходящую длину последовательности для эффективного упаковывания в капсид, что может повышать вероятность того, что трансгены в конечном итоге будут доставлены пациенту надлежащим образом.
[0081] Пептид 2A для полицистронной экспрессии. Короткая последовательность, кодирующая пептид 2A, играет ряд важных ролей. Во-первых, пептид 2A способствует полицистронной экспрессии, которая представляет собой продуцирование двух различных белков с одной и той же мРНК. Это, в свою очередь, позволяет встраивание трансгена недеструктивным образом путем сопряжения транскрипции трансгена с геном-мишенью с высокой экспрессией в представляющей интерес ткани, контролируемым сильным эндогенным промотором. Для направленных на печень терапевтических программ, включающих LB-001, локус альбумина может функционировать как участок встраивания. Посредством процесса, известного как рибосомальное пропускание, пептид 2A способствует продуцированию терапевтического белка на том же уровне, что и альбумина, в каждой модифицированной клетке. Во-вторых, альбумин у пациента продуцируется нормально, за исключением добавления C-концевой метки, которая служит в качестве циркулирующего биомаркера, указывающего на успешное встраивание и экспрессию трансгена. Эта модификация альбумина будет иметь минимальный эффект на его функцию, исходя из результатов клинических испытаний других слитых конструкций белка альбумина. Пептид 2A был включен в другие потенциальные терапевтические средства, такие как химерные рецепторы антигена T-клеток, или CAR-T (Qasim et al. Sci Transl Med 2017).
[0082] Ключевой стадией применения платформы GENERIDE™ является идентификация генетического локуса, являющего мишенью, для встраивания. Это является важным, поскольку положение определяет регуляцию экспрессии трансгена, в частности, уровней и тканей, где продуцируется белок. Для направленных на печень терапевтических программ, включающих LB-001, в качестве участка встраивания можно использовать локус альбумина (см. фиг. 3 и фиг. 4).
[0083] Нацеливание на локус альбумина позволяет задействовать сильный эндогенный промотор, который обеспечивает продуцирование альбумина на высоком уровне для максимизации экспрессии трансгена. Связывание экспрессии трансгена с альбумином может позволить экспрессию трансгена на терапевтических уровнях без необходимости в добавлении экзогенных промоторов или встраивании трансгена в большинство клеток-мишеней.
[0084] Это подтверждается моделями на животных для MMA, гемофилии B и синдрома Криглера-Найяра. В этих моделях встраивание трансгена приблизительно в 1% клеток приводило к терапевтической пользе. Сила промотора альбумина перевешивает умеренные уровни встраивания, обеспечивая потенциально терапевтические уровни экспрессии трансгена.
[0085] На фиг. 5 показаны относительные уровни экспрессии альбумина по сравнению с определенными связанными с заболеванием генами в печени, включая метилмалонил-CoA мутазу, или MUT, дефицитный ген у пациентов с MMA.
[0086] GENERIDE™ приводит к встраиванию корректирующего гена в локус альбумина в доклинических моделях заболевания на мышах, у не являющихся человеком приматов и в клетках человека (in vitro). Кроме того, эффективность HR, которая требуется для экспрессии трансгена с GENERIDE™, повышается в областях активной транскрипции и, вероятно, будет низкой в тканях, где альбумин не экспрессируется активно. Этот признак должен сделать встраивание как в мишени, так и вне мишени, более предсказуемым процессом среди программ, в которых используется локус альбумина для встраивания. Кроме того, поскольку в платформе GENERIDE™ используется HR, продукты-кандидаты GENERIDE™ не содержат никаких бактериальных нуклеаз, уменьшая риск встраивания в мишени в других участках или вне мишени, который ассоциирован с бактериальными нуклеазами. Терапевтический подход GENERIDE™ можно применять для других тканей и заданных положений в геноме. В исследованиях реализуемости in vitro, GENERIDE™ был подвержен встраиванию в другие геномные локусы, включая рДНК, LAMA3 и COL7A1.
[0087] Потенциальные преимущества подхода GENERIDE™ включают следующие:
[0088] Направленное встраивание трансгена в геном. Общепринятые подходы к генной терапии доставляют терапевтические трансгены в клетки-мишени. Основным недостатком большинства из этих подходов является то, что после попадания генов внутрь клетки они не встраиваются в хромосомы клеток-хозяев и не используют природные процессы, которые приводят к репликации и сегрегации ДНК в ходе деления клеток. Это является особенно проблематичным, когда общепринятые средства генной терапии вводят на раннем этапе жизни пациента, поскольку быстрый рост тканей в ходе нормального развития ребенка приведет к снижению и конечной утрате терапевтической пользы, ассоциированной с трансгеном. Не встроенные гены, экспрессируемые вне генома на отдельной цепи ДНК, называют эписомами. Эта эписомальная экспрессия может быть эффективной в первоначальных клетках, которые трансдуцируют, и в некоторых случаях она может длиться в течение длительного периода времени или на протяжении всей жизни пациента. Однако эписомальная экспрессия, как правило, является временной в тканях-мишенях, таких как печень, в которой происходит высокое обновление клеток и которая имеет тенденцию к значительному увеличению в размере в ходе жизни педиатрического пациента. С использованием технологии GENERIDE™ трансген встраивается в геном, что потенциально может обеспечить стабильную и длительную экспрессию трансгена по мере деления клеток и роста тканей пациента, и может приводить к длительной терапевтической пользе.
[0089] Экспрессия трансгена без экзогенных промоторов. С использованием технологии GENERIDE™ трансген экспрессируется в области, где он регулируется мощным эндогенным промотором. В частности, длинные плечи гомологии можно использовать для вставки трансгена в конкретный участок в геноме, который экспрессируется под контролем мощного эндогенного промотора, такого как промотор альбумина. Вследствие не использования экзогенных промоторов для запуска экспрессии трансгена, эта технология лишена потенциального встраивания промоторов вне мишени, которое ассоциировано с увеличенным риском злокачественной опухоли. Выбор мощных эндогенных промоторов может позволить достижение терапевтических уровней экспрессии белка с трансгена с умеренными частотами встраивания, типичными для в высокой степени точного и надежного процесса HR. При использовании технологии GENERIDE™ наблюдалось точное встраивание трансгена и конечная экспрессия клетками в моделях на животных in vivo и в клетках человека in vitro.
[0090] Свободное от нуклеаз редактирование генома. Посредством использования встречающегося в природе процесса HR, GENERIDE™ предназначен для избегания нежелательных побочных эффектов, ассоциированных с экзогенными нуклеазами, используемыми в общепринятых технологиях редактирования генов. Использование этих модифицированных способами инженерии ферментов ассоциировано с генотоксичностью, включая хромосомные изменения, в результате склонной к ошибкам репарации двухцепочечных разрывов ДНК. Избегание применения нуклеаз также уменьшает количество экзогенных компонентов, которые необходимо доставлять в клетку.
[0091] Модульность. Модульный подход позволит GENERIDE™ обеспечивать надежную тканеспецифическую экспрессию генов, которая будет воспроизводимой среди различных терапевтических средств, нацеленных на одну и ту же ткань. Капсид AAV служит в качестве носителя, который позволяет доставку остальных компонентов в клетки организма. Векторы можно конструировать так, чтобы они в высокой степени эффективно доставляли их компоненты в конкретные ткани-мишени, такие как печень. Плечи гомологии, которые не зависят от трансгена, представляют собой сегменты ДНК, каждый из которых имеет длину сотни оснований и направляют встраивание гена-мишени в конкретное положение в геноме. Это положение является ключевым, поскольку оно определяет, какой эндогенный промотор будет экспрессировать трансген. Например, в новом способе терапии на основе экспрессии трансгена в печени может использоваться тот же капсид и плечи гомологии, что и у LB-001, где трансген для новой терапии заменяет ген MUT из LB-001. Путем подстановки другого трансгена в конструкцию GENERIDE™, этот трансген можно доставлять для нового терапевтического показания, одновременно по существу сохраняя все другие компоненты конструкции. Этот подход позволит задействовать общие способы производства и аналитику для различных продуктов-кандидатов GENERIDE™ и может укоротить процесс разработки других программ лечения.
MMA
[0092] MMA может вызываться мутациями в нескольких генах, которые кодируют ферменты, ответственные за нормальный метаболизм определенных аминокислот. Наиболее часто встречающиеся мутации находятся в гене MUT, которые вызывают полный или частичный дефицит его активности. В результате, может накапливаться вещество, называемое метилмалоновой кислотой, и другие потенциально токсичные соединения, вызывая признаки и симптомы MMA. На фиг. 6 проиллюстрирован эффект дефицита MUT в клетках печени.
[0093] Пациенты с MMA страдают от частых потенциально летальных эпизодов метаболической нестабильности, которые отвечают за наблюдаемое тяжелое течение заболевания и раннюю смертность. Эффекты MMA обычно проявляются в раннем младенческом возрасте с симптомами, включающим заторможенность, рвоту, дегидратацию и снижение прибавки в весе. Пациенты с MMA имеют долговременные осложнения, включая отсутствие аппетита, умственную отсталость, заболевание почек и панкреатит. Без лечения MMA приводит к коме и смерти. В настоящее время нет одобренных способов терапии MMA и перспективы для пациентов с MMA остаются плохими. Контроль заболевания ограничивается диетой с низким количеством белка, высоким количеством калорий, лишенной аминокислот, обычно процессируемых посредством каскада MUT. Несмотря на диетотерапию и тщательный уход, пациенты с MMA, особенно пациенты с наиболее тяжелым дефицитом MUT, часто страдают от неврологического повреждения и повреждения почек, обостряющихся в периоды катаболического стресса, когда повреждение, инфекция или заболевание запускает разрушение белка в организме. Ожидаемый срок жизни пациентов с MMA возрос за последние несколько десятилетий, однако все еще оценивается как ограничивающиеся возрастом приблизительно 20-30 лет. Качество жизни как пациентов, так и их семей и лиц, осуществляющих уход, значительно ухудшается из-за заболевания вследствие ограничений, которые оно налагает на школьную жизнь и социальное функционирование. Раннее вмешательство в этой уязвимой группе населения является необходимым для борьбы с проявлением необратимой клинической патологии заболевания.
[0094] Сообщается, что встречаемость MMA в США составляет 1 на 50000 рождений с распространенностью на настоящий момент приблизительно от 1600 до 2400 пациентов в США. Оценивается, что доля пациентов с MMA с мутацией Mut составляет приблизительно 63% от всей популяции с MMA. Согласно оценке, количество пациентов с MMA с генетическим дефицитом, на который нацелен LB-001, составляет от 3400 до 5100 пациентов в основных странах мира, среди которых от 1000 до 1500 пациентов находятся в США.
[0095] С течением времени у пациентов с MMA, как правило, развивается терминальное заболевание почек, требующее трансплантации почек в подростковом возрасте. Комбинированная трансплантация печени-почки, или ранняя трансплантация печени, стали вмешательством, целью которого является улучшение метаболического контроля. Однако ограниченное количество доноров печени, значительные риски, ассоциированные с хирургической операцией, высокая стоимость процедур (в США приблизительно $740000 в среднем за трансплантацию печени и $1,2 миллиона в среднем за комбинированную трансплантацию печени и почки (Milliman Research Report, 2014 U.S. organ and tissue transplant cost estimates)) и пожизненная зависимость от иммуносупрессивных лекарственных средств ограничивает широкое распространение трансплантации печени у пациентов с MMA.
[0096] Поскольку MUT представляет собой митохондриальный фермент, дефицит MUT может быть трудно или невозможно скорректировать посредством фермент-заместительной терапии, в которой проводят инфузию функционального фермента в кровоток. Наиболее эффективным способом получения фермента MUT внутри клетки является его синтез в ней. Для этого было исследовано несколько различных подходов в моделях на животных, включая введение мРНК для кодирования MUT непосредственно в клетки или введение гена MUT в клетки с использованием вирусного вектора. Хотя оба этих подхода помогают подтвердить, что введение функционального гена MUT может облегчать симптомы, они также имеют ключевое ограничение, состоящее в том, что терапевтическая польза является временной. В случае терапии посредством мРНК, еженедельное внутривенное введение мРНК MUT требовалось для поддержания терапевтических уровней MUT, однако непонятно, как часто эту терапию необходимо проводить у пациентов. В случае терапии геном MUT уровни MUT снижались стечением времени. Без лечения, которое является долговременным, потребуется множество доз. Однако развитие у пациента нейтрализующих антител к вирусному вектору, используемому для доставки генной терапии MUT, ограничивает возможность вводить последующие дозы. Кроме того, введение вектора на основе AAV, имеющего сильный экзогенный промотор, коррелирует с печеночно-клеточной карциномой после доставки новорожденным.
[0097] Введение функциональной копии гена MUT в геном пациентов с MMA может обеспечить значительно лучший подход, потенциально обеспечивая пожизненную пользу после однократного введения.
[0098] MMA представляет собой органическую ацидемию с высокой неудовлетворенной потребностью в лечении и отсутствием терапевтических способов лечения. Поскольку GENERIDE™ предназначен для обеспечения длительности терапии, он может обеспечить пожизненную пользу для пациентов с MMA путем вмешательства на ранних этапах их жизни посредством лечения, которое восстанавливает функцию аберрантных генов до того, как может произойти необратимое ухудшение функций. В некоторых вариантах осуществления терапевтические трансгены доставляют с использованием конструкции GENERIDE™, предназначенной для встраивания непосредственно за геном, кодирующим альбумин, имеющий наиболее высокую экспрессию ген в печени. Экспрессия трансгенов "добавляется" к экспрессии альбумина, что может обеспечить достаточные терапевтические уровни желаемых белков, учитывая высокий уровень экспрессии альбумина в печени.
Модели MMA на мышах
[0099] Модели MMA на мышах можно использовать для анализа лечения посредством GENERIDE™. Иллюстративные модели MMA на мышах представлены на фиг. 31A и фиг. 31B. Иллюстративные экспериментальные способы анализа моделей MMA на мышах после введения конструкций GENERIDE™ проиллюстрированы на фиг. 32.
[0100] В одном примере модели MMA на мышах ген Mut делают полностью нефункциональным. Этот нефункциональный аллель Mut обозначают как Mut-/-. Полагают, что мыши, имеющие этот нефункциональный аллель, имеют более тяжелый дефицит, чем дефицит, наблюдаемый в большинстве тяжелых случаев у пациентов с MMA. Без лечения эти мыши умирают в течение первых нескольких дней жизни.
[0101] Модификация мыши Mut-/- является другой моделью на мышах MMA, называемой Mut-/-; TgINS-MCK-Mut. Как используют в рамках изобретения, Mut-/-; TgINS-MCK-Mut может обозначаться как MCK-Mut, или Mut-/-; Mck-Mut, или Mut-/-MCK+. В этой модели на мышах существует функциональная копия гена Mut мыши, помещенного под контроль промотора креатинкиназы. Это позволяет экспрессию Mut в мышечных клетках, что в свою очередь позволяет мышам выживать дольше, все еще демонстрируя многие из фенотипических изменений, наблюдаемых у пациентов с MMA.
ПРИМЕРЫ
Пример 1: Альбумин в качестве геномного локуса для встраивания трансгена посредством GENERIDE™
[0102] В настоящем примере иллюстрируется, что локус альбумина может быть участком встраивания для экспрессии трансгена в печени.
[0103] Локус альбумина имеет несколько привлекательных признаков в качестве локуса для экспрессии трансгена. Сильный эндогенный промотор запускает высокие уровни продуцирования альбумина, и этот сильный промотор может быть использован для максимизации экспрессии трансгена для достижения терапевтических уровней без добавления экзогенных промоторов. Как проиллюстрировано на фиг. 4, альбумин на высоком уровне экспрессируется в печени по сравнению с другими тканями. Этот ассоциированный с печенью паттерн экспрессии можно использовать для локализации экспрессии конструкций GENERIDE™ преимущественно в печени. Кроме того, как показано на фиг. 3, альбумин является геном с наиболее высокой экспрессией в печени и, соответственно, более высокая экспрессия альбумина относительно экспрессии связанных с заболеванием генов в печени может приводить к достижению терапевтических уровней экспрессии трансгена. Например, на фиг. 5 проиллюстрировано, что уровни экспрессии альбумина в 100X превышают экспрессию других определенных генов печени, ассоциированных с моногенными заболеваниями, включая MMA.
Пример 2: LB-001 для лечения метилмалоновой ацидемии (MMA)
[0104] В настоящем примере описан LB-001, продукт-кандидат для лечения MMA. LB-001 содержит трансген, кодирующий фермент MUT, дефицит которого наиболее распространен у пациентов с MMA (фиг. 6). LB-001 сконструирован для нацеливания на клетки печени и встраивания трансгена MUT в локус альбумина.
[0105] LB-001 состоит из конструкции ДНК, включающей ген, кодирующий фермент MUT человека, инкапсулированной в капсид AAV (фиг. 7A). Последовательность, кодирующая фермент MUT, связана с последовательностью пептида 2A и окружена плечами гомологии, которые направляют встраивание последовательности гена MUT и пептида 2A в хромосомный локус гена альбумина. Конструкция встраивается в локус альбумина так, что ген MUT экспрессируется, что приводит к синтезу фермента MUT в качестве отдельного от альбумина белка. в LB-001 используется LK03, капсид AAV, оптимизированный для нацеливания на клетки печени человека.
[0106] Иллюстративная нуклеиновая кислота, которую можно использовать с капсидом AAV-LK03 для экспрессии последовательности Mut человека, представлена на фиг. 7B. Нуклеиновая кислота содержит ITR из AAV2, 5’- и 3’-плечи гомологии длиной 1000 оснований, соответствующие последовательности альбумина, и синтетическую последовательность Mut человека, которой предшествует пептид 2A, для способствования рибосомальному пропусканию. Клиническое показание для этой конструкции включает лечение тяжелой метилмалоновой ацидемии (MMA) в комбинации с диетотерапией. Доставка функционирующей копии гена метилмалонил-CoA мутазы (Mut) в гепатоциты пациентов с MMA с использованием технологии GENERIDE™ предназначена для выведения и блокирования накопления токсичных метаболитов. LB-001 для научных целей был получен посредством тройной трансфекции клеток HEK. Производство клинического материала может проводиться способами, известными в данной области, в том числе с использованием платформы на основе бакуловирусных экспрессирующих векторных систем (BEVS).
Пример 3: Анализ для определения дозы у мышей
[0107] В настоящем примере продемонстрирована иллюстративная схема исследования для поиска дозы суррогатного LB-001 в модели на мышах Mut-MCK. Результаты такого анализа можно использовать для определения эффективной дозы суррогатного LB-001 на мышах с нокаутом MUT при в/в введении. Кроме того, результаты этого анализа могут обеспечить токсикологическую оценку не GLP и повлиять на более крупные исследования на животных и клинические испытания. Для этого примера оцениваемое показание представляет собой метилмалоновую ацидемию (MMA). Могут быть включены другие схемы исследований для других показаний.
[0108] В этом исследовании суррогатный LB-001 содержит 1000 п.н. 5’- и 3’-плечи гомологии. Вектор (Vt-20, партия 4 (CMRI)) вводят в следующих трех дозах: 6e12 (низкая), 6e13 (средняя), 6e14 (высокая) вг/кг. Линия мышей представляет собой Mut-MCK. Ожидаемый размер помета животных составляет 6-8 детенышей. Согласно оценке, для каждой группы введения понадобится 5-6 однопометных животных. В таблице 1 обобщенно представлены группы лечения в исследовании.
Таблица 1. Обобщение групп лечения для анализа с целью поиска дозы
[0109] Сбор образцов для исследования включает следующие: (1) сыворотка; (2) плазма (пробирки с EDTA); (3) печень (свежезамороженная (сухой лед), хранившаяся при -80°C)); и печень, почка, сердце, легкое, головной мозг и скелетная мышца (фиксированные в течение ночи в 10% формалине и хранившиеся при комнатной температуре в 70% этаноле). В таблице 2 обобщенно представлено взятие образцов для исследования.
Таблица 2. Обобщение взятия образцов для анализа с целью поиска дозы
1, 2
(5 посмертных,
5 прижизненных)
1, 2
(5 посмертных,
5 прижизненных)
[0110] Данные для исследования включают следующие: (1) выживаемость; (2) масса тела, измеряемая один раз в неделю; (3) уровень MMA в плазме, начиная на D30, D60 и D90; и (4) интеграция в ткань печени в конце исследования (D90).
Пример 4: Эффективность доставки трансгена MUT в моделях на мышах
[0111] В данном примере представлены доклинические данные для LB-001, которые были получены для двух моделей MMA на мышах. В первой модели ген Mut делали полностью нефункциональным. Эта нефункциональная форма Mut обозначается как Mut-/-. Полагают, что мыши, имеющие этот нефункциональный ген, имеют более тяжелый дефицит, чем наблюдают в большинстве тяжелых случаев MMA у пациентов. Без лечения эти мыши умирают в течение первых нескольких дней жизни. Однократная внутрибрюшинная инъекция конструкции GENERIDE™ LB-001 мыши четырем новорожденным мышам приводила к увеличенной выживаемости для трех из четырех мышей, причем две мыши жили более одного года, как показано на верхней панели фиг. 8. Кроме того, у этих мышей происходило увеличение массы тела при свободном кормлении, как показано на нижней панели фиг. 8.
[0112] Вторая модель MMA на мышах, называемая MCK-Mut, представляет собой модификацию мыши Mut-/-, у которой функциональная копия гена Mut мыши помещена под контроль промотора креатинкиназы. Это позволяет экспрессию Mut в мышечных клетках, что в свою очередь позволяет мышам жить дольше, все еще демонстрируя многие из фенотипических изменений, наблюдаемых у пациентов с MMA. Пяти новорожденным мышам MCK-Mut проводили однократные инъекции конструкции GENERIDE™ LB-001 мыши. У этих мышей наблюдали экспрессию Mut. В возрасте одного месяца эти мыши имели значительное улучшение прибавки в весе по сравнению с мышами MCK-Mut без введения, как показано на фиг. 9. Эти результаты были статистически значимыми. Значение P является стандартной мерой статистической значимости, причем значения p менее 0,05, соответствующие вероятности менее чем один к двадцати того, что результаты получены случайно, обычно считаются статистически значимыми.
[0113] Мыши MCK-Mut, которым вводили GENERIDE™, также имели значимое снижение плазменных уровней метилцитрата и метилмалоновой кислоты, связанных с заболеванием токсических метаболитов и диагностических биомаркеров, которые накапливаются у пациентов с MMA, как показано на фиг. 10.
[0114] Неожиданно, несмотря на относительно низкие уровни хромосомного встраивания, достигнутые путем AAV-направляемого редактирования генов посредством HR, такие способы приводят к терапевтическим уровням экспрессии функционального фермента Mut. Без связи с какой-либо теорией полагают, что этот успех является следствием определенных признаков конструкции LB-001.
[0115] Во-первых, используемый капсид AAV, LK03, был оптимизирован для нацеливания на клетки печени человека. Во-вторых, геномное встраивание нацелено на локус гена альбумина. Альбумин является белком с наиболее высокой экспрессией в печени, и нормальная экспрессия большинства других белков является лишь долей экспрессии альбумина. Таким образом, даже при умеренной частоте встраивания могут экспрессироваться терапевтические уровни белка. Транскрипционно активные гены, одним из которых является альбумин, более подвержены встраиванию трансгена с использованием HR.
[0116] В третьих, наблюдалось, что присутствие самого по себе функционального Mut обеспечивает селективное преимущество гепатоцитам относительно гепатоцитов, лишенных Mut. С течением времени это селективное преимущество приводит к увеличенной доле клеток печени, которые содержат функциональную копию Mut. Это можно наблюдать у мышей, которым введена конструкция GENERIDE™ мыши с и без функционирующей копии Mut в печени. Первоначальные частоты встраивания GENERIDE™ в обеих группах мышей составляли менее 4%. С течением времени количество модифицированных клеток оставалось таким же у мышей, которые естественным образом экспрессируют Mut в печени (Mut+/- в печени). Однако после более чем одного года у мышей с генетическим дефицитом Mut в печени (Mut-/- в печени), процент клеток, экспрессирующих Mut, возрастал до 24%, как показано на фиг. 11. Без связи с какой-либо теорией, это селективное преимущество может быть отнесено к улучшениям митохондриальной функции в результате экспрессии Mut и восстановления дефицитного каскада метаболизма аминокислот.
[0117] Дополнительные доказательства, подтверждающие селективное преимущество у этих мышей, включают (i) количественное определение клеток с геном Mut, встроенным в локус альбумина, посредством ортогональной количественной полимеразной цепной реакции длинных фрагментов, или LR-qPCR, как показано на фиг. 12 и (ii) детекцию увеличенной частоты встраивания в локус альбумина посредством LR-qPCR через один год после введения дозы по сравнению с одним месяцем после введения дозы, как показано на фиг. 13.
[0118] В противоположность общепринятым подходам к генной терапии на основе AAV, в которых процент клеток, входящих в терапию, снижается с течением времени по мере репликации клеток и утрачивания ими кодируемого вирусом трансгена, в исследовании MMA на мышах процент клеток, содержавших конструкцию Mut GENERIDE™, возрастал с течением времени. Этот результат подтверждает возможность того, что однократное введение может обеспечить пожизненную пользу.
Пример 5: Эффективность доставки трансгена MUT в моделях на мышах
[0119] В данном примере подтверждаются данные, представленные в примере 4. Как и в примере 4, в данном примере используется вектор на основе AAV без промотора, в котором используется гомологичная рекомбинация для достижения сайт-специфической вставки гена MUT человека в локус альбумина мыши (Alb). Этот вектор (AAV-Alb-2A-MUT) содержит плечи гомологии, фланкирующие последовательность, кодирующую пептид 2A, проксимально относительно гена MUT, и обеспечивает экспрессию MUT с эндогенного промотора Alb после встраивания. Предшествующие данные показали, что AAV-Alb-2A-MUT, доставляемый в дозе 8,6E11-2,5E12 вг/детеныш при рождении, снижал уровень связанных с заболеванием метаболитов и увеличивал рост и выживаемость в моделях MMA на мышах (Chandler, R.J. et al., Rescue of Mice with Methylmalonic Acidemia from Immediate Neonatal Lethality Using an Albumin Targeted, Promoterless Adeno-Associated Viral Integrating Vector, Molecular Therapy, Abstract 26, 25(5S1): page 13 (May 2017)). В настоящем примере, подобно примеру 4, описаны данные о том, что доставка трансгена MUT с использованием конструкций и способов, описанных в настоящем описании, обеспечивает долговременную эффективность в моделях MMA на мышах.
[0120] Как представлено в примере 4, настоящий пример подтверждает, что лечение гипоморфной MMA в модели на мышах с использованием GENERIDE™ приводит к снижению уровней в плазме метилмалоновой кислоты (фиг. 14). Также, как показано в примере 4, в настоящем примере подтверждается, что встраивание трансгена MUT обеспечивает преимущество в отношении роста клеток печени у мышей с MMA. Например, наблюдалось, что экспрессия белка MUT в печени, процент клеток с мРНК MUT, и количество встраиваний в Alb возрастают с течением времени у мышей, которым вводили MMA (фиг. 15-17). Низкие уровни встраиваний трансгенов и низкие количества положительных по мРНК MUT клеток, наблюдаемые у мышей дикого типа через 13-15 месяцев после введения и у мышей с MMA через 2 месяца после введения (фиг. 15 и 17), являются характерными для коррекции посредством гомологичной рекомбинации in vivo.
[0121] Кроме того, как и в примере 4, в настоящем примере показано, что RNAscope для мышей с MMA, которым вводили AAV-Alb-2A-MUT, продемонстрировал устойчивую экспрессию MUT, и положительные по MUT гепатоциты выглядели как отчетливые и широко рассеянные кластеры, что согласуется с паттерном клональной экспансии. Исследования RNAscope также показывают, что экспрессия MUT присутствовала приблизительно в 5-40% гепатоцитов у мышей с MMA, которым проводили введение, против 1% у контролей дикого типа (фиг. 17). Данные примера 4 и настоящего примера указывают на то, что селективное преимущество скорректированных гепатоцитов может быть достигнуто в моделях MMA на мышах после лечения с использованием MUT GENERIDE™. Это наблюдение имеет клиническое значение для лечения пациентов с MMA.
Пример 6: Эффективность доставки трансгена MUT в моделях на мышах
[0122] В настоящем примере подтверждены данные, представленные в примере 4 для лечения MMA в моделях на мышах с использованием LB001 мыши.
[0123] Как и в примере 4, в настоящем примере описано повышение встраивания ДНК с течением времени для моделей MMA на мышах с дефицитом MUT в печени (фиг. 18). Это повышение наблюдали для различных доз трансгенной конструкции. Без связи с какой-либо теорией, такое повышение встраивания трансгена с использованием конструкций и способов, описанных в настоящем описании, такое наблюдаемое селективное преимущество могут использоваться для целей достижения терапевтических уровней экспрессии трансгена при введении безопасной дозы конструкции пациентам. Например, начиная с относительно низкой дозы конструкции, пациент, страдающий от MMA, может в конечном итоге достигнуть достаточных уровней трансгена MUT для снижения тяжести или лечения заболевания. Наблюдение увеличенного встраивания трансгена с течением времени у пациентов может использоваться для мониторинга лечения.
Пример 7: Исследование активности hLB001 in vivo в модели на гуманизированных мышах
[0124] В этом примере представлен иллюстративный анализ для оценки эффективности сайт-специфического встраивания трансгена MUT в локус ALB человека с использованием рекомбинантного AAV (hLB001) (LK-03-GENERIDE™ MUT) и гуманизированной модели на мышах FRG KO/NOD.
[0125] Вектор для этого анализа представляет собой hLB001, вводимый мышам FRG с гуманизированной печенью на 2 уровнях дозирования (1e13 и 1e14 вг/кг). Конечные результаты для этого анализа включают следующие: (1) Процент геномного встраивания и (2) экспрессия слитой мРНК ALB-2A-MUT. Анализируемый момент времени включает 21 сутки после инфицирования.
Материалы, способы и взятие образцов
[0126] Материалы
a. 3 самки гуманизированных мышей Fah-/-/Rag2-/-/Il2rg-/- NOD (Hu-FRGN) с ≥ 80% заменой гепатоцитов человека на донорские HHM19027/YTW.
b. 12 самок гуманизированных мышей Fah-/-/Rag2-/-/Il2rg-/- NOD (Hu-FRGN) с заменой ≥ 80% гепатоцитов человека на донорские HHF13022/RMG
c. ELISA альбумина человека Yecuris
d. Стерильный шприц 3/10 см3 с иглой 29g
e. Стерильный шприц 1 см3 с иглой 29g
f. Покрытые цитратом натрия пробирки, 0,8 мл
g. PBS, носитель
h. Предварительная фаза: rAAV, титр: 6,43e13 вг/мл
i. Фаза 1: титр rAAV: 9,29e13 вг/мл
j. 1,5-мл пробирки, стерильные
k. Коктейль анестетиков для мыши (7,5 мг/мл кетамина, 1,5 мг/мл ксилазина и 0,25 мг/мл ацепромазина)
l. Кассеты TissueTek
m. 10% нормальный забуференный формалин, свежеприготовленный
n. Этанол, 70%
o. 5-мл полипропиленовая пробирка с навинчивающейся крышкой
p. Жидкий азот
[0127] Способы
Подготовка мышей перед дозированием
[0128] Всех мышей для использования в испытании получают из NTBC ≥ 25 суток и SMX/™P ≥ 3 суток перед началом исследования. Гуманизацию оценивают за ≤ 7 суток до начала исследования.
Подготовка вируса для дозирования:
[0129] Вирус следует разморозить и держать на льду в ходе и после получения. PBS можно размораживать при 37°C или комнатной температуре. Предлагается размораживать PBS ≥ 30 минут и вирус ≥ 5 минут перед подготовкой.
[0130] Предварительное исследование - пилотное:
a. Составление соединения:
i. Для доставки 1e14 вг/кг необходимо 2e13 вг/мл исходного вируса
ii. Внутри бокса биологической безопасности, уровень II, разбавить 6,43e13 вг/мл до исходной культуры 2e13 вг/мл. Принять среднюю массу тела за 25 г.
b. Четырех (4) HuFRGN, которым трансплантирован HHM19027/YTW, разделяют на две группы, и им проводят дозирование указанных соединений в указанной дозе, указанной на схеме ниже
c. На 1 сутки в каждой группе вводят указанную дозу каждого соединения посредством внутривенной доставки через вену ретроорбитального синуса с использованием стерильного шприца 3/10 см3 с иглой 29g:
iii. Каждую мышь взвешивают и регистрируют массу тела (BW).
iv. BW (г) каждой мыши умножают на концентрацию исходного раствора в вг/г для определения общего количества вг соединения, требуемого для достижения желаемой дозы.
v. Общее количество вг делят на концентрацию исходного раствора в вг/мкл для определения объема исходного раствора для применения для дозирования.
vi. Мышей подвергают анестезии с использованием испаряющегося изофлурана перед дозированием.
vii. Вычисленную дозу вируса для каждой мыши отбирают через стерильную иглу 29G в шприц 3/10 см3 и доставляют через вену ретроорбитального синуса
d. Мониторинг всех животных проводят сразу после дозирования, чтобы убедиться в восстановлении после анестезии и отсутствии ненамеренного вреда, причиненного в ходе дозирования животному.
e. Всех мышей подвергают мониторингу каждые сутки в отношении общего состояния здоровья. Если мышь находят умирающей или умершей, мышь подвергают анестезии и проводят взятие образцов, как описано ниже в разделе "Терминальное взятие образцов".
[0131] Терминальное взятие образцов
a. На 22 сутки (через три недели после дозирования) всех мышей взвешивают и подвергают анестезии с использованием коктейля для мышей в соответствии с массой тела.
b. Проводят взятие столько цельной крови, сколько это возможно, посредством пункции сердца с использованием шприца 1 см3 с иглой 27g. Цельную кровь переносят в покрытую цитратом натрия пробирку, плазму выделяют центрифугированием при 1500×g в течение 15 минут при 4°C. Плазму распределяют на аликвоты объемом 100 мкл и хранят при -80°C.
c. Брюшину и грудную полость открывают, обнажая печень, печень извлекают и массу печени регистрируют. Печень разрезают на отдельные доли, каждую долю далее разрезают на две равные части.
d. Для исследования гистологии один фрагмент каждой доли помещают в кассету TissueTek и фиксируют в свежеприготовленном 10% нормальном забуференном формалине в течение 16-32 ч при комнатной температуре, а затем переносят в 70% этанол и хранят при комнатной температуре.
Примечание: не фиксировать при 4°C. Не фиксировать в течение < 16 ч или >32 ч. Замедленная фиксация может вызвать деградацию РНК и генерировать низкий сигнал или не генерировать сигнал. Более короткое время или более низкая температура приведут к недостаточной фиксации.
e. Для биоанализа второй фрагмент каждой доли переносят в 5-мл полипропиленовую пробирку и быстро замораживают в жидком азоте и хранят при -80°C.
[0132] Испытание - фаза 1
a. Состав соединения:
i. Для доставки 1e14 вг/кг необходимо 2e13 вг/мл исходного вируса. Для доставки 1e13 вг/кг необходимо 2e12 вг/мл.
ii. Внутри бокса биологической безопасности, уровень II, разбавить 9,29E+13 вг/мл до исходной культуры 2e13 вг/мл и 2e12 вг/мл. Принять среднюю массу тела за 25 г.
b. Двенадцать (12) HuFRGN, которым трансплантирован HHF13022/RMG, подразделяют на три группы и проводят им дозирование указанных соединений в указанной дозе, показанных в таблице ниже.
c. На 1 сутки в каждой группе вводят указанную дозу каждого соединения посредством внутривенной доставки через вену ретроорбитального синуса с использованием стерильного шприца 3/10 см3 с иглой 29g:
iii. Каждую мышь взвешивают и регистрируют массу тела (BW).
iv. BW (г) каждой мыши умножают на концентрацию исходного раствора в вг/г для определения общего количество вг соединения, требуемого для достижения желаемой дозы.
v. Общее количество вг делят на концентрацию исходного раствора в вг/мкл для определения объема исходного раствора для применения для дозирования.
vi. Мышей подвергают анестезии с использованием испаряющегося изофлурана перед дозированием.
vii. Вычисленную дозу вируса для каждой мыши отбирают через стерильную иглу 29G в шприц 3/10 см3 и доставляют через вену ретроорбитального синуса
d. Мониторинг всех животных проводят сразу после дозирования, чтобы убедиться в восстановлении после анестезии и отсутствии ненамеренного вреда, причиненного в ходе дозирования животному.
e. Всех мышей подвергают мониторингу каждые сутки в отношении общего состояния здоровья. Если мышь находят умирающей или умершей, мышь подвергают анестезии и проводят взятие образцов, как описано ниже в разделе "Терминальное взятие образцов".
[0133] Терминальное взятие образцов
a. На 22 сутки (через три недели после дозирования) подвергают анестезии с использованием коктейля для мышей.
b. Проводят взятие столько цельной крови, сколько это возможно, посредством пункции сердца с использованием шприца 1 см3 с иглой 27g. Цельную кровь переносят в покрытую цитратом натрия пробирку, плазму выделяют центрифугированием при 1500×g в течение 15 минут при 4°C. Плазму распределяют на аликвоты объемом 100 мкл и хранят при -80°C.
c. Брюшину и грудную полость открывают, обнажая печень, печень извлекают и массу печени регистрируют. Печень разрезают на отдельные доли, каждую долю далее разрезают на две равные части.
d. Для исследования гистологии один фрагмент каждой доли помещают в кассету TissueTek и фиксируют в свежеприготовленном 10% нормальном забуференном формалине в течение 16-32 ч при комнатной температуре, а затем переносят в 70% этанол и хранят при комнатной температуре.
Примечание: не фиксировать при 4°C. Не фиксировать в течение < 16 ч или >32 ч. Замедленная фиксация может вызывать деградацию РНК и генерировать низкий сигнал или не генерировать сигнал. Более короткое время или более низкая температура приведут к недостаточной фиксации.
e. Для биоанализа второй фрагмент каждой доли переносят в 5-мл полипропиленовую пробирку и быстро замораживают в жидком азоте и хранят при -80°C.
Пример 8: GENERIDE™ на первичных гепатоцитах человека
[0134] Первичные гепатоциты человека культивировали с использованием культуральной сэндвич-системы. Клетки инфицировали GENERIDE™ hLB001, а затем через 48 часов проводили замену среды. Через 7 суток после инфицирования клетки собирали и экстрагировали РНК с использованием набора Qiagen Allprep kit (каталожный номер №/ID: 80204).
[0135] После экстракции РНК 1 мкг РНК использовали для обратной транскрипции с использованием набора High-Capacity cDNA Reverse Transcription Kit (Thermofisher 4368814). кДНК использовали в качестве матрицы для последующей амплификации посредством ПЦР с использованием праймеров 235/267 (фиг. 19). Продукт ПЦР секвенировали с использованием праймера 235.
[0136] Результат секвенирования показывают, что слитая мРНК экзона 12, экзона 13, экзона 14 ALB перед стоп-кодоном и последовательность 2a, которая указывает на правильную экспрессию слитой мРНК в результате точного встраивания, опосредуемого GENERIDE™, в первичных гепатоцитах человека.
Пример 9: GENERIDE™ в первичных гепатоцитах человека
[0137] Настоящий пример подтверждает результаты, наблюдаемые в примере 8, в том, что вектор GENERIDE™ LB001 может опосредовать эффективное редактирование генома посредством встраивания MUT в локус ALB в первичных гепатоцитах человека.
Способы
[0138] Для анализа инфекционности, встраивания ДНК и уровней белка использовали первичную культуральную сэндвич-систему гепатоцитов человека (фиг. 20). Частоту сайт-специфического встраивания анализировали с использованием кПЦР длинных фрагментов (LR) (фиг. 21). В качестве положительной контрольной ДНК использовали стабильную клеточную линию HepG2-2A-PuroR.
Результаты
[0139] Оценивали относительную экспрессию MUT и ALB (фиг. 22). Для дополнительных испытаний для тестирования GENERIDE™ LB-001 было выбрано три донора первичных гепатоцитов человека с одним и тем же гаплотипом 1 (фиг. 23-25). Эти результаты подтверждают, что GENERIDE™ LB-001 может встраиваться и экспрессировать трансген MUT в первичных гепатоцитах человека.
Пример 10: Трансгены MUT для применения технологии GENERIDE™ для лечения MMA
[0140] В настоящем примере показано, что различные трансгены MUT можно использовать для применений в технологии GENERIDE™. Например, синтетические полинуклеотиды, кодирующие метилмалонил-CoA мутазу человека (synMUT), можно использовать в применениях GENERIDE™. Примеры конструкций synMUT описаны в WO/2014/143884 и в патенте США № 9944918, оба из которых включены в настоящее описание в качестве ссылок. Иллюстративные оптимизированные нуклеотидные последовательности, кодирующие метилмалонил-CoA мутазу человека (synMUT1-4), приведены в качестве SEQ ID NO: 9, 12, 13 и 14, соответственно.
Пример 11: Врожденные ошибки метаболизма
[0141] Печень является ключевым органом, ответственным за многие процессы метаболизма и детоксикации. Десятки моногенных заболеваний, включая MMA, являются результатом дефицита ферментов печени, вовлеченных в метаболические пути. Были получены дополнительные подтверждающие концепцию данные в моделях на животных, направленные на другую редкую врожденную ошибку метаболизма, синдром Криглера-Найяра. Пациенты с синдромом Криглера-Найяра неспособны метаболизировать и устранять билирубин из кровотока, что приводит к пожизненному риску неврологического повреждения и смерти. Сходную конструкцию GENERIDE™, но с геном билирубинуридиндифосфатглюкуронозилтрансферазы, или UGT1A1, в качестве трансгена использовали для коррекции генного дефицита в модели на животных синдрома Криглера-Найяра. Введение UGT1A1 в локус альбумина в клетках печени мыши приводило к нормализации уровней билирубина и долговременной выживаемости мышей с дефицитом UGT1A1 от менее чем двадцать суток до по меньшей мере одного года, как показано на фиг. 26. Дополнительные показания, на которые может быть осуществлено нацеливание в этой категории, включают фенилкетонурию, дефицит орнитинтранскарбамилазы и болезнь запасания гликогена типа 1A.
Пример 12: Другие способы направленной на печень терапии
[0142] Специфичность терапевтических продуктов, являющихся кандидатами, в отношении печени определяется как используемым капсидом AAV, так и областью встраивания в ДНК клетки-хозяина. В LB-001 используется капсид AAV, LK03, который сконструирован так, чтобы быть высокоэффективным для трансдукции печени человека. Трансгены для направленных на печень терапевтических продуктов, являющихся кандидатами, встраивали в локус гена альбумина, который на значительном уровне продуцируется только в печени, где он является наиболее высоко экспрессируемым геном. Считается, что выбор альбумина приведет к повышению специфичности к печени, поскольку активная транскрипция повышает скорость гомологичной рекомбинации, и тканеспецифическая экспрессия гена альбумина запустит продуцирование трансгена в печени.
Пример 13: Использование печени в качестве фабрики белков in vivo
[0143] В этом примере проиллюстрировано, что модулирующую конструкцию GENERIDE™ можно применять для продуцирования белков, которые функционируют вне печени.
[0144] Печень является основным секреторным органом, который продуцирует многие белки, присутствующие в кровотоке. Этот признак может позволить гепатоцитам доставлять ключевые терапевтические белки пациентам с генетическими дефицитами. Например, это было продемонстрировано в модели гемофилии B на животных с использованием конструкции GENERIDE™ LB-101 мыши, кодирующей фактор свертывания IX человека, для коррекции дефицита свертывания. В этой модели экспрессия фактора свертывания IX человека и свертываемость крови восстанавливались до нормальных уровней после однократного введения новорожденным и взрослым больным мышам.
[0145] Кроме того, стабильные и терапевтические уровни фактора IX человека сохранялись в течение 20 недель у новорожденных мышей дикого типа после введения конструкции GENERIDE™ LB-101 мыши, даже после частичной гепатэктомии, или PH, как показано на фиг. 27. PH представляет собой методику, при которой две трети печени удаляют для запуска регенеративного роста органа. При использовании традиционной генной терапии на основе AAV экспрессия трансгена после PH значительно снижалась.
Пример 14: Полиорганные заболевания
[0146] Некоторые генетические мутации приводят как к дефициту белка, так и к сверхэкспрессии вредоносных белков, которые обуславливают патогенез. Одним таким заболеванием является A1ATD. При A1ATD пациенты имеют дефицит циркулирующей A1AT, и у них может развиваться тяжелое повреждение печени, которое может потребовать трансплантации печени. Это является результатом того, что AATD представляет собой доминантно-негативное заболевание, при котором дефектная копия гена ассоциирована с симптомами даже в присутствии нормальной копии. AATD является другим генетическим заболеванием, которое было скорректировано в модели на мышах с использованием конструкции GENERIDE™ LB-201 мыши. Конструкция GENERIDE™, использованная в этой модели на мышах, включала нормальную копию гена, а также микроРНК, сконструированную для снижения экспрессии вредоносного гена. Экспрессия трансгена и подавление мутантного гена наблюдались у этих мышей в течение по меньшей мере восьми месяцев.
Пример 15: Анализ ответа на дозу у мышей с гемофилией B
[0147] В настоящем примере продемонстрирована эффективность способов GENERIDE™ в отношении встраивания фактора IX в различных дозах у мышей.
[0148] Серотип DJ AAV использовали для обеспечения экспрессии FIX-TripleL после встраивания с сильного специфического для печени промотора Alb мыши. Без связи с какой-либо теорией, предполагается, что: промотор Alb должен обеспечить высокие уровни продуцирования фактора свертывания, даже если происходит встраивание только в небольшую часть гепатоцитов; и что высокая активность транскрипции в локусе Alb должна делать его более подверженным встраиванию трансгена посредством гомологичной рекомбинации.
[0149] Подход нацеливания на гены in vivo на основе технологии GENERIDE™ применяли для специфического встраивания версии терапевтической кДНК без промотора в локус альбумина без использования нуклеаз в моделях на мышах с дефицитом FIX. Использовали вариант FIX человека, FIX-TripleL (FIX-V86A/E277A/R338L). Доставка генов аденоассоциированного вируса (AAV) у мышей с гемофилией B показала, что FIX-TripleL имел в 15-раз более высокую специфическую активность свертывания, чем FIX-WT, и эта активность была значительно лучшей, чем у FIX-Triple (в 10 раз) или FIX-R338L (в 6 раз). При более низкой дозе вируса FIX-TripleL повышал активность FIX от субтерапевтических до терапевтических уровней. В физиологических условиях не наблюдали признаков неблагоприятных тромботических событий у мышей C57B 1/6, которых длительно лечили AAV-FIX (Kao et al. Thrombosis and Haemostasis 2013).
Материалы и способы:
[0150] Обобщение схемы эксперимента представлено в таблице 3.
Таблица 3. Обобщение схемы эксперимента
2. Уровни hFIX в плазме
3. Время свертывания
2. ELISA
3. aPTT
2. Раз в месяц
3. 4 неделипосле инъекции
[0151] Содержание животных: Животных содержали и осуществляли уход за ними в соответствии с руководством по уходу за животными как National Institute of Health (NIH), так и Association for Assessment and Accreditation of Laboratory Animal Care (AAALAC). Методики эксперимента были изучены и одобрены Israel Board for Animal Experiments. Мышей содержали в условиях с контролируемой температурой с циклом свет-темнота 12/12 ч со стандартным рационом и водой без ограничений.
[0152] Конструирование плазмиды: геномный сегмент Alb мыши (90474003-90476720 в NCBI эталонной последовательности: NC_000071.6) амплифицировали способом ПЦР и встраивали между ITR AAV2 в участки рестрикции BSRGI и SPEI в модифицированном остове pTRUF. Геномный сегмент охватывает область на 1,3 т.п.н. выше и на 1,4 т.п.н. ниже стоп-кодона Alb. Затем авторы изобретения встраивали в участок рестрикции BPU10I оптимизированную кодирующую P2A последовательность, которой предшествовала кодирующая линкер последовательность (глицин-серин-глицин) и за которой следовал участок рестрикции NHEI. Наконец, авторы изобретения встроили кодон-оптимизированную кДНК (Vector NTI) hFIX-TripleL в участок NHEI с получением LB-Pm-0005 (pAAV-288), который служил для конструирования вектора DJ. Конечные продуцирующие rAAV плазмиды получали с использованием набора EndoFree Plasmid Megaprep Kit (Qiagen).
[0153] Продуцирование AAV: Вектор AAV-FIX-TripleL (LB-Vt-0001), партия № 170824 (общее количество 1.13E13 вг) получали способом очистки с CsCl.
[0154] Инъекции мышам и взятие крови: Мышей с нокаутом F9tm1Dws приобретали от Jackson Laboratory, чтобы они были парами для скрещивания, чтобы получить потомство для инъекций новорожденным. Самцам с нокаутом F9tm1Dws в возрасте двух дней внутрибрюшинно инъецировали 3e11, 3e10, 3e9 и 1e9 геномов вектора AAV-hFIX-TripleL на мышь и взятие крови начинали в возрасте 4 недели путем ретроорбитального взятия крови для ELISA и анализа активированного частичного тромбопластинового времени (с использованием IDEXX Coag Dx Analyzer). Всех мышей умерщвляли через 12 недель и печень извлекали для анализа ДНК/белка.
[0155] Определение FIX в плазме: ELISA для FIX проводили со следующими антителами; первичное IgG-антитело мыши против FIX человека в разведении 1:500 (Sigma F2645), и поликлональное вторичное IgG-антитело козы против FIX человека, конъюгированное с пероксидазой, в разведении 1:4200 (Enzyme Research GAFIX-APHRP).
[0156] Оценка нацеливания на локус Alb посредством анализа с использованием LR-qPCR: Амплификацию геномного Alb с встраиванием, но не нежелательную амплификацию вектора, проводили с использованием праймера, гибридизующегося за пределами плеча гомологии, и праймера для встроенной ДНК, ампликон LR-PCR служил в качестве матрицы для количественных анализов кПЦР TaqMan. В конечном итоге авторы вычисляли уровни встраивания посредством стандартной кривой эталонных встроенных образцов.
Результаты:
[0157] Для лечения новорожденных мышей с гемофилией B проводили внутрибрюшинные (в/б) инъекции мышам с нокаутом F9tm1Dws в возрасте 2 суток с использованием 3e11, 3e10, 3e9 и 1e9 векторных геномов (вг) на мышь (1,5e14, 1,5e13, 1,5e12 и 5e11 на кг) вектора AAV-DJ GENERIDE™, кодирующего гиперактивный вариант FIX человека; FIX-TripleL. Облегчение заболевания было продемонстрировано уже в дозах 1,5E12 вг/кг. Время свертывания через 4 недели после инъекции измеряли посредством анализа активированного частичного тромбопластинового времени (aPTT). Функциональное свертывание, определенное посредством активированного частичного тромбопластинового времени (aPTT) у мышей KO, которым проводили введение, восстанавливалось до уровней, сходных с уровнями у мышей дикого типа (WT) (фиг. 28-29). Эти результаты демонстрируют высокие терапевтические уровни экспрессии hFIX-TripleL в результате встраивания внутри мишени.
Обсуждение:
[0158] Было обнаружено, что 1,5E12 вг/кг hFIX-TripleL облегчают геморрагический диатез у новорожденных мышей с гемофилией B через 4 недель, и их состояние остается стабильным в течение 12 недель. Это демонстрирует терапевтический эффект нацеливания на гены in vivo без нуклеаз и без содержащегося в векторе промотора. Благоприятный профиль безопасности описанной стратегии нацеливания без промотора и нуклеаз для rAAV делает его основным кандидатом для клинической оценки в контексте гемофилии и других генетических дефицитов. В более общем смысле, эту стратегию можно применять всегда, когда терапевтический эффект обеспечивается секретируемым белком или когда нацеливание обеспечивает селективное преимущество.
Пример 16: Несоответствие гаплотипов в плечах гомологии
[0159] В настоящем примере продемонстрирована эффективность GENERIDE™ с несоответствиями в плечах гомологии и воспроизводимость с использованием различных партий векторов.
[0160] Как обсуждалось выше, в GENERIDE™ кодирующая последовательность терапевтического гена без промотора нацеливается посредством безошибочной гомологичной рекомбинации (HR) в локус альбумина. Экспрессия терапевтического гена связана с устойчивой экспрессией альбумина в печени через пептид 2A. В соответствующем локусе альбумина человека существует 2 основных гаплотипа, охватывающих 95% популяции. Гаплотипы различаются 5 SNP в последовательности, соответствующей 5’-плечу гомологии (фиг. 30A - фиг. 30C).
[0161] Серотип DJ AAV использовали для обеспечения экспрессии FIX-TripleL после встраивания с сильного специфического для печени промотора Alb мыши. Технологию GENERIDE™ использовали для специфического встраивания версии терапевтической кДНК без промотора в локус альбумина без использования нуклеаз у мышей C57bl/6 дикого типа. Использовали вариант FIX дикого типа человека, FIX-TripleL (FIX-V86A/E277A/R338L) и несоответствующий по гаплотипу hFIX-TripleL с 6 SNP в плечах гомологии. Гаплотипы различаются 5 SNP в последовательности, соответствующей 5’-плечу гомологии, и одним SNP в последовательности, соответствующей 3’-плечу гомологии.
Материалы и способы:
[0162] Обобщение схемы эксперимента приведено в таблице 4.
Таблица 4. Обобщение схемы эксперимента
Частота интеграции
[0163] Содержание животных: Животных содержали и осуществляли уход за ними в соответствии с руководством по уходу за животными как National Institute of Health (NIH), так и Association for Assessment and Accreditation of Laboratory Animal Care (AAALAC). Методики эксперимента были изучены и одобрены Israel Board for Animal Experiments. Мышей содержали в условиях с контролируемой температурой с циклом свет-темнота 12/12 ч со стандартным рационом и водой без ограничений.
[0164] Конструирование плазмиды: геномный сегмент Alb мыши (90474003-90476720 в NCBI эталонной последовательности: NC_000071.6) амплифицировали способом ПЦР и встраивали между ITR AAV2 в участки рестрикции BSRGI и SPEI в модифицированном остове pTRUF. Геномный сегмент охватывает область на 1,3 т.п.н. выше и на 1,4 т.п.н. ниже стоп-кодона Alb. Затем авторы изобретения встраивали в участок рестрикции BPU10I оптимизированную кодирующую P2A последовательность, который предшествовала кодирующая линкер последовательность (глицин-серин-глицин) и за которой следовал участок рестрикции NHEI. Наконец, авторы изобретения встроили кодон-оптимизированную кДНК (Vector NTI) hFIX-TripleL в участок NHEI с получением LB-Pm-0005 (pAAV-288), который служил для конструирования вектора DJ. Конечные продуцирующие rAAV плазмиды получали с использованием набора EndoFree Plasmid Megaprep Kit (Qiagen).
[0165] Продуцирование AAV: Вектор AAV-FIX-TripleL (LB-Vt-0001), партия № 171102 служил в качестве положительного контроля и три других партии вектора с несоответствием оснований № 171102, 171116, 171130 получали с использованием способа очистки с CsCl.
[0166] Инъекции мышам и взятие крови: Самкам мышей C57bl/6 в возрасте девяти недель инъецировали внутрибрюшинно 1e12 векторных геномов AAV-hFIX-TripleL без несоответствия на мышь, и взятие крови проводили через две, четыре, семь и десять недель после инъекции путем ретроорбитального взятия крови для измерения уровня белков посредством ELISA. Всех мышей умерщвляли через 10 недель и печень извлекали для анализа частоты встраивания ДНК.
[0167] Определение FIX в плазме: ELISA для FIX проводили со следующими антителами; первичное IgG-антитело мыши против FIX человека в разведении 1:500 (Sigma F2645), и поликлональное вторичное IgG-антитело козы против FIX человека, конъюгированное с пероксидазой, в разведении 1:4200 (Enzyme Research GAFIX-APHRP).
[0168] Оценка нацеливания на локус Alb посредством анализа с использованием LR-qPCR: Амплификацию геномного Alb с встраиванием, но не нежелательную амплификацию вектора, проводили с использованием праймера, гибридизующегося за пределами плеча гомологии, и праймера для встроенной ДНК, ампликон LR-PCR служил в качестве матрицы для количественных анализов кПЦР TaqMan. В конечном итоге авторы вычисляли уровни встраивания посредством стандартной кривой эталонных встроенных образцов.
Результаты:
[0169] Для лечения взрослых мышей C57bl/6 проводили внутривенные (в/в) инъекции мышам C57bl/6 в возрасте 9 недель 1e12 векторных геномов (вг) на мышь (5e13 на кг) вектора AAV-DJ GENERIDE™, кодирующего гиперактивный вариант FIX человека; FIX-TripleL без несоответствий. Векторы с синтетическими гаплотипами мыши, имеющие аналогичные мутации, конструировали, и было обнаружено, что GENERIDE™ по большей части не изменяется в результате этого несоответствия гаплотипов. Это наблюдение служит в поддержку возможности использовать одну векторную конструкцию для различных популяций пациентов. Высокое соответствие было обнаружено между различными векторами, продуцируемыми независимо и по отдельности. Наблюдалось стабильное присутствие белка hFIX в плазме в течение 10 недель.
Обсуждение:
[0170] Предшествующие результаты продемонстрировали облегчение геморрагического диатеза у мышей с гемофилией B после однократной инъекции либо взрослым, либо новорожденным мышам 1,5e12 вг/кг вектора GENERIDE™, кодирующего вариант hFIX-TripleL. В этом исследовании было показано, что эффективность GENERIDE™ не снижалась в результате несоответствий между плечами гомологии на векторе и локусом-мишенью, когда несоответствие имитирует распространенные гаплотипы у человека. Эта работа также продемонстрировала устойчивую способность к эффективному и стабильному продуцированию вектора. Благоприятный профиль эффективности безопасности описанной стратегии нацеливания без промотора и нуклеаз для rAAV делает GENERIDE™ основным кандидатом для клинической оценки в контексте гемофилии и других генетических дефицитов. Этот терапевтический эффект может быть достигнут посредством одной векторной конструкции, которая может быть пригодной для всей популяции.
Пример 17: Капсиды для применения в технологии GENERIDE™
[0171] В настоящем примере описаны иллюстративные капсиды, которые можно использовать в применениях технологии GENERIDE™. Иллюстративные капсиды, которые можно использовать для экспрессии трансгена с использованием GENERIDE™, включают AAV8, AAV-DJ, LK03 и NP59.
[0172] SEQ ID NO: 1 представляет собой аминокислотную последовательность белка капсида AAV-DJ. SEQ ID NO: 2 представляет собой нуклеотидную последовательность, кодирующую белок капсида AAV-DJ. Дополнительная информация, касающаяся AAV-DJ, может быть найдена в WO/2007/120542, включенной в настоящее описание в качестве ссылки.
[0172] SEQ ID NO: 1 представляет собой аминокислотную последовательность белка капсида AAV-DJ. SEQ ID NO: 2 представляет собой нуклеотидную последовательность, кодирующую белок капсида AAV-DJ. Дополнительная информация, касающаяся AAV-DJ, может быть найдена в WO/2007/120542, включенной в настоящее описание в качестве ссылки.
[0174] SEQ ID NO: 7 представляет собой нуклеотидную последовательность, кодирующую капсидный белок AAV-NP59. SEQ ID NO: 8 представляет собой аминокислотную последовательность капсидного белка AAV-NP59. Дополнительная информация, касающаяся NP59, может быть найдена в WO/2017/143100, включенной в настоящее описание в качестве ссылки.
Пример 18: Продолжение развития платформы GENERIDE™
[0175] Ключевые аспекты платформы GENERIDE™ с точки зрения конструирования конструкций и капсидов для производства в коммерческом масштабе могут быть оптимизированы.
- капсид AAV. Капсиды AAV конструируют так, чтобы они были высокоэффективными в отношении доставки их содержимого в конкретные ткани-мишени, такие как печень. Идентифицированы капсиды, которые лучше подходят для клинического применения в печени и других показаний. Например, LK03, капсид AAV, используемый в LB-001, был разработан так, чтобы он был селективным в отношении печени.
- Плечи гомологии и участки встраивания. Технология редактирования генома имеет потенциальное преимущество, состоящее в том, что плечи гомологии и участки встраивания для одного терапевтического средства можно применять для других терапевтических средств, которые нацелены в ту же ткань. Выводы, полученные при оптимизации частоты гомологичной рекомбинации и уровней экспрессии генов, можно применять для следующих продуктов-кандидатов.
- Мишени. Потенциальные мишени включают мишени, которые соответствуют генам, в норме экспрессируемым в печени, других тканях, связанных с экспрессией в печени, и мишени, на которые лучше осуществлять нацеливание в других тканях, таких как ЦНС или мышца.
- Селекция. Потенциальным преимуществом технологии редактирования генома GENERIDE™ является ее долговременная природа в результате встраивания в хромосому. Данные указывают на то, что существуют способы терапии, где коррекция дефицита гена может обеспечить селективное преимущество для клеток и запустить увеличение процента клеток, содержащих трансген. Также проводится оценка способов предоставления селективного преимущества обработанным клеткам, даже когда трансген не обеспечивает селективного преимущества на клеточном уровне. Один такой способ вовлекает добавление элемента к конструкции GENERIDE™, так чтобы клетки, которые не включают элемент, имели селективное невыгодное положение, когда пациентов лечат экзогенным средством. Эти и родственные способы позволяют увеличение количества клеток, содержащих желаемый ген, гарантируя длительный терапевтический эффект у пациентов.
ПОСЛЕДОВАТЕЛЬНОСТИ
SEQ ID NO: 1 представляет собой аминокислотную последовательность капсидного белка AAV-DJ.
MAADGYLPDWLEDTLSEGIRQWWKLKPGPPPPKPAERHKDDSRGLVLPGYKYLGPFNGLDKGEPVNEADAAALEHDKAYDRQLDSGDNPYLKYNHADAEFQERLKEDTSFGGNLGRAVFQAKKRLLEPLGLVEEAAKTAPGKKRPVEHSPVEPDSSSGTGKAGQQPARKRLNFGQTGDADSVPDPQPIGEPPAAPSGVGSLTMAAGGGAPMADNNEGADGVGNSSGNWHCDSTWMGDRVITTSTRTWALPTYNNHLYKQISNSTSGGSSNDNAYFGYSTPWGYFDFNRFHCHFSPRDWQRLINNNWGFRPKRLSFKLFNIQVKEVTQNEGTKTIANNLTSTIQVFTDSEYQLPYVLGSAHQGCLPPFPADVFMIPQYGYLTLNNGSQAVGRSSFYCLEYFPSQMLKTGNNFQFTYTFEDVPFHSSYAHSQSLDRLMNPLIDQYLYYLSRTQTTGGTTNTQTLGFSQGGPNTMANQAKNWLPGPCYRQQRVSKTSADNNNSEYSWTGATKYHLNGRDSLVNPGPAMASHKDDEEKFFPQSGVLIFGKQGSEKTNVDIEKVMITDEEEIRTTNPVATEQYGSVSTNLQRGNRQAATADVNTQGVLPGMVWQDRDVYLQGPIWAKIPHTDGHFHPSPLMGGFGLKHPPPQILIKNTPVPADPPTTFNQSKLNSFITQYSTGQVSVEIEWELQKENSKRWNPEIQYTSNYYKSTSVDFAVNTEGVYSEPRPIGTRYLTRNL
SEQ ID NO: 2 представляет собой нуклеотидную последовательность, кодирующую капсидный белок AAV-DJ.
atggctgccgatggttatcttccagattggctcgaggacactctctctgaaggaataagacagtggtggaagctcaaacctggcccaccaccaccaaagcccgcagagcggcataaggacgacagcaggggtcttgtgcttcctgggtacaagtacctcggacccttcaacggactcgacaagggagagccggtcaacgaggcagacgccgcggccctcgagcacgacaaagcctacgaccggcagctcgacagcggagacaacccgtacctcaagtacaaccacgccgacgccgagttccaggagcggctcaaagaagatacgtcttttgggggcaacctcgggcgagcagtcttccaggccaaaaagaggcttcttgaacctcttggtctggttgaggaagcggctaagacggctcctggaaagaagaggcctgtagagcactctcctgtggagccagactcctcctcgggaaccggaaaggcgggccagcagcctgcaagaaaaagattgaattttggtcagactggagacgcagactcagtcccagaccctcaaccaatcggagaacctcccgcagccccctcaggtgtgggatctcttacaatggctgcaggcggtggcgcaccaatggcagacaataacgagggcgccgacggagtgggtaattcctcgggaaattggcattgcgattccacatggatgggcgacagagtcatcaccaccagcacccgaacctgggccctgcccacctacaacaaccacctctacaagcaaatctccaacagcacatctggaggatcttcaaatgacaacgcctacttcggctacagcaccccctgggggtattttgactttaacagattccactgccacttttcaccacgtgactggcagcgactcatcaacaacaactggggattccggcccaagagactcagcttcaagctcttcaacatccaggtcaaggaggtcacgcagaatgaaggcaccaagaccatcgccaataacctcaccagcaccatccaggtgtttacggactcggagtaccagctgccgtacgttctcggctctgcccaccagggctgcctgcctccgttcccggcggacgtgttcatgattccccagtacggctacctaacactcaacaacggtagtcaggccgtgggacgctcctccttctactgcctggaatactttccttcgcagatgctgagaaccggcaacaacttccagtttacttacaccttcgaggacgtgcctttccacagcagctacgcccacagccagagcttggaccggctgatgaatcctctgattgaccagtacctgtactacttgtctcggactcaaacaacaggaggcacgacaaatacgcagactctgggcttcagccaaggtgggcctaatacaatggccaatcaggcaaagaactggctgccaggaccctgttaccgccagcagcgagtatcaaagacatctgcggataacaacaacagtgaatactcgtggactggagctaccaagtaccacctcaatggcagagactctctggtgaatccgggcccggccatggcaagccacaaggacgatgaagaaaagtttttttcctcagagcggggttctcatctttgggaagcaaggctcagagaaaacaaatgtggacattgaaaaggtcatgattacagacgaagaggaaatcaggacaaccaatcccgtggctacggagcagtatggttctgtatctaccaacctccagagaggcaacagacaagcagctaccgcagatgtcaacacacaaggcgttcttccaggcatggtctggcaggacagagatgtgtaccttcaggggcccatctgggcaaagattccacacacggacggacattttcacccctctcccctcatgggtggattcggacttaaacaccctccgcctcagatcctgatcaagaacacgcctgtacctgcggatcctccgaccaccttcaaccagtcaaagctgaactctttcatcacccagtattctactggccaagtcagcgtggagatcgagtgggagctgcagaaggaaaacagcaagcgctggaaccccgagatccagtacacctccaactactacaaatctacaagtgtggactttgctgttaatacagaaggcgtgtactctgaaccccgccccattggcacccgttacctcacccgtaatctgtaa
SEQ ID NO: 3 представляет собой аминокислотную последовательность капсидного белка AAV-2.
MAADGYLPDWLEDTLSEGIRQWWKLKPGPPPPKPAERHKDDSRGLVLPGYKYLGPFNGLDKGEPVNEADAAALEHDKAYDRQLDSGDNPYLKYNHADAEFQERLKEDTSFGGNLGRAVFQAKKRVLEPLGLVEEPVKTAPGKKRPVEHSPVEPDSSSGTGKAGQQPARKRLNFGQTGDADSVPDPQPLGQPPAAPSGLGTNTMATGSGAPMADNNEGADGVGNSSGNWHCDSTWMGDRVITTSTRTWALPTYNNHLYKQISSQSGASNDNHYFGYSTPWGYFDFNRFHCHFSPRDWQRLINNNWGFRPKRLNFKLFNIQVKEVTQNDGTTTIANNLTSTVQVFTDSEYQLPYVLGSAHQGCLPPFPADVFMVPQYGYLTLNNGSQAVGRSSFYCLEYFPSQMLRTGNNFTFSYTFEDVPFHSSYAHSQSLDRLMNPLIDQYLYYLSRTNTPSGTTTQSRLQFSQAGASDIRDQSRNWLPGPCYRQQRVSKTSADNNNSEYSWTGATKYHLNGRDSLVNPGPAMASHKDDEEKFFPQSGVLIFGKQGSEKTNVDIEKVMITDEEEIRTTNPVATEQYGSVSTNLQRGNRQAATADVNTQGVLPGMVWQDRDVYLQGPIWAKIPHTDGHFHPSPLMGGFGLKHPPPQILIKNTPVPANPSTTFSAAKFASFITQYSTGQVSVEIEWELQKENSKRWNPEIQYTSNYNKSVNRGLTVDTNGVYSEPRPIGTRYLTRNL
SEQ ID NO: 4 представляет собой аминокислотную последовательность капсидного белка AAV-8.
MAADGYLPDWLEDNLSEGIREWWALKPGAPKPKANQQKQDDGRGLVLPGYKYLGPFNGLDKGEPVNAADAAALEHDKAYDQQLQAGDNPYLRYNHADAEFQERLQEDTSFGGNLGRAVFQAKKRVLEPLGLVEEGAKTAPGKKRPVEPSPQRSPDSSTGIGKKGQQPARKRLNFGQTGDSESVPDPQPLGEPPAAPSGVGPNTMAAGGGAPMADNNEGADGVGSSSGNWHCDSTWLGDRVITTSTRTWALPTYNNHLYKQISNGTSGGATNDNTYFGYSTPWGYFDFNRFHCHFSPRDWQRLINNNWGFRPKRLSFKLFNIQVKEVTQNEGTKTIANNLTSTIQVFTDSEYQLPYVLGSAHQGCLPPFPADVFMIPQYGYLTLNNGSQAVGRSSFYCLEYFPSQMLRTGNNFQFTYTFEDVPFHSSYAHSQSLDRLMNPLIDQYLYYLSRTQTTGGTANTQTLGFSQGGPNTMANQAKNWLPGPCYRQQRVSTTTGQNNNSNFAWTAGTKYHLNGRNSLANPGIAMATHKDDEERFFPSNGILIFGKQNAARDNADYSDVMLTSEEEIKTTNPVATEEYGIVADNLQQQNTAPQIGTVNSQGALPGMVWQNRDVYLQGPIWAKIPHTDGNFHPSPLMGGFGLKHPPPQILIKNTPVPADPPTTFNQSKLNSFITQYSTGQVSVEIEWELQKENSKRWNPEIQYTSNYYKSTSVDFAVNTEGVYSEPRPIGTRYLTRNL
SEQ ID NO: 5 представляет собой нуклеотидную последовательность, кодирующую капсидный белок AAV-LK03.
atggctgctgacggttatcttccagattggctcgaggacaacctttctgaaggcattcgagagtggtgggcgctgcaacctggagcccctaaacccaaggcaaatcaacaacatcaggacaacgctcggggtcttgtgcttccgggttacaaatacctcggacccggcaacggactcgacaagggggaacccgtcaacgcagcggacgcggcagccctcgagcacgacaaggcctacgaccagcagctcaaggccggtgacaacccctacctcaagtacaaccacgccgacgccgagttccaggagcggctcaaagaagatacgtcttttgggggcaacctcgggcgagcagtcttccaggccaaaaagaggcttcttgaacctcttggtctggttgaggaagcggctaagacggctcctggaaagaagaggcctgtagatcagtctcctcaggaaccggactcatcatctggtgttggcaaatcgggcaaacagcctgccagaaaaagactaaatttcggtcagactggcgactcagagtcagtcccagaccctcaacctctcggagaaccaccagcagcccccacaagtttgggatctaatacaatggcttcaggcggtggcgcaccaatggcagacaataacgagggtgccgatggagtgggtaattcctcaggaaattggcattgcgattcccaatggctgggcgacagagtcatcaccaccagcaccagaacctgggccctgcccacttacaacaaccatctctacaagcaaatctccagccaatcaggagcttcaaacgacaaccactactttggctacagcaccccttgggggtattttgactttaacagattccactgccacttctcaccacgtgactggcagcgactcattaacaacaactggggattccggcccaagaaactcagcttcaagctcttcaacatccaagttaaagaggtcacgcagaacgatggcacgacgactattgccaataaccttaccagcacggttcaagtgtttacggactcggagtatcagctcccgtacgtgctcgggtcggcgcaccaaggctgtctcccgccgtttccagcggacgtcttcatggtccctcagtatggatacctcaccctgaacaacggaagtcaagcggtgggacgctcatccttttactgcctggagtacttcccttcgcagatgctaaggactggaaataacttccaattcagctataccttcgaggatgtaccttttcacagcagctacgctcacagccagagtttggatcgcttgatgaatcctcttattgatcagtatctgtactacctgaacagaacgcaaggaacaacctctggaacaaccaaccaatcacggctgctttttagccaggctgggcctcagtctatgtctttgcaggccagaaattggctacctgggccctgctaccggcaacagagactttcaaagactgctaacgacaacaacaacagtaactttccttggacagcggccagcaaatatcatctcaatggccgcgactcgctggtgaatccaggaccagctatggccagtcacaaggacgatgaagaaaaatttttccctatgcacggcaatctaatatttggcaaagaagggacaacggcaagtaacgcagaattagataatgtaatgattacggatgaagaagagattcgtaccaccaatcctgtggcaacagagcagtatggaactgtggcaaataacttgcagagctcaaatacagctcccacgactagaactgtcaatgatcagggggccttacctggcatggtgtggcaagatcgtgacgtgtaccttcaaggacctatctgggcaaagattcctcacacggatggacactttcatccttctcctctgatgggaggctttggactgaaacatccgcctcctcaaatcatgatcaaaaatactccggtaccggcaaatcctccgacgactttcagcccggccaagtttgcttcatttatcactcagtactccactggacaggtcagcgtggaaattgagtgggagctacagaaagaaaacagcaaacgttggaatccagagattcagtacacttccaactacaacaagtctgttaatgtggactttactgtagacactaatggtgtttatagtgaacctcgccccattggcacccgttaccttacccgtcccctgtaa
SEQ ID NO: 6 представляет собой аминокислотную последовательность капсидного белка AAV-LK03.
MAADGYLPDWLEDNLSEGIREWWALQPGAPKPKANQQHQDNARGLVLPGYKYLGPGNGLDKGEPVNAADAAALEHDKAYDQQLKAGDNPYLKYNHADAEFQERLKEDTSFGGNLGRAVFQAKKRLLEPLGLVEEAAKTAPGKKRPVDQSPQEPDSSSGVGKSGKQPARKRLNFGQTGDSESVPDPQPLGEPPAAPTSLGSNTMASGGGAPMADNNEGADGVGNSSGNWHCDSQWLGDRVITTSTRTWALPTYNNHLYKQISSQSGASNDNHYFGYSTPWGYFDFNRFHCHFSPRDWQRLINNNWGFRPKKLSFKLFNIQVKEVTQNDGTTTIANNLTSTVQVFTDSEYQLPYVLGSAHQGCLPPFPADVFMVPQYGYLTLNNGSQAVGRSSFYCLEYFPSQMLRTGNNFQFSYTFEDVPFHSSYAHSQSLDRLMNPLIDQYLYYLNRTQGTTSGTTNQSRLLFSQAGPQSMSLQARNWLPGPCYRQQRLSKTANDNNNSNFPWTAASKYHLNGRDSLVNPGPAMASHKDDEEKFFPMHGNLIFGKEGTTASNAELDNVMITDEEEIRTTNPVATEQYGTVANNLQSSNTAPTTRTVNDQGALPGMVWQDRDVYLQGPIWAKIPHTDGHFHPSPLMGGFGLKHPPPQIMIKNTPVPANPPTTFSPAKFASFITQYSTGQVSVEIEWELQKENSKRWNPEIQYTSNYNKSVNVDFTVDTNGVYSEPRPIGTRYLTRPL
SEQ ID NO: 7 представляет собой нуклеотидную последовательность, кодирующую капсидный белок AAV-NP59.
atggctgccgatggttatcttccagattggctcgaggacactctctctgaaggaataagacagtggtggaagctcaaacctggcccaccaccaccaaagcccgcagagcggcataaggacgacagcaggggtcttgtgcttcctgggtacaagtacctcggacccttcaacggactcgacaagggagagccggtcaacgaggcagacgccgcggccctcgagcacgacaaagcctacgaccggcagctcgacagcggagacaacccgtacctcaagtacaaccacgccgacgcggagtttcaggagcgccttaaagaagatacgtcttttgggggcaacctcggacgagcagtcttccaggcgaaaaagagggttcttgaacctctgggcctggttgaggaacctgttaagacggctccgggaaaaaagaggccggtagagcactctcctgtggagccagactcctcctcgggaaccggcaagacaggccagcagcccgctaaaaagagactcaattttggtcagactggcgactcagagtcagtcccagaccctcaacctctcggagaaccaccagcagccccctctggtctgggaactaatacgatggctacaggcagtggcgcaccaatggcagacaataacgagggcgccgacggagtgggtaattcctcgggaaattggcattgcgattccacatggatgggcgacagagtcatcaccaccagcacccgaacctgggccctgcccacctacaacaaccatctctacaagcaaatctccagccaatcaggagcttcaaacgacaaccactactttggctacagcaccccttgggggtattttgactttaacagattccactgccacttctcaccacgtgactggcagcgactcattaacaacaactggggattccggcccaagaaactcagcttcaagctcttcaacatccaagttaaagaggtcacgcagaacgatggcacgacgactattgccaataaccttaccagcacggttcaagtgtttactgactcggagtaccagctcccgtacgtcctcggctcggcgcatcaaggatgcctcccgccgttcccagcagacgtcttcatggtgccacagtatggatacctcaccctgaacaacgggagtcaggcagtaggacgctcttcattttactgcctggagtactttccttctcagatgctgcgtaccggaaacaactttaccttcagctacacttttgaggacgttcctttccacagcagctacgctcacagccagagtctggaccgtctcatgaatcctctcatcgaccagtacctgtattacttgagcagaacaaacactccaagtggaaccaccacgcagtcaaggcttcagttttctcaggccggagcgagtgacattcgggaccagtctaggaactggcttcctggaccctgttaccgccagcagcgagtatcaaagacatctgcggataacaacaacagtgaatactcgtggactggagctaccaagtaccacctcaatggcagagactctctggtgaatccgggcccggccatggcaagccacaaggacgatgaagaaaagttttttcctcagagcggggttctcatctttgggaagcaaggctcagagaaaacaaatgtggacattgaaaaggtcatgattacagacgaagaggaaatcaggacaaccaatcccgtggctacggagcagtatggttctgtatctaccaacctccagagaggcaacagacaagcagctaccgcagatgtcgacacacaaggcgttcttccaggcatggtctggcaggacagagatgtgtaccttcagggacccatctgggcaaagattccacacacggacggacattttcacccctctcccctcatgggtggattcggacttaaacaccctcctccacagattctcatcaagaacaccccggtacctgcgaatccttcgaccaccttcagtgcggcaaagtttgcttccttcatcacacagtactccacgggacaggtcagcgtggagatcgagtgggagctgcagaaggaaaacagcaaacgctggaatcccgaaattcagtacacttccaactacaacaagtctgttaatgtggactttactgtggacactaatggcgtgtattcagagcctcgccccattggcaccagatacctgactcgtaatctgtaa
SEQ ID NO: 8 представляет собой аминокислотную последовательность капсидного белка AAV-NP59.
MAADGYLPDWLEDTLSEGIRQWWKLKPGPPPPKPAERHKDDSRGLVLPGYKYLGPFNGLDKGEPVNEADAAALEHDKAYDRQLDSGDNPYLKYNHADAEFQERLKEDTSFGGNLGRAVFQAKKRVLEPLGLVEEPVKTAPGKKRPVEHSPVEPDSSSGTGKTGQQPAKKRLNFGQTGDSESVPDPQPLGEPPAAPSGLGTNTMATGSGAPMADNNEGADGVGNSSGNWHCDSTWMGDRVITTSTRTWALPTYNNHLYKQISSQSGASNDNHYFGYSTPWGYFDFNRFHCHFSPRDWQRLINNNWGFRPKKLSFKLFNIQVKEVTQNDGTTTIANNLTSTVQVFTDSEYQLPYVLGSAHQGCLPPFPADVFMVPQYGYLTLNNGSQAVGRSSFYCLEYFPSQMLRTGNNFTFSYTFEDVPFHSSYAHSQSLDRLMNPLIDQYLYYLSRTNTPSGTTTQSRLQFSQAGASDIRDQSRNWLPGPCYRQQRVSKTSADNNNSEYSWTGATKYHLNGRDSLVNPGPAMASHKDDEEKFFPQSGVLIFGKQGSEKTNVDIEKVMITDEEEIRTTNPVATEQYGSVSTNLQRGNRQAATADVDTQGVLPGMVWQDRDVYLQGPIWAKIPHTDGHFHPSPLMGGFGLKHPPPQILIKNTPVPANPSTTFSAAKFASFITQYSTGQVSVEIEWELQKENSKRWNPEIQYTSNYNKSVNVDFTVDTNGVYSEPRPIGTRYLTRNL
SEQ ID NO: 9 представляет собой оптимизированную нуклеотидную последовательность, кодирующую метилмалонил-CoA мутазу (synMUT1) человека
atgctgagagccaaaaaccagctgttcctgctgagcccccactatctgagacaggtcaaagaaagttccgggagtagactgatccagcagagactgctgcaccagcagcagccactgcatcctgagtgggccgctctggccaagaaacagctgaagggcaaaaacccagaagacctgatctggcacactccagaggggatttcaatcaagcccctgtacagcaaaagggacactatggatctgccagaggaactgccaggagtgaagcctttcacccgcggaccttacccaactatgtatacctttcgaccctggacaattcggcagtacgccggcttcagtactgtggaggaatcaaacaagttttataaggacaacatcaaggctggacagcagggcctgagtgtggcattcgatctggccacacatcgcggctatgactcagataatcccagagtcaggggggacgtgggaatggcaggagtcgctatcgacacagtggaagatactaagattctgttcgatggaatccctctggagaaaatgtctgtgagtatgacaatgaacggcgctgtcattcccgtgctggcaaacttcatcgtcactggcgaggaacagggggtgcctaaggaaaaactgaccggcacaattcagaacgacatcctgaaggagttcatggtgcggaatacttacatttttccccctgaaccatccatgaaaatcattgccgatatcttcgagtacaccgctaagcacatgcccaagttcaactcaattagcatctccgggtatcatatgcaggaagcaggagccgacgctattctggagctggcttacaccctggcagatggcctggaatattctcgaaccggactgcaggcaggcctgacaatcgacgagttcgctcctagactgagtttcttttggggaattggcatgaacttttacatggagatcgccaagatgagggctggccggagactgtgggcacacctgatcgagaagatgttccagcctaagaactctaagagtctgctgctgcgggcccattgccagacatccggctggtctctgactgaacaggacccatataacaatattgtcagaaccgcaatcgaggcaatggcagccgtgttcggaggaacccagagcctgcacacaaactcctttgatgaggccctggggctgcctaccgtgaagtctgctaggattgcacgcaatacacagatcattatccaggaggaatccggaatcccaaaggtggccgatccctggggaggctcttacatgatggagtgcctgacaaacgacgtgtatgatgctgcactgaagctgattaatgaaatcgaggaaatggggggaatggcaaaggccgtggctgagggcattccaaaactgaggatcgaggaatgtgcagctaggcgccaggcacgaattgactcaggaagcgaagtgatcgtcggggtgaataagtaccagctggagaaagaagacgcagtcgaagtgctggccatcgataacacaagcgtgcgcaatcgacagattgagaagctgaagaaaatcaaaagctcccgcgatcaggcactggccgaacgatgcctggcagccctgactgagtgtgctgcaagcggggacggaaacattctggctctggcagtcgatgcctcccgggctagatgcactgtgggggaaatcaccgacgccctgaagaaagtcttcggagagcacaaggccaatgatcggatggtgagcggcgcttatagacaggagttcggggaatctaaagagattaccagtgccatcaagagggtgcacaagttcatggagagagaagggcgacggcccaggctgctggtggcaaagatgggacaggacggacatgatcgcggagcaaaagtcattgccaccgggttcgctgacctgggatttgacgtggatatcggccctctgttccagacaccacgagaggtcgcacagcaggcagtcgacgctgatgtgcacgcagtcggagtgtccactctggcagctggccataagaccctggtgcctgaactgatcaaagagctgaactctctgggcagaccagacatcctggtcatgtgcggcggcgtgatcccaccccaggattacgaattcctgtttgaggtcggggtgagcaacgtgttcggaccaggaaccaggatccctaaggccgcagtgcaggtcctggatgatattgaaaagtgtctggaaaagaaacagcagtcagtgtaa
SEQ ID NO: 10 представляет собой встречающуюся в природе (wt) аминокислотную последовательность метилмалонил-CoA мутазы человека.
MLRAKNQLFLLSPHYLRQVKESSGSRLIQQRLLHQQQPLHPEWAALAKKQLKGKNPEDLIWHTPEGISIKPLYSKRD™DLPEELPGVKPFTRGPYP™YTFRPWTIRQYAGFSTVEESNKFYKDNIKAGQQGLSVAFDLATHRGYDSDNPRVRGDVGMAGVAIDTVEDTKILFDGIPLEKMSVSMTMNGAVIPVLANFIVTGEEQGVPKEKLTGTIQNDILKEFMVRNTYIFPPEPSMKIIADIFEYTAKHMPKFNSISISGYHMQEAGADAILELAYTLADGLEYSRTGLQAGLTIDEFAPRLSFFWGIGMNFYMEIAKMRAGRRLWAHLIEKMFQPKNSKSLLLRAHCQTSGWSLTEQDPYNNIVRTAIEAMAAVFGGTQSLHTNSFDEALGLPTVKSARIARNTQIIIQEESGIPKVADPWGGSYMMECLTNDVYDAALKLINEIEEMGGMAKAVAEGIPKLRIEECAARRQARIDSGSEVIVGVNKYQLEKEDAVEVLAIDNTSVRNRQIEKLKKIKSSRDQALAEHCLAALTECAASGDGNILALAVDASRARCTVGEITDALKKVFGEHKANDRMVSGAYRQEFGESKEITSAIKRVHKFMEREGRRPRLLVAKMGQDGHDRGAKVIATGFADLGFDVDIGPLFQTPREVAQQAVDADVHAVGVSTLAAGHKTLVPELIKELNSLGRPDILVMCGGVIPPQDYEFLFEVGVSNVFGPGTRIPKAAVQVLDDIEKCLEKKQQSV
SEQ ID NO: 11 представляет собой встречающуюся в природе (wt) нуклеотидную последовательность гена метилмалонил-CoA мутазы человека (wtMUT).
atgttaagagctaagaatcagctttttttactttcacctcattacctgaggcaggtaaaagaatcatcaggctccaggctcatacagcaacgacttctacaccagcaacagccccttcacccagaatgggctgccctggctaaaaagcagctgaaaggcaaaaacccagaagacctaatatggcacaccccggaagggatctctataaaacccttgtattccaagagagatactatggacttacctgaagaacttccaggagtgaagccattcacacgtggaccatatcctaccatgtatacctttaggccctggaccatccgccagtatgctggttttagtactgtggaagaaagcaataagttctataaggacaacattaaggctggtcagcagggattatcagttgcctttgatctggcgacacatcgtggctatgattcagacaaccctcgagttcgtggtgatgttggaatggctggagttgctattgacactgtggaagataccaaaattctttttgatggaattcctttagaaaaaatgtcagtttccatgactatgaatggagcagttattccagttcttgcaaattttatagtaactggagaagaacaaggtgtacctaaagagaagcttactggtaccatccaaaatgatatactaaaggaatttatggttcgaaatacatacatttttcctccagaaccatccatgaaaattattgctgacatatttgaatatacagcaaagcacatgccaaaatttaattcaatttcaattagtggataccatatgcaggaagcaggggctgatgccattctggagctggcctatactttagcagatggattggagtactctagaactggactccaggctggcctgacaattgatgaatttgcaccaaggttgtctttcttctggggaattggaatgaatttctatatggaaatagcaaagatgagagctggtagaagactctgggctcacttaatagagaaaatgtttcagcctaaaaactcaaaatctcttcttctaagagcacactgtcagacatctggatggtcacttactgagcaggatccctacaataatattgtccgtactgcaatagaagcaatggcagcagtatttggagggactcagtctttgcacacaaattcttttgatgaagctttgggtttgccaactgtgaaaagtgctcgaattgccaggaacacacaaatcatcattcaagaagaatctgggattcccaaagtggctgatccttggggaggttcttacatgatggaatgtctcacaaatgatgtttatgatgctgctttaaagctcattaatgaaattgaagaaatgggtggaatggccaaagctgtagctgagggaatacctaaacttcgaattgaagaatgtgctgcccgaagacaagctagaatagattctggttctgaagtaattgttggagtaaataagtaccagttggaaaaagaagacgctgtagaagttctggcaattgataatacttcagtgcgaaacaggcagattgaaaaacttaagaagatcaaatccagcagggatcaagctttggctgaacgttgtcttgctgcactaaccgaatgtgctgctagcggagatggaaatatcctggctcttgcagtggatgcatctcgggcaagatgtacagtgggagaaatcacagatgccctgaaaaaggtatttggtgaacataaagcgaatgatcgaatggtgagtggagcatatcgccaggaatttggagaaagtaaagagataacatctgctatcaagagggttcataaattcatggaacgtgaaggtcgcagacctcgtcttcttgtagcaaaaatgggacaagatggccatgacagaggagcaaaagttattgctacaggatttgctgatcttggttttgatgtggacataggccctcttttccagactcctcgtgaagtggcccagcaggctgtggatgcggatgtgcatgctgtgggcataagcaccctcgctgctggtcataaaaccctagttcctgaactcatcaaagaacttaactcccttggacggccagatattcttgtcatgtgtggaggggtgataccacctcaggattatgaatttctgtttgaagttggtgtttccaatgtatttggtcctgggactcgaattccaaaggctgccgttcaggtgcttgatgatattgagaagtgtttggaaaagaagcagcaatctgtataa
SEQ ID NO: 12 представляет собой оптимизированную нуклеотидную последовательность, кодирующую метилмалонил-CoA мутазу человека (synMUT2)
atgctgcgagcgaaaaatcagctttttctgttgagcccacactacctgaggcaggttaaagaatccagcgggagccggctgattcagcagcgactgctccaccagcagcagcctttgcatcccgaatgggctgctttggcgaagaagcagctcaaggggaagaaccctgaagatcttatttggcacaccccagagggcatcagcatcaagcctttgtattccaaaagggacaccatggatctgcctgaagaattgcccggggtcaaaccattcacacgggggccatatccaaccatgtacaccttccggccatggactatcagacagtatgcaggctttagcactgtcgaggaatccaataagttctataaagacaatatcaaagctggccagcaaggtctgtccgtggcattcgatctggctacacatagaggttatgattctgacaatccaagagtacggggagacgtcggaatggcgggagttgccattgacacagtggaggacaccaagatacttttcgatgggattccattggagaaaatgtctgtgtcaatgacgatgaacggcgctgtgattcccgttttggcgaacttcatcgtcaccggggaagagcagggcgtcccgaaggaaaagctcaccgggacaatccaaaacgacattcttaaagaattcatggtgagaaatacctacatctttcctcctgagccttccatgaagatcatcgcggacatctttgaatacacggctaaacacatgcctaaatttaactcaatcagcataagcgggtaccacatgcaggaggccggcgctgacgctatacttgagctcgcatataccctggcagatggactggaatactcaaggaccgggctccaggctggactgacaatcgacgagtttgccccccgactcagttttttctggggtatcgggatgaatttctacatggagatagcgaagatgagggcgggcagacggctttgggcgcatctgatcgagaaaatgttccagcccaagaattcaaagagtctgctgctgagagcccactgccagacctcaggctggagcctgactgaacaggacccatacaacaacattgttagaaccgccatcgaggcgatggcagcggttttcggtgggacacagtcattgcacactaactcatttgacgaagccctcggtctgcctaccgtgaagtcagctcggatcgctaggaacacacagatcatcatccaggaggagagtggcatcccaaaagtcgccgatccttggggaggaagttacatgatggaatgcctcacgaatgacgtatacgatgccgcactcaagctgattaacgagatcgaggaaatgggaggcatggcaaaagctgtcgccgagggcattccaaagctgcgcatagaggagtgtgccgcccgaagacaggcccgcattgactccggctctgaggtgatagtgggcgttaataaatatcagctagagaaggaagacgccgtcgaagttctggcgatagataatacctctgtgcgaaatagacagattgagaaactgaagaagatcaagtcaagccgagaccaggccttggccgagaggtgtctggcagccctcactgagtgcgcggcatctggggacggcaacatattggcacttgccgtcgatgcctccagggcccgatgtacggtcggcgaaattaccgatgccctcaagaaggtttttggcgagcacaaggctaacgacaggatggttagtggagcatacagacaggagtttggcgaaagcaaggaaattacttccgcgattaaaagagtgcacaaattcatggaacgggagggtaggcgaccgaggctcctcgttgccaaaatgggtcaggacggccacgaccggggcgccaaggttatcgctaccggtttcgctgacctgggcttcgatgtggatatcggaccactgtttcaaacccccagagaagttgcccaacaagccgttgacgctgacgtacacgctgtaggcatctccactctcgccgccgggcataagactctcgtcccagagctgataaaggagcttaacagcctcggaagacccgacatcctggttatgtgcggtggagtgattccgccgcaggattacgaattcctcttcgaagtaggagtgtcaaacgtgttcggcccaggcactcggatacccaaggctgccgttcaggtgcttgacgacattgaaaaatgtctggagaagaagcaacaatctgtataa
SEQ ID NO: 13 представляет собой оптимизированную нуклеотидную последовательность, кодирующую метилмалонил-CoA мутазу человека (synMUT3)
atgttgagggctaaaaaccagctctttctgttgagtccacactaccttaggcaagtgaaggaatctagcggtagcaggctgatccagcagcgcctgctgcaccagcagcagcccctgcaccctgagtgggctgcattggcaaagaaacaactgaagggtaaaaatcctgaagatctgatttggcacacaccggaggggatttccataaaacctctctactctaaacgcgatactatggatctgcccgaggaattgccaggagtgaaaccctttacaagggggccctaccccactatgtacacgttcagaccctggactatacgccagtatgccggattttctaccgttgaggaatccaacaagttttataaggacaacatcaaagccgggcagcagggactgtcagtggcatttgatctcgccacccaccgcgggtacgactccgacaacccaagagtccgcggtgacgtcggcatggcaggggttgccattgacacagtagaggatactaaaattttgtttgatgggatccccctagagaagatgtccgtgtctatgacgatgaacggcgcggtaatcccagtgcttgccaacttcatagtcacaggggaagagcagggcgtaccaaaggagaagctcacaggaacaatccaaaatgacattctgaaggaattcatggtgagaaatacttatatctttcctcccgagccctctatgaagattattgccgacatttttgaatacaccgcaaaacatatgcccaagttcaattccatatctattagtggataccacatgcaagaagctggggctgatgcaatacttgagcttgcctacaccctggccgacggactggagtattctcgcactggcctgcaagccgggctgacaattgacgagttcgccccacgccttagcttcttctggggcatcggcatgaatttctatatggagatcgcaaagatgagagcagggcggcgcttgtgggcccatctgatcgaaaagatgtttcagcctaagaatagtaagagcctgctcctgcgggctcactgtcagacgtcaggctggagcctcacagagcaggatccttacaataacatcgtccggactgctattgaggcgatggctgcagtattcggaggaacacaaagcctgcacactaattctttcgatgaggctttggggctccctaccgtgaagtcagccagaattgcaagaaacacccaaataatcatccaagaagaatcagggatcccaaaagttgccgacccctggggaggaagttatatgatggagtgcctgaccaatgacgtctacgacgccgctttgaagctgattaacgagattgaagagatgggcggaatggccaaggcggtcgctgagggcattccgaaactgcgcatagaggagtgtgctgctcgcaggcaggccagaattgattccggttccgaagtgatcgtgggggttaataagtatcaactggaaaaagaggacgctgtcgaagtcctcgcaatcgataataccagcgttagaaaccgacaaattgagaagctgaaaaagatcaaaagttcaagggaccaggccttggctgagcggtgtctcgccgcactgaccgaatgtgccgccagcggcgatggtaacatcctcgccctcgctgtggacgcttccagagcccggtgcaccgtgggcgaaattacggacgcgctgaaaaaagtctttggcgaacacaaggccaatgatagaatggtgagtggcgcctataggcaggagttcggcgagagtaaagaaataacatccgccatcaagagggtccacaaatttatggagcgggaaggacgcagacctagacttctcgtggccaaaatgggtcaggacggtcatgaccggggagccaaagtcatcgcaacgggcttcgccgatttggggtttgacgtggatatcggtcccttgtttcaaacccccagggaggtggctcagcaggctgtggacgctgacgtccacgcagtgggcatttctacactggcagccgggcacaagacgttggtgccagaactgatcaaagagttgaacagcctgggacgccctgacatcctggtaatgtgcggtggggtaatccccccccaagactacgagttccttttcgaagtgggtgtttctaacgtgttcggacctggaacaagaatccctaaggcggcagtgcaggtgcttgacgatatcgagaagtgcctggagaaaaagcaacaatccgtttaa
SEQ ID NO: 14 представляет собой оптимизированную нуклеотидную последовательность, кодирующую метилмалонил-CoA мутазу человека (synMUT4)
atgcttcgcgccaagaaccaactgttcctgctgtccccccactacctccgacaagtcaaggagagctcgggaagccgcctgattcagcagcggctgctgcaccagcagcagcccctgcatccggaatgggcagcgttggcaaagaagcagctgaagggaaagaaccctgaggacctgatctggcacaccccggagggaatctcgatcaagccactgtactccaaaagggacaccatggacttgcctgaagaacttccgggcgtgaagccttttacccgggggccatacccaacaatgtacactttccgcccctggaccatcagacagtacgccggtttctccaccgtcgaagaatccaacaagttctataaggacaacatcaaggccgggcagcagggactgagcgtcgcgtttgacctggcaacccatcgcggctacgactccgacaaccctcgcgtgcggggggacgtgggaatggccggagtggctatcgacaccgtggaggacaccaagattctcttcgacggaatcccgctggaaaagatgtcggtgtccatgaccatgaatggcgccgtgatcccggtgctcgcgaacttcatcgtgacgggagaggaacagggagtgccgaaagagaagctgaccgggactattcagaatgacatcctcaaggagttcatggtccgcaacacttacattttccctcctgaaccctcgatgaagatcatcgctgacatcttcgagtacaccgcgaagcacatgccgaagttcaactcgatctccatctcgggctaccacatgcaggaggccggggccgacgccattctcgaactggcgtacactctggcggatggtctggaatactcacgcaccggactgcaggccggactgacaatcgacgagttcgccccgaggctgtccttcttctggggcattgggatgaacttctatatggaaatcgcgaagatgagagctggaaggcggctgtgggcgcacctgatcgagaagatgttccagcccaagaacagcaaaagccttctcctccgcgcccactgccaaacttccggctggtcactgaccgagcaggatccgtacaacaacattgtccggactgccattgaggccatggccgctgtgttcggaggcactcagtccctccacactaactccttcgacgaggccctgggtctgccgaccgtgaagtccgcccggatagccagaaatactcaaatcattatccaggaggaaagcggaatccccaaggtcgccgacccttggggaggatcttacatgatggagtgtttgaccaatgacgtctacgacgccgccctgaagctcattaacgaaatcgaagagatgggcggaatggccaaggccgtggctgagggcatcccgaagctgagaatcgaggaatgcgccgcccggagacaggcccgcattgatagcggcagcgaggtcattgtgggcgtgaacaagtaccagcttgaaaaggaggacgccgtggaagtgctggcaatcgataacacctccgtgcgcaaccggcagatcgaaaagctcaagaagattaagtcctcacgggaccaggcactggcggagagatgcctcgccgcgctgaccgaatgcgctgcctcgggagatggcaacattctggccctggcagtggacgcctctcgggctcggtgcactgtgggggagatcaccgacgccctcaagaaagtgttcggtgaacataaggccaacgaccggatggtgtccggagcgtaccgccaggaatttggcgaatcaaaggaaatcacgtccgcaatcaagagggtgcacaaattcatggaacgggagggcagacggcccagactgctcgtggctaaaatgggacaagatggtcacgaccgcggcgccaaggtcatcgcgactggcttcgccgatctcggattcgacgtggacatcggacctctgtttcaaactccccgggaagtggcccagcaggccgtggacgcggacgtgcatgccgtcgggatctcaaccctggcggccggccataagaccctggtgccggaactgatcaaggagctgaactcgctcggccgccccgacatcctcgtgatgtgtggcggagtgattccgccacaagactacgagttcctgttcgaagtcggggtgtccaacgtgttcggtcccggaaccagaatcccgaaggctgcggtccaagtgctggatgatattgagaagtgccttgagaaaaagcaacagtcagtgtga
SEQ ID NO: 16 представляет собой нуклеотидную последовательность, кодирующую конструкцию для экспрессии Mut у мышей. Она представляет собой последовательность мыши для LB-001. Компоненты последовательности включают: ITR (инвертированный концевой повтор); плечи гомологии; P2A; и SynMut.
TTGGCCACTCCCTCTCTGCGCGCTCGCTCGCTCACTGAGGCCGGGCGACCAAAGGTCGCCCGACGCCCGGGCTTTGCCCGGGCGGCCTCAGTGAGCGAGCGAGCGCGCAGAGAGGGAGTGGCCAACTCCATCACTAGGGGTTCCTatttaaatCTGAAACTAGACAAAACCCGTGTGACTGGCATCGATTATTCTATTTGATCTAGCTAGTCCTAGCAAAGTGACAACTGCTACTCCCCTCCTACACAGCCAAGATTCCTAAGTTGGCAGTGGCATGCTTAATCCTCAAAGCCAAAGTTACTTGGCTCCAAGATTTATAGCCTTAAACTGTGGCCTCACATTCCTTCCTATCTTACTTTCCTGCACTGGGGTAAATGTCTCCTTGCTCTTCTTGCTTTCTGTCCTACTGCAGGGCTCTTGCTGAGCTGGTGAAGCACAAGCCCAAGGCTACAGCGGAGCAACTGAAGACTGTCATGGATGACTTTGCACAGTTCCTGGATACATGTTGCAAGGCTGCTGACAAGGACACCTGCTTCTCGACTGAGGTCAGAAACGTTTTTGCATTTTGACGATGTTCAGTTTCCATTTTCTGTGCACGTGGTCAGGTGTAGCTCTCTGGAACTCACACACTGAATAACTCCACCAATCTAGATGTTGTTCTCTACGTAACTGTAATAGAAACTGACTTACGTAGCTTTTAATTTTTATTTTCTGCCACACTGCTGCCTATTAAATACCTATTATCACTATTTGGTTTCAAATTTGTGACACAGAAGAGCATAGTTAGAAATACTTGCAAAGCCTAGAATCATGAACTCATTTAAACCTTGCCCTGAAATGTTTCTTTTTGAATTGAGTTATTTTACACATGAATGGACAGTTACCATTATATATCTGAATCATTTCACATTCCCTCCCATGGCCTAACAACAGTTTATCTTCTTATTTTGGGCACAACAGATGTCAGAGAGCCTGCTTTAGGAATTCTAAGTAGAACTGTAATTAAGCAATGCAAGGCACGTACGTTTACTATGTCATTGCCTATGGCTATGAAGTGCAAATCCTAACAGTCCTGCTAATACTTTTCTAACATCCATCATTTCTTTGTTTTCAGGGTCCAAACCTTGTCACTAGATGCAAAGACGCCTTAGCCggcagcggcgccaccaacttcagcctgctgaaacaggccggcgacgtggaagagaaccctggccccCTGAGAGCCAAAAACCAGCTGTTCCTGCTGAGCCCCCACTATCTGAGACAGGTCAAAGAAAGTTCCGGGAGTAGACTGATCCAGCAGAGACTGCTGCACCAGCAGCAGCCACTGCATCCTGAGTGGGCCGCTCTGGCCAAGAAACAGCTGAAGGGCAAAAACCCAGAAGACCTGATCTGGCACACTCCAGAGGGGATTTCAATCAAGCCCCTGTACAGCAAAAGGGACACTATGGATCTGCCAGAGGAACTGCCAGGAGTGAAGCCTTTCACCCGCGGACCTTACCCAACTATGTATACCTTTCGACCCTGGACAATTCGGCAGTACGCCGGCTTCAGTACTGTGGAGGAATCAAACAAGTTTTATAAGGACAACATCAAGGCTGGACAGCAGGGCCTGAGTGTGGCATTCGATCTGGCCACACATCGCGGCTATGACTCAGATAATCCCAGAGTCAGGGGGGACGTGGGAATGGCAGGAGTCGCTATCGACACAGTGGAAGATACTAAGATTCTGTTCGATGGAATCCCTCTGGAGAAAATGTCTGTGAGTATGACAATGAACGGCGCTGTCATTCCCGTGCTGGCAAACTTCATCGTCACTGGCGAGGAACAGGGGGTGCCTAAGGAAAAACTGACCGGCACAATTCAGAACGACATCCTGAAGGAGTTCATGGTGCGGAATACTTACATTTTTCCCCCTGAACCATCCATGAAAATCATTGCCGATATCTTCGAGTACACCGCTAAGCACATGCCCAAGTTCAACTCAATTAGCATCTCCGGGTATCATATGCAGGAAGCAGGAGCCGACGCTATTCTGGAGCTGGCTTACACCCTGGCAGATGGCCTGGAATATTCTCGAACCGGACTGCAGGCAGGCCTGACAATCGACGAGTTCGCTCCTAGACTGAGTTTCTTTTGGGGAATTGGCATGAACTTTTACATGGAGATCGCCAAGATGAGGGCTGGCCGGAGACTGTGGGCACACCTGATCGAGAAGATGTTCCAGCCTAAGAACTCTAAGAGTCTGCTGCTGCGGGCCCATTGCCAGACATCCGGCTGGTCTCTGACTGAACAGGACCCATATAACAATATTGTCAGAACCGCAATCGAGGCAATGGCAGCCGTGTTCGGAGGAACCCAGAGCCTGCACACAAACTCCTTTGATGAGGCCCTGGGGCTGCCTACCGTGAAGTCTGCTAGGATTGCACGCAATACACAGATCATTATCCAGGAGGAATCCGGAATCCCAAAGGTGGCCGATCCCTGGGGAGGCTCTTACATGATGGAGTGCCTGACAAACGACGTGTATGATGCTGCACTGAAGCTGATTAATGAAATCGAGGAAATGGGGGGAATGGCAAAGGCCGTGGCTGAGGGCATTCCAAAACTGAGGATCGAGGAATGTGCAGCTAGGCGCCAGGCACGAATTGACTCAGGAAGCGAAGTGATCGTCGGGGTGAATAAGTACCAGCTGGAGAAAGAAGACGCAGTCGAAGTGCTGGCCATCGATAACACAAGCGTGCGCAATCGACAGATTGAGAAGCTGAAGAAAATCAAAAGCTCCCGCGATCAGGCACTGGCCGAACGATGCCTGGCAGCCCTGACTGAGTGTGCTGCAAGCGGGGACGGAAACATTCTGGCTCTGGCAGTCGATGCCTCCCGGGCTAGATGCACTGTGGGGGAAATCACCGACGCCCTGAAGAAAGTCTTCGGAGAGCACAAGGCCAATGATCGGATGGTGAGCGGCGCTTATAGACAGGAGTTCGGGGAATCTAAAGAGATTACCAGTGCCATCAAGAGGGTGCACAAGTTCATGGAGAGAGAAGGGCGACGGCCCAGGCTGCTGGTGGCAAAGATGGGACAGGACGGACATGATCGCGGAGCAAAAGTCATTGCCACCGGGTTCGCTGACCTGGGATTTGACGTGGATATCGGCCCTCTGTTCCAGACACCACGAGAGGTCGCACAGCAGGCAGTCGACGCTGATGTGCACGCAGTCGGAGTGTCCACTCTGGCAGCTGGCCATAAGACCCTGGTGCCTGAACTGATCAAAGAGCTGAACTCTCTGGGCAGACCAGACATCCTGGTCATGTGCGGCGGCGTGATCCCACCCCAGGATTACGAATTCCTGTTTGAGGTCGGGGTGAGCAACGTGTTCGGACCAGGAACCAGGATCCCTAAGGCCGCAGTGCAGGTCCTGGATGATATTGAAAAGTGTCTGGAAAAGAAACAGCAGTCAGTGTAAACACATCACAACCACAACCTTCTCAGGTAACTATACTTGGGACTTAAAAAACATAATCATAATCATTTTTCCTAAAACGATCAAGACTGATAACCATTTGACAAGAGCCATACAGACAAGCACCAGCTGGCACTCTTAGGTCTTCACGTATGGTCATCAGTTTGGGTTCCATTTGTAGATAAGAAACTGAACATATAAAGGTCTAGGTTAATGCAATTTACACAAAAGGAGACCAAACCAGGGAGAGAAGGAACCAAAATTAAAAATTCAAACCAGAGCAAAGGAGTTAGCCCTGGTTTTGCTCTGACTTACATGAACCACTATGTGGAGTCCTCCATGTTAGCCTAGTCAAGCTTATCCTCTGGATGAAGTTGAAACCATATGAAGGAATATTTGGGGGGTGGGTCAAAACAGTTGTGTATCAATGATTCCATGTGGTTTGACCCAATCATTCTGTGAATCCATTTCAACAGAAGATACAACGGGTTCTGTTTCATAATAAGTGATCCACTTCCAAATTTCTGATGTGCCCCATGCTAAGCTTTAACAGAATTTATCTTCTTATGACAAAGCAGCCTCCTTTGAAAATATAGCCAACTGCACACAGCTATGTTGATCAATTTTGTTTATAATCTTGCAGAAGAGAATTTTTTAAAATAGGGCAATAATGGAAGGCTTTGGCAAAAAAATTGTTTCTCCATATGAAAACAAAAAACTTATTTTTTTATTCAAGCAAAGAACCTATAGACATAAGGCTATTTCAAAATTATTTCAGTTTTAGAAAGAATTGAAAGTTTTGTAGCATTCTGAGAAGACAGCTTTCATTTGTAATCATAGGTAATATGTAGGTCCTCAGAAATGGTGAGACCCCTGACTTTGACACTTGGGGACTCTGAGGGACCAGTGATGAAGAGGGCACAACTTATATCACACATGCACGAGTTGGGGTGAGAGGGTGTCACAACATCTATCAGTGTGTCATCTGCCCACCAAGTAAatttaaatAGGAACCCCTAGTGATGGAGTTGGCCACTCCCTCTCTGCGCGCTCGCTCGCTCACTGAGGCCGCCCGGGCAAAGCCCGGGCGTCGGGCGACCTTTGGTCGCCCGGCCTCAGTGAGCGAGCGAGCGCGCAGAGAGGGAGTGGCCAA
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ:
<110> VENDITTI, Charles P.
CHANDLER, Randy J.
CHAU, B. Nelson
CHIANG, Kyle P.
LIAO, Jing
<120> НЕДЕСТРУКТИВНАЯ ГЕННАЯ ТЕРАПИЯ ДЛЯ ЛЕЧЕНИЯ MMA
<130> 2012538-0062
<150> 62/717,771
<151> 2018-08-10
<160> 19
<170> PatentIn version 3.5
<210> 1
<211> 737
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полипептид
<400> 1
Met Ala Ala Asp Gly Tyr Leu Pro Asp Trp Leu Glu Asp Thr Leu Ser
1 5 10 15
Glu Gly Ile Arg Gln Trp Trp Lys Leu Lys Pro Gly Pro Pro Pro Pro
20 25 30
Lys Pro Ala Glu Arg His Lys Asp Asp Ser Arg Gly Leu Val Leu Pro
35 40 45
Gly Tyr Lys Tyr Leu Gly Pro Phe Asn Gly Leu Asp Lys Gly Glu Pro
50 55 60
Val Asn Glu Ala Asp Ala Ala Ala Leu Glu His Asp Lys Ala Tyr Asp
65 70 75 80
Arg Gln Leu Asp Ser Gly Asp Asn Pro Tyr Leu Lys Tyr Asn His Ala
85 90 95
Asp Ala Glu Phe Gln Glu Arg Leu Lys Glu Asp Thr Ser Phe Gly Gly
100 105 110
Asn Leu Gly Arg Ala Val Phe Gln Ala Lys Lys Arg Leu Leu Glu Pro
115 120 125
Leu Gly Leu Val Glu Glu Ala Ala Lys Thr Ala Pro Gly Lys Lys Arg
130 135 140
Pro Val Glu His Ser Pro Val Glu Pro Asp Ser Ser Ser Gly Thr Gly
145 150 155 160
Lys Ala Gly Gln Gln Pro Ala Arg Lys Arg Leu Asn Phe Gly Gln Thr
165 170 175
Gly Asp Ala Asp Ser Val Pro Asp Pro Gln Pro Ile Gly Glu Pro Pro
180 185 190
Ala Ala Pro Ser Gly Val Gly Ser Leu Thr Met Ala Ala Gly Gly Gly
195 200 205
Ala Pro Met Ala Asp Asn Asn Glu Gly Ala Asp Gly Val Gly Asn Ser
210 215 220
Ser Gly Asn Trp His Cys Asp Ser Thr Trp Met Gly Asp Arg Val Ile
225 230 235 240
Thr Thr Ser Thr Arg Thr Trp Ala Leu Pro Thr Tyr Asn Asn His Leu
245 250 255
Tyr Lys Gln Ile Ser Asn Ser Thr Ser Gly Gly Ser Ser Asn Asp Asn
260 265 270
Ala Tyr Phe Gly Tyr Ser Thr Pro Trp Gly Tyr Phe Asp Phe Asn Arg
275 280 285
Phe His Cys His Phe Ser Pro Arg Asp Trp Gln Arg Leu Ile Asn Asn
290 295 300
Asn Trp Gly Phe Arg Pro Lys Arg Leu Ser Phe Lys Leu Phe Asn Ile
305 310 315 320
Gln Val Lys Glu Val Thr Gln Asn Glu Gly Thr Lys Thr Ile Ala Asn
325 330 335
Asn Leu Thr Ser Thr Ile Gln Val Phe Thr Asp Ser Glu Tyr Gln Leu
340 345 350
Pro Tyr Val Leu Gly Ser Ala His Gln Gly Cys Leu Pro Pro Phe Pro
355 360 365
Ala Asp Val Phe Met Ile Pro Gln Tyr Gly Tyr Leu Thr Leu Asn Asn
370 375 380
Gly Ser Gln Ala Val Gly Arg Ser Ser Phe Tyr Cys Leu Glu Tyr Phe
385 390 395 400
Pro Ser Gln Met Leu Lys Thr Gly Asn Asn Phe Gln Phe Thr Tyr Thr
405 410 415
Phe Glu Asp Val Pro Phe His Ser Ser Tyr Ala His Ser Gln Ser Leu
420 425 430
Asp Arg Leu Met Asn Pro Leu Ile Asp Gln Tyr Leu Tyr Tyr Leu Ser
435 440 445
Arg Thr Gln Thr Thr Gly Gly Thr Thr Asn Thr Gln Thr Leu Gly Phe
450 455 460
Ser Gln Gly Gly Pro Asn Thr Met Ala Asn Gln Ala Lys Asn Trp Leu
465 470 475 480
Pro Gly Pro Cys Tyr Arg Gln Gln Arg Val Ser Lys Thr Ser Ala Asp
485 490 495
Asn Asn Asn Ser Glu Tyr Ser Trp Thr Gly Ala Thr Lys Tyr His Leu
500 505 510
Asn Gly Arg Asp Ser Leu Val Asn Pro Gly Pro Ala Met Ala Ser His
515 520 525
Lys Asp Asp Glu Glu Lys Phe Phe Pro Gln Ser Gly Val Leu Ile Phe
530 535 540
Gly Lys Gln Gly Ser Glu Lys Thr Asn Val Asp Ile Glu Lys Val Met
545 550 555 560
Ile Thr Asp Glu Glu Glu Ile Arg Thr Thr Asn Pro Val Ala Thr Glu
565 570 575
Gln Tyr Gly Ser Val Ser Thr Asn Leu Gln Arg Gly Asn Arg Gln Ala
580 585 590
Ala Thr Ala Asp Val Asn Thr Gln Gly Val Leu Pro Gly Met Val Trp
595 600 605
Gln Asp Arg Asp Val Tyr Leu Gln Gly Pro Ile Trp Ala Lys Ile Pro
610 615 620
His Thr Asp Gly His Phe His Pro Ser Pro Leu Met Gly Gly Phe Gly
625 630 635 640
Leu Lys His Pro Pro Pro Gln Ile Leu Ile Lys Asn Thr Pro Val Pro
645 650 655
Ala Asp Pro Pro Thr Thr Phe Asn Gln Ser Lys Leu Asn Ser Phe Ile
660 665 670
Thr Gln Tyr Ser Thr Gly Gln Val Ser Val Glu Ile Glu Trp Glu Leu
675 680 685
Gln Lys Glu Asn Ser Lys Arg Trp Asn Pro Glu Ile Gln Tyr Thr Ser
690 695 700
Asn Tyr Tyr Lys Ser Thr Ser Val Asp Phe Ala Val Asn Thr Glu Gly
705 710 715 720
Val Tyr Ser Glu Pro Arg Pro Ile Gly Thr Arg Tyr Leu Thr Arg Asn
725 730 735
Leu
<210> 2
<211> 2215
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 2
atggctgccg atggttatct tccagattgg ctcgaggaca ctctctctga aggaataaga 60
cagtggtgga agctcaaacc tggcccacca ccaccaaagc ccgcagagcg gcataaggac 120
gacagcaggg gtcttgtgct tcctgggtac aagtacctcg gacccttcaa cggactcgac 180
aagggagagc cggtcaacga ggcagacgcc gcggccctcg agcacgacaa agcctacgac 240
cggcagctcg acagcggaga caacccgtac ctcaagtaca accacgccga cgccgagttc 300
caggagcggc tcaaagaaga tacgtctttt gggggcaacc tcgggcgagc agtcttccag 360
gccaaaaaga ggcttcttga acctcttggt ctggttgagg aagcggctaa gacggctcct 420
ggaaagaaga ggcctgtaga gcactctcct gtggagccag actcctcctc gggaaccgga 480
aaggcgggcc agcagcctgc aagaaaaaga ttgaattttg gtcagactgg agacgcagac 540
tcagtcccag accctcaacc aatcggagaa cctcccgcag ccccctcagg tgtgggatct 600
cttacaatgg ctgcaggcgg tggcgcacca atggcagaca ataacgaggg cgccgacgga 660
gtgggtaatt cctcgggaaa ttggcattgc gattccacat ggatgggcga cagagtcatc 720
accaccagca cccgaacctg ggccctgccc acctacaaca accacctcta caagcaaatc 780
tccaacagca catctggagg atcttcaaat gacaacgcct acttcggcta cagcaccccc 840
tgggggtatt ttgactttaa cagattccac tgccactttt caccacgtga ctggcagcga 900
ctcatcaaca acaactgggg attccggccc aagagactca gcttcaagct cttcaacatc 960
caggtcaagg aggtcacgca gaatgaaggc accaagacca tcgccaataa cctcaccagc 1020
accatccagg tgtttacgga ctcggagtac cagctgccgt acgttctcgg ctctgcccac 1080
cagggctgcc tgcctccgtt cccggcggac gtgttcatga ttccccagta cggctaccta 1140
acactcaaca acggtagtca ggccgtggga cgctcctcct tctactgcct ggaatacttt 1200
ccttcgcaga tgctgagaac cggcaacaac ttccagttta cttacacctt cgaggacgtg 1260
cctttccaca gcagctacgc ccacagccag agcttggacc ggctgatgaa tcctctgatt 1320
gaccagtacc tgtactactt gtctcggact caaacaacag gaggcacgac aaatacgcag 1380
actctgggct tcagccaagg tgggcctaat acaatggcca atcaggcaaa gaactggctg 1440
ccaggaccct gttaccgcca gcagcgagta tcaaagacat ctgcggataa caacaacagt 1500
gaatactcgt ggactggagc taccaagtac cacctcaatg gcagagactc tctggtgaat 1560
ccgggcccgg ccatggcaag ccacaaggac gatgaagaaa agtttttttc ctcagagcgg 1620
ggttctcatc tttgggaagc aaggctcaga gaaaacaaat gtggacattg aaaaggtcat 1680
gattacagac gaagaggaaa tcaggacaac caatcccgtg gctacggagc agtatggttc 1740
tgtatctacc aacctccaga gaggcaacag acaagcagct accgcagatg tcaacacaca 1800
aggcgttctt ccaggcatgg tctggcagga cagagatgtg taccttcagg ggcccatctg 1860
ggcaaagatt ccacacacgg acggacattt tcacccctct cccctcatgg gtggattcgg 1920
acttaaacac cctccgcctc agatcctgat caagaacacg cctgtacctg cggatcctcc 1980
gaccaccttc aaccagtcaa agctgaactc tttcatcacc cagtattcta ctggccaagt 2040
cagcgtggag atcgagtggg agctgcagaa ggaaaacagc aagcgctgga accccgagat 2100
ccagtacacc tccaactact acaaatctac aagtgtggac tttgctgtta atacagaagg 2160
cgtgtactct gaaccccgcc ccattggcac ccgttacctc acccgtaatc tgtaa 2215
<210> 3
<211> 735
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полипептид
<400> 3
Met Ala Ala Asp Gly Tyr Leu Pro Asp Trp Leu Glu Asp Thr Leu Ser
1 5 10 15
Glu Gly Ile Arg Gln Trp Trp Lys Leu Lys Pro Gly Pro Pro Pro Pro
20 25 30
Lys Pro Ala Glu Arg His Lys Asp Asp Ser Arg Gly Leu Val Leu Pro
35 40 45
Gly Tyr Lys Tyr Leu Gly Pro Phe Asn Gly Leu Asp Lys Gly Glu Pro
50 55 60
Val Asn Glu Ala Asp Ala Ala Ala Leu Glu His Asp Lys Ala Tyr Asp
65 70 75 80
Arg Gln Leu Asp Ser Gly Asp Asn Pro Tyr Leu Lys Tyr Asn His Ala
85 90 95
Asp Ala Glu Phe Gln Glu Arg Leu Lys Glu Asp Thr Ser Phe Gly Gly
100 105 110
Asn Leu Gly Arg Ala Val Phe Gln Ala Lys Lys Arg Val Leu Glu Pro
115 120 125
Leu Gly Leu Val Glu Glu Pro Val Lys Thr Ala Pro Gly Lys Lys Arg
130 135 140
Pro Val Glu His Ser Pro Val Glu Pro Asp Ser Ser Ser Gly Thr Gly
145 150 155 160
Lys Ala Gly Gln Gln Pro Ala Arg Lys Arg Leu Asn Phe Gly Gln Thr
165 170 175
Gly Asp Ala Asp Ser Val Pro Asp Pro Gln Pro Leu Gly Gln Pro Pro
180 185 190
Ala Ala Pro Ser Gly Leu Gly Thr Asn Thr Met Ala Thr Gly Ser Gly
195 200 205
Ala Pro Met Ala Asp Asn Asn Glu Gly Ala Asp Gly Val Gly Asn Ser
210 215 220
Ser Gly Asn Trp His Cys Asp Ser Thr Trp Met Gly Asp Arg Val Ile
225 230 235 240
Thr Thr Ser Thr Arg Thr Trp Ala Leu Pro Thr Tyr Asn Asn His Leu
245 250 255
Tyr Lys Gln Ile Ser Ser Gln Ser Gly Ala Ser Asn Asp Asn His Tyr
260 265 270
Phe Gly Tyr Ser Thr Pro Trp Gly Tyr Phe Asp Phe Asn Arg Phe His
275 280 285
Cys His Phe Ser Pro Arg Asp Trp Gln Arg Leu Ile Asn Asn Asn Trp
290 295 300
Gly Phe Arg Pro Lys Arg Leu Asn Phe Lys Leu Phe Asn Ile Gln Val
305 310 315 320
Lys Glu Val Thr Gln Asn Asp Gly Thr Thr Thr Ile Ala Asn Asn Leu
325 330 335
Thr Ser Thr Val Gln Val Phe Thr Asp Ser Glu Tyr Gln Leu Pro Tyr
340 345 350
Val Leu Gly Ser Ala His Gln Gly Cys Leu Pro Pro Phe Pro Ala Asp
355 360 365
Val Phe Met Val Pro Gln Tyr Gly Tyr Leu Thr Leu Asn Asn Gly Ser
370 375 380
Gln Ala Val Gly Arg Ser Ser Phe Tyr Cys Leu Glu Tyr Phe Pro Ser
385 390 395 400
Gln Met Leu Arg Thr Gly Asn Asn Phe Thr Phe Ser Tyr Thr Phe Glu
405 410 415
Asp Val Pro Phe His Ser Ser Tyr Ala His Ser Gln Ser Leu Asp Arg
420 425 430
Leu Met Asn Pro Leu Ile Asp Gln Tyr Leu Tyr Tyr Leu Ser Arg Thr
435 440 445
Asn Thr Pro Ser Gly Thr Thr Thr Gln Ser Arg Leu Gln Phe Ser Gln
450 455 460
Ala Gly Ala Ser Asp Ile Arg Asp Gln Ser Arg Asn Trp Leu Pro Gly
465 470 475 480
Pro Cys Tyr Arg Gln Gln Arg Val Ser Lys Thr Ser Ala Asp Asn Asn
485 490 495
Asn Ser Glu Tyr Ser Trp Thr Gly Ala Thr Lys Tyr His Leu Asn Gly
500 505 510
Arg Asp Ser Leu Val Asn Pro Gly Pro Ala Met Ala Ser His Lys Asp
515 520 525
Asp Glu Glu Lys Phe Phe Pro Gln Ser Gly Val Leu Ile Phe Gly Lys
530 535 540
Gln Gly Ser Glu Lys Thr Asn Val Asp Ile Glu Lys Val Met Ile Thr
545 550 555 560
Asp Glu Glu Glu Ile Arg Thr Thr Asn Pro Val Ala Thr Glu Gln Tyr
565 570 575
Gly Ser Val Ser Thr Asn Leu Gln Arg Gly Asn Arg Gln Ala Ala Thr
580 585 590
Ala Asp Val Asn Thr Gln Gly Val Leu Pro Gly Met Val Trp Gln Asp
595 600 605
Arg Asp Val Tyr Leu Gln Gly Pro Ile Trp Ala Lys Ile Pro His Thr
610 615 620
Asp Gly His Phe His Pro Ser Pro Leu Met Gly Gly Phe Gly Leu Lys
625 630 635 640
His Pro Pro Pro Gln Ile Leu Ile Lys Asn Thr Pro Val Pro Ala Asn
645 650 655
Pro Ser Thr Thr Phe Ser Ala Ala Lys Phe Ala Ser Phe Ile Thr Gln
660 665 670
Tyr Ser Thr Gly Gln Val Ser Val Glu Ile Glu Trp Glu Leu Gln Lys
675 680 685
Glu Asn Ser Lys Arg Trp Asn Pro Glu Ile Gln Tyr Thr Ser Asn Tyr
690 695 700
Asn Lys Ser Val Asn Arg Gly Leu Thr Val Asp Thr Asn Gly Val Tyr
705 710 715 720
Ser Glu Pro Arg Pro Ile Gly Thr Arg Tyr Leu Thr Arg Asn Leu
725 730 735
<210> 4
<211> 738
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полипептид
<400> 4
Met Ala Ala Asp Gly Tyr Leu Pro Asp Trp Leu Glu Asp Asn Leu Ser
1 5 10 15
Glu Gly Ile Arg Glu Trp Trp Ala Leu Lys Pro Gly Ala Pro Lys Pro
20 25 30
Lys Ala Asn Gln Gln Lys Gln Asp Asp Gly Arg Gly Leu Val Leu Pro
35 40 45
Gly Tyr Lys Tyr Leu Gly Pro Phe Asn Gly Leu Asp Lys Gly Glu Pro
50 55 60
Val Asn Ala Ala Asp Ala Ala Ala Leu Glu His Asp Lys Ala Tyr Asp
65 70 75 80
Gln Gln Leu Gln Ala Gly Asp Asn Pro Tyr Leu Arg Tyr Asn His Ala
85 90 95
Asp Ala Glu Phe Gln Glu Arg Leu Gln Glu Asp Thr Ser Phe Gly Gly
100 105 110
Asn Leu Gly Arg Ala Val Phe Gln Ala Lys Lys Arg Val Leu Glu Pro
115 120 125
Leu Gly Leu Val Glu Glu Gly Ala Lys Thr Ala Pro Gly Lys Lys Arg
130 135 140
Pro Val Glu Pro Ser Pro Gln Arg Ser Pro Asp Ser Ser Thr Gly Ile
145 150 155 160
Gly Lys Lys Gly Gln Gln Pro Ala Arg Lys Arg Leu Asn Phe Gly Gln
165 170 175
Thr Gly Asp Ser Glu Ser Val Pro Asp Pro Gln Pro Leu Gly Glu Pro
180 185 190
Pro Ala Ala Pro Ser Gly Val Gly Pro Asn Thr Met Ala Ala Gly Gly
195 200 205
Gly Ala Pro Met Ala Asp Asn Asn Glu Gly Ala Asp Gly Val Gly Ser
210 215 220
Ser Ser Gly Asn Trp His Cys Asp Ser Thr Trp Leu Gly Asp Arg Val
225 230 235 240
Ile Thr Thr Ser Thr Arg Thr Trp Ala Leu Pro Thr Tyr Asn Asn His
245 250 255
Leu Tyr Lys Gln Ile Ser Asn Gly Thr Ser Gly Gly Ala Thr Asn Asp
260 265 270
Asn Thr Tyr Phe Gly Tyr Ser Thr Pro Trp Gly Tyr Phe Asp Phe Asn
275 280 285
Arg Phe His Cys His Phe Ser Pro Arg Asp Trp Gln Arg Leu Ile Asn
290 295 300
Asn Asn Trp Gly Phe Arg Pro Lys Arg Leu Ser Phe Lys Leu Phe Asn
305 310 315 320
Ile Gln Val Lys Glu Val Thr Gln Asn Glu Gly Thr Lys Thr Ile Ala
325 330 335
Asn Asn Leu Thr Ser Thr Ile Gln Val Phe Thr Asp Ser Glu Tyr Gln
340 345 350
Leu Pro Tyr Val Leu Gly Ser Ala His Gln Gly Cys Leu Pro Pro Phe
355 360 365
Pro Ala Asp Val Phe Met Ile Pro Gln Tyr Gly Tyr Leu Thr Leu Asn
370 375 380
Asn Gly Ser Gln Ala Val Gly Arg Ser Ser Phe Tyr Cys Leu Glu Tyr
385 390 395 400
Phe Pro Ser Gln Met Leu Arg Thr Gly Asn Asn Phe Gln Phe Thr Tyr
405 410 415
Thr Phe Glu Asp Val Pro Phe His Ser Ser Tyr Ala His Ser Gln Ser
420 425 430
Leu Asp Arg Leu Met Asn Pro Leu Ile Asp Gln Tyr Leu Tyr Tyr Leu
435 440 445
Ser Arg Thr Gln Thr Thr Gly Gly Thr Ala Asn Thr Gln Thr Leu Gly
450 455 460
Phe Ser Gln Gly Gly Pro Asn Thr Met Ala Asn Gln Ala Lys Asn Trp
465 470 475 480
Leu Pro Gly Pro Cys Tyr Arg Gln Gln Arg Val Ser Thr Thr Thr Gly
485 490 495
Gln Asn Asn Asn Ser Asn Phe Ala Trp Thr Ala Gly Thr Lys Tyr His
500 505 510
Leu Asn Gly Arg Asn Ser Leu Ala Asn Pro Gly Ile Ala Met Ala Thr
515 520 525
His Lys Asp Asp Glu Glu Arg Phe Phe Pro Ser Asn Gly Ile Leu Ile
530 535 540
Phe Gly Lys Gln Asn Ala Ala Arg Asp Asn Ala Asp Tyr Ser Asp Val
545 550 555 560
Met Leu Thr Ser Glu Glu Glu Ile Lys Thr Thr Asn Pro Val Ala Thr
565 570 575
Glu Glu Tyr Gly Ile Val Ala Asp Asn Leu Gln Gln Gln Asn Thr Ala
580 585 590
Pro Gln Ile Gly Thr Val Asn Ser Gln Gly Ala Leu Pro Gly Met Val
595 600 605
Trp Gln Asn Arg Asp Val Tyr Leu Gln Gly Pro Ile Trp Ala Lys Ile
610 615 620
Pro His Thr Asp Gly Asn Phe His Pro Ser Pro Leu Met Gly Gly Phe
625 630 635 640
Gly Leu Lys His Pro Pro Pro Gln Ile Leu Ile Lys Asn Thr Pro Val
645 650 655
Pro Ala Asp Pro Pro Thr Thr Phe Asn Gln Ser Lys Leu Asn Ser Phe
660 665 670
Ile Thr Gln Tyr Ser Thr Gly Gln Val Ser Val Glu Ile Glu Trp Glu
675 680 685
Leu Gln Lys Glu Asn Ser Lys Arg Trp Asn Pro Glu Ile Gln Tyr Thr
690 695 700
Ser Asn Tyr Tyr Lys Ser Thr Ser Val Asp Phe Ala Val Asn Thr Glu
705 710 715 720
Gly Val Tyr Ser Glu Pro Arg Pro Ile Gly Thr Arg Tyr Leu Thr Arg
725 730 735
Asn Leu
<210> 5
<211> 2211
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 5
atggctgctg acggttatct tccagattgg ctcgaggaca acctttctga aggcattcga 60
gagtggtggg cgctgcaacc tggagcccct aaacccaagg caaatcaaca acatcaggac 120
aacgctcggg gtcttgtgct tccgggttac aaatacctcg gacccggcaa cggactcgac 180
aagggggaac ccgtcaacgc agcggacgcg gcagccctcg agcacgacaa ggcctacgac 240
cagcagctca aggccggtga caacccctac ctcaagtaca accacgccga cgccgagttc 300
caggagcggc tcaaagaaga tacgtctttt gggggcaacc tcgggcgagc agtcttccag 360
gccaaaaaga ggcttcttga acctcttggt ctggttgagg aagcggctaa gacggctcct 420
ggaaagaaga ggcctgtaga tcagtctcct caggaaccgg actcatcatc tggtgttggc 480
aaatcgggca aacagcctgc cagaaaaaga ctaaatttcg gtcagactgg cgactcagag 540
tcagtcccag accctcaacc tctcggagaa ccaccagcag cccccacaag tttgggatct 600
aatacaatgg cttcaggcgg tggcgcacca atggcagaca ataacgaggg tgccgatgga 660
gtgggtaatt cctcaggaaa ttggcattgc gattcccaat ggctgggcga cagagtcatc 720
accaccagca ccagaacctg ggccctgccc acttacaaca accatctcta caagcaaatc 780
tccagccaat caggagcttc aaacgacaac cactactttg gctacagcac cccttggggg 840
tattttgact ttaacagatt ccactgccac ttctcaccac gtgactggca gcgactcatt 900
aacaacaact ggggattccg gcccaagaaa ctcagcttca agctcttcaa catccaagtt 960
aaagaggtca cgcagaacga tggcacgacg actattgcca ataaccttac cagcacggtt 1020
caagtgttta cggactcgga gtatcagctc ccgtacgtgc tcgggtcggc gcaccaaggc 1080
tgtctcccgc cgtttccagc ggacgtcttc atggtccctc agtatggata cctcaccctg 1140
aacaacggaa gtcaagcggt gggacgctca tccttttact gcctggagta cttcccttcg 1200
cagatgctaa ggactggaaa taacttccaa ttcagctata ccttcgagga tgtacctttt 1260
cacagcagct acgctcacag ccagagtttg gatcgcttga tgaatcctct tattgatcag 1320
tatctgtact acctgaacag aacgcaagga acaacctctg gaacaaccaa ccaatcacgg 1380
ctgcttttta gccaggctgg gcctcagtct atgtctttgc aggccagaaa ttggctacct 1440
gggccctgct accggcaaca gagactttca aagactgcta acgacaacaa caacagtaac 1500
tttccttgga cagcggccag caaatatcat ctcaatggcc gcgactcgct ggtgaatcca 1560
ggaccagcta tggccagtca caaggacgat gaagaaaaat ttttccctat gcacggcaat 1620
ctaatatttg gcaaagaagg gacaacggca agtaacgcag aattagataa tgtaatgatt 1680
acggatgaag aagagattcg taccaccaat cctgtggcaa cagagcagta tggaactgtg 1740
gcaaataact tgcagagctc aaatacagct cccacgacta gaactgtcaa tgatcagggg 1800
gccttacctg gcatggtgtg gcaagatcgt gacgtgtacc ttcaaggacc tatctgggca 1860
aagattcctc acacggatgg acactttcat ccttctcctc tgatgggagg ctttggactg 1920
aaacatccgc ctcctcaaat catgatcaaa aatactccgg taccggcaaa tcctccgacg 1980
actttcagcc cggccaagtt tgcttcattt atcactcagt actccactgg acaggtcagc 2040
gtggaaattg agtgggagct acagaaagaa aacagcaaac gttggaatcc agagattcag 2100
tacacttcca actacaacaa gtctgttaat gtggacttta ctgtagacac taatggtgtt 2160
tatagtgaac ctcgccccat tggcacccgt taccttaccc gtcccctgta a 2211
<210> 6
<211> 736
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полипептид
<400> 6
Met Ala Ala Asp Gly Tyr Leu Pro Asp Trp Leu Glu Asp Asn Leu Ser
1 5 10 15
Glu Gly Ile Arg Glu Trp Trp Ala Leu Gln Pro Gly Ala Pro Lys Pro
20 25 30
Lys Ala Asn Gln Gln His Gln Asp Asn Ala Arg Gly Leu Val Leu Pro
35 40 45
Gly Tyr Lys Tyr Leu Gly Pro Gly Asn Gly Leu Asp Lys Gly Glu Pro
50 55 60
Val Asn Ala Ala Asp Ala Ala Ala Leu Glu His Asp Lys Ala Tyr Asp
65 70 75 80
Gln Gln Leu Lys Ala Gly Asp Asn Pro Tyr Leu Lys Tyr Asn His Ala
85 90 95
Asp Ala Glu Phe Gln Glu Arg Leu Lys Glu Asp Thr Ser Phe Gly Gly
100 105 110
Asn Leu Gly Arg Ala Val Phe Gln Ala Lys Lys Arg Leu Leu Glu Pro
115 120 125
Leu Gly Leu Val Glu Glu Ala Ala Lys Thr Ala Pro Gly Lys Lys Arg
130 135 140
Pro Val Asp Gln Ser Pro Gln Glu Pro Asp Ser Ser Ser Gly Val Gly
145 150 155 160
Lys Ser Gly Lys Gln Pro Ala Arg Lys Arg Leu Asn Phe Gly Gln Thr
165 170 175
Gly Asp Ser Glu Ser Val Pro Asp Pro Gln Pro Leu Gly Glu Pro Pro
180 185 190
Ala Ala Pro Thr Ser Leu Gly Ser Asn Thr Met Ala Ser Gly Gly Gly
195 200 205
Ala Pro Met Ala Asp Asn Asn Glu Gly Ala Asp Gly Val Gly Asn Ser
210 215 220
Ser Gly Asn Trp His Cys Asp Ser Gln Trp Leu Gly Asp Arg Val Ile
225 230 235 240
Thr Thr Ser Thr Arg Thr Trp Ala Leu Pro Thr Tyr Asn Asn His Leu
245 250 255
Tyr Lys Gln Ile Ser Ser Gln Ser Gly Ala Ser Asn Asp Asn His Tyr
260 265 270
Phe Gly Tyr Ser Thr Pro Trp Gly Tyr Phe Asp Phe Asn Arg Phe His
275 280 285
Cys His Phe Ser Pro Arg Asp Trp Gln Arg Leu Ile Asn Asn Asn Trp
290 295 300
Gly Phe Arg Pro Lys Lys Leu Ser Phe Lys Leu Phe Asn Ile Gln Val
305 310 315 320
Lys Glu Val Thr Gln Asn Asp Gly Thr Thr Thr Ile Ala Asn Asn Leu
325 330 335
Thr Ser Thr Val Gln Val Phe Thr Asp Ser Glu Tyr Gln Leu Pro Tyr
340 345 350
Val Leu Gly Ser Ala His Gln Gly Cys Leu Pro Pro Phe Pro Ala Asp
355 360 365
Val Phe Met Val Pro Gln Tyr Gly Tyr Leu Thr Leu Asn Asn Gly Ser
370 375 380
Gln Ala Val Gly Arg Ser Ser Phe Tyr Cys Leu Glu Tyr Phe Pro Ser
385 390 395 400
Gln Met Leu Arg Thr Gly Asn Asn Phe Gln Phe Ser Tyr Thr Phe Glu
405 410 415
Asp Val Pro Phe His Ser Ser Tyr Ala His Ser Gln Ser Leu Asp Arg
420 425 430
Leu Met Asn Pro Leu Ile Asp Gln Tyr Leu Tyr Tyr Leu Asn Arg Thr
435 440 445
Gln Gly Thr Thr Ser Gly Thr Thr Asn Gln Ser Arg Leu Leu Phe Ser
450 455 460
Gln Ala Gly Pro Gln Ser Met Ser Leu Gln Ala Arg Asn Trp Leu Pro
465 470 475 480
Gly Pro Cys Tyr Arg Gln Gln Arg Leu Ser Lys Thr Ala Asn Asp Asn
485 490 495
Asn Asn Ser Asn Phe Pro Trp Thr Ala Ala Ser Lys Tyr His Leu Asn
500 505 510
Gly Arg Asp Ser Leu Val Asn Pro Gly Pro Ala Met Ala Ser His Lys
515 520 525
Asp Asp Glu Glu Lys Phe Phe Pro Met His Gly Asn Leu Ile Phe Gly
530 535 540
Lys Glu Gly Thr Thr Ala Ser Asn Ala Glu Leu Asp Asn Val Met Ile
545 550 555 560
Thr Asp Glu Glu Glu Ile Arg Thr Thr Asn Pro Val Ala Thr Glu Gln
565 570 575
Tyr Gly Thr Val Ala Asn Asn Leu Gln Ser Ser Asn Thr Ala Pro Thr
580 585 590
Thr Arg Thr Val Asn Asp Gln Gly Ala Leu Pro Gly Met Val Trp Gln
595 600 605
Asp Arg Asp Val Tyr Leu Gln Gly Pro Ile Trp Ala Lys Ile Pro His
610 615 620
Thr Asp Gly His Phe His Pro Ser Pro Leu Met Gly Gly Phe Gly Leu
625 630 635 640
Lys His Pro Pro Pro Gln Ile Met Ile Lys Asn Thr Pro Val Pro Ala
645 650 655
Asn Pro Pro Thr Thr Phe Ser Pro Ala Lys Phe Ala Ser Phe Ile Thr
660 665 670
Gln Tyr Ser Thr Gly Gln Val Ser Val Glu Ile Glu Trp Glu Leu Gln
675 680 685
Lys Glu Asn Ser Lys Arg Trp Asn Pro Glu Ile Gln Tyr Thr Ser Asn
690 695 700
Tyr Asn Lys Ser Val Asn Val Asp Phe Thr Val Asp Thr Asn Gly Val
705 710 715 720
Tyr Ser Glu Pro Arg Pro Ile Gly Thr Arg Tyr Leu Thr Arg Pro Leu
725 730 735
<210> 7
<211> 2208
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 7
atggctgccg atggttatct tccagattgg ctcgaggaca ctctctctga aggaataaga 60
cagtggtgga agctcaaacc tggcccacca ccaccaaagc ccgcagagcg gcataaggac 120
gacagcaggg gtcttgtgct tcctgggtac aagtacctcg gacccttcaa cggactcgac 180
aagggagagc cggtcaacga ggcagacgcc gcggccctcg agcacgacaa agcctacgac 240
cggcagctcg acagcggaga caacccgtac ctcaagtaca accacgccga cgcggagttt 300
caggagcgcc ttaaagaaga tacgtctttt gggggcaacc tcggacgagc agtcttccag 360
gcgaaaaaga gggttcttga acctctgggc ctggttgagg aacctgttaa gacggctccg 420
ggaaaaaaga ggccggtaga gcactctcct gtggagccag actcctcctc gggaaccggc 480
aagacaggcc agcagcccgc taaaaagaga ctcaattttg gtcagactgg cgactcagag 540
tcagtcccag accctcaacc tctcggagaa ccaccagcag ccccctctgg tctgggaact 600
aatacgatgg ctacaggcag tggcgcacca atggcagaca ataacgaggg cgccgacgga 660
gtgggtaatt cctcgggaaa ttggcattgc gattccacat ggatgggcga cagagtcatc 720
accaccagca cccgaacctg ggccctgccc acctacaaca accatctcta caagcaaatc 780
tccagccaat caggagcttc aaacgacaac cactactttg gctacagcac cccttggggg 840
tattttgact ttaacagatt ccactgccac ttctcaccac gtgactggca gcgactcatt 900
aacaacaact ggggattccg gcccaagaaa ctcagcttca agctcttcaa catccaagtt 960
aaagaggtca cgcagaacga tggcacgacg actattgcca ataaccttac cagcacggtt 1020
caagtgttta ctgactcgga gtaccagctc ccgtacgtcc tcggctcggc gcatcaagga 1080
tgcctcccgc cgttcccagc agacgtcttc atggtgccac agtatggata cctcaccctg 1140
aacaacggga gtcaggcagt aggacgctct tcattttact gcctggagta ctttccttct 1200
cagatgctgc gtaccggaaa caactttacc ttcagctaca cttttgagga cgttcctttc 1260
cacagcagct acgctcacag ccagagtctg gaccgtctca tgaatcctct catcgaccag 1320
tacctgtatt acttgagcag aacaaacact ccaagtggaa ccaccacgca gtcaaggctt 1380
cagttttctc aggccggagc gagtgacatt cgggaccagt ctaggaactg gcttcctgga 1440
ccctgttacc gccagcagcg agtatcaaag acatctgcgg ataacaacaa cagtgaatac 1500
tcgtggactg gagctaccaa gtaccacctc aatggcagag actctctggt gaatccgggc 1560
ccggccatgg caagccacaa ggacgatgaa gaaaagtttt ttcctcagag cggggttctc 1620
atctttggga agcaaggctc agagaaaaca aatgtggaca ttgaaaaggt catgattaca 1680
gacgaagagg aaatcaggac aaccaatccc gtggctacgg agcagtatgg ttctgtatct 1740
accaacctcc agagaggcaa cagacaagca gctaccgcag atgtcgacac acaaggcgtt 1800
cttccaggca tggtctggca ggacagagat gtgtaccttc agggacccat ctgggcaaag 1860
attccacaca cggacggaca ttttcacccc tctcccctca tgggtggatt cggacttaaa 1920
caccctcctc cacagattct catcaagaac accccggtac ctgcgaatcc ttcgaccacc 1980
ttcagtgcgg caaagtttgc ttccttcatc acacagtact ccacgggaca ggtcagcgtg 2040
gagatcgagt gggagctgca gaaggaaaac agcaaacgct ggaatcccga aattcagtac 2100
acttccaact acaacaagtc tgttaatgtg gactttactg tggacactaa tggcgtgtat 2160
tcagagcctc gccccattgg caccagatac ctgactcgta atctgtaa 2208
<210> 8
<211> 735
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полипептид
<400> 8
Met Ala Ala Asp Gly Tyr Leu Pro Asp Trp Leu Glu Asp Thr Leu Ser
1 5 10 15
Glu Gly Ile Arg Gln Trp Trp Lys Leu Lys Pro Gly Pro Pro Pro Pro
20 25 30
Lys Pro Ala Glu Arg His Lys Asp Asp Ser Arg Gly Leu Val Leu Pro
35 40 45
Gly Tyr Lys Tyr Leu Gly Pro Phe Asn Gly Leu Asp Lys Gly Glu Pro
50 55 60
Val Asn Glu Ala Asp Ala Ala Ala Leu Glu His Asp Lys Ala Tyr Asp
65 70 75 80
Arg Gln Leu Asp Ser Gly Asp Asn Pro Tyr Leu Lys Tyr Asn His Ala
85 90 95
Asp Ala Glu Phe Gln Glu Arg Leu Lys Glu Asp Thr Ser Phe Gly Gly
100 105 110
Asn Leu Gly Arg Ala Val Phe Gln Ala Lys Lys Arg Val Leu Glu Pro
115 120 125
Leu Gly Leu Val Glu Glu Pro Val Lys Thr Ala Pro Gly Lys Lys Arg
130 135 140
Pro Val Glu His Ser Pro Val Glu Pro Asp Ser Ser Ser Gly Thr Gly
145 150 155 160
Lys Thr Gly Gln Gln Pro Ala Lys Lys Arg Leu Asn Phe Gly Gln Thr
165 170 175
Gly Asp Ser Glu Ser Val Pro Asp Pro Gln Pro Leu Gly Glu Pro Pro
180 185 190
Ala Ala Pro Ser Gly Leu Gly Thr Asn Thr Met Ala Thr Gly Ser Gly
195 200 205
Ala Pro Met Ala Asp Asn Asn Glu Gly Ala Asp Gly Val Gly Asn Ser
210 215 220
Ser Gly Asn Trp His Cys Asp Ser Thr Trp Met Gly Asp Arg Val Ile
225 230 235 240
Thr Thr Ser Thr Arg Thr Trp Ala Leu Pro Thr Tyr Asn Asn His Leu
245 250 255
Tyr Lys Gln Ile Ser Ser Gln Ser Gly Ala Ser Asn Asp Asn His Tyr
260 265 270
Phe Gly Tyr Ser Thr Pro Trp Gly Tyr Phe Asp Phe Asn Arg Phe His
275 280 285
Cys His Phe Ser Pro Arg Asp Trp Gln Arg Leu Ile Asn Asn Asn Trp
290 295 300
Gly Phe Arg Pro Lys Lys Leu Ser Phe Lys Leu Phe Asn Ile Gln Val
305 310 315 320
Lys Glu Val Thr Gln Asn Asp Gly Thr Thr Thr Ile Ala Asn Asn Leu
325 330 335
Thr Ser Thr Val Gln Val Phe Thr Asp Ser Glu Tyr Gln Leu Pro Tyr
340 345 350
Val Leu Gly Ser Ala His Gln Gly Cys Leu Pro Pro Phe Pro Ala Asp
355 360 365
Val Phe Met Val Pro Gln Tyr Gly Tyr Leu Thr Leu Asn Asn Gly Ser
370 375 380
Gln Ala Val Gly Arg Ser Ser Phe Tyr Cys Leu Glu Tyr Phe Pro Ser
385 390 395 400
Gln Met Leu Arg Thr Gly Asn Asn Phe Thr Phe Ser Tyr Thr Phe Glu
405 410 415
Asp Val Pro Phe His Ser Ser Tyr Ala His Ser Gln Ser Leu Asp Arg
420 425 430
Leu Met Asn Pro Leu Ile Asp Gln Tyr Leu Tyr Tyr Leu Ser Arg Thr
435 440 445
Asn Thr Pro Ser Gly Thr Thr Thr Gln Ser Arg Leu Gln Phe Ser Gln
450 455 460
Ala Gly Ala Ser Asp Ile Arg Asp Gln Ser Arg Asn Trp Leu Pro Gly
465 470 475 480
Pro Cys Tyr Arg Gln Gln Arg Val Ser Lys Thr Ser Ala Asp Asn Asn
485 490 495
Asn Ser Glu Tyr Ser Trp Thr Gly Ala Thr Lys Tyr His Leu Asn Gly
500 505 510
Arg Asp Ser Leu Val Asn Pro Gly Pro Ala Met Ala Ser His Lys Asp
515 520 525
Asp Glu Glu Lys Phe Phe Pro Gln Ser Gly Val Leu Ile Phe Gly Lys
530 535 540
Gln Gly Ser Glu Lys Thr Asn Val Asp Ile Glu Lys Val Met Ile Thr
545 550 555 560
Asp Glu Glu Glu Ile Arg Thr Thr Asn Pro Val Ala Thr Glu Gln Tyr
565 570 575
Gly Ser Val Ser Thr Asn Leu Gln Arg Gly Asn Arg Gln Ala Ala Thr
580 585 590
Ala Asp Val Asp Thr Gln Gly Val Leu Pro Gly Met Val Trp Gln Asp
595 600 605
Arg Asp Val Tyr Leu Gln Gly Pro Ile Trp Ala Lys Ile Pro His Thr
610 615 620
Asp Gly His Phe His Pro Ser Pro Leu Met Gly Gly Phe Gly Leu Lys
625 630 635 640
His Pro Pro Pro Gln Ile Leu Ile Lys Asn Thr Pro Val Pro Ala Asn
645 650 655
Pro Ser Thr Thr Phe Ser Ala Ala Lys Phe Ala Ser Phe Ile Thr Gln
660 665 670
Tyr Ser Thr Gly Gln Val Ser Val Glu Ile Glu Trp Glu Leu Gln Lys
675 680 685
Glu Asn Ser Lys Arg Trp Asn Pro Glu Ile Gln Tyr Thr Ser Asn Tyr
690 695 700
Asn Lys Ser Val Asn Val Asp Phe Thr Val Asp Thr Asn Gly Val Tyr
705 710 715 720
Ser Glu Pro Arg Pro Ile Gly Thr Arg Tyr Leu Thr Arg Asn Leu
725 730 735
<210> 9
<211> 2253
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 9
atgctgagag ccaaaaacca gctgttcctg ctgagccccc actatctgag acaggtcaaa 60
gaaagttccg ggagtagact gatccagcag agactgctgc accagcagca gccactgcat 120
cctgagtggg ccgctctggc caagaaacag ctgaagggca aaaacccaga agacctgatc 180
tggcacactc cagaggggat ttcaatcaag cccctgtaca gcaaaaggga cactatggat 240
ctgccagagg aactgccagg agtgaagcct ttcacccgcg gaccttaccc aactatgtat 300
acctttcgac cctggacaat tcggcagtac gccggcttca gtactgtgga ggaatcaaac 360
aagttttata aggacaacat caaggctgga cagcagggcc tgagtgtggc attcgatctg 420
gccacacatc gcggctatga ctcagataat cccagagtca ggggggacgt gggaatggca 480
ggagtcgcta tcgacacagt ggaagatact aagattctgt tcgatggaat ccctctggag 540
aaaatgtctg tgagtatgac aatgaacggc gctgtcattc ccgtgctggc aaacttcatc 600
gtcactggcg aggaacaggg ggtgcctaag gaaaaactga ccggcacaat tcagaacgac 660
atcctgaagg agttcatggt gcggaatact tacatttttc cccctgaacc atccatgaaa 720
atcattgccg atatcttcga gtacaccgct aagcacatgc ccaagttcaa ctcaattagc 780
atctccgggt atcatatgca ggaagcagga gccgacgcta ttctggagct ggcttacacc 840
ctggcagatg gcctggaata ttctcgaacc ggactgcagg caggcctgac aatcgacgag 900
ttcgctccta gactgagttt cttttgggga attggcatga acttttacat ggagatcgcc 960
aagatgaggg ctggccggag actgtgggca cacctgatcg agaagatgtt ccagcctaag 1020
aactctaaga gtctgctgct gcgggcccat tgccagacat ccggctggtc tctgactgaa 1080
caggacccat ataacaatat tgtcagaacc gcaatcgagg caatggcagc cgtgttcgga 1140
ggaacccaga gcctgcacac aaactccttt gatgaggccc tggggctgcc taccgtgaag 1200
tctgctagga ttgcacgcaa tacacagatc attatccagg aggaatccgg aatcccaaag 1260
gtggccgatc cctggggagg ctcttacatg atggagtgcc tgacaaacga cgtgtatgat 1320
gctgcactga agctgattaa tgaaatcgag gaaatggggg gaatggcaaa ggccgtggct 1380
gagggcattc caaaactgag gatcgaggaa tgtgcagcta ggcgccaggc acgaattgac 1440
tcaggaagcg aagtgatcgt cggggtgaat aagtaccagc tggagaaaga agacgcagtc 1500
gaagtgctgg ccatcgataa cacaagcgtg cgcaatcgac agattgagaa gctgaagaaa 1560
atcaaaagct cccgcgatca ggcactggcc gaacgatgcc tggcagccct gactgagtgt 1620
gctgcaagcg gggacggaaa cattctggct ctggcagtcg atgcctcccg ggctagatgc 1680
actgtggggg aaatcaccga cgccctgaag aaagtcttcg gagagcacaa ggccaatgat 1740
cggatggtga gcggcgctta tagacaggag ttcggggaat ctaaagagat taccagtgcc 1800
atcaagaggg tgcacaagtt catggagaga gaagggcgac ggcccaggct gctggtggca 1860
aagatgggac aggacggaca tgatcgcgga gcaaaagtca ttgccaccgg gttcgctgac 1920
ctgggatttg acgtggatat cggccctctg ttccagacac cacgagaggt cgcacagcag 1980
gcagtcgacg ctgatgtgca cgcagtcgga gtgtccactc tggcagctgg ccataagacc 2040
ctggtgcctg aactgatcaa agagctgaac tctctgggca gaccagacat cctggtcatg 2100
tgcggcggcg tgatcccacc ccaggattac gaattcctgt ttgaggtcgg ggtgagcaac 2160
gtgttcggac caggaaccag gatccctaag gccgcagtgc aggtcctgga tgatattgaa 2220
aagtgtctgg aaaagaaaca gcagtcagtg taa 2253
<210> 10
<211> 750
<212> БЕЛОК
<213> Homo sapiens
<400> 10
Met Leu Arg Ala Lys Asn Gln Leu Phe Leu Leu Ser Pro His Tyr Leu
1 5 10 15
Arg Gln Val Lys Glu Ser Ser Gly Ser Arg Leu Ile Gln Gln Arg Leu
20 25 30
Leu His Gln Gln Gln Pro Leu His Pro Glu Trp Ala Ala Leu Ala Lys
35 40 45
Lys Gln Leu Lys Gly Lys Asn Pro Glu Asp Leu Ile Trp His Thr Pro
50 55 60
Glu Gly Ile Ser Ile Lys Pro Leu Tyr Ser Lys Arg Asp Thr Met Asp
65 70 75 80
Leu Pro Glu Glu Leu Pro Gly Val Lys Pro Phe Thr Arg Gly Pro Tyr
85 90 95
Pro Thr Met Tyr Thr Phe Arg Pro Trp Thr Ile Arg Gln Tyr Ala Gly
100 105 110
Phe Ser Thr Val Glu Glu Ser Asn Lys Phe Tyr Lys Asp Asn Ile Lys
115 120 125
Ala Gly Gln Gln Gly Leu Ser Val Ala Phe Asp Leu Ala Thr His Arg
130 135 140
Gly Tyr Asp Ser Asp Asn Pro Arg Val Arg Gly Asp Val Gly Met Ala
145 150 155 160
Gly Val Ala Ile Asp Thr Val Glu Asp Thr Lys Ile Leu Phe Asp Gly
165 170 175
Ile Pro Leu Glu Lys Met Ser Val Ser Met Thr Met Asn Gly Ala Val
180 185 190
Ile Pro Val Leu Ala Asn Phe Ile Val Thr Gly Glu Glu Gln Gly Val
195 200 205
Pro Lys Glu Lys Leu Thr Gly Thr Ile Gln Asn Asp Ile Leu Lys Glu
210 215 220
Phe Met Val Arg Asn Thr Tyr Ile Phe Pro Pro Glu Pro Ser Met Lys
225 230 235 240
Ile Ile Ala Asp Ile Phe Glu Tyr Thr Ala Lys His Met Pro Lys Phe
245 250 255
Asn Ser Ile Ser Ile Ser Gly Tyr His Met Gln Glu Ala Gly Ala Asp
260 265 270
Ala Ile Leu Glu Leu Ala Tyr Thr Leu Ala Asp Gly Leu Glu Tyr Ser
275 280 285
Arg Thr Gly Leu Gln Ala Gly Leu Thr Ile Asp Glu Phe Ala Pro Arg
290 295 300
Leu Ser Phe Phe Trp Gly Ile Gly Met Asn Phe Tyr Met Glu Ile Ala
305 310 315 320
Lys Met Arg Ala Gly Arg Arg Leu Trp Ala His Leu Ile Glu Lys Met
325 330 335
Phe Gln Pro Lys Asn Ser Lys Ser Leu Leu Leu Arg Ala His Cys Gln
340 345 350
Thr Ser Gly Trp Ser Leu Thr Glu Gln Asp Pro Tyr Asn Asn Ile Val
355 360 365
Arg Thr Ala Ile Glu Ala Met Ala Ala Val Phe Gly Gly Thr Gln Ser
370 375 380
Leu His Thr Asn Ser Phe Asp Glu Ala Leu Gly Leu Pro Thr Val Lys
385 390 395 400
Ser Ala Arg Ile Ala Arg Asn Thr Gln Ile Ile Ile Gln Glu Glu Ser
405 410 415
Gly Ile Pro Lys Val Ala Asp Pro Trp Gly Gly Ser Tyr Met Met Glu
420 425 430
Cys Leu Thr Asn Asp Val Tyr Asp Ala Ala Leu Lys Leu Ile Asn Glu
435 440 445
Ile Glu Glu Met Gly Gly Met Ala Lys Ala Val Ala Glu Gly Ile Pro
450 455 460
Lys Leu Arg Ile Glu Glu Cys Ala Ala Arg Arg Gln Ala Arg Ile Asp
465 470 475 480
Ser Gly Ser Glu Val Ile Val Gly Val Asn Lys Tyr Gln Leu Glu Lys
485 490 495
Glu Asp Ala Val Glu Val Leu Ala Ile Asp Asn Thr Ser Val Arg Asn
500 505 510
Arg Gln Ile Glu Lys Leu Lys Lys Ile Lys Ser Ser Arg Asp Gln Ala
515 520 525
Leu Ala Glu His Cys Leu Ala Ala Leu Thr Glu Cys Ala Ala Ser Gly
530 535 540
Asp Gly Asn Ile Leu Ala Leu Ala Val Asp Ala Ser Arg Ala Arg Cys
545 550 555 560
Thr Val Gly Glu Ile Thr Asp Ala Leu Lys Lys Val Phe Gly Glu His
565 570 575
Lys Ala Asn Asp Arg Met Val Ser Gly Ala Tyr Arg Gln Glu Phe Gly
580 585 590
Glu Ser Lys Glu Ile Thr Ser Ala Ile Lys Arg Val His Lys Phe Met
595 600 605
Glu Arg Glu Gly Arg Arg Pro Arg Leu Leu Val Ala Lys Met Gly Gln
610 615 620
Asp Gly His Asp Arg Gly Ala Lys Val Ile Ala Thr Gly Phe Ala Asp
625 630 635 640
Leu Gly Phe Asp Val Asp Ile Gly Pro Leu Phe Gln Thr Pro Arg Glu
645 650 655
Val Ala Gln Gln Ala Val Asp Ala Asp Val His Ala Val Gly Val Ser
660 665 670
Thr Leu Ala Ala Gly His Lys Thr Leu Val Pro Glu Leu Ile Lys Glu
675 680 685
Leu Asn Ser Leu Gly Arg Pro Asp Ile Leu Val Met Cys Gly Gly Val
690 695 700
Ile Pro Pro Gln Asp Tyr Glu Phe Leu Phe Glu Val Gly Val Ser Asn
705 710 715 720
Val Phe Gly Pro Gly Thr Arg Ile Pro Lys Ala Ala Val Gln Val Leu
725 730 735
Asp Asp Ile Glu Lys Cys Leu Glu Lys Lys Gln Gln Ser Val
740 745 750
<210> 11
<211> 2253
<212> ДНК
<213> Homo sapiens
<400> 11
atgttaagag ctaagaatca gcttttttta ctttcacctc attacctgag gcaggtaaaa 60
gaatcatcag gctccaggct catacagcaa cgacttctac accagcaaca gccccttcac 120
ccagaatggg ctgccctggc taaaaagcag ctgaaaggca aaaacccaga agacctaata 180
tggcacaccc cggaagggat ctctataaaa cccttgtatt ccaagagaga tactatggac 240
ttacctgaag aacttccagg agtgaagcca ttcacacgtg gaccatatcc taccatgtat 300
acctttaggc cctggaccat ccgccagtat gctggtttta gtactgtgga agaaagcaat 360
aagttctata aggacaacat taaggctggt cagcagggat tatcagttgc ctttgatctg 420
gcgacacatc gtggctatga ttcagacaac cctcgagttc gtggtgatgt tggaatggct 480
ggagttgcta ttgacactgt ggaagatacc aaaattcttt ttgatggaat tcctttagaa 540
aaaatgtcag tttccatgac tatgaatgga gcagttattc cagttcttgc aaattttata 600
gtaactggag aagaacaagg tgtacctaaa gagaagctta ctggtaccat ccaaaatgat 660
atactaaagg aatttatggt tcgaaataca tacatttttc ctccagaacc atccatgaaa 720
attattgctg acatatttga atatacagca aagcacatgc caaaatttaa ttcaatttca 780
attagtggat accatatgca ggaagcaggg gctgatgcca ttctggagct ggcctatact 840
ttagcagatg gattggagta ctctagaact ggactccagg ctggcctgac aattgatgaa 900
tttgcaccaa ggttgtcttt cttctgggga attggaatga atttctatat ggaaatagca 960
aagatgagag ctggtagaag actctgggct cacttaatag agaaaatgtt tcagcctaaa 1020
aactcaaaat ctcttcttct aagagcacac tgtcagacat ctggatggtc acttactgag 1080
caggatccct acaataatat tgtccgtact gcaatagaag caatggcagc agtatttgga 1140
gggactcagt ctttgcacac aaattctttt gatgaagctt tgggtttgcc aactgtgaaa 1200
agtgctcgaa ttgccaggaa cacacaaatc atcattcaag aagaatctgg gattcccaaa 1260
gtggctgatc cttggggagg ttcttacatg atggaatgtc tcacaaatga tgtttatgat 1320
gctgctttaa agctcattaa tgaaattgaa gaaatgggtg gaatggccaa agctgtagct 1380
gagggaatac ctaaacttcg aattgaagaa tgtgctgccc gaagacaagc tagaatagat 1440
tctggttctg aagtaattgt tggagtaaat aagtaccagt tggaaaaaga agacgctgta 1500
gaagttctgg caattgataa tacttcagtg cgaaacaggc agattgaaaa acttaagaag 1560
atcaaatcca gcagggatca agctttggct gaacgttgtc ttgctgcact aaccgaatgt 1620
gctgctagcg gagatggaaa tatcctggct cttgcagtgg atgcatctcg ggcaagatgt 1680
acagtgggag aaatcacaga tgccctgaaa aaggtatttg gtgaacataa agcgaatgat 1740
cgaatggtga gtggagcata tcgccaggaa tttggagaaa gtaaagagat aacatctgct 1800
atcaagaggg ttcataaatt catggaacgt gaaggtcgca gacctcgtct tcttgtagca 1860
aaaatgggac aagatggcca tgacagagga gcaaaagtta ttgctacagg atttgctgat 1920
cttggttttg atgtggacat aggccctctt ttccagactc ctcgtgaagt ggcccagcag 1980
gctgtggatg cggatgtgca tgctgtgggc ataagcaccc tcgctgctgg tcataaaacc 2040
ctagttcctg aactcatcaa agaacttaac tcccttggac ggccagatat tcttgtcatg 2100
tgtggagggg tgataccacc tcaggattat gaatttctgt ttgaagttgg tgtttccaat 2160
gtatttggtc ctgggactcg aattccaaag gctgccgttc aggtgcttga tgatattgag 2220
aagtgtttgg aaaagaagca gcaatctgta taa 2253
<210> 12
<211> 2253
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 12
atgctgcgag cgaaaaatca gctttttctg ttgagcccac actacctgag gcaggttaaa 60
gaatccagcg ggagccggct gattcagcag cgactgctcc accagcagca gcctttgcat 120
cccgaatggg ctgctttggc gaagaagcag ctcaagggga agaaccctga agatcttatt 180
tggcacaccc cagagggcat cagcatcaag cctttgtatt ccaaaaggga caccatggat 240
ctgcctgaag aattgcccgg ggtcaaacca ttcacacggg ggccatatcc aaccatgtac 300
accttccggc catggactat cagacagtat gcaggcttta gcactgtcga ggaatccaat 360
aagttctata aagacaatat caaagctggc cagcaaggtc tgtccgtggc attcgatctg 420
gctacacata gaggttatga ttctgacaat ccaagagtac ggggagacgt cggaatggcg 480
ggagttgcca ttgacacagt ggaggacacc aagatacttt tcgatgggat tccattggag 540
aaaatgtctg tgtcaatgac gatgaacggc gctgtgattc ccgttttggc gaacttcatc 600
gtcaccgggg aagagcaggg cgtcccgaag gaaaagctca ccgggacaat ccaaaacgac 660
attcttaaag aattcatggt gagaaatacc tacatctttc ctcctgagcc ttccatgaag 720
atcatcgcgg acatctttga atacacggct aaacacatgc ctaaatttaa ctcaatcagc 780
ataagcgggt accacatgca ggaggccggc gctgacgcta tacttgagct cgcatatacc 840
ctggcagatg gactggaata ctcaaggacc gggctccagg ctggactgac aatcgacgag 900
tttgcccccc gactcagttt tttctggggt atcgggatga atttctacat ggagatagcg 960
aagatgaggg cgggcagacg gctttgggcg catctgatcg agaaaatgtt ccagcccaag 1020
aattcaaaga gtctgctgct gagagcccac tgccagacct caggctggag cctgactgaa 1080
caggacccat acaacaacat tgttagaacc gccatcgagg cgatggcagc ggttttcggt 1140
gggacacagt cattgcacac taactcattt gacgaagccc tcggtctgcc taccgtgaag 1200
tcagctcgga tcgctaggaa cacacagatc atcatccagg aggagagtgg catcccaaaa 1260
gtcgccgatc cttggggagg aagttacatg atggaatgcc tcacgaatga cgtatacgat 1320
gccgcactca agctgattaa cgagatcgag gaaatgggag gcatggcaaa agctgtcgcc 1380
gagggcattc caaagctgcg catagaggag tgtgccgccc gaagacaggc ccgcattgac 1440
tccggctctg aggtgatagt gggcgttaat aaatatcagc tagagaagga agacgccgtc 1500
gaagttctgg cgatagataa tacctctgtg cgaaatagac agattgagaa actgaagaag 1560
atcaagtcaa gccgagacca ggccttggcc gagaggtgtc tggcagccct cactgagtgc 1620
gcggcatctg gggacggcaa catattggca cttgccgtcg atgcctccag ggcccgatgt 1680
acggtcggcg aaattaccga tgccctcaag aaggtttttg gcgagcacaa ggctaacgac 1740
aggatggtta gtggagcata cagacaggag tttggcgaaa gcaaggaaat tacttccgcg 1800
attaaaagag tgcacaaatt catggaacgg gagggtaggc gaccgaggct cctcgttgcc 1860
aaaatgggtc aggacggcca cgaccggggc gccaaggtta tcgctaccgg tttcgctgac 1920
ctgggcttcg atgtggatat cggaccactg tttcaaaccc ccagagaagt tgcccaacaa 1980
gccgttgacg ctgacgtaca cgctgtaggc atctccactc tcgccgccgg gcataagact 2040
ctcgtcccag agctgataaa ggagcttaac agcctcggaa gacccgacat cctggttatg 2100
tgcggtggag tgattccgcc gcaggattac gaattcctct tcgaagtagg agtgtcaaac 2160
gtgttcggcc caggcactcg gatacccaag gctgccgttc aggtgcttga cgacattgaa 2220
aaatgtctgg agaagaagca acaatctgta taa 2253
<210> 13
<211> 2253
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 13
atgttgaggg ctaaaaacca gctctttctg ttgagtccac actaccttag gcaagtgaag 60
gaatctagcg gtagcaggct gatccagcag cgcctgctgc accagcagca gcccctgcac 120
cctgagtggg ctgcattggc aaagaaacaa ctgaagggta aaaatcctga agatctgatt 180
tggcacacac cggaggggat ttccataaaa cctctctact ctaaacgcga tactatggat 240
ctgcccgagg aattgccagg agtgaaaccc tttacaaggg ggccctaccc cactatgtac 300
acgttcagac cctggactat acgccagtat gccggatttt ctaccgttga ggaatccaac 360
aagttttata aggacaacat caaagccggg cagcagggac tgtcagtggc atttgatctc 420
gccacccacc gcgggtacga ctccgacaac ccaagagtcc gcggtgacgt cggcatggca 480
ggggttgcca ttgacacagt agaggatact aaaattttgt ttgatgggat ccccctagag 540
aagatgtccg tgtctatgac gatgaacggc gcggtaatcc cagtgcttgc caacttcata 600
gtcacagggg aagagcaggg cgtaccaaag gagaagctca caggaacaat ccaaaatgac 660
attctgaagg aattcatggt gagaaatact tatatctttc ctcccgagcc ctctatgaag 720
attattgccg acatttttga atacaccgca aaacatatgc ccaagttcaa ttccatatct 780
attagtggat accacatgca agaagctggg gctgatgcaa tacttgagct tgcctacacc 840
ctggccgacg gactggagta ttctcgcact ggcctgcaag ccgggctgac aattgacgag 900
ttcgccccac gccttagctt cttctggggc atcggcatga atttctatat ggagatcgca 960
aagatgagag cagggcggcg cttgtgggcc catctgatcg aaaagatgtt tcagcctaag 1020
aatagtaaga gcctgctcct gcgggctcac tgtcagacgt caggctggag cctcacagag 1080
caggatcctt acaataacat cgtccggact gctattgagg cgatggctgc agtattcgga 1140
ggaacacaaa gcctgcacac taattctttc gatgaggctt tggggctccc taccgtgaag 1200
tcagccagaa ttgcaagaaa cacccaaata atcatccaag aagaatcagg gatcccaaaa 1260
gttgccgacc cctggggagg aagttatatg atggagtgcc tgaccaatga cgtctacgac 1320
gccgctttga agctgattaa cgagattgaa gagatgggcg gaatggccaa ggcggtcgct 1380
gagggcattc cgaaactgcg catagaggag tgtgctgctc gcaggcaggc cagaattgat 1440
tccggttccg aagtgatcgt gggggttaat aagtatcaac tggaaaaaga ggacgctgtc 1500
gaagtcctcg caatcgataa taccagcgtt agaaaccgac aaattgagaa gctgaaaaag 1560
atcaaaagtt caagggacca ggccttggct gagcggtgtc tcgccgcact gaccgaatgt 1620
gccgccagcg gcgatggtaa catcctcgcc ctcgctgtgg acgcttccag agcccggtgc 1680
accgtgggcg aaattacgga cgcgctgaaa aaagtctttg gcgaacacaa ggccaatgat 1740
agaatggtga gtggcgccta taggcaggag ttcggcgaga gtaaagaaat aacatccgcc 1800
atcaagaggg tccacaaatt tatggagcgg gaaggacgca gacctagact tctcgtggcc 1860
aaaatgggtc aggacggtca tgaccgggga gccaaagtca tcgcaacggg cttcgccgat 1920
ttggggtttg acgtggatat cggtcccttg tttcaaaccc ccagggaggt ggctcagcag 1980
gctgtggacg ctgacgtcca cgcagtgggc atttctacac tggcagccgg gcacaagacg 2040
ttggtgccag aactgatcaa agagttgaac agcctgggac gccctgacat cctggtaatg 2100
tgcggtgggg taatcccccc ccaagactac gagttccttt tcgaagtggg tgtttctaac 2160
gtgttcggac ctggaacaag aatccctaag gcggcagtgc aggtgcttga cgatatcgag 2220
aagtgcctgg agaaaaagca acaatccgtt taa 2253
<210> 14
<211> 2253
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 14
atgcttcgcg ccaagaacca actgttcctg ctgtcccccc actacctccg acaagtcaag 60
gagagctcgg gaagccgcct gattcagcag cggctgctgc accagcagca gcccctgcat 120
ccggaatggg cagcgttggc aaagaagcag ctgaagggaa agaaccctga ggacctgatc 180
tggcacaccc cggagggaat ctcgatcaag ccactgtact ccaaaaggga caccatggac 240
ttgcctgaag aacttccggg cgtgaagcct tttacccggg ggccataccc aacaatgtac 300
actttccgcc cctggaccat cagacagtac gccggtttct ccaccgtcga agaatccaac 360
aagttctata aggacaacat caaggccggg cagcagggac tgagcgtcgc gtttgacctg 420
gcaacccatc gcggctacga ctccgacaac cctcgcgtgc ggggggacgt gggaatggcc 480
ggagtggcta tcgacaccgt ggaggacacc aagattctct tcgacggaat cccgctggaa 540
aagatgtcgg tgtccatgac catgaatggc gccgtgatcc cggtgctcgc gaacttcatc 600
gtgacgggag aggaacaggg agtgccgaaa gagaagctga ccgggactat tcagaatgac 660
atcctcaagg agttcatggt ccgcaacact tacattttcc ctcctgaacc ctcgatgaag 720
atcatcgctg acatcttcga gtacaccgcg aagcacatgc cgaagttcaa ctcgatctcc 780
atctcgggct accacatgca ggaggccggg gccgacgcca ttctcgaact ggcgtacact 840
ctggcggatg gtctggaata ctcacgcacc ggactgcagg ccggactgac aatcgacgag 900
ttcgccccga ggctgtcctt cttctggggc attgggatga acttctatat ggaaatcgcg 960
aagatgagag ctggaaggcg gctgtgggcg cacctgatcg agaagatgtt ccagcccaag 1020
aacagcaaaa gccttctcct ccgcgcccac tgccaaactt ccggctggtc actgaccgag 1080
caggatccgt acaacaacat tgtccggact gccattgagg ccatggccgc tgtgttcgga 1140
ggcactcagt ccctccacac taactccttc gacgaggccc tgggtctgcc gaccgtgaag 1200
tccgcccgga tagccagaaa tactcaaatc attatccagg aggaaagcgg aatccccaag 1260
gtcgccgacc cttggggagg atcttacatg atggagtgtt tgaccaatga cgtctacgac 1320
gccgccctga agctcattaa cgaaatcgaa gagatgggcg gaatggccaa ggccgtggct 1380
gagggcatcc cgaagctgag aatcgaggaa tgcgccgccc ggagacaggc ccgcattgat 1440
agcggcagcg aggtcattgt gggcgtgaac aagtaccagc ttgaaaagga ggacgccgtg 1500
gaagtgctgg caatcgataa cacctccgtg cgcaaccggc agatcgaaaa gctcaagaag 1560
attaagtcct cacgggacca ggcactggcg gagagatgcc tcgccgcgct gaccgaatgc 1620
gctgcctcgg gagatggcaa cattctggcc ctggcagtgg acgcctctcg ggctcggtgc 1680
actgtggggg agatcaccga cgccctcaag aaagtgttcg gtgaacataa ggccaacgac 1740
cggatggtgt ccggagcgta ccgccaggaa tttggcgaat caaaggaaat cacgtccgca 1800
atcaagaggg tgcacaaatt catggaacgg gagggcagac ggcccagact gctcgtggct 1860
aaaatgggac aagatggtca cgaccgcggc gccaaggtca tcgcgactgg cttcgccgat 1920
ctcggattcg acgtggacat cggacctctg tttcaaactc cccgggaagt ggcccagcag 1980
gccgtggacg cggacgtgca tgccgtcggg atctcaaccc tggcggccgg ccataagacc 2040
ctggtgccgg aactgatcaa ggagctgaac tcgctcggcc gccccgacat cctcgtgatg 2100
tgtggcggag tgattccgcc acaagactac gagttcctgt tcgaagtcgg ggtgtccaac 2160
gtgttcggtc ccggaaccag aatcccgaag gctgcggtcc aagtgctgga tgatattgag 2220
aagtgccttg agaaaaagca acagtcagtg tga 2253
<210> 15
<211> 4615
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<400> 15
ttggccactc cctctctgcg cgctcgctcg ctcactgagg ccgcccgggc aaagcccggg 60
cgtcgggcga cctttggtcg cccggcctca gtgagcgagc gagcgcgcag agagggagtg 120
gccaactcca tcactagggg ttccttacgt aactccatga aagtggattt tattatcctc 180
atcatgcaga tgagaatatt gagacttata gcggtatgcc tgagccccaa agtactcaga 240
gttgcctggc tccaagattt ataatcttaa atgatgggac taccatcctt actctctcca 300
tttttctata cgtgagtaat gttttttctg tttttttttt ttctttttcc attcaaactc 360
agtgcacttg ttgagcttgt gaaacacaag cccaaggcaa caaaagagca actgaaagct 420
gttatggatg atttcgcagc ttttgtagag aagtgctgca aggctgacga taaggagacc 480
tgctttgccg aggaggtact acagttctct tcattttaat atgtccagta ttcatttttg 540
catgtttggt taggctaggg cttagggatt tatatatcaa aggaggcttt gtacatgtgg 600
gacagggatc ttattttaca aacaattgtc ttacaaaatg aataaaacag cactttgttt 660
ttatctcctg ctctattgtg ccatactgtt aaatgtttat aatgcctgtt ctgtttccaa 720
atttgtgatg cttatgaata ttaataggaa tatttgtaag gcctgaaata ttttgatcat 780
gaaatcaaaa cattaattta tttaaacatt tacttgaaat gtggtggttt gtgatttagt 840
tgattttata ggctagtggg agaatttaca ttcaaatgtc taaatcactt aaaattgccc 900
tttatggcct gacagtaact tttttttatt catttgggga caactatgtc cgtgagcttc 960
cgtccagaga ttatagtagt aaattgtaat taaaggatat gatgcacgtg aaatcacttt 1020
gcaatcatca atagcttcat aaatgttaat tttgtatcct aatagtaatg ctaatatttt 1080
cctaacatct gtcatgtctt tgtgttcagg gtaaaaaact tgttgctgca agtcaagctg 1140
ccttaggctt aggcagcggc gccaccaact tcagcctgct gaaacaggcc ggcgacgtgg 1200
aagagaaccc tggccccctg agagccaaaa accagctgtt cctgctgagc ccccactatc 1260
tgagacaggt caaagaaagt tccgggagta gactgatcca gcagagactg ctgcaccagc 1320
agcagccact gcatcctgag tgggccgctc tggccaagaa acagctgaag ggcaaaaacc 1380
cagaagacct gatctggcac actccagagg ggatttcaat caagcccctg tacagcaaaa 1440
gggacactat ggatctgcca gaggaactgc caggagtgaa gcctttcacc cgcggacctt 1500
acccaactat gtataccttt cgaccctgga caattcggca gtacgccggc ttcagtactg 1560
tggaggaatc aaacaagttt tataaggaca acatcaaggc tggacagcag ggcctgagtg 1620
tggcattcga tctggccaca catcgcggct atgactcaga taatcccaga gtcagggggg 1680
acgtgggaat ggcaggagtc gctatcgaca cagtggaaga tactaagatt ctgttcgatg 1740
gaatccctct ggagaaaatg tctgtgagta tgacaatgaa cggcgctgtc attcccgtgc 1800
tggcaaactt catcgtcact ggcgaggaac agggggtgcc taaggaaaaa ctgaccggca 1860
caattcagaa cgacatcctg aaggagttca tggtgcggaa tacttacatt tttccccctg 1920
aaccatccat gaaaatcatt gccgatatct tcgagtacac cgctaagcac atgcccaagt 1980
tcaactcaat tagcatctcc gggtatcata tgcaggaagc aggagccgac gctattctgg 2040
agctggctta caccctggca gatggcctgg aatattctcg aaccggactg caggcaggcc 2100
tgacaatcga cgagttcgct cctagactga gtttcttttg gggaattggc atgaactttt 2160
acatggagat cgccaagatg agggctggcc ggagactgtg ggcacacctg atcgagaaga 2220
tgttccagcc taagaactct aagagtctgc tgctgcgggc ccattgccag acatccggct 2280
ggtctctgac tgaacaggac ccatataaca atattgtcag aaccgcaatc gaggcaatgg 2340
cagccgtgtt cggaggaacc cagagcctgc acacaaactc ctttgatgag gccctggggc 2400
tgcctaccgt gaagtctgct aggattgcac gcaatacaca gatcattatc caggaggaat 2460
ccggaatccc aaaggtggcc gatccctggg gaggctctta catgatggag tgcctgacaa 2520
acgacgtgta tgatgctgca ctgaagctga ttaatgaaat cgaggaaatg gggggaatgg 2580
caaaggccgt ggctgagggc attccaaaac tgaggatcga ggaatgtgca gctaggcgcc 2640
aggcacgaat tgactcagga agcgaagtga tcgtcggggt gaataagtac cagctggaga 2700
aagaagacgc agtcgaagtg ctggccatcg ataacacaag cgtgcgcaat cgacagattg 2760
agaagctgaa gaaaatcaaa agctcccgcg atcaggcact ggccgaacga tgcctggcag 2820
ccctgactga gtgtgctgca agcggggacg gaaacattct ggctctggca gtcgatgcct 2880
cccgggctag atgcactgtg ggggaaatca ccgacgccct gaagaaagtc ttcggagagc 2940
acaaggccaa tgatcggatg gtgagcggcg cttatagaca ggagttcggg gaatctaaag 3000
agattaccag tgccatcaag agggtgcaca agttcatgga gagagaaggg cgacggccca 3060
ggctgctggt ggcaaagatg ggacaggacg gacatgatcg cggagcaaaa gtcattgcca 3120
ccgggttcgc tgacctggga tttgacgtgg atatcggccc tctgttccag acaccacgag 3180
aggtcgcaca gcaggcagtc gacgctgatg tgcacgcagt cggagtgtcc actctggcag 3240
ctggccataa gaccctggtg cctgaactga tcaaagagct gaactctctg ggcagaccag 3300
acatcctggt catgtgcggc ggcgtgatcc caccccagga ttacgaattc ctgtttgagg 3360
tcggggtgag caacgtgttc ggaccaggaa ccaggatccc taaggccgca gtgcaggtcc 3420
tggatgatat tgaaaagtgt ctggaaaaga aacagcagtc agtgtaacat cacatttaaa 3480
agcatctcag gtaactatat tttgaatttt ttaaaaaagt aactataata gttattatta 3540
aaatagcaaa gattgaccat ttccaagagc catatagacc agcaccgacc actattctaa 3600
actatttatg tatgtaaata ttagctttta aaattctcaa aatagttgct gagttgggaa 3660
ccactattat ttctattttg tagatgagaa aatgaagata aacatcaaag catagattaa 3720
gtaattttcc aaagggtcaa aattcaaaat tgaaaccaaa gtttcagtgt tgcccattgt 3780
cctgttctga cttatatgat gcggtacaca gagccatcca agtaagtgat ggctcagcag 3840
tggaatactc tgggaattag gctgaaccac atgaaagagt gctttatagg gcaaaaacag 3900
ttgaatatca gtgatttcac atggttcaac ctaatagttc aactcatcct ttccattgga 3960
gaatatgatg gatctacctt ctgtgaactt tatagtgaag aatctgctat tacatttcca 4020
atttgtcaac atgctgagct ttaataggac ttatcttctt atgacaacat ttattggtgt 4080
gtccccttgc ctagcccaac agaagaattc agcagccgta agtctaggac aggcttaaat 4140
tgttttcact ggtgtaaatt gcagaaagat gatctaagta atttggcatt tattttaata 4200
ggtttgaaaa acacatgcca ttttacaaat aagacttata tttgtccttt tgtttttcag 4260
cctaccatga gaataagaga aagaaaatga agatcaaaag cttattcatc tgtttttctt 4320
tttcgttggt gtaaagccaa caccctgtct aaaaaacata aatttcttta atcattttgc 4380
ctcttttctc tgtgcttcaa ttaataaaaa atggaaagaa tctaatagag tggtacagca 4440
ctgttatttt tcaaagatgt gttgtacgta aggaacccct agtgatggag ttggccactc 4500
cctctctgcg cgctcgctcg ctcactgagg ccgggcgacc aaaggtcgcc cgacgcccgg 4560
gctttgcccg ggcggcctca gtgagcgagc gagcgcgcag agagggagtg gccaa 4615
<210> 16
<211> 4619
<212> ДНК
<213> Mus sp.
<400> 16
ttggccactc cctctctgcg cgctcgctcg ctcactgagg ccgggcgacc aaaggtcgcc 60
cgacgcccgg gctttgcccg ggcggcctca gtgagcgagc gagcgcgcag agagggagtg 120
gccaactcca tcactagggg ttcctattta aatctgaaac tagacaaaac ccgtgtgact 180
ggcatcgatt attctatttg atctagctag tcctagcaaa gtgacaactg ctactcccct 240
cctacacagc caagattcct aagttggcag tggcatgctt aatcctcaaa gccaaagtta 300
cttggctcca agatttatag ccttaaactg tggcctcaca ttccttccta tcttactttc 360
ctgcactggg gtaaatgtct ccttgctctt cttgctttct gtcctactgc agggctcttg 420
ctgagctggt gaagcacaag cccaaggcta cagcggagca actgaagact gtcatggatg 480
actttgcaca gttcctggat acatgttgca aggctgctga caaggacacc tgcttctcga 540
ctgaggtcag aaacgttttt gcattttgac gatgttcagt ttccattttc tgtgcacgtg 600
gtcaggtgta gctctctgga actcacacac tgaataactc caccaatcta gatgttgttc 660
tctacgtaac tgtaatagaa actgacttac gtagctttta atttttattt tctgccacac 720
tgctgcctat taaataccta ttatcactat ttggtttcaa atttgtgaca cagaagagca 780
tagttagaaa tacttgcaaa gcctagaatc atgaactcat ttaaaccttg ccctgaaatg 840
tttctttttg aattgagtta ttttacacat gaatggacag ttaccattat atatctgaat 900
catttcacat tccctcccat ggcctaacaa cagtttatct tcttattttg ggcacaacag 960
atgtcagaga gcctgcttta ggaattctaa gtagaactgt aattaagcaa tgcaaggcac 1020
gtacgtttac tatgtcattg cctatggcta tgaagtgcaa atcctaacag tcctgctaat 1080
acttttctaa catccatcat ttctttgttt tcagggtcca aaccttgtca ctagatgcaa 1140
agacgcctta gccggcagcg gcgccaccaa cttcagcctg ctgaaacagg ccggcgacgt 1200
ggaagagaac cctggccccc tgagagccaa aaaccagctg ttcctgctga gcccccacta 1260
tctgagacag gtcaaagaaa gttccgggag tagactgatc cagcagagac tgctgcacca 1320
gcagcagcca ctgcatcctg agtgggccgc tctggccaag aaacagctga agggcaaaaa 1380
cccagaagac ctgatctggc acactccaga ggggatttca atcaagcccc tgtacagcaa 1440
aagggacact atggatctgc cagaggaact gccaggagtg aagcctttca cccgcggacc 1500
ttacccaact atgtatacct ttcgaccctg gacaattcgg cagtacgccg gcttcagtac 1560
tgtggaggaa tcaaacaagt tttataagga caacatcaag gctggacagc agggcctgag 1620
tgtggcattc gatctggcca cacatcgcgg ctatgactca gataatccca gagtcagggg 1680
ggacgtggga atggcaggag tcgctatcga cacagtggaa gatactaaga ttctgttcga 1740
tggaatccct ctggagaaaa tgtctgtgag tatgacaatg aacggcgctg tcattcccgt 1800
gctggcaaac ttcatcgtca ctggcgagga acagggggtg cctaaggaaa aactgaccgg 1860
cacaattcag aacgacatcc tgaaggagtt catggtgcgg aatacttaca tttttccccc 1920
tgaaccatcc atgaaaatca ttgccgatat cttcgagtac accgctaagc acatgcccaa 1980
gttcaactca attagcatct ccgggtatca tatgcaggaa gcaggagccg acgctattct 2040
ggagctggct tacaccctgg cagatggcct ggaatattct cgaaccggac tgcaggcagg 2100
cctgacaatc gacgagttcg ctcctagact gagtttcttt tggggaattg gcatgaactt 2160
ttacatggag atcgccaaga tgagggctgg ccggagactg tgggcacacc tgatcgagaa 2220
gatgttccag cctaagaact ctaagagtct gctgctgcgg gcccattgcc agacatccgg 2280
ctggtctctg actgaacagg acccatataa caatattgtc agaaccgcaa tcgaggcaat 2340
ggcagccgtg ttcggaggaa cccagagcct gcacacaaac tcctttgatg aggccctggg 2400
gctgcctacc gtgaagtctg ctaggattgc acgcaataca cagatcatta tccaggagga 2460
atccggaatc ccaaaggtgg ccgatccctg gggaggctct tacatgatgg agtgcctgac 2520
aaacgacgtg tatgatgctg cactgaagct gattaatgaa atcgaggaaa tggggggaat 2580
ggcaaaggcc gtggctgagg gcattccaaa actgaggatc gaggaatgtg cagctaggcg 2640
ccaggcacga attgactcag gaagcgaagt gatcgtcggg gtgaataagt accagctgga 2700
gaaagaagac gcagtcgaag tgctggccat cgataacaca agcgtgcgca atcgacagat 2760
tgagaagctg aagaaaatca aaagctcccg cgatcaggca ctggccgaac gatgcctggc 2820
agccctgact gagtgtgctg caagcgggga cggaaacatt ctggctctgg cagtcgatgc 2880
ctcccgggct agatgcactg tgggggaaat caccgacgcc ctgaagaaag tcttcggaga 2940
gcacaaggcc aatgatcgga tggtgagcgg cgcttataga caggagttcg gggaatctaa 3000
agagattacc agtgccatca agagggtgca caagttcatg gagagagaag ggcgacggcc 3060
caggctgctg gtggcaaaga tgggacagga cggacatgat cgcggagcaa aagtcattgc 3120
caccgggttc gctgacctgg gatttgacgt ggatatcggc cctctgttcc agacaccacg 3180
agaggtcgca cagcaggcag tcgacgctga tgtgcacgca gtcggagtgt ccactctggc 3240
agctggccat aagaccctgg tgcctgaact gatcaaagag ctgaactctc tgggcagacc 3300
agacatcctg gtcatgtgcg gcggcgtgat cccaccccag gattacgaat tcctgtttga 3360
ggtcggggtg agcaacgtgt tcggaccagg aaccaggatc cctaaggccg cagtgcaggt 3420
cctggatgat attgaaaagt gtctggaaaa gaaacagcag tcagtgtaaa cacatcacaa 3480
ccacaacctt ctcaggtaac tatacttggg acttaaaaaa cataatcata atcatttttc 3540
ctaaaacgat caagactgat aaccatttga caagagccat acagacaagc accagctggc 3600
actcttaggt cttcacgtat ggtcatcagt ttgggttcca tttgtagata agaaactgaa 3660
catataaagg tctaggttaa tgcaatttac acaaaaggag accaaaccag ggagagaagg 3720
aaccaaaatt aaaaattcaa accagagcaa aggagttagc cctggttttg ctctgactta 3780
catgaaccac tatgtggagt cctccatgtt agcctagtca agcttatcct ctggatgaag 3840
ttgaaaccat atgaaggaat atttgggggg tgggtcaaaa cagttgtgta tcaatgattc 3900
catgtggttt gacccaatca ttctgtgaat ccatttcaac agaagataca acgggttctg 3960
tttcataata agtgatccac ttccaaattt ctgatgtgcc ccatgctaag ctttaacaga 4020
atttatcttc ttatgacaaa gcagcctcct ttgaaaatat agccaactgc acacagctat 4080
gttgatcaat tttgtttata atcttgcaga agagaatttt ttaaaatagg gcaataatgg 4140
aaggctttgg caaaaaaatt gtttctccat atgaaaacaa aaaacttatt tttttattca 4200
agcaaagaac ctatagacat aaggctattt caaaattatt tcagttttag aaagaattga 4260
aagttttgta gcattctgag aagacagctt tcatttgtaa tcataggtaa tatgtaggtc 4320
ctcagaaatg gtgagacccc tgactttgac acttggggac tctgagggac cagtgatgaa 4380
gagggcacaa cttatatcac acatgcacga gttggggtga gagggtgtca caacatctat 4440
cagtgtgtca tctgcccacc aagtaaattt aaataggaac ccctagtgat ggagttggcc 4500
actccctctc tgcgcgctcg ctcgctcact gaggccgccc gggcaaagcc cgggcgtcgg 4560
gcgacctttg gtcgcccggc ctcagtgagc gagcgagcgc gcagagaggg agtggccaa 4619
<210> 17
<211> 22
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной посследовательности: синтетический праймер
<400> 17
acattcacct tccatgcaga ta 22
<210> 18
<211> 19
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной посследовательности: синтетический праймер
<400> 18
tcagcaggct gaaattggt 19
<210> 19
<211> 247
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полинуклеотид
<220>
<221> модифицированное основание
<222> (1)..(12)
<223> a, c, t, g, неизвестный или другой
<220>
<221> дополнительный признак
<222> (1)..(12)
<223> n представляет собой a, c, g или t
<220>
<221> модифицированное основание
<222> (15)..(16)
<223> a, c, t, g, неизвестный или другой
<220>
<221> дополнительный признак
<222> (15)..(16)
<223> n представляет собой a, c, g или t
<220>
<221> модифицированное основание
<222> (20)..(20)
<223> a, c, t, g, неизвестный или другой
<220>
<221> дополнительный признак
<222> (20)..(20)
<223> n представляет собой a, c, g или t
<220>
<221> модифицированное основание
<222> (22)..(22)
<223> a, c, t, g, неизвестный или другой
<220>
<221> дополнительный признак
<222> (22)..(22)
<223> n представляет собой a, c, g или t
<220>
<221> модифицированное основание
<222> (24)..(24)
<223> a, c, t, g, неизвестный или другой
<220>
<221> дополнительный признак
<222> (24)..(24)
<223> n представляет собой a, c, g или t
<220>
<221> модифицированное основание
<222> (83)..(83)
<223> a, c, t, g, неизвестный или другой
<220>
<221> дополнительный признак
<222> (83)..(83)
<223> n представляет собой a, c, g или t
<220>
<221> модифицированное основание
<222> (234)..(234)
<223> a, c, t, g, неизвестный или другой
<220>
<221> дополнительный признак
<222> (234)..(234)
<223> n представляет собой a, c, g или t
<220>
<221> модифицированное основание
<222> (243)..(243)
<223> a, c, t, g, неизвестный или другой
<220>
<221> дополнительный признак
<222> (243)..(243)
<223> n представляет собой a, c, g или t
<220>
<221> модифицированное основание
<222> (245)..(246)
<223> a, c, t, g, неизвестный или другой
<220>
<221> дополнительный признак
<222> (245)..(246)
<223> n представляет собой a, c, g или t
<400> 19
nnnnnnnnnn nngannagan ananaatcaa gaaacaaact gcacttgttg agcttgtgaa 60
acacaagccc aaggcaacaa aanagcaact gaaagctgtt atggatgatt tcgcagcttt 120
tgtagagaag tgctgcaagg ctgacgataa ggagacctgc tttgccgagg agggtaaaaa 180
acttgttgct gcaagtcaag ctgccttagg cttaggcagc ggcgccacca attnagcctg 240
ctnanna 247
<---
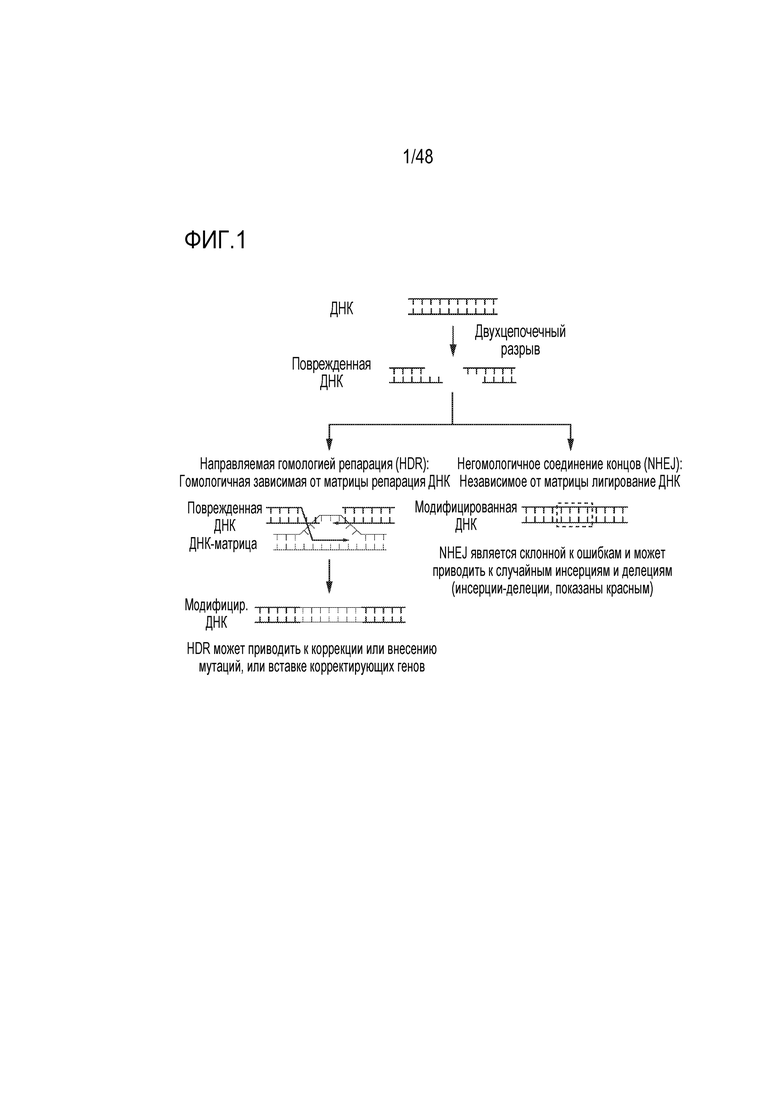
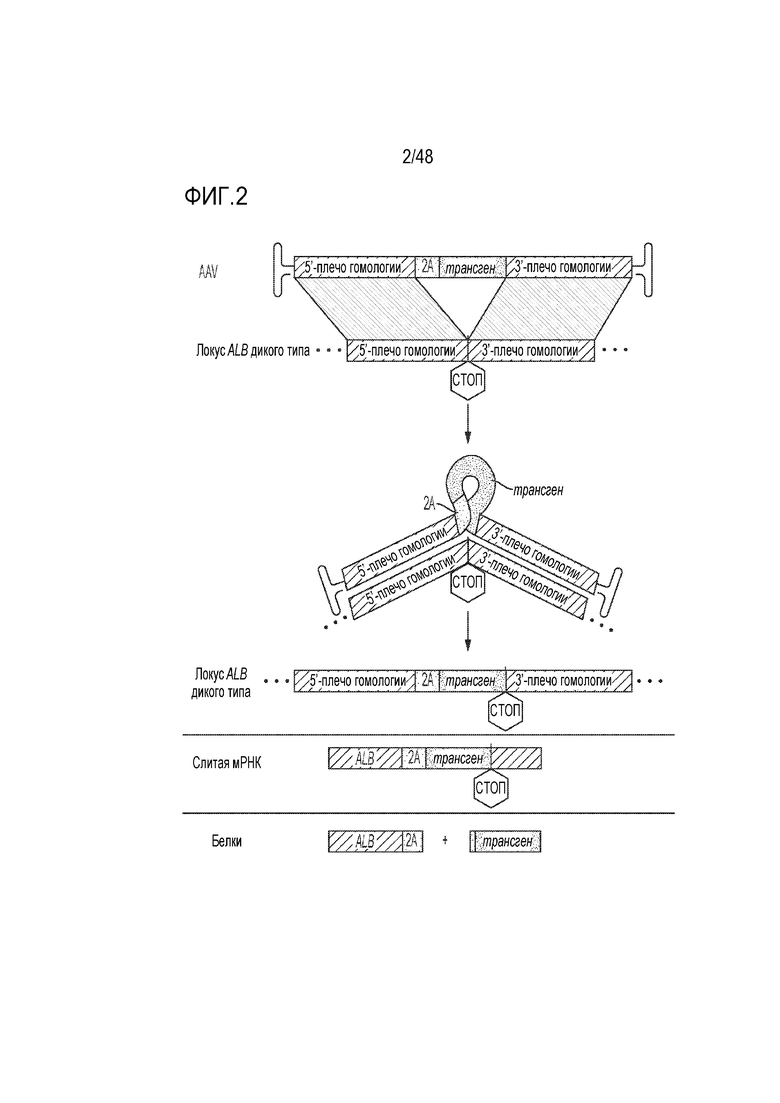
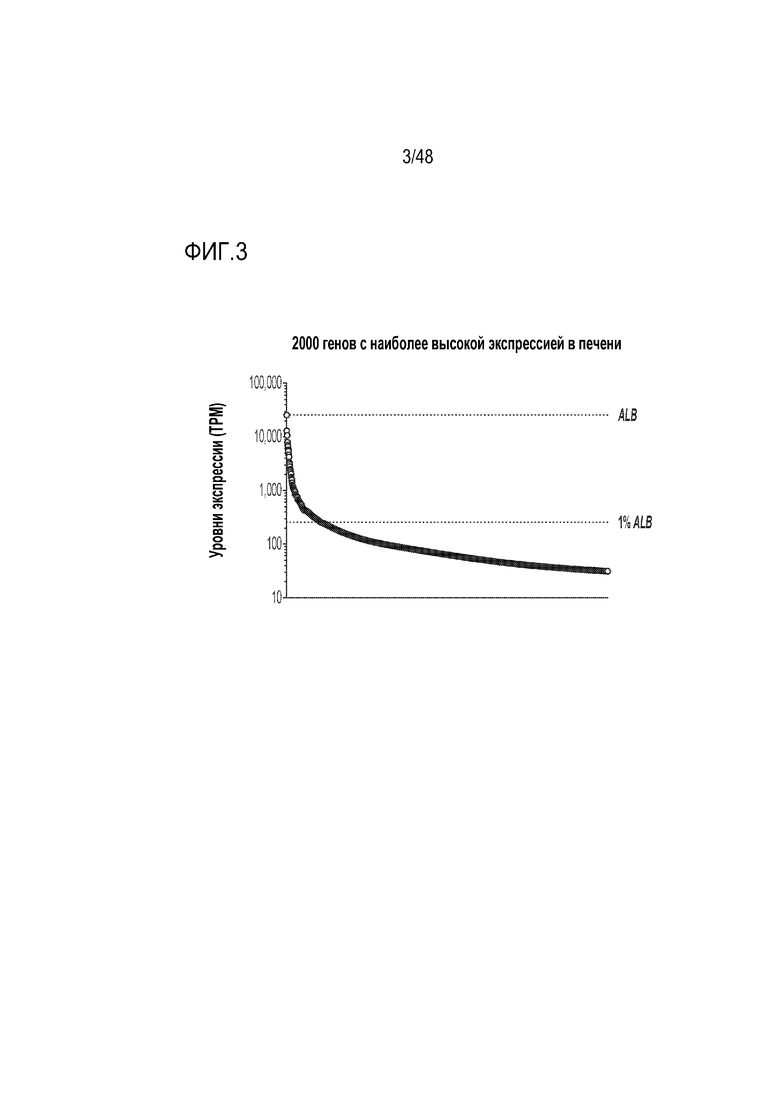


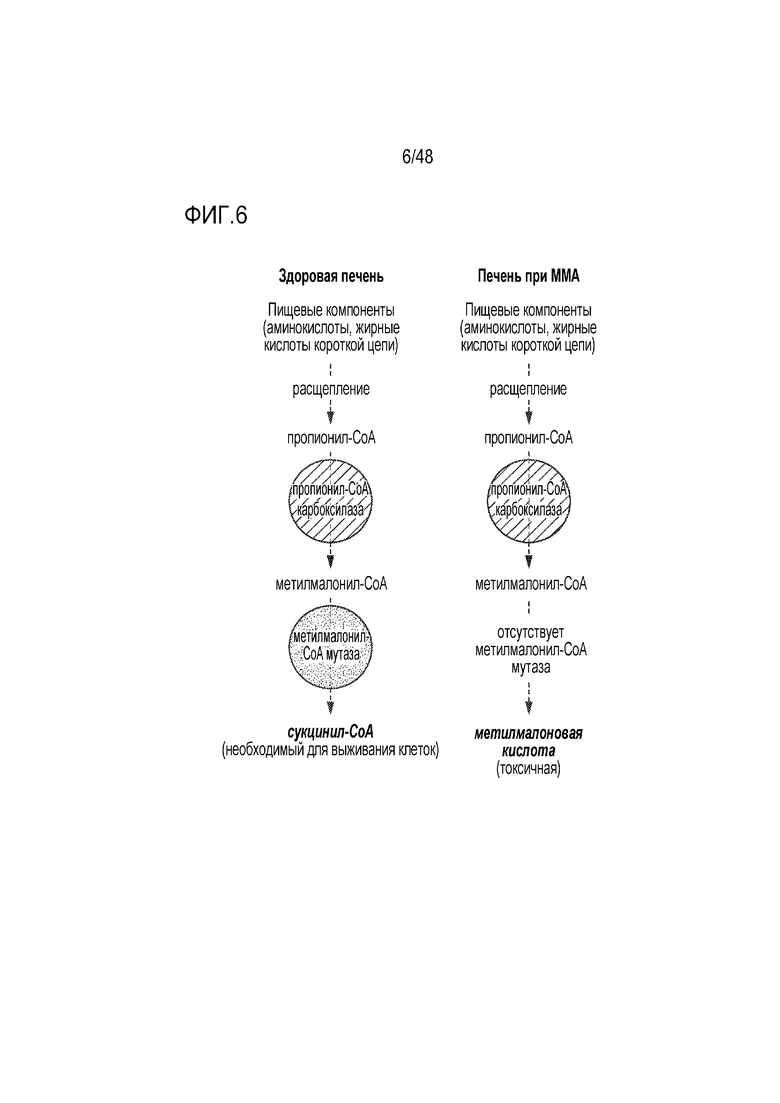

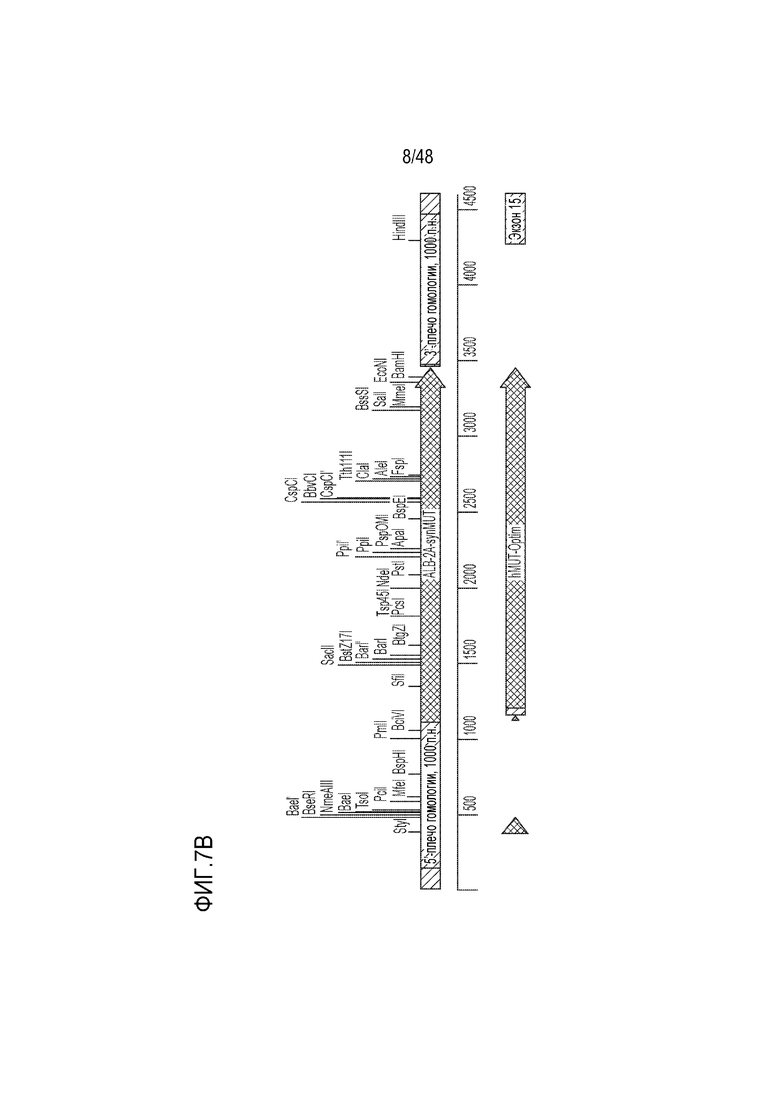


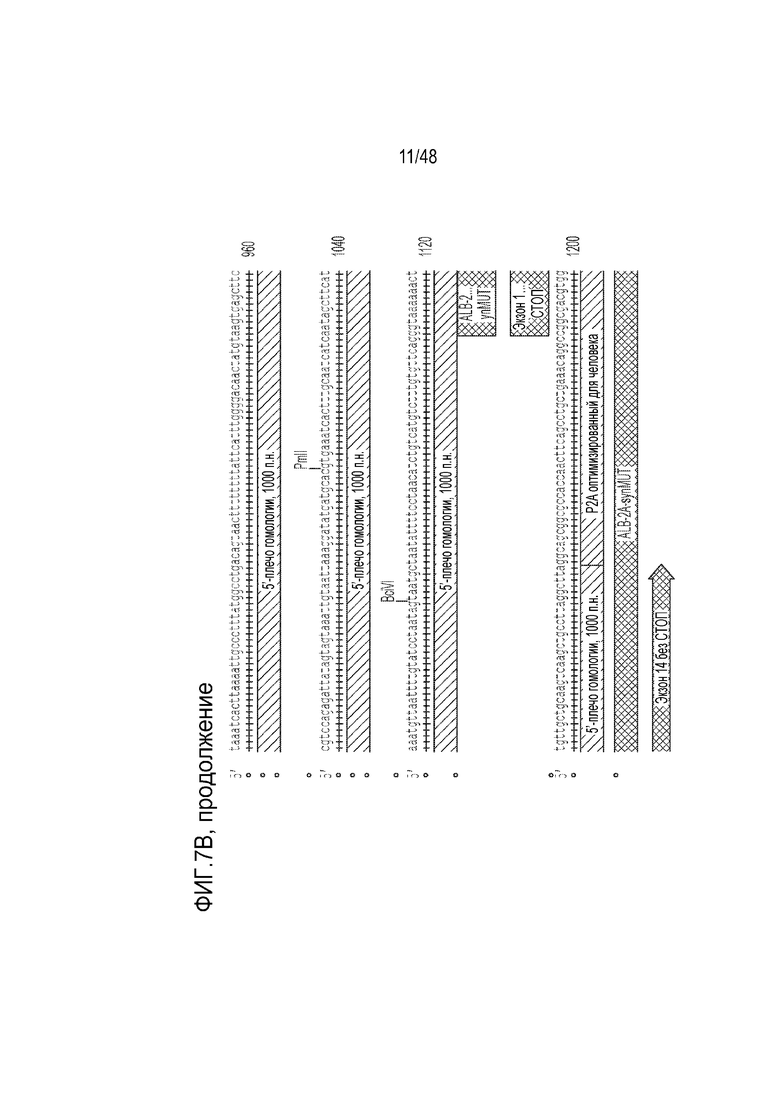
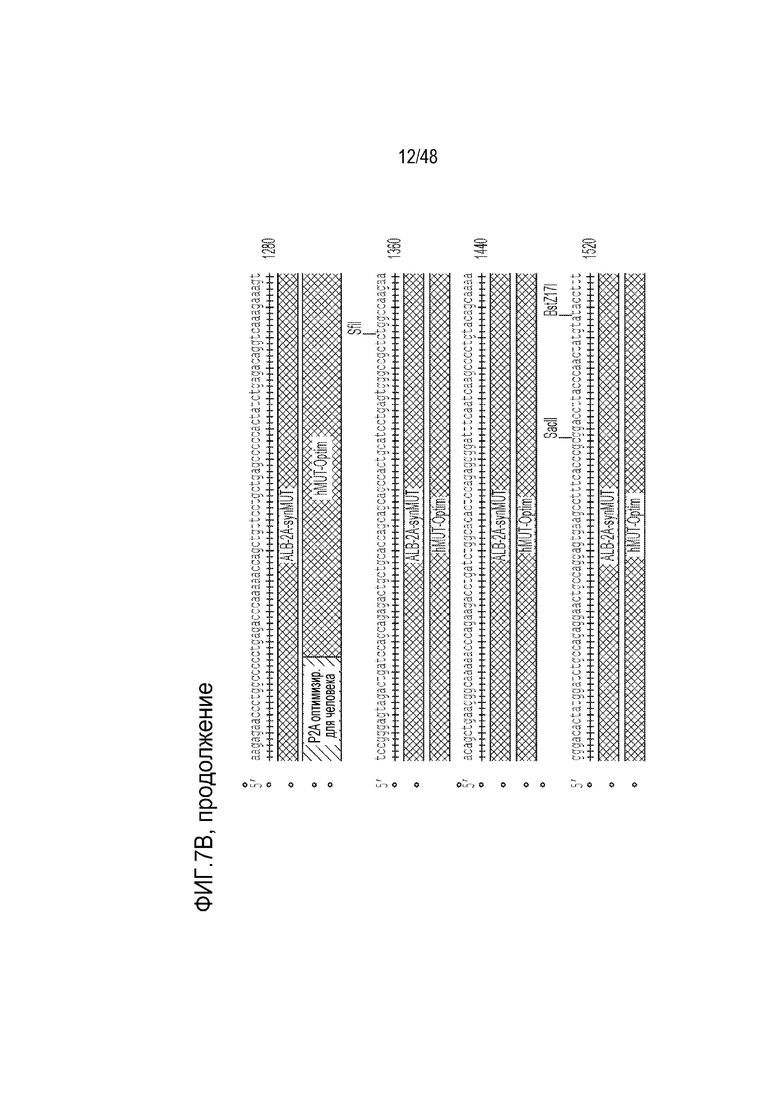
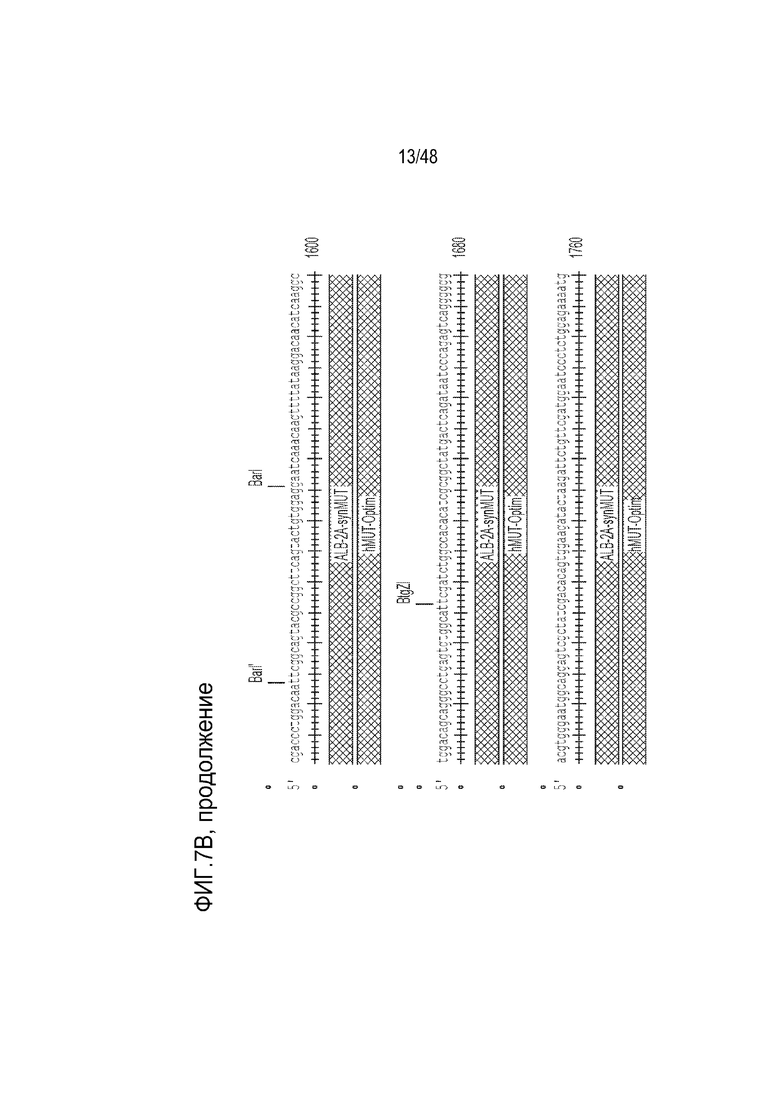
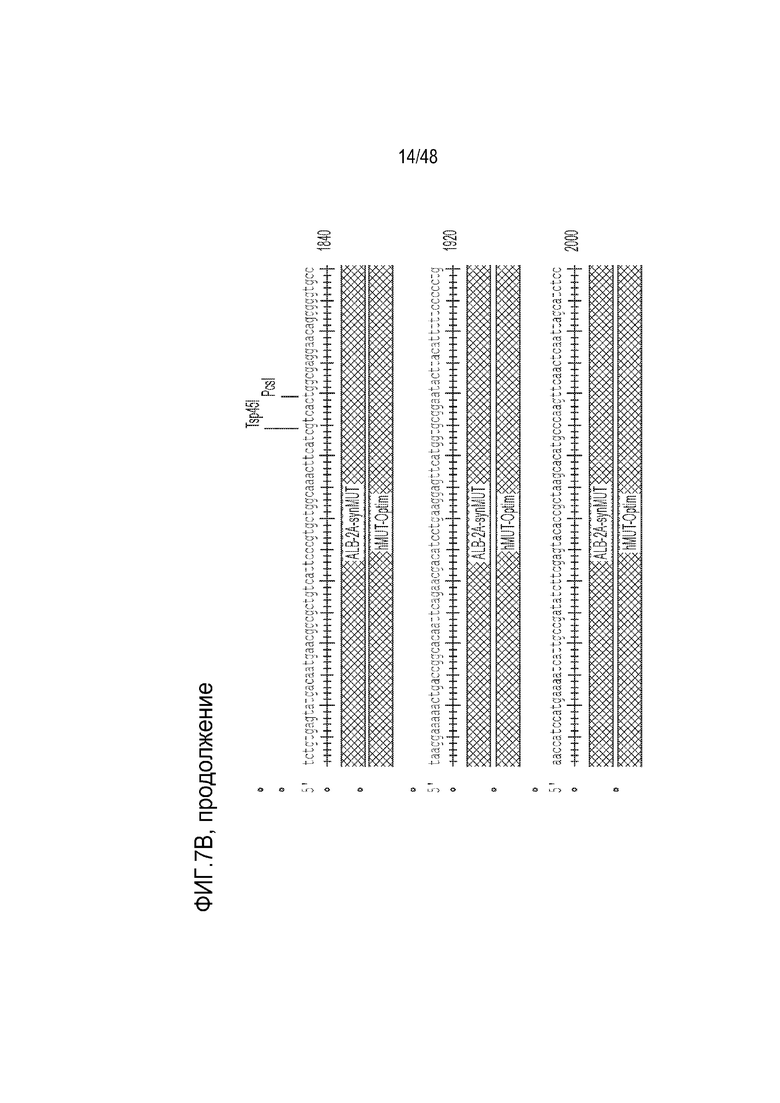
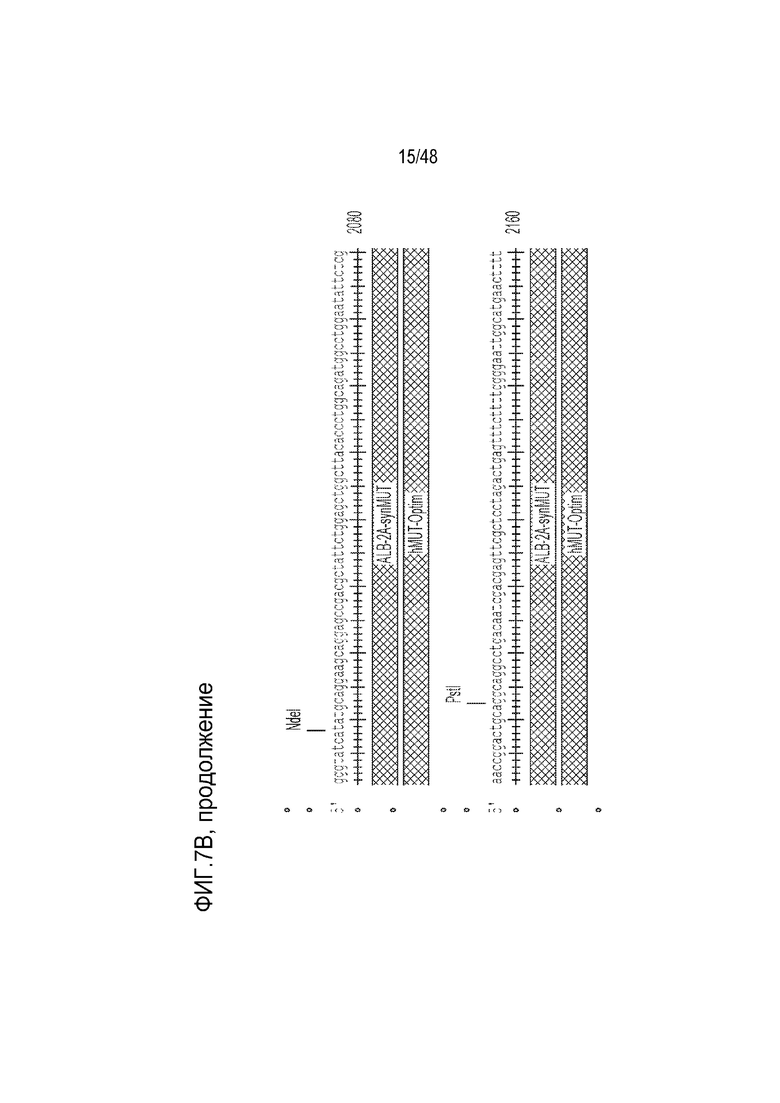
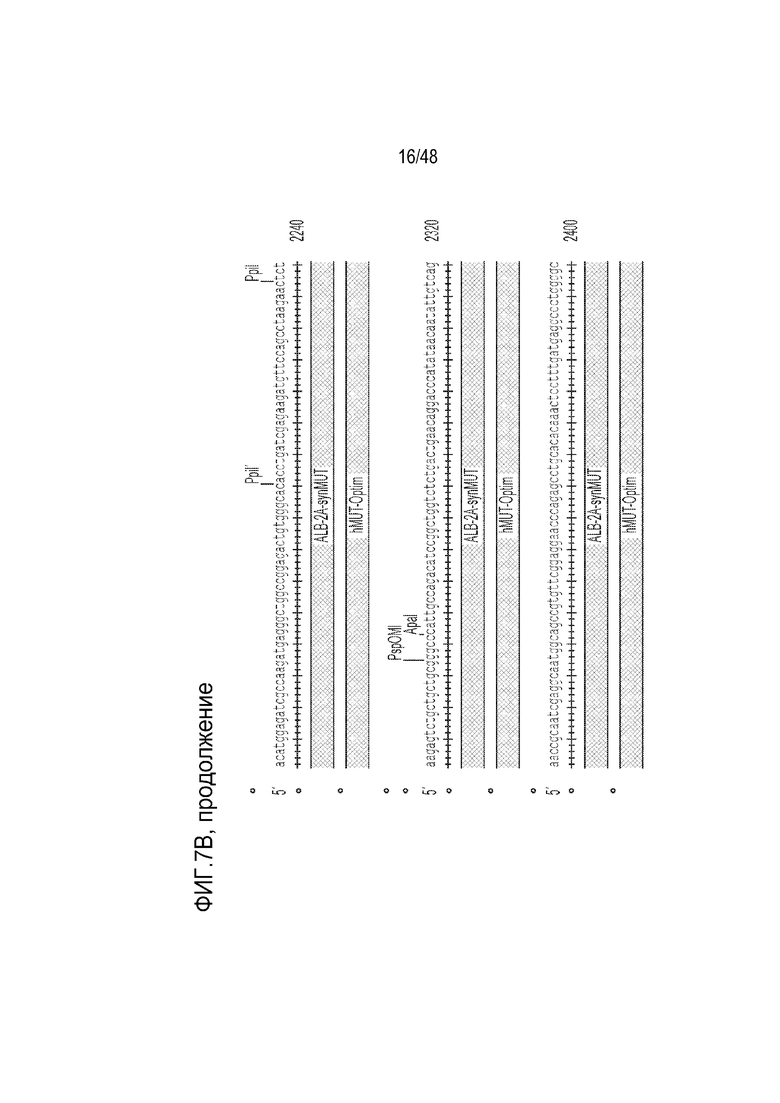
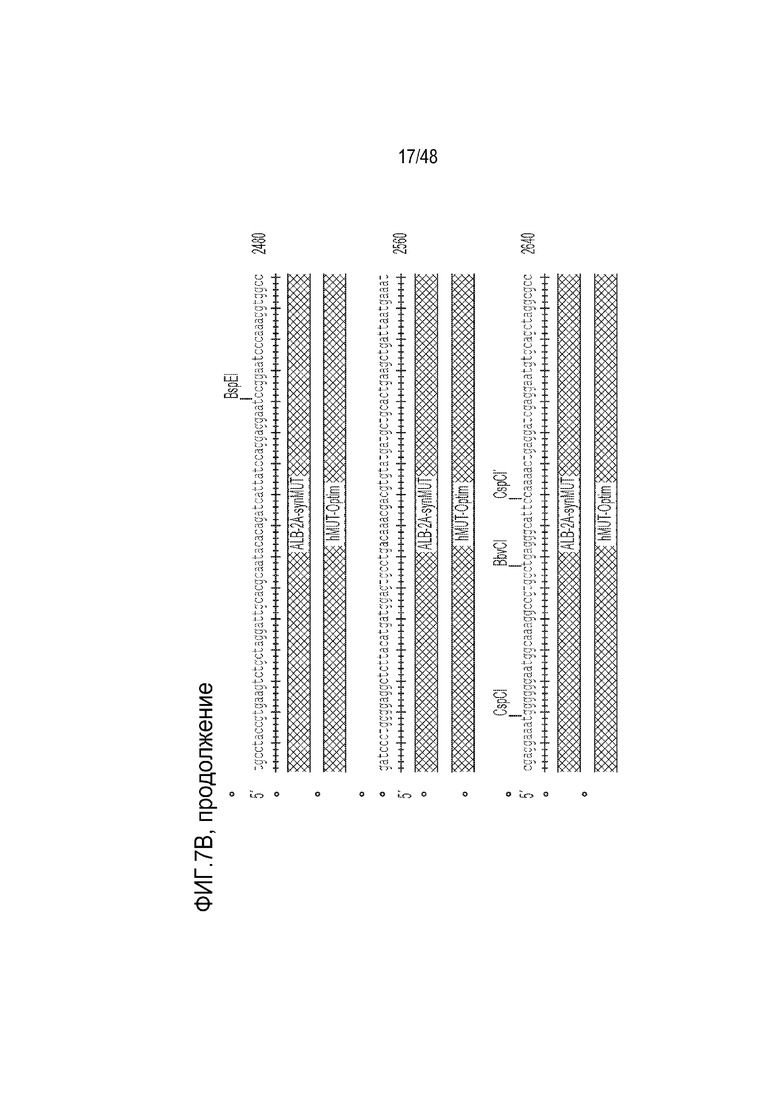
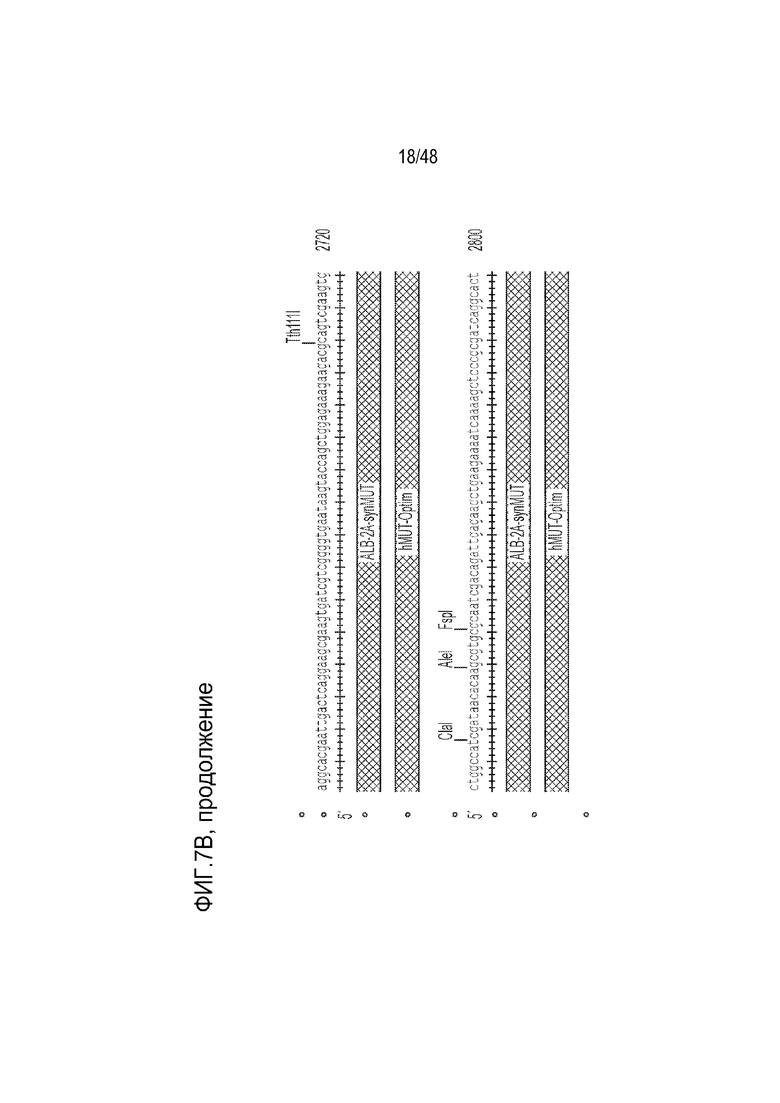


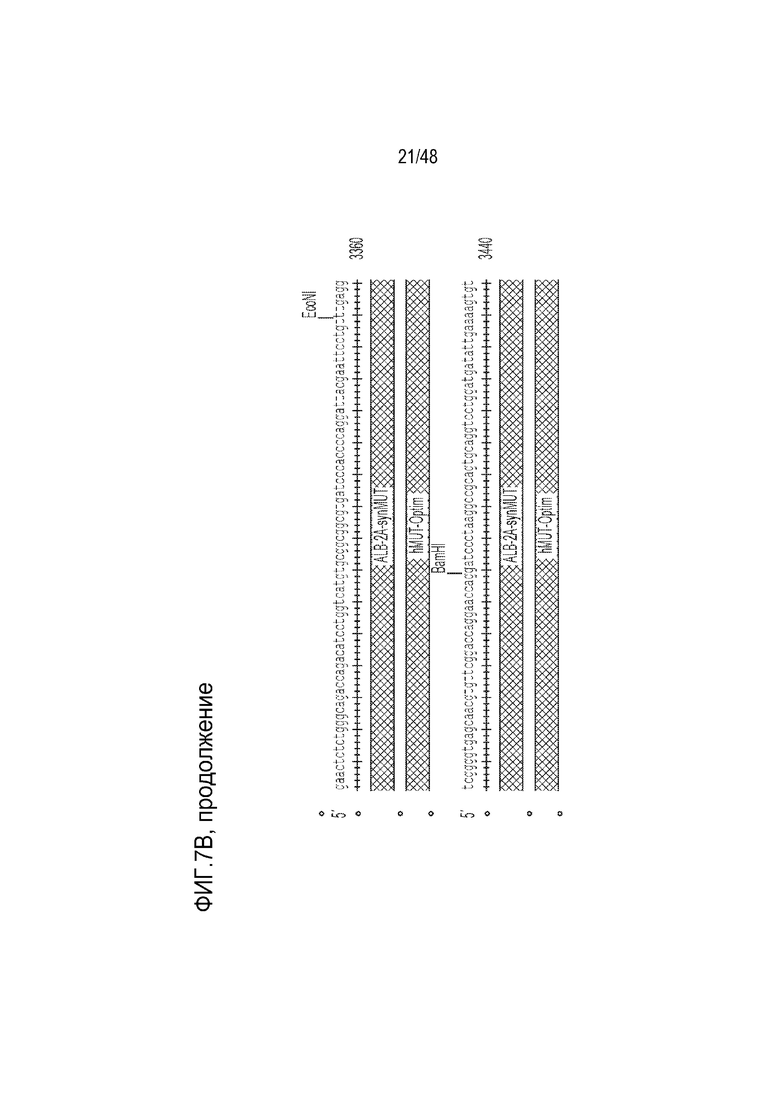



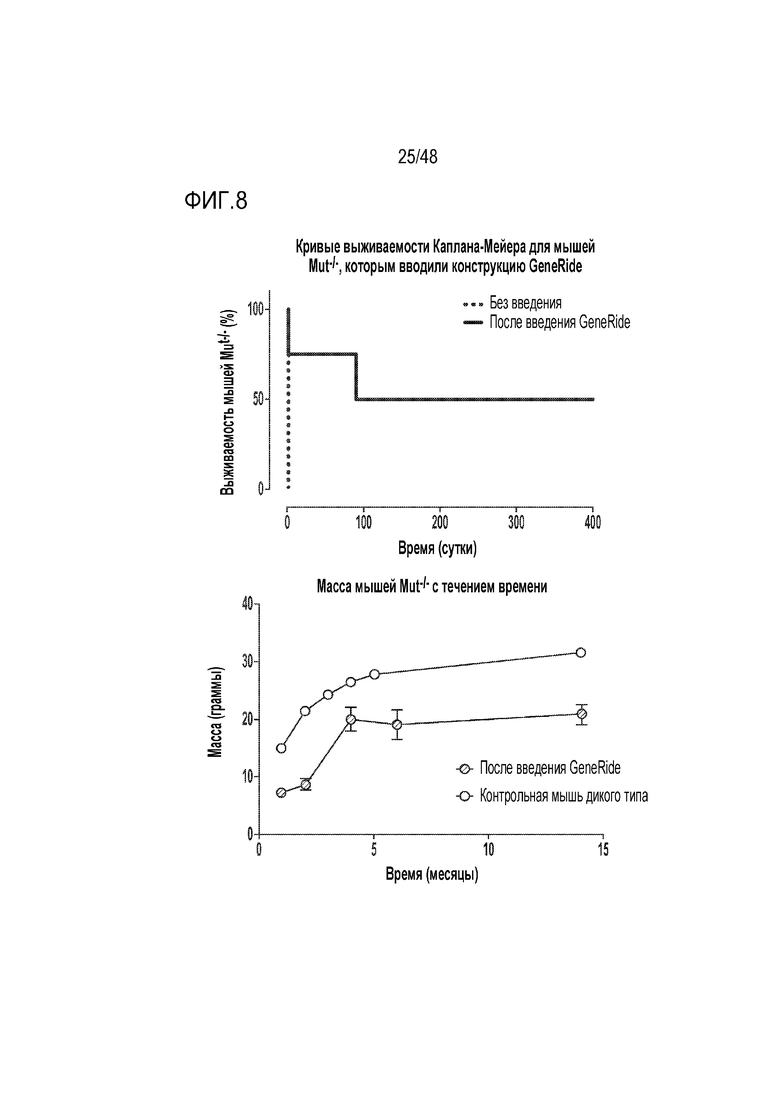
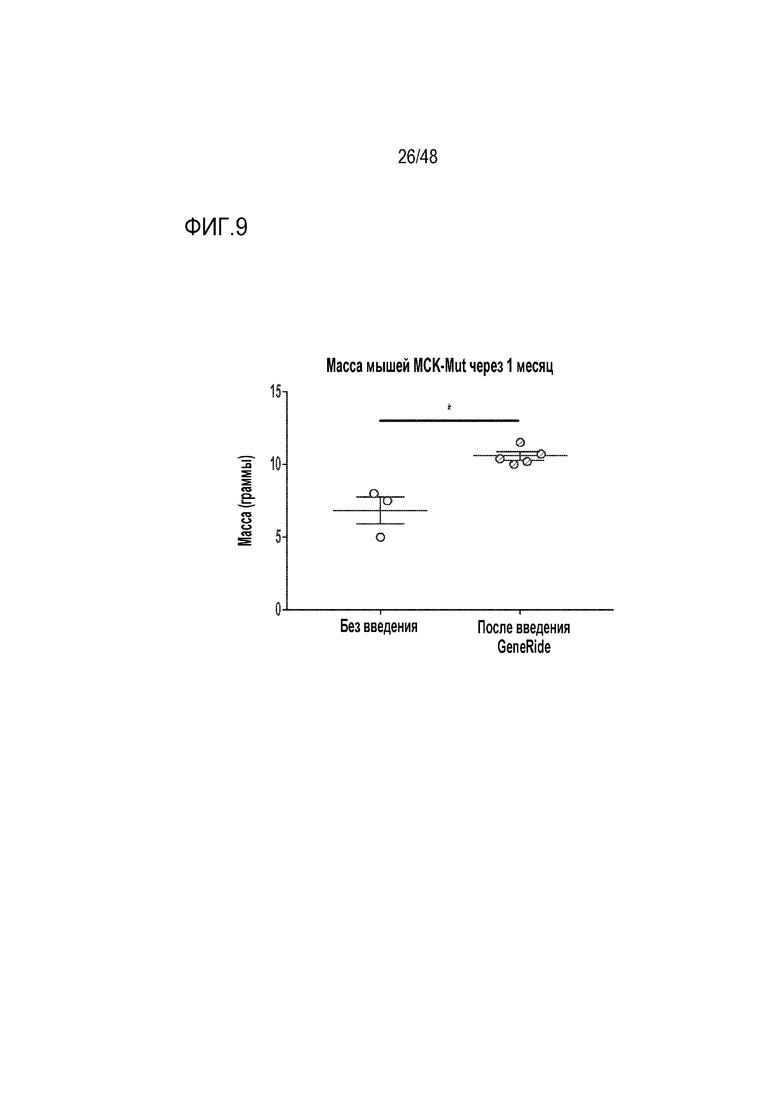
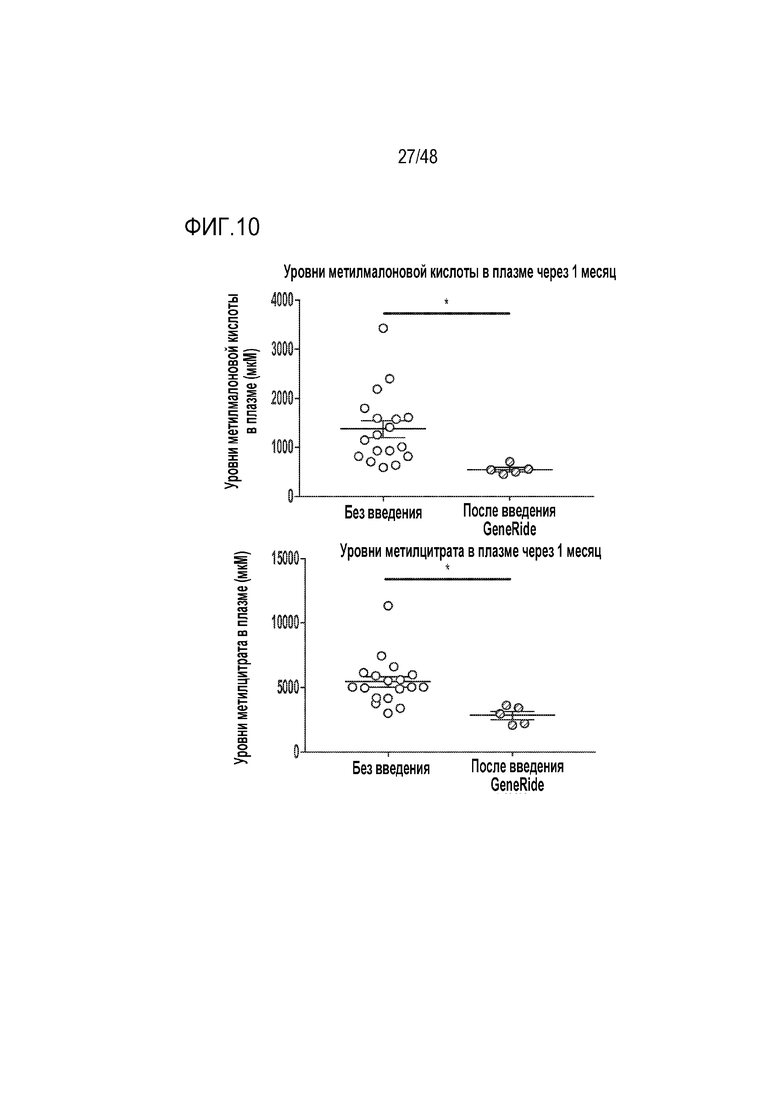
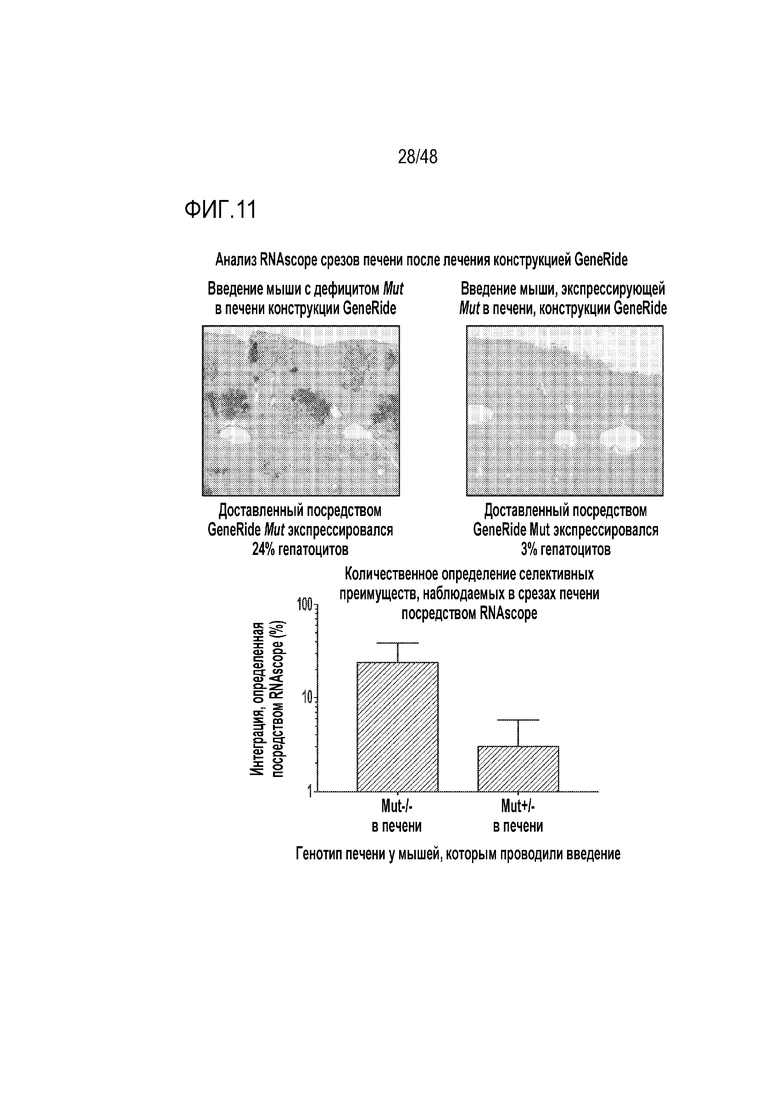
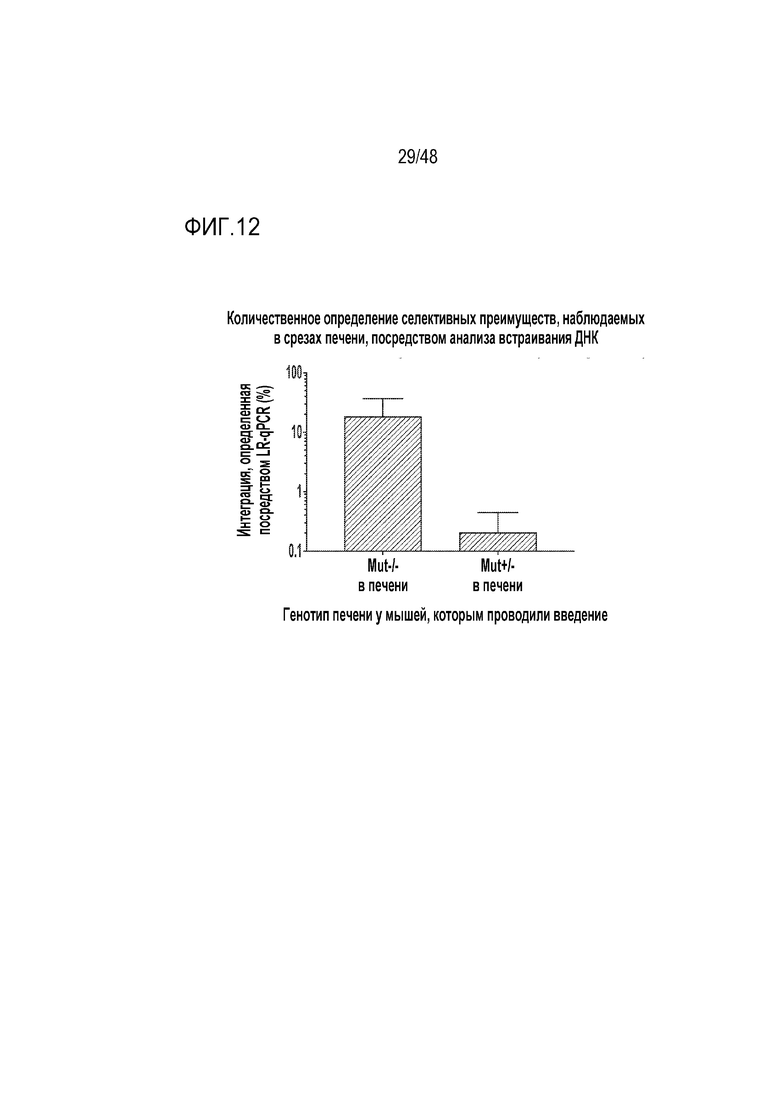
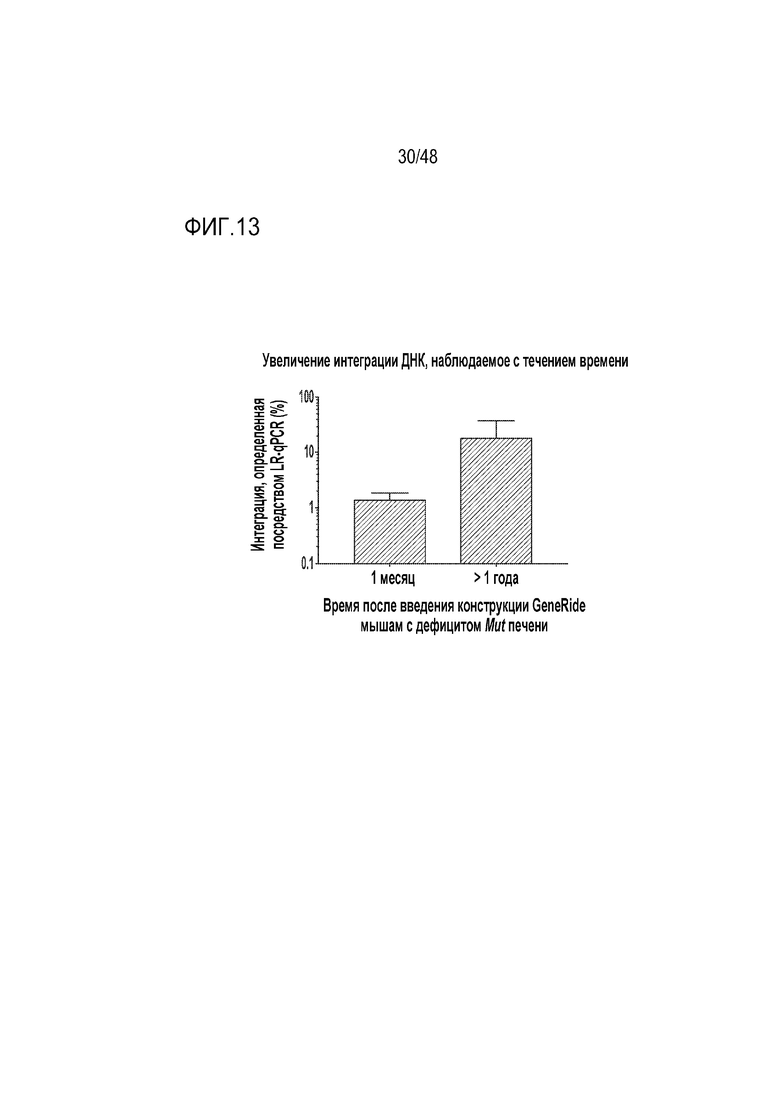
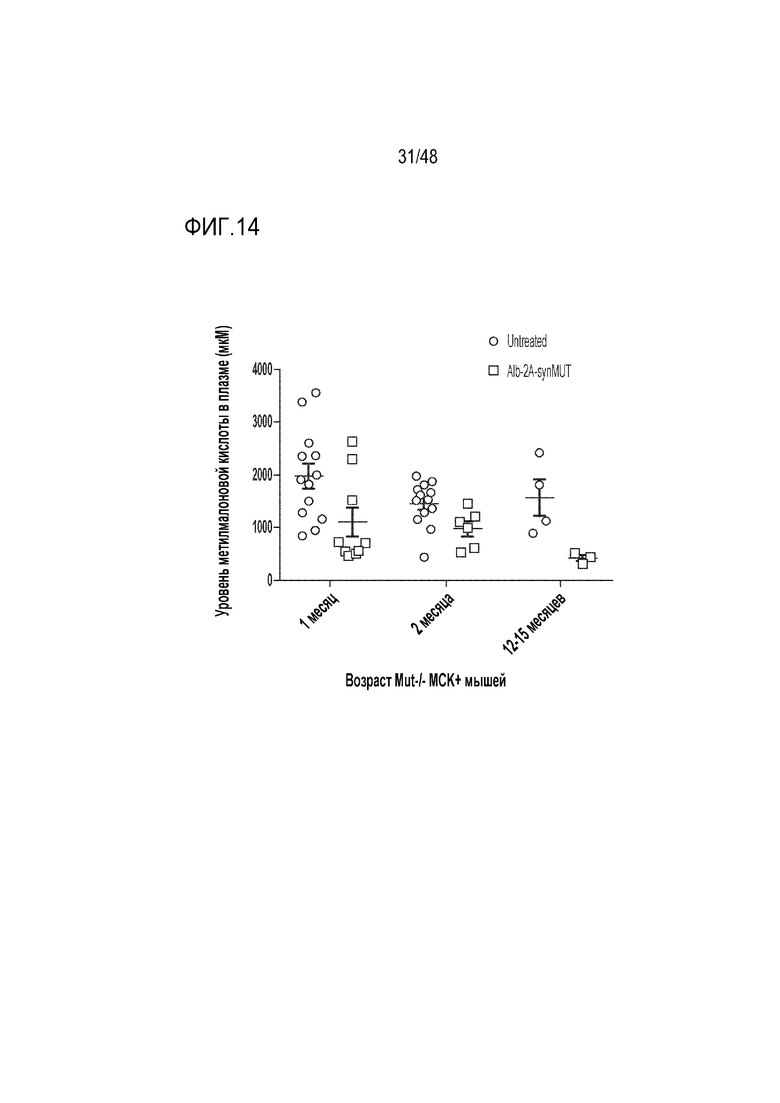
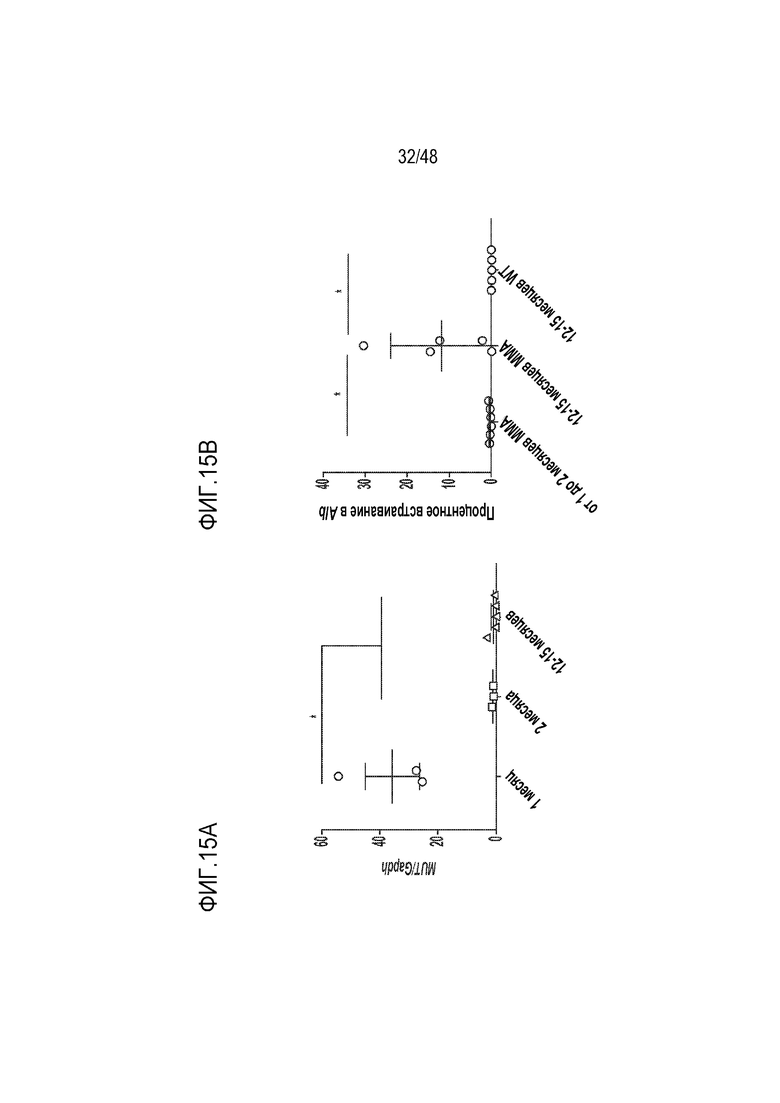
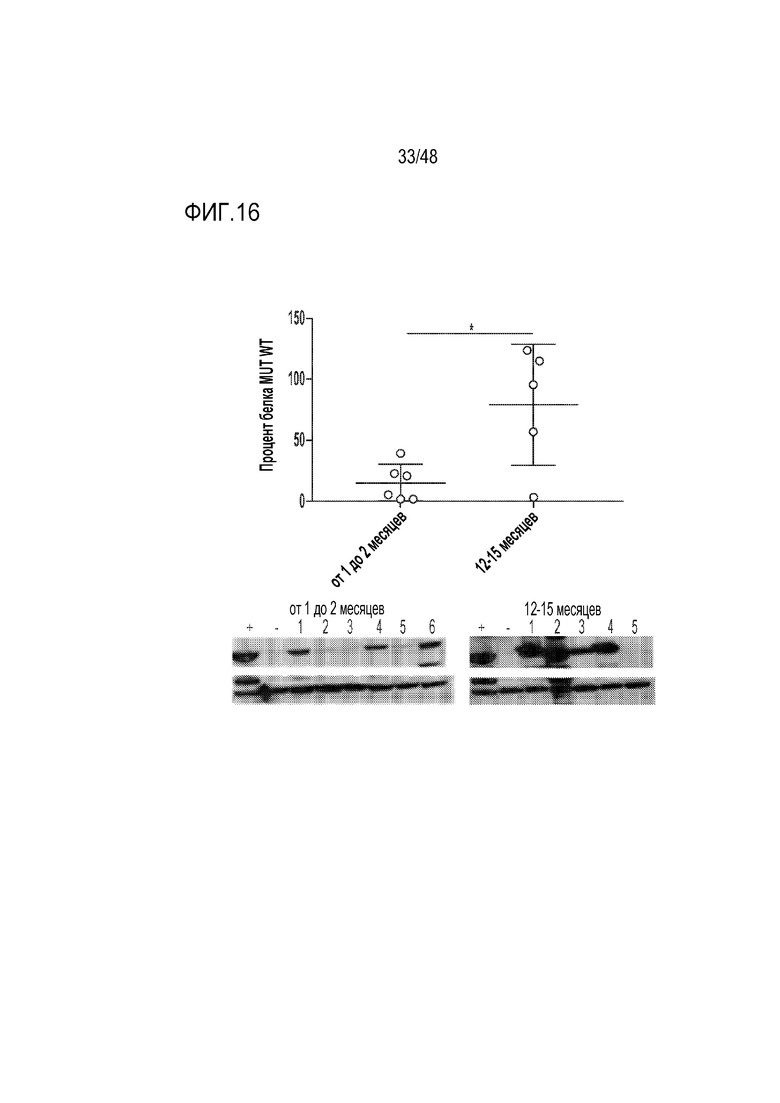
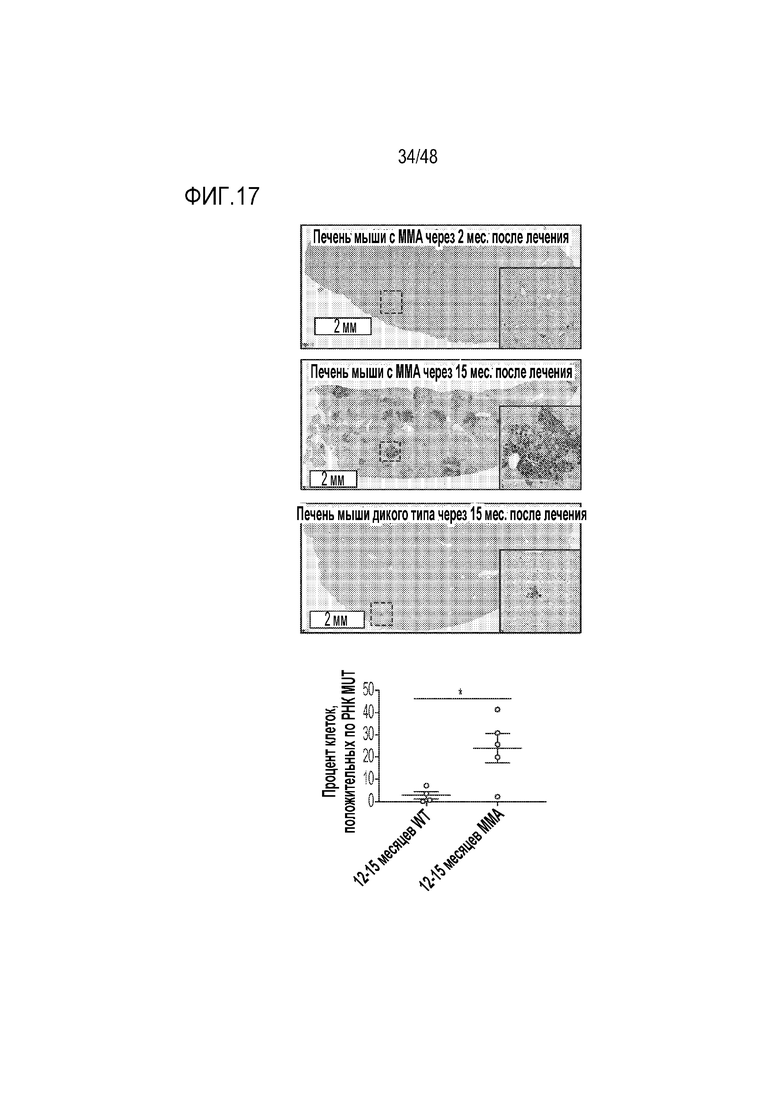
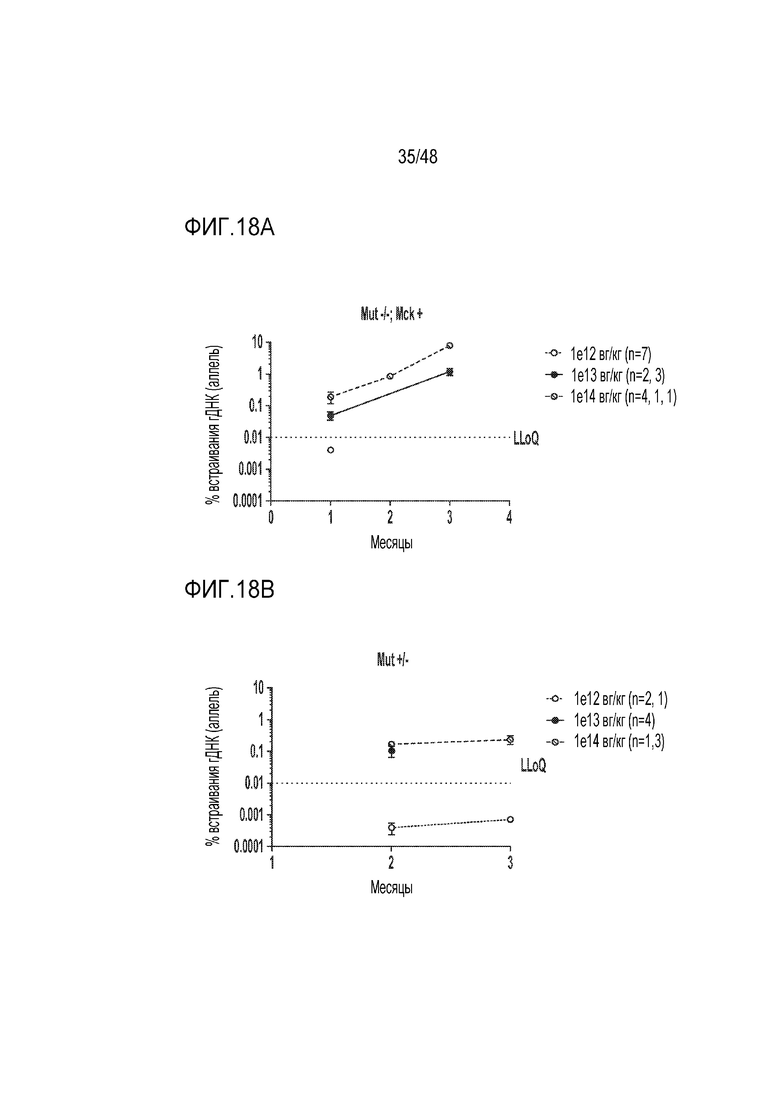
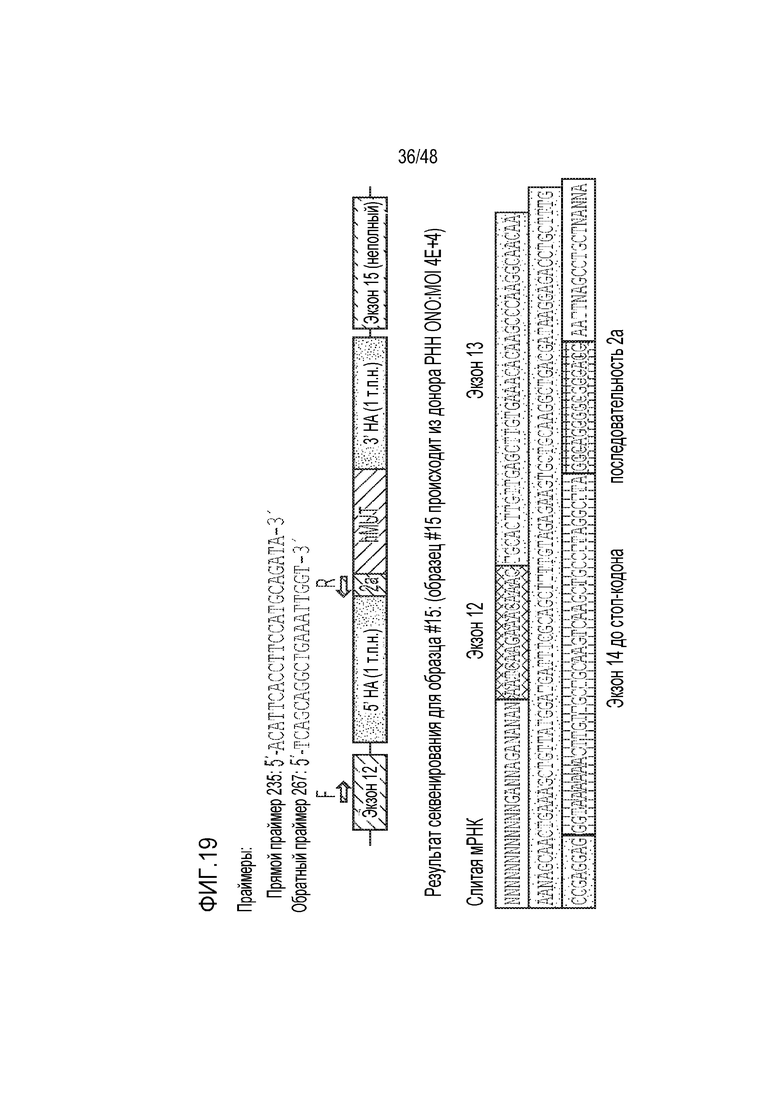
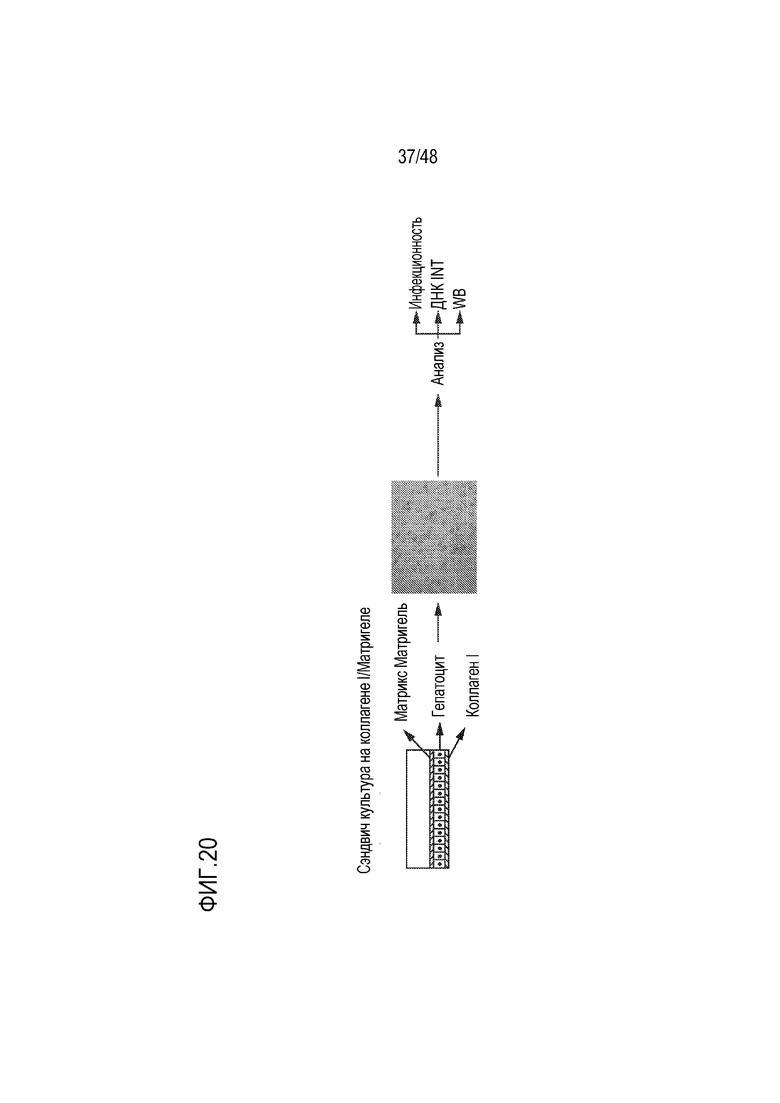
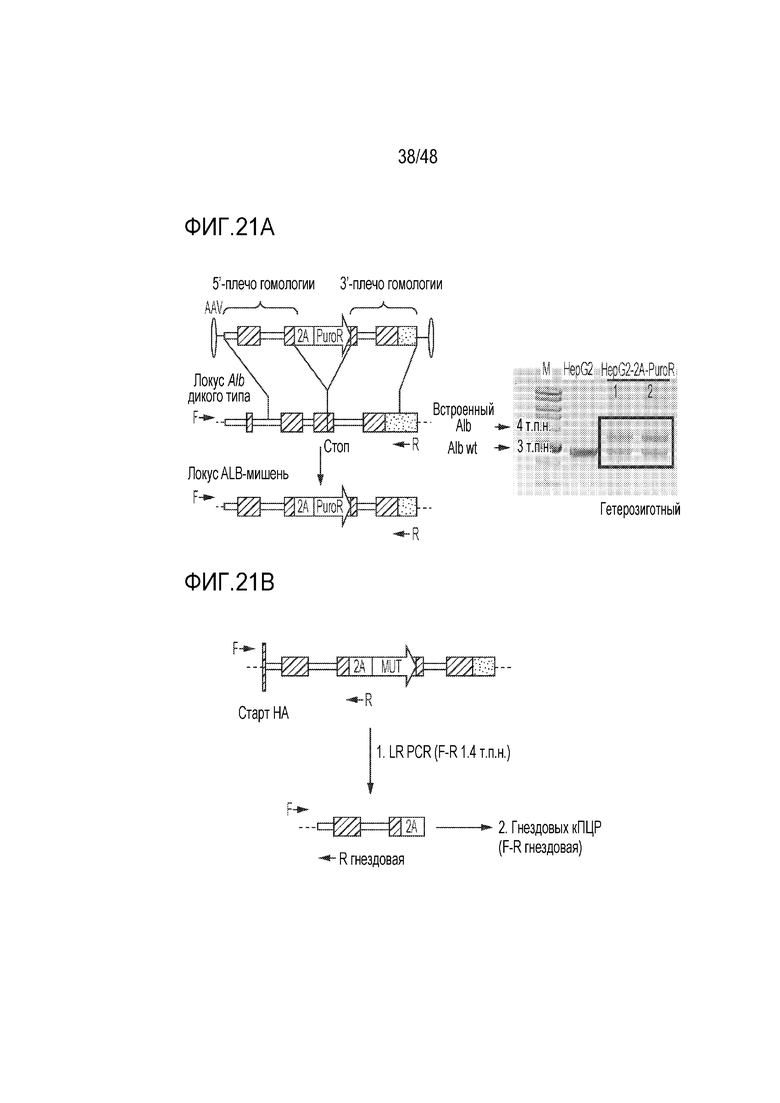
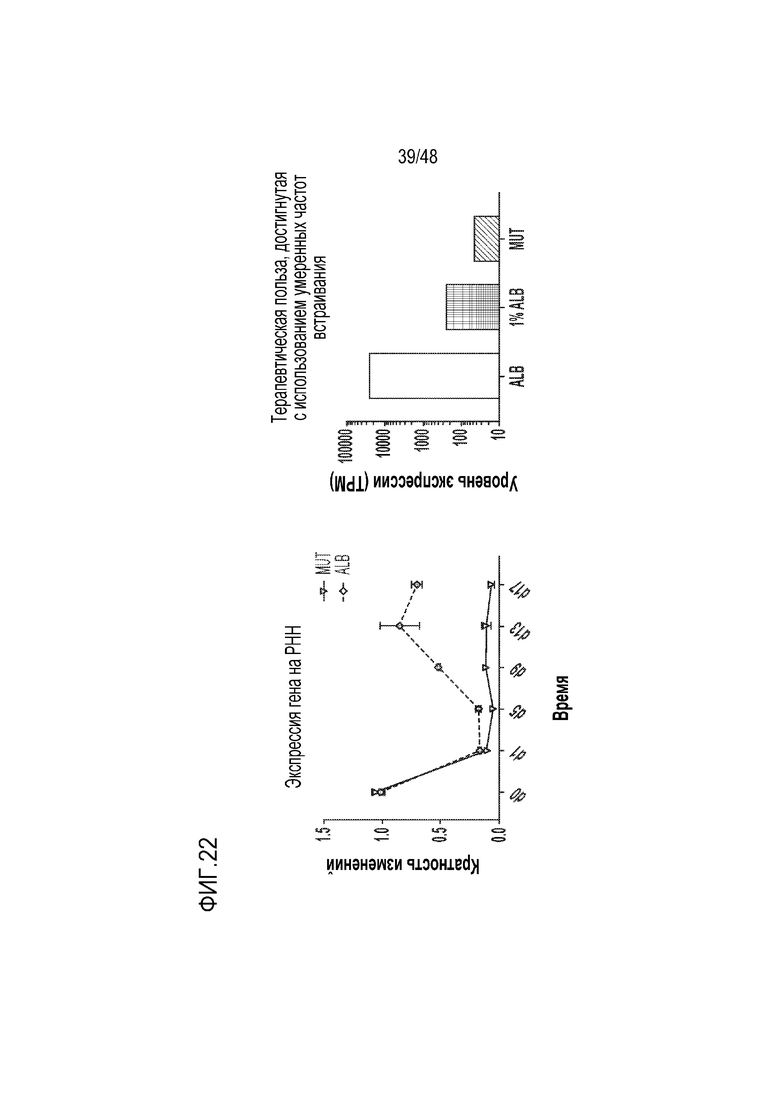
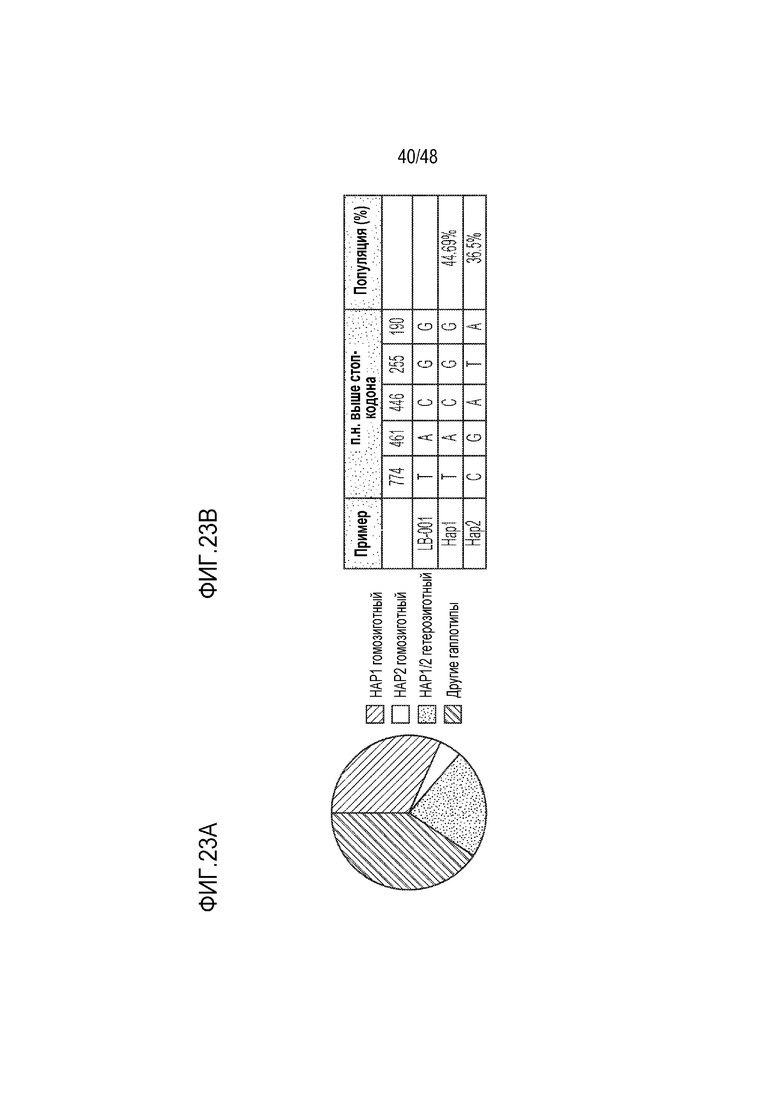
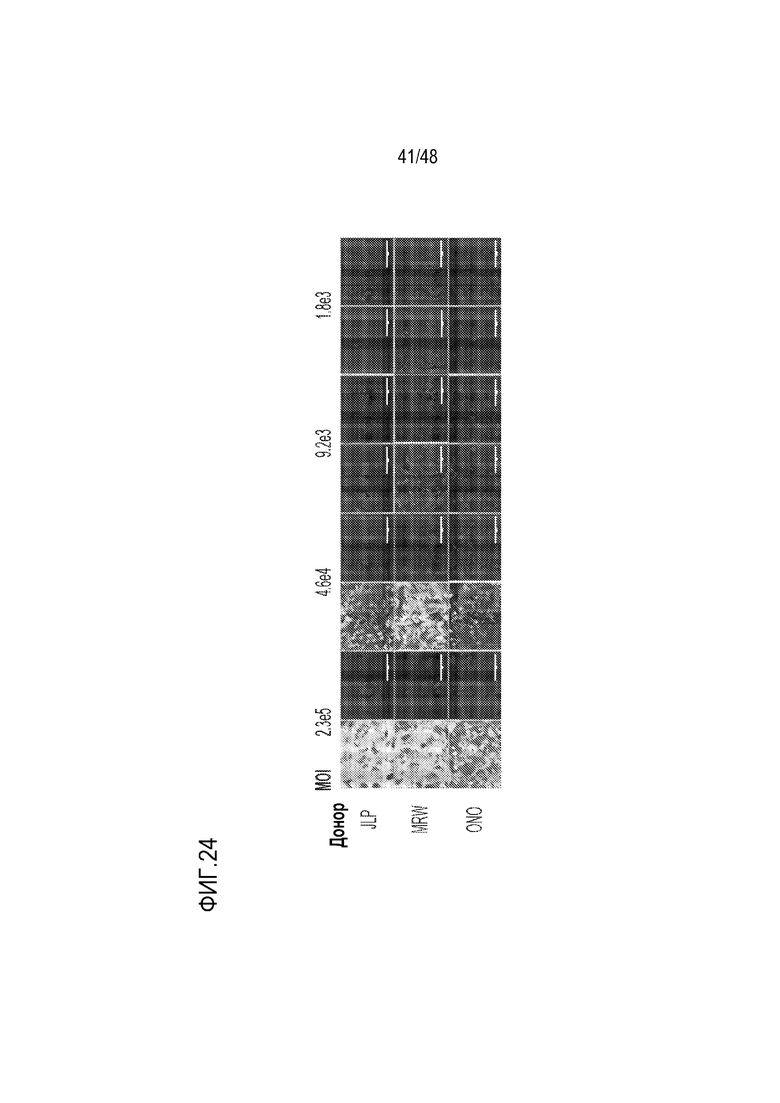
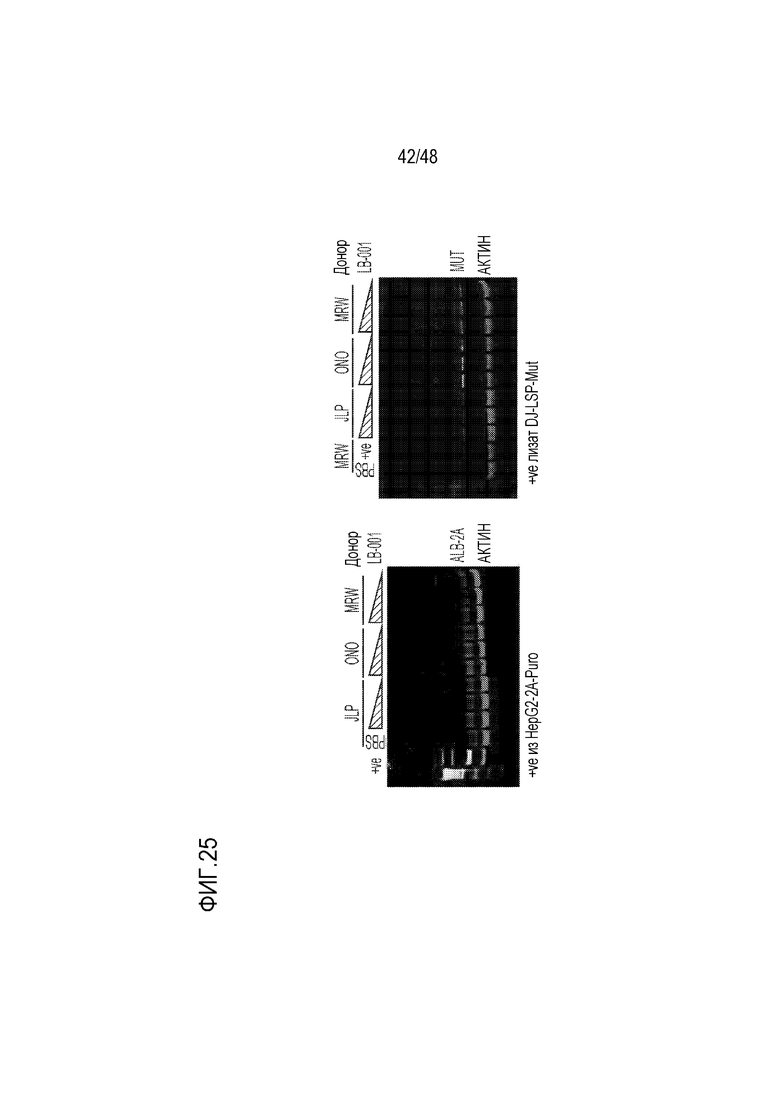
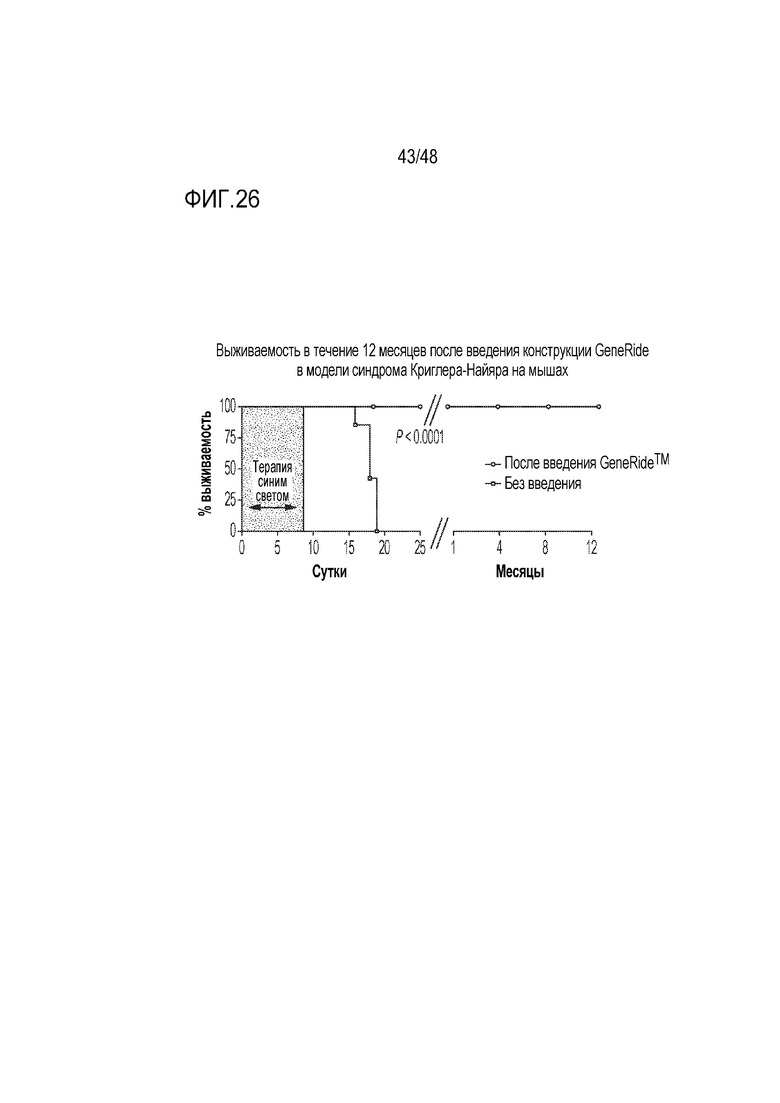
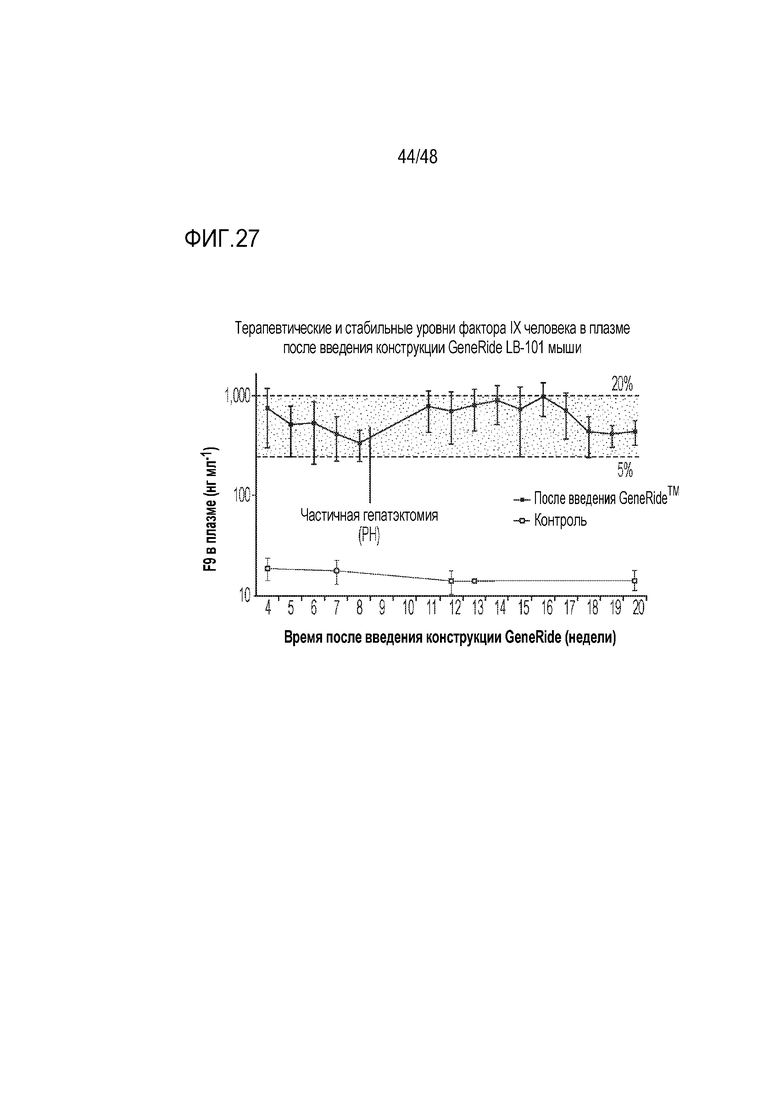
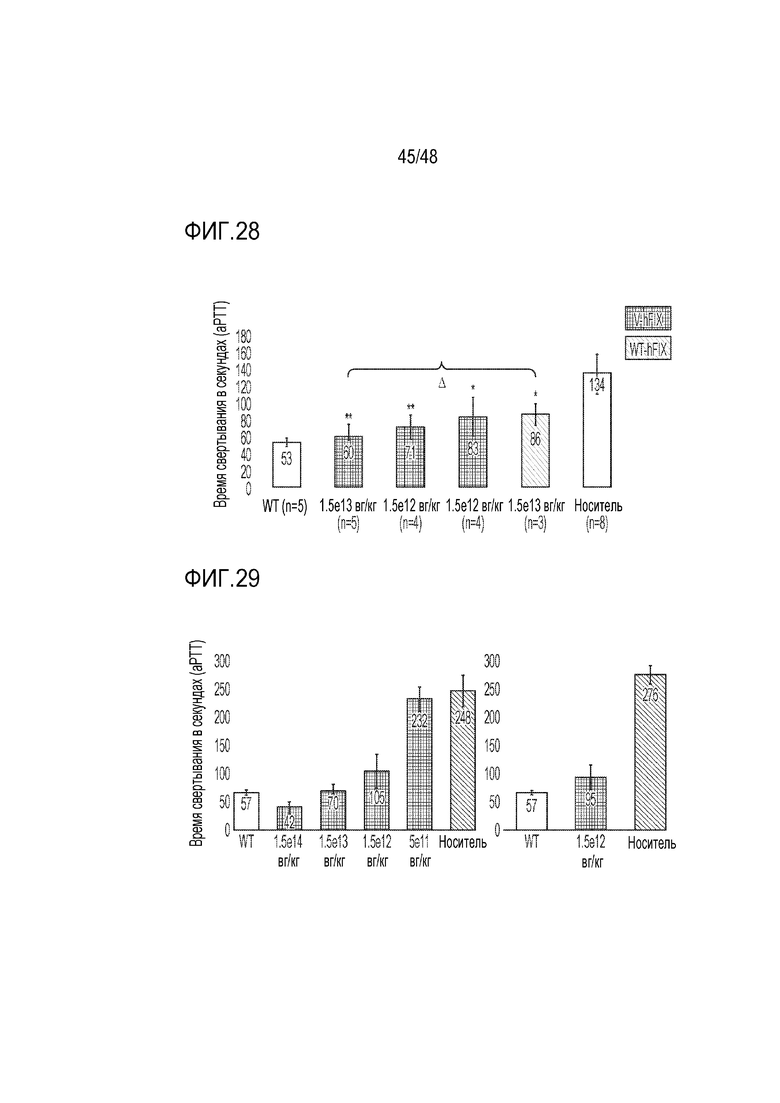
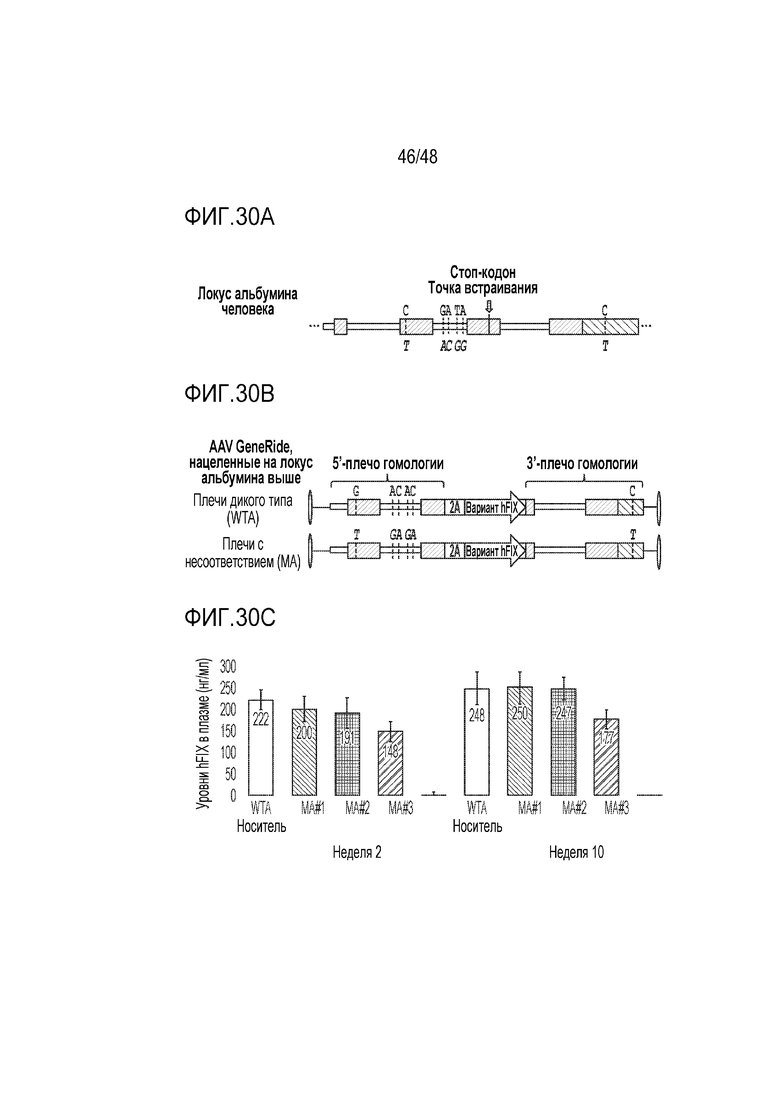
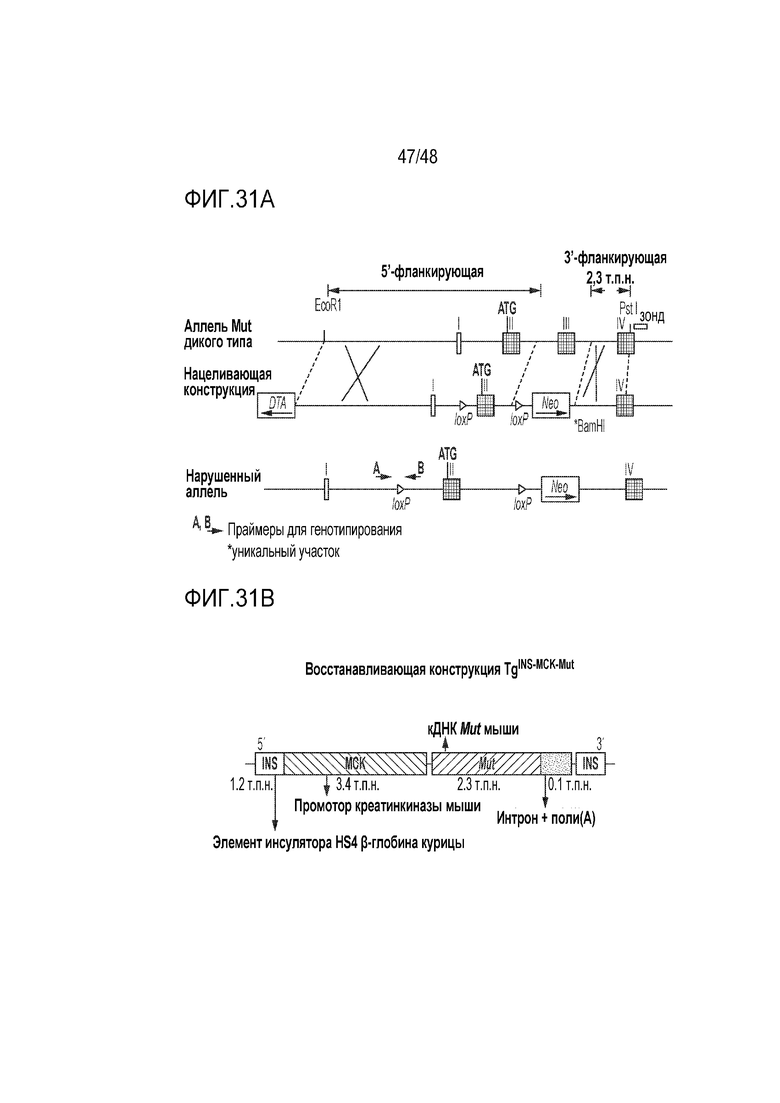
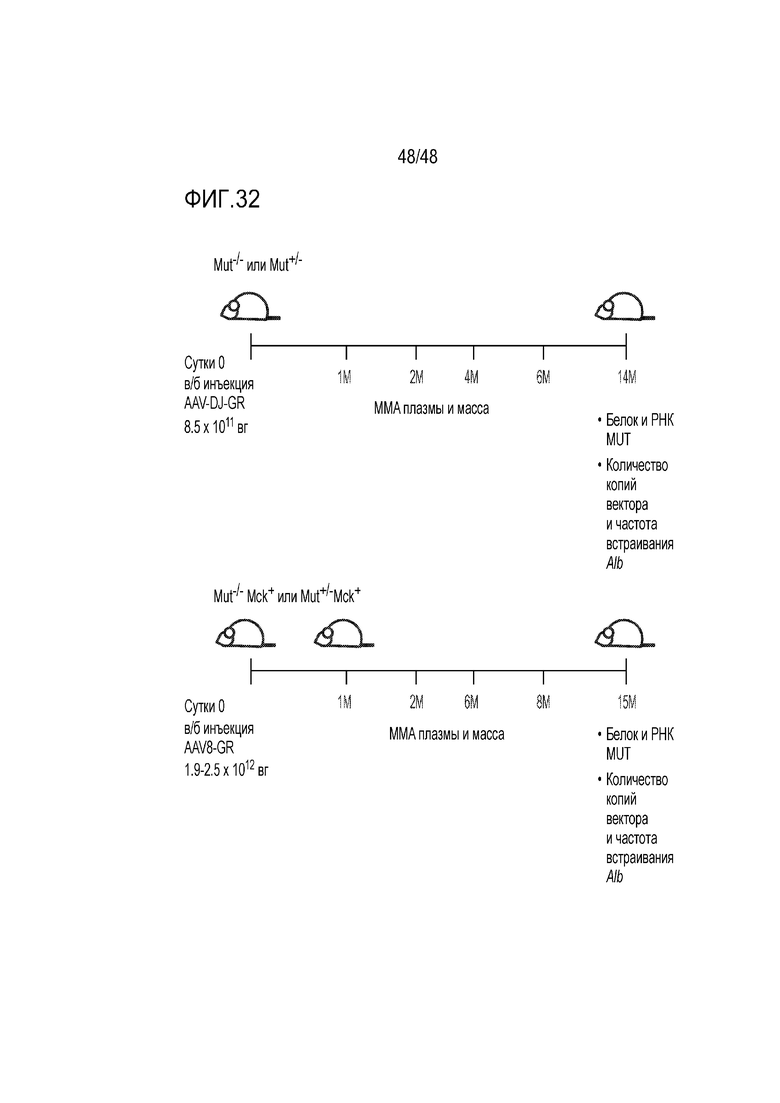
Изобретение относится к области биотехнологии. Описана группа изобретений, включающая способ повышения уровня экспрессии трансгена в ткани и рекомбинантный вирусный вектор для применения при лечении метилмалоновой ацидемии (MMA). В одном варианте реализации способ включает в себя стадию введения индивидууму, нуждающемуся в этом, композиции, которая доставляет трансген, который встраивается в геном по меньшей мере популяции клеток в ткани индивидуума. Изобретение расширяет арсенал средств повышения экспрессии трансгена в ткани. 2 н. и 16 з.п. ф-лы, 32 ил., 4 табл., 18 пр.
1. Способ повышения уровня экспрессии трансгена в ткани, причем указанный способ включает
введение индивидууму, нуждающемуся в этом, композиции, которая доставляет трансген, который встраивается в геном по меньшей мере популяции клеток в ткани индивидуума, где композиция содержит:
полинуклеотидную кассету, содержащую первую последовательность нуклеиновой кислоты и вторую последовательность нуклеиновой кислоты, где первая последовательность нуклеиновой кислоты кодирует трансген, который содержит SEQ ID NO: 9, 12, 13 или 14; и вторая последовательность нуклеиновой кислоты находится с 5’- или 3’-стороны от первой последовательности нуклеиновой кислоты и способствует продуцированию двух независимых продуктов генов при встраивании в участок встраивания, являющийся мишенью, в геноме клетки;
третью последовательность нуклеиновой кислоты, которая имеет длину, равную или превышающую 800 нуклеотидов, и находится с 5’-стороны от полинуклеотидной кассеты, содержащую последовательность, которая по существу гомологична геномной последовательности альбумина человека, находящейся с 5’-стороны от участка встраивания, являющегося мишенью, в геноме клетки; и
четвертую последовательность нуклеиновой кислоты, которая имеет длину, равную или превышающую 800 нуклеотидов, и находится с 3’-стороны от полинуклеотидной кассеты, содержащую последовательность, которая по существу гомологична геномной последовательности альбумина человека, находящейся с 3’-стороны от участка встраивания, являющегося мишенью, в геноме клетки;
где после введения композиции трансген встраивается в геном популяции клеток и уровень экспрессии трансгена в ткани возрастает.
2. Способ по п.1, где встраивание трансгена не включает нуклеазную активность.
3. Способ по п.1 или 2, где увеличенный уровень экспрессии включает увеличенный процент клеток в ткани, экспрессирующих трансген.
4. Способ по любому из пп.1-3, где композиция содержит рекомбинантный вирусный вектор.
5. Способ по п.4, где рекомбинантный вирусный вектор представляет собой рекомбинантный вектор на основе AAV.
6. Способ по п.4, где рекомбинантный вирусный вектор содержит капсидный белок, содержащий аминокислотную последовательность, обладающую по меньшей мере 95% идентичностью последовательности с аминокислотной последовательностью AAV8, представленную последовательностью SEQ ID NO: 4, AAV-DJ, представленную последовательностью SEQ ID NO: 1; AAV-LK03, представленную последовательностью SEQ ID NO: 6, или AAVNP59, представленную последовательностью SEQ ID NO: 8.
7. Способ по п.4, где рекомбинантный вирусный вектор содержит капсидный белок LK03.
8. Способ по п.5, где рекомбинантный вектор на основе AAV содержит нуклеотидную последовательность SEQ ID NO: 15.
9. Способ по любому из пп.1-7, где композиция дополнительно содержит последовательности ITR AAV2.
10. Способ по любому из пп.1-8, где полинуклеотидная кассета не содержит промоторную последовательность.
11. Способ по любому из пп.1-10, где при встраивании полинуклеотидной кассеты в участок встраивания, являющийся мишенью, в геном клетки трансген экспрессируется под контролем эндогенного промотора в участке встраивания, являющемся мишенью.
12. Способ по п.11, где участок встраивания, являющийся мишенью, представляет собой локус альбумина, содержащий эндогенный промотор альбумина и эндогенный ген альбумина.
13. Способ по п.12, где при встраивании полинуклеотидной кассеты в участок встраивания, являющийся мишенью, в геноме клетки трансген экспрессируется под контролем эндогенного промотора альбумина без нарушения экспрессии эндогенного гена альбумина.
14. Способ по любому из пп.1-13, где ткань представляет собой печень.
15. Способ по любому из пп.1-14, где вторая последовательность нуклеиновой кислоты включает:
a) пептид 2A;
b) участок внутренней посадки рибосомы (IRES);
c) N-концевой участок сплайсинга интеина и C-концевой участок сплайсинга интеина; или
d) донор сплайсинга и акцептор сплайсинга.
16. Способ по любому из пп.1-15, где третья и четвертая последовательности нуклеиновых кислот представляют собой плечи гомологии, которые встраивают трансген и вторую последовательность нуклеиновой кислоты в эндогенный локус гена альбумина, содержащий эндогенный промотор альбумина и эндогенный ген альбумина.
17. Способ по п.16, где плечи гомологии направляют встраивание полинуклеотидной кассеты непосредственно с 3'-стороны от инициирующего кодона эндогенного гена альбумина или непосредственно с 5'-стороны от стоп-кодона эндогенного гена альбумина.
18. Рекомбинантный вирусный вектор для применения при лечении метилмалоновой ацидемии (MMA), где рекомбинантный вирусный вектор содержит последовательность SEQ ID NO: 15.
19. Рекомбинантный вирусный вектор по п.18, где рекомбинантный вирусный вектор содержит капсид LK03 AAV.
| US 20170088856 A1, 30.03.2017 | |||
| CA 2864879 A1, 22.08.2013 | |||
| КОМПОЗИЦИИ ВЕКТОРА AAV И СПОСОБЫ ПЕРЕНОСА ГЕНОВ В КЛЕТКИ, ОРГАНЫ И ТКАНИ | 2013 |
|
RU2653444C2 |
| A | |||
| Barzel et al | |||
| Promoterless gene targeting without nucleases ameliorates haemophilia B in mice | |||
| Nature, 2015, V | |||
| МАШИНА ДЛЯ НАКЛЕИВАНИЯ ЭТИКЕТОВ НА БУТЫЛКИ | 1925 |
|
SU517A1 |
| Способ приготовления искусственной массы из продуктов конденсации фенолов с альдегидами | 1920 |
|
SU360A1 |
| Rajiv Sharma et al | |||
| In vivo genome editing of the albumin locus as a platform for protein replacement therapy | |||
| BLOOD, 2015, | |||
Авторы
Даты
2024-06-06—Публикация
2018-10-30—Подача