Изобретение относится к области органической и медицинской химии, к новым биологически активным веществам класса замещенных пирроло[4,5-a]тиено[3,2-e]пиримидинов, а именно к (E)-5-амино-2-оксо-1-(2-(нафталин-2-ил)-2-оксоэтилиден)-1,2,6,7,8,9-гексагидробензо[4,5]тиено[3,2-e]пирроло[1,2-a]пиримидин-3-карбоксамиду формулы:

которое обладает противораковой активностю в терапии рака молочной железы, что позволяет предположить его использование в медицине в качестве лекарственных средств с цитотоксическими свойствами и низкой токсичностью.
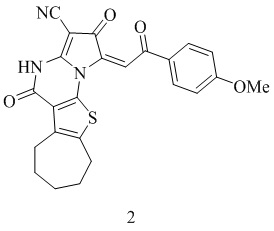
Ближайшим аналогом по структуре для заявляемого соединения является (E)-2,5-диоксо-1-(2-(4-метоксифенил)-2-оксоэтилиден)-1,2,4,5,7,8,9,10-октагидро-6H-циклогепта[4,5]тиено[3,2-e]пирроло[1,2-a]пиримидин-3-карбонитрил 2, обладающий противораковой активностью [European Journal of Medicinal Chemistry, 2023, Vol. 254, pp. 115325] формулы:
Приведены данные по противораковой активности.
4T1
MEF NF2
Эталоном сравнения биологической активности был выбран Карбоплатин формулы:

который был одобрен FDA для лечения рака молочной железы и является аналогом по действию [Łakomska I. Cytotoxic malonate platinum(II) complexes with 1,2,4-triazolo[1,5-a]pyrimidine derivatives: structural characterization and mechanism of the suppression of tumor cell growth / J Inorg Biochem. – 2014 Dec; 141:188-197. – [Electronical resource]. – URL: DOI: 10.1016/j.jinorgbio.2014.08.005.],[ Carboplatin (NSC 241240) . – [Electronical resource]. – URL: https://www.selleckchem.com/products/Carboplatin.html], [Clark CC. Enhancement of synthetic lethality via combinations of ABT-888, a PARP inhibitor, and carboplatin in vitro and in vivo using BRCA1 and BRCA2 isogenic models / Mol Cancer Ther. – 2012 Sep;11(9):1948-58. – [Electronical resource]. – URL: DOI: 10.1158/1535-7163.MCT-11-0597]
Задачей изобретения является поиск в ряду производных замещенных пирроло[4,5-a]тиено[3,2-e]пиримидинов веществ с выраженной противораковой активностью в терапии рака молочной железы и низкой токсичностью в отношении здоровых тканей для расширения арсенала цитотоксических средств.
Технический результат достигается химическим синтезом и применением (E)-5-амино-2-оксо-1-(2-(нафталин-2-ил)-2-оксоэтилиден)-1,2,6,7,8,9-гексагидробензо[4,5]тиено[3,2-e]пирроло[1,2-a]пиримидин-3-карбоксамида, который обладает противораковой активностью в терапии рака молочной железы и низкой токсичностью в отношении здоровых тканей.
Заявляемое соединение 1 синтезируют взаимодействием нитрила (E)-2-((2-оксо-5-(нафталин-2-ил)фуран-3(2H)-илиден)амино)-4,5,6,7-тетрагидробензо[b]тиофен-3-карбоновой кислоты с амидом цианоуксусной кислоты в присутствии 1 эквивалента диизопропилэтиламина. Реакция протекает в диоксане при перемешивании и температуре 50°С в течение 3 часов с последующим выделением целевых продуктов известными методами по схеме:

Однако из патентной и научно-технической литературы не выявлено применение соединения 1 в качестве средств с цитотоксическими свойствами в терапии рака молочной железы.
Изобретение иллюстрируется примерами исследования фармакологических свойств.
Пример 1. Получение соединения 1.
К раствору 3.84 г (0.01 моль) (E)-2-((2-оксо-5-(нафталин-2-ил)фуран-3(2H)-илиден)амино)-4,5,6,7-тетрагидробензо[b]тиофен-3-карбоновой кислоты в 50 мл безводного диоксана прибавляли 0.89 г (0.01 моль) амида цианоуксусной кислоты и нагревали до полного растворения. Затем полученный раствор остужали до 50 °С и добавляли 1.29 г (0.01 моль) диизопропилэтиламина, полученный раствор выдерживали 3 часа при температуре 50 °С при интенсивном перемешивании. Смесь охлаждали до 0°С, выпавший осадок отфильтровывали и перекристаллизовывали.
Выход 74 %, т. пл. 253-254°С (диоксан). Спектр ЯМР 1Н (CDCl3+CF3COOH), δ, м. д.: 2.03 (м, 4H), 2.91 (м, 2H), 2.98 (м, 2H), 7.28 (уш. с, 1Н), 7.41 (с, 1Н), 7.63 (м, 2Н), 7.97 (м, 5Н), 8.49 (уш. с, 1Н). Спектр ЯМР 13C (CDCl3+CF3COOH), δ, м. д.: 20.9, 21.3, 24.2, 24.5, 88.3, 112.3, 120.8, 122.7, 127.0, 127.4, 128.9, 128.9, 129.3, 129.5, 131.7, 131.9, 132.1, 132.8, 134.9, 136.2, 145.6, 145.6, 156.2, 156.9, 166.3, 176.1, 190.7. Найдено, %: C, 66.66; H, 4.27; N, 11.94; S, 6.86. C26H20N4O3S. Вычислено, %: C, 66.65; H, 4.30; N, 11.96; S, 6.84.
Полученное соединение 1 представляет собой желтое кристаллическое вещество, растворимое в ДМСО, при нагревании в толуоле, ацетоне, не растворимое в воде и гексане.

Пример 2. Для оценки противоопухолевой активности соединения 1 использовался стандартный тест с использованием резазурина [Lancaster MV, Fields RD (1996) Antibiotic and cytotoxic drug susceptibility assays using resazurin and poisoning agents. U.S. Patent No. 5,501,959]. Клеточная линия 4T1 культивировалась с использованием среды RPMI (Биолот) + 10% ФБС (фетальной бычьей сыворотки) (Биолот), линия MEF NF2 – ДМЕМ (Биолот) +10% ФБС при температуре 37°С в увлажненной атмосфере 5% CO2 (СО2 инкубатор с воздушной рубашкой Panasonic (Sanyo) MCO-18AC (MCO-18AC-PE)). Пассажировали дважды в неделю (при 80% конкуренции) при плотности 4 x 104 клеток на см2.
В 96 луночный планшет (TC-treated Culture Microplate, Corning) заносили клетки в размере 10 тыс. кл. на лунку + 100 мкл среды. Перед добавлением к клеточным культурам все тестируемые соединения растворяли в ДМСО (500 мкл - 10 мМ); затем разводили в клеточной среде (40 мкл в среде 960 мкл) и получали раствор 400 мкМ. После этого в лунки с клетками (4T1 и MEF NF2) добавляли несколько концентраций тестируемых соединений (0.8, 1.6, 3.2, 6.3, 12.5, 25, 50 мкM). Спустя 48 часов среду заменяли раствором среды + 10% резазурина (Resazurin sodium salt, Sigma-Aldrich) и инкубировали 4 часа. В качестве положительного контроля использовали лунки с клетками без внесения вещества. В качестве отрицательного контроля – лунки без клеток с добавлением среды с резазурином. После инкубации среду с резазурином из всех лунок переносили на чистый планшет и оценивали на спектрофотометре на длинах волн 570 нм и 600 нм. Жизнеспособность оценивали по стандартным формулам.
Пример 3. Острую токсичность (ЛД50, мг/мл) соединения 1 определяли по методу Г. Н. Першина [Першин Г. Н. Методы экспериментальной химиотерапии // М., С. 100, 109-117 (1971)]. Соединение 1 вводили внутрибрюшинно белым мышам массой 16-18 г в виде взвеси в 2% крахмальной слизи и наблюдали за поведением и гибелью животных в течение 10 суток. Для исследуемого соединения 1 ЛД50 составляет > 1500 мг/кг.
Согласно классификации токсичности препаратов соединение 1 относится к V классу практически нетоксичных препаратов [Измеров Н.Ф., Саноцкий И.В., Сидоров К.К. Параметры токсикометрии промышленных ядов при однократном воздействии: Справочник. М., 1977. – с. 196]. Результаты испытаний представлены в таблице:
Противораковая активность соединения 1.
4T1
MEF NF2
Как видно из таблицы, заявляемое соединение 1 проявляет выраженную противораковую активность и превышает таковую препарата сравнения, используемого в медицинской практике по отношению к терапии рака молочной железы. В то же самое время предложенное соединение 1 является более чем в 12 раз менее токсично чем препарат сравнения. Таким образом, (E)-5-амино-2-оксо-1-(2-(нафталин-2-ил)-2-оксоэтилиден)-1,2,6,7,8,9-гексагидробензо[4,5]тиено[3,2-e]пирроло[1,2-a]пиримидин-3-карбоксамид проявляет более высокую активность по сравнению с используемым в медицине препаратом сравнения, что делает возможным его использование для создания новых лекарственных средств целенаправленного действия с низкой токсичностью в отношении здоровых тканей.
Изобретение относится к области органической и медицинской химии, к новым биологически активным веществам класса замещенных пирроло[4,5-a]тиено[3,2-e]пиримидинов, а именно к (E)-5-амино-2-оксо-1-(2-(нафталин-2-ил)-2-оксоэтилиден)-1,2,6,7,8,9-гексагидробензо[4,5]тиено[3,2-e]пирроло[1,2-a]пиримидин-3-карбоксамиду формулы 1, применяющемуся как противораковое средство в терапии рака молочной железы. Технический результат заключается в получении соединения ряда замещенных пирроло[4,5-a]тиено[3,2-e]пиримидинов с выраженной противораковой активностью в терапии рака молочной железы и низкой токсичностью в отношении здоровых тканей. 2 табл., 3 пр.

(E)-5-амино-2-оксо-1-(2-(нафталин-2-ил)-2-оксоэтилиден)-1,2,6,7,8,9-гексагидробензо[4,5]тиено[3,2-e]пирроло[1,2-a]пиримидин-3-карбоксамид формулы:
 ,
,
применяющийся как противораковое средство в терапии рака молочной железы.
| ŁAKOMSKA I | |||
| et al, Cytotoxic malonate platinum(II) complexes with 1,2,4-triazolo[1,5-a]pyrimidine derivatives: structural characterization and mechanism of the suppression of tumor cell growth, J Inorg Biochem, 2014, vol.141, p.188-197 | |||
| CLARK C.C | |||
| et al, Enhancement of synthetic lethality via combinations of ABT-888, a PARP inhibitor, and |
Авторы
Даты
2024-06-07—Публикация
2023-07-14—Подача