Изобретение относится к области медицины, а именно к онкологии, в частности к химиотерапии злокачественных новообразований.
В России ежегодно диагностируются более 600000 новых случаев онкологических заболеваний, из которых 55% подлежат срочному операционно-хирургическому вмешательству, особенно при раке молочной железы, желудка, толстой кишки, матки, щитовидной и предстательной желез, меланоме.
Однако, современные методы диагностирования (эхография, компьютерная и магнитно-резонансная томографии, радионуклидная диагностика и др.) не могут дать точного ответа о наличии или отсутствии микрометастаз в лимфатических узлах, что приводит к неверному дооперационному стадированию заболевания и к ошибкам в выборе хирургической тактики.
В последние годы в мире успешно развивается метод непрямой цветной лимфографии «сторожевых» лимфоузлов.
Пока зарегистрирован только один препарат - «Лимфазурин» и его дженерик «Isosulfan blue injection 1%» («Lymphazurin injection 1%») (США), которые представляют собой буферный раствор красителя Изосульфана синего.
Однако, высокая цена, достигающая 1000 долларов США за флакон (50 мл, 50 мг), и отсутствие поставок этого препарата не только на европейский рынок, но и в Российскую Федерацию, делает его недоступным для широкого клинического применения в российских онкологических клиниках.
Согласно патентам US 1531507; US 1805925; US 1878530; US 2422 445; US 2726252; US 4330476; US 4710322; US 5659053; US 7534911; US 7662992, способ получения красителя «Изосульфан синий» общей формулы
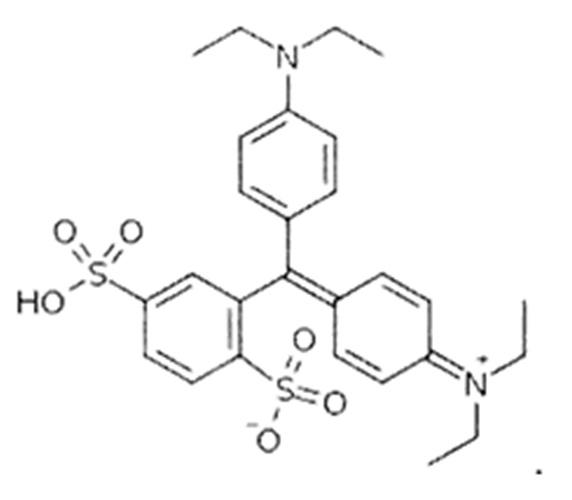
основывается на многостадийном синтезе, в котором в качестве исходного соединения участвует 2-хлорбензальдегид.
Самым близким (прототипом) является способ получения Изосульфана синего (US 7662992). Где предложен способ получения промежуточного соединения, натриевой соли 2-хлорбензальдегид-5-сульфоновой кислоты формулы (2), используемого при его получении, и способ выделения динатриевой соли бензальдегид-2,5-дисульфоновой кислоты формулы (3). Также предложен способ получения изолейкокислоты формулы (4), которая при мягком окислении дает Изосульфан синий фармацевтического качества, который можно использовать для приготовления фармацевтических составов.
Однако, при изучении прототипа, выявлены следующие недостатки получения, а именно: сульфирование 2-хлорбензальдегида осуществлялось в течение 16 часов при 70°С с выходом от 50-56% соответствующей 2-хлорбензальдегид-5-сульфокислоты. Замещение хлора на сульфогруппу осуществлялось с выходом 90-95% соответствующей динатриевой соли 2,5-дисульфобензальдегида. Стадия конденсации динатриевой соли 2,5-дисульфобензальдегида с N,N-диэтиланилином осуществлялся либо в ледяной уксусной кислоте в присутствии каталитических количеств карбамида, либо в среде концентрированной соляной кислоты. Выход соответствующего трифенилмета-нового производного (динатриевой соли изолейкокислоты) или [2-бис(4-диэтиламино) фенил)метилбензол-1,4-дисульфокислоты] составлял всего 25-35%. Окисление динатриевой соли [2-бис(4-диэтиламино) фенил)метилбензол-1,4-дисульфокислоты] осуществлялось с выходом 30-45% в зависимости от используемого окислителя. Таким образом, суммарный выход конечного продукта Изосульфана синего составлял всего от 7,3% до 8,3%.
Из этого следует, что исходный продукт синтеза Изосульфана синего во всех известных патентах являлся 2-хлорбензальдегид, который на территории Российской Федерации не производится.
Следовательно, разработка нового способа получения 2-хлорбензальдегида и последующего синтеза красителя «Изосульфан синий» из отечественного сырья является актуальной задачей.
Задачей изобретения является предоставление способа получения Изосульфана синего из отечественного сырья с высоким выходом.
Указанная задача решается тем, что конечный продукт получают окислением динатриевой соли 2-[бис[4-(диэтиламино)фенил]метил]бензол-1,4-дисульфокислоты, при этом в качестве исходного реагента используют толуол и этапы получения Изосульфана синего включают следующие стадии:
а) каталитическое хлорирование толуола с получением смеси 2-хлортолуола и 4-хлортолуола;
б) объединенное окисление, полученных на стадии (а) 2-хлор- и 4-хлортолуолов в среде серной кислоты до соответствующих альдегидов, с последующим выделением 4-хлорбензальдегида из сульфомассы экстракцией;
в) сульфирование комплекса 2-хлорбензальдегида и концентрированной серной кислоты олеумом до образования 2-хлорбензальдегид-5-сульфокислоты;
г) добавление к водному раствору сульфита натрия, полученной на стадии (в) 2-хлорбензальдегид-5-сульфокислоты с получением динатриевой соли 2,5-дисульфобензальдегида;
д) конденсацию динатриевой соли 2,5-дисульфобензальдегида с N,N-диэтиланилином в присутствии каталитического количества гексахлорфосфазотриена;
e) окисление динатриевой соли изолейконовой кислоты в Изосульфан синий.
Компанией «Скандия Эко» совместно с ИОХ им.Н.Д. Зелинского РАН, ФГБУ «НМИЦ радиологии» Минздрава России, МНИОИ им. П.А. Герцена была разработана новая технология получения красителя «Изосульфан синий», в которой используется исключительно отечественное сырье.
В основу технологии получения Изосульфана синего авторами изобретения заложено использование толуола - широко распространенного химического продукта, производство которого в РФ насчитывает более одного миллиона тонн в год.
Известно, что при хлорировании толуола в присутствии катализаторов образуется смесь монохлортолуолов: 2-хлортолуола и 4-хлортолуола (А.С. СССР №956443). Монохлортолуолы легко окисляются в кислой среде с образованием соответствующих альдегидов (А.С. СССР №50850). Однако разделение соответствующих монохлорбензальдегидов представляло собой серьезную техническую задачу из-за близости физических констант 2-хлор- и 4-хлорбензальдегидов, которая была успешно решена в настоящей заявке. Вышеназванные изомерные альдегиды были легко разделены в серной кислоте, которая образует устойчивый комплекс с 2-хлорбензальдегидом и практически не взаимодействует с 4-хлорбензальдегидом, который легко отделяется от сульфомассы.
Способ осуществляют следующим образом.
В качестве исходного продукта используют толуол, причем смесь 2-хлортолуола и 4-хлортолуола получают каталитическим хлорированием в присутствии ацетонитрила. В среде серной кислоты происходит объединенное окисление орто-хлор- и пара-хлортолуолов до соответствующих альдегидов с последующим выделением 4-хлорбензальдегида из сульфомассы экстракцией хлористым метиленом. К устойчивому комплексу 2-хлорбензальдегида и серной кислоты добавляют 60% олеум и сульфируют до образования соответствующего 2-хлорбензальдегид-5-сульфокислоты, которую выделяют экстракцией этилацетатом с последующим удалением растворителя. К водному раствору сульфита натрия добавляют 2-хлорбензальдегид-5-сульфокислоту и кипятят с обратным холодильником до полной замены хлора на сульфогруппу. Конденсацию динатриевой соли 2,5-дисульфобензальдегида с N,N-диэтиланилина осуществляют в присутствии каталитического количества гексахлорфосфазотриена.
Этапы получения
К сульфомассе, содержащей 2-хлорбензальдегид, добавляют 60% олеум и поднимают температуру до 80° Цельсия (что сократило время сульфирования практически в три раза - 5 часов (вместо 16 часов сульфирование). Выход конечного продукта составил 95%.
Далее, вместо разбавления сульфомассы водой, полученную 2-хлорбензальдегид-5-сульфокислоту экстрагировали этилацетатом, что существенно упрощало стадию выделения выше названного продукта. Этилацетат обрабатывают сухим сульфатом натрия и упаривают в вакууме оставляя в остатке чистую 2-хлорбензальдегид-5-сульфокислоту, которую обрабатывают сульфитом натрия в кипящем водном растворе. После испарения водного раствора и перекристаллизации из спирта получают чистую динатриевую соль бензальдегид-2,5-дисульфокислоты. Выход конечного продукта составил 85-90%.
Известно, что конденсацию диэтиланилина с бензальдегид-2,4-дисульфокислотой в присутствии каталитических количеств гексахлорфосфазотриена (фосфазена) осуществляют в течение одного часа и с высоким выходом (А.С. СССР №219725). Для бензальдегид-2,5-дисульфокислоты данная конденсация с N,N-диэтиланилином не проводилась.
Конденсация динатриевой соли 2,5-дисульфобензальдегида с N,N-диэтиланилином в присутствии каталитического количества гексахлорфосфазотриена
Оказалась, что увеличив количество фосфазена на 5-10% по сравнению с приведенным примером, удалось в течение одного часа провести конденсацию динатриевой соли 2,5-дисульфобензальдегида и N,N-диэтиланилина. Выход конечного продукта динатриевой соли изолейкокислоты составил 89%.
Окисление динатриевой соли 2-[бис[4-(диэтиламино)фенил]метил]бензол-1,4-дисульфокислоты осуществляют перманганатом натрия до получения соответствующего Изосульфана синего. Очистку проводят двухкратным переосаждением из чистой воды натриевой соли Изосульфана синего. Выход конечного продукта составил 90%, чистота продукта составила 99,3%.
Таким образом, поставленная задача перед авторами настоящего изобретения была выполнена успешно и разработан новый способ получения Изосульфана синего из отечественного сырья с общим выходом конечного продукта 73-76%).
Экспериментальная часть получения красителя Изосульфана синего (4-{[4-(диэтиламино)фенил](2,5-дисульфофенил)метилиден}-N,N-диэтилциклогекса-2,5-диен-1-иминий).
1. Получение N-окиси пиридина
В трехгорлой колбе с обратным холодильником и капельной воронкой смешивают 248 мл ледяной уксусной кислоты с 124 мл 30%-ной перекиси водорода и 8 мл концентрированной H2SO4, не прекращая перемешивания к приготовленной окислительной смеси постепенно прибавляют 158 г пиридина, затем нагревают смесь при 75-80°С в течение 6 часов. После 2 ч нагревания в реакционную смесь медленно прикапывают 8 мл второй порции концентрированной H2SO4, после 4 часов нагревания прикапывают 8 мл третьей порции конц. H2SO4. После окончания нагревания реакционную смесь охлаждают, дважды экстрагируют хлороформом, хлороформенную вытяжку промывают водой, высушивают, хлороформ отгоняют, а остаток перегоняют в вакууме. Выход N-окиси пиридина 182 г (96%).
2. Получение гексахлорциклофосфазатриена (фосфазена), катализатора конденсации динатриевой соли бензальдегид-2,5-дисульфокислоты и N,N-диэтиланилина
В 1000 мл трехгорлую колбу, снабженную механической мешалкой, термометром, и обратным холодильником, загружают 500 мл хлорбензола, 104,1 г (0,5 моль) пятихлористого фосфора и 120 г сухого хлорида аммония, а также 4,0 г N-окиси пиридина (0,02 моля на моль PCl5), которую используют в качестве катализатора реакции конденсации. Далее реакционную массу интенсивно перемешивают и нагревают до 130-132°С (до температуры кипения хлорбензола). Кипящую реакционную массу выдерживают в течение 8 часов, затем охлаждают, отгоняют хлорбензол в вакууме, а из оставшейся массы экстрагируют фосфазен петролейным эфиром. Петролейный эфир упаривают в вакууме, остается белое кристаллическое вещество с Т пл. 114-116°С (лит. Т пл. 114-116°С). Выход фосфазена составляет 101,3 г (88,5%).
3. Получение смеси 2-хлор- и 4-хлортолуолов
Через смесь 600 мл толуола и 300 мл ацетонитрила, предварительно насыщенного HCl, при температуре 20-25°С, пропускают газообразный хлор со скорость 12 л/ч, температура реакции 20-25°С, время реакции 60 минут. Конверсия толуола в монохлортолуолы составляет 100%. Соотношение орто-хлортолуола к пара-хлортолуолу составляет 55,6% к 44,4%. Ацетонитрил удаляют в вакууме и возвращают в реакцию хлорирования толуола. Полученную смесь монохлортолуолов передают на стадию окисления в соответствующий моно-хлорбензальдегид.
4. Получение и разделение смеси 2-хлорбензальдегида и 4-хлорбензальдегида
Полученную на предыдущей стадии смесь монохлортолуолов, при перемешивании и охлаждении, медленно добавляют к 98% серной кислоте, а затем добавляют двуокись марганца. Температуру смеси поднимают до 40°С и выдерживают в течение 1 часа. В результате окислительной реакции метильная группа монохлортолуолов окисляется в альдегидную и реакцию окисления останавливают. Причем образовавшийся 2-хлорбензальдегид образует прочный комплекс с 98% серной кислотой, а 4-хлорбензальдегид не вступает в реакцию с 98% серной кислотой и отделяется с помощью экстракции хлористым метиленом. Оставшийся комплекс 2-хлорбензальдегида и серной кислоты используют для дальнейшего сульфирования в 2-хлорбензальдегид-5-сульфокислоту. Наличие сульфата марганца в реакционной смеси не влияет на дальнейшее сульфирование 2-хлорбензальдегида. Физические свойства 4-хлорбензальдегида: Т пл. 45-50°С (лит. 45-51°С (PubChem, CID 7726)).
5. Сульфирование 2-хлорбензальдегида в 2-хлорбензальдегид-5-сульфокислоту
В литровую четырехгорлую колбу с верхней мешалкой, капельной воронкой, обратным холодильником и термометром помещают 250 г комплекса 2-хлорбензальдегида в серной кислоте, содержащего 105-110 г 2-хлорбензальдегида. Из капельной воронки, при охлаждении и интенсивном перемешивании добавляют 40 мл 60% олеума для получения в конечном результате 28-30%-ного олеума. Образовавшуюся реакционную массу перемешивают 1 час при 20°С, а затем температуру реакционной массы увеличивают до 80-85°С и выдерживают 4-5 часов до полного исчезновения 2-хлорбензальдегида. Контроль осуществляют с помощью ТСХ. Реакционную смесь охлаждают до 25-30°С и конечный продукт 2-хлорбензальдегид-5-сульфокислоту экстрагируют этилацетатом. Этилацетат удаляют в вакууме, а 2-хлорбензальдегид-5-сульфокислоту добавляют к концентрированному раствору сульфита натрия. Реакционную смесь нагревают до 100°С с обратным холодильником и выдерживают 5-6 часов. Затем реакционную смесь упаривают в вакууме, а сухой остаток смешивают в 500 мл метанола.
Все образовавшиеся сульфаты отделяют фильтрацией. Раствор метанола упаривают в вакууме и получают динатриевую соль бензальдегид-2,5-дисульфокислоты. Выход динатриевой соли бензальдегид-2,5-дисульфокислоты составляет 78,3 г (89%).
6. Конденсация динатриевой соли 2,5-дисульфобензальдегида с N,N-диэтиланилином и фосфазеном
В колбу с термометром, мешалкой, обратным воздушным холодильником и трубкой для ввода азота помещают 13,0 г (0,04 моль) гексахлорциклофосфазатриена, 37,5 г (0,12 моль) динатриевой соли бензальдегид-2,5-дисульфокислоты, 80 мл диэтиланилина и нагревают смесь в токе азота на глицериновой бане при 120°С и размешивают. Через 40 мин происходит экзотермическая реакция и температура в колбе поднимается до 145°С. При этом реакционная масса делается вязкой и окрашивается в бирюзовый цвет. Массу нагревают еще 50 мин при 140°С (пока она не затвердеет). Ее охлаждают, добавляют 100 мл воды и 26 г соды, а затем добавляют ацетон, который высаживает продукт конденсации, осадок отфильтровывают, промывают на фильтре ацетоном и сушат при 50°С. Получают 53,1 г (83%) динатриевой соли 2-[бис[4-(диэтиламино)фенил]метил]бензол-1,4-дисульфокислоты.
7. Окисление динатриевой соли изолейконовой кислоты в Изосульфан синий
750 мл метанола и 750 мл ацетонитрила загружают в 3-литровую колбу с тремя горлышками с верхней мешалкой, конденсатором и термометром, к этому раствору добавляют 50 г (0,09 М) динатриевой соли 2-[бис[4-(диэтиламино)фенил]метил]бензол-1,4-дисульфокислоты. Суспензию охлаждают до 0…+5°С. Добавляют 35,6 г (0,10 М) перманганата натрия (40% раствор в воде) в одну партию при 0-50°С и перемешивают реакционную массу в течение 1 часа. Реакцию контролируют методом ВЭЖХ и после завершения реакции, реакционную массу отфильтровывают через слой силикагеля и промывают 200 мл метанола. Фильтрат загружают в 3 л колбу и отгоняют фильтрат под вакуумом при температуре 30-35°С. Остаток охлаждают до 25-30°С и добавляют 100 мл воды для получения прозрачного раствора. К прозрачному раствору добавляют 1000 мл третичного бутанола и перемешивают в течение 2 часов при 25-30°С. Полученное таким образом твердое вещество собирают путем фильтрации. Твердое вещество высушивают в вакууме при температуре 50-55°С в течение 10-12 часов. Получают 39 г Изосульфана синего (I), имеющего ТСХ чистоту более 99,0%. Выход конечного продукта составлял 75%. Продукт очищают перекристаллизацией из водного изопропанола. Чистота конечного продукта 99,5%.
8. Окончательная очистка Изосульфана синего
35 г Изосульфана синего загружают в 1 л колбу с тремя горлышками, добавляют 70 мл воды и перемешивают в течение 20 минут при температуре 25-30°С. К реакционной массе добавляют 350 мл третичного бутанола при температуре 25-30°С. Осажденное твердое вещество перемешивают в течение 2 часов при температуре 25-30°С. Твердое вещество собирают путем фильтрования и сушат в вакуумной печи при температуре 40-45°С в течение 10-12 часов для получения 26,6 г чистого Изосульфана синего, имеющего чистоту ТСХ, превышающую 99,8%.
Предложенный новый способ получения красителя Изосульфан синий из отечественного сырья позволил также получить чистый 4-хлорбензальдегид - важный продукт органического синтеза. Благодаря новой технологии выход конечного Изосульфана синего возрос с 3,0% до 75%. Предложенный способ может найти применение в медицине при химиотерапии опухолей.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВЫДЕЛЕНИЯ ЛИМФОТРОПИНА ИЗ ПРОМЫШЛЕННОГО КРАСИТЕЛЯ "ДИСУЛЬФИНОВЫЙ ГОЛУБОЙ" | 2021 |
|
RU2782930C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ИНТРАОПЕРАЦИОННОЙ ВИЗУАЛИЗАЦИИ ЛИМФАТИЧЕСКИХ УЗЛОВ МЕТОДОМ НЕПРЯМОЙ ЦВЕТНОЙ ЛИМФОГРАФИИ | 2018 |
|
RU2687092C2 |
| СПОСОБ ПОЛУЧЕНИЯ СМЕСЕВОГО ПЛАСТИФИКАТОРА | 1999 |
|
RU2148574C1 |
| 3-(3,5-ДИНИТРОПИРАЗОЛ-4-ИЛ)-4-НИТРОФУРАЗАН, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ ЕГО В КАЧЕСТВЕ ТЕРМОСТОЙКОГО ВЗРЫВЧАТОГО ВЕЩЕСТВА | 2007 |
|
RU2343150C1 |
| СПОСОБ ПЕРЕРАБОТКИ ОТХОДОВ ПРОИЗВОДСТВА КОНТАКТНОГО АНТРАХИНОНА | 1991 |
|
RU2072353C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИГИДРОХЛОРИДА 2,7-БИС-[2-(ДИЭТИЛАМИНО)ЭТОКСИ]ФЛУОРЕНОНА-9-ПРОТИВОВИРУСНОГО И ИММУНОМОДУЛИРУЮЩЕГО ПРЕПАРАТА "АМИКСИН" | 1999 |
|
RU2218327C2 |
| ПРОИЗВОДНЫЕ ТЕТРАФУРАЗАНО[3,4-b:3',4'-f:3",4"-j:3'",4'"-N][1,4,5,8,9,12,13,16]ОКТААЗАБ ИЦИКЛО[14.2.2]ЭЙКОЗА-4,8,12-ТРИЕНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2000 |
|
RU2167161C1 |
| 3-(4-Нитратометил-1Н-1,2,3-триазол-1-ил)-4-нитро-1,2,5-оксадиазол и способ его получения | 2023 |
|
RU2813466C1 |
| Азо[5-(4-нитрофуразан-3-ил)-2-(1,3,4-тиадиазол)] и способ его получения | 2023 |
|
RU2818440C1 |
| 3-(3,4-Динитропиразол-5-ил)-4-нитрофуразан и способ его получения | 2021 |
|
RU2760680C1 |
Изобретение относится к области органической химии, конкретно к получению красителя Изосульфана синего, нашедшего применение, в частности, в химиотерапии злокачественных новообразований. Способ получения красителя окислением динатриевой соли 2-[бис[4-(диэтиламино)фенил]метил]бензол-1,4-дисульфокислоты (динатриевой соли изолейконовой кислоты) характеризуется тем, что в качестве исходного реагента используют толуол и включает стадии а-е. На стадии а) осуществляют каталитическое хлорирование толуола с получением смеси 2-хлортолуола и 4-хлортолуола. На этапе б) проводят объединенное окисление полученных на стадии (а) 2-хлор- и 4-хлортолуолов в среде серной кислоты до соответствующих альдегидов, с последующим выделением из сульфомассы 4-хлорбензальдегида экстракцией. Затем на стадии в) проводят сульфирование комплекса 2-хлорбензальдегида и концентрированной серной кислоты олеумом до образования 2-хлорбензальдегид-5-сульфокислоты. На этапе г) добавляют к водному раствору сульфита натрия полученную на стадии (в) 2-хлорбензальдегид-5-сульфокислоту с получением динатриевой соли 2,5-дисульфобензальдегида. Конденсацию динатриевой соли 2,5-дисульфобензальдегида с N,N-диэтиланилином в присутствии каталитического количества гексахлорфосфазотриена осуществляют на стадии д). На этапе е) проводят окисление динатриевой соли изолейконовой кислоты в конечный Изосульфан синий. Техническим результатом изобретения является обеспечение способа получения целевого красителя из отечественного сырья с высоким выходом. 5 з.п. ф-лы, 1 пр.
Способ получения красителя Изосульфан синий (4-{[4-(диэтиламино)фенил](2,5-дисульфофенил)метилиден}-N,N-диэтилциклогекса-2,5-диен-1-иминий) окислением динатриевой соли 2-[бис[4-(диэтиламино)фенил]метил]бензол-1,4-дисульфокислоты (динатриевой соли изолейконовой кислоты), отличающийся тем, что в качестве исходного реагента используют толуол и способ включает следующие стадии:
а) каталитическое хлорирование толуола с получением смеси 2-хлортолуола и 4-хлортолуола;
б) объединенное окисление полученных на стадии (а) 2-хлор- и 4-хлортолуолов в среде серной кислоты до соответствующих альдегидов, с последующим выделением 4-хлорбензальдегида из сульфомассы экстракцией;
в) сульфирование комплекса 2-хлорбензальдегида и концентрированной серной кислоты олеумом до образования 2-хлорбензальдегид-5-сульфокислоты;
г) добавление к водному раствору сульфита натрия полученной на стадии (в) 2-хлорбензальдегид-5-сульфокислоты с получением динатриевой соли 2,5-дисульфобензальдегида;
д) конденсацию динатриевой соли 2,5-дисульфобензальдегида с N,N-диэтиланилином в присутствии каталитического количества гексахлорфосфазотриена;
e) окисление динатриевой соли изолейконовой кислоты в Изосульфан синий.
2. Способ по п. 1, отличающийся тем, что на стадии а) смесь 2-хлортолуола и 4-хлортолуола получают каталитическим хлорированием в присутствии ацетонитрила.
3. Способ по п. 1, отличающийся тем, что выделение 4-хлорбензальдегида из сульфомассы осуществляют экстракцией хлористым метиленом.
4. Способ по п. 1, отличающийся тем, что на этапе в) сульфирование проводят 60% олеумом и образовавшийся 2-хлорбензальдегид-5-сульфокислоты выделяют экстракцией этилацетатом с последующим удалением растворителя.
5. Способ по п. 1, отличающийся тем, что реакцию этапа г) проводят при кипении с обратным холодильником до полной замены хлора на сульфогруппу.
6. Способ по п. 1, отличающийся тем, что после стадии е) осуществляют дополнительную очистку Изосульфана синего в присутствии трет-бутанола.
| WO 2008140564 A1, 20.11.2008 | |||
| Способ получения монохлортолуолов | 1978 |
|
SU956443A1 |
| Способ получения ксиленовых красителей | 1936 |
|
SU50850A1 |
| 0 |
|
SU219725A1 | |
| WO 2018008040 A1, 11.01.2018 | |||
| WO 2017118882 A1, 13.07.2017. | |||
Авторы
Даты
2024-06-25—Публикация
2023-07-28—Подача