Область техники
Изобретение относится к области биомолекулярной фармакологии, биотехнологии и генетической инженерии и касается молекул нуклеиновых кислот и кодируемых ими новых растворимых белков – функциональных антагонистов IL-1 человека, способных блокировать провоспалительный ответ, а также способа их получения. В основе изобретения лежит использование белка IL-1RA (Interleukin-1 receptor antagonist protein), являющегося естественным функциональным антагонистом IL-1, в составе молекулы рецептора-ловушки.
Уровень техники
Цитокины включают класс белков, которые опосредуют воспаление и модулируют иммунитет. Одна группа цитокинов, интерлейкины, носит это название, поскольку считалось, что они опосредуют передачу сигналов между лейкоцитами (отсюда и название интерлейкины) (Dinarello et al., 2011). Цитокины играют решающую роль в развитии многих воспалительных заболеваний (Feldmann, 2008).
Интерлейкин IL-1 входит в число первых признанных цитокинов. Ген IL-1 кодирует две родственные, но функционально различные изоформы: IL-1α и IL-1β (Dinarello, 2011). Эта пара медиаторов оказывает множественное влияние на защитные силы хозяина и играет роль в патогенезе широкого спектра заболеваний. Заметные эффекты IL-1 на многие типы клеток включают следующие события: индукция продукции простагландинов посредством индукции циклооксигеназы-2; выработка оксида азота путем повышения уровней индуцибельной изоформы NO; индукция экспрессии многих цитокинов, в том числе усиление транскрипции собственных генов; повышение экспрессии молекул адгезии лейкоцитов и медиаторов тромбообразования; и активация клеток, участвующих во врожденном иммунитете, в первую очередь мононуклеарных фагоцитов (Dinarello, 2009)
Действие IL-1 контролируется несколькими уровнями регуляции. Семейство IL-1 включает структурно родственный антагонист рецептора IL-1 (IL-1RA). Баланс между провоспалительными изоформами IL-1α и IL-1β и этим эндогенным ингибитором (IL-1RA) представляет собой один из важных уровней контроля. Изоформы IL-1α и IL-1β имеют разные функциональные профили. IL-1α обычно находится на поверхности клетки и передает сигналы на короткие расстояния при прямом контакте. Напротив, IL-1β может действовать на расстоянии (Dinarello, 2011).
Два рецептора связывают основные члены семейства IL-1. Рецептор I IL-1 (IL-1RI) передает сигнал IL-1β. Напротив, рецептор II IL-1 (IL-1RII) связывает лиганды, но не передает сигнал, поскольку у него отсутствует цитоплазматический домен. Таким образом, IL-1RII действует как «приманка», или рецептор-ловушка, обеспечивая еще один уровень негативной регуляции передачи сигналов IL-1. IL-1 может индуцировать экспрессию собственного гена во многих типах клеток (Beltrami-Moreira, Vromman et al., 2016).
Семейство цитокинов IL-1 играет важную роль во врожденных иммунных реакциях, в особенности IL-1α и IL-1β являются основными медиаторами аутовоспалительных заболеваний и провоспалительной активности (Dinarello, 2009; Dinarello, 2011). IL-1β считается ключевым цитокином в патогенезе острого подагрического артрита и ряда других аутовоспалительных заболеваний, а блокирование передачи сигналов IL-1β оказывает терапевтический эффект (Schlesinger, 2014).
IL-1β опосредует провоспалительную реакцию при ревматоидном артрите посредством нескольких механизмов, включая активацию остеокластов, синовиальных фибробластов и эндотелиальных клеток (McInnes and Schett, 2011). Описан антагонист рецептора IL-1, анакинра. Анакинра представляет собой рекомбинантный не гликозилированный IL-1RA белок, соответвующий естественной последовательности IL-1RA с дополнительным метионином на N-конце, который получают путем продукции в E.coli. Препарат одобрен для лечения ревматоидного артрита, но имеет относительно умеренную эффективность. Анакинра, канакинумаб и рилонацепт оказывают выраженное противовоспалительное действие при наследственных системных аутовоспалительных заболеваниях, характеризующихся повышенной выработкой IL-1β. Анакинра эффективна у некоторых пациентов с системными воспалительными заболеваниями, включая ювенильный идиопатический артрит с системным началом, болезнь Стилла у взрослых и другие аутовоспалительные состояния. Клинические испытания дали обнадеживающие результаты при артритах, вызванных патологическим накоплением кристаллов солей, таких как подагра и хондрокальциноз. Сообщалось также об обнадеживающих результатах применения анакинры при сахарном диабете 2-го типа и вялотекущей/ вялотекущей множественной миеломе (Igel, Toprover et al., 2019).
Fc-слитые белки хорошо зарекомендовали себя в качестве терапевтических и профилактических средств. Полученные с помощью этой технологии белки имеют эффекторную часть, связанную с Fc-доменом, который заметно удлиняет период полувыведения белков из плазмы крови, что продлевает их терапевтическую активность, а также приводит к более медленному почечному клиренсу для молекул большего размера. Также, молекулы обладают довольно низкой иммуногенностью, так как составляющие их части представляют собой естественные белки организма человека. Вместе с тем, такие молекулы обладают значительным терапевтическим потенциалом, так как способны связывать необходимые лиганды и, таким образом, блокировать цепочки передачи сигналов. В последнее время ведется активная разработка терапевтических средств на основе Fc-слитых белков (см. например, RU2689522, 28.05.2019; WO2023063842, 20.04.2023 (RU2787060)).
Целью изобретения является разработка эффективных антагонистов IL-1 на основе технологии Fc-слитых белков.
Сущность изобретения
Задачей настоящего изобретения является расширение арсенала технических средств для лечения воспалительных и аутоиммунных заболеваний. В частности, задача касается получения полипептидных препаратов – антагонистов IL-1, обладающих высокой аффинностью к рецептору IL-1RI; также задача касается разработки нуклеотидных последовательностей, кодирующих такие полипептиды и являющихся экспрессионной основой для их получения.
Решение поставленной задачи осуществляется путем создания слитого белка IL-1RA-hFc, являющегося антагонистом IL-1, в структуру которого входит IL-1RA человека, представленный аминокислотами 26-177, соответствующих естественной последовательности IL-1RA (SEQ ID NO: 1), а также константная часть тяжелой цепи (Fc-фрагмент) IgG4 человека, представленная последовательностью SEQ ID NO: 3. При этом Fc-фрагмент IgG4 человека присоединен к фрагменту белка IL-1RA с С-конца посредством линкерной последовательности RS.
В некоторых вариантах осуществления изобретения слитый белок дополнительно включает сигнальную последовательность, локализованную на N-конце слитого белка. В частных вариантах изобретения сигнальная последовательность представлена в последовательности SEQ ID NO: 4.
В некоторых частных вариантах изобретения слитый белок имеет аминокислотную последовательность, представленную SEQ ID NO: 2.
Поставленная задача также решается путем создания изолированной молекулы нуклеиновой кислоты, кодирующей такой слитый белок.
В некоторых частных вариантах осуществления изобретения молекула нуклеиновой кислоты имеет последовательность SEQ ID NO: 5.
Указанная задача также решается путем создания экспрессирующего вектора, несущего нуклеотидную последовательность, соответствующую последовательности изолированной молекулы нуклеиновой кислоты, кодирующей такой слитый белок, под контролем регуляторных элементов, необходимых для экспрессии данной нуклеотидной последовательности в клетке-хозяине; а также путем создания клетки-хозяина, включающей экспрессирующий вектор, описанный в настоящей заявке, обеспечивающей эффективную продукцию такого слитого белка с использованием вышеуказанной молекулы нуклеиновой кислоты. В некоторых вариантах воплощения изобретения в качестве таких клеток выступают клетки млекопитающих (в некоторых частных вариантах воплощения изобретения – клетки яичников китайских хомячков (CHO)).
Решение поставленной задачи также может достигаться при применении вышеуказанного слитого белка для лечения и профилактики широкого спектра воспалительных состояний и аутоиммунных заболеваний. Результатом изобретения является создание ингибитора IL-1, что достигается за счет использования фрагмента IL-1RA в составе слитого белка IL-1RA-hFc, который является рецептором-ловушкой, направленной на снижение способности изоформ IL-1 взаимодействовать с клеточным рецептором IL-1 RI и активировать передачу сигнала. Белок IL-1RA-hFc может вводиться пациенту в терапевтически эффективном количестве, предпочтительно в составе фармацевтической композиции.
При осуществлении изобретения достигаются следующие технические результаты:
- создан вариант терапевтического агента на основе слитого (гибридного) белка IL-1RA-hFc, содержащего функциональную часть IL-1RA, слитую с константной частью (Fc-доменом) иммуноглобулина человека IgG4, и способного блокировать передачу сигнала изоформ IL-1 (провоспалительный ответ), а также
- разработаны нуклеотидные последовательности, кодирующие такие слитые белки и являющиеся экспрессионной основой для их получения;
- благодаря особенностям конструкции, разработанный рекомбинантный полипептид имеет потенциально высокую степень безопасности терапевтического применения в сочетании с улучшенными фармакокинетическими свойствами.
Краткое описание рисунков
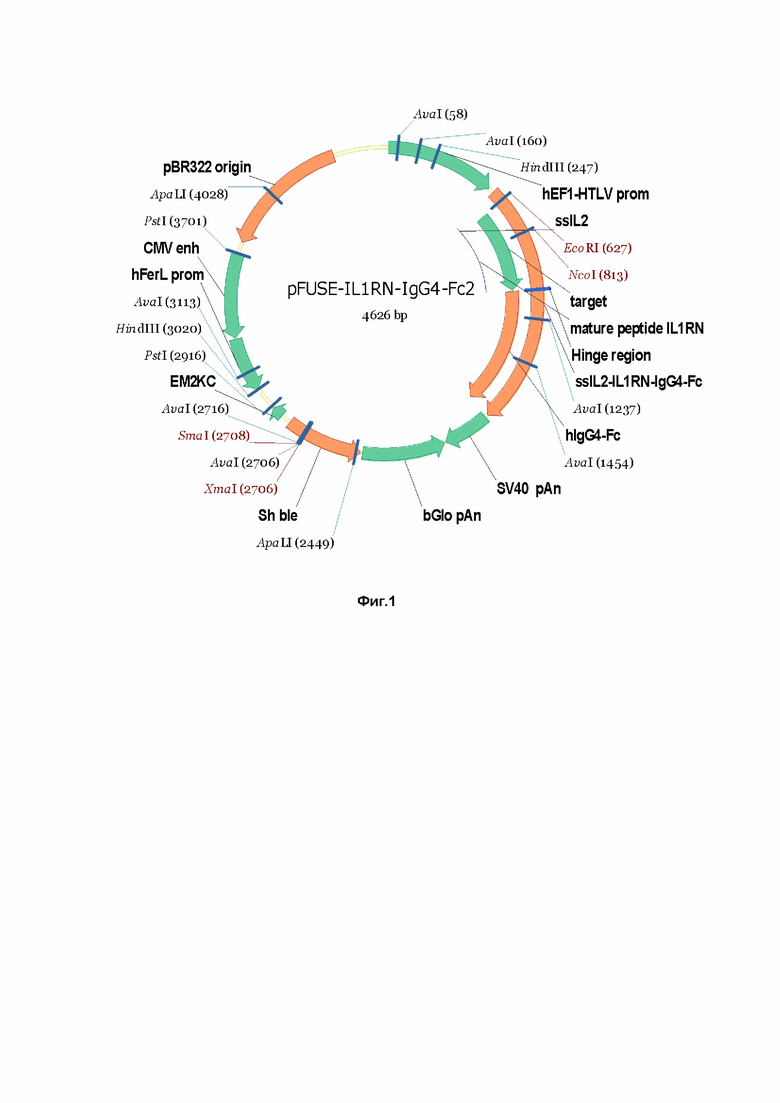
Фиг.1. Схема экспрессирующего вектора, содержащего нуклеотидную последовательность SEQ ID NO: 5, кодирующую слитый белок, имеющий аминокислотную последовательность SEQ ID NO: 2.
Определения и термины
Следующие термины и определения применяются в данном документе, если иное не указано явно. Ссылки на методики, используемые при описании данного изобретения, относятся к хорошо известным методам, включая изменения этих методов и замену их эквивалентными методами, известными специалистам.
В документах данного изобретения термины «включает», «включающий» и т.п., а также «содержит», «содержащий» и т.п. интерпретируются как означающие «включает, помимо всего прочего» (или «содержит, помимо всего прочего»). Указанные термины не предназначены для того, чтобы их истолковывали как «состоит только из».
Термины «полипептид», «белок» и «пептид» используют в настоящем документе взаимозаменяемо, и все они означают полимер из аминокислотных остатков. Эти термины также могут использоваться в настоящем описании взаимозаменяемо при обозначении конечного продукта, получаемого в результате экспрессии в клетке-хозяине последовательности нуклеиновой кислоты.
Под «слитым белком» («гибридным белком», «рекомбинантным белком», «слитым полипептидом», «рекомбинантным полипептидом», «гибридной конструкцией») понимают конструкцию из двух или более частей полипептидной природы, ковалентно связанных между собой, образующейся в результате экспрессии рекомбинантной молекулы ДНК, в которой соединены друг с другом в одной рамке считывания кодирующие участки, соответственно, двух или нескольких разных генов или их фрагментов.
Термин «изолированный» («выделенный») имеет свое общепринятое значение, известное среднему специалисту в данной области техники, и при использовании в отношении выделенной нуклеиновой кислоты или выделенного полипептида используется без ограничения для обозначения нуклеиновой кислоты или полипептида, которые, благодаря человеку, существуют отдельно от своего нативного окружения и поэтому не являются продуктом природы. Выделенная нуклеиновая кислота или полипептид могут существовать в очищенной форме или могут существовать в ненативном окружении, в таком как, например, клетка-хозяин.
Термин «синонимичная замена» относится к нуклеотидной последовательности, имеющей последовательность нуклеотидов, которая может отличаться от референсной последовательности нуклеиновой кислоты на одну или более замен, которые не ведут к изменению аминокислотной последовательности белка, кодируемой данной молекулой нуклеиновой кислоты. В связи с тем, что генетический код является «вырожденным», то есть различные по нуклеотидной последовательности триплеты могут кодировать одну и ту же аминокислоту, синонимичные замены в нуклеотидной последовательности не приводят к изменению аминокислотной последовательности белка.
Термин «рецептор-ловушка» (от англ. Decoy receptor, также трап) относится к гибридным белкам, состоящим из внеклеточного домена молекулы (рецептора) и Fc-домена иммуноглобулина. Внеклеточный домен рецептора отвечает за связывание мишени, а Fc-домен осуществляет димеризацию гибридного белка. Последнее необходимо для увеличения эффективности связывания и обеспечения большей стабильности высокомолекулярного комплекса. В рамках настоящего изобретения «рецептор-ловушка» состоит из функционального фрагмента человеческого белка IL-1RA и константной части тяжелой цепи IgG4 человека.
Термин «лечение» означает излечение, замедление, остановку, либо реверсию прогрессирования заболевания или нарушения. В настоящем документе «лечение» также означает смягчение симптомов, ассоциированных с заболеванием или нарушением. Слитый белок по изобретению может быть использован для применения в лечении заболеваний, опосредованных IL-1. В частности, такое заболевание может выбрано из артрита, энтерита, астмы, легочного фиброза, гломерулонефрита, реакции трансплантат против хозяина, острого повреждения легких, ревматоидного артрита, атопического дерматита и др.
Термин «профилактика», «предотвращение», «превентивная терапия» охватывает устранение факторов риска, а также профилактическое лечение субклинических стадий заболевания у человека, направленное на уменьшение вероятности возникновения клинических стадий заболевания. Пациенты для профилактической терапии отбираются на основе факторов, которые, на основании известных данных, влекут увеличение риска возникновения клинических стадий заболевания по сравнению с общим населением. К профилактической терапии относится а) первичная профилактика и б) вторичная профилактика. Первичная профилактика определяется как профилактическое лечение у пациентов, клиническая стадия заболевания у которых ещё не наступила. Вторичная профилактика – это предотвращение повторного наступления того же или близкого клинического состояния заболевания.
Термин «уменьшение риска» охватывает терапию, которая снижает частоту возникновения клинической стадии заболевания. Примерами уменьшения риска заболевания является первичная и вторичная профилактика заболевания.
Под «терапевтически/профилактически эффективным количеством (терапевтической дозой)» подразумевается количество лекарственного средства, вводимого пациенту, при котором у него с наибольшей вероятностью проявится ожидаемый терапевтический (профилактический) эффект. Точное требуемое количество может меняться от субъекта к субъекту в зависимости от многочисленных факторов, таких как тяжесть заболевания, возраст, масса тела, общее состояние организма, комбинированное лечение с другими препаратами и др. Введение лекарственного средства по изобретению субъекту, нуждающемуся в лечении и/или профилактике заболевания или состояния, осуществляется в дозе, достаточной для достижения терапевтического эффекта. При проведении лечения и/или профилактики введение может осуществляться как разово, так и несколько раз в день, чаще в виде курсового введения на протяжении времени, достаточного для достижения терапевтического эффекта (от нескольких дней до недели, нескольких недель и до месяцев), при этом курсы введения лекарственного средства могут проводиться повторно. В частности, при среднетяжелых формах заболевания разовая доза, кратность и/или длительность введения лекарственного средства по изобретению могут быть увеличены. Предпочтительно слитый белок по изобретению вводят пациенту в составе фармацевтической композиции, включающей, помимо активного компонента, фармацевтически приемлемые носители и/или наполнители.
Если не определено отдельно, технические и научные термины в данной заявке имеют стандартные значения, общепринятые в научной и технической литературе.
Номера последовательностей нуклеотидов и аминокислот, упоминаемых в настоящей заявке, соответствуют номеру в Перечне последовательностей (SEQ ID NO) согласно Стандарту ST.26, являющемуся частью настоящего описания изобретения. В случае наличия разночтений в структуре последовательностей между упоминанием в тексте описания и соответствующей последовательностью в Перечне последовательностей согласно стандарту ST.26, приоритетными являются данные, приведенные в тексте описания.
Подробное описание изобретения
В настоящем изобретении предлагаются конструкции ДНК, кодирующие слитые белки (рекомбинантные полипептиды) – антагонисты IL-1, блокирующие провоспалительный ответ, индуцируемый изоформами α и β IL-1.
Более конкретно, изобретение относится к нуклеотидным конструкциям, кодирующим полипептиды, содержащие IL-1RA, слитый с константной частью (Fc-доменом) иммуноглобулина человека IgG4 (IL-1RA-hFc).
Естественная последовательность белка IL-1RA человека состоит из 177 аминокислот (ак) (SEQ ID NO: 1). В состав нативного белка входит сигнальный пептид (1—25 ак SEQ ID NO: 1) и функциональный домен (26-177 ак SEQ ID NO: 1).
В рамках настоящего изобретения в процессе разработки новых полипептидных препаратов – ингибиторов действия IL-1 было осуществлено клонирование последовательности, соответствующей функциональной части IL-1RA, и ее слияние в одной рамке считывания с последовательностью, кодирующей константную часть тяжелой цепи IgG4 человека. При конструировании гибридного белка по изобретению особое внимание было уделено линкеру, связывающему два активных фрагмента белковой конструкции. Известно, что белковые линкеры должны обеспечивать необходимый интервал между доменами гибридного белка, поддерживая правильную укладку белка в случае, когда взаимодействия N или C концов являются критическими для укладки. Кроме того, предпочтительно, чтобы используемый белковый линкер усиливал стабильность молекулы. Помимо этого, при конструировании гибридного белка по изобретению особое внимание было уделено безопасности белковой конструкции при ее введении пациенту в процессе проведения терапии. Как известно, проявление нежелательной иммуногенности биотехнологических лекарственных препаратов на основе слитых белков является серьезной проблемой, существенно влияющей на их применение в терапии, особенно при лечении заболеваний, требующих длительного системного введения лекарственных препаратов на их основе (Авдеева Ж.И. и др. Проблемы, связанные с нежелательной иммуногенностью биотехнологических лекарственных препаратов (терапевтических белков) // Иммунология т.40, № 3, 2019, с.51-64). Поэтому при конструировании гибридного белка внимание было уделено не только его стабильности и терапевтической эффективности, но и снижению риска потенциальной иммуногенности. Анализируя возможные риски развития иммуногенности, авторы изобретения обратили внимание на то, что несмотря на то, что фрагменты молекул IL-1RA и Fc-фрагмента IgG имеют человеческое происхождение и естественным образом должны иметь низкий иммуногенный профиль, последовательность, получаемая в результате слияния этих молекул, не всегда безопасна. Так, используемые в качестве линкеров длинные гибкие линкерные пептиды обычно состоят из небольших неполярных аминокислотных остатков, таких как глицин, и полярных аминокислотных остатков, таких как серин и треонин: несколько остатков глицина придают линкеру неструктурированную конформацию, что обеспечивает его гибкость, а серин или треонин предоставляют полярный участок поверхности для ограничения гидрофобного взаимодействия в пептиде или с составляющими фрагментами слитого белка. Однако такие пептидные линкеры, богатые глицином, например, повторы последовательности GGGGS, имеют общий мотив с прионовыми доменами (см, например, Kun-Hua Yu et al. The Effect of Octapeptide Repeats on Prion Folding and Misfolding // Int J Mol Sci. 2021 Feb; 22(4): 1800; Kim S. et al. Transmembrane glycine zippers: Physiological and pathological roles in membrane proteins // PNAS, October 4, 2005 vol. 102 no. 40 p. 14278 –14283), что может стать причиной нежелательных структурных изменений в белке, его агрегации, а также иммуногенности. Неструктурированные длинные гибкие пептиды, используемые в качестве линкеров, могут иметь множество поверхностных неоэпитопов, в образовании которых могут участвовать как участки линкерного пептида, так и участки молекул, участвующих в образовании слитого белка, примыкающие к линкеру в месте слияния. Такие поверхностные неоэпитопы, доступные для распознавания иммунной системой, также могут стать причиной нежелательной иммуногенности. Так, например, последовательности GGGGSGGGGS, GGGGSGG, GGGGSAE и EPKSSDK, образующиеся в линкерной части слитых белков IL-1RA-hFc, известных из уровня техники, присутствуют в большом количестве различных видов бактерий, грибов и паразитических простейших (таких как Acinetobacter sp., Cryptosporangium parvum, Bacteroides fragilis, Dermabacter hominis, Toxoplasma gondii, Chryseobacterium sp., Rhodotorula toruloides, Actinomyces oris, Plasmodium vivax, Plasmodium ovale curtisi и др.), многие из которых являются патогенными или условно-патогенными для человека. Воздействие такого пептида на человека может стать причиной перекрестной реактивности с гибридным белком IL-1RA-hFc и последующей иммунной реакции.
В результате проведенной работы было обнаружено, что использование линкера RS не только обеспечивает необходимую стабильность молекулы, но и также, благодаря, по меньшей мере, его длине, обеспечивает получение слитого белка, обладающего низким риском потенциальной иммуногенности. При этом необходимая гибкость молекулы слитого белка по изобретению обеспечивается включением в конструкцию фрагмента шарнирного участка PPCPSCP константной части тяжелой цепи IgG4 человека, представленного ак 1-7 SEQ ID NO: 3, что позволяет обеспечить необходимый поворот и жесткость без излишней неструктурированности, благодаря чему функциональный домен белка IL-1RА и Fc-домен, входящие в молекулу, могут действовать независимо друг от друга за счет увеличения гибкости на данном участке. Таким образом, благодаря особенностям конструкции, рекомбинантный полипептид по изобретению обладает одновременно потенциально улучшенными фармакокинетическими свойствами и низким риском потенциальной иммуногенности.
Использование IgG4-изотипа Fc-фрагмента в составе слитого белка по изобретению обеспечивает дополнительные преимущества: минимальная эффекторная функция для антителозависимой клеточной цитотоксичности (antibody-dependent cellular cytotoxicity - ADCC) и отсутствие комплемент-зависимой цитотоксичности (complement-dependent cytotoxicity - CDC), что снижает возможный риск воспалительных реакций и сенсибилизацию при использовании терапевтического агента на основе гибридного белка IL-1RA-hFc.
Таким образом, гибридный белок по изобретению IL-1RA-hFc (в частном варианте изобретения представленный последовательностью SEQ ID NO: 2), состоящий из функционального домена белка IL-1RА человека, представленной аминокислотами 26-177 SEQ ID NO: 1, и Fc-фрагмента IgG4 человека, представленного последовательностью SEQ ID NO: 3 и присоединенного к фрагменту белка IL-1RА с С-конца посредством линкерной последовательности RS, обладает высокой степенью безопасности терапевтического применения.
Слитый белок IL-1RA-hFc по изобретению также может необязательно содержать сигнальную последовательность, которая может включать любую последовательность, известную квалифицированному специалисту в области управления секрецией полипептида или белка из клетки, и включать природные или синтетические последовательности. Обычно сигнальная последовательность размещается на N-конце слитого белка по настоящему изобретению. В частных вариантах изобретения сигнальный пептид имеет последовательность SEQ ID NO: 4.
Слитый белок (рекомбинантный полипептид), являющийся объектом настоящего изобретения, может быть получен следующим образом.
Растворимые рекомбинантные полипептиды-антагонисты IL-1 производят в результате экспрессии кодирующих их нуклеотидных последовательностей в эукариотических клеточных линиях, с последующей очисткой синтезированных рекомбинантных белков при помощи аффинной, ионобменной или гидрофобной хроматографии, применяемых по отдельности или в различных сочетаниях друг с другом, а также при помощи иных способов очистки белков. Соответствующие нуклеотидные последовательности получают при помощи комбинирования участков ДНК, кодирующих выбранные домены IL-1RA, с последовательностью ДНК, кодирующей Fc-фрагмент IgG4 человека. В некоторых частных вариантах изобретения молекулы нуклеиновой кислоты, кодирующие такие полипептиды-антагонисты IL-1, имеют нуклеотидную последовательность, соответствующую SEQ ID NO: 5.
Также указанная задача решается путем создания экспрессирующего вектора, содержащего данную молекулу нуклеиновой кислоты под контролем регуляторных элементов, необходимых для экспрессии данной нуклеиновой кислоты в клетке-хозяине. В предпочтительных вариантах изобретения в качестве клетки-хозяина, включающей такой экспрессирующий вектор, могут выступать клетки яичников китайских хомячков CHO (например, клеточные линии CHO-К1 или CHO DG44), адаптированные для производства терапевтических белков. В настоящем изобретении экспрессирующий вектор предпочтительно подбирается для экспрессии гетерологичных последовательностей в клетках млекопитающих, но в некоторых вариантах изобретения экспрессирующий вектор может быть выбран для экспрессии в других системах, таких как, например, клетки насекомых, дрожжевые или бактериальные клетки. Соответственно, каждый экспрессирующий вектор имеет свой набор регуляторных элементов, позволяющих проводить экспрессию гетерологичной последовательности (продукта) в клетке-хозяине, таких как промоторы и/или энхансеры, последовательности Козак, polyA последовательности и другие регуляторные последовательности. А также может иметь последовательности, кодирующие лидерные (сигнальные) пептиды, обеспечивающие секрецию рекомбинантных полипептидов во внеклеточную среду. Терминация синтеза белка с заданной изолированной последовательности нуклеиновой кислоты определяется добавлением к ней с 3’-конца в одной рамке считывания одного или нескольких стоп-кодонов.
После трансфекции вектора в клетки эукариотической клеточной линии происходит синтез рекомбинантного полипептида и его секреция в культуральную бессывороточную среду. Полученный рекомбинантный полипептид очищают из среды при помощи, как правило, аффинной хроматографии на белок протеин-A или белок протеин-G, однако могут использоваться и другие методы очистки белков.
Нижеследующие примеры приведены в целях раскрытия характеристик настоящего изобретения, и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения.
Пример 1. Конструирование плазмид
Для конструирования плазмид с заявляемыми нуклеотидными последовательностями была использована последовательность, кодирующая белок человека IL-1RA, полученная из плазмиды RG218518 (OriGene, IL-1RA, Human Tagged ORF clone). Последовательность, кодирующая IL-1RA, была использована для клонирования. Для клонирования участка, соответствующему аминокислотам 26-177 для SEQ ID NO: 2 были подобраны следующие праймеры:
IL-1RA_SENSE (taatgaattcgcgaccctctgggagaaaatc) (SEQ ID NO: 6)
IL-1RA_ANTISENSE (TAATAGATCTCTCGTCCTCCTGGAAGTAGA) (SEQ ID NO: 7)
Проведена ПЦР со следующими условиями: 98оС 1 мин, 30 циклов (98оС 10 сек, 59оС 10 сек, 72оС 1 мин), 72оС 5 мин. Компоненты реакции: полимераза – Phusion (Thermo), буфер, содержащий Mg2+ для Phusion-полимеразы (Thermo), по 10 пкмоль каждого из праймеров и 0,25 мM смеси трифосфатов нуклеотидов (Thermo). Амплификацию осуществляли с последовательности RG218518 (Origene). После ПЦР: ПЦР продукт очищали набором для очистки ПЦР продуктов GeneJet PCR purification kit (Fermentas). Концентрация и соответствие предсказанному молекулярному весу проверяли при помощи гель-электрофореза в 1% агарозе (ТАЕ буфер). Полученные ПЦР продукты были использованы для дальнейшего конструирования.
Для клонирования целевых последовательностей использовался вектор pFUSE-hIgG4e-Fc2 (InvivoGen), который позволяет получить слитые с Fc-доменом IgG4 последовательности и проводить исследование их свойств. В один из праймеров был включен сайт рестрикции EcoRI (IL-1RA_SENSE), а в другой сайт рестрикции BglII (IL-1RA_ANTISENSE), что после амплификации и рестрикции позволило получить фрагмент ДНК липкими EcoRI, BglII концами. Вектор и ПЦР-продукт обрабатывали рестриктазами EcoRI (Thermo) и BglII (Thermo) в течение 1 часа при 37оС, затем очищали с помощью GeneJet PCR purification kit (Fermentas) и лигировали, используя 1 Ед (ME) лигазы (Thermo) по протоколу производителя. Лигазной смесью трансформировали компетентные клетки E. coli XL1-Blue и высевали на среду LB, содержащую зеоцин.
Чашки инкубировали в термостате в течение ночи при 37oC. На следующий день проверяли по 20 колоний из каждой лигазной смеси на присутствие нужной вставки, для этого часть колонии разводили в 20 мкл воды и кипятили в течение 5 минут. После охлаждения смесь откручивали и использовали 1 мкл в качестве матрицы в реакции ПЦР. ПЦР осуществляли при помощи Taq ДНК-полимеразы (Fermentas) и праймеров PROMF2 и FC. Присутствие вставки проверяли после электрофореза ПЦР продуктов. Из двух колоний, содержащих вставку, выделяли плазмидную ДНК, верифицировали длины рестрикционных фрагментов при помощи рестрикции с эндонуклеазами EcoRI и HindIII и секвенировали c использованием праймеров PROMF2 и FC на секвенаторе Applied Biosystems 3500 по инструкции производителя, используя праймеры PROMF2 (прямой) и FC (обратный).
PROMF2: GCCTGACCCTGCTTGCTCAACT (SEQ ID NO: 8)
FC: CTCACGTCCACCACCACGCA (SEQ ID NO: 9)
Сконструированная в результате плазмида, содержащая целевые нуклеотидные последовательности, показана на Фиг. 1.
Пример 2. Продукция гибридного белка
Для продукции гибридного белка проводилась временная трансфекция клеток CHO сконструированной плазмидой, кодирующей гибридный белок.
Линию клеток СНО культивировали на среде Dynamis, с добавлением Glutamax (6 мМ), Anticlumping reagent B (0,5%) и зеоцина (500 мкг/мл). Культивирование осуществляли в шейкере-СО2-инкубаторе Multitron Cell (Infors, Швейцария) в атмосфере 5%-ного СО2 при температуре 37°С и относительной влажности 95% в колбах Эрнленмейера (Сorning, США) объемом 125 мл (перемешивание 120 об/мин).
Для трансфекции клеток CHO выделяли особо чистую («transfection grade») плазмидную ДНК с помощью набора EndoFree Plasmid MaxiKit (Qiagen) по протоколу фирмы-производителя. Линеаризацию сконструированной плазмиды осуществляли по сайту NotI (Thermo). Для трансфекции добавляли 20 мкг линеаризованной плазмиды на 100 мкл клеточной суспензии с концентрацией 5х107 клеток/мл. Электропорация проводилась по протоколу: 3 импульса по 1130 В продолжительностью 20 мс.
Селекцию трансфицированных клеток начинали через 48 часов после трансфекции путем добавления антибиотика зеоцина в концентрации 500 мкг/мл и продолжали ее при дальнейших пересевах.
Продукцию белка анализировали при помощи стандартного гель-электрофореза в полиакриамидном геле (SDS-PAGE). Секретируемый гибридный белок визуализировали с использованием кроличьих антител против человечьего Fc-домена (Jackson Immunoresearch, США). Также целевой белок IL-1RA-hFc из культуральной жидкости очищали путем FPLC хроматографии на колонке HiTrap ProteinA HP (Cytiva) и оценивали методом гель-электрофореза. При культивировании данных пулов была подтверждена продукция слитых полипептидов IL-1RA-hFc и их секреция в культуральной жидкости.
Таким образом, в результате проведенных исследований разработана нуклеотидная последовательность, кодирующая слитый белок IL-1RA-hFc и являющаяся экспрессионной основой для его получения, а также получен слитый белок IL-1RA-hFc, содержащий функциональный домен IL-1RA, слитый с константной частью (Fc-доменом) иммуноглобулина человека IgG4, способный эффективно блокировать IL-1, который может быть использован в терапии и предотвращении развития воспалительных и аутоиммунных заболеваний. Данное изобретение обладает рядом улучшенных свойств по сравнению с аналогами и поэтому расширяет круг имеющихся кандидатов для лечения воспалительных и аутоиммунных заболеваний, в патогенезе которых участвует IL-1.
Несмотря на то, что изобретение описано со ссылкой на раскрываемые варианты воплощения, для специалистов в данной области должно быть очевидно, что конкретные подробно описанные эксперименты приведены лишь в целях иллюстрирования настоящего изобретения, и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения. Должно быть понятно, что возможно осуществление различных модификаций без отступления от сути настоящего изобретения.
--->
<?xml version="1.0" encoding="UTF-8"?>
<!DOCTYPE ST26SequenceListing PUBLIC "-//WIPO//DTD Sequence Listing
1.3//EN" "ST26SequenceListing_V1_3.dtd">
<ST26SequenceListing dtdVersion="V1_3" fileName="IL-1RA-hFc.xml"
softwareName="WIPO Sequence" softwareVersion="2.3.0"
productionDate="2023-12-13">
<ApplicantFileReference>4103762</ApplicantFileReference>
<ApplicantName languageCode="ru">Общество с ограниченной
ответственностью "Пальмира Биофарма" </ApplicantName>
<ApplicantNameLatin>"PALMIRA BIOPHARMA" Limited Liability
Company</ApplicantNameLatin>
<InventionTitle languageCode="ru">Нуклеотидная последовательность,
кодирующая слитый белок, состоящий из функционального фрагмента
человеческого IL-1RА и константной части тяжелой цепи человеческого
IgG4</InventionTitle>
<SequenceTotalQuantity>9</SequenceTotalQuantity>
<SequenceData sequenceIDNumber="1">
<INSDSeq>
<INSDSeq_length>177</INSDSeq_length>
<INSDSeq_moltype>AA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..177</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>protein</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q2">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>Homo sapiens</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>MEICRGLRSHLITLLLFLFHSETICRPSGRKSSKMQAFRIWDVNQKTFY
LRNNQLVAGYLQGPNVNLEEKIDVVPIEPHALFLGIHGGKMCLSCVKSGDETRLQLEAVNITDLSENRKQ
DKRFAFIRSDSGPTTSFESAACPGWFLCTAMEADQPVSLTNMPDEGVMVTKFYFQEDE</INSDSeq_se
quence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="2">
<INSDSeq>
<INSDSeq_length>398</INSDSeq_length>
<INSDSeq_moltype>AA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..398</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>protein</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q19">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>MYRMQLLSCIALSLALVTNSRPSGRKSSKMQAFRIWDVNQKTFYLRNNQ
LVAGYLQGPNVNLEEKIDVVPIEPHALFLGIHGGKMCLSCVKSGDETRLQLEAVNITDLSENRKQDKRFA
FIRSDSGPTTSFESAACPGWFLCTAMEADQPVSLTNMPDEGVMVTKFYFQEDERSPPCPSCPAPEFLGGP
SVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTV
LHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIA
VEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSPGK<
/INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="3">
<INSDSeq>
<INSDSeq_length>224</INSDSeq_length>
<INSDSeq_moltype>AA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..224</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>protein</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q6">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>PPCPSCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPE
VQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQ
PREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTV
DKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSPGK</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="4">
<INSDSeq>
<INSDSeq_length>20</INSDSeq_length>
<INSDSeq_moltype>AA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..20</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>protein</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q8">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>MYRMQLLSCIALSLALVTNS</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="5">
<INSDSeq>
<INSDSeq_length>1194</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..1194</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q10">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>atgtacaggatgcaactcctgtcttgcattgcactaagtcttgcacttg
tcacgaattcgcgaccctctgggagaaaatccagcaagatgcaagccttcagaatctgggatgttaacca
gaagaccttctatctgaggaacaaccaactagttgctggatacttgcaaggaccaaatgtcaatttagaa
gaaaagatagatgtggtacccattgagcctcatgctctgttcttgggaatccatggagggaagatgtgcc
tgtcctgtgtcaagtctggtgatgagaccagactccagctggaggcagttaacatcactgacctgagcga
gaacagaaagcaggacaagcgcttcgccttcatccgctcagacagcggccccaccaccagttttgagtct
gccgcctgccccggttggttcctctgcacagcgatggaagctgaccagcccgtcagcctcaccaatatgc
ctgacgaaggcgtcatggtcaccaaattctacttccaggaggacgagagatctcccccatgcccatcatg
cccagcacctgagttcctggggggaccatcagtcttcctgttccccccaaaacccaaggacactctcatg
atctcccggacccctgaggtcacgtgcgtggtggtggacgtgagccaggaagaccccgaggtccagttca
actggtacgtggatggcgtggaggtgcataatgccaagacaaagccgcgggaggagcagttcaacagcac
gtaccgtgtggtcagcgtcctcaccgtcctgcaccaggactggctgaacggcaaggagtacaagtgcaag
gtctccaacaaaggcctcccgtcctccatcgagaaaaccatctccaaagccaaagggcagccccgagagc
cacaggtgtacaccctgcccccatcccaggaggagatgaccaagaaccaggtcagcctgacctgcctggt
caaaggcttctaccccagcgacatcgccgtggagtgggagagcaatgggcagccggagaacaactacaag
accacgcctcccgtgctggactccgacggctccttcttcctctacagcaggctaaccgtggacaagagca
ggtggcaggaggggaatgtcttctcatgctccgtgatgcatgaggctctgcacaaccactacacacagaa
gagcctctccctgtctccgggtaaa</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="6">
<INSDSeq>
<INSDSeq_length>31</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..31</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q12">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>taatgaattcgcgaccctctgggagaaaatc</INSDSeq_sequence
>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="7">
<INSDSeq>
<INSDSeq_length>30</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..30</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q14">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>taatagatctctcgtcctcctggaagtaga</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="8">
<INSDSeq>
<INSDSeq_length>22</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..22</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q16">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gcctgaccctgcttgctcaact</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="9">
<INSDSeq>
<INSDSeq_length>20</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..20</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q18">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>ctcacgtccaccaccacgca</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
</ST26SequenceListing>
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Нуклеотидная последовательность, кодирующая слитый белок, состоящий из растворимого экстраклеточного фрагмента человеческого IL-6R и константной части тяжелой цепи человеческого IgG4 | 2023 |
|
RU2818329C1 |
| Нуклеотидная последовательность, кодирующая слитый белок, состоящий из растворимого внеклеточного фрагмента человеческого PDGFRa и константной части тяжелой цепи человеческого IgG4 | 2023 |
|
RU2821574C1 |
| НУКЛЕОТИДНАЯ ПОСЛЕДОВАТЕЛЬНОСТЬ, КОДИРУЮЩАЯ СЛИТЫЙ БЕЛОК, СОСТОЯЩИЙ ИЗ РАСТВОРИМОГО ВНЕКЛЕТОЧНОГО ФРАГМЕНТА ЧЕЛОВЕЧЕСКОГО Dll4 И КОНСТАНТНОЙ ЧАСТИ ТЯЖЕЛОЙ ЦЕПИ ЧЕЛОВЕЧЕСКОГО IgG4 | 2021 |
|
RU2787060C1 |
| НУКЛЕОТИДНАЯ ПОСЛЕДОВАТЕЛЬНОСТЬ, КОДИРУЮЩАЯ СЛИТЫЙ БЕЛОК, СОСТОЯЩИЙ ИЗ РАСТВОРИМОГО ВНЕКЛЕТОЧНОГО ДОМЕНА ЧЕЛОВЕЧЕСКОГО TNFR1 И КОНСТАНТНОЙ ЧАСТИ ТЯЖЁЛОЙ ЦЕПИ ЧЕЛОВЕЧЕСКОГО IGG4 | 2018 |
|
RU2689522C1 |
| СЛИТНЫЕ БЕЛКИ ИММУНОГЛОБУЛИНОВ | 2008 |
|
RU2530168C2 |
| МОДИФИЦИРОВАННЫЙ БЕЛОК ИНТЕРЛЕЙКИНА-7 И СПОСОБЫ ЕГО ПРИМЕНЕНИЯ | 2016 |
|
RU2708160C2 |
| IL-1бета-СВЯЗЫВАЮЩИЕ АНТИТЕЛА И ИХ ФРАГМЕНТЫ | 2006 |
|
RU2518295C2 |
| ГУМАНИЗИРОВАННОЕ АНТИТЕЛО (Н14.18) НА ОСНОВАНИИ АНТИТЕЛА 14.18 МЫШИ, СВЯЗЫВАЮЩЕЕСЯ С GD2, И ЕГО СЛИЯНИЕ С IL-2 | 2003 |
|
RU2366664C2 |
| АНТИТЕЛА ПРОТИВ ЧЕЛОВЕЧЕСКОГО VISTA И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2746994C2 |
| ГЕТЕРОДИМЕРНЫЙ БЕЛОК IL-15 И ЕГО ПРИМЕНЕНИЯ | 2014 |
|
RU2689717C2 |
Изобретение относится к области биотехнологии, в частности к слитому белку - антагонисту IL-1. Указанный белок содержит функциональный домен IL-1RA человека, представленный аминокислотной последовательностью, соответствующей положениям 26-177 последовательности SEQ ID NO: 1, Fc-фрагмент IgG4 человека с последовательностью SEQ ID NO: 3 и линкерную последовательность RS. Настоящее изобретение также относится к молекуле нуклеиновой кислоты, кодирующей указанный слитый белок, экспрессирующему вектору и клетке, трансфицированной указанным вектором. Изобретение обеспечивает потенциально высокую степень безопасности терапевтического применения белка в сочетании с улучшенными фармакокинетическими свойствами. 4 н. и 5 з.п. ф-лы, 1 ил., 2 пр.
1. Слитый белок - антагонист IL-1, содержащий
функциональный домен IL-1RA человека, представленный аминокислотной последовательностью, соответствующей положениям 26-177 последовательности SEQ ID NO: 1,
и Fc-фрагмент IgG4 человека, представленный аминокислотной последовательностью SEQ ID NO: 3 и присоединенный к функциональному домену IL-1RA человека с С-конца посредством линкерной последовательности RS.
2. Слитый белок по п.1, дополнительно включающий сигнальную последовательность, локализованную на N-конце слитого белка.
3. Слитый белок по п.2, в котором сигнальная последовательность представлена SEQ ID NO: 4.
4. Слитый белок по п.3, представленный аминокислотной последовательностью SEQ ID NO: 2.
5. Изолированная молекула нуклеиновой кислоты, кодирующая слитый белок по любому из пп.1-4.
6. Изолированная молекула нуклеиновой кислоты по п.5, представленная последовательностью SEQ ID NO: 5.
7. Экспрессирующий вектор, имеющий в своем составе последовательность нуклеиновой кислоты по любому из пп.5-6 под контролем регуляторных элементов, необходимых для ее экспрессии в клетке-хозяине.
8. Клетка, способная экспрессировать слитый белок по любому из пп.1-4, не являющаяся эмбриональной клеткой человека и трансфицированная экспрессирующим вектором по п.7.
9. Клетка по п.8, представляющая собой клетку яичников китайского хомячка (СНО).
| US 6733753 B2, 11.05.2004 | |||
| US 2022195051 A1, 23.06.2022 | |||
| RU 2020127792 A, 28.02.2022 | |||
| US 8883134 B2, 11.11.2014 | |||
| КОСОБОКОВА Е.Н | |||
| и др., Слитные белки на основе антител и цитокинов: получение, функциональность и перспективы применения в онкологии, Современные технологии в медицине, 2013, v | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Транспортер для перевозки товарных вагонов по трамвайным путям | 1919 |
|
SU102A1 |
Авторы
Даты
2024-06-27—Публикация
2023-12-19—Подача