ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
По настоящей заявке по 35 U.S.C. § 119(e) испрашивается приоритет предварительной патентной заявки США серийный No. 62/874287, поданной 15 июля 2019 г., полное содержание которой, таким образом, приведено в качестве ссылки.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к антителам против белков, вовлеченным в костимулирующие или коингибирующие пути передачи сигналов, включая CTLA-4. Более конкретно, настоящее изобретение, кроме того, относится к канинизированным антителам против человеческого CTLA-4, имеющим специфические последовательности и высокую аффинность связывания для собачьего CTLA-4. Настоящее изобретение также относится к применению антител по настоящему изобретению в лечении злокачественной опухоли у собачьих.
УРОВЕНЬ ТЕХНИКИ ДЛЯ ИЗОБРЕТЕНИЯ
Инициация или остановка иммунных ответов опосредована посредством путей передачи сигналов, которые активируются посредством комплексных взаимодействий между группой белков, экспрессированных на поверхности множества иммуноцитов, наиболее примечательно, T-лимфоцитов и антигенпредставляющих клеток (APC). Костимулирующие пути передачи сигналов приводят к развитию иммунных ответов и как показано, опосредованы, наиболее важно, через взаимодействие CD28 на поверхности T-клеток и членов семейства B7.1 (также известного как CD80) и B7.2 (также известного как CD86) на поверхности APC. Считают, что B7.1 и B7.2 осуществляют сходные функции.
В отличие от этого, коингибирующие пути приводят к ингибированию или остановке иммунных ответов и, как показано, опосредованы через взаимодействие между CTLA-4 на T-клетках и белками B7.1/B7.2 на APC. Показано, что дополнительные коингибирующие пути передачи сигналов опосредованы через взаимодействие между рецептором 1 программируемой клеточной смерти (PD-1) на T-клетках и белками лигандами 1 или 2 рецептора программируемой клеточной смерти (PD-L1/PD-L2) на APC. Кроме того, показано также, что взаимодействие между PD-L1 и B7.1 может также приводить к ингибирующим сигналам в T-клетках.
B7.1 и B7.2 являются членами суперсемейства иммуноглобулинов (Ig) [Sharpe and Freeman, Nature Reviews, 2:116-126 (2002)]. B7.1 экспрессируется на активированных B-клетках, активированных T-клетках, так же как макрофагах и дендритных клетках [Swanson and Hall, Eur J. Immunol., 23:295-298 (1993); Razi-Wolfe et al., PNAS, 89:4210-4214 (1992)]. B7.2 конститутивно экспрессируется на дендритных клетках, клетках Лангерганса и B-клетках. Кроме того, B7.2 экспрессируется на моноцитах и подвергается повышающей регуляции после стимуляции IFN-гамма [Larsen et al., Immunol.,152:5208-5219 (1994); Inaba, J. Exp. Med. 180:1849-1860 (1994)].
B7.1 и B7.2 связывают CD28 и CTLA-4 с различными функциональными последствиями [Linsley et al., PNAS, 87:5031-5035 (1990); Linsley et al., J. Exp. Med., 173:721-730(1991); Azuma et al., Nature 366:76-79 (1993); Freeman et al., Science 262:909-912 (1993)]. Связывание B7.1 и B7.2 с CTLA-4 имеет намного более высокую аффинность, чем связывание B7.1/B7.2 с CD28 [van der Merwe, J. Exp. Med. 185:393-402 (1997)].
CD28 представляет собой гомодимерный гликопротеин, который является членом суперсемейства Ig [Aruffo and Seed, PNAS, 84:8573-8577 (1987)]. Зрелый белок имеет одиночный внеклеточный вариабельный домен из 134 аминокислотных остатков, содержащий гексапептидный мотив MYPPPY, который является необходимым для связывания с контр-рецептором [Riley and June, Blood, 105:13-21 (2005)]. 41-аминокислотный цитоплазматический домен CD28 содержит четыре тирозиновых остатка, которые могут быть фосфорилированы после активации [Sharpe and Freeman, Nat. Rev. Immunol., 2:116-126 (2002)]. CD28 экспрессируется на большинстве CD4+ T-клеток и приблизительно 50% CD8+ T-клеток [Gross et al., J. Immunol., 149:380 388 (1992); Riley and June, Blood, 105:13-21 (2005)]. После связывания T-клеточного рецептора (TCR), связывание B7.1/B7.2 с CD28 обеспечивает костимулирующий сигнал T-клетке, позволяющий активацию T-клетки и последующее развитие иммунного ответа [Reiser et al., PNAS, 89:271-275 (1992); Jenkins et al., J. Immunol., 147:2461-2466 (1991)]. Показано, что в отсутствие сигнала CD28, T-клетки подвергаются апоптозу или входят в состояние неспособности отвечать [Jenkins et al., J. Exp. Med. 165:302-319 (1987); Jenkins et al., PNAS, 84:5409-5413 (1987); Schwartz, Science, 248:1349-1356 (1990)]. Связывание CD28-B7.1/B7.2 может изменять пороговый уровень связывания TCR (например, количество комплекса антиген-MHC), необходимый для активации, уменьшать время для стимуляции наивных клеток и увеличивать амплитуду ответа T-клеток [Soskic et al., Advances in Immunology, 124:96-123 (2014)].
CTLA-4 (CD152) также является членом суперсемейства Ig и состоит из одиночного внеклеточного домена, трансмембранного домена и короткого цитоплазматического хвоста [Swanson, Immunology; 1010:169-177 (2000)]. Кроме того, CTLA-4 разделяет приблизительно 30% идентичности аминокислот с CD28. CTLA-4 не эксперессируется конститутивно на наивных T-клетках, хотя он подвергается быстрой повышающей регуляции вскоре после связывания CD28 и активации T-клетки с пиковым уровнем экспрессии CTLA-4 через приблизительно 48-96 часов после первоначальной активации T-клетки [Alegre et al., J. Immunol., 157:4762-4770 (1996); Freeman et al., J. Immunol., 149:3795-3801 (1992)]. CTLA-4 связывается как с B7.1, так и с B7.2 с намного более высокой аффинностью, чем CD28 [van der Merwe et al., J. Exp. Med., 185:393-402 (1997)]. Однако, в отличие от стимулирующих эффектов CD28, связывающего B7.1 или B7.2, CTLA-4 действует в качестве ингибирующего рецептора, который является жизненно необходимым для понижающей модуляции иммунного ответа [Walnus et al., Immunity, 1:405-413 (1994); Walnus, J.Exp. Med., 183:2541-2550 (1996); Krummel and Allison, J. Exp. Med., 183:2533-2540 (1996)]. Механизм, посредством которого CTLA-4 опосредует свои иммуноингибирующие функции, связан с его способностью действовать в качестве конкурентного ингибитора взаимодействия между CD28 и B7.1/B7.2 [обзор приведен в Swanson, Immunology, 1010:169-177 (2000)]. Критическая роль CTLA-4 в иммунной понижающей регуляции показана у мышей с недостаточностью CTLA-4, которые умирают к возрасту 3-5 недель из-за развития лимфопролиферативного заболевания, характеризуемого инфильтрацией T-клеток во множество органов [Tivol et al., Immunity, 3:541-5417 (1995); Waterhouse et al., Science, 270:985-988 (1995)]. Показано также, что последствия нокаута CTLA-4 зависят от взаимодействия CD28 с его лигандами B7.1 и B7.2, как показано по отсутствию заболевания у мышей с тройным нокаутом CTLA-4/B7-1/B7-2 [Mandelbrot et al., J. Exp. Med., 189:435-440 (1999)]. Это подтверждается также посредством защиты против лимфопролиферации, достигаемой посредством повторяющегося введения CTLA-4 Ig у мышей с нокаутом CTLA-4 [Tivol et al., J Immunol., 158:5091-5094 (1997)].
Кроме того, показано, что блокирование эффекта CTLA-4 с использованием антител усиливает ответы T-клеток in vitro и in vivo, и увеличивает противоопухолевые иммунные ответы [Leach et al., Science, 271:1734-1736 (1996)]. На основании этих обнаружений, разработку блокаторов CTLA-4, таких как моноклональные антитела, предпринимали для обеспечения терапевтических вариантов для лечения злокачественных опухолей [Hodi et al., PNAS, 100(8):4712-4717 (2003); Phan GQ et al., PNAS,100(14):8372-8377 (2003); Attia, Journal of Clinical Oncology, 23(25):6043-6053 (2005); Comin-Anduix et al., Journal of Translational Medicine, 6:22-22 (2008); WO2000037504 A2; U.S. 8017114 B2; WO2010097597A1; WO2012120125 A1; и Boutros et al., Nat Rev Clin Oncol., 13(8):473-486 (2016)].
PD-1 является членом семейства CD28/CTLA-4 иммуномодулирующих рецепторов. PD-1 также является членом суперсемейства Ig и содержит внеклеточный вариабельный домен, который связывает его лиганды, и цитоплазматический хвост, который связывает передающие сигналы молекулы [обзор приведен в Zak et al., Cell Structure, 25:1163-1174 (2017)]. Цитоплазматический хвост PD-1 содержит два передающих сигналы мотива на основе тирозина [Zhang et al., Immunity 20:337-347 (2004)]. Экспрессия PD-1 не обнаружена на нестимулированных T-клетках, B-клетках или миелоидных клетках. Однако, экспрессия PD 1 подвергается повышающей регуляции на этих клетках после активации [Chemnitz et al., J. Immunol., 173:945-954 (2004); Petrvas et al., J. Exp. Med., 203:2281-2292 (2006)]. PD-1 является наиболее близко родственным CTLA-4, разделяя приблизительно 24% идентичность аминокислот [Jin et al., Current Topics in Microbiology and Immunology, 350:17-37 (2010)]. PD-1 ослабляет активацию T-клетки при связывании с PD-L1 и PD-L2, которые экспрессированы на поверхности APC. Связывание любого из этих лигандов с PD-1 отрицательно регулирует передачу сигналов антигена через T-клеточный рецептор (TCR). До настоящего времени, обнаружено, что только PD-L1 и PD-L2 функционируют в качестве лигандов для PD-1. Как и для CTLA-4, связывание PD-1, по-видимому, передает отрицательный иммуномодулирующий сигнал. Связывание PD-1 посредством PD-L1 или PD-L2 приводит к ингибированию опосредованной TCR пролиферации и продукции цитокинов [Jin et al., Current Topics in Microbiology and Immunology, 350:17-37 (2010)]. В отличие от животных с недостаточностью CTLA-4, мыши с недостаточностью PD-1 умирают намного позже на протяжении жизни и демонстрируют признаки аутоиммунитета, хотя тяжесть наблюдаемых эффектов не настолько выражена, как эффектов, проявляемых животными с недостаточностью CTLA-4 [Nishimura et al., Immunity, 11(2):141-151 (1999); Nishimura et al., Science, 291(5502):319-322 (2001)]. Несмотря на то, что пути передачи сигналов PD-1 в настоящее время интенсивно исследуют, исследования до настоящего времени позволяют предполагать, что взаимодействия PD-L1/PD-L2/PD-1 вовлечены в отрицательную регуляцию некоторых иммунных ответов из-за ослабления сигналов ниже стимуляции TCR, приводящего к уменьшению секреции цитокинов и нарушению пролиферация T-клетки и к уменьшению продукции цитотоксических молекул T-клетки [Freeman et al., J. Exp. Med., 192 (7):1027-1034 (2000)].
PD-L1 (CD274) представляет собой мембранный белок типа 1 и состоит из IgV-подобных и IgC-подобных внеклеточных доменов, гидрофобного трансмембранного домена, короткого цитоплазматического хвоста, состоящего из 30 аминокислот, с неизвестными свойствами передачи сигнала. PD-L1 известен как член семейства B7 и разделяет приблизительно 20% идентичность аминокислот с членами семейства B7. PD L1 связывается со своим рецептором, PD-1, обнаруженным на активированных T-клетках, B-клетках и миелоидных клетках. PD-L1 также связывается с костимулирующей молекулой B7.1, но не с CD86 [Butte et al., Immunology, 45 (13):3567-3572 (2008)]. Аффинность B7.1 для PD-L1 является промежуточной между его аффинностями для CD28 и CTLA-4. Родственная молекула PD-L2 не имеет аффинности для CD80 или CD86, но разделяет PD-1 в качестве рецептора. Привлечение PD-L1 с использованием его рецептора PD-1 на T-клетках подает сигнал, который ингибирует опосредованную TCR продукцию IL-2 и пролиферацию T-клетки. Связывание PD-L1 с PD-1 также вносит вклад в индуцированную лигандом TCR понижающую модуляцию в ходе представления антигена наивным T-клеткам. Кроме того, связывание PD-L1 с B7.1 на T-клетках приводит к апоптозу T-клеток. Роль PD 1 и PD-L1 в качестве ингибиторов активации T-клетки показана во многих исследованиях. На основании этих обнаружений, разработку блокаторов PD-1 и PD-L1, таких как моноклональные антитела, предпринимали для обеспечения терапевтических вариантов для лечения злокачественных опухолей и инфекционных заболеваний.
Гуманизированные моноклональные антитела, блокирующие связывание и активность собачьего PD-1, PD L1 и CTLA-4, разработаны и в настоящее время доступны для использования в лечении субъектов-людей с диагнозом одна из нескольких различных типов злокачественных опухолей. Подобным образом, канинизированные моноклональные антитела, блокирующие связывание и активность собачьего PD-1 и PD L1, также опубликованы [U.S. 9944704 B2, U.S. 10106607 B2 и U.S.2018/0237535 A1, полное содержание которых, таким образом, приведено в качестве ссылки]. Однако, до настоящего времени не было сообщений о канинизированном моноклональном антителе, блокирующем связывание и активность собачьего CTLA-4.
Цитату из любой ссылки в настоящем описании не следует рассматривать как допущение, что такая ссылка является доступной в качестве «предшествующего уровня техники» для настоящего изобретения.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к канинизированным антителам против человеческого CTLA-4, имеющим специфическую аффинность связывания для собачьего CTLA-4, так же как имеющим способность блокировать связывание собачьего CTLA-4 с собачьим CD80 и/или CD86. Настоящее изобретение также относится к применению таких антител в лечении заболеваний, таких как злокачественная опухоль и/или заболевания, обусловленные инфекциями.
Соответственно, настоящее изобретение относится к выделенному канинизированному антителу, содержащему тяжелую цепь собачьего IgG и собачью легкую цепь каппа или лямбда, или антигенсвязывающий фрагмент канинизированного антитела, которое специфически связывает CTLA-4. В конкретных вариантах осуществления этого типа, собачья легкая цепь каппа или лямбда содержит три определяющие комплементарность области (CDR) легкой цепи, т.е., CDR легкой цепи 1 (CDRL1), CDR легкой цепи 2 (CDRL2) и CDR легкой цепи 3 (CDRL3), и тяжелая цепь собачьего IgG содержит три CDR тяжелой цепи, т.е., CDR тяжелой цепи 1 (CDRH1), CDR тяжелой цепи 2 (CDRH2) и CDR тяжелой цепи 3 (CDRH3), где все шесть из CDR получены из антитела против CTLA-4 млекопитающих. Конкретные варианты осуществления канинизированных антител и их фрагментов по настоящему изобретению связывают собачий CTLA-4 и/или блокируют связывание собачьего CTLA-4 с собачьим CD80 и/или CD86.
В конкретных вариантах осуществления, CDRL1 канинизированного антитела содержит аминокислотную последовательность SEQ ID NO:54, CDRL2 содержит аминокислотную последовательность, содержащую SEQ ID NO:56, и CDRL3 содержит аминокислотную последовательность SEQ ID NO:58. В родственных вариантах осуществления CDRH1 канинизированного антитела содержит аминокислотную последовательность SEQ ID NO:48, CDRH2 содержит аминокислотную последовательность, содержащую SEQ ID NO:50, и CDRH3 содержит аминокислотную последовательность SEQ ID NO:52.
В конкретных вариантах осуществления, CDRL1 канинизированного антитела кодирована нуклеотидной последовательностью SEQ ID NO:53, CDRL2 кодирована нуклеотидной последовательностью SEQ ID NO:55, и CDRL3 кодирована нуклеотидной последовательностью SEQ ID NO:57. В родственных вариантах осуществления CDRH1 канинизированного антитела кодирована нуклеотидной последовательностью SEQ ID NO:47, CDRH2 кодирована нуклеотидной последовательностью SEQ ID NO:49, и CDRH3 кодирована нуклеотидной последовательностью SEQ ID NO:51.
В более конкретном варианте осуществления, CDRL1 канинизированного антитела содержит аминокислотную последовательность SEQ ID NO:54, CDRL2 содержит аминокислотную последовательность, содержащую SEQ ID NO:56, и CDRL3 содержит аминокислотную последовательность SEQ ID NO:58, и кроме того, CDRH1 канинизированного антитела содержит аминокислотную последовательность SEQ ID NO:48, CDRH2 содержит аминокислотную последовательность, содержащую SEQ ID NO:50, и CDRH3 содержит аминокислотную последовательность SEQ ID NO:52.
Для конкретных вариантов осуществления настоящего изобретения, тяжелая цепь канинизированного антитела содержит аминокислотную последовательность SEQ ID NO:34. В более конкретных вариантах осуществления, тяжелая цепь кодирована нуклеотидной последовательностью SEQ ID NO:33. В родственных вариантах осуществления, тяжелая цепь содержит аминокислотные последовательности SEQ ID NO:48, SEQ ID NO:50 и SEQ ID NO:52, внутри консервативного варианта аминокислотной последовательности SEQ ID NO:34. В других вариантах осуществления, тяжелая цепь содержит аминокислотные последовательности SEQ ID NO:48, SEQ ID NO:50 и SEQ ID NO:52, внутри функционально консервативного варианта аминокислотной последовательности SEQ ID NO:34.
В других вариантах осуществления, тяжелая цепь канинизированного антитела содержит аминокислотную последовательность SEQ ID NO:36. В более конкретных вариантах осуществления, тяжелая цепь кодирована нуклеотидной последовательностью SEQ ID NO:35. В родственных вариантах осуществления, тяжелая цепь содержит аминокислотные последовательности SEQ ID NO:48, SEQ ID NO:50 и SEQ ID NO:52, внутри консервативного варианта аминокислотной последовательности SEQ ID NO:36. В других вариантах осуществления, тяжелая цепь содержит аминокислотные последовательности SEQ ID NO:48, SEQ ID NO:50 и SEQ ID NO:52, внутри функционально консервативного варианта аминокислотной последовательности SEQ ID NO:36.
В других вариантах осуществления, тяжелая цепь канинизированного антитела содержит аминокислотную последовательность SEQ ID NO:38. В более конкретных вариантах осуществления, тяжелая цепь кодирована нуклеотидной последовательностью SEQ ID NO:37. В родственных вариантах осуществления, тяжелая цепь содержит аминокислотные последовательности SEQ ID NO:48, SEQ ID NO:50 и SEQ ID NO:52, внутри консервативного варианта аминокислотной последовательности SEQ ID NO:38. В других вариантах осуществления, тяжелая цепь содержит аминокислотные последовательности SEQ ID NO:48, SEQ ID NO:50 и SEQ ID NO:52, внутри функционально консервативного варианта аминокислотной последовательности SEQ ID NO:38.
В других вариантах осуществления, тяжелая цепь канинизированного антитела содержит аминокислотную последовательность SEQ ID NO:40. В более конкретных вариантах осуществления, тяжелая цепь кодирована нуклеотидной последовательностью SEQ ID NO:39. В родственных вариантах осуществления, тяжелая цепь содержит аминокислотные последовательности SEQ ID NO:48, SEQ ID NO:50 и SEQ ID NO:52, внутри консервативного варианта аминокислотной последовательности SEQ ID NO:40. В других вариантах осуществления, тяжелая цепь содержит аминокислотные последовательности SEQ ID NO:48, SEQ ID NO:50 и SEQ ID NO:52, внутри функционально консервативного варианта аминокислотной последовательности SEQ ID NO:40.
Для конкретных вариантов осуществления настоящего изобретения, тяжелая цепь канинизированного антитела содержит аминокислотную последовательность SEQ ID NO:60. В более конкретных вариантах осуществления, тяжелая цепь кодирована нуклеотидной последовательностью SEQ ID NO:59. В родственных вариантах осуществления, тяжелая цепь содержит аминокислотные последовательности SEQ ID NO:48, SEQ ID NO:50 и SEQ ID NO:52, внутри консервативного варианта аминокислотной последовательности SEQ ID NO:60. В других вариантах осуществления, тяжелая цепь содержит аминокислотные последовательности SEQ ID NO:48, SEQ ID NO:50 и SEQ ID NO:52, внутри функционально консервативного варианта аминокислотной последовательности SEQ ID NO:60.
В других вариантах осуществления, тяжелая цепь канинизированного антитела содержит аминокислотную последовательность SEQ ID NO:62. В более конкретных вариантах осуществления, тяжелая цепь кодирована нуклеотидной последовательностью SEQ ID NO:61. В родственных вариантах осуществления, тяжелая цепь содержит аминокислотные последовательности SEQ ID NO:48, SEQ ID NO:50 и SEQ ID NO:52, внутри консервативного варианта аминокислотной последовательности SEQ ID NO:62. В других вариантах осуществления, тяжелая цепь содержит аминокислотные последовательности SEQ ID NO:48, SEQ ID NO:50 и SEQ ID NO:52, внутри функционально консервативного варианта аминокислотной последовательности SEQ ID NO:62.
В других вариантах осуществления, тяжелая цепь канинизированного антитела содержит аминокислотную последовательность SEQ ID NO:64. В более конкретных вариантах осуществления, тяжелая цепь кодирована нуклеотидной последовательностью SEQ ID NO:63. В родственных вариантах осуществления, тяжелая цепь содержит аминокислотные последовательности SEQ ID NO:48, SEQ ID NO:50 и SEQ ID NO:52, внутри консервативного варианта аминокислотной последовательности SEQ ID NO:64. В других вариантах осуществления, тяжелая цепь содержит аминокислотные последовательности SEQ ID NO:48, SEQ ID NO:50 и SEQ ID NO:52, внутри функционально консервативного варианта аминокислотной последовательности SEQ ID NO:64.
В других вариантах осуществления, тяжелая цепь канинизированного антитела содержит аминокислотную последовательность SEQ ID NO:66. В более конкретных вариантах осуществления, тяжелая цепь кодирована нуклеотидной последовательностью SEQ ID NO:65. В родственных вариантах осуществления тяжелая цепь содержит аминокислотные последовательности SEQ ID NO:48, SEQ ID NO:50 и SEQ ID NO:52, внутри консервативного варианта аминокислотной последовательности SEQ ID NO:66. В других вариантах осуществления, тяжелая цепь содержит аминокислотные последовательности SEQ ID NO:48, SEQ ID NO:50 и SEQ ID NO:52, внутри функционально консервативного варианта аминокислотной последовательности SEQ ID NO:66.
В конкретных вариантах осуществления, собачья легкая цепь канинизированного антитела представляет собой цепь каппа. В альтернативных вариантах осуществления, собачья легкая цепь представляет собой цепь лямбда. В конкретных вариантах осуществления, легкая цепь каппа содержит аминокислотную последовательность SEQ ID NO:42. В более конкретных вариантах осуществления, легкая цепь каппа кодирована нуклеотидной последовательностью SEQ ID NO:41. В родственных вариантах осуществления, легкая цепь каппа содержит аминокислотные последовательности SEQ ID NO:54, SEQ ID NO:56 и SEQ ID NO:58, внутри консервативного варианта аминокислотной последовательности SEQ ID NO:42. В других вариантах осуществления, легкая цепь каппа содержит аминокислотные последовательности SEQ ID NO:54, SEQ ID NO:56 и SEQ ID NO:58, внутри функционально консервативного варианта аминокислотной последовательности SEQ ID NO:42.
В конкретных вариантах осуществления, легкая цепь каппа канинизированного антитела содержит аминокислотную последовательность SEQ ID NO:44. В более конкретных вариантах осуществления, легкая цепь каппа кодирована нуклеотидной последовательностью SEQ ID NO:43. В родственных вариантах осуществления, легкая цепь каппа содержит аминокислотные последовательности SEQ ID NO:54, SEQ ID NO:56 и SEQ ID NO:58, внутри консервативного варианта аминокислотной последовательности SEQ ID NO:44. В других вариантах осуществления, легкая цепь каппа содержит аминокислотные последовательности SEQ ID NO:54, SEQ ID NO:56 и SEQ ID NO:58, внутри функционально консервативного варианта аминокислотной последовательности SEQ ID NO:44.
В других вариантах осуществления, легкая цепь каппа канинизированного антитела содержит аминокислотную последовательность SEQ ID NO:46. В более конкретных вариантах осуществления, легкая цепь каппа кодирована нуклеотидной последовательностью SEQ ID NO:45. В родственных вариантах осуществления, легкая цепь каппа содержит аминокислотные последовательности SEQ ID NO:54, SEQ ID NO:56 и SEQ ID NO:58, внутри консервативного варианта аминокислотной последовательности SEQ ID NO:46. В других вариантах осуществления, легкая цепь каппа содержит аминокислотные последовательности SEQ ID NO:54, SEQ ID NO:56 и SEQ ID NO:58, внутри функционально консервативного варианта аминокислотной последовательности SEQ ID NO:46.
Кроме того, настоящее изобретение относится к канинизированным антителам, содержащим любую легкую цепь по настоящему изобретению с любой тяжелой цепью по настоящему изобретению. В конкретных вариантах осуществления, выделенное канинизированное антитело содержит тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO:36, SEQ ID NO:62, или аминокислотные последовательности SEQ ID NO:48, SEQ ID NO:50 и SEQ ID NO:52, внутри консервативного варианта аминокислотной последовательности SEQ ID NO:36 или SEQ ID NO:62, и легкую цепь каппа, содержащую аминокислотную последовательность SEQ ID NO:46 или аминокислотную последовательность, содержащую аминокислотные последовательности SEQ ID NO:54, SEQ ID NO:56 и SEQ ID NO:58, внутри консервативного варианта аминокислотной последовательности SEQ ID NO:46. В более конкретных вариантах осуществления, выделенное канинизированное антитело содержит тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO:36, и легкую цепь каппа, содержащую аминокислотную последовательность SEQ ID NO:46. В других конкретных вариантах осуществления, выделенное канинизированное антитело содержит тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO:62, и легкую цепь каппа, содержащую аминокислотную последовательность SEQ ID NO:46.
В других конкретных вариантах осуществления, выделенное канинизированное антитело содержит тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO:40, SEQ ID NO:66, или содержит аминокислотные последовательности SEQ ID NO:48, SEQ ID NO:50 и SEQ ID NO:52, внутри консервативного варианта аминокислотной последовательности SEQ ID NO:40 или SEQ ID NO:66, и легкую цепь каппа, содержащую аминокислотную последовательность SEQ ID NO:42 или аминокислотную последовательность, содержащую аминокислотные последовательности SEQ ID NO:54, SEQ ID NO:56 и SEQ ID NO:58, внутри консервативного варианта аминокислотной последовательности SEQ ID NO:42. В более конкретных вариантах осуществления, выделенное канинизированное антитело содержит тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO:40, и легкую цепь каппа, содержащую аминокислотную последовательность SEQ ID NO:42. В других конкретных вариантах осуществления, выделенное канинизированное антитело содержит тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO:66, и легкую цепь каппа, содержащую аминокислотную последовательность SEQ ID NO:42.
Кроме того, настоящее изобретение относится к выделенным нуклеиновым кислотам, кодирующим любую из легких цепей канинизированного антитела по настоящему изобретению. Подобным образом, кроме того, настоящее изобретение относится к выделенным нуклеиновым кислотам, кодирующим любую из тяжелых цепей канинизированного антитела по настоящему изобретению. Кроме того, настоящее изобретение относится к экспрессирующим векторам, содержащим одну или несколько выделенных нуклеиновых кислот по настоящему изобретению. Кроме того, настоящее изобретение относится к клеткам-хозяевам, содержащим один или несколько экспрессирующих векторов по настоящему изобретению.
В конкретных вариантах осуществления, антитело представляет собой рекомбинантное антитело или его антигенсвязывающий фрагмент. В родственных вариантах осуществления, вариабельный домен тяжелой цепи и вариабельный домен легкой цепи соединены посредством гибкого линкера с формированием одноцепочечного антитела.
В конкретных вариантах осуществления, антитело или антигенсвязывающий фрагмент представляет собой фрагмент Fab.
В других вариантах осуществления, антитело или антигенсвязывающий фрагмент представляет собой фрагмент Fab’. В других вариантах осуществления, антитело или антигенсвязывающий фрагмент представляет собой фрагмент (Fab')2. В других вариантах осуществления, антитело или антигенсвязывающий фрагмент представляет собой диатело. В конкретных вариантах осуществления, антитело или антигенсвязывающий фрагмент представляет собой доменное антитело. В более конкретных вариантах осуществления, антитело или антигенсвязывающий фрагмент представляет собой камелизированное однодоменное антитело.
В конкретных вариантах осуществления, канинизированное антитело против человеческого CTLA-4 или антигенсвязывающий фрагмент увеличивает иммунный ответ субъекта-собаки, подвергаемого лечению.
Соответственно, кроме того, настоящее изобретение относится к выделенным нуклеиновым кислотам, кодирующим канинизированные антитела против человеческого CTLA-4 или антигенсвязывающие фрагменты, как описано в настоящем описании. В родственных вариантах осуществления такие антитела или антигенсвязывающие фрагменты можно использовать для получения лекарственного средства для лечения злокачественной опухоли у субъекта-собаки. Альтернативно или в сочетании, настоящее изобретение относится к использованию любого из антител или фрагментов антител по настоящему изобретению для диагностического применения. В дополнительных вариантах осуществления, настоящее изобретение относится к набору, содержащему любое из канинизированных антител или антигенсвязывающих фрагментов, описанных в настоящем описании.
В дополнительных вариантах осуществления, настоящее изобретение относится к экспрессирующему вектору, содержащему выделенную нуклеиновую кислоту, кодирующую любое из канинизированных антител против человеческого CTLA-4 или антигенсвязывающих фрагментов по изобретению. Изобретение также относится к клетке-хозяину, содержащей любой из экспрессирующих векторов, описанных в настоящем описании. В конкретных вариантах осуществления, эти нуклеиновые кислоты, экспрессирующие векторы или полипептиды по изобретению можно использовать в способах получения антитела.
Настоящее изобретение, кроме того, относится к фармацевтическим композициям, содержащим канинизированное антитело по настоящему изобретению или его антигенсвязывающий фрагмент вместе с фармацевтически приемлемым носителем или разбавителем. Кроме того, настоящее изобретение относится к способам увеличения активности иммуноцита, включающим введение нуждающемуся в этом субъекту терапевтически эффективного количества таких фармацевтических композиций. В конкретных вариантах осуществления, субъект относится к собачьим. В альтернативных вариантах осуществления, субъект относится к кошачьим. В других вариантах осуществления, субъект относится к лошадиным. В конкретных вариантах осуществления способ используют для лечения злокачественной опухоли. В других вариантах осуществления, способ используют для лечения инфекции или инфекционного заболевания. В других вариантах осуществления, канинизированное антитело по настоящему изобретению или его антигенсвязывающий фрагмент используют в качестве адъюванта вакцины.
Эти и другие аспекты настоящего изобретения станут лучше понятными со ссылкой на следующее краткое описание чертежей и подробное описание.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фигуре 1 показаны результаты ELISA с собачьим CTLA-4 для серий отобранных химерных антител, как указано, показывающие их активность связывания: • 3B10, Δ 8H5,  611,
611,  10D1, ∇ 3B3, O 418, □ 411,
10D1, ∇ 3B3, O 418, □ 411,  1E2, и + изо-контроль. Индивидуальные химерные антитела описаны в таблице 1 ниже. Изо-контроль представляет собой канинизированное мышиное антитело против антигена, не родственного CTLA-4.
1E2, и + изо-контроль. Индивидуальные химерные антитела описаны в таблице 1 ниже. Изо-контроль представляет собой канинизированное мышиное антитело против антигена, не родственного CTLA-4.
На фигуре 2 показаны результаты ELISA для серий канинизированных антител 3B-10, как указано, показывающие, что канинизированные антитела 3B-10 сильно связываются с собачьим CTLA-4. • 3B10 MC,  c3B10L2-H3,
c3B10L2-H3,  c3B10L3-H3, ∇ c3B10L2-H2, O c3B10L3-H2, □ c3B10L3-H4 и Δ c3B10L1-H1. L1, L2 и L3 соответствуют VL1, VL2 и VL3, соответственно, в таблице 5 ниже, и H1, H2, H3 и H4 соответствуют VH1, VH2, VH3 и VH4, соответственно, в таблице 4 ниже. 3B10 MC представляет собой такое же химерное антитело, изображенное на фигуре 1.
c3B10L3-H3, ∇ c3B10L2-H2, O c3B10L3-H2, □ c3B10L3-H4 и Δ c3B10L1-H1. L1, L2 и L3 соответствуют VL1, VL2 и VL3, соответственно, в таблице 5 ниже, и H1, H2, H3 и H4 соответствуют VH1, VH2, VH3 и VH4, соответственно, в таблице 4 ниже. 3B10 MC представляет собой такое же химерное антитело, изображенное на фигуре 1.
На фигуре 3 представлены результаты ELISA с собачьим CD86 и собачьим CTLA-4 в присутствии химерных или канинизированных антител 3B10. • 3B10 MC,  c3B10L1-H1,
c3B10L1-H1,  c3B10L3-H2,
c3B10L3-H2,  c3B10L3-H4 и + изо-контроль. Результаты показывают блокирующую активность антитела по отношению к взаимодействию связывания собачьего CD86 с собачьим CTLA-4 как для химерных, так и для канинизированных антител 3B10. Изо-контроль представляет собой канинизированные мышиное антитело против антигена, не родственного CTLA-4.
c3B10L3-H4 и + изо-контроль. Результаты показывают блокирующую активность антитела по отношению к взаимодействию связывания собачьего CD86 с собачьим CTLA-4 как для химерных, так и для канинизированных антител 3B10. Изо-контроль представляет собой канинизированные мышиное антитело против антигена, не родственного CTLA-4.
На фигуре 4 показано образование IFNγ, продуцированного собачьими PBMC после активации посредством отобранных химерных антител против CTLA-4, как указано [1E2, 3B10, 10D1, 8H5, 611, 411 и 418] и как описано для фигуры 1 выше.
На фигуре 5 идентифицированы эпитопы собачьего CTLA-4, содержащего аминокислотную последовательность из предшествующего уровня техники SEQ ID NO:68, которые взаимодействуют с канинизированным антителом 3B10L3H2 (3B10 VL3VH2).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Сокращения:
На протяжении подробного описания и примеров по изобретению, использованы следующие сокращения:
ADCC Антителозависимая клеточная цитотоксичность
CDC Комплементзависимая цитотоксичность
CDR Определяющая комплементарность область в вариабельных областях иммуноглобулинов, определенная с использованием системы нумерации Kabat
CHO Яичник китайского хомяка
EC50 концентрация, приводящая к 50% эффективности или связыванию
ELISA Твердофазный иммуноферментный анализ
FR Каркасная область антитела: вариабельные области иммуноглобулинов, исключая области CDR.
HRP Пероксидаза хрена
IFN интерферон
IC50 концентрация, приводящая к 50% ингибированию
IgG Иммуноглобулин G
Kabat Система выравнивания и нумерации иммуноглобулинов, впервые предложенная в
Elvin A. Kabat [Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, Md. (1991)].
mAb Моноклональное антитело (также Mab или MAb)
MES 2-(N-морфолино)этансульфоновая кислота
MOA Механизм действия
ПЦР Полимеразная цепная реакция
PK Фармакокинетика
SEB Энтеротоксин B Staphylococcus
TT Токсоид столбняка
V область Фрагмент цепей IgG, который является изменчивым по последовательности между различными антителами. Он простирается до остатка по Kabat 109 в легкой цепи и 113 в тяжелой цепи.
VH Вариабельная область тяжелой цепи иммуноглобулина
VK Вариабельная область легкой цепи каппа иммуноглобулина
Определения:
Так, чтобы изобретение было более понятным, определенные технические и научные термины конкретно определены ниже. Если в другом месте в настоящем описании конкретно не определено иное, все другие технические и научные термины, используемые в настоящем описании, имеют такое же значение, которое является общепринятым для специалиста в области, к которой относится настоящее изобретение.
В рамках изобретения, включая прилагаемую формулу изобретения, формы единственного числа слов включают соответствующие им объекты ссылки множественного числа, если контекст явно не требует иного.
«Активация», как это применимо к клеткам или к рецепторам, относится к активации или обработке клетки или рецептора с использованием лиганда, если не указано иное по контексту или явно. «Лиганд» включает природные и синтетические лиганды, например, цитокины, варианты, аналоги, мутеины цитокинов и связывающие соединения, происходящие из антител. «Лиганд» также включает малые молекулы, например, пептидные миметики цитокинов и пептидные миметики антител. «Активация» может относиться к активации клеток, как регулируется посредством внутренних механизмов, так же как посредством внешних факторов или факторов внешней среды.
«Активность» молекулы может описывать или относиться к связыванию молекулы с лигандом или с рецептором, к каталитической активности; к способности стимулировать экспрессию гена или передачу сигналов в клетке, дифференцировку или созревание клетки; к антигенной активности, к модуляции активности других молекул и т.п. «Активность» молекулы может также относиться к активности при модуляции или поддержании взаимодействий между клетками, например, адгезии, или активности при поддержании структуры клетки, например, клеточных мембран или цитоскелета. «Активность» может также означать специфическую активность, например, [каталитическую активность]/[мг белка] или [иммунологическую активность]/[мг белка], концентрацию в биологическом компартменте или т.п. «Активность» может относиться к модуляции компонентов врожденной или адаптивной иммунных систем.
«Введение» и «обработка», как это применимо к животному, например, к экспериментальному субъекту, клетке, ткани, органу или биологической жидкости собачьих, относится к контакту экзогенного фармацевтического, терапевтического, диагностического средства или композиции с животным, например, субъектом, клеткой, тканью, органом или биологической жидкостью собачьих. Обработка клетки включает контакт реагента с клеткой, так же как контакт реагента с жидкостью, где жидкость находится в контакте с клеткой. «Введение» и «обработка» также обозначает обработки in vitro и ex vivo, например, клетки, посредством реагента, диагностического, связывающего соединения, или посредством другой клетки. Термин «субъект» включает любой организм, предпочтительно, животное, более предпочтительно, млекопитающее (например, собачье, кошачье или лошадиное) и наиболее предпочтительно, собачье.
«Лечить» или «лечение» обозначает введение лекарственного средства, такого как композиция, содержащая любое из антител или антигенсвязывающих фрагментов по настоящему изобретению, внутренним или внешним способом субъекту или пациенту - собачьему, имеющему один или несколько симптомов заболевания, или, как подозревают, имеющему заболевание, против которого средство имеет терапевтическую активность. Как правило, средство вводят в количестве, эффективном для облегчения и/или ослабления одного или нескольких симптомов заболевания у подвергаемых лечению субъекта или популяции, независимо от того, происходит ли это посредством индукции регрессии или ингибирования прогрессирования такого симптома(симптомов) до любой клинически измеримой степени. Количество лекарственного средства, которое является эффективным для облегчения любого конкретного симптома заболевания (также обозначенное в настоящем описании как «терапевтически эффективное количество»), может меняться в соответствии с такими факторами, как состояние заболевания, возраст и масса пациента (например, собачьего, кошачьего или лошадиного), и способность фармацевтической композиции вызывать желательный ответ у субъекта. Был ли симптом заболевания облегчен или ослаблен, можно оценивать посредством любого клинического измерения, как правило, используемого ветеринарами или другими специалистами, поставляющими услуги здравоохранения, для оценки тяжести или статуса прогрессирования этого симптома. В то время как вариант осуществления настоящего изобретения (например, способ или изделие для лечения) может не являться эффективным для облегчения целевого симптома(симптомов) заболевания у каждого субъекта, он должен облегчать целевой симптом(ы) заболевания у статистически значимого количества субъектов, как определено посредством любого статистического теста, известного в данной области, такого как t-критерий Стьюдента, критерий хи2, U-критерий в соответствии с Манном и Уитни, критерий Крускала-Уоллиса (Н-критерий), критерий Джонкхиера-Терпстры и критерий Уилкоксона.
«Лечение», как это применимо к человеческому, ветеринарному (например, собачьему) или исследовательскому субъекту, относится к терапевтическому лечению, так же как к исследовательским и диагностическим применениям. «Лечение», как это применимо к человеческому, ветеринарному (например, собачьему) или исследовательскому субъекту, или клетке, ткани или органу, включает контакт антител или антигенсвязывающих фрагментов по настоящему изобретению с субъектом - собачьим или другим животным (например, кошачьим), клеткой, тканью, физиологическим компартментом или физиологической жидкостью.
Термин «иммунный ответ» относится к действию, например, лимфоцитов, антигенпредставляющих клеток, фагоцитов, гранулоцитов и растворимых макромолекул, продуцированных вышеуказанными клетками или печенью (включая антитела, цитокины, и комплемент), которое приводит к избирательному повреждению, разрушению или выведению из организма млекопитающего (например, организма собачьего) злокачественных клеток, клеток или тканей, инфицированных патогенами, или проникших патогенов.
Канинизированные антитела против человеческого CTLA-4
Настоящее изобретение относится к выделенным канинизированным антителам против человеческого CTLA-4 или их антигенсвязывающим фрагментам, которые связывают собачий CTLA-4, и к применениям таких антител или фрагментов.
В рамках изобретения, канинизированное антитело против человеческого CTLA-4 относится к канинизированному антителу, которое специфически связывается с CTLA-4 млекопитающих. Антитело, которое специфически связывается с CTLA-4 млекопитающих, и в частности, с собачьим CTLA-4, представляет собой антитело, демонстрирующее предпочтительное связывание с CTLA-4 млекопитающих, по сравнению с другими антигенами, но эта специфичность не требует абсолютной специфичности связывания. Канинизированное антитело против человеческого CTLA-4 считают «специфическим» для собачьего CTLA-4, если его связывание является определяющим присутствие собачьего CTLA-4 в биологическом образце, полученном от собачьего, или если оно является способным изменять активность собачьего CTLA-4 без излишних помех для активности других неродственных собачьих белков в собачьем образце, например, без получения нежелательных результатов, таких как ложноположительные в диагностическом контексте или побочные эффекты в терапевтическом контексте. Степень специфичности, необходимая для канинизированного антитела против человеческого CTLA-4, может зависеть от намеченного применения антитела, и в любом случае, определяется пригодностью для использования для намеченной цели. Антитело, или связывание соединение, происходящее из антигенсвязывающего участка антитела, из предусмотренного способа, связывается со своим антигеном, или его вариантом или мутеином, с аффинностью, по меньшей мере в два раза большей, предпочтительно, по меньшей мере в десять раз большей, более предпочтительно, по меньшей мере в 20 раз большей, и наиболее предпочтительно, по меньшей мере в 100 раз большей, чем аффинность для любого другого собачьего антигена. Выделенное антитело, которое специфически связывает собачий CTLA-4, однако, может вступать в перекрестную реакцию с другими антигенами, в частности, близко родственными антигенами, такими как кошачий CTLA-4, лошадиный CTLA-4 и/или человеческий CTLA-4.
В рамках изобретения, говорят, что антитело специфически связывается с полипептидом, содержащим данную последовательность (в этом случае собачьим CTLA-4), если оно связывается с полипептидами, содержащим последовательность собачьего CTLA-4, но связывается далеко не так хорошо, если вообще связывается, с другими собачьими белками, лишенными аминокислотной последовательности собачьего CTLA-4. Например, антитело, которое специфически связывается с полипептидом, содержащим собачий CTLA-4, может связываться с меченной FLAG® формой собачьего CTLA-4, но не может специфически связываться с другими меченными FLAG® собачьими белками.
В рамках изобретения, если не указано иное, «фрагмент антитела» или «антигенсвязывающий фрагмент» относится к антигенсвязывающим фрагментам антител, т.е. фрагментам антител. сохраняющим способность специфического связывания с антигеном (например, собачьим CTLA-4), связываемым полноразмерным антителом, например, фрагментам, сохраняющим одну или несколько областей CDR. Примеры антигенсвязывающих фрагментов включают, но без ограничения, фрагменты Fab, Fab', F(ab')2 и Fv; диатела; линейные антитела; одноцепочечные молекулы антител, например, sc-Fv; наноантитела и мультиспецифические антитела, сформированные из фрагментов антител.
Как правило, канинизированное антитело или его антигенсвязывающий фрагмент по изобретению сохраняет по меньшей мере 10% от своего связывания с собачьим CTLA-4 (при сравнении с соответствующим исходным антителом), когда эта активность выражена на молярной основе. Предпочтительно, антитело или антигенсвязывающий фрагмент по изобретению сохраняет по меньшей мере 20%, 50%, 70%, 80%, 90%, 95% или 100%, или более от аффинности связывания собачьего CTLA-4, как у исходного антитела.
Настоящее изобретение относится к антителам, обозначенным как «консервативные варианты» антитела с определенной аминокислотной последовательностью. В рамках изобретения, «консервативные варианты» имеют одну, две, три или более консервативных аминокислотных замен в своей аминокислотной последовательности, относительно канинизированного антитела по изобретению, имеющего определенную аминокислотную последовательность. Настоящее изобретение, кроме того, относится к антителам, обозначенным как «функционально консервативные варианты» канинизированного антитела с определенной аминокислотной последовательностью. В рамках изобретения, «функционально консервативные варианты» имеют одну, две, три или более неконсервативных аминокислотных замен, относительно аминокислотной последовательности этого канинизированного антитела. Термины «консервативный вариант» и «функционально консервативный вариант» использованы только в отношении замен аминокислотных остатков в собачьей рамке считывания соответствующего канинизированного антитела по изобретению, а не в специфических CDR канинизированного антитела. Важно, что «консервативный вариант» и/или «функционально консервативный вариант» по существу не изменяет биологическую активность соответствующего канинизированного антитела по изобретению, содержащего определенную аминокислотную последовательность.
«Выделенное антитело» относится к статусу очистки и в таком контексте означает, что молекула является в основном свободной от других биологических молекул, таких как нуклеиновые кислоты, белки, липиды, углеводы, или другой материал, такой как клеточный дебрис и среда для выращивания. Как правило, термин «выделенное» не предназначен для обозначения полного отсутствия такого материала или отсутствия воды, буферов или солей, если они не присутствуют в количествах, создающих существенные помехи для экспериментального или терапевтического использования связывающего соединения, как описано в настоящем описании.
Вариабельные области каждой пары легкая/тяжелая цепь формируют антигенсвязывающий участок антитела. Таким образом, как правило, интактное антитело имеет два связывающих участка. За исключением бифункциональных или биспецифических антител, два связывающих участка, как правило, являются одинаковыми.
Как правило, вариабельные домены как тяжелых, так и легких цепей, содержат три гипервариабельные области, называемые также определяющими комплементарность областями (CDR), локализованные внутри относительно консервативных каркасных областей (FR). CDR обычно фланкированы каркасными областями, позволяющими их связывание со специфическим эпитопом. Как правило, от N-конца до C-конца, вариабельные домены как легких, так и тяжелых цепей, содержат FR1, CDR1, FR2, CDR2, FR3, CDR3 и FR4. Приписывание аминокислоты каждому домену осуществляют, как правило, в соответствии с определениями из Sequences of Proteins of Immunological Interest, Kabat, et al.; National Institutes of Health, Bethesda, Md., 5th ed., NIH Publ. No. 91-3242 (1991); Kabat, Adv. Prot. Chem. 32:1-75 (1978); Kabat, et al., J. Biol. Chem. 252:6609-6616 (1977); Chothia, et al., J. Mol. Biol. 196:901-917 (1987) или Chothia, et al., Nature 342:878-883 (1989).
В рамках изобретения, термин «гипервариабельная область» относится к аминокислотным остаткам антитела, ответственным за связывание антигена. Гипервариабельная область содержит аминокислотные остатки из «определяющей комплементарность области» или «CDR» (т.е. CDRL1, CDRL2 и CDRL3 в вариабельном домене легкой цепи, и CDRH1, CDRH2 и CDRH3 в вариабельном домене тяжелой цепи). [См. Kabat et al. Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, Md. (1991), где определены области CDR антитела по последовательности; См. также Chothia and Lesk, J. Mol. Biol. 196: 901-917 (1987), где определены области CDR антитела по структуре].
В рамках изобретения, термин «каркасные» или «FR» остатки относится к остаткам вариабельного домена, отличным от остатков гипервариабельной области, определенных в настоящем описании как остатки CDR. Каркас канинизированного антитела представляет часть собачьей рамки считывания. В рамках изобретения, термин «собачье» включает всех домашних собак, Canis lupus familiaris или Canis familiaris, если не указано иное.
В рамках изобретения, термин «кошачье» относится к любому члену семейства Felidae. Домашние кошки, чистопородные и/или нечистопородные кошки-компаньоны, и дикие или бездомные кошки все являются кошачьими.
В рамках изобретения, термин «собачья рамка считывания» относится к аминокислотной последовательности тяжелой цепи и легкой цепи собачьего антитела, отличной от остатков гипервариабельной области, определенных в настоящем описании как остатки CDR. Применительно к канинизированному антителу, в большинстве вариантов осуществления аминокислотные последовательности природных собачьих CDR заменены на соответствующие чужеродные CDR (например, из мышиного антитела) на обеих цепях. Необязательно, тяжелые и/или легкие цепи собачьего антитела могут содержать некоторые чужеродные не относятся к CDR остатки, например, для сохранения конформации чужеродных CDR внутри собачьего антитела и/или для модификации функции Fc, как обсуждают ниже.
Существует четыре известных подтипа тяжелой цепи IgG собачьего IgG, и они обозначены как IgG-A, IgG-B, IgG-C и IgG-D. Два известных подтипа легкой цепи обозначены как лямбда и каппа.
Помимо связывания и активации собачьих иммуноцитов, собачье или канинизированное антитело против CTLA-4 также можно конструировать с наличием двух дополнительных атрибутов:
1. Отсутствие эффекторных функций, таких как антителозависимая цитотоксичность (ADCC) и комплементзависимая цитотоксичность (CDC), и
2. Простота очистки в крупном масштабе с использованием стандартных промышленных технологий, таких как технологии на основе хроматографии с белком A.
Ни один из природных изотипов собачьего IgG не удовлетворяет обоим критериям. Например, IgG-B может быть очищен с использованием белка A, но имеет высокий уровень активности ADCC. С другой стороны, IgG-A слабо связывается с белком A, но имеет нежелательную активность ADCC. Кроме того, ни IgG-C, ни IgG-D не могут быть очищены на колонках с белком A, хотя IgG-D не имеет активности ADCC. (IgG-C имеет значительную активность ADCC). Настоящее изобретение преодолевает эту сложность посредством предоставления мутантных собачьих антител IgG-B, специфических для CTLA-4 [См. U.S. 10106607 B2, полное содержание которого, таким образом, приведено в качестве ссылки]. Эти антитела как лишены эффекторных функций, таких как ADCC, так и могут быть легко очищены с использованием стандартной промышленной хроматографии с белком A.
В рамках изобретения, термин «канинизированное антитело» относится к антителу, содержащему три CDR тяжелой цепи и три CDR легкой цепи из не относящегося к собачьим источника, например, антитела против человеческого CTLA-4, вместе с собачьей рамкой считывания или модифицированной собачьей рамкой считывания. Модифицированная собачья рамка считывания содержит одну или несколько аминокислотных замен. В конкретных вариантах осуществления, модифицированная собачья рамка считывания дополнительно оптимизирует эффективность канинизированного антитела, например, для увеличения его связывания с собачьим CTLA-4 и/или его способности блокировать связывание собачьего CTLA-4 с собачьим CD80 и/или CD86.
«Гомология» относится к сходству последовательности между двумя полинуклеотидными последовательности или между двумя полипептидными последовательностями, когда они оптимально выровнены. Когда положение в обеих из двух сравниваемых последовательностей занято одинаковой мономерной субъединицей основания или аминокислоты, например, если положение в каждой из двух молекул ДНК занято аденином, тогда молекулы являются гомологичными в этом положении. Процент гомологии представляет собой количество гомологичных положений, общих для двух последовательностей, деленное на общее количество сравненных положений, × 100. Например, если 6 из 10 положений в двух последовательностях являются совпадающими или гомологичными, когда последовательности оптимально выровнены, тогда две последовательности являются на 60% гомологичными. Как правило, сравнение проводят, когда две последовательности выровнены для получения максимального процента гомологии.
В рамках изобретения, одна аминокислотная последовательность является на 100% «идентичной» или имеет 100% «идентичность» с второй аминокислотной последовательностью, когда аминокислотные остатки обеих последовательностей являются идентичными. Соответственно, аминокислотная последовательность является на 50% «идентичной» с второй аминокислотной последовательностью, когда 50% аминокислотных остатков двух аминокислотных последовательностей являются идентичными. Сравнение последовательностей осуществляют на протяжении непрерывного блока из аминокислотных остатков, содержащихся в данном белке, например, белке или части полипептида, подвергаемых сравнению. В конкретном варианте осуществления, избранные делеции или вставки, которые могут в ином случае изменять соответствие между двумя аминокислотными последовательностями, принимают во внимание.
«Выделенная молекула нуклеиновой кислоты» обозначает ДНК или РНК из геномного источника, мРНК, кДНК или синтетического источника, или некоторых их комбинаций, которая не является ассоциированной с всем или частью полинуклеотида, в котором выделенный полинуклеотид обнаружен в природе, или является связанной с полинуклеотидом, с которым она не связана в природе. Для целей по настоящему изобретению, следует понимать, что «молекула нуклеиновой кислоты, содержащая» конкретную нуклеотидную последовательность, не включает интактные хромосомы. Выделенные молекулы нуклеиновой кислоты, «содержащие» указанные последовательности нуклеиновой кислоты, могут включать, в дополнение к указанным последовательностям, кодирующие последовательности для вплоть до десяти или даже вплоть до двадцати или более других белков, или их частей или фрагментов, или могут включать функционально связанные регуляторные последовательности, контролирующие экспрессию кодирующей области перечисленных последовательностей нуклеиновой кислоты, и/или могут включать векторные последовательности.
Фраза «контрольные последовательности» относится к последовательностям ДНК, необходимым для экспрессии функционально связанной кодирующей последовательности в конкретном организме-хозяине. Контрольные последовательности, подходящие для прокариот, например, включают промотор, необязательно, последовательность оператора и участок связывания рибосомы. Известно, что эукариотические клетки используют промоторы, сигналы полиаденилирования и энхансеры.
Нуклеиновая кислота является «функционально связанной», когда она помещена в функциональную взаимосвязь с другой последовательностью нуклеиновой кислоты. Например, ДНК для предпоследовательности или секреторного лидера является функционально связанной с ДНК для полипептида, если она экспрессируется в форме пребелка, который участвует в секреции полипептида; промотор или энхансер является функционально связанным с кодирующей последовательностью если он влияет на транскрипцию последовательности; или участок связывания рибосомы является функционально связанным с кодирующей последовательностью, если он расположен таким образом, чтобы облегчать трансляцию. Как правило, «функционально связанный» означает, что связанные последовательности ДНК являются непрерывными, и, в случае секреторного лидера, непрерывными и находящимися в фазе считывания. Однако, энхансеры не обязательно должны являться непрерывными. Связывание осуществляют посредством лигирования в удобных участках рестрикции. Если таких участков не существует, синтетические олигонуклеотидные адаптеры или линкеры используют в соответствии с общепринятой практикой. Следует также ясно понимать, что когда последовательность нуклеиновой кислоты представлена в настоящем описании, она может включать стоп-кодон. Однако, поскольку стоп-кодоны являются взаимозаменяемыми, включение специфического стоп-кодона в последовательность не следует рассматривать как необходимую часть этой последовательности.
В рамках изобретения, выражения «клетка», «линия клеток» и «культура клеток» использованы взаимозаменяемо, и все такие обозначения включают потомство. Таким образом, слова «трансформанты» и «трансформированные клетки» включают первичные клетки субъекта и культуры, происходящие из них, независимо от количества переносов. Понятно также, что не все потомство будет иметь точно идентичное содержание ДНК, из-за преднамеренных или самопроизвольных мутаций. Включено мутантное потомство, имеющее такую же функцию или биологическую активность, как та, по которой скринировали исходно трансформированную клетку. Когда предусмотрены отличные определения, это ясно из контекста.
В рамках изобретения, «зародышевая последовательность» относится к последовательностям из не перегруппированных последовательностей ДНК иммуноглобулинов. Можно использовать любой источник не перегруппированных последовательностей иммуноглобулинов. Человеческие зародышевые последовательности можно получать, например, из зародышевых баз данных JOINSOLVER® на веб-сайте Национального института артрита и скелетно-мышечных и кожных заболеваний Национального института здравоохранения США. Мышиные зародышевые последовательности можно получать, например, как описано в Giudicelli et al. [Nucleic Acids Res. 33:D256-D261 (2005)].
Свойства иллюстративных канинизированных антител против человеческого CTLA-4
Настоящее изобретение относится к выделенным канинизированным антителам против человеческого CTLA-4 и способам применения антител или их антигенсвязывающих фрагментов в лечении заболевания, например, лечении злокачественной опухоли у собачьих. Примеры канинизированных антител против человеческого CTLA-4, которые связывают собачий CTLA-4, включают, но без ограничения: антитела, содержащие тяжелые цепи собачьих IgG-A, IgG-B, IgG-C и IgG-D и/или собачьи легкие цепи каппа вместе с CDR против человеческого CTLA-4. Соответственно, настоящее изобретение относится к выделенным канинизированным антителам против человеческого CTLA-4 или их антигенсвязывающим фрагментам, которые связываются с собачьим CTLA-4 и блокируют связывание собачьего CTLA-4 с собачьим CD80 и/или CD86.
«Консервативно модифицированные варианты» или «консервативная замена» относится к заменам аминокислот в белке на другие аминокислоты, имеющие сходные характеристики (например, заряд, размер боковой цепи, гидрофобность/гидрофильность, конформацию и жесткость остова, и т.д.), так что изменения часто могут быть выполнены без изменения биологической активности белка. Специалисту в данной области известно, что, как правило, одиночные аминокислотные замены в не являющихся необходимыми областях полипептида существенно не изменяют биологическую активность [См., например, Watson et al., Molecular Biology of the Gene, The Benjamin/Cummings Pub. Co., p. 224 (4th Ed.; 1987)]. Кроме того, замены структурно или функционально сходных аминокислот с меньшей вероятностью нарушают биологическую активность. Различные варианты осуществления антитела или антигенсвязывающего фрагмента по настоящему изобретению содержат полипептидные цепи с последовательностями, описанными в настоящем описании, например, SEQ ID NO:34, 36, 38, 40, 42, 44, 60, 62, 64 или 66, или полипептидные цепи, содержащие вплоть до 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, 15, 20 или более консервативных аминокислотных замен в областях, отличных от CDR. Иллюстративные консервативные замены приведены в таблице A.
ТАБЛИЦА A
Иллюстративные консервативные аминокислотные замены
Функционально-консервативные варианты антител по изобретению также предусмотрены по настоящему изобретению. «Функционально-консервативные варианты», в рамках изобретения, относятся к антителам или фрагментам, в которых один или несколько аминокислотных остатков заменены без изменения желательного свойства, такого как аффинность и/или специфичность для антигена. Такие варианты включают, но без ограничения, замену аминокислоты на аминокислоту, имеющую сходные свойства, такую как консервативные аминокислотные замены из таблицы A.
Нуклеиновые кислоты
Настоящее изобретение, кроме того, относится к нуклеиновым кислотам, кодирующим иммуноглобулиновые цепи канинизированных антител против человеческого CTLA-4 и их антигенсвязывающие фрагменты, описанные в настоящем описании. Например, настоящее изобретение включает все из новых нуклеиновых кислот, перечисленных в таблицах ниже.
Также в настоящее изобретение включены нуклеиновые кислоты, кодирующие полипептиды иммуноглобулинов, содержащие аминокислотные последовательности из собачьей рамки считывания, которые являются по меньшей мере приблизительно на 70% идентичными, предпочтительно, по меньшей мере приблизительно на 80% идентичными, более предпочтительно, по меньшей мере приблизительно на 90% идентичными и наиболее предпочтительно, по меньшей мере приблизительно на 95% идентичными (например, на 95%, 96%, 97%, 98%, 99%, 100%) с аминокислотными последовательностями из собачьей рамки считывания антител, представленных в настоящем описании, когда сравнение проводят посредством алгоритма BLAST, где параметры алгоритма выбирают для получения наибольшего совпадения между соответствующими последовательностями на протяжении полной длины соответствующих эталонных последовательностей. Кроме того, настоящее изобретение относится к нуклеиновым кислотам, которые кодируют собачью рамку считывания полипептидов иммуноглобулинов, содержащую аминокислотные последовательности, которые являются по меньшей мере приблизительно на 70% сходными, предпочтительно, по меньшей мере приблизительно на 80% сходными, более предпочтительно, по меньшей мере приблизительно на 90% сходными и наиболее предпочтительно, по меньшей мере приблизительном на 95% сходными (например, на 95%, 96%, 97%, 98%, 99%, 100%) с любой из эталонных аминокислотных последовательностей, когда сравнение проводят посредством алгоритма BLAST, где параметры алгоритма выбирают для получения наибольшего совпадения между соответствующими последовательностями на протяжении полной длины соответствующих эталонных последовательностей, они также включены в настоящее изобретение.
Идентичность последовательности относится к степени, в которой аминокислоты из двух полипептидов являются одинаковыми в эквивалентных положениях, когда две последовательности оптимально выровнены. Сходство последовательности включает идентичные остатки и неидентичные, биохимически родственные аминокислоты. Биохимически родственные аминокислоты, которые разделяют сходные свойства и могут являться взаимозаменяемыми, обсуждают выше.
Следующие ссылки относятся к алгоритмам BLAST, часто используемым для анализа последовательностей: BLAST ALGORITHMS: Altschul, S.F., et al., J. Mol. Biol. 215:403-410 (1990); Gish, W., et al., Nature Genet. 3:266-272 (1993); Madden, T.L., et al., Meth. Enzymol. 266:131-141(1996); Altschul, S.F., et al., Nucleic Acids Res. 25:3389-3402 (1997); Zhang, J., et al., Genome Res. 7:649-656 (1997); Wootton, J.C., et al., Comput. Chem. 17:149-163 (1993); Hancock, J.M. et al., Comput. Appl. Biosci. 10:67-70 (1994); ALIGNMENT SCORING SYSTEMS: Dayhoff, M.O., et al., «A model of evolutionary change in proteins.» in Atlas of Protein Sequence and Structure, vol. 5, suppl. 3. M.O. Dayhoff (ed.), pp. 345-352, (1978); Natl. Biomed. Res. Found., Washington, DC; Schwartz, R.M., et al., «Matrices for detecting distant relationships.» in Atlas of Protein Sequence and Structure, vol. 5, suppl. 3.» (1978), M.O. Dayhoff (ed.), pp. 353-358 (1978), Natl. Biomed. Res. Found., Washington, DC; Altschul, S.F., J. Mol. Biol. 219:555-565 (1991); States, D.J., et al., Methods 3:66-70(1991); Henikoff, S., et al., Proc. Natl. Acad. Sci. USA 89:10915-10919 (1992); Altschul, S.F., et al., J. Mol. Evol. 36:290-300 (1993); ALIGNMENT STATISTICS: Karlin, S., et al., Proc. Natl. Acad. Sci. USA 87:2264-2268 (1990); Karlin, S., et al., Proc. Natl. Acad. Sci. USA 90:5873-5877 (1993); Dembo, A., et al., Ann. Prob. 22:2022-2039 (1994); и Altschul, S.F. «Evaluating the statistical significance of multiple distinct local alignments.» in Theoretical and Computational Methods in Genome Research (S. Suhai, ed.), pp. 1-14, Plenum, New York (1997).
Настоящее изобретение также относится к экспрессирующим векторам, содержащим выделенные нуклеиновые кислоты по изобретению, где нуклеиновая кислота является функционально связанной с контрольными последовательностями, узнаваемыми клеткой-хозяином, когда клетку-хозяина трансфицируют вектором. Также настоящее изобретение относится к клеткам-хозяевам, содержащим экспрессирующий вектор по настоящему изобретению, и к способам получения антитела или его антигенсвязывающего фрагмента, описанного в настоящем описании, включающим культивирование клетки-хозяина, несущей экспрессирующий вектор, кодирующий антитело или антигенсвязывающий фрагмент, в культуральной среде, и выделение антигена или его антигенсвязывающего фрагмента из клетки-хозяина или культуральной среды.
Связывание и аффинность связывания эпитопа
Кроме того, настоящее изобретение относится к антителам или их антигенсвязывающиим фрагментам, которые связываются с таким же эпитопом на собачьем CTLA-4, как канинизированное антитело против человеческого CTLA-4, содержащее аминокислотную последовательность SEQ ID NO:36 и/или SEQ ID NO:46. Канинизированные антитела против человеческого CTLA-4 или их антигенсвязывающие фрагменты являются способными ингибировать связывание собачьего CTLA-4 с собачьим CD80 и/или CD86.
Канинизированное антитело против человеческого CTLA-4 можно получать рекомбинантным способом, как описано ниже в примерах. Линии клеток млекопитающих, доступные в качестве хозяев для экспрессии антител или фрагментов, описанных в настоящем описании, хорошо известны в данной области и включают множество иммортализованных линий клеток, доступных из Американской коллекции типовых культур (ATCC). Они включают, среди прочего, клетки яичников китайского хомяка (CHO), NSO, клетки SP2, клетки HeLa, клетки почки детеныша хомяка (BHK), клетки почки обезьяны (COS), клетки человеческой печеночно-клеточной карциномы (например, Hep G2), клетки A549, клетки 3T3, клетки HEK-293 и ряд других линий клеток. Клетки-хозяева млекопитающих включают клетки человека, мыши, крысы, собаки, обезьяны, свиньи, козы, быка, лошади и хомяка. Особенно предпочтительные линии клеток выбирают посредством определения того, какие линии клеток имеют высокие уровни экспрессии. Другие линии клеток, которые можно использовать, представляют собой линии клеток насекомых, такие как клетки Sf9, клетки амфибий, бактериальные клетки, клетки растений и клетки грибов. Когда рекомбинантные экспрессирующие векторы, кодирующие тяжелую цепь, или ее антигенсвязывающую часть или фрагмент, легкую цепь и/или ее антигенсвязывающий фрагмент, вводят в клетки-хозяева млекопитающих, антитела продуцируют посредством культивирования клеток-хозяев в течение периода времени, достаточного, чтобы позволять экспрессию антитела в клетках-хозяевах или, более предпочтительно, секрецию антитела в культуральную среду, в которой выращивают клетки-хозяева.
Антитела можно выделять из культуральной среды с использованием стандартных способов очистки белка. Кроме того, экспрессию антител по изобретению (или других групп из них) из линий клеток для продукции можно усиливать с использованием ряда известных способов. Например, система экспрессии генов с использованием глутаминсинтетазы (система GS) является общепринятым способом усиления экспрессии в определенных условиях. Систему GS обсуждают, полностью или частично, в связи с Европейскими патентами No. 0 216 846, 0 256 055 и 0 323 997, и Европейской Патентной заявкой No. 89303964.4.
Как правило, гликопротеины, продуцированные в конкретной линии клеток или трансгенном животном, имеют паттерн гликозилирования, который является характерным для гликопротеинов, продуцированных в линии клеток или трансгенном животном. Таким образом, конкретный паттерн гликозилирования антитела может зависеть от конкретной линии клеток или трансгенного животного, используемых для продукции антитела. Однако, все антитела, кодированные молекулами нуклеиновой кислоты, представленными в настоящем описании, или содержащие аминокислотные последовательности, представленные в настоящем описании, составляют настоящее изобретение, независимо от паттерна гликозилирования, который антитела могут иметь. Сходным образом, в конкретных вариантах осуществления, антитела с паттерном гликозилирования, содержащим только нефукозилированные N-гликаны, могут обеспечивать преимущества, поскольку показано, что эти антитела, как правило, имеют более сильную эффективность, чем их фукозилированные эквивалентны как in vitro, так и in vivo [См., например, Shinkawa et al., J. Biol. Chem. 278: 3466-3473 (2003); Патенты США No. 6946292 и 7214775].
Настоящее изобретение, кроме того, включает фрагменты антител из канинизированных антител против человеческого CTLA-4, описанных в настоящем описании. Фрагменты антител включают фрагменты F(ab)2, которые можно получать посредством ферментного расщепления IgG посредством, например, пепсина. Фрагменты Fab можно получать, посредством, например, восстановления F(ab)2 с использованием дитиотреитола или меркаптоэтиламина. Фрагмент Fab представляет собой цепь VL-CL, присоединенную к цепи VH-CH1 посредством дисульфидного мостика. Фрагмент F(ab)2 представляет собой два фрагмента Fab, которые, в свою очередь, присоединены посредством двух дисульфидных мостиков. Часть Fab молекулы F(ab)2 включает части области Fc, между которыми локализованы дисульфидные мостики. Фрагмент FV представляет собой область VL или VH.
В одном варианте осуществления, антитело или антигенсвязывающий фрагмент содержит константную область тяжелой цепи, например, собачью константную область, такую как константная область тяжелой цепи собачьих IgG-A, IgG-B, IgG-C и IgG D или ее вариант. В другом варианте осуществления, антитело или антигенсвязывающий фрагмент содержит константную область легкой цепи, например, константную область собачьей легкой цепи, такую как область собачьей легкой цепи лямбда или каппа или ее вариант. В качестве примера, а не ограничения, константная область собачьей тяжелой цепи может происходить из IgG-B [например, модифицированного IgG-B, см. U.S. 10106607 B2, полное содержание которой, таким образом, приведено в качестве ссылки], и константная область собачьей легкой цепи может происходить из каппа.
Конструирование антител
Канинизированные антитела против человеческого CTLA-4 по настоящему изобретению сконструированы для включения модификаций в собачью рамку считывания, включая каркасные остатки внутри вариабельных доменов исходного (т.е., собачьего) моноклонального антитела, например, для улучшения свойств антитела.
Экспериментальные и диагностические применения
Канинизированные антитела против человеческого CTLA-4 или их антигенсвязывающие фрагменты по настоящему изобретению могут также являться полезными в диагностических анализах собачьего белка CTLA-4, например, детекции его экспрессии в специфических клетках опухолей, тканях или сыворотке. Такие диагностические способы могут являться полезными при диагностике различных заболеваний, в частности, конкретных злокачественных опухолей, у собачьих.
Например, такой способ включает следующие стадии:
(a) покрытия субстрата (например, поверхности лунки микропланшета для титрования, например, пластикового планшета) канинизированным антителом против человеческого CTLA-4 или его антигенсвязывающим фрагментом;
(b) нанесения образца, подлежащего тестированию по присутствию собачьего CTLA-4, на субстрат;
(c) промывки планшета, так чтобы удалить несвязавшийся материал в образце;
(d) применения меченных поддающейся детекции меткой антител (например, связанных с ферментом антител), которые также являются специфическими для антигена CTLA-4;
(e) промывки субстрата, так чтобы удалить несвязавшиеся, меченые антитела;
(f) если меченые антитела являются связанными с ферментом, применения химического вещества, которое посредством фермента переводят в флуоресцентный сигнал; и
(g) детекции присутствия меченого антитела.
В следующем варианте осуществления, меченое антитело является меченным пероксидазой, которая вступает в реакцию с ABTS [например, 2,2'-азино-бис(3-этилбензтиазолин-6-сульфоновой кислотой)] или 3,3’,5,5’-тетраметилбензидином с получением изменения цвета, которое поддается детекции. Альтернативно, меченое антитело является меченным поддающимся детекции радиоактивным изотопом (например, 3H), который можно детектировать посредством сцинтилляционного счетчика в присутствии сцинтиллятора. Канинизированные антитела против человеческого CTLA-4 по изобретению можно использовать в способе Вестерн-блоттинга или иммуноблоттинга белков.
Такой способ составляет часть настоящего изобретения и включает, например:
(i) приведение мембраны или другого твердого субстрата, подлежащего тестированию по присутствию связанного собачьего CTLA-4 или его фрагмента, в контакт с канинизированным антителом против человеческого CTLA-4 или его антигенсвязывающим фрагментом по настоящему изобретению. Такая мембрана может принимать форму основанной на нитроцеллюлозе или виниле [например, поливинилиденфториде (PVDF)] мембраны, на которую белки, подлежащие тестированию по присутствию собачьего CTLA-4 в геле для неденатурирующего PAGE (электрофореза в полиакриламидном геле) или в геле для SDS-PAGE (электрофореза в полиакриламидном геле с додецилсульфатом натрия), перенесены (например, после электрофоретического разделения в геле). Перед контактом мембраны с канинизированным антителом против человеческого CTLA-4 или его антигенсвязывающим фрагментом, мембрану, необязательно, блокируют, например, с использованием обезжиренного сухого молока или т.п., так чтобы связать неспецифические участки связывания белка на мембране.
(ii) промывку мембраны один или несколько раз для удаления несвязавшегося канинизированного антитела против человеческого CTLA-4 или его антигенсвязывающего фрагмента и других несвязавшихся веществ; и
(iii) детекцию связанного канинизированного антитела против человеческого CTLA-4 или его антигенсвязывающего фрагмента.
Детекцию связанного антитела или антигенсвязывающего фрагмента можно осуществлять посредством связывания антитела или антигенсвязывающего фрагмента с вторичным антителом (антителом против иммуноглобулина), которое является меченным поддающейся детекции меткой, и затем детекции присутствия вторичного антитела.
Канинизированные антитела против человеческого CTLA-4 и их антигенсвязывающие фрагменты, описанные в настоящем описании, можно также использовать для иммуногистохимии. Такой способ составляет часть настоящего изобретения и включает, например, (1) приведение клетки, подлежащей тестированию по присутствию собачьего CTLA-4, в контакт с канинизированным антителом против человеческого CTLA-4 или его антигенсвязывающим фрагментом по настоящему изобретению; и (2) детекцию антитела или фрагмента на или в клетке.
Если собственно антитело или антигенсвязывающий фрагмент является меченным поддающейся детекции меткой, его можно детектировать напрямую. Альтернативно, антитело или антигенсвязывающий фрагмент может связываться посредством меченного поддающейся детекции меткой вторичного антитела, которое детектируют.
Конкретные канинизированные антитела против человеческого CTLA-4 и их антигенсвязывающие фрагменты, описанные в настоящем описании, также можно использовать для визуализации опухоли in vivo. Такой способ может включать инъекцию меченных радиоактивной меткой канинизированных антител против человеческого CTLA-4 или их антигенсвязывающих фрагментов в организм собачьего, подлежащего тестированию по присутствию опухоли, ассоциированной с экспрессией собачьего CTLA-4, с последующей радионуклидной визуализацией организма пациента для детекции присутствия меченого антитела или антигенсвязывающего фрагмента, например, в локализациях, содержащих высокую концентрацию антитела или антигенсвязывающего фрагмента, которые являются связанными с опухолью.
Способы визуализации включают визуализацию посредством SPECT (однофотонной эмиссионной компьютерной томографии) или визуализацию посредством PET (позитронной эмиссионной томографии). Метки включают, например, иод-123 (123I) и технеций-99m (99mTc), например, в сочетании с визуализацией посредством SPECT, или 11C, 13N, 15O или 18F, например, в сочетании с визуализацией посредством PET, или индий-111 [См., например, Gordon et al., International Rev. Neurobiol. 67:385-440 (2005)].
Фармацевтические композиции и введение
Для получения фармацевтических или стерильных композиций, канинизированное антитело против человеческого CTLA-4 или его антигенсвязывающий фрагмент смешивают с фармацевтически приемлемым носителем или наполнителем. [См., например, Remington's Pharmaceutical Sciences and U.S. Pharmacopeia: National Formulary, Mack Publishing Company, Easton, PA (1984)].
Составы терапевтических и диагностических средств можно получать посредством смешивания с приемлемыми носителями, наполнителями или стабилизаторами в форме, например, лиофилизированных порошков, взвесей, водных растворов или суспензий [См., например, Hardman, et al. (2001) Goodman and Gilman’s The Pharmacological Basis of Therapeutics, McGraw-Hill, New York, NY; Gennaro (2000) Remington: The Science and Practice of Pharmacy, Lippincott, Williams, and Wilkins, New York, NY; Avis, et al. (eds.) (1993) Pharmaceutical Dosage Forms: Parenteral Medications, Marcel Dekker, NY; Lieberman, et al. (eds.) (1990) Pharmaceutical Dosage Forms: Tablets, Marcel Dekker, NY; Lieberman, et al. (eds.) (1990) Pharmaceutical Dosage Forms: Disperse Systems, Marcel Dekker, NY; Weiner and Kotkoskie (2000) Excipient Toxicity and Safety, Marcel Dekker, Inc., New York, NY]. В одном варианте осуществления, антитела против CTLA-4 по настоящему изобретению разводят до подходящей концентрации в растворе ацетата натрия, pH 5-6, и NaCl или сахарозу добавляют для тоничности. Дополнительные средства, такие как полисорбат 20 или полисорбат 80, можно добавлять для улучшения стабильности.
Токсичность и терапевтическую эффективность композиций антител, вводимых отдельно или в комбинации с другим средством, можно определять стандартными фармацевтическими способами, в культурах клеток или у экспериментальных животных, например, для определения LD50 (дозы, летальной для 50% популяции) и ED50 (дозы, терапевтически эффективной в 50% популяции). Соотношение доз между токсическими и терапевтическими эффектами представляет собой терапевтический индекс (LD50/ ED50). В конкретных аспектах, антитела, имеющие высокие терапевтические индексы, являются желательными. Данные, полученные из этих анализов культур клеток и исследований на животных, можно использовать для составления диапазона дозирования для использования у собачьих. Доза таких соединений, предпочтительно, лежит в диапазоне циркулирующих концентраций, включающем ED50 при небольшой токсичности или в отсутствие токсичности. Дозу можно менять в пределах этого диапазона, в зависимости от используемых лекарственной формы и способа введения.
Способ введения можно менять. Пригодные способы введения включают пероральный, ректальный, трансмукозальный, желудочный, парентеральный; внутримышечный, подкожный, внутрикожный, интрамедуллярный, интратекальный, прямой интравентрикулярный, внутривенный, внутрибрюшинный, интраназальный, внутриглазной, ингаляционный, инсуффляционный, местный, кожный, чрескожный или внутриартериальный.
В конкретных вариантах осуществления, канинизированное антитело против человеческого CTLA-4 или его антигенсвязывающий фрагмент можно вводить инвазивным способом, например, посредством инъекции. В следующих вариантах осуществления изобретения, канинизированное антитело против человеческого CTLA-4 или его антигенсвязывающий фрагмент, или его фармацевтическую композицию вводят внутривенно, подкожно, внутримышечно, внутриартериально, внутрь опухоли, или посредством ингаляции, аэрозольной доставки. Введение неинвазивными способами (например, перорально; например, в пилюле, капсуле или таблетке) также включено в объем настоящего изобретения.
Композиции можно вводить с использованием медицинских устройств, известных в данной области. Например, фармацевтическую композицию по изобретению можно вводить посредством инъекции с использованием подкожной иглы, включая, например, предварительно заполненный шприц или автоинжектор. Фармацевтические композиции, описанные в настоящем описании, можно также вводить с использованием безыгольного устройства для подкожных инъекций; такого как устройства, описанные в Патентах США No. 6620135; 6096002; 5399163; 5383851; 5312335; 5064413; 4941880; 4790824 или 4596556.
Фармацевтические композиции, описанные в настоящем описании, можно также вводить посредством инфузии. Примеры хорошо известных форм имплантатов и модулей для введения фармацевтических композиций включают: Патент США No. 4487603, в котором описан имплантируемый микроинфузионный насос для дозирования лекарственного средства с контролируемой скоростью; Патент США No. 4447233, в котором описан инфузионный насос для доставки лекарственного средства с точной скоростью инфузии; Патент США No. 4447224, в котором описан имплантируемый инфузионный аппарат с переменным потоком для непрерывной доставки лекарственного средства; Патент США. No. 4439196, в котором описана осмотическая система для доставки лекарственного средства, имеющая многокамерные отсеки. Многие другие такие имплантаты, системы доставки и модули хорошо известны специалисту в данной области.
Альтернативно, можно вводить канинизированное антитело против человеческого CTLA-4 местным, а не системным способом, например, посредством инъекции антитела непосредственно в пораженный артритом сустав или очаг индуцированного патогеном повреждения, характеризующиеся иммунопатологией, часто в составе-депо или составе с замедленным высвобождением. Кроме того, можно вводить канинизированное антитело против человеческого CTLA-4 в системе для направленной доставки лекарственного средства, например, в липосоме, покрытой тканеспецифическим антителом, нацеленным, например, на пораженный артритом сустав или очаг индуцированного патогеном повреждения, характеризующиеся иммунопатологией. Липосомы могут быть нацелены на пораженную ткань и избирательно захватываться ею.
Режим введения зависит от нескольких факторов, включая скорость оборота терапевтического антитела в сыворотке или ткани, уровень симптомов, иммуногенность терапевтического антитела и доступность клеток-мишеней в биологическом матриксе. Предпочтительно, режим введения обеспечивает доставку достаточного количества терапевтического антитела для эффекта улучшения целевого состояния заболевания, в то же время одновременно минимизируя нежелательные побочные эффекты. Следовательно, доставляемое количество биологического вещества частично зависит от конкретного терапевтического антитела и тяжести состояния, подвергаемого лечению. Доступно руководство по выбору подходящих доз терапевтических антител [См., например, Wawrzynczak Antibody Therapy, Bios Scientific Pub. Ltd, Oxfordshire, UK (1996); Kresina (ed.) Monoclonal Antibodies, Cytokines and Arthritis, Marcel Dekker, New York, NY (1991); Bach (ed.) Monoclonal Antibodies and Peptide Therapy in Autoimmune Diseases, Marcel Dekker, New York, NY (1993); Baert, et al. New Engl. J. Med. 348:601-608 (2003); Milgrom et al. New Engl. J. Med. 341:1966-1973 (1999); Slamon et al. New Engl. J. Med. 344:783-792 (2001); Beniaminovitz et al. New Engl. J. Med. 342:613-619 (2000); Ghosh et al. New Engl. J. Med. 348:24-32 (2003); Lipsky et al. New Engl. J. Med. 343:1594-1602 (2000)].
Определение подходящей дозы осуществляет ветеринар, например, с использованием параметров или факторов, как известно или как подозревают в данной области, влияющих на лечение. Как правило, дозу начинают с количества, несколько меньшего, чем оптимальная доза, и затем повышают с небольшими приращениями, пока не будет достигнут желательный или оптимальный эффект, относительно любых отрицательных побочных эффектов. Важные диагностические показатели включают показатели симптомов, например, воспаления или уровня продуцированных воспалительных цитокинов.
Антитела или их антигенсвязывающие фрагменты, описанные в настоящем описании, можно предоставлять посредством непрерывной инфузии, или посредством доз, вводимых, например, ежесуточно, 1-7 раз в неделю, раз в неделю, раз в две недели, раз в месяц, раз в два месяца, раз в четыре месяца, раз в полгода, раз в год и т.д. Дозы можно предоставлять, например, внутривенно, подкожно, местно, перорально, интраназально, ректально, внутримышечно, интрацеребрально, интраспинально или посредством ингаляции. Общая недельная доза обычно составляет по меньшей мере 0,05 мкг/кг массы тела, более обычно, по меньшей мере 0,2 мкг/кг, 0,5 мкг/кг, 1 мкг/кг, 10 мкг/кг, 100 мкг/кг, 0,25 мг/кг, 1,0 мг/кг, 2,0 мг/кг, 5,0 мг/мл, 10 мг/кг, 25 мг/кг, 50 мг/кг или более [См., например, Yang, et al. New Engl. J. Med. 349:427-434 (2003); Herold, et al. New Engl. J. Med. 346:1692-1698 (2002); Liu, et al. J. Neurol. Neurosurg. Psych. 67:451-456 (1999); Portielji, et al. Cancer Immunol. Immunother. 52:133-144 (2003)]. Дозы можно также предоставлять для достижения предопределенной целевой концентрации канинизированного антитела против человеческого CTLA-4 в сыворотке крови субъекта, такой как 0,1, 0,3, 1, 3, 10, 30, 100, 300 мкг/мл или более. В других вариантах осуществления, канинизированное антитело против человеческого CTLA-4 по настоящему изобретению вводят подкожно или внутривенно, на основе введения раз в неделю, раз в две недели, «каждые 4 недели», раз в месяц, раз в два месяца или раз в четыре месяца при 10, 20, 50, 80, 100, 200, 500, 1000 или 2500 мг/субъекта.
В рамках изобретения, «ингибировать» или «лечить», или «лечение» включают отсрочку развития симптомов, ассоциированных с нарушением, и/или уменьшение тяжести симптомов такого нарушения. Термины, кроме того, включают ослабление существующих неконтролируемых или нежелательных симптомов, предотвращение дополнительных симптомов, и ослабление или предотвращение причин, лежащих в основе таких симптомов. Таким образом, термины означают, что обеспечивающий преимущества результат получен у субъекта-позвоночного с нарушением, заболеванием или симптомом, или с потенциалом для развития такого нарушения, заболевания или симптома.
В рамках изобретения, термины «терапевтически эффективное количество», «терапевтически эффективная доза» и «эффективное количество» относятся к количеству канинизированного антитела против человеческого CTLA-4 или его антигенсвязывающего фрагмента по настоящему изобретению, которые при введении отдельно или в комбинации с дополнительным лекарственным средством в клетку, ткань или субъекту, является эффективным для вызова поддающегося измерению улучшения по отношению к одному или нескольким симптомам заболевания или состояния, или прогрессированию такого заболевания или состояния. Терапевтически эффективная доза, кроме того, относится к количеству связывающего соединения, достаточному для получения в результате по меньшей мере частичного ослабления симптомов, например, лечения, заживления, предотвращения или облегчения соответствующего медицинского состояния, или увеличения частоты случаев лечения, заживления, предотвращения или облегчения таких состояний. Применительно к индивидуальному активному ингредиенту, вводимому отдельно, терапевтически эффективная доза относится к этому ингредиенту отдельно. Применительно к комбинации, терапевтически эффективная доза относится к комбинированным количествам активных ингредиентов, которые приводят в результате к терапевтическому эффекту, независимо от того, введены ли они в комбинации, серийно или одновременно. Эффективное количество терапевтического средства может приводить в результате к улучшению диагностического показателя или параметра по меньшей мере на 10%; обычно, по меньшей мере на 20%; предпочтительно, по меньшей мере приблизительно на 30%; более предпочтительно, по меньшей мере на 40%, и наиболее предпочтительно, по меньшей мере на 50%. Эффективное количество может также приводить в результате к улучшению субъективного показателя в тех случаях, когда субъективные показатели используются для оценки тяжести заболевания.
Другие виды комбинированной терапии
Как описано ранее, канинизированное антитело против человеческого CTLA-4 или его антигенсвязывающий фрагмент можно вводить совместно с одним или несколькими другими лекарственными средствами (такими как химиотерапевтическое средство). Антитело можно связывать со средством (в форме иммунокомплекса) или можно вводить отдельно от средства. В последнем случае (отдельное введение), антитело можно вводить до, после или одновременно со средством, или можно вводить совместно с другими известными видами терапии.
Наборы
Кроме того, настоящее изобретение относится к наборам, содержащим один или несколько компонентов, которые включают, но без ограничения, антитело или антигенсвязывающий фрагмент, как обсуждают в настоящем описании, специфически связывающие CTLA-4 (например, канинизированное антитело против человеческого CTLA-4 или его антигенсвязывающий фрагмент по настоящему изобретению), в сочетании с одним или несколькими дополнительными компонентами, включая, но без ограничения, фармацевтически приемлемый носитель и/или химиотерапевтическое средство, как обсуждают в настоящем описании. Связывающую композицию и/или химиотерапевтическое средство можно составлять в форме чистой композиции или в комбинации с фармацевтически приемлемым носителем, в фармацевтической композиции.
В одном варианте осуществления, набор включает связывающую композицию по изобретению, например, канинизированное антитело против человеческого CTLA-4, содержащее аминокислотную последовательность SEQ ID NO:36 и SEQ ID NO:46, или его фармацевтическую композицию в одном контейнере (например, в стерильном стеклянном или пластиковом флаконе), и химиотерапевтическое средство и/или его фармацевтическую композицию в другом контейнере (например, в стерильном стеклянном или пластиковом флаконе).
В другом варианте осуществления, набор содержит комбинацию по изобретению, включающую связывающий компонент композиции (например, канинизированное антитело против человеческого CTLA-4, содержащее аминокислотную последовательность SEQ ID NO:36 и SEQ ID NO:46), вместе с фармацевтически приемлемым носителем, необязательно, в комбинации с одним или несколькими компонентами лекарственного средства, составленными совместно, необязательно, в фармацевтической композиции, в одном, общем контейнере.
Если набор включает фармацевтическую композицию для парентерального введения субъекту, набор может включать устройство для проведения такого введения. Например, набор может включать одну или несколько игл для подкожных инъекций или другие инъекционные устройства, как обсуждают выше. Набор может также включать вкладыш в упаковку, включающий информацию, касающуюся фармацевтических композиций и лекарственных форм в наборе. Как правило, такая информация помогает владельцам домашних животных и ветеринарам в использовании вложенных фармацевтических композиций и лекарственных форм эффективно и безопасно. Например, следующая информация, касающаяся комбинации по изобретению, может быть представлена во вкладыше: фармакокинетика, фармакодинамика, данные клинических исследований, параметры эффективности, показания и применение, противопоказания, предупреждения, меры предосторожности, неблагоприятные реакции, сведения о передозировке, правильной дозировке и введении, сведения о поставке, надлежащие условия хранения, ссылки, информация о производителе/поставщике и патентная информация.
В целях удобства, антитело или специфическое связывающее вещество, описанное в настоящем описании, может быть представлено в наборе, т.е., упакованной комбинации реагентов в предопределенных количествах с инструкциями для проведения диагностического или детектирующего анализа. Когда антитело является меченным ферментом, набор может включать субстраты и кофакторы, необходимые для фермента (например, предшественник субстрата, который обеспечивает поддающейся детекции хромофор или флуорофор). Кроме того, можно включать другие добавки, такие как стабилизаторы, буферы (например, блокирующий буфер или буфер для лизиса) и т.п. Относительные количества различных реагентов можно широко менять для обеспечения концентраций реагентов в растворе, которые существенно оптимизируют чувствительность анализа. В частности, реагенты могут быть представлены в виде сухих порошков, обычно лиофилизированных, включая наполнители, которые при растворении обеспечивают раствор реагента, имеющий подходящую концентрацию.
ПРИМЕРЫ
ПРИМЕР 1
КОНСТРУИРОВАНИЕ ХИМЕРНЫХ АНТИТЕЛ ПРОТИВ CTLA-4
Сочли возможным, что моноклональное антитело из предшествующего уровня техники, образованное против человеческого CTLA-4, которое, как обнаружено, как связывает человеческий CTLA-4, так и блокирует связывание человеческого CTLA-4 с человеческим CD86, может также связывать собачий CTLA-4 и предположительно, блокирует связывание собачьего CTLA-4 с собачьим CD86. Для тестирования этой возможности, известную нуклеотидную последовательность, соответствующую вариабельной области тяжелой цепи моноклонального антитела против человеческого CTLA-4, 3B10 (как описано в WO2012120125), сливали с нуклеотидной последовательностью модифицированной собачьей константной тяжелой цепи (CH1-Шарнир-CH2-3) для получения нуклеотидной последовательности химерной мышиной-собачьей тяжелой цепи, обозначенной как SEQ ID NO:1. Вторую известную нуклеотидную последовательность, кодирующую аминокислотную последовательность, соответствующую вариабельной области легкой цепи моноклонального антитела против человеческого CTLA-4, сливали с нуклеотидной последовательностью собачьего константного домена легкой цепи каппа для получения нуклеотидной последовательности химерной мышиной-собачьей легкой цепи, обозначенной как SEQ ID NO:3. Белок, кодированный нуклеотидной последовательностью химерной мышиной-собачьей тяжелой цепи, содержит аминокислотную последовательность SEQ ID NO:2, и белок, кодированный нуклеотидной последовательностью химерной мышиной-собачьей легкой цепи, содержит аминокислотную последовательность SEQ ID NO:4. Химерные человеческие-собачьи тяжелую и легкую цепи клонировали в отдельные экспрессирующие плазмиды с использованием стандартных способов молекулярной биологии. Плазмиды, содержащие гены тяжелой и легкой цепи, трансфицировали в клетки HEK 293, и экспрессированное антитело очищали из клеточного супернатанта HEK 293 с использованием белка A.
Подобным образом, химерное антитело 8H5, содержащее вариабельные домены, ранее описанные в WO2012120125, также конструировали, как проиллюстрировано посредством антитела, сформированного посредством комбинирования тяжелых и легких цепей с последовательностями ДНК и аминокислотными последовательностями, перечисленными как SEQ ID NO:5-8, соответственно. Кроме того, химерные антитела 411, 418 и 611, содержащие вариабельные домены, описанные в WO2000037504, конструировали, как проиллюстрировано посредством антитела, сформированного посредством комбинирования тяжелых и легких цепей с последовательностями нуклеиновой кислоты и аминокислотными последовательностями, перечисленными как SEQ ID NO:9-20, соответственно. Химерные антитела 10D1 и 1E2, содержащие вариабельные домены, описанные в U.S. 8017114 B2, также конструировали, как проиллюстрировано посредством антитела, сформированного посредством комбинирования тяжелых и легких цепей с нуклеотидными и аминокислотными последовательностями, перечисленными как SEQ ID NO:21-28, соответственно. Кроме того, химерное антитело 3B3, содержащее вариабельные домены, описанные как в WO2010097597, конструировали, как проиллюстрировано посредством антитела, сформированного посредством комбинирования тяжелых и легких цепей с нуклеотидными и аминокислотными последовательностями, перечисленными как SEQ ID NO:29-32, соответственно. Идентификационные номера аминокислотной последовательности для химерных антител представлены в таблице 1 ниже.
ТАБЛИЦА 1
АМИНОКИСЛОТНЫЕ ПОСЛЕДОВАТЕЛЬНОСТИ ДЛЯ ХИМЕРНЫХ АНТИТЕЛ
ПРИМЕР 2
РЕАКЦИОННАЯ СПОСОБНОСТЬ ХИМЕРНЫХ АНТИТЕЛ ПРОТИВ CTLA-4
Химерные антитела из примера 1 экспрессировали в клетках Expi293 [Система экспрессии Expi293, полученная из THERMO FISHER SCIENTIFIC®] и очищали с использованием колонки с белком A. Затем химерные антитела тестировали по реакционной способности по отношению к собачьему CTLA-4 посредством ELISA, следующим образом:
1. Покрывали иммунопланшет 200 нг/лунку CTLA-4 и инкубировали планшет при 4°C в течение ночи.
2. Промывали планшет 3 раза посредством PBS с 0,05% Tween 20 (PBST).
3. Блокировали планшет посредством 0,5% BSA в PBS в течение 45-60 мин при комнатной температуре.
4. Промывали планшет 3 раза посредством PBST.
5. Разводили антитела в три раза в каждом столбце или ряду планшета для разведения.
6. Переносили разведенные антитела в каждый столбец или ряд иммунопланшета, и инкубировали планшет в течение 45-60 мин при комнатной температуре.
7. Промывали планшет 3 раза посредством PBST.
8. Добавляли разведенные 1:2000 меченные пероксидазой хрена Fc против IgG собаки в каждую лунку планшета, и инкубировали планшет в течение 45-60 мин при комнатной температуре.
9. Промывали планшет 3 раза посредством PBST.
10. Добавляли субстрат TMB в каждую лунку планшета, и инкубировали планшет в течение 10-15 мин при комнатной температуре для проявления окрашивания.
11. Добавляли 100 мкл 1,5 M фосфорной кислоты в каждую лунку для остановки реакции.
12. Считывали планшет при 450 нм с использованием эталонной длины волны 540 нм.
Результаты ELISA изображены на фигуре 1, и показывают, что отобранные антитела могли связываться с собачьим CTLA-4. Кроме того, обнаружено, что химерное антитело 3B10 являлось наилучшим связывающим кандидатом среди этой группы химерных антител.
ПРИМЕР 3
КОНСТРУИРОВАНИЕ КАНИНИЗИРОВАННОГО МОНОКЛОНАЛЬНОГО АНТИТЕЛА 3B10 ПРОТИВ ЧЕЛОВЕЧЕСКОГО CTLA-4
После определения, что химерное антитело 3B10 имело наиболее сильную аффинность связывания для собачьего CTLA-4 (см. фигуру 1), группу из 6 CDR этого химерного антитела выбрали для добавления в собачью рамку считывания. Для осуществления способа канинизации, определяли последовательности ДНК, кодирующие тяжелые и легкие цепи собачьего IgG [см. U.S. 10106607 B2, полное содержание которой, таким образом, приведено в качестве ссылки]. Последовательности ДНК и белка собачьих тяжелых и легких цепей известны в данной области и могут быть получены посредством поиска в базах данных генов и белков NCBI. Существует четыре известных подтипа IgG собачьего IgG, и они обозначены как IgG-A, IgG-B, IgG-C и IgG-D. Существует два типа легких цепей в собачьих антителах, обозначенные как каппа и лямбда.
ТАБЛИЦА 2
ПОСЛЕДОВАТЕЛЬНОСТИ ДНК CDR ИЗ ПРЕДШЕСТВУЮЩЕГО УРОВНЯ ТЕХНИКИ В КАНИНИЗИРОВАННЫХ АНТИТЕЛАХ
ТАБЛИЦА 31
АМИНОКИСЛОТНЫЕ ПОСЛЕДОВАТЕЛЬНОСТИ CDR ИЗ ПРЕДШЕСТВУЮЩЕГО УРОВНЯ ТЕХНИКИ В КАНИНИЗИРОВАННЫХ АНТИТЕЛАХ
______________________
1 Последовательности нуклеиновой кислоты и аминокислотные последовательности CDR в таблицах 2 и 3 были получены ранее и описаны в WO2012120125 для гуманизированного антитела против человеческого CTLA-4.
NO:
Без связи с каким-либо конкретным способом, общий способ получения канинизированных тяжелых и легких цепей, которые можно смешивать в различных комбинациях для получения канинизированных mAb против человеческого CTLA-4, может включать следующую схему:
i) Идентификация CDR из цепей H и L желательных mAb против CTLA-4. Обратная трансляция аминокислотных последовательностей CDR в подходящую последовательность ДНК.
ii) Идентификация подходящей последовательности ДНК для цепей H и L собачьего IgG (например, модифицированной тяжелой цепи IgG-B, как описано в U.S. 10106607 B2, и легкой цепи каппа).
iii) Идентификация последовательностей ДНК, кодирующих эндогенные CDR, из ДНК цепей H и L собачьего IgG из вышеуказанной последовательности.
iv) Замена последовательности ДНК, кодирующей эндогенные CDR собачьих цепей H и L, на последовательности ДНК, кодирующие желательные CDR против человеческого CTLA-4. Когда было использовано модифицированное собачье IgG B, модификации в D31A и N63A, как пронумеровано в SEQ ID NO:69, осуществляли в собачьем IgG B, как описано ранее в U.S. 10106607 B2, полное содержание которого, таким образом, приведено в качестве ссылки. Также, необязательно, заменяли ДНК, кодирующую некоторые аминокислотные остатки собачьей рамки считывания, на ДНК, кодирующую избранные аминокислотные остатки из желательных областей собачьего mAb против человеческого CTLA-4. Этот способ называют обратной мутацией. Две группы из четырех вариантов для каждой тяжелой цепи и одна группа из трех вариантов для вариабельной области легкой цепи, перечисленные в таблицах 4 и 5, разработаны для каждого варианта в группе, содержащей различные участки обратной мутации.
v) Синтез ДНК со стадии (iv) и клонирование ее в подходящую экспрессирующую плазмиду.
vi) Трансфекция плазмид, содержащих желательные канинизированные цепи H и L, в клетки HEK 293.
vii) Очистка экспрессированного канинизированного антитела из супернатанта HEK 293.
viii) Тестирование очищенного канинизированного антитела по связыванию с собачьим CTLA-4.
Сконструирована группа канинизированных последовательностей цепей H и L. SEQ ID NO:перечислены в таблицах 4 и 5 ниже.
ТАБЛИЦА 4
SEQ ID NO. КАНИНИЗИРОВАННОЙ ТЯЖЕЛОЙ ЦЕПИ 3B10
Нуклеиновая кислота
Аминокислоты
______________________
2 Как показано в SEQ ID NO:69, ниже.
ТАБЛИЦА 5
SEQ ID NO. КАНИНИЗИРОВАННОЙ ЛЕГКОЙ ЦЕПИ 3B10
Нуклеиновая кислота
Аминокислоты
Настоящее изобретение относится к канинизированным антителам, сформированным посредством любой комбинации канинизированных тяжелых с легкими цепями, перечисленных в таблицах 4 и 5 выше. Затем антитела экспрессировали в клетках Expi293 и затем очищали. Результаты ELISA, показанные на фигуре 2, демонстрируют, что 3B10 было успешно канинизировано, где 3B10L3H2, 3B10L3H3 и 3B10L3H4 все обладали сходной активностью тесного связывания, как исходное мышиное-собачье химерное антитело из 3B10.
ПРИМЕР 4
БЛОКИРУЮЩАЯ АКТИВНОСТЬ ХИМЕРНЫХ И КАНИНИЗИРОВАННЫХ АНТИТЕЛ 3B10 ДЛЯ ВЗАИМОДЕЙСТВИЯ СОБАЧЬЕГО CD86 И CTLA-4
Чтобы убедиться, что канинизированные антитела 3B10 сохраняют нейтрализующую активность для собачьего CTLA-4, как исходное антитело, канинизированные антитела тестировали по блокирующей активности для взаимодействия собачьего-CD-80 и собачьего CTLA-4, посредством ELISA, следующим образом:
1. Покрывали иммунопланшет с использованием 200 нг/лунку CTLA-4 и инкубировали планшет при 4°C в течение ночи.
2. Промывали планшет 3 раза посредством PBS с 0,05% Tween 20 (PBST).
3. Блокировали планшет с использованием 0,5% BSA в PBS в течение 45-60 мин при комнатной температуре.
4. Промывали планшет 3 раза посредством PBST.
5. В три раза разводили антитела в каждом столбце или ряду планшета для разведения и затем добавляли 100 нг/лунку биотинилированного CD-86, и смешивали с антителами.
6. Переносили смесь разведенных антител и CD-86 в каждую колонку или ряд иммунопланшета, и инкубировали планшет в течение 45-60 мин при комнатной температуре.
7. Промывали планшет 3 раза посредством PBST.
8. Добавляли разведенный 1:2000 конъюгированный с пероксидазой хрена стрептавидин в каждую лунку планшета, и инкубировали планшет в течение 45-60 мин при комнатной температуре.
9. Промывали планшет 3 раза с использованием PBST.
10. Добавляли субстрат TMB в каждую лунку планшета, и инкубировали планшет в течение 10-15 мин при комнатной температуре для проявления окрашивания.
11. Добавляли 100 мкл 1,5 M фосфорной кислоты в каждую лунку для остановки реакции.
12. Считывали планшет при 450 нм с использованием эталонной длины волны 540 нм.
График результатов для планшетов для ELISA, изображенный на фигуре 3, показывает, что канинизированные варианты 3B10 имеют сходную блокирующую активность, как исходное 3B10.
ПРИМЕР 5
ОБРАЗОВАНИЕ IFNγ СОБАЧЬИМИ PBMC, АКТИВИРОВАННЫМИ ПОСРЕДСТВОМ ХИМЕРНЫХ АНТИТЕЛ
Введение:
Интерферон-гамма (IFN-γ; также известный как интерферон типа II) в основном продуцируется посредством активированных T-лимфоцитов и возможно, посредством клеток естественных киллеров. Этот атрибут широко используют в качестве показателя активации T-клеток посредством количественного тестирования IFN-γ в анализе на основе ELISA. Для идентификации функциональных антител против CTLA-4 (антител против CTLA-4), отобранные антитела тестировали по их активности стимуляции продукции IFN-γ в собачьих мононуклеарных клетках периферической крови с использованием следующего способа.
Эксперимент и результаты
Выделение собачьих мононуклеарных клеток периферической крови:
1. Собирали ~20 мл цельной крови в пробирку с ЭДТА или гепарином натрия.
2. Переносили кровь в 50 мл полистирольную пробирку и разводили 50:50 с сбалансированным солевым раствором Хенкса (HBSS).
3. Добавляли 15 мл фиколла Ficoll-Plaque Plus в четыре x 50 мл пробирки SepMate™. Затем добавляли ~10 мл разведенной 50:50 крови, медленно и по стенке каждой из пробирок SepMate™, содержащих фиколл.
4. Центрифугировали пробирки при 1200 x g в течение 20 минут.
5. Собирали клетки с поверхности раздела градиента и переносили клетки в 50 мл полипропиленовую пробирку. Добавляли HBSS до отметки 40-45 мл и центрифугировали клетки при 800 x g в течение 10 минут.
6. Отбрасывали супернатант, ресуспендировали клетки в 40-45 мл HBSS, и снова центрифугировали пробирки при 800 x g в течение 10 минут.
7. Отбрасывали супернатант и ресуспендировали клетки из каждой пробирки с использованием 2 мл сред для собачьих лимфоцитов (пулировали клетки от одного и того же животного).
8. Отбирали небольшую аликвоту суспензии клеток, смешивали ее с 0,04% трипанового синего и подсчитывали количество клеток.
9. Сохраняли суспензию клеток при 2-7°C до использования [но не дольше, чем 24 часа перед использованием.]
Анализ пролиферации клеток для собачьих мононуклеарных клеток периферической крови:
1. Разводили антитела в средах для собачьих лимфоцитов [среде RPMI, закупленной из LONZA, каталожный No. 12-167Q, или эквивалентной] для достижения конечной концентрации 40 мкг/мл (подготавливали 160 мкг/мл) и стерилизовали их с использованием шприцевого фильтра 0,2 мкм. Разведенные в два раза антитела помещали в стерильный планшет для разведения и затем отставляли.
2. Разводили клетки до 2,5 X 106 клеток/мл в средах для собачьих лимфоцитов и распределяли по 100 мкл на лунку целого 96-луночного планшета для культивирования тканей.
3. Разводили Con A в средах для собачьих лимфоцитов для достижения конечной концентрации 250 нг/мл (подготавливали 1000 нг/мл), стерилизовали их с использованием шприцевого фильтра 0,2 мкм и добавляли по 50 мкл во все лунки. (Примечание - не добавляли Con A в один столбец из восьми лунок ни для контроля только клетки, ни в лунки, предназначенные для контроля только клетки+mAb.)
4. Добавляли 100 мкл сред для собачьих лимфоцитов на лунку в лунки только с клетками и 50 мкл сред в столбец, содержащий контрольные лунки для Con A (Con A+клетки без обработки mAb).
5. Добавляли 50 мкл разведенных mAb в лунки в двух повторах.
6. Инкубировали планшеты при 36±2°C, 4,0-6,0% CO2 в увлажненном инкубаторе в течение 68-124 часов.
ELISA IFN-гамма:
1. После 68-124-часовой инкубации, центрифугировали планшет при 800 x g в течение 10 минут.
2. Собирали супернатант из каждой лунки и пулировали повторы. Эти образцы можно замораживать при ≤-50°C для позднейшего использования или тестировать немедленно.
3. Разводили образцы супернатанта подходящим образом, при необходимости, и проводили ELISA IFN-гамма в соответствии с инструкциями в наборе для ELISA собачьего IFN-гамма Quantikine™ [R&D Systems, каталожный No. CAIF00].
Результаты, представленные на фигуре 4, показывают, что тестированные химерные антитела, особенно 3B10, 411 и 611, значительно активировали собачьи T-клетки для продукции IFN-гамма.
ПРИМЕР 6
ЭПИТОПНОЕ КАРТИРОВАНИЕ КАНИНИЗИРОВАННОГО АНТИТЕЛА 3B10
Эпитоп для связывания канинизированного антитела 3B10L3H2 на собачьем CTLA-4 (Эталонная последовательность в NCBI: NP_001003106; SEQ ID NO:68) картировали посредством химического сшивания и масс-спектрометрии. Результаты показывают, что антитело связывается с двумя отдельными линейными областями на антигене CTLA-4, включающими аминокислоты R33, R38, S42, T45, R83, T87, Y90, K93 и Y98 (см. фигуру 5). На фигуре 5 аминокислотные остатки для не являющегося непрерывным эпитопа CTLA-4, с которым связывается канинизированное антитело 3B10L3H2, показаны как состоящие из двух линейных частей, аминокислотных остатков 30-50 и аминокислотных остатков 80-100, соответственно.
ПОСЛЕДОВАТЕЛЬНОСТИ
SEQ ID NO:1: ДНК химерной мышиной-собачьей тяжелой цепи (3B10):
GAAGTGCAGCTGCAGCAGTTTGGCGCGGAACTGGTGAAACCGGGCGCGAGCGTGAAAATGAGCTGCAAAGCGAGCGGCTATACCTTTACCGATTATAACATGGATTGGGTGCGCCAGAGCGGCAAAAGCCTGGAATGGATTGGCAACATTAACCCGAACAGCGAAAGCACCAGCTATAACCAGAAATTTAAAGGCAAAGCGACCCTGACCGTGGATAAAAGCAGCAGCACCGCGTATATGGAACTGCGCAGCCTGACCAGCGATGATACCGCGGTGTATTATTGCACCCGCGATGGCAACCGCTATGATGCGTGGTTTGCGTATTGGGGCCAGGGCACCCTGGTGACCGTGAGCAGCGCGAGCACCACCGCGCCGAGCGTGTTTCCGCTGGCGCCGAGCTGCGGCAGCACCAGCGGCAGCACCGTGGCGCTGGCGTGCCTGGTGAGCGGCTATTTTCCGGAACCGGTGACCGTGAGCTGGAACAGCGGCAGCCTGACCAGCGGCGTGCATACCTTTCCGAGCGTGCTGCAGAGCAGCGGCCTGTATAGCCTGAGCAGCATGGTGACCGTGCCGAGCAGCCGCTGGCCGAGCGAAACCTTTACCTGCAACGTGGCGCATCCGGCGAGCAAAACCAAAGTGGATAAACCGGTGCCGAAACGCGAAAACGGCCGCGTGCCGCGCCCGCCGGATTGCCCGAAATGCCCGGCGCCGGAAATGCTGGGCGGCCCGAGCGTGTTTATTTTTCCGCCGAAACCGAAAGATACCCTGCTGATTGCGCGCACCCCGGAAGTGACCTGCGTGGTGGTGGCGCTGGATCCGGAAGATCCGGAAGTGCAGATTAGCTGGTTTGTGGATGGCAAACAGATGCAGACCGCGAAAACCCAGCCGCGCGAAGAACAGTTTGCGGGCACCTATCGCGTGGTGAGCGTGCTGCCGATTGGCCATCAGGATTGGCTGAAAGGCAAACAGTTTACCTGCAAAGTGAACAACAAAGCGCTGCCGAGCCCGATTGAACGCACCATTAGCAAAGCGCGCGGCCAGGCGCATCAGCCGAGCGTGTATGTGCTGCCGCCGAGCCGCGAAGAACTGAGCAAAAACACCGTGAGCCTGACCTGCCTGATTAAAGATTTTTTTCCGCCGGATATTGATGTGGAATGGCAGAGCAACGGCCAGCAGGAACCGGAAAGCAAATATCGCACCACCCCGCCGCAGCTGGATGAAGATGGCAGCTATTTTCTGTATAGCAAACTGAGCGTGGATAAAAGCCGCTGGCAGCGCGGCGATACCTTTATTTGCGCGGTGATGCATGAAGCGCTGCATAACCATTATACCCAGGAAAGCCTGAGCCATAGCCCGGGCAAA
SEQ ID NO:2: Аминокислотная последовательность химерной мышиной-собачьей тяжелой цепи (3B10):
EVQLQQFGAELVKPGASVKMSCKASGYTFTDYNMDWVRQSGKSLEWIGNINPNSESTSYNQKFKGKATLTVDKSSSTAYMELRSLTSDDTAVYYCTRDGNRYDAWFAYWGQGTLVTVSSASTTAPSVFPLAPSCGSTSGSTVALACLVSGYFPEPVTVSWNSGSLTSGVHTFPSVLQSSGLYSLSSMVTVPSSRWPSETFTCNVAHPASKTKVDKPVPKRENGRVPRPPDCPKCPAPEMLGGPSVFIFPPKPKDTLLIARTPEVTCVVVALDPEDPEVQISWFVDGKQMQTAKTQPREEQFAGTYRVVSVLPIGHQDWLKGKQFTCKVNNKALPSPIERTISKARGQAHQPSVYVLPPSREELSKNTVSLTCLIKDFFPPDIDVEWQSNGQQEPESKYRTTPPQLDEDGSYFLYSKLSVDKSRWQRGDTFICAVMHEALHNHYTQESLSHSPGK
SEQ ID NO:3: ДНК химерной мышиной-собачьей легкой цепи (3B10):
CAGATTGTGCTGACCCAGAGCCCGGCGATTATGAGCGCGAGCCCGGGCGAAAAAGTGACCATGACCTGCAGCGCGAGCAGCAGCGTGACCTATATGCATTGGTTTCAGCAGAAACCGGGCACCAGCCCGAAACTGTGGATTTATAGCACCAGCATTCTGGCGAGCGGCGTGCCGGCGCGCTTTAGCGGCAGCGGCAGCGGCACCAGCTATAGCCTGACCATTAGCCGCATGGAAGCGGAAGATGCGGCGACCTATTATTGCCAGCAGCGCACCAGCTATCCGCTGACCTTTGGCACCGGCACCAAACTGGAACTGAAACGCAACGATGCGCAGCCGGCGGTGTATCTGTTTCAGCCGAGCCCGGATCAGCTGCATACCGGCAGCGCGAGCGTGGTGTGCCTGCTGAACAGCTTTTATCCGAAAGATATTAACGTGAAATGGAAAGTGGATGGCGTGATTCAGGATACCGGCATTCAGGAAAGCGTGACCGAACAGGATAGCAAAGATAGCACCTATAGCCTGAGCAGCACCCTGACCATGAGCAGCACCGAATATCTGAGCCATGAACTGTATAGCTGCGAAATTACCCATAAAAGCCTGCCGAGCACCCTGATTAAAAGCTTTCAGCGCAGCGAATGCCAGCGCGTGGAT
SEQ ID NO:4: Аминокислотная последовательность химерной мышиной-собачьей легкой цепи (3B10):
QIVLTQSPAIMSASPGEKVTMTCSASSSVTYMHWFQQKPGTSPKLWIYSTSILASGVPARFSGSGSGTSYSLTISRMEAEDAATYYCQQRTSYPLTFGTGTKLELKRNDAQPAVYLFQPSPDQLHTGSASVVCLLNSFYPKDINVKWKVDGVIQDTGIQESVTEQDSKDSTYSLSSTLTMSSTEYLSHELYSCEITHKSLPSTLIKSFQRSECQRVD
SEQ ID NO:5: ДНК химерной мышиной-собачьей тяжелой цепи (8H5)
CAGGTGCAGCTGCAGCAGAGCGGCGATGATCTGGTGAAACCGGGCGCGAGCGTGAAACTGAGCTGCAAAGCGAGCGGCTATACCTTTACCAGCTATTGGATTAACTGGATTAAACAGCGCCCGGGCCAGGGCCTGGAATGGATTGGCCGCATTGCGCCGGGCAGCGGCACCACCTATTATAACGAAGTGTTTAAAGGCAAAGCGACCCTGACCGTGGATAAATATAGCAGCACCGCGTATATTCAGCTGAGCAGCCTGAGCAGCGAAGATAGCGCGGTGTATTTTTGCGCGCGCGGCGATTATGGCAGCTATTGGGGCCAGGGCACCCTGGTGACCGTGAGCAGCGCGAGCACCACCGCGCCGAGCGTGTTTCCGCTGGCGCCGAGCTGCGGCAGCACCAGCGGCAGCACCGTGGCGCTGGCGTGCCTGGTGAGCGGCTATTTTCCGGAACCGGTGACCGTGAGCTGGAACAGCGGCAGCCTGACCAGCGGCGTGCATACCTTTCCGAGCGTGCTGCAGAGCAGCGGCCTGTATAGCCTGAGCAGCATGGTGACCGTGCCGAGCAGCCGCTGGCCGAGCGAAACCTTTACCTGCAACGTGGCGCATCCGGCGAGCAAAACCAAAGTGGATAAACCGGTGCCGAAACGCGAAAACGGCCGCGTGCCGCGCCCGCCGGATTGCCCGAAATGCCCGGCGCCGGAAATGCTGGGCGGCCCGAGCGTGTTTATTTTTCCGCCGAAACCGAAAGATACCCTGCTGATTGCGCGCACCCCGGAAGTGACCTGCGTGGTGGTGGCGCTGGATCCGGAAGATCCGGAAGTGCAGATTAGCTGGTTTGTGGATGGCAAACAGATGCAGACCGCGAAAACCCAGCCGCGCGAAGAACAGTTTGCGGGCACCTATCGCGTGGTGAGCGTGCTGCCGATTGGCCATCAGGATTGGCTGAAAGGCAAACAGTTTACCTGCAAAGTGAACAACAAAGCGCTGCCGAGCCCGATTGAACGCACCATTAGCAAAGCGCGCGGCCAGGCGCATCAGCCGAGCGTGTATGTGCTGCCGCCGAGCCGCGAAGAACTGAGCAAAAACACCGTGAGCCTGACCTGCCTGATTAAAGATTTTTTTCCGCCGGATATTGATGTGGAATGGCAGAGCAACGGCCAGCAGGAACCGGAAAGCAAATATCGCACCACCCCGCCGCAGCTGGATGAAGATGGCAGCTATTTTCTGTATAGCAAACTGAGCGTGGATAAAAGCCGCTGGCAGCGCGGCGATACCTTTATTTGCGCGGTGATGCATGAAGCGCTGCATAACCATTATACCCAGGAAAGCCTGAGCCATAGCCCGGGCAAA
SEQ ID NO:6. Аминокислотная последовательность химерной мышиной-собачьей тяжелой цепи (8H5):
QVQLQQSGDDLVKPGASVKLSCKASGYTFTSYWINWIKQRPGQGLEWIGRIAPGSGTTYYNEVFKGKATLTVDKYSSTAYIQLSSLSSEDSAVYFCARGDYGSYWGQGTLVTVSSASTTAPSVFPLAPSCGSTSGSTVALACLVSGYFPEPVTVSWNSGSLTSGVHTFPSVLQSSGLYSLSSMVTVPSSRWPSETFTCNVAHPASKTKVDKPVPKRENGRVPRPPDCPKCPAPEMLGGPSVFIFPPKPKDTLLIARTPEVTCVVVALDPEDPEVQISWFVDGKQMQTAKTQPREEQFAGTYRVVSVLPIGHQDWLKGKQFTCKVNNKALPSPIERTISKARGQAHQPSVYVLPPSREELSKNTVSLTCLIKDFFPPDIDVEWQSNGQQEPESKYRTTPPQLDEDGSYFLYSKLSVDKSRWQRGDTFICAVMHEALHNHYTQESLSHSPGK
SEQ ID NO:7: ДНК химерной мышиной-собачьей легкой цепи (8H5):
CAGATTGTGCTGACCCAGAGCCCGGCGATTATGAGCGCGAGCCCGGGCGAAAAAGTGACCATGACCTGCAGCGCGAGCAGCAGCATTAGCTATATGCATTGGTTTCAGCAGAAACCGGGCACCAGCCCGAAACGCTGGATTTATGATACCAGCAAACTGGCGAGCGGCGTGCCGGCGCGCTTTAGCGGCAGCGGCAGCGGCACCAGCTATAGCCTGACCATTAACAGCATGGAAGCGGAAGATGCGGCGACCTATTATTGCCATCAGCGCACCAGCTATCCGCTGACCTTTGGCGCGGGCACCAAACTGGAACTGAAACGCAACGATGCGCAGCCGGCGGTGTATCTGTTTCAGCCGAGCCCGGATCAGCTGCATACCGGCAGCGCGAGCGTGGTGTGCCTGCTGAACAGCTTTTATCCGAAAGATATTAACGTGAAATGGAAAGTGGATGGCGTGATTCAGGATACCGGCATTCAGGAAAGCGTGACCGAACAGGATAGCAAAGATAGCACCTATAGCCTGAGCAGCACCCTGACCATGAGCAGCACCGAATATCTGAGCCATGAACTGTATAGCTGCGAAATTACCCATAAAAGCCTGCCGAGCACCCTGATTAAAAGCTTTCAGCGCAGCGAATGCCAGCGCGTGGAT
SEQ ID NO:8: Аминокислотная последовательность химерной мышиной-собачьей легкой цепи (8H5):
QIVLTQSPAIMSASPGEKVTMTCSASSSISYMHWFQQKPGTSPKRWIYDTSKLASGVPARFSGSGSGTSYSLTINSMEAEDAATYYCHQRTSYPLTFGAGTKLELKRNDAQPAVYLFQPSPDQLHTGSASVVCLLNSFYPKDINVKWKVDGVIQDTGIQESVTEQDSKDSTYSLSSTLTMSSTEYLSHELYSCEITHKSLPSTLIKSFQRSECQRVD
SEQ ID NO:9: ДНК химерной человеческой-собачьей тяжелой цепи (411):
CAGGTGCAGCTGGTGGAAAGCGGCGGCGGCGTGGTGCAGCCGGGCCGCAGCCTGCGCCTGAGCTGCGTGGCGAGCGGCTTTACCTTTAGCAGCCATGGCATGCATTGGGTGCGCCAGGCGCCGGGCAAAGGCCTGGAATGGGTGGCGGTGATTTGGTATGATGGCCGCAACAAATATTATGCGGATAGCGTGAAAGGCCGCTTTACCATTAGCCGCGATAACAGCAAAAACACCCTGTTTCTGCAGATGAACAGCCTGCGCGCGGAAGATACCGCGGTGTATTATTGCGCGCGCGGCGGCCATTTTGGCCCGTTTGATTATTGGGGCCAGGGCACCCTGGTGACCGTGAGCAGCGCGAGCACCACCGCGCCGAGCGTGTTTCCGCTGGCGCCGAGCTGCGGCAGCACCAGCGGCAGCACCGTGGCGCTGGCGTGCCTGGTGAGCGGCTATTTTCCGGAACCGGTGACCGTGAGCTGGAACAGCGGCAGCCTGACCAGCGGCGTGCATACCTTTCCGAGCGTGCTGCAGAGCAGCGGCCTGTATAGCCTGAGCAGCATGGTGACCGTGCCGAGCAGCCGCTGGCCGAGCGAAACCTTTACCTGCAACGTGGCGCATCCGGCGAGCAAAACCAAAGTGGATAAACCGGTGCCGAAACGCGAAAACGGCCGCGTGCCGCGCCCGCCGGATTGCCCGAAATGCCCGGCGCCGGAAATGCTGGGCGGCCCGAGCGTGTTTATTTTTCCGCCGAAACCGAAAGATACCCTGCTGATTGCGCGCACCCCGGAAGTGACCTGCGTGGTGGTGGCGCTGGATCCGGAAGATCCGGAAGTGCAGATTAGCTGGTTTGTGGATGGCAAACAGATGCAGACCGCGAAAACCCAGCCGCGCGAAGAACAGTTTGCGGGCACCTATCGCGTGGTGAGCGTGCTGCCGATTGGCCATCAGGATTGGCTGAAAGGCAAACAGTTTACCTGCAAAGTGAACAACAAAGCGCTGCCGAGCCCGATTGAACGCACCATTAGCAAAGCGCGCGGCCAGGCGCATCAGCCGAGCGTGTATGTGCTGCCGCCGAGCCGCGAAGAACTGAGCAAAAACACCGTGAGCCTGACCTGCCTGATTAAAGATTTTTTTCCGCCGGATATTGATGTGGAATGGCAGAGCAACGGCCAGCAGGAACCGGAAAGCAAATATCGCACCACCCCGCCGCAGCTGGATGAAGATGGCAGCTATTTTCTGTATAGCAAACTGAGCGTGGATAAAAGCCGCTGGCAGCGCGGCGATACCTTTATTTGCGCGGTGATGCATGAAGCGCTGCATAACCATTATACCCAGGAAAGCCTGAGCCATAGCCCGGGCAAA
SEQ ID NO:10: Аминокислотная последовательность химерной человеческой-собачьей тяжелой цепи (411)
QVQLVESGGGVVQPGRSLRLSCVASGFTFSSHGMHWVRQAPGKGLEWVAVIWYDGRNKYYADSVKGRFTISRDNSKNTLFLQMNSLRAEDTAVYYCARGGHFGPFDYWGQGTLVTVSSASTTAPSVFPLAPSCGSTSGSTVALACLVSGYFPEPVTVSWNSGSLTSGVHTFPSVLQSSGLYSLSSMVTVPSSRWPSETFTCNVAHPASKTKVDKPVPKRENGRVPRPPDCPKCPAPEMLGGPSVFIFPPKPKDTLLIARTPEVTCVVVALDPEDPEVQISWFVDGKQMQTAKTQPREEQFAGTYRVVSVLPIGHQDWLKGKQFTCKVNNKALPSPIERTISKARGQAHQPSVYVLPPSREELSKNTVSLTCLIKDFFPPDIDVEWQSNGQQEPESKYRTTPPQLDEDGSYFLYSKLSVDKSRWQRGDTFICAVMHEALHNHYTQESLSHSPGK
SEQ ID NO:11. ДНК химерной человеческой-собачьей легкой цепи (411):
GAAATTGTGCTGACCCAGAGCCCGGGCACCCTGAGCCTGAGCCCGGGCGAACGCGCGACCCTGAGCTGCCGCGCGAGCCAGAGCATTAGCAGCAGCTTTCTGGCGTGGTATCAGCAGCGCCCGGGCCAGGCGCCGCGCCTGCTGATTTATGGCGCGAGCAGCCGCGCGACCGGCATTCCGGATCGCTTTAGCGGCAGCGGCAGCGGCACCGATTTTACCCTGACCATTAGCCGCCTGGAACCGGAAGATTTTGCGGTGTATTATTGCCAGCAGTATGGCACCAGCCCGTGGACCTTTGGCCAGGGCACCAAAGTGGAAATTAAACGCAACGATGCGCAGCCGGCGGTGTATCTGTTTCAGCCGAGCCCGGATCAGCTGCATACCGGCAGCGCGAGCGTGGTGTGCCTGCTGAACAGCTTTTATCCGAAAGATATTAACGTGAAATGGAAAGTGGATGGCGTGATTCAGGATACCGGCATTCAGGAAAGCGTGACCGAACAGGATAGCAAAGATAGCACCTATAGCCTGAGCAGCACCCTGACCATGAGCAGCACCGAATATCTGAGCCATGAACTGTATAGCTGCGAAATTACCCATAAAAGCCTGCCGAGCACCCTGATTAAAAGCTTTCAGCGCAGCGAATGCCAGCGCGTGGAT
SEQ ID NO:12: Аминокислотная последовательность химерной человеческой-собачьей легкой цепи (411):
EIVLTQSPGTLSLSPGERATLSCRASQSISSSFLAWYQQRPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQYGTSPWTFGQGTKVEIKRNDAQPAVYLFQPSPDQLHTGSASVVCLLNSFYPKDINVKWKVDGVIQDTGIQESVTEQDSKDSTYSLSSTLTMSSTEYLSHELYSCEITHKSLPSTLIKSFQRSECQRVD
SEQ ID NO:13. ДНК химерной человеческой-собачьей тяжелой цепи (418)
CAGGTGCAGCTGGTGGAAAGCGGCGGCGGCGTGGTGCAGCCGGGCCGCAGCCTGCGCCTGAGCTGCACCGCGAGCGGCTTTACCTTTAGCAACTATGGCATGCATTGGGTGCGCCAGGCGCCGGGCAAAGGCCTGGAATGGGTGGCGGTGATTTGGTATGATGGCAGCAACAAACATTATGGCGATAGCGTGAAAGGCCGCTTTACCATTAGCAGCGATAACAGCAAAAACACCCTGTATCTGCAGATGAACAGCCTGCGCGCGGAAGATACCGCGGTGTATTATTGCGCGCGCGGCGAACGCCTGGGCAGCTATTTTGATTATTGGGGCCAGGGCACCCTGGTGACCGTGAGCAGCGCGAGCACCACCGCGCCGAGCGTGTTTCCGCTGGCGCCGAGCTGCGGCAGCACCAGCGGCAGCACCGTGGCGCTGGCGTGCCTGGTGAGCGGCTATTTTCCGGAACCGGTGACCGTGAGCTGGAACAGCGGCAGCCTGACCAGCGGCGTGCATACCTTTCCGAGCGTGCTGCAGAGCAGCGGCCTGTATAGCCTGAGCAGCATGGTGACCGTGCCGAGCAGCCGCTGGCCGAGCGAAACCTTTACCTGCAACGTGGCGCATCCGGCGAGCAAAACCAAAGTGGATAAACCGGTGCCGAAACGCGAAAACGGCCGCGTGCCGCGCCCGCCGGATTGCCCGAAATGCCCGGCGCCGGAAATGCTGGGCGGCCCGAGCGTGTTTATTTTTCCGCCGAAACCGAAAGATACCCTGCTGATTGCGCGCACCCCGGAAGTGACCTGCGTGGTGGTGGCGCTGGATCCGGAAGATCCGGAAGTGCAGATTAGCTGGTTTGTGGATGGCAAACAGATGCAGACCGCGAAAACCCAGCCGCGCGAAGAACAGTTTGCGGGCACCTATCGCGTGGTGAGCGTGCTGCCGATTGGCCATCAGGATTGGCTGAAAGGCAAACAGTTTACCTGCAAAGTGAACAACAAAGCGCTGCCGAGCCCGATTGAACGCACCATTAGCAAAGCGCGCGGCCAGGCGCATCAGCCGAGCGTGTATGTGCTGCCGCCGAGCCGCGAAGAACTGAGCAAAAACACCGTGAGCCTGACCTGCCTGATTAAAGATTTTTTTCCGCCGGATATTGATGTGGAATGGCAGAGCAACGGCCAGCAGGAACCGGAAAGCAAATATCGCACCACCCCGCCGCAGCTGGATGAAGATGGCAGCTATTTTCTGTATAGCAAACTGAGCGTGGATAAAAGCCGCTGGCAGCGCGGCGATACCTTTATTTGCGCGGTGATGCATGAAGCGCTGCATAACCATTATACCCAGGAAAGCCTGAGCCATAGCCCGGGCAAA
SEQ ID NO:14. Аминокислотная последовательность химерной человеческой-собачьей тяжелой цепи (418)
QVQLVESGGGVVQPGRSLRLSCTASGFTFSNYGMHWVRQAPGKGLEWVAVIWYDGSNKHYGDSVKGRFTISSDNSKNTLYLQMNSLRAEDTAVYYCARGERLGSYFDYWGQGTLVTVSSASTTAPSVFPLAPSCGSTSGSTVALACLVSGYFPEPVTVSWNSGSLTSGVHTFPSVLQSSGLYSLSSMVTVPSSRWPSETFTCNVAHPASKTKVDKPVPKRENGRVPRPPDCPKCPAPEMLGGPSVFIFPPKPKDTLLIARTPEVTCVVVALDPEDPEVQISWFVDGKQMQTAKTQPREEQFAGTYRVVSVLPIGHQDWLKGKQFTCKVNNKALPSPIERTISKARGQAHQPSVYVLPPSREELSKNTVSLTCLIKDFFPPDIDVEWQSNGQQEPESKYRTTPPQLDEDGSYFLYSKLSVDKSRWQRGDTFICAVMHEALHNHYTQESLSHSPGK
SEQ ID NO:15. ДНК химерной человеческой-собачьей легкой цепи (418)
GAAATTGTGCTGACCCAGAGCCCGGGCACCCTGAGCCTGAGCCCGGGCGAACGCGCGACCCTGAGCTGCCGCACCAGCGTGAGCAGCAGCTATCTGGCGTGGTATCAGCAGAAACCGGGCCAGGCGCCGCGCCTGCTGATTTATGGCGCGAGCAGCCGCGCGACCGGCATTCCGGATCGCTTTAGCGGCAGCGGCAGCGGCACCGATTTTACCCTGACCATTAGCCGCCTGGAACCGGAAGATTTTGCGGTGTATTATTGCCAGCAGTATGGCATTAGCCCGTTTACCTTTGGCGGCGGCACCAAAGTGGAAATTAAACGCAACGATGCGCAGCCGGCGGTGTATCTGTTTCAGCCGAGCCCGGATCAGCTGCATACCGGCAGCGCGAGCGTGGTGTGCCTGCTGAACAGCTTTTATCCGAAAGATATTAACGTGAAATGGAAAGTGGATGGCGTGATTCAGGATACCGGCATTCAGGAAAGCGTGACCGAACAGGATAGCAAAGATAGCACCTATAGCCTGAGCAGCACCCTGACCATGAGCAGCACCGAATATCTGAGCCATGAACTGTATAGCTGCGAAATTACCCATAAAAGCCTGCCGAGCACCCTGATTAAAAGCTTTCAGCGCAGCGAATGCCAGCGCGTGGAT
SEQ ID NO:16. Аминокислотная последовательность химерной человеческой-собачьей легкой цепи (418)
EIVLTQSPGTLSLSPGERATLSCRTSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQYGISPFTFGGGTKVEIKRNDAQPAVYLFQPSPDQLHTGSASVVCLLNSFYPKDINVKWKVDGVIQDTGIQESVTEQDSKDSTYSLSSTLTMSSTEYLSHELYSCEITHKSLPSTLIKSFQRSECQRVD
SEQ ID NO:17. ДНК химерной человеческой-собачьей тяжелой цепи (611)
CAGGTGCAGCTGGTGGAAAGCGGCGGCGGCGTGGTGGAACCGGGCCGCAGCCTGCGCCTGAGCTGCACCGCGAGCGGCTTTACCTTTAGCAGCTATGGCATGCATTGGGTGCGCCAGGCGCCGGGCAAAGGCCTGGAATGGGTGGCGGTGATTTGGTATGATGGCAGCAACAAACATTATGCGGATAGCGCGAAAGGCCGCTTTACCATTAGCCGCGATAACAGCAAAAACACCCTGTATCTGCAGATGAACAGCCTGCGCGCGGAAGATACCGCGGTGTATTATTGCGCGCGCGCGGGCCTGCTGGGCTATTTTGATTATTGGGGCCAGGGCACCCTGGTGACCGTGAGCAGCGCGAGCACCACCGCGCCGAGCGTGTTTCCGCTGGCGCCGAGCTGCGGCAGCACCAGCGGCAGCACCGTGGCGCTGGCGTGCCTGGTGAGCGGCTATTTTCCGGAACCGGTGACCGTGAGCTGGAACAGCGGCAGCCTGACCAGCGGCGTGCATACCTTTCCGAGCGTGCTGCAGAGCAGCGGCCTGTATAGCCTGAGCAGCATGGTGACCGTGCCGAGCAGCCGCTGGCCGAGCGAAACCTTTACCTGCAACGTGGCGCATCCGGCGAGCAAAACCAAAGTGGATAAACCGGTGCCGAAACGCGAAAACGGCCGCGTGCCGCGCCCGCCGGATTGCCCGAAATGCCCGGCGCCGGAAATGCTGGGCGGCCCGAGCGTGTTTATTTTTCCGCCGAAACCGAAAGATACCCTGCTGATTGCGCGCACCCCGGAAGTGACCTGCGTGGTGGTGGCGCTGGATCCGGAAGATCCGGAAGTGCAGATTAGCTGGTTTGTGGATGGCAAACAGATGCAGACCGCGAAAACCCAGCCGCGCGAAGAACAGTTTGCGGGCACCTATCGCGTGGTGAGCGTGCTGCCGATTGGCCATCAGGATTGGCTGAAAGGCAAACAGTTTACCTGCAAAGTGAACAACAAAGCGCTGCCGAGCCCGATTGAACGCACCATTAGCAAAGCGCGCGGCCAGGCGCATCAGCCGAGCGTGTATGTGCTGCCGCCGAGCCGCGAAGAACTGAGCAAAAACACCGTGAGCCTGACCTGCCTGATTAAAGATTTTTTTCCGCCGGATATTGATGTGGAATGGCAGAGCAACGGCCAGCAGGAACCGGAAAGCAAATATCGCACCACCCCGCCGCAGCTGGATGAAGATGGCAGCTATTTTCTGTATAGCAAACTGAGCGTGGATAAAAGCCGCTGGCAGCGCGGCGATACCTTTATTTGCGCGGTGATGCATGAAGCGCTGCATAACCATTATACCCAGGAAAGCCTGAGCCATAGCCCGGGCAAA
SEQ ID NO:18: Аминокислотная последовательность химерной человеческой-собачьей тяжелой цепи (611)
QVQLVESGGGVVEPGRSLRLSCTASGFTFSSYGMHWVRQAPGKGLEWVAVIWYDGSNKHYADSAKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARAGLLGYFDYWGQGTLVTVSSASTTAPSVFPLAPSCGSTSGSTVALACLVSGYFPEPVTVSWNSGSLTSGVHTFPSVLQSSGLYSLSSMVTVPSSRWPSETFTCNVAHPASKTKVDKPVPKRENGRVPRPPDCPKCPAPEMLGGPSVFIFPPKPKDTLLIARTPEVTCVVVALDPEDPEVQISWFVDGKQMQTAKTQPREEQFAGTYRVVSVLPIGHQDWLKGKQFTCKVNNKALPSPIERTISKARGQAHQPSVYVLPPSREELSKNTVSLTCLIKDFFPPDIDVEWQSNGQQEPESKYRTTPPQLDEDGSYFLYSKLSVDKSRWQRGDTFICAVMHEALHNHYTQESLSHSPGK
SEQ ID NO:19: ДНК химерной человеческой-собачьей легкой цепи (611)
GAAATTGTGCTGACCCAGAGCCCGGGCACCCTGAGCCTGAGCCCGGGCGAACGCGCGACCCTGAGCTGCCGCGCGAGCCAGAGCGTGAGCAGCTATCTGGCGTGGTATCAGCAGAAACCGGGCCAGGCGCCGCGCCCGCTGATTTATGGCGTGAGCAGCCGCGCGACCGGCATTCCGGATCGCTTTAGCGGCAGCGGCAGCGGCACCGATTTTACCCTGACCATTAGCCGCCTGGAACCGGAAGATTTTGCGGTGTATTATTGCCAGCAGTATGGCATTAGCCCGTTTACCTTTGGCCCGGGCACCAAAGTGGATATTAAACGCAACGATGCGCAGCCGGCGGTGTATCTGTTTCAGCCGAGCCCGGATCAGCTGCATACCGGCAGCGCGAGCGTGGTGTGCCTGCTGAACAGCTTTTATCCGAAAGATATTAACGTGAAATGGAAAGTGGATGGCGTGATTCAGGATACCGGCATTCAGGAAAGCGTGACCGAACAGGATAGCAAAGATAGCACCTATAGCCTGAGCAGCACCCTGACCATGAGCAGCACCGAATATCTGAGCCATGAACTGTATAGCTGCGAAATTACCCATAAAAGCCTGCCGAGCACCCTGATTAAAAGCTTTCAGCGCAGCGAATGCCAGCGCGTGGAT
SEQ ID NO:20. Аминокислотная последовательность химерной человеческой-собачьей легкой цепи (611)
EIVLTQSPGTLSLSPGERATLSCRASQSVSSYLAWYQQKPGQAPRPLIYGVSSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQYGISPFTFGPGTKVDIKRNDAQPAVYLFQPSPDQLHTGSASVVCLLNSFYPKDINVKWKVDGVIQDTGIQESVTEQDSKDSTYSLSSTLTMSSTEYLSHELYSCEITHKSLPSTLIKSFQRSECQRVD
SEQ ID NO:21. ДНК химерной человеческой-собачьей тяжелой цепи (10D1)
CAGGTGCAGCTGGTGGAAAGCGGCGGCGGCGTGGTGCAGCCGGGCCGCAGCCTGCGCCTGAGCTGCGCGGCGAGCGGCTTTACCTTTAGCAGCTATACCATGCATTGGGTGCGCCAGGCGCCGGGCAAAGGCCTGGAATGGGTGACCTTTATTAGCTATGATGGCAACAACAAATATTATGCGGATAGCGTGAAAGGCCGCTTTACCATTAGCCGCGATAACAGCAAAAACACCCTGTATCTGCAGATGAACAGCCTGCGCGCGGAAGATACCGCGGTGTATTATTGCGCGCGCACCGGCTGGCTGGGCCCGTTTGATTATTGGGGCCAGGGCACCCTGGTGACCGTGAGCAGCGCGAGCACCACCGCGCCGAGCGTGTTTCCGCTGGCGCCGAGCTGCGGCAGCACCAGCGGCAGCACCGTGGCGCTGGCGTGCCTGGTGAGCGGCTATTTTCCGGAACCGGTGACCGTGAGCTGGAACAGCGGCAGCCTGACCAGCGGCGTGCATACCTTTCCGAGCGTGCTGCAGAGCAGCGGCCTGTATAGCCTGAGCAGCATGGTGACCGTGCCGAGCAGCCGCTGGCCGAGCGAAACCTTTACCTGCAACGTGGCGCATCCGGCGAGCAAAACCAAAGTGGATAAACCGGTGCCGAAACGCGAAAACGGCCGCGTGCCGCGCCCGCCGGATTGCCCGAAATGCCCGGCGCCGGAAATGCTGGGCGGCCCGAGCGTGTTTATTTTTCCGCCGAAACCGAAAGATACCCTGCTGATTGCGCGCACCCCGGAAGTGACCTGCGTGGTGGTGGCGCTGGATCCGGAAGATCCGGAAGTGCAGATTAGCTGGTTTGTGGATGGCAAACAGATGCAGACCGCGAAAACCCAGCCGCGCGAAGAACAGTTTGCGGGCACCTATCGCGTGGTGAGCGTGCTGCCGATTGGCCATCAGGATTGGCTGAAAGGCAAACAGTTTACCTGCAAAGTGAACAACAAAGCGCTGCCGAGCCCGATTGAACGCACCATTAGCAAAGCGCGCGGCCAGGCGCATCAGCCGAGCGTGTATGTGCTGCCGCCGAGCCGCGAAGAACTGAGCAAAAACACCGTGAGCCTGACCTGCCTGATTAAAGATTTTTTTCCGCCGGATATTGATGTGGAATGGCAGAGCAACGGCCAGCAGGAACCGGAAAGCAAATATCGCACCACCCCGCCGCAGCTGGATGAAGATGGCAGCTATTTTCTGTATAGCAAACTGAGCGTGGATAAAAGCCGCTGGCAGCGCGGCGATACCTTTATTTGCGCGGTGATGCATGAAGCGCTGCATAACCATTATACCCAGGAAAGCCTGAGCCATAGCCCGGGCAAA
SEQ ID NO:22. Аминокислотная последовательность химерной человеческой-собачьей тяжелой цепи (10D1)
QVQLVESGGGVVQPGRSLRLSCAASGFTFSSYTMHWVRQAPGKGLEWVTFISYDGNNKYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARTGWLGPFDYWGQGTLVTVSSASTTAPSVFPLAPSCGSTSGSTVALACLVSGYFPEPVTVSWNSGSLTSGVHTFPSVLQSSGLYSLSSMVTVPSSRWPSETFTCNVAHPASKTKVDKPVPKRENGRVPRPPDCPKCPAPEMLGGPSVFIFPPKPKDTLLIARTPEVTCVVVALDPEDPEVQISWFVDGKQMQTAKTQPREEQFAGTYRVVSVLPIGHQDWLKGKQFTCKVNNKALPSPIERTISKARGQAHQPSVYVLPPSREELSKNTVSLTCLIKDFFPPDIDVEWQSNGQQEPESKYRTTPPQLDEDGSYFLYSKLSVDKSRWQRGDTFICAVMHEALHNHYTQESLSHSPGK
SEQ ID NO:23. ДНК химерной человеческой-собачьей легкой цепи (10D1)
GAAATTGTGCTGACCCAGAGCCCGGGCACCCTGAGCCTGAGCCCGGGCGAACGCGCGACCCTGAGCTGCCGCGCGAGCCAGAGCGTGGGCAGCAGCTATCTGGCGTGGTATCAGCAGAAACCGGGCCAGGCGCCGCGCCTGCTGATTTATGGCGCGTTTAGCCGCGCGACCGGCATTCCGGATCGCTTTAGCGGCAGCGGCAGCGGCACCGATTTTACCCTGACCATTAGCCGCCTGGAACCGGAAGATTTTGCGGTGTATTATTGCCAGCAGTATGGCAGCAGCCCGTGGACCTTTGGCCAGGGCACCAAAGTGGAAATTAAACGCAACGATGCGCAGCCGGCGGTGTATCTGTTTCAGCCGAGCCCGGATCAGCTGCATACCGGCAGCGCGAGCGTGGTGTGCCTGCTGAACAGCTTTTATCCGAAAGATATTAACGTGAAATGGAAAGTGGATGGCGTGATTCAGGATACCGGCATTCAGGAAAGCGTGACCGAACAGGATAGCAAAGATAGCACCTATAGCCTGAGCAGCACCCTGACCATGAGCAGCACCGAATATCTGAGCCATGAACTGTATAGCTGCGAAATTACCCATAAAAGCCTGCCGAGCACCCTGATTAAAAGCTTTCAGCGCAGCGAATGCCAGCGCGTGGAT
SEQ ID NO:24. Аминокислотная последовательность химерной человеческой-собачьей легкой цепи (10D1)
EIVLTQSPGTLSLSPGERATLSCRASQSVGSSYLAWYQQKPGQAPRLLIYGAFSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQYGSSPWTFGQGTKVEIKRNDAQPAVYLFQPSPDQLHTGSASVVCLLNSFYPKDINVKWKVDGVIQDTGIQESVTEQDSKDSTYSLSSTLTMSSTEYLSHELYSCEITHKSLPSTLIKSFQRSECQRVD
SEQ ID NO:25. ДНК химерной человеческой-собачьей тяжелой цепи (1E2)
CAGGTGCAGCTGGTGGAAAGCGGCGGCGGCGTGGTGCAGCCGGGCCGCAGCCTGCGCCTGAGCTGCGCGGCGAGCGGCTTTACCTTTAGCAGCTATGGCATGCATTGGGTGCGCCAGGCGCCGGGCAAAGGCCTGGAATGGGTGGCGGTGATTTGGTATGATGGCAGCAACAAATATTATGCGGATAGCGTGAAAGGCCGCTTTACCATTAGCCGCGATAACAGCAAAAACACCCTGTATCTGCAGATGAACAGCCTGCGCGCGGAAGATACCGCGGTGTTTTATTGCGCGCGCGCGCCGAACTATATTGGCGCGTTTGATGTGTGGGGCCAGGGCACCATGGTGACCGTGAGCAGCGCGAGCACCACCGCGCCGAGCGTGTTTCCGCTGGCGCCGAGCTGCGGCAGCACCAGCGGCAGCACCGTGGCGCTGGCGTGCCTGGTGAGCGGCTATTTTCCGGAACCGGTGACCGTGAGCTGGAACAGCGGCAGCCTGACCAGCGGCGTGCATACCTTTCCGAGCGTGCTGCAGAGCAGCGGCCTGTATAGCCTGAGCAGCATGGTGACCGTGCCGAGCAGCCGCTGGCCGAGCGAAACCTTTACCTGCAACGTGGCGCATCCGGCGAGCAAAACCAAAGTGGATAAACCGGTGCCGAAACGCGAAAACGGCCGCGTGCCGCGCCCGCCGGATTGCCCGAAATGCCCGGCGCCGGAAATGCTGGGCGGCCCGAGCGTGTTTATTTTTCCGCCGAAACCGAAAGATACCCTGCTGATTGCGCGCACCCCGGAAGTGACCTGCGTGGTGGTGGCGCTGGATCCGGAAGATCCGGAAGTGCAGATTAGCTGGTTTGTGGATGGCAAACAGATGCAGACCGCGAAAACCCAGCCGCGCGAAGAACAGTTTGCGGGCACCTATCGCGTGGTGAGCGTGCTGCCGATTGGCCATCAGGATTGGCTGAAAGGCAAACAGTTTACCTGCAAAGTGAACAACAAAGCGCTGCCGAGCCCGATTGAACGCACCATTAGCAAAGCGCGCGGCCAGGCGCATCAGCCGAGCGTGTATGTGCTGCCGCCGAGCCGCGAAGAACTGAGCAAAAACACCGTGAGCCTGACCTGCCTGATTAAAGATTTTTTTCCGCCGGATATTGATGTGGAATGGCAGAGCAACGGCCAGCAGGAACCGGAAAGCAAATATCGCACCACCCCGCCGCAGCTGGATGAAGATGGCAGCTATTTTCTGTATAGCAAACTGAGCGTGGATAAAAGCCGCTGGCAGCGCGGCGATACCTTTATTTGCGCGGTGATGCATGAAGCGCTGCATAACCATTATACCCAGGAAAGCCTGAGCCATAGCCCGGGCAAA
SEQ ID NO:26. Аминокислотная последовательность химерной человеческой-собачьей тяжелой цепи (1E2)
QVQLVESGGGVVQPGRSLRLSCAASGFTFSSYGMHWVRQAPGKGLEWVAVIWYDGSNKYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVFYCARAPNYIGAFDVWGQGTMVTVSSASTTAPSVFPLAPSCGSTSGSTVALACLVSGYFPEPVTVSWNSGSLTSGVHTFPSVLQSSGLYSLSSMVTVPSSRWPSETFTCNVAHPASKTKVDKPVPKRENGRVPRPPDCPKCPAPEMLGGPSVFIFPPKPKDTLLIARTPEVTCVVVALDPEDPEVQISWFVDGKQMQTAKTQPREEQFAGTYRVVSVLPIGHQDWLKGKQFTCKVNNKALPSPIERTISKARGQAHQPSVYVLPPSREELSKNTVSLTCLIKDFFPPDIDVEWQSNGQQEPESKYRTTPPQLDEDGSYFLYSKLSVDKSRWQRGDTFICAVMHEALHNHYTQESLSHSPGK
SEQ ID NO:27: ДНК химерной человеческой-собачьей легкой цепи (1E2)
GATATTCAGATGACCCAGAGCCCGAGCAGCCTGAGCGCGAGCGTGGGCGATCGCGTGACCATTACCTGCCGCGCGAGCCAGGGCATTAGCAGCTGGCTGGCGTGGTATCAGCAGAAACCGGAAAAAGCGCCGAAAAGCCTGATTTATGCGGCGAGCAGCCTGCAGAGCGGCGTGCCGAGCCGCTTTAGCGGCAGCGGCAGCGGCACCGATTTTACCCTGACCATTAGCAGCCTGCAGCCGGAAGATTTTGCGACCTATTATTGCCAGCAGTATAACAGCTATCCGCCGACCTTTGGCCAGGGCACCAAAGTGGAAATTAAACGCAACGATGCGCAGCCGGCGGTGTATCTGTTTCAGCCGAGCCCGGATCAGCTGCATACCGGCAGCGCGAGCGTGGTGTGCCTGCTGAACAGCTTTTATCCGAAAGATATTAACGTGAAATGGAAAGTGGATGGCGTGATTCAGGATACCGGCATTCAGGAAAGCGTGACCGAACAGGATAGCAAAGATAGCACCTATAGCCTGAGCAGCACCCTGACCATGAGCAGCACCGAATATCTGAGCCATGAACTGTATAGCTGCGAAATTACCCATAAAAGCCTGCCGAGCACCCTGATTAAAAGCTTTCAGCGCAGCGAATGCCAGCGCGTGGAT
SEQ ID NO:28: Аминокислотная последовательность химерной человеческой-собачьей легкой цепи (1E2)
DIQMTQSPSSLSASVGDRVTITCRASQGISSWLAWYQQKPEKAPKSLIYAASSLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYNSYPPTFGQGTKVEIKRNDAQPAVYLFQPSPDQLHTGSASVVCLLNSFYPKDINVKWKVDGVIQDTGIQESVTEQDSKDSTYSLSSTLTMSSTEYLSHELYSCEITHKSLPSTLIKSFQRSECQRVD
SEQ ID NO:29: ДНК химерной мышиной-собачьей тяжелой цепи (3B3)
GAAGTGAAACTGGTGAACAGCGGCGGCGGCCTGGTGCAGCCGGGCAACAGCCTGCGCCTGAGCTGCGCGACCAGCGGCTTTACCTTTACCGATTTTTATATGAGCTGGGTGCGCCAGCCGCCGGGCAAAGCGCTGGAATGGCTGGGCTTTGTGCGCAACCGCGCGAACGGCTATACCACCGAATATAGCGTGAGCGTGAAAGGCCGCTTTATTATTAGCCGCGATAACTTTCAGAGCACCCTGTTTCTGCAGATGAACACCCTGCGCGCGGAAGATAGCGGCACCTATTATTGCGTGCGCGGCCCGGGCGATACCGCGGATTATACCATGGATTATTGGGGCCAGGGCACCAGCGTGACCGTGAGCAGCGCGAGCACCACCGCGCCGAGCGTGTTTCCGCTGGCGCCGAGCTGCGGCAGCACCAGCGGCAGCACCGTGGCGCTGGCGTGCCTGGTGAGCGGCTATTTTCCGGAACCGGTGACCGTGAGCTGGAACAGCGGCAGCCTGACCAGCGGCGTGCATACCTTTCCGAGCGTGCTGCAGAGCAGCGGCCTGTATAGCCTGAGCAGCATGGTGACCGTGCCGAGCAGCCGCTGGCCGAGCGAAACCTTTACCTGCAACGTGGCGCATCCGGCGAGCAAAACCAAAGTGGATAAACCGGTGCCGAAACGCGAAAACGGCCGCGTGCCGCGCCCGCCGGATTGCCCGAAATGCCCGGCGCCGGAAATGCTGGGCGGCCCGAGCGTGTTTATTTTTCCGCCGAAACCGAAAGATACCCTGCTGATTGCGCGCACCCCGGAAGTGACCTGCGTGGTGGTGGCGCTGGATCCGGAAGATCCGGAAGTGCAGATTAGCTGGTTTGTGGATGGCAAACAGATGCAGACCGCGAAAACCCAGCCGCGCGAAGAACAGTTTGCGGGCACCTATCGCGTGGTGAGCGTGCTGCCGATTGGCCATCAGGATTGGCTGAAAGGCAAACAGTTTACCTGCAAAGTGAACAACAAAGCGCTGCCGAGCCCGATTGAACGCACCATTAGCAAAGCGCGCGGCCAGGCGCATCAGCCGAGCGTGTATGTGCTGCCGCCGAGCCGCGAAGAACTGAGCAAAAACACCGTGAGCCTGACCTGCCTGATTAAAGATTTTTTTCCGCCGGATATTGATGTGGAATGGCAGAGCAACGGCCAGCAGGAACCGGAAAGCAAATATCGCACCACCCCGCCGCAGCTGGATGAAGATGGCAGCTATTTTCTGTATAGCAAACTGAGCGTGGATAAAAGCCGCTGGCAGCGCGGCGATACCTTTATTTGCGCGGTGATGCATGAAGCGCTGCATAACCATTATACCCAGGAAAGCCTGAGCCATAGCCCGGGCAAA
SEQ ID NO:30. Аминокислотная последовательность химерной мышиной-собачьей тяжелой цепи (3B3)
EVKLVNSGGGLVQPGNSLRLSCATSGFTFTDFYMSWVRQPPGKALEWLGFVRNRANGYTTEYSVSVKGRFIISRDNFQSTLFLQMNTLRAEDSGTYYCVRGPGDTADYTMDYWGQGTSVTVSSASTTAPSVFPLAPSCGSTSGSTVALACLVSGYFPEPVTVSWNSGSLTSGVHTFPSVLQSSGLYSLSSMVTVPSSRWPSETFTCNVAHPASKTKVDKPVPKRENGRVPRPPDCPKCPAPEMLGGPSVFIFPPKPKDTLLIARTPEVTCVVVALDPEDPEVQISWFVDGKQMQTAKTQPREEQFAGTYRVVSVLPIGHQDWLKGKQFTCKVNNKALPSPIERTISKARGQAHQPSVYVLPPSREELSKNTVSLTCLIKDFFPPDIDVEWQSNGQQEPESKYRTTPPQLDEDGSYFLYSKLSVDKSRWQRGDTFICAVMHEALHNHYTQESLSHSPGK
SEQ ID NO:31: ДНК химерной мышиной-собачьей легкой цепи (3B3)
CAGGCGGTGGTGACCCAGGAAAGCGCGTTTACCACCAGCCCGGGCGGCACCGTGATTCTGACCTGCCGCAGCAGCACCGGCGCGGTGACCACCAACAACTATGCGAACTGGGTGCAGGAAAAACCGGATCATCTGTTTACCGGCCTGATTGGCGGCACCAGCAACCGCGCGCCGGGCGTGCCGGTGCGCTTTAGCGGCAGCCTGATTGGCGATAAAGCGGCGCTGACCATTACCGGCGCGCAGACCGAAGATGATGGCATGTATTTTTGCGCGCTGTGGTATACCACCCATTTTGTGTTTGGCGGCGGCACCAAAGTGACCGTGCTGGGCCAGCCGAAAGCGAGCCCGAGCGTGACCCTGTTTCCGCCGAGCAGCGAAGAACTGGGCGCGAACAAAGCGACCCTGGTGTGCCTGATTAGCGATTTTTATCCGAGCGGCGTGACCGTGGCGTGGAAAGCGGATGGCAGCCCGATTACCCAGGGCGTGGAAACCACCAAACCGAGCAAACAGAGCAACAACAAATATGCGGCGAGCAGCTATCTGAGCCTGACCCCGGATAAATGGAAAAGCCATAGCAGCTTTAGCTGCCTGGTGACCCATGAAGGCAGCACCGTGGAAAAAAAAGTGGCGCCGGCGGAATGCAGC
SEQ ID NO:32: Аминокислотная последовательность химерной мышиной-собачьей легкой цепи (3B3)
QAVVTQESAFTTSPGGTVILTCRSSTGAVTTNNYANWVQEKPDHLFTGLIGGTSNRAPGVPVRFSGSLIGDKAALTITGAQTEDDGMYFCALWYTTHFVFGGGTKVTVLGQPKASPSVTLFPPSSEELGANKATLVCLISDFYPSGVTVAWKADGSPITQGVETTKPSKQSNNKYAASSYLSLTPDKWKSHSSFSCLVTHEGSTVEKKVAPAECS
SEQ ID NO:33: ДНК тяжелой цепи канинизированного 3B10 (VH1)
GAAGTGCAGCTGGTGCAGAGCGGCGCGGAAGTGAAAAAACCGGGCGCGAGCGTGAAAGTGAGCTGCAAAGCGAGCGGCTATACCTTTACCGATTATAACATGGATTGGGTGCGCCAGGCGCCGGGCGCGGGCCTGGATTGGATGGGCAACATTAACCCGAACAGCGAAAGCACCAGCTATAACCAGAAATTTAAAGGCCGCGTGACCCTGACCGCGGATACCAGCACCAGCACCGCGTATATGGAACTGAGCAGCCTGCGCGCGGGCGATATTGCGGTGTATTATTGCACCCGCGATGGCAACCGCTATGATGCGTGGTTTGCGTATTGGGGCCAGGGCACCCTGGTGACCGTGAGCAGCGCGAGCACCACCGCGCCGAGCGTGTTTCCGCTGGCGCCGAGCTGCGGCAGCACCAGCGGCAGCACCGTGGCGCTGGCGTGCCTGGTGAGCGGCTATTTTCCGGAACCGGTGACCGTGAGCTGGAACAGCGGCAGCCTGACCAGCGGCGTGCATACCTTTCCGAGCGTGCTGCAGAGCAGCGGCCTGTATAGCCTGAGCAGCATGGTGACCGTGCCGAGCAGCCGCTGGCCGAGCGAAACCTTTACCTGCAACGTGGCGCATCCGGCGAGCAAAACCAAAGTGGATAAACCGGTGCCGAAACGCGAAAACGGCCGCGTGCCGCGCCCGCCGGATTGCCCGAAATGCCCGGCGCCGGAAATGCTGGGCGGCCCGAGCGTGTTTATTTTTCCGCCGAAACCGAAAGATACCCTGCTGATTGCGCGCACCCCGGAAGTGACCTGCGTGGTGGTGGATCTGGATCCGGAAGATCCGGAAGTGCAGATTAGCTGGTTTGTGGATGGCAAACAGATGCAGACCGCGAAAACCCAGCCGCGCGAAGAACAGTTTAACGGCACCTATCGCGTGGTGAGCGTGCTGCCGATTGGCCATCAGGATTGGCTGAAAGGCAAACAGTTTACCTGCAAAGTGAACAACAAAGCGCTGCCGAGCCCGATTGAACGCACCATTAGCAAAGCGCGCGGCCAGGCGCATCAGCCGAGCGTGTATGTGCTGCCGCCGAGCCGCGAAGAACTGAGCAAAAACACCGTGAGCCTGACCTGCCTGATTAAAGATTTTTTTCCGCCGGATATTGATGTGGAATGGCAGAGCAACGGCCAGCAGGAACCGGAAAGCAAATATCGCACCACCCCGCCGCAGCTGGATGAAGATGGCAGCTATTTTCTGTATAGCAAACTGAGCGTGGATAAAAGCCGCTGGCAGCGCGGCGATACCTTTATTTGCGCGGTGATGCATGAAGCGCTGCATAACCATTATACCCAGGAAAGCCTGAGCCATAGCCCGGGCAAA
SEQ ID NO:34. Аминокислотная последовательность тяжелой цепи канинизированного 3B10 (VH1)
EVQLVQSGAEVKKPGASVKVSCKASGYTFTDYNMDWVRQAPGAGLDWMGNINPNSESTSYNQKFKGRVTLTADTSTSTAYMELSSLRAGDIAVYYCTRDGNRYDAWFAYWGQGTLVTVSSASTTAPSVFPLAPSCGSTSGSTVALACLVSGYFPEPVTVSWNSGSLTSGVHTFPSVLQSSGLYSLSSMVTVPSSRWPSETFTCNVAHPASKTKVDKPVPKRENGRVPRPPDCPKCPAPEMLGGPSVFIFPPKPKDTLLIARTPEVTCVVVDLDPEDPEVQISWFVDGKQMQTAKTQPREEQFNGTYRVVSVLPIGHQDWLKGKQFTCKVNNKALPSPIERTISKARGQAHQPSVYVLPPSREELSKNTVSLTCLIKDFFPPDIDVEWQSNGQQEPESKYRTTPPQLDEDGSYFLYSKLSVDKSRWQRGDTFICAVMHEALHNHYTQESLSHSPGK
SEQ ID NO:35: ДНК тяжелой цепи канинизированного 3B10 (VH2)
GAAGTGCAGCTGGTGCAGAGCGGCGCGGAAGTGAAAAAACCGGGCGCGAGCGTGAAAGTGAGCTGCAAAGCGAGCGGCTATACCTTTACCGATTATAACATGGATTGGGTGCGCCAGGCGCCGGGCGCGAGCCTGGATTGGATTGGCAACATTAACCCGAACAGCGAAAGCACCAGCTATAACCAGAAATTTAAAGGCAAAGCGACCCTGACCGTGGATAAAAGCACCAGCACCGCGTATATGGAACTGAGCAGCCTGCGCGCGGGCGATATTGCGGTGTATTATTGCACCCGCGATGGCAACCGCTATGATGCGTGGTTTGCGTATTGGGGCCAGGGCACCCTGGTGACCGTGAGCAGCGCGAGCACCACCGCGCCGAGCGTGTTTCCGCTGGCGCCGAGCTGCGGCAGCACCAGCGGCAGCACCGTGGCGCTGGCGTGCCTGGTGAGCGGCTATTTTCCGGAACCGGTGACCGTGAGCTGGAACAGCGGCAGCCTGACCAGCGGCGTGCATACCTTTCCGAGCGTGCTGCAGAGCAGCGGCCTGTATAGCCTGAGCAGCATGGTGACCGTGCCGAGCAGCCGCTGGCCGAGCGAAACCTTTACCTGCAACGTGGCGCATCCGGCGAGCAAAACCAAAGTGGATAAACCGGTGCCGAAACGCGAAAACGGCCGCGTGCCGCGCCCGCCGGATTGCCCGAAATGCCCGGCGCCGGAAATGCTGGGCGGCCCGAGCGTGTTTATTTTTCCGCCGAAACCGAAAGATACCCTGCTGATTGCGCGCACCCCGGAAGTGACCTGCGTGGTGGTGGATCTGGATCCGGAAGATCCGGAAGTGCAGATTAGCTGGTTTGTGGATGGCAAACAGATGCAGACCGCGAAAACCCAGCCGCGCGAAGAACAGTTTAACGGCACCTATCGCGTGGTGAGCGTGCTGCCGATTGGCCATCAGGATTGGCTGAAAGGCAAACAGTTTACCTGCAAAGTGAACAACAAAGCGCTGCCGAGCCCGATTGAACGCACCATTAGCAAAGCGCGCGGCCAGGCGCATCAGCCGAGCGTGTATGTGCTGCCGCCGAGCCGCGAAGAACTGAGCAAAAACACCGTGAGCCTGACCTGCCTGATTAAAGATTTTTTTCCGCCGGATATTGATGTGGAATGGCAGAGCAACGGCCAGCAGGAACCGGAAAGCAAATATCGCACCACCCCGCCGCAGCTGGATGAAGATGGCAGCTATTTTCTGTATAGCAAACTGAGCGTGGATAAAAGCCGCTGGCAGCGCGGCGATACCTTTATTTGCGCGGTGATGCATGAAGCGCTGCATAACCATTATACCCAGGAAAGCCTGAGCCATAGCCCGGGCAAA
SEQ ID NO:36: Аминокислотная последовательность тяжелой цепи канинизированного 3B10 (VH2)
EVQLVQSGAEVKKPGASVKVSCKASGYTFTDYNMDWVRQAPGASLDWIGNINPNSESTSYNQKFKGKATLTVDKSTSTAYMELSSLRAGDIAVYYCTRDGNRYDAWFAYWGQGTLVTVSSASTTAPSVFPLAPSCGSTSGSTVALACLVSGYFPEPVTVSWNSGSLTSGVHTFPSVLQSSGLYSLSSMVTVPSSRWPSETFTCNVAHPASKTKVDKPVPKRENGRVPRPPDCPKCPAPEMLGGPSVFIFPPKPKDTLLIARTPEVTCVVVDLDPEDPEVQISWFVDGKQMQTAKTQPREEQFNGTYRVVSVLPIGHQDWLKGKQFTCKVNNKALPSPIERTISKARGQAHQPSVYVLPPSREELSKNTVSLTCLIKDFFPPDIDVEWQSNGQQEPESKYRTTPPQLDEDGSYFLYSKLSVDKSRWQRGDTFICAVMHEALHNHYTQESLSHSPGK
SEQ ID NO:37: ДНК тяжелой цепи канинизированного 3B10 (VH3)
GAAGTGCAGCTGGTGCAGAGCGGCGCGGAAGTGAAAAAACCGGGCGCGAGCGTGAAAGTGAGCTGCAAAGCGAGCGGCTATACCTTTACCGATTATAACATGGATTGGGTGCGCCAGGCGCATGGCGCGAGCCTGGATTGGATTGGCAACATTAACCCGAACAGCGAAAGCACCAGCTATAACCAGAAATTTAAAGGCAAAGCGACCCTGACCGTGGATAAAAGCACCAGCACCGCGTATATGGAACTGAGCAGCCTGCGCGCGGGCGATATTGCGGTGTATTATTGCACCCGCGATGGCAACCGCTATGATGCGTGGTTTGCGTATTGGGGCCAGGGCACCCTGGTGACCGTGAGCAGCGCGAGCACCACCGCGCCGAGCGTGTTTCCGCTGGCGCCGAGCTGCGGCAGCACCAGCGGCAGCACCGTGGCGCTGGCGTGCCTGGTGAGCGGCTATTTTCCGGAACCGGTGACCGTGAGCTGGAACAGCGGCAGCCTGACCAGCGGCGTGCATACCTTTCCGAGCGTGCTGCAGAGCAGCGGCCTGTATAGCCTGAGCAGCATGGTGACCGTGCCGAGCAGCCGCTGGCCGAGCGAAACCTTTACCTGCAACGTGGCGCATCCGGCGAGCAAAACCAAAGTGGATAAACCGGTGCCGAAACGCGAAAACGGCCGCGTGCCGCGCCCGCCGGATTGCCCGAAATGCCCGGCGCCGGAAATGCTGGGCGGCCCGAGCGTGTTTATTTTTCCGCCGAAACCGAAAGATACCCTGCTGATTGCGCGCACCCCGGAAGTGACCTGCGTGGTGGTGGATCTGGATCCGGAAGATCCGGAAGTGCAGATTAGCTGGTTTGTGGATGGCAAACAGATGCAGACCGCGAAAACCCAGCCGCGCGAAGAACAGTTTAACGGCACCTATCGCGTGGTGAGCGTGCTGCCGATTGGCCATCAGGATTGGCTGAAAGGCAAACAGTTTACCTGCAAAGTGAACAACAAAGCGCTGCCGAGCCCGATTGAACGCACCATTAGCAAAGCGCGCGGCCAGGCGCATCAGCCGAGCGTGTATGTGCTGCCGCCGAGCCGCGAAGAACTGAGCAAAAACACCGTGAGCCTGACCTGCCTGATTAAAGATTTTTTTCCGCCGGATATTGATGTGGAATGGCAGAGCAACGGCCAGCAGGAACCGGAAAGCAAATATCGCACCACCCCGCCGCAGCTGGATGAAGATGGCAGCTATTTTCTGTATAGCAAACTGAGCGTGGATAAAAGCCGCTGGCAGCGCGGCGATACCTTTATTTGCGCGGTGATGCATGAAGCGCTGCATAACCATTATACCCAGGAAAGCCTGAGCCATAGCCCGGGCAAA
SEQ ID NO:38. Аминокислотная последовательность тяжелой цепи канинизированного 3B10 (VH3)
EVQLVQSGAEVKKPGASVKVSCKASGYTFTDYNMDWVRQAHGASLDWIGNINPNSESTSYNQKFKGKATLTVDKSTSTAYMELSSLRAGDIAVYYCTRDGNRYDAWFAYWGQGTLVTVSSASTTAPSVFPLAPSCGSTSGSTVALACLVSGYFPEPVTVSWNSGSLTSGVHTFPSVLQSSGLYSLSSMVTVPSSRWPSETFTCNVAHPASKTKVDKPVPKRENGRVPRPPDCPKCPAPEMLGGPSVFIFPPKPKDTLLIARTPEVTCVVVDLDPEDPEVQISWFVDGKQMQTAKTQPREEQFNGTYRVVSVLPIGHQDWLKGKQFTCKVNNKALPSPIERTISKARGQAHQPSVYVLPPSREELSKNTVSLTCLIKDFFPPDIDVEWQSNGQQEPESKYRTTPPQLDEDGSYFLYSKLSVDKSRWQRGDTFICAVMHEALHNHYTQESLSHSPGK
SEQ ID NO:39: ДНК тяжелой цепи канинизированного 3B10 (VH4)
GAAGTGCAGCTGCAGCAGAGCGGCGCGGAAGTGAAAAAACCGGGCGCGAGCGTGAAAGTGAGCTGCAAAGCGAGCGGCTATACCTTTACCGATTATAACATGGATTGGGTGCGCCAGGCGCCGGGCGCGAGCCTGGATTGGATTGGCAACATTAACCCGAACAGCGAAAGCACCAGCTATAACCAGAAATTTAAAGGCAAAGCGACCCTGACCGTGGATAAAAGCACCAGCACCGCGTATATGGAACTGCGCAGCCTGACCGCGGGCGATATTGCGGTGTATTATTGCACCCGCGATGGCAACCGCTATGATGCGTGGTTTGCGTATTGGGGCCAGGGCACCCTGGTGACCGTGAGCAGCGCGAGCACCACCGCGCCGAGCGTGTTTCCGCTGGCGCCGAGCTGCGGCAGCACCAGCGGCAGCACCGTGGCGCTGGCGTGCCTGGTGAGCGGCTATTTTCCGGAACCGGTGACCGTGAGCTGGAACAGCGGCAGCCTGACCAGCGGCGTGCATACCTTTCCGAGCGTGCTGCAGAGCAGCGGCCTGTATAGCCTGAGCAGCATGGTGACCGTGCCGAGCAGCCGCTGGCCGAGCGAAACCTTTACCTGCAACGTGGCGCATCCGGCGAGCAAAACCAAAGTGGATAAACCGGTGCCGAAACGCGAAAACGGCCGCGTGCCGCGCCCGCCGGATTGCCCGAAATGCCCGGCGCCGGAAATGCTGGGCGGCCCGAGCGTGTTTATTTTTCCGCCGAAACCGAAAGATACCCTGCTGATTGCGCGCACCCCGGAAGTGACCTGCGTGGTGGTGGATCTGGATCCGGAAGATCCGGAAGTGCAGATTAGCTGGTTTGTGGATGGCAAACAGATGCAGACCGCGAAAACCCAGCCGCGCGAAGAACAGTTTAACGGCACCTATCGCGTGGTGAGCGTGCTGCCGATTGGCCATCAGGATTGGCTGAAAGGCAAACAGTTTACCTGCAAAGTGAACAACAAAGCGCTGCCGAGCCCGATTGAACGCACCATTAGCAAAGCGCGCGGCCAGGCGCATCAGCCGAGCGTGTATGTGCTGCCGCCGAGCCGCGAAGAACTGAGCAAAAACACCGTGAGCCTGACCTGCCTGATTAAAGATTTTTTTCCGCCGGATATTGATGTGGAATGGCAGAGCAACGGCCAGCAGGAACCGGAAAGCAAATATCGCACCACCCCGCCGCAGCTGGATGAAGATGGCAGCTATTTTCTGTATAGCAAACTGAGCGTGGATAAAAGCCGCTGGCAGCGCGGCGATACCTTTATTTGCGCGGTGATGCATGAAGCGCTGCATAACCATTATACCCAGGAAAGCCTGAGCCATAGCCCGGGCAAA
SEQ ID NO:40: Аминокислотная последовательность тяжелой цепи канинизированного 3B10 (VH4)
EVQLQQSGAEVKKPGASVKVSCKASGYTFTDYNMDWVRQAPGASLDWIGNINPNSESTSYNQKFKGKATLTVDKSTSTAYMELRSLTAGDIAVYYCTRDGNRYDAWFAYWGQGTLVTVSSASTTAPSVFPLAPSCGSTSGSTVALACLVSGYFPEPVTVSWNSGSLTSGVHTFPSVLQSSGLYSLSSMVTVPSSRWPSETFTCNVAHPASKTKVDKPVPKRENGRVPRPPDCPKCPAPEMLGGPSVFIFPPKPKDTLLIARTPEVTCVVVDLDPEDPEVQISWFVDGKQMQTAKTQPREEQFNGTYRVVSVLPIGHQDWLKGKQFTCKVNNKALPSPIERTISKARGQAHQPSVYVLPPSREELSKNTVSLTCLIKDFFPPDIDVEWQSNGQQEPESKYRTTPPQLDEDGSYFLYSKLSVDKSRWQRGDTFICAVMHEALHNHYTQESLSHSPGK
SEQ ID NO:41: ДНК легкой цепи канинизированного 3B10 (VL1)
GATATTGTGATGACCCAGACCCCGCTGAGCCTGAGCGTGAGCCCGGGCGAACCGGCGAGCATTAGCTGCAGCGCGAGCAGCAGCGTGACCTATATGCATTGGTTTCGCCATAAACCGGGCCAGAGCCCGCAGAGCCTGATTTATAGCACCAGCATTCTGGCGAGCGGCGTGCCGGATCGCTTTAGCGGCAGCGGCAGCGGCACCGATTTTACCCTGAAAATTAGCCGCGTGGAAGCGGATGATGCGGGCGTGTATTATTGCCAGCAGCGCACCAGCTATCCGCTGACCTTTGGCACCGGCACCAAACTGGAACTGAAACGCAACGATGCGCAGCCGGCGGTGTATCTGTTTCAGCCGAGCCCGGATCAGCTGCATACCGGCAGCGCGAGCGTGGTGTGCCTGCTGAACAGCTTTTATCCGAAAGATATTAACGTGAAATGGAAAGTGGATGGCGTGATTCAGGATACCGGCATTCAGGAAAGCGTGACCGAACAGGATAGCAAAGATAGCACCTATAGCCTGAGCAGCACCCTGACCATGAGCAGCACCGAATATCTGAGCCATGAACTGTATAGCTGCGAAATTACCCATAAAAGCCTGCCGAGCACCCTGATTAAAAGCTTTCAGCGCAGCGAATGCCAGCGCGTGGAT
SEQ ID NO:42: Аминокислотная последовательность легкой цепи канинизированного 3B10 (VL1)
DIVMTQTPLSLSVSPGEPASISCSASSSVTYMHWFRHKPGQSPQSLIYSTSILASGVPDRFSGSGSGTDFTLKISRVEADDAGVYYCQQRTSYPLTFGTGTKLELKRNDAQPAVYLFQPSPDQLHTGSASVVCLLNSFYPKDINVKWKVDGVIQDTGIQESVTEQDSKDSTYSLSSTLTMSSTEYLSHELYSCEITHKSLPSTLIKSFQRSECQRVD
SEQ ID NO:43: ДНК легкой цепи канинизированного 3B10 (VL2)
CAGATTGTGATGACCCAGACCCCGCTGAGCCTGAGCGTGAGCCCGGGCGAACCGGCGAGCATTAGCTGCAGCGCGAGCAGCAGCGTGACCTATATGCATTGGTTTCAGCAGAAACCGGGCCAGAGCCCGCAGAGCCTGATTTATAGCACCAGCATTCTGGCGAGCGGCGTGCCGGATCGCTTTAGCGGCAGCGGCAGCGGCACCGATTTTACCCTGAAAATTAGCCGCGTGGAAGCGGATGATGCGGGCGTGTATTATTGCCAGCAGCGCACCAGCTATCCGCTGACCTTTGGCACCGGCACCAAACTGGAACTGAAACGCAACGATGCGCAGCCGGCGGTGTATCTGTTTCAGCCGAGCCCGGATCAGCTGCATACCGGCAGCGCGAGCGTGGTGTGCCTGCTGAACAGCTTTTATCCGAAAGATATTAACGTGAAATGGAAAGTGGATGGCGTGATTCAGGATACCGGCATTCAGGAAAGCGTGACCGAACAGGATAGCAAAGATAGCACCTATAGCCTGAGCAGCACCCTGACCATGAGCAGCACCGAATATCTGAGCCATGAACTGTATAGCTGCGAAATTACCCATAAAAGCCTGCCGAGCACCCTGATTAAAAGCTTTCAGCGCAGCGAATGCCAGCGCGTGGAT
SEQ ID NO:44: Аминокислотная последовательность легкой цепи канинизированного 3B10 (VL2)
QIVMTQTPLSLSVSPGEPASISCSASSSVTYMHWFQQKPGQSPQSLIYSTSILASGVPDRFSGSGSGTDFTLKISRVEADDAGVYYCQQRTSYPLTFGTGTKLELKRNDAQPAVYLFQPSPDQLHTGSASVVCLLNSFYPKDINVKWKVDGVIQDTGIQESVTEQDSKDSTYSLSSTLTMSSTEYLSHELYSCEITHKSLPSTLIKSFQRSECQRVD
SEQ ID NO:45: ДНК легкой цепи канинизированного 3B10 (VL3)
CAGATTGTGCTGACCCAGACCCCGCTGAGCCTGAGCGTGAGCCCGGGCGAACCGGCGAGCATTAGCTGCAGCGCGAGCAGCAGCGTGACCTATATGCATTGGTTTCAGCAGAAACCGGGCCAGAGCCCGAAAAGCTGGATTTATAGCACCAGCATTCTGGCGAGCGGCGTGCCGGATCGCTTTAGCGGCAGCGGCAGCGGCACCGATTTTACCCTGAAAATTAGCCGCGTGGAAGCGGATGATGCGGGCGTGTATTATTGCCAGCAGCGCACCAGCTATCCGCTGACCTTTGGCACCGGCACCAAACTGGAACTGAAACGCAACGATGCGCAGCCGGCGGTGTATCTGTTTCAGCCGAGCCCGGATCAGCTGCATACCGGCAGCGCGAGCGTGGTGTGCCTGCTGAACAGCTTTTATCCGAAAGATATTAACGTGAAATGGAAAGTGGATGGCGTGATTCAGGATACCGGCATTCAGGAAAGCGTGACCGAACAGGATAGCAAAGATAGCACCTATAGCCTGAGCAGCACCCTGACCATGAGCAGCACCGAATATCTGAGCCATGAACTGTATAGCTGCGAAATTACCCATAAAAGCCTGCCGAGCACCCTGATTAAAAGCTTTCAGCGCAGCGAATGCCAGCGCGTGGAT
SEQ ID NO:46: Аминокислотная последовательность легкой цепи канинизированного 3B10 (VL3)
QIVLTQTPLSLSVSPGEPASISCSASSSVTYMHWFQQKPGQSPKSWIYSTSILASGVPDRFSGSGSGTDFTLKISRVEADDAGVYYCQQRTSYPLTFGTGTKLELKRNDAQPAVYLFQPSPDQLHTGSASVVCLLNSFYPKDINVKWKVDGVIQDTGIQESVTEQDSKDSTYSLSSTLTMSSTEYLSHELYSCEITHKSLPSTLIKSFQRSECQRVD
SEQ ID NO:59: ДНК тяжелой цепи IgGBm канинизированного 3B10 (VH1)
GAAGTGCAGCTGGTGCAGAGCGGCGCGGAAGTGAAAAAACCGGGCGCGAGCGTGAAAGTGAGCTGCAAAGCGAGCGGCTATACCTTTACCGATTATAACATGGATTGGGTGCGCCAGGCGCCGGGCGCGGGCCTGGATTGGATGGGCAACATTAACCCGAACAGCGAAAGCACCAGCTATAACCAGAAATTTAAAGGCCGCGTGACCCTGACCGCGGATACCAGCACCAGCACCGCGTATATGGAACTGAGCAGCCTGCGCGCGGGCGATATTGCGGTGTATTATTGCACCCGCGATGGCAACCGCTATGATGCGTGGTTTGCGTATTGGGGCCAGGGCACCCTGGTGACCGTGAGCAGCgcgagcaccaccgcgccgagcgtgtttccgctggcgccgagctgcggcagcaccagcggcagcaccgtggcgctggcgtgcctggtgagcggctattttccggaaccggtgaccgtgagctggaacagcggcagcctgaccagcggcgtgcatacctttccgagcgtgctgcagagcagcggcctgtatagcctgagcagcatggtgaccgtgccgagcagccgctggccgagcgaaacctttacctgcaacgtggcgcatccggcgagcaaaaccaaagtggataaaccggtgccgaaacgcgaaaacggccgcgtgccgcgcccgccggattgcccgaaatgcccggcgccggaaatgctgggcggcccgagcgtgtttatttttccgccgaaaccgaaagataccctgctgattgcgcgcaccccggaagtgacctgcgtggtggtggcgctggatccggaagatccggaagtgcagattagctggtttgtggatggcaaacagatgcagaccgcgaaaacccagccgcgcgaagaacagtttgccggcacctatcgcgtggtgagcgtgctgccgattggccatcaggattggctgaaaggcaaacagtttacctgcaaagtgaacaacaaagcgctgccgagcccgattgaacgcaccattagcaaagcgcgcggccaggcgcatcagccgagcgtgtatgtgctgccgccgagccgcgaagaactgagcaaaaacaccgtgagcctgacctgcctgattaaagatttttttccgccggatattgatgtggaatggcagagcaacggccagcaggaaccggaaagcaaatatcgcaccaccccgccgcagctggatgaagatggcagctattttctgtatagcaaactgagcgtggataaaagccgctggcagcgcggcgatacctttatttgcgcggtgatgcatgaagcgctgcataaccattatacccaggaaagcctgagccatagcccgggcaaa
SEQ ID NO:60: Аминокислотная последовательность тяжелой цепи IgGBm канинизированного 3B10 (VH1) EVQLVQSGAEVKKPGASVKVSCKASGYTFTDYNMDWVRQAPGAGLDWMGNINPNSESTSYNQKFKGRVTLTADTSTSTAYMELSSLRAGDIAVYYCTRDGNRYDAWFAYWGQGTLVTVSSasttapsvfplapscgstsgstvalaclvsgyfpepvtvswnsgsltsgvhtfpsvlqssglyslssmvtvpssrwpsetftcnvahpasktkvdkpvpkrengrvprppdcpkcpapemlggpsvfifppkpkdtlliartpevtcvvvAldpedpevqiswfvdgkqmqtaktqpreeqfAgtyrvvsvlpighqdwlkgkqftckvnnkalpspiertiskargqahqpsvyvlppsreelskntvsltclikdffppdidvewqsngqqepeskyrttppqldedgsyflysklsvdksrwqrgdtficavmhealhnhytqeslshspgk
SEQ ID NO:61: ДНК тяжелой цепи IgGBm канинизированного 3B10 (VH2)
GAAGTGCAGCTGGTGCAGAGCGGCGCGGAAGTGAAAAAACCGGGCGCGAGCGTGAAAGTGAGCTGCAAAGCGAGCGGCTATACCTTTACCGATTATAACATGGATTGGGTGCGCCAGGCGCCGGGCGCGAGCCTGGATTGGATTGGCAACATTAACCCGAACAGCGAAAGCACCAGCTATAACCAGAAATTTAAAGGCAAAGCGACCCTGACCGTGGATAAAAGCACCAGCACCGCGTATATGGAACTGAGCAGCCTGCGCGCGGGCGATATTGCGGTGTATTATTGCACCCGCGATGGCAACCGCTATGATGCGTGGTTTGCGTATTGGGGCCAGGGCACCCTGGTGACCGTGAGCAGCgcgagcaccaccgcgccgagcgtgtttccgctggcgccgagctgcggcagcaccagcggcagcaccgtggcgctggcgtgcctggtgagcggctattttccggaaccggtgaccgtgagctggaacagcggcagcctgaccagcggcgtgcatacctttccgagcgtgctgcagagcagcggcctgtatagcctgagcagcatggtgaccgtgccgagcagccgctggccgagcgaaacctttacctgcaacgtggcgcatccggcgagcaaaaccaaagtggataaaccggtgccgaaacgcgaaaacggccgcgtgccgcgcccgccggattgcccgaaatgcccggcgccggaaatgctgggcggcccgagcgtgtttatttttccgccgaaaccgaaagataccctgctgattgcgcgcaccccggaagtgacctgcgtggtggtggcgctggatccggaagatccggaagtgcagattagctggtttgtggatggcaaacagatgcagaccgcgaaaacccagccgcgcgaagaacagtttgccggcacctatcgcgtggtgagcgtgctgccgattggccatcaggattggctgaaaggcaaacagtttacctgcaaagtgaacaacaaagcgctgccgagcccgattgaacgcaccattagcaaagcgcgcggccaggcgcatcagccgagcgtgtatgtgctgccgccgagccgcgaagaactgagcaaaaacaccgtgagcctgacctgcctgattaaagatttttttccgccggatattgatgtggaatggcagagcaacggccagcaggaaccggaaagcaaatatcgcaccaccccgccgcagctggatgaagatggcagctattttctgtatagcaaactgagcgtggataaaagccgctggcagcgcggcgatacctttatttgcgcggtgatgcatgaagcgctgcataaccattatacccaggaaagcctgagccatagcccgggcaaa
SEQ ID NO:62: Аминокислотная последовательность тяжелой цепи IgGBm канинизированного 3B10 (VH2)
EVQLVQSGAEVKKPGASVKVSCKASGYTFTDYNMDWVRQAPGASLDWIGNINPNSESTSYNQKFKGKATLTVDKSTSTAYMELSSLRAGDIAVYYCTRDGNRYDAWFAYWGQGTLVTVSSasttapsvfplapscgstsgstvalaclvsgyfpepvtvswnsgsltsgvhtfpsvlqssglyslssmvtvpssrwpsetftcnvahpasktkvdkpvpkrengrvprppdcpkcpapemlggpsvfifppkpkdtlliartpevtcvvvAldpedpevqiswfvdgkqmqtaktqpreeqfAgtyrvvsvlpighqdwlkgkqftckvnnkalpspiertiskargqahqpsvyvlppsreelskntvsltclikdffppdidvewqsngqqepeskyrttppqldedgsyflysklsvdksrwqrgdtficavmhealhnhytqeslshspgk
SEQ ID NO:63: ДНК тяжелой цепи IgGBm канинизированного 3B10 (VH3)
GAAGTGCAGCTGGTGCAGAGCGGCGCGGAAGTGAAAAAACCGGGCGCGAGCGTGAAAGTGAGCTGCAAAGCGAGCGGCTATACCTTTACCGATTATAACATGGATTGGGTGCGCCAGGCGCATGGCGCGAGCCTGGATTGGATTGGCAACATTAACCCGAACAGCGAAAGCACCAGCTATAACCAGAAATTTAAAGGCAAAGCGACCCTGACCGTGGATAAAAGCACCAGCACCGCGTATATGGAACTGAGCAGCCTGCGCGCGGGCGATATTGCGGTGTATTATTGCACCCGCGATGGCAACCGCTATGATGCGTGGTTTGCGTATTGGGGCCAGGGCACCCTGGTGACCGTGAGCAGCgcgagcaccaccgcgccgagcgtgtttccgctggcgccgagctgcggcagcaccagcggcagcaccgtggcgctggcgtgcctggtgagcggctattttccggaaccggtgaccgtgagctggaacagcggcagcctgaccagcggcgtgcatacctttccgagcgtgctgcagagcagcggcctgtatagcctgagcagcatggtgaccgtgccgagcagccgctggccgagcgaaacctttacctgcaacgtggcgcatccggcgagcaaaaccaaagtggataaaccggtgccgaaacgcgaaaacggccgcgtgccgcgcccgccggattgcccgaaatgcccggcgccggaaatgctgggcggcccgagcgtgtttatttttccgccgaaaccgaaagataccctgctgattgcgcgcaccccggaagtgacctgcgtggtggtggcgctggatccggaagatccggaagtgcagattagctggtttgtggatggcaaacagatgcagaccgcgaaaacccagccgcgcgaagaacagtttgccggcacctatcgcgtggtgagcgtgctgccgattggccatcaggattggctgaaaggcaaacagtttacctgcaaagtgaacaacaaagcgctgccgagcccgattgaacgcaccattagcaaagcgcgcggccaggcgcatcagccgagcgtgtatgtgctgccgccgagccgcgaagaactgagcaaaaacaccgtgagcctgacctgcctgattaaagatttttttccgccggatattgatgtggaatggcagagcaacggccagcaggaaccggaaagcaaatatcgcaccaccccgccgcagctggatgaagatggcagctattttctgtatagcaaactgagcgtggataaaagccgctggcagcgcggcgatacctttatttgcgcggtgatgcatgaagcgctgcataaccattatacccaggaaagcctgagccatagcccgggcaaa
SEQ ID NO:64: Аминокислотная последовательность тяжелой цепи IgGBm канинизированного 3B10 (VH3)
EVQLVQSGAEVKKPGASVKVSCKASGYTFTDYNMDWVRQAHGASLDWIGNINPNSESTSYNQKFKGKATLTVDKSTSTAYMELSSLRAGDIAVYYCTRDGNRYDAWFAYWGQGTLVTVSSasttapsvfplapscgstsgstvalaclvsgyfpepvtvswnsgsltsgvhtfpsvlqssglyslssmvtvpssrwpsetftcnvahpasktkvdkpvpkrengrvprppdcpkcpapemlggpsvfifppkpkdtlliartpevtcvvvAldpedpevqiswfvdgkqmqtaktqpreeqfAgtyrvvsvlpighqdwlkgkqftckvnnkalpspiertiskargqahqpsvyvlppsreelskntvsltclikdffppdidvewqsngqqepeskyrttppqldedgsyflysklsvdksrwqrgdtficavmhealhnhytqeslshspgk
SEQ ID NO:65: ДНК тяжелой цепи IgGBm канинизированного 3B10 (VH4)
GAAGTGCAGCTGCAGCAGAGCGGCGCGGAAGTGAAAAAACCGGGCGCGAGCGTGAAAGTGAGCTGCAAAGCGAGCGGCTATACCTTTACCGATTATAACATGGATTGGGTGCGCCAGGCGCCGGGCGCGAGCCTGGATTGGATTGGCAACATTAACCCGAACAGCGAAAGCACCAGCTATAACCAGAAATTTAAAGGCAAAGCGACCCTGACCGTGGATAAAAGCACCAGCACCGCGTATATGGAACTGCGCAGCCTGACCGCGGGCGATATTGCGGTGTATTATTGCACCCGCGATGGCAACCGCTATGATGCGTGGTTTGCGTATTGGGGCCAGGGCACCCTGGTGACCGTGAGCAGCgcgagcaccaccgcgccgagcgtgtttccgctggcgccgagctgcggcagcaccagcggcagcaccgtggcgctggcgtgcctggtgagcggctattttccggaaccggtgaccgtgagctggaacagcggcagcctgaccagcggcgtgcatacctttccgagcgtgctgcagagcagcggcctgtatagcctgagcagcatggtgaccgtgccgagcagccgctggccgagcgaaacctttacctgcaacgtggcgcatccggcgagcaaaaccaaagtggataaaccggtgccgaaacgcgaaaacggccgcgtgccgcgcccgccggattgcccgaaatgcccggcgccggaaatgctgggcggcccgagcgtgtttatttttccgccgaaaccgaaagataccctgctgattgcgcgcaccccggaagtgacctgcgtggtggtggcgctggatccggaagatccggaagtgcagattagctggtttgtggatggcaaacagatgcagaccgcgaaaacccagccgcgcgaagaacagtttgccggcacctatcgcgtggtgagcgtgctgccgattggccatcaggattggctgaaaggcaaacagtttacctgcaaagtgaacaacaaagcgctgccgagcccgattgaacgcaccattagcaaagcgcgcggccaggcgcatcagccgagcgtgtatgtgctgccgccgagccgcgaagaactgagcaaaaacaccgtgagcctgacctgcctgattaaagatttttttccgccggatattgatgtggaatggcagagcaacggccagcaggaaccggaaagcaaatatcgcaccaccccgccgcagctggatgaagatggcagctattttctgtatagcaaactgagcgtggataaaagccgctggcagcgcggcgatacctttatttgcgcggtgatgcatgaagcgctgcataaccattatacccaggaaagcctgagccatagcccgggcaaa
SEQ ID NO:66: Аминокислотная последовательность тяжелой цепи IgGBm канинизированного 3B10 (VH4)
EVQLQQSGAEVKKPGASVKVSCKASGYTFTDYNMDWVRQAPGASLDWIGNINPNSESTSYNQKFKGKATLTVDKSTSTAYMELRSLTAGDIAVYYCTRDGNRYDAWFAYWGQGTLVTVSSasttapsvfplapscgstsgstvalaclvsgyfpepvtvswnsgsltsgvhtfpsvlqssglyslssmvtvpssrwpsetftcnvahpasktkvdkpvpkrengrvprppdcpkcpapemlggpsvfifppkpkdtlliartpevtcvvvAldpedpevqiswfvdgkqmqtaktqpreeqfAgtyrvvsvlpighqdwlkgkqftckvnnkalpspiertiskargqahqpsvyvlppsreelskntvsltclikdffppdidvewqsngqqepeskyrttppqldedgsyflysklsvdksrwqrgdtficavmhealhnhytqeslshspgk
SEQ ID NO:67: Последовательность н. собачьего CTLA-4 (Эталонная последовательность в NCBI: NP_001003106).
ATGGCGGGCTTTGGCTTTCGCCGCCATGGCGCGCAGCCGGATCTGGCGAGCCGCACCTGGCCGTGCACCGCGCTGTTTAGCCTGCTGTTTATTCCGGTGTTTAGCAAAGGCATGCATGTGGCGCAGCCGGCGGTGGTGCTGGCGAGCAGCCGCGGCGTGGCGAGCTTTGTGTGCGAATATGGCAGCAGCGGCAACGCGGCGGAAGTGCGCGTGACCGTGCTGCGCCAGGCGGGCAGCCAGATGACCGAAGTGTGCGCGGCGACCTATACCGTGGAAGATGAACTGGCGTTTCTGGATGATAGCACCTGCACCGGCACCAGCAGCGGCAACAAAGTGAACCTGACCATTCAGGGCCTGCGCGCGATGGATACCGGCCTGTATATTTGCAAAGTGGAACTGATGTATCCGCCGCCGTATTATGTGGGCATGGGCAACGGCACCCAGATTTATGTGATTGATCCGGAACCGTGCCCGGATAGCGATTTTCTGCTGTGGATTCTGGCGGCGGTGAGCAGCGGCCTGTTTTTTTATAGCTTTCTGATTACCGCGGTGAGCCTGAGCAAAATGCTGAAAAAACGCAGCCCGCTGACCACCGGCGTGTATGTGAAAATGCCGCCGACCGAACCGGAATGCGAAAAACAGTTTCAGCCGTATTTTATTCCGATTAAC
SEQ ID NO:68: Последовательность ак собачьего CTLA-4 (Эталонная последовательность в NCBI: NP_001003106).
MAGFGFRRHGAQPDLASRTWPCTALFSLLFIPVFSKGMHVAQPAVVLASSRGVASFVCEYGSSGNAAEVRVTVLRQAGSQMTEVCAATYTVEDELAFLDDSTCTGTSSGNKVNLTIQGLRAMDTGLYICKVELMYPPPYYVGMGNGTQIYVIDPEPCPDSDFLLWILAAVSSGLFFYSFLITAVSLSKMLKKRSPLTTGVYVKMPPTEPECEKQFQPYFIPIN
SEQ ID NO:69: Генетически модифицированная область cFc собачьего IgG B (из U.S. 10106107 B2)
lggpsvfifppkpkdtlliartpevtcvvvAldpedpevqiswfvdgkqmqtaktqpreeqfAgtyrvvsvlpighqdwlkgkqftckvnnkalpspiertiskargqahqpsvyvlppsreelskntvsltclikdffppdidvewqsngqqepeskyrttppqldedgsyflysklsvdksrwqrgdtficavmhealhnhytqeslshspgk
Во всех из предшествующих нуклеотидных последовательностей вариабельные области выделены жирным шрифтом, в то время как в соответствующих аминокислотных последовательностях последовательности для вариабельных областей выделены жирным шрифтом, и CDR выделены как подчеркиванием, так и жирным шрифтом.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ИНТЕРВЕТ ИНТЕРНЭШНЛ Б.В.
МОРСИ, Мохамад
ЧЖАН, Юаньчжэн
ТАРПИ, Иан
<120> Канинизированные антитела против человеческого CTLA-4
<130> 24721-US-PCT
<150> 62/874287
<151> 2019-07-15
<160> 69
<170> PatentIn версии 3.5
<210> 1
<211> 1362
<212> ДНК
<213> Искусственная последовательность
<220>
<223> мышиная-собачья химера
<400> 1
gaagtgcagc tgcagcagtt tggcgcggaa ctggtgaaac cgggcgcgag cgtgaaaatg 60
agctgcaaag cgagcggcta tacctttacc gattataaca tggattgggt gcgccagagc 120
ggcaaaagcc tggaatggat tggcaacatt aacccgaaca gcgaaagcac cagctataac 180
cagaaattta aaggcaaagc gaccctgacc gtggataaaa gcagcagcac cgcgtatatg 240
gaactgcgca gcctgaccag cgatgatacc gcggtgtatt attgcacccg cgatggcaac 300
cgctatgatg cgtggtttgc gtattggggc cagggcaccc tggtgaccgt gagcagcgcg 360
agcaccaccg cgccgagcgt gtttccgctg gcgccgagct gcggcagcac cagcggcagc 420
accgtggcgc tggcgtgcct ggtgagcggc tattttccgg aaccggtgac cgtgagctgg 480
aacagcggca gcctgaccag cggcgtgcat acctttccga gcgtgctgca gagcagcggc 540
ctgtatagcc tgagcagcat ggtgaccgtg ccgagcagcc gctggccgag cgaaaccttt 600
acctgcaacg tggcgcatcc ggcgagcaaa accaaagtgg ataaaccggt gccgaaacgc 660
gaaaacggcc gcgtgccgcg cccgccggat tgcccgaaat gcccggcgcc ggaaatgctg 720
ggcggcccga gcgtgtttat ttttccgccg aaaccgaaag ataccctgct gattgcgcgc 780
accccggaag tgacctgcgt ggtggtggcg ctggatccgg aagatccgga agtgcagatt 840
agctggtttg tggatggcaa acagatgcag accgcgaaaa cccagccgcg cgaagaacag 900
tttgcgggca cctatcgcgt ggtgagcgtg ctgccgattg gccatcagga ttggctgaaa 960
ggcaaacagt ttacctgcaa agtgaacaac aaagcgctgc cgagcccgat tgaacgcacc 1020
attagcaaag cgcgcggcca ggcgcatcag ccgagcgtgt atgtgctgcc gccgagccgc 1080
gaagaactga gcaaaaacac cgtgagcctg acctgcctga ttaaagattt ttttccgccg 1140
gatattgatg tggaatggca gagcaacggc cagcaggaac cggaaagcaa atatcgcacc 1200
accccgccgc agctggatga agatggcagc tattttctgt atagcaaact gagcgtggat 1260
aaaagccgct ggcagcgcgg cgataccttt atttgcgcgg tgatgcatga agcgctgcat 1320
aaccattata cccaggaaag cctgagccat agcccgggca aa 1362
<210> 2
<211> 454
<212> PRT
<213> Искусственная последовательность
<220>
<223> мышиная-собачья химера
<400> 2
Glu Val Gln Leu Gln Gln Phe Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met Asp Trp Val Arg Gln Ser Gly Lys Ser Leu Glu Trp Ile Gly
35 40 45
Asn Ile Asn Pro Asn Ser Glu Ser Thr Ser Tyr Asn Gln Lys Phe Lys
50 55 60
Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr Met
65 70 75 80
Glu Leu Arg Ser Leu Thr Ser Asp Asp Thr Ala Val Tyr Tyr Cys Thr
85 90 95
Arg Asp Gly Asn Arg Tyr Asp Ala Trp Phe Ala Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Thr Ala Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser Gly Ser Thr Val Ala Leu
130 135 140
Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ser Leu Thr Ser Gly Val His Thr Phe Pro Ser Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Met Val Thr Val Pro Ser
180 185 190
Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys Asn Val Ala His Pro Ala
195 200 205
Ser Lys Thr Lys Val Asp Lys Pro Val Pro Lys Arg Glu Asn Gly Arg
210 215 220
Val Pro Arg Pro Pro Asp Cys Pro Lys Cys Pro Ala Pro Glu Met Leu
225 230 235 240
Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Leu Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val Ala Leu Asp
260 265 270
Pro Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val Asp Gly Lys Gln
275 280 285
Met Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu Gln Phe Ala Gly Thr
290 295 300
Tyr Arg Val Val Ser Val Leu Pro Ile Gly His Gln Asp Trp Leu Lys
305 310 315 320
Gly Lys Gln Phe Thr Cys Lys Val Asn Asn Lys Ala Leu Pro Ser Pro
325 330 335
Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala His Gln Pro Ser
340 345 350
Val Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu Ser Lys Asn Thr Val
355 360 365
Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro Asp Ile Asp Val
370 375 380
Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser Lys Tyr Arg Thr
385 390 395 400
Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu Tyr Ser Lys
405 410 415
Leu Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp Thr Phe Ile Cys
420 425 430
Ala Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Glu Ser Leu
435 440 445
Ser His Ser Pro Gly Lys
450
<210> 3
<211> 651
<212> ДНК
<213> Искусственная последовательность
<220>
<223> мышиная-собачья химера
<400> 3
cagattgtgc tgacccagag cccggcgatt atgagcgcga gcccgggcga aaaagtgacc 60
atgacctgca gcgcgagcag cagcgtgacc tatatgcatt ggtttcagca gaaaccgggc 120
accagcccga aactgtggat ttatagcacc agcattctgg cgagcggcgt gccggcgcgc 180
tttagcggca gcggcagcgg caccagctat agcctgacca ttagccgcat ggaagcggaa 240
gatgcggcga cctattattg ccagcagcgc accagctatc cgctgacctt tggcaccggc 300
accaaactgg aactgaaacg caacgatgcg cagccggcgg tgtatctgtt tcagccgagc 360
ccggatcagc tgcataccgg cagcgcgagc gtggtgtgcc tgctgaacag cttttatccg 420
aaagatatta acgtgaaatg gaaagtggat ggcgtgattc aggataccgg cattcaggaa 480
agcgtgaccg aacaggatag caaagatagc acctatagcc tgagcagcac cctgaccatg 540
agcagcaccg aatatctgag ccatgaactg tatagctgcg aaattaccca taaaagcctg 600
ccgagcaccc tgattaaaag ctttcagcgc agcgaatgcc agcgcgtgga t 651
<210> 4
<211> 217
<212> PRT
<213> Искусственная последовательность
<220>
<223> мышиная-собачья химера
<400> 4
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Ser Ser Ser Val Thr Tyr Met
20 25 30
His Trp Phe Gln Gln Lys Pro Gly Thr Ser Pro Lys Leu Trp Ile Tyr
35 40 45
Ser Thr Ser Ile Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Arg Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Arg Thr Ser Tyr Pro Leu Thr
85 90 95
Phe Gly Thr Gly Thr Lys Leu Glu Leu Lys Arg Asn Asp Ala Gln Pro
100 105 110
Ala Val Tyr Leu Phe Gln Pro Ser Pro Asp Gln Leu His Thr Gly Ser
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Ser Phe Tyr Pro Lys Asp Ile Asn
130 135 140
Val Lys Trp Lys Val Asp Gly Val Ile Gln Asp Thr Gly Ile Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Met Ser Ser Thr Glu Tyr Leu Ser His Glu Leu Tyr Ser
180 185 190
Cys Glu Ile Thr His Lys Ser Leu Pro Ser Thr Leu Ile Lys Ser Phe
195 200 205
Gln Arg Ser Glu Cys Gln Arg Val Asp
210 215
<210> 5
<211> 1350
<212> ДНК
<213> Искусственная последовательность
<220>
<223> мышиная-собачья химера
<400> 5
caggtgcagc tgcagcagag cggcgatgat ctggtgaaac cgggcgcgag cgtgaaactg 60
agctgcaaag cgagcggcta tacctttacc agctattgga ttaactggat taaacagcgc 120
ccgggccagg gcctggaatg gattggccgc attgcgccgg gcagcggcac cacctattat 180
aacgaagtgt ttaaaggcaa agcgaccctg accgtggata aatatagcag caccgcgtat 240
attcagctga gcagcctgag cagcgaagat agcgcggtgt atttttgcgc gcgcggcgat 300
tatggcagct attggggcca gggcaccctg gtgaccgtga gcagcgcgag caccaccgcg 360
ccgagcgtgt ttccgctggc gccgagctgc ggcagcacca gcggcagcac cgtggcgctg 420
gcgtgcctgg tgagcggcta ttttccggaa ccggtgaccg tgagctggaa cagcggcagc 480
ctgaccagcg gcgtgcatac ctttccgagc gtgctgcaga gcagcggcct gtatagcctg 540
agcagcatgg tgaccgtgcc gagcagccgc tggccgagcg aaacctttac ctgcaacgtg 600
gcgcatccgg cgagcaaaac caaagtggat aaaccggtgc cgaaacgcga aaacggccgc 660
gtgccgcgcc cgccggattg cccgaaatgc ccggcgccgg aaatgctggg cggcccgagc 720
gtgtttattt ttccgccgaa accgaaagat accctgctga ttgcgcgcac cccggaagtg 780
acctgcgtgg tggtggcgct ggatccggaa gatccggaag tgcagattag ctggtttgtg 840
gatggcaaac agatgcagac cgcgaaaacc cagccgcgcg aagaacagtt tgcgggcacc 900
tatcgcgtgg tgagcgtgct gccgattggc catcaggatt ggctgaaagg caaacagttt 960
acctgcaaag tgaacaacaa agcgctgccg agcccgattg aacgcaccat tagcaaagcg 1020
cgcggccagg cgcatcagcc gagcgtgtat gtgctgccgc cgagccgcga agaactgagc 1080
aaaaacaccg tgagcctgac ctgcctgatt aaagattttt ttccgccgga tattgatgtg 1140
gaatggcaga gcaacggcca gcaggaaccg gaaagcaaat atcgcaccac cccgccgcag 1200
ctggatgaag atggcagcta ttttctgtat agcaaactga gcgtggataa aagccgctgg 1260
cagcgcggcg atacctttat ttgcgcggtg atgcatgaag cgctgcataa ccattatacc 1320
caggaaagcc tgagccatag cccgggcaaa 1350
<210> 6
<211> 450
<212> PRT
<213> Искусственная последовательность
<220>
<223> мышиная-собачья химера
<400> 6
Gln Val Gln Leu Gln Gln Ser Gly Asp Asp Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Ile Asn Trp Ile Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Arg Ile Ala Pro Gly Ser Gly Thr Thr Tyr Tyr Asn Glu Val Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Tyr Ser Ser Thr Ala Tyr
65 70 75 80
Ile Gln Leu Ser Ser Leu Ser Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Arg Gly Asp Tyr Gly Ser Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Thr Thr Ala Pro Ser Val Phe Pro Leu Ala Pro
115 120 125
Ser Cys Gly Ser Thr Ser Gly Ser Thr Val Ala Leu Ala Cys Leu Val
130 135 140
Ser Gly Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ser
145 150 155 160
Leu Thr Ser Gly Val His Thr Phe Pro Ser Val Leu Gln Ser Ser Gly
165 170 175
Leu Tyr Ser Leu Ser Ser Met Val Thr Val Pro Ser Ser Arg Trp Pro
180 185 190
Ser Glu Thr Phe Thr Cys Asn Val Ala His Pro Ala Ser Lys Thr Lys
195 200 205
Val Asp Lys Pro Val Pro Lys Arg Glu Asn Gly Arg Val Pro Arg Pro
210 215 220
Pro Asp Cys Pro Lys Cys Pro Ala Pro Glu Met Leu Gly Gly Pro Ser
225 230 235 240
Val Phe Ile Phe Pro Pro Lys Pro Lys Asp Thr Leu Leu Ile Ala Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Ala Leu Asp Pro Glu Asp Pro
260 265 270
Glu Val Gln Ile Ser Trp Phe Val Asp Gly Lys Gln Met Gln Thr Ala
275 280 285
Lys Thr Gln Pro Arg Glu Glu Gln Phe Ala Gly Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Pro Ile Gly His Gln Asp Trp Leu Lys Gly Lys Gln Phe
305 310 315 320
Thr Cys Lys Val Asn Asn Lys Ala Leu Pro Ser Pro Ile Glu Arg Thr
325 330 335
Ile Ser Lys Ala Arg Gly Gln Ala His Gln Pro Ser Val Tyr Val Leu
340 345 350
Pro Pro Ser Arg Glu Glu Leu Ser Lys Asn Thr Val Ser Leu Thr Cys
355 360 365
Leu Ile Lys Asp Phe Phe Pro Pro Asp Ile Asp Val Glu Trp Gln Ser
370 375 380
Asn Gly Gln Gln Glu Pro Glu Ser Lys Tyr Arg Thr Thr Pro Pro Gln
385 390 395 400
Leu Asp Glu Asp Gly Ser Tyr Phe Leu Tyr Ser Lys Leu Ser Val Asp
405 410 415
Lys Ser Arg Trp Gln Arg Gly Asp Thr Phe Ile Cys Ala Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Glu Ser Leu Ser His Ser Pro
435 440 445
Gly Lys
450
<210> 7
<211> 651
<212> ДНК
<213> Искусственная последовательность
<220>
<223> мышиная-собачья химера
<400> 7
cagattgtgc tgacccagag cccggcgatt atgagcgcga gcccgggcga aaaagtgacc 60
atgacctgca gcgcgagcag cagcattagc tatatgcatt ggtttcagca gaaaccgggc 120
accagcccga aacgctggat ttatgatacc agcaaactgg cgagcggcgt gccggcgcgc 180
tttagcggca gcggcagcgg caccagctat agcctgacca ttaacagcat ggaagcggaa 240
gatgcggcga cctattattg ccatcagcgc accagctatc cgctgacctt tggcgcgggc 300
accaaactgg aactgaaacg caacgatgcg cagccggcgg tgtatctgtt tcagccgagc 360
ccggatcagc tgcataccgg cagcgcgagc gtggtgtgcc tgctgaacag cttttatccg 420
aaagatatta acgtgaaatg gaaagtggat ggcgtgattc aggataccgg cattcaggaa 480
agcgtgaccg aacaggatag caaagatagc acctatagcc tgagcagcac cctgaccatg 540
agcagcaccg aatatctgag ccatgaactg tatagctgcg aaattaccca taaaagcctg 600
ccgagcaccc tgattaaaag ctttcagcgc agcgaatgcc agcgcgtgga t 651
<210> 8
<211> 217
<212> PRT
<213> Искусственная последовательность
<220>
<223> мышиная-собачья химера
<400> 8
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Ser Ser Ser Ile Ser Tyr Met
20 25 30
His Trp Phe Gln Gln Lys Pro Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Asn Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys His Gln Arg Thr Ser Tyr Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Asn Asp Ala Gln Pro
100 105 110
Ala Val Tyr Leu Phe Gln Pro Ser Pro Asp Gln Leu His Thr Gly Ser
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Ser Phe Tyr Pro Lys Asp Ile Asn
130 135 140
Val Lys Trp Lys Val Asp Gly Val Ile Gln Asp Thr Gly Ile Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Met Ser Ser Thr Glu Tyr Leu Ser His Glu Leu Tyr Ser
180 185 190
Cys Glu Ile Thr His Lys Ser Leu Pro Ser Thr Leu Ile Lys Ser Phe
195 200 205
Gln Arg Ser Glu Cys Gln Arg Val Asp
210 215
<210> 9
<211> 1359
<212> ДНК
<213> Искусственная последовательность
<220>
<223> человеческая-собачья химера
<400> 9
caggtgcagc tggtggaaag cggcggcggc gtggtgcagc cgggccgcag cctgcgcctg 60
agctgcgtgg cgagcggctt tacctttagc agccatggca tgcattgggt gcgccaggcg 120
ccgggcaaag gcctggaatg ggtggcggtg atttggtatg atggccgcaa caaatattat 180
gcggatagcg tgaaaggccg ctttaccatt agccgcgata acagcaaaaa caccctgttt 240
ctgcagatga acagcctgcg cgcggaagat accgcggtgt attattgcgc gcgcggcggc 300
cattttggcc cgtttgatta ttggggccag ggcaccctgg tgaccgtgag cagcgcgagc 360
accaccgcgc cgagcgtgtt tccgctggcg ccgagctgcg gcagcaccag cggcagcacc 420
gtggcgctgg cgtgcctggt gagcggctat tttccggaac cggtgaccgt gagctggaac 480
agcggcagcc tgaccagcgg cgtgcatacc tttccgagcg tgctgcagag cagcggcctg 540
tatagcctga gcagcatggt gaccgtgccg agcagccgct ggccgagcga aacctttacc 600
tgcaacgtgg cgcatccggc gagcaaaacc aaagtggata aaccggtgcc gaaacgcgaa 660
aacggccgcg tgccgcgccc gccggattgc ccgaaatgcc cggcgccgga aatgctgggc 720
ggcccgagcg tgtttatttt tccgccgaaa ccgaaagata ccctgctgat tgcgcgcacc 780
ccggaagtga cctgcgtggt ggtggcgctg gatccggaag atccggaagt gcagattagc 840
tggtttgtgg atggcaaaca gatgcagacc gcgaaaaccc agccgcgcga agaacagttt 900
gcgggcacct atcgcgtggt gagcgtgctg ccgattggcc atcaggattg gctgaaaggc 960
aaacagttta cctgcaaagt gaacaacaaa gcgctgccga gcccgattga acgcaccatt 1020
agcaaagcgc gcggccaggc gcatcagccg agcgtgtatg tgctgccgcc gagccgcgaa 1080
gaactgagca aaaacaccgt gagcctgacc tgcctgatta aagatttttt tccgccggat 1140
attgatgtgg aatggcagag caacggccag caggaaccgg aaagcaaata tcgcaccacc 1200
ccgccgcagc tggatgaaga tggcagctat tttctgtata gcaaactgag cgtggataaa 1260
agccgctggc agcgcggcga tacctttatt tgcgcggtga tgcatgaagc gctgcataac 1320
cattataccc aggaaagcct gagccatagc ccgggcaaa 1359
<210> 10
<211> 453
<212> PRT
<213> Искусственная последовательность
<220>
<223> человеческая-собачья химера
<400> 10
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Val Ala Ser Gly Phe Thr Phe Ser Ser His
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Arg Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly His Phe Gly Pro Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Thr Ala Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Cys Gly Ser Thr Ser Gly Ser Thr Val Ala Leu Ala
130 135 140
Cys Leu Val Ser Gly Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ser Leu Thr Ser Gly Val His Thr Phe Pro Ser Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Met Val Thr Val Pro Ser Ser
180 185 190
Arg Trp Pro Ser Glu Thr Phe Thr Cys Asn Val Ala His Pro Ala Ser
195 200 205
Lys Thr Lys Val Asp Lys Pro Val Pro Lys Arg Glu Asn Gly Arg Val
210 215 220
Pro Arg Pro Pro Asp Cys Pro Lys Cys Pro Ala Pro Glu Met Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys Asp Thr Leu Leu
245 250 255
Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val Ala Leu Asp Pro
260 265 270
Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val Asp Gly Lys Gln Met
275 280 285
Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu Gln Phe Ala Gly Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Pro Ile Gly His Gln Asp Trp Leu Lys Gly
305 310 315 320
Lys Gln Phe Thr Cys Lys Val Asn Asn Lys Ala Leu Pro Ser Pro Ile
325 330 335
Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala His Gln Pro Ser Val
340 345 350
Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu Ser Lys Asn Thr Val Ser
355 360 365
Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro Asp Ile Asp Val Glu
370 375 380
Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser Lys Tyr Arg Thr Thr
385 390 395 400
Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu Tyr Ser Lys Leu
405 410 415
Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp Thr Phe Ile Cys Ala
420 425 430
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Glu Ser Leu Ser
435 440 445
His Ser Pro Gly Lys
450
<210> 11
<211> 657
<212> ДНК
<213> Искусственная последовательность
<220>
<223> человеческая-собачья химера
<400> 11
gaaattgtgc tgacccagag cccgggcacc ctgagcctga gcccgggcga acgcgcgacc 60
ctgagctgcc gcgcgagcca gagcattagc agcagctttc tggcgtggta tcagcagcgc 120
ccgggccagg cgccgcgcct gctgatttat ggcgcgagca gccgcgcgac cggcattccg 180
gatcgcttta gcggcagcgg cagcggcacc gattttaccc tgaccattag ccgcctggaa 240
ccggaagatt ttgcggtgta ttattgccag cagtatggca ccagcccgtg gacctttggc 300
cagggcacca aagtggaaat taaacgcaac gatgcgcagc cggcggtgta tctgtttcag 360
ccgagcccgg atcagctgca taccggcagc gcgagcgtgg tgtgcctgct gaacagcttt 420
tatccgaaag atattaacgt gaaatggaaa gtggatggcg tgattcagga taccggcatt 480
caggaaagcg tgaccgaaca ggatagcaaa gatagcacct atagcctgag cagcaccctg 540
accatgagca gcaccgaata tctgagccat gaactgtata gctgcgaaat tacccataaa 600
agcctgccga gcaccctgat taaaagcttt cagcgcagcg aatgccagcg cgtggat 657
<210> 12
<211> 219
<212> PRT
<213> Искусственная последовательность
<220>
<223> человеческая-собачья химера
<400> 12
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Ser Ser
20 25 30
Phe Leu Ala Trp Tyr Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Thr Ser Pro
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Asn Asp Ala
100 105 110
Gln Pro Ala Val Tyr Leu Phe Gln Pro Ser Pro Asp Gln Leu His Thr
115 120 125
Gly Ser Ala Ser Val Val Cys Leu Leu Asn Ser Phe Tyr Pro Lys Asp
130 135 140
Ile Asn Val Lys Trp Lys Val Asp Gly Val Ile Gln Asp Thr Gly Ile
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Met Ser Ser Thr Glu Tyr Leu Ser His Glu Leu
180 185 190
Tyr Ser Cys Glu Ile Thr His Lys Ser Leu Pro Ser Thr Leu Ile Lys
195 200 205
Ser Phe Gln Arg Ser Glu Cys Gln Arg Val Asp
210 215
<210> 13
<211> 1362
<212> ДНК
<213> Искусственная последовательность
<220>
<223> человеческая-собачья химера
<400> 13
caggtgcagc tggtggaaag cggcggcggc gtggtgcagc cgggccgcag cctgcgcctg 60
agctgcaccg cgagcggctt tacctttagc aactatggca tgcattgggt gcgccaggcg 120
ccgggcaaag gcctggaatg ggtggcggtg atttggtatg atggcagcaa caaacattat 180
ggcgatagcg tgaaaggccg ctttaccatt agcagcgata acagcaaaaa caccctgtat 240
ctgcagatga acagcctgcg cgcggaagat accgcggtgt attattgcgc gcgcggcgaa 300
cgcctgggca gctattttga ttattggggc cagggcaccc tggtgaccgt gagcagcgcg 360
agcaccaccg cgccgagcgt gtttccgctg gcgccgagct gcggcagcac cagcggcagc 420
accgtggcgc tggcgtgcct ggtgagcggc tattttccgg aaccggtgac cgtgagctgg 480
aacagcggca gcctgaccag cggcgtgcat acctttccga gcgtgctgca gagcagcggc 540
ctgtatagcc tgagcagcat ggtgaccgtg ccgagcagcc gctggccgag cgaaaccttt 600
acctgcaacg tggcgcatcc ggcgagcaaa accaaagtgg ataaaccggt gccgaaacgc 660
gaaaacggcc gcgtgccgcg cccgccggat tgcccgaaat gcccggcgcc ggaaatgctg 720
ggcggcccga gcgtgtttat ttttccgccg aaaccgaaag ataccctgct gattgcgcgc 780
accccggaag tgacctgcgt ggtggtggcg ctggatccgg aagatccgga agtgcagatt 840
agctggtttg tggatggcaa acagatgcag accgcgaaaa cccagccgcg cgaagaacag 900
tttgcgggca cctatcgcgt ggtgagcgtg ctgccgattg gccatcagga ttggctgaaa 960
ggcaaacagt ttacctgcaa agtgaacaac aaagcgctgc cgagcccgat tgaacgcacc 1020
attagcaaag cgcgcggcca ggcgcatcag ccgagcgtgt atgtgctgcc gccgagccgc 1080
gaagaactga gcaaaaacac cgtgagcctg acctgcctga ttaaagattt ttttccgccg 1140
gatattgatg tggaatggca gagcaacggc cagcaggaac cggaaagcaa atatcgcacc 1200
accccgccgc agctggatga agatggcagc tattttctgt atagcaaact gagcgtggat 1260
aaaagccgct ggcagcgcgg cgataccttt atttgcgcgg tgatgcatga agcgctgcat 1320
aaccattata cccaggaaag cctgagccat agcccgggca aa 1362
<210> 14
<211> 454
<212> PRT
<213> Искусственная последовательность
<220>
<223> человеческая-собачья химера
<400> 14
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Thr Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Asn Lys His Tyr Gly Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ser Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Glu Arg Leu Gly Ser Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Thr Ala Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser Gly Ser Thr Val Ala Leu
130 135 140
Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ser Leu Thr Ser Gly Val His Thr Phe Pro Ser Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Met Val Thr Val Pro Ser
180 185 190
Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys Asn Val Ala His Pro Ala
195 200 205
Ser Lys Thr Lys Val Asp Lys Pro Val Pro Lys Arg Glu Asn Gly Arg
210 215 220
Val Pro Arg Pro Pro Asp Cys Pro Lys Cys Pro Ala Pro Glu Met Leu
225 230 235 240
Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Leu Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val Ala Leu Asp
260 265 270
Pro Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val Asp Gly Lys Gln
275 280 285
Met Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu Gln Phe Ala Gly Thr
290 295 300
Tyr Arg Val Val Ser Val Leu Pro Ile Gly His Gln Asp Trp Leu Lys
305 310 315 320
Gly Lys Gln Phe Thr Cys Lys Val Asn Asn Lys Ala Leu Pro Ser Pro
325 330 335
Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala His Gln Pro Ser
340 345 350
Val Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu Ser Lys Asn Thr Val
355 360 365
Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro Asp Ile Asp Val
370 375 380
Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser Lys Tyr Arg Thr
385 390 395 400
Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu Tyr Ser Lys
405 410 415
Leu Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp Thr Phe Ile Cys
420 425 430
Ala Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Glu Ser Leu
435 440 445
Ser His Ser Pro Gly Lys
450
<210> 15
<211> 651
<212> ДНК
<213> Искусственная последовательность
<220>
<223> человеческая-собачья химера
<400> 15
gaaattgtgc tgacccagag cccgggcacc ctgagcctga gcccgggcga acgcgcgacc 60
ctgagctgcc gcaccagcgt gagcagcagc tatctggcgt ggtatcagca gaaaccgggc 120
caggcgccgc gcctgctgat ttatggcgcg agcagccgcg cgaccggcat tccggatcgc 180
tttagcggca gcggcagcgg caccgatttt accctgacca ttagccgcct ggaaccggaa 240
gattttgcgg tgtattattg ccagcagtat ggcattagcc cgtttacctt tggcggcggc 300
accaaagtgg aaattaaacg caacgatgcg cagccggcgg tgtatctgtt tcagccgagc 360
ccggatcagc tgcataccgg cagcgcgagc gtggtgtgcc tgctgaacag cttttatccg 420
aaagatatta acgtgaaatg gaaagtggat ggcgtgattc aggataccgg cattcaggaa 480
agcgtgaccg aacaggatag caaagatagc acctatagcc tgagcagcac cctgaccatg 540
agcagcaccg aatatctgag ccatgaactg tatagctgcg aaattaccca taaaagcctg 600
ccgagcaccc tgattaaaag ctttcagcgc agcgaatgcc agcgcgtgga t 651
<210> 16
<211> 217
<212> PRT
<213> Искусственная последовательность
<220>
<223> человеческая-собачья химера
<400> 16
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Thr Ser Val Ser Ser Ser Tyr Leu
20 25 30
Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
35 40 45
Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu
65 70 75 80
Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ile Ser Pro Phe Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Asn Asp Ala Gln Pro
100 105 110
Ala Val Tyr Leu Phe Gln Pro Ser Pro Asp Gln Leu His Thr Gly Ser
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Ser Phe Tyr Pro Lys Asp Ile Asn
130 135 140
Val Lys Trp Lys Val Asp Gly Val Ile Gln Asp Thr Gly Ile Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Met Ser Ser Thr Glu Tyr Leu Ser His Glu Leu Tyr Ser
180 185 190
Cys Glu Ile Thr His Lys Ser Leu Pro Ser Thr Leu Ile Lys Ser Phe
195 200 205
Gln Arg Ser Glu Cys Gln Arg Val Asp
210 215
<210> 17
<211> 1359
<212> ДНК
<213> Искусственная последовательность
<220>
<223> человеческая-собачья химера
<400> 17
caggtgcagc tggtggaaag cggcggcggc gtggtggaac cgggccgcag cctgcgcctg 60
agctgcaccg cgagcggctt tacctttagc agctatggca tgcattgggt gcgccaggcg 120
ccgggcaaag gcctggaatg ggtggcggtg atttggtatg atggcagcaa caaacattat 180
gcggatagcg cgaaaggccg ctttaccatt agccgcgata acagcaaaaa caccctgtat 240
ctgcagatga acagcctgcg cgcggaagat accgcggtgt attattgcgc gcgcgcgggc 300
ctgctgggct attttgatta ttggggccag ggcaccctgg tgaccgtgag cagcgcgagc 360
accaccgcgc cgagcgtgtt tccgctggcg ccgagctgcg gcagcaccag cggcagcacc 420
gtggcgctgg cgtgcctggt gagcggctat tttccggaac cggtgaccgt gagctggaac 480
agcggcagcc tgaccagcgg cgtgcatacc tttccgagcg tgctgcagag cagcggcctg 540
tatagcctga gcagcatggt gaccgtgccg agcagccgct ggccgagcga aacctttacc 600
tgcaacgtgg cgcatccggc gagcaaaacc aaagtggata aaccggtgcc gaaacgcgaa 660
aacggccgcg tgccgcgccc gccggattgc ccgaaatgcc cggcgccgga aatgctgggc 720
ggcccgagcg tgtttatttt tccgccgaaa ccgaaagata ccctgctgat tgcgcgcacc 780
ccggaagtga cctgcgtggt ggtggcgctg gatccggaag atccggaagt gcagattagc 840
tggtttgtgg atggcaaaca gatgcagacc gcgaaaaccc agccgcgcga agaacagttt 900
gcgggcacct atcgcgtggt gagcgtgctg ccgattggcc atcaggattg gctgaaaggc 960
aaacagttta cctgcaaagt gaacaacaaa gcgctgccga gcccgattga acgcaccatt 1020
agcaaagcgc gcggccaggc gcatcagccg agcgtgtatg tgctgccgcc gagccgcgaa 1080
gaactgagca aaaacaccgt gagcctgacc tgcctgatta aagatttttt tccgccggat 1140
attgatgtgg aatggcagag caacggccag caggaaccgg aaagcaaata tcgcaccacc 1200
ccgccgcagc tggatgaaga tggcagctat tttctgtata gcaaactgag cgtggataaa 1260
agccgctggc agcgcggcga tacctttatt tgcgcggtga tgcatgaagc gctgcataac 1320
cattataccc aggaaagcct gagccatagc ccgggcaaa 1359
<210> 18
<211> 453
<212> PRT
<213> Искусственная последовательность
<220>
<223> человеческая-собачья химера
<400> 18
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Glu Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Thr Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Asn Lys His Tyr Ala Asp Ser Ala
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Gly Leu Leu Gly Tyr Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Thr Ala Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Cys Gly Ser Thr Ser Gly Ser Thr Val Ala Leu Ala
130 135 140
Cys Leu Val Ser Gly Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ser Leu Thr Ser Gly Val His Thr Phe Pro Ser Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Met Val Thr Val Pro Ser Ser
180 185 190
Arg Trp Pro Ser Glu Thr Phe Thr Cys Asn Val Ala His Pro Ala Ser
195 200 205
Lys Thr Lys Val Asp Lys Pro Val Pro Lys Arg Glu Asn Gly Arg Val
210 215 220
Pro Arg Pro Pro Asp Cys Pro Lys Cys Pro Ala Pro Glu Met Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys Asp Thr Leu Leu
245 250 255
Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val Ala Leu Asp Pro
260 265 270
Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val Asp Gly Lys Gln Met
275 280 285
Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu Gln Phe Ala Gly Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Pro Ile Gly His Gln Asp Trp Leu Lys Gly
305 310 315 320
Lys Gln Phe Thr Cys Lys Val Asn Asn Lys Ala Leu Pro Ser Pro Ile
325 330 335
Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala His Gln Pro Ser Val
340 345 350
Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu Ser Lys Asn Thr Val Ser
355 360 365
Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro Asp Ile Asp Val Glu
370 375 380
Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser Lys Tyr Arg Thr Thr
385 390 395 400
Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu Tyr Ser Lys Leu
405 410 415
Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp Thr Phe Ile Cys Ala
420 425 430
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Glu Ser Leu Ser
435 440 445
His Ser Pro Gly Lys
450
<210> 19
<211> 654
<212> ДНК
<213> Искусственная последовательность
<220>
<223> человеческая-собачья химера
<400> 19
gaaattgtgc tgacccagag cccgggcacc ctgagcctga gcccgggcga acgcgcgacc 60
ctgagctgcc gcgcgagcca gagcgtgagc agctatctgg cgtggtatca gcagaaaccg 120
ggccaggcgc cgcgcccgct gatttatggc gtgagcagcc gcgcgaccgg cattccggat 180
cgctttagcg gcagcggcag cggcaccgat tttaccctga ccattagccg cctggaaccg 240
gaagattttg cggtgtatta ttgccagcag tatggcatta gcccgtttac ctttggcccg 300
ggcaccaaag tggatattaa acgcaacgat gcgcagccgg cggtgtatct gtttcagccg 360
agcccggatc agctgcatac cggcagcgcg agcgtggtgt gcctgctgaa cagcttttat 420
ccgaaagata ttaacgtgaa atggaaagtg gatggcgtga ttcaggatac cggcattcag 480
gaaagcgtga ccgaacagga tagcaaagat agcacctata gcctgagcag caccctgacc 540
atgagcagca ccgaatatct gagccatgaa ctgtatagct gcgaaattac ccataaaagc 600
ctgccgagca ccctgattaa aagctttcag cgcagcgaat gccagcgcgt ggat 654
<210> 20
<211> 218
<212> PRT
<213> Искусственная последовательность
<220>
<223> человеческая-собачья химера
<400> 20
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Pro Leu Ile
35 40 45
Tyr Gly Val Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ile Ser Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys Arg Asn Asp Ala Gln
100 105 110
Pro Ala Val Tyr Leu Phe Gln Pro Ser Pro Asp Gln Leu His Thr Gly
115 120 125
Ser Ala Ser Val Val Cys Leu Leu Asn Ser Phe Tyr Pro Lys Asp Ile
130 135 140
Asn Val Lys Trp Lys Val Asp Gly Val Ile Gln Asp Thr Gly Ile Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Met Ser Ser Thr Glu Tyr Leu Ser His Glu Leu Tyr
180 185 190
Ser Cys Glu Ile Thr His Lys Ser Leu Pro Ser Thr Leu Ile Lys Ser
195 200 205
Phe Gln Arg Ser Glu Cys Gln Arg Val Asp
210 215
<210> 21
<211> 1359
<212> ДНК
<213> Искусственная последовательность
<220>
<223> человеческая-собачья химера
<400> 21
caggtgcagc tggtggaaag cggcggcggc gtggtgcagc cgggccgcag cctgcgcctg 60
agctgcgcgg cgagcggctt tacctttagc agctatacca tgcattgggt gcgccaggcg 120
ccgggcaaag gcctggaatg ggtgaccttt attagctatg atggcaacaa caaatattat 180
gcggatagcg tgaaaggccg ctttaccatt agccgcgata acagcaaaaa caccctgtat 240
ctgcagatga acagcctgcg cgcggaagat accgcggtgt attattgcgc gcgcaccggc 300
tggctgggcc cgtttgatta ttggggccag ggcaccctgg tgaccgtgag cagcgcgagc 360
accaccgcgc cgagcgtgtt tccgctggcg ccgagctgcg gcagcaccag cggcagcacc 420
gtggcgctgg cgtgcctggt gagcggctat tttccggaac cggtgaccgt gagctggaac 480
agcggcagcc tgaccagcgg cgtgcatacc tttccgagcg tgctgcagag cagcggcctg 540
tatagcctga gcagcatggt gaccgtgccg agcagccgct ggccgagcga aacctttacc 600
tgcaacgtgg cgcatccggc gagcaaaacc aaagtggata aaccggtgcc gaaacgcgaa 660
aacggccgcg tgccgcgccc gccggattgc ccgaaatgcc cggcgccgga aatgctgggc 720
ggcccgagcg tgtttatttt tccgccgaaa ccgaaagata ccctgctgat tgcgcgcacc 780
ccggaagtga cctgcgtggt ggtggcgctg gatccggaag atccggaagt gcagattagc 840
tggtttgtgg atggcaaaca gatgcagacc gcgaaaaccc agccgcgcga agaacagttt 900
gcgggcacct atcgcgtggt gagcgtgctg ccgattggcc atcaggattg gctgaaaggc 960
aaacagttta cctgcaaagt gaacaacaaa gcgctgccga gcccgattga acgcaccatt 1020
agcaaagcgc gcggccaggc gcatcagccg agcgtgtatg tgctgccgcc gagccgcgaa 1080
gaactgagca aaaacaccgt gagcctgacc tgcctgatta aagatttttt tccgccggat 1140
attgatgtgg aatggcagag caacggccag caggaaccgg aaagcaaata tcgcaccacc 1200
ccgccgcagc tggatgaaga tggcagctat tttctgtata gcaaactgag cgtggataaa 1260
agccgctggc agcgcggcga tacctttatt tgcgcggtga tgcatgaagc gctgcataac 1320
cattataccc aggaaagcct gagccatagc ccgggcaaa 1359
<210> 22
<211> 453
<212> PRT
<213> Искусственная последовательность
<220>
<223> человеческая-собачья химера
<400> 22
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Thr Phe Ile Ser Tyr Asp Gly Asn Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Thr Gly Trp Leu Gly Pro Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Thr Ala Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Cys Gly Ser Thr Ser Gly Ser Thr Val Ala Leu Ala
130 135 140
Cys Leu Val Ser Gly Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ser Leu Thr Ser Gly Val His Thr Phe Pro Ser Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Met Val Thr Val Pro Ser Ser
180 185 190
Arg Trp Pro Ser Glu Thr Phe Thr Cys Asn Val Ala His Pro Ala Ser
195 200 205
Lys Thr Lys Val Asp Lys Pro Val Pro Lys Arg Glu Asn Gly Arg Val
210 215 220
Pro Arg Pro Pro Asp Cys Pro Lys Cys Pro Ala Pro Glu Met Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys Asp Thr Leu Leu
245 250 255
Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val Ala Leu Asp Pro
260 265 270
Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val Asp Gly Lys Gln Met
275 280 285
Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu Gln Phe Ala Gly Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Pro Ile Gly His Gln Asp Trp Leu Lys Gly
305 310 315 320
Lys Gln Phe Thr Cys Lys Val Asn Asn Lys Ala Leu Pro Ser Pro Ile
325 330 335
Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala His Gln Pro Ser Val
340 345 350
Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu Ser Lys Asn Thr Val Ser
355 360 365
Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro Asp Ile Asp Val Glu
370 375 380
Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser Lys Tyr Arg Thr Thr
385 390 395 400
Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu Tyr Ser Lys Leu
405 410 415
Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp Thr Phe Ile Cys Ala
420 425 430
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Glu Ser Leu Ser
435 440 445
His Ser Pro Gly Lys
450
<210> 23
<211> 657
<212> ДНК
<213> Искусственная последовательность
<220>
<223> человеческая-собачья химера
<400> 23
gaaattgtgc tgacccagag cccgggcacc ctgagcctga gcccgggcga acgcgcgacc 60
ctgagctgcc gcgcgagcca gagcgtgggc agcagctatc tggcgtggta tcagcagaaa 120
ccgggccagg cgccgcgcct gctgatttat ggcgcgttta gccgcgcgac cggcattccg 180
gatcgcttta gcggcagcgg cagcggcacc gattttaccc tgaccattag ccgcctggaa 240
ccggaagatt ttgcggtgta ttattgccag cagtatggca gcagcccgtg gacctttggc 300
cagggcacca aagtggaaat taaacgcaac gatgcgcagc cggcggtgta tctgtttcag 360
ccgagcccgg atcagctgca taccggcagc gcgagcgtgg tgtgcctgct gaacagcttt 420
tatccgaaag atattaacgt gaaatggaaa gtggatggcg tgattcagga taccggcatt 480
caggaaagcg tgaccgaaca ggatagcaaa gatagcacct atagcctgag cagcaccctg 540
accatgagca gcaccgaata tctgagccat gaactgtata gctgcgaaat tacccataaa 600
agcctgccga gcaccctgat taaaagcttt cagcgcagcg aatgccagcg cgtggat 657
<210> 24
<211> 219
<212> PRT
<213> Искусственная последовательность
<220>
<223> человеческая-собачья химера
<400> 24
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Gly Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Phe Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Pro
85 90 95
Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Asn Asp Ala
100 105 110
Gln Pro Ala Val Tyr Leu Phe Gln Pro Ser Pro Asp Gln Leu His Thr
115 120 125
Gly Ser Ala Ser Val Val Cys Leu Leu Asn Ser Phe Tyr Pro Lys Asp
130 135 140
Ile Asn Val Lys Trp Lys Val Asp Gly Val Ile Gln Asp Thr Gly Ile
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Met Ser Ser Thr Glu Tyr Leu Ser His Glu Leu
180 185 190
Tyr Ser Cys Glu Ile Thr His Lys Ser Leu Pro Ser Thr Leu Ile Lys
195 200 205
Ser Phe Gln Arg Ser Glu Cys Gln Arg Val Asp
210 215
<210> 25
<211> 1362
<212> ДНК
<213> Искусственная последовательность
<220>
<223> человеческая-собачья химера
<400> 25
caggtgcagc tggtggaaag cggcggcggc gtggtgcagc cgggccgcag cctgcgcctg 60
agctgcgcgg cgagcggctt tacctttagc agctatggca tgcattgggt gcgccaggcg 120
ccgggcaaag gcctggaatg ggtggcggtg atttggtatg atggcagcaa caaatattat 180
gcggatagcg tgaaaggccg ctttaccatt agccgcgata acagcaaaaa caccctgtat 240
ctgcagatga acagcctgcg cgcggaagat accgcggtgt tttattgcgc gcgcgcgccg 300
aactatattg gcgcgtttga tgtgtggggc cagggcacca tggtgaccgt gagcagcgcg 360
agcaccaccg cgccgagcgt gtttccgctg gcgccgagct gcggcagcac cagcggcagc 420
accgtggcgc tggcgtgcct ggtgagcggc tattttccgg aaccggtgac cgtgagctgg 480
aacagcggca gcctgaccag cggcgtgcat acctttccga gcgtgctgca gagcagcggc 540
ctgtatagcc tgagcagcat ggtgaccgtg ccgagcagcc gctggccgag cgaaaccttt 600
acctgcaacg tggcgcatcc ggcgagcaaa accaaagtgg ataaaccggt gccgaaacgc 660
gaaaacggcc gcgtgccgcg cccgccggat tgcccgaaat gcccggcgcc ggaaatgctg 720
ggcggcccga gcgtgtttat ttttccgccg aaaccgaaag ataccctgct gattgcgcgc 780
accccggaag tgacctgcgt ggtggtggcg ctggatccgg aagatccgga agtgcagatt 840
agctggtttg tggatggcaa acagatgcag accgcgaaaa cccagccgcg cgaagaacag 900
tttgcgggca cctatcgcgt ggtgagcgtg ctgccgattg gccatcagga ttggctgaaa 960
ggcaaacagt ttacctgcaa agtgaacaac aaagcgctgc cgagcccgat tgaacgcacc 1020
attagcaaag cgcgcggcca ggcgcatcag ccgagcgtgt atgtgctgcc gccgagccgc 1080
gaagaactga gcaaaaacac cgtgagcctg acctgcctga ttaaagattt ttttccgccg 1140
gatattgatg tggaatggca gagcaacggc cagcaggaac cggaaagcaa atatcgcacc 1200
accccgccgc agctggatga agatggcagc tattttctgt atagcaaact gagcgtggat 1260
aaaagccgct ggcagcgcgg cgataccttt atttgcgcgg tgatgcatga agcgctgcat 1320
aaccattata cccaggaaag cctgagccat agcccgggca aa 1362
<210> 26
<211> 454
<212> PRT
<213> Искусственная последовательность
<220>
<223> человеческая-собачья химера
<400> 26
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Phe Tyr Cys
85 90 95
Ala Arg Ala Pro Asn Tyr Ile Gly Ala Phe Asp Val Trp Gly Gln Gly
100 105 110
Thr Met Val Thr Val Ser Ser Ala Ser Thr Thr Ala Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser Gly Ser Thr Val Ala Leu
130 135 140
Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ser Leu Thr Ser Gly Val His Thr Phe Pro Ser Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Met Val Thr Val Pro Ser
180 185 190
Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys Asn Val Ala His Pro Ala
195 200 205
Ser Lys Thr Lys Val Asp Lys Pro Val Pro Lys Arg Glu Asn Gly Arg
210 215 220
Val Pro Arg Pro Pro Asp Cys Pro Lys Cys Pro Ala Pro Glu Met Leu
225 230 235 240
Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Leu Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val Ala Leu Asp
260 265 270
Pro Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val Asp Gly Lys Gln
275 280 285
Met Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu Gln Phe Ala Gly Thr
290 295 300
Tyr Arg Val Val Ser Val Leu Pro Ile Gly His Gln Asp Trp Leu Lys
305 310 315 320
Gly Lys Gln Phe Thr Cys Lys Val Asn Asn Lys Ala Leu Pro Ser Pro
325 330 335
Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala His Gln Pro Ser
340 345 350
Val Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu Ser Lys Asn Thr Val
355 360 365
Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro Asp Ile Asp Val
370 375 380
Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser Lys Tyr Arg Thr
385 390 395 400
Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu Tyr Ser Lys
405 410 415
Leu Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp Thr Phe Ile Cys
420 425 430
Ala Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Glu Ser Leu
435 440 445
Ser His Ser Pro Gly Lys
450
<210> 27
<211> 654
<212> ДНК
<213> Искусственная последовательность
<220>
<223> человеческая-собачья химера
<400> 27
gatattcaga tgacccagag cccgagcagc ctgagcgcga gcgtgggcga tcgcgtgacc 60
attacctgcc gcgcgagcca gggcattagc agctggctgg cgtggtatca gcagaaaccg 120
gaaaaagcgc cgaaaagcct gatttatgcg gcgagcagcc tgcagagcgg cgtgccgagc 180
cgctttagcg gcagcggcag cggcaccgat tttaccctga ccattagcag cctgcagccg 240
gaagattttg cgacctatta ttgccagcag tataacagct atccgccgac ctttggccag 300
ggcaccaaag tggaaattaa acgcaacgat gcgcagccgg cggtgtatct gtttcagccg 360
agcccggatc agctgcatac cggcagcgcg agcgtggtgt gcctgctgaa cagcttttat 420
ccgaaagata ttaacgtgaa atggaaagtg gatggcgtga ttcaggatac cggcattcag 480
gaaagcgtga ccgaacagga tagcaaagat agcacctata gcctgagcag caccctgacc 540
atgagcagca ccgaatatct gagccatgaa ctgtatagct gcgaaattac ccataaaagc 600
ctgccgagca ccctgattaa aagctttcag cgcagcgaat gccagcgcgt ggat 654
<210> 28
<211> 218
<212> PRT
<213> Искусственная последовательность
<220>
<223> человеческая-собачья химера
<400> 28
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Glu Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Asn Asp Ala Gln
100 105 110
Pro Ala Val Tyr Leu Phe Gln Pro Ser Pro Asp Gln Leu His Thr Gly
115 120 125
Ser Ala Ser Val Val Cys Leu Leu Asn Ser Phe Tyr Pro Lys Asp Ile
130 135 140
Asn Val Lys Trp Lys Val Asp Gly Val Ile Gln Asp Thr Gly Ile Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Met Ser Ser Thr Glu Tyr Leu Ser His Glu Leu Tyr
180 185 190
Ser Cys Glu Ile Thr His Lys Ser Leu Pro Ser Thr Leu Ile Lys Ser
195 200 205
Phe Gln Arg Ser Glu Cys Gln Arg Val Asp
210 215
<210> 29
<211> 1374
<212> ДНК
<213> Искусственная последовательность
<220>
<223> мышиная-собачья химера
<400> 29
gaagtgaaac tggtgaacag cggcggcggc ctggtgcagc cgggcaacag cctgcgcctg 60
agctgcgcga ccagcggctt tacctttacc gatttttata tgagctgggt gcgccagccg 120
ccgggcaaag cgctggaatg gctgggcttt gtgcgcaacc gcgcgaacgg ctataccacc 180
gaatatagcg tgagcgtgaa aggccgcttt attattagcc gcgataactt tcagagcacc 240
ctgtttctgc agatgaacac cctgcgcgcg gaagatagcg gcacctatta ttgcgtgcgc 300
ggcccgggcg ataccgcgga ttataccatg gattattggg gccagggcac cagcgtgacc 360
gtgagcagcg cgagcaccac cgcgccgagc gtgtttccgc tggcgccgag ctgcggcagc 420
accagcggca gcaccgtggc gctggcgtgc ctggtgagcg gctattttcc ggaaccggtg 480
accgtgagct ggaacagcgg cagcctgacc agcggcgtgc atacctttcc gagcgtgctg 540
cagagcagcg gcctgtatag cctgagcagc atggtgaccg tgccgagcag ccgctggccg 600
agcgaaacct ttacctgcaa cgtggcgcat ccggcgagca aaaccaaagt ggataaaccg 660
gtgccgaaac gcgaaaacgg ccgcgtgccg cgcccgccgg attgcccgaa atgcccggcg 720
ccggaaatgc tgggcggccc gagcgtgttt atttttccgc cgaaaccgaa agataccctg 780
ctgattgcgc gcaccccgga agtgacctgc gtggtggtgg cgctggatcc ggaagatccg 840
gaagtgcaga ttagctggtt tgtggatggc aaacagatgc agaccgcgaa aacccagccg 900
cgcgaagaac agtttgcggg cacctatcgc gtggtgagcg tgctgccgat tggccatcag 960
gattggctga aaggcaaaca gtttacctgc aaagtgaaca acaaagcgct gccgagcccg 1020
attgaacgca ccattagcaa agcgcgcggc caggcgcatc agccgagcgt gtatgtgctg 1080
ccgccgagcc gcgaagaact gagcaaaaac accgtgagcc tgacctgcct gattaaagat 1140
ttttttccgc cggatattga tgtggaatgg cagagcaacg gccagcagga accggaaagc 1200
aaatatcgca ccaccccgcc gcagctggat gaagatggca gctattttct gtatagcaaa 1260
ctgagcgtgg ataaaagccg ctggcagcgc ggcgatacct ttatttgcgc ggtgatgcat 1320
gaagcgctgc ataaccatta tacccaggaa agcctgagcc atagcccggg caaa 1374
<210> 30
<211> 458
<212> PRT
<213> Искусственная последовательность
<220>
<223> мышиная-собачья химера
<400> 30
Glu Val Lys Leu Val Asn Ser Gly Gly Gly Leu Val Gln Pro Gly Asn
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Thr Ser Gly Phe Thr Phe Thr Asp Phe
20 25 30
Tyr Met Ser Trp Val Arg Gln Pro Pro Gly Lys Ala Leu Glu Trp Leu
35 40 45
Gly Phe Val Arg Asn Arg Ala Asn Gly Tyr Thr Thr Glu Tyr Ser Val
50 55 60
Ser Val Lys Gly Arg Phe Ile Ile Ser Arg Asp Asn Phe Gln Ser Thr
65 70 75 80
Leu Phe Leu Gln Met Asn Thr Leu Arg Ala Glu Asp Ser Gly Thr Tyr
85 90 95
Tyr Cys Val Arg Gly Pro Gly Asp Thr Ala Asp Tyr Thr Met Asp Tyr
100 105 110
Trp Gly Gln Gly Thr Ser Val Thr Val Ser Ser Ala Ser Thr Thr Ala
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser Gly Ser
130 135 140
Thr Val Ala Leu Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ser Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ser Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Met Val
180 185 190
Thr Val Pro Ser Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys Asn Val
195 200 205
Ala His Pro Ala Ser Lys Thr Lys Val Asp Lys Pro Val Pro Lys Arg
210 215 220
Glu Asn Gly Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys Pro Ala
225 230 235 240
Pro Glu Met Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Ala Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val
275 280 285
Asp Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu Gln
290 295 300
Phe Ala Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly His Gln
305 310 315 320
Asp Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn Lys Ala
325 330 335
Leu Pro Ser Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala
340 345 350
His Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu Ser
355 360 365
Lys Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro
370 375 380
Asp Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser
385 390 395 400
Lys Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe
405 410 415
Leu Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp
420 425 430
Thr Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His Tyr Thr
435 440 445
Gln Glu Ser Leu Ser His Ser Pro Gly Lys
450 455
<210> 31
<211> 645
<212> ДНК
<213> Искусственная последовательность
<220>
<223> мышиная-собачья химера
<400> 31
caggcggtgg tgacccagga aagcgcgttt accaccagcc cgggcggcac cgtgattctg 60
acctgccgca gcagcaccgg cgcggtgacc accaacaact atgcgaactg ggtgcaggaa 120
aaaccggatc atctgtttac cggcctgatt ggcggcacca gcaaccgcgc gccgggcgtg 180
ccggtgcgct ttagcggcag cctgattggc gataaagcgg cgctgaccat taccggcgcg 240
cagaccgaag atgatggcat gtatttttgc gcgctgtggt ataccaccca ttttgtgttt 300
ggcggcggca ccaaagtgac cgtgctgggc cagccgaaag cgagcccgag cgtgaccctg 360
tttccgccga gcagcgaaga actgggcgcg aacaaagcga ccctggtgtg cctgattagc 420
gatttttatc cgagcggcgt gaccgtggcg tggaaagcgg atggcagccc gattacccag 480
ggcgtggaaa ccaccaaacc gagcaaacag agcaacaaca aatatgcggc gagcagctat 540
ctgagcctga ccccggataa atggaaaagc catagcagct ttagctgcct ggtgacccat 600
gaaggcagca ccgtggaaaa aaaagtggcg ccggcggaat gcagc 645
<210> 32
<211> 215
<212> PRT
<213> Искусственная последовательность
<220>
<223> мышиная-собачья химера
<400> 32
Gln Ala Val Val Thr Gln Glu Ser Ala Phe Thr Thr Ser Pro Gly Gly
1 5 10 15
Thr Val Ile Leu Thr Cys Arg Ser Ser Thr Gly Ala Val Thr Thr Asn
20 25 30
Asn Tyr Ala Asn Trp Val Gln Glu Lys Pro Asp His Leu Phe Thr Gly
35 40 45
Leu Ile Gly Gly Thr Ser Asn Arg Ala Pro Gly Val Pro Val Arg Phe
50 55 60
Ser Gly Ser Leu Ile Gly Asp Lys Ala Ala Leu Thr Ile Thr Gly Ala
65 70 75 80
Gln Thr Glu Asp Asp Gly Met Tyr Phe Cys Ala Leu Trp Tyr Thr Thr
85 90 95
His Phe Val Phe Gly Gly Gly Thr Lys Val Thr Val Leu Gly Gln Pro
100 105 110
Lys Ala Ser Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu Glu Leu
115 120 125
Gly Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe Tyr Pro
130 135 140
Ser Gly Val Thr Val Ala Trp Lys Ala Asp Gly Ser Pro Ile Thr Gln
145 150 155 160
Gly Val Glu Thr Thr Lys Pro Ser Lys Gln Ser Asn Asn Lys Tyr Ala
165 170 175
Ala Ser Ser Tyr Leu Ser Leu Thr Pro Asp Lys Trp Lys Ser His Ser
180 185 190
Ser Phe Ser Cys Leu Val Thr His Glu Gly Ser Thr Val Glu Lys Lys
195 200 205
Val Ala Pro Ala Glu Cys Ser
210 215
<210> 33
<211> 1365
<212> ДНК
<213> Искусственная последовательность
<220>
<223> канинизированное мышиное антитело
<400> 33
gaagtgcagc tggtgcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cgagcggcta tacctttacc gattataaca tggattgggt gcgccaggcg 120
ccgggcgcgg gcctggattg gatgggcaac attaacccga acagcgaaag caccagctat 180
aaccagaaat ttaaaggccg cgtgaccctg accgcggata ccagcaccag caccgcgtat 240
atggaactga gcagcctgcg cgcgggcgat attgcggtgt attattgcac ccgcgatggc 300
aaccgctatg atgcgtggtt tgcgtattgg ggccagggca ccctggtgac cgtgagcagc 360
gcgagcacca ccgcgccgag cgtgtttccg ctggcgccga gctgcggcag caccagcggc 420
agcaccgtgg cgctggcgtg cctggtgagc ggctattttc cggaaccggt gaccgtgagc 480
tggaacagcg gcagcctgac cagcggcgtg catacctttc cgagcgtgct gcagagcagc 540
ggcctgtata gcctgagcag catggtgacc gtgccgagca gccgctggcc gagcgaaacc 600
tttacctgca acgtggcgca tccggcgagc aaaaccaaag tggataaacc ggtgccgaaa 660
cgcgaaaacg gccgcgtgcc gcgcccgccg gattgcccga aatgcccggc gccggaaatg 720
ctgggcggcc cgagcgtgtt tatttttccg ccgaaaccga aagataccct gctgattgcg 780
cgcaccccgg aagtgacctg cgtggtggtg gatctggatc cggaagatcc ggaagtgcag 840
attagctggt ttgtggatgg caaacagatg cagaccgcga aaacccagcc gcgcgaagaa 900
cagtttaacg gcacctatcg cgtggtgagc gtgctgccga ttggccatca ggattggctg 960
aaaggcaaac agtttacctg caaagtgaac aacaaagcgc tgccgagccc gattgaacgc 1020
accattagca aagcgcgcgg ccaggcgcat cagccgagcg tgtatgtgct gccgccgagc 1080
cgcgaagaac tgagcaaaaa caccgtgagc ctgacctgcc tgattaaaga tttttttccg 1140
ccggatattg atgtggaatg gcagagcaac ggccagcagg aaccggaaag caaatatcgc 1200
accaccccgc cgcagctgga tgaagatggc agctattttc tgtatagcaa actgagcgtg 1260
gataaaagcc gctggcagcg cggcgatacc tttatttgcg cggtgatgca tgaagcgctg 1320
cataaccatt atacccagga aagcctgagc catagcccgg gcaaa 1365
<210> 34
<211> 455
<212> PRT
<213> Искусственная последовательность
<220>
<223> канинизированное мышиное антитело
<400> 34
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met Asp Trp Val Arg Gln Ala Pro Gly Ala Gly Leu Asp Trp Met
35 40 45
Gly Asn Ile Asn Pro Asn Ser Glu Ser Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ala Gly Asp Ile Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Asp Gly Asn Arg Tyr Asp Ala Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Thr Ala Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser Gly Ser Thr Val Ala
130 135 140
Leu Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ser Leu Thr Ser Gly Val His Thr Phe Pro Ser Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Met Val Thr Val Pro
180 185 190
Ser Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys Asn Val Ala His Pro
195 200 205
Ala Ser Lys Thr Lys Val Asp Lys Pro Val Pro Lys Arg Glu Asn Gly
210 215 220
Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys Pro Ala Pro Glu Met
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Leu
260 265 270
Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val Asp Gly Lys
275 280 285
Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu Gln Phe Asn Gly
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly His Gln Asp Trp Leu
305 310 315 320
Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn Lys Ala Leu Pro Ser
325 330 335
Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala His Gln Pro
340 345 350
Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu Ser Lys Asn Thr
355 360 365
Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro Asp Ile Asp
370 375 380
Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser Lys Tyr Arg
385 390 395 400
Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu Tyr Ser
405 410 415
Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp Thr Phe Ile
420 425 430
Cys Ala Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Glu Ser
435 440 445
Leu Ser His Ser Pro Gly Lys
450 455
<210> 35
<211> 1365
<212> ДНК
<213> Искусственная последовательность
<220>
<223> канинизированное мышиное антитело
<400> 35
gaagtgcagc tggtgcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cgagcggcta tacctttacc gattataaca tggattgggt gcgccaggcg 120
ccgggcgcga gcctggattg gattggcaac attaacccga acagcgaaag caccagctat 180
aaccagaaat ttaaaggcaa agcgaccctg accgtggata aaagcaccag caccgcgtat 240
atggaactga gcagcctgcg cgcgggcgat attgcggtgt attattgcac ccgcgatggc 300
aaccgctatg atgcgtggtt tgcgtattgg ggccagggca ccctggtgac cgtgagcagc 360
gcgagcacca ccgcgccgag cgtgtttccg ctggcgccga gctgcggcag caccagcggc 420
agcaccgtgg cgctggcgtg cctggtgagc ggctattttc cggaaccggt gaccgtgagc 480
tggaacagcg gcagcctgac cagcggcgtg catacctttc cgagcgtgct gcagagcagc 540
ggcctgtata gcctgagcag catggtgacc gtgccgagca gccgctggcc gagcgaaacc 600
tttacctgca acgtggcgca tccggcgagc aaaaccaaag tggataaacc ggtgccgaaa 660
cgcgaaaacg gccgcgtgcc gcgcccgccg gattgcccga aatgcccggc gccggaaatg 720
ctgggcggcc cgagcgtgtt tatttttccg ccgaaaccga aagataccct gctgattgcg 780
cgcaccccgg aagtgacctg cgtggtggtg gatctggatc cggaagatcc ggaagtgcag 840
attagctggt ttgtggatgg caaacagatg cagaccgcga aaacccagcc gcgcgaagaa 900
cagtttaacg gcacctatcg cgtggtgagc gtgctgccga ttggccatca ggattggctg 960
aaaggcaaac agtttacctg caaagtgaac aacaaagcgc tgccgagccc gattgaacgc 1020
accattagca aagcgcgcgg ccaggcgcat cagccgagcg tgtatgtgct gccgccgagc 1080
cgcgaagaac tgagcaaaaa caccgtgagc ctgacctgcc tgattaaaga tttttttccg 1140
ccggatattg atgtggaatg gcagagcaac ggccagcagg aaccggaaag caaatatcgc 1200
accaccccgc cgcagctgga tgaagatggc agctattttc tgtatagcaa actgagcgtg 1260
gataaaagcc gctggcagcg cggcgatacc tttatttgcg cggtgatgca tgaagcgctg 1320
cataaccatt atacccagga aagcctgagc catagcccgg gcaaa 1365
<210> 36
<211> 455
<212> PRT
<213> Искусственная последовательность
<220>
<223> канинизированное мышиное антитело
<400> 36
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met Asp Trp Val Arg Gln Ala Pro Gly Ala Ser Leu Asp Trp Ile
35 40 45
Gly Asn Ile Asn Pro Asn Ser Glu Ser Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ala Gly Asp Ile Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Asp Gly Asn Arg Tyr Asp Ala Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Thr Ala Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser Gly Ser Thr Val Ala
130 135 140
Leu Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ser Leu Thr Ser Gly Val His Thr Phe Pro Ser Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Met Val Thr Val Pro
180 185 190
Ser Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys Asn Val Ala His Pro
195 200 205
Ala Ser Lys Thr Lys Val Asp Lys Pro Val Pro Lys Arg Glu Asn Gly
210 215 220
Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys Pro Ala Pro Glu Met
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Leu
260 265 270
Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val Asp Gly Lys
275 280 285
Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu Gln Phe Asn Gly
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly His Gln Asp Trp Leu
305 310 315 320
Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn Lys Ala Leu Pro Ser
325 330 335
Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala His Gln Pro
340 345 350
Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu Ser Lys Asn Thr
355 360 365
Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro Asp Ile Asp
370 375 380
Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser Lys Tyr Arg
385 390 395 400
Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu Tyr Ser
405 410 415
Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp Thr Phe Ile
420 425 430
Cys Ala Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Glu Ser
435 440 445
Leu Ser His Ser Pro Gly Lys
450 455
<210> 37
<211> 1365
<212> ДНК
<213> Искусственная последовательность
<220>
<223> канинизированное мышиное антитело
<400> 37
gaagtgcagc tggtgcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cgagcggcta tacctttacc gattataaca tggattgggt gcgccaggcg 120
catggcgcga gcctggattg gattggcaac attaacccga acagcgaaag caccagctat 180
aaccagaaat ttaaaggcaa agcgaccctg accgtggata aaagcaccag caccgcgtat 240
atggaactga gcagcctgcg cgcgggcgat attgcggtgt attattgcac ccgcgatggc 300
aaccgctatg atgcgtggtt tgcgtattgg ggccagggca ccctggtgac cgtgagcagc 360
gcgagcacca ccgcgccgag cgtgtttccg ctggcgccga gctgcggcag caccagcggc 420
agcaccgtgg cgctggcgtg cctggtgagc ggctattttc cggaaccggt gaccgtgagc 480
tggaacagcg gcagcctgac cagcggcgtg catacctttc cgagcgtgct gcagagcagc 540
ggcctgtata gcctgagcag catggtgacc gtgccgagca gccgctggcc gagcgaaacc 600
tttacctgca acgtggcgca tccggcgagc aaaaccaaag tggataaacc ggtgccgaaa 660
cgcgaaaacg gccgcgtgcc gcgcccgccg gattgcccga aatgcccggc gccggaaatg 720
ctgggcggcc cgagcgtgtt tatttttccg ccgaaaccga aagataccct gctgattgcg 780
cgcaccccgg aagtgacctg cgtggtggtg gatctggatc cggaagatcc ggaagtgcag 840
attagctggt ttgtggatgg caaacagatg cagaccgcga aaacccagcc gcgcgaagaa 900
cagtttaacg gcacctatcg cgtggtgagc gtgctgccga ttggccatca ggattggctg 960
aaaggcaaac agtttacctg caaagtgaac aacaaagcgc tgccgagccc gattgaacgc 1020
accattagca aagcgcgcgg ccaggcgcat cagccgagcg tgtatgtgct gccgccgagc 1080
cgcgaagaac tgagcaaaaa caccgtgagc ctgacctgcc tgattaaaga tttttttccg 1140
ccggatattg atgtggaatg gcagagcaac ggccagcagg aaccggaaag caaatatcgc 1200
accaccccgc cgcagctgga tgaagatggc agctattttc tgtatagcaa actgagcgtg 1260
gataaaagcc gctggcagcg cggcgatacc tttatttgcg cggtgatgca tgaagcgctg 1320
cataaccatt atacccagga aagcctgagc catagcccgg gcaaa 1365
<210> 38
<211> 455
<212> PRT
<213> Искусственная последовательность
<220>
<223> канинизированное мышиное антитело
<400> 38
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met Asp Trp Val Arg Gln Ala His Gly Ala Ser Leu Asp Trp Ile
35 40 45
Gly Asn Ile Asn Pro Asn Ser Glu Ser Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ala Gly Asp Ile Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Asp Gly Asn Arg Tyr Asp Ala Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Thr Ala Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser Gly Ser Thr Val Ala
130 135 140
Leu Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ser Leu Thr Ser Gly Val His Thr Phe Pro Ser Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Met Val Thr Val Pro
180 185 190
Ser Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys Asn Val Ala His Pro
195 200 205
Ala Ser Lys Thr Lys Val Asp Lys Pro Val Pro Lys Arg Glu Asn Gly
210 215 220
Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys Pro Ala Pro Glu Met
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Leu
260 265 270
Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val Asp Gly Lys
275 280 285
Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu Gln Phe Asn Gly
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly His Gln Asp Trp Leu
305 310 315 320
Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn Lys Ala Leu Pro Ser
325 330 335
Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala His Gln Pro
340 345 350
Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu Ser Lys Asn Thr
355 360 365
Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro Asp Ile Asp
370 375 380
Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser Lys Tyr Arg
385 390 395 400
Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu Tyr Ser
405 410 415
Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp Thr Phe Ile
420 425 430
Cys Ala Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Glu Ser
435 440 445
Leu Ser His Ser Pro Gly Lys
450 455
<210> 39
<211> 1365
<212> ДНК
<213> Искусственная последовательность
<220>
<223> канинизированное мышиное антитело
<400> 39
gaagtgcagc tgcagcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cgagcggcta tacctttacc gattataaca tggattgggt gcgccaggcg 120
ccgggcgcga gcctggattg gattggcaac attaacccga acagcgaaag caccagctat 180
aaccagaaat ttaaaggcaa agcgaccctg accgtggata aaagcaccag caccgcgtat 240
atggaactgc gcagcctgac cgcgggcgat attgcggtgt attattgcac ccgcgatggc 300
aaccgctatg atgcgtggtt tgcgtattgg ggccagggca ccctggtgac cgtgagcagc 360
gcgagcacca ccgcgccgag cgtgtttccg ctggcgccga gctgcggcag caccagcggc 420
agcaccgtgg cgctggcgtg cctggtgagc ggctattttc cggaaccggt gaccgtgagc 480
tggaacagcg gcagcctgac cagcggcgtg catacctttc cgagcgtgct gcagagcagc 540
ggcctgtata gcctgagcag catggtgacc gtgccgagca gccgctggcc gagcgaaacc 600
tttacctgca acgtggcgca tccggcgagc aaaaccaaag tggataaacc ggtgccgaaa 660
cgcgaaaacg gccgcgtgcc gcgcccgccg gattgcccga aatgcccggc gccggaaatg 720
ctgggcggcc cgagcgtgtt tatttttccg ccgaaaccga aagataccct gctgattgcg 780
cgcaccccgg aagtgacctg cgtggtggtg gatctggatc cggaagatcc ggaagtgcag 840
attagctggt ttgtggatgg caaacagatg cagaccgcga aaacccagcc gcgcgaagaa 900
cagtttaacg gcacctatcg cgtggtgagc gtgctgccga ttggccatca ggattggctg 960
aaaggcaaac agtttacctg caaagtgaac aacaaagcgc tgccgagccc gattgaacgc 1020
accattagca aagcgcgcgg ccaggcgcat cagccgagcg tgtatgtgct gccgccgagc 1080
cgcgaagaac tgagcaaaaa caccgtgagc ctgacctgcc tgattaaaga tttttttccg 1140
ccggatattg atgtggaatg gcagagcaac ggccagcagg aaccggaaag caaatatcgc 1200
accaccccgc cgcagctgga tgaagatggc agctattttc tgtatagcaa actgagcgtg 1260
gataaaagcc gctggcagcg cggcgatacc tttatttgcg cggtgatgca tgaagcgctg 1320
cataaccatt atacccagga aagcctgagc catagcccgg gcaaa 1365
<210> 40
<211> 455
<212> PRT
<213> Искусственная последовательность
<220>
<223> канинизированное мышиное антитело
<400> 40
Glu Val Gln Leu Gln Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met Asp Trp Val Arg Gln Ala Pro Gly Ala Ser Leu Asp Trp Ile
35 40 45
Gly Asn Ile Asn Pro Asn Ser Glu Ser Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ala Gly Asp Ile Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Asp Gly Asn Arg Tyr Asp Ala Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Thr Ala Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser Gly Ser Thr Val Ala
130 135 140
Leu Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ser Leu Thr Ser Gly Val His Thr Phe Pro Ser Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Met Val Thr Val Pro
180 185 190
Ser Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys Asn Val Ala His Pro
195 200 205
Ala Ser Lys Thr Lys Val Asp Lys Pro Val Pro Lys Arg Glu Asn Gly
210 215 220
Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys Pro Ala Pro Glu Met
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Leu
260 265 270
Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val Asp Gly Lys
275 280 285
Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu Gln Phe Asn Gly
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly His Gln Asp Trp Leu
305 310 315 320
Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn Lys Ala Leu Pro Ser
325 330 335
Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala His Gln Pro
340 345 350
Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu Ser Lys Asn Thr
355 360 365
Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro Asp Ile Asp
370 375 380
Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser Lys Tyr Arg
385 390 395 400
Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu Tyr Ser
405 410 415
Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp Thr Phe Ile
420 425 430
Cys Ala Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Glu Ser
435 440 445
Leu Ser His Ser Pro Gly Lys
450 455
<210> 41
<211> 651
<212> ДНК
<213> Искусственная последовательность
<220>
<223> канинизированное мышиное антитело
<400> 41
gatattgtga tgacccagac cccgctgagc ctgagcgtga gcccgggcga accggcgagc 60
attagctgca gcgcgagcag cagcgtgacc tatatgcatt ggtttcgcca taaaccgggc 120
cagagcccgc agagcctgat ttatagcacc agcattctgg cgagcggcgt gccggatcgc 180
tttagcggca gcggcagcgg caccgatttt accctgaaaa ttagccgcgt ggaagcggat 240
gatgcgggcg tgtattattg ccagcagcgc accagctatc cgctgacctt tggcaccggc 300
accaaactgg aactgaaacg caacgatgcg cagccggcgg tgtatctgtt tcagccgagc 360
ccggatcagc tgcataccgg cagcgcgagc gtggtgtgcc tgctgaacag cttttatccg 420
aaagatatta acgtgaaatg gaaagtggat ggcgtgattc aggataccgg cattcaggaa 480
agcgtgaccg aacaggatag caaagatagc acctatagcc tgagcagcac cctgaccatg 540
agcagcaccg aatatctgag ccatgaactg tatagctgcg aaattaccca taaaagcctg 600
ccgagcaccc tgattaaaag ctttcagcgc agcgaatgcc agcgcgtgga t 651
<210> 42
<211> 217
<212> PRT
<213> Искусственная последовательность
<220>
<223> канинизированное мышиное антитело
<400> 42
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Ser Ala Ser Ser Ser Val Thr Tyr Met
20 25 30
His Trp Phe Arg His Lys Pro Gly Gln Ser Pro Gln Ser Leu Ile Tyr
35 40 45
Ser Thr Ser Ile Leu Ala Ser Gly Val Pro Asp Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Asp
65 70 75 80
Asp Ala Gly Val Tyr Tyr Cys Gln Gln Arg Thr Ser Tyr Pro Leu Thr
85 90 95
Phe Gly Thr Gly Thr Lys Leu Glu Leu Lys Arg Asn Asp Ala Gln Pro
100 105 110
Ala Val Tyr Leu Phe Gln Pro Ser Pro Asp Gln Leu His Thr Gly Ser
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Ser Phe Tyr Pro Lys Asp Ile Asn
130 135 140
Val Lys Trp Lys Val Asp Gly Val Ile Gln Asp Thr Gly Ile Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Met Ser Ser Thr Glu Tyr Leu Ser His Glu Leu Tyr Ser
180 185 190
Cys Glu Ile Thr His Lys Ser Leu Pro Ser Thr Leu Ile Lys Ser Phe
195 200 205
Gln Arg Ser Glu Cys Gln Arg Val Asp
210 215
<210> 43
<211> 651
<212> ДНК
<213> Искусственная последовательность
<220>
<223> канинизированное мышиное антитело
<400> 43
cagattgtga tgacccagac cccgctgagc ctgagcgtga gcccgggcga accggcgagc 60
attagctgca gcgcgagcag cagcgtgacc tatatgcatt ggtttcagca gaaaccgggc 120
cagagcccgc agagcctgat ttatagcacc agcattctgg cgagcggcgt gccggatcgc 180
tttagcggca gcggcagcgg caccgatttt accctgaaaa ttagccgcgt ggaagcggat 240
gatgcgggcg tgtattattg ccagcagcgc accagctatc cgctgacctt tggcaccggc 300
accaaactgg aactgaaacg caacgatgcg cagccggcgg tgtatctgtt tcagccgagc 360
ccggatcagc tgcataccgg cagcgcgagc gtggtgtgcc tgctgaacag cttttatccg 420
aaagatatta acgtgaaatg gaaagtggat ggcgtgattc aggataccgg cattcaggaa 480
agcgtgaccg aacaggatag caaagatagc acctatagcc tgagcagcac cctgaccatg 540
agcagcaccg aatatctgag ccatgaactg tatagctgcg aaattaccca taaaagcctg 600
ccgagcaccc tgattaaaag ctttcagcgc agcgaatgcc agcgcgtgga t 651
<210> 44
<211> 217
<212> PRT
<213> Искусственная последовательность
<220>
<223> канинизированное мышиное антитело
<400> 44
Gln Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Ser Ala Ser Ser Ser Val Thr Tyr Met
20 25 30
His Trp Phe Gln Gln Lys Pro Gly Gln Ser Pro Gln Ser Leu Ile Tyr
35 40 45
Ser Thr Ser Ile Leu Ala Ser Gly Val Pro Asp Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Asp
65 70 75 80
Asp Ala Gly Val Tyr Tyr Cys Gln Gln Arg Thr Ser Tyr Pro Leu Thr
85 90 95
Phe Gly Thr Gly Thr Lys Leu Glu Leu Lys Arg Asn Asp Ala Gln Pro
100 105 110
Ala Val Tyr Leu Phe Gln Pro Ser Pro Asp Gln Leu His Thr Gly Ser
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Ser Phe Tyr Pro Lys Asp Ile Asn
130 135 140
Val Lys Trp Lys Val Asp Gly Val Ile Gln Asp Thr Gly Ile Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Met Ser Ser Thr Glu Tyr Leu Ser His Glu Leu Tyr Ser
180 185 190
Cys Glu Ile Thr His Lys Ser Leu Pro Ser Thr Leu Ile Lys Ser Phe
195 200 205
Gln Arg Ser Glu Cys Gln Arg Val Asp
210 215
<210> 45
<211> 651
<212> ДНК
<213> Искусственная последовательность
<220>
<223> канинизированное мышиное антитело
<400> 45
cagattgtgc tgacccagac cccgctgagc ctgagcgtga gcccgggcga accggcgagc 60
attagctgca gcgcgagcag cagcgtgacc tatatgcatt ggtttcagca gaaaccgggc 120
cagagcccga aaagctggat ttatagcacc agcattctgg cgagcggcgt gccggatcgc 180
tttagcggca gcggcagcgg caccgatttt accctgaaaa ttagccgcgt ggaagcggat 240
gatgcgggcg tgtattattg ccagcagcgc accagctatc cgctgacctt tggcaccggc 300
accaaactgg aactgaaacg caacgatgcg cagccggcgg tgtatctgtt tcagccgagc 360
ccggatcagc tgcataccgg cagcgcgagc gtggtgtgcc tgctgaacag cttttatccg 420
aaagatatta acgtgaaatg gaaagtggat ggcgtgattc aggataccgg cattcaggaa 480
agcgtgaccg aacaggatag caaagatagc acctatagcc tgagcagcac cctgaccatg 540
agcagcaccg aatatctgag ccatgaactg tatagctgcg aaattaccca taaaagcctg 600
ccgagcaccc tgattaaaag ctttcagcgc agcgaatgcc agcgcgtgga t 651
<210> 46
<211> 217
<212> PRT
<213> Искусственная последовательность
<220>
<223> канинизированное мышиное антитело
<400> 46
Gln Ile Val Leu Thr Gln Thr Pro Leu Ser Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Ser Ala Ser Ser Ser Val Thr Tyr Met
20 25 30
His Trp Phe Gln Gln Lys Pro Gly Gln Ser Pro Lys Ser Trp Ile Tyr
35 40 45
Ser Thr Ser Ile Leu Ala Ser Gly Val Pro Asp Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Asp
65 70 75 80
Asp Ala Gly Val Tyr Tyr Cys Gln Gln Arg Thr Ser Tyr Pro Leu Thr
85 90 95
Phe Gly Thr Gly Thr Lys Leu Glu Leu Lys Arg Asn Asp Ala Gln Pro
100 105 110
Ala Val Tyr Leu Phe Gln Pro Ser Pro Asp Gln Leu His Thr Gly Ser
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Ser Phe Tyr Pro Lys Asp Ile Asn
130 135 140
Val Lys Trp Lys Val Asp Gly Val Ile Gln Asp Thr Gly Ile Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Met Ser Ser Thr Glu Tyr Leu Ser His Glu Leu Tyr Ser
180 185 190
Cys Glu Ile Thr His Lys Ser Leu Pro Ser Thr Leu Ile Lys Ser Phe
195 200 205
Gln Arg Ser Glu Cys Gln Arg Val Asp
210 215
<210> 47
<211> 15
<212> ДНК
<213> Mus musculus
<400> 47
gattataaca tggat 15
<210> 48
<211> 5
<212> PRT
<213> Mus musculus
<400> 48
Asp Tyr Asn Met Asp
1 5
<210> 49
<211> 51
<212> ДНК
<213> Mus musculus
<400> 49
aacattaacc cgaacagcga aagcaccagc tataaccaga aatttaaagg c 51
<210> 50
<211> 17
<212> PRT
<213> Mus musculus
<400> 50
Asn Ile Asn Pro Asn Ser Glu Ser Thr Ser Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 51
<211> 33
<212> ДНК
<213> Mus musculus
<400> 51
gatggcaacc gctatgatgc gtggtttgcg tat 33
<210> 52
<211> 11
<212> PRT
<213> Mus musculus
<400> 52
Asp Gly Asn Arg Tyr Asp Ala Trp Phe Ala Tyr
1 5 10
<210> 53
<211> 30
<212> ДНК
<213> Mus musculus
<400> 53
agcgcgagca gcagcgtgac ctatatgcat 30
<210> 54
<211> 10
<212> PRT
<213> Mus musculus
<400> 54
Ser Ala Ser Ser Ser Val Thr Tyr Met His
1 5 10
<210> 55
<211> 21
<212> ДНК
<213> Mus musculus
<400> 55
agcaccagca ttctggcgag c 21
<210> 56
<211> 7
<212> PRT
<213> Mus musculus
<400> 56
Ser Thr Ser Ile Leu Ala Ser
1 5
<210> 57
<211> 27
<212> ДНК
<213> Mus musculus
<400> 57
cagcagcgca ccagctatcc gctgacc 27
<210> 58
<211> 9
<212> PRT
<213> Mus musculus
<400> 58
Gln Gln Arg Thr Ser Tyr Pro Leu Thr
1 5
<210> 59
<211> 1365
<212> ДНК
<213> Искусственная последовательность
<220>
<223> канинизированное мышиное антитело
<400> 59
gaagtgcagc tggtgcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cgagcggcta tacctttacc gattataaca tggattgggt gcgccaggcg 120
ccgggcgcgg gcctggattg gatgggcaac attaacccga acagcgaaag caccagctat 180
aaccagaaat ttaaaggccg cgtgaccctg accgcggata ccagcaccag caccgcgtat 240
atggaactga gcagcctgcg cgcgggcgat attgcggtgt attattgcac ccgcgatggc 300
aaccgctatg atgcgtggtt tgcgtattgg ggccagggca ccctggtgac cgtgagcagc 360
gcgagcacca ccgcgccgag cgtgtttccg ctggcgccga gctgcggcag caccagcggc 420
agcaccgtgg cgctggcgtg cctggtgagc ggctattttc cggaaccggt gaccgtgagc 480
tggaacagcg gcagcctgac cagcggcgtg catacctttc cgagcgtgct gcagagcagc 540
ggcctgtata gcctgagcag catggtgacc gtgccgagca gccgctggcc gagcgaaacc 600
tttacctgca acgtggcgca tccggcgagc aaaaccaaag tggataaacc ggtgccgaaa 660
cgcgaaaacg gccgcgtgcc gcgcccgccg gattgcccga aatgcccggc gccggaaatg 720
ctgggcggcc cgagcgtgtt tatttttccg ccgaaaccga aagataccct gctgattgcg 780
cgcaccccgg aagtgacctg cgtggtggtg gcgctggatc cggaagatcc ggaagtgcag 840
attagctggt ttgtggatgg caaacagatg cagaccgcga aaacccagcc gcgcgaagaa 900
cagtttgccg gcacctatcg cgtggtgagc gtgctgccga ttggccatca ggattggctg 960
aaaggcaaac agtttacctg caaagtgaac aacaaagcgc tgccgagccc gattgaacgc 1020
accattagca aagcgcgcgg ccaggcgcat cagccgagcg tgtatgtgct gccgccgagc 1080
cgcgaagaac tgagcaaaaa caccgtgagc ctgacctgcc tgattaaaga tttttttccg 1140
ccggatattg atgtggaatg gcagagcaac ggccagcagg aaccggaaag caaatatcgc 1200
accaccccgc cgcagctgga tgaagatggc agctattttc tgtatagcaa actgagcgtg 1260
gataaaagcc gctggcagcg cggcgatacc tttatttgcg cggtgatgca tgaagcgctg 1320
cataaccatt atacccagga aagcctgagc catagcccgg gcaaa 1365
<210> 60
<211> 455
<212> PRT
<213> Искусственная последовательность
<220>
<223> канинизированное мышиное антитело
<400> 60
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met Asp Trp Val Arg Gln Ala Pro Gly Ala Gly Leu Asp Trp Met
35 40 45
Gly Asn Ile Asn Pro Asn Ser Glu Ser Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ala Gly Asp Ile Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Asp Gly Asn Arg Tyr Asp Ala Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Thr Ala Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser Gly Ser Thr Val Ala
130 135 140
Leu Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ser Leu Thr Ser Gly Val His Thr Phe Pro Ser Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Met Val Thr Val Pro
180 185 190
Ser Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys Asn Val Ala His Pro
195 200 205
Ala Ser Lys Thr Lys Val Asp Lys Pro Val Pro Lys Arg Glu Asn Gly
210 215 220
Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys Pro Ala Pro Glu Met
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val Ala Leu
260 265 270
Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val Asp Gly Lys
275 280 285
Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu Gln Phe Ala Gly
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly His Gln Asp Trp Leu
305 310 315 320
Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn Lys Ala Leu Pro Ser
325 330 335
Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala His Gln Pro
340 345 350
Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu Ser Lys Asn Thr
355 360 365
Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro Asp Ile Asp
370 375 380
Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser Lys Tyr Arg
385 390 395 400
Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu Tyr Ser
405 410 415
Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp Thr Phe Ile
420 425 430
Cys Ala Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Glu Ser
435 440 445
Leu Ser His Ser Pro Gly Lys
450 455
<210> 61
<211> 1365
<212> ДНК
<213> Искусственная последовательность
<220>
<223> канинизированное мышиное антитело
<400> 61
gaagtgcagc tggtgcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cgagcggcta tacctttacc gattataaca tggattgggt gcgccaggcg 120
ccgggcgcga gcctggattg gattggcaac attaacccga acagcgaaag caccagctat 180
aaccagaaat ttaaaggcaa agcgaccctg accgtggata aaagcaccag caccgcgtat 240
atggaactga gcagcctgcg cgcgggcgat attgcggtgt attattgcac ccgcgatggc 300
aaccgctatg atgcgtggtt tgcgtattgg ggccagggca ccctggtgac cgtgagcagc 360
gcgagcacca ccgcgccgag cgtgtttccg ctggcgccga gctgcggcag caccagcggc 420
agcaccgtgg cgctggcgtg cctggtgagc ggctattttc cggaaccggt gaccgtgagc 480
tggaacagcg gcagcctgac cagcggcgtg catacctttc cgagcgtgct gcagagcagc 540
ggcctgtata gcctgagcag catggtgacc gtgccgagca gccgctggcc gagcgaaacc 600
tttacctgca acgtggcgca tccggcgagc aaaaccaaag tggataaacc ggtgccgaaa 660
cgcgaaaacg gccgcgtgcc gcgcccgccg gattgcccga aatgcccggc gccggaaatg 720
ctgggcggcc cgagcgtgtt tatttttccg ccgaaaccga aagataccct gctgattgcg 780
cgcaccccgg aagtgacctg cgtggtggtg gcgctggatc cggaagatcc ggaagtgcag 840
attagctggt ttgtggatgg caaacagatg cagaccgcga aaacccagcc gcgcgaagaa 900
cagtttgccg gcacctatcg cgtggtgagc gtgctgccga ttggccatca ggattggctg 960
aaaggcaaac agtttacctg caaagtgaac aacaaagcgc tgccgagccc gattgaacgc 1020
accattagca aagcgcgcgg ccaggcgcat cagccgagcg tgtatgtgct gccgccgagc 1080
cgcgaagaac tgagcaaaaa caccgtgagc ctgacctgcc tgattaaaga tttttttccg 1140
ccggatattg atgtggaatg gcagagcaac ggccagcagg aaccggaaag caaatatcgc 1200
accaccccgc cgcagctgga tgaagatggc agctattttc tgtatagcaa actgagcgtg 1260
gataaaagcc gctggcagcg cggcgatacc tttatttgcg cggtgatgca tgaagcgctg 1320
cataaccatt atacccagga aagcctgagc catagcccgg gcaaa 1365
<210> 62
<211> 455
<212> PRT
<213> Искусственная последовательность
<220>
<223> канинизированное мышиное антитело
<400> 62
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met Asp Trp Val Arg Gln Ala Pro Gly Ala Ser Leu Asp Trp Ile
35 40 45
Gly Asn Ile Asn Pro Asn Ser Glu Ser Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ala Gly Asp Ile Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Asp Gly Asn Arg Tyr Asp Ala Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Thr Ala Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser Gly Ser Thr Val Ala
130 135 140
Leu Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ser Leu Thr Ser Gly Val His Thr Phe Pro Ser Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Met Val Thr Val Pro
180 185 190
Ser Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys Asn Val Ala His Pro
195 200 205
Ala Ser Lys Thr Lys Val Asp Lys Pro Val Pro Lys Arg Glu Asn Gly
210 215 220
Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys Pro Ala Pro Glu Met
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val Ala Leu
260 265 270
Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val Asp Gly Lys
275 280 285
Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu Gln Phe Ala Gly
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly His Gln Asp Trp Leu
305 310 315 320
Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn Lys Ala Leu Pro Ser
325 330 335
Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala His Gln Pro
340 345 350
Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu Ser Lys Asn Thr
355 360 365
Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro Asp Ile Asp
370 375 380
Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser Lys Tyr Arg
385 390 395 400
Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu Tyr Ser
405 410 415
Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp Thr Phe Ile
420 425 430
Cys Ala Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Glu Ser
435 440 445
Leu Ser His Ser Pro Gly Lys
450 455
<210> 63
<211> 1365
<212> ДНК
<213> Искусственная последовательность
<220>
<223> канинизированное мышиное антитело
<400> 63
gaagtgcagc tggtgcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cgagcggcta tacctttacc gattataaca tggattgggt gcgccaggcg 120
catggcgcga gcctggattg gattggcaac attaacccga acagcgaaag caccagctat 180
aaccagaaat ttaaaggcaa agcgaccctg accgtggata aaagcaccag caccgcgtat 240
atggaactga gcagcctgcg cgcgggcgat attgcggtgt attattgcac ccgcgatggc 300
aaccgctatg atgcgtggtt tgcgtattgg ggccagggca ccctggtgac cgtgagcagc 360
gcgagcacca ccgcgccgag cgtgtttccg ctggcgccga gctgcggcag caccagcggc 420
agcaccgtgg cgctggcgtg cctggtgagc ggctattttc cggaaccggt gaccgtgagc 480
tggaacagcg gcagcctgac cagcggcgtg catacctttc cgagcgtgct gcagagcagc 540
ggcctgtata gcctgagcag catggtgacc gtgccgagca gccgctggcc gagcgaaacc 600
tttacctgca acgtggcgca tccggcgagc aaaaccaaag tggataaacc ggtgccgaaa 660
cgcgaaaacg gccgcgtgcc gcgcccgccg gattgcccga aatgcccggc gccggaaatg 720
ctgggcggcc cgagcgtgtt tatttttccg ccgaaaccga aagataccct gctgattgcg 780
cgcaccccgg aagtgacctg cgtggtggtg gcgctggatc cggaagatcc ggaagtgcag 840
attagctggt ttgtggatgg caaacagatg cagaccgcga aaacccagcc gcgcgaagaa 900
cagtttgccg gcacctatcg cgtggtgagc gtgctgccga ttggccatca ggattggctg 960
aaaggcaaac agtttacctg caaagtgaac aacaaagcgc tgccgagccc gattgaacgc 1020
accattagca aagcgcgcgg ccaggcgcat cagccgagcg tgtatgtgct gccgccgagc 1080
cgcgaagaac tgagcaaaaa caccgtgagc ctgacctgcc tgattaaaga tttttttccg 1140
ccggatattg atgtggaatg gcagagcaac ggccagcagg aaccggaaag caaatatcgc 1200
accaccccgc cgcagctgga tgaagatggc agctattttc tgtatagcaa actgagcgtg 1260
gataaaagcc gctggcagcg cggcgatacc tttatttgcg cggtgatgca tgaagcgctg 1320
cataaccatt atacccagga aagcctgagc catagcccgg gcaaa 1365
<210> 64
<211> 455
<212> PRT
<213> Искусственная последовательность
<220>
<223> канинизированное мышиное антитело
<400> 64
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met Asp Trp Val Arg Gln Ala His Gly Ala Ser Leu Asp Trp Ile
35 40 45
Gly Asn Ile Asn Pro Asn Ser Glu Ser Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ala Gly Asp Ile Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Asp Gly Asn Arg Tyr Asp Ala Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Thr Ala Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser Gly Ser Thr Val Ala
130 135 140
Leu Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ser Leu Thr Ser Gly Val His Thr Phe Pro Ser Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Met Val Thr Val Pro
180 185 190
Ser Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys Asn Val Ala His Pro
195 200 205
Ala Ser Lys Thr Lys Val Asp Lys Pro Val Pro Lys Arg Glu Asn Gly
210 215 220
Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys Pro Ala Pro Glu Met
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val Ala Leu
260 265 270
Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val Asp Gly Lys
275 280 285
Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu Gln Phe Ala Gly
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly His Gln Asp Trp Leu
305 310 315 320
Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn Lys Ala Leu Pro Ser
325 330 335
Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala His Gln Pro
340 345 350
Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu Ser Lys Asn Thr
355 360 365
Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro Asp Ile Asp
370 375 380
Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser Lys Tyr Arg
385 390 395 400
Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu Tyr Ser
405 410 415
Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp Thr Phe Ile
420 425 430
Cys Ala Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Glu Ser
435 440 445
Leu Ser His Ser Pro Gly Lys
450 455
<210> 65
<211> 1365
<212> ДНК
<213> Искусственная последовательность
<220>
<223> канинизированное мышиное антитело
<400> 65
gaagtgcagc tgcagcagag cggcgcggaa gtgaaaaaac cgggcgcgag cgtgaaagtg 60
agctgcaaag cgagcggcta tacctttacc gattataaca tggattgggt gcgccaggcg 120
ccgggcgcga gcctggattg gattggcaac attaacccga acagcgaaag caccagctat 180
aaccagaaat ttaaaggcaa agcgaccctg accgtggata aaagcaccag caccgcgtat 240
atggaactgc gcagcctgac cgcgggcgat attgcggtgt attattgcac ccgcgatggc 300
aaccgctatg atgcgtggtt tgcgtattgg ggccagggca ccctggtgac cgtgagcagc 360
gcgagcacca ccgcgccgag cgtgtttccg ctggcgccga gctgcggcag caccagcggc 420
agcaccgtgg cgctggcgtg cctggtgagc ggctattttc cggaaccggt gaccgtgagc 480
tggaacagcg gcagcctgac cagcggcgtg catacctttc cgagcgtgct gcagagcagc 540
ggcctgtata gcctgagcag catggtgacc gtgccgagca gccgctggcc gagcgaaacc 600
tttacctgca acgtggcgca tccggcgagc aaaaccaaag tggataaacc ggtgccgaaa 660
cgcgaaaacg gccgcgtgcc gcgcccgccg gattgcccga aatgcccggc gccggaaatg 720
ctgggcggcc cgagcgtgtt tatttttccg ccgaaaccga aagataccct gctgattgcg 780
cgcaccccgg aagtgacctg cgtggtggtg gcgctggatc cggaagatcc ggaagtgcag 840
attagctggt ttgtggatgg caaacagatg cagaccgcga aaacccagcc gcgcgaagaa 900
cagtttgccg gcacctatcg cgtggtgagc gtgctgccga ttggccatca ggattggctg 960
aaaggcaaac agtttacctg caaagtgaac aacaaagcgc tgccgagccc gattgaacgc 1020
accattagca aagcgcgcgg ccaggcgcat cagccgagcg tgtatgtgct gccgccgagc 1080
cgcgaagaac tgagcaaaaa caccgtgagc ctgacctgcc tgattaaaga tttttttccg 1140
ccggatattg atgtggaatg gcagagcaac ggccagcagg aaccggaaag caaatatcgc 1200
accaccccgc cgcagctgga tgaagatggc agctattttc tgtatagcaa actgagcgtg 1260
gataaaagcc gctggcagcg cggcgatacc tttatttgcg cggtgatgca tgaagcgctg 1320
cataaccatt atacccagga aagcctgagc catagcccgg gcaaa 1365
<210> 66
<211> 455
<212> PRT
<213> Искусственная последовательность
<220>
<223> канинизированное мышиное антитело
<400> 66
Glu Val Gln Leu Gln Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met Asp Trp Val Arg Gln Ala Pro Gly Ala Ser Leu Asp Trp Ile
35 40 45
Gly Asn Ile Asn Pro Asn Ser Glu Ser Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ala Gly Asp Ile Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Asp Gly Asn Arg Tyr Asp Ala Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Thr Ala Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Cys Gly Ser Thr Ser Gly Ser Thr Val Ala
130 135 140
Leu Ala Cys Leu Val Ser Gly Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ser Leu Thr Ser Gly Val His Thr Phe Pro Ser Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Met Val Thr Val Pro
180 185 190
Ser Ser Arg Trp Pro Ser Glu Thr Phe Thr Cys Asn Val Ala His Pro
195 200 205
Ala Ser Lys Thr Lys Val Asp Lys Pro Val Pro Lys Arg Glu Asn Gly
210 215 220
Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys Pro Ala Pro Glu Met
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val Ala Leu
260 265 270
Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val Asp Gly Lys
275 280 285
Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu Gln Phe Ala Gly
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly His Gln Asp Trp Leu
305 310 315 320
Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn Lys Ala Leu Pro Ser
325 330 335
Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala His Gln Pro
340 345 350
Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu Ser Lys Asn Thr
355 360 365
Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro Asp Ile Asp
370 375 380
Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser Lys Tyr Arg
385 390 395 400
Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu Tyr Ser
405 410 415
Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp Thr Phe Ile
420 425 430
Cys Ala Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Glu Ser
435 440 445
Leu Ser His Ser Pro Gly Lys
450 455
<210> 67
<211> 669
<212> ДНК
<213> Canis familiaris
<400> 67
atggcgggct ttggctttcg ccgccatggc gcgcagccgg atctggcgag ccgcacctgg 60
ccgtgcaccg cgctgtttag cctgctgttt attccggtgt ttagcaaagg catgcatgtg 120
gcgcagccgg cggtggtgct ggcgagcagc cgcggcgtgg cgagctttgt gtgcgaatat 180
ggcagcagcg gcaacgcggc ggaagtgcgc gtgaccgtgc tgcgccaggc gggcagccag 240
atgaccgaag tgtgcgcggc gacctatacc gtggaagatg aactggcgtt tctggatgat 300
agcacctgca ccggcaccag cagcggcaac aaagtgaacc tgaccattca gggcctgcgc 360
gcgatggata ccggcctgta tatttgcaaa gtggaactga tgtatccgcc gccgtattat 420
gtgggcatgg gcaacggcac ccagatttat gtgattgatc cggaaccgtg cccggatagc 480
gattttctgc tgtggattct ggcggcggtg agcagcggcc tgttttttta tagctttctg 540
attaccgcgg tgagcctgag caaaatgctg aaaaaacgca gcccgctgac caccggcgtg 600
tatgtgaaaa tgccgccgac cgaaccggaa tgcgaaaaac agtttcagcc gtattttatt 660
ccgattaac 669
<210> 68
<211> 223
<212> PRT
<213> Canis familiaris
<400> 68
Met Ala Gly Phe Gly Phe Arg Arg His Gly Ala Gln Pro Asp Leu Ala
1 5 10 15
Ser Arg Thr Trp Pro Cys Thr Ala Leu Phe Ser Leu Leu Phe Ile Pro
20 25 30
Val Phe Ser Lys Gly Met His Val Ala Gln Pro Ala Val Val Leu Ala
35 40 45
Ser Ser Arg Gly Val Ala Ser Phe Val Cys Glu Tyr Gly Ser Ser Gly
50 55 60
Asn Ala Ala Glu Val Arg Val Thr Val Leu Arg Gln Ala Gly Ser Gln
65 70 75 80
Met Thr Glu Val Cys Ala Ala Thr Tyr Thr Val Glu Asp Glu Leu Ala
85 90 95
Phe Leu Asp Asp Ser Thr Cys Thr Gly Thr Ser Ser Gly Asn Lys Val
100 105 110
Asn Leu Thr Ile Gln Gly Leu Arg Ala Met Asp Thr Gly Leu Tyr Ile
115 120 125
Cys Lys Val Glu Leu Met Tyr Pro Pro Pro Tyr Tyr Val Gly Met Gly
130 135 140
Asn Gly Thr Gln Ile Tyr Val Ile Asp Pro Glu Pro Cys Pro Asp Ser
145 150 155 160
Asp Phe Leu Leu Trp Ile Leu Ala Ala Val Ser Ser Gly Leu Phe Phe
165 170 175
Tyr Ser Phe Leu Ile Thr Ala Val Ser Leu Ser Lys Met Leu Lys Lys
180 185 190
Arg Ser Pro Leu Thr Thr Gly Val Tyr Val Lys Met Pro Pro Thr Glu
195 200 205
Pro Glu Cys Glu Lys Gln Phe Gln Pro Tyr Phe Ile Pro Ile Asn
210 215 220
<210> 69
<211> 215
<212> PRT
<213> Искусственная последовательность
<220>
<223> модифицированная собачья
<400> 69
Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys Asp Thr
1 5 10 15
Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val Ala Leu
20 25 30
Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val Asp Gly Lys
35 40 45
Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu Gln Phe Ala Gly
50 55 60
Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly His Gln Asp Trp Leu
65 70 75 80
Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn Lys Ala Leu Pro Ser
85 90 95
Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala His Gln Pro
100 105 110
Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu Ser Lys Asn Thr
115 120 125
Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro Asp Ile Asp
130 135 140
Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser Lys Tyr Arg
145 150 155 160
Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu Tyr Ser
165 170 175
Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp Thr Phe Ile
180 185 190
Cys Ala Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Glu Ser
195 200 205
Leu Ser His Ser Pro Gly Lys
210 215
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛА ПРОТИВ СОБАЧЬЕГО CTLA-4 | 2020 |
|
RU2818586C2 |
| СОБАЧЬИ АНТИТЕЛА С МОДИФИЦИРОВАННЫМИ ПОСЛЕДОВАТЕЛЬНОСТЯМИ CH2-CH3 | 2014 |
|
RU2815059C2 |
| СОБАЧЬИ АНТИТЕЛА С МОДИФИЦИРОВАННЫМИ ПОСЛЕДОВАТЕЛЬНОСТЯМИ CH2-CH3 | 2014 |
|
RU2801209C2 |
| АНТИ-IL31 АНТИТЕЛА ДЛЯ ПРИМЕНЕНИЯ В ВЕТЕРИНАРИИ | 2020 |
|
RU2835543C1 |
| АНТИТЕЛА К СОБАЧЬЕМУ АЛЬФА-РЕЦЕПТОРУ ИНТЕРЛЕЙКИНА-4 | 2020 |
|
RU2840044C1 |
| АНТИТЕЛА К СОБАЧЬЕМУ АЛЬФА-РЕЦЕПТОРУ ИНТЕРЛЕЙКИНА-4 | 2020 |
|
RU2838943C1 |
| АНТИТЕЛА К PD-L1, СВЯЗЫВАЮЩИЕ PD-L1 СОБАКИ | 2015 |
|
RU2722562C2 |
| АНТИТЕЛА К PD-L1, СВЯЗЫВАЮЩИЕ PD-L1 СОБАКИ | 2015 |
|
RU2832918C2 |
| АНТИТЕЛА К PD-1 СОБАК | 2014 |
|
RU2732604C2 |
| АНТИ-IL31 АНТИТЕЛА ДЛЯ ПРИМЕНЕНИЯ В ВЕТЕРИНАРИИ | 2018 |
|
RU2795485C2 |

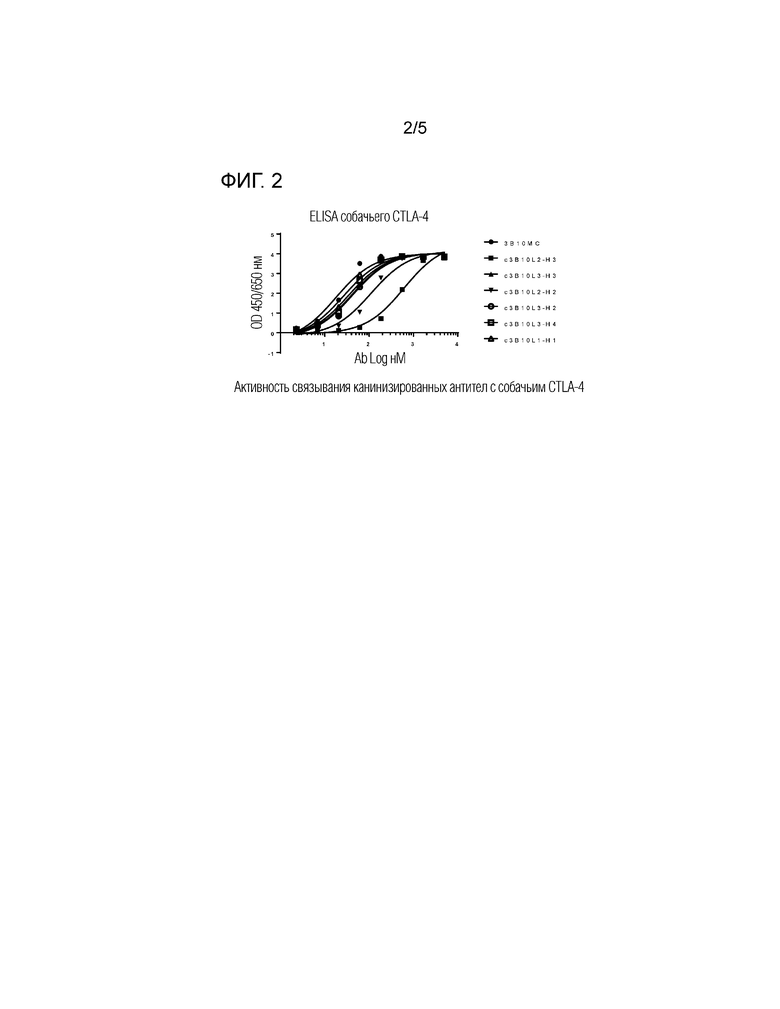
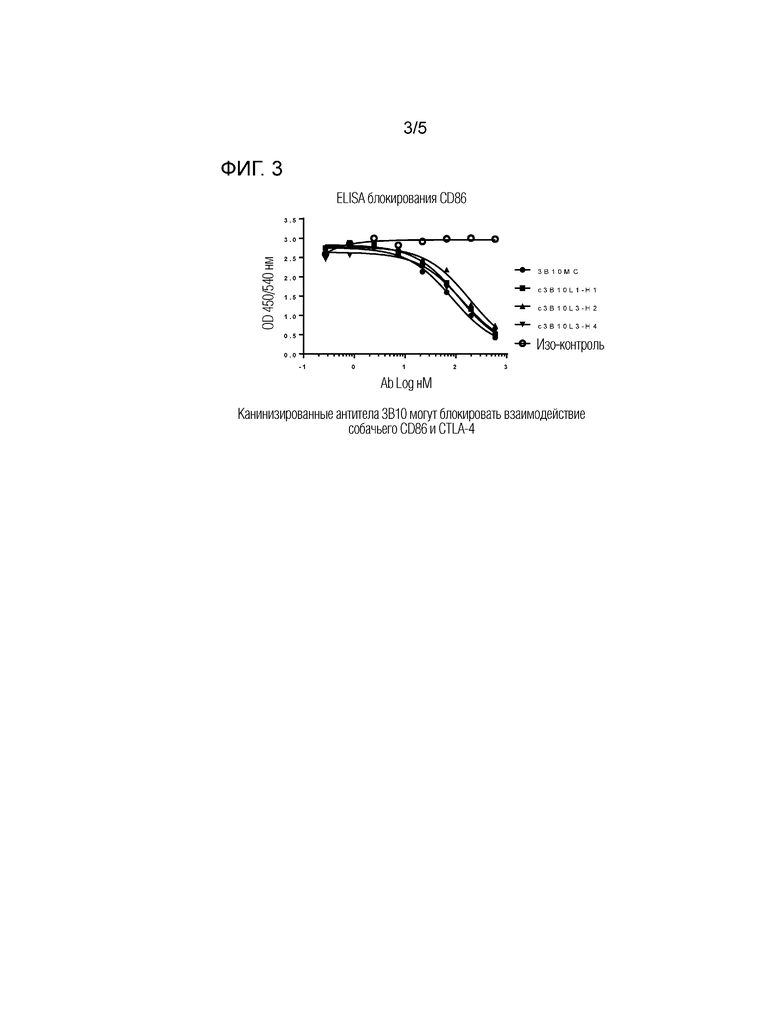

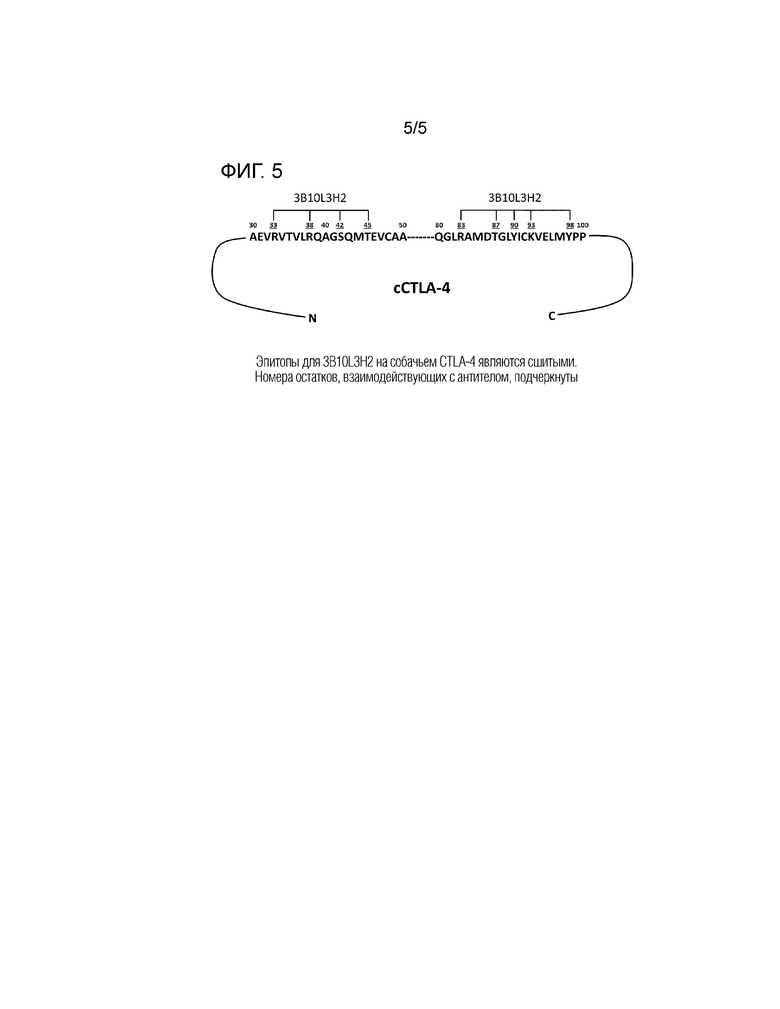
Изобретение относится к области биохимии, в частности к выделенному канинизированному антителу или его антигенсвязывающему фрагменту, которое специфически связывается с собачьим CTLA-4. Также раскрыты нуклеиновая кислота, кодирующая указанное антитело; вектор экспрессии, клетка-хозяин, содержащие указанную нуклеотидную кислоту; фармацевтическая композиция, содержащая указанное антитело. Раскрыты способ повышения активности иммуноцита с помощью указанного антитела; способ получения указанного антитела. Изобретение позволяет эффективно лечить злокачественную опухоль. 8 н. и 4 з.п. ф-лы, 5 ил., 5 табл., 6 пр.
1. Выделенное канинизированное антитело или его антигенсвязывающий фрагмент, которое специфически связывается с собачьим CTLA-4, содержащее тяжелую цепь собачьего IgG и собачью легкую цепь каппа;
где собачья легкая цепь каппа содержит три определяющие комплементарность области (CDR) легкой цепи: CDR легкой цепи 1 (CDRL1), CDR легкой цепи 2 (CDRL2) и CDR легкой цепи 3 (CDRL3); и тяжелая цепь собачьего IgG содержит три CDR тяжелой цепи: CDR тяжелой цепи 1 (CDRH1), CDR тяжелой цепи 2 (CDRH2) и CDR тяжелой цепи 3 (CDRH3):
(a) где CDRL1 содержит аминокислотную последовательность SEQ ID NO:54;
(b) где CDRL2 содержит аминокислотную последовательность, содержащую SEQ ID NO:56;
(c) где CDRL3 содержит аминокислотную последовательность SEQ ID NO:58;
(d) где CDRH1 содержит аминокислотную последовательность SEQ ID NO:48;
(e) где CDRH2 содержит аминокислотную последовательность SEQ ID NO:50; и
(f) где CDRH3 содержит аминокислотную последовательность SEQ ID NO:52.
2. Выделенное канинизированное антитело по п. 1, где тяжелая цепь собачьего IgG содержит аминокислотную последовательность, выбранную из группы, состоящей SEQ ID NO:34, SEQ ID NO:36, SEQ ID NO:38, SEQ ID NO:40, SEQ ID NO:60, SEQ ID NO:62, SEQ ID NO:64 и SEQ ID NO:66.
3. Выделенное канинизированное антитело по п. 1 или 2, где легкая цепь каппа содержит аминокислотную последовательность, выбранную из группы, состоящей SEQ ID NO:42, SEQ ID NO:44 и SEQ ID NO:46.
4. Выделенное канинизированное антитело по п.1, где тяжелая цепь собачьего IgG содержит аминокислотную последовательность SEQ ID NO:36, и собачья легкая цепь каппа содержит аминокислотную последовательность SEQ ID NO:46.
5. Выделенное канинизированное антитело по п. 1, где тяжелая цепь собачьего IgG содержит аминокислотную последовательность SEQ ID NO:62, и собачья легкая цепь каппа содержит аминокислотную последовательность SEQ ID NO:46.
6. Выделенная нуклеиновая кислота, кодирующая собачью легкую цепь каппа канинизированного антитела по пп. 1-4 или 5.
7. Выделенная нуклеиновая кислота, кодирующая тяжелую цепь собачьего IgG канинизированного антитела по пп. 1-4 или 5.
8. Вектор экспрессии, содержащий выделенную нуклеиновую кислоту по п. 6 или 7.
9. Клетка-хозяин для получения канинизированного антитела по любому из пп. 1-5, где клетка содержит вектор экспрессии по п. 8.
10. Фармацевтическая композиция для повышения активности иммуноцита, содержащая антитело по пп. 1-4 или 5 и фармацевтически приемлемый носитель или разбавитель.
11. Способ повышения активности иммуноцита, включающий введение пациенту терапевтически эффективного количества фармацевтической композиции по п. 10.
12. Способ получения канинизированного, антитела или его антигенсвязывающего фрагмента, которое специфически связывается с CTLA-4, включающий:
a. культивирование клетки-хозяина по п. 9 в культуральной среде в условиях, когда нуклеиновая кислота экспрессируется, таким образом продуцируется полипептид, содержащий вариабельные области легкой и тяжелой цепей; и
b. выделение полипептидов из клетки-хозяина или культуральной среды.
| WO 2012120125 A1, 13.09.2012 | |||
| ПЛАНЕТАРНЫЙ РЕДУКТОР | 1996 |
|
RU2112166C1 |
| ПРИМЕНЕНИЕ АНТИТЕЛ К CTLA-4 | 2005 |
|
RU2346702C2 |
| WO 2018025178 A1, 08.02.2018. | |||
Авторы
Даты
2024-07-05—Публикация
2020-07-15—Подача