Изобретение относится к медицине и экологии, а именно к методу обоснования возможного типа: синергетического или антагонистического, комбинированного аэрогенного воздействия трех химических веществ: оксида алюминия, бенз(а)пирена и гидрофторида, на здоровье детей 4-7 лет, с помощью маркерных лабораторных показателей негативных медико-биологических эффектов (нарушение здоровья, развитие заболевания) детей 4-7 лет при комбинированном воздействии на ребенка оксида алюминия, бенз(а)пирена и гидрофторида, для диагностических целей, а также для расширения доказательной базы наличия связи дополнительной заболеваемости и/или связанных с ней функциональных нарушений со стороны иммунной, нервной, костной систем и органов дыхания, у наиболее чувствительных групп населения – детей, в зоне одновременного наличие указанных токсикантов в атмосферном воздухе.
Существующие наработки свидетельствуют, что в большинстве случаев для веществ, токсикология которых изучена достаточно детально, при их комбинированном действии исследователи теоретически прогнозируют более высокую токсичность смеси по сравнению с изолированным действием ее составляющих компонентов. Данный подход основан на концепции суммирования негативного действия веществ в смеси с количественной оценкой суммы эффектов или суммы доз (Жолдакова З.И., Харчевникова Н.В., Мамонов Р.А., Синицына О.О. «Методы оценки комбин6ировнного действия веществ». Гигиена и санитария. 2012; 2:86-89). При этом формально принимается сходство механизмов токсического действия у веществ в смеси и таргетности к критическим органам и системам каждого ее компонента.
Однако токсиканты с разной тропностью к органам-мишеням и метаболизмом часто действуют на организм совместно несколько иначе, чем каждый по отдельности, однако в известных способах это не учитывается, что снижает достоверность этих способов.
При этом следует отметить, что рассматриваемые химические вещества: оксид алюминия, бенз(а)пирен и гидрофторид, также являются токсикантами, причем с разной тропностью на организм человека. Например, органами-мишенями при длительной аэрогенной экспозиции алюминием являются центральная нервная система и органы дыхания, бенз(а)пиреном - иммунная система, гидрофторидом и фторидами твердыми плохо растворимыми - костная система и органы дыхания. А потому актуальным является оценка особенностей комбинированного действия на критические органы и системы детского организма от разных сочетаний указанных химических веществ, базирующихся на анализе причинно-следственных связей, отражающих внешнесредовое воздействие загрязнителей, в том числе бенз(а)пирена, соединений алюминия и фтора, и ответных реакций организма человека в рамках известных типов комбинированного действия.
В настоящее время выделяют следующие три основных типа комбинированного действия веществ – токсикантов, при их одновременном поступлении в организм: аддитивный, синергетический и антагонистический.
Характер комбинированного действия, при котором суммарный эффект комбинированного действия веществ равен сумме эффектов каждого из них при изолированном действии, является аддитивным. В таком случае можно сказать, что смесь веществ ведет себя как одно вещество, и отдельные ее компоненты являются полностью взаимозаменяемыми в изоэффективных дозах или концентрациях.
Если же суммарный эффект комбинированного действия химических веществ превышает сумму эффектов каждого отдельного вещества, то такой тип комбинированного действия оценивается, как синергический. При синергетическом эффекте может наблюдаться биологическое усиление действия компонентов химических веществ на здоровье человека по мере их прохождения по биогеохимическим циклам и одновременном поражении нескольких систем организма, что приводит к более значимым негативным последствиям (негативным эффектам).
При этом разновидностью синергичности в теории систем и других областях знаний (биологии, генетике, экологии) является понятие эмерджентности – появление негативных эффектов, не присущих при изолированном воздействии каждого компонента.
В случае, если суммарный эффект комбинированного действия веществ - токсикантов меньше суммы эффектов отдельных ее компонентов, то такой тип комбинированного действия носит антагонистический характер. При этом вещества могут влиять на кинетику поступления, превращения и выведения друг друга, а также быть конкурентными и неконкурентными антагонистами.
В рамках настоящего изобретения используются следующие термины:
«Негативный эффект» – изменения в морфологии, физиологии, росте, развитии или продолжительности жизни организма, популяции или потомства, проявляющиеся в ухудшении функциональной способности или способности компенсировать дополнительный стресс, или в повышении чувствительности к воздействиям других факторов среды обитания.
«Экспозиция» – контакт организма (рецептора) с химическим, физическим или биологическим агентом.
Зависимость «экспозиция–ответ» − связь между воздействующей экспозицией (соединениями алюминия, бенз(а)пиреном и гидрофторидом), и распространенностью (ответ) негативного эффекта в экспонируемой популяции.
Зависимость «экспозиция – негативный эффект» – связь между экспозицией (химическими веществами) и степенью выраженности негативного эффекта в экспонируемой популяции.
«Лабораторные показатели негативного эффекта» – показатели, количественно или качественно характеризующие биохимическое, физиологическое или иное изменение в организме, в зависимости от степени которого определяется фактическое или потенциальное нарушение здоровья или развитие болезни.
«Лабораторный показатель» – биохимический показатель, определение которого осуществляется методами, направленными на анализ исследуемого материала с помощью различного специализированного лабораторного оборудования;
«Тип комбинированного аэрогенного действия химических веществ: оксида алюминия, бенз(а)пирена и гидрофторида» - характер комбинированного действия нескольких токсичных веществ на организм человека при одном и том же их пути поступления в организм, показывающий превышение суммы негативных эффектов каждого отдельного вещества (синергетический тип) или уменьшение суммы негативных эффектов отдельных ее компонентов (антагонистический тип) по сравнению с характером изолированного воздействия на здоровье человека индивидуальных веществ – токсикантов.
На сегодняшний день научные разработки по изучению типа комбинированного действия химических веществ на биологический организм в основном проведены в экспериментальных исследованиях на биологических объектах (преимущественно на мелких грызунах) при моделировании острой и субхронической токсичности, которая оценивается одним эффектом (как правило, летальным):
Например, в статье Кацнельсон Б.А., Вараксин А.Н., Панов В.Г., Привалова Л.И., Минигалиева И.А., Киреева Е.П. «Экспериментальное моделирование и математическое описание хронической комбинированной токсичности как основа анализа многофакторных химических рисков для здоровья». Токсикологический вестник. 2015; 5(134): 37-45, указывается, что были проведены опыты экспериментального изучения и математического моделирования субхронической комбинированной токсичности (далее - КТ) при бинарном действии на мышах солей никеля, марганца и хрома. Общим математическим выражением при этом служит уравнение:
y = b0 + b1 x1 + b2x2 +….+ bnxn + b12x1 x2 +… + b(n-1)n xn-1xn+…+ b12…nx1 x2...xn,
которое для простейшего и чаще всего рассматриваемого случая бинарной КТ принимает вид: y = b0+b1x1 +b2 x2 + b12x1 x2.
где y - величина рассматриваемого показателя состояния организма при действии токсической комбинации,
b0 – его величина вне такого действия,
xi – доза каждого из n веществ, составляющих комбинацию,
bi – соответствующий коэффициент регрессии для изолированного действия этого вещества,
а члены общего вида b12…nx1 x2...xn (для бинарной КТ – только b12x1 x2) соответствуют дозо-зависимому влиянию взаимодействия эффектов.
Если последнее несущественно, то эти комбинационные (т.н. «перекрестные») члены уравнения значимо не отличаются от нуля, и уравнение выражает аддитивность эффектов. При супер- или субаддитивности эффектов комбинационный член уравнения имеет, соответственно, положительное или отрицательное значение, то есть эффект комбинации оказывается выше (синергизм) или ниже (антагонизм) суммы эффектов, что означает супер- или субаддитивность соответственно.
В статье приведены графики проведенного двухэтапного анализа на примере трех веществ: никеля, марганца и хрома. При этих опытах производили введение в организм мышей указанных химических веществ в разной концентрации и определение лабораторных показателей при этом с построением изоболограмм. На первом этапе оцениваются все варианты КТ для каждого из трёх бинарных сочетаний (в данном случае: Mn+Ni, Mn+Cr, Ni+Cr), а на втором – все эффекты токсического воздействия классифицируются в зависимости от того, оказывается ли на фоне действия третьего фактора тип одной и той же бинарной КТ более неблагоприятным для организма (класс А), менее неблагоприятным для организма (класс B) или остаётся существенно не изменившимся (класс С). Предварительно принимается, какие именно изменения типов КТ определяют эти классы.
В статье Минигалиева И.А., Кацнельсон Б.А., Гурвич В.Б., Привалова Л.И., Панов В.Г., Вараксин А.Н., Сутункова М.П. «О соотношении между общепринятой практикой оценки риска для здоровья при полиметаллических экспозициях и теорией комбинированной токсичности». Токсикологический вестник. 2017; 4(145): 13-18, приводятся результаты экспериментов на крысах, подвергавшихся повторным внутрибрюшинным введениям нескольких бинарных и одной трёхфакторной комбинации химических веществ, главным образом, солей токсичных металлов или металлсодержащих наночастиц. Интоксикации количественно характеризовались десятками функциональных, биохимических и морфометрических показателей. Для описания комбинированной токсичности опирались как на описательную статистику результатов, рассматриваемую с позиций обычной логики, так и на две математические модели, основанные на дисперсионном анализе (ANOVA) и на математической теории поверхности отклика, которые соотносятся с широко признанными парадигмами теории комбинированной токсичности: соответственно, аддитивности эффектов и аддитивности доз. В эксперименте изучалась КТ никеля и марганца. Анализ результатов, проведенный на базе уравнения y = b0+b1x1 +b2 x2 + b12x1 x2, выполнен с использованием метода построения поверхности отклика для построения изоболограммм для трёх типов КТ никеля и марганца, соответствующих традиционным определениям (а) аддитивности, (б) супераддитивности (синергизма) и (в) субаддитивности (антагонизма) однонаправленных эффектов. На осях координат - дозы металлов в долях соответствующих ЛД50; числа над изоболами - заданные уровни эффекта, к которым эти изоболы относятся.
Также в статье: Мирзакаримова М.А. «Сравнительная гигиеническая оценка комбинированного действия сложных смесей химических загрязнений атмосферного воздуха». Гигиена и санитария. 2017; 96(6): 528-531. doi: http://dx.doi.org/10.18821/0016-9900-2017-96-6-528-531, представлены результаты экспериментальных работ по изучению характера совместного токсического действия различных сложных смесей, присутствующих в атмосферном воздухе. Действие сложных смесей на организм лабораторных животных изучалось в двух сериях опытов. В I серии исследовано комбинированное действие диоксида серы, диоксида азота, фтористого водорода и взвешенных частиц, а во II серии - ацетата свинца, формальдегида, диоксида серы, аммиака. Установлено, что характер комбинированного действия ацетата свинца, формальдегида, диоксида серы, аммиака при длительном ингаляционном поступлении в организм проявляется по типу эффекта суммации, а диоксида серы, диоксида азота, фтористого водорода и взвешенных частиц по типу эффекта неполной суммации. При совместном присутствии в атмосферном воздухе ацетата свинца, формальдегида, диоксида серы, аммиака ПДК для каждого вещества не должна превышать 0,25 ПДК, а диоксида серы, диоксида азота, фтористого водорода и взвешенных частиц 0,46 ПДК при их изолированном действии.
Однако все указанные исследования нельзя распространить на человеческий организм. Межвидовые различия организма человека, тем более ребенка, и экспериментальных животных являются источником неопределенностей, которые могут быть связаны с относительно повышенной интенсивностью ответной реакции, а также более широким спектром химических веществ, негативно воздействующих на здоровье человека по сравнению с модельными биологическими объектами.
Кроме этого, все указанные известные исследования связаны с возникновением летального исхода животного, что тем более исключает их преломление на человеческий организм.
Вместе с этим, недостаточность накопленных знаний, полученных в известных эпидемиологических и клинических исследованиях по рассматриваемой проблеме, также увеличивает степень неопределенности, а значит, ставится под сомнение достоверность известных способов.
При этом из уровня техники не были выявлены известные способы дифференциальной оценки преобладающего типа комбинированного аэрогенного воздействия химических веществ: оксида алюминия, бенз(а)пирена и гидрофторида, на здоровье детей 4-7 лет, поэтому сделать выбор ближайшего аналога к заявляемому объекту не представляется возможным.
Технический результат, достигаемый предлагаемым изобретением, заключается в создании информативного и доказательного способа обоснования и установления дифференциальной оценки типа (синергетического или антагонистического) комбинированного аэрогенного одновременного воздействия химических веществ: оксида алюминия, бенз(а)пирена и гидрофторида, на здоровье детей 4-7 лет, за счет анализа параметризированных причинно-следственных связей экспозиции воздействующих веществ и негативных эффектов.
Поставленный технический результат достигается предлагаемым способом дифференциальной оценки преобладающего типа комбинированного аэрогенного воздействия химических веществ: оксида алюминия, бенз(а)пирена и гидрофторида, на здоровье детей 4-7 лет, согласно которому
у детей, проживающих на территории с постоянным присутствием и/или с повышенной, по сравнению с предельно-допустимой концентрацией, в атмосферном воздухе химических веществ: оксида алюминия, бенз(а)пирена и гидрофторида отбирают пробы мочи и пробы крови,
в пробах у детей определяют концентрацию алюминия и фторид-иона в моче, бенз(а)пирена в крови,
при выявлении у ребенка концентрации биомаркеров экспозиции, а именно: содержания в моче ребенка алюминия 0,010-0,012 мг/дм3 и фторид-иона 0,55-0,83 мг/дм3 , и бенз(а)пирена в крови ребенка (0,006-0,008)⋅10-3 мг/дм3, определяют в биосредах ребенка лабораторные показатели, являющиеся биомаркерами негативных эффектов, которые патогенетически связаны с наиболее вероятными негативными эффектами – нарушениями здоровья у детей, со стороны критических органов и систем, возникающими в ответ на воздействие химических веществ: оксида алюминия – нервная система и органы дыхания; бенз(а)пирена – иммунная система; гидрофторида – костная система и органы дыхания, а именно: со стороны иммунной системы - содержание иммуноглобулина G общего (IgG), МЕ/см3; иммуноглобулина G специфического (IgGспец.) к бенз(а)пирену, усл. ед; фагоцитарное число, усл ед, и фагоцитарный индекс в крови, усл ед; со стороны костной системы - показатель тартрат-резистентной кислой фосфатазы в сыворотке крови, ЕД/дм3; со стороны нервной системы - уровень нейронспецифической энолазы в сыворотке крови, мкг/дм3; со стороны органов дыхания - уровень иммуноглобулина Е общего (IgЕ), г/дм3, и уровень малонового диальдегида (МДА), мкмоль/см3, в плазме крови;
при уровне лабораторных показателей ребенка, входящих в количественный диапазон лабораторных показателей вышеуказанных биомаркеров негативных эффектов, а именно: со стороны иммунной системы: уровень IgG 12,98-15,30 г/дм3, IgGспец. к бенз(а)пирену 0,11-0,214 усл. ед., фагоцитарное число 0,83-0,95 усл. ед. и фагоцитарный индекс 1,70-1,81 усл. ед.; костной системы: содержание тартрат-резистентной кислой фосфатазы 2,53-3,09 ЕД/дм3; нервной системы: уровень нейронспецифической энолазы 4,09-5,59 мкг/дм3; органов дыхания: уровень IgE 58,99-196,63 МЕ/см3 и МДА 2,37-2,61 мкмоль/см3, которые патогенетически связаны с воздействием вышеуказанных биомаркеров экспозиции на здоровье детей, такие биомаркеры определяют как патогенетически значимые выявленные биомаркеры негативных эффектов для ребенка;
затем определяют вероятность p каждого выявленного биомаркера негативных эффектов по формуле:
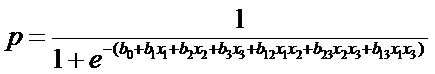
где p – вероятность ответной реакции организма ребенка для каждого выявленного патогенетически значимого биомаркера негативных эффектов при одновременном развитии эффектов изолированного и комбинированного действия трех химических веществ, при их бинарной комбинации;
x1, x2, x3 – концентрация алюминия в моче ребенка, бенз(а)пирена в крови ребенка и фторид-иона в моче ребенка соответственно, при экспозиции оксидом алюминия, бенз(а)пиреном и гидрофторидом, мг/дм3 ;
b0 – коэффициент регрессии, приведенный в таблице 2 описания, характеризующий уровень вероятности ответной реакции организма ребенка для каждого выявленного патогенетически значимого биомаркера негативных эффектов, независимо от влияния изучаемых маркеров экспозиции - фоновый уровень;
b1, b2, b3, b12, b13, b23 – коэффициенты регрессии, приведенные в таблице 2 описания, характеризующие уровень вероятности ответной реакции организма ребенка для каждого выявленного патогенетически значимого биомаркера негативных эффектов, при изолированном действии оксида алюминия, бенз(а)пирена и гидрофторида, а также при их комбинированном действии в бинарной смеси;
определяют вероятность p1 каждого выявленного патогенетически значимого биомаркера негативных эффектов по формуле:
p1 =
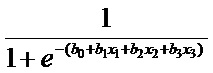
где p1 - вероятность ответной реакции организма ребенка для каждого выявленного патогенетически значимого биомаркера негативных эффектов, при одновременном развитии эффектов действия оксида алюминия, бенз(а)пирена и гидрофторида при их изолированном действии;
определяют дополнительную вероятность Δр выявленного патогенетически значимого биомаркера негативных эффектов по формуле:
Δр= р - p1,
где Δр – дополнительная вероятность ответной реакции организма ребенка для каждого выявленного патогенетически значимого биомаркера негативных эффектов в результате эффектов комбинированного действия оксида алюминия, бенз(а)пирена и гидрофторида;
и для выявленного биомаркера негативных эффектов, при положительном значении Δр преобладающий тип комбинированного аэрогенного воздействия алюминия, бенз(а)пирена и гидрофторида на нарушение здоровья ребенка 4-7 лет оценивают, как синергетический, превышающий сумму негативных эффектов каждого отдельного вещества, а при отрицательном значении Δр – как антагонистический, меньше суммы негативных эффектов каждого отдельного вещества.
Для понимания существа вопроса необходимо пояснение. Обозначенная проблема оценки типа комбинированного аэрогенного воздействия химических веществ: оксида алюминия, бенз(а)пирена и гидрофторида, на здоровье детей 4-7 лет, актуальна для регионов Российской Федерации с размещением и функционированием хозяйствующих субъектов, специализирующихся на производстве алюминия (порядка 40 предприятий), где большая часть населения из зон аэрогенной химической экспозиции подвергается комбинированному действию токсичных веществ, прежде всего, бенз(а)пирена, оксида алюминия, фторсодержащих неорганических соединений. Данные вещества относятся к чрезвычайно и высоко опасным для здоровья человека (1 и 2 класс), оказывающие политропное действие на организм при внешнесредовом поступлении.
Органами-мишенями при длительной аэрогенной экспозиции алюминием являются центральная нервная система и органы дыхания, бенз(а)пиреном - иммунная система, гидрофторидом и фторидами твердыми плохо растворимыми - костная система и органы дыхания.
Как нейротропное вещество оксид алюминия оказывает прямое цитотоксическое действие на нейроны головного мозга и астроциты, нарушая синтез полипептидной цепи белковой молекулы, аксональный транспорт, синтез и активность нейромедиаторов. Также оказывает прямое цитотоксическое действие на рецепторы дыхательных путей с образованием активных форм кислорода, повышением сенсорной чувствительности к алюминию и развитием воспалительного ответа.
Иммунодепрессивное действие бенз(а)пирена характеризуется дисбалансом клеточного и гуморального иммунитета, в том числе, подавлением продукции интерлейкинов и интерферонов, снижением защитной барьерной функции слизистых.
Фторид-ион обладает высокой реакционной способностью, прямым цитотоксическим и декальцинирующим действием на протоплазму клетки. Оказывает митогенное действие на остеобласты, нарушает кальциевый баланс и синтез коллагена в костной ткани, что способствует остеокластической реакции и нарушению ремоделирования костной ткани. Разрушает защитный слой эпителия дыхательных путей и альвеолоцитов с развитием воспалительной реакции.
В связи с этим, актуальным является расширение существующих методических подходов к определению конкретного типа комбинированного действия веществ - токсикантов, базирующихся на анализе причинно-следственных связей, отражающих внешнесредовое воздействие загрязняющих веществ, в том числе бенз(а)пирена, соединений алюминия и фтора, и ответных реакций организма человека, а именно, детей возраста 4-7 лет.
Для установления характера комбинированного действия нескольких веществ целесообразна оценка биологически правдоподобных последовательностей ключевых событий в системе «экспозиция химических веществ – отклонение биомаркеров экспозиции от референтных значений – отклонение биомаркеров негативного эффекта от физиологической нормы», приводящих к наблюдаемому негативному ответу.
При этом типы комбинированной токсичности могут быть не одинаковыми по отношению к разным эффектам.
Предлагаемый способ основан на следующем:
- на использовании параметризированных причинно-следственных связей экспозиции и негативных эффектов, развивающихся со стороны критических органов и систем экспонированных лиц;
- на применении классической модели множественной логистической регрессии, которая теоретически предусматривает оценку вероятности отклонения биомаркера негативного эффекта от физиологической нормы, как при изолированном, так и комбинированном действии веществ независимо от пути их поступления.
Поскольку характер действия сложной системы возможных комбинаций химических веществ – токсикантов, трудно поддается интерпретации, для решения поставленной задачи в предлагаемом способе учитывали бинарные комбинации химических веществ в различных сочетаниях.
В заявляемом способе тот или иной тип комбинированного действия веществ оценивался по бинарному сочетанию веществ, а также по виду негативного эффекта (лабораторный показатель) и уровню биомаркеров экспозиции.
Кроме того, впервые в предлагаемом способе введена количественная оценка дополнительной вероятности Δр, сформированной в результате эффектов комбинированного действия одновременно трех веществ, и ее определение проводится по расчету разницы вероятности отклонения биомаркера эффекта по полученной модели, включающей одновременно параметры изолированного и комбинированного действия трех веществ, и модели, включающей параметры только изолированного действия каждого из трех веществ. Причем было установлено, что при положительном значении дополнительной вероятности преобладающий тип комбинированного действия многокомпонентной смеси химических веществ на здоровье ребенка оценивается как синергетический, при отрицательном – антагонистический. И указанный подход оказался применимым и для человеческого организма, в том числе и для детей, что позволило повысить объективность гигиенической оценки риска здоровью экспонируемого детского населения.
Предлагаемый способ осуществляют следующим образом, реализуя его на конкретном примере.
1. Выделяют территорию наблюдения с постоянным одновременным присутствием в атмосферном воздухе химических веществ: оксида алюминия, бенз(а)пирена и гидрофторида и/или с их повышенной, по сравнению с предельно-допустимой концентрацией (ПДК) в атмосферном воздухе, и выделяют территорию сравнения, характеризующуюся отсутствием превышений гигиенических нормативов содержания указанных химических веществ в атмосферном воздухе.
Гигиеническая оценка качества атмосферного воздуха на территории наблюдения и сравнения по содержанию алюминия, бенз(а)пирена и гидрофторида в селитебной застройке, расположенной в зоне влияния алюминиевого производства, проводилась в точках расположения постов наблюдения управления по гидрометеорологии и мониторингу окружающей среды и/или в точках социально-гигиенического мониторинга (ПДКс.г., ПДКс.с.). При этом проводилось сравнение фактической величины хронической экспозиции с ее референтным значением (Rfc) за тот же период усреднения.
Качество атмосферного воздуха селитебной застройки характеризуется повышенным содержанием бенз(а)пирена до 2,2 ПДКс.г. и до 5,8 ПДКс.с, а также постоянным присутствием оксида алюминия и гидрофторида на уровне 0,1 ПДКс.г. и 0,3 ПДКс.с.
При этом территория наблюдения характеризовалась следующей хронической аэрогенной экспозицией бенз(а)пирена (наблюдения за 5 лет):
- повышенной относительно референтной концентрации (Rfc) бенз(а)пирена 5,8 Rfc (при этом Rfc=0,000001 мг/дм3);
- оксида алюминия (в пересчете на алюминий) на уровне референтной концентрации 0,2 Rfc (при этом Rfc=0,005 мг/дм3)
- содержание гидрофторида (в пересчете на фтор) на уровне референтных значений и составляло 0,3 Rfc (при этом Rfc= 0,013 мг/дм3).
Территория сравнения характеризовалась хронической аэрогенной экспозицией ниже референтных уровней, а именно бенз(а)пирена 0,000001 Rfc, оксида алюминия 0,04 Rfc и гидрофторида 0,12 Rfc.
2. Производят выборку групп детей возраста 4-7 лет на территории наблюдения и на территории сравнения.
На территории наблюдения были отобраны 332 ребенка, вошедшие в группу наблюдения.
На территории сравнения были отобраны 132 ребенка, составляющие группу сравнения.
Выборки по половозрастному составу, социально-бытовым условиям проживания, среднему уровню материального обеспечения, по частоте и характеру вредных привычек и профессиональных вредностей у родителей отобранных детей, были сопоставимыми. На момент обследования дети не имели острых инфекционных заболеваний не менее, чем в течение 4 недель до начала исследования, не принимали лекарственных препаратов, оказывающих выраженное влияние на изучаемые функции/заболевания со стороны критических органов и систем, менее чем за 30 дней до начала исследования.
3. У детей из групп наблюдения и сравнения отбирают пробы мочи и пробы крови.
Определяют в пробах мочи концентрацию алюминия и фторид-иона. В пробе крови определяют содержание бенз(а)пирена. Определение указанных химических веществ производят по следующим методикам:
МУК 4.1.3589-19. Измерение массовой концентрации алюминия в биологических средах (кровь, моча) методом масс-спектрометрии с индуктивно связанной плазмой. – М.: Федеральный центр госсанэпиднадзора Минздрава России, 2019. – 24 с.
МУК 4.1.3040-12 «Измерение массовой концентрации бенз(а)пирена в крови методом высокоэффективной жидкостной хроматографии». – М.: Федеральный центр гигиены и эпидемиологии Роспотребнадзора, 2013. – 46 с.
Количественное определение ионов фтора в моче с использованием ионселективного электрода. Определение химических соединений в биологических средах: Сборник методических указаний. МУК 4.1.773-99. – М.: Федеральный центр госсанэпиднадзора Минздрава России, 2000. – 152 с.
Оценка установленного содержания алюминия и фтор-ионов в моче и бенз(а)пирена в крови проводилась относительно референтных уровней (Тиц Н.У. Клиническое руководство по лабораторным тестам. М.: ЮНИМЕД–пресс; 2003).
4. Обосновывают биомаркеры экспозиции на основании установления достоверных связей между аэрогенной экспозицией химических веществ: оксида алюминия, бенз(а)пирена и гидрофторида, на соответствующей территории и концентрацией изучаемых химических веществ в биосредах у каждого ребенка территории наблюдения и территории сравнения, с помощью построения модели линейной регрессии, описываемой уравнением вида:
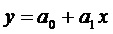
где y – маркер экспозиции: содержание химического вещества в биосредах, мг/дм3;
x – уровень экспозиции: суммарная и изолированная доза для условий годового периода осреднения химического вещества при поступлении в организм ребенка с атмосферным воздухом на соответствующей территории, мг/кг х день;
а0, а1 - параметры регрессионной модели.
В результате этой операции биомаркерами экспозиции (на конкретном примере аэрогенного воздействия оксида алюминия, бенз(а)пирена и гидрофторида на детей 4-7 лет) обоснованы следующие значения уровней алюминия (0,010-0,012 мг/дм3) и фторид-иона (0,55-0,83 мг/дм3) в моче, бенз(а)пирена в крови ((0,006-0,008)⋅10-3 мг/дм3).
5. Далее устанавливают перечень лабораторных показателей, которые этиопатогенетически связаны с наиболее вероятными негативными эффектами – нарушениями здоровья у детей со стороны критических органов и систем, возникающими в ответ на воздействие химических веществ: оксида алюминия – нервная система и органы дыхания, бенз(а)пирена – иммунная система, гидрофторида – костная система и органы дыхания.
В качестве источников информации о тропности алюминия, бенз(а)пирена и гидрофторида использованы следующие нормативно-методические документы и справочные материалы:
- Руководство по оценке риска здоровью населения при воздействии химических веществ // Руководство 2.1.10.1920-04. – М.: Федеральный центр Госсанэпиднадзора Минздрава России, 2004. – 143 с.
- Воздействие на организм человека опасных и вредных экологических факторов. Метрологические аспекты. В 2-х томах. // Под ред. Исаева Л. К. Том I. – М.: ПАИМС, 1997. – 512 с.
- Воздействие на организм человека опасных и вредных экологических факторов. Метрологические аспекты. В 2-х томах. // Под ред. Исаева Л. К. Том II. – М.: ПАИМС, 1997. – 496 с.
- Справочник «Вредные вещества в окружающей среде и их соединения» [Вредные вещества в окружающей среде. Элементы I-IV групп периодической системы и их неорганические соединения: Справ.-энц. изд. / Пол ред. В.А. Филова и др. — СПб.: НПО «Профессионал», 2012. — 464 с.
Сформированный перечень лабораторных показателей для исследования ответных реакций организма детей, исходя из наиболее вероятных негативных эффектов – нарушений здоровья у детей со стороны критических органов и систем, возникающих в ответ на воздействие бенз(а)пирена, алюминия и фторида, был следующим:
- со стороны иммунной системы - уровень сывороточных иммуноглобулинов А, М, G; содержание иммуноглобулина Е общего (IgE), иммуноглобулина G специфического (IgGспец.) к бенз(а)пирену, алюминию и фтору, фагоцитарное число и фагоцитарный индекс в крови;
- со стороны костной системы – содержание N-остеокальцина, тартрат-резистентной кислой фосфатазы в сыворотке крови, уровень ионизированного кальция в плазме крови;
- со стороны нервной системы – содержание глутаминовой кислоты, γ-аминомасляной кислоты (ГАМК), серотонина, кортизола, нейротропина-3, уровень нейронспецифической энолазы в сыворотке крови;
- со стороны органов дыхания – содержание лимфоцитов, моноцитов, эозинофилов в крови, эозинофильно-лимфоцитарный индекс; содержание эозинофилов, нейтрофилов в назальном секрете, индекс эозинофилии; уровень иммуноглобулина G общего (IgG), уровень антиоксидантной активности плазмы крови и малонового диальдегида (МДА).
6. В биосредах детей группы наблюдения и сравнения определяют лабораторные показатели из установленного перечня, отражающие состояние критических органов и систем.
Далее в группе наблюдения выделяют те лабораторные показатели, уровень которых достоверно отличается от физиологической нормы и/или от уровня показателей группы сравнения (p≤0,05) и, имеющие достоверную причинно-следственную связь с содержанием алюминия (0,010-0,012 мг/дм3) и фторид-иона (0,55-0,83 мг/дм3) в моче, бенз(а)пирена в крови ((0,006-0,008)⋅10-3 мг/дм3).
Далее осуществляли математическое моделирование причинно-следственных связей между содержанием химического вещества в моче/крови - биомаркер экспозиции, и ответной реакцией организма ребенка через отклонения лабораторных показателей от физиологической нормы и/или по сравнению с показателем группы сравнения - биомаркера негативного эффекта, которое выполняют для каждого указанного лабораторного показателя по формуле:
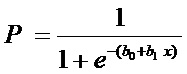
где Р - вероятность отклонения маркера негативного эффекта - лабораторного показателя, от физиологической нормы и/или от уровня показателей группы сравнения, при воздействии маркера экспозиции – химического вещества: оксида алюминия, бенз(а)пирена, гидрофторида;
х – концентрация маркера экспозиции - концентрация химического вещества в моче/в крови, мг/дм3;
b0, b1 – параметры математической модели.
Оценка достоверности параметров и адекватности модели проводилась на основании однофакторного дисперсионного анализа по критерию Фишера при заданном уровне значимости р≤0,05. При построении математических моделей определялись 95%-ные доверительные границы. В качестве адекватных моделей выбирались модели, соответствующие статистическому критерию и отвечающие требованию биологического правдоподобия.
7. В результате было обосновано, что биомаркерами негативных эффектов (на конкретном примере) со стороны иммунной системы: повышенный (относительно физиологической нормы / или уровня показателей группы сравнения) уровень иммуноглобулина G общего (IgG) в пределах 12,98-15,30 г/дм3, наличие иммуноглобулина G специфического (IgGспец.) к бенз(а)пирену в пределах 0,11-0,214 усл. ед., понижение фагоцитарного числа в пределах 0,83-0,95 усл. ед. и фагоцитарного индекса 1,70-1,81 усл. ед.в крови; костной системы – повышенное содержание тартрат-резистентной кислой фосфатазы в сыворотке крови в пределах 2,53-3,09 ЕД/дм3; нервной системы – повышенный уровень нейронспецифической энолазы в сыворотке крови в пределах 4,09-5,59 мкг/дм3; органов дыхания – повышенный уровень иммуноглобулина Е общего (IgE) в сыворотке крови в пределах 58,99-196,63 МЕ/см3и малонового диальдегида (МДА) в плазме крови в пределах 2,37-2,61 мкмоль/см3; изменение которых патогенетически связанно с воздействием факторов экспозиции: оксид алюминия, бенз(а)пирен и гидрофторид.
8. Далее производят определение вероятности отклонения биомаркера негативного эффекта у детей группы наблюдения от физиологической нормы или уровня показателей группы сравнения при одновременном развитии эффектов изолированного и комбинированного действия трех указанных химических веществ, но при их бинарной комбинации в различных сочетаниях, по следующей формуле:
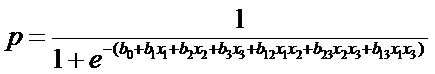
где p – вероятность отклонения биомаркера негативного эффекта от физиологической нормы или уровня показателей группы сравнения при одновременном развитии эффектов изолированного и комбинированного действия трех химических веществ, при их бинарной комбинации;
x1, x2, x3 – концентрация каждого вещества в биосреде ребенка при экспозиции оксидом алюминия, бенз(а)пиреном и гидрофторидом соответственно, мг/дм3;
b0 – коэффициент регрессии, характеризующий уровень вероятности отклонения биомаркера негативного эффекта от физиологической нормы, независимо от влияния изучаемых маркеров экспозиции (фоновый уровень);
b1, b2, b3, b12, b13, b23 – коэффициенты регрессии, характеризующие скорость нарастания вероятности отклонения биомаркера негативного эффекта от физиологической нормы при изолированном действии химических веществ, а также при комбинированном действии указанных химических веществ в бинарной смеси.
9. Определяют предварительный тип комбинированного действия химических веществ путем сопоставительного анализа смены знаков коэффициентов регрессии при изолированном действии каждого вещества (b1, b2, b3) и комбинации веществ в паре (b12, b13, b23): положительный, отрицательный или равный нулю, полученных моделей, используя следующую матрицу, в которой химическое вещество i и химическое вещество j есть оксид алюминия, или бенз(а)пирен, или гидрофторид (таблица 1):
При этом, используя данные о предварительном типе комбинированного действия веществ в бинарном сочетании, в каждой бинарной смеси химических веществ оценивается направление негативного эффекта (5-й столбик таблицы 1): если в указанной матрице коэффициент регрессии bij химических веществ не отличается от нуля, т.е. bij =0, то действие химических веществ в их бинарной комбинации оценивается, как адекватное простой суммации негативных эффектов при изолированном действии каждого из веществ i и j; если коэффициент регрессии имеет положительное значение bij>0, то действие химических веществ оценивается как усиление негативного эффекта; если коэффициент регрессии имеет отрицательное значение bij<0, то действие химических веществ оценивается как ослабление негативного эффекта.
Таким образом получается таблица с предварительным типом комбинированного действия алюминия, бенз(а)пирена и фторид-иона (таблица 2).
Данные, приведенные в таблице 2, показывают следующее. Анализ полученных параметров моделей с использованием разработанной матрицы экспертной оценки позволил установить, что при содержании в крови бенз(а)пирена, в моче алюминия и фторид-иона на уровнях, превышающих в 1,7-1,9 раза референтные значения, и при биомаркере экспозиции: содержанием в моче ребенка алюминия (0,010-0,012 мг/дм3) и фторид-иона (0,55-0,83 мг/дм3) в моче, бенз(а)пирена в крови ((0,006-0,008)⋅10-3 мг/дм3), формируются различные варианты комбинированного действия изучаемых химических веществ в отношении негативных эффектов.
В зависимости от бинарного сочетания трех химических веществ и выбора биомаркера негативного эффекта (8 лабораторных показателей) выявлены различные варианты комбинированного действия (т.е. всего установлено 24 варианта, а именно: b1b2 (8)+ b1b3(8)+ b2b3(8)=24). Для 10 из них (синергизм + эмерджентность+антагонизм) (42,0 % от их общего количества) установлена вероятность усиления негативного эффекта (таблица 2), свойственная действию фторида в комбинации с алюминием и с бенз(а)пиреном.
Ниже приведены пояснения о порядке установления предварительного типа комбинированного действия химических веществ: алюминия, бенз(а)пирена и фторида, на примере биомаркера негативного эффекта - иммуноглобулина IgG, от влияния бинарной смеси: алюминий и бенз(а)пирен.
Рассмотрим совокупность коэффициентов регрессии, приведенных в таблице 2, для данных веществ в отношении IgG:
b1 =132,3 (т.е. b1 >0); b2 = 0; b1b2 = 0;
Находим по матрице, приведенной в таблице 1, такое сочетание коэффициентов регрессии (таблица 3):
Таблица 3
действие химического вещества i
(bi)
действие химического вещества j
(bj)
действие химических веществ i и j при бинарной комбинации (bij)
Делаем следующий вывод:
Предварительный тип комбинированного действия алюминия и бенз(а)пирена в их бинарном сочетании – «Изолированное действие алюминия».
Аналогичным образом был установлен в таблице 2 предварительный тип комбинированного действия других веществ в их бинарной комбинации.
10. Наряду с сопоставительным анализом смены знаков коэффициентов регрессии, также определяют частоту встречаемости соответствующих им выявленных вариантов комбинированного действия химических веществ. Поскольку особую опасность представляет комбинированное действие веществ, обуславливающее усиление негативного эффекта, именно этот тип является ключевым для оценки негативных последствий при комбинированной экспозиции и именно он принимается в дальнейший расчет частоты встречаемости типа комбинированного действия веществ.
Для этого определяют % каждого из выявленного предварительного типа комбинированного действия веществ (синергизм, или антагонизм, или эмерджентность, или аддитивность) от общего числа вариантов с усилением негативного эффекта, соответствующих бинарной комбинации веществ и с учетом установленной вероятности отклонения патогенетически значимых биомаркеров негативных эффектов.
Ниже приведены пояснения о порядке установления частоты встречаемости предварительного типа комбинированного действия бинарной смеси: алюминий и фтора.
В комбинации фторида и алюминия (колонка b1b3 таблицы 2) установлено 6 вариантов типа предварительного действия химических веществ с усилением негативного эффекта по отношению к органам-мишеням: 4 синергизма и 2 антагонизм (в таблице 2 отмечены знаком*) (Таблица 4):
Таблица 4
и фтор
Примечание:* - типы взаимодействий химических веществ с усилением негативного эффекта
6 вариантов действия с усилением негативного эффекта составляют для данной комбинации веществ 100 %; 4 варианта синергизма от общего количества – х %.
т.е. (4·100)/6=66,7 %.
6 варианта действия с усилением негативного эффекта составляют для данной комбинации веществ 100 %; 2 варианта антагонизма от общего количества – х %.
т.е. (2·100)/6=33,3 %.
Таким образом, анализ частоты встречаемости выявленных типов действия веществ в комбинации алюминия и фтора показал, что преобладающим из 6-ти вариантов с усилением негативного эффекта является синергизм, установленный в 67,0 % случаев при действии на иммунную, нервную системы и органы дыхания; антагонизм – в 33,0 % на костную систему.
Аналогично просчитываем частоту встречаемости предварительного типа комбинированного действия бинарной комбинации бенз(а)пирена и фтора (Таблица 5).
Таблица 5
и фтор
Примечание:* - типы взаимодействий химических веществ с усилением негативного эффекта
В комбинации бенз(а)пирена и фтора (колонка b2b3 таблицы 2) установлено 4 вариантов типа предварительного действия химических веществ с усилением негативного эффекта по отношению к органам-мишеням: 3 синергизма и 1 эмерджентность (в таблице 2 отмечены знаком*):
4 варианта действия с усилением негативного эффекта составляют для данной комбинации веществ 100 %; 1 варианта эмерджентности от общего количества – х %.
т.е. (1·100)/4=25,0 %.
4 варианта действия с усилением негативного эффекта составляют для данной комбинации веществ 100 %; 3 варианта синергизма от общего количества – х %.
т.е. (3·100)/4=75,0 %.
Таким образом, в комбинации бенз(а)пирена и фтора (колонка b2b3 таблицы 2) выявлены синергизм и эмерджентность с усилением негативного эффекта. Синергизм установлен в 75,0 % случаев при действии на органы дыхания и костную систему, эмерджентность в 25,0 % случаев – на иммунную систему.
В бинарной комбинации алюминия и бенз(а)пирена (колонка b1b2 таблицы 2) усиления негативных эффектов со стороны иммунной, костной систем и органов дыхания не выявлено. Вещества в этом случае действуют адекватно изолированному, а значит, их не берем в дальнейший анализ.
С учетом установленной вероятности p отклонения патогенетически значимых биомаркеров негативных эффектов и наибольшей частоты встречаемости соответствующих им выявленных предварительных типов комбинированного действия химических веществ применительно к критическим органам и системам, устанавливают уточненный предварительный тип комбинированного действия бинарной смеси химических веществ: оксида алюминия, бенз(а)пирена и гидрофторида, на каждый критический орган или систему
11. Затем определяют дополнительную вероятность Δр отклонения биомаркера негативного эффекта, по расчету разницы вероятности p отклонения биомаркера негативного эффекта в полученной модели, включающей одновременно параметры изолированного и комбинированного действия трех веществ в их бинарной комбинации, и вероятности p1 отклонения биомаркера негативного эффекта в модели, включающей параметры только изолированного действия химических веществ:
Δр= р - p1,
где Δр – дополнительная вероятность отклонения биомаркера негативного эффекта в результате эффектов комбинированного действия трех веществ: оксида алюминия, бенз(а)пирена и гидрофторида,
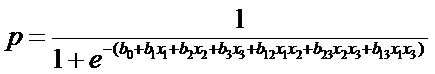
p1 =
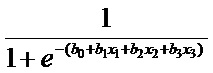
т.е. Δ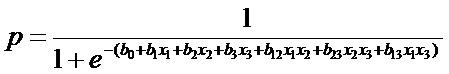
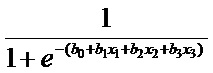
И по указанной дополнительной вероятности Δр производят дифференциальную оценку преобладающего типа комбинированного аэрогенного воздействия химических веществ: оксида алюминия, бенз(а)пирена и гидрофторида, на здоровье детей 4-7 лет, а именно: при положительном значении дополнительной вероятности Δр тип комбинированного аэрогенного воздействия многокомпонентной смеси химических веществ на нарушение здоровья детей оценивают как синергетический, при отрицательном значении дополнительной вероятности Δр – антагонистический. Полученные данные приведены в таблице 6.
Ниже приведены пояснения о порядке расчета вероятности р, вероятности р1 и дополнительной вероятности Δp, приведенных в таблице 6, на примере биомаркера негативного эффекта - иммуноглобулина IgG и преобладающего типа комбинированного действия трех веществ на этот показатель, который отражает здоровье детей в отношении иммунной системы.
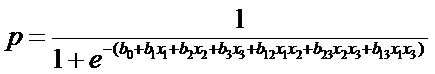
p1 =
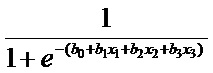
Δр= р – p1 = 0,267 – 0,340 = - 0,073
т.к. значение Δр является отрицательным числом, то преобладающий тип комбинированного аэрогенного воздействия многокомпонентной смеси химических веществ: оксида алюминия, бенз(а)пирена и гидрофторида, на нарушение здоровья детей в отношении иммунной системы в части показателя IgG оценивают как антагонистический, то есть меньше суммы негативных эффектов каждого отдельного вещества.
Интегральная оценка преобладающего типа комбинированного действия одновременно трех веществ по совокупности негативных эффектов позволила установить в 75,0 % случаев синергетический тип действия алюминия, фторида и бенз(а)пирена (повышение IgG специфического к бенз(а)пирену, тартрат-резистентной кислой фосфатазы, нейронспецифической энолазы, МДА; снижение фагоцитарного числа и индекса).
Антагонистический характер действия изучаемых веществ выявлен только в 25,0 % случаев (повышение IgG и IgE общего).
Это значит, что преобладающим типом комбинированного действия одновременно трех веществ алюминия, фторида и бенз(а)пирена по совокупности негативных эффектов является синергизм.
Пример конкретной реализации предлагаемого способа:
1 этап.
Качество атмосферного воздуха селитебной застройки характеризуется повышенным содержанием бенз(а)пирена до 2,2 ПДКс.г. и до 5,8 ПДКс.с, а также постоянным присутствием оксида алюминия и гидрофторида на уровне 0,1 ПДКс.г. и 0,3 ПДКс.с.
При этом территория наблюдения характеризовалась следующей хронической аэрогенной экспозицией бенз(а)пирена (наблюдения за 5 лет):
- повышенной относительно референтной концентрации (Rfc) бенз(а)пирена 5,8 Rfc (при этом Rfc=0,000001 мг/дм3);
- оксида алюминия (в пересчете на алюминий) алюминия на уровне референтной концентрации 0,2 Rfc (при этом Rfc=0,005 мг/дм3)
- содержание гидрофторида (в пересчете на фтор) на уровне референтных значений и составляло 0,3 Rfc (при этом Rfc= 0,013 мг/дм3).
Территория сравнения характеризовалась хронической аэрогенной экспозицией ниже референтных уровней, а именно бенз(а)пирена 0,000001 Rfc, оксида алюминия 0,04 Rfc и гидрофторида 0,12 Rfc.
2 этап.
На территории наблюдения были отобраны 332 ребенка 4-7 лет, вошедшие в группу наблюдения.
На территории сравнения были отобраны 132 ребенка 4-7 лет, составляющие группу сравнения.
Выборки по половозрастному составу, социально-бытовым условиям проживания, среднему уровню материального обеспечения, по частоте и характеру вредных привычек и профессиональных вредностей у родителей отобранных детей, были сопоставимыми. На момент обследования дети не имели острых инфекционных заболеваний не менее, чем в течение 4 недель до начала исследования, не принимали лекарственных препаратов, оказывающих выраженное влияние на изучаемые функции/заболевания со стороны критических органов и систем, менее чем за 30 дней до начала исследования.
3 этап.
В условиях существующей хронической экспозиции при ингаляционном поступлении бенз(а)пирена, оксида алюминия и гидрофторида установлено, что у детей группы наблюдения среднее содержание бенз(а)пирена в крови регистрируется на уровне 0,007±0,001 мг/дм3, что в 1,8 раза выше относительно аналогичного показателя у детей группы сравнения.
Среднее содержание фторид-иона в моче у детей группы наблюдения составило 0,69±0,14 мг/дм3, что в 1,2-1,9 раза выше относительно данного показателя в группе сравнения и референтного уровня (р=0,0001).
Концентрация алюминия в моче детей группы наблюдения составила 0,011±0,001 мг/дм3, что превысило в 1,7 раза референтный уровень и 2,8 раза концентрацию алюминия в моче детей группы сравнения (р=0,0001-0,045).
Данные о содержании химических веществ в биосредах детей группы наблюдения и группы сравнения приведены в таблице 7.
4 этап.
Моделирование зависимости «концентрация химического вещества в крови/моче от концентрации химического вещества в атмосферном воздухе» позволило получить адекватные модели зависимости (таблица 8): содержание бенз(а)пирена в крови от дозы бенз(а)пирена в атмосферном воздухе (R2=0,10; р=0,01), содержание фторид-иона в моче от дозы гидрофторида в атмосферном воздухе (R2=0,08; р=0,04), содержание алюминия в моче от дозы оксида алюминия в атмосферном воздухе (R2=0,07; р=0,0001), что позволило обосновать концентрации указанных химических веществ в качестве маркеров ингаляционной экспозиции, а уровни алюминия (0,010-0,012 мг/дм3) и фторид-иона (0,55-0,83 мг/дм3) в моче, бенз(а)пирена в крови ((0,006-0,008)⋅10-3 мг/дм3) могут свидетельствовать о повышенной опасности вероятности возникновения негативных эффектов со стороны органов, тропных к негативному действию перечисленных химических веществ.
5 этап.
Сформирован перечень лабораторных показателей для исследования ответных реакций организма детей исходя из наиболее вероятных негативных эффектов – нарушений здоровья у детей со стороны критических органов и систем, возникающих в ответ на воздействие бенз(а)пирена, алюминия и фторида:
- со стороны иммунной системы - уровень сывороточных иммуноглобулинов А, М, G; содержание иммуноглобулина Е общего (IgE), иммуноглобулина G специфического (IgGспец.) к бенз(а)пирену, алюминию и фтору, фагоцитарное число и фагоцитарный индекс в крови;
- со стороны костной системы – содержание N-остеокальцина, тартрат-резистентной кислой фосфатазы в сыворотке крови, уровень ионизированного кальция в плазме крови;
- со стороны нервной системы – содержание глутаминовой кислоты, γ-аминомасляной кислоты (ГАМК), серотонина, кортизола, нейротропина-3, уровень нейронспецифической энолазы в сыворотке крови;
- со стороны органов дыхания – содержание лимфоцитов, моноцитов, эозинофилов в крови, эозинофильно-лимфоцитарный индекс; содержание эозинофилов, нейтрофилов в назальном секрете, индекс эозинофилии; уровень иммуноглобулина Е общего (IgЕ), уровень антиоксидантной активности плазмы крови и малонового диальдегида (МДА).
6 этап.
В биосредах детей группы наблюдения установлены уровни лабораторных показателей достоверно отличающиеся от физиологической нормы и/или от уровня показателей группы сравнения (p≤0,05), при этом отражающие состояние критических органов и систем, тропных к действию бенз(а)пирена, оксида алюминия и гидрофторида (таблица 9).
На основании моделирования причинно-следственных связей между содержанием химического вещества в моче/крови и отклонения лабораторных показателей от физиологической нормы и/или по сравнению с показателем группы сравнения, установлены адекватности модели зависимости (таблица 10):
7 этап.
В результате установленных адекватных моделей зависимости обосновано 8 биомаркеров негативных эффектов:
- со стороны иммунной системы: повышенный (относительно физиологической нормы / или уровня показателей группы сравнения) уровень иммуноглобулина G общего (IgG) в пределах 12,98-15,30 г/дм3, наличие иммуноглобулина G специфического (IgGспец.) к бенз(а)пирену в пределах 0,11-0,214 усл. ед., понижение фагоцитарного числа в пределах 0,83-0,95 усл. ед. и фагоцитарного индекса 1,70-1,81 усл. ед.в крови;
- костной системы – повышенное содержание тартрат-резистентной кислой фосфатазы в сыворотке крови в пределах 2,53-3,09 ЕД/дм3;
- нервной системы – повышенный уровень нейронспецифической энолазы в сыворотке крови в пределах 4,09-5,59 мкг/дм3;
- органов дыхания – повышенный уровень иммуноглобулина Е общего (IgE) в сыворотке крови в пределах 58,99-196,63 МЕ/см3и малонового диальдегида (МДА) в плазме крови в пределах 2,37-2,61 мкмоль/см3; изменение которых патогенетически связанно с воздействием факторов экспозиции (оксид алюминия, бенз(а)пирен и гидрофторид).
8 этап.
Проведено определение вероятности отклонения биомаркера негативного эффекта от физиологической нормы или уровня показателей группы сравнения при одновременном развитии эффектов изолированного и комбинированного действия трех указанных химических веществ, но при их бинарной комбинации в различных сочетаниях. Получают коэффициенты регрессии, характеризующие скорость нарастания вероятности отклонения биомаркера негативного эффекта от физиологической нормы при изолированном действии химических веществ, а также при комбинированном действии указанных химических веществ в бинарной смеси (таблица 2).
9 этап.
Экспертная оценка предварительного типа комбинированного действия химических веществ путем сопоставительного анализа смены знаков коэффициентов регрессии при изолированном действии каждого вещества (b1, b2, b3) и комбинации веществ в паре (b12, b13, b23) позволила установить, что при содержании в крови бенз(а)пирена, в моче алюминия и фторид-иона на уровнях, превышающих в 1,7-1,9 раза референтные значения, и при биомаркере экспозиции: содержанием в моче ребенка алюминия (0,010-0,012 мг/дм3) и фторид-иона (0,55-0,83 мг/дм3) в моче, бенз(а)пирена в крови ((0,006-0,008)⋅10-3 мг/дм3), формируются различные варианты комбинированного действия изучаемых химических веществ в отношении негативных эффектов.
В зависимости от бинарного сочетания трех химических веществ и выбора биомаркера негативного эффекта (8 лабораторных показателей) выявлены различные варианты комбинированного действия (всего 24 варианта, а именно: (8)b1b2+(8)b1b3+ (8)b2b3=24). Для 10 из них (синергизм + эмерджентность+антагонизм) (42,0 % от их общего количества) установлена вероятность усиления негативного эффекта (таблица 2), свойственная действию фторида в комбинации с алюминием и с бенз(а)пиреном.
10 этап.
Определение частоты встречаемости соответствующих выявленных вариантов комбинированного действия химических веществ позволило установить, что в комбинации фторида и алюминия (колонка b1b3 таблицы 2) установлено 2 типа действия с усилением негативного эффекта: синергизм и антагонизм. Анализ частоты встречаемости выявленных типов действия веществ показал, что преобладающим является синергизм, установленный в 67,0 % случаев при действии на иммунную, нервную системы и органы дыхания; антагонизм – в 33,0 % на костную систему.
В комбинации фторида и бенз(а)пирена (колонка b2b3 таблицы 2) выявлены синергизм и эмерджентность с усилением негативного эффекта. Синергизм установлен в 75,0 % случаев при действии на органы дыхания и костную систему, эмерджентность в 25,0 % случаев – на иммунную систему.
В бинарной комбинации алюминия и бенз(а)пирена (колонка b1b2 таблицы 2) усиления негативных эффектов со стороны иммунной, костной систем и органов дыхания не выявлено. Вещества в этом случае действуют адекватно изолированному.
11 этап.
Определение дополнительной вероятности отклонения биомаркера негативного эффекта в результате эффектов комбинированного действия трех веществ: оксида алюминия, бенз(а)пирена и гидрофторида позволила установить, что по совокупности негативных эффектов в 75,0 % случаев преобладает синергетический тип действия алюминия, фторида и бенз(а)пирена (повышение IgG специфического к бенз(а)пирену, тартрат-резистентной кислой фосфатазы, нейронспецифической энолазы, МДА; снижение фагоцитарного числа и индекса) (таблица 6). Антагонистический характер действия изучаемых веществ выявлен только в 25,0 % случаев (повышение IgG и IgE общего).
Таким образом, интегральная оценка типа комбинированного действия бинарной смеси веществ на каждый орган-мишень при их выявленном разнообразии выполняется с учетом установленной вероятности отклонения патогенетически значимых биомаркеров негативных эффектов и наибольшей частоты встречаемости соответствующих им выявленных типов действия.
Для доказательства достоверности предлагаемого способа ниже приведены примеры его реализации на примерах конкретных детей.
Пример 1. Девочка 5 лет, постоянно проживает на территории наблюдения. Пробы биосред характеризуются одновременным наличием алюминия, фторид-иона в моче, бенз(а)пирена в крови. Содержание в моче алюминия 0,009 мг/дм3, фторид-иона в моче 0,545 мг/дм3, бенз(а)пирена в крови 0,002·10-6 мг/дм3. В крови были определены следующие лабораторные показатели:
уровень IgG – 13,12 г/дм3,
уровень IgGспец. к бенз(а)пирену – 0,11 усл. ед.,
фагоцитарное число - 0,72 усл. ед.
фагоцитарный индекс – 1,68 усл. ед.в крови;
содержание тартрат-резистентной кислой фосфатазы в сыворотке крови - 2,93 ЕД/дм3;
уровень нейронспецифической энолазы в сыворотке крови – 5,80 мкг/дм3;
уровень IgE общего в сыворотке крови – 115,3 МЕ/см3
уровень МДА в плазме крови – 2,49 мкмоль/см3.
Было установлено, что у ребенка повышены уровни IgE общего и МДА по сравнению с физиологической нормой и уровни данных показателей входят в диапазон этих показателей, характеризующих состояние органов дыхания (повышенный уровень IgE общего в сыворотке крови в пределах 58,99-196,63 МЕ/см3 и МДА в плазме крови в пределах 2,37-2,61 мкмоль/см3) в предлагаемом способе, изменение которых патогенетически связанно с воздействием оксида алюминия, бенз(а)пирена и гидрофторида. А согласно данным, приведенным в таблице 2, показано, что влияние указанных химических веществ характеризуется усилением окислительной модификации белков эпителиальных клеток и последующим дисбалансом оксидантно-антиоксидантных процессов, что приводит к запуску IgE-зависимых реакций, воспалительных процессов, сопровождающихся высвобождением медиаторов воспаления. Таким образом, следует ожидать, что ребенок подвержен заболеваниям органов дыхания, т.к. преобладающим типом комбинированного аэрогенного воздействия этих химических веществ на органы дыхания является синергизм. Изучение анамнеза в поликлинике показало, что ребенок страдает хроническим ринитом (МКБ-10: J31.0). Таким образом, было доказано, что предлагаемый способ является достоверным.
Пример 2. Мальчик 7 лет, постоянно проживает на территории наблюдения. Пробы биосред характеризуются одновременным наличием алюминия, фторид-иона в моче, бенз(а)пирена в крови. Содержание в моче алюминия 0,010 мг/дм3, фторид-иона в моче 0,703 мг/дм3, бенз(а)пирена в крови 0,001·10-6 мг/дм3. В крови были определены следующие лабораторные показатели:
уровень IgG – 11,25 г/дм3,
уровень IgGспец. к бенз(а)пирену – 0,13 усл. ед.,
фагоцитарное число - 0,93 усл. ед.
фагоцитарный индекс – 1,75 усл. ед.в крови;
содержание тартрат-резистентной кислой фосфатазы в сыворотке крови - 3,00 ЕД/дм3;
уровень нейронспецифической энолазы в сыворотке крови – 6,12 мкг/дм3;
уровень IgE общего в сыворотке крови – 48,7 МЕ/см3
уровень МДА в плазме крови – 2,38 мкмоль/см3.
Было установлено, что у ребенка уровень тартрат-резистентной кислой фосфатазы повышен относительно среднегруппового уровня группы наблюдения и входит в диапазон показателя, характеризующего состояние костной системы (уровень тартрат-резистентной кислой фосфатазы в сыворотке крови в пределах 2,53-3,09 ЕД/дм3;) в предлагаемом способе, изменение которого патогенетически связанно с воздействием оксида алюминия, бенз(а)пирена и гидрофторида. А согласно данным, приведенным в таблице 2, показано, что влияние указанных химических веществ усиливает ремоделирование костной ткани в сторону процесса резорбции, т.е. следует ожидать, что ребенок подвержен заболеваниям со стороны костной системы, т.к. преобладающим типом комбинированного аэрогенного воздействия этих химических веществ на костную систему является синергизм. Изучение анамнеза в поликлинике показало, что ребенок страдает деформирующей дорсопатией (МКБ-10: M43.9). Таким образом, было доказано, что предлагаемый способ является достоверным.
Предлагаемый способ обеспечивает повышение объективность гигиенической оценки рисков здоровью и их реализации, обусловленных комбинированным воздействием химических веществ на детей 4-7 лет из зон экспозиции.
Таблица 1. Матрица для экспертной оценки предварительного типа комбинированного действия химических веществ
Таблица 2. Предварительный тип комбинированного действия бинарных смесей алюминия, бенз(а)пирена, алюминия и фторид-иона
ний
(х1)
пирен
(х2)
(х3)
пирен
(х12)
и фтор
(х13)
пирен и фтор
(х23)
и фтор
и фтор
Примечание:* - типы взаимодействий химических веществ с усилением негативного эффекта
Таблица 6. Дополнительная вероятность отклонения биомаркера негативного эффекта в результате эффектов комбинированного действия трех веществ: оксида алюминия, бенз(а)пирена и гидрофторида и преобладающий тип комбинированного действия
Таблица 7. Содержание химических веществ в биосредах детей исследуемых групп, мг/дм3
мг/дм3
р1 – достоверность различий группы наблюдения и группы сравнения
р2– достоверность различий группы наблюдения и референтного уровня
Статистическая обработка полученных результатов выполнялась с учетом описания количественных признаков с использованием значения среднего (М) и ошибки репрезентативности (m), так как случайные величины анализируемых показателей соответствовали закону нормального распределения.
Таблица 8. Модели зависимости содержания химических веществ в биосредах детей от концентрации (среднесуточной) в атмосферном воздухе
в атмосферном воздухе, мг/м3
(концентрация вещества
в биосреде), мг/дм3
циент
детерминации (R2)
(F≥3,65)
достовер
ности
(p≤0,05)
Таблица 9. Сравнительный анализ изменения лабораторных показателей у детей группы наблюдения и группы сравнения, отражающих состояние критических органов и систем
различий средних между группами (p≤0,05)
Таблица 10. Модели зависимости изменения биохимических показателей у детей группы наблюдения и сравнения от содержания химических веществ в биосредах
изменения показателя
различий
(р≤0,05)
в моче
Изобретение относится к медицине, а именно к медицинской экологии, и может быть использовано для дифференциальной оценки преобладающего типа комбинированного аэрогенного воздействия химических веществ: оксида алюминия, бенз(а)пирена и гидрофторида, на здоровье детей 4-7 лет. У детей, проживающих на территории с постоянным присутствием и/или с повышенной, по сравнению с предельно-допустимой концентрацией, в атмосферном воздухе химических веществ: оксида алюминия, бенз(а)пирена и гидрофторида отбирают пробы мочи и пробы крови. В пробах у детей определяют концентрацию алюминия и фторид-иона в моче, бенз(а)пирена в крови. При выявлении у ребенка концентрации биомаркеров экспозиции, а именно: содержания в моче ребенка алюминия 0,010-0,012 мг/дм3 и фторид-иона 0,55-0,83 мг/дм3, и бенз(а)пирена в крови ребенка (0,006-0,008)⋅10-3 мг/дм3, определяют в биосредах ребенка лабораторные показатели, являющиеся биомаркерами негативных эффектов, которые патогенетически связаны с наиболее вероятными негативными эффектами – нарушениями здоровья у детей, со стороны критических органов и систем, возникающими в ответ на воздействие химических веществ: оксида алюминия – нервная система и органы дыхания; бенз(а)пирена – иммунная система; гидрофторида – костная система и органы дыхания, а именно: со стороны иммунной системы - содержание иммуноглобулина G общего (IgG), МЕ/см3; иммуноглобулина G специфического (IgGспец.) к бенз(а)пирену, усл. ед; фагоцитарное число, усл ед, и фагоцитарный индекс в крови, усл ед; со стороны костной системы - показатель тартрат-резистентной кислой фосфатазы в сыворотке крови, ЕД/дм3; со стороны нервной системы - уровень нейронспецифической энолазы в сыворотке крови, мкг/дм3; со стороны органов дыхания - уровень иммуноглобулина Е общего (IgЕ), г/дм3, и уровень малонового диальдегида (МДА), мкмоль/см3, в плазме крови. При уровне лабораторных показателей ребенка, входящих в количественный диапазон лабораторных показателей вышеуказанных биомаркеров негативных эффектов, а именно: со стороны иммунной системы: уровень IgG 12,98-15,30 г/дм3, IgGспец. к бенз(а)пирену 0,11-0,214 усл. ед., фагоцитарное число 0,83-0,95 усл. ед. и фагоцитарный индекс 1,70-1,81 усл. ед.; костной системы: содержание тартрат-резистентной кислой фосфатазы 2,53-3,09 ЕД/дм3; нервной системы: уровень нейронспецифической энолазы 4,09-5,59 мкг/дм3; органов дыхания: уровень IgE 58,99-196,63 МЕ/см3 и МДА 2,37-2,61 мкмоль/см3, которые патогенетически связаны с воздействием вышеуказанных биомаркеров экспозиции на здоровье детей, такие биомаркеры определяют как патогенетически значимые выявленные биомаркеры негативных эффектов для ребенка.
Определяют вероятность p каждого выявленного биомаркера негативных эффектов по формуле: 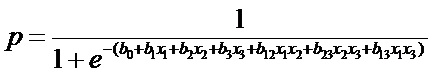 , где p – вероятность ответной реакции организма ребенка для каждого выявленного патогенетически значимого биомаркера негативных эффектов при одновременном развитии эффектов изолированного и комбинированного действия трех химических веществ, при их бинарной комбинации; x1, x2, x3 – концентрация алюминия в моче ребенка, бенз(а)пирена в крови ребенка и фторид-иона в моче ребенка соответственно, при экспозиции оксидом алюминия, бенз(а)пиреном и гидрофторидом, мг/дм3; b0 – коэффициент регрессии, приведенный в таблице 2 описания, характеризующий уровень вероятности ответной реакции организма ребенка для каждого выявленного патогенетически значимого биомаркера негативных эффектов, независимо от влияния изучаемых маркеров экспозиции - фоновый уровень; b1, b2, b3, b12, b13, b23 – коэффициенты регрессии, приведенные в таблице 2 описания, характеризующие уровень вероятности ответной реакции организма ребенка для каждого выявленного патогенетически значимого биомаркера негативных эффектов, при изолированном действии оксида алюминия, бенз(а)пирена и гидрофторида, а также при их комбинированном действии в бинарной смеси. Определяют вероятность p1 каждого выявленного патогенетически значимого биомаркера негативных эффектов по формуле: p1 =
, где p – вероятность ответной реакции организма ребенка для каждого выявленного патогенетически значимого биомаркера негативных эффектов при одновременном развитии эффектов изолированного и комбинированного действия трех химических веществ, при их бинарной комбинации; x1, x2, x3 – концентрация алюминия в моче ребенка, бенз(а)пирена в крови ребенка и фторид-иона в моче ребенка соответственно, при экспозиции оксидом алюминия, бенз(а)пиреном и гидрофторидом, мг/дм3; b0 – коэффициент регрессии, приведенный в таблице 2 описания, характеризующий уровень вероятности ответной реакции организма ребенка для каждого выявленного патогенетически значимого биомаркера негативных эффектов, независимо от влияния изучаемых маркеров экспозиции - фоновый уровень; b1, b2, b3, b12, b13, b23 – коэффициенты регрессии, приведенные в таблице 2 описания, характеризующие уровень вероятности ответной реакции организма ребенка для каждого выявленного патогенетически значимого биомаркера негативных эффектов, при изолированном действии оксида алюминия, бенз(а)пирена и гидрофторида, а также при их комбинированном действии в бинарной смеси. Определяют вероятность p1 каждого выявленного патогенетически значимого биомаркера негативных эффектов по формуле: p1 =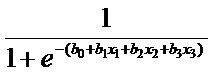 , где p1 - вероятность ответной реакции организма ребенка для каждого выявленного патогенетически значимого биомаркера негативных эффектов, при одновременном развитии эффектов действия оксида алюминия, бенз(а)пирена и гидрофторида при их изолированном действии. Определяют дополнительную вероятность Δр выявленного патогенетически значимого биомаркера негативных эффектов по формуле: Δр= р - p1, где Δр – дополнительная вероятность ответной реакции организма ребенка для каждого выявленного патогенетически значимого биомаркера негативных эффектов в результате эффектов комбинированного действия оксида алюминия, бенз(а)пирена и гидрофторида. Для выявленного биомаркера негативных эффектов, при положительном значении Δр преобладающий тип комбинированного аэрогенного воздействия алюминия, бенз(а)пирена и гидрофторида на нарушение здоровья ребенка 4-7 лет оценивают, как синергетический, превышающий сумму негативных эффектов каждого отдельного вещества, а при отрицательном значении Δр – как антагонистический, меньше суммы негативных эффектов каждого отдельного вещества. Способ обеспечивает возможность информативного и доказательного обоснования и установления дифференциальной оценки типа: синергетического или антагонистического, комбинированного аэрогенного одновременного воздействия оксида алюминия, бенз(а)пирена и гидрофторида, на здоровье детей 4-7 лет, за счет за счет анализа параметризированных причинно-следственных связей экспозиции воздействующих веществ и негативных эффектов. 10 табл., 2 пр.
, где p1 - вероятность ответной реакции организма ребенка для каждого выявленного патогенетически значимого биомаркера негативных эффектов, при одновременном развитии эффектов действия оксида алюминия, бенз(а)пирена и гидрофторида при их изолированном действии. Определяют дополнительную вероятность Δр выявленного патогенетически значимого биомаркера негативных эффектов по формуле: Δр= р - p1, где Δр – дополнительная вероятность ответной реакции организма ребенка для каждого выявленного патогенетически значимого биомаркера негативных эффектов в результате эффектов комбинированного действия оксида алюминия, бенз(а)пирена и гидрофторида. Для выявленного биомаркера негативных эффектов, при положительном значении Δр преобладающий тип комбинированного аэрогенного воздействия алюминия, бенз(а)пирена и гидрофторида на нарушение здоровья ребенка 4-7 лет оценивают, как синергетический, превышающий сумму негативных эффектов каждого отдельного вещества, а при отрицательном значении Δр – как антагонистический, меньше суммы негативных эффектов каждого отдельного вещества. Способ обеспечивает возможность информативного и доказательного обоснования и установления дифференциальной оценки типа: синергетического или антагонистического, комбинированного аэрогенного одновременного воздействия оксида алюминия, бенз(а)пирена и гидрофторида, на здоровье детей 4-7 лет, за счет за счет анализа параметризированных причинно-следственных связей экспозиции воздействующих веществ и негативных эффектов. 10 табл., 2 пр.
Способ дифференциальной оценки преобладающего типа комбинированного аэрогенного воздействия химических веществ: оксида алюминия, бенз(а)пирена и гидрофторида, на здоровье детей 4-7 лет, характеризующийся тем, что
у детей, проживающих на территории с постоянным присутствием и/или с повышенной, по сравнению с предельно-допустимой концентрацией, в атмосферном воздухе химических веществ: оксида алюминия, бенз(а)пирена и гидрофторида отбирают пробы мочи и пробы крови,
в пробах у детей определяют концентрацию алюминия и фторид-иона в моче, бенз(а)пирена в крови,
при выявлении у ребенка концентрации биомаркеров экспозиции, а именно: содержания в моче ребенка алюминия 0,010-0,012 мг/дм3 и фторид-иона 0,55-0,83 мг/дм3 , и бенз(а)пирена в крови ребенка (0,006-0,008)⋅10-3 мг/дм3, определяют в биосредах ребенка лабораторные показатели, являющиеся биомаркерами негативных эффектов, которые патогенетически связаны с наиболее вероятными негативными эффектами – нарушениями здоровья у детей, со стороны критических органов и систем, возникающими в ответ на воздействие химических веществ: оксида алюминия – нервная система и органы дыхания; бенз(а)пирена – иммунная система; гидрофторида – костная система и органы дыхания, а именно: со стороны иммунной системы - содержание иммуноглобулина G общего (IgG), МЕ/см3; иммуноглобулина G специфического (IgGспец.) к бенз(а)пирену, усл. ед; фагоцитарное число, усл ед, и фагоцитарный индекс в крови, усл ед; со стороны костной системы - показатель тартрат-резистентной кислой фосфатазы в сыворотке крови, ЕД/дм3; со стороны нервной системы - уровень нейронспецифической энолазы в сыворотке крови, мкг/дм3; со стороны органов дыхания - уровень иммуноглобулина Е общего (IgЕ), г/дм3, и уровень малонового диальдегида (МДА), мкмоль/см3, в плазме крови;
при уровне лабораторных показателей ребенка, входящих в количественный диапазон лабораторных показателей вышеуказанных биомаркеров негативных эффектов, а именно: со стороны иммунной системы: уровень IgG 12,98-15,30 г/дм3, IgGспец. к бенз(а)пирену 0,11-0,214 усл. ед., фагоцитарное число 0,83-0,95 усл. ед. и фагоцитарный индекс 1,70-1,81 усл. ед.; костной системы: содержание тартрат-резистентной кислой фосфатазы 2,53-3,09 ЕД/дм3; нервной системы: уровень нейронспецифической энолазы 4,09-5,59 мкг/дм3; органов дыхания: уровень IgE 58,99-196,63 МЕ/см3 и МДА 2,37-2,61 мкмоль/см3, которые патогенетически связаны с воздействием вышеуказанных биомаркеров экспозиции на здоровье детей, такие биомаркеры определяют как патогенетически значимые выявленные биомаркеры негативных эффектов для ребенка;
затем определяют вероятность p каждого выявленного биомаркера негативных эффектов по формуле:
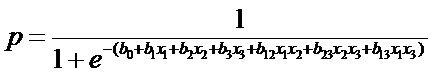 ,
,
где p – вероятность ответной реакции организма ребенка для каждого выявленного патогенетически значимого биомаркера негативных эффектов при одновременном развитии эффектов изолированного и комбинированного действия трех химических веществ, при их бинарной комбинации;
x1, x2, x3 – концентрация алюминия в моче ребенка, бенз(а)пирена в крови ребенка и фторид-иона в моче ребенка соответственно, при экспозиции оксидом алюминия, бенз(а)пиреном и гидрофторидом, мг/дм3 ;
b0 – коэффициент регрессии, приведенный в таблице 2 описания, характеризующий уровень вероятности ответной реакции организма ребенка для каждого выявленного патогенетически значимого биомаркера негативных эффектов, независимо от влияния изучаемых маркеров экспозиции - фоновый уровень;
b1, b2, b3, b12, b13, b23 – коэффициенты регрессии, приведенные в таблице 2 описания, характеризующие уровень вероятности ответной реакции организма ребенка для каждого выявленного патогенетически значимого биомаркера негативных эффектов, при изолированном действии оксида алюминия, бенз(а)пирена и гидрофторида, а также при их комбинированном действии в бинарной смеси;
определяют вероятность p1 каждого выявленного патогенетически значимого биомаркера негативных эффектов по формуле:
p1 =
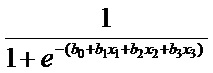 ,
,
где p1 - вероятность ответной реакции организма ребенка для каждого выявленного патогенетически значимого биомаркера негативных эффектов, при одновременном развитии эффектов действия оксида алюминия, бенз(а)пирена и гидрофторида при их изолированном действии;
определяют дополнительную вероятность Δр выявленного патогенетически значимого биомаркера негативных эффектов по формуле:
Δр= р - p1,
где Δр – дополнительная вероятность ответной реакции организма ребенка для каждого выявленного патогенетически значимого биомаркера негативных эффектов в результате эффектов комбинированного действия оксида алюминия, бенз(а)пирена и гидрофторида;
и для выявленного биомаркера негативных эффектов, при положительном значении Δр преобладающий тип комбинированного аэрогенного воздействия алюминия, бенз(а)пирена и гидрофторида на нарушение здоровья ребенка 4-7 лет оценивают, как синергетический, превышающий сумму негативных эффектов каждого отдельного вещества, а при отрицательном значении Δр – как антагонистический, меньше суммы негативных эффектов каждого отдельного вещества.
| Способ обоснования возникновения у детей негативного эффекта в виде заболевания, связанного с центральной или вегетативной нервной системой, ассоциированного с аэрогенной экспозицией алюминия | 2017 |
|
RU2666924C1 |
| Способ обоснования возникновения у детей негативного эффекта в виде заболевания костной системы, ассоциированного с аэрогенным воздействием соединений фтора | 2017 |
|
RU2670769C1 |
| ТИХОНОВА И.В | |||
| Гигиеническая оценка воздействия химических компонентов производства глинозема на органы дыхания у детей для совершенствования системы социально-гигиенического мониторинга | |||
| Автореф | |||
| диссер | |||
| Способ восстановления спиралей из вольфрамовой проволоки для электрических ламп накаливания, наполненных газом | 1924 |
|
SU2020A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| ЗОРИНА А.С | |||
| и др | |||
| Исследования содержания бенз(а)пирена в крови | |||
Авторы
Даты
2024-08-07—Публикация
2023-11-15—Подача