Изобретение относится к аналитической химии и может быть использовано при подготовке пробы премиксов, кормов или кормового сырья для количественного определения содержания витамина А в форме ретинола ацетата в диапазоне 500 тыс.-1,5 млн МЕ/г или витамина D3 в форме холекальциферола в диапазоне 300-700 тыс. МЕ/г методом высокоэффективной жидкостной хроматографии (ВЭЖХ).
Известен способ определения витамина А в биологическом материале методом ВЭЖХ, включающий добавление к навеске пробы экстрагента, состоящего из изопропилового спирта и воды, омыление в течение 10 мин при температуре 75°С, охлаждение полученной смеси до комнатной температуры и отделение фильтрата (см. а.с. СССР № 1790895, МПК A23K 1/00, дата публикации 30.01.1993 г.).
Однако известное решение относится только к определению содержания витамина А в количестве до 500000 МЕ/г.
В качестве ближайшего аналога (прототипа) принят способ определения витамина А в биологическом материале методом ВЭЖХ, содержащий добавление к пробе исследуемого образца последовательно антиоксиданта и водно-спиртового раствора гидроксида калия в этаноле с соотношением 2 г KOH : 2 см3 воды для анализа : 18 см3 ректификованного этилового спирта, омыление полученной смеси в течение 30 мин с последующим охлаждением до комнатной температуры, добавление к полученному гидролизату воды, последовательная тройная экстракция гексаном с объединением экстрактов, промывание объединенного гексанового экстракта дистиллированной водой, внесение безводного сульфата натрия с последующим упариванием, растворение полученного сухого остатка в жидкости с последующей выдержкой в темной месте, и фильтрацию перед проведением высокоэффективной жидкостной хроматографии (см. ГОСТ 32043-2012, введен в действие с 01.07.2014 г.).
Недостатками прототипа являются ограниченный диапазон определяемых концентраций витаминов - до 10000 МЕ/г и высокие значения относительной погрешности метода - до 35%.
Проблемой, на решение которой направлена заявляемое изобретение, является разработка эффективного способа количественного определения содержания витамина А в форме ретинола ацетата в диапазоне 500 тыс.-1,5 млн МЕ/г или витамина D3 в форме холекальциферола в диапазоне 300-700 тыс. МЕ/г методом высокоэффективной жидкостной хроматографии (ВЭЖХ).
Технический результат, проявляющийся при решении поставленной проблемы, выражается в следующем:
- возможность количественного определения содержания жирорастворимого витамина в высоких концентрациях, в частности витамина А в форме ретинола ацетата в диапазоне 500 тыс.-1,5 млн МЕ/г или витамина D3 в форме холекальциферола в диапазоне 300-700 тыс. МЕ/г;
- снижение показателя погрешности методики до 15%.
Поставленная проблема решается тем, что способ подготовки пробы для количественного определения содержания жирорастворимого витамина в исследуемом образце методом ВЭЖХ, содержащий добавление к пробе исследуемого образца последовательно антиоксиданта и водно-спиртового раствора гидроксида калия в этаноле с соотношением 2 г KOH : 2 см3 воды для анализа : 18 см3 ректификованного этилового спирта, омыление полученной смеси в течение 30 мин с последующим охлаждением до комнатной температуры, добавление к полученному гидролизату воды, последовательная тройная экстракция гексаном с объединением экстрактов, промывание объединенного гексанового экстракта дистиллированной водой, внесение безводного сульфата натрия с последующим упариванием, растворение полученного сухого остатка в жидкости с последующей выдержкой в темной месте, и фильтрацию перед проведением высокоэффективной жидкостной хроматографии отличается тем, что к навеске пробы исследуемого образца в качестве антиоксиданта добавляют 10%-ный водный раствор аскорбиновой кислоты, омыление проводят при температуре 70°С, после упаривания полученный сухой остаток растворяют в изопропиловом спирте и подвергают обращенно-фазной высокоэффективной жидкостной хроматографии.
Кроме того, в исследуемом образце определяют содержание витамина А в форме ретинола ацетата в диапазоне 500 тыс.-1,5 млн МЕ/г.
Кроме того, в исследуемом образце определяют содержание витамина D3 в форме холекальциферола в диапазоне 300-700 тыс. МЕ/г.
Сопоставительный анализ признаков заявляемого изобретения с признаками прототипа и аналогов свидетельствует о соответствии заявляемого решения критерию «новизна».
При этом отличительные признаки формулы изобретения обеспечивают решение следующих функциональных задач.
Признак, указывающий что используют «навеску пробы исследуемого образца», позволяет не готовить дополнительно растворы и как следствие упростить методику при экономии реагентов.
Признак, указывающий, что к навеске пробы исследуемого образца «в качестве антиоксиданта добавляют 10%-ный водный раствор аскорбиновой кислоты» обеспечивает сокращение потерь нестабильного витамина в условиях контакта с кислородом и УФ-облучения.
Признак, указывающий что «омыление проводят при температуре 70°С», обеспечивает сохранность жирорастворимого витамина, который разрушается при более высокой температуре.
Признаки, указывающие что «сухой остаток растворяют в изопропиловом спирте и подвергают обращенно-фазной высокоэффективной жидкостной хроматографии», позволяют получить более достоверные результаты ВЭЖХ при более низких затратах.
Зависимые пункты формулы описывают виды, формы и концентрацию жирорастворимых витаминов.
Другие отличительные признаки и преимущества изобретения ясно вытекают из описания, приведенного ниже для иллюстрации и не являющегося ограничительным, со ссылками на прилагаемые чертежи:
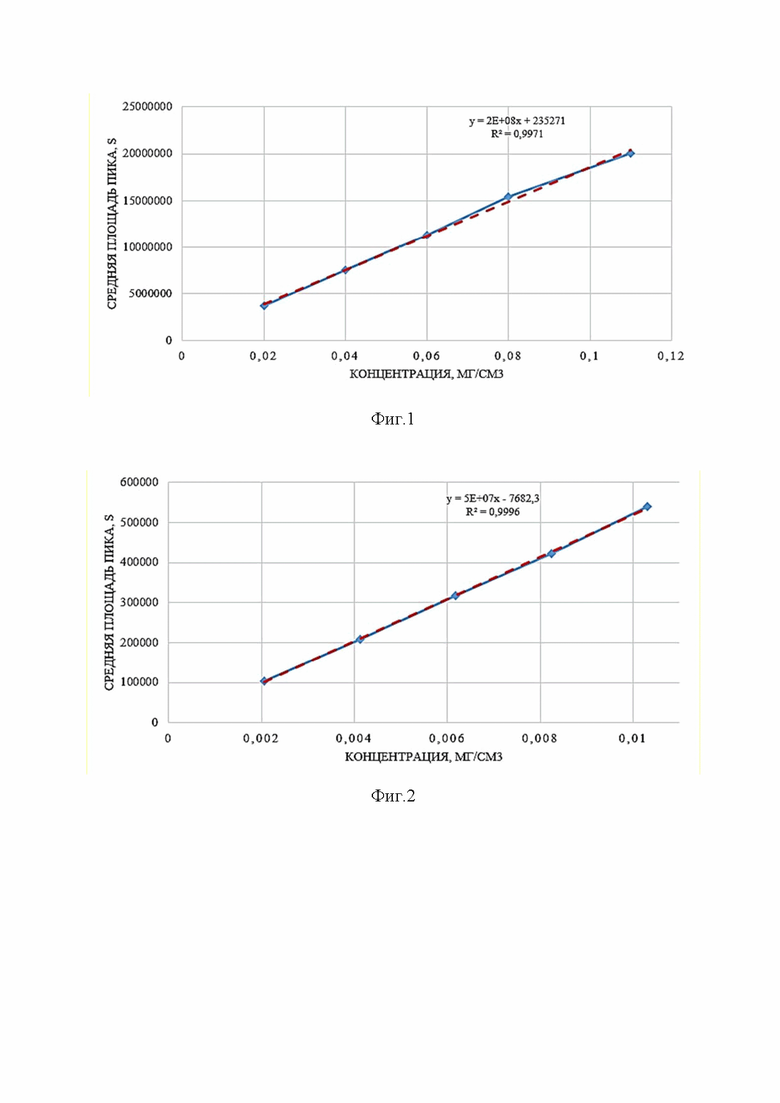
на фиг.1 изображена линейная калибровочная зависимость для витамина А в форме ретинола ацетата;
на фиг.2 изображена линейная калибровочная зависимость для витамина D3 в форме холекальциферола.
Заявляемый способ осуществляют на стандартном оборудовании в несколько этапов.
1. Отбор исследуемого образца - осуществляют в соответствии с ГОСТ 13496.0, при необходимости указанный образец гомогенизируют до фракции 0,8 мм.
2. Взятие навески пробы исследуемого образца.
2.1. Для витамина А для первого определения (методика которого описана в этапах 3-5) берут навеску пробы 0,070 г с погрешностью взвешивания ±0,0001 г.
В случае, если окончательный результат первого определения лежит в диапазоне 750 тыс.-1,25 млн МЕ/г витамина А, то его считают приемлемым.
В случае если окончательный результат первого определения лежит в диапазоне 500-750 тыс. МЕ/г, то этапы 3-5 повторяют, используя навеску пробы 0,011 г.
В случае если результат анализа лежит в диапазоне 1,250-1,500 млн МЕ/г, то этапы 3-5 повторяют, используя навеску пробы 0,050 г.
Для витамина D3 берут навеску пробы 0,011 г с погрешностью взвешивания ±0,0001 г.
3. Подготовка навески пробы исследуемого образца для обращенно-фазной высокоэффективной жидкостной хроматографии.
Навеску пробы исследуемого образца, взятую на этапе 2, переносят в коническую колбу вместимостью 100 см3 и добавляют 10 см3 антиоксиданта, в качестве которого используют 10%-ный водный раствор аскорбиновой кислоты, аккуратно перемешивают так, чтобы вся проба была смочена внесенным раствором.
После этого вносят 20 см3 водно-спиртового раствора гидроксида калия в этаноле с соотношением 2 г KOH : 2 см3 воды для анализа : 18 см3 ректификованного этилового спирта.
Содержимое колбы тщательно, но аккуратно перемешивают, соединяют с обратным холодильником и подвергают омылению в течение 30 мин на водяной бане при температуре 70°С.
После охлаждения реакционной смеси до комнатной температуры к полученному гидролизату пробы добавляют 10 см3 дистиллированной воды, содержимое колбы перемешивают, переносят в делительную воронку вместимостью 100 см3, следя за тем, чтобы как можно меньше осадка анализируемой пробы попадало в делительную воронку.
Трижды экстрагируют н-гексаном, внося поочередно 10, 10 и 5 см3. Тщательно ополаскивают очередным объемом экстрагента колбу, в которой проводился гидролиз. Продолжительность каждой экстракции - не менее 1 мин.
Гексановые экстракты объединяют в мерной колбе вместимостью 25 см3, объем содержимого доводят до метки н-гексаном и перемешивают.
Объединенный гексановый экстракт декантируют в делительную воронку и промывают дистиллированной водой порциями по 15 см3 до нейтральной реакции промывных вод (проверка по индикаторной бумаге).
Промытый экстракт сливают в чистую коническую колбу вместимостью 100 см3 и добавляют 5 г безводного сульфата натрия.
Из полученного гексанового экстракта отбирают 1 см3, переносят в круглодонную колбу на 10 см3 для удаления растворителя и упаривают досуха.
В сухой остаток сразу же добавляют 10 см3 изопропилового спирта, выдерживают 10 мин в темном месте с периодическим перемешиванием.
Полученный экстракт в изопропиловом спирте отфильтровывают через мембранный фильтр в хроматографическую виалу. Образец готов к вводу в хроматограф.
4. Проведение обращенно-фазной высокоэффективной жидкостной хроматографии.
Образец, подготовленный на этапе 3, вводят в хроматограф и подвергают обращенно-фазной высокоэффективной жидкостной хроматографии при параметрах, приведенных в таблице 1.
Параметры обращенно-фазной ВЭЖХ
Использование подвижной фазы метанол : вода в соотношении 98:2 обеспечивает эффективное разделение сложных смесей витаминов (А, D3) при минимальном времени анализа. Обычно применяют нормально-фазовое разделение синтетических жирорастворимых витаминов, основанном на элюировании их неполярными органическими растворителями после сорбции на полярных сорбентах. В обращенно-фазовом варианте используется подвижная фаза на основе полярного растворителя и неполярного сорбента. Применение неполярных сорбентов обеспечивает высокую скорость достижения равновесия.
Проведение хроматографических измерений при скорости потока 1,0 мл/мин позволяет увеличить время удерживания слабоудерживающих компонентов с целью исключения асимметрии пиков и возникновения «хвостов».
5. Обработка полученных результатов.
Для количественного анализа можно использовать, например колонки хроматографические с привитой обращенной фазой С18 длиной 250 мм, внутренним диаметром 4,6 мм, зернением 5 мкм.
За результат единичного измерения принимали значение, рассчитанное с помощью программного обеспечения хроматографа, результат из двух параллельных измерений одного раствора. За результат анализа принимали среднее арифметическое значение двух результатов единичных измерений. Для каждого образца для оценивания было получено по 20 результатов анализа.
Оценка метрологических характеристик методики анализа для проб рассчитывалась согласно РМГ 61-2010.
В таблицах 2 и 3 представлены значения площадей пиков исследуемых витаминов; на фиг. 1 и 2 приведены линейные калибровочные зависимости. Коэффициенты пригодности линейной зависимости были рассчитаны по п. 6.5 ГОСТ Р ИСО 11095-2007.
С помощью программного обеспечения хроматографа вычисляют массовую концентрацию определяемых витаминов в растворе по линейной градуировочной зависимости, реализуемой в соответствии с требованиями МИ 2175-91.
Зависимость площади пика от концентрации для витамина А
Зависимость площади пика от концентрации для витамина D3
По результатам статистической обработки данных, полученных в результате анализа, были установлены границы относительной суммарной погрешности ± δ,% и подтверждены диапазоны определения массовых концентраций витаминов А и D3, представленные в таблице 4.
Метрологические характеристики методики
Таким образом, заявляемый способ подготовки пробы исследуемого образца для количественного определения витамина А в форме ретинола ацетата или витамина D3 в форме холекальциферола методом высокоэффективной жидкостной хроматографии позволяет расширить диапазон определяемых концентраций и снизить границы относительной суммарной погрешности до 15%.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения витамина А в форме ретинол ацетата в исследуемом образце | 2022 |
|
RU2825784C2 |
| Биорелевантная среда двенадцатиперстной кишки свиньи натощак | 2022 |
|
RU2799589C1 |
| Биорелевантная среда двенадцатиперстной кишки крупного рогатого скота натощак | 2022 |
|
RU2799319C1 |
| Биорелевантная среда кишечника крупного рогатого скота натощак | 2022 |
|
RU2799519C1 |
| Биорелевантная среда желудка сельскохозяйственной птицы натощак | 2023 |
|
RU2822250C1 |
| Биорелевантная среда желудка свиньи натощак | 2023 |
|
RU2822251C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ОБЩИХ И ПОЛИЦИКЛИЧЕСКИХ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ В КОМПОНЕНТАХ ЭКОСИСТЕМЫ | 2015 |
|
RU2589897C1 |
| Биорелевантная среда желудка крупного рогатого скота натощак | 2023 |
|
RU2822252C1 |
| Способ определения витамина А в биологическом материале | 1990 |
|
SU1790895A1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ 3,4-БЕНЗ(А)ПИРЕНА ИЗ ПОЧВ, ДОННЫХ ОТЛОЖЕНИЙ И ОСАДКОВ СТОЧНЫХ ВОД | 2012 |
|
RU2485109C1 |
Изобретение относится к пищевой и химической промышленности. Способ подготовки пробы для количественного определения содержания витамина А в форме ретинола ацетата в диапазоне 500 тыс.-1,5 млн МЕ/г или витамина D3 в форме холекальциферола в диапазоне 300-700 тыс. МЕ/г в исследуемом образце методом ВЭЖХ содержит добавление к пробе исследуемого образца последовательно антиоксиданта и водно-спиртового раствора гидроксида калия в этаноле с соотношением 2 г KOH : 2 см3 воды для анализа : 18 см3 ректификованного этилового спирта, омыление полученной смеси в течение 30 минут с последующим охлаждением до комнатной температуры, добавление к полученному гидролизату воды, последовательную тройную экстракцию гексаном с объединением экстрактов, промывание объединенного гексанового экстракта дистиллированной водой, внесение безводного сульфата натрия с последующим упариванием, растворение полученного сухого остатка в жидкости с последующей выдержкой в темном месте и фильтрацию перед проведением высокоэффективной жидкостной хроматографии, отличается тем, что к навеске пробы исследуемого образца в качестве антиоксиданта добавляют 10%-ный водный раствор аскорбиновой кислоты, омыление проводят при температуре 70 °С, после упаривания полученный сухой остаток растворяют в изопропиловом спирте и подвергают обращенно-фазной высокоэффективной жидкостной хроматографии. Изобретение позволяет снизить показатели погрешности методики до 15%. 2 ил., 4 табл.
Способ подготовки пробы для количественного определения содержания витамина А в форме ретинола ацетата в диапазоне 500 тыс.-1,5 млн МЕ/г или витамина D3 в форме холекальциферола в диапазоне 300-700 тыс. МЕ/г в исследуемом образце методом ВЭЖХ, содержащий добавление к пробе исследуемого образца последовательно антиоксиданта и водно-спиртового раствора гидроксида калия в этаноле с соотношением 2 г KOH : 2 см3 воды для анализа : 18 см3 ректификованного этилового спирта, омыление полученной смеси в течение 30 минут с последующим охлаждением до комнатной температуры, добавление к полученному гидролизату воды, последовательную тройную экстракцию гексаном с объединением экстрактов, промывание объединенного гексанового экстракта дистиллированной водой, внесение безводного сульфата натрия с последующим упариванием, растворение полученного сухого остатка в жидкости с последующей выдержкой в темном месте и фильтрацию перед проведением высокоэффективной жидкостной хроматографии, отличающийся тем, что к навеске пробы исследуемого образца в качестве антиоксиданта добавляют 10%-ный водный раствор аскорбиновой кислоты, омыление проводят при температуре 70 °С, после упаривания полученный сухой остаток растворяют в изопропиловом спирте и подвергают обращенно-фазной высокоэффективной жидкостной хроматографии.
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ВИТАМИНА E (α-ТОКОФЕРОЛ АЦЕТАТА) МЕТОДОМ ДИФФЕРЕНЦИАЛЬНОЙ ВОЛЬТАМПЕРОМЕТРИИ | 2000 |
|
RU2180747C1 |
| Способ количественного определения витамина Д @ в растительных кормах | 1988 |
|
SU1562849A2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЖИРОРАСТВОРИМЫХ ВИТАМИНОВ А, D2, Е И В-КАРОТИНА ПРИ СОВМЕСТНОМ ПРИСУТСТВИИ МЕТОДОМ ТОНКОСЛОЙНОЙ ХРОМАТОГРАФИИ | 2013 |
|
RU2530620C1 |
| CN 102435700 A, 02.05.2012 | |||
| CN 109142564 A, 04.01.2019. | |||
Авторы
Даты
2024-08-07—Публикация
2023-10-20—Подача