Область техники
[1] Настоящее изобретение относится к соединению, выбранному из нового производного соединения бензотриазола, обладающего ингибирующей активностью в отношении эктонуклеотидпирофосфатазы-фосфодиэстеразы (ENPP), его фармацевтически приемлемой соли, его гидрата и его стереоизомера, способу получения соединения и фармацевтической композиции для профилактики, облегчения или лечения рака, содержащей это соединение.
Уровень техники
Раскрытие
[2] Рак представляет собой заболевание, связанное с неконтролируемой пролиферацией клеток, которые проникают или пролиферируют в другие органы, снижая, таким образом, качество жизни и, в конечном счете, приводя к смерти. Хотя генетические аберрации являются прямой причиной неконтролируемой пролиферации раковых клеток, недостаточность иммунного надзора и/или отсутствие адекватного иммунного противодействия иммунной системы раковым клеткам является еще одной причиной пролиферации раковых клеток. Кроме того, это приводит к образованию первичных опухолей, имеющих микроокружение опухоли (ТМЕ) с подавленным противораковым иммунитетом. Терапевтические агенты для лечения таких летальных заболеваний могут быть в общих чертах разделены на две категории. Первая категория непосредственно воздействует на сами раковые клетки, и вторая категория воздействует на компоненты микроокружения опухоли (ТМЕ), чтобы предотвратить дальнейшую пролиферацию или выживание раковых клеток.
[3] Иммунотерапия рака представляет собой терапевтический подход, который нацелен на иммунные факторы, присутствующие в ТМЕ, чтобы вызвать атаку иммунных клеток на опухолевые клетки. В некоторых случаях иммунотерапия рака направлена на стимулирование распознавания опухолевых клеток посредством высвобождения опухолеассоциированных антигенов в ТМЕ (например, противораковые вакцины). В других случаях иммунотерапия рака направлена на стимулирование атаки на опухолевые клетки путем регулирования активности врожденных и/или адаптивных иммунных клеток (например, блокада иммунных контрольных точек).
[4] Микробные инфекции вызывают множество заболеваний по всему миру. Патогенные микроорганизмы разнообразны и включают вирусы, бактерии, грибы и простейшие. В некоторых случаях терапевтический агент представляет собой химическое вещество, которое непосредственно предотвращает микробный рост. В других случаях терапевтические агенты представляют собой терапевтические вещества для усиления или стимуляции иммунной функции организма-хозяина против патогенных микроорганизмов.
[5] Микроокружение опухоли (ТРМ) содержит злокачественные опухолевые клетки, а также различные типы иммунных клеток (например, макрофаги, лимфоциты, NK-клетки и дендритные клетки) и неиммунных клеток (например, опухолеассоциированные фибробласты, перициты, эндотелиальные клетки и адипоциты). В то же время сообщалось, что присутствие инфильтрирующих опухоль лимфоцитов приводит к положительным клиническим результатам в ответ на множество методов иммунотерапии при различных видах рака. Доклинические исследования показали, что модуляция или повышающая регуляция других типов иммунных клеток, отличных от лимфоцитов, в частности врожденных иммунных клеток, модулирует ответную реакцию противораковой терапии на опухоли. Врожденная иммунная система является одним из двух основных компонентов системы иммунной защиты организма-хозяина у позвоночных. К основным функциям врожденного иммунитета относятся 1) выявление и удаление инородных веществ (например, бактерий, вирусов) из тканей организма, 2) привлечение иммунных клеток к определенным участкам путем продуцирования цитокинов и стимулирования адаптивных иммунных ответов, и 3) активация каскада комплемента. Такой врожденный иммунитет может быть активирован путем распознавания молекулярных паттернов, полученных от микробных патогенов (ассоциированные с патогеном молекулярные паттерны, РАМР) или остатков разрушенных клеток (ассоциированные с повреждением молекулярные паттерны, DAMP).
[6] Паттерн-распознающие рецепторы (PRR) представляют собой несколько различных типов рецепторов, которые в основном экспрессируются врожденными иммунными клетками и могут распознавать специфические РАМР или DAMP в зависимости от их лигандной специфичности. Цитоплазматическая ДНК представляет собой тип молекулярного паттерна, распознаваемый рецепторами цитоплазматической ДНК (тип PRR) и запускающий врожденный иммунный ответ. Сигнальный путь cGAS-STING (cGAS, циклическая GMP-AMP синтаза; STING, стимулятор генов интерферонов), являющийся типом сенсора цитоплазматической ДНК, участвует в интерферонах (IFN) 1 типа путем 1) распознавания цитоплазматической ДНК в результате микробной инфекции или повреждения собственной ДНК, и 2) выработки химических факторов, главным образом активации фактора транскрипции IRE3.
[7] IFN 1 типа, продуцируемый ТМЕ из-за трансформированных раковых клеток, способствует рекрутингу и активации воспалительных клеток, включая NK-клетки, в месте опухоли и индуцирует как гибель опухолевых клеток, так и выработку хемоаттрактантов, которые способствуют адаптивным иммунным ответам.
[8] Системное введение IFN 1 типа показало подтвержденную эффективность в раковых средах, основанную на регрессе опухоли и улучшении выживаемости при системном введении IFN-бета на доклинической мышиной модели. Однако системное введение IFN 1 типа имеет проблему, заключающуюся в том, что требуется высокая доза для достижения терапевтически эффективного количества и получения терапевтической эффективности. В этом случае сообщалось о проблемах с переносимостью.
[9] Недавно опубликованные клинические результаты применения экзогенных агонистов STING (модифицированных циклических динуклеотидов) показали более низкие показатели контроля заболевания, чем ожидалось, несмотря на очевидное увеличение продукции провоспалительных цитокинов.
[10] Таким образом, существует потребность в исследовании новых терапевтических способов, которые могут активировать сигнальный путь cGAS-STING.
[11][Документы известного уровня техники]
[12][Патентные документы]
[13] Патентная публикация Китая CN 110575458 А
[14] Международная публикация WO 2019/233300 А1
[15] Международная публикация WO 2018/119325 А1
[16] Международная публикация WO 2018/119328 А1
[17] Международная публикация WO 2019/046778 А1
[18] Международная публикация WO 2019/177971 А1
[19] Патентная публикация Японии JP 2020-15670
[20] Международная публикация WO 2019/051269 А1
[21] Патентная публикация США US 2020/0039979 А1
[22] Международная публикация WO 2019/023635 А1
[23] Международная публикация WO 2019/051269 А1
Раскрытие
Техническая проблема
[24] Для решения указанных выше проблем настоящее изобретение предлагает способ повышения активности сигнального пути cGAS-STING.
[25] Одной из задач настоящего изобретения является предложить новое производное соединение бензотриазола, обладающее ингибирующей активностью в отношении ENPP1. Другим аспектом настоящего изобретения является предложить новое производное соединение бензотриазола для улучшения и/или модулирования выработки интерферонов (IFN) 1 типа in vivo.
[26] Еще одной задачей настоящего изобретения является предложить фармацевтическую композицию, подходящую для лечения, профилактики и облегчения рака, содержащую в качестве активного ингредиента новое производное соединение бензотриазола, его фармацевтически приемлемую соль, его гидрат, его сольват или его стереоизомер.
[27] Еще одной задачей настоящего изобретения является предложить способ профилактики, облегчения или лечения рака, предусматривающий введение нового производного соединения бензотриазола или фармацевтической композиции, его содержащей, нуждающемуся в этом пациенту или субъекту.
[28] Еще одной задачей настоящего изобретения является предложить способ профилактики, облегчения или лечения инфекционного заболевания, предусматривающий введение нового производного соединения бензотриазола или фармацевтической композиции, его содержащей, нуждающемуся в этом пациенту или субъекту.
[29] Еще одной задачей настоящего изобретения является предложить способ профилактики, облегчения или лечения пародонтоза, предусматривающий введение нового производного соединения бензотриазола или фармацевтической композиции, его содержащей, нуждающемуся в этом пациенту или субъекту.
[30] Еще одной задачей настоящего изобретения является предложить способ профилактики, облегчения или лечения вирусного заболевания, предусматривающий введение нового производного соединения бензотриазола или фармацевтической композиции, его содержащей, нуждающемуся в этом пациенту или субъекту.
[31] Еще одной задачей настоящего изобретения является предложить способ профилактики, облегчения или лечения патологической минерализации мягких тканей, предусматривающий введение нового производного соединения бензотриазола или фармацевтической композиции, его содержащей, нуждающемуся в этом пациенту или субъекту.
[32] Еще одной задачей настоящего изобретения является осуществление следующего механизма с активным ингредиентом нового производного соединения бензотриазола, его фармацевтически приемлемой соли, его гидрата, его сольвата или его изомера. Б одном аспекте способ предусматривает примирование рака агентом для индуцирования иммуногенной гибели клеток (ICD) перед стимуляцией сигнального пути cGAS-STING. В другом аспекте способ предусматривает блокирование деградации эндогенного лиганда STING перед примированием раковой опухоли агентом для индуцирования ICD. Б другом аспекте способ предусматривает применение ингибитора для 2', 3'-cGAMP-деградирующего полипептида в сочетании с агентом для индукции ICD для лечения рака. В одном аспекте настоящее изобретение предлагает способ разработки ингибитора для 2', 3'-cGAMP-разрушающего полипептида и подробный способ анализа для оценки ферментативной активности cGAMP-разрушающего полипептида.
Техническое решение
[33] Для решения описанных выше технических проблем в одном аспекте настоящее изобретение предлагает соединение, выбранное из производного соединения бензотриазола, представленного следующей формулой 1, его таутомера, его фармацевтически приемлемой соли, его гидрата, его сольвата и его стереоизомера:
[34][Формула 1]
[35]
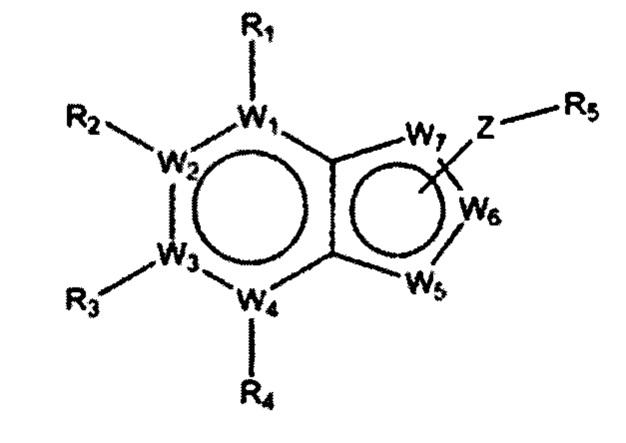
[36] где
[37] W1 представляет собой N или CRa,
[38] W2 представляет собой N или CRb,
[39] W3 представляет собой N или CRc,
[40] W4 представляет собой N или CRd
[41] W5 представляет собой N или CRe,
[42] W6 представляет собой N или CRf,
[43] W7 представляет собой N или CRg,
[44] где каждый Ra, Rb, Rc, Rd, Re, Rf и Rg независимо выбран из группы, состоящей из водорода, галогена, циано, нитро, алкила, алкенила, алкинила, циклоалкила, гетероциклила, арила и гетероарила,
[45] каждый из R1, R2, R3 и R4 независимо представляет собой водород, гидроксильную группу, галогенную группу, -CF3, -(O)CF3, C1-C13 алкильную группу, C1-C6 алкоксигруппу, аминогруппу (-NR7R8), нитрогруппу (-N(O)2), амидную группу (-(С=O)NR7R8), карбоксильную группу (-С(О)ОН), нитрильную группу (-CN), С6-С10 арильную группу, С3-С10 циклическую группу, С3-С10 гетероарильную группу, С3-С10 гетероциклическую группу, или-С(О)-(С1-С13 алкил),
[46] Z присутствует или отсутствует, при этом, когда Z присутствует, Z представляет собой -O-, -СО-, -COO-, -CnHn+2-, O(CnHn+2)-, -(OC2H4)n-, -(C2H4O)n-, -(CnHn+2)O-, -(CnHn+2)CO-, -(CnHn+2)O(CmHm+2)-, -NR7 (CnHn+2)-, - (NR7C2H4)n-, -(C2H4NR7)n- или-(CnHn+2)NR7-,
[47] n является целым числом от 0 до 8,
[48] R5 представляет собой-A-(R6)y,
[49] где А представляет собой С3-С10 циклическую группу, С5-С10 бициклическую группу, С3-С10 гетероциклическую группу, С6-С10арильную группу или С3-С10гетероарильную группу,
[50] R6 представляет собой водород, гидроксильную группу, галогенную группу, С1-С13 алкильную группу, C1-C6 алкоксигруппу, С1-С6 алкенильную группу, С6-С10 арильную группу, С3-С10 циклическую группу, С3-С10 гетероарильную группу, С3-С10 гетероциклическую группу, -С(О)-(C1-C1-C13 алкил), трет-бутоксикарбонильную группу (Boc), аминогруппу (-NR7R8), (CmHm+2) NR7R8, нитрогруппу (-N(O)2), амидную группу (-(С=O)NR7R8), сложноэфирную группу (-(CmHm+2)С(О)OR7), карбоксильную группу (-С(О)ОН), нитрильную группу (-CN), сульфонамидную группу (-(CmHm+2)NHS(О)2R7), мочевинную группу, сульфамоильную группу (-(CmHm+2)NHS(О)2NHR7), сульфонамидную группу, сульфамоилалкильную группу (- (CmHm+2) NHS(О)2NHR7), сульфамоилалкильную группу (-(CmHm+2)NR7S(O)2NHR8), сульфидную группу (-(CmHm+2)SR7), сульфоновую группу (-(CmHm+2)S(О)2R7), или фосфорильную группу (-(CmHm+2)P(О)R7R8), или связан с тем же углеродом, что и углерод, связанный с А, с образованием 3-10-членного насыщенного кольца, связан с тем же углеродом, что и углерод, связанный с А, с образованием 3-10-членного насыщенного гетероцикла, содержащего по меньшей мере один гетероатом из N, О и S, связан с углеродом, смежным с углеродом, связанным с А, с образованием 3-10-членного насыщенного кольца, или связан с углеродом, смежным с углеродом, связанным с А, с образованием 3-10-членного насыщенного гетероцикла, содержащего по меньшей мере один гетероатом из N, О и S,
[51] m является целым числом от 0 до 4; и
[52] у является целым числом от 0 до 4,
[53] при этом С1-С13 алкильная группа, C1-C6 алкоксигруппа, C1-Сб алкенильная группа или-С(О)-(С1-С13 алкил-включает в себя по меньшей мере один заместитель, выбранный из группы, состоящей из водорода, гидроксильной группы, галогенной группы, С1-С13 алкильной группы, C1-C6 алкоксигруппы, аминогруппы (-NR7R8), нитрогруппы (-N(O)2), амидной группы (-(С=O)NR7R8), карбоксильной группы (-С(О)ОН), нитрильной группы (-CN), мочевинной группы (-NR7(С=O)NR8-), сульфонамидной группы (-NHS(O)2-), сульфидной группы (-S-), сульфонильной группы (-S(O)2-), фосфорильной группы (-P(O)R7R8), С6-С10 арильной группы, С3-С10 гетероарильной группы и С3-С10гетероциклической группы,
[54] С6-С10 арильная группа, С3-С10 гетероарильная группа, С3-С10 циклическая группа, С3-С10 гетероциклическая группа или С5-С10 бициклическая группа включает в себя по меньшей мере один заместитель, выбранный из группы, состоящей из водорода, гидроксильной группы, галогенной группы, карбонильной группы (-(C=O)R7R8), C1-C3 алкильной группы, замещенной или незамещенной галогеном или С3-С10 гетероциклической группой, С1-С3 алкоксигруппы, замещенной или незамещенной галогеном или С3-С10 гетероциклической группой, С6-С10 фенокси, аминогруппы (-NR7R8), нитрогруппы (-N(O)2), амидной группы (-(С=O)NR7R8), карбоксильной группы (-С(О)ОН), нитрильной группы (-CN), мочевинной группы (-NR7 (С=O)NR8-), сульфонамидной группы (-NHS(O)2-), сульфидной группы (-S-), сульфонильной группы (-S(O)2-), фосфорильной группы (-P(O)R7R8), С6-С10 арильной группы, С3-С10 гетероарильной группы и С3-С10 гетероциклической группы, и
[55] каждый из R7 и R8 независимо представляет собой водород, С1-С6 алкильную группу, С1-С6 алкенильную группу, С1-С6 алкинильную группу, С6-С10 арильную группу, С3-С10 гетероарильную группу, С3-С10 гетероциклическую группу, аминогруппу (-NH2), нитрогруппу (-N(O)2), -Boc, или-NHBoc, или R7, вместе с атомом азота или углерода, связанным с R8, образует 3-7-членное насыщенное кольцо, включающее по меньшей мере одно из N, О, S, NH, C=N, С=O, -NHC(O)-, -NHC(O)NH-, -NHS(O)2-, или SO2, и является замещенным по меньшей мере одним из водорода, С1-С13 алкильной группы, С6-С10 арильной группы, С3-С10 гетероарильной группы, гидроксильной группы, галогенидной группы или цианогруппы,
[56] где С3-С10 гетероарильная группа и С3-С10 гетероциклическая группа включает в себя по меньшей мере один гетероатом, выбранный из группы, состоящей из N, О и S.
Полезные эффекты
[57] Соединение в соответствии с настоящим изобретением способно эффективно ингибировать активность ENPP1.
Соответственно, соединение может быть использовано для лечения, профилактики и облегчения раковых заболеваний, вызванных аномальным клеточным ростом.
[58] Соединение согласно настоящему изобретению, его фармацевтически приемлемая соль или гидрат, и фармацевтическая композиция для профилактики или лечения рака, содержащая его в качестве активного ингредиента, эффективно ингибируют ENPP1 с активацией сигнального пути STING и, таким образом, применимо для профилактики или лечения рака.
[59] Раковые заболевания, которые можно лечить, предотвращать и облегчать введением соединения по настоящему изобретению, включают рак желудка, рак легких, рак печени, колоректальный рак, рак тонкой кишки, рак поджелудочной железы, рак головного мозга, рак костей, меланому, рак молочной железы, склеродермию, рак матки, рак шейки матки, рак головы и шеи, рак пищевода, рак щитовидной железы, рак паращитовидных желез, рак почки, саркому, рак предстательной железы, рак уретры, рак мочевого пузыря, рак крови (включая лейкоз, множественную миелому и миелодиспластический синдром), лимфому (включая болезнь Ходжкина и неходжкинскую лимфому), псориаз, фиброаденому, и тому подобное.
[60] Соединение по настоящему изобретению, его фармацевтически приемлемая соль или гидрат, и композиция, содержащая его в качестве активного ингредиента, может использоваться в качестве противовирусного терапевтического агента.
[61] В частности, соединение по настоящему изобретению эффективно для предупреждения, облегчения или лечения заболеваний, связанных с ENPP 1.
Наилучший вариант осуществления
[62] Определения
[63] Если из контекста явно не следует иное, все числа, цифровые значения и/или выражения, которые представляют ингредиенты, условия реакции, полимерные композиции, а также количества смесей, используемые в описании, являются приближениями, которые отражают, среди прочего, различные погрешности измерений, неизбежно происходящих в процессе получения этих цифровых значений. По этой причине следует понимать, что во всех случаях термин «примерно» должен рассматриваться как модификация всех чисел, цифровых значений и/или выражений. Кроме того, когда в описании раскрываются числовые диапазоны, эти диапазоны являются непрерывными и включают все числа от минимального до максимального, включая максимум в каждом диапазоне, если не указано иное. Кроме того, когда диапазон относится к целому числу, он включает все целые числа от минимального до максимального, включая максимум в пределах диапазона, если не указано иное.
[64] Следует понимать, что в описании, когда диапазон упоминается в отношении параметра, параметр охватывает все цифровые значения, включая конечные точки, раскрытые в пределах диапазона. Например, диапазон «5-10» включает цифровые значения 5, 6, 7, 8, 9 и 10, а также произвольные поддиапазоны, такие как диапазоны 6-10, 7-10, 6-9 и 7-9, и любые цифровые значения, такие как 5, 5, 6, 5, 7, 5, 5, 5-8, 5 и 6, 5-9, между соответствующими целыми числами, которые попадают в пределы данного диапазона. Кроме того, например, диапазон «от 10% до 30%» охватывает все целые числа, включая такие числа, как 10%, 11%, 12% и 13%, а также 30%, и любые поддиапазоны, такие как диапазоны от 10% до 15%, от 12% до 18%, или от 20% до 30%, а также любые числа, такие как 10, 5%, 15, 5% и 25, 5%, между соответствующими целыми числами, которые попадают в пределы данного диапазона.
[65] Используемые здесь термины «индивидуум» («индивидуумы»), «субъект» («субъекты») и «пациент» («пациенты») означают любое млекопитающее (млекопитающих). В некоторых вариантах осуществления млекопитающее представляет собой человека. В некоторых вариантах осуществления млекопитающее не является человеком. Ни один из терминов не требует ситуации, характеризующейся наблюдением (например, постоянным или периодическим) медицинских работников (например, врачей, штатных медсестер, младших медсестер-стажеров, помощников врача, вспомогательного персонала или работников хосписа), и не ограничивается данной ситуацией.
[66] Термин «лечение» относится к попытке предотвратить развитие или изменение связанного с заболеванием повреждения. Соответственно, термин «лечение» относится как к терапевтическим, так и к профилактическим действиям. Нуждающиеся в лечении включают состояние, в котором заболевание развивается, и состояние, в котором заболевание должно быть предотвращено. При лечении опухолей терапевтический агент может воздействовать для непосредственного снижения патологии опухолевых клеток или чтобы сделать опухолевые клетки более восприимчивыми к лечению с помощью других терапевтических агентов, например, радиации, химиотерапии и/или иммунотерапии. Используемый в настоящем описании термин «облегченный» или «подвергнутый лечению» означает признак, который приближается к нормализованному значению, измеряемому с помощью обычных статистических тестов. Признаком, приближающимся к нормализованному значению, является, например, значение, полученное от здорового пациента или индивидуума, которое отличается от нормализованного значения менее чем на 50%, предпочтительно менее чем на 25%, и более предпочтительно менее чем на 10%, и еще более предпочтительно имеет небольшое отличие от нормализованного значения.
[67] Термин «лечение рака» означает любое одно или более из следующих воздействий: 1) ингибирование роста опухоли, включающее i) замедление или ii) полную остановку роста; 2) снижение количества опухолевых клеток; 3) поддержание размера опухоли; 4) уменьшение размера опухоли; 5) ингибирование инфильтрации опухолевых клеток в периферические органы, включающее i) уменьшение или ii) замедление или iii) полное предотвращение; 6) ингибирование метастазирования, включающее i) уменьшение или ii) замедление, или iii) полное предотвращение; и 7) усиление противоопухолевого иммунного ответа, который может вызвать i) поддержание размера опухоли, ii) уменьшение размера опухоли, iii) замедление роста опухоли или iv) уменьшение, замедление или предотвращение инвазии.
[68] Используемый здесь термин «эффективное количество» или «терапевтически эффективное количество» относится к достаточному количеству раскрываемого здесь соединения, которое в некоторой степени облегчает симптомы заболевания или состояния, подлежащего лечению (такого как рак или воспалительное заболевание, пародонтоз или минерализация мягких тканей). В некоторых вариантах осуществления результатом является 1) уменьшение и/или облегчение признаков, симптомов или причин заболевания, или 2) любое другое желаемое изменение биологической системы в клинических условиях. В некоторых вариантах осуществления подходящее «эффективное» количество для любого индивидуального случая определяется с использованием таких методик, как исследование с повышением дозы.
[69] В некоторых вариантах осуществления термин «эффективное количество» относится к эффективному количеству для ингибирования ENPP1 на примерно 20% (20% ингибирование), по меньшей мере примерно 30% (30% ингибирование), по меньшей мере примерно 40% (40% ингибирование), по меньшей мере примерно 50% (50% ингибирование), по меньшей мере примерно 60% (60% ингибирование), по меньшей мере примерно 70% (70% ингибирование), по меньшей мере примерно 80% (80% ингибирование), или по меньшей мере примерно 90% (90% ингибирование), при введении количества соединения, раскрываемого в настоящем документе, т.е. одной или более доз, в рамках монотерапии или комбинированной терапии, при сравнении с активностью ENPP1 у субъекта, не получавшего соединение, или при сравнении активности ENPP1 до или после лечения соединением.
[70] В некоторых вариантах осуществления термин «терапевтически эффективное количество» относится к эффективному количеству для уменьшения опухолевой нагрузки субъекта на примерно 20%, по меньшей мере примерно 30%, по меньшей мере примерно 40%, по меньшей мере примерно 50%, по меньшей мере примерно 60%, по меньшей мере примерно 70%, по меньшей мере примерно 80% или по меньшей мере примерно 90%, при введении количества соединения, раскрываемого в настоящем документе, т.е. одной или более доз, в рамках монотерапии или комбинированной терапии, при сравнении с опухолевой нагрузкой у субъекта, не получавшего соединение, или при сравнении опухолевой нагрузки до или после лечения соединением. Используемый здесь термин «опухолевая нагрузка» означает общую массу опухолевой ткани субъекта, больного раком.
[71] В некоторых вариантах осуществления термин «терапевтически эффективное количество» относится к дозе, используемой для радиотерапии, необходимой для наблюдения уменьшения опухоли у субъекта на примерно 20%, по меньшей мере примерно 30%, по меньшей мере примерно 40%, по меньшей мере примерно 50%, по меньшей мере примерно 60%, по меньшей мере примерно 70%, по меньшей мере примерно 80% или по меньшей мере примерно 90%, при введении количества соединения, раскрываемого в настоящем документе, т.е. одной или более доз, в рамках монотерапии или комбинированной терапии, по сравнению с дозой радиотерапии, необходимой для наблюдения уменьшения опухоли у субъекта, не получавшего соединение.
[72]
[73] Далее настоящее изобретение будет описано подробно.
[74] В результате непрерывных исследований, направленных на решение указанных выше проблем, авторы настоящего изобретения разработали соединение для ингибирования ENPP1, композицию для ингибирования ENPP1 и способ ингибирования ENPP1. В одном аспекте авторы настоящего изобретения разработали новое производное соединение бензотриазола для ингибирования ENPP1, его фармацевтически приемлемую соль, гидрат и стереоизомер, способ их получения и фармацевтическую композицию для профилактики или лечения рака, содержащую их в качестве активного ингредиента. В одном варианте осуществления способ предусматривает обработку образца проникающим в клетки ингибитором ENPP1 для ингибирования гидролиза cGAMP, связанного с ENPP1. В одном варианте осуществления способ предусматривает введение пациенту или субъекту терапевтически эффективного количества проникающего в клетки ингибитора ENPP1 для лечения рака. Соединение согласно одному из аспектов настоящего изобретения, содержащая его композиция, или соединение и композиция могут быть использованы для различных применений или заболеваний, требующих ингибирования ENPP1.
[75] Сигнальный путь cGAS-STING, иммуногенный апоптоз и продуцирование IFN 1 типа
[76] Цитоплазматическая двухцепочечная ДНК может быть введена вне клеток в результате микробной инфекции или везикулярного переноса из соседних мертвых клеток. Цитоплазматическая ДНК также может быть получена из поврежденной геномной ДНК или митохондриальной ДНК внутри клеток. Если цитоплазматическая ДНК присутствует, она может быть обнаружена различными сенсорами ДНК, такими как РНК-полимераза III, DDX41, DAI, IFI6, cGAS, LEEFIP1, DHX9, DHX36, Ku70 и AIM2.
[77] Циклическая GMP-AMP-синтаза (cGAS) представляет собой цитоплазматический белок, присутствующий в виде димера и состоящий из двух ДНК-связывающих доменов и домена нуклеотидилтрансферазы (который преобразует АТР и GTP в циклический динуклеотид 2',3-cGAMP, имеющий 2',5' и 3',5' фосфодиэфирные связи). Кроме того, cGAMP действует как вторичный мессенджер и связывается с STING с высокой аффинностью (Kd ~ 4 нМ), индуцируя экспрессию IFN 1 типа.
[78] STING (также известный как ТМЕМ173, MITA или MPYS) представляет собой якорный белок эндоплазматического ретикулума (ER), содержащий четыре трансмембранных домена на N-конце и домен димеризации на С-конце. После связывания с cGAMP, STING образует тетрамер и перемещается из ER в промежуточный компартмент ER-Гольджи. В аппарате Гольджи STING притягивает и активирует tank-связывающую киназу 1 (ТВК1), активированный ТВК1 фосфорилирует С-концевой домен STING, и STING рекрутирует и активирует регуляторный фактор интерферонов 3 (IRF3). Затем активированный IRF3 мигрирует в ядро и способствует экспрессии иммуностимулируемых генов (ISG) и IFN 1 типа. После активации STING переносится в эндолизосомы и затем разрушается. В этот момент активация сигнального пути cGAS-STING прекращается.
[7 9] Иммуногенная гибель клеток (ICD)
[80] Иммуногенная гибель клеток (ICD), которая является одним из видов клеточной гибели, относится к клеточному феномену, который индуцирует активацию контролируемого иммунного ответа. Гибель клеток характеризуется апоптотической морфологией и поддерживает целостность биологической мембраны. ICD также характеризуется секрецией DAMP (например, кальретикулина, белка 1 высокомобильной группы (HMGB1), АТР и Hsp70/90 белков), а также воздействием полипептидов, образованных нативными или мутировавшими белками, на клетки. Экспонированные полипептиды (действующие в качестве антигенов) распознаются дендритными клетками (DC) и впоследствии основными эффекторными Т-клеточными лимфоцитами для активации адаптивного иммунного ответа.
[81] ICD также может быть дополнительно классифицирована на основе различных типов индукторов ICD, таких как 1) излучение (например, ультрафиолетовое излучение или гамма-излучение), 2) малые молекулы химиотерапии (например, доксорубицин или паклитаксел) и 3) биологические агенты (например, полипептиды, олигосахариды, липиды или нуклеиновые кислоты).
[82] Лучевая терапия
[83] Лучевая терапия хорошо известна и применяется для лечения пациентов, страдающих различными заболеваниями. Лучевая терапия обычно используется для подавления отмирания или роста нежелательной ткани (например, раковой ткани). Определенное количество высокоэнергетического электромагнитного излучения и/или частиц высокой энергии направлено на сведение к минимуму непреднамеренного повреждения желаемой или здоровой ткани при одновременном непосредственном повреждении нежелательных тканей или поражений на пути прохождения излучения.
[84] Результаты проводившихся до сих пор исследований показали, что, поскольку воздействие на нормальную ткань в большей степени зависит от размера фракции, чем от дозы, фракция дозы 1, 8-2, 0 Гр считается стандартной для традиционной лучевой терапии, и, соответственно время лечения увеличивается. Фактически, малая доза за фракцию индуцирует опухолевый эффект путем митотической гибели раковых клеток и восстанавливает сублетальное повреждение нормальных тканей после введения. Стереотаксическая лучевая терапия тела (SBRT) представляет собой усовершенствованную лучевую терапию, которая использует сложное наведение изображения для точного определения трехмерной локализации опухолей, благодаря чему излучение может быть доставлено более точно к раковым клеткам. Кроме прямой цитотоксичности, SBRT оказывает существенное влияние на гибель опухолевых клеток в высоких дозах, сопровождающуюся микроваскулярным повреждением, тем самым добавляя новый механизм радиационно-индуцированного повреждения. Однако в недавнем сообщении было показано, что высокодозовое излучение индуцирует экспрессию ферментов нуклеазы с ослаблением воздействия излучения на опосредованную STING активацию врожденного иммунитета.
[85] Неоадгьювантная терапия
[86] Неоадъювантная терапия представляет собой способ лечения, который направлен на облегчение основной терапии или повышения эффективности основной терапии путем уменьшения размера и прогрессирования опухоли за счет введения терапевтического агента до введения или процедуры основной терапии. Терапевтические агенты, пригодные для неоадъювантной терапии, включают 1) системную терапию (химиотерапия, иммунотерапия или гормональная терапия) и 2) местную терапию (лучевая терапия). Неоадъювантная терапия, к сожалению, неприменима ко всем пациентам, поскольку используемый терапевтический агент может вызывать различную токсичность у пациентов и определяет возможность или невозможность проведения основной терапии. В недавнем сообщении было показано, что, когда сопутствующее введение агониста пути STING и ингибитора контрольных точек иммунного ответа с интерлейкином 2 использовалась в качестве неоадъювантной терапии, выживаемость была выше, чем в случае, когда агонист пути STING не использовался, что подтверждает потенциальную применимость терапевтических агентов, активирующих путь STING, для неоадъювантной терапии (Lauren Е. Milling, et al., can, imm, res, (2021), 10.1158/2326-6066.CIR-21-0247).
[87] Противораковая вакцина
[88] Противораковая вакцина представляет собой способ лечения, который активирует дендритные клетки, являющиеся маркирующими антиген клетками, путем введения выбранных раковых антигенов вместе с адъювантом, и направлен на подавление роста опухоли и гибель опухоли путем стимулирования приобретенной иммунной системы пациента к распознаванию и атаке специфических раковых антигенов. В зависимости от способа введения раковых антигенов антигенные вакцины могут быть разделены на специфические антигенные вакцины (одно или более очищенных антигенов или антиген-продуцирующих веществ, которые выбирают и вводят) и неспецифические антигенные вакцины (вызывающие гибель раковых клеток в опухоли для высвобождения антигенов). В зависимости от типа введения специфических антигенных вакцин в организм антигенные вакцины могут быть подразделены на ДНК-вакцины, РНК-вакцины и белковые вакцины. В недавнем сообщении было показано, что сопутствующее введение агониста STING с белковой противораковой вакциной проявило синергический эффект, заключающийся в увеличении выживаемости и предотвращении метастазирования, что подтверждает потенциальную применимость терапевтических агентов, активирующих путь STING для комбинированной терапии с противораковыми вакцинами (ДНК вакцинами, РНК-вакцинами и белковыми вакцинами) (Matteo Rossi, et al., front. In imm. (2021), 10. 338 9/fimmu. 2 021. 6 95056).
[89] CAR-T терапия
[90] CAR-T-клеточная терапия включает выделение Т-клеток, присутствующих у пациента, экспрессию специального рецептора (CAR, химерный антигенный рецептор), способного распознавать раковые клетки, пролиферацию рецептора и введение рецептора в организм пациента для побуждения CAR-T-клеток к избирательной атаке антигенов на раковые клетки, находящиеся на их поверхности. В недавнем сообщении было показано, что при сочетании CAR-T терапии с терапевтическим агентом, активирующим путь STING, повышение уровня интерферона 1 типа улучшает инфильтрацию опухоли и апоптоз CAR-T-клеток, тем самым повышая эффективность терапевтического агента для CAR-T клеточной терапии, что подтверждает потенциальную применимость комбинированной терапии терапевтического агента, индуцирующего активацию пути STING, CAR-T клетками в микроокружении опухоли (Feng Ji, et. Al., (2021) J Hematol Oncol (2021) 14:152).
[91] Патоген
[92] Как описано выше, внутриклеточная инвазия нуклеиновых кислот, полученных из патогенов, активирует сигнальный путь cGAS-STING, тем самым усиливая иммунный ответ на патогены. В некоторых случаях патоген представляет собой вирус, такой как ДНК-вирус или РНК-вирус. В некоторых случаях патоген представляет собой ретровирус. Примеры вирусов, которые активируют сигнальный путь cGAS-STING, включают, без ограничения, вирус простого герпеса 1 (HSV-1), герпесвирус, ассоциированный с саркомой Капоши (KSHV), вирус осповакцины (VACV), аденовирус, вирус папилломы человека (HPV), вирус гепатита В (HBV), вирус гепатита С (HCV), вирус денге (DENV), вирус Зика (ZIKV), вирус гриппа A (IAV), вирус иммунодефицита человека (HIV), или цитомегаловирус человека (HCMV). В других вариантах осуществления патоген представляет собой бактерию. Примеры бактерий включают, без ограничения, Listeria monocytogenes, Mycobacterium tuberculosis, Francisella novicida, Legionella pneumophila, Chlamydia trachomatis, Streptococcus pneumoniae и Neisseria gonorrhoeae.
[93] Инфаркт миокарда
[94] Инфаркт миокарда является одной из основных причин систолической сердечной недостаточности. После инфаркта миокарда в сердечную ткань поступают различные типы клеток для регенерации или заживления пораженной сердечной ткани. На процесс заживления большое влияние оказывают коммуникация и регуляция между поступающими клетками. Завершившееся заживление значительно влияет на функциональное восстановление ткани миокарда. Существует высокая потребность в лекарственных средствах, которые помогают или способствуют такой регенерации тканей миокарда. В недавнем сообщении было показано, что адениновые и пуриновые нуклеотиды изменяются за счет активности фермента ENPP1, экспрессируемого фибробластами в пораженной сердечной ткани, что приводит к увеличению апоптоза не являющихся кардиомиоцитами и иммунных клеток и мешает регенерации сердечной ткани. Показана возможность стимуляции функционального восстановления ткани миокарда путем ингибирования активности фермента ENPP1 (Shen Li, et al., J. Clin. Inv. (2021), 10.1172/JCI149711).
[95] Терапевтический агент для лечения генетических заболеваний, связанных с гипофосфатемией
[96] Гипофосфатазия представляет собой врожденное метаболическое нарушение и генетическое заболевание, при котором регенерация и минерализация кости нарушаются из-за дефицита щелочной фосфатазы, которая является необходимым ферментом для таких клеточных процессов, как метаболизм мышц и формирование костей. Для пациентов с диагнозом гипофосфатемия важно облегчить симптомы, связанные с костной патологией, с помощью малоинтенсивной физической активности и упражнений в качестве профилактики, а для облегчения симптомов, вызванных гипофосфатемией, и предотвращения осложнений необходимо квалифицированное лечение. Сообщалось о случаях, когда эффекты достигались с помощью трансплантации костного мозга у тяжелых пациентов, но их эффективность еще не доказана. В недавнем сообщении было показано, что гипофосфатазия вызвана увеличением избытка пирофосфата в организме из-за дефицита щелочной фосфатазы, а также тем, что пирофосфат образуется в результате активности ENPP1, и поэтому ингибирование активности ENPP1 способно уменьшить симптомы гипофосфатемии (корпоративная презентация RallyBio (2021)).
[97] Фосфодиэстеразы
[98] Фосфодиэстеразы (PDE) включают циклические нуклеотидные фосфодиэстеразы, фосфолипазы С и D, аутотаксин, сфингомиелиновые фосфодиэстеразы, ДНКазы, РНКазы, рестрикционные эндонуклеазы и ряд менее известных низкомолекулярных фосфодиэстераз. Группа типичных ферментов PDE важна для гидролиза циклических нуклеотидов аденозин-3', 5'-циклического монофосфата (сАМР) и гуанозин-3', 5'-циклического монофосфата (cGMP) в их неактивные 5'-монофосфаты.
[99] Циклические нуклеотидные фосфодиэстеразы содержат группу ферментов, которые расщепляют сложные фосфодиэфирные связи циклических нуклеотидных молекул вторичных мессенджеров, а именно сАМР и cGMP. Они регулируют локализацию, персистенцию и амплификацию циклических нуклеотидных сигналов в субклеточных доменах.
[100] Эктонуклеотидные пирофосфатазы/фосфодизстеразы
[101] Класс фосфодиэстераз также включает эктонуклеотидные пирофосфатазы/фосфодизстеразы. Эктонуклеотидная пирофосфатаза/фосфодиэстераза (ENPP) или нуклеотидпирофосфатаза/фосфодиэстераза (NPP) представляют собой группу ферментов эктонуклеотидаз, которые гидролизуют пирофосфатные и сложные фосфодиэфирные связи их субстратов с образованием нуклеотид-5'-монофосфатов (или фосфолипидов и фосфохолинов). В некоторых вариантах осуществления группа ферментов ENPP включает семь ферментов эктонуклеотидаз (ENPP-1, ENPP-2, ENPP-3, ENPP-4, ENPP-5, ENPP-6 и ENPP-7), имеющих сходную белковую структуру на поверхности клетки.
[102] Ферменты ENPP обычно имеют модульную структуру, включающую каталитический домен из 400 аминокислот. Данный каталитический домен не связан с фосфолипазой, Nudix гидролазой или эктонуклеозидтрифосфатдифосфогидролазой, хотя он проявляет частично перекрывающиеся активности. Предполагается, что ENPP 1 и ENPP 3 имеют трансмембранный домен на своем N-конце и нуклеазоподобный домен на своем С-конце и являются однократно пронизывающими мембрану трансмембранными белками типа 2, каталитические домены которых направлены к внеклеточному домену. Ожидается, что ENPP 2, у которого отсутствует трансмембранный домен либо на N-, либо на С-конце, будет иметь сигнальный пептид на N-конце и будет секретироваться вне клетки. Предполагается, что ENPP 4, ENPP 5, ENPP 6 и ENPP 7, содержащие предполагаемые N-концевые сигнальные пептиды и С-концевые трансмембранные домены, также являются однократно пронизывающими мембрану трансмембранными белками типа 1, каталитические домены которых направлены во внеклеточный домен.
[103] Известно, что ENPP 1, ENPP 2 и ENPP 3 образуют нуклеозидмонофосфаты (ENPP 1, ENPP 2 и ENPP 3) или нуклеозиддифосфаты (ENPP 1 и ENPP 2), используя нуклеотиды и их производные в качестве субстратов. Известно, что только ENPP2 использует лизофосфолипиды. Известно, что ENPP 6 и ENPP 7 продуцируют холинфосфаты, используя сложные холинфосфатные эфиры в качестве субстратов. Для ENPP 4 и ENPP 5 не существует известного субстрата.
[104] ENPP1, который также называют NPP1 или РС-1, представляет собой трансмембранный гликопротеин типа 2 и экспрессируется в ряде тканей (поджелудочной железы, почек, мочевого пузыря и печени). ENPP1 необходим для пуринергической передачи сигналов, которая играет важную роль в регуляции сердечно-сосудистой, нейрональной, иммунной функций и функций крови у млекопитающих. ENPP1 катализирует гидролиз АТР или GTP до AMP или GMP с образованием неорганического пирофосфата (PPi). В целом, поскольку неорганический пирофосфат регулирует минерализацию костей и хрящей, выработка PPi посредством ENPP1 делает ENPP1 центральным регулятором развития костей и хрящей. В отличие от ингибирующего эффекта избыточного PPi, продуцируемого ENPP1 в суставной ткани, образование фосфата кальция из PPi, продуцируемого ENPP1, необходимо для минерализации костной ткани. ENPP1 имеет широкую специфичность и гидролизует различные субстраты, включая сложные фосфодиэфирные связи нуклеотидов и нуклеотидных сахаров и пирофосфатные связи нуклеотидов и нуклеотидных сахаров.
[105] Недавно было обнаружено, что ENPP1 играет важную роль в иммунологическом ответе на различные внешние сигналы, которые активируют сигнальный путь cGAS-STING. Предварительное исследование ферментативной активности, разрушающей молекулы cGAMP, показало, что ENPP1 функционирует в качестве основной гидролазы cGAMP. В соответствии с этими результатами сообщалось, что время полужизни cGAMP в значительной степени зависело от ENPP1, на основе верификации намного более длительного времени полужизни cGAMP у мышей с нокаутом ENPP1.
[106] Было показано, что бисфосфотионатный аналог cGAMP, который устойчив к гидролизу ENPP1, активирует STING в десять раз эффективнее, чем cGAMP, что указывает на то, что задержка или уменьшение гидролиза cGAMP путем ингибирования ENPP1 может значительно увеличить активацию STING. Сообщалось, что ингибирование ENPP1 индуцирует присутствие персистирующего cGAMP для активации пути STING, тем самым ослабляя инфекцию вирусом псевдобешенства и снижая инфицирование Mycobacterium tuberculosis.
[107]
[108] Соответственно, в одном аспекте настоящее изобретение предлагает ингибитор ENPP1, который представляет собой cGAMP-разрушающий полипептид.
[109] В одном аспекте ингибитор ENPP1 представляет собой обратимый ингибитор.
[110] В одном аспекте ингибитор ENPP1 представляет собой конкурентный ингибитор.
[111] В другом аспекте ингибитор ENPP1 представляет собой аллостерический ингибитор.
[112] В другом аспекте ингибитор ENPP1 представляет собой необратимый ингибитор.
[113] В одном аспекте ингибитор ENPP1 связывается с каталитическим доменом фосфодиэстеразы (PDE), с которым связан AMP или GMP.
[114] В одном аспекте ингибитор ENPP1 связывается с каталитическим доменом PDE, но слабо связывается с ним, когда с ним связан AMP.
[115] В другом аспекте ингибитор ENPP1 не ингибирует гидролитическую активность АТР каталитического домена или слабо ингибирует его гидролитическую активность АТР.
[116] Способ ингибирования ENPP1
[117] Как указано выше, настоящее изобретение включает следующие конфигурации: 1) ингибитор ENPP1; 2) способ ингибирования фермента ENPP1 с использованием ингибитора ENPP1; 3) способ ингибирования гидролазной активности ENPP1 к cGAMP; 4) способ улучшения выходного сигнала активации пути STING; и 5) способ ингибирования роста опухоли на соответствующей мышиной модели опухоли в условиях монотерапии или комбинированной терапии.
[118] В некоторых вариантах осуществления ингибирование ENPP1 означает, что активность ENPP1 снижается на 10% или более, например, 20% или более, 30% или более, 40% или более, 50% или более, 60% или более, 70% или более, 80% или более, 90% или более, или 95% или более, по сравнению с контролем, не обработанным соединением. В некоторый вариантах осуществления, ингибирование ENPP1 означает, что активность ENPP1 уменьшается по меньшей мере в 2 раза, например, по меньшей мере в 3 раза, по меньшей мере в 5 раз, по меньшей мере в 10 раз, по меньшей мере в 100 раз, или по меньшей мере в 1000 раз, по сравнению с контролем, не обработанным соединением.
[119] В некоторых вариантах осуществления проникающий в клетку ингибитор ENPP1 представляет собой ингибитор, описанный в настоящем документе. В некоторых вариантах осуществления, проникающий в клетку ингибитор ENPP1 представляет собой ингибитор для любого одного соединения, выбранного из производного соединения бензотриазола, представленного формулой 1, его таутомера, его фармацевтически приемлемой соли, его гидрата и его стереоизомера.
[120][Формула 1]
[121] 
[122] В некоторых вариантах осуществления проникающий в клетку ингибитор ENPP1 представляет собой любое из следующих соединений:
[123] Соединение 1: 5-метокси-1-(пиперидин-4-ил)-1Н-бензо[d][1,2,3]триазол гидрохлорид;
[124] Соединение 2: 4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)циклогексил)метананилин;
[125] Соединение 3: 5-метокси-1-(пиперидин-4-илметил)-1Н-бензо[d][1,2,3] триазол;
[126] Соединение 4: 4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)анилин гидрохлорид;
[127] Соединение 5: 4-(1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
[128] Соединение 6: 4-(4-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
[129] Соединение 7: 4-(6-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
[130] Соединение 8: 4-(7-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
[131] Соединение 9: 4-(4, 6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
[132] Соединение 10: 4-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
[133] Соединение 11: 2-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)этан-1-амин гидрохлорид;
[134] Соединение 12: 1-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)-N-метилметанамин гидрохлорид;
[135] Соединение 13: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-бензил)циклопропанамин гидрохлорид;
[136] Соединение 14: (S)-1-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)этан-1-амин гидрохлорид;
[137] Соединение 15: 3-хлор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
[138] Соединение 16: 3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
[139] Соединение 17: 2, 5-дифтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин;
[140] Соединение 18: 2, 6-дифтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин;
[141] Соединение 19: 4-(5-этокси-1Н-бензо[d][1,2,3]триазол1-ил)-3-фторфенил)метанамин;
[142] Соединение 20: 3-фтор-4-(5-изопропокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин;
[143] Соединение 21: 4-(5-(1, 1-дифторэтил)-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин;
[144] Соединение 22: 4-(5-(1, 1-дифторэтил)-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторфенил)метанамин;
[145] Соединение 23: 3-фтор-4-(5-фторметокси)-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин;
[146] Соединение 24: 4-(5-дифторметокси)-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторфенил)метанамин;
[147] Соединение 25: 7-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-1,2,3,4-тетрагидройзохинолин гидрохлорид;
[148] Соединение 26: 7-фтор-6-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-1,2,3,4-тетрагидройзохинолин гидрохлорид;
[149] Соединение 27: 8-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-2,3,4,5-тетрагидро-1Н-бензо[с]азепин гидрохлорид;
[150] Соединение 28: 4-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)-2,5-дифторфенил)метанамин;
[151] Соединение 29: 1-(изоиндолин-5-ил)-5,6-диметокси-1Н бензо[d][1,2,3]триазол гидрохлорид;
[152] Соединение 30: 3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бицикло[1.1.1]пентан-1-ил)метанамин;
[153] Соединение 31: 3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-5-метилтиофен-2-ил)метанамин гидрохлорид;
[154] Соединение 32: трет-бутил-((4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)пиперидин-1-ил)сульфонил)карбамат;
[155] Соединение 33: трет-бутил-((4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)метил)пиперидин-1-ил)сульфонил)карбамат;
[156] Соединение 34: трет-бутил(N-(1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфонил)карбамат;
[157] Соединение 35: трет-бутил(N-(4-(4-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфонил)карбамат;
[158] Соединение 36: трет-бутил(N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфонил)карбамат;
[159] Соединение 37: трет-бутил(N-(4-(6-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфонил)карбамат;
[160] Соединение 38: трет-бутил(N-(4-(7-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфонил)карбамат;
[161] Соединение 39: трет-бутил((S)-N-(1-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)этил)сульфонил)карбамат;
[162] Соединение 40: трет-бутил-((6-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3, 4-дигидройзохинолин-2(1Н)-ил)сульфонил)карбамат;
[163] Соединение 41: N-((3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)циклопентил)метил)сульфамид;
[164] Соединение 42: 4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)пиперидин-1-сульфонамид;
[165] Соединение 43: N-((4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)циклогексил)метил)сульфамид;
[166] Соединение 44: 2-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)пиперидин-1-ил)этан-1-сульфонамид;
[167] Соединение 45: 4-((5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)метил)пиперидин-1-сульфонамид;
[168] Соединение 46: N-(4-(1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[169] Соединение 47: N-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)сульфамид;
[170] Соединение 48: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)сульфамид гидрохлорид;
[171] Соединение 49: N-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[172] Соединение 50: N-(4-(4-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[173] Соединение 51: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид гидрохлорид;
[174] Соединение 52: N-(4-(6-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[175] Соединение 53: N-(4-(7-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[176] Соединение 54: N-(4-(4,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[177] Соединение 55: N-(4-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[178] Соединение 56: N-(4-(1Н-бензо[d][1,2,3]триазол-1-ил-3-фторбензил)сульфамид;
[179] Соединение 57: N-(4-(1Н-бензо[d][1,2,3]триазол-1-ил)-2,3-дифторбензил)сульфамид;
[180] Соединение 58: N-(4-(1Н-бензо[d][1,2,3]триазол-1-ил-3,5-дифторбензил)сульфамид;
[181] Соединение 59: N-(3-хлор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[182] Соединение 60: N-(2-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[183] Соединение 61: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторбензил)сульфамид;
[184] Соединение 62: N-(2, 5-дифтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[185] Соединение 63: N-(2, 6-дифтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[186] Соединение 64: N-(3, 5-дифтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-бензил)сульфамид;
[187] Соединение 65: N-(2, 3-дифтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-бензил)сульфамид;
[188] Соединение 66: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3-метилбензил)сульфамид;
[189] Соединение 67: N-(3-циано-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3-бензил)сульфамид;
[190] Соединение 68: N-(3-метокси-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[191] Соединение 69: N-(4-(5-метокси-6-метил-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[192] Соединение 70: N-(3-фтор-4-(5-метокси-6-метил-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[193] Соединение 71: N-(4-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторбензил)сульфамид;
[194] Соединение 72: N-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенэтил)сульфамид;
[195] Соединение 73: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенэтил)сульфамид гидрохлорид;
[196] Соединение 74: N-(3-фтор-4-(5-гидрокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[197] Соединение 75: N-(3-фтор-4-(5-метил-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[198] Соединение 76: N-(4-(5-этокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторбензил)сульфамид;
[199] Соединение 77: N-(3-фтор-4-(5-изопропокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[200] Соединение 78: N-(5-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил-пиридин-2-ил)метил)сульфамид;
[201] Соединение 79: (N-(6-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил-пиридин-3-ил)метил)сульфамид;
[202] Соединение 80: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)-N-метил)сульфамид;
[203] Соединение 81: N-(3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)-N-метилсульфамид;
[204] Соединение 82: N-циклопропил-N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[205] Соединение 83: (S)-N-(1-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)этил)сульфамид;
[206] Соединение 84: N-(4-(5-трифторметил)-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[207] Соединение 85: N-(3-фтор-4-(5-трифторметил)-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[208] Соединение 86: 4-(5-(1,1-дифторэтил)-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метан амин;
[209] Соединение 87: N-(4-(5-диметиламино)-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторбензил)сульфамид;
[210] Соединение 88: N-(3-фтор-4-(5-фторметокси)-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[211] Соединение 89: N-(4-(5-трифторметокси)-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[212] Соединение 90: N-(3-фтор-4-(5-трифторметокси)-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[213] Соединение 91: N-(4-(5-дифторметокси)-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторбензил)сульфамид;
[214] Соединение 92: N-(4-(6-фтор-5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[215] Соединение 93: N-(3-фтор-4-(6-фтор-5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[216] Соединение 94: 5-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)изоиндолин-2-сульфонамид;
[217] Соединение 95: N-5-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-2,3-дигидро-1Н-инден-2-ил)сульфамид;
[218] Соединение 96: 6-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3,4-дигидройзохинолин-2(1Н)сульфонамид;
[219] Соединение 97: 7-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3,4-дигидройзохинолин-2(1Н)сульфонамид;
[220] Соединение 98: 8-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-1,3,4,5-тетрагидро-2Н-бензо[d]азепин-2-сульфонамид;
[221] Соединение 99: N-(4-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)-2,5-дифторбензил)сульфамид;
[222] Соединение 100: N-(4-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)-2,6-дифторбензил)сульфамид;
[223] Соединение 101: 7-фтор-6-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3,4-дигидроизохинолин-2 (1Н)-сульфонамид;
[224] Соединение 102: 5-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)-изоиндолин-2-сульфонамид;
[225] Соединение 103: N-(5-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)-дигидро-1Н-инден-2 -ил)сульфамид;
[226] Соединение 104: N-(4-((5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)метил)фенил)сульфамид гидрохлорид;
[227] Соединение 105: N-(4-((5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)метил)бензил)сульфамид гидрохлорид;
[228] Соединение 106: N-((5-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)тиофен-2-ил)метил)сульфамид;
[229] Соединение 107: N-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-5-метоксилтиофен-2-ил)метил)сульфамид;
[230] Соединение 108: N-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-бицикло[1.1.1]пентан-1-ил)сульфамид;
[231] Соединение 109: N-(4-(5-метокси-2Н-бензо[d][1,2,3]триазол-2-ил)фенил)сульфамид гидрохлорид;
[232] Соединение 110: N-(4-((5-метокси-2Н-бензо[d][1,2,3]триазол-2-ил)бензил)сульфамид гидрохлорид;
[233] Соединение 111: 2-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)пиперидин-1-ил)этан-1-сульфонилфторид;
[234] Соединение 112: N-(3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)метансульфонамид;
[235] Соединение 113: N-(3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)этансульфонамид;
[236] Соединение 114: N-(3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)-4-метилбензолсульфонамид;
[237] Соединение 115: N-(3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)метансульфонимидамид;
[238] Соединение 116: 3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензойная кислота;
[239] Соединение 117: диэтил-(3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)фосфоамидит;
[240] Соединение 118: 4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)фосфоновая кислота;
[241] Соединение 119: 4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)фосфоновая кислота;
[242] Соединение 120: 3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)бороновая кислота;
[243] Соединение 121: 4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенэтил)бороновая кислота;
[244] Соединение 122: N-(4-(5-метокси-1Н-индол-1-ил)бензил)сульфамид;
[245] Соединение 123: N-(4-(5-метокси-1Н-бензо[d]имидазол-1-ил)бензил)сульфамид; и
[246] Соединение 124: N-(4-(5-метокси-1Н-индазол-1-ил)бензил)сульфамид.
[247]
[248] В некоторых вариантах осуществления соединения настоящего изобретения имеют профиль ингибирования ENPP1, который отражает активность в отношении дополнительных ферментов. В некоторых вариантах осуществления соединения настоящего изобретения специфически ингибируют ENPP1 без непреднамеренного ингибирования одного или более других ферментов.
[249] В некоторых вариантах осуществления соединения настоящего изобретения ингибируют ENPP 1, что может быть определено с помощью анализа для определения активности ферментов в бесклеточных или клеточных системах после обработки соединениями настоящего изобретения, по сравнению с контрольной группой путем анализа ингибирования, например, путем измерения IC50 или ЕС50. В некоторых вариантах осуществления соединения настоящего изобретения имеют IC50 (или ЕС50)10 мкМ или менее, такое как 3 мкМ или менее, 1 мкМ или менее, 500 нМ или менее, 300 нМ или менее, 200 нМ или менее, 100 нМ или менее, 50 нМ или менее, 30 нМ или менее, 10 нМ или менее, 5 нМ или менее, 3 нМ или менее, 1 нМ или менее, или даже более низкое значение.
[250] Методика анализа, которая может быть использована для определения активности ENPP1, может включать, без ограничения, следующие методики анализа, включая бесклеточные системы анализа, такие как анализы авидности, анализы с использованием очищенных ферментов, клеточные анализы для определения фенотипов клеток, такие как анализы экспрессии генов и анализы in vivo с участием специфических животных.
[251] В некоторых вариантах осуществления способ настоящего изобретения представляет собой способ подавления пролиферации раковых клеток, причем способ включает обработку клеток эффективным количеством соединения настоящего изобретения для подавления пролиферации раковых клеток. В некоторых вариантах осуществления способ может выполняться в комбинации с химиотерапией. Любые раковые клетки могут использоваться, если они доступны.
[252] Способ лечения
[253] Как упоминалось выше, настоящее изобретение включает способы ингибирования активности ENPP1 в отношении cGAMP, чтобы вызвать повышенные уровни cGAMP и/или модуляцию нижерасположенных факторов пути STING. В недавнем сообщении показано, что ингибирование ENPP1 может модулировать активность STING in vivo и, таким образом, может быть использовано для лечения различных заболеваний, как например, при иммунотерапии рака или лечении инфекционных заболеваний. Как описано выше, способ по настоящему изобретению представляет собой способ усиления STING-опосредованного ответа и регуляции иммунного ответа у субъекта.
[254] В некоторых вариантах осуществления STING-опосредованный ответ включает увеличение выработки интерферона (например, интерферона 1 типа, интерферона 3 типа)у субъекта. Интерфероны (IFN)представляют собой группу сигнальных белков, продуцируемых и высвобождаемых клетками-хозяевами в ответ на присутствие одного или более патогенов для усиления защиты окружающих клеток от патогенов. IFN также выполняют множество других функций: 1)активируют иммунные клетки, такие как NK-клетки и макрофаги, и 2)стимулируют защиту организма-хозяина повышающей регуляцией презентации антигена за счет повышенной экспрессии антигенов главного комплекса гистосовместимости (МНС). IFN обычно подразделяются на три класса: IFN 1 типа, IFN 2 типа и IFN 3 типа. IFN 1 типа млекопитающих включают IFN-α (альфа), IFN-β (бета), IFN-δ (дельта), I FN-ε (эпсилон), IFN-κ (каппа), IFN-τ (тау), IFN-ω (омега)и IFN-ζ (дзета). Все IFN 1 типа связываются со специфическим комплексом рецепторов клеточной поверхности, известным как IFN-α/β рецептор (IFNAR), который состоит из цепей IFNAR1 и IFNAR2.
[255] Интерфероны изучались как противораковые средства вследствие их противоопухолевой активности, которая характеризуется двумя различными эффектами, а именно внутренним противоопухолевым и/или иммуномодулирующим эффектом. IFN регулируют экспрессию ряда генов, которые непосредственно влияют на рост, пролиферацию, дифференцировку, выживание, миграцию опухолевых клеток и другие специфические функции. В некоторых случаях лечение in vitro с использованием IFN 1 типа оказывает прямой антипролиферативный эффект за счет продления всех фаз клеточного цикла с помощью IFN. В некоторых случаях, CRKL, который является типом белка CRK, активируемого IFN 1 типа, взаимодействует с онкосупрессором, малым G-белком RAP1A, ингибируя GТРазу семейства RAS, что приводит к остановке роста раковых клеток. Известно, что IFN регулируют два основных апоптотических ответа. Двумя апоптотическими ответами являются внешние (путь, опосредованный апоптотическими рецепторами)и внутренние (митохондриальные)пути. В ответ на IFN 1 типа происходит повышающая регуляция активации сенсорного белка (например, рецептора DR), что вызывает апоптоз опухолевых клеток.
[256] IFN оказывают внешнее воздействие на опухоли посредством регуляции таких процессов, как ангиогенез, остеокластогенез и иммунитет. Как эндогенные, так и экзогенные IFN 1 типа играют важную роль в активности противоракового иммунитета. Например, IFN 1 типа усиливают активность α/β Т-клеток, γ/δ Т-клеток, NK-клеток и дендритных клеток, и ингибируют активность иммуносупрессорных клеток, например, превращение регуляторных Т-клеток, супрессорных клеток костного мозга и опухолеассоциированных макрофагов. IFN 1 типа также действует непосредственно на опухолевые клетки, улучшая экспрессию антигена и повышая регуляцию многочисленных взаимодействующих с иммунитетом молекул (например, стресс-лигандов, распознаваемых главным комплексом гистосовместимости класса 1 (MHCI)) и иммунорецепторов зародышевой линии.
[257] В одном аспекте способ предусматривает введение терапевтически эффективного количества ингибитора ENPP1 субъекту, страдающему раком, для лечения рака у субъекта. В одном варианте осуществления субъект может быть субъектом с диагнозом или подозрением на рак. Любой подходящий ингибитор ENPP1 может использоваться у субъекта. В одном варианте осуществления рак выбирают из рака надпочечников, рака печени, рака почки, рака мочевого пузыря, рака молочной железы, рака толстой кишки, рака желудка, рака яичников, рака шейки матки, рака матки, рака пищевода, колоректального рака, рака предстательной железы, рака поджелудочной железы, рака легких (мелкоклеточного и немелкоклеточного), рака щитовидной железы, карциномы, саркомы, глиобластомы, меланомы и рака головы и шеи. В одном варианте осуществления рак представляет собой лимфому.
[258] В одном варианте осуществления эффективное количество соединения варьирует в диапазоне от примерно 10 нг до примерно 100 мг, например, от примерно 10 нг до примерно 50 нг, от примерно 50 нг до примерно 150 нг, от примерно 150 нг до примерно 250 нг, от примерно 250 нг до примерно 500 нг, от примерно 500 нг до примерно 750 нг, от примерно 750 нг до примерно 1 мкг, от примерно 1 мкг до примерно 10 мкг, от примерно 10 мкг до примерно 50 мкг, от примерно 50 мкг до примерно 150 мкг, от примерно 150 мкг до примерно 250 мкг, от примерно 250 мкг до примерно 500 мкг, от примерно 500 мкг до примерно 750 мкг, от примерно 750 мкг до примерно 1 мг, от примерно 1 мг до примерно 50 мг, от примерно 1 мг до примерно 100 мг, или от примерно 50 мг до примерно 100 мг. Количество может быть однократной дозой или общей суточной дозой. Общее суточное количество может находиться в диапазоне от 10 нг до 100 мг, или от 100 мг до примерно 500 мг, или от 500 мг до примерно 1000 мг.
[259] В одном варианте осуществления соединение вводят в однократной дозе. В других вариантах осуществления вводят многократные дозы. Когда многократные дозы вводятся в течение определенного периода времени, соединение вводят два раза в день (bid), один раз в день (qd), через день (qod), каждые 3 дня, 3 раза в неделю (tiw)или два раза в неделю (biw).
[260] Комбинированная терапия
[261] Соединение-ингибитор ENPP1 по настоящему изобретению может вводиться субъекту отдельно или в комбинации с дополнительным активным агентом или дополнительной терапией, например, лучевой терапией. Термины «агент», «соединение» и «лекарственное средство» используются здесь взаимозаменяемо. В одном варианте осуществления способ настоящего изобретения кроме того предусматривает введение субъекту дополнительного агента, например, малой молекулы, химиотерапевтического агента, антитела, конъюгата антитело-лекарственное средство, аптамера, белка, ингибитора контрольных точек иммунного ответа или лучевой терапии сопутствующим образом или последовательно в комбинации.
[262] Термин «совместное введение» или «в комбинации с» включает введение двух или более терапевтических агентов одновременно, параллельно или последовательно, без какого-либо конкретного ограничения по времени. В некоторых вариантах осуществления агонисты или агенты одновременно присутствуют в клетках или субъектах или одновременно оказывают биологическое или терапевтическое воздействие. В некоторых вариантах осуществления терапевтические агенты представлены в виде идентичной композиции или стандартной лекарственной формы. В некоторых вариантах осуществления терапевтические агенты представляют собой отдельные композиции или стандартные лекарственные формы. В некоторых вариантах осуществления первый терапевтический агент вводят перед введением второго терапевтического агента (например, за 5 минут до, за 15 минут до, за 30 минут до, за 45 минут до, за 1 час до, за 2 часа до, за 4 часа до, за 6 часов до, за 12 часов до, за 24 часа до, за 48 часов до, за 72 часа до, за 96 часов до, за 1 неделю до, за 2 недели до, за 3 недели до, за 4 недели до, за 5 недель до, за 6 недель до, за 8 недель до или за 12 недель до), при сопутствующем введении с введением второго терапевтического агента, или после введения второго терапевтического агента (например, через 5 минут после, через 15 минут после, через 30 минут после, через 45 минут после, через 1 час после, через 2 часа после, через 4 часа после, через 6 часов после, через 12 часов после, через 24 часа после, через 48 часов после, через 72 часа после, через 96 часов после, через 1 неделю после, через 2 недели после, через 3 недели после, через 4 недели после, через 5 недель после, через 6 недель после, через 8 недель после или через 12 недель после).
[263] «Сопутствующее введение» дополнительной терапии на основе известного терапевтического агента или композиции, включающей описанное соединение по настоящему изобретению, означает комбинацию соединения и второго агента или дополнительную терапию, такую, что как известный агент, так и композиция, включающая описанное соединение, обладают терапевтическими эффектами. Сопутствующее введение может включать одновременное или предшествующее введение лекарственных средств в сочетании с введением соединения по настоящему изобретению. Пути введения этих двух агентов могут различаться, и типичные пути введения подробно описаны ниже. Специалистам в данной области не составит труда определить подходящее время введения, последовательность и дозировку для лекарственного средства или терапии и соединения, описанных в настоящем документе.
[264] Для лечения рака соединения-ингибиторы ENPP1 могут вводиться в комбинации с химиотерапевтическим агентом, выбранным из группы, состоящей из алкилирующих агентов, антиметаболитов, противоопухолевых антибиотиков, растительных алкалоидов, таксанов, аналогов нуклеозидов, антрациклинов, препаратов с нацеливанием на тимидилат, модуляторов апоптоза, ингибиторов контроля клеточного цикла, ингибиторов рецептора колониестимулирующего фактора 1, CD47 ингибиторов и тому подобного.
[265] Комбинация с иммунотерапевтическими агентами
[266] Для лечения рака соединения-ингибиторы ENPP1 могут вводиться в комбинации с иммунотерапевтическим агентом. Иммунотерапевтический агент представляет собой агонист, подходящий для лечения рака путем индуцирования, усиления или ингибирования иммунного ответа. В некоторых вариантах осуществления иммунотерапевтический агент представляет собой ингибитор контрольных точек иммунного ответа. Можно использовать любой иммуносупрессор. Например, ингибитор контрольных точек иммунного ответа может представлять собой ингибитор ассоциированного с цитотоксическими Т-лимфоцитами антигена 4 (CTLA-4), ингибитор белка 1 запрограммированной смерти клеток (PD-1) или ингибитор лиганда 1 запрограммированной смерти клеток (PD-L1), но этим не ограничивается. Примеры ингибитора контрольных точек иммунного ответа включают, без ограничения, ипилимумаб, пембролизумаб, ниволумаб, атезолизумаб, авелумаб, дурвалумаб, цемиплимаб и тому подобное. В некоторых вариантах осуществления иммунотерапевтический агент представляет собой иммуноклеточную терапию. Может применяться любая подходящая клеточная терапия, и ее примеры включают, без ограничения, химерную антигенную рецепторную Т-клеточную терапию, химерную антигенную рецепторную NK-клеточную терапию и другие клеточные терапии.
[267] Для лечения рака соединение-ингибитор ENPP1 может вводиться в комбинации с подходящим режимом вакцинации против рака, например, вакциной на основе дендритных клеток, которая способствует Th1/Th17 иммунитету. В некоторых случаях соединение-ингибитор ENPP1 подходит для использования в качестве адъювантной терапии в комбинации с вакцинацией, индуцирующей Th-17.
[268] Комбинация с лучевой терапией
[269] Для лечения рака соединение-ингибитор ENPP1 может вводиться в комбинации с лучевой терапией. В некоторых вариантах осуществления соединение-ингибитор ENPP1 может вводиться до или после лучевой терапии. Комбинация лучевой терапии и введения соединения по настоящему изобретению может дать синергический терапевтический эффект. Когда субъект подвергается лучевой терапии (ЛТ) в соответствующей дозе и/или с соответствующей частотой в ходе лучевой терапии (ЛТ), у субъекта может вырабатываться cGAMP. Соединение-ингибитор ENPP1 может повышать терапевтическую эффективность для субъекта за счет предотвращения разрушения продуцируемого cGAMP, в сравнении с уровнем cGAMP, полученным, например, только при ЛТ. В связи с этим, детали способов настоящего изобретения предусматривают введение сниженной дозы и/или частоты и/или режима лучевой терапии по сравнению с дозой и/или частотой и/или снижением терапевтического эффекта одной только лучевой терапии. В некоторых вариантах осуществления лучевую терапию проводят в комбинации с соединением по настоящему изобретению в дозировке и/или частоте, эффективных для снижения риска радиационного повреждения, например, риска радиационного повреждения субъекта, ожидаемого при терапевтически эффективном количестве.
[270] В одном варианте осуществления способ включает введение субъекту ингибитора ENPP1 перед лучевой терапией. В одном варианте осуществления способ включает введение ингибитора ENPP1 субъекту после подвергания субъекта воздействию лучевой терапии. В другом варианте осуществления способ включает последовательное назначение субъекту, нуждающемуся в этом, лучевой терапии, за которой следует ингибитор ENPP1, после чего следует ингибитор контрольных точек иммунного ответа.
[271] Комбинация с противораковой вакциной
[272] Для лечения рака соединение-ингибитор ENPP1 может вводиться в сочетании с противораковой вакциной. В некоторых вариантах осуществления соединение-ингибитор ENPP1 может вводиться до или после введения противораковой вакцины.
[273] Комбинация с CAR-T
[274] Для лечения рака соединение-ингибитор ENPP1 может вводиться в сочетании с CAR-T-клеточным терапевтическим агентом. В некоторых вариантах осуществления соединение-ингибитор ENPP1 может вводиться до или после введения CAR-T-клеточного терапевтического агента.
[275] Монотерапия
[276] Терапия, способствующая регенерации миокарда
[277] В одном аспекте терапия для регенерации миокарда может включать введение терапевтически эффективного количества ингибитора ENPP1 субъекту, имеющему патологическое изменение вследствие инфаркта миокарда, для лечения субъекта.
[278] Схема лечения гипофосфатемии
[279] В одном аспекте способы лечения гипофосфатемии могут включать введение терапевтически эффективного количества ингибитора ENPP1 субъекту, имеющему патологическое изменение, вызванное наследственной гипофосфатемией, для лечения субъекта.
[280] Фармацевтическая композиция
[281] Фармацевтически приемлемые эксципиенты, такие как наполнители, адъюванты, носители или разбавители, легко доступны специалистам в данной области. Фармацевтически приемлемые вспомогательные вещества, такие как модификаторы рН, буферы, модификаторы изотоничности, стабилизаторы, смачивающие вещества и тому подобное, легко доступны специалистам в данной области.
[282] В некоторых вариантах осуществления соединение настоящего изобретения готовят в водном буфере. Подходящие водные буферы включают, без ограничения, ацетатный, сукцинатный, цитратный и фосфатный буферы в различных концентрациях в диапазоне от 5 мМ до 1000 мМ. В некоторых вариантах осуществления водные буферы включают реагенты, которые обеспечивают получение изотонических растворов. Такие реагенты включают, без ограничения, хлорид натрия, сахара, такие как маннит, декстроза и сахароза, и тому подобное. В некоторых вариантах осуществления, водный буфер кроме того включает в себя неионогенное поверхностно-активное вещество, такое как полисорбат 20 или 80. Необязательно, композиция может дополнительно включать консервант. Подходящие консерванты включают, без ограничения, бензиловый спирт, фенол, хлорбутанол, бензалконийхлорид, и тому подобное. В другом варианте осуществления композицию хранят при температуре примерно 4°С. Композиция также может быть лиофилизирована и обычно содержит криопротектор, такой как сахароза, трегалоза, лактоза, мальтоза или маннит. Лиофилизированные препараты могут храниться даже при комнатной температуре в течение длительного периода времени.
[283] Здесь фармацевтическая композиция может включать в себя или по существу состоять из соединения, описанного в настоящем документе, или его фармацевтически приемлемой соли, его изомера или его таутомера, и дополнительно включает или по существу состоит из одного или более представляющих интерес активаторов. Любой благоприятный активатор может использоваться в настоящем способе в комбинации с соединением настоящего изобретения. В одном варианте осуществления соединение настоящего изобретения и ингибитор контрольных точек иммунного ответа, а также дополнительный терапевтический агент, как описано в настоящем документе, для комбинированной терапии, может вводиться перорально, подкожно, внутримышечно, интраназально, парентерально или другими путями. В другом варианте осуществления соединение настоящего изобретения, химиотерапевтический агент (в частности, химиотерапевтический агент, способный индуцировать выработку cGAMP in vivo)и дополнительный терапевтический агент, описанный здесь для комбинированной терапии, может вводиться перорально, подкожно, внутримышечно, интраназально, парентерально или другими путями. Соединение настоящего изобретения и второй активатор (если присутствует)могут быть введены одинаковыми или различными путями. Терапевтический агент может быть введен любым подходящим способом, включая, без ограничения, пероральный, ректальный, назальный, местный, вагинальный, парентеральный, внутривенный, интраназальный, а также внутриопухолевую инъекцию в пораженный орган.
[284] Соединения настоящего изобретения могут вводиться в стандартной лекарственной форме и могут быть получены с помощью любого способа, хорошо известного в области техники. Такие способы включают комбинирование соединения настоящего изобретения с фармацевтически приемлемым носителем или разбавителем, который представляет собой один из одного или более вспомогательных ингредиентов. Фармацевтически приемлемый носитель выбирают на основе выбранного пути введения и стандартной фармацевтической практики. Каждый носитель должен быть «фармацевтически приемлемым» в том смысле, что он совместим с другими ингредиентами композиции и не наносит вреда субъекту или пациенту. Этот носитель может быть твердым или жидким, его тип обычно выбирают в соответствии со способом введения.
[285] Примеры подходящих твердых носителей включают лактозу, сахарозу, желатин, агар и сыпучий порошок. Примеры подходящих жидких носителей включают воду, фармацевтически приемлемые жиры и масла, спирты или другие органические растворители, такие как сложные эфиры, эмульсии, сиропы или эликсиры, суспензии и растворы и/или суспензии, восстановленные из невспенивающикся гранул. Такие жидкие носители могут содержать, например, подходящие растворители, консерванты, эмульгаторы, суспендирующие агенты, разбавители, подсластители, загустители и размягчители.
[286]
[287] Ниже будут описаны различные аспекты настоящего изобретения.
[288] В одном аспекте настоящее изобретение предлагает соединение, выбранное из производного соединения бензотриазола, представленного следующей формулой 1, его таутомера, его фармацевтически приемлемой соли, его гидрата, его сольвата и его стереоизомера:
[289][Формула 1]
[290]

[291] где
[292] W1 представляет собой N или CRa,
[293] W2 представляет собой N или CRb,
[294] W3 представляет собой N или CRc,
[295] W4 представляет собой N или CRd,
[296] W5 представляет собой N или CRe,
[297] W6 представляет собой N или CRf,
[298] W7 представляет собой N или CRg,
[299] где каждый Ra, Rb, Rc, Rd, Re, Rf и Rg независимо выбран из группы, состоящей из водорода, галогена, циано, нитро, алкила, алкенила, алкинила, циклоалкила, гетероциклила, арила и гетероарила,
[300] каждый из R1, R2, R3 и R4 независимо представляет собой водород, гидроксильную группу, галогенную группу, -CF3, -(O)CF3, C1-C13 алкильную группу, C1-C6 алкоксигруппу, аминогруппу (-NR7R8), нитрогруппу (-N(O)2), амидную группу (- (С=O)NR7R8), карбоксильную группу (-С(О)ОН), нитрильную группу (-CN), С6-С10 арильную группу, С3-С10 циклическую группу, С3-С10 гетероарильную группу, С3-С10 гетероциклическую группу или -С(О)-(С1-С13 алкил),
[301] Z присутствует или отсутствует, при этом, когда Z присутствует, Z представляет собой -O-, -СО-, -COO-, -CnHn+2-, -О(CnHn+2)-,-(ОС2Н4)n-,-(С2Н4О)n-,-(CnHn+2)О-,-(CnHn+2)СО-, (CnHn+2)О (CmHm+2)-, -NR7 (CnHn+2)-, - (NR7C2H4)n-,-(C2H4NR7)n- или-(CnHn+2)NR7-,
[302] n является целым числом от 0 до 8,
[303] R5 представляет собой -A-(R6)y,
[304] где А представляет собой С3-С10 циклическую группу, С5-С10 бициклическую группу, С3-С10 гетероциклическую группу, С6-С10 арильную группу или С3-С10 гетероарильную группу,
[305] R6 представляет собой водород, гидроксильную группу, галогенную группу, C1-C13 алкильную группу, С1-С6 алкоксигруппу, С1-С6 алкенильную группу, С6-С10 арильную группу, С3-С10 циклическую группу, С3-С10 гетероарильную группу, С3-С10 гетероциклическую группу, -С(О)-(С1-С13 алкил), трет-бутоксикарбонильную группу (Boc), аминогруппу (-NR7R8), (CmHm+2)NR7R8, нитрогруппу (-N(O)2), амидную группу (- (С=O)NR7R8), сложноэфирную группу (- (CmHm+2)С(О)OR7), карбоксильную группу (-С(О)ОН), нитрильную группу (-CN), сульфонамидную группу (-(CmHm+2)NHS (О)2R7), мочевинную группу, сульфамоильную группу (-(CmHm+2)NHS (О)2NHR7), сульфонамидную группу, сульфамоилалкильную группу (- (CmHm+2)NHS (О)2NHR7), сульфамоилалкильную группу (-(CmHm+2)NR7S (О)2NHR8), сульфидную группу (- (CmHm+2)SR7), сульфоновую группу (-(CmHm+2)S(О)2R7), или фосфорильную группу (-(CmHm+2)Р(О)R7R8), или связан с тем же углеродом, что и углерод, связанный с А, с образованием 3-10-членного насыщенного кольца, связан с тем же углеродом, что и углерод, связанный с А, с образованием 3-10-членного насыщенного гетероцикла, содержащего по меньшей мере один гетероатом из N, О и S, связан с углеродом, смежным с углеродом, связанным с А, с образованием 3-10-членного насыщенного кольца, или связан с углеродом, смежным с углеродом, связанным с А, с образованием 3-10-членного насыщенного гетероцикла, содержащего по меньшей мере один гетероатом из N, О и S,
[306] m является целым числом от 0 до 4; и
[307] у является целым числом от 0 до 4,
[308] при этом С1-С13 алкильная группа, Cl-C6 алкоксигруппа, С1-С6 алкенильная группа или -С(О)-(С1-С13 алкил)включает в себя по меньшей мере один заместитель, выбранный из группы, состоящей из водорода, гидроксильной группы, галогенной группы, С1-С13 алкильной группы, С1-С6 алкоксигруппы, аминогруппы (-NR7R8), нитрогруппы (-N(O)2), амидной группы (-(С=O)NR7R8), карбоксильной группы (-С(О)ОН), нитрильной группы (-CN), мочевинной группы (-NR7 (С=O)NR8 -), сульфонамидной группы (-NHS(O)2-), сульфидной группы (-S-), сульфонильной группы (-S(O)2-), фосфорильной группы (-P(O)R7R8), С6-С10 арильной группы, С3-С10 гетероарильной группы и С3-С10 гетероциклической группы,
[309] С6-С10 арильная группа, С3-С10 гетероарильная группа, С3-С10 циклическая группа, С3-С10 гетероциклическая группа или С5-С10 бициклическая группа включает в себя по меньшей мере один заместитель, выбранный из группы, состоящей из водорода, гидроксильной группы, галогенной группы, карбонильной группы (-(C=O)R7R8), С1-С3 алкильной группы, замещенной или незамещенной галогеном или С3-С10 гетероциклической группой, С1-С3 алкоксигруппы, замещенной или незамещенной галогеном или С3-С10гетероциклической группой, С6-С10 фенокси, аминогруппы (-NR7R8), нитрогруппы (-N(O)2), амидной группы (- (С=O)NR7R8), карбоксильной группы (-С(О)ОН), нитрильной группы (-CN), мочевинной группы (-NR7 (С=O)NR8-), сульфонамидной группы (-NHS(O)2-), сульфидной группы (-S-), сульфонильной группы (-S(O)2-), фосфорильной группы (-P(O)R7R8), С6-С10 арильной группы, С3-С10 гетероарильной группы и С3-С10 гетероциклической группы, и
[310] каждый из R7 и R8 независимо представляет собой водород, C1-С6 алкильную группу, C1-C6 алкенильную группу, C1-C6 алкинильную группу, С6-С10 арильную группу, С3-С10 гетероарильную группу, С3-С10 гетероциклическую группу, аминогруппу (-NH2), нитрогруппу (-N(O)2), -Вос, или -NHBoc, или R7, вместе с атомом азота или углерода, связанным с R8, образует 3-7-членное насыщенное кольцо, включающее по меньшей мере одно из N, О, S, NH, C=N, С=О, -NHC(O)-, -NHC(O)NH-, -NHS(O)2-, или SO2, и является замещенным по меньшей мере одним из водорода, С1-С13 алкильной группы, С6-С10 арильной группы, С3-С10 гетероарильной группы, гидроксильной группы, галогенидной группы или цианогруппы,
[311] где С3-С10 гетероарильная группа и С3-С10 гетероциклическая группа включает в себя по меньшей мере один гетероатом, выбранный из группы, состоящей из N, О и S.
[312]
[313] В определении заместителя в настоящем изобретении термин «алкил» означает алифатический углеводородный радикал. Алкил может быть «насыщенным алкилом», не содержащим алкенильного или алкинильного фрагмента, или «ненасыщенным алкилом», содержащим по меньшей мере один алкенильный или алкинильный фрагмент. Термин «алкенил» означает группу, содержащую по меньшей мере одну двойную углерод-углеродную связь, и термин «алкинил» означает группу, содержащую по меньшей мере одну тройную углерод-углеродную связь. Алкил может быть циклическим, с разветвленной или прямоцепочечной структурой при использовании по отдельности или в комбинации.
[314] Термин «арил» означает ароматическую монокарбоциклическую С6 группу, которая может быть дополнительно конденсирована, отдельно или в комбинации с другим радикалом, с 5- или 6-членной карбоциклической группой, которая может быть ароматической и может быть насыщенной или ненасыщенной. Примеры арила могут включать, без ограничения, фенил, инданил, 1-нафтил, 2-нафтил, тетрагидронафтил, и тому подобное. Арил может быть связан с другими группами в соответствующих положениях на ароматическом кольце.
[315] Термин «алкокси» обозначает алкильную группу, связанную с другой группой посредством атома кислорода (т.е. -O-алкил). Алкоксигруппа может быть незамещенной или замещенной одним или более подходящим заместителем. Примеры алкоксигруппы включают, без ограничения, (C1-C6)алкоксигруппу, такую как -О-метил, -О-этил, -О-пропил, -О-изопропил, -О-2-метил-1-пропил, -О-2-метил-2-пропил, -О-2-метил-1-бутил, -О-3-метил-1-бутил, -О-2-метил-3-бутил, -О-2,2-диметил-1-пропил, -О-2-метил-1-пентил, 3-О-метил-1-пентил, -О-4-метил-1-пентил, -О-2-метил-2-пентил, -О-3-метил-2-пентил, -О-4-метил-2-пентил, -О-2,2-диметил-1-бутил, -О-3,3-диметилбутил, -О-2-этил-1-бутил, -О-бутил, -О-изобутил, -О-трет-бутил, -О-пентил, -О-изопентил, -О-неопентил и -О-гексил.
[316] Термин «фенокси» обозначает фенильную группу, связанную с другой группой посредством атома кислорода (т.е. -О-арил). Фенокси является незамещенной или замещенной по меньшей мере одной из групп: галогенной, алкильной, арильной или гетероарильной, но не ограничивается ими.
[317] Термин «аминогруппа» обозначает алкильную группу, связанную с другой группой посредством атома азота (т.е. -NH-или -N-алкил). Аминогруппа может быть незамещенной или замещенной одним или более подходящим заместителем. Примеры аминогруппы включают, без ограничения, (C1-C6)амино, например, NH-метил, -NH-этил, -NH-пропил, -NH-изопропил, -NH-2-метил-1-пропил, -NH-2-метил-2-пропил, -NH-2-метил-1-бутил, -NH-3-метил-1-бутил, -NH-2-метил-3-бутил, -NH-2,2-диметил-1-пропил, -NH-2-метил-1-пентил, 3-NH-метил-1-пентил, -NH-4-метил-1-пентил, -NH-2-метил-2-пентил, -NH-3-метил-2-пентил, -NH-4-метил-2-пентил, NH-2,2-диметил-1-бутил, -NH-3,3-диметилбутил, -NH-2-этил-1-бутил, -NH-бутил, -NH-изобутил, -NH-трет-бутил, -NH-пентил, -NH-изопентил, -NH-неопентил, -NH-гексил, -N,N-диметил, -N-метил-N-этил, -N-метил-N-пропил, -N-метил-изопропил, -N-метил-N-бутил, -N-метил-N-изобутил, -N-метил-N-пентил, -N-метил-N-изопентил, N-метил-N-гексил, N-метил-N-изогексил, -N,N-диэтил, -N-этил-N-пропил, -N-этил-N-изопропил, -N-этил-N-бутил, -N-этил-N-изобутил, -N-этил-N-пентил, -N-этил-N-изопентил, -N-этил-N-гексил, -N-этил-N-изогексил, -N,N-дипропил, -N-пропил-N-изопропил, -N-пропил-N-бутил, -N-пропил-N-изобутил, -N-пропил-N-пентил, -N-пропил-N-изопентил, -N-пропил-N-гексил, -N-пропил-N-изогексил, -N,N-дибутил, -N-бутил-N-изобутил, -N-бутил-N-пентил, -N-бутил-N-изопентил, -N-бутил-N-гексил, -N-бутил-N-изогексил, N,N-дипентил, -N-пентил-N-гексил, -N-пентил-N-изогексил и -N,N-дигексил.
[318] Под термином «галогенная группа» подразумевается фтор, хлор, бром или иод.
[319] Термин «гетероциклическая группа» означает
гетероароматическое соединение, содержащее по меньшей мере один гетероатом, выбранный из группы, состоящей из N, О и S, если не указано иное. Предпочтительно гетероциклическая группа может включать, без ограничения, пирролидиновые, фурановые, морфолиновые, пиперазиновые и пиперидиновые группы, более предпочтительно пирролидиновые, пиперидиновые, пиперазиновые и морфолиновые группы.
[320] Термин «гетероарильная группа» относится к гетероароматическому соединению, содержащему по меньшей мере один гетероатом, выбранный из группы, состоящей из N, О и S, если не указано иное. Предпочтительно гетероарильная группа может включать, без ограничения, пиридиновые, пиразиновые, пиримидиновые, пиридазиновые, пиразольные, имидазольные, триазольные, индольные, оксадиазольные, тиадиазольные, хинолиновые, изохинолиновые, изоксазольные, оксазольные, тиазольные и пиррольные группы.
[321] В одном аспекте настоящее изобретение предлагает соединение, выбранное из производного соединения бензотриазола, представленного формулой 1, его таутомера, его фармацевтически приемлемой соли, его гидрата, его сольвата и его стереоизомера, где каждый из W1, W2, W3 и W4 представляет собой -СН-.
[322] В одном аспекте настоящее изобретение предлагает соединение, выбранное из производного соединения бензотриазола, представленного формулой 1, его таутомера, его фармацевтически приемлемой соли, его гидрата, его сольвата и его стереоизомера, где А представляет собой С5-С6 циклическую группу, С5-С7 бициклическую группу, С5-С8 гетероциклическую группу, С6-С10 арильную группу или С4-С7 гетероарильную группу.
[323] В одном аспекте настоящее изобретение предлагает соединение, выбранное из производного соединения бензотриазола, представленного формулой 1, его таутомера, его фармацевтически приемлемой соли, его гидрата, его сольвата и его стереоизомера, где А представляет собой замещенный или незамещенный циклопентан, замещенный или незамещенный циклогексан, замещенный или незамещенный бензол, замещенный или незамещенный бициклопентан, замещенный или незамещенный тиофен, замещенный или незамещенный пиридин, замещенный или незамещенный бензофуран, замещенный или незамещенный хинолин, замещенный или незамещенный индол, замещенный или незамещенный бензоазепин, замещенный или незамещенный пиперидин, замещенный или незамещенный фуран, замещенный или незамещенный нафталин, замещенный или незамещенный антрацен, или замещенный или незамещенный фенантрен, замещенный или незамещенный пиридазин, замещенный или незамещенный пиразин, замещенный или незамещенный имидазол, замещенный или незамещенный пиразол, замещенный или незамещенный пиримидин, замещенный или незамещенный пиррол, замещенный или незамещенный индол, или замещенный или незамещенный пурин.
[324] В одном аспекте настоящее изобретение предлагает соединение, выбранное из производного соединения бензотриазола, представленного формулой 1, его таутомера, его фармацевтически приемлемой соли, его гидрата, его сольвата и его стереоизомера, где А представляет собой замещенный или незамещенный циклопентан, замещенный или незамещенный циклогексан, замещенный или незамещенный бензол, замещенный или незамещенный бициклопентан, замещенный или незамещенный тиофен, замещенный или незамещенный пиридин, замещенный или незамещенный бензофуран, замещенный или незамещенный хинолин, замещенный или незамещенный индол, замещенный или незамещенный бензоазепин, или замещенный или незамещенный пиперидин.
[325] В одном аспекте настоящее изобретение предлагает соединение, выбранное из производного соединения бензотриазола, представленного формулой 1, его фармацевтически приемлемой соли, его гидрата, его сольвата и его стереоизомера, где каждый из R1, R2, R3 и R4 независимо представляет собой водород, гидроксильную группу, галогенную группу, -CF3,-(O)CF3, С1-С13 алкильную группу, С1-С6 алкоксигруппу, аминогруппу (-NR7R8), Z присутствует или отсутствует, при этом, когда Z присутствует, Z представляет собой -CnHn+2-, и n является целым числом от 1 до 4.
[326] В одном аспекте настоящее изобретение предлагает соединение, выбранное из производного соединения бензотриазола, представленного формулой 1, его таутомера, его фармацевтически приемлемой соли, его гидрата, его сольвата и его стереоизомера, где каждый из W1, W2, W3 и W4 представляет собой -СН-, А представляет собой замещенный или незамещенный циклопентан, замещенный или незамещенный циклогексан, замещенный или незамещенный бензол, замещенный или незамещенный бициклопентан, замещенный или незамещенный тиофен, замещенный или незамещенный пиридин, замещенный или незамещенный бензофуран, замещенный или незамещенный хинолин, замещенный или незамещенный индол, замещенный или незамещенный бензоазепин, или замещенный или незамещенный пиперидин, каждый из R1, R2, R3 и R4 независимо представляет собой водород, гидроксильную группу, галогенную группу, -CF3,-(O)CF3, С1-С13 алкильную группу, C1-C6 алкоксигруппу или аминогруппу (-NR7R8), Z присутствует или отсутствует, при этом, когда Z присутствует, Z представляет собой -CnHn+2-, и n является целым числом от 1 до 4.
[327] В одном аспекте настоящее изобретение предлагает соединение, выбранное из производного соединения бензотриазола, представленного формулой 1, его фармацевтически приемлемой соли, его гидрата, его сольвата и его стереоизомера, при этом соединение выбрано из группы, состоящей из следующих соединений №№1-124:
[328] Соединение 1: 5-метокси-1-(пиперидин-4-ил)-1Н-бензо[d][1,2,3]триазол гидрохлорид;
[329] Соединение 2: 4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)циклогексил)метананилин;
[330] Соединение 3: 5-метокси-1-(пиперидин-4-илметил)-1Н-бензо[d][1,2,3]триазол;
[331] Соединение 4: 4-(5-метокси-1Н-бензо[d][1,2,3]триазол 1-ил)анилин гидрохлорид;
[332] Соединение 5: 4-(1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
[333] Соединение 6: 4-(4-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
[334] Соединение 7: 4-(б-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
[335] Соединение 8: 4-(7-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
[336] Соединение 9: 4-(4,б-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
[337] Соединение 10: 4-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
[338] Соединение 11: 2-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)этан-1-амин гидрохлорид;
[339] Соединение 12: 1-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)-N-метилметанамин гидрохлорид;
[340] Соединение 13: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-бензил)циклопропанамин гидрохлорид;
[341] Соединение 14: (S)-1-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)этан-1-амин гидрохлорид;
[342] Соединение 15: 3-хлор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
[343] Соединение 16: 3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
[344] Соединение 17: 2,5-дифтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин;
[345] Соединение 18: 2,6-дифтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин;
[346] Соединение 19: 4-(5-этокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторфенил)метанамин;
[347] Соединение 20: 3-фтор-4-(5-изопропокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин;
[348] Соединение 21: 4-(5-(1,1-дифторэтил)-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин;
[349] Соединение 22: 4-(5-(1,1-дифторэтил)-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторфенил)метанамин;
[350] Соединение 23: 3-фтор-4-(5-фторметокси)-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин;
[351] Соединение 24: 4-(5-дифторметокси)-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторфенил)метанамин;
[352] Соединение 25: 7-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-1,2,3,4-тетрагидройзохинолин гидрохлорид;
[353] Соединение 26: 7-фтор-6-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-1,2,3,4-тетрагидройзохинолин гидрохлорид;
[354] Соединение 27: 8-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-2,3,4,5-тетрагидро-1Н-бензо[с]азепин гидрохлорид;
[355] Соединение 28: 4-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)-2,5-дифторфенил)метанамин;
[356] Соединение 29: 1-(изоиндолин-5-ил)-5,6-диметокси-1Н-бензо[d][1,2,3]триазол гидрохлорид;
[357] Соединение 30: 3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бицикло[1.1.1]пентан-1-ил)метанамин;
[358] Соединение 31: 3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-5-метилтиофен-2-ил)метанамин гидрохлорид;
[359] Соединение 32: трет-бутил-((4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)пиперидин-1-ил)сульфонил)карбамат;
[360] Соединение 33: трет-бутил-((4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)метил)пиперидин-1-ил)сульфонил)карбамат;
[361] Соединение 34: трет-бутил(N-(1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфонил)карбамат;
[362] Соединение 35: трет-бутил(N-(4-(4-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфонил)карбамат;
[363] Соединение 36: трет-бутил(N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфонил)карбамат;
[364] Соединение 37: трет-бутил(N-(4-(6-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфонил)карбамат;
[365] Соединение 38: трет-бутил(N-(4-(7-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфонил)карбамат;
[366] Соединение 39: трет-бутил((S)-N-(1-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)этил)сульфонил)карбамат;
[367] Соединение 40: трет-бутил-((6-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3,4-дигидроизохинолин-2 (1Н)-ил)сульфонил)карбамат;
[368] Соединение 41: N-((3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)циклопентил)метил)сульфамид;
[369] Соединение 42: 4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)пиперидин-1-сульфонамид;
[370] Соединение 43: N-((4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)циклогексил)метил)сульфамид;
[371] Соединение 44: 2-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)пиперидин-1-ил)этан-1 - сульфонамид;
[372] Соединение 45: 4-((5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)метил)пиперидин-1-сульфонамид;
[373] Соединение 46: N-(4-(1Н-бензо[d][1,2,3]триазол-1 ил)бензил)сульфамид;
[374] Соединение 47: N-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)сульфамид;
[375] Соединение 48: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)сульфамид гидрохлорид;
[376] Соединение 49: N-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[377] Соединение 50: N-(4-(4-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[378] Соединение 51: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид гидрохлорид;
[379] Соединение 52: N-(4-(6-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[380] Соединение 53: N-(4-(7-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[381] Соединение 54: N-(4-(4,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[382] Соединение 55: N-(4-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[383] Соединение 56: N-(4-(1Н-бензо[d][1,2,3]триазол-1-ил)3-фторбензил)сульфамид;
[384] Соединение 57: N-(4-(1Н-бензо[d][1,2,3]триазол-1-ил)2,3-дифторбензил)сульфамид;
[385] Соединение 58: N-(4-(1Н-бензо[d][1,2,3]триазол-1-ил)3,5-дифторбензил)сульфамид;
[386] Соединение 59: N-(3-хлор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[387] Соединение 60: N-(2-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[388] Соединение 61: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторбензил)сульфамид;
[389] Соединение 62: N-(2,5-дифтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[390] Соединение 63: N-(2,6-дифтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[391] Соединение 64: N-(3,5-дифтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-бензил)сульфамид;
[392] Соединение 65: N-(2,3-дифтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-бензил)сульфамид;
[393] Соединение 66: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3-метилбензил)сульфамид;
[394] Соединение 67: N-(3-циано-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3-бензил)сульфамид;
[395] Соединение 68: N-(3-метокси-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[396] Соединение 69: N-(4-(5-метокси-6-метил-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[397] Соединение 70: N-(3-фтор-4-(5-метокси-6-метил-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[398] Соединение 71: N-(4-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторбензил)сульфамид;
[399] Соединение 72: N-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенэтил)сульфамид;
[400] Соединение 73: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенэтил)сульфамид гидрохлорид;
[401] Соединение 74: N-(3-фтор-4-(5-гидрокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[402] Соединение 75: N-(3-фтор-4-(5-метил-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[403] Соединение 76: N-(4-(5-этокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторбензил)сульфамид;
[404] Соединение 77: N-(3-фтор-4-(5-изопропокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[405] Соединение 78: N-(5-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)пиридин-2-ил)метил)сульфамид;
[406] Соединение 79: (N-(6-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)пиридин-3-ил)метил)сульфамид;
[407] Соединение 80: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)-N-метил)сульфамид;
[408] Соединение 81: N-(3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)-N-метил сульфамид;
[409] Соединение 82: N-циклопропил-N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[410] Соединение 83: (S)-N-(1-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)этил)сульфамид;
[411] Соединение 84: N-(4-(5-трифторметил)-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[412] Соединение 85: N-(3-фтор-4-(5-трифторметил)-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[413] Соединение 86: 4-(5-(1,1-дифторэтил)-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метан амин;
[414] Соединение 87: N-(4-(5-диметиламино)-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторбензил)сульфамид;
[415] Соединение 88: N-(3-фтор-4-(5-фторметокси)-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[416] Соединение 89: N-(4-(5-трифторметокси)-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[417] Соединение 90: N-(3-фтор-4-(5-трифторметокси)-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[418] Соединение 91: N-(4-(5-дифторметокси)-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторбензил)сульфамид;
[419] Соединение 92: N-(4-(6-фтор-5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[420] Соединение 93: N-(3-фтор-4-(6-фтор-5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[421] Соединение 94: 5-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)изоиндолин-2-сульфон амид;
[422] Соединение 95: N-5-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-2,3-дигидро-1Н-инден-2-ил)сульфамид;
[423] Соединение 96: 6-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3,4-дигидроизохинолин-2(1Н)сульфонамид;
[424] Соединение 97: 7-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3,4-дигидроизохинолин-2(1Н)сульфонамид;
[425] Соединение 98: 8-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-1,3,4,5-тетрагидро-2Н-бензо[с]азепин-2-сульфонамид;
[426] Соединение 99: N-(4-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)-2,5-дифторбензил)сульфамид;
[427] Соединение 100: N-(4-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)-2,6-дифторбензил)сульфамид;
[428] Соединение 101: 7-фтор-6-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3,4-дигидроизохинолин-2 (1Н)-сульфонамид;
[429] Соединение 102: 5-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)-изоиндолин-2-сульфонамид;
[430] Соединение 103: N-(5-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)-дигидро-1Н-инден-2 -ил)сульфамид;
[431] Соединение 104: N-(4-((5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)метил)фенил)сульфамид гидрохлорид;
[432] Соединение 105: N-(4-((5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)метил)бензил)сульфамид гидрохлорид;
[433] Соединение 106: N-((5-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)тиофен-2-ил)метил)сульфамид;
[434] Соединение 107: N-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-5-метоксилтиофен-2-ил)метил)сульфамид;
[435] Соединение 108: N-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-бицикло[1.1.1]пентан-1-ил)сульфамид;
[436] Соединение 109: N-(4-(5-метокси-2Н-бензо[d][1,2,3]триазол-2-ил)фенил)сульфамид гидрохлорид;
[437] Соединение 110: N-(4-((5-метокси-2Н-бензо[d][1,2,3]триазол-2-ил)бензил)сульфамид гидрохлорид;
[438] Соединение 111: 2-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)пиперидин-1-ил)этан-1-сульфонилфторид;
[439] Соединение 112: N-(3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)метансульфонамид;
[440] Соединение 113: N-(3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)этансульфонамид;
[441] Соединение 114: N-(3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)-4-метилбензолсульфонамид;
[442] Соединение 115: N-(3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)метансульфонимидамид;
[443] Соединение 116: 3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензойная кислота;
[444] Соединение 117: диэтил-(3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)фосфоамидит;
[445] Соединение 118: 4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)фосфоновая кислота;
[446] Соединение 119: 4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)фосфоновая кислота;
[447] Соединение 120: 3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)бороновая кислота;
[448] Соединение 121: 4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенэтил)бороновая кислота;
[449] Соединение 122: N-(4-(5-метокси-1Н-индол-1-ил)бензил)сульфамид;
[450] Соединение 123: N-(4-(5-метокси-1Н-бензо[d]имидазол-1-ил)бензил)сульфамид; и
[451] Соединение 124: N-(4-(5-метокси-1Н-индазол-1-ил)бензил)сульфамид.
[452]
[453] Соединение формулы 1 по настоящему изобретению может быть использовано в форме фармацевтически приемлемой соли, полученной из неорганической или органической кислоты, и соль предпочтительно включает по меньшей мере одну, выбранную из группы, состоящей из соляной кислоты, бромистоводородной кислоты, серной кислоты, фосфорной кислоты, азотной кислоты, уксусной кислоты, гликолевой кислоты, молочной кислоты, пировиноградной кислоты, малоновой кислоты, янтарной кислоты, глутаровой кислоты, фумаровой кислоты, яблочной кислоты, миндальной кислоты, винной кислоты, лимонной кислоты, аскорбиновой кислоты, пальмитиновой кислоты, малеиновой кислоты, гидроксималеиновой кислоты, бензойной кислоты, гидроксибензойной кислоты, фенилуксусной кислоты, коричной кислоты, салициловой кислоты, метансульфоновой кислоты, бензолсульфоновой кислоты и толуолсульфоновой кислоты.
[454] Соединение формулы 1 по настоящему изобретению или его фармацевтически приемлемая соль могут включать гидрат и сольват. Гидрат может быть образован путем связывания соединения формулы 1 с молекулой воды.
[455] В другом аспекте настоящее изобретение предлагает фармацевтическую композицию для профилактики, облегчения или лечения рака, содержащую соединение в соответствии с одним аспектом настоящего изобретения в качестве активного ингредиента.
[456] В другом аспекте настоящее изобретение предлагает ингибитор ENPP 1, содержащий соединение в соответствии с одним аспектом настоящего изобретения в качестве активного ингредиента.
[457] В другом аспекте настоящее изобретение предлагает активатор сигнального пути STING, содержащий соединение в соответствии с одним аспектом настоящего изобретения в качестве активного ингредиента.
[458] В другом аспекте настоящее изобретение предлагает фармацевтическую композицию для профилактики, облегчения или лечения рака, где рак связан с ингибированием ENPP 1.
[459]
[460] В другом аспекте настоящее изобретение предлагает фармацевтическую композицию для профилактики, облегчения или лечения рака, содержащую соединение в соответствии с настоящим изобретением, выбранное из соединения формулы 1, его фармацевтически приемлемой соли, его гидрата или его стереоизомера в качестве активного ингредиента.
[461] Фармацевтическая композиция по настоящему изобретению обладает превосходной способностью ингибировать активность ENPP 1.
[462] Соответственно, фармацевтическая композиция настоящего изобретения может использоваться для лечения, профилактики и облегчения раковых заболеваний, вызванных аномальным клеточным ростом. Раковые заболевания, которые могут быть предотвращены, вылечены или облегчены введением фармацевтической композиции по настоящему изобретению, включают рак желудка, рак легких, рак печени, колоректальный рак, рак тонкой кишки, рак поджелудочной железы, рак головного мозга, рак костей, меланому, рак молочной железы, фиброзное уплотнение, рак матки, рак шейки матки, рак головы и шеи, рак пищевода, рак щитовидной железы, рак паращитовидных желез, рак почки, саркому, рак предстательной железы, рак уретры, рак мочевого пузыря, рак крови (включая лейкоз, множественную миелому, миелодиспластический синдром), лимфому (включая болезнь Ходжкина и неходжкинскую лимфому), псориаз и фиброаденому.
[463] В другом аспекте настоящее изобретение предлагает ингибитор ENPP 1, содержащий любое из описанных выше соединений в качестве активного ингредиента.
[464] В другом аспекте настоящее изобретение предлагает активатор сигнального пути STING, содержащий любое из описанных выше соединений в качестве активного ингредиента.
[465] Фармацевтическая композиция может быть применена к экспериментальным животным, таким как мыши, кролики, крысы, морские свинки или хомяки, предпочтительно к приматам, включая людей, более предпочтительно к людям, без ограничения перечисленным.
[466] Используемый в настоящем описании термин «лечение» включает облегчение или ослабление симптомов, уменьшение распространенности заболевания, задержку или облегчение прогрессирования заболевания, уменьшение, облегчение или стабилизацию болезненного состояния, частичное или полное выздоровление, продление выживаемости и другие благоприятные результаты лечения.
[467] Кроме того, в данном описании лечение рака означает лечение всех раковых клеток, и рак включает ангиогенез эндотелиальных клеток и их митоз (солидные опухоли, метастазы опухолей и доброкачественные опухоли). Например, рак включает, без ограничения, рак молочной железы, рак яичников, рак шейки матки, рак предстательной железы, рак яичка, рак мочеполовой системы, рак пищевода, рак гортани, глиобластому, рак желудка, рак кожи, кератоакантомы, рак легких, сквамозно-клеточную карциному, крупноклеточную карциному, мелкоклеточную карциному, аденокарциному легкого, рак костей, рак толстой кишки, аденому, рак поджелудочной железы, аденокарциному, канцерогенный рак, фолликулярную карциному, недифференцированный рак, папиллярный рак, нормальную гематому, меланому, саркому, рак мочевого пузыря, рак печени, рак желчных протоков, рак почки, миелоидные заболевания, лимфоидные заболевания, болезнь Ходжкина, рак волосковых клеток, рак полости рта, фарингеальный (оральный) рак, рак губ, рак языка, рак тонкой кишки, колоректальный рак, рак толстой кишки, рак прямой кишки, рак головного мозга, рак центральной нервной системы, лейкоз, гемангиому, трахому и гнойную саркому.
[468] Содержание активного ингредиента, а именно соединения, представленного формулой 1, его фармацевтически приемлемой соли, его гидрата или его сольвата соответствующим образом регулируют путем выбора специалистами в данной области в зависимости от режима применения и способа применения фармацевтической композиции настоящего изобретения.
[469] Например, фармацевтическая композиция содержит соединение, представленное формулой 1, его фармацевтически приемлемую соль, его гидрат, или его сольват в количестве 0,1-10% масс., более предпочтительно 0,5-5% масс., в расчете на общую массу фармацевтической композиции.
[470] Соединение, представленное формулой 1, его фармацевтически приемлемая соль, его гидрат или его сольват может присутствовать отдельно или в комбинации с фармакологически приемлемым носителем, эксципиентом, разбавителем или дополнительным ингредиентом в фармацевтической композиции.
[471] Например, фармацевтически приемлемый носитель, эксципиент и разбавитель включают, без ограничения, одно или более, выбранное из группы, состоящей из лактозы, декстрозы, сахарозы, сорбита, маннита, ксилита, эритрита, мальтита, крахмала, гуммиарабика, альгината, желатина, фосфата кальция, силиката кальция, целлюлозы, метилцеллюлозы, микрокристаллической целлюлозы, поливинилпирролидона, воды, метилгидроксибензоата, пропилгидроксибензоата, талька, стеарата магния, минерального масла, декстрина, карбоната кальция, пропиленгликоля, жидкого парафина и физиологического раствора, и может использоваться обычный носитель, эксципиент или разбавитель. В дополнение к этому, фармацевтическая композиция может также включать традиционный наполнитель, сухой разбавитель, связующее, разрыхлитель, антикоагулянт, скользящее вещество, увлажняющее средство, регулятор кислотности, питательное вещество, витамин, электролит, альгиновую кислоту или ее соль, пектиновую кислоту или ее соль, защитный коллоид, глицерин, ароматизатор, эмульгатор, консервант или тому подобное.
[472] При введении в комбинации с другим противоопухолевым лекарственным средством для лечения рака или опухолей соединение, представленное формулой 1, или его фармацевтически приемлемая соль могут проявлять синергический терапевтический эффект с противоопухолевым лекарственным средством.
[473] В частности, фармацевтическая композиция может дополнительно включать по меньшей мере один другой противораковый агент или терапевтический агент, который, как известно, эффективен для лечения или профилактики рака, в дополнение к активному ингредиенту, и соответственно, может использоваться в качестве одновременно или отдельно применяемой комбинированной терапии. Другие противораковые агенты или терапевтические агенты, которые могут применяться для комбинированной терапии, могут включать, например, по меньшей мере одно соединение, выбранное из группы, включающей Gleevec® (иматиниб), Sutent® (сунитиниб), Herceptin® (трастузумаб), Velcade® (бортезомиб), дексаметазон, Nexavar® (сорафениб), ингибиторы ароматазы и ингибиторы киназы, без ограничения перечисленным.
[474] Фармацевтическая композиция может вводиться перорально или парентерально, и, например, может вводиться различными путями, включая пероральный, трансдермальный, подкожный, внутривенный или внутримышечный. Кроме того, лекарственная форма композиции может варьировать в зависимости от способа применения и может быть приготовлена с использованием способов, хорошо известных в данной области, для обеспечения быстрого, пролонгированного или отсроченного высвобождения активного ингредиента после введения млекопитающим. Как правило, твердые препараты для перорального применения включают таблетки, драже, мягкие или твердые капсулы, пилюли, порошки, гранулы и тому подобное. Эти препараты могут быть приготовлены, например, путем смешивания крахмала, карбоната кальция, сахарозы, лактозы, желатина или тому подобного. Кроме того, также могут использоваться скользящие вещества, такие как стеарат магния и тальк, в дополнение к простым эксципиентам. Жидкие препараты для перорального введения включают суспензии, жидкости и растворы, эмульсии, сиропы и тому подобное. В дополнение к воде и жидкому парафину, которые являются обычными простыми разбавителями, могут быть включены различные эксципиенты, такие как смачивающие агенты, подсластители, ароматизаторы и консерванты. Лекарственные формы для парентерального введения включают кремы, лосьоны, мази, гипс, жидкости и растворы, аэрозоли, жидкие экстракты, эликсиры, настои, саше, пластыри, инъекционные растворы и тому подобное. Инъекционные лекарственные формы предпочтительно представляют собой изотонический водный раствор или суспензию.
[475] Фармацевтическая композиция может дополнительно включать адъювант, такой как стерилизатор, консервант, стабилизатор, увлажняющий агент или ускоритель эмульгирования, соль и/или буфер для регулирования осмотического давления и другие терапевтически полезные вещества. В качестве альтернативы, фармацевтическая композиция может быть приготовлена в соответствии с обычным способом смешивания, грануляции или покрытия оболочкой, или с использованием подходящего способа, известного в данной области.
[476] Кроме того, дозировка фармацевтической композиции может быть определена с учетом способа введения, возраста, пола, тяжести заболевания и состояния пациента, скорости всасывания активного ингредиента в организме и скорости инактивации активного ингредиента и лекарственных средств, используемых с ним в комбинации, и фармацевтическую композицию можно вводить однократно или многократно порциями. Активный ингредиент фармацевтической композиции предпочтительно вводится перорально или парентерально млекопитающему, включая человека, в количестве 0,001-100 мг/кг массы тела, предпочтительно 0,01-35 мг/кг массы тела, ежедневно, и может вводиться однократно или разделяться на несколько приемов в течение дня.
[477] В другом аспекте настоящее изобретение предлагает способ лечения рака, предусматривающий введение терапевтически эффективного количества соединения, представленного формулой 1, его фармацевтически приемлемой соли или его гидрата.
[478] Предпочтительно, способ лечения может дополнительно включать выявление пациента, нуждающегося в профилактике или лечении рака, до введения препарата.
[479] Используемый в настоящем описании термин «терапевтически эффективное количество» означает количество активного ингредиента, которое эффективно для профилактики или лечения рака у млекопитающего, и терапевтически эффективное количество может контролироваться различными факторами, такими как тип заболевания, тяжесть течения заболевания, тип и содержание активного ингредиента и других ингредиентов, содержащихся в композиции, тип композиции, возраст, вес, общее состояние здоровья, пол и диета пациента, время введения, путь введения, скорость выведения композиции из крови, продолжительность лечения и лекарственные средства, применяемые одновременно с этим. Предпочтительно, как описано выше, соединение может быть введено в количестве 0,001-100 мг/кг массы тела, предпочтительно 0,01-35 мг/кг массы тела, ежедневно, однократно или несколько pаз в день порциями, пероральным или парентеральным путями.
[480] В другом аспекте настоящее изобретение предлагает способ получения соединения, выбранного из производного соединения бензотриазола, представленного формулой 1, его фармацевтически приемлемой соли, его гидрата и его стереоизомера.
[481] В то же время настоящее изобретение предлагает способ получения производного соединения бензотриазола, представленного формулой 1. Способ получения по настоящему изобретению будет описан подробно далее.
[482]
[483] В одном варианте осуществления соединение, представленное формулой 1 по настоящему изобретению, может быть получено по меньшей мере одним из следующих способов получения с 1 по 3.
[484] Способ получения 1
[485] Производное соединение бензотриазола формулы 1 согласно одному аспекту настоящего изобретения может быть получено в соответствии со способом получения на основе следующей схемы реакции 1.
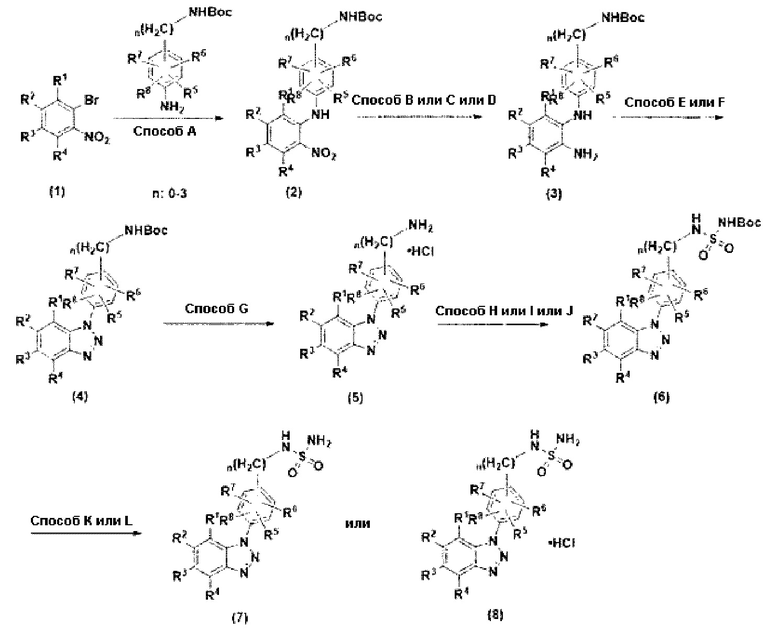
[486]
[487] [Схема реакции 1]
[488]
[489] Способ получения 2
[490] Производное соединение бензотриазола формулы 1 согласно одному аспекту настоящего изобретения может быть получено в соответствии со способом получения на основе следующей схемы реакции 2.
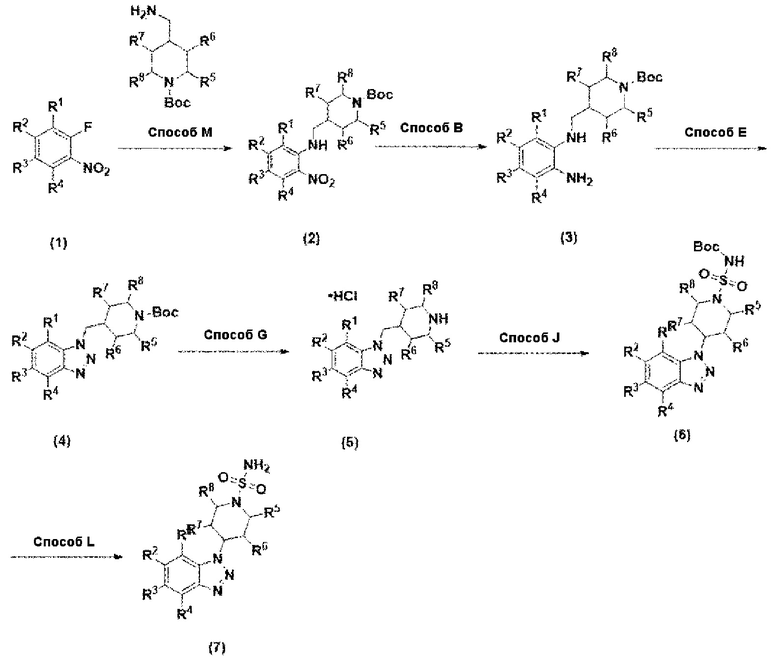
[491]
[492] [Схема реакции 2]
[493]
[494] Способ получения 3
[495] Производное соединение бензотриазола формулы 1 согласно одному аспекту настоящего изобретения может быть получено в соответствии со способом получения на основе следующей схемы реакции 3.
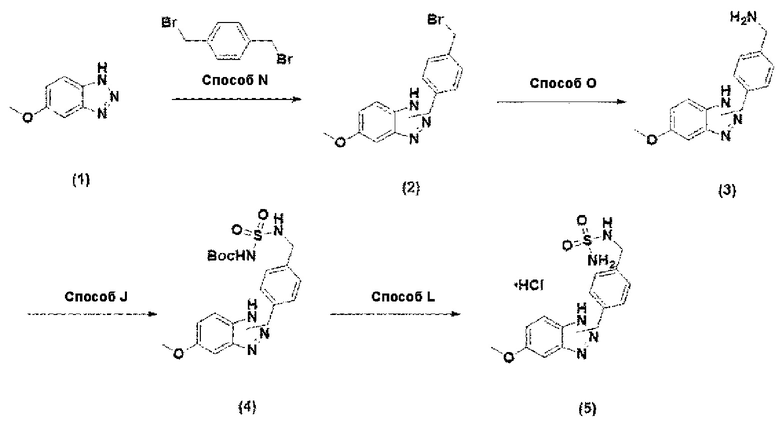
[496]
[497] [Схема реакции 3]
[498]
[499] Способ А
[500] После удаления воздуха из колбы, высушенной в печи и продутой газообразным азотом, в колбу добавляли Pd2(dba)3 (0,05 экв.), рац-BINAP (0,1 экв.), Cs2CO3 (5 экв.), бромнитробензол (1 экв.), анилин (1,05 экв.) и дегазированный толуол. Газообразный азот добавляли в реакционную смесь в течение 15 мин, с последующим нагреванием при 110°С в течение 14 ч. Смешанному раствору давали возможность остыть до комнатной температуры, разбавляли этилацетатом, фильтровали через целит и промывали насыщенным солевым раствором. Органический слой сушили над безводным сульфатом магния, фильтровали и упаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (н-гексан/этилацетат) с использованием ЖХСД для получения целевого соединения с высоким выходом.
[501]
[502] Способ В
[503] Pd/C (10%, 50% влажности, 0,05 экв.) добавляли к раствору нитроинтермедиата (1 экв.) в метаноле, после чего перемешивали при комнатной температуре в присутствии газообразного водорода в течение 12 ч. Реакционную смесь отфильтровывали через целит и затем концентрировали для получения целевого соединения с высоким выходом.
[504]
[505] Способ С
[506] Порошок железа (5 экв.) и водный раствор хлорида аммония (10 экв.) добавляли к раствору нитроинтермедиата (1 экв.) в этаноле. Реакционный раствор перемешивали при 65°С в течение 2 ч. Реакционный раствор фильтровали через целит, добавляли к нему водный раствор бикарбоната натрия и полученную смесь трижды экстрагировали этилацетатом. Органический слой сушили над безводным сульфатом магния и упаривали при пониженном давлении для получения целевого соединения с высоким выходом.
[507]
[508] Способ D:
[509] Порошок железа (5 экв.) и водный раствор хлорида аммония (10 экв.) добавляли к раствору нитроинтермедиата (1 экв.) в этаноле. Реакционный раствор перемешивали при 65°С в течение 2 ч. Реакционный раствор фильтровали через целит, добавляли к нему водный раствор бикарбоната натрия и полученную смесь трижды экстрагировали этилацетатом. Органический слой сушили над безводным сульфатом магния и упаривали при пониженном давлении для получения целевого соединения с высоким выходом.
[510]
[511] Способ Е:
[512] Водный раствор нитрита натрия (2 экв.) медленно добавляли при 0°С к раствору анилинового интермедиата (1 экв.) в уксусной кислоте, после чего перемешивали при комнатной температуре в течение 12 ч. Реакционную смесь концентрировали при пониженном давлении, туда добавляли водный раствор гидрокарбоната натрия, и полученную смесь экстрагировали этилацетатом трижды. Органический слой промывали насыщенным солевым раствором, сушили над безводным сульфатом магния и упаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (н-гексан/этилацетат) с использованием ЖХСД для получения целевого соединения.
[513]
[514] Способ F
[515] Водный раствор нитрита натрия (2 экв.) медленно добавляли при 0°С к раствору анилинового интермедиата (1 экв.) в уксусной кислоте, после чего перемешивали при комнатной температуре в течение 12 ч. Реакционный раствор концентрировали при пониженном давлении, туда добавляли водный раствор гидрокарбоната натрия, и полученную смесь экстрагировали этилацетатом трижды. Органический слой промывали насыщенным солевым раствором, сушили над безводным сульфатом магния и упаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (н-гексан/этилацетат) с использованием ЖХСД для получения целевого соединения.
[516]
[517] Способ G
[518] Избыток 4 н. водного раствора соляной кислоты (в диоксане) добавляли в раствор Boc-защищенного амина или анилинового интермедиата в этилацетате, после чего перемешивали при комнатной температуре в течение 4 ч. Реакционную смесь концентрировали при пониженном давлении и промывали дихлорметаном для получения заданного количества целевого соединения в виде гидрохлоридной соли.
[519]
[520] Способ Н
[521] Амингидрохлоридный интермедиат (1 экв.), полученный с помощью способа G, растворяли в дихлорметане и добавляли к нему триэтиламин (8 экв.) при 0°С в атмосфере азота. Раствор трет-бутил(хлорсульфонил)карбамата (8 экв.) в дихлорметане добавляли в реакционный раствор, после чего перемешивали при комнатной температуре в течение 3 ч. Реакционную смесь концентрировали при пониженном давлении, разбавляли водным раствором бикарбоната натрия и трижды экстрагировали этилацетатом. Органический слой промывали насыщенным солевым раствором, сушили над безводным сульфатом магния и упаривали при пониженном давлении. Остаток очищали посредством колоночной хроматографии на силикагеле (н-гексан/этилацетат) с использованием ЖХСД для получения целевого соединения.
[522]
[523] Способ I:
[524] DMAP (2 экв.) добавляли в водный раствор анилингидрохлорида (1 экв.) в ацетонитриле при 0°С в атмосфере азота. Раствор трет-бутил(хлорсульфонил)карбамата (2 экв.) в дихлорметане добавляли к реакционной смеси, после чего перемешивали при комнатной температуре в течение 3 ч. Реакционную смесь концентрировали при пониженном давлении, разбавляли водным раствором бикарбоната натрия и трижды экстрагировали этилацетатом. Органический слой промывали насыщенным солевым раствором, сушили над безводным сульфатом магния и упаривали при пониженном давлении. Остаток очищали посредством колоночной хроматографии на силикагеле (н-гексан/этилацетат) с использованием ЖХСД для получения целевого соединения.
[525]
[526] Способ J:
[527] Трет-бутанол медленно добавляли при 0°С к раствору хлорсульфонилизоцианата в безводном дихлорметане. Через 30 мин смешанный раствор медленно добавляли при 0°С к раствору амингидрохлоридного интермедиата в безводном дихлорметане в присутствии триэтиламина, после чего перемешивали при комнатной температуре в течение 2 ч. Реакционную смесь разбавляли дихлорметаном и промывали 0,1 н. водным раствором соляной кислоты и водой. Органический слой сушили над безводным сульфатом магния и упаривали при пониженном давлении. Остаток очищали посредством колоночной хроматографии на силикагеле с использованием ЖХСД для получения целевого соединения.
[528]
[529] Способ K
[530] Избыток 4 н. водного раствора соляной кислоты (в диоксане) добавляли в раствор Boc-защищенного сульфонамидного интермедиата (1 экв.) в этилацетате, после чего перемешивали при комнатной температуре в течение 4 ч. Реакционную смесь концентрировали при пониженном давлении, разбавляли водным раствором гидрокарбоната натрия и трижды экстрагировали этилацетатом. Органический слой промывали насыщенным солевым раствором, сушили над безводным сульфатом магния и упаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с использованием ЖХСД для получения целевого соединения.
[531]
[532] Способ L
[533] Избыток 4 н. водного раствора соляной кислоты (в диоксане) добавляли к Boc-защищенному сульфонамидному интермедиату (1 экв.), после чего перемешивали при комнатной температуре в течение 4-12 ч. Реакционную смесь концентрировали при пониженном давлении, промывали этилацетатом и затем метанолом, и сушили с получением целевого соединения в виде гидрохлорида.
[534]
[535] Способ М
[536] Нитрофторбензол, N-Boc-пиперидин-4-илметанамин и карбонат калия растворяли в DMSO, после чего перемешивали при комнатной температуре в течение 16 ч. Реакционную смесь разбавляли водой и экстрагировали этилацетатом. Органический слой промывали насыщенным солевым раствором, сушили над безводным сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с использованием ЖХСД для получения целевого соединения.
[537]
[538] Способ N
[539] Водный раствор NaOH (1,1 экв.) добавляли к раствору 5-метокси-1Н-бензо[d][1,2,3]триазола (1 экв.) в ацетонитриле. 1,4-бис(бромэтил)бензол (1,1 экв.) добавляли к смешанному раствору, после чего перемешивали при комнатной температуре в течение 3 ч. Реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой сушили над безводным сульфатом магния и растворитель концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле с использованием ЖХСД (этилацетат/гексан), с получением двух структурных изомеров с высоким выходом.
[540]
[541] Способ О
[542] Азид натрия (3 экв.) добавляли к раствору а бензилбромидного интермедиата (1 экв.) в ацетонитриле, после чего перемешивали при 75°С в течение 16 ч. Реакционную смесь экстрагировали этилацетатом и водным раствором гидрокарбоната натрия. Органический слой сушили над безводным сульфатом магния и концентрировали при пониженном давлении, с получением неочищенного азидного интермедиата с высоким выходом. Трифенилфосфин (2 экв.) медленно добавляли при 0°С к раствору азидного интермедиата (1 экв.) в тетрагидрофуране. К ним добавляли воду, после чего перемешивали при 70°С в течение 12 ч. Растворитель концентрировали при пониженном давлении и добавляли к нему раствор соляной кислоты в диоксане для получения целевого соединения с высоким выходом.
Вариант осуществления изобретения
[543] Далее настоящее изобретение будет описано более подробно со ссылкой на примеры синтеза, примеры получения, примеры, экспериментальные примеры и примеры композиций. Однако приведенные ниже примеры синтеза, примеры получения, примеры, экспериментальные примеры и примеры композиций приведены только для иллюстрации и не должны рассматриваться как ограничивающие объем настоящего изобретения.
[544]
[545] [Пример получения 1] Получение соединения 47
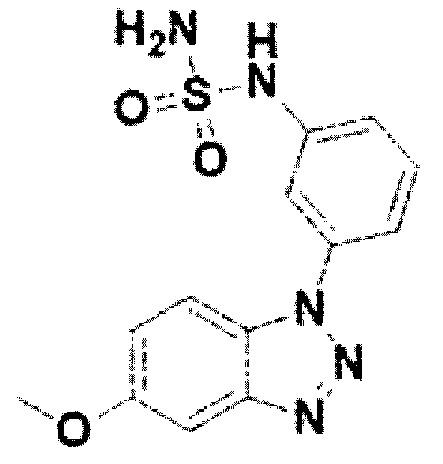
[546]
[547] Пример получения 1:
[548] [Схема реакции 1]
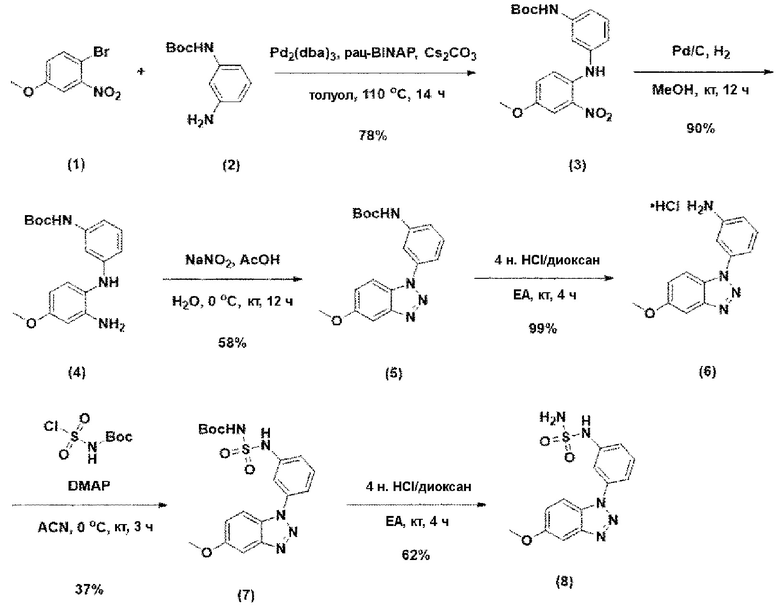
[549]
[550] трет-бутил(3-((4-метокси-2-нитрофенил)амино)фенил)карбамат (3)
[551]
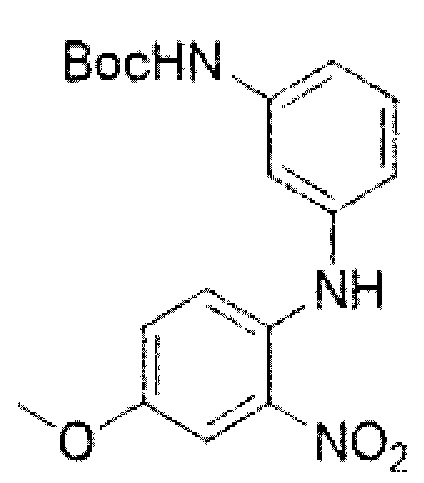
[552] Смесь 1-бром-4-метокси-2-нитробензола (1,16 г, 5 ммоль), трет-бутил-(3-аминофенил)карбамата (1,9 г, 5,25 ммоль), Pd2(dba)3 (229 мг, 0,25 ммоль), рац-BINAP (311 мг, 0,5 ммоль), и Cs2CO3 (8,15 г, 25 ммоль) в толуоле (17 мл, 0,3 М) продували газообразным азотом в течение 15 мин. Реакционный раствор нагревали и перемешивали при 110°С в течение 14 ч в присутствии газообразного азота. Реакционному раствору давали возможность остыть до комнатной температуры, разбавляли этилацетатом, фильтровали через целит и промывали насыщенным солевым раствором. Органический слой сушили над безводным сульфатом магния, концентрировали и очищали посредством колоночной хроматографии с использованием ЖХСД с получением целевого соединения (1,40 г) с выходом 78%.
[553]
[554] 1Н ЯМР (400 МГц, CDCl3) δ 9,31 (ушир.с, 1Н), 7,66 (д, J=3,2 Гц, 1Н), 7,45 (д, J=2,2 Гц, 1Н), 7,36-7,25 (м, 2Н), 7,18-7,02 (м, 2Н), 7,01-6,88 (м, 1Н), 6,53 (с, 1Н), 3,86 (с, 3Н), 1,61-1,49 (м, 9Н).
[555]
[556] трет-бутил-(3-((2-амино-4-метоксифенил)амино)фенил)карбамат (4)
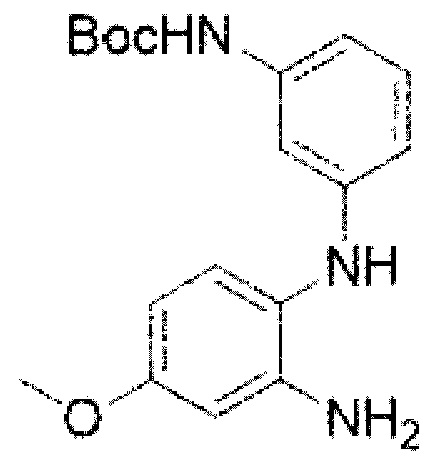
[557]
[558]
[559] Pd/C (10%, 50% влажности, 480 мг, 0,22 ммоль) добавляли к раствору трет-бутил(3-((4-метокси-2-нитрофенил)амино)фенил)карбамата (1,60 г, 4,45 ммоль) в метаноле (15 мл, 0,3 М), после чего перемешивали при комнатной температуре в течение 12 ч в присутствии газообразного водорода. Реакционный раствор отфильтровывали через целит и затем концентрировали с получением целевого соединения (1,32 г) с выходом 90%.
[560]
[561] 1Н ЯМР (400 МГц, CDCl3) δ 7, 29 (с, 1Н), 7,15-7,05 (м, 2Н), 6,94-6,83 (м, 1Н), 6,81 (ушир.с, 1Н), 6,66 (ушир.с, 1Н), 6,64-6,56 (м, 1Н), 6,50 (с, 1Н), 3,66 (с, 3Н), 1,39 (с, 9Н).
[562]
[563] трет-бутил-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)карбамат (5)
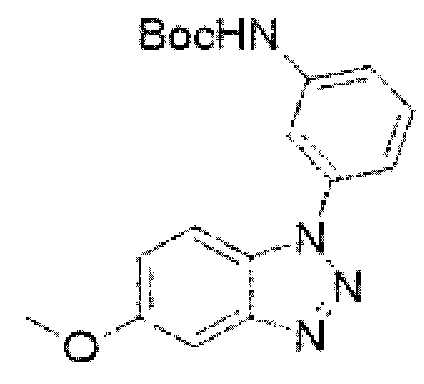
[564]
[565]
[566] Водный раствор нитрита натрия (544 мг, 7,89 ммоль) медленно добавляли при 0°С к раствору трет-бутил-(3-((2-амино-4-метоксифенил)амино)фенил) карбамата (1,30 г, 3,95 ммоль) в уксусной кислоте (13,2 мл, 0,3 М), после чего перемешивали при комнатной температуре в течение 12 ч. Реакционный раствор концентрировали при пониженном давлении, туда добавляли водный раствор гидрокарбоната натрия, и полученную смесь экстрагировали этилацетатом трижды. Органический слой промывали насыщенным солевым раствором, сушили над безводным сульфатом магния и упаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (н-гексан/этилацетат) с использованием ЖХСД для получения целевого соединения (780 мг) с выходом 58%.
[567]
[568] 1H ЯМР (400 МГц, CDCl3) δ 7,94 (с, 1Н), 7,62 (д, J=9,0 Гц, 1Н), 7,45-7,31 (м, 4Н), 7,15 (дд, J=2,3, 9,2 Гц, 1Н), 6,93 (с, 1Н), 3,85 (с, 3Н), 1,46 (с, 9Н).
[569]
[570] 3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)анилин гидрохлорид (6)
[571]
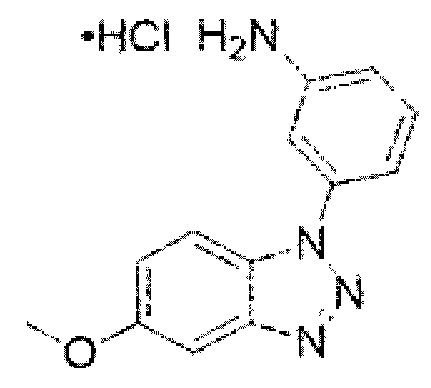
[572]
[573] Избыток 4 н. водного раствора соляной кислоты (в диоксане) добавляли к раствору трет-бутил-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)карбамата (800 мг, 2,35 ммоль) в этилацетате (2,35 мл, 1 М), после чего перемешивали в течение 4 ч. Реакционный раствор концентрировали при пониженном давлении, и остаток промывали дихлорметаном и сушили с получением целевого соединения в виде гидрохлоридной соли с выходом 99% (645 мг).
[574]
[575] трет-бутил(N-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)сульфамоил)карбамат (7)
[576]
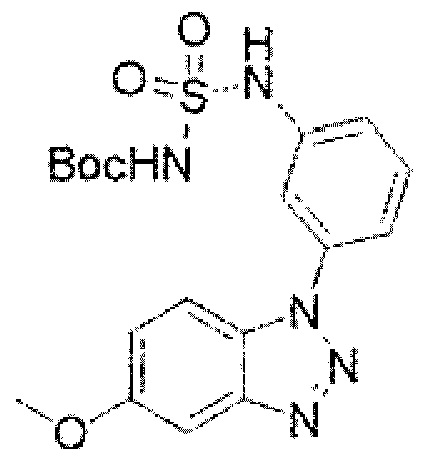
[577]
[578] DMAP (123 мг, 1 ммоль) добавляли при 0°С к раствору 3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)анилина гидрохлорида (139 мг, 0,5 ммоль) в ацетонитриле (2,5 мл, 0,2 М) в присутствии газообразного азота. Раствор трет-бутил(хлорсульфонил)карбамата (432 мг, 1 ммоль) в ацетонитриле медленно добавляли в смешанный раствор, после чего перемешивали в течение 3 ч. Растворитель концентрировали при пониженном давлении, разбавляли водным раствором бикарбоната натрия и трижды экстрагировали этилацетатом. Органический слой промывали насыщенным солевым раствором и сушили над безводным сульфатом магния, и растворитель упаривали при пониженном давлении. Остаток очищали посредством колоночной хроматографии на силикагеле (н-гексан/этилацетат) с использованием ЖХСД для получения целевого соединения (78 мг) с выходом 37%.
[579]
[580] 1Н ЯМР (400 МГц, Метанол-d4) δ 7,81 (д, J=9,1 Гц, 1Н), 7,78 (р, J=1,0 Гц, 1Н), 7,67-7,60 (м, 2Н), 7,49 (д, J=2,3 Гц, 1Н), 7,42 (с, 1Н), 7,32 (дд, J=9,1, 2,3 Гц, 1Н), 3,96 (с, 3Н), 1,39 (с, 9Н).
[581]
[582] N-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)сульфамид (8)
[583]
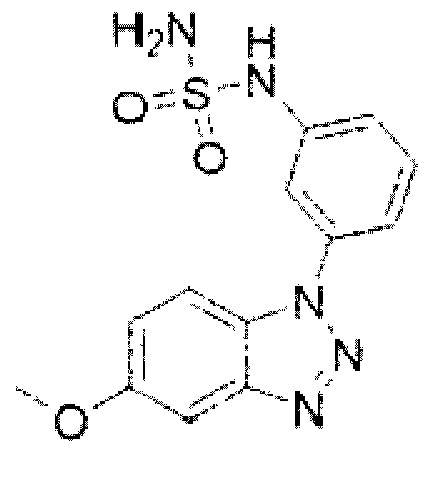
[584]
[585] Избыток 4 н. водного раствора соляной кислоты (в диоксане) добавляли к раствору трет-бутил(N-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)сульфамоил)карбамата (70 мг, 0,17 ммоль) в этилацетате (1,7 мл, 0,1 М), после чего перемешивали при комнатной температуре в течение 4 ч. Реакционный раствор концентрировали при пониженном давлении, разбавляли водным раствором бикарбоната натрия и трижды экстрагировали этилацетатом. Органический слой промывали насыщенным солевым раствором и сушили над безводным сульфатом магния, и растворитель упаривали при пониженном давлении. Остаток очищали посредством колоночной хроматографии на силикагеле (н-гексан/этилацетат) с использованием ЖХСД для получения целевого соединения (33 мг) с выходом 62%.
[586] 1H ЯМР (400 МГц, ДМСО-d6) δ 9,96 (с, 1Н), 7,82 (д, J=9,0 Гц, 1Н), 7,68 (т, J=2,0 Гц, 1Н), 7,63 (д, J=2,4 Гц, 1Н), 7,59 (т, J=7,9 Гц, 1Н), 7,52-7,47 (м, 1Н), 7,41-7,23 (м, 4Н), 3,91 (с, 3Н).
[587]
[588] Соединения следующих примеров синтезировали со ссылкой на пример получения 1 и схемы реакции 1-4, описанные выше.
[589]
[590] Пример 1: 5-метокси-1-(пиперидин-4-ил)-1Н-бензо[d][1,2,3]триазол гидрохлорид;
[591]
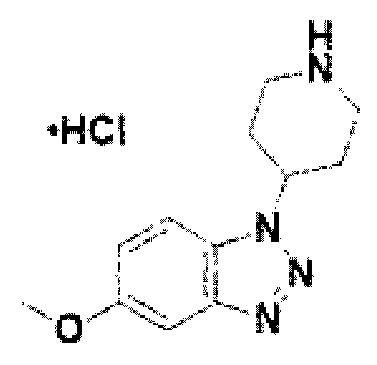
[592] ЖХМС (ESI) рассчитано для C12H16N4O [М+Н]+ 232,12, найдено m/z 233,1
[593]
[594] Пример 2: 4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)циклогексил)метананилин;
[595]
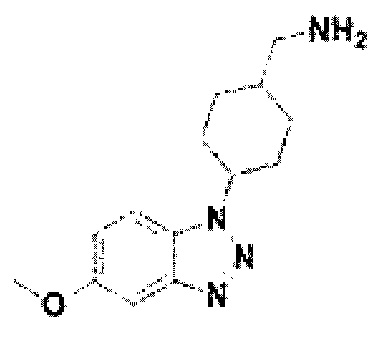
[596] 1H ЯМР (400 МГц, ДМСО-d6) δ 7,83 (м, 2Н), 7,46 (д, J=2,1 Гц, 1Н), 7,18 (дд, J=9,0, 2,2 Гц, 1Н), 4,95 (с, 1Н), 3,85 (с, 3Н) 2,90 (д, 1Н), 2,17 (S, 2Н), 1,97 (с, 3Н), 1,74 (с, 3Н), 1,24 (с, 2Н).
[597]
[598] Пример 3: 5-метокси-1-(пиперидин-4-илметил)-1Н-бензо[d][1,2,3]триазол;
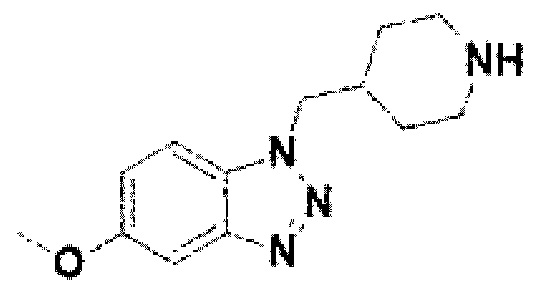
[599]
[600] ЖХМС (ESI) рассчитано для C13H18N4O [М+Н]+ 246,15, найдено m/z 247,2
[601]
[602] Пример 4: 4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)анилин гидрохлорид;
[603]
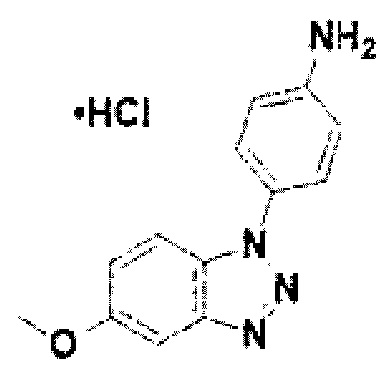
[604] ЖХМС (ESI) рассчитано для C13H12N4O [М+Н]+ 240,10, найдено m/z 341,1
[605]
[606] Пример 5: 4-(1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
[607]
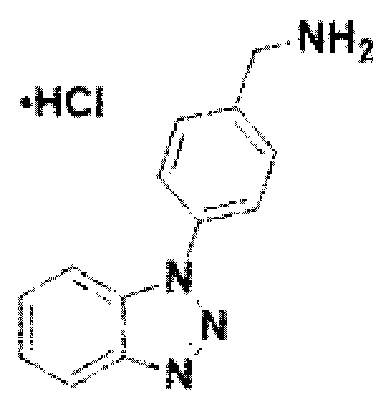
[608] ЖХМС (ESI) рассчитано для C13H12N4 [М+Н]+ 224,11, найдено m/z 225,1
[609]
[610] Пример 6: 4-(4-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
[611]
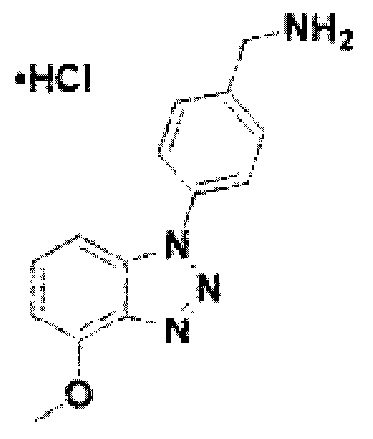
[612] ЖХМС (ESI) рассчитано для C14H14N4O [М+Н]+ 254,12, найдено m/z 255,1
[613]
[614] Пример 7: 4-(6-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
[615]
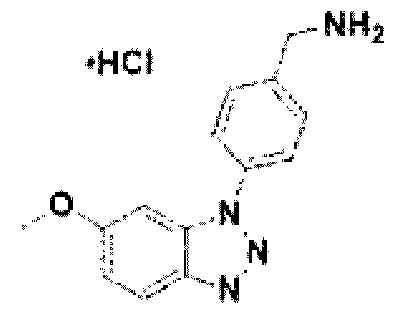
[616] ЖХМС (ESI) рассчитано для C14H14N4O [М+Н]+ 254,12, найдено m/z 255,1
[617]
[618] Пример 8: 4-(7-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
[619]
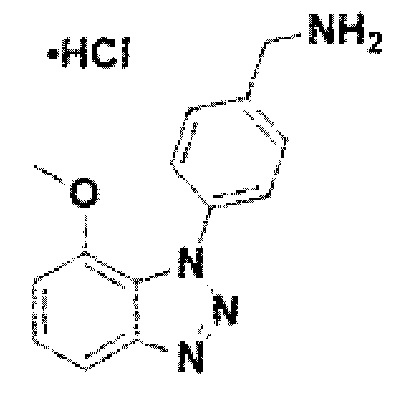
[620] ЖХМС (ESI) рассчитано для C14H14N4O [М+Н]+ 254,12, найдено m/z 255,1
[621]
[622] Пример 9: 4-(4,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
[623]
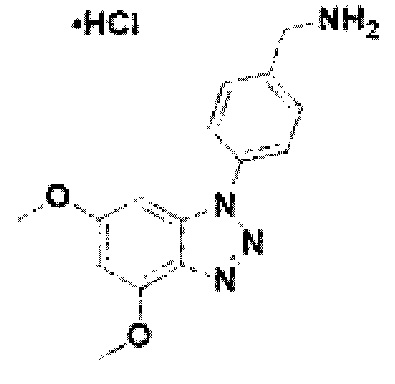
[624] ЖХМС (ESI) рассчитано для C15H16N4O2 [М+Н]+ 284,13, найдено m/z 285,1
[625]
[626] Пример 10: 4-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
[627]
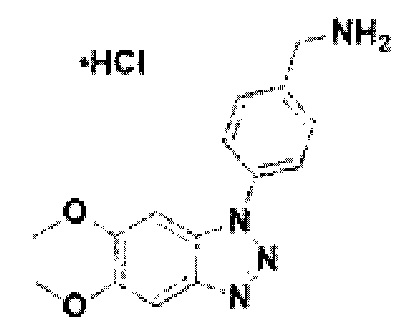
[628] ЖХМС (ESI) рассчитано для C15H16N4O2 [М+Н]+ 284,13, найдено m/z 285,1
[629]
[630] Пример 11: 2-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)этан-1-амин гидрохлорид;
[631]
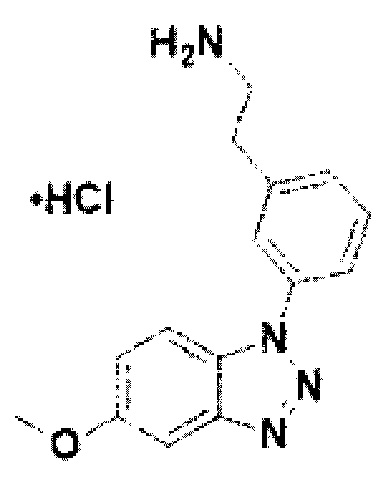
[632] ЖХМС (ESI) рассчитано для C15H16N4O [М+Н]+ 268,13, найдено m/z 269,1
[633]
[634] Пример 12: 1-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)-N-метилметанамин гидрохлорид;
[635]
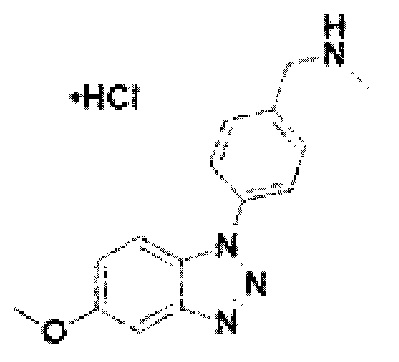
[636] ЖХМС (ESI) рассчитано для C15H16N4O [М+Н]+ 268,13, найдено m/z 269,1
[637]
[638] Пример 13: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-бензил)циклопропанамин гидрохлорид;
[639]
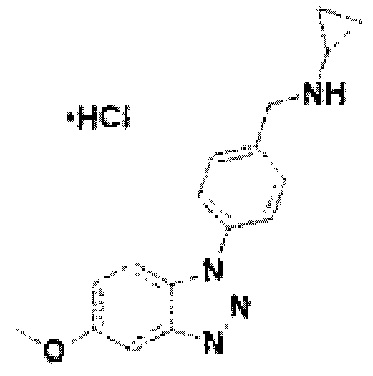
[640] 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,74 (д, J=4,1 Гц, 2Н), 7,96 (д, J=8,6 Гц, 2Н), 7,90 (д, J=8,6 Гц, 2Н), 7,86 (д, J=9,1 Гц, 1Н), 7,63 (д, J=2,2 Гц, 1Н), 7,31 (дд, J=9,1, 2,3 Гц, 1Н), 4,36 (д, J=5,7 Гц, 2Н), 3,90 (с, 3Н), 2,71 (д, J=3,6 Гц, 1Н), 0,97 (т, J=4,4 Гц, 2Н), 0,76 (кв, J=7,0 Гц, 2Н).
[641]
[642] Пример 14: (S)-1-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)этан-1-амин гидрохлорид;
[643]
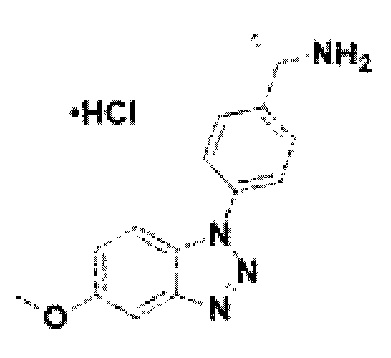
[644] ЖХМС (ESI) рассчитано для C15H16N4O [М+Н]+ 268,13, найдено m/z 269,1
[645]
[646] Пример 15: 3-хлор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
[647]
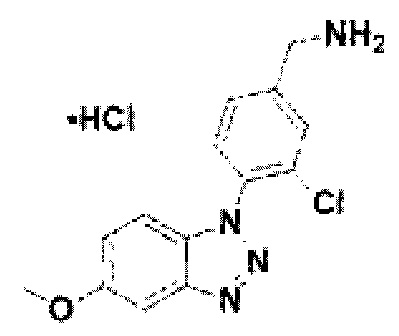
[648] ЖХМС (ESI) рассчитано для C14H13ClN4O [М+Н]+ 288,08, найдено m/z 289,1
[649]
[650] Пример 16: 3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид
[651]
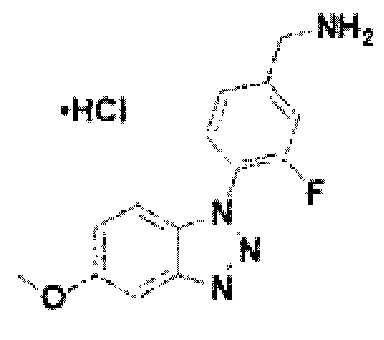
[652] ЖХМС (ESI) рассчитано для C14H13F1N4O [М+Н]+ 272,11, найдено m/z 273,1
[653]
[654] Пример 17: 2,5-дифтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин;
[655]
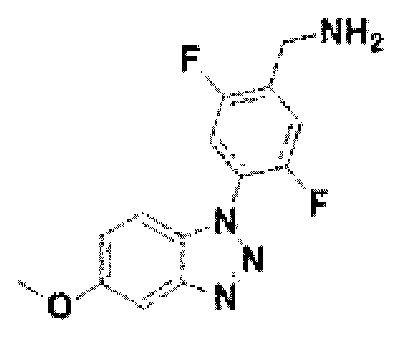
[656] ЖХМС (ESI) рассчитано для C14H12F2N4O [М+Н]+ 290,14, найдено m/z 291,1
[657]
[658] Пример 18: 2,6-дифтор-4-(5-метокси-1H-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин;
[659]
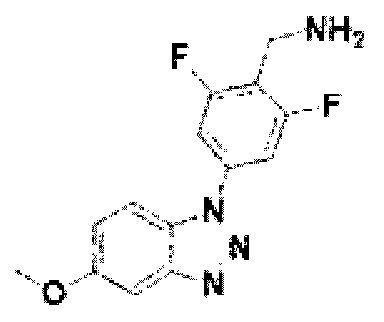
[660] ЖХМС (ESI) рассчитано для C14H12F2N4O [М+Н]+ 290,14, найдено m/z 291,1
[661]
[662] Пример 19: 4-(5-этокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторфенил)метанамин;
[663]
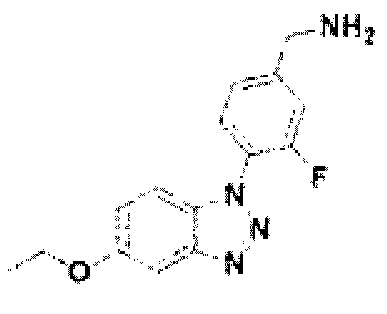
[664] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,75 (т, J=8,0 Гц, 1Н), 7,64-7,58 (м, 2Н), 7,53-7,43 (м, 2Н), 7,26 (дд, J=9,0, 2,3 Гц, 1Н), 4,16 (д, J=7,0 Гц, 2Н), 3,87 (с, 2Н), 1,40 (т, J=7,0 Гц, 3Н), 1,24 (с, 2Н).
[665]
[666] Пример 20: 3-фтор-4-(5-изопропокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин;
[667]
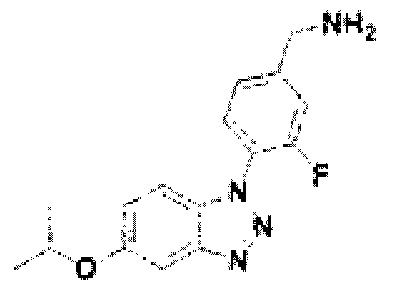
[668] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,75 (т, J=8,0 Гц, 1Н), 7,67-7,57 (м, 2Н), 7,52-7,42 (м, 2Н), 7,23 (дд, J=9,0, 2,2 Гц, 1Н), 4,82-4,74 (м, 1Н), 3,88 (с, 2Н), 1,34 (с, 3Н), 1,32 (с, 3Н), 1,18 (т, J=7,1 Гц, 1Н).
[669]
[670] Пример 21: 4-(5-(1,1-дифторэтил)-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин;
[671]
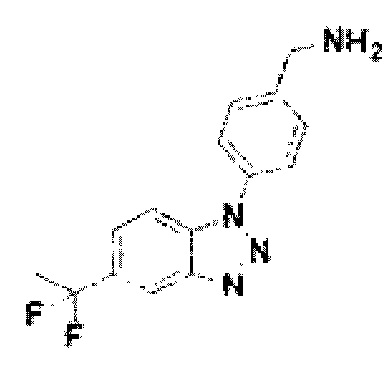
[672] ЖХМС (ESI) рассчитано для C15H14F2N4 [М+Н]+ 288,10 г найдено m/z 289
[673]
[674] Пример 22: 4-(5-(1,1-дифторэтил)-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторфенил)метанамин;
[675]
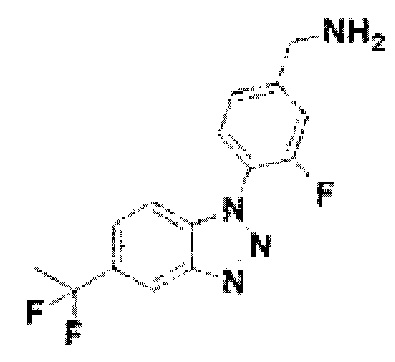
[676]
[677] ЖХМС (ESI) рассчитано для C15H13F3N4 [М+Н]+ 306,37, найдено m/z 307,1
[678]
[679] Пример 23: 3-фтор-4-(5-фторметокси)-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин;
[680]
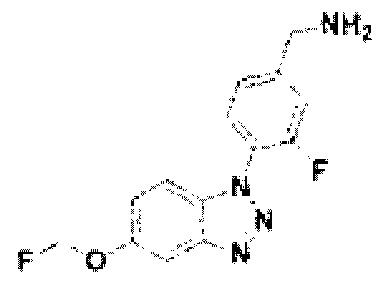
[681] ЖХМС (ESI) рассчитано для C14H12F2N4O [М+Н]+ 290,27, найдено m/z 291
[682] Пример 24: 4-(5-дифторметокси)-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторфенил)метанамин;
[683]
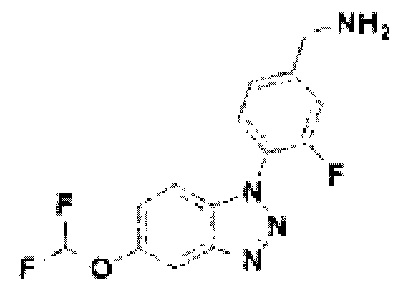
[684] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,78 (т, J=8,0 Гц, 2Н), 7,71 (дд, J=9,0, 1,9 Гц, 2Н), 7,63 (д, J=11,6 Гц, 2Н), 7,52 (д, J=2,2 Гц, 1Н), 7,51-7,49 (м, 1Н), 7,38 (с, 1Н), 3,88 (с, 2Н).
[685]
[686] Пример 25: 7-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-1,2,3,4-тетрагидроизохинолин гидрохлорид;
[687]
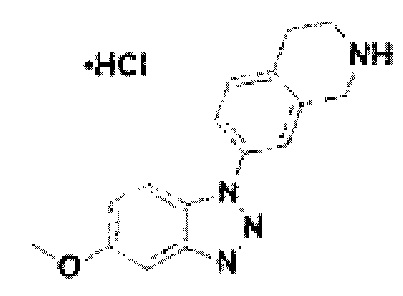
[688] 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,75 (с, 2Н), 7,89 (д, J=9,1 Гц, 1Н), 7,79 (д, J=8,5 Гц, 2Н), 7,62 (д, J=2,2 Гц, 1Н), 7,54 (д, J=8,1 Гц, 1Н), 7,32 (д, J=2,3 Гц, 1Н), 4,42 (д, J=4,4 Гц, 2Н), 3,91 (с, 3Н), 3,44 (д, J=5,6 Гц, 2Н), 3,15 (т, J=6,1 Гц, 2Н).
[689]
[690] Пример 26: 7-фтор-6-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-1,2,3,4-тетрагидроизохинолин гидрохлорид;
[691]
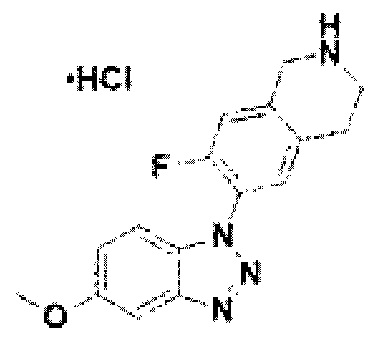
[692] ЖХМС (ESI) рассчитано для C16H15FN4O [М+Н]+ 298,12, найдено m/z 299,1
[693]
[694] Пример 27: 8-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-2,3,4,5-тетрагидро-1Н-бензо[с]азепин гидрохлорид;
[695]
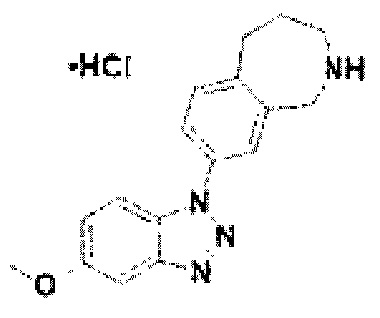
[696] ЖХМС (ESI) рассчитано для C17H18N4O [М+Н]+ 294,15, найдено m/z 295,2
[697]
[698] Пример 28: 4-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)-2,5-дифторфенил)метанамин;
[699]
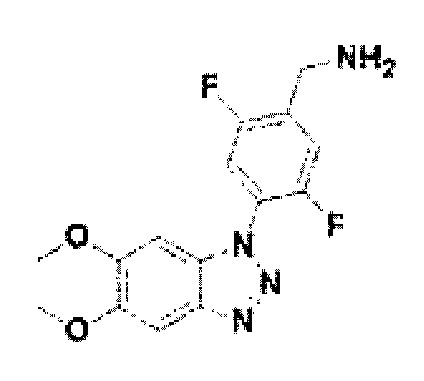
[700] ЖХМС (ESI) рассчитано для C15H14F2N4O2 [М+Н]+ 320, 17, найдено m/z 321,1
[701]
[702] Пример 29: 1-(изоиндолин-5-ил)-5,6-диметокси-1Н-бензо[d][1,2,3]триазол гидрохлорид;
[703] 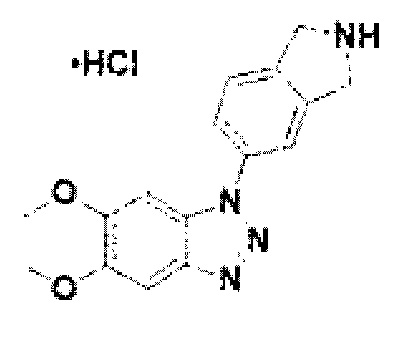
[704] 1Н ЯМР (400 МГц, ДМСО-d6) δ 10,23 (с, 2Н), 7,93 (с, 1Н), 7,87 (дд, J=8,2, 1,8 Гц, 1Н), 7,70 (д, J=8,2 Гц, 1Н), 7,59 (с, 1Н), 7,24 (с, 1Н), 4,71-4,50 (м, 4Н), 3,92 (с, 3Н), 3,90 (с, 3Н).
[705]
[706] Пример 30: 3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бицикло[1.1.1]пентан-1-ил)метанамин;
[707]
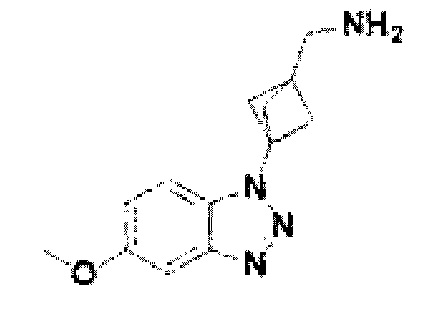
[708] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7, 78 (д, J=9,0 Гц, 1Н), 7,49 (д, J=2,2 Гц, 1Н), 7,25-7,13 (м, 2Н), 6,75 (д, J=8,6 Гц, 1Н), 3,85 (с, 3Н), 1,24 (с, 6Н), 0,85 (д, J=7,2 Гц, 2Н).
[709]
[710] Пример 31: 3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-5-метилтиофен-2-ил)метанамин гидрохлорид;
[711]
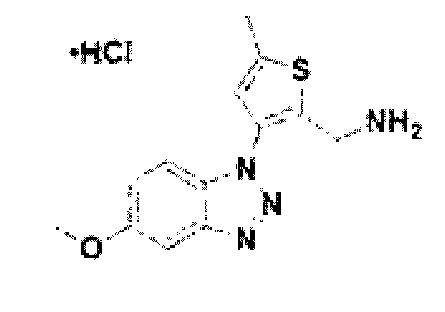
[712] 1Н ЯМР (400 МГц, ДМСО-d6) δ 8,40 (с, 2Н), 7,72 (д, J=9,1 Гц, 1Н), 7,63 (д, J=2,1 Гц, 1Н), 7,31 (дд, J=8,8, 2,5 Гц, 2Н), 7,16 (м, 1Н) 6,76 (дд, J=5,9, 3,5 Гц, 2Н), 4,23 (д, J=5,4 Гц, 2Н), 3,90 (с, 3Н), 2,57 (с, 3Н).
[713]
[714] Пример 32: трет-бутил-((4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)пиперидин-1-ил)сульфонил)карбамат;
[715]
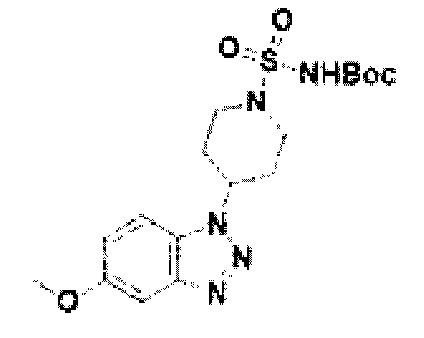
[716] ЖХМС (ESI) рассчитано для C17H25N5O5S [М+Н]+ 411,16, найдено m/z 412,2
[717]
[718] Пример 33: трет-бутил-((4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)метил)пиперидин-1-ил)сульфонил)карбамат;
[719]
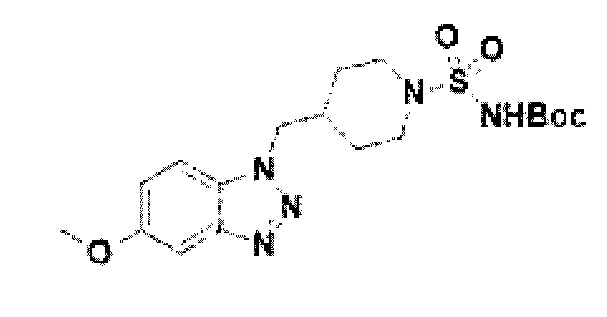
[720] ЖХМС (ESI) рассчитано для C18H27N5O5S [М+Н]+ 425,17, найдено m/z 426,2
[721]
[722] Пример 34: трет-бутил(N-(1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфонил)карбамат;
[723]
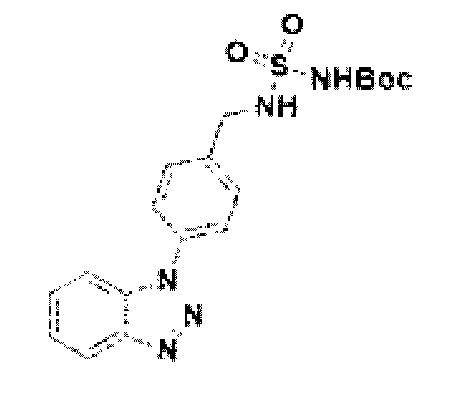
[724] ЖХМС (ESI) рассчитано для C18H21N5O4S [М+Н]+ 403,13, найдено m/z 404,1
[725]
[726] Пример 35: трет-бутил(N-(4-(4-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфонил)карбамат;
[727] 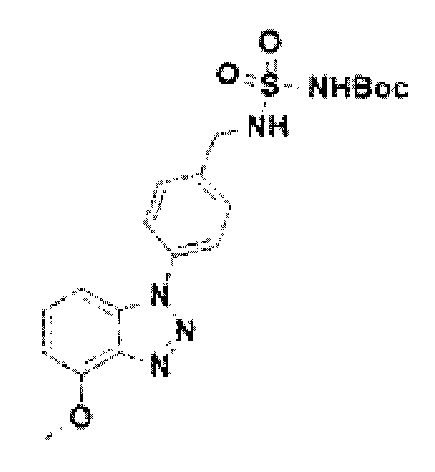
[728] ЖХМС (ESI) рассчитано для C19H23N5O5S [М+Н]+ 433,14, найдено m/z 434,1
[729]
[730] Пример 36: трет-бутил(N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфонил)карбамат;
[731]
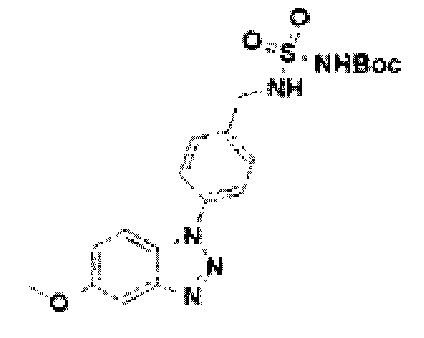
[732] ЖХМС (ESI) рассчитано для C19H23N5O5S [М+Н]+ 433,14, найдено m/z 434,1
[733]
[734] Пример 37: трет-бутил(N-(4-(6-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфонил)карбамат;
[735]
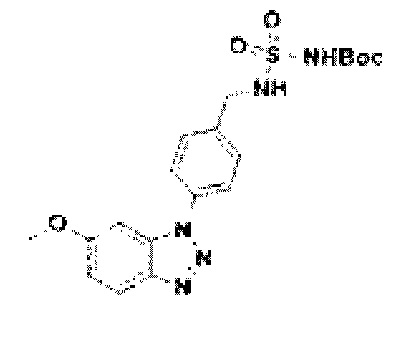
[736] ЖХМС (ESI) рассчитано для C19H23N5O5S [М+Н]+ 433,14, найдено m/z 434,1
[737]
[738] Пример 38: трет-бутил(N-(4-(7-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфонил)карбамат;
[739]
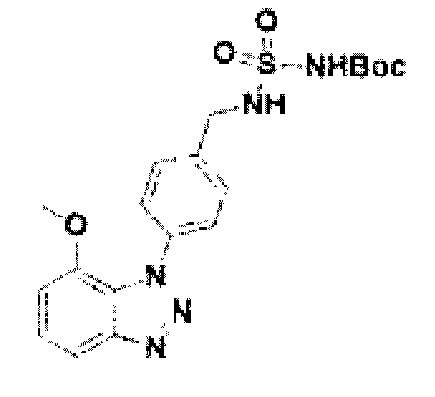
[740] ЖХМС (ESI) рассчитано для C19H23N5O5S [М+Н]+ 433,14, найдено m/z 434,1
[741]
[742] Пример 39: трет-бутил((S)-N-(1-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)этил)сульфонил)карбамат;
[743]
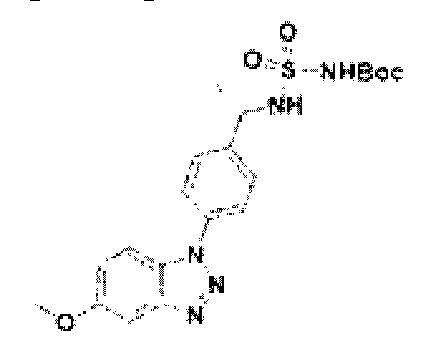
[744] ЖХМС (ESI) рассчитано для C20H25N5O5S [М+Н]+ 447,16, найдено m/z 448,2
[745]
[746] Пример 40: трет-бутил-((6-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3,4-дипидроизохинолин-2(1Н)-ил)сульфонил)карбамат;
[747]
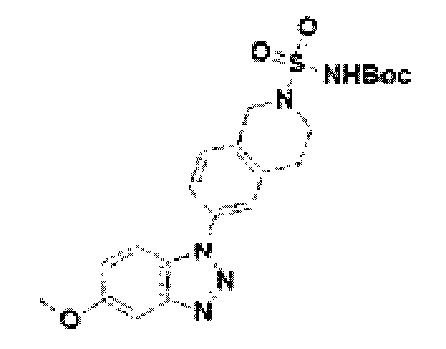
[748] ЖХМС (ESI) рассчитано для C21H25N5O5S [М+Н]+ 459,16, найдено m/z 460,2
[749]
[750] Пример 41: N-((3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)циклопентил)метил)сульфамид;
[751]
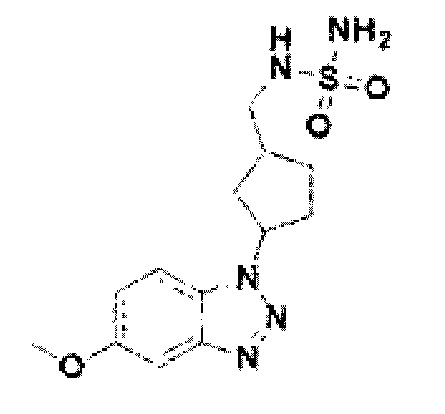
[752] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,79 (д, J=9,0 Гц, 1Н), 7,45 (д, J=2,1 Гц, 1Н), 7,18 (дд, J=9,0, 2,3 Гц, 1Н), 6,65 (т, J=6,l Гц, 1Н), 6,51 (с, 2Н), 5,31 (дд, J=15,9, 7,9 Гц, 1Н), 3,84 (с, 3Н), 2,99 (дд, J=10,0, 6,8 Гц, 2Н), 2,40-2,21 (м, 2Н), 2,20-2,06 (м, 1Н), 1,90 (дд, J=21,3, 14,1, 7,9 Гц, 2Н), 1,74-1,59 (м, 1Н), 1,24 (с, 2H).
[753]
[754] Пример 42: 4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)пиперидин-1-сульфонамид;
[755]
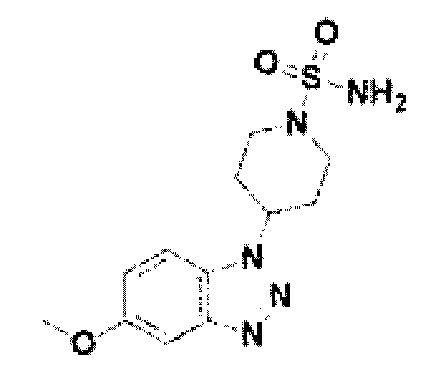
[756] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7, 82 (д, J=8,4 Гц, 1Н), 7,44 (с, 1Н), 7,18 (д, J=8,2 Гц, 1Н), 4,97 (ушир. с, 1Н), 3,86 (с, 3Н), 3,69 (д, J=11,4 Гц, 2Н), 2,95 (т, J=10,7 Гц, 2Н), 2,29-2,23 (м, 4Н).
[757]
[758] Пример 43: N-((4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)циклогексил)метил)сульфамид;
[759]
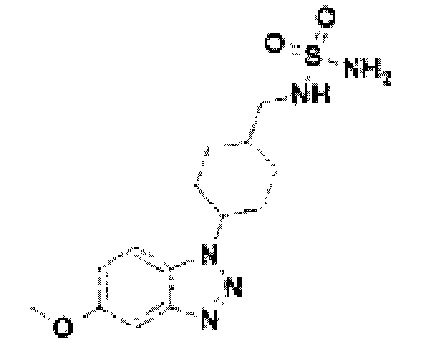
[760] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,81 (дд, J=20,1, 9,2 Гц, 1Н), 7,45 (д, J=2,2 Гц, 1Н), 7,17 (дд, J=9,0, 2,3 Гц, 1Н), 6,59 (т, J=6,2 Гц, 1Н), 6,52 (д, J=11,1 Гц, 1Н), 4,91 (дд, J=8,9, 4,3 Гц, 1Н), 3,84 (с, 3Н), 2,96 (т, J=6,9 Гц, 2Н), 2,14 (дт, J=15,3, 6,5 Гц, 2Н), 1,91 (дд, J=13,6, 4,5 Гц, 0Н), 1,73 (д, J=4,7 Гц, 3Н), 1,24 (с, 1Н).
[761]
[762] Пример 44: 2-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)пиперидин-1-ил)этан-1-сульфонамид;
[763]
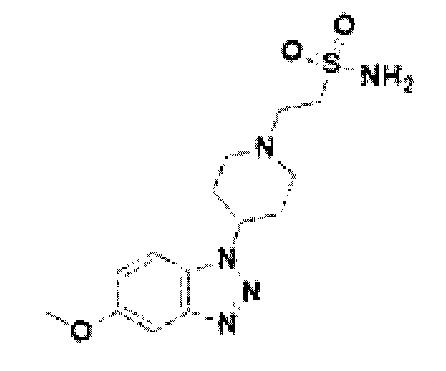
[764] ЖХМС (ESI) рассчитано для C20H25N5O5S [М+Н]+ 447,16, найдено m/z 448,2
[765]
[766] Пример 45: 4-((5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)метил)пиперидин-1-сульфонамид;
[767]
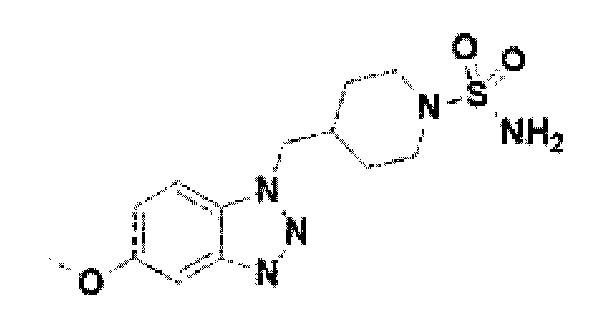
[768] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7, 83 (д, J=9,0 Гц, 1Н), 7,44 (д, J=1,6 Гц, 1Н), 7,19 (д, J=7,2 Гц, 1Н), 4,60 (д, J=6,9 Гц, 2Н), 3,85 (с, 3Н), 3,44 (д, J=11,4 Гц, 2Н), 2,44 (т, J=11,3 Гц, 2Н), 2,01 (ушир. с, 1Н), 1,57 (д, J=11,2 Гц, 2Н), 1,37-1,29 (м, 2Н).
[769]
[770] Пример 46: N-(4-(1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[771]
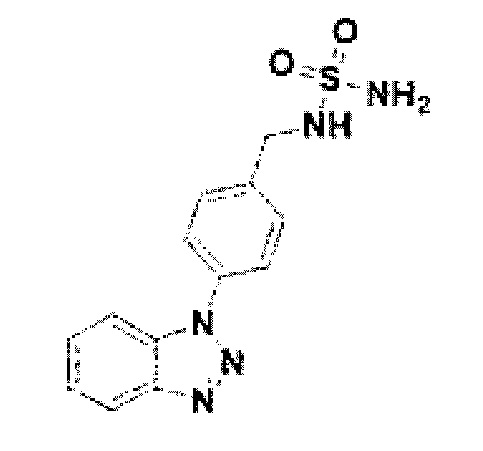
[772] 1Н ЯМР (400 МГц, ДМСО-d6) δ 8,20 (д, J=8,4 Гц, 1Н), 7,89 (дд, J=27,8, 8,4 Гц, 3Н), 7,68 (дт, J=7,4, 2,9 Гц, 3Н), 7,58-7,49 (м, 1Н), 7,27 (с, 1Н), 6,73 (с, 2Н), 4,23 (д, J=6,5 Гц, 2Н).
[773]
[774] Пример 47: N-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)сульфамид;
[775]
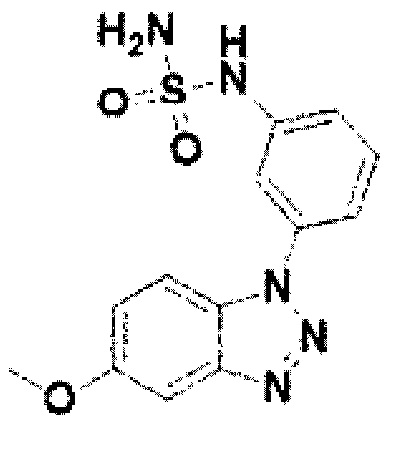
[776] 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,96 (с, 1Н), 7,82 (д, J=9,0 Гц, 1H), 7,68 (т, J=2,0 Гц, 1H), 7,63 (д, J=2,4 Гц, 1H), 7,59 (т, J=7,9 Гц, 1H), 7,52-7,47 (м, 1H), 7,41-7,23 (м, 4H), 3,91 (с, 3Н).
[777]
[778] Пример 48: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)сульфамид гидрохлорид;
[779]
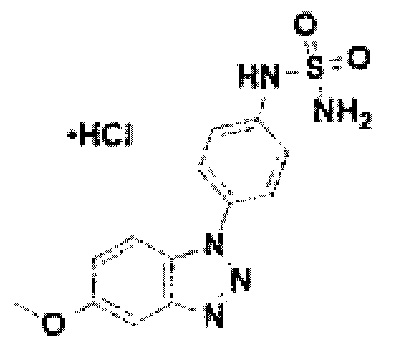
[780] 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,78 (ушир.с, 1Н), 7,75-7,71 (м, 2Н), 7,56 (с, 1Н), 7,42 (д, J=7,6 Гц, 2Н), 7,26-7,17 (м, 2Н), 3,88 (с, 3Н).
[781]
[782] Пример 49: N-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[783]
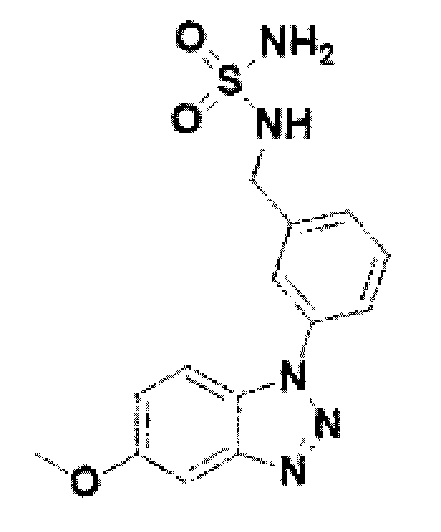
[784] 1Н ЯМР (400 МГц, ДМСО-d6) δ 8,05-7,80 (м, 2Н), 7,77 (д, J=8,0 Гц, 1Н), 7,64 (дд, J=12,0, 4,7 Гц, 2Н), 7,56 (д, J=7,7 Гц, 1Н), 7,30 (тд, J=8,9, 4,4 Гц, 2Н), 6,73 (с, 2Н), 4,26 (д, J=6,4 Гц, 2Н), 3,91 (с, 3Н).
[785]
[786] Пример 50: N-(4-(4-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[787]
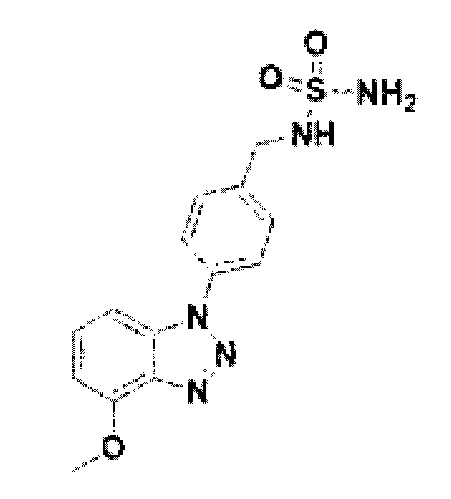
[788] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,95-7,75 (м, 2Н), 7,66 (д, J=8,6 Гц, 2Н), 7,63-7,51 (м, 1Н), 7,45-7,33 (м, 1Н), 7,26 (т, J=6,5 Гц, 1Н), 6,97 (д, J=7,6 Гц, 1Н), 6,73 (с, 2Н), 4,22 (д, J=6,5 Гц, 2Н), 4,08 (с, 3Н).
[789]
[790] Пример 51: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид гидрохлорид;
[791]
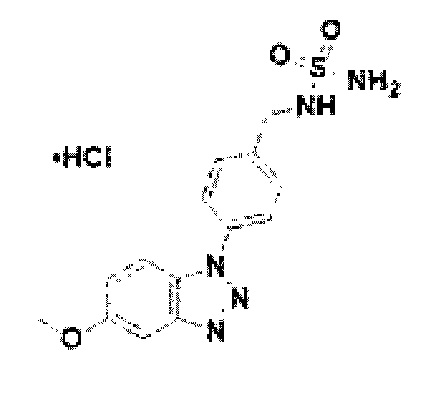
[792] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,82-7,78 (м, 3Н), 7,65 (д, J=8,4 Гц, 2Н), 7,59 (д, J=2,1 Гц, 1Н), 7,28 (дд, J=9,0, 2,2 Гц, 1Н), 4,22 (с, 2Н), 3,90 (с, 3Н).
[793]
[794] Пример 52: N-(4-(6-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[795]
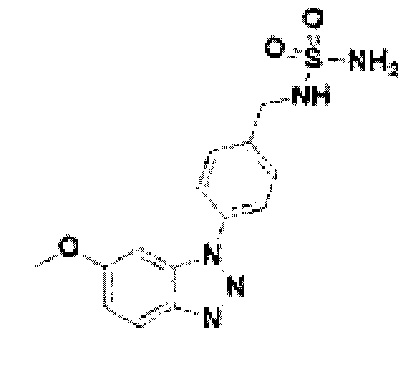
[796] 1Н ЯМР (400 МГц, ДМСО-d6) δ 8,05 (д, J=9,1 Гц, 1Н), 7,84 (д, J=8,5 Гц, 2Н), 7,67 (д, J=8,5 Гц, 2Н), 7,26 (с, 1Н), 7,20 (д, J=2,1 Гц, 1Н), 7,13 (дд, J=9,1, 2,2 Гц, 1Н), 6,73 (с, 2Н), 4,22 (д, J=6,5 Гц, 2Н), 3,90 (с, 3Н).
[797]
[798] Пример 53: N-(4-(7-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[799]
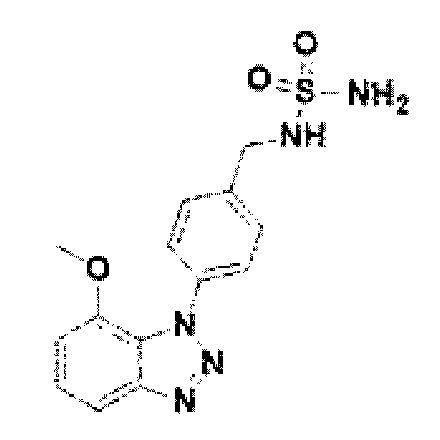
[800] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,71 (дд, J=8,4, 0,6 Гц, 1Н), 7,68-7,62 (м, 2Н), 7,57 (д, J=8,7 Гц, 2Н), 7,42 (дд, J=8,3, 7,8 Гц, 1Н), 7,24 (д, J=6,5 Гц, 1Н), 7,12 (д, J=7,5 Гц, 1Н), 6,73 (с, 2Н), 4,22 (д, J=6,5 Гц, 2Н), 3,84 (с, 3Н).
[801]
[802] Пример 54: N-(4-(4,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[803]
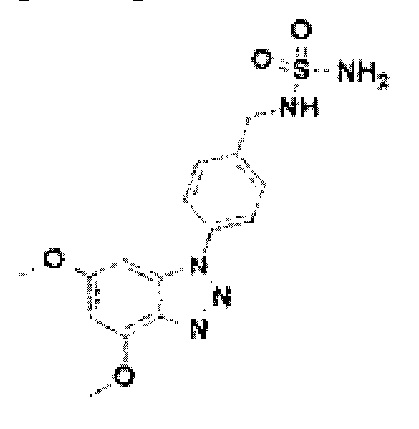
[804] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,86-7,74 (м, 2Н), 7,65 (д, J=8,6 Гц, 2Н), 7,26 (т, J=6,5 Гц, 1Н), 6,82-6,67 (м, 3Н), 6,56 (д, J=1,8 Гц, 1Н), 4,22 (д, J=6,5 Гц, 2Н), 4,03 (с, 3Н), 3,87 (с, 3Н).
[805]
[806] Пример 55: N-(4-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[807]
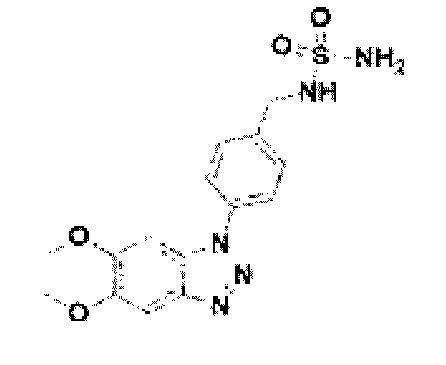
[808] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,84 (д, J=8,5 Гц, 2Н), 7,66 (д, J=8,5 Гц, 2Н), 7,59 (с, 1Н), 7,25 (д, J=6,5 Гц, 1Н), 7,21 (с, 1Н), 6,72 (с, 2Н), 4,23 (с, 2Н), 3,92 (с, 3Н), 3,90 (с, 3Н).
[809]
[810] Пример 56: N-(4-(1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторбензил)сульфамид;
[811]
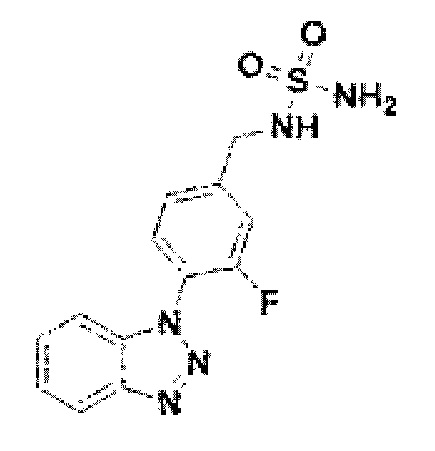
[812] 1Н ЯМР (400 МГц, Метанол-d4) δ 8,13 (д, J=8,4 Гц, 1Н), 7,73 (т, J=7,8 Гц, 1Н), 7,65 (д, J=7,0 Гц, 1Н), 7,63-7,57 (м, 2Н), 7,54 (т, J=7,6 Гц, 2Н), 4,40 (с, 2Н).
[813]
[814] Пример 57: N-(4-(1Н-бензо[d][1,2,3]триазол-1-ил)-2,3-дифторбензил)сульфамид;
[815]
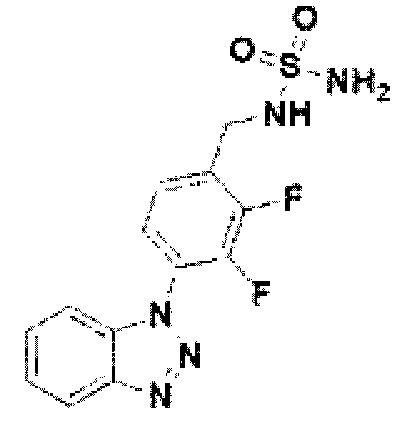
[816] 1H ЯМР (400 МГц, Метанол-d4) δ 8,13 (д, J=8,4 Гц, 1Н), 7,73 (т, J=7,8 Гц, 1Н), 7,70-7,63 (м, 1Н), 7,63-7,57 (м, 2Н), 7,57-7,52 (м, 2Н), 4,40 (с, 2Н).
[817]
[818] Пример 58: N-(4-(1Н-бензо[d][1,2,3]триазол-1-ил)-3,5-дифторбензил)сульфамид;
[819]
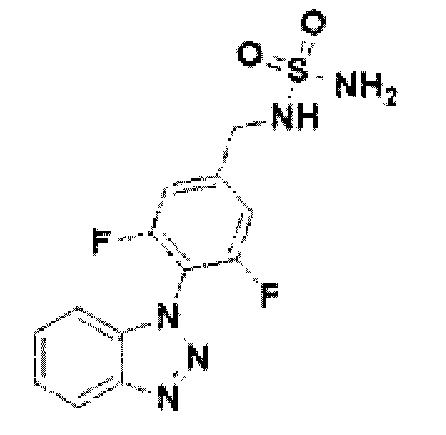
[820] 1H ЯМР (400 МГц, Метанол-d4) δ 8,16 (д, J=8,4 Гц, 1Н), 7,71-7,64 (м, 1Н), 7,60-7,50 (м, 2Н), 7,46 (д, J=8,9 Гц, 2Н), 4,40 (с, 2Н).
[821]
[822] Пример 59: N-(3-клор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[823]
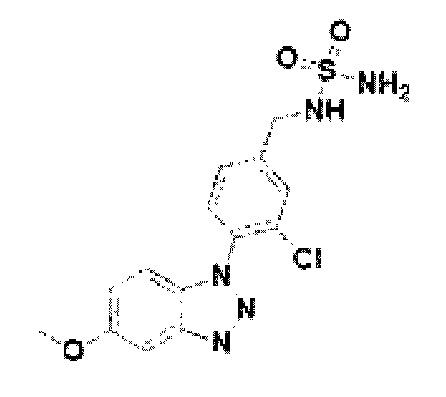
[824] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,83 (д, J=1,6 Гц, 1Н), 7,75 (д, J=8,1 Гц, 1Н), 7,63 (дд, J=6,3, 1,9 Гц, 2Н), 7,38 (дд, J=12,2, 7,8 Гц, 2Н), 7,26 (дд, J=9,0, 2,3 Гц, 1Н), 6,78 (с, 2Н), 4,27 (д, J=6,5 Гц, 2Н), 3,91 (с, 3Н).
[825]
[826] Пример 60: N-(2-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[827]
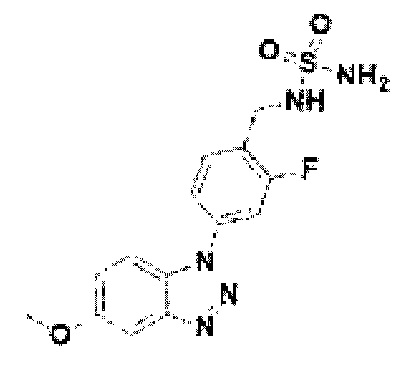
[828] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,89 (д, J=9,1 Гц, 1Н), 7,82-7,73 (м, 3Н), 7,64 (д, J=2,2 Гц, 1Н), 7,31 (дд, J=9,1, 2,4 Гц, 1Н), 7,26 (т, J=6,5 Гц, 1Н), 6,76 (с, 2Н), 4,24 (д, J=6,4 Гц, 2Н), 3,90 (с, 3Н).
[829]
[830] Пример 61: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторбензил)сульфамид;
[831] 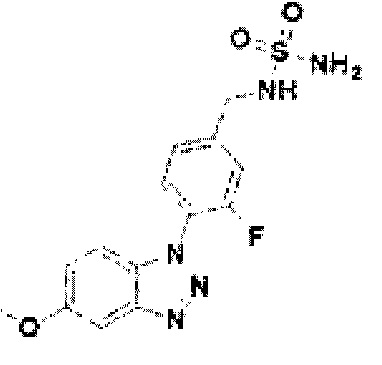
[832] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,80 (т, J=7,9 Гц, 1Н), 7,62 (дд, J=10,4, 2,0 Гц, 2Н), 7,54 (дд, J=9,0, 2,2 Гц, 1Н), 7,51-7,45 (м, 1Н), 7,36 (т, J=6,5 Гц, 1Н), 7,29 (дд, J=9,0, 2,3 Гц, 1Н), 6,77 (с, 2Н), 4,26 (д, J=6,5 Гц, 2Н), 3,90 (с, 3Н).
[833]
[834] Пример 62: N-(2,5-дифтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[835]
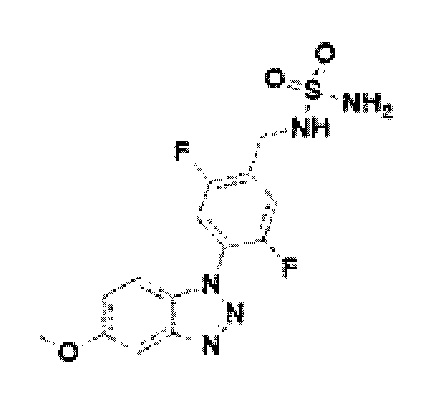
[836] ЖХМС (ESI) рассчитано для C14H13F2N5O3S [М+Н]+ 369,35, найдено m/z 370,1
[837]
[838] Пример 63: N-(2,6-дифтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[839]
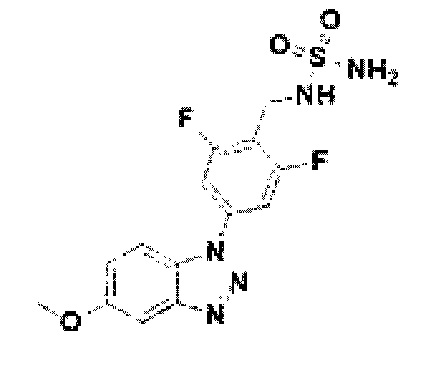
[840] ЖХМС (ESI) рассчитано для C14H13F2N5O3S [М+Н]+ 369,35, найдено m/z 370,1
[841]
[842] Пример 64: N-(3,5-дифтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-бензил)сульфамид;
[843]
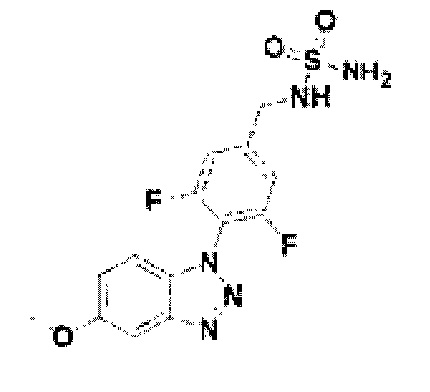
[844] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,67 (д, J=2,1 Гц, 1Н), 7,54 (д, J=9,0 Гц, 3Н), 7,44 (с, 1Н), 7,31 (дд, J=9,0, 2,3 Гц, 1Н), 6,80 (с, 2Н), 4,28 (д, J=6,5 Гц, 2Н), 3,90 (с, 3Н).
[845]
[846] Пример 65: N-(2,3-дифтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-бензил)сульфамид;
[847]
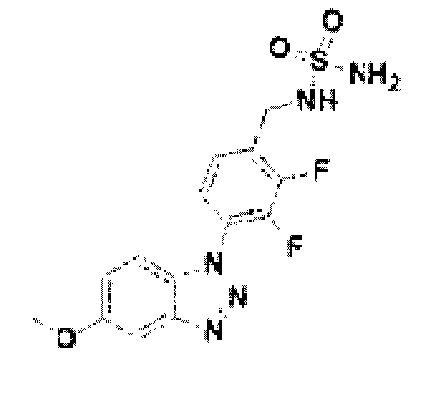
[848] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,75-7,57 (м, 4Н), 7,36 (т, J=6,2 Гц, 1Н), 7,31 (дд, J=9,1, 2,3 Гц, 1Н), 6,80 (с, 2Н), 4,30 (д, J=6,4 Гц, 2Н), 3,90 (с, 3Н).
[849]
[850] Пример 66: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3-метилбензил)сульфамид;
[851]
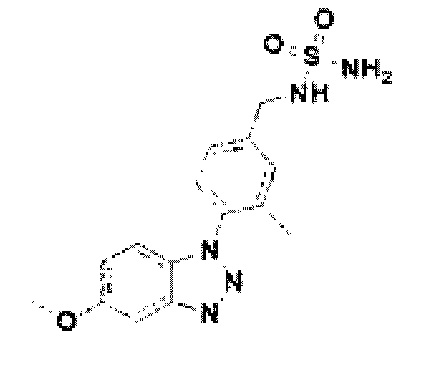
[852] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,62 (д, J=2,1 Гц, 1Н), 7,55 (с, 1Н), 7,47 (с, 2Н), 7,37 (д, J=9,0 Гц, 1Н), 7,28-7,19 (м, 2Н), 6,72 (с, 2Н), 4,21 (д, J=6,5 Гц, 2Н), 3,90 (с, 3Н), 2,05 (с, 3Н).
[853]
[854] Пример 67: N-(3-циано-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3-бензил)сульфамид;
[855]
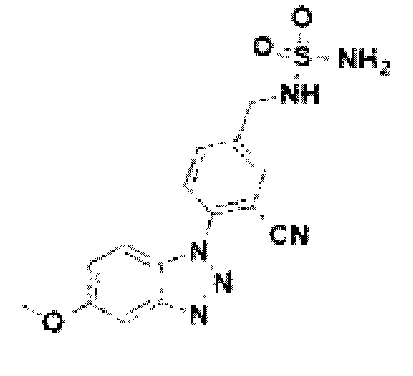
[856] ЖХМС (ESI) рассчитано для C15H14N6O3S [М+Н]+ 358,08, найдено m/z 359,1
[857]
[858] Пример 68: N-(3-метокси-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[859]
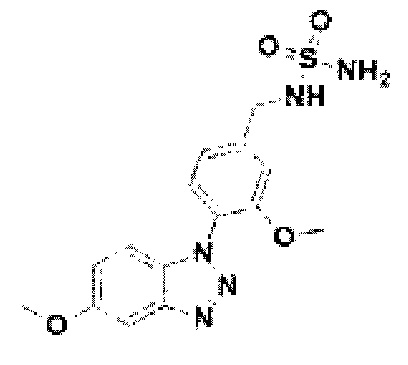
[860] ЖХМС (ESI) рассчитано для C15H17N5O4S [М+Н]+ 363,1, найдено m/z 364,1
[861]
[862] Пример 69: N-(4-(5-метокси-6-метил-1Н-бензо[d][1,2,3] триазол-1-ил)бензил)сульфамид;
[863]
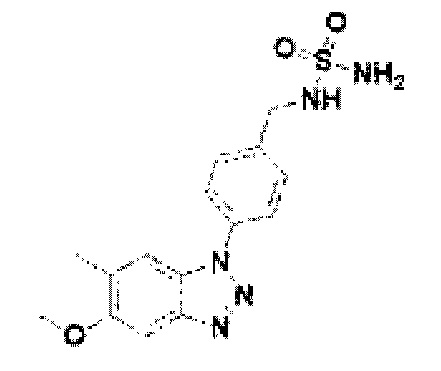
[864] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,82 (д, J=8,2 Гц, 2Н), 7,73 (с, 1Н), 7,65 (д, J=8,3 Гц, 2Н), 7,55 (с, 1Н), 7,25 (т, J=6,4 Гц, 1Н), 6,72 (с, 2Н), 4,21 (д, J=6,l Гц, 2Н), 3,93 (с, 3Н), 2,35 (с, 3Н).
[865]
[866] Пример 70: N-(3-фтор-4-(5-метокси-6-метил-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[867]
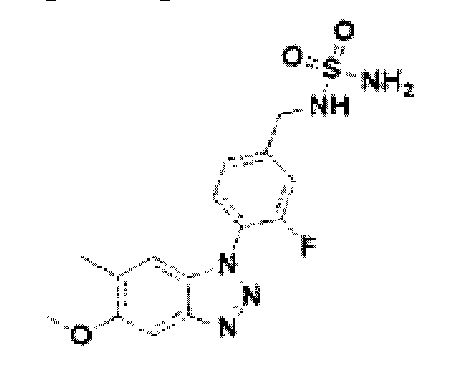
[868] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,77 (т, J=7,9 Гц, 1Н), 7,61 (д, J=11,4 Гц, 1Н), 7,57 (с, 1Н), 7,49 (д, J=7,9 Гц, 1Н), 7,42 (с, 1Н), 7,36 (т, J=6,5 Гц, 1Н), 6,77 (с, 2Н), 4,25 (д, J=6,5 Гц, 2Н), 3,93 (с, 3Н), 2,31 (с, 3Н).
[869]
[870] Пример 71: N-(4-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторбензил)сульфамид;
[871]
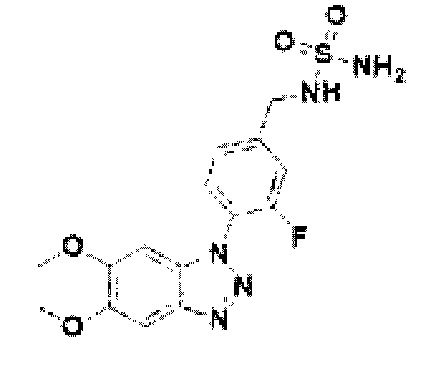
[872] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,77 (т, J=7,9 Гц, 1Н), 7,61 (д, J=10,6 Гц, 2Н), 7,49 (д, J=8,1 Гц, 1Н), 7,36 (т, J=6,5 Гц, 1Н), 6,97 (с, 1Н), 6,77 (с, 2Н), 4,25 (д, J=6,5 Гц, 2Н), 3,90 (с, 3Н), 3,84 (с, 3Н).
[873]
[874] Пример 72: N-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенэтил)сульфамид;
[875]
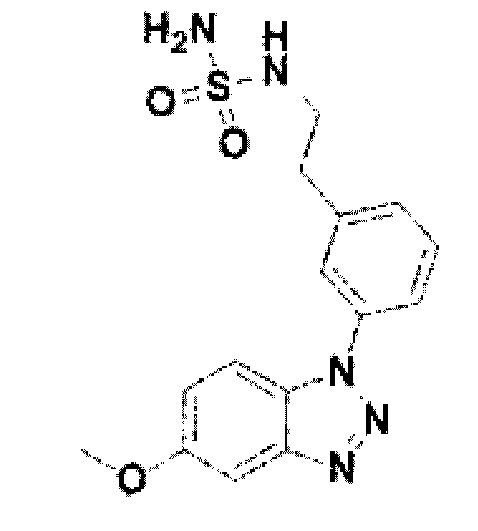
[876] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,87 (д, J=9,1 Гц, 1Н), 7,80-7,68 (м, 2Н), 7,67-7,58 (м, 2Н), 7,46 (д, J=7,7 Гц, 1Н), 7,29 (дд, J=9,1, 2,3 Гц, 1Н), 6,67 (т, J=5,9 Гц, 1Н), 6,58 (с, 2Н), 3,91 (с, 3Н), 3,34 (с, 2Н), 3,22 (дд, J=13,5, 7,1 Гц, 2Н), 2,97 (т, J=7,3 Гц, 2Н), 2,57-2,47 (м, 4Н).
[877]
[878] Пример 73: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенэтил)сульфамид гидрохлорид;
[879]
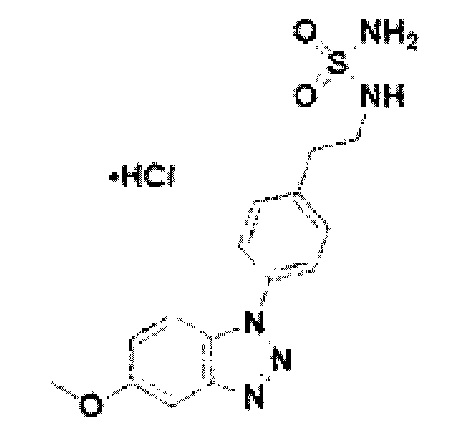
[880] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,80 (м, 2Н), 7,60-7,55 (м, 2Н), 7,29-7,27 (м, 1Н), 6,66-6,60 (ушир.с, 2Н), 3,89 (с, 3Н), 3,18 (ушир.с, 2Н), 2,93 (ушир.с, 2Н).
[881]
[882] Пример 74: N-(3-фтор-4-(5-гидрокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[883]
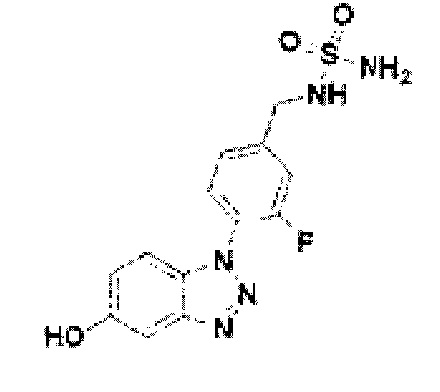
[884] 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,92 (с, 1Н), 7,77 (т, J=8,0 Гц, 1Н), 7,60 (д, J=11,7 Гц, 1Н), 7,51-7,42 (м, 2Н), 7,35 (дд, J=8,5, 4,3 Гц, 2Н), 7,17 (дд, J=8,9, 2,2 Гц, 1Н), 6,77 (с, 2Н), 4,25 (д, J=6,5 Гц, 2Н).
[885]
[886] Пример 75: N-(3-фтор-4-(5-метил-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[887]
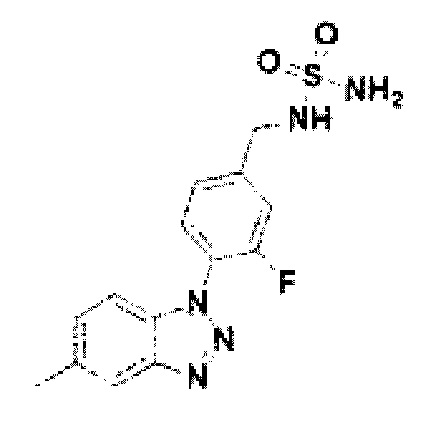
[888] ЖХМС (ESI) рассчитано для C14H14FN5O2S [М+Н]+ 335,09, найдено m/z 336,1
[889]
[890] Пример 76: N-(4-(5-этокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторбензил)сульфамид;
[891]
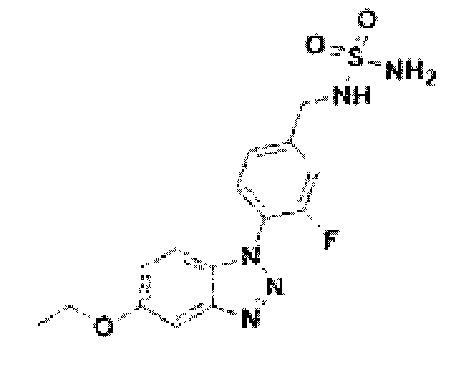
[892] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,80 (т, J=8,0 Гц, 1Н), 7,62 (д, J=9,5 Гц, 2Н), 7,51 (т, J=9,6 Гц, 2Н), 7,36 (д, J=6,3 Гц, 1Н), 7,27 (д, J=8,8 Гц, 1Н), 6,77 (с, 2Н), 4,25 (д, J=6,5 Гц, 2Н), 4,16 (д, J=6,9 Гц, 2Н), 1,40 (т, J=6,9 Гц, 3Н).
[893]
[894] Пример 77: N-(3-фтор-4-(5-изопропокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[895]
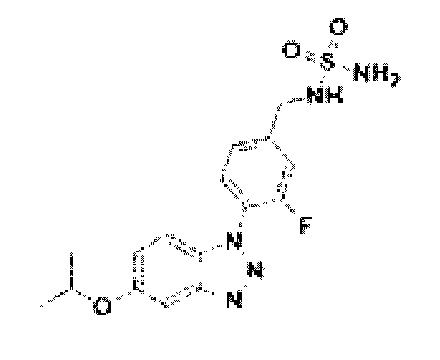
[896] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,79 (т, J=8,0 Гц, 1Н), 7,62 (т, J=7,5 Гц, 2Н), 7,51 (дд, J=11,8, 5,0 Гц, 2Н), 7,36 (т, J=6,5 Гц, 1Н), 7,24 (дд, J=9,0, 2,2 Гц, 1Н), 6,77 (с, 2Н), 4,84-4,73 (м, 1Н), 4,25 (д, J=6,5 Гц, 2Н), 1,34 (с, 3Н), 1,33 (с, 3Н).
[897]
[898] Пример 78: N-(5-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)пиридин-2-ил)метил)сульфамид;
[899]
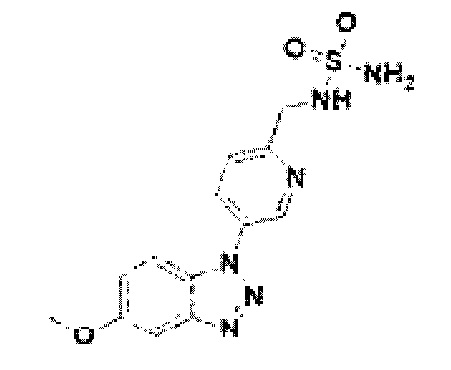
[900] 1Н ЯМР (400 МГц, ДМСО-d6) δ 9,03 (д, J=2,4 Гц, 1Н), 8,36 (дд, J=8,4, 2,6 Гц, 1Н), 7,89 (д, J=9,1 Гц, 1Н), 7,81 (д, J=8,5 Гц, 1Н), 7,65 (д, J=2,2 Гц, 1Н), 7,39-7,28 (м, 2Н), 6,78 (с, 2Н), 4,34 (д, J=6,5 Гц, 2Н), 3,90 (с, 3Н).
[901]
[902] Пример 79: (N-(6-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)пиридин-3-ил)метил)сульфамид;
[903]
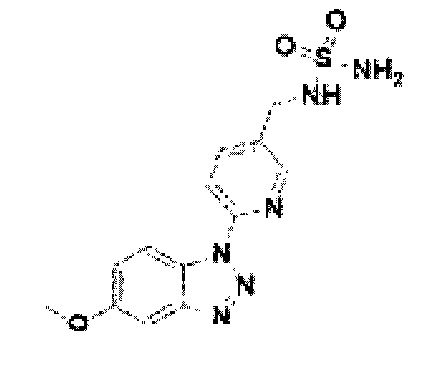
[904] 1Н ЯМР (400 МГц, ДМСО-d6) δ 8,64 (с, 1Н), 8,45 (д, J=9,2 Гц, 2Н), 8,21 (с, 1Н), 8,13 (с, 1Н), 7,64 (с, 1Н), 7,38-7,33 (м, 2Н), 6,77 (с, 1Н), 4,36-4,30 (м, 2Н), 3,90 (с, 3Н).
[905]
[906] Пример 80: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)-N-метил)сульфамид;
[907]
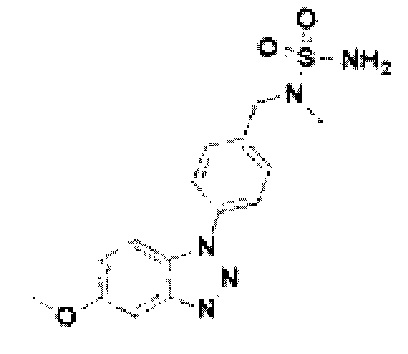
[908] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,88 (т, J=9,3 Гц, 3Н), 7,64 (дд, J=13,2, 5,3 Гц, 3Н), 7,30 (дд, J=9,1, 2,3 Гц, 1Н), 6,98 (с, 2Н), 4,23 (с, 2Н), 3,91 (с, 3H), 2,63 (с, 3H).
[909]
[910] Пример 81: N-(3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)-N-метилсульфамид;
[911]
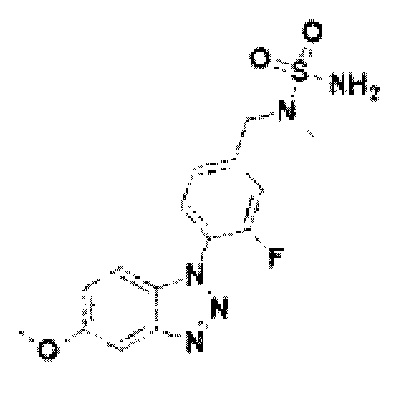
[912] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,84 (т, J=7,9 Гц, 1Н), 7,65-7,55 (м, 3H), 7,49 (д, J=8,5 Гц, 1Н), 7,29 (дд, J=9,1, 2,3 Гц, 1Н), 7,03 (с, 2Н), 4,27 (с, 2Н), 3,90 (с, 3H), 2,67 (с, 3H).
[913]
[914] Пример 82: N-циклопропил-N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[915]
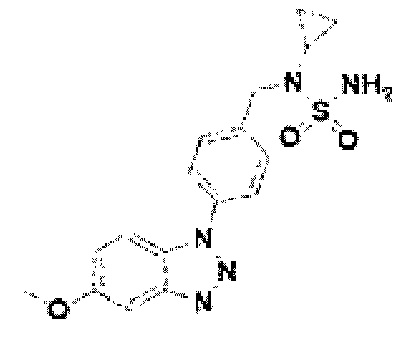
[916] 1H ЯМР (400 МГц, ДМСО-d6) δ 7,83 (дд, J=8,8, 3,7 Гц, 3H), 7,66-7,53 (м, 3H), 7,29 (дд, J=9,1, 2,3 Гц, 1Н), 7,05 (с, 2Н), 4,40 (с, 2Н), 3,90 (с, 3H), 2,46-2,38 (м, 1Н), 0,75-0,43 (м, 4Н).
[917]
[918] Пример 83: (S)-N-(1-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)этил)сульфамид;
[919]
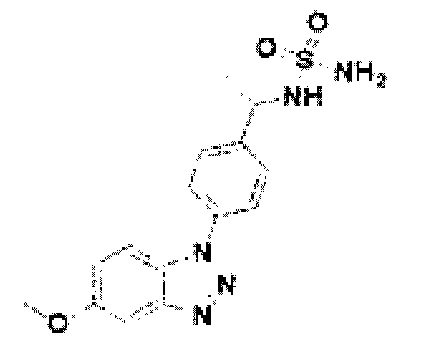
[920] ЖХМС (ESI) рассчитано для C15H17N5O3S [М+Н]+ 34 7, 11, найдено m/z 348,1.
[921]
[922] Пример 84: N-(4-(5-трифторметил)-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[923]
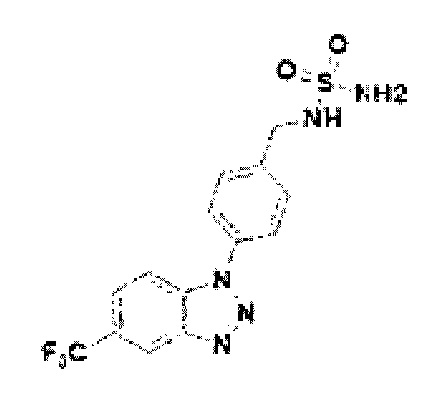
[924] ЖХМС (ESI) рассчитано для C14H12F3N5O2S [М+Н]+ 371,07, найдено m/z 372,1.
[925]
[926] Пример 85: N-(3-фтор-4-(5-трифторметил)-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[927]
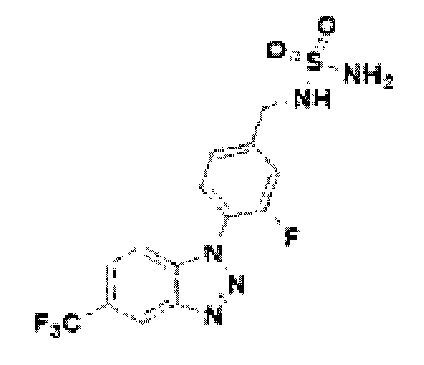
[928] 1Н ЯМР (400 МГц, ДМСО-d6) δ 8,76 (с, 1Н), 7,98 (дд, J=8,9, 1,3 Гц, 1Н), 7,88 (дд, J=13,7, 5,8 Гц, 2Н), 7,66 (д, J=11,5 Гц, 1Н), 7,54 (д, J=8,2 Гц, 1Н), 7,38 (т, J=6,5 Гц, 1Н), 6,78 (с, 2Н), 4,28 (д, J=6,5 Гц, 2Н).
[929]
[930] Пример 86: 4-(5-(1,1-дифторэтил)-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин;
[931]
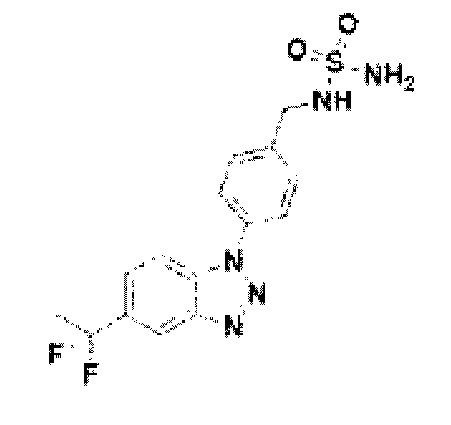
[932] ЖХМС (ESI) рассчитано для C15H14F2N4 [М+Н]+ 288,10, найдено m/z 289
[933]
[934] Пример 87: N-(4-(5-диметиламино)-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторбензил)сульфамид;
[935]
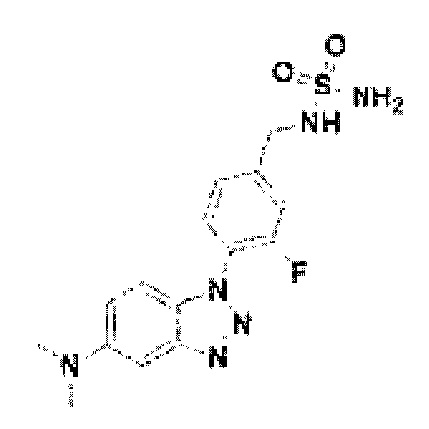
[936] ЖХМС (ESI) рассчитано для C15H17FN6O2S [М+Н]+ 364,11, найдено m/z 365,1
[937]
[938] Пример 88: N-(3-фтор-4-(5-фторметокси)-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[939]
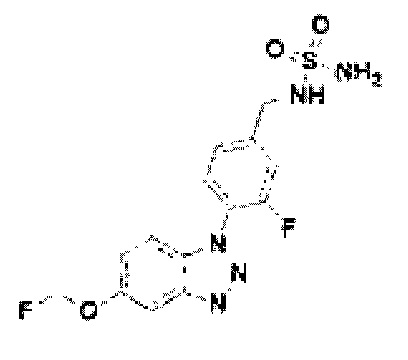
[940] ЖХМС (ESI) рассчитано для C14H13F2N5O3S [М+Н]+ 369,35, найдено m/z 370,1
[941]
[942] Пример 89: N-(4-(5-трифторметокси)-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[943]
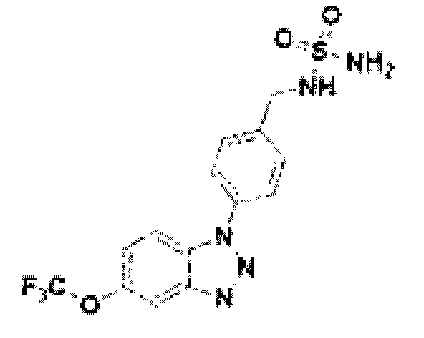
[944] 1Н ЯМР (400 МГц, ДМСО-d6) δ 8,33 (с, 1Н), 8,04 (д, J=9,0 Гц, 1Н), 7,87 (д, J=8,5 Гц, 2Н), 7,77-7,60 (м, 3H), 7,27 (т, J=6,5 Гц, 1Н), 6,73 (с, 2Н), 4,23 (д, J=6,5 Гц, 2Н).
[945]
[946] Пример 90: N-(3-фтор-4-(5-трифторметокси)-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[947]
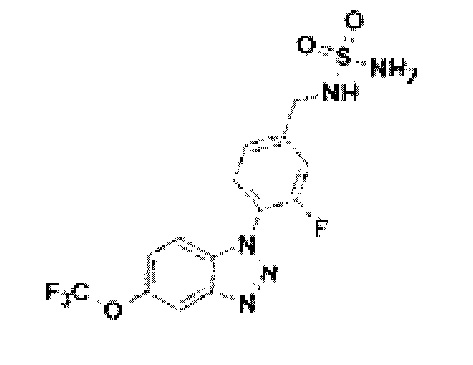
[948] 1Н ЯМР (400 МГц, ДМСО-d6) δ 8,36 (с, 1Н), 7,89-7,77 (м, 2Н), 7,72-7,61 (м, 2Н), 7,52 (д, J=8,2 Гц, 1Н), 7,37 (т, J=6,5 Гц, 1Н), 6,77 (с, 2Н), 4,27 (д, J=6,5 Гц, 2Н).
[949]
[950] Пример 91: N-(4-(5-дифторметокси)-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторбензил)сульфамид;
[951]
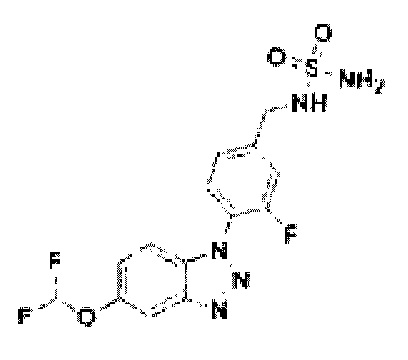
[952] 1Н ЯМР (400 МГц, ДМСО-d6) δ 8,04 (д, J=2,0 Гц, 1Н), 7,83 (т, J=8,0 Гц, 1Н), 7,72 (дд, J=9,0, 2,0 Гц, 1Н), 7,64 (д, J=10,2 Гц, 1Н), 7,52 (дд, J=8,9, 2,3 Гц, 2Н), 7,38 (д, J=7,7 Гц, 2Н), 6,77 (с, 2Н), 4,26 (д, J=6, 5 Гц, 2Н).
[953]
[954] Пример 92: N-(4-(6-фтор-5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[955]
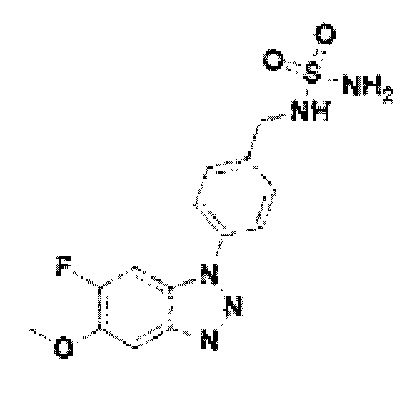
[956] 1H ЯМР (400 МГц, ДМСО-d6) δ 7,88 (дд, J=9,0, 6,0 Гц, 2Н), 7,84 (д, J=8,5 Гц, 2Н), 7,65 (д, J=8,5 Гц, 2Н), 7,26 (т, J=6,5 Гц, 1Н), 6,72 (с, 2Н), 4,21 (д, J=6, 5 Гц, 2Н), 3,99 (с, 3H).
[957]
[958] Пример 93: N-(3-фтор-4-(6-фтор-5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
[959]
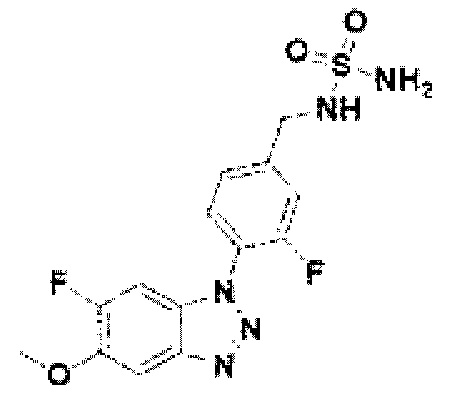
[960] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,89 (д, J=7,6 Гц, 1Н), 7,80 (т, J=8,0 Гц, 1Н), 7,69-7,57 (м, 2Н), 7,49 (д, J=8,1 Гц, 1Н), 7,37 (т, J=6,5 Гц, 1Н), 6,76 (с, 2Н), 4,25 (д, J=6,4 Гц, 2Н), 3,98 (с, 3H).
[961]
[962] Пример 94: 5-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)изоиндолин-2-сульфонамид;
[963]
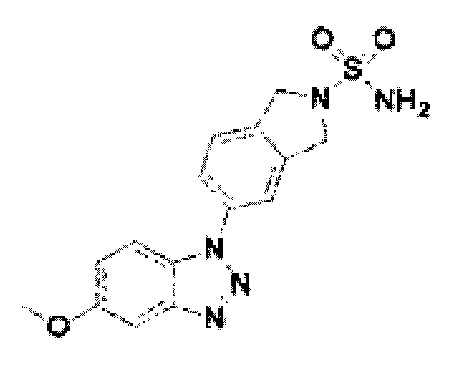
[964] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,80 (с, 1Н), 7,78 (д, J=9,1 Гц, 1Н), 7,72 (дд, J=8,1, 2,0 Гц, 1Н), 7,58-7,53 (м, 2Н), 7,22 (дд, J=9,1, 2,3 Гц, 1Н), 6,95 (с, 2Н), 4,57 (с, 2Н), 4,55 (с, 2Н), 3,82 (с, 3H).
[965]
[966] Пример 95: N-5-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-2,3-дигидро-1Н-инден-2-ил)сульфамид;
[967]
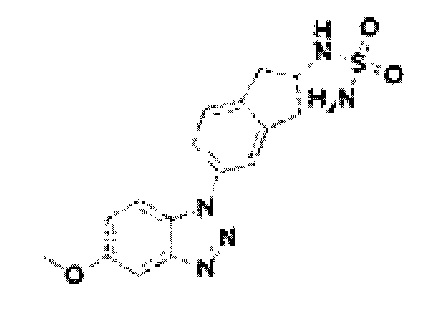
[968] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,80 (д, J=9,0 Гц, 1Н), 7,68 (с, 1Н), 7,62-7,58 (м, 2Н), 7,48 (д, J=3,8 Гц, 1Н), 7,27 (дд, J=9,1, 2,3 Гц, 1Н), 7,02 (д, J=7,0 Гц, 1Н), 6,68 (с, 2Н), 4,17 (дд, J=14,6, 7,3 Гц, 1Н), 3,89 (с, 3H), 3,30 (дд, J=10,4, 5,8 Гц, 2Н), 3,06-2,94 (м, 2Н).
[969]
[970] Пример 96: 6-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3,4-дигидроизохинолин-2(1Н)сульфонамид;
[971]
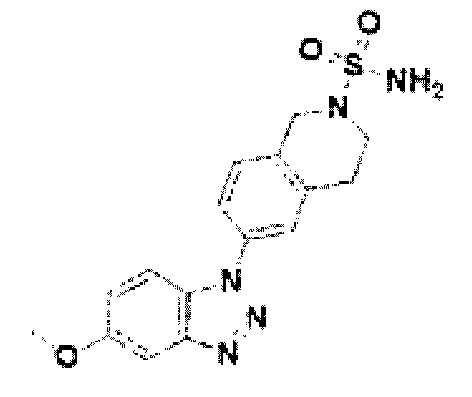
[972] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,84 (д, J=9,1 Гц, 1Н), 7,68-7,67 (м, 2Н), 7,60 (д, J=2,1 Гц, 1Н), 7,49 (д, J=9,0 Гц, 1Н), 7,28 (дд, J=9,1, 2,3 Гц, 1Н), 7,00 (с, 2Н), 4,33 (с, 2Н), 3,89 (с, 3H), 3,07 (т, J=5,7 Гц, 2Н), 2,50 (т, J=3,4 Гц, 2Н).
[973]
[974] Пример 97: 7-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3,4-дигидроизохинолин-2(1Н)сульфонамид;
[975]
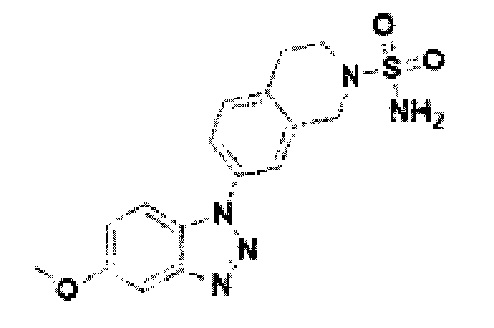
[976] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,89 (д, J=9,1 Гц, 1Н), 7,69 (дд, J=11,8, 3,6 Гц, 2Н), 7,61 (д, J=2,1 Гц, 1Н), 7,48 (д, J=8,2 Гц, 1Н), 7,29 (дд, J=9,1, 2,3 Гц, 1Н), 6,99 (с, 2Н), 4,39 (с, 2Н), 3,91 (с, 3H), 3,37 (т, J=5,9 Гц, 2Н), 3,05 (т, J=5,8 Гц, 2Н).
[977]
[978] Пример 98: 8-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-1,3,4,5-тетрагидро-2Н-бензо[с]азепин-2-сульфонамид;
[979]
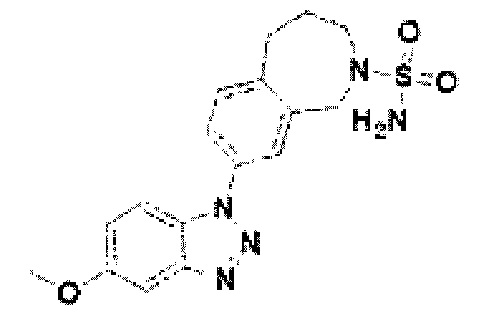
[980] ЖХМС (ESI) рассчитано для C17H19N5O3S [М+Н]+ 373,12, найдено m/z 374,1
[981]
[982] Пример 99: N-(4-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)-2,5-дифторбензил)сульфамид;
[983]
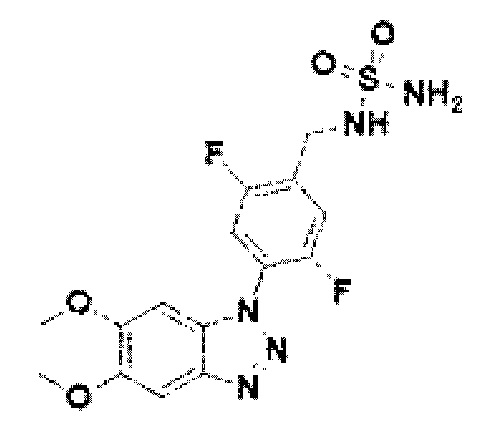
[984] ЖХМС (ESI) рассчитано для C14H15F2N5O4S [М+Н]+ 399,08, найдено m/z 400,1
[985]
[986] Пример 100: N-(4-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)-2,6-дифторбензил)сульфамид;
[987]
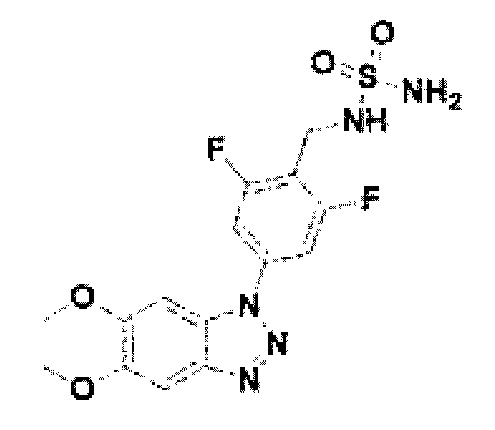
[988] ЖХМС (ESI) рассчитано для C14H15F2N5O4S [М+Н]+ 399, 08, найдено m/z 400,1
[989]
[990] Пример 101: 7-фтор-6-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3,4-дигидроизохинолин-2(1Н)-сульфонамид;
[991]
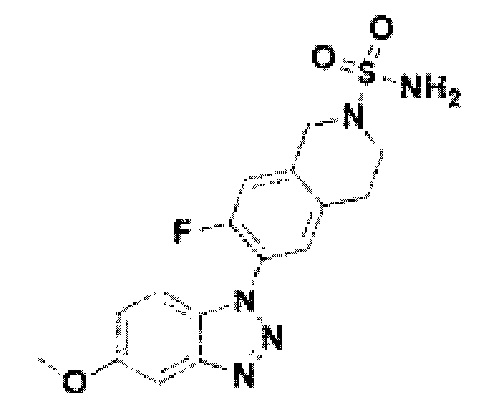
[992] ЖХМС (ESI) рассчитано для C16H16FN5O3S [М+Н]+ 377,1, найдено m/z 378,1
[993]
[994] Пример 102: 5-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)-изоиндолин-2-сульфонамид;
[995]
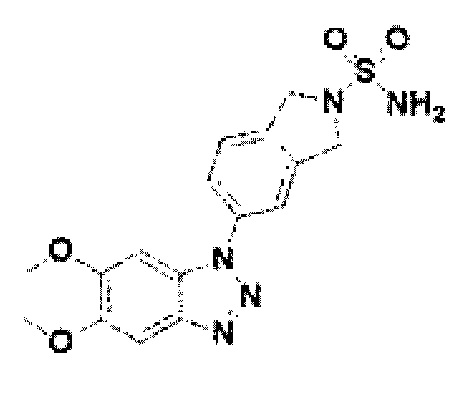
[996] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,85 (с, 1Н), 7,79 (дд, J=8,1, 1,8 Гц, 1Н), 7,63 (д, J=8,2 Гц, 1Н), 7,58 (с, 1Н), 7,23 (с, 1Н), 7,03 (с, 2Н), 4,66 (с, 2Н), 4,63 (с, 2Н), 3,91 (с, 3H), 3,90 (с, 3H).
[997]
[998] Пример 103: N-(5-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)-дигидро-1Н-инден-2-ил)сульфамид;
[999]
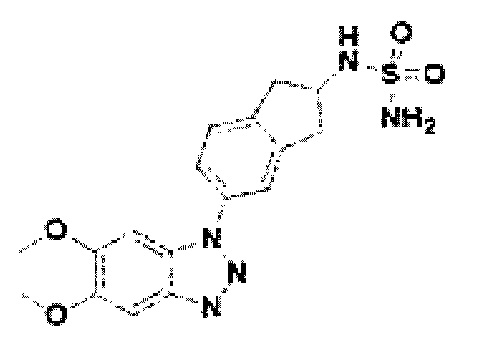
[1000] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,67 (с, 1Н), 7,61 (д, J=7,9 Гц, 1Н), 7,57 (д, J=5,6 Гц, 1Н), 7,49 (д, J=8,2 Гц, 1Н), 7,17 (с, 1Н), 7,02 (д, J=7,0 Гц, 1Н), 6,68 (с, 2Н), 4,17 (дд, J=14,7, 7,3 Гц, 1Н), 3,90 (с, 3H), 3,89 (с, 3H), 3,34-3,25 (м, 2Н), 3,06-2,97 (м, 2Н).
[1001]
[1002] Пример 104: N-(4-((5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)метил)фенил)сульфамид гидрохлорид;
[1003]
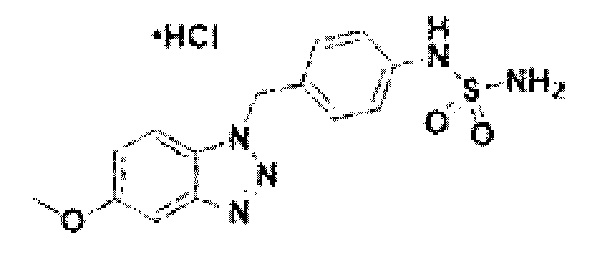
[1004] ЖХМС (ESI) рассчитано для C14H16ClN5O3S [М+Н]+ 369,07, найдено m/z 370,1
[1005]
[1006] Пример 105: N-(4-((5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)метил)бензил)сульфамид гидрохлорид;
[1007]
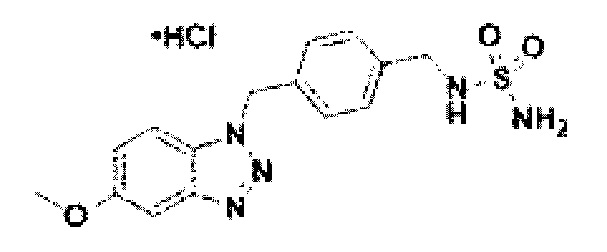
[1008] ЖХМС (ESI) рассчитано для C14H16ClN5O3S [М+Н]+ 383,08, найдено m/z 384,1
[1009]
[1010] Пример 106: N-((5-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)тиофен-2-ил)метил)сульфамид;
[1011]
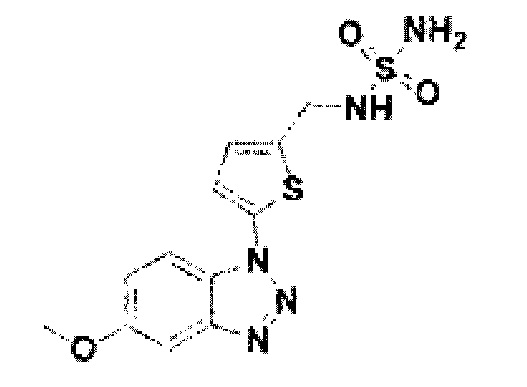
[1012] ЖХМС (ESI) рассчитано для C24H13N5O3S2 [М+Н]+ 339,41, найдено m/z 340
[1013]
[1014] Пример 107: N-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-5-метоксилтиофен-2-ил)метил)сульфамид;
[1015]
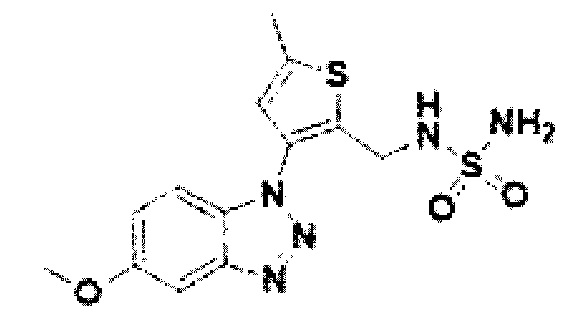
[1016] 1H ЯМР (400 МГц, MeOH-d4) δ 6,03 (д, J=9,6 Гц, 1Н), 5,91 (с, 1Н), 5,74 (д, J=8,7 Гц, 1Н), 5,47 (с, 1Н), 3,08 (с, 2Н), 2,75 (с, 2Н), 2,39 (с, 3Н), 1,03 (с, 3Н).
[1017]
[1018] Пример 108: N-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-бицикло[1.1.1]пентан-1-ил)сульфамид;
[1019]
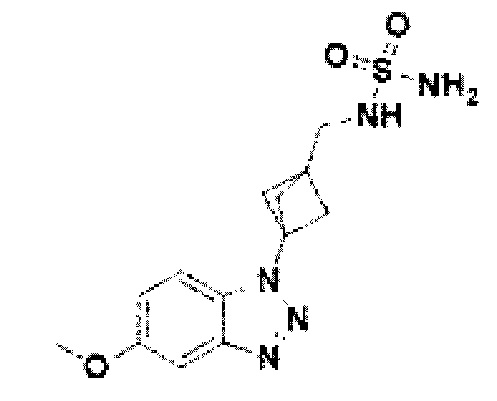
[1020] 1H ЯМР (400 МГц, ДМСО-d6) δ 7,78 (д, J=9,0 Гц, 1Н), 7,49 (д, J=2,0 Гц, 1Н), 7,21 (дд, J=9,0, 2,2 Гц, 1Н), 6,76 (т, J=6,2 Гц, 1Н), 6,58 (с, 2Н), 3,85 (с, 3Н), 3,23 (д, J=6,2 Гц, 2Н), 2,45 (с, 6Н).
[1021]
[1022] Пример 109: N-(4-(5-метокси-2Н-бензо[d][1,2,3]триазол-2-ил)фенил)сульфамид гидрохлорид;
[1023]
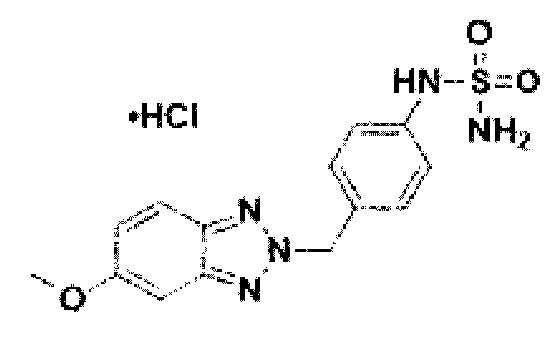
[1024] ЖХМС (ESI) рассчитано для C14H15N5O3S [М+Н]+ 333,09, найдено m/z 334,1.
[1025]
[1026] Пример 110: N-(4-((5-метокси-2Н-бензо[d][1,2,3]триазол-2-ил)бензил)сульфамид гидрохлорид;
[1027]
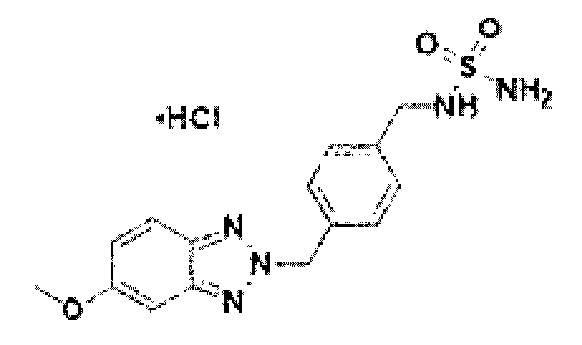
[1028] 1H ЯМР (400 МГц, ДМСО-d6) δ 7,90 (д, J=9,0 Гц, 1Н), 7,33-7,31 (м, 5Н), 7,00 (дд, J=9,1, 2,2 Гц, 1Н), 5,88 (с, 2Н), 4,03 (с, 2Н), 3,84 (с, 3Н).
[1029]
[1030] Пример 111: 2-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)пиперидин-1-ил)этан-1-сульфонилфторид;
[1031]
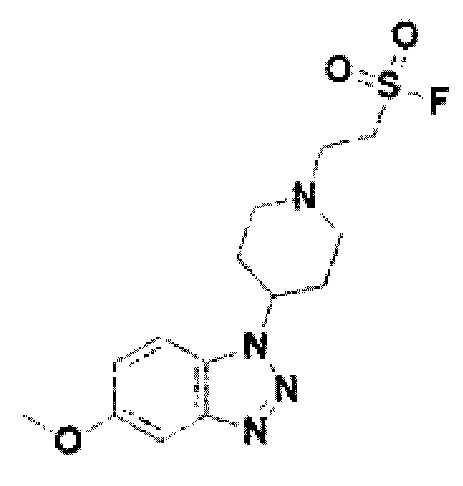
[1032] ЖХМС (ESI) рассчитано для C14H19FN4O3S [М+Н]+ 342, 12, найдено m/z 343,1
[1033]
[1034] Пример 112: N-(3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)метансульфонамид;
[1035]
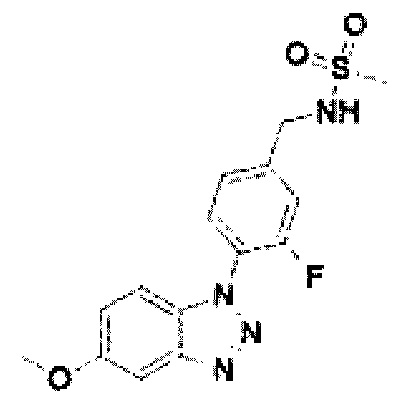
[1036] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,82 (д, J=7,9 Гц, 2Н), 7,63 (д, J=2,1 Гц, 1Н), 7,60 (д, J=11,6 Гц, 1Н), 7,57 (с, 1Н), 7,50 (д, J=7,3 Гц, 1Н), 7,28 (дд, J=9,0, 2,3 Гц, 1Н), 4,35 (д, J=6,4 Гц, 2H), 3,90 (с, 3Н), 2,98 (с, 3Н).
[1037]
[1038] Пример 113: N-(3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)этансульфонамид;
[1039]
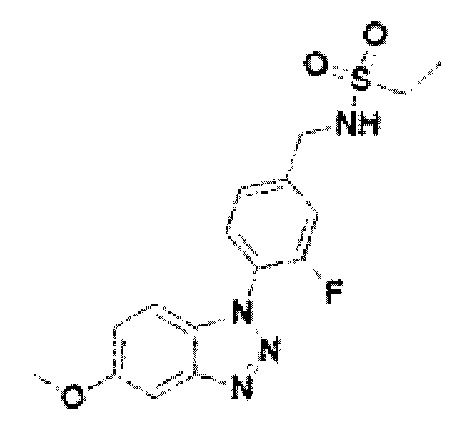
[1040] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,83 (дд, J=9,9, 6,1 Гц, 2Н), 7,64-7,59 (м, 1Н), 7,57 (д, J=6,9 Гц, 1Н), 7,55-7,46 (м, 1Н), 7,28 (дд, J=9,1, 2,3 Гц, 1Н), 4,33 (д, J=6,3 Гц, 2Н), 3,90 (с, 3Н), 3,07 (д, J=7,4 Гц, 2Н), 1,24 (д, J=2,6 Гц, 3Н).
[1041]
[1042] Пример 114: N-(3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)-4-метилбензолсульфонамид;
[1043]
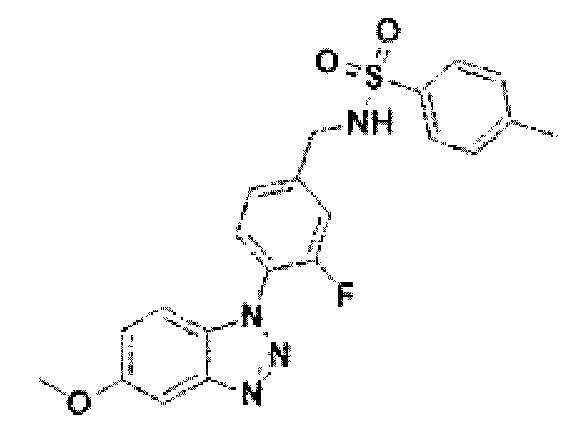
[1044] 1H ЯМР (400 МГц, ДМСО-d6) δ 8,33 (т, J=6,4 Гц, 1Н), 7,71 (дд, J=16,0, 8,1 Гц, 3Н), 7,62 (д, J=2,1 Гц, 1Н), 7,51-7,41 (м, 2Н), 7,38 (д, J=8,0 Гц, 3Н), 7,29 (дд, J=9,0, 2,3 Гц, 1Н), 4,17 (д, J=6,4 Гц, 2Н), 3,90 (с, 3Н), 2,35 (с, 3Н).
[1045]
[1046] Пример 115: N-(3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)метансульфонимидамид;
[1047]
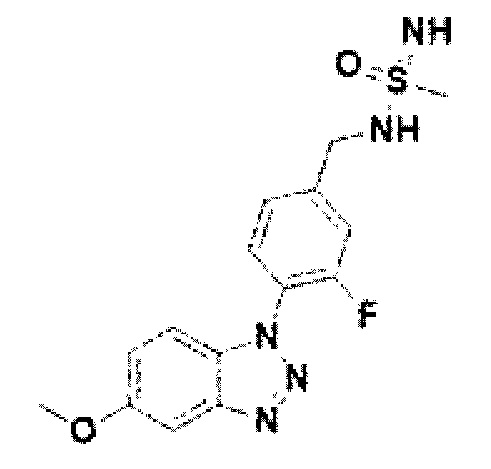
[1048] ЖХМС (ESI) рассчитано для C15H16FN5O2S [М+Н]+ 349,1 найдено m/z 350,1
[1049]
[1050] Пример 116: 3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензойная кислота;
[1051]
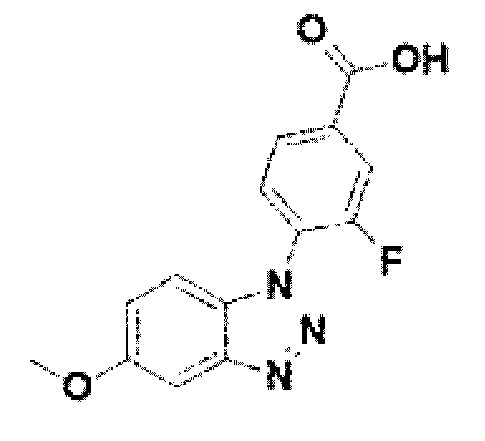
[1052] 1Н ЯМР (400 МГц, ДМСО-d6) δ 13,86 (ушир.с, 1Н), 8,12-7,93 (м, 3Н), 7,64 (дд, J=9,1, 2,5 Гц, 2Н), 7,31 (дд, J=9,1, 2,2 Гц, 1Н), 3,90 (с, 3Н).
[1053]
[1054] Пример 117: диэтил-(3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)фосфоамидит;
[1055]
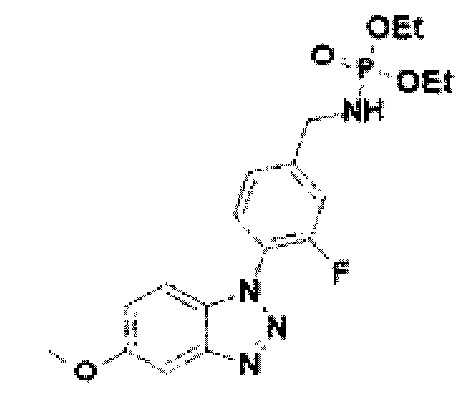
[1056] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,80 (т, J=8,0 Гц, 1Н), 7,63 (д, J=2,1 Гц, 1Н), 7,58 (д, J=11,6 Гц, 1Н), 7,52 (дд, J=9,0, 2,1 Гц, 1Н), 7,48 (д, J=8,2 Гц, 1Н), 7,28 (дд, J=9,0, 2,2 Гц, 1Н), 5,70 (дд, J=7,3, 4,6 Гц, 1Н), 4,16-4,09 (м, 2Н), 3,98-3,90 (м, 4Н), 3,89 (с, 3Н), 1,21 (т, J=7,1 Гц, 42, 6Н).
[1057]
[1058] Пример 118: 4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)фосфоновая кислота;
[1059]
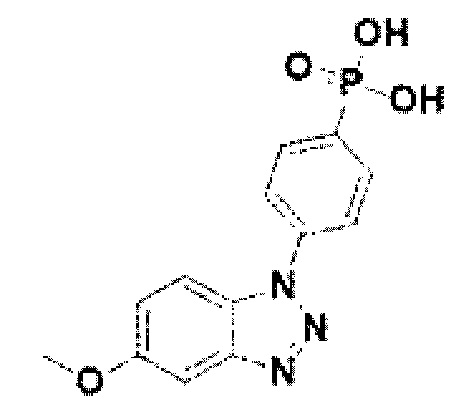
[1060] 1Н ЯМР (400 МГц, ДМСО-d6) δ 8,09-7,87 (м, 5Н), 7,64 (д, J=2,2 Гц, 1Н), 7,32 (дд, J=9,1, 2,3 Гц, 1Н), 3,90 (с, 3Н).
[1061]
[1062] Пример 119: 4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)фосфоновая кислота;
[1063]
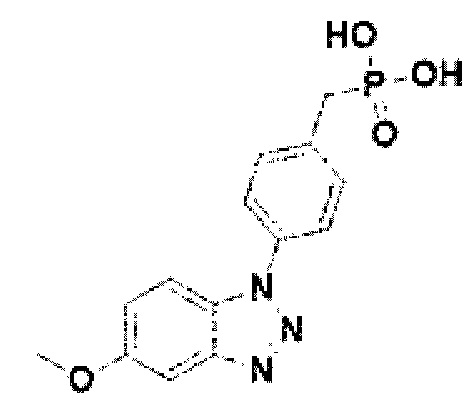
[1064] 1Н ЯМР (400 МГц, ДМСО-d6) δ 7,79 (дд, J=8,6, 6,2 Гц, 3Н), 7,60 (д, J=2,2 Гц, 1Н), 7,54 (дд, J=8,5, 2,2 Гц, 2Н), 7,28 (дд, J=9,1, 2,3 Гц, 1Н), 3,89 (с, 3Н), 3,11 (д, J=21,5 Гц, 2Н).
[1065]
[1066] Пример 120: 3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)бороновая кислота;
[1067]
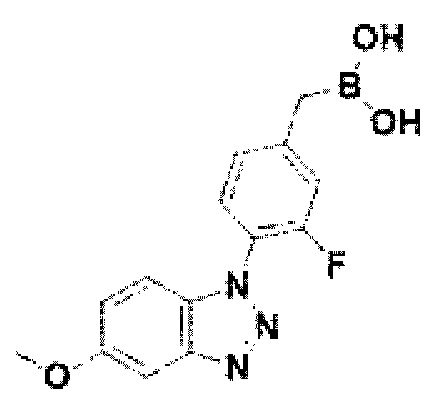
[1068] ЖХМС (ESI) рассчитано для C14H13BFN3O3 [М+Н]+ 301,10, найдено m/z 302,1
[1069]
[1070] Пример 121: 4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенэтил)бороновая кислота;
[1071]
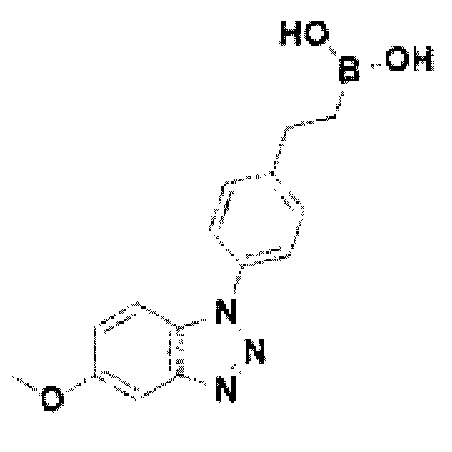
[1072] ЖХМС (ESI) рассчитано для C15H16BN3O3 [М+Н]+ 297,13, найдено m/z 298,1
[1073]
[1074] Пример 122: N-(4-(5-метокси-1Н-индол-1-ил)бензил)сульфамид;
[1075]
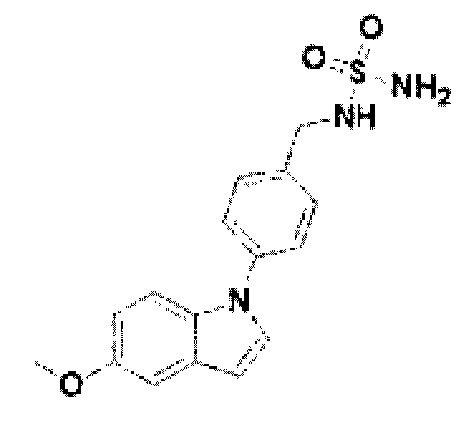
[1076] ЖХМС (ESI) рассчитано для C16H17N3O3S [М+Н]+ 330,24, найдено m/z 331,1
[1077]
[1078] Пример 123: N-(4-(5-метокси-1Н-бензо[d]имидазол-1-ил)бензил)сульфамид
[1079]
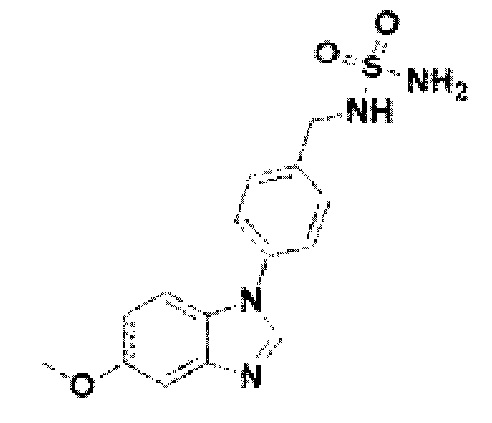
[1080] ЖХМС (ESI) рассчитано для C15H16N4O3S [М+Н]+ 332,09, найдено m/z 333,1
[1081]
[1082] Пример 124: N-(4-(5-метокси-1Н-индазол-1-ил)бензил)сульфамид;
[1083]
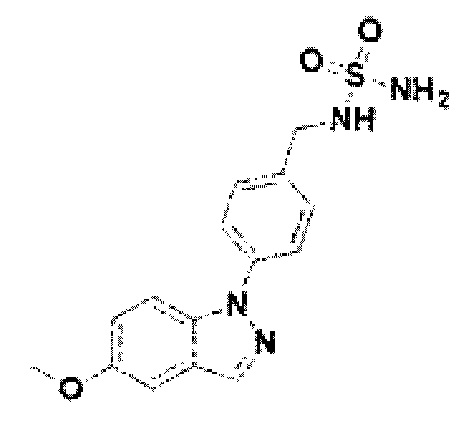
[1084] ЖХМС (ESI) рассчитано для C15H16N4O3S [М+Н]+ 332,09, найдено m/z 333,1
[1085]
[1086] [Экспериментальный пример]
[1087] Следующие эксперименты проводили на примерах 1-124, полученных, как описано выше.
[1088]
[1089] Экспериментальный пример 1: Анализ фермента ENPP1 с субстратом cGAMP
[1090] ENPP1 гидролизует нуклеотиды или производные нуклеотидов с образованием нуклеозид-5'-монофосфата и пирофосфата. Кроме того, ENPP1 гидролизует 2',3'-cGAMP с образованием 5'-аденозинмонофосфата (AMP) и 5'-гуанозинмонофосфата (GMP). AMP, полученный в результате реакции, измеряли с помощью набора AMP-Glo® (Promega). Набор AMP-Glo® содержит два реагента. Первый реагент прекращает ферментативную реакцию получения AMP, удаляет АТР и преобразует полученный AMP в ADP. Второй реагент преобразует ADP в АТР, который используется для генерации люминесценции в люциферазной реакции. Измеряемая величина люминесценции пропорциональна количеству AMP, вырабатываемого ENPP1.
[1091] Конечный реакционный раствор содержал 50 мМ Трис-буфера (рН 8,5), 250 мМ NaCl, 0,5 мМ CaCl2, 1 мкМ ZnCl2, 5% глицерина и 1% ДМСО. Последовательно разбавленные ингибиторы ENPP1 (обычно в диапазоне от 10 мкМ до 0,5 нМ) предварительно сохраняли с рекомбинантными ферментами ENPP1 человека (R & D системы) при 3 нг/реакция и комнатной температуре (КТ) в течение 5-10 мин. Реакцию инициировали добавлением cGAMP (в конечной концентрации 5 мкМ) и осуществляли при 37°С в течение 90 мин. В конце реакции добавляли 10 мкл первого реагента AMP-Glo, чтобы остановить реакцию, и продукт хранили при комнатной температуре в течение 1 ч. После хранения добавляли 20 мкл раствора для обнаружения AMP (смесь реагента II AMP-Glo и Kinase-Glo в соотношении 1:100) и хранили при комнатной температуре в течение 1 ч. Сигналы люминесценции измеряли с помощью планшет-ридера Victor® (Perkin Elmer). Контроль максимальной активности (содержащий ферменты и субстраты в присутствии 1% ДМСО; МАХ) и контроль минимальной активности (содержащий субстраты и 1% ДМСО; MIN) оценивали одновременно. В каждом эксперименте также тестировали последовательно разбавленные эталонные ингибиторы ENPP1. IC50, показывающий % остаточной активности в зависимости от концентрации соединения, определяли путем подгонки кривых ингибирования с использованием 3-параметрового анализа на основе программного обеспечения GraphPad Prism®. Последовательно разбавленные образцы одного соединения тестировали два или более раз и рассчитывали среднее значение IC50 для каждого соединения.
[1092]
[1093] Экспериментальные результаты показаны в таблицах 1 и 2 ниже.
[1094]
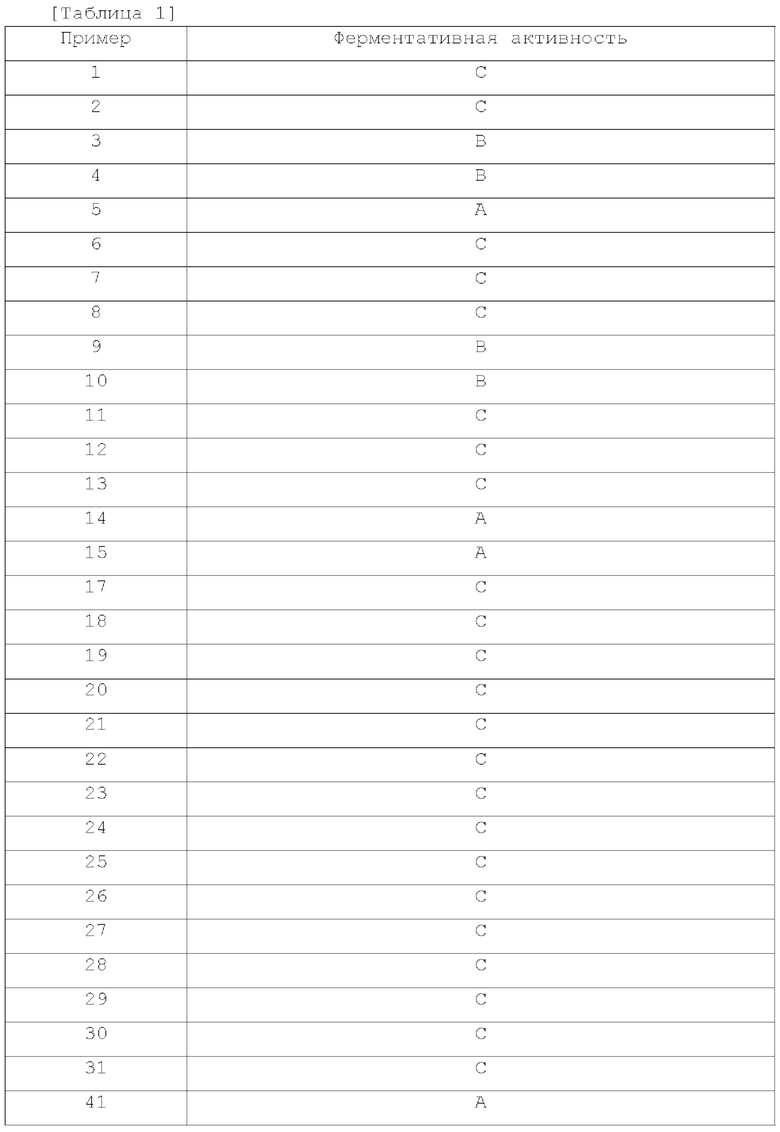
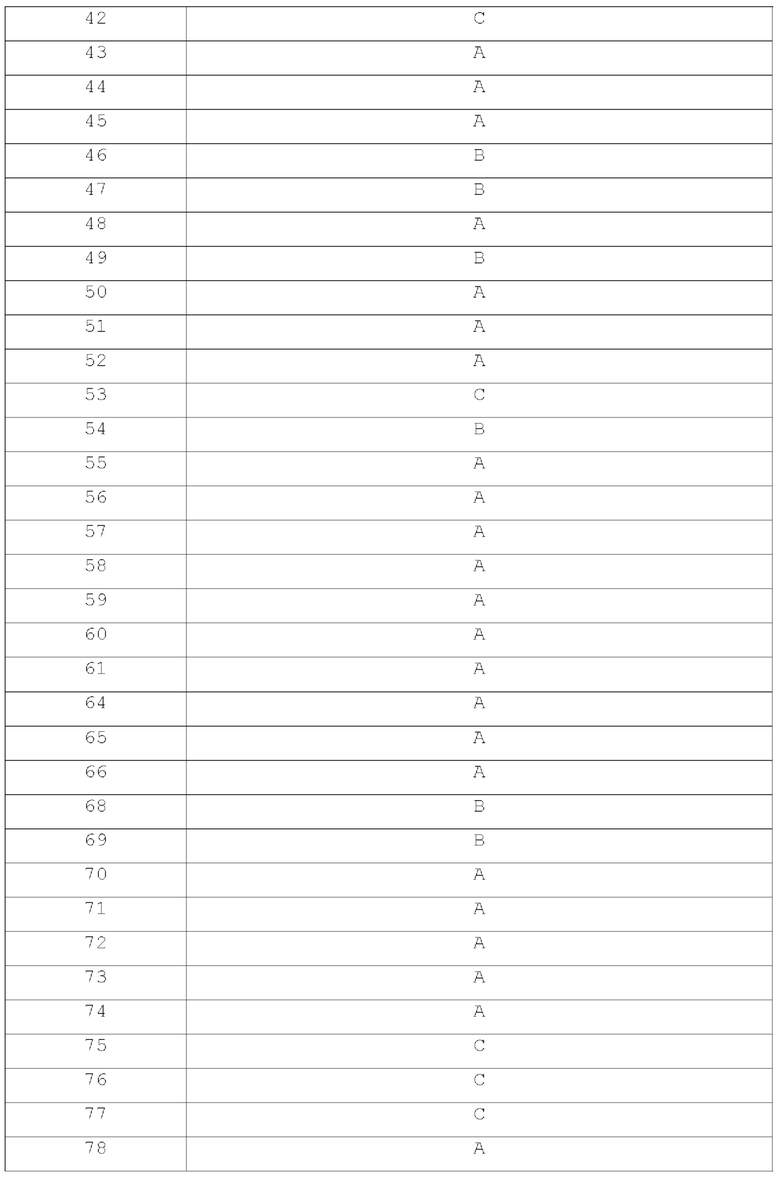
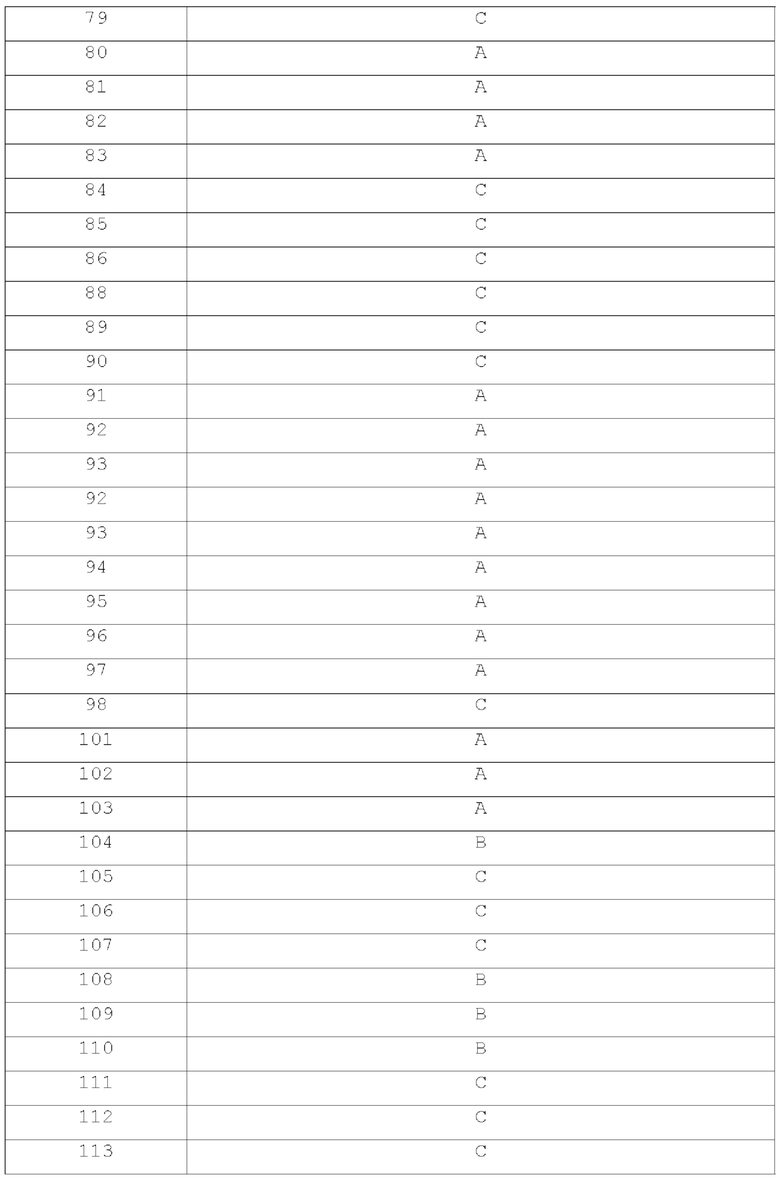

[1095]
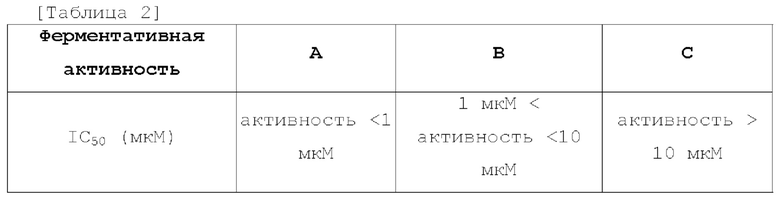
[1096] [Экспериментальный пример 2]
[1097] Следующие эксперименты проводили на примерах, полученных, как описано выше.
[1098] Экспериментальный пример 2: Люциферазный анализ клеток НСТ116-Dual
[1099] Клетки НСТ116-Dual™ экспрессируют гены, кодирующие люциферазу, секретируемую под контролем промотора стимулируемого интерфероном гена 54 (ISG54), наряду с пятью элементами ответа, простимулированными интерфероном. Клеточная линия НСТ116-Dual™ использовалась для измерения и мониторинга активности регуляторного фактора интерферона 3 (IRF3), который индуцирует выработку интерферона I типа и связан с нисходящей передачей сигналов, и Lucia, секретируемый в культуральной среде, использовался для создания люминесценции в люциферазной реакции.
[1100] Клетки НСТ116-Dual™ культивировали при 2×104 клеток/лунку (93,4 мкл) в 96-луночном планшете в течение одного дня в среде DMEM, содержащей 10% FBS и 25 мМ HEPES (рН 7,2-7,5). Клетки обрабатывали 3,3 мкл ингибитора ENPP1 (обычно 10 мкМ) и затем 3,3 мкл cGAMP (10 мкМ), чтобы довести конечный объем до 100 мкл (конечная доля ДМСО составляла 0,1%). Клетки, обработанные ингибитором ENPP1 и cGAMP, культивировали при 37°С в течение 48 ч, и к 20 мкл среды для культивирования клеток добавляли 50 мкл реакционного раствора Quanti-Luc для измерения активности люциферазы. Повышение регуляторного фактора интерферона 3 (IRF3), вызванное соединением, по сравнению с cGAMP, определяли как кратность.
[1101] Экспериментальные результаты показаны в таблицах 3 и 4 ниже.
[1102]
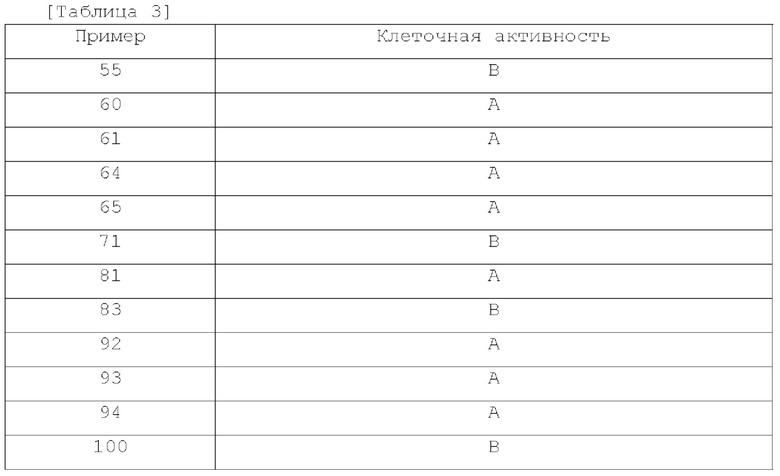
[1103]

[1104] [Пример композиции]
[1105] Вместе с тем, новое соединение, представленное формулой 1 в соответствии с настоящим изобретением, может быть приготовлено в различных формах в соответствии с назначением. Ниже приведены примеры некоторых способов получения композиций для включения соединения, представленного формулой 1 по настоящему изобретению, в качестве активного ингредиента, но настоящее изобретение этим не ограничивается.
[1106]
[1107] Пример композиции 1: Таблетка (прямое прессование)
[1108] 5,0 мг активного ингредиента просеивали, смешивали с ним 14,1 мг лактозы, 0,8 мг кросповидона USNF и 0,1 мг стеарата магния, и смесь спрессовывали в таблетки.
[1109] Пример композиции 2: Таблетка (влажное гранулирование)
[1110] 5,0 мг активного ингредиента просеивали и смешивали с 16,0 мг лактозы и 4,0 мг крахмала. 0,3 мг полисорбата 80 растворяли в чистой воде и соответствующее количество полученного раствора добавляли к полученной смеси, с последующим гранулированием. Гранулы высушивали, просеивали и смешивали с 2,7 мг коллоидного диоксида кремния и 2,0 мг стеарата магния. Гранулы спрессовывали в таблетки.
[1111] Пример композиции 3: Порошки и капсулы
[1112] 5,0 мг активного ингредиента просеивали и затем смешивали с 14,8 мг лактозы, 10,0 мг поливинилпирролидона и 0,2 мг стеарата магния. Твердые желатиновые капсулы №5 заполняли полученной смесью с использованием подходящего устройства.
[1113] Пример композиции 4: Инъекционный раствор
[1114] Инъекционные растворы готовили путем добавления 100 мг активного ингредиента, а также 180 мг маннита, 26 мг Na2HPO4⋅12H2O и 2,974 мг дистиллированной воды.
[1115]
[1116] Хотя варианты осуществления настоящего изобретения были описаны выше, специалистам в данной области техники будет очевидно, что настоящее изобретение может быть реализовано в других конкретных вариантах осуществления без изменения технических концепций или существенных признаков настоящего изобретения. Поэтому следует понимать, что указанные выше варианты осуществления являются иллюстративными, но не ограничивающими во всех отношениях.
| название | год | авторы | номер документа |
|---|---|---|---|
| Новые соединения пиридопиримидинона для модулирования каталитической активности гистонлизиндеметилаз (KDMS) | 2015 |
|
RU2684396C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ ТРИАЗОЛОПИРАЗИНА И ИХ ПРИМЕНЕНИЕ | 2013 |
|
RU2643361C2 |
| НОВОЕ СОЕДИНЕНИЕ БИФЕНИЛА ИЛИ ЕГО СОЛЬ | 2016 |
|
RU2726622C2 |
| НОВОЕ ПРОИЗВОДНОЕ ПИПЕРИДИНА И СОДЕРЖАЩАЯ ЕГО ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ИНГИБИРОВАНИЯ АУТОТАКСИНА | 2022 |
|
RU2834850C2 |
| СПИРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ | 2016 |
|
RU2745069C2 |
| 4-(ИМИДАЗО[1,2-а]ПИРИДИН-3-ИЛ)-ПИРИМИДИНОВЫЕ ПРОИЗВОДНЫЕ | 2020 |
|
RU2822388C2 |
| ПРОИЗВОДНЫЕ ХИНОЛИН-2-ОНА В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗЫ C-KIT | 2016 |
|
RU2754858C2 |
| ЗАМЕЩЕННЫЕ ПИРАЗОЛОПИРИМИДИНЫ И ЗАМЕЩЕННЫЕ ПУРИНЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ УБИКВИТИН-СПЕЦИФИЧЕСКОЙ ПРОЦЕССИРУЮЩЕЙ ПРОТЕАЗЫ 1 (USP1) | 2019 |
|
RU2833222C2 |
| 1, 2, 4-ТРИАЗОЛЬНОЕ ПРОИЗВОДНОЕ, СПОСОБЫ ЕГО ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПРОМЕЖУТОЧНОЕ СОЕДИНЕНИЕ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2003 |
|
RU2288223C2 |
| ИНГИБИТОРЫ СЕРИН/ТРЕОНИН КИНАЗЫ ДЛЯ ЛЕЧЕНИЯ ГИПЕРПРОЛИФЕРАТИВНЫХ ЗАБОЛЕВАНИЙ | 2013 |
|
RU2644947C2 |
Настоящее изобретение относится производным бензотриазола, а именно к соединению формулы 1 или его фармацевтически приемлемой соли, в котором W1 представляет собой С; W2 представляет собой С; W3 представляет собой С; W4 представляет собой С; W5 представляет собой N; W6 представляет собой N; W7 представляет собой N; где каждый из R1, R2, R3 и R4 независимо представляет собой водород, гидроксильную группу, галогенную группу, -CF3, -(O)CF3, C1-С6 алкильную группу, C1-С6 алкоксигруппу или аминогруппу -NR7R8; Z присутствует или отсутствует, при этом, когда Z присутствует, Z представляет собой -СН2 или -С2Н4; R5 представляет собой -А-R6, где А представляет собой С3-С6 циклоалкил, С5 бициклоалкил, С4-С6 гетероциклическую группу, содержащую один гетероатом N, необязательно конденсированную с фенилом, фенильную группу или С4-С5 гетероарильную группу, содержащую один гетероатом, выбранный из группы, состоящей из N и S, R6 представляет собой карбоксильную группу (-С(О)ОН), нитрильную группу (-CN), -S(O)2NHR7, -CH2NHS(О)2NHR7, СН(СН3)NHS(О)2NHR7, -СН(СН3)NHS(О)2NH2, -CH2NHS(О)2NH2, CH2NR7S(О)2NH2, -S(O)2NH2, -C2H4NHS(О)2NH2, -CH2NHS(О)2R7, CH2NHSO(NH)R7, -CH2NHP(О)OR7OR8, или -CH2NHP(O)(ОН)2, А может быть дополнительно замещен одним или двумя заместителями, независимо выбранными из группы, состоящей из галогеновой группы, метильной группы, нитрильной группы (-CN) и метоксигруппы, помимо R6, и каждый из R7 и R8 независимо представляет собой водород, C1-С6 алкильную группу, фенильную группу, замещенную или незамещенную C1-С6 алкилом, аминогруппу (-NH2), -Вос, или -NHBoc. Изобретение также относится к фармацевтической композиции, ингибитору ENPP 1 и активатору сигнального пути STING на основе указанного соединения. Технический результат заключается в создании альтернативных соединений для лечения ENPP1-опосредованных заболеваний, а также заболеваний, опосредованных сигнальным путём STING. 5 н. и 2 з.п. ф-лы, 4 табл., 124 пр.
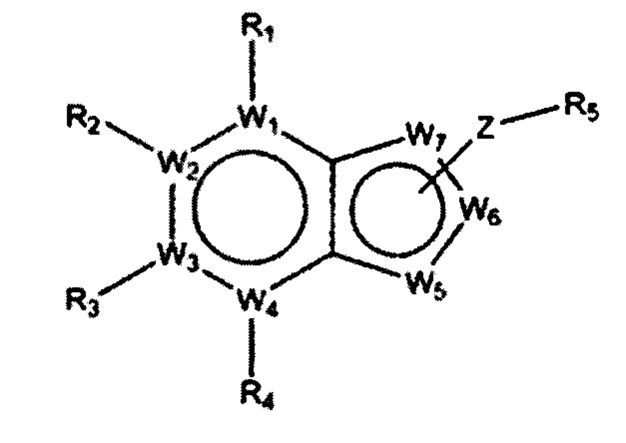
1. Соединение, выбранное из соединения, представленного следующей формулой 1, или его фармацевтически приемлемой соли:
[Формула 1]
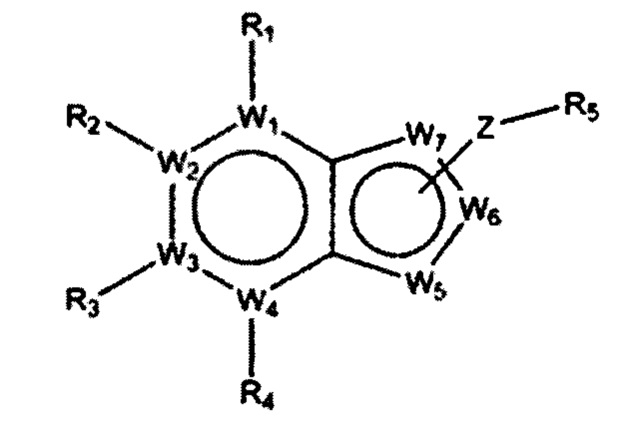
где
W1 представляет собой С;
W2 представляет собой С;
W3 представляет собой С;
W4 представляет собой С;
W5 представляет собой N;
W6 представляет собой N;
W7 представляет собой N;
где каждый из R1, R2, R3 и R4 независимо представляет собой водород, гидроксильную группу, галогенную группу, -CF3, -(O)CF3, C1-С6 алкильную группу, C1-С6 алкоксигруппу или аминогруппу -NR7R8;
Z присутствует или отсутствует, при этом, когда Z присутствует, Z представляет собой -СН2 или -С2Н4;
R5 представляет собой -А-R6,
где А представляет собой С3-С6 циклоалкил, С5 бициклоалкил, С4-С6 гетероциклическую группу, содержащую один гетероатом N, необязательно конденсированную с фенилом, фенильную группу или С4-С5 гетероарильную группу, содержащую один гетероатом, выбранный из группы, состоящей из N и S,
R6 представляет собой карбоксильную группу (-С(О)ОН), нитрильную группу (-CN), -S(O)2NHR7, -CH2NHS(О)2NHR7, СН(СН3)NHS(О)2NHR7, -СН(СН3)NHS(О)2NH2, -CH2NHS(О)2NH2, CH2NR7S(О)2NH2, -S(O)2NH2, -C2H4NHS(О)2NH2, -CH2NHS(О)2R7, CH2NHSO(NH)R7, -CH2NHP(О)OR7OR8, или -CH2NHP(O)(ОН)2,
А может быть дополнительно замещен одним или двумя заместителями, независимо выбранными из группы, состоящей из галогеновой группы, метильной группы, нитрильной группы (-CN) и метоксигруппы, помимо R6, и
каждый из R7 и R8 независимо представляет собой водород, C1-С6 алкильную группу, фенильную группу, замещенную или незамещенную C1-С6 алкилом, аминогруппу (-NH2), -Вос, или -NHBoc.
2. Соединение по п. 1, в котором А представляет собой замещенный или незамещенный циклопентан, замещенный или незамещенный циклогексан, замещенный или незамещенный бензол, замещенный или незамещенный бициклопентан, замещенный или незамещенный тиофен, замещенный или незамещенный пиридин, замещенный или незамещенный пиперидин или замещенный или незамещенный пиррол.
3. Соединение, выбранное из группы, состоящей из следующих соединений №№1-124, или его фармацевтически приемлемая соль:
Соединение 1: 5-метокси-1-(пиперидин-4-ил)-1Н-бензо[d][1,2,3]триазол гидрохлорид;
Соединение 2: 4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)циклогексил)метананилин;
Соединение 3: 5-метокси-1-(пиперидин-4-илметил)-1Н-бензо[d][1,2,3]триазол;
Соединение 4: 4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)анилин гидрохлорид;
Соединение 5: 4-(1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
Соединение 6: 4-(4-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
Соединение 7: 4-(6-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
Соединение 8: 4-(7-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
Соединение 9: 4-(4,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
Соединение 10: 4-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин гидрохлорид;
Соединение 11: 2-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)этан-1-амин гидрохлорид;
Соединение 12: 1-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)-N-метилметанамин гидрохлорид;
Соединение 13: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-бензил)циклопропанамин гидрохлорид;
Соединение 14: (S)-1-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)этан-1-амин гидрохлорид;
Соединение 15: 3-хлор-4-(5-метокси-1Н-бензо[d][1,2,3] триазол-1-ил)фенил)метанамин гидрохлорид;
Соединение 16: 3-фтор-4-(5-метокси-1Н-бензо[d][1, 2, 3] триазол-1-ил)фенил)метанамин гидрохлорид;
Соединение 17: 2,5-дифтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин;
Соединение 18: 2,6-дифтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин;
Соединение 19: 4-(5-этокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторфенил)метанамин;
Соединение 20: 3-фтор-4-(5-изопропокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин;
Соединение 21: 4-(5-(1,1-дифторэтил)-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин;
Соединение 22: 4-(5-(1,1-дифторэтил)-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторфенил)метанамин;
Соединение 23: 3-фтор-4-(5-фторметокси)-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин;
Соединение 24: 4-(5-дифторметокси)-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторфенил)метанамин;
Соединение 25: 7-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-1.2.3.4- тетрагидроизохинолин гидрохлорид;
Соединение 26: 7-фтор-6-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-1,2,3,4-тетрагидроизохинолин гидрохлорид;
Соединение 27: 8-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-2.3.4.5- тетрагидро-1Н-бензо[с]азепин гидрохлорид;
Соединение 28: 4-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)-2,5-дифторфенил)метанамин;
Соединение 29: 1-(изоиндолин-5-ил)-5,6-диметокси-1Н-бензо[d][1,2,3]триазол гидрохлорид;
Соединение 30: 3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бицикло[1.1.1]пентан-1-ил)метанамин;
Соединение 31: 3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-5-метилтиофен-2-ил)метанамин гидрохлорид;
Соединение 32: трет-бутил-((4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)пиперидин-1-ил)сульфонил) карбамат;
Соединение 33: трет-бутил-((4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)метил)пиперидин-1-ил)сульфонил)карбамат;
Соединение 34: трет-бутил(N-(1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфонил)карбамат;
Соединение 35: трет-бутил(N-(4-(4-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфонил)карбамат;
Соединение 36: трет-бутил(N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфонил)карбамат;
Соединение 37: трет-бутил(N-(4-(6-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфонил)карбамат;
Соединение 38: трет-бутил(N-(4-(7-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфонил)карбамат;
Соединение 39: трет-бутил((S)-N-(1-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)этил)сульфонил)карбамат;
Соединение 40: трет-бутил-((6-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3,4-дигидроизохинолин-2(1Н)-ил)сульфонил)карбамат;
Соединение 41: N-((3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)циклопентил)метил)сульфамид;
Соединение 42: 4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)пиперидин-1-сульфонамид;
Соединение 43: N-((4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)циклогексил)метил)сульфамид;
Соединение 44: 2-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)пиперидин-1-ил)этан-1-сульфонамид;
Соединение 45: 4-((5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)метил)пиперидин-1-сульфонамид;
Соединение 46: N-(4-(1Н-бензо[d] [1,2,3]триазол-1-ил)бензил)сульфамид;
Соединение 47: N-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)сульфамид;
Соединение 48: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)сульфамид гидрохлорид;
Соединение 49: N-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
Соединение 50: N-(4-(4-метокси-1Н-бензо[d] [1,2,3]триазол-1-ил)бензил)сульфамид;
Соединение 51: N-(4-(5-метокси-1Н-бензо[d] [1,2,3]триазол-1-ил)бензил)сульфамид гидрохлорид;
Соединение 52: N-(4-(6-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
Соединение 53: N-(4-(7-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
Соединение 54: N-(4-(4,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
Соединение 55: N-(4-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
Соединение 56: N-(4-(1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторбензил)сульфамид;
Соединение 57: N-(4-(1Н-бензо[d][1,2,3]триазол-1-ил)-2,3-дифторбензил)сульфамид;
Соединение 58: N-(4-(1Н-бензо[d][1,2,3]триазол-1-ил)-3,5-дифторбензил)сульфамид;
Соединение 59: N-(3-хлор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
Соединение 60: N-(2-фтор-4-(5-метокси-1Н-бензо[d] [1,2,3]триазол-1-ил)бензил)сульфамид;
Соединение 61: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторбензил)сульфамид;
Соединение 62: N-(2,5-дифтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
Соединение 63: N-(2,6-дифтор-4-(5-метокси-1Н-бензо[d] [1,2,3]триазол-1-ил)бензил)сульфамид;
Соединение 64: N-(3,5-дифтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-бензил)сульфамид;
Соединение 65: N-(2,3-дифтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-бензил)сульфамид;
Соединение 66: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3-метилбензил)сульфамид;
Соединение 67: N-(3-циано-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3-бензил)сульфамид;
Соединение 68: N-(3-метокси-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
Соединение 69: N-(4-(5-метокси-6-метил-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
Соединение 70: N-(3-фтор-4-(5-метокси-6-метил-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
Соединение 71: N-(4-(5,6-диметокси-1Н-бензо[d] [1,2,3]триазол-1-ил)-3-фторбензил)сульфамид;
Соединение 72: N-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенэтил)сульфамид;
Соединение 73: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенэтил)сульфамид гидрохлорид;
Соединение 74: N-(3-фтор-4-(5-гидрокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил) сульфамид;
Соединение 75: N-(3-фтор-4-(5-метил-1Н-бензо[d] [1,2,3]триазол-1-ил)бензил)сульфамид;
Соединение 76: N-(4-(5-этокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторбензил)сульфамид;
Соединение 77: N-(3-фтор-4-(5-изопропокси-1Н-бензо[d] [1,2,3]триазол-1-ил)бензил)сульфамид;
Соединение 78: N-(5-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)пиридин-2-ил)метил)сульфамид;
Соединение 79: (N-(6-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)пиридин-3-ил)метил)сульфамид;
Соединение 80: N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)-N-метил)сульфамид;
Соединение 81: N-(3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)-N-метилсульфамид;
Соединение 82: N-циклопропил-N-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
Соединение 83: (S)-N-(1-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)этил)сульфамид;
Соединение 84: N-(4-(5-трифторметил)-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
Соединение 85: N-(3-фтор-4-(5-трифторметил)-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
Соединение 86: 4-(5-(1,1-дифторэтил)-1Н-бензо[d][1,2,3]триазол-1-ил)фенил)метанамин;
Соединение 87: N-(4-(5-диметиламино)-1Н-бензо[d][1,2,3]триазол-1-ил) -3-фторбензил)сульфамид;
Соединение 88: N-(3-фтор-4-(5-фторметокси)-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
Соединение 89: N-(4-(5-трифторметокси)-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
Соединение 90: N-(3-фтор-4-(5-трифторметокси)-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
Соединение 91: N-(4-(5-дифторметокси)-1Н-бензо[d][1,2,3]триазол-1-ил)-3-фторбензил)сульфамид;
Соединение 92: N-(4-(6-фтор-5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)сульфамид;
Соединение 93: N-(3-фтор-4-(6-фтор-5-метокси-1Н-бензо[d] [1,2,3]триазол-1-ил)бензил)сульфамид;
Соединение 94: 5-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)изоиндолин-2-сульфонамид;
Соединение 95: N-5-(5-метокси-1Н-бензо[d] [1,2,3]триазол-1-ил)-2,3-дигидро-1Н-инден-2-ил)сульфамид;
Соединение 96: 6-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3,4-дигидроизохинолин-2(1Н)сульфонамид;
Соединение 97: 7-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3,4-дигидроизохинолин-2(1Н)сульфонамид;
Соединение 98: 8-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-1,3,4,5-тетрагидро-2Н-бензо[с]азепин-2-сульфонамид;
Соединение 99: N-(4-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)-2,5- дифторбензил)сульфамид;
Соединение 100: N-(4-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)-2,6-дифторбензил)сульфамид;
Соединение 101: 7-фтор-6-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-3,4-дигидроизохинолин-2(1Н)-сульфонамид;
Соединение 102: 5-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)-изоиндолин-2-сульфонамид;
Соединение 103: N-(5-(5,6-диметокси-1Н-бензо[d][1,2,3]триазол-1-ил)-дигидро-1Н-инден-2-ил)сульфамид;
Соединение 104: N-(4-((5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)метил)фенил)сульфамид гидрохлорид;
Соединение 105: N-(4-((5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)метил)бензил)сульфамид гидрохлорид;
Соединение 106: N-((5-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)тиофен-2 -ил)метил)сульфамид;
Соединение 107: N-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-5-метоксилтиофен-2-ил)метил)сульфамид;
Соединение 108: N-(3-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)-бицикло[1.1.1]пентан-1-ил)сульфамид;
Соединение 109: N-(4-(5-метокси-2Н-бензо[d][1,2,3]триазол-2-ил)фенил)сульфамид гидрохлорид;
Соединение 110: N-(4-((5-метокси-2Н-бензо[d][1,2,3]триазол-2- ил)бензил)сульфамид гидрохлорид;
Соединение 111: 2-(4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)пиперидин-1-ил)этан-1-сульфонилфторид;
Соединение 112: N-(3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)метансульфонамид;
Соединение 113: N-(3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)этансульфонамид;
Соединение 114: N-(3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)-4-метилбензолсульфонамид;
Соединение 115: N-(3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)метансульфонимидамид;
Соединение 116: 3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензойная кислота;
Соединение 117: диэтил-(3-фтор-4-(5-метокси-1Н-бензо[d][1,2,3]триазол-1-ил)бензил)фосфоамидит;
Соединение 122: N-(4-(5-метокси-1Н-индол-1-ил)бензил)сульфамид;
Соединение 123: N-(4-(5-метокси-1Н-бензо[d]имидазол-1-ил)бензил)сульфамид; и
Соединение 124: N-(4-(5-метокси-1Н-индазол-1-ил)бензил)сульфамид.
4. Соединение по п. 1, в котором фармацевтически приемлемая соль представляет собой соль неорганической кислоты или органической кислоты, выбранной из группы, состоящей из соляной кислоты, бромистоводородной кислоты, серной кислоты, фосфорной кислоты, азотной кислоты, уксусной кислоты, гликолевой кислоты, молочной кислоты, пировиноградной кислоты, малоновой кислоты, янтарной кислоты, глутаровой кислоты, фумаровой кислоты, яблочной кислоты, миндальной кислоты, винной кислоты, лимонной кислоты, аскорбиновой кислоты, пальмитиновой кислоты, малеиновой кислоты, гидроксималеиновой кислоты, бензойной кислоты, гидроксибензойной кислоты, фенилуксусной кислоты, коричной кислоты, салициловой кислоты, метансульфоновой кислоты, бензолсульфоновой кислоты и толуолсульфоновой кислоты.
5. Фармацевтическая композиция для профилактики, облегчения или лечения рака, связанного с ингибированием ENPP 1, содержащая терапевтически эффективное количество соединения по любому из пп. 1-4 в качестве активного ингредиента и фармацевтически приемлемый эксципиент.
6. Ингибитор ENPP 1, содержащий соединение по любому из пп. 1-4 в качестве активного ингредиента.
7. Активатор сигнального пути STING, содержащий соединение по любому из пп. 1-4 в качестве активного ингредиента.
| WO 2020210649 A1, 15.10.2020 | |||
| BIAGI G | |||
| et al., Some structural changes on triazolyl-benzotriazoles and triazolyl-benzimidazolones as potential potassium channel activators | |||
| III, Il Farmaco, 2001, vol | |||
| Приспособление для разматывания лент с семенами при укладке их в почву | 1922 |
|
SU56A1 |
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| Приспособление к паровозному реверсу | 1924 |
|
SU841A1 |
| FENG P | |||
| et al., Electrooxidative and Regioselective C−H Azolation of Phenol and Aniline Derivatives, Angewandte Chemie | |||
Авторы
Даты
2024-08-12—Публикация
2022-01-28—Подача