Изобретение относится к новым биологически активным производным замещенных 2,3-дигидрофуран-3-онов и может быть использовано в качестве противовирусных средств с широким спектром противовирусной активности.
Производные фуранонов обладают широким спектром биологической активности. Из уровня развития техники широко известно использование производных фуранонов в качестве ароматизаторов.
Возможно их использование для лечения расстройств центральной нервной системы (Ripka, Amy; Shapiro, Gideon; Chesworth, Richard 1,2-Disubstituted heterocyclic compounds as phosphodiesterase 10 inhibitors and their preparation, pharmaceutical compositions and use in the treatment of CNS disorders and disorders affected by CNS function, WO2009158393).
Кроме того, они могут демонстрировать активность в отношении ферментов из каскада митоген-активируемых протеинкиназ (Schiltz, Gary Е.; Izquierdo-Ferrer, Javier; Vagadia, Purav; Clutter, Matthew R.; Mishra, Rama K.; Platanias, Leonidas C. SUBSTITUTED AROMATIC N-HETEROCYCLIC COMPOUNDS AS INHIBITORS OF MITOGEN-ACTIVATED PROTEIN KINASE INTERACTING KINASE 1 (MNK1) AND 2 (MNK2), US20180244654).
Известно, что фураноны являются структурным компонентом природных соединений, в частности сорбифуранонов, которые замедляют рост опухолевых клеток в культуре (BRINGMANN GERHARD (DE) и др. Sorbifuranone, sorbivinetone, sorbivinetol and derivatives of these compounds, process for their preparation, medicines containing them and their use DE-102004005106-A1).
Фураноны выступают в качестве противопаразитарных агентов (Li, Honglin; Zhao, Zhenjiang; Huang, Jin; Xu, Yufang; Xu, Minghao; Diao, Yanyan; Zhou, Hongchang; Jin, Huangtao; Gao, Rui; Zhu, Junsheng Preparation of heterocycles as DHODH inhibitors, WO 2013075596).
Также известно, что ряд производных фуранонов обладает антибактериальной активностью (WO 01/85664 А2).
Наиболее близким структурным аналогом к соединениям изобретения является производное фуранона nivefuranone, продуцируемое грибами Aspergillus niveus, которое обладает активностью против Т-лимфотропного вируса (в тестах in vitro на культуре лимфоцитов человека, инфицированных Т-лимфотропным вирусом 2 В типа с IC50 0.78 μg/mL) (Fujiwara Т, Sato А, Kawamura Y, Matsumoto К, Itazaki H. Nivefuranone manufacture with Aspergillus niveusJapanese Kokai Tokkyo Koho, Patent, 1994).
Из предшествующего уровня техники не выявлено соединений -производных фуранона с широким спектром противовирусной активности, в том числе, и по отношению к РНК вирусам, в частности имеющих активность в отношении коронавирусов, таких как MERS, SARS и SARS-CoV-2. Масштабная пандемия коронавируса COVID-19 требует незамедлительной разработки эффективных и безопасных противовирусных средств нового поколения, так как существующие противовирусные препараты и вакцины обладают ограниченной эффективностью в отношении вируса SARS-CoV-2, в особенности его резистентных штаммов.
Способность разработанных новых соединений эффективно подавлять репликацию РНКовых вирусов различных типов, в т.ч. SARS-CoV-2, свидетельствует о потенциальной применимости структурного класса 2,3-дигидрофуран-3-онов для терапии инфекционных заболеваний у людей и других животных.
Раскрытие изобретения
Задачей настоящего изобретения является разработка и создание новых соединений эффективных для терапии заболеваний, вызванных РНК-вирусами, в частности, но не ограничиваясь, для терапии заболеваний, вызываемых коронавирусами HCoV-OC43, HCoV-HKUl, HCoV-229E, HCoV-NL63, SARS, MERS и SARS-CoV-2.
Техническим результатом изобретения является разработка и получение новых химических соединений, обладающих высокой эффективностью для лечения заболеваний, вызванных РНК вирусами.
Раскрытые соединения являются перспективными для применения в терапии инфекционных заболеваний, в том числе, но не ограничиваясь, коронавирусами, в частности вирусом SARS-CoV-2, а также рядом других видов вирусов.
Указанный технический результат достигается посредством разработки и создания соединений общей формулы (I),
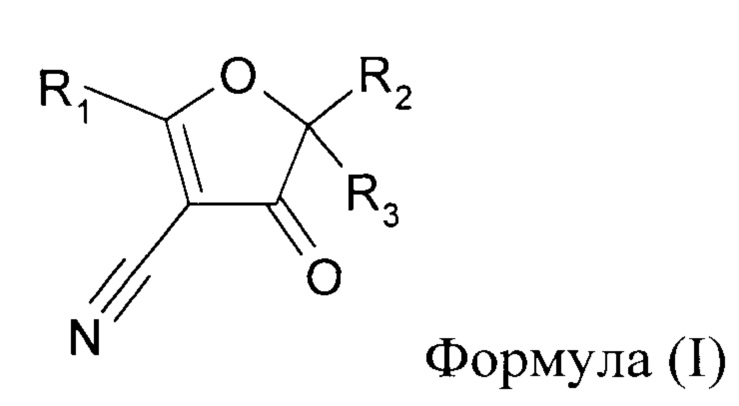
где R1 представляет собой заместители вида
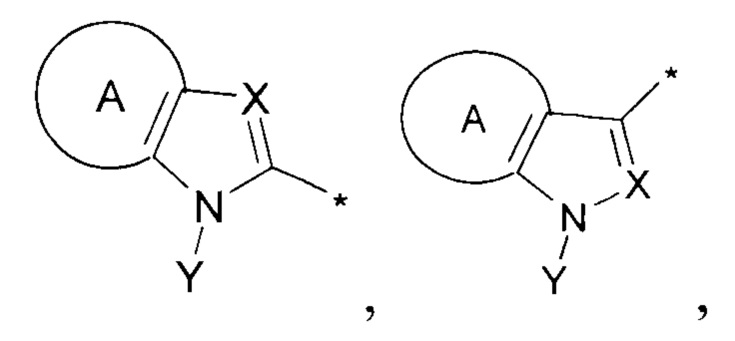
где А представляет собой конденсированный С6-арил или его производное, -5÷6-членный-гетероарил или его производное, содержащий от 1 до 3 гетероатомов, независимо выбранных из N, S и/или О, причем звездочкой указано место присоединения заместителя;
X представляет собой N или заместитель вида CR4,
где R4 выбирается независимо и представляет собой -Н, -D, -F, -Cl, -Br, -I, -CN,
-CH2F, -CHF2, -CF3, -NO2, алкил или его производное, алкенил или его производное, алкинил или его производное, С6-арил, -5÷6-членный-гетероарил или его производное, содержащий от 1 до 4 гетероатомов, независимо выбранных из N, S и/или О, -С3-С9-циклоалкил или его производное, или -4÷9-членный гетероцикл, содержащий от 1 до 4 гетероатомов, независимо выбранных из N, S и/или О, а также заместители вида -CH2ORa; -CH2N(Ra)2, где
Ra выбирается независимо и представляет собой -Н, замещенный или незамещенный -C1-С6-алкил, алкенил или его производное, -С3-С9-циклоалкил или его производное, -С6-арил или его производное, 5÷6-членный-гетероарил или его производное, содержащий от 1 до 4 гетероатомов, независимо выбранных из N, S и/или О, или 4÷9-членный гетероцикл или его производное, содержащий от 1 до 4 гетероатомов, независимо выбранных из N, S и/или О;
Y выбирается независимо и представляет собой -Н или заместители вида
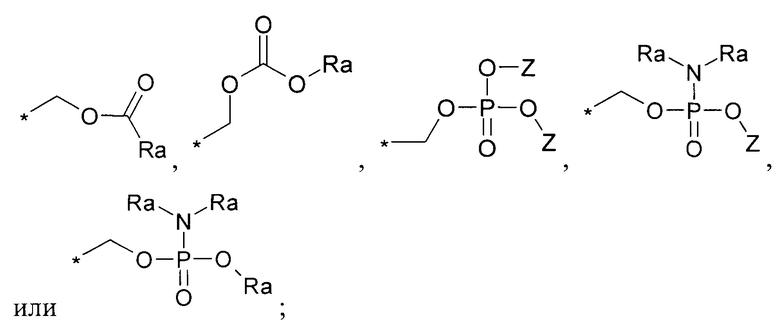
Z выбирается независимо и представляет собой -Н, -Li+, -Na+, -K+, -[N(Rf)4]+;
Rf выбирается независимо и представляет собой -Н, или -алкил;
R2 и R3 выбирается независимо и представляет собой алкил или его производное, алкенил или его производное, -С6-С10 арил или его производное, -5÷10-членный-гетероарил или его производное, содержащий от 1 до 4 гетероатомов, независимо выбранных из N, S и/или О, С3-С9-циклоалкил или его производное, или замещенный или незамещенный 4+9-членный гетероцикл или его производное, содержащий от 1 до 4 гетероатомов, независимо выбранных из N, S и/или О, также заместители вида, причем зездочкой обозначена точка прикрепления заместителя
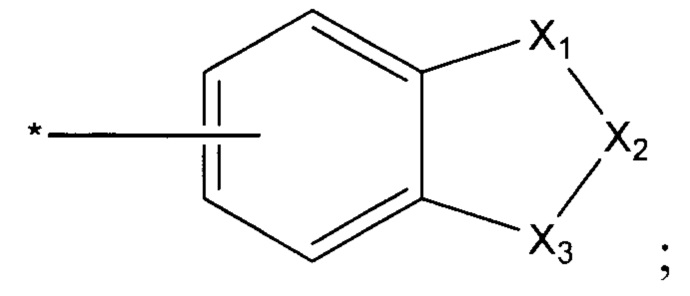
X1, Х2 и Х3 выбираются независимо и представляют собой -(СН2)n-,-O-, -S-, -S(=O)- -S(=O)2-, или заместители вида:
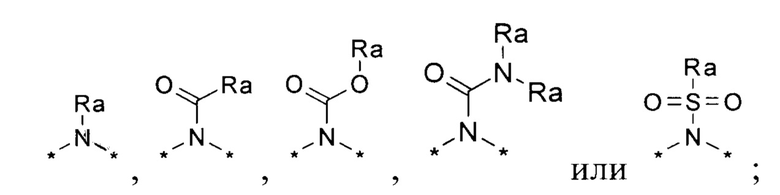
причем n выбирается независимо для X1, Х2 и Х3 и может принимать значения от 1 до 4;
Заместители R2 и R3 вместе с атомом углерода, к которому они присоединены, могут образовывать 8÷14-членный спироцикл.
При этом соединение формулы (I) может представлять собой фармацевтически приемлемую соль или оптические изомеры.
В некоторых частных вариантах воплощения изобретения заместитель R1 выбирается из группы бициклических конденсированных -8÷9-членных-гетероарилов вида
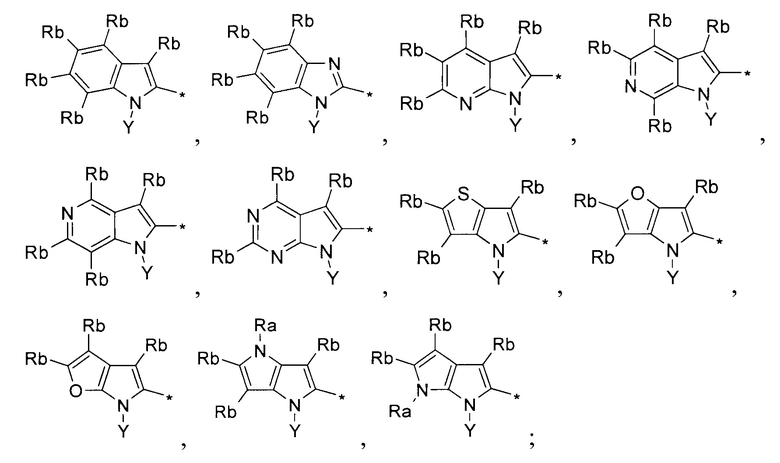
Rb выбирается независимо и представляет собой -Н, -D, -F, -Cl, -Br, -I, -CH2F,
-CHF2, -CF3, -OCF3, -OCHF2, -CN, -NO2, алкил или его производное, алкенилил или его производное, С3-С9-циклоалкил или его производное, а также аместителей типа -ORc, -SRc, -N(Rc)2, -CON(Rc)2,-COORc; -SO2Rc, -SO2N(Rc)2;
Rc выбирается независимо и представляет собой -Н, замещенный или незамещенный -C1-С6-алкил, замещенный или незамещенный -С3-С9-циклоалкил, замещенный или незамещенный С6-арил, замещенный или незамещенный -5÷6-членный-гетероарил, содержащий от 1 до 4 гетероатомов, независимо выбранных из N, S и/или О, или замещенный или незамещенный 4÷9-членный гетероцикл, содержащий от 1 до 4 гетероатомов, независимо выбранных из N, S и/или О.
Отдельный подкласс соединений, представляющих интерес, включает соединения общей формулы (Ib),
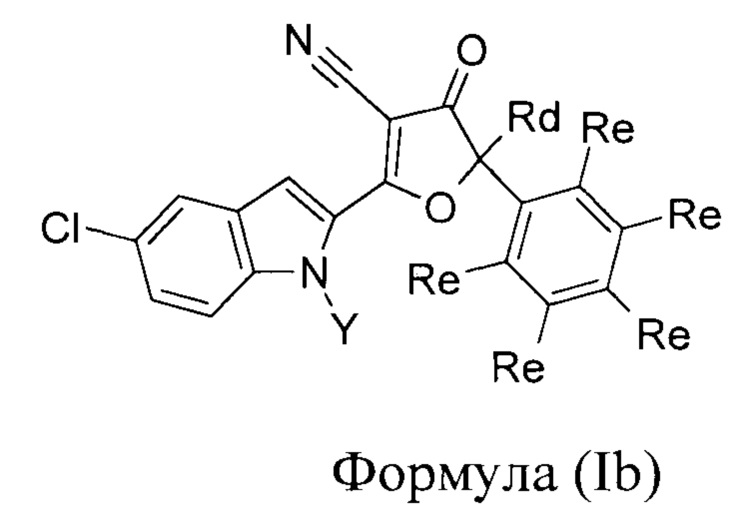
Rd выбирается независимо и представляет собой алкил или его производное, С3-С9-циклоалкил или его производное;
Re выбирается независимо и представляет собой -Н, -D, -F, -Cl, -Br, I, -CH2F,
-CHF2, -CF3, -OCF3, -OCHF2, -OAlk, -CN, -NO2, алкил или его производное, алкинил или его производное, С3-С6-циклоалкил или его производное С6-арил или его производное, -5÷6-членный-гетероарил или его производное, содержащий от 1 до 4 гетероатомов, независимо выбранных из N, S и/или О, или 4÷9-членный гетероциклил или его производное, содержащий от 1 до 4 гетероатомов, независимо выбранных из N, S и/или О, а также заместителей типа -ORa, -N(Ra)2, -SRa, -SO2Ra, -C(=O)N(Ra)2.
В некоторых частных вариантах воплощения изобретения соединения, представляющие интерес, могут быть выбраны из группы:
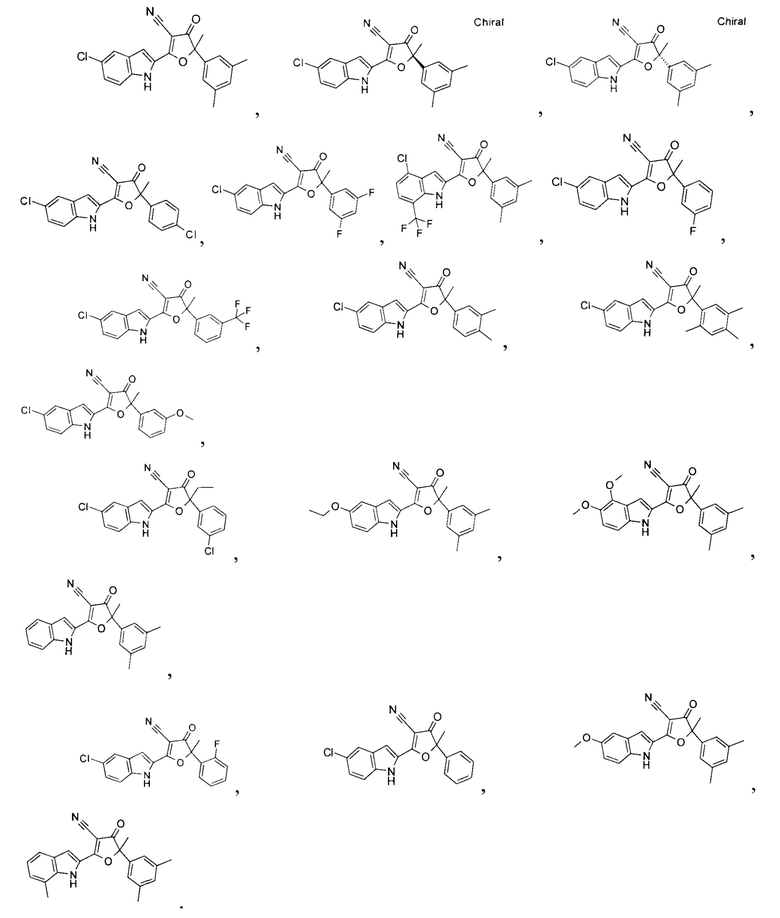
Определения (термины)
Следующие определения применяются в данном документе, если иное не указано явно. Кроме того, если не указано иное, все вхождения функциональных групп выбираются независимо, два вхождения могут быть как одинаковыми, так и разными.
Термин «алкил» сам по себе или как часть другого заместителя, относится к насыщенным углеводородным группам с прямой или разветвленной цепью, включая углеводородные группы, имеющие указанное число атомов углерода (то есть, C1-6-алкил подразумевает от одного до шести атомов углерода). Примеры алкилов включают метил, этил, н-пропил, изо-пропил.
Термин «алкинил» сам по себе или как часть другого заместителя относится к углеводородным группам, в которых по крайней мере одна углерод-углеродная связь является тройной связью, в то время как остальные связи могут представлять собой простые, двойные или дополнительные тройные связи, включая углеводородные группы, от 2 до 6 атомов углерода. Примеры алкинильных групп включают этинил, 1-пропинил, 2-пропинил и т.д.
Термин «алкенил» сам по себе или как часть другого заместителя относится к углеводородным группам, в которых по крайней мере одна углерод-углеродная связь является двойной связью, в то время как остальные связи могут представлять собой либо простые связи, либо дополнительные двойные связи, включая углеводородные группы, содержащие от 2 до 6 атомов углерода. Примеры алкенильных групп включают этенил, 1-пропенил, 2-пропенил, 1-бутенил, 2-бутенил, 3-бутенил, 2-метил-1-пропенил, 2-метил-2-пропенил и т.п.
Термин «галоген» сам по себе или в части другого термина относится к атому фтора, хлора, брома или йода.
Термин «циклоалкил» в настоящем документе относится к группам, имеющим от 3 до 12 атомов углерода в моно- или полициклической структуре, включая спироциклы. В качестве иллюстрации, циклоалкилы включают, но не ограничиваются, следующими радикалами: циклопропил, циклопентил, циклогексил, бицикло[2.2.2]октанил, спиро[5.5]ундеканил, которые, как и в случае других алифатических или гетероалифатических или гетероциклических заместителей, могут быть замещенными. Термин «гетероцикл», или «гетероциклический» означает в настоящем документе неароматические моно- или полициклические системы (насыщенные или частично ненасыщенные), имеющие от трех до двенадцати атомов, содержащие гетероатомы N, О или S. Гетероцикл может быть присоединен к основному фрагменту молекулы через атом азота (N-гетероцикл) либо через атом углерода. Гетероциклы также могут быть замещенными.
Термин «циклоалкенил» означает в настоящем документе частично ненасыщенный циклоалкил, содержащий от 5 до 12 атомов углерода, имеющий в своем составе от одной до двух двойных углерод-углеродных связей.
Термин «арил» в настоящем документе означает группы, содержащие ароматический цикл, имеющий от пяти до десяти атомов углерода. Примером арильных циклических групп является фенил.
Термин «гетероарил», «гетероарильный цикл» как он используется здесь, означает стабильный гетероциклический и полигетероциклический ароматический фрагмент, имеющий 5-10 атомов в цикле. Гетероарильная группа может быть замещенной или незамещенной и может состоять из одного или несколько колец. Возможные заместители включают, помимо прочего, любой из ранее упомянутых заместителей. Примерами типичных гетероарильных циклов являются пяти- и шестичленные моноциклические группы, такие как тиенил, пирролил, имидазолил, пиразолил, пиридил, пиримидинил, пиридазинил, триазинил, тетразолил и т.п.; а также полициклические гетероциклические группы, такие как бензо[b]тиенил, изобензофуранил, изоиндолил, бензимидазолил, и т.п.. Термин «гетероарил» может использоваться эквивалентно с терминами «гетероарильный цикл» или «гетероароматический».
Арильная группа или гетероарильная группа (включая гетероарильную часть гетероаралкилов или гетероаралкокси фрагментов и т.п.) могут содержать один или несколько заместителей. Примеры подходящего заместителя на ненасыщенном атоме углерода арильной или гетероарильной группы включают, но не ограничиваются, галоген (F, Cl, Br или I), С1-3-алкил, -CN, -ОН, -C1-3-алкил и другие.
Термин «замещенный» должен обозначать, что один или более атом водорода при атоме или группе, упоминаемой как «замещенный», заменен на любую из перечисленных групп, при условии, что упоминаемый атом обладает нормальной валентностью, или что валентность замещаемого соответствующего атома группы не является избыточной, и что замещение приводит к стабильному соединению. Термин «замещенный или незамещенный» означает, что данное соединение или подструктура является либо незамещенным, либо замещенным, как определено в заявке, одним или более заместителями, как упоминается или как определено ниже.
В данном документе алкильная, алкенильная, алкинильная, алкиленовая, циклоалкильная, циклоалкенильная, гетероциклическая, арильная и гетероарильная группы, а также другие подструктуры, содержащие в своем составе по крайней мере один атом водорода, могут замещаться одним или более заместителями:
-F, -Cl, -Br, -CN, -ОН, -NO2, -NH2, -CF3, -CHF2, -CH2F, -С1-С4-алкил, -С2-С4-алкенил, -С2-С4-алкинил, -С3-С9-циклоалкил, -4÷9-членный-гетероцикл, присоединенный через С или N-атомы, -фенил, -5÷6-членный-гетероарил, присоединенный через С или N-атомы, -O-Rz, -N(Rz)2, -NRz-C(=O)-Rz, -NRz-S(=O)2-Rz, -S-Rz, -C(=O)-Rz, -C(=O)-ORz, -C(=O)-N(Rz)2, -O-C(=O)-Rz, -O-C(=O)-(NRz)2, -SO-N(Rz)2, -SO2-Rz, в которых каждый Rz независимо выбран и представляет собой -Н, -C1-С6-алкил, -С3-С9-циклоалкил, -5÷6-членный гетероарил, содержащий от 1 до 4 гетероатомов, независимо выбранных из N, S и/или О, или замещенный или незамещенный 4÷9-членный гетероцикл, содержащий от 1 до 4 гетероатомов.
Данное изобретение содержит только такие комбинации заместителей и производных, которые образуют стабильное или химически возможное соединение. Стабильным или химически возможным соединением называется такое соединение, стабильности которого достаточно для его синтеза и аналитического детектирования. Предпочтительные соединения данного изобретения являются достаточно стабильными и не разлагаются при температуре до 40°С в отсутствие химически активных условий, в течение, по крайней мере, одной недели.
Некоторые соединения данного изобретения могут существовать в таутомерных формах, и это изобретение включает в себя все такие таутомерные формы таких соединений, если не указано иное.
Под термином «изомер», «оптический изомер», «стереоизомер» понимают любые изомеры - структурные и оптические изомеры, т.е. стереоизомеры. При этом, если не указано иначе, изображенные здесь структуры также подразумевают и все стереоизомеры, то есть R- и S-изомеры для каждого ассиметричного центра. Кроме того, отдельные стереохимические изомеры, равно как и энантиомеры и диастереомерные смеси настоящих соединений, также являются предметом данного изобретения. Таким образом, данное изобретение охватывает каждый диастереомер или энантиомер, свободный в значительной степени от других изомеров (>90%, а предпочтительно >95% мольной чистоты), так же как и смесь таких изомеров.
Конкретный оптический изомер может быть получен разделением рацемической смеси в соответствии со стандартной процедурой, например путем получения диастереоизомерных солей путем обработки оптически активной кислотой или основанием с последующим разделением смеси диастереомеров кристаллизацией с последующим выделением оптически активных оснований из этих солей. Примерами соответствующих кислот являются винная, диацетилвинная, дибензоилвинная, дитолуолвинная и камфорсульфоновая кислота. Другая методика разделения оптических изомеров заключается в использовании хиральной хроматографической колонки. Кроме того, другой метод разделения включает синтез ковалентных диастереомерных молекул путем реакции соединений изобретения с оптически чистой кислотой в активированной форме или оптически чистым изоцианатом. Полученные диастереомеры можно разделить обычными способами, например хроматографией, дистилляцией, кристаллизаций или сублимацией, а затем гидролизовать для получения энантиомерно чистого соединения.
Оптически активные соединения данного изобретения могут быть получены с использованием оптически активных исходных материалов. Такие изомеры могут находиться в форме свободной кислоты, свободного основания, эфира или соли.
Настоящее изобретение включает все фармацевтически приемлемые изотопно меченые соединения по настоящему изобретению, в которых один или несколько атомов замещен атомами, имеющими такой же атомный номер, но атомную массу или массовое число, отличные от атомной массы или массового числа, обычно встречающихся в природе.
Примеры изотопов, подходящих для включения в соединения по изобретению, включают изотопы водорода, такие как 2Н и 3Н, углерода, такие как 11С, 13С и 14С, хлора, такие как 36CI, фтора, такие как 18F, йода, такие как 123I и 125I, азота, такие как 13N и 15N, кислорода, такие как 15O, 17О и 18O, фософора, такие как 32Р, и серы, такие как 35S.
Некоторые изотопно меченые соединения формулы (I), например, те, которые включают радиоактивный изотоп, используют в исследованиях распределения лекарственного препарата и/или субстрата в тканях. В частности, с этой целью используют радиоактивные изотопы, такие как тритий, то есть 3Н, и углерод-14, то есть 14С, ввиду легкости их введения и доступности средств их обнаружения.
Замещение более тяжелыми изотопами, такими как дейтерий, то есть 2Н, может обеспечить определенные терапевтические эффекты, обусловленные метаболической стабильностью, например, увеличением периода полувыведения in vivo или снижением норм дозирования, и, следовательно, может быть предпочтительным в некоторых случаях.
Изотопно меченые соединения по изобретению могут быть получены обычными способами, известными специалисту в данной области или способами, аналогичными описанным в прилагаемых примерах способов синтеза, при использовании соответствующих изотопно меченых реагентов вместо немеченого ранее применяемого реагента.
Фармацевтически приемлемые сольваты в соответствии с изобретением включают сольваты, где растворитель кристаллизации может быть изотопно замещен, например, D2O, d6-ацетон, (d6-ДМСО.
Термин «сольват» относится к ассоциации или комплексу из одной или нескольких молекул растворителя и соединения по изобретению. Примеры растворителей, образующих сольваты, включают, но ими не ограничиваются, воду, изопропанол, этанол, метанол, ДМСО, этилацетат, уксусную кислоту и этаноламин.
Термин «гидрат» относится к комплексу, где молекулами растворителя является вода.
Соединения настоящего изобретения могут существовать в свободной форме или, если требуется, в виде фармацевтически приемлемой соли или другого производного. Используемый здесь термин «фармацевтически приемлемая соль» относится к таким солям, которые, в рамках проведенного медицинского заключения, пригодны для использования в контакте с тканями человека и животных без излишней токсичности, раздражения, аллергической реакции и т.д., и отвечают разумному соотношению пользы и риска. Фармацевтически приемлемые соли аминов, карбоновых кислот, фосфонатов и другие типы соединений хорошо известны в медицине. Соли могут быть получены in situ в процессе выделения или очистки соединений изобретения, а также могут быть получены отдельно, путем взаимодействия свободной кислоты или свободного основания соединения изобретения с подходящим основанием или кислотой, соответственно. Примером фармацевтически приемлемых, нетоксичных солей кислот могут служить соли аминогруппы, образованные неорганическими кислотами, такими как соляная, бромоводородная, фосфорная, серная и хлорная кислоты, или органическими кислотами, такими как уксусная, щавелевая, малеиновая, винная, янтарная или малоновая кислоты, или полученные другими методами, используемыми в данной области, например, с помощью ионного обмена. К другим фармацевтически приемлемым солям относятся адипинат, альгинат, аскорбат, аспартат, бензолсульфонат, бензоат, бисульфат, борат, бутират, камфорат, камфорсульфонат, цитрат, циклопентанпропионат, диглюконат, додецилсульфат, этансульфонат, формиат, фумарат, глюкогептонат, глицерофосфат, глюконат, гемисульфат, гептанат, гексанат, гидройодид, 2-гидрокси-этансульфонат, лактобионат, лактат, лаурат, лаурил сульфат, малат, малеат, малонат, метансульфонат, 2-нафталинсульфонат, никотинат, нитрат, олеат, оксалат, пальмитат, памоат, пектинат, персульфат, 3-фенилпропионат, фосфат, пикрат, пивалат, пропионат, стеарат, сукцинат, сульфат, тартрат, тиоцианат, п-толуолсульфонат, ундеканат, валериат и подобные. Типичные соли щелочных и щелочноземельных металлов содержат натрий, литий, калий, кальций, магний и другие. Кроме того, фармацевтически приемлемые соли могут содержать, если требуется, нетоксичные катионы аммония, четвертичного аммония и амина, полученные с использованием таких противоионов, как галогениды, гидроксиды, карбоксилаты, сульфаты, фосфаты, нитраты, низшие алкил сульфонаты и арил сульфонаты.
Соединения общей формулы (I) могут быть получены по реакции взаимодействия производных α,β-ацетилен γ-гидрокси нитрила с производными карбоновой кислотой по описанному в литературе методу [Synthetic Communications, 45: 2718-2729, 2015].
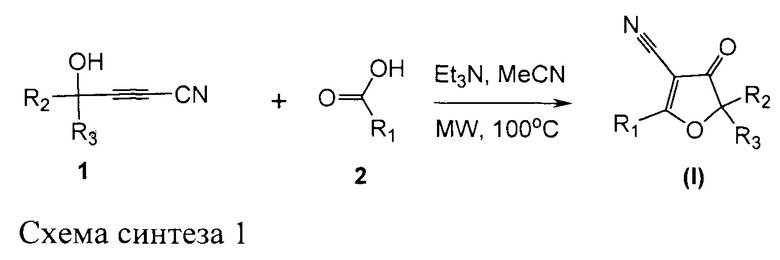
В качестве исходных соединений для синтеза структуры, отвечающей формуле (I) использовали широкий ряд производных α,β-ацетилен γ-гидрокси нитрила и карбоновой кислоты, известных ранее из уровня техники, которые могут быть коммерчески доступными, либо получены методами, известными для специалиста.
Ниже приведены примеры, иллюстрирующие схему синтеза, а также приведены сведения, подтверждающие получение заявленных структур.
Пример 1. Синтез 2-(5-Хлоро-1Н-индол-2-ил)-5-(3,5-диметилфенил)-5-метил-4-оксо-4,5-дигидрофуран-3-нитрил (НТ 2020081).
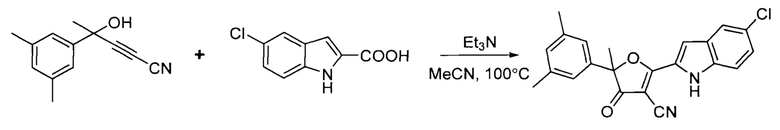
4-(3,5-диметилфенил)-4-гидроксипент-2-инитрил (1 экв., 1⋅10-3 моль, 200 мг), 5-хлор-1Н-индол-2-карбоновую кислоту (1.1 экв., 1.1⋅10-3 моль, 215 мг) и триэтиламин (1.3 экв., 1.3⋅10-3 моль, 132 мг/ 180 мкл) смешали в 6 мл ацетонитрила во флаконе. Флакон продули аргоном и закупорили. Смесь нагрели до 100°С и перешивали при данной температуре в течение 12 ч. По охлаждении смесь упарили, остаток очистили методом препаративной колоночной хроматографии на силикагеле (элюент - n-гексан: этилацетат=3:1 (об.), Rf=0.40 (n-гексан: этилацетат=1:1 (об.))).
Желтый порошок, 210 мг (56%).
ЯМР 1Н (400 МГц, CDCl3, δ, м.д., J, Гц): 1.92 (с, 3Н), 2.32 (с, 6Н), 7.01 (с, 1H), 7.08 (с, 2Н), 7.40 (дд, 1H, h=2.0 Гц, J2=8.9 Гц), 7.44-7.48 (м, 1Н), 7.73-7.77 (м, 1Н), 7.83 (дд, 1Н, J,=O.8 Гц, J2=2.2 Гц), 9.32 (уш. с, 1Н).
Пример 2. Синтез 2-(5-Хлоро-1Н-индол-2-ил)-5-(3,5-диметилфенил)-5-метил-4-оксо-4,5-дигидрофуран-3-нитрил (НТ 2020078).
Был получен по методике, описанной в Примере 1 из цианоацетилена и кислоты:
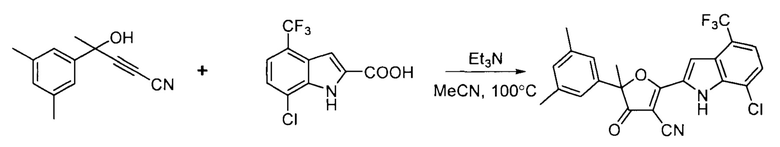
Желтый порошок, 362 мг (81%).
ЯМР 1Н (400 МГц, CDCl3, δ, м.д., J, Гц): 1.90 (с, 3Н), 2.35 (с, 6Н), 7.02 (с, 1Н), 7.08 (с, 2Н), 7.55 (2Н, с), 8.05 (уш. с, 1Н), 9.55 (уш. с, 1Н).
В описанном способе могут использовать любые подходящие растворители, преимущественно апротонные с высоким показателем диэлектрической проницаемости, предпочтительно выбранные из триэтиламина, ацетонитрила, диметилформамида и пр.
Кроме того, нагревание является необязательной стадией, поскольку при исключении стадии нагревания синтез осуществим, иногда с увеличением времени реакциит
Использование среды инертного газа является необязательным условием, поскольку его использование определяется подбором реагентов и условий проведения реакции.
Используя общую Схему синтеза 1 для получения соединения (I), в качестве исходных соединений были приведены химические структуры, содержащие следующие заместители:
где R1 представляет собой заместители вида
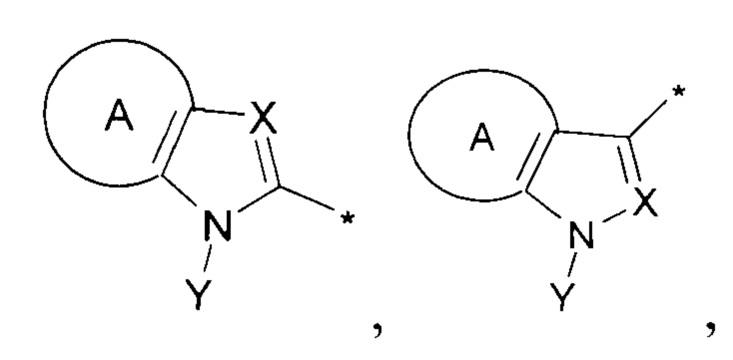
где А представляет собой конденсированный С6-арил или его производное, -5÷6-членный-гетероарил или его производное, содержащий от 1 до 3 гетероатомов, независимо выбранных из N, S и/или О, причем звездочкой указано место присоединения заместителя; X представляет собой N или заместитель вида CR4,
где R4 выбирается независимо и представляет собой -Н, -D, -F, -О, -Br, -I, -CN, -CH2F, -CHF2, -CF3, -NO2, алкил или его производное, алкенил или его производное, алкинил или его производное, С6-арил, -5÷6-членный-гетероарил или его производное, содержащий от 1 до 4 гетероатомов, независимо выбранных из N, S и/или О, -С3-С9-циклоалкил или его производное, или -4÷9-членный гетероцикл, содержащий от 1 до 4 гетероатомов, независимо выбранных из N, S и/или О, а также заместители вида -CH2ORa; -CH2N(Ra)2, где
Ra выбирается независимо и представляет собой -Н, замещенный или незамещенный -C1-С6-алкил, алкенил или его производное, -С3-С9-циклоалкил или его производное, -С6-арил или его производное, 5÷6-членный-гетероарил или его производное, содержащий от 1 до 4 гетероатомов, независимо выбранных из N, S и/или О, или 4÷9-членный гетероцикл или его производное, содержащий от 1 до 4 гетероатомов, независимо выбранных из N, S и/или О;
Y выбирается независимо и представляет собой -Н или заместители вида
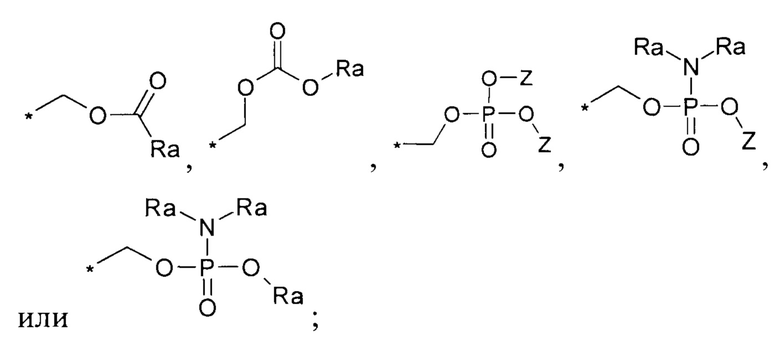
Z выбирается независимо и представляет собой -Н, -Li+, -Na+, -K+, -[N(Rf)4]+;
Rf выбирается независимо и представляет собой -Н, или -алкил;
R2 и R3 выбирается независимо и представляет собой алкил или его производное, алкенил или его производное, -С6-С10 арил или его производное, -5÷10-членный-гетероарил или его производное, содержащий от 1 до 4 гетероатомов, независимо выбранных из N, S и/или О, С3-С9-циклоалкил или его производное, или замещенный или незамещенный 4÷9-членный гетероцикл или его производное, содержащий от 1 до 4 гетероатомов, независимо выбранных из N, S и/или О, также заместители вида, причем зездочкой обозначена точка прикрепления заместителя
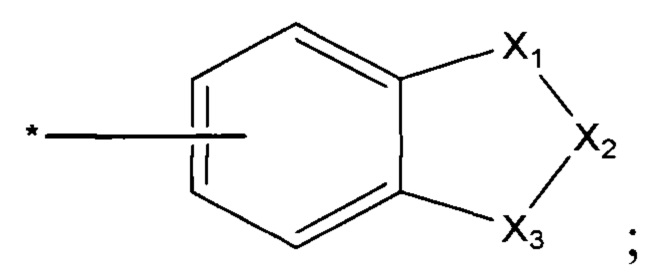
X1, Х2 и Х3 выбираются независимо и представляют собой -(СН2)n-, -O-, -S-, -S(=O)-, -S(=O)2-, или заместители вида:
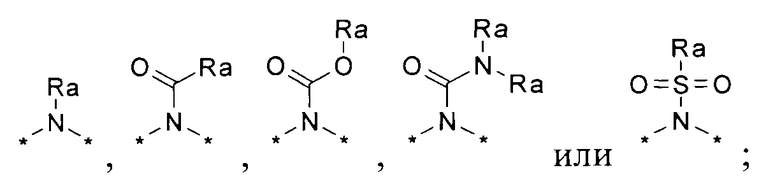
причем п выбирается независимо для X1, Х2 и Х3 и может принимать значения от 1 до 4;
Заместители R2 и R3 вместе с атомом углерода к которому они присоединены, могут образовывать 8÷14-членный спироцикл, где соединение формулы (I) представляет собой фармацевтически приемлемую соль или оптические изомеры.
В некоторых частных вариантах воплощения изобретения заместитель R1 выбирается из группы бициклических конденсированных -8÷9-членных-гетероарилов вида
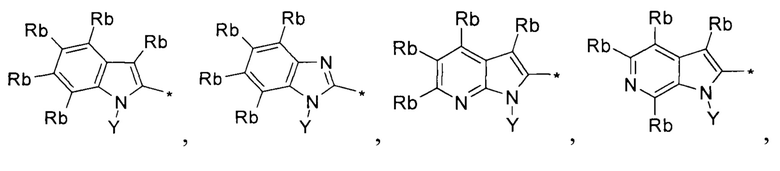
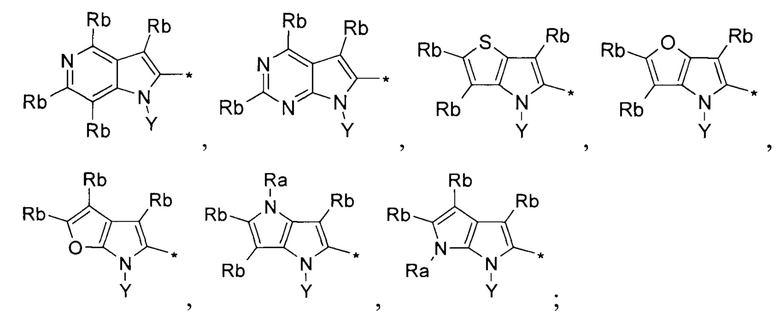
Rb выбирается независимо и представляет собой -Н, -D, -F, -Cl, -Br, -I, -CH2F,
-CHF2, -CF3, -OCF3, -OCFLF2, -CN, -NO2, алкил или его производное, алкенилил или его производное, С3-С9-гциклоалкил или его производное, а также аместителей типа -ORc, -SRc, -N(Rc)2, -CON(Rc)2,-COORc; -SO2Rc, -SO2N(Rc)2;
Rc выбирается независимо и представляет собой -Н, замещенный или незамещенный -C1-С6-алкил, замещенный или незамещенный -С3-С9-циклоалкил, замещенный или незамещенный С6-арил, замещенный или незамещенный -5÷6-членный-гетероарил, содержащий от 1 до 4 гетероатомов, независимо выбранных из N, S и/или О, или замещенный или незамещенный 4÷9-членный гетероцикл, содержащий от 1 до 4 гетероатомов, независимо выбранных из N, S и/или О.
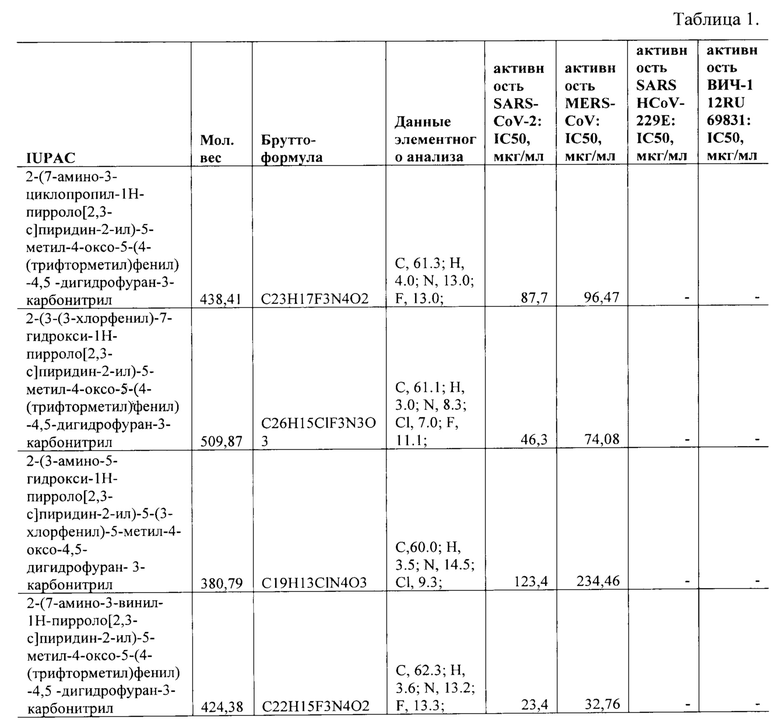
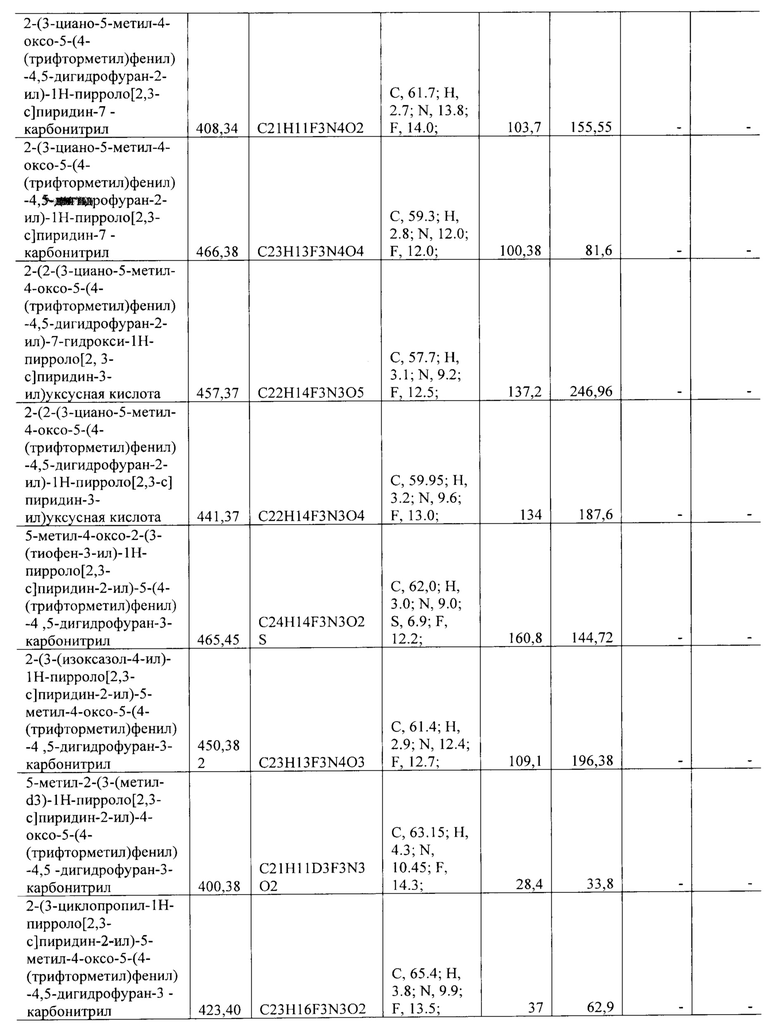
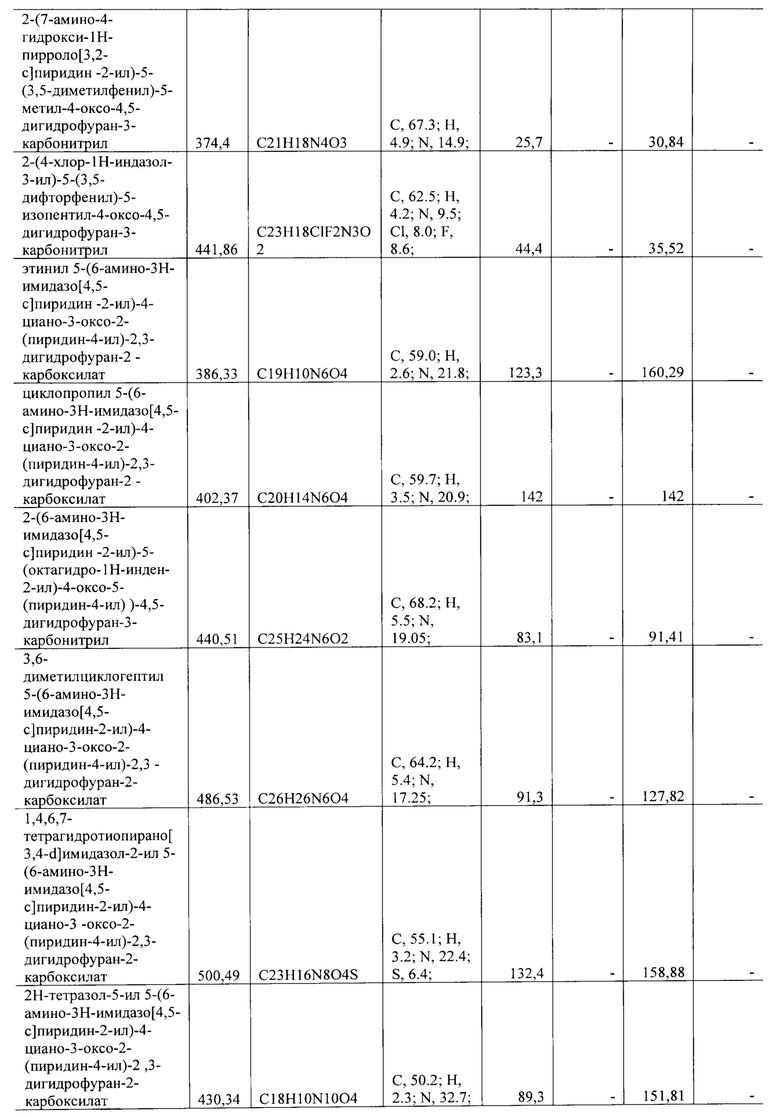
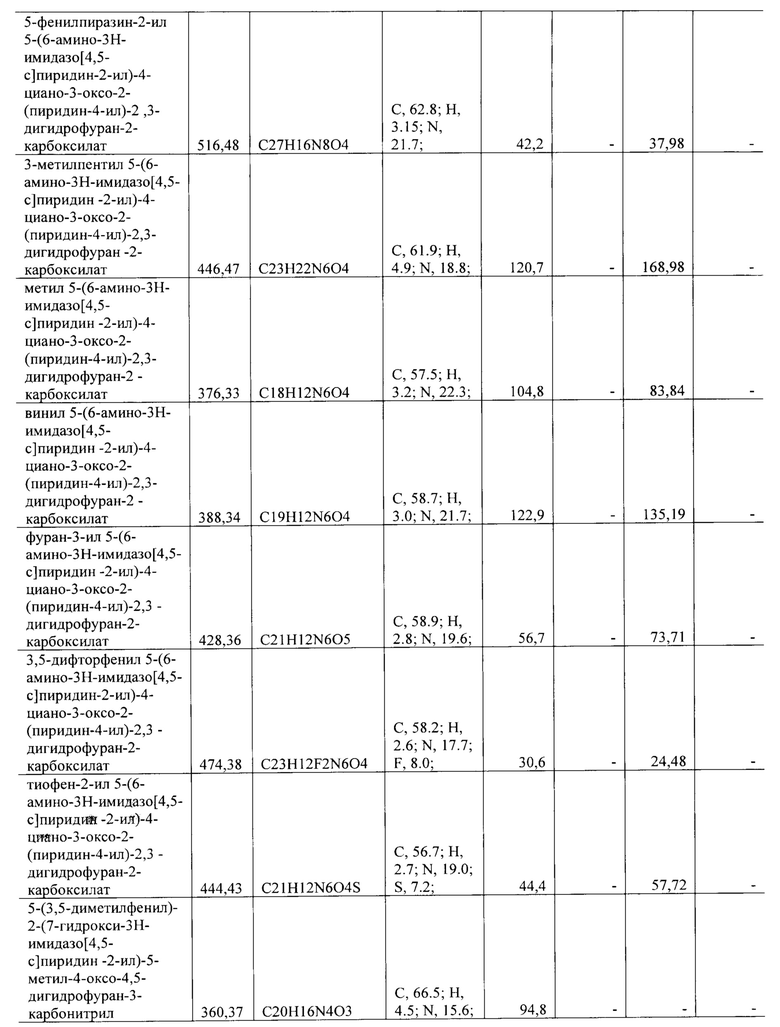
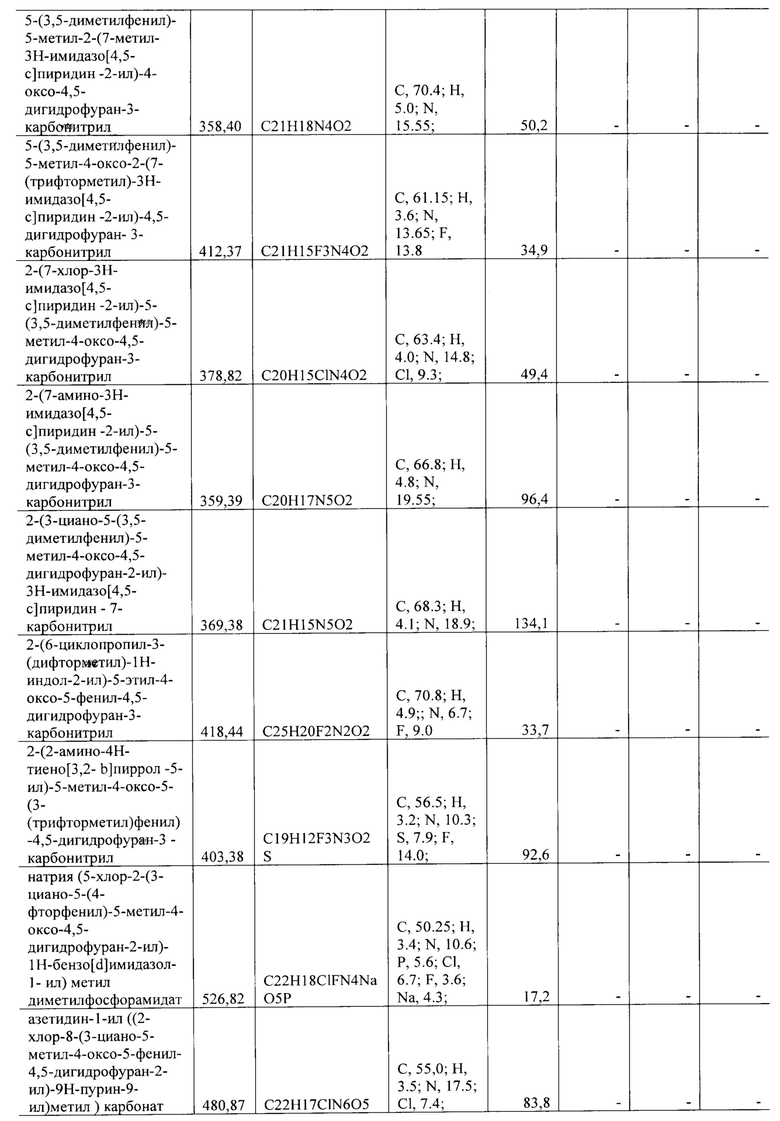
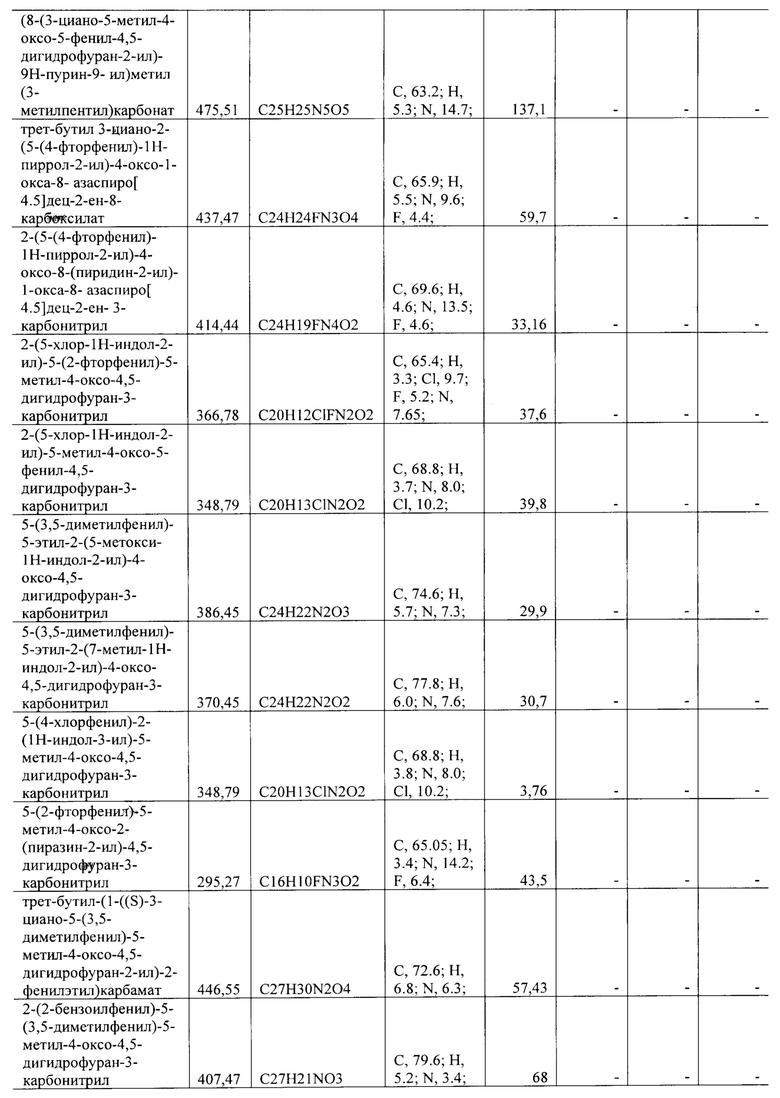
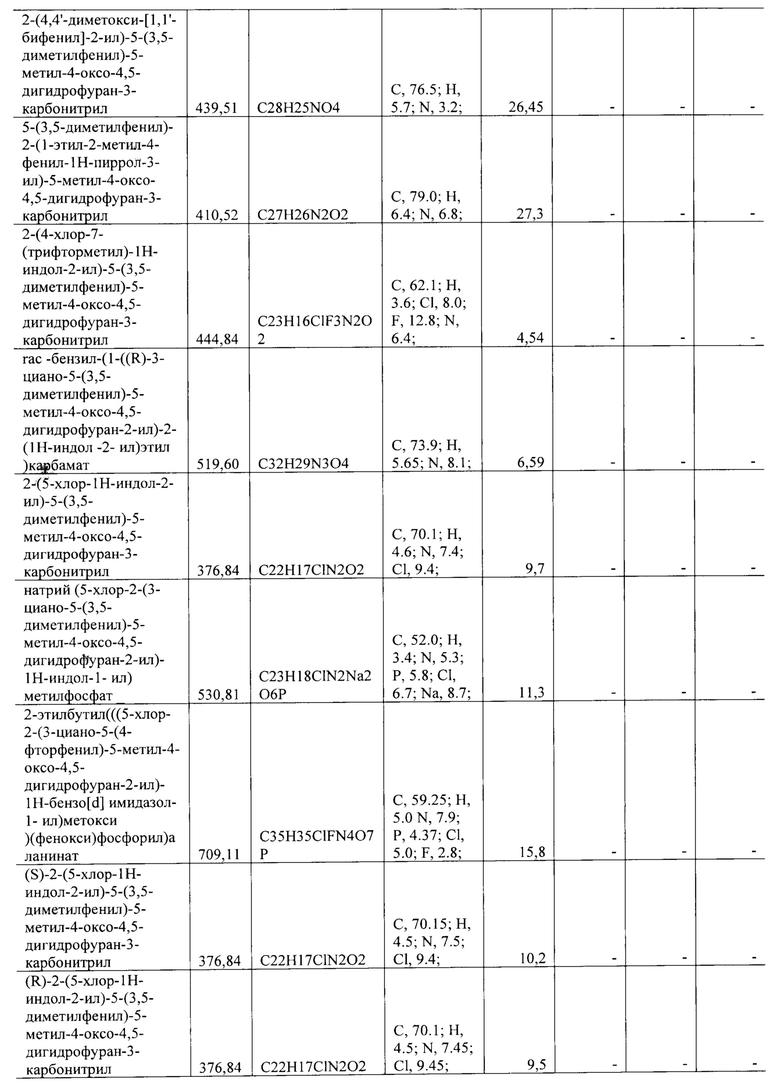
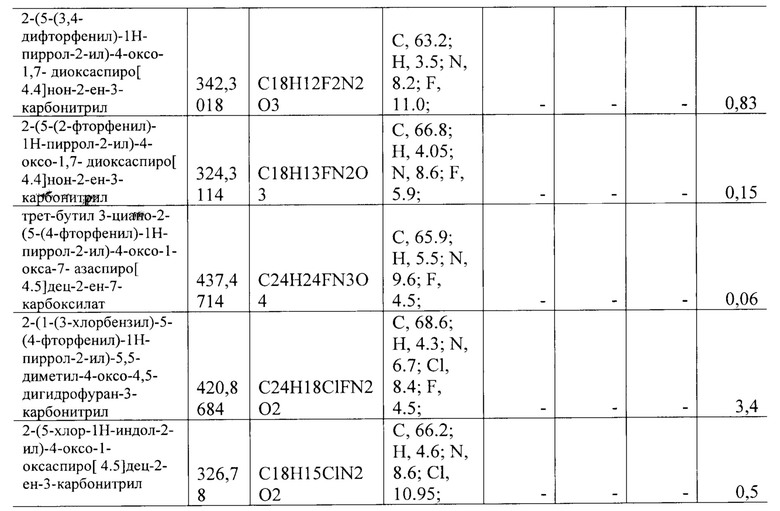
Строение полученных структур подверждено данными элементного анализа. Элементный анализ на содержание углерода, водорода, азота и серы проведен на элементном анализаторе Flash ЕА 1112 CHNS-O/MAS 200 (Thermo Scientific, США). Элементный анализ на содержание фтора, натрия, хлора, брома и фосфора выполнен на энергодисперсионном рентгенофлуоресцентном спектрометре EDX-8100 (Shimadzu, Япония).
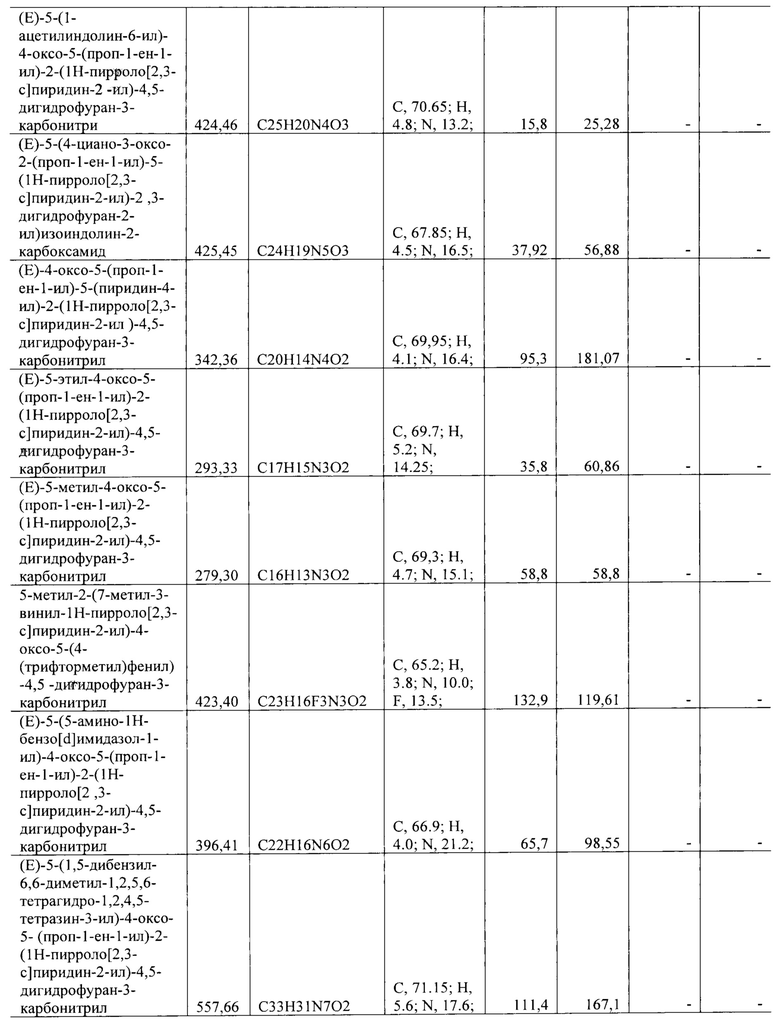
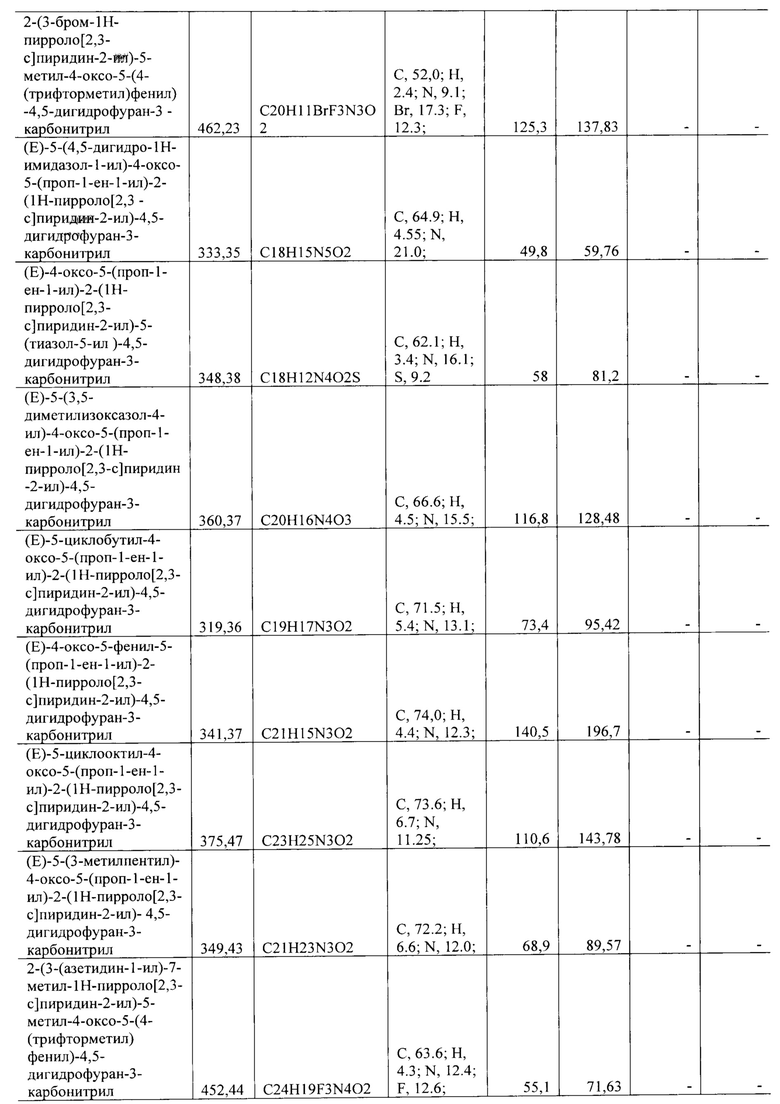
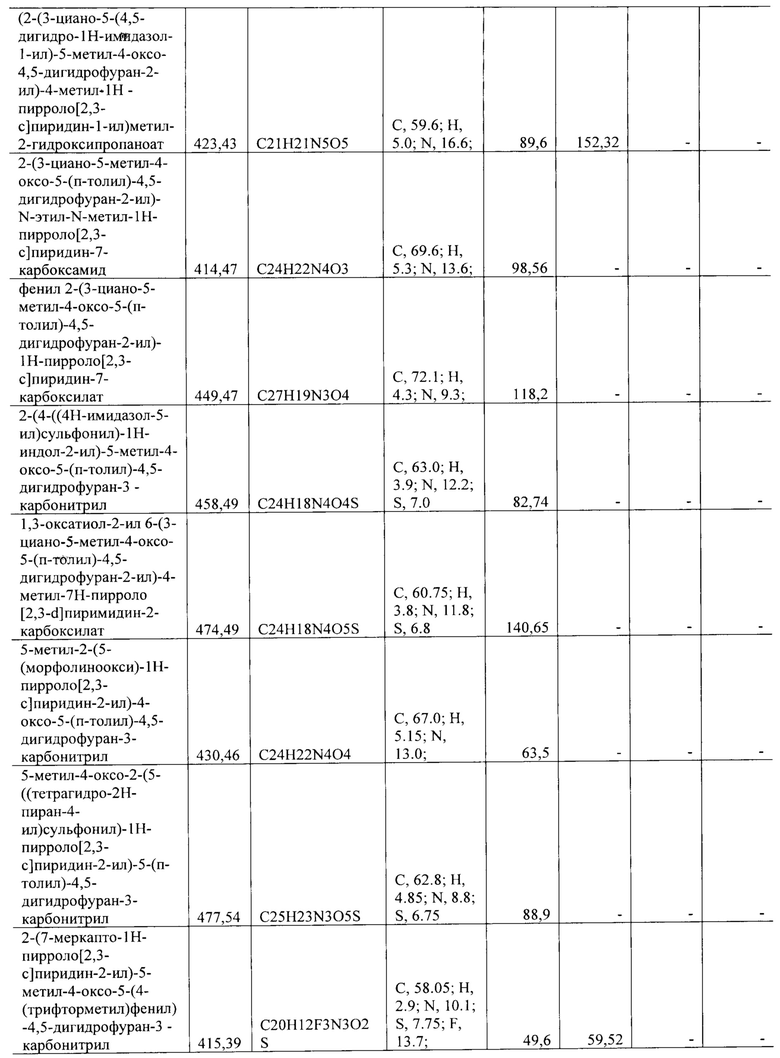
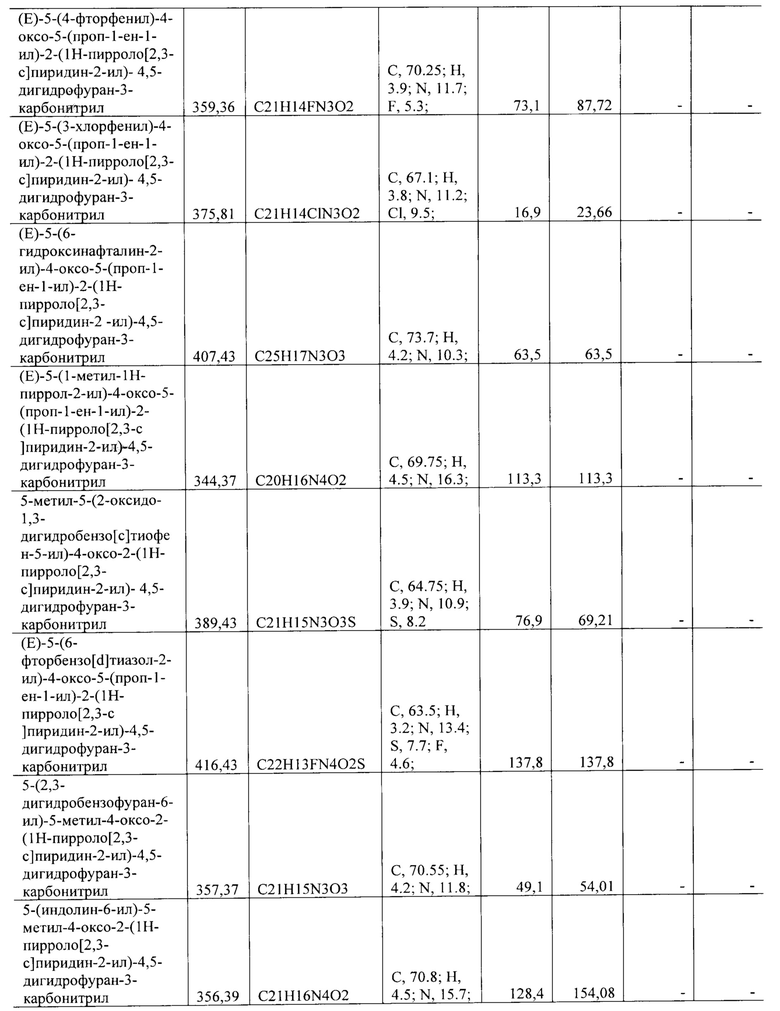
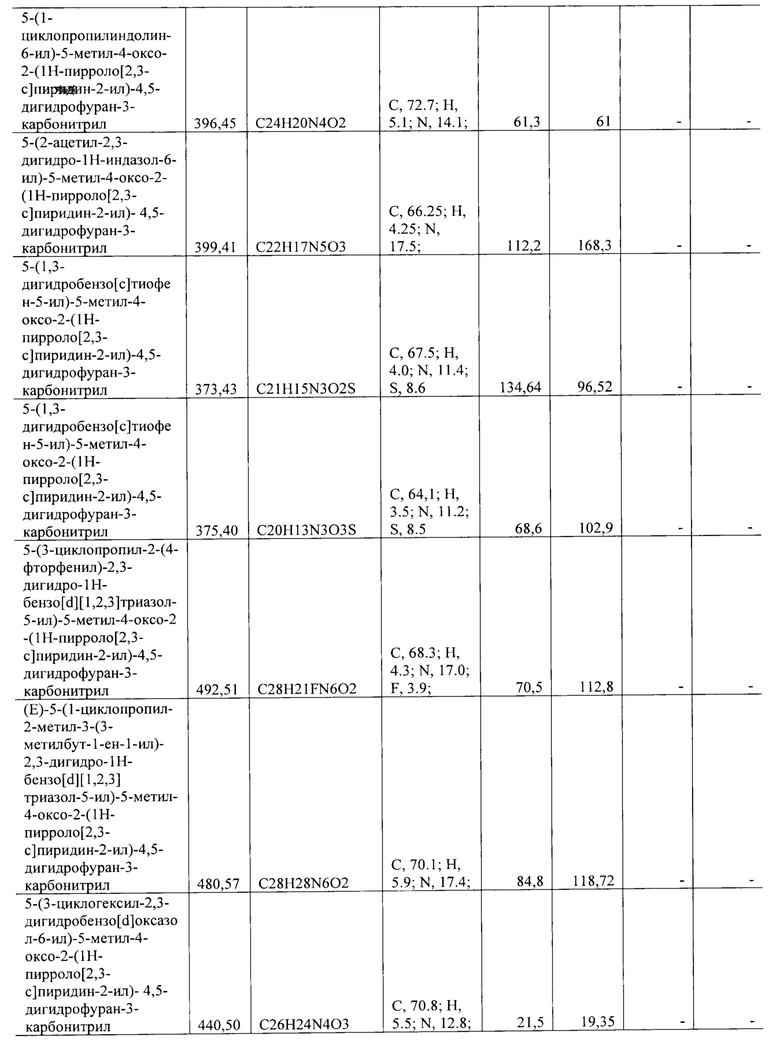
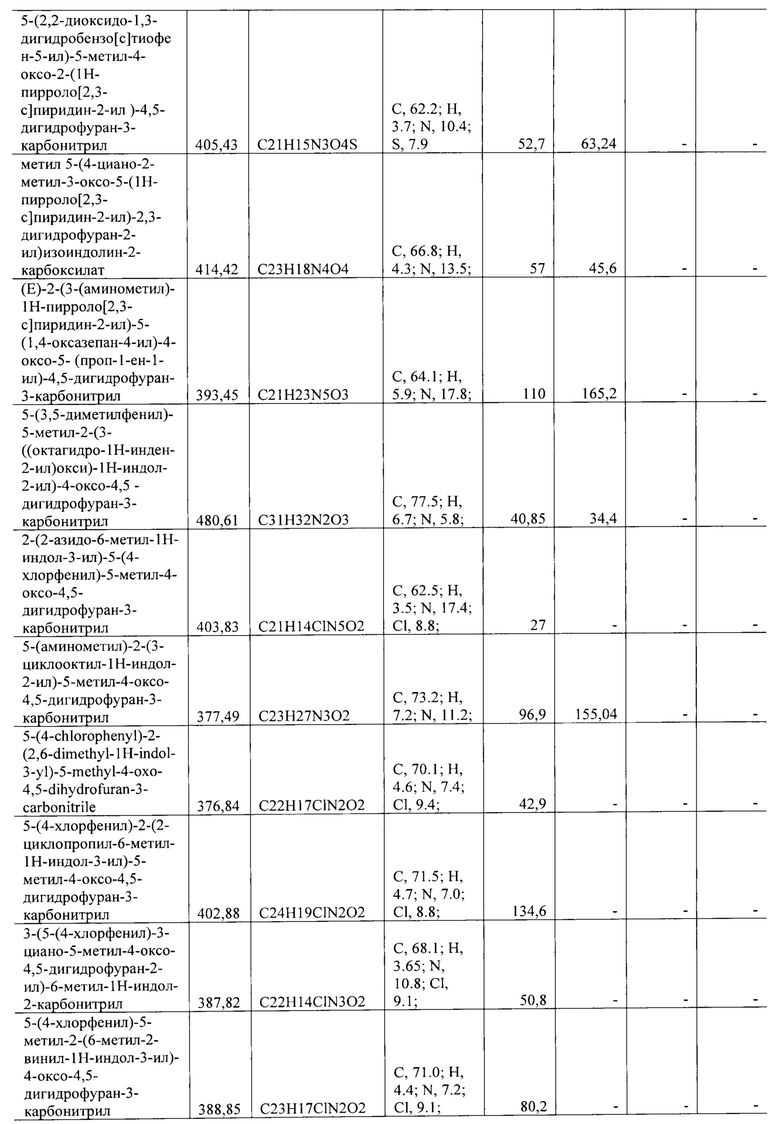
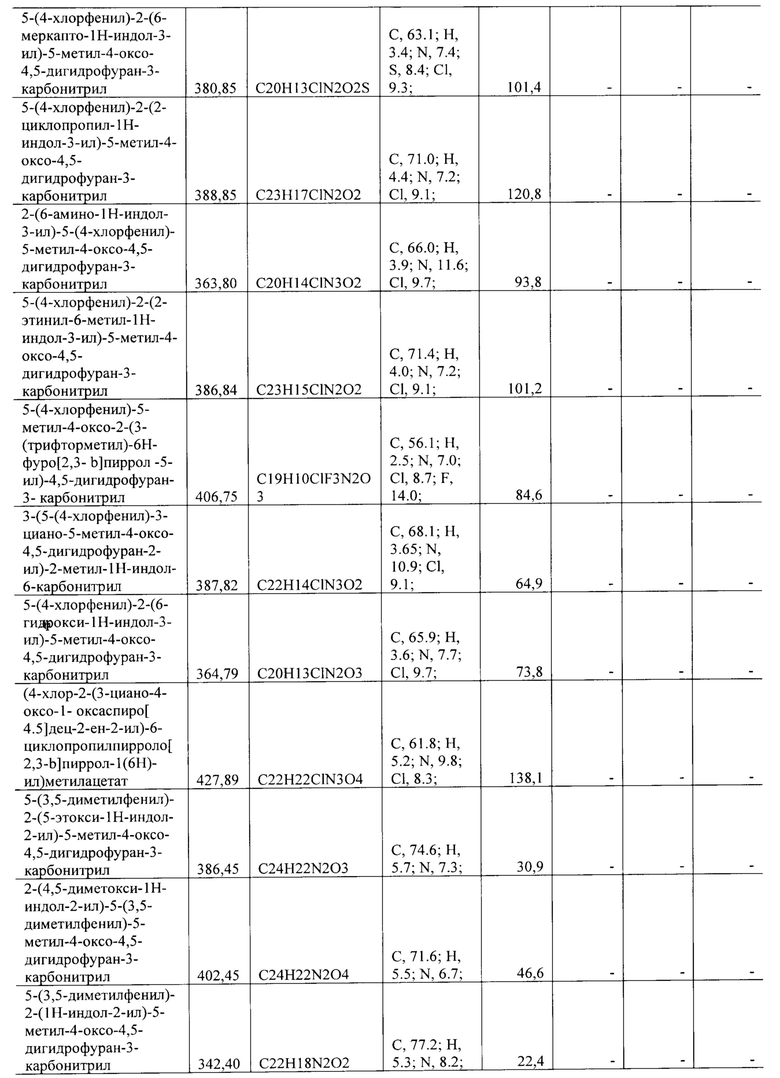
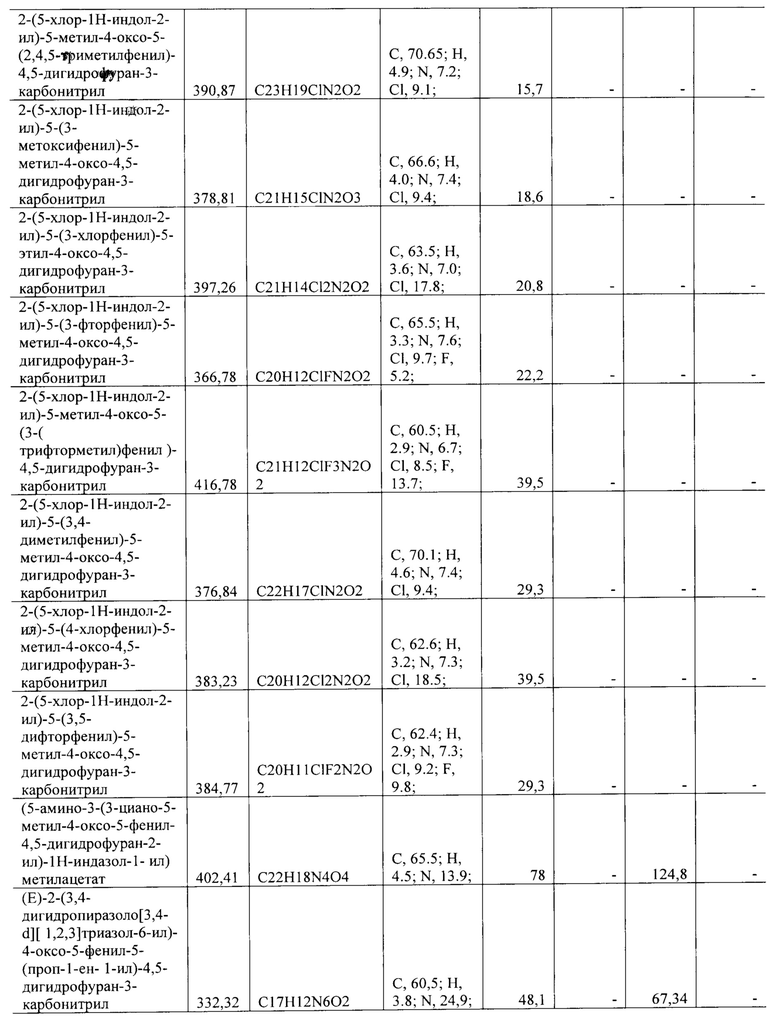
Все синтезированные соединения с активностью в отношении группы вирусов описаны в Таблице 1.
Пример 3
Исследование противовирусной активности в отношении вирусов MERS, SARS, SARS-CoV-2 проведено на культуре клеток Vero Е6, Клетки культивировались на среде DMEM с добавлением 10% FBS, смеси антибиотиков и L-глутамина при 37°С во влажной атмосфере с 5% содержанием С02. Для заражения культуры использованы штаммы вирусов SARS-CoV-2 (VIC01/2020 и SPE-RII-3524V/2020), HCoV-229E и HCoV-ЕМС/2012.
Для изучения противовирусной активности субстанций растворы исследуемых веществ в ДМСО вносили в поддерживающую питательную среду в 10-кратных разведениях в диапазоне концентраций, не вызывающих цитотоксичность. На планшеты с суточным монослоем клеток Vero вносили вирус в концентрации 1000 TCID50 в 100 мкл среды. Через 1 час после инфицирования инфицированных вирусом вносили разведения исследуемых веществ по 100 мкл на лунку в 2 повторностях. Также использовали контроль вируса (100 мкл среды с вирусом в концентрации 1000 TCID50 + 100 мкл поддерживающей среды) и отрицательный контроль клеток (в лунки вносили 200 мкл среды). После 72-часовой инкубации при 37С в атмосфере 5% СО2 регистрировали цитопатическое действие вируса с использованием МТТ теста. По кривой оптической плотности определяли IC50 исследуемого вещества.
Исследование противовирусной активности в отношении вируса ВИЧ-1 проведено на культуре клеток человека МТ-4. Среда для культивирования клеток: RPMI-1640, содержащая 0,2% бикарбоната натрия, с добавлением 10% инактивированной фетальной сыворотки, 2 mM L-глютамина и 20 мкг/мл гентамицина.
Перед определением противовирусной активности исследовалась цитотоксичность исследуемых веществ МТТ-методом. В дальнейшем для определения противовирусной активности в отношении ВИЧ-1 использовались разведения исследуемого вещества в зоне нетоксичности.
Определение концентрации живых клеток, не разрушенных ВИЧ-1, в присутствии ВИЧ и исследуемых соединений проводили на 96-луночном планшете МТТ-методом. В лунки планшета вносили по 30 000 клеток МТ-4 в 100 мкл полной среды RPMI-1640. Затем в отдельной посуде готовили разведения исследуемого вещества с 5-кратным шагом разведения, используя нетоксические для клеток концентрации веществ. Далее по 3 повтора каждого разведения препарата в объеме 50 мкл добавляли в соответствующие лунки планшета с культурой клеток. Объем жидкости в каждой лунке доводили до 200 мкл путем добавления 50 мкл полной среды RPMI-1640.
Инкубирование клеток МТ-4 с исследуемыми разведениями препарата проводили 5 суток в CO2 инкубаторе при температуре 37°С и 5% СО2. После этого добавляли раствор МТТ-реагента в объеме 20 мкл., дополнительно инкубировали в течение 1.5 часов, и по кривой оптической плотности определяли IC50 исследуемого вещества.
Полученные значения 50% ингибирующей концентрации IC50 представлены в Таблице 1.
Пример 4.
Используя соединения, отвечающие формуле (I), которые включают указанные выше заместители, а таже могут быть фармацевтически приемлемыми солями или оптическими изомерами, структура и активность которых описаны в Таблице 1, были получены фармацевтические композиции, включающие активное вещество и фармацевтически приемлемые дополнительные соединения (эксципиенты), широко известные специалисту.
Подходящие носители и эксципиенты хорошо известны специалистам в данной области техники и подробно описаны, например, в Ansel, Howard С, et al., Ansel's Pharmaceutical Dosage Forms and Drug Delivery Systems. Philadelphia: Lippincott, Williams & Wilkins, 2004; Gennaro, Alfonso R., et al. Remington: The Science and Practice of Pharmacy. Philadelphia: Lippincott, Williams & Wilkins, 2000; and Rowe, Raymond C. Handbook of Pharmaceutical Excipients. Chicago, Pharmaceutical Press, 2005. Композиции могут также включать один или более буферов, стабилизирующих агентов, поверхностно-активные вещества, смачивающие агенты, смазывающие агенты, эмульгаторы, суспендирующие агенты, консерванты, антиоксиданты, кроющие агенты, глиданты, технологические добавки, красители, подсластители, отдушки, ароматизаторы, разбавители и другие известные добавки для обеспечения элегантной презентации препарата (например, соединения по настоящему изобретению или его фармацевтической композиции) или помощи в изготовлении фармацевтического продукта (например, лекарственного средства).
Композиции были составлены сочетанием одного или нескольких соединений, описанных в Таблице 1 и подходящих эксципиентов.
Способы приготовления различных композиций могут быть найдены в Remington's Pharmaceutical Sciences, A. Gennaro (ред), 18-ое издание, 1990, изд. Mack Publishing Co., Истон, Пенсильвания.
Приводимые ниже примеры предназначены только для иллюстрации и их не следует рассматривать в качестве ограничений изобретения. Термин "активный компонент" обозначает одно или более соединений, описанных в Таблице 1.
Пример 5. Получение композиции.
Просеянный порошок субстанции активный компонент в количестве 10,0 г, кросповидона в количестве 10,0 г, макрогола 6000 в количестве 8,0 г загружают в шаровую мельницу и микронизируют в течение 30 минут. Активный компонент в смеси с макроголом 6000 и кросповидоном гранулируют в псевдоожиженном слое 20% раствор лактозы и маннита. Полученный гранульный порошок опудривают натрия стеарилфумаратом в количестве 2,0 г в конусном смесителе.
Получаемая фармацевтическая композиция имеет следующий состав (мас. %)
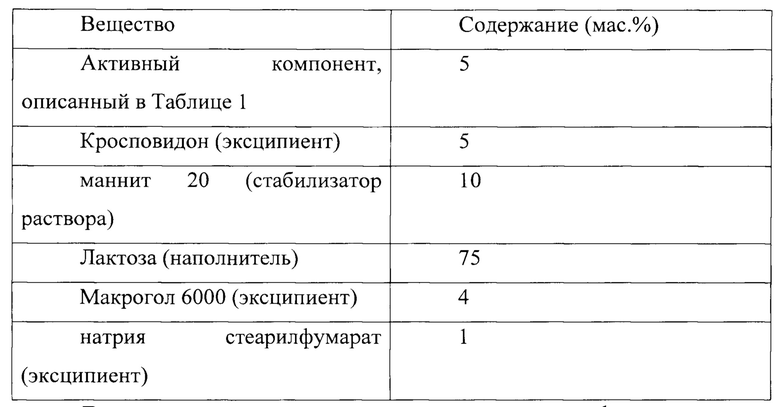
Другие примеры, описывающие получение фармацевтических композиций, могут включать как твердые, так и жидкие приемлемые эксципиенты, при этом образуются следующие составы, например:
Активный компонент - 95-99,99 мас. %
Приемлемый эксципиент - 0,1-5 мас. %,
Или
Активный компонент - 0,1-4 мас. %
Приемлемый эксципиент - 96-99,99 мас. %,
Твердые готовые лекарственные формы включают порошки, таблетки, диспергируемые гранулы, капсулы, крахмальные облатки и суппозитории. Порошки и таблетки могут содержать от 0,1 до 100% активного ингредиента.
Жидкие готовые лекарственные формы включают растворы, суспензии и эмульсии.
Аэрозольные препараты могут включать растворы и твердые вещества в порошкообразной форме, которые могут находиться в комбинации с фармацевтически приемлемы носителем.
Предпочтительно фармацевтический препарат находится в виде унифицированной дозы. В такой форме препарат существует в стандартных дозах подходящей величины, содержащие соответствующее количества активного компонента.
Пример 6. Форма в виде таблетки.
6.1. Формы таблеток получали при помощи влажной грануляции ингредиентов и прессовки.
Активный компонент смешивали с подходящими эксципиентами и ноштелями, при помощи влажной грануляции ингредиентов и прессовки.
6.2. Формы таблеток получали при помощи непосредственной прессовки смешанных ингредиентов.
Активный компонент смешивали с подходящими эксципиентами и носителями, приведенными выше при прессовке.
Пример 7. Капсулы.
Капсулу получали при помощи диспергирования активного ингредиента в подходящих эксципиентах и заполнении капсул.
Пример 8. Форма для инъекции.
Активный компонент смешивали с жидкими эксципиентами, затем смесь фильтровали через стерильный микропористый фильтр и плотно закрывали в стерильные в стеклянные ампулы.
Пример 9. Суспензии. Активный компонент с подходящим эксципиентом смешивали для образования суспензий.
Представленные значения активностей этих соединений указывают на то, что и соединения, и их любое сочетание в композициях проявляют положительный эффект в области лечения и профилактики противовирусных заболеваний.
Способы лечения и/или профилактики вирусных заболеваний.
Способ лечения и/или профилактики сводится к введению соединения формулы I, одного или несколько, и/или его фармацевтически приемлемой соли и/или одного или нескольких изомеров (рацемической смеси или отдельного стереоизомера), фармацевтической композиции, описанной выше, и/или их сочетания, которое специально не ограничивается и определяется в зависимости от различных форм препарата, возраста пациента, пола и других условий и тяжести заболевания.
Таблетки, пилюли, жидкости и растворы, суспензии, эмульсии, гранулы и капсулы вводились перорально. Инъекции вводились внутривенно в чистом виде или после смешивания с обычным жидким заместителем, таким как глюкоза, аминокислоты и т.д., и при необходимости вводятся в чистом виде внутримышечно, внутрикожно, подкожно или внутрибрюшинно. Суппозитории вводятся внутриректально.
Дозировка вышеупомянутого фармацевтического препарата выбирается в зависимости от направления применения, возраста пациента, пола и других условий, и тяжести заболевания, и количество активного компонента определяется индивидуально.
| название | год | авторы | номер документа |
|---|---|---|---|
| 2-АМИДО-4-АРИЛОКСИ-1-КАРБОНИЛПИРРОЛИДИНОВЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ СЕРИНПРОТЕАЗ, В ЧАСТНОСТИ ПРОТЕАЗЫ NS3-NS4A HCV | 2004 |
|
RU2440368C2 |
| МАКРОЦИКЛИЧЕСКИЕ ИНГИБИТОРЫ СЕРИНПРОТЕАЗЫ | 2009 |
|
RU2490272C2 |
| ПРОИЗВОДНЫЕ ПИПЕРИДИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И ПРИМЕНЕНИЕ | 2002 |
|
RU2316553C2 |
| СОЕДИНЕНИЕ, НАЦЕЛЕННОЕ НА БЕЛОК И ЕГО ДЕГРАДАЦИЮ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2021 |
|
RU2829459C1 |
| АРИЛЬНЫЕ, ГЕТЕРОАРИЛЬНЫЕ И ГЕТЕРОЦИКЛИЧЕСКИЕ ФАРМАЦЕВТИЧЕСКИЕ СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ МЕДИЦИНСКИХ НАРУШЕНИЙ | 2018 |
|
RU2801278C2 |
| СОЕДИНЕНИЕ 3,4-ДИГИДРОИЗОХИНОЛИНА И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2825312C1 |
| СОЕДИНЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ 2-АМИНОПИРИМИДИНА И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2795914C1 |
| ПРОИЗВОДНЫЕ ПИПЕРИДИНИЛПИПЕРАЗИНА, ПРИМЕНИМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ХЕМОКИНОВЫХ РЕЦЕПТОРОВ | 2006 |
|
RU2411241C2 |
| ПРОТИВОВИРУСНЫЙ АКТИВНЫЙ КОМПОНЕНТ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ЛЕКАРСТВЕННОЕ СРЕДСТВО, СПОСОБ ЛЕЧЕНИЯ ВИРУСНЫХ ЗАБОЛЕВАНИЙ | 2009 |
|
RU2407738C1 |
| КЛАСС КОНДЕНСИРОВАННЫХ КОЛЬЦЕВЫХ СОЕДИНЕНИЙ И ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2021 |
|
RU2831125C1 |
Изобретение относится к новым биологически активным производным замещенных 2,3-дигидрофуран-3-онов формулы I
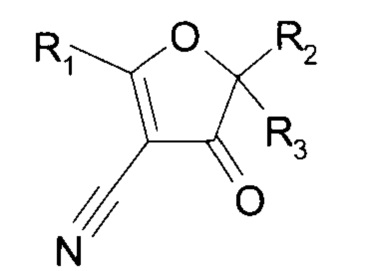 ,
,
где R1 представляет собой заместителей вида 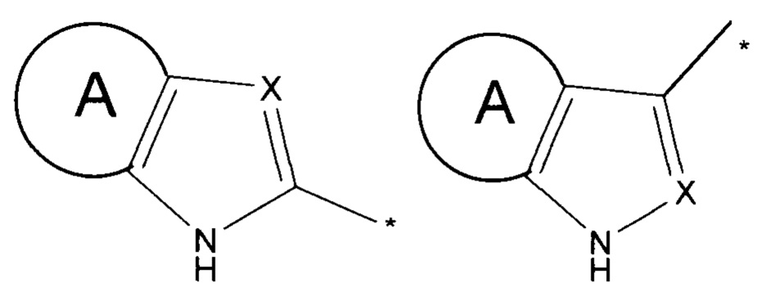 ,
,
где А представляет собой конденсированный С6-арил или 5-6-членный гетероарил, содержащий от 1 до 3 гетероатомов, независимо выбранных из N, S или О, замещенный от 1 до 3 заместителями, независимо выбранными из -F, Cl, NH2, CF3, C1-С3-алкила, С3-циклоалкила, CN, ОН, O-Rz, SO2-Rz, причем звездочкой указано место присоединения заместителя; X представляет собой N или заместитель вида CR4, где R4 выбирается независимо и представляет собой Н, Br, CN, С2-С4-алкенил, 5-членный гетероарил, содержащий 2 гетероатома, выбранных из N и О, С6-арил с заместителями Cl, С3-циклоалкил или 4-членный гетероцикл, содержащий 1 гетероатом N, R2 и R3 выбираются независимо и представляют собой -C1-С6-алкил, который может быть замещен O-Rz; С2-С6-алкенил, С6-арил, который может быть замещен одним, двумя или тремя заместителями, выбранными из F, Cl, CF3, Сl-алкил, O-Rz, O-R2; С3-С9-циклоалкил, или R2 и R3 вместе с атомом, к которому они присоединены, образуют 10-членный спироцикл; каждый Rz независимо выбран и представляет собой -Н; -C1-С6-алкил, 5-членный гетероарил, содержащий 2 гетероатома, выбранных из N, 6-членный гетероцикл, содержащий от 2 гетероатомов, выбранных из N и О, тетрагидропиранил, исключая 2-(1Н-индол-2-ил)-5,5-диметил-4-оксо-4,5-дигидрофуран-3-карбонитрил, а также к фармацевтической композиции, способу профилактики вирусного заболевания, где вирус относится к РНК вирусам, применению соединений для производства лекарственного средства и лекарственному средству, обладающему противовирусной активностью, где вирус относится к РНК вирусам. Технический результат: разработка и получение новых химических соединений, обладающих высокой эффективностью для лечения заболеваний, вызванных РНК вирусами. 11 н. и 11 з.п. ф-лы, 1 табл., 9 пр.
1. Соединение, представленное формулой I, его фармацевтически приемлемая соль или изомер
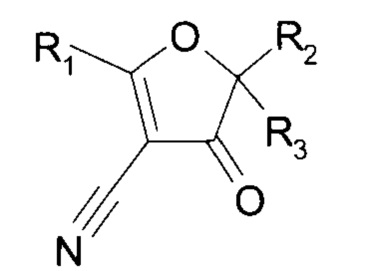
Формула (I),
где R1 представляет собой заместителей вида
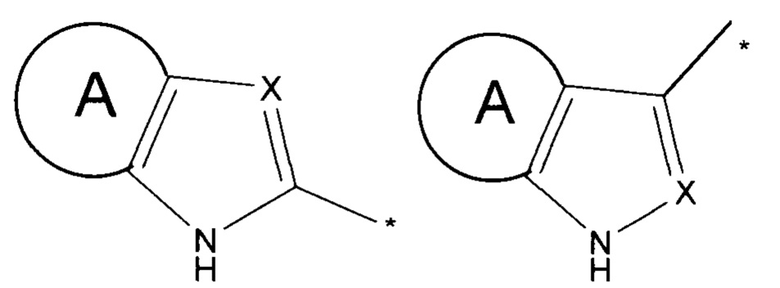 ,
,
где А представляет собой конденсированный С6-арил или 5-6-членный гетероарил, содержащий от 1 до 3 гетероатомов, независимо выбранных из N, S или О, замещенный от 1 до 3 заместителями, независимо выбранными из -F, Cl, NH2, CF3, C1-С3-алкила, С3-циклоалкила, CN, ОН, O-Rz, SO2-Rz,
причем звездочкой указано место присоединения заместителя;
X представляет собой N или заместитель вида CR4,
где R4 выбирается независимо и представляет собой
Н, Br, CN, С2-С4-алкенил, 5-членный гетероарил, содержащий 2 гетероатома, выбранных из N и О, С6-арил с заместителями Cl, С3-циклоалкил или 4-членный гетероцикл, содержащий 1 гетероатом N,
R2 и R3 выбирается независимо и представляет собой -C1-С6 алкил, который может быть замещен O-Rz; С2-С6 - алкенил, С6-арил, который может быть замещен одним, двумя или тремя заместителями, выбранными из F, Cl, CF3, С1-алкил, O-Rz, O-R2; С3-С9-циклоалкил, или
R2 и R3 вместе с атомом, к которому они присоединены, образуют 10-членный спироцикл;
каждый Rz независимо выбран и представляет собой -Н; -C1-С6-алкил, 5-членный гетероарил, содержащий 2 гетероатома, выбранных из N, 6-членный гетероцикл, содержащий от 2 гетероатомов, выбранных из N и О, тетрагидропиранил, исключая 2-(1Н-индол-2-ил)-5,5-диметил-4-оксо-4,5-дигидрофуран-3-карбонитрил.
2. Соединение по п. 1, где заместитель R1 выбирается из группы бициклических конденсированных 8-9-членных гетероарилов вида
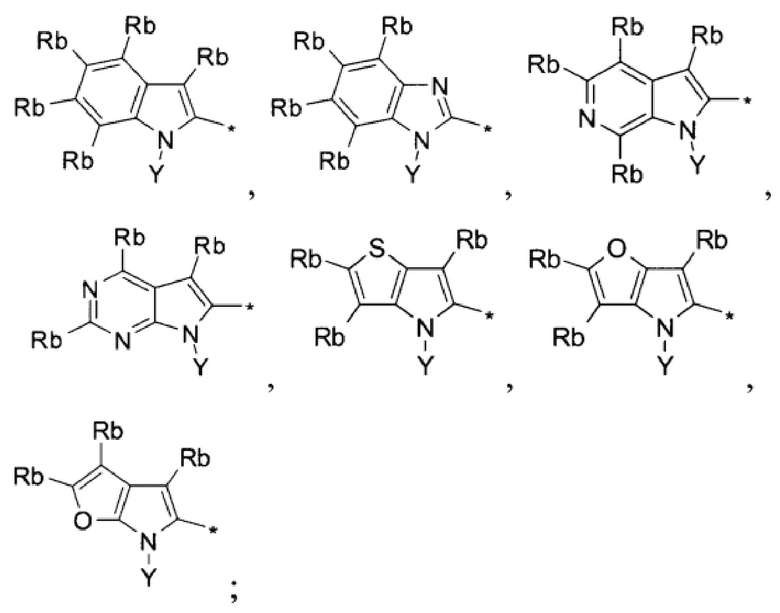
Y представляет собой Н;
Rb выбирается независимо и представляет собой Н, F, Cl, Br, CF3, CN, С1-С3-алкила, -С2-С4-алкенила, С3-циклоалкил, а также аместителей типа ORc, SO2Rc;
Rc независимо выбран и представляет собой Н, C1-С6-алкил, 5-членный гетероарил, содержащий 2 гетероатома, выбранных из N, 6-членный гетероцикл, содержащий от 2 гетероатомов, выбранных из N и О.
3. Соединение общей формулы (Ib)
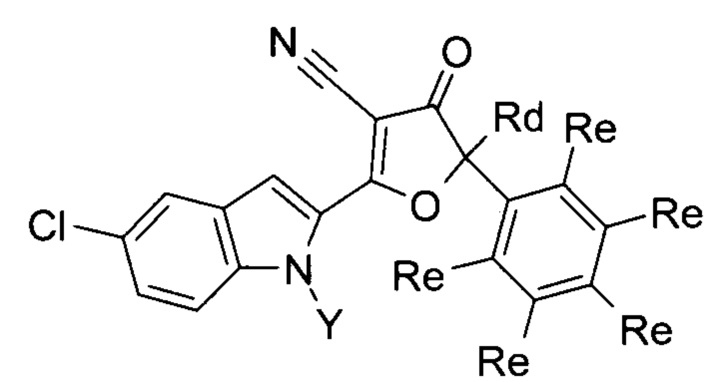
Формула (Ib)
Y представляет собой Н
Rd выбирается независимо и представляет собой С1-С6-алкил;
Re выбирается независимо и представляет собой Н, F, Cl, Br, ОСН3.
4. Соединение, его фармацевтически приемлемая соль или оптический изомер, соответствующие по структуре формуле, выбранной из ряда
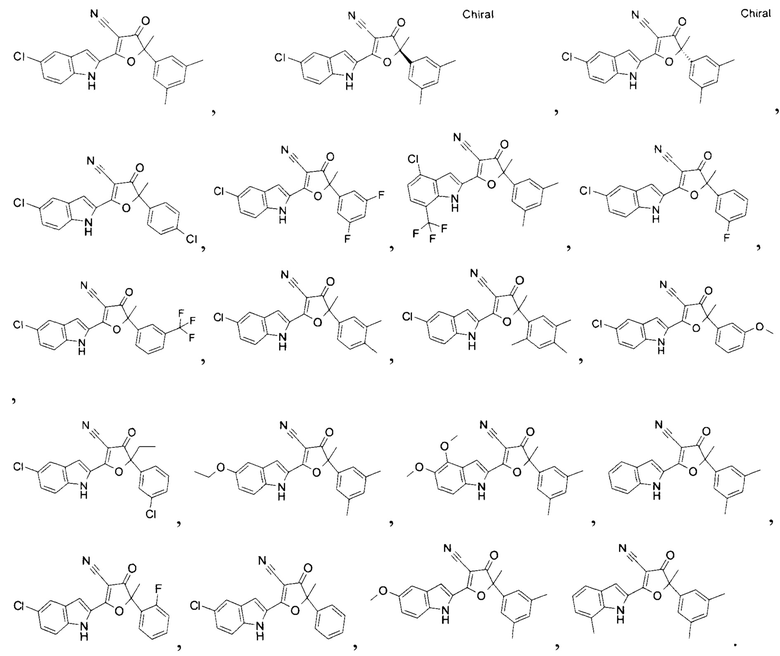
5. Соединение, его фармацевтически приемлемые соли или изомеры, соответствующие
по структуре формуле
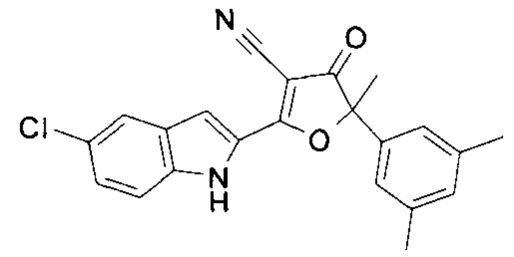
6. Соединение по любому из пп. 1-5, и/или одна или несколько его фармацевтически приемлемых солей, и/или один или несколько изомеров для применения в качестве лекарственного средства с противовирусной активностью, где вирус относится к РНК вирусам.
7. Соединение по п. 3, и/или одна или несколько его фармацевтически приемлемых солей, и/или один или несколько изомеров для применения в качестве лекарственного средства с противовирусной активностью, где вирус относится к РНК вирусам.
8. Соединение по п. 4, и/или одна или несколько его фармацевтически приемлемых солей, и/или один или несколько изомеров для применения в качестве лекарственного средства с противовирусной активностью, где вирус относится к РНК вирусам.
9. Соединение по п. 5, и/или одна или несколько его фармацевтически приемлемых солей, и/или один или несколько изомеров для применения в качестве лекарственного средства с противовирусной активностью, где вирус относится к РНК вирусам.
10. Соединение по любому из пп. 1-5, и/или одна или несколько его фармацевтически приемлемых солей, и/или один или несколько изомеров для получения лекарственного средства с противовирусной активностью, где вирус относится к РНК вирусам.
11. Соединение по п. 3, и/или одна или несколько его фармацевтически приемлемых солей, и/или один или несколько изомеров, для получения лекарственного средства с противовирусной активностью, где вирус относится к РНК вирусам.
12. Соединение по п. 4, и/или одна или несколько его фармацевтически приемлемых солей, и/или один или несколько изомеров для получения лекарственного средства с противовирусной активностью, где вирус относится к РНК вирусам.
13. Соединение по п. 5, и/или одна или несколько его фармацевтически приемлемых солей, и/или один или несколько его изомеров для получения лекарственного средства с противовирусной активностью, где вирус относится к РНК вирусам.
14. Фармацевтическая композиция с противовирусной активностью, где вирус относится к РНК вирусам, включающая от 0,1 до 99,9 мас.% одного или нескольких соединений по пп. 1-5, и/или одну или несколько их фармацевтически приемлемых солей, и/или один или несколько изомеров, и один или более эксципиент.
15. Фармацевтическая композиция по п. 14 для применения в качестве лекарственного средства с противовирусной активностью, где вирус относится к РНК вирусам.
16. Фармацевтическая композиция по п. 14 для получения лекарственного средства с противовирусной активностью, где вирус относится к РНК вирусам.
17. Способ профилактики вирусного заболевания, где вирус относится к РНК вирусам, заключающийся во введении субъекту терапевтически эффективного и безопасного количества одного или несколько соединений по пп. 1-5, и/или одной или нескольких их фармацевтически приемлемых солей, и/или одного или нескольких изомеров.
18. Способ профилактики вирусного заболевания, где вирус относится к РНК вирусам, заключающийся во введении субъекту терапевтически эффективного и безопасного количества одного или нескольких соединений по пп. 1-5 и/или одной или нескольких фармацевтических композиций по п. 14.
19. Способ профилактики вирусного заболевания, где вирус относится к РНК вирусам, заключающийся во введении субъекту терапевтически эффективного и безопасного количества одной или нескольких фармацевтических композиций по п. 14.
20. Применение одного или несколько соединений по любому из пп. 1-5, и/или одной или нескольких их фармацевтически приемлемых солей, и/или одного или нескольких изомеров для производства лекарственного средства с противовирусной активностью, где вирус относится к РНК вирусам.
21. Применение одной или нескольких фармацевтических композиций по п. 14 для производства лекарственного средства с противовирусной активностью, где вирус относится к РНК вирусам.
22. Лекарственное средство, обладающее противовирусной активностью, где вирус относится к РНК вирусам в виде таблеток, капсул, порошков, диспергируемых гранул, крахмальных облаток или инъекций, растворов, суспензии или эмульсии, содержащих одно или несколько соединений по любому из пп. 1-5, и/или одну или несколько их фармацевтически приемлемых солей, и/или одно или несколько их изомеров, и/или фармацевтическую композицию по п. 14.
| MAL'KINA A | |||
| G | |||
| ET AL, Synthesis 48(12), 2016, рр | |||
| Способ закрепления основных красителей на растительных волокнах | 1924 |
|
SU1880A1 |
| FRANCESCA ESPOSITO ET AL, ELSEVIER, Antiviral Research, vol | |||
| Способ прикрепления барашков к рогулькам мокрых ватеров | 1922 |
|
SU174A1 |
| БД PubChem, PubChem CID 136653509, 24.01.2019, PubChem CID 136647557, 24.01.2019 | |||
| J | |||
| HFN ET AL, ELSEVIER, European Journal of Medicinal Chemistry 188 (2020) | |||
Авторы
Даты
2024-10-04—Публикация
2021-10-09—Подача