ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к вариантным антигенсвязывающим доменам, которые специфично связываются с TRBC2 (константной областью 2 бета-цепи Т-клеточного рецептора). Настоящее изобретение также относится к клеткам и агентам, которые можно применять при лечении и диагностике Т-клеточных злокачественных новообразований.
Уровень техники
Лимфоидные злокачественные новообразования в большинстве случаев можно разделить на имеющие Т-клеточное и В-клеточное происхождение. Т-клеточные злокачественные новообразования представляют собой клинически и биологически гетерогенную группу расстройств, в совокупности составляющих 10-20% неходжкинских лимфом и 20% острых лейкозов. Наиболее часто выявляемыми гистологическими подтипами являются: периферическая Т-клеточная лимфома, неспецифицированная (ПТКЛн); ангиоиммунобластная Т-клеточная лимфома (АИТЛ) и анапластическая крупноклеточная лимфома (АККЛ). Из всех острых лимфобластных лейкозов (ОЛЛ) приблизительно 20% имеют Т-клеточный фенотип.
Эти заболевания, как правило, ведут себя агрессивно по сравнению, например, с B-клеточными злокачественными новообразованиями, при этом выживаемость в течение 5 лет составляет всего 30%. В случае Т-клеточной лимфомы, данные заболевания ассоциированы с высокой долей пациентов с диссеминированным заболеванием, неблагоприятным значением Международного прогностического индекса (IPI) и распространенностью экстранодальной формы заболевания. Химиотерапия сама по себе обычно неэффективна, и существующие терапевтические подходы приводят к исцелению менее 30% пациентов.
Кроме того, в отличие от В-клеточных злокачественных новообразований, при которых иммунотерапевтические средства, такие как моноклональное антитело к CD20 ритуксимаб, значительно улучшают результаты, в настоящее время не существует равнозначно эффективного, минимально токсичного иммунотерапевтического средства для лечения Т-клеточных злокачественных новообразований. Серьезной проблемой в разработке иммунотерапевтических средств для Т-клеточных расстройств является значительное частичное совпадение экспрессии маркеров клональных и нормальных Т-клеток, при этом не существует единственного антигена, который позволял бы однозначно идентифицировать клональные (злокачественные) клетки.
Т-клетки c химерными антигенными рецепторами (CAR) показали себя в качестве перспективного средства в лечении рефрактерных В-клеточных злокачественных новообразований. Нацеливание на Т-клеточные злокачественные новообразования, вероятно, будет столь же эффективным, однако применение CAR при таких заболеваниях, как Т-клеточная лимфома, проблематично в связи с недостаточным количеством целевых антигенов. В отличие от В-клеточных лимфом, в которых абляция В-клеточного компартмента представляет собой управляемую токсичность и может лечиться внутривенным введением иммуноглобулина, разрушение Т-клеточного компартмента будет плохо переноситься и приведет к осложнениям, связанным с супрессией клеточно-опосредованного иммунитета.
Способ лечения Т-клеточных лимфом и лейкозов, заключающийся в нацеливании на константную область бета-цепи Т-клеточного рецептора (TRBC), был ранее описан в WO2015/132598. Данный подход основан на уникальной особенности Т-клеточного рецептора, т.е. на том, что каждый TCR кодирует или TRBC1, или TRBC2 взаимоисключающим образом. Поскольку Т-клеточные лимфомы и лейкозы представляют собой клональную популяцию клеток, каждая лимфома будет экспрессировать один TCR, с TRBC1 или TRBC2 на поверхности.
Моноклональное антитело Jovi-1 специфично связывается с TRBC1 и используется в качестве связывающего домена CAR для лечения Т-клеточных лимфом (Maciocia et al., 2017, Nat Med 23:1416-23; WO2015/132598). Данная предлагаемая терапия позволяет осуществлять лечение субпопуляции пациентов, у которых экспрессируются TCR с константной областью TRBC1.
Для лечения всей популяции пациентов необходимы связывающая молекула/CAR, нацеленные на TRBC2. Одним из способов получения антител, специфичных к TRBC2, является отбор фагов в фаговой библиотеке антител человека. Другой способ состоит в иммунизации животных пептидами, происходящими от TRBC2, с последующим отбором специфичных антител. Оба этих подхода были успешно реализованы, и были созданы различные связывающие молекулы, специфичные для TRBC2, как описано в WO2015/132598.
В настоящем изобретении предложены альтернативные связывающие молекулы, специфичные для TRBC2, которые можно использовать в качестве терапевтических агентов для лечения TRBC2-положительных.лимфом или лейкозов.
Краткое изложение аспектов изобретения
Авторы настоящего изобретения определили кристаллическую структуру JOVI-1 (Viney et al., 1992, Hybridoma 11:701-13) - моноклонального антитела, специфичного к TRBC1, в комплексе с TRBC1-TCR с разрешением 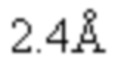 (Фиг. 3). На основании данных о кристаллической структуре, стало возможно модифицировать исходное антитело Jovi-1 так, чтобы оно связывалось с TRBC2. Данный способ является особенно привлекательным, так как ряд аминокислот в составе этого антитела образуют паратоп, который обеспечивает комплементарную форму для которая делает возможным взаимодействие с TCR, в то время как для специфичности к TRBC1 требуется лишь несколько аминокислот. С помощью способов вычислительной биологии и инженерии белков авторы настоящего изобретения, исходя из принципов рациональности, спроектировали мутантные версии связывающих молекул к TRBC1, которые специфичны к TRBC2 и имеют уменьшенную аффинность к TRBC1.
(Фиг. 3). На основании данных о кристаллической структуре, стало возможно модифицировать исходное антитело Jovi-1 так, чтобы оно связывалось с TRBC2. Данный способ является особенно привлекательным, так как ряд аминокислот в составе этого антитела образуют паратоп, который обеспечивает комплементарную форму для которая делает возможным взаимодействие с TCR, в то время как для специфичности к TRBC1 требуется лишь несколько аминокислот. С помощью способов вычислительной биологии и инженерии белков авторы настоящего изобретения, исходя из принципов рациональности, спроектировали мутантные версии связывающих молекул к TRBC1, которые специфичны к TRBC2 и имеют уменьшенную аффинность к TRBC1.
Таким образом, в первом аспекте настоящего изобретения предложен вариантный антигенсвязывающий домен, который содержит по меньшей мере одну мутацию в домене VH (вариабельный домен тяжелой цепи) по сравнению с эталонным антителом, имеющим домен VH с последовательностью с SEQ ID: 1, и домен VL (вариабельный домен легкой цепи) с последовательностью с SEQ ID: 2, в котором по меньшей мере одна мутация в домене VH выбрана из T28K, Y32K и A100N, причем указанный вариантный антигенсвязывающий домен демонстрирует увеличенную аффинность к TRBC2 по сравнению с указанным эталонным антителом.
Указанный вариантный антигенсвязывающий домен может содержать по меньшей мере две мутации в домене VH, выбранные из T28K, Y32K и A100N. Например, указанный домен может содержать мутации Y32K и A100N. Вариантный антигенсвязывающий домен может дополнительно содержать мутацию T28R в домене VH или, в качестве альтернативы - мутацию G31K в домене VH.
Вариантный антигенсвязывающий домен может содержать мутации T28K, Y32K и A100N.
Вариантный антигенсвязывающий домен может дополнительно содержать по меньшей мере одну мутацию в положении, выбранном из группы, состоящей из V2, Y27, G31, R98, Y102, N103 и A107 в домене VH, N35 в домене VL и R55 в домене VL.
По меньшей мере одна дополнительная мутация может быть выбрана из:
a) в домене VH:
- V2K, V2R,
- Y27F, Y27M, Y27N, Y27W,
- G31K, G31R, G31S,
- R98K,
- Y102F, Y102L,
- N103A, N103E, N103F, N103H, N103L, N103M, N103Q, N103S, N103W, N103Y,
- A107S,
и
b) в домене VL:
- N35M, N35F, N35Y, N35K, N35R, и
- R55K.
Вариантный антигенсвязывающий домен может быть выбран из вариантных антигенсвязывающих доменов, содержащих следующие комбинации мутаций:
- T28K, Y32F, A100N в домене VH и N35K в домене VL,
- T28K, Y32F, A100N в домене VH,
- T28K, Y32F, A100N, Y27N в домене VH
- T28K, Y32F, A100N, G31K в домене VH
- T28K, Y32F, A100N, Y27M в домене VH
- T28K, Y32F, A100N, Y27W в домене VH
- T28K, Y32F, A100N в домене VH и R55K в домене VL,
- T28K, Y32F, A100N, N103H в домене VH
- T28K, Y32F, A100N, N103A в домене VH
- T28K, Y32F, A100N, N103Y в домене VH
- T28K, Y32F, A100N в домене VH и N35R в домене VL,
- T28K, Y32F, A100N, N103S в домене VH и N35M в домене VL,
- T28K, Y32F, A100N, N103M, в домене VH,
- T28K, Y32F, A100N, N103W в домене VH и N35R в домене VL,
- T28K, Y32F, A100N в домене VH и N35F в домене VL,
- T28K, Y32F, A100N, N103S в домене VH и N35K в домене VL,
- T28K, Y32F, A100N, R98K в домене VH,
- T28K, Y32F, A100N, N103S в домене VH и N35R в домене VL,
- T28K, Y32F, A100N, N103L в домене VH,
- T28K, Y32F, A100N, N103S в домене VH и N35F в домене VL,
- T28K, Y32F, A100N, N103S в домене VH и N35Y в домене VL,
- T28K, Y32F, A100N, N103L в домене VH и N35M в домене VL,
- T28K, Y32F, A100N, N103L в домене VH и N35R в домене VL,
- T28K, Y32F, A100N, N103W в домене VH и N35K в домене VL,
- T28K, Y32F, A100N, N103L в домене VH и N35Y в домене VL,
- T28K, Y32F, A100N, N103F в домене VH,
- T28K, Y32F, A100N, N103W в домене VH,
- T28K, Y32F, A100N, N103L в домене VH и N35K в домене VL,
- T28K, Y32F, A100N, N103L в домене VH и N35F в домене VL,
- T28K, Y32F, A100N, N103W в домене VH и N35M в домене VL,
- T28K, Y32F, A100N, N103F в домене VH и N35Y в домене VL,
- T28K, Y32F, A100N, Y27F в домене VH,
- T28K, Y32F, A100N, N103Q в домене VH,
- T28K, Y32F, A100N, N103S в домене VH,
- T28K, Y32F, A100N, N103M в домене VH и N35F в домене VL,
- T28K, Y32F, A100N, N103F в домене VH и N35M в домене VL,
- T28K, Y32F, A100N, N103F в домене VH и N35F в домене VL,
- T28K, Y32F, A100N, G31R в домене VH,
- T28K, Y32F, A100N, N103W в домене VH и N35F в домене VL,
- T28K, Y32F, A100N, V2R в домене VH,
- T28K, Y32F, A100N, G31S в домене VH,
- T28K, Y32F, A100N, A107S в домене VH,
- T28K, Y32F, A100N, N103E в домене VH и N35M в домене VL,
- T28K, Y32F, A100N, V2K в домене VH,
- T28K, Y32F, A100N, N103E в домене VH
- T28K, Y32F, A100N, Y102F, N103M в домене VH и N35K в домене VL,
- T28K, Y32F, A100N, Y102F, N103M в домене VH и N35F в домене VL,
- T28K, Y32F, A100N, Y102F, N103M в домене VH и N35R в домене VL,
- T28K, Y32F, A100N, Y102F в домене VH и N35R в домене VL,
- T28K, Y32F, A100N, N103M в домене VH и N35M в домене VL,
- T28K, Y32F, A100N, N103M в домене VH и N35Y в домене VL,
- T28K, Y32F, A100N, N103M в домене VH и N35R в домене VL,
- T28K, Y32F, A100N, N103F в домене VH и N35K в домене VL,
- T28K, Y32F, A100N, Y102L, N103W в домене VH и N35R в домене VL,
- T28K, Y32F, A100N, Y102L, N103W в домене VH и N35K в домене VL,
- T28K, Y32F, A100N, Y102F в домене VH, и
- T28K, Y32F, A100N, Y102L, N103M в домене VH и N35R в домене VL.
Вариантный антигенсвязывающий домен может содержать мутации T28K, Y32F, A100N в домене VH и мутацию N35K в домене VL.
Вариантный антигенсвязывающий домен может содержать мутации T28K, Y32F и A100N в домене VH.
Вариантный антигенсвязывающий домен может дополнительно демонстрировать уменьшенную аффинность к TRBC1 по сравнению с эталонным антителом.
Отношение аффинности вариантного антигенсвязывающего домена к TRBC2 и к TRBC1 должно быть не менее 2.
Отношение аффинности вариантного антигенсвязывающего домена к TRBC2 и к TRBC1 должно быть не менее 5.
Отношение аффинности вариантного антигенсвязывающего домена к TRBC2 и к TRBC1 должно быть не менее 10.
Вариантный антигенсвязывающий домен может дополнительно содержать домен олигомеризации.
Во втором аспекте настоящего изобретения предложено антитело, содержащее вариантный антигенсвязывающий домен в соответствии с первым аспектом настоящего изобретения.
В третьем аспекте настоящего изобретения предложен химерный антигенный рецептор (CAR), содержащий вариантный антигенсвязывающий домен по первому аспекту настоящего изобретения, спейсер, трансмембранный домен и эндодомен.
Спейсер может быть выбран из следующих: «стебель» CD8 человека, представленный в SEQ ID: 7, и спейсер COMP (олигомерного матриксного белка хряща), представленный в SEQ ID: 19.
В четвертом аспекте настоящего изобретения предложен биспецифичный активатор Т-клеток (BiTE), содержащий вариантный антигенсвязывающий домен по первому аспекту настоящего изобретения и домен активации Т-клеток.
В пятом аспекте настоящего изобретения предложена последовательность нуклеиновой кислоты, кодирующая вариантный антигенсвязывающий домен по первому аспекту настоящего изобретения, антитело по второму аспекту настоящего изобретения, CAR по третьему аспекту настоящего изобретения, или BiTE по четвертому аспекту настоящего изобретения.
В шестом аспекте настоящего изобретения предложен вектор, содержащий последовательность нуклеиновой кислоты по пятому аспекту настоящего изобретения.
В седьмом аспекте настоящего изобретения предложена клетка, которая содержит CAR по третьему аспекту настоящего изобретения.
В восьмом аспекте настоящего изобретения предложен способ получения клетки по седьмому аспекту настоящего изобретения, включающий этап трансдукции или трансфекции клетки вектором по шестому аспекту настоящего изобретения, который содержит последовательность нуклеиновой кислоты, кодирующую CAR.
В девятом аспекте настоящего изобретения предложен конъюгат, содержащий вариантный антигенсвязывающий домен по первому аспекту настоящего изобретения или антитело по второму аспекту настоящего изобретения, и детектируемый компонент или химиотерапевтический компонент.
Данный конъюгат может содержать химиотерапевтический компонент.
В десятом аспекте настоящего изобретения предложен способ лечения Т-клеточных лимфомы или лейкоза у субъекта, включающий этап введения клетки по седьмому аспекту настоящего изобретения или антитела по второму аспекту настоящего изобретения, или BiTE по четвертому аспекту настоящего изобретения, или конъюгата по девятому аспекту настоящего изобретения субъекту, в организме которого злокачественные Т-клетки экспрессируют TRBC2.
Т-клеточные лимфома или лейкоз могут быть выбраны из следующего: неспецифицированная периферическая Т-клеточная лимфома (ПТКЛн); ангиоиммунобластная Т-клеточная лимфома (АИТЛ), анапластическая крупноклеточная лимфома (АККЛ), Т-клеточная лимфома, ассоциированная с энтеропатией (EATL), гепатолиенальная Т-клеточная лимфома (ГЛТЛ), экстранодальная NK/T-клеточная лимфома назального типа, Т-клеточная лимфома кожи, первичная АККЛ кожи, Т-клеточный пролимфоцитарный лейкоз и Т-клеточный острый лимфобластный лейкоз.
В одиннадцатом аспекте настоящего изобретения предложена клетка по седьмому аспекту настоящего изобретения или антитело по второму аспекту настоящего изобретения, или BiTE по четвертому аспекту настоящего изобретения, или конъюгат по девятому аспекту настоящего изобретения для применения в медицине.
В двенадцатом аспекте настоящего изобретения предложена клетка по седьмому аспекту настоящего изобретения или антитело по второму аспекту настоящего изобретения, или BiTE по четвертому аспекту настоящего изобретения, или конъюгат по девятому аспекту настоящего изобретения для применения в лечении Т-клеточных лимфомы или лейкоза, при которой(ом) злокачественные Т-клетки экспрессируют TRBC2.
Т-клеточные лимфома или лейкоз могут быть выбраны из следующего: неспецифицированная периферическая Т-клеточная лимфома (ПТКЛн); ангиоиммунобластная Т-клеточная лимфома (АИТЛ), анапластическая крупноклеточная лимфома (АККЛ), Т-клеточная лимфома, ассоциированная с энтеропатией (EATL), гепатолиенальная Т-клеточная лимфома (ГЛТЛ), экстранодальная NK/T-клеточная лимфома назального типа, Т-клеточная лимфома кожи, первичная АККЛ кожи, Т-клеточный пролимфоцитарный лейкоз и Т-клеточный острый лимфобластный лейкоз.
В тринадцатом аспекте настоящего изобретения предложено применение клетки по седьмому аспекту настоящего изобретения или антитела по второму аспекту настоящего изобретения, или BiTE по четвертому аспекту настоящего изобретения, или конъюгата по девятому аспекту настоящего изобретения при изготовлении лекарственного средства для лечения Т-клеточных лимфомы или лейкоза, при которой(ом) злокачественные Т-клетки экспрессируют TRBC2.
Т-клеточные лимфома или лейкоз могут быть выбраны из следующего: неспецифицированная периферическая Т-клеточная лимфома (ПТКЛн); ангиоиммунобластная Т-клеточная лимфома (АИТЛ), анапластическая крупноклеточная лимфома (АККЛ), Т-клеточная лимфома, ассоциированная с энтеропатией (EATL), гепатолиенальная Т-клеточная лимфома (ГЛТЛ), экстранодальная NK/T-клеточная лимфома назального типа, Т-клеточная лимфома кожи, первичная АККЛ кожи, Т-клеточный пролимфоцитарный лейкоз и Т-клеточный острый лимфобластный лейкоз.
В четырнадцатом аспекте настоящего изобретения предложен диагностический агент, который содержит вариантный антигенсвязывающий домен по первому аспекту настоящего изобретения или антитело по второму аспекту настоящего изобретения.
Данный диагностический агент может быть предназначен для диагностики Т-клеточных лимфомы или лейкоза.
Т-клеточные лимфома или лейкоз могут быть выбраны из следующего: неспецифицированная периферическая Т-клеточная лимфома (ПТКЛн); ангиоиммунобластная Т-клеточная лимфома (АИТЛ), анапластическая крупноклеточная лимфома (АККЛ), Т-клеточная лимфома, ассоциированная с энтеропатией (EATL), гепатолиенальная Т-клеточная лимфома (ГЛТЛ), экстранодальная NK/T-клеточная лимфома назального типа, Т-клеточная лимфома кожи, первичная АККЛ кожи, Т-клеточный пролимфоцитарный лейкоз и Т-клеточный острый лимфобластный лейкоз.
В пятнадцатом аспекте настоящего изобретения предложен способ диагностики Т-клеточной лимфомы или лейкоза у субъекта, включающий этап приведения в контакт вариантного антигенсвязывающего домена по первому аспекту настоящего изобретения или антитела по второму аспекту настоящего изобретения с содержащим Т-клетки образцом, полученным у данного субъекта.
Способ диагностики Т-клеточных лимфомы или лейкоза у субъекта может дополнительно включать этап определения процентной доли TRBC2-положительных Т-клеток в образце.
Процент, составляющий 70% или более TRBC2-положительных Т-клеток в образце может указывать на наличие Т-клеточных лимфомы или лейкоза.
Образец может представлять собой образец крови или может быть получен из него.
Т-клеточные лимфома или лейкоз могут быть выбраны из следующего: неспецифицированная периферическая Т-клеточная лимфома (ПТКЛн); ангиоиммунобластная Т-клеточная лимфома (АИТЛ), анапластическая крупноклеточная лимфома (АККЛ), Т-клеточная лимфома, ассоциированная с энтеропатией (EATL), гепатолиенальная Т-клеточная лимфома (ГЛТЛ), экстранодальная NK/T-клеточная лимфома назального типа, Т-клеточная лимфома кожи, первичная АККЛ кожи, Т-клеточный пролимфоцитарный лейкоз и Т-клеточный острый лимфобластный лейкоз.
В шестнадцатом аспекте настоящего изобретения предложен способ идентификации субъектов с Т-клеточными лимфомой или лейкозом, соответствующих критериям для лечения с применением клетки по седьмому аспекту настоящего изобретения или антитела по второму аспекту настоящего изобретения, или BiTE по четвертому аспекту настоящего изобретения, или конъюгата по девятому аспекту настоящего изобретения, включающий определение процента TRBC2-положительных Т-клеток в полученном от субъекта образце, содержащем Т-клетки.
Субъект может соответствовать критериям для вышеуказанного лечения с применением клетки по седьмому аспекту настоящего изобретения или антитела по второму аспекту настоящего изобретения, или BiTE по четвертому аспекту настоящего изобретения, или конъюгата по девятому аспекту настоящего изобретения, если процент TRBC2-положительных Т-клеток в образце составляет 70% или более.
Образец может представлять собой образец крови или может быть получен из него.
Т-клеточные лимфома или лейкоз могут быть выбраны из следующего: неспецифицированная периферическая Т-клеточная лимфома (ПТКЛн); ангиоиммунобластная Т-клеточная лимфома (АИТЛ), анапластическая крупноклеточная лимфома (АККЛ), Т-клеточная лимфома, ассоциированная с энтеропатией (EATL), гепатолиенальная Т-клеточная лимфома (ГЛТЛ), экстранодальная NK/T-клеточная лимфома назального типа, Т-клеточная лимфома кожи, первичная АККЛ кожи, Т-клеточный пролимфоцитарный лейкоз и Т-клеточный острый лимфобластный лейкоз.
В семнадцатом аспекте настоящего изобретения предложен способ выбора терапии, включающей клетку по седьмому аспекту настоящего изобретения или антитело по второму аспекту настоящего изобретения, или BiTE по четвертому аспекту настоящего изобретения, или конъюгат по девятому аспекту настоящего изобретения для лечения субъекта, включающий определение процентной доли TRBC2-положительных Т-клеток в полученном от указанного субъекта образце, содержащем Т-клетки.
Указанная терапия может быть выбрана для лечения указанного субъекта, если процент TRBC2-положительных Т-клеток в образце составляет 70% или более.
Образец может представлять собой образец крови или может быть получен из него.
Т-клеточные лимфома или лейкоз могут быть выбраны из следующего: неспецифицированная периферическая Т-клеточная лимфома (ПТКЛн); ангиоиммунобластная Т-клеточная лимфома (АИТЛ), анапластическая крупноклеточная лимфома (АККЛ), Т-клеточная лимфома, ассоциированная с энтеропатией (EATL), гепатолиенальная Т-клеточная лимфома (ГЛТЛ), экстранодальная NK/T-клеточная лимфома назального типа, Т-клеточная лимфома кожи, первичная АККЛ кожи, Т-клеточный пролимфоцитарный лейкоз и Т-клеточный острый лимфобластный лейкоз.
Описание ЧЕРТЕЖЕЙ
Фиг. 1. Схема комплекса Т-клеточный рецептор αβ/CD3.
Т-клеточный рецептор формируется из 6 различных белковых цепей, сборка которых происходит в эндоплазматическом ретикулуме, чтобы они экспрессировались на поверхности клеток. Четыре белка комплекса CD3 (CD3ζ, CD3γ, CD3ε и CD3ε) формируют окружение Т-клеточного рецептора (TCR). Указанный TCR придает комплексу специфичность к определенному антигену и состоит из двух цепей: TCRα и TCRβ. Каждая цепь TCR имеет вариабельный участок, дистальный по отношению к мембране, и константный участок, проксимальный по отношению к мембране. Почти все Т-клеточные лимфомы и многие Т-клеточные лейкозы экспрессируют комплекс TCR/CD3.
Фиг. 2: Сегрегация константной области β-цепи Т-клеточного рецептора (TRBC)-1 и TRBC2 во время реаранжировки Т-клеточного рецептора. Каждая бета-цепь TCR формируется в результате геномной рекомбинации конкретных вариабельной (variable; V), обеспечивающей разнообразие (diversity; D), соединительной (joining; J) и константной (TRBC) областей бета-цепи. Геном человека содержит два очень похожих и функционально эквивалентных локуса TRBC, известных как TRBC1 и TRBC2. Во время реаранжировки генов TCR происходит рекомбинация J-области с TRBC1 или TRBC2. Данная реаранжировка является постоянной. Т-клетки экспрессируют множество копий одного TCR на своей поверхности, следовательно, каждая Т-клетка будет экспрессировать TCR, константная область β-цепи которого кодируется или TRBC1, или TRBC2.
Фиг. 3. Структурная область контакта между бета-цепью TCR и фрагментом Fab антитела Jovi-1, специфичного к TRBC1.
Фиг. 4. Схема структуры химерных антигенных рецепторов (CAR), специфичных к TRBC1 и TRBC2.
Фиг. 5. Функциональная характеристика CAR к TRBC2.
Продуцирование IFN-γ (A) содержащим три мутации CAR к TRBC2 и (B) CAR к TRBC1, инкубированным в присутствии TRBC1 или TRBC2.
Фиг. 6. Цитотоксическая активность (A) T-клеток с содержащим три мутации CAR к TRBC2 и (B) Т-клеток с CAR к TRBC1, совместно инкубированных с клетками Raji WT, Raji TRBC1+ или Raji TRBC2+.
Фигура 7. Антиген-специфичная активация клеток Jurkat, трансдуцированных CAR против TRBC2, которые были совместно инкубированы с клетками HPB (периферической крови человека) с TRBC1 и HPB с TRBC2. Клетки Jurkat (TRBC1+) трансдуцировали конструкциями CAR против TRBC2 второго поколения и совместно инкубировали с клетками HPB с TRBC1 и HPB с TRBC2 при соотношении Э:М (эффектор:мишень) 1:1. Контрольные группы включали нетрансдуцированные клетки Jurkat (NT), клетки HPB-ALL (клетки периферической крови человека, полученные при остром лимфобластном лейкозе) с нокаутом TCR (обозначены: HPB KO) и трансдуцированные клетки Jurkat, посеянные в чистом виде в качестве отрицательного контроля, или с антителами αCD3/αCD28 - в качестве положительного контроля для анализа, соответственно. N35K: связывающая молекула, имеющая мутации T28K, Y32F, A100N в домене VH и N35K в домене VL антитела hJovi-1; N103L: связывающая молекула, имеющая мутации T28K, Y32F, A100N, N103L в домене VH антитела hJovi-1; N103M-N35Y: связывающая молекула, имеющая мутации T28K, Y32F, A100N, N103M в домене VH и N35Y в домене VL антитела hJovi-1; Y102F-N103M-N35R: связывающая молекула, имеющая мутации T28K, Y32F, A100N, Y102F, N103M в домене VH и N35R в домене VL антитела hJovi-1; и Y102L-N103M-N35R: связывающая молекула, имеющая мутации T28K, Y32F, A100N, Y102L, N103M в домене VH и N35R в домене VL антитела hJovi-1.
Фиг. 8. Цитотоксическая активность T-клеток с CAR к TRBC2, инкубированных совместно с клетками TRBC1+HPB-ALL и TRBC2+HPB-ALL. Мононуклеарные клетки периферической крови (МКПК) трансдуцировали конструкциями CAR против TRBC2 второго поколения. Трансдуцированные МКПК инкубировали совместно с клетками TRBC1+HPB-ALL и TRBC2+HPB-ALL при соотношении Э:М 1:2. Контрольные группы включали нетрансдуцированные клетки (NT), клетки, трансдуцированные CAR против TRBC1 hJovi-1 (JOVI), и клетки HPB-ALL с нокаутированным TCR (HPB-KO). N35K: связывающая молекула, имеющая мутации T28K, Y32F, A100N в домене VH и N35K в домене VL антитела hJovi-1; N103L: связывающая молекула, имеющая мутации T28K, Y32F, A100N, N103L в домене VH антитела hJovi-1; N103M-N35Y: связывающая молекула, имеющая мутации T28K, Y32F, A100N, N103M в домене VH и N35Y в домене VL антитела hJovi-1; Y102F-N103M-N35R: связывающая молекула, имеющая мутации T28K, Y32F, A100N, Y102F, N103M в домене VH и N35R в домене VL антитела hJovi-1; и Y102L-N103M-N35R: связывающая молекула, имеющая мутации T28K, Y32F, A100N, Y102L, N103M в домене VH и N35R в домене VL антитела hJovi-1.
Фиг. 9: Анализ влияния различных форматов антител на связывание антител к TRBC2 посредством поверхностного плазмонного резонанса (SPR).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Авторы настоящего изобретения определили кристаллическую структуру моноклонального антитела Jovi-1, что помогло идентифицировать два ключевых остатка, необходимых для формирования специфичности к TRBC1 (Фиг. 1). Интересен тот факт, что данные остатки расположены в CDR (участок, определяющей комплементарность) 1, а не в CDR 3, который, как правило, определяет специфичность антитела. Кроме того, другие остатки, которые расположены в непосредственной близости от эпитопа TRBC1, вероятно, будут играть важную роль в конструировании специфичности области TRBC1 по отношению к TRBC2. В настоящей заявке приведено описание остатков, содержащихся в Jovi-1, которые участвуют в связывании TRBC1 или которые играют важную роль в формировании специфичности к TRBC2.
В настоящем изобретении предложены варианты антигенсвязывающего домена антитела JOVI-1, обладающие увеличенной аффинностью к константной области 2 бета-цепи TCR (TRBC2) по сравнению с JOVI-1.
1. Константная область β-цепи TCR (TRBC)
Т-клеточный рецептор (TCR) экспрессируется на поверхности Т-лимфоцитов и отвечает за распознавание антигенов, связанных с молекулами главного комплекса гистосовместимости (ГКГС). При взаимодействии TCR с антигенным пептидом и ГКГС (пептид/ГКГС), T-лимфоцит активируется посредством ряда биохимических событий, опосредованных ассоциированными ферментами, корецепторами, специализированными адаптерными молекулами и активированными или высвобожденными транскрипционными факторами.
TCR представляет собой связанный дисульфидной связью, заякоренный на мембране гетеродимер, обычно состоящий из высоковариабельных альфа (α) и бета (β) цепей, экспрессируемых как часть комплекса с инвариантными молекулами цепи CD3. Т-клетки, экспрессирующие данный рецептор, называют α:β (или αβ) Т-клетками (~95% от общего количества Т-клеток). Меньшая часть Т-клеток экспрессирует альтернативный рецептор, образованный вариабельными гамма (γ) и дельта (δ) цепями, и эти клетки называются γδ Т-клетками (~5% от общего количества Т-клеток).
Каждая α и β цепь состоит из двух внеклеточных доменов: вариабельной (V) и константной (C) областей, причем оба домена, принадлежащие к суперсемейству Иммуноглобулинов (IgSF), образуют антипараллельные β-листы. Константная область расположена проксимально к клеточной мембране, за ней расположена трансмембранная область и короткий цитоплазматический концевой сегмент, тогда как вариабельная область связывается с комплексом пептид/ГКГС. Константная область TCR состоит из коротких соединительных последовательностей, в которых остаток цистеина образует дисульфидные связи, которые образуют связь между двумя цепями две цепи.
Вариабельные домены α-цепи и β-цепи TCR имеют три гипервариабельных или определяющих комплементарность участка (CDR). Вариабельная область β-цепи также имеет дополнительный участок гипервариабельности (HV4), однако обычно она не контактирует с антигеном и поэтому не считается CDR.
TCR также содержит до пяти инвариантных цепей γ, δ, ε (совместно именуемые CD3) и ζ. Субъединицы CD3 и ζ опосредуют передачу сигналов TCR через особые цитоплазматические домены, которые взаимодействуют с молекулами вторичного мессенджера и адаптерными молекулами после распознавания антигена клетками αβ или γδ. Экспрессии комплекса TCR на поверхности клеток предшествует попарная сборка субъединиц, в которой участвуют трансмембранные и внеклеточные домены цепей α и β TCR, и цепей γ и δ CD3.
Таким образом, TCR обычно состоят из комплекса CD3 и цепей α и β TCR, которые, в свою очередь, состоят из вариабельных и константных областей (Фиг. 1).
Локус (Chr7:q34), в котором расположена константная область β-цепи TCR (TRBC), в ходе эволюции удвоился с образованием двух почти идентичных и функционально равнозначных генов: TRBC1 и TRBC2 (Фиг. 2). Каждый TCR может содержать взаимоисключающим образом или TRBC1, или TRBC2, и, таким образом, каждая T-клетка из αβ будет экспрессировать или TRBC1, или TRBC2 взаимоисключающим образом.
Авторы настоящего изобретения ранее определили, что, несмотря на сходство между последовательностями TRBC1 и TRBC2, их можно отличить друг от друга. Авторы изобретения также ранее определили, что аминокислотные последовательности TRBC1 и TRBC2 могут быть распознаны in situ на поверхности клетки, например, Т-клетки (WO2015/132598).
2. Вариантный антигенсвязывающий домен
В первом аспекте настоящего изобретения предложен вариантный антигенсвязывающий домен (далее - «вариантный антигенсвязывающий домен согласно настоящему изобретению»), который содержит по меньшей мере одну мутацию в домене VH по сравнению с эталонным антителом, имеющим домен VH с последовательностью с SEQ ID: 1, и домен VL с последовательностью с SEQ ID: 2, в котором по меньшей мере одна мутация в домене VH выбрана из T28K, Y32K и A100N, причем данный вариантный антигенсвязывающий домен демонстрирует увеличенную аффинность к TRBC2 по сравнению с эталонным антителом.
Термин «вариантный» или «мутантный» в контексте настоящей заявки относится к полипептиду, отличающемуся от конкретно указанного полипептида, т.е. эталонного или родительского полипептида аминокислотными вставками, делециями и/или заменами, сделанными с помощью, например, способов рекомбинантной ДНК или синтеза de novo. Понятия «вариантный» или «мутантный» в контексте настоящего изобретения используют без ограничения их смысла. Вариантные антигенсвязывающие домены по настоящему изобретению включают антигенсвязывающие молекулы, в которых один или несколько аминокислотных остатков модифицированы заменой, вставкой и/или делецией таким образом, что это оказывает существенное влияние на аффинность эталонного или родительского антигенсвязывающего домена по связыванию антигена.
Термин «антигенсвязывающий домен» в контексте настоящей заявки относится к вариабельным областям каждой пары легкой и тяжелой цепей антитела, то есть к доменам VL и VH соответственно, которые формируют его участок связывания. Они характеризуются одинаковой общей структурой, состоящей из относительно сохранившихся участков, называемых каркасными (FR), соединенных тремя гипервариабельными участками, называемыми участками, определяющими комплементарность (CDR) (Kabat et al., 1991, Sequences of Proteins of Immunological Interest, 5th Ed., NIH Publication No. 91-3242, Bethesda, MD.; Chothia & Lesk, 1987, J Mol Biol 196:901-17). Термин «определяющий комплементарность участок» или «CDR» в контексте настоящей заявки относится к области антитела, которая является комплементарной форме антигена. Таким образом, CDR определяют аффинность белка (проще говоря, силу связывания) и специфичность к конкретным антигенам. CDR двух цепей каждой пары выравниваются за счет каркасных областей, приобретая функцию связывания с конкретным эпитопом.
Вариантный антигенсвязывающий домен согласно настоящему изобретению содержит по меньшей мере одну мутацию в домене VH по сравнению с эталонным антителом. Термин «эталонное антитело» в контексте настоящей заявки относится к гуманизированному антителу JOVI-1, т.е. hJOVI-1, которое содержит домен VH с последовательностью согласно SEQ ID: 1, и домен VL с последовательностью согласно SEQ ID: 2. Антитело мыши JOVI-1 было ранее описано Viney et al. (1992; как было приведено выше) и является доступным на рынке (Abcam, ab5465). Ранее было определено, что JOVI-1 способно различать клетки исходя из специфичной экспрессии TRBC1 или TRBC2 посредством специфичного связывания исключительно с TRBC1 (WO 2015/132598).
SEQ ID: 1 (домен VH антитела hJOVI-1):
QVQLVQSGAEVKKPGASVKVSCKASGYTFTGYVMHWVRQAPGQGLEWMGFINPYNDDIQSNERFRGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARGAGYNFDGAYRFFDFWGQGTMVTVSS
SEQ ID: 2 (домен VL антитела hJOVI-1):
DIVMTQSPLSLPVTPGEPASISCRSSQRLVHSNGNTYLHWYLQKPGQSPRLLIYRVSNRFPGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCSQSTHVPYTFGQGTKLEIK
Далее любое упоминание домена VH означает домен VH антитела hJOVI-1 согласно SEQ ID: 1, если не указано иное, и любое упоминание домена VL означает домен VL антитела hJOVI-1 согласно SEQ ID: 2., если не указано иное.
Авторы настоящего изобретения определили, что наличие по меньшей мере одной мутации, выбранной из T28K, Y32F и A100N, в домене VH эталонного антитела, вызывает увеличение аффинности вариантного антигенсвязывающего домена согласно настоящему изобретению к TRBC2 по сравнению с эталонным антителом (Пример 1).
Термин «аффинность» в контексте настоящей заявки относится к силе взаимодействия между участком связывания антигена антитела и эпитопом. Антитела с высокой аффинностью будут связывать большее количество антигена за более короткий период времени, чем антитела с низкой аффинностью. Аффинность обычно количественно определяется в качестве равновесной константы диссоциации (KD), которая равна отношению kконеч/kначал между антителом и антигеном. Аффинность антигенсвязывающего домена к какому-либо определенному антигену может быть количественно определена с помощью какого-либо общепринятого способа, включая, без ограничения, способы, основанные на меченных клетках, такие как прямой и непрямой иммуноферментный анализ (ELISA) и радиоиммуноанализ, и способы без применения меток, которые позволяют осуществлять непосредственное обнаружение и количественное определение взаимодействий в реальном времени, такие как поверхностный плазмонный резонанс и интерференция биослоя.
Аффинность вариантного антигенсвязывающего домена согласно настоящему изобретению к TRBC2 увеличена по сравнению с аффинностью эталонного антитела. Аффинность вариантного антигенсвязывающего домена к TRBC2 может быть увеличена по меньшей мере на 1%, по меньшей мере на 5%, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 100%, по меньшей мере на 150%, по меньшей мере на 200%, по меньшей мере на 300%, по меньшей мере на 400%, по меньшей мере на 500%, по меньшей мере на 600%, по меньшей мере на 700%, по меньшей мере на 800%, по меньшей мере на 900%, по меньшей мере на 1000%, по меньшей мере на 5000% или по меньшей мере на 10000% по сравнению с аффинностью эталонного антитела к TRBC2.
Вариантный антигенсвязывающий домен согласно настоящему изобретению может содержать мутацию T28K в домене VH. Вариантный антигенсвязывающий домен согласно настоящему изобретению может содержать мутацию Y32F в домене VH. Вариантный антигенсвязывающий домен согласно настоящему изобретению может содержать мутацию A100N в домене VH.
Вариантный антигенсвязывающий домен согласно настоящему изобретению может содержать по меньшей мере две мутации в домене VH, выбранные из T28K, Y32F и A100N. По меньшей мере две мутации могут быть мутациями Y32F и A100N. В одном из вариантов реализации настоящего изобретения вариантный антигенсвязывающий домен согласно настоящему изобретению может содержать мутации Y32F и A100N, и дополнительно содержать мутацию T28R в домене VH. В другом варианте реализации вариантный антигенсвязывающий домен согласно настоящему изобретению может содержать мутации Y32F и A100N, и дополнительно содержать мутацию G31R в домене VH.
Вариантный антигенсвязывающий домен согласно настоящему изобретению может содержать мутации T28K, Y32F и A100N в домене VH.
В другом варианте реализации вариантный антигенсвязывающий домен согласно настоящему изобретению содержит мутации T28K, Y32F и A100N в домене VH, и дополнительно содержит по меньшей мере одну мутацию в положении, выбранном из группы, состоящей из V2, Y27, G31, R98, Y102, N103 и A107 в домене VH, и N35 и R55 в домене VL. Вариантный антигенсвязывающий домен согласно настоящему изобретению может содержать одну, две, три, четыре, пять, шесть или семь мутаций в положении, выбранном из группы, состоящей из V2, Y27, G31, R98, Y102, N103 и A107 в домене VH, и N35 и R55 в домене VL.
Вариантный антигенсвязывающий домен согласно настоящему изобретению может содержать мутации T28K, Y32F и A100N в домене VH, и может дополнительно содержать мутацию в положении V2 в домене VH, мутацию в положении Y27 в домене VH, мутацию в положении G31 в домене VH, мутацию в положении R98 в домене VH, мутацию в положении Y102 в домене VH, мутацию в положении N103 в домене VH, мутацию в положении A107 в домене VH, мутацию в положении N35 в домене VL и мутацию в положении R55 в домене VL.
Вариантный антигенсвязывающий домен по настоящему изобретению может содержать мутации T28K, Y32F и A100N в домене VH, и дополнительно содержать по меньшей мере одну мутацию, выбранную из:
a) в домене VH:
- V2K, V2R,
- Y27F, Y27M, Y27N, Y27W,
- G31K, G31R, G31S,
- R98K,
- Y102F, Y102L,
- N103A, N103E, N103F, N103H, N103L, N103M, N103Q, N103S, N103W, N103Y и
- A107S,
и
b) в домене VL:
- N35M, N35F, N35Y, N35K, N35R и
- R55K.
Вариантный антигенсвязывающий домен согласно настоящему изобретению может быть выбран из вариантных антигенсвязывающих доменов, содержащих следующие комбинации мутаций:
- T28K, Y32F, A100N, Y27N в домене VH,
- T28K, Y32F, A100N, G31K в домене VH,
- T28K, Y32F, A100N, Y27M в домене VH,
- T28K, Y32F, A100N, Y27W в домене VH,
- T28K, Y32F, A100N в домене VH,
- T28K, Y32F, A100N в домене VH и R55K в домене VL,
- T28K, Y32F, A100N в домене VH и N35K в домене VL,
- T28K, Y32F, A100N, N103H в домене VH,
- T28K, Y32F, A100N, N103A в домене VH,
- T28K, Y32F, A100N, N103Y в домене VH,
- T28K, Y32F, A100N в домене VH и N35R в домене VL,
- T28K, Y32F, A100N, N103S в домене VH и N35M в домене VL,
- T28K, Y32F, A100N, N103M, в домене VH,
- T28K, Y32F, A100N, N103W в домене VH и N35R в домене VL,
- T28K, Y32F, A100N в домене VH и N35F в домене VL,
- T28K, Y32F, A100N, N103S в домене VH и N35K в домене VL,
- T28K, Y32F, A100N, R98K в домене VH,
- T28K, Y32F, A100N, N103S в домене VH и N35R в домене VL,
- T28K, Y32F, A100N, N103L в домене VH,
- T28K, Y32F, A100N, N103S в домене VH и N35F в домене VL,
- T28K, Y32F, A100N, N103S в домене VH и N35Y в домене VL,
- T28K, Y32F, A100N, N103L в домене VH и N35M в домене VL,
- T28K, Y32F, A100N, N103L в домене VH и N35R в домене VL,
- T28K, Y32F, A100N, N103W в домене VH и N35K в домене VL,
- T28K, Y32F, A100N, N103L в домене VH и N35Y в домене VL,
- T28K, Y32F, A100N, N103F в домене VH,
- T28K, Y32F, A100N, N103W в домене VH,
- T28K, Y32F, A100N, N103L в домене VH и N35K в домене VL,
- T28K, Y32F, A100N, N103L в домене VH и N35F в домене VL,
- T28K, Y32F, A100N, N103W в домене VH и N35M в домене VL,
- T28K, Y32F, A100N, N103F в домене VH и N35Y в домене VL,
- T28K, Y32F, A100N, Y27F в домене VH,
- T28K, Y32F, A100N, N103Q в домене VH,
- T28K, Y32F, A100N, N103S в домене VH,
- T28K, Y32F, A100N, N103M в домене VH и N35F в домене VL,
- T28K, Y32F, A100N, N103F в домене VH и N35M в домене VL,
- T28K, Y32F, A100N, N103F в домене VH и N35F в домене VL,
- T28K, Y32F, A100N, G31R в домене VH,
- T28K, Y32F, A100N, N103W в домене VH и N35F в домене VL,
- T28K, Y32F, A100N, V2R в домене VH,
- T28K, Y32F, A100N, G31S в домене VH,
- T28K, Y32F, A100N, A107S в домене VH,
- T28K, Y32F, A100N, N103E в домене VH и N35M в домене VL,
- T28K, Y32F, A100N, V2K в домене VH,
- T28K, Y32F, A100N, N103E в домене VH,
- T28K, Y32F, A100N, Y102F, N103M в домене VH и N35K в домене VL,
- T28K, Y32F, A100N, Y102F, N103M в домене VH и N35F в домене VL,
- T28K, Y32F, A100N, Y102F, N103M в домене VH и N35R в домене VL,
- T28K, Y32F, A100N, Y102F в домене VH и N35R в домене VL,
- T28K, Y32F, A100N, N103M в домене VH и N35M в домене VL,
- T28K, Y32F, A100N, N103M в домене VH и N35Y в домене VL,
- T28K, Y32F, A100N, N103M в домене VH и N35R в домене VL,
- T28K, Y32F, A100N, N103F в домене VH и N35K в домене VL,
- T28K, Y32F, A100N, Y102L, N103W в домене VH и N35R в домене VL,
- T28K, Y32F, A100N, Y102L, N103W в домене VH и N35K в домене VL,
- T28K, Y32F, A100N, Y102F в домене VH и
- T28K, Y32F, A100N, Y102L, N103M в домене VH и N35R в домене VL.
Было продемонстрировано, что эти конкретные комбинированные мутации изменяют связывание с TRBC2 и TRBC1 таким образом, что оно может быть эффективно применено для нацеливания на TRBC2 (см. Таблицу 1).
КД TRBC1
(M)
Н/Д - нет данных; связывание с TRBC1 практически равно нулю и находится за пределами обнаружения прибора.
В конкретном варианте реализации настоящего изобретения вариантный антигенсвязывающий домен согласно настоящему изобретению содержит мутации T28K, Y32F, A100N в домене VH.
В другом конкретном варианте реализации вариантный антигенсвязывающий домен согласно настоящему изобретению содержит мутации T28K, Y32F, A100N и Y27N в домене VH.
В еще одном конкретном варианте реализации вариантный антигенсвязывающий домен согласно настоящему изобретению содержит мутации T28K, Y32F, A100N и N103M в домене VH.
В еще одном конкретном варианте реализации вариантный антигенсвязывающий домен согласно настоящему изобретению содержит мутации T28K, Y32F, A100N в домене VH и N35K в домене VL.
В еще одном конкретном варианте реализации вариантный антигенсвязывающий домен согласно настоящему изобретению содержит мутации T28K, Y32F, A100N, N103L в домене VH.
В еще одном конкретном варианте реализации вариантный антигенсвязывающий домен согласно настоящему изобретению содержит мутации T28K, Y32F, A100N, N103M в домене VH и мутацию N35Y в домене VL.
В еще одном конкретном варианте реализации вариантный антигенсвязывающий домен согласно настоящему изобретению содержит мутации T28K, Y32F, A100N, Y102F, N103M в домене VH и мутацию N35R в домене VL.
В еще одном конкретном варианте реализации вариантный антигенсвязывающий домен согласно настоящему изобретению содержит мутации T28K, Y32F, A100N, Y102L, N103M в домене VH и мутацию N35R в домене VL.
Особое преимущество обеспечил бы вариант реализации, в котором вариантный антигенсвязывающий домен согласно настоящему изобретению не только демонстрирует увеличенную аффинность к TRBC2 по сравнению с эталонным антителом, но также его аффинность к TRBC1 уменьшается по сравнению с аффинностью эталонного антитела. Такое изменение специфичности к антигену позволило бы вариантному антигенсвязывающему домену отличать TRBC2 и TRBC1 друг от друга посредством предпочтения к связыванию с TRBC2. Таким образом, в еще одном варианте реализации вариантный антигенсвязывающий домен дополнительно демонстрирует уменьшенную аффинность к TRBC1 по сравнению с эталонным антителом.
Аффинность вариантного антигенсвязывающего домена согласно настоящему изобретению к TRBC1 уменьшена по сравнению с аффинностью эталонного антитела. Аффинность вариантного антигенсвязывающего домена к TRBC2 может быть увеличена по меньшей мере на 1%, по меньшей мере на 5%, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 100%, по меньшей мере на 150%, по меньшей мере на 200%, по меньшей мере на 300%, по меньшей мере на 400%, по меньшей мере на 500%, по меньшей мере на 600%, по меньшей мере на 700%, по меньшей мере на 800%, по меньшей мере на 900%, по меньшей мере на 1000%, по меньшей мере на 5000% или по меньшей мере на 10000% по сравнению с аффинностью эталонного антитела к TRBC1.
Отношения аффинности вариантного антигенсвязывающего домена по настоящему изобретению к TRBC2 к его аффинности к TRBC1 может составлять по меньшей мере 2, или по меньшей мере 3, или по меньшей мере 4, или по меньшей мере 5, или по меньшей мере 6, или по меньшей мере 7, или по меньшей мере 8, или по меньшей мере 9, или по меньшей мере 10, или по меньшей мере 15, или по меньшей мере 20, или по меньшей мере 25, или по меньшей мере 50, или по меньшей мере 100, или по меньшей мере 500, или по меньшей мере 1000 или более.
При увеличении авидности вариантного антигенсвязывающего домена согласно настоящему изобретению в Примере 6, авторы настоящего изобретения неожиданно обнаружили, что не только повышалась авидность вариантного антигенсвязывающего домена согласно настоящему изобретению в отношении TRBC2, но также сохранялась его низкая аффинность к TRBC1, и, следовательно, значительно улучшилась специфичность вариантного антигенсвязывающего домена согласно настоящему изобретению к TRBC2.
Авидность вариантного антигенсвязывающего домена согласно настоящему изобретению к TRBC2 может быть увеличена при помощи домена, обладающего способностью образовывать олигомеры или мультимеры. Таким образом, вариантный антигенсвязывающий домен согласно настоящему изобретению может дополнительно содержать домен олигомеризации. Термин «домен олигомеризации» в контексте настоящей заявки относится к домену, который самоассоцируется с образованием олигомера, такого как димер или тример, или мультимера. Таким образом, в контексте настоящей заявки термин «домен олигомеризации» также относится к домену мультимеризации. Домены олигомеризации хорошо известны специалистам в этой области, и применение какого-либо домена олигомеризации совместно с вариантным антигенсвязывающим доменом согласно настоящему изобретению возможно при условии, что полученный олигомер поддерживает или улучшает аффинность мономерного вариантного антигенсвязывающего домена к TRBC2. Примеры доменов олигомеризации включают, без ограничения, область Fc, спейсер COMP (олигомерный матриксный белок хряща) согласно SEQ ID: 18 или укороченный COMP, как описано ниже в контексте информации о химерном антигенном рецепторе (CAR) согласно настоящему изобретению.
В настоящем изобретении также рассматриваются различные форматы вариантного антигенсвязывающего домена согласно настоящему изобретению, включая, без ограничения, scFv, диатело, тримерное тело, минитело, фрагменты F(ab) and F(ab')2, и полноразмерное антитело, т.е. IgG, IgM, IgA, IgD, IgE.
Таким образом, еще один аспект настоящего изобретения относится к антителу, именуемому далее «антитело согласно настоящему изобретению», которое содержит вариантный антигенсвязывающий домен согласно настоящему изобретению.
3. Химерные антигенные рецепторы
В еще одном аспекте настоящего изобретения предложен химерный антигенный рецептор (CAR) (далее - «CAR согласно настоящему изобретению»), содержащий вариантный антигенсвязывающий домен согласно настоящему изобретению, трансмембранный домен и эндодомен.
Термин «вариантный антигенсвязывающий домен согласно настоящему изобретению» был подробно раскрыт в контексте первого аспекта настоящего изобретения, и его признаки и варианты реализации в равной степени применимы к данному аспекту настоящего изобретения.
Термин «химерный антигенный рецептор» или «CAR», или «химерный Т-клеточный рецептор», или «искусственные Т-клеточные рецепторы», или «химерные иммунорецепторы» в контексте настоящей заявки относится к химерному трансмембранному белку I типа, который соединяет распознающий антиген внеклеточный домен (связывающая молекула) с внутриклеточным сигнальным доменом (эндодомен). Связывающая молекула обычно представляет собой одноцепочечный вариабельный фрагмент (scFv), происходящий из моноклонального антитела (mAb), однако его основой могут быть другие форматы, которые содержат участок связывания антигена. Спейсерный домен обычно необходим для того, чтобы отделять связывающую молекулу от мембраны и позволять ему занимать подходящее положение в пространстве. Обычно используют спейсерный домен Fc иммуноглобулина IgG1. В зависимости от антигена могут быть достаточны более компактные спейсеры, например, «стебель» CD8α и даже один только шарнир IgG1. Трансмембранный домен заякоривает белок в клеточной мембране и соединяет спейсер с эндодоменом.
Ранние конструкции CAR имели эндодомены, происходящие из внутриклеточных фрагментов γ-цепи молекул FcεR1 или CD3ζ. Следовательно, эти рецепторы первого поколения передавали иммунологический сигнал 1, которого было достаточно, чтобы запустить уничтожение Т-клетками когнатных клеток-мишеней, но не могли полностью активировать Т-клетки для пролиферации и выживания. Чтобы преодолеть это ограничение, были сконструированы составные эндодомены: слияние внутриклеточного фрагмента костимулирующей молекулы Т-клетки с фрагментом CD3ζ привело к созданию рецепторов второго поколения, которые могут передавать активирующий и костимулирующий сигналы одновременно после распознавания антигена. Наиболее часто используемым костимулирующим доменом является CD28. Это обеспечивает наиболее мощный костимулирующий сигнал, а именно иммунологический сигнал 2, который запускает пролиферацию Т-клеток. Также были описаны некоторые рецепторы, которые включают эндодомены семейства рецепторов TNF (ФНО - фактор некроза опухоли), такие как близкородственные OX40 и 4-1BB, которые передают сигналы выживания. На сегодняшний день описаны еще более эффективные CAR третьего поколения, которые имеют эндодомены, способные передавать сигналы активации, пролиферации и выживания.
При связывании CAR с целевым антигеном происходит передача активирующего сигнала Т-клетке, на которой он экспрессируется. Таким образом, CAR направляет специфичность и цитотоксичность Т-клетки на опухолевые клетки, экспрессирующие целевой антиген.
Таким образом CAR обычно содержат: (i) антигенсвязывающий домен; (ii) спейсер; (iii) трансмембранный домен; и (iii) внутриклеточный домен, который включает сигнальный домен или ассоциирован с ним (см. Фиг. 4).
CAR может иметь следующую общую структуру:
Антигенсвязывающий домен - спейсерный домен - трансмембранный домен - внутриклеточный сигнальный домен (эндодомен).
3.1. Сигнальный пептид
CAR по настоящему изобретению может содержать сигнальный пептид, таким образом, когда CAR экспрессируется внутри клетки, такой как Т-клетка, образующийся белок направляется в эндоплазматический ретикулум, а затем на поверхность клетки, где он экспрессируется.
Кор сигнального пептида может содержать длинный участок гидрофобных аминокислот, который имеет тенденцию образовывать единую альфа-спираль. Сигнальный пептид может начинаться с короткого положительно заряженного участка аминокислот, который помогает обеспечить правильную топологию полипептида во время транслокации. На конце сигнального пептида обычно находится участок из аминокислот, который распознается и расщепляется сигнальной пептидазой. Сигнальная пептидаза может расщепляться во время или после завершения транслокации с образованием свободного сигнального пептида и зрелого белка. Затем свободные сигнальные пептиды расщепляются специфичными протеазами.
Сигнальный пептид может быть расположен на аминоконце молекулы.
Сигнальный пептид может содержать последовательность с SEQ ID от 3 до 5 или ее вариант, имеющий 5, 4, 3, 2 или 1 аминокислотных мутаций (вставки, замены или добавления), при условии, что данный сигнальный пептид продолжает выполнять свою функцию, вызывая экспрессию белка на поверхности клеток.
SEQ ID: 3: MGTSLLCWMALCLLGADHADG
Сигнальный пептид с SEQ ID: 3 является компактным и высокоэффективным. Предполагается, что после концевого глицина будет происходить расщепление примерно на 95%, что обеспечит эффективное удаление сигнальной пептидазой.
SEQ ID: 4: MSLPVTALLLPLALLLHAARP
Сигнальный пептид с SEQ ID: 4 происходит из IgG1.
SEQ ID: 5: MAVPTQVLGLLLLWLTDARC
Сигнальный пептид с SEQ ID : 5 происходит из CD8.
3.2. Спейсерный домен
CAR содержат спейсерную последовательность для соединения антигенсвязывающего домена с трансмембранным доменом и пространственного отделения антигенсвязывающего домена от эндодомена. Гибкий спейсер позволяет антигенсвязывающему домену располагаться в разных направлениях для облегчения связывания.
В CAR по настоящему изобретению спейсерная последовательность может содержать, например, область Fc IgG1, шарнир IgG1, «стебель» CD8 человека или «стебель» CD8 мыши. В альтернативном варианте спейсер может содержать альтернативную линкерную последовательность, которая имеет сходную длину и/или способность располагать домен в пространстве, что и область Fc IgG1, шарнир IgG1 или «стебель» CD8. Спейсер IgG1 человека может быть изменен для удаления мотивов, связывающих Fc. Спейсер может содержать суперспиральный домен, например, как описано в WO2016/151315.
CAR по настоящему изобретению может содержать последовательность, выбранную из последовательностей с SEQ ID: от 6 до 10 или ее вариант, имеющий по меньшей мере 80%-ную идентичность последовательности.
SEQ ID: 6 (шарнир-CH2CH3 IgG1 человека)
AEPKSPDKTHTCPPCPAPPVAGPSVFLFPPKPKDTLMIARTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGKKD
SEQ ID: 7 («стебель» CD8 человека):
TTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDI
SEQ ID: 8 (шарнир IgG1 человека):
AEPKSPDKTHTCPPCPKDPK
SEQ ID: 9 (эктодомен CD2)
KEITNALETWGALGQDINLDIPSFQMSDDIDDIKWEKTSDKKKIAQFRKEKETFKEKDTYKLFKNGTLKIKHLKTDDQDIYKVSIYDTKGKNVLEKIFDLKIQERVSKPKISWTCLLKTGTGTLKERVSKPKISWTCLKNVLKTGTGTGTKVSKPKISWTCMINTTGTG
EKGLD
SEQ ID: 10 (эктодомен CD34)
SLDNNGTATPELPTQGTFSNVSTNVSYQETTTPSTLGSTSLHPVSQHGNEATTNITETTVKFTSTSVITSVYGNTNSSVQSQTSVISTVFTTPANVSTPETTLKPSLSPGNVSDLSTTSTSLATSPTKPYTSSSPILSDIKAEIKCSGIREVKLTQGICLEQNKTSSCAEFKKDRGEGLARVLCGEEQADADAGAQVCSLLLAQSEVRPQCLLLVLANRTEISSKLQLMKKHQSDLKKLGILDFTEQDVASHQSYSQKT
SEQ ID: 19 (COMP)
DLGPQMLRELQETNAALQDVRELLRQQVREITFLKNTVMECDACG
Возможно укорочение домена из суперспирального COMP (олигомерный матриксный белок хряща) на N-конце и сохранение экспрессии на поверхности клеток. Таким образом, спейсер из суперспирального COMP может содержать или состоять из укороченного варианта последовательности с SEQ ID: 18, укороченного на N-конце. Укороченный COMP может содержать 5 C-концевых аминокислот с SEQ ID: 19, т.е. последовательность CDACG (SEQ ID: 20). Укороченный COMP может содержать от 5 до 44 аминокислот, например, по меньшей мере 5, 10, 15, 20, 25, 30, 35 или 40 аминокислот. Укороченный COMP может соответствовать C-концу последовательности с SEQ ID: 19. Например, укороченный COMP, состоящий из 20 аминокислот, может содержать последовательность QQVREITFLKNTVMECDACG (SEQ ID: 21). Укороченный COMP может сохранять остатки цистеина, участвующие в мультимеризации. Укороченный COMP может сохранять способность образовывать мультимеры.
3.3. Трансмембранный домен
Трансмембранный домен представляет собой последовательность CAR, которая проходит через мембрану.
Трансмембранный домен может представлять собой любую белковую структуру, термодинамически стабильную в мембране. Как правило, это альфа-спираль, состоящая из нескольких гидрофобных остатков. Трансмембранный домен любого трансмембранного белка может быть применен для обеспечения трансмембранного участка согласно настоящему изобретению. Наличие и протяженность трансмембранного домена белка могут быть определены специалистами в данной области при помощи алгоритма TMHMM (http://www.cbs.dtu.dk/services/TMHMM-2.0/). Кроме того, с учетом того, что трансмембранный домен белка представляет собой сравнительно простую структуру, то есть предполагается, что полипептидная последовательность образует гидрофобную альфа-спираль достаточной длины, чтобы проходить через мембрану, искусственно созданный TM домен также может быть применен (в US 7052906 B1 описываются компоненты искусственного трансмембранного домена).
Трансмембранный домен может быть получен из CD28, CD8a или TYRP-1, что обеспечивает хорошую стабильность рецептора.
В одном из вариантов реализации трансмембранный домен получен из CD8a.
SEQ ID: 11: трансмембранный домен из CD8a.
IYIWAPLAGTCGVLLLSLVIT
В другом варианте реализации трансмембранный домен получен из TYRP-1.
SEQ ID: 12: трансмембранный домен из TYRP-1.
IIAIAVVGALLLVALIFGTASYLI
3.4. Эндодомен
Эндодомен является участком CAR, передающим сигнал. После распознавания антигена кластер рецепторов, нативные CD45 и CD148 исключаются из синапса, и сигнал передается в клетку. Наиболее часто используемым компонентом эндодомена является CD3ζ, который содержит 3 ITAM (активирующий мотив иммунорецептора на основе тирозина). Он передает сигнал активации Т-клетке после связывания антигена. CD3ζ может не обеспечивать полностью компетентный сигнал активации, и может потребоваться дополнительная передача костимулирующего сигнала. Примеры костимулирующих доменов включают эндодомены из CD28, OX40, 4-1BB, CD27 и ICOS, которые можно использовать вместе с CD3ζ для передачи сигнала пролиферации/выживания.
В одном из вариантов реализации по меньшей мере один костимулирующий эндодомен используют вместе с CD3ζ. В конкретном варианте реализации костимулирующий эндодомен выбран из группы, включающей эндодомены из CD28, OX40, 4-1BB, CD27 и ICOS.
В другом варианте реализации по меньшей мере два костимулирующих эндодомена используют вместе с CD3ζ. В конкретном варианте реализации два костимулирующих эндодомена выбраны из группы, состоящей из эндодоменов из CD28, OX40, 4-1BB, CD27 и ICOS в любой комбинации и порядке. Особенно подходящие комбинации включают эндодомены из CD28 и CD3ζ, эндодомены из OX40 и CD3ζ, эндодомены из 4-1BB и CD3ζ, эндодомены из CD28, OX40 и CD3ζ, и эндодомены из CD28, 4-1BB и CD3ζ.
Трансмембранный и внутриклеточный сигнальный домен Т-клеток (эндодомен) CAR с активирующим эндодоменом может содержать последовательность с SEQ ID: от 13 до 18 или ее вариант, имеющий не менее 80% идентичности с ней.
SEQ ID: 13, содержащая трансмембранный домен CD28 и эндодомен CD3ζ.
FWVLVVVGGVLACYSLLVTVAFIIFWVRRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLDALSTATKD
SEQ ID: 14, содержащая трансмембранный домен CD28 и эндодомены CD28 и CD3ζ.
FWVLVVVGGVLACYSLLVTVAFIIFWVRSKRSRLLHSDYMNMTPRRPGPTRKHYQPYAPPRDFAAYRSRVKFSRSADAPAYQQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNGLGMMAKPRRKNLGPRGLGMAKGKPRRKNGLGMAXMMAKPRRKNLGMA
SEQ ID: 15, содержащая трансмембранный домен CD28 и эндодомены CD28, OX40 и CD3ζ.
FWVLVVVGGVLACYSLLVTVAFIIFWVRSKRSRLLHSDYMNMTPRRPGPTRKHYQPYAPPRDFAAYRSRDQRLPPDAHKPPGGGSFRTPIQEEQADAHSTLAKIRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR
SEQ ID: 16, содержащая трансмембранный домен CD8a и эндодомен CD3ζ.
IYIWAPLAGTCGVLLLSLVITRVLYCKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYPPRH
SEQ ID: 17, содержащая трансмембранный домен CD8a и эндодомены 4-1BB и CD3ζ.
IYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYN
SEQ ID: 18, содержащая трансмембранный домен TYRP-1 и эндодомены 4-1BB и CD3ζ.
IIAIAVVGALLLVALIFGTASYLIKRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGGKPRRKAYDVLDKRRGRDPEMGGGKPRRKAYPQEGLYNELQ
Вариант последовательности может иметь по меньшей мере 80%, 85%, 90%, 95%, 98% или 99% идентичности последовательности с SEQ ID: с 13 по 18, при условии, что данная последовательность обеспечивает эффективный трансмембранный домен и эффективный внутриклеточный Т-клеточный сигнальный домен.
CAR согласно настоящему изобретению может содержать последовательность из группы последовательностей с SEQ ID: с 25 по 36.
SEQ ID: 25: CAR, содержащий мутации T28K, Y32F, A100N в домене VH, мутацию N35K в домене VL, шарнирный спейсер IgG1, трансмембранный домен TYRP-1, эндодомены 4-1BB и CD3ζ.
QVQLVQSGAEVKKPGASVKVSCKASGYKFTGFVMHWVRQAPGQGLEWMGFINPYNDDIQSNERFRGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARGNGYNFDGAYRFFDFWGQGTMVTVSSGGGGSGGGGSGGGGSDIVMTQSPLSLPVTPGEPASISCRSSQRLVHSNGKTYLHWYLQKPGQSPRLLIYRVSNRFPGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCSQSTHVPYTFGQGTKLEIKRSDPAEPKSPDKTHTCPPCPKDPKIIAIAVVGALLLVALIFGTASYLIKRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCELRRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR
SEQ ID: 26: CAR, содержащий мутации T28K, Y32F, A100N в домене VH, шарнирный спейсер IgG1, трансмембранный домен TYRP-1, эндодомены 4-1BB и CD3ζ.
QVQLVQSGAEVKKPGASVKVSCKASGYKFTGFVMHWVRQAPGQGLEWMGFINPYNDDIQSNERFRGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARGNGYNFDGAYRFFDFWGQGTMVTVSSGGGGSGGGGSGGGGSDIVMTQSPLSLPVTPGEPASISCRSSQRLVHSNGNTYLHWYLQKPGQSPRLLIYRVSNRFPGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCSQSTHVPYTFGQGTKLEIKRSDPAEPKSPDKTHTCPPCPKDPKIIAIAVVGALLLVALIFGTASYLIKRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCELRRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR
SEQ ID: 27: CAR, содержащий мутации T28K, Y32F, A100N, N103L в домене VH, шарнирный спейсер IgG1, трансмембранный домен TYRP-1 и эндодомены 4-1BB и CD3ζ.
QVQLVQSGAEVKKPGASVKVSCKASGYKFTGFVMHWVRQAPGQGLEWMGFINPYNDDIQSNERFRGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARGNGYLFDGAYRFFDFWGQGTMVTVSSGGGGSGGGGSGGGGSDIVMTQSPLSLPVTPGEPASISCRSSQRLVHSNGNTYLHWYLQKPGQSPRLLIYRVSNRFPGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCSQSTHVPYTFGQGTKLEIKRSDPAEPKSPDKTHTCPPCPKDPKIIAIAVVGALLLVALIFGTASYLIKRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCELRRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR
SEQ ID: 28: CAR, содержащий мутации T28K, Y32F, A100N, N103M в домене VH, мутацию N35Y в домене VL, шарнирный спейсер IgG1, трансмембранный домен TYRP-1, эндодомены 4-1BB и CD3ζ.
QVQLVQSGAEVKKPGASVKVSCKASGYKFTGFVMHWVRQAPGQGLEWMGFINPYNDDIQSNERFRGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARGNGYMFDGAYRFFDFWGQGTMVTVSSGGGGSGGGGSGGGGSDIVMTQSPLSLPVTPGEPASISCRSSQRLVHSNGYTYLHWYLQKPGQSPRLLIYRVSNRFPGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCSQSTHVPYTFGQGTKLEIKRSDPAEPKSPDKTHTCPPCPKDPKIIAIAVVGALLLVALIFGTASYLIKRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCELRRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR
SEQ ID: 29: CAR, содержащий мутации T28K, Y32F, A100N, N103M в домене VH, мутацию N35R в домене VL, шарнирный спейсер IgG1, трансмембранный домен TYRP-1, эндодомены 4-1BB и CD3ζ.
QVQLVQSGAEVKKPGASVKVSCKASGYKFTGFVMHWVRQAPGQGLEWMGFINPYNDDIQSNERFRGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARGNGFMFDGAYRFFDFWGQGTMVTVSSGGGGSGGGGSGGGGSDIVMTQSPLSLPVTPGEPASISCRSSQRLVHSNGRTYLHWYLQKPGQSPRLLIYRVSNRFPGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCSQSTHVPYTFGQGTKLEIKRSDPAEPKSPDKTHTCPPCPKDPKIIAIAVVGALLLVALIFGTASYLIKRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCELRRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR
SEQ ID: 30: CAR, содержащий мутации T28K, Y32F, A100N, Y102L, N103M в домене VH, мутации N35R в домене VL, шарнирный спейсер IgG1, трансмембранный домен TYRP-1, эндодомены 4-1BB и CD3ζ.
QVQLVQSGAEVKKPGASVKVSCKASGYKFTGFVMHWVRQAPGQGLEWMGFINPYNDDIQSNERFRGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARGNGLMFDGAYRFFDFWGQGTMVTVSSGGGGSGGGGSGGGGSDIVMTQSPLSLPVTPGEPASISCRSSQRLVHSNGRTYLHWYLQKPGQSPRLLIYRVSNRFPGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCSQSTHVPYTFGQGTKLEIKRSDPAEPKSPDKTHTCPPCPKDPKIIAIAVVGALLLVALIFGTASYLIKRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCELRRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR
SEQ ID: 31: CAR, содержащий мутации T28K, Y32F, A100N в домене VH, спейсер-«стебель» CD8, трансмембраный домен TYRP-1 и эндодомены 4-1BB и CD3ζ.
QVQLVQSGAEVKKPGASVKVSCKASGYKFTGFVMHWVRQAPGQGLEWMGFINPYNDDIQSNERFRGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARGNGYNFDGAYRFFDFWGQGTMVTVSSGGGGSGGGGSGGGGSDIVMTQSPLSLPVTPGEPASISCRSSQRLVHSNGNTYLHWYLQKPGQSPRLLIYRVSNRFPGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCSQSTHVPYTFGQGTKLEIKRSDPTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDIIIAIAVVGALLLVALIFGTASYLIKRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCELRRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR
SEQ ID: 32: CAR, содержащий мутации T28K, Y32F, A100N в домене VH, спейсер-«стебель» CD8, трансмембранный домен TYRP-1 и эндодомены CD28 и CD3ζ.
QVQLVQSGAEVKKPGASVKVSCKASGYKFTGFVMHWVRQAPGQGLEWMGFINPYNDDIQSNERFRGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARGNGYNFDGAYRFFDFWGQGTMVTVSSGGGGSGGGGSGGGGSDIVMTQSPLSLPVTPGEPASISCRSSQRLVHSNGNTYLHWYLQKPGQSPRLLIYRVSNRFPGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCSQSTHVPYTFGQGTKLEIKRSDPTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDIIIAIAVVGALLLVALIFGTASYLIRSKRSRLLHSDYMNMTPRRPGPTRKHYQPYAPPRDFAAYRSRRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR
SEQ ID: 33: CAR, содержащий мутации T28K, Y32F, A100N в домене VH, шарнирный спейсер IgG1, трансмембранный домен TYRP-1, эндодомены CD28 и CD3ζ.
QVQLVQSGAEVKKPGASVKVSCKASGYKFTGFVMHWVRQAPGQGLEWMGFINPYNDDIQSNERFRGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARGNGYNFDGAYRFFDFWGQGTMVTVSSGGGGSGGGGSGGGGSDIVMTQSPLSLPVTPGEPASISCRSSQRLVHSNGNTYLHWYLQKPGQSPRLLIYRVSNRFPGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCSQSTHVPYTFGQGTKLEIKRSDPAEPKSPDKTHTCPPCPKDPKIIAIAVVGALLLVALIFGTASYLIRSKRSRLLHSDYMNMTPRRPGPTRKHYQPYAPPRDFAAYRSRRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR
SEQ ID: 34: CAR, содержащий мутации T28K, Y32F, A100N в домене VH, мутацию N35K в домене VL, шарнирный спейсер IgG1, трансмембранный домен TYRP-1, эндодомены CD28 и CD3ζ.
QVQLVQSGAEVKKPGASVKVSCKASGYKFTGFVMHWVRQAPGQGLEWMGFINPYNDDIQSNERFRGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARGNGYNFDGAYRFFDFWGQGTMVTVSSGGGGSGGGGSGGGGSDIVMTQSPLSLPVTPGEPASISCRSSQRLVHSNGKTYLHWYLQKPGQSPRLLIYRVSNRFPGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCSQSTHVPYTFGQGTKLEIKRSDPAEPKSPDKTHTCPPCPKDPKIIAIAVVGALLLVALIFGTASYLIRSKRSRLLHSDYMNMTPRRPGPTRKHYQPYAPPRDFAAYRSRRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR
SEQ ID: 35: CAR, содержащий мутации T28K, Y32F, A100N в домене VH, мутацию N35K в домене VL, спейсер-«стебель» CD8, трансмембранный домен TYRP-1 и эндодомены 4-1BB и CD3ζ.
QVQLVQSGAEVKKPGASVKVSCKASGYKFTGFVMHWVRQAPGQGLEWMGFINPYNDDIQSNERFRGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARGNGYNFDGAYRFFDFWGQGTMVTVSSGGGGSGGGGSGGGGSDIVMTQSPLSLPVTPGEPASISCRSSQRLVHSNGKTYLHWYLQKPGQSPRLLIYRVSNRFPGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCSQSTHVPYTFGQGTKLEIKRSDPTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDIIIAIAVVGALLLVALIFGTASYLIKRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCELRRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR
SEQ ID: 36: CAR, содержащий мутации T28K, Y32F, A100N в домене VH, мутацию N35K в домене VL, спейсер-«стебель» CD8, трансмембранный домен TYRP-1, эндодомены CD28 и CD3ζ.
QVQLVQSGAEVKKPGASVKVSCKASGYKFTGFVMHWVRQAPGQGLEWMGFINPYNDDIQSNERFRGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARGNGYNFDGAYRFFDFWGQGTMVTVSSGGGGSGGGGSGGGGSDIVMTQSPLSLPVTPGEPASISCRSSQRLVHSNGKTYLHWYLQKPGQSPRLLIYRVSNRFPGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCSQSTHVPYTFGQGTKLEIKRSDPTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDIIIAIAVVGALLLVALIFGTASYLIRSKRSRLLHSDYMNMTPRRPGPTRKHYQPYAPPRDFAAYRSRRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR
4. Биспецифичный активатор Т-клеток
Был разработан широкий спектр молекул, которые основаны на базовой концепции наличия двух антителоподобных связывающих доменов.
Биспецифичные молекулы, рекрутирующие Т-клетки, представляют собой класс биспецифичных антителоподобных молекул, которые были разработаны прежде всего для применения в качестве противораковых лекарственных средств. Они направляют иммунную систему хозяина, точнее цитотоксическую активность Т-клеток, против клетки-мишени, такой как раковая клетка. В этих молекулах один связывающий домен связывается с Т-клеткой через рецептор CD3, а другой - с клетками-мишенями, такими как опухолевая клетка (через специфичную для опухоли молекулу). Поскольку биспецифичная молекула связывает как клетку-мишень, так и Т-клетку, она сближает клетку-мишень с Т-клеткой, таким образом, чтобы Т-клетка могла оказывать свое воздействие, например, цитотоксическое действие на раковую клетку. Образование комплекса «Т-клетка:биспецифичное Ат:раковая клетка» индуцирует передачу сигналов в Т-клетке, приводя, например, к высвобождению цитотоксических медиаторов. В идеале агент индуцирует желаемую передачу сигналов только в присутствии клетки-мишени, что приводит к избирательному уничтожению.
Биспецифичные молекулы, рекрутирующие Т-клетки, были разработаны в нескольких различных форматах, но одним из наиболее распространенных является слитая молекула, состоящая из двух тандемно расположенных одноцепочечных вариабельных фрагментов (scFv) различных антител. Иногда их называют BiTE (биспецифичные активаторы Т-клеток).
В настоящем изобретении также рассматривается биспецифичная молекула, которая избирательно распознает TRBC2 и способна активировать Т-клетки. Например, данная молекула может представлять собой BiTE.
Таким образом, в еще одном аспекте настоящего изобретения предложен биспецифичный активатор Т-клеток (BiTE) (далее - «BiTE согласно настоящему изобретению»), содержащий вариантный антигенсвязывающий домен согласно настоящему изобретению и домен активации Т-клеток.
Термин «вариантный антигенсвязывающий домен согласно настоящему изобретению» был подробно раскрыт в контексте первого аспекта настоящего изобретения, и его признаки и варианты реализации в равной степени применимы к данному аспекту настоящего изобретения.
Термин «домен активации Т-клеток» в контексте настоящей заявки относится ко второму домену, способному активировать Т-клетки. Домен активации Т-клеток может представлять собой scFv, который специфично связывается с CD3. Примеры scFv к CD3, которые подходят для целей настоящего изобретения, хорошо известны в данной области и включают, без ограничения, scFv, полученный из OKT3.
Биспецифичная молекула может содержать сигнальный пептид, способствующий ее продуцированию. Сигнальный пептид может вызывать секрецию биспецифичной молекулы клеткой-хозяином, таким образом, биспецифичная молекула может быть собрана из супернатанта клетки-хозяина.
Сигнальный пептид может быть расположен на аминоконце молекулы. Биспецифичная молекула может иметь следующую общую формулу: сигнальный пептид - вариантный антигенсвязывающий домен согласно настоящему изобретению - домен активации Т-клеток.
Биспецифичная молекула может содержать спейсерную последовательность для соединения вариантного антигенсвязывающего домена согласно настоящему изобретению и домена активации Т-клеток, и для пространственного разделения двух доменов.
Спейсерная последовательность может, например, содержать шарнир IgG1 или «стебель» CD8. В альтернативном варианте линкер может содержать альтернативную линкерную последовательность, которая имеет такие же характеристики длины и/или расстояния между доменами, что и шарнир IgG1 или «стебель» CD8.
5. Нуклеиновая кислота
В еще одном аспекте настоящего изобретения также предложена последовательность нуклеиновой кислоты, кодирующая вариантный антигенсвязывающий домен согласно настоящему изобретению (далее «первая нуклеиновая кислота согласно настоящему изобретению»).
В другом аспекте настоящего изобретения также предложена последовательность нуклеиновой кислоты, кодирующая антитело согласно настоящему изобретению, (далее - «вторая нуклеиновая кислота согласно настоящему изобретению»).
В еще одном аспекте настоящего изобретения также предложена последовательность нуклеиновой кислоты, кодирующая CAR согласно настоящему изобретению (далее - «третья нуклеиновая кислота согласно настоящему изобретению»).
В еще одном аспекте настоящего изобретения также предложена последовательность нуклеиновой кислоты, кодирующая BiTE согласно настоящему изобретению (далее - «четвертая нуклеиновая кислота согласно настоящему изобретению»).
Термины «вариантный антигенсвязывающий домен согласно настоящему изобретению», «антитело согласно настоящему изобретению» и «BiTE согласно настоящему изобретению» были подробно раскрыты в контексте предыдущих аспектов изобретения, и их признаки и варианты реализации в равной степени применимы к данным аспектам изобретения.
В контексте настоящей заявки термины «полинуклеотид», «нуклеотид» и «нуклеиновая кислота» предназначены для применения в качестве синонимов друг друга.
Специалисту в данной области будет понятно, что многочисленные различные полинуклеотиды и нуклеиновые кислоты могут кодировать один и тот же полипептид вследствие вырожденности генетического кода. Кроме того, следует понимать, что квалифицированные специалисты могут, используя обычные способы, делать замены нуклеотидов, которые не влияют на полипептидную последовательность, кодируемую полинуклеотидами, описанными в настоящей заявке, чтобы отразить применение кодонов в любом конкретном организме-хозяине, в котором должны быть экспрессированы полипептиды.
Последовательности нуклеиновых кислот и конструкции по настоящему изобретению могут содержать альтернативные кодоны в областях последовательностей, кодирующих идентичные или схожие аминокислотные последовательности для того, чтобы избежать гомологичной рекомбинации.
В соответствии с настоящим изобретением нуклеиновые кислоты могут содержать ДНК или РНК. Они могут быть одноцепочечными или двухцепочечными. Они также могут представлять собой полинуклеотиды, которые включают синтетические или модифицированные нуклеотиды. В данной области известен ряд различных типов модификации олигонуклеотидов. Они включают метилфосфонатные и фосфоротиоатные остовы, добавление акридиновых или полилизиновых цепей на 3' и/или 5' концах молекулы. Для целей применения в соответствии с настоящей заявкой, следует понимать, что полинуклеотиды могут быть модифицированы любым способом, доступным в данной области техники. Такие модификации могут быть выполнены с целью увеличения активности in vivo или продолжительности жизни представляющих интерес полинуклеотидов.
Термины «вариант», «гомолог» или «производное» в отношении нуклеотидной последовательности включают какую-либо замену, видоизменение, модификацию, перестановку, делецию или добавление одной или нескольких нуклеиновых кислот в последовательность или из нее.
6. Вектор
В настоящем изобретении также предложен вектор или набор векторов, который содержит одну или несколько последовательностей нуклеиновых кислот согласно настоящему изобретению. Такой вектор может быть применен для введения последовательности нуклеиновой кислоты в клетку-хозяина для того, чтобы она экспрессировала вариантную антигенсвязывающую молекулу или антитело, или CAR, или BiTE согласно настоящему изобретению.
Термины «вариантный антигенсвязывающий домен согласно настоящему изобретению», «антитело согласно настоящему изобретению» и «BiTE согласно настоящему изобретению» были подробно раскрыты в контексте предыдущих аспектов изобретения, и их признаки и варианты реализации в равной степени применимы к данным аспектам изобретения.
Вектор может, например, представлять собой плазмиду или вирусный вектор, такой как ретровирусный или лентивирусный вектор, или вектор на основе транспозона, или или синтетическую мРНК.
Вектор может быть способен к трансфекции или трансдукции цитолитической иммунной клетки, такой как Т-клетка или NK-клетка.
7. Клетка
Еще один аспект настоящего изобретения относится к клетке (далее - «клетка согласно настоящему изобретению»), которая содержит CAR согласно настоящему изобретению.
Клетка может содержать нуклеиновую кислоту или вектор по настоящему изобретению.
Термины «CAR согласно настоящему изобретению», «нуклеиновая кислота согласно настоящему изобретению», «вектор согласно настоящему изобретению» были подробно раскрыты в контексте предыдущих аспектов изобретения, и их признаки и варианты реализации в равной степени применимы к данным аспектам изобретения.
Клетка может представлять собой цитолитическую иммунную клетку, такую как Т-клетка или NK-клетка.
Т-клетки или Т-лимфоциты представляют собой вид лимфоцитов, которые играют центральную роль в клеточном иммунитете. Их можно отличить от других лимфоцитов, таких как В-клетки и естественные клетки-киллеры (NK-клетки), по наличию Т-клеточного рецептора (TCR) на поверхности клетки. Ниже приведен краткий обзор различных типов Т-клеток.
Хелперные Т-клетки (Th-клетки) помогают другим лейкоцитам в иммунологических процессах, включая созревание В-клеток в плазматические клетки и В-клетки памяти, и в активации цитотоксических Т-клеток и макрофагов. Th-клетки экспрессируют CD4 на своей поверхности. Th-клетки активируются, когда молекулы ГКГС II класса презентируют им пептидные антигены на поверхности антигенпрезентирующих клеток (АПК). Эти клетки могут дифференцироваться в один из нескольких подтипов, включая TH1, TH2, TH3, TH17, Th9 или TFH, которые секретируют различные цитокины для облегчения различных типов иммунных ответов.
Цитолитические Т-клетки (клетки TC или CTL) разрушают инфицированные вирусом клетки и опухолевые клетки, и участвуют в отторжении трансплантата. CTL экспрессируют CD8 на своей поверхности. Эти клетки распознают свои мишени путем связывания с антигеном, ассоциированным с ГКГС I класса, который присутствует на поверхности всех содержащих ядро клеток. Через IL-10, аденозин и другие молекулы, секретируемые регуляторными Т-клетками, клетки CD8+ могут быть инактивированы до состояния анергии, что предотвращает аутоиммунные заболевания, такие как экспериментальный аутоиммунный энцефаломиелит.
Т-клетки памяти представляют собой подгруппу антиген-специфичных Т-клеток, которые сохраняются в течение длительного времени после устранения инфекции. Они быстро размножаются с образованием большого количества эффекторных Т-клеток при повторном контакте с родственным им антигеном, таким образом обеспечивая иммунную систему «памятью» против прошлых инфекций. Т-клетки памяти включают три подтипа: Т-клетки центральной памяти (клетки TCM) и два типа T-клеток эффекторной памяти (клетки TEM и клетки TEMRA). Клетки памяти могут представлять собой CD4+ или CD8+. Т-клетки памяти обычно экспрессируют белок клеточной поверхности CD45RO.
Регуляторные Т-клетки (T-reg-клетки), ранее известные как супрессорные Т-клетки, имеют решающее значение для поддержания иммунологической толерантности. Их основная роль заключается в отключении опосредованного Т-клетками иммунитета к концу иммунной реакции и в подавлении аутореактивных Т-клеток, которые избежали процесса негативного отбора в тимусе.
Были описаны два основных типа CD4+ Treg клеток -Treg естественного происхождения и адаптивные Treg.
T-reg-клетки естественного происхождения (также известные как T-reg-клетки CD4+CD25+FoxP3+) образуются в тимусе и связаны с взаимодействиями между развивающимися Т-клетками как с миелоидными (CD11c+), так и с плазмацитоидными (CD123+) дендритными клетками, которые были активированы с помощью TSLP (тимусный стромальный лимфопоэтин). T-reg-клетки естественного происхождения можно отличить от других Т-клеток по наличию внутриклеточной молекулы, называемой FoxP3. Мутации гена FOXP3 могут предотвращать развитие регуляторных Т-клеток, вызывая смертельное аутоиммунное заболевание IPEX (Х-сцепленный синдром иммунной дисрегуляции, полиэндокринопатии и энтеропатии).
Адаптивные клетки Treg (также известные как клетки Tr1 или клетки Th3) могут образовываться во время нормального иммунного ответа.
Клетка может представлять собой естественную клетку-киллер (или NK-клетку). NK-клетки являются частью врожденной иммунной системы. NK-клетки обеспечивают быстрые ответы на рефлекторные сигналы от инфицированных вирусом клеток независимо от ГКГС.
NK-клетки, принадлежащие к группе врожденных лимфоидных клеток, характеризуются как крупные гранулярные лимфоциты (LGL) и представляют собой третий тип клеток, дифференцированных от общего лимфоидного предшественника, генерирующего В- и Т-лимфоциты. Известно, что NK-клетки дифференцируются и созревают в костном мозге, лимфатическом узле, селезенке, миндалинах и тимусе, откуда они затем попадают в кровоток.
Клетка согласно настоящему изобретению может представлять собой клетку любого из вышеупомянутых типов. В одном из вариантов реализации клетка согласно настоящему изобретению представляет собой Т-клетку. В другом варианте реализации клетка согласно настоящему изобретению представляет собой NK-клетку.
Клетки по данному аспекту настоящего изобретения могут быть получены ex vivo или из собственной периферической крови пациента (1-я сторона), или (в условиях трансплантации гемопоэтических стволовых клеток) - из периферической крови донора (2-я сторона), или из периферической крови неподключенного донора (3-я сторона).
В альтернативном варианте реализации клетки по данному аспекту настоящего изобретения могут быть получены в результате дифференциации ex vivo индуцибельных клеток-предшественников или эмбриональных клеток-предшественников в цитолитические клетки. В качестве альтернативы можно использовать линию иммортализованных цитолитических клеток, таких как Т- или NK-клетки, которые сохраняют свою литическую функцию и могут действовать как терапевтическое средство.
Во всех этих вариантах реализации экспрессирующие CAR клетки получают путем введения ДНК или РНК, кодирующей химерный полипептид, одним из многих способов, включая трансдукцию вирусным вектором, трансфекцию ДНК или РНК.
Клетка согласно настоящему изобретению может представлять собой клетку ex vivo, полученную у субъекта. Клетка может быть из образца мононуклеарных клеток периферической крови (МКПК). Клетка, в частности цитолитическая клетка, такая как Т- или NK-клетка, может быть активирована и/или размножена перед трансдукцией нуклеиновой кислотой, кодирующей молекулы, обеспечивающие CAR согласно настоящему изобретению, например, обработкой моноклональным антителом к анти-CD3.
Клетка согласно настоящему изобретению может быть получена способом, включающим этап трансдукции или трансфекции клетки вектором согласно настоящему изобретению, который содержит последовательность нуклеиновой кислоты, кодирующую CAR.
Способ получения клетки согласно настоящему изобретению может дополнительно включать этап выделения клетки из содержащего клетки образца, полученного у субъекта или из других источников, перечисленных выше, перед этапом трансдукции или трансфекции. В случае если клетка является цитолитической клеткой, образец представляет собой полученный у субъекта образец, содержащий цитолитические клетки.
Термин «субъект» или «индивидуум», используемый в контексте настоящего изобретения, относится к представителям видов млекопитающих, предпочтительно к человеку мужского или женского пола любого возраста или расы.
Затем клетка согласно настоящему изобретению может быть очищена, например, путем отбора на основе экспрессии антигенсвязывающего домена CAR.
8. Конъюгат
Вариантный антигенсвязывающий домен или антитело согласно настоящему изобретению может представлять собой конъюгат вариантного антигенсвязывающего домена или антитела, например, конъюгат может быть детектируемым компонентом или химиотерапевтическим компонентом.
Термины «вариантный антигенсвязывающий домен согласно настоящему изобретению» и «антитело согласно настоящему изобретению» были подробно раскрыты в контексте предыдущих аспектов настоящего изобретения, и их признаки и варианты реализации в равной степени применимы к данным аспектам изобретения.
Детектируемый компонент может представлять собой флуоресцентную группу, например флуоресцентный пептид. Термин «флуоресцентный пептид» в контексте настоящей заявки относится к полипептиду, который при возбуждении излучает свет с детектируемой длиной волны. Примеры флуоресцентных белков включают, но не ограничиваются ими: изотиоцианат флуоресцеина (FITC), фикоэритрин (PE), аллофикоцианин (APC), зеленый флуоресцентный белок (GFP), усиленный GFP, красный флуоресцентный белок (RFP), синий флуоресцентный белок (BFP) и белок mCherry.
Вариантный антигенсвязывающий домен или антитело согласно настоящему изобретению, конъюгированные с детектируемым компонентом, могут быть применены для определения TRBC злокачественной Т-клетки.
Термин «химиотерапевтический компонент» в контексте настоящей заявки относится к компоненту, который является разрушительным для клетки, то есть такой компонент уменьшает жизнеспособность клетки. Полученные конъюгаты в дальнейшем названы «химиотерапевтический конъюгат согласно настоящему изобретению». Химиотерапевтический компонент может представлять собой цитотоксический лекарственный препарат. Предполагаемый химиотерапевтический компонент включает, без ограничения: алкилирующие агенты, нитрозомочевины, этиленимины/метилмеламин, алкилсульфонаты, антиметаболиты, аналоги пиримидина, эпиподофилотоксины, ферменты, такие как L-аспарагиназа; модификаторы биологического ответа, такие как IFNα, IL-2, G-CSF и GM-CSF; координационные комплексы платины, такие как цисплатин и карбоплатин, антрацендионы, замещенная мочевина, такая как гидроксимочевина, производные метилгидразина, включая N-метилгидразин (MIH) и прокарбазин, адренокортикальные супрессоры, такие как митотан (o,p'-DDD) и аминоглутетимид; гормоны и антагонисты, в том числе антагонисты адренокортикостероидов, такие как преднизон и его эквиваленты, дексаметазон и аминоглютетимид; прогестин, в частности, гидроксипрогестерона капроат, медроксипрогестерона ацетат и мегестрола ацетат; эстроген, в частности, эквиваленты диэтилстильбэстрола и этинилэстрадиола; антиэстроген, в частности, тамоксифен; андрогены, включая пропионат тестостерона и флуоксиместерон/эквиваленты; антиандрогены, в частности, флутамид, аналоги гонадотропин-рилизинг гормона и лейпролид; и нестероидные антиандрогены, в частности, флутамид.
Вариантный антигенсвязывающий домен или антитело согласно настоящему изобретению, конъюгированные с химиотерапевтическим компонентом, обеспечивают направленную доставку химиотерапевтического компонента в клетки, экспрессирующие TRBC2.
9. Фармацевтическая композиция
Настоящее изобретение также относится к фармацевтической композиции, содержащей клетку или множество клеток, или антитело, или BiTE (биспецифичный активатор Т-клеток), или химиотерапевтический конъюгат согласно настоящему изобретению, далее - «фармацевтическая композиция согласно настоящему изобретению».
Фармацевтическая композиция может дополнительно содержать фармацевтически приемлемый носитель, разбавитель или вспомогательное вещество. Фармацевтическая композиция может необязательно содержать один или несколько дополнительных фармацевтически активных полипептидов и/или соединений. Такой состав может, например, быть в форме, подходящей для внутривенной инфузии.
Термины «клетка согласно настоящему изобретению», «антитело согласно настоящему изобретению», «BiTE согласно настоящему изобретению» и «химиотерапевтический конъюгат согласно настоящему изобретению» были подробно описаны в контексте предыдущих аспектов изобретения, и их характеристики и варианты реализации в равной степени применимы к данным аспектам настоящего изобретения.
Введение препарата
Введение клетки или группы клеток, или антитела, или BiTE, или химиотерапевтического конъюгата согласно настоящему изобретению может осуществляться каким-либо из нескольких путей, которые делают активный ингредиент биодоступным. Например, агент можно вводить пероральным и парентеральным путем, внутрибрюшинно, внутривенно, подкожно, чрескожно, внутримышечно, местной доставкой, например, с помощью катетера или стента.
Как правило, фактическая дозировка, которая будет наиболее подходящей для конкретного субъекта, определяется врачом, и она будет зависеть от возраста, веса и ответа конкретного пациента. Дозировка должна быть такой, чтобы ее было достаточно для сокращения количества или деплеции клональных Т-клеток, экспрессирующих TRBC1 или TRBC2.
10. Способ лечения
В еще одном аспекте настоящего изобретения предложена клетка или антитело, или BiTE, или химиотерапевтический конъюгат согласно настоящему изобретению для применения в медицине.
В другом аспекте настоящего изобретения предложен способ лечения Т-клеточных лимфомы или лейкоза у субъекта (далее - «способ лечения согласно настоящему изобретению»), который включает этап введения клетки или антитела, или BiTE, или химиотерапевтичесого конъюгата согласно настоящему изобретению субъекту, в организме которого злокачественные Т-клетки экспрессируют TRBC2. Препарат можно вводить в форме фармацевтической композиции, как указано выше.
Альтернативная формулировка данного аспекта изобретения может быть следующей: клетка или антитело, или BiTE, или химиотерапевтический конъюгат согласно настоящему изобретению для применения в лечении Т-клеточных лимфомы или лейкоза, далее - «клетка, антитело, BiTE или химиотерапевтический конъюгат для применения согласно настоящему изобретению» при экспрессировании TRBC2 злокачественными Т-клетками.
Альтернативная формулировка данного аспекта изобретения может быть следующей: клетка или антитело, или BiTE, или химиотерапевтический конъюгат согласно настоящему изобретению для применения в изготовлении лекарственного средства для лечения Т-клеточных лимфомы или лейкоза, при котором злокачественные Т-клетки экспрессируют TRBC2.
Термины «клетка согласно настоящему изобретению», «антитело согласно настоящему изобретению», «BiTE согласно настоящему изобретению» и «химиотерапевтический конъюгат согласно настоящему изобретению» были подробно раскрыты в контексте предыдущих аспектов настоящего изобретения, и их характеристики и варианты реализации в равной степени применимы к данным аспектам настоящего изобретения.
Способ лечения Т-клеточных лимфомы и/или лейкоза относится к терапевтическому применению клетки, антитела, BiTE или химиотерапевтического конъюгата согласно настоящему изобретению. Согласно указанному способу, клетку, антитело, BiTE или химиотерапевтический конъюгат согласно настоящему изобретению можно вводить субъекту, больному Т-клеточными лимфомой и/или лейкозом с целью ослабления, уменьшения, облегчения по меньшей мере одного симптома, связанного с данным заболеванием и/или для замедления, уменьшения или остановки прогрессирования заболевания.
Способ предотвращения Т-клеточных лимфомы и/или лейкоза относится к профилактическому применению клетки, антитела, BiTE или химиотерапевтического конъюгата согласно настоящему изобретению. Согласно указанному способу, такую клетку, антитело, BiTE или химиотерапевтический конъюгат можно вводить субъекту, у которого еще не проявились Т-клеточные лимфома и/или лейкоз, и/или у которого не проявляются какие-либо симптомы Т-клеточных лимфомы и/или лейкоза, с целью предотвратить или ослабить факторы, вызывающие данное заболевание, или уменьшить или предотвратить развитие по крайней мере одного симптома, связанного с заболеванием. Субъект может иметь предрасположенность или считаться подверженным риску развития Т-клеточных лимфомы и/или лейкоза.
Данный способ может включать следующие этапы:
(i) выделение образца, содержащего цитотоксические клетки;
(ii) трансдукция или трансфекция такой клетки последовательностью нуклеиновой кислоты или вектором по настоящему изобретению; и
(iii) введение субъекту клетки по п. (ii).
Образец, содержащий цитотоксические клетки, может быть выделен у субъекта или из других источников, например, как было сказано выше. Цитотоксическая клетка, такая как T- или NK-клетка, может быть выделена из собственной периферической крови субъекта (1-я сторона), или в условиях трансплантации гемопоэтических стволовых клеток - из периферической крови донора (2-я сторона), или из периферической крови несвязанного донора (3-я сторона).
Способ лечения Т-клеточных лимфомы и/или лейкоза относится к терапевтическому применению агента. Согласно указанному способу, агент можно вводить субъекту, имеющему Т-клеточные лимфому и/или лейкоз, с целью уменьшить, снизить или облегчить по меньшей мере один симптом, связанный с данным заболеванием, и/или замедлить, снизить или остановить прогрессирование заболевания.
Данные виды терапевтического применения будут включать введение терапевтически эффективного количества клетки, антитела, BiTE или химиотерапевтического конъюгата по настоящему изобретению.
Термин «терапевтически эффективное количество» в контексте настоящей заявки относится к количеству клетки, антитела, BiTE или химиотерапевтического конъюгата по настоящему изобретению, которое требуется для достижения заметного прогресса в плане профилактики, лечения, отсрочки проявления, уменьшения тяжести или облегчения одного или нескольких симптомов TRBC2-положительных Т-клеточных лимфомы и/или лейкоза.
Способ по настоящему изобретению может быть применен для лечения любого вида лимфомы и/или лейкоза, ассоциированных с клональной экспансией клеток, экспрессирующих Т-клеточные рецепторы (TCR), содержащие TRBC2. Таким образом, настоящее изобретение относится к способу лечения заболевания, в котором задействованы злокачественные Т-клетки, которые экспрессируют TCR, содержащие TRBC2.
Способ по настоящему изобретению может быть применен для лечения Т-клеточной лимфомы, при которой злокачественные Т-клетки экспрессируют TCR, содержащие TRBC2. Термин «лимфома» используют в настоящей заявке в соответствии с общепринятым значением для обозначения рака, который обычно развивается в лимфатических узлах, но также может поражать селезенку, костный мозг, кровь и другие органы. Лимфома обычно представляет собой солидную опухоль из лимфоидных клеток. Первичным симптомом, ассоциированным с лимфомой, является лимфаденопатия, хотя вторичные (B) симптомы могут включать увеличение температуры, ночную потливость, потерю веса, потерю аппетита, увеличенную утомляемость, респираторный дистресс и зуд.
Способ по настоящему изобретению может быть применен для лечения Т-клеточного лейкоза, при котором злокачественные Т-клетки экспрессируют TCR, содержащие TRBC2. Термин «лейкоз» используют в настоящей заявке в соответствии с общепринятым значением для обозначения рака крови или костного мозга.
Ниже приведен иллюстративный неисчерпывающий перечень заболеваний, которые можно лечить способом по настоящему изобретению.
ПЕРИФЕРИЧЕСКАЯ Т-КЛЕТОЧНАЯ ЛИМФОМА
Периферические Т-клеточные лимфомы являются сравнительно редкими лимфомами и составляют менее 10% всех неходжкинских лимфом (НХЛ). Однако они связаны с агрессивным клиническим течением, а причины и точное клеточное происхождение большинства Т-клеточных лимфом до сих пор не определены.
Лимфома обычно сначала проявляется в виде припухлости в области шеи, подмышек или паха. Последующее вздутие может появиться там, где расположены другие лимфатические узлы, например, в селезенке. Как правило, увеличенные лимфатические узлы могут вторгаться в пространство кровеносных сосудов, нервов или желудка, вызывая отеки рук и ног, покалывание и онемение или распирающее чувство соответственно. Симптомы лимфомы также включают неспецифические симптомы, такие как увеличение температуры, озноб, необъяснимая потеря веса, ночная потливость, сонливость и зуд.
Для установления прогностически и терапевтически значимой категоризации периферических Т-клеточных лимфом в классификации ВОЗ используют морфологические и иммунофенотипические особенности в сочетании с клиническими аспектами и в некоторых случаях с генетикой (Swerdlow et al.; WHO classification of tumours of haematopoietic and lymphoid tissues. 4th ed.; Lyon: IARC Press; 2008). Анатомическая локализация неопластических Т-клеток частично соответствует их предполагаемым нормальным клеточным аналогам и функциям, и, как таковые, Т-клеточные лимфомы связаны с лимфатическими узлами и периферической кровью. Данный подход позволяет лучше понять некоторые проявления Т-клеточных лимфом, включая их распределение в клетках, некоторые аспекты морфологии и даже связанные с ними клинические данные.
Наиболее распространенной из Т-клеточных лимфом является неспецифицированная периферическая Т-клеточная лимфома (ПТКЛн), на которую приходится 25% от общего количества случаев, на втором месте ангиоиммунобластная Т-клеточная лимфома (АИТЛ) (18,5%).
ПЕРИФЕРИЧЕСКАЯ Т-КЛЕТОЧНАЯ ЛИМФОМА, НЕСПЕЦИФИЦИРОВАННАЯ (ПТКЛН)
На ПТКЛн приходится более 25% от всех периферических Т-клеточных и NK/Т-клеточных лимфом, и она является наиболее распространенным подтипом. Ее определяют диагностикой способом исключения, когда заболевание не соответствует ни одному из известных случаев зрелых Т-клеточных лимфом, перечисленных в действующем перечне ВОЗ за 2008 год. В этом она схожа с неспецифицированной диффузной В-крупноклеточной лимфомой (ДВККЛн).
Большинство пациентов - взрослые, средний возраст которых составляет 60 лет, а соотношение мужчин и женщин составляет 2:1. Большинство случаев имеют узловое происхождение, однако экстранодальные проявления встречаются примерно у 13% пациентов и чаще всего затрагивают кожу и желудочно-кишечный тракт.
Цитологический спектр очень широк - от полиморфных до мономорфных видов. Описаны три морфологически определенные разновидности, включая лимфоэпителиоидную (Lennert), Т-зональную и фолликулярную лимфомы. Лимфоэпителиоидная разновидность ПТКЛ характеризуется содержанием большого количества фоновых эпителиоидных гистиоцитов и как правило является положительной по CD8. Это связывают с благоприятным прогнозом. Фолликулярная разновидность ПТКЛн проявляет себя как потенциально отдельный клиникопатологический компонент.
Большинство ПТКЛн имеют фенотип зрелых Т-клеток и в большинстве случаев являются CD4-положительными. В 75% случаев наблюдаются переменные потери по меньшей мере одного Т-клеточного маркера (CD3, CD2, CD5 или CD7), причем чаще всего сокращается количество CD7 и CD5. Могут экспрессироваться CD30 и редко CD15, причем экспрессия CD15 является неблагоприятным прогностическим признаком. Экспрессия CD56, хотя и встречается редко, также оказывает негативное влияние на прогноз. Прочие неблагоприятные патологические прогностические факторы включают степень пролиферации более 25% по экспрессии KI-67 и наличие более 70% трансформированных клеток. Иммунофенотипический анализ данных лимфом дал мало сведений об их биологии.
АНГИОИММУНОБЛАСТНАЯ Т-КЛЕТОЧНАЯ ЛИМФОМА (АИТЛ)
АИТЛ является системным заболеванием, которое характеризуется полиморфным инфильтратом, затрагивающим лимфатические узлы, выступающими наружными эндотелиальными венулами (НЭВ) и периваскулярной экспансией сетей фолликулярных дендритных клеток (ФДК). АИТЛ считается новым видом T-клеточной лимфомы, происходящим из фолликулярных хелперных T-клеток (TFH) αβ, обычно встречающихся в зародышевых центрах.
АИТЛ является вторым по распространенности заболеванием среди периферических T-клеточных и NK/T-клеточных лимфом, на которое приходится около 18,5% случаев. Она встречается у людей среднего и пожилого возраста, средний возраст заболевших составляет 65 лет, причем заболеваемость у мужчин и женщин примерно одинакова. По данным клинических исследований пациенты обычно имеют запущенную стадию заболевания с генерализованной лимфаденопатией, гепатоспленомегалией и выраженными конституциональными симптомами. Обычно имеет место кожная сыпь с сопутствующим зудом. Часто встречается поликлональная гипергаммаглобулинемия, связанная с аутоиммунными явлениями.
Описаны три различных морфологических паттерна АИТЛ. На ранних стадиях поражения АИТЛ (Паттерн I) обычно наблюдается ненарушенная архитектура с характерными гиперпластическими фолликулами. Неопластическая пролиферация локализована на периферии фолликулов. У Паттерна II архитектура узлов частично смазана с сохранением нескольких регрессированных фолликулов. Субкапсулярные синусы сохранены и даже расширены. Паракортикальная область содержит разветвляющиеся НЭВ, и имеет место пролиферация ФДК за пределы B-клеточного фолликула. Неопластические клетки имеют размер от малого до среднего с минимальной цитологической атипией. Они часто имеют прозрачную или бледную цитоплазму и могут иметь хорошо различимые Т-клеточные мембраны. Как правило, очевидно наличие полиморфного воспалительного фона.
Хотя АИТЛ является злокачественным Т-клеточным новообразованием, имеет место характерная экспансия В-клеток и плазматических клеток, что, по-видимому, отражает функцию неопластических клеток в качестве клеток TFH. Присутствуют как EBV-положительные, так и EBV-отрицательные B-клетки. Иногда атипичные B-клетки имеют морфологическую и иммунофенотипическую схожесть с клетками Ходжкина/Рида-Штернберга, что в некоторых случаях приводит к путанице при диагностике данного заболевания. Пролиферация B-клеток при АИТЛ может быть обширной, и у некоторых пациентов развивают вторичные EBV-положительные диффузные В-крупноклеточные лимфомы (ДВККЛ) или (реже) EBV-отрицательные B-клеточные опухоли, часто с плазмоцитарной дифференциацией.
Неопластические CD4-положительные Т-клетки АИТЛ демонстрируют сильную экспрессию CD10 и CD279 (PD-1) и являются положительными по CXCL13. Наличие CXCL13 приводит к увеличению рекрутирования B-клеток в лимфатические узлы за счет адгезии к НЭВ, активации B-клеток, плазмоцитарной дифференциации и экспансии сетей ФДК, что составляет морфологические и клинические особенности АИТЛ. Интенсивная экспрессия PD-1 в перифолликулярных опухолевых клетках особенно полезна для того, чтобы отличать Паттерн I АИТЛ от реактивной фолликулярной и паракортикальной гиперплазии.
Фолликулярная разновидность ПТКЛн представляет собой еще одно заболевание с фенотипом TFH. В отличие от АИТЛ, при нем не наблюдают выступающие НЭВ или внефолликулярная экспансия сетей ФДК. Неопластические клетки могут образовывать внутрифолликулярные агрегаты, имитирующие В-клеточную фолликулярную лимфому, но также могут иметь межфолликулярный паттерн роста или затрагивать расширенные мантийные зоны. Клинически фолликулярная разновидность ПТКЛн отличается от АИТЛ, поскольку чаще у пациентов наблюдается ранняя стадия заболевания с частичным поражением лимфатических узлов и могут отсутствовать конституциональные симптомы, связанные с АИТЛ.
АНАПЛАСТИЧЕСКАЯ КРУПНОКЛЕТОЧНАЯ ЛИМФОМА (АККЛ)
АККЛ можно разделить на АККЛ-«киназа анапластической лимфомы» (КАЛ)+ и АККЛ-КАЛ-.
АККЛ-КАЛ+ является одним из наиболее четко определенных заболеваний среди периферических Т-клеточных лимфом с характерными «отличительными клетками», несущими подковообразные ядра и экспрессирующими КАЛ и CD30. На его долю приходится около 7% всех периферических Т-клеточных и NK-клеточных лимфом, и оно наиболее распространено в первые три десятилетия жизни. Пациенты часто страдают лимфаденопатией, но поражение экстранодальных участков (кожи, костей, мягких тканей, легких, печени) и В-симптомы являются распространенным явлением.
АККЛ-КАЛ+ демонстрирует широкий морфологический спектр с 5 различными описанными паттернами, но все варианты содержат некоторые отличительные клетки. Клетки с характерными признаками имеют эксцентричные подковообразные или почковидные ядра и заметную перинуклеарную эозинофильную область Гольджи. Рост опухолевых клеток имеет когезионный характер с предрасположенностью к вовлечению синуса. Меньшие опухолевые клетки преобладают в мелкоклеточном варианте, а в лимфогистиоцитарном варианте обильные гистиоциты маскируют присутствие опухолевых клеток, многие из которых являются небольшими.
По определению, во всех случаях наблюдается КАЛ и CD30-положительность, причем их экспрессия обычно слабее в более мелких опухолевых клетках. Часто наблюдают потерю пан-Т-клеточных маркеров, в 75% случаев отсутствует экспрессия CD3 на поверхности.
Экспрессия ALK является результатом характерного рекуррентного генетического изменения, заключающегося в перестройке гена ALK на хромосоме 2p23 в один из множества партнерских генов, что приводит к экспрессии химерного белка.
Наиболее распространенным партнерским геном, встречающимся в 75% случаев, является ген Нуклеофозмина (NPM1) на хромосоме 5q35, что приводит к t(2;5)(p23;q35). Клеточное распределение КАЛ в разных вариантах транслокации может варьироваться в зависимости от гена-партнера.
АККЛ-КАЛ- включена в классификацию ВОЗ 2008 года в качестве предварительной категории. Ее определяют как CD30-положительную Т-клеточную лимфому, которая морфологически неотличима от АККЛ-КАЛ+ с когезионным характером роста и наличием отличительных клеток, но лишенная экспрессии белка КАЛ.
Пациенты, как правило, представляют собой взрослых в возрасте от 40 до 65 лет, в отличие от АККЛ-КАЛ +, которая чаще встречается у детей и молодых взрослых. АККЛ-КАЛ- может поражать как лимфатические узлы, так и экстранодальные ткани, хотя последнее наблюдается реже, чем в АККЛ-КАЛ+. Большинство случаев АККЛ-КАЛ- демонстрируют сглаживание архитектуры лимфатических узлов листами когезионных неопластических клеток с типичными «отличительными» чертами. В отличие от АККЛ-КАЛ+, мелкоклеточный морфологический вариант не выявляют.
В отличие от своего аналога КАЛ+, АККЛ-КАЛ- демонстрирует большее сохранение экспрессии поверхностного Т-клеточного маркера, в то время как экспрессия цитотоксических маркеров и эпителиального мембранного антигена (ЭМА) менее вероятна. Сигнатуры экспрессии генов и рекуррентный хромосомный дисбаланс различны в АККЛ-КАЛ- и АККЛ-КАЛ+, подтверждая, что они являются различными заболеваниями на молекулярном и генетическом уровне.
АККЛ-КАЛ- клинически отличается от АККЛ-КАЛ+ и ПТКЛН со значительными различиями в прогнозе между этими тремя различными заболеваниями. Общая 5-летняя выживаемость у АККЛ-КАЛ- составляет 49%, что не так хорошо, как у АККЛ-КАЛ+ (при 70%), но в то же время значительно лучше, чем у ПТКЛН (32%).
Т-КЛЕТОЧНАЯ ЛИМФОМА, АССОЦИИРОВАННАЯ С ЭНТЕРОПАТИЕЙ (ТКЛЭ)
ТКЛЭ - это агрессивное новообразование, которое, как считается, происходит от интраэпителиальных Т-клеток кишечника. В классификации ВОЗ 2008 года признаны два морфологически, иммуногистохимически и генетически различных типа ТКЛЭ: тип I (представляющий большинство ТКЛЭ) и тип II (составляющий 10-20% случаев).
ТКЛЭ типа I обычно ассоциируют с явной или бессимптомной глютен-чувствительной энтеропатией и чаще встречается у пациентов из Северной Европы в связи с высокой распространенностью целиакии в этой популяции.
Чаще всего поражения ТКЛЭ обнаруживаю в тощей кишке или подвздошной кишке (90% случаев) с редкими проявлениями в двенадцатиперстной кишке, толстой кишке, желудке или в областях за пределами желудочно-кишечного тракта. Кишечные поражения обычно многоочаговые с изъязвлением слизистой оболочки. Клиническое течение ТКЛЭ является агрессивным, большинство пациентов умирает от заболевания или осложнений заболевания в течение 1 года.
Цитологический спектр ТКЛЭ типа I широк, и в некоторых случаях может содержать анапластические клетки. Существует полиморфный воспалительный фон, который в некоторых случаях может скрывать неопластический компонент. Слизистая оболочка кишечника в участках, прилегающих к опухоли, часто демонстрирует признаки целиакии с притуплением ворсинок и увеличением числа интраэпителиальных лимфоцитов (IEL), которые могут представлять собой пораженные клетки-предшественники.
По данным иммуногистохимии, неопластические клетки часто являются CD3+CD4-CD8-CD7+CD5-CD56-βF1+ и содержат цитотоксические белки, связанные с гранулами (TIA-1, гранзим B, перфорин). CD30 частично экспрессирован почти во всех случаях. CD103, который является рецептором хоминга слизистой оболочки, может быть экспрессирован в ТКЛЭ.
ТКЛЭ типа II, также называемая CD56+ мономорфной эпителиотропной Т-клеточной лимфомой кишечника, определяют как опухоль кишечника, состоящую из мономорфных T-клеток малого и среднего размера, которые экспрессируют CD8 и CD56. Часто наблюдают латеральное распространение опухоли в слизистой оболочке и отсутствие воспалительного фона. В большинстве случаев экспрессируется γδ TCR, однако есть случаи, связанные с αβ TCR.
ТКЛЭ типа II имеет более широкое распространение во всем мире, чем ТКЛЭ типа I, и его часто наблюдают в азиатских или испаноязычных популяциях, в которых целиакия встречается редко. У лиц европейского происхождения ТКЛЭ II составляет около 20% Т-клеточных лимфом кишечника, с историей целиакии, по крайней мере, в ряде случаев. Клиническое течение является агрессивным.
ГЕПАТОЛИЕНАЛЬНАЯ Т-КЛЕТОЧНАЯ ЛИМФОМА (ГЛТЛ)
ГЛТЛ является агрессивным системным новообразованием, обычно возникающим из цитотоксических γδ Т-клеток врожденной иммунной системы, однако в редких случаях оно также может возникнуть из αβ Т-клеток. Это одна из самых редких Т-клеточных лимфом, которая обычно поражает подростков и молодых взрослых (средний возраст 35 лет) с сильным преобладанием мужчин.
ЭКСТРАНОДАЛЬНАЯ NK/T-КЛЕТОЧНАЯ ЛИМФОМА, НАЗАЛЬНЫЙ ТИП
Экстранодальная NK/T-клеточная лимфома, назальный тип, является агрессивным заболеванием, часто с деструктивными поражениями средней линии и некрозом. Большинство случаев имеют NK-клеточное происхождение, но некоторые случаи происходят от цитотоксических T-клеток. Общепризнано, что данное заболевание ассоциировано с вирусом Эпштейна-Барра (EBV).
Т-КЛЕТОЧНАЯ ЛИМФОМА КОЖИ
Способ согласно настоящему изобретению также может быть применен для лечения Т-клеточной лимфомы кожи.
Т-клеточная лимфома кожи (ТКЛК) характеризуется миграцией злокачественных Т-клеток в кожу, что вызывает появление различных поражений. Эти поражения меняют форму по мере прогрессирования заболевания, обычно начиная с того, что кажется сыпью, и, в конечном итоге, образуя бляшки и опухоли перед метастазированием в другие части тела.
Т-клеточные лимфомы кожи включают те, которые упомянуты в следующем иллюстративном, неисчерпывающем списке; грибовидный микоз, педжетоидный ретикулез, синдром Сезари, гранулематозная вялая кожа, лимфоматоидный папулез, парапсориаз лихеноидный хронический, CD30+ кожная Т-клеточная лимфома, вторичная кожная CD30+ крупноклеточная лимфома, CD30- кожная крупноклеточная Т-клеточная лимфома не грибовидный микоз, плеоморфная Т-клеточная лимфома, лимфома Леннерта, подкожная Т-клеточная лимфома и ангиоцентрическая лимфома.
Признаки и симптомы ТКЛК варьируют в зависимости от конкретного заболевания, из которых два наиболее распространенных типа - грибовидный микоз и синдром Сезари. Классический грибовидный микоз делится на три стадии:
- Пятна (атрофические или неатрофические): неспецифический дерматит, пятна на нижней части туловища и ягодицах; минимальный/отсутствующий кожный зуд;
- Зубной налет: бляшки с сильным зудом, лимфаденопатия; и
- Опухоль: тенденция к образованию язв
Синдром Сезари определяется эритродермией и лейкозом. Признаки и симптомы включают отечную кожу, лимфаденопатию, ладонный и/или подошвенный гиперкератоз, алопецию, дистрофию ногтей, эктропион и гепатоспленомегалию.
Из всех первичных кожных лимфом 65% относятся к Т-клеточному типу. Наиболее распространенным иммунофенотипом является CD4-положительный. Общей патофизиологии для этих заболеваний не существует, так как термин Т-клеточная лимфома кожи охватывает широкий спектр нарушений.
Первичные этиологические механизмы развития Т-клеточной лимфомы кожи (то есть грибовидного микоза) не выяснены. Грибовидному микозу может предшествовать опосредованная Т-клетками хроническая воспалительная болезнь кожи, которая может иногда прогрессировать до фатальной лимфомы.
ПЕРВИЧНАЯ АККЛ КОЖИ (АКЛК)
АККЛК часто неотличима от АККЛ-КАЛ- по морфологии. Ее определяют как кожную опухоль из крупных клеток с анапластической, плеоморфной или иммунобластной морфологией с более чем 75% клеток, экспрессирующих CD30. Вместе с лимфоматоидным папулезом (LyP) АКЛК относится к спектру первичных CD30-положительных Т-клеточных лимфопролиферативных нарушений, которые как группа составляют вторую наиболее распространенную после грибовидного микоза группу Т-клеточных лимфопролифераций.
Профиль иммуногистохимического окрашивания достаточно схож с АККЛ-КАЛ- с большей долей случаев, окрашивающих положительно на цитотоксические маркеры. По крайней мере 75% опухолевых клеток должны быть положительными по CD30. CD15 также может быть экспрессирован, и когда происходит вовлечение лимфатического узла, дифференциация с классической лимфомой Ходжкина может быть затруднена. Редкие случаи АККЛ-КАЛ+ могут иметь локализованные кожные повреждения и напоминать C-ALCL.
Т-КЛЕТОЧНЫЙ ОСТРЫЙ ЛИМФОБЛАСТНЫЙ ЛЕЙКОЗ
Т-клеточный острый лимфобластный лейкоз (Т-ОЛЛ) составляет около 15% и 25% от общего количества ОЛЛ в педиатрической и взрослой когортах соответственно. Пациенты обычно имеют высокое количество лейкоцитов и могут иметь органомегалию, особенно увеличение средостения и вовлечение ЦНС.
Способ согласно настоящему изобретению может быть применен для лечения Т-ОЛЛ, который связан со злокачественной Т-клеткой, которая экспрессирует TCR, включающий TRBC1.
Т-КЛЕТОЧНЫЙ ПРОЛИМФОЦИТАРНЫЙ ЛЕЙКОЗ (Т-ПЛЛ)
Т-клеточный пролимфоцитарный лейкоз (Т-ПЛЛ) представляет собой зрелый Т-клеточный лейкоз с агрессивным поведением и склонностью к поражению крови, костного мозга, лимфатических узлов, печени, селезенки и кожи. Т-ПЛЛ поражает, главным образом, взрослых в возрасте старше 30 лет. Другие названия включают Т-клеточный хронический лимфоцитарный лейкоз, «холмистый» тип Т-клеточного лейкоза и Т-пролимфоцитарный лейкоз/Т-клеточный лимфоцитарный лейкоз.
В периферической крови Т-ПЛЛ состоит из лимфоцитов среднего размера с одиночными ядрышками и базофильной цитоплазмой со случайными пузырьками или выступами. Ядра, как правило, имеют округлую или овальную форму, причем у отдельных пациентов имеются клетки с более нерегулярным ядерным контуром, сходным с церебриформной ядерной формой, наблюдаемой при синдроме Сезари. Мелкоклеточный вариант составляет 20% всех случаев Т-ПЛЛ, а вариант, подобный клеткам Сезари (церебриформный), наблюдается в 5% случаев.
Т-ПЛЛ обладает иммунофенотипом зрелого (посттимического) T-лимфоцита, и неопластические клетки, как правило, положительны по пан-Т-антигенам CD2, CD3 и CD7 и негативны по TdT и CD1a. Иммунофенотип CD4+/CD8- присутствует в 60% случаев, иммунофенотип CD4+/CD8+ присутствует в 25%, а иммунофенотип CD4-/CD8+ присутствует в 15% случаев.
Диагностирумые Т-клеточные лимфома или лейкоз могут быть выбраны из следующего: неспецифицированная периферическая Т-клеточная лимфома (ПТКЛн); ангиоиммунобластная Т-клеточная лимфома (АИТЛ), анапластическая крупноклеточная лимфома (АККЛ), Т-клеточная лимфома, ассоциированная с энтеропатией (EATL), гепатолиенальная Т-клеточная лимфома (ГЛТЛ), экстранодальная NK/T-клеточная лимфома назального типа, Т-клеточная лимфома кожи, первичная АККЛ кожи, Т-клеточный пролимфоцитарный лейкоз и Т-клеточный острый лимфобластный лейкоз.
Способ лечения может включать этап введения терапевтического количества клетки или группы клеток, или антитела, или BiTE, или химиотерапевтического конъюгата согласно настоящему изобретению. Специалист сможет определить количество клетки или группы клеток, или антитела, или BiTE, или химиотерапевтического конъюгата согласно настоящему изобретению, которое способно оказать терапевтическое действие на пациента, общепринятыми способами.
11. Диагностический агент
Ранее было определено, что доля Т-клеток TRBC2+ от здоровых доноров составляет 35%, а Т-клеток TRBC1+ - 65%, то есть средняя процентная доля от общего количества Т-клеток, экспрессирующих TRBC1, составляла 35% (диапазон 25-47%) (Maciocia et al., 2017, Nat Med 23:1416-23). Поскольку Т-клеточные лимфомы или лейкозы являются клональными раковыми образованиями (Maciocia et al., 2017; как было сказано выше), нерегулируемая пролиферация злокачественных Т-клеток, характерная для Т-клеточных лимфомы или лейкоза, будет приводить к тому, что доля T-клеток TRBC1+ или TRBC2+ (например, Т-клетки TRBC2- или TRBC1-) будет значительно отличаться от первоначальной. Соответственно, за счет способности различать TRBC1 и TRBC2 благодаря специфичному связыванию с TRBC2, вариантный антигенсвязывающий домен и антитело согласно настоящему изобретению представляют собой агенты, которые можно применять для диагностики Т-клеточных лимфом или лейкозов.
Таким образом, в еще одном аспекте настоящего изобретения предложен диагностический агент (далее - «первый диагностический агент согласно настоящему изобретению»), котороый содержит вариантный антигенсвязывающий домен согласно настоящему изобретению.
В другом аспекте настоящего изобретения предложен диагностический агент, (далее - «второй диагностический агент согласно настоящему изобретению», который содержит антитело согласно настоящему изобретению.
Термины «вариантный антигенсвязывающий домен согласно настоящему изобретению» и «антитело согласно настоящему изобретению» были подробно раскрыты в контексте предыдущих аспектов настоящего изобретения, и их признаки и варианты реализации в равной степени применимы к данным аспектам изобретения.
Вариантный антигенсвязывающий домен или антитело согласно настоящему изобретению, предназначенные для применения в этих анализах, могут быть мечеными или немечеными. Термин «детектируемая метка» или «агент для мечения» в контексте настоящей заявки относится к молекулярной метке, которая позволяет обнаруживать, определять местоположение и/или идентифицировать молекулу, к которой она присоединена с помощью соответствующих способов и оборудования для обнаружения, например, с помощью спектроскопических, фотохимических, биохимических, иммунохимических или химических средств. Агенты для мечения, пригодные для мечения антител, включают радионуклиды, энзимы, флуорофоры, хемилюминесцентные реагенты, ферментные субстраты или кофакторы, ингибиторы ферментов, частицы, красители и их производные, и т. п. Для специалиста в данной области очевидно, что обнаружение немеченых вариантных антигенсвязывающих доменов и антител должно производиться с помощью дополнительного реагента, например, меченого вторичного антитела. Это особенно полезно для увеличения чувствительности способа обнаружения, поскольку позволяет усилить сигнал. Существует широкий спектр стандартных анализов, которые могут быть применены в настоящем изобретении, в которых используются немеченые антитела согласно настоящему изобретению (первичное антитело) и меченые антитела согласно настоящему изобретению (вторичные антитела). Данные способы включают вестерн-блоттинг или иммуноблотирование, ELISA (иммуноферментный анализ), RIA (радиоиммуноанализ), конкурентный EIA (конкурентный иммуноферментный анализ), DAS-ELISA (сэндвич-ELISA с двумя антителами), иммуноцитохимические и иммуногистохимические способы, проточную цитометрию или мультиплексные способы обнаружения, основанные на применении белковых микросфер, биочипов или микрочипов, которые включают антитела согласно настоящему изобретению. Другие способы обнаружения и количественной оценки TRBC2 с применением вариантного антигенсвязывающего домена или антитела согласно настоящему изобретению включают способы аффинной хроматографии или анализы связывания лиганда.
Данный диагностический агент может быть применен для диагностики Т-клеточных лимфомы или лейкоза.
Т-клеточные лимфома или лейкоз могут быть выбраны из следующего: неспецифицированная периферическая Т-клеточная лимфома (ПТКЛн); ангиоиммунобластная Т-клеточная лимфома (АИТЛ), анапластическая крупноклеточная лимфома (АККЛ), Т-клеточная лимфома, ассоциированная с энтеропатией (EATL), гепатолиенальная Т-клеточная лимфома (ГЛТЛ), экстранодальная NK/T-клеточная лимфома назального типа, Т-клеточная лимфома кожи, первичная АККЛ кожи, Т-клеточный пролимфоцитарный лейкоз и Т-клеточный острый лимфобластный лейкоз.
12. Способ диагностики
В еще одном аспекте настоящего изобретения предложен способ диагностики Т-клеточных лимфомы или лейкоза у субъекта, (далее - «способ диагностики согласно настоящему изобретению», который включает этап приведения в контакт вариантного антигенсвязывающего домена или антитела согласно настоящему изобретению с образцом, содержащим Т-клетки, полученные у субъекта.
Термины «вариантный антигенсвязывающий домен согласно настоящему изобретению», «антитело согласно настоящему изобретению» и «субъект» были подробно раскрыты в контексте предыдущих аспектов изобретения, и их признаки и варианты реализации в равной степени применимы к данному аспекту настоящего изобретения.
Способ диагностики согласно настоящему изобретению может дополнительно включать этап определения процентной доли TRBC2-положительных Т-клеток в образце.
Для применения первого способа согласно настоящему изобретению на практике, у исследуемого субъекта получают образец, содержащий Т-клетки, такой как биологический образец. Термин «образец» или «биологический образец» в контексте настоящей заявки означает различные виды биологических жидкостей или участков тканей пораженных органов, которые содержат Т-клетки. Иллюстративные неограничивающие примеры образцов, используемых в данном способе диагностики согласно настоящему изобретению, включают различные виды биологических жидкостей, содержащих Т-клетки, такие как кровь, лимфатическая и спинномозговая жидкости. Такие образцы биологической жидкости можно получить любым стандартным способом, известным специалистам. В альтернативном варианте указанный образец также может представлять собой фрагмент образца ткани пораженного органа, например, из лимфатической железы, селезенки, миндалин или тимуса, который может быть получен любым общепринятым способом, например, с помощью биопсии или хирургической резекции, и из замороженных фрагментов, взятых для гистологических целей.
В соответствии с первым этапом способа диагностики согласно настоящему изобретению вариантный антигенсвязывающий домен или антитело согласно настоящему изобретению контактирует с образцом, полученным у исследуемого субъекта, в соответствующих условиях, известных специалистам в данной области.
Специалист в данной области может использовать ряд стандартных способов для обнаружения TRBC2 в образце, которые подходят для выполнения второго этапа способа диагностики согласно настоящему изобретению. Особенно полезны иммунологические способы. Таким образом, применение первого или второго диагностического агента согласно настоящему изобретению может быть особенно полезным для применения способа диагностики согласно настоящему изобретению. Признаки и конкретные варианты реализации, касающиеся диагностических агентов согласно настоящему изобретению были определены ранее и в равной степени применимы к способу диагностики согласно настоящему изобретению.
В способе диагностики согласно настоящему изобретению процентное содержание TRBC2-положительных Т-клеток в образце, составляющее 70%, или 75%, или 80%, или 85%, или 90%, или 95%, или 96%, или 97%, или 98%, или 99%, или более может указывать на наличие Т-клеточных лимфомы или лейкоза.
Специалистам в данной области техники будет понятно, что несмотря на то, что прогноз отражает наиболее вероятный вариант, он не обязательно должен быть правильным для 100% субъектов, подлежащих диагностике или обследованию. Однако данный термин подразумевает, что статистически значимая доля субъектов может быть определена как имеющие увеличенную вероятность получения данного результата. Специалист в данной области может достаточно быстро определить, являются ли полученные у субъекта данные статистически значимыми, при помощи различных хорошо известных средств статистической оценки, например, способом определения доверительных интервалов, определением значения p, способом классификационных норм с перекрестной валидацией и т. п. Подробную информацию можно найти в Dowdy and Wearden, Statistics for Research, John Wiley & Sons, New York, 1983. Предпочтительные доверительные интервалы составляют по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90% или по меньшей мере 95%. В предпочтительном варианте реализации значения p составляют 0,01 или 0,005 или меньше.
Кроме того, вариантный антигенсвязывающий домен или антитело согласно настоящему изобретению ввиду их способности специфично связывать TRBC2-положительные Т-клетки также могут быть применены для диагностики Т-клеточных лимфомы или лейкоза in vivo. Например, они могут быть применены в медицинской визуализации, то есть в комплексе способов и технологий, используемых для создания изображений тела (или его частей и функций), например, тела человека, для клинических целей, таких как медицинские процедуры, направленные на выявление, диагностику или исследование заболеваний.
Для этой цели вариантный антигенсвязывающий домен или антитело согласно настоящему изобретению маркируют подходящими способами, известными в данной области, и применяют в качестве агентов для способов диагностической визуализации, таких как радиоиммунодиагностика, позитронно-эмиссионная томография (ПЭТ), иммунофлуоресцентная эндоскопия и т. п., например, посредством связывания и/или загрузки соответствующими молекулами, например радиоактивными изотопами или флуоресцентными красителями. Вариантный антигенсвязывающий домен и антитело согласно настоящему изобретению могут быть ассоциированы с изотопами, излучающими гамма-лучи, и применяться в радиоиммуноцинтиграфии с применением гамма-камер или однофотонной эмиссионной компьютерной томографии. Вариантный антигенсвязывающий домен и антитело согласно настоящему изобретению могут быть ассоциированы с излучателями позитронов и использоваться в ПЭТ. Вариантный антигенсвязывающий домен и антитело согласно настоящему изобретению могут быть ассоциированы с флуоресцентными красителями, такими как Cy3, Cy2, Cy5 или FITC (флуоресцеин изотиоцианат), и использоваться в иммунофлуоресцентной эндоскопии. Вариантный антигенсвязывающий домен и антитело согласно настоящему изобретению, модифицированные вышеописанным образом, вводятся любым подходящим путем, например внутривенно, в дозе, подходящей для индивидуума, и обнаружение, определение местоположения или количественные измерения TRBC2-положительных Т-клеток осуществляются способами, хорошо известными в данной области. Используемые здесь способы и технологии, включая диагностическую визуализацию, известны квалифицированным специалистам, которые также могут предоставить подходящие лекарственные формы.
Диагностируемые Т-клеточные лимфома или лейкоз могут быть выбраны из следующего: неспецифицированная периферическая Т-клеточная лимфома (ПТКЛн); ангиоиммунобластная Т-клеточная лимфома (АИТЛ), анапластическая крупноклеточная лимфома (АККЛ), Т-клеточная лимфома, ассоциированная с энтеропатией (EATL), гепатолиенальная Т-клеточная лимфома (ГЛТЛ), экстранодальная NK/T-клеточная лимфома назального типа, Т-клеточная лимфома кожи, первичная АККЛ кожи, Т-клеточный пролимфоцитарный лейкоз и Т-клеточный острый лимфобластный лейкоз.
Образец может представлять собой образец крови или может быть получен из него.
13. Способы персонализированной медицины
В еще одном аспекте настоящего изобретения предложен способ выявления субъектов с Т-клеточными лимфомой или лейкозом, соответствующих критериям для лечения на основе клеток, антител, BiTE или химиотерапевтического конъюгата согласно настоящему изобретению (далее - «первый способ персонализированной медицины согласно настоящему изобретению»), включающий определение процентной доли TRBC2-положительных Т-клеток в образце, содержащем Т-клетки, полученные у субъекта.
Термины «клетка согласно настоящему изобретению», «антитело согласно настоящему изобретению», «BiTE согласно настоящему изобретению», «химиотерапевтический агент согласно настоящему изобретению», «субъект» и «образец, содержащий Т-клетки» были подробно раскрыты в контексте предыдущих аспектов настоящего изобретения, и их признаки и варианты реализации в равной степени применимы к данному аспекту настоящего изобретения.
В первом способе персонализированной медицины согласно настоящему изобретению субъект соответствует критериям для вышеупомянутого лечения на основе клеток, антител, BiTE или химиотерапевтического конъюгата согласно настоящему изобретению, если процент TRBC2-положительных Т-клеток в образце составляет 70% или 75%, или 80%, или 85%, или 90%, или 95%, или 96%, или 97%, или 98%, или 99% или более.
В еще одном аспекте настоящего изобретения предложен способ выбора терапии, включающей клетку, антитело, BiTE или химиотерапевтический конъюгат согласно настоящему изобретению, для лечения субъекта (далее - «второй способ персонализированной медицины согласно настоящему изобретению»), включающий определение процентной доли TRBC2-положительных Т-клеток в образце, содержащем Т-клетки, полученные у субъекта.
Термины «клетка согласно настоящему изобретению», «антитело согласно настоящему изобретению», «BiTE согласно настоящему изобретению», «химиотерапевтический агент согласно настоящему изобретению», «субъект» и «образец, содержащий Т-клетки» были подробно раскрыты в контексте предыдущих аспектов настоящего изобретения, и их признаки и варианты реализации в равной степени применимы к данному аспекту настоящего изобретения.
Во втором способе персонализированной медицины согласно настоящему изобретению терапия, включающая клетку, антитело, BiTE или химиотерапевтический конъюгат согласно настоящему изобретению, выбирается для лечения указанного субъекта, если процент TRBC2-положительных Т-клеток в образце составляет 70%, или 75%, или 80%, или 85%, или 90%, или 95%, или 96%, или 97%, или 98%, или 99% или более.
Образец может представлять собой образец крови или может быть получен из него.
Т-клеточные лимфома или лейкоз могут быть выбраны из следующего: неспецифицированная периферическая Т-клеточная лимфома (ПТКЛн); ангиоиммунобластная Т-клеточная лимфома (АИТЛ), анапластическая крупноклеточная лимфома (АККЛ), Т-клеточная лимфома, ассоциированная с энтеропатией (EATL), гепатолиенальная Т-клеточная лимфома (ГЛТЛ), экстранодальная NK/T-клеточная лимфома назального типа, Т-клеточная лимфома кожи, первичная АККЛ кожи, Т-клеточный пролимфоцитарный лейкоз и Т-клеточный острый лимфобластный лейкоз.
Далее настоящее изобретение будет описано с помощью Примеров, которые предназначены для помощи среднему специалисту в данной области техники в реализации изобретения, и никоим образом не предназначены для ограничения объема данного изобретения.
ПРИМЕРЫ
Пример 1: Анализ связывания антител к TRBC2 способом поверхностного плазмонного резонанса (SPR)
Кристаллическая структура моноклонального антитела hJovi-1, специфичного к TRBC1, была определена в комплексе с TRBC1-TCR в разрешении 2,4 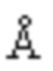 (Фиг. 3). С помощью вычислительной биологии и белковой инженерии, основываясь на принципах рациональности, было сконструировано несколько мутантных версий связывающей молекулы к TRBC1 для того, чтобы перенаправить специфичность с TRBC1 на TRBC2. Было создано некоторое количество связывающих молекул к TRBC2 в формате IgG. В Таблице 1 показаны данные по мутациям, содержащимся в доменах VH и VL антитела hJovi-1.
(Фиг. 3). С помощью вычислительной биологии и белковой инженерии, основываясь на принципах рациональности, было сконструировано несколько мутантных версий связывающей молекулы к TRBC1 для того, чтобы перенаправить специфичность с TRBC1 на TRBC2. Было создано некоторое количество связывающих молекул к TRBC2 в формате IgG. В Таблице 1 показаны данные по мутациям, содержащимся в доменах VH и VL антитела hJovi-1.
Сенсорный чип CM5 серии S иммобилизовали посредством аминового связывания с антителом к Fc человека до плотности 9000-10000 ЕО при помощи прибора Biacore T200. В качестве рабочего буфера во всех условиях эксперимента использовали буфер HBS-P+. Тестируемые антитела к TRBC2 (Таблица 1) улавливали в проточных кюветах 2, 3 и 4 до плотности 100-300 ЕО. Рекомбинантный очищенный TRBC1 или TRBC2 в известных концентрациях использовали в качестве «исследуемого вещества» и вводили через соответствующие проточные кюветы при времени контакта 150 с и диссоциации в течение 300 с при скорости потока 30 мкл/мин. В каждом эксперименте проточную кювету 1 не подвергали модификации и использовали для вычитания эталонных значений. Сенсограмму «0 концентраций» только буфера использовали в качестве двойного вычитания эталонных значений к коэффициенту отклонения. Данные соответствовали модели связывания Ленгмюра 1:1. Поскольку использовали захватывающее устройство, для подбора данных в каждом случае использовали локальный параметр Rmax.
Результаты определения аффинности к TRBC1 и TRBC2, полученные для каждого из антител к TRBC2, показаны в Таблице 1. Тестируемые антитела к TRBC2 продемонстрировали предпочтение к связыванию с TRBC2 в большинстве случаев в диапазоне нМ, с различными кинетическими свойствами ka и kd. В большинстве случаев оценка связывания с TRBC1 составила >1 мкМ со значениями, приближающимися к пределу чувствительности прибора.
Пример 2: Создание CAR к TRBC2 на основе связывающей молекулы KFN
Конструкции CAR второго поколения были созданы на основе антитела к TRBC2, полученного в результате тройной мутации (мутации T28K, Y32F, A100N в домене VH антитела hJovi-1, последовательность с SEQ ID: 26), и гуманизированного антитела Jovi-1 (hJovi-1) (Фиг. 4). Эти конструкции CAR клонировали в ретровирусный вектор и использовали для трансдукции активированных МКПК, полученных от здоровых доноров.
Пример 3: Функциональная характеристика CAR к TRBC2: Продукция цитокинов
Для оценки функциональной способности T-клеток с CAR к TRBC2 с тройной мутацией по отношению к TRBC2 использовали анализ связывания, проводимый на планшете (plate bound assay), в котором TRBC1 или TRBC2 иммобилизовали перед добавлением CAR-T-клеток. Через 72 часа культуральные супернатанты собирали и продукцию IFN-γ определяли с помощью ИФА (ELISA). На Фиг. 5A T-клетки с CAR к TRBC2 с тройной мутацией продемонстрировали более интенсивное высвобождение IFN-γ в присутствии лиганда TRBC2 по сравнению с TRBC1. Напротив, Т-клетки с CAR на основе антитела hJovi-1 показали высокий уровень продукции IFN-γ только при культивировании с лигандом TRBC1 (Фиг. 5B). Данные результаты демонстрируют, что Т-клетки с CAR, трансдуцированные мутантом с тройной мутацией, нацеленным на TRBC2, обладают большей активацией и высвобождением цитокинов по отношению TRBC2, чем при взаимодействии с TRBC1.
Пример 4: Функциональная характеристика CAR к TRBC2: Анализ цитотоксичности
Для определения способности анти-TRBC2 Т-клеток с CAR с тройной мутацией нацеливаться на TRBC2, были проведены анализы цитотоксичности с применением клеток Raji, трансдуцированных для экспрессии TRBC1 или TRBC2 в качестве клеток-мишеней и совместно культивируемых с Т-клетками с CAR. T-клетки с CAR на основе антитела hJovi-1 или анти-TRBC2 Т-клетки CAR с тройной мутацией культивировали в соотношении Э:М 1:1 с клетками Raji WT, Raji TRBC1+ или Raji TRBC2+. Выделение клеток-мишеней количественно определяли через 72 часа после культивирования с помощью проточной цитометрии и использовали для определения цитотоксической способности T-клеток с CAR. Культуры, содержащие анти-TRBC2 Т-клетки с CAR с тройной мутацией продемонстрировали ограниченную выживаемость клеток-мишеней Raji TRBC2+ (Фиг. 6). Напротив, анти-TRBC2 Т-клетки с CAR с тройной мутацией не устраняли клетки-мишени Raji TRBC1+, что указывает на их увеличенную способность нацеливаться на клетки TRBC2+.
Авторы настоящего изобретения использовали сконструированное моноклональное антитело для создания анти-TRBC2 CAR 2-го поколения. Созданные авторами настоящего изобретения анти-TRBC2 CAR продемонстрировали специфичность, высвобождение цитокинов и цитотоксичность на культурах, совместно культивируемых в течение 72-часов, в отношении линий клеток TRBC2+, в противоположность результатам у линий клеток TRBC1+ или линий клеток, которые не экспрессировали TCR на поверхности. Т-клетки с анти-TRBC2 CAR также продемонстрировали пролиферативную способность в продолжительных по времени анализах при совместном культивировании.
Пример 5: Функциональная характеристика CAR к TRBC2: Анализ киллинга
Дополнительные конструкции CAR второго поколения были созданы на основе связывающих молекул TRBC2, приведенных в Таблице 1, которые имеют следующие мутации:
- Мутации T28K, Y32F, A100N в домене VH и N35K в домене VL антитела hJovi-1 (обозначены как N35K, SEQ ID: 25),
- Мутации T28K, Y32F, A100N, N103L в домене VH антитела hJovi-1 (обозначены как N103L, SEQ ID: 27),
- Мутации T28K, Y32F, A100N, N103M в домене VH и N35Y в домене VL антитела hJovi-1 (обозначены как N103M-N35Y, SEQ ID: 28),
- Мутации T28K, Y32F, A100N, Y102F, N103M в домене VH и N35R в домене VL антитела hJovi-1 (обозначены как Y102F-N103M-N35R, SEQ ID: 29),
- Мутации T28K, Y32F, A100N, Y102L, N103M в домене VH и N35R в домене VL антитела hJovi-1 (обозначены как Y102L-N103M-N35R, SEQ ID: 30).
Эти конструкции CAR и молекулы анти-TRBC2 с тройной мутацией (мутации T28K, Y32F, A100N в домене VH антитела hJovi-1, обозначены как KFN, SEQ ID: 26) клонировали в ретровирусный вектор и использовали для трансдукции (a) клеток Jurkat или (b) активированных МКПК, полученных от здоровых доноров. Контрольный CAR к TRBC1, то есть конструкцию CAR на основе антитела hJovi-1 использовали в качестве контроля в анализе киллинга с применением активированных МКПК.
а) клетки Jurkat
Чтобы определить, были ли созданные связывающие молекулы специфичными к антигену TRBC2, клетки Jurkat, которые представляют собой TRBC1+, трансдуцировали вышеуказанными конструкциями CAR к TRBC2. Со-культуры трансдуцированных клеток Jurkat получали при соотношении эффектора к мишени (Э:М) 1:1 с применением клеток HPB-ALL, трансдуцированных для экспрессии только TRBC1 или TRBC2 (обозначены как HPB TRBC1 и HPB TRBC2 соответственно) в качестве клеток-мишеней с клетками HPB-ALL, имеющими нокаутированный TCR (обозначены как HPB KO) в качестве отрицательного контроля. Трансдуцированные клетки Jurkat высевали отдельно или с антителами αCD3/αCD28 для применения в качестве соответственно отрицательного или положительного контроля для анализа. Антиген-специфичную активацию оценивали по окрашиванию CD69 способом проточной цитометрии через 24 часа.
Результаты, показанные на Фиг. 7, продемонстрировали, что все трансдуцированные клетки Jurkat были избирательно активированы после совместной инкубации с клетками HPB TRBC2. Данные результаты демонстрируют, что все протестированные CAR проявляли специфичность к мишеням TRBC2, поскольку не наблюдали увеличение количества CD69 при совместном культивировании Jurkat с мишенями TRBC1+ или HPB KO.
b) МКПК
Вначале МКПК (мононуклеарные клетки периферической крови) были разделены на клетки TRBC1+ и TRBC2+ при помощи магнитных гранул с покрытием анти-биотин после окрашивания 10 мкг/мл биотинилированным антителом мыши JOVI-1, которое связывается только с TRBC1. Популяцию TRBC2+ трансдуцировали CAR на основе антитела hJovi-1 (JOVI), а популяцию TRBC1+ - вышеуказанным CAR к TRBC2. Данная дифференциальная трансдукция обеспечила, чтобы активация антигенов и уничтожение мишеней запускались только при добавлении мишеней в контролируемых условиях культивирования (таких как, например, отношение эффекторов к мишеням и временные точки), а не в смешанной популяции, где условия различны для каждого донора МКПК.
Затем анализы киллинга были организированы c применением клеток HPB-ALL, трансдуцированных для экспрессии только TRBC1 или TRBC2 (обозначены как TRBC1+HPB-ALL and TRBC2+HPB-ALL соответственно) в качестве клеток-мишеней с клетками HPB-ALL, имеющими деактивированный TCR (обозначены как HPB-KO) в качестве контроля. Через 10 дней после трансдукции клетки культивировали совместно при соотношении Э:М 1:2. Киллинг клеток оценивали способом проточной цитометрии через 72 часа после настройки параметров анализа.
Результаты продемонстрировали, что Т-клетки с CAR на основе hJovi-1 обеспечивали киллинг только клеток TRBC1+ HPB-ALL, а все T-клетки с CAR к TRBC2 обеспечивали киллинг только клеток TRBC2+ HPB-ALL (Фиг. 8). Сходные уровни фонового киллинга наблюдали у всех TRBC1- и TRBC2-специфичных T-клеток с CAR в отношении контрольных клеток HPB-KO, что указывает на то, что все протестированные CAR были специфичны к когнатному им антигену.
Пример 6: Анализ влияния различных форматов строения антител на связывание антител к TRBC2 посредством поверхностного плазмонного резонанса (SPR).
Эффект мультимеризации связывающих молекул к TRBC2 анализировали способом SPR. Для этого использовали антитела к TRBC2 с мутациями T28K, Y32F, A100N, Y102L и N103M в домене VH и мутацией N35R в домене VL антитела hJovi-1, имеющие три различных формата, а именно scFv (SEQ ID: 22), scFv-Fc (SEQ ID: 23) и scFv-COMP (SEQ ID: 24).
SEQ ID: 22
QVQLVQSGAEVKKPGASVKVSCKASGYKFTGFVMHWVRQAPGQGLEWMGFINPYNDDIQSNERFRGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARGNGLMFDGAYRFFDFWGQGTMVTVSSGGGGSGGGGSGGGGSDIVMTQSPLSLPVTPGEPASISCRSSQRLVHSNGRTYLHWYLQKPGQSPRLLIYRVSNRFPGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCSQSTHVPYTFGQGTKLEIKR
SEQ ID: 23
QVQLVQSGAEVKKPGASVKVSCKASGYKFTGFVMHWVRQAPGQGLEWMGFINPYNDDIQSNERFRGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARGNGLMFDGAYRFFDFWGQGTMVTVSSGGGGSGGGGSGGGGSDIVMTQSPLSLPVTPGEPASISCRSSQRLVHSNGRTYLHWYLQKPGQSPRLLIYRVSNRFPGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCSQSTHVPYTFGQGTKLEIKRSDPRGPTIKPCPPCKCPAPNLLGGPSVFIFPPKIKDVLMISLSPIVTCVVVDVSEDDPDVQISWFVNNVEVHTAQTQTHREDYNSTLRVVSALPIQHQDWMSGKEFKCKVNNKDLPAPIERTISKPKGSVRAPQVYVLPPPEEEMTKKQVTLTCMVTDFMPEDIYVEWTNNGKTELNYKNTEPVLDSDGSYFMYSKLRVEKKNWVERNSYSCSVVHEGLHNHHTTKSFSRTPGK
SEQ ID: 24
QVQLVQSGAEVKKPGASVKVSCKASGYKFTGFVMHWVRQAPGQGLEWMGFINPYNDDIQSNERFRGRVTMTRDTSISTAYMELSRLRSDDTAVYYCARGNGLMFDGAYRFFDFWGQGTMVTVSSGGGGSGGGGSGGGGSDIVMTQSPLSLPVTPGEPASISCRSSQRLVHSNGRTYLHWYLQKPGQSPRLLIYRVSNRFPGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCSQSTHVPYTFGQGTKLEIKRSGGGGSGGGGSGGGGSAGSDLGPQMLRELQETNAALQDVRELLRQQVREITFLKNTVMECDACGSGKKDPKSGGGGSYPYDVPDYA
Для изучения взаимодействия связывания 1:1 scFv к TRBC2, сенсорный чип серии S CM5 иммобилизовали посредством аминового связывания с антителом для захвата к Fc человека до плотности 9000-10000 ЕО при помощи прибора Biacore T200. В качестве рабочего буфера во всех условиях эксперимента использовали буфер HBS-P+. Исследуемое антитело к TRBC2 было захвачено в потоке 4 до плотности 200-250 ЕО. Рекомбинантный очищенный TRBC1 или TRBC2 в известных концентрациях использовали в качестве «исследуемого вещества» и вводили через соответствующие проточные кюветы при времени контакта 150 с и диссоциации в течение 300 с при скорости потока 30 мкл/мин. Проточную кювету 1 не подвергали модификации и использовали для вычитания эталонных значений. Сенсограмму «0 концентраций» только буфера использовали в качестве двойного вычитания эталонных значений к коэффициенту отклонения. Данные соответствовали модели связывания Ленгмюра 1:1. Поскольку использовали захватывающее устройство, для подбора данных в каждом случае использовали локальный параметр Rmax. Определяли скорость диссоциации и рассчитывали период полужизни по формуле: t½=ln2/kd.
Результаты, показанные на Фиг. 9A, продемонстрировали, что данная связывающая молекула scFv к TRBC2 имеет период полужизни 8 с. Аффинность связывания данной связывающей молекулы приведена в Таблице 1.
Для изучения поливалентного взаимодействия форматов антител scFv-Fc и scFv-COMP чип серии S CAP иммобилизовали захватывающим биотин реагентом до плотности 2500-5000 ЕО. Растворимые рекомбинантные биотинилированные TRBC1 и TRBC2 улавливали на проточных кюветах 3 в независимых экспериментальных циклах до плотности 90-110 ЕО. Очищенные антитела scFv-Fc или scFv-COMP к TRBC2 вводили в проточную кювету со временем контакта 150 с и диссоциацией в течение 300 с при скорости потока 30 мкл/мин. Биотинилированный белок в проточной кювете 1 не учитывали и использовали для вычитания эталонных значений. Сенсограмму «0 концентраций» только буфера использовалаи в качестве двойного вычитания эталонных значений к коэффициенту отклонения. Данные соответствовали модели связывания Ленгмюра 1:1. Поскольку использовалои захватывающее устройство, для подбора данных в каждом случае использовали локальный параметр Rmax. Определяли скорость диссоциации и рассчитывали период полужизни по формуле: t½=ln2/kd.
Результаты, показанные на Фиг. 9B и 9C, продемонстрировали, что периоды полужизни антител формата scFv-Fc и scFv-COMP составляют 16,2 с и 7,3 мин соответственно.
Таким образом, данные результаты демонстрируют, что мультимеризация улучшает связывание антител к TRBC2 с низкой аффинностью/высокой специфичностью.
Настоящая заявка испрашивает приоритет на основании заявки Соединенного Королевства № 1817822.8, поданной 31 октября 2018 г. Данная заявка полностью включена в настоящую заявку посредством ссылки.
Все публикации, процитированные в приведенном выше описании, включены в настоящую заявку посредством ссылки. Различные модификации и варианты описанных способов и систем согласно настоящему изобретению будут понятны специалистам в данной области без отклонения от объема и сущности настоящего изобретения. Несмотря на то, что настоящее изобретение было описано в связи с конкретными предпочтительными вариантами реализации, следует понимать, что заявленное изобретение не должно быть чрезмерно ограничено данными конкретными вариантами реализации. Безусловно, предполагается, что различные модификации описанных вариантов реализации настоящего изобретения, которые являются понятными для специалистов в области молекулярной биологии или близких к ней областях, должны входить в объем нижеприведенной формулы изобретения.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Autolus Limited
<120> Связывающий домен
<130> P116251PCT
<150> GB 1817822.8
<151> 2018-10-31
<160> 36
<170> PatentIn версии 3.5
<210> 1
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH (тяжелой цепи) домен hJOVI-1, гуманизированного
антитела JOVI-1
<400> 1
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Asn Pro Tyr Asn Asp Asp Ile Gln Ser Asn Glu Arg Phe
50 55 60
Arg Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Gly Tyr Asn Phe Asp Gly Ala Tyr Arg Phe Phe Asp
100 105 110
Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 2
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL (легкой цепи) домен hJOVI-1, гуманизированного антитела JOVI-1
<400> 2
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Arg Leu Val His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Arg Leu Leu Ile Tyr Arg Val Ser Asn Arg Phe Pro Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser
85 90 95
Thr His Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 3
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> сигнальный пептид
<400> 3
Met Gly Thr Ser Leu Leu Cys Trp Met Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Asp His Ala Asp Gly
20
<210> 4
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> сигнальный пептид, происходящий из IgG1
<400> 4
Met Ser Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro
20
<210> 5
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> сигнальный пептид, происходящий из CD8
<400> 5
Met Ala Val Pro Thr Gln Val Leu Gly Leu Leu Leu Leu Trp Leu Thr
1 5 10 15
Asp Ala Arg Cys
20
<210> 6
<211> 234
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> последовательность спейсера, шарнир-CH2CH3 IgG1 человека
<400> 6
Ala Glu Pro Lys Ser Pro Asp Lys Thr His Thr Cys Pro Pro Cys Pro
1 5 10 15
Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
20 25 30
Lys Asp Thr Leu Met Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val
35 40 45
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
50 55 60
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
65 70 75 80
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
85 90 95
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
100 105 110
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
115 120 125
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
130 135 140
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
145 150 155 160
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
165 170 175
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
180 185 190
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
195 200 205
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
210 215 220
Ser Leu Ser Leu Ser Pro Gly Lys Lys Asp
225 230
<210> 7
<211> 46
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> последовательность спейсера, стебель CD8 человека
<400> 7
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
1 5 10 15
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
20 25 30
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
35 40 45
<210> 8
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> последовательность спейсера, шарнир IgG1 человека
<400> 8
Ala Glu Pro Lys Ser Pro Asp Lys Thr His Thr Cys Pro Pro Cys Pro
1 5 10 15
Lys Asp Pro Lys
20
<210> 9
<211> 185
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> последовательность спейсера, эктодомен CD2
<400> 9
Lys Glu Ile Thr Asn Ala Leu Glu Thr Trp Gly Ala Leu Gly Gln Asp
1 5 10 15
Ile Asn Leu Asp Ile Pro Ser Phe Gln Met Ser Asp Asp Ile Asp Asp
20 25 30
Ile Lys Trp Glu Lys Thr Ser Asp Lys Lys Lys Ile Ala Gln Phe Arg
35 40 45
Lys Glu Lys Glu Thr Phe Lys Glu Lys Asp Thr Tyr Lys Leu Phe Lys
50 55 60
Asn Gly Thr Leu Lys Ile Lys His Leu Lys Thr Asp Asp Gln Asp Ile
65 70 75 80
Tyr Lys Val Ser Ile Tyr Asp Thr Lys Gly Lys Asn Val Leu Glu Lys
85 90 95
Ile Phe Asp Leu Lys Ile Gln Glu Arg Val Ser Lys Pro Lys Ile Ser
100 105 110
Trp Thr Cys Ile Asn Thr Thr Leu Thr Cys Glu Val Met Asn Gly Thr
115 120 125
Asp Pro Glu Leu Asn Leu Tyr Gln Asp Gly Lys His Leu Lys Leu Ser
130 135 140
Gln Arg Val Ile Thr His Lys Trp Thr Thr Ser Leu Ser Ala Lys Phe
145 150 155 160
Lys Cys Thr Ala Gly Asn Lys Val Ser Lys Glu Ser Ser Val Glu Pro
165 170 175
Val Ser Cys Pro Glu Lys Gly Leu Asp
180 185
<210> 10
<211> 259
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> последовательность спейсера, эктодомен CD34
<400> 10
Ser Leu Asp Asn Asn Gly Thr Ala Thr Pro Glu Leu Pro Thr Gln Gly
1 5 10 15
Thr Phe Ser Asn Val Ser Thr Asn Val Ser Tyr Gln Glu Thr Thr Thr
20 25 30
Pro Ser Thr Leu Gly Ser Thr Ser Leu His Pro Val Ser Gln His Gly
35 40 45
Asn Glu Ala Thr Thr Asn Ile Thr Glu Thr Thr Val Lys Phe Thr Ser
50 55 60
Thr Ser Val Ile Thr Ser Val Tyr Gly Asn Thr Asn Ser Ser Val Gln
65 70 75 80
Ser Gln Thr Ser Val Ile Ser Thr Val Phe Thr Thr Pro Ala Asn Val
85 90 95
Ser Thr Pro Glu Thr Thr Leu Lys Pro Ser Leu Ser Pro Gly Asn Val
100 105 110
Ser Asp Leu Ser Thr Thr Ser Thr Ser Leu Ala Thr Ser Pro Thr Lys
115 120 125
Pro Tyr Thr Ser Ser Ser Pro Ile Leu Ser Asp Ile Lys Ala Glu Ile
130 135 140
Lys Cys Ser Gly Ile Arg Glu Val Lys Leu Thr Gln Gly Ile Cys Leu
145 150 155 160
Glu Gln Asn Lys Thr Ser Ser Cys Ala Glu Phe Lys Lys Asp Arg Gly
165 170 175
Glu Gly Leu Ala Arg Val Leu Cys Gly Glu Glu Gln Ala Asp Ala Asp
180 185 190
Ala Gly Ala Gln Val Cys Ser Leu Leu Leu Ala Gln Ser Glu Val Arg
195 200 205
Pro Gln Cys Leu Leu Leu Val Leu Ala Asn Arg Thr Glu Ile Ser Ser
210 215 220
Lys Leu Gln Leu Met Lys Lys His Gln Ser Asp Leu Lys Lys Leu Gly
225 230 235 240
Ile Leu Asp Phe Thr Glu Gln Asp Val Ala Ser His Gln Ser Tyr Ser
245 250 255
Gln Lys Thr
<210> 11
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> трансмембранный домен CD8a
<400> 11
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
1 5 10 15
Ser Leu Val Ile Thr
20
<210> 12
<211> 24
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> трансмембранный домен TYRP-1
<400> 12
Ile Ile Ala Ile Ala Val Val Gly Ala Leu Leu Leu Val Ala Leu Ile
1 5 10 15
Phe Gly Thr Ala Ser Tyr Leu Ile
20
<210> 13
<211> 140
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> последовательность, содержащая трансмембранный домен CD28
и эндодомен CD3zeta
<400> 13
Phe Trp Val Leu Val Val Val Gly Gly Val Leu Ala Cys Tyr Ser Leu
1 5 10 15
Leu Val Thr Val Ala Phe Ile Ile Phe Trp Val Arg Arg Val Lys Phe
20 25 30
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
35 40 45
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
50 55 60
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
65 70 75 80
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
85 90 95
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
100 105 110
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
115 120 125
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
130 135 140
<210> 14
<211> 180
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> последовательность, содержащая трансмембранный домен
CD28 и эндодомены CD28 и CD3zeta
<400> 14
Phe Trp Val Leu Val Val Val Gly Gly Val Leu Ala Cys Tyr Ser Leu
1 5 10 15
Leu Val Thr Val Ala Phe Ile Ile Phe Trp Val Arg Ser Lys Arg Ser
20 25 30
Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr Pro Arg Arg Pro Gly
35 40 45
Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala
50 55 60
Ala Tyr Arg Ser Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala
65 70 75 80
Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg
85 90 95
Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu
100 105 110
Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn
115 120 125
Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met
130 135 140
Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly
145 150 155 160
Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala
165 170 175
Leu Pro Pro Arg
180
<210> 15
<211> 216
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> последовательность, содержащая трансмембранный домен CD28
и эндодомены CD28, OX40 и CD3zeta
<400> 15
Phe Trp Val Leu Val Val Val Gly Gly Val Leu Ala Cys Tyr Ser Leu
1 5 10 15
Leu Val Thr Val Ala Phe Ile Ile Phe Trp Val Arg Ser Lys Arg Ser
20 25 30
Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr Pro Arg Arg Pro Gly
35 40 45
Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala
50 55 60
Ala Tyr Arg Ser Arg Asp Gln Arg Leu Pro Pro Asp Ala His Lys Pro
65 70 75 80
Pro Gly Gly Gly Ser Phe Arg Thr Pro Ile Gln Glu Glu Gln Ala Asp
85 90 95
Ala His Ser Thr Leu Ala Lys Ile Arg Val Lys Phe Ser Arg Ser Ala
100 105 110
Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
115 120 125
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
130 135 140
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
145 150 155 160
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
165 170 175
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
180 185 190
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
195 200 205
His Met Gln Ala Leu Pro Pro Arg
210 215
<210> 16
<211> 136
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> последовательность, содержащая трансмембранный домен CD8a
и эндодомен CD3zeta
<400> 16
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
1 5 10 15
Ser Leu Val Ile Thr Arg Val Leu Tyr Cys Lys Phe Ser Arg Ser Ala
20 25 30
Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
35 40 45
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
50 55 60
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
65 70 75 80
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
85 90 95
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
100 105 110
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
115 120 125
His Met Gln Ala Leu Pro Pro Arg
130 135
<210> 17
<211> 178
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> последовательность, содержащая трансмембранный домен CD8a
и эндодомен 4-1BB и CD3zeta
<400> 17
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
1 5 10 15
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
20 25 30
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
35 40 45
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
50 55 60
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln
65 70 75 80
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
85 90 95
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
100 105 110
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
115 120 125
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
130 135 140
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
145 150 155 160
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
165 170 175
Pro Arg
<210> 18
<211> 178
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> последовательность, содержащая трансмембранный
домен TYRP-1 и эндодомены 4-1BB и CD3zeta
<400> 18
Ile Ile Ala Ile Ala Val Val Gly Ala Leu Leu Leu Val Ala Leu Ile
1 5 10 15
Phe Gly Thr Ala Ser Tyr Leu Ile Lys Arg Gly Arg Lys Lys Leu Leu
20 25 30
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
35 40 45
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
50 55 60
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln
65 70 75 80
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
85 90 95
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
100 105 110
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
115 120 125
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
130 135 140
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
145 150 155 160
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
165 170 175
Pro Arg
<210> 19
<211> 45
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> последовательность спейсера, COMP
<400> 19
Asp Leu Gly Pro Gln Met Leu Arg Glu Leu Gln Glu Thr Asn Ala Ala
1 5 10 15
Leu Gln Asp Val Arg Glu Leu Leu Arg Gln Gln Val Arg Glu Ile Thr
20 25 30
Phe Leu Lys Asn Thr Val Met Glu Cys Asp Ala Cys Gly
35 40 45
<210> 20
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> укороченный COMP, 5 C-концевых ак
<400> 20
Cys Asp Ala Cys Gly
1 5
<210> 21
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> укороченный COMP, 20 C-концевых ак
<400> 21
Gln Gln Val Arg Glu Ile Thr Phe Leu Lys Asn Thr Val Met Glu Cys
1 5 10 15
Asp Ala Cys Gly
20
<210> 22
<211> 252
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> одноцепочечный вариабельный фрагмент, scFv
<400> 22
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Gly Phe
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Asn Pro Tyr Asn Asp Asp Ile Gln Ser Asn Glu Arg Phe
50 55 60
Arg Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Gly Leu Met Phe Asp Gly Ala Tyr Arg Phe Phe Asp
100 105 110
Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr
130 135 140
Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser Ile
145 150 155 160
Ser Cys Arg Ser Ser Gln Arg Leu Val His Ser Asn Gly Arg Thr Tyr
165 170 175
Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Arg Leu Leu Ile
180 185 190
Tyr Arg Val Ser Asn Arg Phe Pro Gly Val Pro Asp Arg Phe Ser Gly
195 200 205
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
210 215 220
Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser Thr His Val Pro Tyr
225 230 235 240
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg
245 250
<210> 23
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> scFv-Fc
<400> 23
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Gly Phe
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Asn Pro Tyr Asn Asp Asp Ile Gln Ser Asn Glu Arg Phe
50 55 60
Arg Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Gly Leu Met Phe Asp Gly Ala Tyr Arg Phe Phe Asp
100 105 110
Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr
130 135 140
Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser Ile
145 150 155 160
Ser Cys Arg Ser Ser Gln Arg Leu Val His Ser Asn Gly Arg Thr Tyr
165 170 175
Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Arg Leu Leu Ile
180 185 190
Tyr Arg Val Ser Asn Arg Phe Pro Gly Val Pro Asp Arg Phe Ser Gly
195 200 205
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
210 215 220
Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser Thr His Val Pro Tyr
225 230 235 240
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Ser Asp Pro Arg
245 250 255
Gly Pro Thr Ile Lys Pro Cys Pro Pro Cys Lys Cys Pro Ala Pro Asn
260 265 270
Leu Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Ile Lys Asp
275 280 285
Val Leu Met Ile Ser Leu Ser Pro Ile Val Thr Cys Val Val Val Asp
290 295 300
Val Ser Glu Asp Asp Pro Asp Val Gln Ile Ser Trp Phe Val Asn Asn
305 310 315 320
Val Glu Val His Thr Ala Gln Thr Gln Thr His Arg Glu Asp Tyr Asn
325 330 335
Ser Thr Leu Arg Val Val Ser Ala Leu Pro Ile Gln His Gln Asp Trp
340 345 350
Met Ser Gly Lys Glu Phe Lys Cys Lys Val Asn Asn Lys Asp Leu Pro
355 360 365
Ala Pro Ile Glu Arg Thr Ile Ser Lys Pro Lys Gly Ser Val Arg Ala
370 375 380
Pro Gln Val Tyr Val Leu Pro Pro Pro Glu Glu Glu Met Thr Lys Lys
385 390 395 400
Gln Val Thr Leu Thr Cys Met Val Thr Asp Phe Met Pro Glu Asp Ile
405 410 415
Tyr Val Glu Trp Thr Asn Asn Gly Lys Thr Glu Leu Asn Tyr Lys Asn
420 425 430
Thr Glu Pro Val Leu Asp Ser Asp Gly Ser Tyr Phe Met Tyr Ser Lys
435 440 445
Leu Arg Val Glu Lys Lys Asn Trp Val Glu Arg Asn Ser Tyr Ser Cys
450 455 460
Ser Val Val His Glu Gly Leu His Asn His His Thr Thr Lys Ser Phe
465 470 475 480
Ser Arg Thr Pro Gly Lys
485
<210> 24
<211> 338
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> scFv-COMP
<400> 24
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Gly Phe
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Asn Pro Tyr Asn Asp Asp Ile Gln Ser Asn Glu Arg Phe
50 55 60
Arg Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Gly Leu Met Phe Asp Gly Ala Tyr Arg Phe Phe Asp
100 105 110
Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr
130 135 140
Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser Ile
145 150 155 160
Ser Cys Arg Ser Ser Gln Arg Leu Val His Ser Asn Gly Arg Thr Tyr
165 170 175
Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Arg Leu Leu Ile
180 185 190
Tyr Arg Val Ser Asn Arg Phe Pro Gly Val Pro Asp Arg Phe Ser Gly
195 200 205
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
210 215 220
Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser Thr His Val Pro Tyr
225 230 235 240
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Ser Gly Gly Gly
245 250 255
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ala Gly Ser Asp
260 265 270
Leu Gly Pro Gln Met Leu Arg Glu Leu Gln Glu Thr Asn Ala Ala Leu
275 280 285
Gln Asp Val Arg Glu Leu Leu Arg Gln Gln Val Arg Glu Ile Thr Phe
290 295 300
Leu Lys Asn Thr Val Met Glu Cys Asp Ala Cys Gly Ser Gly Lys Lys
305 310 315 320
Asp Pro Lys Ser Gly Gly Gly Gly Ser Tyr Pro Tyr Asp Val Pro Asp
325 330 335
Tyr Ala
<210> 25
<211> 454
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CAR, содержащий мутации T28K, Y32F, A100N в домене VH,
мутацию N35K в VL domain, спейсер-шарнир IgG1, трансмембранный
домен TYRP-1 , и эндодомены 4-1BB и CD3zeta
<400> 25
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Gly Phe
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Asn Pro Tyr Asn Asp Asp Ile Gln Ser Asn Glu Arg Phe
50 55 60
Arg Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Gly Tyr Asn Phe Asp Gly Ala Tyr Arg Phe Phe Asp
100 105 110
Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr
130 135 140
Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser Ile
145 150 155 160
Ser Cys Arg Ser Ser Gln Arg Leu Val His Ser Asn Gly Lys Thr Tyr
165 170 175
Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Arg Leu Leu Ile
180 185 190
Tyr Arg Val Ser Asn Arg Phe Pro Gly Val Pro Asp Arg Phe Ser Gly
195 200 205
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
210 215 220
Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser Thr His Val Pro Tyr
225 230 235 240
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Ser Asp Pro Ala
245 250 255
Glu Pro Lys Ser Pro Asp Lys Thr His Thr Cys Pro Pro Cys Pro Lys
260 265 270
Asp Pro Lys Ile Ile Ala Ile Ala Val Val Gly Ala Leu Leu Leu Val
275 280 285
Ala Leu Ile Phe Gly Thr Ala Ser Tyr Leu Ile Lys Arg Gly Arg Lys
290 295 300
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
305 310 315 320
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
325 330 335
Gly Gly Cys Glu Leu Arg Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
340 345 350
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
355 360 365
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
370 375 380
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
385 390 395 400
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
405 410 415
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
420 425 430
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
435 440 445
Gln Ala Leu Pro Pro Arg
450
<210> 26
<211> 454
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CAR, содержащий мутации T28K, Y32F, A100N в домене VH,
спейсер-шарнир IgG1, трансмембранный домен TYRP-1, и
эндодомены 4-1BB и CD3zeta
<400> 26
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Gly Phe
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Asn Pro Tyr Asn Asp Asp Ile Gln Ser Asn Glu Arg Phe
50 55 60
Arg Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Gly Tyr Asn Phe Asp Gly Ala Tyr Arg Phe Phe Asp
100 105 110
Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr
130 135 140
Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser Ile
145 150 155 160
Ser Cys Arg Ser Ser Gln Arg Leu Val His Ser Asn Gly Asn Thr Tyr
165 170 175
Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Arg Leu Leu Ile
180 185 190
Tyr Arg Val Ser Asn Arg Phe Pro Gly Val Pro Asp Arg Phe Ser Gly
195 200 205
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
210 215 220
Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser Thr His Val Pro Tyr
225 230 235 240
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Ser Asp Pro Ala
245 250 255
Glu Pro Lys Ser Pro Asp Lys Thr His Thr Cys Pro Pro Cys Pro Lys
260 265 270
Asp Pro Lys Ile Ile Ala Ile Ala Val Val Gly Ala Leu Leu Leu Val
275 280 285
Ala Leu Ile Phe Gly Thr Ala Ser Tyr Leu Ile Lys Arg Gly Arg Lys
290 295 300
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
305 310 315 320
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
325 330 335
Gly Gly Cys Glu Leu Arg Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
340 345 350
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
355 360 365
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
370 375 380
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
385 390 395 400
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
405 410 415
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
420 425 430
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
435 440 445
Gln Ala Leu Pro Pro Arg
450
<210> 27
<211> 454
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CAR, содержащий мутации T28K, Y32F, A100N, N103L в
домене VH, спейсер-шарнир IgG1, трансмембранный домен TYRP-1,
и эндодомены 4-1BB и CD3zeta
<400> 27
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Gly Phe
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Asn Pro Tyr Asn Asp Asp Ile Gln Ser Asn Glu Arg Phe
50 55 60
Arg Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Gly Tyr Leu Phe Asp Gly Ala Tyr Arg Phe Phe Asp
100 105 110
Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr
130 135 140
Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser Ile
145 150 155 160
Ser Cys Arg Ser Ser Gln Arg Leu Val His Ser Asn Gly Asn Thr Tyr
165 170 175
Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Arg Leu Leu Ile
180 185 190
Tyr Arg Val Ser Asn Arg Phe Pro Gly Val Pro Asp Arg Phe Ser Gly
195 200 205
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
210 215 220
Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser Thr His Val Pro Tyr
225 230 235 240
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Ser Asp Pro Ala
245 250 255
Glu Pro Lys Ser Pro Asp Lys Thr His Thr Cys Pro Pro Cys Pro Lys
260 265 270
Asp Pro Lys Ile Ile Ala Ile Ala Val Val Gly Ala Leu Leu Leu Val
275 280 285
Ala Leu Ile Phe Gly Thr Ala Ser Tyr Leu Ile Lys Arg Gly Arg Lys
290 295 300
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
305 310 315 320
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
325 330 335
Gly Gly Cys Glu Leu Arg Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
340 345 350
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
355 360 365
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
370 375 380
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
385 390 395 400
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
405 410 415
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
420 425 430
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
435 440 445
Gln Ala Leu Pro Pro Arg
450
<210> 28
<211> 454
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CAR, содержащий мутации T28K, Y32F, A100N, N103M в домене
VH,мутацию N35Y в домене VL, спейсер-шарнир IgG1, трансмембранный
домен TYRP-1, и эндодомены 4-1BB и CD3zeta
<400> 28
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Gly Phe
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Asn Pro Tyr Asn Asp Asp Ile Gln Ser Asn Glu Arg Phe
50 55 60
Arg Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Gly Tyr Met Phe Asp Gly Ala Tyr Arg Phe Phe Asp
100 105 110
Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr
130 135 140
Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser Ile
145 150 155 160
Ser Cys Arg Ser Ser Gln Arg Leu Val His Ser Asn Gly Tyr Thr Tyr
165 170 175
Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Arg Leu Leu Ile
180 185 190
Tyr Arg Val Ser Asn Arg Phe Pro Gly Val Pro Asp Arg Phe Ser Gly
195 200 205
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
210 215 220
Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser Thr His Val Pro Tyr
225 230 235 240
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Ser Asp Pro Ala
245 250 255
Glu Pro Lys Ser Pro Asp Lys Thr His Thr Cys Pro Pro Cys Pro Lys
260 265 270
Asp Pro Lys Ile Ile Ala Ile Ala Val Val Gly Ala Leu Leu Leu Val
275 280 285
Ala Leu Ile Phe Gly Thr Ala Ser Tyr Leu Ile Lys Arg Gly Arg Lys
290 295 300
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
305 310 315 320
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
325 330 335
Gly Gly Cys Glu Leu Arg Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
340 345 350
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
355 360 365
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
370 375 380
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
385 390 395 400
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
405 410 415
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
420 425 430
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
435 440 445
Gln Ala Leu Pro Pro Arg
450
<210> 29
<211> 454
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CAR, содержащий мутации T28K, Y32F, A100N, N103M в домене VH,
мутацию N35R в домене VL, спейсер-шарнир IgG1, трансмембранный
домен TYRP-1, и эндодомены 4-1BB и CD3zeta
<400> 29
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Gly Phe
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Asn Pro Tyr Asn Asp Asp Ile Gln Ser Asn Glu Arg Phe
50 55 60
Arg Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Gly Phe Met Phe Asp Gly Ala Tyr Arg Phe Phe Asp
100 105 110
Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr
130 135 140
Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser Ile
145 150 155 160
Ser Cys Arg Ser Ser Gln Arg Leu Val His Ser Asn Gly Arg Thr Tyr
165 170 175
Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Arg Leu Leu Ile
180 185 190
Tyr Arg Val Ser Asn Arg Phe Pro Gly Val Pro Asp Arg Phe Ser Gly
195 200 205
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
210 215 220
Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser Thr His Val Pro Tyr
225 230 235 240
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Ser Asp Pro Ala
245 250 255
Glu Pro Lys Ser Pro Asp Lys Thr His Thr Cys Pro Pro Cys Pro Lys
260 265 270
Asp Pro Lys Ile Ile Ala Ile Ala Val Val Gly Ala Leu Leu Leu Val
275 280 285
Ala Leu Ile Phe Gly Thr Ala Ser Tyr Leu Ile Lys Arg Gly Arg Lys
290 295 300
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
305 310 315 320
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
325 330 335
Gly Gly Cys Glu Leu Arg Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
340 345 350
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
355 360 365
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
370 375 380
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
385 390 395 400
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
405 410 415
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
420 425 430
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
435 440 445
Gln Ala Leu Pro Pro Arg
450
<210> 30
<211> 454
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CAR, содержащий мутации T28K, Y32F, A100N, Y102L, N103M
в домене VH, мутацию N35R в домене VL, спейсер-шарнир
IgG1, трансмембранный домен TYRP-1, и эндодомены 4-1BB и CD3zeta
<400> 30
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Gly Phe
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Asn Pro Tyr Asn Asp Asp Ile Gln Ser Asn Glu Arg Phe
50 55 60
Arg Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Gly Leu Met Phe Asp Gly Ala Tyr Arg Phe Phe Asp
100 105 110
Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr
130 135 140
Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser Ile
145 150 155 160
Ser Cys Arg Ser Ser Gln Arg Leu Val His Ser Asn Gly Arg Thr Tyr
165 170 175
Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Arg Leu Leu Ile
180 185 190
Tyr Arg Val Ser Asn Arg Phe Pro Gly Val Pro Asp Arg Phe Ser Gly
195 200 205
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
210 215 220
Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser Thr His Val Pro Tyr
225 230 235 240
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Ser Asp Pro Ala
245 250 255
Glu Pro Lys Ser Pro Asp Lys Thr His Thr Cys Pro Pro Cys Pro Lys
260 265 270
Asp Pro Lys Ile Ile Ala Ile Ala Val Val Gly Ala Leu Leu Leu Val
275 280 285
Ala Leu Ile Phe Gly Thr Ala Ser Tyr Leu Ile Lys Arg Gly Arg Lys
290 295 300
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
305 310 315 320
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
325 330 335
Gly Gly Cys Glu Leu Arg Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
340 345 350
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
355 360 365
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
370 375 380
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
385 390 395 400
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
405 410 415
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
420 425 430
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
435 440 445
Gln Ala Leu Pro Pro Arg
450
<210> 31
<211> 480
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CAR, содержащий мутации T28K, Y32F, A100N в домене VH,
спейсер-стебель CD8, трансмембранный домен TYRP-1, и
эндодомены 4-1BB и CD3zeta
<400> 31
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Gly Phe
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Asn Pro Tyr Asn Asp Asp Ile Gln Ser Asn Glu Arg Phe
50 55 60
Arg Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Gly Tyr Asn Phe Asp Gly Ala Tyr Arg Phe Phe Asp
100 105 110
Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr
130 135 140
Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser Ile
145 150 155 160
Ser Cys Arg Ser Ser Gln Arg Leu Val His Ser Asn Gly Asn Thr Tyr
165 170 175
Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Arg Leu Leu Ile
180 185 190
Tyr Arg Val Ser Asn Arg Phe Pro Gly Val Pro Asp Arg Phe Ser Gly
195 200 205
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
210 215 220
Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser Thr His Val Pro Tyr
225 230 235 240
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Ser Asp Pro Thr
245 250 255
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
260 265 270
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
275 280 285
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Ile Ile Ala
290 295 300
Ile Ala Val Val Gly Ala Leu Leu Leu Val Ala Leu Ile Phe Gly Thr
305 310 315 320
Ala Ser Tyr Leu Ile Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
325 330 335
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
340 345 350
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
355 360 365
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
370 375 380
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
385 390 395 400
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
405 410 415
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
420 425 430
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
435 440 445
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
450 455 460
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
465 470 475 480
<210> 32
<211> 479
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CAR, содержащий мутации T28K, Y32F, A100N в домене VH,
спейсер-стебель CD8, трансмембранный домен TYRP-1, и эндодомены
CD28 и CD3zeta
<400> 32
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Gly Phe
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Asn Pro Tyr Asn Asp Asp Ile Gln Ser Asn Glu Arg Phe
50 55 60
Arg Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Gly Tyr Asn Phe Asp Gly Ala Tyr Arg Phe Phe Asp
100 105 110
Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr
130 135 140
Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser Ile
145 150 155 160
Ser Cys Arg Ser Ser Gln Arg Leu Val His Ser Asn Gly Asn Thr Tyr
165 170 175
Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Arg Leu Leu Ile
180 185 190
Tyr Arg Val Ser Asn Arg Phe Pro Gly Val Pro Asp Arg Phe Ser Gly
195 200 205
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
210 215 220
Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser Thr His Val Pro Tyr
225 230 235 240
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Ser Asp Pro Thr
245 250 255
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
260 265 270
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
275 280 285
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Ile Ile Ala
290 295 300
Ile Ala Val Val Gly Ala Leu Leu Leu Val Ala Leu Ile Phe Gly Thr
305 310 315 320
Ala Ser Tyr Leu Ile Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp
325 330 335
Tyr Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr
340 345 350
Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Arg Arg
355 360 365
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
370 375 380
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
385 390 395 400
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
405 410 415
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
420 425 430
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
435 440 445
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
450 455 460
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
465 470 475
<210> 33
<211> 453
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CAR, содержащий мутации T28K, Y32F, A100N в домене VH,
спейсер-шарнир IgG1, трансмембранный домен TYRP-1, и
эндодомены CD28 и CD3zeta
<400> 33
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Gly Phe
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Asn Pro Tyr Asn Asp Asp Ile Gln Ser Asn Glu Arg Phe
50 55 60
Arg Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Gly Tyr Asn Phe Asp Gly Ala Tyr Arg Phe Phe Asp
100 105 110
Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr
130 135 140
Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser Ile
145 150 155 160
Ser Cys Arg Ser Ser Gln Arg Leu Val His Ser Asn Gly Asn Thr Tyr
165 170 175
Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Arg Leu Leu Ile
180 185 190
Tyr Arg Val Ser Asn Arg Phe Pro Gly Val Pro Asp Arg Phe Ser Gly
195 200 205
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
210 215 220
Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser Thr His Val Pro Tyr
225 230 235 240
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Ser Asp Pro Ala
245 250 255
Glu Pro Lys Ser Pro Asp Lys Thr His Thr Cys Pro Pro Cys Pro Lys
260 265 270
Asp Pro Lys Ile Ile Ala Ile Ala Val Val Gly Ala Leu Leu Leu Val
275 280 285
Ala Leu Ile Phe Gly Thr Ala Ser Tyr Leu Ile Arg Ser Lys Arg Ser
290 295 300
Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr Pro Arg Arg Pro Gly
305 310 315 320
Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala
325 330 335
Ala Tyr Arg Ser Arg Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
340 345 350
Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
355 360 365
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
370 375 380
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
385 390 395 400
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
405 410 415
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
420 425 430
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
435 440 445
Ala Leu Pro Pro Arg
450
<210> 34
<211> 453
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CAR, содержащий мутации T28K, Y32F, A100N в домене VH, мутацию N35K
в домене VL, спейсер-шарнир IgG1, трансмембранный домен
TYRP-1, и эндодомены CD28 и CD3zeta
<400> 34
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Gly Phe
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Asn Pro Tyr Asn Asp Asp Ile Gln Ser Asn Glu Arg Phe
50 55 60
Arg Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Gly Tyr Asn Phe Asp Gly Ala Tyr Arg Phe Phe Asp
100 105 110
Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr
130 135 140
Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser Ile
145 150 155 160
Ser Cys Arg Ser Ser Gln Arg Leu Val His Ser Asn Gly Lys Thr Tyr
165 170 175
Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Arg Leu Leu Ile
180 185 190
Tyr Arg Val Ser Asn Arg Phe Pro Gly Val Pro Asp Arg Phe Ser Gly
195 200 205
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
210 215 220
Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser Thr His Val Pro Tyr
225 230 235 240
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Ser Asp Pro Ala
245 250 255
Glu Pro Lys Ser Pro Asp Lys Thr His Thr Cys Pro Pro Cys Pro Lys
260 265 270
Asp Pro Lys Ile Ile Ala Ile Ala Val Val Gly Ala Leu Leu Leu Val
275 280 285
Ala Leu Ile Phe Gly Thr Ala Ser Tyr Leu Ile Arg Ser Lys Arg Ser
290 295 300
Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr Pro Arg Arg Pro Gly
305 310 315 320
Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala
325 330 335
Ala Tyr Arg Ser Arg Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
340 345 350
Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
355 360 365
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
370 375 380
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
385 390 395 400
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
405 410 415
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
420 425 430
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
435 440 445
Ala Leu Pro Pro Arg
450
<210> 35
<211> 480
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CAR, содержащий мутации T28K, Y32F, A100N в домене VH,
мутацию N35K в домене VL, спейсер-стебель CD8, трансмембранный
домен TYRP-1, и эндодомены 4-1BB и CD3zeta
<400> 35
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Gly Phe
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Asn Pro Tyr Asn Asp Asp Ile Gln Ser Asn Glu Arg Phe
50 55 60
Arg Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Gly Tyr Asn Phe Asp Gly Ala Tyr Arg Phe Phe Asp
100 105 110
Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr
130 135 140
Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser Ile
145 150 155 160
Ser Cys Arg Ser Ser Gln Arg Leu Val His Ser Asn Gly Lys Thr Tyr
165 170 175
Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Arg Leu Leu Ile
180 185 190
Tyr Arg Val Ser Asn Arg Phe Pro Gly Val Pro Asp Arg Phe Ser Gly
195 200 205
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
210 215 220
Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser Thr His Val Pro Tyr
225 230 235 240
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Ser Asp Pro Thr
245 250 255
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
260 265 270
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
275 280 285
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Ile Ile Ala
290 295 300
Ile Ala Val Val Gly Ala Leu Leu Leu Val Ala Leu Ile Phe Gly Thr
305 310 315 320
Ala Ser Tyr Leu Ile Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
325 330 335
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
340 345 350
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
355 360 365
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
370 375 380
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
385 390 395 400
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
405 410 415
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
420 425 430
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
435 440 445
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
450 455 460
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
465 470 475 480
<210> 36
<211> 479
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CAR, содержащий мутации T28K, Y32F, A100N в домене VH, мутацию
N35K в домене VL, спейсер-стебель CD8, трансмембранный домен TYRP-1,
и эндодомены CD28 и CD3zeta
<400> 36
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Lys Phe Thr Gly Phe
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Asn Pro Tyr Asn Asp Asp Ile Gln Ser Asn Glu Arg Phe
50 55 60
Arg Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Gly Tyr Asn Phe Asp Gly Ala Tyr Arg Phe Phe Asp
100 105 110
Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr
130 135 140
Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser Ile
145 150 155 160
Ser Cys Arg Ser Ser Gln Arg Leu Val His Ser Asn Gly Lys Thr Tyr
165 170 175
Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Arg Leu Leu Ile
180 185 190
Tyr Arg Val Ser Asn Arg Phe Pro Gly Val Pro Asp Arg Phe Ser Gly
195 200 205
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
210 215 220
Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser Thr His Val Pro Tyr
225 230 235 240
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Ser Asp Pro Thr
245 250 255
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
260 265 270
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
275 280 285
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Ile Ile Ala
290 295 300
Ile Ala Val Val Gly Ala Leu Leu Leu Val Ala Leu Ile Phe Gly Thr
305 310 315 320
Ala Ser Tyr Leu Ile Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp
325 330 335
Tyr Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr
340 345 350
Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Arg Arg
355 360 365
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
370 375 380
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
385 390 395 400
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
405 410 415
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
420 425 430
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
435 440 445
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
450 455 460
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
465 470 475
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР (CAR) С АНТИГЕНСВЯЗЫВАЮЩИМИ ДОМЕНАМИ К КОНСТАНТНОЙ ОБЛАСТИ β Т-КЛЕТОЧНОГО РЕЦЕПТОРА | 2015 |
|
RU2830064C2 |
| ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР (CAR) С АНТИГЕНСВЯЗЫВАЮЩИМИ ДОМЕНАМИ К КОНСТАНТНОЙ ОБЛАСТИ β Т-КЛЕТОЧНОГО РЕЦЕПТОРА | 2015 |
|
RU2744046C2 |
| АНТИГЕНСВЯЗЫВАЮЩИЕ ДОМЕНЫ ПРОТИВ TRBC1 | 2018 |
|
RU2791327C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, НАЦЕЛЕННЫЕ НА FLT3 | 2018 |
|
RU2820859C2 |
| CD3-СПЕЦИФИЧЕСКИЕ СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2020 |
|
RU2826453C2 |
| Т-КЛЕТКИ С ДВУМЯ ХИМЕРНЫМИ АНТИГЕННЫМИ РЕЦЕПТОРАМИ CAR | 2021 |
|
RU2839662C1 |
| KIR3DL3 - ИНГИБИРУЮЩИЙ РЕЦЕПТОР ИММУННОЙ СИСТЕМЫ И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2827900C1 |
| АНТИТЕЛА, СПЕЦИФИЧНЫЕ К FLT3, И ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2758513C2 |
| КЛЕТКА | 2015 |
|
RU2768019C2 |
| АНТИ-ROR1/АНТИ-CD3 БИСПЕЦИФИЧЕСКИЕ СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2020 |
|
RU2831608C2 |
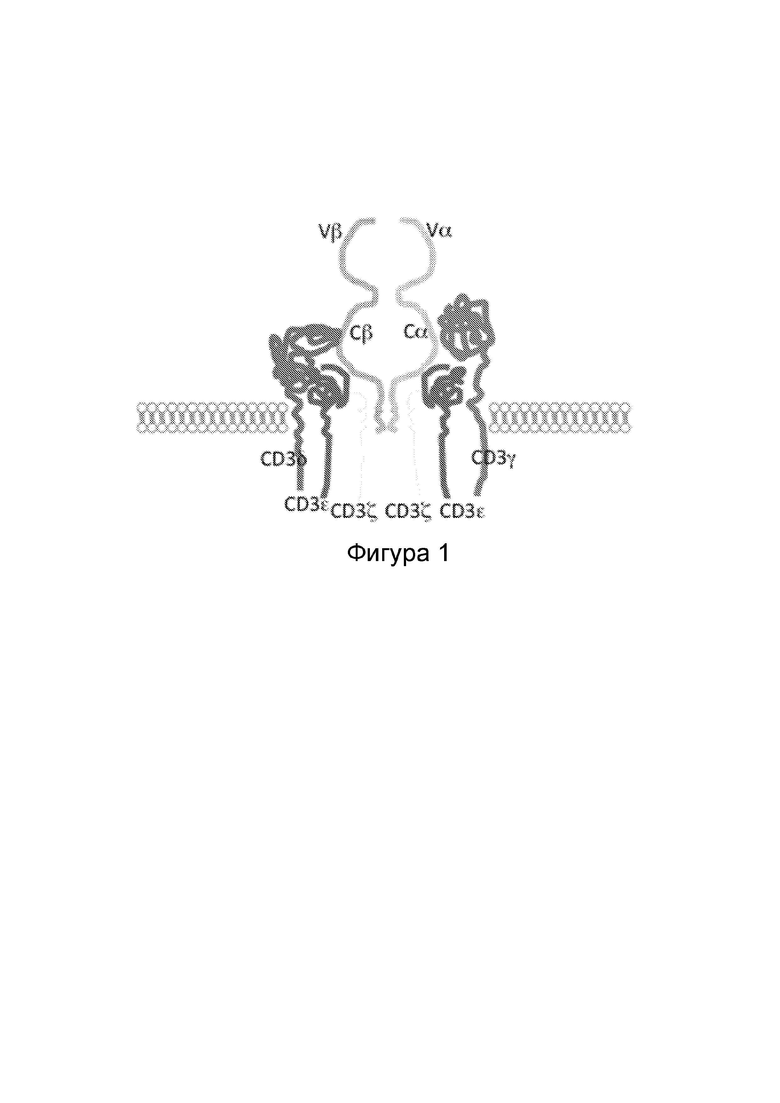
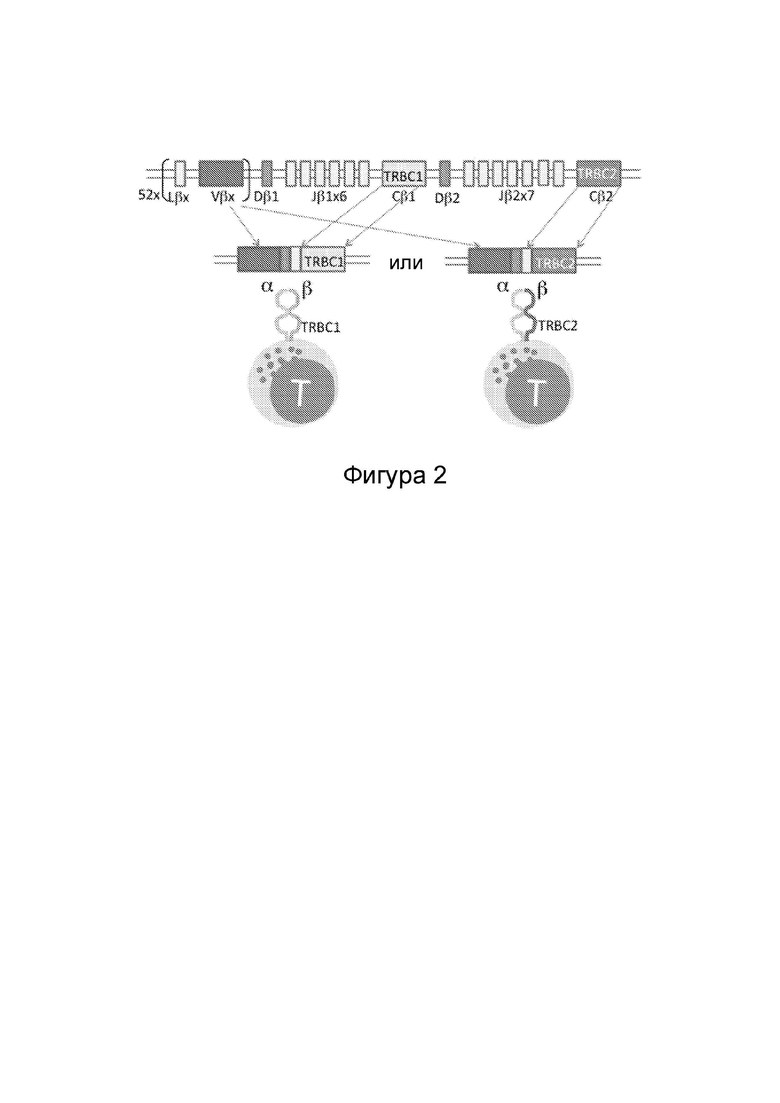
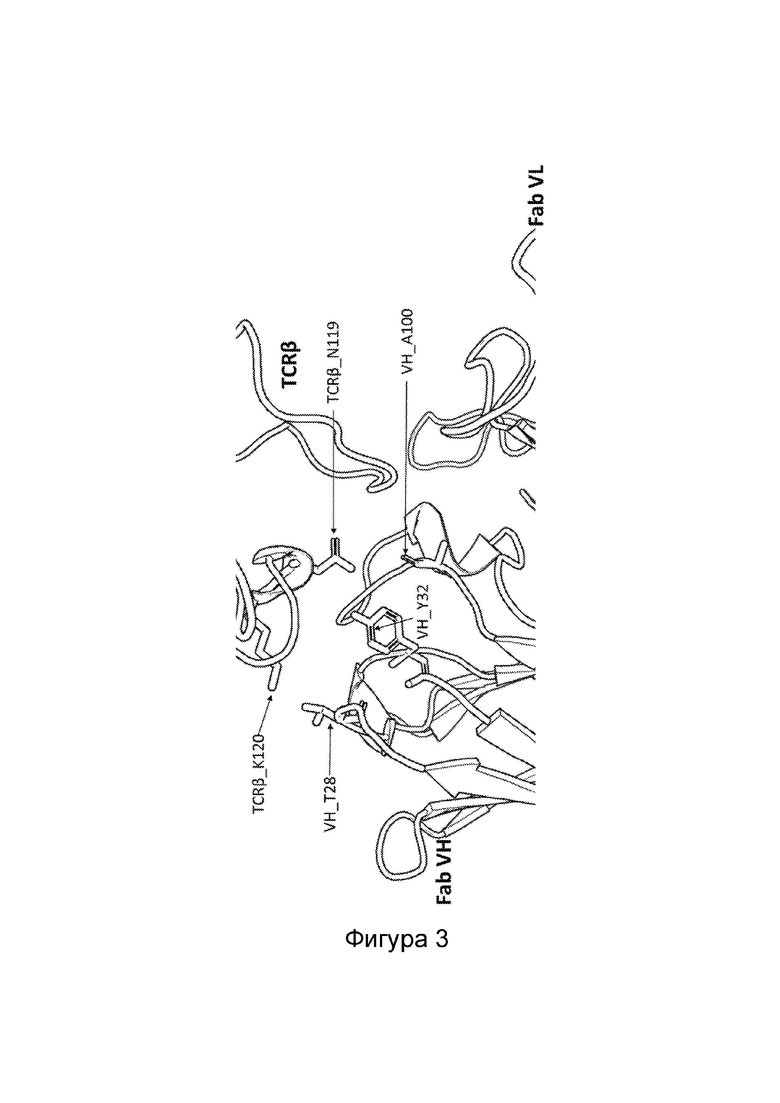
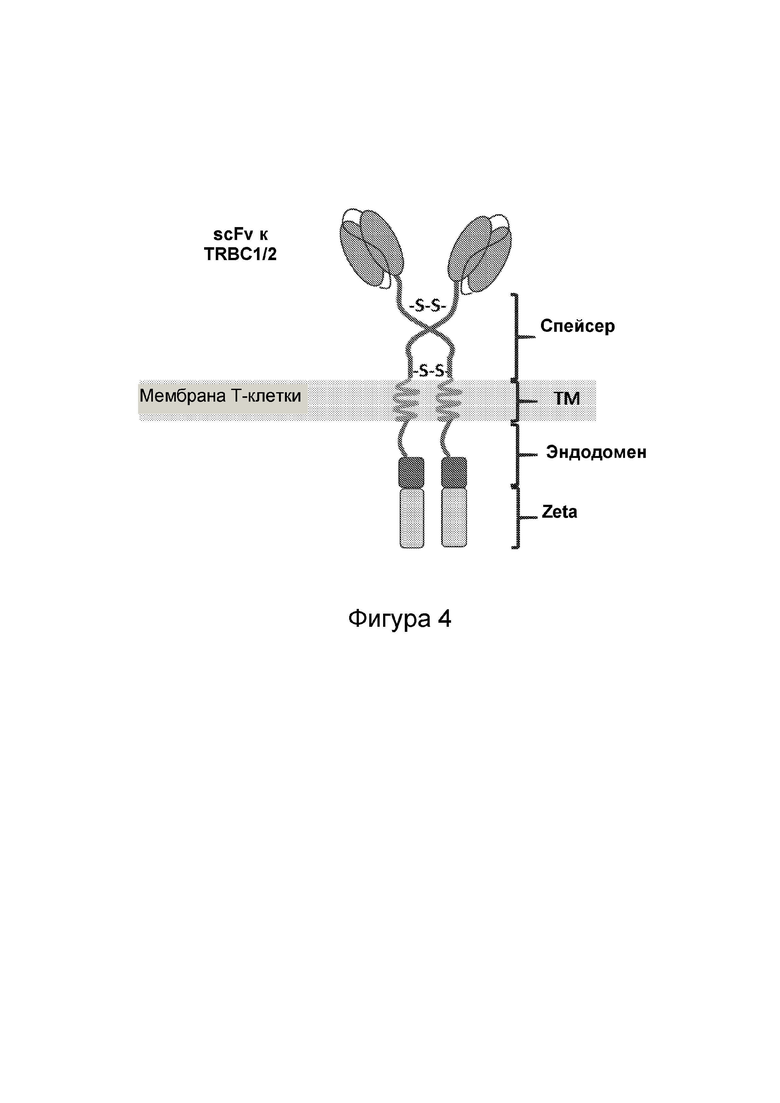
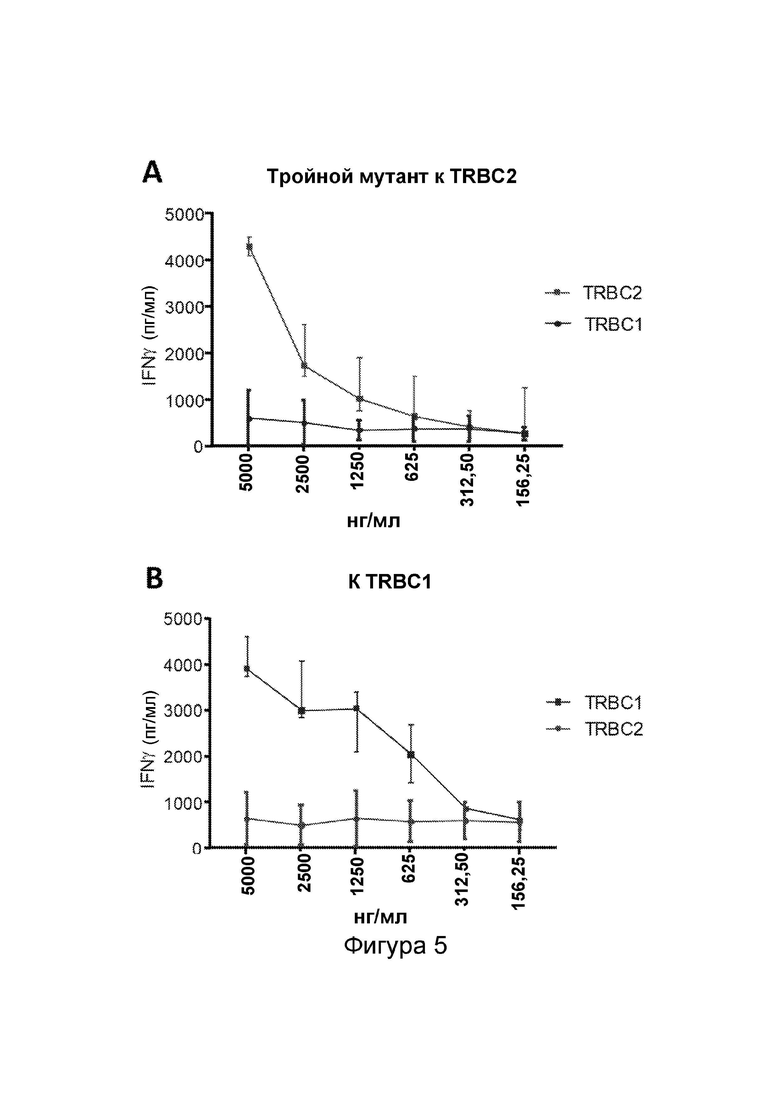
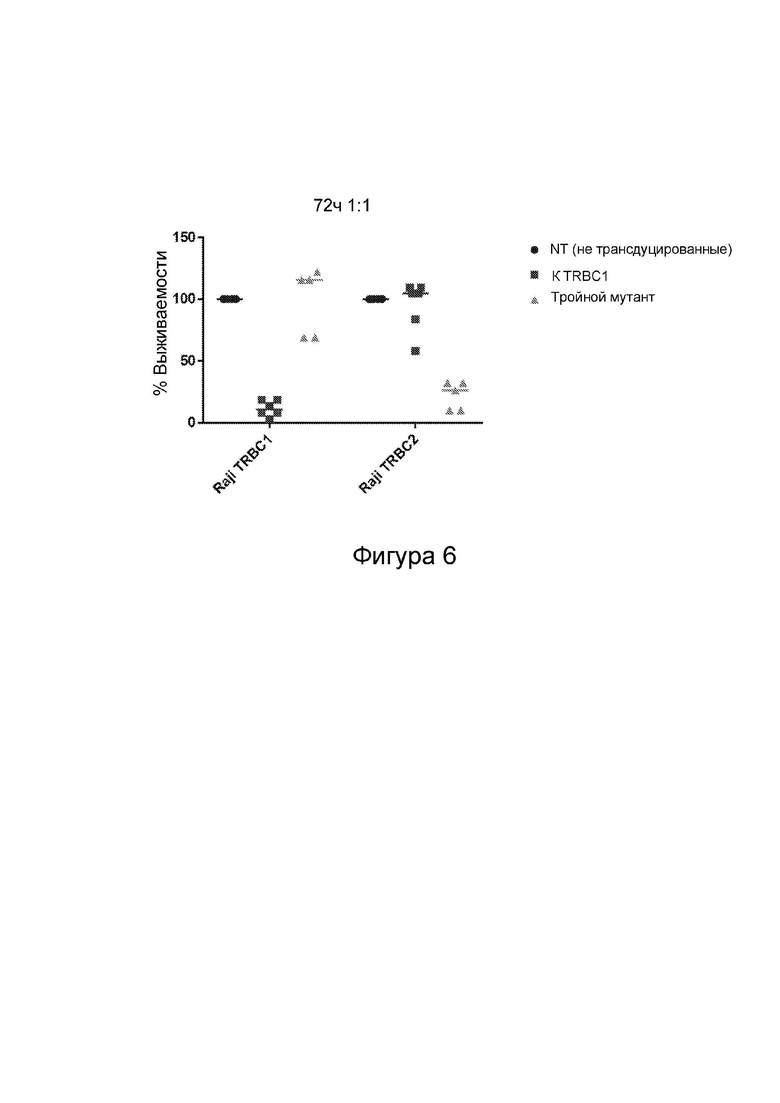
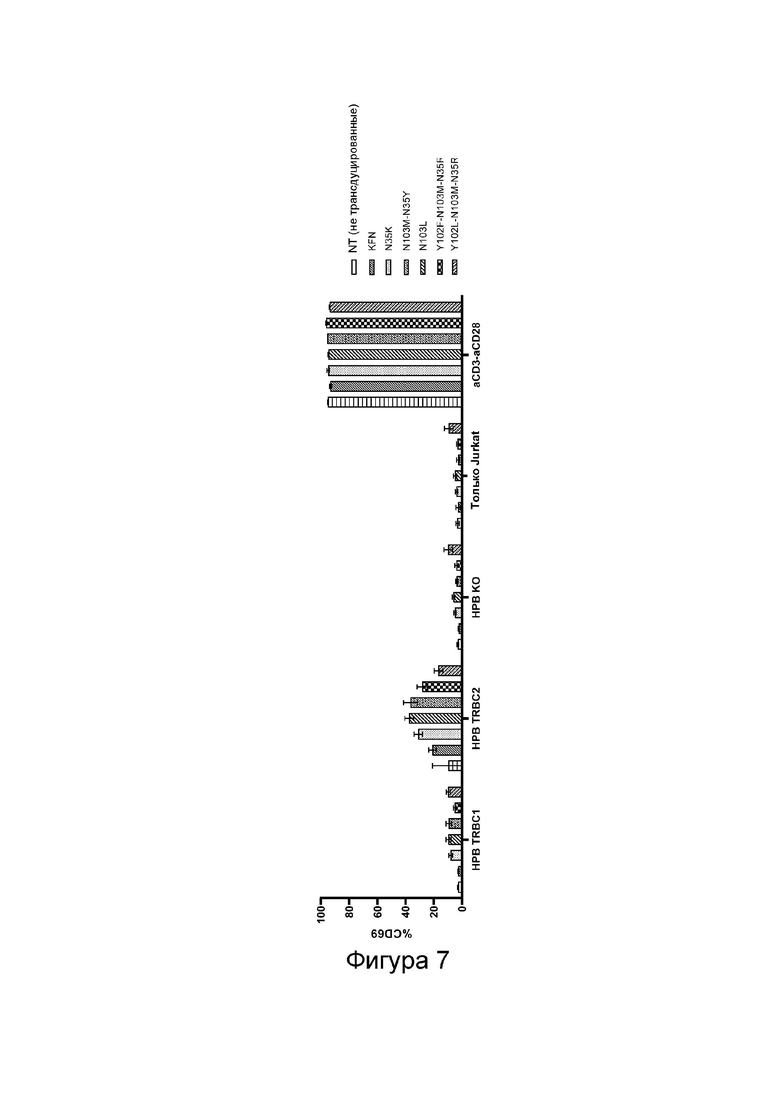
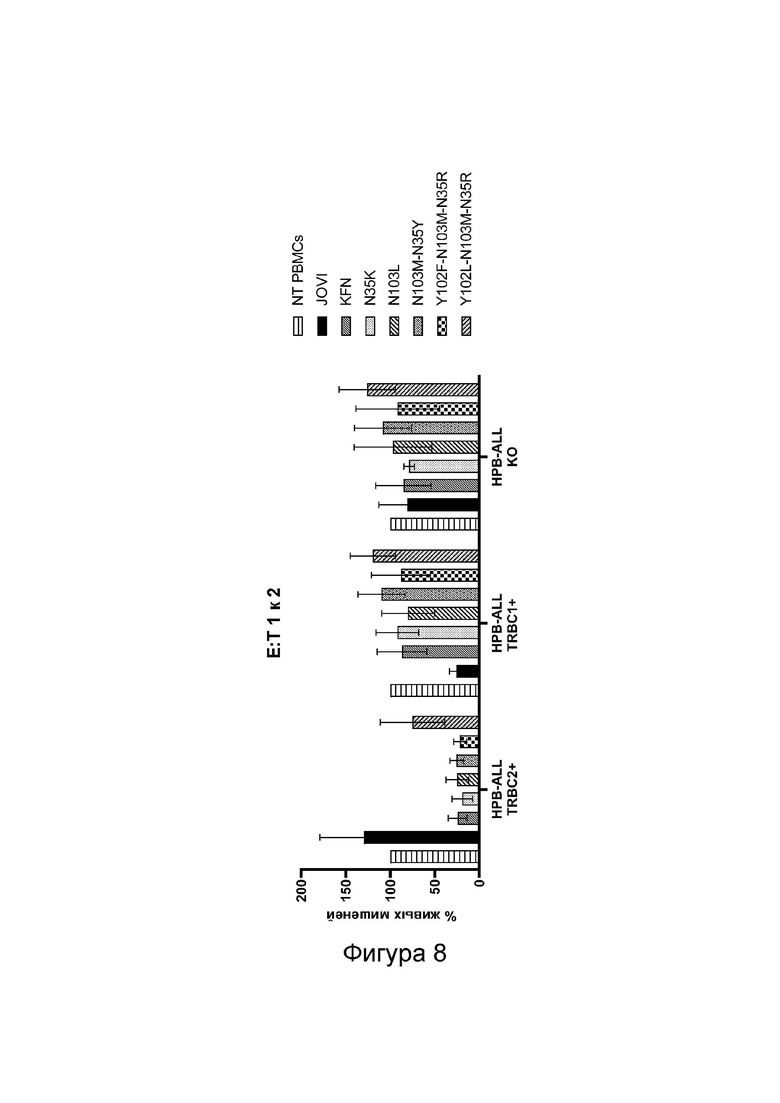
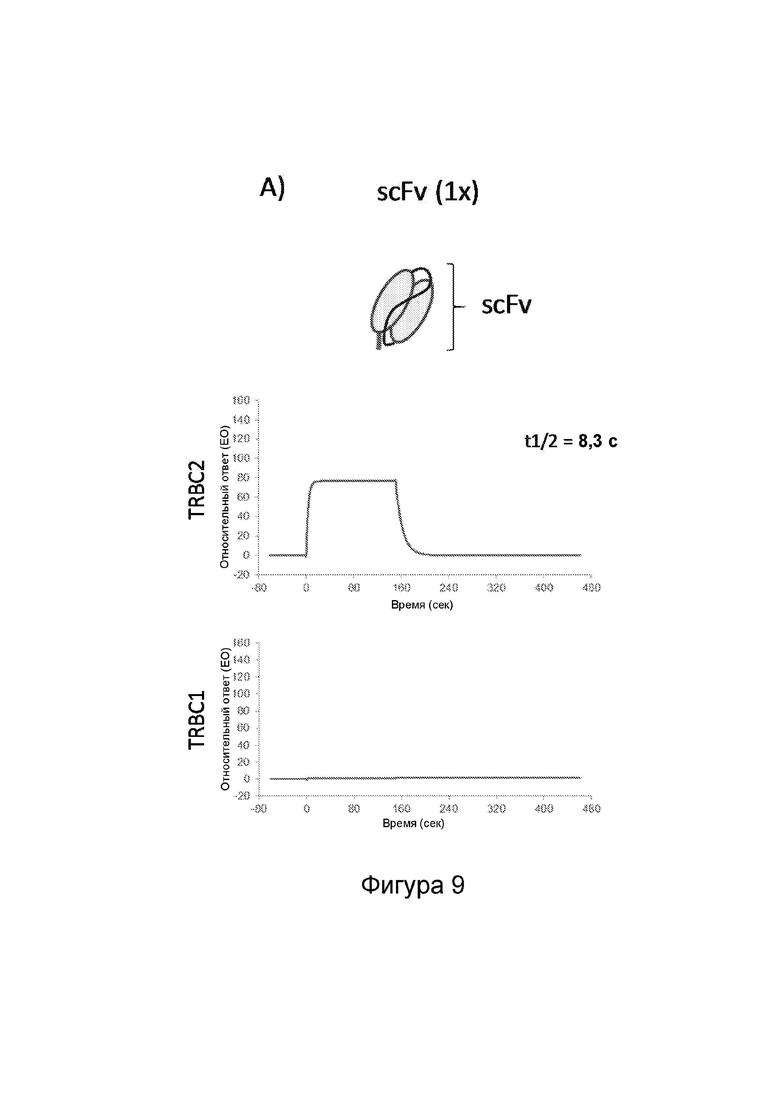
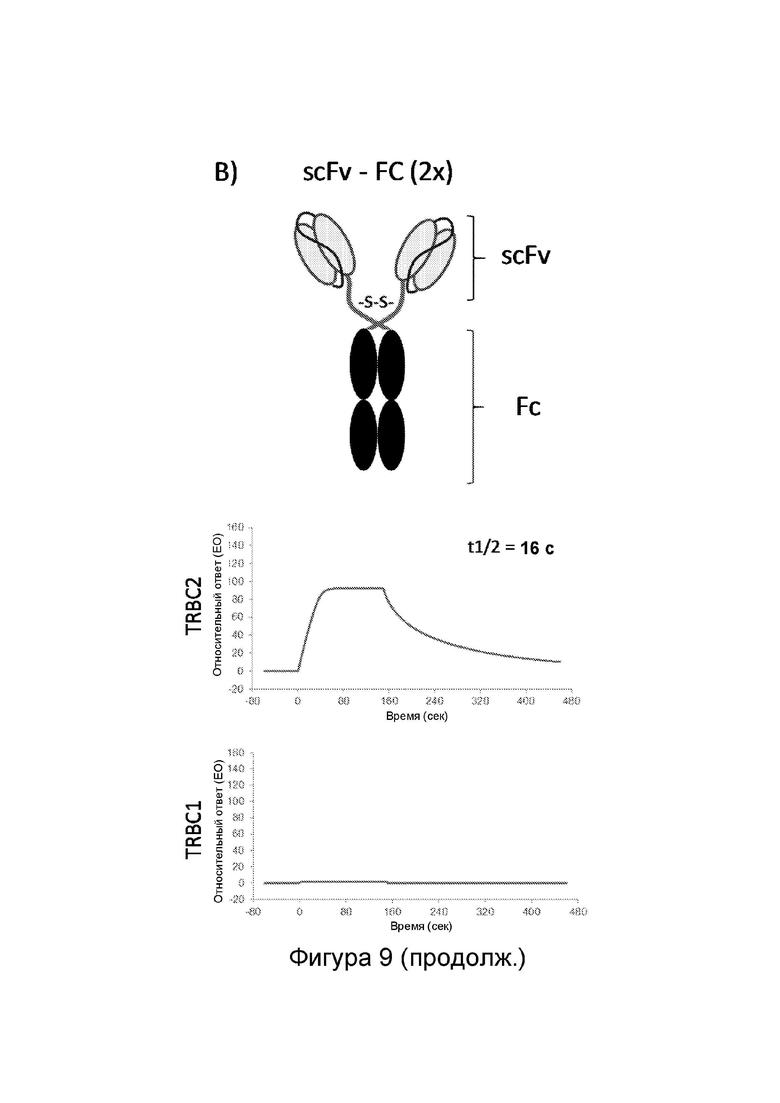
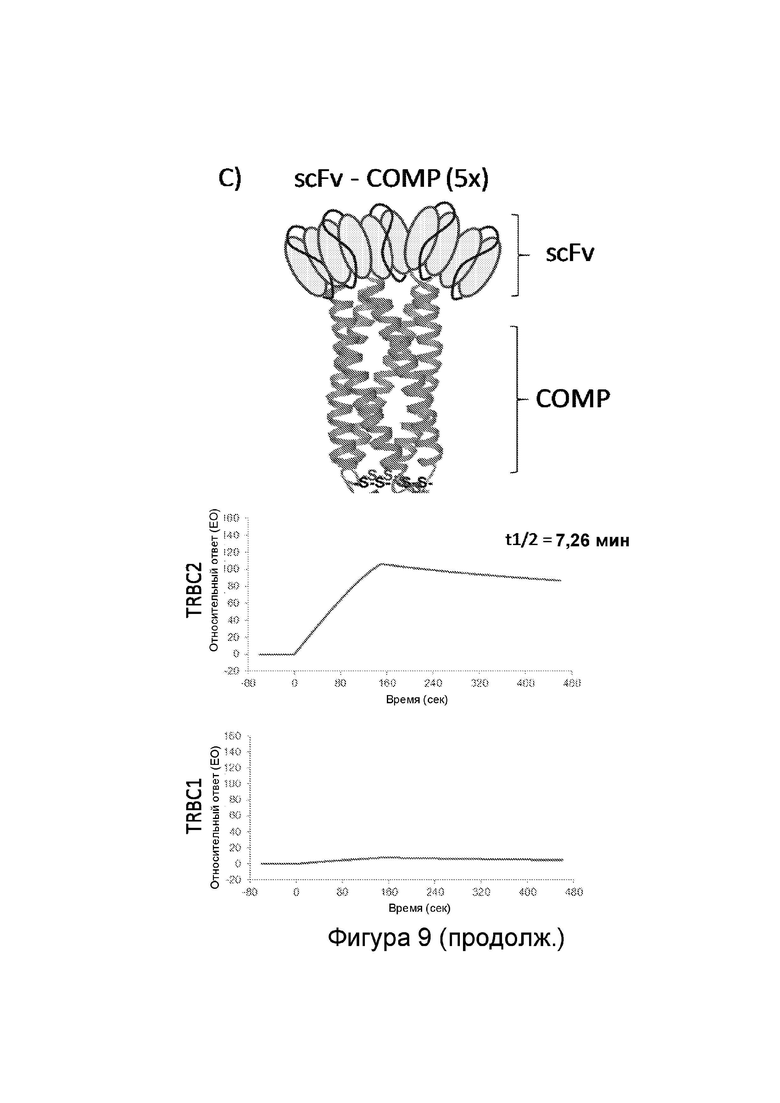
Группа изобретений относится к биотехнологии. Предложен вариантный антигенсвязывающий домен, который содержит по меньшей мере одну мутацию в домене VH по сравнению с эталонным антителом и который проявляет увеличенную аффинность к TRBC2 по сравнению с указанным эталонным антителом. Также предложено антитело, химерный антигенный рецептор (CAR) и биспецифичный активатор Т-клеток (BiTE), клетка, которая содержит указанный CAR, и конъюгат, содержащие указанный вариантный антигенсвязывающий домен или указанное антитело. Кроме того, предложены варианты применения в медицине, способы диагностики и способы персонализированной медицины, в которых применяют продукты согласно настоящему изобретению. Группа изобретений может быть использована для лечения Т-клеточного злокачественного новообразования, выбранного из Т-клеточных лимфомы или лейкоза у субъекта. 19 н. и 23 з.п. ф-лы, 1 табл., 9 ил., 6 пр.
1. Вариантный антигенсвязывающий домен, который содержит домен VH с последовательностью согласно SEQ ID NO: 1 с мутациями Y32F и A100N и одной дополнительной мутацией, выбранной из T28K, T28R или G31R, в указанном домене VH, и домен VL с последовательностью согласно SEQ ID NO: 2, и при этом указанный вариантный антигенсвязывающий домен содержит по меньшей мере три мутации в домене VH и/или VL и демонстрирует увеличенную аффинность к TRBC2 по сравнению с эталонным антителом, которое имеет домен VH с последовательностью согласно SEQ ID NO: 1 и домен VL с последовательностью согласно SEQ ID NO: 2.
2. Вариантный антигенсвязывающий домен по п. 1, который содержит мутации T28K, Y32F и A100N, дополнительно содержащий по меньшей мере одну мутацию в положении, выбранном из группы, состоящей из V2, Y27, G31, R98, Y102, N103 и A107 в домене VH, N35 в домене VL и R55 в домене VL.
3. Вариантный антигенсвязывающий домен по п. 2, в котором указанная по меньшей мере одна дополнительная мутация выбрана из следующих:
а) в домене VH:
- V2К, V2R,
- Y27F, Y27M, Y27N, Y27W,
- G31К, G31R, G31S,
- R98K,
- Y102F, Y102L,
- N103A, N103E, N103F, N103H, N103L, N103M, N103Q, N103S, N103W, N103Y,
- А107S,
и
b) в домене VL:
- N35M, N35F, N35Y, N35K, N35R и
- R55K.
4. Вариантный антигенсвязывающий домен по п. 3, который выбран из вариантных антигенсвязывающих доменов, содержащих следующие комбинации мутаций:
- T28K, Y32F, A100N в домене VH и N35K в домене VL,
- T28K, Y32F, A100N в домене VH,
- T28K, Y32F, A100N, Y27N в домене VH,
- T28K, Y32F, A100N, G31K в домене VH,
- T28K, Y32F, A100N, Y27M в домене VH,
- T28K, Y32F, A100N, Y27W в домене VH,
- T28K, Y32F, A100N в домене VH и R55K в домене VL,
- T28K, Y32F, A100N, N103H в домене VH,
- T28K, Y32F, A100N, N103A в домене VH,
- T28K, Y32F, A100N, N103Y в домене VH,
- T28K, Y32F, A100N в домене VH и N35R в домене VL,
- T28K, Y32F, A100N, N103S в домене VH и N35M в домене VL,
- T28K, Y32F, A100N, N103M в домене VH,
- T28K, Y32F, A100N, N103W в домене VH и N35R в домене VL,
- T28K, Y32F, A100N в домене VH и N35F в домене VL,
- T28K, Y32F, A100N, N103S в домене VH и N35K в домене VL,
- T28K, Y32F, A100N, R98K в домене VH,
- T28K, Y32F, A100N, N103S в домене VH и N35R в домене VL,
- T28K, Y32F, A100N, N103L в домене VH,
- T28K, Y32F, A100N, N103S в домене VH и N35F в домене VL,
- T28K, Y32F, A100N, N103S в домене VH и N35Y в домене VL,
- T28K, Y32F, A100N, N103L в домене VH и N35M в домене VL,
- T28K, Y32F, A100N, N103L в домене VH и N35R в домене VL,
- T28K, Y32F, A100N, N103W в домене VH и N35K в домене VL,
- T28K, Y32F, A100N, N103L в домене VH и N35Y в домене VL,
- T28K, Y32F, A100N, N103F в домене VH,
- T28K, Y32F, A100N, N103W в домене VH,
- T28K, Y32F, A100N, N103L в домене VH и N35K в домене VL,
- T28K, Y32F, A100N, N103L в домене VH и N35F в домене VL,
- T28K, Y32F, A100N, N103W в домене VH и N35M в домене VL,
- T28K, Y32F, A100N, N103F в домене VH и N35Y в домене VL,
- T28K, Y32F, A100N, Y27F в домене VH,
- T28K, Y32F, A100N, N103Q в домене VH,
- T28K, Y32F, A100N, N103S в домене VH,
- T28K, Y32F, A100N, N103M в домене VH и N35F в домене VL,
- T28K, Y32F, A100N, N103F в домене VH и N35M в домене VL,
- T28K, Y32F, A100N, N103F в домене VH и N35F в домене VL,
- T28K, Y32F, A100N, G31R в домене VH,
- T28K, Y32F, A100N, N103W в домене VH и N35F в домене VL,
- T28K, Y32F, A100N, V2R в домене VH,
- T28K, Y32F, A100N, G31S в домене VH,
- T28K, Y32F, A100N, A107S в домене VH,
- T28K, Y32F, A100N, N103E в домене VH и N35M в домене VL,
- T28K, Y32F, A100N, V2K в домене VH,
- T28K, Y32F, A100N, N103E в домене VH,
- T28K, Y32F, A100N, Y102F, N103M в домене VH и N35K в домене VL,
- T28K, Y32F, A100N, Y102F, N103M в домене VH и N35F в домене VL,
- T28K, Y32F, A100N, Y102F, N103M в домене VH и N35R в домене VL,
- T28K, Y32F, A100N, Y102F в домене VH и N35R в домене VL,
- T28K, Y32F, A100N, N103M в домене VH и N35M в домене VL,
- T28K, Y32F, A100N, N103M в домене VH и N35Y в домене VL,
- T28K, Y32F, A100N, N103M в домене VH и N35R в домене VL,
- T28K, Y32F, A100N, N103F в домене VH и N35K в домене VL,
- T28K, Y32F, A100N, Y102L, N103W в домене VH и N35R в домене VL,
- T28K, Y32F, A100N, Y102L, N103W в домене VH и N35K в домене VL,
- T28K, Y32F, A100N, Y102F в домене VH и
- T28K, Y32F, A100N, Y102L, N103M в домене VH и N35R в домене VL.
5. Вариантный антигенсвязывающий домен по п. 4, который содержит мутации T28K, Y32F и A100N в домене VH и мутацию N35K в домене VL.
6. Вариантный антигенсвязывающий домен по п. 4, который содержит мутации T28K, Y32F и A100N в домене VH.
7. Вариантный антигенсвязывающий домен по любому из пп. 1-6, который дополнительно содержит домен олигомеризации.
8. Антитело, которое специфично связывается с TRBC2, содержащее вариантный антигенсвязывающий домен по любому из пп. 1-6.
9. Химерный антигенный рецептор (CAR), который специфично связывается с TRBC2, содержащий вариантный антигенсвязывающий домен по любому из пп. 1-7, спейсер, трансмембранный домен и эндодомен.
10. Биспецифичный активатор Т-клеток (BiTE), который специфично связывается с TRBC2, содержащий вариантный антигенсвязывающий домен по любому из пп. 1-7 и домен активации Т-клеток.
11. Молекула нуклеиновой кислоты, кодирующая вариантный антигенсвязывающий домен по любому из пп. 1-7.
12. Молекула нуклеиновой кислоты, кодирующая CAR по п. 9.
13. Вектор, который обеспечивает экспрессию молекулы нуклеиновой кислоты по п. 12, содержащий молекулу нуклеиновой кислоты по п. 12.
14. Цитолитическая клетка для устранения клеток, которые экспрессируют TRBC2, которая содержит CAR по п. 9.
15. Способ получения клетки по п. 14, который включает этап трансдукции или трансфекции клетки вектором по п. 13, который содержит последовательность нуклеиновой кислоты, кодирующую CAR.
16. Конъюгат для применения при лечении Т-клеточного злокачественного новообразования, выбранного из Т-клеточных лимфомы или лейкоза, содержащий вариантный антигенсвязывающий домен по любому из пп. 1-7 или антитело по п. 8 и детектируемый компонент или химиотерапевтический компонент.
17. Конъюгат по п. 16, который содержит химиотерапевтический компонент.
18. Способ лечения Т-клеточного злокачественного новообразования, выбранного из Т-клеточных лимфомы или лейкоза у субъекта, включающий этап введения субъекту клетки по п. 14, или антитела по п. 8, или BiTE по п. 10, или конъюгата по п. 16 или 17, при этом злокачественные Т-клетки экспрессируют TRBC2.
19. Способ по п. 18, отличающийся тем, что указанные Т-клеточные лимфома или лейкоз выбраны из неспецифицированной периферической Т-клеточной лимфомы (ПТКЛн), ангиоиммунобластной Т-клеточной лимфомы (АИТЛ), анапластической крупноклеточной лимфомы (АККЛ), Т-клеточной лимфомы, ассоциированной с энтеропатией (EATL), гепатолиенальной Т-клеточной лимфомы (ГЛТЛ), экстранодальной NK/T-клеточной лимфомы назального типа, Т-клеточной лимфомы кожи, первичной АККЛ кожи, Т-клеточного пролимфоцитарного лейкоза и Т-клеточного острого лимфобластного лейкоза.
20. Применение клетки по п. 14 для устранения клеток, которые экспрессируют TRBC2.
21. Применение по п. 20, отличающееся тем, что клетку по п. 14 применяют для лечения Т-клеточных лимфомы или лейкоза, при этом злокачественные Т-клетки экспрессируют TRBC2.
22. Применение по п. 20, отличающееся тем, что клетку по п. 14 применяют для изготовления лекарственного средства для лечения Т-клеточных лимфомы или лейкоза, при этом злокачественные Т-клетки экспрессируют TRBC2.
23. Применение по п. 21 или 22, отличающееся тем, что указанные Т-клеточные лимфома или лейкоз выбраны из неспецифицированной периферической Т-клеточной лимфомы (ПТКЛн), ангиоиммунобластной Т-клеточной лимфомы (АИТЛ), анапластической крупноклеточной лимфомы (АККЛ), Т-клеточной лимфомы, ассоциированной с энтеропатией (EATL), гепатолиенальной Т-клеточной лимфомы (ГЛТЛ), экстранодальной NK/T-клеточной лимфомы назального типа, Т-клеточной лимфомы кожи, первичной АККЛ кожи, Т-клеточного пролимфоцитарного лейкоза и Т-клеточного острого лимфобластного лейкоза.
24. Применение антитела по п. 8 для специфичного связывания TRBC2.
25. Применение по п. 24, отличающееся тем, что антитело по п. 8 применяют для лечения Т-клеточных лимфомы или лейкоза, при этом злокачественные Т-клетки экспрессируют TRBC2.
26. Применение по п. 24, отличающееся тем, что антитело по п. 8 применяют для изготовления лекарственного средства для лечения Т-клеточных лимфомы или лейкоза, при этом злокачественные Т-клетки экспрессируют TRBC2.
27. Применение по п. 25 или 26, отличающееся тем, что указанные Т-клеточные лимфома или лейкоз выбраны из неспецифицированной периферической Т-клеточной лимфомы (ПТКЛн), ангиоиммунобластной Т-клеточной лимфомы (АИТЛ), анапластической крупноклеточной лимфомы (АККЛ), Т-клеточной лимфомы, ассоциированной с энтеропатией (EATL), гепатолиенальной Т-клеточной лимфомы (ГЛТЛ), экстранодальной NK/T-клеточной лимфомы назального типа, Т-клеточной лимфомы кожи, первичной АККЛ кожи, Т-клеточного пролимфоцитарного лейкоза и Т-клеточного острого лимфобластного лейкоза.
28. Применение BiTE по п. 10 для специфичного связывания TRBC2.
29. Применение по п. 28, отличающееся тем, что BiTE по п. 10 применяют для лечения Т-клеточных лимфомы или лейкоза, при этом злокачественные Т-клетки экспрессируют TRBC2.
30. Применение по п. 28, отличающееся тем, что BiTE по п. 10 применяют для изготовления лекарственного средства для лечения Т-клеточных лимфомы или лейкоза, при этом злокачественные Т-клетки экспрессируют TRBC2.
31. Применение по п. 29 или 30, отличающееся тем, что указанные Т-клеточные лимфома или лейкоз выбраны из неспецифицированной периферической Т-клеточной лимфомы (ПТКЛн), ангиоиммунобластной Т-клеточной лимфомы (АИТЛ), анапластической крупноклеточной лимфомы (АККЛ), Т-клеточной лимфомы, ассоциированной с энтеропатией (EATL), гепатолиенальной Т-клеточной лимфомы (ГЛТЛ), экстранодальной NK/T-клеточной лимфомы назального типа, Т-клеточной лимфомы кожи, первичной АККЛ кожи, Т-клеточного пролимфоцитарного лейкоза и Т-клеточного острого лимфобластного лейкоза.
32. Применение конъюгата по п. 16 или 17 при лечении Т-клеточного злокачественного новообразования, клетки которого экспрессируют TRBC2.
33. Применение по п. 32, отличающееся тем, что конъюгат по п. 16 или 17 применяют для лечения Т-клеточных лимфомы или лейкоза, при этом злокачественные Т-клетки экспрессируют TRBC2.
34. Применение по п. 32, отличающееся тем, что конъюгат по п. 16 или 17 применяют для изготовления лекарственного средства для лечения Т-клеточных лимфомы или лейкоза, при этом злокачественные Т-клетки экспрессируют TRBC2.
35. Применение по п. 33 или 34, отличающееся тем, что указанные Т-клеточные лимфома или лейкоз выбраны из неспецифицированной периферической Т-клеточной лимфомы (ПТКЛн), ангиоиммунобластной Т-клеточной лимфомы (АИТЛ), анапластической крупноклеточной лимфомы (АККЛ), Т-клеточной лимфомы, ассоциированной с энтеропатией (EATL), гепатолиенальной Т-клеточной лимфомы (ГЛТЛ), экстранодальной NK/T-клеточной лимфомы назального типа, Т-клеточной лимфомы кожи, первичной АККЛ кожи, Т-клеточного пролимфоцитарного лейкоза и Т-клеточного острого лимфобластного лейкоза.
36. Агент для диагностики Т-клеточного злокачественного новообразования, который содержит вариантный антигенсвязывающий домен по любому из пп. 1-7 или антитело по п. 8.
37. Aгент по п. 36, причём Т-клеточное злокачественное новообразование выбрано из Т-клеточных лимфомы или лейкоза.
38. Способ диагностики Т-клеточного злокачественного новообразования, выбранного из Т-клеточных лимфомы или лейкоза у субъекта, включающий этап приведения в контакт вариантного антигенсвязывающего домена по любому из пп. 1-7 или антитела по п. 8 с содержащим T-клетки образцом, полученным от указанного субъекта.
39. Способ по п. 38, дополнительно включающий этап определения процента TRBC2-положительных Т-клеток в образце.
40. Способ по п. 39, отличающийся тем, что процент, составляющий 70% или более TRBC2-положительных Т-клеток в образце, указывает на наличие Т-клеточных лимфомы или лейкоза.
41. Способ идентификации субъекта с Т-клеточным злокачественным новообразованием, выбранным из Т-клеточных лимфомы или лейкоза, соответствующих критериям для лечения клеткой по п. 14, или антителом по п. 8, или BiTE по п. 10, или конъюгатом по п. 16 или 17, включающий определение процента TRBC2-положительных Т-клеток в содержащем Т-клетки образце, полученном от указанного субъекта, причём определение процента TRBC2-положительных Т-клеток в содержащем Т-клетки образце, полученном от указанного субъекта, включает этап приведения в контакт вариантного антигенсвязывающего домена по любому из пп. 1-7 или антитела по п. 8 с указанным содержащим T-клетки образцом, при этом указанного субъекта идентифицируют как соответствующего критериям для указанного лечения, если процент TRBC2-положительных Т-клеток в указанном образце составляет 70% или более.
42. Способ выбора терапии при лечении Т-клеточного злокачественного новообразования, включающей клетку по п. 14, или антитело по п. 8, или BiTE по п. 10, или конъюгат по п. 16 или 17, для лечения субъекта, включающий определение процента TRBC2-положительных Т-клеток в содержащем Т-клетки образце, полученном от указанного субъекта, причём определение процента TRBC2-положительных Т-клеток в содержащем Т-клетки образце, полученном от указанного субъекта, включает этап приведения в контакт вариантного антигенсвязывающего домена по любому из пп. 1-7 или антитела по п. 8 с указанным содержащим T-клетки образцом, при этом указанную терапию выбирают для лечения указанного субъекта, если процент TRBC2-положительных Т-клеток в указанном образце составляет 70% или более.
| PAUL M MACIOCIA ET AL: "Targeting the T cell receptor [beta]-chain constant region for immunotherapy of T cell malignancies: Supplemental Figures", NATURE MEDICINE vol | |||
| Прибор для равномерного смешения зерна и одновременного отбирания нескольких одинаковых по объему проб | 1921 |
|
SU23A1 |
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| WO 2015132598 Al, 11.09.2015 | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2024-11-11—Публикация
2019-10-31—Подача