ЗАЯВЛЕНИЕ О ГОСУДАРСТВЕННОЙ ПОДДЕРЖКЕ
[0001] Настоящее изобретение выполнено при государственной поддержке в рамках грантов № R01CA175498 и R01DK100525, выданных национальными институтами здравоохранения. Правительство имеет определенные права на изобретение.
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0002] По настоящей заявке испрашивается приоритет предварительной заявки на патент США № 62/911,169, поданной 4 октября 2019 г., содержание которой полностью включено посредством ссылки.
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[0003] Настоящая заявка содержит список последовательностей, который представлен в формате ASCII через USPTO EFS-Web и настоящим полностью включен посредством ссылки. Копия ASCII, созданная 1 октября 2020 года, называется SequenceListing.txt и имеет размер 140 килобайт.
УРОВЕНЬ ТЕХНИКИ
[0004] Иммуноглобулин-подобные рецепторы киллерных клеток (KIR) - это белки, которые включают два (KIR2D) или три (KIR3D) иммуноглобулин-подобных внеклеточных домена (Beziat 2017). KIR3DL3 является членом семейства KIR, но его функции ранее были неизвестны (Beziat 2017). В настоящем изобретении представлены результаты, демонстрирующие, что KIR3DL3 является ингибирующим рецептором иммунной системы. В настоящем изобретении дополнительно предлагаются антитела и их иммуногенные фрагменты к KIR3DL3 или одному или более его эпитопам, а также композиции и способы их применения. В соответствии с некоторыми вариантами осуществления, представленными в настоящем описании, блокирование функции KIR3DL3 антителами или их иммуногенными фрагментами, слитыми посредством лигандов полипептидами или малыми молекулами можно использовать для лечения рака и инфекций, тогда как стимуляцию функции KIR3DL3 антителами или их иммуногенными фрагментами, слитыми посредством лигандов полипептидами или малыми молекулами можно использовать для лечения аутоиммунных заболеваний и в случаях, связанных с трансплантацией.
[0005] Лекарственные вещества, подавляющие иммунный ответ, можно использовать для эффективного лечения пациентов с аутоиммунными заболеваниями или для предотвращения отторжения трансплантата. Например, среди доступных в настоящее время средств для лечения ревматоидного артрита и в случае трансплантации почки являются абатацепт (Orencia®) и бетацепт (Nulojix®), модифицированные слитые полипептиды антител, содержащие внеклеточный домен человеческого цитотоксического Т-лимфоцит-ассоциированного антигена 4 (CTLA-4), связанного с Fc-областью IgG1. И наоборот, препараты, активирующие иммунный ответ, могут быть использованы для эффективного лечения заболеваний или расстройств, включая рак или инфекционные заболевания. Например, ипилимумаб (Ервой®) представляет собой моноклональное антитело, которое активирует иммунный ответ путем нацеливания на CTLA-4 и может использоваться для лечения меланомы. Пембролизумаб (Кейтруда®) представляет собой гуманизированное антитело к человеческому рецептору запрограммированной смерти-1 (PD-1) и назначается в качестве анти-PD-1 иммунотерапии против некоторых видов рака. Ниволумаб (Опдиво®) является еще одним анти-PD-1 антителом, используемым в качестве иммунотерапии для лечения некоторых видов рака.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0006] В одном из аспектов изобретение относится к антителу или его иммуногенному фрагменту, которое специфически связывается с белком KIR3DL3 (SEQ ID NO: 335). В некоторых вариантах осуществления изобретение относится к антителу или его иммуногенному фрагменту, которое специфически связывается с белком KIR3DL3, где антитело или его иммуногенный фрагмент специфически связывается с эпитопом KIR3DL3, содержащим полноразмерный внеклеточный домен или его часть. В некоторых вариантах осуществления антитело или его иммуногенный фрагмент связывается с доменом D0 KIR3DL3 (SEQ ID NO: 337), доменом D1 KIR3DL3 (SEQ ID NO: 338) или доменом D2 KIR3DL3 (SEQ ID NO: 339).
[0007] В одном из аспектов антитела или их иммуногенные фрагменты, представленные в настоящем описании, содержат область VH, содержащую CDR1, CDR2 и CDR3, имеющие аминокислотную последовательность SEQ ID NO: 7, 9, 11, 31, 33, 35, 54, 56, 76, 78, 80, 100, 102, 104, 124, 126, 128, 148, 150, 152, 172, 174, 176, 196, 198, 200, 220, 222, 224, 244, 246, 248, 268, 270, 272, 292, 294, 296, 316, 318 или 320.
[0008] В одном из аспектов антитела или их иммуногенные фрагменты, представленные в настоящем описании, содержат область VH, содержащую по меньшей мере одну CDR, которая на 80% идентична аминокислотной последовательности, выбранной из SEQ ID NO: 7, 9, 11, 31, 33, 35, 54, 56, 76, 78, 80, 100, 102, 104, 124, 126, 128, 148, 150, 152, 172, 174, 176, 196, 198, 200, 220, 222, 224, 244, 246, 248, 268, 270, 272, 292, 294, 296, 316, 318 или 320.
[0009] В одном из аспектов антитела или их иммуногенные фрагменты, представленные в настоящем описании, содержат область VH, содержащую по меньшей мере две CDR, которые на 80% идентичны аминокислотной последовательности, выбранной из SEQ ID NO: 7, 9, 11, 31, 33, 35, 54, 56, 76, 78, 80, 100, 102, 104, 124, 126, 128, 148, 150, 152, 172, 174, 176, 196, 198, 200, 220, 222, 224, 244, 246, 248, 268, 270, 272, 292, 294, 296, 316, 318 или 320.
[0010] В одном из аспектов антитела или их иммуногенные фрагменты, представленные в настоящем описании, содержат область VH, содержащую по меньшей мере три CDR, которые на 80% идентичны аминокислотной последовательности, выбранной из SEQ ID NO: 7, 9, 11, 31, 33, 35, 54, 56, 76, 78, 80, 100, 102, 104, 124, 126, 128, 148, 150, 152, 172, 174, 176, 196, 198, 200, 220, 222, 224, 244, 246, 248, 268, 270, 272, 292, 294, 296, 316, 318 или 320.
[0011] В одном из аспектов антитела или их иммуногенные фрагменты, представленные в настоящем описании, содержат область VL, содержащую CDR1, CDR2 и CDR3, имеющие аминокислотную последовательность SEQ ID NO: 19, 21, 23, 43, 45, 47, 64, 66, 68, 88, 90, 92, 112, 114, 116, 136, 138, 140, 160, 162, 164, 184, 186, 188, 208, 210, 212, 232, 234, 236, 256, 258, 260, 280, 282, 284, 304, 306, 308, 328, 330 или 332.
[0012] В одном из аспектов антитела или их иммуногенные фрагменты, представленные в настоящем описании, содержат область VL, содержащую по меньшей мере одну CDR, которая на 80% идентична аминокислотной последовательности, выбранной из SEQ ID NO: 19, 21, 23, 43, 45, 47, 64, 66, 68, 88, 90, 92, 112, 114, 116, 136, 138, 140, 160, 162, 164, 184, 186, 188, 208, 210, 212, 232, 234, 236, 256, 258, 260, 280, 282, 284, 304, 306, 308, 328, 330 или 332.
[0013] В одном из аспектов антитела или их иммуногенные фрагменты, представленные в настоящем описании, содержат область VL, содержащую по меньшей мере две CDR, которые на 80% идентичны аминокислотной последовательности, выбранной из SEQ ID NO: 19, 21, 23, 43, 45, 47, 64, 66, 68, 88, 90, 92, 112, 114, 116, 136, 138, 140, 160, 162, 164, 184, 186, 188, 208, 210, 212, 232, 234, 236, 256, 258, 260, 280, 282, 284, 304, 306, 308, 328, 330 или 332.
[0014] В одном из аспектов антитела или их иммуногенные фрагменты, представленные в настоящем описании, содержат область VL, содержащую по меньшей мере три CDR, которые на 80% идентичны аминокислотной последовательности, выбранной из SEQ ID NO: 19, 21, 23, 43, 45, 47, 64, 66, 68, 88, 90, 92, 112, 114, 116, 136, 138, 140, 160, 162, 164, 184, 186, 188, 208, 210, 212, 232, 234, 236, 256, 258, 260, 280, 282, 284, 304, 306, 308, 328, 330 или 332.
[0015] В некоторых аспектах антитела или их иммуногенные фрагменты, предложенные в настоящем описании, содержат моноклональное антитело.
[0016] В некоторых аспектах антитела или их иммуногенные фрагменты, представленные в настоящем описании, содержат химерное антитело, человеческое антитело или гуманизированное антитело.
[0017] В одном из аспектов антитела или их иммуногенные фрагменты, представленные в настоящем описании, содержат аминокислотную последовательность, выбранную из SEQ ID NO: 7, 9, 11, 19, 21, 23, 31, 33, 35, 43, 45, 47, 54, 56, 64, 66, 68, 76, 78, 80, 88, 90, 92, 100, 102, 104, 112, 114, 116, 124, 126, 128, 136, 138, 140, 148, 150, 152, 160, 162, 164, 172, 174, 176, 184, 186, 188, 196, 198, 200, 208, 210, 212, 220, 222, 224, 232, 234, 236, 244, 246, 248, 256, 258, 260, 268, 270, 272, 280, 282, 284, 292, 294, 296, 304, 306, 308, 316, 318, 320, 328, 330 или 332.
[0018] В одном из аспектов в настоящем описании представлены антитела или их иммуногенные фрагменты, где антитело представляет собой моноклональное 8G7, моноклональное 26E10, моноклональное 26E2, моноклональное 31C4, моноклональное 34B10, моноклональное 37A3, моноклональное 12A10, моноклональное 3B7, моноклональное 11G8, моноклональное 14F8, моноклональное 15D2, моноклональное 29H7, моноклональное 30D10 или моноклональное 51C3.
[0019] В одном из аспектов в настоящем документе представлены антитела или их иммуногенные фрагменты, где антитело представляет собой гуманизированное 8G7, гуманизированное 26E10, гуманизированное 26E2, гуманизированное 31C4, гуманизированное 34B10, гуманизированное 37A3, гуманизированное 12A10, гуманизированное 3B7, гуманизированное 11G8, гуманизированное 14F8, гуманизированное 15D2, гуманизированное 29H7, гуманизированное 30D10 или гуманизированное 51C3.
[0020] В другом аспекте представлены слитые полипептиды, содержащие антитело или его иммуногенный фрагмент согласно настоящему изобретению.
[0021] В некоторых аспектах представлены композиции, содержащие антитело или его иммуногенный фрагмент, или слитые белки согласно настоящему изобретению.
[0022] В другом аспекте композиции, представленные в настоящем описании, дополнительно содержат фармацевтически приемлемый носитель.
[0023] В другом аспекте композиции, представленные в настоящем описании, дополнительно содержат фармацевтически приемлемое вспомогательное вещество.
[0024] В некоторых аспектах антитела или их иммуногенные фрагменты, слитые полипептиды или композиции согласно настоящему изобретению могут представлять собой или содержать компонент химерного антигенного рецептора или конъюгат антитело-лекарственное вещество (например, антитело или его иммуногенный фрагмент, присоединенный к цитотоксическому агенту или молекуле).
[0025] В некоторых аспектах представлены антитела или их иммуногенные фрагменты, слитые полипептиды или композиции согласно настоящему изобретению для применения в терапии.
[0026] В некоторых аспектах представлены антитела или их иммуногенные фрагменты, слитые полипептиды или композиции согласно настоящему изобретению для применения в производстве лекарственного средства.
[0027] В другом аспекте представлены нуклеиновые кислоты, содержащие нуклеиновую кислоту, кодирующую антитело или его иммуногенный фрагмент согласно настоящему изобретению.
[0028] В другом аспекте представлены нуклеиновые кислоты, содержащие нуклеиновую кислоту, кодирующую слитый полипептид согласно настоящему изобретению.
[0029] В некоторых аспектах представлены способы лечения субъекта, страдающего от состояния, включающие введение субъекту терапевтически эффективного количества антитела или его иммуногенного фрагмента, слитого полипептида или композиции согласно настоящему изобретению.
[0030] В некоторых аспектах представлены способы лечения субъекта, страдающего от состояния, включающие введение субъекту терапевтически эффективного количества антитела или его иммуногенного фрагмента, слитого полипептида или композиции согласно настоящему изобретению, где субъект имеет состояние, представляющее собой рак. В некоторых вариантах осуществления рак выбирают из группы, состоящей из хронического лимфолейкоза (CLL), острого лейкоза, острого лимфолейкоза (ALL), В-клеточного острого лимфолейкоза (В-ALL), Т-клеточной лимфомы, В-клеточной лимфомы, Т-клеточного острого лимфолейкоза (Т-ALL), хронического миелогенного лейкоза (CML), В-клеточного пролимфоцитарного лейкоза, Т-клеточной лимфомы, болезни Ходжкина, В-клеточной неходжкинской лимфомы, бластной плазмоцитоидной дендритно-клеточной опухоли, лимфомы Беркитта, диффузной крупноклеточной В-клеточной лимфомы, фолликулярной лимфомы, волосатоклеточного лейкоза, мелкоклеточной фолликулярной лимфомы, крупноклеточной фолликулярной лимфомы, злокачественных лимфопролиферативных состояний, лимфомы, ассоциированной со слизистой оболочкой (MALT), лимфомы из мантийных клеток, лимфомы маргинальной зоны, множественной миеломы, миелодисплазии и миелодиспластического синдрома, неходжкинской лимфомы, лимфомы Ходжкина, плазмобластной лимфомы, новообразования из плазмоцитоидных дендритных клеток, макроглобулинемии Вальденстрема или прелейкемии. В других вариантах осуществления рак выбирают из группы, состоящей из рака толстой кишки, рака прямой кишки, почечно-клеточного рака, рака печени, рака легких, рака почки, рака желудка, рака желчного пузыря, рака тонкой кишки, рака пищевода, меланомы, рака костей, рака поджелудочной железы, рака кожи, рака головы или шеи, кожной или внутриглазной злокачественной меланомы, рака матки, рака яичников, рака прямой кишки, рака анальной области, рака желудка, рака яичек, рака матки, карциномы фаллопиевых труб, карциномы эндометрия, карциномы шейки матки, карциномы влагалища, карциномы вульвы, рака эндокринной системы, рака щитовидной железы, рака паращитовидной железы, рака надпочечников, саркомы мягких тканей, рака уретры, рака полового члена, солидных опухолей детского возраста, рака мочевого пузыря, рака почки или мочеточника, рака почечной лоханки, новообразования центральной нервной системы (ЦНС), первичной лимфомы ЦНС, ангиогенеза опухоли, опухоли спинного мозга, глиомы ствола головного мозга, аденомы гипофиза, саркомы Капоши, эпидермоидного рака, плоскоклеточного рака, рака, индуцированного окружающей средой, комбинации раковых заболеваний и метастатических поражений, вызванных раковыми заболеваниями. В других вариантах осуществления рак представляет собой гематологическое злокачественное новообразование у человека. В некоторых вариантах осуществления гематологическое злокачественное новообразование у человека выбирают из миелоидного новообразования, острого миелоидного лейкоза (AML), AML с рецидивирующими генетическими аномалиями, AML с изменениями, связанными с миелодисплазией, AML, связанного с терапией, острых лейкозов неоднозначного происхождения, миелопролиферативного новообразования, эссенциальной тромбоцитемии, истинной полицитемии, миелофиброза (MF), первичного миелофиброза, системного мастоцитоза, миелодиспластических синдромов (MDS), миелопролиферативных/миелодиспластических синдромов, хронического миелоидного лейкоза, хронического нейтрофильного лейкоза, хронического эозинофильного лейкоза, миелодиспластических синдромов (MDS), рефрактерной анемии с кольцевидными сидеробластами, рефрактерной цитопении с многолинейной дисплазией, рефрактерной анемии с избытком бластов (тип 1), рефрактерной анемии с избытком бластов (тип 2), MDS с изолированной делецией (5q), неклассифицируемого MDS, миелопролиферативных/миелодиспластических синдромов, хронического миеломоноцитарного лейкоза, атипичного хронического миелоидного лейкоза, ювенильного миеломоноцитарного лейкоза, неклассифицируемых миелопролиферативных/миелодисплатических синдромов, лимфоидных новообразований, предраковых лимфоидных новообразований, В-лимфобластного лейкоза, В-лимфобластной лимфомы, Т-лимфобластного лейкоза, Т-лимфобластной лимфомы, новообразований из зрелых В-клеток, диффузной крупноклеточной В-клеточной лимфомы, первичной лимфомы центральной нервной системы, первичной медиастинальной В-клеточной лимфомы, лимфомы/лейкемии Беркитта, фолликулярной лимфомы, хронического лимфолейкоза, малой лимфоцитарной лимфомы, В-клеточного пролимфоцитарного лейкоза, лимфоплазмоцитарной лимфомы, макроглобулинемии Вальденстрема, лимфомы из мантийных клеток, лимфомы маргинальной зоны, посттрансплантационных лимфопролиферативных заболеваний, ВИЧ-ассоциированных лимфом, первичной выпотной лимфомы, внутрисосудистой крупноклеточной В-клеточной лимфомы, первичной кожной В-клеточной лимфомы, волосатоклеточного лейкоза, множественной миеломы, моноклональной гаммапатии неясного генеза (MGUS), тлеющей множественной миеломы или солитарных плазмоцитом (солитарных костных и экстрамедуллярных).
[0031] В некоторых вариантах осуществления рак представляет собой метастатический рак.
[0032] В некоторых вариантах осуществления способы лечения страдающего от рака субъекта, включающие введение субъекту терапевтически эффективного количества антитела или его иммуногенного фрагмента, слитого полипептида или композиции согласно настоящему изобретению, дополнительно включают предоставление субъекту одного или более дополнительных видов терапии рака, выбранных из химиотерапии, лучевой терапии, иммунотерапии, хирургии и их комбинации.
[0033] В некоторых аспектах представлены способы лечения субъекта, страдающего от состояния, включающие введение субъекту терапевтически эффективного количества антитела или его иммуногенного фрагмента, слитого полипептида или композиции согласно настоящему изобретению, где субъект имеет состояние, представляющее собой инфекцию. В некоторых вариантах осуществления инфекция вызвана патогеном. В некоторых вариантах осуществления патоген представляет собой вирус. В некоторых вариантах осуществления вирус выбирают из группы, состоящей из вирусов иммунодефицита человека, вирусов гриппа, папилломавирусов, коронавирусов, вирусов гепатита или герпесвирусов. В других вариантах осуществления патоген представляет собой бактерию. В некоторых вариантах осуществления бактерия представляет собой микобактерию туберкулеза. В других вариантах осуществления патоген представляет собой прион. В других вариантах осуществления патоген представляет собой грибок. В некоторых вариантах осуществления грибок представляет собой Pneumocystis jirovecii (PJP). В других вариантах осуществления патоген представляет собой паразита.
[0034] В некоторых аспектах представлены способы лечения субъекта, страдающего от состояния, включающие введение субъекту терапевтически эффективного количества антитела или его иммуногенного фрагмента, слитого полипептида или композиции согласно настоящему изобретению, где субъект имеет состояние, представляющее собой аутоиммунное заболевание или расстройство. В некоторых вариантах осуществления аутоиммунное заболевание или расстройство выбирают из группы, состоящей из острого диссеминированного энцефаломиелита (ADEM), очаговой алопеции, антифосфолипидного синдрома, аутоиммунной кардиомиопатии, аутоиммунной гемолитической анемии, аутоиммунного гепатита, аутоиммунного заболевания внутреннего уха, аутоиммунного липопролиферативного синдрома, аутоиммунной периферической невропатии, аутоиммунного панкреатита, аутоиммунного полиэндокринного синдрома, аутоиммунного прогестеронового дерматита, аутоиммунной тромбоцитопенической пурпуры, аутоиммунной крапивницы, аутоиммунного увеита, болезни Бехчета, глютеновой болезни, болезни Шагаса, болезни холодовых агглютининов, болезни Крона, дерматомиозита, сахарного диабета 1 типа, эозинофильного фасциита, пемфигоида желудочно-кишечного тракта, синдрома Гудпасчера, синдрома Грейвса, синдрома Гийена-Барре, энцефалопатии Хашимото, тиреоидита Хашимото, красной волчанки, синдрома Миллера-Фишера, смешанного заболевания соединительной ткани, тяжелой миастении, вульгарной пузырчатки, пернициозной анемии, полимиозита, псориаза, псориатического артрита, рецидивирующего полихондрита, ревматоидного артрита, ревматической атаки, синдрома Шегрена, височного артериита, поперечного миелита, язвенного колита, недифференцированного заболевания соединительной ткани, васкулита и гранулематоза Вегенера. В некоторых вариантах осуществления аутоиммунное заболевание или расстройство представляет собой ревматоидный артрит взрослых.
[0035] В некоторых аспектах представлены способы лечения субъекта, страдающего от состояния, включающие введение субъекту терапевтически эффективного количества антитела или его иммуногенного фрагмента, слитого полипептида или композиции согласно настоящему изобретению, где субъект имеет состояние, представляющее собой наличие трансплантата. В некоторых вариантах осуществления трансплантат выбирают из трансплантата стволовых клеток или трансплантата костного мозга. В некоторых вариантах осуществления трансплантат выбирают из группы, состоящей из трансплантата почки, трансплантата легкого, трансплантата сердца, трансплантата поджелудочной железы, трансплантата роговицы или трансплантата печени.
[0036] В некоторых аспектах представлены композиции, содержащие антитело, его иммуногенный фрагмент, слитый полипептид или их комбинацию согласно настоящему изобретению, для применения при лечении субъекта, страдающего от состояния.
[0037] Некоторые аспекты относятся к композициям, содержащим антитело, его иммуногенный фрагмент, слитый полипептид или их комбинацию согласно настоящему изобретению, для применения при лечении субъекта, страдающего от состояния, представляющее собой рак. В некоторых вариантах осуществления рак выбирают из группы, состоящей из хронического лимфолейкоза (CLL), острого лейкоза, острого лимфолейкоза (ALL), В-клеточного острого лимфолейкоза (В-ALL), Т-клеточной лимфомы, В-клеточной лимфомы, Т-клеточного острого лимфолейкоза (Т-ALL), хронического миелогенного лейкоза (CML), В-клеточного пролимфоцитарного лейкоза, Т-клеточной лимфомы, болезни Ходжкина, В-клеточной неходжкинской лимфомы, бластной плазмоцитоидной дендритно-клеточной опухоли, лимфомы Беркитта, диффузной крупноклеточной В-клеточной лимфомы, фолликулярной лимфомы, волосатоклеточного лейкоза, мелкоклеточной фолликулярной лимфомы, крупноклеточной фолликулярной лимфомы, злокачественных лимфопролиферативных состояний, лимфомы, ассоциированной со слизистой оболочкой (MALT), лимфомы из мантийных клеток, лимфомы маргинальной зоны, множественной миеломы, миелодисплазии и миелодиспластического синдрома, неходжкинской лимфомы, лимфомы Ходжкина, плазмобластной лимфомы, новообразования из плазмоцитоидных дендритных клеток, макроглобулинемии Вальденстрема или прелейкемии. В других вариантах осуществления рак выбирают из группы, состоящей из рака толстой кишки, рака прямой кишки, почечно-клеточного рака, рака печени, рака легких, рака почки, рака желудка, рака желчного пузыря, рака тонкой кишки, рака пищевода, меланомы, рака костей, рака поджелудочной железы, рака кожи, рака головы или шеи, кожной или внутриглазной злокачественной меланомы, рака матки, рака яичников, рака прямой кишки, рака анальной области, рака желудка, рака яичек, рака матки, карциномы фаллопиевых труб, карциномы эндометрия, карциномы шейки матки, карциномы влагалища, карциномы вульвы, рака эндокринной системы, рака щитовидной железы, рака паращитовидной железы, рака надпочечников, саркомы мягких тканей, рака уретры, рака полового члена, солидных опухолей детского возраста, рака мочевого пузыря, рака почки или мочеточника, рака почечной лоханки, новообразования центральной нервной системы (ЦНС), первичной лимфомы ЦНС, ангиогенеза опухоли, опухоли спинного мозга, глиомы ствола головного мозга, аденомы гипофиза, саркомы Капоши, эпидермоидного рака, плоскоклеточного рака, рака, индуцированного окружающей средой, комбинации раковых заболеваний и метастатических поражений, вызванных раковыми заболеваниями. В других вариантах осуществления рак представляет собой гематологическое злокачественное новообразование у человека. В некоторых вариантах осуществления гематологическое злокачественное новообразование у человека выбирают из миелоидного новообразования, острого миелоидного лейкоза (AML), AML с рецидивирующими генетическими аномалиями, AML с изменениями, связанными с миелодисплазией, AML, связанного с терапией, острых лейкозов неоднозначного происхождения, миелопролиферативного новообразования, эссенциальной тромбоцитемии, истинной полицитемии, миелофиброза (MF), первичного миелофиброза, системного мастоцитоза, миелодиспластических синдромов (MDS), миелопролиферативных/миелодиспластических синдромов, хронического миелоидного лейкоза, хронического нейтрофильного лейкоза, хронического эозинофильного лейкоза, миелодиспластических синдромов (MDS), рефрактерной анемии с кольцевидными сидеробластами, рефрактерной цитопении с многолинейной дисплазией, рефрактерной анемии с избытком бластов (тип 1), рефрактерной анемии с избытком бластов (тип 2), MDS с изолированной делецией (5q), неклассифицируемого MDS, миелопролиферативных/миелодиспластических синдромов, хронического миеломоноцитарного лейкоза, атипичного хронического миелоидного лейкоза, ювенильного миеломоноцитарного лейкоза, неклассифицируемых миелопролиферативных/миелодисплатических синдромов, лимфоидных новообразований, предраковых лимфоидных новообразований, В-лимфобластного лейкоза, В-лимфобластной лимфомы, Т-лимфобластного лейкоза, Т-лимфобластной лимфомы, новообразований из зрелых В-клеток, диффузной крупноклеточной В-клеточной лимфомы, первичной лимфомы центральной нервной системы, первичной медиастинальной В-клеточной лимфомы, лимфомы/лейкемии Беркитта, фолликулярной лимфомы, хронического лимфолейкоза, малой лимфоцитарной лимфомы, В-клеточного пролимфоцитарного лейкоза, лимфоплазмоцитарной лимфомы, макроглобулинемии Вальденстрема, лимфомы из мантийных клеток, лимфомы маргинальной зоны, посттрансплантационных лимфопролиферативных заболеваний, ВИЧ-ассоциированных лимфом, первичной выпотной лимфомы, внутрисосудистой крупноклеточной В-клеточной лимфомы, первичной кожной В-клеточной лимфомы, волосатоклеточного лейкоза, множественной миеломы, моноклональной гаммапатии неясного генеза (MGUS), тлеющей множественной миеломы или солитарных плазмоцитом (солитарных костных и экстрамедуллярных).
[0038] В некоторых вариантах осуществления рак представляет собой метастатический рак.
[0039] В некоторых вариантах осуществления представлены композиции, содержащие антитело, его иммуногенный фрагмент, слитый полипептид или их комбинацию согласно настоящему изобретению, для применения при лечении субъекта, страдающего от состояния, где композицию вводят субъекту вместе с одним или более дополнительными видами терапии рака, выбранными из химиотерапии, лучевой терапии, иммунотерапии, хирургии или их комбинации.
[0040] В некоторых аспектах представлены композиции, содержащие антитело, его иммуногенный фрагмент, слитый полипептид или их комбинацию согласно настоящему изобретению, для применения при лечении субъекта, страдающего от состояния, где состояние представляет собой инфекцию. В некоторых вариантах осуществления инфекция вызвана патогеном. В некоторых вариантах осуществления патоген представляет собой вирус. В некоторых вариантах осуществления вирус выбирают из группы, состоящей из вирусов иммунодефицита человека, вирусов гриппа, папилломавирусов, коронавирусов, вирусов гепатита или герпесвирусов. В других вариантах осуществления патоген представляет собой бактерию. В некоторых вариантах осуществления бактерия представляет собой микобактерию туберкулеза. В других вариантах осуществления патоген представляет собой прион. В других вариантах осуществления патоген представляет собой грибок. В некоторых вариантах осуществления грибок представляет собой Pneumocystis jirovecii (PJP). В других вариантах осуществления патоген представляет собой паразита.
[0041] В некоторых аспектах представлены композиции, содержащие антитело, его иммуногенный фрагмент, слитый полипептид или их комбинацию согласно настоящему изобретению, для применения при лечении субъекта, страдающего от состояния, где состояние представляет собой аутоиммунное заболевание или расстройство. В некоторых вариантах осуществления аутоиммунное заболевание или расстройство выбирают из группы, состоящей из острого диссеминированного энцефаломиелита (ADEM), очаговой алопеции, антифосфолипидного синдрома, аутоиммунной кардиомиопатии, аутоиммунной гемолитической анемии, аутоиммунного гепатита, аутоиммунного заболевания внутреннего уха, аутоиммунного липопролиферативного синдрома, аутоиммунной периферической невропатии, аутоиммунного панкреатита, аутоиммунного полиэндокринного синдрома, аутоиммунного прогестеронового дерматита, аутоиммунной тромбоцитопенической пурпуры, аутоиммунной крапивницы, аутоиммунного увеита, болезни Бехчета, глютеновой болезни, болезни Шагаса, болезни холодовых агглютининов, болезни Крона, дерматомиозита, сахарного диабета 1 типа, эозинофильного фасциита, пемфигоида желудочно-кишечного тракта, синдрома Гудпасчера, синдрома Грейвса, синдрома Гийена-Барре, энцефалопатии Хашимото, тиреоидита Хашимото, красной волчанки, синдрома Миллера-Фишера, смешанного заболевания соединительной ткани, тяжелой миастении, вульгарной пузырчатки, пернициозной анемии, полимиозита, псориаза, псориатического артрита, рецидивирующего полихондрита, ревматоидного артрита, ревматической атаки, синдрома Шегрена, височного артериита, поперечного миелита, язвенного колита, недифференцированного заболевания соединительной ткани, васкулита и гранулематоза Вегенера. В некоторых вариантах осуществления аутоиммунное заболевание или расстройство представляет собой ревматоидный артрит взрослых.
[0042] В некоторых аспектах представлены композиции, содержащие антитело, его иммуногенный фрагмент, слитый полипептид или их комбинацию согласно настоящему изобретению, для применения при лечении субъекта, страдающего от состояния, где состояние представляет собой наличие трансплантата. В некоторых вариантах осуществления трансплантат выбирают из трансплантата стволовых клеток или трансплантата костного мозга. В некоторых вариантах осуществления трансплантат выбирают из группы, состоящей из трансплантата почки, трансплантата легкого, трансплантата сердца, трансплантата поджелудочной железы, трансплантата роговицы и трансплантата печени.
[0043] Этот список приведен в качестве примера и является иллюстративным, а не исчерпывающим и ограничивающим. Дополнительные аспекты и варианты осуществления могут быть изложены или вытекать из остальной части описания изобретения и формулы изобретения.
ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0044] На фигурах (фиг.) 1A-1B показано, что белок KIR3DL3 экспрессируется на клеточной поверхности клеток адаптивного иммунитета человека и клеток врожденного иммунитета. На фиг. 1A представлен ряд графиков, показывающих анализ мононуклеарных клеток периферической крови (PBMC), выполненный методом сортировки флуоресцентно-активированных клеток (FACS). FACS-анализ показал, что белок KIR3DL3 детектируется на поверхности клеток врожденного иммунитета человека, включая натуральные киллеры (NK), T-натуральные киллеры (NKT) и γδ T-клетки, а также на поверхности клеток адаптивного иммунитета, включая CD8+ T-клетки и CD4+ T-клетки. Фиг. 1B представляет собой диаграмму, демонстрирующую процент KIR3DL3-положительных клеток в различных популяциях иммунных клеток в PBMC от шести различных доноров.
[0045] На фиг. 2A-2C показано, что HHLA2 связывается с KIR3DL3, но не с его ближайшими гомологами KIR3DL1 и KIR3DL2, и что с HHLA2 связываются домен D0 и вся внеклеточная часть KIR3DL3. На фиг. 2A представлены гистограммы клеточных линий 3T3, экспрессирующих KIR3DL1, KIR3DL2 или KIR3DL3, окрашенный слитым полипептидом HHLA2-Ig (незаштрихованные гистограммы) или контрольным Ig (заштрихованные гистограммы). На. Фиг. 2B представлен график, показывающий результаты анализа межклеточного конъюгата, которые указывают на то, что клеточная линия 3T3, экспрессирующая HHLA2, связывается с клеточной линией 3T3, экспрессирующей KIR3DL3, но не с контрольной клеточной линией 3T3. На фиг. 2C представлены гистограммы клеточной линии 3T3, экспрессирующей HHLA2, связанного с доменом D0 (красный) и всей внеклеточной частью (красная) KIR3DL3.
[0046] На фиг. 3A-3B показаны результаты, указывающие на то, что TMIGD2 и KIR3DL3 связываются с неперекрывающимися участками на HHLA2. Фиг. 3A представляет собой диаграмму, изображающую среднюю интенсивность флуоресценции (MFI) клеток 3T3, экспрессирующих HHLA2, которые инкубировали со слитым полипептидом TMIGD2-mIg или контрольным mIgG в указанных концентрациях перед окрашиванием 10 мкг/мл KIR3DL3-hIg с последующим окрашиванием анти-человеческим IgG Fc, конъюгированным с аллофикоцианином (APC). Фиг. 3B представляет собой диаграмму, изображающую MFI клеток 3T3, экспрессирующих HHLA2, которые инкубировали со слитым полипептидом KIR3DL3-hIg или контрольным hIgG в указанных концентрациях перед окрашиванием 10 мкг/мл TMIGD2-mIg с последующим окрашиванием APC конъюгатом анти-мышиного IgG Fc.
[0047] На фиг. 4A-4B показаны результаты, указывающие на то, что KIR3DL3 ингибирует функции иммунных клеток. На фиг. 4A представлены графики FACS-анализа и диаграммы количественного определения специфического лизиса. Клетки KIR3DL3+ или KIR3DL3-NK92 сортировали и экспрессию KIR3DL3 исследовали с помощью FACS. Анализы цитотоксичности выполняли путем инкубации клеток NK92 с целевым контролем K562 или K562, экспрессирующими HHLA2 (HHLA2/K562), при указанных соотношениях эффекторных клеток и целевых клеток (E:T=1, 2, 5, 10). Фиг. 4B представляет собой диаграмму, изображающую проценты специфического лизиса после анализа цитотоксичности в KIR3DL3+ CD8+ T-клетках (терминально дифференцированных эффекторных клетках) из PBMC, которые были отсортированы методом FACS и размножены в присутствии анти-CD3/CD28, IL-2 и фидерных клеток in vitro. Анализы цитотоксичности выполняли путем инкубации KIR3DL3+ CD8+ Т-клеток с целевым контролем K562 или HHLA2/K562 при указанных соотношениях эффекторных клеток и целевых клеток. *Р <0,05; **Р <0,01.
[0048] На фиг. 5A-5B показано, что моноклональные антитела (mAb), блокирующие KIR3DL3, нейтрализуют подавление иммунитета, вызванное KIR3DL3. На фиг. 5A представлена серия гистограмм клеток KIR3DL3+ NK92, предварительно инкубированных с анти-KIR3DL3 mAb (клоны 26E10, 34B10, 30D10, 8G7) в течение 45 мин при комнатной температуре (RT). На фиг. 5В представлена диаграмма, демонстрирующая процент специфического лизиса в указанных клетках после анализа цитотоксичности. Анализы цитотоксичности проводили с целевым контролем K562 или HHLA2/K562 при E:T соотношении, равном 5:1. *Р <0,05; **Р <0,01.
[0049] На фиг. 6A-6B показано, что моноклональные антитела к домену IgV1 HHLA2 могут блокировать связывание HHLA2 с KIR3DL3 и нейтрализовать подавление иммунитета, вызванное KIR3DL3. Фиг. 6A представляет собой диаграмму, демонстрирующую среднюю интенсивность флуоресценции (MFI) HHLA2-экспрессирующих клеток 3T3, которые были предварительно инкубированы с анти-HHLA2 mAb или контрольным мышиным IgG, а затем окрашены белком KIR3DL3-Ig в различных концентрациях. Связывание белка KIR3DL3-Ig с HHLA2 определяли методом FACS. Фиг. 6B представляет собой диаграмму, демонстрирующую проценты специфического лизиса после анализа токсичности в целевых клетках HHLA2/K562, которые были предварительно инкубированы с анти-HHLA2 mAb (клон B5B5, A3H11, 566.1) или изотипом mIgG1. Анализы цитотоксичности выполняли путем инкубации клеток KIR3DL3+ NK92 с контрольными клетками K562 или HHLA2/K562 при E:T соотношении, равном 5:1, при 37°C в течение 4 часов. *Р <0,05; **Р <0,01.
[0050] На фиг. 7 представлена серия графиков FACS, демонстрирующих характер экспрессии двух рецепторов KIR3DL3 и TMIGD2 на человеческих NK-клетках, CD8+ T-клетках и CD4+ T-клетках.
[0051] На фиг. 8 представлены две диаграммы, изображающие гистограммы клеточных линий 3T3, экспрессирующих TMIGD2, окрашенных с помощью слитого полипептида HHLA2 EC-Ig-Fc (слева, красные гистограммы), слитого полипептида HHLA2-IgV1-hIgG (справа, красные гистограммы) или контрольного Ig (черные гистограммы).
[0052] На фиг. 9 KIR3DL3 представлена таблица, демонстрирующая соответствующие выделенные цветом проценты потенциала экспрессии уровней мРНК KIRDL3 в 1425 опухолевых линиях человека. мРНК KIR3DL3 экспрессировали во многих опухолевых линиях гематологических злокачественных новообразований человека. На фиг. 9 показаны 40 верхних линий, экспрессирующих самые высокие уровни мРНК KIR3DL3.
[0053] На фиг. 10A-10D показано, что мотив ITIM в KIR3DL3 опосредует супрессию NK-клеток посредством рекрутирования SHR1/2. На фиг. 10А показаны KIR3DL3 дикого типа (WT) и ITIM-мутант (Y381F) KIR3DL3 с мутацией тирозина (Y) на фенилаланин (F) в последовательностях ITIM (YAQL) и их экспрессия, определенная с помощью проточной цитометрии. На фиг. 10В показано фосфорилирование тирозина у KIR3DL3 WT и мутанта Y381F после обработки перванадатом. На фиг. 10C показаны анализы цитотоксичности, проведенные путем инкубации клеток KIR3DL3 WT или Y381F NK92 с K562 (вверху, контроль K562 или HHLA2/K562) или Raji (внизу, контроль Raji или HHLA2/Raji) при указанных соотношениях E:T. Показан один представитель 3 независимых экспериментов. *Р <0,05, **Р <0,01; NS, не существенно. На фиг. 10D показана коиммунопреципитация, демонстрирующая, что KIR3DL3 взаимодействует как с SHP-1, так и с SHP-2.
[0054] На фиг. 11 показано, что KIR3DL3 экспрессируется на инфильтрирующих опухоль иммунных клетках при различных видах рака человека, включая рак почки, рак желудка, рак легкого, желчного пузыря и поджелудочной железы. Репрезентативные изображения указанного рака человека с коэкспрессией KIR3DL3 и CD45 (DAPI: синий, CD45: красный, KIR3DL3: зеленый). Слева: наложение всех маркеров; Середина: CD45 и DAPI; Справа: KIR3DL3 и DAPI. Масштабные линейки, 50 мкм.
[0055] На фиг. 12A-12F показано, что блокада KIR3DL3 способствует противоопухолевому иммунитету. На фиг. 12A-12B показаны мышиные модели внутрибрюшинной опухоли, обработанные первичными NK-клетками и анти-KIR3DL3 mAb. На фиг. 12А изображена схема процедуры эксперимента. На фиг. 12В показано биолюминесцентное измерение роста опухоли в группах 26Е10 (синяя линия) и mIgG1 (черная линия). Данные представляют собой среднее значение ± SEM общего потока при визуализации в вентральной плоскости для каждой мыши. На фиг. 12C-12D показаны мышиные модели с метастазами опухоли в легкие, обработанные первичными NK-клетками и анти-KIR3DL3 mAb. На фиг. 12C изображена схема процедуры эксперимента. На фиг. 12D показано биолюминесцентное измерение роста опухоли в группе 26E10 (синий) и mIgG1 (черный). Данные представляют собой среднее значение ± SEM арифметического среднего общего потока при визуализации в дорсальной и вентральной плоскостях для каждой мыши. P-значения двухфакторного дисперсионного анализа (ANOVA). На фиг. 12E-12F показаны мышиные модели подкожной опухоли, обработанные первичными NK-клетками и анти-KIR3DL3 mAb. На фиг. 12E изображена схема процедуры эксперимента. На фиг. 12F изображена оценка роста опухоли. Показаны средние объемы опухоли ± SEM. i.p., внутрибрюшинно; i.v., внутривенно; s.c., подкожно.
ПОДРОБНОЕ ОПИСАНИЕ
[0056] Иммуноглобулин-подобные рецепторы киллерных клеток (KIR) - это белки, которые включают два (KIR2D) или три (KIR3D) иммуноглобулин-подобных внеклеточных домена (Beziat 2017). KIR3DL3 является членом семейства KIR, но его функции ранее были неизвестны (Beziat 2017). Белок KIR3DL3 экспрессируется на поверхности клеток адаптивного иммунитета человека и клеток врожденного иммунитета. Согласно представленным в настоящем описании результатам, KIR3DL3 ингибирует функции иммунных клеток человека. Следовательно, блокирование функции KIR3DL3 антителами, слитыми посредством лигандов полипептидами или малыми молекулами можно использовать для лечения рака или инфекций, тогда как стимуляцию функции KIR3DL3 антителами, слитыми посредством лигандов полипептидами или малыми молекулами можно использовать для лечения аутоиммунных заболеваний или случаев, связанных с трансплантацией. KIR3DL3 экспрессируется при различных гематологических злокачественных новообразованиях человека, поэтому использование антител и других молекул для уничтожения KIR3DL3-положительных опухолевых клеток можно использовать для лечения гематологических злокачественных новообразований человека. Настоящее изобретение относится к антителам к KIR3DL3 или одному или более его эпитопов, а также композиции и способам их применения.
[0057] Результаты, обеспечиваемые настоящим изобретением, демонстрируют, что KIR3DL3 ингибирует функцию иммунных клеток. Кроме того, введение mAb, блокирующих KIR3DL3, таких как представленные в настоящем описании, нейтрализует вызванное KIR3DL3 подавление иммунитета. Таким образом, выделенные анти-KIR3DL3 антитела, включая моноклональные антитела, анти-KIR3DL3 антитела могут блокировать функцию KIR3DL3, тем самым усиливая функцию иммунных клеток. Более того, дополнительные результаты, представленные в настоящем описании, демонстрируют, что HHLA2 связывается с KIR3DL3, но не с его близкими гомологами KIR3DL1 и KIR3DL2. Таким образом, антитела к домену IgV1 HHLA2 могут блокировать связывание HHLA2 с KIR3DL3, тем самым нейтрализуя подавление иммунитета, вызванное KIR3DL3.
Определения и сокращения
[0058] Если не указано иное, каждый из приведенных ниже терминов имеет значение, приведенное в этом разделе.
[0059] Неопределенные артикли означают по меньшей мере одно из ассоциированных существительных и используется взаимозаменяемо с терминами «по меньшей мере один» и «один или более». Например, фраза «модуль» означает по меньшей мере один модуль или один или более модулей.
[0060] Союзы «или» и «и/или» используются взаимозаменяемо.
[0061] В контексте настоящего описания термин «антитело» используется для обозначения, помимо природных антител, генно-модифицированных или иным образом модифицированных форм иммуноглобулинов, включая химерные антитела, человеческие антитела, гуманизированные антитела или синтетические антитела. Раскрытые в настоящем описании антитела могут быть моноклональными или поликлональными антителами. В тех вариантах осуществления, где антитело представляет собой иммуногенно активную часть молекулы иммуноглобулина, антитело может включать, помимо прочего, одноцепочечное Fv-антитело (scFv), связанный дисульфидной связью Fv, однодоменное антитело (dAb), Fab, Fab', фрагмент Fab, F(ab')2 или диатело. Описанные в настоящем описании антитела, включая антитела, которые содержат иммуногенно активную часть молекулы иммуноглобулина, сохраняют способность связываться со специфическим антигеном, например, KIR3DL3, или одним или более его эпитопами.
[0062] «Домен» используется для описания сегмента белка или нуклеиновой кислоты. Если не указано иное, не требуется, чтобы домен обладал каким-либо определенным функциональным свойством.
[0063] «Субъект» означает человека, мышь или примата, отличного от человека. Субъект-человек может быть любого возраста (например, младенец, ребенок, молодой взрослый или взрослый) и может страдать от заболевания, такого как рак. В некоторых вариантах осуществления субъект страдает от соответствующего заболевания, расстройства или состояния. В некоторых вариантах осуществления субъект подвержен заболеванию, расстройству или состоянию. В некоторых вариантах осуществления у субъекта проявляются один или более симптомов или признаков заболевания, расстройства или состояния. В некоторых вариантах осуществления у субъекта не проявляются какие-либо симптомы или признаки заболевания, расстройства или состояния. В некоторых вариантах осуществления субъект представляет собой лицо с одним или более признаками, свидетельствующими о предрасположенности к заболеванию, расстройству или состоянию или риске возникновения заболевания, расстройства или состояния. В некоторых вариантах осуществления субъект представляет собой пациента. В некоторых вариантах осуществления субъект представляет собой индивидуума, которому ставят диагноз и/или предоставляют терапию.
[0064] «Лечить», «лечащий» и «лечение», используемые в настоящем описании, означают лечение заболевания у субъекта (например, человека), включая одно или более из подавления заболевания, т.е. остановку или предотвращение его развития или прогрессирования; облегчения заболевания, т.е. регресса болезненного состояния; облегчения одного или более симптомов заболевания; и излечения болезни.
[0065] «Предотвратить», «предупреждение» и «профилактика», используемые в настоящем описании, означают профилактику заболевания у субъекта, например, у человека, включая (а) предотвращение или профилактику заболевания; (b) уменьшение предрасположенности к заболеванию; (c) предотвращение или отсрочку возникновения и/или снижение частоты и/или тяжести по меньшей мере одного симптома заболевания.
[0066] Термины «полинуклеотид», «нуклеотидная последовательность», «нуклеиновая кислота», «молекула нуклеиновой кислоты», «последовательность нуклеиновой кислоты» и «олигонуклеотид» относятся к последовательности нуклеотидных оснований (также называемых «нуклеотидами») в ДНК и РНК и означают любую цепь из двух или более нуклеотидов. Полинуклеотиды могут быть химерными смесями или производными или их модифицированными вариантами, одноцепочечными или двухцепочечными. Олигонуклеотид может быть модифицирован в основном фрагменте, сахарном фрагменте или фосфатном остове, например, для улучшения стабильности молекулы, параметров ее гибридизации и т.д. Последовательность нуклеотидов обычно несет генетическую информацию, включая информацию, используемую клеточным механизмом для создания белков и ферментов. Эти термины включают двух- или одноцепочечную геномную ДНК, РНК, любые синтетические и генетически измененные полинуклеотиды, а также смысловые и антисмысловые полинуклеотиды. Сюда же относятся нуклеиновые кислоты, содержащие модифицированные основания.
[0067] В нуклеотидных последовательностях, представленных в настоящем описании, используются общепринятые обозначения IUPAC, как показано в Таблице 1 ниже (см. также Cornish-Bowden 1985, включенный в настоящее описание посредством ссылки). Однако следует отметить, что «Т» означает «тимин или урацил», поскольку указанная последовательность (такая как последовательность гРНК) может кодироваться либо ДНК, либо РНК.
[0068] Термины «белок», «пептид» и «полипептид» используются взаимозаменяемо для обозначения последовательной цепи аминокислот, связанных друг с другом пептидными связями. Термины включают отдельные белки, группы или комплексы совместно ассоциированных белков, а также фрагменты, варианты, производные и аналоги таких белков. Пептидные последовательности представлены с помощью общепринятых обозначений, начиная с амино- или N-конца слева и заканчивая карбоксильным или С-концом справа. Можно использовать стандартные однобуквенные или трехбуквенные сокращения.
Создание и последовательности mAb к человеческому KIR3DL3
[0069] KIR3DL3 является членом семейства KIR, но его функции ранее были неизвестны (Beziat 2017). Внеклеточная часть KIR3DL3 состоит из трех доменов (D0, D1 и D2). В соответствии с вариантами осуществления, представленными в настоящем описании, были получены следующие слитые полипептиды: 1) слитый полипептид KIR3DL3 D0-Ig путем слияния кодирующей области KIR3DL3 D0 (Q26-A128) с Fc-меткой человеческого IgG1; и 2) слитый полипептид KIR3DL3 D0D1D2-Ig путем слияния кодирующей области KIR3DL3 D0D1D2 (Q26-L325) с Fc-меткой человеческого IgG1, с помощью ранее описанных методов (Zhao 2013). В некоторых вариантах осуществления слитые полипептиды экспрессировали в системе S2, а затем очищали. Мышей иммунизировали слитым полипептидом KIR3DL3 D0(Q26-A128)-Ig или слитым полипептидом KIR3DL3 D0(Q26-A128)-Ig, и из спленоцитов, слитых с клетками миеломы NS0, стандартными методами получали гибридомы. Последовательности человеческого KIR3DL3 показаны ниже в таблице 2.
atgtcgctcatggtcgtcagcatggcgtgtgttgggttcttcttgctggaggggccctggccacatgtgggtggtcaggacaagcccttcctctctgcctggcccggcactgtggtgtctgaaggacaacatgtgactcttcagtgtcgctctcgtcttgggtttaatgaattcagtctgtccaaagaagacgggatgcctgtccctgagctctacaacagaatattccggaacagctttctcatgggccctgtgaccccagcacatgcagggacctacagatgttgcagttcacacccacactcccccactgggtggtcggcacccagcaaccctgtggtgatcatggtcacaggagtccacagaaaaccttccctcctggcccacccaggtcccctggtgaaatcaggagagacggtcatcctgcaatgttggtcagatgtcaggtttgagcgcttccttctgcacagagaggggatcactgaggaccccttgcgcctcgttggacagctccacgatgcgggttcccaggtcaactattccatgggtcccatgacacctgcccttgcagggacctacagatgctttggttctgtcactcacttaccctatgagttgtcggctcccagtgaccctctggacatcgtggtcgtaggtctatatgggaaaccttctctctcagcccagccgggccccacggttcaggcaggagagaatgtgaccttgtcctgcagctcccggagcttgtttgacatttaccatctatccagggaggcggaggccggtgaacttaggctcactgcagtgctgagggtcaatggaacattccaggccaacttccctctgggccctgtgacccacggagggaactacagatgcttcggctctttccgtgccctgccccatgcgtggtcagacccgagtgacccactgcccgtttctgtcacaggtaactccagaaacctgcacgttctgattgggacctcagtggtcatcatcccctttgctatcctcctcttctttctccttcatcgctggtgtgccaacaaaaagaatgctgttgtaatggaccaagagcctgcagggaacagaacagtgaacagggaggactctgatgaacaagaccctcaggaggtgacatacgcacagttgaatcactgcgttttcacacagagaaaaatcactcgcccttctcagaggcccaagacacccccaacagataccagcgtgtaa
MSLMVVSMACVGFFLLEGPWPHVGGQDKPFLSAWPGTVVSEGQHVTLQCRSRLGFNEFSLSKEDGMPVPELYNRIFRNSFLMGPVTPAHAGTYRCCSSHPHSPTGWSAPSNPVVIMVTGVHRKPSLLAHPGPLVKSGETVILQCWSDVRFERFLLHREGITEDPLRLVGQLHDAGSQVNYSMGPMTPALAGTYRCFGSVTHLPYELSAPSDPLDIVVVGLYGKPSLSAQPGPTVQAGENVTLSCSSRSLFDIYHLSREAEAGELRLTAVLRVNGTFQANFPLGPVTHGGNYRCFGSFRALPHAWSDPSDPLPVSVTGNSRNLHVLIGTSVVIIPFAILLFFLLHRWCANKKNAVVMDQEPAGNRTVNREDSDEQDPQEVTYAQLNHCVFTQRKITRPSQRPKTPPTDTSV
MSLMVVSMACVGFFLLEGPWPHVGG
WPGTVVSEGQHVTLQCRSRLGFNEFSLSKEDGMPVPELYNRIFRNSFLMGPVTPAHAGTYRCCSSHPHSPTGWSAPSNPVVIMVT
HPGPLVKSGETVILQCWSDVRFERFLLHREGITEDPLRLVGQLHDAGSQVNYSMGPMTPALAGTYRCFGSVTHLPYELSAPSDPLDIVVV
QPGPTVQAGENVTLSCSSRSLFDIYHLSREAEAGELRLTAVLRVNGTFQANFPLGPVTHGGNYRCFGSFRALPHAWSDPSDPLPVSVTGNSRNLHVL
NLHVLIGTSVVIIPFAILLFFLL
HRWCANKKNAVVMDQEPAGNRTVNREDSDEQDPQEVTYAQLNHCVFTQRKITRPSQRPKT
VTYAQL
[0070] В некоторых вариантах осуществления mAb к белку KIR3DL3 получали из гибридом, описанных выше, и определяли сродство связывания каждого mAb, показанное ниже в таблице 3.
[0071] В некоторых вариантах осуществления после оценки сродства связывания гибридомы секвенировали. Секвенирование показало, что каждое из 14 полученных mAb имело уникальные последовательности VH и VL. Каждая VH или VL имеет три CDR (CDR1, CDR2 и CDR3). Эти последовательности представлены в SEQ ID NO: 1-333 и аннотированы ниже в таблице 4.





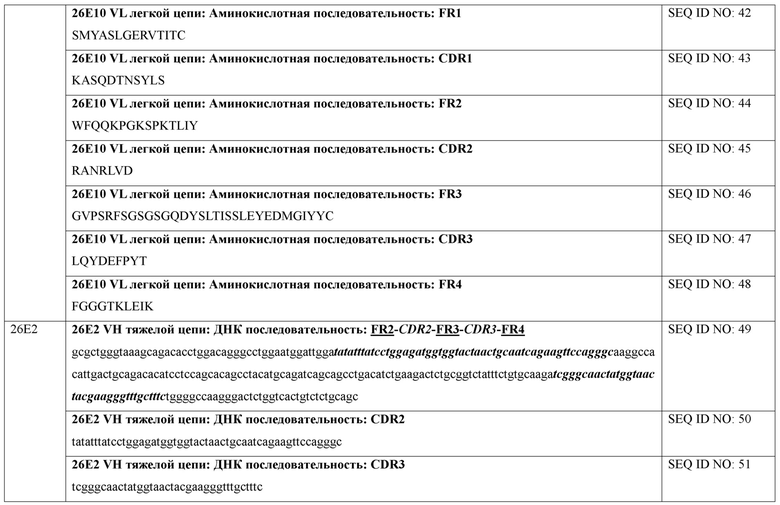

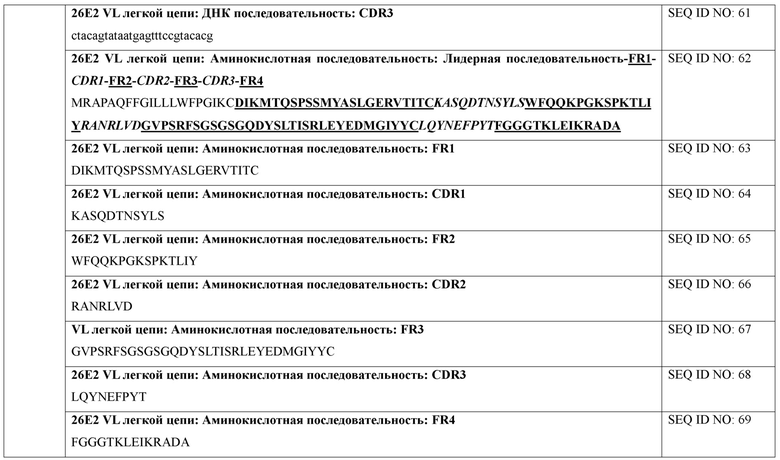













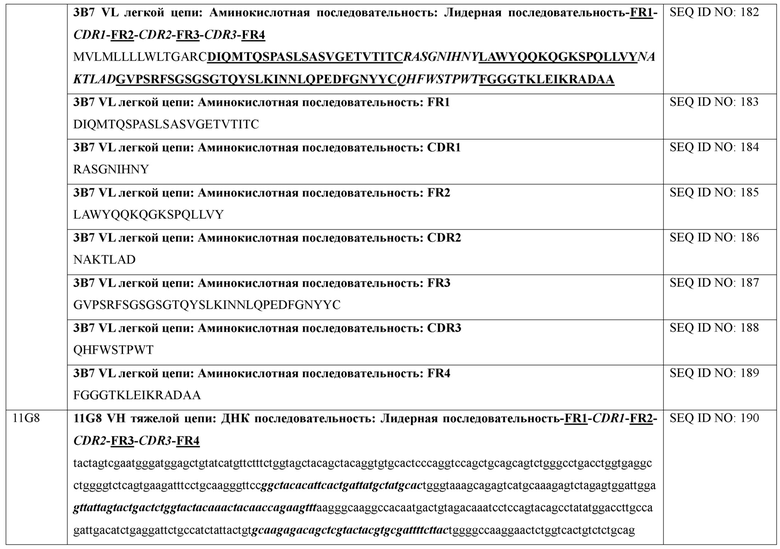















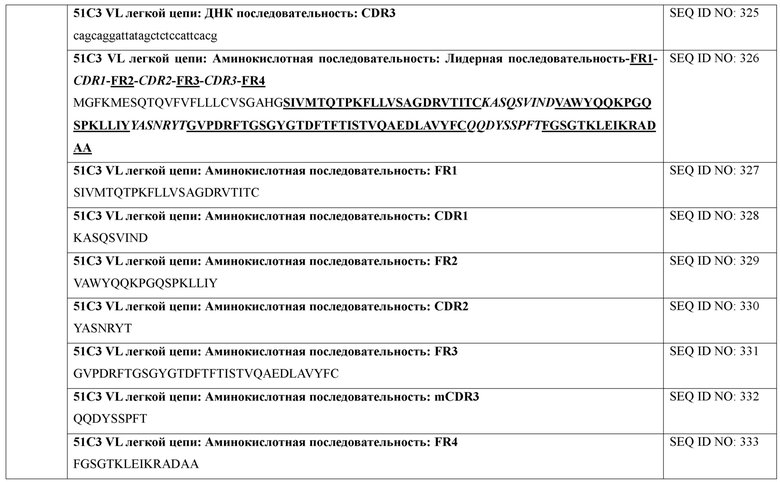
[0072] В некоторых вариантах осуществления представленные антитела или их иммуногенные фрагменты содержат последовательность, которая на по меньшей мере на 80% идентична (например, на по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% идентична) одной или более определяющим комплементарность областям (CDR) (например, CDR1, CDR2 или CDR3), перечисленным в таблице 4. В некоторых вариантах осуществления представленные антитела или их иммуногенные фрагменты содержат последовательность, которая на по меньшей мере 80% идентична одной или более CDR VH, перечисленным в таблице 4. В некоторых вариантах осуществления представленные антитела или их иммуногенные фрагменты содержат последовательность, которая на по меньшей мере 80% идентична двум или более CDR VH, перечисленным в таблице 4. В некоторых вариантах осуществления представленные антитела или их иммуногенные фрагменты содержат последовательность, которая на по меньшей мере 80% идентична трем CDR VH, перечисленным в таблице 4. В некоторых вариантах осуществления представленные антитела или их иммуногенные фрагменты содержат последовательность, которая на по меньшей мере 80% идентична одной или более CDR VL, перечисленным в таблице 4. В некоторых вариантах осуществления представленные антитела или их иммуногенные фрагменты содержат последовательность, которая на по меньшей мере 80% идентична двум или более CDR VL, перечисленным в таблице 4. В некоторых вариантах осуществления представленные антитела или их иммуногенные фрагменты содержат последовательность, которая на по меньшей мере 80% идентична трем CDR VL, перечисленным в таблице 4.
[0073] В некоторых вариантах осуществления антитело представляет собой или содержит гуманизированное антитело. «Гуманизированная» форма не относящегося к человеческому антитела (например, грызуна) представляет собой химерное антитело, включающее последовательность, полученную из нечеловеческого антитела. Во многих случаях гуманизированное антитело представляет собой человеческий иммуноглобулин, в котором остаток в гипервариабельном домене исследуемого вида заменен остатком в гипервариабельном домене вида, отличного от человека (донорское антитело), с желаемой специфичностью, сродством и способностью, например, мыши, крысы, кролика или примата, не являющегося человеком. В некоторых случаях остаток в каркасной области (FR) человеческого иммуноглобулина заменяют соответствующим остатком нечеловеческого происхождения. Кроме того, гуманизированное антитело может включать остаток, отсутствующий в реципиентном или донорском антителе. В некоторых вариантах осуществления такая модификация может быть выполнена для дальнейшего улучшения характеристик антитела. Как правило, гуманизированное антитело, по существу, может включать по меньшей мере один или, как правило, оба из двух вариабельных доменов, и в этом случае все или практически все гипервариабельные петли соответствуют гипервариабельным петлям нечеловеческого иммуноглобулина, и все или практически все FR соответствуют FR последовательности человеческого иммуноглобулина. Кроме того, гуманизированное антитело может необязательно включать по меньшей мере часть константного домена (Fc) иммуноглобулина или, как правило, константного домена человеческого иммуноглобулина. Методы, используемые для гуманизации моноклонального антитела, хорошо известны специалистам в данной области и были описаны ранее. См., например, патенты США №№ 4,816,567; 5,807,715; 5,866,692; 6,331,415; 5,530,101; 5,693,761; 5,693,762; 5,585,089; and 6,180,370; Jones 1986; Riechmann 1988; Vaswani & Hamilton 1998; Harris 1995; Hurle & Gross 1994. В некоторых аспектах настоящее изобретение относится к нуклеиновой кислоте, кодирующей гуманизированное антитело. Такая нуклеиновая кислота по настоящему изобретению может присутствовать в клетке, лизате клеток, в выделенной форме, частично очищенной форме или в по существу очищенной форме. Нуклеиновая кислота является «выделенной», «частично очищенной» или «по существу очищенной», когда она отделена от отличающихся от нее клеточных компонентов или других клеточных компонентов, например нуклеиновых кислот или белков других клеток, с помощью методов, известных специалистам в данной области, включая, без ограничений, обработку щелочью/SDS, окрашивание CsCl, колоночную хроматографию, электрофорез в агарозном геле или любой другой подходящий метод. Нуклеиновая кислота по настоящему изобретению может представлять собой, например, ДНК или РНК и может включать или не включать интронную последовательность.
Нуклеиновые кислоты
[0074] Настоящее изобретение включает нуклеиновые кислоты, содержащие одну или более нуклеотидных последовательностей, кодирующих одну или более тяжелых цепей, вариабельных доменов тяжелых цепей, каркасных областей тяжелых цепей, CDR тяжелых цепей, константных доменов тяжелых цепей, легких цепей, вариабельных доменов легких цепей, каркасных областей легких цепей, CDR легких цепей, константных доменов легких цепей или других иммуноглобулин-подобных последовательностей, антитела или связывающие молекулы, раскрытые в настоящем описании. В некоторых вариантах осуществления такие нуклеотидные последовательности могут присутствовать в векторе (например, в плазмидном или вирусном векторе). В некоторых вариантах осуществления такие нуклеотиды могут присутствовать в геноме клетки (например, клетки нуждающегося в лечении субъекта) или клетки, используемой для продуцирования антитела (например, клетки млекопитающего).
Экспрессия и связывание белка KIR3DL3
[0075] С помощью анализа РВМС методом сортинга флуоресцентно-активированных клеток (FACS) с использованием моноклональных анти-KIR3DL3 антител, представленных в настоящем описании, было показано, что белок KIR3DL3 широко экспрессируется на клеточной поверхности клеток врожденного иммунитета (NK-клеток, NKT-клеток, γδT-клеток) и клеток адаптивного иммунитета (CD8 Т-клетках и CD4 Т-клетках) (фиг. 1). В CD8 Т-клетках KIR3DL3 в основном экспрессируется на терминально дифференцированных эффекторных CD8 Т-клетках.
[0076] В ранее проведенных исследованиях было показано, что недавно обнаруженный HHLA2 является членом семейства B7 и продемонстрировали, что он способен ингибировать пролиферацию и функцию Т-клеток (Zhao 2013; патент США № 10,093,737). Последующие исследования показали, что HHLA2 сверхэкспрессируется при различных типах рака человека (Cheng 2018; Cheng 2017; Koirala 2016; Janakiram 2015). Для проверки связывания HHLA2 с KIR3DL1, KIR3DL2 и KIR3DL3 создавали клеточные линии 3T3, стабильно экспрессирующие KIR3DL1, KIR3DL2 или KIR3DL3 на клеточной поверхности. Результаты анализа FACS показали, что белок HHLA2 связывается с клетками 3T3, экспрессирующими KIR3DL3, но не с клетками 3T3, экспрессирующими KIR3DL1 или KIR3DL2 (фиг. 2A). Кроме того, анализ межклеточного конъюгата показывает, что клеточная линия 3T3, экспрессирующая HHLA2, связывается с клеточной линией 3T3, экспрессирующей KIR3DL3, но не с контрольной клеточной линией 3T3 (фиг. 2B). Эти результаты демонстрируют, что HHLA2 связывается с KIR3DL3, но не с его близкими гомологами KIR3DL1 и KIR3DL2.
[0077] Результаты, представленные в настоящем описании, дополнительно демонстрируют, что с HHLA2 связываются домен D0 и вся внеклеточная часть KIR3DL3 (фиг. 2C), предполагая, что домен D0 KIR3DL3 является функциональным доменом при взаимодействии между KIR3DL3 и HHLA2.
[0078] Поскольку HHLA2 может связываться как с KIR3DL3, так и/или с TMIGD2, используя метод FACS, выполняли конкурентные анализы, которые продемонстрировали, что TMIGD2 не может ингибировать связывание KIR3DL3 с HHLA2 (фиг. 3A), и что KIR3DL3 не может ингибировать связывание TMIGD2 с HHLA2 (фиг. 3B), предполагая, что KIR3DL3 и TMIGD2 связываются с неперекрывающимися участками на HHLA2.
KIR3DL3 ингибирует функции человеческих иммунных клеток, и mAb, блокирующие KIR3DL3, нейтрализуют подавление иммунитета, вызванное KIR3DL3.
[0079] В отличие от KIR3DL1 и KIR3DL2, которые связываются с HLA-A и/или HLA-B, KIR3DL3 связывается с HHLA2, но функция KIR3DL3 ранее была неизвестна (Beziat 2017). Для выяснения функции KIR3DL3 выполняли эксперименты, используя метод FACS для сортировки линии человеческих NK-клеток NK92 на KIR3DL3-положительную популяцию (KIR3DL3+ NK92) и KIR3DL3-отрицательную популяцию (KIR3DL3- NK92) по функции NK-опосредованного уничтожения. Результаты показывают, что клетки KIR3DL3- NK92 в равной степени убивают как HHLA2-положительные клетки K562 (HHLA2+ K562), так и HHLA2-отрицательные клетки K562 (HHLA2- K562) (фиг. 4A), но клетки KIR3DL3+ NK92 убивают клетки HHLA2- K562 намного эффективнее, чем клетки HHLA2+ K562 (фиг. 4А). Затем FACS использовали для сортировки KIR3DL3+CD8 Т-клеток (терминально дифференцированных эффекторных клеток) и размножения этих клеток в присутствии анти-CD3/CD28, IL-2 и фидерных клеток in vitro для получения достаточного количества клеток. Затем выполняли анализ опосредованного CD8 Т-клетками уничтожения, который показал, что KIR3DL3+ CD8 Т-клетки убивали клетки K562 намного эффективнее, чем клетки HHLA2+ K562 (фиг. 4B). Эти результаты демонстрируют, что KIR3DL3 ингибирует функции иммунных клеток при связывании с HHLA2.
[0080] После демонстрации того, что KIR3DL3 индуцирует иммунную супрессию (фиг. 4A-4B), выполняли эксперименты для определения, способны ли анти-KIR3DL3 mAb (такие как представленные в настоящем описании) блокировать функцию KIR3DL3. Чтобы проверить это, клетки KIR3DL3+ NK92 предварительно инкубировали либо с анти-KIR3DL3 mAb, либо с мышиными антителами IgG1 в качестве отрицательного контроля. В качестве доказательства принципа исследовали четыре анти-KIR3DL3 mAb (26E10, 34B10, 30D10, 8G7). После предварительной инкубации клетки анализировали на опосредованное NK-клетками уничтожение, как показано на фиг. 4А. После анализа цитотоксичности клетки, предварительно инкубированные с мышиным IgG1, не показали эффекта, в то время как клетки, предварительно инкубированные с анти-KIR3DL3 mAb (26E10, 34B10, 30D10, 8G7), продемонстрировали в значительной степени усиленное уничтожение целевых клеток HHLA2+ К562, опосредованное клетками KIR3DL3+ NK92 (фиг. 5А, 5В).
[0081] Внеклеточная часть HHLA2 включает домены IgV1, IgC и IgV2 (Zhao 2013). В ранее проведенной работе было получено анти-HHLA2 mAb, которое распознает части IgCIgV2 (566.1) (Zhao 2013). Впоследствии были сгенерированы два дополнительных анти-HHLA2 mAb (A3H11 и B5B5). Эти два антитела распознают домен IgV1. С помощью конкурентного анализа связывания было показано, что A3H11 и B5B5, а не 566.1, блокируют связывание белка KIR3DL3 с HHLA2 (фиг. 6A). Кроме того, в анализах уничтожения NK-клеток mAb A3H11 и B5B5, а не 566.1, нейтрализовали индуцированную KIR3DL3 супрессию иммунной системы (фиг. 6B). Эти результаты демонстрируют, что домен IgV1 HHLA2 может связываться с KIR3DL3, приводя к ингибированию иммунных клеток, и что mAb к домену IgV1 HHLA2 способны блокировать связывание HHLA2 с KIR3DL3 и нейтрализовать индуцированное KIR3DL3 подавление иммунитета.
[0082] Различные паттерны экспрессии между KIR3DL3 и TMIGD2 не известны. Поэтому были выполнены эксперименты с помощью метода FACS для изучения экспрессии этих двух рецепторов на человеческих иммунных клетках в PBMC. Эти эксперименты показали, что KIR3DL3-положительные CD8 и CD4 Т-клетки являются TMIGD2-отрицательными, тогда как NK-клетки могут быть KIR3DL3+/TMIGD2+, KIR3DL3+/TMIGD2-, KIR3DL3-/TMIGD2+ или KIR3DL3-/TMIGD2- (фиг. 7). Эти результаты показывают, что, хотя оба белка являются рецепторами для HHLA2, TMIGD2 и KIR3DL3 имеют разные паттерны экспрессии.
[0083] Для изучения связывания TMIGD2 с HHLA2 клеточные линии 3T3, экспрессирующие TMIGD2, окрашивали слитым полипептидом HHLA2 EC-Ig-Fc, слитым полипептидом HHLA-2-IgV1-hIgG или Ig (контроль) (фиг. 8). Полученные результаты показывают, что с TMIGD2 связывались домен IgV1 и вся внеклеточная часть HHLA2 (фиг. 8), предполагая, что домен IgV1 HHLA2 является функциональным доменом при взаимодействии между HHLA2 и TMIGD2.
KIR3DL3 ингибирует функции человеческих иммунных клеток путем рекрутинга SHP1/2 через мотив ITIM.
[0084] Для дальнейшего изучения механизма, с помощью которого KIR3DL3 опосредует подавление иммунных клеток, получали мутант KIR3DL3, Y381F, путем замены остатка тирозина (Y) в положении 381, расположенного в последовательности YAQL в мотиве ITIM, на остаток фенилаланина (F) (фиг. 10А). KIR3DL3-отрицательные (KIR3DL3-) клетки NK92 трансдуцировали конструкциями мутанта Y381F или KIR3DL3 WT и исследовали на экспрессию KIR3DL3 методом проточной цитометрии. Экспрессию KIR3DL3 WT и Y381F детектировали в клетках, трансдуцированных соответствующей конструкцией (фиг. 10А). Затем исследовали фосфорилирование тирозина у мутанта Y381F и KIR3DL3 WT. Вкратце, трансфицированные клетки NK92 культивировали в присутствии (+) или в отсутствие (-) перванадата (VO4, 1 мМ) в течение 5 минут при 37°C. Перванадат является ингибитором протеинтирозинфосфатазы и способствует фосфорилированию белков по остаткам тирозина. Клеточные лизаты подвергали иммунопреципитации анти-KIR3DL3 антителами и исследовали на предмет фосфорилирования тирозина с помощью иммуноблотов, используя анти-KIR3DL3 антитела и антитела к фосфорилированному тирозину (4G10). Показаны результаты как для лизатов цельных клеток (WCL), так и для образцов иммунопреципитации (IP) (фиг. 10B). Как и ожидалось, фосфорилирование тирозина было обнаружено в KIR3DL3WT, но не в Y381F.
[0085] Затем выполняли анализы цитотоксичности путем инкубации клеток NK92, экспрессирующих KIR3DL3 WT или Y381F, с клетками K562 или клетками Raji, экспрессирующими HHLA2 или контроль, при различных соотношениях эффектор/мишень (E:T) (фиг. 10C). Процент специфического лизиса вычисляли и наносили на график в зависимости от отношения E:T. Как показано, как в случае клеток K562, так и в случае клеток Raji цитотоксичность клеток NK92, экспрессирующих KIR3DL3 WT, и инкубированных с клетками, экспрессирующими HHLA2, существенно отличалась по сравнению с контролем, что согласуется с результатами, наблюдаемыми ранее. Однако цитотоксичность клеток NK92, экспрессирующих KIR3DL3 Y381F, не отличалась, что свидетельствует о том, что обеспечиваемое KIR3DL3 HHLA2-индуцированное подавление функции иммунных клеток осуществляется через мотив ITIM в KIR3DL3.
[0086] Наконец, учитывая важность фосфорилирования тирозина в мотиве ITIM в функционировании KIR3DL3 и роль протеинтирозинфосфатаз SHP-1/SHP-2 в иммунных клетках, проверяли, взаимодействует ли KIR3DL3 с SHP-1 или SHP-2. Вкратце, первичные KIR3DL3+ NK-клетки (35×106 клеток) обрабатывали с (+) или без (-) перванадата (VO4, 1 мМ) в течение 5 минут при 37°C. Анти-KIR3DL3 (дорожки 2, 4) или mIgG1 (дорожки 1, 3) иммунопреципитаты (IP) и лизаты цельных клеток (WCL) последовательно анализировали в отношении KIR3LD3, SHP-1 и SHP-2 с помощью вестерн-блоттинга. Как показано на фиг. 10D, эксперименты по совместной иммунопреципитации продемонстрировали, что KIR3DL3 взаимодействует как с SHP-1, так и с SHP-2, что свидетельствует о том, что KIR3DL3 ингибирует функции человеческих иммунных клеток путем рекрутинга SHP1/2 с участием мотива ITIM.
Экспрессия KIR3DL3 при раке
[0087] Для изучения уровней экспрессии мРНК KIR3DL3 в опухолях человека выполняли поиск среди 1425 линий опухолей человека. 40 лучших опухолевых линий, экспрессирующих самые высокие уровни мРНК KIR3DL3, представлены на фиг. 9. Из 40 исследованных опухолей (демонстрирующих самые высокие уровни мРНК KIR3DL3) многие линии опухолей являются гематологическими злокачественными новообразованиями человека, что предполагает особую роль нацеливания на KIR3DL3 в лечении этих состояний.
[0088] В опухолях человека также исследовали экспрессию KIR3DL3 на уровне белка, и было обнаружено, что KIR3DL3 экспрессируется на инфильтрирующих опухоль иммунных клетках при различных видах рака человека, включая рак почки, рак желудка, рак легких, желчного пузыря и поджелудочной железы (фиг. 11). В совокупности, эти данные свидетельствуют о том, что путь KIR3DL3 представляет собой новый иммуносупрессивный механизм в микроокружении опухоли и привлекательную мишень для терапии рака человека.
Композиции
[0089] В некоторых аспектах настоящее изобретение относится к композициям, содержащим антитело, слитый полипептид, нуклеиновую кислоту или малую молекулу в соответствии с раскрытым и представленным в настоящем описании вариантом осуществления.
[0090] В некоторых вариантах осуществления композиция дополнительно содержит фармацевтически приемлемое вспомогательное вещество. Неограничивающие примеры фармацевтически приемлемых вспомогательных веществ включают, например, описанные в «Remington: The Science and Practice of Pharmacy», 19-е изд. (1995) или последнем издании, Mack Publishing Co; A. Gennaro (2000) "Remington: The Science and Practice of Pharmacy", 20th ed., Lippincott, Williams, & Wilkins; Pharmaceutical Dosage Forms and Drug Delivery Systems (1999) H. C. Ansel et al., eds., 7th ed., Lippincott, Williams, & Wilkins; and Handbook of Pharmaceutical Excipients (2000) A. H. Kibbe et al., eds., 3rd ed. Amer. Pharmaceutical Assoc. В некоторых вариантах осуществления композиция подходит для введения субъекту, например стерильная композиция. В некоторых вариантах осуществления композиция подходит для введения субъекту-человеку, например, композиция является стерильной и не содержит поддающихся обнаружению пирогенов и/или других токсинов.
[0091] В некоторых вариантах осуществления композиция содержит другие компоненты, такие как маннит фармацевтической чистоты, лактозу, крахмал, стеарат магния, сахаринат натрия, тальк, целлюлозу, глюкозу, сахарозу, магний, карбонат и т.п. В некоторых вариантах осуществления композиции содержат фармацевтически приемлемое вспомогательное вещество, необходимое для приближения к физиологическим условиям, такое как агенты, регулирующие рН и буферные агенты, агенты, регулирующие токсичность, и т.п., например, ацетат натрия, хлорид натрия, хлорид калия, хлорид кальция, лактат натрия, гидрохлоридные, сульфатные соли, сольваты (например, смешанные ионные соли, вода, органические соединения), гидраты (например, вода) и т.п.
[0092] В некоторых вариантах осуществления композиции представлены в виде водного раствора, порошка, гранул, таблеток, пилюль, суппозиториев, капсул, суспензий, спреев и т.п. Композиция может содержать фармацевтически приемлемое вспомогательное вещество, фармацевтически приемлемую соль, разбавители, носители, несущие среды и аналогичные другие неактивные агенты, хорошо известные специалистам в данной области. Носители и вспомогательные вещества, обычно используемые в фармацевтических препаратах, включают, например, тальк, гуммиарабик, лактозу, крахмал, стеарат магния, масло какао, водные или неводные растворители, масла, производные парафина, гликоли и т.д. Растворы можно приготовить с помощью воды или физиологически совместимых органических растворителей, таких как этанол, 1,2-пропиленгликоль, полигликоли, диметилсульфоксид, жирные спирты, триглицериды, неполные сложные эфиры глицерина и т.п. Парентеральные композиции могут быть приготовлены с помощью обычных способов, которые могут включать стерильный изотонический раствор, воду, 1,3-бутандиол, этанол, 1,2-пропиленгликоль, полигликоли, смешанные с водой, раствор Рингера и т.д. В одном из аспектов для облегчения определения локализации и надлежащего размещения композиции в предполагаемом месте лечения добавляют краситель.
[0093] Композиции могут включать консервант и/или стабилизатор. Неограничивающие примеры консервантов включают метил-, этил-, пропил-парабены, бензоат натрия, бензойную кислоту, сорбиновую кислоту, сорбат калия, пропионовую кислоту, хлорид бензалкония, бензиловый спирт, тимеросал, соли фенилмеркурата, хлоргексидин, фенол, 3-крезол, четвертичные аммониевые соединения (QAC), хлорбутанол, 2-этоксиэтанол и имидомочевину.
[0094] Для контроля тоничности композиция может содержать физиологическую соль, такую как натриевая соль. Предпочтительным является хлорид натрия (NaCl), который может присутствовать в количестве от 1 до 20 мг/мл. Другие соли, которые могут присутствовать, включают хлорид калия, дигидрофосфат калия, динатрийфосфата дегидрат, хлорид магния и хлорид кальция.
[0095] Композиции могут включать один или более буферов. Типичные буферы включают: фосфатный буфер; трис-буфер; боратный буфер; сукцинатный буфер; гистидиновый буфер; или цитратный буфер. Буферы обычно включают в концентрации от 5 до 20 мМ. Значение pH композиции обычно составляет от 5 до 8, а чаще от 6 до 8, например, от 6,5 до 7,5 или от 7,0 до 7,8.
[0096] Композицию можно вводить любым подходящим способом, который будет очевиден специалисту в данной области, в зависимости от заболевания или состояния, подлежащего лечению. Типичные пути введения включают внутривенный, внутриартериальный, внутримышечный, подкожный, внутричерепной, интраназальный или внутрибрюшинный.
[0097] В некоторых вариантах осуществления композиция может включать криопротектор. Неограничивающие примеры криопротекторов включают гликоль (например, этиленгликоль, пропиленгликоль и глицерин), диметилсульфоксид (ДМСО), формамид, сахарозу, трегалозу, декстрозу и любые их комбинации.
[0098] Композиция может содержать фармацевтически приемлемое вспомогательное вещество, фармацевтически приемлемую соль, разбавители, носители, наполнители и аналогичные другие неактивные агенты, хорошо известные специалистам в данной области. Носители и вспомогательные вещества, обычно используемые в фармацевтических препаратах, включают, например, тальк, гуммиарабик, лактозу, крахмал, стеарат магния, масло какао, водные или неводные растворители, масла, производные парафина, гликоли и т.д. Растворы можно приготовить с помощью воды или физиологически совместимых органических растворителей, таких как этанол, 1,2-пропиленгликоль, полигликоли, диметилсульфоксид, жирные спирты, триглицериды, неполные сложные эфиры глицерина и т.п. Парентеральные композиции могут быть приготовлены обычными способами, которые могут включать стерильный изотонический раствор, воду, 1,3-бутандиол, этанол, 1,2-пропиленгликоль, полигликоли, смешанные с водой, раствор Рингера и т.д. В одном из аспектов для облегчения определения локализации и надлежащего размещения композиции в предполагаемом месте лечения добавляют краситель.
[0099] В некоторых аспектах в настоящем описании представлена молекула нуклеиновой кислоты, кодирующая антитела или их иммуногенные фрагменты.
[0100] В одном из аспектов представлен вектор, кодирующий молекулу нуклеиновой кислоты, раскрытую в настоящем описании. В некоторых аспектах представлена клетка-хозяин, содержащая молекулу нуклеиновой кислоты, раскрытую в настоящем описании, или вектор, раскрытый в настоящем описании.
[0101] В некоторых вариантах осуществления антитело является гуманизированным.
[0102] В одном из аспектов представлен набор частей, содержащий указанную выше композицию. Набор может дополнительно содержать документ или руководство пользователя, в котором описан протокол получения антител, слитого полипептида, нуклеиновых кислот и/или малых молекул и/или введения нуждающемуся в этом субъекту.
Способы применения и лечения
[0103] В настоящем описании представлены способы применения и лечения нуждающегося в этом субъекта. В некоторых вариантах осуществления в настоящем описании представлены антитела, слитый полипептид, нуклеиновая кислота и/или малые молекулы для применения в терапии. В других вариантах осуществления в настоящем описании представлены антитела, слитый полипептид, нуклеиновые кислоты и/или малые молекулы для применения в производстве лекарственного средства.
[0104] В настоящем описании также представлены способы лечения субъекта, включающие введение субъекту терапевтически эффективного количества антитела, слитого полипептида, нуклеиновой кислоты и/или малой молекулы в соответствии с раскрытым и представленным в настоящем описании вариантом осуществления.
[0105] В настоящем описании также представлены композиции, содержащие антитело, его иммуногенный фрагмент, слитый полипептид или их комбинацию (например, в составе химерного антигенного рецептора и/или конъюгата антитело-лекарственное средство) в соответствии с раскрытыми и представленными в настоящем описании вариантами осуществления, для применения при лечении субъекта, страдающего от состояния.
[0106] В некоторых вариантах осуществления введение антитела, представленного в настоящем описании, достигается путем введения субъекту нуклеиновой кислоты, кодирующей антитело. Нуклеиновые кислоты, кодирующие антитело, представленное в настоящем описании, могут быть включены в генную конструкцию для использования в качестве части протокола генной терапии для доставки этих нуклеиновых кислот, которые можно использовать для экспрессии и продуцирования антитела внутри клеток. Экспрессионные конструкции таких компонентов можно вводить в любом терапевтически эффективном носителе, например, в любом составе или композиции, способной эффективно доставлять ген компонента в клетки in vivo. Подходы включают вставку нуклеиновой кислоты, кодирующей представленное в настоящем описании антитело, в вирусные векторы, включая рекомбинантные ретровирусы, аденовирусы, аденоассоциированные вирусы, лентивирусы, вирус простого герпеса-1 (HSV-1), или рекомбинантные бактериальные или эукариотические плазмиды. Вирусные векторы можно трансфицировать непосредственно в клетки; плазмидная ДНК может быть доставлена с помощью, например, катионных липосом (например, Lipofectin®), дериватизации, полилизиновых конъюгатов, грамицидина S, искусственных вирусных оболочек или других подходящих внутриклеточных носителей, прямой инъекции или CaPO4 осаждения (см., например, WO 04/060407). Примеры подходящих ретровирусов включают, без ограничения, pLJ, pZIP, pWE и pEM, известные специалистам в данной области (см., например, Eglitis 1985; Danos & Mulligan 1988; Wilson 1988; Armentano 1990; Huber 1991; Ferry 1991; Chowdhury 1991; van Beusechem 1992; Kay 1992; Dai 1992; Hwu 1993; патенты США № 4,868,116 и 4,980,286; публикации РСТ № WO89/07136; WO89/02468; WO89/05345; и WO92/07573). В другой системе вирусной доставки гена, которую можно использовать для доставки антитела или нуклеиновой кислоты, кодирующей антитело согласно настоящему изобретению, используются векторы, полученные из аденовируса (см., например, Berkner 1988; Rosenfeld 1991; Rosenfeld 1992). Подходящие аденовирусные векторы, полученные из штамма аденовируса Ad типа 5 dl324 или других штаммов аденовируса (например, Ad2, Ad3, Ad7 и т.д.), известны специалистам в данной области. Еще одной вирусной векторной системой, которую можно использовать для доставки антитела или нуклеиновой кислоты, кодирующей антитело согласно настоящему изобретению, является аденоассоциированный вирус (AAV). См., например, Flotte 1992; Samulski 1989; and McLaughlin 1988.
[0107] В некоторых вариантах осуществления субъект имеет состояние, при котором усиление иммунного ответа может принести пользу, такое как инфекция, заболевание или рак. В этих вариантах осуществления композиции, представленные в настоящем описании (включая антитела, слитые полипептиды, нуклеиновые кислоты и/или малые молекулы), можно использовать для блокирования функции KIR3DL3. В других вариантах осуществления субъект имеет состояние, при котором может помочь подавление иммунного ответа, такое как аутоиммунное заболевание или случаи, связанные с трансплантацией. В этих вариантах осуществления композиции, представленные в настоящем описании (включая антитела, слитые полипептиды, нуклеиновые кислоты и/или малые молекулы), можно использовать для стимуляции функции KIR3DL3.
[0108] В некоторых вариантах осуществления рак представляет собой хронический лимфолейкоз (CLL), острый лейкоз, острый лимфолейкоз (ALL), В-клеточный острый лимфолейкоз (В-ALL), Т-клеточный острый лимфолейкоз (Т-ALL), Т-клеточную лимфому, В-клеточную лимфому, хронический миелогенный лейкоз (CML), острый миелогенный лейкоз, В-клеточный пролимфоцитарный лейкоз, бластную плазмоцитоидную дендритно-клеточную опухоль, лимфому Беркитта, диффузную крупноклеточную В-клеточную лимфому, фолликулярную лимфому, волосатоклеточный лейкоз, мелкоклеточную фолликулярную лимфому, крупноклеточную фолликулярную лимфому, злокачественные лимфопролиферативные состояния, лимфому, ассоциированную со слизистой оболочкой (MALT), лимфому из мантийных клеток, лимфому маргинальной зоны, множественную миелому, миелодисплазиию и миелодиспластический синдром, неходжкинскую лимфому, лимфому Ходжкина, плазмобластную лимфому, новообразование из плазмоцитоидных дендритных клеток, макроглобулинемию Вальденстрема или прелейкемию.
[0109] В некоторых вариантах осуществления рак представляет собой гематологическое злокачественное новообразование человека. Например, в некоторых вариантах осуществления гематологическое злокачественное новообразование человека может быть выбрано из миелоидного новообразования, острого миелоидного лейкоза (AML), AML с рецидивирующими генетическими аномалиями, AML с изменениями, связанными с миелодисплазией, AML, связанного с терапией, острых лейкозов неоднозначного происхождения, миелопролиферативного новообразования, эссенциальной тромбоцитемии, истинной полицитемии, миелофиброза (MF), первичного миелофиброза, системного мастоцитоза, миелодиспластических синдромов (MDS), миелопролиферативных/миелодиспластических синдромов, хронического миелоидного лейкоза, хронического нейтрофильного лейкоза, хронического эозинофильного лейкоза, миелодиспластических синдромов (MDS), рефрактерной анемии с кольцевидными сидеробластами, рефрактерной цитопении с многолинейной дисплазией, рефрактерной анемии с избытком бластов (тип 1), рефрактерной анемии с избытком бластов (тип 2), MDS с изолированной делецией (5q), неклассифицируемого MDS, миелопролиферативных/миелодиспластических синдромов, хронического миеломоноцитарного лейкоза, атипичного хронического миелоидного лейкоза, ювенильного миеломоноцитарного лейкоза, неклассифицируемых миелопролиферативных/миелодисплатических синдромов, лимфоидных новообразований, предраковых лимфоидных новообразований, В-лимфобластного лейкоза, В-лимфобластной лимфомы, Т-лимфобластного лейкоза, Т-лимфобластной лимфомы, новообразований из зрелых В-клеток, диффузной крупноклеточной В-клеточной лимфомы, первичной лимфомы центральной нервной системы, первичной медиастинальной В-клеточной лимфомы, лимфомы/лейкемии Беркитта, фолликулярной лимфомы, хронического лимфолейкоза, малой лимфоцитарной лимфомы, В-клеточного пролимфоцитарного лейкоза, лимфоплазмоцитарной лимфомы, макроглобулинемии Вальденстрема, лимфомы из мантийных клеток, лимфомы маргинальной зоны, посттрансплантационных лимфопролиферативных заболеваний, ВИЧ-ассоциированных лимфом, первичной выпотной лимфомы, внутрисосудистой крупноклеточной В-клеточной лимфомы, первичной кожной В-клеточной лимфомы, волосатоклеточного лейкоза, множественной миеломы, моноклональной гаммапатии неясного генеза (MGUS), тлеющей множественной миеломы или солитарных плазмоцитом (солитарных костных и экстрамедуллярных).
[0110] В некоторых вариантах осуществления рак представляет собой рак надпочечников, рак анального канала, базальноклеточный и плоскоклеточный рак кожи, рак желчных протоков, рак мочевого пузыря, рак костей, опухоли головного и спинного мозга, рак молочной железы, рак шейки матки, колоректальный рак, рак эндометрия, рак пищевода, опухоли семейства Юинга, рак глаза (меланома глаза), рак желчного пузыря, рак желудка, гастроинтестинальные нейроэндокринные (карциноидные) опухоли, гастроинтестинальную стромальную опухоль (GIST), гестационную трофобластическую болезнь, саркому Капоши, рак почки, рак гортани и гипофоренгиальный рак, рак печени, рак легкого, карциноидную опухоль легкого, злокачественную мезотелиому, меланому кожи, рак кожи из клеток Меркеля, рак полости носа и придаточных пазух, рак носоглотки, нейробластому, немелкоклеточный рак легкого, новообразования центральной нервной системы (ЦНС), рак полости рта и ротоглотки, остеосаркому, рак яичников, рак поджелудочной железы, нейроэндокринную опухоль поджелудочной железы (NET), рак полового члена, опухоли гипофиза, рак простаты, ретинобластому, рабдомиосаркому, рак слюнных желез, рак кожи, мелкоклеточный рак легкого, рак тонкой кишки, саркому мягких тканей, рак желудка, рак яичка, рак вилочковой железы, рак щитовидной железы, саркому матки, рак влагалища, рак вульвы, макроглобулинемию Вальденстрема, опухоль Вильмса, плоскоклеточный рак, рак, вызванный окружающей средой, комбинацию раковых заболеваний и метастатических поражений, вызванных раковыми заболеваниями. В некоторых вариантах осуществления рак представляет собой лейкоз или лимфому, например, лимфобластную лимфому или В-клеточную неходжкинскую лимфому. В некоторых вариантах осуществления рак представляет собой метастатический рак.
[0111] В некоторых вариантах осуществления способы лечения субъекта, страдающего от рака, включают введение субъекту терапевтически эффективного количества антитела, слитого полипептида, нуклеиновой кислоты и/или малой молекулы в соответствии с раскрытым и представленным в настоящем описании вариантом осуществления, в комбинации с одной или более дополнительными видами терапии рака, нацеленными на конкретный тип рака, в течение длительного периода времени для получения улучшенных или синергетических терапевтических эффектов. В некоторых вариантах осуществления один или более дополнительных видов терапии рака выбирают из химиотерапии, лучевой терапии, иммунотерапии, хирургии и их комбинации. Например, антитело, слитый полипептид, нуклеиновая кислота, малая молекула и/или их композиция могут быть введены в комбинации с одним или более дополнительными химиотерапевтическими агентами. В другом примере антитело, слитый полипептид, нуклеиновую кислоту, малую молекулу и/или их композицию можно вводить в комбинации с одним или более дополнительными иммунотерапевтическими агентами. Такие способы можно использовать для лечения любого ракового заболевания или типа опухоли, где KIR3DL3 играет роль в регуляции функций иммунных клеток, включая, помимо прочего, первичный, рецидивирующий и метастатический рак, как указано выше.
[0112] «Терапевтически эффективное количество» антитела, слитого полипептида, нуклеиновой кислоты и/или малой молекулы, в контексте настоящего описания, представляет собой количество антитела, слитого полипептида, нуклеиновой кислоты и/или малой молекулы, которое обеспечивает желаемый эффект у субъекта для лечения и/или профилактики состояния, например, терапевтический эффект. В некоторых вариантах осуществления терапевтически эффективное количество представляет собой количество антитела, слитого полипептида, нуклеиновой кислоты и/или малой молекулы, которое обеспечивает максимальный терапевтический эффект. В других вариантах осуществления терапевтически эффективное количество обеспечивает терапевтический эффект, меньший, чем максимальный терапевтический эффект. Например, терапевтически эффективное количество может представлять собой количество, которое оказывает терапевтическое действие, не вызывая при этом одного или более побочных эффектов, связанных с дозой, обеспечивающей максимальный терапевтический эффект. Терапевтически эффективное количество конкретной композиции будет меняться в зависимости от множества факторов, включая, помимо прочего, характеристики терапевтической композиции (например, активность, фармакокинетику, фармакодинамику и биодоступность), физиологическое состояние субъекта (например, возраст, массу тела, пол, тип и стадию заболевания, историю болезни, общее физическое состояние, реакцию на данную дозу и другие присутствующие лекарственные средства), природу любых фармацевтически приемлемых носителей, наполнителей и консервантов в композиции, и путь введения. Специалист в клинической и фармакологической области сможет определить терапевтически эффективное количество с помощью рутинных экспериментов, а именно путем мониторинга реакции у субъекта на введение антитела, слитого полипептида, нуклеиновой кислоты и/или малой молекулы и соответствующего регулирования дозировки. Для получения дополнительных рекомендаций см., например, Remington: The Science and Practice of Pharmacy, 22-е изд., Pharmaceutical Press, London, 2012, и Goodman & Gilman's The Pharmacological Basis of Therapeutics, 12-е изд., McGraw-Hill, New York, NY, 2011, полное раскрытие которого включено в настоящее описание посредством ссылки.
[0113] В некоторых вариантах осуществления терапевтически эффективное количество антитела, слитого полипептида, нуклеиновой кислоты и/или малой молекулы, раскрытых в настоящем описании, находится в диапазоне от примерно 10 мг/кг до примерно 150 мг/кг, от 30 мг/кг до примерно 120 мг/кг, от 60 мг/кг до примерно 90 мг/кг. В некоторых вариантах осуществления терапевтически эффективное количество антитела, слитого полипептида, нуклеиновой кислоты и/или малой молекулы, раскрытых в настоящем описании, составляет примерно 15 мг/кг, примерно 30 мг/кг, примерно 45 мг/кг, примерно 60 мг/кг, примерно 75 мг/кг, примерно 90 мг/кг, примерно 105 мг/кг, примерно 120 мг/кг, примерно 135 мг/кг или примерно 150 мг/кг. Субъекту можно вводить одну дозу или более доз антитела, слитого полипептида, нуклеиновой кислоты и/или малой молекулы. В некоторых вариантах осуществления антитело, слитый полипептид, нуклеиновую кислоту и/или малую молекулу вводят один или более раз в сутки.
[0114] Специалистам в данной области известно множество способов, которые в соответствующих обстоятельствах можно использовать для введения субъекту, например человеку. Например, в некоторых вариантах осуществления введение может быть системным или местным. В некоторых вариантах осуществления введение может быть энтеральным или парентеральным. Кроме того, в компетенцию специалиста в данной области входит выбор подходящего пути введения, такого как пероральное введение, подкожное введение, внутривенное введение, внутримышечное введение, внутрикожное введение, подоболочечное введение или внутрибрюшинное введение. Для лечения нуждающегося в этом субъекта антитело, слитый полипептид, нуклеиновую кислоту и/или малую молекулу можно вводить непрерывно или периодически, для обеспечения немедленного высвобождения, контролируемого высвобождения или замедленного высвобождения. Кроме того, антитело, слитый полипептид, нуклеиновую кислоту и/или малую молекулу можно вводить один раз в сутки, два раза в сутки, три раза в сутки или четыре раза в сутки в течение 3 дней, 5 дней, 7 дней, 10 дней, 2 недель, 3 недель, 4 недель, 8 недель или 12 недель. В некоторых вариантах осуществления антитело, слитый полипептид, нуклеиновую кислоту и/или малую молекулу можно вводить ежедневно, через день, каждый третий день, еженедельно, раз в две недели (т.е. каждую вторую неделю), каждую третью неделю, ежемесячно, раз в два месяца или каждый третий месяц. Антитело, слитый полипептид, нуклеиновую кислоту и/или малую молекулу можно вводить в течение предварительно определенного периода времени. Альтернативно, антитело, слитый полипептид, нуклеиновую кислоту и/или малую молекулу можно вводить до тех пор, пока не будет достигнут конкретный терапевтический контрольный показатель. В некоторых вариантах осуществления способы, представленные в настоящем описании, включают стадию оценки одного или более терапевтических контрольных показателей, таких как, без ограничения, уровень определенных биомаркеров в биологическом образце, таком как циркулирующие в крови опухолевые клетки, образце биопсии или мочи для определения необходимости в продолжении введения антитела, слитого полипептида, нуклеиновой кислоты и/или малой молекулы. В некоторых вариантах осуществления, связанных с раком, антитело, слитый полипептид, нуклеиновую кислоту и/или малую молекулу можно вводить до тех пор, пока не будет остановлен или обращен вспять рост опухоли, пока не будет уничтожена одна или более опухолей или пока количество раковых клеток не уменьшится до определенного уровня.
[0115] Как показано в рабочих примерах, блокада KIR3DL3 с помощью антител способствует противоопухолевому иммунитету и подавляет рост опухоли в мышиных моделях аденокарциномы легкого. В качестве стандартного лечения, лечение ранних стадий рака легкого, включая немелкоклеточный рак легкого (NSCLC), включает хирургическое вмешательство, фотодинамическую терапию, лазерную терапию, брахитерапию, химиотерапию и лучевую терапию и/или любую их комбинацию. Для более поздних стадий рака легких стандартное лечение включает химиотерапию, лучевую терапию, иммунотерапию и/или любую их комбинацию. В некоторых вариантах осуществления химиотерапевтические средства для лечения рака легкого включают, без ограничения, цисплатин (Платинол), карбоплатин (Параплатин), доцетаксел (Таксотер), гемцитабин (Гемзар), паклитаксел (Таксол), винорелбин (Навельбин), пеметрексед (Алимта), связанный с альбумином паклитаксел (Абраксан), этопозид (Вепесид или Этопофос), доксорубицин (Адриамицин), ифосфамид (Ифекс), иринотекан (Камптозар), топотекан (Гикамтин), винбластин (Онковир) и винкристин (Онковин). В некоторых вариантах осуществления иммунотерапевтические средства для лечения рака легкого включают, без ограничения, пембролизумаб (Кейтруда), ниволумаб (Опдиво), ипилимумаб (Ервой), бевацизумаб (Авастин), атезолизумаб (Тецентрик) и нецитумумаб (Портрацца).
[0116] В некоторых вариантах осуществления инфекция вызывана патогеном. В некоторых вариантах осуществления патоген может представлять собой вирус, бактерию, прион, грибок или паразит. Неограничивающие примеры вирусов, которые поддаются лечению с помощью изобретения, включают вирусы иммунодефицита человека (ВИЧ) (например, ВИЧ-1 и ВИЧ-2), вирусы гриппа (например, вирусы гриппа А, В и С), папилломавирусы, коронавирусы (например, респираторный коронавирус человека), вирусы гепатита (например, вирусы гепатита A-G) или герпесвирусы (например, HSV 1-9), вирус Западного Нила, вирус Зика, вирус энцефаломиокардита, вирус денге или эболавирус. Неограничивающие примеры бактерий, которые поддаются лечению с помощью изобретения, включают Mycobacterium tuberculosis, Campylobacter jejuni, Staphylococcus aureus, Borrelia burgdorferi, Helicobacter pylori, Salmonella enterica, E. coli, Streptococcus pyogenes, multiple drug resistant S. aureus, Chlamydia pneumoniae, Clostridium botulinum, Vibrio vulnificus, Parachlamydia, Corynebacterium amycolatum, Klebsiella pneumoniae, резистентные к линезолиду энтерококки (E. faecalis и E. faecium) и Acinetobacter baumannii с множественной лекарственной устойчивостью. Неограничивающие примеры грибов, которые поддаются лечению с помощью изобретения, включают Pneumocystis jirovecii (PJP), Candida, Blastomyces, Coccidioides, Cryptococcus, Histoplasma, Paracoccidioides, Aspergillus, Talaromyces и Sporothrix. В некоторых вариантах осуществления инфекция может представлять собой ВИЧ, пневмоцисту или микобактерии туберкулеза.
[0117] В некоторых вариантах осуществления аутоиммунное заболевание выбирают из группы, состоящей из острого диссеминированного энцефаломиелита (ADEM), очаговой алопеции, антифосфолипидного синдрома, аутоиммунной кардиомиопатии, аутоиммунной гемолитической анемии, аутоиммунного гепатита, аутоиммунного заболевания внутреннего уха, аутоиммунного липопролиферативного синдрома, аутоиммунной периферической невропатии, аутоиммунного панкреатита, аутоиммунного полиэндокринного синдрома, аутоиммунного прогестеронового дерматита, аутоиммунной тромбоцитопенической пурпуры, аутоиммунной крапивницы, аутоиммунного увеита, болезни Бехчета, глютеновой болезни, болезни Шагаса, болезни холодовых агглютининов, болезни Крона, дерматомиозита, сахарного диабета 1 типа, эозинофильного фасциита, пемфигоида желудочно-кишечного тракта, синдрома Гудпасчера, синдрома Грейвса, синдрома Гийена-Барре, энцефалопатии Хашимото, тиреоидита Хашимото, красной волчанки, синдрома Миллера-Фишера, смешанного заболевания соединительной ткани, тяжелой миастении, вульгарной пузырчатки, пернициозной анемии, полимиозита, псориаза, псориатического артрита, рецидивирующего полихондрита, ревматоидного артрита, ревматической атаки, синдрома Шегрена, височного артериита, поперечного миелита, язвенного колита, недифференцированного заболевания соединительной ткани, васкулита и гранулематоза Вегенера.
[0118] В одном из вариантов осуществления подлежащее лечению аутоиммунное заболевание представляет собой ревматоидный артрит взрослых.
[0119] В некоторых вариантах осуществления состояние представляет собой наличие трансплантата. В этих вариантах осуществления композиции и способы, представленные в настоящем описании, могут быть использованы для подавления отторжения трансплантата. В некоторых вариантах осуществления трансплантат представляет собой трансплантат стволовых клеток или костного мозга, например, у субъекта с болезнью «трансплантат против хозяина». В некоторых вариантах осуществления трансплантат выбирают из группы, состоящей из трансплантата почки, трансплантата легкого, трансплантата сердца, трансплантата поджелудочной железы, трансплантата роговицы или трансплантата печени.
[0120] В некоторых вариантах осуществления антитело, представленное в настоящем описании, может быть включено в курс лечения, который дополнительно включает введение субъекту по меньшей мере одного дополнительного агента.
[0121] В некоторых вариантах осуществления способы, представленные в настоящем описании, могут применяться в сочетании с дополнительной терапией, например, в виде комбинированной терапии. В некоторых вариантах осуществления дополнительная терапия может представлять собой терапию иммуноассоциированного расстройства или состояния, включая раскрытое в настоящем описании. Например, раскрытая в настоящем описании композиция может быть введена субъекту одновременно, до или после лучевой терапии, химиотерапии, гормональной терапии, клеточной терапии и/или другой противоопухолевой или антиаутоиммунной терапии. В некоторых вариантах осуществления композицию можно вводить субъекту одновременно, до или после трансплантации органа.
[0122] В некоторых вариантах осуществления дополнительный агент, вводимый в комбинации с антителом, представленным в настоящем описании, можно вводить одновременно с антителом, в тот же день, что и антитело, или в пределах той же недели, что и антитело. В некоторых вариантах осуществления дополнительный агент, вводимый в комбинации с антителом, представленным в настоящем описании, можно вводить в одном составе. В некоторых вариантах осуществления введение дополнительного агента может быть отделено от введения антитела, представленного в настоящем описании, временным интервалом, таким как, один или более часов до или после, один или более дней до или после, одна или более недель до или после или один или более месяцев до или после введения представленного антитела. В различных вариантах осуществления частота введения одного или более дополнительных агентов может быть такой же, аналогичной или отличной от частоты введения антитела, представленного в настоящем описании.
[0123] В некоторых вариантах осуществления комбинированная терапия может представлять собой схему лечения, которая включает введение двух разных антител, представленных в настоящем описании, и/или режим лечения, который включает введение антитела, представленного в настоящем описании, в виде множества составов и/или способов введения.
[0124] В некоторых вариантах осуществления дополнительный агент может представлять собой или включать одно или более лекарственных веществ. Например, в некоторых вариантах осуществления дополнительный агент может представлять собой или включать одно или более лекарственных веществ, действие которых направлено на подавление иммунных ответов, например, для эффективного лечения пациентов с аутоиммунными заболеваниями или для предотвращения отторжения трансплантата. Например, доступные в настоящее время средства для лечения ревматоидного артрита и в случае трансплантации почки включают абатацепт (Orencia®) и бетацепт (Nulojix®), модифицированные слитые полипептиды антител, содержащие внеклеточный домен человеческого цитотоксического Т-лимфоцит-ассоциированного антигена 4 (CTLA-4), связанный с Fc-областью IgG1. И наоборот, лекарственные вещества, которые активируют или инактивируют иммунные реакции, могут быть использованы в качестве дополнительных агентов для эффективного лечения заболеваний или расстройств, включая рак или инфекционные заболевания. Например, ипилимумаб (Ервой®) представляет собой моноклональное антитело, которое активирует иммунный ответ путем нацеливания на CTLA-4 и может использоваться для лечения меланомы. Пембролизумаб (Кейтруда®) представляет собой гуманизированное антитело к человеческому рецептору запрограммированной смерти-1 (PD-1) и назначается в качестве анти-PD-1 иммунотерапии против некоторых видов рака. Ниволумаб (Опдиво®) является еще одним анти-PD-1 антителом, используемым в качестве иммунотерапии для лечения некоторых видов рака.
[0125] Исходя из вышеизложенного понятно, что конкретные варианты осуществления изобретения раскрыты в настоящем описании в иллюстративных целях, при этом могут быть сделаны различные модификации без отклонения от объема изобретения. Соответственно, изобретение не является ограниченным ничем, кроме прилагаемой формулы изобретения.
ПРИМЕР 1
[0126] В этом рабочем примере показана эффективность блокады KIR3DL3 с помощью антител в стимулировании противоопухолевого иммунитета и подавлении роста опухоли в мышиных моделях аденокарциномы легкого (фиг. 12A-12B). Модель мышиной внутрибрюшинной опухоли формировали путем внутрибрюшинной (i.p.) инъекции 4×106 клеток HHLA2+ HCC827, трансдуцированных люциферазой (Luc2-HCC827), мышам NSG (n=6 для каждой группы) (фиг. 12A). Четыре дня спустя мышей распределяли по группам 26E10 (анти-KIR3DL3 mAb) или mIgG1 на основании исходной биолюминесценции. Затем каждой мыши внутрибрюшинно вводили 1×107 размноженных KIR3DL3+ NK-клеток вместе с 1 мкг IL-2, 1 мкг IL-15 и 200 мкг 26E10 (или mIgG1) через день (всего 5 раз). Биолюминесценцию измеряли с помощью устройства визуализации IVIS spectrum (Capiler Perkin Elmer) с началом визуализации через 5-10 минут после внутрибрюшинной инъекции D-люциферина (150 мкг/г массы тела) и анализировали с помощью программного обеспечения Living Image 3.0. Биолюминесцентное измерение роста опухоли показывает, что моноклональное анти-KIR3DL3 антитело снижает рост опухоли по сравнению с контролем (фиг. 12B), что свидетельствует о том, что направленное воздействие на KIR3DL3-опосредованную иммуносупрессию является эффективным подходом к терапии рака посредством стимуляции противоопухолевого иммунитета.
[0127] Эффективность блокады KIR3DL3 антителами также тестировали на мышиных моделях метастатического рака легкого (фиг. 12C-12D). 5×105 клеток Luc2-HCC827 вводили внутривенно мышам NSG (n=4 для каждой группы). Четыре дня спустя мышей распределяли по группам 26E10 (анти-KIR3DL3) или mIgG1 на основании исходной биолюминесценции. Затем каждая мышь получала внутривенно 7×106 KIR3DL3+ NK-клеток вместе с 1 мкг IL-2, 1 мкг IL-15 и 200 мкг 26E10 (или mIgG1) через день (всего 3 раза). Биолюминесценцию измеряли с помощью устройства визуализации IVIS spectrum (Capiler Perkin Elmer) с началом визуализации через 10-18 минут после внутрибрюшинной инъекции D-люциферина (150 мкг/г массы тела) и анализировали с помощью программного обеспечения Living Image 3.0 (фиг. 12C). И в этом случае, было обнаружено, что моноклональное анти-KIR3DL3 антитело значительно снижает рост опухоли по сравнению с контролем (фиг. 12D), что свидетельствует о том, что ингибирование KIR3DL3-опосредованной иммунной супрессии и, как следствие, усиление противоопухолевого иммунитета также эффективны при лечении метастатического рака.
[0128] Наконец, эффективность блокады KIR3DL3 подтверждали на моделях подкожной опухоли у мышей (фиг. 12E-12F). Клетки аденокарциномы легкого человека HCC827 (3×106) вводили подкожно мышам NSG. Двенадцать дней спустя мышей с опухолями рандомизировали по группам 26E10 или mIgG1 (n=4 в каждой группе) и затем обрабатывали KIR3DL3+ NK-клетками (10×106 клеток) и 26E10 или изотипом mIgG1 (200 мкг) через день в течение двух недель (фиг. 12Е). Рост опухоли оценивали, как и раньше. В соответствии с предыдущими наблюдениями, моноклональное анти-KIR3DL3 антитело значительно снижало рост опухоли по сравнению с контролем (фиг. 12F), подтверждая, что KIR3DL3 является потенциальной новой мишенью для иммунотерапии рака.
[0129] Антитело или его иммуногенный фрагмент, которое специфически связывается с белком KIR3DL3.
[0130] Антитело или его иммуногенный фрагмент по п. 129, где антитело или его иммуногенный фрагмент специфически связывается с эпитопом KIR3DL3, содержащим полноразмерный внеклеточный домен или его часть.
[0131] Антитело или его иммуногенный фрагмент по п. 130, где антитело или его иммуногенный фрагмент связывается с доменом D0 KIR3DL3, доменом D1 KIR3DL3 или доменом D2 KIR3DL3.
[0132] Антитело или его иммуногенный фрагмент по п. 129 или п. 130, содержащее область VH, содержащую CDR1, CDR2 и CDR3, имеющие аминокислотную последовательность SEQ ID NO: 7, 9, 11, 31, 33, 35, 54, 56, 76, 78, 80, 100, 102, 104, 124, 126, 128, 148, 150, 152, 172, 174, 176, 196, 198, 200, 220, 222, 224, 244, 246, 248, 268, 270, 272, 292, 294, 296, 316, 318 или 320.
[0133] Антитело или его иммуногенный фрагмент по п. 129 или п. 130, содержащее область VH, содержащую по меньшей мере одну CDR, которая на 80% идентична аминокислотной последовательности, выбранной из SEQ ID NO: 7, 9, 11, 31, 33, 35, 54, 56, 76, 78, 80, 100, 102, 104, 124, 126, 128, 148, 150, 152, 172, 174, 176, 196, 198, 200, 220, 222, 224, 244, 246, 248, 268, 270, 272, 292, 294, 296, 316, 318 или 320.
[0134] Антитело или его иммуногенный фрагмент по п. 129 или п. 130, содержащее область VH, содержащую по меньшей мере две CDR, которые на 80% идентичны аминокислотной последовательности, выбранной из SEQ ID NO: 7, 9, 11, 31, 33, 35, 54, 56, 76, 78, 80, 100, 102, 104, 124, 126, 128, 148, 150, 152, 172, 174, 176, 196, 198, 200, 220, 222, 224, 244, 246, 248, 268, 270, 272, 292, 294, 296, 316, 318 или 320.
[0135] Антитело или его иммуногенный фрагмент по п. 129 или п. 130, содержащее область VH, содержащую по меньшей мере три CDR, которые на 80% идентичны аминокислотной последовательности, выбранной из SEQ ID NO: 7, 9, 11, 31, 33, 35, 54, 56, 76, 78, 80, 100, 102, 104, 124, 126, 128, 148, 150, 152, 172, 174, 176, 196, 198, 200, 220, 222, 224, 244, 246, 248, 268, 270, 272, 292, 294, 296, 316, 318 или 320.
[0136] Антитело или его иммуногенный фрагмент по п. 129 или п. 130, содержащее область VL, содержащую CDR1, CDR2 и CDR3, имеющие аминокислотную последовательность SEQ ID NO: 19, 21, 23, 43, 45, 47, 64, 66, 68, 88, 90, 92, 112, 114, 116, 136, 138, 140, 160, 162, 164, 184, 186, 188, 208, 210, 212, 232, 234, 236, 256, 258, 260, 280, 282, 284, 304, 306, 308, 328, 330 или 332.
[0137] Антитело или его иммуногенный фрагмент по п. 129 или п. 130, содержащее область VL, содержащую по меньшей мере одну CDR, которая на 80% идентична аминокислотной последовательности, выбранной из SEQ ID NO: 19, 21, 23, 43, 45, 47, 64, 66, 68, 88, 90, 92, 112, 114, 116, 136, 138, 140, 160, 162, 164, 184, 186, 188, 208, 210, 212, 232, 234, 236, 256, 258, 260, 280, 282, 284, 304, 306, 308, 328, 330 или 332.
[0138] Антитело или его иммуногенный фрагмент по п. 129 или п. 130, содержащее область VL, содержащую по меньшей мере две CDR, которые на 80% идентичны аминокислотной последовательности, выбранной из SEQ ID NO: 19, 21, 23, 43, 45, 47, 64, 66, 68, 88, 90, 92, 112, 114, 116, 136, 138, 140, 160, 162, 164, 184, 186, 188, 208, 210, 212, 232, 234, 236, 256, 258, 260, 280, 282, 284, 304, 306, 308, 328, 330 или 332.
[0139] Антитело или его иммуногенный фрагмент по п. 129 или п. 130, содержащее область VL, содержащую по меньшей мере три CDR, которые на 80% идентичны аминокислотной последовательности, выбранной из SEQ ID NO: 19, 21, 23, 43, 45, 47, 64, 66, 68, 88, 90, 92, 112, 114, 116, 136, 138, 140, 160, 162, 164, 184, 186, 188, 208, 210, 212, 232, 234, 236, 256, 258, 260, 280, 282, 284, 304, 306, 308, 328, 330 или 332.
[0140] Антитело по любому из пп. 129-139, где указанное антитело представляет собой моноклональное антитело.
[0141] Антитело по любому из пп. 129-139, где антитело представляет собой химерное антитело, человеческое антитело или гуманизированное антитело.
[0142] Антитело или его иммуногенный фрагмент по любому из пп. 129-139, содержащее аминокислотную последовательность, выбранную из SEQ ID NO: 7, 9, 11, 19, 21, 23, 31, 33, 35, 43, 45, 47, 54, 56, 64, 66, 68, 76, 78, 80, 88, 90, 92, 100, 102, 104, 112, 114, 116, 124, 126, 128, 136, 138, 140, 148, 150, 152, 160, 162, 164, 172, 174, 176, 184, 186, 188, 196, 198, 200, 208, 210, 212, 220, 222, 224, 232, 234, 236, 244, 246, 248, 256, 258, 260, 268, 270, 272, 280, 282, 284, 292, 294, 296, 304, 306, 308, 316, 318, 320, 328, 330 или 332.
[0143] Антитело по п. 140, где антитело представляет собой моноклональное 8G7, моноклональное 26E10, моноклональное 26E2, моноклональное 31C4, моноклональное 34B10, моноклональное 37A3, моноклональное 12A10, моноклональное 3B7, моноклональное 11G8, моноклональное 14F8, моноклональное 15D2, моноклональное 29H7, моноклональное 30D10 или моноклональное 51C3.
[0144] Антитело по п. 141, где антитело представляет собой гуманизированное 8G7, гуманизированное 26E10, гуманизированное 26E2, гуманизированное 31C4, гуманизированное 34B10, гуманизированное 37A3, гуманизированное 12A10, гуманизированное 3B7, гуманизированное 11G8, гуманизированное 14F8, гуманизированное 15D2, гуманизированное 29H7, гуманизированное 30D10 или гуманизированное 51C3.
[0145] Слитый полипептид, содержащий антитело или его иммуногенный фрагмент по любому из пп. 129-144.
[0146] Композиция, содержащая антитело или его иммуногенный фрагмент по любому из пп. 129-144 или слитый полипептид по п. 145.
[0147] Композиция по п. 146, дополнительно содержащая фармацевтически приемлемый носитель.
[0148] Композиция по п. 146 или п. 147, дополнительно содержащая фармацевтически приемлемое вспомогательное вещество.
[0149] Антитело или его иммуногенный фрагмент по любому из пп. 129-144, слитый полипептид по п. 145 или композиция по любому из пп. 146-148 для применения в терапии.
[0150] Антитело или его иммуногенный фрагмент по любому из пп. 129-144, слитый полипептид по п. 145 или композиция по любому из пп. 146-148 для применения в производстве лекарственного средства.
[0151] Нуклеиновая кислота, содержащая нуклеиновую кислоту, кодирующую антитело или его иммуногенный фрагмент, где антитело или его иммуногенный фрагмент представляет собой антитело или его иммуногенный фрагмент по любому из пп. 129-144.
[0152] Нуклеиновая кислота, содержащая нуклеиновую кислоту, кодирующую слитый полипептид, где слитый полипептид представляет собой слитый полипептид по п. 145.
[0153] Способ лечения субъекта, страдающего от состояния, включающий введение субъекту терапевтически эффективного количества антитела или его иммуногенного фрагмента по любому из пп. 129-144, слитого полипептида по п. 145 или композиции по любой из пп. 146-148.
[0154] Способ по п. 153, где состояние представляет собой рак.
[0155] Способ по п. 154, где рак выбирают из группы, состоящей из хронического лимфолейкоза (CLL), острого лейкоза, острого лимфолейкоза (ALL), В-клеточного острого лимфолейкоза (В-ALL), Т-клеточной лимфомы, В-клеточной лимфомы, Т-клеточного острого лимфолейкоза (Т-ALL), хронического миелогенного лейкоза (CML), В-клеточного пролимфоцитарного лейкоза, Т-клеточной лимфомы, болезни Ходжкина, В-клеточной неходжкинской лимфомы, бластной плазмоцитоидной дендритно-клеточной опухоли, лимфомы Беркитта, диффузной крупноклеточной В-клеточной лимфомы, фолликулярной лимфомы, волосатоклеточного лейкоза, мелкоклеточной фолликулярной лимфомы, крупноклеточной фолликулярной лимфомы, злокачественных лимфопролиферативных состояний, лимфомы, ассоциированной со слизистой оболочкой (MALT), лимфомы из мантийных клеток, лимфомы маргинальной зоны, множественной миеломы, миелодисплазии и миелодиспластического синдрома, неходжкинской лимфомы, лимфомы Ходжкина, плазмобластной лимфомы, новообразования из плазмоцитоидных дендритных клеток, макроглобулинемии Вальденстрема или прелейкемии.
[0156] Способ по п. 154, где рак выбирают из группы, состоящей из рака толстой кишки, рака прямой кишки, почечно-клеточного рака, рака печени, рака легких, рака почки, рака желудка, рака желчного пузыря, рака тонкой кишки, рака пищевода, меланомы, рака костей, рака поджелудочной железы, рака кожи, рака головы или шеи, кожной или внутриглазной злокачественной меланомы, рака матки, рака яичников, рака прямой кишки, рака анальной области, рака желудка, рака яичек, рака матки, карциномы фаллопиевых труб, карциномы эндометрия, карциномы шейки матки, карциномы влагалища, карциномы вульвы, рака эндокринной системы, рака щитовидной железы, рака паращитовидной железы, рака надпочечников, саркомы мягких тканей, рака уретры, рака полового члена, солидных опухолей детского возраста, рака мочевого пузыря, рака почки или мочеточника, рака почечной лоханки, новообразования центральной нервной системы (ЦНС), первичной лимфомы ЦНС, ангиогенеза опухоли, опухоли спинного мозга, глиомы ствола головного мозга, аденомы гипофиза, саркомы Капоши, эпидермоидного рака, плоскоклеточного рака, рака, индуцированного окружающей средой, комбинации раковых заболеваний и метастатических поражений, вызванных раковыми заболеваниями.
[0157] Способ по п. 154, где рак представляет собой гематологическое злокачественное новообразование человека.
[0158] Способ по п. 157, где гематологическое злокачественное новообразование человека выбирают из миелоидного новообразования, острого миелоидного лейкоза (AML), AML с рецидивирующими генетическими аномалиями, AML с изменениями, связанными с миелодисплазией, AML, связанного с терапией, острых лейкозов неоднозначного происхождения, миелопролиферативного новообразования, эссенциальной тромбоцитемии, истинной полицитемии, миелофиброза (MF), первичного миелофиброза, системного мастоцитоза, миелодиспластических синдромов (MDS), миелопролиферативных/миелодиспластических синдромов, хронического миелоидного лейкоза, хронического нейтрофильного лейкоза, хронического эозинофильного лейкоза, миелодиспластических синдромов (MDS), рефрактерной анемии с кольцевидными сидеробластами, рефрактерной цитопении с многолинейной дисплазией, рефрактерной анемии с избытком бластов (тип 1), рефрактерной анемии с избытком бластов (тип 2), MDS с изолированной делецией (5q), неклассифицируемого MDS, миелопролиферативных/миелодиспластических синдромов, хронического миеломоноцитарного лейкоза, атипичного хронического миелоидного лейкоза, ювенильного миеломоноцитарного лейкоза, неклассифицируемых миелопролиферативных/миелодисплатических синдромов, лимфоидных новообразований, предраковых лимфоидных новообразований, В-лимфобластного лейкоза, В-лимфобластной лимфомы, Т-лимфобластного лейкоза, Т-лимфобластной лимфомы, новообразований из зрелых В-клеток, диффузной крупноклеточной В-клеточной лимфомы, первичной лимфомы центральной нервной системы, первичной медиастинальной В-клеточной лимфомы, лимфомы/лейкемии Беркитта, фолликулярной лимфомы, хронического лимфолейкоза, малой лимфоцитарной лимфомы, В-клеточного пролимфоцитарного лейкоза, лимфоплазмоцитарной лимфомы, макроглобулинемии Вальденстрема, лимфомы из мантийных клеток, лимфомы маргинальной зоны, посттрансплантационных лимфопролиферативных заболеваний, ВИЧ-ассоциированных лимфом, первичной выпотной лимфомы, внутрисосудистой крупноклеточной В-клеточной лимфомы, первичной кожной В-клеточной лимфомы, волосатоклеточного лейкоза, множественной миеломы, моноклональной гаммапатии неясного генеза (MGUS), тлеющей множественной миеломы или солитарных плазмоцитом (солитарных костных и экстрамедуллярных).
[0159] Способ по п. 154, где рак представляет собой метастатический рак.
[0160] Способ по п. 154, дополнительно включающий предоставление субъекту одного или более дополнительных видов терапии рака, выбранных из химиотерапии, лучевой терапии, иммунотерапии, хирургии и их комбинации.
[0161] Способ по п. 153, где состояние представляет собой инфекцию.
[0162] Способ по п. 161, где инфекция вызвана патогеном.
[0163] Способ по пункту 162, где патоген представляет собой вирус.
[0164] Способ по п. 163, где вирус выбирают из группы, состоящей из вирусов иммунодефицита человека, вирусов гриппа, папилломавирусов, коронавирусов, вирусов гепатита или герпесвирусов.
[0165] Способ по п. 162, где патоген представляет собой бактерию.
[0166] Способ по п. 165, где бактерия представляет собой микобактерию туберкулеза.
[0167] Способ по п. 162, где патоген представляет собой прион.
[0168] Способ по п. 162, где патоген представляет собой грибок.
[0169] Способ по п. 168, где грибок представляет собой Pneumocystis jirovecii (PJP).
[0170] Способ по п. 162, где патоген представляет собой паразита.
[0171] Способ по п. 153, где состояние представляет собой аутоиммунное заболевание или расстройство.
[0172] Способ по п. 171, где аутоиммунное заболевание или расстройство выбирают из группы, состоящей из острого диссеминированного энцефаломиелита (ADEM), очаговой алопеции, антифосфолипидного синдрома, аутоиммунной кардиомиопатии, аутоиммунной гемолитической анемии, аутоиммунного гепатита, аутоиммунного заболевания внутреннего уха, аутоиммунного липопролиферативного синдрома, аутоиммунной периферической невропатии, аутоиммунного панкреатита, аутоиммунного полиэндокринного синдрома, аутоиммунного прогестеронового дерматита, аутоиммунной тромбоцитопенической пурпуры, аутоиммунной крапивницы, аутоиммунного увеита, болезни Бехчета, глютеновой болезни, болезни Шагаса, болезни холодовых агглютининов, болезни Крона, дерматомиозита, сахарного диабета 1 типа, эозинофильного фасциита, пемфигоида желудочно-кишечного тракта, синдрома Гудпасчера, синдрома Грейвса, синдрома Гийена-Барре, энцефалопатии Хашимото, тиреоидита Хашимото, красной волчанки, синдрома Миллера-Фишера, смешанного заболевания соединительной ткани, тяжелой миастении, вульгарной пузырчатки, пернициозной анемии, полимиозита, псориаза, псориатического артрита, рецидивирующего полихондрита, ревматоидного артрита, ревматической атаки, синдрома Шегрена, височного артериита, поперечного миелита, язвенного колита, недифференцированного заболевания соединительной ткани, васкулита и гранулематоза Вегенера.
[0173] Способ по п. 171, где аутоиммунное заболевание или расстройство представляет собой ревматоидный артрит взрослых.
[0174] Способ по п. 153, где состояние представляет собой наличие трансплантата.
[0175] Способ по п. 174, где трансплантат выбирают из трансплантата стволовых клеток или трансплантата костного мозга.
[0176] Способ по п. 174, где трансплантат выбирают из группы, состоящей из трансплантата почки, трансплантата легкого, трансплантата сердца, трансплантата поджелудочной железы, трансплантата роговицы или трансплантата печени.
[0177] Композиция по любому из пп. 146-148 для применения в способе лечения субъекта, страдающего от состояния.
[0178] Композиция по п. 177, где состояние представляет собой рак.
[0179] Композиция по п. 178, где рак выбирают из группы, состоящей из хронического лимфолейкоза (CLL), острого лейкоза, острого лимфолейкоза (ALL), В-клеточного острого лимфолейкоза (В-ALL), Т-клеточной лимфомы, В-клеточной лимфомы, Т-клеточного острого лимфолейкоза (Т-ALL), хронического миелогенного лейкоза (CML), В-клеточного пролимфоцитарного лейкоза, Т-клеточной лимфомы, болезни Ходжкина, В-клеточной неходжкинской лимфомы, бластной плазмоцитоидной дендритно-клеточной опухоли, лимфомы Беркитта, диффузной крупноклеточной В-клеточной лимфомы, фолликулярной лимфомы, волосатоклеточного лейкоза, мелкоклеточной фолликулярной лимфомы, крупноклеточной фолликулярной лимфомы, злокачественных лимфопролиферативных состояний, лимфомы, ассоциированной со слизистой оболочкой (MALT), лимфомы из мантийных клеток, лимфомы маргинальной зоны, множественной миеломы, миелодисплазии и миелодиспластического синдрома, неходжкинской лимфомы, лимфомы Ходжкина, плазмобластной лимфомы, новообразования из плазмоцитоидных дендритных клеток, макроглобулинемии Вальденстрема или прелейкемии.
[0180] Композиция по п. 178, где рак выбирают из группы, состоящей из рака толстой кишки, рака прямой кишки, почечно-клеточного рака, рака печени, рака легких, рака почки, рака желудка, рака желчного пузыря, рака тонкой кишки, рака пищевода, меланомы, рака костей, рака поджелудочной железы, рака кожи, рака головы или шеи, кожной или внутриглазной злокачественной меланомы, рака матки, рака яичников, рака прямой кишки, рака анальной области, рака желудка, рака яичек, рака матки, карциномы фаллопиевых труб, карциномы эндометрия, карциномы шейки матки, карциномы влагалища, карциномы вульвы, рака эндокринной системы, рака щитовидной железы, рака паращитовидной железы, рака надпочечников, саркомы мягких тканей, рака уретры, рака полового члена, солидных опухолей детского возраста, рака мочевого пузыря, рака почки или мочеточника, рака почечной лоханки, новообразования центральной нервной системы (ЦНС), первичной лимфомы ЦНС, ангиогенеза опухоли, опухоли спинного мозга, глиомы ствола головного мозга, аденомы гипофиза, саркомы Капоши, эпидермоидного рака, плоскоклеточного рака, рака, индуцированного окружающей средой, комбинации раковых заболеваний и метастатических поражений, вызванных раковыми заболеваниями.
[0181] Композиция по п. 178, где рак представляет собой гематологическое злокачественное новообразование человека.
[0182] Композиция по п. 181, где гематологическое злокачественное новообразование человека выбирают из миелоидного новообразования, острого миелоидного лейкоза (AML), AML с рецидивирующими генетическими аномалиями, AML с изменениями, связанными с миелодисплазией, AML, связанного с терапией, острых лейкозов неоднозначного происхождения, миелопролиферативного новообразования, эссенциальной тромбоцитемии, истинной полицитемии, миелофиброза (MF), первичного миелофиброза, системного мастоцитоза, миелодиспластических синдромов (MDS), миелопролиферативных/миелодиспластических синдромов, хронического миелоидного лейкоза, хронического нейтрофильного лейкоза, хронического эозинофильного лейкоза, миелодиспластических синдромов (MDS), рефрактерной анемии с кольцевидными сидеробластами, рефрактерной цитопении с многолинейной дисплазией, рефрактерной анемии с избытком бластов (тип 1), рефрактерной анемии с избытком бластов (тип 2), MDS с изолированной делецией (5q), неклассифицируемого MDS, миелопролиферативных/миелодиспластических синдромов, хронического миеломоноцитарного лейкоза, атипичного хронического миелоидного лейкоза, ювенильного миеломоноцитарного лейкоза, неклассифицируемых миелопролиферативных/миелодисплатических синдромов, лимфоидных новообразований, предраковых лимфоидных новообразований, В-лимфобластного лейкоза, В-лимфобластной лимфомы, Т-лимфобластного лейкоза, Т-лимфобластной лимфомы, новообразований из зрелых В-клеток, диффузной крупноклеточной В-клеточной лимфомы, первичной лимфомы центральной нервной системы, первичной медиастинальной В-клеточной лимфомы, лимфомы/лейкемии Беркитта, фолликулярной лимфомы, хронического лимфолейкоза, малой лимфоцитарной лимфомы, В-клеточного пролимфоцитарного лейкоза, лимфоплазмоцитарной лимфомы, макроглобулинемии Вальденстрема, лимфомы из мантийных клеток, лимфомы маргинальной зоны, посттрансплантационных лимфопролиферативных заболеваний, ВИЧ-ассоциированных лимфом, первичной выпотной лимфомы, внутрисосудистой крупноклеточной В-клеточной лимфомы, первичной кожной В-клеточной лимфомы, волосатоклеточного лейкоза, множественной миеломы, моноклональной гаммапатии неясного генеза (MGUS), тлеющей множественной миеломы или солитарных плазмоцитом (солитарных костных и экстрамедуллярных).
[0183] Композиция по п. 178, где рак представляет собой метастатический рак.
[0184] Композиция по п. 178, где композицию вводят субъекту вместе с одним или более дополнительными видами терапии рака, выбранными из химиотерапии, лучевой терапии, иммунотерапии, хирургии и их комбинации.
[0185] Композиция по п. 177, где состояние представляет собой инфекцию.
[0186] Композиция по п. 185, где инфекция вызвана патогеном.
[0187] Композиция по п. 186, где патоген представляет собой вирус.
[0188] Композиция по п. 187, где вирус выбирают из группы, состоящей из вирусов иммунодефицита человека, вирусов гриппа, папилломавирусов, коронавирусов, вирусов гепатита или герпесвирусов.
[0189] Композиция по п. 186, где патоген представляет собой бактерию.
[0190] Композиция по п. 189, где бактерия представляет собой микобактерию туберкулеза.
[0191] Композиция по п. 186, где патоген представляет собой прион.
[0192] Композиция по п. 186, где патоген представляет собой грибок.
[0193] Композиция по п. 192, где грибок представляет собой Pneumocystis jirovecii (PJP).
[0194] Композиция по п. 186, где патоген представляет собой паразита.
[0195] Композиция по п. 177, где состояние представляет собой аутоиммунное заболевание или расстройство.
[0196] Композиция по п. 195, где аутоиммунное заболевание или расстройство выбирают из группы, состоящей из острого диссеминированного энцефаломиелита (ADEM), очаговой алопеции, антифосфолипидного синдрома, аутоиммунной кардиомиопатии, аутоиммунной гемолитической анемии, аутоиммунного гепатита, аутоиммунного заболевания внутреннего уха, аутоиммунного липопролиферативного синдрома, аутоиммунной периферической невропатии, аутоиммунного панкреатита, аутоиммунного полиэндокринного синдрома, аутоиммунного прогестеронового дерматита, аутоиммунной тромбоцитопенической пурпуры, аутоиммунной крапивницы, аутоиммунного увеита, болезни Бехчета, глютеновой болезни, болезни Шагаса, болезни холодовых агглютининов, болезни Крона, дерматомиозита, сахарного диабета 1 типа, эозинофильного фасциита, пемфигоида желудочно-кишечного тракта, синдрома Гудпасчера, синдрома Грейвса, синдрома Гийена-Барре, энцефалопатии Хашимото, тиреоидита Хашимото, красной волчанки, синдрома Миллера-Фишера, смешанного заболевания соединительной ткани, тяжелой миастении, вульгарной пузырчатки, пернициозной анемии, полимиозита, псориаза, псориатического артрита, рецидивирующего полихондрита, ревматоидного артрита, ревматической атаки, синдрома Шегрена, височного артериита, поперечного миелита, язвенного колита, недифференцированного заболевания соединительной ткани, васкулита и гранулематоза Вегенера.
[0197] Композиция по п. 195, где аутоиммунное заболевание или расстройство представляет собой ревматоидный артрит взрослых.
[0198] Композиция по п. 177, где состояние представляет собой наличие трансплантата.
[0199] Композиция по п. 198, где трансплантат выбирают из трансплантата стволовых клеток или трансплантата костного мозга.
[0200] Композиция по п. 198, где трансплантат выбирают из группы, состоящей из трансплантата почки, трансплантата легкого, трансплантата сердца, трансплантата поджелудочной железы, трансплантата роговицы или трансплантата печени.
ЛИТЕРАТУРА
Armentano et al. Proc Natl Acad Sci USA 87(16):6141-6145 (1990)
Berkner Biotechniques 6(7):616-629 (1988)
Beziat et al. Immunology 150(3):248-264 (2017)
Cheng et al. Clin Cancer Res 24(8):1954-1964 (2018)
Cheng et al. Clin Cancer Res 23(3):825-832 (2017)
Chowdhury et al. Science 254(5039):1802-1805 (1991)
Dai et al. Proc Natl Acad Sci USA 89(22):10892-10895 (1992)
Danos & Mulligan Proc Natl Acad Sci USA 85(17):6460-6464 (1988)
Eglitis et al. Science 230(4732):1395-1398 (1985)
Ferry et al. Proc Natl Acad Sci USA 88(19):8377-8381 (1991)
Flotte et al. Am J Respir Cell Mol Biol 7(3):349-356 (1992)
Harris Biochem Soc Trans 23(4):1035-1038 (1995)
Huber et al. Proc Natl Acad Sci USA 88(18):8039-8043 (1991)
Hurle & Gross Curr Opin Biotechnol 5(4):428-433 (1994)
Hwu et al. J Immunol 150(9):4104-4115 (1993)
Janakiram et al. Clin Cancer Res 21(10):2359-2366 (2015)
Jones et al. Nature 321(6069):522-525 (1986)
Kay et al. Hum Gene Ther 3(6):641-647 (1992)
Koirala et al. Sci Rep 6:31154 (2016)
McLaughlin et al. J Virol 62(6):1963-1973 (1988)
Presta Curr Opin Biotechnol 3(4):394-398 (1992)
Riechmann et al. Nature 332(6162):323-327 (1988)
Rosenfeld et al. Science 252(5004):431-434 (1991)
Rosenfeld et al. Cell 68(1):143-155 (1992)
Samulski et al. J Virol 63(9):3822-3828 (1989)
van Beusechem et al. Proc Natl Acad Sci USA 89(16):7640-7644 (1992)
Vaswani & Hamilton Ann Allergy Asthma Immunol 81(2):105-115 (1998)
Wilson et al. Proc Natl Acad Sci USA 85(9):3014-3018 (1988)
Zhao et al. Proc Natl Acad Sci USA 110(24):9879-9884 (2013)
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> АЛЬБЕРТ ЭЙНШТЕЙН КОЛЛЕДЖ ОФ МЕДСИН
<120> KIR3DL3 - ИНГИБИРУЮЩИЙ РЕЦЕПТОР ИММУННОЙ СИСТЕМЫ И ЕГО
ПРИМЕНЕНИЕ
<130> 129807-8002.WO0
<140> PCT/US20/053857
<141> 2020-10-01
<150> US 62/911,169
<151> 2019-10-04
<160> 342
<170> PatentIn version 3.5
<210> 1
<211> 411
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 8G7
<220>
<221> misc_feature
<222> (1)..(57)
<223> Лидерная последовательность
<220>
<221> misc_feature
<222> (58)..(132)
<223> FR1
<220>
<221> misc_feature
<222> (133)..(162)
<223> CDR1
<220>
<221> misc_feature
<222> (163)..(207)
<223> FR2
<220>
<221> misc_feature
<222> (208)..(255)
<223> CDR2
<220>
<221> misc_feature
<222> (256)..(345)
<223> FR3
<220>
<221> misc_feature
<222> (346)..(378)
<223> CDR3
<220>
<221> misc_feature
<222> (379)..(408)
<223> FR4
<400> 1
atgaactttg ggttgagatt gattttcctt gtccttgttt taaaaggtgt ccagtgtgaa 60
gtgatgctgg tggagtctgg gggaggctta gtgaagcctg gagggtccct gaaactctcc 120
tgtgcagcct ctggattcac tttcagtacc tatgccatgt cttgggttcg ccagactccg 180
gagaagaggc tggagtgggt cgcaaccatt cttagtggtg gtaattacac ctactatcca 240
gacagtgtga aggggcgatt caccatctcc agagacaatg ccaagaacac cctgaacctg 300
caaatgagca gtctgaggtc tgaggacacg gccatgtatt actgtgtaat cccctatggt 360
agtagtcctt ttgactattg gggccaaggc accactctca cagtctctct a 411
<210> 2
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 8G7: CDR1
<400> 2
ggattcactt tcagtaccta tgccatgtct 30
<210> 3
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 8G7: CDR2
<400> 3
attcttagtg gtggtaatta cacctactat ccagacagtg tgaagggg 48
<210> 4
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 8G7: CDR3
<400> 4
gtaatcccct atggtagtag tccttttgac tat 33
<210> 5
<211> 136
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 8G7
<220>
<221> MISC_FEATURE
<222> (1)..(19)
<223> Лидерная последовательность
<220>
<221> MISC_FEATURE
<222> (20)..(44)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (45)..(54)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (55)..(68)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (69)..(85)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (86)..(115)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (116)..(126)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (127)..(136)
<223> FR4
<400> 5
Met Asn Phe Gly Leu Arg Leu Ile Phe Leu Val Leu Val Leu Lys Gly
1 5 10 15
Val Gln Cys Glu Val Met Leu Val Glu Ser Gly Gly Gly Leu Val Lys
20 25 30
Pro Gly Gly Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe
35 40 45
Ser Thr Tyr Ala Met Ser Trp Val Arg Gln Thr Pro Glu Lys Arg Leu
50 55 60
Glu Trp Val Ala Thr Ile Leu Ser Gly Gly Asn Tyr Thr Tyr Tyr Pro
65 70 75 80
Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn
85 90 95
Thr Leu Asn Leu Gln Met Ser Ser Leu Arg Ser Glu Asp Thr Ala Met
100 105 110
Tyr Tyr Cys Val Ile Pro Tyr Gly Ser Ser Pro Phe Asp Tyr Trp Gly
115 120 125
Gln Gly Thr Thr Leu Thr Val Ser
130 135
<210> 6
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 8G7: FR1
<400> 6
Glu Val Met Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser
20 25
<210> 7
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 8G7: CDR1
<400> 7
Gly Phe Thr Phe Ser Thr Tyr Ala Met Ser
1 5 10
<210> 8
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 8G7: FR2
<400> 8
Trp Val Arg Gln Thr Pro Glu Lys Arg Leu Glu Trp Val Ala
1 5 10
<210> 9
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 8G7: CDR2
<400> 9
Thr Ile Leu Ser Gly Gly Asn Tyr Thr Tyr Tyr Pro Asp Ser Val Lys
1 5 10 15
Gly
<210> 10
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 8G7: FR3
<400> 10
Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Asn Leu Gln
1 5 10 15
Met Ser Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys
20 25 30
<210> 11
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 8G7: CDR3
<400> 11
Val Ile Pro Tyr Gly Ser Ser Pro Phe Asp Tyr
1 5 10
<210> 12
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 8G7: FR4
<400> 12
Trp Gly Gln Gly Thr Thr Leu Thr Val Ser
1 5 10
<210> 13
<211> 423
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 8G7
<220>
<221> misc_feature
<222> (28)..(87)
<223> Лидерная последовательность
<220>
<221> misc_feature
<222> (88)..(156)
<223> FR1
<220>
<221> misc_feature
<222> (157)..(183)
<223> CDR1
<220>
<221> misc_feature
<222> (184)..(234)
<223> FR2
<220>
<221> misc_feature
<222> (235)..(255)
<223> CDR2
<220>
<221> misc_feature
<222> (256)..(352)
<223> FR3
<220>
<221> misc_feature
<222> (353)..(378)
<223> CDR3
<220>
<221> misc_feature
<222> (379)..(408)
<223> FR4
<400> 13
ttattactag tcgacacggg catcaagatg aagtcacaga cccaggtctt cgtatttcta 60
ctgctctgtg tgtctggtgc tcatgggagt attgtgatga cccagactcc caaattcctg 120
cttgtatcag caggagacag ggttaccata acctgcaagg ccagtcagag tgtgagtaat 180
gatgtagctt ggtaccaaca gaagccaggg cagtctccta aactgctgat atactatgca 240
tccaatcgct acactggagt ccctgatcgc ttcactggca gtggatatgg gacggatttc 300
actttcacca tcagcactgt gcaggctgaa gacctggcag tttatttctg tcagcaggat 360
tatagctctc cgtggacgtt cggtggaggc accaagctgg aaatcaaacg ggctgatgct 420
gca 423
<210> 14
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 8G7: CDR1
<400> 14
aaggccagtc agagtgtgag taatgat 27
<210> 15
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 8G7: CDR2
<400> 15
tatgcatcca atcgctacac t 21
<210> 16
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 8G7: CDR3
<400> 16
cagcaggatt atagctctcc gtggacg 27
<210> 17
<211> 127
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 8G7
<220>
<221> MISC_FEATURE
<222> (1)..(20)
<223> Лидерная последовательность
<220>
<221> MISC_FEATURE
<222> (21)..(43)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (44)..(52)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (53)..(69)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (70)..(76)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (77)..(108)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (109)..(117)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (118)..(127)
<223> FR4
<400> 17
Met Lys Ser Gln Thr Gln Val Phe Val Phe Leu Leu Leu Cys Val Ser
1 5 10 15
Gly Ala His Gly Ser Ile Val Met Thr Gln Thr Pro Lys Phe Leu Leu
20 25 30
Val Ser Ala Gly Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser
35 40 45
Val Ser Asn Asp Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro
50 55 60
Lys Leu Leu Ile Tyr Tyr Ala Ser Asn Arg Tyr Thr Gly Val Pro Asp
65 70 75 80
Arg Phe Thr Gly Ser Gly Tyr Gly Thr Asp Phe Thr Phe Thr Ile Ser
85 90 95
Thr Val Gln Ala Glu Asp Leu Ala Val Tyr Phe Cys Gln Gln Asp Tyr
100 105 110
Ser Ser Pro Trp Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
115 120 125
<210> 18
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 8G7: FR1
<400> 18
Ser Ile Val Met Thr Gln Thr Pro Lys Phe Leu Leu Val Ser Ala Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys
20
<210> 19
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 8G7: CDR1
<400> 19
Lys Ala Ser Gln Ser Val Ser Asn Asp
1 5
<210> 20
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 8G7: FR2
<400> 20
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile
1 5 10 15
Tyr
<210> 21
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 8G7: CDR2
<400> 21
Tyr Ala Ser Asn Arg Tyr Thr
1 5
<210> 22
<211> 32
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 8G7: FR3
<400> 22
Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Tyr Gly Thr Asp Phe Thr
1 5 10 15
Phe Thr Ile Ser Thr Val Gln Ala Glu Asp Leu Ala Val Tyr Phe Cys
20 25 30
<210> 23
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 8G7: CDR3
<400> 23
Gln Gln Asp Tyr Ser Ser Pro Trp Thr
1 5
<210> 24
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 8G7: FR4
<400> 24
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
1 5 10
<210> 25
<211> 431
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 26E10
<220>
<221> misc_feature
<222> (11)..(67)
<223> Лидерная последовательность
<220>
<221> misc_feature
<222> (68)..(142)
<223> FR1
<220>
<221> misc_feature
<222> (143)..(172)
<223> CDR1
<220>
<221> misc_feature
<222> (173)..(214)
<223> FR2
<220>
<221> misc_feature
<222> (215)..(265)
<223> CDR2
<220>
<221> misc_feature
<222> (266)..(361)
<223> FR3
<220>
<221> misc_feature
<222> (362)..(397)
<223> CDR3
<220>
<221> misc_feature
<222> (398)..(430)
<223> FR4
<400> 25
tggggaattc atggaatgga gctgggtttt tctcttcctc ctgtcaataa ctacaggtgt 60
ccactcccag gcttatctac agcagtctgg ggctgagctg gtgaggtctg gggcctcagt 120
gaagatgtcc tgcaaggctt ctggctacac atttaccagt tacaatatac actgggtaaa 180
gcagacacct ggacagggcc tggaatggat tggatatatt tatcctggag atggtgttac 240
taactacaat cagaagttca agggcaaggc cacattgact gcagacacat cctccagcac 300
agcctacatg cagatcagca gcctgacatc tgaagactct gcggtctatt tctgtgcaag 360
atcgggcaac tatggtaact acgaagggtt tgcttactgg ggccaaggga ctctggtcac 420
tgtctctgct a 431
<210> 26
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 26E10: CDR1
<400> 26
ggctacacat ttaccagtta caatatacac 30
<210> 27
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 26E10: CDR2
<400> 27
tatatttatc ctggagatgg tgttactaac tacaatcaga agttcaaggg c 51
<210> 28
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 26E10: CDR3
<400> 28
tcgggcaact atggtaacta cgaagggttt gcttac 36
<210> 29
<211> 140
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 26E10
<220>
<221> MISC_FEATURE
<222> (1)..(19)
<223> Лидерная последовательность
<220>
<221> MISC_FEATURE
<222> (20)..(44)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (45)..(54)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (55)..(68)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (69)..(85)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (86)..(117)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (118)..(129)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (130)..(140)
<223> FR4
<400> 29
Met Glu Trp Ser Trp Val Phe Leu Phe Leu Leu Ser Ile Thr Thr Gly
1 5 10 15
Val His Ser Gln Ala Tyr Leu Gln Gln Ser Gly Ala Glu Leu Val Arg
20 25 30
Ser Gly Ala Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe
35 40 45
Thr Ser Tyr Asn Ile His Trp Val Lys Gln Thr Pro Gly Gln Gly Leu
50 55 60
Glu Trp Ile Gly Tyr Ile Tyr Pro Gly Asp Gly Val Thr Asn Tyr Asn
65 70 75 80
Gln Lys Phe Lys Gly Lys Ala Thr Leu Thr Ala Asp Thr Ser Ser Ser
85 90 95
Thr Ala Tyr Met Gln Ile Ser Ser Leu Thr Ser Glu Asp Ser Ala Val
100 105 110
Tyr Phe Cys Ala Arg Ser Gly Asn Tyr Gly Asn Tyr Glu Gly Phe Ala
115 120 125
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala
130 135 140
<210> 30
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 26E10: FR1
<400> 30
Gln Ala Tyr Leu Gln Gln Ser Gly Ala Glu Leu Val Arg Ser Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser
20 25
<210> 31
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 26E10: CDR1
<400> 31
Gly Tyr Thr Phe Thr Ser Tyr Asn Ile His
1 5 10
<210> 32
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 26E10: FR2
<400> 32
Trp Val Lys Gln Thr Pro Gly Gln Gly Leu Glu Trp Ile Gly
1 5 10
<210> 33
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 26E10: CDR2
<400> 33
Tyr Ile Tyr Pro Gly Asp Gly Val Thr Asn Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 34
<211> 32
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 26E10: FR3
<400> 34
Lys Ala Thr Leu Thr Ala Asp Thr Ser Ser Ser Thr Ala Tyr Met Gln
1 5 10 15
Ile Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys Ala Arg
20 25 30
<210> 35
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 26E10: CDR3
<400> 35
Ser Gly Asn Tyr Gly Asn Tyr Glu Gly Phe Ala Tyr
1 5 10
<210> 36
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 26E10: FR4
<400> 36
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala
1 5 10
<210> 37
<211> 296
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 26E10
<220>
<221> misc_feature
<222> (2)..(43)
<223> FR1
<220>
<221> misc_feature
<222> (44)..(76)
<223> CDR1
<220>
<221> misc_feature
<222> (77)..(121)
<223> FR2
<220>
<221> misc_feature
<222> (122)..(142)
<223> CDR2
<220>
<221> misc_feature
<222> (143)..(238)
<223> FR3
<220>
<221> misc_feature
<222> (239)..(265)
<223> CDR3
<220>
<221> misc_feature
<222> (266)..(295)
<223> FR4
<400> 37
ttccatgtat gcatctctag gagagagagt cactatcact tgcaaggcga gtcaggacac 60
taatagctat ttaagctggt tccagcagaa accagggaaa tctcctaaga ccctgatcta 120
tcgtgcaaac agattggtag atggggtccc atcaaggttc agtggcagtg gatctgggca 180
agattattct ctcaccatca gcagcctgga gtatgaagat atgggaattt attattgtct 240
acagtatgat gagtttccgt acacgttcgg aggggggacc aagctggaaa taaaac 296
<210> 38
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 26E10: CDR1
<400> 38
aaggcgagtc aggacactaa tagctattta agc 33
<210> 39
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 26E10: CDR2
<400> 39
cgtgcaaaca gattggtaga t 21
<210> 40
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 26E10: CDR3
<400> 40
ctacagtatg atgagtttcc gtacacg 27
<210> 41
<211> 98
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 26E10
<220>
<221> MISC_FEATURE
<222> (1)..(14)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (15)..(25)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (26)..(40)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (41)..(47)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (48)..(79)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (80)..(88)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (89)..(98)
<223> FR4
<400> 41
Ser Met Tyr Ala Ser Leu Gly Glu Arg Val Thr Ile Thr Cys Lys Ala
1 5 10 15
Ser Gln Asp Thr Asn Ser Tyr Leu Ser Trp Phe Gln Gln Lys Pro Gly
20 25 30
Lys Ser Pro Lys Thr Leu Ile Tyr Arg Ala Asn Arg Leu Val Asp Gly
35 40 45
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Gln Asp Tyr Ser Leu
50 55 60
Thr Ile Ser Ser Leu Glu Tyr Glu Asp Met Gly Ile Tyr Tyr Cys Leu
65 70 75 80
Gln Tyr Asp Glu Phe Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu
85 90 95
Ile Lys
<210> 42
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 26E10: FR1
<400> 42
Ser Met Tyr Ala Ser Leu Gly Glu Arg Val Thr Ile Thr Cys
1 5 10
<210> 43
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 26E10: CDR1
<400> 43
Lys Ala Ser Gln Asp Thr Asn Ser Tyr Leu Ser
1 5 10
<210> 44
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 26E10: FR2
<400> 44
Trp Phe Gln Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile Tyr
1 5 10 15
<210> 45
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 26E10: CDR2
<400> 45
Arg Ala Asn Arg Leu Val Asp
1 5
<210> 46
<211> 32
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 26E10: FR3
<400> 46
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Gln Asp Tyr Ser
1 5 10 15
Leu Thr Ile Ser Ser Leu Glu Tyr Glu Asp Met Gly Ile Tyr Tyr Cys
20 25 30
<210> 47
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 26E10: CDR3
<400> 47
Leu Gln Tyr Asp Glu Phe Pro Tyr Thr
1 5
<210> 48
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 26E10: FR4
<400> 48
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
1 5 10
<210> 49
<211> 264
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 26E2
<220>
<221> misc_feature
<222> (2)..(46)
<223> FR2
<220>
<221> misc_feature
<222> (47)..(97)
<223> CDR2
<220>
<221> misc_feature
<222> (98)..(193)
<223> FR3
<220>
<221> misc_feature
<222> (194)..(229)
<223> CDR3
<220>
<221> misc_feature
<222> (230)..(262)
<223> FR4
<400> 49
gcgctgggta aagcagacac ctggacaggg cctggaatgg attggatata tttatcctgg 60
agatggtggt actaactgca atcagaagtt ccagggcaag gccacattga ctgcagacac 120
atcctccagc acagcctaca tgcagatcag cagcctgaca tctgaagact ctgcggtcta 180
tttctgtgca agatcgggca actatggtaa ctacgaaggg tttgctttct ggggccaagg 240
gactctggtc actgtctctg cagc 264
<210> 50
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 26E2: CDR2
<400> 50
tatatttatc ctggagatgg tggtactaac tgcaatcaga agttccaggg c 51
<210> 51
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 26E2: CDR3
<400> 51
tcgggcaact atggtaacta cgaagggttt gctttc 36
<210> 52
<211> 87
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 26E2
<220>
<221> MISC_FEATURE
<222> (1)..(15)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (16)..(32)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (33)..(64)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (65)..(76)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (77)..(87)
<223> FR4
<400> 52
Arg Trp Val Lys Gln Thr Pro Gly Gln Gly Leu Glu Trp Ile Gly Tyr
1 5 10 15
Ile Tyr Pro Gly Asp Gly Gly Thr Asn Cys Asn Gln Lys Phe Gln Gly
20 25 30
Lys Ala Thr Leu Thr Ala Asp Thr Ser Ser Ser Thr Ala Tyr Met Gln
35 40 45
Ile Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys Ala Arg
50 55 60
Ser Gly Asn Tyr Gly Asn Tyr Glu Gly Phe Ala Phe Trp Gly Gln Gly
65 70 75 80
Thr Leu Val Thr Val Ser Ala
85
<210> 53
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 26E2: FR2
<400> 53
Arg Trp Val Lys Gln Thr Pro Gly Gln Gly Leu Glu Trp Ile Gly
1 5 10 15
<210> 54
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 26E2: CDR2
<400> 54
Tyr Ile Tyr Pro Gly Asp Gly Gly Thr Asn Cys Asn Gln Lys Phe Gln
1 5 10 15
Gly
<210> 55
<211> 32
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 26E2: FR3
<400> 55
Lys Ala Thr Leu Thr Ala Asp Thr Ser Ser Ser Thr Ala Tyr Met Gln
1 5 10 15
Ile Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys Ala Arg
20 25 30
<210> 56
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 26E2: CDR3
<400> 56
Ser Gly Asn Tyr Gly Asn Tyr Glu Gly Phe Ala Phe
1 5 10
<210> 57
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 26E2: FR4
<400> 57
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala
1 5 10
<210> 58
<211> 394
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 26E2
<220>
<221> misc_feature
<222> (1)..(60)
<223> Лидерная последовательность
<220>
<221> misc_feature
<222> (61)..(129)
<223> FR1
<220>
<221> misc_feature
<222> (130)..(162)
<223> CDR1
<220>
<221> misc_feature
<222> (163)..(207)
<223> FR2
<220>
<221> misc_feature
<222> (208)..(228)
<223> CDR2
<220>
<221> misc_feature
<222> (229)..(324)
<223> FR3
<220>
<221> misc_feature
<222> (325)..(351)
<223> CDR3
<220>
<221> misc_feature
<222> (352)..(393)
<223> FR4
<400> 58
atgagggccc ctgctcagtt ttttgggatc ttgttgctct ggtttccagg tatcaaatgt 60
gacatcaaga tgacccagtc tccatcctcc atgtatgcat ctctaggaga gagagtcact 120
atcacttgca aggcgagtca ggacactaat agctatttaa gctggttcca gcagaaacca 180
gggaaatctc ctaagaccct gatctatcgt gcaaacagat tggtagatgg ggtcccatca 240
aggttcagtg gcagtggatc tgggcaagat tattctctca ccatcagccg cctggagtat 300
gaagatatgg gaatttatta ttgtctacag tataatgagt ttccgtacac gttcggaggg 360
gggaccaagc tggaaataaa acgggctgat gctg 394
<210> 59
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 26E2: CDR1
<400> 59
aaggcgagtc aggacactaa tagctattta agc 33
<210> 60
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 26E2: CDR2
<400> 60
cgtgcaaaca gattggtaga t 21
<210> 61
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 26E2: CDR3
<400> 61
ctacagtata atgagtttcc gtacacg 27
<210> 62
<211> 131
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 26E2
<220>
<221> MISC_FEATURE
<222> (1)..(20)
<223> Лидерная последовательность
<220>
<221> MISC_FEATURE
<222> (21)..(43)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (44)..(54)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (55)..(69)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (70)..(76)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (77)..(108)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (109)..(117)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (118)..(131)
<223> FR4
<400> 62
Met Arg Ala Pro Ala Gln Phe Phe Gly Ile Leu Leu Leu Trp Phe Pro
1 5 10 15
Gly Ile Lys Cys Asp Ile Lys Met Thr Gln Ser Pro Ser Ser Met Tyr
20 25 30
Ala Ser Leu Gly Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp
35 40 45
Thr Asn Ser Tyr Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ser Pro
50 55 60
Lys Thr Leu Ile Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser
65 70 75 80
Arg Phe Ser Gly Ser Gly Ser Gly Gln Asp Tyr Ser Leu Thr Ile Ser
85 90 95
Arg Leu Glu Tyr Glu Asp Met Gly Ile Tyr Tyr Cys Leu Gln Tyr Asn
100 105 110
Glu Phe Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
115 120 125
Ala Asp Ala
130
<210> 63
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 26E2: FR1
<400> 63
Asp Ile Lys Met Thr Gln Ser Pro Ser Ser Met Tyr Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Thr Ile Thr Cys
20
<210> 64
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 26E2: CDR1
<400> 64
Lys Ala Ser Gln Asp Thr Asn Ser Tyr Leu Ser
1 5 10
<210> 65
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 26E2: FR2
<400> 65
Trp Phe Gln Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile Tyr
1 5 10 15
<210> 66
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 26E2: CDR2
<400> 66
Arg Ala Asn Arg Leu Val Asp
1 5
<210> 67
<211> 32
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 26E2: FR3
<400> 67
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Gln Asp Tyr Ser
1 5 10 15
Leu Thr Ile Ser Arg Leu Glu Tyr Glu Asp Met Gly Ile Tyr Tyr Cys
20 25 30
<210> 68
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 26E2: CDR3
<400> 68
Leu Gln Tyr Asn Glu Phe Pro Tyr Thr
1 5
<210> 69
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 26E2: FR4
<400> 69
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Ala Asp Ala
1 5 10
<210> 70
<211> 435
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 31C4
<220>
<221> misc_feature
<222> (14)..(70)
<223> Лидерная последовательность
<220>
<221> misc_feature
<222> (71)..(145)
<223> FR1
<220>
<221> misc_feature
<222> (146)..(175)
<223> CDR1
<220>
<221> misc_feature
<222> (176)..(217)
<223> FR2
<220>
<221> misc_feature
<222> (218)..(268)
<223> CDR2
<220>
<221> misc_feature
<222> (269)..(358)
<223> FR3
<220>
<221> misc_feature
<222> (359)..(400)
<223> CDR3
<220>
<221> misc_feature
<222> (401)..(433)
<223> FR4
<400> 70
tgtggggaat tccatggaat ggagctgggt ttttctcttc ctcctgtcaa taactacagg 60
tgtccactcc caggcttatc tacagcagtc tggggctgag ctggtgaggt ctggggcctc 120
agtgaagatg tcctgcaagg cttctggcta cacatttacc agttacaata tgcactgggt 180
aaagcagaca cctggacagg gcctggaatg gattggatat atttttcctg gagatggtgg 240
tactaactac aatcagaagt tcaagggcaa ggccacattg actgcagaca catcctccag 300
cacagcctac atgcagatca gcagcctgac atctgaagac tctgcggtct atttctgtgc 360
aagatcgggc aactatggta actacgaagg gtttgcttac tggggccaag ggactctggt 420
cactgtctct gctag 435
<210> 71
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 31C4: CDR1
<400> 71
ggctacacat ttaccagtta caatatgcac 30
<210> 72
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 31C4: CDR2
<400> 72
tatatttttc ctggagatgg tggtactaac tacaatcaga agttcaaggg c 51
<210> 73
<211> 42
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 31C4: CDR3
<400> 73
gcaagatcgg gcaactatgg taactacgaa gggtttgctt ac 42
<210> 74
<211> 140
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 31C4
<220>
<221> MISC_FEATURE
<222> (1)..(19)
<223> Лидерная последовательность
<220>
<221> MISC_FEATURE
<222> (20)..(44)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (45)..(54)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (55)..(68)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (69)..(85)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (86)..(115)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (116)..(129)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (130)..(140)
<223> FR4
<400> 74
Met Glu Trp Ser Trp Val Phe Leu Phe Leu Leu Ser Ile Thr Thr Gly
1 5 10 15
Val His Ser Gln Ala Tyr Leu Gln Gln Ser Gly Ala Glu Leu Val Arg
20 25 30
Ser Gly Ala Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe
35 40 45
Thr Ser Tyr Asn Met His Trp Val Lys Gln Thr Pro Gly Gln Gly Leu
50 55 60
Glu Trp Ile Gly Tyr Ile Phe Pro Gly Asp Gly Gly Thr Asn Tyr Asn
65 70 75 80
Gln Lys Phe Lys Gly Lys Ala Thr Leu Thr Ala Asp Thr Ser Ser Ser
85 90 95
Thr Ala Tyr Met Gln Ile Ser Ser Leu Thr Ser Glu Asp Ser Ala Val
100 105 110
Tyr Phe Cys Ala Arg Ser Gly Asn Tyr Gly Asn Tyr Glu Gly Phe Ala
115 120 125
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala
130 135 140
<210> 75
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 31C4: FR1
<400> 75
Gln Ala Tyr Leu Gln Gln Ser Gly Ala Glu Leu Val Arg Ser Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser
20 25
<210> 76
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 31C4: CDR1
<400> 76
Gly Tyr Thr Phe Thr Ser Tyr Asn Met His
1 5 10
<210> 77
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 31C4: FR2
<400> 77
Trp Val Lys Gln Thr Pro Gly Gln Gly Leu Glu Trp Ile Gly
1 5 10
<210> 78
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 31C4: CDR2
<400> 78
Tyr Ile Phe Pro Gly Asp Gly Gly Thr Asn Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 79
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 31C4: FR3
<400> 79
Lys Ala Thr Leu Thr Ala Asp Thr Ser Ser Ser Thr Ala Tyr Met Gln
1 5 10 15
Ile Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
20 25 30
<210> 80
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 31C4: CDR3
<400> 80
Ala Arg Ser Gly Asn Tyr Gly Asn Tyr Glu Gly Phe Ala Tyr
1 5 10
<210> 81
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 31C4: FR4
<400> 81
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala
1 5 10
<210> 82
<211> 407
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 31C4
<220>
<221> misc_feature
<222> (3)..(71)
<223> Лидерная последовательность
<220>
<221> misc_feature
<222> (72)..(140)
<223> FR1
<220>
<221> misc_feature
<222> (141)..(173)
<223> CDR1
<220>
<221> misc_feature
<222> (174)..(218)
<223> FR2
<220>
<221> misc_feature
<222> (219)..(239)
<223> CDR2
<220>
<221> misc_feature
<222> (240)..(335)
<223> FR3
<220>
<221> misc_feature
<222> (336)..(362)
<223> CDR3
<220>
<221> misc_feature
<222> (363)..(407)
<223> FR4
<400> 82
tactagtcga catgaggccc cctgctcagt tttttgggat cttgttgctc tggtttccag 60
gtatcaaatg tgacatcaag atgacccagt ctccatcttc catgtatgca tctctaggag 120
agagagtcac tatcacttgc aaggcgagtc aggacattaa tagctattta agctggttcc 180
agcagaaacc agggaaatct cctaagaccc tgatctatcg tgcaaacaga ttggtagatg 240
gggtcccatc aaggttcagt ggcagtggat ctgggcaaga ttattctctc accatcagca 300
gcctggagta tgaagatatg ggaatttatt attgtctaca gtatgatgaa tttccgtaca 360
cgttcggagg ggggaccaag ctggaaataa aacgggctga tgctgca 407
<210> 83
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 31C4: CDR1
<400> 83
aaggcgagtc aggacattaa tagctattta agc 33
<210> 84
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 31C4: CDR2
<400> 84
cgtgcaaaca gattggtaga t 21
<210> 85
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 31C4: CDR3
<400> 85
ctacagtatg atgaatttcc gtacacg 27
<210> 86
<211> 135
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 31C4
<220>
<221> MISC_FEATURE
<222> (1)..(23)
<223> Лидерная последовательность
<220>
<221> MISC_FEATURE
<222> (24)..(46)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (47)..(57)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (58)..(72)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (73)..(79)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (80)..(111)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (112)..(120)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (121)..(135)
<223> FR4
<400> 86
Leu Val Asp Met Arg Pro Pro Ala Gln Phe Phe Gly Ile Leu Leu Leu
1 5 10 15
Trp Phe Pro Gly Ile Lys Cys Asp Ile Lys Met Thr Gln Ser Pro Ser
20 25 30
Ser Met Tyr Ala Ser Leu Gly Glu Arg Val Thr Ile Thr Cys Lys Ala
35 40 45
Ser Gln Asp Ile Asn Ser Tyr Leu Ser Trp Phe Gln Gln Lys Pro Gly
50 55 60
Lys Ser Pro Lys Thr Leu Ile Tyr Arg Ala Asn Arg Leu Val Asp Gly
65 70 75 80
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Gln Asp Tyr Ser Leu
85 90 95
Thr Ile Ser Ser Leu Glu Tyr Glu Asp Met Gly Ile Tyr Tyr Cys Leu
100 105 110
Gln Tyr Asp Glu Phe Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu
115 120 125
Ile Lys Arg Ala Asp Ala Ala
130 135
<210> 87
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 31C4: FR1
<400> 87
Asp Ile Lys Met Thr Gln Ser Pro Ser Ser Met Tyr Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Thr Ile Thr Cys
20
<210> 88
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 31C4: CDR1
<400> 88
Lys Ala Ser Gln Asp Ile Asn Ser Tyr Leu Ser
1 5 10
<210> 89
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 31C4: FR2
<400> 89
Trp Phe Gln Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile Tyr
1 5 10 15
<210> 90
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 31C4: CDR2
<400> 90
Arg Ala Asn Arg Leu Val Asp
1 5
<210> 91
<211> 32
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 31C4: FR3
<400> 91
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Gln Asp Tyr Ser
1 5 10 15
Leu Thr Ile Ser Ser Leu Glu Tyr Glu Asp Met Gly Ile Tyr Tyr Cys
20 25 30
<210> 92
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 31C4: CDR3
<400> 92
Leu Gln Tyr Asp Glu Phe Pro Tyr Thr
1 5
<210> 93
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 31C4: FR4
<400> 93
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Ala Asp Ala Ala
1 5 10 15
<210> 94
<211> 430
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 34B10
<220>
<221> misc_feature
<222> (11)..(67)
<223> Лидерная последовательность
<220>
<221> misc_feature
<222> (68)..(142)
<223> FR1
<220>
<221> misc_feature
<222> (143)..(172)
<223> CDR1
<220>
<221> misc_feature
<222> (173)..(214)
<223> FR2
<220>
<221> misc_feature
<222> (215)..(271)
<223> CDR2
<220>
<221> misc_feature
<222> (272)..(367)
<223> FR3
<220>
<221> misc_feature
<222> (368)..(397)
<223> CDR3
<220>
<221> misc_feature
<222> (398)..(430)
<223> FR4
<400> 94
tggggaattc atggagttgg ggttcagctg gattttcctt ggaacacttt taaatggtat 60
ccagtgtgag gtgaagctgg tggagtctgg aggagtcttg gtacagcctg ggggttctct 120
gagactctcc tgtgcaactt ctggattcac cttcactgat tactacatgg gctgggtccg 180
ccagcctcca ggaaaggcgc ttgagtggtt gggttttatt agaaacaaag ctaatggtta 240
cacaacagag tccagtgcat ctgtgaaggg tcggttcacc atctccagag ataattccca 300
aagcatcctc tatcttcaaa tgaacaccct gagagctgag gacagtgcca cttattactg 360
tgcaagagat tactactccg gtagtagcct tgactactgg ggccaaggca ccactctcac 420
agtctcctca 430
<210> 95
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 34B10: CDR1
<400> 95
ggattcacct tcactgatta ctacatgggc 30
<210> 96
<211> 57
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 34B10: CDR2
<400> 96
tttattagaa acaaagctaa tggttacaca acagagtcca gtgcatctgt gaagggt 57
<210> 97
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 34B10: CDR3
<400> 97
gattactact ccggtagtag ccttgactac 30
<210> 98
<211> 140
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 34B10
<220>
<221> MISC_FEATURE
<222> (1)..(19)
<223> Лидерная последовательность
<220>
<221> MISC_FEATURE
<222> (20)..(44)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (45)..(54)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (55)..(68)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (69)..(87)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (88)..(119)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (120)..(129)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (130)..(140)
<223> FR4
<400> 98
Met Glu Leu Gly Phe Ser Trp Ile Phe Leu Gly Thr Leu Leu Asn Gly
1 5 10 15
Ile Gln Cys Glu Val Lys Leu Val Glu Ser Gly Gly Val Leu Val Gln
20 25 30
Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Thr Ser Gly Phe Thr Phe
35 40 45
Thr Asp Tyr Tyr Met Gly Trp Val Arg Gln Pro Pro Gly Lys Ala Leu
50 55 60
Glu Trp Leu Gly Phe Ile Arg Asn Lys Ala Asn Gly Tyr Thr Thr Glu
65 70 75 80
Ser Ser Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Gln Ser Ile Leu Tyr Leu Gln Met Asn Thr Leu Arg Ala Glu Asp Ser
100 105 110
Ala Thr Tyr Tyr Cys Ala Arg Asp Tyr Tyr Ser Gly Ser Ser Leu Asp
115 120 125
Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val Ser Ser
130 135 140
<210> 99
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 34B10: FR1
<400> 99
Glu Val Lys Leu Val Glu Ser Gly Gly Val Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Thr Ser
20 25
<210> 100
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 34B10: CDR1
<400> 100
Gly Phe Thr Phe Thr Asp Tyr Tyr Met Gly
1 5 10
<210> 101
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 34B10: FR2
<400> 101
Trp Val Arg Gln Pro Pro Gly Lys Ala Leu Glu Trp Leu Gly
1 5 10
<210> 102
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 34B10: CDR2
<400> 102
Phe Ile Arg Asn Lys Ala Asn Gly Tyr Thr Thr Glu Ser Ser Ala Ser
1 5 10 15
Val Lys Gly
<210> 103
<211> 32
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 34B10: FR3
<400> 103
Arg Phe Thr Ile Ser Arg Asp Asn Ser Gln Ser Ile Leu Tyr Leu Gln
1 5 10 15
Met Asn Thr Leu Arg Ala Glu Asp Ser Ala Thr Tyr Tyr Cys Ala Arg
20 25 30
<210> 104
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 34B10: CDR3
<400> 104
Asp Tyr Tyr Ser Gly Ser Ser Leu Asp Tyr
1 5 10
<210> 105
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 34B10: FR4
<400> 105
Trp Gly Gln Gly Thr Thr Leu Thr Val Ser Ser
1 5 10
<210> 106
<211> 406
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 34B10
<220>
<221> misc_feature
<222> (1)..(75)
<223> Лидерная последовательность
<220>
<221> misc_feature
<222> (76)..(144)
<223> FR1
<220>
<221> misc_feature
<222> (145)..(177)
<223> CDR1
<220>
<221> misc_feature
<222> (178)..(222)
<223> FR2
<220>
<221> misc_feature
<222> (223)..(243)
<223> CDR2
<220>
<221> misc_feature
<222> (244)..(339)
<223> FR3
<220>
<221> misc_feature
<222> (340)..(366)
<223> CDR3
<220>
<221> misc_feature
<222> (367)..(405)
<223> FR4
<400> 106
tctatactag tcgacaggag gaccccggct cagatttgtg gtctcctgtt gctctttttt 60
caaggtacca gatgtgatat ccagatgaca cagactacat cctccctgtc tgcctctctg 120
ggagacagag tcaccatcag ttgcagggca agtcaggaca ttagcaatta tttaaattgg 180
tatcagcaga aaccagatgg aactgttaaa ctcctgatct actacacatc aagattacac 240
tcaggagtcc catcaaggtt cagtggcagt gggtctggaa cagattattc tctctccatt 300
agcaacctgg agcaagaaga tattgccact tacttttgcc aacagggtta tacgcttccg 360
tacacgttcg gaggggggac caagcttgaa ataaaacggg ctgatg 406
<210> 107
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 34B10: CDR1
<400> 107
agggcaagtc aggacattag caattattta aat 33
<210> 108
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 34B10: CDR2
<400> 108
tacacatcaa gattacactc a 21
<210> 109
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 34B10: CDR3
<400> 109
caacagggtt atacgcttcc gtacacg 27
<210> 110
<211> 135
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 34B10
<220>
<221> MISC_FEATURE
<222> (1)..(25)
<223> Лидерная последовательность
<220>
<221> MISC_FEATURE
<222> (26)..(48)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (49)..(59)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (60)..(74)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (75)..(81)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (82)..(113)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (114)..(122)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (123)..(135)
<223> FR4
<400> 110
Ser Ile Leu Val Asp Arg Arg Thr Pro Ala Gln Ile Cys Gly Leu Leu
1 5 10 15
Leu Leu Phe Phe Gln Gly Thr Arg Cys Asp Ile Gln Met Thr Gln Thr
20 25 30
Thr Ser Ser Leu Ser Ala Ser Leu Gly Asp Arg Val Thr Ile Ser Cys
35 40 45
Arg Ala Ser Gln Asp Ile Ser Asn Tyr Leu Asn Trp Tyr Gln Gln Lys
50 55 60
Pro Asp Gly Thr Val Lys Leu Leu Ile Tyr Tyr Thr Ser Arg Leu His
65 70 75 80
Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr
85 90 95
Ser Leu Ser Ile Ser Asn Leu Glu Gln Glu Asp Ile Ala Thr Tyr Phe
100 105 110
Cys Gln Gln Gly Tyr Thr Leu Pro Tyr Thr Phe Gly Gly Gly Thr Lys
115 120 125
Leu Glu Ile Lys Arg Ala Asp
130 135
<210> 111
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 34B10: FR1
<400> 111
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys
20
<210> 112
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 34B10: CDR1
<400> 112
Arg Ala Ser Gln Asp Ile Ser Asn Tyr Leu Asn
1 5 10
<210> 113
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 34B10: FR2
<400> 113
Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile Tyr
1 5 10 15
<210> 114
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 34B10: CDR2
<400> 114
Tyr Thr Ser Arg Leu His Ser
1 5
<210> 115
<211> 32
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 34B10: FR3
<400> 115
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Ser
1 5 10 15
Leu Ser Ile Ser Asn Leu Glu Gln Glu Asp Ile Ala Thr Tyr Phe Cys
20 25 30
<210> 116
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 34B10: CDR3
<400> 116
Gln Gln Gly Tyr Thr Leu Pro Tyr Thr
1 5
<210> 117
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 34B10: FR4
<400> 117
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Ala Asp
1 5 10
<210> 118
<211> 411
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 37A3
<220>
<221> misc_feature
<222> (1)..(57)
<223> Лидерная последовательность
<220>
<221> misc_feature
<222> (58)..(132)
<223> FR1
<220>
<221> misc_feature
<222> (133)..(162)
<223> CDR1
<220>
<221> misc_feature
<222> (163)..(204)
<223> FR2
<220>
<221> misc_feature
<222> (205)..(261)
<223> CDR2
<220>
<221> misc_feature
<222> (262)..(351)
<223> FR3
<220>
<221> misc_feature
<222> (352)..(381)
<223> CDR3
<220>
<221> misc_feature
<222> (382)..(411)
<223> FR4
<400> 118
atgtacttgg gactgagctg tgtatttctt gtggctcttt tgaatggtgt ccagtgtcag 60
gtgcagcttg tagagaccgg gggaggcttg gtgaggcctg gaaattctct gaaactctcc 120
tgtgttacct cgggattcac tttcagtaac taccggatgc actggcttcg ccagcctcca 180
gggaagaggc tggagtggat tgctgtaatt acagtcaaat ctgataatta tggagcaaat 240
tttgcagagt ctgtgaaagg cagattcact atttcaagag atgattcaaa aagcagtgtc 300
tacctgcaga tgaacagatt aagagaggaa gacactgcca cttattattg tagtagaggt 360
agtggcccag ggtttgctta ctggggccaa gggactctgg tcactgtctc t 411
<210> 119
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 37A3: CDR1
<400> 119
ggattcactt tcagtaacta ccggatgcac 30
<210> 120
<211> 57
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 37A3: CDR2
<400> 120
gtaattacag tcaaatctga taattatgga gcaaattttg cagagtctgt gaaaggc 57
<210> 121
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 37A3: CDR3
<400> 121
agtagaggta gtggcccagg gtttgcttac 30
<210> 122
<211> 137
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 37A3
<220>
<221> MISC_FEATURE
<222> (1)..(19)
<223> Лидерная последовательность
<220>
<221> MISC_FEATURE
<222> (20)..(44)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (45)..(54)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (55)..(68)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (69)..(87)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (88)..(117)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (118)..(127)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (128)..(137)
<223> FR4
<400> 122
Met Tyr Leu Gly Leu Ser Cys Val Phe Leu Val Ala Leu Leu Asn Gly
1 5 10 15
Val Gln Cys Gln Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Arg
20 25 30
Pro Gly Asn Ser Leu Lys Leu Ser Cys Val Thr Ser Gly Phe Thr Phe
35 40 45
Ser Asn Tyr Arg Met His Trp Leu Arg Gln Pro Pro Gly Lys Arg Leu
50 55 60
Glu Trp Ile Ala Val Ile Thr Val Lys Ser Asp Asn Tyr Gly Ala Asn
65 70 75 80
Phe Ala Glu Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser
85 90 95
Lys Ser Ser Val Tyr Leu Gln Met Asn Arg Leu Arg Glu Glu Asp Thr
100 105 110
Ala Thr Tyr Tyr Cys Ser Arg Gly Ser Gly Pro Gly Phe Ala Tyr Trp
115 120 125
Gly Gln Gly Thr Leu Val Thr Val Ser
130 135
<210> 123
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 37A3: FR1
<400> 123
Gln Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Arg Pro Gly Asn
1 5 10 15
Ser Leu Lys Leu Ser Cys Val Thr Ser
20 25
<210> 124
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 37A3: CDR1
<400> 124
Gly Phe Thr Phe Ser Asn Tyr Arg Met His
1 5 10
<210> 125
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 37A3: FR2
<400> 125
Trp Leu Arg Gln Pro Pro Gly Lys Arg Leu Glu Trp Ile Ala
1 5 10
<210> 126
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 37A3: CDR2
<400> 126
Val Ile Thr Val Lys Ser Asp Asn Tyr Gly Ala Asn Phe Ala Glu Ser
1 5 10 15
Val Lys Gly
<210> 127
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 37A3: FR3
<400> 127
Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Ser Val Tyr Leu Gln
1 5 10 15
Met Asn Arg Leu Arg Glu Glu Asp Thr Ala Thr Tyr Tyr Cys
20 25 30
<210> 128
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 37A3: CDR3
<400> 128
Ser Arg Gly Ser Gly Pro Gly Phe Ala Tyr
1 5 10
<210> 129
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 37A3: FR4
<400> 129
Trp Gly Gln Gly Thr Leu Val Thr Val Ser
1 5 10
<210> 130
<211> 411
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 37A3
<220>
<221> misc_feature
<222> (1)..(72)
<223> Лидерная последовательность
<220>
<221> misc_feature
<222> (73)..(141)
<223> FR1
<220>
<221> misc_feature
<222> (142)..(192)
<223> CDR1
<220>
<221> misc_feature
<222> (193)..(237)
<223> FR2
<220>
<221> misc_feature
<222> (238)..(258)
<223> CDR2
<220>
<221> misc_feature
<222> (259)..(354)
<223> FR3
<220>
<221> misc_feature
<222> (355)..(381)
<223> CDR3
<220>
<221> misc_feature
<222> (382)..(411)
<223> FR4
<400> 130
atgggcttca agatggagtc acagactcag gtcctcatct ccttgctgtt ctgggtatct 60
ggtacctgtg gggacattgt gatgacacag tctccatcct ccctgagtgt gtcagcagga 120
gagaaggtca ctatgagctg caagtccagt cagagtctgt taaacagtgg aaatcaaaag 180
aactacttgg cctggtacca gcagaaacca gggcagcctc ctaaactgtt gatctacggg 240
gcatccacta gggaatctgg ggtccctgat cgcttcacag gcagtggatc tggaaccgat 300
ttcactctta ccatcagcag tgtgcaggct gaagacctgg cagtttatta ctgtcagaat 360
gatcatagtt atccattcac gttcggctcg gggacaaagt tggaaataaa a 411
<210> 131
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 37A3: CDR1
<400> 131
aagtccagtc agagtctgtt aaacagtgga aatcaaaaga actacttggc c 51
<210> 132
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 37A3: CDR2
<400> 132
ggggcatcca ctagggaatc t 21
<210> 133
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 37A3: CDR3
<400> 133
cagaatgatc atagttatcc attcacg 27
<210> 134
<211> 137
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 37A3
<220>
<221> MISC_FEATURE
<222> (1)..(24)
<223> Лидерная последовательность
<220>
<221> MISC_FEATURE
<222> (25)..(47)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (48)..(64)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (65)..(79)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (80)..(86)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (87)..(118)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (119)..(127)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (128)..(137)
<223> FR4
<400> 134
Met Gly Phe Lys Met Glu Ser Gln Thr Gln Val Leu Ile Ser Leu Leu
1 5 10 15
Phe Trp Val Ser Gly Thr Cys Gly Asp Ile Val Met Thr Gln Ser Pro
20 25 30
Ser Ser Leu Ser Val Ser Ala Gly Glu Lys Val Thr Met Ser Cys Lys
35 40 45
Ser Ser Gln Ser Leu Leu Asn Ser Gly Asn Gln Lys Asn Tyr Leu Ala
50 55 60
Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile Tyr Gly
65 70 75 80
Ala Ser Thr Arg Glu Ser Gly Val Pro Asp Arg Phe Thr Gly Ser Gly
85 90 95
Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Val Gln Ala Glu Asp
100 105 110
Leu Ala Val Tyr Tyr Cys Gln Asn Asp His Ser Tyr Pro Phe Thr Phe
115 120 125
Gly Ser Gly Thr Lys Leu Glu Ile Lys
130 135
<210> 135
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 37A3: FR1
<400> 135
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Ser Val Ser Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys
20
<210> 136
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 37A3: CDR1
<400> 136
Lys Ser Ser Gln Ser Leu Leu Asn Ser Gly Asn Gln Lys Asn Tyr Leu
1 5 10 15
Ala
<210> 137
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 37A3: FR2
<400> 137
Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile Tyr
1 5 10 15
<210> 138
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 37A3: CDR2
<400> 138
Gly Ala Ser Thr Arg Glu Ser
1 5
<210> 139
<211> 32
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 37A3: FR3
<400> 139
Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr
1 5 10 15
Leu Thr Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys
20 25 30
<210> 140
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 37A3: CDR3
<400> 140
Gln Asn Asp His Ser Tyr Pro Phe Thr
1 5
<210> 141
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 37A3: FR4
<400> 141
Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
1 5 10
<210> 142
<211> 432
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 12A10
<220>
<221> misc_feature
<222> (12)..(68)
<223> Лидерная последовательность
<220>
<221> misc_feature
<222> (69)..(143)
<223> FR1
<220>
<221> misc_feature
<222> (144)..(173)
<223> CDR1
<220>
<221> misc_feature
<222> (174)..(215)
<223> FR2
<220>
<221> misc_feature
<222> (216)..(266)
<223> CDR2
<220>
<221> misc_feature
<222> (267)..(356)
<223> FR3
<220>
<221> misc_feature
<222> (357)..(398)
<223> CDR3
<220>
<221> misc_feature
<222> (399)..(431)
<223> FR4
<400> 142
tggggaattc catggaatgg agctgggttt ttctcttcct cctgtcaata actacaggtg 60
tccactccca ggcttatcta cagcagtctg gggctgagct ggtgaggtct ggggcctcag 120
tgaagatgtc ctgcaaggct tctggctaca catttaccag ttacaatatg cactgggtaa 180
agcagacacc tggacagggc ctggaatgga ttggatatat ttttcctgga gatggtggta 240
ctaactacaa tcagaagttc aagggcaagg ccacattgac tgcagacaca tcctccagca 300
cagcctacat gcagatcagc agcctgacat ctgaagactc tgcggtctat ttctgtgcaa 360
gatcgggcta ctatggtaac tacgaagggt ttgcttactg gggccaaggg actctggtca 420
ctgtctctgc ag 432
<210> 143
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 12A10: CDR1
<400> 143
ggctacacat ttaccagtta caatatgcac 30
<210> 144
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 12A10: CDR2
<400> 144
tatatttttc ctggagatgg tggtactaac tacaatcaga agttcaaggg c 51
<210> 145
<211> 42
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 12A10: CDR3
<400> 145
gcaagatcgg gctactatgg taactacgaa gggtttgctt ac 42
<210> 146
<211> 140
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 12A10
<220>
<221> MISC_FEATURE
<222> (1)..(19)
<223> Лидерная последовательность
<220>
<221> MISC_FEATURE
<222> (20)..(44)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (45)..(54)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (55)..(68)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (69)..(85)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (86)..(115)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (116)..(129)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (130)..(140)
<223> FR4
<400> 146
Met Glu Trp Ser Trp Val Phe Leu Phe Leu Leu Ser Ile Thr Thr Gly
1 5 10 15
Val His Ser Gln Ala Tyr Leu Gln Gln Ser Gly Ala Glu Leu Val Arg
20 25 30
Ser Gly Ala Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe
35 40 45
Thr Ser Tyr Asn Met His Trp Val Lys Gln Thr Pro Gly Gln Gly Leu
50 55 60
Glu Trp Ile Gly Tyr Ile Phe Pro Gly Asp Gly Gly Thr Asn Tyr Asn
65 70 75 80
Gln Lys Phe Lys Gly Lys Ala Thr Leu Thr Ala Asp Thr Ser Ser Ser
85 90 95
Thr Ala Tyr Met Gln Ile Ser Ser Leu Thr Ser Glu Asp Ser Ala Val
100 105 110
Tyr Phe Cys Ala Arg Ser Gly Tyr Tyr Gly Asn Tyr Glu Gly Phe Ala
115 120 125
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala
130 135 140
<210> 147
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 12A10: FR1
<400> 147
Gln Ala Tyr Leu Gln Gln Ser Gly Ala Glu Leu Val Arg Ser Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser
20 25
<210> 148
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 12A10: CDR1
<400> 148
Gly Tyr Thr Phe Thr Ser Tyr Asn Met His
1 5 10
<210> 149
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 12A10: FR2
<400> 149
Trp Val Lys Gln Thr Pro Gly Gln Gly Leu Glu Trp Ile Gly
1 5 10
<210> 150
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 12A10: CDR2
<400> 150
Tyr Ile Phe Pro Gly Asp Gly Gly Thr Asn Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 151
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 12A10: FR3
<400> 151
Lys Ala Thr Leu Thr Ala Asp Thr Ser Ser Ser Thr Ala Tyr Met Gln
1 5 10 15
Ile Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
20 25 30
<210> 152
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 12A10: CDR3
<400> 152
Ala Arg Ser Gly Tyr Tyr Gly Asn Tyr Glu Gly Phe Ala Tyr
1 5 10
<210> 153
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 12A10: FR4
<400> 153
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala
1 5 10
<210> 154
<211> 303
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 12A10
<220>
<221> misc_feature
<222> (3)..(44)
<223> FR1
<220>
<221> misc_feature
<222> (45)..(77)
<223> CDR1
<220>
<221> misc_feature
<222> (78)..(122)
<223> FR2
<220>
<221> misc_feature
<222> (123)..(143)
<223> CDR2
<220>
<221> misc_feature
<222> (144)..(239)
<223> FR3
<220>
<221> misc_feature
<222> (240)..(266)
<223> CDR3
<220>
<221> misc_feature
<222> (267)..(302)
<223> FR4
<400> 154
cttccatgta tgcatctcta ggagagagag tcactatcac ttgcaaggcg agtcaggaca 60
ttaatagcta tttaagctgg ttccagcaga aaccagggaa atctcctaag accctgatct 120
atcgtgcaaa cagattggta gatggggtcc catcaaggtt cagtggcagt ggatctgggc 180
aagattattc tctcaccatc agcagcctgg aatatgaaga tatgggaatt tattattgtc 240
tacattatgc tgagtttccg tacacgttcg gaggggggac caagctggaa ataaaacggg 300
ctg 303
<210> 155
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 12A10: CDR1
<400> 155
aaggcgagtc aggacattaa tagctattta agc 33
<210> 156
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 12A10: CDR2
<400> 156
cgtgcaaaca gattggtaga t 21
<210> 157
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 12A10: CDR3
<400> 157
ctacattatg ctgagtttcc gtacacg 27
<210> 158
<211> 100
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 12A10
<220>
<221> MISC_FEATURE
<222> (1)..(14)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (15)..(25)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (26)..(40)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (41)..(47)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (48)..(79)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (80)..(88)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (89)..(100)
<223> FR4
<400> 158
Ser Met Tyr Ala Ser Leu Gly Glu Arg Val Thr Ile Thr Cys Lys Ala
1 5 10 15
Ser Gln Asp Ile Asn Ser Tyr Leu Ser Trp Phe Gln Gln Lys Pro Gly
20 25 30
Lys Ser Pro Lys Thr Leu Ile Tyr Arg Ala Asn Arg Leu Val Asp Gly
35 40 45
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Gln Asp Tyr Ser Leu
50 55 60
Thr Ile Ser Ser Leu Glu Tyr Glu Asp Met Gly Ile Tyr Tyr Cys Leu
65 70 75 80
His Tyr Ala Glu Phe Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu
85 90 95
Ile Lys Arg Ala
100
<210> 159
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 12A10: FR1
<400> 159
Ser Met Tyr Ala Ser Leu Gly Glu Arg Val Thr Ile Thr Cys
1 5 10
<210> 160
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 12A10: CDR1
<400> 160
Lys Ala Ser Gln Asp Ile Asn Ser Tyr Leu Ser
1 5 10
<210> 161
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 12A10: FR2
<400> 161
Trp Phe Gln Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile Tyr
1 5 10 15
<210> 162
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 12A10: CDR2
<400> 162
Arg Ala Asn Arg Leu Val Asp
1 5
<210> 163
<211> 32
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 12A10: FR3
<400> 163
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Gln Asp Tyr Ser
1 5 10 15
Leu Thr Ile Ser Ser Leu Glu Tyr Glu Asp Met Gly Ile Tyr Tyr Cys
20 25 30
<210> 164
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 12A10: CDR3
<400> 164
Leu His Tyr Ala Glu Phe Pro Tyr Thr
1 5
<210> 165
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 12A10: FR4
<400> 165
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Ala
1 5 10
<210> 166
<211> 434
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 3B7
<220>
<221> misc_feature
<222> (12)..(68)
<223> Лидерная последовательность
<220>
<221> misc_feature
<222> (69)..(143)
<223> FR1
<220>
<221> misc_feature
<222> (144)..(173)
<223> CDR1
<220>
<221> misc_feature
<222> (174)..(215)
<223> FR2
<220>
<221> misc_feature
<222> (216)..(266)
<223> CDR2
<220>
<221> misc_feature
<222> (267)..(356)
<223> FR3
<220>
<221> misc_feature
<222> (357)..(401)
<223> CDR3
<220>
<221> misc_feature
<222> (402)..(431)
<223> FR4
<400> 166
tactagtcga catgggatgg agctgtatca tgttctttct ggtagcaaca gctacaggtg 60
tgcactccca ggtccagctg cagcagtctg ggcctgaggt ggtgaggcct ggggtctcag 120
tgaagatttc ctgcaagggt tccggctaca cattcagtga ttatactatg cactgggtga 180
agcagagtca tgcaaagagt ctagagtgga ttggagttat tagtactgac aatggtaata 240
caaactataa ccagaagttt aagggcaagg ccacaatgac tgtagacaaa tcctccagca 300
ctgcctatat ggaacttgcc agattgacat ctgaggattc tgccatctat tactgtgcaa 360
gggaggcccg ggactacggt agtatctatg ctttggacta ctggggtcaa ggaacctcag 420
tcaccgtctc tcag 434
<210> 167
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 3B7: CDR1
<400> 167
ggctacacat tcagtgatta tactatgcac 30
<210> 168
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 3B7: CDR2
<400> 168
gttattagta ctgacaatgg taatacaaac tataaccaga agtttaaggg c 51
<210> 169
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 3B7: CDR3
<400> 169
gcaagggagg cccgggacta cggtagtatc tatgctttgg actac 45
<210> 170
<211> 140
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 3B7
<220>
<221> MISC_FEATURE
<222> (1)..(19)
<223> Лидерная последовательность
<220>
<221> MISC_FEATURE
<222> (20)..(44)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (45)..(54)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (55)..(68)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (69)..(85)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (86)..(115)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (116)..(130)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (131)..(140)
<223> FR4
<400> 170
Met Gly Trp Ser Cys Ile Met Phe Phe Leu Val Ala Thr Ala Thr Gly
1 5 10 15
Val His Ser Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Val Val Arg
20 25 30
Pro Gly Val Ser Val Lys Ile Ser Cys Lys Gly Ser Gly Tyr Thr Phe
35 40 45
Ser Asp Tyr Thr Met His Trp Val Lys Gln Ser His Ala Lys Ser Leu
50 55 60
Glu Trp Ile Gly Val Ile Ser Thr Asp Asn Gly Asn Thr Asn Tyr Asn
65 70 75 80
Gln Lys Phe Lys Gly Lys Ala Thr Met Thr Val Asp Lys Ser Ser Ser
85 90 95
Thr Ala Tyr Met Glu Leu Ala Arg Leu Thr Ser Glu Asp Ser Ala Ile
100 105 110
Tyr Tyr Cys Ala Arg Glu Ala Arg Asp Tyr Gly Ser Ile Tyr Ala Leu
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Ser Val Thr Val Ser
130 135 140
<210> 171
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 3B7: FR1
<400> 171
Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Val Val Arg Pro Gly Val
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Gly Ser
20 25
<210> 172
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 3B7: CDR1
<400> 172
Gly Tyr Thr Phe Ser Asp Tyr Thr Met His
1 5 10
<210> 173
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 3B7: FR2
<400> 173
Trp Val Lys Gln Ser His Ala Lys Ser Leu Glu Trp Ile Gly
1 5 10
<210> 174
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 3B7: CDR2
<400> 174
Val Ile Ser Thr Asp Asn Gly Asn Thr Asn Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 175
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 3B7: FR3
<400> 175
Lys Ala Thr Met Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr Met Glu
1 5 10 15
Leu Ala Arg Leu Thr Ser Glu Asp Ser Ala Ile Tyr Tyr Cys
20 25 30
<210> 176
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 3B7: CDR3
<400> 176
Ala Arg Glu Ala Arg Asp Tyr Gly Ser Ile Tyr Ala Leu Asp Tyr
1 5 10 15
<210> 177
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 3B7: FR4
<400> 177
Trp Gly Gln Gly Thr Ser Val Thr Val Ser
1 5 10
<210> 178
<211> 395
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 3B7
<220>
<221> misc_feature
<222> (15)..(59)
<223> Лидерная последовательность
<220>
<221> misc_feature
<222> (60)..(128)
<223> FR1
<220>
<221> misc_feature
<222> (129)..(155)
<223> CDR1
<220>
<221> misc_feature
<222> (156)..(206)
<223> FR2
<220>
<221> misc_feature
<222> (207)..(227)
<223> CDR2
<220>
<221> misc_feature
<222> (228)..(323)
<223> FR3
<220>
<221> misc_feature
<222> (324)..(350)
<223> CDR3
<220>
<221> misc_feature
<222> (351)..(395)
<223> FR4
<400> 178
tattactagt cgacatggtt cttatgttgc tgctgctatg gcttacaggt gccagatgtg 60
acatccagat gactcagtct ccagcctccc tatctgcatc tgtgggagaa actgtcacca 120
tcacatgtcg agcaagtggg aatattcaca attatttagc atggtatcag cagaaacagg 180
gaaaatctcc tcagctcctg gtctataatg caaaaacctt agcagatggt gtgccatcaa 240
ggttcagtgg cagtggatca ggaacacaat attctctcaa gatcaacaac ctgcagcctg 300
aggattttgg gaattattac tgtcaacatt tttggagtac tccgtggacg ttcggtggag 360
gcaccaagct ggaaatcaaa cgggctgatg ctgca 395
<210> 179
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 3B7: CDR1
<400> 179
cgagcaagtg ggaatattca caattat 27
<210> 180
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 3B7: CDR2
<400> 180
aatgcaaaaa ccttagcaga t 21
<210> 181
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 3B7: CDR3
<400> 181
caacattttt ggagtactcc gtggacg 27
<210> 182
<211> 127
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 3B7
<220>
<221> MISC_FEATURE
<222> (1)..(15)
<223> Лидерная последовательность
<220>
<221> MISC_FEATURE
<222> (16)..(38)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (39)..(47)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (48)..(64)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (65)..(71)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (72)..(103)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (104)..(112)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (113)..(127)
<223> FR4
<400> 182
Met Val Leu Met Leu Leu Leu Leu Trp Leu Thr Gly Ala Arg Cys Asp
1 5 10 15
Ile Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Val Gly Glu
20 25 30
Thr Val Thr Ile Thr Cys Arg Ala Ser Gly Asn Ile His Asn Tyr Leu
35 40 45
Ala Trp Tyr Gln Gln Lys Gln Gly Lys Ser Pro Gln Leu Leu Val Tyr
50 55 60
Asn Ala Lys Thr Leu Ala Asp Gly Val Pro Ser Arg Phe Ser Gly Ser
65 70 75 80
Gly Ser Gly Thr Gln Tyr Ser Leu Lys Ile Asn Asn Leu Gln Pro Glu
85 90 95
Asp Phe Gly Asn Tyr Tyr Cys Gln His Phe Trp Ser Thr Pro Trp Thr
100 105 110
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Ala Asp Ala Ala
115 120 125
<210> 183
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 3B7: FR1
<400> 183
Asp Ile Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Glu Thr Val Thr Ile Thr Cys
20
<210> 184
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 3B7: CDR1
<400> 184
Arg Ala Ser Gly Asn Ile His Asn Tyr
1 5
<210> 185
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 3B7: FR2
<400> 185
Leu Ala Trp Tyr Gln Gln Lys Gln Gly Lys Ser Pro Gln Leu Leu Val
1 5 10 15
Tyr
<210> 186
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 3B7: CDR2
<400> 186
Asn Ala Lys Thr Leu Ala Asp
1 5
<210> 187
<211> 32
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 3B7: FR3
<400> 187
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Gln Tyr Ser
1 5 10 15
Leu Lys Ile Asn Asn Leu Gln Pro Glu Asp Phe Gly Asn Tyr Tyr Cys
20 25 30
<210> 188
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 3B7: CDR3
<400> 188
Gln His Phe Trp Ser Thr Pro Trp Thr
1 5
<210> 189
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 3B7: FR4
<400> 189
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Ala Asp Ala Ala
1 5 10 15
<210> 190
<211> 425
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 11G8
<220>
<221> misc_feature
<222> (11)..(67)
<223> Лидерная последовательность
<220>
<221> misc_feature
<222> (68)..(142)
<223> FR1
<220>
<221> misc_feature
<222> (143)..(172)
<223> CDR1
<220>
<221> misc_feature
<222> (173)..(214)
<223> FR2
<220>
<221> misc_feature
<222> (215)..(259)
<223> CDR2
<220>
<221> misc_feature
<222> (260)..(355)
<223> FR3
<220>
<221> misc_feature
<222> (356)..(391)
<223> CDR3
<220>
<221> misc_feature
<222> (392)..(424)
<223> FR4
<400> 190
tactagtcga atgggatgga gctgtatcat gttctttctg gtagctacag ctacaggtgt 60
gcactcccag gtccagctgc agcagtctgg gcctgacctg gtgaggcctg gggtctcagt 120
gaagatttcc tgcaagggtt ccggctacac attcactgat tatgctatgc actgggtaaa 180
gcagagtcat gcaaagagtc tagagtggat tggagttatt agtactgact ctggtactac 240
aaactacaac cagaagttta agggcaaggc cacaatgact gtagacaaat cctccagtac 300
agcctatatg gaccttgcca gattgacatc tgaggattct gccatctatt actgtgcaag 360
agacagctcg tactacgtgc gattttctta ctggggccaa ggaactctgg tcactgtctc 420
tgcag 425
<210> 191
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 11G8: CDR1
<400> 191
ggctacacat tcactgatta tgctatgcac 30
<210> 192
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 11G8: CDR2
<400> 192
gttattagta ctgactctgg tactacaaac tacaaccaga agttt 45
<210> 193
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 11G8: CDR3
<400> 193
gcaagagaca gctcgtacta cgtgcgattt tcttac 36
<210> 194
<211> 138
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 11G8
<220>
<221> MISC_FEATURE
<222> (1)..(19)
<223> Лидерная последовательность
<220>
<221> MISC_FEATURE
<222> (20)..(44)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (45)..(54)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (55)..(68)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (69)..(83)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (84)..(115)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (116)..(127)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (128)..(138)
<223> FR4
<400> 194
Met Gly Trp Ser Cys Ile Met Phe Phe Leu Val Ala Thr Ala Thr Gly
1 5 10 15
Val His Ser Gln Val Gln Leu Gln Gln Ser Gly Pro Asp Leu Val Arg
20 25 30
Pro Gly Val Ser Val Lys Ile Ser Cys Lys Gly Ser Gly Tyr Thr Phe
35 40 45
Thr Asp Tyr Ala Met His Trp Val Lys Gln Ser His Ala Lys Ser Leu
50 55 60
Glu Trp Ile Gly Val Ile Ser Thr Asp Ser Gly Thr Thr Asn Tyr Asn
65 70 75 80
Gln Lys Phe Lys Gly Lys Ala Thr Met Thr Val Asp Lys Ser Ser Ser
85 90 95
Thr Ala Tyr Met Asp Leu Ala Arg Leu Thr Ser Glu Asp Ser Ala Ile
100 105 110
Tyr Tyr Cys Ala Arg Asp Ser Ser Tyr Tyr Val Arg Phe Ser Tyr Trp
115 120 125
Gly Gln Gly Thr Leu Val Thr Val Ser Ala
130 135
<210> 195
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 11G8: FR1
<400> 195
Gln Val Gln Leu Gln Gln Ser Gly Pro Asp Leu Val Arg Pro Gly Val
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Gly Ser
20 25
<210> 196
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 11G8: CDR1
<400> 196
Gly Tyr Thr Phe Thr Asp Tyr Ala Met His
1 5 10
<210> 197
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 11G8: FR2
<400> 197
Trp Val Lys Gln Ser His Ala Lys Ser Leu Glu Trp Ile Gly
1 5 10
<210> 198
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 11G8: CDR2
<400> 198
Val Ile Ser Thr Asp Ser Gly Thr Thr Asn Tyr Asn Gln Lys Phe
1 5 10 15
<210> 199
<211> 32
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 11G8: FR3
<400> 199
Lys Gly Lys Ala Thr Met Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
1 5 10 15
Met Asp Leu Ala Arg Leu Thr Ser Glu Asp Ser Ala Ile Tyr Tyr Cys
20 25 30
<210> 200
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 11G8: CDR3
<400> 200
Ala Arg Asp Ser Ser Tyr Tyr Val Arg Phe Ser Tyr
1 5 10
<210> 201
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 11G8: FR4
<400> 201
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala
1 5 10
<210> 202
<211> 420
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 11G8
<220>
<221> misc_feature
<222> (25)..(84)
<223> Лидерная последовательность
<220>
<221> misc_feature
<222> (85)..(153)
<223> FR1
<220>
<221> misc_feature
<222> (154)..(180)
<223> CDR1
<220>
<221> misc_feature
<222> (181)..(231)
<223> FR2
<220>
<221> misc_feature
<222> (232)..(252)
<223> CDR2
<220>
<221> misc_feature
<222> (253)..(360)
<223> FR3
<220>
<221> misc_feature
<222> (361)..(375)
<223> CDR3
<220>
<221> misc_feature
<222> (376)..(420)
<223> FR4
<400> 202
tactagttgt atattggctt caagatggag tcacagaccc aggtcttcgt atttctactg 60
ctctgtgtgt ctggtgctca tgggagtatt gtgatgaccc agactcccaa attcctgctt 120
gtttcagtag gagacagggt taccataacc tgtaaggcca gtcagagtgt gagtaatgat 180
gtagcttggt accaacagaa gccagggcag tctcctaaac tgctaatata ctatgcatcc 240
aatcgctaca ctggagtccc tgatcgcttc actggcagtg gatatgggac ggatttcact 300
ttcaccatca gcactgtgca ggctgaagac ctggcagttt atttctgtca gcaggattat 360
agttctccgt ggacgttcgg tggaggcacc aagctggaaa tcaaacgggc tgatgctgca 420
<210> 203
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 11G8: CDR1
<400> 203
aaggccagtc agagtgtgag taatgat 27
<210> 204
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 11G8: CDR2
<400> 204
tatgcatcca atcgctacac t 21
<210> 205
<211> 15
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 11G8: CDR3
<400> 205
agttctccgt ggacg 15
<210> 206
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 11G8
<220>
<221> MISC_FEATURE
<222> (1)..(20)
<223> Лидерная последовательность
<220>
<221> MISC_FEATURE
<222> (21)..(43)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (44)..(52)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (53)..(69)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (70)..(76)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (77)..(108)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (109)..(117)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (118)..(132)
<223> FR4
<400> 206
Met Glu Ser Gln Thr Gln Val Phe Val Phe Leu Leu Leu Cys Val Ser
1 5 10 15
Gly Ala His Gly Ser Ile Val Met Thr Gln Thr Pro Lys Phe Leu Leu
20 25 30
Val Ser Val Gly Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser
35 40 45
Val Ser Asn Asp Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro
50 55 60
Lys Leu Leu Ile Tyr Tyr Ala Ser Asn Arg Tyr Thr Gly Val Pro Asp
65 70 75 80
Arg Phe Thr Gly Ser Gly Tyr Gly Thr Asp Phe Thr Phe Thr Ile Ser
85 90 95
Thr Val Gln Ala Glu Asp Leu Ala Val Tyr Phe Cys Gln Gln Asp Tyr
100 105 110
Ser Ser Pro Trp Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
115 120 125
Ala Asp Ala Ala
130
<210> 207
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 11G8: FR1
<400> 207
Ser Ile Val Met Thr Gln Thr Pro Lys Phe Leu Leu Val Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys
20
<210> 208
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 11G8: CDR1
<400> 208
Lys Ala Ser Gln Ser Val Ser Asn Asp
1 5
<210> 209
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 11G8: FR2
<400> 209
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile
1 5 10 15
Tyr
<210> 210
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 11G8: CDR2
<400> 210
Tyr Ala Ser Asn Arg Tyr Thr
1 5
<210> 211
<211> 32
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 11G8: FR3
<400> 211
Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Tyr Gly Thr Asp Phe Thr
1 5 10 15
Phe Thr Ile Ser Thr Val Gln Ala Glu Asp Leu Ala Val Tyr Phe Cys
20 25 30
<210> 212
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 11G8: CDR3
<400> 212
Gln Gln Asp Tyr Ser Ser Pro Trp Thr
1 5
<210> 213
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 11G8: FR4
<400> 213
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Ala Asp Ala Ala
1 5 10 15
<210> 214
<211> 434
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 14F8
<220>
<221> misc_feature
<222> (12)..(68)
<223> Лидерная последовательность
<220>
<221> misc_feature
<222> (69)..(143)
<223> FR1
<220>
<221> misc_feature
<222> (144)..(173)
<223> CDR1
<220>
<221> misc_feature
<222> (174)..(215)
<223> FR2
<220>
<221> misc_feature
<222> (216)..(266)
<223> CDR2
<220>
<221> misc_feature
<222> (267)..(356)
<223> FR3
<220>
<221> misc_feature
<222> (357)..(401)
<223> CDR3
<220>
<221> misc_feature
<222> (402)..(431)
<223> FR4
<400> 214
tacttgtcga catgggatgg agctgtatca tgttctttct ggtagcaaca gctacaggtg 60
tgcactccca ggtccagctg cagcagtctg ggcctgaggt ggtgaggcct ggggtctcag 120
tgaagatttc ctgcaagggt tccggctaca cattcactga ttatactatg cactgggtga 180
agcagagtca tgcaaagagt ctagagtgga ttggagttat tagtacttac aatggtaata 240
caaactacaa ccagaacttt gagggcaagg ccacaatgac tgtagacaaa tcctccagca 300
cagcctatat ggaacttgcc agattgacat ctgaggattc tgccatctat tactgtgcaa 360
gagagagggg gggggatggt tactacagtg ctgtggacta ctggggtcaa ggaacctcag 420
tcaccgtctc tcag 434
<210> 215
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 14F8: CDR1
<400> 215
ggctacacat tcactgatta tactatgcac 30
<210> 216
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 14F8: CDR2
<400> 216
gttattagta cttacaatgg taatacaaac tacaaccaga actttgaggg c 51
<210> 217
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 14F8: CDR3
<400> 217
gcaagagaga ggggggggga tggttactac agtgctgtgg actac 45
<210> 218
<211> 140
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 14F8
<220>
<221> MISC_FEATURE
<222> (1)..(19)
<223> Лидерная последовательность
<220>
<221> MISC_FEATURE
<222> (20)..(44)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (45)..(54)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (55)..(68)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (69)..(85)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (86)..(115)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (116)..(130)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (131)..(140)
<223> FR4
<400> 218
Met Gly Trp Ser Cys Ile Met Phe Phe Leu Val Ala Thr Ala Thr Gly
1 5 10 15
Val His Ser Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Val Val Arg
20 25 30
Pro Gly Val Ser Val Lys Ile Ser Cys Lys Gly Ser Gly Tyr Thr Phe
35 40 45
Thr Asp Tyr Thr Met His Trp Val Lys Gln Ser His Ala Lys Ser Leu
50 55 60
Glu Trp Ile Gly Val Ile Ser Thr Tyr Asn Gly Asn Thr Asn Tyr Asn
65 70 75 80
Gln Asn Phe Glu Gly Lys Ala Thr Met Thr Val Asp Lys Ser Ser Ser
85 90 95
Thr Ala Tyr Met Glu Leu Ala Arg Leu Thr Ser Glu Asp Ser Ala Ile
100 105 110
Tyr Tyr Cys Ala Arg Glu Arg Gly Gly Asp Gly Tyr Tyr Ser Ala Val
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Ser Val Thr Val Ser
130 135 140
<210> 219
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 14F8: FR1
<400> 219
Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Val Val Arg Pro Gly Val
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Gly Ser
20 25
<210> 220
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 14F8: CDR1
<400> 220
Gly Tyr Thr Phe Thr Asp Tyr Thr Met His
1 5 10
<210> 221
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 14F8: FR2
<400> 221
Trp Val Lys Gln Ser His Ala Lys Ser Leu Glu Trp Ile Gly
1 5 10
<210> 222
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 14F8: CDR2
<400> 222
Val Ile Ser Thr Tyr Asn Gly Asn Thr Asn Tyr Asn Gln Asn Phe Glu
1 5 10 15
Gly
<210> 223
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 14F8: FR3
<400> 223
Lys Ala Thr Met Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr Met Glu
1 5 10 15
Leu Ala Arg Leu Thr Ser Glu Asp Ser Ala Ile Tyr Tyr Cys
20 25 30
<210> 224
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 14F8: CDR3
<400> 224
Ala Arg Glu Arg Gly Gly Asp Gly Tyr Tyr Ser Ala Val Asp Tyr
1 5 10 15
<210> 225
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 14F8: FR4
<400> 225
Trp Gly Gln Gly Thr Ser Val Thr Val Ser
1 5 10
<210> 226
<211> 313
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 14F8
<220>
<221> misc_feature
<222> (3)..(47)
<223> FR1
<220>
<221> misc_feature
<222> (48)..(74)
<223> CDR1
<220>
<221> misc_feature
<222> (75)..(125)
<223> FR2
<220>
<221> misc_feature
<222> (126)..(146)
<223> CDR2
<220>
<221> misc_feature
<222> (147)..(242)
<223> FR3
<220>
<221> misc_feature
<222> (243)..(269)
<223> CDR3
<220>
<221> misc_feature
<222> (270)..(311)
<223> FR4
<400> 226
ccaaattcct gcttgtatca gcaggagaca gggttaccat aacctgcaag gccagtcaga 60
gtgtgattaa tgatgtagct tggtaccaac agaagccagg gcagtctcct aaactgctga 120
tatactatgc atccaatcgc tacactggag tccctgatcg cttcactggc agtggatatg 180
ggacggattt cactttcacc atcagcactg tgcaggctga agacctggca gtttatttct 240
gtcagcagga ttatagctct ccgtacacgt tcggaggggg gaccaagctg gaaataaaac 300
gggctgatgc tgc 313
<210> 227
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 14F8: CDR1
<400> 227
aaggccagtc agagtgtgat taatgat 27
<210> 228
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 14F8: CDR2
<400> 228
tatgcatcca atcgctacac t 21
<210> 229
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 14F8: CDR3
<400> 229
cagcaggatt atagctctcc gtacacg 27
<210> 230
<211> 103
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 14F8
<220>
<221> MISC_FEATURE
<222> (1)..(15)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (16)..(24)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (25)..(41)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (42)..(48)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (49)..(80)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (81)..(89)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (90)..(103)
<223> FR4
<400> 230
Lys Phe Leu Leu Val Ser Ala Gly Asp Arg Val Thr Ile Thr Cys Lys
1 5 10 15
Ala Ser Gln Ser Val Ile Asn Asp Val Ala Trp Tyr Gln Gln Lys Pro
20 25 30
Gly Gln Ser Pro Lys Leu Leu Ile Tyr Tyr Ala Ser Asn Arg Tyr Thr
35 40 45
Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Tyr Gly Thr Asp Phe Thr
50 55 60
Phe Thr Ile Ser Thr Val Gln Ala Glu Asp Leu Ala Val Tyr Phe Cys
65 70 75 80
Gln Gln Asp Tyr Ser Ser Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu
85 90 95
Glu Ile Lys Arg Ala Asp Ala
100
<210> 231
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 14F8: FR1
<400> 231
Lys Phe Leu Leu Val Ser Ala Gly Asp Arg Val Thr Ile Thr Cys
1 5 10 15
<210> 232
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 14F8: CDR1
<400> 232
Lys Ala Ser Gln Ser Val Ile Asn Asp
1 5
<210> 233
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 14F8: FR2
<400> 233
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile
1 5 10 15
Tyr
<210> 234
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 14F8: CDR2
<400> 234
Tyr Ala Ser Asn Arg Tyr Thr
1 5
<210> 235
<211> 32
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 14F8: FR3
<400> 235
Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Tyr Gly Thr Asp Phe Thr
1 5 10 15
Phe Thr Ile Ser Thr Val Gln Ala Glu Asp Leu Ala Val Tyr Phe Cys
20 25 30
<210> 236
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 14F8: CDR3
<400> 236
Gln Gln Asp Tyr Ser Ser Pro Tyr Thr
1 5
<210> 237
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 14F8: FR4
<400> 237
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Ala Asp Ala
1 5 10
<210> 238
<211> 421
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 15D2
<220>
<221> misc_feature
<222> (11)..(67)
<223> Лидерная последовательность
<220>
<221> misc_feature
<222> (68)..(142)
<223> FR1
<220>
<221> misc_feature
<222> (143)..(172)
<223> CDR1
<220>
<221> misc_feature
<222> (173)..(214)
<223> FR2
<220>
<221> misc_feature
<222> (215)..(265)
<223> CDR2
<220>
<221> misc_feature
<222> (266)..(355)
<223> FR3
<220>
<221> misc_feature
<222> (356)..(388)
<223> CDR3
<220>
<221> misc_feature
<222> (389)..(418)
<223> FR4
<400> 238
tggggaattc atggagttgg ggttcagctt gattttcctt gtccttgttt taaaaggtgt 60
ccagtgtgaa gtgatgctgg tggagtctgg gggaggctta gtgaagcctg gagggtccct 120
gaaactctcc tgtgcagcct ctggattcac tttcagtaac tatgccatgt cttgggttcg 180
ccagactccg gagaagaggc tggagtgggt cgcaacctct cttagtggtg gtaattacac 240
ctactatcca gacagtgtga aggggcgatt caccatctcc agagacaatg ccaagagcac 300
cctgtacctg caaatgagca gtctgaggtc tgaggacacg gccatgtatt actgtgtaat 360
cccccaaggt agtagtcctt ttgactattg gggccaaggc accactctca cagtctctca 420
g 421
<210> 239
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 15D2: CDR1
<400> 239
ggattcactt tcagtaacta tgccatgtct 30
<210> 240
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 15D2: CDR2
<400> 240
acctctctta gtggtggtaa ttacacctac tatccagaca gtgtgaaggg g 51
<210> 241
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 15D2: CDR3
<400> 241
gtaatccccc aaggtagtag tccttttgac tat 33
<210> 242
<211> 136
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 15D2
<220>
<221> MISC_FEATURE
<222> (1)..(19)
<223> Лидерная последовательность
<220>
<221> MISC_FEATURE
<222> (20)..(44)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (45)..(54)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (55)..(68)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (69)..(85)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (86)..(115)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (116)..(126)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (127)..(136)
<223> FR4
<400> 242
Met Glu Leu Gly Phe Ser Leu Ile Phe Leu Val Leu Val Leu Lys Gly
1 5 10 15
Val Gln Cys Glu Val Met Leu Val Glu Ser Gly Gly Gly Leu Val Lys
20 25 30
Pro Gly Gly Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe
35 40 45
Ser Asn Tyr Ala Met Ser Trp Val Arg Gln Thr Pro Glu Lys Arg Leu
50 55 60
Glu Trp Val Ala Thr Ser Leu Ser Gly Gly Asn Tyr Thr Tyr Tyr Pro
65 70 75 80
Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Ser
85 90 95
Thr Leu Tyr Leu Gln Met Ser Ser Leu Arg Ser Glu Asp Thr Ala Met
100 105 110
Tyr Tyr Cys Val Ile Pro Gln Gly Ser Ser Pro Phe Asp Tyr Trp Gly
115 120 125
Gln Gly Thr Thr Leu Thr Val Ser
130 135
<210> 243
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 15D2: FR1
<400> 243
Glu Val Met Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser
20 25
<210> 244
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 15D2: CDR1
<400> 244
Gly Phe Thr Phe Ser Asn Tyr Ala Met Ser
1 5 10
<210> 245
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 15D2: FR2
<400> 245
Trp Val Arg Gln Thr Pro Glu Lys Arg Leu Glu Trp Val Ala
1 5 10
<210> 246
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 15D2: CDR2
<400> 246
Thr Ser Leu Ser Gly Gly Asn Tyr Thr Tyr Tyr Pro Asp Ser Val Lys
1 5 10 15
Gly
<210> 247
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 15D2: FR3
<400> 247
Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Ser Thr Leu Tyr Leu Gln
1 5 10 15
Met Ser Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys
20 25 30
<210> 248
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 15D2: CDR3
<400> 248
Val Ile Pro Gln Gly Ser Ser Pro Phe Asp Tyr
1 5 10
<210> 249
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 15D2: FR4
<400> 249
Trp Gly Gln Gly Thr Thr Leu Thr Val Ser
1 5 10
<210> 250
<211> 417
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 15D2
<220>
<221> misc_feature
<222> (12)..(83)
<223> Лидерная последовательность
<220>
<221> misc_feature
<222> (84)..(152)
<223> FR1
<220>
<221> misc_feature
<222> (153)..(185)
<223> CDR1
<220>
<221> misc_feature
<222> (186)..(230)
<223> FR2
<220>
<221> misc_feature
<222> (231)..(251)
<223> CDR2
<220>
<221> misc_feature
<222> (252)..(347)
<223> FR3
<220>
<221> misc_feature
<222> (348)..(374)
<223> CDR3
<220>
<221> misc_feature
<222> (375)..(404)
<223> FR4
<400> 250
tactagtcga catgggcttc aagatggagt cacagattca ggttttggta tttttactgc 60
tctgtgtgtg tggtggtcat gggagtattg tgatgaccca gactcccaaa ttccctattg 120
tttcagtagg agacagggtt accataacct gtaaggccag tcagagtgtg aaaaatgatg 180
tagcatggta ccaacagaag ccagggcagt ctggtaaaat gttaatatat tatgcatgca 240
atcgctacac gggagtcctt gatcgcttca ctgtcagtgg atatgtgacg gatttcactt 300
tcaccatcac cactgtgcag gctgaagacc tggcagttta cttttgtcag caggatcata 360
gttatccgtg gacgttcggt gctgggacca agctggagct gaaacgggct gatgctg 417
<210> 251
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 15D2: CDR1
<400> 251
aaggccagtc agagtgtgaa aaatgatgta gca 33
<210> 252
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 15D2: CDR2
<400> 252
tatgcatgca atcgctacac g 21
<210> 253
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 15D2: CDR3
<400> 253
cagcaggatc atagttatcc gtggacg 27
<210> 254
<211> 131
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 15D2
<220>
<221> MISC_FEATURE
<222> (1)..(24)
<223> Лидерная последовательность
<220>
<221> MISC_FEATURE
<222> (25)..(47)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (48)..(58)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (59)..(73)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (74)..(80)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (81)..(112)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (113)..(121)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (122)..(131)
<223> FR4
<400> 254
Met Gly Phe Lys Met Glu Ser Gln Ile Gln Val Leu Val Phe Leu Leu
1 5 10 15
Leu Cys Val Cys Gly Gly His Gly Ser Ile Val Met Thr Gln Thr Pro
20 25 30
Lys Phe Pro Ile Val Ser Val Gly Asp Arg Val Thr Ile Thr Cys Lys
35 40 45
Ala Ser Gln Ser Val Lys Asn Asp Val Ala Trp Tyr Gln Gln Lys Pro
50 55 60
Gly Gln Ser Gly Lys Met Leu Ile Tyr Tyr Ala Cys Asn Arg Tyr Thr
65 70 75 80
Gly Val Leu Asp Arg Phe Thr Val Ser Gly Tyr Val Thr Asp Phe Thr
85 90 95
Phe Thr Ile Thr Thr Val Gln Ala Glu Asp Leu Ala Val Tyr Phe Cys
100 105 110
Gln Gln Asp His Ser Tyr Pro Trp Thr Phe Gly Ala Gly Thr Lys Leu
115 120 125
Glu Leu Lys
130
<210> 255
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 15D2: FR1
<400> 255
Ser Ile Val Met Thr Gln Thr Pro Lys Phe Pro Ile Val Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys
20
<210> 256
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 15D2: CDR1
<400> 256
Lys Ala Ser Gln Ser Val Lys Asn Asp Val Ala
1 5 10
<210> 257
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 15D2: FR2
<400> 257
Trp Tyr Gln Gln Lys Pro Gly Gln Ser Gly Lys Met Leu Ile Tyr
1 5 10 15
<210> 258
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 15D2: CDR2
<400> 258
Tyr Ala Cys Asn Arg Tyr Thr
1 5
<210> 259
<211> 32
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 15D2: FR3
<400> 259
Gly Val Leu Asp Arg Phe Thr Val Ser Gly Tyr Val Thr Asp Phe Thr
1 5 10 15
Phe Thr Ile Thr Thr Val Gln Ala Glu Asp Leu Ala Val Tyr Phe Cys
20 25 30
<210> 260
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 15D2: CDR3
<400> 260
Gln Gln Asp His Ser Tyr Pro Trp Thr
1 5
<210> 261
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 15D2: FR4
<400> 261
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
1 5 10
<210> 262
<211> 438
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 29H7
<220>
<221> misc_feature
<222> (15)..(71)
<223> Лидерная последовательность
<220>
<221> misc_feature
<222> (72)..(146)
<223> FR1
<220>
<221> misc_feature
<222> (147)..(176)
<223> CDR1
<220>
<221> misc_feature
<222> (177)..(218)
<223> FR2
<220>
<221> misc_feature
<222> (219)..(269)
<223> CDR2
<220>
<221> misc_feature
<222> (270)..(359)
<223> FR3
<220>
<221> misc_feature
<222> (360)..(404)
<223> CDR3
<220>
<221> misc_feature
<222> (405)..(437)
<223> FR4
<400> 262
tattactagt cgccatggga tggagctgta tcatgttctt tctggtagca acagctacag 60
gtgtgcactc ccaggtccag ctgcagcagt ctgggcctga ggtggtgagg cctggggtct 120
cagtgaagat ttcctgcaag ggttccggct acacattcac tgattatgtt atgcactggg 180
tgaagcagag tcatggaaag agtctagagt ggattggagt tattagtact tacaatggta 240
atacaaacta caaccagaag tttaagggca aggccacaat gactgtagac aaatcctcca 300
gcacagccta tatggaactt gccagattga catctgagga ttctgccatc tattactgtg 360
caagagagag ggggggggat ggttactaca gtgctatgga ctactggggt caaggaacct 420
cagtcaccgt ctcctcag 438
<210> 263
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 29H7: CDR1
<400> 263
ggctacacat tcactgatta tgttatgcac 30
<210> 264
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 29H7: CDR2
<400> 264
gttattagta cttacaatgg taatacaaac tacaaccaga agtttaaggg c 51
<210> 265
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 29H7: CDR3
<400> 265
gcaagagaga ggggggggga tggttactac agtgctatgg actac 45
<210> 266
<211> 141
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 29H7
<220>
<221> MISC_FEATURE
<222> (1)..(19)
<223> Лидерная последовательность
<220>
<221> MISC_FEATURE
<222> (20)..(44)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (45)..(54)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (55)..(68)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (69)..(85)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (86)..(115)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (116)..(130)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (131)..(141)
<223> FR4
<400> 266
Met Gly Trp Ser Cys Ile Met Phe Phe Leu Val Ala Thr Ala Thr Gly
1 5 10 15
Val His Ser Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Val Val Arg
20 25 30
Pro Gly Val Ser Val Lys Ile Ser Cys Lys Gly Ser Gly Tyr Thr Phe
35 40 45
Thr Asp Tyr Val Met His Trp Val Lys Gln Ser His Gly Lys Ser Leu
50 55 60
Glu Trp Ile Gly Val Ile Ser Thr Tyr Asn Gly Asn Thr Asn Tyr Asn
65 70 75 80
Gln Lys Phe Lys Gly Lys Ala Thr Met Thr Val Asp Lys Ser Ser Ser
85 90 95
Thr Ala Tyr Met Glu Leu Ala Arg Leu Thr Ser Glu Asp Ser Ala Ile
100 105 110
Tyr Tyr Cys Ala Arg Glu Arg Gly Gly Asp Gly Tyr Tyr Ser Ala Met
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Ser Val Thr Val Ser Ser
130 135 140
<210> 267
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 29H7: FR1
<400> 267
Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Val Val Arg Pro Gly Val
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Gly Ser
20 25
<210> 268
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 29H7: CDR1
<400> 268
Gly Tyr Thr Phe Thr Asp Tyr Val Met His
1 5 10
<210> 269
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 29H7: FR2
<400> 269
Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile Gly
1 5 10
<210> 270
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 29H7: CDR2
<400> 270
Val Ile Ser Thr Tyr Asn Gly Asn Thr Asn Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 271
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 29H7: FR3
<400> 271
Lys Ala Thr Met Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr Met Glu
1 5 10 15
Leu Ala Arg Leu Thr Ser Glu Asp Ser Ala Ile Tyr Tyr Cys
20 25 30
<210> 272
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 29H7: CDR3
<400> 272
Ala Arg Glu Arg Gly Gly Asp Gly Tyr Tyr Ser Ala Met Asp Tyr
1 5 10 15
<210> 273
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 29H7: FR4
<400> 273
Trp Gly Gln Gly Thr Ser Val Thr Val Ser Ser
1 5 10
<210> 274
<211> 389
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 29H7
<220>
<221> misc_feature
<222> (3)..(53)
<223> Лидерная последовательность
<220>
<221> misc_feature
<222> (54)..(122)
<223> FR1
<220>
<221> misc_feature
<222> (123)..(149)
<223> CDR1
<220>
<221> misc_feature
<222> (150)..(200)
<223> FR2
<220>
<221> misc_feature
<222> (201)..(221)
<223> CDR2
<220>
<221> misc_feature
<222> (222)..(317)
<223> FR3
<220>
<221> misc_feature
<222> (318)..(344)
<223> CDR3
<220>
<221> misc_feature
<222> (345)..(389)
<223> FR4
<400> 274
acaggagccg ggtgttggta tttctactgc tctgtgtgtc tggtgctcat gggagtattg 60
tgatgaccca gactcccaaa ttcctgcttg tttcagcagg agacagggtt accatagcct 120
gcaaggccag tcagagtgtg attaataatg tagcttggta ccaacagaag ccagggcagt 180
ctcctgaact gctgatatac tatgcatcca atcgctacac tggagtccct gatcgcttca 240
ctggcagtgg atatgggacg gatttcactt tcaccatcac cactgtgcag gctgaagacc 300
tggcagttta tttctgtcag caggattata gctctccgta cacgttcgga ggggggacca 360
agctggaaat aaaacgggct gatgctgca 389
<210> 275
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 29H7: CDR1
<400> 275
aaggccagtc agagtgtgat taataat 27
<210> 276
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 29H7: CDR2
<400> 276
Thr Ala Thr Gly Cys Ala Thr Cys Cys Ala Ala Thr Cys Gly Cys Thr
1 5 10 15
Ala Cys Ala Cys Thr
20
<210> 277
<211> 27
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 29H7: CDR3
<400> 277
Cys Ala Gly Cys Ala Gly Gly Ala Thr Thr Ala Thr Ala Gly Cys Thr
1 5 10 15
Cys Thr Cys Cys Gly Thr Ala Cys Ala Cys Gly
20 25
<210> 278
<211> 129
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 29H7
<220>
<221> MISC_FEATURE
<222> (1)..(17)
<223> Лидерная последовательность
<220>
<221> MISC_FEATURE
<222> (18)..(40)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (41)..(49)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (50)..(66)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (67)..(73)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (74)..(105)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (106)..(114)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (115)..(129)
<223> FR4
<400> 278
Arg Ser Arg Val Leu Val Phe Leu Leu Leu Cys Val Ser Gly Ala His
1 5 10 15
Gly Ser Ile Val Met Thr Gln Thr Pro Lys Phe Leu Leu Val Ser Ala
20 25 30
Gly Asp Arg Val Thr Ile Ala Cys Lys Ala Ser Gln Ser Val Ile Asn
35 40 45
Asn Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Glu Leu Leu
50 55 60
Ile Tyr Tyr Ala Ser Asn Arg Tyr Thr Gly Val Pro Asp Arg Phe Thr
65 70 75 80
Gly Ser Gly Tyr Gly Thr Asp Phe Thr Phe Thr Ile Thr Thr Val Gln
85 90 95
Ala Glu Asp Leu Ala Val Tyr Phe Cys Gln Gln Asp Tyr Ser Ser Pro
100 105 110
Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Ala Asp Ala
115 120 125
Ala
<210> 279
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 29H7: FR1
<400> 279
Ser Ile Val Met Thr Gln Thr Pro Lys Phe Leu Leu Val Ser Ala Gly
1 5 10 15
Asp Arg Val Thr Ile Ala Cys
20
<210> 280
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 29H7: CDR1
<400> 280
Lys Ala Ser Gln Ser Val Ile Asn Asn
1 5
<210> 281
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 29H7: FR2
<400> 281
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Glu Leu Leu Ile
1 5 10 15
Tyr
<210> 282
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 29H7: CDR2
<400> 282
Tyr Ala Ser Asn Arg Tyr Thr
1 5
<210> 283
<211> 32
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 29H7: FR3
<400> 283
Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Tyr Gly Thr Asp Phe Thr
1 5 10 15
Phe Thr Ile Thr Thr Val Gln Ala Glu Asp Leu Ala Val Tyr Phe Cys
20 25 30
<210> 284
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 29H7: CDR3
<400> 284
Gln Gln Asp Tyr Ser Ser Pro Tyr Thr
1 5
<210> 285
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 29H7: FR4
<400> 285
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Ala Asp Ala Ala
1 5 10 15
<210> 286
<211> 424
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 30D10
<220>
<221> misc_feature
<222> (2)..(67)
<223> Лидерная последовательность
<220>
<221> misc_feature
<222> (68)..(142)
<223> FR1
<220>
<221> misc_feature
<222> (143)..(172)
<223> CDR1
<220>
<221> misc_feature
<222> (173)..(217)
<223> FR2
<220>
<221> misc_feature
<222> (218)..(265)
<223> CDR2
<220>
<221> misc_feature
<222> (266)..(355)
<223> FR3
<220>
<221> misc_feature
<222> (356)..(391)
<223> CDR3
<220>
<221> misc_feature
<222> (392)..(421)
<223> FR4
<400> 286
tggggaattc caggaatgga gctgggtttt tctcttcctg atggcagtgg ttacaggggt 60
caattcagag gttcagctgc agcagtctgg ggctgagctt gtgaggccag gggccttagt 120
caagttgtcc tgcaaagctt ctggcttcaa ctttaaagac tactttatgc actgggtgaa 180
gcagaggcct gaacagggcc tggagtggat tggatggatt gatcctgaaa atggtaatac 240
tatatatgaa ccgaagttcc agggcaaggc cagtataaca gcagacacat cctccaacac 300
agcctacctg cagctcagca gcctgacatc tgaggacact gccgtctatt actgtgctag 360
agggggggta ggtcactggt acttcgatgt ctggggcgca gggaccacgg tcaccgtctc 420
tcag 424
<210> 287
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 30D10: CDR1
<400> 287
ggcttcaact ttaaagacta ctttatgcac 30
<210> 288
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 30D10: CDR2
<400> 288
attgatcctg aaaatggtaa tactatatat gaaccgaagt tccagggc 48
<210> 289
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 30D10: CDR3
<400> 289
gctagagggg gggtaggtca ctggtacttc gatgtc 36
<210> 290
<211> 140
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 30D10
<220>
<221> MISC_FEATURE
<222> (1)..(22)
<223> Лидерная последовательность
<220>
<221> MISC_FEATURE
<222> (23)..(47)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (48)..(57)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (58)..(72)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (73)..(88)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (89)..(118)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (119)..(130)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (131)..(140)
<223> FR4
<400> 290
Gly Glu Phe Gln Glu Trp Ser Trp Val Phe Leu Phe Leu Met Ala Val
1 5 10 15
Val Thr Gly Val Asn Ser Glu Val Gln Leu Gln Gln Ser Gly Ala Glu
20 25 30
Leu Val Arg Pro Gly Ala Leu Val Lys Leu Ser Cys Lys Ala Ser Gly
35 40 45
Phe Asn Phe Lys Asp Tyr Phe Met His Trp Val Lys Gln Arg Pro Glu
50 55 60
Gln Gly Leu Glu Trp Ile Gly Trp Ile Asp Pro Glu Asn Gly Asn Thr
65 70 75 80
Ile Tyr Glu Pro Lys Phe Gln Gly Lys Ala Ser Ile Thr Ala Asp Thr
85 90 95
Ser Ser Asn Thr Ala Tyr Leu Gln Leu Ser Ser Leu Thr Ser Glu Asp
100 105 110
Thr Ala Val Tyr Tyr Cys Ala Arg Gly Gly Val Gly His Trp Tyr Phe
115 120 125
Asp Val Trp Gly Ala Gly Thr Thr Val Thr Val Ser
130 135 140
<210> 291
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 30D10: FR1
<400> 291
Glu Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Ala
1 5 10 15
Leu Val Lys Leu Ser Cys Lys Ala Ser
20 25
<210> 292
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 30D10: CDR1
<400> 292
Gly Phe Asn Phe Lys Asp Tyr Phe Met His
1 5 10
<210> 293
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 30D10: FR2
<400> 293
Trp Val Lys Gln Arg Pro Glu Gln Gly Leu Glu Trp Ile Gly Trp
1 5 10 15
<210> 294
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 30D10: CDR2
<400> 294
Ile Asp Pro Glu Asn Gly Asn Thr Ile Tyr Glu Pro Lys Phe Gln Gly
1 5 10 15
<210> 295
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 30D10: FR3
<400> 295
Lys Ala Ser Ile Thr Ala Asp Thr Ser Ser Asn Thr Ala Tyr Leu Gln
1 5 10 15
Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
20 25 30
<210> 296
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 30D10: CDR3
<400> 296
Ala Arg Gly Gly Val Gly His Trp Tyr Phe Asp Val
1 5 10
<210> 297
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 30D10: FR4
<400> 297
Trp Gly Ala Gly Thr Thr Val Thr Val Ser
1 5 10
<210> 298
<211> 417
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 30D10
<220>
<221> MISC_FEATURE
<222> (10)..(69)
<223> Лидерная последовательность
<220>
<221> MISC_FEATURE
<222> (70)..(138)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (139)..(177)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (178)..(228)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (229)..(249)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (250)..(345)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (346)..(372)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (373)..(402)
<223> FR4
<400> 298
Thr Gly Gly Gly Ala Ala Thr Thr Cys Ala Thr Gly Gly Ala Gly Ala
1 5 10 15
Cys Ala Gly Ala Cys Ala Cys Ala Cys Thr Cys Cys Thr Gly Cys Thr
20 25 30
Ala Thr Gly Gly Gly Thr Gly Cys Thr Gly Cys Thr Gly Cys Thr Thr
35 40 45
Thr Gly Gly Gly Thr Thr Cys Cys Ala Gly Gly Cys Thr Cys Cys Ala
50 55 60
Cys Thr Gly Gly Thr Gly Ala Cys Ala Thr Thr Gly Thr Gly Cys Thr
65 70 75 80
Gly Ala Cys Cys Cys Ala Ala Thr Cys Thr Cys Cys Ala Gly Cys Thr
85 90 95
Thr Cys Thr Thr Thr Gly Gly Cys Thr Gly Thr Gly Thr Cys Thr Cys
100 105 110
Thr Ala Gly Gly Gly Cys Ala Gly Ala Gly Gly Gly Cys Cys Ala Cys
115 120 125
Cys Ala Thr Cys Thr Cys Thr Thr Gly Cys Ala Ala Gly Gly Cys Cys
130 135 140
Ala Gly Cys Cys Ala Ala Ala Gly Thr Gly Thr Thr Gly Ala Thr Thr
145 150 155 160
Ala Thr Gly Ala Thr Gly Gly Thr Gly Ala Thr Ala Gly Thr Thr Ala
165 170 175
Thr Ala Thr Gly Ala Ala Cys Thr Gly Gly Thr Ala Cys Cys Ala Ala
180 185 190
Cys Ala Gly Ala Ala Ala Cys Cys Ala Gly Gly Ala Cys Ala Gly Cys
195 200 205
Cys Ala Cys Cys Cys Ala Ala Ala Cys Thr Cys Cys Thr Cys Ala Thr
210 215 220
Thr Thr Ala Thr Gly Thr Thr Gly Cys Ala Thr Cys Cys Ala Ala Thr
225 230 235 240
Cys Thr Ala Ala Ala Ala Thr Cys Thr Gly Gly Gly Ala Thr Cys Cys
245 250 255
Cys Ala Gly Cys Cys Ala Gly Gly Thr Thr Thr Ala Gly Thr Gly Gly
260 265 270
Cys Ala Gly Thr Gly Gly Gly Thr Gly Thr Gly Gly Gly Ala Cys Ala
275 280 285
Gly Ala Cys Thr Thr Cys Ala Cys Cys Cys Thr Cys Ala Ala Cys Ala
290 295 300
Thr Cys Cys Ala Thr Cys Cys Thr Gly Thr Gly Gly Ala Gly Gly Ala
305 310 315 320
Gly Gly Ala Gly Gly Ala Thr Gly Gly Thr Gly Cys Ala Ala Cys Cys
325 330 335
Thr Ala Thr Thr Ala Cys Thr Gly Thr Cys Ala Gly Cys Ala Ala Ala
340 345 350
Cys Thr Ala Ala Thr Gly Ala Gly Gly Ala Thr Cys Cys Gly Thr Gly
355 360 365
Gly Ala Cys Gly Thr Thr Cys Gly Gly Thr Gly Gly Ala Gly Gly Cys
370 375 380
Ala Cys Cys Ala Ala Gly Cys Thr Gly Gly Ala Ala Ala Thr Cys Ala
385 390 395 400
Ala Ala Cys Gly Gly Gly Cys Thr Gly Ala Thr Gly Cys Thr Gly Cys
405 410 415
Ala
<210> 299
<211> 39
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 30D10: CDR1
<400> 299
aaggccagcc aaagtgttga ttatgatggt gatagttat 39
<210> 300
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 30D10: CDR2
<400> 300
gttgcatcca atctaaaatc t 21
<210> 301
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 30D10: CDR3
<400> 301
cagcaaacta atgaggatcc gtggacg 27
<210> 302
<211> 131
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 30D10
<220>
<221> MISC_FEATURE
<222> (1)..(20)
<223> Лидерная последовательность
<220>
<221> MISC_FEATURE
<222> (21)..(43)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (44)..(56)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (57)..(73)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (74)..(80)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (81)..(112)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (113)..(121)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (122)..(131)
<223> FR4
<400> 302
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala
20 25 30
Val Ser Leu Gly Gln Arg Ala Thr Ile Ser Cys Lys Ala Ser Gln Ser
35 40 45
Val Asp Tyr Asp Gly Asp Ser Tyr Met Asn Trp Tyr Gln Gln Lys Pro
50 55 60
Gly Gln Pro Pro Lys Leu Leu Ile Tyr Val Ala Ser Asn Leu Lys Ser
65 70 75 80
Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Cys Gly Thr Asp Phe Thr
85 90 95
Leu Asn Ile His Pro Val Glu Glu Glu Asp Gly Ala Thr Tyr Tyr Cys
100 105 110
Gln Gln Thr Asn Glu Asp Pro Trp Thr Phe Gly Gly Gly Thr Lys Leu
115 120 125
Glu Ile Lys
130
<210> 303
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 30D10: FR1
<400> 303
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys
20
<210> 304
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 30D10: CDR1
<400> 304
Lys Ala Ser Gln Ser Val Asp Tyr Asp Gly Asp Ser Tyr
1 5 10
<210> 305
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 30D10: FR2
<400> 305
Met Asn Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile
1 5 10 15
Tyr
<210> 306
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 30D10: CDR2
<400> 306
Val Ala Ser Asn Leu Lys Ser
1 5
<210> 307
<211> 32
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 30D10: FR3
<400> 307
Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Cys Gly Thr Asp Phe Thr
1 5 10 15
Leu Asn Ile His Pro Val Glu Glu Glu Asp Gly Ala Thr Tyr Tyr Cys
20 25 30
<210> 308
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 30D10: CDR3
<400> 308
Gln Gln Thr Asn Glu Asp Pro Trp Thr
1 5
<210> 309
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 30D10: FR4
<400> 309
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
1 5 10
<210> 310
<211> 424
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 51C3
<220>
<221> misc_feature
<222> (1)..(66)
<223> Лидерная последовательность
<220>
<221> misc_feature
<222> (67)..(138)
<223> FR1
<220>
<221> misc_feature
<222> (139)..(171)
<223> CDR1
<220>
<221> misc_feature
<222> (172)..(213)
<223> FR2
<220>
<221> misc_feature
<222> (214)..(264)
<223> CDR2
<220>
<221> misc_feature
<222> (265)..(354)
<223> FR3
<220>
<221> misc_feature
<222> (355)..(390)
<223> CDR3
<220>
<221> misc_feature
<222> (391)..(423)
<223> FR4
<400> 310
tggggaattc aggaatggag ctgggttttt ctctttctcc tgtcaggaac tgcaggtgtc 60
ctctctgagg tccagctgca acagtctgga cctgagctgg tgaagcctgg ggcttcagtg 120
aagatatcct gcaagacttc tggatacaca ttcactgaat acatcatgca ctgggtgaaa 180
cagagccatg gaaagagcct tgagtggatt ggaggtatta atcctaataa tggtggtact 240
aactacaacc agaagtttaa gggcaaggcc acattgactg tagacacgtc ctccagcata 300
gcctacatgg aactccgcag cctgacatct gaagattctg cagtctatta ttgtgcaaga 360
gacgatggtt actacgtaaa gttcgcttac tggggccaag ggactctggt cactgtctct 420
gcag 424
<210> 311
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 51C3: CDR1
<400> 311
tctggataca cattcactga atacatcatg cac 33
<210> 312
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 51C3: CDR2
<400> 312
ggtattaatc ctaataatgg tggtactaac tacaaccaga agtttaaggg c 51
<210> 313
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 51C3: CDR3
<400> 313
gcaagagacg atggttacta cgtaaagttc gcttac 36
<210> 314
<211> 141
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 51C3
<220>
<221> MISC_FEATURE
<222> (1)..(22)
<223> Лидерная последовательность
<220>
<221> MISC_FEATURE
<222> (23)..(46)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (47)..(57)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (58)..(71)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (72)..(88)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (89)..(118)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (119)..(130)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (131)..(141)
<223> FR4
<400> 314
Trp Gly Ile Gln Glu Trp Ser Trp Val Phe Leu Phe Leu Leu Ser Gly
1 5 10 15
Thr Ala Gly Val Leu Ser Glu Val Gln Leu Gln Gln Ser Gly Pro Glu
20 25 30
Leu Val Lys Pro Gly Ala Ser Val Lys Ile Ser Cys Lys Thr Ser Gly
35 40 45
Tyr Thr Phe Thr Glu Tyr Ile Met His Trp Val Lys Gln Ser His Gly
50 55 60
Lys Ser Leu Glu Trp Ile Gly Gly Ile Asn Pro Asn Asn Gly Gly Thr
65 70 75 80
Asn Tyr Asn Gln Lys Phe Lys Gly Lys Ala Thr Leu Thr Val Asp Thr
85 90 95
Ser Ser Ser Ile Ala Tyr Met Glu Leu Arg Ser Leu Thr Ser Glu Asp
100 105 110
Ser Ala Val Tyr Tyr Cys Ala Arg Asp Asp Gly Tyr Tyr Val Lys Phe
115 120 125
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala
130 135 140
<210> 315
<211> 24
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 51C3: FR1
<400> 315
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr
20
<210> 316
<211> 27
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 51C3: CDR1
<400> 316
Cys His Glu Ala Val Tyr Cys His Ala Ile Asn Val His Cys Asp Arg
1 5 10 15
Ser Gly Tyr Thr Phe Thr Glu Tyr Ile Met His
20 25
<210> 317
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 51C3: FR2
<400> 317
Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile Gly
1 5 10
<210> 318
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 51C3: CDR2
<400> 318
Gly Ile Asn Pro Asn Asn Gly Gly Thr Asn Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 319
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 51C3: FR3
<400> 319
Lys Ala Thr Leu Thr Val Asp Thr Ser Ser Ser Ile Ala Tyr Met Glu
1 5 10 15
Leu Arg Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
20 25 30
<210> 320
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 51C3: CDR3
<400> 320
Ala Arg Asp Asp Gly Tyr Tyr Val Lys Phe Ala Tyr
1 5 10
<210> 321
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH тяжелой цепи 51C3: FR4
<400> 321
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala
1 5 10
<210> 322
<211> 419
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 51C3
<220>
<221> misc_feature
<222> (12)..(83)
<223> Лидерная последовательность
<220>
<221> misc_feature
<222> (84)..(152)
<223> FR1
<220>
<221> misc_feature
<222> (153)..(179)
<223> CDR1
<220>
<221> misc_feature
<222> (180)..(230)
<223> FR2
<220>
<221> misc_feature
<222> (231)..(251)
<223> CDR2
<220>
<221> misc_feature
<222> (252)..(347)
<223> FR3
<220>
<221> misc_feature
<222> (348)..(374)
<223> CDR3
<220>
<221> misc_feature
<222> (375)..(419)
<223> FR4
<400> 322
tactagttga catgggcttc aagatggagt cacagactca ggtcttcgta tttctactgc 60
tctgtgtgtc tggtgctcat gggagtattg tgatgaccca gactcccaaa ttcctgcttg 120
tatcagcagg agacagggtt accataacct gcaaggccag tcagagtgtg attaatgatg 180
tagcttggta ccaacagaag ccagggcagt ctcctaaact gctgatatac tatgcatcca 240
atcgctacac tggagtccct gatcgcttca ctggcagtgg atatgggacg gatttcactt 300
tcaccatcag cactgtgcag gctgaagacc tggcagttta tttctgtcag caggattata 360
gctctccatt cacgttcggc tcggggacaa agttggaaat aaaacgggct gatgctgca 419
<210> 323
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 51C3: CDR1
<400> 323
aaggccagtc agagtgtgat taatgat 27
<210> 324
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 51C3: CDR2
<400> 324
tatgcatcca atcgctacac t 21
<210> 325
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 51C3: CDR3
<400> 325
cagcaggatt atagctctcc attcacg 27
<210> 326
<211> 136
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 51C3
<220>
<221> MISC_FEATURE
<222> (1)..(24)
<223> Лидерная последовательность
<220>
<221> MISC_FEATURE
<222> (25)..(47)
<223> FR1
<220>
<221> MISC_FEATURE
<222> (48)..(56)
<223> CDR1
<220>
<221> MISC_FEATURE
<222> (57)..(73)
<223> FR2
<220>
<221> MISC_FEATURE
<222> (74)..(80)
<223> CDR2
<220>
<221> MISC_FEATURE
<222> (81)..(112)
<223> FR3
<220>
<221> MISC_FEATURE
<222> (113)..(121)
<223> CDR3
<220>
<221> MISC_FEATURE
<222> (122)..(136)
<223> FR4
<400> 326
Met Gly Phe Lys Met Glu Ser Gln Thr Gln Val Phe Val Phe Leu Leu
1 5 10 15
Leu Cys Val Ser Gly Ala His Gly Ser Ile Val Met Thr Gln Thr Pro
20 25 30
Lys Phe Leu Leu Val Ser Ala Gly Asp Arg Val Thr Ile Thr Cys Lys
35 40 45
Ala Ser Gln Ser Val Ile Asn Asp Val Ala Trp Tyr Gln Gln Lys Pro
50 55 60
Gly Gln Ser Pro Lys Leu Leu Ile Tyr Tyr Ala Ser Asn Arg Tyr Thr
65 70 75 80
Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Tyr Gly Thr Asp Phe Thr
85 90 95
Phe Thr Ile Ser Thr Val Gln Ala Glu Asp Leu Ala Val Tyr Phe Cys
100 105 110
Gln Gln Asp Tyr Ser Ser Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu
115 120 125
Glu Ile Lys Arg Ala Asp Ala Ala
130 135
<210> 327
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 51C3: FR1
<400> 327
Ser Ile Val Met Thr Gln Thr Pro Lys Phe Leu Leu Val Ser Ala Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys
20
<210> 328
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 51C3: CDR1
<400> 328
Lys Ala Ser Gln Ser Val Ile Asn Asp
1 5
<210> 329
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 51C3: FR2
<400> 329
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile
1 5 10 15
Tyr
<210> 330
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 51C3: CDR2
<400> 330
Tyr Ala Ser Asn Arg Tyr Thr
1 5
<210> 331
<211> 32
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 51C3: FR3
<400> 331
Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Tyr Gly Thr Asp Phe Thr
1 5 10 15
Phe Thr Ile Ser Thr Val Gln Ala Glu Asp Leu Ala Val Tyr Phe Cys
20 25 30
<210> 332
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 51C3: CDR3
<400> 332
Gln Gln Asp Tyr Ser Ser Pro Phe Thr
1 5
<210> 333
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL легкой цепи 51C3: FR4
<400> 333
Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys Arg Ala Asp Ala Ala
1 5 10 15
<210> 334
<211> 1233
<212> ДНК
<213> Homo sapiens
<400> 334
atgtcgctca tggtcgtcag catggcgtgt gttgggttct tcttgctgga ggggccctgg 60
ccacatgtgg gtggtcagga caagcccttc ctctctgcct ggcccggcac tgtggtgtct 120
gaaggacaac atgtgactct tcagtgtcgc tctcgtcttg ggtttaatga attcagtctg 180
tccaaagaag acgggatgcc tgtccctgag ctctacaaca gaatattccg gaacagcttt 240
ctcatgggcc ctgtgacccc agcacatgca gggacctaca gatgttgcag ttcacaccca 300
cactccccca ctgggtggtc ggcacccagc aaccctgtgg tgatcatggt cacaggagtc 360
cacagaaaac cttccctcct ggcccaccca ggtcccctgg tgaaatcagg agagacggtc 420
atcctgcaat gttggtcaga tgtcaggttt gagcgcttcc ttctgcacag agaggggatc 480
actgaggacc ccttgcgcct cgttggacag ctccacgatg cgggttccca ggtcaactat 540
tccatgggtc ccatgacacc tgcccttgca gggacctaca gatgctttgg ttctgtcact 600
cacttaccct atgagttgtc ggctcccagt gaccctctgg acatcgtggt cgtaggtcta 660
tatgggaaac cttctctctc agcccagccg ggccccacgg ttcaggcagg agagaatgtg 720
accttgtcct gcagctcccg gagcttgttt gacatttacc atctatccag ggaggcggag 780
gccggtgaac ttaggctcac tgcagtgctg agggtcaatg gaacattcca ggccaacttc 840
cctctgggcc ctgtgaccca cggagggaac tacagatgct tcggctcttt ccgtgccctg 900
ccccatgcgt ggtcagaccc gagtgaccca ctgcccgttt ctgtcacagg taactccaga 960
aacctgcacg ttctgattgg gacctcagtg gtcatcatcc cctttgctat cctcctcttc 1020
tttctccttc atcgctggtg tgccaacaaa aagaatgctg ttgtaatgga ccaagagcct 1080
gcagggaaca gaacagtgaa cagggaggac tctgatgaac aagaccctca ggaggtgaca 1140
tacgcacagt tgaatcactg cgttttcaca cagagaaaaa tcactcgccc ttctcagagg 1200
cccaagacac ccccaacaga taccagcgtg taa 1233
<210> 335
<211> 410
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> MISC_FEATURE
<222> (1)..(25)
<223> Сигнальный пепетид
<220>
<221> MISC_FEATURE
<222> (34)..(118)
<223> домен D0
<220>
<221> MISC_FEATURE
<222> (129)..(218)
<223> домен D1
<220>
<221> MISC_FEATURE
<222> (229)..(325)
<223> домен D2
<220>
<221> MISC_FEATURE
<222> (321)..(343)
<223> Трансмембранный домен
<220>
<221> MISC_FEATURE
<222> (344)..(403)
<223> Цитоплазматический хвост
<220>
<221> MISC_FEATURE
<222> (379)..(384)
<223> Тирозин-содержащий ингибирующий мотив иммунорецептора (ITIM)
<400> 335
Met Ser Leu Met Val Val Ser Met Ala Cys Val Gly Phe Phe Leu Leu
1 5 10 15
Glu Gly Pro Trp Pro His Val Gly Gly Gln Asp Lys Pro Phe Leu Ser
20 25 30
Ala Trp Pro Gly Thr Val Val Ser Glu Gly Gln His Val Thr Leu Gln
35 40 45
Cys Arg Ser Arg Leu Gly Phe Asn Glu Phe Ser Leu Ser Lys Glu Asp
50 55 60
Gly Met Pro Val Pro Glu Leu Tyr Asn Arg Ile Phe Arg Asn Ser Phe
65 70 75 80
Leu Met Gly Pro Val Thr Pro Ala His Ala Gly Thr Tyr Arg Cys Cys
85 90 95
Ser Ser His Pro His Ser Pro Thr Gly Trp Ser Ala Pro Ser Asn Pro
100 105 110
Val Val Ile Met Val Thr Gly Val His Arg Lys Pro Ser Leu Leu Ala
115 120 125
His Pro Gly Pro Leu Val Lys Ser Gly Glu Thr Val Ile Leu Gln Cys
130 135 140
Trp Ser Asp Val Arg Phe Glu Arg Phe Leu Leu His Arg Glu Gly Ile
145 150 155 160
Thr Glu Asp Pro Leu Arg Leu Val Gly Gln Leu His Asp Ala Gly Ser
165 170 175
Gln Val Asn Tyr Ser Met Gly Pro Met Thr Pro Ala Leu Ala Gly Thr
180 185 190
Tyr Arg Cys Phe Gly Ser Val Thr His Leu Pro Tyr Glu Leu Ser Ala
195 200 205
Pro Ser Asp Pro Leu Asp Ile Val Val Val Gly Leu Tyr Gly Lys Pro
210 215 220
Ser Leu Ser Ala Gln Pro Gly Pro Thr Val Gln Ala Gly Glu Asn Val
225 230 235 240
Thr Leu Ser Cys Ser Ser Arg Ser Leu Phe Asp Ile Tyr His Leu Ser
245 250 255
Arg Glu Ala Glu Ala Gly Glu Leu Arg Leu Thr Ala Val Leu Arg Val
260 265 270
Asn Gly Thr Phe Gln Ala Asn Phe Pro Leu Gly Pro Val Thr His Gly
275 280 285
Gly Asn Tyr Arg Cys Phe Gly Ser Phe Arg Ala Leu Pro His Ala Trp
290 295 300
Ser Asp Pro Ser Asp Pro Leu Pro Val Ser Val Thr Gly Asn Ser Arg
305 310 315 320
Asn Leu His Val Leu Ile Gly Thr Ser Val Val Ile Ile Pro Phe Ala
325 330 335
Ile Leu Leu Phe Phe Leu Leu His Arg Trp Cys Ala Asn Lys Lys Asn
340 345 350
Ala Val Val Met Asp Gln Glu Pro Ala Gly Asn Arg Thr Val Asn Arg
355 360 365
Glu Asp Ser Asp Glu Gln Asp Pro Gln Glu Val Thr Tyr Ala Gln Leu
370 375 380
Asn His Cys Val Phe Thr Gln Arg Lys Ile Thr Arg Pro Ser Gln Arg
385 390 395 400
Pro Lys Thr Pro Pro Thr Asp Thr Ser Val
405 410
<210> 336
<211> 25
<212> БЕЛОК
<213> Homo sapiens
<400> 336
Met Ser Leu Met Val Val Ser Met Ala Cys Val Gly Phe Phe Leu Leu
1 5 10 15
Glu Gly Pro Trp Pro His Val Gly Gly
20 25
<210> 337
<211> 85
<212> БЕЛОК
<213> Homo sapiens
<400> 337
Trp Pro Gly Thr Val Val Ser Glu Gly Gln His Val Thr Leu Gln Cys
1 5 10 15
Arg Ser Arg Leu Gly Phe Asn Glu Phe Ser Leu Ser Lys Glu Asp Gly
20 25 30
Met Pro Val Pro Glu Leu Tyr Asn Arg Ile Phe Arg Asn Ser Phe Leu
35 40 45
Met Gly Pro Val Thr Pro Ala His Ala Gly Thr Tyr Arg Cys Cys Ser
50 55 60
Ser His Pro His Ser Pro Thr Gly Trp Ser Ala Pro Ser Asn Pro Val
65 70 75 80
Val Ile Met Val Thr
85
<210> 338
<211> 90
<212> БЕЛОК
<213> Homo sapiens
<400> 338
His Pro Gly Pro Leu Val Lys Ser Gly Glu Thr Val Ile Leu Gln Cys
1 5 10 15
Trp Ser Asp Val Arg Phe Glu Arg Phe Leu Leu His Arg Glu Gly Ile
20 25 30
Thr Glu Asp Pro Leu Arg Leu Val Gly Gln Leu His Asp Ala Gly Ser
35 40 45
Gln Val Asn Tyr Ser Met Gly Pro Met Thr Pro Ala Leu Ala Gly Thr
50 55 60
Tyr Arg Cys Phe Gly Ser Val Thr His Leu Pro Tyr Glu Leu Ser Ala
65 70 75 80
Pro Ser Asp Pro Leu Asp Ile Val Val Val
85 90
<210> 339
<211> 97
<212> БЕЛОК
<213> Homo sapiens
<400> 339
Gln Pro Gly Pro Thr Val Gln Ala Gly Glu Asn Val Thr Leu Ser Cys
1 5 10 15
Ser Ser Arg Ser Leu Phe Asp Ile Tyr His Leu Ser Arg Glu Ala Glu
20 25 30
Ala Gly Glu Leu Arg Leu Thr Ala Val Leu Arg Val Asn Gly Thr Phe
35 40 45
Gln Ala Asn Phe Pro Leu Gly Pro Val Thr His Gly Gly Asn Tyr Arg
50 55 60
Cys Phe Gly Ser Phe Arg Ala Leu Pro His Ala Trp Ser Asp Pro Ser
65 70 75 80
Asp Pro Leu Pro Val Ser Val Thr Gly Asn Ser Arg Asn Leu His Val
85 90 95
Leu
<210> 340
<211> 23
<212> БЕЛОК
<213> Homo sapiens
<400> 340
Asn Leu His Val Leu Ile Gly Thr Ser Val Val Ile Ile Pro Phe Ala
1 5 10 15
Ile Leu Leu Phe Phe Leu Leu
20
<210> 341
<211> 60
<212> БЕЛОК
<213> Homo sapiens
<400> 341
His Arg Trp Cys Ala Asn Lys Lys Asn Ala Val Val Met Asp Gln Glu
1 5 10 15
Pro Ala Gly Asn Arg Thr Val Asn Arg Glu Asp Ser Asp Glu Gln Asp
20 25 30
Pro Gln Glu Val Thr Tyr Ala Gln Leu Asn His Cys Val Phe Thr Gln
35 40 45
Arg Lys Ile Thr Arg Pro Ser Gln Arg Pro Lys Thr
50 55 60
<210> 342
<211> 6
<212> БЕЛОК
<213> Homo sapiens
<400> 342
Val Thr Tyr Ala Gln Leu
1 5
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Т-КЛЕТКИ С ХИМЕРНЫМИ АНТИГЕННЫМИ РЕЦЕПТОРАМИ (CAR-T) ДЛЯ ЛЕЧЕНИЯ РАКА | 2019 |
|
RU2811466C2 |
| ИММУНОЦИТОКИНЫ НА ОСНОВЕ IL-15 И IL-15Rα ДОМЕНА SUSHI | 2012 |
|
RU2763298C2 |
| ПРИМЕНЕНИЕ АНТИТЕЛА ПРОТИВ О-АЦЕТИЛИРОВАННОГО ГАНГЛИОЗИДА GD2 ДЛЯ УЛУЧШЕНИЯ ТЕРАПЕВТИЧЕСКОГО ПОТЕНЦИАЛА ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2017 |
|
RU2771173C2 |
| СОБАЧЬИ АНТИТЕЛА С МОДИФИЦИРОВАННЫМИ ПОСЛЕДОВАТЕЛЬНОСТЯМИ CH2-CH3 | 2014 |
|
RU2815059C2 |
| СОБАЧЬИ АНТИТЕЛА С МОДИФИЦИРОВАННЫМИ ПОСЛЕДОВАТЕЛЬНОСТЯМИ CH2-CH3 | 2014 |
|
RU2801209C2 |
| СУБСТРАТЫ МАТРИКСНОЙ МЕТАЛЛОПРОТЕИНАЗЫ И ДРУГИЕ РАСЩЕПЛЯЕМЫЕ ФРАГМЕНТЫ И СПОСОБЫ ИХ ИСПОЛЬЗОВАНИЯ | 2014 |
|
RU2832636C2 |
| ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ КОНЪЮГАТА ТРОЙНОГО АГОНИСТА ДЛИТЕЛЬНОГО ДЕЙСТВИЯ, ОБЛАДАЮЩЕГО АКТИВНОСТЯМИ В ОТНОШЕНИИ ВСЕХ ИЗ РЕЦЕПТОРОВ ГЛЮКАГОНА /GLP-1/GIP, ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЯ ЛЕГКОГО | 2020 |
|
RU2829342C1 |
| МОЛЕКУЛЫ, СВЯЗЫВАЮЩИЕ ADAM9, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2783619C2 |
| АНТИТЕЛА, НАПРАВЛЕННЫЕ ПРОТИВ РЕЦЕПТОРА ИНТЕРЛЕЙКИНА 36 (IL-36R) | 2016 |
|
RU2745898C2 |
| IL-17A-связывающие полипептиды | 2016 |
|
RU2749712C2 |

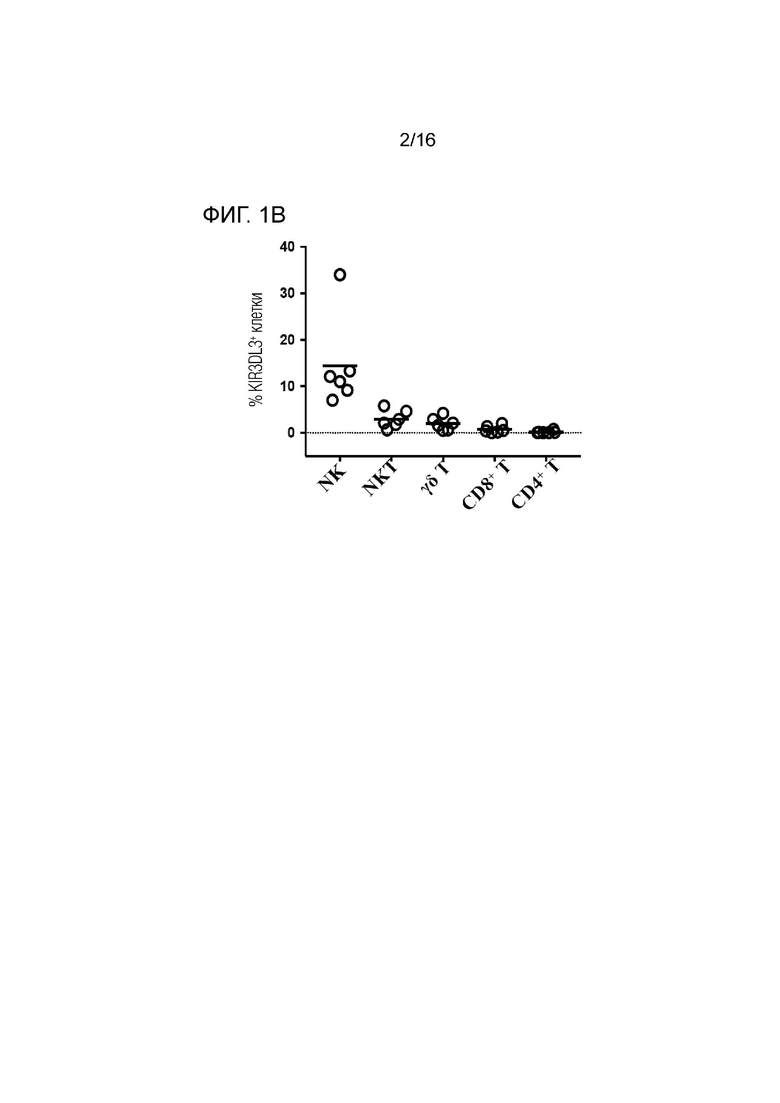
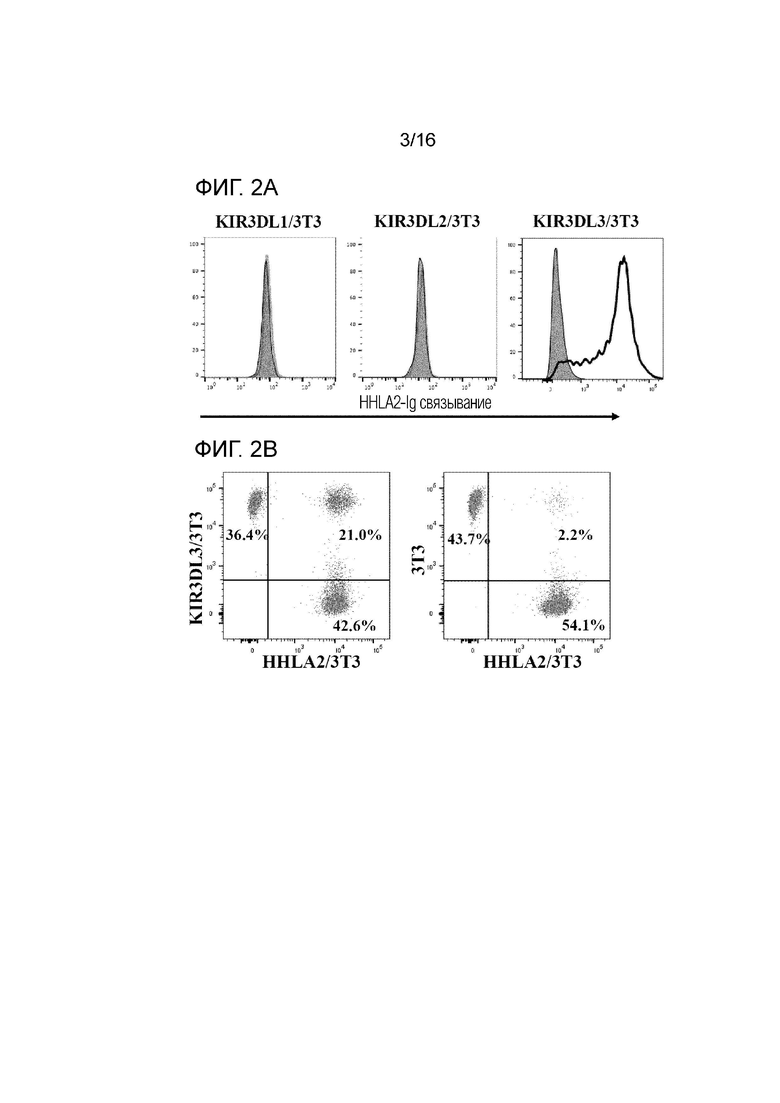
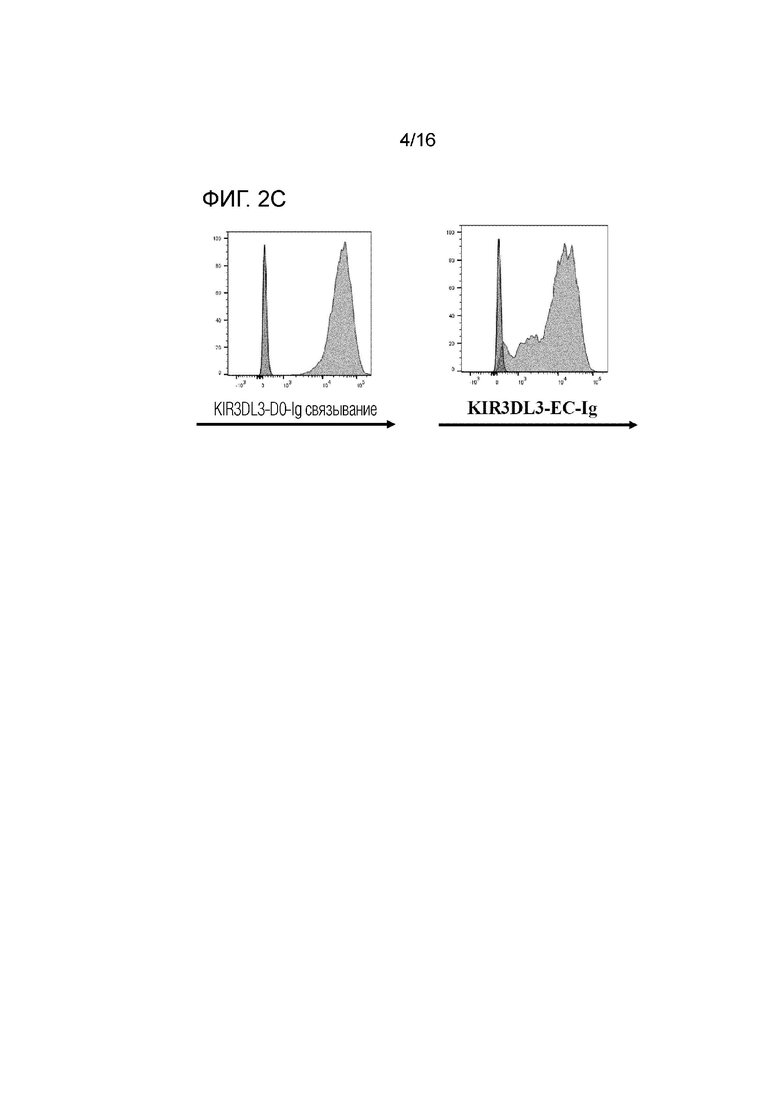
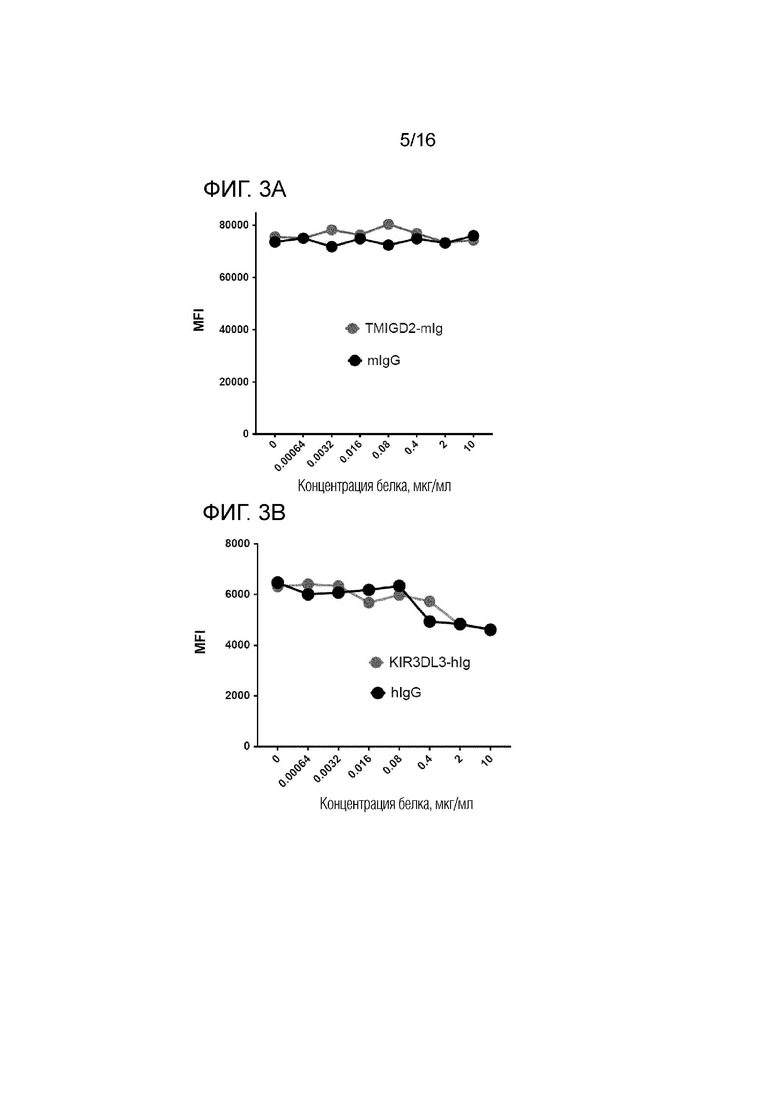
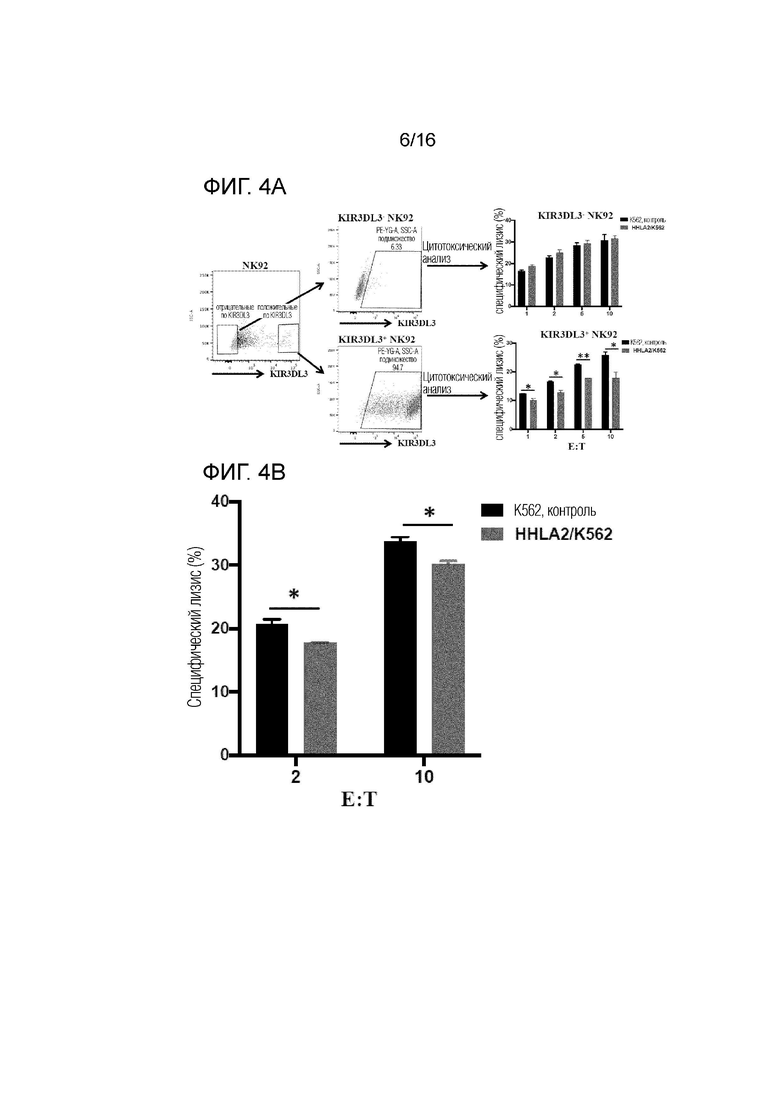
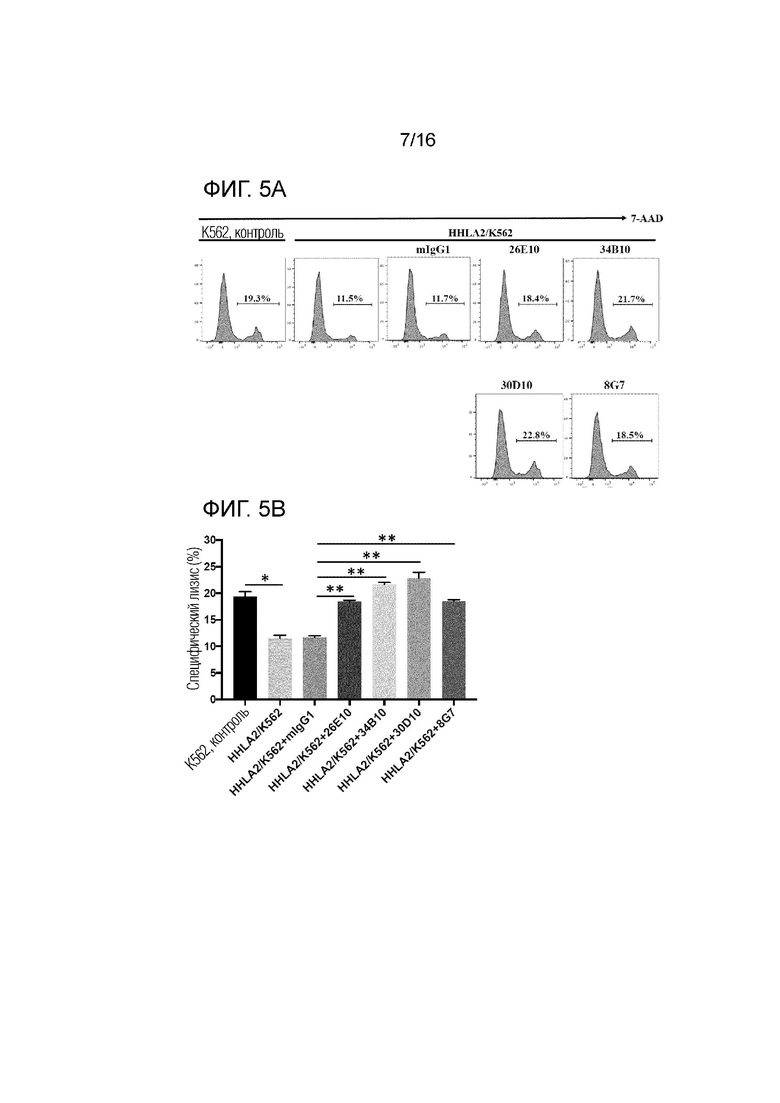
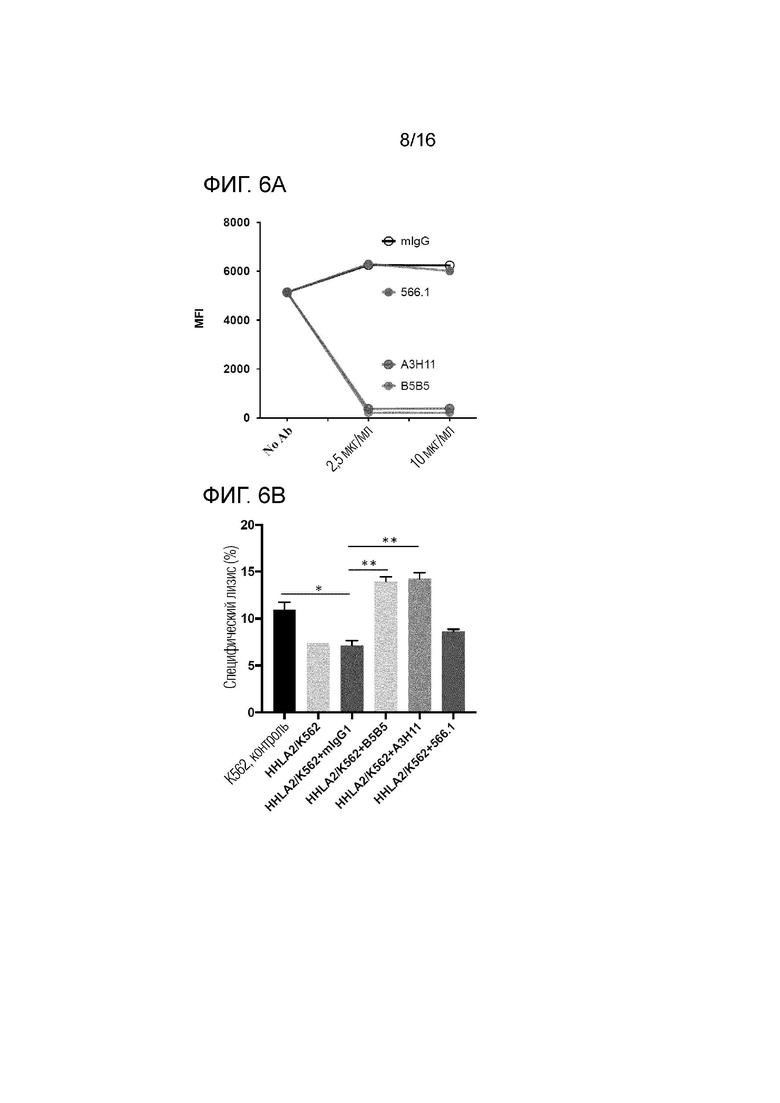
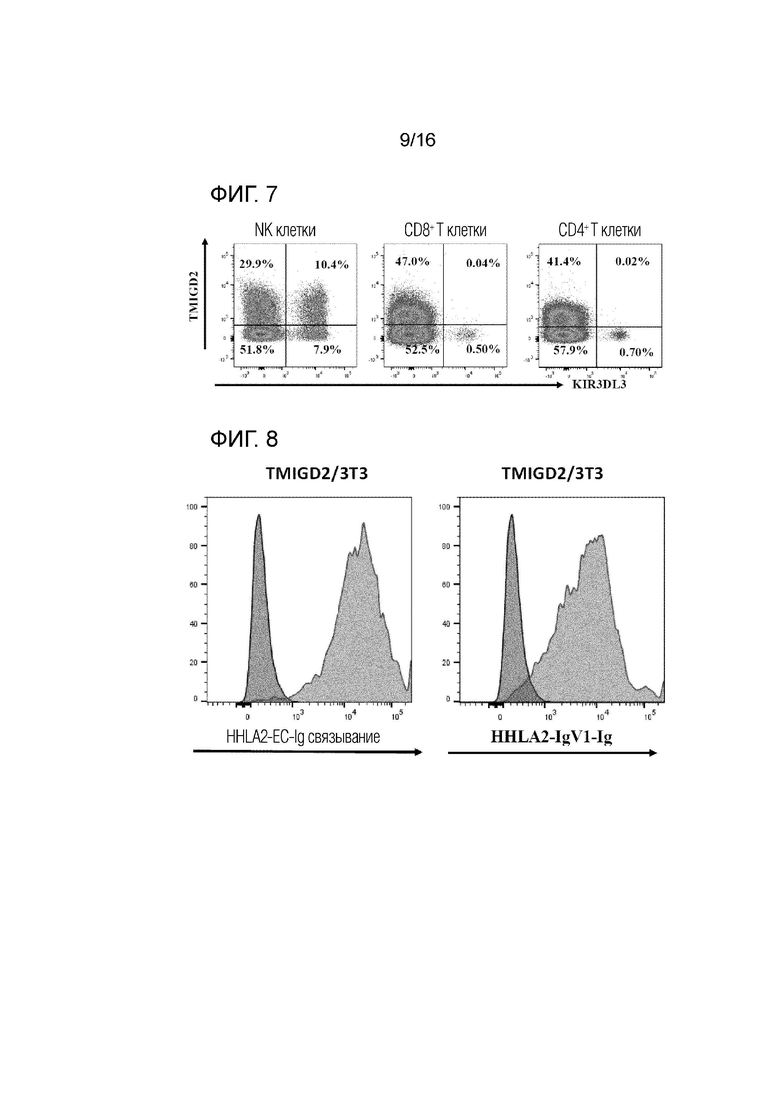
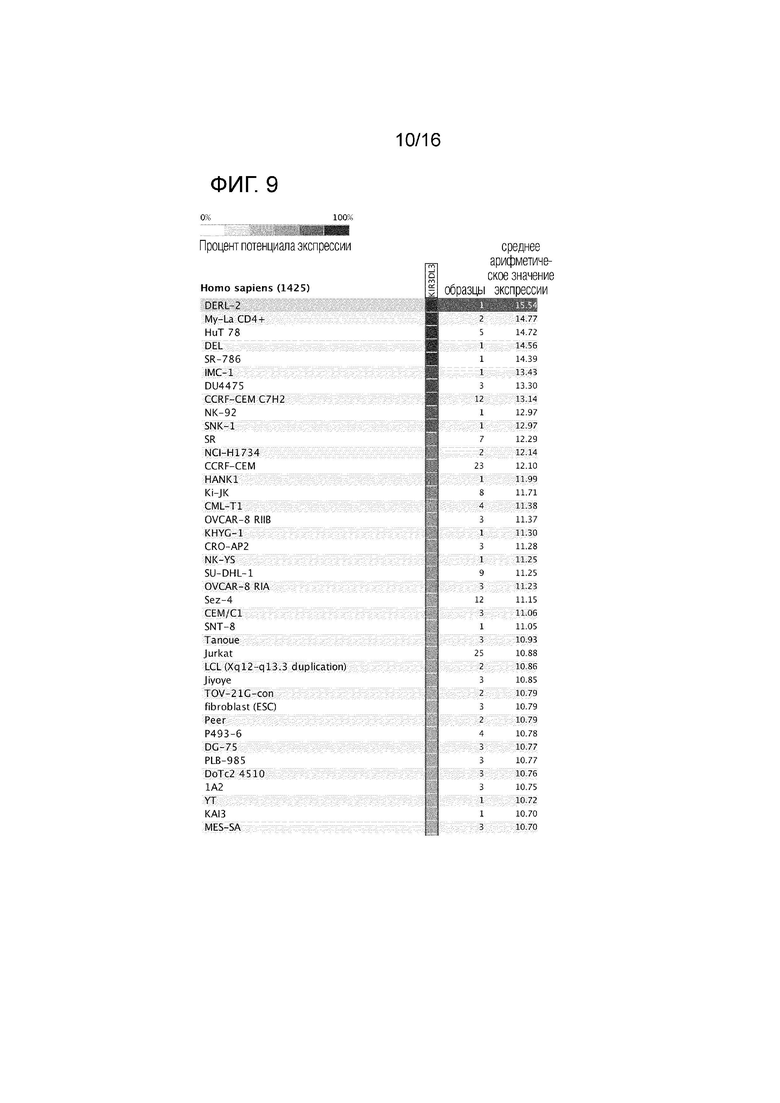
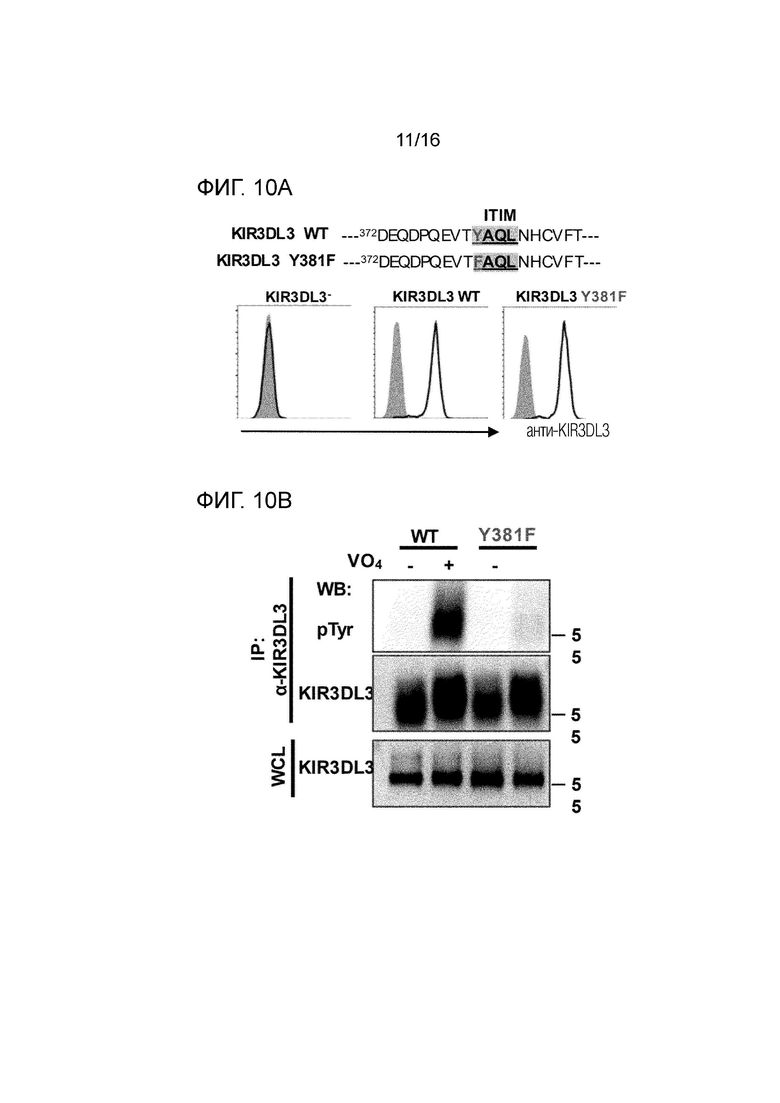
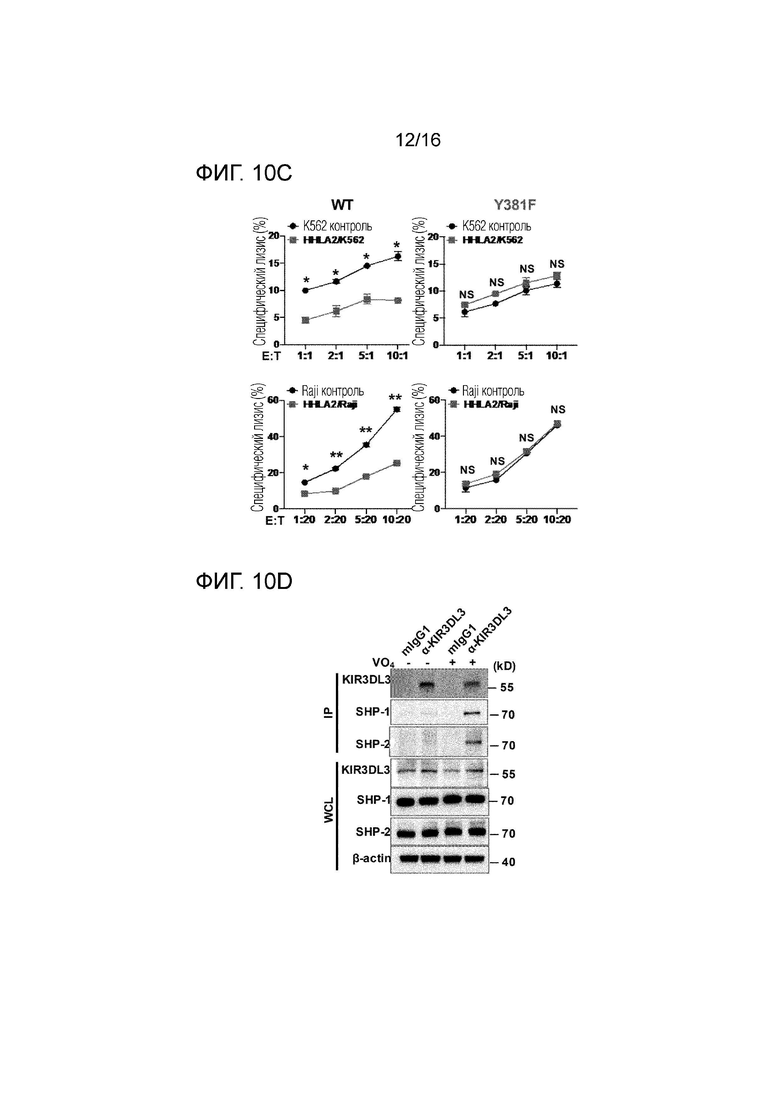
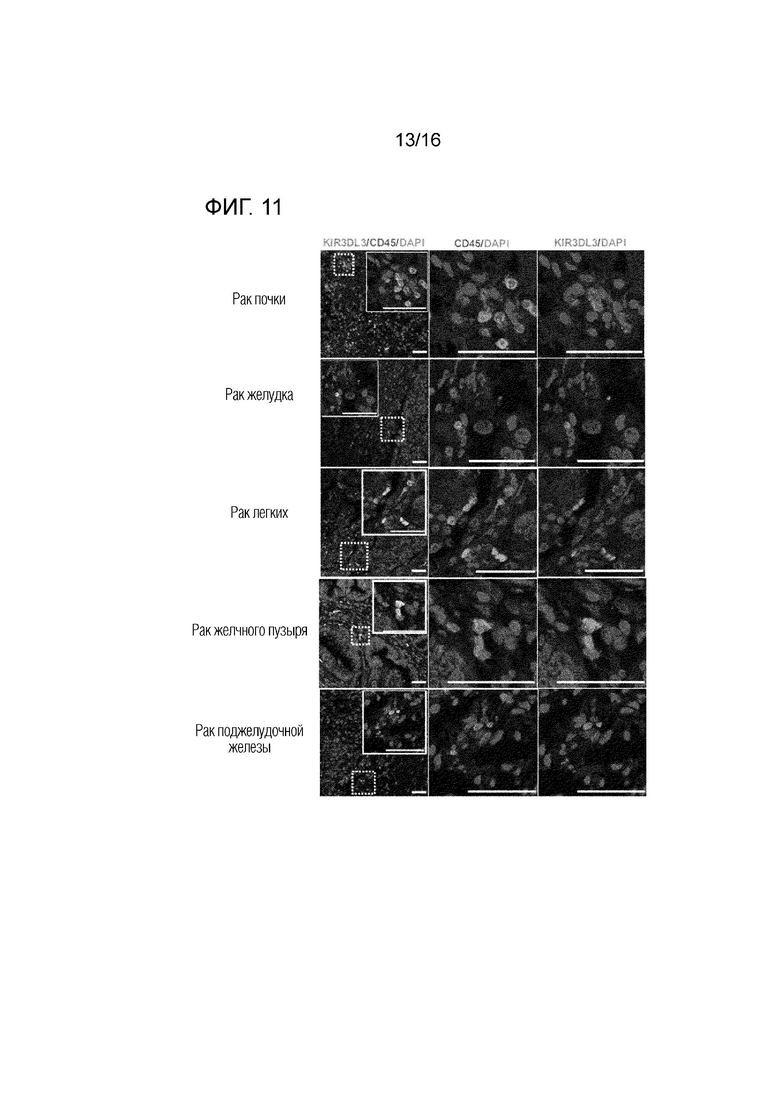
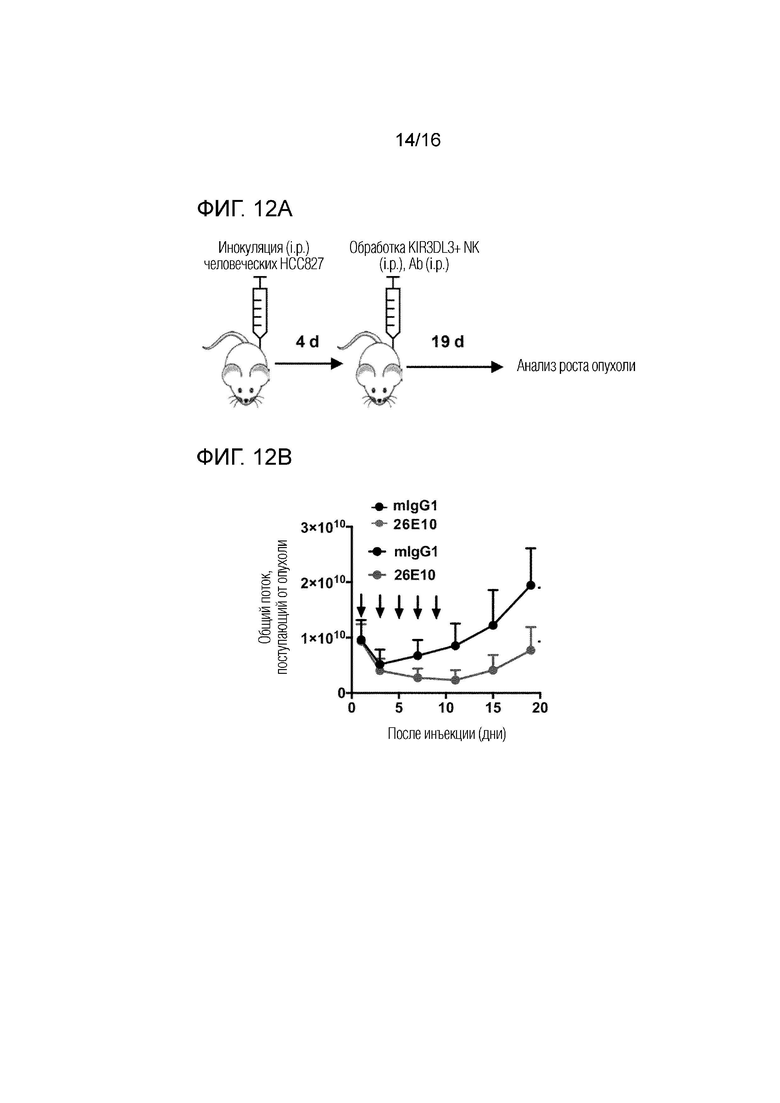
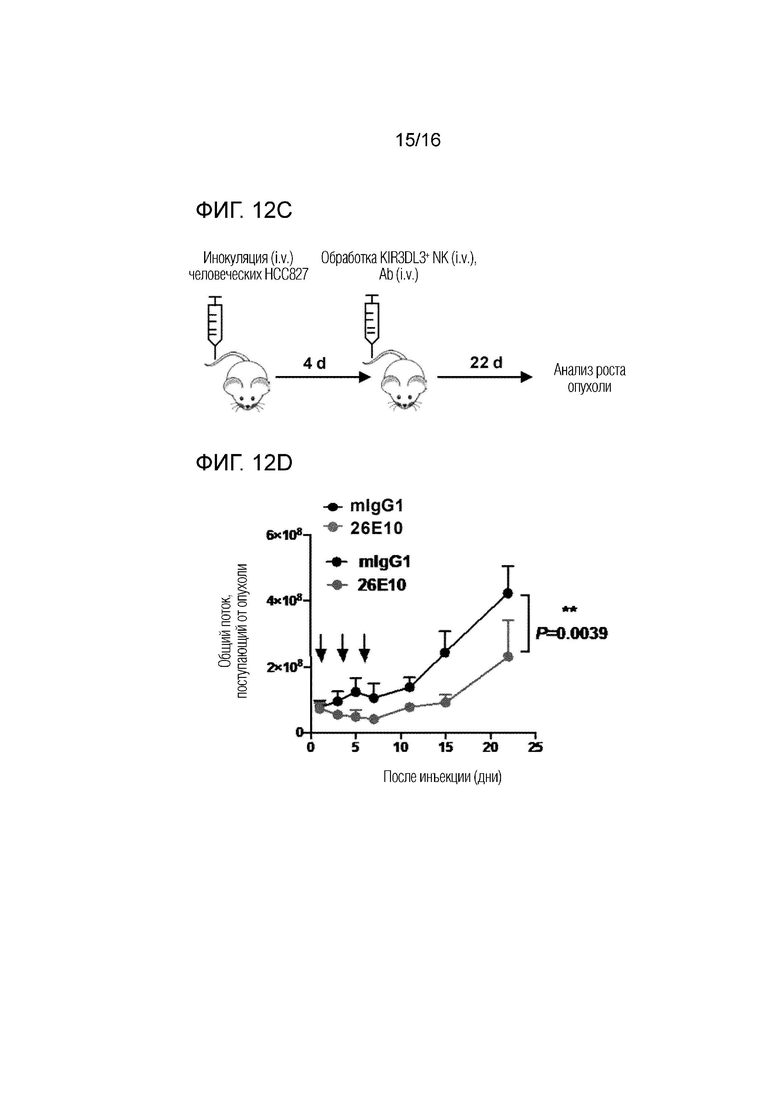
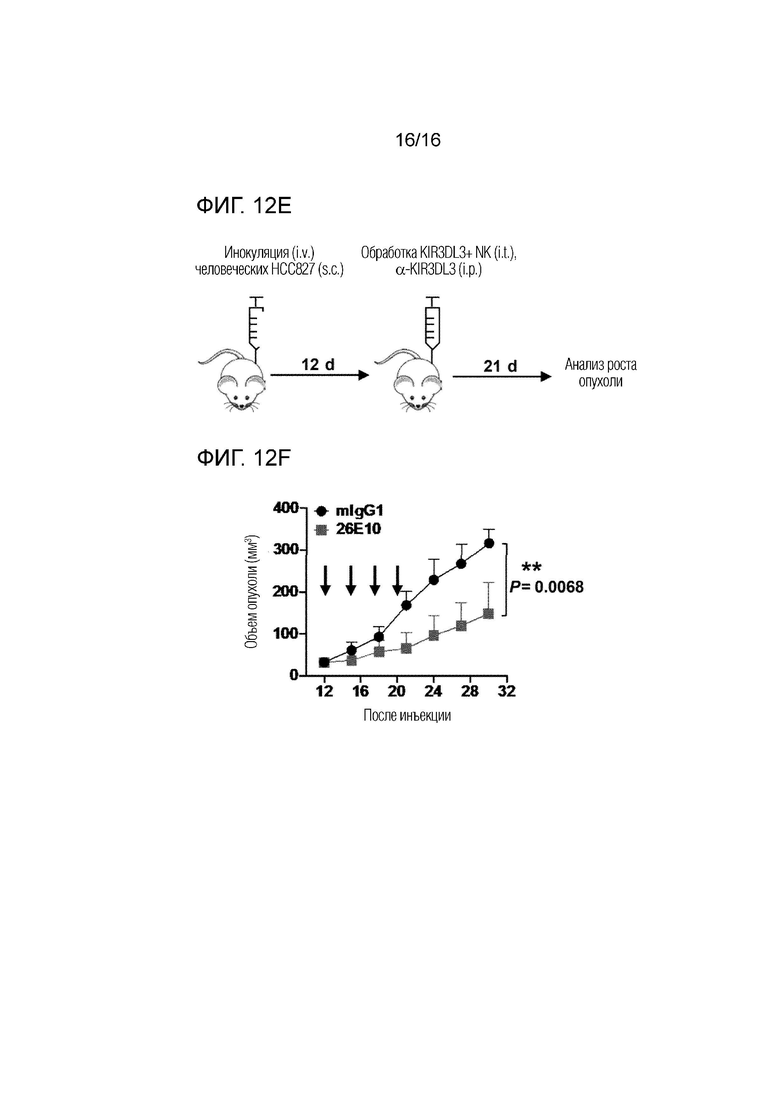
Изобретение относится к области биотехнологии. Предложены антитело или его фрагмент, которые специфически связываются с белком KIR3DL3, слитый полипептид и конъюгат, содержащие указанные антитело или его фрагмент, композиции на их основе. Также изобретение относится к способам применения антител для лечения заболеваний человека, связанных с высокой экспрессией белка KIR3DL3, включая рак. Изобретение обеспечивает нейтрализацию вызванного KIR3DL3 подавления иммунитета. 9 н. и 36 з.п. ф-лы, 27 ил., 4 табл., 1 пр.
1. Антитело или его фрагмент, которые специфически связываются с белком KIR3DL3, включающие вариабельную область тяжелой цепи (VH), содержащую CDR1, представленный в SEQ ID NO: 31, CDR2, представленный в SEQ ID NO: 33, и CDR3, представленный в SEQ ID NO: 35; и вариабельную область легкой цепи (VL), содержащую CDR1, представленный в SEQ ID NO: 43, CDR2, представленный в SEQ ID NO: 45, и CDR3, представленный в SEQ ID NO: 47.
2. Антитело по п. 1, где антитело представляет собой моноклональное антитело.
3. Антитело по п. 1 или 2, где антитело представляет собой химерное антитело, человеческое антитело или гуманизированное антитело.
4. Слитый полипептид, который специфически связывается с белком KIR3DL3, содержащий антитело или его фрагмент по любому из пп. 1-3 в составе химерного антигенного рецептора.
5. Конъюгат, который специфически связывается с белком KIR3DL3, содержащий антитело или его фрагмент по любому из пп. 1-3 и цититоксический агент.
6. Композиция для лечения состояния, связанного с высокой экспрессией белка KIR3DL3, содержащая антитело или его фрагмент по любому из пп. 1-3, или слитый полипептид по п. 4, или конъюгат по п. 5 и фармацевтически приемлемый носитель или наполнитель.
7. Применение антитела или его фрагмента по любому из пп. 1-3, слитого полипептида по п. 4, или конъюгата по п. 5, или композиции по п. 6 в производстве лекарственного средства для лечения состояния, связанного с высокой экспрессией белка KIR3DL3.
8. Нуклеиновая кислота, кодирующая антитело или его фрагмент по любому из пп. 1-3.
9. Нуклеиновая кислота, кодирующая слитый полипептид по п. 4.
10. Способ лечения состояния, связанного с высокой экспрессией белка KIR3DL3 у субъекта, включающий введение субъекту терапевтически эффективного количества антитела или его фрагмента по любому из пп. 1-3, слитого полипептида по п. 4, или конъюгата по п. 5, или композиции по п. 6.
11. Способ по п. 10, где субъект страдает от состояния, представляющего собой рак.
12. Способ по п. 11, где рак выбирают из группы, состоящей из хронического лимфолейкоза (CLL), острого лейкоза, острого лимфолейкоза (ALL), В-клеточного острого лимфолейкоза (В-ALL), Т-клеточной лимфомы, В-клеточной лимфомы, Т-клеточного острого лимфолейкоза (Т-ALL), хронического миелогенного лейкоза (CML), В-клеточного пролимфоцитарного лейкоза, Т-клеточной лимфомы, болезни Ходжкина, В-клеточной неходжкинской лимфомы, бластной плазмоцитоидной дендритно-клеточной опухоли, лимфомы Беркитта, диффузной крупноклеточной В-клеточной лимфомы, фолликулярной лимфомы, волосатоклеточного лейкоза, мелкоклеточной фолликулярной лимфомы, крупноклеточной фолликулярной лимфомы, злокачественных лимфопролиферативных состояний, лимфомы, ассоциированной со слизистой оболочкой (MALT), лимфомы из мантийных клеток, лимфомы маргинальной зоны, множественной миеломы, миелодисплазии и миелодиспластического синдрома, неходжкинской лимфомы, лимфомы Ходжкина, плазмобластной лимфомы, новообразования из плазмоцитоидных дендритных клеток, макроглобулинемии Вальденстрема или прелейкемии.
13. Способ по п. 11, где рак выбирают из группы, состоящей из рака толстой кишки, рака прямой кишки, почечно-клеточного рака, рака печени, рака легких, рака почки, рака желудка, рака желчного пузыря, рака тонкой кишки, рака пищевода, меланомы, рака костей, рака поджелудочной железы, рака кожи, рака головы или шеи, кожной или внутриглазной злокачественной меланомы, рака матки, рака яичников, рака прямой кишки, рака анальной области, рака желудка, рака яичек, рака матки, карциномы фаллопиевых труб, карциномы эндометрия, карциномы шейки матки, карциномы влагалища, карциномы вульвы, рака эндокринной системы, рака щитовидной железы, рака паращитовидной железы, рака надпочечников, саркомы мягких тканей, рака уретры, рака полового члена, солидных опухолей детского возраста, рака мочевого пузыря, рака почки или мочеточника, рака почечной лоханки, новообразования центральной нервной системы (ЦНС), первичной лимфомы ЦНС, ангиогенеза опухоли, опухоли спинного мозга, глиомы ствола головного мозга, аденомы гипофиза, саркомы Капоши, эпидермоидного рака, плоскоклеточного рака, рака, индуцированного окружающей средой, комбинации раковых заболеваний и метастатических поражений, вызванных раковыми заболеваниями.
14. Способ по п. 11, где рак представляет собой гематологическое злокачественное новообразование человека.
15. Способ по п. 14, где гематологическое злокачественное новообразование человека выбирают из миелоидного новообразования, острого миелоидного лейкоза (AML), AML с рецидивирующими генетическими аномалиями, AML с изменениями, связанными с миелодисплазией, AML, связанного с терапией, острых лейкозов неоднозначного происхождения, миелопролиферативного новообразования, эссенциальной тромбоцитемии, истинной полицитемии, миелофиброза (MF), первичного миелофиброза, системного мастоцитоза, миелодиспластических синдромов (MDS), миелопролиферативных/миелодиспластических синдромов, хронического миелоидного лейкоза, хронического нейтрофильного лейкоза, хронического эозинофильного лейкоза, миелодиспластических синдромов (MDS), рефрактерной анемии с кольцевидными сидеробластами, рефрактерной цитопении с многолинейной дисплазией, рефрактерной анемии с избытком бластов (тип 1), рефрактерной анемии с избытком бластов (тип 2), MDS с изолированной делецией (5q), неклассифицируемого MDS, миелопролиферативных/миелодиспластических синдромов, хронического миеломоноцитарного лейкоза, атипичного хронического миелоидного лейкоза, ювенильного миеломоноцитарного лейкоза, неклассифицируемых миелопролиферативных/миелодисплатических синдромов, лимфоидных новообразований, предраковых лимфоидных новообразований, В-лимфобластного лейкоза, В-лимфобластной лимфомы, Т-лимфобластного лейкоза, Т-лимфобластной лимфомы, новообразований из зрелых В-клеток, диффузной крупноклеточной В-клеточной лимфомы, первичной лимфомы центральной нервной системы, первичной медиастинальной В-клеточной лимфомы, лимфомы/лейкемии Беркитта, фолликулярной лимфомы, хронического лимфолейкоза, малой лимфоцитарной лимфомы, В-клеточного пролимфоцитарного лейкоза, лимфоплазмоцитарной лимфомы, макроглобулинемии Вальденстрема, лимфомы из мантийных клеток, лимфомы маргинальной зоны, посттрансплантационных лимфопролиферативных заболеваний, ВИЧ-ассоциированных лимфом, первичной выпотной лимфомы, внутрисосудистой крупноклеточной В-клеточной лимфомы, первичной кожной В-клеточной лимфомы, волосатоклеточного лейкоза, множественной миеломы, моноклональной гаммапатии неясного генеза (MGUS), тлеющей множественной миеломы или солитарных плазмоцитом (солитарных костных и экстрамедуллярных).
16. Способ по п. 11, где рак представляет собой метастатический рак.
17. Способ по п. 11, дополнительно включающий предоставление субъекту одного или более дополнительных видов терапии рака, выбранных из химиотерапии, лучевой терапии, иммунотерапии, хирургии и их комбинации.
18. Способ по п. 10, где субъект страдает от состояния, представляющего собой инфекцию.
19. Способ по п. 18, где инфекция вызвана патогеном.
20. Способ по п. 19, где патоген представляет собой вирус.
21. Способ по п. 20, где вирус выбирают из группы, состоящей из вирусов иммунодефицита человека, вирусов гриппа, папилломавирусов, коронавирусов, вирусов гепатита или герпесвирусов.
22. Способ по п. 19, где патоген представляет собой бактерию.
23. Способ по п. 22, где бактерия представляет собой микобактерию туберкулеза.
24. Способ по п. 19, где патоген представляет собой прион.
25. Способ по п. 19, где патоген представляет собой грибок.
26. Способ по п. 25, где грибок представляет собой Pneumocystis jirovecii (PJP).
27. Способ по п. 19, где патоген представляет собой паразита.
28. Применение композиции по п. 6 при лечении субъекта, страдающего от состояния, связанного с высокой экспрессией белка KIR3DL3 у субъекта.
29. Применение по п. 28, где состояние представляет собой рак.
30. Применение по п. 29, где рак выбирают из группы, состоящей из хронического лимфолейкоза (CLL), острого лейкоза, острого лимфолейкоза (ALL), В-клеточного острого лимфолейкоза (В-ALL), Т-клеточной лимфомы, В-клеточной лимфомы, Т-клеточного острого лимфолейкоза (Т-ALL), хронического миелогенного лейкоза (CML), В-клеточного пролимфоцитарного лейкоза, Т-клеточной лимфомы, болезни Ходжкина, В-клеточной неходжкинской лимфомы, бластной плазмоцитоидной дендритно-клеточной опухоли, лимфомы Беркитта, диффузной крупноклеточной В-клеточной лимфомы, фолликулярной лимфомы, волосатоклеточного лейкоза, мелкоклеточной фолликулярной лимфомы, крупноклеточной фолликулярной лимфомы, злокачественных лимфопролиферативных состояний, лимфомы, ассоциированной со слизистой оболочкой (MALT), лимфомы из мантийных клеток, лимфомы маргинальной зоны, множественной миеломы, миелодисплазии и миелодиспластического синдрома, неходжкинской лимфомы, лимфомы Ходжкина, плазмобластной лимфомы, новообразования из плазмоцитоидных дендритных клеток, макроглобулинемии Вальденстрема или прелейкемии.
31. Применение по п. 29, где рак выбирают из группы, состоящей из рака толстой кишки, рака прямой кишки, почечно-клеточного рака, рака печени, рака легких, рака почки, рака желудка, рака желчного пузыря, рака тонкой кишки, рака пищевода, меланомы, рака костей, рака поджелудочной железы, рака кожи, рака головы или шеи, кожной или внутриглазной злокачественной меланомы, рака матки, рака яичников, рака прямой кишки, рака анальной области, рака желудка, рака яичек, рака матки, карциномы фаллопиевых труб, карциномы эндометрия, карциномы шейки матки, карциномы влагалища, карциномы вульвы, рака эндокринной системы, рака щитовидной железы, рака паращитовидной железы, рака надпочечников, саркомы мягких тканей, рака уретры, рака полового члена, солидных опухолей детского возраста, рака мочевого пузыря, рака почки или мочеточника, рака почечной лоханки, новообразования центральной нервной системы (ЦНС), первичной лимфомы ЦНС, ангиогенеза опухоли, опухоли спинного мозга, глиомы ствола головного мозга, аденомы гипофиза, саркомы Капоши, эпидермоидного рака, плоскоклеточного рака, рака, индуцированного окружающей средой, комбинации раковых заболеваний и метастатических поражений, вызванных раковыми заболеваниями.
32. Применение по п. 29, где рак представляет собой гематологическое злокачественное новообразование человека.
33. Применение по п. 32, где гематологическое злокачественное новообразование человека выбирают из миелоидного новообразования, острого миелоидного лейкоза (AML), AML с рецидивирующими генетическими аномалиями, AML с изменениями, связанными с миелодисплазией, AML, связанного с терапией, острых лейкозов неоднозначного происхождения, миелопролиферативного новообразования, эссенциальной тромбоцитемии, истинной полицитемии, миелофиброза (MF), первичного миелофиброза, системного мастоцитоза, миелодиспластических синдромов (MDS), миелопролиферативных/миелодиспластических синдромов, хронического миелоидного лейкоза, хронического нейтрофильного лейкоза, хронического эозинофильного лейкоза, миелодиспластических синдромов (MDS), рефрактерной анемии с кольцевидными сидеробластами, рефрактерной цитопении с многолинейной дисплазией, рефрактерной анемии с избытком бластов (тип 1), рефрактерной анемии с избытком бластов (тип 2), MDS с изолированной делецией (5q), неклассифицируемого MDS, миелопролиферативных/миелодиспластических синдромов, хронического миеломоноцитарного лейкоза, атипичного хронического миелоидного лейкоза, ювенильного миеломоноцитарного лейкоза, неклассифицируемых миелопролиферативных/миелодисплатических синдромов, лимфоидных новообразований, предраковых лимфоидных новообразований, В-лимфобластного лейкоза, В-лимфобластной лимфомы, Т-лимфобластного лейкоза, Т-лимфобластной лимфомы, новообразований из зрелых В-клеток, диффузной крупноклеточной В-клеточной лимфомы, первичной лимфомы центральной нервной системы, первичной медиастинальной В-клеточной лимфомы, лимфомы/лейкемии Беркитта, фолликулярной лимфомы, хронического лимфолейкоза, малой лимфоцитарной лимфомы, В-клеточного пролимфоцитарного лейкоза, лимфоплазмоцитарной лимфомы, макроглобулинемии Вальденстрема, лимфомы из мантийных клеток, лимфомы маргинальной зоны, посттрансплантационных лимфопролиферативных заболеваний, ВИЧ-ассоциированных лимфом, первичной выпотной лимфомы, внутрисосудистой крупноклеточной В-клеточной лимфомы, первичной кожной В-клеточной лимфомы, волосатоклеточного лейкоза, множественной миеломы, моноклональной гаммапатии неясного генеза (MGUS), тлеющей множественной миеломы или солитарных плазмоцитом (солитарных костных и экстрамедуллярных).
34. Применение по п. 29, где рак представляет собой метастатический рак.
35. Применение по п. 29, где композицию вводят субъекту вместе с одним или более дополнительными видами терапии рака, выбранными из химиотерапии, лучевой терапии, иммунотерапии, хирургии и их комбинации.
36. Применение по п. 28, где состояние представляет собой инфекцию.
37. Применение по п. 36, где инфекция вызвана патогеном.
38. Применение по п. 37, где патоген представляет собой вирус.
39. Применение по п. 38, где вирус выбирают из группы, состоящей из вирусов иммунодефицита человека, вирусов гриппа, папилломавирусов, коронавирусов, вирусов гепатита или герпесвирусов.
40. Применение по п. 37, где патоген представляет собой бактерию.
41. Применение по п. 40, где бактерия представляет собой микобактерию туберкулеза.
42. Применение по п. 37, где патоген представляет собой прион.
43. Применение по п. 37, где патоген представляет собой грибок.
44. Применение по п. 43, где грибок представляет собой Pneumocystis jirovecii (PJP).
45. Применение по п. 37, где патоген представляет собой паразита.
| WO 2015187359 A1, 10.12.2015 | |||
| US 2016272709 A1, 22.09.2016 | |||
| GHANADI K | |||
| et al., Colorectal cancer and the KIR genes in the human genome: A meta-analysis, Genomics Data, 2016, Volume 10, pp.118-126 | |||
| TRUNDLEY A.E | |||
| et al., Molecular characterization of KIR3DL3, Immunogenetics, 2006, vol.7(12), pp.904-916 | |||
| СВЯЗЫВАЮЩИЕ KIR3DL2 АГЕНТЫ | 2013 |
|
RU2682449C2 |
Авторы
Даты
2024-10-03—Публикация
2020-10-01—Подача