ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к клеткам и агентам, полезным для лечения Т-клеточной лимфомы или лейкемии.
ПРЕДШЕСТВУЮЩИЙ ИЗОБРЕТЕНИЮ УРОВЕНЬ ТЕХНИКИ
Лимфоидные злокачественные новообразования по большей части могут быть разделены на опухоли, происходящие или из T-клеток, или из B-клеток. Т-клеточные злокачественные новообразования представляют собой клинически и биологически гетерогенную группу нарушений, в общей сложности, включающую 10-20% неходжкинских лимфом и 20% острых лейкемий. Наиболее часто выявляемыми гистологическими подтипами являются периферическая Т-клеточная лимфома, неуточненная (ПТКЛ-НУ); ангиоиммунобластная Т-клеточная лимфома (АИТКЛ) и анапластическая крупноклеточная лимфома (АККЛ). Из всех острых лимфобластных лейкемий (ОЛЛ) около 20% имеют Т-клеточный фенотип.
Эти заболевания, как правило, ведут себя агрессивно по сравнению, например, с B-клеточными злокачественными новообразованиями, с предполагаемой пятилетней выживаемостью всего лишь 30%. В случае Т-клеточной лимфомы они ассоциированы с высокой долей пациентов, демонстрирующих диссеминированное заболевание, неблагоприятное значение международного прогностического индикатора (IPI) и преобладание внеузлового заболевания. Химиотерапия по отдельности, как правило, неэффективна, и менее чем 30% пациентов излечиваются при помощи современных способов лечения.
Более того, в отличие от В-клеточных злокачественных новообразований, где иммунотерапевтические средства, такие как моноклональное антитело против CD20 ритуксимаб, значительно улучшают исход болезни, в настоящее время не существует такого же эффективного иммунотерапевтического средства с минимальной токсичностью, подходящего для лечения Т-клеточных злокачественных новообразований. Существенной трудностью в разработке иммунотерапии для Т-клеточных заболеваний является значительное перекрытие экспрессии маркеров клональных и нормальных T-клеток, и отсутствие отдельного антигена, способного четко идентифицировать клональные (злокачественные) клетки.
Аналогичная проблема существует при нацеливании пан-В-клеточного антигена для лечения В-клеточного злокачественного новообразования. Однако, в этом случае, сопутствующее истощение В-клеточного компартмента приводит к относительно незначительной иммуносупрессии, которая легко переносится большинством пациентов. Более того, при терапевтическом лечении, которое приводит к особенно длительному истощению нормального B-компартмента, его потеря может быть в значительной степени нейтрализована введением смешанного иммуноглобулина. Ситуация совершенно иная при нацеливании на Т-клеточные злокачественные новообразования. В этом случае, сопутствующее истощение Т-клеточного компартмента приводит к тяжелой иммуносупрессии и тяжелой токсичности. Более того, не существует удовлетворительного способа для уменьшения потери Т-клеточного компартмента.
Токсичность частично иллюстрируется клиническими эффектами терапевтического моноклонального антитела Алемтузумаб. Этот препарат разрушает клетки, которые экспрессируют CD52, и обладает некоторой эффективностью при Т-клеточных злокачественных новообразованиях. Полезность этого препарата сильно ограничена глубоким клеточным иммунодефицитом, в основном, за счет истощения популяции Т-клеток, с заметно повышенным риском инфицирования.
Существует, таким образом, потребность в новом способе для адресной терапии Т-клеточных злокачественных новообразований, который не ассоциирован с вышеизложенными недостатками.
ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фигура 1: Диаграмма комплекса Т-клеточного рецептора αβ/CD3. Т-клеточный рецептор формируется из 6 различных белковых цепей, которые должны собираться в эндоплазматическом ретикулуме, чтобы экпрессироваться на клеточной поверхности. Четыре белка из комплекса CD3 (CD3ζ, CD3γ, CD3ε и CD3δ) охватывают Т-клеточный рецептор (TCR). Этот TCR наполняет комплекс специфичностью к конкретному антигену и состоит из двух цепей: TCRα и TCRβ. Каждая цепь TCR имеет вариабельный компонент, расположенный дистально по отношению к мембране, и константный компонент, расположенный проксимально по отношению к мембране. Почти все Т-клеточные лимфомы и многие из Т-клеточных лейкемий экспрессируют комплекс TCR/CD3.
Фигура 2: Сегрегация константных областей β Т-клеточного рецептора (TRBC)-1 и TRBC2 во время реаранжировки Т-клеточного рецептора. Каждая бета-цепь TCR образуется путем геномной рекомбинации определенных вариабельной (V), определяющей разнообразие (D), соединительной (J) и константной (TRBC) бета-областей. Геном человека содержит два очень похожих и функционально эквивалентных локуса TRBC, известных как TRBC1 и TRBC2. Во время реаранжировки гена TCR, J-область рекомбинирует или с TRBC1, или с TRBC2. Эта реаранжировка является постоянной. T-клетки экспрессируют много копий одиночного TCR на поверхности, таким образом, каждая Т-клетка будет экспрессировать TCR, у которого константная область β-цепи кодируется или TRBC1, или TRBC2.
Фигура 3: Выравнивание TRBC1 и TRBC2 человека на аминокислотном уровне. Константные цепи TCRβ, кодируемые TRBC1 и TRBC2, различаются только по четырем аминокислотам: K/N в положении 3 TRBC, N/K в положении 4 TRBC; F/Y в положении 36 TRBC; V/E в положении 135 TRBC.
Фигура 4: Однозначная демонстрация того, что антитело JOVI-1 связывается с TRBC1, а не с TRBC2. Использовали генетическую инженерию клеток для однозначного доказательства того, что моноклональное антитело JOVI-1 распознает вариант TRBC1 константной цепи TCRβ. Получали трехцистронную ретровирусную кассету. Она кодирует обе цепи TCRα и TCRβ человеческого TCR, который распознает минорный антиген гистосовместимости антиген HA1, вместе с укороченным человеческим CD34 в качестве подходящего маркерного гена. HA1 TCR исходно представляет собой TRBC2. Получали вторую ретровирусную кассету, которая была идентична первой, за исключением того, что четыре остатка в константной области TCRβ, которые отличают TRBC1 от TRBC2, были заменены на остатки, кодируемые TRBC1. T-клетки Юркат, нокаутные по обеим цепям TCRα и TCRβ, трансдуцировали одним из двух векторов. Эти клетки окрашивали или пан-TCR/CD3 антителом, или моноклональным JOVI-1, конъюгированным вместе с антителами против CD34, и анализировали в проточном цитометре. Верхний ряд демонстрирует окрашивание пан-TCR/CD3 антителом по сравнению с CD34 (маркером трансдукции), нижний ряд демонстрирует окрашивание JOVI-1 по сравнению с CD34. Трансдуцированные клетки демонстрируют сходное окрашивание TCR/CD3, но только TRBC1-положительные клетки окрашиваются JOVI-1. Таким образом, JOVI-1 является специфическим антителом для TRBC1, и, более того, возможно использовать антитело для различения TRBC1 и двух TCR.
ФИГУРА 5: Моноклональное антитело JOVI-1 отличает TRBC1 от TRBC2, распознавая остатки 3 и 4 в TRBC. Для точного определения того, как JOVI-1 отличает TRBC1 от TRBC2, вышеописанная конструкция TRBC2 TCR HA1 была мутирована для получения двух гибридов TRBC1/2. Дополнительный вариант получали таким образом, что только остатки 3 и 4 константной цепи TCRβ были заменены с остатков TRBC2 на остатки TRBC1. Получали дополнительный вариант, в котором только остаток 36 был изменен с остатка TRBC2 на остаток TRBC1. T-клетки Юркат, нокаутные по TCR, трансдуцировали этими новыми конструкциями. В качестве контролей использовали исходные клетки Юркат, трансдуцированные TRBC2 и TRBC1 и описанные в фигуре 4. T-клетки Юркат окрашивали JOVI-1 и анализировали в проточном цитометре. Окрашивание JOVI-1 перекрывалось с окрашиванием T-клеток Юркат, нокаутных по TCR и не трансдуцированных TCR. JOVI-1 окрасило клетки Юркат, экспрессирующие TRBC1 TCR, а не TRBC2 TCR. JOVI-1 окрасило TRBC1/гибрид 2, в котором только TRBC остатки 3 и 4 TRBC были из TRBC1. JOVI-1 не окрасило T-клетки Юркат, в которых только остаток 36 TRBC был из TRBC1.
ФИГУРА 6: Пример Т-клеточной экспрессии TRBC1 у здорового донора. Мононуклеарные клетки периферической крови здорового донора окрашивали антителами против CD3, CD4, CD8 и JOVI-1 и анализировали путем проточной цитометрии. Популяции Т-клеток CD4+ и CD8+ показаны на верхней панели. Каждая из этих популяций дала сигнал выше порогового значения, и прямое рассеяние относительно окрашивания JOVI-1 показано на осях Y и X, соответственно. Эти данные показывают, что оба компартмента, CD4+ и CD8+, содержат клетки, которые являются TRBC1-положительными и -отрицательными. Это репрезентативные данные от одного донора.
Фигура 7: TRBC1+ T-клетки у нескольких здоровых доноров. Производили забор крови у десяти здоровых доноров и окрашивали мононуклеарные клетки периферической крови, как описано выше в фигуре 4. Совокупные данные доли TRBC1 T-клеток в обоих компартментах, CD4 и CD8, показаны на линейчатой диаграмме вместе с медианой и интервалом. Все доноры имели компартменты TRBC1+ и TRBC1-. Медиана TRBC1+ клеток в %=36%.
Фигура 8: Клеточные линии, полученные из Т-клеточного злокачественного новообразования, окрашены JOVI-1. Было получено несколько клеточных линий из Т-клеточных злокачественных новообразований. Многие из этих клеточных линий все еще экспрессируют TCR. Мы выбрали для исследования клетки Юркат (клеточная линия Т-клеточной лейкемии), HPB-ALL (другая клеточная линия Т-клеточной лейкемии) и HD-Mar-2 (клеточная линия Т-клеточной лимфомы). Путем окрашивания этих клеточных линий пан-TCR/CD3 антителом, мы смогли продемонстрировать, что все три линии экспрессируют TCR (левые панели, окрашивание перекрывается с контрольным окрашиванием изотипов). Затем, путем окрашивания JOVI-1 мы смогли определить, что эти T-клеточные линии либо TRBC1-отрицательные, либо TRBC1-положительные. Только клетки Юркат (TRBC1+), а не клетки HPB-ALL или HD-Mar-2 (TRBC2+), окрашивались JOVI-1, подтверждая исключительную экспрессию или TRBC1, или TRBC2.
Фигура 9: Селективный лизис TRBC1 T-клеток моноклональным антителом (МАТ) JOVI-1. T-клетки Юркат дикого типа (CD34-, TRBC1+) смешивали с Т-клетками Юркат, нокаутными по TCRαβ и трансдуцированными TRBC2 с коэкспрессией маркерного гена CD34 (CD34+TRBC2+). Эти клетки инкубировали с JOVI-1 по отдельности, или инкубировали с JOVI-1 и комплементом в течение 1 часа. Клетки отмывали и окрашивали по CD34, аннексину V и 7-аминоактиномицину (7-AAD). Клетки анализировали проточной цитометрией. Ниже показана экспрессия CD34 в живой популяции, определенной по отрицательному аннексину-V и слабой экспрессии 7-AAD. (a) JOVI-1 отдельно; (b) JOVI-1 с комплементом. Наблюдали селективный лизис TRBC1 T-клеток (CD34-).
Фигура 10: Поликлональные Т-клетки, специфичные к вирусу Эпштейна-Барр (EBV), можно разделить на две приблизительно равные популяции TRBC1/2. С использованием общепринятых способов, авторы изобретения избирательно нарастили T-клетки, специфичные к EBV, из периферической крови здорового донора. Последующая линия имела высокую степень селективности против аутологичных В-клеток, зараженных EBV (аутолимфобластные клеточные линии, ауто-ЛКЛ), и не проявляла активности против аллогенных Т-клеток, зараженных EBV (алло-ЛКЛ), и не имела неспецифической активности естественных киллеров (при измерении тестом против клеток K562). Такая линия является репрезентативной для донорского иммунитета к EBV. (b) При окрашивании JOVI-1 эти T-клетки типируются в равных долях, как TRBC1 и TRBC2.
Фигура 11: Аннотированная последовательность VH и VL JOVI-1. Гипервариабельные области подчеркнуты и выделены жирным шрифтом.
Фигура 12: Демонстрация того, что периферическая Т-клеточная лимфома ограничена по TRBC, а нормально циркулирующие T-клетки - нет. Получали T-клетки из периферической крови пациента с циркулирующими клетками Т-клеточной лимфомы. Периферические мононуклеарные клетки выделяли и окрашивали при помощи панели антител, включающей CD5, TCR и JOVI-1. Нормальные и злокачественные T-клетки можно было различить в цитометре по интенсивности экспрессии CD5. Яркий CD5 (нормальные T-клетки) имели приблизительно равные популяции TRBC1 и 2. Популяции с промежуточной яркостью и слабой яркостью CD5 (опухоль) были все TRBC2-позитивные. Если бы этот пациент получал TRBC2-направленную терапию, лимфома была бы уничтожена, и приблизительно половина T-клеток была бы сохранена.
Фигура 13: Демонстрация того, что VH и VL полученные из JOVI-1 верны, и что они могут складываться в виде одноцепочечного вариабельного фрагмента. Использовали супернатант исходной гибридомы, рекомбинантное антитело JOVI-1 и scFv-Fc, произведенный трансфецированными клетками 293T для окрашивания ряда клеточных линий: Юркат, нокаутных по TCR, Юркат дикого типа, Юркат, нокаутных по TCR и трансдуцированных TRBC1 TCR в векторе с совместной экспрессией eBFP2, Юркат, нокаутных по TCR и трансдуцированных TRBD2 TCR в векторе с совместной экспрессией eBFP2. Окрашивание анализировали проточной цитометрией. И рекомбинантное антитело, и scFv связались с клетками, экспрессирующими TRBC2.
Фигура 14: CAR на основе JOVI-1 в различных форматах. CAR, как правило, содержат связывающий домен, спейсер, трансмембранный домен и домен для внутриклеточной передачи сигнала. В этом исследовании получали CAR, которые содержат scFv JOVI-1, спейсер, полученный или из «стебля» CD8, домена шарнир-CH2-CH3 человеческого IgG1 с мутациями, которые исключают связывание с FcR; или спейсер, полученный из IgG1 человека.
Фигура 15: Функция CAR на основе JOVI-1. T-клетки из периферической крови здорового донора трансдуцировали различными вышеописанными CAR. T-клетки также трансдуцировали CAR, специфичным к CD19, в качестве контроля. Эти T-клетки затем объединяли с клетками-мишенями: Юркат, нокаутными по TCR, и Юркат дикого типа и клетками Раджи (линия CD19+ В-клеточной лимфомы). Данные по высвобождению хрома показаны для эффекторов против различных мишеней. T-клетки с CAR JOVI-1 лизировали клетки Юркат, но не клетки Раджи и клетки Юркат, нокаутные по TCR.
Фигура 16: Самоочищение T-клеточных культур с CAR JOVI-1. Поскольку T-клетки содержат приблизительно равное количество T-клеток, позитивных или по TRBC1, или по TRBC2, возможно, что после введения CAR может происходить определенное количество «братоубийства» или самоочищения культуры. Было показано, что это имело место. В этом примере, T-клетки с CAR окрашивали после трансдукции и анализировали проточной цитометрией. При сравнении суррогатно трансдуцированных и трансдуцированных клеток можно наблюдать, что Т-клеточная популяция теряет TRBC1-позитивные T-клетки.
Фигура 17: Исследование клональности Т-клеточной лейкемии из больших гранулярных лимфоцитов (ТЛ-БГЛ) -Пациент A
Фигура 18: Исследование клональности Т-клеточной лейкемии из больших гранулярных лимфоцитов (ТЛ-БГЛ) -Пациент B
Фигура 19: Исследование клональности Т-клеточной лейкемии из больших гранулярных лимфоцитов (ТЛ-БГЛ) -Пациент C
Фигура 20: Исследование клональности поликлональной Т-клеточной лимфомы (ПКТЛ) -Пациент D
Фигура 21: Стратегии отбора фагов по пептидам TRBC. A) Два раунда отбора фагового дисплея на твердой фазе по пептидам TRBC, иммобилизованных на поверхности прямо или опосредованно. B) Три раунда отбора фагового дисплея в жидкой фазе по биотинилированным пептидам TRBC.
Фигура 22: Анализ результатов по поликлональным фагам из отборов фагового дисплея по пептидам TRBC. Анализ связывания посредством TRF с использованием поликлонального фага из отборов на твердой фазе проводили на пептидах TRBC, непосредственно иммобилизованных в виде конъюгатов БСА/OA (A), отборы на твердой фазе по пептидам TRBC, иммобилизованным на стрептавидине/нейтравидине (B) и из отборов в жидкой фазе (C).
фигура 23: Схематическое представление вектора pSANG10-3F вектор. Ген, кодирующий одноцепочечное антитело (scFv), клонируют по сайту NcoI/NotI после промотора T7 и лидерной последовательности pelB (для периплазматической транслокации). Вектор также содержит C-концевую гекса-гистидиновую метку (His6) для очистки и три-FLAG метку для детекции.
Фигура 24: Первичный скрининг агентов, специфически связывающихся с TRBC1 и TRBC2. Связывание девяносто четырех scFv из отборов по TRBC1 (A) и TRBC2 (B) с биотинилированными TRBC1 и TRBC2 (0,5 мкг/мл), иммобилизованными на 96-луночных планшетах Nunc Maxisorp™, покрытых нейтравидином (10 мкг/мл). Связывание scFv с иммобилизованными пептидами определяли с использованием антитела к FLAG, конъюгированного с европием.
Фигура 25: Связывание сыворотки с поликлональными антителами от кролика #13174, иммунизированного TRBC1, с пептидами TRBC1 и TRBC2. (A) После третьей иммунизации (B) После третьей иммунизации и очистки TRBC1-специфичных антител.
Фигура 26: Связывание сыворотки с поликлональными антителами от кролика #17363, иммунизированного пептидом TRBC2, с пептидами TRBC1 и TRBC2. (A) После третьей иммунизации (B) После третьей иммунизации и очистки TRBC2-специфичных антител.
Фигура 27: Связывание сыворотки с поликлональными антителами от кролика #17364, иммунизированного пептидом TRBC2, с пептидами TRBC1 и TRBC2. (A) После третьей иммунизации (B) После третьей иммунизации и очистки TRBC2-специфичных антител.
СУЩНОСТЬ АСПЕКТов ИЗОБРЕТЕНИЯ
Авторы настоящего изобретения разработали способ, за счет которого возможно истощить популяцию злокачественных T-клеток у индивидуума, не затрагивая значительную часть здоровых T-клеток. В частности, они разработали химерные антигенные рецепторы (CAR), специфичные для TRBC1 и TRBC2, для применения в лечении Т-клеточных злокачественных новообразований.
Таким образом, в первом аспекте настоящее изобретение относится к химерному антигенному рецептору (CAR), который содержит антигенсвязывающий домен, селективно связывающийся с константной областью 1 TCR-бета (TRBC1) или TRBC2.
В первом варианте осуществления первого аспекта изобретения предлагается CAR, который селективно связывается с TRBC1. В этом варианте осуществления CAR может содержать антигенсвязывающий домен, который имеет вариабельную область тяжелой цепи (VH) и вариабельную область легкой цепи (VL), которые содержат следующие определяющие комплементарность области (CDR):
VH CDR1: SEQ ID No. 7;
VH CDR2: SEQ ID No. 8;
VH CDR3: SEQ ID No. 9;
VL CDR1: SEQ ID No. 10;
VL CDR2: SEQ ID No. 11; и
VL CDR3: SEQ ID No. 12.
CAR может содержать антигенсвязывающий домен, который имеет вариабельную область тяжелой цепи (VH) с последовательностью, показанной в виде SEQ ID No. 1 и вариабельную область легкой цепи (VL) с последовательностью, показанной в виде SEQ ID No. 2.
CAR может содержать антигенсвязывающий домен, который включает scFv с аминокислотной последовательностью, показанной в виде SEQ ID No. 3.
CAR может содержать аминокислотную последовательность, выбранную из SEQ ID No. 33, 34 и 35.
CAR может содержать CDR3 VH и/или CDR3 VL из перечисленных в таблице 1.
CAR может включать антитело или его функциональный фрагмент, который содержит:
(i) CDR3 тяжелой цепи и/или CDR3 легкой цепи;
(ii) CDR1, CDR2 и CDR3 тяжелой цепи и/или CDR1, CDR2 и CDR3 легкой цепи; или
(iii) вариабельную область тяжелой цепи (VH) и/или вариабельную область легкой цепи (VL);
из одного из scFv, показанных в виде SEQ ID No. от 13 до 22.
Во втором варианте осуществления первого аспекта изобретения предлагается CAR, который селективно связывается с TRBC2.
В связи с этим вариантом осуществления, CAR может содержать CDR3 VH и/или CDR3 VL из перечисленных в таблице 2.
CAR может включать антитело или его функциональный фрагмент, который содержит:
(i) CDR3 тяжелой цепи и/или CDR3 легкой цепи;
(ii) CDR1, CDR2 и CDR3 тяжелой цепи и/или CDR1, CDR2 и CDR3 легкой цепи; или
(iii) вариабельную область тяжелой цепи (VH) и/или вариабельную область легкой цепи (VL);
из одного из scFv, показанных в виде SEQ ID No. от 23 до 32.
Во втором аспекте, настоящее изобретение относится к последовательности нуклеиновой кислоты, кодирующей CAR по первому аспекту изобретения.
В третьем аспекте, предлагается вектор, который содержит последовательность нуклеиновой кислоты по второму аспекту изобретения.
В четвертом аспекте, предлагается клетка, которая содержит CAR по первому аспекту изобретения. Клетка может быть цитолитической иммунной клеткой, такой как Т-клетка или клеткой-естественным киллером (NK).
В пятом аспекте предлагается способ для получения клетки по четвертому аспекту изобретения, который включает этап трансдукции или трансфекции клетки последовательностью нуклеиновой кислоты по второму аспекту изобретения или вектором по третьему аспекту изобретения.
В шестом аспекте предлагается клетка по четвертому аспекту изобретения для применения в способе лечения Т-клеточной лимфомы или лейкемии у индивидуума, который включает этап введения клетки, содержащей TCRB1- или TCRB2-селективный CAR индивидууму, для того чтобы вызвать селективное истощение популяции злокачественных T-клеток, вместе с нормальными T-клетками, экспрессирующими ту же TRBC, что и злокачественные T-клетки, но не вызвать истощение популяции нормальных T-клеток, экспрессирующих TRBC, которая не экспрессируется злокачественными T-клетками.
Способ может также включать этап исследования константной области TCR-бета (TCRB) злокачественной Т-клетки от индивидуума, чтобы определить, экспрессирует она TRBC1 или TRBC2.
Также предлагается способ лечения Т-клеточной лимфомы или лейкемии у индивидуума, который включает этап введения TCRB1- или TCRB2-селективного агента индивидууму, где агент вызывает селективное истощение популяции злокачественных T-клеток, вместе с нормальными T-клетками, экспрессирующими ту же TRBC, что и злокачественные T-клетки, но не вызывает истощение популяции нормальных T-клеток, экспрессирующих TRBC, которая не экспрессируется злокачественными T-клетками.
В первом варианте осуществления этого аспекта изобретения, агент представляет собой TCRB1-селективный агент. Во втором варианте осуществления этого аспект изобретения, агент представляет собой TCRB2-селективный агент.
Способ может также включать перед этапом введения этап исследования константной области TCR-бета (TCRB) злокачественной Т-клетки от индивидуума, чтобы определить, экспрессирует она TRBC1 или TRBC2.
Агент может быть истощающим моноклональным антителом или его фрагментом. Агент может быть конъюгированным антителом, которое может содержать химиотерапевтическую часть.
Агент может быть биспецифическим Т-клеточным активатором. Агент может быть химерным антигенным рецептором (CAR), который экспрессируется Т-клетками. CAR может содержать аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID No. 33, 34 и 35.
Агент может содержать антитело JOVI-1 или его функциональный фрагмент.
Агент может содержать антитело или его функциональный фрагмент с вариабельной областью тяжелой цепи (VH) и вариабельной областью легкой цепи (VL), которые содержат следующие определяющие комплементарность области (CDR):
VH CDR1: SEQ ID No. 7;
VH CDR2: SEQ ID No. 8;
VH CDR3: SEQ ID No. 9;
VL CDR1: SEQ ID No. 10;
VL CDR2: SEQ ID No. 11; и
VL CDR3: SEQ ID No. 12.
Агент может содержать антитело или его функциональный фрагмент с вариабельной областью тяжелой цепи (VH) с аминокислотной последовательностью, показанной в виде SEQ ID No. 1, и вариабельную область легкой цепи (VL) с аминокислотной последовательностью, показанной в виде SEQ ID No. 2.
Агент может содержать ScFv с аминокислотной последовательностью, показанной в виде SEQ ID No. 3. Агент может быть предложен в виде фармацевтической композиции.
Т-клеточную лимфому или лейкемию можно выбирать из периферической Т-клеточной лимфомы, неуточненной (ПТКЛ-НУ); ангиоиммунобластной Т-клеточной лимфомы (АИТКЛ), анапластической крупноклеточной лимфомы (АККЛ), Т-клеточной лимфомы, ассоциированной с энтеропатией (ТКЛЭ), гепатоспленической Т-клеточной лимфомы (ГСТЛ), экстранодальной NK/Т-клеточной лимфомы назального типа, Т-клеточной лимфомы кожи, первичной АККЛ кожи, Т-клеточной пролимфоцитарной лейкемии и Т-клеточной острой лимфобластной лейкемии.
Настоящее изобретение также относится к агенту для применения в лечении Т-клеточной лимфомы или лейкемии согласно такому способу.
Настоящее изобретение также относится к набору, содержащему агент для применения в вышеописанном качестве.
Настоящее изобретение также относится к использованию агента для производства лекарственного средства для лечения Т-клеточной лимфомы или лейкемии по вышеописанному способу.
Настоящее изобретение также относится к способу для диагностики Т-клеточной лимфомы или лейкемии у индивидуума, который включает этап определения процента Т-клеток, которые являются TRBC1- или TRBC2-положительными, от общего числа T-клеток в образце.
Процентное содержание TRBC1- или TRBC2-положительных T-клеток, которое составляет больше чем приблизительно 80%, может указывать на наличие Т-клеточной лимфомы или лейкемии.
Образец может быть образцом периферической крови или биопсией.
Агент, который связывается со всеми T-клетками, может связываться с CD3.
ПОДРОБНОЕ ОПИСАНИЕ
Настоящее изобретение относится к агентам, таким как химерные антигенные рецепторы (CAR), которые селективно связываются с TRBC1 или TRBC2. Такие агенты пригодны для способов лечения Т-клеточной лимфомы или лейкемии у индивидуума. Т-клеточные злокачественные новообразования являются клональными, поэтому они экспрессируют либо TRBC1, либо TRBC2. При введении TCRB1- или TCRB2-селективного агента индивидууму, агент вызывает селективное истощение популяции злокачественных T-клеток, вместе с нормальными T-клетками, экспрессирующими ту же TRBC, что и злокачественные T-клетки, но не вызывает истощение популяции нормальных T-клеток, экспрессирующих TRBC, которая не экспрессируется злокачественными T-клетками.
КОНСТАНТНАЯ ОБЛАСТЬ TCR β (TRBC)
Т-клеточный рецептор (TCR) экспрессируется на поверхности T-лимфоцитов и отвечает за распознавание антигенов, связанных с молекулами главного комплекса гистосовместимости (MHC). Когда TCR взаимодействует с антигенным пептидом и MHC (пептид/MHC), T-лимфоцит активируется посредством серии биохимических событий, которые опосредуются связанными с ними ферментами, ко-рецепторами, специализированными адапторными молекулами и активированными или высвобожденными факторами транскрипции.
TCR представляет собой закрепленный в мембране гетеродимер, соединенный дисульфидными связями, который в норме состоит из высоко вариабельных альфа (α) и бета (β) цепей, экспрессирующихся как часть комплекса с неизменяющимися молекулами цепей CD3. T-клетки, экспрессирующие этот рецептор обозначают как α:β (или αβ) T-клетки (~95% от общего числа T-клеток). Меньшая часть T-клеток экспрессирует альтернативный рецептор, образованный вариабельными цепями гамма (γ) и дельта (δ), и обозначается как γδ T-клетки (~5% от общего числа T-клеток).
Каждая α и β цепь состоит из двух внеклеточных доменов: вариабельной области (V) и константной области (C), оба относятся к доменам иммуноглобулинового суперсемейства, образующим антипараллельные β-складки. Константная область расположена проксимально по отношению к клеточной мембране, затем следует трансмембранная область и короткий цитоплазматический хвост, в то время как вариабельная область связывается с комплексом пептид/MHC (см. фигура 1). Константная область TCR состоит из коротких соединительных последовательностей, в которых остаток цистеина образует дисульфидные связи, которые соединяют две цепи.
Вариабельные домены и α-цепи, и β-цепи TCR имеют три гипервариабельные или определяющие комплементарность области (CDR). Вариабельная область β-цепи также имеет дополнительную область гипервариабельности (HV4), однако, в норме она не контактирует с антигеном и, таким образом, не рассматривается как CDR.
TCR также содержит до пяти неизменяемых цепей γ,δ,ε (в совокупности обозначаемых CD3) и ζ. Субъединицы CD3 и ζ опосредуют передачу сигнала с TCR через специфические цитоплазматические домены, которые взаимодействуют с молекулами-вторичными мессенджерами и адапторными молекулами после распознавания антигена посредством αβ или γδ. Экспрессии комплекса TCR на поверхности клетки предшествует парная сборка субъединиц, в которой играют роль и трансмембранные, и внеклеточные домены α и β TCR, и γ и δ CD3.
TCR, таким образом, обычно состоит из комплекса CD3 и α- и β-цепей TCR, которые, в свою очередь состоят из вариабельных и константных областей (фигура 1).
Локус (Chr7:q34), который поставляет β-константную область TCR (TRBC) был дуплицирован в ходе эволюционной истории с получением двух практически идентичных и функционально эквивалентных генов: TRBC1 и TRBC2 (фигура 2), которые различаются только по четырем аминокислотам в зрелом белке, производимом обоими генами (фигура 3). Каждый TCR будет содержать, взаимоисключающим образом, или TRBC1 или TRBC2, и по существу, каждая αβ Т-клетка будет экспрессировать или TRBC1, или TRBC2, взаимоисключающим образом.
Авторы настоящего изобретения установили, что, несмотря на сходство между последовательностью TRBC1 и TRBC2, их возможно различить. Авторы изобретения также установили, что аминокислотные последовательности TRBC1 и TRBC2 можно различать, когда они находятся in situ на поверхности клетки, например, Т-клетки.
ЗЛОКАЧЕСТВЕННЫЕ КЛЕТКИ
Термин «злокачественный» применяют в настоящем документе в соответствии с его стандартным значением по отношению к клетке, у которой отсутствует самоограничение по росту, которая может быть способна прорастать в соседние ткани и может быть способна распространяться в отдаленную ткань. По существу, термин «злокачественная Т-клетка» применяют в настоящем документе для обозначения клонально разрастающейся Т-клетки в отношении лимфомы или лейкемии.
Способ по настоящему изобретению включает определение TRBC злокачественной Т-клетки. Его можно проводить с использованием известных в данной области способов. Например, можно определять при помощи способов ПЦР, вестерн-блоттинга, проточной цитометрии или флуоресцентной микроскопии.
После того, как определен TRBC, экспрессируемый злокачественной Т-клеткой, индивидууму вводят соответствующий TRBC1- или TRBC2-селективный агент. «Соответствующий TRBC-селективный агент» означает, что если определяют, что злокачественная Т-клетка экспрессирует TRBC1, то вводят TRBC1-селективный агент, в то время как если определяют, что злокачественная Т-клетка экспрессирует TRBC2, то вводят TRBC2-селективный агент.
СЕЛЕКТИВНЫЙ АГЕНТ
Селективный агент связывается или с TRBC1, или с TRBC2, взаимоисключающим образом.
Как указано выше, каждая αβ Т-клетка экспрессирует TCR, который содержит или TRBC1, или TRBC2. При клональном Т-клеточном нарушении, таком как Т-клеточная лимфома или лейкемия, злокачественные T-клетки, происходящие из одного клона, будут все экспрессировать или TRBC1, или TRBC2.
Таким образом, настоящий способ включает этап введения TRBC1- или TRBC2-селективного агента индивидууму, где агент вызывает селективное истощение популяции злокачественных T-клеток, вместе с нормальными T-клетками, которые экспрессируют такую же TRBC, что и злокачественные T-клетки, но не вызывает значительного истощения популяции нормальных T-клеток, экспрессирующих TRBC, отличную от TRBC злокачественных T-клеток.
Поскольку TRBC-селективный агент не вызывает значительного истощения популяции нормальных T-клеток, экспрессирующих TRBC, отличную от TRBC злокачественных T-клеток, он не вызывает истощения всего компартмента Т-клеток. Сохранение части Т-клеточного компартмента индивидуума (т.е. T-клеток, которые не экспрессируют такую же TRBC, что и злокачественные Т-клетки) приводит к уменьшению токсичности и снижению клеточного и гуморального иммунодефицита, а, следовательно, снижению риска инфицирования.
Введение TRBC1-селективного агента в соответствии со способом по настоящему изобретению может приводить к 5, 10, 20, 50, 75, 90, 95 или 99% истощению, т.е. уменьшению числа T-клеток, экспрессирующих TRBC1.
Введение TRBC2-селективного агента в соответствии со способом по настоящему изобретению может приводить к 5, 10, 20, 50, 75, 90, 95 или 99% истощению, т.е. уменьшению числа T-клеток, экспрессирующих TRBC2.
TRBC1-селективный агент может связываться с TRBC1 с аффинностью, по меньшей мере, в 2, 4, 5, 7 или 10 раз большей, чем с TRBC2. Аналогично, TRBC2-селективный агент может связываться с TRBC2 с аффинностью, по меньшей мере, в 2, 4, 5, 7 или 10 раз большей, чем с TRBC1.
TRBC1-селективный агент вызывает истощение большей доли TRBC1-экспрессирующих T-клеток в клеточной популяции, чем TRBC2-экспрессирующих клеток. Например, соотношение истощения TRBC1-экспрессирующих T-клеток к TRBC2-экспрессирующим клеткам может составлять, по меньшей мере, 60%:40%, 70%:30%, 80%:20%, 90%:10% или 95%:5%. Аналогично, TRBC2-селективный агент вызывает истощение большей доли TRBC2-экспрессирующих T-клеток в клеточной популяции, чем TRBC1-экспрессирующих клеток. Например, соотношение истощения TRBC2-экспрессирующих T-клеток к TRBC1-экспрессирующим клеткам может составлять, по меньшей мере, 60%:40%, 70%:30%, 80%:20%, 90%:10% или 95%:5%.
При помощи способа по изобретению у индивидуума удаляют злокачественные T-клетки, не затрагивая значительную долю здоровых Т-клеток. Под «значительной долей» подразумевают, что выживает доля T-клеток, экспрессирующих TRBC, отличную от TRBC злокачественных T-клеток, достаточная для того чтобы поддержать Т-клеточную функцию у индивидуума. Агент может вызывать истощение менее чем 20%, 15%, 10% или 5% Т-клеточной популяции, экспрессирующей другую TRBC.
Селективный агент может быть селективным или для TRBC1, или для TRBC2, поскольку он отличает остатки, как перечислено ниже:
(i) N от K в положении 3 TRBC;
(ii) K от N в положении 3 TRBC;
(iii) K от N в положении 4 TRBC;
(iv) N от K в положении 4 TRBC;
(v) F от Y в положении 36 TRBC;
(vi) Y от F в положении 36 TRBC;
(vii) V от E в положении 135 TRBC; и/или
(viii) E от V в положении 135 TRBC.
Селективный агент может различить любую комбинацию из вышеуказанных различий.
АНТИТЕЛО
Агент, применяемый в способе по настоящему изобретению, может быть истощающим моноклональным антителом (МАТ) или его функциональным фрагментом, или миметиком антитела.
Термин «истощающее антитело» применяют в общепринятом смысле по отношению к антителу, которое связывается с антигеном, присутствующим на Т-клетке-мишени и опосредует смерть Т-клетки-мишени. Введение истощающего антитела индивидууму, таким образом, приводит к снижению/уменьшению числа клеток у индивидуума, экспрессирующих целевой антиген.
Как применяют в настоящем документе, «антитело» означает полипептид с антигенсвязывающим участком, который содержит, по меньшей мере, одну определяющую комплементарность область CDR. Антитело может содержать 3 CDR и иметь антигенсвязывающий участок, который эквивалентен таковому в доменном антителе (ДАТ). Антитело может содержать 6 CDR и иметь антигенсвязывающий участок, который эквивалентен таковому у классической молекулы антитела. Остальная часть полипептида может представлять собой любую последовательность, которая обеспечивает подходящий каркас для антигенсвязывающего участка и располагает его подходящим образом для связывания с антигеном. Антитело может быть целой молекулой иммуноглобулина или ее частью, такой как Fab, F(ab)'2, Fv, одиночная цепь Fv (ScFv) фрагмента или нанотело. Антитело может быть бифункциональным антителом. Антитело может представлять собой антитело, не принадлежащее человеку, химерное, гуманизированное или полностью человеческое антитело.
Антитело, таким образом, может быть любым функциональным фрагментом, который сохраняет антигенную специфичность полноразмерного антитела.
TRBC1-СЕЛЕКТИВНЫЕ АНТИТЕЛА
Агент для применения в способе по настоящему изобретению может содержать антитело или его функциональный фрагмент с вариабельной областью тяжелой цепи (VH) и вариабельной областью легкой цепи (VL), которая включает одну или несколько из следующих определяющих комплементарность областей (CDR):
VH CDR1: GYTFTGY (SEQ ID No. 7);
VH CDR2: NPYNDD (SEQ ID No. 8);
VH CDR3: GAGYNFDGAYRFFDF (SEQ ID No. 9);
VL CDR1: RSSQRLVHSNGNTYLH (SEQ ID No. 10);
VL CDR2: RVSNRFP (SEQ ID No. 11); и
VL CDR3: SQSTHVPYT (SEQ ID No. 12).
Одна или несколько CDR, каждая независимо, могут содержать или не содержать одну или несколько аминокислотных мутаций (например, замен) по сравнению с последовательностями, приведенными в SEQ ID No. с 7 до 12, при условии, что полученное антитело сохраняет способность селективно связываться с TRBC1.
Исследования показали, что CDR L3 и H3 преимущественно отвечают за высокоэнергетические взаимодействия с антигеном, таким образом, антитело или его функциональный фрагмент может содержать CDR3 VH и/или CDR3 VL, описанную выше.
При помощи фагового дисплея были идентифицированы несколько дополнительных связывающих доменов антител, которые являются высокоселективными для связывания TRBC1 по сравнению с TRBC2, как описано в примере 12.
Агент может содержать антитело или его функциональный фрагмент с вариабельной областью тяжелой цепи (VH) и/или вариабельной областью легкой цепи (VL), которая включает одну или несколько определяющих комплементарность областей (CDR3), показанных в таблице 1.
Таблица 1
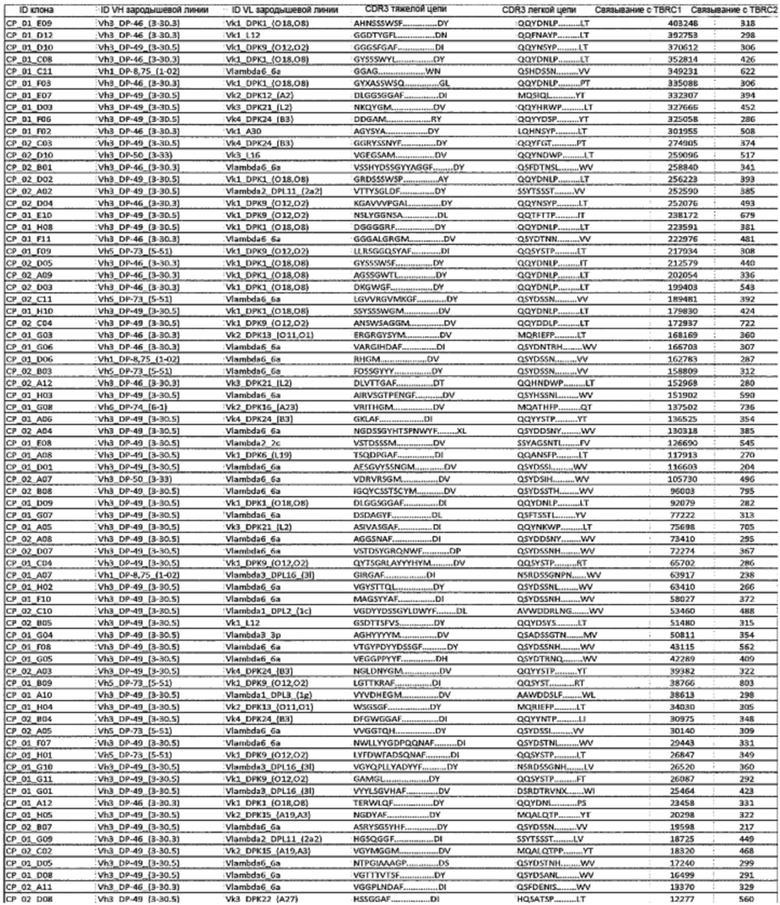
Если агент представляет собой доменное антитело, он может содержать 3 CDR, т.е. или CDR1-CDR3 VH, или CDR1-CDR3 VL.
Агент может содержать антитело или его функциональный фрагмент, который содержит вариабельную область тяжелой цепи (VH) с аминокислотной последовательностью, показанной в виде SEQ ID No. 1, и вариабельную область легкой цепи (VL) с аминокислотной последовательностью, показанной в виде SEQ ID No. 2.
SEQ_ID_1 Jovi-1 VH
EVRLQQSGPDLIKPGASVKMSCKASGYTFTGYVMHWVKQRPGQGLEWIGFINPYNDDIQSNERFRGKATLTSDKSSTTAYMELSSLTSEDSAVYYCARGAGYNFDGAYRFFDFWGQGTTLTVSS
SEQ_ID_2 Jovi-1 VL
DVVMTQSPLSLPVSLGDQASISCRSSQRLVHSNGNTYLHWYLQKPGQSPKLLIYRVSNRFPGVPDRFSGSGSGTDFTLKISRVEAEDLGIYFCSQSTHVPYTFGGGTKLEIKR
Агент может содержать ScFv с аминокислотной последовательностью, показанной в виде SEQ ID No. 3.
SEQ_ID_3 Jovi-1 scFv
EVRLQQSGPDLIKPGASVKMSCKASGYTFTGYVMHWVKQRPGQGLEWIGFINPYNDDIQSNERFRGKATLTSDKSSTTAYMELSSLTSEDSAVYYCARGAGYNFDGAYRFFDFWGQGTTLTVSSGGGGSGGGGSGGGGSDVVMTQSPLSLPVSLGDQASISCRSSQRLVHSNGNTYLHWYLQKPGQSPKLLIYRVSNRFPGVPDRFSGSGSGTDFTLKISRVEAEDLGIYFCSQSTHVPYTFGGGTKLEIKR
Альтернативно, агент может содержать антитело или его функциональный фрагмент, который включает:
(i) CDR3 тяжелой цепи и/или CDR3 легкой цепи;
(ii) CDR1, CDR2 и CDR3 тяжелой цепи и/или CDR1, CDR2 и CDR3 легкой цепи; или
(iii) вариабельную область тяжелой цепи (VH) и/или вариабельную область легкой цепи (VL);
из одного из scFv, показанных в виде SEQ ID No. 13-22.
В последовательностях, показанных в виде SEQ ID No. 13-22, части VH и VL в последовательности показаны жирным шрифтом, а последовательности CDR1 и CDR2 для тяжелых и легких цепей подчеркнуты. Последовательности CDR3 для VH и VL приведены в таблице 1.
SEQ ID No. 13_(CP_01_E09)
QVQLVESGGGVVQPGRSLRLSCAASGFTFSSYAMHWVRQAPGKGLEWVAVISYDGSNKYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARAHNSSSWSFDYWGQGTLVTVSSGGGGSGGGGSGGGASDIQMTQSPSSLSASVGDRVTITCRASQSISSYLNWYQQKPGKAPKLLIYDASNLETGVPSRFSGSGSGTDFTFTISSLQPEDIATYYCQQYDNLPLTFGGGTKVDIKRTAAA
SEQ ID No. 14 (CP_01_D12)
EVQLLESGGGVVQPGRSLRLSCAASGFTFSSYAMHWVRQAPGKGLEWVAVISYDGSNKYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKGGDTYGFLDNWGQGTMVTVSSGGGGSGGGGSGGGASDIQMTQSPSTLSASVGDRVTITCRASQSISSWLAWYQQKPGKAPKLLIYKASSLESGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQFNAYPLTFGGGTKVEIKRTAAA
SEQ ID No. 15 (CP_01_D10)
QVQLVESGGGLVQPGRSLRLSCAASGFTFSSYAMHWVRQAPGKGLEWVAVISYDGSSKYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKGGGSFGAFDIWGQGTLVTVSSGGGGSGGGGSGGGASDIQMTQSPSSLSASVGDRVTITCRASQSISRYLNWYQQKPGKAPNLLIYAASSLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYNSYPLTFGGGTKLEIKRTAAA
SEQ ID No. 16 (CP_01_C08)
EVQLLESGGGAVQPGRSLRLSCAASGFTFSSYAMHWVRQAPGKGLEWVAVISYDGSNKYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCASGYSSSWYLDYWGQGTLVTVSSGGGGSGGGGSGGGASDIQMTQSPSSVSASVGDRVTITCQASQDISNYLNWYQQKPGKAPKLLIYDASNLETGVPSRFSGSGSGTDFTFTISSLQPEDIATYYCQQYDNLPLTFGGGTKVEIKRTAAA
SEQ ID No. 17 (CP_01_C11)
QVQLVESGAEVKKPGASVKVSCKASGYTFTGYYMHWVRQAPGQGLEWMGRINPNSGGTNYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCASGGAGWNWGQGTMVTVSSGGGGSGGGGSGGGASNFMLTQPHSVSESPGKTATISCTRSSGSIASNYVQWYQQRPGSAPTTVIYEDNQRPFGVPDRFSGSIDSSSNSASLTISGLKTEDEADYYCQSHDSSNVVFGGGTQLTVLGQPAA
SEQ ID No. 18 (CP_01_F03)
EVQLVESGGGVVQPGRSLRLSCAASGFTFSSYAMHWVRQAPGKGLEWVAVISYDGSNKYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARGY?ASSWSQGLWGQGTLVTVSSGGGGSGGGGSGGGASDIQMTQSPSSLSASVRDRVTITCQASQDISNYLNWYQQKPGKAPKLLIYDASNLETGVPSRFSGSGSGTDFTFTISSLQPEDIATYYCQQYDNLPPTFGGGTKVEIKRTAAA
SEQ ID No. 19 (CP_01_E07)
QVQLVESGGGVVQPGRSLRLSCAASGFTFSSYGMHWVRQAPGKGLEWVAVISYDGSNKYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKDLGGSGGAFDIWGQGTLVTVSSGGGGSGGGGSGGGASDIVMTQTPHSLSVTPGQPASISCKSSQSLLYSDGKTYLYWYLQKPGQPPQLLIYEVSNRFSGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCMQSIQLYTFGQGTKVDIKRTAAA
SEQ ID No. 20 (CP_01_D03)
QVQLVESGGGVVQPGRSLRLSCAAPGFTFSSYGMHWVRQAPGKGLEWVAVISYDGSNKYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARNKQYGMDVWGQGTLVTVSSGGGGSGGGGSGGGASDIVMTQSPATLSLAPGERATLSCRASQSVGSNLAWYQQKPGQAPSLLIYDASTRATGIPARFSGSGSGTDFTLTISSLQSEDIAVYYCQQYHRWPLTFGGGTKVEIKRTAAA
SEQ ID No. 21 (CP_01_F06)
EVQLLESGGGVVQPGRSLRLSCAASGFTFSSYGMHWVRQAPGKGLEWVAVISYDGSNKYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKDDGAMRYWGQGTMVTVSSGGGGSGGGGSGGGASDIQMTQSPDSLAVSLGERATINCKSSQSVLYSSNNKNYLAWYQQKPGQPPKLLIYWASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVAVYYCQQYYDSPYTFGQGTKVDIKRTAAA
SEQ ID No. 22 (CP_01_F02)
QVQLVESGGGVVQPGRPLRLSCAASGFTFSSYAMHWVRQAPGKGLEWVAVISYDGSNKYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARAGYSYADYWGQGTMVTVSSGGGGSGGGGSGGGASDIQMTQSPSSLSASVGDRVTITCRASQGIRNDLGWYQQKPGKAPKRLIYAASSLQSGVPSRFSGSGSGTEFTLTISSLQPEDFATYYCLQHNSYPLTFGGGTKVDIKRTAAA
TRBC2-СПЕЦИФИЧНЫЕ АГЕНТЫ
При помощи фагового дисплея были идентифицированы несколько дополнительных связывающих доменов антител, которые являются высокоселективными для связывания TRBC2 по сравнению с TRBC1, как описано в примере 12.
Агент может содержать антитело или его функциональный фрагмент с вариабельной областью тяжелой цепи (VH) и/или вариабельной областью легкой цепи (VL), которая включает одну или несколько определяющих комплементарность областей (CDR3), показанных в таблице 2.
Таблица 2
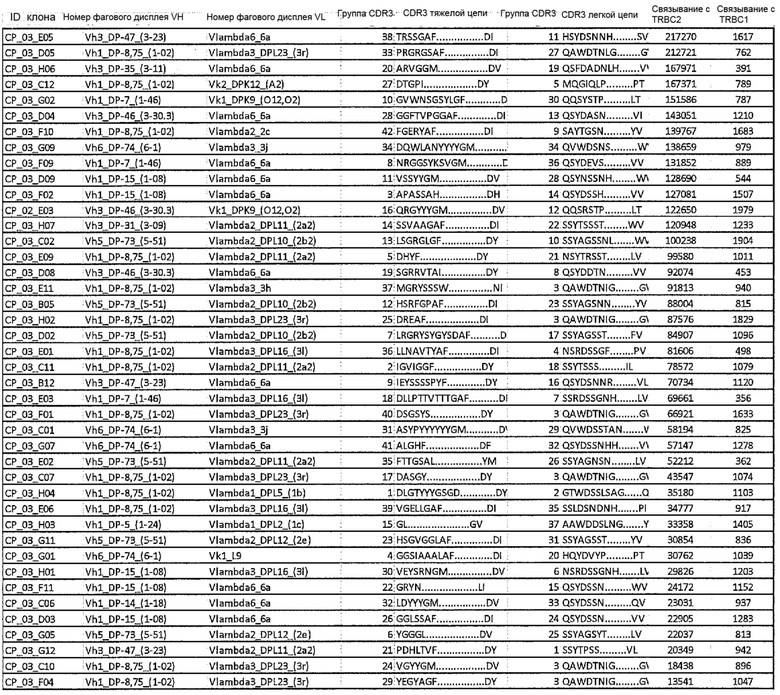
Агент может содержать антитело или его функциональный фрагмент, который включает:
(i) CDR3 тяжелой цепи и/или CDR3 легкой цепи;
(ii) CDR1, CDR2 и CDR3 тяжелой цепи и/или CDR1, CDR2 и CDR3 легкой цепи; или
(iii) вариабельную область тяжелой цепи (VH) и/или вариабельную область легкой цепи (VL);
из одного из scFv, показанных в виде SEQ ID No. 23-32.
В последовательностях, показанных в виде SEQ ID No. 23-32, части VH и VL в последовательности показаны жирным шрифтом, а последовательности CDR1 и CDR2 для тяжелых и легких цепей подчеркнуты. Последовательности CDR3 для VH и VL приведены в таблице 2.
SEQ ID No. 23 (CP_03_E05)
EVQLVESGGGVVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSAISGSGGSTYYADSVKGRFSISRDNSKNTLYLQMNSLRAEDTAVYYCARTRSSGAFDIWGQGTLVTVSSGGGGSGGGGSGGGASNFMLTQPHSVSESPGKTVTISCTRSSGSIASKYVQWYQQRPGSSPTTVIYEDNQRPSGVPDRFSGSIDTSSNSASLTISGLRTEDEADYYCHSYDSNNHSVFGGGTKVTVLGQPAA
SEQ ID No. 24 (CP_03_D05)
QVQLVESGAEVKKPGASVKVSCKASGYTFTGYYMHWVRQAPGQGLEWMGRINPNSGGTNYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCASPRGRGSAFDIWGQGTLVTVSSGGGGSGGGGSGGGASSYELTQPPSVSVSPGQTATISCSGDQLGGKYGHWYQKKPGQSPVLVLYQDRKRPAGIPERFSGSSSGNTITLTISGTQAVDEADYYCQAWDTNLGGVFGGGTKVTVLGQPAA
SEQ ID No. 25 (CP_03_H06)
QVQLVESGGGLVKPGGSLRLSCAASGFTFSDYYMSWIRQAPGKGLEWVSYISSSGSTIYYADSVEGRFTISRDNAKNSLYLQMNSLRTEDTAVYYCARARVGGMDVWGQGTMVTVSSGGGGSGGGGSGGGASNFMLTQPHSVSESPGKTVTISCTRSSGSIASNYVQWYQQRPGSSPTTVIYEDNQRPSGVPDRFSGSIDSSSNSASLTISGLKTEDEADYYCQSFDADNLHVVFGGGTKLTVLGQPAA
SEQ ID No. 26 (CP_03_C12)
EVQLVQSGAEVKKPGASVKVSCKASGYTFTGYYMHWVRQAPGQGLEWMGWINPNSGGTNYAQKFQGRVTMTRDTSISTAYMELSSLRSEDTAVYYCARDTGPIDYWGQGTMVTVSSGGGGSGGGGSGGGASDIVMTQTPLSLSVTPGQPASISCKSSQSLLHSDGKTYLYWYLQKPGQPPQLLVYEVSNRFSGVPDKFSGSGSGTDFTLKISRVEAEDVGVYYCMQGIQLPPTFGGGTKVDIKRTAAA
SEQ ID No. 27 (CP_03_G02)
EVQLVQSGAEVKKPGSSVKVSCKASGGTFSSYAISWVRQAPGQGLEWMGIINPSGGSTSYAQKFQGRVTMTRDTSTSIVYMELSSLRSEDTAVYYCARGVWNSGSYLGFDYWGQGTLVTVSSGGGGSGGGGSGGGASDIQMTQSPSSLSASVGDRVTITCQASQDISNYLNWYQQKPGKAPKLLIYAASSLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQSYSTPLTFGGGTKLEIKRTAAA
SEQ ID No. 28 (CP_03_D04)
EVQLVESGGGVVQPGRSLRLSCAASGFTFSSYAMHWVRQAPGKGLEWVAVISYDGSNKYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARGGFTVPGGAFDIWGQGTLVTVSSGGGGSGGGGSGGGASNFMLTQPHSVSDSPGKTVTISCTRSSGRIGSNFVQWYQQRPGSSPTTVIYEDDQRPSGVPARFSGSIDSSSNSASLTISGLTTADEAGYYCQSYDASNVIFGGGTKLTVLGQPAA
SEQ ID No. 29 (CP_03_F10)
EVQLVESGAEVKKPGASVKVSCKASGYTFTGYYMHWVRQAPGQGLEWMGRINPNSGGTNYAQKFQGRVTMTRDTSISTAYMELSSLRSEDTAVYYCARFGERYAFDIWGQGTLVTVSSGGGGSGGGGSGGGASQSELTQPPSASGSPGQSVTISCTGTSTDVGAFHFVSWYQHTPGKAPKLLISEVRKRASGVPDRFSGSRSGNTASLTVSGLQSEDEADYFCSAYTGSNYVFGSGTKLTVLGQPAA
SEQ ID No. 30 (CP_03_G09)
QVQLQQSGPGLVKPSQTLSLTCAISGDSVSSNSAAWNWIRQSPSRGLEWLGRTYYRSKWYNDYAVSVKSRITINPDTSKNQFSLQLNSVTPEDTAVYYCARDQWLANYYYYGMDVWGQGTLVTVSSGGGGSGGGGSGGGASSYELTQPLSVSVALGQTARITCGGNNIGSKNVHWYQQKPGQAPVLVIYRDNNRPSGIPERFSGSNSGNTATLTISKAQAGDEADYYCQVWDSNSWVFGGGTKLTVLGQPAA
SEQ ID No. 31 (CP_03_F09)
QMQLVQSGAEVKKPGASVKVSCKASGYTFASYYMHWVRQAPGQGLEWMGIINPSGGSTSYAQKFQGRVTMTRDTSTSTVYMELSRLRSDDTAVYYCASNRGGSYKSVGMDVWGQGTTVTVSSGGGGSGGGGSGGGASNFMLTQPQSVSESPGKTVTISCTRSSGNFASKYVQWYQQRPGSSPTTVIYENYQRPSGVPDRFSGSIDSSSNSATLTISGLKTEDEADYYCQSYDEVSVVFGGGTQLTVLGQPAA
SEQ ID No. 32 (CP_03_D09)
EVQLVQSGAEVKKPGSSVKVSCEASGYTFTSYAISWVRQAPGQGLEWMGWMNPNSGNTGYAQKFQGRVTMTRNTSISTAYMELSSLRSEDTAVYYCARVSSYYGMDVWGQGTLVTVSSGGGGSGGGGSGGGASNFMLTQPLSVSESPGKTVTISCTRSSGSIASNYVQWYQQRPGSAPTTVIYEDNQRPSGVPDRFSGSIDSSSNSASLTISGLKTEDEADYYCQSYNSSNHWVFGGGTKVTVLGQPAA
Варианты вышеуказанных аминокислотных последовательностей также можно использовать в настоящем изобретении, при условии, что полученное антитело связывается с TRBC1 или TRBC2 без значительного перекрестного реагирования. Как правило, такие варианты имеют высокую степень идентичности последовательности с одной из вышеуказанных последовательностей.
Способы выравнивания последовательностей для сравнения хорошо известны в данной области.
Средство поиска основного локального выравнивания (BLAST) NCBI доступно в нескольких источниках, включая Национальный центр биологической информации (NCBI, Bethesda, Md.) и Интернет, для применения в связи с программами анализа последовательностей blastp, blastn, blastx, tblastn и tblastx. Описание определения идентичности последовательности с использованием этой программы доступно на веб-сайте NCBI в Интернет.
Варианты доменов VL или VH или scFv, как правило, имеют, по меньшей мере, приблизительно 75%, например, по меньшей мере, приблизительно 80%, 90%, 95%, 96%, 97%, 98% или 99% идентичности последовательности с последовательностями, приведенными в виде SEQ ID No 1-3, 13-32.
Как правило, варианты могут содержать одну или несколько консервативных аминокислотных замен по сравнению с исходной аминокислотной последовательностью или последовательностью нуклеиновой кислоты. Консервативные замены представляют собой такие замены, которые по существу не влияют на аффинность или не снижают аффинность антитела относительно связывания с TRBC1 или TRBC2. Например, антитело человека, которое специфически связывается с TRBC1 или TRBC2, может включать до 1, до 2, до 5, до 10, или до 15 консервативных замен, в любом из или в обоих VH или VL по сравнению с любой из последовательностей, приведенных в виде SEQ ID No. 1-3 или 13-32, и сохраняет специфическое связывание с TRBC1 или TRBC2.
Функционально похожие аминокислоты, которые можно заменять путем консервативной замены, хорошо известны специалисту в данной области. Следующие шесть групп представляют собой примеры аминокислот, которые считаются консервативными заменами одна для другой: 1) Аланин (A), Серин (S), Треонин (T); 2) Аспарагиновая кислота (D), Глутаминовая кислота (E); 3) Аспарагин (N), Глутамин (Q); 4) Аргинин (R), Лизин (K); 5) Изолейцин (I), Лейцин (L), Метионин (M), Валин (V); и 6) Фенилаланин (F), Тирозин (Y), Триптофан (W).
ПОЛУЧЕНИЕ АНТИТЕЛ
Получение антител можно проводить с использованием стандартных лабораторных способов. Антитела можно получать из сыворотки животных, или, в случае моноклональных антител или их фрагментов, производить в клеточной культуре. Для получения антител можно использовать технологию рекомбинантных ДНК в соответствии с общеизвестным способом в клеточной культуре бактерий или млекопитающих.
Способы для продукции моноклональных антител хорошо известны в данной области. В кратком изложении, моноклональные антитела, как правило, производят путем слияния миеломных клеток с клетками селезенки от мыши или кролика, которые были иммунизированы желаемым антигеном. В настоящем документе, желаемый антиген представляет собой пептид TRBC1 или TRBC2, или цепь TCRβ, содержащую или TRBC1, или TRBC2.
Альтернативно, антитела и родственные молекулы, в частности scFv, можно производить вне иммунной системы путем комбинирования библиотек цепей VH и VL рекомбинантным образом. Такие библиотеки могут быть сконструированы и отобраны с использованием технологии фагового дисплея, как описано в примере 12.
ИДЕНТИФИКАЦИЯ TRBC1/TRBC2-СЕЛЕКТИВНЫХ АНТИТЕЛ
Антитела, которые являются селективными или для TRBC1, или для TRBC2, можно идентифицировать с использованием способов, которые являются стандартными в данной области. Способы для определения специфичности связывания антитела в качестве неограничивающих примеров включают иммуноферментный анализ (ELISA), вестерн-блоттинг, иммуногистохимию, проточную цитометрию, способ резонансного переноса энергии флуоресценции (FRET), библиотеки фагового дисплея, скрининги двойных гибридов дрожжей, ко-иммунопреципитацию, бимолекулярную комплементацию флуоресценции и тандемную аффинную очистку.
Для выявления антитела, которое является селективным или для TRBC1, или для TRBC2, оценивают связывание антитела с каждым из TRBC1 и TRBC2. Как правило, оценку производят, определяя связывание антитела с каждой TRBC раздельно. Антитело, которое является селективным, связывается или с TRBC1, или с TRBC2, без значительного связывания с другой TRBC.
МИМЕТИКИ АНТИТЕЛ
Агент альтернативно может быть молекулой, которая не была получена из иммуноглобулина или на его основе. Был разработан ряд "антителомиметических" сконструированных белков с повторами (DRP) для изучения связывающих свойств не-антительных полипептидов.
Белки с повторами, такие как анкирин или белки, богатые лейциновыми повторами, являются повсеместно распространенными связывающими молекулами, которые встречаются, в отличие от антител, внутри- и внеклеточно. Их уникальная модульная архитектура отличается повторяющимися структурными единицами (повторами), которые уложены вместе в стопку с образованием удлиненных доменов с повторами, выставляя вариабельные и модульные поверхности для связывания мишеней. На основании этой модульности можно получать комбинаторные библиотеки полипептидов с весьма разнообразной специфичностью связывания. DARPins (сконструированные белки с анкириновыми повторами) являются одним из примеров миметика антитела на основе этой технологии.
Для антикалинов специфичность связывания получена от липокалинов, семейства белков, которые исполняют целый ряд функций in vivo, связанных с физиологическим транспортом и хранением химически чувствительных или нерастворимых соединений. Липокалины имеют прочную внутреннюю структуру, содержащую высоко консервативный β-цилиндр, который поддерживает четыре петли на одном конце белка. Эти петли для входа в карман для связывания и конформационные различия в этой части молекулы отвечают за изменения в специфичности связывания между различными липокалинами.
Авимеры получены из большого семейства доменов внеклеточного рецептора человека при помощи перемешивания экзонов in vitro и фагового дисплея, создающих мультидоменные белки со связывающими и ингибиторными свойствами.
Версатела представляют собой небольшие белки с массой 3-5 кДа с >15% цистеинов, которые образуют каркас с высокой плотностью дисульфидов, замещая гидрофобную сердцевину, присутствующую у большинства белков. Замещение большого числа гидрофобных аминокислот, составляющих гидрофобную сердцевину, небольшим числом дисульфидов приводит к белку, который меньше по размеру, более гидрофильный, более устойчивый к протеазам и нагреванию и имеет низкую плотность Т-клеточных эпитопов. Все четыре этих свойства приводят в результате к белку со значительно сниженной иммуногенностью. Версатела можно также производить в E. coli, и они являются хорошо растворимыми и стабильными.
КОНЪЮГАТЫ
Антитело или миметик может быть конъюгатом антитела или миметика и другого агента или антитела, например конъюгат может быть детектируемой частью или химиотерапевтической частью.
Детектируемая часть может быть флуоресцентным фрагментом, например, флуоресцентным пептидом. «Флуоресцентный пептид» относится к полипептиду, который при возбуждении излучает свет на детектируемой длине волны. Примеры флуоресцентных белков в качестве неограничивающих примеров включают флуоресцеинизотиоцианат (FITC), фикоэритрин (PE), аллофикоцианин (APC), зеленый флуоресцентный белок (GFP), улучшенный GFP, красный флуоресцентный белок (RFP), синий флуоресцентный белок (BFP) и mCherry.
TRBC1- или TRBC2-селективный агент, конъюгированный с детектируемой частью, можно использовать для определения TRBC злокачественной Т-клетки.
Химиотерапевтическая часть, как применяют в настоящем документе, относится к части, которая является разрушительной для клетки и которая представляет собой часть, снижающую жизнеспособность клетки. Химиотерапевтическая часть может быть цитотоксическим лекарственным средством. Химиотерапевтическое средство, рассматриваемое в качестве неограничивающих примеров, включает алкилирующие средства, нитрозомочевины, этиленимины/метилмеламин, алкилсульфонаты, антиметаболиты, аналоги пиримидина, эпиподофилотоксины, ферменты, такие как L-аспарагиназа; модификаторы биологического ответа, такие как IFNα, IL-2, G-CSF и GM-CSF; координационные комплексы с платиной, такие как цисплатин и карбоплатин, антрацендионы, замещенную мочевину, такую как гидроксимочевина, производные метилгидразина, включая N-метилгидразин (MIH) и прокарбазин, препараты, подавляющие надпочечники, такие как митотан (o,p'-DDD) и аминоглютетимид; гормоны и антагонисты, включая антагонисты адренокортикостероидов, такие как преднизон и эквиваленты, дексаметазон и аминоглютетимид; прогестин, такой как гидроксипрогестерона капроат, медроксипрогестерона ацетат и мегестрола ацетат; эстроген, такой как эквиваленты диэтилстилбестрола и этинилэстрадиола; антиэстроген, такой как тамоксифен; андрогены, включая тестостерона пропионат и флуоксиместерон/эквиваленты; антиандрогены, такие как флутамид, аналоги гонадотропин-рилизинг гормона и леупролид; и нестероидные антиандрогены, такие как флутамид.
TRBC-селективный агент, конъюгированный с химиотерапевтической частью, способен осуществлять направленную доставку химиотерапевтической части к клеткам, которые экспрессируют или TRBC1, или TRBC2.
БИСПЕЦИФИЧЕСКИЕ Т-КЛЕТОЧНЫЕ АКТИВАТОРЫ
Был разработан широкий спектр молекул на основании базовой концепции о наличии двух антитело-подобных связывающих доменов.
Биспецифические молекулы, активирующие Т-клетки, представляют собой класс биспецифических антитело подобных молекул, которые были первично разработаны для применения в качестве противоопухолевых лекарственных средств. Они направляют иммунную систему хозяина, более конкретно, цитотоксическую активность T-клеток, против клетки-мишени, такой как злокачественная клетка. В этих молекулах, один связывающий домен связывается с Т-клеткой через рецептор CD3, а другой с клетками-мишенями, такими как опухолевая клетка (через опухоль-специфическую молекулу). Поскольку биспецифическая молекула связывается и с клеткой-мишенью, и с Т-клеткой, она приводит клетку-мишень в сближение с Т-клеткой, так что Т-клетка может оказывать свой эффект, например, цитотоксический эффект, на злокачественную клетку. Образование комплекса Т-клетка:биспецифическое АТ:злокачественная клетка вызывает передачу сигнала в Т-клетке. приводя, например, к высвобождению цитотоксических медиаторов. В идеале, агент только вызывает желаемую передачу сигнала в присутствии клетки-мишени, приводя к избирательному лизису.
Биспецифические молекулы, активирующие Т-клетки, были разработаны в ряде различных форматов, но один из наиболее распространенных представляет собой слияние двух одноцепочечных вариабельных фрагментов (scFvs) различных антител. Эти молекулы иногда обозначают BiTEs (Биспецифические Т-клеточные активаторы).
Агент, применяемый в способе по настоящему изобретению, может быть биспецифической молекулой, которая селективно распознает TRBC1 или TRBC2 и способна активировать Т-клетку. Например, агент может быть BiTE. Агент, применяемый в способе, может содержать:
(i) первый домен, который связывается или с TRBC1, или с TRBC2; и
(ii) второй домен, способный активировать Т-клетку.
Биспецифическая молекула может содержать сигнальный пептид для облегчения своей продукции. Сигнальный пептид может вызывать секрецию биспецифической молекулы клеткой-хозяином, так что биспецифическую молекулу можно выделить из супернатанта клетки-хозяина.
Сигнальный пептид может находиться на аминоконце молекулы. Биспецифическая молекула может иметь общую формулу: сигнальный пептид-первый домен-второй домен.
Биспецифическая молекула может содержать спейсерную последовательность для соединения первого домена со вторым доменом и пространственного разделения двух доменов.
Спейсерная последовательность может, например, включать шарнир из IgG1 или «стебель» из CD8. Линкер может альтернативно содержать альтернативную линкерную последовательность, которая имеет аналогичную длину и/или доменные спейсерные свойства, как и шарнир IgG1 или «стебель» CD8.
Биспецифическая молекула может содержать JOVI-1, или его функциональный фрагмент, как определено выше.
ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР (CAR)
Химерные антигенные рецепторы (CARs), также известные как химерные Т-клеточные рецепторы, искусственные Т-клеточные рецепторы и химерные иммунорецепторы, представляют собой сконструированные рецепторы, которые прививают произвольную специфичность на иммунную эффекторную клетку. В классическом CAR, специфичность моноклонального антитела прививают на Т-клетку. Нуклеиновые кислоты, кодирующие CAR, могут быть перенесены в T-клетки при помощи, например, ретровирусных векторов. Таким образом, можно получать большое количество опухоль-специфических T-клеток для переноса адоптивных клеток. Клинические исследования Фазы I этого подхода продемонстрировали эффективность.
Связывающий домен CAR для целевого антигена обычно сливают через спейсер и трансмембранный домен с эндодоменом, который содержит внутриклеточный Т-клеточный сигнальный домен или ассоциирован с ним. Когда CAR связывается с антигеном-мишенью, это приводит к передаче активирующего сигнала на ту Т-клетку, которая экспрессирует CAR на своей поверхности.
Агент, применяемый в способе по настоящему изобретению, может быть CAR, который селективно распознает TRBC1 или TRBC2. Агент может быть Т-клеткой, которая экспрессирует CAR, селективно распознающий TRBC1 или TRBC2.
CAR может также содержать трансмембранный домен, который перекрывает мембрану. Он может содержать гидрофобную альфа-спираль. Трансмембранный домен может быть получен из CD28, который придает хорошую стабильность рецептору.
Эндодомен представляет собой часть CAR, участвующую в передаче сигнала. Эндодомен или содержит внутриклеточный Т-клеточный сигнальный домен или ассоциирован с ним. После распознавания антигена рецепторы кластеризуются, и сигнал передается клетке. Наиболее широко используемым компонентом для Т-клеточной передачи сигнала является тот из CD3-зета, который содержит три иммунорецепторных тирозиновых активирующих мотива (ITAM). Он передает сигнал активации на Т-клетку после связывания с антигеном. CD3-зета может не обеспечивать полностью компетентный сигнал активации, и может быть необходима дополнительная ко-стимуляторная передача сигнала. Например, можно использовать химерные CD28 и OX40 с CD3-зета для передачи пролиферативного сигнала/сигнала выживаемости, или можно использовать все три вместе.
Эндодомен CAR может содержать эндодомен CD28, и OX40 и эндодомен CD3-зета.
CAR может содержать сигнальный пептид, так что когда CAR экспрессируется внутри клетки, такой как Т-клетка, формирующийся белок направляется в эндоплазматический ретикулум и затем к клеточной поверхности, где он экспрессируется.
CAR может содержать спейсерную последовательность для соединения TRBC-связывающего домена с трансмембранным доменом и пространственного разделения TRBC-связывающего домена и эндодомена. Гибкий спейсер позволяет TRBC-связывающему домену ориентироваться в различных направлениях, чтобы делать возможным связывание TRBC.
Спейсерная последовательность может, например, включать Fc-область IgG1, шарнир IgG1 или «стебель» CD8, или их сочетание. Линкер может альтернативно содержать альтернативную линкерную последовательность, которая имеет аналогичную длину и/или доменные спейсерные свойства, как и Fc-область IgG1, шарнир IgG1 или «стебель» CD8.
Выявлено, что CAR, содержащие спейсер на основе шарнира IgG1 или «стебля» CD8, показали наилучшую эффективность против клеток Юркат (фигура 15). Спейсер, таким образом, может содержать шарнир IgG1 или «стебель» CD8, или спейсер, который имеет аналогичную длину и/или доменные спейсерные свойства, как и шарнир IgG1 или «стебель» CD8.
Спейсер из человеческого IgG1 может быть изменен для удаления Fc-связывающих мотивов.
CAR может содержать антитело JOVI-1 или его функциональный фрагмент, как определено выше.
CAR может содержать аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID No. 33, 34 и 35.
>SEQ_ID_33 JOVI-1 CAR со спейсером из «стебля» CD8
METDTLLLWVLLVWIPGSTGEVRLQQSGPDLIKPGASVKMSCKASGYTFTGYVMHWVKQRPGQGLEWIGFINPYNDDIQSNERFRGKATLTSDKSSTTAYMELSSLTSEDSAVYYCARGAGYNFDGAYRFFDFWGQGTTLTVSSGGGGSGGGGSGGGGSDVVMTQSPLSLPVSLGDQASISCRSSQRLVHSNGNTYLHWYLQKPGQSPKLLIYRVSNRFPGVPDRFSGSGSGTDFTLKISRVEAEDLGIYFCSQSTHVPYTFGGGTKLEIKRSDPTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDIFWVLVVVGGVLACYSLLVTVAFIIFWVRSKRSRLLHSDYMNMTPRRPGPTRKHYQPYAPPRDFAAYRSRDQRLPPDAHKPPGGGSFRTPIQEEQADAHSTLAKIRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR
>SEQ_ID_34 JOVI-1 CAR со спейсером шарнир-CH2-CH3pvaa
METDTLLLWVLLVWIPGSTGEVRLQQSGPDLIKPGASVKMSCKASGYTFTGYVMHWVKQRPGQGLEWIGFINPYNDDIQSNERFRGKATLTSDKSSTTAYMELSSLTSEDSAVYYCARGAGYNFDGAYRFFDFWGQGTTLTVSSGGGGSGGGGSGGGGSDVVMTQSPLSLPVSLGDQASISCRSSQRLVHSNGNTYLHWYLQKPGQSPKLLIYRVSNRFPGVPDRFSGSGSGTDFTLKISRVEAEDLGIYFCSQSTHVPYTFGGGTKLEIKRSDPAEPKSPDKTHTCPPCPAPPVAGPSVFLFPPKPKDTLMIARTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGKKDPKFWVLVVVGGVLACYSLLVTVAFIIFWVRSKRSRLLHSDYMNMTPRRPGPTRKHYQPYAPPRDFAAYRSRDQRLPPDAHKPPGGGSFRTPIQEEQADAHSTLAKIRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR
>SEQ_ID_35 JOVI-1 CAR со спейсером из шарнира IgG1
METDTLLLWVLLVWIPGSTGEVRLQQSGPDLIKPGASVKMSCKASGYTFTGYVMHWVKQRPGQGLEWIGFINPYNDDIQSNERFRGKATLTSDKSSTTAYMELSSLTSEDSAVYYCARGAGYNFDGAYRFFDFWGQGTTLTVSSGGGGSGGGGSGGGGSDVVMTQSPLSLPVSLGDQASISCRSSQRLVHSNGNTYLHWYLQKPGQSPKLLIYRVSNRFPGVPDRFSGSGSGTDFTLKISRVEAEDLGIYFCSQSTHVPYTFGGGTKLEIKRSDPAEPKSPDKTHTCPPCPKDPKFWVLVVVGGVLACYSLLVTVAFIIFWVRSKRSRLLHSDYMNMTPRRPGPTRKHYQPYAPPRDFAAYRSRDQRLPPDAHKPPGGGSFRTPIQEEQADAHSTLAKIRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR
В приведенных выше последовательностях CAR одна или несколько из 6 CDR независимо могут содержать или не содержать одну или несколько аминокислотных мутаций (например, замен) по сравнению с последовательностями, приведенными в виде SEQ ID No. С 7 до 12, при условии, что полученный CAR сохраняет способность связываться с TRBC1.
Варианты вышеуказанных аминокислотных последовательностей также можно использовать в настоящем изобретении, при условии, что полученный CAR связывается с TRBC1 или TRBC2 и не имеет значительного перекрестного реагирования. Как правило, такие варианты имеют высокую степень идентичности последовательности с одной из последовательностей, приведенных в виде SEQ ID No. 33, 34 или 35.
Варианты CAR, как правило, имеют, по меньшей мере, приблизительно 75%, например, по меньшей мере, приблизительно 80%, 90%, 95%, 96%, 97%, 98% или 99% идентичности последовательности с одной из последовательностей, приведенных в виде SEQ ID No 33, 34 и 35.
НУКЛЕИНОВАЯ КИСЛОТА
Настоящее изобретение дополнительно относится к нуклеиновой кислоте, кодирующей агент, такой как BiTE или CAR по первому аспекту изобретения.
Последовательность нуклеиновой кислоты может кодировать CAR, содержащий одну из аминокислотных последовательностей, показанных в виде SEQ ID No. 33, 34 и 35.
Как применяют в настоящем документе, термины «полинуклеотид», «нуклеотид», и «нуклеиновая кислота» предназначены для того, чтобы быть синонимами друг для друга.
Специалисту следует понимать, что многочисленные различные полинуклеотиды и нуклеиновые кислоты могут кодировать одинаковый полипептид в результате вырожденности генетического кода. Кроме того, следует понимать, что специалисты с использованием рутинных способов могут производить нуклеотидные замены, которые не влияют на полипептидную последовательность, кодируемую полинуклеотидами, описанными в настоящем документе, для соответствия использованию кодонов любого конкретного организма-хозяина, в котором предполагается экспрессировать полипептиды.
Нуклеиновые кислоты по изобретению могут содержать ДНК или РНК. Они могут быть одноцепочечными или двухцепочечными. Они могут также быть полинуклеотидами, которые включают в себя синтетические или модифицированные нуклеотиды. Ряд различных типов модификации олигонуклеотидов известен в данной области. Эти модификации включают метилфосфонатные и тиофосфатные остовы, добавление акридиновых или полилизиновых цепей на 3' и/или 5'-концах молекулы. Для целей применения, описанных в настоящем документе, следует понимать, что полинуклеотиды могут быть модифицированы любым способом, доступным в данной области. Такие модификации можно проводить для того чтобы улучшить активность in vivo или продолжительность жизни интересующих полинуклеотидов.
Термины «вариант», «гомолог» или «производное» по отношению к нуклеотидной последовательности включают любую замену, вариацию, модификацию, замещение, делецию или добавление одной (или более) нуклеиновых кислот в последовательности или к последовательности.
ВЕКТОР
Настоящее изобретение также относится к вектору или набору векторов, которые содержат одну или несколько последовательностей нуклеиновой кислоты/кислот по изобретению. Такой вектор можно использовать для введения последовательности нуклеиновой кислоты/кислот в клетку-хозяина, таким образом, что он экспрессирует CAR по первому аспекту изобретения.
Вектор, например, может быть плазмидой или вирусным вектором, таким как ретровирусный вектор или лентивирусный вектор, или вектор на основе транспозона или синтетическая мРНК.
Вектор может быть способен к трансфекции или трансдукции Т-клеток или NK-клеток.
КЛЕТКА
Настоящее изобретение также относится к клетке, такой как иммунная клетка, содержащая CAR по первому аспекту изобретения.
Клетка может содержать нуклеиновую кислоту или вектор по настоящему изобретению.
Клетка может быть Т-клеткой или клеткой-естественным киллером (NK).
Т-клетки могут быть T-клетками или T-лимфоцитами, которые представляют собой тип лимфоцита, играющего центральную роль в клеточном иммунитете. Их можно отличить от других лимфоцитов, таких как B-клетки и клетки-естественные киллеры (NK-клетки) по наличию Т-клеточного рецептора (TCR) на клеточной поверхности. Существуют различные типы Т-клеток, резюмированные ниже.
Хелперные T-клетки (TH-клетки) помогают другим лейкоцитам в иммунологических процессах, включая созревание B-клеток в плазматические клетки и B-клетки памяти, и активацию цитотоксических T-клеток и макрофагов. TH-клетки экспрессируют на поверхности CD4. TH-клетки активируются, когда им презентируют пептидные антигены при помощи молекул MHC класса II на поверхности антигенпредставляющих клеток (APC). Эти клетки могут относиться к одному из нескольких подтипов, включая TH1, TH2, TH3, TH17, Th9, или TFH, которые секретируют различные цитокины для облегчения различных типов иммунных ответов.
Цитолитические T-клетки (TC-клетки, или ЦТЛ) разрушает клетки, инфицированные вирусами, и опухолевые клетки, и также вовлечены в отторжение трансплантата. ЦТЛ экспрессируют CD8 на поверхности. Эти клетки распознают свои мишени при связывании с антигеном, ассоциированным с MHC класса I, который присутствует на поверхности всех ядросодержащих клеток. При помощи IL-10, аденозина и других молекул, секретируемых регуляторными T-клетками, клетки CD8+ можно инактивировать до анергического статуса, который предотвращает аутоиммунные заболевания, такие как экспериментальный аутоиммунный энцефаломиелит.
T-клетки памяти представляют собой подтип антиген-специфических T-клеток, которые персистируют длительное время после того как инфекция устранена. Они быстро нарастают до большого количества эффекторных T-клеток после повторной презентации распознанного ими антигена, таким образом, обеспечивая иммунную систему "памятью" против прошлых инфекций. T-клетки памяти включают три подтипа: T-клетки центральной памяти (TCM-клетки) и два типа T-клеток эффекторной памяти (TEM-клетки и TEMRA-клетки). Клетки памяти могут быть или CD4+, или CD8+. T-клетки памяти, как правило, экспрессируют белок клеточной поверхности CD45RO.
Регуляторные T-клетки (Treg-клетки), ранее известные как супрессорные T-клетки, являются ключевыми для поддержания иммунологической толерантности. Их основная роль заключается в выключении T-клеточного иммунитета в направлении к концу иммунной реакции и в подавлении аутореактивных T-клеток, которые избежали процесса негативной селекции в тимусе.
Были описаны два главных класса CD4+ Treg-клеток - природные Treg-клетки и адаптивные Treg-клетки.
Природные Treg-клетки (также известные как CD4+CD25+FoxP3+ Treg-клетки) появляются в тимусе и связаны с взаимодействиями между развивающимися T-клетками с миелоидными (CD11c+) и плазмоцитарными (CD123+) дендритными клетками, которые были активированы тимусным стромальным лимфопоэтином (TSLP). Природные Treg-клетки можно отличить от других T-клеток по наличию внутриклеточной молекулы, называемой FoxP3. Мутации в гене FOXP3 могут предотвращать развитие регуляторных Т-клеток, вызывая летальное аутоиммунное заболевание - синдром дисрегуляции иммунитета, полиэндокринопатии и энтеропатии (IPEX).
Адаптивные Treg-клетки (также известные как Tr1-клетки или Th3-клетки) могут возникать во время нормального иммунного ответа.
Клетка может быть клеткой-естественным киллером (или NK-клеткой). NK-клетки образуют часть врожденной иммунной системы. NK-клетки обеспечивают быстрые ответы на внутренние сигналы от клеток, инфицированных вирусами, независимым от MHC образом.
NK-клетки (принадлежащие к группе врожденных лимфоидных клеток) определяются как большие гранулярные лимфоциты (БГЛ) и составляют третий тип клеток, дифференцирующихся от общего лимфоидного предшественника, производящего B и T-лимфоциты. Известно, что NK-клетки дифференцируются и созревают в костном мозге, лимфоузле, селезенке, миндалинах и тимусе, где они затем попадают в циркуляцию.
Клетки с CAR по изобретению могут быть любым из вышеупомянутых типов клеток.
T-клетки или NK-клетки, экспрессирующие CAR по первому аспекту изобретения, могут быть созданы ex vivo или из собственной периферической крови пациента (первая партия), или в окружении трансплантата гематопоэтических стволовых клеток из периферической крови донора (вторая партия), или из периферической крови неродственного донора (третья партия).
Альтернативно, T-клетки или NK-клетки, экспрессирующие CAR по первому аспекту изобретения, могут быть получены при дифференцировке ex vivo индуцибельных клеток-предшественников или эмбриональных клеток-предшественников в T- или NK-клетки. Альтернативно, можно использовать иммортализованную T-клеточную линию, которая сохраняет свою литическую функцию и могла бы действовать в качестве терапевтического средства.
Во всех этих вариантах осуществления, клетки с CAR получают путем введения ДНК или РНК, кодирующей CAR, одним из многих способов, включающих трансдукцию вирусным вектором, трансфекцию ДНК или РНК.
Клетка с CAR по изобретению может быть ex vivo T- или NK-клетка от индивидуума. T- или NK-клетка может быть из образца мононуклеарной клетки периферической крови (PBMC). T- или NK-клетки можно активировать и/или наращивать перед тем как их трансдуцируют нуклеиновой кислотой, кодирующей CAR по первому аспекту изобретения, например, путем обработки моноклональным антителом против CD3.
T- или NK-клетку по изобретению можно производить путем:
(i) выделения образца, содержащего T- или NK-клетку у индивидуума или из других вышеуказанных источников; и
(ii) трансдукции или трансфекции T- или NK-клеток последовательностью нуклеиновой кислоты/кислот, кодирующих CAR по изобретению.
T- или NK клетки можно затем выделять, например, отбирать на основе экспрессии антигенсвязывающего домена антигенсвязывающего полипептида.
Настоящее изобретение также относится к набору, который включает T- или NK-клетку, содержащую CAR по первому аспекту изобретения.
ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ
Настоящее изобретение также относится к фармацевтической композиции, содержащей множество клеток, экспрессирующих CAR по первому аспекту изобретения. Фармацевтическая композиция может дополнительно содержать фармацевтически приемлемый носитель, разбавитель или эксципиент. Фармацевтическая композиция может необязательно содержать один или несколько дополнительных фармацевтически активных полипептидов и/или соединений. Такой состав может находиться, например, в форме, подходящей для внутривенного вливания.
Т-КЛЕТОЧНАЯ ЛИМФОМА И/ИЛИ ЛЕЙКЕМИЯ
Настоящее изобретение относится к агентам, клеткам и способам лечения Т-клеточной лимфомы и/или лейкемии.
Способ лечения Т-клеточной лимфомы и/или лейкемии относится к терапевтическому применению агента. В настоящем изобретении агент можно вводить индивидууму, у которого есть в наличии заболевание, Т-клеточная лимфома и/или лейкемия, для того чтобы уменьшить, снизить, улучшить, по меньшей мере, один симптом, ассоциированный с заболеванием и/или для того чтобы замедлить, уменьшить или блокировать прогрессирование заболевания.
Способ по настоящему изобретению можно использовать для лечения любой лимфомы и/или лейкемии, ассоциированной с клональным распространением клетки, экспрессирующей Т-клеточный рецептор (TCR), содержащий константную область β. По существу настоящее изобретение относится к способу лечения заболевания, которое включает злокачественные T-клетки, экспрессирующие TCR, который содержит TRBC.
Способ по настоящему изобретению можно использовать для лечения Т-клеточной лимфомы, при которой злокачественная Т-клетка экспрессирует TCR, который содержит TRBC. «Лимфому» применяют в настоящем документе в соответствии с ее стандартным значением по отношению к злокачественной опухоли, которая, как правило, развивается в лимфоузлах, но может также поражать селезенку, костный мозг, кровь и другие органы. Лимфома, как правило, присутствует в виде плотной опухоли из лимфоидных клеток. Первичным симптомом, ассоциированным с лимфомой, является лимфоаденопатия, хотя вторичные (B) симптомы могут включать лихорадку, ночную потливость, потерю массы, потерю аппетита, утомляемость, дыхательную недостаточность и кожный зуд.
Способ по настоящему изобретению можно использовать для лечения Т-клеточной лейкемии, при которой злокачественная Т-клетка экспрессирует TCR, который содержит TRBC. «Лейкемию» применяют в настоящем документе в соответствии с ее стандартным значением по отношению к злокачественной опухоли крови или костного мозга.
Ниже представлен иллюстративный, не исчерпывающий перечень заболеваний, которые можно лечить способом по настоящему изобретению.
ПЕРИФЕРИЧЕСКАЯ Т-КЛЕТОЧНАЯ ЛИМФОМА
Периферические Т-клеточные лимфомы представляют собой относительно редкие лимфомы, и на них приходится менее 10% от всех неходжкинских лимфом (НХЛ). Однако они ассоциированы с аггресивным клинически течением, и причины и точное клеточное происхождение большинства Т-клеточн лимфом все еще не определены.
Лимфома, как правило, впервые манифестирует в виде опухания на шее, подмышкой или в паху. Дополнительное опухание может происходить там, где расположены другие лимфоузлы, например, в селезенке. Как правило, увеличенные лимфоузлы могут вторгаться в пространство кровеносных сосудов, нервов или желудка, приводя к опуханию рук и ног, покалыванию и онемению, или к ощущениям наполненности, соответственно. Симптомы лимфомы также включают неспецифические симптомы, такие как лихорадка, озноб, необъяснимая потеря массы, ночная потливость, вялость и зуд.
Классификация ВОЗ использует морфологические и иммунофенотипические отличительные признаки в сочетании с клиническими аспектами и, в некоторых случаях, с генетикой для того чтобы определить прогностически и терапевтически значимую классификацию для периферических Т-клеточных лимфом (Swerdlow et al.; WHO classification of tumours of haematopoietic and lymphoid tissues. 4th ed.; Lyon: IARC Press; 2008). Анатомическая локализация неопластических T-клеток частично соответствует их предполагаемым нормальным клеточным партнерам и функциям и, как таковые, Т-клеточные лимфомы ассоциированы с лимфоузлами и периферической кровью. Этот подход позволяет лучше понимать некоторые из проявлений Т-клеточных лимфом, включая распределение клеток, некоторые аспекты морфологии и даже связанные с ними клинические результаты.
Наиболее распространенными Т-клеточными лимфомами являются периферическая Т-клеточная лимфома, не уточненная (ПТКЛ-НУ) включающая 25% от общего числа, а затем ангиоиммунобластная Т-клеточная лимфома (АИТКЛ) (18,5%).
ПЕРИФЕРИЧЕСКАЯ Т-КЛЕТОЧНАЯ ЛИМФОМА, НЕ УТОЧНЕННАЯ (ПТКЛ-НУ)
ПТКЛ-НУ включает более 25% от всех периферических Т-клеточных лимфом и NK/Т-клеточных лимфом, и является наиболее распространенным субтипом. Ее диагностируют по исключению, как не соответствующую ни одной из конкретных зрелых Т-клеточных лимфом, перечисленных в действующем на данный момент списке ВОЗ 2008. Как таковая, она является аналогом диффузной крупноклеточной В-клеточной лимфомы, не уточненной (ДКБКЛ-НУ).
Большинство пациентов являются взрослыми со средним возрастом от 60 лет и соотношением мужчин к женщинам 2:1. Большинство случаев являются по своей природе узловыми, однако, внеузловое расположение встречается приблизительно у 13% пациентов и наиболее часто включает кожу и желудочно-кишечный тракт.
Цитологический спектр очень широк, в диапазоне от полиморфологического до мономорфологического. Были описаны три морфологически определенных варианта, включая лимфоэпителиоидный (Леннерта) вариант, вариант T-зоны и фолликулярный вариант. Лимфоэпителиоидный вариант ПТКЛ включает обилие сопутствующих эпителиоидных гистиоцитов и обычно является положительным по CD8. Его ассоциируют с лучшим прогнозом. Фолликулярный вариант ПТКЛ-НУ проявляется как потенциально отличающаяся клинико-патологическая форма.
Большинство ПТКЛ-НУ имеют зрелый Т-клеточный фенотип и большинство случаев являются положительными по CD4. 75% случаев демонстрируют вариабельную потерю, по меньшей мере, одного пан-Т-клеточного маркера (CD3, CD2, CD5 или CD7), с наиболее частым подавлением CD7 и CD5. Могут экспрессироваться CD30 и редко CD15, при этом CD15 является неблагоприятным прогностическим признаком. Экспрессия CD56, хотя и редкая, также имеет отрицательное прогностическое влияние. Дополнительные неблагоприятные прогностические патологические факторы включают скорость пролиферации больше чем 25% на основании экспрессии KI-67, и присутствия более чем 70% трансформированных клеток. Иммунофенотипический анализ этих лимфом предлагает малое понимание их биологии.
АНГИОИММУНОБЛАСТНАЯ Т-КЛЕТОЧНАЯ ЛИМФОМА (АИТКЛ)
АИТКЛ представляет собой системное заболевание, характеризующееся полиморфным инфильтратом, захватывающим лимфоузлы, выраженные наружные эндотелиальные венулы (НЭВ) и периваскулярное расширение сетей фолликулярных дендритных клеток (ФДК). АИТКЛ рассматривается как Т-клеточная лимфома de-novo, происходящая из αβ T-клеток фолликулярного хелперного типа (TFH), которые обычно находятся в зародышевых центрах.
АИТКЛ представляет собой вторую наиболее частую нозологическую форму среди периферических Т-клеточных лимфом и NK/Т-клеточных лимфом, составляя приблизительно 18,5% случаев. Она встречается в интервале от среднего до пожилого возраста, со средним возрастом 65 лет, и приблизительно равной встречаемостью у мужчин и женщин. Клинически, пациенты, как правило, имеют позднюю стадию заболевания с генерализованной лимфоаденопатией, гепатоспленомегалией и выраженными системными симптомами. Обычно присутствует кожная сыпь с ассоциированным зудом. Часто присутствует поликлональная гипергаммаглобулинемия, ассоциированная с аутоиммунными явлениями.
При АИТКЛ описаны три различных морфологических паттерна. Раннее поражение при АИТКЛ (Паттерн I), как правило, демонстрирует сохранившуюся архитектуру с характерными гиперпластическими фолликулами. Неопластическая пролиферация локализована на периферии фолликулов. При Паттерне II узловая архитектура частично стерта с сохранением нескольких регрессировавших фолликулов. Субкапсулярные синусы сохранены и даже расширены. Паракортикальная область содержит разветвленные НЭВ и присутствует пролиферация ФДК за пределами В-клеточного фолликула. Неопластические клетки имеют размер от небольшого до среднего, с минимальной цитологической атипией. Они часто имеют прозрачную или бледную цитоплазму, и могут демонстрировать четкие клеточные мембраны. Как правило, очевиден полиморфный воспалительный фон.
Хотя АИТКЛ представляет собой Т-клеточное злокачественное новообразование, присутствует характерное размножение B-клеток и плазматических клеток, которое вероятно отражает функцию неопластических клеток как TFH-клеток. Присутствуют и EBV-положительные и EBV-отрицательные B-клетки. Иногда, атипичные B-клетки могут напоминать Ходжкин/Рид-Штернберг-подобные клетки морфологически и иммунофенотипически, что иногда приводит к диагностической путанице с этой формой. B-клеточная пролиферация при АИТКЛ может быть обширной, и у некоторых пациентов развиваются вторичные EBV-положительные диффузные крупноклеточные В-клеточные лимфомы (ДККБКЛ) или - более редко - EBV-отрицательные В-клеточные опухоли, часто с плазмоцитарной дифференцировкой.
Неопластические CD4-положительные T-клетки при АИТКЛ демонстрируют устойчивую экспрессию CD10 и CD279 (PD-1) и являются положительными по CXCL13. CXCL13 приводит к увеличенному рекрутингу В-клеток в лимфоузлы через адгезию к НЭВ, активацию В-клеток, плазмоцитарную дифференцировку и распространение сетей ФДК; все факторы вносят вклад в морфологические и клинические признаки АИТКЛ. Интенсивная экспрессия PD-1 в перифолликулярных опухолевых клетках особенно полезна при различении Паттерна I АИТКЛ с реактивной фолликулярной и паракортикальной гиперплазией.
Фолликулярный вариант ПТКЛ-НУ представляет собой другую форму с фенотипом TFH. В противоположность АИТКЛ, у него нет выраженных НЭВ или экстрафолликулярной пролиферации сетей ФДК. Неопластические клетки могут формировать внутрифолликулярные агрегаты, имитируя В-клеточную фолликулярную лимфому, но могут также иметь паттерн внутрифолликулярного роста или включать расширенные зоны мантии. Клинически, фолликулярный вариант ПТКЛ-НУ отличается от АИТКЛ, поскольку у пациентов чаще присутствует ранняя стадия заболевания с частичным включением лимфоузлов и могут отсутствовать системные симптомы, ассоциированные с АИТКЛ.
АНАПЛАСТИЧЕСКАЯ КРУПНОКЛЕТОЧНАЯ ЛИМФОМА (АККЛ)
АККЛ могут быть подразделены как АККЛ-«киназа анапластической лимфомы» (ALK)+ или АККЛ-ALK-.
АККЛ-ALK+ является одной из хорошо охарактеризованных форм периферических Т-клеточных лимфом, с характерными «отличительными клетками» с подковообразными ядрами и экспрессирующими ALK и CD30. На ее долю приходится приблизительно 7% от всех периферических Т-клеточных и NK-клеточных лимфом, и она наиболее часто встречается в первые три декады жизни. У пациентов часто присутствует лимфоаденопатия, но общим является вовлеченность внеузловых участков (кожа, кости, мягкие ткани, легкое, печень) и B-симптомы.
АККЛ-ALK+ демонстрирует широкий морфологический спектр, с пятью описанными различными паттернами, но все варианты содержат какие-то отличительные клетки. Отличительные клетки имеют эксцентрические подковообразные или почкообразные ядра, и выраженную перинуклеарную эозинофильную область Гольджи. Опухолевые клетки растут сцепленным образом с предрасположенностью к вовлечению синуса. Мелкие опухолевые клетки преобладают в мелкоклеточном варианте, а в лимфогистиоцитарном варианте обилие гистиоцитов маскирует присутствие опухолевых клеток, многие из которых невелики.
По определению, все случаи показывают положительность по ALK и CD30, как правило, с более слабой экспрессией в мелких опухолевых клетках. Часто наблюдают потерю пан-Т-клеточных маркеров, в 75% случаев с потерей поверхностной экспрессии CD3.
Экспрессия ALK является результатом характерного рецидивирующего генетического изменения, состоящего в транслокации гена ALK на хромосоме 2p23 в один из многих генов-партнеров, что приводит к экспрессии химерного белка. Наиболее распространенным геном-партнером, встречающимся в 75% случаев, является ген нуклеофосмина (NPM1) на хромосоме 5q35, что приводит к t(2;5)(p23;q35). Клеточное распределение ALK в различных вариантах транслокации может варьировать в зависимости от гена-партнера.
АККЛ-ALK- включена в виде предварительной категории в классификацию ВОЗ 2008. Ее определяют как CD30-положительную Т-клеточную лимфому, которая морфологически неотличима от АККЛ-ALK+ со сцепленной моделью роста и присутствием отличительных клеток, но с отсутствием экспрессии белка ALK.
Пациентами, как правило, являются взрослые в возрасте между 40 и 65 годами, в отличие от АККЛ-ALK+, которая более распространена у детей и молодых людей. АККЛ-ALK- может захватывать и лимфоузлы, и внеузловые ткани, хотя последнее наблюдают менее часто, чем при АККЛ-ALK+. Большинство случаев АККЛ-ALK- демонстрируют архитектуру лимфоузла со складками сцепленных неопластических клеток с типичными «отличительными» признаками. В отличие от АККЛ-ALK+, мелкоклеточный морфологический вариант не распознается.
В отличие от формы ALK+, АККЛ-ALK- демонстрирует большее сохранение экспрессии Т-клеточных маркеров, в то время как экспрессия цитотоксических маркеров и поверхностного антигена эпителиоцитов (EMA) менее вероятна. Профили экспрессии генов и рекуррентный хромосомный дисбаланс различны при АККЛ-ALK- и АККЛ-ALK+, подтверждая, что они являются различными формами на молекулярном и генетическом уровне.
АККЛ-ALK- клинически отличается как от АККЛ-ALK+, так и от ПТКЛ-НУ, со значимыми отличиями в прогнозе между этими тремя различными формами. Сообщают, что пятилетняя общая выживаемость при АККЛ-ALK- составляет 49%, и она не так хороша, как выживаемость при АККЛ-ALK+ (около 70%), но в то же время значительно лучше, чем выживаемость при ПТКЛ-НУ (32%).
Т-КЛЕТОЧНАЯ ЛИМФОМА, АССОЦИИРОВАННАЯ С ЭНТЕРОПАТИЕЙ (ТКЛЭ)
ТКЛЭ представляет собой агрессивную неоплазию, которая, как считают, происходит из внутриэпителиальных T-клеток кишечника. В классификации ВОЗ 2008 различают два морфологически, иммуногистохимически и генетически различных типа ТКЛЭ: Тип I (представляющий большинство ТКЛЭ) и Тип II (составляющий 10-20% случаев).
Тип I ТКЛЭ, как правило, ассоциирован с явной или бессимптомной глютено-чувствительной энтеропатией, и более часто наблюдается у пациентов северно-европейской выборки из-за высокой распространенности глютеновой болезни в этой популяции.
Наиболее часто, бляшки ТКЛЭ обнаруживают в тощей или подвздошной кишке (90% случаев), с редкими случаями в двенадцатиперстной кишке, толстой кишке, желудке, или областях вне желудочно-кишечного тракта. Кишечные поражения, как правило, являются многоочаговыми с изъязвлением слизистой. Клиническое течение ТКЛЭ является агрессивным, и большинство пациентов умирают от заболевания или осложнений заболевания в течение одного года.
Цитологический спектр ТКЛЭ типа I является широким, и некоторые случаи могут содержать анапластические клетки. Присутствует полиморфный воспалительный фон, который в некоторых случаях может скрывать неопластический компонент. Слизистая оболочка кишечника в областях, прилегающих к опухоли, часто демонстрирует признаки глютеновой болезни с «притуплением» ворсинок и увеличенным числом внутриэпителиальных лимфоцитов (ВЭЛ), которые могут представлять поврежденные клетки-предшественники.
Согласно иммуногистохимии, неопластические клетки часто являются CD3+CD4-CD8-CD7+CD5-CD56-βF1+ и содержат цитотоксические белки, ассоциированные с гранулами (TIA-1, гранзим B, перфорин). CD30 частично экспрессируется практически во всех случаях. CD103, который представляет собой хоминг-рецептор слизистой, может экспрессироваться при ТКЛЭ.
Тип II ТКЛЭ, также обозначаемый как мономорфная CD56+ кишечная Т-клеточная лимфома, определяют как опухоль кишечника, которая состоит из мономорфных T-клеток размером от небольшого до среднего, экспрессирующих и CD8, и CD56. Часто присутствует латеральное распространение опухоли внутрь слизистой, и отсутствие воспалительного фона. Большинство случаев экспрессируют γδ TCR, однако, есть случаи, ассоциированные с αβ TCR.
Тип II ТКЛЭ имеет более широкое распространение в мире, чем Тип I ТКЛЭ и часто наблюдается в азиатских или латиноамериканских популяциях, у которых редко наблюдается глютеновая болезнь. У индивидуумов европейского происхождения ТКЛЭ, типа II составляет приблизительно 20% от кишечных Т-клеточных лимфом, с историей глютеновой болезни, по меньшей мере, в подгруппе случаев. Клиническое течение является агрессивным.
ГЕПАТОСПЛЕНИЧЕСКАЯ Т-КЛЕТОЧНАЯ ЛИМФОМА (ГСТЛ)
ГСТЛ представляет собой агрессивную системную неоплазию, в основном, происходящую из γδ цитотоксических T-клеток врожденной иммунной системы, однако, в редких случаях она может также происходить из αβ T-клеток. Это одна из наиболее редких Т-клеточных лимфом, и, как правило, она поражает подростков и молодых людей (средний возраст, 35 лет) с сильным преобладанием мужчин.
ЭКСТРАНОДАЛЬНАЯ NK/Т-КЛЕТОЧНАЯ ЛИМФОМА НАЗАЛЬНОГО ТИПА
Экстранодальная NK/Т-клеточная лимфома назального типа представляет собой агрессивное заболевание, часто с деструктивными поражениями средней линии и некрозом. Большинство случаев являются производными NK-клеток, но некоторые происходят из цитотоксических T-клеток. Она везде ассоциирована с вирусом Эпштейна-Барр (EBV).
Т-КЛЕТОЧНАЯ ЛИМФОМА КОЖИ
Способ по настоящему изобретению также можно использовать для лечения Т-клеточной лимфомы кожи.
Т-клеточная лимфома кожи (ТКЛК) характеризуется миграцией злокачественных T-клеток к коже, что вызывает появление различных повреждений. Эти повреждения меняют форму с прогрессированием заболевания, как правило, сначала появляется то, что выглядит как сыпь, и, в конечном итоге, формируются бляшки и опухоли перед метастазированием в другие части организма.
Кожные Т-клеточные лимфомы включают те, которые упомянуты в следующем иллюстративном неисчерпывающем списке: фунгоидный микоз, восходящий ретикулез, синдром Сезари, гранулематозная дряблая кожа, лимфоматозный папулез, хронический лихеноидный парапсориаз, CD30+ кожная Т-клеточная лимфома, вторичная кожная CD30+ крупноклеточная лимфома, CD30- кожная крупноклеточная Т-клеточная лимфома без фунгоидного микоза, плеоморфная Т-клеточная лимфома, лимфома Леннерта, подкожная Т-клеточная лимфома и лимфангиома.
Признаки и симптомы ТКЛК варьируют в зависимости от конкретного заболевания, из которых два наиболее распространенных типа представляют собой фунгоидный микоз и синдром Сезари. Классический фунгоидный микоз делится на три стадии:
Пятно (атрофическое или неатрофическое): Неспецифический дерматит, пятна на нижней части туловища и ягодиц; минимальный/отсутствующий зуд;
Бляшка: интенсивно зудящие бляшки, лимфоаденопатия; и
Опухоль: Склонная к изъязвлению.
Синдром Сезари определяется эритродермией и лейкозом. Признаки и симптомы включают отечную кожу, лимфоаденопатию, ладонный и/или подошвенный гиперкератоз, алопецию, дистрофию ногтей, выворот века и гепатоспленомегалию.
Из всех первичных кожных лимфом, 65% представляют собой T-тип клеток. Наиболее распространенным иммунофенотипом является CD4-положительный. Для этих заболеваний не существует общей патофизиологии, поскольку термин Т-клеточная лимфома кожи охватывает широкий спектр нарушений.
Первичные этиологические механизмы для развития Т-клеточной лимфомы кожи (например, фунгоидного микоза) не выяснены. Фунгоидному микозу может предшествовать хроническое воспалительное заболевание кожи, опосредованное Т-клетками, которое может иногда прогрессировать в летальную лимфому.
ПЕРВИЧНАЯ КОЖНАЯ АККЛ (К-АККЛ)
К-АККЛ часто неотличима от ALC-ALK- по морфологии. Она определяется как кожная опухоль из крупных клеток с анапластической, плеоморфной или иммунобластной морфологией с более чем 75% клеток, экспрессирующих CD30. Вместе с лимфоматоидным папулезом (ЛП) К-АККЛ относится к спектру первичных кожных CD30-положительных Т-клеточных лимфопролиферативных нарушений, которые как группа включают вторую наиболее распространенную группу кожных Т-клеточных лимфопролифераций после фунгоидного микоза.
Профиль иммуногистохимического окрашивания очень похож на АККЛ-ALK- с большей долей случаев с положительным окрашиванием по цитотоксическим маркерам. По меньшей мере, 75% опухолевых клеток должны быть положительными по CD30. CD15 также может экспрессироваться, и, когда происходит поражение лимфоузлов, дифференциальный диагноз с классической лимфомой Ходжкина может быть трудным. Редкие случаи АККЛ-ALK+ могут происходить с кожными повреждениями, и могут напоминать К-АККЛ.
Т-КЛЕТОЧНАЯ ОСТРАЯ ЛИМФОБЛАСТНАЯ ЛЕЙКЕМИЯ
Т-клеточная острая лимфобластная лейкемия (Т-ОЛЛ) составляет приблизительно 15% и 25% от ОЛЛ в детской и взрослой когортах, соответственно. Пациенты, как правило, имеют высокое число лейкоцитов, и может проявляться органомегалия, в частности, медиастинальное расширение, и поражение ЦНС.
Способ по настоящему изобретению можно использовать для лечения T-ОЛЛ, которая ассоциирована с злокачественной Т-клеткой, экспрессирующей TCR, который содержит TRBC.
Т-КЛЕТОЧНАЯ ПРОЛИМФОЦИТАРНАЯ ЛЕЙКЕМИЯ
Т-клеточный пролимфоцитарный лейкоз (T-ПЛЛ) представляет собой лейкемию со зрелыми Т-клетками с агрессивным поведением и предрасположенностью к крови, костному мозгу, лимфоузлам, печени, селезенке, и поражению кожи. T-ПЛЛ первично поражает взрослых в возрасте старше 30 лет. Другие названия включают Т-клеточную хроническую лимфоцитарную лейкемию, "узловатый тип" Т-клеточной лейкемии, и T-пролимфоцитарную лейкемию/Т-клеточную лимфоцитарную лейкемию.
В периферической крови T-ПЛЛ состоит из лимфоцитов среднего размера с одиночными ядрышками и базофильной цитоплазмой с единичными полостями или отростками. Ядрышки, как правило, имеют форму от круглой до овальной, и единичные пациенты имеют клетки с более неправильной формой границ ядра, которая сходна с мозговидной формой ядра, наблюдаемой при синдроме Сезари. Мелкоклеточный вариант составляет 20% от всех случаев T-ПЛЛ, и вариант с клетками, подобными клеткам Сезари, (мозговидный) наблюдают в 5% случаев.
T-ПЛЛ имеет иммунофенотип зрелого (пост-тимического) T-лимфоцита, и неопластические клетки, как правило, положительны по пан-T-антигенам CD2, CD3, и CD7 и отрицательны по TdT и CD1a. Иммунофенотип CD4+/CD8- присутствует в 60% случаев, иммунофенотип CD4+/CD8+ присутствует в 25%, и иммунофенотип CD4-/CD8+ присутствует в 15% случаев.
ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ
Способ по настоящему изобретению может включать этап введения агента в форме фармацевтической композиции.
Агент можно вводить с фармацевтически приемлемым носителем, разбавителем, эксципиентом или адъювантом. Фармацевтический носитель, эксципиент или разбавитель можно выбирать с учетом намеченного пути введения и стандартной фармацевтической практики. Фармацевтические композиции могут содержать в качестве носителя, эксципиента или разбавителя или в дополнение к носителю, эксципиенту или разбавителю любое подходящее связывающее средство/средства, смазочное средство/средства, суспендирующее средство/средства, покрывающее средство/средства, агент/агенты, повышающие растворимость, и другие носители.
ВВЕДЕНИЕ
Введение агента можно производить при помощи любого из ряда путей, которые делают активный ингредиент биодоступным. Например, агент можно вводить пероральным и парентеральным путями, интраперитонеально, внутривенно, подкожно, чрезкожно, внутримышечно, путем местной доставки, например, через катетер или стент.
Как правило, терапевт определит фактическую дозировку, которая будет наиболее подходящей для индивидуума, и она будет варьировать в зависимости от возраста, массы и ответа конкретного пациента. Дозировка такова, что она достаточна для уменьшения или истощения числа клональных T-клеток, экспрессирующих или TRBC1, или TRBC2.
ПРИМЕНЕНИЕ
Настоящее изобретение также относится к агенту для применения в лечении Т-клеточной лимфомы в соответствии со способом по первому аспекту. Агент может быть любым агентом, определенным выше.
Настоящее изобретение также относится к применению агента, определенного выше, в производстве лекарственного средства для лечения Т-клеточной лимфомы в соответствии со способом по первому аспекту.
НАБОР
Настоящее изобретение дополнительно относится к набору, включающему агент, определенный выше, для применения для лечения Т-клеточной лимфомы в соответствии со способом по первому аспекту.
Набор может также содержать реагент(-ы), подходящие для определения TRBC злокачественной Т-клетки. Например, набор может содержать праймеры для ПЦР или антитело (антитела), которые специфичны или для TRBC1, или для TRBC2.
СПОСОБ ДЛЯ ОПРЕДЕЛЕНИЯ Т-КЛЕТОЧНОЙ ЛИМФОМЫ И/ИЛИ ЛЕЙКЕМИИ
Настоящее изобретение дополнительно относится к способу определения наличия Т-клеточной лимфомы или лейкемии у индивидуума, включающему этап определения доли T-клеток в образце от индивидуума, которые являются или TRBC1-, или TRBC2-положительными.
Т-клеточные лимфомы включают клональное размножение отдельных злокачественных T-клеток. Как таковое, наличие Т-клеточной лимфомы у индивидуума можно выявить, определяя долю T-клеток или с TRBC1, или с TRBC2 в образце, полученном от пациента.
Образец может быть образцом периферической крови, образцом лимфы или образцом, взятым напрямую из опухоли, например, биопсийным образцом.
Доля Т-клеток от общего числа, которые являются TRBC1- или TRBC2-положительными, указывающая на наличие Т-клеточной лимфомы или лейкемии, может составлять, например 80, 85, 90, 95, 98 или 99% от общей популяции клеток.
Способ может включать определение инфильтрации отдельными популяциями T-клеток в биопсии или образце. В настоящем изобретении на наличие Т-клеточной лимфомы или лейкемии указывает то, если 80, 85, 90, 95, 98 или 99% от общей популяции Т-клеток в образце являются или TRBC1, или TRBC2.
Общее число T-клеток в образце можно выявлять, определяя число клеток в образце, экспрессирующих CD3, CD4, CD8 и/или CD45. Также можно использовать сочетание этих маркеров.
Долю от общего числа T-клеток в образце, которые экспрессируют или TRBC1, или TRBC2 можно определять при помощи способов, известных в данной области, например, проточной цитометрии, иммуногистохимии или флуоресцентной микроскопии.
Изобретение будет теперь дополнительно описано в виде примеров, которые призваны помочь специалисту в данной области в осуществлении изобретения и никоим образом не ограничивают объем изобретения.
ПРИМЕРЫ
Пример 1 - Распознавание TRBC1 и TRBC2-экспрессирующих клеток
Антитело JOVI-1 ранее было описано у Viney et al. (Hybridoma; 1992; 11(6); 701- 713) и доступно коммерчески (Abcam, ab5465). Авторы настоящего изобретения определили, что JOVI-1 способно распознавать клетки на основании специфической экспрессии TRBC1 или TRBC2.
Авторы изобретения создали два плазмидных вектора, доставляющих полные вариабельные и константные области TCR, которые различаются только по экспрессии или TRBC1, или TRBC2. Эти плазмиды применяли для получения ретровирусного супернатанта путем временной трансфекции клеток 293T. Этот супернатант применяли, чтобы стабильно трансдуцировать T-клетки Юркат, нокаутные по TCR (клеточная линия T-ALL с мутацией в локусе бета-цепи TCR, препятствующей экспрессии этой цепи, и, таким образом, полного поверхностного комплекса TCR/CD3). Это привело к получению клеточных линий, которые идентичны, за исключением экспрессии или TRBC1, или TRBC2. Окрашивание этих клеточных линий выявило полную экспрессию поверхностного комплекса TCR/CD3, и только клетки, экспрессирующие TRBC1, окрашивались при помощи антитела JOVI-1 (фигура 4).
Пример 2 CD4+ и CD8+ T-клетки здорового донора содержат раздельные TRBC1-положительные и TRBC1-отрицательные популяции
Авторы изобретения тестировали антитело JOVI-1 на первичных T-клетках человека от здоровых доноров. Эти анализы выявили, что все доноры имели доли и CD4+, и CD8+ T-клеток, которые экспрессировали TRBC1, и доли каждых из них, которые не экспрессировали. Приблизительно 20-50% нормальных CD4+ и CD8+ T-клеток являются TRBC1-положительными (фигуры 6 и 7).
Пример 3 - Клональные T-клеточные линии, экспрессирующие TCR, являются TRBC1-положительными или отрицательными
Клеточные линии были получены из исходной популяции клональной опухоли у пациента. Окрашивание T-клеточных линий, экспрессирующих TCR, выявило, что T-клетки экспрессируют или TRBC1, или TRBC2, подтверждая, что он является маркером клональности. Из трех протестированных T-клеточных линий, клетки Юркат (известные как TRBC1+), но не клетки HPB-ALL или HD-Mar-2 (известные как TRBC2+), окрашиваются JOVI-1, подтверждая эксклюзивную экспрессию или TRBC1, или TRBC 2 (фигура 8).
Пример 4 - Первичные клональные Т-клетки у пациентов с T-пролимфоцитарной лейкемий являются TRBC1-положительными или отрицательными
Клональные T-клетки, выделенные из периферической крови пациентов с T-пролимфоцитарной лейкемией (T-ПЛЛ), являются или однородно TRBC1-положительными, или TRBC1-отрицательными.
Пример 5 - Влияние мутации остатков, которые являются уникальными для TCBC1
Получали плазмидные векторы, кодирующие TCR, которые являются идентичными, за исключением мутаций гибрида TRBC1/2 в константной области β-цепи TCR. Анализ показал, что JOVI-1 распознает различия в остатках в положениях 3 и 4 константной цепи TCRβ, указывая на то, что эти остатки доступны для распознавания антителом и являются, вероятно, наилучшими мишенями для создания агентов, отличающих TRBC1 от TRBC2, или TRBC2 от TRBC1 (фигура 5).
Пример 6 - Специфический лизис TRBC1-, а не TRBC2-TCR-экспрессирующих T-клеток.
T-клетки Юркат дикого типа (CD34-, TRBC1+) смешивали с T-клетками Юркат, нокаутными по TCRαβ и трансдуцированными TRBC2 с коэкспрессией маркерного гена CD34 (CD34+TRBC2+). Эти клетки инкубировали с JOVI-1 отдельно или инкубировали с JOVI-1 и комплементом в течение 1 часа. Клетки отмывали и окрашивали по CD34, аннексину V и 7-AAD. Клетки анализировали проточной цитометрией.
На фигуре 9 показана экспрессия CD34 в живых популяциях, определенных как популяции, отрицательные по аннексину-V и со слабой экспрессией 7-AAD. Наблюдали селективный лизис T-клеток с TRBC1 (CD34-) (фигура 9).
T-клетки Юркат дикого типа в норме являются TRBC1+ и не экспрессируют укороченный маркерный ген CD34. Как описано выше, авторы изобретения получили линию Юркат TRBC2+ путем трансдукции T-клеток Юркат, нокаутных по TCRαβ, ретровирусным вектором, который кодирует TRBC2 TCR, а также укороченный маркерный ген CD34. Эти T-клетки затем смешивали вместе. Затем, авторы изобретения инкубировали T-клетки или с JOVI-1 по отдельности или с JOVI-1 и комплементом в течение 1 часа. Для удобства, авторы изобретения могли различать популяции TRBC1 и TRBC2 по окрашиванию по маркерному гену CD34 и, таким образом, избежали невыявления TRBC1 TCR из-за интернализации TCR после длительной инкубации с МАТ против TCR. Клетки отмывали и окрашивали на CD34, аннексин V и 7-AAD. Клетки анализировали проточной цитометрией. Путем гейтинга живых клеток (т.е. клеток, которые были отрицательными по аннексину V и имели слабую яркость 7-AAD) авторы изобретения смогли определить, что TRBC1 T-клетки подвергаются селективному лизису JOVI-1 в присутствии комплемента (фигура 9).
Пример 7 - Поликлональные T-клетки, специфичные по вирусу Эпштейна-Барр (EBV), можно разделить на две приблизительно равные популяции TRBC1/2.
T-клетки периферической крови были получены от здорового донора крови. Выделяли мононуклеарные клетки, и большинство клеток были криоконсервированы. Небольшое количество клеток было заражено лабораторным штаммом EBV (B95-8). Через несколько недель возникла иммортализованная зараженная EBV клеточная линия, известная как лимфобластная клеточная линия (ЛКЛ). Известно, что такая клеточная линия представляет большую коллекцию различных антигенов EBV. Предварительно криоконсервированные мононуклеарные клетки были разморожены и повторно стимулированы этой линией ЛКЛ еженедельно в течение 4 недель в присутствии IL2. Этот способ селективно наращивает EBV-специфические T-клетки из мононуклеарной популяции периферической крови. Известно, что такой способ приводит к поликлональной линии, где >90% T-клеток являются EBV-специфическими и отражают донорский иммунитет к EBV. Специфичность проверяли, демонстрируя высокий уровень лизиса аутологических клеток ЛКЛ, но не аллогенных клеток ЛКЛ или K562 (фигура 10a). Эту клеточную линию затем окрашивали JOVI-1, и было показана, что она содержит приблизительно равную смесь TRBC1 и TRBC2 T-клеток (фигура 10b).
Таким образом, если вводят терапевтическое средство, которое истощает или TRBC-1-, или TRBC2-компартмент, адекватный иммунитет к EBV будет сохраняться. Поскольку иммунитет к EBV рассматривается в качестве модельной системы иммунного ответа, резонно предположить, что иммунитет к другим патогенам будет в равной степени сохранен.
Пример 8 - Окрашивание при помощи JOV1 циркулирующей периферической Т-клеточной лимфомы
Гипотеза состояла в том, что Т-клеточные лимфомы, являясь клональными, будут экспрессировать или TRBC1, или TRBC2 Т-клеточные рецепторы, в то время как нормальные T-клетки, являясь поликлональными, будут включать популяцию T-клеток, которая представляет собой смесь T-клеток с TRBC1 или TRBC2. Чтобы продемонстрировать это, получали образец крови Т-клеточной лимфомы от пациента, чья лимфома циркулировала в периферической крови. Мононуклеарные клетки периферической крови выделяли и окрашивали панелью антител, которая включала CD5 и JOVI1. Сначала выявляли общую Т-клеточную популяцию (которая содержит и лимфомные, и нормальные T-клетки). Эта популяция содержала T-клетки с нормальной (яркой) экспрессией CD5 и T-клетки со промежуточной/слабой экспрессией CD5. Первые представляют собой нормальные T-клетки, в то время как последние представляют лимфому. Далее исследовали связывание с JOVI-1, и результаты показаны на фигуре 12.
Популяции с промежуточным и слабым CD5 (опухоль) были все TRBC2-положительными.
Пример 9 - Выявление последовательностей VH/VL JOVI-1
С использованием быстрой амплификации концов кДНК (5' RACE) с праймерами, которые отжигаются на константных областях CH1 IgG мыши и константной области каппа мыши, мы выделили единичную функциональную последовательность VH и единичную функциональную последовательность VL из гибридомы JOVI-1. Последовательности VH и VL представляют собой SEQ ID 1 и 2, соответственно (см. выше). Аннотированная последовательность VH и VL показана на фигуре 11.
Эти последовательности VH и VL клонировали обратно в рамку считывания с тяжелой цепью IgG мыши и легкой цепью каппа, соответственно. Кроме того, VH и VL были слиты для образования одноцепочечного вариабельного фрагмента (scFv), который был затем слит с областью шарнир-CH2-CH3 IgG2a мыши для создания scFv-Fv. Аминокислотная последовательность scFv приведена в подробном описании в виде SEQ ID No. 3. Рекомбинантное антитело и рекомбинантный scFv-Fc получали путем трансфекции клеток 293T. Вместе с JOVI-1 из гибридомы, окрашивали следующие клетки: клетки Юркат, нокаутные по TCR; клетки Юркат дикого типа; клетки Юркат, нокаутные по TCR и трансдуцированные TRBC1 с ко-экспрессией eBFP2 и клетки Юркат, нокаутные по TCR и трансдуцированные TRBC2 с ко-экспрессией eBFP2. И рекомбинантное антитело, и scFv-Fc, полученный из JOVI, связывали TRBC2, подтверждая, что мы идентифицировали правильные VH/VL, и что VH/VL JOVI-1 можно сложить в виде scFv. Эти данные по связыванию показаны на фигуре 13.
Пример 10 - Функция CAR на основе JOVI-1
scFv JOVI-1 клонировали в форматах CAR. Для выявления, какая длина спейсера будет приводить к оптимальному CAR JOVI-1, получали третье поколение CAR или с Fc-спейсером человека, спейсером из стебля CD8 человека или со спейсером, полученным из шарнира IgG1 (фигура 4). Первичные T-клетки человека от нормальных доноров трансдуцировали этими CAR и сравнивали лизис клеток Юркат и клеток Юркат, нокаутных по TCR. CAR с scFv JOVI-1, которые имели спейсер или из шарнира IgG1 или из стебля CD8, лизировали клетки Юркат, но не клетки Юркат, нокаутные по TCR (фигура 5), демонстрируя ожидаемую специфичность. Поскольку T-клетки здоровых доноров, трансдуцированые CAR, должны иметь смесь TRBC 1/2 T-клеток, то ожидалось, что культуры будут «самоочищаться». Фактически, это и наблюдали. Окрашивание JOVI-1 T-клеточных культур с CAR, которые стали 100% TRBC2-отрицательными, показано на фигуре 6.
МАТЕРИАЛЫ И СПОСОБЫ
ДЕМОНСТРАЦИЯ СПЕЦИФИЧНОСТИ JOVI-1
Получали трехцистронную ретровирусную кассету, которая кодировала хорошо охарактеризованный TCR человека, а также подходящий маркерный ген. Кодирующие последовательности для TCRα- и β-цепей получали при помощи синтеза гена de novo из перекрывающихся олигонуклеотидов. Эти цепи были соединены в рамке считывания с пептидом 2А ящура для ко-экспрессии. Укороченный маркерный ген CD34 клонировали из кДНК путем ПЦР и экспрессировали совместно с цепями TCR с использованием участка внутренней посадки рибосомы (IRES). Эту кассету вставляли в ретровирусный вектор. Варианты этой конструкции получали путем соединения перекрывающейся ПЦР с праймерами, которые вносили желаемые мутации. Точность конструкций подтверждали секвенированием по Сэнгеру. Клетки Юркат линии 76 представляют собой хорошо охарактеризованное производное T-клеточной линии Юркат, нокаутной по обеим цепям TCR, α и β. Эту линию Юркат трансдуцировали вышеуказанными ретровирусными векторами с использованием стандартных способов.
ОКРАШИВАНИЕ И АНАЛИЗ КЛЕТОК ЮРКАТ, T-КЛЕТОК ПЕРИФЕРИЧЕСКОЙ КРОВИ И КЛЕТОЧНЫХ ЛИНИЙ
Клетки Юркат получали из Европейской коллекции клеточных культур животных (ECACC) и конструировали, как описано выше. Другие T-клеточные линии также получали от ECACC. Периферическую кровь брали путем венозной пункции у здоровых доноров. Кровь обрабатывали фиколлом для выделения мононуклеарных клеток. Клетки окрашивали JOVI-1, а также коммерчески доступными моноклональными антителами, которые распознают все TCR и CD3. В случае сконструированных T-клеток, клетки окрашивали антителами, которые распознают CD34. В случае мононуклеарных клеток периферической крови, клетки окрашивали антителами, которые распознают CD4 и CD8. Антитела приобретали, конъюгированными с подходящими флуорофорами, так что можно было получать независимые флуоресцентные сигналы с одновременным анализом клеток в проточном цитометре.
ДЕМОНСТРАЦИЯ СПЕЦИФИЧЕСКОГО ЛИЗИСА T-КЛЕТОК С TRBC1
T-клетки Юркат дикого типа (TRBC1 - TCR), и T-клетки Юркат TCR KO с введенным TRBC2 TCR смешивали вместе в соотношении 1:1. Эту смесь клеток Юркат затем инкубировали с моноклональным антителом JOVI-1 в концентрации 1 мкг/мл в отсутствие или в присутствии комплемента. Через четыре часа клетки окрашивали аннексином-V и 7AAD, и CD34. Удобно то, что по маркерному гену CD34 можно различать клетки Юркат дикого типа (TRBC1) и трансгенные (TRBC2). Клеточные популяции анализировали проточной цитометрией. Живые клетки селективно исследовали путем гейтинга цитометрических событий, которые были отрицательными по аннексину-V и имели слабую яркость по 7AAD. Таким образом, была исследована выживаемость трансгенных T-клеток (TRBC2) по сравнению с Т-клетками дикого типа (TRBC1).
Пример 11 - Исследование клональности Т-клеточных лимфопролиферативных нарушений
Четырех пациентов, трех с Т-клеточным лимфопролиферативным заболеванием с большими гранулярными лимфоцитами (TЛ-БГЛ) и одного с периферической Т-клеточной лимфомой (ПТКЛ) тестировали чтобы подтвердить, что злокачественные клетки были однородно или TRBC1- положительными, или отрицательными.
У пациентов с T-лимфопролиферативными заболеваниями собирали цельную кровь или костный мозг. Мононуклеарные клетки периферической крови (PBMC) получали путем центрифугирования в градиенте Фиколл. Свежеполученные PBMC осаждали и окрашивали в течение 20 минут соответствующими предварительно конъюгированными антителами. Клетки затем отмывали и ресуспендировали в фосфатно-солевом буфере и сразу же анализировали проточной цитометрией на BD LSR Fortessa II. Живые лимфоциты идентифицировали по свойствам прямого/бокового светорассеяния (FSc/SSc) и по неспособности поглощать краситель для выявления мертвых клеток. T-клетки идентифицировали по окрашиванию с анти-TCR альфа/бета антителом. Опухолевые и нормальные Т-клеточные популяции идентифицировали с использованием соответствующих красителей для клеточной поверхности для каждого образца, в зависимости от иммунофенотипа, предварительно определенного в клиническом лабораторном анализе.
Результаты показаны на фигурах с 18 до 21.
У пациента A (TЛ-БГЛ, фигура 18), нормальные T-клетки были яркие по CD7, и содержали смесь CD4/CD8 клеток и смешанную популяцию TRBC1+ или TRBC1- клеток. Напротив, злокачественные клетки были CD7- или CD7-слабыми, были однородно CD8+CD4-, и были однородно TRBC1-.
У пациента B (TЛ-БГЛ, фигура 19), злокачественные клетки были идентифицированы как CD4-, CD8+, CD7+ CD57+ и были клонально TRBC1- (выделенная панель). Нормальные CD4+CD8- и CD4-CD8+ T-клетки содержали TRBC1+ и TRBC1-популяции.
У пациента C (TЛ-БГЛ, фигура 20), нормальные CD4+ и CD8+ T- клеточные популяции были на 30-40% TRBC1+. Злокачественные клетки были идентифицированы как CD4-, CD8+, CD7+ CD57+ и были клонально TRBC1+ (выделенная панель, следует заметить, что 84% клеток являются TRBC1, оставшиеся 16%, вероятно, загрязнены «нормальными» T-клетками). Нормальные CD4+CD8- и CD4-CD8+ T-клетки содержали TRBC1+ и TRBC1-популяции.
У пациента D (ПТКЛ-НУ, фигура 21), злокачественные клетки в костном мозге, выявленные на основании высокого прямого светорассеяния (FSC) и слабой яркости CD5 и CD4, были однородно TRBC1+, в то время как CD4+CD8- и CD4-CD8+ T-клетки содержали и TRBC1+, и TRBC1-популяции.
Пример 12 - Получение моноклональных антител человека, которые различают две изоформы константного домена β-цепи Т-клеточного рецептора, с использованием фагового дисплея
Для того чтобы получить антитела, которые различают TRBC2 и TRBC1, были синтезированы пептидные фрагменты, покрывающие область различия между двумя изоформами TRBC. Из четырех аминокислотных различий между TRBC2 и TRBC1, два были обнаружены в начале константных доменов. Были синтезированы пептиды (см. ниже), представляющие эти области, и использованы для создания антител.
TRBC2 VLEDLKNVFPPEVAV (SEQ ID No. 36)
TRBC1 VLEDLNKVFPPEVAV (SEQ ID No. 37)
Эти пептиды получали в биотинилированной, не-биотинилированной и модифицированной цистеином формах (путем добавления цистеина на C-конце). Модифицированные цистеином формы TRBC1 и TRBC2 затем конъюгировали с модифицированным бычьим сывороточным альбумином (Imm-Link БСА, Innova 462-001) или овальбумином (Imm-Link Ovalbumin, Innova 461-001) в соответствии с условиями, рекомендованными производителем.
Результаты
Отборы антител фагового дисплея
Конструировали библиотеки фагового дисплея человека и проводили отборы фагов, как описано в (Schofieldetal.,2007 Геном Biol8, R254). Для того чтобы идентифицировать TRBC1- и TRBC2-специфичные антитела в библиотеке антител, проводили множественные раунды отборов фагового дисплея. Использовали параллельно две стратегии отбора фагов для того, чтобы максимизировать шанс получения большой панели специфических связывающих агентов. Эти стратегии известны как отбор на твердой фазе и отбор в жидкой фазе (фигура 21). При отборе на твердой фазе, фаговые антитела имеют возможность связываться с целевым антигеном, иммобилизованным на твердой поверхности (Schofieldetal.,2007,как выше). При отборе в жидкой фазе, фаговые антитела связываются с биотинилированным антигеном в растворе, и комплекс фаговое антитело-антиген затем захватывается парамагнитными гранулами, покрытыми стрептавидином или нейтравидином. В пределах стратегии отбора на твердой фазе использовали два различных подхода иммобилизации или презентации антигена. При использовании первого подхода, пептиды TRBC, конъюгированные с бычьим сывороточным альбумином (БСА) или овальбумином (ОА) были иммобилизованы в иммунопробирках Maxisorp™ путем прямой абсорбции. При использовании второго подхода, биотинилированные пептиды TRBC были опосредованно иммобилизованы в иммунопробирках Maxisorp™, которые были предварительно покрыты стрептавидином или нейтравидином.
Для того чтобы отобрать антитела, которые специфичны к желаемому пептиду, все отборы проводили в присутствии избытка противоположного пептида. Например, все отборы по TRBC1 проводили в присутствии 10-кратного молярного избытка не-биотинилированного TRBC2. Этот способ известен как «деселекция» и ожидалось, что он истощит антитела, которые распознают общие эпитопы на обоих пептидах TRBC, поскольку эти антитела предпочтительно связываются с избытком TRBC2 в растворе. Во избежание обогащения клонами с антителами, которые связываются с белком-носителем (БСА или ОА) или партнером по иммобилизации (стрептавидином или нейтравидином от Thermo fisher scientific), использовали комбинацию двух стратегий.
Первая стратегия заключалась в смене партнера по конъюгации или иммобилизации между раундами отбора. Для пептидов, иммобилизованных напрямую, первый раунд отборов проводили на БСА-пептиде, а для раунда 2 использовали конъюгат OA-пептид. Аналогично, биотинилированные пептиды TRBC были иммобилизованы на стрептавидине в раунде 1, и применяли нейтравидин для иммобилизации в раунде 2.
Вторая стратегия заключалась в истощении фаговой библиотеки любых связывающих агентов к партнерам по конъюгации/иммобилизации при проведении «деселекции» в раунде 1. Для пептидов, иммобилизованных напрямую, «деселекцию» проводили при помощи этапа связывания фаг-пептид в присутствии 10-кратного молярного избытка свободного БСА в растворе. В случае биотинилированных пептидов, иммобилизованных на стрептавидине, фаговую библиотеку предварительно инкубировали с парамагнитными гранулами, покрытыми стрептавидином. Гранулы удаляли перед добавлением фага к пробиркам с антигеном, таким образом, ограничивая попадание в отбор агента, связываюшего стрептавидин. Различные использованные условия отбора обобщены на фигуре 21. См. таблицу 3 для подробной информации об условиях отбора.
Поликлональный фаг, полученный в результате раунда 2 отбора, тестировали при помощи ELISA с использованием различных презентаций пептидов или вспомогательных белков. Они включают пептиды TRBC, напрямую иммобилизированные в виде конъюгатов БСА или ОА, или биотинилированные пептиды, иммобилизованные опосредованно на стрептавидине или нейтравидине. Контрольные белки включали стрептавидин, нейтравидин, БСА и неродственный антиген. Связывание фагов выявляли при помощи антитела мыши к M13 (GE healthcare) с последующим антителом против мышиного Fc, меченным европием (Perkin Elmers), с использованием флуоресценции с временным разрешением (TRF) (фигура 22). Этот результат демонстрирует предпочтительное связывание популяций поликлональных фагов с соответствующим пептидом TRBC (по сравнению с противоположным пептидом TRBC). Например, поликлональный фаг, полученный при отборе по TRBC1, показал значительно более высокий сигнал связывания с TRBC1, чем с TRBC2, и наоборот. Присутствовало слабое связывание или связывание отсутствовало с партнерами по иммобилизации или конъюгации и с неродственным антигеном.
Субклонирование одноцепочечного антитела (scFv) и моноклональный скрининг
Популяции scFv на выходе из раунда-2 и раунда-3 отбора субклонировали в экспрессирующий вектор pSANG10-3F и трансформировали клетки E.coli BL21 (DE3). 1128 индивидуальных трансформантов (564 клона/пептида TRBC) высаживали в 12×96-луночные культуральные планшеты (94 клонов/плашку) и индуцировали экспрессию антител при помощи среды для аутоиндуцирования. Рекомбинантные моноклональные антитела, секретируемые в культуральный супернатант в течение ночи после индукции, тестировали на связывание с биотинилированными TRBC1 и TRBC2, иммобилизованными на 96-луночных планшетах Nunc Maxisorp™, покрытых нейтравидином. Из 564 клонов, отсортированных из отборов по TRBC1, 255 клонов были признаны специфичными для TRBC1 (>10000 единиц TRF для TRBC1 и <1000 единиц TRF для TRBC2). 138 TRBC2-специфичных связывающих агентов (>10000 единиц TRF для TRBC2 и <2000 единиц TRF для TRBC1) были идентифицированы из 564 клонов, отсортированных из отборов по TRBC2. На фигуре 24 представлен репрезентативный профиль связывания от одного 96-луночного планшета, полученного из отбора или по TRBC1 (фигура 24A) или по TRBC2 (фигура 24B). Подробности конкретных связывающих агентов, полученных с использованием различных условий отбора, обобщены в таблице 5.
142 и 138 специфичных связывающих агентов были выбраны из отборов по TRBC1 и TRBC2, соответственно, для анализа последовательности и дальнейшей характеризации. Последовательности тщательно выбранных клонов получали путем секвенирования по Сэнгеру с использованием набора BigDye® terminator v3.1 cycle sequencing (Life technologies). Последовательности ДНК анализировали для определения белковой последовательности, и были идентифицированы CDR доменов VH и VL. Анализ областей CDR3 VH и VL выявил 74 уникальных клона TRBC1 и 42 уникальных клона TRBC2 (где уникальность определяли как любую комбинацию последовательностей CDR3 VH и CDR3 VL). TRBC1-специфичные клоны и последовательности их CDR3 VH и CDR3 VL обобщены в таблице 1 выше. TRBC2-специфичные клоны и последовательности их CDR3 VH и CDR3 VL обобщены в таблице 2 выше.
Таблица 3A. Подробности отбора по TRBC на твердой фазе
ОА TRBC1 (Раунд 2)
ОА TRBC2 (Раунд 2)
(Раунд 2)
(Раунд 2)
Таблица 3B Подробности отбора по TRBC в жидкой фазе
(5 мкМ)
(5 мкМ)
Таблица 4: Количества в результате отборов
Таблица 5: Подробности моноклонального скрининга
Пример 13 - Выработка поликлонального антитела к TRBC путем иммунизации кроликов пептидами
Для того чтобы получить антитела, которые различают TRBC2 и TRBC1, синтезировали два пептида, которые покрывают основную область дифференцировки между двумя изоформами TRBC и использовали для иммунизации кроликов. Использовали следующие пептидные последовательности:
TRBC1: VLEDLNKVFPPEVAVC (SEQ ID No. 38)
TRBC2: VLEDLKNVFPPEVAVC (SEQ ID No. 39).
Синтезировали 15 мг пептидов TRBC1 и TRBC2. Конъюгировали гемоцианин моллюска фиссуреллы (KLH) с пептидами TRBC1 и TRBC2 через C-концевые цистеины, присутствующие на пептидах. Для каждого пептида иммунизировали по два новоанглийских кролика; всего три раза при помощи пептида TRBC1 или TRBC2, конъюгированного с KLH. После третьей иммунизации кроликов умерщвляли и обескровливали, и собирали сыворотку для очистки. Неочищенную сыворотку, полученную от кроликов пропускали через колонку с гранулами перекрестно-сшитой агарозной смолы, вместе с пептидом, использованным для иммунизации, для сбора антител, специфичных для общих сегментов и эпитопу пептида, специфичному для изоформы TRBC. Первоначально очищенный супернатант затем очищали дополнительно с использованием колонки с иммобилизованным альтернативным пептидом для удаления антител, специфичных к общим сегментам пептида.
Протокол ELISA
Покрывающий антиген(-ы):
A:пептид TRBC1
B:пептид TRBC2
Покрывающая концентрация: 4 мкг/мл, 100 мкл/лунку
Покрывающий буфер: Фосфатно-солевой буфер, pH7,4
Вторичное антитело: Козлиное антитело против кроличьего IgG (H&L), конъюгированное с пероксидазой
Результаты показаны на фигурах 25 и 26. Этим способом возможно создать поликлональную сыворотку, содержащую антитела, специфические к TRBC1 или TRBC2.
--->
Список последовательностей
<110> UCL Business PLC
<120> Способ
<130> P104381PCT
<150> GB 1403905.1
<151> 2014-03-05
<150> GB 1416908.0
<151> 2014-09-25
<160> 272
<170> PatentIn version 3.5
<210> 1
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Вариабельный домен тяжелой цепи (VH) Jovi-1 VH
<400> 1
Glu Val Arg Leu Gln Gln Ser Gly Pro Asp Leu Ile Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Val Met His Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Phe Ile Asn Pro Tyr Asn Asp Asp Ile Gln Ser Asn Glu Arg Phe
50 55 60
Arg Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser Ser Thr Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Gly Tyr Asn Phe Asp Gly Ala Tyr Arg Phe Phe Asp
100 105 110
Phe Trp Gly Gln Gly Thr Thr Leu Thr Val Ser Ser
115 120
<210> 2
<211> 113
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Вариабельный домен легкой цепи(VL) Jovi-1 VL
<400> 2
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Arg Leu Val His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Lys Leu Leu Ile Tyr Arg Val Ser Asn Arg Phe Pro Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Ile Tyr Phe Cys Ser Gln Ser
85 90 95
Thr His Val Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg
<210> 3
<211> 252
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Jovi-1 scFv
<400> 3
Glu Val Arg Leu Gln Gln Ser Gly Pro Asp Leu Ile Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Val Met His Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Phe Ile Asn Pro Tyr Asn Asp Asp Ile Gln Ser Asn Glu Arg Phe
50 55 60
Arg Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser Ser Thr Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Gly Tyr Asn Phe Asp Gly Ala Tyr Arg Phe Phe Asp
100 105 110
Phe Trp Gly Gln Gly Thr Thr Leu Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr
130 135 140
Gln Ser Pro Leu Ser Leu Pro Val Ser Leu Gly Asp Gln Ala Ser Ile
145 150 155 160
Ser Cys Arg Ser Ser Gln Arg Leu Val His Ser Asn Gly Asn Thr Tyr
165 170 175
Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile
180 185 190
Tyr Arg Val Ser Asn Arg Phe Pro Gly Val Pro Asp Arg Phe Ser Gly
195 200 205
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
210 215 220
Glu Asp Leu Gly Ile Tyr Phe Cys Ser Gln Ser Thr His Val Pro Tyr
225 230 235 240
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
245 250
<210> 4
<400> 4
000
<210> 5
<400> 5
000
<210> 6
<400> 6
000
<210> 7
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Определяющая комплементарность область(CDR) вариабельного домена
тяжелой цепи (VH) CDR1
<400> 7
Gly Tyr Thr Phe Thr Gly Tyr
1 5
<210> 8
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH CDR2
<400> 8
Asn Pro Tyr Asn Asp Asp
1 5
<210> 9
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH CDR3
<400> 9
Gly Ala Gly Tyr Asn Phe Asp Gly Ala Tyr Arg Phe Phe Asp Phe
1 5 10 15
<210> 10
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Вариабельная область легкой цепи (VL) CDR1
<400> 10
Arg Ser Ser Gln Arg Leu Val His Ser Asn Gly Asn Thr Tyr Leu His
1 5 10 15
<210> 11
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL CDR2
<400> 11
Arg Val Ser Asn Arg Phe Pro
1 5
<210> 12
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL CDR3
<400> 12
Ser Gln Ser Thr His Val Pro Tyr Thr
1 5
<210> 13
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Одноцепочечный фрагмент вариабельного домена (scFv) CP_01_E09
<400> 13
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala His Asn Ser Ser Ser Trp Ser Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Ala Ser Asp Ile Gln Met Thr Gln Ser Pro Ser
130 135 140
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
145 150 155 160
Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Lys Ala Pro Lys Leu Leu Ile Tyr Asp Ala Ser Asn Leu Glu Thr Gly
180 185 190
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe
195 200 205
Thr Ile Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln
210 215 220
Gln Tyr Asp Asn Leu Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Asp
225 230 235 240
Ile Lys Arg Thr Ala Ala Ala
245
<210> 14
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> scFv CP_01_D12
<400> 14
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Gly Gly Asp Thr Tyr Gly Phe Leu Asp Asn Trp Gly Gln Gly
100 105 110
Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Ala Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Thr
130 135 140
Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser
145 150 155 160
Gln Ser Ile Ser Ser Trp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys
165 170 175
Ala Pro Lys Leu Leu Ile Tyr Lys Ala Ser Ser Leu Glu Ser Gly Val
180 185 190
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
195 200 205
Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln
210 215 220
Phe Asn Ala Tyr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile
225 230 235 240
Lys Arg Thr Ala Ala Ala
245
<210> 15
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> scFv CP_01_D10
<400> 15
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Ser Ser Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Gly Gly Gly Ser Phe Gly Ala Phe Asp Ile Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Ala Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser
130 135 140
Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser
145 150 155 160
Gln Ser Ile Ser Arg Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys
165 170 175
Ala Pro Asn Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val
180 185 190
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
195 200 205
Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln
210 215 220
Tyr Asn Ser Tyr Pro Leu Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
225 230 235 240
Lys Arg Thr Ala Ala Ala
245
<210> 16
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> scFv CP_01_C08
<400> 16
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Ala Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Gly Tyr Ser Ser Ser Trp Tyr Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Ala Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser
130 135 140
Val Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser
145 150 155 160
Gln Asp Ile Ser Asn Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys
165 170 175
Ala Pro Lys Leu Leu Ile Tyr Asp Ala Ser Asn Leu Glu Thr Gly Val
180 185 190
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr
195 200 205
Ile Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln
210 215 220
Tyr Asp Asn Leu Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile
225 230 235 240
Lys Arg Thr Ala Ala Ala
245
<210> 17
<211> 245
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> scFv CP_01_C11
<400> 17
Gln Val Gln Leu Val Glu Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Gly Gly Ala Gly Trp Asn Trp Gly Gln Gly Thr Met Val Thr
100 105 110
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Ala Ser Asn Phe Met Leu Thr Gln Pro His Ser Val Ser Glu Ser Pro
130 135 140
Gly Lys Thr Ala Thr Ile Ser Cys Thr Arg Ser Ser Gly Ser Ile Ala
145 150 155 160
Ser Asn Tyr Val Gln Trp Tyr Gln Gln Arg Pro Gly Ser Ala Pro Thr
165 170 175
Thr Val Ile Tyr Glu Asp Asn Gln Arg Pro Phe Gly Val Pro Asp Arg
180 185 190
Phe Ser Gly Ser Ile Asp Ser Ser Ser Asn Ser Ala Ser Leu Thr Ile
195 200 205
Ser Gly Leu Lys Thr Glu Asp Glu Ala Asp Tyr Tyr Cys Gln Ser His
210 215 220
Asp Ser Ser Asn Val Val Phe Gly Gly Gly Thr Gln Leu Thr Val Leu
225 230 235 240
Gly Gln Pro Ala Ala
245
<210> 18
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> scFv CP_01_F03
<220>
<221> прочий_признак
<222> (101)..(101)
<223> Xaa может быть любой встречающейся в природе аминокислотой
<400> 18
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Tyr Xaa Ala Ser Ser Trp Ser Gln Gly Leu Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Ala Ser Asp Ile Gln Met Thr Gln Ser Pro Ser
130 135 140
Ser Leu Ser Ala Ser Val Arg Asp Arg Val Thr Ile Thr Cys Gln Ala
145 150 155 160
Ser Gln Asp Ile Ser Asn Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Lys Ala Pro Lys Leu Leu Ile Tyr Asp Ala Ser Asn Leu Glu Thr Gly
180 185 190
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe
195 200 205
Thr Ile Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln
210 215 220
Gln Tyr Asp Asn Leu Pro Pro Thr Phe Gly Gly Gly Thr Lys Val Glu
225 230 235 240
Ile Lys Arg Thr Ala Ala Ala
245
<210> 19
<211> 251
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> scFv CP_01_E07
<400> 19
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Leu Gly Gly Ser Gly Gly Ala Phe Asp Ile Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Ala Ser Asp Ile Val Met Thr Gln Thr Pro His
130 135 140
Ser Leu Ser Val Thr Pro Gly Gln Pro Ala Ser Ile Ser Cys Lys Ser
145 150 155 160
Ser Gln Ser Leu Leu Tyr Ser Asp Gly Lys Thr Tyr Leu Tyr Trp Tyr
165 170 175
Leu Gln Lys Pro Gly Gln Pro Pro Gln Leu Leu Ile Tyr Glu Val Ser
180 185 190
Asn Arg Phe Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly
210 215 220
Val Tyr Tyr Cys Met Gln Ser Ile Gln Leu Tyr Thr Phe Gly Gln Gly
225 230 235 240
Thr Lys Val Asp Ile Lys Arg Thr Ala Ala Ala
245 250
<210> 20
<211> 244
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> scFv CP_01_D03
<400> 20
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Pro Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Lys Gln Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Ala Ser Asp Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser
130 135 140
Leu Ala Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser
145 150 155 160
Val Gly Ser Asn Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
165 170 175
Ser Leu Leu Ile Tyr Asp Ala Ser Thr Arg Ala Thr Gly Ile Pro Ala
180 185 190
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
195 200 205
Ser Leu Gln Ser Glu Asp Ile Ala Val Tyr Tyr Cys Gln Gln Tyr His
210 215 220
Arg Trp Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg
225 230 235 240
Thr Ala Ala Ala
<210> 21
<211> 249
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> scFv CP_01_F06
<400> 21
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Asp Gly Ala Met Arg Tyr Trp Gly Gln Gly Thr Met Val
100 105 110
Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Ala Ser Asp Ile Gln Met Thr Gln Ser Pro Asp Ser Leu Ala Val
130 135 140
Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Val
145 150 155 160
Leu Tyr Ser Ser Asn Asn Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys
165 170 175
Pro Gly Gln Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu
180 185 190
Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
195 200 205
Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr
210 215 220
Cys Gln Gln Tyr Tyr Asp Ser Pro Tyr Thr Phe Gly Gln Gly Thr Lys
225 230 235 240
Val Asp Ile Lys Arg Thr Ala Ala Ala
245
<210> 22
<211> 244
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> scFv CP_01_F02
<400> 22
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Pro Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Gly Tyr Ser Tyr Ala Asp Tyr Trp Gly Gln Gly Thr Met
100 105 110
Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Ala Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser
130 135 140
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly
145 150 155 160
Ile Arg Asn Asp Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
165 170 175
Lys Arg Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser
180 185 190
Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser
195 200 205
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln His Asn
210 215 220
Ser Tyr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Asp Ile Lys Arg
225 230 235 240
Thr Ala Ala Ala
<210> 23
<211> 249
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> scFv CP_03_E05
<400> 23
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Ser Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Thr Arg Ser Ser Gly Ala Phe Asp Ile Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Ala Ser Asn Phe Met Leu Thr Gln Pro His Ser Val Ser
130 135 140
Glu Ser Pro Gly Lys Thr Val Thr Ile Ser Cys Thr Arg Ser Ser Gly
145 150 155 160
Ser Ile Ala Ser Lys Tyr Val Gln Trp Tyr Gln Gln Arg Pro Gly Ser
165 170 175
Ser Pro Thr Thr Val Ile Tyr Glu Asp Asn Gln Arg Pro Ser Gly Val
180 185 190
Pro Asp Arg Phe Ser Gly Ser Ile Asp Thr Ser Ser Asn Ser Ala Ser
195 200 205
Leu Thr Ile Ser Gly Leu Arg Thr Glu Asp Glu Ala Asp Tyr Tyr Cys
210 215 220
His Ser Tyr Asp Ser Asn Asn His Ser Val Phe Gly Gly Gly Thr Lys
225 230 235 240
Val Thr Val Leu Gly Gln Pro Ala Ala
245
<210> 24
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> scFv CP_03_D05
<400> 24
Gln Val Gln Leu Val Glu Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Pro Arg Gly Arg Gly Ser Ala Phe Asp Ile Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Ala Ser Ser Tyr Glu Leu Thr Gln Pro Pro Ser Val
130 135 140
Ser Val Ser Pro Gly Gln Thr Ala Thr Ile Ser Cys Ser Gly Asp Gln
145 150 155 160
Leu Gly Gly Lys Tyr Gly His Trp Tyr Gln Lys Lys Pro Gly Gln Ser
165 170 175
Pro Val Leu Val Leu Tyr Gln Asp Arg Lys Arg Pro Ala Gly Ile Pro
180 185 190
Glu Arg Phe Ser Gly Ser Ser Ser Gly Asn Thr Ile Thr Leu Thr Ile
195 200 205
Ser Gly Thr Gln Ala Val Asp Glu Ala Asp Tyr Tyr Cys Gln Ala Trp
210 215 220
Asp Thr Asn Leu Gly Gly Val Phe Gly Gly Gly Thr Lys Val Thr Val
225 230 235 240
Leu Gly Gln Pro Ala Ala
245
<210> 25
<211> 249
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> scFv CP_03_H06
<400> 25
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Tyr Met Ser Trp Ile Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Glu Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Thr Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Arg Val Gly Gly Met Asp Val Trp Gly Gln Gly Thr Met
100 105 110
Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Ala Ser Asn Phe Met Leu Thr Gln Pro His Ser Val Ser Glu
130 135 140
Ser Pro Gly Lys Thr Val Thr Ile Ser Cys Thr Arg Ser Ser Gly Ser
145 150 155 160
Ile Ala Ser Asn Tyr Val Gln Trp Tyr Gln Gln Arg Pro Gly Ser Ser
165 170 175
Pro Thr Thr Val Ile Tyr Glu Asp Asn Gln Arg Pro Ser Gly Val Pro
180 185 190
Asp Arg Phe Ser Gly Ser Ile Asp Ser Ser Ser Asn Ser Ala Ser Leu
195 200 205
Thr Ile Ser Gly Leu Lys Thr Glu Asp Glu Ala Asp Tyr Tyr Cys Gln
210 215 220
Ser Phe Asp Ala Asp Asn Leu His Val Val Phe Gly Gly Gly Thr Lys
225 230 235 240
Leu Thr Val Leu Gly Gln Pro Ala Ala
245
<210> 26
<211> 248
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> scFv CP_03_C12
<400> 26
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Thr Gly Pro Ile Asp Tyr Trp Gly Gln Gly Thr Met Val
100 105 110
Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Ala Ser Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val
130 135 140
Thr Pro Gly Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu
145 150 155 160
Leu His Ser Asp Gly Lys Thr Tyr Leu Tyr Trp Tyr Leu Gln Lys Pro
165 170 175
Gly Gln Pro Pro Gln Leu Leu Val Tyr Glu Val Ser Asn Arg Phe Ser
180 185 190
Gly Val Pro Asp Lys Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
195 200 205
Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys
210 215 220
Met Gln Gly Ile Gln Leu Pro Pro Thr Phe Gly Gly Gly Thr Lys Val
225 230 235 240
Asp Ile Lys Arg Thr Ala Ala Ala
245
<210> 27
<211> 249
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> scFv CP_03_G02
<400> 27
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Ile Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Val Trp Asn Ser Gly Ser Tyr Leu Gly Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Ala Ser Asp Ile Gln Met Thr Gln Ser
130 135 140
Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys
145 150 155 160
Gln Ala Ser Gln Asp Ile Ser Asn Tyr Leu Asn Trp Tyr Gln Gln Lys
165 170 175
Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln
180 185 190
Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
195 200 205
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr
210 215 220
Cys Gln Gln Ser Tyr Ser Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys
225 230 235 240
Leu Glu Ile Lys Arg Thr Ala Ala Ala
245
<210> 28
<211> 251
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> scFv CP_03_D04
<400> 28
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Phe Thr Val Pro Gly Gly Ala Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Ala Ser Asn Phe Met Leu Thr Gln Pro His
130 135 140
Ser Val Ser Asp Ser Pro Gly Lys Thr Val Thr Ile Ser Cys Thr Arg
145 150 155 160
Ser Ser Gly Arg Ile Gly Ser Asn Phe Val Gln Trp Tyr Gln Gln Arg
165 170 175
Pro Gly Ser Ser Pro Thr Thr Val Ile Tyr Glu Asp Asp Gln Arg Pro
180 185 190
Ser Gly Val Pro Ala Arg Phe Ser Gly Ser Ile Asp Ser Ser Ser Asn
195 200 205
Ser Ala Ser Leu Thr Ile Ser Gly Leu Thr Thr Ala Asp Glu Ala Gly
210 215 220
Tyr Tyr Cys Gln Ser Tyr Asp Ala Ser Asn Val Ile Phe Gly Gly Gly
225 230 235 240
Thr Lys Leu Thr Val Leu Gly Gln Pro Ala Ala
245 250
<210> 29
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> scFv CP_03_F10
<400> 29
Glu Val Gln Leu Val Glu Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Phe Gly Glu Arg Tyr Ala Phe Asp Ile Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Ala Ser Gln Ser Glu Leu Thr Gln Pro Pro Ser Ala Ser
130 135 140
Gly Ser Pro Gly Gln Ser Val Thr Ile Ser Cys Thr Gly Thr Ser Thr
145 150 155 160
Asp Val Gly Ala Phe His Phe Val Ser Trp Tyr Gln His Thr Pro Gly
165 170 175
Lys Ala Pro Lys Leu Leu Ile Ser Glu Val Arg Lys Arg Ala Ser Gly
180 185 190
Val Pro Asp Arg Phe Ser Gly Ser Arg Ser Gly Asn Thr Ala Ser Leu
195 200 205
Thr Val Ser Gly Leu Gln Ser Glu Asp Glu Ala Asp Tyr Phe Cys Ser
210 215 220
Ala Tyr Thr Gly Ser Asn Tyr Val Phe Gly Ser Gly Thr Lys Leu Thr
225 230 235 240
Val Leu Gly Gln Pro Ala Ala
245
<210> 30
<211> 252
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> scFv CP_03_G09
<400> 30
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Ala Ala Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Asn Asp Tyr Ala
50 55 60
Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ala Arg Asp Gln Trp Leu Ala Asn Tyr Tyr Tyr Tyr Gly
100 105 110
Met Asp Val Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Ala Ser Ser Tyr Glu
130 135 140
Leu Thr Gln Pro Leu Ser Val Ser Val Ala Leu Gly Gln Thr Ala Arg
145 150 155 160
Ile Thr Cys Gly Gly Asn Asn Ile Gly Ser Lys Asn Val His Trp Tyr
165 170 175
Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr Arg Asp Asn
180 185 190
Asn Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser Asn Ser Gly
195 200 205
Asn Thr Ala Thr Leu Thr Ile Ser Lys Ala Gln Ala Gly Asp Glu Ala
210 215 220
Asp Tyr Tyr Cys Gln Val Trp Asp Ser Asn Ser Trp Val Phe Gly Gly
225 230 235 240
Gly Thr Lys Leu Thr Val Leu Gly Gln Pro Ala Ala
245 250
<210> 31
<211> 252
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> scFv CP_03_F09
<400> 31
Gln Met Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ala Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Asn Arg Gly Gly Ser Tyr Lys Ser Val Gly Met Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Ala Ser Asn Phe Met Leu Thr Gln Pro
130 135 140
Gln Ser Val Ser Glu Ser Pro Gly Lys Thr Val Thr Ile Ser Cys Thr
145 150 155 160
Arg Ser Ser Gly Asn Phe Ala Ser Lys Tyr Val Gln Trp Tyr Gln Gln
165 170 175
Arg Pro Gly Ser Ser Pro Thr Thr Val Ile Tyr Glu Asn Tyr Gln Arg
180 185 190
Pro Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Ile Asp Ser Ser Ser
195 200 205
Asn Ser Ala Thr Leu Thr Ile Ser Gly Leu Lys Thr Glu Asp Glu Ala
210 215 220
Asp Tyr Tyr Cys Gln Ser Tyr Asp Glu Val Ser Val Val Phe Gly Gly
225 230 235 240
Gly Thr Gln Leu Thr Val Leu Gly Gln Pro Ala Ala
245 250
<210> 32
<211> 249
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> scFv CP_03_D09
<400> 32
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Glu Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Met Asn Pro Asn Ser Gly Asn Thr Gly Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asn Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Ser Ser Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Ala Ser Asn Phe Met Leu Thr Gln Pro Leu Ser Val Ser
130 135 140
Glu Ser Pro Gly Lys Thr Val Thr Ile Ser Cys Thr Arg Ser Ser Gly
145 150 155 160
Ser Ile Ala Ser Asn Tyr Val Gln Trp Tyr Gln Gln Arg Pro Gly Ser
165 170 175
Ala Pro Thr Thr Val Ile Tyr Glu Asp Asn Gln Arg Pro Ser Gly Val
180 185 190
Pro Asp Arg Phe Ser Gly Ser Ile Asp Ser Ser Ser Asn Ser Ala Ser
195 200 205
Leu Thr Ile Ser Gly Leu Lys Thr Glu Asp Glu Ala Asp Tyr Tyr Cys
210 215 220
Gln Ser Tyr Asn Ser Ser Asn His Trp Val Phe Gly Gly Gly Thr Lys
225 230 235 240
Val Thr Val Leu Gly Gln Pro Ala Ala
245
<210> 33
<211> 537
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Химерный антигенный рецептор (CAR), JOVI-1 CAR со «стеблевым»
спейсером CD8
<400> 33
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Val Trp Ile Pro
1 5 10 15
Gly Ser Thr Gly Glu Val Arg Leu Gln Gln Ser Gly Pro Asp Leu Ile
20 25 30
Lys Pro Gly Ala Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr
35 40 45
Phe Thr Gly Tyr Val Met His Trp Val Lys Gln Arg Pro Gly Gln Gly
50 55 60
Leu Glu Trp Ile Gly Phe Ile Asn Pro Tyr Asn Asp Asp Ile Gln Ser
65 70 75 80
Asn Glu Arg Phe Arg Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser Ser
85 90 95
Thr Thr Ala Tyr Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Gly Ala Gly Tyr Asn Phe Asp Gly Ala Tyr
115 120 125
Arg Phe Phe Asp Phe Trp Gly Gln Gly Thr Thr Leu Thr Val Ser Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Ser Leu Gly Asp
165 170 175
Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Arg Leu Val His Ser Asn
180 185 190
Gly Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro
195 200 205
Lys Leu Leu Ile Tyr Arg Val Ser Asn Arg Phe Pro Gly Val Pro Asp
210 215 220
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser
225 230 235 240
Arg Val Glu Ala Glu Asp Leu Gly Ile Tyr Phe Cys Ser Gln Ser Thr
245 250 255
His Val Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
260 265 270
Ser Asp Pro Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
275 280 285
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
290 295 300
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
305 310 315 320
Ile Phe Trp Val Leu Val Val Val Gly Gly Val Leu Ala Cys Tyr Ser
325 330 335
Leu Leu Val Thr Val Ala Phe Ile Ile Phe Trp Val Arg Ser Lys Arg
340 345 350
Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr Pro Arg Arg Pro
355 360 365
Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro Pro Arg Asp Phe
370 375 380
Ala Ala Tyr Arg Ser Arg Asp Gln Arg Leu Pro Pro Asp Ala His Lys
385 390 395 400
Pro Pro Gly Gly Gly Ser Phe Arg Thr Pro Ile Gln Glu Glu Gln Ala
405 410 415
Asp Ala His Ser Thr Leu Ala Lys Ile Arg Val Lys Phe Ser Arg Ser
420 425 430
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
435 440 445
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
450 455 460
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
465 470 475 480
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
485 490 495
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
500 505 510
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
515 520 525
Leu His Met Gln Ala Leu Pro Pro Arg
530 535
<210> 34
<211> 727
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> JOVI-1 CAR со спейсером H-CH2-CH3pvaa
<400> 34
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Val Trp Ile Pro
1 5 10 15
Gly Ser Thr Gly Glu Val Arg Leu Gln Gln Ser Gly Pro Asp Leu Ile
20 25 30
Lys Pro Gly Ala Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr
35 40 45
Phe Thr Gly Tyr Val Met His Trp Val Lys Gln Arg Pro Gly Gln Gly
50 55 60
Leu Glu Trp Ile Gly Phe Ile Asn Pro Tyr Asn Asp Asp Ile Gln Ser
65 70 75 80
Asn Glu Arg Phe Arg Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser Ser
85 90 95
Thr Thr Ala Tyr Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Gly Ala Gly Tyr Asn Phe Asp Gly Ala Tyr
115 120 125
Arg Phe Phe Asp Phe Trp Gly Gln Gly Thr Thr Leu Thr Val Ser Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Ser Leu Gly Asp
165 170 175
Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Arg Leu Val His Ser Asn
180 185 190
Gly Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro
195 200 205
Lys Leu Leu Ile Tyr Arg Val Ser Asn Arg Phe Pro Gly Val Pro Asp
210 215 220
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser
225 230 235 240
Arg Val Glu Ala Glu Asp Leu Gly Ile Tyr Phe Cys Ser Gln Ser Thr
245 250 255
His Val Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
260 265 270
Ser Asp Pro Ala Glu Pro Lys Ser Pro Asp Lys Thr His Thr Cys Pro
275 280 285
Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro
290 295 300
Pro Lys Pro Lys Asp Thr Leu Met Ile Ala Arg Thr Pro Glu Val Thr
305 310 315 320
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
325 330 335
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
340 345 350
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
355 360 365
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
370 375 380
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
385 390 395 400
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp
405 410 415
Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
420 425 430
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
435 440 445
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
450 455 460
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
465 470 475 480
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
485 490 495
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Lys Asp Pro Lys Phe
500 505 510
Trp Val Leu Val Val Val Gly Gly Val Leu Ala Cys Tyr Ser Leu Leu
515 520 525
Val Thr Val Ala Phe Ile Ile Phe Trp Val Arg Ser Lys Arg Ser Arg
530 535 540
Leu Leu His Ser Asp Tyr Met Asn Met Thr Pro Arg Arg Pro Gly Pro
545 550 555 560
Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala
565 570 575
Tyr Arg Ser Arg Asp Gln Arg Leu Pro Pro Asp Ala His Lys Pro Pro
580 585 590
Gly Gly Gly Ser Phe Arg Thr Pro Ile Gln Glu Glu Gln Ala Asp Ala
595 600 605
His Ser Thr Leu Ala Lys Ile Arg Val Lys Phe Ser Arg Ser Ala Asp
610 615 620
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
625 630 635 640
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
645 650 655
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
660 665 670
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
675 680 685
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
690 695 700
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
705 710 715 720
Met Gln Ala Leu Pro Pro Arg
725
<210> 35
<211> 511
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> JOVI-1 CAR с шарнирным спейсером IgG1
<400> 35
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Val Trp Ile Pro
1 5 10 15
Gly Ser Thr Gly Glu Val Arg Leu Gln Gln Ser Gly Pro Asp Leu Ile
20 25 30
Lys Pro Gly Ala Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr
35 40 45
Phe Thr Gly Tyr Val Met His Trp Val Lys Gln Arg Pro Gly Gln Gly
50 55 60
Leu Glu Trp Ile Gly Phe Ile Asn Pro Tyr Asn Asp Asp Ile Gln Ser
65 70 75 80
Asn Glu Arg Phe Arg Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser Ser
85 90 95
Thr Thr Ala Tyr Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Gly Ala Gly Tyr Asn Phe Asp Gly Ala Tyr
115 120 125
Arg Phe Phe Asp Phe Trp Gly Gln Gly Thr Thr Leu Thr Val Ser Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Ser Leu Gly Asp
165 170 175
Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Arg Leu Val His Ser Asn
180 185 190
Gly Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro
195 200 205
Lys Leu Leu Ile Tyr Arg Val Ser Asn Arg Phe Pro Gly Val Pro Asp
210 215 220
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser
225 230 235 240
Arg Val Glu Ala Glu Asp Leu Gly Ile Tyr Phe Cys Ser Gln Ser Thr
245 250 255
His Val Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
260 265 270
Ser Asp Pro Ala Glu Pro Lys Ser Pro Asp Lys Thr His Thr Cys Pro
275 280 285
Pro Cys Pro Lys Asp Pro Lys Phe Trp Val Leu Val Val Val Gly Gly
290 295 300
Val Leu Ala Cys Tyr Ser Leu Leu Val Thr Val Ala Phe Ile Ile Phe
305 310 315 320
Trp Val Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn
325 330 335
Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr
340 345 350
Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Arg Asp Gln Arg Leu
355 360 365
Pro Pro Asp Ala His Lys Pro Pro Gly Gly Gly Ser Phe Arg Thr Pro
370 375 380
Ile Gln Glu Glu Gln Ala Asp Ala His Ser Thr Leu Ala Lys Ile Arg
385 390 395 400
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
405 410 415
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
420 425 430
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
435 440 445
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
450 455 460
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
465 470 475 480
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
485 490 495
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
500 505 510
<210> 36
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетический пептид для TRBC2
<400> 36
Val Leu Glu Asp Leu Lys Asn Val Phe Pro Pro Glu Val Ala Val
1 5 10 15
<210> 37
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетический пептид для TRBC1
<400> 37
Val Leu Glu Asp Leu Asn Lys Val Phe Pro Pro Glu Val Ala Val
1 5 10 15
<210> 38
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> синтетический пептид для TRBC1
<400> 38
Val Leu Glu Asp Leu Asn Lys Val Phe Pro Pro Glu Val Ala Val Cys
1 5 10 15
<210> 39
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический пептид для TRBC2
<400> 39
Val Leu Glu Asp Leu Lys Asn Val Phe Pro Pro Glu Val Ala Val Cys
1 5 10 15
<210> 40
<211> 175
<212> БЕЛОК
<213> Homo sapiens
<400> 40
Asp Leu Asn Lys Val Phe Pro Pro Glu Val Ala Val Phe Glu Pro Ser
1 5 10 15
Glu Ala Glu Ile Ser His Thr Gln Lys Ala Thr Leu Val Cys Leu Ala
20 25 30
Thr Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp Val Asn Gly
35 40 45
Lys Glu Val His Ser Gly Val Ser Thr Asp Pro Gln Pro Leu Lys Glu
50 55 60
Gln Pro Ala Leu Asn Asp Ser Arg Tyr Cys Leu Ser Ser Arg Leu Arg
65 70 75 80
Val Ser Ala Thr Phe Trp Gln Asn Pro Arg Asn His Phe Arg Cys Gln
85 90 95
Val Gln Phe Tyr Gly Leu Ser Glu Asn Asp Glu Trp Thr Gln Asp Arg
100 105 110
Ala Lys Pro Val Thr Gln Ile Val Ser Ala Glu Ala Trp Gly Arg Ala
115 120 125
Asp Cys Gly Phe Thr Ser Val Ser Tyr Gln Gln Gly Val Leu Ser Ala
130 135 140
Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val
145 150 155 160
Leu Val Ser Ala Leu Val Leu Met Ala Met Val Lys Arg Lys Asp
165 170 175
<210> 41
<211> 175
<212> БЕЛОК
<213> Homo sapiens
<400> 41
Asp Leu Lys Asn Val Phe Pro Pro Glu Val Ala Val Phe Glu Pro Ser
1 5 10 15
Glu Ala Glu Ile Ser His Thr Gln Lys Ala Thr Leu Val Cys Leu Ala
20 25 30
Thr Gly Phe Tyr Pro Asp His Val Glu Leu Ser Trp Trp Val Asn Gly
35 40 45
Lys Glu Val His Ser Gly Val Ser Thr Asp Pro Gln Pro Leu Lys Glu
50 55 60
Gln Pro Ala Leu Asn Asp Ser Arg Tyr Cys Leu Ser Ser Arg Leu Arg
65 70 75 80
Val Ser Ala Thr Phe Trp Gln Asn Pro Arg Asn His Phe Arg Cys Gln
85 90 95
Val Gln Phe Tyr Gly Leu Ser Glu Asn Asp Glu Trp Thr Gln Asp Arg
100 105 110
Ala Lys Pro Val Thr Gln Ile Val Ser Ala Glu Ala Trp Gly Arg Ala
115 120 125
Asp Cys Gly Phe Thr Ser Glu Ser Tyr Gln Gln Gly Val Leu Ser Ala
130 135 140
Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val
145 150 155 160
Leu Val Ser Ala Leu Val Leu Met Ala Met Val Lys Arg Lys Asp
165 170 175
<210> 42
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_E09
<400> 42
Ala His Asn Ser Ser Ser Trp Ser Phe
1 5
<210> 43
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_D12
<400> 43
Gly Gly Asp Thr Tyr Gly Phe Leu
1 5
<210> 44
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_D10
<400> 44
Gly Gly Gly Ser Phe Gly Ala Phe
1 5
<210> 45
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_C08
<400> 45
Gly Tyr Ser Ser Ser Trp Tyr Leu
1 5
<210> 46
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_C11
<400> 46
Gly Gly Ala Gly
1
<210> 47
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_F03
<220>
<221> прочий_признак
<222> (3)..(3)
<223> Xaa может быть любой встречающейся в природе аминокислотой
<400> 47
Gly Tyr Xaa Ala Ser Ser Trp Ser Gln
1 5
<210> 48
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_E07
<400> 48
Asp Leu Gly Gly Ser Gly Gly Ala Phe
1 5
<210> 49
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_D03
<400> 49
Asn Lys Gln Tyr Gly Met
1 5
<210> 50
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_F06
<400> 50
Asp Asp Gly Ala Met
1 5
<210> 51
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_F02
<400> 51
Ala Gly Tyr Ser Tyr Ala
1 5
<210> 52
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_C03
<400> 52
Gly Gly Arg Tyr Ser Ser Asn Tyr Phe
1 5
<210> 53
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_D10
<400> 53
Val Gly Glu Gly Ser Ala Met
1 5
<210> 54
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_B01
<400> 54
Val Ser Ser His Tyr Asp Ser Ser Gly Tyr Tyr Ala Gly Gly Phe
1 5 10 15
<210> 55
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_D02
<400> 55
Gly Arg Asp Ser Ser Ser Trp Ser Pro
1 5
<210> 56
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_A02
<400> 56
Val Thr Thr Tyr Ser Gly Leu Asp Phe
1 5
<210> 57
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_D04
<400> 57
Lys Gly Ala Val Val Val Pro Gly Ala Leu
1 5 10
<210> 58
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_E10
<400> 58
Asn Ser Leu Tyr Gly Gly Asn Ser Ala
1 5
<210> 59
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_H08
<400> 59
Asp Gly Gly Gly Gly Arg Phe
1 5
<210> 60
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_F11
<400> 60
Gly Gly Gly Ala Leu Gly Arg Gly Met
1 5
<210> 61
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_F09
<400> 61
Leu Leu Arg Ser Gly Gly Gln Ser Tyr Ala Phe
1 5 10
<210> 62
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_D05
<400> 62
Gly Tyr Ser Ser Ser Trp Ser Phe
1 5
<210> 63
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_A09
<400> 63
Ala Gly Ser Ser Gly Trp Thr Leu
1 5
<210> 64
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_D03
<400> 64
Asp Lys Gly Trp Gly Phe
1 5
<210> 65
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_C11
<400> 65
Leu Gly Val Val Arg Gly Val Met Lys Gly Phe
1 5 10
<210> 66
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_H10
<400> 66
Ser Ser Tyr Ser Ser Ser Trp Gly Met
1 5
<210> 67
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_C04
<400> 67
Ala Asn Ser Trp Ser Ala Gly Gly Met
1 5
<210> 68
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_G03
<400> 68
Glu Arg Gly Arg Gly Tyr Ser Tyr Met
1 5
<210> 69
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_G06
<400> 69
Val Ala Arg Gly Ile His Asp Ala Phe
1 5
<210> 70
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_D06
<400> 70
Arg His Gly Met
1
<210> 71
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_B03
<400> 71
Phe Asp Ser Ser Gly Tyr Tyr Tyr
1 5
<210> 72
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_A12
<400> 72
Asp Leu Val Thr Thr Gly Ala Phe
1 5
<210> 73
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_H03
<400> 73
Ala Ile Arg Val Ser Gly Thr Pro Glu Asn Gly Phe
1 5 10
<210> 74
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_G08
<400> 74
Val Arg Ile Thr His Gly Met
1 5
<210> 75
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_A06
<400> 75
Gly Lys Leu Ala Phe
1 5
<210> 76
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_A04
<400> 76
Asn Gly Asp Ser Ser Gly Tyr His Thr Ser Pro Asn Trp Tyr Phe
1 5 10 15
<210> 77
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_E08
<400> 77
Val Ser Thr Asp Ser Ser Ser Met
1 5
<210> 78
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_A08
<400> 78
Thr Ser Gln Asp Pro Gly Ala Phe
1 5
<210> 79
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_D01
<400> 79
Ala Glu Ser Gly Val Tyr Ser Ser Asn Gly Met
1 5 10
<210> 80
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_A07
<400> 80
Val Asp Arg Val Arg Ser Gly Met
1 5
<210> 81
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_B08
<400> 81
Ile Gly Gln Tyr Cys Ser Ser Thr Ser Cys Tyr Met
1 5 10
<210> 82
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_D09
<400> 82
Asp Leu Gly Gly Ser Gly Gly Ala Phe
1 5
<210> 83
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_G07
<400> 83
Asp Ser Asp Ala Gly Tyr Phe
1 5
<210> 84
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_A05
<400> 84
Ala Ser Ile Val Ala Ser Gly Ala Phe
1 5
<210> 85
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_A08
<400> 85
Ala Gly Gly Ser Asn Ala Phe
1 5
<210> 86
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_D07
<400> 86
Val Ser Thr Asp Ser Tyr Gly Arg Gln Asn Trp Phe
1 5 10
<210> 87
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_C04
<400> 87
Gln Tyr Thr Ser Gly Arg Leu Ala Tyr Tyr Tyr His Tyr Met
1 5 10
<210> 88
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_A07
<400> 88
Gly Ile Arg Gly Ala Phe
1 5
<210> 89
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_H02
<400> 89
Val Gly Tyr Ser Thr Thr Gln Leu
1 5
<210> 90
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_F10
<400> 90
Met Ala Gly Ser Tyr Tyr Ala Phe
1 5
<210> 91
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_C10
<400> 91
Val Gly Asp Tyr Tyr Asp Ser Ser Gly Tyr Leu Asp Trp Tyr Phe
1 5 10 15
<210> 92
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_B05
<400> 92
Gly Ser Asp Thr Thr Ser Phe Val Ser
1 5
<210> 93
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_G04
<400> 93
Ala Gly His Tyr Tyr Tyr Tyr Met
1 5
<210> 94
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_F08
<400> 94
Val Thr Gly Tyr Pro Asp Tyr Tyr Asp Ser Ser Gly Phe
1 5 10
<210> 95
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_G05
<400> 95
Val Glu Gly Gly Pro Pro Tyr Tyr Phe
1 5
<210> 96
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_A03
<400> 96
Asn Gly Leu Asp Asn Tyr Gly Met
1 5
<210> 97
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_B09
<400> 97
Leu Gly Thr Thr Lys Arg Ala Phe
1 5
<210> 98
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_A10
<400> 98
Val Tyr Val Asp His Glu Gly Met
1 5
<210> 99
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_H04
<400> 99
Trp Ser Gly Ser Gly Phe
1 5
<210> 100
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_B04
<400> 100
Asp Phe Gly Trp Gly Gly Ala Phe
1 5
<210> 101
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_A05
<400> 101
Val Val Gly Gly Thr Gln His
1 5
<210> 102
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_F07
<400> 102
Asn Trp Leu Leu Tyr Tyr Gly Asp Pro Gln Gln Asn Ala Phe
1 5 10
<210> 103
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_H01
<400> 103
Leu Tyr Phe Asp Trp Phe Ala Asp Ser Gln Asn Ala Phe
1 5 10
<210> 104
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_G10
<400> 104
Val Gly Tyr Gln Pro Leu Leu Tyr Ala Asp Tyr Tyr Phe
1 5 10
<210> 105
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_G11
<400> 105
Gly Ala Met Gly Leu
1 5
<210> 106
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_G01
<400> 106
Val Tyr Tyr Leu Ser Gly Val His Ala Phe
1 5 10
<210> 107
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_A12
<400> 107
Thr Glu Arg Trp Leu Gln Phe
1 5
<210> 108
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_H05
<400> 108
Asn Gly Asp Tyr Ala Phe
1 5
<210> 109
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_B07
<400> 109
Ala Ser Arg Tyr Ser Gly Ser Tyr His Phe
1 5 10
<210> 110
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_G09
<400> 110
His Gly Ser Gln Gly Gly Phe
1 5
<210> 111
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_C02
<400> 111
Val Gly Tyr Met Gly Gly Met
1 5
<210> 112
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_D05
<400> 112
Asn Thr Pro Gly Ile Ala Ala Ala Gly Pro
1 5 10
<210> 113
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_01_D08
<400> 113
Val Gly Thr Thr Thr Val Thr Ser Phe
1 5
<210> 114
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_A11
<400> 114
Val Gly Gly Pro Leu Asn Asp Ala Phe
1 5
<210> 115
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_D08
<400> 115
His Ser Ser Gly Gly Ala Phe
1 5
<210> 116
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_E09
<400> 116
Gln Gln Tyr Asp Asn Leu Pro
1 5
<210> 117
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_D12
<400> 117
Gln Gln Phe Asn Ala Tyr Pro
1 5
<210> 118
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_D10
<400> 118
Gln Gln Tyr Asn Ser Tyr Pro
1 5
<210> 119
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_C08
<400> 119
Gln Gln Tyr Asp Asn Leu Pro
1 5
<210> 120
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_C11
<400> 120
Gln Ser His Asp Ser Ser Asn
1 5
<210> 121
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_F03
<400> 121
Gln Gln Tyr Asp Asn Leu Pro
1 5
<210> 122
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_E07
<400> 122
Met Gln Ser Ile Gln Leu
1 5
<210> 123
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_D03
<400> 123
Gln Gln Tyr His Arg Trp Pro
1 5
<210> 124
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_F06
<400> 124
Gln Gln Tyr Tyr Asp Ser Pro
1 5
<210> 125
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_F02
<400> 125
Leu Gln His Asn Ser Tyr Pro
1 5
<210> 126
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_C03
<400> 126
Gln Gln Tyr Phe Gly Thr
1 5
<210> 127
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_D10
<400> 127
Gln Gln Tyr Asn Asp Trp Pro
1 5
<210> 128
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_B01
<400> 128
Gln Ser Phe Asp Thr Asn Ser Leu
1 5
<210> 129
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_D02
<400> 129
Gln Gln Tyr Asp Asn Leu Pro
1 5
<210> 130
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_A02
<400> 130
Ser Ser Tyr Thr Ser Ser Ser Thr
1 5
<210> 131
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_D04
<400> 131
Gln Gln Tyr Asn Ser Tyr Pro
1 5
<210> 132
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_E10
<400> 132
Gln Gln Thr Phe Thr Thr Pro
1 5
<210> 133
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_H08
<400> 133
Gln Gln Tyr Asp Asn Leu Pro
1 5
<210> 134
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_F11
<400> 134
Gln Ser Tyr Asp Thr Asn Asn
1 5
<210> 135
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_F09
<400> 135
Gln Gln Ser Tyr Ser Thr Pro
1 5
<210> 136
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_D05
<400> 136
Gln Gln Tyr Asp Asn Leu Pro
1 5
<210> 137
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_A09
<400> 137
Gln Gln Tyr Asp Asn Leu Pro
1 5
<210> 138
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_D03
<400> 138
Gln Gln Tyr Asp Asn Leu Pro
1 5
<210> 139
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_C11
<400> 139
Gln Ser Tyr Asp Ser Ser Asn
1 5
<210> 140
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_H10
<400> 140
Gln Gln Tyr Asp Asn Leu Pro
1 5
<210> 141
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_C04
<400> 141
Gln Gln Tyr Asp Asp Leu Pro
1 5
<210> 142
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_G03
<400> 142
Met Gln Arg Ile Glu Phe Pro
1 5
<210> 143
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_G06
<400> 143
Gln Ser Tyr Asp Asn Thr Arg His
1 5
<210> 144
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_D06
<400> 144
Gln Ser Tyr Asp Ser Ser Asn
1 5
<210> 145
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_B03
<400> 145
Gln Ser Tyr Asp Ser Ser Asn
1 5
<210> 146
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_A12
<400> 146
Gln Gln His Asn Asp Trp Pro
1 5
<210> 147
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_H03
<400> 147
Gln Ser Tyr His Ser Ser Asn Leu
1 5
<210> 148
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_G08
<400> 148
Met Gln Ala Thr His Phe Pro
1 5
<210> 149
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_A06
<400> 149
Gln Gln Tyr Tyr Ser Thr Pro
1 5
<210> 150
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_A04
<400> 150
Gln Ser Tyr Asp Asp Ser Asn Tyr
1 5
<210> 151
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_E08
<400> 151
Ser Ser Tyr Ala Gly Ser Asn Thr Leu
1 5
<210> 152
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_A08
<400> 152
Gln Gln Ala Asn Ser Phe Pro
1 5
<210> 153
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_D01
<400> 153
Gln Ser Tyr Asp Ser Ser Ile
1 5
<210> 154
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_A07
<400> 154
Gln Ser Tyr Asp Ser Ile His
1 5
<210> 155
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_B08
<400> 155
Gln Ser Tyr Asp Ser Ser Thr His
1 5
<210> 156
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_D09
<400> 156
Gln Gln Tyr Asp Asn Leu Pro
1 5
<210> 157
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_G07
<400> 157
Gln Ser Phe Thr Ser Ser Thr Leu
1 5
<210> 158
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_A05
<400> 158
Gln Gln Tyr Asn Lys Trp Pro
1 5
<210> 159
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_A08
<400> 159
Gln Ser Tyr Asp Asp Ser Asn Tyr
1 5
<210> 160
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_D07
<400> 160
Gln Ser Tyr Asp Ser Ser Asn His
1 5
<210> 161
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_C04
<400> 161
Gln Gln Ser Tyr Ser Thr Pro
1 5
<210> 162
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_A07
<400> 162
Asn Ser Arg Asp Ser Ser Gly Asn Pro Asn
1 5 10
<210> 163
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_H02
<400> 163
Gln Ser Tyr Asp Ser Ser Asn Leu
1 5
<210> 164
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_F10
<400> 164
Gln Ser Tyr Asp Ser Ser Asn His
1 5
<210> 165
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_C10
<400> 165
Ala Val Trp Asp Asp Arg Leu Asn Gly
1 5
<210> 166
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_B05
<400> 166
Gln Gln Tyr Asp Ser Tyr Ser
1 5
<210> 167
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_G04
<400> 167
Gln Ser Ala Asp Ser Ser Gly Thr Asn
1 5
<210> 168
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_F08
<400> 168
Gln Ser Tyr Asp Ser Ser Asn His
1 5
<210> 169
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_G05
<400> 169
Gln Ser Tyr Asp Thr Arg Asn Gln
1 5
<210> 170
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_A03
<400> 170
Gln Gln Tyr Tyr Ser Thr Pro
1 5
<210> 171
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_B09
<400> 171
Gln Gln Ser Tyr Ser Thr
1 5
<210> 172
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_A10
<400> 172
Ala Ala Trp Asp Asp Ser Leu Phe
1 5
<210> 173
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_H04
<400> 173
Met Gln Arg Ile Glu Phe Pro
1 5
<210> 174
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_B04
<400> 174
Gln Gln Tyr Tyr Asn Thr Pro
1 5
<210> 175
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_A05
<400> 175
Gln Ser Tyr Asp Ser Ser Ile
1 5
<210> 176
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_F07
<400> 176
Gln Ser Tyr Asp Ser Thr Asn Leu
1 5
<210> 177
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_H01
<400> 177
Gln Gln Ser Tyr Ser Thr Pro
1 5
<210> 178
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_G10
<400> 178
Asn Ser Arg Asp Ser Ser Gly Asn His
1 5
<210> 179
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_G11
<400> 179
Gln Gln Ser Tyr Ser Thr Pro
1 5
<210> 180
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_G01
<220>
<221> прочий_признак
<222> (9)..(9)
<223> Xaa может быть любой встречающейся в природе аминокислотой
<400> 180
Asp Ser Arg Asp Thr Arg Val Asn Xaa
1 5
<210> 181
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_A12
<400> 181
Gln Gln Tyr Asp Asn Leu
1 5
<210> 182
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_H05
<400> 182
Met Gln Ala Leu Gln Thr Pro
1 5
<210> 183
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_B07
<400> 183
Gln Ser Tyr Asp Ser Ser Asn
1 5
<210> 184
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_G09
<400> 184
Ser Ser Tyr Thr Ser Ser Ser Thr
1 5
<210> 185
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_C02
<400> 185
Met Gln Ala Leu Gln Thr Pro Pro
1 5
<210> 186
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_D05
<400> 186
Gln Ser Tyr Asp Ser Thr Asn His
1 5
<210> 187
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_01_D08
<400> 187
Gln Ser Tyr Asp Ser Ala Asn Leu
1 5
<210> 188
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_A11
<400> 188
Gln Ser Phe Asp Glu Asn Ile Ser
1 5
<210> 189
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_D08
<400> 189
His Gln Ser Ala Thr Ser Pro
1 5
<210> 190
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_E05
<400> 190
Thr Arg Ser Ser Gly Ala Phe
1 5
<210> 191
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_D05
<400> 191
Pro Arg Gly Arg Gly Ser Ala Phe
1 5
<210> 192
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_H06
<400> 192
Ala Arg Val Gly Gly Met
1 5
<210> 193
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_C12
<400> 193
Asp Thr Gly Pro Ile
1 5
<210> 194
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_G02
<400> 194
Gly Val Trp Asn Ser Gly Ser Tyr Leu Gly Phe
1 5 10
<210> 195
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_D04
<400> 195
Gly Gly Phe Thr Val Pro Gly Gly Ala Phe
1 5 10
<210> 196
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_F10
<400> 196
Phe Gly Glu Arg Tyr Ala Phe
1 5
<210> 197
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_G09
<400> 197
Asp Gln Trp Leu Ala Asn Tyr Tyr Tyr Tyr Gly Met
1 5 10
<210> 198
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_F09
<400> 198
Asn Arg Gly Gly Ser Tyr Lys Ser Val Gly Met
1 5 10
<210> 199
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_D09
<400> 199
Val Ser Ser Tyr Tyr Gly Met
1 5
<210> 200
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_F02
<400> 200
Ala Pro Ala Ser Ser Ala His
1 5
<210> 201
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_02_E03
<400> 201
Gln Arg Gly Tyr Tyr Tyr Gly Met
1 5
<210> 202
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_H07
<400> 202
Ser Ser Val Ala Ala Gly Ala Phe
1 5
<210> 203
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_C02
<400> 203
Leu Ser Gly Arg Gly Leu Gly Phe
1 5
<210> 204
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_E09
<400> 204
Asp His Tyr Phe
1
<210> 205
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_D08
<400> 205
Ser Gly Arg Arg Val Thr Ala Ile
1 5
<210> 206
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_E11
<400> 206
Met Gly Arg Tyr Ser Ser Ser Trp
1 5
<210> 207
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_B05
<400> 207
His Ser Arg Phe Gly Pro Ala Phe
1 5
<210> 208
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_H02
<400> 208
Asp Arg Glu Ala Phe
1 5
<210> 209
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_D02
<400> 209
Leu Arg Gly Arg Tyr Ser Tyr Gly Tyr Ser Asp Ala Phe
1 5 10
<210> 210
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_E01
<400> 210
Leu Leu Asn Ala Val Thr Tyr Ala Phe
1 5
<210> 211
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_C11
<400> 211
Ile Gly Val Ile Gly Gly Phe
1 5
<210> 212
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_B12
<400> 212
Ile Glu Tyr Ser Ser Ser Ser Pro Tyr Phe
1 5 10
<210> 213
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_E03
<400> 213
Asp Leu Leu Pro Thr Thr Val Thr Thr Thr Gly Ala Phe
1 5 10
<210> 214
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_F01
<400> 214
Asp Ser Gly Ser Tyr Ser
1 5
<210> 215
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_C01
<400> 215
Ala Ser Tyr Pro Tyr Tyr Tyr Tyr Tyr Tyr Gly Met
1 5 10
<210> 216
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_G07
<400> 216
Ala Leu Gly His Phe
1 5
<210> 217
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_E02
<400> 217
Phe Thr Thr Gly Ser Ala Leu
1 5
<210> 218
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_C07
<400> 218
Asp Ala Ser Gly Tyr
1 5
<210> 219
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_H04
<400> 219
Asp Leu Gly Thr Tyr Tyr Tyr Gly Ser Gly Asp
1 5 10
<210> 220
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_E06
<400> 220
Val Gly Glu Leu Leu Gly Ala Phe
1 5
<210> 221
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_E05
<400> 221
His Ser Tyr Asp Ser Asn Asn His
1 5
<210> 222
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_G11
<400> 222
His Ser Gly Val Gly Gly Leu Ala Phe
1 5
<210> 223
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_G01
<400> 223
Gly Gly Ser Ile Ala Ala Ala Leu Ala Phe
1 5 10
<210> 224
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_H01
<400> 224
Val Glu Tyr Ser Arg Asn Gly Met
1 5
<210> 225
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_F11
<400> 225
Gly Arg Tyr Asn
1
<210> 226
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_C06
<400> 226
Leu Asp Tyr Tyr Tyr Gly Met
1 5
<210> 227
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_D03
<400> 227
Gly Gly Leu Ser Ser Ala Phe
1 5
<210> 228
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_G05
<400> 228
Tyr Gly Gly Gly Leu
1 5
<210> 229
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_G12
<400> 229
Pro Asp His Leu Thr Val Phe
1 5
<210> 230
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_C10
<400> 230
Val Gly Tyr Tyr Gly Met
1 5
<210> 231
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 тяжелой цепи, клон CP_03_F04
<400> 231
Tyr Glu Gly Tyr Ala Gly Phe
1 5
<210> 232
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_D05
<400> 232
Gln Ala Trp Asp Thr Asn Leu Gly
1 5
<210> 233
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_H06
<400> 233
Gln Ser Phe Asp Ala Asp Asn Leu His
1 5
<210> 234
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_C12
<400> 234
Met Gln Gly Ile Gln Leu Pro
1 5
<210> 235
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_G02
<400> 235
Gln Gln Ser Tyr Ser Thr Pro
1 5
<210> 236
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_D04
<400> 236
Gln Ser Tyr Asp Ala Ser Asn
1 5
<210> 237
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_F10
<400> 237
Ser Ala Tyr Thr Gly Ser Asn
1 5
<210> 238
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_G09
<400> 238
Gln Val Trp Asp Ser Asn Ser
1 5
<210> 239
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_F09
<400> 239
Gln Ser Tyr Asp Glu Val Ser
1 5
<210> 240
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_D09
<400> 240
Gln Ser Tyr Asn Ser Ser Asn His
1 5
<210> 241
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_F02
<400> 241
Gln Ser Tyr Asp Ser Ser His
1 5
<210> 242
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_02_E03
<400> 242
Gln Gln Ser Arg Ser Thr Pro
1 5
<210> 243
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_H07
<400> 243
Ser Ser Tyr Thr Ser Ser Ser Thr
1 5
<210> 244
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_C02
<400> 244
Ser Ser Tyr Ala Gly Ser Ser Asn Leu
1 5
<210> 245
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_E09
<400> 245
Asn Ser Tyr Thr Arg Ser Ser Thr
1 5
<210> 246
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_D08
<400> 246
Gln Ser Tyr Asp Asp Thr Asn
1 5
<210> 247
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_E11
<400> 247
Gln Ala Trp Asp Thr Asn Ile Gly
1 5
<210> 248
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_B05
<400> 248
Ser Ser Tyr Ala Gly Ser Asn Asn
1 5
<210> 249
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_H02
<400> 249
Gln Ala Trp Asp Thr Asn Ile Gly
1 5
<210> 250
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_D02
<400> 250
Ser Ser Tyr Ala Gly Ser Ser Thr
1 5
<210> 251
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_E01
<400> 251
Asn Ser Arg Asp Ser Ser Gly Phe
1 5
<210> 252
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_C11
<400> 252
Ser Ser Tyr Thr Ser Ser Ser
1 5
<210> 253
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_B12
<400> 253
Gln Ser Tyr Asp Ser Asn Asn Arg
1 5
<210> 254
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_E03
<400> 254
Ser Ser Arg Asp Ser Ser Gly Asn His
1 5
<210> 255
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_F01
<400> 255
Gln Ala Trp Asp Thr Asn Ile Gly
1 5
<210> 256
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_C01
<400> 256
Gln Val Trp Asp Ser Ser Thr Ala Asn
1 5
<210> 257
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_G07
<400> 257
Gln Ser Tyr Asp Ser Ser Asn His His
1 5
<210> 258
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_E02
<400> 258
Ser Ser Tyr Ala Gly Asn Ser Asn
1 5
<210> 259
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_C07
<400> 259
Gln Ala Trp Asp Thr Asn Ile Gly
1 5
<210> 260
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_H04
<400> 260
Gly Thr Trp Asp Ser Ser Leu Ser Ala Gly
1 5 10
<210> 261
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_E06
<400> 261
Ser Ser Leu Asp Ser Asn Asp Asn His
1 5
<210> 262
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_H03
<400> 262
Ala Ala Trp Asp Asp Ser Leu Asn Gly
1 5
<210> 263
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_G11
<400> 263
Ser Ser Tyr Ala Gly Ser Ser Thr
1 5
<210> 264
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_G01
<400> 264
His Gln Tyr Asp Val Tyr Pro
1 5
<210> 265
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_H01
<400> 265
Asn Ser Arg Asp Ser Ser Gly Asn His
1 5
<210> 266
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_F11
<400> 266
Gln Ser Tyr Asp Ser Ser Asn
1 5
<210> 267
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_C06
<400> 267
Gln Ser Tyr Asp Ser Ser Asn
1 5
<210> 268
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_D03
<400> 268
Gln Ser Tyr Asp Ser Ser Asn
1 5
<210> 269
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_G05
<400> 269
Ser Ser Tyr Ala Gly Ser Tyr Thr
1 5
<210> 270
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_G12
<400> 270
Ser Ser Tyr Thr Pro Ser Ser
1 5
<210> 271
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_C10
<400> 271
Gln Ala Trp Asp Thr Asn Ile Gly
1 5
<210> 272
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR3 легкой цепи, клон CP_03_F04
<400> 272
Gln Ala Trp Asp Thr Asn Ile Gly
1 5
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР (CAR) С АНТИГЕНСВЯЗЫВАЮЩИМИ ДОМЕНАМИ К КОНСТАНТНОЙ ОБЛАСТИ β Т-КЛЕТОЧНОГО РЕЦЕПТОРА | 2015 |
|
RU2830064C2 |
| ВЫСОКОАФФИННЫЙ Т-КЛЕТОЧНЫЙ РЕЦЕПТОР ДЛЯ РАСПОЗНАВАНИЯ АНТИГЕНА AFP | 2019 |
|
RU2836365C2 |
| АНТИГЕНСВЯЗЫВАЮЩИЕ ДОМЕНЫ ПРОТИВ TRBC1 | 2018 |
|
RU2791327C2 |
| Т-КЛЕТОЧНЫЕ РЕЦЕПТОРЫ | 2018 |
|
RU2762255C2 |
| Т-КЛЕТОЧНЫЕ РЕЦЕПТОРЫ, СПЕЦИФИЧНЫЕ В ОТНОШЕНИИ КОМПЛЕКСА ОПУХОЛЕВЫЙ АНТИГЕН NY-ESO-1/HLA-A*02 | 2016 |
|
RU2775394C2 |
| Химерные антигенные рецепторы, нацеливающиеся на CD70 | 2019 |
|
RU2801824C2 |
| Т-КЛЕТОЧНЫЕ РЕЦЕПТОРЫ | 2017 |
|
RU2775623C2 |
| ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР | 2019 |
|
RU2810092C2 |
| СВЯЗЫВАЮЩИЙ ДОМЕН | 2019 |
|
RU2829934C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, НАЦЕЛЕННЫЕ НА РЕЦЕПТОР, СВЯЗАННЫЙ С G-БЕЛКАМИ, И ИХ ПРИМЕНЕНИЕ | 2015 |
|
RU2762359C2 |
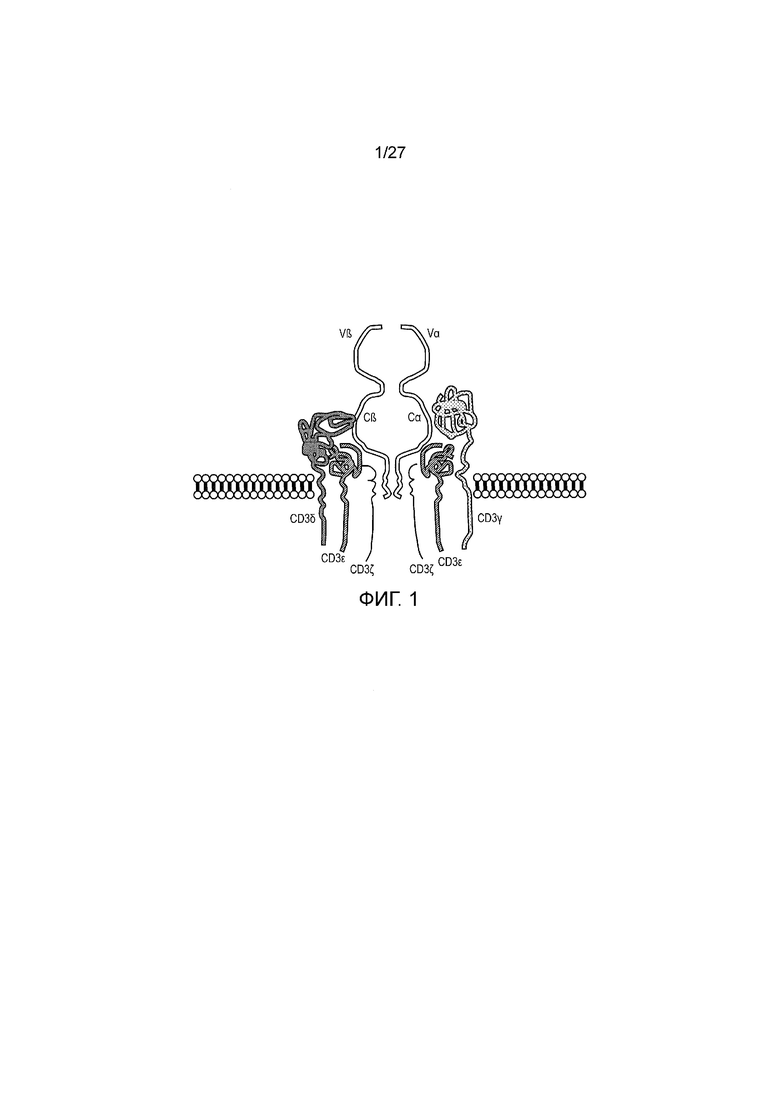
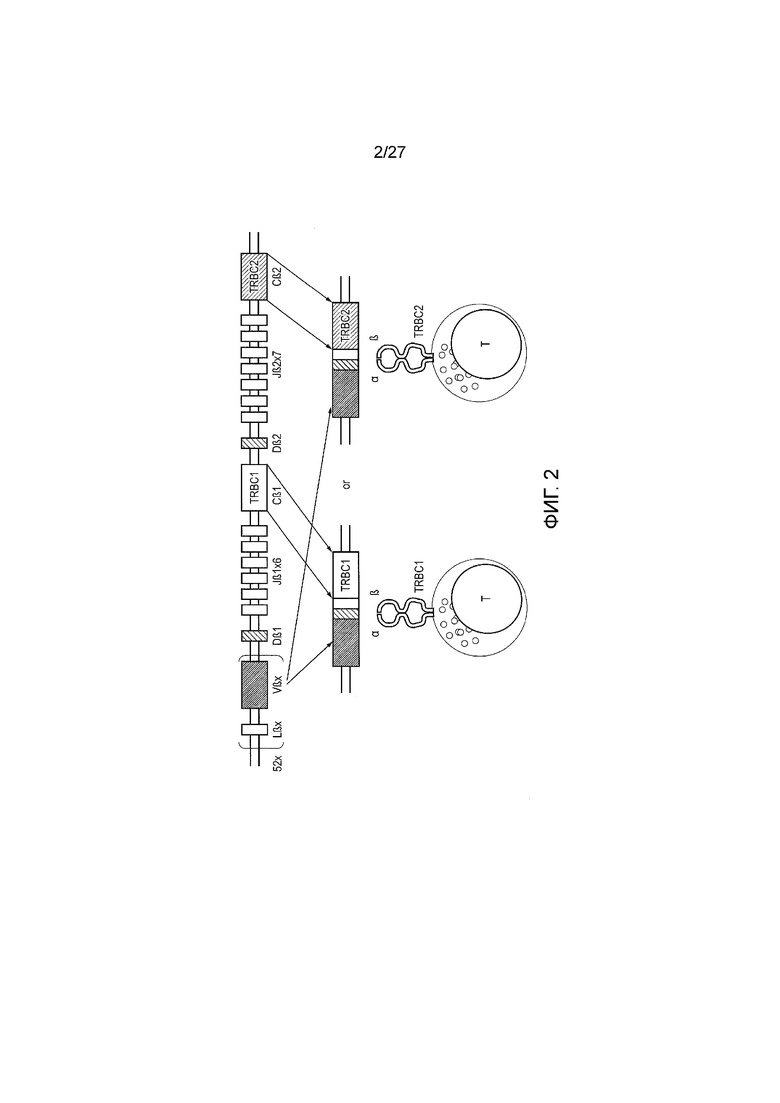
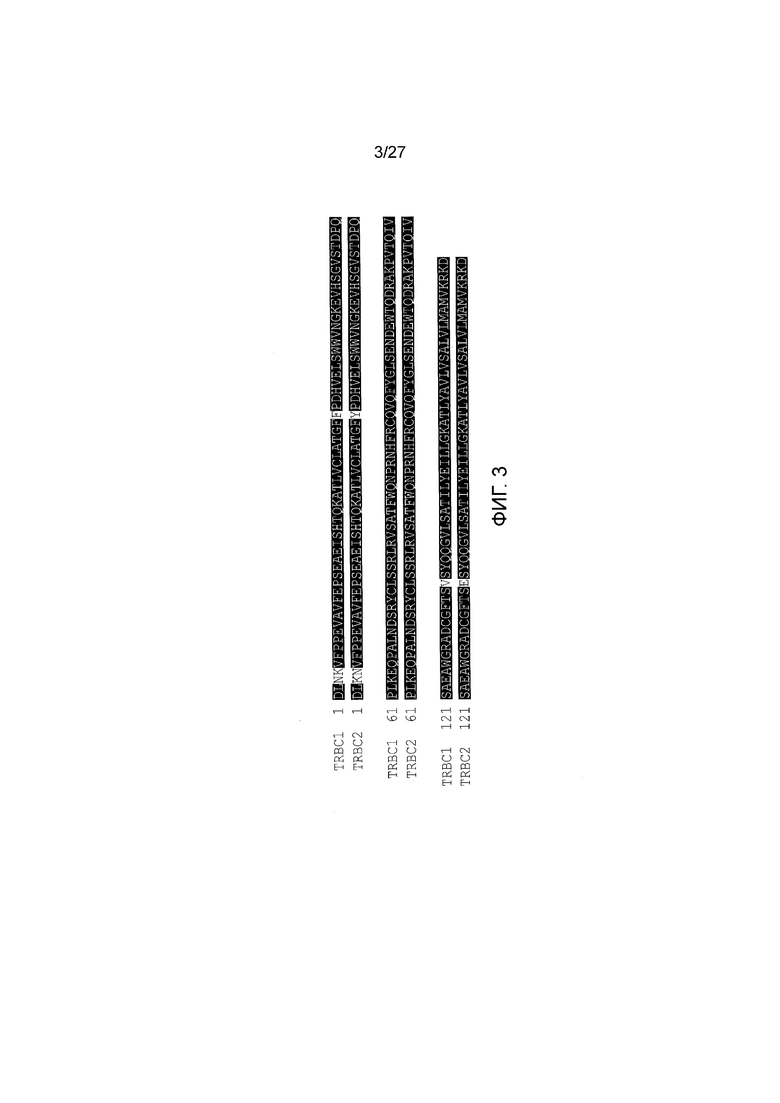
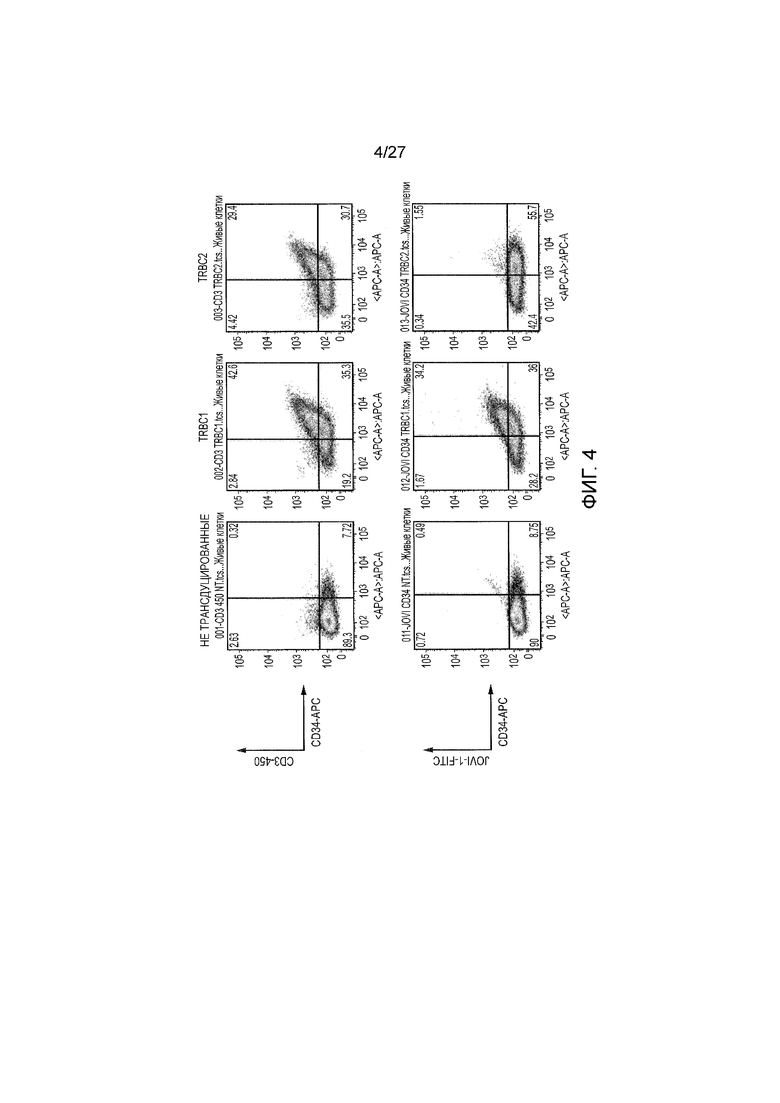
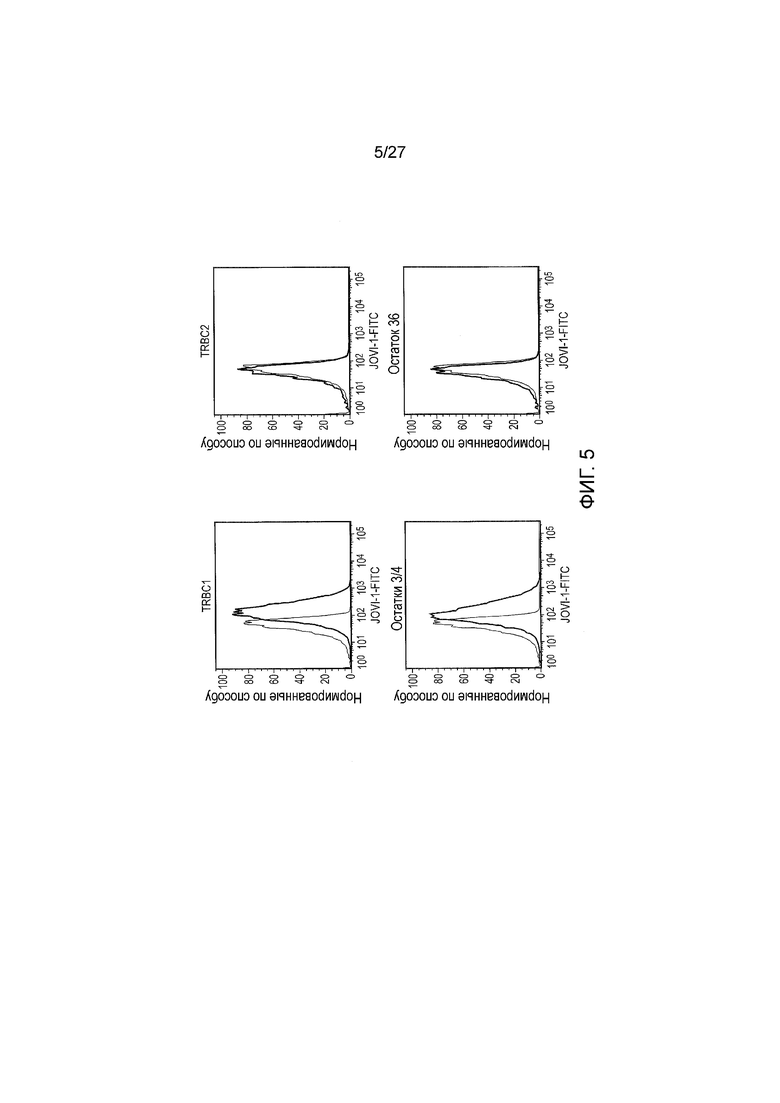
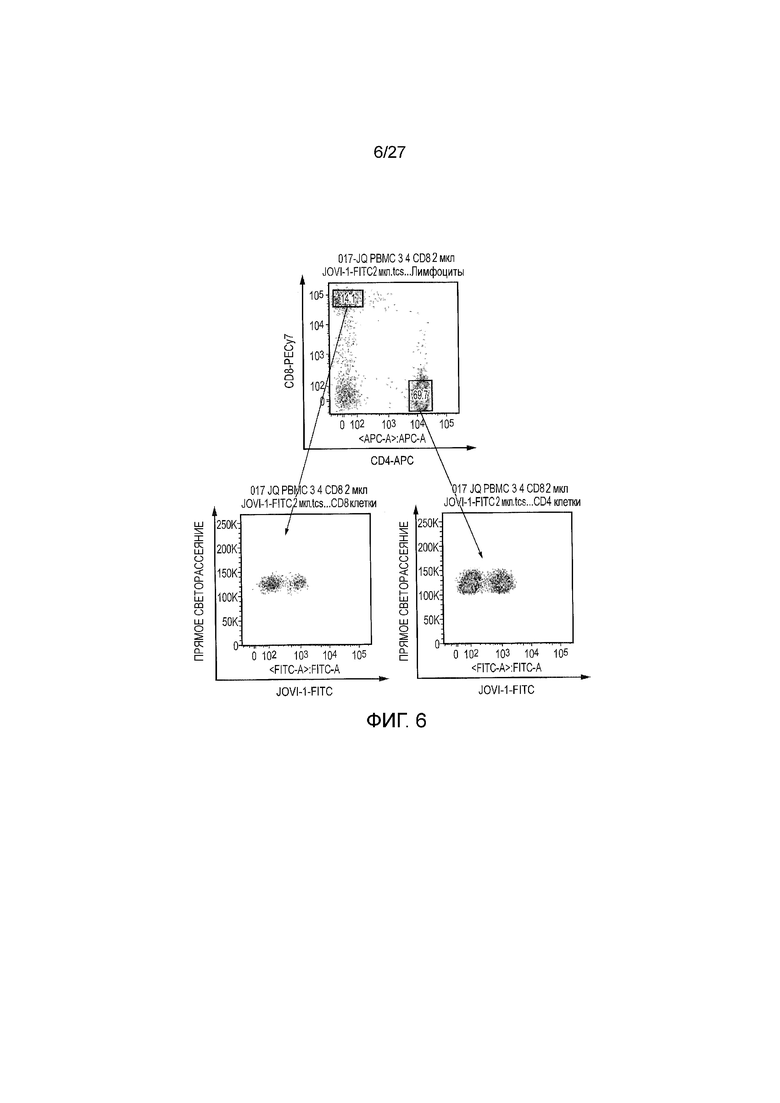
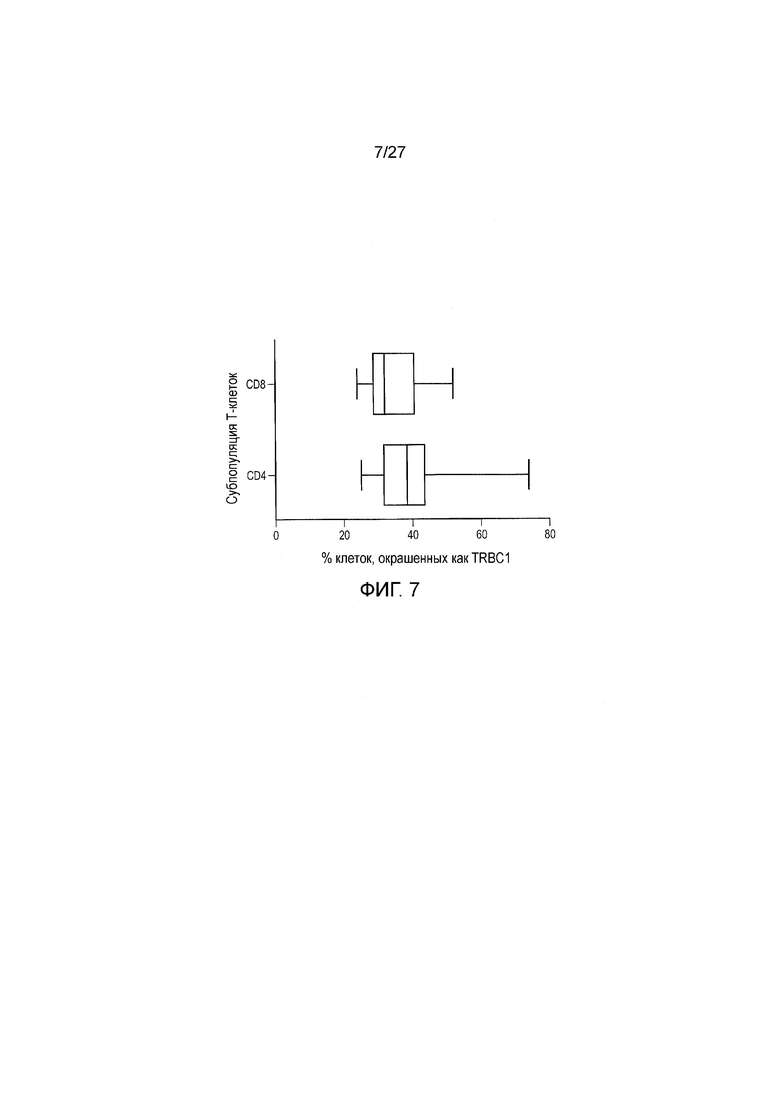
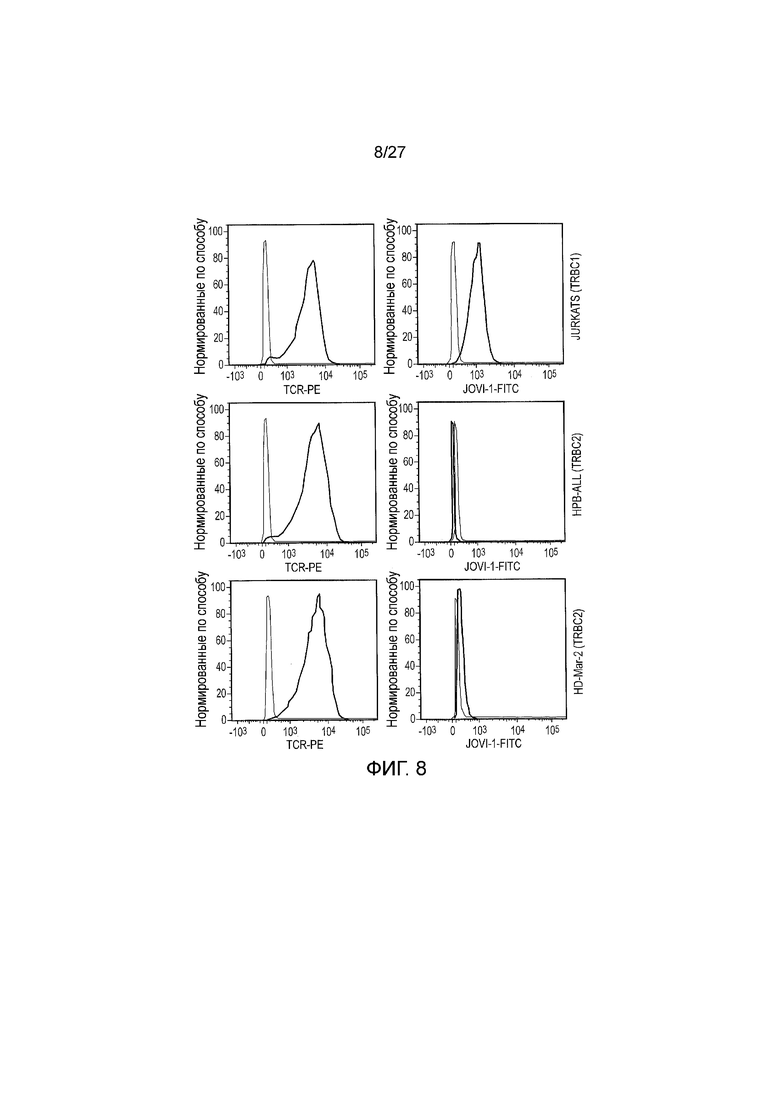
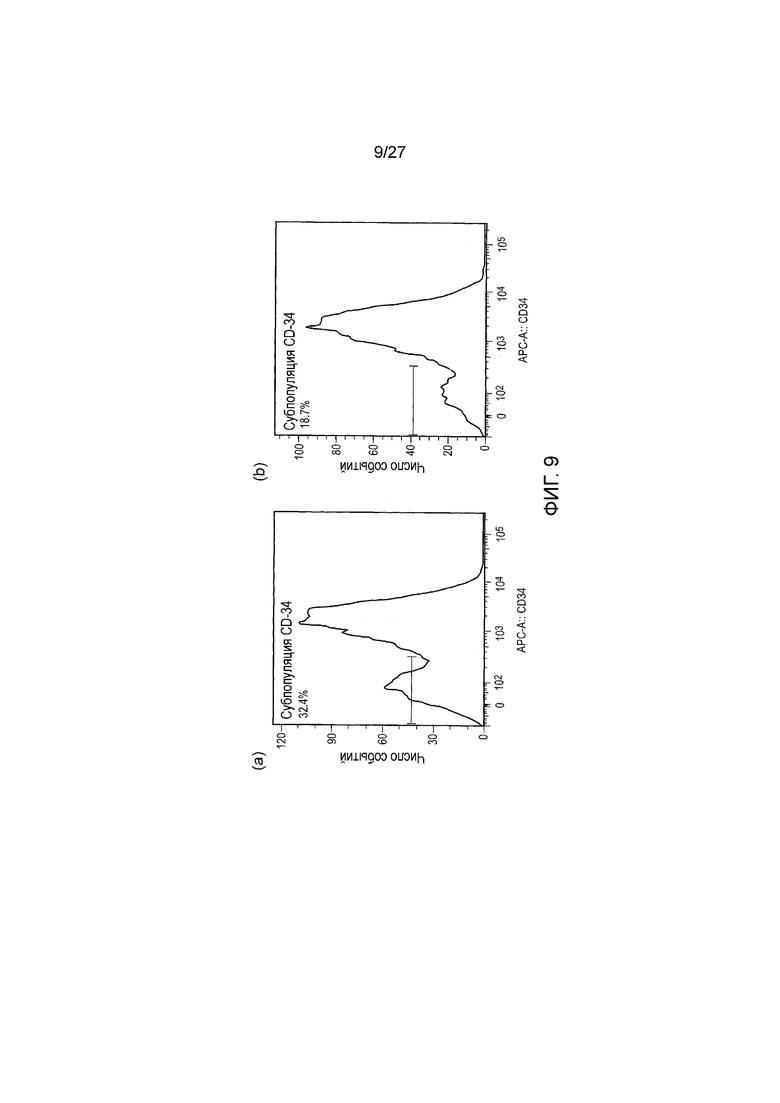
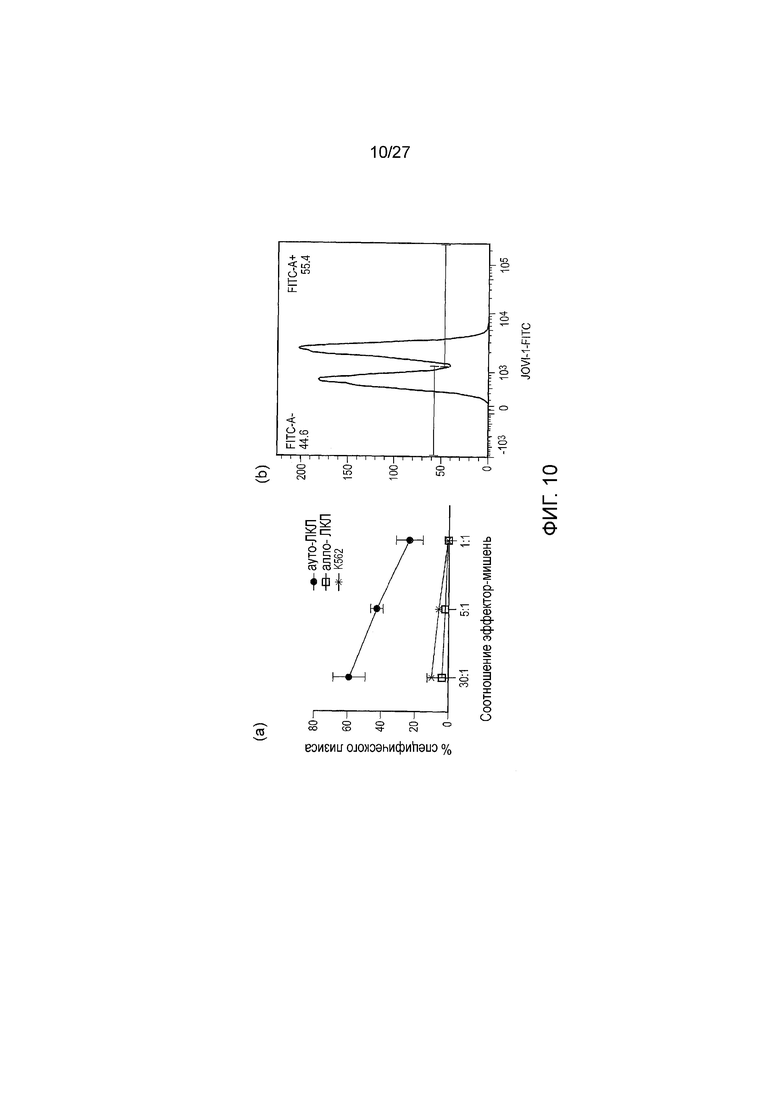

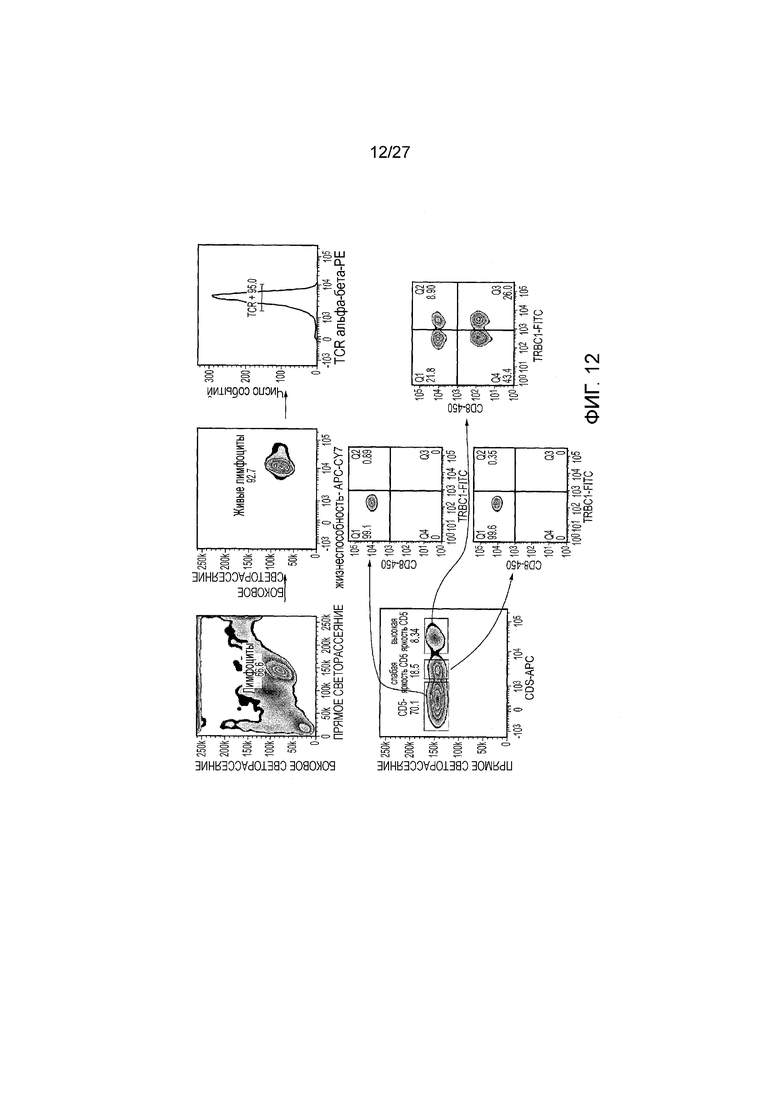
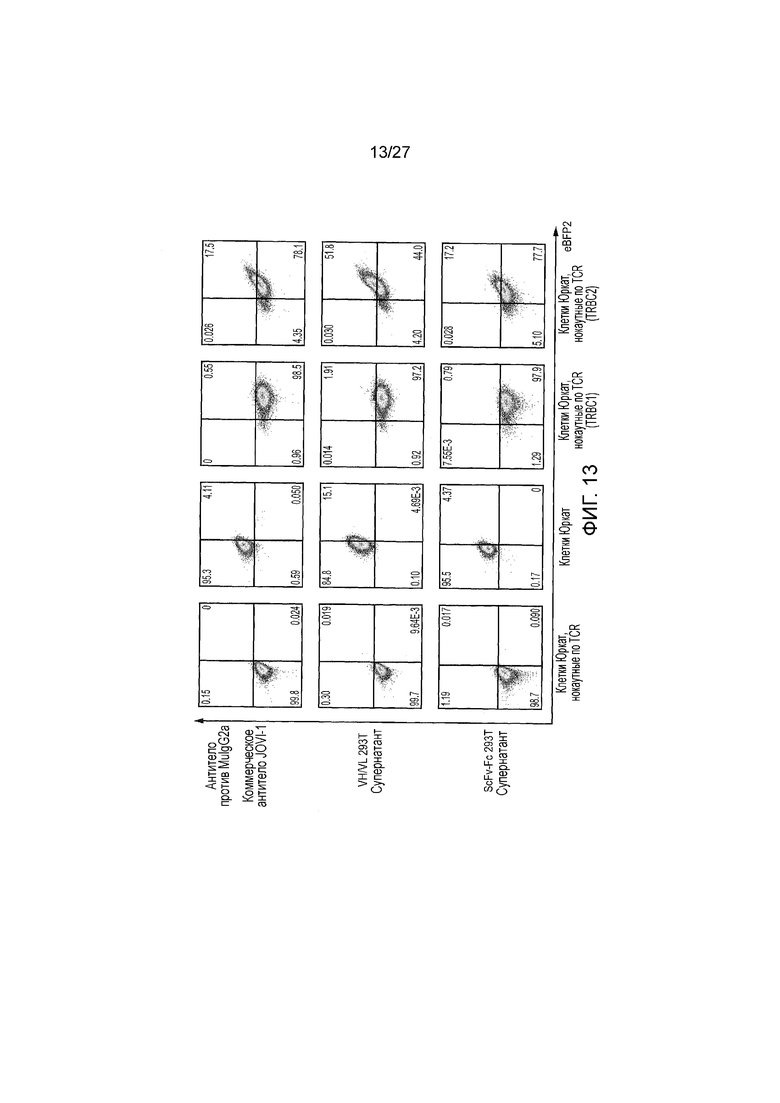
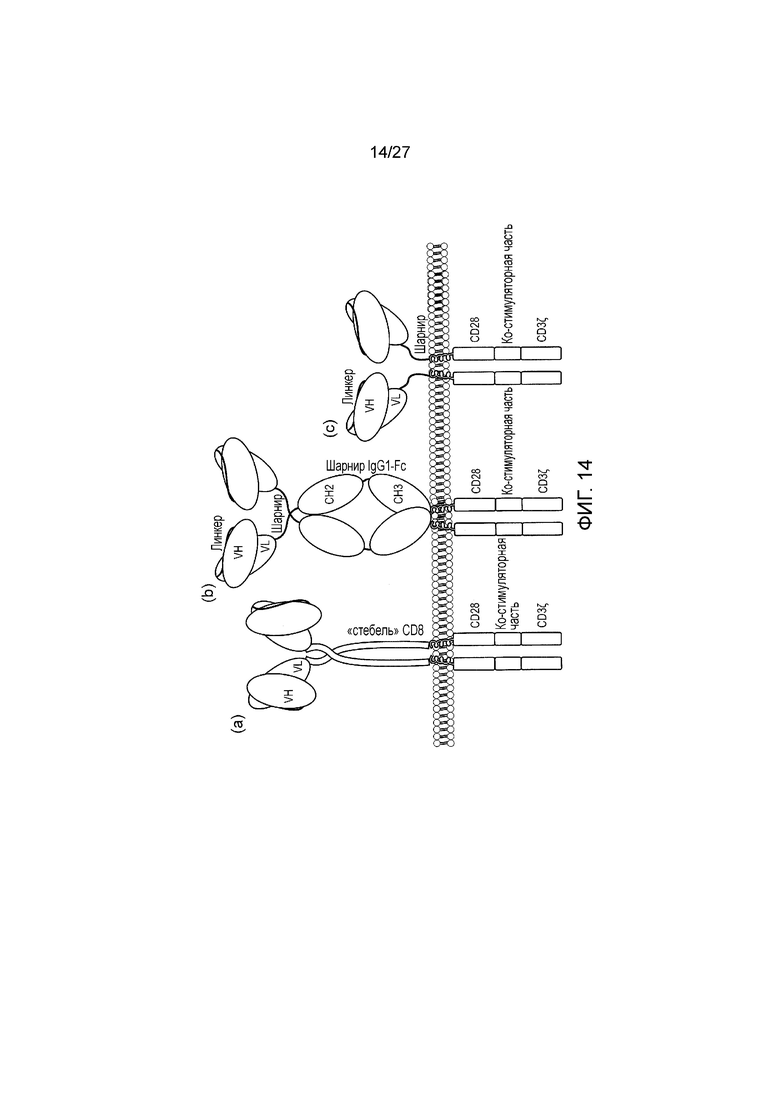
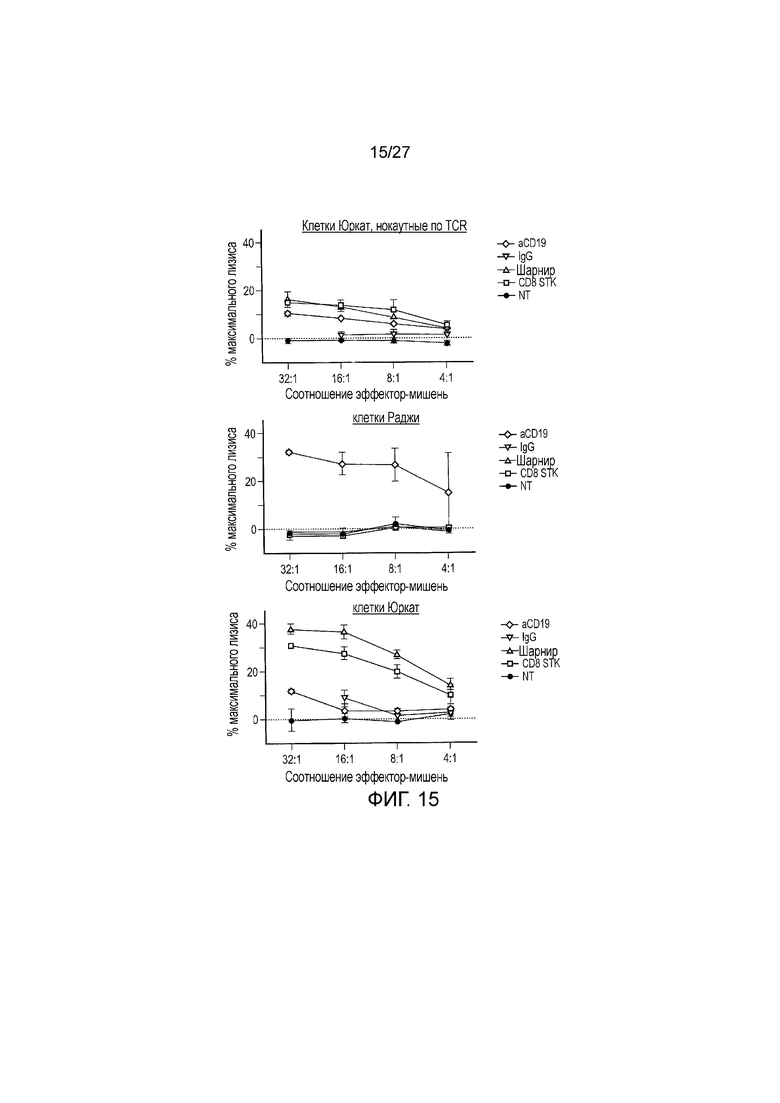
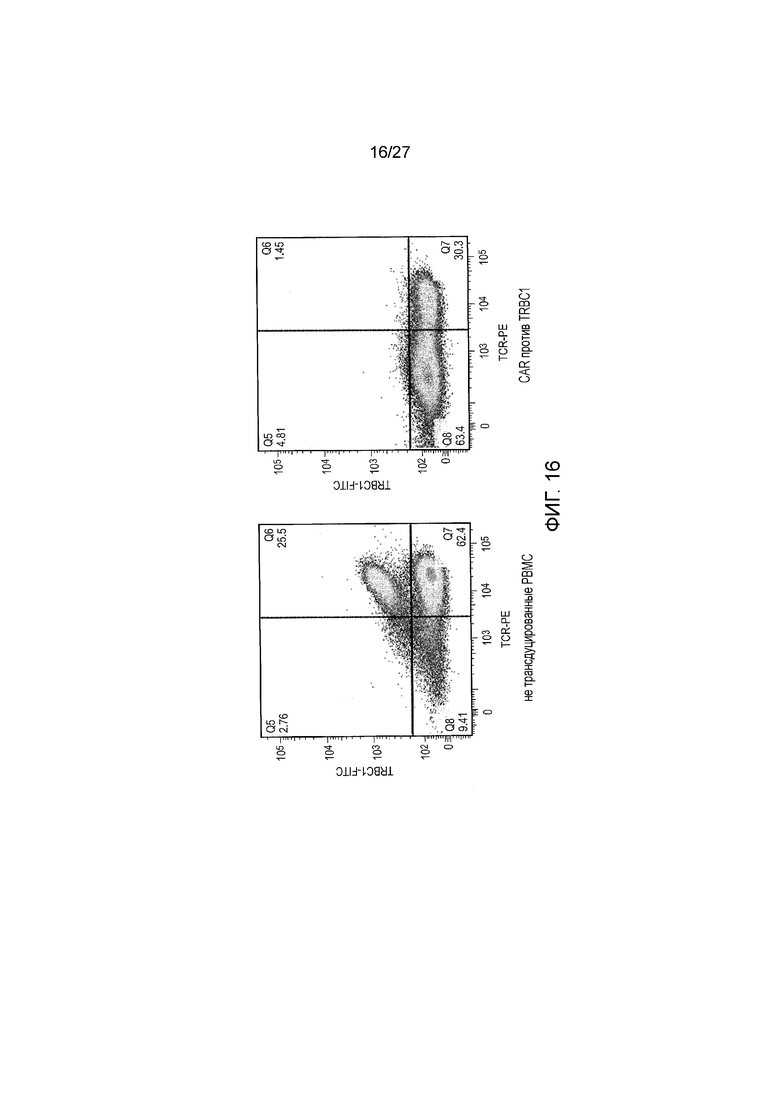
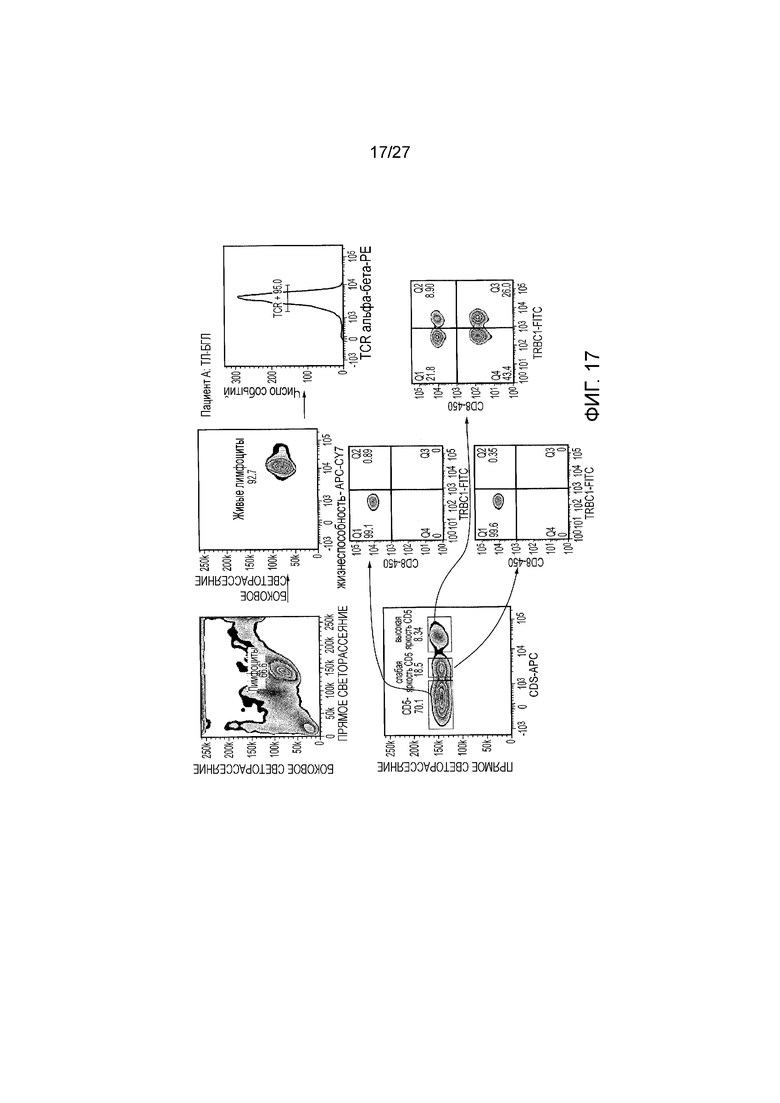
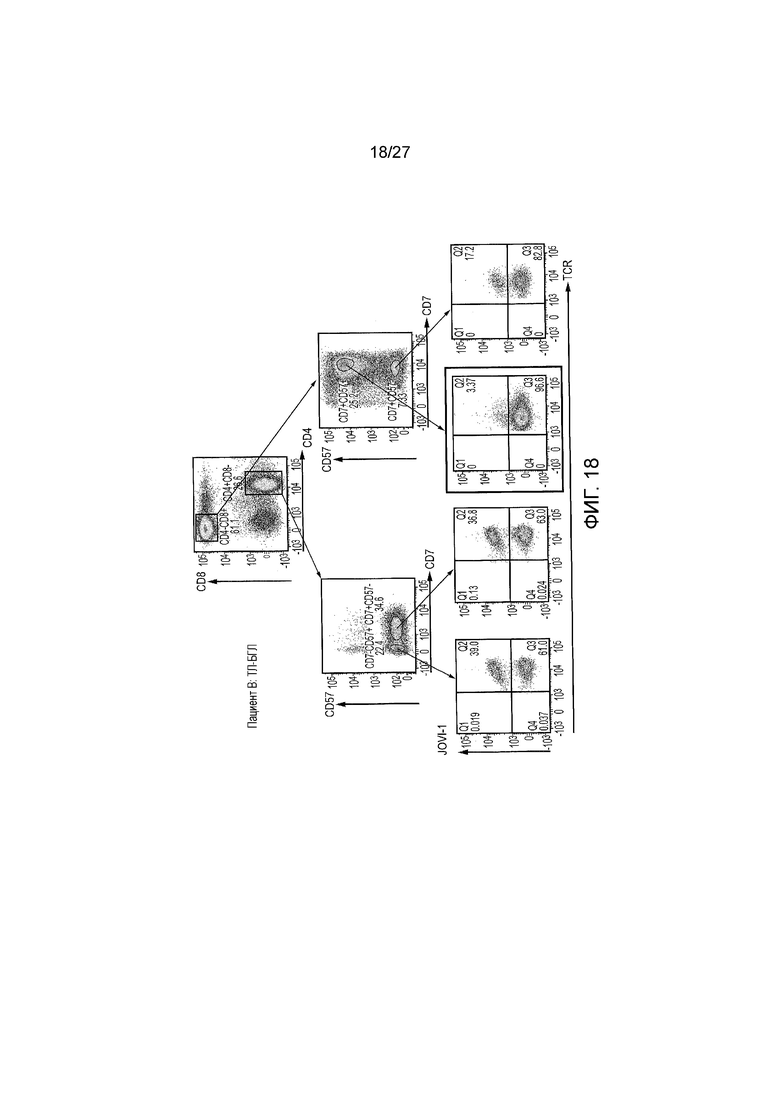
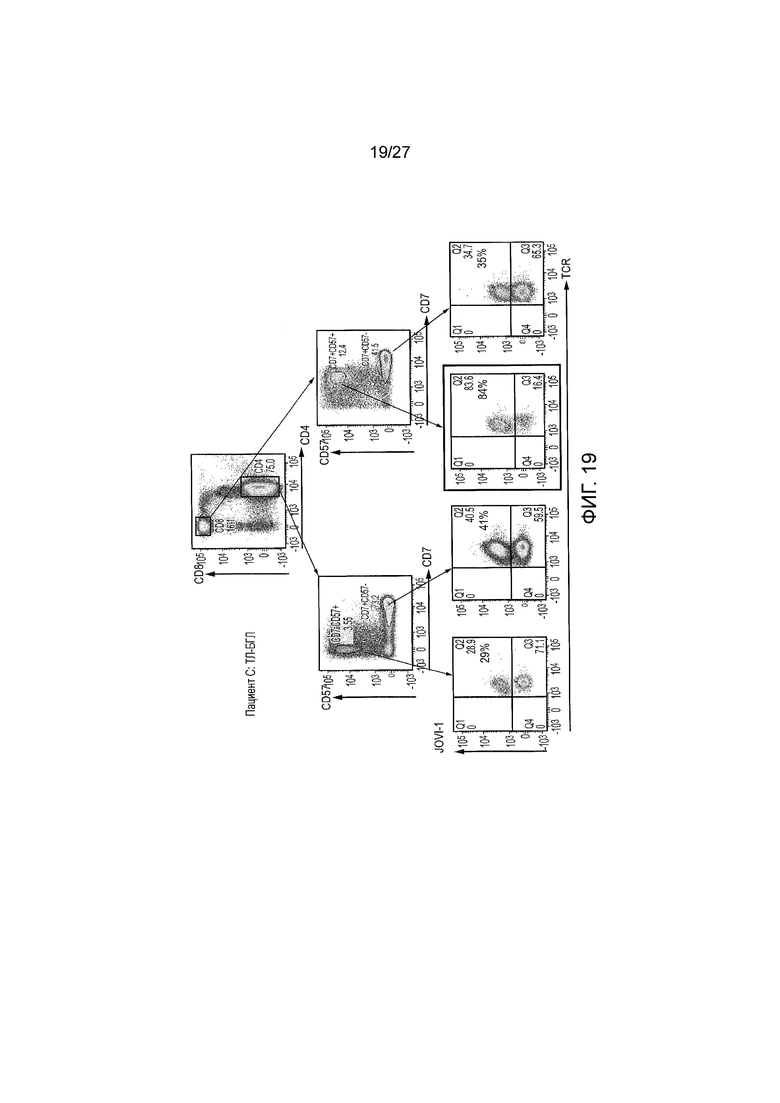
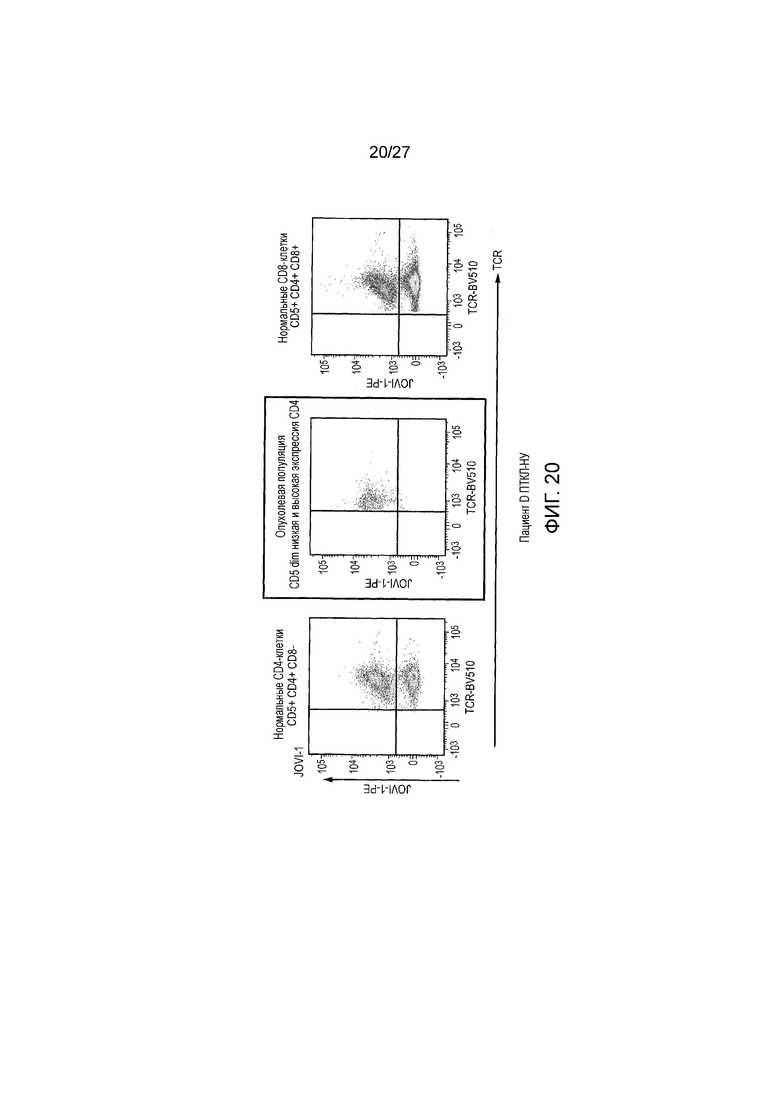

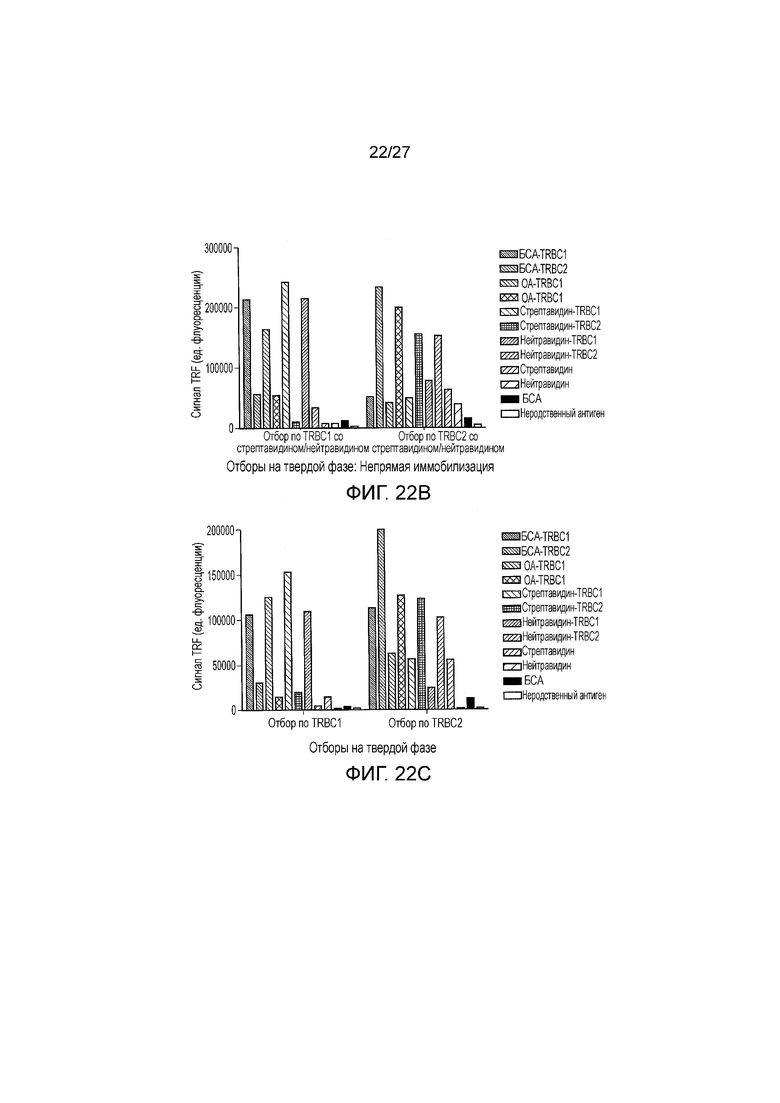
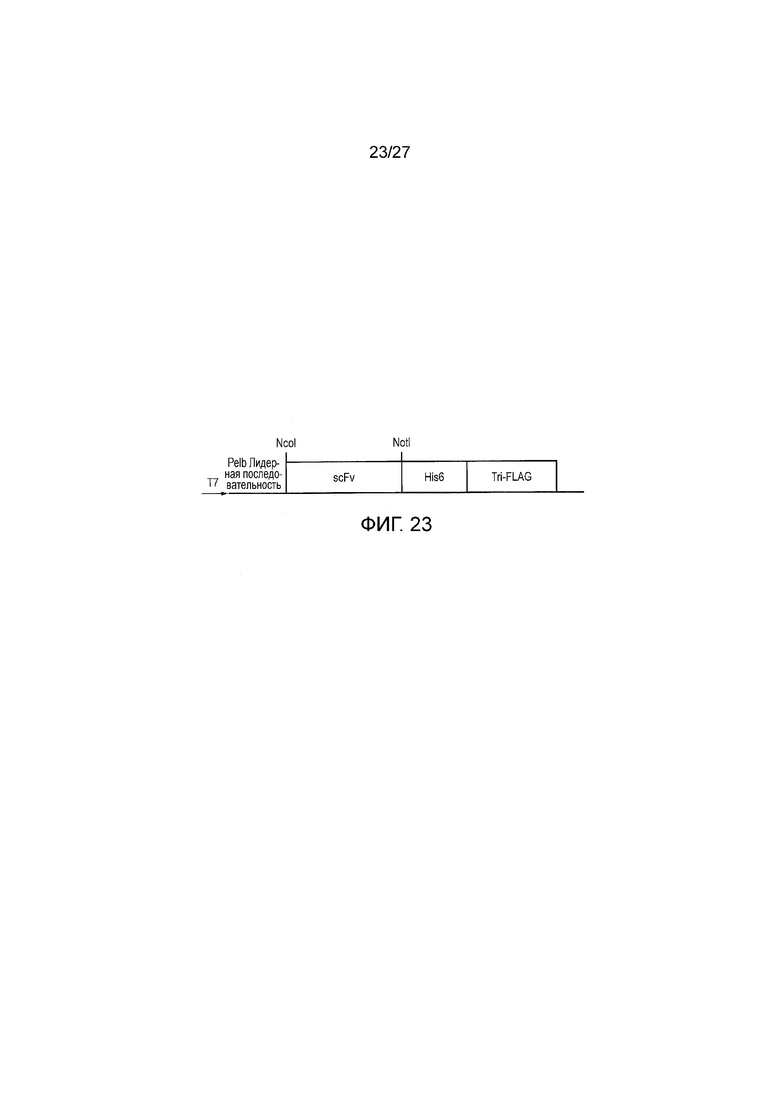
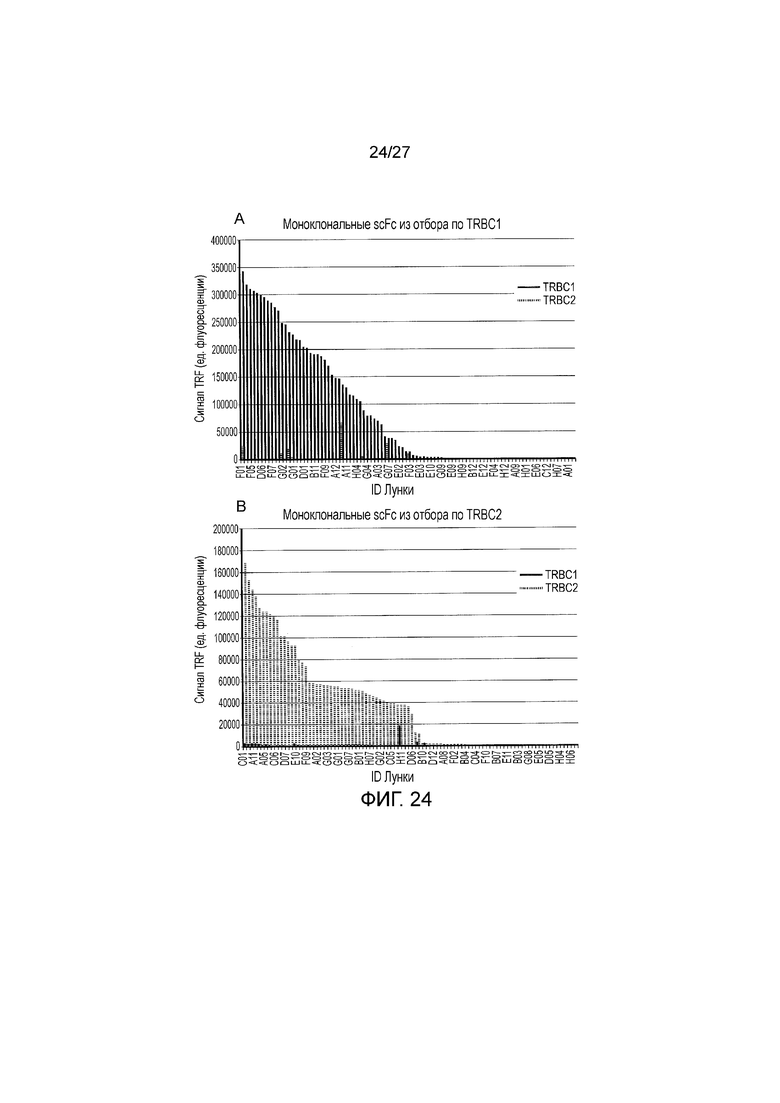
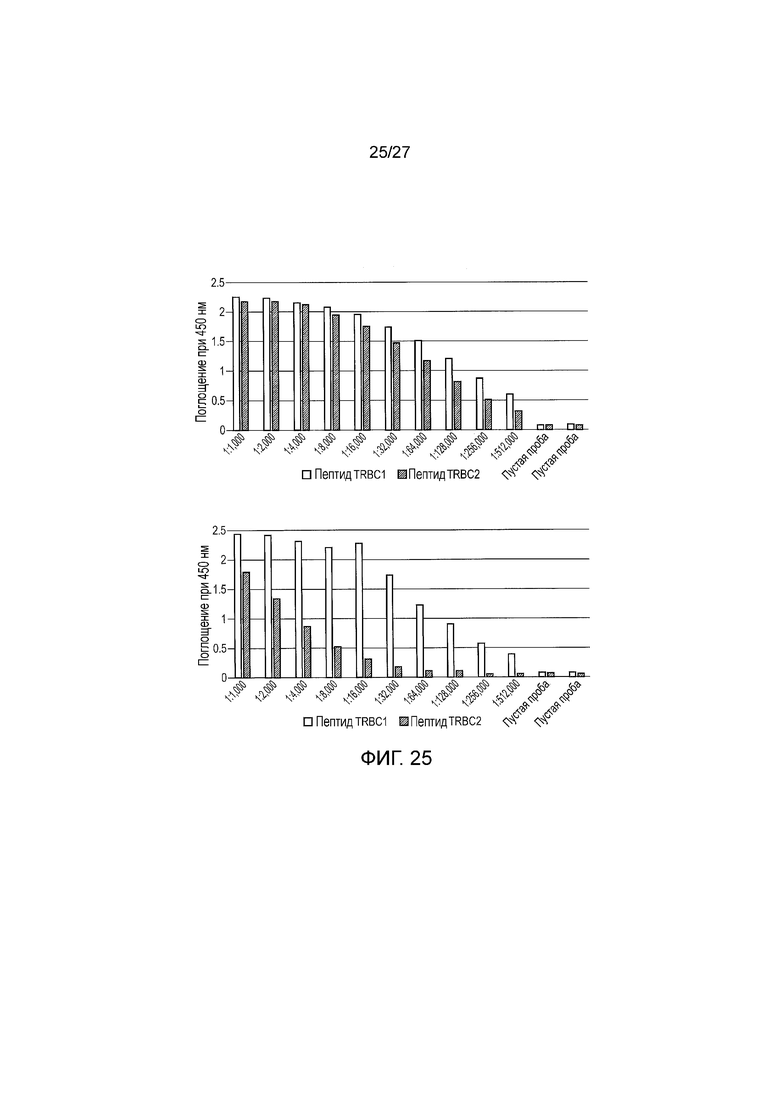

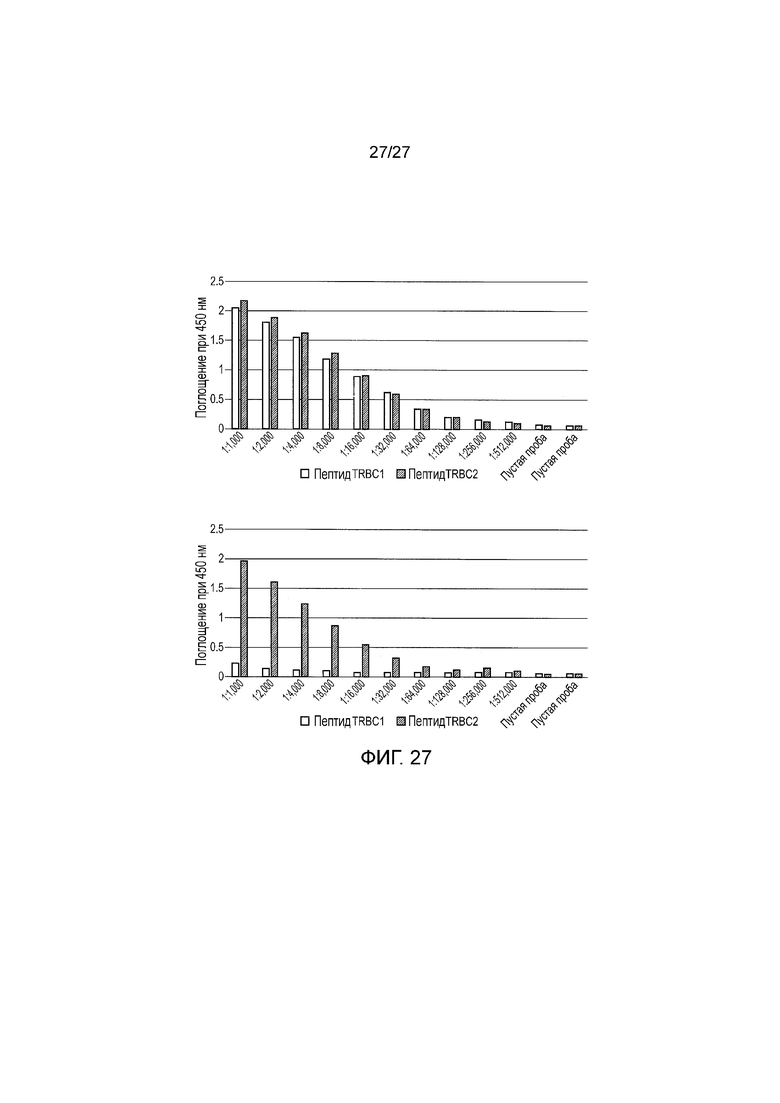
Настоящее изобретение относится к области иммунологии. Предложены применение цитолитической Т-клетки, цитолитическая Т-клетка, CAR. Также рассмотрены молекула нуклеиновой кислоты, вектор экспрессии, способ получения клетки, способ лечения Т-клеточной лимфомы или лейкемии. Данное изобретение может найти дальнейшее применение в терапии онкологических заболеваний, связанных со злокачественными Т-клетками. 7 н. и 11 з.п. ф-лы, 29 ил., 6 табл., 13 пр.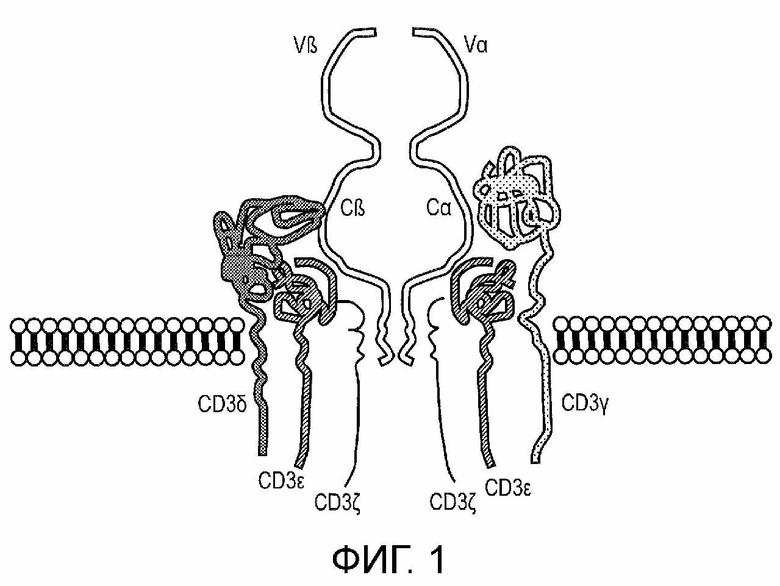
1. Применение цитолитической Т-клетки, содержащей химерный антигенный рецептор (CAR), содержащий антигенсвязывающий домен, который селективно связывается с константной областью TCR бета (TRBC) для лечения Т-клеточной лимфомы или лейкемии у индивидуума, чтобы вызвать селективное истощение злокачественных T-клеток вместе с нормальными T-клетками, экспрессирующими ту же TRBC, что и злокачественные T-клетки, но не вызывать истощения нормальных T-клеток, экспрессирующих TRBC, которую не экспрессируют злокачественные Т-клетки, где указанная TRBC выбрана из TRBC1 и TRBC2.
2. Применение по п. 1, которое включает этап исследования константной области TCR бета (TRBС) злокачественной Т-клетки у указанного субъекта для определения того, экспрессирует ли указанная клетка TRBC1 или TRBC2.
3. Применение по п. 1 или 2, где Т-клеточная лимфома или лейкемия выбрана из периферической Т-клеточной лимфомы, из периферической Т-клеточной лимфомы, неуточненной (ПТКЛ-НУ); ангиоиммунобластной Т-клеточной лимфомы (АИТКЛ), анапластической крупноклеточной лимфомы (АККЛ), Т-клеточной лимфомы, ассоциированной с энтеропатией (ТКЛЭ), гепатоспленической Т-клеточной лимфомы (ГСТЛ), экстранодальной NK/Т-клеточной лимфомы назального типа, Т-клеточной лимфомы кожи, первичной АККЛ кожи, Т-клеточной пролимфоцитарной лейкемии и Т-клеточной острой лимфобластной лейкемии.
4. Применение по любому из пп. 1-3, где указанный CAR селективно связывается с TRBC1.
5. Применение по п. 4, где антигенсвязывающий домен указанного CAR имеет вариабельную область тяжелой цепи (VH) и вариабельную область легкой цепи (VL), которые содержат следующие определяющие комплементарность области (CDR):
VH CDR1: SEQ ID No. 7;
VH CDR2: SEQ ID No. 8;
VH CDR3: SEQ ID No. 9;
VL CDR1: SEQ ID No. 10;
VL CDR2: SEQ ID No. 11; и
VL CDR3: SEQ ID No. 12.
6. Применение по п. 4, где антигенсвязывающий домен содержит вариабельную область тяжелой цепи (VH) с последовательностью, показанной в виде SEQ ID No. 1, и вариабельную область легкой цепи (VL) с последовательностью, показанной в виде SEQ ID No. 2.
7. Применение по п. 4, где антигенсвязывающий домен содержит scFv с аминокислотной последовательностью, показанной в виде SEQ ID No. 3.
8. Применение по п. 4, где указанный CAR содержит аминокислотную последовательность, выбранную из SEQ ID No. 4, 5 и 6.
9. Применение по любому из пп. 1-3, где указанный CAR селективно связывается с TRBC2.
10. Цитолитическая Т-клетка, способная уничтожать клетку-мишень, экспрессирующую TRBC1, которая содержит CAR, указанный CAR содержит антигенсвязывающий домен, который селективно связывается с TRBC1, где указанный антигенсвязывающий домен содержит вариабельную область тяжелой цепи (VH) и вариабельную область легкой цепи (VL), которые содержат следующие определяющие комплементарность участки (CDR):
VH CDR1: SEQ ID NO: 7;
VH CDR2: SEQ ID NO: 8;
VH CDR3: SEQ ID NO: 9;
VL CDR1: SEQ ID NO: 10;
VL CDR2: SEQ ID NO: 11; и
VL CDR3: SEQ ID NO: 12.
11. CAR, который содержит антигенсвязывающий домен, который селективно связывается с TRBC1, где указанный антигенсвязывающий домен содержит вариабельную область тяжелой цепи (VH) и вариабельную область легкой цепи (VL), которые содержат следующие определяющие комплементарность участки (CDR):
VH CDR1: SEQ ID NO: 7;
VH CDR2: SEQ ID NO: 8;
VH CDR3: SEQ ID NO: 9;
VL CDR1: SEQ ID NO: 10;
VL CDR2: SEQ ID NO: 11; и
VL CDR3: SEQ ID NO: 12.
12. Молекула нуклеиновой кислоты, кодирующая CAR по п. 11.
13. Вектор экспрессии, который содержит молекулу нуклеиновой кислоты по п. 12.
14. Способ получения клетки по п. 10, который включает этап трансдукции или трансфекции клетки молекулой нуклеиновой кислоты по п. 12 или вектором по п. 13.
15. Клетка по п. 10 для применения в способе лечения TRBC1+ Т-клеточной лимфомы или лейкемии у индивидуума, который включает этап введения клетки, содержащей TRBC1-селективный CAR индивидууму, для того чтобы вызвать селективное истощение популяции злокачественных T-клеток, вместе с нормальными T-клетками, экспрессирующими ту же TRBC, что и злокачественные T-клетки, но не вызвать истощение популяции нормальных T-клеток, экспрессирующих TRBC, которая не экспрессируется злокачественными T-клетками.
16. Клетка для применения по п. 15, где способ также включает этап исследования константной области TCR бета (TRBC) злокачественной Т-клетки от индивидуума, чтобы определить, экспрессирует она TRBC1 или TRBC2.
17. Клетка для применения по п. 15 или 16, где Т-клеточная лимфома или лейкемия выбрана из периферической Т-клеточной лимфомы, неуточненной (ПТКЛ-НУ); ангиоиммунобластной Т-клеточной лимфомы (АИТКЛ), анапластической крупноклеточной лимфомы (АККЛ), Т-клеточной лимфомы, ассоциированной с энтеропатией (ТКЛЭ), гепатоспленической Т-клеточной лимфомы (ГСТЛ), экстранодальной NK/Т-клеточной лимфомы назального типа, Т-клеточной лимфомы кожи, первичной АККЛ кожи, Т-клеточной пролимфоцитарной лейкемии и Т-клеточной острой лимфобластной лейкемии.
18. Способ лечения Т-клеточной лимфомы или лейкемии у индивидуума, включающий этап введения в эффективном количестве цитолитической Т-клетки, содержащей химерный антигенный рецептор (CAR), содержащий антигенсвязывающий домен, который селективно связывается с константной областью TCR бета (TRBC) указанному субъекту, чтобы вызвать селективное истощение злокачественных T-клеток вместе с нормальными T-клетками, экспрессирующими ту же TRBC, что и злокачественные T-клетки, но не вызывать истощения нормальных T-клеток, экспрессирующих TRBC, которую не экспрессируют злокачественные Т-клетки, где указанная TRBC выбрана из TRBC1 и TRBC2.
| Колосоуборка | 1923 |
|
SU2009A1 |
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| BERGER CL et | |||
| al | |||
| "The growth of cutaneous T-cell lymphoma is stimulated by immature dendritic cells", Blood, 99(8), pp | |||
| Стенной мусорный ящик | 1924 |
|
SU2929A1 |
| VINEY JL et | |||
| al | |||
| "Generation of monoclonal antibodies against a human T cell receptor beta chain expressed in | |||
Авторы
Даты
2021-03-02—Публикация
2015-03-05—Подача