ОБЛАСТЬ ТЕХНИКИ
[001] Данное раскрытие относится к способам лечения рака. В частности, в данном раскрытии предложены способы лечения различных видов рака путем введения ингибитора фермента, активирующего малый убиквитин-подобный модификатор (SUMO - англ.: small ubiquitin-like modifier) (SAE), в комбинации с одним или более ингибиторами контрольных точек.
УРОВЕНЬ ТЕХНИКИ
[002] В 2012 году по всему миру было диагностировано около 14 миллионов случаев рака и зарегистрировано около 8,2 миллиона смертей. Глобальное бремя рака растет угрожающими темпами; ожидается, что только в 2030 году возникнет около 21,3 миллиона новых случаев заболевания раком и 13,1 миллиона смертей от рака и это просто из-за роста и старения населения. Рак является второй по распространенности причиной смерти в США, уступая лишь сердечно-сосудистым заболеваниям, на долю которых приходится примерно одна из каждых четырех смертей. По оценкам Национального института рака, в 2014 году в живых осталось около 14,5 миллиона американцев, страдавших раком. У некоторых из этих людей не было рака, в то время как у других все еще были признаки рака и, возможно, они проходили лечение. Несмотря на то, что достижения медицины улучшили показатели выживаемости при раке, существует постоянная потребность в новых и более эффективных способах лечения.
[003] Лечение рака в большинстве случаев основывается на проведении операций, радиотерапии, цитотоксической химиотерапии и их комбинаций. Однако в последнее десятилетие таргетные терапии рака открыли новую эру в области онкологии. Таргетные терапии рака - это препараты, разработанные для воздействия на определенные молекулы, необходимые для роста и прогрессирования опухоли, и могут включать в себя малые молекулы и более крупные химические соединения, такие как моноклональные антитела (мАт).
[004] Рак легкого является основной причиной смертности, связанной с онкологическими заболеваниями, во всем мире, а в 2019 году в Соединенных Штатах Америки (США) было зарегистрировано 142670 смертей. Siegel, R.L., et al., СА Cancer J Clin. 69(1): 7-34 (2019) ("Siegel"). Более 80% случаев рака легкого классифицируются как немелкоклеточный рак легкого (НМРЛ). Несмотря на то, что таргетные терапии привнесли новые варианты лечения пациентов с молекулярно определенным местнораспространенным или метастатическим НМРЛ (например, НМРЛ с мутацией рецептора эпидермального фактора роста [EGFR], НМРЛ с перестройкой гена киназы анапластической лимфомы [ALK]), эти терапии являются неэффективными для пациентов, в опухолях которых отсутствуют такие генетические изменения, что составляет большинство пациентов с НМРЛ. Однако иммунотерапия стала частью первой линии лечения таких пациентов, что привело к улучшению выживаемости. Однако, несмотря на положительный эффект ингибиторов контрольных точек (ИКТ) на общую выживаемость (ОВ) при НМРЛ, заболевание на поздней стадии является неизлечимым и в конечном итоге будет прогрессировать. В исследовании фазы 1b KEYNOTE-001 пембролизумаба у пациентов с распространенным НМРЛ 5-летняя ОВ у пациентов, не получавших лечения, с экспрессией PD-L1≥50% составила 29,6%, 15,7%, если уровень PD-L1 составлял <50%. У пациентов, ранее получавших лечение, у которых уровни экспрессии PD-L1 составляли ≥50%, от 1 до 49% и <1%, 5-летняя ОВ составила 25%, 12,6% и 3,5%, соответственно.
[005] Внедрение иммунотерапии первой линии изменило прежние парадигмы лечения при НМРЛ. У пациентов, опухоли которых прогрессировали после терапии на основе ИКТ, выбор лечения комбинацией двух препаратов платины или доцетакселом зависит от схемы химиотерапии, ассоциированной с ИКТ в рамках терапии первой линии. Лечение доцетакселом плюс рамуцирумабом в рамках терапии второй линии показало общую частоту ответа (ОЧО) 23%, среднюю выживаемость без прогрессирования (ВВП) 4,5 месяца (отношение рисков [ОР]: 0,76, 95% ДИ 0,68-0,86) и среднюю ОВ 10,5 месяцев (ОР: 0,86, 95% ДИ 0,75-0,98). Garon, Е.В., et at., Lancet 384 (9944): 665-73 (2014). Сочетание ИКТ с активацией пути интерферона типа I (ИФН) может активизировать ранее существовавший иммунный ответ и инициировать новый противоопухолевый иммунный ответ, а также имеет потенциал улучшения исходов при НМРЛ, включая пациентов с опухолями, отрицательными на экспрессию PD-L1.
[006] Рак шейки матки является четвертой основной причиной смертности от рака у женщин во всем мире, в 2019 году в Соединенных Штатах Америки было зарегистрировано 13 170 новых случаев и 4250 смертей. Siegel, 7-34. В отличие от пациентов с ранней стадией рака шейки матки, прогноз для пациентов с рецидивирующим или метастатическим заболеванием является неблагоприятным. За последние 30 лет комбинированная химиотерапия на основе цисплатина показала наилучшие показатели ВВП и средней ОВ: 5 месяцев и 10-13 месяцев, соответственно. Moore D.H., et at., J. Clin. Oncol. 22(15): 3113-9 (2004); Long H.J., 3rd, et at., J. Clin. Oncol. 23(21): 4626-33 (2005); Monk B.J., et at., J. Clin. Oncol. 27(28): 4649-55 (2009). Кроме того, добавление бевацизумаба к стандартной химиотерапии первой линии значительно улучшило среднюю ВВП (8,2 против 5,9 месяцев; ОР: 0,67, 95% ДИ, 0,54-0,82) и среднюю ОВ (17,0 против 13,3 месяцев; OP: 0,71, 95% ДИ, 0,54-0,95) по сравнению с проведением только химиотерапии.
[007] Лечение после неэффективности препаратов платины представляет собой серьезную проблему, и имеющиеся в настоящее время препараты для монотерапии, такие как топотекан, винорелбин, гемцитабин, доцетаксел и наб-паклитаксел, показали неудовлетворительную активность. Совсем недавно, в июне 2018 года, моноклональное антитело (мАт) к PD-1, пембролизумаб, получило ускоренное одобрение для лечения распространенного рака шейки матки с прогрессированием заболевания во второй линии на основании результатов KEYNOTE-158 (NCT02628067), многоцентрового нерандомизированного, открытого, мультикогортного исследования. В этом исследовании пациенты получали пембролизумаб внутривенно в дозе 200 мг каждые три недели до неприемлемой токсичности или документально подтвержденного прогрессирования заболевания. Среди 98 пациентов одобрение основывалось на 77 (79%) пациентах, у которых были опухоли с экспрессией PD-L1 с комбинированным показателем позитивности (CPS) ≥1, и которые получали по меньшей мере одну линию химиотерапии для лечения метастатического заболевания.
[008] При средней продолжительности периода последующего наблюдения 11,7 месяцев общая частота ответа (ОЧО) у 77 пациентов составила 14,3% (95% ДИ: 7,4, 24,1), включая 2,6% полных ответов (ПО) и 11,7% частичных ответов (ЧО). Расчетная средняя продолжительность ответа (ПО), основанная на 11 пациентах с ответом в независимом анализе, не была достигнута (диапазон от 4,1 до 18,6+ месяцев), в то время как у 91% ПО была больше или равна 6 месяцам.
[009] Колоректальный рак (КРР) является второй по основной причиной смерти от рака во всем мире: в 2019 году в Соединенных Штатах Америки умерло 51020 человек. Siegel, 7-34. Приблизительно 25% пациентов с КРР впервые обращаются за помощью при распространенном метастатической заболевании IV стадии, а еще 25-50% пациентов обращаются за помощью, когда заболевание находится на ранней стадии, но в дальнейшем развивается метастатическое заболевание. Несмотря на разработку нескольких схем химиотерапии и добавление мАт, направленных на EGFR/сосудистый эндотелиальный фактор роста A (VEGFA), прогноз для пациентов с метастатическим КРР остается плохим, а средняя 5-летняя выживаемость в США составляет всего 12,5%. Siegel R., et al., СА Cancer J Clin. 64(1): 9-29 (2014).
[010] Пациенты с КРР, которым иммунотерапия приносит пользу, - это пациенты с сильно мутировавшими опухолями с дефицитом репарации неспаренных оснований (dMMR) или с высокими уровнями микросателлитной нестабильности (MSI-H). Для этой подгруппы пациентов ИКТ пембролизумаб, ниволумаб и комбинация ниволумаба и ипилимумаба получили одобрение регулирующих органов в США в 2017, 2017 и 2018 годах, соответственно. Одобрения были основаны на данных 225 пациентов с КРР с MSI-Н, которые перешли на применение схем, содержащих фтор пиримидин, оксалиплатин и иринотекан. ЧОО, продемонстрированная пембролизумабом, ниволумабом или комбинацией ипилимумаба и ниволумаба, составила 36%, 28% и 46%, соответственно; а ПО составляла более шести месяцев у 78%, 67% и 89% ответивших на лечение соответствующими ИКТ пациентов. Le, D.T., et al., New Eng. J. Med. 372(26):2509-20 (2015); O'Neil, B.H., et al., PLoS One 12(12): e0189848 (2017); Overman, M.J., et al., Lancet Oncol. 18(9):1182-91 (2017); Overman, M.J., et al., J. Clin. Oncol. 36(8): 773-9 (2018); Le D.T., et al., J. Clin. Oncol. 36 (15 suppl.) 3514 (2018).
[011] К сожалению, опухоли dMMR/MSI-H составляют только 5% случаев метастатического КРР (Oliveira A.F., et al., Front Oncol. 9:396 (2019)), и современные ИКТ неэффективны в опухолях, имеющих гены репарации неспаренных оснований (pMMR), и опухолях микросателлитной стабильностью (MSS) или опухолях с низким уровнем микросателлитной нестабильности (MSI-L). В этих опухолях низкая мутационная нагрузка опухоли и отсутствие инфильтрации иммунных клеток считаются механизмами иммунной резистентности. И после того, как опухоль прогрессировала до необходимости перехода на химиотерапевтические схемы на основе мАт, два доступных терапевтических варианта, регорафениб и трифлуридин-типирацил, показали низкую ЧОО от 1,6 до 3%, со средней ВВП и средней ОВ 2 и 7 месяцев, соответственно. Mayer, R.J., et al., New Eng. J. Med. 372(20):1909-19 (2015). Van Cutsem, E., et al., J. Clin. Oncol. 30(28):3499-506 (2012).
[012] Ингибиторы фермента, активирующего малый убиквитин-подобный модификатор (SUMO) (SAE) являются примером небольших молекул, которые могут использоваться для таргетной терапии. SUMO является членом семейства убиквитин-подобных белков (Ubl), которые ковалентно конъюгируются с клеточными белками аналогично конъюгации убиквитина (Ub) (Kerscher, О. et al., Annu Rev Cell Dev Biol. 22:159-80 (2006)). Клетки млекопитающих экспрессируют три основные изоформы SUMO: SUMO1, SUMO2 и SUMO3. SUMO2 и SUMO3 имеют приблизительно 95% гомологию аминокислотной последовательности, но имеют приблизительно 45% гомологию последовательности с SUMO1 (Kamitani, Т., et al., J Biol Chem. 273(18):11349-53 (1998)). Белки SUMO могут конъюгироваться с одним остатком лизина белка (моносумоилирование) или со вторым белком SUMO, который уже конъюгирован с белком, образующим цепь SUMO (полисумоилировапие). Только SUMO2/3 может образовывать такие цепи, поскольку они обладают внутренними консенсусными сайтами модификации SUMO (Tatham, М.Н., et al., J Biol Chem. 276(38):35368-74 (2001)). Дополнительная изоформа, SUMO4, обнаруживается в клетках почек, лимфатических узлов и селезенки, но неизвестно, может ли SUMO4 конъюгироваться с клеточными белками.
[013] SUMO1, SUMO2 и SUMO3 активируются АТФ-зависимым образом посредством SAE (см., например, публикацию патентной заявки США №2010/0160177 А1 (фиг. 1B), патент США 9434765 В2 (ФИГ. 2) и Gareau, J.R., et al., Nat Rev Mol Cell Biol. 11:861-871 (2010) (Фигура 1)). SAE представляет собой гетеродимер, состоящий из SAE1 (субъединица 1 SUMO-активирующего фермента) и SAE2 (UBA2). SAE, как и другие ферменты, активирующие Е1, использует АТФ для аденилирования С-концевого остатка глицина SUMO. На второй стадии между С-концевым глицином SUMO и остатком цистеина в SAE2 образуется промежуточный тиоэфир. Затем SUMO переносится с Е1 на остаток цистеина SUMO-конъюгирующего фермента (Е2), UBC9. В отличие от пути Ub, который содержит множество ферментов Е2, Ubc9 в настоящее время является единственным известным конъюгирующим ферментом для SUMO и функционирует с белками SUMO1, SUMO2 и SUMO3. Затем белки SUMO конъюгируются с целевым белком либо напрямую, либо в сочетании с лигазой Е3 посредством образования изопептидной связи с эпсилон-аминогруппой боковой цепи лизина на целевом белке. Было идентифицировано несколько лигаз SUMO Е3, включая белки PIAS (белковый ингибитор активированного преобразователя сигнала и активатор белка транскрипции) и Ran-связывающий белок 2 (RanBP2) и polycomb 2 (Рс2) (Johnson, Е.S., and Gupta, А.А, Cell. 106(6):735-44 (2001); Pichler, A., et al., Cell. 108(1):109-20 (2002); Kagey, M.H., et al., Cell. 113(1):127-37 (2003)). После присоединения к клеточным мишеням SUMO модулирует функцию, субклеточную локализацию, комплексообразование и/или стабильность субстратных белков (Müller S., et al., Nat Rev Mol Cell Biol. 2(3):202-10 (2001)). SUMO-конъюгация является обратимой за счет действия десумоилирующих ферментов, называемых SENP (Hay, R.Т., Trends Cell Biol. 17(8):370-6 (2007)), и затем белки SUMO могут участвовать в дополнительных циклах конъюгации.
[014] SAE-инициированная SUMO-конъюгация играет важную роль в регуляции различных клеточных процессов, включая регуляцию клеточного цикла, регуляцию транскрипции, нацеливание на клеточные белки, поддержание целостности генома, сегрегацию хромосом и стабильность белка (Hay, R.Т., Mol Cell. 18(1):1-12 (2005); Gill, G., Genes Dev. 18(17):2046-59 (2004)). Например, SUMO-конъюгация вызывает изменения в субклеточной локализации RanGAP1, направляя его на комплекс ядерных пор (Mahajan, R., et al., Cell. 88(1):97-1070 (1997)). Сумоилирование противодействует убиквитинированию и впоследствии блокирует деградацию 1 кВ, тем самым негативно регулируя активацию NF-κВ (Desterro, J.М., et al., Mol Cell. 2(2):233-9 (1998)). Сообщалось, что сумоилирование играет важную роль в транскрипции, проявляя как репрессивные, так и стимулирующие эффекты. Многие из модулируемых транскрипционных узлов играют важную роль при раке. Например, сумоилирование стимулирует транскрипционную активность факторов транскрипции, таких как р53 и HSF2 (Rodriguez, М.S., et al., EMBO J. 18(22):6455-61 (1999); Goodson, M.L., et al., J Biol Chem. 276(21):18513-8 (2001)). Напротив, SUMO-конъюгация подавляет транскрипционную активность факторов транскрипции, таких как LEF (Sachdev, S., et al., Genes Dev. 15(23):3088-103 (2001)) and c-Myb (Bies, J., et al., J Biol Chem. 277(11):8999-9009 (2002)). Таким образом, SUMO-конъюгация контролирует экспрессию генов и пути контроля роста, которые важны для выживания раковых клеток.
[015] Измененная экспрессия компонентов пути SAE была отмечена при различных типах рака: (Moschos, S.J., et al., Hum Pathol. 41(9):1286-980 (2010)); включая множественную миелому (Driscoll, J.J., et al., Blood. 115(14):2827-34 (2010)); и рак молочной железы (Chen, S.F., et al., Chin J Cancer. 30(9):638-44 (2011)). Кроме того, доклинические исследования показывают, что рак, управляемый Мус, может быть особенно чувствительным к ингибированию SAE (Kessler, J.D., et al., Science. 335(6066):348-53 (2012); Hoellein, A., et al., Blood. 124(13):2081-90 (2014)). Поскольку SUMO-конъюгация регулирует основные клеточные функции, которые способствуют росту и выживанию опухолевых клеток, нацеливание на SAE может представлять подход к лечению пролиферативных нарушений, таких как рак. (Не, X., et al., Nature Chemical Biology. 13:1164-1171 (2017)). Таким образом, некоторые виды рака могут быть SAE-опосредованными расстройствами.
[016] Ингибиторы SAE также могут применяться для лечения других заболеваний и состояний помимо онкологии. Например, SUMO модифицирует белки, которые играют важную роль в нейродегенеративных заболеваниях (Steffan, J.S., et al., Science. 304(5667):100-4 (2004); Dorval, V., and Fraser, P.E., J Biol Chem. 281(15):9919-24 (2006); Ballatore, C., et al., Nat Rev Neurosci. 8(9):663-72(2007)). Также сообщалось, что сумоилирование играет важную роль в патогенных вирусных инфекциях, воспалении и сердечной функции (Lee, Н.R., et al., J Virol. 78(12):6527-42 (2004); Liu, В., and Shuai, K., Mol Cell. 35(6):731-2 (2009); Wang, J., and Schwartz, R.J., CircRes. 107(1):19-29 (2010)).
[017] Помимо малых молекул, таргетная терапия может включать моноклональные антитела. Например, среди множества известных таргетных терапий с применением моноклональных антител есть моноклональные антитела к PD-1 (например, ниволумаб/Opdivo® и пембролизумаб/Keytruda®), моноклональные антитела к PD-L1 (например, атезолизумаб/Tecentriq®, дурвалумаб/Imfinzi® и авелумаб/Bavencio®) и моноклональные антитела к CTLA-4 (например, ипилимумаб/Yervoy®). Таким образом, некоторые виды рака могут представлять собой PD-1 -опосредованные нарушения, PD-L1-опосредованные нарушения и CTLA-4-опосредованные нарушения. Дополнительные таргетные терапии с применением моноклональных антител включают, но не ограничиваются ими, моноклональные антитела к CD20 (например, ритуксимаб/Rituxan®), CD52 (например, алемтузумаб/Campath®), VEGF (например, бевацизумаб/Avastin®), HER2 (например, трастузумаб/Herceptin® для лечения Her2+ рака молочной железы и желудка) и EGFR (например, цетуксимаб/Erbitux® для лечения колоректального рака).
[018] Новые комбинации терапевтических средств, которые обеспечивают положительный эффект при лечении рака, желательны для продления жизни пациента при сохранении высокого качества жизни. Новые комбинации могут обеспечить повышенную пользу по сравнению с каждым из средств по отдельности. В частности, комбинированные схемы лечения могут быть полезны для пациентов, страдающих заболеваниями, включая пролиферативные нарушения, аутоиммунные заболевания, воспалительные заболевания, фиброзные заболевания и заболевания почек, и потенциально могут даже снизить частоту рецидивов или помочь преодолеть резистентность к определенному противораковому средству, которая иногда наблюдается у этих пациентов. Это действительно так в случае, когда рак может быть устойчивым или невосприимчивым к доступным в настоящее время терапевтическим схемам.
[019] Таким образом, существует потребность в новых схемах лечения рака, включая комбинированные терапии.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[020] В одном аспекте данное раскрытие относится к способам лечения рака, включающим введение ингибитора SAE и ингибитора контрольных точек в комбинации субъекту, нуждающемуся в таком лечении.
[021] В одном аспекте данное раскрытие относится к способам лечения пациента, имеющего рак, включающим введение пациенту, нуждающемуся в таком лечении, комбинации [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамата (соединения I-263а) или его фармацевтически приемлемой соли, и ингибитора контрольных точек. Соединение I-263а также называется в данном документе TAK-981.
[022] В некоторых вариантах осуществления ингибитор контрольных точек представляет собой антитело к PD-1.
[023] В некоторых вариантах осуществления антитело к PD-1 выбрано из группы, состоящей из ниволумаба, пембролизумаба, ламбролизумаба, пидилизумаба, BMS-936559 и АМР-224.
[024] В некоторых вариантах осуществления ингибитор контрольных точек представляет собой антитело к PD-L1.
[025] В некоторых вариантах осуществления антитело к PD-L1 выбрано из группы, состоящей из атезолизумаба, дурвалумаба, авелумаба, YW243.55.S70, MEDI-4736, MSB-0010718С, LY3300054, BMS-936559, MPDL3280A и MDX-1105.
[026] В некоторых вариантах осуществления ингибитор контрольных точек представляет собой антитело к CTLA-4.
[027] В некоторых вариантах осуществления антитело к CTLA-4 выбрано из группы, состоящей из ипилимумаба и тремелимумаба.
[028] В некоторых вариантах осуществления [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его фармацевтически приемлемую соль вводят перорально.
[029] В некоторых вариантах осуществления [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его фармацевтически приемлемую соль вводят внутривенно.
[030] В некоторых вариантах осуществления [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его фармацевтически приемлемую соль вводят путем внутривенной инфузии.
[031] В некоторых вариантах осуществления ингибитор контрольных точек вводят внутривенно.
[032] В некоторых вариантах осуществления ингибитор контрольных точек вводят путем внутривенной инфузии.
[033] В некоторых вариантах осуществления ингибитор контрольных точек вводят путем подкожной инъекции.
[034] В некоторых вариантах осуществления ингибитор контрольных точек вводят подкожно.
[035] В некоторых вариантах осуществления [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат и ингибитор контрольных точек вводят одновременно.
[036] В некоторых вариантах осуществления [(1R,2S,4Я)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат и ингибитор контрольных точек вводят последовательно в отдельных фармацевтических композициях.
[037] В некоторых вариантах осуществления рак представляет собой PD-1-положительный рак, PD-L1-положительный рак или CTLA-4-положительный рак.
[038] В некоторых вариантах осуществления рак представляет собой солидную опухоль или гематологическую злокачественную опухоль. В некоторых вариантах осуществления солидная опухоль представляет собой распространенную солидную опухоль. В некоторых вариантах осуществления солидная опухоль представляет собой метастатическую солидную опухоль. В некоторых вариантах осуществления солидная опухоль представляет собой неоперабельную солидную опухоль.
[039] В некоторых вариантах осуществления рак представляет собой меланому, рак легкого, рак почек, лимфому, рак головы и шеи, уротелиальный рак, рак предстательной железы, рак мочевого пузыря, рак молочной железы, рак желудка, колоректальный рак, лейкоз, рак шейки матки, рак с высоким уровнем микросателлитной нестабильности, гепатоцеллюлярную карциному или карциному из клеток Мерке ля.
[040] В некоторых вариантах осуществления рак представляет собой рак шейки матки. В некоторых вариантах осуществления рак представляет собой рак шейки матки, при котором ранее не проводилось лечение с применением ИКТ. В некоторых вариантах осуществления рак представляет собой плоскоклеточную карциному, аденосквамозную карциному или аденокарциному шейки матки.
[041] В некоторых вариантах осуществления рак представляет собой колоректальный рак. В некоторых вариантах осуществления рак представляет собой колоректальный рак с микросателлитной стабильностью (МСС-КРР). В некоторых вариантах осуществления рак представляет собой МСС-КРР, при котором ранее не проводилось лечение с применением ИКТ.
[042] В некоторых вариантах осуществления меланома представляет собой метастатическую меланому, неоперабельную меланому или меланому кожи.
[043] В некоторых вариантах осуществления рак легкого представляет собой немелкоклеточный рак легкого (НМРЛ) или мелкоклеточный рак легкого.
[044] В некоторых вариантах осуществления немелкоклеточный рак легкого представляет собой метастатический немелкоклеточный рак легкого, метастатический плоскоклеточный немелкоклеточный рак легкого или метастатический неплоскоклеточный немелкоклеточный рак легкого. В некоторых вариантах осуществления немелкоклеточный рак легкого представляет собой аденокарциному немелкоклеточного рака легкого.
[045] В некоторых вариантах осуществления рак почки представляет собой почечно-клеточную карциному.
[046] В некоторых вариантах осуществления лимфома представляет собой классическую лимфому Ходжкина или первичную В-крупноклеточную лимфому средостения.
[047] В некоторых вариантах осуществления рак головы и шеи представляет собой плоскоклеточный рак головы и шеи.
[048] В некоторых вариантах осуществления уротелиальный рак представляет собой уротелиальную карциному.
[049] В некоторых вариантах осуществления рак предстательной железы представляет собой гормонорезистентный рак предстательной железы.
[050] В некоторых вариантах осуществления рак желудка представляет собой аденокарциному гастроэзофагеального перехода.
[051] В некоторых вариантах осуществления [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его фармацевтически приемлемую соль вводят один раз в две недели, один раз в неделю, два раза в неделю, три раза в неделю или ежедневно.
[052] В некоторых вариантах осуществления [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его фармацевтически приемлемую соль вводят два раза в неделю.
[053] В некоторых вариантах осуществления [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его фармацевтически приемлемую соль вводят один раз в неделю.
[054] В некоторых вариантах осуществления [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его фармацевтически приемлемую соль вводят в дни 1, 4, 8 и 11 21-дневного цикла.
[055] В некоторых вариантах осуществления ингибитор контрольных точек вводят один раз в двенадцать недель, один раз в четыре недели, один раз в три недели, один раз в две недели, один раз в неделю, два раза в неделю, три раза в неделю или ежедневно.
[056] В некоторых вариантах осуществления ингибитор контрольных точек вводят один раз в две недели.
[057] В некоторых вариантах осуществления ингибитор контрольных точек вводят один раз в три недели.
[058] В некоторых вариантах осуществления ингибитор контрольных точек вводят один раз в четыре недели.
[059] В некоторых вариантах осуществления ингибитор контрольных точек вводят один раз в двенадцать недель.
[060] В некоторых вариантах осуществления ингибитор контрольных точек вводят в день 1 цикла лечения.
[061] В некоторых вариантах осуществления цикл лечения составляет 14 дней, 21 день, 28 дней или 84 дня.
[062] В некоторых вариантах осуществления [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его фармацевтически приемлемую соль и ингибитор контрольных точек вводят одновременно один раз в двенадцать недель, один раз в четыре недели, один раз в три недели, один раз в две недели, один раз в неделю, два раза в неделю, три раза в неделю, ежедневно или в дни 1, 4, 8 и 11 21-дневного цикла.
[063] В некоторых вариантах осуществления [(R1,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его фармацевтически приемлемую соль вводят один раз в две недели, один раз в неделю, два раза в неделю, три раза в неделю, ежедневно или в дни 1, 4, 8 и 11 21-дневного цикла; а ингибитор контрольных точек вводят отдельно один раз в двенадцать недель, один раз в четыре недели, один раз в три недели, один раз в две недели, один раз в неделю, два раза в неделю, три раза в неделю или ежедневно.
[064] В одном аспекте данное раскрытие относится к набору, содержащему лекарственное средство для применения при лечении рака у субъекта, нуждающегося в таком лечении. Набор содержит лекарственное средство, содержащее ингибитор SAE, и инструкцию по введению ингибитора SAE и одного или более ингибиторов контрольных точек; или набор содержит лекарственное средство, содержащее один или более ингибиторов контрольных точек, и инструкцию по введению одного или более ингибиторов контрольных точек и ингибитора SAE. Набор может содержать как лекарственное средство, содержащее ингибитор SAE, так и лекарственное средство, содержащее один или более ингибиторов контрольных точек, и инструкцию по введению ингибитора SAE и одного или более ингибиторов контрольных точек. Набор также может содержать одно или более дополнительных терапевтических средств.
[065] В одном аспекте данное раскрытие относится к лекарственному средству для применения при лечении рака у субъекта, нуждающегося в таком лечении. Лекарственное средство содержит ингибитор SAE и один или более ингибиторов контрольных точек. Лекарственное средство также может содержать одно или более дополнительных терапевтических средств.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[066] На ФИГ. 1а показан график индивидуального объема опухоли в зависимости от времени на сингенной опухолевой модели СТ26 после введения мышам соединения I-263а и носителя.
[067] На ФИГ. 1b показан график индивидуального объема опухоли в зависимости от времени на сингенной опухолевой модели СТ26 после введения мышам носителя и антимышиного антитела к PD-1 («анти-mPD-1»).
[068] На ФИГ. 1с показан график индивидуального объема опухоли как функции времени на сингенной опухолевой модели СТ26 после введения мышам носителя и комбинации соединения I-263а и анти-mPD-1 антитела.
[069] На ФИГ. 2а показан график индивидуального объема опухоли как функции времени на сингенной опухолевой модели СТ26 после введения мышам соединения I-263а и носителя.
[070] На ФИГ. 2b показан график индивидуального объема опухоли в зависимости от времени на сингенной опухолевой модели СТ26 после введения мышам носителя и анти-mPD-1 антитела.
[071] На ФИГ. 2с показан график индивидуального объема опухоли как функции времени на сингенной опухолевой модели СТ26 после введения мышам носителя и комбинации соединения I-263а и анти-mPD-1 антитела.
[072] На ФИГ. 3а показан график индивидуального объема опухоли как функции времени на сингенной опухолевой модели А20 после введения мышам соединения I-263а и носителя.
[073] На ФИГ. 3b показан график индивидуального объема опухоли в зависимости от времени на сингенной опухолевой модели А20 после введения мышам носителя и анти-mPD-1 антитела.
[074] На ФИГ. 3с показан график индивидуального объема опухоли как функции времени на сингенной опухолевой модели А20 после введения мышам носителя и комбинации соединения I-263а и анти-mPD-1 антитела.
[075] На ФИГ. 4а показан график индивидуального объема опухоли как функции времени на сингенной опухолевой модели WEHI-3 после введения мышам соединения I-263а и носителя.
[076] На ФИГ. 4b показан график индивидуального объема опухоли в зависимости от времени на сингенной опухолевой модели WEHI-3 после введения мышам анти-mPD-1 антитела и носителя.
[077] На ФИГ. 4с показан график индивидуального объема опухоли в зависимости от времени на сингенной опухолевой модели WEHI-3 после введения мышам антимышиного антитела к CTLA-4 («анти-mCTLA-4») и носителя.
[078] На ФИГ. 4d показан график индивидуального объема опухоли как функции времени на сингенной опухолевой модели WEHI-3 после введения мышам носителя и комбинации соединения I-263а и анти-mPD-1 антитела.
[079] На ФИГ. 4е показан график индивидуального объема опухоли как функции времени на сингенной опухолевой модели WEHI-3 после введения мышам носителя и комбинации соединения I-263а и анти-mCTLA-4 антитела.
[080] На ФИГ. 5а показан график индивидуального объема опухоли как функции времени на сингенной опухолевой модели WEHI-3 после введения мышам соединения I-263а и носителя.
[081] На ФИГ. 5b показан график индивидуального объема опухоли в зависимости от времени на сингенной опухолевой модели WEHI-3 после введения мышам анти-mPD-1 антитела и носителя.
[082] На ФИГ. 5с показан график индивидуального объема опухоли в зависимости от времени на сингенной опухолевой модели WEHI-3 после введения мышам анти-mCTLA-4 антитела и носителя.
[083] На ФИГ. 5d показан график индивидуального объема опухоли как функции времени на сингенной опухолевой модели WEHI-3 после введения мышам носителя и комбинации соединения I-263а и анти-mPD-1 антитела.
[084] На ФИГ. 5е показан график индивидуального объема опухоли как функции времени на сингенной опухолевой модели WEHI-3 после введения мышам носителя и комбинации соединения I-263а и анти-mCTLA-4 антитела.
[085] На ФИГ. 6а показан график индивидуального объема опухоли как функции времени на сингенной опухолевой модели JC после введения мышам соединения I-263а и носителя.
[086] На ФИГ. 6b показан график индивидуального объема опухоли в зависимости от времени на сингенной опухолевой модели JC после введения мышам анти-mPD-1 антитела и носителя.
[087] На ФИГ. 6с показан график индивидуального объема опухоли в зависимости от времени на сингенной опухолевой модели JC после введения мышам анти-mCTLA-4 антитела и носителя.
[088] На ФИГ. 6d показан график индивидуального объема опухоли как функции времени на сингенной опухолевой модели JC после введения мышам носителя и комбинации соединения I-263а и анти-mPD-1 антитела.
[089] На ФИГ. 6е показан график индивидуального объема опухоли как функции времени на сингенной опухолевой модели JC после введения мышам носителя и комбинации соединения I-263а и анти-mCTLA-4 антитела.
[090] На ФИГ. 7а показан график индивидуального объема опухоли как функции времени на сингенной опухолевой модели B16-F10 после введения мышам соединения I-263а и носителя.
[091] На ФИГ. 7b показан график индивидуального объема опухоли в зависимости от времени на сингенной опухолевой модели B16-F10 после введения мышам анти-mPD-1 антитела и носителя.
[092] На ФИГ. 7с показан график индивидуального объема опухоли в зависимости от времени на сингенной опухолевой модели B16-F10 после введения мышам анти-mCTLA-4 антитела и носителя.
[093] На ФИГ. 7d показан график индивидуального объема опухоли как функции времени на сингенной опухолевой модели B16-F10 после введения мышам носителя и комбинации соединения I-263а и анти-mPD-1 антитела.
[094] На ФИГ. 7е показан график индивидуального объема опухоли как функции времени на сингенной опухолевой модели B16-F10 после введения мышам носителя и комбинации соединения I-263а и анти-mCTLA-4 антитела.
[095] На ФИГ. 8а показан график индивидуального объема опухоли как функции времени на сингенной опухолевой модели МС38 после введения мышам соединения I-263а и носителя.
[096] На ФИГ. 8b показан график индивидуального объема опухоли в зависимости от времени на сингенной опухолевой модели МС38 после введения мышам анти-mPD-1 антитела и носителя.
[097] На ФИГ. 8с показан график индивидуального объема опухоли в зависимости от времени на сингенной опухолевой модели МС38 после введения мышам анти-mCTLA-4 антитела и носителя.
[098] На ФИГ. 8d показан график индивидуального объема опухоли как функции времени на сингенной опухолевой модели МС38 после введения мышам носителя и комбинации соединения I-263а и анти-mPD-1 антитела.
[099] На ФИГ. 8е показан график индивидуального объема опухоли как функции времени на сингенной опухолевой модели МС38 после введения мышам носителя и комбинации соединения I-263а и анти-mCTLA-4 антитела.
ПОДРОБНОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Определения и сокращения
[0100] Для облегчения понимания данного раскрытия ниже приведены определения для ряда сокращений, терминов и фраз.
SAE
SUMO-активирующий фермент
МСС-КРР
колоректальный рак с микросателлитной стабильностью
[0101] Если не указано иное, все технические и научные термины, используемые в настоящем документе, имеют то же значение, которое обычно понимается специалистом в области, к которой принадлежит настоящее раскрытие. Все патенты и публикации, упоминаемые в данном документе, в полном объеме включены в данный документ посредством ссылки.
[0102] В контексте данного документа термин «рак» относится к клеточному нарушению, характеризующемуся неконтролируемой или нерегулируемой клеточной пролиферацией, снижением клеточной дифференцировки, несоответствующей способностью проникать в окружающие ткани и/или способностью устанавливать новый рост на эктопических участках. Термин «рак» включает солидные опухоли и несолидные опухоли, такие как, например, гематологические опухоли. Термин «рак» охватывает заболевания кожи, тканей, органов, костей, хрящей, крови и сосудов. Термин «рак» также подразумевает первичный и метастатический рак.
[0103] В контексте данного документа термин «аутоиммунное заболевание» относится к нарушению, возникающему в результате аномального иммунного ответа на здоровую часть тела. Термин «аутоиммунное заболевание» охватывает нарушения, включая, но не ограничиваясь ими, ревматоидный артрит (РА), гранулематоз с полиангиитом (GPA) (гранулематоз Вегенера) и микроскопический полиангиит (MPA).
[0104] Термин «PD-1» (также известный как белок 1 программируемой гибели клеток, PDCD1, CD279, SLEB2 или SLE1) относится к любому нативному PD-1, если не указано иное. Термин «PD-1» охватывает «полноразмерный» непроцессированный PD-1, а также любую форму PD-1, которая является результатом процессинга в клетке. Термин также включает встречающиеся в природе варианты PD-1, например, сплайс-варианты, аллельные варианты и изоформы.
[0105] Термин «PD-L1» (также известный как лиганд программируемой гибели клеток 1) относится к любому нативному PD-L1, если не указано иное. Термин «PD-L1» охватывает «полноразмерный» непроцессированный PD-L1, а также любую форму PD-L1, которая является результатом процессинга в клетке. Термин также включает встречающиеся в природе варианты PD-L1, например, сплайс-варианты, аллельные варианты и изоформы.
[0106] Термин «CTLA-4» (также известный как антиген 4, ассоциированный с цитотоксическими Т-лимфоцитами) относится к любому нативному CTLA-4, если не указано иное. Термин «CTLA-4» охватывает «полноразмерный» непроцессированный CTLA-4, а также любую форму CTLA-4, который является результатом процессинга в клетке. Термин также включает встречающиеся в природе варианты CTLA-4, например, сплайс-варианты, аллельные варианты и изоформы.
[0107] Термин «антитело» означает молекулу иммуноглобулина, которая распознает и специфически связывается с мишенью, такой как белок, полипептид, пептид, углевод, полинуклеотид, липид, или комбинацией вышеперечисленного, через по меньшей мере один сайт распознавания антигена в вариабельной области молекулы иммуноглобулина. В контексте данного документа термин «антитело» включает интактные поликлональные антитела, интактные моноклональные антитела, фрагменты антител (такие как Fab, Fab', F(ab')2 и Fv), одноцепочечные мутанты Fv (scFv), мультиспецифические антитела, такие как биспецифические антитела, полученные по меньшей мере из двух интактных антител, химерные антитела, гуманизированные антитела, человеческие антитела, слитые белки, содержащие часть антитела, определяющую антиген, и любую другую модифицированную молекулу иммуноглобулина, содержащую сайт распознавания антигена, при условии, что антитела проявляют желаемую биологическую активность. Антитело может принадлежать к любому из пяти основных классов иммуноглобулинов: IgA, IgD, IgE, IgG и IgM или их подклассов (изотипов) (например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2), на основании идентичности их константных доменов тяжелой цепи называемых альфа, дельта, эпсилон, гамма и мю, соответственно. Различные классы иммуноглобулинов имеют различные и хорошо известные структуры субъединиц и трехмерные конфигурации. Антитела могут быть неконъюгированными или конъюгированными с другими молекулами, такими как токсины, радиоизотопы и т.д.
[0108] «Блокирующее» антитело или «антагонистическое» антитело представляет собой антитело, которое ингибирует или снижает биологическую активность антигена, который оно связывает, такой как, например, PD-1, PD-L1 или CTLA-4. В определенном варианте осуществления блокирующие антитела или антагонистические антитела по существу или полностью подавляют биологическую активность антигена. Желательно, чтобы биологическая активность снижалась на 10%, 20%, 30%, 50%, 70%, 80%, 90%, 95% или даже 100%.
[0109] Термин «антитело к PD-1» или «антитело, которое связывается с PD-1» относятся к антителу, которое способно связывать PD-1 с достаточной аффинностью, так что антитело становится пригодным в качестве диагностического и/или терапевтического средства нацеливания на PD-1. Степень связывания анти-PD-1 антитела с неродственным белком, не являющимся PD-1, составляет менее чем около 10% от связывания антитела с PD-1, как измерено, например, с помощью радиоиммунологического анализа (РИА). В определенных вариантах осуществления антитело, которое связывается с PD-1, имеет константу диссоциации (Kd)≤1 мкМ, ≤100 нМ, ≤10 нМ, ≤1 нМ или ≤0,1 нМ.
[0110] Термин «антитело к PD-1» или «антитело, которое связывается с PD-L1» относятся к антителу, которое способно связывать PD-L1 с достаточной аффинностью, так что антитело становится пригодным в качестве диагностического и/или терапевтического средства нацеливания на PD-L1. Степень связывания анти-PD-L1 антитела с неродственным белком, не являющимся PD-L1, составляет менее чем около 10% от связывания антитела с PD-L1, как измерено, например, с помощью радиоиммунологического анализа (РИА). В определенных вариантах осуществления антитело, которое связывается с PD-L1, имеет константу диссоциации (Kd)≤1 мкМ, ≤100 нМ, ≤10 нМ, ≤1 нМ или ≤0,1 нМ.
[0111] Термин «антитело к CTLA-4» или «антитело, которое связывается с CTLA-4» относятся к антителу, которое способно связывать CTLA-4 с достаточной аффинностью, так что антитело становится пригодным в качестве диагностического и/или терапевтического средства нацеливания на CTLA-4. Степень связывания анти-CTLA-4 антитела с неродственным белком, не являющимся CTLA-4, составляет менее чем около 10% от связывания антитела с CTLA-4, как измерено, например, с помощью радиоиммунологического анализа (РИА). В определенных вариантах осуществления антитело, которое связывается с CTLA-4, имеет константу диссоциации (Kd)≤1 мкМ, ≤100 нМ, ≤10 нМ, ≤1 нМ или ≤0,1 нМ.
[0112] «Моноклональное антитело» относится к гомогенной популяции антител, вовлеченной в высокоспецифическое распознавание и связывание одной антигенной детерминанты или эпитопа. Этим они отличаются от поликлональных антител, которые обычно включают различные антитела, направленные против различных антигенных детерминант. Термин «моноклональное антитело» охватывает как интактные, так и полноразмерные моноклональные антитела, а также фрагменты антител (такие как Fab, Fab', F(ab')2, Fv), одноцепочечные (scFv) мутанты, слитые белки, содержащие часть антитела, и любую другую модифицированную молекулу иммуноглобулина, содержащую сайт распознавания антигена. Кроме того, «моноклональное антитело» относится к таким антителам, полученным любым количеством способов, включая, но не ограничиваясь, гибридомой, селекции с помощью фагового дисплея, рекомбинантной экспрессией и трансгенными животными.
[0113] Термин «химерные антитела» относится к антителам, в которых аминокислотная последовательность молекулы иммуноглобулина получена от двух или более видов. Как правило, вариабельная область как легкой, так и тяжелой цепей соответствует вариабельной области антител, происходящих от одного вида млекопитающих (например, мыши, крысы, кролика и т.д.) с желаемой специфичностью, аффинностью и характеристиками, в то время как константные области гомологичны последовательностям антител, полученных из другого источника (как правило, человека), чтобы избежать иммунного ответа у этого вида.
[0114] В контексте данного документа термин «эффективное количество» или «терапевтически эффективное количество» относится к количеству соединения или комбинации одного или более соединений, которые при введении (последовательно или одновременно) вызывают желаемый биологический или лекарственный ответ, например, либо уничтожают раковые клетки-мишени, либо замедляют, либо останавливают прогрессирование рака у пациента. Терапевтически эффективное количество может варьироваться в зависимости от предполагаемого применения (in vitro или in vivo) или от пациента и заболевания, которое лечат, например, от массы тела и возраста пациента, тяжести заболевания, способа введения и тому подобного, что может легко определить специалист в данной области. Этот термин также применяется к дозе, которая будет вызывать конкретный ответ в клетках-мишенях, например, снижение адгезии тромбоцитов и/или миграции клеток. Например, в некоторых вариантах осуществления «терапевтически эффективное количество» в контексте данного документа относится к количеству [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамата или его фармацевтически приемлемой соли, и количеству ингибитора контрольных точек, которые при применении по отдельности или в комбинации оказывают положительный эффект. В некоторых вариантах осуществления комбинированный эффект является аддитивным. В некоторых вариантах осуществления комбинированный эффект является синергическим. Кроме того, специалистам в данной области будет понятно, что в случае комбинированной терапии количество [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамата или его фармацевтически приемлемой соли и/или количество ингибитора контрольных точек могут быть использованы в «субтерапевтическом количестве», т.е. в количестве меньшем терапевтически эффективного количества [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамата или его фармацевтически приемлемой соли, или только ингибитора контрольных точек.
[0115] В любой форме или композиции вводимая доза(ы) или терапевтически эффективное (общее) количество может быть выражено в виде количества терапевтического вещества(веществ) на пациента либо на основе (i) ППТ, например, в мг/м2, либо (ii) количества, например, в мг.
[0116] Термин «около» означает приблизительно, в области, примерно или около. Термин «около», когда речь идет о числе или числовом диапазоне, означает, что упомянутые число или числовой диапазон являются приближением в пределах экспериментальной изменчивости (или в пределах статистической погрешности эксперимента), и, таким образом, число или числовой диапазон может варьироваться от 1% до 15% от указанного числа или числового диапазона. В общем, термин «около» применяется в данном документе для изменения числового значения выше и ниже указанного значения с отклонением в ± 10%.
[0117] В контексте данного документа термин «пациент» как правило означает млекопитающее (например, человека), у которого диагностировано, проявляются симптомы или который, как полагают, страдает от заболевания, нарушения или состояния (например, рака).
[0118] В контексте данного документа термин «площадь поверхности тела» (ППТ) рассчитывается с помощью стандартной номограммы, например,
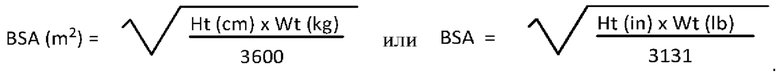
[0119] Термин «комбинированное введение», «введение в комбинации» и «введение комбинации» относится к введению пациенту более чем одного фармацевтически активного ингредиента (включая, но не ограничиваясь ими, [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его фармацевтически приемлемую соль, и ингибитор контрольных точек, как раскрыто в данном документе). Комбинированное введение может относиться к одновременному введению или может относиться к последовательному введению [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамата или его фармацевтически приемлемой соли, а также ингибитора контрольных точек, как раскрыто в данном документе.
[0120] Термины «одновременный» и «одновременно» относятся к введению пациенту [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-l-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамата или его фармацевтически приемлемой соли, а также ингибитора контрольных точек, как раскрыто в данном документе, одновременно или в двух разных временных точках, разделенных по времени не более чем на 2 часа. Одновременное введение [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамата или его фармацевтически приемлемой соли, а также ингибитора контрольных точек может осуществляться в одной лекарственной форме или в отдельных лекарственных формах.
[0121] Термины «последовательный» и «последовательно» относятся к введению пациенту [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамата или его фармацевтически приемлемой соли, а также ингибитора контрольных точек, как раскрыто в данном документе, в двух разных временных точках, разделенных более чем на 2 часа, например, около 3 часа, около 4 часа, около 5 часа, около 8 часов, около 12 часов, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней или даже дольше.
[0122] Термин «перерыв» относится к периоду, который следует после введения пациенту одного или более конкретных фармацевтически активных ингредиентов в схеме с перерывами. Перерыв относится к периоду отдыха, когда конкретный фармацевтически активный ингредиент не вводят в течение по меньшей мере одного дня.
[0123] Термин «синергетический эффект» относится к ситуации, когда комбинация двух или более средств дает больший эффект, чем сумма эффектов каждого из отдельных средств. Термин охватывает не только снижение выраженности симптомов заболевания, которое подлежит лечению, но также улучшенный профиль побочных эффектов, улучшенную переносимость, улучшенное соблюдение пациентом режима и схемы лечения, улучшенную эффективность или любой другой улучшенный клинический результат.
[0124] Используемые в данном документе иллюстративные термины «включать», «такой как», «например» и т.п. (и их варианты, например, «включает» и «включая», «примеры»), если не указано иное, не предназначены для ограничения. То есть, если явно не указано иное, такие термины предназначены для обозначения «но не ограничиваясь этим», например, «включая» означает включая, но не ограничиваясь этим.
[0125] Если не указано иное, подразумевается, что изображенные в данном документе структуры включают химические соединения, которые отличаются только присутствием одного или более изотопно обогащенных атомов. Например, химические соединения, имеющие структуру, за исключением замещения атома водорода дейтерием или тритием или замещения атома углерода 13С- или 14С-обогащенным углеродом, входят в объем этого изобретения.
[0126] Если стереохимическая конфигурация не обозначена, подразумевается, что изображенные в данном документе структуры включают все стереохимические формы структуры, то есть R- и S-конфигурации для каждого асимметричного центра. Следовательно, если не указано иное, одиночные стереохимические изомеры, а также энантиомерные, диастереомерные смеси присутствующих химических соединений входят в объем изобретения. Когда стереохимическая конфигурация обозначается для соединения, диастереоизомерный или энантиомерный избыток соединения составляет по меньшей мере 99,0%, 99,5%, 99,6%, 99,7%, 99,8% или 99,9%.
Ингибитор SAE
[0127] В данном раскрытии предложено комбинированное лечение для пациентов с раком или аутоиммунным заболеванием. Комбинированное лечение включает, среди прочего, введение нуждающемуся в нем субъекту терапевтически эффективного количества по меньшей мере одного ингибитора SAE.
[0128] В некоторых вариантах осуществления ингибитор SAE представляет собой [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его фармацевтически приемлемую соль, имеющее следующую структуру:
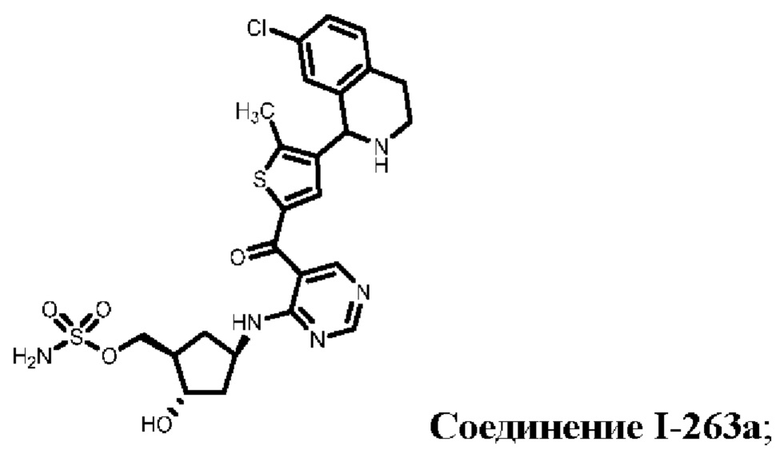
[(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат в данном документе также называется соединением I-263а.
[0129] В некоторых вариантах осуществления ингибитор SAE представляет собой [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его фармацевтически приемлемую соль.
[0130] В некоторых вариантах осуществления ингибитор SAE представляет собой [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или Соединение I-263а.
[0131] Ингибиторы SAE, согласно раскрытию в данном документе, описаны, например, в US 2016/0009744 и US 9695154. Они могут быть получены способами, известными специалисту в данной области, и/или в соответствии со способами, описанными в US 2016/0009744 и US 9695154, которые полностью включены в данный документ посредством ссылки. Центральным в механизме действия применимых ингибиторов SAE, таких как Соединение I-263а, в комбинациях и способах по данному раскрытию является продукция ИФН типа 1 и индукция врожденного иммунного ответа с активацией дендритных клеток, естественных клеток-киллеров (NK) и макрофагов. Биохимические анализы продемонстрировали, что Соединение I-263а представляет собой основанный на механизме ингибитор SUMO-активирующего фермента, который мощно ингибирует активность фермента, образуя ковалентный аддукт с SUMO. Сильная селективность для SUMO-активирующего фермента наблюдалась по сравнению с другими близкородственными убиквитин-активирующими ферментами, Nedd8-активирующим ферментом и ферментом, связанным с аутофагией 7. Селективное и мощное ингибирование SUMO-активирующего фермента и SUMOилирования соединением I-263а было продемонстрировано на культивируемых линиях опухолевых клеток мыши и человека, а антипролиферативная активность соединения I-263а была определена на панели из 7 мышиных клеточных линиях гематологических и солидных опухолей.
[0132] В некоторых вариантах осуществления ингибитор SAE представляет собой [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его кристаллическую форму.
[0133] В некоторых вариантах осуществления ингибитор SAE или его фармацевтическая соль представляет собой кристаллическую форму 1 [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамата, как описано в опубликованной заявке на патент США № US 2016/0009744.
[0134] В некоторых вариантах осуществления ингибитор SAE или его фармацевтическая соль представляет собой кристаллическую форму 2 [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамата, как описано в опубликованной заявке на патент США № US 2016/0009744.
[0135] В некоторых вариантах осуществления ингибитор SAE или его фармацевтическая соль представляет собой кристаллическую форму 3 [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамата, описанную в опубликованной заявке на патент США № US 2016/0009744.
Ингибиторы контрольных точек
[0136] В данном раскрытии предложено комбинированное лечение, включающее, помимо прочего, введение нуждающемуся в нем субъекту терапевтически эффективного количества по меньшей мере одного ингибитора контрольных точек (например, ниволумаба, пембролизумаба, атезолизумаба, дурвалумаба, авелумаба и ипилимумаба). В некоторых вариантах осуществления ингибитор контрольных точек представляет собой антитело к PD-1. В некоторых вариантах осуществления ингибитор контрольных точек представляет собой антитело к PD-L1. В некоторых вариантах осуществления ингибитор контрольных точек представляет собой антитело к CTLA-4.
[0137] PD-1 представляет собой трансмембранный белок типа I, который является одной из основных молекул иммунных контрольных точек (Blanket al., 2005, Cancer Immunotherapy, 54:307-314). PD-1 преимущественно экспрессируется на активированных Т-клетках, и он взаимодействует с лигандами PD-L1 (В7-Н1 или CD274) и PD-L2 (B7-DC или CD273) для индукции сигнала ингибирования, приводящего к снижению пролиферации Т-клеток, продукции цитокинов и цитотоксической активности (Freemanetal., 2000, J. Exp. Med., 192:1027-34).
[0138] В некоторых вариантах осуществления анти-PD-1 антитело представляет собой полностью человеческое моноклональное антитело. В некоторых вариантах осуществления анти-PD-1 антитело представляет собой гуманизированное моноклональное антитело класса IgG.
[0139] В некоторых вариантах осуществления антитело к PD-1 представляет собой полноразмерное (интактное) антитело. В некоторых вариантах осуществления антитело к PD-1 состоит из PD-1-связывающих фрагментов, включая, но не ограничиваясь ими, Fab, Fab', F(ab')2 и Fv, одноцепочечные фрагменты Fv и одноцепочечные доменные фрагменты.
[0140] В некоторых вариантах осуществления антитело к PD-1 представляет собой дериватизированное антитело. В некоторых вариантах осуществления антитело к PD-1 дериватизируется путем гликозилирования, ацетилирования, пегилирования, фосфорилирования и амидирования. В некоторых вариантах осуществления антитело к PD-1 дериватизируется известными защитными/блокирующими группами, протеолитическим расщеплением, связыванием с клеточным лигандом или другим белком. В некоторых вариантах осуществления дериватизированное антитело к PD-1 может содержать одну или более неприродных аминокислот, например, с использованием технологии ambrx (см., например, Wolfson, 2006, Chem. Biol. 13(10):1011-2).
[0141] В некоторых вариантах осуществления антитело к PD-1 представляет собой ниволумаб.
[0142] Ниволумаб представляет собой человеческое моноклональное антитело, которое блокирует взаимодействие между PD-1 и его лигандами, PD-L1 и PD-L2. Ниволумаб представляет собой каппа-иммуноглобулин IgG4 с расчетной молекулярной массой 146 кДа. Он экспрессируется в рекомбинантной клеточной линии яичника китайского хомячка (СНО). Ниволумаб одобрен FDA для лечения неоперабельной или метастатической меланомы, меланомы, метастатического немелкоклеточного рака легкого, распространенной почечно-клеточной карциномы, классической лимфомы Ходжкина, плоскоклеточного рака головы и шеи, уротелиальной карциномы, метастатического колоректального рака с высоким уровнем микросателлитной нестабильности (MSI-H) или с дефицитом репарации неспаренных оснований (dMMR) и гепатоцеллюлярной карциномы. Ниволумаб коммерчески доступен под названием Opdivo®.
[0143] В некоторых вариантах осуществления изобретения антитело к PD-1 представляет собой пембролизумаб.
[0144] Пембролизумаб представляет собой гуманизированное моноклональное антитело, которое блокирует взаимодействие между PD-1 и его лигандами, PD-L1 и PD-L2. Пембролизумаб представляет собой каппа-иммуноглобулин IgG4 с приблизительной молекулярной массой 149 кДа. Пембролизумаб продуцируется в рекомбинантных клетках яичника китайского хомячка (СНО). Пембролизумаб одобрен FDA для лечения меланомы, немелкоклеточного рака легкого, рака головы и шеи, классической лимфомы Ходжкина, первичной В-крупноклеточной лимфомы средостения, уротелиальной карциномы, рака с высоким уровнем микросателлитной нестабильностью, рака желудка и рака шейки матки. Пембролизумаб коммерчески доступен под названием Keytruda®.
[0145] В некоторых вариантах осуществления антитело к PD-1 представляет собой цемиплимаб.
[0146] Цемиплимаб представляет собой человеческое моноклональное антитело, которое связывается с PD-1 и блокирует его взаимодействие с PD-L1 и PD-L2. Цемиплимаб представляет собой иммуноглобулин IgG4 с приблизительной молекулярной массой 146 кДа. Цемиплимаб получают с помощью технологии рекомбинантной ДНК в суспензии клеток яичника китайского хомячка (СНО). Цемиплимаб одобрен FDA для лечения метастатической плоскоклеточной карциномы кожи (CSCC) или местнораспространенной CSCC, которые не являются кандидатами на излечивающее оперативное вмешательство или излечивающее облучение. Цемиплимаб коммерчески доступен под названием Libtayo®.
[0147] Дополнительные антитела к PD-1 включают, например, пидилизумаб (Medivation), BMS-936559 (Bristol-Myers Squibb) и AMP-224.
[0148] В некоторых вариантах осуществления антитело к PD-1, используемое в способах (и наборах), описанных в данном документе, представляет собой ниволумаб или антитело к PD-1, которое связывается с тем же эпитопом, что и ниволумаб. В некоторых вариантах осуществления антитело к PD-1 представляет собой ниволумаб.
[0149] В некоторых вариантах осуществления антитело к PD-1, используемое в способах (и наборах), описанных в данном документе, представляет собой пембролизумаб или антитело к PD-1, которое связывается с тем же эпитопом, что и пембролизумаб. В некоторых вариантах осуществления изобретения антитело к PD-1 представляет собой пембролизумаб.
[0150] PD-L1 представляет собой трансмембранный белок типа I, который включает содержит Ig-V-подобный домен, Ig-C-подобный домен, трансмембранный домен и внутриклеточный С-концевой домен. PD-L1 экспрессируется в широком диапазоне видов рака с высокой частотой, включая опухолевые клетки и/или инфильтрирующие опухоль иммунные клетки, и может способствовать ингибированию противоопухолевого иммунного ответа в микроокружении опухоли. При некоторых видах рака экспрессия PD-L1 была связана с уменьшением выживаемости и неблагоприятным прогнозом. PD-L1 экспрессируется на многих типах клеток, включая Т-клетки, В-клетки, эндотелиальные, эпителиальные и антигенпрезентирующие клетки, на клетках тканей легких, печени и сердца, а также на некоторых типах опухолевых клеток. Также было показано, что экспрессия PD-L1 на клеточной поверхности повышается за счет стимуляции ИФН-γ. Существует по меньшей мере 4 варианта PD-1, которые были клонированы из активированных Т-клеток человека, включая транскрипты, в которых отсутствуют (i) экзон 2, (ii) экзон 3, (iii) экзоны 2 и 3 или (iv) экзоны 2-4. Nielsen et al., Cell. Immunol. 235: 109-16 (2005). Аминокислотная последовательность PD-L1 человека представлена под номером доступа в GenBank NP 054862.1.
[0151] В некоторых вариантах осуществления антитело к PD-L1 представляет собой полноразмерное (интактное) антитело. В некоторых вариантах осуществления антитело к PD-L1 состоит из PD-L1-связывающих фрагментов, включая, но не ограничиваясь ими, фрагменты Fab, F(ab')2, Fd, Fv и dAb, одноцепочечные фрагменты Fv и иммуноглобулиновые слитые белки с PD-Ll-связывающим доменом.
[0152] В некоторых вариантах осуществления антитело к PD-L1 представляет собой атезолизумаб.
[0153] Атезолизумаб представляет собой антитело, блокирующее лиганд 1 программируемой гибели клеток (PD-L1). Атезолизумаб представляет собой сконструированный с помощью Fc гуманизированный негликозилированный каппа-иммуноглобулин IgG1, расчетная молекулярная масса которого составляет 145 кДа. Атезолизумаб одобрен FDA для лечения местнораспространенной или метастатической уротелиальной карциномы и метастатического немелкоклеточного рака легкого. Атезолизумаб коммерчески доступен под названием Tecentriq®.
[0154] В некоторых вариантах осуществления антитело к PD-L1 представляет собой дурвалумаб.
[0155] Дурвалумаб представляет собой антитело, блокирующее лиганд 1 программируемой гибели клеток (PD-L1). Дурвалумаб представляет собой человеческое моноклональное антитело класса каппа-иммуноглобулина G1 (IgG1κ), которое получают с помощью технологии рекомбинантной ДНК в культуре суспензии клеток яичника китайского хомячка (СНО). Дурвалумаб одобрен FDA для лечения уротелиальной карциномы и немелкоклеточного рака легкого. Дурвалумаб коммерчески доступен под названием Imfinzi®.
[0156] В некоторых вариантах осуществления антитело к PD-L1 представляет собой авелумаб.
[0157] Авелумаб представляет собой антитело, блокирующее лиганд 1 программируемой гибели клеток (PD-L1). Авелумаб представляет собой человеческое моноклональное антитело класса IgG1 лямбда, молекулярная масса которого составляет приблизительно 147 кДа. Авелумаб одобрен FDA для лечения метастатической карциномы из клеток Меркеля и местнораспространенной или метастатической уротелиальной карциномы. Авелумаб коммерчески доступен под названием Bavencio®.
[0158] Дополнительные антитела к PD-L1 включают, например, YW243.55.S70 (патент США №8217149), MEDI-4736, MSB-0010718C, LY3300054 (Eli Lilly and Co.), BMS-936559 (Bristol-Meyers Squibb), MPDL3280A и MDX-1105.
[0159] В некоторых вариантах осуществления антитело к PD-L1, используемое в способах (и наборах), описанных в данном документе, представляет собой атезолизумаб или антитело к PD-L1, которое связывается с тем же эпитопом, что и атезолизумаб. В некоторых вариантах осуществления антитело к PD-L1 представляет собой атезолизумаб.
[0160] В некоторых вариантах осуществления антитело к PD-L1, используемое в способах (и наборах), описанных в данном документе, представляет собой дурвалумаб или антитело к PD-L1, которое связывается с тем же эпитопом, что и дурвалумаб. В некоторых вариантах осуществления антитело к PD-L1 представляет собой дурвалумаб.
[0161] В некоторых вариантах осуществления антитело к PD-L1, используемое в способах (и наборах), описанных в данном документе, представляет собой авелумаб или антитело к PD-L1, которое связывается с тем же эпитопом, что и авелумаб. В некоторых вариантах осуществления антитело к PD-L1 представляет собой авелумаб.
[0162] CTLA-4 представляет собой трансмембранный белок типа I, кодируемый у человека геном CTLA-4. Было установлено, что CTLA-4 имеет связь с ростом и развитием рака из-за его негативной роли в иммунном ответе. CTLA-4 экспрессируется на клеточной поверхности активированных CD4+ и CD8+ Т-клеток и является важным негативным регулятором функции Т-клеток. Было показано, что CTLA-4 негативно регулирует иммунную активацию через внутренние и внешние механизмы (Grosso and Kunkel, Cancer Immunity (2013) 13:5). Было показано, что ингибирование негативной регуляции CTLA-4 способствует стимуляции адаптивного иммунного ответа и активации Т-клеток. Репрезентативную аминокислотную последовательность CTLA-4 человека можно найти под номером доступа в GenBank: AAL07473.1, а репрезентативную последовательность нуклеиновой кислоты мРНК, кодирующую CTLA-4 человека, можно найти под номером доступа в GenBank: AF414120.1.
[0163] В некоторых вариантах осуществления антитело к CTLA-4 представляет собой полноразмерное (интактное) антитело. В некоторых вариантах осуществления антитело к CTLA-4 состоит из анти-CTLA-4-связывающих фрагментов, включая, но не ограничиваясь ими, Fab, Fab', F(ab')2, Fv и одноцепочечные фрагменты, диатело, стабилизированный дисульфидом фрагмент Fv (dsFv), (dsFv)2, биспецифический dsFv (dsFv-dsFv'), диатело, стабилизированное дисульфидом (ds-диатело), молекулу одноцепочечного антитела (scFv), димер scFv (двухвалентное диатело), мультиспецифическое антитело, вер блюд изированное однодоменное антитело, нанотело, доменное антитело и двухвалентное доменное антитело.
[0164] В некоторых вариантах осуществления антитело к CTLA-4 представляет собой ипилимумаб.
[0165] Ипилимумаб представляет собой рекомбинантное человеческое моноклональное антитело, которое связывается с цитотоксическим антигеном 4, ассоциированным с Т-лимфоцитами (CTLA-4). Ипилимумаб представляет собой каппа-иммуноглобулин IgG1 с приблизительной молекулярной массой 148 кДа. Ипилимумаб продуцируется в культуре клеток млекопитающих (яичника китайского хомячка). Ипилимумаб одобрен FDA для лечения неоперабельной или метастатической меланомы, адъювантного лечения меланомы и распространенной почечно-клеточной карциномы. Ипилимумаб коммерчески доступен под названием Yervoy®.
[0166] Дополнительные антитела к CTLA-4 включают, например, тремелимумаб.
[0167] В некоторых вариантах осуществления антитело к CTLA-4, используемое в способах (и наборах), описанных в данном документе, представляет собой ипилимумаб или антитело к CTLA-4, которое связывается с тем же эпитопом, что и ипилимумаб. В некоторых вариантах осуществления антитело к CTLA-4 представляет собой ипилимумаб. Способы лечения рака или аутоиммунных заболеваний
[0168] В некоторых вариантах осуществления данное раскрытие относится к способу лечения рака у пациента путем введения пациенту, нуждающемуся в указанном лечении, комбинации ингибитора SAE или его фармацевтически приемлемой соли и одного или более ингибиторов контрольных точек.
[0169] В некоторых вариантах осуществления данное раскрытие относится к способу лечения рака путем введения пациенту, нуждающемуся в указанном лечении, комбинации ингибитора SAE и ингибитора контрольных точек.
[0170] В некоторых вариантах осуществления данное раскрытие относится к применению ингибитора SAE в комбинации с ингибитором контрольных точек для лечения рака у пациента.
[0171] В некоторых вариантах осуществления данное раскрытие относится к композиции, содержащей ингибитор SAE, для применения при лечении рака у пациента, причем пациента также лечат ингибитором контрольных точек. В некоторых аспектах изобретение относится к композиции, содержащей ингибитор SAE, для применения при лечении рака у пациента, причем ингибитор SAE находится в комбинации с ингибитором контрольных точек. В некоторых вариантах осуществления ингибитор SAE можно вводить одновременно или последовательно с ингибитором контрольных точек.
[0172] В некоторых вариантах осуществления данное раскрытие относится к композиции, содержащей Соединение I-263а или его фармацевтически приемлемую соль, и ингибитор контрольных точек или его фармацевтически приемлемую соль, в виде совместного состава или отдельных составов, при этом введение композиций является одновременным, последовательным или чередующимся. В некоторых вариантах осуществления данное раскрытие предусматривает введение соединения I-263а или его фармацевтически приемлемой соли, ингибитора контрольных точек или его фармацевтически приемлемой соли и одного или более дополнительных терапевтических средств или его фармацевтически приемлемой соли, в виде совместного состава или отдельных составов, при этом введение композиций является одновременным, последовательным или чередующимся.
[0173] В некоторых вариантах осуществления данное раскрытие относится к способам лечения рака, включающим введение пациенту, нуждающемуся в таком лечении, терапевтически эффективного количества комбинации ингибитора SAE и ингибитора контрольных точек.
[0174] В некоторых вариантах осуществления данное раскрытие относится к способу лечения рака путем введения пациенту комбинации соединения I-263а или его фармацевтически приемлемой соли и ингибитора контрольных точек.
[0175] В другом аспекте данное раскрытие относится к применению соединения I-263а или его фармацевтически приемлемой соли в комбинации с ингибитором контрольных точек для лечения рака.
[0176] В некоторых вариантах осуществления способы лечения рака, как описано в данном документе, могут включать комбинацию ингибитора SAE, ингибитора контрольных точек и одного или более дополнительных терапевтических средств. В некоторых вариантах осуществления одно или более дополнительных терапевтических средств могут представлять собой химиотерапевтические средства. В некоторых вариантах осуществления одно или более дополнительных терапевтических средств могут включать, но не ограничиваются ими, флударабин, циклофосфамид, доксорубицин, винкристин, метотрексат, химиотерапевтические средства на основе антрациклинов, преднизон, метилпреднизолон, глюкокортикоиды, ибритумомаб тиуксетан, ацетаминофен, антигистаминные препараты и их комбинации. В другом варианте осуществления ингибитор контрольных точек вводят совместно с гиалуронидазой человека.
[0177] В некоторых вариантах осуществления данное раскрытие относится к способу лечения нарушения, причем нарушение представляет собой рак.
[0178] В некоторых вариантах осуществления рак представляет собой солидную опухоль. В некоторых вариантах осуществления солидная опухоль представляет собой распространенную солидную опухоль. В некоторых вариантах осуществления солидная опухоль представляет собой метастатическую солидную опухоль. В некоторых вариантах осуществления солидная опухоль представляет собой неоперабельную солидную опухоль.
[0179] Неограничивающие примеры солидных опухолей включают рак поджелудочной железы; рак мочевого пузыря, включая инвазивный рак мочевого пузыря; колоректальный рак, включая метастатический колоректальный рак с высоким уровнем микросателлитной нестабильности (MSI-H) или с дефицитом репарации неспаренных оснований (dMMR); колоректальный рак с микросателлитной стабильностью (MSS); рак щитовидной железы; рак желудка; рак молочной железы, включая метастатический рак молочной железы; рак предстательной железы, включая андроген-зависимый и андроген-независимый рак предстательной железы; рак почек, включая, например, метастатическую почечно-клеточную карциному и распространенную почечно-клеточную карциному; уротелиальную карциному, включая местнораспространенную или метастатическую уротелиальную карциному; рак с высокой микросателлитной нестабильностью; рак печени, включая, например.ю гепатоцеллюлярную карциному и рак внутрипеченочных желчных протоков; рак легкого и бронхов, включая немелкоклеточный рак легкого (НМРЛ), аденокарциному НМРЛ, плоскоклеточный рак легкого, брохиолоальвеолярную карциному (ВАС), аденокарциному легкого и мелкоклеточный рак легкого (МРЛ); рак яичников, включая, например, прогрессирующий эпителиальный и первичный перитонеальный рак; рак шейки матки, включая рак шейки матки, при котором ранее не проводилось лечение с применением ИКТ; плоскоклеточную карциному; аденосквамозную карциному; аденокарциному шейки матки; рак матки, включая, например, тело матки и шейку матки; рак эндометрия; рак пищевода; рак головы и шеи, включая, например, плоскоклеточную карциному головы и шеи, рак носоглотки, ротовой полости и глотки; меланому, включая неоперабельную или метастатическую меланому, и адъювантное лечение меланомы; метастатическую карциному из клеток Меркеля; нейроэндокринный рак, включая метастатические нейроэндокринные опухоли; рак головного мозга, включая, например, глиому/глиобластому, анапластическую олигодендроглиому, мультиформную глиобластому взрослых и анапластическую астроцитому взрослых; нейроэндокринный рак, включая метастатические нейроэндокринные опухоли; рак костей; рак гастроэзофагеального перехода и саркому мягких тканей.
[0180] В некоторых вариантах осуществления рак представляет собой имеет гематологический рак. Неограничивающие примеры гематологических злокачественных новообразований включают острый миелоидный лейкоз (ОМЛ); хронический миелолейкоз (ХМЛ), включая ускоренную фазу ХМЛ и бластную фазу ХМЛ (ХМЛ-БФ); острый лимфобластный лейкоз (ОЛЛ); хронический лимфоцитарный лейкоз (ХЛЛ); лимфому Ходжкина (ЛХ), включая классическую лимфому Ходжкина; неходжкинскую лимфому (НХЛ), включая В-клеточную лимфому, Т-клеточную лимфому, фолликулярную лимфому (ФЛ), лимфому маргинальной зоны (ЛМЗ), мантийноклеточную лимфому (МКЛ), диффузную В-крупноклеточную лимфому (ДВККЛ), первичную В-крупноклеточную лимфому средостения и лимфому Беркитта; множественную миелому (ММ); амилоидоз; макроглобулинемию Вальденстрема; миелодиспластические синдромы (МДС), включая рефрактерную анемию (РА), рефрактерную анемию с кольцевидными сидеробластами (РАКС), рефрактерную анемию с избытком бластов (РАИБ) и РАИБ в процессе трансформации (РАИБ-Т); и миелопролиферативные синдромы. В некоторых вариантах осуществления рак представляет собой хронический лимфоцитарный лейкоз (ХЛЛ), лимфому Ходжкина или неходжкинскую лимфому, включая фолликулярную лимфому (ФЛ), лимфому маргинальной зоны (ЛМЗ), мантийноклеточную лимфому (МКЛ), диффузную В-крупноклеточную лимфому (ДВККЛ) и лимфому Беркитта.
[0181] В некоторых вариантах осуществления рак представляет собой меланому, рак легкого, рак почек, лимфому, рак головы и шеи, уротелиальный рак, рак предстательной железы, рак мочевого пузыря, рак молочной железы, рак желудка, колоректальный рак, лейкоз, рак шейки матки, рак с высоким уровнем микросателлитной нестабильности, гепатоцеллюлярную карциному или карциному из клеток Меркеля.
[0182] В некоторых вариантах осуществления меланома представляет собой метастатическую меланому, неоперабельную меланому или меланому кожи.
[0183] В некоторых вариантах осуществления рак легкого представляет собой немелкоклеточный рак легкого или мелкоклеточный рак легкого.
[0184] В некоторых вариантах осуществления немелкоклеточный рак легкого представляет собой метастатический немелкоклеточный рак легкого, метастатический плоскоклеточный немелкоклеточный рак легкого или метастатический немелкоклеточный рак легкого. В некоторых вариантах осуществления немелкоклеточный рак легкого представляет собой аденокарциному немелкоклеточного рака легкого.
[0185] В некоторых вариантах осуществления рак представляет собой рак шейки матки. В некоторых вариантах осуществления рак представляет собой рак шейки матки, при котором ранее не проводилось лечение с применением ИКТ. В некоторых вариантах осуществления рак представляет собой плоскоклеточную карциному, аденосквамозную карциному или аденокарциному шейки матки.
[0186] В некоторых вариантах осуществления рак представляет собой колоректальный рак. В некоторых вариантах осуществления рак представляет собой колоректальный рак с микросателлитной стабильностью (МСС-КРР). В некоторых вариантах осуществления рак представляет собой МСС-КРР, при котором ранее не проводилось лечение с применением ИКТ.
[0187] В некоторых вариантах осуществления рак почки представляет собой почечно-клеточную карциному.
[0188] В некоторых вариантах осуществления лимфома представляет собой классическую лимфому Ходжкина или первичную В-крупноклеточную лимфому средостения.
[0189] В некоторых вариантах осуществления рак головы и шеи представляет собой плоскоклеточный рак головы и шеи.
[0190] В некоторых вариантах осуществления уротелиальный рак представляет собой уротелиальную карциному.
[0191] В некоторых вариантах осуществления рак предстательной железы представляет собой гормонорезистентный рак предстательной железы.
[0192] В некоторых вариантах осуществления рак желудка представляет собой аденокарциному гастроэзофагеального перехода.
[0193] В некоторых вариантах осуществления рак представляет является рецидивирующим. В некоторых вариантах осуществления рецидив рака представляет собой рак, который вернулся после периода времени, в течение которого рак не мог быть обнаружен.
[0194] В некоторых вариантах осуществления рак является рефрактерным. В некоторых вариантах осуществления рефрактерный рак не отвечает на противораковое лечение; он также известен как резистентный рак. В некоторых вариантах осуществления рак является устойчивым к ритуксимабу. В некоторых вариантах осуществления рак не отвечает на лечение ритуксимабом. В некоторых вариантах осуществления рак представляет собой рецидивирующий рак, устойчивый к ритуксимабу. В некоторых вариантах осуществления пациент стал рефрактерным к схеме, содержащей ритуксимаб. В некоторых вариантах осуществления опухоль является неоперабельной. В некоторых вариантах осуществления неоперабельная опухоль не может быть удалена хирургическим путем. В некоторых вариантах осуществления лечение рака ранее не проводилось. В некоторых вариантах осуществления рак является местнораспространенным. В некоторых вариантах осуществления «местнораспространенный» относится к раку, который несколько обширен, но все еще ограничен одной областью. В некоторых случаях «местнораспространенный» может относиться к небольшой опухоли, которая не распространилась, но инфильтрировала близлежащие органы или ткани, что затрудняет ее удаление только хирургическим путем. В некоторых вариантах осуществления рак является метастатическим. В некоторых вариантах осуществления метастатический рак представляет собой рак, который распространился из той части тела, где он появился (первичный очаг), в другие части тела.
[0195] В некоторых вариантах осуществления у пациента имеется прогрессирующая метастатическая или неоперабельная солидная опухоль, для которой по меньшей мере одна предшествующая схема лечения оказалась неэффективной.
[0196] В некоторых вариантах осуществления пациент имеет рецидивирующую или рефрактерную PD-1-положительную или PD-L1-положительную аденокарциному немелкоклеточного рака легкого. В некоторых вариантах осуществления у пациента имеется как PD-1-положительная аденокарцинома немелкоклеточного рака легкого, так и рецидивирующая или рефрактерная аденокарцинома немелкоклеточного рака легкого. В некоторых вариантах осуществления у пациента имеется как PD-L1-положительная аденокарцинома немелкоклеточного рака легкого, так и рецидивирующая или рефрактерная аденокарцинома немелкоклеточного рака легкого.
[0197] В некоторых вариантах осуществления у пациента имеется рецидивирующая или рефрактерная PD-1-положительная или PD-L1-положительная аденокарцинома немелкоклеточного рака легкого и наблюдается прогрессирование на фоне по меньшей мере одной предшествующей схемы лечения.
[0198] В некоторых вариантах осуществления пациент имеет рецидивирующую или рефрактерную PD-1-положительную или PD-L1-положительную аденокарциному немелкоклеточного рака легкого и является рефрактерным к любому ИКТ. В некоторых вариантах осуществления у пациента имеется рецидивирующая или рефрактерная PD-1-положительная или PD-L1-положительная аденокарцинома немелкоклеточного рака легкого и наблюдается прогрессирование на фоне по меньшей мере одной предшествующей схемы лечения и является рефрактерным к любому ИКТ.
[0199] В некоторых вариантах осуществления пациент имеет рецидивирующий или рефрактерный PD-1-положительный рак шейки матки, при котором ранее не проводилось лечение с применением ИКТ. В некоторых вариантах осуществления у пациента имеется как PD-1-положительный рак шейки матки, при котором ранее не проводилось лечение с применением ИКТ, так и рецидивирующий или рефрактерный рак шейки матки, при котором ранее не проводилось лечение с применением ИКТ.
[0200] В некоторых вариантах осуществления у пациента имеется рецидивирующий или рефрактерный PD-1-положительная рак шейки матки, при котором ранее не проводилось лечение с применением ИКТ, и наблюдается прогрессирование на фоне по меньшей мере одной предшествующей схемы лечения.
[0201] В некоторых вариантах осуществления пациент имеет рецидивирующий или рефрактерный PD-1-положительный рак шейки матки, при котором ранее не проводилось лечение с применением ИКТ, и который является рефрактерным к любому ИКТ. В некоторых вариантах осуществления пациент имеет рецидивирующий или рефрактерный PD-1-положительный рак шейки матки, при котором ранее не проводилось лечение с применением ИКТ и наблюдается прогрессирование на фоне по меньшей мере одной предшествующей схемы лечения, и который является рефрактерным к любому ИКТ.
[0202] В некоторых вариантах осуществления пациент имеет рецидивирующий или рефрактерный PD-1-положительный колоректальный рак с микросателлитной стабильностью (МСС-КРР), при котором ранее не проводилось лечение с применением ИКТ. В некоторых вариантах осуществления у пациента имеется как PD-1-положительный МСС-КРР, при котором ранее не проводилось лечение с применением ИКТ, так и рецидивирующий или рефрактерный МСС-КРР, при котором ранее не проводилось лечение с применением ИКТ.
[0203] В некоторых вариантах осуществления пациент имеет рецидивирующий или рефрактерный PD-1-положительный МСС-КРР, при котором ранее не проводилось лечение с применением ИКТ и наблюдается прогрессирование на фоне по меньшей мере одной предшествующей схемы лечения. В некоторых вариантах осуществления пациент имеет рецидивирующий или рефрактерный PD-1-положительный МСС-КРР, при котором ранее не проводилось лечение с применением ИКТ и наблюдается прогрессирование на фоне по меньшей мере двух предшествующих схем лечения. В некоторых вариантах осуществления у пациента имеется рецидивирующий или рефрактерный PD-1-положительный МСС-КРР, при котором ранее не проводилось лечение с применением ИКТ, и наблюдается прогрессирование на фоне по меньшей мере одной предшествующей схемы лечения.
[0204] В некоторых вариантах осуществления пациент имеет рецидивирующий или рефрактерный PD-1-положительный МСС-КРР, при котором ранее не проводилось лечение с применением ИКТ, и который является рефрактерным к любому ИКТ. В некоторых вариантах осуществления пациент имеет рецидивирующий или рефрактерный PD-1-положительный МСС-КРР, при котором ранее не проводилось лечение с применением ИКТ и наблюдается прогрессирование на фоне по меньшей мере одной предшествующей схемы лечения, и который является рефрактерным к любому ИКТ. В некоторых вариантах осуществления пациент имеет рецидивирующий или рефрактерный PD-1-положительный МСС-КРР, при котором ранее не проводилось лечение с применением ИКТ и наблюдается прогрессирование на фоне по меньшей мере двух предшествующих схем лечения, и который является рефрактерным к любому ИКТ. В некоторых вариантах осуществления пациент имеет рецидивирующий или рефрактерный PD-1-положительный МСС-КРР, при котором ранее не проводилось лечение с применением ИКТ и наблюдается прогрессирование на фоне по меньшей мере трех предшествующих схем лечения, и который является рефрактерным к любому ИКТ.
[0205] В некоторых вариантах осуществления данное раскрытие относится к способу лечения нарушения, причем нарушение представляет собой с аутоиммунное заболевание.
[0206] В некоторых вариантах осуществления нарушение является SAE-опосредованным нарушением. В некоторых вариантах осуществления нарушение является SAE-опосредованным нарушением, отличным от рака.
[0207] В некоторых вариантах осуществления нарушение представляет собой PD-1-положительный рак. PD-1-положительный рак включает рак, при котором PD-1 экспрессируется на раковых клетках.
[0208] В некоторых вариантах осуществления PD-1-положительный рак представляет собой PD-1-положительный рак легкого. В некоторых вариантах осуществления PD-1-положительный рак представляет собой PD-1-положительный немелкоклеточный рак легкого. В некоторых вариантах осуществления PD-1-положительный рак представляет собой PD-1-положительный метастатический немелкоклеточный рак легкого.
[0209] В некоторых вариантах осуществления PD-1-положительный рак представляет собой PD-1-положительный рак шейки матки.
[0210] В некоторых вариантах осуществления PD-1-положительный рак представляет собой PD-1-положительный колоректальный рак. В некоторых вариантах осуществления PD-1-положительный рак представляет собой PD-1-положительный колоректальный рак с микросателлитной стабильностью. В некоторых вариантах осуществления PD-1-положительный рак представляет собой PD-1-положительный колоректальный рак с высоким уровнем микросателлитной нестабильности (MSI-H). В некоторых вариантах осуществления изобретения PD-1-положительный рак представляет собой PD-1-положительный метастатический колоректальный рак с дефицитом репарации неспаренных оснований (dMMR).
[0211] В некоторых вариантах осуществления PD-1-положительный рак представляет собой PD-1-положительную меланому. В некоторых вариантах осуществления PD-1-положительный рак представляет собой PD-1-положительную неоперабельную или метастатическую меланому.
[0212] В некоторых вариантах осуществления PD-1-положительный рак представляет собой PD-1-положительный рак почек. В некоторых вариантах осуществления PD-1-положительный рак представляет собой PD-1-положительную распространенную почечно-клеточную карциному.
[0213] В некоторых вариантах осуществления PD-1-положительный рак представляет собой PD-1-положительную лимфому. В некоторых вариантах осуществления PD-1-положительный рак представляет собой PD-1-положительную классическую лимфому Ходжкина.
[0214] В некоторых вариантах осуществления PD-1-положительный рак представляет собой PD-1-положительный рак головы и шеи. В некоторых вариантах осуществления PD-1-положительный рак представляет собой PD-1-положительную рецидивирующую или метастатическую плоскоклеточную карциному головы и шеи.
[0215] В некоторых вариантах осуществления PD-1-положительный рак представляет собой PD-1-положительный уротелиальный рак. В некоторых вариантах осуществления PD-1-положительный рак представляет собой PD-1-положительную распространенную или метастатическую уротелиальную карциному.
[0216] В некоторых вариантах осуществления PD-1-положительный рак представляет собой PD-1-положительную гепатоцеллюлярную карциному.
[0217] В некоторых вариантах осуществления PD-1-положительный рак представляет собой PD-1-положительную плоскоклеточную карциному. В некоторых вариантах осуществления PD-1-положительный рак представляет собой PD-1-положительную метастатическую плоскоклеточную карциному кожи.
[0218] В некоторых вариантах осуществления нарушение представляет собой PD-L1-положительный рак. PD-L1-положительный рак включает рак, при котором PD-L1 экспрессируется на раковых клетках.
[0219] В некоторых вариантах осуществления PD-L1-положительный рак представляет собой PD-L1-положительный рак легкого. В некоторых вариантах осуществления PD-L1-положительный рак представляет собой PD-L1-положительный немелкоклеточный рак легкого. В некоторых вариантах осуществления PD-L1-положительный рак представляет собой PD-L1-положительный метастатический немелкоклеточный рак легкого. В некоторых вариантах осуществления PD-L1-положительный рак представляет собой PD-L1-положительный немелкоклеточный рак легкого III-й стадии.
[0220] В некоторых вариантах осуществления PD-L1-положительный рак представляет собой PD-L1-положительный уротелиальный рак. В некоторых вариантах осуществления PD-L1-положительный рак представляет собой PD-L1-положительную распространенную или метастатическую уротелиальную карциному. В некоторых вариантах осуществления PD-L1-положительный рак представляет собой PD-L1-положительную распространенную или метастатическую уротелиальную карциному.
[0221] В некоторых вариантах осуществления PD-L1-положительный рак представляет собой PD-L1-положительную метастатическую карциному из клеток Меркеля.
[0222] В некоторых вариантах осуществления нарушение представляет собой CTLA-4-положительный рак. CTLA-4-положительный рак включает рак, при котором CTLA-4 экспрессируется на раковых клетках.
[0223] В некоторых вариантах осуществления CTLA-4-положительный рак представляет собой CTLA-4-положительную меланому. В некоторых вариантах осуществления CTLA-4-положительный рак представляет собой CTLA-4-положительную неоперабельную или метастатическую меланому. В некоторых вариантах осуществления CTLA-4-положительный рак представляет собой CTLA-4-положительную меланому кожи.
[0224] В некоторых вариантах осуществления CTLA-4-положительный рак представляет собой CTLA-4-положительный рак почек. В некоторых вариантах осуществления CTLA-4-положительный рак представляет собой CTLA-4-положительную распространенную почечно-клеточную карциному.
Лекарственное средство
[0225] В некоторых вариантах осуществления данное раскрытие относится к лекарственному средству для применения при лечении рака у пациента, нуждающегося в таком лечении. Лекарственное средство включает ингибитор SAE и ингибитор контрольных точек и находится в одной лекарственной форме или в отдельных лекарственных формах.
[0226] В некоторых вариантах осуществления лекарственное средство, как описано в данном документе, может включать комбинацию ингибитора SAE, ингибитора контрольных точек и, необязательно, одного или более дополнительных терапевтических средств.
[0227] В некоторых вариантах осуществления данное раскрытие относится к применению ингибитора SAE при производстве лекарственного средства для лечения рака, причем ингибитор SAE вводят с ингибитором контрольных точек, и причем лекарственное средство находится в одной лекарственной форме или в отдельных лекарственных формах. В некоторых вариантах осуществления ингибитор SAE вводят с ингибитором контрольных точек и одним или более дополнительными терапевтическими средствами.
[0228] В некоторых вариантах осуществления данное раскрытие относится к применению ингибитора SAE при производстве лекарственного средства для лечения рака у пациента, причем пациента также лечат ингибитором контрольных точек и, необязательно, одним или более дополнительными терапевтическими средствами. В некоторых вариантах осуществления ингибитор SAE можно вводить одновременно или последовательно с ингибитором контрольных точек. В некоторых аспектах данное раскрытие относится к применению ингибитора SAE при производстве лекарственного средства для лечения рака у пациента, причем ингибитор SAE находится в комбинации с ингибитором контрольных точек и, необязательно, с одним или более дополнительными терапевтическими средствами. В некоторых вариантах осуществления ингибитор SAE находится в той же композиции, что и ингибитор контрольных точек. В некоторых вариантах осуществления ингибитор SAE находится в отдельной композиции, как и ингибитор контрольных точек. В некоторых вариантах осуществления ингибитор SAE находится в той же композиции, что и одно или более дополнительных терапевтических средств. В некоторых вариантах осуществления ингибитор SAE находится в той же композиции, что и ингибитор контрольных точек и, необязательно, одно или более дополнительных терапевтических средств. В некоторых вариантах осуществления ингибитор SAE находится в отдельной композиции, как одно или более дополнительных терапевтических средств. В некоторых вариантах осуществления ингибитор SAE находится в отдельной композиции, как и ингибитор контрольных точек и, необязательно, одно или более дополнительных терапевтических средств.
[0229] В другом аспекте данное раскрытие относится к применению соединения I-263а или его фармацевтически приемлемой соли в комбинации с ингибитором контрольных точек при производстве лекарственного средства для лечения рака. В некоторых вариантах осуществления данное раскрытие относится к применению соединения I-263а или его фармацевтически приемлемой соли в комбинации с ингибитором контрольных точек и, необязательно, одним или более дополнительными терапевтическими средствами при производстве лекарственного средства для применения при лечении рака.
[0230] В другом аспекте данное раскрытие относится к применению соединения I-263а или его фармацевтически приемлемой соли при производстве лекарственного средства для лечения рака, причем Соединение I-263а или его фармацевтически приемлемую соль вводят с ингибитором контрольных точек и, необязательно, одним или более дополнительными терапевтическими средствами.
[0231] В другом аспекте данное раскрытие относится к соединению I-263а или его фармацевтически приемлемой соли для применения в качестве лекарственного средства в комбинации с ингибитором контрольных точек, причем Соединение I-263а и ингибитор контрольных точек можно вводить одновременно или последовательно.
[0232] В другом аспекте данное раскрытие относится к применению соединения I-263а или его фармацевтически приемлемой соли и ингибитора контрольных точек при производстве лекарственного средства для лечения рака у субъекта. В некоторых вариантах осуществления данное раскрытие относится к применению соединения I-263а или его фармацевтически приемлемой соли и ингибитора контрольных точек при производстве лекарственного средства для лечения рака у субъекта, причем соединение I-263а составлено для одновременного или последовательного введения субъекту с дополнительным терапевтическим средством. В некоторых вариантах осуществления данное раскрытие относится к применению соединения I-263а или его фармацевтически приемлемой соли и ингибитора контрольных точек при производстве лекарственного средства для лечения рака у субъекта, причем Соединение I-263а и ингибитор контрольных точек составлены для одновременного или последовательного введения субъекту с дополнительным терапевтическим средством.
[0233] В некоторых вариантах осуществления одно или более дополнительных терапевтических средств могут представлять собой химиотерапевтические средства. В некоторых вариантах осуществления одно или более дополнительных терапевтических средств могут включать, но не ограничиваются ими, флударабин, циклофосфамид, доксорубицин, винкристин, метотрексат, химиотерапевтические средства на основе антрациклинов, преднизон, метилпреднизолон, глюкокортикоиды, ибритумомаб тиуксетан, ацетаминофен, антигистаминные препараты и их комбинации. В другом варианте осуществления ингибитор контрольных точек вводят совместно с гиалуронидазой человека.
Введение комбинации
[0234] Соединение I-263а или его фармацевтически приемлемую соль можно вводить в комбинации с ингибитором контрольных точек и, необязательно, одним или более дополнительными терапевтическими средствами в одной лекарственной форме или в виде отдельных лекарственных форм. В некоторых вариантах осуществления при введении в виде отдельной лекарственной формы ингибитор контрольных точек можно вводить до, одновременно или после введения I-263а или его фармацевтически приемлемой соли. В некоторых вариантах осуществления при введении в виде отдельной лекарственной формы одну или более доз I-263а или его фармацевтически приемлемой соли можно вводить до ингибитора контрольных точек. В некоторых вариантах осуществления ингибитор контрольных точек вводят до введения соединения I-263а или его фармацевтически приемлемой соли. В контексте данного документа введение в «комбинации» соединения I-263а или его фармацевтически приемлемой соли, ингибитора контрольных точек и, необязательно, одного или более дополнительных терапевтических средств относится не только к одновременному или последовательному введению средств, но также и к введение средств в рамках одного цикла лечения, как будет понятно специалисту в данной области. При введении соединения I-263а или его фармацевтически приемлемой соли в комбинации с ингибитором контрольных точек и, необязательно, одним или более дополнительными терапевтическими средствами, вводят терапевтически эффективное количество комбинации.
[0235] Ингибитор SAE можно вводить любым способом, известным специалисту в данной области. Например, в некоторых вариантах осуществления ингибитор SAE можно вводить в форме фармацевтической композиции ингибитора SAE и фармацевтически приемлемого носителя, таких как описаны в данном документе. В некоторых вариантах осуществления фармацевтическая композиция подходит для перорального введения. В некоторых вариантах осуществления фармацевтическая композиция представляет собой таблетку или капсулу, подходящую для перорального введения. В некоторых других вариантах осуществления фармацевтическая композиция представляет собой жидкую лекарственную форму, подходящую для перорального введения. В некоторых вариантах осуществления фармацевтическая композиция подходит для парентеральный введения. В некоторых вариантах осуществления фармацевтическая композиция подходит для внутривенного введения. В некоторых вариантах осуществления фармацевтическая композиция подходит для внутривенной инфузии. В некоторых вариантах осуществления фармацевтическая композиция подходит для инъекции. В некоторых вариантах осуществления фармацевтическая композиция подходит для внутривенной инъекции. В некоторых вариантах осуществления фармацевтическая композиция подходит для подкожной инъекции. В некоторых вариантах осуществления данные композиции необязательно дополнительно содержат одно или более дополнительных терапевтических средств.
[0236] Ингибитор контрольных точек можно вводить любым способом, известным специалисту в данной области. В некоторых вариантах осуществления ингибитор контрольных точек вводят внутривенно (в/в). В некоторых вариантах осуществления ингибитор контрольных точек вводят подкожно (п/к). В некоторых вариантах осуществления ингибитор контрольных точек вводят перорально. Например, в некоторых вариантах осуществления ингибитор контрольных точек можно вводить в форме второй композиции, фармацевтической композиции ингибитора контрольных точек и фармацевтически приемлемого носителя, таких как описаны в данном документе. В некоторых аспектах фармацевтическая композиция подходит для перорального введения. В некоторых вариантах осуществления фармацевтическая композиция представляет собой таблетку или капсулу, подходящую для перорального введения. В некоторых других вариантах осуществления фармацевтическая композиция представляет собой жидкую лекарственную форму, подходящую для перорального введения. В некоторых вариантах осуществления данные композиции необязательно дополнительно содержат одно или более дополнительных терапевтических средств.
[0237] В некоторых вариантах осуществления ингибитор контрольных точек можно вводить перорально, парентерально, с помощью спрея для ингаляции, местно, ректально, назально, буккально, вагинально или через имплантированный резервуар. В контексте данного документа термин «парентеральный» включает подкожную, внутривенную, внутрибрюшинную, внутримышечную, внутрисуставную, интрасиновиальную, интрастернальную, интратекальную, внутрипеченочную, внутриочаговую и внутричерепную инъекцию или инфузию. В некоторых вариантах осуществления ингибитор контрольных точек вводят перорально, внутривенно или подкожно. В некоторых вариантах осуществления ингибитор контрольных точек вводят перорально. В некоторых вариантах осуществления ингибитор контрольных точек вводят внутривенно. В некоторых вариантах осуществления внутривенное введение может представлять собой внутривенную инфузию или внутривенную инъекцию. В некоторых вариантах осуществления ингибитор контрольных точек вводят путем внутривенной инфузии. В некоторых вариантах осуществления ингибитор контрольных точек вводят путем внутривенной инъекции. В некоторых вариантах осуществления ингибитор контрольных точек вводят путем подкожной инъекции. В некоторых вариантах осуществления ингибитор контрольных точек вводят путем внутривенной инфузии, а затем вводят путем подкожной инъекции. В другом варианте осуществления ингибитор контрольных точек вводят совместно с гиалуронидазой человека подкожно. Эти способы введения могут иметь кратковременное действие, длительное действие или иметь быстрое высвобождение. Кроме того, ингибитор контрольных точек можно посредством местных, а не системных способов, например, посредством введения (например, путем инъекции) в место опухоли.
[0238] В некоторых вариантах осуществления каждое терапевтическое средство в раскрытой в данном документе комбинации (например, Соединение I-263а и ингибитор контрольных точек) можно вводить одним и тем же путем или разными путями. Например, первое терапевтическое средство комбинации можно вводить путем внутривенной инъекции, тогда как другое терапевтическое средство или средства комбинации можно вводить перорально. Альтернативно, например, все терапевтические средства можно вводить перорально или все терапевтические средства можно вводить путем внутривенной инъекции. Терапевтические средства также можно вводить поочередно.
[0239] В некоторых вариантах осуществления ингибитор контрольных точек также можно вводить с помощью назального аэрозоля или ингаляции. Ингибитор контрольных точек может быть получен в соответствии с методиками, хорошо известными в данной области, и может быть получен в виде в виде растворов в физиологическом растворе с использованием бензилового спирта или других подходящих консервантов, промоторов абсорбции для повышения биодоступности, фторуглеродов и/или других принятых солюбилизирующих или диспергирующих агентов.
[0240] Количества или подходящие дозы способов по данному раскрытию зависят от ряда факторов, включая природу тяжести состояния, подлежащего лечению, конкретный ингибитор, способ введения и возраст, массу тела, общее состояние здоровья и ответ отдельного пациента. В некоторых вариантах осуществления подходящий уровень дозы представляет собой такой уровень, при котором достигается терапевтический ответ, измеренный по регрессии опухоли или другим стандартным показателям прогрессирования заболевания, выживаемости без прогрессирования или общей выживаемости. В некоторых вариантах осуществления подходящим уровнем дозы является такой уровень, при котором достигается этот терапевтический ответ, а также сводятся к минимуму любые побочные эффекты, ассоциированные с введением терапевтического средства. Подходящие уровни доз могут быть такими, которые продлевают терапевтический ответ и/или продлевают жизнь.
[0241] Следует понимать, что подходящая доза ингибитора SAE, ингибитора контрольных точек и, необязательно, одного или более дополнительных терапевтических средств может быть принята в любое время дня или ночи. В некоторых вариантах осуществления подходящую дозу каждого средства принимают утром. В некоторых других вариантах осуществления подходящую дозу каждого средства принимают вечером. В некоторых вариантах осуществления подходящую дозу каждого из средств принимают как утром, так и вечером. Следует понимать, что подходящую дозу каждого средства можно принимать независимо от приема пищи. В некоторых вариантах осуществления подходящую дозу средства принимают во время приема пищи. В некоторых вариантах осуществления подходящую дозу средства принимают натощак.
[0242] В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят ежедневно. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят один раз в два дня. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят один раз в три дня. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят по схеме два раза в неделю. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят по схеме три раза в неделю. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят еженедельно. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят по схеме один раз в две недели.
[0243] В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят по меньшей мере 3 раза в разные дни в рамках 7-дневного цикла. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят в день 1 и день 4 7-дневного цикла. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят в последовательные дни 7-дневного цикла с последующим перерывом. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят в течение 2 дней подряд с перерывом в 5 дней подряд в рамках по меньшей мере одного 7-дневного цикла. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят в течение 3 дней подряд с перерывом в 4 дней подряд в рамках по меньшей мере одного 7-дневного цикла. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят в течение 4 дней подряд с перерывом в 3 дней подряд в рамках по меньшей мере одного 7-дневного цикла. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят в течение 5 дней подряд с перерывом в 2 дней подряд в рамках по меньшей мере одного 7-дневного цикла. В некоторых вариантах осуществления между одним или более 7-дневными циклами лечения будут периоды с перерывом. В некоторых вариантах осуществления между одним или более 7-дневными циклами лечения будет 7-дневный перерыв.
[0244] В данном раскрытии предполагается введение ингибитора SAE в течение одного или более циклов лечения, например 1, 2, 3, 4, 5, 6 или более циклов лечения. В некоторых вариантах осуществления цикл лечения составляет от около 7 дней до около 56 дней или более. В некоторых вариантах осуществления цикл лечения составляет 7 дней, 14 дней, 21 день, 28 дней, 35 дней, 42 дня, 49 дней или 56 дней. В некоторых вариантах осуществления цикл лечения составляет 21 день или 28 дней. В некоторых вариантах осуществления будут периоды перерыва в рамках одного или более циклов лечения или между ними. Например, в некоторых вариантах осуществления в конце цикла лечения будет период перерыва. В некоторых вариантах осуществления между вторым и третьим циклами лечения будет период перерыва, но не между первым и вторым циклами лечения. В другом варианте осуществления может быть период перерыва между первым и вторым циклами лечения, но не между вторым и третьим циклами лечения. Схемы введения включают, например, введение ингибитора SAE один раз за схему лечения, например, в день 1 21-дневного цикла, дважды во время цикла лечения, например, в дни 1 и 15 в рамках 21-дневного цикла или в дни 1 и 15 в рамках 28-дневного цикла, три раза в течение цикла лечения, например, в дни 1, 8 и 15 в рамках 21-дневного цикла или в дни 1, 8 и 15 в рамках 28-дневного цикла, и четыре раза в течение цикла лечения, например, в дни 1, 4, 8 и 11 в рамках 21-дневного цикла или в дни 1, 4, 8 и 11 в рамках 28-дневного цикла. Другие схемы введения входят в объем данного изобретения.
[0245] В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят в день в рамках 21-дневного цикла. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят по меньшей мере два раза в рамках 21-дневного цикла. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят по меньшей мере четыре раза в рамках 21-дневного цикла. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят в день 1 в рамках 21-дневного цикла. В некоторых вариантах осуществления соединение I-263а или его фармацевтически приемлемую соль вводят в день 4 в рамках 21-дневного цикла. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят в день 8 в рамках 21-дневного цикла. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят в день 11 в рамках 21-дневного цикла. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят в дни 1, 4, 8 и 11 в рамках 21-дневного цикла.
[0246] В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят на протяжении 1 года или менее. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят в течение 1 года или более. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят в течение 24 месяцев или менее. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят в течение 24 месяцев или более.
[0247] В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят один раз в неделю. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят один раз в неделю в течение двух недель. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят один раз в неделю в течение двух недель в рамках 21-дневного цикла.
[0248] В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет от около 0,5 мг до около 200 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет от около 0,5 мг до около 100 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет от около 0,5 мг до около 50 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет от около 0,5 мг до около 10 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет от около 0,5 мг до около 5 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет от около 1 мг до около 3 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет от около 2 мг до около 5 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет от около 5 мг до около 10 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет от около 5 мг до около 15 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет от около 10 мг до около 20 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет от около 15 мг до около 25 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет от около 20 мг до около 30 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет от около 25 мг до около 35 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет от около 30 мг до около 40 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет от около 35 мг до около 45 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет от около 40 мг до около 50 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет от около 55 мг до около 65 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет от около 50 мг до около 100 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет от около 90 мг до около 150 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет от около 140 мг до около 200 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет около 0,5 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет около 1 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет около 2 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет около 3 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет около 4 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет около 6 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет около 8 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет около 10 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет около 12 мг. Все вводимые количества относятся к количеству введенного соединения I-263а и не включают массовое количество какой-либо фармацевтически приемлемой соли.
[0249] В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет около 1 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет около 3 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет около 6 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет около 10 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет около 15 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет около 25 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет около 40 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет около 60 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет около 90 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет около 120 мг. В некоторых вариантах осуществления количество соединения I-263а или его фармацевтически приемлемой соли, вводимое в каждый день дозирования, составляет около 160 мг.
[0250] В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят посредством внутривенной (в/в) инфузии. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят посредством в/в инфузии в течение 60±10 минут. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят посредством в/в инфузии в течение 300 минут или менее. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят посредством в/в инфузии в течение от 60 до 300 минут.
[0251] В некоторых вариантах осуществления ингибитор контрольных точек вводят ежедневно. В некоторых вариантах осуществления ингибитор контрольных точек вводят через день. В некоторых вариантах осуществления ингибитор контрольных точек вводят один раз в три дня. В некоторых вариантах осуществления ингибитор контрольных точек вводят по схеме два раза в неделю. В некоторых вариантах осуществления ингибитор контрольных точек вводят по схеме три раза в неделю. В некоторых вариантах осуществления ингибитор контрольных точек вводят еженедельно. В некоторых вариантах осуществления ингибитор контрольных точек вводят по схеме один раз в две недели. В некоторых вариантах осуществления ингибитор контрольных точек вводят по схеме один раз в три недели. В некоторых вариантах осуществления ингибитор контрольных точек вводят по схеме один раз в четыре недели. В некоторых вариантах осуществления ингибитор контрольных точек вводят по схеме один раз в восемь недель. В некоторых вариантах осуществления ингибитор контрольных точек вводят по схеме один раз в двенадцать недель.
[0252] В некоторых вариантах осуществления ингибитор контрольных точек вводят по меньшей мере 3 раза через день в рамках 7-дневного цикла. В некоторых вариантах осуществления ингибитор контрольных точек вводят в день 1 цикла лечения. В некоторых вариантах осуществления ингибитор контрольных точек вводят в день 1 и день 4 7-дневного цикла. В некоторых вариантах осуществления ингибитор контрольных точек вводят в последовательные дни 7-дневного цикла с последующим перерывом. В некоторых вариантах осуществления ингибитор контрольных точек вводят в течение 2 дней подряд с последующим перерывом в 5 дней подряд в течение по меньшей мере одного 7-дневного цикла. В некоторых вариантах осуществления ингибитор контрольных точек вводят в течение 3 дней подряд с последующим перерывом в 4 дней подряд в течение по меньшей мере одного 7-дневного цикла. В некоторых вариантах осуществления ингибитор контрольных точек вводят в течение 4 дней подряд с последующим перерывом в 3 дней подряд в течение по меньшей мере одного 7-дневного цикла. В некоторых вариантах осуществления ингибитор контрольных точек вводят в течение 5 дней подряд с последующим перерывом в 2 дней подряд в течение по меньшей мере одного 7-дневного цикла.
[0253] В данном раскрытии предполагается введение ингибитора контрольных точек в течение одного или более циклов лечения, например 1, 2, 3, 4, 5, 6 или более циклов лечения. В некоторых вариантах осуществления цикл лечения составляет от около 7 дней до около 84 дней или более. В некоторых вариантах осуществления цикл лечения составляет 7 дней, 14 дней, 21 день, 28 дней, 35 дней, 42 дня, 49 дней, 56 дней или 84 дня. В некоторых вариантах осуществления цикл лечения составляет 21 день или 28 дней. В некоторых вариантах осуществления будут периоды перерыва в рамках одного или более циклов лечения или между ними. Например, в некоторых вариантах осуществления в конце цикла лечения будет период перерыва. В некоторых вариантах осуществления между вторым и третьим циклами лечения будет период перерыва, но не между первым и вторым циклами лечения. В другом варианте осуществления может быть период перерыва между первым и вторым циклами лечения, но не между вторым и третьим циклами лечения. Схемы введения включают, например, введение ингибитора контрольных точек один раз за схему лечения, например, в день 1 21-дневного цикла, дважды во время цикла лечения, например, в дни 1 и 15 в рамках 21-дневного цикла или в дни 1 и 15 в рамках 28-дневного цикла, три раза в течение цикла лечения, например, в дни 1, 8 и 15 в рамках 21-дневного цикла или в дни 1, 8 и 15 в рамках 28-дневного цикла, и четыре раза в течение цикла лечения, например, в дни 1, 4, 8 и 11 в рамках 21-дневного цикла или в дни 1, 4, 8 и 11 в рамках 28-дневного цикла. Другие схемы введения входят в объем данного изобретения.
[0254] В некоторых вариантах осуществления ингибитор контрольных точек вводят путем внутривенной (в/в) инфузии. В некоторых вариантах осуществления ингибитор контрольных точек вводят путем в/в инфузии в течение 30±10 минут.
[0255] В некоторых вариантах осуществления ингибитор контрольных точек вводят в рамках 21-дневного цикла. В некоторых вариантах осуществления ингибитор контрольных точек вводят в день 1 в рамках 21-дневного цикла.
[0256] В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят в тот же день, что и ингибитор контрольных точек. В некоторых вариантах осуществления Соединение I-263а или его фармацевтически приемлемую соль вводят перед ингибитором контрольных точек, когда оба вводят в один и тот же день. В некоторых вариантах осуществления ингибитор контрольных точек вводят перед соединением I-263а или его фармацевтически приемлемой солью, когда оба вводятся в один и тот же день.
[0257] В некоторых вариантах осуществления введение дозы соединения I-263а или его фармацевтически приемлемой соли откладывается на период от 1 до 3 дней в рамках 21-дневного цикла. В некоторых вариантах осуществления введение дозы ингибитора контрольных точек откладывается на период от 1 до 3 дней в рамках 21-дневного цикла. В некоторых вариантах осуществления введение дозы как соединения I-263а или его фармацевтически приемлемой соли, так и ингибитора контрольных точек откладывается на период от 1 до 3 дней в рамках 21-дневного цикла.
[0258] В некоторых вариантах осуществления ингибитор контрольных точек вводят путем подкожной инъекции. В некоторых вариантах осуществления ингибитор контрольных точек вводят путем внутривенной инфузии с последующими одной или более подкожными инъекциями. В некоторых вариантах осуществления внутривенная инфузия и одна или более последующих подкожных инъекций вводятся в соответствии со схемами введения и способами, раскрытыми в данном документе.
[0259] В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 0,5 мг до около 1000 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 0,5 мг до около 900 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 0,5 мг до около 800 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 0,5 мг до около 700 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 0,5 мг до около 600 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 0,5 мг до около 500 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 1 мг до около 500 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 10 мг до около 500 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 50 мг до около 500 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 100 мг до около 500 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 150 мг до около 500 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 200 мг до около 500 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 220 мг до около 500 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 240 мг до около 500 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 260 мг до около 500 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 280 мг до около 500 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 300 мг до около 500 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 320 мг до около 500 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 340 мг до около 500 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 360 мг до около 500 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 380 мг до около 500 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 400 мг до около 500 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 200 мг до около 480 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 200 мг до около 460 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 200 мг до около 440 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 200 мг до около 420 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 200 мг до около 400 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 200 мг до около 380 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 200 мг до около 360 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 200 мг до около 340 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 200 мг до около 320 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 200 мг до около 300 мг.
[0260] В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 100 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 120 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 140 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 160 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 180 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 200 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 220 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 240 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 260 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 280 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 300 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 320 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 340 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 360 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 380 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 400 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 420 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 440 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 460 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 480 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 500 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 600 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 700 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 800 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 900 мг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 1000 мг.
[0261] В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 0,5 мг/кг до около 10 мг/кг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 0,5 мг/кг до около 7,5 мг/кг. В некоторых вариантах осуществления количество антитела к PD-1, вводимого в каждый день дозирования, составляет от около 0,5 мг/кг до около 5 мг/кг. В некоторых вариантах осуществления количество антитела к PD-1, вводимого в каждый день дозирования, составляет от около 1 мг/кг до около 4 мг/кг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет от около 1 мг/кг до около 3 мг/кг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 0,5 мг/кг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 1 мг/кг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 1,5 мг/кг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 2 мг/кг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 2,5 мг/кг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 3 мг/кг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 3,5 мг/кг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 4 мг/кг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 4,5 мг/кг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 5 мг/кг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 7,5 мг/кг. В некоторых вариантах осуществления количество антитела к PD-1, вводимое в каждый день дозирования, составляет около 10 мг/кг.
[0262] В некоторых вариантах осуществления антитело к PD-1 представляет собой ниволумаб или его фармацевтически приемлемую соль. В некоторых вариантах осуществления антитело к PD-1 представляет собой пембролизумаб или его фармацевтически приемлемую соль. В некоторых вариантах осуществления антитело к PD-1 представляет собой цемиплимаб или его фармацевтически приемлемую соль.
[0263] В некоторых вариантах осуществления введение ниволумаба, пембролизумаба и цемиплимаба осуществляется в соответствии с инструкциями по применению, утвержденными органами здравоохранения, например, выпущенными FDA или ЕМА, которые полностью включены в данный документ.
[0264] В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 0,5 мг до около 2000 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 0,5 мг до около 1800 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 0,5 мг до около 1600 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 0,5 мг до около 1400 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 0,5 мг до около 1200 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 0,5 мг до около 1000 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 1 мг до около 2000 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 10 мг до около 2000 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 100 мг до около 2000 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 200 мг до около 2000 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 400 мг до около 2000 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 600 мг до около 2000 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 800 мг до около 2000 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 1000 мг до около 2000 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 1200 мг до около 2000 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 1500 мг до около 2000 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 1000 мг до около 2000 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 1000 мг до около 1800 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 1000 мг до около 1600 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 1000 мг до около 1400 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 1000 мг до около 1200 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 1200 мг до около 1400 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 1100 мг до около 1300 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 1100 мг до около 1200 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 1200 мг до около 1300 мг.
[0265] В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 100 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 200 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 300 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 400 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 500 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 600 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 700 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 800 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 900 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 1000 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 1100 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 1200 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 1300 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 1400 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 1500 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 1600 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 1700 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 1800 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 1900 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 2000 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 2500 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 3000 мг.
[0266] В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 0,5 мг/кг до около 20 мг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимого в каждый день дозирования, составляет от около 1 мг/кг до около 20 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимого в каждый день дозирования, составляет от около 5 мг/кг до около 20 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 5 мг/кг до около 15 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 5 мг/кг до около 10 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 6 мг/кг до около 10 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 7 мг/кг до около 10 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 8 мг/кг до около 10 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 9 мг/кг до около 10 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 10 мг/кг до около 15 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 10 мг/кг до около 14 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 10 мг/кг до около 13 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 10 мг/кг до около 12 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет от около 10 мг/кг до около 11 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 1 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 2 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 3 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 4 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 5 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 6 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 7 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 8 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 9 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 10 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 11 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 12 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 13 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 14 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 15 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 16 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 17 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 18 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 19 мг/кг. В некоторых вариантах осуществления количество антитела к PD-L1, вводимое в каждый день дозирования, составляет около 20 мг/кг.
[0267] В некоторых вариантах осуществления антитело к PD-L1 представляет собой атезолизумаб или его фармацевтически приемлемую соль. В некоторых вариантах осуществления антитело к PD-L1 представляет собой дурвалумаб или его фармацевтически приемлемую соль. В некоторых вариантах осуществления антитело к PD-L1 представляет собой авелумаб или его фармацевтически приемлемую соль.
[0268] В некоторых вариантах осуществления введение атезолизумаба, дурвалумаба и авелумаба осуществляется в соответствии с инструкциями по применению, утвержденными органами здравоохранения, например, выпущенными FDA или ЕМА, которые полностью включены в данный документ.
[0269] В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет от около 0,5 мг до около 2000 мг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет от около 1 мг до около 2000 мг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет от около 10 мг до около 2000 мг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет от около 50 мг до около 2000 мг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет от около 100 мг до около 2000 мг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 1 мг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 10 мг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 100 мг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 200 мг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 400 мг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 600 мг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 800 мг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 1000 мг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 1200 мг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 1400 мг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 1600 мг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 1800 мг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 2000 мг.
[0270] В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет от около 0,5 мг/кг до около 20 мг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимого в каждый день дозирования, составляет от около 1 мг/кг до около 20 мг/кг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимого в каждый день дозирования, составляет от около 1 мг/кг до около 18 мг/кг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимого в каждый день дозирования, составляет от около 1 мг/кг до около 16 мг/кг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет от около 1 мг/кг до около 14 мг/кг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимого в каждый день дозирования, составляет от около 1 мг/кг до около 12 мг/кг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимого в каждый день дозирования, составляет от около 1 мг/кг до около 10 мг/кг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 1 мг/кг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 2 мг/кг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 3 мг/кг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 4 мг/кг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 5 мг/кг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 6 мг/кг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 7 мг/кг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 8 мг/кг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 9 мг/кг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 10 мг/кг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 11 мг/кг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 12 мг/кг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 13 мг/кг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 14 мг/кг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 15 мг/кг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 16 мг/кг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 17 мг/кг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 18 мг/кг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 19 мг/кг. В некоторых вариантах осуществления количество антитела к CTLA-4, вводимое в каждый день дозирования, составляет около 20 мг/кг.
[0271] В некоторых вариантах осуществления антитело к CTLA-4 представляет собой ипилимумаб или его фармацевтически приемлемую соль.
[0272] В некоторых вариантах осуществления введение ипилимумаба осуществляется в соответствии с инструкциями по применению, утвержденными органами здравоохранения выпущенными FDA или ЕМА, которые полностью включены в данный документ.
Фармацевтические композиции
[0273] Ингибиторы SAE и ингибиторы контрольных точек, используемые в описанных в данном документе способах и наборах, могут быть составлены в виде фармацевтических композиций, подходящих для введения. Фармацевтические композиции могут содержать фармацевтически приемлемые вспомогательные вещества. Фармацевтически приемлемый вспомогательные вещества, используемые в данном документе, включают, но не ограничиваются ими, любые и все растворители, дисперсионные среды или другие жидкие носители, дисперсионные или суспензионные добавки, разбавители, гранулирующие и/или диспергирующие вещества, поверхностно-активные вещества, изотонические вещества, загустители или эмульгирующие вещества, консерванты, связующие вещества, смазывающие вещества или масла, красители, подсластители или ароматизаторы, стабилизаторы, антиоксиданты, противомикробные или противогрибковые вещества, вещества, регулирующие осмоляльность, вещества, регулирующие рН, буферы, хелатирующие вещества, криопротекторы и/или объемообразующие вещества, которые подходят для конкретной желаемой лекарственной формы. В данной области известны различные вспомогательные вещества для составления фармацевтических композиций и методы получения композиции (см. публикацию Remington: The Science and Practice of Pharmacy, 21st Ed., A.R. Gennaro (Lippincott, Williams & Wilkins, Baltimore, MD), 2006; которая полностью включена в данный документ посредством ссылки).
[0274] Любое из терапевтических средств, описанных в данном документе, может быть в форме фармацевтически приемлемой соли. В некоторых вариантах осуществления такие соли получены из неорганических или органических кислот или оснований. Обзор подходящих солей см., например, в публикации Berge et al., J. Pharm. Sci., 1977, 66, 1-19 and Remington: The Science and Practice of Pharmacy, 20th Ed., A. Gennaro (ed.), Lippincott Williams & Wilkins (2000).
[0275] Примеры подходящих солей присоединения кислоты включают ацетат, адипат, альгинат, аспартат, бензоат, бензолсульфонат, бисульфат, бутират, цитрат, камфорат, камфорсульфонат, циклопентанепропионат, диглюконат, додецилсульфат, этансульфонат, фумарат, люкогептаноат, глицерофосфат, гемисульфат, гептаноат, гексаноат, гидрохлорид, гидробромид, гидроиодид, 2-гидроксиэтансульфонат, лактат, малеат, метансульфонат, 2-нафталинсульфонат, никотинат, оксалат, памоат, пектинат, персульфат, 3-фенил-пропионат, пикрат, пивалат, пропионат, сукцинат, тартрат, тиоцианат, тозилат и ундеканоат.
[0276] Примеры подходящих солей присоединения основания включают соли аммония; соли щелочных металлов, такие как соли натрия и калия; соли щелочноземельных металлов, такие как соли кальция и магния; соли с органическими основаниями, такие как соли дициклогексиламина, N-метил-D-глюкамин; и соли с аминокислотами, такими как аргинин, лизин и т.п.
[0277] Например, Berge перечисляет следующие одобренные FDA коммерчески продаваемые соли: анионы ацетат, безилат (бензолсульфонат), бензоат, бикарбонат, битартрат, бромид, эдетат кальция (этилендиаминтетраацетат), камсилат (камфорсульфонат), карбонат, хлорид, цитрат, дигидрохлорид, эдетат (этилендиаминтетраацетат), эдизилат (1,2-этандисульфонат), эстолат (лаурилсульфат), эзилат (этансульфонат), фумарат, глюцептат (глюкогептонат), глюконат, глутамат, гликоллиларсанилат (гликолламидофениларсонат), гексилрезорцинат, гидрабамин (N,N'-ди(дегидроабиетил)этилендиамин), гидробромид, гидрохлорид, гидроксинафтоат, иодид, изетионат (2-гидроксиэтансульфонат), лактат, лактобионат, малат, малеат, манделат, мезилат (метансульфонат), метилбромид, метилнитрат, метилсульфат, мукат, напсилат (2-нафталинсульфонат), нитрат, памоат (эмбонат), пантотенат, фосфат/дифосфат, полигалактуронат, салицилат, стеарат, субацетат, сукцинат, сульфат, таннат, тартрат, теоклат (8-хлортеофиллинат) и триэтиодид; органические катионы бензатин (N,N'-дибензилэтилендиамин), хлорпрокаин, холин, диэтаноламин, этилендиамин, меглюмин (N-метилглюкамин) и прокаин; и металлические катионы алюминия, кальция, лития, магния, калия, натрия и цинка.
[0278] Berge дополнительно перечисляет следующие не одобренные FDA коммерчески продаваемые (за пределами США) соли: анионы адипат, альгинат, аминосалицилат, ангидрометиленцитрат, ареколин, аспартат, бисульфат, бутилбромид, камфорат, диглюконат, дигидробромид, дисукцинат, глицерофосфат, гемисульфат, гидрофторид, гидроиодид, метиленбис(салицилат), нападисилат (1,5-нафталиндисульфонат), оксалат, пектинат, персульфат, фенилэтилбарбитурат, пикрат, пропионат, тиоцианат, тозилат и ундеканоат; органические катионы бенетамин (N-бензилфенэтиламин), клемизол (1-n-хлорбензил-2-пирролилдин-1'-илметилбензимидазол), диэтиламин, пиперазин и трометамин (трис(гидроксиметил)аминометан); и металлические катионы бария и висмута.
[0279] Фармацевтические композиции могут содержать фармацевтически приемлемые носители. В контексте данного документа термин «фармацевтически приемлемый носитель» относится к материалу, который совместим с субъектом-реципиентом (человеком) и подходит для доставки действующего вещества в целевой сайт без прекращения действия вещества. Токсичность или побочные эффекты, если таковые имеются, связанные с носителем, предпочтительно соизмеримы с разумным соотношением риск/польза для предполагаемого использования действующего вещества.
[0280] Фармацевтически приемлемые носители, которые можно использовать в данных композициях, включают ионообменники, оксид алюминия, стеарат алюминия, лецитин, сывороточные белки, такие как сывороточный альбумин человека, буферные вещества, такие как фосфаты или карбонаты, глицин, сорбиновая кислота, сорбат калия, частичные глицеридные смеси насыщенных растительных жирных кислот, вода, соли или электролиты, такие как протаминсульфат, динатрийгидрофосфат, гидрофосфат калия, хлорид натрия, соли цинка, коллоидный кремнезем, трисиликат магния, поливинилпирролидон, вещества на основе целлюлозы, полиэтиленгликоль, натрийкарбоксиметилцеллюлоза, полиакрилаты, воски, полиэтилен-полиоксипропиленовые блок-полимеры, полиэтиленгликоль и ланолин.
[0281] Фармацевтические композиции для применения в способах по данному раскрытия могут быть получены способами, хорошо известными в данной области, такими как, среди прочего, обычные процессы гранулирования, смешивания, растворения, инкапсулирования, лиофилизации или эмульгирования. Композиции могут быть получены в различных формах, включая гранулы, преципитаты или частицы, порошки, включая лиофилизированные порошки, порошки, полученные с помощью ротоционной или распылительной сушки, аморфные порошки, таблетки, капсулы, сироп, суппозитории, инъекции, эмульсии, эликсиры, суспензии или растворы. Составы могут содержать стабилизаторы, модификаторы рН, поверхностно-активные вещества, солюбилизирующие вещества, модификаторы биодоступности и их комбинации. Эти фармацевтические композиции составлены для фармацевтического введения человеку. Такие композиции можно вводить перорально, парентерально, с помощью спрея для ингаляции, местно, ректально, назально, буккально, вагинально или через имплантированный резервуар. В контексте данного документа термин «парентеральный» включает подкожную, внутривенную, внутрибрюшинную, внутримышечную, внутрисуставную, интрасиновиальную, интрастернальную, интратекальную, внутрипеченочную, внутриочаговую и внутричерепную инъекцию или инфузию. В некоторых вариантах осуществления композиции вводят перорально, внутривенно или подкожно. В некоторых вариантах осуществления композиции вводят перорально. В некоторых вариантах осуществления композиции вводят внутривенно. В некоторых вариантах осуществления внутривенное введение может представлять собой внутривенную инфузию или внутривенную инъекцию. В некоторых вариантах осуществления композиции вводят посредством внутривенной инфузии. В некоторых вариантах осуществления композиции вводят посредством внутривенной инъекции. В некоторых вариантах осуществления композиции вводят посредством подкожной инъекции. В некоторых вариантах осуществления композиции вводят путем внутривенной инфузии, а затем вводят путем подкожной инъекции. В другом варианте осуществления ингибитор контрольных точек вводят совместно с гиалуронидазой человека подкожно. Эти составы могут иметь кратковременное действие, длительное действие или иметь быстрое высвобождение. Кроме того, композиции можно вводить посредством местных, а не системных способов, например, посредством введения (например, путем инъекции) в место опухоли.
[0282] Фармацевтические составы могут быть получены в виде жидких суспензий или растворов с применением жидкости, такой как масло, вода, спирт и их комбинаций. Могут быть включены солюбилизирующие вещества, такие как циклодекстрины. Фармацевтически подходящие поверхностно-активные вещества, суспендирующие вещества или эмульгирующие вещества могут быть добавлены для перорального или парентерального введения. Суспензии могут включать в себя масла, такие как арахисовое масло, кунжутное масло, хлопковое масло, кукурузное масло и оливковое масло. Суспензионные препараты могут содержать также сложные эфиры жирных кислот, такие как этилолеат, изопропилмиристат, глицериды жирных кислот и глицериды ацетилированных жирных кислот. Суспензионные составы могут включать спирты, такие как этанол, изопропиловый спирт, гексадециловый спирт, глицерин и пропиленгликоль; простые эфиры, такие как поли(этиленгликоль); углеводороды нефти, такие как минеральное масло и вазелин; и воду.
[0283] Стерильные формы этих фармацевтических композиций для инъекций могут представлять собой водные или масляные суспензии. Эти суспензии могут быть составлены согласно методикам, известным в данной области техники, с использованием подходящих диспергирующих или смачивающих веществ и суспендирующих веществ. Стерильный препарат для инъекций может находиться в виде стерильного раствора для инъекций или суспензии в нетоксичном парентерально-приемлемом разбавителе или растворителе, например, в виде раствора в 1,3-бутандиоле. К приемлемым носителям и растворителям, которые можно использовать, относятся вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, стерильные нелетучие масла обычно используются в качестве растворителя или суспендирующей среды. Для данной цели можно использовать любое нелетучее масло со слабовыраженным вкусом, включая синтетические моно- или диглицериды. Жирные кислоты, такие как олеиновая кислота и ее глицеридные производные подходят при приготовлении инъекционных растворов, также как и натуральные фармацевтически приемлемые масла, такие как оливковое масло или касторовое масло, особенно в форме их полиоксиэтилированных производных. Эти масляные растворы или суспензии могут также содержать разбавитель или диспергирующее средство на основе длинноцепочечного спирта, такие как карбоксиметилцеллюлоза или аналогичные диспергирующие средства, которые обычно используются в составлении фармацевтически приемлемых лекарственных форм, включая эмульсии и суспензии. Другие обычно используемые поверхностно-активные вещества, такие как алкиловые сложные эфиры сорбитана, например, Tween или Span и другие эмульгаторы или усилители биодоступности, которые обычно используются при изготовлении фармацевтически приемлемых твердых, жидких или других лекарственных форм, также могут быть использованы для целей составления. Соединения могут быть составлены для парентерального введения путем инъекции, такой как болюсная инъекция или непрерывная инфузия. Единичная лекарственная форма для инъекций может быть представлена в ампулах или в многодозных контейнерах.
[0284] Такие фармацевтические композиции можно вводить перорально в любой приемлемой для перорального применения лекарственной форме, включая капсулы, таблетки, водные суспензии или растворы. Когда водные суспензии необходимы для перорального применения, активный ингредиент объединяют с эмульгирующими и суспендирующими веществами. Если желательно, могут быть добавлены определенные подслащивающие, ароматизирующие или красящие вещества. Для перорального введения в форме капсулы полезные разбавители включают лактозу и сухой кукурузный крахмал. В случае таблеток для перорального применения носители, которые обычно используются, включают лактозу и кукурузный крахмал. Также обычно добавляют смазывающие вещества, такие как стеарат магния. Покрытия можно использовать для различных целей, например, для маскировки вкуса, для воздействия на место растворения или абсорбции или для продления действия лекарственного препарата. Покрытия можно наносить на таблетку или гранулированные частицы для применения в капсуле.
[0285] Альтернативно, эти фармацевтические композиции можно вводить в виде суппозиториев для ректального введения. Они могут быть получены путем смешивания данного вещества с подходящим не раздражающим вспомагательным веществом, который является твердым при комнатной температуре, но жидким при ректальной температуре и, следовательно, расплавится в прямой кишке, чтобы высвободить лекарственное средство. К таким материалам относятся масло какао, пчелиный воск и полиэтиленгликоли.
[0286] Данные фармацевтические композиции также могут вводиться местно, особенно когда мишень лечения включает области или органы, легко доступные посредством местного применения, включая заболевания глаз, кожи или нижнего отдела кишечного тракта. Подходящие местные составы можно легко получить для каждой из этих областей или органов.
[0287] Местное применение для нижнего отдела кишечного тракта может быть осуществлено с помощью препарата ректального суппозитория (см. выше) или подходящего состава для клизмы. Также могут быть применяться трансдермальные пластыри для местного применения. Для местного применения фармацевтические композиции могут быть составлены в подходящей мази, содержащей активный компонент, суспендированный или растворенный в одном или более носителей. Носители для местного введения соединений по данному раскрытию включают минеральное масло, жидкий вазелин, белый вазелин, пропиленгликоль, полиоксиэтилен, соединение полиоксипропилена, эмульгирующий воск и воду. Альтернативно, фармацевтические композиции могут быть составлены в подходящем лосьоне или креме, содержащем активные компоненты, суспендированные или растворенные в одном или более фармацевтически приемлемых носителях. Подходящие носители включают минеральное масло, моностеарат сорбитана, полисорбат 60, воск цетиловых эфиров, цетеариловый спирт, 2-октилдодеканол, бензиловый спирт и воду.
[0288] Для офтальмологического применения фармацевтические композиции могут быть составлены в виде микронизированных суспензий в изотоническом стерильном физиологическом растворе с откорректированным рН или, предпочтительно, в виде растворов в изотоническом стерильном физиологическом растворе с откорректированным рН, либо с добавлением консерванта, такого как хлорид бензилалкония, либо без него. Альтернативно, для офтальмологического применения фармацевтические композиции могут быть составлены в виде мази, такой как вазелин.
[0289] Фармацевтические композиции также можно вводить с помощью назального аэрозоля или путем ингаляции. Такие композиции получают в соответствии с методами, хорошо известными в области получения фармацевтического состава, и могут быть получены в виде растворов в физиологическом растворе с использованием бензилового спирта или других подходящих консервантов, промоторов абсорбции для повышения био доступности, фторуглеродов и/или других принятых солюбилизирующих или диспергирующих веществ.
[0290] В некоторых вариантах осуществления соединение формулы I-263а составлено в виде раствора для внутривенной инфузии. В некоторых вариантах осуществления соединение формулы I-263а составляют в растворе с буферным веществом или веществом, модифицирующим рН, и циклодекстрином, таким как бета-цикл о декстрин. В некоторых вариантах осуществления раствор включает фосфорную кислоту и каптизол (бетадекс сульфобутиловый эфир натрия) в воде. В некоторых вариантах осуществления раствор для внутривенной инфузии содержит 10 мг/мл соединения формулы I-263а.
[0291] В некоторых вариантах осуществления соединение формулы I-263а составлено в виде лекарственного препарата, причем лекарственный препарат содержит соединение I-263а в растворе фосфорной кислоты и каптизола (бетадекс сульфобутиловый эфир натрия) в воде. В некоторых вариантах осуществления лекарственный препарат упакован в объеме 10 мл стерильного раствора соединения I-263а.
[0292] В некоторых вариантах осуществления ингибитор контрольных точек составлен в виде раствора для инъекций, содержащего 100 мг/4 мл ингибитора контрольных точек. В некоторых вариантах осуществления ингибитор контрольных точек составлен в виде порошка для раствора для инфузий, содержащего 50 мг ингибитора контрольных точек. В некоторых вариантах осуществления ингибитор контрольных точек представляет собой пембролизумаб.
[0293] В другом аспекте данное раскрытие относится к фармацевтической композиции для применения при лечении или профилактике рака у субъекта, нуждающегося в этом, содержащей Соединение I-263а или его фармацевтически приемлемую соль и ингибитор контрольных точек. В некоторых вариантах осуществления данное раскрытие относится к фармацевтической композиции для применения при лечении или профилактике рака у субъекта, нуждающегося в этом, содержащей Соединение I-263а или его фармацевтически приемлемую соль, а также ингибитор контрольных точек и один или более дополнительных терапевтических средств. В некоторых вариантах осуществления фармацевтическая композиция составленадля одновременного или последовательного введения указанного соединения I-263а или его фармацевтически приемлемой соли и указанного одного или более дополнительных терапевтических средств. В некоторых вариантах осуществления фармацевтическая композиция составленадля одновременного или последовательного введения указанного соединения I-263а или его фармацевтически приемлемой соли, указанного ингибитора контрольных точек и указанного одного или более дополнительных терапевтических средств.
Наборы
[0294] В некоторых вариантах осуществления описанный в данном документе ингибитор SAE или ингибитор контрольных точек может быть изготовлен для включения в набор. «Набор» представляет собой любое изделие (например, упаковку или контейнер), содержащее по меньшей мере один реагент или химиотерапевтическое средство. Набор для применения в описанных в данном документе способах может содержать ингибитор SAE, такой как соединение формулы I-263а или его фармацевтически приемлемая соль. В некоторых вариантах осуществления набор может дополнительно включать ингибитор контрольных точек и, необязательно, один или более дополнительных терапевтических средств. В некоторых вариантах осуществления набор может включать соединение формулы I-263а или его фармацевтически приемлемую соль, ингибитор контрольных точек и, необязательно, один или более дополнительных терапевтических средств. В некоторых вариантах осуществления набор может включать один или более ингибиторов SAE или их фармацевтически приемлемых солей. В некоторых вариантах осуществления набор может включать один или более ингибиторов контрольных точек.
[0295] В некоторых вариантах осуществления данное раскрытие относится к набору, содержащему лекарственное средство для применения при лечении рака у пациента, нуждающегося в таком лечении. Набор содержит лекарственное средство, содержащее ингибитор SAE, и инструкцию по введению ингибитора SAE и ингибитора контрольных точек; или набор содержит лекарственное средство, содержащее ингибитор контрольных точек, и инструкцию по введению ингибитора контрольных точек и ингибитора SAE. Набор может содержать лекарственное средство, содержащее ингибитор SAE и ингибитор контрольных точек, а также инструкцию по введению ингибитора SAE и ингибитора контрольных точек, причем лекарственное средство находится в одной лекарственной форме или в отдельных лекарственных формах. В некоторых вариантах осуществления набор необязательно содержит один или более дополнительных терапевтических средств.
[0296] В некоторых вариантах осуществления набор, содержащий ингибитор SAE и ингибитор контрольных точек, может дополнительно включать другой компонент или реагент.В некоторых вариантах осуществления реагент в наборе может представлять собой разбавитель для подготовки ингибитора SAE для введения. В некоторых вариантах осуществления реагент в наборе может представлять собой разбавитель для подготовки ингибитора контрольной точки для введения. В некоторых вариантах осуществления компонент в наборе может представлять собой сосуд для смешивания комбинации ингибитора SAE и ингибитора контрольных точек.
[0297] В другом аспекте данное раскрытие относится к набору для лечения рака, содержащему по меньшей мере одно лекарственное средство, содержащее по меньшей мере одну дозу соединения I-263а или его фармацевтически приемлемой соли, и по меньшей мере одно лекарственное средство, содержащее по меньшей мере одну дозу ингибитора контрольных точек, причем указанный набор для лечения рака дополнительно содержит инструкции по дозированию для введения лекарственных средств для лечения пациента, признанного нуждающимся в них.
[0298] Следующие примеры приведены для лучшего понимания данного раскрытия. Эти примеры являются только иллюстративными и никоим образом не предназначены для ограничения объема данного раскрытия.
ПРИМЕРЫ
[0299] Сокращения
[0300] Пример 1: Противоопухолевая эффективность in vivo
[0301] Общие аналитические методы
[0302] Если не указано иное, спектры ЯМР 1H получали с использованием прибора Varian 300 МГц. Если не указано иное, ВЭЖХ получали с использование прибора Agilent серии 1100, а СЭЖХ получали с использование прибора Water Acuity Systems.
[0303] Соединение I-263а, используемое в приведенных ниже примерах, можно синтезировать в соответствии с процедурами, изложенными в примере 201 в публикации РСТ № WO 2016/004136.
[0304] Общие экспериментальные условия противоопухолевой эффективности на мышиных опухолевых моделях
[0305] Мышиные сингенные опухолевые модели
[0306] Следующие сингенные модели использовали в каждом из исследований 1-8, как указано ниже.
[0307] СТ26, исследование 1: СТ26 представляет собой мышиную клеточную линию карциномы толстой кишки из фибробластов. Мышиная сингенная опухолевая модель СТ26 была создана путем подкожной инокуляции 0,2×106 клеток СТ-26 (клеточная суспензия) 12-недельным самкам мышей линии BALB/c (Jackson Laboratory, 600 Main St, г. Бар-Харбор, штат Мэн) в бок. Когда средний объем опухоли достигал приблизительно 60 мм3, животных рандомизировали в одну контрольную группу, получавшую носитель и три группы лечения (n=8/группу). Затем мышам вводили дозу 20% HPβCD или соединения I-263а, или антимышиного антитела к PD-1 в течение 14-дневного периода. Рост опухоли и массу тела измеряли дважды в неделю во время периода лечения и периода последующего наблюдения, и мышей подвергали гуманному умерщвлению, когда они достигали своей гуманной конечной точки.
[0308] СТ26, исследование 2: СТ26 представляет собой мышиную клеточную линию карциномы толстой кишки из фибробластов. Мышиная сингенная опухолевая модель СТ26 была создана путем подкожной инокуляции 0,2×106 клеток СТ-26 (клеточная суспензия) 10-недельным самкам мышей линии BALB/c (Vital River Laboratory Animal Technology Co., Ltd., г. Пекин, Китай) в бок. Когда средний объем опухоли достигал приблизительно 40 мм3, животных рандомизировали в одну контрольную группу, получавшую носитель и три группы лечения (n=9/группу). Затем мышам вводили дозу 20% HPβCD или соединения I-263а, или антимышиного антитела к PD-1 в течение 14-дневного периода. Рост опухоли и массу тела измеряли дважды в неделю во время периода лечения и периода последующего наблюдения, и мышей подвергали гуманному умерщвлению, когда они достигали своей гуманной конечной точки.
[0309] А20, исследование 3: А20 представляет собой мышиную клеточную линию В-клеточной лимфомы. Мышиная сингенная опухолевая модель А20 была создана путем подкожной инокуляции 1,0×106 клеток А20 (клеточная суспензия) 8-недельным самкам мышей линии BALB/c (Jackson Laboratory, 600 Main St, г. Бар-Харбор, штат Мэн) в бок. Когда средний объем опухоли достигал приблизительно 50 мм3, животных рандомизировали в одну контрольную группу, получавшую носитель и три группы лечения (n=7/группу). Затем мышам вводили дозу 20% HPβCD или соединения I-263а, или антимышиного антитела к PD-1 в течение 11-дневного периода. Рост опухоли и массу тела измеряли дважды в неделю во время периода лечения и периода последующего наблюдения, и мышей подвергали гуманному умерщвлению, когда они достигали своей гуманной конечной точки.
[0310] WEHI-3, исследование 4: WEHI-3 представляет собой мышиную клеточную линию миеломоноцитарного лейкоза. Мышиная сингенная опухолевая модель WEHI-3 была создана путем подкожной инокуляции 0,1×106 клеток WEHI-3 (клеточная суспензия) 13-недельным самкам мышей линии BALB/c (Jackson Laboratory, 600 Main St, г. Бар-Харбор, штат Мэн) в бок. Когда средний объем опухоли достигал приблизительно 50 мм3, животных рандомизировали в одну контрольную группу, получавшую носитель и пять групп лечения (n=8/группу). Затем мышам вводили дозу 20% HPβCD или соединения I-263а, или антимышинного антитела к PD-1 или антимышинного антитела к CTLA-4 в течение 21-дневного периода. Рост опухоли и массу тела измеряли дважды в неделю во время периода лечения и периода последующего наблюдения, и мышей подвергали гуманному умерщвлению, когда они достигали своей гуманной конечной точки.
[0311] WEHI-3, исследование 5: WEHI-3 представляет собой мышиную клеточную линию миеломоноцитарного лейкоза. Мышиная сингенная опухолевая модель WEHI-3 была создана путем подкожной инокуляции 0,1×106 клеток WEHI-3 (клеточная суспензия) 9-недельным самкам мышей линии BALB/c (SINO-British SIPPR/BK Lab Animal Ltd. г. Шанхай, Китай) в бок. Когда средний объем опухоли достигал приблизительно 30 мм3, животных рандомизировали в одну контрольную группу, получавшую носитель и пять групп лечения (n=8/группу). Затем мышам вводили дозу 20% HPβCD или соединения I-263а, или антимышинного антитела к PD-1 или антимышинного антитела к CTLA-4 в течение 21-дневного периода. Рост опухоли и массу тела измеряли дважды в неделю во время периода лечения и периода последующего наблюдения, и мышей подвергали гуманному умерщвлению, когда они достигали своей гуманной конечной точки.
[0312] JC, исследование 6: JC представляет собой мышиную клеточную линию аденокарциномы молочной железы. Мышиная сингенная опухолевая модель JC была создана путем подкожной инокуляции 0,2×106 клеток JC (клеточная суспензия) 10-недельным самкам мышей линии BALB/c (Vital River Laboratory Animal Technology Co., Ltd., г. Пекин, Китай) в бок. Когда средний объем опухоли достигал приблизительно 45 мм3, животных рандомизировали в одну контрольную группу, получавшую носитель и пять групп лечения (n=8/группу). Затем мышам вводили дозу 20% HPβCD или соединения I-263а, или антимышиного антитела к PD-1 в течение 21-дневного периода. Рост опухоли и массу тела измеряли дважды в неделю во время периода лечения и периода последующего наблюдения, и мышей подвергали гуманному умерщвлению, когда они достигали своей гуманной конечной точки.
[0313] B16-F10, исследование 7: B16-F10 представляет собой мышиную клеточную линию меланомы. Мышиная сингенная опухолевая модель B16-F10 была создана путем подкожной инокуляции 0,08×106 клеток B16-F10 (клеточная суспензия) 11-недельным самкам мышей линии C57BL/6 (Taconic Biosciences, г. Ренсселер, штат Нью-Йорк) в бок. Когда средний объем опухоли достигал приблизительно 50 мм3, животных рандомизировали в одну контрольную группу, получавшую носитель и пять групп лечения (n=8/группу). Затем мышам вводили дозу 20% HPβCD или соединения I-263а, или антимышиного антитела к PD-1 в течение 17-дневного периода. Рост опухоли и массу тела измеряли дважды в неделю во время периода лечения и периода последующего наблюдения, и мышей подвергали гуманному умерщвлению, когда они достигали своей гуманной конечной точки.
[0314] МС38, исследование 8: МС38 представляет собой мышиную клеточную линию аденокарциномы толстой кишки. Мышиная сингенная опухолевая модель МС38 была создана путем подкожной инокуляции 1,0×106 клеток МС38 (клеточная суспензия) 11-недельным самкам мышей линии C57BL/6 (SINO-British SIPPR7BK Lab Animal Ltd., г. Шанхай, Китай) в бок. Когда средний объем опухоли достигал приблизительно 60 мм3, животных рандомизировали в одну контрольную группу, получавшую носитель и пять групп лечения (n=8/группу). Затем мышам вводили дозу 20% HPβCD или соединения I-263а, или антимышиного антитела к PD-1 в течение 21-дневного периода. Рост опухоли и массу тела измеряли дважды в неделю во время периода лечения и периода последующего наблюдения, и мышей подвергали гуманному умерщвлению, когда они достигали своей гуманной конечной точки.
[0315] Исследуемые вещества
[0316] Следующие исследуемые вещества использовали в каждом из исследований 1-8, как указано ниже.
[0317] Исследование 1. Исходный раствор соединения I-263а с концентрацией 0,825 мг/мл еженедельно составляли в 20% HPβCD и вводили внутривенно (в/в) на основе точной массы тела животного в каждый день лечения с использованием вводимого объема 10 мл/кг массы тела. Общая концентрация полученных доз составляла 7,5 мг/кг. Вводимый объем соединения I-263а составлял 0,2 мл. Антимышиное антитело к PD1 (анти-mPD-1) (Bio X Cell, 10 Technology Drive, Suite 2B, Западный Ливан, NH 03784) составляли перед каждой инъекцией в концентрации 2,2 мг/мл в фосфатно-солевом буфере (ФСБ) и вводили внутрибрюшинно (в/б) на основе точной массы тела в каждый день лечения с использованием вводимого объема 5 мл/кг с получением дозы 10 мг/кг. Вводимый объем соединения анти-mPD-1 составлял 0,1 мл. Соединение I-263а вводили по схеме два раза в неделю в течение 1 недели (дни 1 и 4), а анти-mPD-1 вводили по схеме два раза в неделю в течение 2 недель (дни 1, 4, 8 и 11).
[0318] Исследование 2. Исходный раствор соединения I-263а с концентрацией 0,75 мг/мл еженедельно составляли в 20% HPβCD и вводили внутривенно (в/в) на основе точной массы тела животного в каждый день лечения с использованием вводимого объема 10 мл/кг массы тела. Общая концентрация полученных доз составляла 7,5 мг/кг. Вводимый объем соединения I-263а составлял 0,2 мл. Антимышиное антитело к PD1 (анти-mPD-1) (Bio X Cell, 10 Technology Drive, Suite 2B, Западный Ливан, NH 03784) составляли перед каждой инъекцией в концентрации 2,0 мг/мл в фосфатно-солевом буфере (ФСБ) и вводили внутрибрюшинно (в/б) на основе точной массы тела в каждый день лечения с использованием вводимого объема 5 мл/кг с получением дозы 10 мг/кг. Вводимый объем соединения анти-mPD-1 составлял 0,1 мл. Соединение I-263а вводили по схеме два раза в неделю в течение 3 недель до дня 14 (дни 0, 3, 7, 10 и 14) и анти-mPD-1 вводили по схеме два раза в неделю в течение 3 недель до дня 14 (дни 0, 3, 7, 10 и 14)
[0319] Исследование 3. Исходный раствор соединения I-263а с концентрацией 1,65 мг/мл еженедельно составляли в 20% HPβCD и вводили внутривенно (в/в) на основе точной массы тела животного в каждый день лечения с использованием вводимого объема 10 мл/кг массы тела. Общая концентрация полученных доз составляла 15 мг/кг. Вводимый объем соединения I-263а составлял 0,2 мл. Антимышиное антитело к PD1 (анти-mPD-1) (Bio X Cell, 10 Technology Drive, Suite 2B, Западный Ливан, NH 03784) составляли перед каждой инъекцией в концентрации 2,0 мг/мл в фосфатно-солевом буфере (ФСБ) и вводили внутрибрюшинно (в/б) на основе точной массы тела в каждый день лечения с использованием вводимого объема 5 мл/кг с получением дозы 10 мг/кг. Вводимый объем соединения анти-mPD-1 составлял 0,1 мл. Соединение I-263а вводили по схеме два раза в неделю в течение 1 недели (день 1), а анти-mPD-1 вводили по схеме два раза в неделю в течение 2 недель до дня 11 (дни 1, 4, 8 и 11).
[0320] Исследование 4. Исходный раствор соединения I-263а с концентрацией 1,01 мг/мл еженедельно составляли в 20% HPβCD и вводили внутривенно (в/в) на основе точной массы тела животного в каждый день лечения с использованием вводимого объема 10 мл/кг массы тела. Общая концентрация полученных доз составляла 7,5 мг/кг. Вводимый объем соединения I-263а составлял 0,2 мл. Антимышиное антитело к PD1 (анти-mPD-1) (Bio X Cell, 10 Technology Drive, Suite 2B, Западный Ливан, NH 03784) составляли перед каждой инъекцией в концентрации 2,7 мг/мл в фосфатно-солевом буфере (ФСБ) и вводили внутрибрюшинно (в/б) на основе точной массы тела в каждый день лечения с использованием вводимого объема 5 мл/кг с получением дозы 10 мг/кг. Вводимый объем соединения анти-mPD-1 составлял 0,1 мл. Антимышиное антитело к CTLA-4 (анти-mCTLA-4) (Bio X Cell, 10 Technology Drive, Suite 2B, Западный Ливан, NH 03784) составляли перед каждой инъекцией в концентрации 2,7 мг/мл в фосфатно-солевом буфере (ФСБ) и вводили внутрибрюшинно (в/б) на основе точной массы тела в каждый день лечения с использованием вводимого объема 5 мл/кг с получением дозы 10 мг/кг. Вводимый объем анти-mCTLA-4 составлял 0,1 мл. Соединение I-263а, анти-mPD-1 и анти-mCTLA-4 вводили по схеме два раза в неделю в течение 3 недель до дня 17 (дни 0, 3, 7, 10, 14 и 17).
[0321] Исследование 5. Исходный раствор соединения I-263а с концентрацией 0,75 мг/мл еженедельно составляли в 20% HPβCD и вводили внутривенно (в/в) на основе точной массы тела животного в каждый день лечения с использованием вводимого объема 10 мл/кг массы тела. Общая концентрация полученных доз составляла 7,5 мг/кг. Вводимый объем соединения I-263а составлял 0,2 мл. Антимышиное антитело к PD1 (анти-mPD-1) (Bio X Cell, 10 Technology Drive, Suite 2B, Западный Ливан, NH 03784) составляли перед каждой инъекцией в концентрации 2,0 мг/мл в фосфатно-солевом буфере (ФСБ) и вводили внутрибрюшинно (в/б) на основе точной массы тела в каждый день лечения с использованием вводимого объема 5 мл/кг с получением дозы 10 мг/кг. Вводимый объем соединения анти-mPD-1 составлял 0,1 мл. Антимышиное антитело к CTLA-4 (анти-mCTLA-4) (Bio X Cell, 10 Technology Drive, Suite 2B, Западный Ливан, NH 03784) составляли перед каждой инъекцией в концентрации 2,0 мг/мл в фосфатно-солевом буфере (ФСБ) и вводили внутрибрюшинно (в/б) на основе точной массы тела в каждый день лечения с использованием вводимого объема 5 мл/кг с получением дозы 10 мг/кг. Вводимый объем анти-mCTLA-4 составлял 0,1 мл. Соединение I-263а вводили по схеме два раза в неделю в течение 3 недель до дня 14 (дни 0, 3, 7, 10 и 14). Анти-mPD-1 вводили по схеме два раза в неделю в течение 2 недель до дня 10 (дни 0, 3, 7 и 10) в группе монотерапии, и по схеме два раза в неделю в течение 3 недель до дня 14 (дни 0, 3, 7, 10 и 14) в группе комбинированного лечения. Анти-mCTLA-4 вводили по схеме один раз в четыре дня в течение 3 циклов до дня 8 (дни 0, 4 и 8).
[0322] Исследование 6. Исходный раствор соединения I-263а с концентрацией 0,75 мг/мл еженедельно составляли в 20% HPβCD и вводили внутривенно (в/в) на основе точной массы тела животного в каждый день лечения с использованием вводимого объема 10 мл/кг массы тела. Общая концентрация полученных доз составляла 7,5 мг/кг. Вводимый объем соединения I-263а составлял 0,2 мл. Антимышиное антитело к PD1 (анти-mPD-1) (Bio X Cell, 10 Technology Drive, Suite 2B, Западный Ливан, NH 03784) составляли перед каждой инъекцией в концентрации 2,0 мг/мл в фосфатно-солевом буфере (ФСБ) и вводили внутрибрюшинно (в/б) на основе точной массы тела в каждый день лечения с использованием вводимого объема 5 мл/кг с получением дозы 10 мг/кг. Вводимый объем соединения анти-mPD-1 составлял 0,1 мл. Антимышиное антитело к CTLA-4 (анти-mCTLA-4) (Bio X Cell, 10 Technology Drive, Suite 2B, Западный Ливан, NH 03784) составляли перед каждой инъекцией в концентрации 2,0 мг/мл в фосфатно-солевом буфере (ФСБ) и вводили внутрибрюшинно (в/б) на основе точной массы тела в каждый день лечения с использованием вводимого объема 5 мл/кг с получением дозы 10 мг/кг. Вводимый объем анти-mCTLA-4 составлял 0,1 мл. Соединение I-263а вводили по схеме два раза в неделю в течение 3 недель до дня 14 (дни 0, 3, 7, 10 и 14). Анти-mPD-1 вводили по схеме два раза в неделю в течение 3 недель до дня 14 (дни 0, 3, 7, 10 и 14). Анти-mCTLA-4 вводили по схеме один раз в четыре дня в течение 3 циклов до дня 8 (дни 0, 4 и 8).
[0323] Исследование 7. Исходный раствор соединения I-263а с концентрацией 0,75 мг/мл еженедельно составляли в 20% HPβCD и вводили внутривенно (в/в) на основе точной массы тела животного в каждый день лечения с использованием вводимого объема 10 мл/кг массы тела. Общая концентрация полученных доз составляла 7,5 мг/кг. Вводимый объем соединения I-263а составлял 0,2 мл. Антимышиное антитело к PD1 (анти-mPD-1) (Bio X Cell, 10 Technology Drive, Suite 2B, Западный Ливан, NH 03784) составляли перед каждой инъекцией в концентрации 2,0 мг/мл в фосфатно-солевом буфере (ФСБ) и вводили внутрибрюшинно (в/б) на основе точной массы тела в каждый день лечения с использованием вводимого объема 5 мл/кг с получением дозы 10 мг/кг. Вводимый объем соединения анти-mPD-1 составлял 0,1 мл. Антимышиное антитело к CTLA-4 (анти-mCTLA-4) (Bio X Cell, 10 Technology Drive, Suite 2B, Западный Ливан, NH 03784) составляли перед каждой инъекцией в концентрации 2,0 мг/мл в фосфатно-солевом буфере (ФСБ) и вводили внутрибрюшинно (в/б) на основе точной массы тела в каждый день лечения с использованием вводимого объема 5 мл/кг с получением дозы 10 мг/кг. Вводимый объем анти-mCTLA-4 составлял 0,1 мл. Соединение I-263а вводили по схеме два раза в неделю в течение 3 недель до дня 17 (дни 0, 3, 7, 10, 14 и 17). Анти-mPD-1 вводили по схеме два раза в неделю в течение 3 недель до дня 17 (дни 0, 3, 7, 10, 14 и 17). Анти-mCTLA-4 вводили по схеме два раза в неделю в течение 3 недель до дня 17 (дни 0, 3, 7, 10, 14 и 17).
[0324] Исследование 8. Исходный раствор соединения I-263а с концентрацией 0,75 мг/мл еженедельно составляли в 20% HPβCD и вводили внутривенно (в/в) на основе точной массы тела животного в каждый день лечения с использованием вводимого объема 10 мл/кг массы тела. Общая концентрация полученных доз составляла 7,5 мг/кг. Вводимый объем соединения I-263а составлял 0,2 мл. Антимышиное антитело к PD1 (анти-mPD-1) (Bio X Cell, 10 Technology Drive, Suite 2B, Западный Ливан, NH 03784) составляли перед каждой инъекцией в концентрации 2,0 мг/мл в фосфатно-солевом буфере (ФСБ) и вводили внутрибрюшинно (в/б) на основе точной массы тела в каждый день лечения с использованием вводимого объема 5 мл/кг с получением дозы 10 мг/кг. Вводимый объем соединения анти-mPD-1 составлял 0,1 мл. Антимышиное антитело к CTLA-4 (анти-mCTLA-4) (Bio X Cell, 10 Technology Drive, Suite 2B, Западный Ливан, NH 03784) составляли перед каждой инъекцией в концентрации 2,0 мг/мл в фосфатно-солевом буфере (ФСБ) и вводили внутрибрюшинно (в/б) на основе точной массы тела в каждый день лечения с использованием вводимого объема 5 мл/кг с получением дозы 10 мг/кг. Вводимый объем анти-mCTLA-4 составлял 0,1 мл. Соединение I-263а вводили по схеме два раза в неделю в течение 3 недель до дня 17 (дни 0, 3, 7, 10, 14 и 17). Анти-mPD-1 вводили по схеме два раза в неделю в течение 3 недель до дня 17 (дни 0, 3, 7, 10, 14 и 17). Анти-mCTLA-4 вводили по схеме два раза в неделю в течение 3 недель до дня 17 (дни 0, 3, 7, 10, 14 и 17).
[0325] Измерения размера опухоли
[0326] Размер опухолей измеряли два раза в неделю с помощью штангенциркуля. Объемы опухоли рассчитывали с использованием стандартного уравнения: V=W2×L/2, где V=объем, W=ширина и L=длина опухоли. Когда средний объем опухоли достиг приблизительно 60 мм3 для исследования 1, 40 мм3 для исследования 2, 50 мм3 для исследования 3, 50 мм3 для исследования 4, 30 мм3 для исследования 5, 45 мм3 для исследования 6, 50 мм3 для исследования 7, 60 мм3 для исследования 8, мыши были рандомизированы на группы по 4 особи (n=8 на группу) в исследовании 1, группы по 4 особи (n=8/группа) в исследовании 2, группы по 4 особи (n=8/группа) в исследовании 3, группы по 6 особей (n=8/группа) в исследовании 4, группы по 6 особей (n=8/группа) в исследовании 5, группы по 6 особей (n=8/группа) в исследовании 6, группы по 6 особей (n=8/группа) в исследовании 7 и группы по 6 особей (n=8/группа) в исследовании 8, и им вводили носитель (20% HPβCD), Соединение I-263а, анти-mPD-1, анти-mCTLA-4 или комбинацию соединения I-263а плюс анти-mPD-1 или анти-mCTLA-4 в различных дозах и по различным схемах. Размер опухоли и массу тела измеряли два раза в неделю на протяжении всего исследования. Мышей умерщвляли, когда объем их опухоли превышал приблизительно 2500 мм3 или, когда отдельная опухоль превышала показатель гуманной конечной точки по размеру (длина опухоли превышала 2 см).
[0327] Результаты
[0328] Для оценки комбинированного действия in vivo соединения I-263а и анти-mPD-1 или анти-mCTLA-4 использовали мышиные сингенные опухолевые модели, выполненные, как описано в разделе Общие способы выше.
[0329] Индивидуальные кривые роста опухоли показаны на фигурах 1a, 1b, 1с, 2а, 2b, 2с, 3а, 3b, 3с, 4а, 4b, 4с, 4d, 4е, 5а, 5b, 5с, 5d, 5е, 6а, 6b, 6с, 6d, 6е, 7а, 7b, 7с, 7d, 7е, 8а, 8b, 8с, 8d и 8е. Каждая диаграмма показывает кривые роста для каждой опухоли, обработанной носителем, вместе с индивидуальными кривыми роста опухоли у мышей, получавших I-263а, или с ингибитором контрольных точек, или с комбинацией I-263а и ингибитором контрольных точек.
ИССЛЕДОВАНИЕ 1: МЫШИНАЯ СИНГЕННАЯ ОПУХОЛЕВАЯ МОДЕЛЬ СТ26
[0330] В подкожной мышиной сингенной опухолевой модели, полученной из карциномы толстой кишки из фибробластов СТ26, мышей инокулировали, рандомизировали в день 0 (6 дней после инокуляции), и лечение начинали в день 1 для всех групп.
[0331] Соединение I-263а тестировали в дозе 7,5 мг/кг, вводимой внутривенно по схеме 2 р/нед. (два раза в неделю) в течение одной недели (дни 1 и 4). Анти-mPD-1 тестировали в дозе 10 мг/кг, вводимой внутрибрюшинно по схеме два раза в неделю в течение двух недель (дни 1, 4, 8 и 11). В группе комбинированного лечения сначала вводили Соединение I-263а, а затем сразу же вводили анти-mPD-1. Одна группа служила группой, обрабатываемой носителем (группа 1), которая получала внутривенное лечение носителем для соединения I-263а (20% HPβCD) по схеме два раза в неделю в течение двух недель (дни 1, 4, 8 и 11).
[0332] Монотерапия соединением I-263а в дозе 7,5 мг/кг два раза в неделю (день 1 и день 4) в течение одной недели или анти-mPD-1 в дозе 10 мг/кг два раза в неделю в течение двух недель (дни 1, 4, 8 и 11) не продемонстрировала какого-либо ингибирования роста опухоли по сравнению с опухолями, обработанными носителем (фигуры 1a, b). Комбинированное лечение соединением I-263а в дозе 7,5 мг/кг два раза в неделю (день 1 и день 4) в течение одной недели и анти-mPD-1 в дозе 10 мг/кг два раза в неделю в течение двух недель (дни 1, 4, 8 и 11) приводило к выраженной противоопухолевой активности с 2 случаями полной регрессии опухоли (2 ПО), определяемыми как отсутствие какой-либо поддающейся измерению опухоли (фигура 1с), достигнутыми в дни 7 и 32 лечения и сохраняющимися до конца мониторинга в день 35. Кроме того, комбинированное лечение также привело к очень длительному стазу опухоли до дня 28. Эти результаты демонстрируют заметно улучшенное ингибирование роста опухоли в комбинации I-263а с анти-mPD-1 по сравнению с активностью любой монотерапии.
[0333] Исследование 2: Мышиная сингенная опухолевая модель СТ26
[0334] В подкожной мышиной сингенной опухолевой модели, полученной из карциномы толстой кишки из фибробластов СТ26, мышей инокулировали, рандомизировали в день 0 (4 дней после инокуляции), и лечение начинали в день 0 для всех групп.
[0335] Соединение I-263а тестировали в дозе 7,5 мг/кг, вводимой внутривенно по схеме 2 р/нед. (два раза в неделю) в течение трех недель до дня 14 (дни 0, 3, 7, 10 и 14). Анти-mPD-1 тестировали в дозе 10 мг/кг, вводимой внутрибрюшинно по схеме два раза в неделю в течение трех недель до дня 14 (дни 0, 3, 7, 10 и 14). В группе комбинированного лечения сначала вводили Соединение I-263а, а затем сразу же вводили анти-mPD-1. Одна группа, которая служила группой, обрабатываемой носителем (группа 1), получала внутривенное лечение носителем для соединения I-263а (20% HPβCD) по схеме два раза в неделю в течение трех недель до дня 14 (дни 0, 3, 7, 10 и 14).
[0336] Монотерапия соединением I-263а в дозе 7,5 мг/кг (в/в) по схеме 2 раза в неделю х 3 (до дня 14) не показала какого-либо ингибирования роста опухоли в этом исследовании по сравнению с опухолями, обработанными носителем (фигура 2а). В результате лечения с применением только анти-mPD-1 в дозе 10 мг/кг (в/б, по схеме 2 раза в неделю х 3 до дня 14) было получено два ПО, один из которых был достигнут на день 14 лечения, а другой - на день 30, без заметного ингибирования роста в оставшихся 7 опухолях (фигура 2b). В результате комбинированного лечения с применением I-263а в дозе 7,5 мг/кг (в/в, два раза в неделю х 3 до дня 14) плюс анти-mPD-1 в дозе 10 мг/кг (в/б, два раза в неделю х 3 до дня 14) был получен 1 ПО, достигнутый к дню 9, без заметного ингибирования роста в оставшихся 8 опухолях, что указывает на отсутствие пользы от комбинации соединения I-263а с анти-mPD-1 по сравнению с активностью одного средства, достигнутой с применением анти-mPD-1, в этом исследовании (фигура 2с).
[0337] Исследование 3: Мышиная сингенная опухолевая модель А20
[0338] В подкожной мышиной сингенной опухолевой модели, полученной из В-клеточной лимфомы А20, мышей инокулировали, рандомизировали в день 0 (5 дней после инокуляции), и лечение начинали в день 1 для всех групп.
[0339] Соединение I-263а тестировали в дозе 15 мг/кг, вводимой внутривенно по схеме 1 р/нед. (один раз в неделю) в течение одной недели (день 1). Анти-mPD-1 тестировали при введении дозы 10 мг/кг внутрибрюшинно по схеме два раза в неделю в течение двух недель до дня 11 (дни 1, 4, 8 и 11). В группе комбинированного лечения сначала вводили Соединение I-263а, а затем сразу же вводили анти-mPD-1. Одна группа, которая служила группой, обрабатываемой носителем (группа 1), получала внутривенное лечение носителем для соединения I-263а (20% HPβCD) по схеме два раза в неделю в течение двух недель до дня 11 (дни 1, 4, 8 и 11).
[0340] Монотерапия соединением I-263а в дозе 15 мг/кг (в/в) по схеме один раз в неделю х 1 продемонстрировала умеренное ингибирование роста подкожных опухолей, происходящих из В-клеточной лимфомы мышей А20, у самок мышей линии Balb/c, что привело к стазу 2, из 7 имплантированных опухолей на день 8 лечения с последующим быстрым ростом (фигура 3а). Лечение с применением анти-mPD-1 в дозе 10 мг/кг (в/б, два раза в неделю × 2 до дня 11) привело к задержке роста 1 опухоли в дни 8-11 и 2 опухолей в день 8 (фигура 3b). В результате комбинированного лечения с применением I-263а в дозе 15 мг/кг (в/в, два раза в неделю × 1 до дня 11) плюс анти-mPD-1 в дозе 10 мг/кг (в/б, два раза в неделю × 2 до дня 11) был получен 1 ПО с дня 4, который сохранялся до конца мониторинга, и 4 регрессии опухолей, которые возобновили рост в дни 8, 11, 18 и 18, демонстрируют улучшенное ингибирование роста опухоли в условиях комбинированного лечения по сравнению с активностью лечения одним средством (фигура 3с).
[0341] Исследование 4: Мышиная сингенная опухолевая модель WEHI-3
[0342] В подкожной мышиной сингенной опухолевой модели, полученной из миеломоноцитарного лейкоза WEHI-3, мышей инокулировали, рандомизировали в день 0 (9 дней после инокуляции), и лечение начинали в день 0 для всех групп.
[0343] Соединение I-263а тестировали в дозе 7,5 мг/кг, вводимой внутривенно по схеме 2 р/нед. (два раза в неделю) в течение трех недель (дни 0, 3, 7, 10, 14 и 17). Анти-mPD-1 тестировали в дозе 10 мг/кг, вводимой внутрибрюшинно по схеме два раза в неделю в течение трех недель (дни 0, 3, 7, 10, 14 и 17). Анти-mCTLA-4 тестировали в дозе 10 мг/кг, вводимой внутрибрюшинно по схеме два раза в неделю в течение трех недель (дни 0, 3, 7, 10, 14 и 17). В группе комбинированного лечения сначала вводили соединение I-263a, а затем сразу же вводили анти-mPD-1 или анти-mCTLA-4. Одна группа, которая служила группой, обрабатываемой носителем (группа 1), получала внутривенное лечение носителем для соединения I-263а (20% HPβCD) по схеме два раза в неделю в течение трех недель (дни 0, 3, 7, 10, 14 и 17).
[0344] Лечение соединением I-263а в дозе 7,5 мг/кг (в/в) по схеме два раза в неделю х 3 оказала очень небольшое влияние на рост подкожных опухолей, происходящих от миеломоноцитарного лейкоза мышей WEHI-3, у самок мышей линии Balb/c, что привело к 2 незначительным задержкам роста опухоли из 8 имплантированных опухолей к дню 14 (фигура 4а). Подобным образом, лечение с применением анти-mPD-1 в дозе 10 мг/кг (в/б, два раза в неделю × 3 до дня 17) привело к 1 небольшой задержке роста опухоли к дню 17 (фигура 4b). Лечение с применением анти-mCTLA-4 в дозе 10 мг/кг (в/б, два раза в неделю х 2 до дня 17) привело к 2 незначительным задержкам роста опухоли к дням 14-17 (фигура 4с). Комбинированное лечение соединением I-263а в дозе 7,5 мг/кг (в/в, два раза в неделю × 3 до дня 17) плюс анти-mPD-1 в дозе 10 мг/кг (в/б, два раза в неделю × 2 до дня 17) привело к 2 ПО, один был достигнут в день 6, один - в день 10 и одна задержка роста опухоли до дня 17, что продемонстрировало заметно улучшенное ингибирование роста опухоли после лечения комбинацией I-263а с анти-mPD-1, по сравнению с активностью лечения любым одним средством (фигура 4d). В результате комбинированного лечения с применением I-263а в дозе 7,5 мг/кг (в/в, два раза в неделю × 3 до дня 17) плюс анти-mCTLA-4 в дозе 10 мг/кг (в/б, два раза в неделю × 2 до дня 17) был получен 1 ПО, достигнутый к дню 14, и одна задержка роста опухоли до дня 6, что демонстрирует улучшенное ингибирование роста опухоли после лечения комбинацией I-263а с анти-mCTLA4, по сравнению с активностью лечения любым одним средством (фигура 4е).
[0345] Исследование 5: Мышиная сингенная опухолевая модель WEHI-3
[0346] В подкожной мышиной сингенной опухолевой модели, полученной из миеломоноцитарного лейкоза WEHI-3, мышей инокулировали, рандомизировали в день 0 (4 дней после инокуляции), и лечение начинали в день 0 для всех групп.
[0347] Соединение I-263а тестировали в дозе 7,5 мг/кг, вводимой внутривенно по схеме 2 р/нед. (два раза в неделю) в течение трех недель до дня 14 (дни 0, 3, 7, 10 и 14). Анти-mPD-1 тестировали в дозе 10 мг, вводимой в/б по схеме два раза в неделю в течение 2 недель до дня 10 (дни 0, 3, 7 и 10) в группе монотерапии, и по схеме два раза в неделю в течение 3 недель до дня 14 (дни 0, 3, 7, 10 и 14) в группе комбинированного лечения. Анти-mCTLA-4 тестировали в дозе 10 мг/кг, вводимой по схеме один раз в четыре дня в течение 2 недель до дня 8 (дни 0, 4 и 8). В группе комбинированного лечения сначала вводили соединение I-263a, а затем сразу же вводили анти-mPD-1 или анти-mCTLA-4. Одна группа, которая служила группой, обрабатываемой носителем (группа 1), получала внутривенное лечение носителем для соединения I-263а (20% HPβCD) по схеме один раз в неделю в течение двух недель (дни 0, и 7).
[0348] Лечение соединением I-263а в дозе 7,5 мг/кг (в/в) по схеме два раза в неделю в течение трех недель до дня 14 (дни 0, 3, 7, 10 и 14) продемонстрировало умеренное ингибирование роста подкожных опухолей, происходящих от миеломоноцитарного лейкоза WEHI-3 мышей у самок мышей линии Balb/c, что привело к одной задержке роста опухоли до дней 11-14 и множественным незначительным задержкам роста опухолей до дней 7-11 в 6 из 8 имплантированных опухолях (фигура 5а). Лечение с применением анти-mPD-1 в дозе 10 мг/кг (в/б, два раза в неделю х 2 до дня 10) не приводило к какой-либо заметной противоопухолевой активности (фигура 5b). Лечение с применением анти-mCTLA-4 в дозе 10 мг/кг (в/б, по схеме один раз в четыре дня в течение 2 недель до дня 8) привело к заметному увеличению ингибирования роста опухоли по сравнению с обработкой носителем (фигура 5с). Комбинированное лечение соединением I-263а в дозе 7,5 мг/кг (в/в, два раза в неделю х 3 до дня 14) плюс анти-mPD-1 в дозе 10 мг/кг (в/б, два раза в неделю х 3 до дня 14) привело к умеренной задержке роста опухоли в период между днями 9-16 для всех 8 имплантированных опухолей, что не свидетельствует о каком-либо заметном улучшении ингибирования роста опухоли для комбинации I-263а с анти-mPD-1 по сравнению с активностью одного средства I-263а (фигура 5d). В результате комбинированного лечения с применением I-263а в дозе 7,5 мг/кг (в/в, два раза в неделю х 3 до дня 14) плюс анти-mCTLA-4 в дозе 10 мг/кг (в/б, один раз в четыре дня в течение двух недель до дня 8) наблюдалась регрессия опухоли с последующим стазом начиная со дня 14, для 2 из 8 имплантированных опухолей наблюдалось очень выраженное ингибирование роста опухоли для 1 опухоли, начинающееся в день 9, и менее заметное ингибирование роста опухоли для 1 опухоли, начинающееся в день 7, что демонстрирует улучшенное ингибирование роста опухоли после комбинации I-263а с анти-mCTLA4 по сравнению с активностью лечения любым одним средством (фигура 5е).
[0349] Исследование 6: Мышиная сингенная опухолевая модель JC
[0350] В подкожной мышиной сингенной опухолевой модели, полученной из аденокарцинома молочной железы JC, мышей инокулировали, рандомизировали в день 0 (12 дней после инокуляции), и лечение начинали в день 0 для всех групп.
[0351] Соединение I-263а тестировали в дозе 7,5 мг/кг, вводимой внутривенно по схеме 2 р/нед. (два раза в неделю) в течение трех недель до дня 14 (дни 0, 3, 7, 10 и 14). Анти-mPD-1 тестировали при введении дозы 10 мг/кг внутрибрюшинно по схеме два раза в неделю в течение 3 недель до дня 14 (дни 0, 3, 7, 10 и 14). Анти-mCTLA-4 тестировали вдозе 10 мг/кг, вводимой по схеме один раз в четыре дня в течение 3 недель до дня 8 (дни 0, 4 и 8). В группе комбинированного лечения сначала вводили Соединение I-263а, а затем сразу же вводили анти-mPD-1 или анти-mCTLA-4. Одна группа, которая служила группой, обрабатываемой носителем (группа 1), получала внутривенное лечение носителем для соединения I-263а (20% HPβCD) по схеме один раз в неделю в течение трех недель (дни 0, 7 и 14).
[0352] Лечение соединением I-263а в дозе 7,5 мг/кг (в/в, два раза в неделю х 3, до дня 14) продемонстрировало очень слабое ингибирование роста опухоли в одной имплантированной опухоли из 8, что показало незначительную задержку роста с день 16 по день 18 (фигура 6а). Лечение с применением анти-mPD-1 в дозе 10 мг/кг (в/б, два раза в неделю х 3 до дня 14) привело к сравнительно незначительной противоопухолевой активностью, причем в одной опухоли наблюдалась незначительная задержка роста опухоли с дня 16 по день 18 (фигура 6b). Лечение с применением анти-mCTLA-4 в дозе 10 мг/кг (в/б, по схеме один раз в четыре дня х 3) привело к задержке роста 2 опухолей в дни 14-21 (фигура 6с). Комбинированное лечение соединением I-263а в дозе 7,5 мг/кг (в/в, два раза в неделю х 3 до дня 14) плюс анти-mPD-1 в дозе 10 мг/кг (в/б, два раза в неделю х 3 до дня 14) привело к одной выраженной задержке роста опухоли в дни 14-18, что продемонстрировало незначительно улучшенное ингибирование роста опухоли после лечения комбинацией I-263а с анти-mPD-1, по сравнению с активностью лечения любым одним средством (фигура 6d). Комбинированное лечение соединением I-263а в дозе 7,5 мг/кг (в/в, два раза в неделю х 3 до дня 14) плюс анти-mCTLA-4 в дозе 10 мг/кг (в/б, по схеме один раз в четыре дня х 3) привело задержке роста опухоли для 2 опухолей в дни 14-21, что не свидетельствует о каком-либо заметном улучшении ингибирования роста опухоли для комбинации I-263а с анти-mCTLA-4 по сравнению с активностью одного средства анти-mCTLA-4 (фигура 6е).
[0353] Исследование 7: Мышиная сингенная опухолевая модель B16-F10
[0354] В подкожной мышиной сингенной опухолевой модели, полученной из меланомы B16-F10, мышей инокулировали, рандомизировали в день 0 (8 дней после инокуляции), и лечение начинали в день 0 для всех групп.
[0355] Соединение I-263а тестировали в дозе 7,5 мг/кг, вводимой внутривенно по схеме 2 р/нед. (два раза в неделю) в течение трех недель до дня 17 (дни 0, 3, 7, 10, 14 и 17). Анти-mPD-1 тестировали при введении дозы 10 мг/кг внутрибрюшинно по схеме два раза в неделю в течение 3 недель до дня 17 (дни 0, 3, 7, 10, 14 и 17). Анти-mCTLA-4 тестировали при введении дозы 10 мг/кг по схеме два раза в неделю в течение 3 недель до дня 17 (дни 0, 3, 7, 10, 14 и 17). В группе комбинированного лечения сначала вводили соединение I-263а, а затем сразу же вводили анти-mPD-1 или анти-mCTLA-4. Одна группа, которая служила группой, обрабатываемой носителем (группа 1), получала внутривенное лечение носителем для соединения I-263а (20% HPβCD) по схеме два раза в неделю в течение двух недель до дня 10 (дни 0, 3, 7 и 10).
[0356] Лечение соединением I-263а в дозе 7,5 мг/кг (в/в, два раза в неделю х 3, до дня 17) привело к задержке роста опухоли для 2 из 8 имплантированных опухолей с дня 7 по дни 10-12 (фигура 7а). Лечение с применением анти-mPD-1 в дозе 10 мг/кг (в/б, два раза в неделю х 3 до дня 17) привело к задержке роста 2 опухолей в дни 7-17, 2 опухолей в дни 7-12 и 1 опухоли в день 10 (фигура 7b). Лечение с применением анти-mCTLA-4 в дозе 10 мг/кг (в/б, два раза в неделю х 3 до дня 17) привело к задержке роста 2 опухолей в дни 10-14 и 1 опухоли в день 10 (фигура 7с). Комбинированное лечение соединением I-263а в дозе 7,5 мг/кг (в/в, два раза в неделю х 3 до дня 17) плюс анти-mPD-1 в дозе 10 мг/кг (в/б, два раза в неделю х 3 до дня 17) привело к задержке роста 1 опухоли с дня 7 по день 14, что свидетельствует об отсутствии улучшения ингибирования роста опухоли для комбинации I-263а с анти-mPD-1, по сравнению с активностью одного любого средства (фигура 7d) Комбинированное лечение соединением I-263а в дозе 7,5 мг/кг (в/в, два раза в неделю х 3 до дня 17) плюс анти-mCTLA-4 в дозе 10 мг/кг (в/б, два раза в неделю х 3 до дня 17) привело к задержке роста 2 опухолей в день 10, что свидетельствует об отсутствии улучшения ингибирования роста опухоли для комбинации I-263а с анти-mCTLA-4 по сравнению с активностью одного средства (фигура 7е).
[0357] Исследование 8: Мышиная сингенная опухолевая модель МС38
[0358] В подкожной мышиной сингенной опухолевой модели, полученной из аденокарциномы толстой кишки МС38, мышей инокулировали, рандомизировали в день 0 (5 дней после инокуляции), и лечение начинали в день 0 для всех групп.
[0359] Соединение I-263а тестировали в дозе 7,5 мг/кг, вводимой внутривенно по схеме 2 р/нед. (два раза в неделю) в течение трех недель до дня 17 (дни 0, 3, 7, 10, 14 и 17). Анти-mPD-1 тестировали при введении дозы 10 мг/кг внутрибрюшинно по схеме два раза в неделю в течение 3 недель до дня 17 (дни 0, 3, 7, 10, 14 и 17). Анти-mCTLA-4 тестировали при введении дозы 10 мг/кг по схеме два раза в неделю в течение 3 недель до дня 17 (дни 0, 3, 7, 10, 14 и 17). В группе комбинированного лечения сначала вводили соединение I-263а, а затем сразу же вводили анти-mPD-1 или анти-mCTLA-4. Одна группа, которая служила группой, обрабатываемой носителем (группа 1), получала внутривенное лечение носителем для соединения I-263а (20% HPβCD) по схеме два раза в неделю в течение 3 недель до дня 10 (дни 0, 3, 7, 10, 14 и 17).
[0360] Лечение соединением I-263а в дозе 7,5 мг/кг (в/в, два раза в неделю х 3, до дня 17) привело к задержке роста опухоли для 2 из 8 имплантированных опухолей в дни 7-18 и для 1 опухоли в дни 11-14 (фигура 8а). Лечение с применением анти-mPD-1 в дозе 10 мг/кг (в/б, два раза в неделю х 3 до дня 17) приводило к заметной задержке роста опухоли с регрессией для 3 опухолей в дни 9-18, 11-18 и 14-18, и задержке роста опухоли для 1 опухоли в дни 4-9 и 3 опухолей в дни 11-14 (фигура 8b). Монотерапия с применением анти-mCTLA-4 в дозе 10 мг/кг (в/б, два раза в неделю х 3 до дня 17) привела к 2 регрессиям опухоли в дни 14-23 день и дни 16-21, а также к 1 задержке роста опухоли в дни 4-20, и задержкам роста 2 опухолей в дни 11-14/16 (фигура 8с). Комбинированное лечение соединением I-263а в дозе 7,5 мг/кг (в/в, два раза в неделю х 3, до дня 17) плюс анти-mPD-1 в дозе 10 мг/кг (в/б, два раза в неделю х 3, до дня 17) привело к регрессии 3 опухолей в дни 7-11, 7-14 и 7-21, а также задержке роста 1 опухоли в дни 7-18, что представляет незначительную пользу, если таковая имеется, комбинации по сравнению с активностью одного средства анти-mPD-1 (фигура 8d). Комбинированное лечение соединением I-263а в дозе 7,5 мг/кг (в/в, два раза в неделю х 3) плюс анти-mCTLA-4 в дозе 10 мг/кг (в/б, два раза в неделю х 3) привело к 3 ПО в дни 14, 25 и 35, что представляло собой длительное явление до конца мониторинга в день 49 и к одной заметной и продолжительной задержке роста с дня 4 по день 28, что продемонстрировало заметное улучшение ингибирования роста опухоли для комбинации I-263а с анти-mCTLA-4 (фигура 8е).
[0361] Пример 2. Клиническое исследование по оценке соединения I-263а в комбинации с ингибитором контрольных точек при лечении пациентов с немелкоклеточным раком легкого, раком шейки матки или колоректальным раком.
[0362] Клиническое исследование фазы 1b/2 будет проводиться для оценки эффектов комбинированной терапии, состоящей из проведения внутривенной инфузии пембролизумаба и внутривенной инфузии соединения I-263а, у взрослых пациентов с немелкоклеточным раком легкого (НМРЛ), раком шейки матки или колоректальным раком с микросателлитной стабильностью (МСС-КРР).
[0363] Исследование будет состоять из периода скрининга (с дня -28 по день -1), периода лечения, визита завершения лечения и визита в рамках периода последующего наблюдения через 30 дней после введения последней дозы, после прекращения лечения по любой причине, и периода наблюдения с выживаемостью без прогрессирования заболевания продолжительностью не более 12 месяцев для каждого пациента после введения последней дозы исследуемого препарата для мониторинга статуса выживаемости. День 1 исследования (исходный уровень) будет определяться как первый день, когда пациент получит соединение I-263а. Один цикл лечения будет определяться как 21 день. Пациентов попросят регулярно приходить на визиты в клинику во время исследования для оценки безопасности и эффективности.
[0364] Пациенты будут получать лечение соединением I-263а и пембролизумабом в течение периода до 24 месяцев или до тех пор, пока не будет подтверждено прогрессирование заболевания, неприемлемая токсичность или соответствие любому критерию для исключения из исследования или прекращения приема исследуемых препаратов. Лечение может быть продолжено после установления прогрессирования заболевания, если у пациента сохраняется клиническая эффективность.
[0365] Исследование будет разделено на 2 части: часть фазы 1b и часть фазы 2. Часть исследования фазы 1b представляет собой исследование с повышением дозы соединения I-263а в комбинации с пембролизумабом в фиксированной дозе у пациентов с немелкоклеточным раком легкого (НМРЛ), раком шейки матки или микросателлитным колоректальным раком с микросателлитной стабильностью (МСС-КРР) для определения безопасности и переносимости комбинации. При повышении дозы соединения I-263а будут руководствоваться дизайном байесовского оптимального интервала (BOIN), чтобы определить рекомендуемую дозу для фазы 2 (RP2D) для комбинированной терапии. RP2D будет определяться на основе коллективного опыта в клинике с учетом данных безопасности, предварительных данных по ФК, предварительных данных по фармакодинамике и любой наблюдаемой ранней противоопухолевой активности, вместе со статистическими выводами из BOIN.
[0366] В исследовании фазы 2 будет определена эффективность и безопасность соединения I-263а в комбинации с пембролизумабом у пациентов с некоторыми видами рака. В исследование будут включены следующие когорты: когорта А: аденокарцинома НМРЛ; когорта В: рак шейки матки; когорта С: МСС-КРР. Каждая когорта будет оцениваться отдельно с использованием адаптивного двухстадийного дизайна для одной доли пациентов.
[0367] На стадии I каждая когорта будет проанализирована, после зачисления в исследование предварительно определенного количества пациентов и установления возможности проведения по меньшей мере одного сканирования после лечения (т.е. после первой оценки заболевания, через 2 месяца после цикла 1, дня 1 (Ц1Д1)). Если предварительно определенная минимальная частота ответов не будет достигнута на первой стадии для данной когорты, зачисление в данную когорта будет прекращено. Однако, если у пациентов в когорте наблюдалась явная клиническая эффективность (например, у большинства пациентов было зарегистрировано стабильное заболевание на неделе 8, и не регистрировался полный ответ (ПО) или частичный ответ (ЧО)), то включение в стадию II может быть разрешено для этой когорты.
[0368] Если необходимая частота ответа во время стадии I или хорошая клиническая эффективность наблюдается для конкретной когорты, как упомянуто выше, то дополнительные пациенты будут включаться во вторую стадию соответствующей когорты до тех пор, пока не будет достигнуто предварительно определенное количество дополнительных пациентов для этой когорты. Итоговый анализ основных конечных точек для каждой когорты будет проводиться, когда все пациенты, проходящие лечение, будут иметь возможность завершить 6-месячную оценку заболевания.
[0369] Начальная доза соединения I-263а будет составлять 3 мг для внутривенного введения. Соединение I-263а будут вводить в виде 1-часовой внутривенной (в/в) инфузии в дни 1, 4, 8 и 11 в рамках 21-дневного цикла. Пембролизумаб будут вводить в дозе 200 мг в день 1 в рамках 21-дневного цикла. Соединение I-263а будут вводить перед пембролизумабом в дни введения как соединения I-263а, так и пембролизумаба в один и тот же день визита. Между завершением инфузии первого исследуемого препарата и началом инфузии второго исследуемого препарата должно пройти не менее 30 минут.
[0370] Соединение I-263а будут вводить в виде внутривенной инфузии в течение 60±10 минут. В случае возникновения инфузионные реакции, продолжительность инфузии может быть увеличена до 4 часов для всех пациентов без необходимости изменения протокола. Пембролизумаб будут вводить в виде внутривенной инфузии в течение 30±10 минут.Повышение или снижение дозы пембролизумаба не допускается.
[0371] В части фазы 1b исследования будут повышать только дозировку соединения I-263а. Начальный уровень дозы будет определен спонсором и участвующими исследователями после изучения новых данных по безопасности из продолжающегося исследования одного средства FIH (исследование TAK-981-1002). Будут рассмотрены следующие уровни доз соединения I-263а: 25 мг, 40 мг, 60 мг, 90 мг, 120 мг и 160 мг. Оценка более низких или промежуточных уровней доз может использоваться, если такие меры необходимы для безопасности пациента или для лучшего понимания токсичности, воздействия или фармакодинамики соединения I-263а.
[0372] При повышении дозы будут придерживаться дизайна байесовского оптимального интервала (BOIN). Yuan Y, et at., Clin. Cancer Res. 22(17):4291-301 (2016). В соответствии с дизайном BOIN решение о повышении или снижении дозы соединения I-263а основывается на уровне кумулятивной дозолимитирующей токсичность (ДЛТ) при текущем уровне дозы и предварительно определенном пороговом значении ДЛТ для пределов повышения/снижения дозы. Целевой показатель ДЛТ для этого исследования составляет 0,3. Правила повышения и снижения дозы для соединения I-263а следующие: 1) если наблюдаемый показатель ДЛТ при текущем уровне дозы составляет ≤0,236, уровень дозы будет повышен; 2) если наблюдаемый показатель ДЛТ при текущем уровне дозы составляет ≥0,359, уровень дозы будет снижен; и 3) если наблюдаемая наблюдаемый показатель ДЛТ при текущем уровне дозы составляет от 0,236 до 0,359, уровень дозы останется прежним.
[0373] Соединение I-263а и пембролизумаб будут вводиться внутривенно до тех пор, пока не будет подтверждено прогрессирование заболевания или неприемлемая токсичность. Токсичность будет оцениваться на основании общих терминологических критериев нежелательных явлений (СТСАЕ) Национального института рака (NCI)., версия 5.0.
[0374] В этом исследовании будет участвовать приблизительно 93 субъекта, из которых приблизительно 24 субъекта будут задействованы в части исследования с повышением дозы фазы 1b и приблизительно от 27 до 69 субъектов в части исследования фазы 2 (приблизительно от 9 до 23 для каждой из трех когорт).
[0375] Первичные конечные точки фазы 1b
[0376] Первичные конечные точки для исследования фазы 1b будут включать: частоту, тяжесть и продолжительность нежелательных явлений, возникших в ходе лечения (НЯВЛ), и лабораторных отклонений для всех групп доз в соответствии с NCI СТСАЕ версии 5.0; и возникновение ДЛТ в течение первого 21 дня лечения в цикле 1.
[0377] Первичные конечные точки фазы 2
[0378] Первичные конечные точки для исследования фазы 2 будут включать: частоту общего ответа (ЧОО) (полный ответ + частичный ответ), как будет определено исследователем в соответствии с критериями оценки ответа при солидных опухолях (RECIST) версии 1.1.
[0379] Вторичные конечные точки фазы 1b
[0380] Вторичные конечные точки для исследования фазы 1b будут включать: ЧОО, уровень контроля заболевания (УКЗ), продолжительность ответа (ПрО), время до прогрессирования (ВДП), выживаемость без прогрессирования (ВБП) и общую выживаемость (ОВ), как будет определено исследователем в соответствии с RECIST версии 1.1 и модифицированными критериями RECIST 1.1, а также в соответствии с согласованными рекомендациями RECIST (iRECIST).
[0381] Вторичные конечные точки фазы 2
[0382] Вторичные конечные точки для исследования фазы 2 будут включать: частоту, тяжесть и продолжительность НЯВЛ и лабораторных отклонений для всех групп доз в соответствии с NCI СТСАЕ версии 5.0; УКЗ, ПрО, ВДП, ВБП и ОВ, как будет определено исследователем в соответствии с RECIST версии 1.1 и iRECIST; ЧОО по оценке исследователем согласно iRECIST; и данным по концентрации соединения I-263а в плазме в зависимости от времени.
[0383] Исследование будет проводиться в соответствии с Надлежащей клинической практикой.
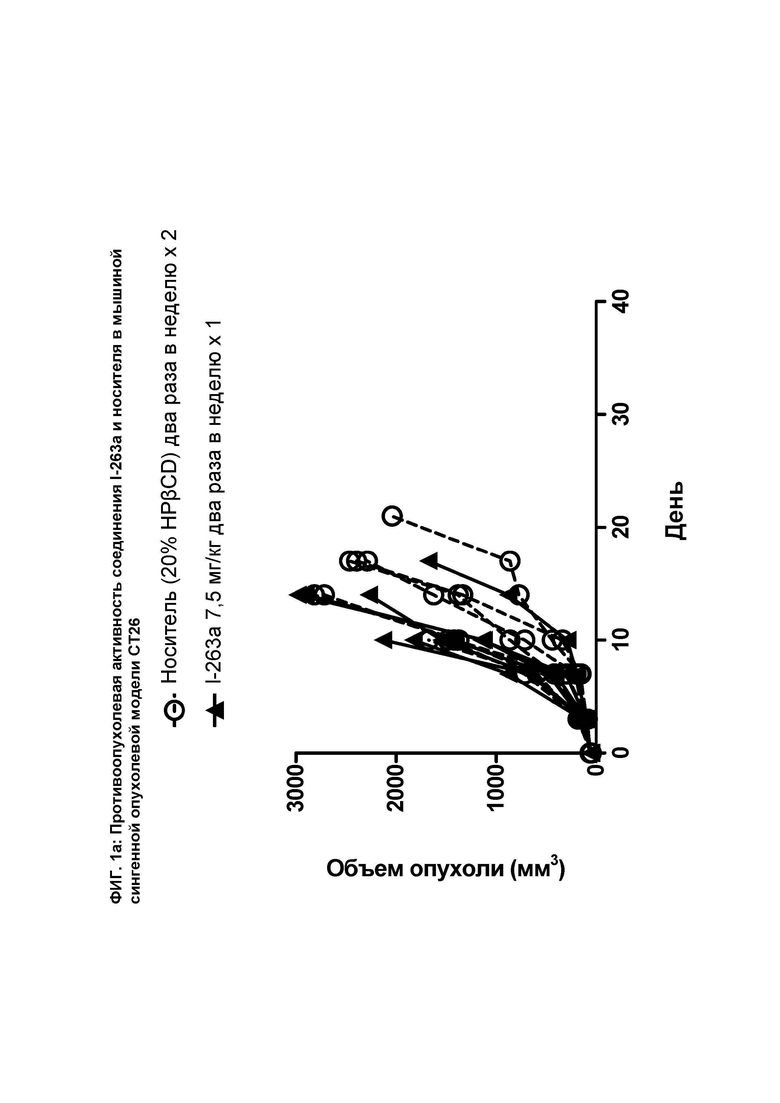
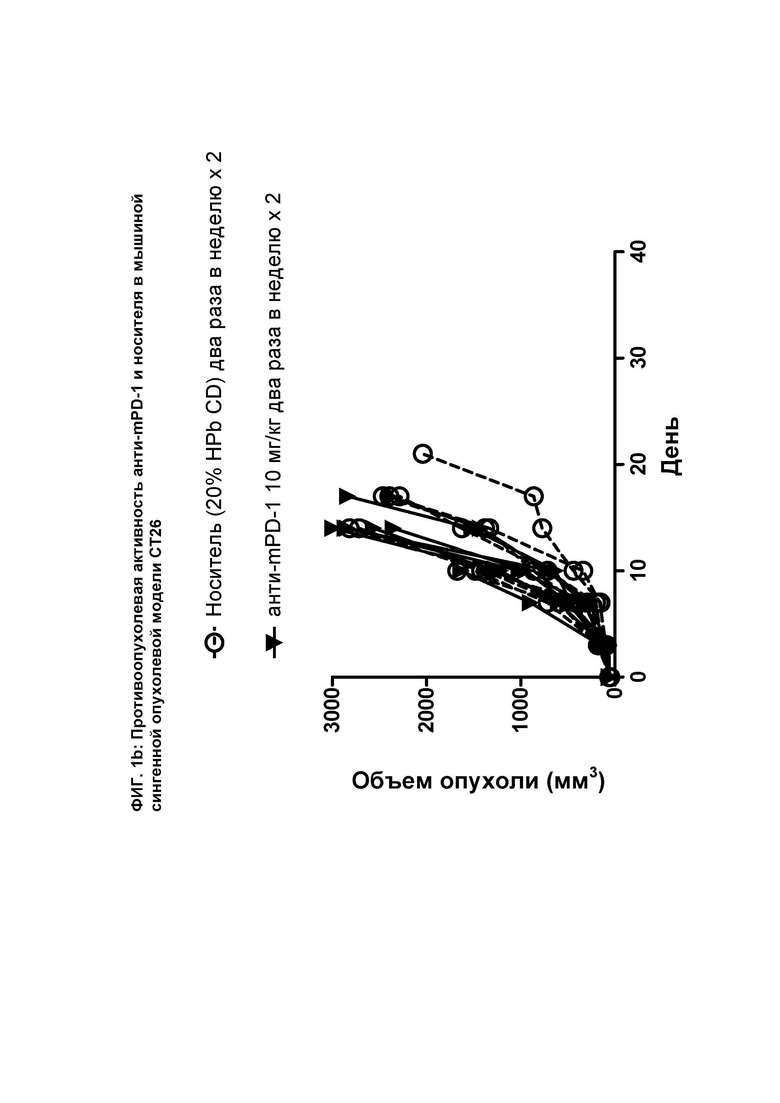
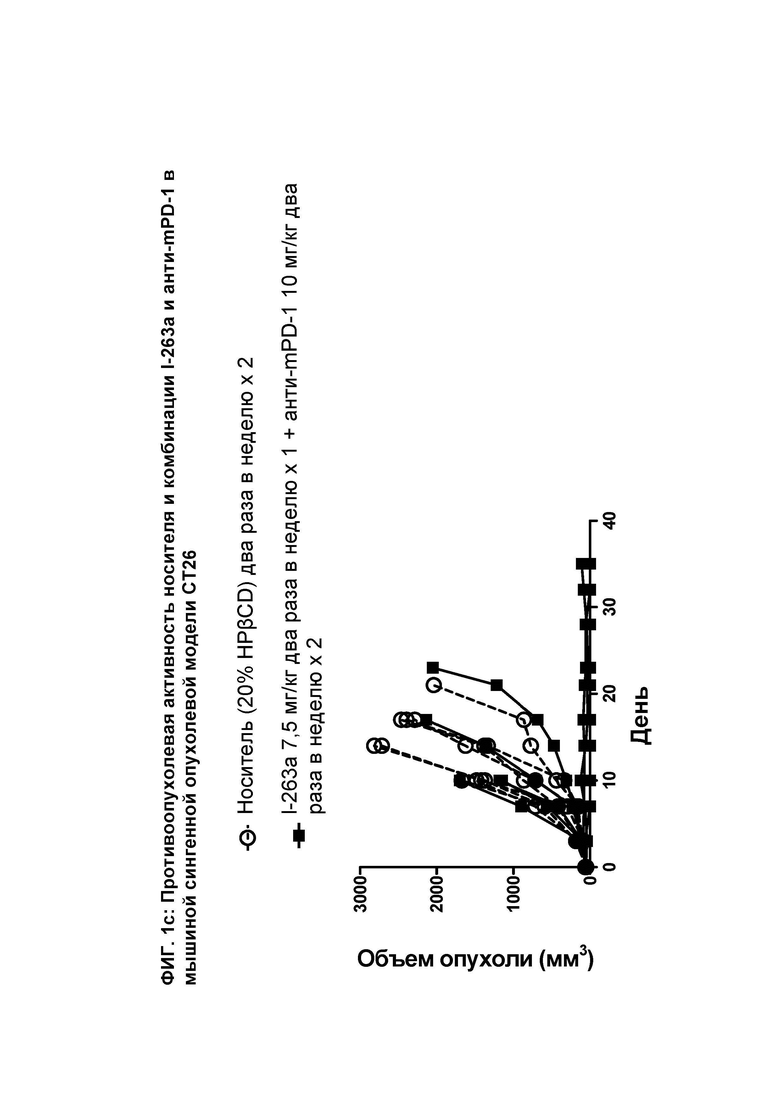
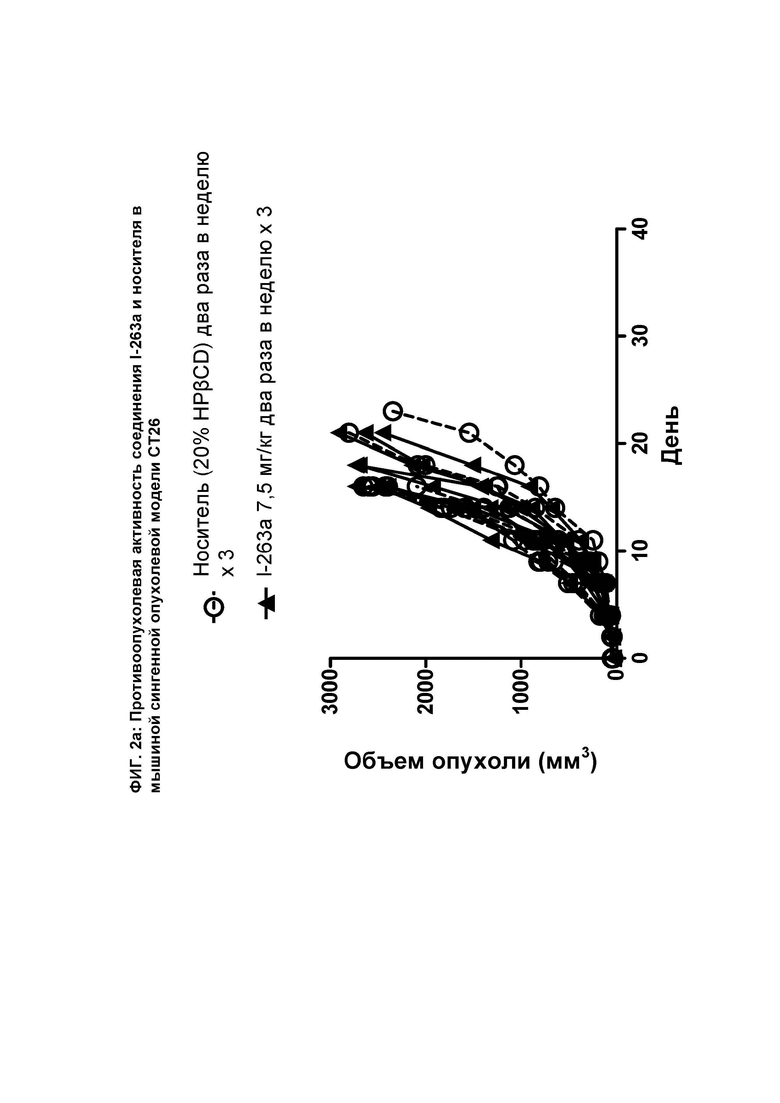
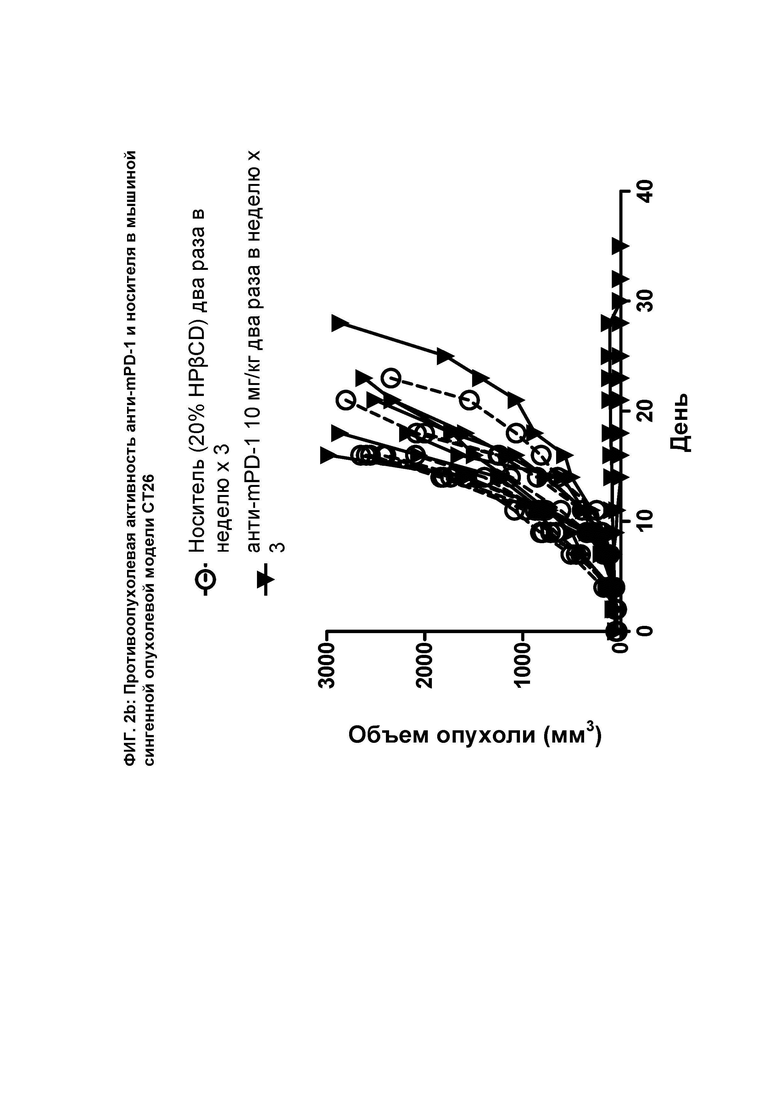
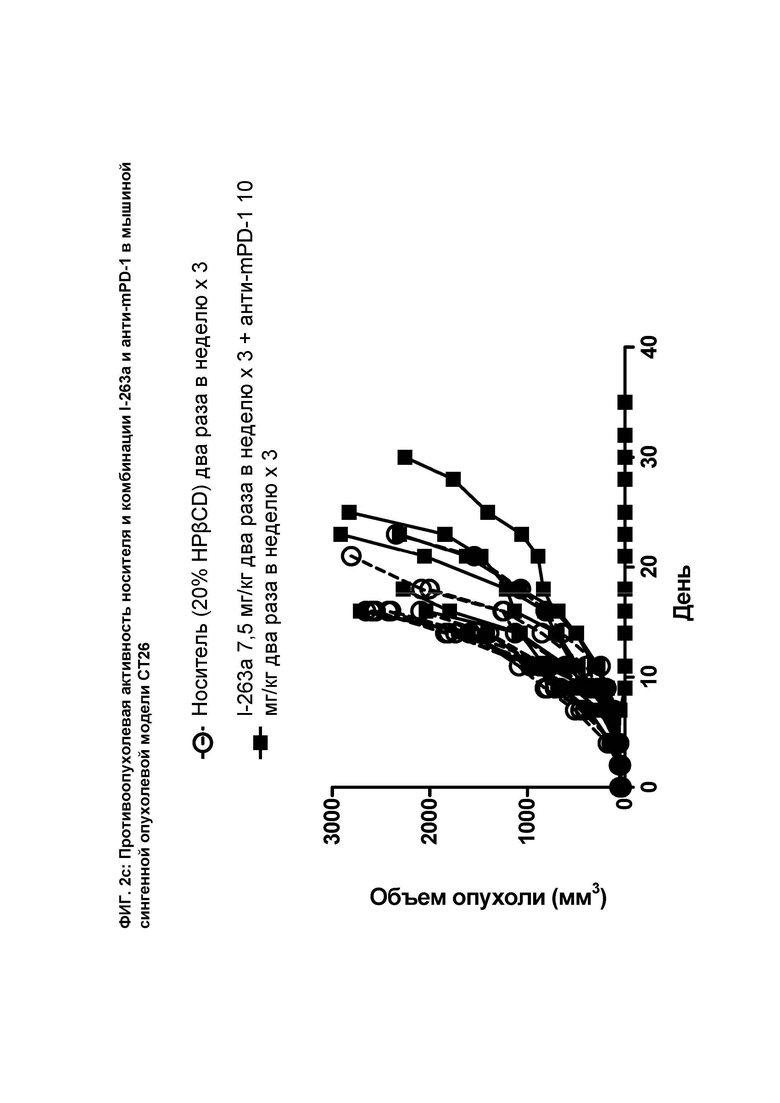
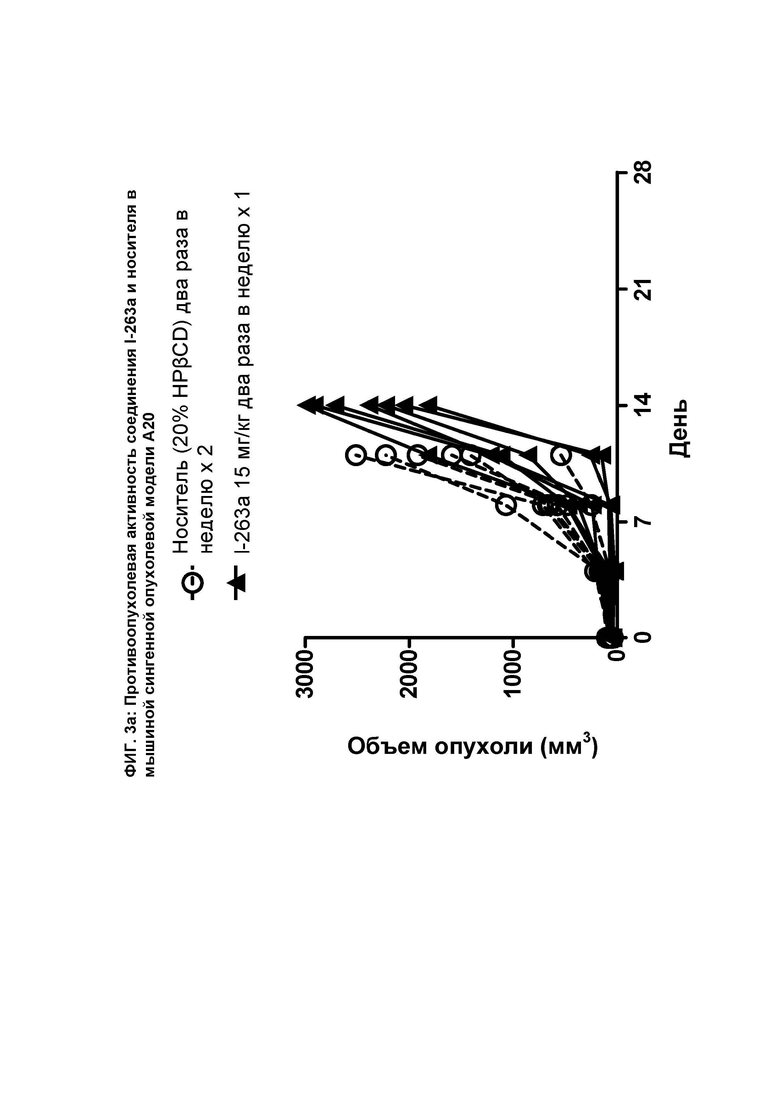
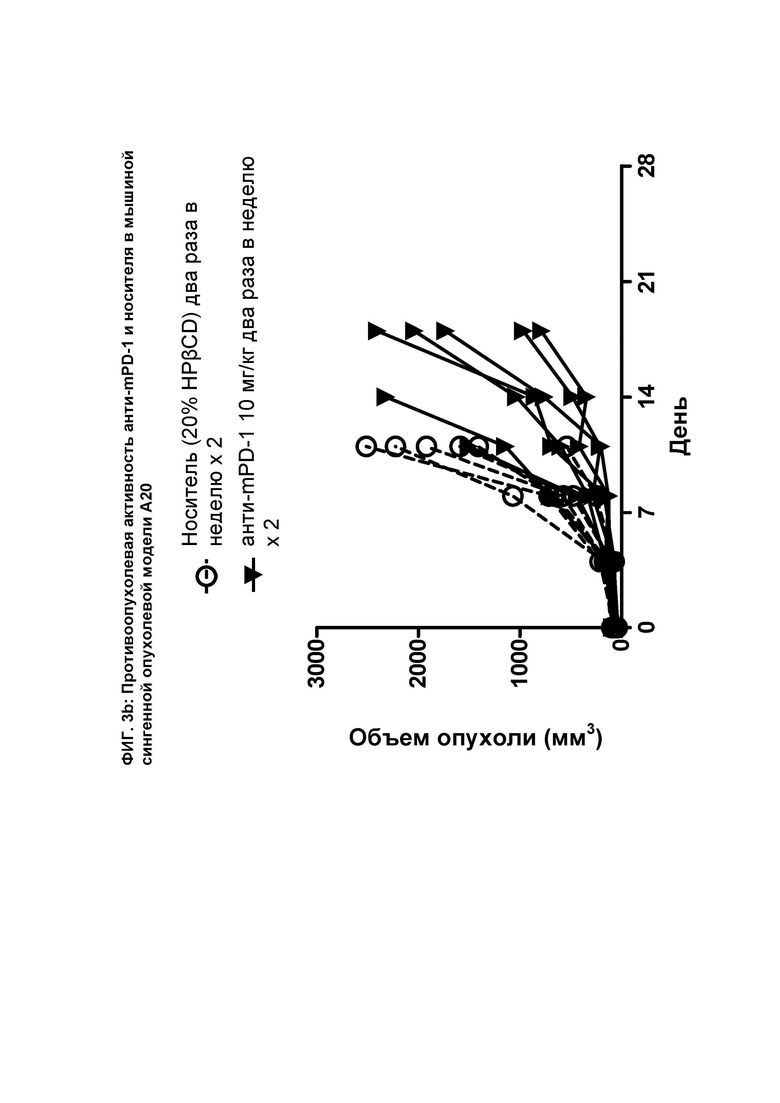
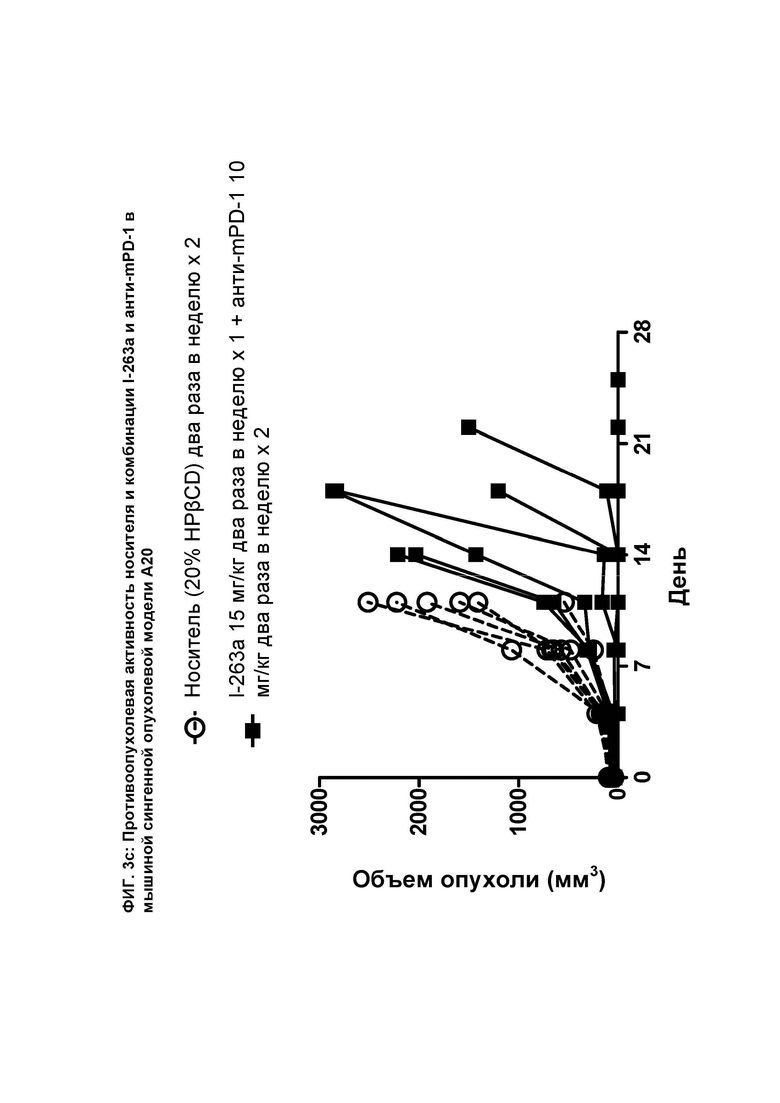
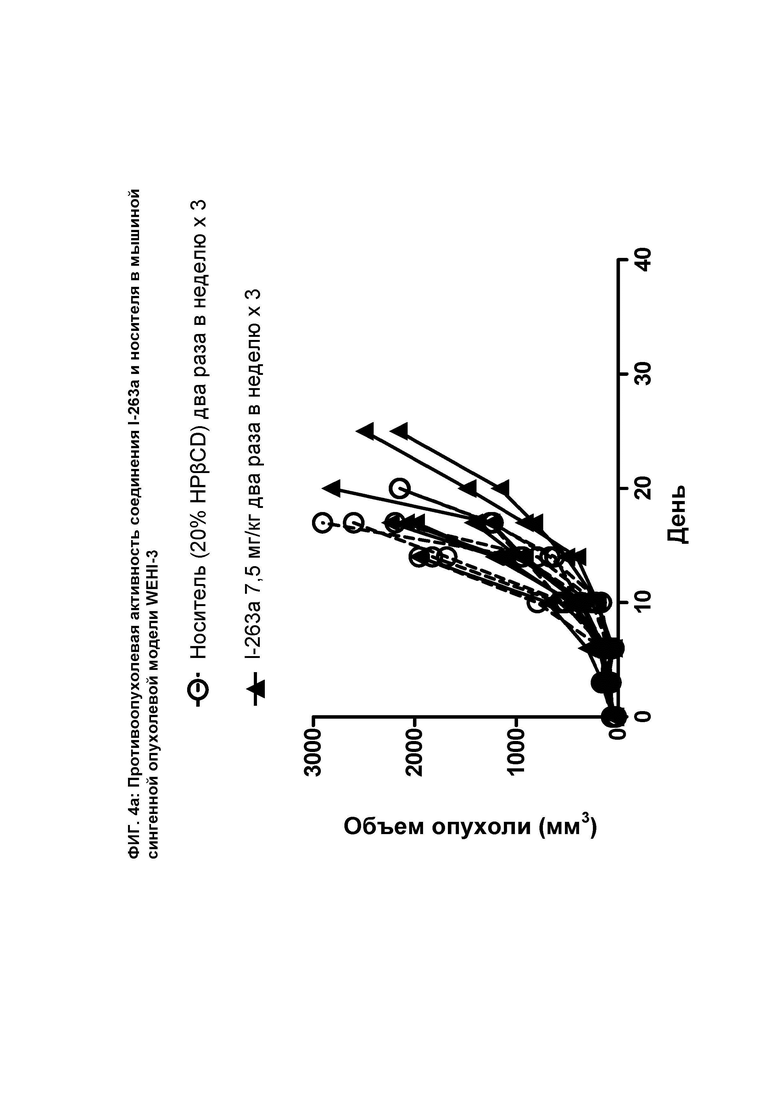
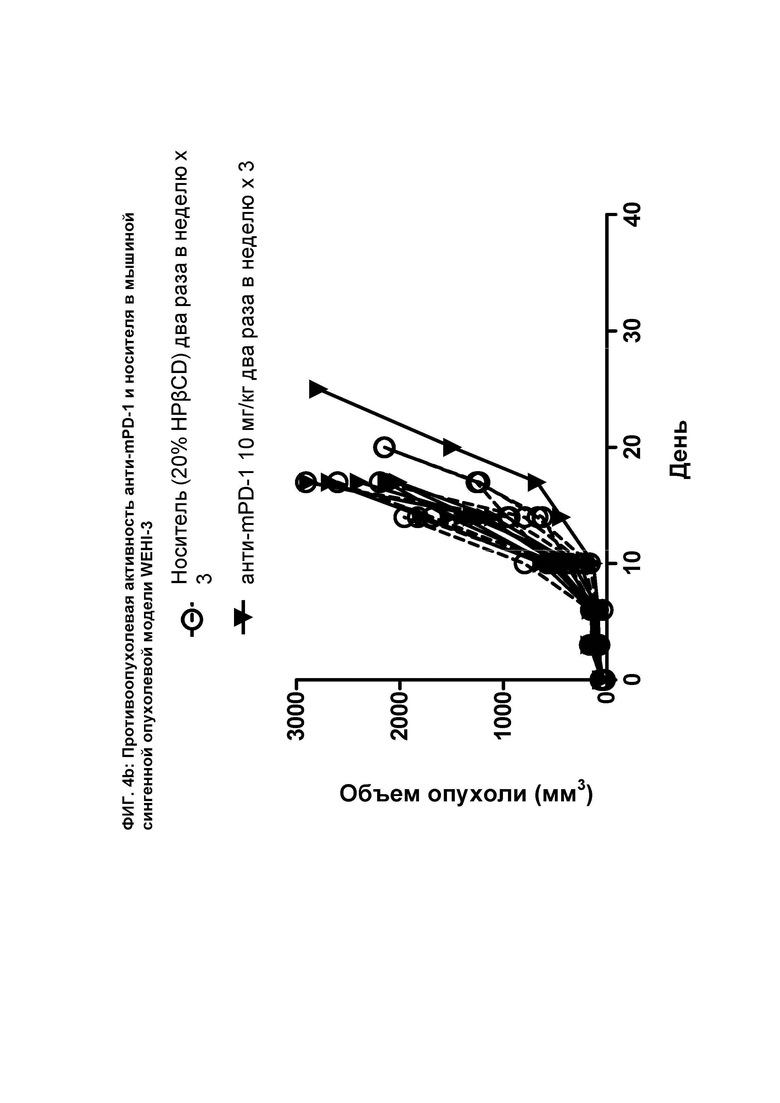
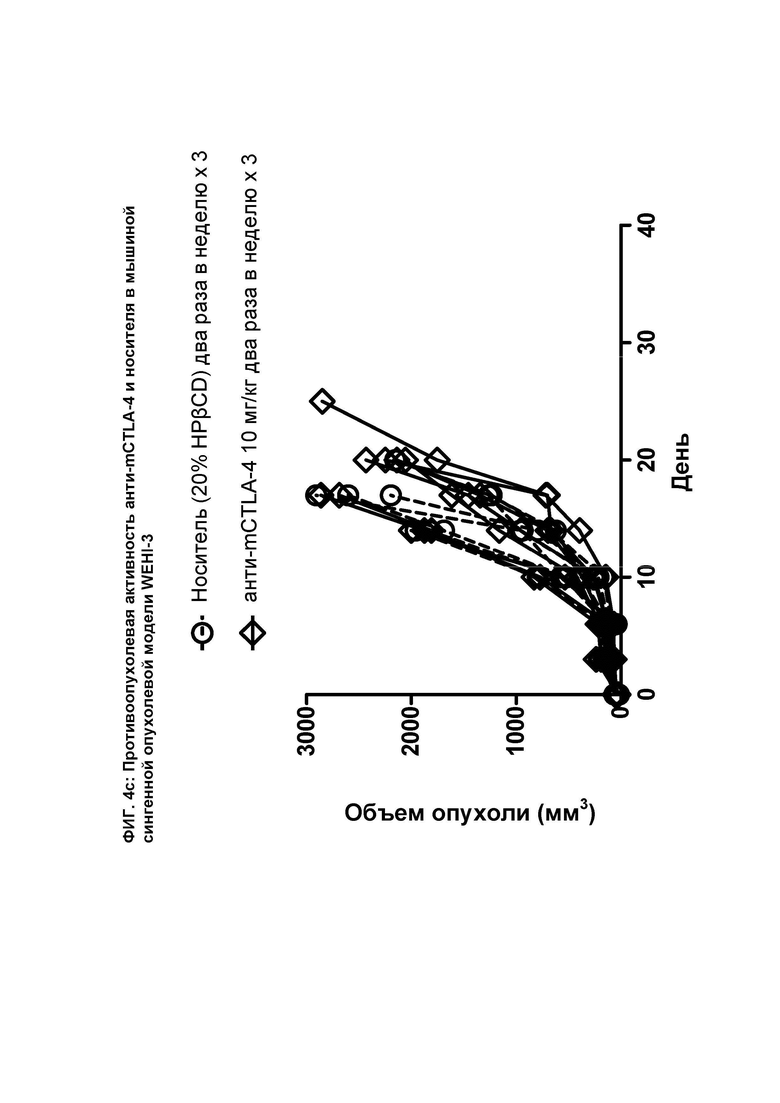
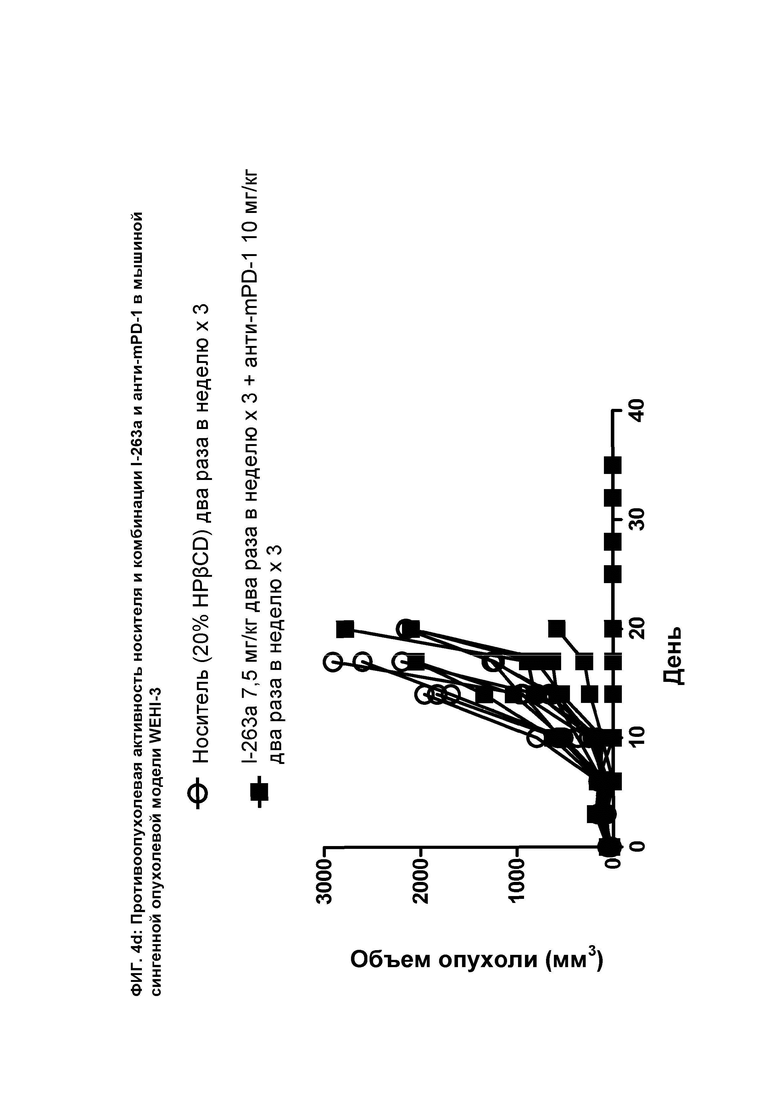
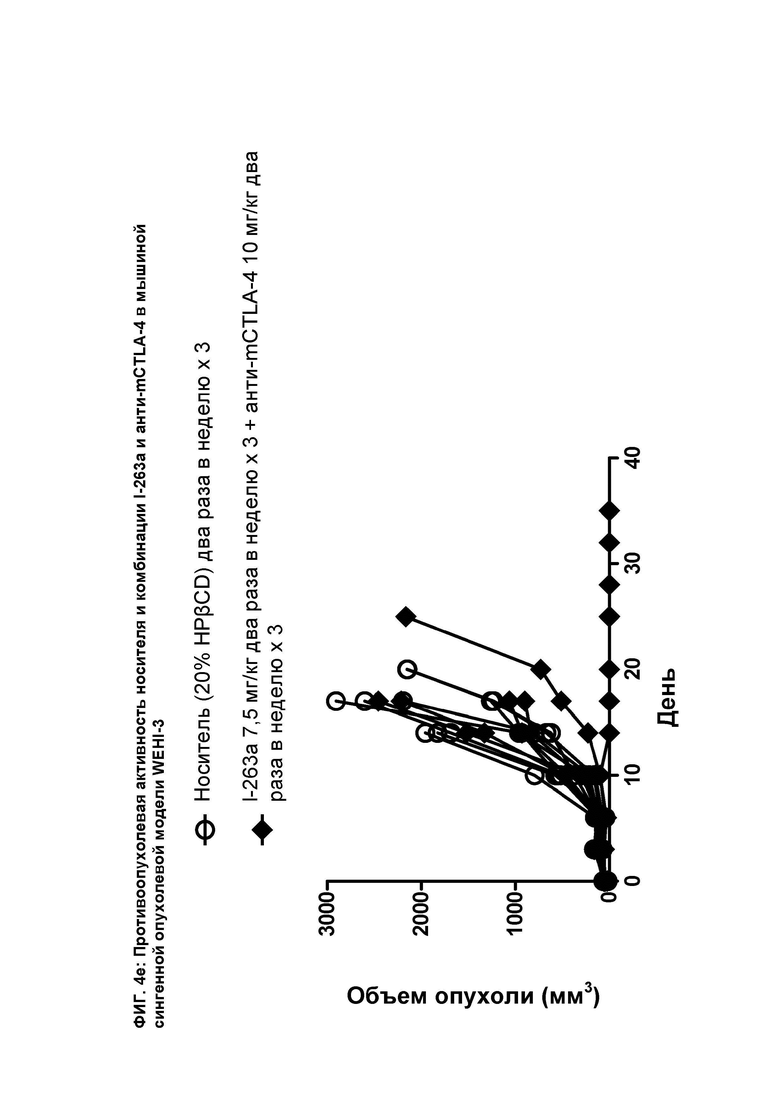
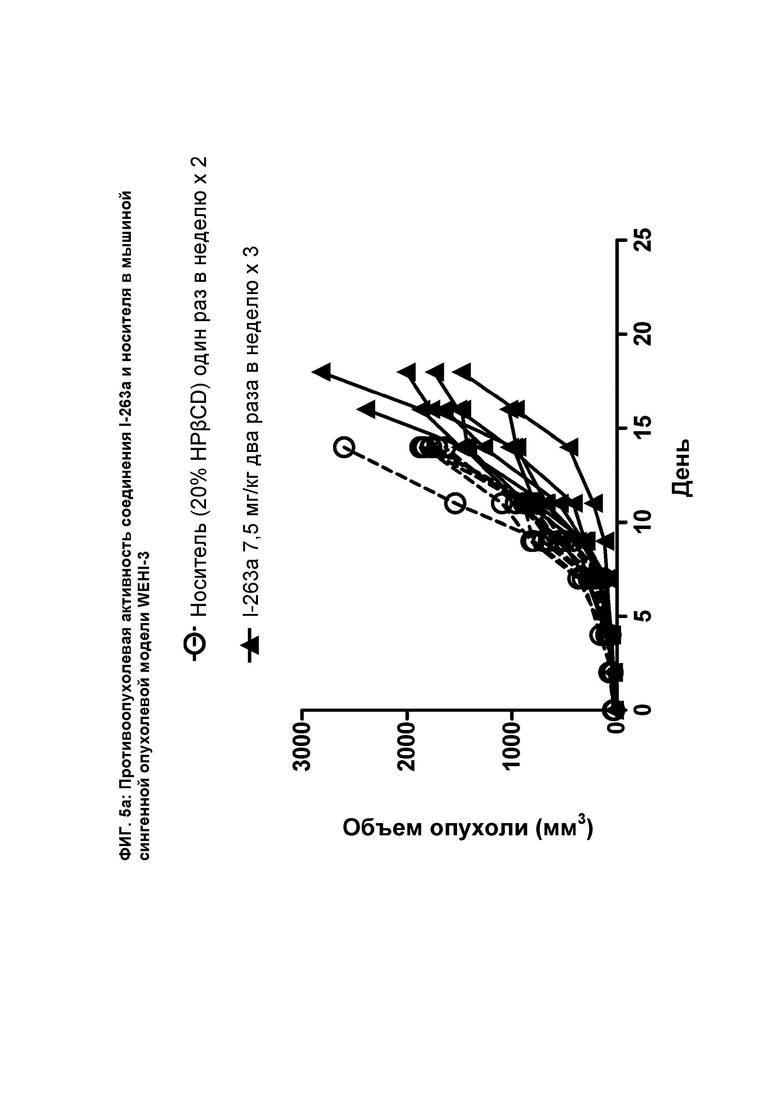
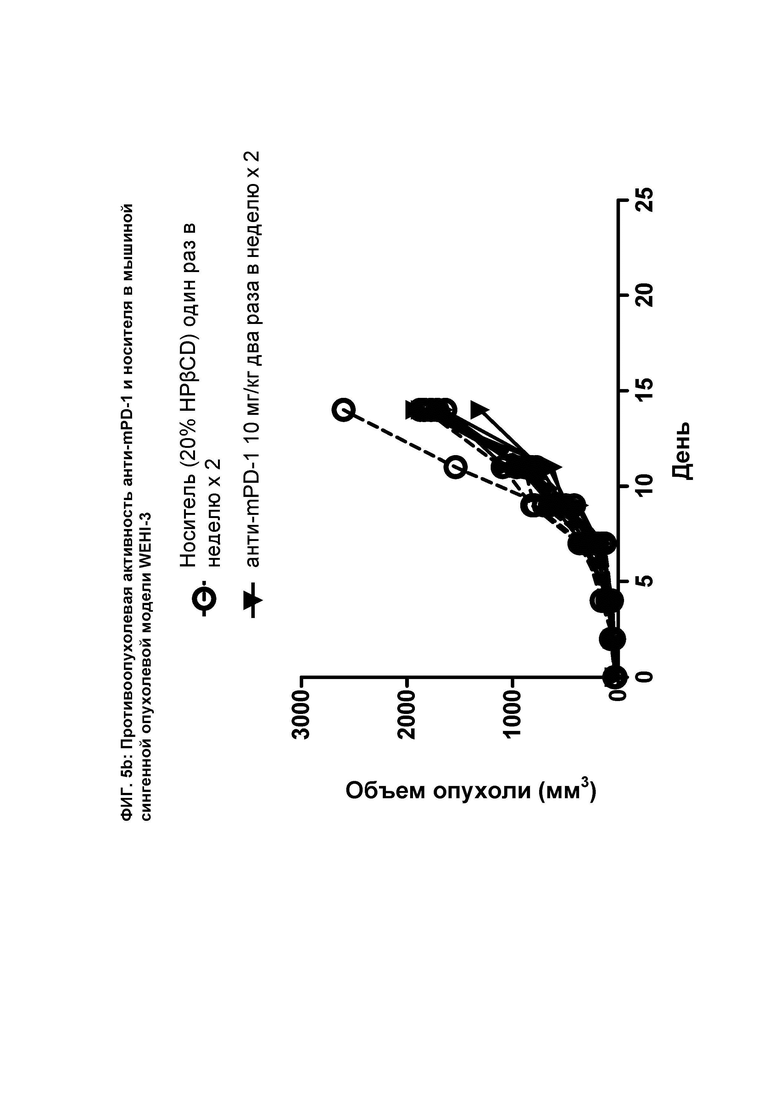
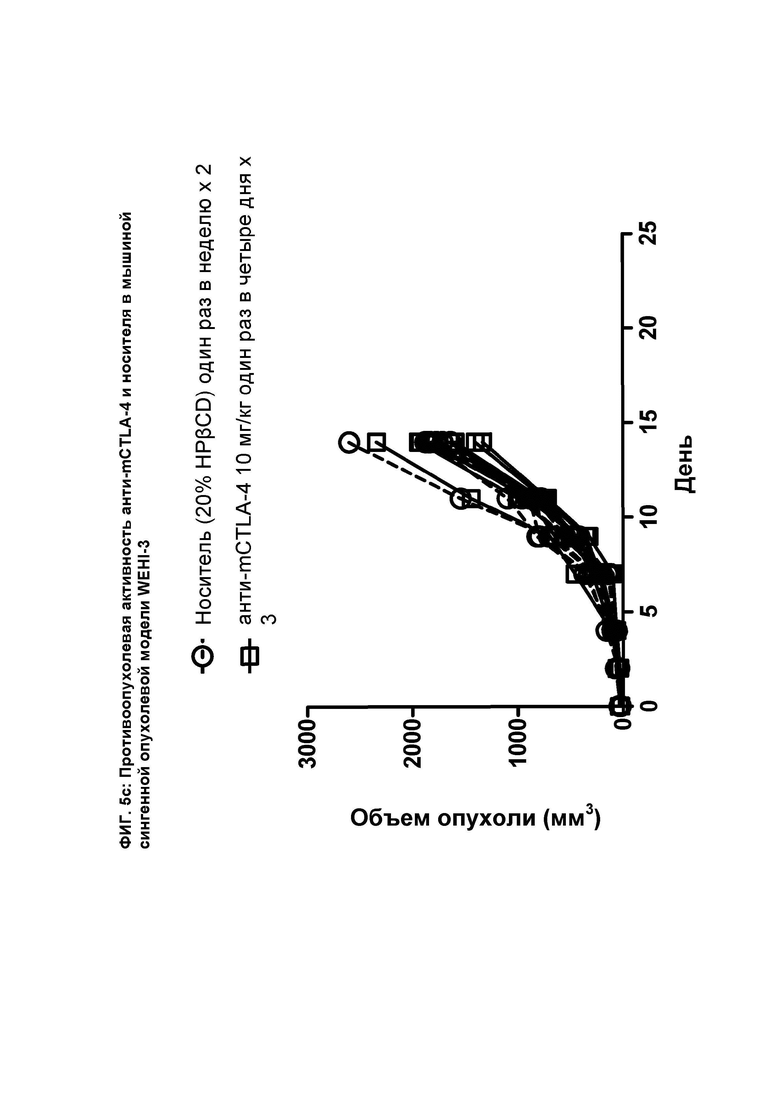
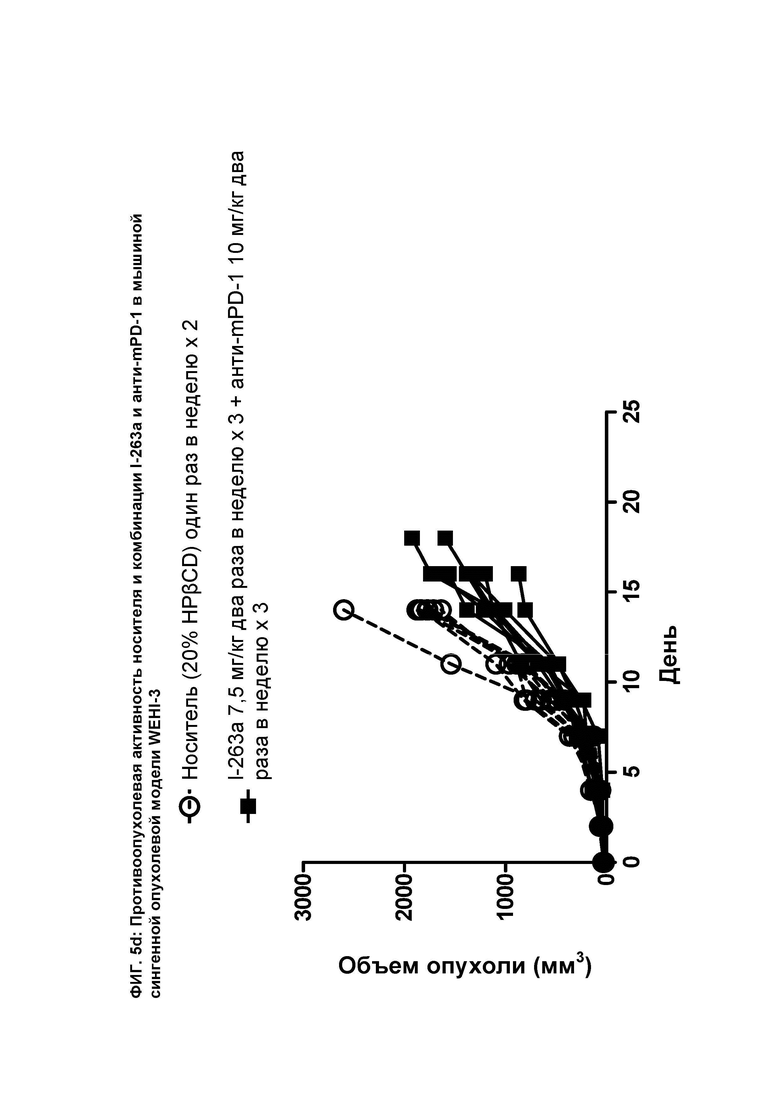
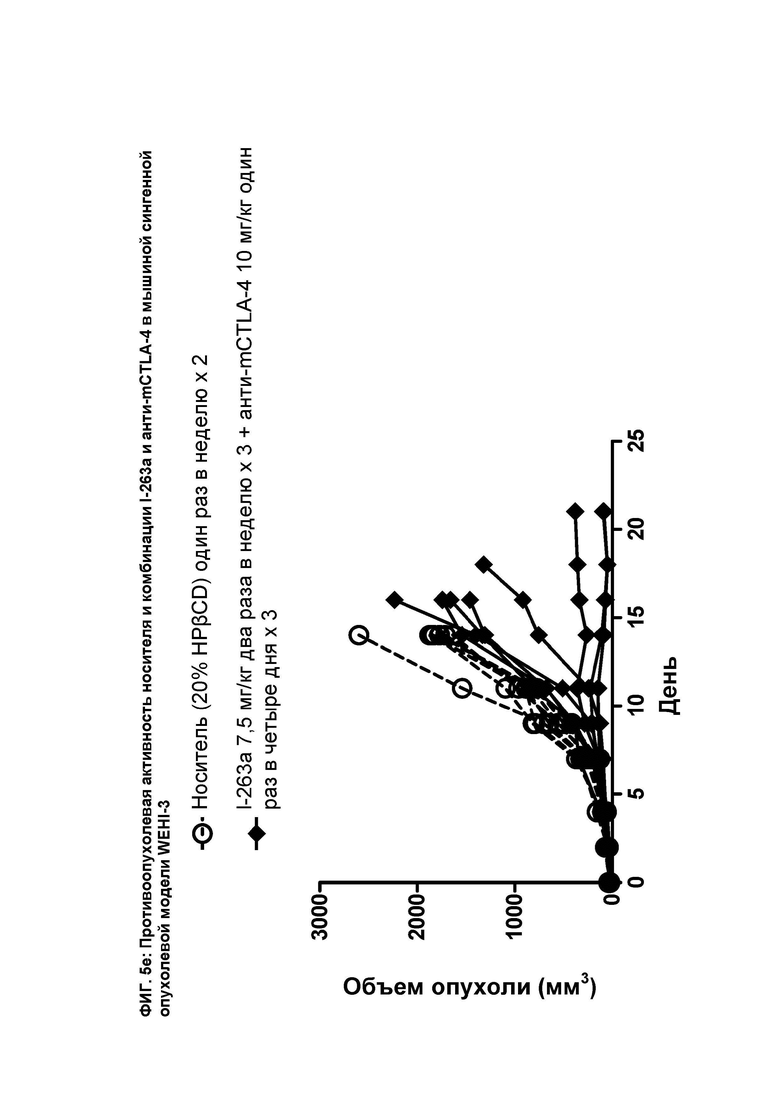
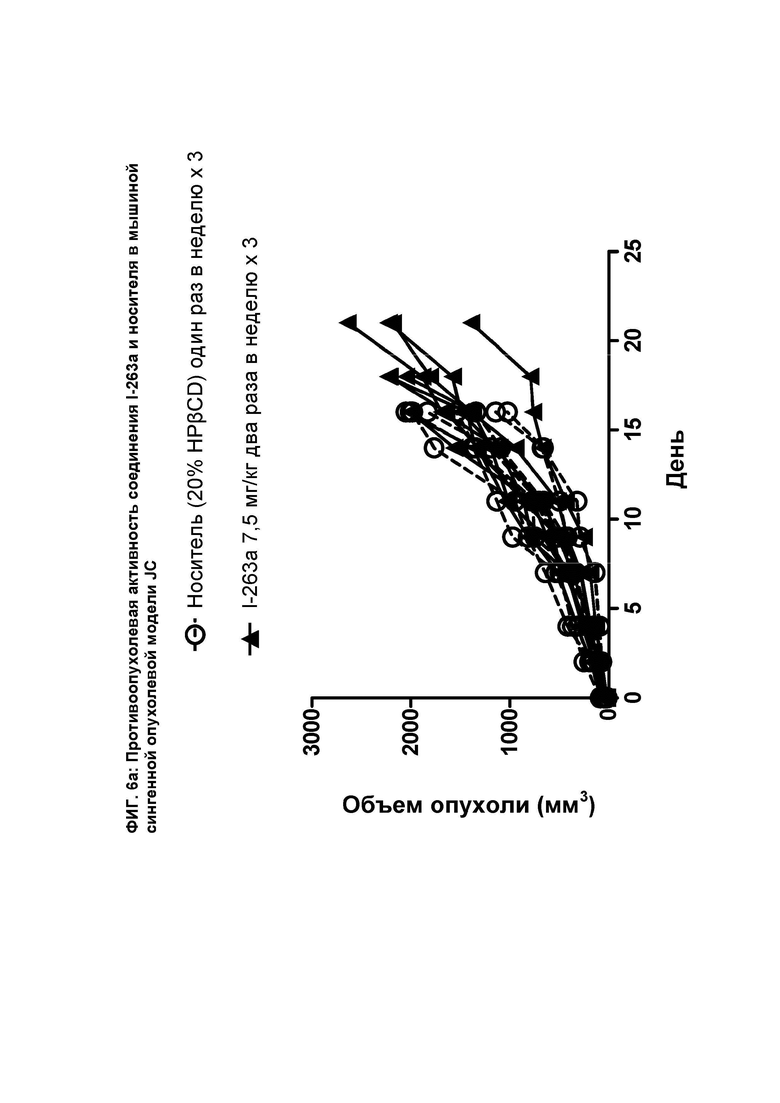
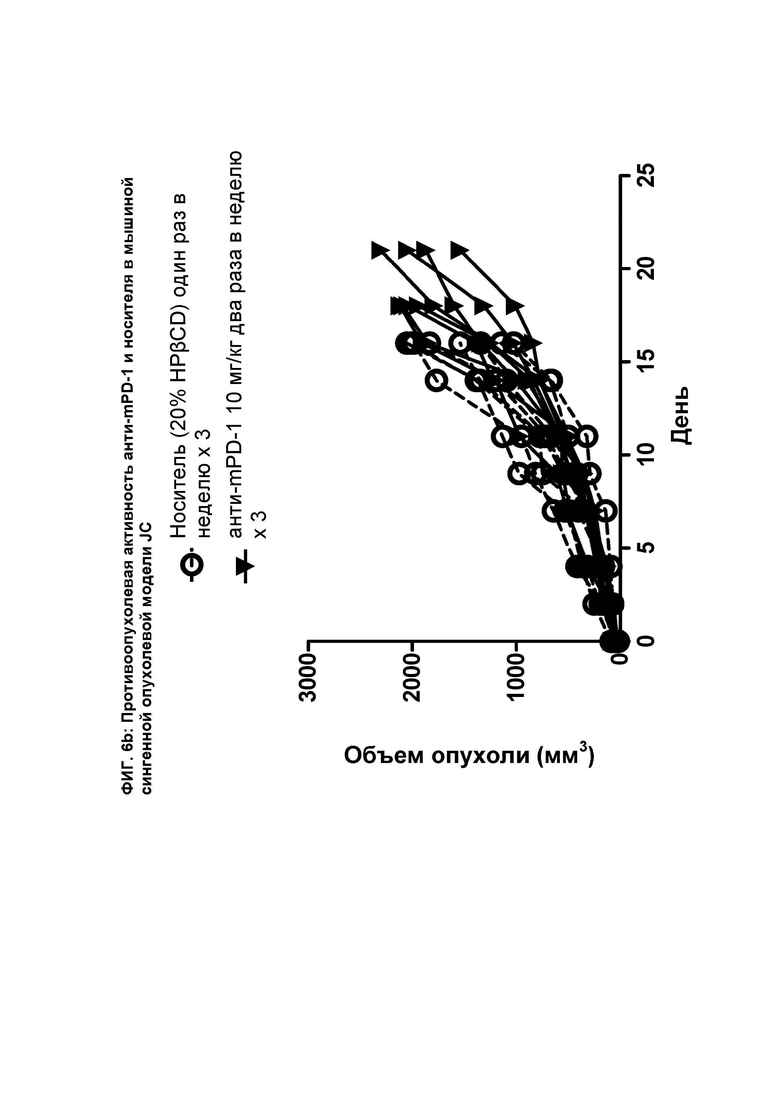
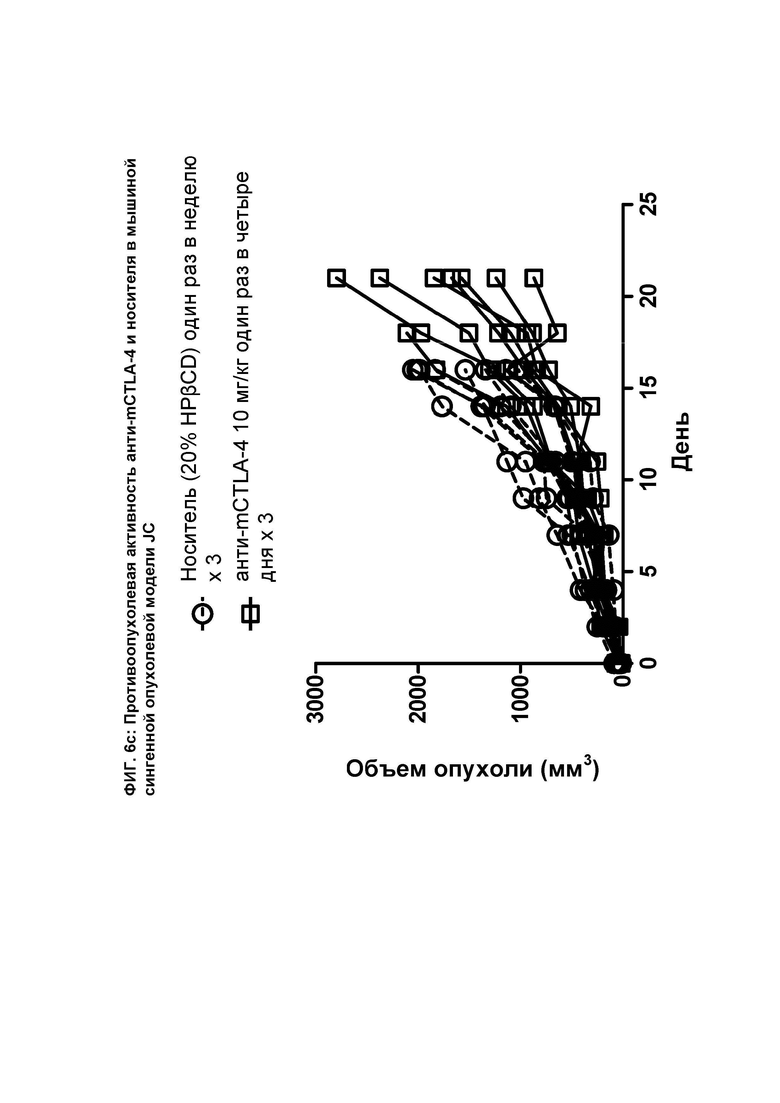
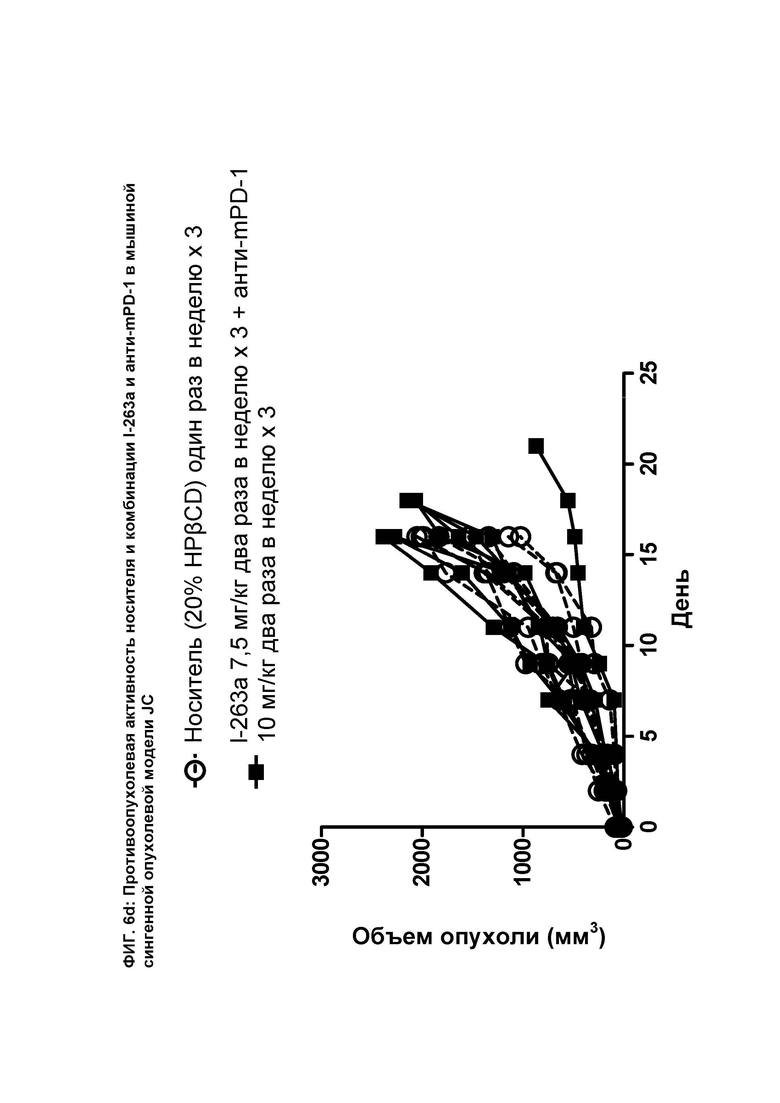
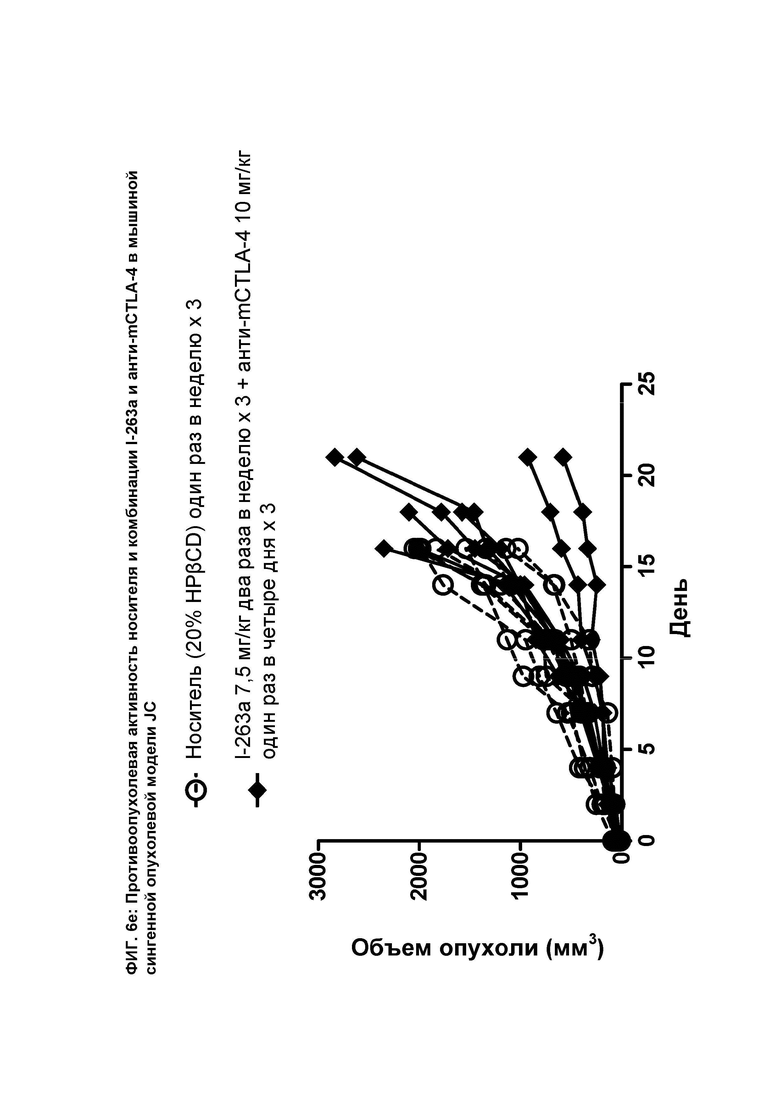
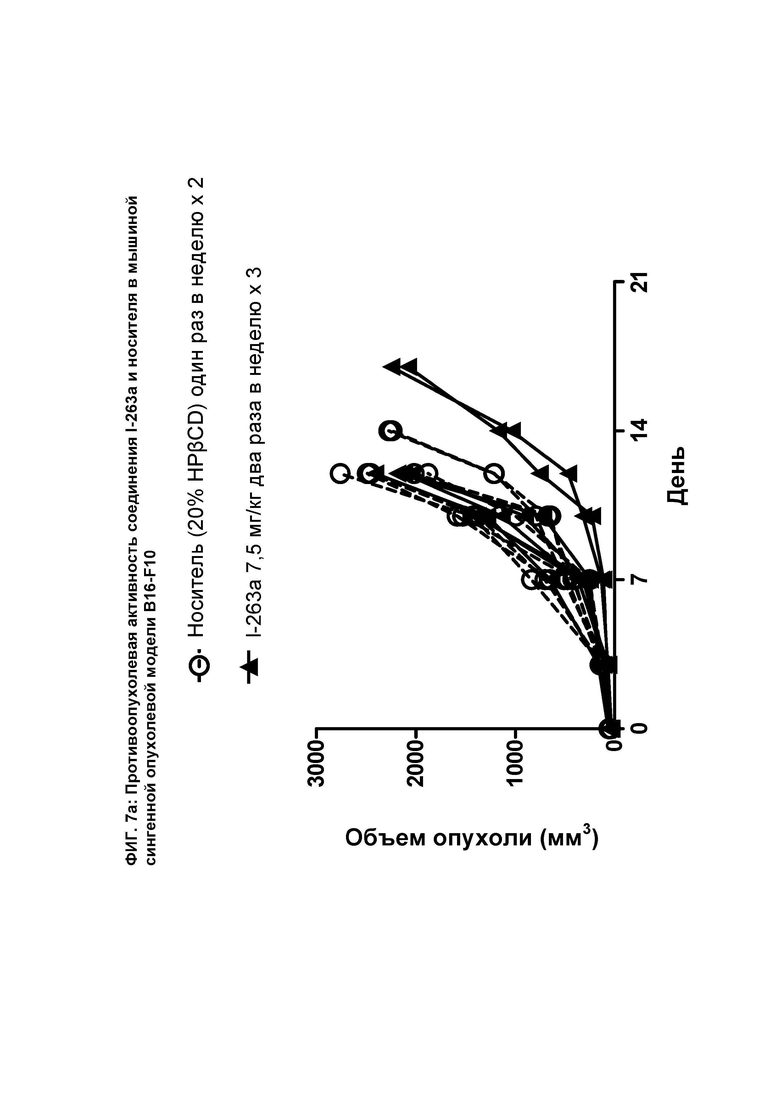
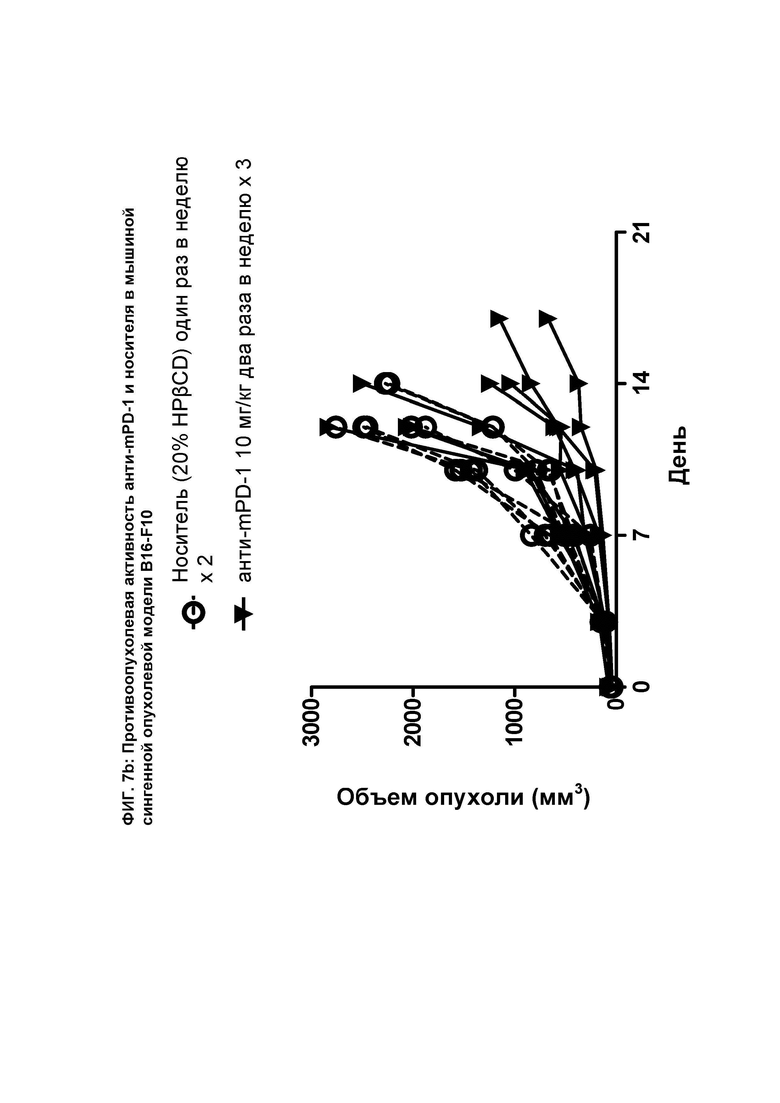
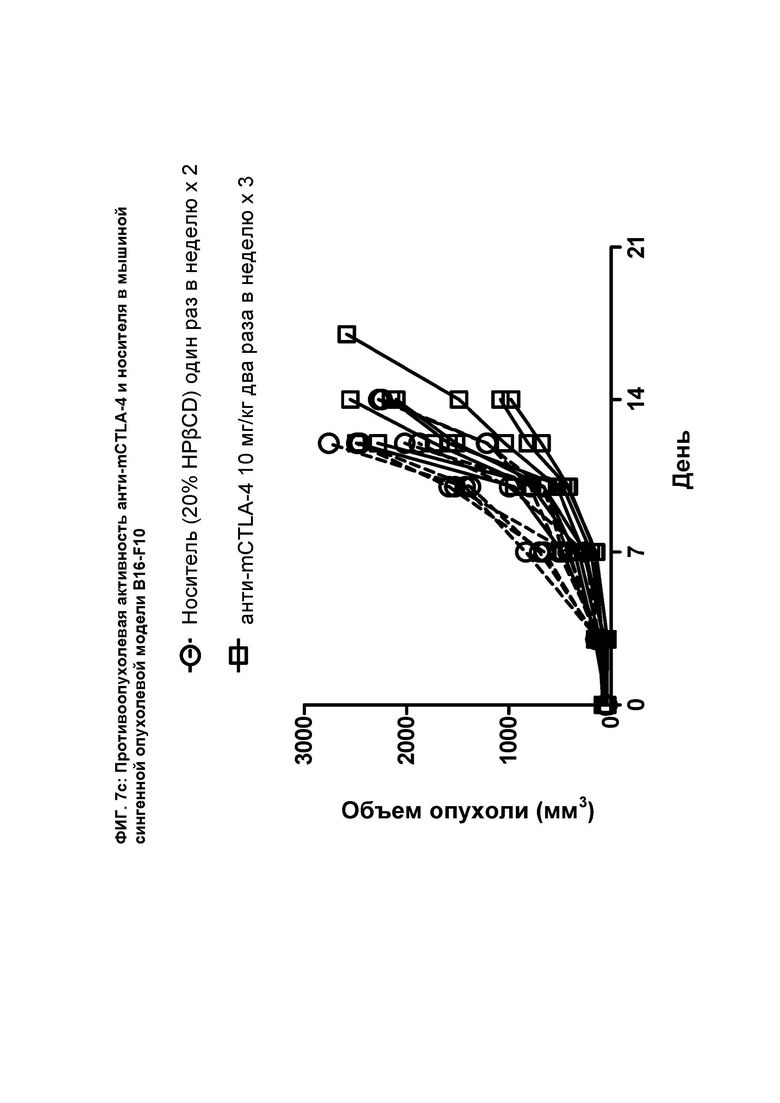
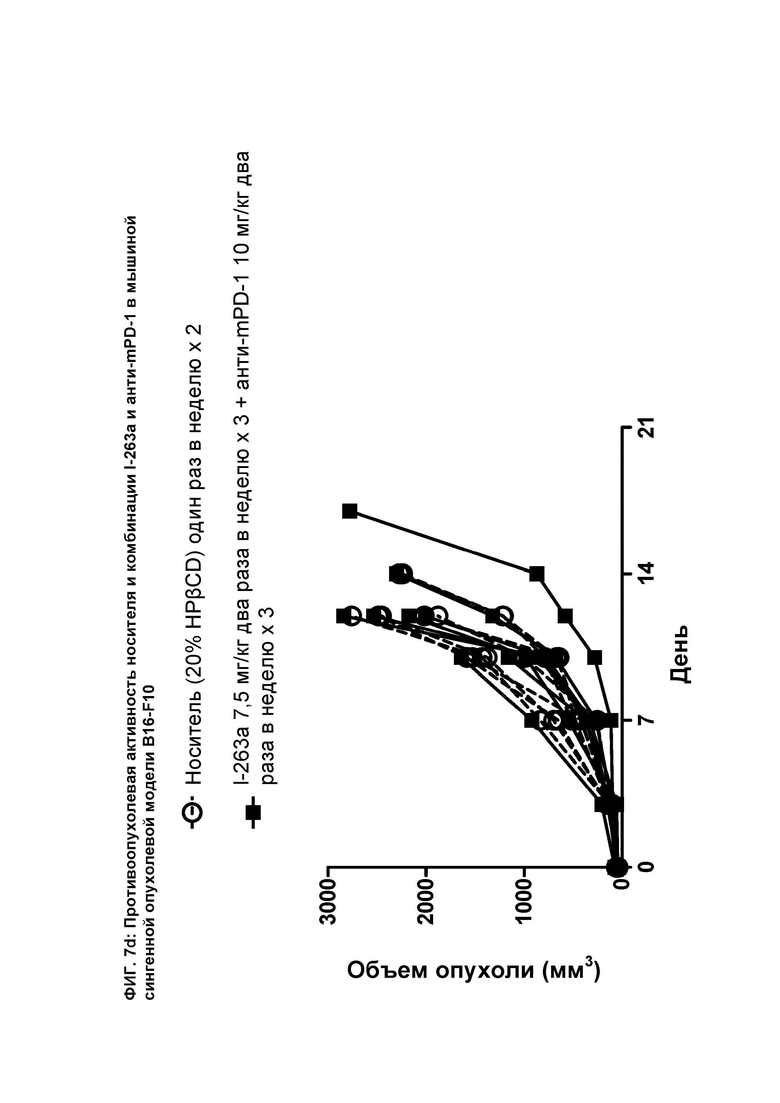
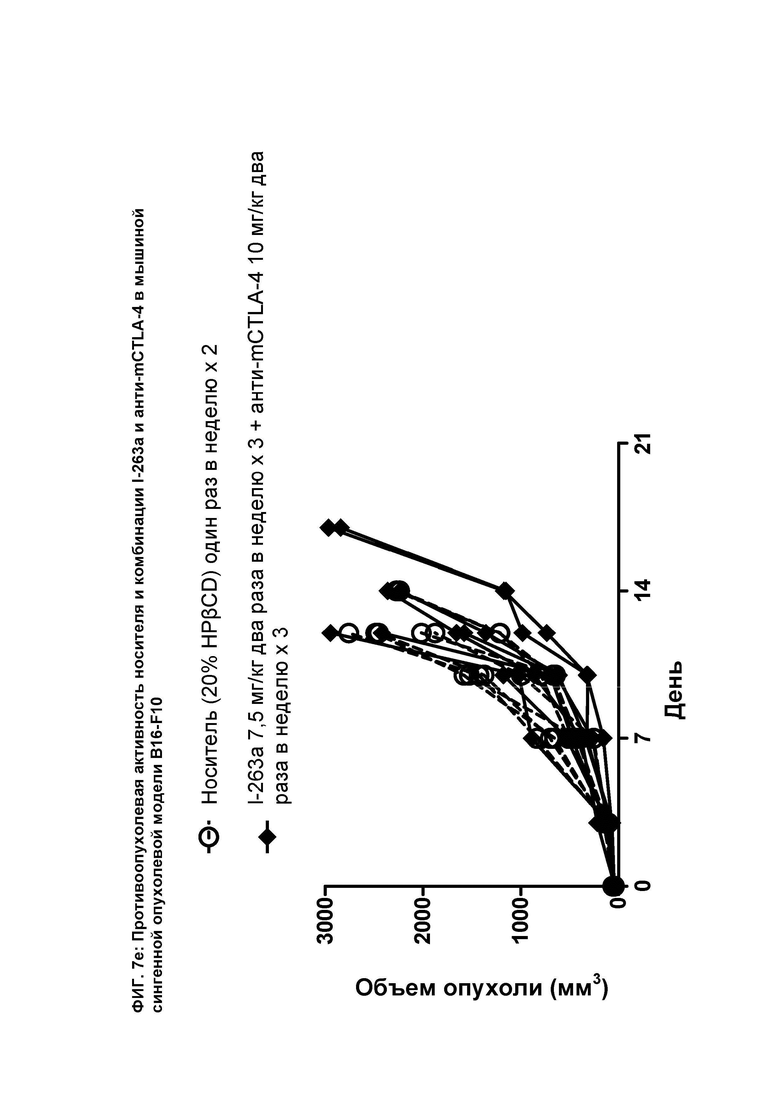
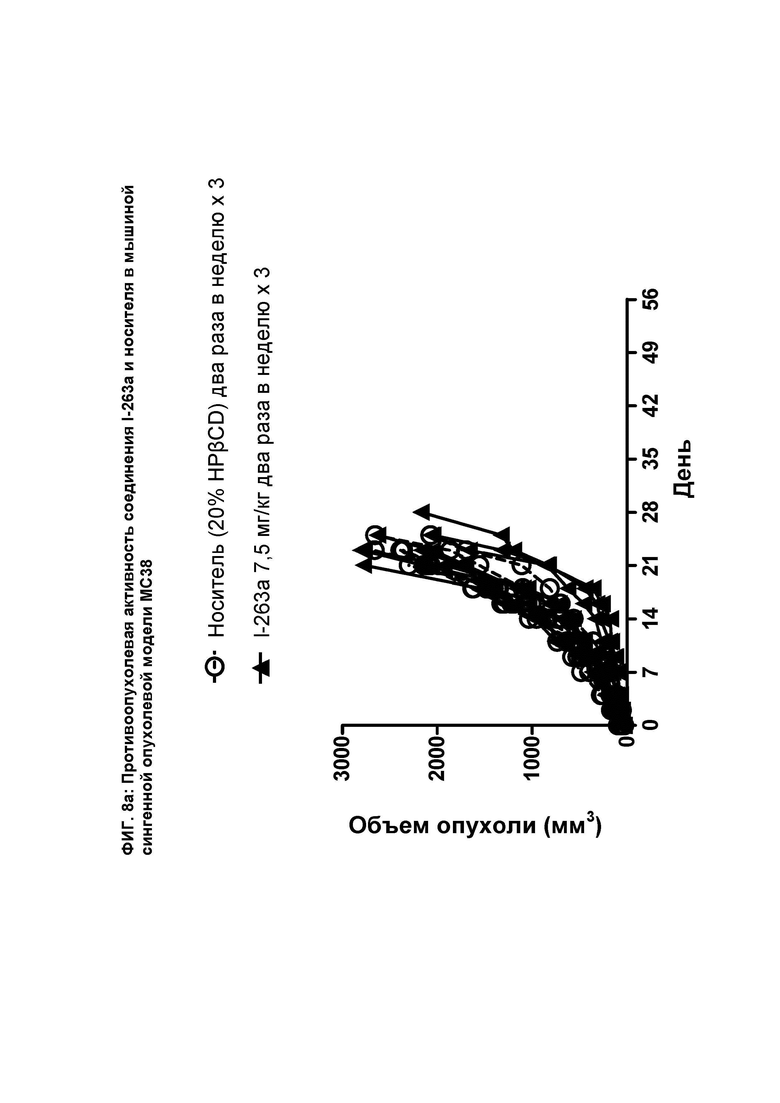
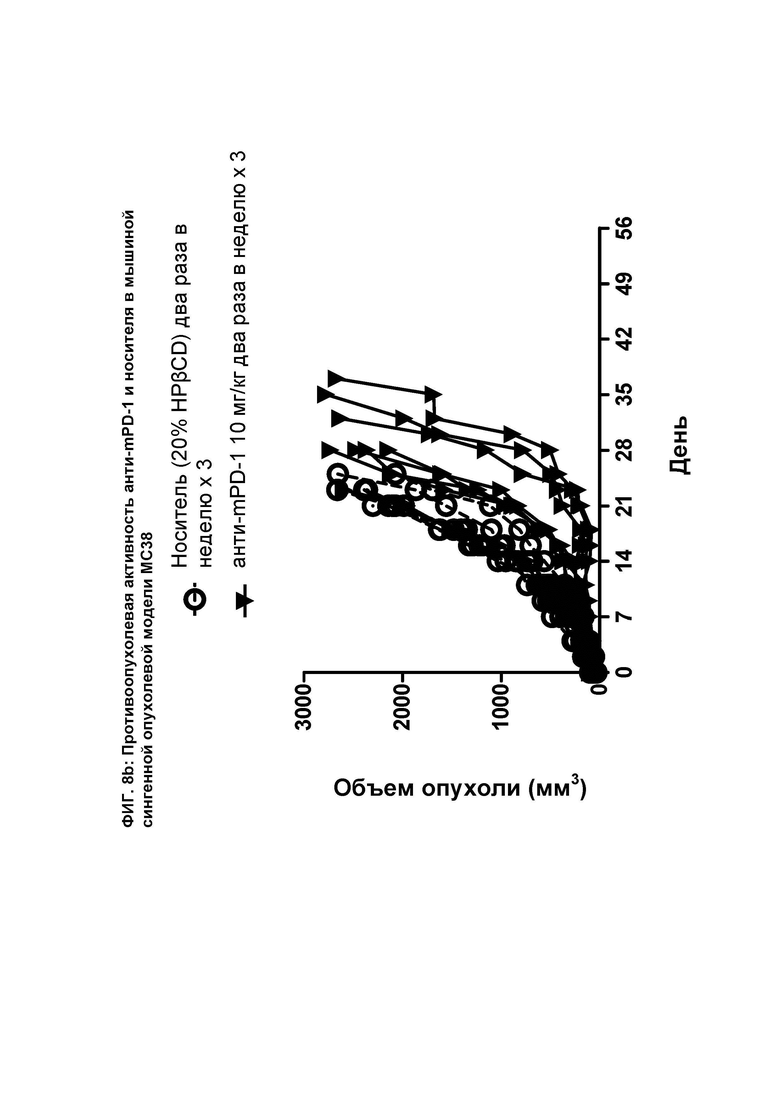
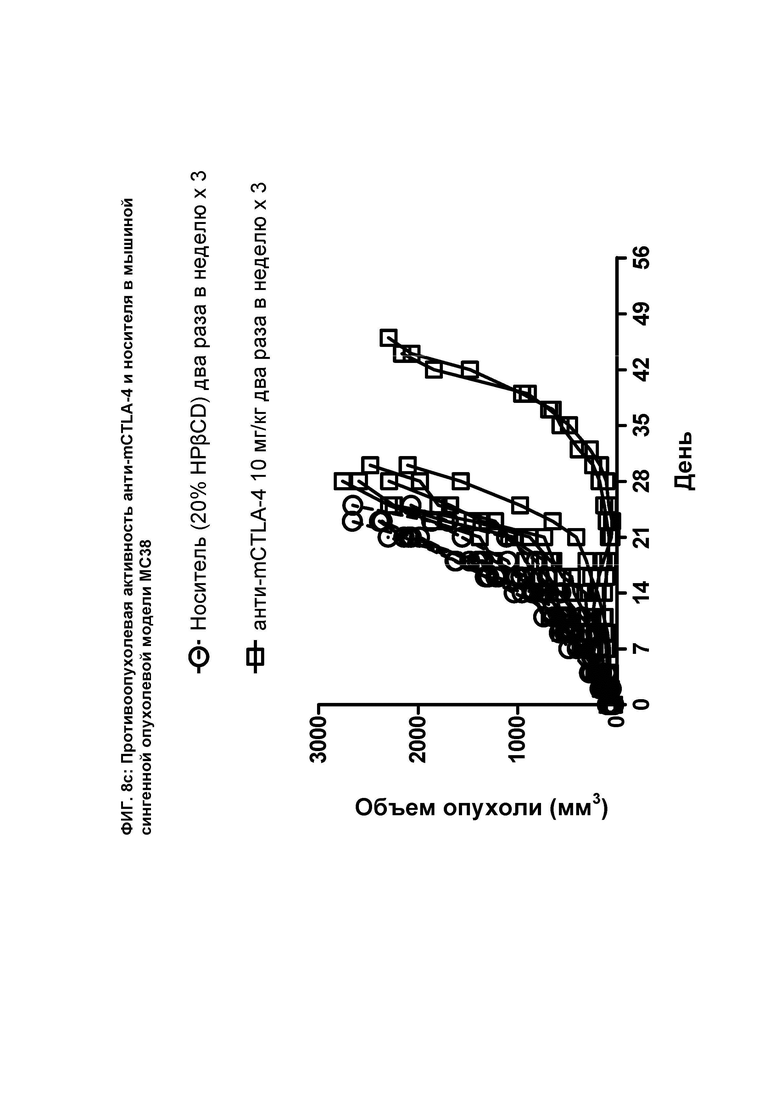
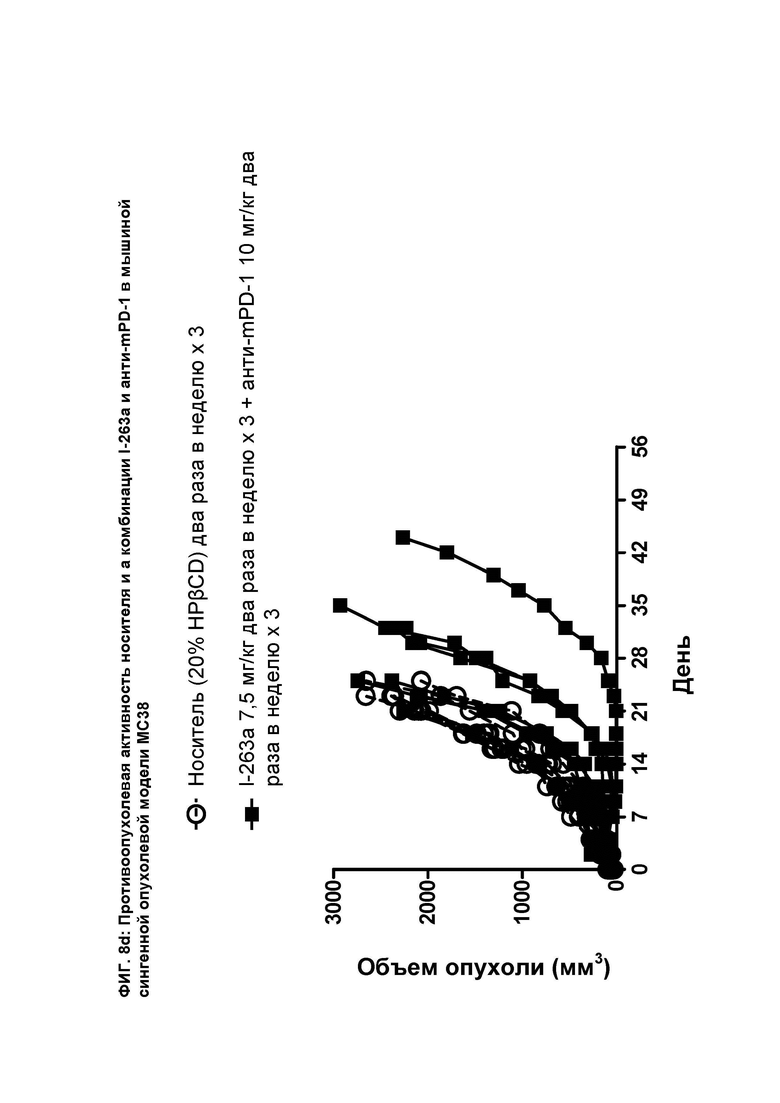
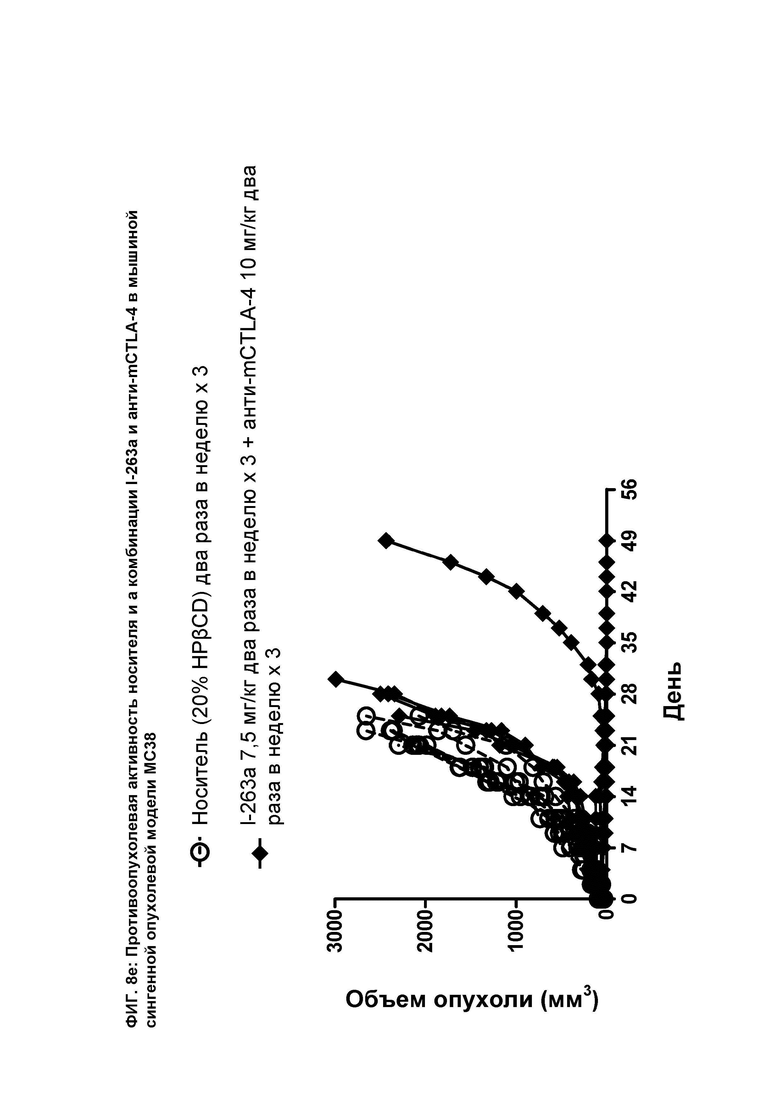
Настоящее изобретение относится к применению [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамата или его фармацевтически приемлемой соли для лечения пациента, страдающего раком, в комбинации с ингибитором контрольных точек, выбранным из антитела к PD-1 и антитела к CTLA-4, причем рак выбран из колоректального рака, лимфомы, лейкоза и рака легкого. Настоящее изобретение обеспечивает синергический эффект комбинации [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамата (соединения I-263a) с ингибитором контрольных точек. 31 з.п. ф-лы, 34 ил., 2 пр.
1. Применение [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамата или его фармацевтически приемлемой соли для лечения пациента, страдающего раком, в комбинации с ингибитором контрольных точек, выбранным из антитела к PD-1 и антитела к CTLA-4, причем рак выбран из колоректального рака, лимфомы, лейкоза и рака легкого.
2. Применение по п. 1, в котором ингибитор контрольных точек представляет собой антитело к PD-1.
3. Применение по п. 2, в котором антитело к PD-1 выбрано из группы, состоящей из ниволумаба, пембролизумаба, ламбролизумаба, пидилизумаба, BMS-936559 и AMP-224.
4. Применение по п. 3, в котором антитело к PD-1 представляет собой пембролизумаб.
5. Применение по п. 1, в котором ингибитор контрольных точек представляет собой антитело к CTLA-4.
6. Применение по п. 5, в котором антитело к CTLA-4 выбрано из группы, состоящей из ипилимумаба и тремелимумаба.
7. Применение по любому из пп. 1-6, в котором [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его фармацевтически приемлемую соль вводят перорально.
8. Применение по любому из пп. 1-6, в котором [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его фармацевтически приемлемую соль вводят внутривенно.
9. Применение по любому из пп. 1-6, в котором [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его фармацевтически приемлемую соль вводят путем внутривенной инфузии.
10. Применение по любому из пп. 1-9, в котором [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат и ингибитор контрольных точек вводят одновременно.
11. Применение по любому из пп. 1-9, в котором [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат и ингибитор контрольных точек вводят последовательно в отдельных фармацевтических композициях.
12. Применение по любому из пп. 1-11, в котором рак представляет собой PD-1-положительный рак, PD-L1-положительный рак или CTLA-4-положительный рак.
13. Применение по п. 1, в котором рак легкого представляет собой немелкоклеточный рак легкого или мелкоклеточный рак легкого.
14. Применение по п. 13, в котором немелкоклеточный рак легкого представляет собой метастатический немелкоклеточный рак легкого, метастатический плоскоклеточный немелкоклеточный рак легкого или метастатический неплоскоклеточный немелкоклеточный рак легкого.
15. Применение по п. 1, в котором лимфома представляет собой классическую лимфому Ходжкина или первичную B-крупноклеточную лимфому средостения.
16. Применение по п. 1, в котором колоректальный рак представляет собой колоректальный рак с микросателлитной стабильностью.
17. Применение по любому из пп. 1-16, в котором [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его фармацевтически приемлемую соль вводят один раз в две недели, один раз в неделю, два раза в неделю, три раза в неделю или ежедневно.
18. Применение по п. 17, в котором [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его фармацевтически приемлемую соль вводят два раза в неделю.
19. Применение по п. 17, в котором [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его фармацевтически приемлемую соль вводят один раз в неделю.
20. Применение по любому из пп. 1-16, в котором [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его фармацевтически приемлемую соль вводят в дни 1, 4, 8 и 11 в рамках 21-дневного цикла.
21. Применение по любому одному из пп. 1-16, в котором ингибитор контрольных точек вводят один раз в двенадцать недель, один раз в четыре недели, один раз в три недели, один раз в две недели, один раз в неделю, два раза в неделю, три раза в неделю или ежедневно.
22. Применение по п. 21, в котором ингибитор контрольных точек вводят один раз в две недели.
23. Применение по п. 21, в котором ингибитор контрольных точек вводят один раз в три недели.
24. Применение по п. 21, в котором ингибитор контрольных точек вводят один раз в четыре недели.
25. Применение по п. 21, в котором ингибитор контрольных точек вводят один раз в двенадцать недель.
26. Применение по любому из пп. 1-16, в котором ингибитор контрольных точек вводят в день 1 цикла лечения.
27. Применение по п. 26, в котором цикл лечения составляет 14 дней, 21 день, 28 дней или 84 дня.
28. Применение по любому из пп. 1-16, в котором [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его фармацевтически приемлемую соль и ингибитор контрольных точек вводят одновременно один раз в двенадцать недель, один раз в четыре недели, один раз в три недели, один раз в две недели, один раз в неделю, два раза в неделю, три раза в неделю, ежедневно или в дни 1, 4, 8 и 11 в рамках 21-дневного цикла.
29. Применение по любому из пп. 1-16, в котором:
[(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его фармацевтически приемлемую соль вводят один раз в две недели, один раз в неделю, два раза в неделю, три раза в неделю, ежедневно или в дни 1, 4, 8 и 11 в рамках 21-дневного цикла; и
ингибитор контрольных точек вводят отдельно один раз в двенадцать недель, один раз в четыре недели, один раз в три недели, один раз в две недели, один раз в неделю, два раза в неделю, три раза в неделю или ежедневно.
30. Применение по любому из пп. 1-16, в котором:
[(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его фармацевтически приемлемую соль вводят в дни 1, 4, 8 и 11 в рамках 21-дневного цикла; и
ингибитор контрольных точек вводят отдельно в день 1 в рамках 21-дневного цикла.
31. Применение по п. 1, в котором [(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его фармацевтически приемлемую соль вводят в количестве 90 мг каждый день дозирования.
32. Применение по п. 1, в котором:
ингибитор контрольных точек представляет собой пембролизумаб;
[(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его фармацевтически приемлемую соль вводят в количестве 90 мг каждый день дозирования;
[(1R,2S,4R)-4-{[5-({4-[(1R)-7-хлор-1,2,3,4-тетрагидроизохинолин-1-ил]-5-метил-2-тиенил}карбонил)пиримидин-4-ил]амино}-2-гидроксициклопентил]метилсульфамат или его фармацевтически приемлемую соль вводят дважды в неделю в течение одного или более циклов лечения, с последующим введением один раз каждую неделю в течение одного или более циклов лечения; и
пембролизумаб вводят отдельно в количестве 200 мг один раз каждые три недели.
| US 20180311239 A1, 01.11.2018 | |||
| WO 2018154529 A1, 30.08.2018 | |||
| WO 2017059224 A3, 06.04.2017 | |||
| WO 2017139231 A1, 17.08.2017. |
Авторы
Даты
2024-11-12—Публикация
2020-02-27—Подача