Область техники
Группа изобретений относится к области биотехнологии, в частности к рекомбинантным нуклеиновым кислотам, которые могут быть использованы при производстве препаратов на основе мРНК.
Уровень техники
Препараты на основе рибонуклеиновой кислоты (мРНК), особенно мРНК-вакцины, широко зарекомендовали себя как многообещающая стратегия лечения в иммунотерапии. Исключительные преимущества мРНК-вакцин, в том числе их высокая эффективность, сниженная частота и тяжесть, побочных реакций, а также относительно низкие затраты на производство, объясняют большое количество доклинических и клинических испытаний мРНК-вакцинных препаратов против различных инфекционных заболеваний и онкологических заболеваний. Недавние технологические достижения смягчили некоторые проблемы, которые препятствуют разработке мРНК-вакцины, такие как низкая эффективность, которая существует как при трансляции генов, так и при доставке in vivo. Эффективность вакцины в первую очередь зависит от стабильности и структуры разработанной мРНК.
Существуют различные подходы к решению проблемы повышения стабильности и/или трансляционной активности мРНК. Одним из таких подходов является использование гетерологичных нетранслируемых областей РНК, способных стабилизировать мРНК и/или повышать эффективность трансляции, что, в конечном итоге должно приводить к увеличению количества синтезируемого белка.
Нетранслируемые области (UTR или НТО) представляют собой некодирующие части последовательности мРНК, расположенные выше (5'-НТО) и ниже (3'-НТО) кодирующей области мРНК. Известно, что НТО связаны с процессами репликации и трансляции мРНК, и они, взаимодействуя с РНК-связывающими белками, могут влиять на устойчивость мРНК к факторам деградации и на эффективность трансляции [Schlake Т, Thess А, Fotin-Mleczek М, et al. Developing mRNA-vaccine technologies. RNA Biol. 2012 Nov; 9(11):1319-30. doi: 10.4161/rna.22269; Linares-Fernandez S, Lacroix C, Exposito JY, et al. Tailoring mRNA Vaccine to Balance Innate/Adaptive Immune Response. Trends Mol Med. 2020 Mar; 26(3):311-323. doi: 10.1016/j.molmed.2019.10.002; Xu S, Yang K, Li R, Zhang L. mRNA Vaccine Era-Mechanisms, Drag Platform and Clinical Prospection. Int J Mol Sci. 2020 Sep 9; 21(18):6582. doi: 10.3390/ijms21186582; Kim SC, Sekhon SS, Shin WR, et al. Modifications of mRNA vaccine structural elements for improving mRNA stability and translation efficiency. Mol Cell Toxicol. 2022; 18(1):l-8. doi: 10.1007/s13273-021-00171-4].
Некоторые регуляторные элементы могут усиливать экспрессию белка на уровне инициации трансляции и на посттранскрипционном уровне [Kaufman RJ. Identification of the components necessary for adenovirus trans1ational control and their utilization in cDNA expression vectors. Proc Natl Acad Sci USA. 1985 Feb; 82(3):689-93. doi: 10.1073/pnas.82.3.689. PMID: 2983309; PMCID: РМС397111].
Среди наиболее известных нетранслируемых последовательностей, которые приводят к высокой трансляционной эффективности, можно выделить последовательности глобиновых генов. В частности, для повышения трансляционной эффективности гетерологичных мРНК используются последовательности человеческого α и β-глобина [Babendure JR, Babendure JL, Ding JH, et al. Control of mammalian trans1ation by mRNA structure near caps. RNA. 2006 May; 12(5):851-61. doi: 10.1261/rna.2309906; Kozak M. Features in the 5' non-coding sequences of rabbit alpha and beta-globin mRNAs that affect trans1ational efficiency. JMolBiol. 1994 Jan 7; 235(1):95-110. doi: 10.1016/S0022-2836(05)80019-1] и кроличьего β-глобина [Annweiler A, Hipskind RA, Wirth T. A strategy for efficient in vitro trans1ation of cDNAs using the rabbit beta-globin leader sequence. Nucleic Acids Res. 1991 Jul 11; 19(13):3750. doi: 10.1093/паг/19.13.3750]. Считается, что 5'-HTO кроличьего β-глобина обеспечивает эффективную зависимую от кэпа трансляцию и не содержит каких-либо вторичных структур или элементов последовательности, которые могут негативно влиять на трансляцию [Kozak М. Features in the 5' non-coding sequences of rabbit alpha and beta-globin mRNAs that affect trans1ational efficiency. J Mol Biol. 1994 Jan 7; 235(1):95-110. doi: 10.1016/S0022-2836(05)80019-1]. Регуляторные последовательности глобиновых генов человека также используются в качестве 3'-НТО и обеспечивают высокую стабильность и трансляционную активность мРНК [Leppek К, Byeon GW, Kladwang W, et al. Combinatorial optimization of mRNA structure, stability, and trans1ation for RNA-based therapeutics. Nat Commun. 2022 Mar 22; 13(1): 1536. doi: 10.1038/s41467-022-28776-w].
Помимо регуляторных элементов глобиновых генов человека, в качестве гетерологичных НТО также используют последовательности 5'-НТО белка теплового шока 70 (БТШ70 или HSP70) и гистона НЗ [Rubtsova MP, Sizova DV, Dmitriev SE, et al. Distinctive properties of the 5'-untrans1ated region of human hsp70 mRNA. J Biol Chem. 2003 Jun 20; 278(25):22350-6. doi: 10.1074/jbc.M303213200, Morris T, Marashi F, Weber L, et al. Involvement of the 5'-leader sequence in coupling the stability of a human H3 histone mRNA with DNA replication. Proc Natl Acad Sci USA. 1986 Feb;83(4):981-5. doi: 10.1073/pnas.83.4.981]. Способность 5'-HTO БТШ70 обеспечивать высокий уровень трансляции гетерологичной мРНК, вероятно, связана с наличием IRES-подобных элементов и оптимальным GC составом [Schlake Т, Thess А, Fotin-Mleczek М, et al. Developing mRNA-vaccine technologies. RNA Biol. 2012 Nov; 9(11):1319-30. doi: 10.4161 /rna.22269, Rubtsova MP, Sizova DV, Dmitriev SE, et al. Distinctive properties of the 5'-untrans1ated region of human hsp70 mRNA. J Biol Chem. 2003 Jun 20; 278(25):22350-6. doi: 10.1074/jbc.M303213200]. Эффект 5'-НТО БТШ70 наблюдался в нескольких различных клеточных линиях [10.1046/j.1432-1327.2001.02064.x], показывая, что воздействие 5'-НТО, вероятно, не является специфичным для типа клеток. Известна последовательность 5'-НТО кроличьего β-глобина [GenBank: V00882.1, 224-276 позиции].
Суммируя данные по природным 3'-НТО, можно сделать вывод, что для усиления трансляционной эффективности гетерологичных мРНК часто используются регуляторные элементы конститутивно (постоянно) экспрессирующихся генов.
mtRNR1 представляет собой митохондриальную некодирующую 12S рРНК, которая участвует в трансляции 13 генов в митохондриях, кодирующих белки [Chinnery PF, Hudson G. Mitochondrial genetics. Br Med Bull. 2013; 106(1):135-59. doi: 10.1093/bmb/ldt017].
AES является отдельным членом семейства Groucho/Transducin-подобных энхансеров расщепленных генов, регулирует транскрипционную активность рецепторов андрогенов и передачу сигналов Notch и Wnt и действует как ген-супрессор опухолей [Costa AM, Pereira-Castro I, Ricardo E, et al. GRG5/AES interacts with T-cell factor 4 (TCF4) and downregulates Wnt signaling in human cells and zebrafish embryos. PLoS One. 2013 Jul 1; 8(7):e67694. doi: 10.1371/journal.pone.0067694;].
Орландини фон Ниссен с соавторами показали, что 3'-НТО, содержащие mtRNR1 и AES в любом порядке, способствуют повышенной экспрессии расположенного выше гена [патенты РФ №2720934 и 2783165; Orlandini von Niessen AG, Poleganov MA, Rechner C, et al. Improving mRNA-Based Therapeutic Gene Delivery by Expression-Augmenting 3' UTRs Identified by Cellular Library Screening. Mol Ther. 2019 Apr 10; 27(4):824-836. doi: 10.1016/j.ymthe.2018.12.011].
Существует мало данных об использовании 3'-НТО вируса энцефаломиокардита (EMCV), однако в статье: Marzbany М and Rasekhian М Effect of encephalomyocarditis virus 3'Untrans1ated region on GFP transient expression: implications in recombinant protein production. Boletin Latinoamericano у del Caribe de Plantas Medicinales у Aromáticas, 2020, 19 (6): 542-554 раскрыто использование 3'-НТО EMCV для увеличения эффективности трансляции гетерологичного гена. Авторы использовали в качестве 3'-НТО последовательность 3'-НТО EMCV, представляюгцую собой 122-нуклеотидную последовательность, взятую из позиции 7713-7835 генома EMCV, последовательность NC_001479 в базе данных NCBI https://www.ncbi.nlm.nih.gov, дата обращения 14.09.2023/
В настоящее время в мире известны мРНК-вакцины, дошедшие до стадии коммерческого использования, двух производителей: ModeRNA и BioNTech.
В мРНК-вакцинах компании ModeRNA используют:
5'-НТО с последовательностью Seq Id №:3 [источники: US10881730B2 Seq Id No.:181; Jeong D.-E., McCoy M., Amies K., et al. Assemblies-of-Putative-SARS-CoV2-Spike-Encoding-mRNA-Sequences-for-Vaccines-BNT-162b2-and-mRNA-1273, доступна онлайн по адресу: https://virological.org/t/assemblies-of-putative-sars-cov2-spike-encoding-mrna-sequences-for-vaccines-bnt-162b2-and-mina-1273/663, дата обращения 21.08.2023; Xia X. Detailed Dissection and Critical Evaluation of the Pfizer/BioNTech and ModeRNA mRNA Vaccines. Vaccines (Basel). 2021 Jul 3; 9(7):734. doi: 10.3390/vaccmes9070734];
3'-НТО с последовательностью Seq Id №:4 [Jeong D.-E., McCoy M., Artiles K., et al. Assemblies-of-Putative-SARS-CoV2-Spike-Encoding-mRNA-Sequences-for-Vaccines-BNT-162b2-and-mRNA-1273, доступна онлайн по адресу: https://virological.org/t/assemblies-of-putative-sars-cov2-spike-encoding-mrna-sequences-for-vaccines-bnt-162b2-and-mrna-1273/663, дата обращения 21.08.2023].
В мРНК-вакцинах компании BioNTech используют:
5'-НТО с последовательностью Seq Id №:6 и 3'-НТО с последовательностью Seq Id №: 7 [источники: BioNTech from World Health Organization Messenger RNA Encoding the Full-Length SARS-CoV-2 Spike Glycoprotein. [(accessed on 7 June 2021)];2020 Available online: https://web.archive.org/web/20210105162941/https://mednet-commimities.net/irm/db/media/docs/11889.doc; Jeong D.-E., McCoy M., Artiles K., et al. Assemblies-of-rAiMive-SARS-CoV2-Spike-Encoding-mRNA-Sequences-for-Vaccines-BNT-162b2-and-niRNA-1273, доступна онлайн по адресу: https://virological.org/t/assemblies-of-putative-sars-cov2-spike-encoding-mma-sequences-for-vaccines-bnt-162b2-and-mrna-1273/663, дата обращения 21.08.2023; Xia X. Detailed Dissection and Critical Evaluation of the Pfizer/BioNTech and ModeRNA mRNA Vaccines. Vaccines (Basel). 2021 Jul 3; 9(7):734. doi: 10.3390/vaccmes9070734]. 3'-НТО состоит из последовательности 3'-НТО гена AES и последовательности 3'-НТО mtRNR1.
Помимо применения природных регуляторных элементов, в настоящее время проводится интенсивный поиск оптимальной искусственной, не встречающейся в природе, последовательности НТО [Cao J, Novoa ЕМ, Zhang Z, et al. High-throughput 5' UTR engineering for enhanced protein production in non-viral gene therapies. Nat Commun. 2021 Jul 6; 12(1):4138. doi: 10.103 8/s41467-021-24436-7].
Несмотря на интенсивный поиск регуляторных элементов для использования в составе гетерологичных рекомбинантных РНК, уровень трансляции белка на матрице мРНК с наилучшими регуляторными элементами, драматически снижается уже через 24 часа после введения препарата мРНК [патенты РФ №2720934 и 2783165]. Поэтому поиск оптимальной комбинации 5'- и 3'-НТО, которая будет более эффективна по сравнению с существующими аналогами, является приоритетной задачей.
Технической задачей, на решение которой направлено настоящее изобретение, является решение как минимум одной из вышеуказанных в уровне техники проблем.
Сущность изобретения
Одной из возможных технических задач, на решение которой может быть направлено настоящее изобретение, являлось создание рекомбинантной РНК, обладающей повышенной стабильностью и/или эффективностью трансляции, а также средств для получения такой РНК.
Недостаточная трансляционная эффективность молекул матричной РНК, приводит к низкому уровню экспрессии целевого белка. За эффективность трансляции отвечают регуляторные элементы РНК: 5'- и 3'-нетранслируемые области (НТО). Оптимальная комбинация регуляторных элементов позволяет значительно увеличить экспрессию целевого белка.
Технический результат, достигаемый при осуществлении настоящего изобретения, состоит в статистически значимом увеличении количества белка, транслируемого с нуклеиновой кислоты, содержащей Seq Id №:1 в составе 3'-НТО и Seq Id №:2 в составе 3'-НТО, по сравнению с количеством белка, транслируемого с нуклеиновой кислоты, содержащей 5'- и 3'-НТО, используемые в составе мРНК-вакцин известных производителей: ModeRNA или BioNTech, через 72 часа после введения в клетки, и по сравнению с количеством белка, транслируемого с нуклеиновой кислоты, содержащей 5'-и 3'-НТО ModeRNA через 48 часов после введения мышам.
Задача может решаться созданием молекулы РНК, содержащей комбинацию нетранслируемых элементов, активных в отношении эффективности трансляции и/или стабильности нуклеиновой кислоты.
Задача может решаться тем, что создана нуклеиновая кислота, содержащая, в направлении транскрипции 5'→3':
(а) промотор;
(б) последовательность нуклеиновой кислоты, которая, будучи транскрибированной под контролем промотора (а), кодирует 5'-нетранслируемую область транскрипта;
(в) транскрибируемую последовательность нуклеиновой кислоты, кодирующую пептид или белок;
(г) последовательность нуклеиновой кислоты, которая, будучи транскрибированной под контролем промотора (а), кодирует 3'-нетранслируемую область транскрипта,
причем упомянутая 3'-нетранслируемая область содержит последовательность Seq Id №:1, а упомянутая 3'-нетранслируемая область содержит последовательность Seq Id №:2,
где последовательности нуклеиновой кислоты (б)-(г) под контролем промотора (а) могут быть транскрибированы с образованием общего транскрипта, в котором последовательности нуклеиновой кислоты, транскрибированные с последовательностей нуклеиновой кислоты (б) и (г), являются активными в отношении повышения эффективности трансляции и/или стабильности последовательности нуклеиновой кислоты, транскрибированной с транскрибируемой последовательности нуклеиновой кислоты (в).
В одном из вариантов осуществления изобретения предлагается РНК с повышенной стабильностью и/или трансляционной эффективностью, получаемая в результате транскрипции с применением любого варианта молекулы нуклеиновой кислоты, описанного выше.
В одном из вариантов осуществления изобретения РНК с повышенной стабильностью содержит в направлении 5'→3':
(а) 5'-нетранслируемую область;
(б) последовательность нуклеиновой кислоты, кодирующую пептид или белок;
(в) 3'-нетранслируемую область,
причем упомянутая 5'-нетранслируемая область содержит последовательность Seq Id №:1, а упомянутая 3'-нетранслируемая область содержит последовательность Seq Id№: 2,
где последовательности нуклеиновой кислоты (а) и (в) являются активными в отношении повышения эффективности трансляции и/или стабильности последовательности нуклеиновой кислоты, кодирующей пептид или белок.
Нуклеиновая кислота по настоящему изобретению может быть использована для in vitro синтеза РНК, которая в дальнейшем может быть капсулирована в липидные наночастицы для получения РНК-вакцины.
Изобретение иллюстрируется следующими графическими материалами:
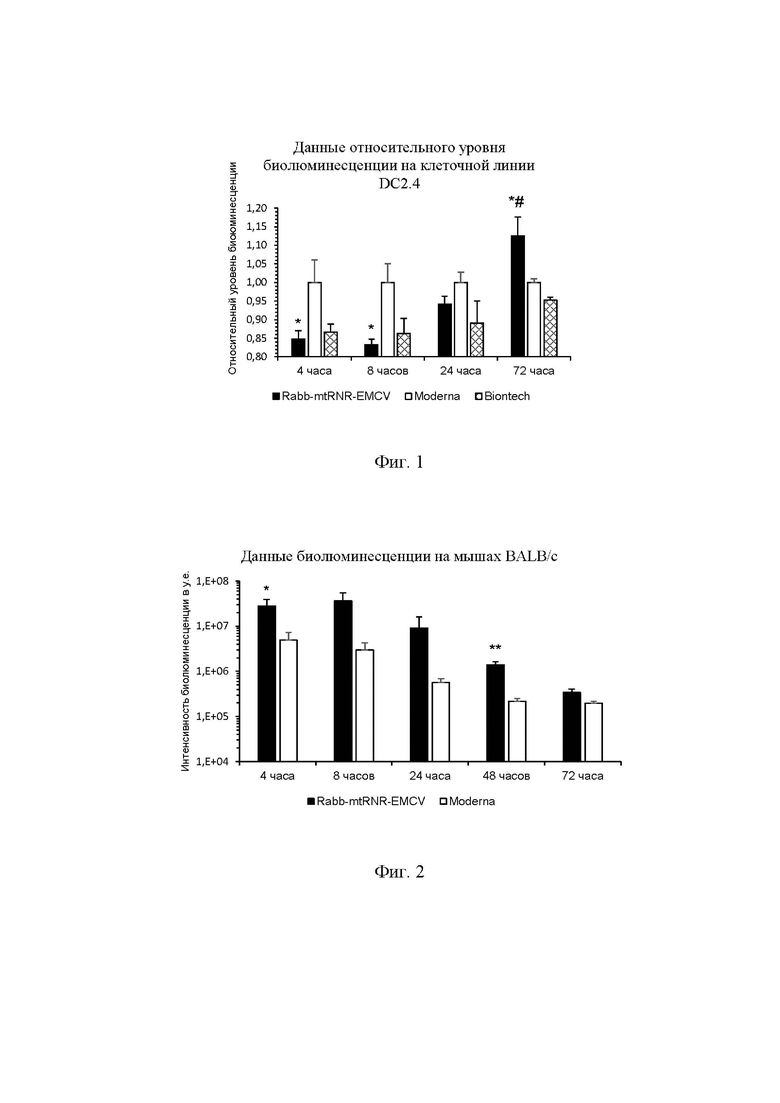
На Фиг. 1 представлены результаты оценки относительной биолюминесценции люциферазы, синтезированной с матричных РНК с различными вариантами 5'- и 3'-НТО в клеточной линии DC2.4.
Данные представлены как среднее ± стандартная ошибка среднего. Статистически достоверные различия обозначены:
по сравнению с мРНК ModeRNA * - p-values <0,05;
по сравнению с мРНК BioNTech # - p-values <0,05;
Условные обозначения: Rabb-mtRNR-EMCV - РНК с 5'-НТО, содержащей Seq Id No.: 1, и 3'-НТО, содержащей Seq Id No.: 2; Moderna - РНК, содержащая Seq Id No.: 3 в качестве 5'-HTO и Seq Id No.: 4 в качестве 3'-НТО; Biontech - РНК, содержащая Seq Id No.: 5 в качестве 5'-НТО и Seq Id No.: 6 в качестве 3'-НТО.
На Фиг. 2 представлены результаты прижизненного анализа абсолютной биолюминесценции люциферазы, синтезированной с матричных мРНК с различными вариантами 5'- и 3'-НТО в мышах линии Balb/c. Данные представлены как среднее ± стандартная ошибка среднего. Статистически достоверные различия по сравнению с мРНК с ModeRNA обозначены: * - р-values <0.05, ** - p-values<0.01, *** - p-values <0.001.
Условные обозначения: Rabb-mtRNR-EMCV - РНК с 5'-НТО, содержащей Seq Id No.: 1, и 3'-НТО, содержащей Seq Id No.: 2; Moderna - РНК, содержащая последовательность Seq Id No.: 3 в качестве 5'-НТО и Seq Id No.: 4 в качестве 3'-НТО.
Детальное описание изобретения
Если не указано иначе, предполагается, что все термины, обозначения и другие научные термины, используемые в данной заявке, имеют значения, которые обычно понимают специалисты в области, к которой относится настоящее изобретение. В некоторых случаях определения терминов с общепринятыми значениями приведены в данной заявке для ясности и/или для быстрой справки и понимания, и включение таких определений в настоящее описание не должно истолковываться как наличие существенного отличия значения термина от обычно подразумеваемого в данной области.
Кроме того, если по контексту не требуется иное, термины в единственном числе включают в себя термины во множественном числе, и термины во множественном числе включают в себя термины в единственном числе. Как правило, используемая классификация и методы культивирования клеток, молекулярной биологии, иммунологии, микробиологии, генетики, аналитической химии, химии органического синтеза, медицинской и фармацевтической химии, а также гибридизации и химии белка и нуклеиновых кислот, описанные в настоящем документе, хорошо известны специалистам и широко применяются в данной области. Ферментативные реакции и способы очистки осуществляют в соответствии с инструкциями производителя, как это обычно осуществляется в данной области, или как описано в настоящем документе.
Изобретение основано на неожиданном повышении эффективности трансляции на матрице мРНК, содержащей комбинацию модифицированной последовательности 5'-НТО транскрипта гена β-глобина кролика в составе 5'-нетранслируемой области мРНК и модифицированной последовательности 3'-нетранслируемой области генома EMCV в сочетании с 3'-нетранслируемой областью mtRNR1 в составе 3'-нетранслируемой области.
В одном из вариантов осуществления настоящего изобретения предлагается нуклеиновая кислота, содержащая, в направлении транскрипции 5'→3':
(а) промотор
(б) последовательность нуклеиновой кислоты, которая, будучи транскрибированной под контролем промотора (а), кодирует 5'-нетранслируемую область транскрипта;
(в) транскрибируемую последовательность нуклеиновой кислоты, кодирующую пептид или белок;
(г) последовательность нуклеиновой кислоты, которая, будучи транскрибированной под контролем промотора (а), кодирует 3'-нетранслируемую область транскрипта,
причем упомянутая 5'-нетранслируемая область содержит последовательность Seq Id №:1, а упомянутая 3'-нетранслируемая область содержит последовательность Seq Id №:2,
где последовательности нуклеиновой кислоты (б)-(г) под контролем промотора (а) могут быть транскрибированы с образованием общего транскрипта, в котором последовательности нуклеиновой кислоты, транскрибированные с последовательностей нуклеиновой кислоты (б) и (г), являются активными в отношении повышения эффективности трансляции и/или стабильности последовательности нуклеиновой кислоты, транскрибированной с транскрибируемой последовательности нуклеиновой кислоты (в).
Выражение «промотор» относится к последовательности нуклеиновой кислоты, которая распознается РНК-полимеразой как стартовая площадка для начала транскрипции.
Выражение «последовательность нуклеиновой кислоты, которая, будучи транскрибированной, кодирует 5'-нетранслируемую область транскрипта» относится к последовательности нуклеиновой кислоты антисмысловой цепи, кодирующей упомянутую 5'-нетранслируемую область, что предусматривает наличие у данной нуклеиновой кислоты смысловой цепи, содержащей ту же последовательность, что и у 5'-нетранслируемой области транскрипта, за исключением замены урацила на тимин. Аналогично, «последовательность нуклеиновой кислоты, которая, будучи транскрибированной, кодирует 3'-нетранслируемую область транскрипта» относится к последовательности нуклеиновой кислоты антисмысловой цепи, кодирующей упомянутую 3'-нетранслируемую область, что предусматривает наличие у данной нуклеиновой кислоты смысловой цепи, содержащей ту же последовательность, что и у 3'-нетранслируемой области транскрипта, за исключением замены урацила на тимин.
Термин «5'-нетранслируемая область» или «5'-НТО» относится к лидерной последовательности: некодирующему участку мРНК, располагающемуся сразу после промотора, но перед кодирующей областью. Используемый здесь термин «5'-нетранслируемая область» или «5'-НТО» также охватывает последовательность ДНК, которая может быть транскрибирована в последовательность РНК, представляющую собой 5'-нетранслируемую область.
Термин «3'-нетранслируемая область» (3'-НТО) относится к некодирующему участку РНК, располагающемуся после последовательности РНК, кодирующей белок или пептид интереса. Используемый здесь термин «3'-нетранслируемая область» или «3'-НТО» также охватывает последовательность ДНК, которая может быть транскрибирована в последовательность РНК, представляющую собой 3'-нетранслируемую область.
Термин «AES» относится к амино-концевому энхансеру Split, а также к гену AES. Белок, кодируемый этим геном, принадлежит к семейству белков groucho/TLE, может функционировать как гомо-олигомер или как гетеро-олигомер вместе с другими представителями семейства преимущественно для подавления экспрессии генов других представителей семейства.
Выражение «нетранслируемая область гена» относится к последовательности НТО как в самом гене, так и в его транскрипте.
Выражение «последовательность нуклеиновой кислоты 5'-нетранслируемой области гена кроличьего β-глобина» относится к последовательности нуклеиновой кислоты из 53 нуклеотидов (последовательность с 224 по 276 нуклеотид локуса V00882 гена β-глобина кролика согласно базе данных NCBI https://www.ncbi.nlm.nih.gov, дата обращения 13.09.2023).
Выражение «последовательность нуклеиновой кислоты 3'-нетранслируемой области гена AES» относится к последовательности нуклеиновой кислоты из 142 нуклеотидов (последовательность с 1218 по 1353 нуклеотид локуса ХМ_006722664 гена AES согласно базе данных NCBI https://www.ncbi.nlm.nih.gov, дата обращения 30.08.2023).
Термин «mtRNR1» относится митохондриальной 12S РНК, а также к гену mtRNR1, кодирующему упомянутую РНК.
Выражение «последовательность нуклеиновой кислоты 3'-нетранслируемой области mtRNR1» относится к последовательности транскрипта с 760 по 898 нуклеотид локуса OQ884979 митохондриальной ДНК согласно базе данных NCBI https://www.ncbi.nlm.nih, дата обращения 30.08.2023).
Последовательность Seq Id No.: 1 представляет собой модифицированную последовательность 5'-НТО транскрипта гена кроличьего β-глобина, состоящую из 52 нуклеотидов и отличающуюся от последовательности нуклеиновой кислоты 5'-нетранслируемой области гена кроличьего β-глобина делецией одного нуклеотида в 9-й позиции (232-й нуклеотид локуса V00882 гена β-глобина кролика согласно базе данных NCBI https://www.ncbi.nlm.nih.gov, дата обращения 13.09.2023.
Последовательность Seq Id No.: 2 представляет собой последовательность 3'-НТО mtRNR1, модифицированную делецией 75-го аденина, соединенную с последовательностью 3'-НТО EMCV, представляющей собой последовательности регуляторного элемента генома EMCV с 680 по 845 нуклеотид локуса NC_001479 согласно базе данных NCBI https://www.ncbi.nlm.nih, дата обращения 14.09.2023.
В одном из вариантов осуществления изобретения предлагается РНК с повышенной стабильностью и/или трансляционной эффективностью, получаемая в результате транскрипции с применением любого варианта молекулы нуклеиновой кислоты, описанного выше. РНК по настоящему изобретению может быть получена любым известным из уровня техники способом транскрипции с матрицы нуклеиновой кислоты. Специалисту в данной области известны такие способы, выбор конкретного не является существенным и зависит от целей и задач исследования или личных предпочтений специалиста.
В одном из вариантов осуществления изобретения РНК с повышенной стабильностью содержит в направлении 5'→3':
(а) 5'-нетранслируемую область;
(б) последовательность нуклеиновой кислоты, кодирующую пептид или белок;
(в) 3'-нетранслируемую область,
причем упомянутая 5'-нетранслируемая область содержит последовательность Seq Id №:1, а упомянутая 3'-нетранслируемая область содержит последовательность Seq Id №:2,
где последовательности нуклеиновой кислоты (а) и (в) являются активными в отношении повышения эффективности трансляции и/или стабильности последовательности нуклеиновой кислоты, кодирующей пептид или белок.
Нуклеиновая кислота по настоящему изобретению может быть использована для in vitro синтеза РНК, которая в дальнейшем может быть капсулирована в липидные наночастицы для получения РНК-вакцины.
Способы введения РНК по настоящему изобретению в живые клетки, векторы для такого введения, капсулирование в липидные наночастицы и сам состав липидных наночастиц, описываемые в примерах осуществления настоящего изобретения, не являются существенными, не влияют на технический результат изобретения и не ограничивают объем прав настоящего изобретения.
Использование нуклеиновой кислоты по настоящему изобретению, содержащей сочетание последовательностей Seq Id No.: 1 в составе 5'-НТО и Seq Id No.: 2 в составе 3'-НТО, демонстрирует увеличение количества транслируемого белка по сравнению с другими вариантами, в том числе коммерчески доступными, по меньшей мере через 72 часа после введения мРНК в клетки и через 48 часов после введения мРНК в мышей.
Сущность и промышленная применимость изобретения поясняется следующими примерами осуществления изобретения.
Пример 1. Получение конструкции 5'-НТО, содержащей последовательность Seq Id No.: 1, и 3'-НТО, содержащей последовательность Seq Id No.: 2.
В качестве вектора для вставки была использована плазмида pSmart (Lucigen, США), содержащая последовательность Т7 промотора, гена устойчивости к ампициллину и гена, кодирующего люциферазу светлячка (Photinus pyralis) и последовательность из 110 аденинов (поли(А)-хвост) после 3'-НТО.
Амплификацию целевой последовательности осуществляли путем сшивки фрагментов ДНК методом ПЦР с перекрывающимися праймерами. Затем методом ПЦР с перекрьшающимися праймерами ампликоны целевых последовательностей, кодирующих 5'-НТО и 3'-НТО, были соединены с последовательностью, кодирующей люциферазу светлячка (Photinus pyralis), которая была амплифицирована с вектора pSmart. В результате был получен ампликон 5'-НТО-люцифераза-3'-НТО. Затем методом ПЦР с фланкирующими праймерами к полученному ампликону были добавлены последовательности сайтов рестрикции EcoRI (G/AATTC) и BglII (A/GATCT). Полученный ампликон с введенными сайтами для эндонуклеаз рестрикции ДНК инкубировали с эндонуклеазами рестрикции EcoRI и BglII, очищали на агарозном геле и лигировали с аналогично подготовленным коммерческим вектором pSmart (Lucigen, США).
Для трансформации использовали штамм Escherichia coli NEB-stable (New England Biolabs, UK). Клоны отбирали методом ПЦР с колоний и подтверждали последовательность вставки секвенированием. Культивирование Е. coli для наработки верифицированной плазмиды проводили на шейкере-инкубаторе при 30°С и 180 оборотах в минуту. Затем с помощью набора QIAGEN Plasmid Maxi Kit (Qiagen, США) проводили выделение плазмидной ДНК из бактериальных клеток. Полученный препарат плазмиды линеаризовали по уникальному сайту рестрикции Spel с последующей визуализацией в агарозном геле.
Пример 2. Транскрипция мРНК in vitro
С матрицы плазмиды, полученной как описано в Примере 1, синтезировали мРНК in vitro.
In vitro транскрипцию проводили в буфере, содержащем 20 мМ дитиотреитола (ДТТ), 2 мМ спермидина, 80 мМ HEPES-KOH рН 7,4, 24 мМ MgCl2. Реакционная смесь также содержала по 3 мМ каждого из рибонуклеозидтрифосфатов (Биосан, Новосибирск), 12 мМ аналога кэпа ARCA (Биолабмикс, Новосибирск), а также остальные компоненты реакции транскрипции, из расчета на 100 мкл реакции: 40 единиц ингибитора рибонуклеаз RiboCare (Евроген, Москва), 500 единиц Т7 РНК-полимеразы (Биолабмикс, Новосибирск), 5 мкг линеаризованной плазмиды и 1 мкл смеси ферментов из набора RiboMAX Large Scale RNA Production System (Promega, США) в качестве источника неорганической пирофосфатазы. Реакцию проводили 2 часа при температуре 37°С, после чего в реакцию добавляли еще по 3 мМ каждого из рибонуклеозидтрифосфатов и дополнительно инкубировали в течение 2 часов. ДНК гидролизовали при помощи нуклеазы RQ1 (Promega, США), РНК осаждали добавлением LiCl до концентрации 0,32М и EDTA рН 8,0 до концентрации 20 мМ с последующей инкубацией на льду в течение часа. Далее раствор центрифугировали в течение 15 минут при 25000 g и 4°С. Осадок РНК промывали 70% этанолом, растворяли в ультрачистой воде и переосаждали спиртом по стандартной методике. Концентрацию РНК определяли спектрофотометрически по оптической плотности (ОП) при длине волны 260 нм.
Пример 3. Эффективность трансляции in vitro на антиген-презентующих клетках DC2.4
Эффективность трансляции in vitro оценивали по количеству синтезированного белка (люциферазы светлячка, Photinus pyralis) с мРНК в культуре дендритных клеток мыши DC2.4. Измерение биолюминесценции белка после добавления субстрата проводили через 4, 8, 24 и 72 часа после введения мРНК. В качестве вектора для доставки мРНК в культуры клеток использовали трансфекционный агент липофектамин (Lipofectamine® 3000, Thermo Fisher Scientific).
Клетки DC2.4 выращивали в среде RPMI-1640 (Capricorn), содержащей 10% FBS (HyClone), 50 мкм бета-меркаптоэтанола, аланил-глутамин и витамины. За сутки до трансфекции клетки DC2.4 высевали в лунки 96-луночного планшета, содержащие по 0,1 мл культуральной среды, в количестве 30 тыс. клеток на лунку. Все мРНК разводили до концентрации 100 нг/мкл, аликвотировали, замораживали и хранили на -80°С. Для трансфекции в отдельной пробирке готовили раствор референсной мРНК и экспериментальной мРНК в стерильном фосфатном буфере (рН=7,5) из расчета 25 мкл буфера и 50 нг каждой РНК на одну лунку. Референсная мРНК содержала последовательность люциферазы Nanoluc (Seq Id No.: 8) и использовалась в качестве внутреннего контроля экспрессии люциферазы. Далее в отдельной пробирке приготовляли раствор трансфицирующего реагента липофектамина (Lipofectamine® 3000, Thermo Fisher Scientific) в стерильном фосфатном буфере рН=7,5 из расчета 0,25 мкл реагента и 25 мкл PBS на лунку. В соответствии с протоколом фирмы-производителя реагент инкубировали в PBS при комнатной температуре в течение 10 минут, после чего смешивали 25 мкл раствора PBS, содержащей экспериментальную и референсную мРНК, с 25 мкл раствора трансфекционного агента, затем инкубировали смесь 15 минут. Далее трансфицирующую смесь в объеме 50 мкл на лунку добавляли по каплям к клеткам и инкубировали клетки 4, 8, 24 или 72 часа. Затем удаляли кондиционированную среду, промывали клетки фосфатным буфером рН 7,5, снимали с субстрата, лизировали при помощи лизирующего буфера Dual Luciferase Assay (Promega, США) и анализировали интенсивность биолюминесценции люциферазы при помощи набора Dual Luciferase Assay (Promega, США). Для сравнения брали мРНК, отличающиеся 5'- и 3'-НТО: мРНК с НТО от компании ModeRNA содержала последовательность 5'-НТО Seq Id №:3 и последовательность 3'-НТО Seq Id №:4, мРНК с НТО от компании BioNTech содержала последовательность 5'-НТО Seq Id №:6 и последовательность 3'-НТО Seq Id №:7. мРНК были получены, как описано в Примере 1 и 2. Результаты представлены на Фиг. 1.
Результаты in vitro на клеточной линии DC2.4 свидетельствуют о том, что интенсивность биолюминесценции, после трансфекции мРНК с регуляторными элементами по настоящему изобретению была выше во всех временных точках по сравнению с BioNTech (р<0,05), а также выше по сравнению с мРНК с регуляторными элементами ModeRNA через 72 часа после трансфекции (р=0,05). Интенсивность биолюминесценции отражает эффективность трансляции, таким образом полученные результаты свидетельствуют о достижении технического результата in vitro.
Статистический анализ данных проводили с помощью одно факторного дисперсионного анализа (ANOVA). Попарные сравнения проводили с помощью критерия Фишера (Fisher LSD в качестве post hoc). Статистические расчеты проводили в программе STATISTICA 8.
Пример 4. Создание липидных наночастиц (ЛНЧ), содержащих мРНК
Капсулирование мРНК в липидные наночастицы проводили путем смешивания водного раствора мРНК в 10 мМ цитратном буфере (рН 3,0) со спиртовым раствором смеси липидов. Липидная смесь содержала следующие компоненты: ионизируемый катионный липид ALC-0315 (BroadPharm, США), дистеароилфосфатидилхолин (ДСФХ или DSPC) (Avanti Polar Lipids, США), холестерин (Sigma-Aldrich, США), DMG-PEG-2000 (BroadPharm, США) в молярном соотношении 46,3:9,4:42,7:1,6. Массовая доля мРНК в ЛНЧ составляла 0,04% масс. Смешивание проводили в микрофлюидном картридже на приборе The NanoAssemblr™ Benchtop (Precision Nanosystems, США) по стандартной методике [Prikazchikova ТА, Abakumova ТО, Sergeeva OV, et al. Design and Validation of siRNA Targeting Gankyrin in the Murine Liver. Russ J Bioorg Chem., 2021, 47:441-446].
Для формирования частиц раствор липидов в этаноле смешивали с раствором мРНК в 10 мМ цитратном буферном растворе, рН 3,0 в соотношении 1:3 по объему на скорости 10 мл/мин в микрофлюидном картридже The NanoAssemblr™ Benchtop. Затем сформированные частицы диализовали против 500-кратного объема фосфатно-солевого буферного раствора, рН 7,4, при температуре 4°С в течение 12 часов. Полученные после диализа частицы фильтровали в стерильных условиях через полиэфирсульфоновую мембрану с диаметром пор 0,2 мкм и при необходимости хранили при 4°С. После фильтрации качество полученных частиц анализировали по двум параметрам: размер частиц и содержание мРНК в частицах. Размер частиц определяли методом динамического рассеяния света (ДРС) с использованием прибора ZetasizerNano ZSP (Malvern Panalitycal, США). Содержание мРНК в частицах определяли по разнице значений уровня флуоресцентного сигнала при окрашивании реагентом RiboGreen (Thermo Fischer Scientific, США) суспензии частиц до их разрушения и после. Для разрушения частиц использовали детергент Triton Х-100 (Sigma-Aldrich, США).
Пример 5. Эффективность трансляции in vivo
Эффективность трансляции in vitro оценивали по количеству синтезированного белка (люциферазы светлячка, Photinus pyralis) с мРНК в мышах линии Balb/c. В качестве вектора доставки мРНК в мышей были использованы липидные наночастицы, полученные, как описано в Примере 4.
В эксперименте использовали самцов мышей линии Balb/c в возрасте 8-9 недель. Мышам внутримышечно вводили липидные наночастицы, содержащие 10 мкг мРНК, кодирующей люциферазу светлячка Photinus pyralis, с различными 5'- и 3'-НТО. Биолюминесценцию оценивали через 4, 8, 24, 48 и 72 часа после введения ЛНЧ с мРНК. За 20 минут до оценки биолюминесценции мышам внутрибрюшинную вводили инъекцию раствора D-люциферина с концентрацией 15 мг/мл (Goldbio, USA) из расчета 10 мкл на 1 г массы тела животного. Затем животные получали ингаляционный наркоз из 2,0% Изофлурана (Laboratories Karizoo, S.A., Испания) в смеси с кислородом в течение 5 минут. Прижизненный анализ люминесценции проводили на приборе IVIS Lumina Series III (PerkinElmer, USA). Результаты анализа представлены на Фиг. 2.
Результаты in vivo на мышах BALB/c свидетельствуют о том, что интенсивность биолюминесценции после введения мРНК с регуляторными элементами по настоящему изобретению, транслирующей светлячковую люциферазу (FLuc), была выше по сравнению с мРНК с регуляторными регионами ModeRNA через 24 часа (t=2.36, р=0.028) после введения.
Полученные результаты показали, что введение мышам мРНК с 5'-НТО, содержащей последовательность Seq Id No.: 1, и 3'-НТО, содержащей последовательность Seq Id No.: 2, приводит к более высокой эффективности синтеза люциферазы и увеличению количества белка по сравнению с мРНК с регуляторными элементами ModeRNA. Через 72 часа интенсивность биолюминесценции после введения сравниваемых мРНК статистически не различалась, что можно трактовать как то, что результат экспрессии после введения мРНК с регуляторными элементами по настоящему изобретению по меньшей мере не ниже мРНК с регуляторными элементами ModeRNA. мРНК с регуляторными элементами компании BioNTech не использовали для эксперимента на живой модели, поскольку она показала худшие результаты в эксперименте in vitro.
Статистический анализ данных проводили с помощью Т теста (t) Стьюдента. Статистические расчеты проводили в программе STATISTICA 8.
Приведенные выше примеры, не ограничивая объем прав настоящего изобретения, подтверждают достижение технического результата при осуществлении настоящего изобретения, а именно статистически значимого увеличения количества белка, транслируемого с нуклеиновой кислоты, содержащей Seq Id №: 1 в составе 5'-НТО и Seq Id №:2 в составе 3'-НТО, по сравнению с количеством белка, транслируемого с нуклеиновой кислоты, содержащей 5'- и 3'-НТО, используемые в составе мРНК-вакцин известных производителей: ModeRNA или BioNTech, через 72 часа после введения в клетки, и по сравнению с количеством белка, транслируемого с нуклеиновой кислоты, содержащей 5'- и 3'-НТО ModeRNA через 48 часов после введения мышам.
Все публикации, патенты и заявки на патенты включены в настоящий документ посредством ссылки. Хотя в вышеприведенном описании это изобретение было описано в отношении некоторых предпочтительных вариантов его осуществления, и многие детали были изложены в целях иллюстрации, для специалистов в данной области техники будет очевидно, что изобретение допускает дополнительные варианты осуществления и что некоторые детали, описанные в данном документе, могут значительно изменяться без отклонения от сущности изобретения.
Использование терминов в единственном числе в контексте описания изобретения должно толковаться как охватывающее как единственное, так и множественное число, если иное не указано в данном документе или явно не противоречит контексту. Термины «состоящий из», «имеющий», «включающий» и «содержащий» следует толковать как неограничивающие термины, т.е. означающие «включая, но не ограничиваясь», если не указано иное. Перечисление диапазонов значений в данном документе просто предназначено для использования в качестве сокращенного способа индивидуальной ссылки на каждое отдельное значение, попадающее в этот диапазон, если здесь не указано иное, и каждое отдельное значение включено в спецификацию, как если бы оно было отдельно изложено в данном документе. Все способы, описанные в данном документе, могут выполняться в любом подходящем порядке, если иное не указано в данном документе или иным образом явно не противоречит контексту. Использование любых и всех примеров или иллюстративного языка (например, «такой как»), представленных в данном документе, предназначено просто для лучшего описания изобретения и не налагает ограничения на объем изобретения, если иное не заявлено. Никакие формулировки в описании не следует истолковывать как указывающие на какой-либо не заявленный элемент как существенный для практического применения изобретения.
Здесь описаны варианты осуществления этого изобретения, включая лучший из известных изобретателям способа осуществления изобретения. Разновидности этих вариантов осуществления могут стать очевидными для специалистов в данной области техники после прочтения предшествующего описания. Авторы ожидают, что квалифицированные специалисты будут использовать такие варианты в зависимости от обстоятельств, и авторы предполагают, что изобретение будет реализовано на практике иначе, чем конкретно описано в данном документе. Соответственно, это изобретение включает в себя все модификации и эквиваленты признаков, изложенных в прилагаемой формуле изобретения, как это разрешено действующим законодательством. Более того, любая комбинация вышеописанных признаков во всех их возможных вариациях охватывается изобретением, если иное не указано в данном документе или иным образом явно не противоречит контексту.
Заявитель просит рассмотреть представленные материалы заявки «Нуклеиновая кислота, содержащая регуляторные элементы гена кроличьего β-глобина, mtRNR1 и EMCV» на предмет выдачи патента на изобретение.
--->
<?xml version="1.0" encoding="UTF-8"?>
<!DOCTYPE ST26SequenceListing PUBLIC "-//WIPO//DTD Sequence Listing
1.3//EN" "ST26SequenceListing_V1_3.dtd">
<ST26SequenceListing dtdVersion="V1_3"
fileName="2023124285_RABB-mtRNR1-EMCV_listing.xml" softwareName="WIPO
Sequence" softwareVersion="2.3.0" productionDate="2024-07-08">
<ApplicationIdentification>
<IPOfficeCode>RU</IPOfficeCode>
<ApplicationNumberText>2023124285</ApplicationNumberText>
<FilingDate>2023-09-20</FilingDate>
</ApplicationIdentification>
<ApplicantName languageCode="ru">Автономная некоммерческая
образовательная организация высшего образования
"Научно-Технологический Университет
"Сириус"</ApplicantName>
<ApplicantNameLatin>Sirius University of Science and
Technology</ApplicantNameLatin>
<InventionTitle languageCode="ru">Нуклеиновая кислота, содержащая
регуляторные элементы гена кроличьего β-глобина, mtRNR1 и
EMCV</InventionTitle>
<SequenceTotalQuantity>7</SequenceTotalQuantity>
<SequenceData sequenceIDNumber="1">
<INSDSeq>
<INSDSeq_length>52</INSDSeq_length>
<INSDSeq_moltype>RNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..52</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other RNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q9">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>acacttgctttgacacaactgtgtttacttgcaatcccccaaaacagac
aga</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="2">
<INSDSeq>
<INSDSeq_length>350</INSDSeq_length>
<INSDSeq_moltype>RNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..350</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other RNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q8">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>caagcacgcagcaatgcagctcaaaacgcttagcctagccacaccccca
cgggaaacagcagtgattaacctttgcaataaacgaaagtttaactaagctatactaaccccagggttgg
tcaatttcgtgccagccacaccctggagctagcggggctgaaggatgcccagaaggtaccccattgtatg
ggatctgatctggggcctcggtgcacatgctttacatgtgtttagtcgaggttaaaaagcgtctaggccc
cccgaaccacggggacgtggttttcctttgaaaaacacgatgataatatggccacaaccggcttctgcct
aataaagaatgttcagctcaa</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="3">
<INSDSeq>
<INSDSeq_length>57</INSDSeq_length>
<INSDSeq_moltype>RNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..57</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other RNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q3">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gggaaataagagagaaaagaagagtaagaagaaatataagaccccggcg
ccgccacc</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="4">
<INSDSeq>
<INSDSeq_length>111</INSDSeq_length>
<INSDSeq_moltype>RNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..111</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other RNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q4">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gctggagcctcggtggcctagcttcttgccccttgggcctccccccagc
ccctcctccccttcctgcacccgtacccccgtggtctttgaataaagtctgagtgggcggca</INSDSe
q_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="5">
<INSDSeq>
<INSDSeq_length>54</INSDSeq_length>
<INSDSeq_moltype>RNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..54</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other RNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q5">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gagaataaactagtattcttctggtccccacagactcagagagaacccg
ccacc</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="6">
<INSDSeq>
<INSDSeq_length>295</INSDSeq_length>
<INSDSeq_moltype>RNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..295</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other RNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q6">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>ctcgagctggtactgcatgcacgcaatgctagctgcccctttcccgtcc
tgggtaccccgagtctcccccgacctcgggtcccaggtatgctcccacctccacctgccccactcaccac
ctctgctagttccagacacctcccaagcacgcagcaatgcagctcaaaacgcttagcctagccacacccc
cacgggaaacagcagtgattaacctttagcaataaacgaaagtttaactaagctatactaaccccagggt
tggtcaatttcgtgccagccacaccctggagctagc</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="7">
<INSDSeq>
<INSDSeq_length>513</INSDSeq_length>
<INSDSeq_moltype>RNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..513</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other RNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q7">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>atggtcttcacactcgaagatttcgttggggactggcgacagacagccg
gctacaacctggaccaagtccttgaacagggaggtgtgtccagtttgtttcagaatctcggggtgtccgt
aactccgatccaaaggattgtcctgagcggtgaaaatgggctgaagatcgacatccatgtcatcatcccg
tatgaaggtctgagcggcgaccaaatgggccagatcgaaaaaatttttaaggtggtgtaccctgtggatg
atcatcactttaaggtgatcctgcactatggcacactggtaatcgacggggttacgccgaacatgatcga
ctatttcggacggccgtatgaaggcatcgccgtgttcgacggcaaaaagatcactgtaacagggaccctg
tggaacggcaacaaaattatcgacgagcgcctgatcaaccccgacggctccctgctgttccgagtaacca
tcaacggagtgaccggctggcggctgtgcgaacgcattctggcg</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
</ST26SequenceListing>
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Нуклеиновая кислота, содержащая регуляторные элементы гена кроличьего β-глобина, mtRNR1 и AES | 2023 |
|
RU2831164C1 |
| Нуклеиновая кислота, содержащая регуляторные элементы TPL, AES и mtRNR1 | 2023 |
|
RU2831163C1 |
| Нуклеиновая кислота, содержащая регуляторные элементы H4C2, AES и mtRNR1 | 2023 |
|
RU2831168C1 |
| Нуклеиновая кислота, содержащая синтетическую регуляторную последовательность | 2024 |
|
RU2835583C1 |
| Вектор на основе мРНК для увеличенной продукции целевого белка в клетках млекопитающих (варианты) | 2022 |
|
RU2792231C1 |
| ПОСЛЕДОВАТЕЛЬНОСТИ 3'-UTR ДЛЯ СТАБИЛИЗАЦИИ РНК | 2016 |
|
RU2783165C1 |
| ПОСЛЕДОВАТЕЛЬНОСТИ 3'-UTR ДЛЯ СТАБИЛИЗАЦИИ РНК | 2016 |
|
RU2720934C2 |
| Плазмидная ДНК-кассета pVAX-C3-PolyA, плазмидная ДНК-матрица pVAX-C3-RBD-PolyA для синтеза мРНК и полинуклеотидная вакцина против SARS-CoV-2, представляющая собой молекулы мРНК-C3-RBD-PolyA, индуцирующие SARS-CoV-2-специфические антитела | 2024 |
|
RU2839841C1 |
| Регуляторная последовательность для увеличения экспрессии генов | 2022 |
|
RU2804421C1 |
| НОВЫЕ МИНИМАЛЬНЫЕ UTR-ПОСЛЕДОВАТЕЛЬНОСТИ | 2017 |
|
RU2759737C2 |
Изобретение относится к области биотехнологии, в частности к нуклеиновой кислоте, предназначенной для транскрипции последовательности нуклеиновой кислоты, кодирующей пептид или белок. Указанная нуклеиновая кислота содержит последовательность, которая кодирует 5’-нетранслируемую область транскрипта с Seq Id №: 1, и последовательность, которая кодирует 3’-нетранслируемую область транскрипта с Seq Id №: 2. Настоящее изобретение также относится к молекулам РНК, предназначенным для трансляции последовательности нуклеиновой кислоты. Настоящее изобретение обеспечивает статистически значимое увеличение количества белка, транслируемого с нуклеиновой кислоты, содержащей SEQ ID NO: 1 в составе 5’-НТО и SEQ ID NO: 2 в составе 3’-НТО. 3 н.п. ф-лы, 2 ил., 5 пр.
1. Нуклеиновая кислота, предназначенная для транскрипции последовательности нуклеиновой кислоты, кодирующей пептид или белок, содержащая в направлении транскрипции 5’→3’:
(а) промотор;
(б) последовательность нуклеиновой кислоты, которая, будучи транскрибированной под контролем промотора (a), кодирует 5’-нетранслируемую область транскрипта;
(в) транскрибируемую последовательность нуклеиновой кислоты, кодирующую пептид или белок;
(г) последовательность нуклеиновой кислоты, которая, будучи транскрибированной под контролем промотора (a), кодирует 3’-нетранслируемую область транскрипта,
причем упомянутая 5’-нетранслируемая область содержит последовательность Seq Id №: 1, а упомянутая 3’-нетранслируемая область содержит последовательность Seq Id №: 2,
где последовательности нуклеиновой кислоты (б)-(г) под контролем промотора (а) могут быть транскрибированы с образованием общего транскрипта, в котором последовательности нуклеиновой кислоты, транскрибированные с последовательностей нуклеиновой кислоты (б) и (г), являются активными в отношении повышения эффективности трансляции и/или стабильности последовательности нуклеиновой кислоты, транскрибированной с транскрибируемой последовательности нуклеиновой кислоты (в).
2. РНК с повышенной стабильностью, предназначенная для трансляции последовательности нуклеиновой кислоты, кодирующей пептид или белок, получаемая в результате транскрипции с применением молекулы нуклеиновой кислоты по п. 1 в качестве матрицы, причем указанная РНК содержит, в направлении 5’→3’:
(а) 5’-нетранслируемую область;
(б) последовательность нуклеиновой кислоты, кодирующую пептид или белок;
(в) 3’-нетранслируемую область,
причем упомянутая 5’-нетранслируемая область содержит последовательность Seq Id: 1, а упомянутая 3’-нетранслируемая область содержит последовательность Seq Id: 2,
где последовательности нуклеиновой кислоты (а) и (в) являются активными в отношении повышения эффективности трансляции и/или стабильности последовательности нуклеиновой кислоты, кодирующей пептид или белок.
3. РНК, предназначенная для трансляции последовательности нуклеиновой кислоты, кодирующей пептид или белок, содержащая, в направлении 5’→3’:
(а) 5’-нетранслируемую область;
(б) последовательность нуклеиновой кислоты, кодирующую пептид или белок;
(в) 3’-нетранслируемую область,
причем упомянутая 5’-нетранслируемая область содержит последовательность Seq Id №: 1, а упомянутая 3’-нетранслируемая область содержит последовательность Seq Id №: 2,
где последовательности нуклеиновой кислоты (а) и (в) являются активными в отношении повышения эффективности трансляции и/или стабильности последовательности нуклеиновой кислоты, кодирующей пептид или белок.
| WO 2017060314 A2, 13.04.2017 | |||
| WO 2017011766A1, 19.01.2017 | |||
| СПОСОБ ПОВЫШЕНИЯ ЭКСПРЕССИИ КОДИРУЕМЫХ РНК БЕЛКОВ | 2014 |
|
RU2733424C2 |
| KOZAK M., Features in the 5' non-coding sequences of rabbit alpha and beta-globin mRNAs that affect translational efficiency, Journal of molecular biology, 1994, vol | |||
| Упругая металлическая шина для велосипедных колес | 1921 |
|
SU235A1 |
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
| АНДРЕЕВ Д.Е., Роль 5’ нетранслируемых областей мРНК в регуляции синтеза | |||
Авторы
Даты
2024-12-02—Публикация
2023-09-20—Подача