Изобретение относится к биохимии и молекулярной биологии и может быть использовано в медицине для оценки активности системы эксцизионной репарации нуклеотидов (ДНК) в отношении объемных повреждений, возникающих в ДНК нормальных и опухолевых клеток как результат спонтанного действия эндогенных и экзогенных генотоксических факторов, а также повреждений, появление которых индуцировано действием химиотерапевтических препаратов.
Система эксцизионной репарации нуклеотидов (ЭРН) с широчайшей специфичностью удаляет из ДНК объемные повреждения, которые представляют собой вызывающие значительные нарушения регулярной структуры ДНК ковалентные аддукты, сформированные гетероциклическими основаниями нуклеотидных звеньев.
ЭРН (NER) - многоэтапный процесс, в котором участвуют около 30 специализированных ферментов и факторов, работа которых обеспечивает удаление из ДНК повреждения в составе окружающего его фрагмента размером 24-32 нуклеотида и последующее восстановление исходной последовательности и целостности молекулы ДНК-полимеразами с использованием в качестве матрицы неповрежденной цепи (Петрусева И.О. и др. Acta Naturae, 2014, Т. 6, №1, с. 24-36). То, насколько быстро происходит удаление объемных повреждений, определяется функциональным состоянием системы ЭРН, последовательностью нуклеотидов в поврежденной ДНК, а также структурой самого повреждения (Petruseva et al, Front Cell Dev Biol., 2021; V9:617160.). Скорость удаления из ДНК поврежденного участка позволяет судить об эффективности работы системы ЭРН.
Мутации в ряде белков ЭРН приводят к накоплению повреждений ДНК и как следствие - мутаций, проявлениям наследственных синдромов, таких как пигментная ксеродерма и нейродегенеративные заболевания (Martens, М. С, et al. Xeroderma pigmentosum: gene variants and splice variants, Genes, 2021, 12, V.8, P. 1173). Снижение активности ЭРН ассоциировано также со старением (Petruseva, et al. Acta Naturae, 2017, Т. 9, №4, c.32-43). В раковых клетках, напротив, часто наблюдается повышенная активность систем репарации ДНК (MacRae SL, et al. Aging (Albany NY), 2015, V. 12, P. 1171-84.). Учитывая то, что действие многих противоопухолевых химиопрепаратов основано на их взаимодействии с ДНК с образованием ковалентных аддуктов, активное удаление индуцированных повреждений может снижать результативность химиотерапии. Возможность оценки скорости удаления объемных повреждений репаративным аппаратом клетки имеет, таким образом, прикладное (клинико-диагностическое) значение.
Результаты оценки репаративного статуса, основанные на непосредственной оценке количества повреждений ДНК, в некоторых случаях расходятся, что может быть связано с несовершенством использованных методик, особенностями структуры исследуемых повреждений и типа образцов. Подобные расхождения особенно характерны для образцов тканей пациента, опухолевых тканей, перевиваемых опухолей, культивируемых клеток пациента и «жидких биопсий», взятых у пациентов - особенно в тех случаях, когда используется комплексная (комбинированная) терапия (Stornetta A., et al. Chem. Res. Toxicol., 2017, V. 30, №l,p.388-409).
Высокую точность оценки количества и специфичность в отношении типа повреждений обеспечивает использование масс-спектрометрических подходов, однако существенным ограничением для их широкого применения является необходимость использования изотопно-меченого внутреннего стандарта (Tretyakova N, et al. Chem Res Toxicol., 2012, V. 25, P. 2007-2035.).
Существующие способы измерения эффективности удаления (эксцизии) из ДНК участка с объемным повреждением (специфической эксцизионной активности системы ЭРН) in vitro различаются уровнями чувствительности и способами детекции продуктов эксцизии. В качестве модельной белковой системы в таких способах чаще всего используются приготовленные по стандартной методике препараты клеточных экстрактов, содержащие все необходимые для протекания реакции эксцизии белки ЭРН.
Модельные ДНК-субстраты, которые используются в большинстве работ для оценки эксцизионной активности ЭРН, представляют собой протяженные (длиной более 100 пар нуклеотидов) линейные ДНК-дуплексы, содержащие повреждение, расположенное в одной из цепей дуплекса, примерно на равном удалении от ее концов. Такие синтетические аналоги субстратов могут быть получены путем ферментативного лигирования набора дезоксиолигонуклеотидов, один из которых содержит модифицированное звено (Н.В. Лукьянчикова и др. БИОХИМИЯ, 2016, Т. 81, вып.3, с. 387-401).
Совершенствование способов оценки количества повреждений ДНК имеет важное значение как для выявления нежелательных токсических воздействий на ДНК живого организма, так и для получения объективных данных о терапевтическом воздействии, выраженных в количестве сохранившихся в ДНК индуцированных повреждений.
Принцип определения активности ЭРН (NER) с помощью количественной ПЦР (qPCR) основан на разнице в эффективности копирования неповрежденной модельной ДНК и ДНК того же размера и последовательности, содержащей в одной из цепей (цепь 1) объемное повреждение, способное блокировать удлинение комплементарного ей олигодезоксинуклеотидного праймера ДНК-полимеразой. Удлинение праймера с использованием в качестве матрицы цепи 1 приводит к наработке комплементарной цепи лишь в случае его успешной элиминации. Восстановление нативной структуры поврежденной ДНК (субстрата ЭРН) в результате катализируемой белками ЭРН-компетентного экстракта специфической эксцизии поврежденного фрагмента и последующей ДНК-полимеразной реакции обеспечивает появление полноразмерных копий неповрежденной ДНК-матрицы, амплификацию в ходе ПНР. Разница значений порогового цикла C(t) при использовании в качестве матрицы образцов ДНК после обработки белками ЭРН-компетентного экстракта и ДНК-полимеразой и контрольной поврежденной ДНК (dC(t)) позволяет судить об эффективности удаления повреждения. Уменьшение значения dC(t) говорит о накоплении в реакционной смеси молекул ДНК, прошедших процесс удаления повреждения, и позволяет определить их количество (концентрацию).
К настоящему моменту известны примеры применения ГЩР для оценки эффективности ЭРН ex vivo. Описанные методики включают трансфекцию культивируемых эукариотических клеток, содержащими процессированный продукт ДНК-белковой сшивки плазмидной ДНК (Chesner), либо шпилечной структурой, содержащей УФ-повреждение (циклобутанпиримидиновый димер) (A Rapid Assay for Measuring Nucleotide Excision Repair by Oligonucleotide Retrieval, Scientific Rep.2014, Loeb). Ограничением для широкого использования этих методик в практике является их относительная сложность, трудоемкость получения субстратов, а также необходимость оптимизации условий эксперимента при работе с различными с клеточными культурами.
Наиболее близким к заявляемому способу - прототипом, является способ оценки активности системы эксцизионной репарации нуклеотидов, включающий получение модельной ДНК и ее инкубацию с белками экстракта млекопитающего в присутствии матричного олигонуклеотида, содержащего олиго дГ тракт на 5' конце, с последующим детектированием получившихся в результате полимеразной реакции радиоактивных продуктов длиной 25-36 нуклеотидов с помощью секвенирующего гель-электрофореза в денатурирующих условиях, при этом оценку активности системы эксцизионной репарации нуклеотидов делают на основе относительной интенсивности полос, соответствующих радиоактивным продуктам длиной 25-36 нуклеотидов. Используемая в прототипе реакционная смесь включает 16-160 нМ модельную ДНК, представляющей собой ДНК-дуплекс (137 п. н.), содержащий в одной из цепей ненуклеозидную вставку с объемным заместителем, 0,3-10,0 мкг/мкл белков клеточного экстракта, а также 45 мМ NaCl, 4,4 мМ MgCb, 0,1 мМ ЭДТА, 4 мМ АТФ и олигонуклеотид-матрицу, комплементарный продуктам специфической эксцизии с олиго дезоксигуанозин (дГ) трактом на 5' конце, в 25 мМ трис-HCl буфере (рН 7,8). После 30-60 минут инкубации при 30°С останавливают реакцию и проводят гибридизацию продуктов эксцизии с комплементарной матрицей для чего смесь нагревают до 95°С и медленно охлаждают. Радиоактивную метку вводят в состав удаленных из состава ДНК-дуплекса олигонуклеотидов с помощью ДНК-полимеразы и реакционной смеси, в которой один из четырех дезоксинуклеотидтрифосфатов (дЦТФ) несет Р32 метку в а положении.
Недостатками прототипа, ограничивающими его применение, являются:
1. Необходимость использования радиоактивной метки (32Р) для детекции продуктов эксцизии.
2. Многостадийная и длительная процедура обработки проб; электрофоретический метод анализа продуктов.
3. Использование при создании ДНК-субстрата протяженного фрагмента последовательности ДНК плазмиды pBR322, хозяином которой является E.coli.
Отмеченные недостатки снижают возможности использования этого способа в практике.
Задачей изобретения является повышение чувствительности способа, а также сокращение временных затрат на проведение измерения и, как результат, расширение возможностей для применения данного способа на практике.
Технический результат: повышение чувствительности способа, а также сокращение временных затрат на проведение измерения.
Поставленная задача достигается предлагаемым способом, заключающимся в следующем.
Для осуществления способа предварительно получают реагент: модельную ДНК, представляющую собой протяженный линейный ДНК-дуплекс (160 пн), обе цепи которого содержат модификации, введенные путем автоматического твердофазного синтеза. Синтез протяженных цепей ДНК осуществляется с помощью фермента Т4 ДНК-лигазы с использованием более коротких фрагментов. При этом в каждой цепи один из фрагментов содержит модификации. На фиг. 1 представлена структура модельной ДНК, где в середине цепи 1 (позиция 91) путем твердофазного синтеза с использованием амидофосфита производства НаноТех-С (Новосибирск, Россия), введено модифицированное звено, представляющее собой эффективно удаляемое системой ЭРН объемное повреждение (-N[6-(дипивалоил-5'(6)-флуоресцеинилкарбамоил)гексаноил]-01-(4,4'-диметокситритил)-02-[(диизопропиламино)(2-цианоэтокси)фосфино]-3-амино-1,2пропандиол) (nFlu). Комплементарная цепь 2 ДНК-дуплекса предлагаемой структуры содержит модифицированное звено 12-0-диметокситритил-тетраэтил ен гликоль, 1-[(2-цианоэтил)-(N,N-диизопропил)] (TEG), введенное с использованием амидофосфита производства ОДО Праймтех (Россия, Новосибирск) и примыкающую к нему фосфотиоатную группу (PS) (позиции 140 и 139-140 соответственно), для введения которой на стадии окисления использовали серосодержащий окислитель (W. J. Stec, G. Zon and W. Egan, J. Am. Chem. Soc, 1984,106, 6077-6079).
В качестве базовой последовательности для модельной ДНК выступает фрагмент гена полиэдрина вируса ядерного полиэдроза (ВЯП) насекомых (GenBank №KJ685906.1). Праймеры 1 и 2 для проведения ПЦР при детекции продуктов репарации (Таблица 1), как и сама последовательность (Фиг. 1), не имеют гомологии с геномом человека при проверке специфичности с помощью программы Primer-BLAST (https://www.ncbi.nlm.nih.gov/tools/primer-blast/index.cgi?LINK_LOC=BlastHome).
Далее готовят реакционную смесь, содержащую ДНК-дуплекс с модификациями в обеих цепях (3-16 нМ); белки клеточного экстракта (0,3-3,0 мкг/мкл); смесь дНТФ (500 мкМ); полностью некомплементарный ДНК-субстрату одноцепочечный олигонуклеотид (ОДН, 65 нт, 0,5 мкМ) для защиты от нуклеаз, специфичных в отношении одноцепочечных участков ДНК; Taq ДНК-полимеразу (0,06 ед.акт/мкл); 1хЭРН буфер (25 мМ Tris-HCl рН 7.8, 45 мМ NaCl, 4,4 мМ MgCl2, 0,1 мМ EDTA, 4 мМ АТР). В результате реакции, под воздействием белков ЭРН, содержащихся в клеточных экстрактах, происходит удаление объемного повреждения в модельной ДНК в составе окружающего повреждение 24-32 звенного фрагмента цепи ДНК. Восстановление целостности цепи обеспечивается присутствием в реакционной смеси Taq ДНК-полимеразы и дНТФ. Восстановленную ДНК детектируют в ходе последующей ПЦР с использованием Taq ДНК-полимеразы с «горячим стартом», а также праймеров 1 и 2, комплементарных к позициям 140-160 и 141-160 первой и второй цепей соответственно (фиг. 1). Структуры использованных праймеров и одноцепочечного олигонуклеотида представлены в таблице 1.
Реакционная смесь для проведения ПЦР содержит следующие компоненты: восстановленная ДНК-матрица; праймеры 1 и 2 (0,3 мкМ); Taq-ДНК-полимераза с «горячим стартом» (0,06 ед.акт./мкл); смесь дНТФ (0,25 мМ); краситель SYBR Green I (0,5х); 1xPCR-буфер (75 мМ Tris-HCl, рН 8.8, 2 мМ (NH4)2SO4, 0,01% Tween 20, 3 мМ MgC12). Реакцию проводят в 96-луночных планшетах на амплификаторе при заданной программе PCR:
- 5 мин при 95°С;
- 15 сек при 95°С;
- 15 сек при 58°С;
- 10 сек при 72°С - считывание сигнала;
- Повторение 2-4 в течение 35 циклов;
- Охлаждение.
Эксцизионную активность системы ЭРН in vitro измеряют путем количественного ПНР-анализа амплификации ДНК-матрицы, которая представляет собой продукт репарации модельной ДНК (фиг.2) белками клеточных экстрактов.
Предлагаемый способ позволяет повысить чувствительность анализа в 10 раз, а также сократить временные затраты на проведение измерения в 20-25 раз.
Предлагаемый способ, по сравнению с прототипом, имеет следующие отличия:
1). В качестве модельной ДНК используют линейный ДНК-дуплекс размером 160 пар нуклеотидов, обе цепи которого содержат модифицированные звенья, при этом в одной из цепей содержится ненуклеозидная вставка на основе пропандиола с объемным заместителем, а комплементарная цепь содержит ненуклеозидную вставку на основе тетраэтиленгликоля, с 5'-стороны фланкированную фосфотиоатной группой. При этом, в цепи 1 содержится объемное повреждение -ненуклеозидная вставка на основе пропандиола с объемным заместителем (nFlu), что позволяет исключить возможность полноразмерного копирования и последующей амплификации этой цепи, а комплементарная цепь (цепь 2) также содержит модификацию в виде ненуклеозидной вставки на основе аналога АП-сайта - тетраэтиленгликоля (TEG), с 5'-стороны фланкированную фосфотиоатной группой (PS), что позволяет исключить возможность полноразмерного копирования данной цепи, а наличие PS-группы не допускает ее расщепления по TEG эндогенной АП-эндонуклеазой экстрактов.
2) Реакционная смесь для определения эксцизионной активности системы ЭРН, содержит следующие компоненты: ДНК-дуплекс с модификациями в обеих цепях (3-16 нМ); белки клеточного экстракта (0,3-3,0 мкг/мкл); смесь дНТФ (500 мкМ); полностью некомплементарный ДНК-субстрату одноцепочечный олигонуклеотид (ОДН, 65 нт, 0,5 мкМ) для защиты от нуклеаз, специфичных в отношении одноцепочечных участков ДНК; Taq ДНК-полимераза (0,06 ед.акт/мкл) в присутствии ЭРН буфера и не содержит радиоактивного дЦТФ и матричного олигонуклеотида с дГ-трактом (прототип).
3) Готовые реакционные смеси выдерживают при 30°С в течение 30-60 минут, после остановки реакции эксцизии прогревом (65°С, 20 мин) реакционную смесь разбавляют до концентрации ДНК 1⋅10-9-110-13 М и используют при проведении ГЩР-анализа.
Полученные в ходе количественного анализа кривые амплификации ДНК значения порогового цикла C(t) используют для определения эффективности процесса репарации модельной ДНК с модификациями.
Определяющими отличиями предлагаемого способа, по сравнению с прототипом, являются:
1. Структура субстрата (протяженного ДНК-дуплекса), используемого для оценки активности системы ЭРН, позволяющая использовать высокочувствительный метод - ПЦР в реальном времени.
2. Детектируемым продуктом реакции является ДНК, не содержащая повреждения.
Изобретение иллюстрируется следующими примерами конкретного выполнения.
Пример 1. Определение рабочего диапазона концентраций, построение калибровочной кривой и расчет эффективности ПЦР в проводимых условиях.
Собирали реакционную смесь объемом 25 мкл для проведения ПЦР-анализа, которая содержала следующие компоненты (указаны финальные концентрации): 0,3 мкМ праймеры 1 и 2; 0,06 ед.акт./мкл Taq ДНК-полимеразы с «горячим стартом»; nm/TEG-ДНК (4⋅10-11 - 4 -10-15 М); 0,25 мМ смесь дНТФ; 0,5х краситель SYBR Green I; 1х ПЦР-буфер (75 мМ Трис-НС1, рН 8,8, 2 мМ (NH4)2SO4, 0,01% Tween 20, 3 мМ MgCl2). Реакцию проводили в 96-луночных планшетах (белый низкопрофильный пластик; BIOplastics BV, Нидерланды) на амплификаторе LightCycler 96 (Roche, Швейцария) при заданной программе ПЦР:
1. 5 мин при 95°С;
2. 15 сек при 95°С;
3. 15 сек при 58°С;
4. 10 сек при 72°С - считывание сигнала;
5. Повторение 2-4 в течение 35 циклов;
6. Плавление продуктов ПЦР;
7. Охлаждение.
На фиг.2 представлены кривые амплификации стандартных образцов nm/TEG-ДНК в 10-кратно убывающей концентрациях (А), построение калибровочного графика (Б) и расчет эффективности ПЦР (В).
Пример 2. Сравнительная оценка эксцизионной активности системы NER с использованием разработанного метода и белков экстракта клеток мыши {Mus musculus) и голого землекопа {Heterocephalus glaber).
Проводили ПЦР-анализ ДНК, содержащейся в реакционной смеси для проведения реакции ЭРН, после 30 минут инкубации с белками экстракта эмбриональных фибробластов мыши {Mus musculus) или с белками экстракта кожных фибробластов голого землекопа {Heterocephalus glaber).
На первой стадии готовили реакционную смесь для проведения реакции ЭРН (30 мкл), которая содержала 16 нМ ДНК-субстрат (nFlu/TEG-ДНК), 0,4 мкг/мкл ЭРН-компетентного экстракта клеток М. Musculus или H. glaber, 0,5 мМ смесь дНТФ, 0,06 ед.акт./мкл Taq ДНК-полимеразы и 0,5 мкМ олигонуклеотид (ОДН) для защиты от нуклеаз, специфичных к одноцепочечным участкам ДНК в буфере (25 мМ Трис-HCl, рН 7,8; 45 мМ NaCl; 4,4 мМ MgCl2; 0,1 мМ ЭДТА; 4 мМ АТФ), затем смесь инкубировали при 30°С в течение 30 мин. Реакцию останавливали прогревом реакционной смеси при 65°С в течение 20 мин. Инактивированную реакционную смесь разбавляли до концентрации ДНК 0,1 нМ (1⋅10-10 М), после чего использовали для анализа с помощью ПНР в режиме реального времени.
Далее собирали реакционную смесь для проведения ПЦР-анализа общим объемом 25 мкл. Смесь содержала 1 мкл разбавленной инактивированной реакционной смеси, полученной на первой стадии, и следующие компоненты: 0,3 мкМ праймеры 1 и 2; 0,06 ед.акт./мкл Taq ДНК-полимеразы с «горячим стартом»; 0,25 мМ смесь дНТФ; 0,5х краситель SYBR Green I; 1х ПЦР-буфер (75 мМ Трис-HCl, рН 8,8, 2 мМ (NH4)2SO4, 0,01% Tween 20, 3 мМ MgCl2). Реакцию проводили в 96-луночных планшетах (белый низкопрофильный пластик; BIOplastics BV, Нидерланды) на амплификаторе LightCycler 96 (Roche, Швейцария) при заданной программе ПЦР:
1. 5 мин при 95°С;
2. 15 сек при 95°С;
3. 15 сек при 58°С;
4. 10 сек при 72°С - считывание сигнала;
5. Повторение 2-4 в течение 35 циклов;
6. Плавление продуктов ПЦР;
7. Охлаждение.
Полученные в ходе анализа кривых амплификации значения порогового цикла C(t) были использованы для расчета разницы dC(t) по формуле:
dC(t)=С(1)nFlu/TEG-ДНК - C(t)x, где C(t)x - значение C(t) для анализируемой пробы; C(t)nFlu/TEG-ДНК - значение C(t) для nFlu/TEG-ДНК в контрольном образце, который не подвергался воздействию белков клеточного экстракта. Для расчета эффективности репарации рассчитанные значения dC(t) были переведены в проценты, где 100% - это разница значений dC(t) между nFlu/TEG- и nm/TEG-ДНК в контрольных образцах.
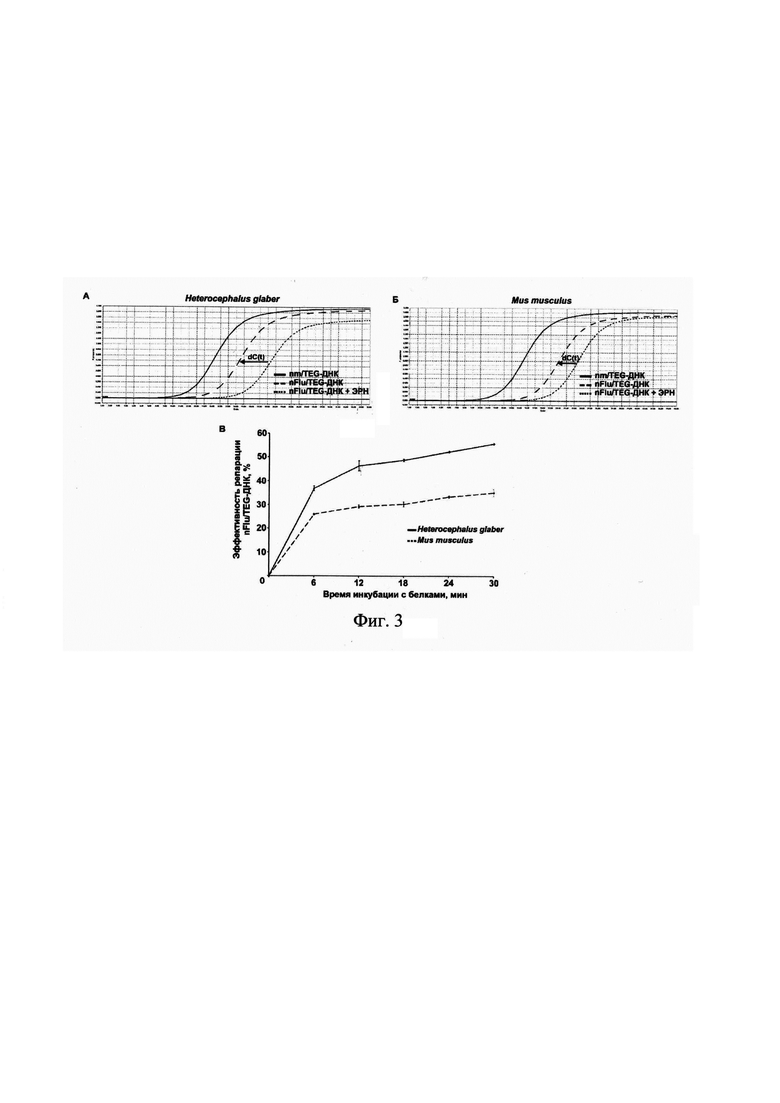
На фиг. 3 представлены кривые амплификации для образцов ДНК после 30 минут инкубации с белками экстракта клеток Heterocephalus glaber (А) и Mus musculus (Б), а также график зависимости эффективности репарации nFlu/TEG-ДНК от времени инкубации с белками клеточных экстрактов.
Данные, представленные на фиг. 2 и 3, демонстрируют, что предлагаемый способ применим для оценки активности системы ЭРН в широком диапазоне концентраций ДНК и позволяет определить количество ДНК с восстановленной нативной структурой. Одновременно с многократным повышением чувствительности за счет использования ПЦР для оценки эффективности удаления из ДНК объемного повреждения, предлагаемый способ позволит значительно сократить время от начала эксперимента до получения первичных результатов в 20-25 раз (до 2-2,5 часов).
Перечень последовательностей
--->
<?xml version="1.0" encoding="UTF-8"?>
<!DOCTYPE ST26SequenceListing PUBLIC "-//WIPO//DTD Sequence Listing
1.3//EN" "ST26SequenceListing_V1_3.dtd">
<ST26SequenceListing dtdVersion="V1_3" fileName="Способ оценки
активности системы эксцизионной репарации нуклеотидов
млекопитающих.xml" softwareName="WIPO Sequence"
softwareVersion="2.3.0" productionDate="2024-11-05">
<ApplicationIdentification>
<IPOfficeCode>RU</IPOfficeCode>
<ApplicationNumberText>2024110015/10</ApplicationNumberText>
<FilingDate>2024-04-11</FilingDate>
</ApplicationIdentification>
<ApplicantFileReference>022859</ApplicantFileReference>
<EarliestPriorityApplicationIdentification>
<IPOfficeCode>RU</IPOfficeCode>
<ApplicationNumberText>2024110015/10(022859)</ApplicationNumberText>
<FilingDate>2024-04-11</FilingDate>
</EarliestPriorityApplicationIdentification>
<ApplicantName languageCode="ru">Федеральное государственное
бюджетное учреждение науки Институт химической биологии и
фундаментальной медицины Сибирского отделения Российской академии
наук</ApplicantName>
<ApplicantNameLatin>Federalnoe gosudarstvennoe byudzhetnoe
uchrezhdenie nauki Institut himicheskoj biologii i fundamentalnoj
mediciny Sibirskogo otdeleniya Rossijskoj akademii
nauk</ApplicantNameLatin>
<InventorName languageCode="ru">Попов Алексей
Алексеевич</InventorName>
<InventorNameLatin>Popov Aleksej Alekseevich</InventorNameLatin>
<InventionTitle languageCode="ru">Способ оценки активности системы
эксцизионной репарации нуклеотидов млекопитающих</InventionTitle>
<SequenceTotalQuantity>3</SequenceTotalQuantity>
<SequenceData sequenceIDNumber="1">
<INSDSeq>
<INSDSeq_length>20</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..20</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q2">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>cgccacgaacttgtagcatc</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="2">
<INSDSeq>
<INSDSeq_length>19</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..19</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q4">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>cgatgaagctggtggtcaa</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="3">
<INSDSeq>
<INSDSeq_length>65</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..65</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>genomic DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q6">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>Nuclear polyhedrosis virus
</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>agctgctgctcatctcgagatctgagtacattggattgccattctccga
gtgtattaccgtgacg</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
</ST26SequenceListing>
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОЦЕНКИ АКТИВНОСТИ СИСТЕМЫ ЭКСЦИЗИОННОЙ РЕПАРАЦИИ НУКЛЕОТИДОВ МЛЕКОПИТАЮЩИХ | 2012 |
|
RU2492242C1 |
| МОЛЕКУЛА СУБСТРАТА | 2016 |
|
RU2755495C2 |
| СПОСОБ АМПЛИФИКАЦИИ НУКЛЕИНОВЫХ КИСЛОТ С ИСПОЛЬЗОВАНИЕМ ФОСФОРИЛГУАНИДИНОВЫХ ОЛИГОНУКЛЕОТИДОВ | 2017 |
|
RU2698134C2 |
| Способ штрихкодирования ампликонов при подготовке таргетных библиотек ДНК к массовому параллельному секвенированию | 2020 |
|
RU2752840C1 |
| ХИМИЧЕСКИ МОДИФИЦИРОВАННЫЙ ТЕРМОСТАБИЛЬНЫЙ ФЕРМЕНТ, СПОСОБ ЕГО ПОЛУЧЕНИЯ, СПОСОБ АМПЛИФИКАЦИИ СОДЕРЖАЩЕЙСЯ В ОБРАЗЦЕ НУКЛЕИНОВОЙ КИСЛОТЫ, РЕАКЦИОННАЯ СМЕСЬ ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ И НАБОР ДЛЯ ПРОВЕДЕНИЯ ЦЕПНОЙ РЕАКЦИИ | 1996 |
|
RU2174556C2 |
| СПОСОБ ГОМОГЕННОЙ ДЕТЕКЦИИ ПО МЕНЬШЕЙ МЕРЕ ОДНОГО ПРОДУКТА ОДНОЦЕПОЧЕЧНОЙ АМПЛИФИКАЦИИ | 2005 |
|
RU2460804C2 |
| МОДИФИЦИРОВАННАЯ ТЕРМОСТАБИЛЬНАЯ ДНК-ПОЛИМЕРАЗА, СПОСОБ ЕЁ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ | 1997 |
|
RU2235773C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АКТИВНОСТИ ТЕЛОМЕРАЗЫ МЕТОДОМ ДВОЙНОЙ АМПЛИФИКАЦИИ ТЕЛОМЕРНЫХ ПОВТОРОВ В РЕАЛЬНОМ ВРЕМЕНИ | 2017 |
|
RU2681165C1 |
| Способ защиты от контаминации реакционных смесей для ПЦР | 2022 |
|
RU2796504C1 |
| КОМПОЗИЦИИ, СПОСОБЫ И НАБОРЫ ДЛЯ СИНТЕЗА И ОБНАРУЖЕНИЯ НУКЛЕИНОВЫХ КИСЛОТ | 2017 |
|
RU2757416C2 |

Изобретение относится к биохимии и молекулярной биологии. Предложен способ оценки активности системы эксцизионной репарации нуклеотидов (ЭРН) млекопитающих. Получают модельную ДНК, представляющую собой ДНК-дуплекс с размером 160 пар нуклеотидов, обе цепи которого содержат ненуклеозидные вставки. Полученную модельную ДНК подвергают воздействию клеточных экстрактов, содержащих белки ЭРН, что приводит к удалению объемного повреждения в составе прилежащего фрагмента цепи ДНК. Восстановление целостности цепи обеспечивается присутствием в реакционной смеси Taq-ДНК полимеразы и дНТФ. Восстановленную ДНК амплифицируют в ходе последующей ПЦР. Предложенный способ обладает повышеннной чувствительностью способа, а также позволяет сократить временные затраты на проведение измерения. 3 ил., 1 табл., 2 пр.
Способ оценки активности системы эксцизионной репарации нуклеотидов (ЭРН) млекопитающих, включающий получение модельной ДНК, подготовку реакционной смеси для проведения реакции ЭРН, инкубацию реакционной смеси при 30°С в течение 30-60 минут, добавление к полученной реакционной смеси модельной ДНК и инкубацию последней с белками экстракта клеток млекопитающего в присутствии олигонуклеотида, и буферного раствора для проведения реакции ЭРН, нагревание реакционной смеси для остановки реакции и последующее детектирование получившихся продуктов, отличающийся тем, что в качестве модельной ДНК используют линейный ДНК-дуплекс размером 160 пар нуклеотидов, обе цепи которого содержат модифицированные звенья, причем в одной из цепей содержится ненуклеозидная вставка на основе пропандиола с объемным заместителем, а комплементарная цепь содержит ненуклеозидную вставку на основе тетраэтиленгликоля, с 5’-стороны фланкированную фосфотиоатной группой, при этом реакционная смесь для проведения реакции ЭPH содержит 3-16 нM ДНК-дуплекс, 0,3-3,0 мкг/мкл белков клеточного экстракта, 500 мкМ смесь дНТФ, 0,5 мкм одноцепочечный олигонуклеотид длиной 65 звеньев, некомплементарный модельной ДНК, и 0,06 ед.акт./мкл Taq ДНК-полимеразы в буфере для ЭРН, при этом буфер для ЭPH содержит 25 мM Tris-HCl pH 7.8, 45 мM NaCl, 4,4 мM MgCl2, 0,1 мM EDTA, 4 мM ATP, при этом реакцию эксцизии останавливают прогревом в течение 20 минут при 65°С, после чего инактивированную реакционную смесь разбавляют и анализируют с помощью количественной ПЦР в реальном времени с использованием праймеров 1 и 2, комплементарных к позициям 140-160 и 141-160 первой и второй цепей ДНК-дуплекса соответственно.
| POPOV A.A | |||
| et al | |||
| Methods for Assessment of Nucleotide Excision Repair Efficiency, Biochemistry (Mosc), 2023, vol | |||
| Шланговое соединение | 0 |
|
SU88A1 |
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| Прибор для указания трамвайных и железнодорожных станций | 1923 |
|
SU1844A1 |
| WANG L | |||
| et al | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Способ получения камфоры | 1921 |
|
SU119A1 |
| Скоропечатный станок для печатания со стеклянных пластинок | 1922 |
|
SU35A1 |
| СПОСОБ ОЦЕНКИ АКТИВНОСТИ СИСТЕМЫ ЭКСЦИЗИОННОЙ РЕПАРАЦИИ НУКЛЕОТИДОВ МЛЕКОПИТАЮЩИХ | 2012 |
|
RU2492242C1 |
Авторы
Даты
2024-12-02—Публикация
2024-04-11—Подача