ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Данная заявка заявляет приоритет предварительной заявки на патент США № 62/953089, поданной 23 декабря 2019 г., раскрытие которой включено в данный документ посредством ссылки во всей своей полноте.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
[0002] Соединение N6-((2-азидоэтокси)карбонил)лизин и два энантиомера, N6-((2-азидоэтокси)карбонил)-L-лизин и N6-((2-азидоэтокси)карбонил)-D-лизин являются пригодными в получении полипептидов и белков в качестве средств изучения и терапевтических продуктов. Например, было продемонстрировано, что ортогональная пара MS пирролизил-tRNA-синтетаза/tRNA Methanosarcina barkeri может контролировать эффективное сайт-специфическое встраивание N6-((2-азидоэтокси)карбонил)-L-лизина в рекомбинантные белки в Escherichia coli. Белки, содержащие азидную функциональную группу, могут быть связаны посредством реакций циклоприсоединения [3+2] для присоединения к белкам флуоресцентных меток и других функциональных фрагментов. Способы получения N6-((2-азидоэтокси)карбонил)лизина, включая два энантиомера, из предшествующего уровня техники обеспечивают низкие выходы или зависят от химических промежуточных соединений, которые могут представлять значительную угрозу безопасности (Milles, S. et al., J. Am. Chem. Soc. (2012), Vol. 134, 5187-5195; US 2016/0297855). Следовательно, существует необходимость в воспроизводимом способе, обеспечивающем высокий выход продукта, предназначенном для получения таких соединений, который зависит от получения химических промежуточных соединений, которые могут представлять меньшую угрозу безопасности.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0003] В определенных вариантах осуществления в данном документе описаны способы получения N6-((2-азидоэтокси)карбонил)лизина и промежуточных соединений, пригодных для этого.
[0004] Охватываются следующие варианты осуществления.
[0005] Вариант осуществления 1 представляет собой способ получения соединения формулы (VI),
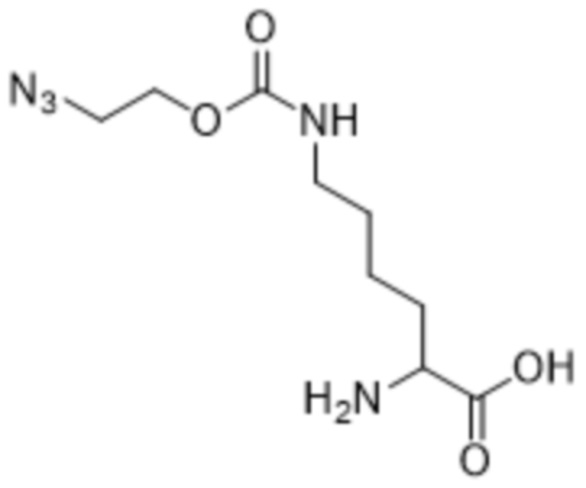
(VI),
или его соли,
включающий осуществление реакции соединения формулы (III),
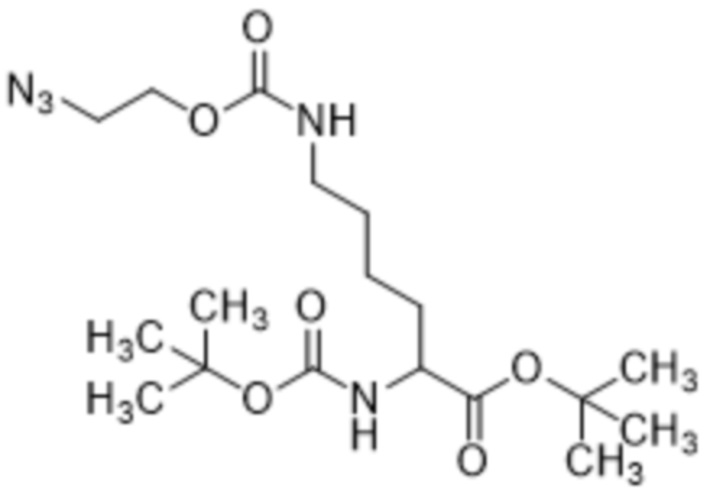
(III),
с кислотой с получением соединения формулы (VI) или его соли.
[0006] Вариант осуществления 2 представляет собой способ согласно варианту осуществления 1, где кислота представляет собой одну или несколько из фосфорной кислоты, хлористоводородной кислоты, уксусной кислоты и трифторуксусной кислоты.
[0007] Вариант осуществления 3 представляет собой способ согласно варианту осуществления 1 или 2, где кислота представляет собой хлористоводородную кислоту.
[0008] Вариант осуществления 4 представляет собой способ согласно любому из вариантов осуществления 1-3, где реакцию соединения формулы (III) с кислотой проводят в растворе, содержащем апротонный растворитель, выбранный из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, 2-метилтетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400 и полиэтиленгликолей.
[0009] Вариант осуществления 5 представляет собой способ согласно варианту осуществления 4, где апротонный растворитель представляет собой 1,4-диоксан.
[0010] Вариант осуществления 6 представляет собой способ согласно любому из вариантов осуществления 1-5, где способ дополнительно включает добавление основания.
[0011] Вариант осуществления 7 представляет собой способ согласно варианту осуществления 6, где основание представляет собой одно или несколько из гидроксида аммония, гидроксида натрия или гидроксида калия.
[0012] Вариант осуществления 8 представляет собой способ согласно варианту осуществления 6 или 7, где основание представляет собой гидроксид аммония.
[0013] Вариант осуществления 9 представляет собой способ согласно любому из вариантов осуществления 6-8, где добавление основания обеспечивает раствор, характеризующийся pH в диапазоне от 4 до 10.
[0014] Вариант осуществления 10 представляет собой способ согласно любому из вариантов осуществления 6-9, где добавление основания обеспечивает раствор, характеризующийся pH в диапазоне от 8 до 9.
[0015] Вариант осуществления 11 представляет собой способ согласно любому из вариантов осуществления 1-10, где соединение формулы (VI) представляет собой соединение формулы (VIa),
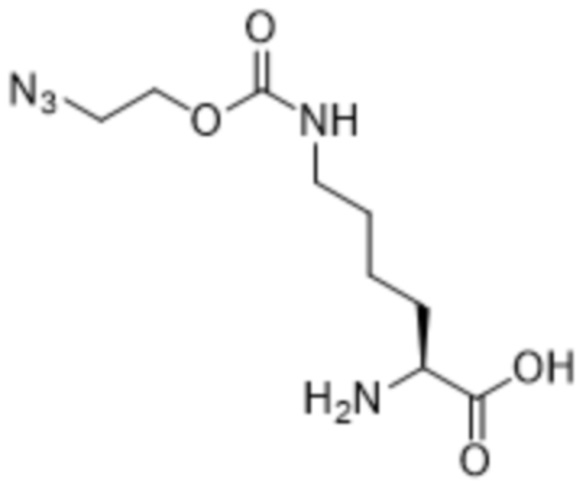
(VIa).
[0016] Вариант осуществления 12 представляет собой способ получения соединения формулы (III),

(III),
включающий осуществление реакции соединения формулы (II),
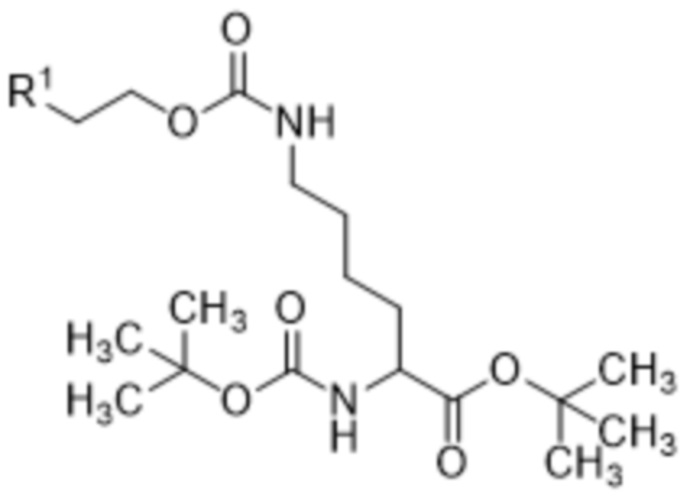
(II),
где R1 выбран из хлора, брома и йода,
с азидной солью щелочного металла с получением соединения формулы (III).
[0017] Вариант осуществления 13 представляет собой способ согласно варианту осуществления 12, где R1 представляет собой хлор.
[0018] Вариант осуществления 14 представляет собой способ согласно варианту осуществления 12 или 13, где азидная соль щелочного металла выбрана из азида лития, азида натрия и азида калия.
[0019] Вариант осуществления 15 представляет собой способ согласно любому из вариантов осуществления 12-14, где азидная соль щелочного металла представляет собой азид натрия.
[0020] Вариант осуществления 16 представляет собой способ согласно любому из вариантов осуществления 12-15, где реакцию соединения формулы (II) с азидной солью щелочного металла проводят в растворе, содержащем апротонный растворитель, выбранный из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, 2-метилтетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400, полиэтиленгликолей.
[0021] Вариант осуществления 17 представляет собой способ согласно варианту осуществления 16, где апротонный растворитель представляет собой ацетонитрил.
[0022] Вариант осуществления 18 представляет собой способ согласно варианту осуществления 16 или 17, где раствор дополнительно содержит воду.
[0023] Вариант осуществления 19 представляет собой способ согласно любому из вариантов осуществления 12-18, где соединение формулы (III) представляет собой соединение формулы (IIIa),
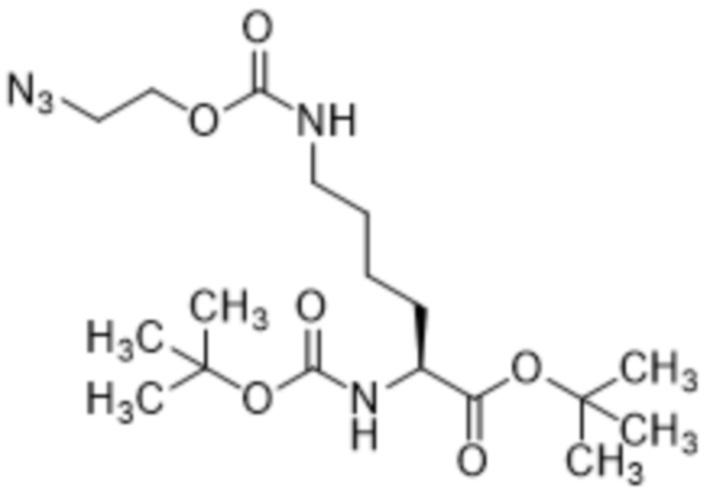
(IIIa),
и соединение формулы (II) представляет собой соединение формулы (IIa),
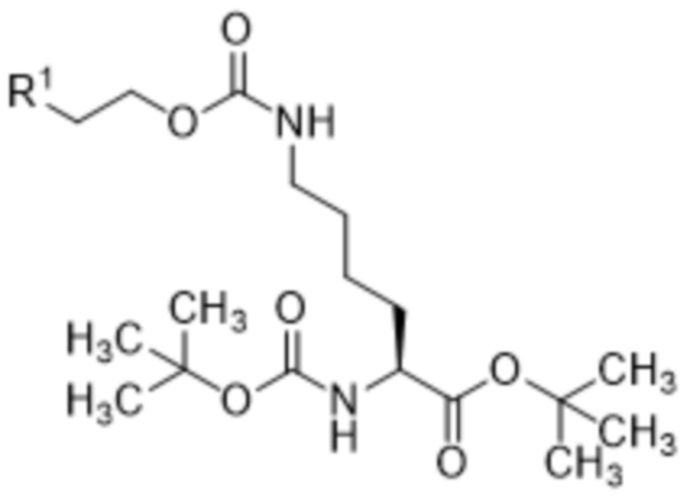
(IIa).
[0024] Вариант осуществления 20 представляет собой способ получения соединения формулы (II),

(II),
включающий осуществление реакции соединения формулы (I),
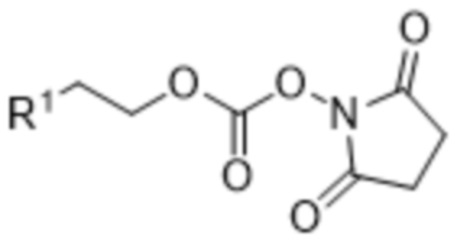
(I),
с соединением формулы (V),
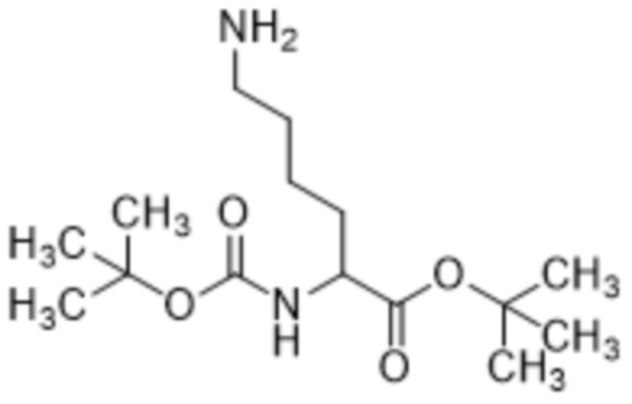
(V),
с получением соединения формулы (II),
при этом в каждом из соединений формулы (I) и формулы (II) R1 является одинаковым и выбран из хлора, брома и йода.
[0025] Вариант осуществления 21 представляет собой способ согласно варианту осуществления 20, где R1 в каждом из соединений формулы (I) и формулы (II) представляет собой хлор.
[0026] Вариант осуществления 22 представляет собой способ согласно варианту осуществления 20 или 21, где реакцию соединения формулы (V) с соединением формулы (I) проводят в растворе, содержащем апротонный растворитель, выбранный из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, 2-метилтетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400 и полиэтиленгликолей.
[0027] Вариант осуществления 23 представляет собой способ согласно варианту осуществления 22, где апротонный растворитель представляет собой 2-метилтетрагидрофуран или N,N-диметилформамид.
[0028] Вариант осуществления 24 представляет собой способ согласно любому из вариантов осуществления 20-23, где соединение формулы (II) представляет собой соединение формулы (IIa),

(IIa),
и соединение формулы (V) представляет собой соединение формулы (Va),
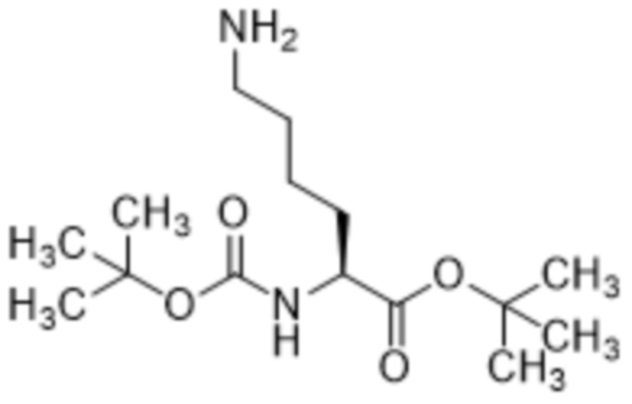
(Va).
[0029] Вариант осуществления 25 представляет собой способ получения соединения формулы (I),

(I),
включающий осуществление реакции соединения формулы (IV),
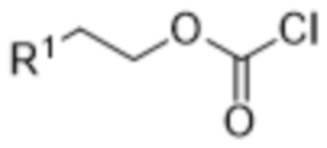
(IV),
с N-гидроксисукцинимидом с получением соединения формулы (I),
при этом в каждом из соединений формулы (I) и формулы (IV) R1 является одинаковым и выбран из хлора, брома и йода.
[0030] Вариант осуществления 26 представляет собой способ согласно варианту осуществления 25, где R1 представляет собой хлор.
[0031] Вариант осуществления 27 представляет собой способ согласно варианту осуществления 25 или 26, где реакцию соединения формулы (IV) с N-гидроксисукцинимидом проводят в растворе, содержащем апротонный растворитель, выбранный из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, 2-метилтетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400 и полиэтиленгликолей.
[0032] Вариант осуществления 28 представляет собой способ согласно варианту осуществления 27, где апротонный растворитель представляет собой ацетонитрил или 2-метилтетрагидрофуран.
[0033] Вариант осуществления 29 представляет собой способ согласно варианту осуществления 27 или 28, где раствор дополнительно содержит основание.
[0034] Вариант осуществления 30 представляет собой способ согласно варианту осуществления 29, где основание представляет собой триалкиламин.
[0035] Вариант осуществления 31 представляет собой способ согласно варианту осуществления 29 или 30, где основание представляет собой триэтиламин.
[0036] Вариант осуществления 32 представляет собой способ получения соединения формулы (VIa) или его соли, включающий следующие стадии:
(i) осуществление реакции 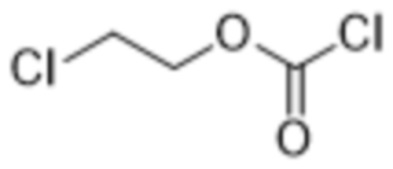 с
с 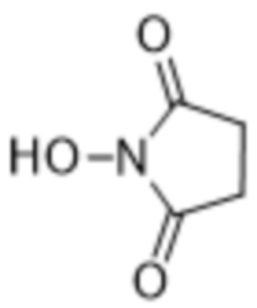 с образованием
с образованием 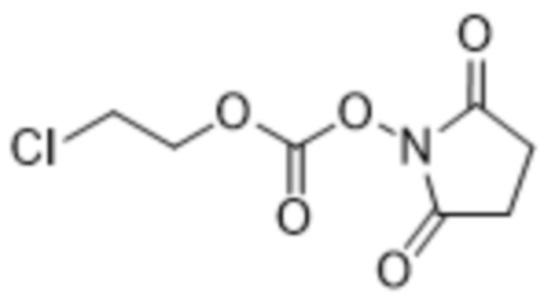 ;
;
(ii) осуществление реакции  с
с 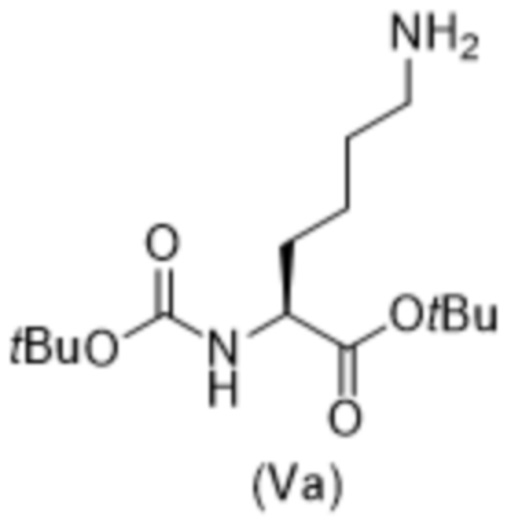 с образованием
с образованием 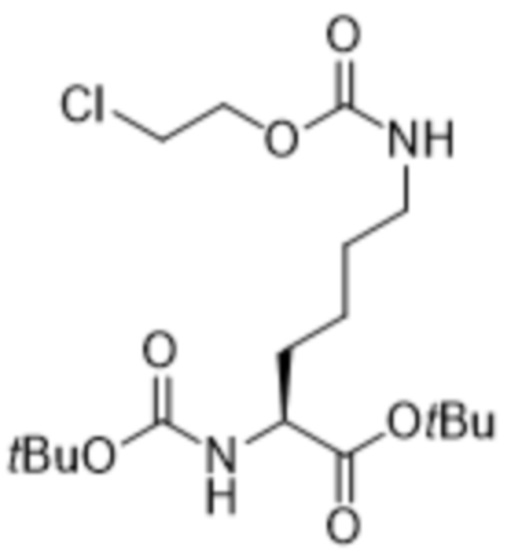 ;
;
(iii) осуществление реакции  с NaN3 с образованием
с NaN3 с образованием 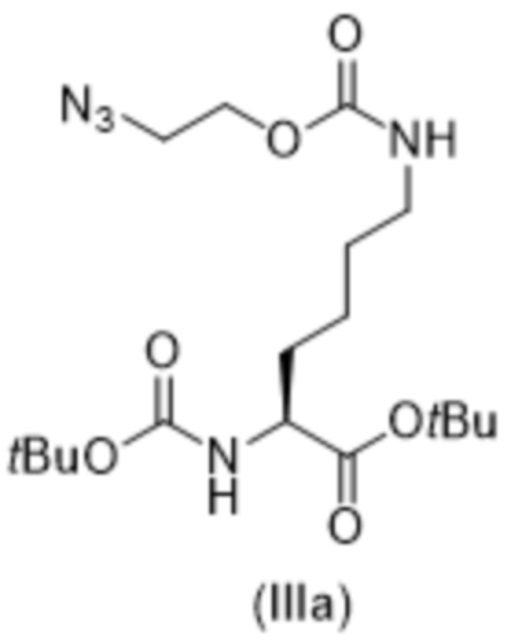 и
и
(iv) осуществление реакции  с HCl с образованием
с HCl с образованием 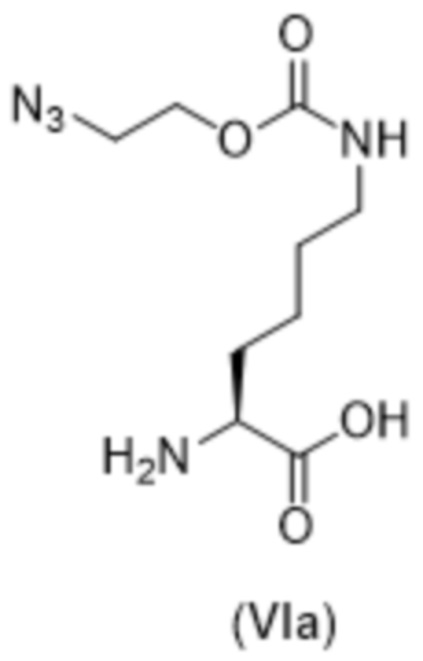 или его соли.
или его соли.
[0037] Вариант осуществления 33 представляет собой соединение формулы (I),

(I),
где R1 выбран из хлора, брома и йода.
[0038] Вариант осуществления 34 представляет собой соединение согласно варианту осуществления 33, где R1 представляет собой хлор.
[0039] Вариант осуществления 35 представляет собой соединение формулы (II),

(II),
где R1 выбран из хлора, брома и йода.
[0040] Вариант осуществления 36 представляет собой соединение согласно варианту осуществления 35, где R1 представляет собой хлор.
[0041] Вариант осуществления 37 представляет собой соединение согласно варианту осуществления 35 или 36, где соединение формулы (II) представляет собой соединение формулы (IIa),

(IIa).
[0042] Вариант осуществления 38 представляет собой соединение формулы (III),

(III).
[0043] Вариант осуществления 39 представляет собой соединение согласно варианту осуществления 38, где соединение формулы (III) представляет собой соединение формулы (IIIa),

(IIIa).
[0044] Вариант осуществления 40 представляет собой соединение формулы (VII),
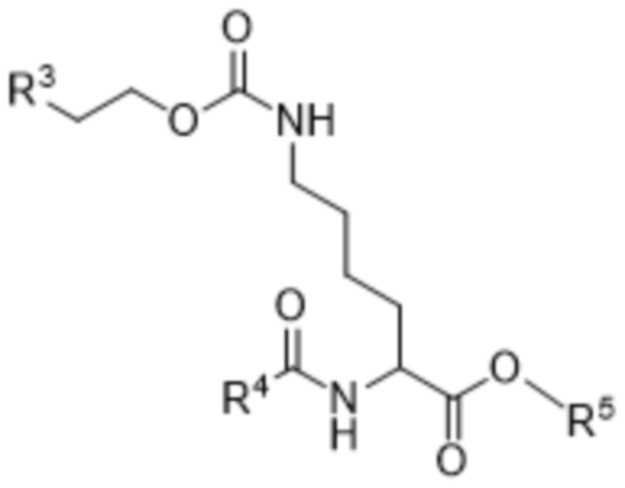
(VII),
где
R3 выбран из хлора, брома и йода;
R4 выбран из -OR6, -CF3, -CH2C6-C12арила и C1-C6алкила;
R5 представляет собой -CH2C6-C12арил или C1-C6алкил; и
R6 выбран из C1-C6алкила, C6-C12арила и -CH2C6-C12арила.
[0045] Вариант осуществления 41 представляет собой соединение формулы (VIII),
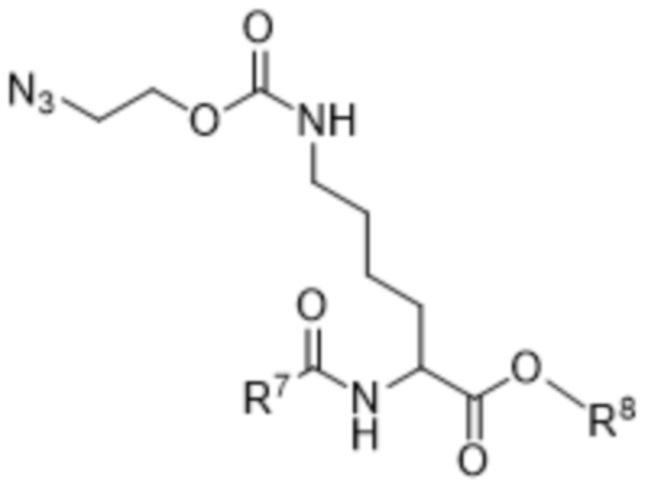
(VIII),
где
R7 выбран из -OR9, -CF3, -CH2C6-C12арила и C1-C6алкила;
R8 представляет собой -CH2C6-C12арил или C1-C6алкил; и
R9 выбран из C1-C6алкила, C6-C12арила и -CH2C6-C12арила.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[0046] Новые признаки настоящего изобретения конкретно изложены в прилагаемой формуле изобретения. Лучшее понимание признаков и преимуществ настоящего изобретения будет достигнуто посредством ссылки на следующее подробное описание, в котором изложены иллюстративные варианты осуществления, в которых используются принципы настоящего изобретения, и прилагаемые графические материалы, на которых представлено следующее.
[0047] На фиг. 1 показаны графики зависимости самонагревания и давления от температуры для N6-((2-азидоэтокси)карбонил)-N2-(трет-бутоксикарбонил)-L-лизината (формула (IIIa)) для исследования ARC, описанного в примере 10.
[0048] На фиг. 2 показаны графики зависимости температуры и давления от времени для N6-((2-азидоэтокси)карбонил)-N2-(трет-бутоксикарбонил)-L-лизината (формула (IIIa)) для исследования ARC, описанного в примере 10.
[0049] На фиг. 3 показан график согласно уравнению Антуана для N6-((2-азидоэтокси)карбонил)-N2-(трет-бутоксикарбонил)-L-лизината (формула (IIIa)) для исследования ARC, описанного в примере 10.
[0050] На фиг. 4 показан график отношения времени к максимальной скорости для N6-((2-азидоэтокси)карбонил)-N2-(трет-бутоксикарбонил)-L-лизината (формула (IIIa)) для исследования ARC, описанного в примере 10.
[0051] На фиг. 5 показан график зависимости времени (логарифмическая шкала) от температуры для N6-((2-азидоэтокси)карбонил)-N2-(трет-бутоксикарбонил)-L-лизината (формула (IIIa)) для исследования ARC, описанного в примере 10.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Определения
[0052] Если не указано иное, все технические и научные термины, используемые в данном документе, имеют то же значение, которое обычно понимается специалистом в области техники, к которой принадлежит заявляемый объект изобретения. Следует учитывать, что подробные описания являются исключительно иллюстративными и пояснительными и не ограничивают какой-либо заявляемый объект изобретения. В настоящей заявке применение единственного числа предусматривает множественное число, если специально не указано иное. Следует отметить, что используемая в данном описании форма единственного числа включает ссылки на множественное число, если контекстом явно не предписывается иное. В настоящей заявке использование "или" означает "и/или", если не указано иное. Кроме того, использование термина "включающий", а также других форм, таких как "включать", "включает" и "включенный", не является ограничивающим.
[0053] Хотя различные признаки настоящего изобретения могут быть описаны в контексте одного варианта осуществления, эти признаки также могут быть представлены отдельно или в любой подходящей комбинации. И наоборот, хотя настоящее изобретение может быть описано в данном документе в контексте отдельных вариантов осуществления для ясности, настоящее изобретение также может быть представлено в одном варианте осуществления.
[0054] Ссылка в настоящем описании на "некоторые варианты осуществления", "вариант осуществления", "один вариант осуществления" или "другие варианты осуществления" означает, что конкретные признак, структура или характеристика, описанные в связи с вариантами осуществления, включены в по меньшей мере некоторые варианты осуществления, но не обязательно во все варианты осуществления, настоящего изобретения.
[0055] Используемые в данном документе диапазоны и количества могут быть выражены как "приблизительно" конкретное значение или диапазон. "Приблизительно" также включает точное количество. Следовательно, "приблизительно 0°C" означает "приблизительно 0°C", а также "0°C." Как правило, термин "приблизительно" включает количество, которое, как ожидается, будет находиться в пределах экспериментальной погрешности, как, например, в пределах 15%, 10% или 5%.
[0056] Заголовки разделов, используемые в данном документе, предназначены исключительно для организационных целей и не должны толковаться как ограничивающие описываемый объект изобретения.
[0057] Термин "C1-C6алкил", применяемый в данном документе, означает aциклическую насыщенную углеводородную группу формулы CnH2n+1, содержащую от 1 до 6 атомов углерода и которая может быть линейной или разветвленной. Примеры таких групп включают без ограничения, метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, пентил, изоамил и гексил.
[0058] Термин "C6-C12арил", применяемый в данном документе, означает ароматический моноциклический или бициклический углеводород содержащий от шести до 12 атомов углерода в кольце, которые могут быть присоединены посредством одного из атомов углерода в кольце. Если C6-C12арил замещен, заместитель может быть расположена на атоме углерода в кольце. Конкретные примеры включают без ограничения фенил, толил, ксилил, триметилфенил и нафтил. Примеры заместителей арила включают без ограничения алкил, гидроксил, галоген, нитрил, алкокси, трифторметил, карбоксамидо, SO2CH3, бензил и замещенный бензил.
[0059] Хотя различные признаки настоящего изобретения могут быть описаны в контексте одного варианта осуществления, эти признаки также могут быть представлены отдельно или в любой подходящей комбинации. И наоборот, хотя настоящее изобретение может быть описано в данном документе в контексте отдельных вариантов осуществления для ясности, настоящее изобретение также может быть представлено в одном варианте осуществления.
Соединения и способы получения
Соединения формулы (I)
[0060] В данном документе описаны соединения формулы (I),
 (I),
(I),
где R1 выбран из хлора, брома и йода. В некоторых вариантах осуществления R1 представляет собой хлор. В некоторых вариантах осуществления R1 представляет собой бром. В некоторых вариантах осуществления R1 представляет собой йод.
[0061] Связь C-R1, где R1 представляет собой хлор, бром или йод, соединения формулы (I) имеет достаточную реакционную способность, чтобы обеспечить возможность протекания дополнительной реакции, например, с соединением формулы (V). В некоторых вариантах осуществления соединение формулы (I) является более реакционноспособным, чем фтористый аналог 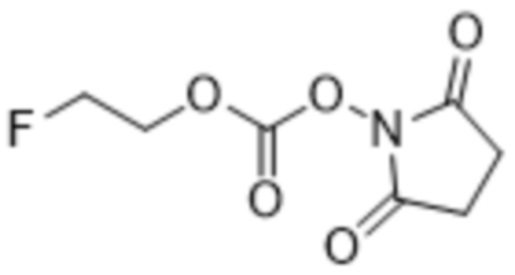 (документ WO2012/019299), например, с соединением формулы (V) с образованием соединения формулы (II). В некоторых вариантах осуществления скорость реакции соединения формулы (I) с соединением формулы (V) с образованием соединения формулы (II) быстрее, чем скорость реакции соответствующего фтористого аналога. В некоторых вариантах осуществления скорость реакции соединения формулы (I) с соединением формулы (V) с образованием соединения формулы (II) является более применимым для химического синтеза, чем скорость реакции с применением соответствующего фтористого аналога.
(документ WO2012/019299), например, с соединением формулы (V) с образованием соединения формулы (II). В некоторых вариантах осуществления скорость реакции соединения формулы (I) с соединением формулы (V) с образованием соединения формулы (II) быстрее, чем скорость реакции соответствующего фтористого аналога. В некоторых вариантах осуществления скорость реакции соединения формулы (I) с соединением формулы (V) с образованием соединения формулы (II) является более применимым для химического синтеза, чем скорость реакции с применением соответствующего фтористого аналога.
[0062] Соединения формулы (I) могут быть получены с применением исходных материалов, которые являются коммерчески доступными или легкодоступными благодаря способам, известным специалистам в данной области техники. Например, соединение формулы (I), где R1 представляет собой хлор, может быть получено посредством обеспечения проведения реакции 2-хлорэтилхлорформиата с N-гидроксисукцинимидом, оба из которых являются коммерчески доступными, или может быть получен способами, известными специалистам в данной области техники. Реакция 2-хлорэтилхлорформиата с N-гидроксисукцинимидом может быть проведена в растворе, содержащем апротонный растворитель, такой как ацетонитрил, ацетон, метилэтилкетон, дихлорметан, хлороформ, тетрагидрофуран, N-метилпирролидин, диметилсульфоксид, N,N-диметилформамид, диметилацетамид, 1,4-диоксан, сульфолан, гамма-бутиролактон, пирролидоны, 1-метил-2-пирролидинон, метилпирролин, монометиловый эфир этиленгликоля, монометиловый эфир диэтиленгликоля, PEG400 и полиэтиленгликоли. В некоторых вариантах осуществления апротонный растворитель, который можно применять, выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида и 1,4-диоксана. В других вариантах осуществления апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана и N,N-диметилформамида. В других дополнительных вариантах осуществления апротонный растворитель представляет собой ацетонитрил, ацетон, метилэтилкетон, дихлорметан, хлороформ или тетрагидрофуран. В некоторых вариантах осуществления апротонный растворитель, который можно применять, представляет собой 2-метилтетрагидрофуран. Раствор, в котором обеспечена возможность вступления в реакцию 2-галогенэтилхлорформиата с N-гидроксисукцинимидом, может дополнительно содержать основание, которое может содержать органическое основание, или неорганическое основание, или как органическое основание, так и неорганическое основание. В некоторых случаях применяемое органическое основание может быть выбрано из гетероциклического основания и триалкиламина или их смеси. Кроме того, если применяют гетероциклическое основание, то оно может быть выбрано из ароматического гетероциклического основания, или неароматического гетероциклического основания, или смеси ароматического гетероциклического основания и неароматического гетероциклического основания. Примеры ароматических гетероциклических оснований включают без ограничения пиридин, 1-алкилпиррол и 1-алкилимидазол или их смесь. Дополнительные примеры ароматических гетероциклических оснований, которые можно применять, включают пиридин, 1-метилпиррол и 1-метилимидазол или их смесь. В некоторых случаях применяемое гетероциклическое основание может представлять собой неароматическое гетероциклическое основание, включающее без ограничения N-алкилпирролидин, N-алкилпиперидин, N-алкилморфолин и 1,4-диалкилпиперазин или их смесь. Дополнительные примеры неароматических гетероциклических оснований, которые можно применять, включают без ограничения N-метилпирролидин, N-метилпиперидин и N-метилморфолин. В других случаях специалист в данной области техники может применять основание, которое представляет собой триалкиламин, примеры которого включают без ограничения триметиламин, триэтиламин, три-н-пропиламин, три-н-бутиламин, трипентиламин, тригексиламин и диизопропилэтиламин. В некоторых вариантах осуществления основание представляет собой триэтиламин. Реакция соединения 2-галогенэтилхлорформиата с N-гидроксисукцинимидом может быть дополнительно проведена при температуре в диапазоне от приблизительно -25oC до приблизительно 100oC или в диапазоне от приблизительно 0oC до приблизительно комнатной температуры. В некоторых вариантах осуществления реакцию проводят при температуре приблизительно 0°C. В приведенных выше вариантах осуществления и любых вариантах осуществления, описанных в данном документе, где применяют апротонный растворитель, реакционный растворитель может по сути не содержать или не содержать протонные растворители. "По сути не содержит" означает, что упомянутое вещество отсутствует или присутствует в достаточно низком количестве, чтобы оказывать незначительное воздействие на реакцию (например, влияние менее 15%, 10% или 5%, оказываемое на выход реакции).
[0063] Пример способа, который можно применять для получения соединения формулы (I), где R1 представляет собой хлор, показан ниже на схеме 1.
Схема 1
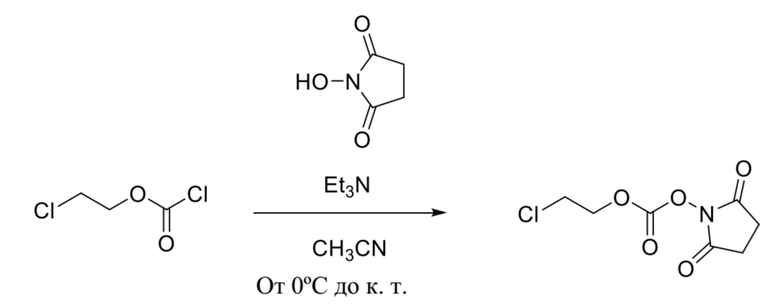
Подобные способы можно применять для получения соединений формулы (I), где R1 представляет собой бром или йод с применением 2-бромэтилхлорформиата или 2-йодметилхлорформиата соответственно. Соединение 2-бромэтилхлорформиат является коммерчески доступным или может быть получено способами, известными специалистам в данной области техники. Получение 2-йодметилхлорформиата описано в Grimshaw et al., Journal of the Chemical Society, 1965, pp. 7136-9.
[0064] В одном аспекте, представленном в данном документе, предусмотрены способы получения соединения формулы (I),
 (I),
(I),
включающие обеспечение проведения реакции соединения формулы (IV),
 (IV),
(IV),
с N-гидроксисукцинимидом с получением соединения формулы (I), где в каждом из соединений формулы (I) и (IV) R1 является одинаковым и выбран из хлора, брома и йода. В некоторых вариантах осуществления способов R1 представляет собой хлор. В некоторых вариантах осуществления способов R1 представляет собой бром. В некоторых вариантах осуществления способов R1 представляет собой йод.
[0065] В некоторых вариантах осуществления способов получения соединения формулы (I), раскрытых в данном документе, реакцию соединения формулы (IV) с N-гидроксисукцинимидом проводят в растворе, содержащем апротонный растворитель. В некоторых вариантах осуществления апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400 и полиэтиленгликолей. В некоторых вариантах осуществления апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида и 1,4-диоксана. В некоторых вариантах осуществления апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана и N,N-диметилформамида. В некоторых вариантах осуществления апротонный растворитель представляет собой ацетонитрил. В некоторых вариантах осуществления апротонный растворитель представляет собой ацетон. В некоторых вариантах осуществления апротонный растворитель представляет собой метилэтилкетон. В некоторых вариантах осуществления апротонный растворитель представляет собой дихлорметан. В некоторых вариантах осуществления апротонный растворитель представляет собой хлороформ. В некоторых вариантах осуществления апротонный растворитель представляет собой тетрагидрофуран. В некоторых вариантах осуществления апротонный растворитель представляет собой 2-метилтетрагидрофуран. В некоторых вариантах осуществления апротонный растворитель представляет собой N,N-диметилформамид.
[0066] В некоторых вариантах осуществления раствор дополнительно содержит основание. В некоторых вариантах осуществления основание выбрано из органического основания и неорганического основания. В некоторых вариантах осуществления органическое основание выбрано из гетероциклического основания и триалкиламина или их смеси. В некоторых вариантах осуществления гетероциклическое основание представляет собой ароматическое гетероциклическое основание, или неароматическое гетероциклическое основание, или смесь ароматического гетероциклического основания и неароматического гетероциклического основания. В некоторых вариантах осуществления гетероциклическое основание представляет собой ароматическое гетероциклическое основание. В некоторых вариантах осуществления ароматическое гетероциклическое основание выбрано из пиридина, 1-алкилпиррола и 1-алкилимидазола или их смеси. В некоторых вариантах осуществления ароматическое гетероциклическое основание выбрано из пиридина, 1-метилпиррола и 1-метилимидазола или их смеси. В некоторых вариантах осуществления ароматическое гетероциклическое основание представляет собой пиридин. В некоторых вариантах осуществления ароматическое гетероциклическое основание представляет собой 1-метилпиррол. В некоторых вариантах осуществления ароматическое гетероциклическое основание представляет собой 1-метилимидазол. В некоторых вариантах осуществления гетероциклическое основание представляет собой неароматическое гетероциклическое основание. В некоторых вариантах осуществления неароматическое гетероциклическое основание выбрано из N-алкилпирролидина, N-алкилпиперидина, N-алкилморфолина и 1,4-диалкилпиперазина или их смеси. В некоторых вариантах осуществления неароматическое гетероциклическое основание представляет собой N-алкилпирролидин. В некоторых вариантах осуществления неароматическое гетероциклическое основание представляет собой N-алкилпиперидин. В некоторых вариантах осуществления неароматическое гетероциклическое основание представляет собой N-алкилморфолин. В некоторых вариантах осуществления неароматическое гетероциклическое основание представляет собой 1,4-диалкилпиперазин. В некоторых вариантах осуществления неароматическое гетероциклическое основание выбрано из N-метилпирролидина, N-метилпиперидина и N-метилморфолина. В некоторых вариантах осуществления неароматическое гетероциклическое основание представляет собой N-метилпирролидин. В некоторых вариантах осуществления неароматическое гетероциклическое основание представляет собой N-метилпиперидин. В некоторых вариантах осуществления неароматическое гетероциклическое основание представляет собой N-метилморфолин. В некоторых вариантах осуществления органическое основание представляет собой триалкиламин. В некоторых вариантах осуществления триалкиламин выбран из триметиламина, триэтиламина, три-н-пропиламина, три-н-бутиламина, трипентиламина, тригексиламина и диизопропилэтиламина. В некоторых вариантах осуществления триалкиламин выбран из триметиламина, триэтиламина, три-н-пропиламина и диизопропилэтиламина. В некоторых вариантах осуществления триалкиламин выбран из триэтиламина, три-н-пропиламина и диизопропилэтиламина. В некоторых вариантах осуществления триалкиламин представляет собой триэтиламин или диизопропилэтиламин. В некоторых вариантах осуществления триалкиламин представляет собой триэтиламин. В некоторых вариантах осуществления триалкиламин представляет собой диизопропилэтиламин.
[0067] В некоторых вариантах осуществления способов получения соединения формулы (I), раскрытых в данном документе, R1 в соединении формулы (I) представляет собой хлор, и апротонный растворитель представляет собой ацетонитрил. В некоторых вариантах осуществления раствор дополнительно содержит основание. В некоторых вариантах осуществления основание выбрано из триалкиламина. В некоторых вариантах осуществления триалкиламин выбран из триметиламина, триэтиламина, три-н-пропиламина, три-н-бутиламина, трипентиламина, тригексиламина и диизопропилэтиламина. В некоторых вариантах осуществления триалкиламин выбран из триметиламина, триэтиламина, три-н-пропиламина и диизопропилэтиламина. В некоторых вариантах осуществления триалкиламин выбран из триэтиламина, три-н-пропиламина и диизопропилэтиламина. В некоторых вариантах осуществления триалкиламин представляет собой триэтиламин или диизопропилэтиламин. В некоторых вариантах осуществления триалкиламин представляет собой триэтиламин. В некоторых вариантах осуществления триалкиламин представляет собой диизопропилэтиламин.
[0068] В некоторых вариантах осуществления способов получения соединения формулы (I), раскрытых в данном документе, R1 в соединении формулы (I) представляет собой бром, и апротонный растворитель представляет собой ацетонитрил. В некоторых вариантах осуществления раствор дополнительно содержит основание. В некоторых вариантах осуществления основание выбрано из триалкиламина. В некоторых вариантах осуществления триалкиламин выбран из триметиламина, триэтиламина, три-н-пропиламина, три-н-бутиламина, трипентиламина, тригексиламина и диизопропилэтиламина. В некоторых вариантах осуществления триалкиламин выбран из триметиламина, триэтиламина, три-н-пропиламина и диизопропилэтиламина. В некоторых вариантах осуществления триалкиламин выбран из триэтиламина, три-н-пропиламина и диизопропилэтиламина. В некоторых вариантах осуществления триалкиламин представляет собой триэтиламин или диизопропилэтиламин. В некоторых вариантах осуществления триалкиламин представляет собой триэтиламин. В некоторых вариантах осуществления триалкиламин представляет собой диизопропилэтиламин.
[0069] В некоторых вариантах осуществления способов получения соединения формулы (I), раскрытых в данном документе, R1 в соединении формулы (I) представляет собой йод, и апротонный растворитель представляет собой ацетонитрил. В некоторых вариантах осуществления раствор дополнительно содержит основание. В некоторых вариантах осуществления основание выбрано из триалкиламина. В некоторых вариантах осуществления триалкиламин выбран из триметиламина, триэтиламина, три-н-пропиламина, три-н-бутиламина, трипентиламина, тригексиламина и диизопропилэтиламина. В некоторых вариантах осуществления триалкиламин выбран из триметиламина, триэтиламина, три-н-пропиламина и диизопропилэтиламина. В некоторых вариантах осуществления триалкиламин выбран из триэтиламина, три-н-пропиламина и диизопропилэтиламина. В некоторых вариантах осуществления триалкиламин представляет собой триэтиламин или диизопропилэтиламин. В некоторых вариантах осуществления триалкиламин представляет собой триэтиламин. В некоторых вариантах осуществления триалкиламин представляет собой диизопропилэтиламин.
Соединения формулы (II)
[0070] Также в данном документе раскрыты соединения формулы (II),
 (II),
(II),
где R1 выбран из хлора, брома и йода.
[0071] В некоторых вариантах осуществления соединений формулы (II) R1 представляет собой хлор. В некоторых вариантах осуществления соединений формулы (II) R1 представляет собой бром. В некоторых вариантах осуществления соединений формулы (II) R1 представляет собой йод.
[0072] Также в данном документе раскрыты соединения формулы (IIa),
 (IIa),
(IIa),
где R1 выбран из хлора, брома и йода.
[0073] В некоторых вариантах осуществления соединений формулы (IIa) R1 представляет собой хлор. В некоторых вариантах осуществления соединений формулы (IIa) R1 представляет собой бром. В некоторых вариантах осуществления соединений формулы (IIa) R1 представляет собой йод.
[0074] Также в данном документе раскрыты соединения формулы (IIb),
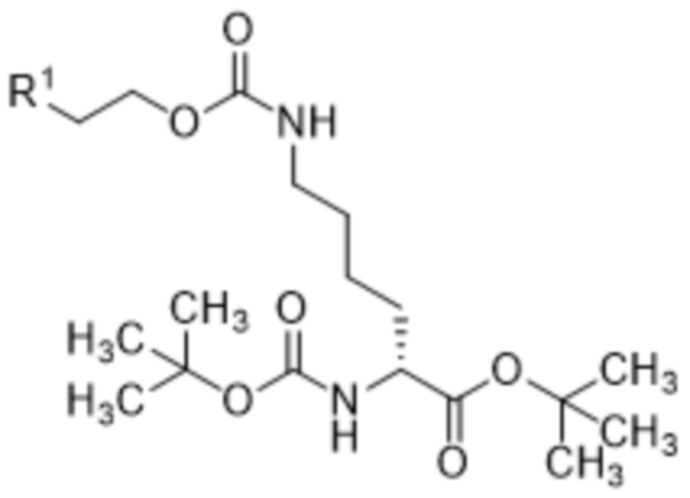 (IIb),
(IIb),
где R1 выбран из хлора, брома и йода.
[0075] В некоторых вариантах осуществления соединений формулы (IIb) R1 представляет собой хлор. В некоторых вариантах осуществления соединений формулы (IIb) R1 представляет собой бром. В некоторых вариантах осуществления соединений формулы (IIb) R1 представляет собой йод.
[0076] Соединения формулы (II) могут быть получены посредством обеспечения проведения реакции соединения формулы (I), где R1 выбран из хлора, брома и йода,
 (I),
(I),
с соединением формулы (V),
 (V),
(V),
с получением соединения формулы (II). В некоторых вариантах осуществления R1 представляет собой хлор. В некоторых вариантах осуществления R1 представляет собой бром. В некоторых вариантах осуществления R1 представляет собой йод.
[0077] Реакция соединения формулы (I) с соединением формулы (V) может быть проведена в растворе, содержащем апротонный растворитель, такой как ацетонитрил, ацетон, метилэтилкетон, дихлорметан, хлороформ, тетрагидрофуран, N-метилпирролидин, диметилсульфоксид, N,N-диметилформамид, диметилацетамид, 1,4-диоксан, сульфолан, гамма-бутиролактон, пирролидоны, 1-метил-2-пирролидинон, метилпирролин, монометиловый эфир этиленгликоля, монометиловый эфир диэтиленгликоля, PEG400 и полиэтиленгликоли. В некоторых вариантах осуществления апротонный растворитель, который можно применять, выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида и 1,4-диоксана. В других вариантах осуществления апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана и N,N-диметилформамида. В других дополнительных вариантах осуществления апротонный растворитель представляет собой ацетонитрил, или ацетон, или метилэтилкетон, или дихлорметан, или хлороформ, или тетрагидрофуран. В некоторых вариантах осуществления апротонный растворитель представляет собой ацетонитрил. В некоторых вариантах осуществления апротонный растворитель представляет собой ацетон. В некоторых вариантах осуществления апротонный растворитель представляет собой метилэтилкетон. В некоторых вариантах осуществления апротонный растворитель представляет собой дихлорметан. В некоторых вариантах осуществления апротонный растворитель представляет собой хлороформ. В некоторых вариантах осуществления апротонный растворитель представляет собой тетрагидрофуран. В некоторых вариантах осуществления апротонный растворитель представляет собой 2-метилтетрагидрофуран. В некоторых вариантах осуществления апротонный растворитель представляет собой N,N-диметилформамид.
[0078] Раствор, в котором обеспечивается проведение реакции соединения формулы (I) с соединением формулы (V), может дополнительно содержать основание, которое может предусматривать органическое основание, или неорганическое основание, или как органическое основание, так и неорганическое основание. В некоторых случаях применяемое органическое основание может быть выбрано из гетероциклического основания и триалкиламина или их смеси. Кроме того, если применяют гетероциклическое основание, то оно может быть выбрано из ароматического гетероциклического основания, или неароматического гетероциклического основания, или смеси ароматического гетероциклического основания и неароматического гетероциклического основания. Примеры ароматических гетероциклических оснований включают без ограничения пиридин, 1-алкилпиррол и 1-алкилимидазол или их смесь. Дополнительные примеры ароматических гетероциклических оснований, которые можно применять, включают пиридин, 1-метилпиррол и 1-метилимидазол или их смесь. В некоторых случаях применяемое гетероциклическое основание может представлять собой неароматическое гетероциклическое основание, включающее без ограничения N-алкилпирролидин, N-алкилпиперидин, N-алкилморфолин и 1,4-диалкилпиперазин или их смесь. Дополнительные примеры неароматических гетероциклических оснований, которые можно применять, включают без ограничения N-метилпирролидин, N-метилпиперидин и N-метилморфолин. В других случаях специалист в данной области техники может применять основание, которое представляет собой триалкиламин, примеры которого включают без ограничения триметиламин, триэтиламин, три-н-пропиламин, три-н-бутиламин, трипентиламин, тригексиламин и диизопропилэтиламин. В некоторых вариантах осуществления основание представляет собой диизопропилэтиламин.
[0079] Реакция соединения формулы (I) с соединением формулы (V) может быть дополнительно проведена при температуре в диапазоне от приблизительно -25°C до приблизительно 100°C или в диапазоне от приблизительно 0°C до приблизительно комнатной температуры. В некоторых вариантах осуществления реакцию проводят при температуре приблизительно 10°C.
[0080] Пример способа, который можно применять для получения соединения формулы (II), показан ниже на схеме 2.
Схема 2
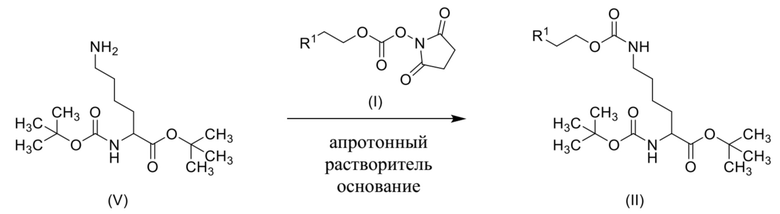
Пример способа, который можно применять для получения соединения формулы (II), где R1 представляет собой хлор, показан ниже на схеме 3.
Схема 3
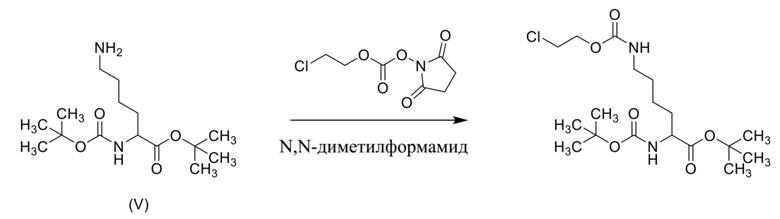
[0081] Соединения формулы (IIa) и (IIb) могут быть получены с применением способов, которые подобны способам, описанным выше, с применением L-энантиомера или D-энантиомера соединения формулы (V), как показано ниже на схеме 4 и схеме 5.
Схема 4
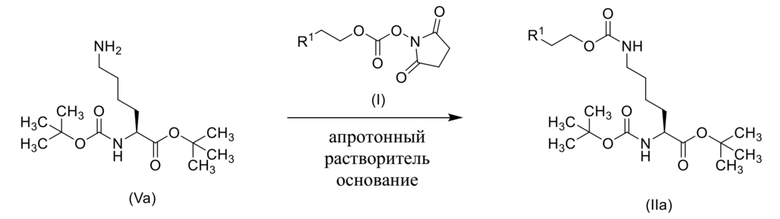
Схема 5
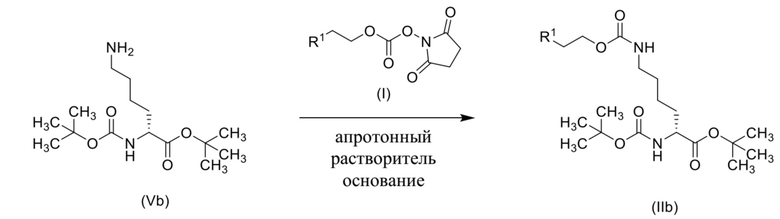
[0082] Также в данном документе раскрыты способы получения соединения формулы (IIa),
 (IIa),
(IIa),
включающие обеспечение проведения реакции соединения формулы (I),
 (I),
(I),
с соединением формулы (Va),
 (Va),
(Va),
с получением соединения формулы (IIa), где R1 выбран из хлора, брома и йода. В некоторых вариантах осуществления способов R1 представляет собой хлор. В некоторых вариантах осуществления способов R1 представляет собой бром. В некоторых вариантах осуществления способов R1 представляет собой йод. В некоторых вариантах осуществления реакцию соединения формулы (Va) с соединением формулы (I) проводят в растворе, содержащем апротонный растворитель. В некоторых вариантах осуществления апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N, N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400 и полиэтиленгликолей. В некоторых вариантах осуществления апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида и 1,4-диоксана. В некоторых вариантах осуществления апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана и N,N-диметилформамида. В некоторых вариантах осуществления апротонный растворитель представляет собой ацетонитрил. В некоторых вариантах осуществления апротонный растворитель представляет собой ацетон. В некоторых вариантах осуществления апротонный растворитель представляет собой метилэтилкетон. В некоторых вариантах осуществления апротонный растворитель представляет собой дихлорметан. В некоторых вариантах осуществления апротонный растворитель представляет собой хлороформ. В некоторых вариантах осуществления апротонный растворитель представляет собой тетрагидрофуран. В некоторых вариантах осуществления апротонный растворитель представляет собой 2-метилтетрагидрофуран. В некоторых вариантах осуществления апротонный растворитель представляет собой N,N-диметилформамид.
[0083] Также в данном документе раскрыты способы получения соединения формулы (IIb),
 (IIb),
(IIb),
включающие обеспечение проведения реакции соединения формулы (I),
 (I),
(I),
с соединением формулы (Vb),
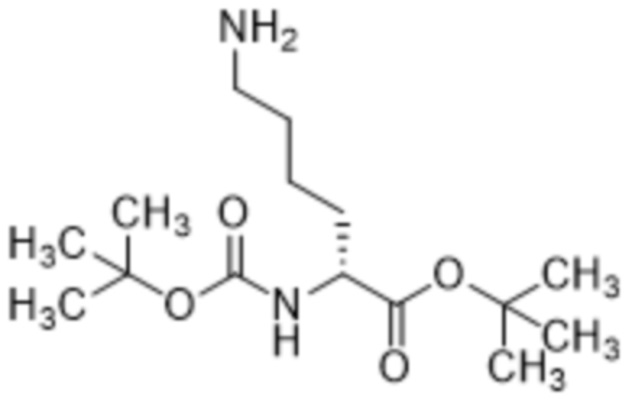 (Vb),
(Vb),
с получением соединения формулы (IIb), где R1 выбран из хлора, брома и йода. В некоторых вариантах осуществления способов R1 представляет собой хлор. В некоторых вариантах осуществления способов R1 представляет собой бром. В некоторых вариантах осуществления способов R1 представляет собой йод. В некоторых вариантах осуществления реакцию соединения формулы (Vb) с соединением формулы (I) проводят в растворе, содержащем апротонный растворитель. В некоторых вариантах осуществления апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400 и полиэтиленгликолей. В некоторых вариантах осуществления апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида и 1,4-диоксана. В некоторых вариантах осуществления апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана и N,N-диметилформамида. В некоторых вариантах осуществления апротонный растворитель представляет собой ацетонитрил. В некоторых вариантах осуществления апротонный растворитель представляет собой ацетон. В некоторых вариантах осуществления апротонный растворитель представляет собой метилэтилкетон. В некоторых вариантах осуществления апротонный растворитель представляет собой дихлорметан. В некоторых вариантах осуществления апротонный растворитель представляет собой хлороформ. В некоторых вариантах осуществления апротонный растворитель представляет собой тетрагидрофуран. В некоторых вариантах осуществления апротонный растворитель представляет собой 2-метилтетрагидрофуран. В некоторых вариантах осуществления апротонный растворитель представляет собой N, N-диметилформамид.
[0084] Соединения формулы (V), содержащие L-энантиомер и D-энантиомер, являются коммерчески доступными или могут быть получены способами, известными специалистам в данной области техники.
Соединения формулы (III)
[0085] Также в данном документе раскрыты соединения формулы (III),
 (III).
(III).
[0086] В некоторых вариантах осуществления соединение формулы (III) представляет собой соединение формулы (IIIa),
 (IIIa).
(IIIa).
[0087] В некоторых вариантах осуществления соединение формулы (III) представляет собой соединение формулы (IIIb),
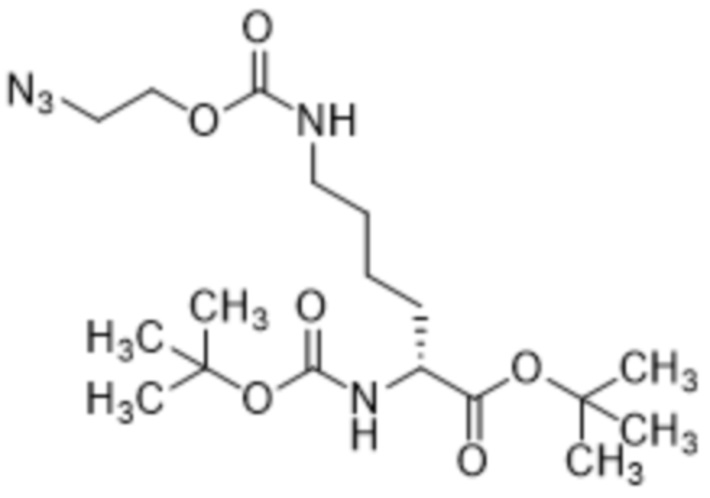 (IIIb).
(IIIb).
[0088] Соединения формулы (III) могут быть получены посредством обеспечения проведения реакции соединения формулы (II), где R1 выбран из хлора, брома и йода, с азидной солью щелочного металла с получением соединения формулы (III). В некоторых вариантах осуществления азидная соль щелочного металла выбрана из азида лития, азида натрия и азида калия. В некоторых случаях азидная соль щелочного металла представляет собой азид лития. В других случаях азидная соль щелочного металла представляет собой азид натрия. В других дополнительных случаях азидная соль щелочного металла представляет собой азид калия. Реакция соединения формулы (II) с азидной солью щелочного металла может быть проведена в растворе, содержащем апротонный растворитель, протонный растворитель или их смесь. Апротонный растворитель, который можно применять, может быть выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400 и полиэтиленгликолей. В некоторых случаях апротонный растворитель выбран из ацетонитрила, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида и 1,4-диоксана. В некоторых вариантах осуществления апротонный растворитель представляет собой ацетонитрил. В некоторых вариантах осуществления апротонный растворитель представляет собой тетрагидрофуран. В некоторых вариантах осуществления апротонный растворитель представляет собой 2-метилтетрагидрофуран. В некоторых вариантах осуществления апротонный растворитель представляет собой N,N-диметилформамид. В некоторых вариантах осуществления апротонный растворитель представляет собой 1,4-диоксан. В некоторых случаях реакция соединения формулы (II) с азидной солью щелочного металла может быть проведена в растворе, содержащем смесь апротонного растворителя и протонного растворителя, где апротонный растворитель является таким, как описано выше, а протонный растворитель может быть выбран из воды и спирта. В некоторых вариантах осуществления протонный растворитель представляет собой воду. В некоторых вариантах осуществления протонный растворитель представляет собой спирт. Примеры спиртов, которые можно применять, включают без ограничения метанол, этанол, н-пропанол, изопропанол, н-бутанол, изобутанол, н-пентанол и изопентанол. В некоторых вариантах осуществления спирт выбран из метанола, этанола, н-пропанола и изопропанола. В некоторых случаях раствор может содержать смесь воды и 1,4-диоксана. В некоторых случаях раствор может содержать смесь воды и ацетонитрила. Реакция соединения формулы (II), где R1 выбран из хлора, брома и йода, с азидной солью щелочного металла может быть проведена при температуре в диапазоне от приблизительно 25°C до приблизительно 150°C или от приблизительно 75°C до приблизительно 80°C. В некоторых вариантах осуществления реакцию проводят при температуре приблизительно 80°C.
[0089] Пример способа, который можно применять для получения соединения формулы (III) посредством реакции соединения формулы (II), где R1 выбран из хлора, брома и йода, для проведения реакции с азидной солью щелочного металла, показан ниже на схеме 6.
Схема 6
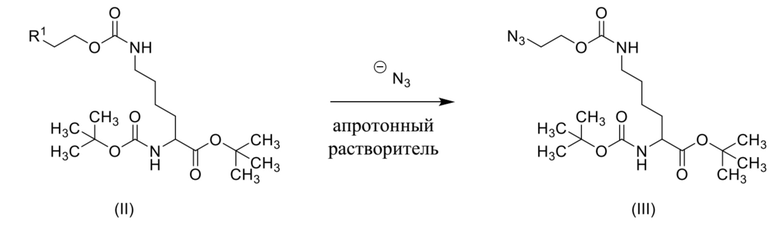
Пример способа, который можно применять для получения соединения формулы (III) посредством реакции соединения формулы (II), где R1 представляет собой хлор, и азида натрия, показан ниже на схеме 7.
Схема 7
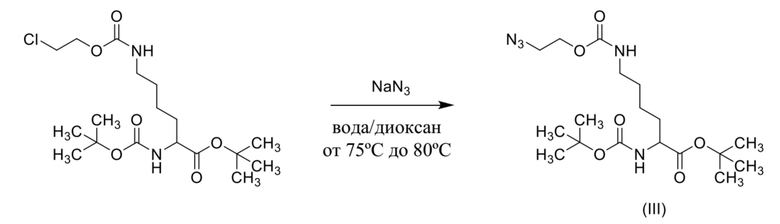
[0090] Соединения формулы (IIIa) и (IIIb) могут быть получены с применением способов, которые подобны способам, описанным выше, с применением L-энантиомера или D-энантиомера соединения формулы (II), как показано ниже на схеме 8 и схеме 9.
Схема 8
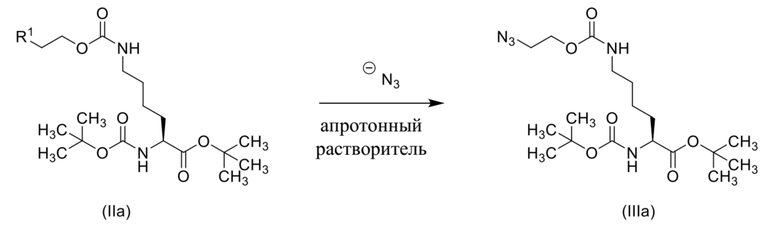
Схема 9
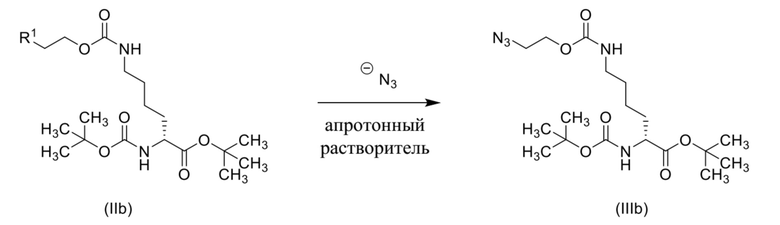
[0091] Также в данном документе раскрыты способы получения соединения формулы (IIIa),
 (IIIa),
(IIIa),
включающие обеспечение проведения реакции соединения формулы (IIa),
 (IIa),
(IIa),
где R1 выбран из хлора, брома и йода, с азидной солью щелочного металла с получением соединения формулы (IIIa). В некоторых вариантах осуществления азидная соль щелочного металла выбрана из азида лития, азида натрия и азида калия. В некоторых вариантах осуществления азидная соль щелочного металла представляет собой азид лития. В некоторых вариантах осуществления азидная соль щелочного металла представляет собой азид натрия. В некоторых вариантах осуществления азидная соль щелочного металла представляет собой азид калия. В некоторых вариантах осуществления реакцию соединения формулы (IIa) с азидной солью щелочного металла проводят в растворе, содержащем апротонный растворитель, протонный растворитель или их смесь. В некоторых вариантах осуществления апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N, N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400 и полиэтиленгликолей. В некоторых вариантах осуществления апротонный растворитель выбран из ацетонитрила, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N, N-диметилформамида, диметилацетамида и 1,4-диоксана. В некоторых вариантах осуществления апротонный растворитель выбран из ацетонитрила, тетрагидрофурана, N, N-диметилформамида и 1,4-диоксана. В некоторых вариантах осуществления апротонный растворитель представляет собой ацетонитрил. В некоторых вариантах осуществления апротонный растворитель представляет собой тетрагидрофуран. В некоторых вариантах осуществления апротонный растворитель представляет собой 2-метилтетрагидрофуран. В некоторых вариантах осуществления апротонный растворитель представляет собой N, N-диметилформамид. В некоторых вариантах осуществления апротонный растворитель представляет собой 1,4-диоксан. В некоторых вариантах осуществления реакцию соединения формулы (IIa) с азидной солью щелочного металла проводят в растворе, содержащем смесь апротонного растворителя и протонного растворителя. В некоторых вариантах осуществления протонный растворитель выбран из воды и спирта. В некоторых вариантах осуществления протонный растворитель представляет собой воду. В некоторых вариантах осуществления протонный растворитель представляет собой спирт. В некоторых вариантах осуществления спирт выбран из метанола, этанола, н-пропанола, изопропанола, н-бутанола, изобутанола, н-пентанола и изопентанола. В некоторых вариантах осуществления спирт выбран из метанола, этанола, н-пропанола и изопропанола. В некоторых вариантах осуществления раствор содержит смесь воды и 1,4-диоксана. В некоторых вариантах осуществления раствор содержит смесь воды и ацетонитрила.
[0092] Также в данном документе раскрыты способы получения соединения формулы (IIIb),
 (IIIb),
(IIIb),
включающие обеспечение проведения реакции соединения формулы (IIb),
 (IIb),
(IIb),
где R1 выбран из хлора, брома и йода, с азидной солью щелочного металла с получением соединения формулы (IIIb). В некоторых вариантах осуществления азидная соль щелочного металла выбрана из азида лития, азида натрия и азида калия. В некоторых вариантах осуществления азидная соль щелочного металла представляет собой азид лития. В некоторых вариантах осуществления азидная соль щелочного металла представляет собой азид натрия. В некоторых вариантах осуществления азидная соль щелочного металла представляет собой азид калия. В некоторых вариантах осуществления реакцию соединения формулы (IIb) с азидной солью щелочного металла проводят в растворе, содержащем апротонный растворитель, протонный растворитель или их смесь. В некоторых вариантах осуществления апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N, N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400 и полиэтиленгликолей. В некоторых вариантах осуществления апротонный растворитель выбран из ацетонитрила, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N, N-диметилформамида, диметилацетамида и 1,4-диоксана. В некоторых вариантах осуществления апротонный растворитель выбран из ацетонитрила, тетрагидрофурана, N, N-диметилформамида и 1,4-диоксана. В некоторых вариантах осуществления апротонный растворитель представляет собой ацетонитрил. В некоторых вариантах осуществления апротонный растворитель представляет собой тетрагидрофуран. В некоторых вариантах осуществления апротонный растворитель представляет собой 2-метилтетрагидрофуран. В некоторых вариантах осуществления апротонный растворитель представляет собой N, N-диметилформамид. В некоторых вариантах осуществления апротонный растворитель представляет собой 1,4-диоксан. В некоторых вариантах осуществления реакцию соединения формулы (IIb) с азидной солью щелочного металла проводят в растворе, содержащем смесь апротонного растворителя и протонного растворителя. В некоторых вариантах осуществления протонный растворитель выбран из воды и спирта. В некоторых вариантах осуществления протонный растворитель представляет собой воду. В некоторых вариантах осуществления протонный растворитель представляет собой спирт. В некоторых вариантах осуществления спирт выбран из метанола, этанола, н-пропанола, изопропанола, н-бутанола, изобутанола, н-пентанола и изопентанола. В некоторых вариантах осуществления спирт выбран из метанола, этанола, н-пропанола и изопропанола. В некоторых вариантах осуществления раствор содержит смесь воды и 1,4-диоксана. В некоторых вариантах осуществления раствор содержит смесь воды и ацетонитрила.
Соединения формулы (VI)
[0093] Также в данном документе раскрыты способы получения соединения формулы (VI),
 (VI),
(VI),
или его соли, включающие обеспечение проведения реакции соединения формулы (III),
 (III),
(III),
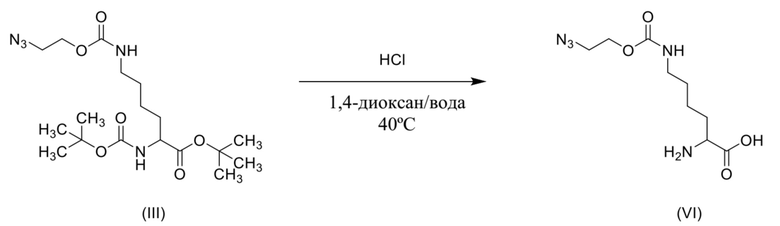
с кислотой с получением соединения формулы (VI) или его соли. В некоторых вариантах осуществления соединение формулы (VI) выделено в виде его соли. В некоторых вариантах осуществления соединение формулы (VI) превращают в его соль с применением способов, известных из уровня техники специалисту в данной области техники. В некоторых вариантах осуществления реакцию соединения формулы (III) с кислотой проводят в растворе, содержащем апротонный растворитель, протонный растворитель или их смесь. Апротонные растворители, которые можно применять для проведения реакции, включают без ограничения ацетонитрил, ацетон, метилэтилкетон, дихлорметан, хлороформ, тетрагидрофуран, N-метилпирролидин, диметилсульфоксид, N,N-диметилформамид, диметилацетамид, 1,4-диоксан, сульфолан, гамма-бутиролактон, пирролидоны, 1-метил-2-пирролидинон, метилпирролин, монометиловый эфир этиленгликоля, монометиловый эфир диэтиленгликоля, PEG400 и полиэтиленгликоли. В некоторых вариантах осуществления апротонный растворитель выбран из ацетонитрила, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида и 1,4-диоксана. В других случаях апротонный растворитель выбран из ацетонитрила, тетрагидрофурана, N,N-диметилформамида и 1,4-диоксана. В некоторых вариантах осуществления апротонный растворитель представляет собой ацетонитрил. В некоторых вариантах осуществления апротонный растворитель представляет собой тетрагидрофуран. В некоторых вариантах осуществления апротонный растворитель представляет собой 2-метилтетрагидрофуран. В некоторых вариантах осуществления апротонный растворитель представляет собой N,N-диметилформамид. В некоторых вариантах осуществления апротонный растворитель представляет собой 1,4-диоксан. В некоторых случаях реакцию соединения формулы (III) с кислотой проводят в растворе, содержащем смесь протонного растворителя и апротонного растворителя, где протонный растворитель предусматривает, например, воду. В некоторых вариантах осуществления реакцию соединения формулы (III) с кислотой проводят в растворе, содержащем смесь 1,4-диоксана и воды. Реакция соединения формулы (III) с кислотой может быть проведена с применением кислот, которые включают без ограничения фосфорную кислоту, хлористоводородную кислоту, уксусную кислоту и трифторуксусную кислоту. В некоторых случаях кислота может представлять собой фосфорную кислоту. В других случаях кислота может представлять собой хлористоводородную кислоту. В других случаях кислота может представлять собой уксусную кислоту. В дополнительных случаях кислота может представлять собой трифторуксусную кислоту. В некоторых вариантах осуществления основание добавляют к кислотной смеси, содержащей соединение формулы (III). В некоторых вариантах осуществления основание представляет собой гидроксид аммония, гидроксид натрия или гидроксид калия. В некоторых вариантах осуществления основание представляет собой гидроксид аммония. В некоторых вариантах осуществления основание добавляют к смеси кислоты, содержащей соединение формулы (III), чтобы довести pH раствора до значения в диапазоне от приблизительно 4 до 10. В некоторых вариантах осуществления основание добавляют к смеси кислоты, содержащей соединение формулы (III), чтобы довести pH раствора до значения в диапазоне от приблизительно 7 до 9,5. В некоторых вариантах осуществления pH раствора регулируют до значения в диапазоне от приблизительно 8 до 9,5. В некоторых вариантах осуществления основание добавляют к смеси кислоты, содержащей соединение формулы (III), чтобы довести pH раствора до значения в диапазоне от приблизительно 7 до 9. В некоторых вариантах осуществления pH раствора регулируют до значения в диапазоне от приблизительно 7 до 8. В некоторых вариантах осуществления pH раствора регулируют до значения в диапазоне от приблизительно 8 до 9. В некоторых вариантах осуществления pH раствора регулируют до приблизительно 4. В некоторых вариантах осуществления pH раствора регулируют до приблизительно 5. В некоторых вариантах осуществления pH раствора регулируют до приблизительно 6. В некоторых вариантах осуществления pH раствора регулируют до приблизительно 7. В некоторых вариантах осуществления pH раствора регулируют до приблизительно 8. В некоторых вариантах осуществления pH раствора регулируют до приблизительно 9. В некоторых вариантах осуществления pH раствора регулируют до приблизительно 10. Реакция может быть проведена при температуре в диапазоне от приблизительно 0°C до приблизительно 100°C, или от приблизительно 25°C до приблизительно 75°C, или от приблизительно 25°C до приблизительно 50°C, или при приблизительно 40°C. В некоторых вариантах осуществления реакцию проводят при температуре в диапазоне от приблизительно 0°C до приблизительно 50°C, такой как от приблизительно 10°C до приблизительно 45°C.
[0094] Пример, в котором обеспечено проведение реакции соединения формулы (III) с кислотой с получением соединение формулы (VI), показан ниже, при этом в нем обеспечено проведение реакции соединения формулы (III) с хлористоводородной кислотой в смеси ацетонитрила и воды при температуре 40oC с получением соединения формулы (VI). Соединение формулы (VI) может быть выделено в виде соли, например гидрохлоридной соли, или оно может быть выделено в виде цвиттер-ионной формы соединения посредством нейтрализации реакционной смеси после реакции соединения формулы (III) с кислотой, как показано на схеме 10.
Схема 10
[0095] Соединения формулы (VIa) и (VIb) могут быть получены, как описано выше для соединений формулы (VI), где соединению формулы (IIIa) или формулы (IIIb) обеспечена возможность вступления в реакцию с кислотой, как описано выше и как показано ниже на схемах 11 и 12.
Схема 11
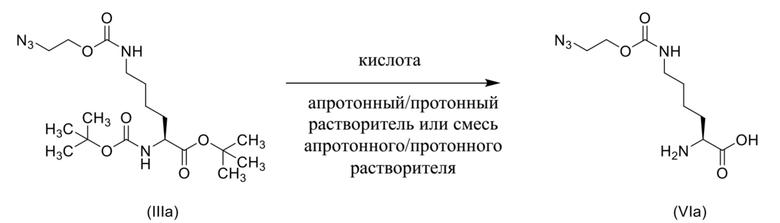
Схема 12
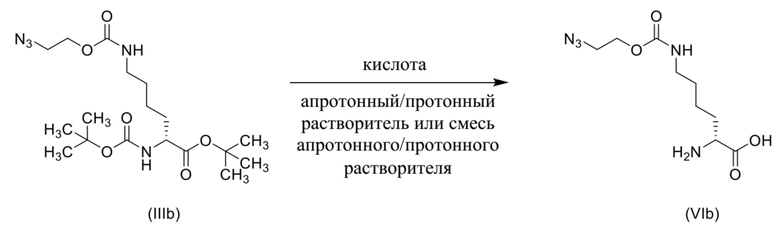
[0096] Также в данном документе раскрыты способы получения соединения формулы (VIa),
 (VIa),
(VIa),
или его соли, включающие обеспечение проведения реакции соединения формулы (IIIa)
 (IIIa),
(IIIa),
с кислотой с получением соединения формулы (VIa) или его соли. В некоторых вариантах осуществления реакцию соединения формулы (IIIa) с кислотой проводят в растворе, содержащем апротонный растворитель, протонный растворитель или их смесь. В некоторых вариантах осуществления апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N, N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400 и полиэтиленгликолей. В некоторых вариантах осуществления апротонный растворитель выбран из ацетонитрила, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида и 1,4-диоксана. В некоторых вариантах осуществления апротонный растворитель выбран из ацетонитрила, тетрагидрофурана, N,N-диметилформамида и 1,4-диоксана. В некоторых вариантах осуществления апротонный растворитель представляет собой ацетонитрил. В некоторых вариантах осуществления апротонный растворитель представляет собой тетрагидрофуран. В некоторых вариантах осуществления апротонный растворитель представляет собой 2-метилтетрагидрофуран. В некоторых вариантах осуществления апротонный растворитель представляет собой N,N-диметилформамид. В некоторых вариантах осуществления апротонный растворитель представляет собой 1,4-диоксан. В некоторых вариантах осуществления реакцию соединения формулы (IIIa) с кислотой проводят в растворе, содержащем смесь протонного растворителя и апротонного растворителя, где протонный растворитель может представлять собой воду. В некоторых вариантах осуществления реакцию соединения формулы (IIIa) с кислотой проводят в растворе, содержащем смесь 1,4-диоксана и воды. В некоторых вариантах осуществления кислота выбрана из фосфорной кислоты, хлористоводородной кислоты, уксусной кислоты и трифторуксусной кислоты. В некоторых вариантах осуществления кислота представляет собой фосфорную кислоту. В некоторых вариантах осуществления кислота представляет собой хлористоводородную кислоту. В некоторых вариантах осуществления кислота представляет собой уксусную кислоту. В некоторых вариантах осуществления кислота представляет собой трифторуксусную кислоту. В некоторых вариантах осуществления основание добавляют к кислотной смеси, содержащей формулу (IIIa). В некоторых вариантах осуществления основание представляет собой гидроксид аммония, гидроксид натрия или гидроксид калия. В некоторых вариантах осуществления основание представляет собой гидроксид аммония. В некоторых вариантах осуществления основание добавляют к смеси кислоты, содержащей формулу (IIIa), чтобы довести pH раствора до значения в диапазоне от приблизительно 4 до 10. В некоторых вариантах осуществления основание добавляют к смеси кислоты, содержащей формулу (IIIa), чтобы довести pH раствора до значения в диапазоне от приблизительно 7 до 9. В некоторых вариантах осуществления pH раствора регулируют до значения в диапазоне от приблизительно 8 до 9. В некоторых вариантах осуществления pH раствора регулируют до приблизительно 4. В некоторых вариантах осуществления pH раствора регулируют до приблизительно 5. В некоторых вариантах осуществления pH раствора регулируют до приблизительно 6. В некоторых вариантах осуществления pH раствора регулируют до приблизительно 7. В некоторых вариантах осуществления pH раствора регулируют до приблизительно 8. В некоторых вариантах осуществления pH раствора регулируют до приблизительно 9. В некоторых вариантах осуществления pH раствора регулируют до приблизительно 10.
[0097] Также в данном документе раскрыты способы получения соединения формулы (VIb),
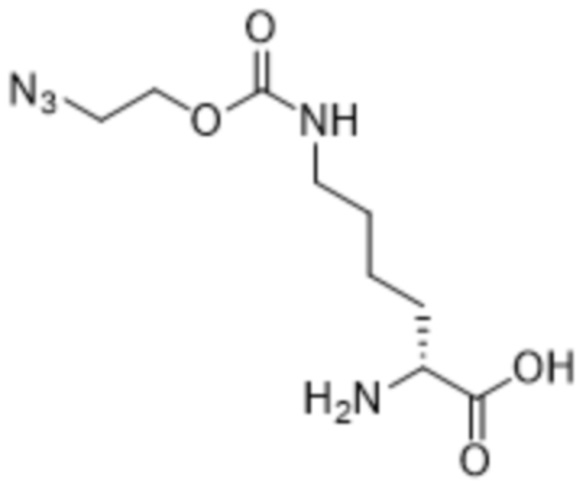 (VIb),
(VIb),
или его соли, включающие обеспечение проведения реакции соединения формулы (IIIb)
 (IIIb),
(IIIb),
с кислотой с получением соединения формулы (VIb) или его соли. В некоторых вариантах осуществления реакцию соединения формулы (IIIb) с кислотой проводят в растворе, содержащем апротонный растворитель, протонный растворитель или их смесь. В некоторых вариантах осуществления апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400 и полиэтиленгликолей. В некоторых вариантах осуществления апротонный растворитель выбран из ацетонитрила, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида и 1,4-диоксана. В некоторых вариантах осуществления апротонный растворитель выбран из ацетонитрила, тетрагидрофурана, N,N-диметилформамида и 1,4-диоксана. В некоторых вариантах осуществления апротонный растворитель представляет собой ацетонитрил. В некоторых вариантах осуществления апротонный растворитель представляет собой тетрагидрофуран. В некоторых вариантах осуществления апротонный растворитель представляет собой 2-метилтетрагидрофуран. В некоторых вариантах осуществления апротонный растворитель представляет собой N,N-диметилформамид. В некоторых вариантах осуществления апротонный растворитель представляет собой 1,4-диоксан. В некоторых вариантах осуществления реакцию соединения формулы (IIIb) с кислотой проводят в растворе, содержащем смесь протонного растворителя и апротонного растворителя, где протонный растворитель может представлять собой воду. В некоторых вариантах осуществления реакцию соединения формулы (IIIb) c кислотой проводят в растворе, содержащем смесь 1,4-диоксана и воды. В некоторых вариантах осуществления кислота выбрана из фосфорной кислоты, хлористоводородной кислоты, уксусной кислоты и трифторуксусной кислоты. В некоторых вариантах осуществления кислота представляет собой фосфорную кислоту. В некоторых вариантах осуществления кислота представляет собой хлористоводородную кислоту. В некоторых вариантах осуществления кислота представляет собой уксусную кислоту. В некоторых вариантах осуществления кислота представляет собой трифторуксусную кислоту. В некоторых вариантах осуществления основание добавляют к кислотной смеси, содержащей формулу (IIIb). В некоторых вариантах осуществления основание представляет собой гидроксид аммония, гидроксид натрия или гидроксид калия. В некоторых вариантах осуществления основание представляет собой гидроксид аммония. В некоторых вариантах осуществления основание добавляют к смеси кислоты, содержащей формулу (IIIb), чтобы довести pH раствора до значения в диапазоне от приблизительно 4 до 10. В некоторых вариантах осуществления основание добавляют к смеси кислоты, содержащей формулу (IIIb), чтобы довести pH раствора до значения в диапазоне от приблизительно 7 до 9. В некоторых вариантах осуществления pH раствора регулируют до значения в диапазоне от приблизительно 8 до 9. В некоторых вариантах осуществления pH раствора регулируют до приблизительно 4. В некоторых вариантах осуществления pH раствора регулируют до приблизительно 5. В некоторых вариантах осуществления pH раствора регулируют до приблизительно 6. В некоторых вариантах осуществления pH раствора регулируют до приблизительно 7. В некоторых вариантах осуществления pH раствора регулируют до приблизительно 8. В некоторых вариантах осуществления pH раствора регулируют до приблизительно 9. В некоторых вариантах осуществления pH раствора регулируют до приблизительно 10.
[0098] В одном аспекте в данном документе предлагается способ получения соединения формулы (VI) или его соли, как указано на схеме 13.
Схема 13
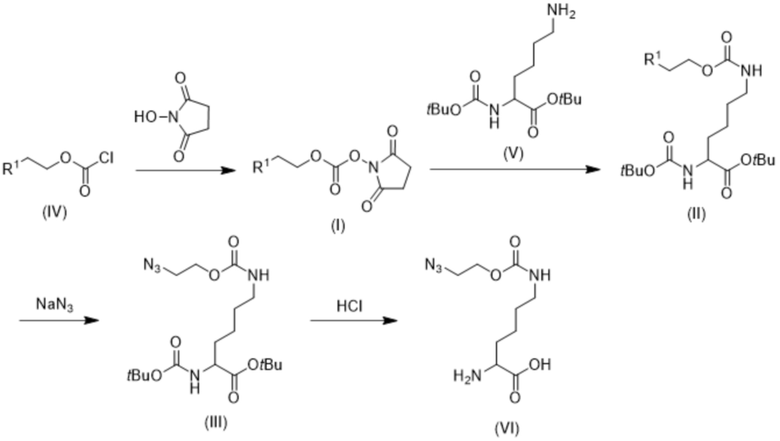
где R1 представляет собой хлор, бром или йод.
[0099] В некоторых вариантах осуществления, где R1 представляет собой хлор, соединение формулы (VI) получают, как указано на схеме 14.
Схема 14
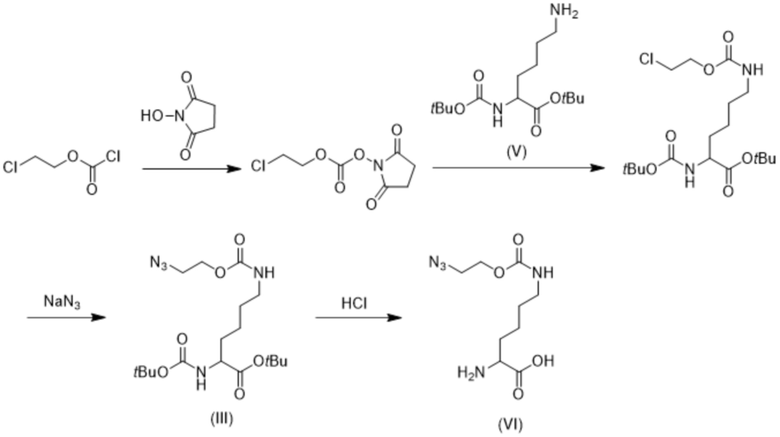
В некоторых вариантах соединения формулы (VIa) и (VIb) или их соли получают, как указано на схеме 15 и схеме 16.
Схема 15
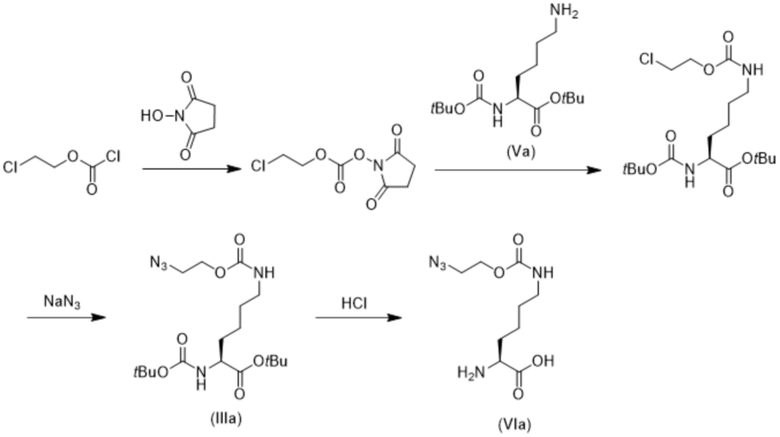
Схема 16
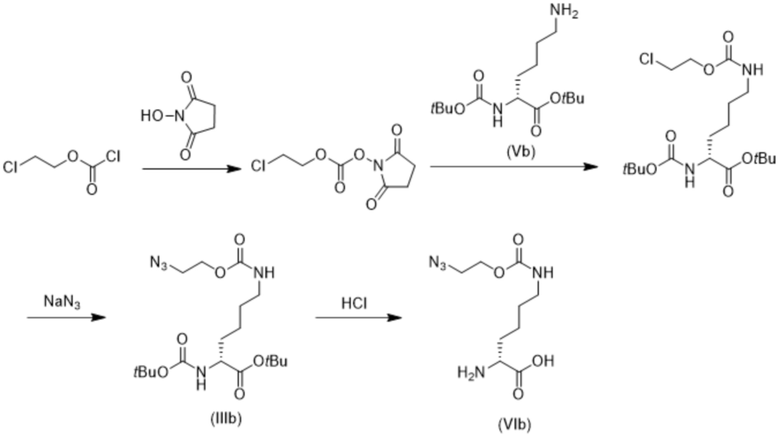
Соединения формулы (VII)
[0100] Также в данном документе раскрыты соединения формулы (VII),
 (VII),
(VII),
где
R3 выбран из хлора, брома и йода;
R4 выбран из -OR6, -CF3, -CH2C6-C12арила и C1-C6алкила;
R5 представляет собой -CH2C6-C12арил или C1-C6алкил; и
R6 выбран из C1-C6алкила, C6-C12арила и -CH2C6-C12арила.
[0101] В некоторых вариантах осуществления соединений формулы (VII) R4 представляет собой -OR6, и R5 представляет собой C1-C6алкил. В некоторых вариантах осуществления R6 представляет собой C1-C6алкил. В некоторых вариантах осуществления C1-C6алкил представляет собой трет-бутил. В некоторых вариантах осуществления R5 представляет собой трет-бутил.
[0102] В некоторых вариантах осуществления соединений формулы (VII) R3 представляет собой хлор. В некоторых вариантах осуществления R6 представляет собой C1-C6алкил. В некоторых вариантах осуществления C1-C6алкил представляет собой трет-бутил. В некоторых вариантах осуществления R5 представляет собой трет-бутил. В некоторых вариантах осуществления R4 представляет собой -OR6, и R5 представляет собой C1-C6алкил.
[0103] В некоторых вариантах осуществления соединений формулы (VII) R3 представляет собой бром. В некоторых вариантах осуществления R6 представляет собой C1-C6алкил. В некоторых вариантах осуществления C1-C6алкил представляет собой трет-бутил. В некоторых вариантах осуществления R5 представляет собой трет-бутил. В некоторых вариантах осуществления R4 представляет собой -OR6, и R5 представляет собой C1-C6алкил.
[0104] В некоторых вариантах осуществления соединений формулы (VII) R3 представляет собой йод. В некоторых вариантах осуществления R6 представляет собой C1-C6алкил. В некоторых вариантах осуществления C1-C6алкил представляет собой трет-бутил. В некоторых вариантах осуществления R5 представляет собой трет-бутил. В некоторых вариантах осуществления R4 представляет собой -OR6, и R5 представляет собой C1-C6алкил.
[0105] Также в данном документе раскрыты соединения формулы (VIIa),
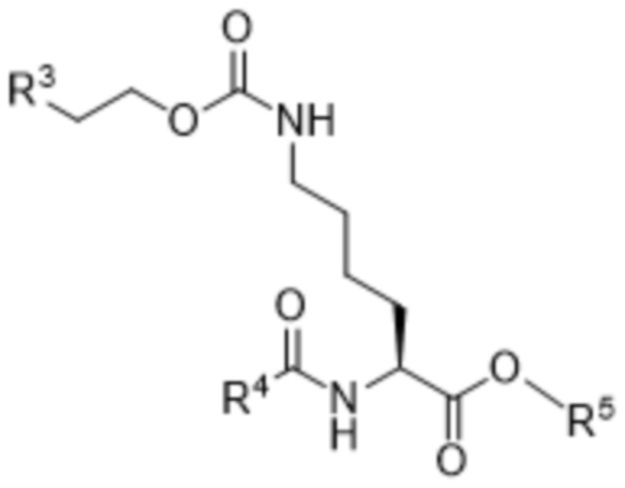 (VIIa),
(VIIa),
где
R3 выбран из хлора, брома и йода;
R4 выбран из -OR6, -CF3, -CH2C6-C12арила и C1-C6алкила;
R5 представляет собой -CH2C6-C12арил или C1-C6алкил; и
R6 выбран из C1-C6алкила, C6-C12арила и -CH2C6-C12арила.
[0106] В некоторых вариантах осуществления соединений формулы (VIIa) R6 выбран из C1-C6алкила, C6-C12арила и -CH2C6-C12арила. В некоторых вариантах осуществления R4 представляет собой -OR6, и R5 представляет собой C1-C6алкил. В некоторых вариантах осуществления R6 представляет собой C1-C6алкил. В некоторых вариантах осуществления C1-C6алкил представляет собой трет-бутил. В некоторых вариантах осуществления R5 представляет собой трет-бутил.
[0107] В некоторых вариантах осуществления соединений формулы (VIIa) R3 представляет собой хлор. В некоторых вариантах осуществления R6 представляет собой C1-C6алкил. В некоторых вариантах осуществления C1-C6алкил представляет собой трет-бутил. В некоторых вариантах осуществления R5 представляет собой трет-бутил. В некоторых вариантах осуществления R4 представляет собой -OR6, и R5 представляет собой C1-C6алкил.
[0108] В некоторых вариантах осуществления соединений формулы (VIIa) R3 представляет собой бром. В некоторых вариантах осуществления R6 представляет собой C1-C6алкил. В некоторых вариантах осуществления C1-C6алкил представляет собой трет-бутил. В некоторых вариантах осуществления R5 представляет собой трет-бутил. В некоторых вариантах осуществления R4 представляет собой -OR6, и R5 представляет собой C1-C6алкил.
[0109] В некоторых вариантах осуществления соединений формулы (VIIa) R3 представляет собой йод. В некоторых вариантах осуществления R6 представляет собой C1-C6алкил. В некоторых вариантах осуществления C1-C6алкил представляет собой трет-бутил. В некоторых вариантах осуществления R5 представляет собой трет-бутил. В некоторых вариантах осуществления R4 представляет собой -OR6, и R5 представляет собой C1-C6алкил.
[0110] Также в данном документе раскрыты соединения формулы (VIIb),
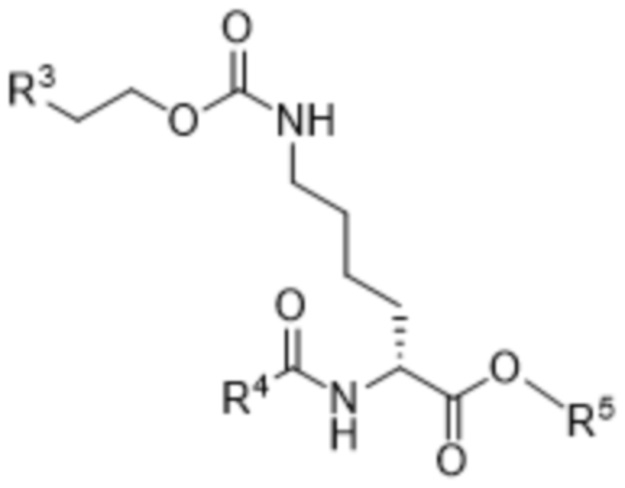 (VIIb),
(VIIb),
где
R3 выбран из хлора, брома и йода;
R4 выбран из -OR6, -CF3, -CH2C6-C12арила и C1-C6алкила;
R5 представляет собой -CH2C6-C12арил или C1-C6алкил; и
R6 выбран из C1-C6алкила, C6-C12арила и -CH2C6-C12арила. В некоторых вариантах осуществления R6 выбран из C1-C6алкила, C6-C12арила и -CH2C6-C12арила.
[0111] В некоторых вариантах осуществления соединений формулы (VIIb) R4 представляет собой -OR6, и R5 представляет собой C1-C6алкил. В некоторых вариантах осуществления R6 представляет собой C1-C6алкил. В некоторых вариантах осуществления C1-C6алкил представляет собой трет-бутил. В некоторых вариантах осуществления R5 представляет собой трет-бутил.
[0112] В некоторых вариантах осуществления соединений формулы (VIIb) R3 представляет собой хлор. В некоторых вариантах осуществления R6 выбран из C1-C6алкила, C6-C12арила и -CH2C6-C12арила. В некоторых вариантах осуществления R4 представляет собой -OR6, и R5 представляет собой C1-C6алкил. В некоторых вариантах осуществления R6 представляет собой C1-C6алкил. В некоторых вариантах осуществления C1-C6алкил представляет собой трет-бутил. В некоторых вариантах осуществления R5 представляет собой трет-бутил.
[0113] В некоторых вариантах осуществления соединений формулы (VIIb) R3 представляет собой бром. В некоторых вариантах осуществления R6 выбран из C1-C6алкила, C6-C12арила и -CH2C6-C12арила. В некоторых вариантах осуществления R4 представляет собой -OR6, и R5 представляет собой C1-C6алкил. В некоторых вариантах осуществления R6 представляет собой C1-C6алкил. В некоторых вариантах осуществления C1-C6алкил представляет собой трет-бутил. В некоторых вариантах осуществления R5 представляет собой трет-бутил.
[0114] В некоторых вариантах осуществления соединений формулы (VIIb) R3 представляет собой йод. В некоторых вариантах осуществления R6 выбран из C1-C6алкила, C6-C12арила и -CH2C6-C12арила. В некоторых вариантах осуществления R4 представляет собой -OR6, и R5 представляет собой C1-C6алкил. В некоторых вариантах осуществления R6 представляет собой C1-C6алкил. В некоторых вариантах осуществления C1-C6алкил представляет собой трет-бутил. В некоторых вариантах осуществления R5 представляет собой трет-бутил.
Соединения формулы (VIII)
[0115] Также в данном документе раскрыты соединения формулы (VIII),
 (VIII),
(VIII),
где
R7 выбран из -OR9, -CF3, -CH2C6-C12арила и C1-C6алкила;
R8 представляет собой -CH2C6-C12арил или C1-C6алкил; и
R9 выбран из C1-C6алкила, C6-C12арила и -CH2C6-C12арила.
[0116] В некоторых вариантах осуществления соединений формулы (VIII) R7 представляет собой -OR9, и R8 представляет собой C1-C6алкил. В некоторых вариантах осуществления R9 представляет собой C1-C6алкил. В некоторых вариантах осуществления C1-C6алкил представляет собой трет-бутил. В некоторых вариантах осуществления R8 представляет собой трет-бутил.
[0117] Также в данном документе раскрыты соединения формулы (VIIIa),
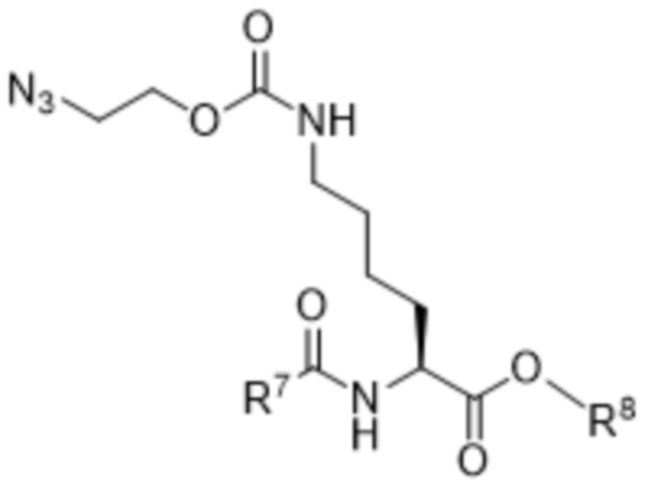 (VIIIa),
(VIIIa),
где
R7 выбран из -OR9, -CF3, -CH2C6-C12арила и C1-C6алкила;
R8 представляет собой -CH2C6-C12арил или C1-C6алкил; и
R9 выбран из C1-C6алкила, C6-C12арила и -CH2C6-C12арила. В некоторых вариантах осуществления R7 представляет собой -OR9, и R8 представляет собой C1-C6алкил.
[0118] В некоторых вариантах осуществления соединений формулы (VIIIa) R9 представляет собой C1-C6алкил. В некоторых вариантах осуществления C1-C6алкил представляет собой трет-бутил. В некоторых вариантах осуществления R8 представляет собой трет-бутил.
[0119] Также в данном документе раскрыты соединения формулы (VIIIb),
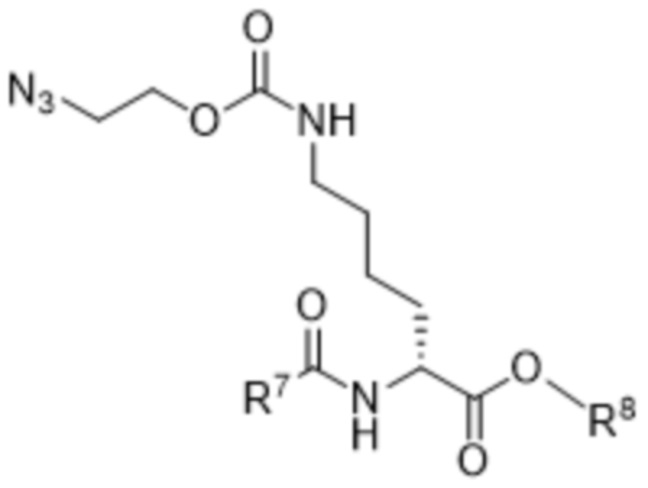 (VIIIb),
(VIIIb),
где
R7 выбран из -OR9, -CF3, -CH2C6-C12арила и C1-C6алкила;
R8 представляет собой -CH2C6-C12арил или C1-C6алкил; и
R9 выбран из C1-C6алкила, C6-C12арила и -CH2C6-C12арила.
[0120] В некоторых вариантах осуществления соединений формулы (VIIIb) R7 представляет собой -OR9, и R8 представляет собой C1-C6алкил. В некоторых вариантах осуществления R9 представляет собой C1-C6алкил. В некоторых вариантах осуществления C1-C6алкил представляет собой трет-бутил. В некоторых вариантах осуществления R8 представляет собой трет-бутил.
[0121] Все соединения формулы (I), (II), (III), (IV), (V), (VI), (VII) или (VIII) или любые их варианты, как описано в данном документе, которые существуют в форме свободного основании или кислоты, могут быть превращены в их соли посредством обработки подходящим неорганическим или органическим основанием или кислотой посредством способов, известных специалисту в данной области техники. Соли соединений согласно настоящему изобретению могут быть превращены в форму их свободного основания или кислоты посредством стандартных методик.
Иллюстративные варианты осуществления
[0122] Настоящее изобретение дополнительно описано с помощью следующих вариантов осуществления. Признаки каждого варианта осуществления комбинируются с любым таковым других вариантов осуществления, где это уместно и осуществимо на практике.
[0123] Вариант осуществления P1. Соединение формулы (I),
 (I),
(I),
где R1 выбран из хлора, брома и йода.
[0124] Вариант осуществления P2. Соединение согласно варианту осуществления P1, где R1 представляет собой хлор.
[0125] Вариант осуществления P3. Соединение согласно варианту осуществления P1, где R1 представляет собой бром.
[0126] Вариант осуществления P4. Соединение согласно варианту осуществления P1, где R1 представляет собой йод.
[0127] Вариант осуществления P5. Соединение формулы (II),
 (II),
(II),
где R1 выбран из хлора, брома и йода.
[0128] Вариант осуществления P6. Соединение согласно варианту осуществления P5, где R1 представляет собой хлор.
[0129] Вариант осуществления P7. Соединение согласно варианту осуществления P5, где R1 представляет собой бром.
[0130] Вариант осуществления P8. Соединение согласно варианту осуществления P5, где R1 представляет собой йод.
[0131] Вариант осуществления P9. Соединение формулы (IIa),
 (IIa),
(IIa),
где R1 выбран из хлора, брома и йода.
[0132] Вариант осуществления P10. Соединение согласно варианту осуществления P9, где R1 представляет собой хлор.
[0133] Вариант осуществления P11. Соединение согласно варианту осуществления P9, где R1 представляет собой бром.
[0134] Вариант осуществления P12. Соединение согласно варианту осуществления P9, где R1 представляет собой йод.
[0135] Вариант осуществления P13. Соединение формулы (IIb),
 (IIb),
(IIb),
где R1 выбран из хлора, брома и йода.
[0136] Вариант осуществления P14. Соединение согласно варианту осуществления P13, где R1 представляет собой хлор.
[0137] Вариант осуществления P15. Соединение согласно варианту осуществления P13, где R1 представляет собой бром.
[0138] Вариант осуществления P16. Соединение согласно варианту осуществления P13, где R1 представляет собой йод.
[0139] Вариант осуществления P17. Соединение формулы (III),
 (III).
(III).
[0140] Вариант осуществления P18. Соединение формулы (IIIa),
 (IIIa).
(IIIa).
[0141] Вариант осуществления P19. Соединение формулы (IIIb),
 (IIIb).
(IIIb).
[0142] Вариант осуществления P20. Способ получения соединения формулы (I),
 (I),
(I),
включающие обеспечение проведения реакции соединения формулы (IV),
 (IV),
(IV),
с N-гидроксисукцинимидом с получением соединения формулы (I), где в каждом из соединений формулы (I) и (IV) R1 является одинаковым и выбран из хлора, брома и йода.
[0143] Вариант осуществления P21. Способ согласно варианту осуществления P20, где R1 представляет собой хлор.
[0144] Вариант осуществления P22. Способ согласно варианту осуществления P20, где R1 представляет собой бром.
[0145] Вариант осуществления P23. Способ согласно варианту осуществления P20, где R1 представляет собой йод.
[0146] Вариант осуществления P24. Способ согласно любому из вариантов осуществления P20-P23, где реакцию соединения формулы (IV) с N-гидроксисукцинимидом проводят в растворе, содержащем апротонный растворитель.
[0147] Вариант осуществления P25. Способ согласно варианту осуществления P24, где апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400 и полиэтиленгликолей.
[0148] Вариант осуществления P26. Способ согласно варианту осуществления P25, где апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида и 1,4-диоксана.
[0149] Вариант осуществления P27. Способ согласно варианту осуществления P26, где апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана и N,N-диметилформамида.
[0150] Вариант осуществления P28. Способ согласно варианту осуществления P27, где апротонный растворитель представляет собой ацетонитрил.
[0151] Вариант осуществления P29. Способ согласно варианту осуществления P27, где апротонный растворитель представляет собой ацетон.
[0152] Вариант осуществления P30. Способ согласно варианту осуществления P27, где апротонный растворитель представляет собой метилэтилкетон.
[0153] Вариант осуществления P31. Способ согласно варианту осуществления P27, где апротонный растворитель представляет собой дихлорметан.
[0154] Вариант осуществления P32. Способ согласно варианту осуществления P27, где апротонный растворитель представляет собой хлороформ.
[0155] Вариант осуществления P33. Способ согласно варианту осуществления P27, где апротонный растворитель представляет собой тетрагидрофуран.
[0156] Вариант осуществления P34. Способ согласно варианту осуществления P27, где апротонный растворитель представляет собой N,N-диметилформамид.
[0157] Вариант осуществления P35. Способ согласно любому из вариантов осуществления P24-P34, где раствор дополнительно содержит основание.
[0158] Вариант осуществления P36. Способ согласно варианту осуществления P35, где основание выбрано из органического основания и неорганического основания.
[0159] Вариант осуществления P37. Способ согласно варианту осуществления P36, где органическое основание выбрано из гетероциклического основания и триалкиламина или их смеси.
[0160] Вариант осуществления P38. Способ согласно варианту осуществления P36, где гетероциклическое основание представляет собой ароматическое гетероциклическое основание, или неароматическое гетероциклическое основание, или смесь ароматического гетероциклического основания и неароматического гетероциклического основания.
[0161] Вариант осуществления P39. Способ согласно варианту осуществления P38, где гетероциклическое основание представляет собой ароматическое гетероциклическое основание.
[0162] Вариант осуществления P40. Способ согласно варианту осуществления P39, где ароматическое гетероциклическое основание выбрано из пиридина, 1-алкилпиррола и 1-алкилимидазола или их смеси.
[0163] Вариант осуществления P41. Способ согласно варианту осуществления P40, где ароматическое гетероциклическое основание выбрано из пиридина, 1-метилпиррола и 1-метилимидазола или их смеси.
[0164] Вариант осуществления P42. Способ согласно варианту осуществления P41, где ароматическое гетероциклическое основание представляет собой пиридин.
[0165] Вариант осуществления P43. Способ согласно варианту осуществления P41, где ароматическое гетероциклическое основание представляет собой 1-метилпиррол.
[0166] Вариант осуществления P44. Способ согласно варианту осуществления P41, где ароматическое гетероциклическое основание представляет собой 1-метилимидазол.
[0167] Вариант осуществления P45. Способ согласно варианту осуществления P38, где гетероциклическое основание представляет собой неароматическое гетероциклическое основание.
[0168] Вариант осуществления P46. Способ согласно варианту осуществления P38, где неароматическое гетероциклическое основание выбрано из N-алкилпирролидина, N-алкилпиперидина, N-алкилморфолина и 1,4-диалкилпиперазина или их смеси.
[0169] Вариант осуществления P47. Способ согласно варианту осуществления P46, где неароматическое гетероциклическое основание представляет собой N-алкилпирролидин.
[0170] Вариант осуществления P48. Способ согласно варианту осуществления P46, где неароматическое гетероциклическое основание представляет собой N-алкилпиперидин.
[0171] Вариант осуществления P49. Способ согласно варианту осуществления P46, где неароматическое гетероциклическое основание представляет собой N-алкилморфолин.
[0172] Вариант осуществления P50. Способ согласно варианту осуществления P46, где неароматическое гетероциклическое основание представляет собой 1,4-диалкилпиперазин.
[0173] Вариант осуществления P51. Способ согласно варианту осуществления P46, где неароматическое гетероциклическое основание выбрано из N-метилпирролидина, N-метилпиперидина и N-метилморфолина.
[0174] Вариант осуществления P52. Способ согласно варианту осуществления P51, где неароматическое гетероциклическое основание представляет собой N-метилпирролидин.
[0175] Вариант осуществления P53. Способ согласно варианту осуществления P51, где неароматическое гетероциклическое основание представляет собой N-метилпиперидин.
[0176] Вариант осуществления P54. Способ согласно варианту осуществления P51, где неароматическое гетероциклическое основание представляет собой N-метилморфолин.
[0177] Вариант осуществления P55. Способ согласно варианту осуществления P37, где органическое основание представляет собой триалкиламин.
[0178] Вариант осуществления P56. Способ согласно варианту осуществления P55, где триалкиламин выбран из триметиламина, триэтиламина, три-н-пропиламина, три-н-бутиламина, трипентиламина, тригексиламина и диизопропилэтиламина.
[0179] Вариант осуществления P57. Способ согласно варианту осуществления P56, где триалкиламин выбран из триметиламина, триэтиламина, три-н-пропиламина и диизопропилэтиламина.
[0180] Вариант осуществления P58. Способ согласно варианту осуществления P57, где триалкиламин выбран из триэтиламина, три-н-пропиламина и диизопропилэтиламина.
[0181] Вариант осуществления P59. Способ согласно варианту осуществления P58, где триалкиламин представляет собой триэтиламин или диизопропилэтиламин.
[0182] Вариант осуществления P60. Способ согласно варианту осуществления P58, где триалкиламин представляет собой триэтиламин.
[0183] Вариант осуществления P61. Способ согласно варианту осуществления P58, где триалкиламин представляет собой диизопропилэтиламин.
[0184] Вариант осуществления P62. Способ согласно варианту осуществления P24, где R1 представляет собой хлор, и апротонный растворитель представляет собой ацетонитрил.
[0185] Вариант осуществления P63. Способ согласно варианту осуществления P62, где раствор дополнительно содержит основание.
[0186] Вариант осуществления P64. Способ согласно варианту осуществления P63, где основание выбрано из триалкиламина.
[0187] Вариант осуществления P65. Способ согласно варианту осуществления P64, где триалкиламин выбран из триметиламина, триэтиламина, три-н-пропиламина, три-н-бутиламина, трипентиламина, тригексиламина и диизопропилэтиламина.
[0188] Вариант осуществления P66. Способ согласно варианту осуществления P65, где триалкиламин выбран из триметиламина, триэтиламина, три-н-пропиламина и диизопропилэтиламина.
[0189] Вариант осуществления P67. Способ согласно варианту осуществления P66, где триалкиламин выбран из триэтиламина, три-н-пропиламина и диизопропилэтиламина.
[0190] Вариант осуществления P68. Способ согласно варианту осуществления P67, где триалкиламин представляет собой триэтиламин или диизопропилэтиламин.
[0191] Вариант осуществления P69. Способ согласно варианту осуществления P68, где триалкиламин представляет собой триэтиламин.
[0192] Вариант осуществления P70. Способ согласно варианту осуществления P68, где триалкиламин представляет собой диизопропилэтиламин.
[0193] Вариант осуществления P71. Способ согласно варианту осуществления P24, где R1 представляет собой хлор, и апротонный растворитель представляет собой ацетонитрил.
[0194] Вариант осуществления P72. Способ согласно варианту осуществления P71, где раствор дополнительно содержит основание.
[0195] Вариант осуществления P73. Способ согласно варианту осуществления P72, где основание выбрано из триалкиламина.
[0196] Вариант осуществления P74. Способ согласно варианту осуществления P73, где триалкиламин выбран из триметиламина, триэтиламина, три-н-пропиламина, три-н-бутиламина, трипентиламина, тригексиламина и диизопропилэтиламина.
[0197] Вариант осуществления P75. Способ согласно варианту осуществления P74, где триалкиламин выбран из триметиламина, триэтиламина, три-н-пропиламина и диизопропилэтиламина.
[0198] Вариант осуществления P76. Способ согласно варианту осуществления P75, где триалкиламин выбран из триэтиламина, три-н-пропиламина и диизопропилэтиламина.
[0199] Вариант осуществления P77. Способ согласно варианту осуществления P76, где триалкиламин представляет собой триэтиламин или диизопропилэтиламин.
[0200] Вариант осуществления P78. Способ согласно варианту осуществления P77, где триалкиламин представляет собой триэтиламин.
[0201] Вариант осуществления P79. Способ согласно варианту осуществления P77, где триалкиламин представляет собой диизопропилэтиламин.
[0202] Вариант осуществления P80. Способ согласно варианту осуществления P24, где R1 представляет собой йод, и апротонный растворитель представляет собой ацетонитрил.
[0203] Вариант осуществления P81. Способ согласно варианту осуществления P80, где раствор дополнительно содержит основание.
[0204] Вариант осуществления P82. Способ согласно варианту осуществления P81, где основание выбрано из триалкиламина.
[0205] Вариант осуществления P83. Способ согласно варианту осуществления P82, где триалкиламин выбран из триметиламина, триэтиламина, три-н-пропиламина, три-н-бутиламина, трипентиламина, тригексиламина и диизопропилэтиламина.
[0206] Вариант осуществления P84. Способ согласно варианту осуществления P83, где триалкиламин выбран из триметиламина, триэтиламина, три-н-пропиламина и диизопропилэтиламина.
[0207] Вариант осуществления P85. Способ согласно варианту осуществления P84, где триалкиламин выбран из триэтиламина, три-н-пропиламина и диизопропилэтиламина.
[0208] Вариант осуществления P86. Способ согласно варианту осуществления P85, где триалкиламин представляет собой триэтиламин или диизопропилэтиламин.
[0209] Вариант осуществления P87. Способ согласно варианту осуществления P86, где триалкиламин представляет собой триэтиламин.
[0210] Вариант осуществления P88. Способ согласно варианту осуществления P86, где триалкиламин представляет собой диизопропилэтиламин.
[0211] Вариант осуществления P89. Способ получения соединения формулы (II),
 (II),
(II),
включающий обеспечение проведения реакции соединения формулы (I),
 (I),
(I),
с соединением формулы (V),
 (V),
(V),
с получением соединения формулы (II), где R1 в каждом из соединений формулы (I) и (II) является одинаковым и выбран из хлора, брома и йода.
[0212] Вариант осуществления P90. Способ согласно варианту осуществления P89, где реакцию соединения формулы (V) с соединением формулы (I) проводят в растворе, содержащем апротонный растворитель.
[0213] Вариант осуществления P91. Способ согласно варианту осуществления P90, где апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400 и полиэтиленгликолей.
[0214] Вариант осуществления P92. Способ согласно варианту осуществления P91, где апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида и 1,4-диоксана.
[0215] Вариант осуществления P93. Способ согласно варианту осуществления P92, где апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана и N,N-диметилформамида.
[0216] Вариант осуществления P94. Способ согласно варианту осуществления P93, где апротонный растворитель представляет собой ацетонитрил.
[0217] Вариант осуществления P95. Способ согласно варианту осуществления P93, где апротонный растворитель представляет собой ацетон.
[0218] Вариант осуществления P96. Способ согласно варианту осуществления P93, где апротонный растворитель представляет собой метилэтилкетон.
[0219] Вариант осуществления P97. Способ согласно варианту осуществления P93, где апротонный растворитель представляет собой дихлорметан.
[0220] Вариант осуществления P98. Способ согласно варианту осуществления P93, где апротонный растворитель представляет собой хлороформ.
[0221] Вариант осуществления P99. Способ согласно варианту осуществления P93, где апротонный растворитель представляет собой тетрагидрофуран.
[0222] Вариант осуществления P100. Способ согласно варианту осуществления P93, где апротонный растворитель представляет собой N,N-диметилформамид.
[0223] Вариант осуществления P101. Способ согласно любому из вариантов осуществления P89-P100, где R1 в каждом из соединений формулы (I) и (II) представляет собой хлор.
[0224] Вариант осуществления P102. Способ согласно любому из вариантов осуществления P89-P100, где R1 в каждом из соединений формулы (I) и (II) представляет собой бром.
[0225] Вариант осуществления P103. Способ согласно любому из вариантов осуществления P89-P100, где R1 в каждом из соединений формулы (I) и (II) представляет собой йод.
[0226] Вариант осуществления P104. Способ получения соединения формулы (IIa),
 (IIa),
(IIa),
включающие обеспечение проведения реакции соединения формулы (I),
 (I),
(I),
с соединением формулы (Va),
 (Va),
(Va),
с получением соединения формулы (IIa), где R1 в каждом из соединений формулы (I) и (IIa) является одинаковым и выбран из хлора, брома и йода.
[0227] Вариант осуществления P105. Способ согласно варианту осуществления P104, где реакцию соединения формулы (Va) с соединением формулы (I) проводят в растворе, содержащем апротонный растворитель.
[0228] Вариант осуществления P106. Способ согласно варианту осуществления P105, где апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400 и полиэтиленгликолей.
[0229] Вариант осуществления P107. Способ согласно варианту осуществления P106, где апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида и 1,4-диоксана.
[0230] Вариант осуществления P108. Способ согласно варианту осуществления P107, где апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана и N,N-диметилформамида.
[0231] Вариант осуществления P109. Способ согласно варианту осуществления P108, где апротонный растворитель представляет собой ацетонитрил.
[0232] Вариант осуществления P110. Способ согласно варианту осуществления P108, где апротонный растворитель представляет собой ацетон.
[0233] Вариант осуществления P111. Способ согласно варианту осуществления P108, где апротонный растворитель представляет собой метилэтилкетон.
[0234] Вариант осуществления P112. Способ согласно варианту осуществления P108, где апротонный растворитель представляет собой дихлорметан.
[0235] Вариант осуществления P113. Способ согласно варианту осуществления P108, где апротонный растворитель представляет собой хлороформ.
[0236] Вариант осуществления P114. Способ согласно варианту осуществления P108, где апротонный растворитель представляет собой тетрагидрофуран.
[0237] Вариант осуществления P115. Способ согласно варианту осуществления P108, где апротонный растворитель представляет собой N,N-диметилформамид.
[0238] Вариант осуществления P116. Способ согласно любому из вариантов осуществления P104-P115, где R1 в каждом из соединений формулы (I) и (IIa) представляет собой хлор.
[0239] Вариант осуществления P117. Способ согласно любому из вариантов осуществления P104-P115, где R1 в каждом из соединений формулы (I) и (IIa) представляет собой бром.
[0240] Вариант осуществления P118. Способ согласно любому из вариантов осуществления P104-P115, где R1 в каждом из соединений формулы (I) и (IIa) представляет собой йод.
[0241] Вариант осуществления P119. Способ получения соединения формулы (IIb),
 (IIb),
(IIb),
включающие обеспечение проведения реакции соединения формулы (I),
 (I),
(I),
с соединением формулы (Vb),
 (Vb),
(Vb),
с получением соединения формулы (IIb), где R1 в каждом из соединений формулы (I) и (IIb) является одинаковым и выбран из хлора, брома и йода.
[0242] Вариант осуществления P120. Способ согласно варианту осуществления P119, где реакцию соединения формулы (Vb) с соединением формулы (I) проводят в растворе, содержащем апротонный растворитель.
[0243] Вариант осуществления P121. Способ согласно варианту осуществления P120, где апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400 и полиэтиленгликолей.
[0244] Вариант осуществления P122. Способ согласно варианту осуществления P121, где апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида и 1,4-диоксана.
[0245] Вариант осуществления P123. Способ согласно варианту осуществления P122, где апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана и N,N-диметилформамида.
[0246] Вариант осуществления P124. Способ согласно варианту осуществления P123, где апротонный растворитель представляет собой ацетонитрил.
[0247] Вариант осуществления P125. Способ согласно варианту осуществления P123, где апротонный растворитель представляет собой ацетон.
[0248] Вариант осуществления P126. Способ согласно варианту осуществления P123, где апротонный растворитель представляет собой метилэтилкетон.
[0249] Вариант осуществления P127. Способ согласно варианту осуществления P123, где апротонный растворитель представляет собой дихлорметан.
[0250] Вариант осуществления P128. Способ согласно варианту осуществления P123, где апротонный растворитель представляет собой хлороформ.
[0251] Вариант осуществления P129. Способ согласно варианту осуществления P123, где апротонный растворитель представляет собой тетрагидрофуран.
[0252] Вариант осуществления P130. Способ согласно варианту осуществления P123, где апротонный растворитель представляет собой N,N-диметилформамид.
[0253] Вариант осуществления P131. Способ согласно любому из вариантов осуществления P119-P130, где R1 в каждом из соединений формулы (I) и (IIb) представляет собой хлор.
[0254] Вариант осуществления P132. Способ согласно любому из вариантов осуществления P119-P130, где R1 в каждом из соединений формулы (I) и (IIb) представляет собой бром.
[0255] Вариант осуществления P133. Способ согласно любому из вариантов осуществления P119-P130, где R1 в каждом из соединений формулы (I) и (IIb) представляет собой йод.
[0256] Вариант осуществления P134. Способ получения соединения формулы (III),
 (III),
(III),
включающий обеспечение проведения реакции соединения формулы (II),
 (II),
(II),
где R1 выбран из хлора, брома и йода, с азидной солью щелочного металла с получением соединения формулы (III).
[0257] Вариант осуществления P135. Способ согласно варианту осуществления P134, где азидная соль щелочного металла щелочного металла выбрана из азида лития, азида натрия и азида калия.
[0258] Вариант осуществления P136. Способ согласно варианту осуществления P135, где азидная соль щелочного металла представляет собой азид лития.
[0259] Вариант осуществления P137. Способ согласно варианту осуществления P135, где азидная соль щелочного металла представляет собой азид натрия.
[0260] Вариант осуществления P138. Способ согласно варианту осуществления P135, где азидная соль щелочного металла представляет собой азид калия.
[0261] Вариант осуществления P139. Способ согласно любому из вариантов осуществления P134-P138, где реакцию соединения формулы (II) с азидной солью щелочного металла проводят в растворе, содержащем апротонный растворитель, протонный растворитель или их смесь.
[0262] Вариант осуществления P140. Способ согласно варианту осуществления P139, где апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400 и полиэтиленгликолей.
[0263] Вариант осуществления P141. Способ согласно варианту осуществления P140, где апротонный растворитель выбран из ацетонитрила, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида и 1,4-диоксана.
[0264] Вариант осуществления P142. Способ согласно варианту осуществления P141, где апротонный растворитель выбран из ацетонитрила, тетрагидрофурана, N,N-диметилформамида и 1,4-диоксана.
[0265] Вариант осуществления P143. Способ согласно варианту осуществления P142, где апротонный растворитель представляет собой ацетонитрил.
[0266] Вариант осуществления P144. Способ согласно варианту осуществления P142, где апротонный растворитель представляет собой тетрагидрофуран.
[0267] Вариант осуществления P145. Способ согласно варианту осуществления P142, где апротонный растворитель представляет собой N,N-диметилформамид.
[0268] Вариант осуществления P146. Способ согласно варианту осуществления P142, где апротонный растворитель представляет собой 1,4-диоксан.
[0269] Вариант осуществления P147. Способ согласно варианту осуществления P139, где реакцию соединения формулы (II) с азидной солью щелочного металла проводят в растворе, содержащем смесь апротонного растворителя и протонного растворителя.
[0270] Вариант осуществления P148. Способ согласно варианту осуществления P147, где раствор дополнительно содержит протонный растворитель.
[0271] Вариант осуществления P149. Способ согласно варианту осуществления P148, где протонный растворитель выбран из воды и спирта.
[0272] Вариант осуществления P150. Способ согласно варианту осуществления P149, где протонный растворитель представляет собой воду.
[0273] Вариант осуществления P151. Способ согласно варианту осуществления P149, где протонный растворитель представляет собой спирт.
[0274] Вариант осуществления P152. Способ согласно варианту осуществления P151, где спирт выбран из метанола, этанола, н-пропанола, изопропанола, н-бутанола, изобутанола, н-пентанола и изопентанола.
[0275] Вариант осуществления P153. Способ согласно варианту осуществления P152, где спирт выбран из метанола, этанола, н-пропанола и изопропанола.
[0276] Вариант осуществления P154. Способ согласно варианту осуществления P139, где раствор содержит смесь воды и 1,4-диоксана.
[0277] Вариант осуществления P155. Способ получения соединения формулы (IIIa),
 (IIIa),
(IIIa),
включающие обеспечение проведения реакции соединения формулы (IIa),
 (IIa),
(IIa),
где R1 выбран из хлора, брома и йода, с азидной солью щелочного металла с получением соединения формулы (IIIa).
[0278] Вариант осуществления P156. Способ согласно варианту осуществления P155, где азидная соль щелочного металла выбрана из азида лития, азида натрия и азида калия.
[0279] Вариант осуществления P157. Способ согласно варианту осуществления P156, где азидная соль щелочного металла представляет собой азид лития.
[0280] Вариант осуществления P158. Способ согласно варианту осуществления P156, где азидная соль щелочного металла представляет собой азид натрия.
[0281] Вариант осуществления P159. Способ согласно варианту осуществления P156, где азидная соль щелочного металла представляет собой азид калия.
[0282] Вариант осуществления P160. Способ согласно любому из вариантов осуществления P155-P159, где реакцию соединения формулы (IIa) с азидной солью щелочного металла проводят в растворе, содержащем апротонный растворитель, протонный растворитель или их смесь.
[0283] Вариант осуществления P161. Способ согласно варианту осуществления P160, где апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400 и полиэтиленгликолей.
[0284] Вариант осуществления P162. Способ согласно варианту осуществления P161, где апротонный растворитель выбран из ацетонитрила, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида и 1,4-диоксана.
[0285] Вариант осуществления P163. Способ согласно варианту осуществления P162, где апротонный растворитель выбран из ацетонитрила, тетрагидрофурана, N,N-диметилформамида и 1,4-диоксана.
[0286] Вариант осуществления P164. Способ согласно варианту осуществления P163, где апротонный растворитель представляет собой ацетонитрил.
[0287] Вариант осуществления P165. Способ согласно варианту осуществления P163, где апротонный растворитель представляет собой тетрагидрофуран.
[0288] Вариант осуществления P166. Способ согласно варианту осуществления P163, где апротонный растворитель представляет собой N,N-диметилформамид.
[0289] Вариант осуществления P167. Способ согласно варианту осуществления P163, где апротонный растворитель представляет собой 1,4-диоксан.
[0290] Вариант осуществления P168. Способ согласно варианту осуществления P160, где реакцию соединения формулы (IIa) с азидной солью щелочного металла проводят в растворе, содержащем смесь апротонного растворителя и протонного растворителя.
[0291] Вариант осуществления P169. Способ согласно любому из вариантов осуществления P161-P168, где раствор дополнительно содержит протонный растворитель.
[0292] Вариант осуществления P170. Способ согласно варианту осуществления P169, где протонный растворитель выбран из воды и спирта.
[0293] Вариант осуществления P171. Способ согласно варианту осуществления P170, где протонный растворитель представляет собой воду.
[0294] Вариант осуществления P172. Способ согласно варианту осуществления P170, где протонный растворитель представляет собой спирт.
[0295] Вариант осуществления P173. Способ согласно варианту осуществления P172, где спирт выбран из метанола, этанола, н-пропанола, изопропанола, н-бутанола, изобутанола, н-пентанола и изопентанола.
[0296] Вариант осуществления P174. Способ согласно варианту осуществления P173, где спирт выбран из метанола, этанола, н-пропанола и изопропанола.
[0297] Вариант осуществления P175. Способ согласно варианту осуществления P160, где раствор содержит смесь воды и 1,4-диоксана.
[0298] Вариант осуществления P176. Способ получения соединения формулы (IIIb),
 (IIIb),
(IIIb),
включающие обеспечение проведения реакции соединения формулы (IIb),
 (IIb),
(IIb),
где R1 выбран из хлора, брома и йода, с азидной солью щелочного металла с получением соединения формулы (IIIb).
[0299] Вариант осуществления P177. Способ согласно варианту осуществления P176, где азидная соль щелочного металла выбрана из азида лития, азида натрия и азида калия.
[0300] Вариант осуществления P178. Способ согласно варианту осуществления P177, где азидная соль щелочного металла представляет собой азид лития.
[0301] Вариант осуществления P179. Способ согласно варианту осуществления P177, где азидная соль щелочного металла представляет собой азид натрия.
[0302] Вариант осуществления P180. Способ согласно варианту осуществления P177, где азидная соль щелочного металла представляет собой азид калия.
[0303] Вариант осуществления P181. Способ согласно любому из вариантов осуществления P176-P180, где реакцию соединения формулы (IIb) с азидной солью щелочного металла проводят в растворе, содержащем апротонный растворитель, протонный растворитель или их смесь.
[0304] Вариант осуществления P182. Способ согласно варианту осуществления P181, где апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400 и полиэтиленгликолей.
[0305] Вариант осуществления P183. Способ согласно варианту осуществления P182, где апротонный растворитель выбран из ацетонитрила, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида и 1,4-диоксана.
[0306] Вариант осуществления P184. Способ согласно варианту осуществления P183, где апротонный растворитель выбран из ацетонитрила, тетрагидрофурана, N,N-диметилформамида и 1,4-диоксана.
[0307] Вариант осуществления P185. Способ согласно варианту осуществления P184, где апротонный растворитель представляет собой ацетонитрил.
[0308] Вариант осуществления P186. Способ согласно варианту осуществления P184, где апротонный растворитель представляет собой тетрагидрофуран.
[0309] Вариант осуществления P187. Способ согласно варианту осуществления P184, где апротонный растворитель представляет собой N,N-диметилформамид.
[0310] Вариант осуществления P188. Способ согласно варианту осуществления P184, где апротонный растворитель представляет собой 1,4-диоксан.
[0311] Вариант осуществления P189. Способ согласно варианту осуществления P181, где реакцию соединения формулы (IIb) с азидной солью щелочного металла проводят в растворе, содержащем смесь апротонного растворителя и протонного растворителя.
[0312] Вариант осуществления P190. Способ согласно любому из вариантов осуществления P182-P188, где раствор дополнительно содержит протонный растворитель.
[0313] Вариант осуществления P191. Способ согласно варианту осуществления P190, где протонный растворитель выбран из воды и спирта.
[0314] Вариант осуществления P192. Способ согласно варианту осуществления P191, где протонный растворитель представляет собой воду.
[0315] Вариант осуществления P193. Способ согласно варианту осуществления P191, где протонный растворитель представляет собой спирт.
[0316] Вариант осуществления P194. Способ согласно варианту осуществления P193, где спирт выбран из метанола, этанола, н-пропанола, изопропанола, н-бутанола, изобутанола, н-пентанола и изопентанола.
[0317] Вариант осуществления P195. Способ согласно варианту осуществления P194, где спирт выбран из метанола, этанола, н-пропанола и изопропанола.
[0318] Вариант осуществления P196. Способ согласно варианту осуществления P195, где раствор содержит смесь воды и 1,4-диоксана.
[0319] Вариант осуществления P197. Способ получения соединения формулы (VI),
 (VI),
(VI),
или его соли, включающие обеспечение проведения реакции соединения формулы (III),
 (III),
(III),
с кислотой с получением соединения формулы (VI).
[0320] Вариант осуществления P198. Способ согласно варианту осуществления P197, где реакцию соединения формулы (III) с кислотой проводят в растворе, содержащем апротонный растворитель, протонный растворитель или их смесь.
[0321] Вариант осуществления P199. Способ согласно варианту осуществления P198, где апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400 и полиэтиленгликолей.
[0322] Вариант осуществления P200. Способ согласно варианту осуществления P199, где апротонный растворитель выбран из ацетонитрила, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида и 1,4-диоксана.
[0323] Вариант осуществления P201. Способ согласно варианту осуществления P200, где апротонный растворитель выбран из ацетонитрила, тетрагидрофурана, N,N-диметилформамида и 1,4-диоксана.
[0324] Вариант осуществления P202. Способ согласно варианту осуществления P201, где апротонный растворитель представляет собой ацетонитрил.
[0325] Вариант осуществления P203. Способ согласно варианту осуществления P201, где апротонный растворитель представляет собой тетрагидрофуран.
[0326] Вариант осуществления P204. Способ согласно варианту осуществления P201, где апротонный растворитель представляет собой N,N-диметилформамид.
[0327] Вариант осуществления P205. Способ согласно варианту осуществления P201, где апротонный растворитель представляет собой 1,4-диоксан.
[0328] Вариант осуществления P206. Способ согласно варианту осуществления P198, где реакцию соединения формулы (III) с кислотой проводят в растворе, содержащем смесь протонного растворителя и апротонного растворителя.
[0329] Вариант осуществления P207. Способ согласно любому из вариантов осуществления P198-P206, где протонный растворитель представляет собой воду.
[0330] Вариант осуществления P208. Способ согласно варианту осуществления P198, где реакцию соединения формулы (III) с кислотой проводят в растворе, содержащем смесь 1,4-диоксана и воды.
[0331] Вариант осуществления P209. Способ согласно любому из вариантов осуществления P197-P208, где кислота выбрана из фосфорной кислоты, хлористоводородной кислоты, уксусной кислоты и трифторуксусной кислоты.
[0332] Вариант осуществления P210. Способ согласно варианту осуществления P209, где кислота представляет собой фосфорную кислоту.
[0333] Вариант осуществления P211. Способ согласно варианту осуществления P209, где кислота представляет собой хлористоводородную кислоту.
[0334] Вариант осуществления P212. Способ согласно варианту осуществления P209, где кислота представляет собой уксусную кислоту.
[0335] Вариант осуществления P213. Способ согласно варианту осуществления P209, где кислота представляет собой трифторуксусную кислоту.
[0336] Вариант осуществления P214. Способ получения соединения формулы (VIa),
 (VIa),
(VIa),
или его соли, включающий обеспечение проведения реакции соединения формулы (IIIa),
 (IIIa),
(IIIa),
с кислотой с получением соединения формулы (VIa).
[0337] Вариант осуществления P215. Способ согласно варианту осуществления P214, где реакцию соединения формулы (IIIa) с кислотой проводят в растворе, содержащем апротонный растворитель, протонный растворитель или их смесь.
[0338] Вариант осуществления P216. Способ согласно варианту осуществления P215, где апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400 и полиэтиленгликолей.
[0339] Вариант осуществления P217. Способ согласно варианту осуществления P216, где апротонный растворитель выбран из ацетонитрила, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида и 1,4-диоксана.
[0340] Вариант осуществления P218. Способ согласно варианту осуществления P217, где апротонный растворитель выбран из ацетонитрила, тетрагидрофурана, N,N-диметилформамида и 1,4-диоксана.
[0341] Вариант осуществления P219. Способ согласно варианту осуществления P218, где апротонный растворитель представляет собой ацетонитрил.
[0342] Вариант осуществления P220. Способ согласно варианту осуществления P218, где апротонный растворитель представляет собой тетрагидрофуран.
[0343] Вариант осуществления P221. Способ согласно варианту осуществления P218, где апротонный растворитель представляет собой N,N-диметилформамид.
[0344] Вариант осуществления P222. Способ согласно варианту осуществления P218, где апротонный растворитель представляет собой 1,4-диоксан.
[0345] Вариант осуществления P223. Способ согласно варианту осуществления P214, где реакцию соединения формулы (IIIa) с кислотой проводят в растворе, содержащем смесь протонного растворителя и апротонного растворителя.
[0346] Вариант осуществления P224. Способ согласно любому из вариантов осуществления P215-P223, где протонный растворитель представляет собой воду.
[0347] Вариант осуществления P225. Способ согласно варианту осуществления P215, где реакцию соединения формулы (IIIa) с кислотой проводят в растворе, содержащем смесь 1,4-диоксана и воды.
[0348] Вариант осуществления P226. Способ согласно любому из вариантов осуществления P214-P225, где кислота выбрана из фосфорной кислоты, хлористоводородной кислоты, уксусной кислоты и трифторуксусной кислоты.
[0349] Вариант осуществления P227. Способ согласно варианту осуществления P226, где кислота представляет собой фосфорную кислоту.
[0350] Вариант осуществления P228. Способ согласно варианту осуществления P226, где кислота представляет собой хлористоводородную кислоту.
[0351] Вариант осуществления P229. Способ согласно варианту осуществления P226, где кислота представляет собой уксусную кислоту.
[0352] Вариант осуществления P230. Способ согласно варианту осуществления P226, где кислота представляет собой трифторуксусную кислоту.
[0353] Вариант осуществления P231. Способ получения соединения формулы (VIb),
 (VIb),
(VIb),
или его соли, включающий обеспечение проведения реакции соединения формулы (IIIb),
 (IIIb),
(IIIb),
с кислотой с получением соединения формулы (VIb).
[0354] Вариант осуществления P232. Способ согласно варианту осуществления P231, где реакцию соединения формулы (IIIb) с кислотой проводят в растворе, содержащем апротонный растворитель, протонный растворитель или их смесь.
[0355] Вариант осуществления P233. Способ согласно варианту осуществления P232, где апротонный растворитель выбран из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400 и полиэтиленгликолей.
[0356] Вариант осуществления P234. Способ согласно варианту осуществления P233, где апротонный растворитель выбран из ацетонитрила, тетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида и 1,4-диоксана.
[0357] Вариант осуществления P235. Способ согласно варианту осуществления P234, где апротонный растворитель выбран из ацетонитрила, тетрагидрофурана, N,N-диметилформамида и 1,4-диоксана.
[0358] Вариант осуществления P236. Способ согласно варианту осуществления P235, где апротонный растворитель представляет собой ацетонитрил.
[0359] Вариант осуществления P237. Способ согласно варианту осуществления P235, где апротонный растворитель представляет собой тетрагидрофуран.
[0360] Вариант осуществления P238. Способ согласно варианту осуществления P235, где апротонный растворитель представляет собой N,N-диметилформамид.
[0361] Вариант осуществления P239. Способ согласно варианту осуществления P235, где апротонный растворитель представляет собой 1,4-диоксан.
[0362] Вариант осуществления P240. Способ согласно варианту осуществления P232, где реакцию соединения формулы (IIIb) с кислотой проводят в растворе, содержащем смесь протонного растворителя и апротонного растворителя.
[0363] Вариант осуществления P241. Способ согласно любому из вариантов осуществления P232-P240, где протонный растворитель представляет собой воду.
[0364] Вариант осуществления P242. Способ согласно варианту осуществления P232, где реакцию соединения формулы (IIIb) с кислотой проводят в растворе, содержащем смесь 1,4-диоксана и воды.
[0365] Вариант осуществления P243. Способ согласно любому из вариантов осуществления P231-P242, где кислота выбрана из фосфорной кислоты, хлористоводородной кислоты, уксусной кислоты и трифторуксусной кислоты.
[0366] Вариант осуществления P244. Способ согласно варианту осуществления P243, где кислота представляет собой фосфорную кислоту.
[0367] Вариант осуществления P245. Способ согласно варианту осуществления P243, где кислота представляет собой хлористоводородную кислоту.
[0368] Вариант осуществления P246. Способ согласно варианту осуществления P243, где кислота представляет собой уксусную кислоту.
[0369] Вариант осуществления P247. Способ согласно варианту осуществления P243, где кислота представляет собой трифторуксусную кислоту.
[0370] Вариант осуществления P248. Соединение формулы (VII),
 (VII),
(VII),
где
R3 выбран из хлора, брома и йода;
R4 выбран из -OR6, -CF3, -CH2C6-C12арила и C1-C6алкила;
R5 представляет собой -CH2C6-C12арил или C1-C6алкил; и
R6 выбран из C1-C6алкила, C6-C12арила и -CH2C6-C12арила.
[0371] Вариант осуществления P249. Соединение согласно варианту осуществления P248, где R3 представляет собой хлор.
[0372] Вариант осуществления P250. Соединение согласно варианту осуществления P248, где R3 представляет собой бром.
[0373] Вариант осуществления P251. Соединение согласно варианту осуществления P248, где R3 представляет собой йод.
[0374] Вариант осуществления P252. Соединение согласно варианту осуществления P249, где R4 представляет собой -OR6, и R5 представляет собой C1-C6алкил.
[0375] Вариант осуществления P253. Соединение согласно варианту осуществления P252, где R6 представляет собой C1-C6алкил.
[0376] Вариант осуществления P254. Соединение согласно варианту осуществления P253, где C1-C6алкил представляет собой трет-бутил.
[0377] Вариант осуществления P255. Соединение согласно варианту осуществления P254, где R5 представляет собой трет-бутил.
[0378] Вариант осуществления P256. Соединение согласно варианту осуществления P250, где R4 представляет собой -OR6, и R5 представляет собой C1-C6алкил.
[0379] Вариант осуществления P257. Соединение согласно варианту осуществления P256, где R6 представляет собой C1-C6алкил.
[0380] Вариант осуществления P258. Соединение согласно варианту осуществления P257, где C1-C6алкил представляет собой трет-бутил.
[0381] Вариант осуществления P259. Соединение согласно варианту осуществления P258, где R5 представляет собой трет-бутил.
[0382] Вариант осуществления P260. Соединение согласно варианту осуществления P251, где R4 представляет собой -OR6, и R5 представляет собой C1-C6алкил.
[0383] Вариант осуществления P261. Соединение согласно варианту осуществления P260, где R6 представляет собой C1-C6алкил.
[0384] Вариант осуществления P262. Соединение согласно варианту осуществления P261, где C1-C6алкил представляет собой трет-бутил.
[0385] Вариант осуществления P263. Соединение согласно варианту осуществления P262, где R5 представляет собой трет-бутил.
[0386] Вариант осуществления P264. Соединение формулы (VIIa),
 (VIIa),
(VIIa),
где
R3 выбран из хлора, брома и йода;
R4 выбран из -OR6, -CF3, -CH2C6-C12арила и C1-C6алкила;
R5 представляет собой -CH2C6-C12арил или C1-C6алкил; и
R6 выбран из C1-C6алкила, C6-C12арила и -CH2C6-C12арила.
[0387] Вариант осуществления P265. Соединение согласно варианту осуществления P264, где R3 представляет собой хлор.
[0388] Вариант осуществления P266. Соединение согласно варианту осуществления P264, где R3 представляет собой бром.
[0389] Вариант осуществления P267. Соединение согласно варианту осуществления P264, где R3 представляет собой йод.
[0390] Вариант осуществления P268. Соединение согласно варианту осуществления P265, где R4 представляет собой -OR6, и R5 представляет собой C1-C6алкил.
[0391] Вариант осуществления P269. Соединение согласно варианту осуществления P268, где R6 представляет собой C1-C6алкил.
[0392] Вариант осуществления P270. Соединение согласно варианту осуществления P269, где C1-C6алкил представляет собой трет-бутил.
[0393] Вариант осуществления P271. Соединение согласно варианту осуществления P270, где R5 представляет собой трет-бутил.
[0394] Вариант осуществления P272. Соединение согласно варианту осуществления P266, где R4 представляет собой -OR6, и R5 представляет собой C1-C6алкил.
[0395] Вариант осуществления P273. Соединение согласно варианту осуществления P272, где R6 представляет собой C1-C6алкил.
[0396] Вариант осуществления P274. Соединение согласно варианту осуществления P273, где C1-C6алкил представляет собой трет-бутил.
[0397] Вариант осуществления P275. Соединение согласно варианту осуществления P274, где R5 представляет собой трет-бутил.
[0398] Вариант осуществления P276. Соединение согласно варианту осуществления P267, где R4 представляет собой -OR6, и R5 представляет собой C1-C6алкил.
[0399] Вариант осуществления P277. Соединение согласно варианту осуществления P276, где R6 представляет собой C1-C6алкил.
[0400] Вариант осуществления P278. Соединение согласно варианту осуществления P277, где C1-C6алкил представляет собой трет-бутил.
[0401] Вариант осуществления P279. Соединение согласно варианту осуществления P278, где R5 представляет собой трет-бутил.
[0402] Вариант осуществления P280. Соединение формулы (VIIb),
 (VIIb),
(VIIb),
где
R3 выбран из хлора, брома и йода;
R4 выбран из -OR6, -CF3, -CH2C6-C12арила и C1-C6алкила;
R5 представляет собой -CH2C6-C12арил или C1-C6алкил; и
R6 выбран из C1-C6алкила, C6-C12арила и -CH2C6-C12арила.
[0403] Вариант осуществления P281. Соединение согласно варианту осуществления P280, где R3 представляет собой хлор.
[0404] Вариант осуществления P282. Соединение согласно варианту осуществления P280, где R3 представляет собой бром.
[0405] Вариант осуществления P283. Соединение согласно варианту осуществления P280, где R3 представляет собой йод.
[0406] Вариант осуществления P284. Соединение согласно варианту осуществления P281, где R4 представляет собой -OR6, и R5 представляет собой C1-C6алкил.
[0407] Вариант осуществления P285. Соединение согласно варианту осуществления P284, где R6 представляет собой C1-C6алкил.
[0408] Вариант осуществления P286. Соединение согласно варианту осуществления P285, где C1-C6алкил представляет собой трет-бутил.
[0409] Вариант осуществления P287. Соединение согласно варианту осуществления P286, где R5 представляет собой трет-бутил.
[0410] Вариант осуществления P288. Соединение согласно варианту осуществления P282, где R4 представляет собой -OR6, и R5 представляет собой C1-C6алкил.
[0411] Вариант осуществления P289. Соединение согласно варианту осуществления P288, где R6 представляет собой C1-C6алкил.
[0412] Вариант осуществления P290. Соединение согласно варианту осуществления P289, где C1-C6алкил представляет собой трет-бутил.
[0413] Вариант осуществления P291. Соединение согласно варианту осуществления P290, где R5 представляет собой трет-бутил.
[0414] Вариант осуществления P292. Соединение согласно варианту осуществления P283, где R4 представляет собой -OR6, и R5 представляет собой C1-C6алкил.
[0415] Вариант осуществления P293. Соединение согласно варианту осуществления P292, где R6 представляет собой C1-C6алкил.
[0416] Вариант осуществления P294. Соединение согласно варианту осуществления P293, где C1-C6алкил представляет собой трет-бутил.
[0417] Вариант осуществления P295. Соединение согласно варианту осуществления P294, где R5 представляет собой трет-бутил.
[0418] Вариант осуществления P296. Соединение формулы (VIII),
 (VIII),
(VIII),
где
R7 выбран из -OR9, -CF3, -CH2C6-C12арила и C1-C6алкила;
R8 представляет собой -CH2C6-C12арил или C1-C6алкил; и
R9 выбран из C1-C6алкила, C6-C12арила и -CH2C6-C12арила.
[0419] Вариант осуществления P297. Соединение согласно варианту осуществления P281, где R7 представляет собой -OR9, и R8 представляет собой C1-C6алкил.
[0420] Вариант осуществления P298. Соединение согласно варианту осуществления P297, где R9 представляет собой C1-C6алкил.
[0421] Вариант осуществления P299. Соединение согласно варианту осуществления P298, где C1-C6алкил представляет собой трет-бутил.
[0422] Вариант осуществления P300. Соединение согласно варианту осуществления P299, где R8 представляет собой трет-бутил.
[0423] Вариант осуществления P301. Соединение формулы (VIIIa),
 (VIIIa),
(VIIIa),
где
R7 выбран из -OR9, -CF3, -CH2C6-C12арила и C1-C6алкила;
R8 представляет собой -CH2C6-C12арил или C1-C6алкил; и
R9 выбран из C1-C6алкила, C6-C12арила и -CH2C6-C12арила.
[0424] Вариант осуществления P302. Соединение согласно варианту осуществления P301, где R7 представляет собой -OR9, и R8 представляет собой C1-C6алкил.
[0425] Вариант осуществления P303. Соединение согласно варианту осуществления P302, где R9 представляет собой C1-C6алкил.
[0426] Вариант осуществления P304. Соединение согласно варианту осуществления P303, где C1-C6алкил представляет собой трет-бутил.
[0427] Вариант осуществления P305. Соединение согласно варианту осуществления P304, где R8 представляет собой трет-бутил.
[0428] Вариант осуществления P306. Соединение формулы (VIIIb),
 (VIIIb),
(VIIIb),
где
R7 выбран из -OR9, -CF3, -CH2C6-C12арила и C1-C6алкила;
R8 представляет собой -CH2C6-C12арил или C1-C6алкил; и
R9 выбран из C1-C6алкила, C6-C12арила и -CH2C6-C12арила.
[0429] Вариант осуществления P307. Соединение согласно варианту осуществления P306, где R7 представляет собой -OR9, и R8 представляет собой C1-C6алкил.
[0430] Вариант осуществления P308. Соединение согласно варианту осуществления P307, где R9 представляет собой C1-C6алкил.
[0431] Вариант осуществления P309. Соединение согласно варианту осуществления P308, где C1-C6алкил представляет собой трет-бутил.
[0432] Вариант осуществления P310. Соединение согласно варианту осуществления P309, где R8 представляет собой трет-бутил.
ПРИМЕРЫ
[0433] Данные примеры представлены исключительно для иллюстративных целей и не ограничивают объем формулы изобретения, представленной в данном документе.
[0434] Пример 1. Получение 2-хлорэтил-(2,5-диоксопирролидин-1-ил)карбоната
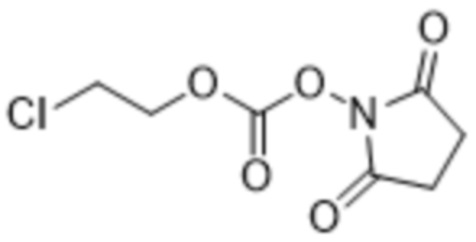
[0435] Реактор с рубашкой объемом 100 л был оснащен верхнеприводной мешалкой, датчиком термопары и обратным холодильником. В реактор добавляли приблизительно 750 грамм 2-хлорэтилхлорформиата и приблизительно 15 литров ацетонитрила. Полученную реакционную смесь охлаждали до 0°C и перемешивали. К смеси добавляли приблизительно 786 грамм N-гидроксисукцинимида (1,3 эквивалента), а затем к смеси добавляли приблизительно 954 мл триэтиламина в течение 1 часа, при этом поддерживая температуру смеси на уровне 3°C или ниже в течение периода приблизительно одного часа, после чего обеспечивали постепенное нагревание реакционной смеси до температуры окружающей среды. За ходом реакции наблюдали с применением тонкослойной хроматографии (TLC) с использованием смеси этилацетат/гексаны (1/3 об./об.) для разделения на пластине для TLC, а для визуализации применяли пары йода и окрашивающий раствор перманганата калия. Обеспечивали продолжение перемешивания реакционной смеси до тех пор, пока присутствие 2-хлорэтилхлорформиата не переставали обнаруживать посредством TLC, после чего добавляли приблизительно 30 литров деионизированной воды с получением прозрачного раствора. В реактор затем добавляли приблизительно 12 литров этилацетата и полученную смесь перемешивали. После перемешивания обеспечивали разделение слоев смеси, нижний водный слой удаляли и помещали в чистые контейнеры в виде бутылей, после чего оставшийся органический слой удаляли и помещали в чистые контейнеры в виде бутылей. Водную фазу возвращали в реактор и в реактор добавляли еще одну порцию этилацетата (приблизительно 12 литров), полученную смесь перемешивали, после чего обеспечивали разделение фаз. Нижнюю водную фазу удаляли из реактора и помещали в чистые контейнеры в виде бутылей, после чего оставшуюся органическую фазу удаляли и помещали в чистые контейнеры в виде бутылей. Данный способ повторяли в третий раз, после чего оставшиеся водные фазы отбрасывали. Безводный сульфат магния добавляли к органическим слоям, смесь перемешивали с помощью стеклянной палочки, и обеспечивали отстаивание раствора в течение не менее часа до тех пор, пока их не сочли высохшими. Смесь фильтровали через фильтр средней пористости, и оставшийся осадок на фильтре промывали двумя объемами этилацетата. Полученную смесь концентрировали на роторном испарителе при пониженном давлении до тех пор, пока не наблюдалось отсутствие дистиллята (максимальная температура бани 60°C), после чего добавляли приблизительно 1,8 литра гексана в оставшийся остаток с образованием твердого вещества. Твердое вещество затем фильтровали через фильтр средней пористости, оставшийся осадок на фильтре промывали несколькими объемами гексана, и затем обеспечивали высушивание оставшегося твердого вещества при пониженном давлении с получением указанного в заголовке соединения. 1H ЯМР (500 МГц, Хлороформ-d) δ 4,56 (t, J=5,8, 5,8 Гц, 2H), 3,76 (t, J=5,8, 5,8 Гц, 2H), 2,85 (s, 4H).
[0436] Пример 2. Получение сложного 1,1-диметилэтилового эфира N2-[(1,1-диметилэтокси)карбонил]-L-лизина (формула (Va))
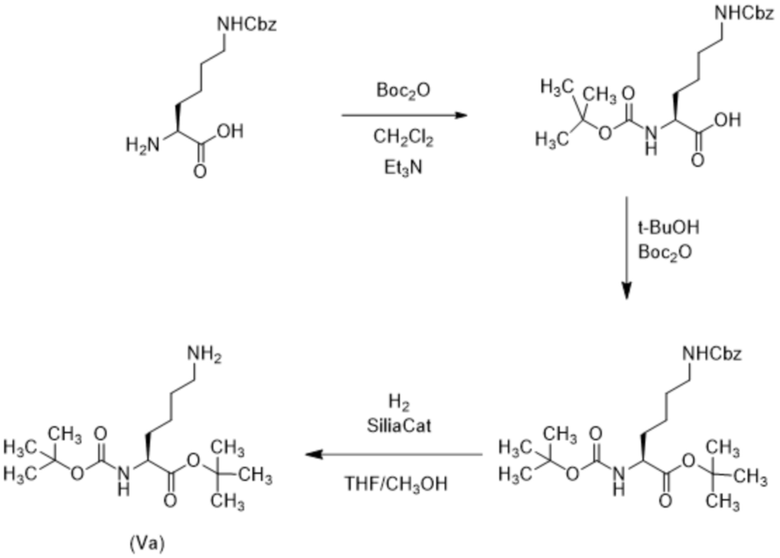
N2-[(1,1-диметилэтокси)карбонил]-N6-[(фенилметокси)карбонил]-L-лизин
[0437] Реактор с рубашкой объемом 100 л был оснащен верхнеприводной мешалкой, датчиком термопары и обратным холодильником. В реактор добавляли приблизительно 3,8 килограмма N6-[(фенилметокси)карбонил]-L-лизина, приблизительно 40 литров деионизированной воды и приблизительно 2,05 килограмма (1,1 экв.) карбоната калия. В отдельный контейнер добавляли приблизительно 3,1 килограмма (1,05 экв.) ди-трет-бутилдикарбоната и приблизительно 16 литров 1,4-диоксана. Раствор ди-трет-бутилдикарбоната затем постепенно добавляли к раствору N6-[(фенилметокси)карбонил]-L-лизина в течение 1 часа, при этом температуру реакционной смесь поддерживали при температуре от приблизительно 20°C до 25°C, и полученную реакционную смесь перемешивали до тех пор, пока не было определено присутствие менее 1% материала, представляющего собой N6-[(фенилметокси)карбонил]-L-лизин. Полученную смесь концентрировали при пониженном давлении с применением роторного испарителя при температуре бани приблизительно 45°C до объема примерно 20 литров, после чего добавляли приблизительно 7 литров деионизированной воды. Затем pH полученной смеси регулировали до pH от примерно 3 до 4 посредством постепенного добавления 1 н. хлористоводородной кислоты (примерно 22,4 литра). К полученной смеси добавляли приблизительно 20 литров этилацетата, смесь перемешивали, обеспечивали разделение фаз, водную фазу отделяли и помещали в чистые контейнеры и оставшуюся органическую фазу помещали в чистые контейнеры. Водную фазу возвращали в реактор, добавляли дополнительную порцию (приблизительно 20 литров) этилацетата, смесь перемешивали, обеспечивали разделение фаз и разделяли водный и органический слои. Данный способ повторяли во второй раз, после чего оставшиеся водные фазы отбрасывали. Объединенные органические фазы возвращали в реактор, добавляли приблизительно 13 литров 1 н. хлористоводородной кислоты, полученную смесь перемешивали, обеспечивали разделение фаз и водные фазы удаляли и отбрасывали. К оставшейся органической фазе добавляли приблизительно 13 литров деионизированной воды, полученную смесь перемешивали, обеспечивали разделение слоев и водный слой отделяли и отбрасывали. В органическую фазу добавляли приблизительно 10 литров насыщенного водного раствора хлорида натрия, смесь перемешивали, обеспечивали разделение фаз и нижнюю водную фазу удаляли и отбрасывали. Добавляли еще одну порцию хлорида натрия, составляющую приблизительно 10 литров, смесь перемешивали, обеспечивали разделение фаз и нижние водные фазы удаляли и отбрасывали. К оставшейся органической фазе добавляли приблизительно 2 килограмма безводного сульфата магния, смесь перемешивали с помощью стеклянной палочки и затем обеспечивали отстаивание в течение не менее часа. Полученную смесь фильтровали через фильтр средней пористости, и осадок на фильтре промывали несколькими объемами этилацетата. Полученный раствор концентрировали на роторном испарителе при температуре бани приблизительно 45°C (максимальная температура бани 60°C) и при пониженном давлении до тех пор, пока не наблюдалось отсутствие дополнительной потери веса, с получением N2-[(1,1-диметилэтокси)карбонил]-N6-[(фенилметокси)карбонил]-L-лизина в виде твердого вещества. Полученное твердое вещество высушивали при периодическом перемешивании твердого вещества в вакуумной печи с температурой печи приблизительно 50°C, до тех пор, пока потери при высушивании не составляли менее приблизительно 0,2% в час.
Сложный 1,1-диметилэтиловый эфир N2-[(1,1-диметилэтокси)карбонил]-N6-[(фенилметокси)карбонил]-L-лизина
[0438] Реактор с рубашкой объемом 100 л был оснащен верхнеприводной мешалкой, датчиком термопары и обратным холодильником. В реактор добавляли приблизительно 3,75 килограмма N2-[(1,1-диметилэтокси)карбонил]-N6-[(фенилметокси)карбонил]-L-лизина и приблизительно 22 литра трет-бутанола. Обеспечивали перемешивание полученной смеси при температуре от приблизительно 20°C до приблизительно 23°C до наблюдения образования прозрачного раствора, после чего добавляли приблизительно 2,85 килограмма (1,1 экв.) ди-трет-бутилдикарбоната в реактор и полученную смесь перемешивали при температуре от приблизительно 20°C до приблизительно 25°C до наблюдения получения прозрачного раствора с последующим добавлением приблизительно 290 грамм (0,2 экв.) 4-диметиламинопиридина. Полученную смесь перемешивали в течение не менее приблизительно 1,5 часа при температуре от приблизительно 20oC до приблизительно 24°C, и за реакцией наблюдали до тех пор, пока не осталось менее приблизительно 1% N2-[(1,1-диметилэтокси)карбонил]-N6-[(фенилметокси)карбонил]-L-лизина, после чего добавляли приблизительно 105 грамм (0,1 экв.) 1,1-диметилэтилендиамина и полученную смесь перемешивали в течение не менее 15 минут при температуре приблизительно 20°C. Реакционную смесь затем охлаждали до температуры от приблизительно -2°C до приблизительно 3°C и добавляли приблизительно 40 литров 0,5 молярного водного раствора хлористоводородной кислоты и приблизительно 20 литров этилацетата с получение смеси, которую перемешивали, обеспечивали разделение фаз и водный и органический слои разделяли и помещали в чистые контейнеры. Водную фазу возвращали в реактор, в который добавляли приблизительно 20 литров этилацетата, смесь перемешивали, обеспечивали разделение фаз и водную фазу удаляли и отбрасывали. Объединенные органические фазы возвращали в реактор, добавляли приблизительно 20 литров насыщенного раствора бикарбоната натрия, полученную смесь перемешивали, обеспечивали разделение фаз и водные фазы удаляли и выбрасывали. В органическую фазу добавляли приблизительно 10 литров водного раствора хлорида натрия, смесь перемешивали, обеспечивали разделение фаз и водную фазу удаляли и отбрасывали. Приблизительно 2 килограмм безводного сульфата магния добавляли в органический слой, смесь перемешивали с помощью стеклянной палочки и затем обеспечивали ее отстаивание в течение не менее 1 часа. Смесь затем фильтровали через фильтр средней пористости, осадок на фильтре промывали несколькими объемами этилацетата и полученный раствор концентрировали при пониженном давлении с применением роторного испарителя при температуре бани приблизительно 45°C (максимальная температура бани приблизительно 60oC) до тех пор, пока не наблюдалось отсутствие дополнительной потери веса, с получением сложного 1,1-диметилэтилового эфира N2-[(1,1-диметилэтокси)карбонил]-N6-[(фенилметокси)карбонил]-L-лизина в виде твердого вещества. Полученное твердое вещество высушивали в вакуумной печи при температуре приблизительно 50°C с периодическим перемешиванием твердого вещества до тех пор, пока не определяли, что потери при высушивании составляют менее приблизительно 0,2% в час.
Сложный 1,1-диметилэтиловый эфир N2-[(1,1-диметилэтокси)карбонил]-L-лизина (формула (Va))
[0439] Реактор высокого давления из нержавеющей стали с рубашкой объемом 100 литров был оснащен верхнеприводной механической мешалкой и впускными отверстиями для водорода/азота. В реактор добавляли приблизительно 4360 грамм сложного 1,1-диметилэтилового эфира N2-[(1,1-диметилэтокси)карбонил]-N6-[(фенилметокси)карбонил]-L-лизина, приблизительно 600 грамм 10% палладия на угле и приблизительно 50 литров тетрагидрофурана (THF). Затем в реакторе нагнетали давление с помощью азота в диапазоне от приблизительно 20 фунтов/кв. дюйм до 40 фунтов/кв. дюйм и затем давление сбрасывали. Способ нагнетания/сбрасывания давления с помощью азота повторяли три раза, после чего в реакторе нагнетали давление водородом в диапазоне от приблизительно 20 фунтов/кв. дюйм до 40 фунтов/кв. дюйм, после чего давление сбрасывали. Способ нагнетания/сбрасывания давления с помощью водорода повторяли три раза, после чего в реакторе нагнетали давление приблизительно 40 фунтов/кв. дюйм с помощью водорода. Реакционную смесь затем нагревали до температуры от приблизительно 40°C до приблизительно 60°C и перемешивали. За ходом реакции наблюдали до тех пор, пока не присутствовало менее приблизительно 1% реагирующего вещества, сложного 1,1-диметилэтилового эфира N2-[(1,1-диметилэтокси)карбонил]-N6-[(фенилметокси)карбонил]-L-лизина, после чего обеспечивали охлаждение смеси и ее поддерживали при температуре от приблизительно 20°C до 25°C в течение не менее 4 часов. Затем в реакторе сбрасывали давление, нагнетали давление с помощью азота и сбрасывали давление три раза. Полученную смесь фильтровали через слой Celite®, суспендированного в THF, с применением фильтра средней пористости и полученный осадок на фильтре промывали несколькими объемами THF. Полученные органические фазы объединяли и концентрировали при пониженном давлении с применением роторного испарителя до тех пор, пока не наблюдалось отсутствие дополнительной потери веса (максимальная температура бани 60°C), с получением сложного 1,1-диметилэтилового эфира N2-[(1,1-диметилэтокси)карбонил]-L-лизина (формула (Va)). 1H ЯМР (500 МГц, DMSO-d6) δ 7,06 (d, J=7,7 Гц, 1H), 3,77-3,69 (m, 1H), 2,62 (t, J=7,3, 7,3 Гц, 2H), 1,62-1,50 (m, 2H), 1,50-1,26 (m, 26H). Масс-спектрометрия в режиме положительной ионизации: масса/заряд 303,4 (M+H).
[0440] Пример 3. Получение сложного 1,1-диметилэтилового эфира N2-[(1,1-диметилэтокси)карбонил]-L-лизина (формула (Va))
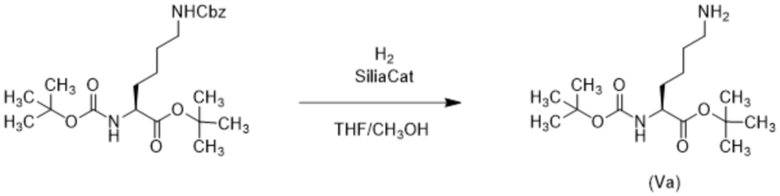
[0441] Реактор высокого давления из нержавеющей стали с рубашкой объемом 100 литров был оснащен верхнеприводной механической мешалкой, трубкой для подачи газообразного водорода. В реактор добавляли приблизительно 4,53 килограмма сложного 1,1-диметилэтилового эфира N2-[(1,1-диметилэтокси)карбонил]-N6-[(фенилметокси)карбонил]-L-лизина, приблизительно 15 литров тетрагидрофурана (THF), приблизительно 15 литров метанола, приблизительно 1,5 литра ледяной уксусной кислоты и приблизительно 1 килограмм 10% палладия на угле SiliaCat. Полученную смесь перемешивали в атмосфере азота в течение приблизительно 15 минут, после чего в реактор загружали водород, температуру нагревающей рубашки регулировали до температуры от приблизительно 20°C до приблизительно 25°C и полученную смесь перемешивали то тех пор, пока не осталось менее приблизительно 1% исходного материала. Полученную смесь фильтровали через фильтр средней пористости, при этом увеличивая количество тетрагидрофурана. Полученный раствор концентрировали до объема приблизительно 6-7 литров с применением роторного испарителя при температуре бани приблизительно 30°C, после чего оставшиеся материалы переносили в реактор с последующим добавлением приблизительно 8 литров метил-трет-бутилового эфира. Приблизительно 13 литров водного раствора бикарбоната натрия добавляли в раствор, смесь перемешивали и фазы разделяли. Водную фазу промывали еще одной порцией метил-трет-бутилового эфира, составляющей приблизительно 4 литра (x2), смесь перемешивали и фазы разделяли. Органический слой промывали приблизительно 4 литрами насыщенного водного раствора бикарбоната натрия и слои разделяли. Полученный органический слой промывали приблизительно 4 литрами насыщенного водного раствора хлорида натрия, слои разделяли и к органическому слою добавляли приблизительно 1 килограмм безводного сульфата магния. Обеспечивали отстаивание смеси в течение приблизительно часа, после чего ее фильтровали с применением фильтра средней пористости и осадок на фильтре промывали несколькими порциями метил-трет-бутилового эфира. Полученный раствор концентрировали с применением роторного испарителя при температуре бани приблизительно 35°C с получением сложного 1,1-диметилэтилового эфира N2-[(1,1-диметилэтокси)карбонил]-L-лизина (формула (Va)) в виде твердого вещества. Твердое вещество высушивали в вакуумной печи при температуре печи приблизительно 35°C с периодическим перемешиванием до тех пор, пока не определяли, что потери при высушивании составляют менее приблизительно 0,2% в час. 1H ЯМР (500 МГц, DMSO-d6) δ 7,06 (d, J=7,7 Гц, 1H), 3,77-3,69 (m, 1H), 2,62 (t, J=7,3, 7,3 Гц, 2H), 1,62-1,50 (m, 2H), 1,50-1,26 (m, 26H). Масс-спектрометрия в режиме положительной ионизации: масса/заряд 303,4 (M+H).
[0442] Пример 4. Получение трет-бутил-N2-(трет-бутоксикарбонил)-N6-((2-хлорэтокси)карбонил)-L-лизината
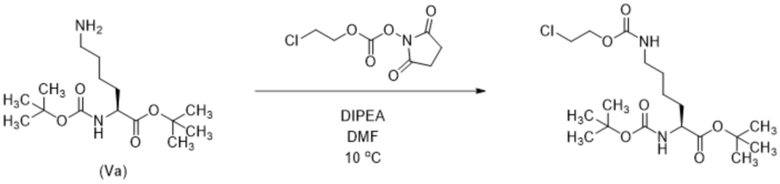
[0443] Реактор с рубашкой объемом 100 литров был оснащен крышкой реактора, перемешивающим узлом, перемешивающим валом, перемешивающей лопастью, термопарой с тефлоновым покрытием и верхнеприводной мешалкой и в нем создавали поток положительного аргона. В реактор добавляли приблизительно 2,9 кг сложного 1,1-диметилэтилового эфира N2-[(1,1-диметилэтокси)карбонил]-L-лизина и приблизительно 19 литров безводного N, N-диметилформамида. Полученную смесь охлаждали до 0°C-5°C при перемешивании с последующим добавлением приблизительно 1,5 литра диизопропилэтиламина. В полученную смесь постепенно порциями добавляли приблизительно 2,11 кг 2-хлорэтил-(2,5-диоксопирролидин-1-ил)карбоната в виде твердого вещества, ожидая приблизительно 10 минут между добавлением каждой порции, при этом внутреннюю температуру смеси поддерживали при температуре от 2°C до 7°C. После завершения добавления 2-хлорэтил-(2,5-диоксопирролидин-1-ил)карбоната обеспечивали перемешивание полученной смеси при температуре от 2°C до 7°C в течение как минимум 4 часов. За ходом реакции наблюдали с помощью определения посредством HPLC того, когда количество сложного 1,1-диметилэтилового эфира N2-[(1,1-диметилэтокси)карбонил]-L-лизина составляло приблизительно менее 1%. Смесь затем охлаждали до температуры от приблизительно -5oC до приблизительно 0oC и добавляли 12 литров гептана с последующим добавлением приблизительно 12 литров этилацетата. В отдельном сосуде получали приблизительно 30 литров 0,5 молярного водного раствора хлористоводородной кислоты посредством добавления приблизительно 28,75 литра воды и приблизительно 1,25 литра концентрированной хлористоводородной кислоты в сосуд, который затем перемешивали и обеспечивали его охлаждение до температуры окружающей среды. Приблизительно 30 литров 0,5 молярного раствора хлористоводородной кислоты затем добавляли к реакционной смеси в другом сосуде, полученную смесь перемешивали, температуру регулировали до уровня от приблизительно 15°C до 25°C, перемешивание продолжали в течение приблизительно 15 минут, после чего перемешивание останавливали и обеспечивали разделение фаз. Водный слой отделяли, помещали в отдельные контейнеры и затем помещали в реактор объемом 50 литров. К водному слою добавляли приблизительно 2 литра гептана и 2 литра этилацетата, полученную смесь перемешивали в течение 10 минут и затем обеспечивали разделение слоев. Водный слой отделяли и помещали в отдельные контейнеры. Данный способ повторяли. Объединенные органические слои переносили из реактора объемом 50 литров в реактор объемом 100 литров вместе с оставшимся органическим слоем из первого разделения и затем добавляли приблизительно 12 литров воды, смесь перемешивали в течение 15 минут, после чего обеспечивали разделение слоев. К оставшимся органическим слоям добавляли приблизительно 4 литра насыщенного раствора хлорида натрия, смесь перемешивали, обеспечивали разделение слоев и водный слой удаляли. Данный способ повторяли со второй порцией 4 литра насыщенного раствора хлорида натрия. К оставшемуся органическому слою добавляли приблизительно 1,5 кг безводного сульфата магния, смесь перемешивали и затем фильтровали через воронку со средней фриттой. Полученный раствор концентрировали при пониженном давлении с применением роторного испарителя и с применением прошедшего через фильтр доочистки этилацетата для завершения переноса из реактора в сосуд роторного испарителя, при этом температуру бани устанавливали на уровне 25°C с максимальной температурой бани 40°C для данного способа. В оставшийся остаток добавляли приблизительно 4 литра ацетонитрила, который затем удаляли при пониженном давлении с применением роторного испарителя. Добавляли вторую порцию ацетонитрила, составляющую приблизительно 4 литра, и удаляли при пониженном давлении с применением роторного испарителя. Оставшийся остаток переносили в сушильный лоток и высушивали при пониженном давлении в вакуумной печи с установленной температурой на уровне приблизительно 25°C. Твердое вещество в сушильном лотке периодически перемешивали и высушивание в вакуумной печи при приблизительно 25°C продолжали до тех пор, пока потери при высушивании не составляли менее приблизительно 0,2% в час, с получением трет-бутил-N2-(трет-бутоксикарбонил)-N6-((2-хлорэтокси)карбонил)-L-лизината в виде твердого вещества. 1H ЯМР (500 МГц, DMSO-d6) δ 7,24-7,16 (m, 1H), 7,02 (d, J=7,6 Гц, 1H), 4,08 (dd, J=5,7, 4,4 Гц, 2H), 3,76-3,69 (m, 1H), 3,50-3,44 (m, 2H), 2,94 (h, J=7,1, 7,1, 7,1, 7,1, 7,1 Гц, 2H), 1,63-1,47 (m, 3H), 1,37 (d, J=2,2 Гц, 22H), 1,30-1,22 (m, 2H), 1,19-1,11 (m, 1H). Масс-спектрометрия в режиме положительной ионизации: масса/заряд 409,4 (M+H).
[0444] Пример 5. Получение трет-бутил-N6-((2-азидоэтокси)карбонил)-N2-(трет-бутоксикарбонил)-L-лизината (формула (IIIa))
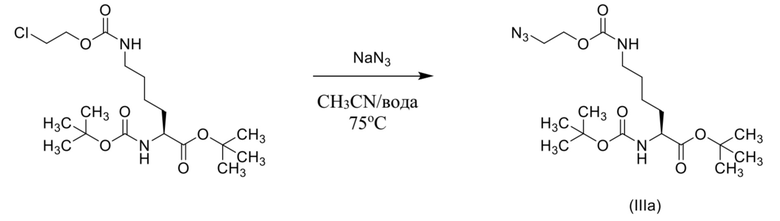
[0445] Реактор с рубашкой объемом 100 литров был оснащен крышкой реактора, перемешивающим узлом, перемешивающим валом, перемешивающей лопастью, термопарой с тефлоновым покрытием и верхнеприводной мешалкой и в нем создавали поток положительного аргона. В реактор добавляли приблизительно 3,75 кг трет-бутил-N2-(трет-бутоксикарбонил)-N6-((2-хлорэтокси)карбонил)-L-лизината и приблизительно 19 литров ацетонитрила. В отдельный реакционный сосуд помещали приблизительно 3 кг азида натрия и приблизительно 19 литров воды и содержимое перемешивали до растворения твердых веществ. Раствор азида натрия затем добавляли к раствору трет-бутил-N2-(трет-бутоксикарбонил)-N6-((2-хлорэтокси)карбонил)-L-лизината, полученную смесь перемешивали и нагревали до температуры от приблизительно 70°C до приблизительно 80°C и перемешивание продолжали в течение приблизительно 30 часов. За ходом реакции наблюдали посредством HPLC до того момента, пока не было определено, что осталось менее приблизительно 1% трет-бутил-N2-(трет-бутоксикарбонил)-N6-((2-хлорэтокси)карбонил)-L-лизината, после чего обеспечивали охлаждение реакционной смеси до температуры от приблизительно 15°C до 25°C с последующим добавлением приблизительно 12 литров гептана и приблизительно 24 литра этилацетата. Обеспечивали перемешивание полученной смеси в течение приблизительно 15 минут, обеспечивали разделение слоев и водный слой удаляли и отбрасывали. К оставшемуся органическому слою добавляли дополнительную порцию воды (приблизительно 5 литров), смесь перемешивали, обеспечивали разделение слоев и водный слой отделяли и отбрасывали. Данный способ повторяли с применением дополнительной порции (приблизительно 5 литров) воды. К органическому слою добавляли 2 литра насыщенного раствора хлорида натрия, полученную смесь перемешивали в течение приблизительно 15 минут, обеспечивали разделение слоев и водный слой отделяли и отбрасывали. Данный способ повторяли с применением дополнительной порции (приблизительно 2 литра) насыщенного раствора хлорида натрия. Оставшиеся органические слои фильтровали с применением воронки со средней фриттой и растворители удаляли при пониженном давлении с применением роторного испарителя при температуре бани 25°C и максимальной температуре бани 40oC. Оставшееся твердое вещество переносили в сушильный лоток и высушивали в вакуумной печи, которую продували аргоном и в которой устанавливали температуру на уровне 35°C. Высушивание продолжали до тех пор, пока потери при высушивании не составляли менее приблизительно 0,2% в час, с последующим высушиванием в течение по меньшей мере 2 дополнительных часов с получением трет-бутил-N6-((2-азидоэтокси)карбонил)-N2-(трет-бутоксикарбонил)-L-лизината (формула (IIIa)) в виде твердого вещества. 1H ЯМР (500 МГц, DMSO-d6) δ 7,20 (t, J=5,7, 5,7 Гц, 1H), 7,02 (d, J=7,5 Гц, 1H), 4,15-4,05 (m, 2H), 3,72 (td, J=8,3, 7,8, 5,1 Гц, 1H), 3,50-3,45 (m, 2H), 3,01-2,89 (m, 2H), 1,60-1,49 (m, 2H), 1,44-1,24 (m, 25H), 1,19-1,12 (m, 1H). Масс-спектрометрия в режиме положительной ионизации: масса/заряд 416,7 (M+H).
[0446] Пример 6. Получение N6-((2-азидоэтокси)карбонил)-L-лизина (формула (VIa))
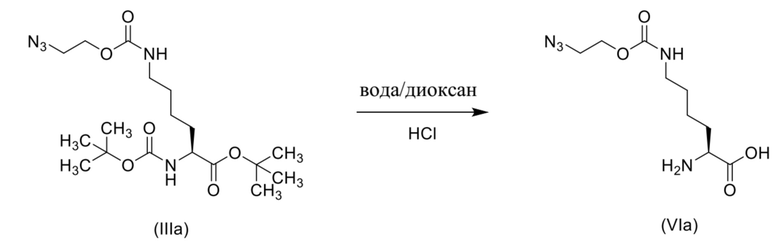
[0447] Реактор с рубашкой объемом 100 литров был оснащен крышкой реактора, перемешивающим узлом, перемешивающим валом, перемешивающей лопастью, термопарой с тефлоновым покрытием, верхнеприводной мешалкой и ловушкой газа, и в нем создавали поток положительного аргона. В реактор добавляли приблизительно 4,53 кг трет-бутил-N6-((2-азидоэтокси)карбонил)-N2-(трет-бутоксикарбонил)-L-лизината (формула (IIIa)) и 11 литров 1,4-диоксана. Полученную смесь перемешивали и охлаждали до температуры от 5°C до 10°C. В смесь добавляли приблизительно 9,4 литра концентрированной хлористоводородной кислоты порциями по 0,5 литра в течение 2 часов, чтобы температуру реакционной смеси находилась в диапазоне от приблизительно 10°C до 15°C. После завершения добавления раствора хлористоводородной кислоты смесь перемешивали, и постепенно нагревали до температуры от 42°C до 47°C, и перемешивание продолжали при этой температуре в течение приблизительно 3 часов. Реакционную смесь затем охлаждали до температуры от приблизительно 15°C до приблизительно 25°C и затем фильтровали через воронку со средней фриттой в отдельные контейнеры. Приблизительно 6-7 литров растворителя удаляли при пониженном давлении с применением роторного испарителя с температурой бани приблизительно 30°C с максимальной температурой бани приблизительно 35°C. Оставшееся содержимое роторного испарителя переносили в реактор с рубашкой, перемешивали и регулировали температуру до температуры на уровне от приблизительно 15°C до приблизительно 25°C. В реактор медленно добавляли от приблизительно 0,9 литра до 1,2 литра водного раствора гидроксида аммония для поддержания внутренней температуры менее 40°C до тех пор, пока не было достигнуто значение pH от приблизительно 7 и до 8. Полученную суспензию охлаждали до температуры от приблизительно 5°C до 10°C, после чего твердое вещество собирали с применением воронки со средней фриттой, ополаскивали с помощью приблизительно 3 литров воды и удаляли избыток воды из осадка на фильтре с применением латексной перемычки. Полученное твердое вещество затем переносили в сушильные лотки и высушивали в вакуумной печи при продувке аргоном, при этом температура печи была установлена на уровне 35oC. Обеспечивали продолжение высушивания твердого вещества при пониженном давлении с периодическим перемешиванием до тех пор, пока не определяли, что потери при высушивании составляют менее приблизительно 0,2% в час, после чего обеспечивали продолжение его высушивания в течение дополнительных 2 часов с получением N6-((2-азидоэтокси)карбонил)-L-лизина (формула (VIa)). 1H ЯМР (500 МГц, Оксид дейтерия) δ 4,12 (t, J=4,8 Гц, 2H), 3,94 (t, J=6,3 Гц, 1H), 3,43-3,37 (m, 2H), 3,04 (t, J=6,7 Гц, 2H), 1,93-1,75 (m, 2H), 1,49-1,38 (m, 2H), 1,38-1,26 (m, 2H). Масс-спектрометрия в режиме положительной ионизации: масса/заряд 260,3 (M+H).
[0448] Пример 7. Модифицированное получение 2-хлорэтил(2,5-диоксопирролидин-1-ил)карбоната
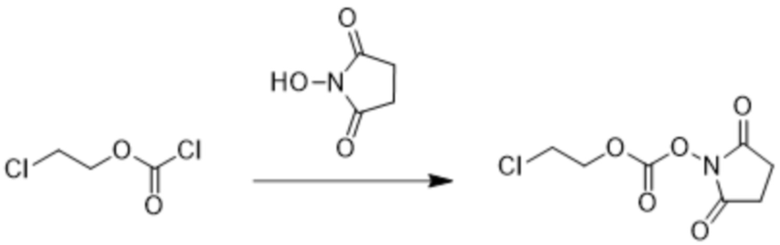
[0449] Получение 2-хлорэтил-(2,5-диоксопирролидин-1-ил)карбоната в соответствии с примером 1 было модифицировано для облегчения промышленного синтеза в большом масштабе. В частности, были проведены модификации для уменьшения реакционных объемов реакции и объемов раствора для обработки, а также для замены высушивания органической фазы c помощью MgSO4 на азеотропную дистилляцию для высушивания. Это было частично достигнуто путем применения 2-метилтетрагидрофурана (2-MeTHF) в качестве реакционного растворителя.
[0450] 3-горлая реакционная колба объемом 1 л с рубашкой была оснащена верхнеприводной мешалкой, регулятором температуры (TC) и капельной воронкой (60 мл) с впускным отверстием для азота, ведущим в барботер. Колбу продували азотом и в нее загружали 2-хлорэтилхлорформиат (40,0 г, 0,280 моль), 2-Me-THF (512,8 г) и N-гидроксисукцинимид (41,9 г, 0,364 моль). Перемешиваемую смесь охлаждали до -4°C. Триэтиламин (36,8 г, 0,364 моль) медленно добавляли в течение 37 минут, поддерживая температуру ≤ 1°C. Во время добавления был образован густой осадок. Температуру регулировали до 11°C в течение 1 часа и смесь перемешивали при 11°C в течение 1 часа. Температуру регулировали до 6°C и медленно добавляли воду (399 г) в течение 16 минут, поддерживая температуру ≤ 10°C. Все твердые вещества растворяли во время добавления воды с получением смеси с 2 жидкими фазами. Смесь перемешивали при 10-11°C в течение 40 минут. Перемешивание останавливали и удаляли нижнюю (водную) фазу. Содержание воды в органической фазе измеряли посредством KF (4,670%). Реакционная колба была оснащена для вакуумной перегонки: короткой насадкой для перегонки с приемной колбой на ацетоновой бане/бане с сухим льдом, системой вакуума собственной разработки с выпускным клапаном. Начинали вакуумную перегонку. Температуру рубашки регулировали от 10 до 35°C во время начала перегонки. Перегонку останавливали, когда объем чаши снижался до 200 мл. Диапазон температуры чаши во время перегонки составлял 11-21°C (обнаруживали, что KF мутного раствора чаши составлял 4,908%). После этого в чашу добавляли 2-Me-THF (400 мл, 337,2 г). Растворитель перегоняли при пониженном вакууме до тех пор, пока объем чаши не был снижен до 200 мл. Диапазон температуры чаши во время перегонки составлял 31-27°C. В конце перегонки образовывался осадок (обнаружили, что KF супернатанта чаши составлял 0,550%). Температуру регулировали до 21°C и разбавленную взвесь перемешивали в течение 30 минут. В течение 10 минут медленно добавляли н-гептан (400 мл, 273,4 г), и полученную взвесь перемешивали при 21°C в течение 16 ч. Взвесь фильтровали (9 см воронка Бюхнера, 1 качественная фильтровальная бумага) и ополаскивали н-гептаном (2×100 мл, 2×67 г). Влажный осадок на фильтре высушивали до постоянного веса (-30 дюймов ртутного столба, 20°C, 1 ч) с получением 56,12 г указанного в заголовке соединения в виде твердого вещества (90,5%).
[0451] Пример 8. Альтернативное получение трет-бутил-N2-(трет-бутоксикарбонил)-N6-((2-хлорэтокси)карбонил)-L-лизината
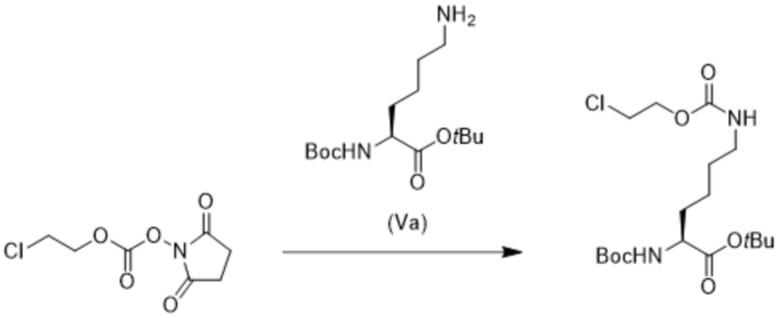
[0452] Получение трет-бутил-N2-(трет-бутоксикарбонил)-N6-((2-хлорэтокси)карбонил)-L-лизината в соответствии с примером 4 было модифицировано для облегчения промышленного синтеза в большом масштабе. Это было частично достигнуто с применением 2-MeTHF в качестве реакционного растворителя с последующей заменой растворителя на ацетонитрил и последующим перемещением реакционной смеси на следующую стадию.
[0453] 3-горлая реакционная колба объемом 500 мл, содержащая (S)-трет-бутил-6-амино-2-(трет-бутоксикарбониламино)гексанoат (формула (Va)) (примерно 49,3 ммоль) в виде неочищенного раствора в 2-MeTHF, была оснащена верхнеприводной мешалкой, TC и капельной воронкой (60 мл) с впускным отверстием для азота, ведущим в барботер. Перемешиваемый раствор охлаждали до 6°C. После этого добавляли одной порцией 2-хлорэтил-(2,5-диоксопирролидин-1-ил)карбонат (10,9 г, 49,2 ммоль), что приводило к увеличению температуры до 14°C. Раствор охлаждали до 9°C и добавляли диизопропилэтиламин (DIPEA) (6,70 г, 51,8 ммоль) посредством капельной воронки в течение 2 минут, ополаскивая с помощью 2-Me-THF (1,5 г). Температуру рубашки повышали с 5 до 20°C в течение 1 ч. Температуру регулировали до 18°C и в течение 5 минут медленно добавляли раствор уксусной кислоты (5 вес. % в H2O, 90 г), поддерживая температуру ≤ 20°C. Смесь перемешивали при 20-22°C в течение 15 минут. Нижнюю водную фазу удаляли и отбрасывали (pH ~5, 102,6 г). Органическую фазу перемешивали с раствором Na2CO3 (5 вес. % в H2O, 90 г) в течение 15 минут. Нижнюю водную фазу удаляли и отбрасывали (pH ~10, 101,3 г). Органическую фазу перемешивали с водой (90 г) в течение 15 минут. Нижнюю водную фазу удаляли и отбрасывали (pH 8-9, 104,1 г). Темную органическую фазу подвергали фильтрации через фильтр доочистки (мембранный фильтр с размером пор 0,2 мкм Polycap PTFE через насос FMI), ополаскивая с помощью 2-Me-THF (2×42 г). Растворитель подвергали вакуумной перегонки (температура рубашки 45°C) до тех пор, пока объем чаши не был снижен до 100 мл (температура чаши в диапазоне 44-32°C). Добавляли ацетонитрил (200 мл, 157,0 г) и растворитель подвергали вакуумной перегонке (температура рубашки 45°C) до тех пор, пока объем чаши не был снижен до 100 мл (температура чаши в диапазоне 44-28°C). Температуру регулировали до 20°C. Раствор, содержащий указанное в заголовке соединение, непосредственно переносили на следующую стадию.
[0454] Пример 9. Альтернативное получение трет-бутил-N6-((2-азидоэтокси)карбонил)-N2-(трет-бутоксикарбонил)-L-лизината (формула (IIIa))
[0455] Получение трет-бутил-N6-((2-азидоэтокси)карбонил)-N2-(трет-бутоксикарбонил)-L-лизината (формула (IIIa)) в соответствии с примером 5 было модифицировано для облегчения промышленного синтеза в большом масштабе. Это было частично достигнуто посредством замены высушивания органической фазы с MgSO4 на азеотропную дистилляцию для высушивания.
[0456] 3-горлая реакционная колба объемом 500 мл, содержащая трет-бутил-N2-(трет-бутоксикарбонил)-N6-((2-хлорэтокси)карбонил)-L-лизинат (примерно 20,1 г, 49,3 ммоль) в виде неочищенного раствора в ацетонитриле, была оснащена верхнеприводной мешалки, регулятором температуры (TC), капельной воронкой (60 мл) и впускным отверстием для азота, присоединенным к барботеру. В рубашке реактора устанавливали температуру на уровне 25°C. Азид натрия (14,4 г, 220 ммоль) растворяли в деионизированной воде (101 мл) при 25°C в колбе Эрленмейера объемом 250 мл. Раствор азида натрия загружали одной порцией в реактор, создавая небольшую эндотерму (+1°C). Температуру рубашки устанавливали на уровне 80°C. Как только внутренняя температура достигала 75°C, реакционную смесь перемешивали в течение не менее (NLT) 20 ч. В рубашке реактора устанавливали на уровне 25°C. Этилацетат (120 мл) загружали в реактор с последующим добавлением н-гептана (60 мл). Реакционную смесь перемешивали при 25°C в течение NLT 20 мин. Фазы разделяли в течение NLT 15 мин. Нижнюю водную фазу удаляли и хранили в точно взвешенной полипропиленовой бутылке (119,1 г). Органическую фазу загружали обратно в реактор вместе с H2O (30 мл). Смесь перемешивали при 25°C в течение NLT 20 мин. Затем разделяли фазы в течение NLT 15 мин. Нижнюю водную фазу удаляли и хранили в точно взвешенной полипропиленовой бутылке (36,3 г). Органическую фазу загружали обратно в реактор вместе с H2O (30 мл) и смесь перемешивали при 25°C в течение NLT 20 мин. Фазы разделяли в течение NLT 15 мин. Нижнюю водную фазу удаляли хранили в точно взвешенной полипропиленовой бутылке (36,7 г). Органическую фазу загружали обратно в реактор вместе с H2O (30 мл). Смесь перемешивали при 25°C в течение NLT 20 мин. Фазы разделяли в течение NLT 15 мин. Нижнюю водную фазу удаляли и хранили в точно взвешенной полипропиленовой бутылке (35,2 г). Органическую фазу загружали обратно в реактор вместе с солевым раствором (17,9 г). Смесь перемешивали при 25°C в течение NLT 20 мин. Фазы разделяли в течение NLT 15 мин. Нижнюю водную фазу удаляли и хранили в точно взвешенной полипропиленовой бутылке (21,4 г). Органическую фазу загружали обратно в реактор вместе с солевым раствором (17,9 г). Смесь перемешивали при 25°C в течение NLT 20 мин. Фазы разделяли в течение NLT 15 мин. Нижнюю водную фазу удаляли и хранили в точно взвешенной полипропиленовой бутылке. (11,51 г). Органическую фазу загружали обратно в реактор и в рубашке устанавливали температуру на уровне 45°C. После этого растворитель отпаривали до примерно 100 мл. 1,4-Диоксан (200 мл, 207 г) загружали в реактор, и раствор снова перегоняли под вакуумом до примерно 100 мл. Коричневую органическую фазу подвергали фильтрации через фильтр доочистки (мембранный фильтр с размером пор 0,2 мкм Polycap PTFE через насос FMI) и ополаскивали с помощью 1,4-диоксана (2×103 г). В рубашке устанавливали температуру на уровне 65°C и растворитель отпаривали до ~ 100 мл. После этого в рубашке устанавливали температуру на уровне 25°C. Раствор 1,4-диоксана, содержащий указанное в заголовке соединение, непосредственно переносили на следующую стадию.
[0457] Пример 10. Исследования посредством калориметрии при степени ускорения (ARC) трет-бутил-N6-((2-азидоэтокси)карбонил)-N2-(трет-бутоксикарбонил)-L-лизината (формула (IIIa))
[0458] С целью оценки безопасности обращения с N6-((2-азидоэтокси)карбонил)-N2-(трет-бутоксикарбонил)-L-лизинатом (формула (IIIa)) проводили исследования посредством калориметрии при степени ускорения (ARC). Данные ARC обеспечивают представление о потенциальной термической опасности, связанной с образованием N6-((2-азидоэтокси)карбонил)-N2-(трет-бутоксикарбонил)-L-лизината (формула (IIIa)), которая вовлекает применение высокой температуры (~80°C) в течение времени реакции 20 ч.
Экспериментальная цель
[0459] Тест ARC определяет начало любой самоускоряющейся экзотермической активности и образования газа в химической системе в псевдоадиабатических условиях, обычно встречаемых во время крупномасштабного изготовления и/или транспортировки. В ARC применяются данные для определения энтальпии реакции или разложения и нахождения максимального повышения температуры в случае неуспешного охлаждения или перемешивания во время критической стадии обработки.
[0460] Тест ARC проводили в баллоне для образца (10 см3), соединенном сверху с датчиком давления. Образец был запечатан внутри корпуса адиабатического баллона, а корпус баллона находился внутри предохранительной камеры аппарата. На стенке баллона помещали термопару. Адиабатический корпус состоял из двух типов нагревателей: (i) инфракрасных нагревателей, применяемых для нагревания образца до его начальной температуры, и (ii) нагревателей, применяемых для контроля за адиабатической средой. При обнаружении тепловыделения из образца такие нагреватели поддерживают адиабатическую среду, точно согласовывая температуру печи с температурой образца. Для определения очень малых изменений температуры реакционной массы применяют очень точную систему контроля и, таким образом, адиабатический контроль является очень эффективным. Калориметр был размещен внутри прочной камеры, способной к выдерживанию разрыва баллона, который может возникнуть вследствие чрезвычайно быстро разлагающихся или детонирующих материалов.
Результаты
[0461] Тесты были проведены в ARC в режиме "нагревание-ожидание-поиск" (HWS). Это предусматривало нагревание образца при регулярных скачках температуры (например, 10°C) и оставление образца для уравновешивания при данной температуры в течение установленного периода. Затем система контроля осуществляла поиск любого небольшого увеличения температуры вследствие экзотермической активности. Если повышение температуры, обнаруженное на протяжении всего периода поиска, составляло менее 0,02 K⋅мин-1, цикл повторяли до определения экзотермической активности. Система контроля ARC переключалась в адиабатический режим, когда обнаруживали скорость увеличения температуры выше 0,02 K⋅мин-1. Затем нагреватели образцов применяли для контроля за окружающей средой баллона при той же температуре, что и сам баллон.
[0462] Образец N6-((2-азидоэтокси)карбонил)-N2-(трет-бутоксикарбонил)-L-лизината (формула (IIIa)) тестировали с применением режима HWS в ARC в адиабатических условиях. Экспериментальные параметры для исследования кратко представлены в таблице 1.
Таблица 1. Экспериментальные параметры для исследования ARC N6-((2-азидоэтокси)карбонил)-N2-(трет-бутоксикарбонил)-L-лизината (формула (IIIa))
* Значение теплоемкости является оценкой, которая представляет собой среднее значение для наиболее распространенных органических соединений.
[0463] Во время теста наблюдали две экзотермы самонагревания (таблицы 2 и 3). Основная экзотерма началась при температуре начала 160,5°C, что приводило к повышению давления и увеличению температуры. Максимальная зарегистрированная скорость самонагревания составляла 2,098 K/мин при 211,5°C, тогда как максимальная скорость изменения давления составляла 2,756 бар/мин при 208,5°C. Общее количество тепла для двух экзотерм было относительно небольшим и составляло 236,0 Дж/г. При приблизительно 380°C давление достигало точки отключения, установленной на уровне 150 бар, на которой эксперимент вынужденно останавливали, прежде чем была достигнута целевая конечная температура 400°C.
Таблица 2. Краткое изложение данных ARC для N6-((2-азидоэтокси)карбонил)-N2-(трет-бутоксикарбонил)-L-лизината (формула (IIIa))
грамм
Таблица 3. Данные ARC для N6-((2-азидоэтокси)карбонил)-N2-(трет-бутоксикарбонил)-L-лизината (формула (IIIa))
[0464] Графики зависимости самонагревания и скорости изменения давления от температуры показаны на фиг. 1, а графики зависимости температуры и давления от времени показаны на фиг. 2. На графике Антуана, показанном на фиг. 3, показано, что давление отклоняется от характеристик Антуана при приблизительно 59,7°C, 227,2°C, 307,7°C и 379,2°C. Неконденсируемый газ с 35,5 бар избыточного давления оставался в баллоне после завершения теста и охлаждения до температуры, близкой к температуре окружающей среды 30,7°C.
Время до обеспечения максимальной скорости
[0465] Данные тестов, полученные из ARC, можно использовать для оценки температуры самоускоряющегося разложения образца (J. K. Wilberforce, "The Use of the Accelerating Rate Calorimeter to determine the SADT of organic peroxides", Columbia Scientific Industries, Milton Keynes; Harold G. Fisher and David D. Goetz, "Determination of self-accelerating decomposition temperature using the accelerating rate calorimeter", J. Loss Prev. Process Ind., 1991, Vol 4., 305-316). Время до достижения максимальной скорости (TMR) определено как количество времени, которое необходимое для того, чтобы реакция достигала своей максимальной скорости самонагревания или скорости изменения давления в реакции неуправляемого нагревания. Данные TMR получали из данных теста, скорректированных на фи-фактор, и создавали график зависимости Ln(TMR) от -1000/T (фиг. 4).
[0466] Следующее уравнение было взято из фиг. 4, чтобы обеспечить возможность определения времени до достижения максимальной скорости как функции температуры:
Ln(TMR(s))=-16,389*(-1000/(T(K))) - 29,262
TMR увеличивается по мере уменьшения температуры бани. Измеренную экзотерму применяли для оценки TMR. Результаты представлены лишь в качестве ссылки, поскольку они основаны на одном тесте ARC, а не на подробном кинетическом исследовании (фиг. 5). Результаты в отношении времени до достижения максимальной скорости кратко представлены в таблице 4.
Таблица 4. Данные TMR для N6-((2-азидоэтокси)карбонил)-N2-(трет-бутоксикарбонил)-L-лизината (формула (IIIa))
* При 129,0°C время до достижения максимальной скорости (TMR) составляет ~24 часа. TMR24 представляет собой хорошую основу для оценки безопасности, но зависит от условий способа.
** Температура начала 2-й экзотермы.
[0467] Данные демонстрируют, что при получении N6-((2-азидоэтокси)карбонил)-N2-(трет-бутоксикарбонил)-L-лизината (формула (IIIa)) в соответствии с реакциями, описанными в данном документе, отсутствует значительная термическая опасность.
[0468] Пример 11. Альтернативное получение N6-((2-азидоэтокси)карбонил)-L-лизина (формула (VIa))
[0469] Получение N6-((2-азидоэтокси)карбонил)-L-лизина (формула (VIa)) в соответствии с примером 6 было модифицировано для облегчения промышленного синтеза в большом масштабе. Это было частично достигнуто посредством регулирования pH раствора для улучшения осаждения указанного в заголовке соединения.
[0470] 3-горлая реакционная колба объемом 500 мл, содержащая трет-бутил-N6-((2-азидоэтокси)карбонил)-N2-(трет-бутоксикарбонил)-L-лизинат (формула (IIIa)) (примерно 20,4 г, 49,3 ммоль) в виде неочищенного раствора в 1,4-диоксане, была оснащена верхнеприводной мешалкой, регулятором температуры (TC), капельной воронкой (60 мл) и впускным отверстием для азота, присоединенным к барботеру. В рубашке реактора устанавливали температуру на уровне 10°C. Как только температура содержимого стабилизировалась на уровне 10,3°C, в реактор медленно загружали концентрированную хлористоводородную кислоту (61,2 г, 51 мл, 220 ммоль) в течение 1 ч. Наблюдали экзотерму при приблизительно от +3 до +5 °C. Внутреннюю температуру поддерживали при 20±5°C во время загрузки. Как только загрузка HCl была завершена, температуру рубашки повышали до 45°C в течение 30 мин. Раствор перемешивали при 45°C в течение не менее (NLT) 3 ч. После этого температуру рубашки понижали от 45°C до 25°C в течение 1 ч. Раствор подвергали фильтрации через доочистки (мембранный фильтр с размером пор 0,2 мкм Polycap PTFE через насос FMI) и ополаскивали с помощью 1,4-диоксана (2×103 г). Раствор загружали обратно в реактор и температуру рубашки устанавливали на уровне 60°C. Раствор отпаривали до 5 об. под вакуумом с температурой рубашки 60°C. После этого температуру рубашки устанавливали на уровне 10°C. Гидроксид аммония (35 мл) медленно добавляли в реактор в течение 1 ч при стабилизации температуры содержимого на уровне 10,4°C. Экзотерму от +5 до +15°C можно наблюдать в зависимости от скорости добавления. Температуру содержимого поддерживали на уровне 25°C. По мере продолжения добавления NH4OH раствор превращался в грязно-белую взвесь. Гидроксид аммония добавляли до тех пор, пока pH не достигал значения 8-9. Как только добавление было завершено, температуру рубашки устанавливали на уровне 5°C и взвесь выдерживали в течение 16 ч. Взвесь фильтровали на воронке с «тонкой» фриттой. Влажный осадок на фильтре промывали H2O, ранее охлажденной до 5°C (2×30 г). Твердые вещества высушивали на воздухе на покрытой воронке с фриттой в течение 12 ч, затем под вакуумом при 25°C в течение 72 ч с получением указанного в заголовке соединения в виде твердого вещества (7,22 г, 57%).
[0471] Пример 12. Влияние pH на растворимость N6-((2-азидоэтокси)карбонил)-L-лизина (формула (VIa)) в воде
[0472] Чтобы дополнительно очистить N6-((2-азидоэтокси)карбонил)-L-лизин (формула (VIa)) получали суспензию N6-((2-азидоэтокси)карбонил)-L-лизина (формула (VIa)) в воде с последующим добавлением HCl с образованием раствора. Нейтрализация полученного раствора гидроксидом аммония обеспечивает повторное осаждение продукта и дополнительную очистку материала от остаточных примесей, которые остаются в растворе. Чтобы улучшить выход продукта исследовали влияние, оказываемое pH на растворимость N6-((2-азидоэтокси)карбонил)-L-лизина (формула (VIa)). Вкратце, данное исследование предусматривало суспендирование N6-((2-азидоэтокси)карбонил)-L-лизина (формула (VIa)) в воде, постепенное повышение основности смеси и определение количества N6-((2-азидоэтокси)карбонил)-L-лизина (формула (VIa)) в супернатанте в зависимости от pH.
[0473] N6-((2-Азидоэтокси)карбонил)-L-лизин (формула (VIa)) (0,95 г) загружали в стеклянный сцинтилляционный флакон объемом 20 мл вместе с водой (7,2 г). Полученную суспензию тщательно перемешивали в вихревом аппарате в течение 60 секунд и затем обеспечивали отстаивание в течение 5 минут. Измеренное значение pH супернатанта 4,44 и аликвоту отбирали и разбавляли элюентом для HPLC (H2O:CH3CN 1:1, 0,1% TFA). Образец анализировали посредством HPLC (колонка: ACE Excel 3 Super C18, 4,6×150 мм, 3,0 мкм, скорость потока: 1,2 мл/мин, фаза A: 0,1% TFA в воде, фаза B: 0,1% TFA в ацетонитриле) и содержание N6-((2-азидоэтокси)карбонил)-L-лизина (формула (VIa)) рассчитывали на основе анализа HPLC стандартов формулы (VIa).
[0474] Повышали основность содержимого сцинтилляционного флакона посредством добавления капли 28-30% гидроксида аммония и суспензию перемешивали вихревым способом, обеспечивали ее декантирование, снова отбирали образцы супернатанта и анализировали посредством HPLC. Данную процедуру повышения основности/анализа повторяли еще 5 раз и результаты показаны в таблице 5.
Таблица 5. Влияние pH на растворимость N6-((2-азидоэтокси)карбонил)-L-лизина (формула (VIa))
[0475] Анализ HPLC показывает, что в диапазоне значений pH от 4 до 8 насыщенный водный раствор N6-((2-азидоэтокси)карбонил)-L-лизина (формула (VIa)) содержит примерно одинаковое количество продукта в своем супернатанте. Извлечение N6-((2-азидоэтокси)карбонил)-L-лизина (формула (VIa)) может быть достигнуто посредством осаждения продукта при pH в диапазоне от 4 до 10, таком как pH в диапазоне от приблизительно 7 до 8, или от 8 до 9, или от приблизительно 8 до 8,5.
[0476] Хотя в данном документе были показаны и описаны предпочтительные варианты осуществления настоящего изобретения, для специалистов в данной области техники будет очевидно, что такие варианты осуществления предусмотрены исключительно в качестве примера. Многочисленные вариации, изменения и замены теперь будут очевидны специалистам в данной области техники без отступления от настоящего изобретения. Следует понимать, что различные альтернативы вариантов осуществления настоящего изобретения, описанного в данном документе, могут быть использованы при осуществлении настоящего изобретения на практике. Подразумевается, что следующая формула изобретения определяет объем настоящего изобретения и таким образом охватывает способы и структуры в пределах объема данной формулы изобретения, а также их эквиваленты. Раскрытия всех патентов и научной литературы, приведенных в данном документе, явным образом включены в данный документ посредством ссылки во всей своей полноте. В той мере, в какой какой-либо включенный материал не соответствует прямому содержанию настоящего раскрытия, явное содержание имеет преимущественную силу.
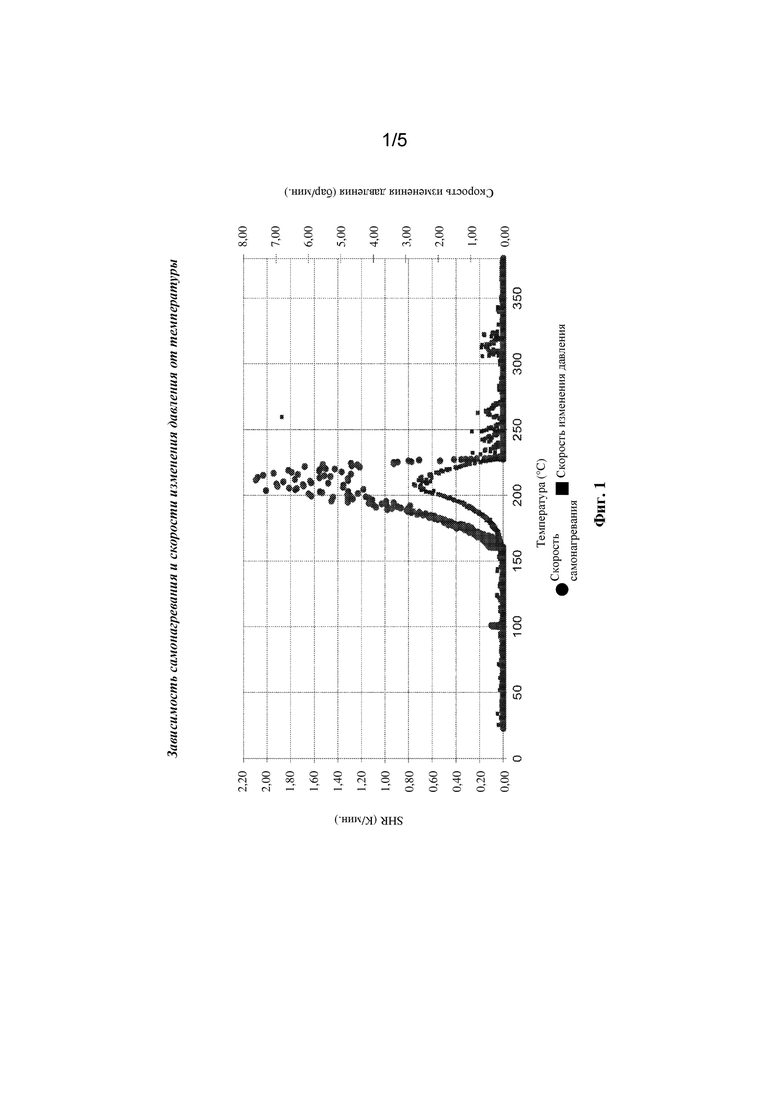
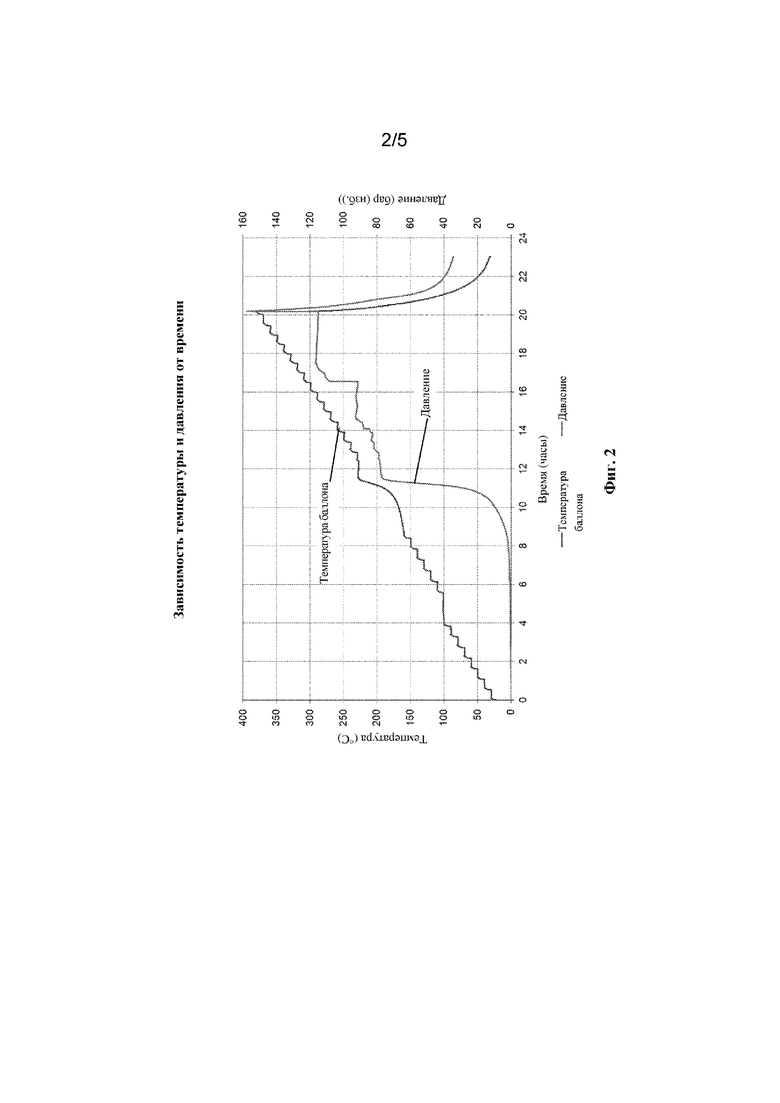
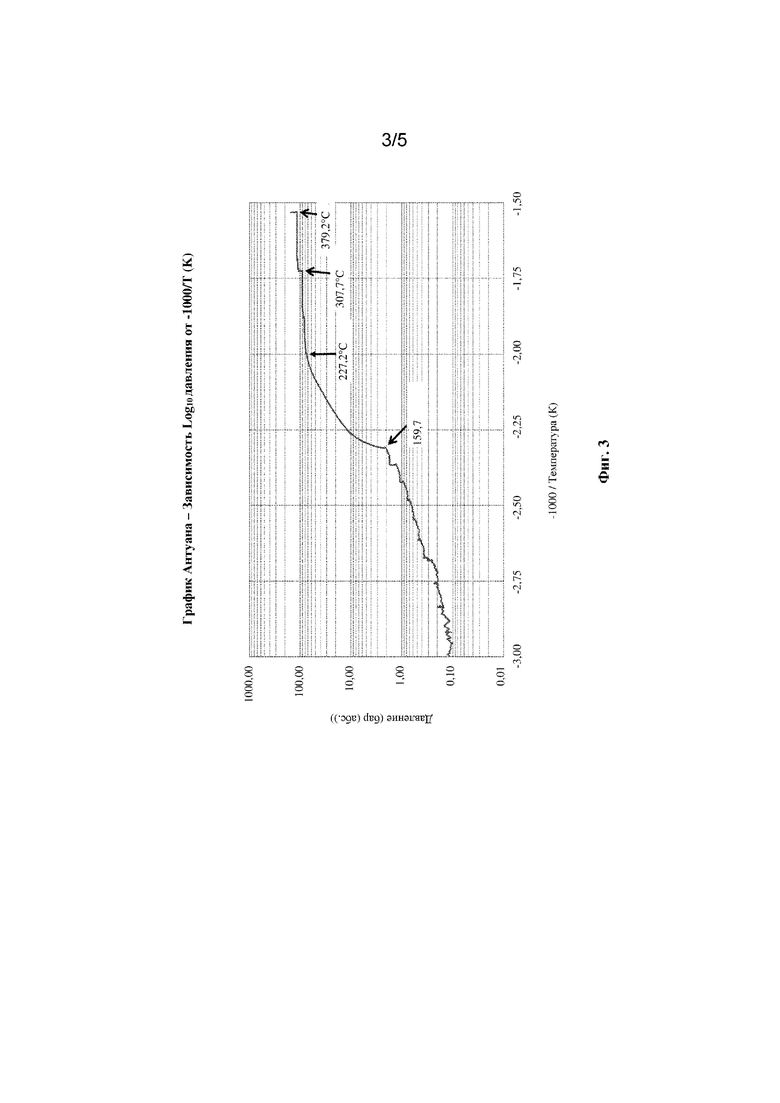
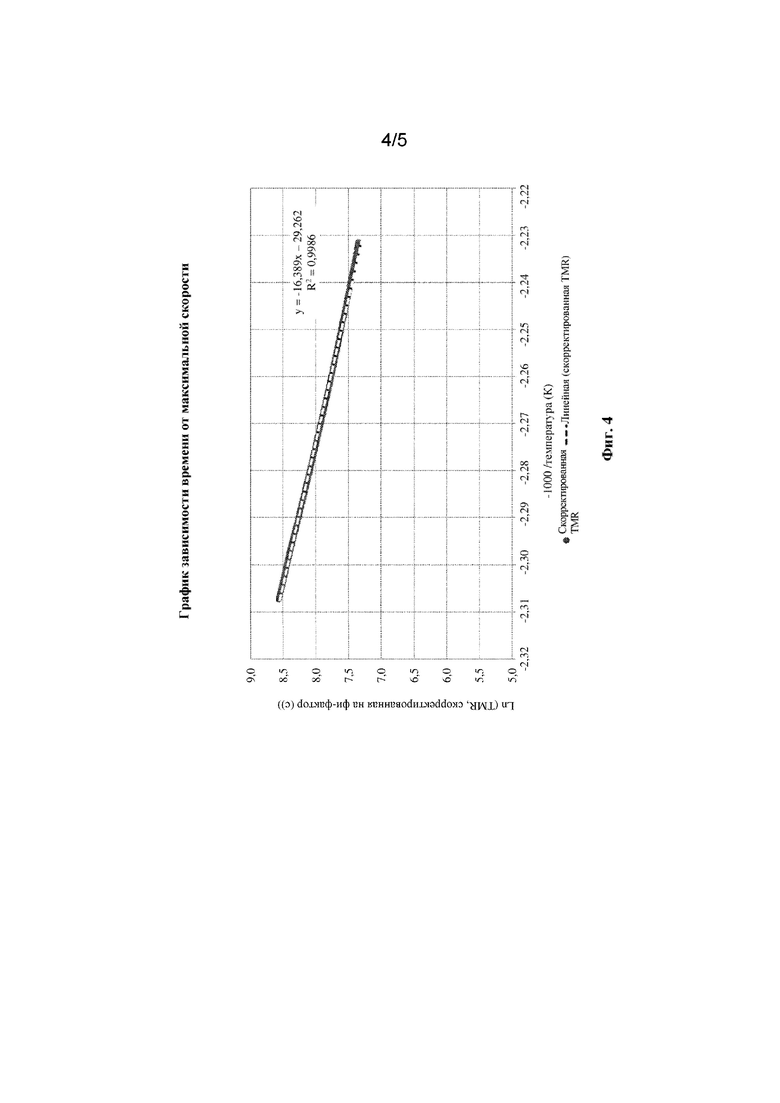
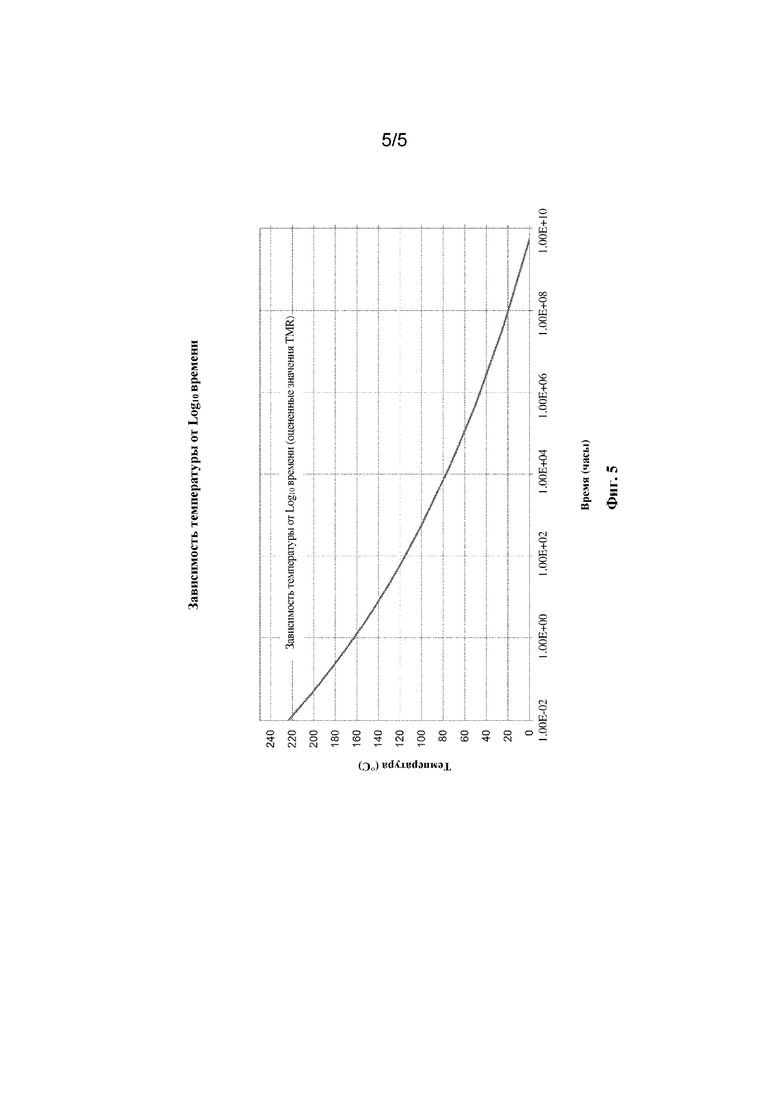
В настоящем изобретении раскрыты методы получения N6-((2-азидоэтокси)карбонил)лизина, синтеза его промежуточных соединений и конкретные промежуточные соединения и пути их применения. N6-((2-азидоэтокси)карбонил)лизин и его два энантиомера, N6-((2-азидоэтокси)карбонил)-L-лизин и N6-((2-азидоэтокси)карбонил)-D-лизин являются пригодными для получения полипептидов и белков в качестве средств изучения и терапевтических продуктов. Способ получения целевого соединения формулы (VI) или его соли включает осуществление реакции соединения формулы (III) с кислотой. Технический результат - воспроизводимый способ, обеспечивающий высокий выход целевого продукта и увеличение безопасности применения промежуточных соединений. 8 н. и 3 з.п. ф-лы, 5 ил., 5 табл., 12 пр.
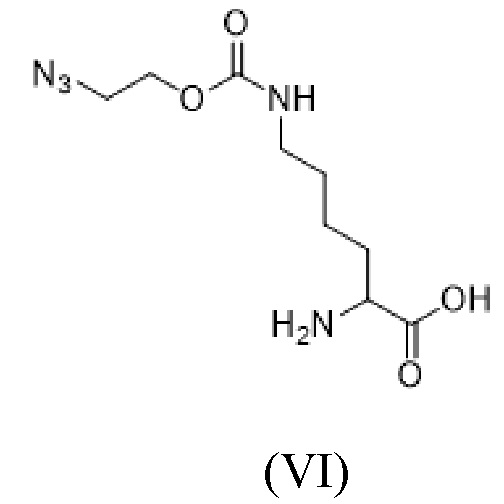
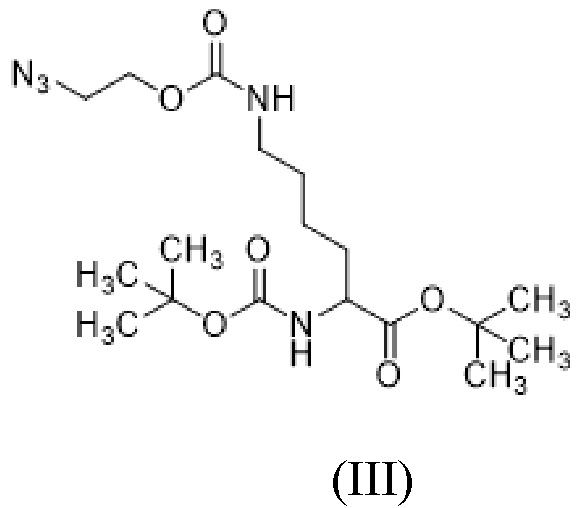
1. Способ получения соединения формулы (VI),
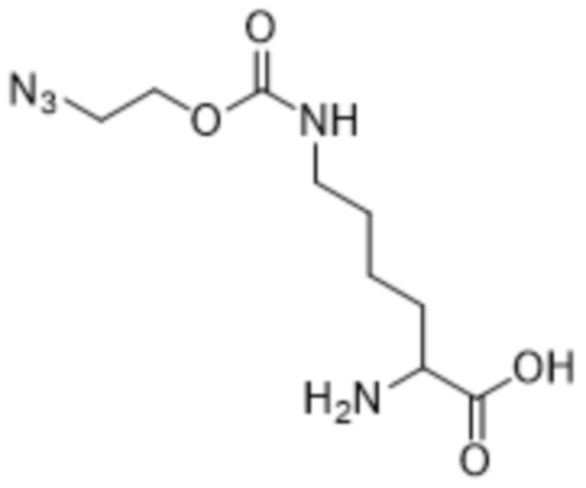
(VI),
или его соли,
включающий осуществление реакции соединения формулы (III),
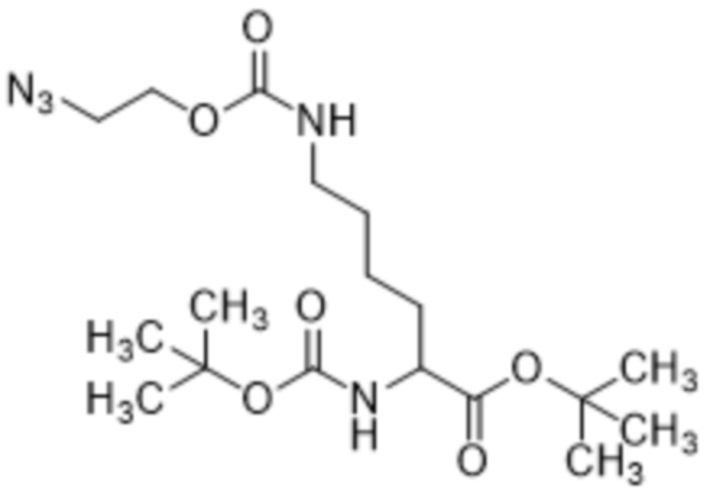
(III),
с кислотой с получением соединения формулы (VI) или его соли.
2. Способ по п. 1, где кислота представляет собой одну или несколько из фосфорной кислоты, хлористоводородной кислоты, уксусной кислоты и трифторуксусной кислоты.
3. Способ по п. 1 или 2, где кислота представляет собой хлористоводородную кислоту.
4. Способ по любому из пп. 1-3, где реакцию соединения формулы (III) с кислотой проводят в растворе, содержащем апротонный растворитель, выбранный из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, 2-метилтетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400 и полиэтиленгликолей.
5. Способ по п. 4, где апротонный растворитель представляет собой 1,4-диоксан.
6. Способ по любому из пп. 1-5, где способ дополнительно включает добавление основания.
7. Способ по п. 6, где основание представляет собой одно или несколько из гидроксида аммония, гидроксида натрия или гидроксида калия.
8. Способ по п. 6 или 7, где основание представляет собой гидроксид аммония.
9. Способ по любому из пп. 6-8, где добавление основания обеспечивает раствор, характеризующийся pH в диапазоне от 4 до 10.
10. Способ по любому из пп. 6-9, где добавление основания обеспечивает раствор, характеризующийся pH в диапазоне от 8 до 9.
11. Способ по любому из пп. 1-10, где соединение формулы (VI) представляет собой соединение формулы (VIa),
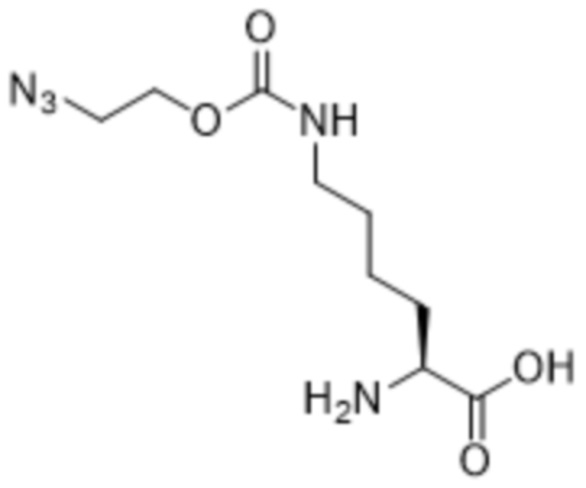
(VIa).
12. Способ получения соединения формулы (III),

(III),
включающий осуществление реакции соединения формулы (II),
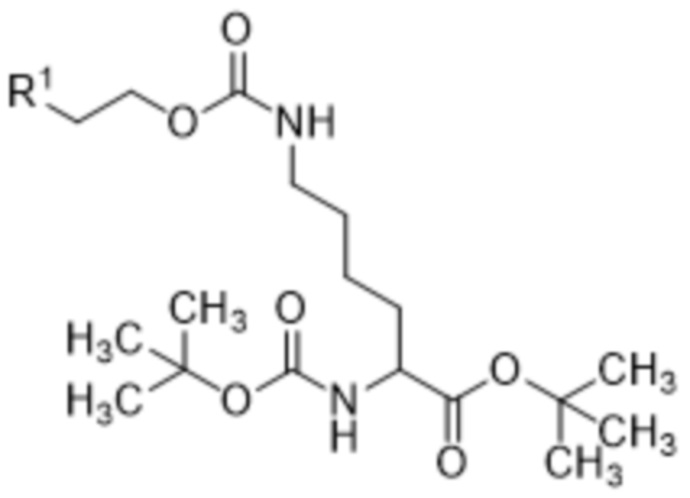
(II),
где R1 выбран из хлора, брома и йода,
с азидной солью щелочного металла с получением соединения формулы (III).
13. Способ по п. 12, где R1 представляет собой хлор.
14. Способ по п. 12 или 13, где азидная соль щелочного металла выбрана из азида лития, азида натрия и азида калия.
15. Способ по любому из пп. 12-14, где азидная соль щелочного металла представляет собой азид натрия.
16. Способ по любому из пп. 12-15, где реакцию соединения формулы (II) с азидной солью щелочного металла проводят в растворе, содержащем апротонный растворитель, выбранный из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, 2-метилтетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400, полиэтиленгликолей.
17. Способ по п. 16, где апротонный растворитель представляет собой ацетонитрил.
18. Способ по п. 16 или 17, где раствор дополнительно содержит воду.
19. Способ по любому из пп. 12-18, где соединение формулы (III) представляет собой соединение формулы (IIIa),
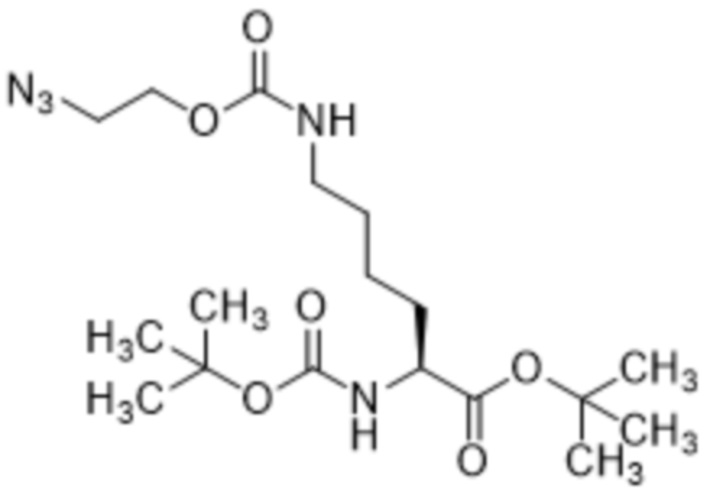
(IIIa),
и соединение формулы (II) представляет собой соединение формулы (IIa),
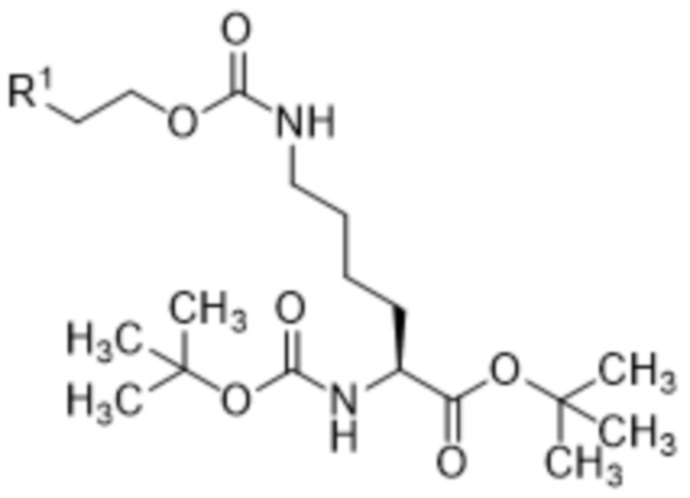
(IIa).
20. Способ получения соединения формулы (II),

(II),
включающий осуществление реакции соединения формулы (I),
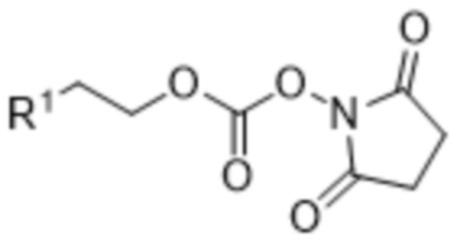
(I),
с соединением формулы (V),
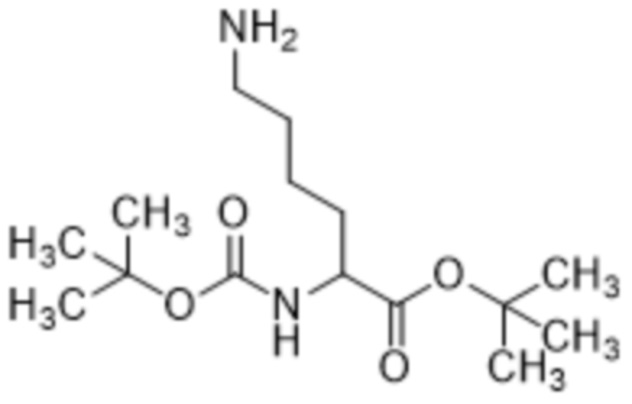
(V),
с получением соединения формулы (II),
при этом в каждом из соединений формулы (I) и формулы (II) R1 является одинаковым и выбран из хлора, брома и йода.
21. Способ по п. 20, где R1 в каждом из соединений формулы (I) и формулы (II) представляет собой хлор.
22. Способ по п. 20 или 21, где реакцию соединения формулы (V) с соединением формулы (I) проводят в растворе, содержащем апротонный растворитель, выбранный из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, 2-метилтетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400 и полиэтиленгликолей.
23. Способ по п. 22, где апротонный растворитель представляет собой 2-метилтетрагидрофуран или N,N-диметилформамид.
24. Способ по любому из пп. 20-23, где соединение формулы (II) представляет собой соединение формулы (IIa),

(IIa),
и соединение формулы (V) представляет собой соединение формулы (Va),
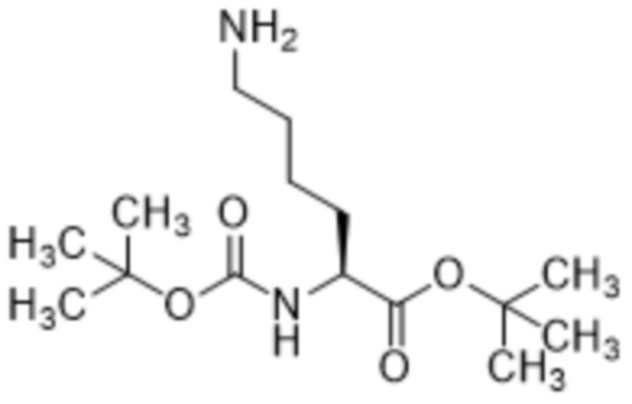
(Va).
25. Способ получения соединения формулы (I),

(I),
включающий осуществление реакции соединения формулы (IV),
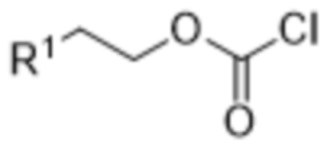
(IV),
с N-гидроксисукцинимидом с получением соединения формулы (I),
при этом в каждом из соединений формулы (I) и формулы (IV) R1 является одинаковым и выбран из хлора, брома и йода.
26. Способ по п. 25, где R1 представляет собой хлор.
27. Способ по п. 25 или 26, где реакцию соединения формулы (IV) с N-гидроксисукцинимидом проводят в растворе, содержащем апротонный растворитель, выбранный из ацетонитрила, ацетона, метилэтилкетона, дихлорметана, хлороформа, тетрагидрофурана, 2-метилтетрагидрофурана, N-метилпирролидина, диметилсульфоксида, N,N-диметилформамида, диметилацетамида, 1,4-диоксана, сульфолана, гамма-бутиролактона, пирролидонов, 1-метил-2-пирролидинона, метилпирролина, монометилового эфира этиленгликоля, монометилового эфира диэтиленгликоля, PEG400 и полиэтиленгликолей.
28. Способ по п. 27, где апротонный растворитель представляет собой ацетонитрил или 2-метилтетрагидрофуран.
29. Способ по п. 27 или 28, где раствор дополнительно содержит основание.
30. Способ по п. 29, где основание представляет собой триалкиламин.
31. Способ по п. 29 или 30, где основание представляет собой триэтиламин.
32. Способ получения соединения формулы (VIa) или его соли, включающий следующие стадии:
(i) осуществление реакции 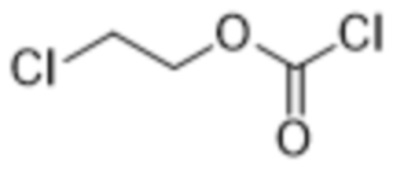 с
с 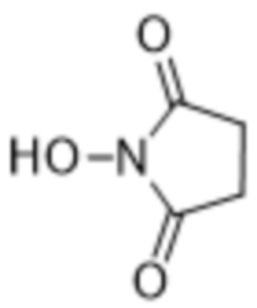 с образованием
с образованием 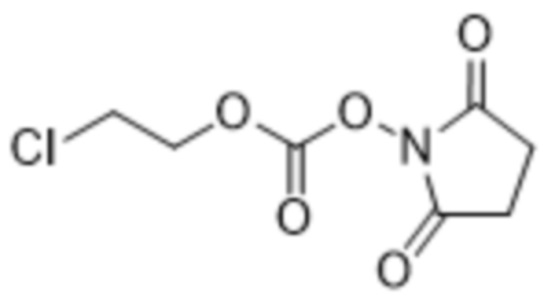 ;
;
(ii) осуществление реакции  с
с 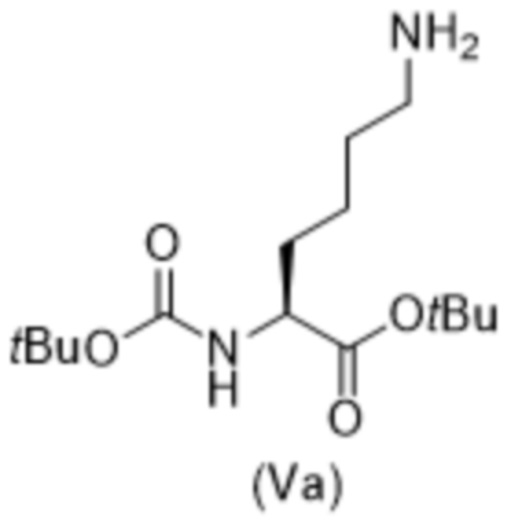 с образованием
с образованием 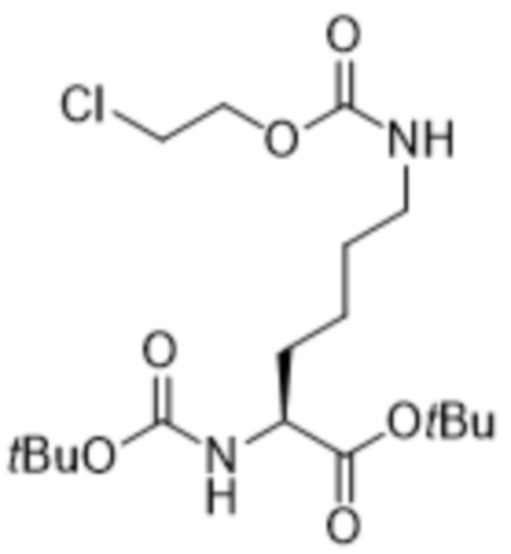 ;
;
(iii) осуществление реакции  с NaN3 с образованием
с NaN3 с образованием 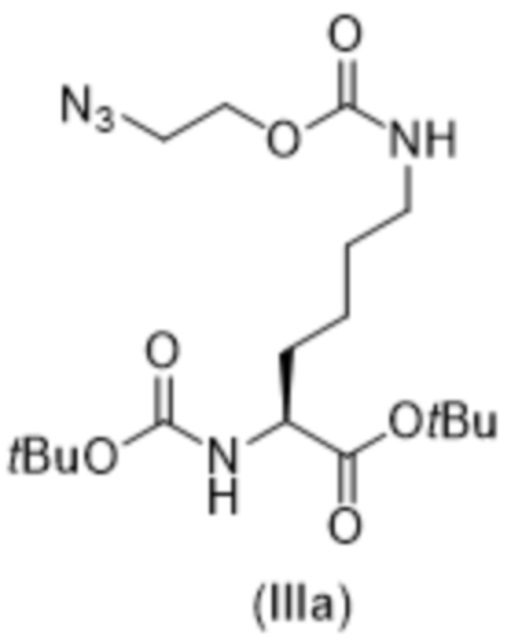 и
и
(iv) осуществление реакции  с HCl с образованием
с HCl с образованием 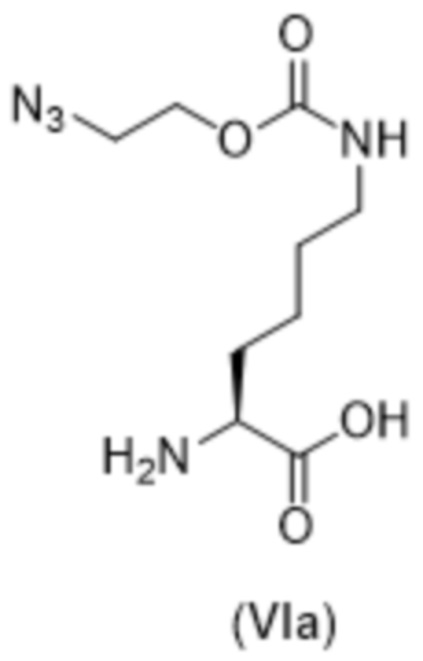 или его соли.
или его соли.
33. Соединение формулы (I),

(I),
где R1 выбран из хлора, брома и йода.
34. Соединение по п. 33, где R1 представляет собой хлор.
35. Соединение формулы (II),

(II),
где R1 выбран из хлора, брома и йода.
36. Соединение по п. 35, где R1 представляет собой хлор.
37. Соединение по п. 35 или 36, где соединение формулы (II) представляет собой соединение формулы (IIa),

(IIa).
38. Соединение формулы (III),

(III).
39. Соединение по п. 38, где соединение формулы (III) представляет собой соединение формулы (IIIa),

(IIIa).
| Milles S | |||
| et al., Click Strategies for Single-Molecule Protein Fluorescence | |||
| Jour | |||
| Of The American Chemical Society, v | |||
| Халат для профессиональных целей | 1918 |
|
SU134A1 |
| Домкрат с зубчатой рейкой | 1926 |
|
SU5187A1 |
| EP 3070095 B1, 21.09.2016 | |||
| Tatsuo Y | |||
| et al., Structural Basis for Genetic-Code Expansion with Buiky Lysine Derivatives by an Engineered Pyrrolysyl-tRNA Synthetase | |||
| Cell Chemical Biology, v | |||
| Прибор для получения стереоскопических впечатлений от двух изображений различного масштаба | 1917 |
|
SU26A1 |
Авторы
Даты
2024-12-18—Публикация
2020-12-22—Подача