ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0001] Настоящее изобретение относится к области психотерапии, в частности к кластерам золота (AuCs), связанным с лигандами, композициям, включающим кластеры золота, применению кластеров золота, связанных с лигандами, для получения лекарственных средств для лечения депрессии, а также к способам, в которых используются кластеры золота, связанные с лигандами, и композиции для лечения депрессии.
УРОВЕНЬ ТЕХНИКИ
[0002] Депрессия представляет собой психическое расстройство с высокой распространенностью среди людей, достигающей 21% населения земного шара, и является причиной тяжелых симптомов, включая печаль, гнев, разочарование, безнадежность, тревогу, раздражительность, отсутствие мотивации и чувство вины.
[0003] Хотя предполагается, что в этом процессе участвует целый ряд факторов, включая биологические различия, химический состав мозга, гормоны, наследственные особенности и хроническое воспаление, точный фактор, вызывающий депрессию, или точный механизм, посредством которого какой-либо фактор вызывает депрессию, не известен, что создает серьезные проблемы для проведения исследований и разработки способов лечения депрессии.
[0004] В настоящее время для лечения депрессии используются антидепрессанты, которые непосредственно воздействуют на химические процессы в головном мозге и, предположительно, достигают терапевтического эффекта за счет устранения химической дисрегуляции, вызывающей депрессию. К ним относятся трициклические антидепрессанты, селективные ингибиторы обратного захвата серотонина (СИОЗС, например, флуоксетин, пароксетин, сертралин, флувоксамин, циталопрам и эсциталопрам), ингибиторы обратного захвата серотонина и норадреналина (СИОЗСН, представители которых - венлафаксин и дулоксетин).
[0005] В исследованиях предпринимались попытки изучить влияние наночастиц на депрессию. Оксид цинка (NanoZnO) размером 20-80 нм уменьшал время неподвижности в тесте принудительного плавания (FST) в мышиной модели депрессии, вызванной липополисахаридами (ЛПС) (Xie 2012). Наночастицы железа (НЧЖ) размером 20 нм облегчали симптомы депрессии в модели депрессии у крыс, вызванной ЛПС (Saeidienik 2018). Однако наносеребро (nanoAg) размером 10 нм при пероральном введении в дозе 0,2 мг/кг массы тела вызывало морфологические нарушения в миелиновых оболочках, проявляя токсичность в отношении центральной нервной системы (ЦНС) у крыс (Dabrowska-Bouta 2016). Наночастицы Al2O3 (NPs), введенные респираторным путем, вызывали депрессивноподобное поведение у самок мышей (Zhang 2015). Очевидно, что проведенные ранее исследования не дают единого мнения и рекомендаций относительно влияния наночастиц на течение депрессии.
[0006] В настоящее время сохраняется потребность в разработке эффективного способа и лекарственных препаратов для лечения депрессии.
РАСКРЫТИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
[0007] Настоящее изобретение относится к кластерам золота, связанным с лигандами, для применения в лечении депрессии у субъекта.
[0008] В определенных вариантах осуществления настоящего изобретения для лечения депрессии у субъекта применяется кластер золота, связанный с лигандом, при этом кластер золота, связанный с лигандом, включает золотое ядро и лиганд, связанный с золотым ядром.
[0009] В определенных вариантах терапевтического применения золотое ядро имеет диаметр в интервале 0,5-3 нм. В определенных вариантах осуществления изобретения золотое ядро имеет диаметр в интервале 0,5-2,6 нм.
[0010] В определенных вариантах терапевтического применения лиганд представляет собой лиганд, выбранный из группы, состоящей из L-цистеина и его производных, D-цистеина и его производных, цистеинсодержащих олигопептидов и их производных, а также других тиолсодержащих соединений.
[0011] В определенных вариантах терапевтического применения L-цистеин и его производные выбирают из группы, состоящей из L-цистеина, N-изобутирил-L-цистеина (L-NIBC) и N-ацетил-L-цистеина (L-NAC), а D-цистеин и его производные выбирают из группы, состоящей из D-цистеина, N-изобутирил-D-цистеина (D-NIBC) и N-ацетил-D-цистеина (D-NAC).
[0012] В определенных вариантах терапевтического применения цистеинсодержащие олигопептиды и их производные представляют собой цистеинсодержащие дипептиды, где цистеинсодержащие дипептиды выбирают из группы, состоящей из L(D)-цистеин-L(D)-аргинин дипептида (CR), L(D)-аргинин-L(D)-цистеин дипептида (RC), L(D)- гистидин-L(D)-цистеин дипептида (НС) и L(D)-цистеин-L(D)-гистидин дипептида (СН).
[0013] В определенных вариантах терапевтического применения цистеинсодержащие олигопептиды и их производные представляют собой цистеинсодержащие трипептиды, где цистеинсодержащие трипептиды выбирают из группы, состоящей из глицин-L(D)-цистеин-L(D)-аргининового трипептида (GCR), L(D)-пролин-L(D)-цистеин-L(D)-аргинин трипептида (PCR), L(D)-лизин-L(D)-цистеин-L(D)-пролин трипептида (KCP) и L(D)-глутатиона (GSH).
[0014] В определенных вариантах терапевтического применения цистеинсодержащие олигопептиды и их производные представляют собой цистеинсодержащие тетрапептиды, где цистеинсодержащие тетрапептиды выбирают из группы, состоящей из глицин-L(D)-серин-L(D)-цистеин-L(D)-аргинин тетрапептида (GSCR) и глицин-L(D)-цистеин-L(D)-серин-L(D)-аргинин тетрапептида (GCSR).
[0015] В определенных вариантах терапевтического применения цистеинсодержащие олигопептиды и их производные представляют собой цистеинсодержащий пентапептид, где цистеинсодержащие пентапептиды выбирают из группы, состоящей из цистеинил-аспарагинил-глутаминил-валинил-аспарагина (CDEVD) и аспарагинил-глутаминил-валинил-аспарагинил-цистеина (DEVDC).
[0016] В определенных вариантах терапевтического применения другие тиолсодержащие соединения выбирают из группы, состоящей из 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L(D)-пролина, тиогликолевой кислоты, меркаптоэтанола, тиофенола, D-3-троловола, N-(2-меркаптопропионил)-глицина, додецилмеркаптана, 2-аминоэтанэтиола (CSH), 3-меркаптопропионовой кислоты (МРА) и 4-меркаптобеновой кислоты (р-МВА).
[0017] Задачи и преимущества изобретения будут раскрыты из следующего подробного описания предпочтительных вариантов его осуществления в совокупности с прилагаемыми чертежами.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0018] Предпочтительные варианты осуществления настоящего изобретения будут описаны далее со ссылками на Фигуры, на которых одинаковые цифры обозначают одинаковые элементы.
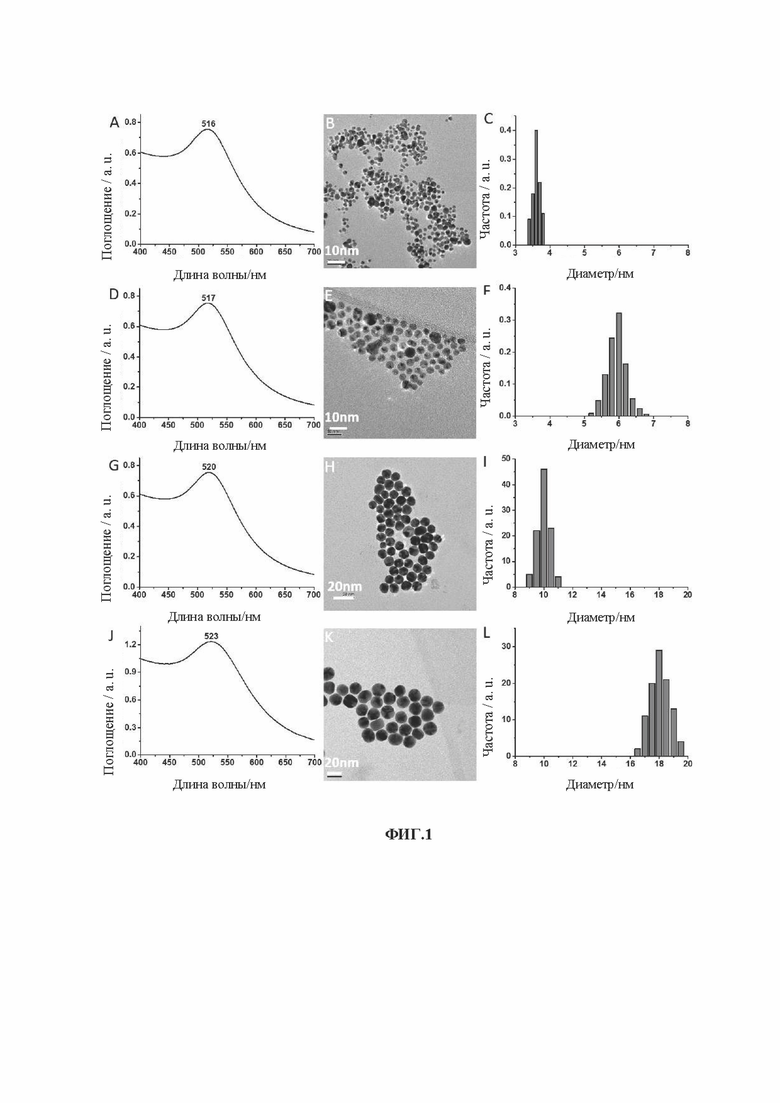
[0019] На фиг. 1 показаны ультрафиолетово-видимые (УФ) спектры, изображения просвечивающего электронного микроскопа (ПЭМ) и диаграммы распределения частиц по размерам лиганда L-NIBC, модифицированного наночастицами золота (L-NIBC-AuNPs) с различными размерами частиц.
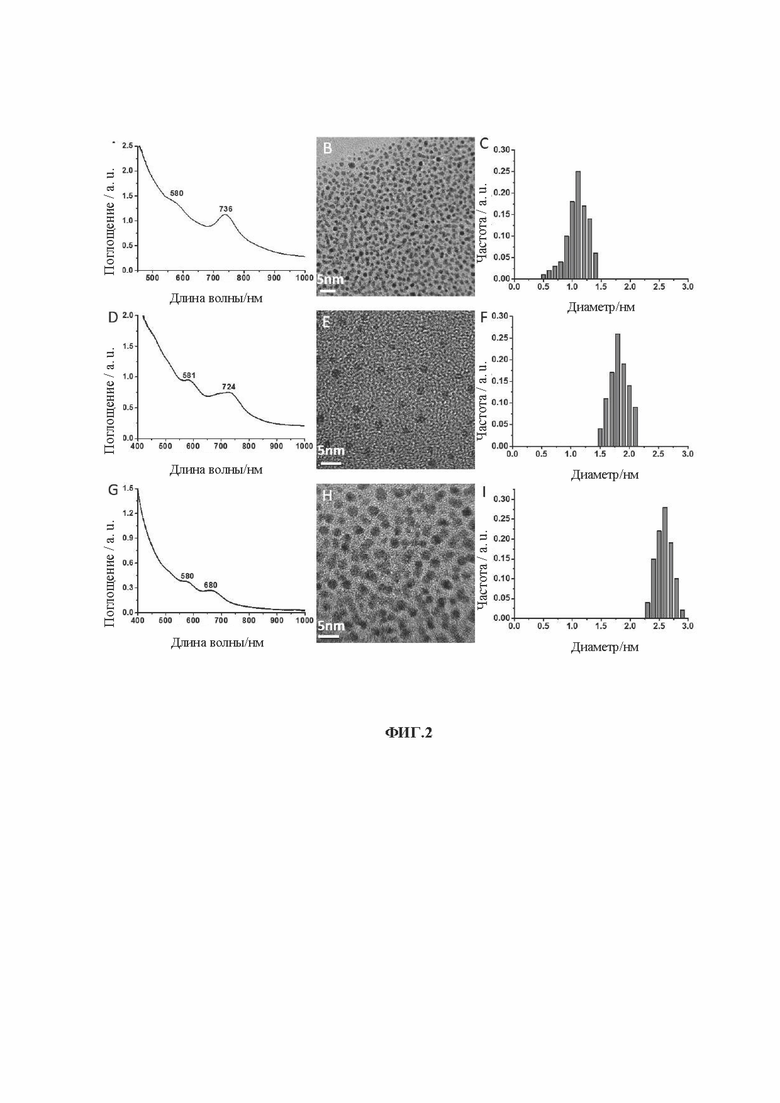
[0020] На фиг. 2 показаны ультрафиолетово-видимые (УФ) спектры, изображения ПЭМ и диаграммы распределения частиц по размерам кластеров золота, связанных с лигандом L-NIBC (L-NIBC-AuCs) с различными размерами частиц.
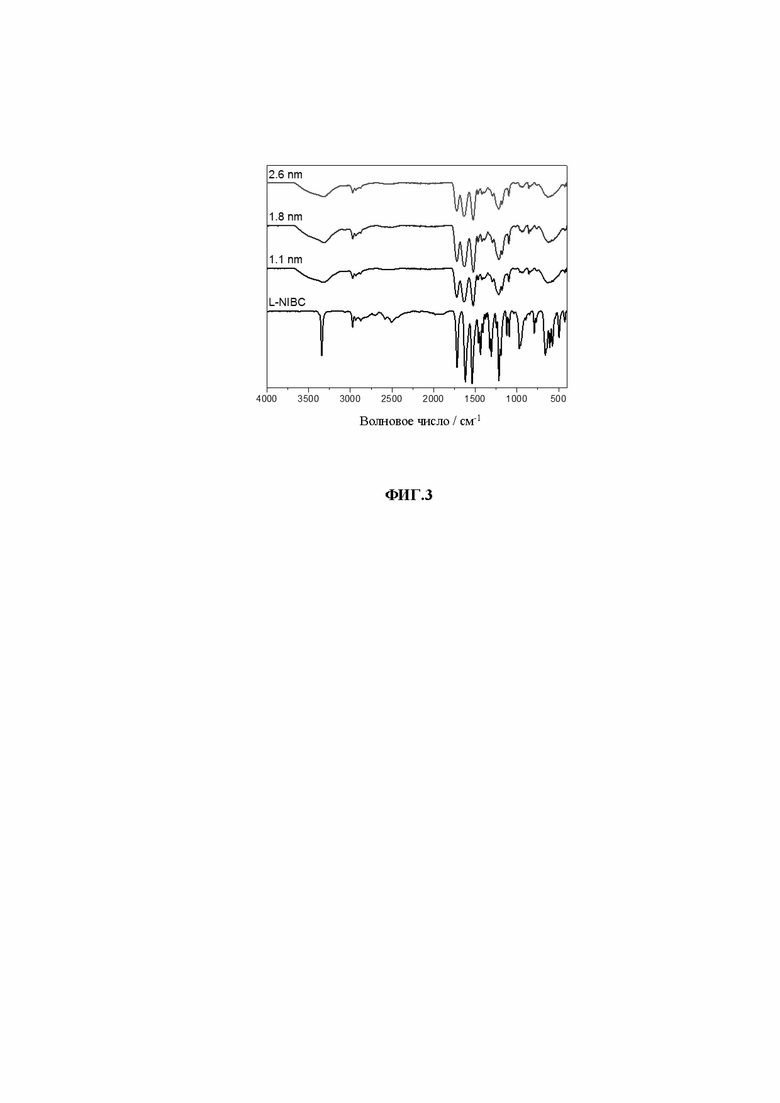
[0021] На фиг. 3 показаны инфракрасные спектры L-NIBC-AuCs с различными размерами частиц.
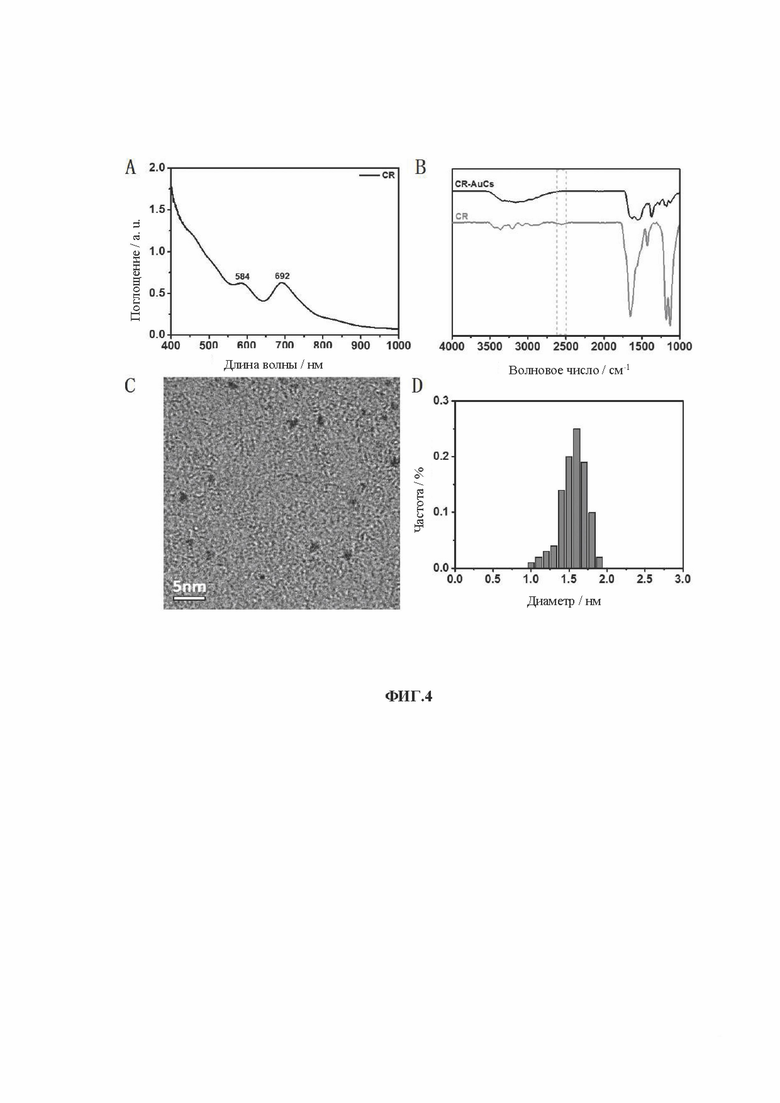
[0022] На фиг. 4 показаны УФ-, ИК-, ПЭМ- и диаграммы распределения частиц по размерам кластеров золота, связанных с лигандом CR (CR-AuCs).
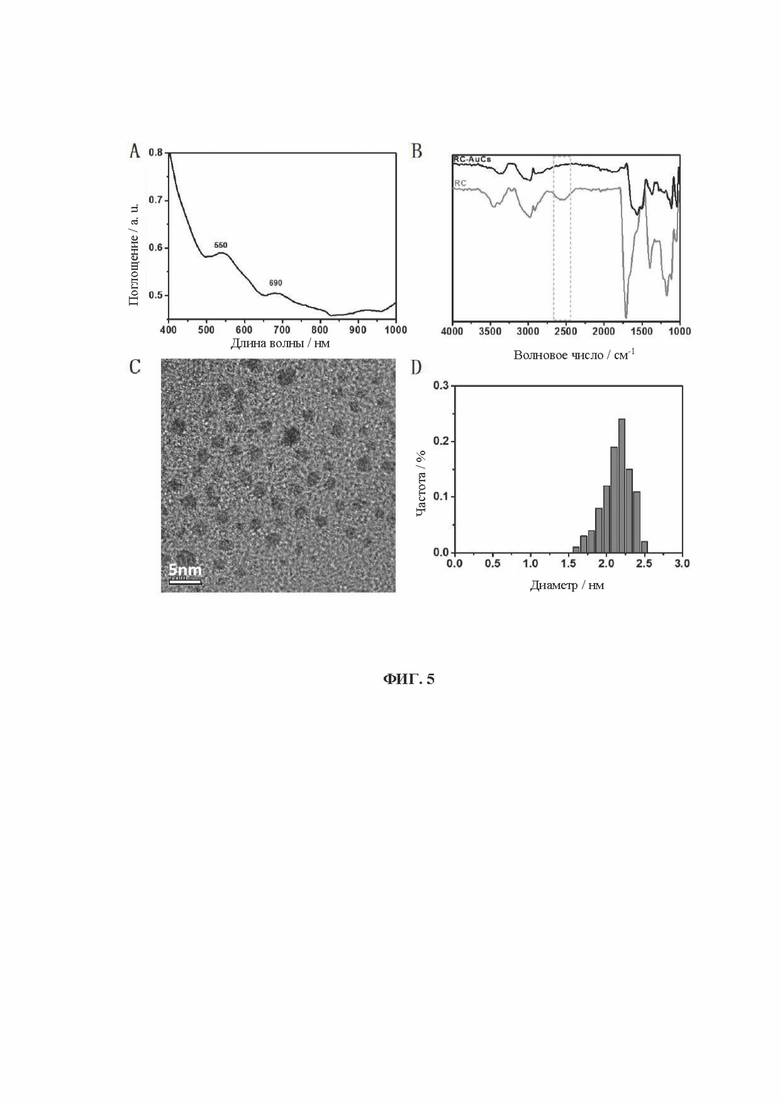
[0023] На фиг. 5 показаны УФ-, ИК-, ПЭМ- и диаграммы распределения частиц по размерам кластеров золота, связанных с лигандом RC (RC-AuCs).
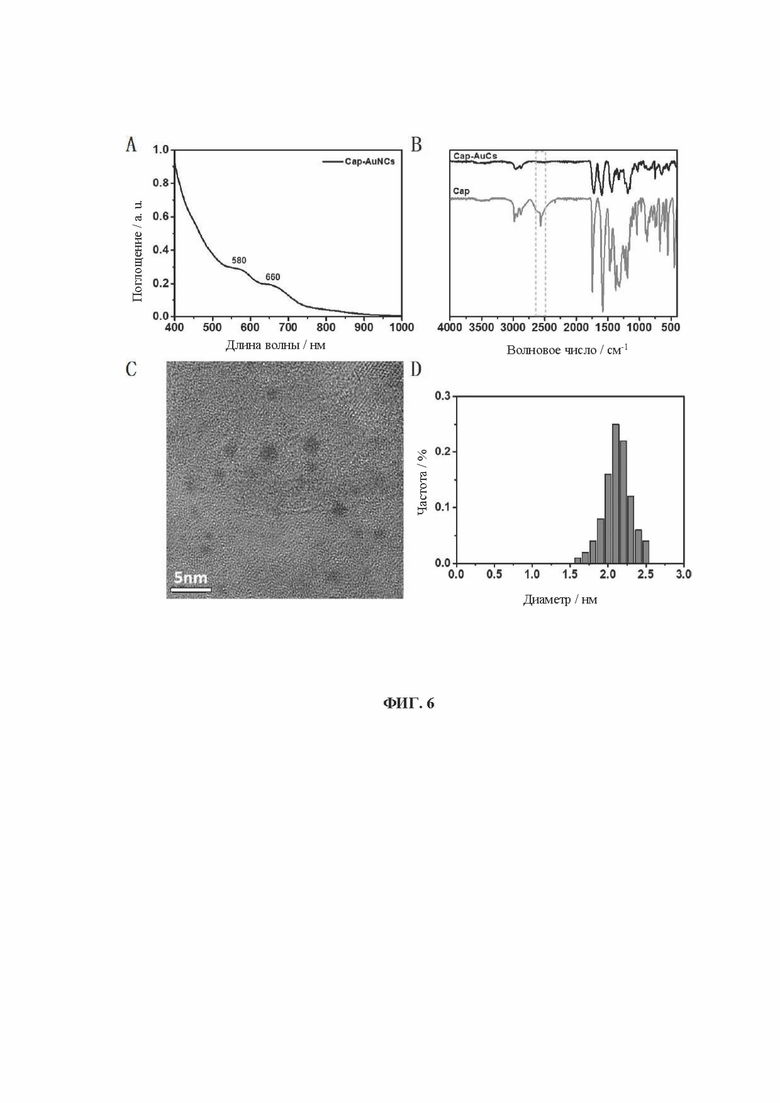
[0024] На фиг. 6 показаны УФ-, ИК-, ПЭМ- и диаграммы распределения частиц по размерам кластеров золота, связанных с лигандом 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L-пролин (т.е. Сар).
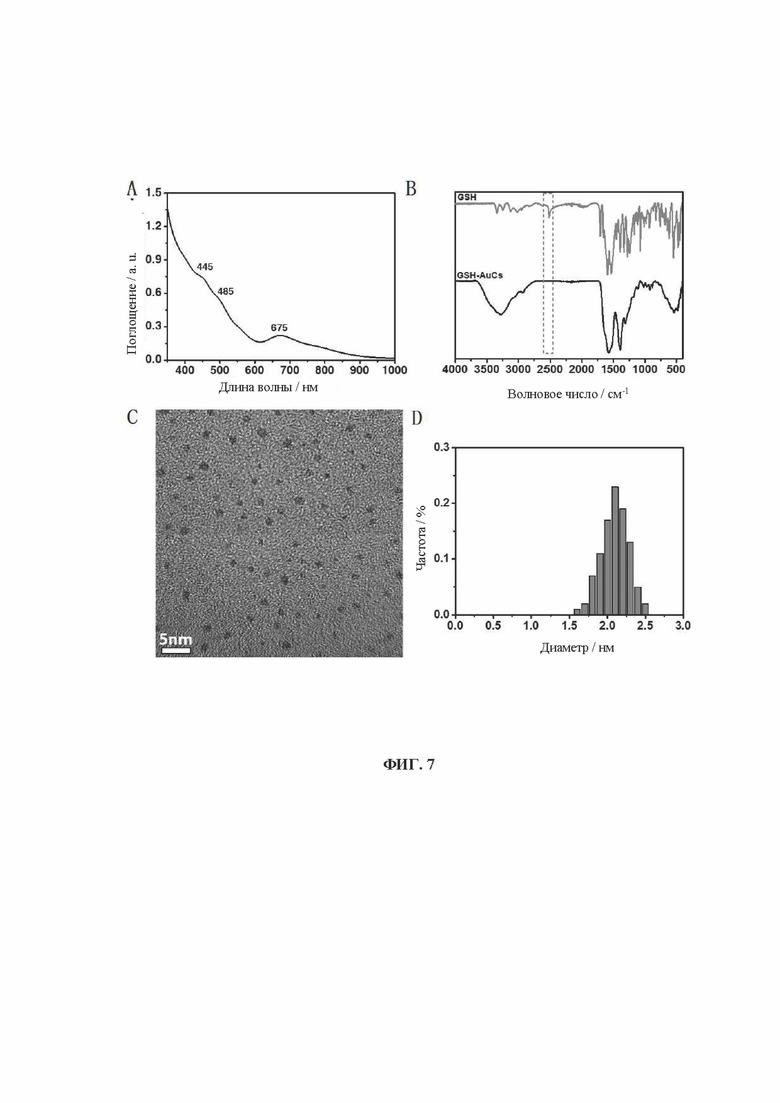
[0025] На фиг. 7 показаны УФ-, ИК- и ПЭМ- и диаграммы распределения частиц по размерам кластеров золота, связанных с лигандом GSH (GSH-AuCs).
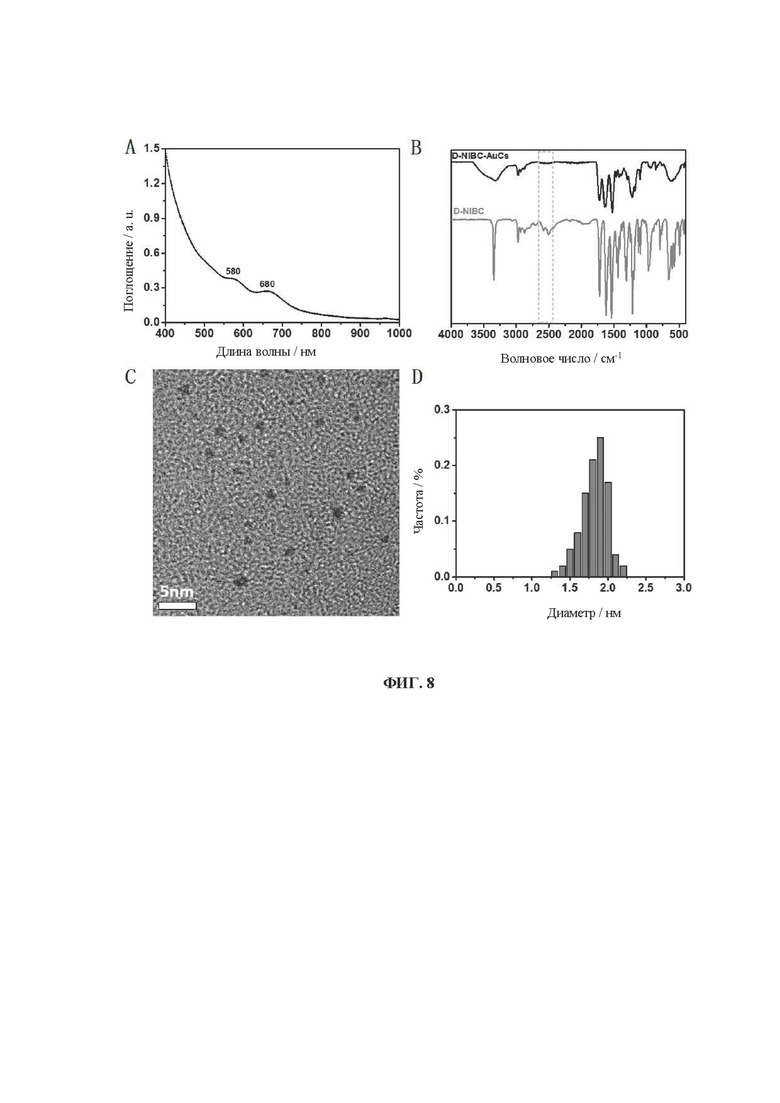
[0026] На фиг. 8 показаны УФ-, ИК-, ПЭМ- и диаграммы распределения частиц по размерам кластеров золота, связанных с лигандом D-NIBC (D-NIBC-AuCs).
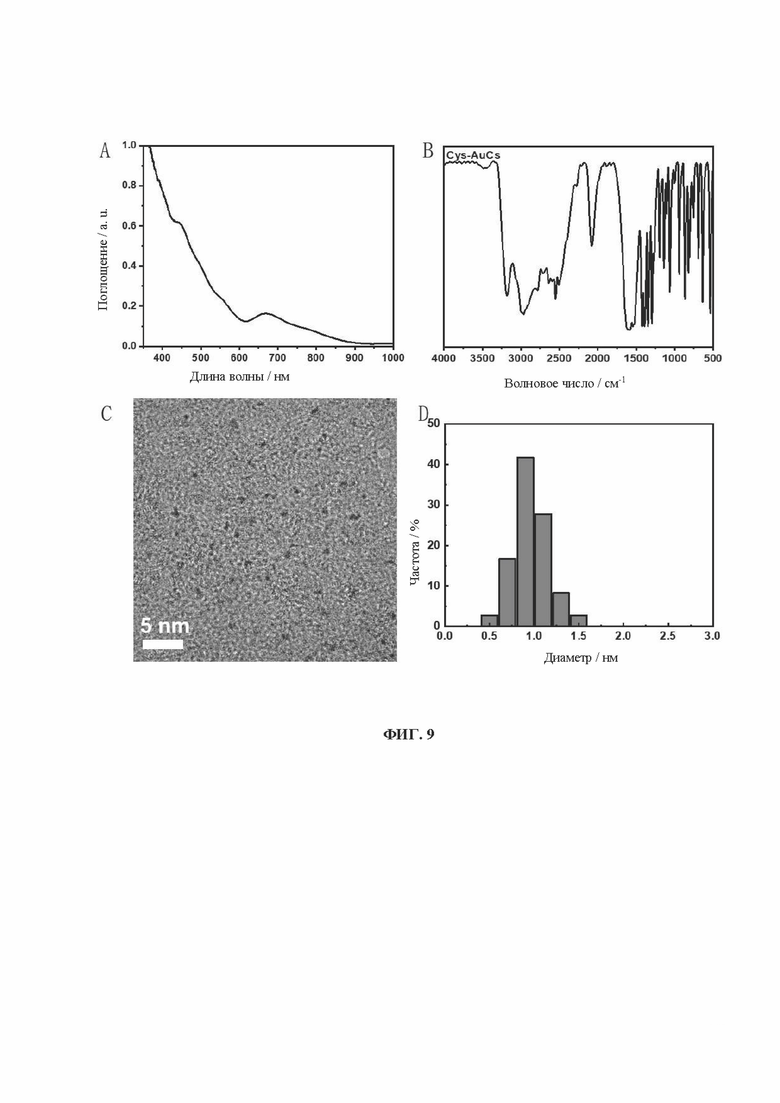
[0027] На фиг. 9 показаны УФ-, ИК-, ПЭМ- и диаграммы распределения частиц по размерам кластеров золота, связанных с лигандом L-цистеином (L-Cys-AuCs).
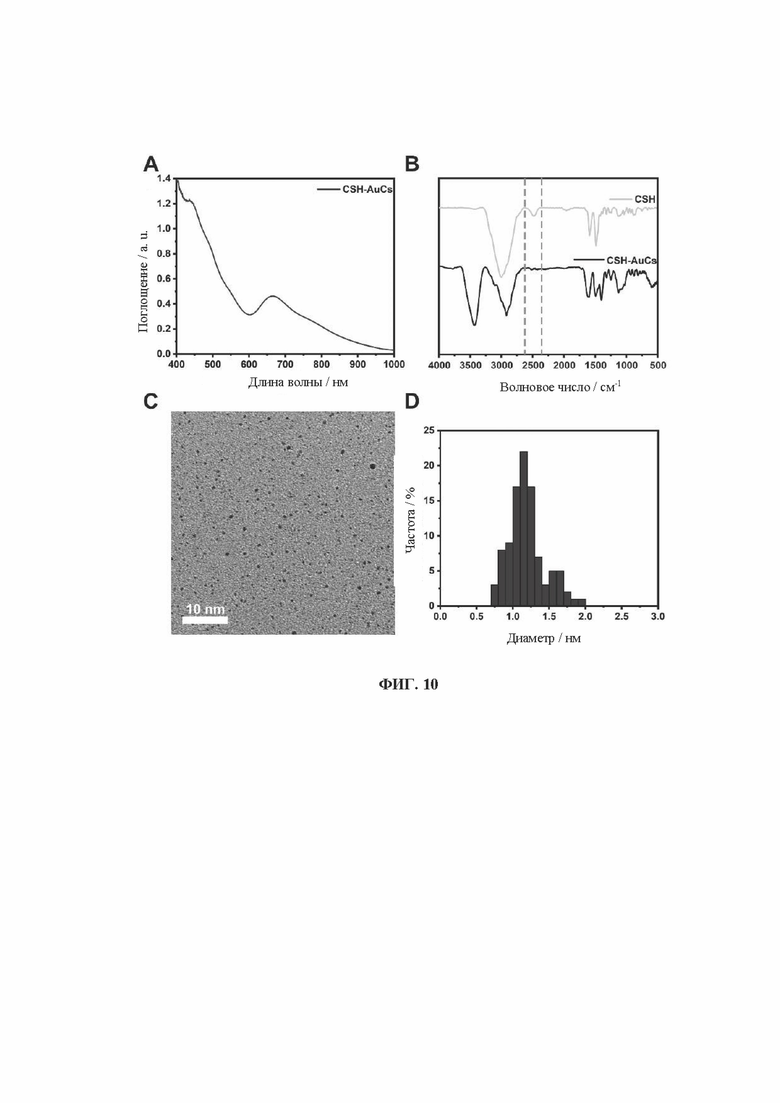
[0028] На фиг. 10 показаны УФ-, ИК-, ПЭМ- и диаграммы распределения частиц по размерам кластеров золота, связанных с лигандом 2-аминоэтандиолом (CSH-AuCs).
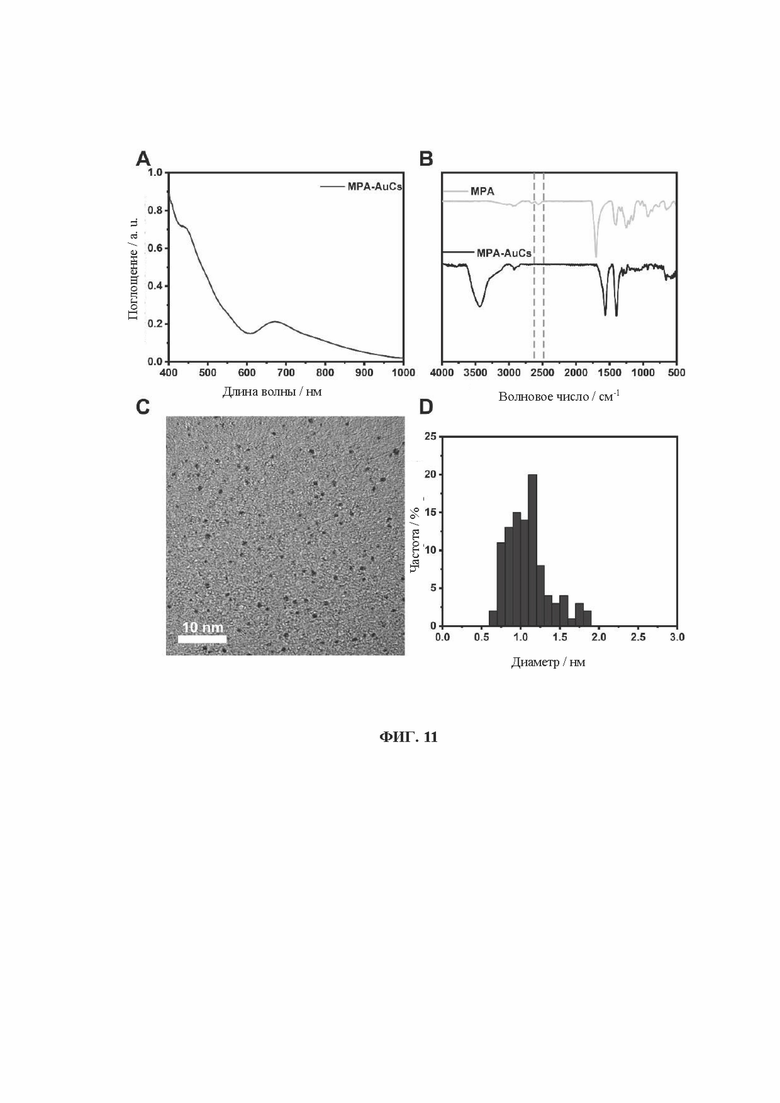
[0029] На фиг. 11 показаны УФ-, ИК-, ПЭМ- и диаграммы распределения частиц по размерам кластеров золота, связанных с лигандом 3-меркаптопропионовой кислотой (MPA-AuCs).
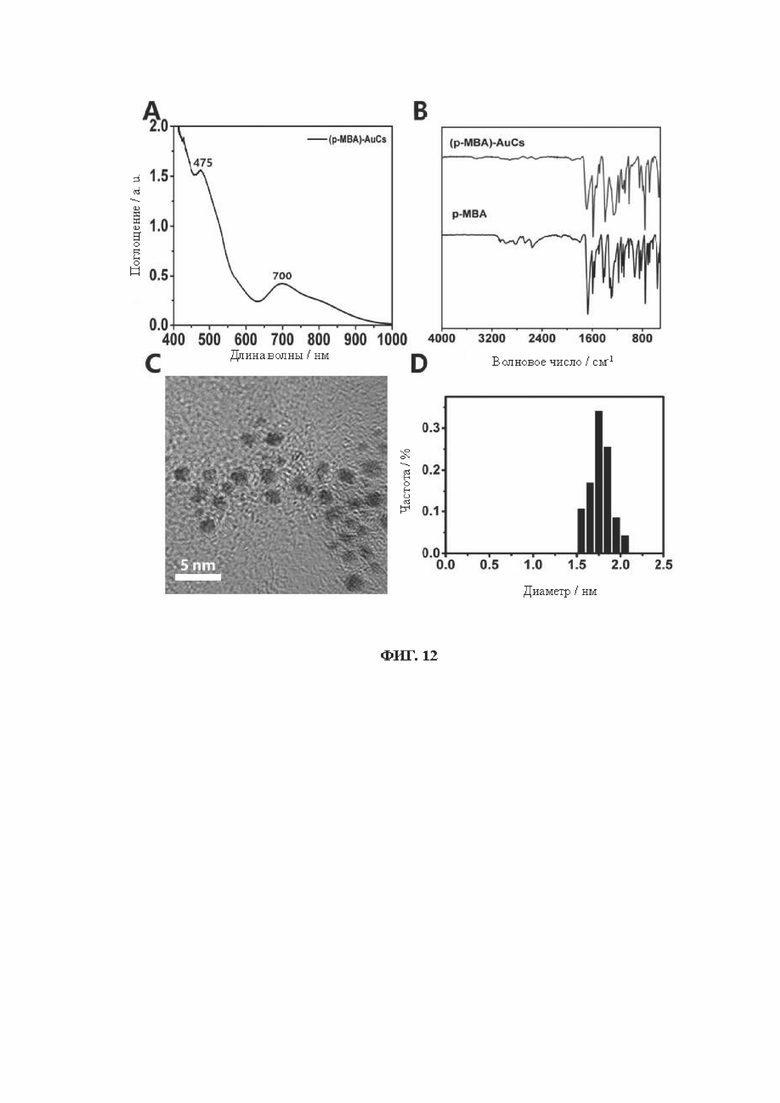
[0030] На фиг. 12 показаны УФ-, ИК-, ПЭМ- и диаграммы распределения частиц по размерам кластеров золота, связанных с лигандом 4-меркаптобеновой кислоты (p-MBA-AuCs).
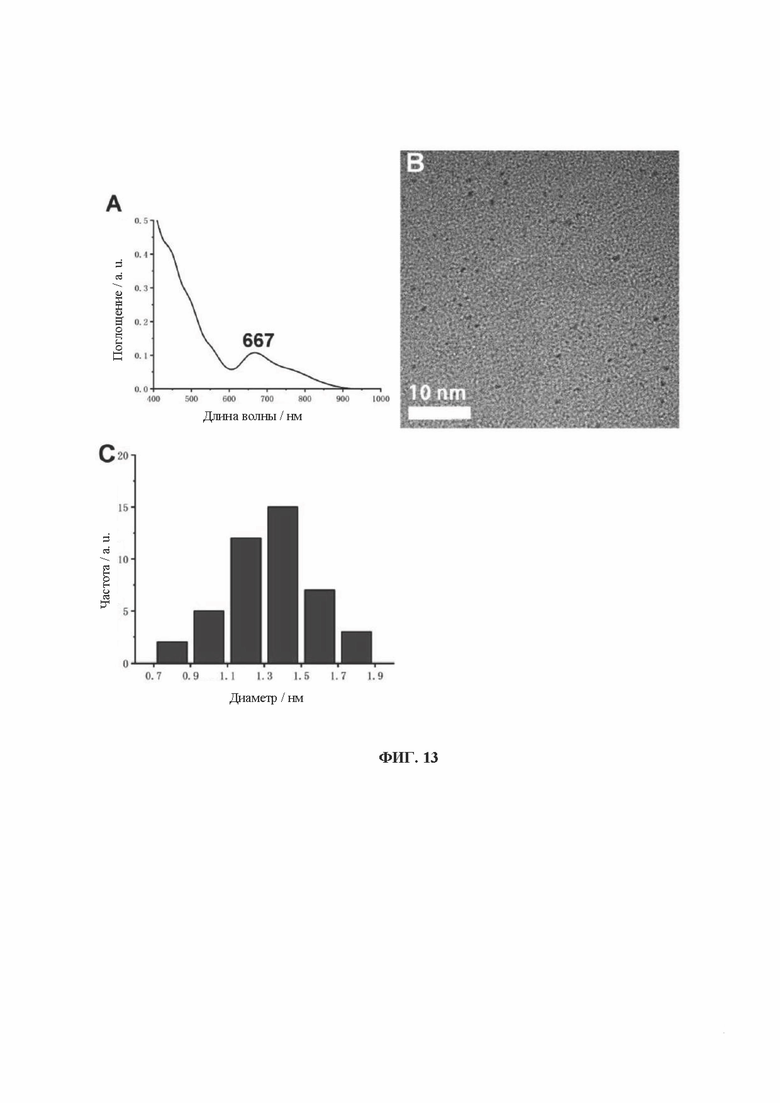
[0031] На фиг. 13 показаны УФ-, ПЭМ- и диаграммы распределения частиц по размерам кластеров золота, связанных лигандом 4-цистеинил-аспарагинил-глутаминил-валинил-аспарагин (CDEVD).
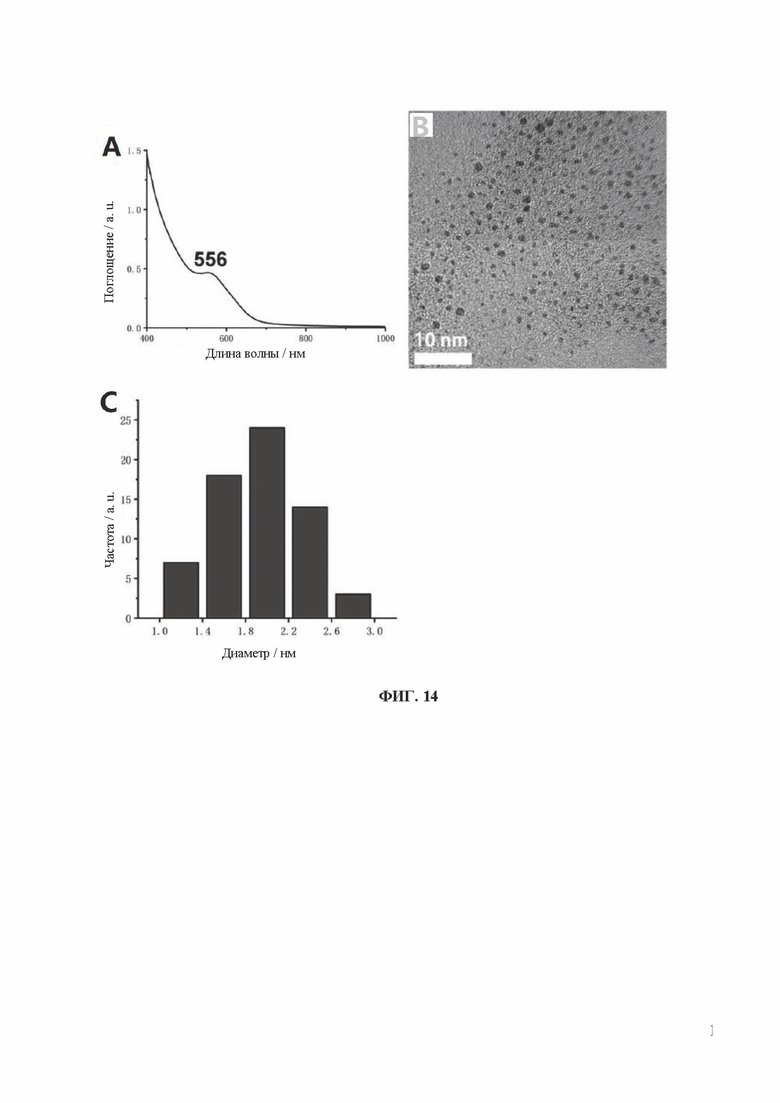
[0032] На фиг. 14 показаны УФ-, ПЭМ- и диаграммы распределения частиц по размерам кластеров золота, связанных лигандом 4-аспарагиновая кислота-глутаминовая кислота-валин-аспарагиновая кислота-цистеин (DEVDC) (DEVDC-AuCs).
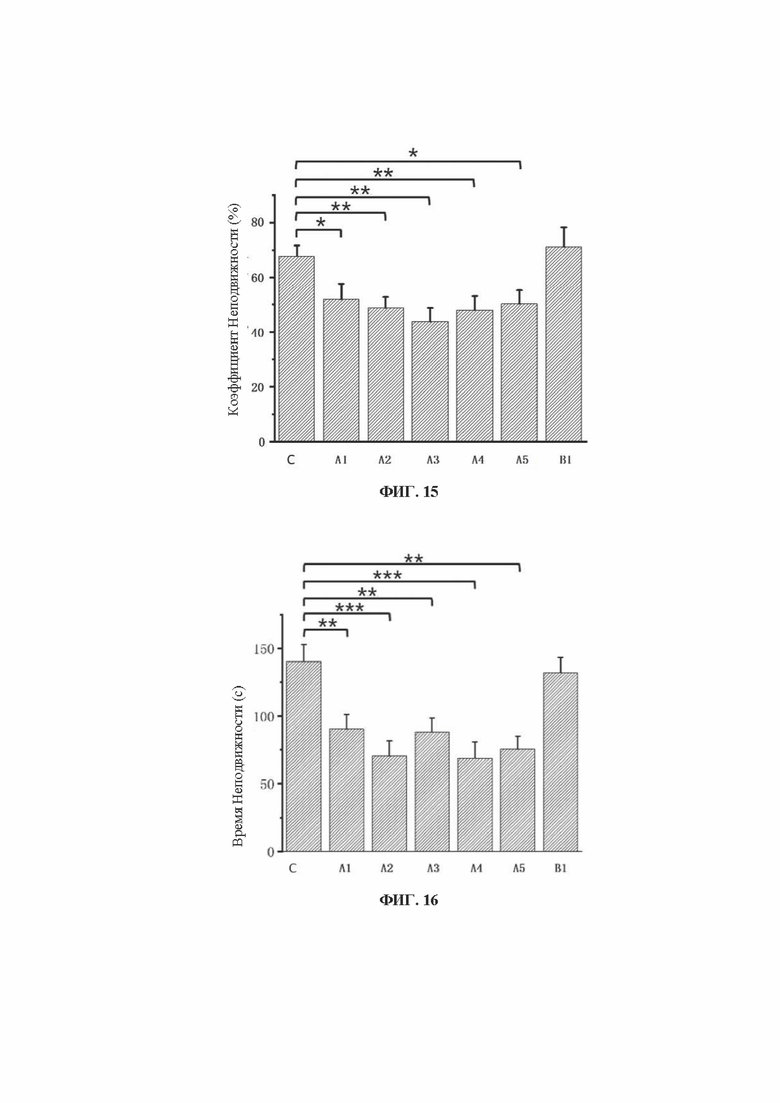
[0033] На фиг. 15 представлена гистограмма, отражающая результаты тестов принудительного плавания.
[0034] На фиг. 16 представлена гистограмма, отражающая результаты тестов подвешивания за хвост.
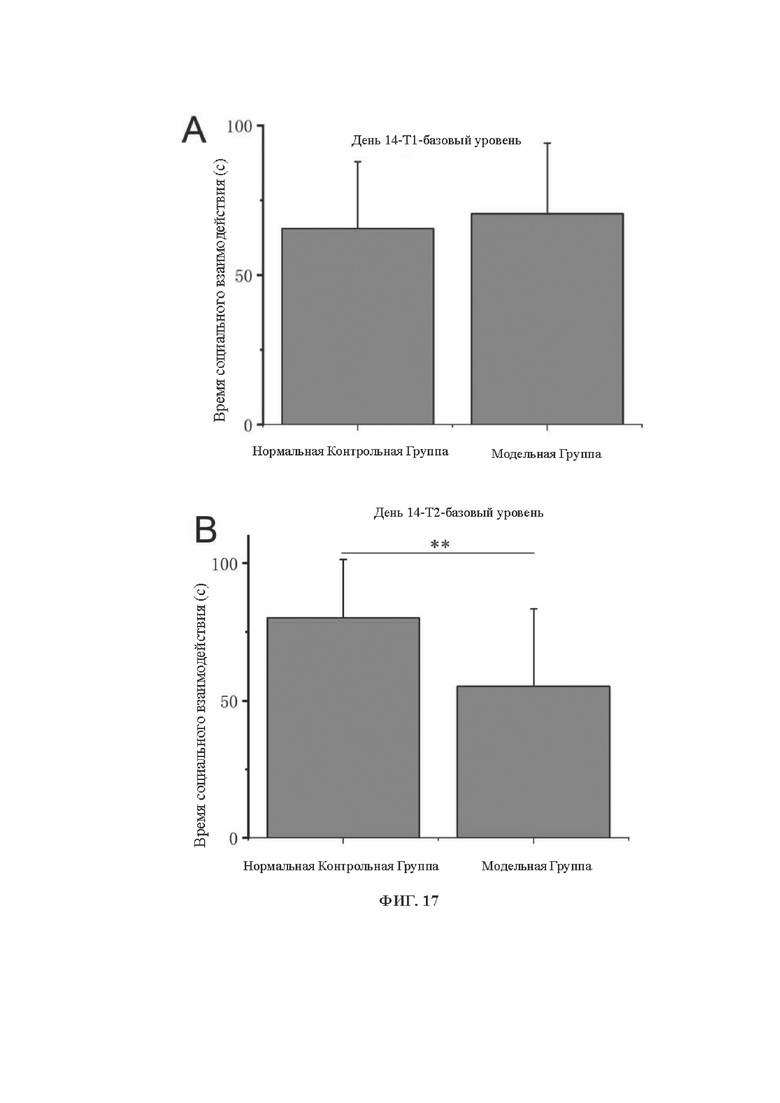
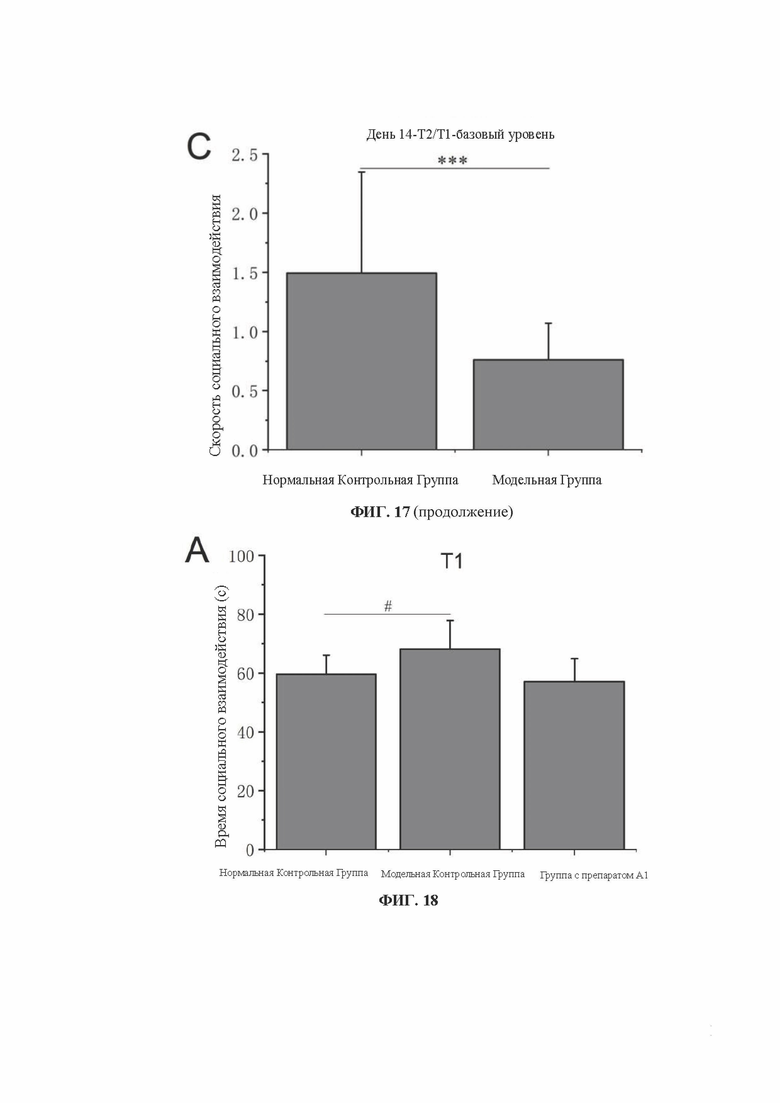
[0035] На фиг. 17 показаны результаты теста социального поведения мышей с хроническим социальным стрессом: А - время социального взаимодействия Т1 у мышей с нормальным уровнем стресса и модельных мышей в зоне социального взаимодействия на первом этапе теста; В - время социального взаимодействия Т2 у мышей с нормальным уровнем стресса и модельных мышей в зоне социального взаимодействия на втором этапе теста; С - соотношение социального взаимодействия Т2/Т1 у мышей с нормальным уровнем стресса и модельных мышей в тесте социального поведения. Данные приведены в формате Среднее ± Стд. откл., ** Р<0,01 и *** Р<0,001 по сравнению с нормальными мышами в группе нормального контроля.
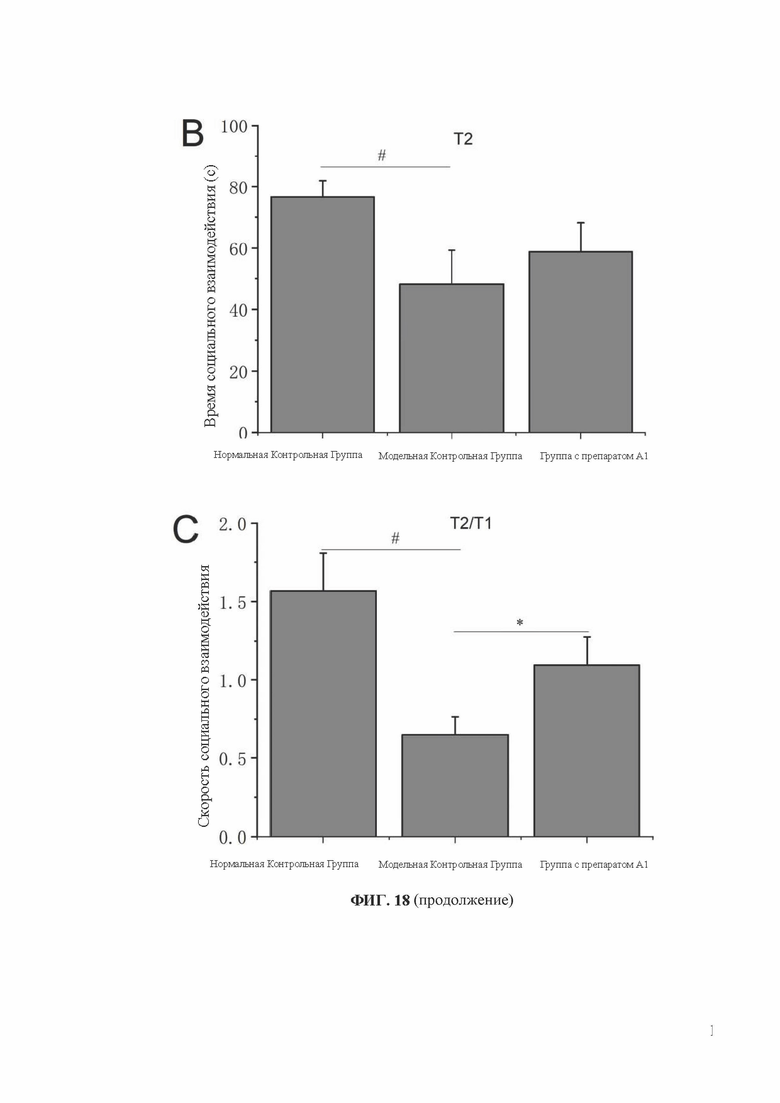
[0036] На фиг. 18 показаны результаты теста социального поведения мышей в группе введения препарата A1: А - на первом этапе теста - время социального взаимодействия Т1 мышей нормальной контрольной группы, модельной контрольной группы и группы введения препарата А1 в зоне социального взаимодействия; В - на втором этапе - время социального взаимодействия Т2 мышей нормальной контрольной группы, модельной контрольной группы и группы введения препарата А1 в зоне социального взаимодействия; С - коэффициент социального взаимодействия Т2/Т1 мышей нормальной контрольной группы, модельной контрольной группы и группы введения препарата А1 в тесте социального поведения. Данные представлены в формате Среднее ± Стд. откл., # Р<0,05 по сравнению с группой нормального контроля, * Р<0,05 по сравнению с группой модельного контроля.
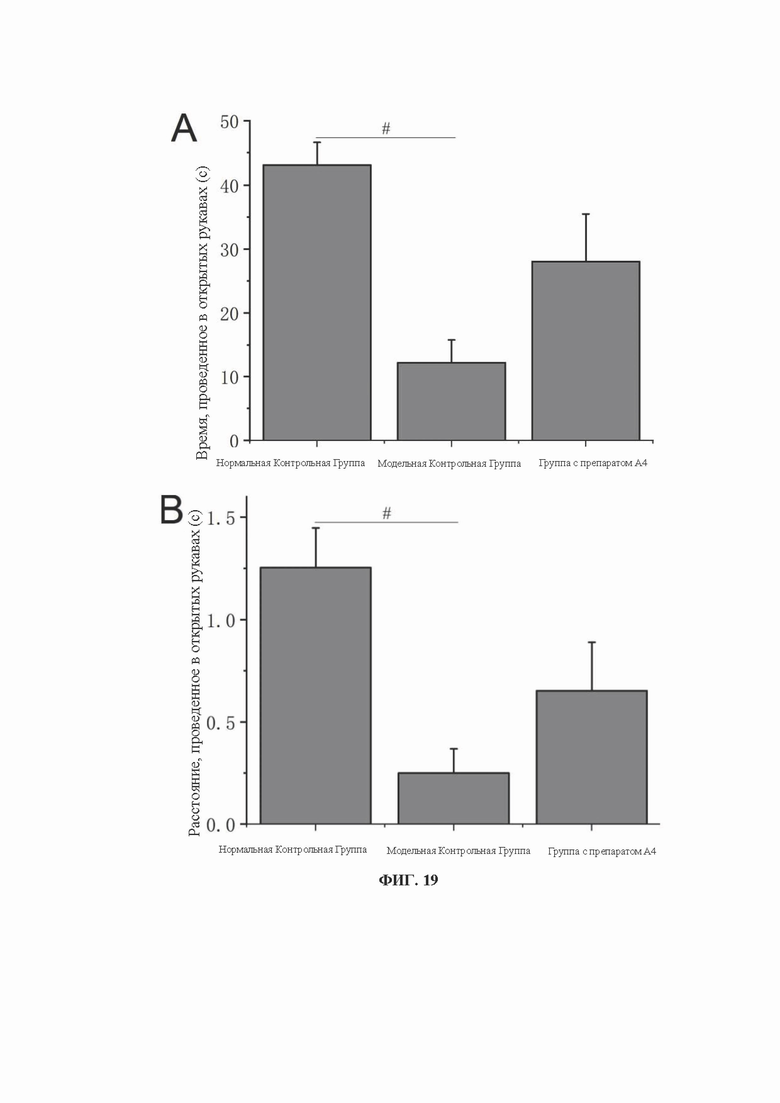
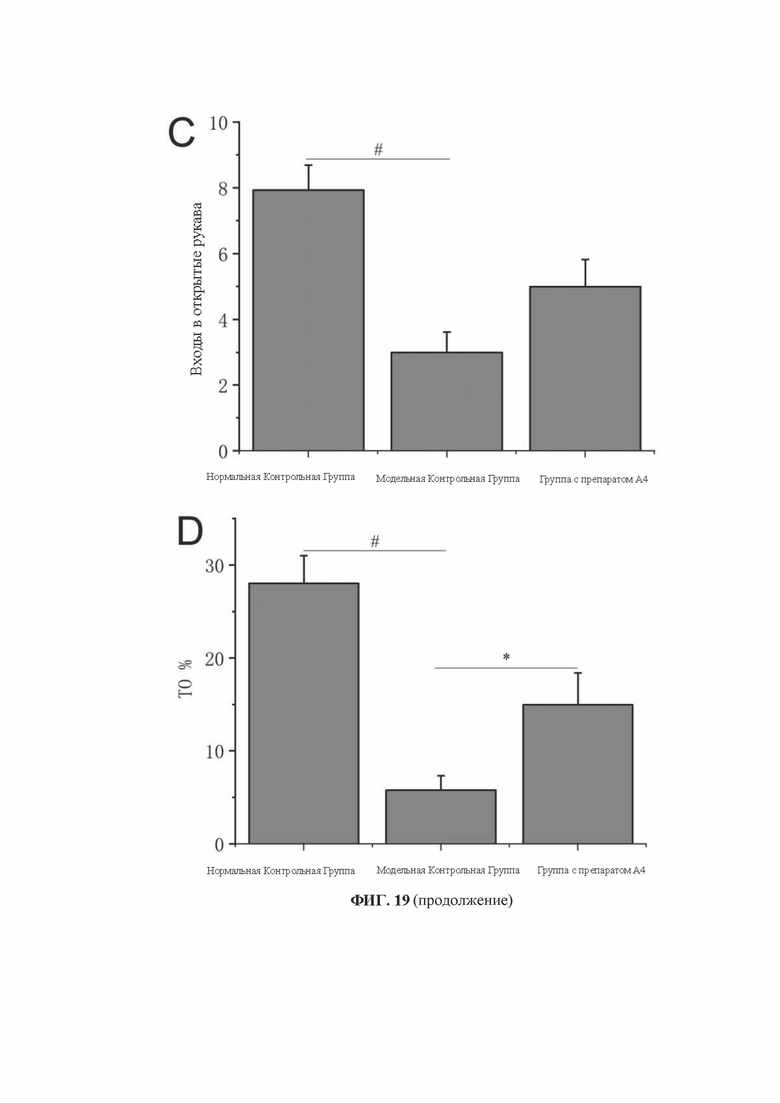
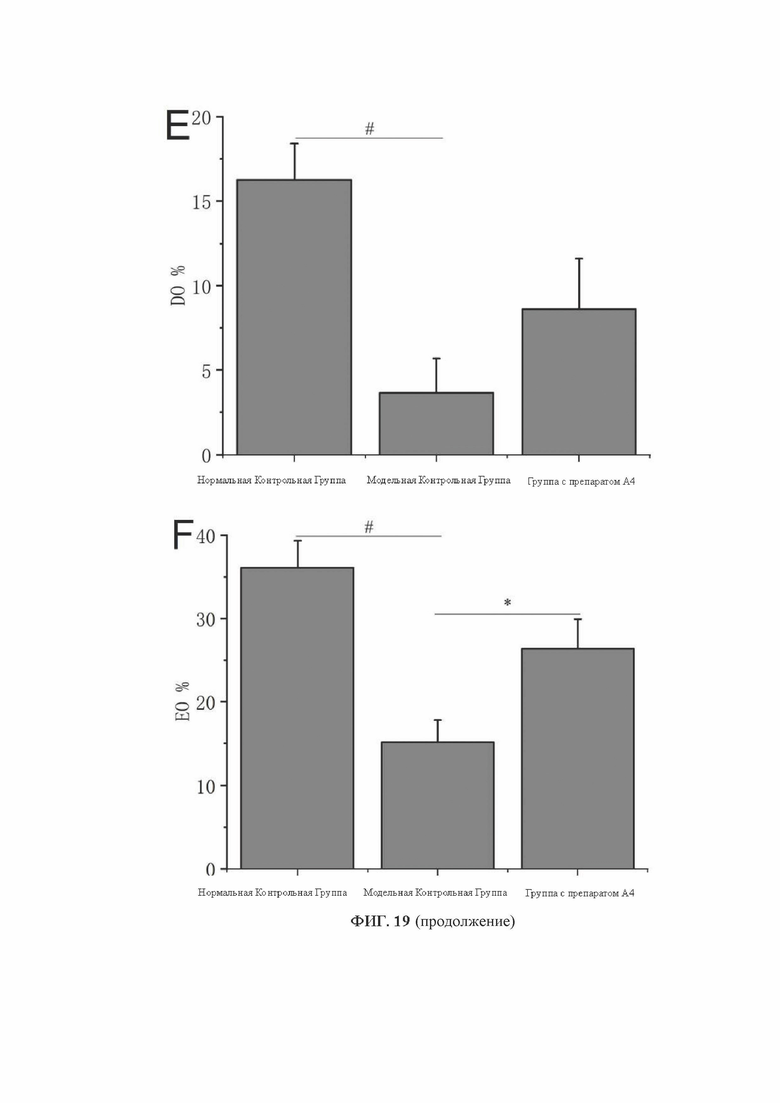
[0037] На фиг. 19 показаны результаты теста приподнятого крестообразного лабиринта на мышах в группе введения препарата А4: А - время перемещения мышей нормальной контрольной группы, модельной контрольной группы и группы введения препарата А4 в открытом рукаве; В - расстояние перемещения мышей нормальной контрольной группы, модельной контрольной группы и группы введения препарата А4 в открытом рукаве; С - время перемещения мышей нормальной контрольной группы, модельной контрольной группы и группы введения препарата А4 в открытом рукаве; D - процентное соотношение времени перемещения в открытом рукаве к времени перемещения в открытом рукаве + закрытом рукаве (ТО%) мышей нормальной контрольной группы, модельной контрольной группы и группы введения препарата А4; Е - процентное соотношение расстояния перемещения в открытом рукаве к общему расстоянию перемещения (DO%) для нормальной контрольной группы, модельной контрольной группы и мышей группы введения препарата А4; F - процентное соотношение времени перемещения в открытом рукаве и общего времени перемещения в закрытом рукаве (ЕО%) для нормальной контрольной группы, модельной контрольной группы и мышей группы введения препарата А4. Данные на рисунке представлены в виде Среднее ± Стд. откл., # Р<0,05 по сравнению с нормальной контрольной группой, * Р<0,05 по сравнению с модельной контрольной группой.
ПОДРОБНОЕ ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
[0038] Следующее подробное описание некоторых вариантов осуществления изобретения даст возможность лучше понять настоящее изобретение.
[0039] В настоящей заявке, где даны ссылки на различные публикации, описания этих публикаций включаются в настоящую заявку в полном объеме для более полного описания уровня техники, к которому относится настоящее изобретение.
[0040] В настоящем документе «введение» означает пероральное («ро») введение, введение в виде суппозитория, местное введение, внутривенное («iv»), внутрибрюшинное («ip»), внутримышечное («im»), интралезиональное, интрагиппокампальное, интрацеребровентрикулярное, интраназальное или подкожное («sc») введение, или имплантацию субъекту устройства замедленного высвобождения, например, мини-осмотического насоса или разъедаемого имплантата. Введение осуществляется любым способом, включая парентеральный и трансмукозальный (например, пероральный, назальный, вагинальный, ректальный или трансдермальный). Парентеральное введение включает, в частности, внутривенное, внутримышечное, внутриартериальное, внутрикожное, подкожное, внутрибрюшинное, внутрижелудочковое и внутричерепное. Другие способы введения включают, не ограничиваясь, использование липосомальных составов, внутривенную инфузию, трансдермальные пластыри и т.д.
[0041] Под «системным введением» и «систематическим введением» понимается способ введения соединения или композиции млекопитающему таким образом, что соединение или композиция доставляются к участкам тела, включая целевой участок фармацевтического воздействия, через систему кровообращения. Системное введение включает, не ограничиваясь, пероральное, интраназальное, ректальное и парентеральное (т.е. введение не через пищеварительный тракт, а внутримышечно, внутривенно, внутриартериально, трансдермально и подкожно) введение, с оговоркой, что в настоящем документе системное введение не включает прямое введение в участок мозга не через систему кровообращения, например, интратекальное введение и внутричерепное введение.
[0042] Под «лечением» и «терапией» в настоящем документе понимается замедление возникновения, приостановление или обращение вспять прогрессирования, облегчение или предотвращение заболевания или состояния, к которому применяется данный термин, или одного или нескольких симптомов такого заболевания или состояния.
[0043] Под «пациентом», «субъектом» или «индивидуумом» взаимозаменяемо понимается млекопитающее, например, человек или другое млекопитающее, включая приматов (например, макак, обыкновенных шимпанзе, понго), одомашненных млекопитающих (например, кошачьи, собачьи), сельскохозяйственное млекопитающее (например, бычьи, овиные, свиные, лошадиные) и лабораторных млекопитающих или грызунов (например, крысиные, мышиные, зайцеобразные, хомяковые, морские свинки).
[0044] Кластеры золота (AuCs) - это особая форма золота, существующая между атомами золота и наночастицами золота. AuCs имеют размер менее 3 нм и состоят всего из от нескольких до нескольких сотен атомов золота, что приводит к разрушению гранецентрированной кубической структуры наночастиц золота. В результате AuC проявляют молекулоподобные дискретные электронные свойства с четко выраженным промежутком HOMO-LUMO в отличие от непрерывных или квазинепрерывных энергетических уровней наночастиц золота. Это приводит к исчезновению эффекта поверхностного плазмонного резонанса и соответствующей полосы поглощения плазмонного резонанса (520 ± 20 нм) в UV-Vis спектре, которой обладают обычные наночастицы золота.
[0045] Настоящее изобретение относится к AuC, связанным с лигандами.
[0046] В определенных вариантах осуществления изобретения AuC, связанный с лигандами, включает лиганд и золотое ядро, где лиганд связан с золотым ядром. Связывание лигандов с золотым ядром означает, что лиганды образуют стабильные в растворе комплексные соединения с золотым ядром посредством ковалентной связи, водородной связи, электростатической силы, гидрофобной силы, силы Ван-дер-Ваальса и т.д. В определенных вариантах осуществления диаметр золотого ядра составляет от 0,5 до 3 нм. В определенных вариантах осуществления диаметр золотого ядра составляет 0,5-2,6 нм
[0047] В определенных вариантах осуществления изобретения AuC, связанный с лигандами, представляет собой тиолсодержащее соединение или олигопептид. В определенных вариантах осуществления лиганд связывается с золотым ядром с образованием AuC, связанного с лигандом, через связь Au-S.
[0048] В определенных вариантах осуществления изобретения лиганд представляет собой, не ограничиваясь, L-цистеин, D-цистеин или производное цистеина. В определенных вариантах осуществления производное цистеина представляет собой N-изобутирил-L-цистеин (L-NIBC), N-изобутирил-D-цистеин (D-NIBC), N-ацетил-L-цистеин (L-NAC) или N-ацетил-D-цистеин (D-NAC).
[0049] В определенных вариантах осуществления лиганд представляет собой, не ограничиваясь, цистеинсодержащий олигопептид и его производные. В определенных вариантах осуществления цистеинсодержащий олигопептид представляет собой цистеинсодержащий дипептид. В определенных вариантах осуществления изобретения цистеинсодержащий дипептид представляет собой L(D)-цистеин-L(D)-аргинин дипептид (CR), L(D)-аргинин-L(D)-цистеин дипептид (RC) или L(D)-цистеин-L-гистидин дипептид (СН). В определенных вариантах осуществления цистеинсодержащий олигопептид представляет собой цистеинсодержащий трипептид. В определенных вариантах осуществления изобретения цистеинсодержащий трипептид представляет собой глицин-L(D)-цистеин-L(D)-аргинин трипептид (GCR), L(D)-пролин-L(D)-цистеин-L(D)-аргинин трипептид (PCR) или L(D)-глутатион (GSH). В определенных вариантах осуществления цистеинсодержащий олигопептид представляет собой цистеинсодержащий тетрапептид. В определенных вариантах осуществления изобретения цистеинсодержащий тетрапептид представляет собой глицин-L(D)-серин-L(D)-цистеин-L(D)-аргинин тетрапептид (GSCR) или глицин-L(D)-цистеин-L(D)-серин-L(D)-аргинин тетрапептид (GCSR). В определенных вариантах осуществления цистеинсодержащий олигопептид представляет собой цистеинсодержащий пентапептид. В определенных вариантах осуществления изобретения цистеинсодержащий пентапептид представляет собой цистеинил-аспарагинил-глутаминил-валинил-аспарагин (CDEVD) или аспарагинил-глутаминил-валинил-аспарагинил-цистеин (DEVDC).
[0050] В определенных вариантах осуществления изобретения лиганд представляет собой тиолсодержащее соединение. В определенных вариантах осуществления тиолсодержащее соединение представляет собой 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L(D)-пролин, тиогликолевую кислоту, меркаптоэтанол, тиофенол, D-3-троловол, додецилмеркаптан, 2-аминоэтанэтиол (CSH), 3-меркаптопропионовую кислоту (MPA) или 4-меркаптобеновую кислоту (р-МВА).
[0051] Настоящее изобретение относится к фармацевтической композиции для лечения депрессии. В определенных вариантах осуществления субъектом является человек. В определенных вариантах осуществления субъектом является домашнее животное, например, собака.
[0052] В определенных вариантах осуществления фармацевтическая композиция включает AuC, связанный с лигандами, как описано выше, и фармацевтически приемлемый эксципиент. В определенных вариантах осуществления эксципиент представляет собой фосфатно-буферный раствор или физиологический солевой раствор.
[0053] Настоящее изобретение раскрывает применение вышеописанных AuCs, связанных с лигандами, для получения лекарственного средства для лечения депрессии.
[0054] Настоящее изобретение раскрывает применение описанных выше AuCs, связанных с лигандами, для лечения субъекта с депрессией или способ лечения субъекта с депрессией с использованием описанных выше AuCs, связанных с лигандами. В определенных вариантах осуществления способ лечения включает введение субъекту фармацевтически эффективного количества AuCs, связанных с лигандами. Фармацевтически эффективное количество может быть определено с помощью обычных исследований in vivo. В определенных вариантах осуществления изобретения фармацевтически эффективное количество AuCs, связанных с лигандами, составляет по меньшей мере 0,001 мг/кг/день, 0,005 мг/кг/день, 0,01 мг/кг/день, 0,05 мг/кг/день, 0,1 мг/кг/день, 0,5 мг/кг/день, 1 мг/кг/день, 2 мг/кг/день, 3 мг/кг/день, 4 мг/кг/день, 5 мг/кг/день, 6 мг/кг/день, 7 мг/кг/день, 8 мг/кг/день, 9 мг/кг/день, 10 мг/кг/день, 15 мг/кг/день, 20 мг/кг/день, 30 мг/кг/день, 40 мг/кг/день, 50 мг/кг/день, 60 мг/кг/день, 70 мг/кг/день, 80 мг/кг/день, 100 мг/кг/день, 200 мг/кг/день, 300 мг/кг/день, 400 мг/кг/день, 500 мг/кг/день, 600 мг/кг/день, 700 мг/кг/день, 800 мг/кг/день, 900 мг/кг/день или 1000 мг/кг/день. [0055] Следующие примеры приведены исключительно с целью демонстрации основных положений настоящего изобретения; они ни в коем случае не предназначены для ограничения объема настоящего изобретения.
[0056] Варианты осуществления
[0057] Вариант осуществления 1. Получение AuCs, связанных с лигандами
[0058] 1.1 Растворяют HAuCl4 в метаноле, воде, этаноле, н-пропаноле или этилацетате для получения раствора А, в котором концентрация HAuCl4 составляет 0,01~0,03М;
[0059] 1.2 Растворяют лиганд в растворителе, чтобы получить раствор В, в котором концентрация лиганда составляет 0,01~0,18 М; лиганд включает, не ограничиваясь, L-цистеин, D-цистеин и другие производные цистеина, такие как N-изобутирил-L-цистеин (L-NIBC), N-изобутирил-D-цистеин (D-NIBC), N-ацетил-L-цистеин (L-NAC) и N-ацетил-D-цистеин (D-NAC), цистеинсодержащие олигопептиды и их производные, включая, не ограничиваясь, дипептиды, трипептид, тетрапептид, пентапептид и другие пептиды, содержащие цистеин, такие как L(D)-цистеин-L(D)-аргинин дипептид (CR), L(D)-аргинин-L(D)-цистеин дипептид (RC), L(D)-цистеин-L(D)-гистидин (СН), глицин-L(D)-цистеин-L(D)-аргинин трипептид (GCR), L(D)-пролин-L(D)-цистеин-L(D)-аргинин трипептид (PCR), L(D)-глутатион (GSH), глицин-L(D)-серин-L(D)-цистеин-L(D)-аргинин тетрапептид (GSCR), глицин-L(D)-цистеин-L(D)-серин-L(D)-аргинин тетрапептид (GCSR), цистеин-аспарагинил-глутаминил-валинил-аспарагин (CDEVD) и аспарагинил-глутаминил-валинин-аспарагинил-цистеин (DEVDC), и другие тиолсодержащие соединения, такие как одно или более из 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L(D)-пролина, тиогликолевой кислоты, меркаптоэтанола, тиофенола, D-3-троловола, додецилмеркаптана, 2-аминоэтанэтиола (CSH), 3-меркаптопропионовой кислоты (MPA) и 4-меркаптобеновой кислоты (р-МВА); растворитель представляет собой один или более из метанола, этилацетата, воды, этанола, н-пропанола, пентана, муравьиной кислоты, уксусной кислоты, диэтилового эфира, ацетона, анизола, 1-пропанола, 2-пропанола, 1-бутанола, 2-бутанола, пентанола, бутилацетата, трибутилметилового эфира, изопропилацетата, диметилсульфоксида, этилформиата, изобутилацетата, метилацетата, 2-метил-1-пропанола и пропилацетата;
[0060] 1.3 Смешивают раствор А и раствор В так, чтобы мольное соотношение между HAuCl4 и лигандом составляло 1:(0,01~100), перемешивают в ледяной бане в течение 0,1~48 ч, добавляют 0,025~0,8 М раствора NaBH4 в воде, этаноле или метаноле, продолжают перемешивание в ледяной водяной бане и проводят реакцию в течение 0,1~12 ч. Мольное соотношение между NaBH4 и лигандом составляет 1:(0,01~100);
[0061] 1.4 Используя ультрафильтрационные трубки MWCO 3K~30K, центрифугируют реакционный раствор при 8000~17500 об/мин по градиенту в течение 10~100 мин после окончания реакции для получения осадка AuCs, связанных с лигандами, с различным средним размером частиц. Апертура фильтрационных мембран для ультрафильтрационных трубок с различными MWCO непосредственно определяет размер AuCs, связанных с лигандами, которые могут пройти через мембраны. По желанию этот этап может быть пропущен;
[0062] 1.5 Растворяют осадок AuCs, связанных с лигандами, в различных средних размерах частиц, полученных на этапе (1.4), в воде, помещают его в диализный мешок и диализируют в воде при комнатной температуре в течение 1~7 дней;
[0063] 1.6 Проводят сублимационную сушку AuCs, связанных с лигандами, в течение 12~24 ч после диализа для получения порошкообразного или флокулирующего вещества, т.е. AuCs, связанных с лигандами.
[0064] Авторами было неожиданно обнаружено, что размер частиц порошкообразного или флокулянтного вещества, полученного вышеописанным способом, составляет менее 3 нм (в целом распределяется в пределах 0,5-2,6 нм). Очевидный пик поглощения при 520 нм отсутствует. Было установлено, что полученный порошок или флок является AuCs, связанными с лигандами.
[0065] Вариант осуществления 2. Получение и характеристики AuCs, связанных с различными лигандами
[0066] 2.1 Получение AuCs, связанных с L-NIBC, т.е. L-NIBC-AuCs
[0067] На примере лиганда L-NIBC подробно описано получение и характеристики AuCs, связанных с лигандом L-NIBC.
[0068] 2.1.1 Взвешивают 1,00 г HAuCl4 и растворяют в 100 мл метанола для получения 0,03 М раствора А;
[0069] 2.1.2 Взвешивают 0,57 г L-NIBC и растворяют его в 100 мл ледяной уксусной кислоты (уксусной кислоты) для получения 0,03 М раствора В;
[0070] 2.1.3 Отмеряют 1 мл раствора А, смешивают его с 0,5 мл, 1 мл, 2 мл, 3 мл, 4 мл или 5 мл раствора В соответственно (т.е. мольное соотношение между HAuCl4 и L-NIBC составляет 1:0,5, 1:1, 1:2, 1:3, 1:4, 1:5 соответственно), проводят реакцию в ледяной бане при перемешивании в течение 2 ч, когда раствор из ярко-желтого становится бесцветным, быстро добавляют 1 мл свежеприготовленного 0,03 М (приготовленного путем взвешивания 11,3 мг NaBH4 и растворения его в 10 мл этанола) этанольного раствора NaBH4, продолжают реакцию в течение 30 мин после того, как раствор станет темно-коричневым, и добавляют 10 мл ацетона для завершения реакции.
[0071] 2.1.4 После проведения реакции реакционный раствор подвергают градиентному центрифугированию для получения порошка L-NIBC-AuCs с различными размерами частиц. Специфический способ: после завершения реакции реакционный раствор переносят в ультрафильтрационную пробирку с MWCO 30K и объемом 50 мл, центрифугируют при 10000 об/мин в течение 20 мин, а ретентат во внутренней пробирке растворяют в сверхчистой воде для получения порошка с размером частиц около 2,6 нм. Затем смешанный раствор во внешней пробирке переносят в ультрафильтрационную пробирку объемом 50 мл с MWCO 10K и центрифугируют при 13000 об/мин в течение 30 мин. Ретентат во внутренней пробирке растворяют в сверхчистой воде для получения порошка с размером частиц около 1,8 нм. Затем смешанный раствор во внешней пробирке переносят в ультрафильтрационную пробирку объемом 50 мл с MWCO 3K и центрифугируют при 17 500 об/мин в течение 40 мин. Ретентат во внутренней пробирке растворяют в сверхчистой воде для получения порошка с размером частиц около 1,1 нм.
[0072] 2.1.5 Осаждают порошок трех различных размеров частиц, полученных градиентным центрифугированием, удаляют растворитель, высушивают сырой продукт N2, растворяют его в 5 мл сверхчистой воды, помещают в диализный мешок (MWCO составляет 3KDa), помещают диализный мешок в 2 л сверхчистой воды, воду меняют каждые два дня, проводят диализ в течение 7 дней, подвергают сублимационной сушке и сохраняют для дальнейшего использования.
[0073] 2.2 Характеристика L-NIBC-AuCs
[0074] Эксперимент по определению характеристик был проведен для полученного выше порошка (L-NIBC-AuCs). Между тем наночастицы золота, модифицированные лигандом L-NIBC (L-NIBC-AuNPs), используются как контроль. Способ получения наночастиц золота с лигандом L-NIBC приведен в источнике (W. Yan, L. Xu, С.Xu, W. Ma, H. Kuang, L. Wang and N. A. Kotov, Journal of the American Chemical Society 2012, 134, 15114; X. Yuan, B. Zhang, Z. Luo, Q. Yao, D. T. Leong, N. Yan and J. Xie, Angewandte Chemie International Edition 2014, 53, 4623).
[0075] 2.2.1 Исследование морфологии с помощью просвечивающего электронного микроскопа (ПЭМ)
[0076] Тестовые порошки (образец L-NIBC-AuCs и образец L-NIBC-AuNPs) были растворены в сверхчистой воде до 2 мг/л в качестве образцов, а затем тестовые образцы были подготовлены методом висячей капли. Более конкретно, 5 мкл образцов капали на ультратонкую углеродную пленку, испаряли естественным образом до исчезновения капли воды, а затем наблюдали морфологию образцов с помощью полевой эмиссионной ПЭМ высокого разрешения JEM-2100F STEM/EDS.
[0077] Четыре ПЭМ-изображения L-NIBC-AuNPs показаны на панелях В, Е, Н и K фиг. 1; три ПЭМ-изображения L-NIBC-AuCs показаны на панелях В, Е и Н фиг. 2.
[0078] Изображения на фиг. 2 показывают, что каждый из образцов L-NIBC-AuCs имеет однородный размер частиц и хорошую дисперсность, а средний диаметр L-NIBC-AuCs (относится к диаметру золотого ядра) составляет 1,1 нм, 1,8 нм и 2,6 нм соответственно, что соответствует результатам на панелях С, F и I фиг. 2. Для сравнения образцы L-NIBC-AuNPs имеют больший размер частиц. Их средний диаметр (относится к диаметру золотого ядра) составляет 3,6 нм, 6,0 нм, 10,1 нм и 18,2 нм, соответственно, что полностью соответствует результатам на панелях С, F, I и L фиг. 1.
[0079] 2.2.2 Ультрафиолетовые (УФ) - видимые (vis) спектры поглощения
[0080] Тестовые порошки (образец L-NIBC-AuCs и образец L-NIBC-AuNPs) были растворены в сверхчистой воде до концентрации 10 мг⋅л-1, после чего при комнатной температуре были измерены спектры поглощения УФ-vis. Диапазон измерения составлял 190-1100 нм, кювета для образца представляла собой стандартную кварцевую ячейку с оптическим путем 1 см, а контрольная кювета была заполнена сверхчистой водой.
[0081] УФ-vis спектры поглощения четырех образцов L-NIBC-AuNPs различных размеров показаны на панелях A, D, G и J на фиг. 1, а статистическое распределение размеров частиц показано на панелях С, F, I и L на фиг. 1; УФ-vis спектры поглощения трех образцов L-NIBC-AuCs различных размеров показаны на панелях A, D и G на фиг. 2, а статистическое распределение размеров частиц показано на панелях С, F и I на фиг. 2.
[0082] На фиг. 1 показано, что благодаря эффекту поверхностного плазмона пик поглощения L-NIBC-AuNPs наблюдался при длине волны около 520 нм. Положение пика поглощения зависит от размера частиц. При размере частиц 3,6 нм УФ пик поглощения появляется при 516 нм; когда размер частиц составляет 6,0 нм, УФ пик поглощения появляется при 517 нм; когда размер частиц составляет 10,1 нм, УФ пик поглощения появляется при 520 нм, а когда размер частиц составляет 18,2 нм, пик поглощения появляется при 523 нм. Ни один из четырех образцов не имеет пика поглощения выше 560 нм.
[0083] На фиг. 2 показано, что в УФ-спектрах поглощения трех образцов L-NIBC-AuCs с различными размерами частиц пик поглощения поверхностного плазмонного эффекта при 520 нм исчез, а два очевидных пика поглощения появились выше 560 нм, и положения пиков поглощения немного изменялись в зависимости от размеров частиц AuCs. Это объясняется тем, что AuCs проявляют молекулоподобные свойства из-за распада гранецентрированной кубической структуры, что приводит к разрыву в плотности соединений AuCs, расщеплению энергетического уровня, исчезновению эффекта плазмонного резонанса и появлению нового пика поглощения в длинноволновом направлении. Можно сделать вывод, что все три образца порошка с разным размером частиц, полученные выше, представляют собой AuCs, связанные с лигандами.
[0084] 2.2.3 Инфракрасная спектроскопия с преобразованием Фурье
[0085] Инфракрасные спектры измерялись на инфракрасном спектрометре с преобразованием Фурье VERTEX80V фирмы Bruker в режиме полного отражения в твердом порошке в высоком вакууме. Диапазон сканирования составляет 4000-400 см-1, число сканирований - 64. Для примера взяты образцы L-NIBC-AuCs, тестовые образцы представляли собой сухой порошок L-NIBC-AuCs с тремя различными размерами частиц, а контрольный образец представлял собой чистый порошок L-NIBC. Результаты показаны на фиг. 3.
[0086] На фиг. 3 показан инфракрасный спектр L-NIBC-AuCs с различными размерами частиц. По сравнению с чистым L-NIBC (кривая внизу), S-H валентные колебания L-NIBC-AuCs с различными размерами частиц полностью исчезли при 2500-2600 см-1, в то время как другие характерные пики L-NIBC по-прежнему наблюдались, что подтверждает, что молекулы L-NIBC были успешно связаны с поверхностью AuCs через связь Au-S. На фигуре также видно, что инфракрасный спектр AuCs, связанных с лигандами, не зависит от их размера.
[0087] AuCs, связанные с другими лигандами, были получены способом, аналогичным описанному выше, за исключением того, что растворитель для раствора В, соотношение между HAuCl4 и лигандом, время проведения реакции и количество добавленного NaBH4 были слегка скорректированы. Например, когда в качестве лиганда используют L-цистеин, D-цистеин, N-изобутирил-L-цистеин (L-NIBC) или N-изобутирил-D-цистеин (D-NIBC), в качестве растворителя выбирают уксусную кислоту; когда в качестве лиганда используют дипептид CR, дипептид RC или 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L-пролин, в качестве растворителя выбирают воду, и проч.; другие стадии аналогичны, поэтому дальнейшие сведения здесь не приводятся.
[0088] В рамках настоящего изобретения вышеописанным способом была получена серия AuCs, связанных с лигандами. Лиганды и характеристики способа получения приведены в таблице 1.

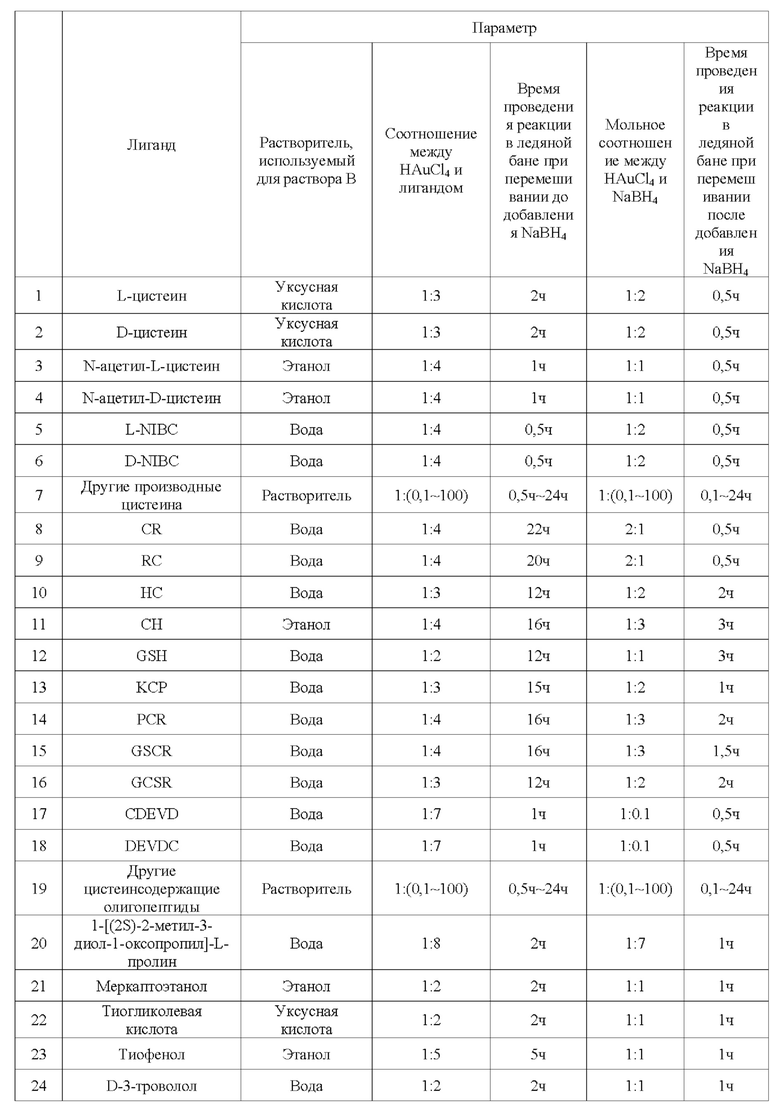
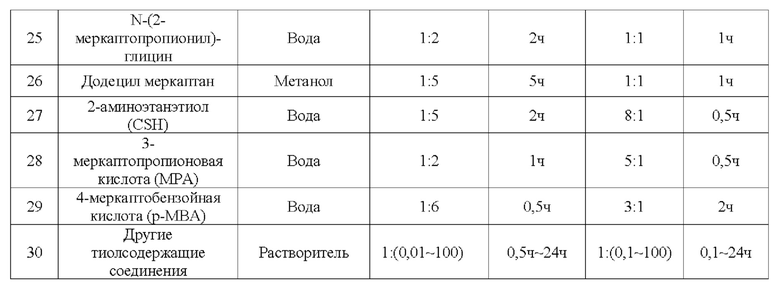
[0090] Образцы, перечисленные в Таблице 1, были получены вышеуказанными способами. Характеристики одиннадцати (11) различных AuCs, связанных с лигандами, показаны на фиг. 4 (CR-AuCs), на фиг. 5 (RC-AuCs), на фиг. 6 (Cap-AuCs) (Сар обозначает 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L-пролин), на фиг. 7 (GSH-AuCs), на фиг. 8 (D-NIBC-AuCs), на фиг. 9 (L-Cys-AuCs), на фиг. 10 (CSH-AuCs), на фиг. 11 (MPA-AuCs), на фиг. 12 (p-MBA-AuCs), на фиг. 13 (CDEVD-AuCs) и на фиг. 14 (DEVDC-AuCs). На фиг. 4-12 показаны УФ-спектры (панель А), инфракрасные спектры (панель В), ПЭМ-изображения (панель С) и распределение частиц по размерам (панель D). На фиг. 13 и 14 показаны УФ-спектры (панель А), ПЭМ-изображения (панель В) и распределение частиц по размерам (панель С).
[0091] Результаты показывают, что диаметры AuCs, связанных с различными лигандами, полученными в Таблице 1, составляют менее 3 нм. Ультрафиолетовые спектры также показывают исчезновение пика при 520±20 нм и появление пика поглощения в других положениях. Положение пика поглощения может меняться в зависимости от лигандов и размеров частиц, равно как и от структуры. В определенных случаях пик поглощения отсутствует, в основном из-за образования смесей AuCs с различными размерами и структурами частиц или некоторых специальных AuCs, которые перемещают положение пика поглощения за пределы УФ-vis спектра. Между тем инфракрасные спектры с преобразованием Фурье также показывают исчезновение инфракрасного пика поглощения тиола лиганда (между пунктирными линиями на панели В на фиг. 4-8), в то время как другие инфракрасные характеристические пики сохраняются, предположительно потому, что все молекулы лиганда были успешно связаны с атомами золота для образования AuCs, связанных с лигандами, и в настоящем изобретении успешно были получены AuCs, связанные с лигандами, перечисленными в таблице 1.
[0092] Вариант осуществления 3. Тестовые образцы для исследований на животных
[0093] А1: кластеры золота, связанные с лигандом L-NIBC (L-NIBC-AuCs), диаметр золотого ядра в интервале 0,5-3,0 нм.
[0094] А2: кластеры золота, связанные с лигандом N-ацетил-Е-цистеином (L-NAC-AuCs), диаметр золотого ядра в интервале 0,5-3,0 нм.
[0095] A3: кластеры золота, связанные с лигандом CR (CR-AuCs), диаметр золотого ядра в интервале 0,5-3,0 нм.
[0096] А4: кластеры золота, связанные с лигандом L-цистеином (L-C-AuCs), диаметр золотого ядра в интервале 0,5-3,0 нм.
[0097] А5: кластеры золота, связанные с лигандом DEVDC (DEVDC-AuCs), диаметр золотого ядра в интервале 0,5-3,0 нм.
[0098] В1: наночастицы золота, связанные с L-NIBC (L-NIBC-AuNPs), распределение по размерам в диапазоне 6,2±1,2 нм.
[0099] Все тестовые образцы были получены в соответствии с описанным выше способом с небольшими изменениями, и их качество было оценено с помощью описанных выше способов.
[0100] Вариант осуществления 4. Тест принудительного плавания (FST)
[0101] В тесте FST мышей помещали в цилиндрическую бочку с глубиной воды 18 см и температурой воды 26°С. Мыши плавали в бочке в течение 6 минут. В течение этого времени прибор регистрирует время плавания мышей, а для анализа данных используется время плавания за последние 4 минуты. Коэффициент неподвижности (т.е. время плавания) (%) рассчитывается как 100 х время неподвижности/время тестирования. Чем выше коэффициент неподвижности, тем выше степень депрессии у мышей.
[0102] Все данные были проанализированы с помощью программы prism 6.01 (односторонний ANOVA плюс тест множественного сравнения Даннетта).
[0103] 84 мыши ICR были случайным образом разделены на следующие 7 групп (n-12): С - контрольная группа, которой вводили обычный физиологический раствор; А1 - группа введения препарата (L-NIBC-AuCs); А2 - группа введения препарата (L-NAC-AuCs); A3 - группа введения препарата (CR-AuCs); А4 - группа введения препарата (L-C-AuCs); А5 - группа введения препарата (DEVDC-AuCs); В1 - группа введения препарата (L-NIBC-AuNPs). Все препараты растворяли в обычном физиологическом растворе. Мышам групп A1, А2, A3, А4, А5 и В1 препарат вводили внутрибрюшинно один раз в сутки в дозе 20 мг/кг массы тела, объем инъекции составлял 50 мкл, а мышам контрольной группы внутрибрюшинно вводили такой же объем обычного физиологического раствора. На 7-й день (день 7) препарат вводили после адаптации мышей к лабораторным условиям в течение 60 минут, а через 30 минут после введения проводили тест принудительного плавания (FST).
[0104] На фиг. 15 показаны результаты теста принудительного плавания у мышей в контрольной группе и каждой из групп введения препарата. В контрольной группе мышей коэффициент неподвижности составил 67,8%±3,9%; в группах введения кластеров золота A1, А2, A3, А4 и А5 коэффициент неподвижности составил 52,0%±5. 7%, 48,7%±4,0%, 43,9%±4,9%, 47,9%±5,2% или 50,2%±5,0% соответственно, что значительно ниже, чем в контрольной группе (*: Р<0,05; **: Р<0,01; ***: Р<0,001). В отличие от этого в группе мышей, которым вводили наночастицы золота В1, значительных изменений по сравнению с контрольной группой не наблюдалось.
[0105] Вариант осуществления 5. Тест подвешивания за хвост
[0106] В тесте подвешивания за хвост (TST) у мышей кончик хвоста длиной 2 см наклеивают на горизонтальную деревянную палочку, чтобы животные висели. Расстояние между мышами и окружающей обстановкой составляет 5 см. Наблюдают и регистрируют время неподвижности мышей (в секундах) в течение 6 минут. Чем больше время неподвижности, тем выше степень депрессии у мышей. Все данные анализируются, как описано выше.
[0107] 84 мыши ICR участвовали в тесте подвешивания за хвост. Схема введения препаратов по группам соответствовала тесту принудительного плавания, описанному выше.
[0108] На фиг. 16 показаны результаты теста подвешивания за хвост у мышей в контрольной группе и в каждой из групп введения препарата. В контрольной группе время неподвижности мышей составило 140,3±12,4 секунды, в то время как в группах введения кластеров золота A1, А2, A3, А4 и А5 время неподвижности мышей составило 90,2±11,1 секунды, 70?4±11,4 секунды, 88,0±10,6 секунды, 68,8±12,2 секунды и 75,5±9,7 секунды, соответственно, значительно уменьшилось по сравнению с контрольной группой (*: Р<0,05; **: Р<0,01; ***: Р<0,001). В отличие от этого в группе введения наночастиц золота В1 существенных различий по сравнению с контрольной группой не наблюдалось.
[0109] Полученные результаты показывают, что пять препаратов кластера золота оказывают значительное терапевтическое действие на депрессию, но наночастицы золота оказываются неэффективными.
[0110] Вариант осуществления 6. Социальный стресс-тест на животной модели
[0111] 6.1. Моделирование и введение препаратов
[0112] Животная модель социального стресса моделирует ситуацию, когда человек сталкивается с фрустрацией от изоляции и беспомощности в повседневном общении, позволяя агрессивным мышам CD-1 нападать на мышей C57BL/6J (сокращенно С57) в течение короткого периода времени, и позволяя мышам С57 находиться в угрозе и страхе перед агрессивными мышами CD-1 в течение длительного времени. При многократном воздействии на мышей давлением социальной неудачи это вызывает явные депрессивноподобные проявления, характеризующиеся отсутствием интереса, тревожностью и социально-избегающим поведением. Эта модель является животной моделью, которая ближе к этиологии человеческой депрессии.
[0113] Сначала обычные мыши С57 были подвергнуты испытанию агрессивными мышами CD-1.
[0114] (1) агрессивных мышей CD-1 помещали с одной стороны клетки для мышей, разделенной перфорированной прозрачной перегородкой, и держали в течение 24 часов;
[0115] (2) обычных мышей С57 в соответствии с их нумерацией помещали в одну сторону клетки с агрессивными мышами CD-1 и стимулировали в течение 5 минут (избегая травм); затем мышей С57 вынимали и помещали в другую сторону той же клетки, разделенную перфорированной прозрачной перегородкой (две стороны были разделены прозрачной перегородкой), так что мыши С57 могли видеть агрессивных мышей CD-1 и чувствовать запах мышей CD-1; мыши С57 и мыши CD-1 оставались вместе на ночь в течение 24 часов;
[0116] (3) в ходе эксперимента каждая мышь С57 постоянно подвергалась стрессу в течение 20 дней. В течение 20 дней мышей С57 разных модельных групп в соответствии с их нумерацией помещали в клетки с агрессивными мышами CD-1 для ежедневной стимуляции. В течение 20 дней между любыми двумя мышами осуществлялось не более одного контакта (т.е. не было повторных контактов, чтобы избежать привыкания);
[0117] (4) в группе нормального контроля вместо агрессивных мышей CD-1 использовали мышей С57, разделенных прозрачными перегородками, и мышей С57 в группе нормального контроля меняли ежедневно в соответствии с нумерацией;
[0118] (5) в конце последнего дня моделирования модельных мышей С57 и обычных мышей контрольной группы С57 держали в одиночных клетках отдельно в течение 24 часов, а затем проводили поведенческие тесты.
[0119] На 15-й день пребывания в состоянии социального стресса модельным мышам С57 в течение 9 дней подряд вводили препараты A1, А2, A3, А4, А5 и В1 один раз в день путем внутрибрюшинной инъекции в дозе 20 мг/кг, в результате чего были выделены группа введения А1, группа введения А2, группа введения A3, группа введения А4, группа введения А5 и группа введения В1. Начиная с 7-го дня введения препарата (21-й день от начала моделирования), поведенческие тесты проводились через час после введения препарата. Группа нормального контроля и группа модельного контроля получали одинаковый объем физиологического раствора, и поведенческие тесты проводились в соответствующие дни. В каждой группе было по 15 мышей.
[0120] 6.2. Поведенческие тесты
[0121] Первым поведенческим тестом был тест социального поведения, который использовался для выявления у мышей поведения социального избегания (типичного признака депрессии). Этот тест проводился соответственно на 14-е и 21-е сутки от начала моделирования. Первый тест на 14-е сутки проводился для оценки успешности моделирования, а второй - на 21-е сутки для оценки влияния препаратов на социальное поведение мышей.
[0122] Тест социального поведения состоял из двух этапов, каждый из которых длился 2,5 мин с интервалом 30 с. На первом этапе (этап без цели) газопроницаемый цилиндр радиусом 4 см помещается на боковой стороне открытого участка, а область в пределах 8 см от центра цилиндра определяется как зона взаимодействия (ЗВ). Время нахождения в зоне взаимодействия успешно смоделированных мышей С57 фиксировалось и обозначалось как Т1. На втором этапе (целевом) мышь CD-1, не контактировавшую с мышью на этапе моделирования, помещают в цилиндр, обеспечивая визуальное и обонятельное взаимодействие между ними (но не допуская физического контакта), фиксируют время визуального и обонятельного взаимодействия между ними на этом этапе в зоне взаимодействия и обозначают его как Т2. Отношение Т2 к T1 (Т2/Т1) называется коэффициентом социального взаимодействия (КСВ). Чем меньше это значение, тем очевиднее поведение социального избегания. И наоборот, тем лучше антидепрессивная способность препарата.
[0123] Вторым поведенческим тестом был тест приподнятого крестообразного лабиринта, который использовался для выявления тревожного (еще один характерный признак депрессии) поведения у мышей. Тест приподнятого крестообразного лабиринта начинался на 23-й день моделирования. Модельные мыши С57 помещались на платформу приподнятого крестообразного лабиринта, затем наблюдалось и регистрировалось время перемещения, расстояние перемещения и время перемещения мышей в каждом рукаве в течение 5 минут. Рассчитывались следующие данные: (1) процентное соотношение времени, проведенного мышами в открытом рукаве, к времени, проведенному мышами как в открытом, так и в закрытом рукаве: ТО%=100%*время нахождения в открытом рукаве/(время нахождения в открытом рукаве + время нахождения в закрытом рукаве); (2) процентное соотношение расстояния перемещения в открытом рукаве к общему расстоянию перемещения: DO%=100%*расстояние перемещения в открытом рукаве/(расстояние перемещения в открытом рукаве + расстояние перемещения в закрытом рукаве); (3) процентное соотношение количества челночных перемещений в открытом рукаве к общему количеству челночных перемещений: ЕО%=100%*количество челночных перемещений в открытом рукаве/(количество челночных перемещений в открытом рукаве + количество челночных перемещений в закрытом рукаве). Чем больше указанные значения, тем выше противотревожное действие препарата.
[0124] Все данные были проанализированы с помощью программы prism 6.01 (односторонний ANOVA плюс тест множественного сравнения Даннетта).
[0125] 6.3. Результаты исследований
[0126] 6.3.1. Успешное создание модели
[0127] Способность мышей к социальному поведению проверяли на 14-й день (за 1 день до введения препарата). Результаты показаны на фиг. 17. На фиг. 17А - 17С представлены результаты T1, Т2 и Т2 / Т1 мышей в тесте социального поведения. Результаты показали, что значение Т2/Т1 у модельных мышей было значительно ниже, чем у обычных мышей, причем разница была весьма значительной (Р<0,001, ***), что свидетельствует о том, что социальные способности модельных мышей были значительно ниже, чем у обычных мышей, и модель была успешно создана.
[0128] 6.3.2. Влияние препаратов на социальное поведение модельных мышей
[0129] На фиг. 18 показано влияние препаратов кластера золота на тест социального поведения мышей с хроническим социальным стрессом, в качестве примера использован препарат А1. Результаты показали, что пять препаратов кластера золота А1-А5 могут значительно улучшить соотношение Т2/Т1 у модельных мышей, причем разница была значительной по сравнению с контрольной группой (Р<0,05, *), что указывает на то, что пять препаратов кластера золота могут эффективно улучшать социальные поведенческие способности и обладают значительным антидепрессивным действием. Однако по сравнению с контрольной группой значение Т2/Т1 в группе В1 не улучшилось, что свидетельствует об отсутствии антидепрессивного эффекта.
[0130] На фиг. 19 показаны результаты воздействия препаратов кластеров золота на мышей с хроническим социальным стрессом в тесте приподнятого крестообразного лабиринта на примере препарата А4. Результаты показали, что на 23-й день моделирования пять препаратов кластеров золота А1-А5 могут значительно увеличить время перемещения в открытом рукаве (ФИГ. 19А), расстояние перемещения в открытом рукаве (ФИГ. 19В), время перемещения в открытом рукаве (ФИГ. 19С), процентное соотношение (ТО%) времени в открытом рукаве к времени в открытом рукаве+закрытом рукаве (FIG. 19D), процентное соотношение (DO%) расстояния перемещения в открытом рукаве к общему расстоянию перемещения (FIG. 19Е) и процентное соотношение (ЕО%) времени перемещения в открытом рукаве к общему времени перемещения (FIG. 19F). На примере препарата А4 можно отметить, что значения ТО% и ЕО% в группе введения препарата имели значительные отличия по сравнению с группой модельного контроля (Р<0,05, *). Эти результаты свидетельствуют о том, что препараты кластера золота обладают выраженным противотревожным действием. Однако препарат В1 не привел к улучшению показателей теста, что свидетельствует о том, что наночастицы золота размером более 3,0 нм не оказывают влияния на тревожно-подобное поведение модельных мышей.
[0131] Полученные результаты свидетельствуют о том, что препараты на основе кластеров золота способны значительно улучшать социальное поведение и тревожно-подобное поведение модельных мышей и могут быть использованы в качестве антидепрессантов. Однако наночастицы золота размером более 3,0 нм не обладают подобным эффектом и не могут быть использованы для разработки антидепрессивных препаратов.
[0132] Подобными эффектами обладают и другие AuC, связанные с лигандами, имеющие различные размеры, хотя их эффекты в определенной степени варьируются. Их подробное описание здесь не приводится.
[0133] Несмотря на то, что настоящее изобретение было раскрыто с указанием конкретных вариантов осуществления, предполагается, что варианты осуществления являются иллюстративными и объем изобретения не ограничивают. Альтернативные варианты осуществления настоящего изобретения будут очевидны тем, кто обладает обычными навыками в области, к которой относится настоящее изобретение. Такие альтернативные варианты осуществления считаются включенными в объем настоящего изобретения. Соответственно, объем настоящего изобретения определяется прилагаемой формулой изобретения и подтверждается приведенным выше описанием.
Ссылки
 Skalska J, Sulkowski G, Frontczak-Baniewicz M, Talarek S, Listos J,
Skalska J, Sulkowski G, Frontczak-Baniewicz M, Talarek S, Listos J,  Influence of a Low Dose of Silver Nanoparticles on Cerebral Myelin and Behavior of Adult Rats. Toxicology. 2016 Jul l;363-364:29-36.
Influence of a Low Dose of Silver Nanoparticles on Cerebral Myelin and Behavior of Adult Rats. Toxicology. 2016 Jul l;363-364:29-36.
Saeidienik F, Shahraki MR, Fanaei H, Badini F. The Effects of Iron Oxide Nanoparticles Administration on Depression Symptoms Induced by LPS in Male Wistar Rats. Basic Clin Neurosci. 2018;9(3):209-216.
Xie Y, Wang Y, Zhang T, Ren G, Yang Z. Effects of Nanoparticle Zinc Oxide on Spatial Cognition and Synaptic Plasticity in Mice With Depressive-Like Behaviors. JBiomedSci. 2012 Feb 3; 19(1): 14. Zhang X, Xu Y, Zhou L, Zhang C, Meng Q, Wu S, Wang S, Ding Z, Chen X, Li X, Chen R. Sex-Dependent Depression-Like Behavior Induced by Respiratory Administration of Aluminum Oxide Nanoparticles. Int J Environ Res Public Health. 2015 Dec 9;12(12):15692-705.
Изобретение относится к области медицины и фармакологии, а именно раскрывается применение кластера золота, связанного с лигандами, для лечения депрессии у субъекта, где указанный кластер золота включает золотое ядро; и лиганд, связанный с золотым ядром; где золотое ядро имеет диаметр в интервале 0,5-3 нм; лиганд является одним из выбранных из группы, состоящей из L-цистеина и его производных, D-цистеина и его производных, цистеинсодержащих олигопептидов и их производных и других тиолсодержащих соединений; L-цистеин и его производные выбраны из группы, состоящей из L-цистеина, N-изобутирил-L-цистеина (L-NIBC) и N-ацетил-L-цистеина (L-NAC); D-цистеин и его производные выбраны из группы, состоящей из D-цистеина, N-изобутирил-D-цистеина(D-NIBC) и N-ацетил-D-цистеина (D-NAC); цистеинсодержащие олигопептиды и их производные представляют собой цистеинсодержащие дипептиды, цистеинсодержащие трипептиды, цистеинсодержащие тетрапептиды или цистеинсодержащие пентапептиды; и другие тиолсодержащие соединения выбраны из группы, состоящейиз1-[(2S)-2-метил-3-тиол-1-оксопропил]-L(D)-пролина, тиогликолевой кислоты, меркаптоэтанола, тиофенола, D-3-троловола, N-(2-меркаптопропионил)-глицина, додецилмеркаптана, 2-аминоэтанэтиола (CSH), 3-меркаптопропионовой кислоты (MPA) и 4-меркаптобеновой кислоты (p-MBA). 5 з.п. ф-лы, 19 ил., 1 табл., 1 пр.
1. Применение кластера золота, связанного с лигандами, для лечения депрессии у субъекта, при этом кластер золота, связанный с лигандами, включает:
золотое ядро; и
лиганд, связанный с золотым ядром;
где золотое ядро имеет диаметр в интервале 0,5-3 нм;
лиганд является одним из выбранных из группы, состоящей из L-цистеина и его производных, D-цистеина и его производных, цистеинсодержащих олигопептидов и их производных и других тиолсодержащих соединений;
L-цистеин и его производные выбраны из группы, состоящей из L-цистеина, N-изобутирил-L-цистеина (L-NIBC) и N-ацетил-L-цистеина (L-NAC); D-цистеин и его производные выбраны из группы, состоящей из D-цистеина, N-изобутирил-D-цистеина(D-NIBC) и N-ацетил-D-цистеина (D-NAC);
цистеинсодержащие олигопептиды и их производные представляют собой цистеинсодержащие дипептиды, цистеинсодержащие трипептиды, цистеинсодержащие тетрапептиды или цистеинсодержащие пентапептиды; и
другие тиолсодержащие соединения выбраны из группы, состоящей из 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L(D)-пролина, тиогликолевой кислоты, меркаптоэтанола, тиофенола, D-3-троловола, N-(2-меркаптопропионил)-глицина, додецилмеркаптана, 2-аминоэтанэтиола (CSH), 3-меркаптопропионовой кислоты (MPA) и 4-меркаптобеновой кислоты (p-MBA).
2. Применение по п.1, где золотое ядро имеет диаметр в интервале 0,5-2,6 нм.
3. Применение по п.1, где цистеинсодержащие дипептиды выбраны из группы, состоящей из L(D)-цистеин-L(D)-аргинин дипептида (CR), L(D)-аргинин-L(D)-цистеин дипептида (RC), L(D)-гистидин-L(D)-цистеин дипептида (HC) и L(D)-цистеин-L(D)-гистидин дипептида (CH).
4. Применение по п.1, где цистеинсодержащие трипептиды выбраны из группы, состоящей из глицин-L(D)-цистеин-L(D)-аргинин трипептида (GCR), L(D)-пролин-L(D)-цистеин-L(D)-аргинин трипептида (PCR), L(D)-лизин-L(D)-цистеин-L(D)-пролин трипептида (KCP) и L(D)-глутатиона (GSH).
5. Применение по п.1, где цистеинсодержащие тетрапептиды выбраны из группы, состоящей из глицин-L(D)-серин-L(D)-цистеин-L(D)-аргинин тетрапептида (GSCR) и глицин-L(D)-цистеин-L(D)-серин-L(D)-аргининтетрапептида (GCSR).
6. Применение по п.1, где цистеинсодержащие пентапептиды выбраны из группы, состоящей из цистеинил-аспарагинил-глутаминил-валинил-аспарагина (CDEVD) и аспарагинил-глутаминил-валинил-аспарагинил-цистеина (DEVDC).
| CN 111035653 A, 21.04.2020 | |||
| US 20160015742 A1, 21.01.2016 | |||
| Rodrigues, Matheus Scarpatto et al | |||
| Nanotechnology as a therapeutic strategy to prevent neuropsychomotor alterations associated with hypercholesterolemia | |||
| Colloids and surfaces | |||
| B, Biointerfaces.2021, v | |||
| Питательное приспособление к трепальным машинам для лубовых растений | 1922 |
|
SU201A1 |
| CN 111848471 A, 30.10.2020 | |||
| CN 111848472 A, 30.10.2020 | |||
| КОМПОЗИТ ГЕКСАПЕПТИДА СО СТАБИЛИЗИРОВАННОЙ ДИСУЛЬФИДНОЙ СВЯЗЬЮ С ВЕЩЕСТВОМ МЕТАЛЛОМ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ЕГО ОСНОВЕ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ НА ОСНОВЕ РЕГУЛЯЦИИ МЕТАБОЛИЗМА, ПРОЛИФЕРАЦИИ, ДИФФЕРЕНЦИРОВКИ И МЕХАНИЗМОВ АПОПТОЗА В НОРМАЛЬНЫХ И ПАТОЛОГИЧЕСКИ ИЗМЕНЕННЫХ ТКАНЯХ | 1999 |
|
RU2153350C1 |
Авторы
Даты
2024-12-19—Публикация
2021-04-25—Подача