ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[1] Настоящее изобретение относится к области лечения заболеваний головного мозга, в частности к кластерам золота (AuCs), связанным с лигандами, к композиции, включающей кластеры золота, связанные с лигандами, к применению кластеров золота, связанных с лигандами, для приготовления лекарств для лечения ишемического церебрального инсульта, а также к способам применения кластеров золота, связанных с лигандами, и композиции для лечения ишемического церебрального инсульта.
УРОВЕНЬ ТЕХНИКИ
[2] Инсульт происходит, когда кровеносный сосуд либо закупоривается тромбом, либо разрывается. Существует три типа инсульта: геморрагический церебральный инсульт, ишемический церебральный инсульт и транзиторная ишемическая атака (ТИА).
[3] Причиной геморрагического церебрального инсульта является разрыв кровеносного сосуда, препятствующий поступлению крови в мозг. Общие симптомы включают внезапную слабость, паралич любой части тела, нарушение речи, рвоту, трудности при ходьбе, кому, потерю сознания, скованность мышц шеи и головокружение. Специализированного лечения не существует.
[4] Ишемический церебральный инсульт, также известный как ишемия головного мозга и церебральная ишемия, представляет собой одну из наиболее распространенных патологий у человека и является одной из ведущих причин смерти и инвалидности. На долю ишемического инсульта приходится около 87 процентов всех случаев инсульта. Ишемический церебральный инсульт является следствием закупоривания, например, тромбом или бляшкой, артерии, снабжающей кровью мозг. Закупоривание возникает в области шеи или в черепе и уменьшает приток крови и кислорода к мозгу, что приводит к повреждению или гибели клеток мозга. Если кровообращение не восстанавливается быстро, повреждение мозга может быть необратимым.
[5] Характерные симптомы ишемического церебрального инсульта зависят от того, какая область мозга поражена. Общими симптомами большинства случаев ишемического церебрального инсульта являются проблемы со зрением, слабость или паралич конечностей, головокружение и вертиго, спутанность сознания, потеря координации и
опущение лица с одной стороны. После появления симптомов очень важно как можно быстрее начать лечение, чтобы снизить вероятность того, что повреждения станут необратимыми.
[6] Основным способом лечения ишемического церебрального инсульта является внутривенное введение тканевого активатора плазминогена (t-PA), который расщепляет тромбы. Для достижения эффективности t-PA должен быть введен в течение четырех с половиной часов с возникновения приступа инсульта. Однако t-PA вызывает кровотечение, поэтому пациентам нельзя вводить t-PA, если у них в анамнезе есть геморрагический инсульт, кровоизлияние в мозг, а также недавняя серьезная операция или травма головы. Долгосрочное лечение включает аспирин или антикоагулянт для предотвращения дальнейшего образования тромбов.
[7] В публикации Amani et al. говорится, что OX26@GNPs, образованные путем конъюгирования OX26-PEG с поверхностью 25 нм коллоидных наночастиц золота, значительно увеличили инфарктную ткань мозга, а свободные GNPs и PEGylated GNPs не повлияли на интенсивность инфаркта; результаты исследования показали, что OX26@GNPs не подходят для лечения ишемического инсульта.
[8] В публикации Zheng et al. говорится, что у их модельной крысы с травмой OGD/R 20 нм Au-NPs повысили жизнеспособность клеток, уменьшили апоптоз нейронов и окислительный стресс, а также улучшили митохондриальное дыхание. Однако в исследовании Zheng et al. также продемонстрировано, что 5 нм Au-NPs показали противоположные эффекты, не подходящие для лечения ишемического инсульта.
[9] ТИА возникает из-за временного тромба. Общие симптомы включают слабость, онемение или паралич одной стороны тела, неразборчивую или спутанную речь, слепоту и головокружение. Специализированного лечения не существует.
[10] В настоящее время сохраняется потребность в эффективных способах и препаратах для лечения ишемического церебрального инсульта.
РАСКРЫТИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
[11] Настоящее изобретение раскрывает применение кластеров золота, связанных с лигандами, для лечения ишемического церебрального инсульта у субъекта.
[12] В определенных вариантах осуществления настоящего изобретения для лечения ишемического церебрального инсульта у субъекта используется кластер золота, связанный
с лигандом, где кластер золота, связанный с лигандом, включает золотое ядро и лиганд, связанный с золотым ядром.
[13] В определенных вариантах терапевтического применения золотое ядро имеет диаметр в интервале 0,5-3 нм. В определенных вариантах осуществления золотое ядро имеет диаметр в интервале 0,5-2,6 нм.
[14] В определенных вариантах терапевтического применения лиганд представляет собой выбранный из группы, состоящей из L-цистеина и его производных, D-цистеина и его производных, цистеинсодержащих олигопептидов и их производных и других тиолсодержащих соединений.
[15] В определенных вариантах терапевтического применения L-цистеин и его производные выбирают из группы, состоящей из L-цистеина, N-изобутирил-L-цистеина (L-NIBC) и N-ацетил-L-цистеина (L-NAC), а D-цистеин и его производные выбирают из группы, состоящей из D-цистеина, N-изобутирил-D-цистеина (D-NIBC) и N-ацетил-D- цистеина (D-NAC).
[16] В определенных вариантах терапевтического применения цистеинсодержащие олигопептиды и их производные представляют собой цистеинсодержащие дипептиды, где цистеинсодержащие дипептиды выбраны из группы, состоящей из L(D)-цистеин-L(D)- аргинин дипептида (CR), L(D)-аргинин-L(D)-цистеин дипептида (RC), L(D)-гистидин- L(D)-цистеин дипептида (HC) и L(D)-цистеин-L(D)-гистидин дипептида (CH).
[17] В определенных вариантах терапевтического применения цистеинсодержащие олигопептиды и их производные представляют собой цистеинсодержащие трипептиды, где цистеинсодержащие трипептиды выбраны из группы, состоящей из глицин-L(D)- цистеин-L(D)-аргинин трипептида (GCR), L(D)-пролин-L(D)-цистеин-L(D)-аргинин трипептида (PCR), L(D)-лизин-L(D)-цистеин-L(D)-пролин трипептида (KCP) и L(D)- глутатиона (GSH).
[18] В определенных вариантах терапевтического применения цистеинсодержащие олигопептиды и их производные представляют собой цистеинсодержащие тетрапептиды, где цистеинсодержащие тетрапептиды выбраны из группы, состоящей из глицин-L(D)- серин-L(D)-цистеин-L(D)-аргининового тетрапептида (GSCR) и глицин-L(D)-цистеин- L(D)-серин-L(D)-аргининового тетрапептида (GCSR).
[19] В определенных вариантах терапевтического применения цистеинсодержащие олигопептиды и их производные представляют собой цистеинсодержащий пентапептид, где цистеинсодержащие пентапептиды выбраны из группы, состоящей из цистеинил-
аспарагинил-глутаминил-валинил-аспарагина (CDEVD) и аспаргинил-глутаминил- валинил-аспарагинил-цистеина (DEVDC).
[20] В определенных вариантах терапевтического применения другие тиолсодержащие соединения выбирают из группы, состоящей из 1-[(2S)-2-метил-3-тиол-1-оксопропил]- L(D)-пролина, тиогликолевой кислоты, меркаптоэтанола, тиофенола, D-3-троловола, N-(2- меркаптопропионил)-глицина, додецилмеркаптана, 2-аминоэтанэтиола (CSH), 3- меркаптопропионовой кислоты (MPA) и 4-меркаптобеновой кислоты (p-MBA).
[21] Задачи и преимущества от применения заявленного изобретения будут раскрыты из следующего подробного описания предпочтительных вариантов его осуществления в совокупности с прилагаемыми чертежами.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[22] Предпочтительные варианты осуществления настоящего изобретения будут описаны далее со ссылкой на фигуры, на которых одинаковые цифры обозначают одинаковые элементы.
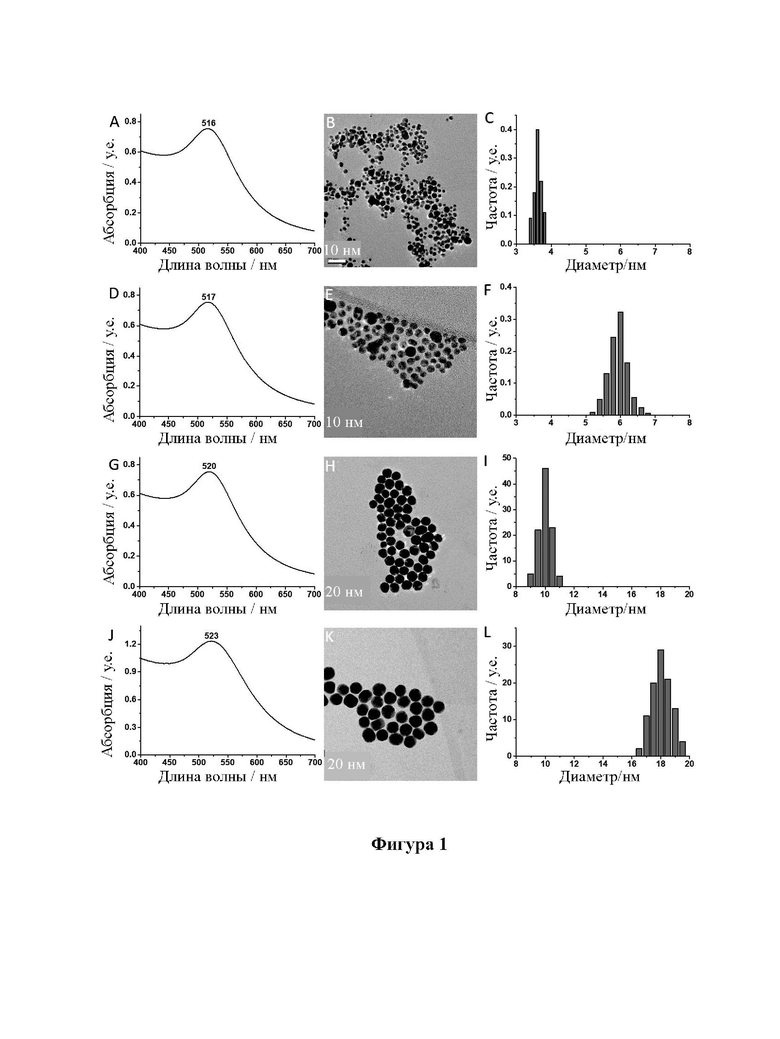
[23] На фиг. 1 показаны ультрафиолетово-видимые (УФ) спектры, изображения просвечивающего электронного микроскопа (ПЭМ) и диаграммы распределения размеров частиц лиганда L-NIBC, модифицированного наночастицами золота (L-NIBC-AuNPs) с различными размерами частиц.
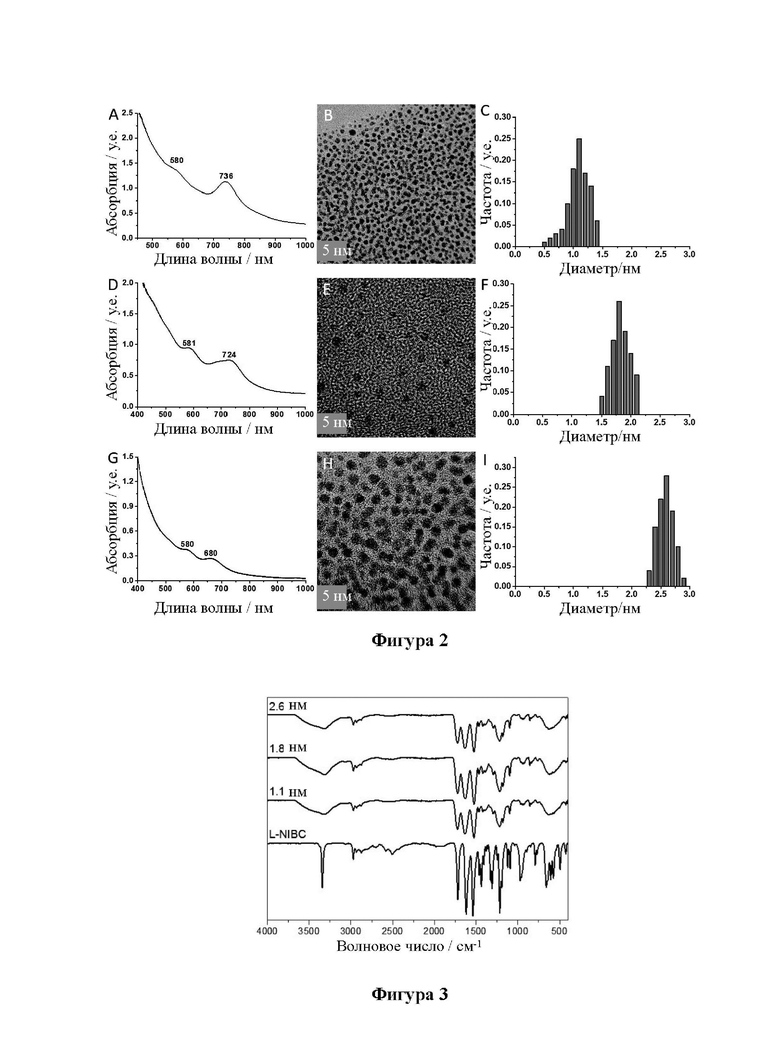
[24] На фиг. 2 показаны ультрафиолетово-видимые (УФ) спектры, изображения ПЭМ и диаграммы распределения частиц по размерам кластеров золота, связанных с лигандом L- NIBC (L-NIBC-AuCs) с различными размерами частиц.
[25] На фиг. 3 показаны инфракрасные спектры L-NIBC-AuCs с различными размерами частиц.
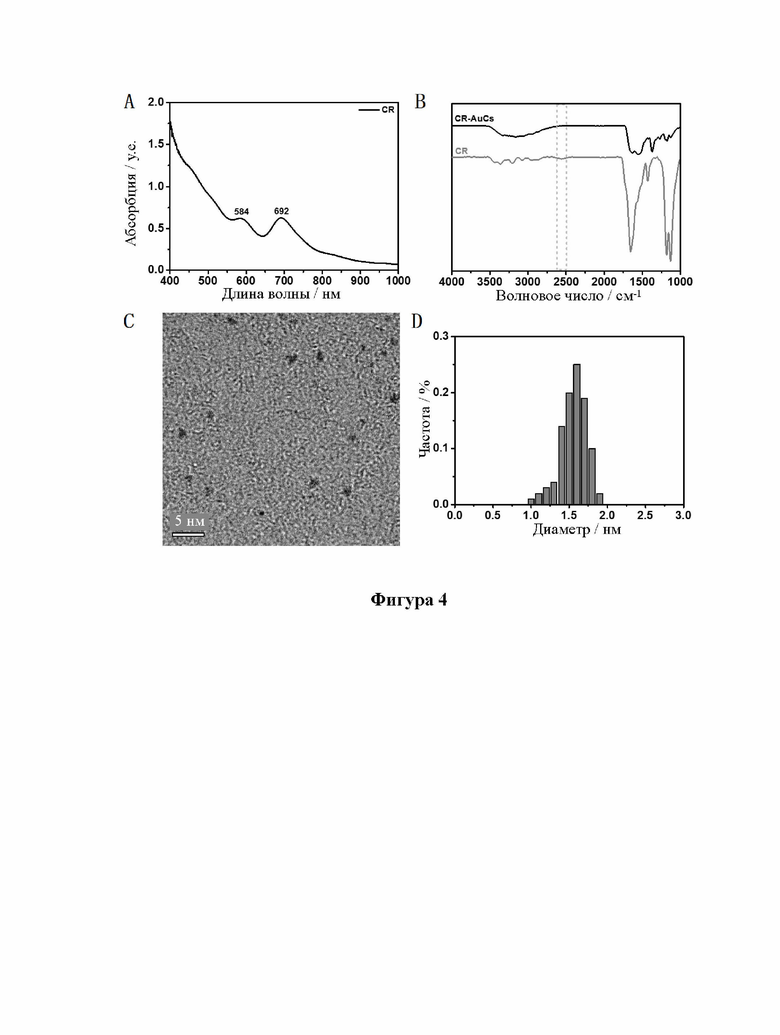
[26] На фиг. 4 показаны УФ, ИК, ПЭМ и диаграммы распределения частиц по размерам кластеров золота, связанных с лигандом CR (CR-AuCs).
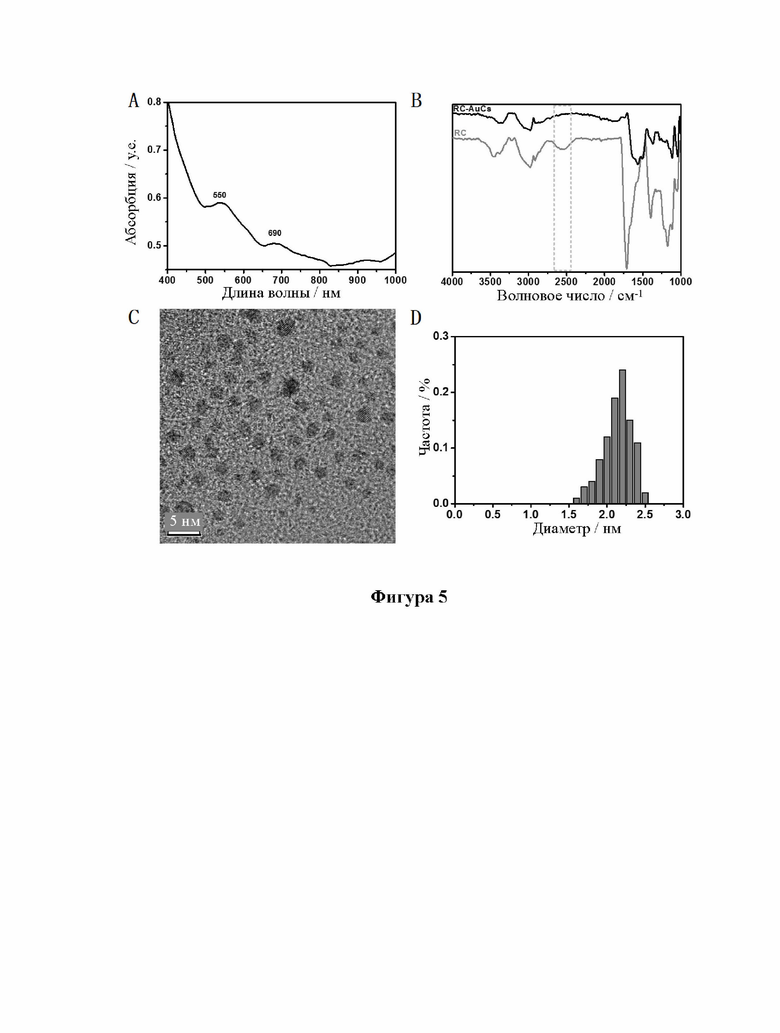
[27] На фиг. 5 показаны УФ, ИК, ПЭМ и диаграммы распределения частиц по размерам кластеров золота, связанных с лигандом RC (RC-AuCs).
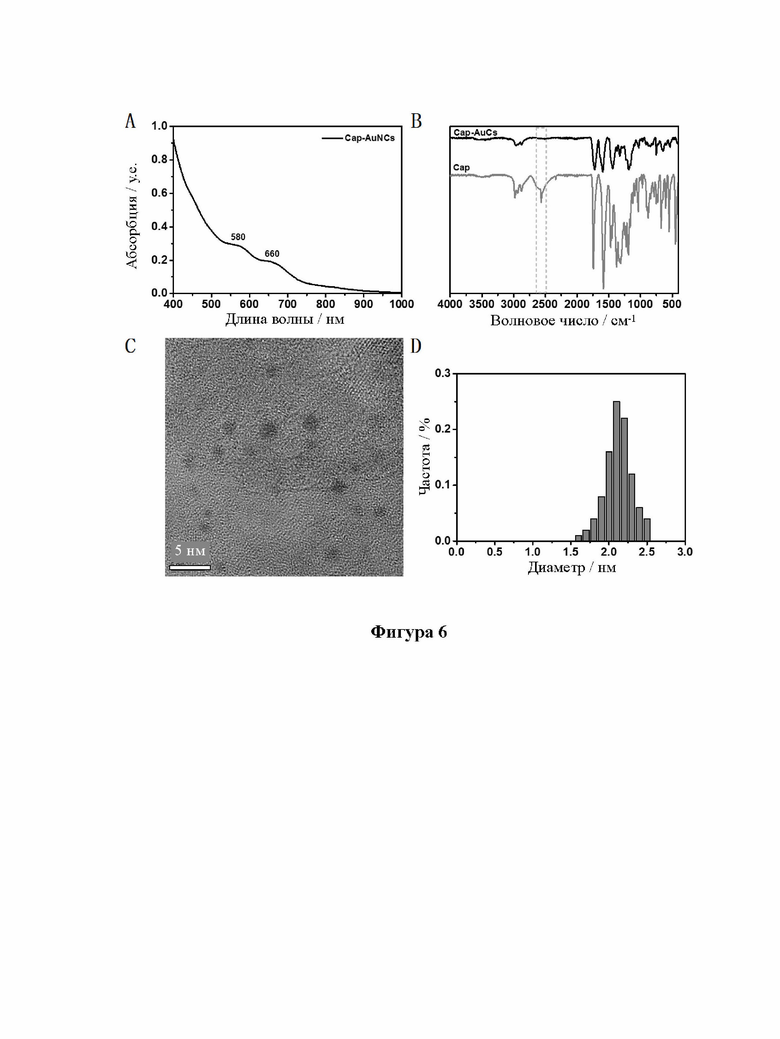
[28] На фиг. 6 показаны УФ, ИК, ПЭМ и диаграммы распределения частиц по размерам лиганда 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L-пролина (т.е. Cap), связанного с кластерами золота (Cap-AuCs).
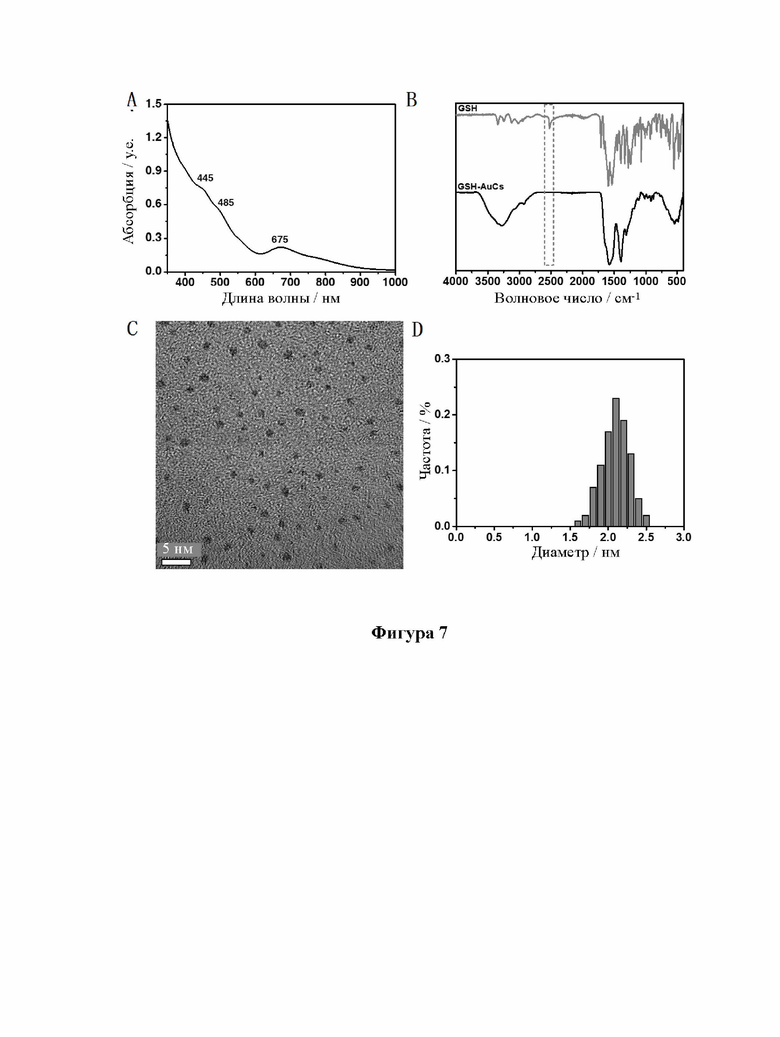
[29] На фиг. 7 показаны диаграммы УФ, ИК, ПЭМ и диаграммы распределения частиц по размерам кластеров золота, связанных с лигандом GSH (GSH-AuCs).
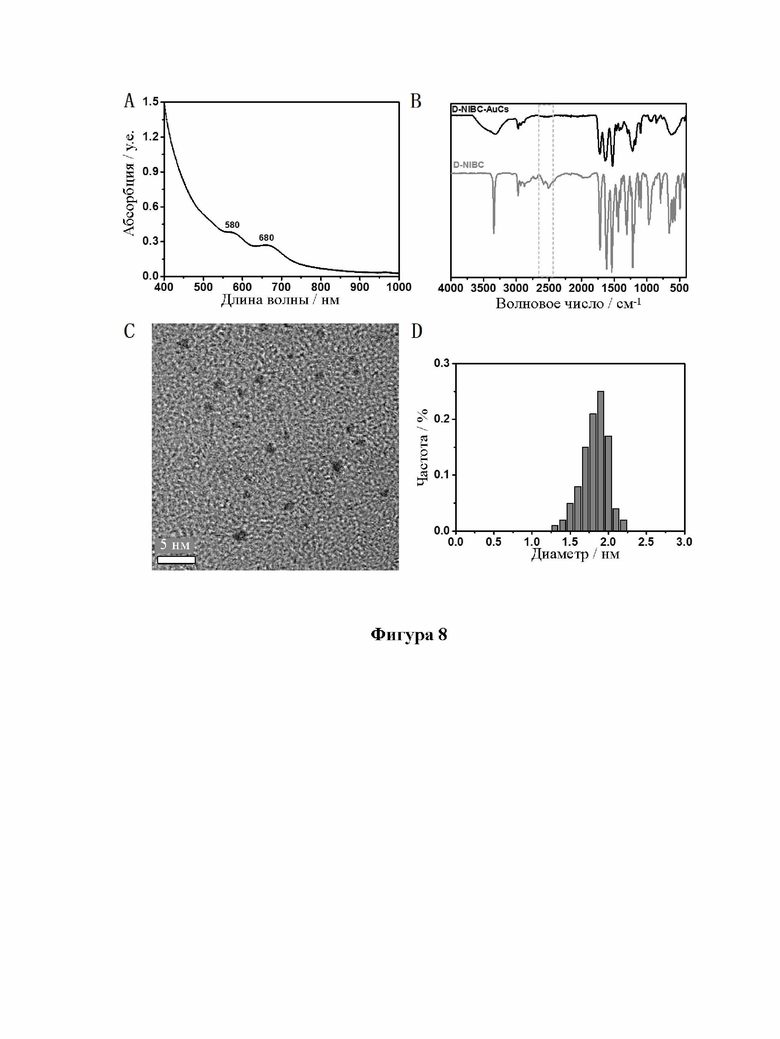
[30] На фиг. 8 показаны УФ, ИК, ПЭМ и диаграммы распределения частиц по размерам кластеров золота, связанных с лигандом D-NIBC (D-NIBC-AuCs).
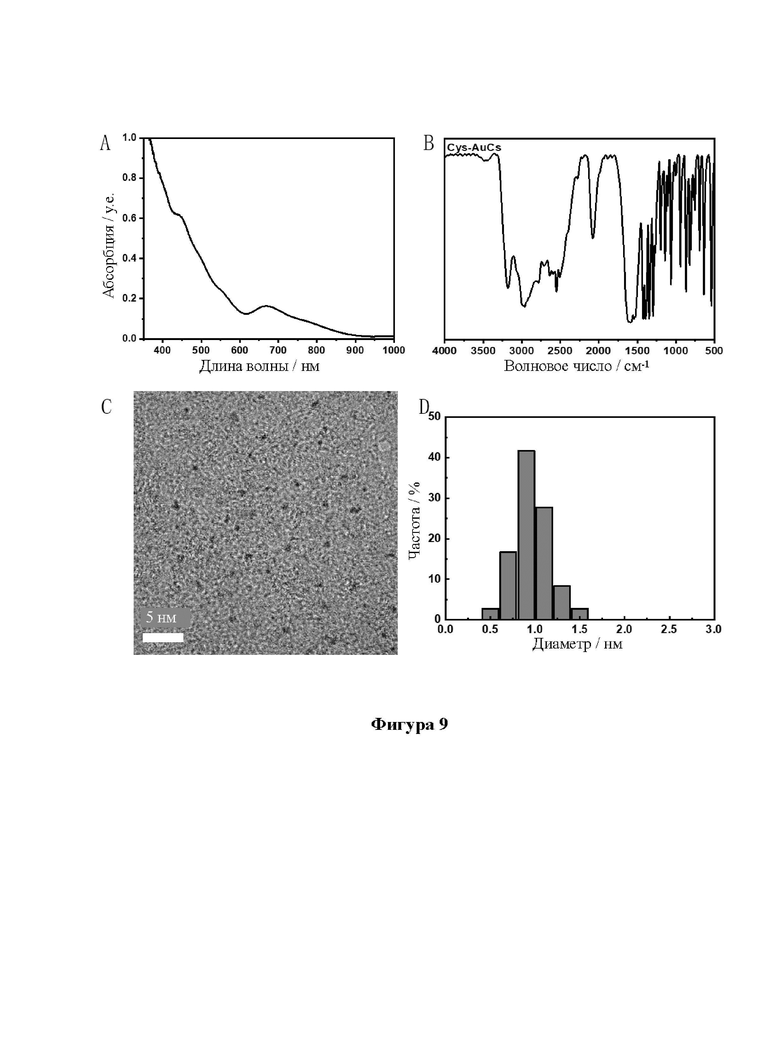
[31] На фиг. 9 показаны УФ, ИК, ПЭМ и диаграммы распределения частиц по размерам кластеров золота, связанных с лигандом L-цистеином (L-Cys-AuCs).
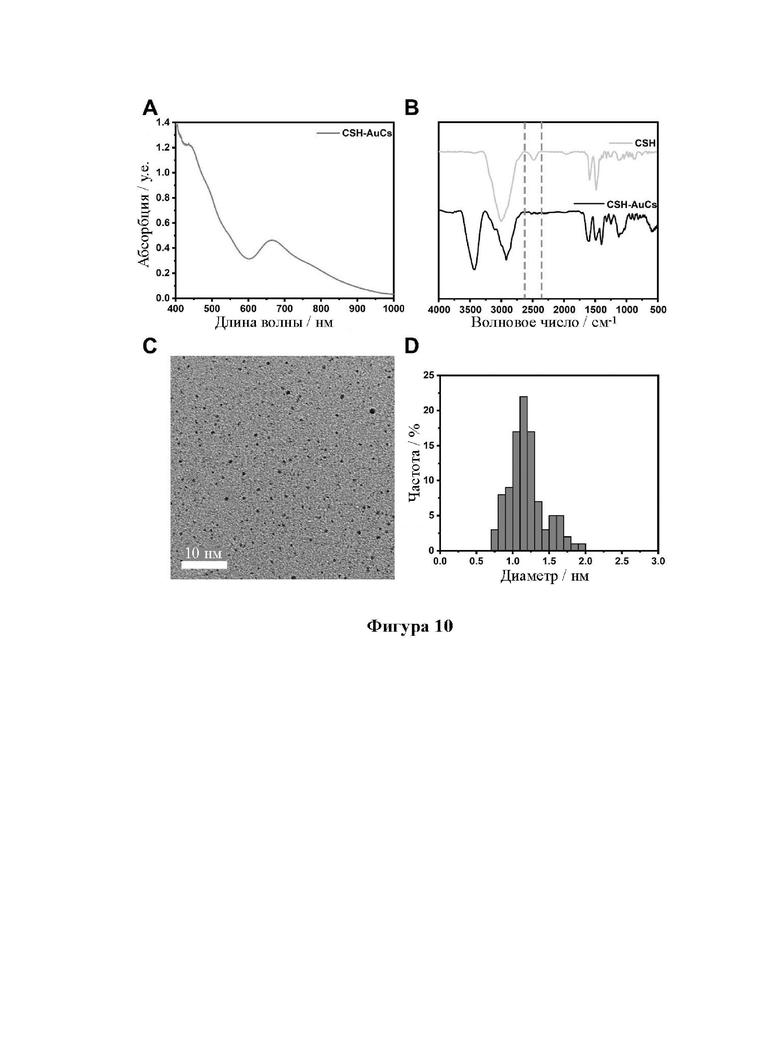
[32] На фиг. 10 показаны УФ, ИК, ПЭМ и диаграммы распределения частиц по размерам кластеров золота, связанных с лигандом 2-аминоэтанэтиолом (CSH-AuCs).
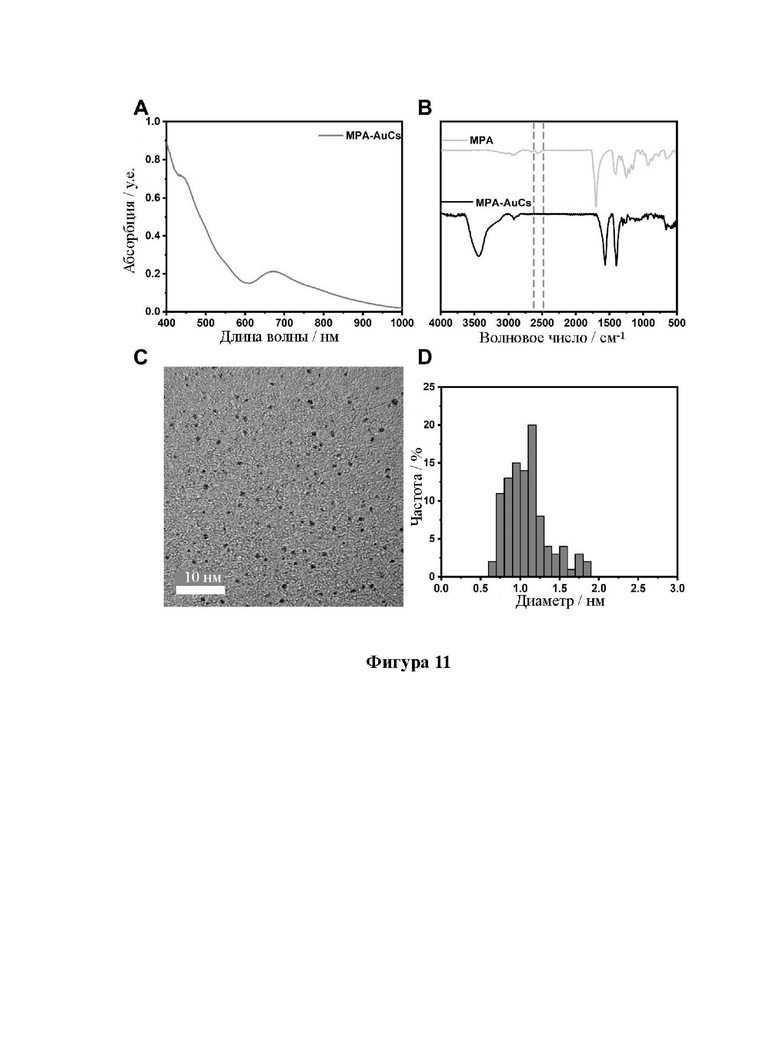
[33] На фиг. 11 показаны УФ, ИК, ПЭМ и диаграммы распределения частиц по размерам кластеров золота, связанных с лигандом 3-меркаптопропионовой кислоты (MPA-AuCs).
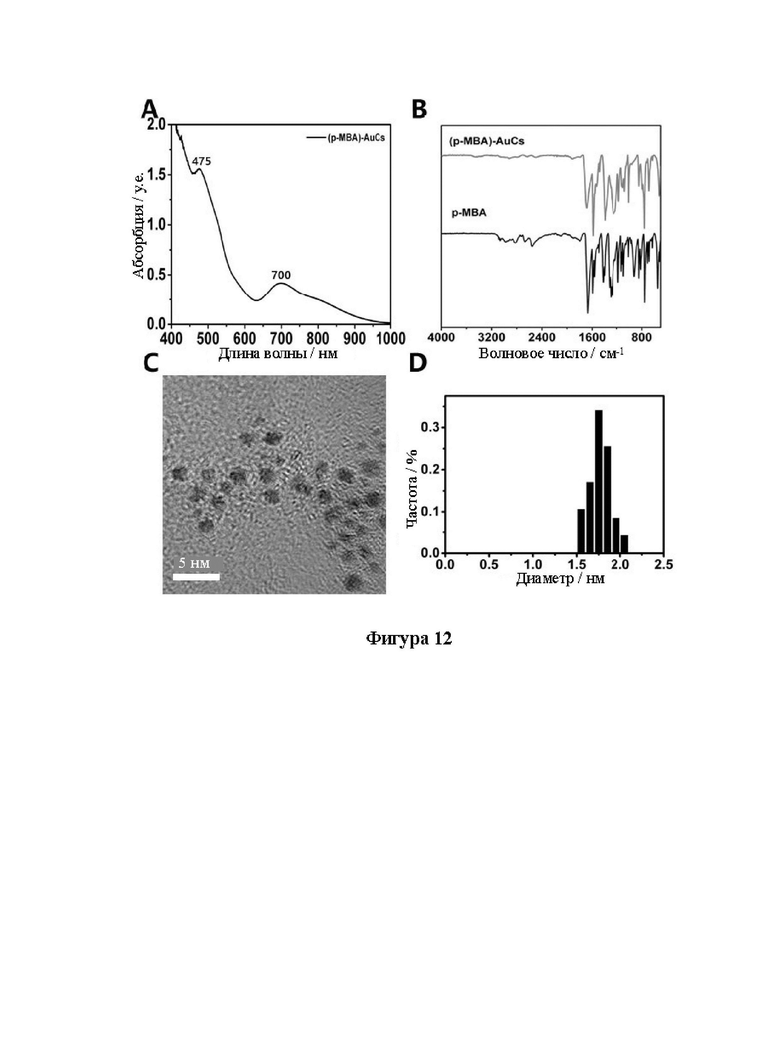
[34] На фиг. 12 представлены УФ, ИК, ПЭМ и диаграммы распределения частиц по размерам кластеров золота, связанных с лигандом 4-меркаптобеновой кислоты (p-MBA- AuCs).
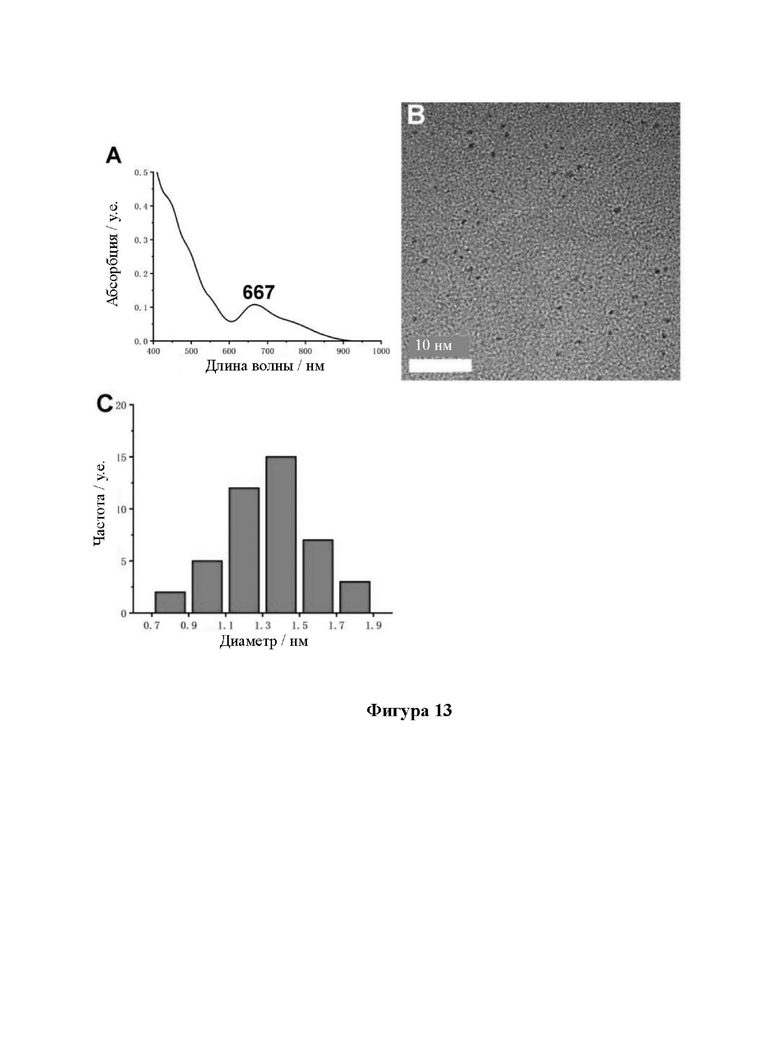
[35] На фиг. 13 показаны УФ, ПЭМ и диаграммы распределения частиц по размерам кластеров золота, связанных с лигандом 4-цистеинил-аспарагинил-глутаминил-валинил- аспарагина (CDEVD) (CDEVD-AuCs).
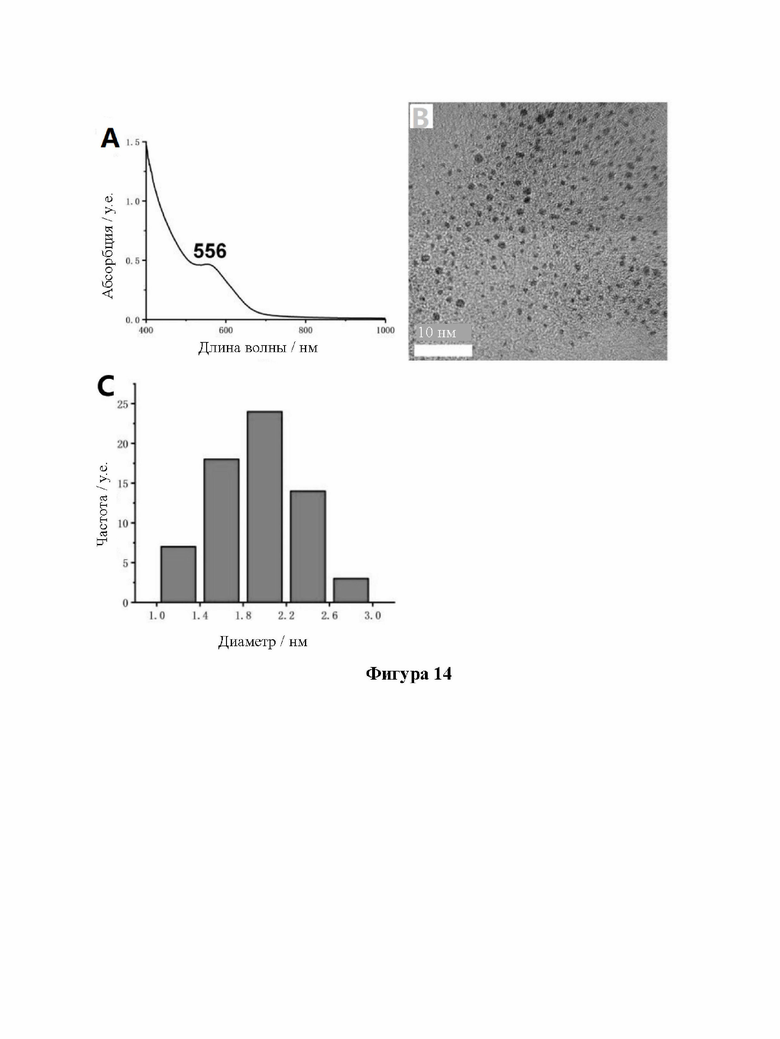
[36] На фиг. 14 показаны УФ, ПЭМ и диаграммы распределения частиц по размерам кластеров золота, связанных с лигандом 4-аспаргинил-глутаминил-валинил-аспарагинил- цистеина (DEVDC) (DEVDC-AuCs).
[37] На фиг. 15 показана оценка результатов рефлекторного поведения крыс в каждой группе (на гистограмме в каждой временной точке слева направо: группа плацебо (пустая), группа модельного контроля, группа A1 с низкой дозировкой, группа A1 с высокой дозировкой, группа A2 с низкой дозировкой, группа A2 с высокой дозировкой, группа A3 с низкой дозировкой, группа A3 с высокой дозировкой, группа A4 с низкой дозировкой, группа A4 с высокой дозировкой, группа B1 с низкой дозировкой, группа B1 с высокой дозировкой, группа B2 с низкой дозировкой и группа B2 с высокой дозировкой).
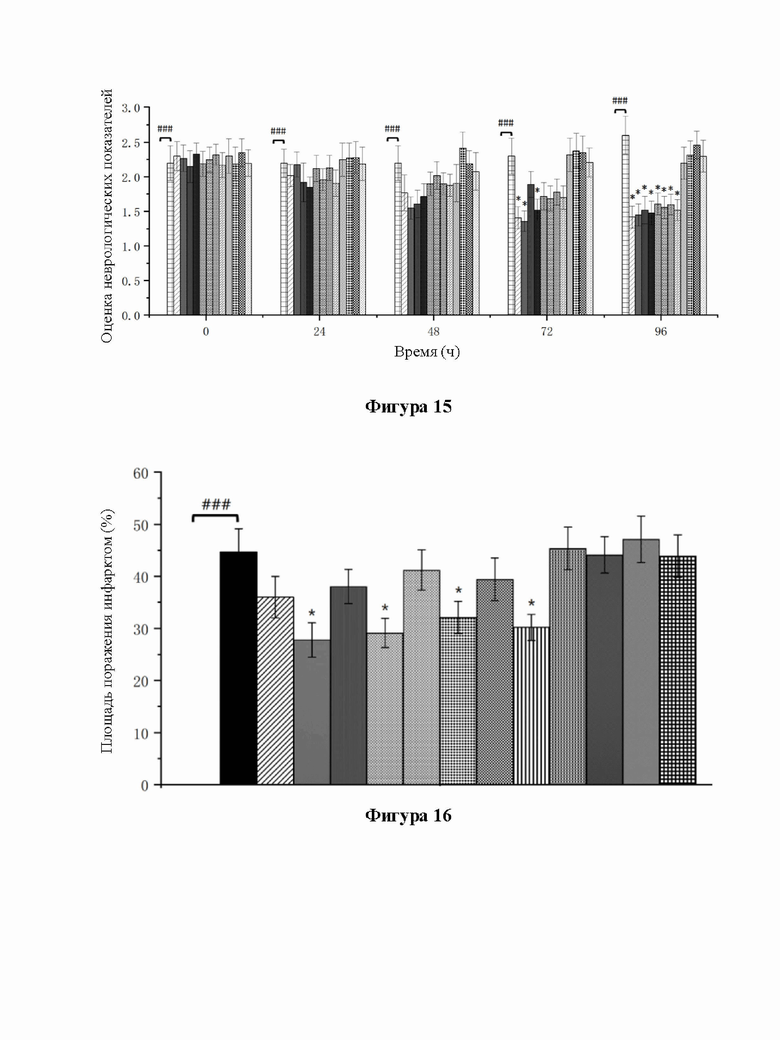
[38] На фиг. 16 показан процент поражения головного мозга крыс в каждой группе (на гистограмме слева направо: группа плацебо (пустая), группа модельного контроля, группа A1 с низкой дозировкой, группа A1 с высокой дозировкой, группа A2 с низкой дозировкой, группа A2 с высокой дозировкой, группа A3 с низкой дозировкой, группа A3 с высокой дозировкой, группа A4 с низкой дозировкой, группа A4 с высокой дозировкой, группа B1 с низкой дозировкой, группа B1 с высокой дозировкой, группа B2 с низкой дозировкой и группа B2 с высокой дозировкой).
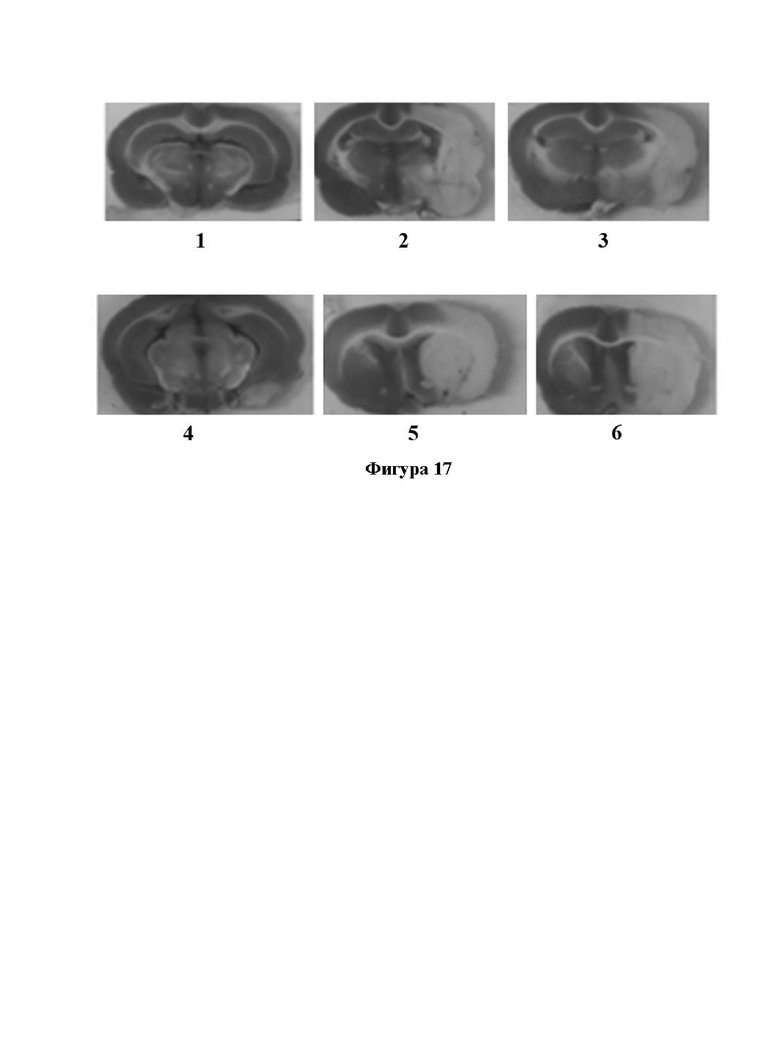
[39] На фиг. 17 показаны примерные изображения окрашивания TTC тканей мозга крыс после введения препаратов кластера золота и наночастиц золота, где (1) группа плацебо;
(2) группа модельного контроля; (3) группа A1 с низкой дозировкой; (4) группа A1 с высокой дозировкой; (5) группа B1 с низкой дозировкой; (6) группа B1 с высокой дозировкой.
ПОДРОБНОЕ ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
[40] Настоящее изобретение станет более понятным, если обратиться к следующему подробному описанию некоторых вариантов осуществления изобретения.
[41] В настоящей заявке, где даны ссылки на различные публикации, описания этих публикаций включаются в настоящую заявку в полном объеме для более полного описания уровня техники, к которому относится настоящее изобретение.
[42] В настоящем документе «введение» означает пероральное («po») введение, введение в виде суппозитория, местное введение, внутривенное («iv»), внутрибрюшинное («ip»), в н у т р и м ы ш еч н о е ( « i m » ) , и н т р а л е з и о н а л ь н о е , и н т р а г и п п о ка м п а л ь н о е , интрацеребровентрикулярное, интраназальное или подкожное («sc») введение, или имплантацию субъекту устройства замедленного высвобождения, например, мини- осмотического насоса или разъедаемого имплантата. Введение осуществляется любым способом, включая парентеральный и трансмукозальный (например, пероральный, назальный, вагинальный, ректальный или трансдермальный). Парентеральное введение включает, в частности, внутривенное, внутримышечное, внутриартериальное, внутрикожное, подкожное, внутрибрюшинное, внутрижелудочковое и внутричерепное. Другие способы введения включают, не ограничиваясь, использование липосомальных составов, внутривенную инфузию, трансдермальные пластыри и т.д.
[43] Под «системным введением» и «систематическим введением» понимается способ введения соединения или композиции млекопитающему таким образом, что соединение или композиция доставляются к участкам тела, включая целевой участок фармацевтического воздействия, через систему кровообращения. Системное введение включает, не ограничиваясь, пероральное, интраназальное, ректальное и парентеральное (т.е. введение не через пищеварительный тракт, а внутримышечно, внутривенно, внутриартериально, трансдермально и подкожно) введение, с оговоркой, что в настоящем документе системное введение не включает прямое введение в участок мозга не через систему кровообращения, например, интратекальное введение и внутричерепное введение.
[44] Под «лечением» и «терапией» в настоящем документе понимается замедление возникновения, приостановление или обращение вспять прогрессирования, облегчение или предотвращение заболевания или состояния, к которому применяется данный термин, или одного или нескольких симптомов такого заболевания или состояния.
[45] Под «пациентом», «субъектом» или «индивидуумом» взаимозаменяемо понимается млекопитающее, например, человек или другое млекопитающее, включая приматов (например, макак, обыкновенных шимпанзе, понго), одомашненных млекопитающих (например, кошачьи, собачьи), сельскохозяйственное млекопитающее (например, бычьи, овиные, свиные, лошадиные) и лабораторных млекопитающих или грызунов (например, крысиные, мышиные, зайцеобразные, хомяковые, морские свинки).
[46] Кластеры золота (AuCs) - это особая форма золота, существующая между атомами золота и наночастицами золота. AuCs имеют размер менее 3 нм и состоят всего из нескольких сотен атомов золота, что приводит к разрушению гранецентрированной кубической структуры наночастиц золота. В результате AuCs проявляют молекулоподобные дискретные электронные свойства с четко выраженным промежутком HOMO-LUMO в отличие от непрерывных или квазинепрерывных энергетических уровней наночастиц золота. Это приводит к исчезновению эффекта поверхностного плазмонного резонанса и соответствующей полосы поглощения плазмонного резонанса (520 ± 20 нм) в UV-Vis спектре, которой обладают обычные наночастицы золота.
[47] Настоящее изобретение раскрывает AuC, связанный с лигандами.
[48] В определенных вариантах осуществления изобретения AuC, связанный с лигандами, включает лиганд и золотое ядро, где лиганд связан с золотым ядром. Связывание лигандов с золотым ядром означает, что лиганды образуют стабильные в растворе комплексные соединения с золотым ядром посредством ковалентной связи, водородной связи, электростатической силы, гидрофобной силы, силы Ван-дер-Ваальса и т.д. В некоторых вариантах осуществления диаметр золотого ядра составляет от 0,5 до 3 нм. В некоторых вариантах осуществления диаметр золотого ядра составляет 0,5 - 2,6 нм.
[49] В некоторых вариантах осуществления изобретения AuC, связанный с лигандами, представляет собой тиолсодержащее соединение или олигопептид. В некоторых вариантах реализации лиганд связывается с золотым ядром с образованием AuC, связанного с лигандом, через связь Au-S.
[50] В некоторых вариантах осуществления изобретения лиганд представляет собой, не ограничиваясь, L-цистеин, D-цистеин или производное цистеина. В некоторых вариантах
осуществления производное цистеина представляет собой N-изобутирил-L-цистеин (L- NIBC), N-изобутирил-D-цистеин (D-NIBC), N-ацетил-L-цистеин (L-NAC) или N-ацетил-D- цистеин (D-NAC).
[51] В определенных вариантах осуществления лиганд представляет собой, не ограничиваясь, цистеинсодержащий олигопептид и его производные. В определенных вариантах осуществления цистеинсодержащий олигопептид представляет собой цистеинсодержащий дипептид. В определенных вариантах осуществления изобретения цистеинсодержащий дипептид представляет собой L(D)-цистеин-L(D)-аргинин дипептид (CR), L(D)-аргинин-L(D)-цистеин дипептид (RC) или L(D)-цистеин-L-гистидин дипептид (CH). В определенных вариантах осуществления цистеинсодержащий олигопептид представляет собой цистеинсодержащий трипептид. В определенных вариантах осуществления изобретения цистеинсодержащий трипептид представляет собой глицин- L(D)-цистеин-L(D)-аргинин трипептид (GCR), L(D)-пролин-L(D)-цистеин-L(D)-аргинин трипептид (PCR) или L(D)-глутатион (GSH). В определенных вариантах осуществления цистеинсодержащий олигопептид представляет собой цистеинсодержащий тетрапептид. В определенных вариантах осуществления изобретения цистеинсодержащий тетрапептид представляет собой глицин-L(D)-серин-L(D)-цистеин-L(D)-аргинин тетрапептид (GSCR) или глицин-L(D)-цистеин-L(D)-серин-L(D)-аргинин тетрапептид (GCSR). В определенных вариантах осуществления цистеинсодержащий олигопептид представляет собой цистеинсодержащий пентапептид. В определенных вариантах осуществления изобретения цистеинсодержащий пентапептид представляет собой цистеинил-аспарагинил- глутаминил-валинил-аспарагин (CDEVD) или аспаргинил-глутаминил-валинил- аспарагинил-цистеин (DEVDC).
[52] В определенных вариантах осуществления изобретения лиганд представляет собой тиолсодержащее соединение. В определенных вариантах осуществления тиолсодержащее соединение представляет собой 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L(D)-пролин, тиогликолевую кислоту, меркаптоэтанол, тиофенол, D-3-троловол, додецилмеркаптан, 2- аминоэтанэтиол (CSH), 3-меркаптопропионовую кислоту (MPA) или 4-меркаптобеновую кислоту (p-MBA).
[53] Настоящее изобретение раскрывает фармацевтическую композицию для лечения ишемического церебрального инсульта. В определенных вариантах осуществления субъектом является человек. В определенных вариантах осуществления субъектом является домашнее животное, например, собака.
[54] В определенных вариантах осуществления фармацевтическая композиция включает AuC, связанный с лигандами, как описано выше, и фармацевтически приемлемый эксципиент. В определенных вариантах осуществления вспомогательное вещество представляет собой фосфатно-буферный раствор или физиологический солевой раствор.
[55] Настоящее изобретение раскрывает применение вышеописанных AuCs, связанных с лигандами, для получения лекарственного средства для лечения ишемического церебрального инсульта.
[56] Настоящее изобретение раскрывает применение описанных выше AuCs, связанных с лигандами, для лечения субъекта с ишемическим церебральным инсультом или способ лечения субъекта с ишемическим церебральным инсультом с использованием описанных выше AuCs, связанных с лигандами. В определенных вариантах осуществления способ лечения включает введение субъекту фармацевтически эффективного количества AuCs, связанных с лигандами. Фармацевтически эффективное количество может быть определено с помощью обычных исследований in vivo. В определенных вариантах осуществления изобретения фармацевтически эффективное количество AuCs, связанных с лигандами, составляет по меньшей мере 0,001 мг/кг/день, 0,005 мг/кг/день, 0,01 мг/кг/ день, 0,05 мг/кг/день, 0,1 мг/кг/день, 0,5 мг/кг/день, 1 мг/кг/день, 2 мг/кг/день, 3 мг/кг/ день, 4 мг/кг/день, 5 мг/кг/день, 6 мг/кг/день, 7 мг/кг/день, 8 мг/кг/день, 9 мг/кг/день, 10 мг/кг/день, 15 мг/кг/день, 20 мг/кг/день, 30 мг/кг/день, 40 мг/кг/день, 50 мг/кг/день, 60 мг/ кг/день, 70 мг/кг/день, 80 мг/кг/день или 100 мг/кг/день.
[57] Следующие примеры приведены исключительно с целью демонстрации основных положений настоящего изобретения; они ни в коем случае не предназначены для ограничения объема настоящего изобретения.
[58] Варианты осуществления
[59] Вариант осуществления 1. Получение AuCs, связанных с лигандами
[60] 1.1 Растворяют HAuCl4 в метаноле, воде, этаноле, н-пропаноле или этилацетате для получения раствора А, в котором концентрация HAuCl4 составляет 0,01~0,03М;
[61] 1.2 Растворяют лиганд в растворителе, чтобы получить раствор B, в котором концентрация лиганда составляет 0,01~0,18 M; лиганд включает, не ограничиваясь, L- цистеин, D-цистеин и другие производные цистеина, такие как N-изобутирил-L-цистеин (L-NIBC), N-изобутирил-D-цистеин (D-NIBC), N-ацетил-L-цистеин (L-NAC) и N-ацетил- D-цистеин (D-NAC), цистеинсодержащие олигопептиды и их производные, включая, не ограничиваясь, дипептиды, трипептид, тетрапептид, пентапептид и другие пептиды,
содержащие цистеин, такие как L(D)-цистеин-L(D)-аргинин дипептид (CR), L(D)-аргинин- L(D)-цистеин дипептид (RC), L(D)-цистеин-L(D)-гистидин (CH), глицин-L(D)-цистеин- L(D)-аргинин трипептид (GCR), L(D)-пролин-L(D)-цистеин-L(D)-аргинин трипептид (PCR), L(D)-глутатион (GSH), глицин-L(D)-серин-L(D)-цистеин-L(D)-аргинин тетрапептид (GSCR), глицин-L(D)-цистеин-L(D)-серин-L(D)-аргинин тетрапептид (GCSR), цистеинил- аспарагинил-глутаминил-валинил-аспарагин (CDEVD) и аспаргинил-глутаминил-валинил- аспарагинил-цистеин (DEVDC), и другие тиолсодержащие соединения, такие как одно или более из 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L(D)-пролина, тиогликолевой кислоты, меркаптоэтанола, тиофенола, D-3-троловола, додецилмеркаптана, 2-аминоэтанэтиола (CSH), 3-меркаптопропионовой кислоты (MPA) и 4-меркаптобеновой кислоты (p-MBA); растворитель представляет собой один или более из метанола, этилацетата, воды, этанола, н-пропанола, пентана, муравьиной кислоты, уксусной кислоты, диэтилового эфира, ацетона, анизола, 1-пропанола, 2-пропанола, 1-бутанола, 2-бутанол, пентанол, бутилацетат, трибутилметиловый эфир, изопропилацетат, диметилсульфоксид, этилформиат, изобутилацетат, метилацетат, 2-метил-1-пропанол и пропилацетат;
[62] 1.3 Смешивают раствор A и раствор B так, чтобы мольное соотношение между HAuCl4 и лигандом составляло 1:(0,01~100), перемешивают в ледяной бане в течение 0,1~48 ч, добавляют 0,025~0,8 М раствора NaBH4 в воде, этаноле или метаноле, продолжают перемешивание в ледяной водяной бане и проводят реакцию в течение 0,1~12 ч. Мольное соотношение между NaBH4 и лигандом составляет 1:(0,01~100).
[63] 1.4 Используя ультрафильтрационные трубки MWCO 3K~30K, центрифугируют реакционный раствор при 8000~17500 об/мин по градиенту в течение 10~100 мин после окончания реакции для получения осадка AuCs, связанных с лигандами, с различным с р е д н и м р а з м е р ом ч а с т и ц . А п е р т у р а ф и л ьт р а ц и о н н ы х м е м б р а н д л я ультрафильтрационных трубок с различными MWCO непосредственно определяет размер AuCs, связанных с лигандами, которые могут пройти через мембраны. По желанию этот этап может быть пропущен.
[64] 1.5 Растворяют осадок AuCs, связанных с лигандами, в различных средних размерах частиц, полученных на этапе (1.4), в воде, помещают его в диализный мешок и диализируют в воде при комнатной температуре в течение 1~7 дней.
[65] 1.6 Проводят сублимационную сушку AuCs, связанных с лигандами, в течение 12~24 ч после диализа для получения порошкообразного или флокулирующего вещества, т.е. AuCs, связанных с лигандами.
[66] Авторами было неожиданно обнаружено, что размер частиц порошкообразного или флокулянтного вещества, полученного вышеописанным способом, составляет менее 3 нм (в целом распределяется в пределах 0,5-2,6 нм). Очевидный пик поглощения при 520 нм отсутствует. Было установлено, что полученный порошок или флок является AuCs, связанными с лигандами.
[67] Вариант осуществления 2. Получение и характеристики AuCs, связанных с различными лигандами
[68] 2.1 Получение AuCs, связанных с L-NIBC, т.е. L-NIBC-AuCs
[69] На примере лиганда L-NIBC подробно описано получение и характеристики AuCs, связанных с лигандом L-NIBC.
[70] 2.1.1 Взвешивают 1,00 г HAuCl4 и растворяют в 100 мл метанола для получения 0,03 М раствора А;
[71] 2.1.2 Взвешивают 0,57 г L-NIBC и растворяют его в 100 мл ледяной уксусной кислоты (уксусной кислоты) для получения 0,03 М раствора B;
[72] 2.1.3 Отмеряют 1 мл раствора A, смешивают его с 0,5 мл, 1 мл, 2 мл, 3 мл, 4 мл или 5 мл раствора B соответственно (т.е. мольное соотношение между HAuCl4 и L-NIBC составляет 1:0,5, 1:1, 1:2, 1:3, 1:4, 1:5 соответственно), проводят реакцию в ледяной бане при перемешивании в течение 2 ч, быстро добавляют 1 мл свежеприготовленного 0,03 M (приготовленного путем взвешивания 11,3 мг NaBH4 и растворения его в 10 мл этанола) этанольного раствора NaBH4, когда раствор из ярко-желтого становится бесцветным, продолжают реакцию в течение 30 мин после того, как раствор станет темно-коричневым, и добавляют 10 мл ацетона для завершения реакции.
[73] 2.1.4 После реакции реакционный раствор подвергают градиентному центрифугированию для получения порошка L-NIBC-AuCs с различными размерами частиц. Специфический способ: после завершения реакции реакционный раствор переносят в ультрафильтрационную пробирку с MWCO 30K и объемом 50 мл, центрифугируют при 10000 об/мин в течение 20 мин, а ретентат во внутренней пробирке растворяют в сверхчистой воде для получения порошка с размером частиц около 2,6 нм. Затем смешанный раствор во внешней пробирке переносят в ультрафильтрационную пробирку объемом 50 мл с MWCO 10K и центрифугируют при 13000 об/мин в течение 30 мин. Ретентат во внутренней пробирке растворяют в сверхчистой воде для получения порошка с размером частиц около 1,8 нм. Затем смешанный раствор во внешней пробирке переносят в ультрафильтрационную пробирку объемом 50 мл с MWCO 3K и
центрифугируют при 17 500 об/мин в течение 40 мин. Ретентат во внутренней пробирке растворяют в сверхчистой воде для получения порошка с размером частиц около 1,1 нм.
[74] 2.1.5 Осаждают порошок трех различных размеров частиц, полученных градиентным центрифугированием, удаляют растворитель, высушивают сырой продукт N2, растворяют его в 5 мл сверхчистой воды, помещают в диализный мешок (MWCO составляет 3KDa), помещают диализный мешок в 2 л сверхчистой воды, воду меняют каждые два дня, проводят диализ в течение 7 дней, подвергают сублимационной сушке и сохраняют для дальнейшего использования.
[75] 2.2 Характеристика L-NIBC-AuCs
[76] Эксперимент по определению характеристик был проведен для полученного выше порошка (L-NIBC-AuCs). Между тем наночастицы золота, модифицированные лигандом L-NIBC (L-NIBC-AuNPs), используются как контроль. Способ получения наночастиц золота с лигандом L-NIBC приведен в источнике (W. Yan, L. Xu, C. Xu, W. Ma, H. Kuang, L. Wang and N. A. Kotov, Journal of the American Chemical Society 2012, 134, 15114; X. Yuan, B. Zhang, Z. Luo, Q. Yao, D. T. Leong, N. Yan and J. Xie, Angewandte Chemie International Edition 2014, 53, 4623).
[77] 2.2.1 Исследование морфологии с помощью просвечивающего электронного микроскопа (ПЭМ)
[78] Тестовые порошки (образец L-NIBC-AuCs и образец L-NIBC-AuNPs) были растворены в сверхчистой воде до 2 мг/л в качестве образцов, а затем тестовые образцы были подготовлены методом висячей капли. Более конкретно, 5 мкл образцов капали на ультратонкую углеродную пленку, испаряли естественным образом до исчезновения капли воды, а затем наблюдали морфологию образцов с помощью полевой эмиссионной ПЭМ высокого разрешения JEM-2100F STEM/EDS.
[79] Четыре ПЭМ-изображения L-NIBC-AuNPs показаны на панелях B, E, H и K фиг. 1; три ПЭМ-изображения L-NIBC-AuCs показаны на панелях B, E и H фиг. 2.
[80] Изображения на фиг. 2 показывают, что каждый из образцов L-NIBC-AuCs имеет однородный размер частиц и хорошую дисперсность, а средний диаметр L-NIBC-AuCs (относится к диаметру золотого ядра) составляет 1,1 нм, 1,8 нм и 2,6 нм соответственно, что соответствует результатам на панелях C, F и I фиг. 2. Для сравнения образцы L-NIBC- AuNPs имеют больший размер частиц. Их средний диаметр (относится к диаметру золотого ядра) составляет 3,6 нм, 6,0 нм, 10,1 нм и 18,2 нм, соответственно, что полностью соответствует результатам на панелях C, F, I и L фиг. 1.
[81] 2.2.2 Ультрафиолетовые (УФ) - видимые (vis) спектры поглощения
[82] Тестовые порошки (образец L-NIBC-AuCs и образец L-NIBC-AuNPs) были растворены в сверхчистой воде до концентрации 10 мг·л-1, после чего при комнатной температуре были измерены спектры поглощения УФ-vis. Диапазон измерения составлял 190-1100 нм, кювета для образца представляла собой стандартную кварцевую ячейку с оптическим путем 1 см, а контрольная кювета была заполнена сверхчистой водой.
[83] УФ-vis спектры поглощения четырех образцов L-NIBC-AuNPs различных размеров показаны на панелях A, D, G и J на фиг. 1, а статистическое распределение размеров частиц показано на панелях C, F, I и L на фиг. 1; УФ-vis спектры поглощения трех образцов L-NIBC-AuCs различных размеров показаны на панелях A, D и G на фиг. 2, а статистическое распределение размеров частиц показано на панелях C, F и I на фиг. 2.
[84] На фиг. 1 показано, что благодаря эффекту поверхностного плазмона L-NIBC-AuNPs наблюдался пик поглощения при длине волны около 520 нм. Положение пика поглощения зависит от размера частиц. При размере частиц 3,6 нм УФ пик поглощения появляется при 516 нм; когда размер частиц составляет 6,0 нм, УФ пик поглощения появляется при 517 нм; когда размер частиц составляет 10,1 нм, УФ пик поглощения появляется при 520 нм, а когда размер частиц составляет 18,2 нм, пик поглощения появляется при 523 нм. Ни один из четырех образцов не имеет пика поглощения выше 560 нм.
[85] На фиг. 2 показано, что в УФ-спектрах поглощения трех образцов L-NIBC-AuCs с различными размерами частиц пик поглощения поверхностного плазмонного эффекта при 520 нм исчез, а два очевидных пика поглощения появились выше 560 нм, и положения пиков поглощения немного изменялись в зависимости от размеров частиц AuCs. Это объясняется тем, что AuCs проявляют молекулоподобные свойства из-за распада гранецентрированной кубической структуры, что приводит к разрыву в плотности соединений AuCs, расщеплению энергетического уровня, исчезновению эффекта плазмонного резонанса и появлению нового пика поглощения в длинноволновом направлении. Можно сделать вывод, что все три образца порошка с разным размером частиц, полученные выше, представляют собой AuCs, связанные с лигандами.
[86] 2.2.3 Инфракрасная спектроскопия с преобразованием Фурье
[87] Инфракрасные спектры измерялись на инфракрасном спектрометре с преобразованием Фурье VERTEX80V фирмы Bruker в режиме полного отражения в твердом порошке в высоком вакууме. Диапазон сканирования составляет 4000-400 см-1, число сканирований - 64. Для примера взяты образцы L-NIBC-AuCs, тестовые образцы
представляли собой сухой порошок L-NIBC-AuCs с тремя различными размерами частиц, а контрольный образец представлял собой чистый порошок L-NIBC. Результаты показаны на фиг. 3.
[88] На фиг. 3 показан инфракрасный спектр L-NIBC-AuCs с различными размерами частиц. По сравнению с чистым L-NIBC (кривая внизу), S-H валентные колебания L- NIBC-AuCs с различными размерами частиц полностью исчезли при 2500-2600 см-1, в то время как другие характерные пики L-NIBC по-прежнему наблюдались, что подтверждает, что молекулы L-NIBC были успешно связаны с поверхностью AuCs через связь Au-S. На фигуре также видно, что инфракрасный спектр AuCs, связанных с лигандами, не зависит от их размера.
[89] AuCs, связанные с другими лигандами, были получены способом, аналогичным описанному выше, за исключением того, что растворитель для раствора B, соотношение подачи между HAuCl4 и лигандом, время проведения реакции и количество добавленного NaBH4 были слегка скорректированы. Например, когда в качестве лиганда используют L- цистеин, D-цистеин, N-изобутирил-L-цистеин (L-NIBC) или N-изобутирил-D-цистеин (D- NIBC), в качестве растворителя выбирают уксусную кислоту; когда в качестве лиганда используют дипептид CR, дипептид RC или 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L- пролин, в качестве растворителя выбирают воду, и проч.; другие стадии аналогичны, поэтому дальнейшие сведения здесь не приводятся.
[90] В рамках настоящего изобретения вышеописанным способом была получена серия AuCs, связанных с лигандами. Лиганды и характеристики способа получения приведены в таблице 1.
[91] Таблица 1. Характеристики получения AuCs, связанных с различными лигандами, согласно настоящему изобретению
добавлени
и после
кислота
кислота
цистеина
(0.1~100)
цистеинсодержащие олигопептиды
диол-1-оксопропил]- L-пролин
кислота
кислота
меркаптопропионил)- глицин
(CSH)
меркаптопропионовая кислота (MPA)
кислота (p-MBA)
тиолсодержащие соединения
[92] Образцы, перечисленные в таблице 1, были получены вышеуказанными способами. Характеристики одиннадцати (11) различных AuCs, связанных с лигандами, показаны на фиг. 4 (CR-AuCs), на фиг. 5 (RC-AuCs), на фиг. 6 (Cap-AuCs) (Cap обозначает 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L-пролин), на фиг. 7 (GSH-AuCs), на фиг. 8 (D-NIBC-AuCs), на фиг. 9 (L-Cys-AuCs), на фиг. 10 (CSH-AuCs), на фиг. 11 (MPA-AuCs), на фиг. 12 (p-MBA- AuCs), на фиг. 13 (CDEVD-AuCs) и на фиг. 13 (DEVDC-AuCs). На фиг. 4-12 показаны УФ- спектры (панель А), инфракрасные спектры (панель В), ПЭМ-изображения (панель С) и распределение частиц по размерам (панель D). На фиг. 13 и 14 показаны УФ-спектры (панель А), ПЭМ-изображения (панель В) и распределение частиц по размерам (панель С).
[93] Результаты показывают, что диаметры AuCs, связанных с различными лигандами, полученными в таблице 1, составляют менее 3 нм. Ультрафиолетовые спектры также показывают исчезновение пика при 520±20 нм и появление пика поглощения в других положениях. Положение пика поглощения может меняться в зависимости от лигандов и размеров частиц, равно как и от структуры. В определенных случаях пик поглощения отсутствует, в основном из-за образования смесей AuCs с различными размерами и структурами частиц или некоторых специальных AuCs, которые перемещают положение пика поглощения за пределы УФ-vis спектра. Между тем инфракрасные спектры с преобразованием Фурье также показывают исчезновение инфракрасного пика поглощения лиганда тиола (между пунктирными линиями на панели B на фиг. 4-8), в то время как другие инфракрасные характеристические пики сохраняются, предположительно потому, что все молекулы лиганда были успешно связаны с атомами золота для образования AuCs, связанных с лигандами, и в настоящем изобретении успешно были получены AuCs, связанные с лигандами, перечисленными в таблице 1.
[94] Вариант осуществления 3. Проведение исследования ишемического церебрального инсульта на животной модели
[95] 3.1 Тестовые образцы
[96] Кластеры золота:
[97] A1: кластеры золота, связанные с лигандом L-NIBC (L-NIBC-AuCs), распределение по размерам в диапазоне 0,5-3,0 нм;
[98] A2: кластеры золота, связанные с лигандом L-цистеином (L-Cys-AuCs), распределение по размерам в диапазоне 0,5-3,0 нм;
[99] A3: кластеры золота, связанные с лигандом N-ацетил-L-цистеином (L-NAC-AuCs), распределение по размерам в диапазоне 0,5-3,0 нм; и
[100] A4: кластеры золота, связанные с лигандом DEVDC (DEVDC-AuCs), распределение по размерам в диапазоне 0,5-3,0 нм.
[101] Наночастицы золота:
[102] B1: наночастицы золота, связанные с L-NIBC (L-NIBC-AuNPs), диапазон распределения по размерам 6,1±1,5 нм; и
[103] B2: наночастицы золота, связанные с L-NAC (L-NAC-AuNPs), диапазон распределения по размерам 9,0±2,4 нм.
[104] Все тестовые образцы были получены в соответствии с описанным выше способом с небольшими изменениями, и их качество было оценено с помощью описанных выше способов.
[105] 3.2 Протоколы исследований
[106] 3.2.1 Создание модели окклюзии средней мозговой артерии (ОСМА) у крыс и введение исследуемых веществ
[107] Самцы крыс Sprague Dawley (SD) класса SPF (220-260 г) были приобретены у Shanghai Shrek Experimental Animal Co., Ltd. Все крысы прошли 7-дневный период адаптации к условиям окружающей среды перед началом исследования. Крысы были случайным образом разделены на 14 групп (n=10), включая группу плацебо, группу модельного контроля, группу низкой (2 мг/кг массы тела крысы) и высокой дозировок (10 мг/кг массы тела крысы) препаратов кластера золота A1, A2, A3 и A4, а также группу низкой (2 мг/кг массы тела крысы) и высокой дозировки (10 мг/кг массы тела крысы) наночастиц золота B1 и B2. В день проведения исследования крысам вводили в качестве наркоза 10% хлоралгидрат (350 мг/кг массы тела). Правая общая сонная артерия, внутренняя сонная артерия и наружная сонная артерия были открыты через срединный разрез. Во внутреннюю сонную артерию (ВСА) вводили шов на 18 мм ± 0,5 мм через наружную сонную артерию (НСА), пока не блокировалось регионарное кровоснабжение СМА, что приводило к церебральному инфаркту. Через 1,5 ч шов снимали до входа в ВСА для реперфузии. Показатели мозгового кровообращения (CBF) до операции и после эмболизации измеряли с помощью флоуметра. Животные, у которых CBF постоянно снижались (rCBF ≥ 70%), считались результативной моделью окклюзии средней мозговой артерии (ОСМА). После реперфузии крысам внутрибрюшинно вводили лекарства или растворители (физиологический раствор) в течение 0 ч, 24 ч, 48 ч и 72 ч соответственно. Неврологические показатели поведения оценивались через 0, 24, 48, 72 и 96 часов. Исследование было прекращено через 96 часов после проведения операции. Забор образцов мозга и окрашивание TTC проводили после эвтаназии. Были сделаны снимки срезов мозга и рассчитан процент площади церебрального инфаркта.
[108] 3.2.2 Оценка неврологических показателей
[109] 0 баллов: нет отличий от обычных крыс; 1 балл: разгибание правой передней лапы не прямое, голова запрокидывается на противоположную сторону; 2 балла: ходьба прерывистыми кругами на открытом пространстве; 3 балла: ходьба непрерывными кругами на открытом пространстве; 4 балла: потеря сознания при ходьбе, заваливание на одну сторону; 5 баллов: смерть.
[110] 3.2.3 Область поражения головного мозга (окрашивание TTC)
[111] Крысам проводили эвтаназию посредством ингаляции углекислого газа. Мозг извлекали и помещали в ванночку для коронального среза (2 мм). Окрашивание проводили 2% TTC в темноте при комнатной температуре. После фотографирования площадь поражения головного мозга измеряли с помощью программы ImageJ. Процент площади поражения мозга (%) = (площадь контралатерального полушария - (площадь ипсилатерального полушария - площадь поражения мозга)) / площадь контралатерального полушария × 100%.
[112] 3.2.4 Статистический анализ
[113] Статистический анализ проводился с помощью программы Graph Pad Prism Software 7.0 (Калифорния, США). Данные были выражены как среднее ± статистическая ошибка, статистический анализ проводился с помощью теста Даннетта. P < 0,05 означает статистическую значимость.
[114] 3.3 Результаты
[115] 3.3.1 Мозговое кровообращение в зоне ишемического поражения головного мозга
[116] Снижение мозгового кровообращения у крыс более чем на 70% (снижение мозгового кровообращения, rCBF≥70%) свидетельствует об успешном создании модели ОСМА. Во всех остальных группах, за исключением группы плацебо, показатель rCBF был более 70%, в среднем около 80%, что свидетельствует об успешном создании модели ОСМА.
[117] 3.3.2 Влияние исследуемых препаратов на неврологические показатели у крыс
[118] На фиг. 15 показана оценка неврологических показателей у крыс в каждой группе (на гистограмме в каждой временной точке слева направо: группа плацебо (пустая), группа модельного контроля, группа A1 с низкой дозировкой, группа A1 с высокой дозировкой, группа A2 с низкой дозировкой, группа A2 с высокой дозировкой, группа A3 с низкой дозировкой, группа A3 с высокой дозировкой, группа A4 с низкой дозировкой, группа A4 с высокой дозировкой, группа B1 с низкой дозировкой, группа B1 с высокой дозировкой, группа B2 с низкой дозировкой и группа B2 с высокой дозировкой). У крыс в группе плацебо были обычные неврологические показатели, и оценка результатов была равна 0;
крысы в группе модельного контроля показали серьезные поведенческие функциональные дефекты через 0 ч, 24 ч, 48 ч, 72 ч и 96 ч после операции (по сравнению с группой плацебо, P<0,001, ###). По сравнению с контрольной группой неврологические показатели в группах A1, A2, A3, A4 с низкой дозировкой и группах с высокой дозировкой не имели значительного улучшения через 24 часа после проведения операции. Через 48 часов после операции неврологические показатели в группах A1, A2, A3 и A4 с низкой дозировкой и группах с высокой дозировкой начали снижаться, но статистической разницы не было (по сравнению с контрольной группой, P > 0,05). Через 72 часа после операции неврологические показатели у животных, получавших четыре вида препаратов, еще больше снизились, причем у группы A1 с низкой дозировкой, группы A1 с высокой дозировкой и группы A2 с высокой дозировкой наблюдались значительные различия (по сравнению с контрольной группой, P < 0,05, *). Через 96 часов после операции наблюдались значительные различия для всех групп с низкими дозировками и групп с высокими дозировками указанных четырех препаратов (по сравнению с контрольной группой, P < 0,05, *). Данные результаты свидетельствуют о том, что все четыре препарата кластера золота могут значительно улучшить неврологические показатели после поражения головного мозга, вызванного ишемическим инсультом, и этот эффект в определенной степени зависит от дозировки.
[119] По сравнению с контрольной модельной группой в группах с низкой и высокой дозировками наночастиц золота B1 и B2 не наблюдалось значительного улучшения неврологических показателей у модельных крыс MACO через 24 ч, 48 ч, 72 ч и 96 ч после операции, что указывает на то, что наночастицы золота не могут в значительной степени восстановить поведенческие функции, вызванные ишемическим церебральным инсультом.
[120] 3.3.3.3 Влияние каждого из препаратов на площадь поражения головного мозга у модельных крыс MACO
[121] На фиг. 16 показан процент площади поражения головного мозга крыс в каждой группе (на гистограмме слева направо: группа плацебо (пустая), группа модельного контроля, группа A1 с низкой дозировкой, группа A1 с высокой дозировкой, группа A2 с низкой дозировкой, группа A2 с высокой дозировкой, группа A3 с низкой дозировкой, группа A3 с высокой дозировкой, группа A4 с низкой дозировкой, группа A4 с высокой дозировкой, группа B1 с низкой дозировкой, группа B1 с высокой дозировкой, группа B2 с низкой дозировкой и группа B2 с высокой дозировкой). В группе плацебо мозговая ткань была в норме, инфаркта не наблюдалось; площадь очага поражения составила 0%.
Площадь поражения головного мозга в группе модельного контроля составила 44,7% ± 4,5% (P < 0,001, ###). По сравнению с контрольной группой процент площади поражения головного мозга в группах A1, A2, A3, A4 с низкой и высокой дозировками явно снизился, но в группах с низкой дозировкой существенной разницы не было, в то время как в группах с высокой дозировкой была обнаружена существенная разница (по сравнению с контрольной группой, P < 0,05, *). Если взять в качестве примера группу A1, то площадь очага поражения в группе с низкой дозировкой уменьшилась с 44,7 ± 4,5% до 36,0 ± 4,0% (по сравнению с контрольной группой, P > 0,05), а в группе с высокой дозировкой уменьшилась до 27,8 ± 3,4% (по сравнению с контрольной группой, P < 0,05, *).
[122] На фиг. 17 показаны примерные изображения окрашивания TTC тканей головного мозга крыс с ОСМА после введения препаратов кластеров золота, представленных группой А1, и наночастиц золота, представленных группой В1. На фиг. 17, (1) группа плацебо; (2) группа модельного контроля; (3) группа A1 с низкой дозировкой; (4) группа A1 с высокой дозировкой; (5) группа B1 с низкой дозировкой; (6) группа B1 с высокой дозировкой. Как видно на фиг. 17, у крыс в группе плацебо не развился инфаркт головного мозга, в то время как в группе модельного контроля наблюдался обширный инфаркт головного мозга (белая часть фигуры справа). Площадь поражения головного мозга после введения низкой дозировки препарата группе A1 уменьшилась (белая часть справа уменьшилась), в то же время площадь поражения головного мозга значительно уменьшилась при введении высокой дозировки препарата A1 (белая часть справа значительно уменьшилась), в то время как введение низкой и высокой дозировки препарата B1 не оказало никакого влияния на площадь поражения головного мозга (белая часть справа не уменьшилась). Группы A2, A3 и A4 показали сходный с A1 эффект в уменьшении площади очага поражения, в то время как результат в группе B2 был схож с группой B1: площадь очага поражения не уменьшилась.
[123] Другие AuCs, связанные с лигандами, оказывают аналогичное действие при лечении ишемического церебрального инсульта, но их действие варьируется в определенных пределах. В данном разделе они не будут описаны подробно.
[124] Вариант осуществления 4. Исследования геморрагического церебрального инсульта на модельных животных
[125] 4.1 Регент
[126] Кластеры золота, связанные с лигандом L-цистеин (L-Cys-AuCs), распределение частиц по размерам в диапазоне 0,5-3,0 нм; наночастицы золота, связанные с L-NIBC (L- NIBC-AuNPs), распределение частиц по размерам в диапазоне 6,1±1,5 нм.
[127] 4.2 Протокол исследования и результаты
[128] Крысам вводят анестезию и помещают в стереотаксическую рамку. В день 0 коллагеназу типа VII стереотаксически вводили в правый стриатум (координаты: 0,0 мм рострально и 3,0 мм латерально от брегмы, 5,5 мм ниже черепа) со скоростью 0,4 мкл/мин в течение 5 мин. Исследуемые препараты вводятся внутривенно с 0 по 4 день в дозировке 10 мг/кг веса крысы. Локомоция оценивалась на третий день. На четвертый день крыс умерщвляют и проводят анализ и гистохимическое окрашивание. Исследуемый препарат AuCs и наночастицы золота показали схожие результаты при геморрагическом церебральном инсульте, что указывает на отсутствие явного терапевтического эффекта.
[129] Несмотря на то, что настоящее изобретение было раскрыто с указанием конкретных вариантов осуществления, предполагается, что варианты осуществления являются иллюстративными и объем изобретения не ограничивают. Альтернативные варианты осуществления настоящего изобретения будут очевидны тем, кто обладает обычными навыками в области, к которой относится настоящее изобретение. Такие альтернативные варианты осуществления считаются включенными в объем настоящего изобретения. Соответственно, объем настоящего изобретения определяется прилагаемой формулой изобретения и подтверждается приведенным выше описанием.
Ссылки
Amani H., Mostafavi E., Mahmoud Reza Alebouyeh M.R., Arzaghi H., Akbarzadeh A., Pazoki- Toroudi H., Webster T.J. Would Colloidal Gold Nanocarriers Present An Effective Diagnosis Or Treatment For Ischemic Stroke? Int J Nanomedicine. 2019 Oct 7;14:8013-8031.
Zheng Y., Wu Y., Liu Y., Guo Z., Bai T., Zhou P., Wu J., Yang Q., Liu Z., Lu X. Intrinsic Effects of Gold Nanoparticles on Oxygen-Glucose Deprivation/Reperfusion Injury in Rat Cortical Neurons. Neurochem Res. 2019 Jul;44(7):1549-1566.
Изобретение относится к области лечения заболеваний головного мозга. Раскрыто применение кластера золота, связанного с лигандом, для лечения ишемического церебрального инсульта у субъекта, где кластер золота, связанный с лигандом, содержит золотое ядро и лиганд, связанный с золотым ядром, при этом золотое ядро имеет диаметр в диапазоне 0,5-3 нм; лиганд представляет собой один, выбранный из группы, состоящей из L-цистеина и его производных, D-цистеина и его производных, цистеинсодержащих олигопептидов и их производных и других тиолсодержащих соединений; L-цистеин и его производные выбраны из группы, состоящей из L-цистеина, N-изобутирил-L-цистеина (L-NIBC) и N-ацетил-L-цистеина (L-NAC), и где D-цистеин и его производные выбраны из группы, состоящей из D-цистеина, N-изобутирил-D-цистеина (D-NIBC) и N-ацетил-D-цистеина (D-NAC); цистеинсодержащие олигопептиды и их производные представляют собой цистеинсодержащие дипептиды, цистеинсодержащие трипептиды, цистеинсодержащие тетрапептиды или цистеинсодержащие пентапептиды; и где другие тиолсодержащие соединения выбраны из группы, состоящей из 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L(D)-пролина, тиогликолевой кислоты, меркаптоэтанола, тиофенола, D-3-троловола, N-(2-меркаптопропионил)-глицина, додецилмеркаптана, 2-аминоэтанэтиола (CSH), 3-меркаптопропионовой кислоты (MPA) и 4-меркаптобеновой кислоты (p-MBA). Изобретение обеспечивает применение кластера золота в лечении ишемического церебрального инсульта. 5 з.п. ф-лы, 17 ил., 1 табл., 4 пр.
1. Применение кластера золота, связанного с лигандом, для лечения ишемического церебрального инсульта у субъекта, где кластер золота, связанный с лигандом, содержит:
золотое ядро; и
лиганд, связанный с золотым ядром;
при этом золотое ядро имеет диаметр в диапазоне 0,5-3 нм;
где лиганд представляет собой один, выбранный из группы, состоящей из L-цистеина и его производных, D-цистеина и его производных, цистеинсодержащих олигопептидов и их производных и других тиолсодержащих соединений;
L-цистеин и его производные выбраны из группы, состоящей из L-цистеина, N-изобутирил-L-цистеина (L-NIBC) и N-ацетил-L-цистеина (L-NAC), и где D-цистеин и его производные выбраны из группы, состоящей из D-цистеина, N-изобутирил-D-цистеина (D-NIBC) и N-ацетил-D-цистеина (D-NAC);
цистеинсодержащие олигопептиды и их производные представляют собой цистеинсодержащие дипептиды, цистеинсодержащие трипептиды, цистеинсодержащие тетрапептиды или цистеинсодержащие пентапептиды;
и где другие тиолсодержащие соединения выбраны из группы, состоящей из 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L(D)-пролина, тиогликолевой кислоты, меркаптоэтанола, тиофенола, D-3-троловола, N-(2-меркаптопропионил)-глицина, додецилмеркаптана, 2-аминоэтанэтиола (CSH), 3-меркаптопропионовой кислоты (MPA) и 4-меркаптобеновой кислоты (p-MBA).
2. Применение по п. 1, где золотое ядро имеет диаметр в интервале 0,5-2,6 нм.
3. Применение по п. 1, где цистеинсодержащие дипептиды выбраны из группы, состоящей из L(D)-цистеин-L(D)-аргинин дипептида (CR), L(D)-аргинин-L(D)-цистеин дипептида (RC), L(D)-гистидин-L(D)-цистеин дипептида (HC) и L(D)-цистеин-L(D)-гистидин дипептида (CH).
4. Применение по п. 1, где цистеинсодержащие трипептиды выбраны из группы, состоящей из глицин-L(D)-цистеин-L(D)-аргинин трипептида (GCR), L(D)-пролин-L(D)-цистеин-L(D)-аргинин трипептида (PCR), L(D)-лизин-L(D)-цистеин-L(D)-пролин трипептида (KCP) и L(D)-глутатиона (GSH).
5. Применение по п. 1, где цистеинсодержащие тетрапептиды выбраны из группы, состоящей из глицин-L(D)-серин-L(D)-цистеин-L(D)-аргининового тетрапептида (GSCR) и глицин-L(D)-цистеин-L(D)-серин-L(D)-аргининового тетрапептида (GCSR).
6. Применение по п. 1, где цистеинсодержащие пентапептиды выбраны из группы, состоящей из цистеинил-аспарагинил-глутаминил-валинил-аспарагина (CDEVD) и аспаргинил-глутаминил-валинил-аспарагинил-цистеина (DEVDC).
| CN 111035653 А, 21.04.2020 | |||
| US 20190175753 A1, 13.06.2019 | |||
| НОВЫЕ НАНОКРИСТАЛЛЫ НА ОСНОВЕ ЗОЛОТА ДЛЯ ТЕРАПЕВТИЧЕСКОГО ЛЕЧЕНИЯ И ПРОЦЕССЫ ИХ ЭЛЕКТРОХИМИЧЕСКОГО ПРОИЗВОДСТВА | 2010 |
|
RU2568850C2 |
| GAO G | |||
| et al | |||
| Gold nanoclusters for Parkinson's disease treatment // Biomaterials, 2019, V | |||
| Кран машиниста для автоматических тормозов с сжатым воздухом | 1921 |
|
SU194A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| ВЕРЕЩАГИНА Я.А | |||
| Физическая химия наноматериалов // Казанский федеральный университет, Казань, 2016, стр | |||
| Способ получения камфоры | 1921 |
|
SU119A1 |
| ХОЛОДОВ Л.Е | |||
| и др | |||
| Клиническая | |||
Авторы
Даты
2024-07-03—Публикация
2020-11-27—Подача