ОБЛАСТЬ ТЕХНИКИ
1. Настоящее изобретение относится к области лечения цирроза печени, в частности, к кластерам золота (AuCs), связанным с лигандами, композициям, включающим AuCs, связанные лигандами, и способам, использующим AuCs, связанные с лигандами, для лечения цирроза печени.
УРОВЕНЬ ТЕХНИКИ
2. Печень - самый большой твердый орган человеческого тела, выполняющий множество важных функций, включая: производство белков крови, которые помогают свертыванию, переносу кислорода и иммунной системе; хранение избыточных питательных веществ и возвращение части питательных веществ в кровь; производство желчи для переваривания пищи; помощь организму в хранении сахара (глюкозы) в виде гликогена; очищение организма от вредных веществ в крови, включая наркотики и алкоголь; расщепление насыщенных жиров и производство холестерина.
3. Цирроз печени - это медленно прогрессирующее заболевание, развивающееся в течение многих лет вследствие длительного, непрерывного повреждения печени. Вместе с развитием цирроза печени здоровая ткань печени постепенно разрушается и заменяется рубцовой тканью. Рубцовая ткань блокирует кровоток через печень и замедляет способность печени перерабатывать питательные вещества, гормоны, лекарства и естественные токсины. Она также снижает выработку белков и других веществ, производимых печенью. Цирроз может в конечном итоге привести к печеночной недостаточности, что может потребовать пересадки печени, и/или раку печени.
4. На ранней стадии цирроза печени нет явных симптомов из-за сильной компенсаторной функции печени. На поздней стадии симптомы включают нарушение функции печени, портальную гипертензию, кровотечения в верхних отделах желудочно-кишечного тракта, печеночную энцефалопатию, вторичную инфекцию, гиперфункцию селезенки, асцит, рак и другие осложнения. Цирроз печени возникает в результате постепенной деформации и затвердения печени. Гистопатологически цирроз печени характеризуется обширным некрозом печеночных клеток, узелковым перерождением остаточных гепатоцитов, гиперплазией соединительной ткани и формированием фиброзных перегородок, что приводит к разрушению дольковой структуры печени и образованию псевдолобул.
5. Цирроз печени имеет разные причины. У некоторых людей с циррозом печени имеется более одной причины поражения печени. К распространенным причинам цирроза печени относятся длительное злоупотребление алкоголем, хронический гепатит В и С, жировая болезнь печени, токсичные металлы, генетические заболевания, нарушения питания, промышленные яды, наркотики, нарушения кровообращения, нарушения обмена веществ, холестаз, шистосомоз и др.
6. Цирроз печени может быть диагностирован с помощью многих тестов/методов. Например, анализ крови может свидетельствовать о циррозе печени, если уровень ферментов печени, включая аланиновую трансаминазу (ALT), аспартатаминотрансаминазу (AST) и щелочную фосфатазу (ALP), а также билирубина повышен, а уровень белков крови понижен.
7. В настоящее время, хотя лечение может задержать прогрессирование цирроза печени путем устранения его причин, специфических способов лечения цирроза печени не существует.
РАСКРЫТИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
8. Настоящее изобретение раскрывает применение кластеров золота, связанных с лигандами, для лечения цирроза печени у субъекта и способ лечения цирроза печени у субъекта с помощью кластеров золота, связанных с лигандами.
9. В некоторых вариантах осуществления настоящего изобретения для лечения цирроза печени у субъекта используется кластер золота, связанный с лигандами, где кластер золота, связанный с лигандами, включает золотое ядро и лиганд, связанный с золотым ядром.
10. В некоторых вариантах осуществления применения для лечения золотое ядро имеет диаметр в интервале 0,5-3 нм. В некоторых вариантах осуществления изобретения золотое ядро имеет диаметр в интервале 0,5-2,6 нм.
11. В некоторых вариантах осуществления применения для лечения лиганд представляет собой выбранный из группы, состоящей из L-цистеина и его производных, D-цистеина и его производных, цистеинсодержащих олигопептидов и их производных и других тиолсодержащих соединений.
12. В некоторых вариантах осуществления применения ля лечения L-цистеин и его производные выбирают из группы, состоящей из L-цистеина, N-изобутирил-L-цистеина (L-NIBC) и N-ацетил-L-цистеина (L-NAC), а D-цистеин и его производные выбирают из группы, состоящей из D-цистеина, N-изобутирил-D-цистеина (D-NIBC) и N-ацетил-D-цистеина (D-NAC).
13. В некоторых вариантах осуществления применения для лечения цистеинсодержащие олигопептиды и их производные представляют собой цистеинсодержащие дипептиды, цистеинсодержащие трипептиды или цистеинсодержащие тетрапептиды.
14. В некоторых вариантах осуществления применения для лечения цистеинсодержащие дипептиды выбирают из группы, состоящей из L(D)-цисте ил-L(D)-аргинин дипептида (CR), L(D)-аргинил-L(D)-цистеин дипептида (RC), L(D)-гистидил-L(D)-цистеин дипептида (НС) и L(D)-цистеил-L(D)-гистидин дипептида (СН).
15. В некоторых вариантах осуществления применения для лечения цистеинсодержащие трипептиды выбирают из группы, состоящей из глицил-L(D)-цистеил-L(D)-аргинин трипептида (GCR), L(D)-пролил-L(D)-цистеил-L(D)-аргинин трипептид (PCR), L(D)-лизил-L(D)-цистеил-L(D)-пролин трипептид (КСР) и L(D) -глутатиона (GSH).
16. В некоторых вариантах осуществления применения цистеинсодержащие тетрапептиды выбирают из группы, состоящей из глицил-L(D)-серил-L(D)-цистеил-L(D)-аргинин тетрапептида (GSCR) и глицил-L(D)-цистеил-L(D)-серил-L(D)-аргинин тетрапептида (GCSR).
17. В некоторых вариантах осуществления применения другие тиолсодержащие соединения выбирают из группы, состоящей из 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L(D)-пролина, тиогликолевой кислоты, меркаптоэтанола, тиофенола, D-3-троловола, N-(2-меркаптопропионил)-глицина и додецилмеркаптана.
18. Цели и преимущества изобретения станут очевидны из следующего подробного описания предпочтительных вариантов его осуществления в связи с прилагаемыми чертежами.
ОПИСАНИЕ ЧЕРТЕЖЕЙ
19. Предпочтительные варианты осуществления настоящего изобретения теперь будут описаны со ссылкой на Фигуры, на которых одинаковые номера позиций обозначают одинаковые элементы.
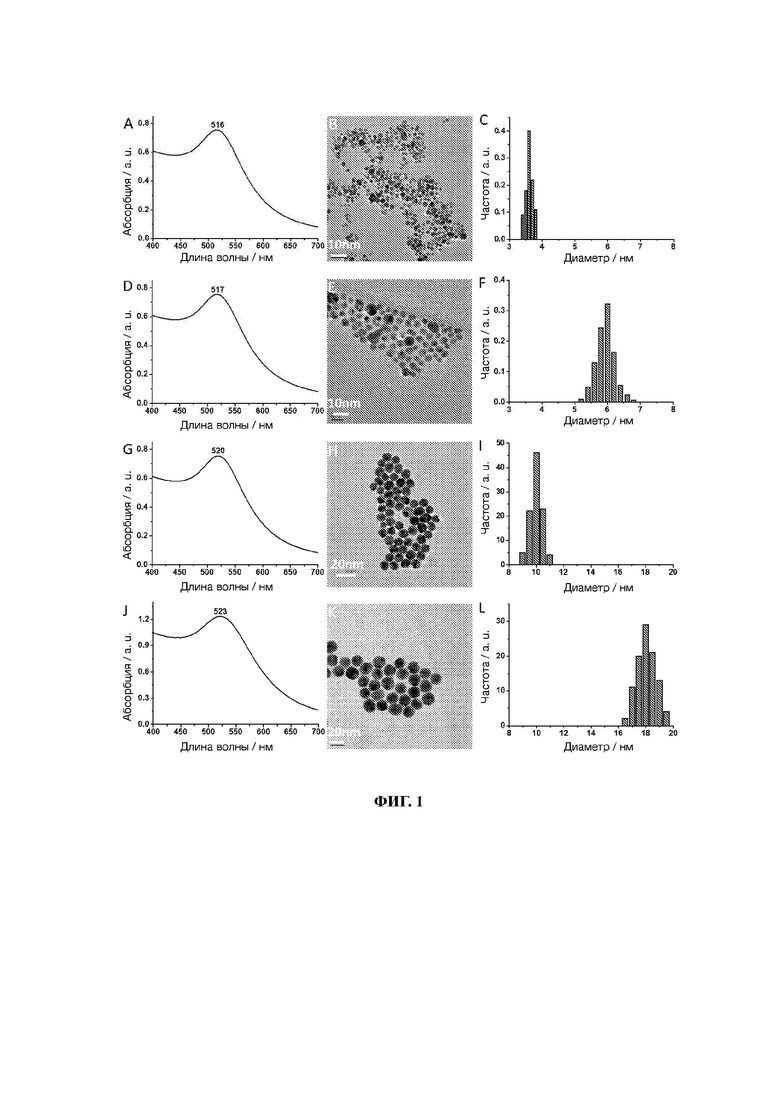
20. На фиг. 1 показаны ультрафиолетовые (УФ) спектры изображения просвечивающего электронного микроскопа (ПЭМ) и диаграммы распределения частиц по размерам наночастиц золота, модифицированных лигандом L-NIBC (L-NIBC-AuNPs) с различными размерами частиц.
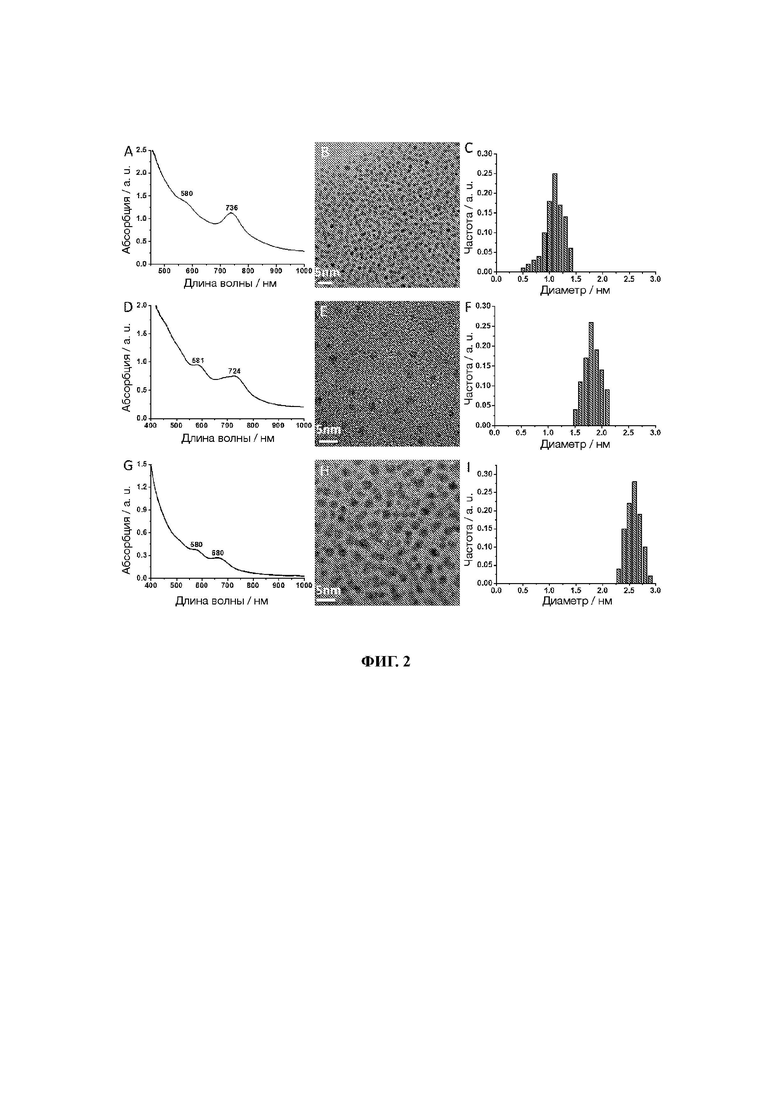
21. На фиг. 2 показаны ультрафиолетовые (УФ) спектры изображения ПЭМ и диаграммы распределения частиц по размерам кластеров золота, связанных с лигандом L-NIBC (L-NIBC-AuCs), с различными размерами частиц.
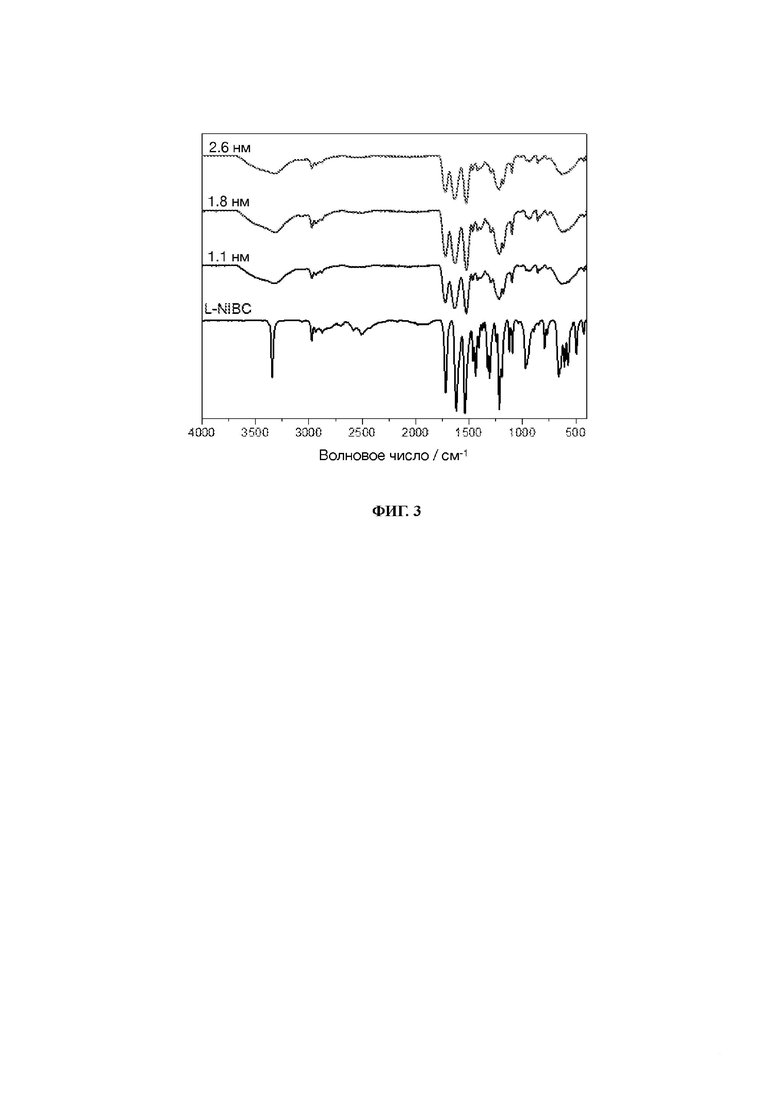
22. На фиг. 3 показаны инфракрасные спектры L-NIBC-AuCs с различными размерами частиц.
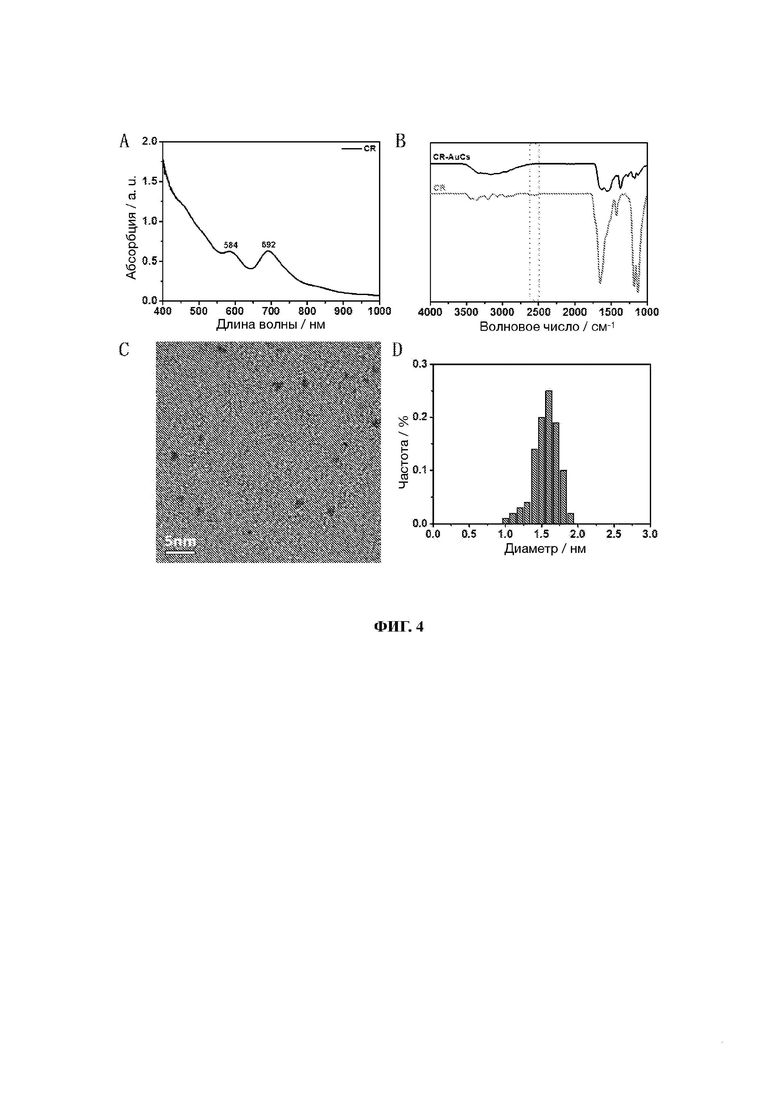
23. На фиг. 4 показаны диаграммы УФ, ИК, ПЭМ и распределения частиц по размерам кластеров золота, связанных с лигандом CR (CR-AuCs).
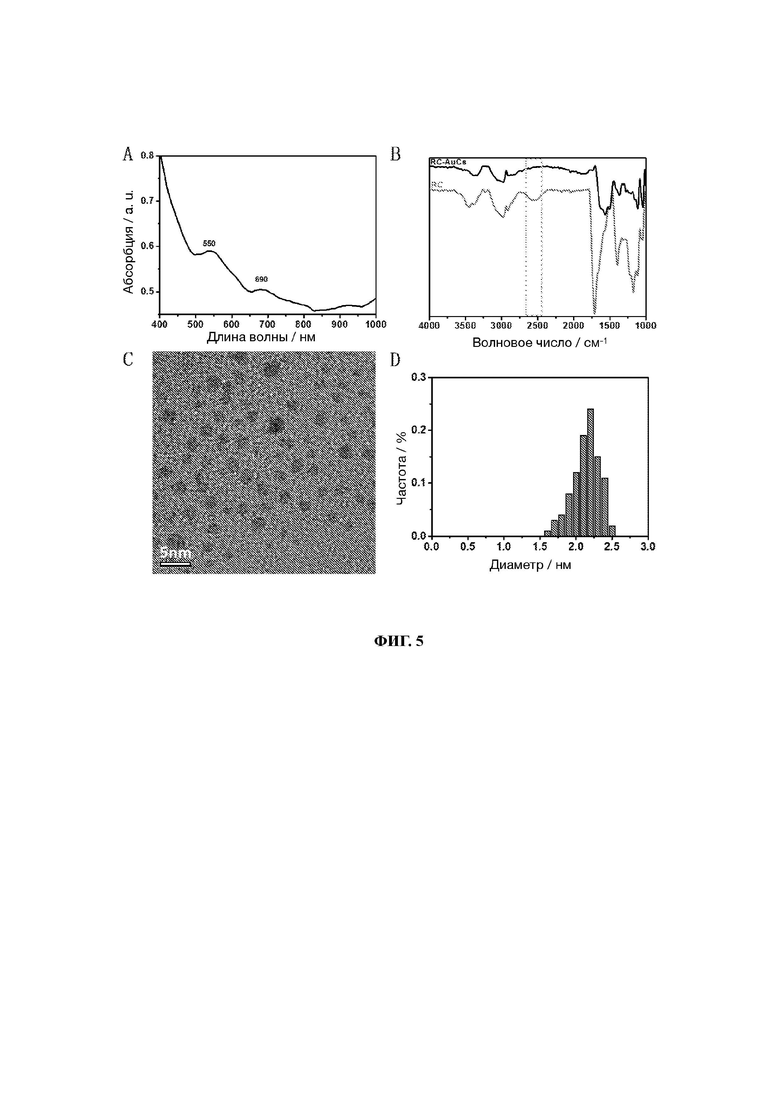
24. На фиг. 5 показаны диаграммы УФ, ИК, ПЭМ и распределения частиц по размерам кластеров золота, связанных с лигандом RC (RC-AuCs).
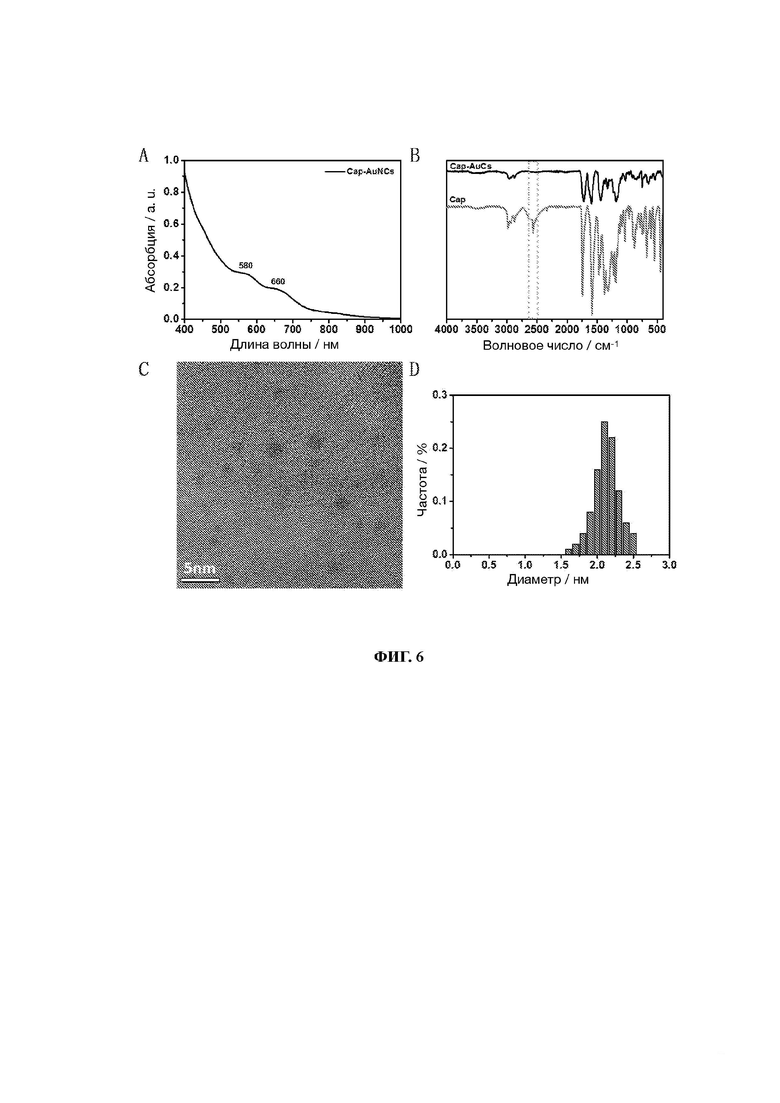
25. На фиг. 6 показаны диаграммы УФ, ИК, ПЭМ и распределения частиц по размерам кластеров золота, связанных с лигандом 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L-пролина (т.е. Cap) (Cap-AuCs).
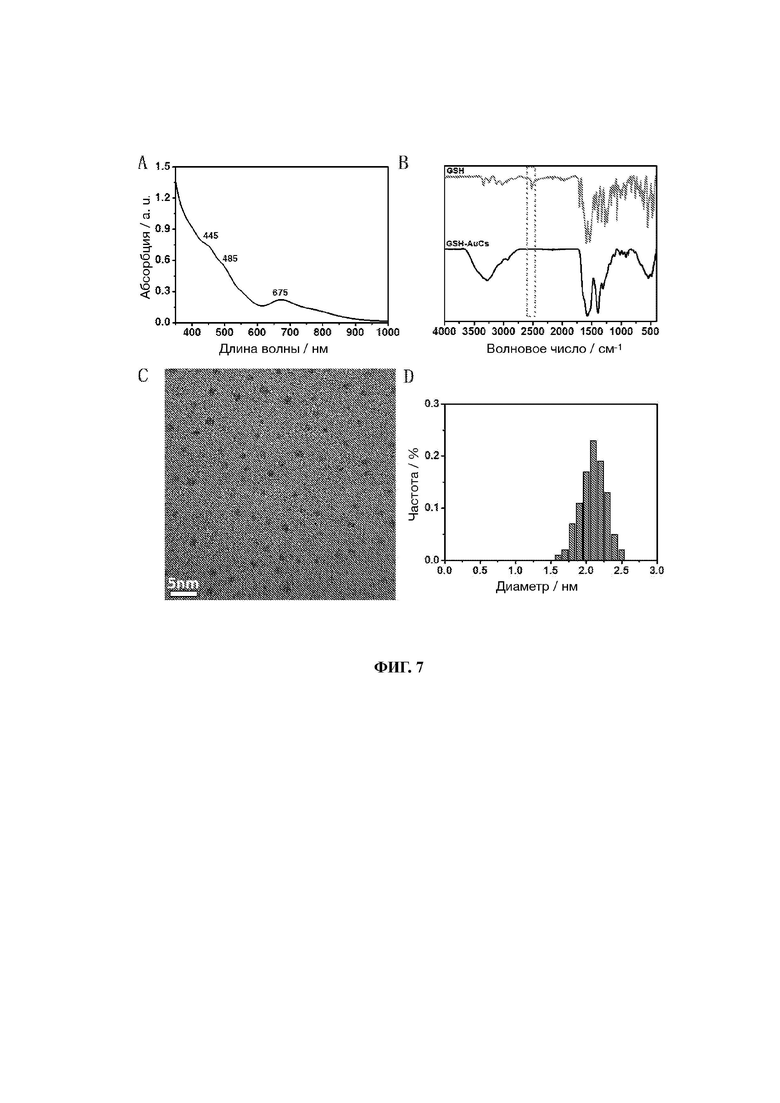
26. На ФИГ. 7 показаны диаграммы УФ, ИК, ПЭМ и распределения частиц по размерам кластеров золота, связанных с лигандом GSH (GSH-AuCs).
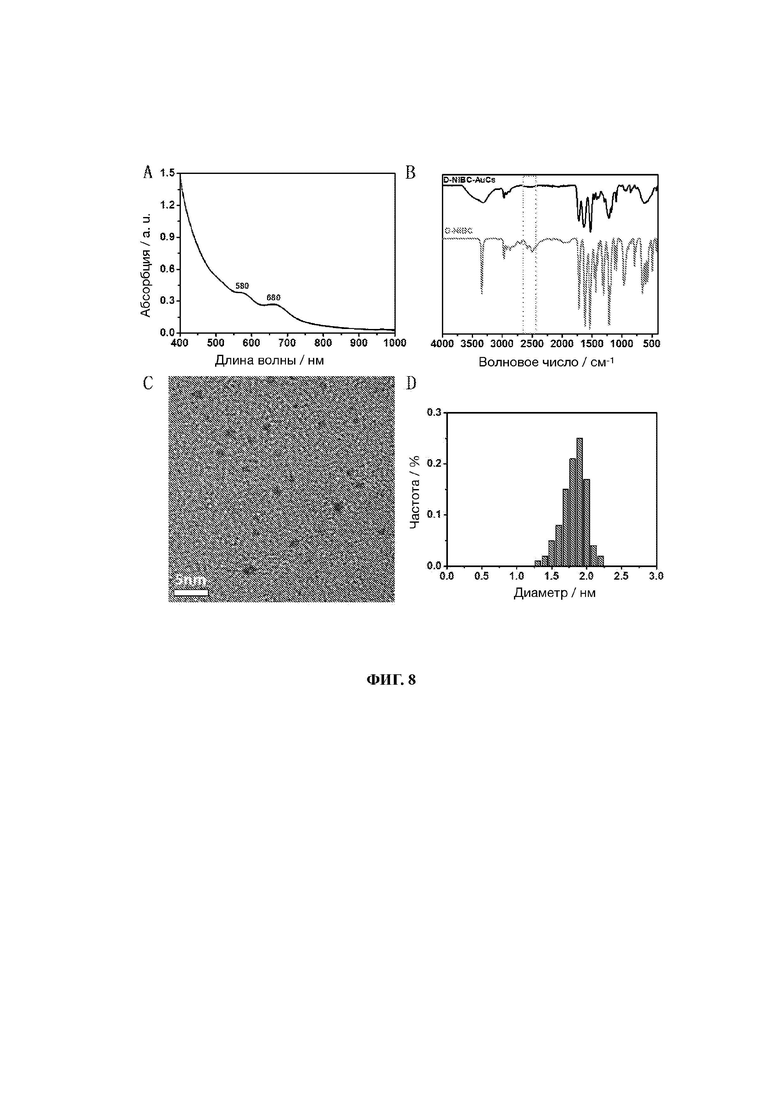
27. На фиг. 8 показаны диаграммы УФ, ИК, ПЭМ и распределения частиц по размерам кластеров золота, связанных с лигандом D-NIBC (D-NIBC-AuCs).
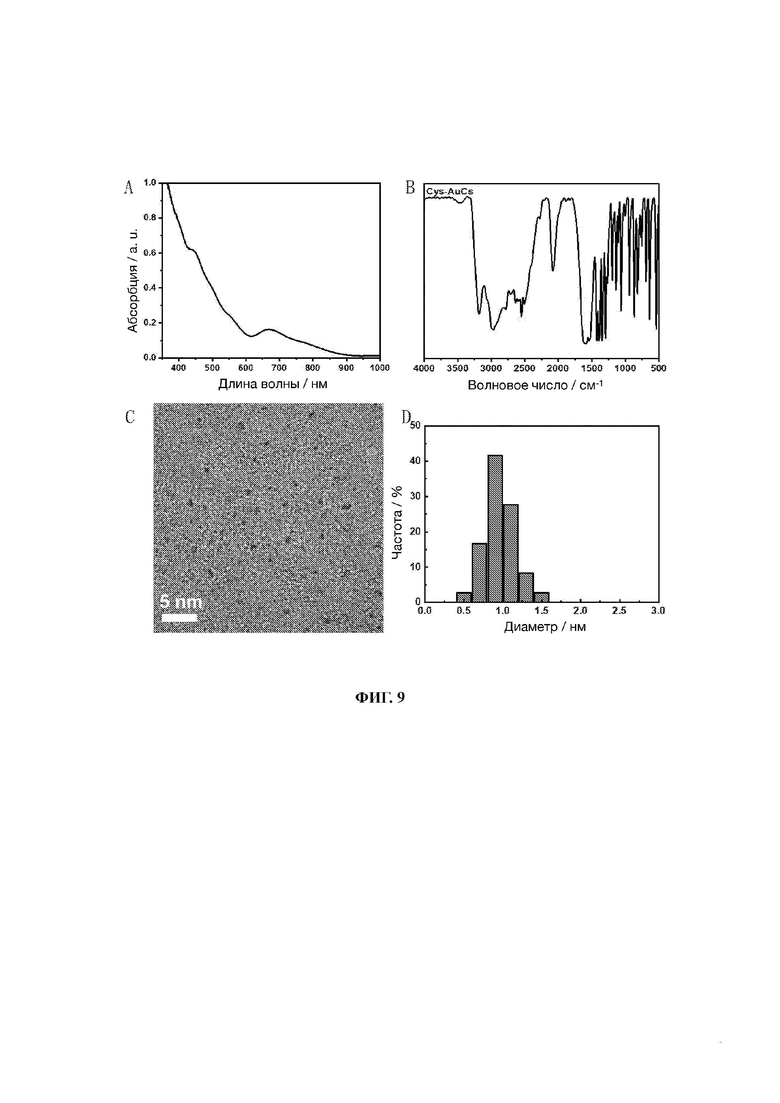
28. На фиг. 9 показаны диаграммы УФ, ИК, ПЭМ и распределения частиц по размерам кластеров золота, связанных с лигандом L-цистеином (L-Cys-AuCs).
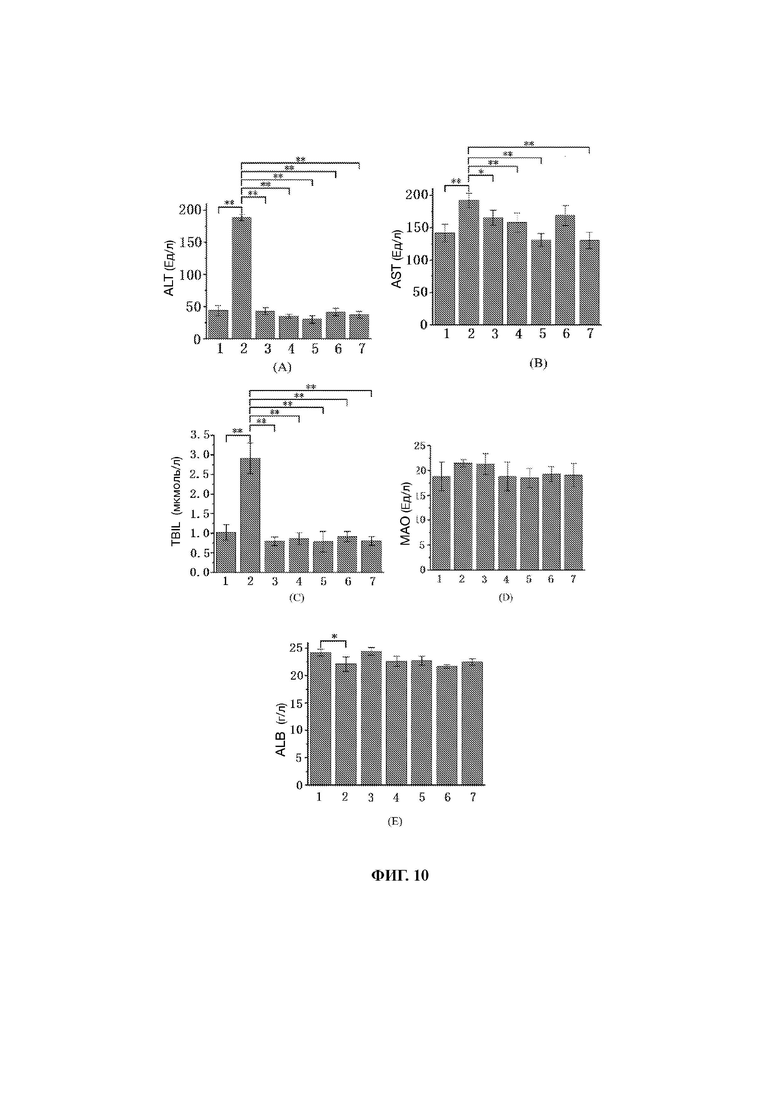
29. На фиг. 10 представлены гистограммы, показывающие влияние различных доз А-01 и А-02 на уровни (A) ALT, (В) AST, (С) TBIL, (D) МАО и (Е) ALB в сыворотке крови мышиной модели цирроза, где 1) обозначает пустую контрольную группу, 2) модельную группу, 3) положительную группу, получавшую сорафениб, 4) группу низкой дозы А-01, 5) группу высокой дозы А-01, 6) группу низкой дозы А-02 и 7) группу высокой дозы А-02.
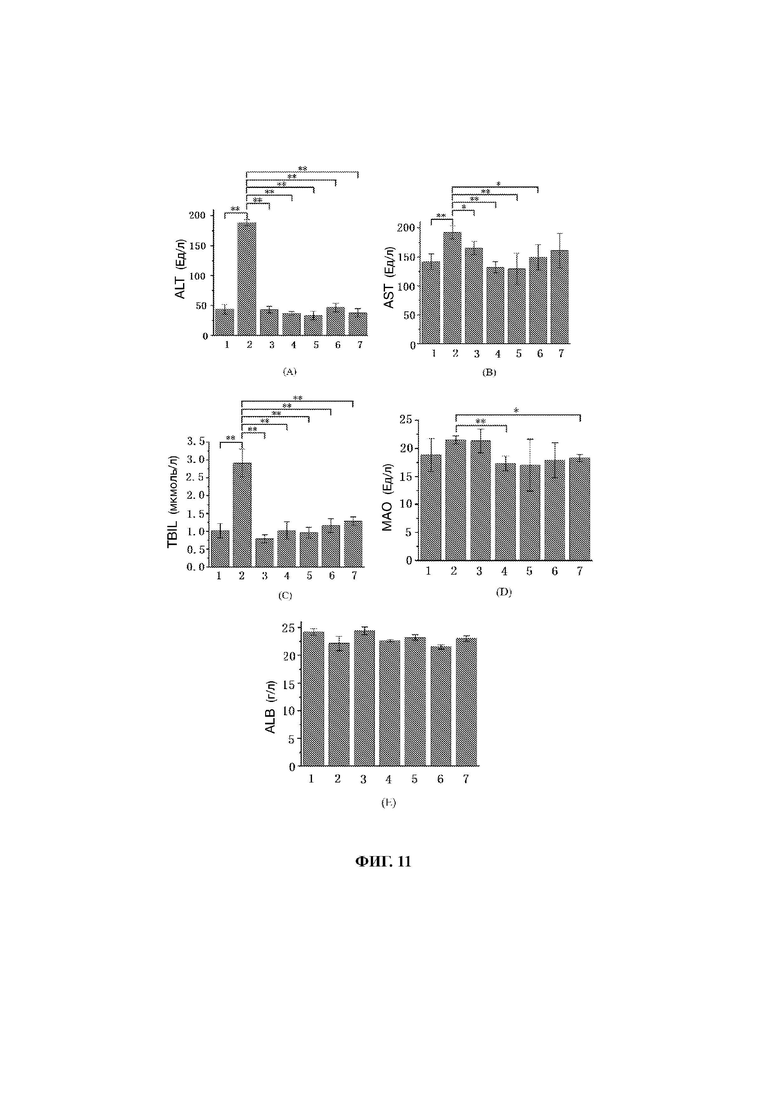
30. На фиг. 11 представлены гистограммы, показывающие влияние различных доз В-01 и В-02 на уровни (A) ALT, (В) AST, (С) TBIL, (D) МАО и (Е) ALB в сыворотке крови больных циррозом моделей мышей, где 1) обозначает пустую контрольную группу, 2) модельную группу, 3) положительную группу, получавшую сорафениб, 4) группу низкой дозы В-01, 5) группу высокой дозы В-01, 6) группу низкой дозы В-02 и 7) группу высокой дозы В-02.
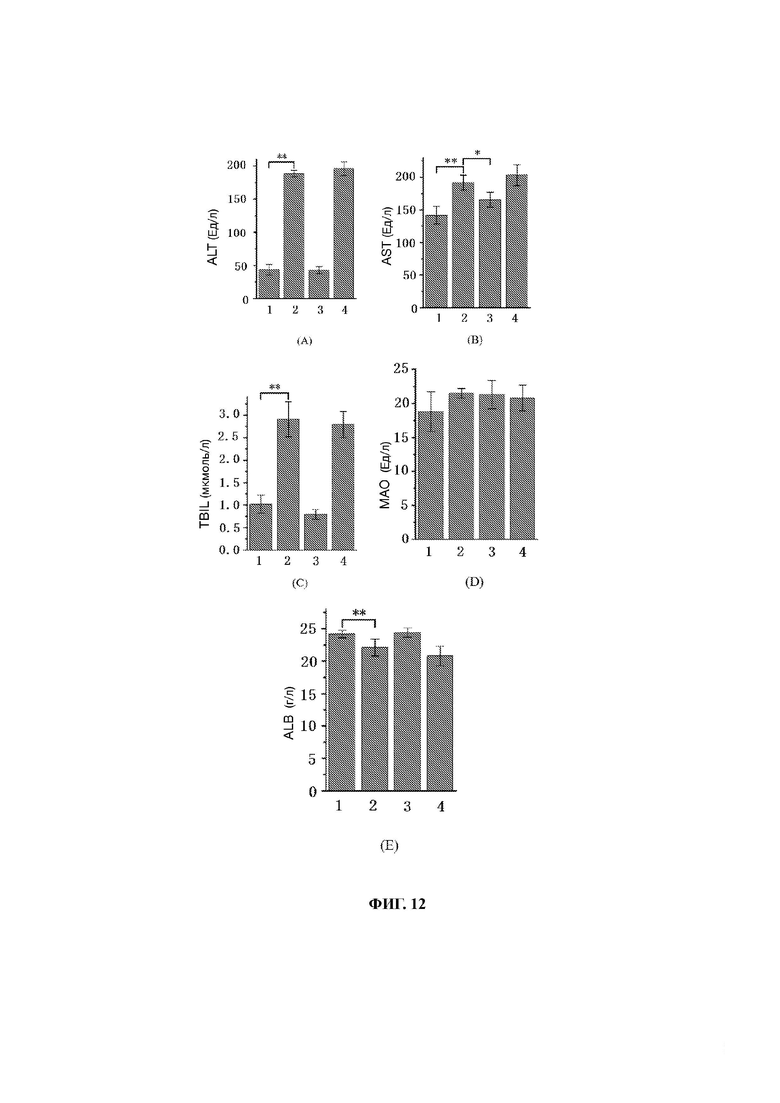
31. На фиг. 12 представлены гистограммы, показывающие влияние высокой дозы С на уровни (A) ALT, (В) AST, (С) TBIL, (D) МАО и (Е) ALB в сыворотке крови у больных циррозом моделей мышей, где 1) обозначает пустую контрольную группу, 2) модельную группу, 3) положительную группу, получавшую сорафениб, 4) группу высокой дозы препарата С.
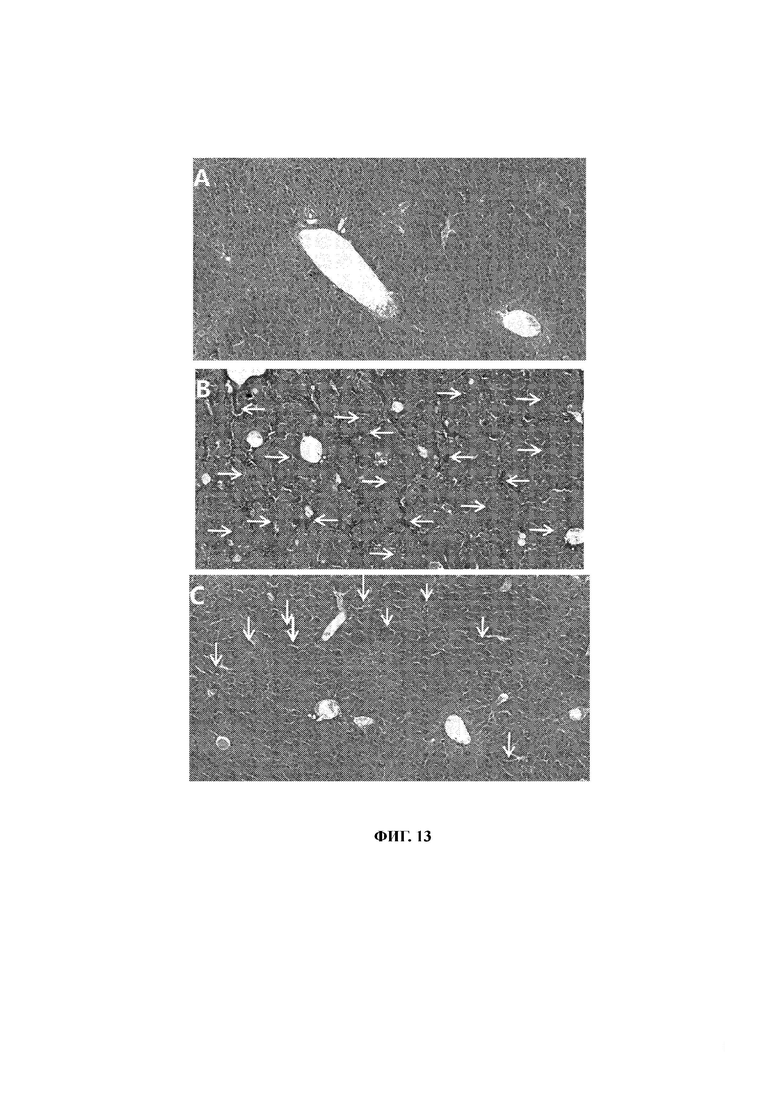
32. На фиг. 13 представлены изображения окрашивания ГЭ: (А) пустая контрольная группа; (В) модельная группа; (С) группа положительного контроля; (D) группа низкой дозы А-01; (Е) группа высокой дозы А-01.
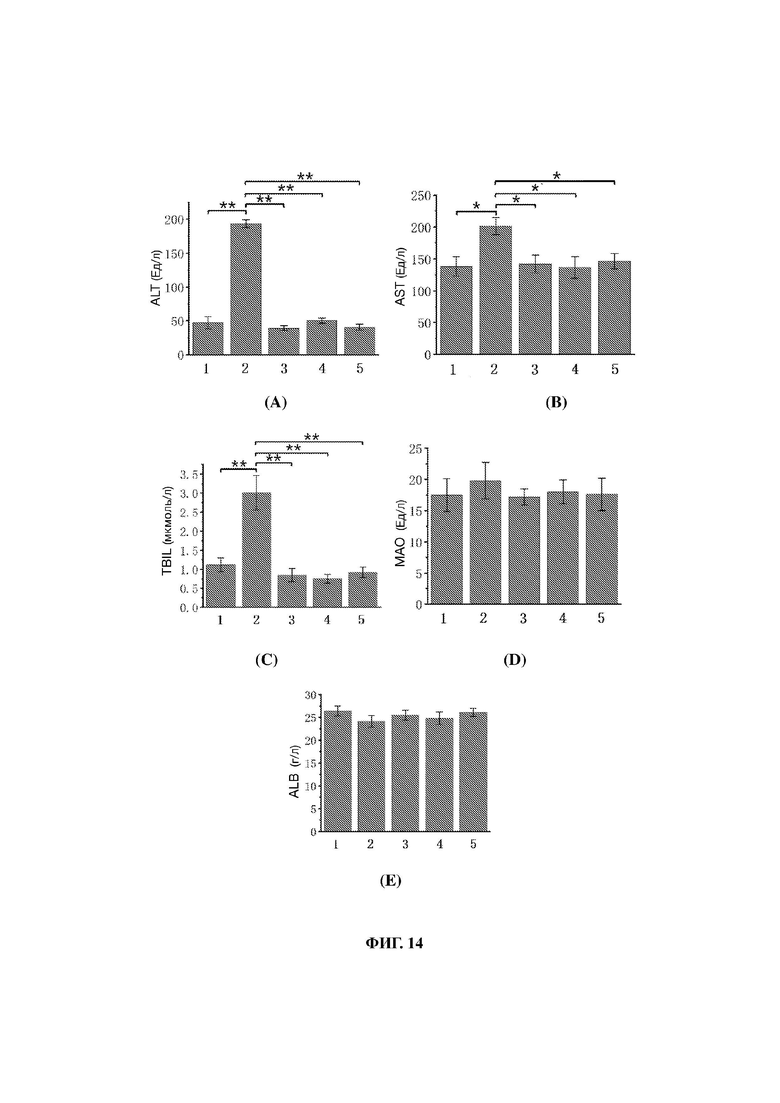
33. На фиг. 14 представлены гистограммы, показывающие влияние препаратов D, Е и F на уровни (A) ALT, (В) AST, (С) TBIL, (D) МАО и (Е) ALB в сыворотке крови больных циррозом моделей мышей, где 1) обозначает пустую контрольную группу, 2) модельную группу, 3) группу препаратов D, 4) группу препаратов Е и 5) группу препаратов F.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
34. Настоящее изобретение может быть более понятным из следующего подробного описания некоторых вариантов осуществления изобретения.
35. В настоящей заявке, где имеются ссылки на публикации, раскрытия этих публикаций включены в настоящую заявку посредством ссылки во всей их полноте для более полного описания уровня техники, к которому относится настоящее изобретение.
36. Кластеры золота (AuCs) - это особая форма золота, существующая между атомами золота и наночастицами золота. AuCs имеют размер менее 3 нм и состоят всего из нескольких сотен атомов золота, что приводит к разрушению гранецентрированной кубической структуры наночастиц золота. В результате AuCs образуют молекулоподобные дискретные электронные структуры с четко выраженным зазором HOMO-LUMO в отличие от непрерывных или квазинепрерывных энергетических уровней наночастиц золота. Это приводит к исчезновению эффекта поверхностного плазмонного резонанса и соответствующей полосы поглощения плазмонного резонанса (520±20 нм) в ультрафиолетовом спектре, которыми обладают традиционные наночастицы золота.
37. Настоящее изобретение раскрывает АuС, связанный с лигандами.
38. В некоторых вариантах осуществления изобретения АuС, связанный с лигандом, включает лиганд и золотое ядро, где лиганд связан с золотым ядром. Присоединение лиганда к золотому ядру означает, что лиганд образует стабильные в растворе комплексные соединения с золотым ядром посредством ковалентной связи, водородной связи, электростатической силы, гидрофобной силы, силы Ван-дер-Ваальса и т.д. В некоторых вариантах осуществления изобретения диаметр золотого ядра находится в интервале 0,5-3 нм. В некоторых вариантах осуществления изобретения диаметр золотого ядра находится в интервале 0,5-2,6 нм.
39. В некоторых вариантах осуществления изобретения лиганд связанного с лигандом АuС, представляет собой тиолсодержащее соединение или олигопептид. В некоторых вариантах осуществления изобретения лиганд присоединяется к золотому ядру с образованием АuС, связанного с лигандом, через связь Au-S.
40. В некоторых вариантах осуществления изобретения лиганд представляет собой следующий, но не ограничивается, L-цистеин, D-цистеин или производное цистеина. В некоторых вариантах осуществления изобретения производное цистеина представляет собой N-изобутирил-L-цистеин (L-NIBC), N-изобутирил-D-цистеин (D-NIBC), N-ацетил-L-цистеин (L-NAC) или N-ацетил-D-цистеин (D-NAC).
41. В некоторых вариантах осуществления изобретения лиганд представляет собой следующий, но не ограничивается, цистеинсодержащий олигопептид и его производные. В некоторых вариантах осуществления изобретения цистеинсодержащий олигопептид представляет собой цистеинсодержащий дипептид. В некоторых вариантах осуществления изобретения цистеинсодержащий дипептид представляет собой L(D)-цистеил-L(D)-аргинин дипептид (CR), L(D)-аргинил-L(D)-цистеин дипептид (RC) или L(D)-цистеил-L-гистидин дипептид (СН). В некоторых вариантах осуществления изобретения цистеинсодержащий олигопептид представляет собой цистеинсодержащий трипептид. В некоторых вариантах осуществления изобретения цистеинсодержащий трипептид представляет собой глицил-L(D)-цистеил-L(D)-аргинин трипептид (GCR), L(D)-пролил-L(D)-цистеил-L(D)-аргинин трипептид (PCR) или L(D)-глутатион (GSH). В некоторых вариантах осуществления изобретения цистеинсодержащий олигопептид представляет собой цистеинсодержащий тетрапептид. В некоторых вариантах осуществления изобретения цистеинсодержащий тетрапептид представляет собой глицил-L(D)-серил-L(D)-цистеил-L(D)-аргинин тетрапептид (GSCR) или глицил-L(D)-цистеил-L(D)-серил-L(D)-аргинин тетрапептид (GCSR).
42. В некоторых вариантах осуществления изобретения лиганд представляет собой тиолсодержащее соединение. В некоторых вариантах осуществления изобретения тиолсодержащее соединение представляет собой 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L(D)-пролин, тиогликолевую кислоту, меркаптоэтанол, тиофенол, D-3-троловол или додецилмеркаптан.
43. Настоящее изобретение предоставляет фармацевтическую композицию для лечения цирроза печени у субъекта. В некоторых вариантах осуществления изобретения субъектом является человек. В некоторых вариантах осуществления изобретения субъектом является домашнее животное, например, собака.
44. В некоторых вариантах осуществления изобретения фармацевтическая композиция включает АuС, связанный с лигандом, как раскрыто выше, и фармацевтически приемлемое вспомогательное вещество. В некоторых вариантах осуществления изобретения вспомогательным веществом является фосфатно-буферный раствор или физиологический солевой раствор.
45. Настоящее изобретение предусматривает применение раскрытых выше AuCs, связанных с лигандом, для приготовления лекарственного средства для лечения цирроза печени у субъекта.
46. Настоящее изобретение предусматривает применение раскрытых выше AuCs, связанных с лигандом, для лечения цирроза печени у субъекта или способ лечения цирроза печени у субъекта с применением раскрытых выше AuCs, связанных с лигандом. В некоторых вариантах осуществления изобретения способ лечения включает введение субъекту фармацевтически эффективного количества AuCs, связанных с лигандом. Фармацевтически эффективное количество может быть определено с помощью обычных исследований in vivo.
47. Следующие примеры приведены исключительно для иллюстрации основных положений настоящего изобретения; они ни в коем случае не предназначены для ограничения объема настоящего изобретения.
48. Варианты осуществления изобретения
49. Вариант 1. Получение AuCs, связанных с лигандами
50. 1.1 Растворение НАuСl4 в метаноле, воде, этаноле, н-пропаноле или этилацетате для получения раствора А, в котором концентрация НАuСl4 составляет 0,01-0,03 М;
51. 1.2 Растворение лиганда в растворителе для получения раствора В, в котором концентрация лиганда составляет 0,01-0,18 М; лиганд включает, не ограничиваясь, L-цистеин, D-цистеин и другие производные цистеина, такие как N-изобутирил-L-цистеин (L-NIBC), N-изобутирил-D-цистеин (D-NIBC), N-ацетил-L-цистеин (L-NAC) и N-ацетил-D-цистеин (D-NAC), цистеинсодержащие олигопептиды и их производные, включая, но не ограничиваясь ими, дипептиды, трипептиды, тетрапептиды и другие пептиды, содержащие цистеин, такие как L(D)-цистеил-L(D)-аргинин дипептид (CR), L(D)-аргинил-L(D)-цистеин дипептид (RC), L(D)-цистеил-L(D)-гистидин (СН), глицил-L(D)-цистеил-L(D)-аргинин трипептид (GCR), L(D)-пролил-L(D)-цистеил-L(D)-аргинин трипептид (PCR), L(D)-глутатион (GSH), глицил-L(D)-серил-L(D)-цистеил-L(D)-аргинин тетрапептид (GSCR) и глицил-L(D)-цистеил-L(D)-серил-L(D)-аргинин тетрапептид (GCSR), и другие тиолсодержащие соединения, такие как одно или более из 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L(D)-пролина, тиогликолевой кислоты, меркаптоэтанола, тиофенола, D-3-троловола и додецилмеркаптана; растворитель представляет собой один или более из метанола, этилацетата, воды, этанола, н-пропанола, пентана, муравьиной кислоты, уксусной кислоты, диэтилового эфира, ацетона, анизола, 1-пропанола, 2-пропанола, 1-бутанола, 2-бутанола, пентанола, бутилацетата, трибутилметилового эфира, изопропилацетата, диметилсульфоксида, этилформиата, изо бутилацетата, метилацетата, 2-метил- 1-пропанола и пропилацетата;
52. 1.3 Смешивание раствора А и раствора В так, чтобы мольное соотношение между HAuCl4 и лигандом составляло 1: (0,01~100), перемешивание в ледяной бане в течение 0,1~48 ч, добавление 0,025~0,8 М раствора NaBH4 в воде, этаноле или метаноле, продолжение перемешивания в ледяной водяной бане и реакции в течение 0,1~12 ч. Мольное соотношение между NaBH4 и лигандом составляет 1: (0,01~100);
53. 1.4 Использование ультрафильтрационных трубок MWCO 3К~30К для центрифугирования реакционного раствора при 8000~17500 об/мин по градиенту в течение 10~100 мин после окончания реакции для получения осадка AuCs, связанных с лигандами, с различным средним размером частиц. Апертура фильтрационных мембран для ультрафильтрационных трубок с различными MWCO непосредственно определяет размер AuCs, связанных с лигандами, которые могут пройти через мембраны. Этот этап может быть по желанию пропущен;
54. 1.5 Растворение осадка AuCs, связанных с лигандом, с частицами различных средних размеров, полученных на этапе (1.4), в воде, помещение его в диализный мешок и диализ в воде при комнатной температуре в течение 1~7 дней;
55. 1.6 Сушка AuCs, связанных с лигандом, в течение 12~24 ч после диализа для получения порошкообразного или флокулирующего вещества, т.е. AuCs, связанных с лигандами.
56. Как было обнаружено, размер частиц порошкообразного или флокулянтного вещества, полученного вышеописанным способом, составляет менее 3 нм (в целом распределяется в пределах 0,5-2,6 нм). Отсутствует очевидный пик поглощения при 520 нм. Установлено, что полученный порошок или флок является AuCs, связанными с лигандами.
57. Вариант 2. Подготовка и определение характеристик AuCs, связанных с различными лигандами
58. 2.1 Получение AuCs, связанных с L-NIBC, т.е. L-NIBC-AuCs
59. На примере лиганда L-NIBC подробно описано приготовление и исследование AuCs, связанных с лигандом L-NIBC.
60. 2.1.1 Взвесьте 1,00 г HAuCl4 и растворите его в 100 мл метанола, чтобы получить 0,03 М раствор А;
61. 2.1.2 Взвесьте 0,57 г L-NIBC и растворите его в 100 мл ледяной уксусной кислоты (уксусной кислоты) для получения 0,03М раствора В;
62. 2.1.3 Отмерьте 1 мл раствора А, смешайте его с 0,5 мл, 1 мл, 2 мл, 3 мл, 4 мл или 5 мл раствора В соответственно (т.е. мольное соотношение между HAuCl4 и L-NIBC составляет 1:0,5, 1:1, 1:2, 1:3, 1:4, 1:5 соответственно), проведите реакцию в ледяной бане при перемешивании в течение 2 ч, быстро добавьте 1 мл свежеприготовленного 0,03 М (приготовленного путем взвешивания 11,3 мг NaBH4 и растворения его в 10 мл этанола) этанолового раствора NaBH4, когда раствор из ярко-желтого станет бесцветным, продолжайте реакцию в течение 30 мин после того, как раствор станет темно-коричневым, и добавьте 10 мл ацетона для завершения реакции.
63. 2.1.4 После реакции реакционный раствор подвергают градиентному центрифугированию для получения порошка L-NIBC-AuCs с различными размерами частиц. Конкретный способ: после завершения реакции реакционный раствор переносят в ультрафильтрационную пробирку с MWCO 30К и объемом 50 мл, центрифугируют при 10000 об/мин в течение 20 мин, а ретентат во внутренней пробирке растворяют в сверхчистой воде для получения порошка с размером частиц около 2,6 нм. Затем смешанный раствор во внешней пробирке переносят в ультрафильтрационную пробирку объемом 50 мл с MWCO 10К и центрифугируют при 13000 об/мин в течение 30 мин. Ретентат во внутренней пробирке растворяют в сверхчистой воде для получения порошка с размером частиц около 1,8 нм. Затем смешанный раствор во внешней пробирке переносят в ультрафильтрационную пробирку объемом 50 мл с MWCO 3К и центрифугируют при 17 500 об/мин в течение 40 мин. Ретентат во внутренней пробирке растворяют в сверхчистой воде для получения порошка с размером частиц около 1,1 нм.
64. 2.1.5 Осаждают порошок трех различных размеров частиц, полученных градиентным центрифугированием, удаляют растворитель соответственно, высушивают сырой продукт при помощи N2, растворяют его в 5 мл сверхчистой воды, помещают в диализный мешок (MWCO составляет 3кДа), помещают диализный мешок в 2 л сверхчистой воды, меняют воду каждые два дня, диализуют в течение 7 дней, высушивают замораживанием и хранят для дальнейшего использования.
65. 2.2 Определение характеристик L-NIBC-AuCs
66. Эксперимент по определению характеристик проводился для полученного выше порошка (L-NIBC-AuCs). В качестве контроля использовались модифицированные лигандом L-NIBC наночастицы золота (L-NIBC-AuNPs). Метод приготовления наночастиц золота с лигандом L-NIBC основан на источниках (W. Yan, L. Xu, С.Xu, W. Ma, H. Kuang, L. Wang и N. A. Kotov, Journal of the American Chemical Society 2012, 134, 15114; X. Yuan, B. Zhang, Z. Luo, Q. Yao, D. T. Leong, N. Yan и J. Xie, Angewandte Chemie International Edition 2014, 53, 4623).
67. 2.2.1 Наблюдение морфологии с помощью просвечивающего электронного микроскопа (ПЭМ)
68. Тест-порошки (образец L-NIBC-AuCs и образец L-NIBC-AuNPs) были растворены в сверхчистой воде до 2 мг/л в качестве образцов, а затем тест-образцы были подготовлены методом висячей капли. Более конкретно, 5 мкл образцов капали на ультратонкую углеродную пленку, испаряли естественным образом до исчезновения капли воды, а затем наблюдали морфологию образцов с помощью полевой эмиссионной ПЭМ высокого разрешения JEM-2100F STEM/EDS.
69. Четыре ПЭМ-изображения L-NIBC-AuNPs показаны на панелях В, Е, Н и К фиг. 1; три ПЭМ-изображения L-NIBC-AuCs показаны на панелях В, Е и Н фиг. 2.
70. Изображения на фиг. 2 показывают, что каждый из образцов L-NIBC-AuCs имеет однородный размер частиц и хорошую дисперсность, а средний диаметр L-NIBC-AuCs (относится к диаметру золотого ядра) составляет 1,1 нм, 1,8 нм и 2,6 нм, соответственно, в точном соответствии с результатами на панелях С, F и I фиг. 2. Для сравнения, образцы L-NIBC-AuNPs имеют больший размер частиц. Их средний диаметр (относится к диаметру золотого ядра) составляет 3,6 нм, 6,0 нм, 10,1 нм и 18,2 нм, соответственно, что точно соответствует результатам на панелях С, F, I и L фиг. 1.
71. 2.2.2 Ультрафиолетовые (УФ)-видимые (вис) спектры поглощения
72. Тест-порошки (образец L-NIBC-AuCs и образец L-NIBC-AuNPs) растворяли в сверхчистой воде до концентрации 10 мг~л-1, и спектры поглощения УФ-вис измеряли при комнатной температуре. Диапазон сканирования составлял 190-1100 нм, кювета для образца представляла собой стандартную кварцевую кювету с оптическим путем 1 см, а контрольная кювета была заполнена сверхчистой водой.
73. УФ-вис спектры поглощения четырех образцов L-NIBC-AuNPs с разными размерами показаны на панелях A, D, G и J фиг. 1, а статистическое распределение размера частиц показано на панелях С, F, I и L фиг. 1; УФ-вис спектры поглощения трех образцов L-NIBC-AuCs с разными размерами показаны на панелях A, D и G фиг. 2, а статистическое распределение размера частиц показано на панелях С, F и I фиг. 2.
74. Фиг. 1 показывает, что благодаря эффекту поверхностного плазмона L-NIBC-AuNPs имели пик поглощения при длине волны около 520 нм. Положение пика поглощения зависит от размера частиц. Когда размер частиц составляет 3,6 нм, УФ пик поглощения появляется при 516 нм; когда размер частиц составляет 6,0 нм, УФ пик поглощения появляется при 517 нм; когда размер частиц составляет 10,1 нм, УФ пик поглощения появляется при 520 нм, а когда размер частиц составляет 18,2 нм, пик поглощения появляется при 523 нм. Ни один из четырех образцов не имеет пика поглощения выше 560 нм.
75. Фиг. 2 показывает, что в УФ-спектрах поглощения трех образцов L-NIBC-AuCs с различными размерами частиц, пик поглощения поверхностного плазмонного эффекта при 520 нм исчез, а два очевидных пика поглощения появились выше 560 нм, и положения пиков поглощения немного изменялись в зависимости от размеров частиц AuCs. Это объясняется тем, что AuCs проявляет молекулоподобные свойства из-за распада гранецентрированной кубической структуры, что приводит к разрыву плотности состояний AuCs, расщеплению энергетического уровня, исчезновению эффекта плазмонного резонанса и появлению нового пика поглощения в длинноволновом направлении. Можно сделать вывод, что все три образца порошка с разным размером частиц, полученные выше, представляют собой AuCs, связанные с лигандами.
76. 2.2.3 Инфракрасная спектроскопия с преобразованием Фурье
77. Инфракрасные спектры были измерены на инфракрасном спектрометре с преобразованием Фурье VERTEX80V фирмы Bruker в режиме полного отражения в твердом порошке в высоком вакууме. Диапазон сканирования 4000-400 см-1 и число сканирований 64. Взяв для примера образцы L-NIBC-AuCs, тест-образцы представляли собой сухой порошок L-NIBC-AuCs с тремя различными размерами частиц, а контрольный образец представлял собой чистый порошок L-NIBC. Результаты показаны на фиг. 3.
78. На фиг. 3 показан инфракрасный спектр L-NIBC-AuCs с различными размерами частиц. По сравнению с чистым L-NIBC (кривая внизу), S-H растягивающие колебания L-NIBC-AuCs с различными размерами частиц полностью исчезли при 2500-2600 см-1, в то время как другие характерные пики L-NIBC все еще наблюдались, подтверждая, что молекулы L-NIBC были успешно связаны с поверхностью AuCs через связь Au-S. На фигуре также видно, что инфракрасный спектр AuCs, связанных с лигандами, не зависит от их размера.
79. AuCs, связанные с другими лигандами, были приготовлены методом, аналогичным описанному выше, за исключением того, что растворитель раствора В, соотношение подачи между HAuCl4 и лигандом, время реакции и количество добавленного NaBH4 были незначительно скорректированы. Например: когда в качестве лиганда используют L-цистеин, D-цистеин, N-изобутирил-L-цистеин (L-NIBC) или N-изобутирил-D-цистеин (D-NIBC), в качестве растворителя выбирают уксусную кислоту; когда в качестве лиганда используют дипептид CR, дипептид RC или 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L-пролин, в качестве растворителя выбирают воду, и так далее и тому подобное; другие стадии аналогичны, поэтому дальнейшие детали здесь не приводятся.
80. Настоящее изобретение предусматривает приготовление и получение серии AuCs, связанных с лигандами, вышеописанным способом. Лиганды и параметры процесса приготовления показаны в таблице 1.
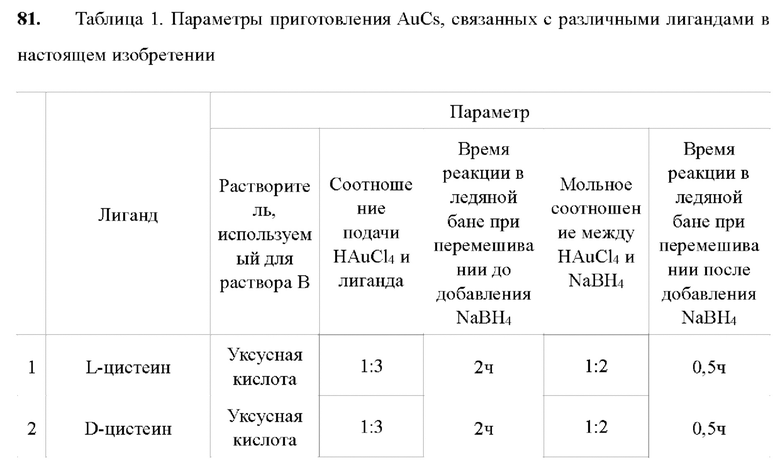
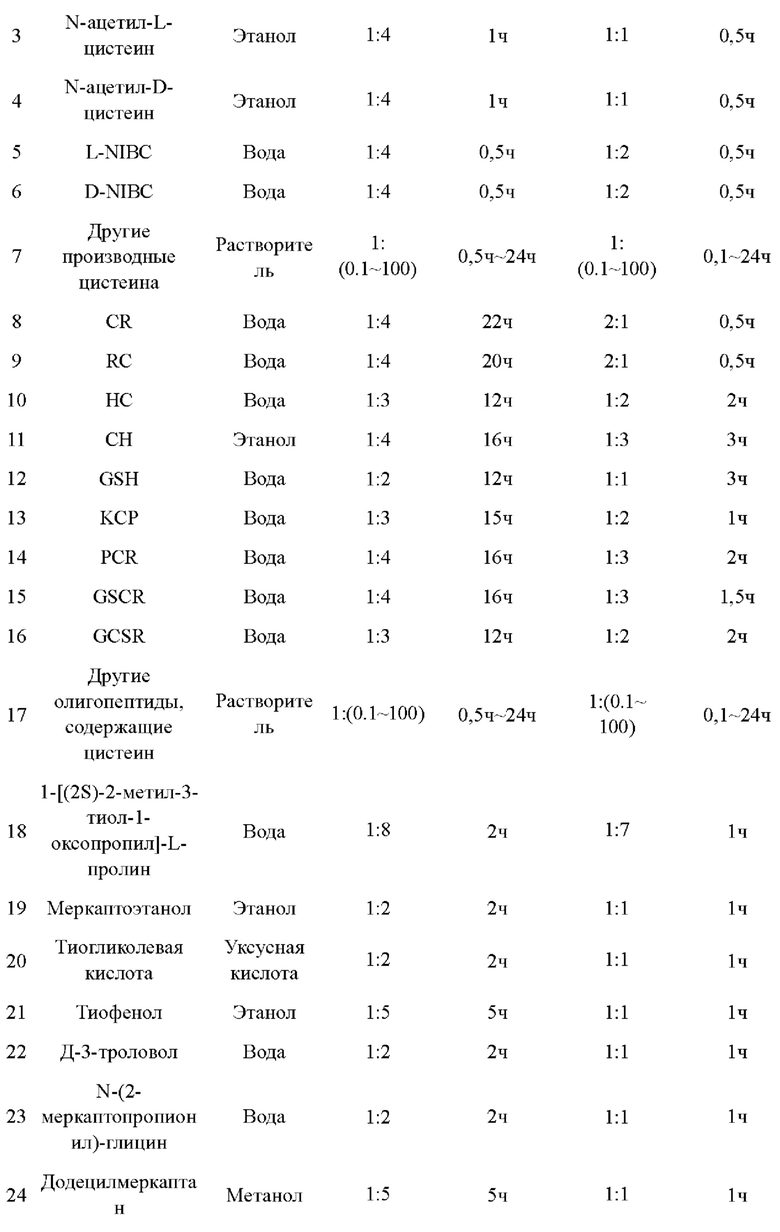

82. Образцы, перечисленные в Таблице 1, подтверждены вышеуказанными способами. Характеристики шести различных AuCs, связанных с лигандами, показаны на фиг. 4 (CR-AuCs), на фиг. 5 (RC-AuCs), на фиг. 6 (Cap-AuCs) (Сар обозначает 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L-пролин), на фиг. 7 (GSH-AuCs), на фиг. 8 (D-NIBC-AuCs) и на фиг. 9 (L-Cys-AuCs). На фиг. 4-фиг. 9 представлены УФ-спектры (панель А), ИК-спектры (панель В), ПЭМ-изображения (панель С) и распределение частиц по размерам (панель D).
83. Результаты показывают, что диаметры AuCs, связанных с различными лигандами, полученные из таблицы 1, все меньше 3 нм. Ультрафиолетовые спектры также показывают исчезновение пика при 520±20 нм и появление пика поглощения в других положениях. Положение пика поглощения может меняться в зависимости от лигандов и размеров частиц, а также структуры. В некоторых ситуациях пик поглощения отсутствует, в основном из-за образования смесей AuCs с различными размерами и структурами частиц или некоторых специальных AuCs, которые перемещают положение пика поглощения за пределы УФ-вис спектра. Между тем, инфракрасные спектры с преобразованием Фурье также показывают исчезновение инфракрасного пика поглощения лиганда тиола (между пунктирными линиями на панели В фиг. 4-8), в то время как другие инфракрасные характерные пики сохраняются, предполагая, что все молекулы лиганда были успешно связаны с атомами золота для образования AuCs, связанных с лигандами, и в рамках настоящего изобретения были успешно получены AuCs, связанные с лигандами, перечисленными в таблице 1.
84. Вариант 3
85. 3.1 Материалы и животные
86. 3.1.1 Тест-образец
87. А-01: кластеры золота, связанные с лигандом L-NIBC (L-NIBC-AuCs), 0,9±0,2 нм.
88. А-02: кластеры золота, связанные с лигандом L-NIBC (L-NIBC-AuCs), 1,9±0,5 нм.
89. В-01: кластеры золота, связанные с лигандом L-Cys (L-Cys-AuCs), 1,0±0,2 нм.
90. В-02: кластеры золота, связанные с лигандом L-Cys (L-Cys-AuCs), 1,7±0,3 нм.
91. С: L-NIBC-модифицированные наночастицы (L-NIBC-AuNPs), 6,3±1,5 нм.
92. Все контрольные образцы были приготовлены по описанному выше способу с незначительными изменениями, и их качество было охарактеризовано с помощью описанных выше способов.
93. 3.1.2 Положительный контрольный образец
94. Сорафениб.
95. 3.1.3 Подопытные животные и группы
96. 120 SPF самцов мышей C57BL/6N, возраст 6-8 недель, масса тела 16-20 г, были приобретены у Beijing Huafukang Experimental Animal Technology Co., Ltd. (номер лицензии на производство: SCXK (Jing) 2019-0008). В соответствии с массой тела они были случайным образом разделены на 12 групп (n=10): пустая контрольная группа, модельная группа, группа положительного контроля, группа низкой дозы А-01, группа высокой дозы А-01, группа низкой дозы А-02, группа высокой дозы А-02, группа низкой дозы В-01, группа высокой дозы В-01, группа низкой дозы В-02, группа высокой дозы В-02 и группа высокой дозы С.
97. 3.2 Модельный протокол
98. За исключением пустой контрольной группы, мышиная модель цирроза печени в других группах была подготовлена с помощью индукционной терапии четыреххлористым углеродом (ССl4). Модельный протокол был следующим: (1) каждой мыши внутрибрюшинно вводили 10% CCl4 (разбавленный оливковым маслом) в дозе 7 мкл/г массы тела дважды в неделю в течение 8 недель; мышам пустой контрольной группы внутрибрюшинно вводили такое же количество растворителя оливкового масла. (2) начиная с 6-й недели, каждую неделю отбирали двух мышей и умерщвляли их через 48 часов после последней инъекции. Наблюдали за внешним видом печени. После того как внешний вид приобретал признаки цирроза (8-я неделя), ткань печени фиксировали формалином. Для оценки модели цирроза использовали окрашивание НЕ и окрашивание по Массону.
99. 3.3 Введение
100. После успешного моделирования мышам в группе положительного контроля вводили внутрижелудочно 25 мг/кг сорафениба; мышам в группах низкой или высокой дозы А-01, А-02, В-01 и В-02 вводили внутрибрюшинно в дозировке 2,5 или 10 мг/кг соответственно соответствующего тест-материала; мышам в группе с высокой дозой С вводили внутрибрюшинно в дозировке 40 мг/кг С; а мышам в пустой контрольной группе и модельной группе вводили внутрибрюшинно физиологический солевой раствор в дозировке 10 мл/кг. Введение проводилось один раз в день в течение 20 дней подряд.
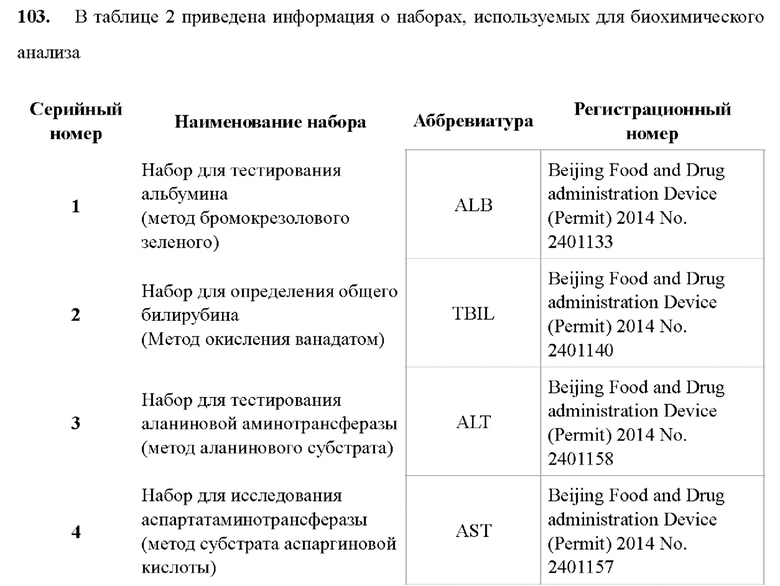
101. 3.4 Биохимический анализ
102. По окончании введения препарата кровь собирали из мышиной орбиты и получали сыворотки для биохимического анализа альбумина (ALbumin, ALB), общего билирубина (TBIL), аминотрансферазы аланина (ALT), аминотрансферазы аспартата (AST) и моноаминоксидазы (МАО) с использованием набора Zhongsheng Beikong Kit и биохимического анализатора (Siemens). Определение проводилось в строгом соответствии с инструкцией к набору.
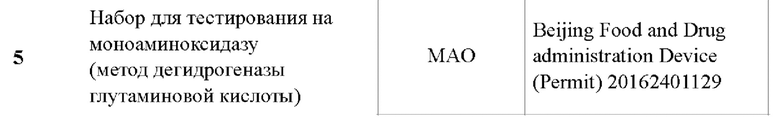
104. 3.5 Патологическое исследование
105. 3.5.1 Окрашивание НЕ
106. После умерщвления образцы ткани печени мышей фиксировали 4% параформальдегидным фиксатором в течение более 48 ч. После фиксации образцы печени обезвоживали с помощью спиртового градиента и обрабатывали ксилолом и этанолом. Затем ткани печени окунали и погружали в парафин. После того, как погруженный материал был обрезан, закреплен и восстановлен, ткани печени были срезаны с помощью парафинового микротома, толщина срезов составляла 4 мкм. Основной процесс окрашивания НЕ заключается в следующем: после запекания в печи при 65°С срезы обрабатывали ксилолом и обезвоживали градиентным этанолом. Срезы последовательно окрашивали гематоксилином, раствором, усиливающим синий цвет, и 0,5% эозином, затем обрабатывали градиентным этанолом и ксилолом и запечатывали нейтральной камедью. Фиброз ткани печени наблюдали с помощью микроскопа.
107. 3.5.2 Окрашивание по Массону
108. После высушивания срезы ткани печени мыши подвергались депарафинизации и обезвоживанию. После хромирования ядра окрашивали раствором гематоксилина по Рего. После промывки водой срезы окрашивали кислотным фуксином Массона с красным Понсо, погружали в 2% водный раствор ледяной уксусной кислоты и дифференцировали с помощью 1% раствора фосфомолибденовой кислоты. После окрашивания анилиновым синим или светло-зеленым раствором срезы на некоторое время погружали в 0,2% водный раствор ледяной уксусной кислоты, затем просвечивали 95% спиртом, безводным спиртом и ксилолом, а затем запечатывали нейтральной камедью. Ткань печени наблюдали с помощью микроскопа.
109. 3.6. Результаты
110. 3.6.1 Успешное моделирование
111. Печень мышей в модельной группе была разделена на круглые или овальные массы разных размеров пролиферирующими фиброзными перегородками. Показатели ALT, TBIL и AST в сыворотке крови значительно увеличились по сравнению с контрольной группой, ALB в сыворотке крови значительно снизился по сравнению с контрольной группой, а показатель МАО не имел существенных отличий от контрольной группы, но его значение также увеличилось. Все вышеперечисленные результаты свидетельствуют о том, что данное экспериментальное моделирование было успешным.
112. 3.6.2 Влияние тест-препаратов на аланин-аминотрансферазу (ALT), общий билирубин (TBIL), аспартат-аминотрансферазу (AST), моноаминоксидазу (МАО) и альбумин (ALB)
113. 3.6.2.1 Тест-препараты А-01 и А-02
114. Как показано на фиг. 10А, активность ALT в модельной группе значительно выше, чем в пустой контрольной группе (увеличилась с 43,5±8,1 Ед/л до 188,5±4,9 Ед/л; Р<0,01), что указывает на патологические изменения функций печени у больных циррозом модельных мышей. После введения А-01 и А-02 в высоких и низких дозах активность ALT во всех группах значительно снизилась (самая высокая - 41,5±5,4 Ед/л в группе низких доз А-02; самая низкая - 30,0±5,9 Ед/л в группе высоких доз А-01; и 42,8±5,4 Ед/л в группе положительного контроля) и вернулась к аналогичному уровню пустой контрольной группы или даже ниже, что значительно отличается от показателей модельной группы (Р<0,01).
115. Как показано на фиг. 10 В, активность AST в сыворотке крови в модельной группе была значительно увеличена по сравнению с пустой контрольной группой (увеличилась с 141,9±13,5 Ед/л до 192,0±11,3 Ед/л; Р<0,05). После введения А-01 и А-02 активность AST во всех группах снизилась, причем введение высоких доз А-01 и А-02 значительно снизило активность AST (130±12,8 Ед/л для группы высокой дозы А-01; 131,3±9,9 Ед/л для группы высокой дозы А-02; оба Р<0,01), явно превосходя группу положительного контроля (165,5±11,6 Ед/л).
116. Как показано на фиг. 10С, концентрация TBIL в модельной группе была значительно выше, чем в пустой контрольной группе (увеличилась с 1,02±0,20 мкмоль/л до 2,91±0,39 мкмоль/л), и наблюдалось значительное отличие от пустой контрольной группы (Р<0,01). После введения высоких и низких доз А-01 и А-02 концентрации TBIL были значительно снижены (самая высокая - 0,91±0,13 мкмоль/л; самая низкая - 0,78±0,25 мкмоль/л); они находятся на аналогичном уровне пустой контрольной группы, но значительно отличаются от модельной группы (Р<0,01).
117. Как показано на фиг. 10D, активность МАО в модельной группе повышена по сравнению с пустой контрольной группой (18,8±2,9 Ед/л для пустой контрольной группы; 21,5±0,7 Ед/л для модельной группы), но статистической разницы нет, что говорит о том, что изменения активности МАО у мышей с циррозом печени, вызванным четыреххлористым углеродом, незначительны. Введение А-01 и А-02 не оказало существенного влияния на активность МАО во всех получавших терапию группах, но активность МАО во всех получавших терапию группах снизилась (самая высокая -19,3±1,5 Ед/л и самая низкая - 18,5±1,9 Ед/л); они находятся на уровне контрольной группы. Для сравнения активность МАО в группе положительного контроля не снизилась (21,3±2,1 Ед/л). Этот результат позволяет предположить, что А-01 и А-02 могут регулировать активность МАО до уровня пустой контрольной группы, играя роль в восстановлении функций печени у мышей с циррозом.
118. Как показано на фиг. 10Е, уровень ALB в модельной группе значительно снизился по сравнению с пустой контрольной группой (снизился с 24,2±0,6 г/л до 22,1±1,3 г/л), причем имеется значительное отличие от пустой контрольной группы (Р<0,05), что свидетельствует о том, что введение четыреххлористого углерода может значительно снизить уровень ALB в сыворотке крови. Введение различных доз А-01 и А-02, а также положительного контроля d не оказало существенного влияния на уровень ALB в сыворотке крови.
119. Препарат положительного контроля сорафениб значительно снижал уровни ALT, AST и TBIL, но не оказывал облегчающего действия на больных циррозом мышей по показателю МАО. Результаты показывают, что А-01 и А-02 оказывают восстанавливающее действие на функцию печени у больных циррозом мышей, причем эффект лучше, чем у положительного контрольного препарата.
120. 3.6.2.2 Тест-препараты В-01 и В-02
121. Как показано на фиг. 11А, низкая и высокая дозы В-01 и В-02 могли значительно снизить активность ALT (самая высокая - 46,3±7,4 Ед/л; самая низкая - 33,0±7,1 Ед/л); они находятся на уровне, аналогичном уровню пустой контрольной группы, но значительно отличаются от модельной группы (188,5±4,9 Ед/л; Р<0,01).
122. Как показано на фиг. 11 В, по сравнению с модельной группой (192,0±11,3 Ед/л), введение В-01 в низкой или высокой дозировке может значительно снизить активность AST до нормального уровня (132,3±10,0 Ед/л и 129,7±26,6 Ед/л соответственно; Р<0,01), и введение В-02 в низкой дозировке может значительно снизить активность AST (149,6±21,8 Ед/л; Р<0,05); они находятся на том же уровне, что и в пустой контрольной группе. Однако введение высоких доз В-02 в некоторой степени снижает активность AST, но существенной разницы нет (Р>0,05). Для сравнения положительный препарат сорафениб также может снизить активность AST до 165,5±11,6 Ед/л (Р<0,05), но эффект не такой хороший, как при применении В-01 в низкой и высокой дозировках и В-02 в низкой дозировке.
123. Как показано на фиг. 11С, низкие и высокие дозы В-01 и В-02 значительно снижали TBIL (самая высокая - 1,28±0,12 мкмоль/л; самая низкая - 0,96±0,15 мкмоль/л); они находятся на уровне, аналогичном уровню пустой контрольной группы (1,02±0,20 мкмоль/ л), но значительно отличаются от модельной группы (2,91±0,39 мкмоль/л; Р<0,01).
124. Как показано на фиг. 11D, по сравнению с модельной группой (21,5±0,7 Ед/л), низкая доза В-01 (17,3±1,3 Ед/л; Р<0,01) и высокая доза В-02 (18,3±0,6 Ед/л; Р<0,05) значительно снижали уровень МАО в сыворотке крови до уровня пустой контрольной группы (18,8±2,9 Ед/л), но препарат положительного контроля не оказывал влияния на уровень МАО в сыворотке крови (21,3±2,1 Ед/л).
125. Как показано на фиг. 11Е, введение тест-препарате в и положительного контрольного препарата не оказало существенного влияния на уровень ALB.
126. Приведенные выше результаты показывают, что В-01 и В-02 значительно снижают уровни ALT, AST, TBIL и МАО, а также оказывают определенный дозозависимый эффект на восстановление функции печени больных циррозом мышей, и их действие, по крайней мере, по некоторым показателям лучше, чем у препаратов положительного контроля.
127. 3.6.2.3 Тест- препараты С
128. Как показано на фиг. 12, по сравнению с модельной группой, введение высоких доз препарата С не привело к значительному улучшению уровней (A) ALT, (В) AST, (С) TBIL, (D) МАО и (Е) ALB по сравнению с модельной контрольной группой, и даже наблюдается тенденция к ухудшению, что говорит о неэффективности препарата С в улучшении функций печени больных циррозом мышей и его возможной токсичности.
129. 3.6.3 Анализы на патологии
130. Цирроз печени патологически характеризуется диффузным фиброзом ткани печени и образованием псевдолобул. Результаты анализов на предмет патологий с окрашиванием НЕ показали, что, как показано на фиг. 13А, нормальная ткань печени мышей пустой контрольной группы имела четкую структуру, неповрежденные печеночные дольки, аккуратно расположенные гепатоциты, радиальное расположение с центром на центральной вене, нормальное ядро гепатоцитов и лишь небольшое количество фиброзной ткани в зоне захвата. Как показано на фиг. 13 В, в ткани печени модельной группы гепатоциты были неупорядочены, появились шаровидные структуры, печеночные дольки почти исчезли, обильно формировались псевдолобулы (на фиг. 13 В указаны стрелками, направленными вправо), в ткани печени присутствовало большое количество пролиферированных протофибрилл, образующих фиброзные перегородки круглой или овальной формы (на фиг. 13 В указаны стрелками, направленными влево). Как показано на фиг. 13С, по сравнению с модельной контрольной группой, в группе положительного контроля наблюдалось значительное уменьшение повреждений печени; гепатоциты, очевидно, имели аккуратное расположение; фиброзная гиперплазия, хотя и была увеличена, очевидно, уменьшилась, не образуя фиброзных септ; псевдолобулины почти исчезли; но по сравнению с нормальными тканями печени, в тканях печени группы положительного контроля наблюдалось явное увеличение межклеточных щелей (на что указывают стрелки, направленные вниз). По сравнению с модельной контрольной группой, в 4 группах, которым вводили препараты с кластерами золота (А-01, А-02, В-01 и В-02), гепатоциты значительно восстановились после повреждения печени, о чем свидетельствует явное уменьшение фиброзной гиперплазии и псевдолобул, и это восстановление в определенной степени зависит от дозы.
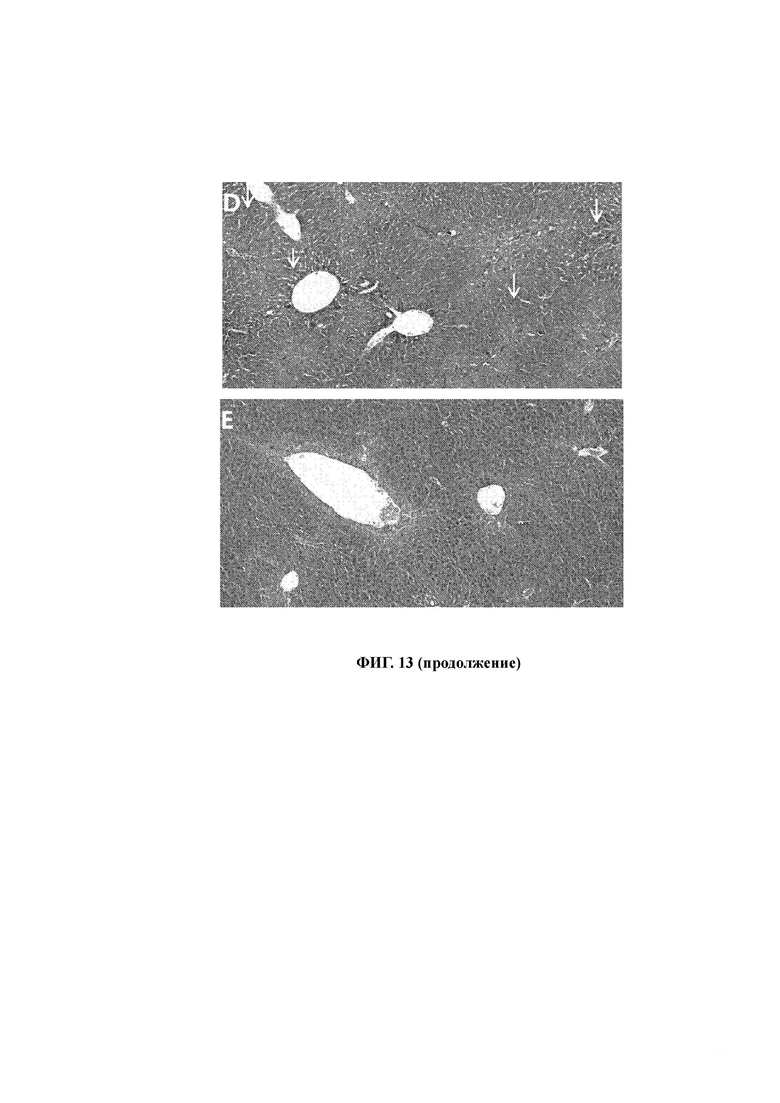
131. На фиг. 13D и фиг. 13Е показаны изображения НЕ, демонстрирующие эффекты снижения и повышения дозы препарата А-01, соответственно, на восстановление повреждений печени. Как показано на фиг. 13D, в группе введения низкой дозы препарата А-01 наблюдается относительно чистое размещение гепатоцитов, почти полное исчезновение псевдолобул, явное уменьшение фиброзной гиперплазии, но межгепатоцитарные щели, по сравнению с нормальной тканью печени, в определенной степени увеличены (на что указывают направленные вниз стрелки на фиг. 13D). Как показано на фиг. 13Е, по сравнению с группой введения низкой дозы препарата А-01, группа введения высокой дозы препарата А-01 имела более хороший эффект в виде уменьшения повреждений печени, полного исчезновения псевдолобул, отсутствия фиброзной гиперплазии, отсутствия заметного увеличения межгепатоцитарных щелей и отсутствия видимых отличий от нормальных тканей печени. В заключение, препарат А-01 показал лучшее воздействие на восстановление повреждений печени, чем препарат положительного контроля.
132. Результаты окрашивания по Массону дали те же выводы, что и результаты окрашивания по НЕ.
133. Остальные три препарата также показали аналогичное препарату А-01 действие; подробное описание не требуется.
134. В целом, четыре тест-препарата А-01, А-02, В-01 и В-02 значительно уменьшили фиброзную гиперплазию печени и псевдолобулины печени. Результаты тестирования показателей функции печени также показали восстановление функции печени. Наиболее значительными изменениями были аланин-аминотрансфераза (ALT) и общий билирубин (TBIL). Аспартатаминотрансфераза (AST) и моноаминооксидаза (МАО) также значительно восстановились, в то время как альбумин (ALB) существенно не изменился. Четыре препарата из кластеров золота могут значительно улучшить функцию печени и часть патологической структуры печени у больных циррозом мышей, а общий эффект превосходит положительный контрольный препарат сорафениб, обеспечивая экспериментальную основу для дальнейшего применения в будущем. Однако препарат С не обладает очевидным терапевтическим эффектом и не может быть использован для лечения цирроза печени.
135. Вариант 4
136. 4.1 Материалы и животные
137. 4.1.1 Тест-образец
138. D: кластеры золота, связанные с лигандом L-NAC (L-NAC-AuCs), 0,5-3 нм.
139. Е: кластеры золота, связанные с лигандом CR (CR-AuCs), 0,5-3 нм.
140. F: кластеры золота, связанные с лигандом RC (RC-AuCs), 0,-3 нм.
141. Все тест-образцы были приготовлены по описанному выше способу с небольшими изменениями, и их качество было охарактеризовано с помощью описанных выше способов.
142. 4.1.2 Подопытные животные и группы
143. 50 SPF самцов мышей C57BL/6N, возраст 6-8 недель, масса тела 16-20 г, были приобретены в Beijing Huafukang Experimental Animal Technology Co. (номер производственной лицензии: SCXK (Jing) 2019-0008). В соответствии с массой тела они были случайным образом разделены на 5 групп (n=10): пустая контрольная группа, модельная группа, группа введения препарата D, группа введения препарата Е и группа введения препарата F.
144. 4.2 Модельный протокол
145. За исключением пустой контрольной группы, модель цирроза печени у мышей в других группах была подготовлена с помощью индукционной терапии четыреххлористым углеродом (ССl4). Модельный протокол был следующим: (1) каждой мыши внутрибрюшинно вводили 10% ССl4 (разбавленный оливковым маслом) в дозировке 7 мкл/г массы тела дважды в неделю в течение 8 недель; мышам пустой контрольной группы внутрибрюшинно вводили такое же количество растворителя оливкового масла. (2) начиная с 6-й недели, каждую неделю отбирали двух мышей и умерщвляли их через 48 часов после последней инъекции. Наблюдали за внешним видом печени. После того как внешний вид приобретал признаки цирроза (8-я неделя), ткань печени фиксировали формалином. Для оценки модели цирроза использовали окрашивание НЕ и окрашивание по Массону.
146. 4.3 Введение
147. После успешного моделирования, мышам в трех группах вводили путем внутрибрюшинной инъекции в дозировке 40 мг/кг соответственно соответствующие препараты кластеров золота; и мышам в пустой контрольной группе и модельной группе вводили внутрибрюшинно физиологический солевой раствор в дозировке 10 мл/кг. Введение осуществлялось один раз в день в течение 20 дней подряд.
148. 4.4 Биохимический анализ
149. Реактивы и протоколы были такими же, как описано в разделе 3.4.
150. 4.5 Результаты
151. 4.5.1 Успешное моделирование
152. Печень мышей в модельной группе была разделена на круглые или овальные массы разных размеров пролиферирующими фиброзными перегородками. Показатели ALT, TBIL и AST в сыворотке крови значительно увеличились по сравнению с контрольной группой, ALB в сыворотке крови значительно снизился по сравнению с контрольной группой, а показатель МАО не имел существенных отличий от контрольной группы, но его значение также увеличилось. Все вышеперечисленные результаты свидетельствуют о том, что данное экспериментальное моделирование было успешным.
153. 4.5.2 Влияние тест-препаратов на аланин-аминотрансферазу (ALT), общий билирубин (TBIL), аспартат-аминотрансферазу (AST), моноаминоксидазу (МАО) и альбумин (ALB)
154. Как показано на фиг. 14А, активность ALT в модельной группе выше, чем в пустой контрольной группе (Р<0,01, **), что указывает на патологические изменения функций печени у больных циррозом мышей. После введения препаратов D, Е или F активность ALT во всех получавших терапию группах значительно снизилась и вернулась к аналогичному уровню пустой контрольной группы, что значительно отличается от таковой в модельной группе (Р<0,01).
155. Как показано на фиг. 14 В, активность AST в модельной группе значительно выше, чем в пустой контрольной группе (Р<0,05, *). После введения препаратов D, Е или F активность AST во всех получавших терапию группах значительно снизилась (Р<0,05, *).
156. Как показано на фиг. 14С, концентрация TBIL в модельной группе значительно выше, чем в пустой контрольной группе (Р<0,01, **). После введения препаратов D, Е или F концентрация TBIL во всех получавших терапию группах значительно снизилась до уровня пустой контрольной группы, но значительно отличается от концентрации TBIL в модельной контрольной группе (Р<0,01, **).
157. Как показано на фиг. 14D, активность МАО в модельной группе была увеличена по сравнению с пустой контрольной группой, но статистической разницы нет (Р>0,5), что говорит о том, что изменения активности МАО у мышей с циррозом печени, вызванным четыреххлористым углеродом, не являются значительными. Введение препаратов D, Е или F не оказало существенного влияния на активность МАО, но активность МАО во всех группах введения препаратов снизилась до уровня пустой контрольной группы.
158. Как показано на фиг. 14Е, концентрация ALB в модельной группе снижается по сравнению с концентрацией ALB в пустой контрольной группе, но разница не является значительной (Р>0,05). Однако введение препаратов D, Е или F увеличивало концентрацию ALB в сыворотке крови, но разница не была значительной (Р>0,05).
159. В итоге, три препарата кластера золота D, Е и F значительно улучшили функцию печени. Аланин-аминотрансфераза (ALT) и общий билирубин (TBIL) показали наиболее значительные изменения, аспартат-аминотрансфераза (AST) и моноаминооксидаза (МАО) показали очевидное восстановление, и альбумин (ALB) также был улучшен, хотя и не значительно. Эти результаты создают экспериментальную основу для дальнейшего применения в будущем.
160. Другие размеры L-Cys-AuCs, L-NIBC-AuCs, L-NAC-AuCs, CR-AuCs, RC-AuCs и другие AuCs, связанные с лигандами, с различными размерами также имеют подобные эффекты, хотя их эффекты варьируются в определенных пределах. Они не будут подробно описаны здесь.
161. Хотя настоящее изобретение было описано со ссылкой на конкретные варианты осуществления, следует понимать, что эти варианты являются иллюстративными и не ограничивают объем изобретения. Альтернативные варианты осуществления настоящего изобретения станут очевидными для тех, кто обладает обычными навыками в области, к которой относится настоящее изобретение. Такие альтернативные варианты осуществления считаются включенными в объем настоящего изобретения. Соответственно, объем настоящего изобретения определяется прилагаемой формулой изобретения и подтверждается приведенным выше описанием.
Изобретение относится к области медицины, а именно, к лечению цирроза печени. Предлагается применение кластера золота, связанного с лигандом, для лечения цирроза печени у субъекта, где кластер золота, связанный с лигандом, содержит золотое ядро, имеющее диаметр в интервале 0,5-3 нм, и лиганд, связанный с золотым ядром. При этом лиганд выбран из группы, состоящей из L-цистеина и его производных, D-цистеина и его производных, цистеинсодержащих олигопептидов и их производных и других тиолсодержащих соединений, где L-цистеин и его производные выбирают из группы, состоящей из L-цистеина, N-изобутирил-L-цистеина (L-NIBC) и N-ацетил-L-цистеина (L-NAC), и где D-цистеин и его производные выбирают из группы, состоящей из D-цистеина, N-изобутирил-D-цистеина (D-NIBC) и N-ацетил-D-цистеина (D-NAC); цистеинсодержащие олигопептиды и их производные представляют собой цистеинсодержащие дипептиды, цистеинсодержащие трипептиды или цистеинсодержащие тетрапептиды; и другие тиолсодержащие соединения выбирают из группы, состоящей из 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L-пролина, 1-[(2S)-2-метил-3-тиол-1-оксопропил]-D-пролина, тиогликолевой кислоты, меркаптоэтанола, тиофенола, D-3-троловола, N-(2-меркаптопропионил)-глицина и додецилмеркаптана. Использование изобретения позволяет улучшить функцию печени. 4 з.п. ф-лы, 2 табл, 14 ил.
1. Применение кластера золота, связанного с лигандом, для лечения цирроза печени у субъекта, где кластер золота, связанный с лигандом, содержит:
золотое ядро; и
лиганд, связанный с золотым ядром;
характеризуется тем, что золотое ядро имеет диаметр в интервале 0,5-3 нм, и
лиганд представляет собой выбранный из группы, состоящей из L-цистеина и его производных, D-цистеина и его производных, цистеинсодержащих олигопептидов и их производных и других тиолсодержащих соединений;
L-цистеин и его производные выбирают из группы, состоящей из L-цистеина, N-изобутирил-L-цистеина (L-NIBC) и N-ацетил-L-цистеина (L-NAC), и где D-цистеин и его производные выбирают из группы, состоящей из D-цистеина, N-изобутирил-D-цистеина (D-NIBC) и N-ацетил-D-цистеина (D-NAC);
цистеинсодержащие олигопептиды и их производные представляют собой цистеинсодержащие дипептиды, цистеинсодержащие трипептиды или цистеинсодержащие тетрапептиды; и
другие тиолсодержащие соединения выбирают из группы, состоящей из 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L-пролина, 1-[(2S)-2-метил-3-тиол-1-оксопропил]-D-пролина, тиогликолевой кислоты, меркаптоэтанола, тиофенола, D-3-троловола, N-(2-меркаптопропионил)-глицина и додецилмеркаптана.
2. Применение кластера золота, связанного с лигандом, по п. 1, где золотое ядро имеет диаметр в интервале 0,5-2,6 нм.
3. Применение кластера золота, связанного с лигандом, по п. 1, где цистеинсодержащие дипептиды выбирают из группы, состоящей из цистеил-аргинин дипептида (CR), аргинил-цистеин дипептида (RC), гистидил-цистеин дипептида (HC) и цистеил-гистидин дипептида (CH).
4. Применение кластера золота, связанного с лигандом, по п. 1, где цистеинсодержащие трипептиды выбирают из группы, состоящей из глицил-цистеил-аргинин трипептида (GCR), пролил-цистеил-аргинин трипептида (PCR), лизил-цистеил-пролин трипептида (KCP) и глутатиона (GSH).
5. Применение кластера золота, связанного с лигандом, по п. 1, где цистеинсодержащие тетрапептиды выбирают из группы, состоящей из глицил-серил-цистеил-аргинин тетрапептида (GSCR) и глицил-цистеил-серил-аргинин тетрапептида (GCSR).
| WO 2013176468 A1, 28.11.2013 | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| Устройство для определения усилий в статически неопределенных системах | 1931 |
|
SU25758A1 |
| MAJOUGA A | |||
| et al | |||
| New separation materials based on gold nanoparticles | |||
| Journal of Manufacturing Technology Management, 2010, V | |||
| Выбрасывающий ячеистый аппарат для рядовых сеялок | 1922 |
|
SU21A1 |
| Приспособление для остановки поезда с пути | 1924 |
|
SU950A1 |
| [онлайн], [найдено | |||
Авторы
Даты
2023-11-02—Публикация
2020-10-28—Подача