ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
1. Настоящее изобретение относится к области рассеянного склероза, в частности, к композиции и способам лечения рассеянного склероза.
УРОВЕНЬ ТЕХНИКИ
2. Рассеянный склероз (PC), представляющий собой "рубцовую ткань во множественных областях", является аутоиммунным заболеванием, при котором иммунная система атакует миелиновую оболочку, которая окружает и защищает нервные волокна центральной нервной системы (ЦНС), вызывая воспаление. Когда миелин или нервные волокна повреждены или разрушены при PC, повреждение областей ЦНС может вызывать множество неврологических симптомов, которые различаются у людей с PC по типу и тяжести. Существует четыре типа PC: клинически изолированный синдром (КИС), ремиттирующий рассеянный склероз (РРС), первично-прогрессирующий рассеянный склероз (ППРС) и вторично-прогрессирующий рассеянный склероз (ВПРС). Общие симптомы включают мышечную слабость, онемение и покалывание, симптом Лермитта, проблемы с мочевым пузырем, проблемы с кишечником, усталость, головокружение и вертиго, сексуальную дисфункцию, спастичность и мышечные спазмы, тремор, проблемы со зрением, изменения походки и подвижности, эмоциональные изменения и депрессию, проблемы с обучением и памятью, а также боль.
3. Причина возникновения PC неизвестна, но считается, что она связана с генетической предрасположенностью, нарушениями в иммунной системе и факторами окружающей среды, которые в совокупности провоцируют заболевание.
4. В то время как доступные лекарства помогают замедлить прогрессировать, изменяя способ функционирования иммунной системы или облегчая симптомы во время внезапного обострения болезни, когда человек испытывает ухудшение симптомов, по-прежнему существует серьезная потребность в новых лекарствах и способах лечения PC.
РАСКРЫТИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
5. Целью настоящего изобретения является создание фармацевтической композиции и способа для лечения рассеянного склероза у субъекта.
6. В некоторых вариантах осуществления настоящего изобретения способ лечения субъекта с рассеянным склерозом включает введение фармацевтической композиции субъекту с рассеянным склерозом в эффективном количестве; где указанная фармацевтическая композиция содержит кластер золота (AuC); причем указанный AuC содержит золотое ядро; и лиганд, связанный с золотым ядром.
7. В некоторых вариантах осуществления способа по настоящему изобретению золотое ядро имеет диаметр менее 3 нм. В некоторых вариантах осуществления способа золотое ядро имеет диаметр в интервале 0,5-2,6 нм.
8. В некоторых вариантах осуществления способа по настоящему изобретению лиганд представляет собой выбранный из группы, состоящей из L-цистеина и его производных, D-цистеина и его производных, цистеинсодержащих олигопептидов и их производных и других тиолсодержащих соединений.
9. В некоторых вариантах осуществления способа по настоящему изобретению L-цистеин и его производные выбирают из группы, включающей L-цистеин, N-изобутирил-L-цистеин (L-NIBC) и N-ацетил-L-цистеин (L-NAC), и где D-цистеин и его производные выбирают из группы, содержащей D-цистеин, N-изобутирил-D-цистеин (D-NIBC) и N-ацетил-D-цистеин (D-NAC).
10. В некоторых вариантах осуществления способа по настоящему изобретению цистеинсодержащие олигопептиды и их производные представляют собой цистеинсодержащие дипептиды, цистеинсодержащие трипептиды или цистеинсодержащие тетрапептиды.
11. В некоторых вариантах осуществления способа по настоящему изобретению цистеинсодержащие дипептиды выбирают из группы, состоящей из L-цистеин-L-аргинин дипептида (CR), L-аргинин-L-цистеин дипептида (RC), L-гистидин-L-цистеин дипептида (НС) и L-цистеин-L-гистидин дипептида (СН).
12. В некоторых вариантах осуществления способа по настоящему изобретению цистеинсодержащие трипептиды выбирают из группы, состоящей из глицин-L-цистеин-L-аргинин трипептида (GCR), L-пролин-L-цистеин-L-аргинин трипептида (PCR), L-лизин-L-цистеин-L-пролин трипептида (KCP) и L-глутатиона (GSH).
13. В некоторых вариантах осуществления способа по настоящему изобретению цистеинсодержащие тетрапептиды выбирают из группы, состоящей из глицин-L-серин-L-цистеин-L-аргинин тетрапептида (GSCR) и глицин-L-цистеин-L-серин-L-аргинин тетрапептида (GCSR).
14. В некоторых вариантах осуществления способа по настоящему изобретению другие тиолсодержащие соединения выбирают из группы, состоящей из 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L-пролина, тиогликолевой кислоты, меркаптоэтанола, тиофенола, D-3-троловола, N-(2-меркаптопропионил)-глицина и додецилмеркаптана.
15. В некоторых вариантах осуществления настоящего изобретения используется кластер золота (AuC) для приготовления лекарственного средства для лечения рассеянного склероза у субъекта, где указанный AuC содержит золотое ядро; и лиганд, связанный с золотым ядром.
16. В некоторых вариантах применения по настоящему изобретению золотое ядро имеет диаметр менее 3 нм. В некоторых вариантах применения золотое ядро имеет диаметр в интервале 0,5-2,6 нм.
17. В некоторых вариантах применения по настоящему изобретению лиганд представляет собой выбранный из группы, состоящей из L-цистеина и его производных, D-цистеина и его производных, цистеинсодержащих олигопептидов и их производных и других тиолсодержащих соединений.
18. В некоторых вариантах применения по настоящему изобретению L-цистеин и его производные выбирают из группы, состоящей из L-цистеина, N-изобутирил-L-цистеина (L-NIBC) и N-ацетил-L-цистеина (L-NAC), и где D-цистеин и его производные выбирают из группы, состоящей из D-цистеина, N-изобутирил-D-цистеина (D-NIBC) и N-ацетил-D-цистеина (D-NAC).
19. В некоторых вариантах применения по настоящему изобретению цистеинсодержащие олигопептиды и их производные представляют собой цистеинсодержащие дипептиды, цистеинсодержащие трипептиды или цистеинсодержащие тетрапептиды.
20. В некоторых вариантах применения по настоящему изобретению цистеинсодержащие дипептиды выбирают из группы, состоящей из L-цистеин-L-аргинин дипептида (CR), L-аргинин-L-цистеин дипептида (RC), L-гистидин-L-цистеин дипептида (НС) и L-цистеин-L-гистидин дипептида (СН).
21. В некоторых вариантах применения по настоящему изобретению цистеинсодержащие трипептиды выбирают из группы, состоящей из глицин-L-цистеин-L-аргинин трипептида (GCR), L-пролин-L-цистеин-L-аргинин трипептида (PCR), L-лизин-L-цистеин-L-пролин трипептида (KCP) и L-глутатиона (GSH).
22. В некоторых вариантах применения по настоящему изобретению цистеинсодержащие тетрапептиды выбирают из группы, состоящей из глицин-L-серин-L-цистеин-L-аргинин тетрапептида (GSCR) и глицин-L-цистеин-L-серин-L-аргинин тетрапептида (GCSR).
23. В некоторых вариантах применения по настоящему изобретению другие тиолсодержащие соединения выбирают из группы, состоящей из 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L-пролина, тиогликолевой кислоты, меркаптоэтанола, тиофенола, D-3-троловола, N-(2-меркаптопропионил)-глицина и додецилмеркаптана.
24. Цели и преимущества изобретения станут очевидными из следующего подробного описания предпочтительных вариантов его осуществления и прилагаемых чертежей.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
25. Предпочтительные варианты осуществления в соответствии с настоящим изобретением далее будут раскрыты со ссылкой на фигуры, на которых ссылочные цифры обозначают конкретные элементы.
26. На фиг. 1 показаны УФ-видимые области спектра, изображения полученные с помощью просвечивающего электронного микроскопа (ТЕМ) и диаграммы распределения частиц по размерам, модифицированных лигандом L-NIBC наночастиц золота (L-NIBC-AuNPs) с различными размерами частиц.
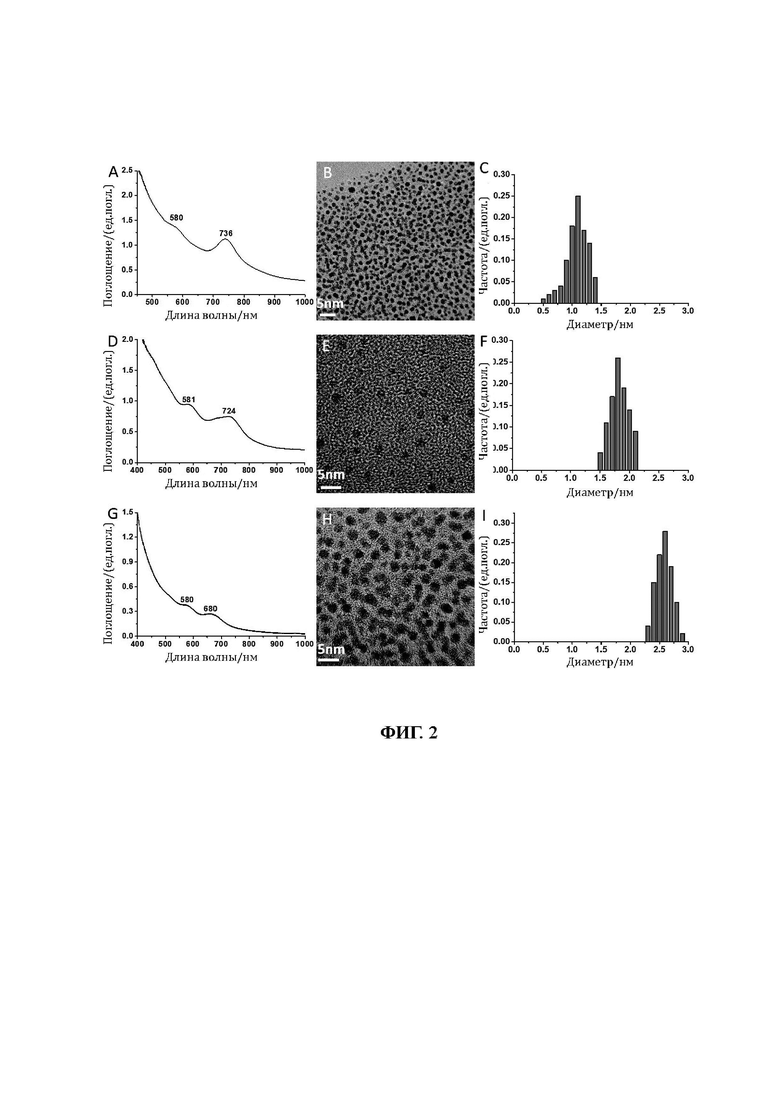
27. На фиг. 2 показаны УФ-видимые области спектра, изображения полученные с помощью ТЕМ и диаграммы распределения частиц по размерам, связанных лигандом L-NIBC кластеров золота (L-NIBC-AuCs) с различными размерами частиц.
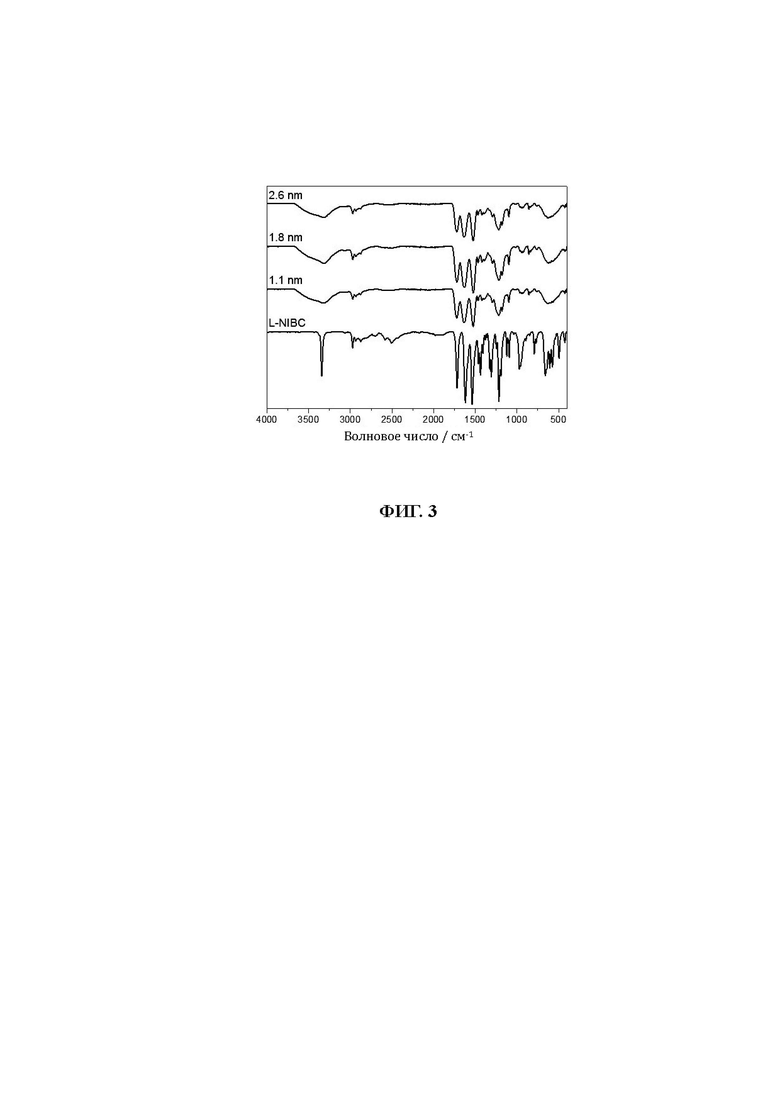
28. На фиг. 3 показаны инфракрасные области спектра L-NIBC-AuCs с различными размерами частиц.
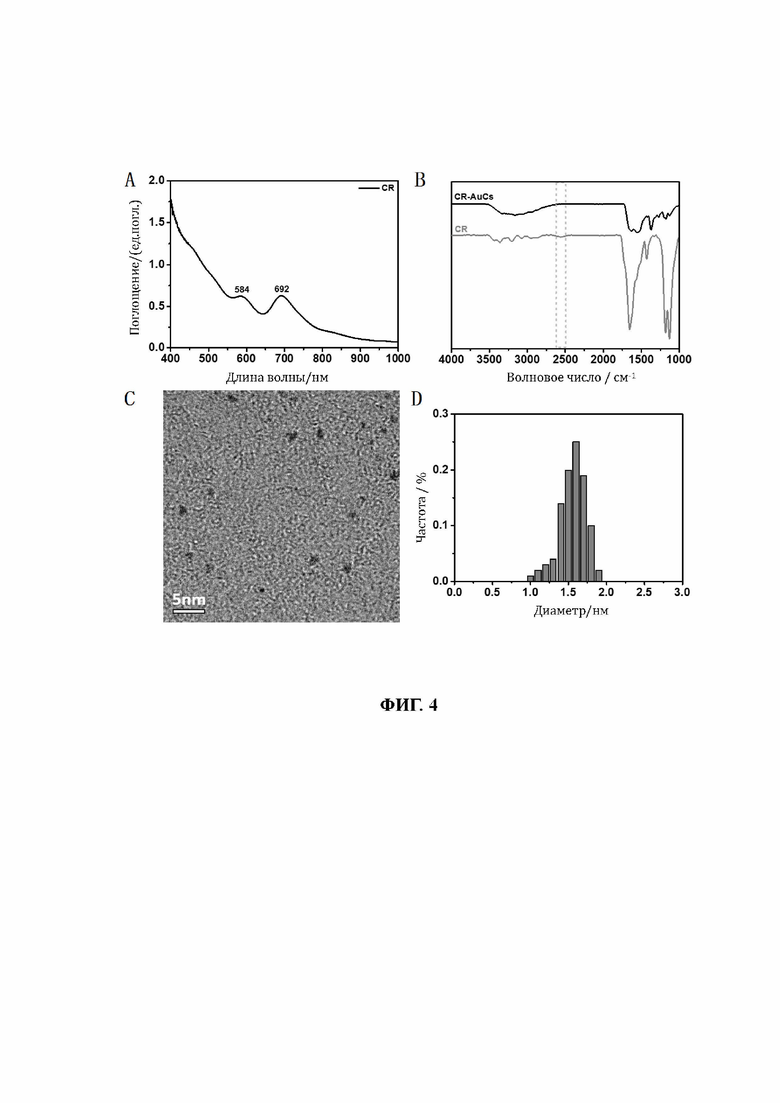
29. На фиг. 4 показаны УФ-видимые области спектра, инфракрасные области спектра, изображения полученные с помощью ТЕМ и диаграммы распределения частиц по размерам, связанных CR-лигандом кластеров золота (CR-AuCs).
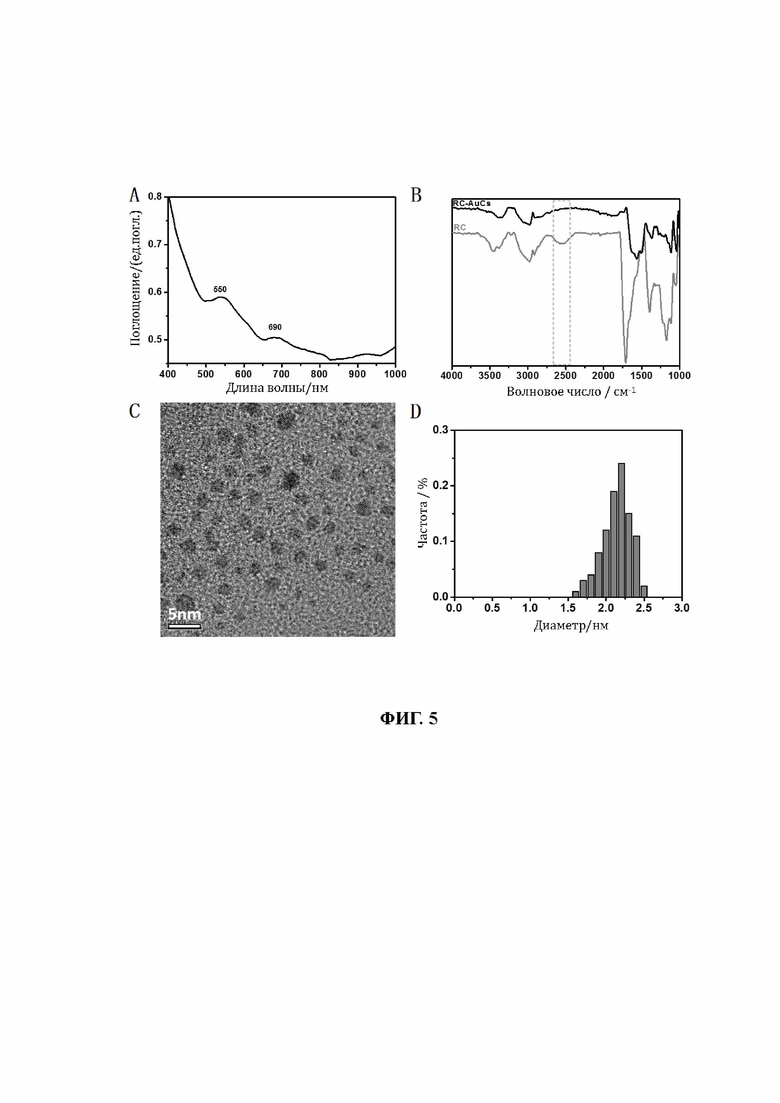
30. На фиг. 5 показаны УФ-видимые области спектра, инфракрасные области спектра, изображения полученные с помощью ТЕМ и диаграммы распределения частиц по размерам, связанных RC-лигандом кластеров золота (RC-AuCs).
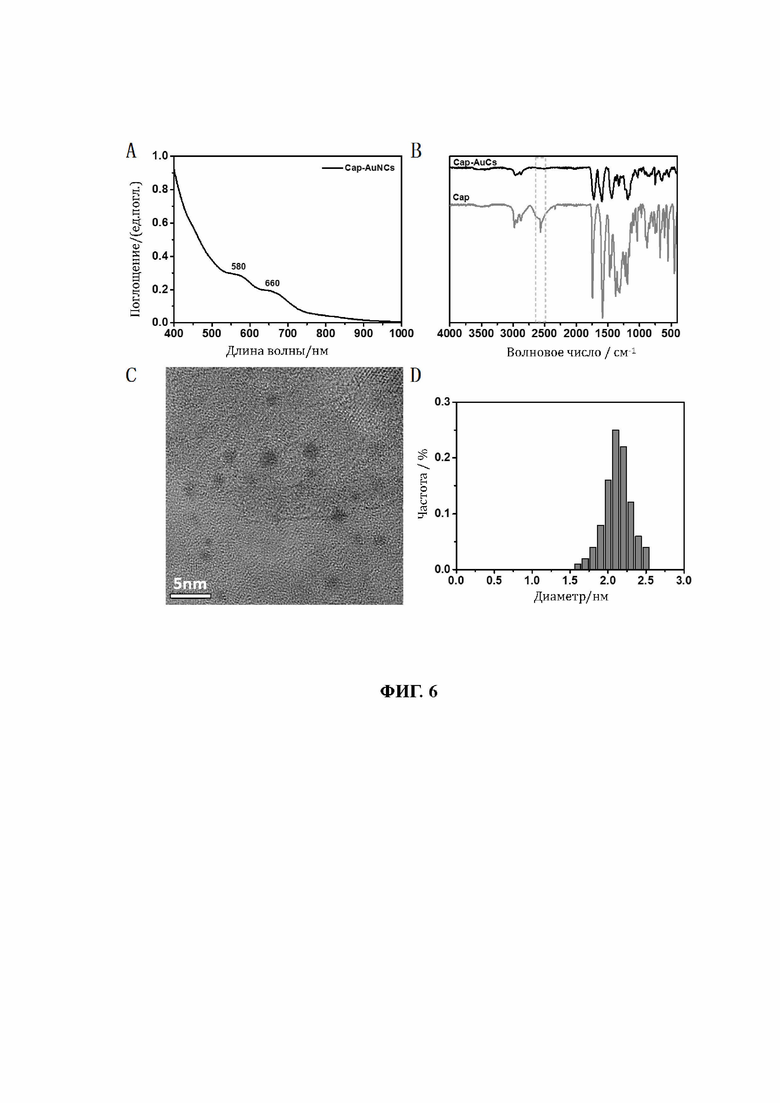
31. На фиг. 6 показаны УФ-видимые области спектра, инфракрасные области спектра, изображения полученные с помощью ТЕМ и диаграммы распределения частиц по размерам, связанных лигандом 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L-пролина (т.е. Сар) кластеров золота (Cap-AuCs).
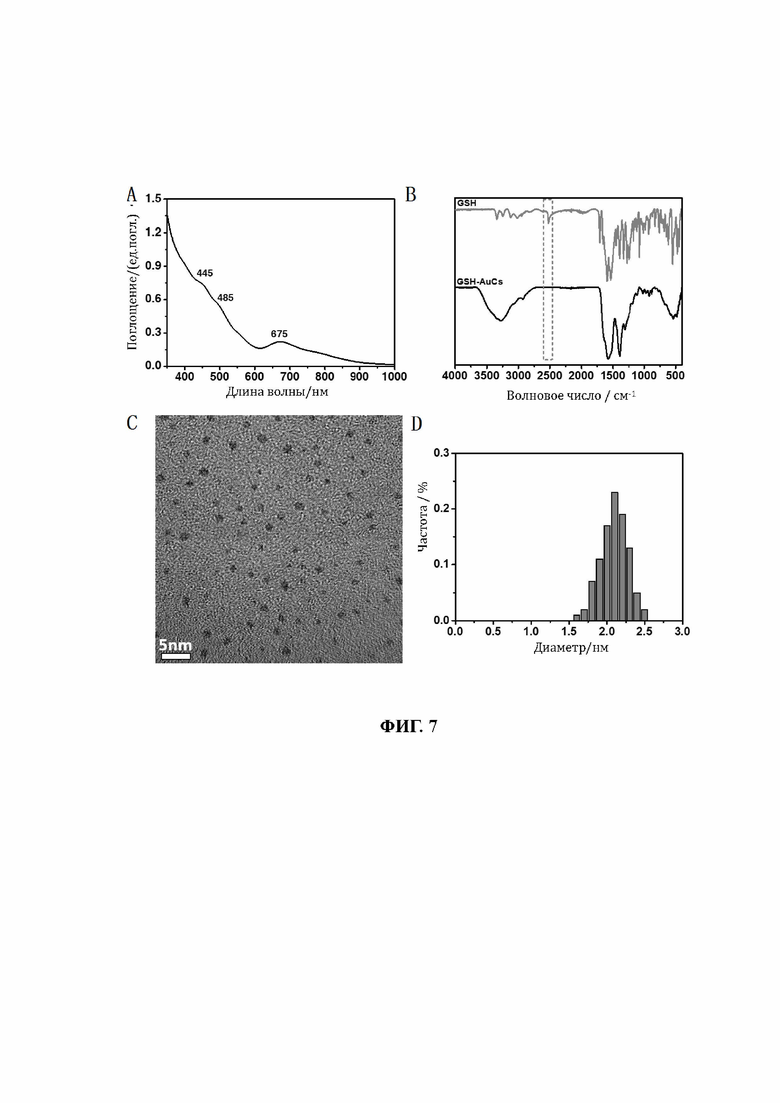
32. На фиг. 7 показаны УФ-видимые области спектра, инфракрасные области спектра, изображения полученные с помощью ТЕМ и диаграммы распределения частиц по размерам, связанных лигандом GSH кластеров золота (GSH-AuCs).
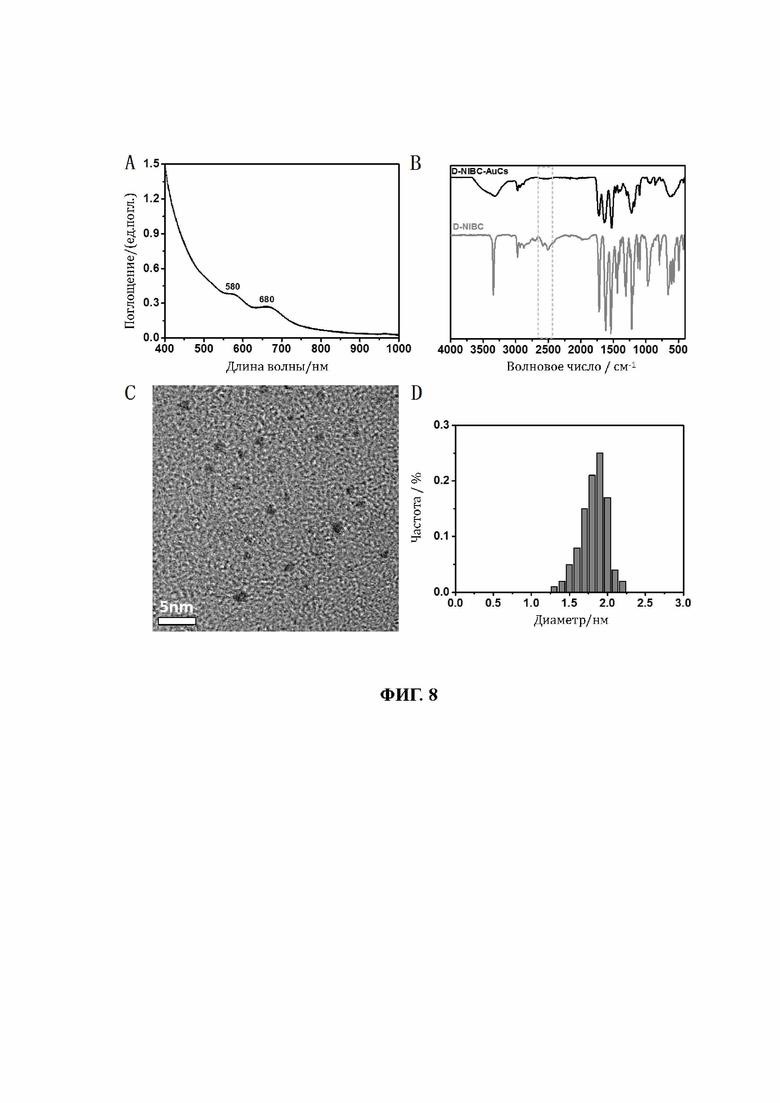
33. На фиг. 8 показаны УФ-видимые области спектра, инфракрасные области спектра, изображения полученные с помощью ТЕМ и диаграммы распределения частиц по размерам, связанных лигандом D-NIBC кластеров золота (D-NIBC-AuCs).
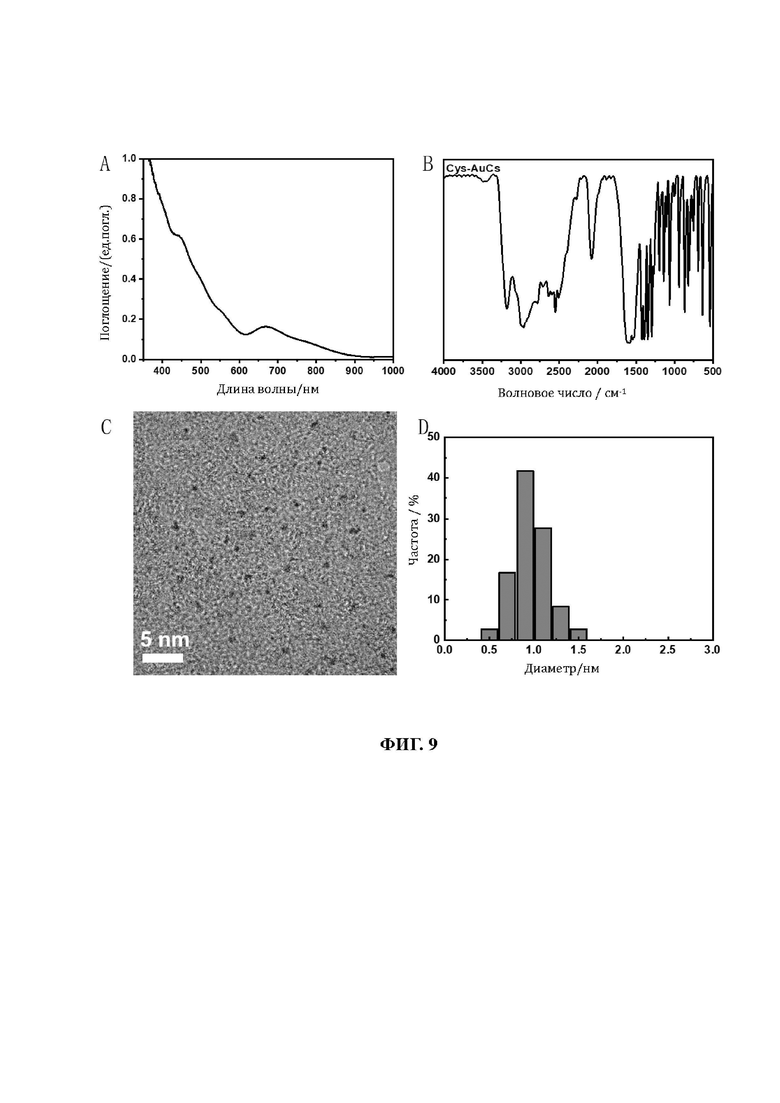
34. На фиг. 9 показаны УФ-видимые области спектра, инфракрасные области спектра, изображения полученные с помощью ТЕМ и диаграммы распределения частиц по размерам, связанных лигандом L-цистеином кластеров золота (L-Cys-AuCs).
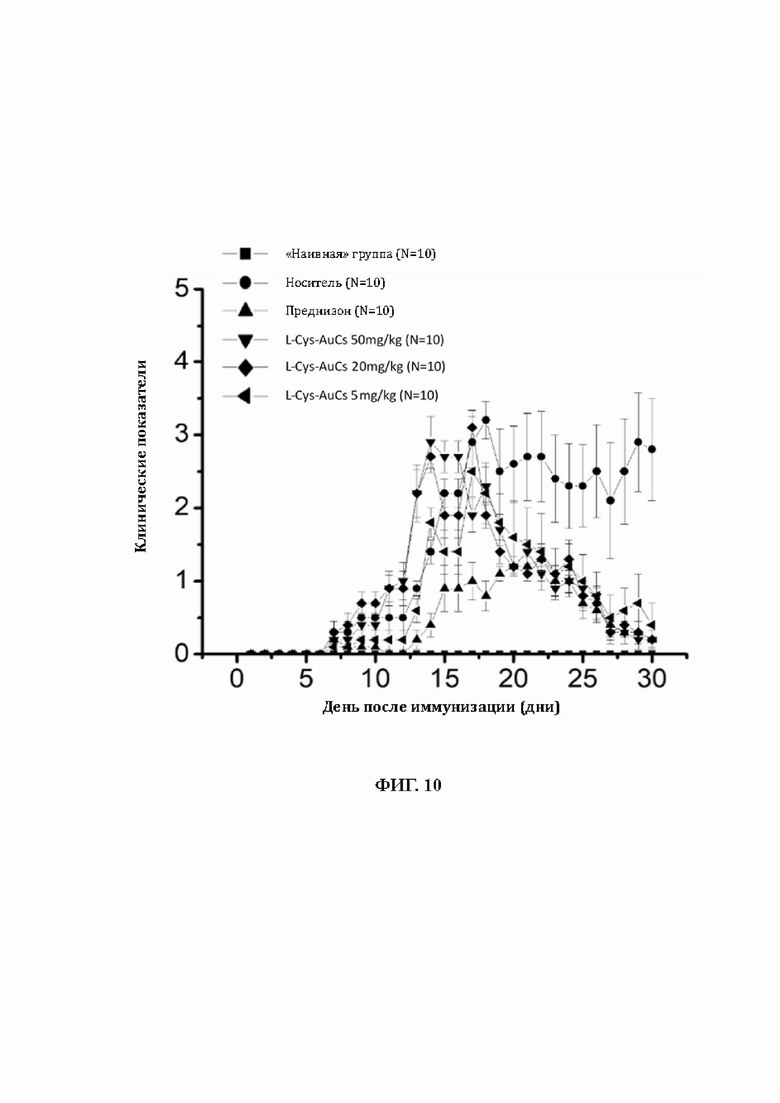
35. На фиг. 10 представлен график, показывающий клинические показатели ЕАЕ.
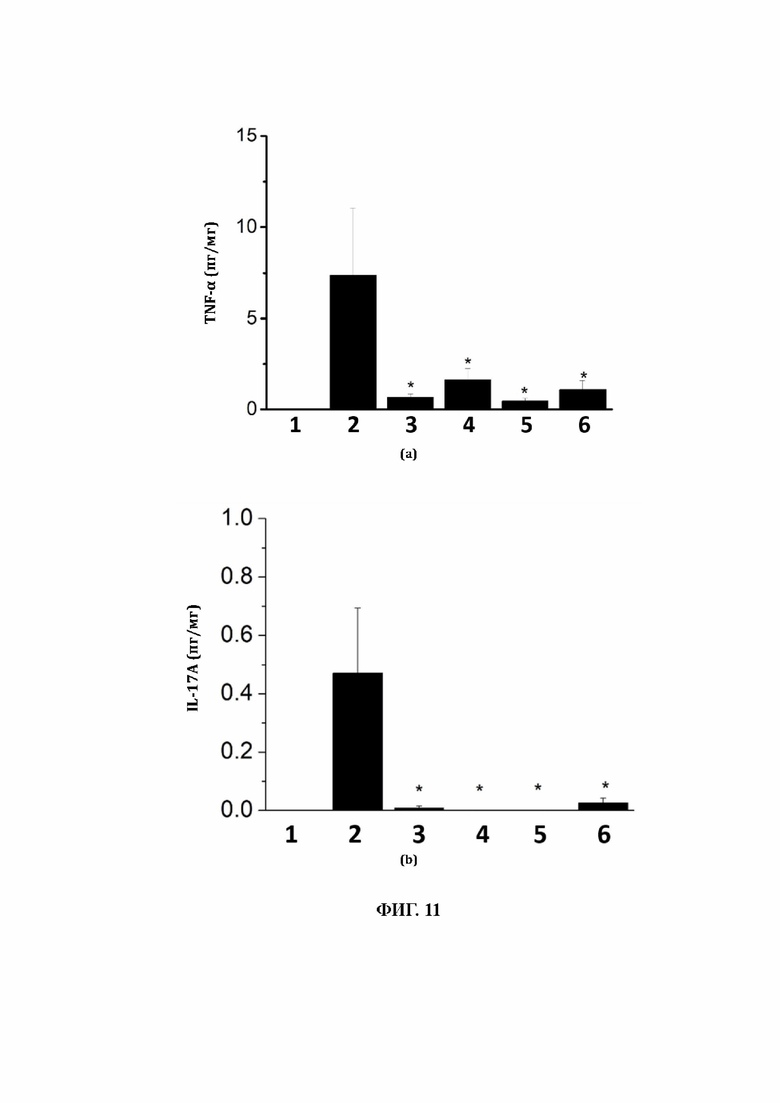
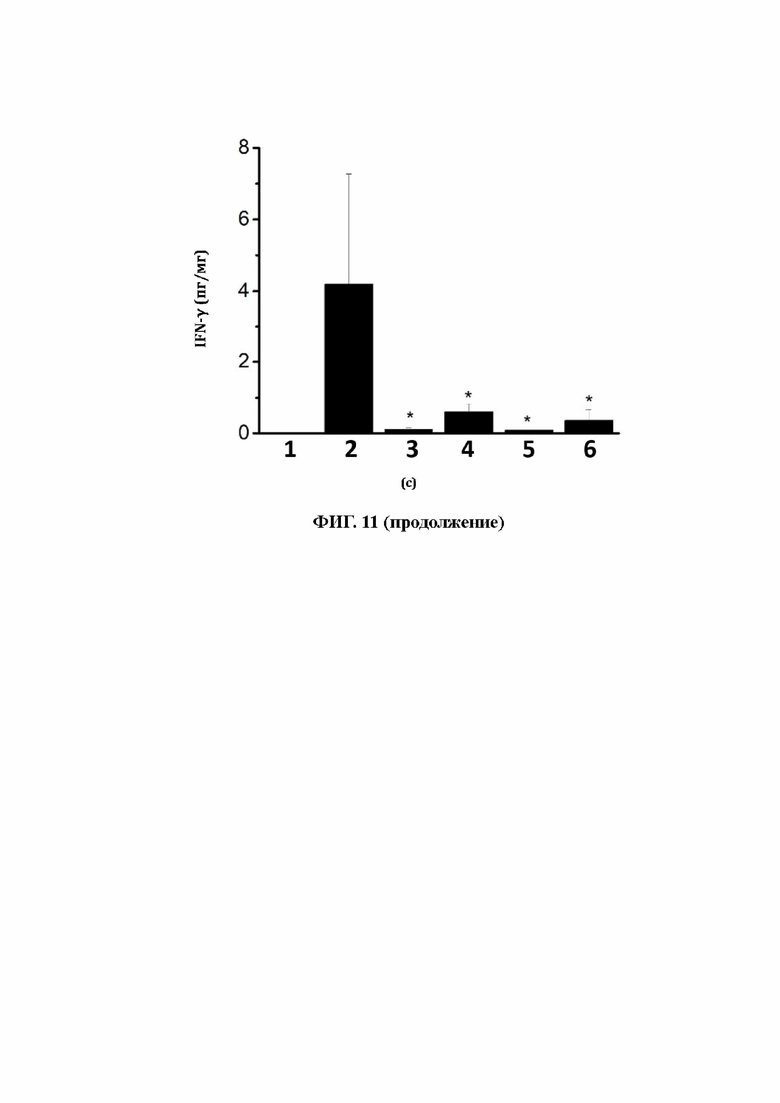
36. На фиг. 11 показаны уровни (a) TNF-α, (b) IL-17 и (с) IFN-γ в спинном мозге, где 1 обозначает «наивную» группу, 2 обозначает группу, получавшую физиологический раствор, 3 обозначает группу, получавшую преднизон, 4 обозначает группу, получавшую 50 мг/кг L-Cys-AuCs, 5 обозначает группу, получавшую 20 мг/кг L-Cys-AuCs, и 6 обозначает группу, получавшую 5 мг/кг L-Cys-AuCs.
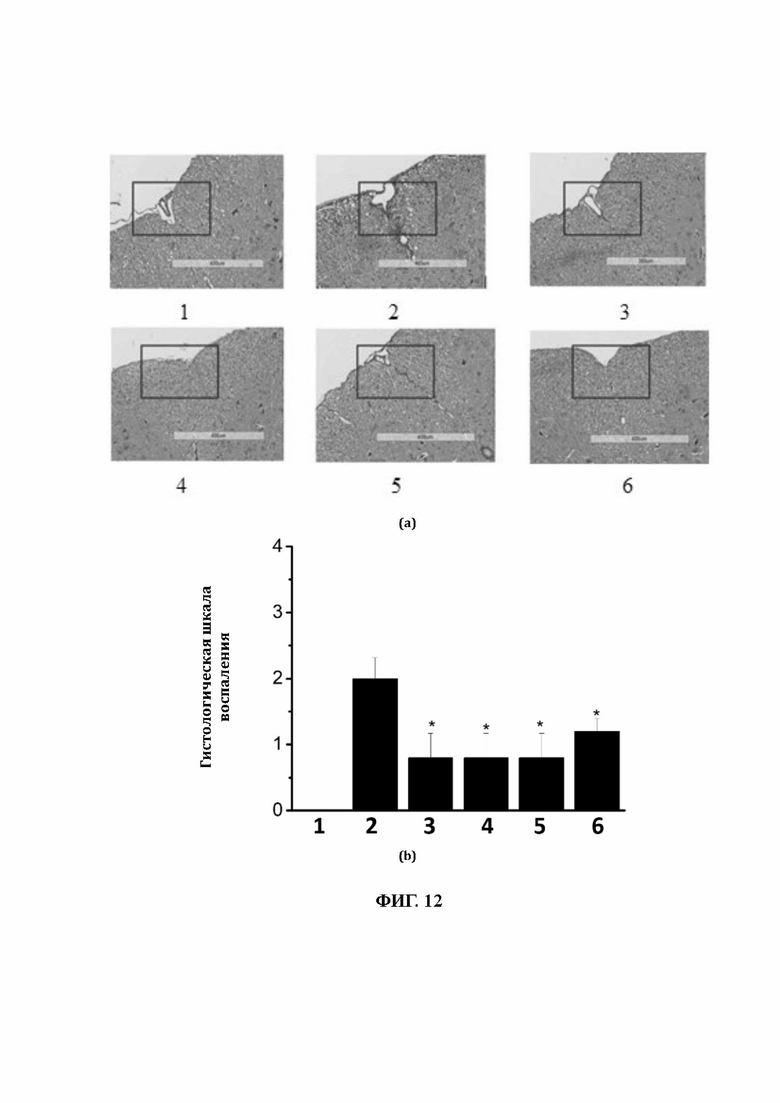
37. На фиг. 12 показаны (а) изображения окрашивания спинного мозга методом с использованием красителей гематоксилина и эозина (НЕ), показывающие инфильтрацию иммунных клеток в спинной мозг, и (b) гистограмма, показывающая гистологические масштабы воспаления; где 1 обозначает «наивную» группу, 2 обозначает группу, получавшую физиологический раствор, 3 обозначает группу, получавшую преднизон, 4 обозначает группу, получавшую 50 мг/кг L-Cys-AuCs, 5 обозначает группу, получавшую 20 мг/кг L-Cys-AuCs, и 6 обозначает группу, получавшую 5 мг/кг L-Cys-AuCs.
ОСУЩЕСТВЛЕНИЕ ИЗОБРЕТЕНИЯ
38. Следующее подробное описание некоторых вариантов осуществления изобретения даст возможность лучше понять настоящее изобретение.
39. По всему тексту данной заявки, где есть ссылки на публикации, полные описания этих публикаций включены в эту заявку в виде ссылок, для более полного раскрытия уровня техники, к которому относится данное изобретение.
40. Кластеры золота (AuCs) - это особая форма золота, существующая между атомами золота и наночастицами золота. AuCs имеют размер менее 3 нм и состоят из атомов золота в количестве от всего нескольких до нескольких сотен, что приводит к разрушению гранецентрированной кубической структуры укладки наночастиц золота. В результате AuCs демонстрируют молекулоподобные дискретные электронные структуры с отчетливым HOMO-LUMO-зазором, в отличие от непрерывных или квазинепрерывных энергетических уровней наночастиц золота. Это приводит к исчезновению эффекта поверхностного плазмонного резонанса и соответствующей полосы поглощения плазмонного резонанса (520±20 нм) в УФ-видимой области спектра, которой обладают обычные наночастицы золота.
41. В настоящем изобретении представлен AuC, связанный лигандами.
42. В некоторых вариантах осуществления изобретения AuC, связанный с лигандами, содержит лиганд и золотое ядро, где лиганд связан с золотым ядром. В некоторых вариантах осуществления изобретения диаметр золотого ядра находится в интервале 0,5-3 нм. В некоторых вариантах осуществления изобретения диаметр золотого ядра находится в интервале 0,5-2,6 нм.
43. В некоторых вариантах осуществления изобретения лиганд AuC, связанного с лигандами, представляет собой тиолсодержащее соединение или олигопептид. В некоторых вариантах лиганд связывается с золотым ядром с образованием связанного лигандами AuC через связь Au-S.
44. В некоторых вариантах осуществления изобретения лиганд представляет собой, но не ограничивается, L-цистеин, D-цистеин или производное цистеина. В некоторых вариантах осуществления изобретения производным цистеина является N-изобутирил-L-цистеин (L-NIBC), N-изобутирил-D-цистеин (D-NIBC), N-ацетил-L-цистеин (L-NAC) или N-ацетил-D-цистеин (D-NAC).
45. В некоторых вариантах осуществления изобретения лиганд представляет собой, но не ограничивается, цистеинсодержащий олигопептид и его производные. В некоторых вариантах осуществления изобретения цистеинсодержащий олигопептид представляет собой цистеинсодержащий дипептид. В некоторых вариантах осуществления изобретения цистеинсодержащий дипептид представляет собой L-цистеин-L-аргинин дипептид (CR), L-аргинин-L-цистеин дипептид (RC) или L-цистеин-L-гистидин дипептид (СН). В некоторых вариантах осуществления изобретения цистеинсодержащий олигопептид представляет собой цистеинсодержащий трипептид. В некоторых вариантах осуществления изобретения цистеинсодержащий трипептид представляет собой глицин-L-цистеин-L-аргинин трипептид (GCR), L-пролин-L-цистеин-L-аргинин трипептид (PCR) или L-глутатион (GSH). В некоторых вариантах осуществления изобретения цистеинсодержащий олигопептид представляет собой цистеинсодержащий тетрапептид. В некоторых вариантах осуществления изобретения цистеинсодержащий тетрапептид представляет собой глицин-L-серин-L-цистеин-L-аргинин тетрапептид (GSCR) или глицин-L-цистеин-L-серин-L-аргинин тетрапептид (GCSR).
46. В некоторых вариантах осуществления изобретения лиганд представляет собой тиолсодержащее соединение. В некоторых вариантах тиолсодержащее соединение представляет собой 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L-пролин, тиогликолевую кислоту меркаптоэтанол, тиофенол, D-3-троловол или додецилмеркаптан.
47. Настоящее изобретение раскрывает фармацевтическую композицию для лечения рассеянного склероза у субъекта. В некоторых вариантах осуществления изобретения субъектом является человек. В некоторых вариантах осуществления изобретения субъектом является домашнее животное, такое как собака.
48. В некоторых вариантах осуществления изобретения фармацевтическая композиция содержит AuC, связанный с лигандами, как описано выше, и фармацевтически приемлемое вспомогательное вещество. В некоторых вариантах осуществления изобретения вспомогательным веществом является фосфатно-буферный раствор или физиологический раствор.
49. Настоящее изобретение раскрывает применение описанных выше AuCs, связанных лигандами, для приготовления лекарственного средства для лечения рассеянного склероза у субъекта.
50. Настоящее изобретение раскрывает применение описанных выше AuCs, связанных лигандами, для лечения рассеянного склероза у субъекта, или способ лечения рассеянного склероза у субъекта с применением описанных выше AuCs, связанных лигандами. В некоторых вариантах осуществления изобретения способ лечения включает введение субъекту фармацевтически эффективного количества AuCs, связанных лигандами. Фармацевтически эффективное количество может быть установлено с помощью обычных исследований in vivo.
51. Следующие примеры приведены с единственной целью проиллюстрировать принципы настоящего изобретения; они никоим образом не ограничивают объем настоящего изобретения.
52. Примеры
53. 1. Получение AuCs, связанных лигандами
54. 1.1 Растворяют HAuCl4 в метаноле, воде, этаноле, n-пропаноле или этилацетате для получения раствора А, где концентрация HAuCl4 составляет 0,01~0,03М;
55. 1.2 Растворяют лиганд с помощью растворителя для получения раствора В, где концентрация лиганда составляет 0,01~0,18М; лиганд включает, но не ограничивается, L-цистеин, D-цистеин и другие производные цистеина, такие как N-изобутирил-L-цистеин (L-NIBC), N-изобутирил-D-цистеин (D-NIBC), N-ацетил-L-цистеин (L-NAC), и N-ацетил-D-цистеин (D-NAC), цистеинсодержащие олигопептиды и их производные, включая, но не ограничиваясь, дипептиды, трипептиды, тетрапептиды и другие цистеинсодержащие пептиды, такие как L-цистеин-L-аргинин дипептид (CR), L-аргинин-L-цистеин дипептид (RC), L-цистеин L-гистидин дипептид (СН), глицин-L-цистеин-L-аргинин трипептид (GCR), L-пролин-L-цистеин-L-аргинин трипептид (PCR), L-глутатион (GSH), глицин-L-серин-L-цистеин-L-аргинин тетрапептид (GSCR) и глицин-L-цистеин-L-серин-L-аргинин тетрапептид (GCSR), и другие тиолсодержащие соединения, такие как одно или более, выбранные из 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L-пролина, тиогликолевой кислоты, меркаптоэтанола, тиофенола, D-3-троловола и додецилмеркаптана; растворителем является один или более, выбранный из метанола, этилацетата, воды, этанола, n-пропанола, пентана, муравьиной кислоты, уксусной кислоты, диэтилового эфира, ацетона, анизола, 1-пропанола, 2-пропанола, 1-бутанола, 2-бутанола, пентанола, бутилацетата, трибутилметилового эфира, изопропилацетата, диметилсульфоксида, этилформиата, изобутилацетата, метилацетата, 2-метил-1-пропанолаи пропилацетата;
56. 1.3 Смешивают раствор А и раствор В так, что мольное соотношение между HAuCl4 и лигандом составляет 1:(0,01~100), перемешивают их на ледяной бане в течение 0,1~48 часов, добавляют 0,025~0,8 М раствора NaBH4, этанола или метанола, продолжают перемешивать на водяной бане со льдом и проводят реакцию в течение 0,1~12 часов. Мольное соотношение между NaBH4 и лигандом составляет 1:(0,01~100);
57. 1.4 Используют ультрафильтрационные пробирки 3K~30K MWCO для градиентного центрифугирования реакционного раствора при 8000~17500 об/мин в течение 10~100 мин после окончания реакции для получения осадка AuCs, связанного лигандами, с различными средними размерами частиц. Апертура фильтрующих мембран для ультрафильтрационных трубок различных пределов отсечения по молекулярной массе (MWCO) напрямую определяет размер AuCs, связанных лигандами, которые могут проходить через мембраны. Этот этап может быть при необходимости исключен;
58. 1.5 Растворяют осадок AuCs, связанных лигандами, с различными средними размерами частиц, полученный на этапе (1.4), в воде, помещая его в диализный мешок и подвергая его диализу в воде при комнатной температуре в течение 1~7 дней;
59. 1.6 Проводят лиофильную сушку AuCs, связанных лигандами, в течение 12~24 часов после диализа для получения порошкообразного или флокулянтного вещества, т.е. AuCs, связанных лигандами.
60. Как было обнаружено, размер частиц порошкообразного или флокулирующего вещества, полученного вышеуказанным способом, составляет менее 3 нм (в основном в пределах 0,5-2,6 нм). Нет очевидного пика поглощения при 520 нм. Определено, что полученные порошок или хлопья представляют собой AuCs, связанные лигандами.
61. 2. Получение и характеристика AuCs, связанных различными лигандами
62. 2.1 Получение AuCs, связанных L-NIBC, т.е. L-NIBC-AuCs
63. На примере лиганда L-NIBC подробно описано получение и подтверждение AuCs, связанных лигандом L-NIBC.
64. 2.1.1 Взвешивают 1,00 г HAuCl4 и растворяют его в 100 мл метанола для получения 0,03 М раствора А;
65. 2.1.2 Взвешивают 0,57 г L-NIBC и растворяют его в 100 мл ледяной уксусной кислоты (уксусной кислоты) для получения 0,03 М раствора В;
66. 2.1.3 Отмеряют 1 мл раствора А, смешивают его с 0,5 мл, 1 мл, 2 мл, 3 мл, 4 мл или 5 мл раствора В соответственно (т.е. мольное соотношение между HAuCl4 и L-NIBC равно 1:0.5, 1:1, 1:2, 1:3, 1:4, 1:5 соответственно), проводят реакцию на ледяной бане при перемешивании в течение 2 часов, быстро добавляют 1 мл свежеприготовленного 0,03 М (приготовленного путем взвешивания 11,3 мг NaBH4 и растворения его в 10 мл этанола) этанольного раствора NaBH4, когда раствор из ярко-желтого превратится в бесцветный, продолжают реакцию в течение 30 мин, далее после того как раствор приобретет темно-коричневый цвет, добавляют 10 мл ацетона для прекращения реакции.
67. 2.1.4 После реакции реакционный раствор подвергают градиентному центрифугированию для получения порошка L-NIBC-AuCs с различными размерами частиц. Конкретный способ: после завершения реакции реакционный раствор переносят в ультрафильтрационную пробирку 30К MWCO объемом 50 мл и центрифугируют при 10000 об/мин в течение 20 мин, а ретентат во внутренней пробирке растворяют в сверхчистой воде для получения порошка с размером частиц около 2,6 нм. Затем смешанный раствор во внешней пробирке переносят в ультрафильтрационную пробирку 10К MWCO объемом 50 мл и центрифугируют при 13000 об/мин в течение 30 мин. Ретентат во внутренней трубке растворяют в сверхчистой воде для получения порошка с размером частиц около 1,8 нм. Затем смешанный раствор во внешней пробирке переносят в ультрафильтрационную пробирку 3K MWCO объемом 50 мл и центрифугируют при 17500 об/мин в течение 40 мин. Ретентат во внутренней трубке растворяют в сверхчистой воде для получения порошка с размером частиц около 1,1 нм.
68. 2.1.5 Осаждают порошок с тремя различными размерами частиц, полученный градиентным центрифугированием, удаляют растворитель, соответственно, высушивают сырой продукт N2, растворяют его в 5 мл сверхчистой воды, помещают в диализный мешок (MWCO составляет 3 кДа), помещают диализный мешок в 2 л сверхчистой воды, меняют воду каждый последующий день, подвергают его диализу в течение 7 дней, высушивают посредством лиофилизации и сохраняют для дальнейшего использования.
69. 2.2 Определение характеристики L-NIBC-AuCs
70. Эксперимент по определению характеристик был проведен в отношении порошка, полученного выше (L-NIBC-AuCs). Между тем, в качестве контроля используются модифицированные лигандом L-NIBC наночастицы золота (L-NIBC-AuNPs). Способ получения наночастиц золота, модифицированных лигандом, представляющим собой L-NIBC, относится к ссылке (W. Yan, L. Xu, С. Xu, W. Ma, H. Kuang, L. Wang и N.A. Kotov, Journal of the American Chemical Society 2012, 134, 15114; X. Yuan, B. Zhang, Z. Luo, Q. Yao, D.T. Leong, N. Yan and J. Xie, Angewandte Chemie International Edition 2014, 53, 4623).
71. 2.2.1 Наблюдение за морфологией с помощью просвечивающего электронного микроскопа (ТЕМ)
72. Тестовые порошки (образец L-NIBC-AuCs и образец L-NIBC-AuNPs) растворяли в сверхчистой воде до 2 мг/л, а затем способом висячей капли готовили тестовые образцы. Более конкретно, образцы объемом 5 мкл капали на ультратонкую углеродную пленку, где они испарялись естественным путем до полного исчезновения капли воды, а затем наблюдали за морфологией образцов с помощью ТЕМ высокого разрешения с полевой эмиссией JEM-2100F STEM/EDS.
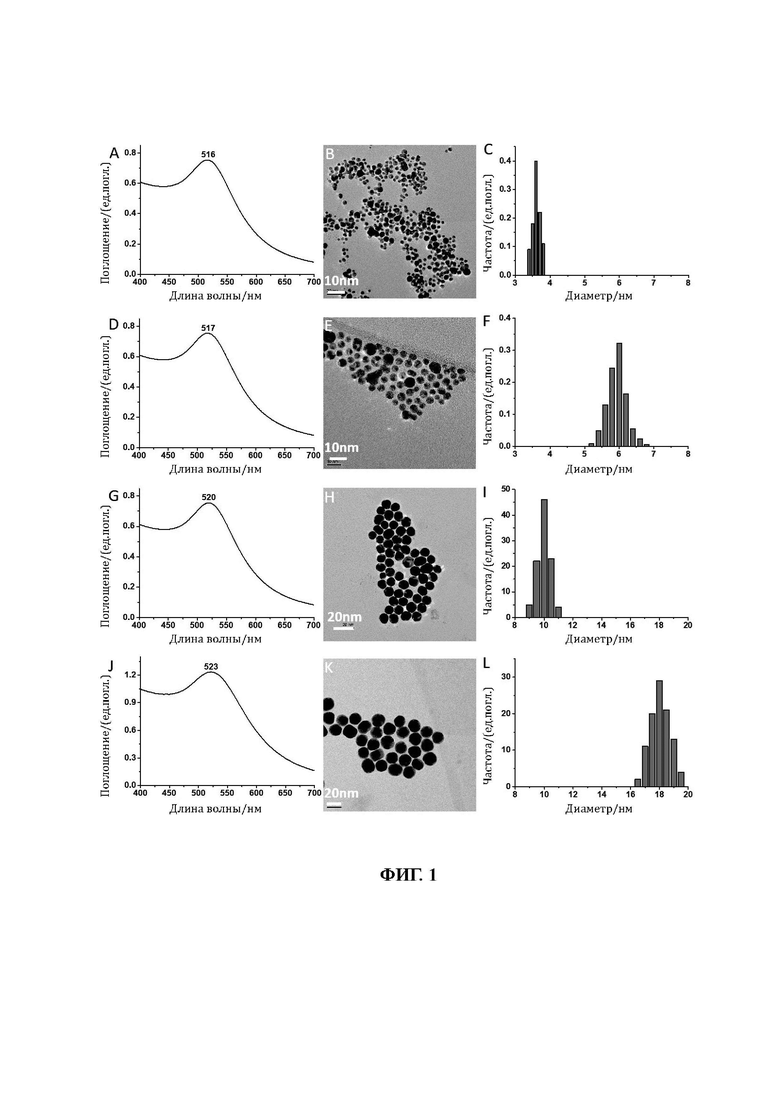
73. Четыре изображения L-NIBC-AuNPs, сделанных с помощью ТЕМ, показаны на снимках В, Е, Н и K на фиг. 1; три изображения L-NIBC-AuCs, сделанных с помощью ТЕМ, показаны на снимках В, Е и Н на фиг. 2.
74. Изображения на фиг.2 показывают, что каждый из образцов L-NIBC-AuCs имеет однородный размер частиц и хорошую диспергируемость, а средний диаметр L-NIBC-AuCs (см. диаметр золотого ядра) составляет 1,1 нм, 1,8 нм и 2,6 нм соответственно, что хорошо согласуется с результатами на снимках С, F и I на фиг. 2. Для сравнения образцы L-NIBC-AuNPs имеют больший размер частиц. Их средний диаметр (см. диаметр золотого ядра) составляет 3,6 нм, 6,0 нм, 10,1 нм и 18,2 нм соответственно, что хорошо согласуется с результатами на снимках С, F, I и L на фиг. 1.
75. 2.2.2 УФ-видимые спектры поглощения (UV-vis)
76. Тестируемые порошки (образец L-NIBC-AuCs и образец L-NIBC-AuNPs) растворяли в сверхчистой воде до концентрации 10 мг⋅л-1, и УФ-видимые спектры поглощения измеряли при комнатной температуре. Диапазон сканирования составлял 190-1100 нм, ячейка для образца представляла собой стандартную кварцевую кювету с длиной оптического пути 1 см, а эталонная ячейка была заполнена сверхчистой водой.
77. УФ-видимые спектры поглощения четырех образцов L-NIBC-AuNPs различных размеров показаны на снимках A, D, G и J на фиг. 1, а статистическое распределение размера частиц показано на снимках С, F, I и L на фиг. 1; УФ-видимые спектры поглощения трех образцов L-NIBC-AuCs с различных размеров показаны на снимках A, D и G на фиг. 2, а статистическое распределение размеров частиц показано на снимках С, F и I на фиг. 2.
78. На фиг.1 показано, что из-за эффекта поверхностного плазмона L-NIBC-AuNPs имели пик поглощения около 520 нм. Положение пика поглощения зависит от размера частиц. Когда размер частиц составляет 3,6 нм, пик поглощения УФ-излучения возникает при 516 нм; когда размер частиц составляет 6,0 нм, пик поглощения УФ-излучения возникает при 517 нм; когда размер частиц составляет 10,1 нм, пик поглощения УФ-излучения возникает при 520 нм, а когда размер частиц составляет 18,2 нм, пик поглощения УФ-излучения возникает при 523 нм. Ни один из четырех образцов не имеет пика поглощения выше 560 нм.
79. На фиг. 2 показано, что в УФ-видимых спектрах поглощения трех образцов L-NIBC-AuCs с различными размерами частиц, пик поглощения эффекта поверхностного плазмона при 520 нм исчез, а два очевидных пика поглощения возникли выше 560 нм, и положение пиков поглощения незначительно менялось в зависимости от размеров частиц AuCs. Это связано с тем, что AuCs проявляют молекулоподобные свойства из-за разрушения гранецентрированной кубической структуры, что приводит к разрыву плотности состояний AuCs, расщеплению энергетического уровня, исчезновению эффекта плазмонного резонанса и возникновению нового пика поглощения в длинноволновом направлении. Можно сделать вывод, что все три образца порошка с различными размерами частиц, полученные выше, являются AuCs, связанными лигандами.
80. 2.2.3 Инфракрасная спектроскопия с преобразованием Фурье
81. Инфракрасные спектры измерялись на инфракрасном спектрометре с преобразованием Фурье VERTEX80V производства Bruker в режиме полного отражения плотного порошка в глубоком вакууме. Диапазон сканирования составляет 4000-400 см-1, а количество сканирований - 64. В качестве примера были взяты образцы L-NIBC-AuCs, таким образом тестовые образцы представляли собой сухой порошок L-NIBC-AuCs с тремя различными размерами частиц, а контрольный образец представлял собой чистый порошок L-NIBC. Результаты показаны на фиг. 3.
82. На фиг. 3 показан инфракрасный спектр L-NIBC-AuCs с различными размерами частиц. По сравнению с чистым L-NIBC (кривая внизу), все колебания растяжения S-Н L-NIBC-AuCs с различными размерами частиц полностью исчезли при 2500-2600 см-1, в то время как другие характеристические пики L-NIBC все еще наблюдались, подтверждая, что молекулы L-NIBC были успешно связаны с поверхностью AuCs через связь Au-S. На фигуре также показано, что инфракрасный спектр AuCs, связанных лигандами, не имеет отношения к его размеру.
83. AuCs, связанные другими лигандами, получали способом, аналогичным вышеуказанному, за исключением того, что растворитель для раствора В, соотношение подачи между HAuCl4 и лигандом, время реакции и количество добавляемого NaBH4 были слегка скорректированы. Например: когда в качестве лиганда используют L-цистеин, D-цистеин, N-изобутирил-L-цистеин (L-NIBC) или N-изобутирил-D-цистеин (D-NIBC), в качестве растворителя выбирают уксусную кислоту; когда в качестве лиганда используют дипептид CR, дипептид RC или 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L-пролин, в качестве растворителя выбирают воду, и так далее, и тому подобное; другие этапы аналогичны, поэтому никакой дополнительной информации здесь не приводится.
84. С помощью настоящего изобретения вышеуказанным способом был подготовлен и получен ряд AuCs, связанных лигандами. Лиганды и параметры процесса получения приведены в таблице 1.
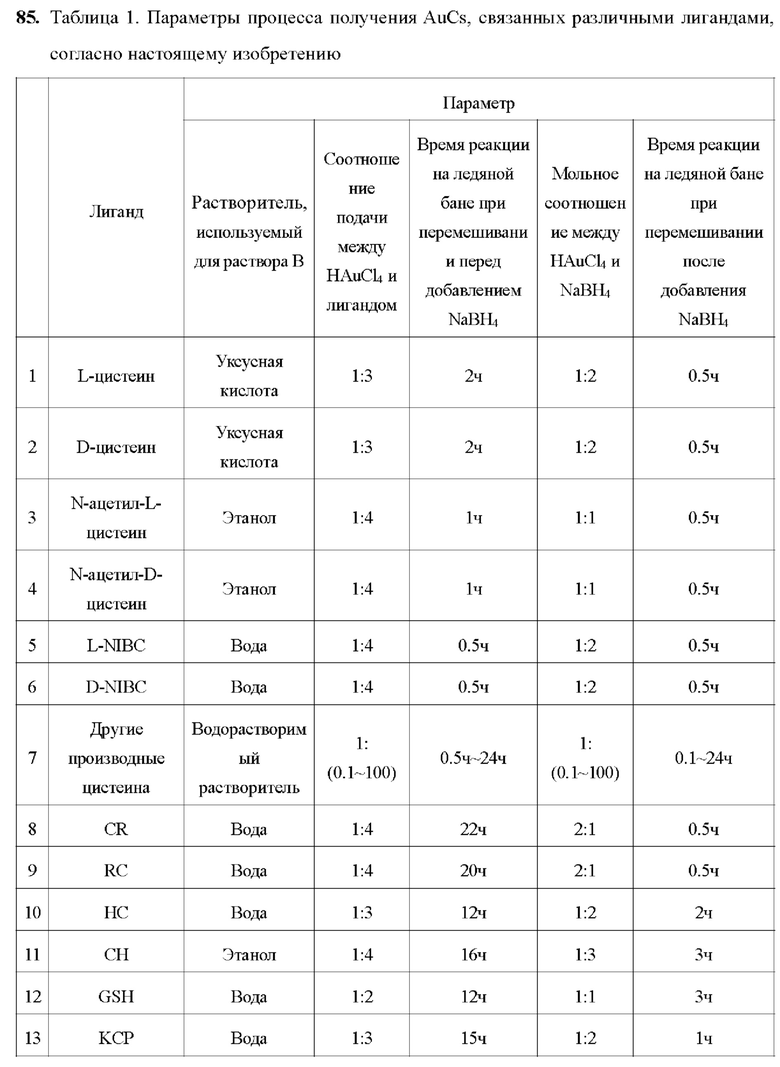
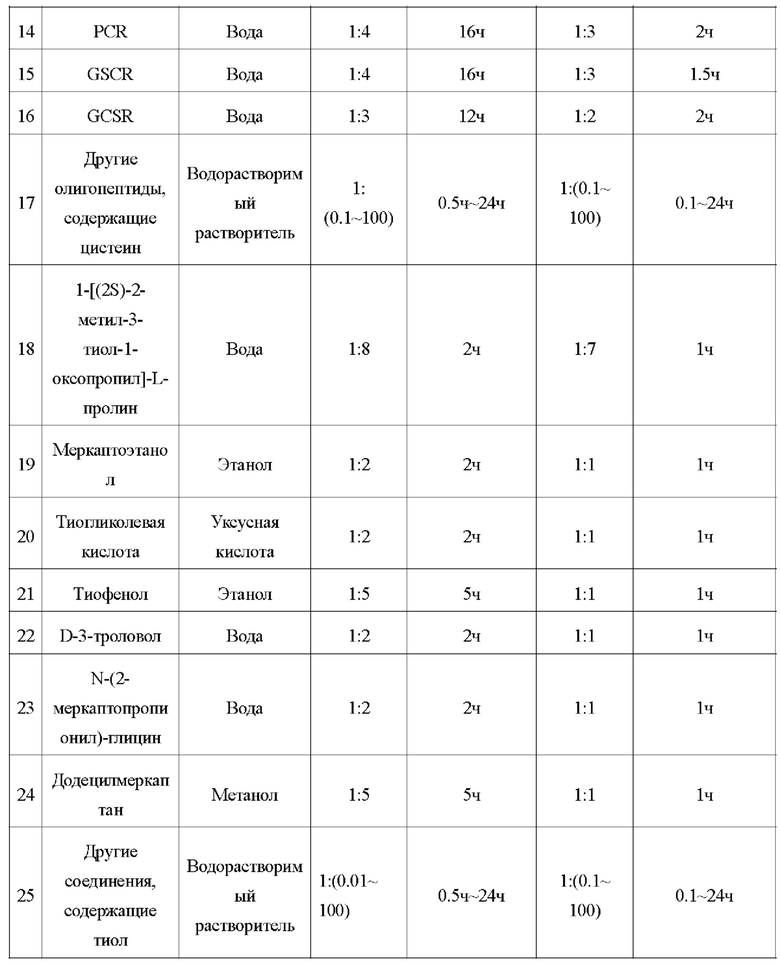
86. Образцы, перечисленные в таблице 1, подтверждены вышеуказанными способами. Характеристики пяти различных AuCs, связанных лигандами, показаны на фиг. 4 (CR-AuCs), на фиг. 5 (RC-AuCs), на фиг. 6 (Cap-AuCs) (Сар обозначает 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L-пролин), на фиг. 7 (GSH-AuCs) и на фиг. 8 (D-NIBC-AuCs). На фигурах 4-8 показаны УФ-спектры (снимок А), инфракрасные спектры (снимок В), изображения полученные с помощью ТЕМ (снимок С) и распределение частиц по размерам (снимок D).
87. Результаты показывают, что все диаметры AuCs, связанных различными лигандами, полученными как показано в таблице 1, меньше 3 нм. УФ-спектры также показывают исчезновение пика при 520±20 нм и возникновение пика поглощения в других положениях. Положение пика поглощения может варьироваться в зависимости от лигандов и размеров частиц, а также структуры. В некоторых ситуациях не возникает характеристического пика поглощения, в основном из-за образования смесей AuCs с различными размерами частиц и структурами или определенных особых AuCs, которые перемещают положение пика поглощения за пределы диапазона УФ-видимой области спектра. Между тем, инфракрасные спектры с преобразованием Фурье также показывают исчезновение пика инфракрасного поглощения тиола лиганда (между пунктирными линиями на снимке В, фиг. 4-8), в то же время все другие характеристические инфракрасные пики сохраняются, что позволяет предположить, что все молекулы лиганда были успешно связаны с атомами золота с образованием AuCs, связанных лигандами, и, таким образом, в соответствии с настоящим изобретением были успешно получены AuCs, связанные лигандами, перечисленные в таблице 1.
88. 3. Исследования на животных
89. 3.1 Материалы и животные
90. 3.1.1 Тестируемый образец
91. В качестве тестируемого образца использовали L-Cys-AuCs с диаметром золотого ядра в интервале 0,5-1,5 нм (1,0±0,5 нм); способ получения соответствовал описанному выше с небольшими изменениями. На фиг. 9 показаны УФ-видимые области спектра, инфракрасные области спектра, изображения полученные с помощью ТЕМ и диаграммы распределения частиц по размерам, связанных лигандом L-цистеином кластеров золота (L-Cys-AuCs).
92. 3.1.2 Положительный контрольный образец
93. Преднизон (Shanghai Yuanye Biotechnology Co., Ltd).
94. 3.1.3 Состав дозы
95. Преднизон взвешивали в необходимом количестве и добавляли соответствующий объем физиологического раствора, осторожно перемешивали состав вихревым методом для обеспечения надлежащего перемешивания. L-Cys-AuCs взвешивали, добавляли соответствующий объем физиологического раствора и перемешивали вихревым методом для полного смешивания суспензии. Все соединения были свежеприготовленными и готовились ежедневно.
96. 3.1.4 Животные для экспериментов
97. Использовали самок мышей C57BL/6N в возрасте 7-9 недель. Животные содержались и за ними ухаживали в соответствии с правилами.
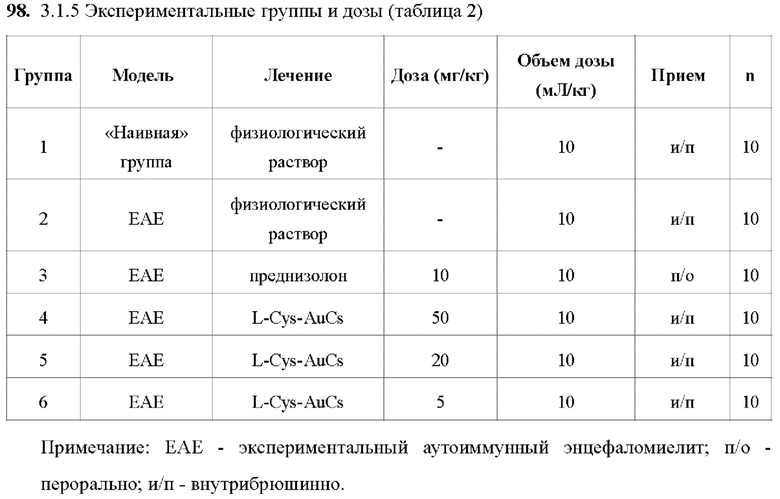
99. 3.1.6 Процедуры
100. На 0-й день мышей случайным образом группировали по массе тела, а затем вводили подкожно 200 мкг пептида миелинового олигодендроцитарного гликопротеина (MOG) в полном адъюванте Фрейнда (CFA) в правый и левый бок, по 100 мкл на каждый. Коклюшный токсин (РТХ) вводили внутрибрюшинно через 0 и 48 часов после иммунизации MOG. Соединения вводили с 1-го по 28-й день в соответствии с таблицей 2. Животных (10 мышей) ежедневно оценивали на наличие клинических признаков ЕАЕ. В конце экспериментов для НЕ-окрашивания (5 мышей) и анализа TNF-α, IL-17, IFN-γ с помощью набора Elisa использовали спинной мозг.
101. 3.2 Результаты
102. Животных ежедневно проверяли на наличие клинических признаков ЕАЕ в соответствии с рубрикой клинических оценок для группы ЕАЕ (таблица 3). Как показано на фиг.10, L-Cys-AuCs в дозах 50 мг/кг (50 mpK), 20 мг/кг (20 mpK) и 5 мг/кг (5mpK) предупреждали паралич у мышей группы ЕАЕ с 17-го дня; преднизон является положительным контролем, он способствовал значительному уменьшению клинических проявлений у группы ЕАЕ с 13-го дня.

104. Анализ TNF-α, IL-17 и IFN-γ в спинном мозге с помощью набора ELISA. TNF-α, IL-17 и IFN-γ являются индикаторами воспаления. L-Cys-AuCs в дозах 50 мг/кг, 20 мг/кг и 5 мг/кг способствовали значительному снижению выработки этих факторов воспаления у мышей с ЕАЕ (фиг. 11).
105. НЕ-окрашивание спинного мозга использовали для изучения инфильтрации иммунных клеток в спинной мозг. Во время индукции ЕАЕ мононуклеарные воспалительные клетки проникают в спинной мозг, вызывая паралич у мышей с ЕАЕ, НЕ-окрашивание выявило значительное увеличение воспалительных клеток у мышей с ЕАЕ, а L-Cys-AuCs в дозах 50 мг/кг, 20 мг/кг и 5 мг/кг способствовали снижению инфильтрации иммунных клеток (фиг. 12(a)) и показали значительно более низкие гистологические масштабы воспаления (фиг. 12(b)).
106. L-Cys-AuCs другого размера и другие AuCs, связанные лигандами, различных размеров также оказывают влияние на ингибирование ЕАЕ, в то же время их влияние в определенной степени различается. Они не будут здесь подробно описаны.
107. Промышленная применимость
108. AuCs, связанные лигандами, могут применяться для лечения рассеянного склероза. Они подходят для промышленного применения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЛЕЧЕНИЕ ПОБОЧНЫХ ЭФФЕКТОВ, ВЫЗВАННЫХ АТИПИЧНЫМИ АНТИПСИХОТИКАМИ | 2020 |
|
RU2808320C1 |
| КЛАСТЕРЫ ЗОЛОТА, КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ ДЕПРЕССИИ | 2021 |
|
RU2832089C2 |
| КЛАСТЕРЫ ЗОЛОТА, КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ ИШЕМИЧЕСКОГО ЦЕРЕБРАЛЬНОГО ИНСУЛЬТА | 2020 |
|
RU2822218C1 |
| КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ ДИАБЕТА | 2020 |
|
RU2801902C1 |
| КЛАСТЕРЫ ЗОЛОТА (AuCs), КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ ЦИРРОЗА ПЕЧЕНИ | 2020 |
|
RU2806634C1 |
| КЛАСТЕРЫ ЗОЛОТА, КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ ЦЕРЕБРАЛЬНОГО ИНСУЛЬТА | 2021 |
|
RU2822217C1 |
| КЛАСТЕРЫ МЕДИ, КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ ЦИРРОЗА ПЕЧЕНИ | 2020 |
|
RU2806633C1 |
| ПЕПТИДЫ ЛАТАРЦИНЫ, ПРОЯВЛЯЮЩИЕ АНТИМИКРОБНУЮ АКТИВНОСТЬ | 2006 |
|
RU2306148C1 |
| ПЕПТИД, ОБЛАДАЮЩИЙ НЕЙРОТРОПНОЙ АКТИВНОСТЬЮ | 2008 |
|
RU2394836C2 |
| ТЕРАПЕВТИЧЕСКИЕ АГЕНТЫ ДЛЯ СНИЖЕНИЯ УРОВНЕЙ ПАРАТИРЕОИДНОГО ГОРМОНА | 2010 |
|
RU2557654C2 |
Группа изобретений относится к области медицины, а именно к неврологии, иммунологии и терапии, и предназначена для лечения рассеянного склероза. Способ лечения субъекта, страдающего рассеянным склерозом, включает введение фармацевтической композиции, содержащей кластер золота (AuC). Указанный AuC содержит золотое ядро и лиганд, связанный с золотым ядром. Также представлено применение кластера золота (AuC) для приготовления лекарственного средства для лечения рассеянного склероза у субъекта, где указанный AuC содержит золотое ядро и лиганд, связанный с золотым ядром. Использование группы изобретений позволяет повысить эффективность лечения рассеянного склероза. 2 н. и 18 з.п. ф-лы, 12 ил., 3 табл., 1 пр.
1. Способ лечения субъекта, страдающего рассеянным склерозом, включающий:
введение фармацевтической композиции субъекту с рассеянным склерозом в эффективном количестве;
где указанная фармацевтическая композиция содержит кластер золота (AuC); причем указанный AuC содержит:
золотое ядро; и
лиганд, связанный с золотым ядром.
2. Способ по п.1, где золотое ядро имеет диаметр менее 3 нм.
3. Способ по п.1, где золотое ядро имеет диаметр в интервале 0,5-2,6 нм.
4. Способ по п.1, где лиганд представляет собой выбранный из группы, состоящей из L-цистеина и его производных, D-цистеина и его производных, цистеинсодержащих олигопептидов и их производных и других тиолсодержащих соединений.
5. Способ по п.4, где L-цистеин и его производные выбирают из группы, включающей L-цистеин, N-изобутирил-L-цистеин (L-NIBC) и N-ацетил-L-цистеин (L-NAC), и где D-цистеин и его производные выбирают из группы, содержащей D-цистеин, N-изобутирил-D-цистеин (D-NIBC) и N-ацетил-D-цистеин (D-NAC).
6. Способ по п.4, где цистеинсодержащие олигопептиды и их производные представляют собой цистеинсодержащие дипептиды, цистеинсодержащие трипептиды или цистеинсодержащие тетрапептиды.
7. Способ по п.6, где цистеинсодержащие дипептиды выбирают из группы, состоящей из L-цистеин-L-аргинин дипептида (CR), L-аргинин-L-цистеин дипептида (RC), L-гистидин-L-цистеин дипептида (HC) и L-цистеин-L-гистидин дипептида (CH).
8. Способ по п.6, где цистеинсодержащие трипептиды выбирают из группы, состоящей из глицин-L-цистеин-L-аргинин трипептида (GCR), L-пролин-L-цистеин-L-аргинин трипептида (PCR), L-лизин-L-цистеин-L-пролин трипептида (KCP) и L-глутатиона (GSH).
9. Способ по п.6, где цистеинсодержащие тетрапептиды выбирают из группы, состоящей из глицин-L-серин-L-цистеин-L-аргинин тетрапептида (GSCR) и глицин-L-цистеин-L-серин-L-аргинин тетрапептида (GCSR).
10. Способ по п.4, где другие тиолсодержащие соединения выбирают из группы, содержащей 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L-пролин, тиогликолевую кислоту, меркаптоэтанол, тиофенол, D-3-троловол, N-(2-меркаптопропионил)-глицин и додецилмеркаптан.
11. Применение кластера золота (AuC) для приготовления лекарственного средства для лечения рассеянного склероза у субъекта, где указанный AuC содержит:
- золотое ядро; и
- лиганд, связанный с золотым ядром.
12. Применение по п.11, где золотое ядро имеет диаметр менее 3 нм.
13. Применение по п.11, где золотое ядро имеет диаметр в интервале 0,5-2,6 нм.
14. Применение по п.11, где лиганд представляет собой выбранный из группы, состоящей из L-цистеина и его производных, D-цистеина и его производных, цистеинсодержащих олигопептидов и их производных и других тиолсодержащих соединений.
15. Применение по п.14, где L-цистеин и его производные выбирают из группы, состоящей из L-цистеина, N-изобутирил-L-цистеина (L-NIBC) и N-ацетил-L-цистеина (L-NAC), и где D-цистеин и его производные выбирают из группы, состоящей из D-цистеина, N-изобутирил-D-цистеина (D-NIBC) и N-ацетил-D-цистеина (D-NAC).
16. Применение по п.14, где цистеинсодержащие олигопептиды и их производные представляют собой цистеинсодержащие дипептиды, цистеинсодержащие трипептиды или цистеинсодержащие тетрапептиды.
17. Применение по п.16, где цистеинсодержащие дипептиды выбирают из группы, состоящей из L-цистеин-L-аргинин дипептида (CR), L-аргинин-L-цистеин дипептида (RC), L-гистидин-L-цистеин дипептида (HC) и L-цистеин-L-гистидин дипептида (CH).
18. Применение по п.16, где цистеинсодержащие трипептиды выбирают из группы, состоящей из глицин-L-цистеин-L-аргинин трипептида (GCR), L-пролин-L-цистеин-L-аргинин трипептида (PCR), L-лизин-L-цистеин-L-пролин трипептида (KCP) и L-глутатиона (GSH).
19. Применение по п.16, где цистеинсодержащие тетрапептиды выбирают из группы, состоящей из глицин-L-серин-L-цистеин-L-аргинин тетрапептида (GSCR) и глицин-L-цистеин-L-серин-L-аргинин тетрапептида (GCSR).
20. Применение по п.14, где другие тиолсодержащие соединения выбирают из группы, состоящей из 1-[(2S)-2-метил-3-тиол-1-оксопропил]-L-пролина, тиогликолевой кислоты, меркаптоэтанола, тиофенола, D-3-троловола, N-(2-меркаптопропионил)-глицина и додецилмеркаптана.
| СПОСОБ ИЗМЕРЕНИЯ ГАЗОПРОНИЦАЕМОСТИ ТАРЫ И УПЛОТНИТЕЛЬНЫХ ЭЛЕМЕНТОВ ВООБЩЕ | 2007 |
|
RU2451284C2 |
| WO 2018024111 A1, 08.02.2018 | |||
| WO 2017178685 A1, 19.10.2017 | |||
| US 2018057551 A1, 01.03.2018. | |||
Авторы
Даты
2023-07-05—Публикация
2019-12-27—Подача