ССЫЛКА НА ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Данная заявка включает Перечень последовательностей, поданный в электронной форме в виде текстового файла под названием 18923802302SEQ, созданного 12 марта 2020 г. и имеющего размер 136 килобайт. Перечень последовательностей включен в данный документ посредством ссылки.
Область техники
Настоящее изобретение в целом относится к лечению субъектов с гипергликемией ингибиторами члена 5 семейства 39 транспортеров растворенных веществ (SLC39A5), способам идентификации субъектов, имеющих высокий риск развития гипергликемии, и способам обнаружения вариантных молекул нуклеиновой кислоты и вариантных полипептидов SLC39A5.
Уровень техники
SLC39A5 принадлежит к суперсемейству транспортеров ионов металлов ZIP (Zrt и Irt-подобные белки). У мышей идентифицировано 14 членов этого семейства, и почти все эти гены являются консервативными у людей. Белки ZIP имеют 8 предсказанных трансмембранных доменов (SLC39A5 имеет 6 трансмембранных доменов), содержащих внутриклеточную петлю между трансмембранными доменами 3 и 4 и внеклеточный аминоконец, который богат гистидином и может играть роль в транспорте металлов. Этот транспортер цинка локализуется на базолатеральной мембране клетки и экспрессируется в тонком кишечнике, поджелудочной железе, почках и печени с аналогичным профилем экспрессии у мышей. SLC39A5 содержится в большом количестве, в частности, в кишечных энтероцитах, ацинарных клетках поджелудочной железы и эмбриональных клетках висцеральной энтодермы. Регуляция SLC39A5 также, по-видимому, уникальна тем, что этот белок интернализуется и координированно деградирует в каждом из этих типов клеток в периоды дефицита цинка в пище. Трансляция мРНК SLC39A5 останавливается во время дефицита цинка по механизму, который включает консервативную 3'-нетранслируемую область, которая, как предполагается, образует стабильную структуру петля-стержень и взаимодействует со специфическими микроРНК. SLC39A4 и SLC39A5 совместно экспрессируются в нескольких тканях с антагонистическими функциями в поддержании гомеостаза цинка. Считается, что SLC39A4 способствует усвоению пищевого цинка, тогда как SLC39A5 может функционировать при выведении цинка из организма. Предыдущие исследования показали роль энтероцитов SLC39A5 в экскреции цинка и роль ацинарных клеток поджелудочной железы SLC39A5 в протекции от токсичности цинка.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В данном изобретении также представлены способы лечения субъекта, имеющего пониженный уровень цинка в сыворотке, при этом способы включают введение субъекту ингибитора члена 5 семейства 39 транспортеров растворенных веществ (SLC39A5).
В данном изобретении также представлены способы лечения субъекта, имеющего повышенный уровень глюкозы в сыворотке крови, при этом способы включают введение субъекту ингибитора SLC39A5.
В данном изобретении представлены способы лечения субъекта, имеющего гипергликемию, при этом способы включают введение пациенту ингибитора SLC39A5.
В настоящем изобретении также представлены способы лечения субъекта терапевтическим агентом, который нормализует или ингибирует пониженный уровень цинка в сыворотке, повышенный уровень глюкозы в сыворотке и/или гипергликемию, при которых субъект страдает пониженным уровнем цинка в сыворотке, повышенным уровнем глюкозы в сыворотке и/или гипергликемией, способы, включающие стадии: определения того, имеет ли субъект вариантную молекулу нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5, кодирующую полипептид SLC39A5 человека, путем: получения или осуществления получения биологического образца от субъекта; и выполнения или осуществления выполнения генотипирования биологического образца, чтобы определить, имеет ли субъект генотип, имеющий молекулу нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5; а когда субъект является эталонным по SLC39A5, то введения или продолжения введения субъекту терапевтического агента, который нормализует или ингибирует пониженный уровень цинка в сыворотке, повышенный уровень глюкозы в сыворотке и/или гипергликемию в стандартной дозировке, и введения субъекту ингибитора SLC39A5; а когда субъект является гетерозиготным по варианту с прогнозируемой потерей функции SLC39A5, то введения или продолжения введения субъекту терапевтического агента, который нормализует или ингибирует пониженный уровень цинка в сыворотке, повышенный уровень глюкозы в сыворотке и/или гипергликемию в количестве, которое равно или ниже стандартной дозировки, и введения субъекту ингибитора SLC39A5; при этом наличие генотипа, имеющего молекулы нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5, кодирующей полипептид SLC39A5 человека, указывает на то, что у субъекта снижен риск развития пониженного уровня цинка в сыворотке, повышенного уровня глюкозы в сыворотке и/или гипергликемии.
В настоящем изобретении также представлены способы идентификации субъекта-человека, имеющего высокий риск развития пониженного уровня цинка в сыворотке, повышенного уровня глюкозы в сыворотке и/или гипергликемии, при этом способы включают: определение или осуществление определения наличия или отсутствия вариантной молекулы нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5, кодирующей полипептид SLC39A5 человека, в биологическом образце, полученном от субъекта; при этом: когда субъект-человек является эталонным по SLC39A5, тогда указанный субъект-человек имеет высокий риск развития пониженного уровня цинка в сыворотке, повышенного уровня глюкозы в сыворотке и/или гипергликемии; и когда субъект-человек является гетерозиготным по варианту с прогнозируемой потерей функции SLC39A5 или гомозиготным по варианту с прогнозируемой потерей функции SLC39A5, тогда указанный субъект-человек имеет низкий риск развития пониженного уровня цинка в сыворотке, повышенного уровня глюкозы в сыворотке, и/или гипергликемии.
В настоящем изобретении также представлены способы обнаружения вариантной молекулы нуклеиновой кислоты варианта человеческого SLC39A5 у субъекта-человека, включающие анализ образца, полученного от субъекта-человека, для определения того, содержит ли молекула нуклеиновой кислоты в образце нуклеотидную последовательность, содержащую: i) цитозин в положении, соответствующем положению 5604 согласно SEQ ID NO: 4, или ее комплементарной цепи; ii) цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 11, или ее комплементарной цепи; iii) цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 18, или ее комплементарной цепи; iv) цитозин в положении, соответствующем положению 6899 согласно SEQ ID NO: 6, или ее комплементарной цепи; v) цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 13, или ее комплементарной цепи; vi) цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 20, или ее комплементарной цепи; vii) аденин или гуанин в положении, соответствующем положению 1353 согласно SEQ ID NO: 2 или SEQ ID NO: 3, или их комплементарным цепям; viii) аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 9 или SEQ ID NO: 10, или их комплементарным цепям; ix) аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 16 или SEQ ID NO: 17, или их комплементарным цепям; x) тимин в положении, соответствующем положению 6352 согласно SEQ ID NO: 5, или ее комплементарной цепи; xi) урацил в положении, соответствующем положению 1194 согласно SEQ ID NO: 12, или ее комплементарной цепи; xii) тимин в положении, соответствующем положению 1194 согласно SEQ ID NO: 19, или ее комплементарной цепи; xiii) тимин в положении, соответствующем положению 5624 согласно SEQ ID NO: 7, или ее комплементарной цепи; xiv) урацил в положении, соответствующем положению 1161 согласно SEQ ID NO: 14, или ее комплементарной цепи; или xv) тимин в положении, соответствующем положению 1161 согласно SEQ ID NO: 21, или ее комплементарной цепи.
В настоящем изобретении также представлены способы обнаружения присутствия варианта полипептида SLC39A5 человека, включающие выполнение анализа образца, полученного от субъекта-человека, для определения того, содержит ли белок SLC39A5 в образце: i) треонин в положении, соответствующем положению 304 согласно SEQ ID NO: 24; ii) аланин в положении, соответствующем положению 413 согласно SEQ ID NO: 26; iii) представляет ли он собой усеченный вариант полипептида SLC39A5, имеющий аминокислотную последовательность, состоящую из SEQ ID NO: 23; iv) представляет ли он собой усеченный вариант полипептида SLC39A5, имеющий аминокислотную последовательность, состоящую из SEQ ID NO: 25; или v) представляет ли он собой усеченный вариант полипептида SLC39A5, имеющий аминокислотную последовательность, состоящую из SEQ ID NO: 27.
В настоящем изобретении также представлены терапевтические агенты, которые нормализуют или ингибируют пониженный уровень цинка в сыворотке, повышенный уровень глюкозы в сыворотке и/или гипергликемию, для применения при лечении пониженного уровня цинка в сыворотке, повышенного уровня глюкозы в сыворотке и/или гипергликемии у субъекта-человека, имеющего: i) молекулу геномной нуклеиновой кислоты, имеющую нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, при этом нуклеотидная последовательность содержит: цитозин в положении, соответствующем положению 5604 согласно SEQ ID NO: 4, или ее комплементарной цепи; цитозин в положении, соответствующем положению 6899 согласно SEQ ID NO: 6, или ее комплементарной цепи; аденин или гуанин в положении, соответствующем положению 1353 согласно SEQ ID NO: 2 или SEQ ID NO: 3, или их комплементарным цепям; тимин в положении, соответствующем положению 6352 согласно SEQ ID NO: 5, или ее комплементарной цепи; или тимин в положении, соответствующем положению 5624 согласно SEQ ID NO: 7, или ее комплементарной цепи; ii) молекулу мРНК, имеющую нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, при этом нуклеотидная последовательность содержит: цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 11, или ее комплементарной цепи; цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 13, или ее комплементарной цепи; аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 9 или SEQ ID NO: 10, или их комплементарным цепям; урацил в положении, соответствующем положению 1194 согласно SEQ ID NO: 12, или ее комплементарной цепи; или урацил в положении, соответствующем положению 1161 согласно SEQ ID NO: 14, или ее комплементарной цепи; или iii) молекулу кДНК, имеющую нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, при этом нуклеотидная последовательность содержит: цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 18, или ее комплементарной цепи; цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 20, или ее комплементарной цепи; аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 16 или SEQ ID NO: 17, или их комплементарным цепям; тимин в положении, соответствующем положению 1194 согласно SEQ ID NO: 19, или ее комплементарной цепи; или тимин в положении, соответствующем положению 1161 согласно SEQ ID NO: 21, или ее комплементарной цепи.
В настоящем изобретении также представлены ингибиторы SLC39A5 для применения в лечении пониженного уровня цинка в сыворотке, повышенного уровня глюкозы в сыворотке и/или гипергликемии у субъекта-человека, имеющего: i) молекулу геномной нуклеиновой кислоты, имеющую нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, при этом нуклеотидная последовательность содержит: цитозин в положении, соответствующем положению 5604 согласно SEQ ID NO: 4, или ее комплементарной цепи; цитозин в положении, соответствующем положению 6899 согласно SEQ ID NO: 6, или ее комплементарной цепи; аденин или гуанин в положении, соответствующем положению 1353 согласно SEQ ID NO: 2 или SEQ ID NO: 3, или их комплементарным цепям; тимин в положении, соответствующем положению 6352 согласно SEQ ID NO: 5, или ее комплементарной цепи; или тимин в положении, соответствующем положению 5624 согласно SEQ ID NO: 7, или ее комплементарной цепи; ii) молекулу мРНК, имеющую нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, при этом нуклеотидная последовательность содержит: цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 11, или ее комплементарной цепи; цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 13, или ее комплементарной цепи; аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 9 или SEQ ID NO: 10, или их комплементарным цепям; урацил в положении, соответствующем положению 1194 согласно SEQ ID NO: 12, или ее комплементарной цепи; или урацил в положении, соответствующем положению 1161 согласно SEQ ID NO: 14, или ее комплементарной цепи; или iii) молекулу кДНК, имеющую нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, при этом нуклеотидная последовательность содержит: цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 18, или ее комплементарной цепи; цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 20, или ее комплементарной цепи; аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 16 или SEQ ID NO: 17, или их комплементарным цепям; тимин в положении, соответствующем положению 1194 согласно SEQ ID NO: 19, или ее комплементарной цепи; или тимин в положении, соответствующем положению 1161 согласно SEQ ID NO: 21, или ее комплементарной цепи.
Краткое описание графических материалов
Сопроводительные фигуры, которые включены и составляют часть этого описания изобретения, иллюстрируют несколько аспектов и вместе с описанием служат для пояснения принципов настоящего изобретения.
На Фиг. 1А показана экспрессия мутанта SLC39A5 в репортерной системе dsRED.
На Фиг. 1B показано, что мутации SLC39A5 приводят к потере функции.
На Фиг. 2А показан хронометраж эксперимента по исследованию лечения стеатоза печени и толерантности к глюкозе с помощью добавок цинка.
На Фиг. 2В показаны уровни цинка в сыворотке у мышей после 4-недельной диеты с высоким содержанием жиров с добавлением цинка или без него.
На Фиг. 2С показаны уровни цинка в печени у мышей после 4-недельной диеты с высоким содержанием жиров с добавлением цинка или без него.
На Фиг. 2D показаны уровни цинка в сыворотке у мышей после 6-недельной диеты с высоким содержанием жиров с добавлением цинка или без него.
На Фиг. 2E показаны уровни цинка в печени у мышей после 6-недельной диеты с высоким содержанием жиров с добавлением цинка или без него.
На Фиг. 3А показаны результаты теста на толерантность к глюкозе у мышей после 4-недельной диеты с высоким содержанием жиров с добавлением цинка или без него.
На Фиг. 3В показана площадь под кривой у мышей после 4-недельной диеты с высоким содержанием жиров с добавлением цинка или без него.
На Фиг. 3С показаны результаты теста на толерантность к глюкозе у мышей после 6-недельной диеты с высоким содержанием жиров с добавлением цинка или без него.
На Фиг. 3D показана площадь под кривой у мышей после 6-недельной диеты с высоким содержанием жиров.
На Фиг. 4 показаны микрофотографии поперечных срезов печени мышей после диеты с высоким содержанием жиров с добавлением цинка или без него.
На Фиг. 5А показана масса тела самок мышей в возрасте 12 недель, имеющих гетерозиготный или гомозиготный нокаут SLC39A5.
На Фиг. 5В показаны уровни глюкозы в крови натощак у самок мышей в возрасте 12 недель, имеющих гетерозиготный или гомозиготный нокаут SLC39A5.
На Фиг. 5C показаны уровни цинка в сыворотке у самцов и самок мышей в возрасте 12 недель, имеющих гетерозиготный или гомозиготный нокаут SLC39A5.
На Фиг. 5D показана масса тела самцов мышей в возрасте 12 недель, имеющих гетерозиготный или гомозиготный нокаут SLC39A5.
На Фиг. 5E показаны уровни глюкозы в крови натощак у самцов мышей в возрасте 12 недель, имеющих гетерозиготный или гомозиготный нокаут SLC39A5.
На Фиг. 5F показаны уровни цинка в печени у самцов и самок мышей в возрасте 12 недель, имеющих гетерозиготный или гомозиготный нокаут SLC39A5.
На Фиг. 6А показаны уровни цинка в сыворотке после 25 недель диеты с высоким содержанием жиров у 31-недельных мышей, имеющих нокаут SLC39A5.
На Фиг. 6B показаны уровни глюкозы в крови натощак после 25 недель диеты с высоким содержанием жиров у 31-недельных мышей, имеющих нокаут SLC39A5.
На Фиг. 6С показаны уровни лептина после 25 недель диеты с высоким содержанием жиров у 31-недельных мышей, имеющих нокаут SLC39A5.
На Фиг. 6D показаны уровни инсулина после 25 недель диеты с высоким содержанием жиров у 31-недельных мышей, имеющих нокаут SLC39A5.
На Фиг. 6E показаны уровни с-пептида после 25 недель диеты с высоким содержанием жиров у 31-недельных мышей, имеющих нокаут SLC39A5.
На Фиг. 6F показаны соотношения инсулин/с-пептид после 25 недель диеты с высоким содержанием жиров у 31-недельных мышей, имеющих нокаут SLC39A5.
На Фиг. 7A показана масса тела 12-недельных самок мышей, имеющих нокаут SLC39A5, нокаут рецептора лептина (LEPR) или двойный нокаут SLC39A5/LEPR.
На Фиг. 7B показаны уровни глюкозы в крови натощак у 12-недельных самок мышей, имеющих нокаут SLC39A5, нокаут рецептора лептина (LEPR), или двойной нокаут SLC39A5/LEPR.
На Фиг. 7С показаны уровни цинка в сыворотке у 12-недельных самок мышей, имеющих нокаут SLC39A5, нокаут рецептора лептина (LEPR) или двойной нокаут SLC39A5/LEPR.
На Фиг. 7D показана масса тела 12-недельных самцов мышей, имеющих нокаут SLC39A5, нокаут рецептора лептина (LEPR) или двойной нокаут SLC39A5/LEPR.
На Фиг. 7E показаны уровни глюкозы в крови натощак у 12-недельных самцов мышей, имеющих нокаут SLC39A5, нокаут рецептора лептина (LEPR), или двойной нокаут SLC39A5/LEPR.
На Фиг. 7F показаны уровни цинка в сыворотке у 12-недельных самцов мышей, имеющих нокаут SLC39A5, нокаут рецептора лептина (LEPR) или двойной нокаут SLC39A5/LEPR.
На Фиг. 8A показана масса тела 10-недельных самок мышей, имеющих нокаут SLC39A5, нокаут рецептора лептина (LEPR) или двойный нокаут SLC39A5/LEPR.
На Фиг. 8B показаны уровни глюкозы в крови натощак у 10-недельных самок мышей, имеющих нокаут SLC39A5, нокаут рецептора лептина (LEPR), или двойной нокаут SLC39A5/LEPR.
На Фиг. 8C показаны уровни β-гидроксибутирата у 10-недельного самок мышей, имеющих нокаут SLC39A5, нокаут рецептора лептина (LEPR) или двойной нокаут SLC39A5/LEPR.
На Фиг. 8D показана масса тела 10-недельных самцов мышей, имеющих нокаут SLC39A5, нокаут рецептора лептина (LEPR) или двойной нокаут SLC39A5/LEPR.
На Фиг. 8E показаны уровни глюкозы в крови натощак у 10-недельных самцов мышей, имеющих нокаут SLC39A5, нокаут рецептора лептина (LEPR), или двойной нокаут SLC39A5/LEPR.
На Фиг. 9А показаны результаты теста на толерантность к глюкозе, введенного внутривенно у мышей с нокаутом SLC39A5 после 14-недельной диеты с высоким содержанием жиров.
На Фиг. 9В показаны уровни инсулина в крови у мышей с нокаутом SLC39A5 после 16-недельной диеты с высоким содержанием жиров.
На Фиг. 10 показаны сравнительные значения нетрансформированных показателей для различных показателей у мышей дикого типа и мышей с нокаутом SLC39A5.
На Фиг. 11 показано, что потеря SLC39A5 приводит к увеличению уровней цинка в сыворотке и костях у обоих полов, тогда как цинк в печени незначительно повышается только у самок мышей.
На Фиг. 12 показано, что потеря SLC39A5 улучшает стеатоз печени у самок мышей в результате индуцированного диетой ожирения.
На Фиг. 13 показано, что потеря SLC39A5 улучшает функцию печени и определенные липидные показатели у самок мышей после индуцированного диетой ожирения.
На Фиг. 14 показано, что потеря SLC39A5 приводит к снижению содержания триглицеридов в печени и усилению кетогенеза у самок мышей при стимуляции диетой с высоким содержанием жира.
На Фиг. 15 показано, что потеря функции SLC39A5 улучшает функцию печени у мышей с дефицитом рецептора лептина.
На Фиг. 16 показано, что потеря функции SLC39A5 улучшает гликемические показатели у мышей с дефицитом рецептора лептина.
На Фиг. 17 показано, что потеря SLC39A5 приводит к активации активируемой АМФ протеинкиназы печени у самок мышей на HFD.
На Фиг. 18 показан выбор целевого пептида SLC39A5 для иммунизации мышей из объединенных графиков гидрофобности Кайта-Дулитла (зеленый) и гидрофильности Хоппа-Вудса (красный) по последовательности SLC39L5; фрагмент, выбранный для использования в качестве пептида для иммунизации (GPSGWGDQEESKAPDLHG; SEQ ID NO: 67), выделен фиолетовым цветом.
На Фиг. 19 показан скрининг моноклональных антител к Slc39a5 в HEK, сверхэкспрессирующем Slc39a5 мыши.
На Фиг. 20 показан скрининг моноклонального антитела к Slc39a5 в HEK, сверхэкспрессирующем Slc39a5 человека.
На Фиг. 21 показано, что потеря функции Slc39a5 способствует повышению уровня глюкозы в крови натощак при нагрузке диетой с высоким содержанием жиров и фруктозы. Диета с высоким содержанием жиров и фруктозы приводит к значительному увеличению массы тела по всем генотипам у обоих полов. Потеря функции Slc39a5 улучшает функцию печени по оценке сывороточных АЛТ и АСТ у обоих полов через 16 недель. Потеря функции Slc39a5 значительно улучшает гипергликемию, оцениваемую по уровням глюкозы в крови натощак в конечной точке (29 недель). «NC»: обычный корм (NC); «HFFD»: диета с высоким содержанием жиров и фруктозы.
На Фиг. 22 показано, что потеря функции Slc39a5 улучшает чувствительность к инсулину у мышей, которых стимулировали диетой с высоким содержанием жиров и фруктозы. Мыши, гомозиготные по потере функции Slc39a5 (независимо от пола), демонстрируют заметное улучшение чувствительности к инсулину по сравнению с мышами дикого типа, что оценивается с помощью перорального теста толерантности к глюкозе («ТТГ»).
На Фиг. 23 показано, что потеря функции Slc39a5 вызывает регресс стеатоза печени после стимуляции HFFD. Самки мышей с потерей функции Slc39a5 более защищены, чем самцы мышей. Комплексная оценка НАЖБП в баллах (оцениваемая двумя независимыми патологами), представляющая собой совокупный балл для макровезикулярного стеатоза, микровезикулярного стеатоза, гепатоцеллюлярной гипертрофии, воспаления и фиброза, демонстрирует значительное улучшение у самок мышей с нокаутом Slc39a5 по сравнению с аналогами дикого типа; тогда как у самцов мышей с потерей Slc39a5 регрессирует стеатоз печени при употреблении нормального корма и не обеспечивает защиты при диете с высоким содержанием жиров и фруктозы, что подтверждается гистопатологией и оценками НАЖБП в баллах.
На Фиг. 24A и 24B показано, что потеря функции Slc39a5 приводит к увеличению уровней цинка в печени и, как следствие, к повышению экспрессии металлотионеина в печени («Mt1» и «Mt2»). Потеря функции Slc39a5 существенно не влияет на уровни железа, меди, кобальта, кальция и магния в печени (Фиг. 24A: самки мышей; Фиг. 24: самцы мышей).
На Фиг. 25A и 25B показано, что цинк быстро активирует сигнальные пути LKB1/AMPK и AKT дозозависимым образом в клетках гепатомы человека HepG2 (Фиг. 25A) и первичных гепатоцитах человека (Фиг. 25B).
На Фиг. 26A показано, что потеря функции Slc39a5 вызывает регресс стеатоза печени у самок мышей, которые были на диете с высоким содержанием жиров и фруктозы. Потеря функции Slc39a5 приводит к увеличению уровней цинка в печени с одновременной активацией сигналинга печеночных AMPK и AKT у самок мышей, которые получали диету с высоким содержанием жиров и фруктозы. Уровни триглицеридов в печени были снижены с увеличением уровней бета-гидроксибутирата в печени, что свидетельствует об усилении β-окисления. Потеря функции Slc39a5 приводит к подавлению экспрессии генов Fasn и G6pc, участвующих в липогенезе de novo и глюконеогенезе в печени, соответственно.
На Фиг. 26B показано, что потеря функции Slc39a5 улучшает стеатоз печени у самцов мышей, получавших нормальный корм. Потеря Slc39a5 у самцов мышей, получающих HFFD, приводит к незначительному повышению уровней цинка в печени с умеренной активацией сигналинга AMPK в печени. Уровни печеночных триглицеридов немного снижаются с увеличением печеночных уровней бета-гидроксибутирата. Потеря функции Slc39a5 приводит к умеренной репрессии Fasn и значительному подавлению экспрессии G6pc, генов, участвующих в липогенезе de novo и глюконеогенезе в печени, соответственно.
На Фиг. 27 показано, что потеря функции Slc39a5 улучшает функцию печени и уровень глюкозы в крови натощак у мышей с дефицитом рецепторов лептина. Врожденная недостаточность рецепторов лептина приводит к значительному увеличению массы тела у Lepr-/- и Slc39a5-/-;Lepr-/- мышей у обоих полов. Потеря функции Slc39a5 улучшает функцию печени у мышей с дефицитом рецепторов лептина (обоих полов), что оценивают по сывороточным АЛТ и АСТ через 22 недели. Потеря функции Slc39a5 значительно улучшает гипергликемию у мышей с дефицитом рецепторов лептина (обоих полов), о чем свидетельствует снижение уровня глюкозы в крови натощак на 34 неделе.
На Фиг. 28 показано, что потеря функции Slc39a5 у мышей с дефицитом рецептора лептина (оба пола) приводит к улучшенной чувствительности к инсулину по сравнению с
(Lepr-/-) дефицитными по рецептору лептина мышами, что оценивается с помощью перорального ТТГ.
На Фиг. 29 показано, что потеря функции Slc39a5 улучшает стеатоз печени у дефицитных по рецептору лептина мышей (оба пола).
На Фиг. 30 показано, что потеря функции Slc39a5 приводит к увеличению уровней цинка в печени и, как следствие, к повышению экспрессии печеночного металлотионеина («Mt1» и «Mt2») у дефицитных по рецептору лептина мышей (оба пола). Кроме того, потеря функции Slc39a5 не оказывает значительного влияния на уровни железа в печени у этих мышей.
На Фиг. 31A и 31B показано, что потеря функции Slc39a5 вызывает регресс стеатоза печени у дефицитных по рецептору лептина мышей у обоих полов (Фиг. 31A, самка; Фиг. 31B, самец). Потеря функции Slc39a5 приводит к увеличению уровней цинка в печени у дефицитных по рецептору лептина мышей (оба пола) с сопутствующей активацией сигналинга печеночного AMPK. Уровни триглицеридов в печени снижают с увеличением уровней бета-гидроксибутирата в печени что свидетельствует об усилении β-окисления. Более того, потеря Slc39a5 приводит к подавлению экспрессии Fasn, что свидетельствует о снижении липогенеза de novo.
На Фиг. 32 показана ассоциация мутаций с потерей функции в SLC39A5 с увеличением уровней циркулирующего цинка и снижением риска T2D (RR: гомозигота по эталонному аллелю; RA: гетерозигота; AA: гомозигота по альтернативному аллелю; случаи: T2D и HbA1c ≥ 6,5%; контроль: ни T1D, ни T2D, ни HbA1c ≥ 6,5%; M1.1: только варианты p.LoF (AAF ≤ 1%).
На Фиг. 33A показана зависимость активности тирозинфосфатазы от концентрации цинка (красная линия) и магния (синяя линия).
На Фиг. 33B показана зависимость активности серин/треонинфосфатазы от концентрации цинка (красная линия) и магния (синяя линия).
На Фиг. 34A показано, что потеря SLC39A5 приводит к опосредованному цинком подавлению активности тирозинфосфатазы у самок мышей, получавших либо диету NC (справа), либо диету HFFD (слева).
На Фиг. 34B показано, что потеря SLC39A5 приводит к опосредованному цинком подавлению активности серин/треонинфосфатазы у самок мышей на диете NC (справа) или диете HFFD (слева).
На Фиг. 34C показано, что потеря SLC39A5 приводит к опосредованному цинком подавлению активности тирозинфосфатазы у самцов мышей на диете NC (справа) или диете HFFD (слева).
На Фиг. 34D показано, что потеря SLC39A5 приводит к опосредованному цинком подавлению активности серин/треонинфосфатазы у самцов мышей на диете NC (справа) или диете HFFD (слева).
Описание
В описании и формуле изобретения применяются различные термины, относящиеся к аспектам настоящего изобретения. Таким терминам следует придавать их обычное значение в данной области техники, если не указано иное. Другие конкретно определенные термины следует толковать в соответствии с определениями, приведенными в данном документе.
Если прямо не указано иное, никоим образом не предусматривается, чтобы какой-либо способ или аспект, изложенные в данном документе, толковались как требующие, чтобы их стадии выполнялись в определенном порядке. Соответственно, если в формуле изобретения или описании способа конкретно не указано, что стадии должны быть ограничены конкретным порядком, никоим образом не предусматривается, что подразумевается порядок, в любом отношении. Это справедливо для любого возможного неявного основания для интерпретации, включая логические выводы в отношении упорядочения этапов или рабочего процесса, очевидного значения, полученного из грамматического построения или пунктуации или число или тип аспектов, описанных в изобретении.
В контексте данного документа формы единственного числа включают в себя также формы множественного числа, если из контекста явно не следует иное.
Используемый в данном документе термин «субъект» включает любое животное, включая млекопитающих. Млекопитающие включают в себя, помимо прочего, сельскохозяйственных животных (таких как, например, лошадь, корова, свинья), домашних животных (таких как, например, собака, кошка), лабораторных животных (таких как, например, мышь, крыса, кролики) и приматов, отличных от человека. В некоторых вариантах осуществления субъектом является человек.
В контексте данного документа термины «нуклеиновая кислота», «молекула нуклеиновой кислоты», «последовательность нуклеиновой кислоты», «полинуклеотид» или «олигонуклеотид» могут включать в себя полимерную форму нуклеотидов любой длины, могут включать в себя ДНК и/или РНК, и могут быть одноцепочечными, двухцепочечными или многоцепочечными. Одна цепь нуклеиновой кислоты также относится к ее комплементарной последовательности.
В контексте данного документа термин «содержащая» может быть заменен на «состоящая из» или «по существу состоящая из» в конкретных вариантах осуществления произвольно.
В соответствии с настоящим изобретением был идентифицирован редкий вариант гена SLC39A5, связанный с повышенными уровнями цинка в сыворотке и низким риском развития повышенного уровня глюкозы в сыворотке и/или гипергликемии, а также с улучшением функции печени у людей. Например, генетическое изменение, которое изменяет нуклеотид тимин в положении 5604 в эталонном SLC39A5 человека (см. SEQ ID NO: 1) на цитозин, или нуклеотид гуанин в положении 6899 в эталонном SLC39A5 человека (см. SEQ ID NO: 1) на цитозин, или нуклеотид цитозина в положении 1353 в ссылке на SLC39A5 человека (см. SEQ ID NO: 1) на аденин или гуанин, или нуклеотид цитозин в положении 6352 в эталонном SLC39A5 человека (см. SEQ ID NO: 1) на тимин, или нуклеотид цитозин в положении 5624 в эталонном SLC39A5 человека (см. SEQ ID NO: 1) на тимин, что указывает на то, что у человека, имеющего такое изменение, возможно повышение уровня цинка в сыворотке и низкий риск развития повышенного уровня глюкозы в сыворотке крови и/или гипергликемии. Считается, что никакие варианты гена или белка SLC39A5 не имеют какой-либо известной связи с повышенным уровнем цинка в сыворотке и низким риском развития повышенного уровня глюкозы в сыворотке и/или гипергликемии. В целом генетический анализ, описанный в данном документе, неожиданно демонстрирует, что ген SLC39A5 и, в частности, вариант гена SLC39A5, ассоциируется с повышенным уровнем цинка в сыворотке и низким риском развития повышенного уровня глюкозы в сыворотке и/или гипергликемии. Следовательно, субъектов-людей, которые являются эталонными по SLC39A5, которые имеют высокий риск развития повышенного уровня глюкозы в сыворотке и/или гипергликемии, можно нормализовать таким образом, чтобы предотвратить повышенный уровень глюкозы в сыворотке и/или гипергликемию, уменьшить их симптомы и/или подавить развитие симптомов. Соответственно, в настоящем изобретении представлены способы применения идентификации таких вариантов у субъектов для выявления или стратификации риска у таких субъектов развития повышенного уровня глюкозы в сыворотке и/или гипергликемии, или для диагностики субъектов как имеющих высокий риск развития повышенного уровня глюкозы в сыворотке, и/или гипергликемии, так что субъектов из группы риска или субъектов с активным заболеванием можно лечить соответствующим образом. Кроме того, в настоящем изобретении представлены выделенные вариантные молекулы геномной нуклеиновой кислоты SLC39A5, вариантные молекулы мРНК и вариантные молекулы кДНК. Соответственно, в данном документе представлены вариантной молекулы нуклеиновой кислоты с потерей функции SLC39A5, которые, как обнаружено, связаны с повышенными уровнями цинка в сыворотке и низким риском развития повышенного уровня глюкозы в сыворотке и/или гипергликемии.
Для целей данного изобретения любой конкретный человек может быть классифицирован как имеющий один из трех генотипов SLC39A5: i) эталонный по SLC39A5; ii) гетерозиготный по варианту с прогнозируемой потерей функции SLC39A5; или iii) гомозиготный по варианту с прогнозируемой потерей функции SLC39A5. Человек является эталонным по SLC39A5, когда у данного человека нет копии вариантной молекулы нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5. Человек является гетерозиготным по варианту с прогнозируемой потерей функции SLC39A5, когда у данного человека есть единственная копия вариантной молекулы нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5. Вариантная молекула нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 представляет собой любую молекулу нуклеиновой кислоты SLC39A5 (например, молекулу геномной нуклеиновой кислоты, молекулу мРНК или молекулу кДНК), кодирующую полипептид SLC39A5, имеющий частичную потерю функции, полную потерю функции, прогнозируемую частичную потерю функции или прогнозируемую полную потерю функции. Человек, имеющий полипептид SLC39A5 с частичной потерей функции (или прогнозируемой частичной потерей функции), является гипоморфным по SLC39A5. Вариантная молекула нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 может представлять собой любую молекулу нуклеиновой кислоты, кодирующую SLC39A5 M304T, G413A, Y47Stop, R322Stop, или R311Stop. SLC39A5 M304T и G413A являются вариантными молекулами нуклеиновой кислоты с прогнозируемой частичной потерей функции. В некоторых вариантах осуществления вариантная молекула нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 кодирует SLC39A5 Y47Stop, R322Stop или R311Stop. Человек является гомозиготным по варианту с прогнозируемой потерей функции SLC39A5, когда у данного человека есть две копии любой из вариантных молекул нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5.
Касательно субъектов-людей, которые генотипированы или определены как эталонные по SLC39A5, то такие субъекты-люди имеют высокий риск развития повышенного уровня глюкозы в сыворотке и/или гипергликемии. Касательно субъектов-людей, которые генотипированы или определены как эталонные по SLC39A5 или гетерозиготные по варианту с прогнозируемой потерей функции SLC39A5, то таких субъектов-людей можно лечить ингибитором SLC39A5. В некоторых вариантах осуществления таких людей можно лечить цинком. В некоторых вариантах осуществления таких субъектов-людей можно лечить терапевтическим агентом, который нормализует или ингибирует повышенный уровень глюкозы в сыворотке и/или гипергликемию. В некоторых вариантах осуществления субъект-человек представляет собой субъекта-человека женского пола. В некоторых вариантах осуществления субъект-человек представляет собой субъекта-человека мужского пола.
В настоящем изобретении представлены способы лечения субъекта, имеющего пониженный уровень цинка в сыворотке, при этом способы включают введение субъекту ингибитора SLC39A5.
В данном изобретении представлены способы лечения субъекта, имеющего повышенный уровень глюкозы в сыворотке крови, при этом способы включают введение субъекту ингибитора SLC39A5.
В данном изобретении представлены способы лечения субъекта, имеющего гипергликемию, при этом способы включают введение пациенту ингибитора SLC39A5.
В некоторых вариантах осуществления ингибитор SLC39A5 включает антитело или его антигенсвязывающий фрагмент. В некоторых вариантах осуществления антитело специфически связывается с белком, содержащим SEQ ID NO: 22, или его фрагментом. В некоторых вариантах осуществления антитело специфически связывается с белком, содержащим SEQ ID NO: 23, SEQ ID NO: 25 или SEQ ID NO: 27, или его фрагментом. В некоторых вариантах осуществления антитело специфически связывается с пептидом, содержащим аминокислотную последовательность GPSGWGDQEESKAPDLHG (SEQ ID NO: 67). В некоторых вариантах осуществления антитело содержит тяжелую цепь, содержащую аминокислотную последовательность согласно SEQ ID NO: 58. В некоторых вариантах осуществления тяжелая цепь кодируется полинуклеотидом, содержащим нуклеотидную последовательность согласно SEQ ID NO: 57. В некоторых вариантах осуществления антитело содержит легкую цепь, содержащую аминокислотную последовательность согласно SEQ ID NO: 60. В некоторых вариантах осуществления легкая цепь кодируется полинуклеотидом, содержащим нуклеотидную последовательность согласно SEQ ID NO: 59. В некоторых вариантах осуществления антитело содержит тяжелую цепь, содержащую аминокислотную последовательность согласно SEQ ID NO: 58, и легкую цепь, содержащую аминокислотную последовательность согласно SEQ ID NO: 60. В некоторых вариантах осуществления тяжелая цепь антитела содержит одну или более определяющих комплементарность областей (CDR), выбранных из: FSLTGYAVN (SEQ ID NO:61), WLGVIWGDGRTDY (SEQ ID NO:62), и ARFGNSYALDY (SEQ ID NO:63). В некоторых вариантах осуществления легкая цепь антитела содержит одну или более CDR, выбранных из: QSLLNSRTRKNYLA (SEQ ID NO: 64), LLIYWASTRES (SEQ ID NO: 65) и KQSYNLH (SEQ ID NO: 66). В некоторых вариантах осуществления фрагмент антитела может содержать одноцепочечный (scFv), диатела, Fv и (Fab′)2, триатела, Fc, Fab, CDR1, CDR2, CDR3, комбинации CDR, вариабельные области, тетратела, бифункциональный гибридные антитела, каркасные области, константные области и т. п.
В некоторых вариантах осуществления ингибитор SLC39A5 содержит антисмысловую молекулу. Примеры антисмысловых молекул включают в себя, помимо прочего, молекулы антисмысловых нуклеиновых кислот, малые интерферирующие РНК (миРНК) и короткие шпилечные РНК (кшРНК). Такие антисмысловые молекулы могут быть сконструированы для нацеливания на любую область мРНК SLC39A5. В некоторых вариантах осуществления антисмысловая РНК, миРНК или кшРНК гибридизуется с последовательностью в молекуле геномной нуклеиновой кислоты SLC39A5 или молекуле мРНК и снижает экспрессию полипептида SLC39A5 в клетке субъекта. В некоторых вариантах осуществления ингибитор SLC39A5 содержит антисмысловую РНК, которая гибридизуется с молекулой геномной нуклеиновой кислоты SLC39A5 или молекулой мРНК и снижает экспрессию полипептида SLC39A5 в клетке субъекта. В некоторых вариантах осуществления ингибитор SLC39A5 содержит антисмысловую миРНК, которая гибридизуется с молекулой геномной нуклеиновой кислоты SLC39A5 или молекулой мРНК и снижает экспрессию полипептида SLC39A5 в клетке субъекта. В некоторых вариантах осуществления ингибитор SLC39A5 содержит антисмысловую кшРНК, которая гибридизуется с молекулой геномной нуклеиновой кислоты SLC39A5 или молекулой мРНК и снижает экспрессию полипептида SLC39A5 в клетке субъекта.
В некоторых вариантах осуществления ингибитор SLC39A5 содержит нуклеазный агент, который индуцирует один или более одноцепочечных разрывов или двухцепочечных разрывов в последовательности (-ях) распознавания или ДНК-связывающем белке, который связывается с последовательностью распознавания, в молекуле геномной нуклеиновой кислоты SLC39A5. Последовательность распознавания может быть расположена в кодирующей области гена SLC39A5 или в регуляторных областях, которые влияют на экспрессию данного гена. Последовательность распознавания ДНК-связывающего белка или нуклеазного агента может быть расположена в интроне, экзоне, промоторе, энхансере, регуляторной области или любой области, не кодирующей белок. Последовательность распознавания может включать в себя или располагаться вблизи старт-кодона гена SLC39A5. Например, последовательность распознавания может располагаться от около 10, 20, 30, 40, 50, 100, 200, 300, 400, 500 или 1000 нуклеотидов стартового кодона. В качестве другого примера, можно применять два или большее количество нуклеазных агентов, каждый из которых нацелен на последовательность распознавания нуклеазы, включающую в себя или расположенную вблизи старт-кодона. В качестве другого примера, можно применять два нуклеазных агента, один - нацеленный на последовательность распознавания нуклеазы, включающую в себя или расположенную вблизи старт-кодона, и один - нацеленный на последовательность распознавания нуклеазы, включающую в себя или расположенную вблизи старт-кодона, при этом расщепление нуклеазными агентами может привести к удалению кодирующей области между двумя последовательностями распознавания нуклеазы. Любой нуклеазный агент, который индуцирует одноцепочечный разрыв или двухцепочечный разрыв в желаемой последовательности распознавания, может применяться в описанных в данном документе способах и композициях. Любой ДНК-связывающий белок, который связывается с желаемой последовательностью распознавания, может применяться в описанных в данном документе способах и композициях.
Подходящие нуклеазные агенты и ДНК-связывающие белки для применения в данном изобретении включают в себя, но не ограничиваются ими, белок «цинковые пальцы» или пару нуклеаз с «цинковыми пальцами» (ZFN), эффекторный белок, подобный активаторам транскрипции (TALE), или эффекторную нуклеазу, подобную активаторам транскрипции (TALEN), или системы коротких палиндромных повторов, регулярно расположенных группами (CRISPR) / CRISPR-ассоциированных белков (Cas). Длина последовательности распознавания может варьировать и включает в себя, например, последовательности распознавания, которые составляют около 30-36 п. о. для белка «цинковые пальцы» или пары ZFN (например, около 15-18 п. о. для каждого ZFN), около 36 п. о. для белка TALE или TALEN и около 20 п. о. для направляющих РНК CRISPR/Cas.
В некоторых вариантах осуществления системы CRISPR/Cas могут применяться для модификации молекулы геномной нуклеиновой кислоты SLC39A5 в клетке. В способах и композициях, описанных в данном документе, могут применяться системы CRISPR-Cas путем использования комплексов CRISPR (содержащих направляющую РНК (нРНК), связанную в комплекс с белком Cas) для сайт-направленного расщепления молекул нуклеиновых кислот SLC39A5.
Белки Cas обычно содержат по меньшей мере один домен распознавания или связывания РНК, который может взаимодействовать с нРНК. Белки Cas также могут содержать нуклеазные домены (такие как, например, домены ДНКазы или РНКазы), домены связывания ДНК, домены геликазы, домены белок-белковых взаимодействий, домены димеризации и другие домены. Подходящие белки Cas включают в себя, например, белок Cas9 дикого типа и белок Cpf1 дикого типа (например, FnCpf1). Белок Cas может обладать полной активностью расщепления для создания двухцепочечного разрыва в геномной молекуле нуклеиновой кислоты SLC39A5, или он может представлять собой никазу, которая создает одноцепочечный разрыв в молекуле геномной нуклеиновой кислоты SLC39A5. Дополнительные примеры белков Cas включают в себя, но не ограничиваются ими, Cas1, Cas1B, Cas2, Cas3, Cas4, Cas5, Cas5e (CasD), Cas6, Cas6e, Cas6f, Cas7, Cas8a1, Cas8a2, Cas8b, Cas8c, Cas9 (Csn1 или Csx12), Cas10, Cas10d, CasF, CasG, CasH, Csy1, Csy2, Csy3, Cse1 (CasA), Cse2 (CasB), Cse3 (CasE), Cse4 (CasC), Csc1, Csc2, Csa5, Csn2, Csm2, Csm3, Csm4, Csm5, Csm6, Cmr1 , Cmr3, Cmr4, Cmr5, Cmr6, Csb1, Csb2, Csb3, Csx17, Csx14, Csx10, Csx16, CsaX, Csx3, Csx1, Csx15, Csf1, Csf2, Csf3, Csf4 и Cu1966, а также их гомологи или модифицированные версии. Белки Cas также могут быть функционально связаны с гетерологичными полипептидами как слитые белки. Например, белок Cas может быть слит с доменом расщепления, доменом эпигенетической модификации, доменом активации транскрипции или доменом репрессии транскрипции. Белки Cas могут быть предоставлены в любой форме. Например, белок Cas может быть предоставлен в форме белка, такого как белок Cas, объединенный в комплекс с нРНК. Альтернативно, белок Cas может быть предоставлен в виде молекулы нуклеиновой кислоты, кодирующей белок Cas, такой молекулы, как РНК или ДНК.
В некоторых вариантах осуществления целевые генетические модификации молекул геномной нуклеиновой кислоты SLC39A5 могут быть получены путем приведения в контакт клетки с белком Cas и одной или большим числом нРНК, которые гибридизуются с одной или большим числом последовательностей распознавания нРНК в целевом геномном локусе в молекуле геномной нуклеиновой кислоты SLC39A5 . Например, последовательность распознавания нРНК может быть расположена в области SEQ ID NO: 1. Последовательность распознавания нРНК может также включать или находиться рядом с положением, соответствующим положению i) 5604, ii) 6899, iii) 1353, iv) 6352 или v) 5624 согласно SEQ ID NO: 1. Например, последовательность распознавания нРНК может располагаться от около 1000, 500, 400, 300, 200, 100, 50, 45, 40, 35, 30, 25, 20, 15, 10 или 5 нуклеотидов в положении, соответствующем положению i) 5604, ii) 6899, iii) 1353, iv) 6352 или v) 5624 согласно SEQ ID NO: 1. Последовательность распознавания нРНК может включать или находиться рядом со старт-кодоном молекулы геномной нуклеиновой кислоты SLC39A5 или стоп-кодоном молекулы геномной нуклеиновой кислоты SLC39A5. Например, последовательность распознавания нРНК может располагаться от около 10, 20, 30, 40, 50, 100, 200, 300, 400, 500 или 1000 нуклеотидов стартового кодона или стоп-кодона.
Последовательности распознавания нРНК в целевом геномном локусе в молекуле геномной нуклеиновой кислоты SLC39A5 расположены рядом с последовательностью мотива, примыкающего к протоспейсеру (Protospacer Adjacent Motif, PAM), которая представляет собой последовательность ДНК из 2-6 пар оснований, непосредственно следующую за последовательностью ДНК, на которую нацелена нуклеаза Cas9. Каноническим PAM является последовательность 5'-NGG-3', где «N» представляет собой любое нуклеиновое основание, за которым следуют два гуаниновых («G») нуклеиновых основания. нРНК могут транспортировать Cas9 в любую точку генома для редактирования генов, но никакое редактирование не может происходить в каком-либо сайте, кроме того, в котором Cas9 распознает PAM. Кроме того, 5'-NGA-3' может представлять собой высокоэффективный неканонический PAM для клеток человека. Как правило, PAM расположен на расстоянии около 2-6 нуклеотидов ниже последовательности ДНК, на которую нацелена нРНК. PAM может фланкировать последовательность распознавания нРНК. В некоторых вариантах осуществления последовательность распознавания нРНК может быть фланкирована PAM на 3’- конце. В некоторых вариантах осуществления последовательность распознавания нРНК может быть фланкирована PAM на 5’- конце. Например, сайт расщепления белков Cas может быть расположен на расстоянии от 1 до 10, от 2 до 5 пар оснований или на три пары оснований выше или ниже последовательности PAM. В некоторых вариантах осуществления (например, когда применяется Cas9 из S. pyogenes или близкородственный Cas9), последовательность PAM некомплементарной цепи может представлять собой 5’-NGG-3’, где N представляет собой любой нуклеотид ДНК и сразу равен 3’ последовательности распознавания нРНК некомплементарной цепи целевой ДНК. Таким образом, последовательность PAM комплементарной цепи будет представлять собой 5’-CCN-3’, где «N» представляет собой любой ДНК-нуклеотид и расположен непосредственно в положении 5’ к последовательности распознавания нРНК комплементарной цепи целевой ДНК.
нРНК представляет собой молекулу РНК, которая связывается с белком Cas и нацеливает белок Cas на определенное место в молекуле геномной нуклеиновой кислоты SLC39A5. Иллюстративная нРНК представляет собой нРНК, эффективную для направления фермента Cas связываться с молекулой геномной нуклеиновой кислоты SLC39A5 или расщеплять ее, при этом нРНК содержит нацеливающий на ДНК сегмент, который гибридизуется с последовательностью распознавания нРНК в молекуле геномной нуклеиновой кислоты SLC39A5, которая включает или находится рядом с положением, соответствующим положению i) 5604, ii) 6899, iii) 1353, iv) 6352 или v) 5624 согласно SEQ ID NO: 1. Например, нРНК может быть выбрана так, чтобы она гибридизовалась с последовательностью распознавания нРНК, которая расположена от около 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 100, 200, 300, 400, 500 или 1000 нуклеотидов в положении, соответствующем положению i) 5604, ii) 6899, iii) 1353, iv) 6352 или v) 5624 согласно SEQ ID NO: 1. Другие иллюстративные нРНК содержат нацеливающий на ДНК сегмент, который гибридизуется с последовательностью распознавания нРНК в молекуле геномной нуклеиновой кислоты SLC39A5, которая включает или находится рядом со старт-кодоном или стоп-кодоном. Например, нРНК может быть выбрана так, чтобы она гибридизовалась с последовательностью распознавания нРНК, которая расположена от около 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 100, 200, 300, 400, 500 или 1000 нуклеотидов стартового кодона или расположена от около 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 100, 200, 300, 400, 500 или 1000 нуклеотидов стартового кодона или стоп-кодона. Дизайн и синтез нРНК описаны, например, в публикациях Mali et al., Science, 2013, 339, 823-826; Jinek et al., Science, 2012, 337, 816-821; Hwang et al., Nat. Biotechnol., 2013, 31, 227-229; Jiang et al., Nat. Biotechnol., 2013, 31, 233-239; и Cong et al., Science, 2013, 339, 819-823. Пригодные нРНК могут содержать от около 17 до около 23 нуклеотидов, от около 18 до около 22 нуклеотидов или от около 19 до около 21 нуклеотида. В некоторых вариантах осуществления нРНК могут содержать 20 нуклеотидов.
Примеры подходящих последовательностей распознавания нРНК, расположенных в пределах эталонного гена SLC39A5 человека, приведены в таблице 1 как последовательности SEQ ID NO: 28-56.
Таблица 1. Последовательности распознавания направляющих РНК вблизи вариантного SLC39A5
Белок Cas и нРНК образуют комплекс, и белок Cas расщепляет целевую молекулу геномной нуклеиновой кислоты SLC39A5. Белок Cas может расщеплять молекулу нуклеиновой кислоты на участке внутри или снаружи последовательности нуклеиновой кислоты, присутствующей в целевой молекуле геномной нуклеиновой кислоты SLC39A5, с которой будет связываться ДНК-нацеливающийся сегмент нРНК. Например, образование комплекса CRISPR (содержащего нРНК, гибридизованную с последовательностью распознавания нРНК и объединенную в комплекс с белком Cas) может привести к расщеплению одной или обеих цепей внутри или вблизи (например, в пределах 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 50 или более пар оснований) последовательности нуклеиновой кислоты, присутствующей в геномной молекуле нуклеиновой кислоты SLC39A5, с которой будет связываться нацеливающийся на ДНК сегмент нРНК.
Результатом таких способов могут быть, например, молекула геномной нуклеиновой кислоты SLC39A5, в которой нарушена область SEQ ID NO: 1, нарушен старт-кодон, нарушен стоп-кодон или нарушена либо удалена кодирующая последовательность. Необязательно, клетка может быть дополнительно приведена в контакт с одной или большим количеством дополнительных нРНК, которые гибридизуются с дополнительными последовательностями распознавания нРНК в целевом геномном локусе в молекуле геномной нуклеиновой кислоты SLC39A5. Пyтем приведения клетки в контакт с одной или большим количеством дополнительных нРНК (таких как, например, вторая нРНК, которая гибридизуется со второй последовательностью распознавания нРНК), расщепление белком Cas может создать два или большее количество двухцепочечных разрывов или два или большее количество одноцепочечных разрывов.
В некоторых вариантах осуществления способы лечения дополнительно включают обнаружение присутствия или отсутствия вариантной молекулы нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5, кодирующей полипептид SLC39A5 человека, в биологическом образце от субъекта. Как применяется по всему тексту данного документа «вариантная молекула нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5» представляет собой любую молекулу нуклеиновой кислоты SLC39A5 (такую как, например, молекулу нуклеиновой геномной кислоты, молекулу мРНК или молекулу кДНК), кодирующую полипептид SLC39A5, имеющий частичную потерю функции, полную потерю функции, прогнозируемую частичную потерю функции или прогнозируемую полную потерю функции.
В настоящем изобретении также представлены способы лечения субъекта терапевтическим агентом, который нормализует или ингибирует повышенный уровень глюкозы в сыворотке и/или гипергликемию, при которых субъект страдает повышенным уровнем глюкозы в сыворотке и/или гипергликемией, способ, включающий стадии: определения того, имеет ли субъект вариантную молекулу нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5, кодирующую полипептид SLC39A5 человека, путем: получения или осуществления получения биологического образца от субъекта; и выполнения или осуществления выполнения генотипирования биологического образца, чтобы определить, имеет ли субъект генотип, имеющий молекулу нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5; а когда субъект является эталонным по SLC39A5, то введения или продолжения введения субъекту терапевтического агента, который нормализует или ингибирует повышенный уровень глюкозы в сыворотке и/или гипергликемию в стандартной дозировке, и введения субъекту ингибитора SLC39A5; а когда субъект является гетерозиготным по варианту с прогнозируемой потерей функции SLC39A5, то путем введения или продолжения введения субъекту терапевтического агента, который нормализует или ингибирует повышенный уровень глюкозы в сыворотке и/или гипергликемию в количестве, которое равно или ниже стандартной дозировки, и введения субъекту ингибитора SLC39A5; при этом наличие генотипа, имеющего молекулы нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5, кодирующей полипептид SLC39A5 человека, указывает на то, что у субъекта снижен риск развития повышенного уровня глюкозы в сыворотке и/или гипергликемии. В некоторых вариантах осуществления субъект является эталонным по SLC39A5. В некоторых вариантах осуществления субъект является гетерозиготным по варианту с прогнозируемой потерей функции SLC39A5.
Касательно субъектов-людей, которые генотипированы или определены либо как эталонные по SLC39A5, либо как гетерозиготные по варианту с прогнозируемой потерей функции SLC39A5, таких субъектов-людей можно лечить с помощью ингибитора SLC39A5, как описано в данном документе.
В любом из описанных в данном документе вариантов осуществления вариантная молекула нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 может представлять собой любую молекулу нуклеиновой кислоты SLC39A5 (такую как, например, молекулу геномной нуклеиновой кислоты, молекулу мРНК или молекулу кДНК), кодирующую полипептид SLC39A5, имеющий частичную потерю функции, полную потерю функции, прогнозируемую частичную потерю функции или прогнозируемую полную потерю функции. Например, вариантная молекула нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 может быть любой молекулой нуклеиновой кислоты, кодирующей любой из полипептидов SLC39A5, описанных в данном документе, включая, например, SLC39A5 M304T, G413A, Y47Stop, R322Stop или R311Stop.
В любом из вариантов осуществления, описанных в данном документе, вариантная молекула нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 также может быть любой молекулой нуклеиновой кислоты SLC39A5 (такой как, например, молекула геномной нуклеиновой кислоты, молекула мРНК или молекула кДНК), которая содержит: i) точечную мутацию в экзоне эталонного гена SLC39A5; ii) полную или частичную делецию кодирующей последовательности эталонного гена SLC39A5, такую как, например, делеция, которая включает экзон 1, полностью или частично, и/или экзон 2, полностью или частично. В некоторых вариантах осуществления делеция включает кодирующую часть экзона 1 и часть экзона 2 эталонного гена SLC39A5. В некоторых вариантах осуществления делеция включает последовательность нуклеиновой кислоты от нуклеотида после старт-кодона ATG в экзоне 1 до пятого нуклеотида перед 3'-концом экзона 2 эталонного гена SLC39A5.
Обнаружение присутствия или отсутствия вариантной молекулы нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 в биологическом образце от субъекта и/или определение того, имеет ли субъект вариантную молекулу нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5, можно выполнять любым из способов, описанных в данном документе. В некоторых вариантах осуществления указанные способы можно выполнять in vitro. В некоторых вариантах осуществления указанные способы можно выполнять in situ. В некоторых вариантах осуществления указанные способы можно выполнять in vivo. В любом из данных вариантов осуществления молекула нуклеиновой кислоты может присутствовать в клетке, полученной от субъекта-человека.
В некоторых вариантах осуществления, когда субъект является эталонным по SLC39A5, субъекту также вводят терапевтический агент, который нормализует или ингибирует повышенный уровень глюкозы в сыворотке и/или гипергликемию, в стандартной дозировке. В некоторых вариантах осуществления, когда субъект является гетерозиготным по варианту с прогнозируемой потерей функции SLC39A5, субъекту также вводят терапевтический агент, который нормализует или ингибирует повышенный уровень глюкозы в сыворотке и/или гипергликемию в дозировке, которая является такой же, как или ниже стандартной дозировки.
В некоторых вариантах осуществления способы лечения дополнительно включают обнаружение присутствия или отсутствия полипептида SLC39A5 с прогнозируемой потерей функции в биологическом образце от субъекта. В некоторых вариантах осуществления, когда субъект не имеет полипептида с прогнозируемой потерей функции SLC39A5, субъекту также вводят терапевтический агент, который нормализует или ингибирует повышенный уровень глюкозы в сыворотке и/или гипергликемию в стандартной дозировке. В некоторых вариантах осуществления, когда субъект имеет полипептид с прогнозируемой потерей функции SLC39A5, субъекту также вводят терапевтический агент, который нормализует или ингибирует повышенный уровень глюкозы в сыворотке и/или гипергликемию в дозировке, которая равна или ниже стандартной дозировки.
В настоящем изобретении также представлены способы лечения субъекта терапевтическим агентом, который нормализует или ингибирует повышенный уровень глюкозы в сыворотке и/или гипергликемию, при этом субъект страдает от повышенного уровня глюкозы в сыворотке и/или гипергликемии, причем способ включает стадии: определения того, имеет ли субъект полипептид с прогнозируемой потерей функции SLC39A5 путем: получения или осуществления получения биологического образца от субъекта; и выполнения или осуществления выполнения анализа биологического образца, чтобы определить, есть ли у субъекта полипептид с прогнозируемой потерей функции SLC39A5; и когда у субъекта нет полипептида с прогнозируемой потерей функции SLC39A5, то введения или продолжения введения субъекту терапевтического агента, который нормализует или ингибирует повышенный уровень глюкозы в сыворотке и/или гипергликемию в стандартной дозировке, и введения субъекту ингибитора SLC39A5; а когда у субъекта есть полипептид с прогнозируемой потерей функции SLC39A5, то введения или продолжения введения субъекту терапевтического агента, который нормализует или ингибирует повышенный уровень глюкозы в сыворотке и/или гипергликемию, в количестве, равном или меньшем, чем стандартная дозировка, и введения субъекту ингибитора SLC39A5; при этом присутствие полипептида с прогнозируемой потерей функции SLC39A5 указывает на то, что у субъекта снижен риск развития повышенного уровня глюкозы в сыворотке и/или гипергликемии. В некоторых вариантах осуществления субъект имеет полипептид с прогнозируемой потерей функции SLC39A5. В некоторых вариантах осуществления субъект не имеет полипептид с прогнозируемой потерей функции SLC39A5.
В любом из описанных в данном документе вариантов осуществления полипептид с прогнозируемой потерей функции SLC39A5 может представлять собой любой полипептид SLC39A5, имеющий частичную потерю функции, полную потерю функции, прогнозируемую частичную потерю функции или прогнозируемую полную потерю функции. В любом из вариантов осуществления, описанных в данном документе, полипептид с прогнозируемой потерей функции SLC39A5 может быть любым из полипептидов SLC39A5, описанных в данном документе, включая, например, SLC39A5 M304T, G413A, Y47Stop, R322Stop или R311Stop. В некоторых вариантах осуществления полипептид SLC39A5 представляет собой SLC39A5 Y47Stop, R322Stop или R311Stop.
Обнаружение присутствия или отсутствия полипептида с прогнозируемой потерей функции SLC39A5 в биологическом образце от субъекта и/или определение того, имеет ли субъект полипептид с прогнозируемой потерей функции SLC39A5, можно выполнять любым из способов, описанных в данном документе. В некоторых вариантах осуществления указанные способы можно выполнять in vitro. В некоторых вариантах осуществления указанные способы можно выполнять in situ. В некоторых вариантах осуществления указанные способы можно выполнять in vivo. В любом из данных вариантов осуществления указанный полипептид может присутствовать в клетке, полученной от субъекта-человека.
В любом из вариантов осуществления, описанных в данном документе, у субъекта может быть пониженный уровень цинка в сыворотке или пониженный уровень цинка в костях, или и то, и другое. В любом из вариантов осуществления, описанных в данном документе, субъект может иметь любое одно или более из следующего: повышенный уровень глюкозы в сыворотке, гипергликемия, диабет 2 типа, стероид-индуцированный диабет, повышенный уровень липопротеинов низкой плотности (ЛПНП) и пониженный уровень липопротеинов высокой плотности (ЛПВП). В любом из вариантов осуществления, описанных в данном документе, у субъекта может быть повышенный уровень глюкозы в сыворотке крови, и его можно лечить способами, описанными в данном документе. В любом из вариантов осуществления, описанных в данном документе, у субъекта может быть гипергликемия, и его можно лечить способами, описанными в данном документе. В любом из вариантов осуществления, описанных в данном документе, у субъекта может быть стероид-индуцированный диабет и его можно лечить способами, описанными в данном документе. В любом из вариантов осуществления, описанных в данном документе, у субъекта может быть повышенный уровень ЛПНП, и его можно лечить способами, описанными в данном документе. В любом из вариантов осуществления, описанных в данном документе, у субъекта может быть пониженный уровень ЛПВП, и его можно лечить способами, описанными в данном документе. В любом из вариантов осуществления, описанных в данном документе, у субъекта может быть диабет 2 типа, и его можно лечить способами, описанными в данном документе. В любом из вариантов осуществления, описанных в данном документе, субъект может иметь любое одно или более из повышенного уровня глюкозы в сыворотке, гипергликемии, диабета 2 типа, стероид-индуцированного диабета, повышенного ЛПНП и пониженного ЛПВП, с сопутствующей дисфункцией печени или без нее. Дисфункция печени включает любое одно или более из следующего: жировая болезнь печени (включая алкогольную жировую болезнь печени (АЖБП) и неалкогольная жировая болезнь печени (НАЖБП)), стеатогепатит, печеночная энцефалопатию, фиброз печени, повышение ферментов печени (включая аланинтрансаминазу (АЛТ) и аспартаттрансаминазу (АСТ)), а также заболевания, связанные с перегрузкой железом, такие как гемохроматоз. В любом из вариантов осуществления, описанных в данном документе, субъект может иметь одно или более из следующего: повышенный уровень глюкозы в сыворотке, гипергликемия, диабет 2 типа, стероид-индуцированный диабет, повышенный уровень ЛПНП и пониженный уровень ЛПВП, со сниженным уровнем цинка в сыворотке или сниженным уровнем цинка в костях, или и то, и другое.
Примеры терапевтических агентов, которые нормализуют или ингибируют повышенный уровень глюкозы в сыворотке и/или гипергликемию, включают, но не ограничиваются ими: статин, агонист PPAR, гормон, агент на основе сульфонилмочевины, бигуанид, ингибитор α-глюкозидазы и агонист GLP-1.
Статины включают, но не ограничиваются ими: аторвастатин, правастатин, флувастатин, ловастатин, симвастатин и церивастатин.
Агонисты PPAR включают тиазолидиндионы и фибраты. Тиазолидиндионы включают, но не ограничиваются ими: 5-((4-(2-(метил-2-пиридиниламино)этокси)фенил)метил)-2,4-тиазолидиндион, троглитазон, пиоглитазон, циглитазон, WAY-120,744, англитазон, AD 5075, дарглитазон и розиглитазон. Фибраты включают, но не ограничиваются ими: гемфиброзил, фенофибрат, клофибрат или ципрофибрат.
Гормоны включают, помимо прочего: гормон щитовидной железы, эстроген и инсулин. Подходящие инсулины включают, но не ограничиваются ими: инсулин для инъекций, трансдермальный инсулин, инсулин для ингаляции или любую их комбинацию. В качестве альтернативы инсулину можно использовать производное инсулина, средство, усиливающее секрецию, сенсибилизатор или миметик. Средства, стимулирующие секрецию инсулина, включают, но не ограничиваются ими: форсколин, дибутрил-цАМФ или изобутилметилксантин (IBMX).
Агенты на основе сульфонилмочевины включают, но не ограничиваются ими: глизоксепид, глибурид, ацетогексамид, хлорпропамид, глиборнурид, толбутамид, толазамид, глипизид, гликлазид, гликидон, глигексамид, фенбутамид и толцикламид.
Бигуаниды включают, но не ограничиваются ими: метформин, фенформин и буформин.
Ингибиторы α-глюкозидазы включают, но не ограничиваются ими: акарбозу и миглитол.
Агонисты GLP-1 включают, но не ограничиваются ими: VICTOZA® или SAXENDA® (лираглутид), BYETTA® или BYDUREON® (экзенатид), LYXUMIA® (ликсисенатид), TANZEUM® (альбиглутид), TRULICITY® (дулаглутид) и OZEMPIC® (семаглутид).
В некоторых вариантах осуществления доза терапевтических агентов, которые нормализуют или ингибируют повышенный уровень глюкозы в сыворотке и/или гипергликемию, может быть снижена на около 10%, около 20%, около 30%, около 40%, около 50%, около 60%, около 70%, около 80% или на около 90% для субъектов, которые являются гетерозиготными по варианту с прогнозируемой потерей функции SLC39A5, (т.е. меньшая дозировка, чем стандартная дозировка) по сравнению с субъектами, которые являются эталонными по SLC39A5 (которые могут получать стандартную дозировку). В некоторых вариантах осуществления доза терапевтических агентов, которые нормализуют или ингибируют повышенный уровень глюкозы в сыворотке и/или гипергликемию, может быть снижена на около 10%, около 20%, около 30%, около 40% или на около 50%. Кроме того, доза терапевтических агентов, которые нормализуют или ингибируют повышенный уровень глюкозы в сыворотке и/или гипергликемию у субъектов, которые являются гетерозиготными по варианту с прогнозируемой потерей функции SLC39A5, можно вводить менее часто по сравнению с субъектами, которые являются эталонными по SLC39A5.
Введение терапевтических агентов, которые нормализуют или ингибируют повышенный уровень глюкозы в сыворотке и/или гипергликемию, и/или ингибиторы SLC39A5, можно повторять, например, через один день, два дня, три дня, пять дней, одну неделю, две недели, три недели, один месяц, пять недель, шесть недель, семь недель, восемь недель, два месяца или три месяца. Повторное введение можно проводить в той же дозе или в другой дозе. Введение можно повторить один раз, два раза, три раза, четыре раза, пять раз, шесть раз, семь раз, восемь раз, девять раз, десять раз или большее число раз. Например, в соответствии с определенными схемами введения доз, субъект может получать терапию в течение продолжительного периода времени, такого как, например, 6 месяцев, 1 год или дольше.
Введение терапевтических агентов, которые нормализуют или ингибируют повышенный уровень глюкозы в сыворотке и/или гипергликемию, и/или ингибиторов SLC39A5 можно осуществлять любым подходящим путем, включая следующие, но не ограничиваясь ими: парентерально, внутривенно, перорально, подкожно, внутриартериально, внутричерепно, интратекально, внутрибрюшинно, местно, интраназально или внутримышечно. Фармацевтические композиции для введения предпочтительно являются стерильными и по существу изотоничными, и произведены согласно условиям правил производства и контроля качества лекарственных средств (GMP). Фармацевтические композиции могут быть представлены в единичной лекарственной форме (т. е. дозированной форме для единичного введения). Фармацевтические композиции могут быть составлены с использованием одного или большего количества физиологически и фармацевтически приемлемых носителей, разбавителей, эксципиентов или вспомогательных веществ. Подходящий лекарственный состав зависит от выбранного пути введения. Термин «фармацевтически приемлемый» означает, что носитель, разбавитель, эксципиент или вспомогательное вещество совместимы с другими ингредиентами лекарственного состава и по существу не являются вредными для их реципиента.
В любом из вариантов осуществления, описанных в данном документе, субъекту-человеку можно вводить цинк. Цинк можно вводить перорально в виде соли цинка, такой как, например, сульфат цинка или глюконат цинка. Цинк можно вводить в количестве от около 5 до около 100 мг/день, от около 5 до около 80 мг/день, от около 5 до около 60 мг/день, от около 5 до около 50 мг/день, от около 5 до около 40 мг/день, от около 5 до около 25 мг/день, от около 5 до около 15 мг/день, от около 10 до около 100 мг/день, от около 15 до около 100 мг/день, от около 20 до около 100 мг/день, от около 25 до около 100 мг/день, от около 10 до около 50 мг/день, от около 15 до около 40 мг/день или от около 20 до около 30 мг/день.
Термины «лечить», «лечат» и «лечение», и «предотвращать», «предотвращение» и «профилактика», используемые в контексте данного документа, относятся к вызыванию желаемого биологического ответа, такого как терапевтический и профилактический эффект, соответственно. В некоторых вариантах осуществления терапевтический эффект включает одно или более из следующего: снижение/уменьшение повышенного уровня глюкозы в сыворотке и/или гипергликемии, снижение/уменьшение степени тяжести повышенного уровня глюкозы в сыворотке и/или гипергликемии (например, таких как снижение или ингибирование развития повышенного уровня глюкозы в сыворотке и/или гипергликемии), снижение/уменьшение симптомов и эффектов, связанных с повышенным уровнем глюкозы в сыворотке и/или гипергликемией, задержка появления симптомов и эффектов, связанных с повышенным уровнем глюкозы в сыворотке и/или гипергликемией, уменьшение степени тяжести симптомов и/или эффектов, связанные с повышенным уровнем глюкозы в сыворотке и/или гипергликемией, уменьшение степени тяжести острого эпизода, уменьшение количества симптомов и эффектов, связанных с повышенным уровнем глюкозы в сыворотке и/или гипергликемией, уменьшение латентного периода симптомов и эффектов, связанных с повышенным уровнем глюкозы в сыворотке и/или гипергликемией, уменьшение интенсивности симптомов и эффектов, связанных с повышенным уровнем глюкозы в сыворотке и/или гипергликемией, уменьшение вторичных симптомов, уменьшение вторичных инфекций, предотвращение рецидива повышенного уровня глюкозы в сыворотке и/или гипергликемии, уменьшение количества или частоты эпизодов рецидива, увеличение латентного периода между симптоматическими эпизодами, увеличение времени до устойчивого прогрессирования, ускорение ремиссии, индукция ремиссии, усиление ремиссии, ускорение выздоровления или повышение эффективности или снижение устойчивости к альтернативным терапевтическим средствам и/или увеличение времени выживаемости заболевшего животного-хозяина после введения агента или композиции, содержащей агент. Профилактический эффект может включать полное или частичное предотвращение/ингибирование или задержку развития/прогрессирования повышенного уровня глюкозы в сыворотке и/или гипергликемии (например, полное или частичное предотвращение/ингибирование или задержка) и увеличение времени выживаемости заболевшего животного-хозяина после применения терапевтического протокола. Лечение повышенного уровня глюкозы в сыворотке и/или гипергликемии включает лечение субъектов, у которых уже диагностирована какая-либо форма повышенного уровня глюкозы в сыворотке и/или гипергликемии на любой клинической стадии или проявлении, задержку начала или развития, или обострения, или ухудшения симптомов или признаков повышенного уровня глюкозы в сыворотке и/или гипергликемии, и/или предотвращение, и/или уменьшение степени тяжести повышенного уровня глюкозы в сыворотке и/или гипергликемии.
В настоящем изобретении также представлены способы идентификации субъекта-человека, имеющего высокий риск развития повышенного уровня глюкозы в сыворотке и/или гипергликемии, при этом способ включает: определение или осуществление определения в биологическом образце, полученном от субъекта, наличия или отсутствия вариантной молекулы нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 (такой как молекула геномной нуклеиновой кислоты, молекула мРНК и/или молекула кДНК), кодирующей полипептид SLC39A5 человека; где: i) когда субъект-человек не имеет молекулы нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 (т.е. субъект-человек генотипически классифицируется как эталонный по SLC39A5), то субъект-человек имеет высокий риск развития повышенного уровня глюкозы в сыворотке и/или гипергликемии; и ii) когда субъект-человек имеет молекулу нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 (т.е. субъект-человек классифицируется как гетерозиготный по варианту с прогнозируемой потерей функции SLC39A5 или гомозиготный по варианту с прогнозируемой потерей функции SLC39A5), то субъект-человек имеет низкий риск развития повышенного уровня глюкозы в сыворотке и/или гипергликемии. Наличие единственной копии вариантной молекулы нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 может в большей степени защищать субъекта-человека от развития повышенного уровня глюкозы в сыворотке и/или гипергликемии, чем отсутствие копий молекул вариантной нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5.
Без намерения ограничиваться какой-либо конкретной теорией или механизмом действия, считается, что одна копия молекулы нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 (т. е. гетерозиготность по варианту с прогнозируемой потерей функции SLC39A5) защищает субъекта-человека от развития повышенного уровня глюкозы в сыворотке и/или гипергликемии, а также считается, что наличие двух копий вариантной молекулы нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 (т. е. гомозиготной по варианту с прогнозируемой потерей функции SLC39A5) может в большей степени защищать субъекта-человека от развития повышенного уровня глюкозы в сыворотке и/или гипергликемии, по сравнению с субъектом-человеком с единственной копией. Таким образом, в некоторых вариантах осуществления одна копия вариантной молекулы нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 может не обеспечить полную защиту, но вместо этого может частично или не полностью защитить субъекта-человека от развития повышенного уровня глюкозы в сыворотке и/или гипергликемии. Не желая связывать себя какой-либо конкретной теорией, могут быть дополнительные факторы или молекулы, участвующие в развитии повышенного уровня глюкозы в сыворотке и/или гипергликемии, которые все еще присутствуют у субъекта-человека, имеющего единственную копию вариантной молекулы нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5, что приводит к неполной защите от развития повышенного уровня глюкозы в сыворотке и/или гипергликемии.
В любом из описанных в данном документе вариантов осуществления вариантная молекула нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 может представлять собой любую молекулу нуклеиновой кислоты SLC39A5 (такую как, например, молекулу геномной нуклеиновой кислоты, молекулу мРНК или молекулу кДНК), кодирующую полипептид SLC39A5, имеющий частичную потерю функции, полную потерю функции, прогнозируемую частичную потерю функции или прогнозируемую полную потерю функции. Например, вариантная молекула нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 может представлять собой любую молекулу нуклеиновой кислоты, кодирующую SLC39A5 M304T, G413A, Y47Stop, R322Stop, или R311Stop. В некоторых вариантах осуществления вариантная молекула нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 кодирует SLC39A5 Y47Stop, R322Stop или R311Stop.
Определение того, имеет ли субъект-человек вариантную молекулу нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 в биологическом образце, может быть выполнено любым из способов, описанных в данном документе. В некоторых вариантах осуществления указанные способы можно выполнять in vitro. В некоторых вариантах осуществления указанные способы можно выполнять in situ. В некоторых вариантах осуществления указанные способы можно выполнять in vivo. В любом из данных вариантов осуществления молекула нуклеиновой кислоты может присутствовать в клетке, полученной от субъекта-человека.
В любом из вариантов осуществления, описанных в данном документе, у субъекта может быть пониженный уровень цинка в сыворотке или пониженный уровень цинка в костях, или и то, и другое. В любом из вариантов осуществления, описанных в данном документе, субъект может иметь любое одно или более из следующего: повышенный уровень глюкозы в сыворотке, гипергликемия, диабет 2 типа, стероид-индуцированный диабет, повышенный уровень липопротеинов низкой плотности (ЛПНП) и пониженный уровень липопротеинов высокой плотности (ЛПВП). В любом из вариантов осуществления, описанных в данном документе, у субъекта может быть повышенный уровень глюкозы в сыворотке крови, и его можно лечить способами, описанными в данном документе. В любом из вариантов осуществления, описанных в данном документе, у субъекта может быть гипергликемия, и его можно лечить способами, описанными в данном документе. В любом из вариантов осуществления, описанных в данном документе, у субъекта может быть стероид-индуцированный диабет и его можно лечить способами, описанными в данном документе. В любом из вариантов осуществления, описанных в данном документе, у субъекта может быть повышенный уровень ЛПНП, и его можно лечить способами, описанными в данном документе. В любом из вариантов осуществления, описанных в данном документе, у субъекта может быть пониженный уровень ЛПВП, и его можно лечить способами, описанными в данном документе. В любом из вариантов осуществления, описанных в данном документе, у субъекта может быть диабет 2 типа, и его можно лечить способами, описанными в данном документе. В любом из вариантов осуществления, описанных в данном документе, субъект может иметь любое одно или более из повышенного уровня глюкозы в сыворотке, гипергликемии, диабета 2 типа, стероид-индуцированного диабета, повышенного ЛПНП и пониженного ЛПВП, с сопутствующей дисфункцией печени или без нее. Дисфункция печени включает любое одно или более из следующего: жировая болезнь печени (включая алкогольную жировую болезнь печени (АЖБП) и неалкогольная жировая болезнь печени (НАЖБП)), стеатогепатит, печеночная энцефалопатию, фиброз печени, повышение ферментов печени (включая аланинтрансаминазу (АЛТ) и аспартаттрансаминазу (АСТ)), а также заболевания, связанные с перегрузкой железом, такие как гемохроматоз. В любом из вариантов осуществления, описанных в данном документе, субъект может иметь одно или более из следующего: повышенный уровень глюкозы в сыворотке, гипергликемия, диабет 2 типа, стероид-индуцированный диабет, повышенный уровень ЛПНП и пониженный уровень ЛПВП, со сниженным уровнем цинка в сыворотке или сниженным уровнем цинка в костях, или и то, и другое.
В некоторых вариантах осуществления, когда субъект-человек идентифицирован как высокий риск развития повышенного уровня глюкозы в сыворотке и/или гипергликемии, тогда указанного субъекта-человека дополнительно лечат терапевтическим агентом, который нормализует или ингибирует повышенный уровень глюкозы в сыворотке и/или гипергликемию, и/или ингибитор SLC39A5, как описано в данном документе. Например, когда субъект-человек является эталонным по SLC39A5 и, следовательно, имеет высокий риск развития повышенного уровня глюкозы в сыворотке и/или гипергликемии, тогда указанному субъекту-человеку вводят ингибитор SLC39A5. В некоторых вариантах осуществления такому субъекту также вводят терапевтический агент, который нормализует или ингибирует повышенный уровень глюкозы в сыворотке и/или гипергликемию. В некоторых вариантах осуществления, когда субъект является гетерозиготным по варианту с прогнозируемой потерей функции SLC39A5, субъекту вводят терапевтический агент, который нормализует или ингибирует повышенный уровень глюкозы в сыворотке и/или гипергликемию в дозировке, которая является такой же, как или ниже стандартной дозировки, и также вводят ингибитор SLC39A5. В некоторых вариантах осуществления субъект является эталонным по SLC39A5. В некоторых вариантах осуществления субъект является гетерозиготным по варианту с прогнозируемой потерей функции SLC39A5.
В данном изобретении также представлены способы обнаружения наличия вариантной молекулы геномной нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5, молекулы мРНК с прогнозируемой потерей функции SLC39A5 и/или молекулы кДНК с прогнозируемой потерей функции SLC39A5 в биологическом образце от субъекта-человека. Следует понимать, что генные последовательности в пределах популяции и молекулы мРНК, кодируемые такими генами, могут варьировать из-за полиморфизмов, таких как однонуклеотидные полиморфизмы. Представленные в данном документе последовательности вариантной молекулы геномной нуклеиновой кислоты SLC39A5, вариантной молекулы мРНК SLC39A5 и вариантной молекулы кДНК SLC39A5 являются только иллюстративными последовательностями. Также возможны другие последовательности вариантной молекулы геномной нуклеиновой кислоты SLC39A5, вариантной молекулы мРНК и вариантной молекулы кДНК.
Биологический образец может быть получен из любой клетки, ткани или биологической жидкости субъекта. Образец может содержать любую клинически значимую ткань, например, образец костного мозга, биопсию опухоли, тонкоигольный аспират, или образец жидкости организма, такой как кровь, зубодесневая жидкость, плазма крови, сыворотка крови, лимфа, асцитная жидкость, кистозная жидкость или моча. В некоторых случаях образец содержит буккальный соскоб. Образец, применяемый в описанных в данном документе способах, будет варьировать в зависимости от формата анализа, природы способа обнаружения и тканей, клеток или экстрактов, которые применяются в качестве образца. Биологический образец может проходить разную обработку в зависимости от применяемого анализа. Например, когда проводят обнаружение вариантной молекулы нуклеиновой кислоты SLC39A5, можно применять предварительную обработку с целью выделения или обогащения образца геномной ДНК. В этих целях можно применять множество известных способов. Когда проводят обнаружение уровня любой вариантной мРНК SLC39A5, можно применять разные методики для обогащения биологического образца мРНК. Можно применять различные способы для обнаружения наличия или уровня молекулы мРНК или наличия конкретного локуса вариантной геномной ДНК.
В некоторых вариантах осуществления обнаружение вариантной молекулы нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 человека у субъекта-человека включает в себя анализ или генотипирование биологического образца, полученного от указанного субъекта-человека, для определения того, содержит ли молекула геномной нуклеиновой кислоты SLC39A5, молекула мРНК SLC39A5, или молекула кДНК SLC39A5, в биологическом образце одну или большее количество вариаций, которые вызывают потерю функции (частичную или полную), или, как прогнозируется, вызывают потерю функции (частичную или полную).
В некоторых вариантах осуществления способы обнаружения присутствия или отсутствия вариантной молекулы нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 (такой как, например, молекулы геномной нуклеиновой кислоты, молекулы мРНК и/или молекулы кДНК) у субъекта-человека, включают: выполнение анализа биологического образца, полученного от субъекта-человека, который определяет, содержит ли молекула нуклеиновой кислоты в биологическом образце конкретную нуклеотидную последовательность. В некоторых вариантах осуществления нуклеотидная последовательность содержит: i) цитозин в положении, соответствующем положению 5604 согласно SEQ ID NO: 4 (для молекул геномной нуклеиновой кислоты); ii) цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 11 (для молекул мРНК); или iii) цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 18 (для молекул кДНК, полученных из молекул мРНК).
В некоторых вариантах осуществления нуклеотидную последовательность содержит: i) цитозин в положении, соответствующем положению 6899 согласно SEQ ID NO: 6 (для молекул геномной нуклеиновой кислоты); ii) цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 13 (для молекул мРНК); или iii) цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 20 (для молекул кДНК, полученных из молекул мРНК).
В некоторых вариантах осуществления нуклеотидная последовательность содержит: i) аденин или гуанин в положении, соответствующем положению 1353, согласно SEQ ID NO: 2 или SEQ ID NO: 3 (для молекул геномной нуклеиновой кислоты); ii) аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 9 или SEQ ID NO: 10 (для молекул мРНК); или iii) аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 16 или SEQ ID NO: 17 (для молекул кДНК, полученных из молекул мРНК).
В некоторых вариантах осуществления нуклеотидная последовательность содержит: i) тимин в положении, соответствующем положению 6352 согласно SEQ ID NO: 5 (для молекул геномной нуклеиновой кислоты); ii) урацил в положении, соответствующем положению 1194 согласно SEQ ID NO: 12 (для молекул мРНК); или iii) тимин в положении, соответствующем положению 1194 согласно SEQ ID NO: 19 (для молекул кДНК, полученных из молекул мРНК).
В некоторых вариантах осуществления нуклеотидная последовательность содержит: i) тимин в положении, соответствующем положению 5624 согласно SEQ ID NO: 7 (для молекул геномной нуклеиновой кислоты); ii) урацил в положении, соответствующем положению 1161 согласно SEQ ID NO: 14 (для молекул мРНК); или iii) тимин в положении, соответствующем положению 1161 согласно SEQ ID NO: 21 (для молекул кДНК, полученных из молекул мРНК).
В некоторых вариантах осуществления биологический образец содержит клетку или клеточный лизат. Такие способы могут дополнительно включать в себя, например, получение от субъекта биологического образца, содержащего молекулу геномной нуклеиновой кислоты SLC39A5 или молекулу мРНК, и, в случае с мРНК, необязательно - проведение обратной транскрипции мРНК в кДНК. Такие анализы могут включать в себя, например, идентификацию указанных положений конкретной молекулы нуклеиновой кислоты SLC39A5. В некоторых вариантах осуществления указанный способ представляет собой способ in vitro.
В некоторых вариантах осуществления стадия определения, стадия обнаружения или генотипирование включают в себя секвенирование по меньшей мере части нуклеотидной последовательности молекулы геномной нуклеиновой кислоты SLC39A5, молекулы мРНК SLC39A5 или молекулы кДНК SLC39A5 в биологическом образце, при этом секвенированная часть содержит одну или большее число вариаций, которые вызывают потерю функции (частичную или полную) или, как прогнозируется, вызывают потерю функции (частичную или полную).
В некоторых вариантах осуществления стадия определения, стадия обнаружения или генотипирование включают в себя секвенирование по меньшей мере части: i) нуклеотидной последовательности молекулы геномной нуклеиновой кислоты SLC39A5 в биологическом образце, при этом секвенированная часть содержит положение, соответствующее положению 5604 согласно SEQ ID NO: 4 или ее комплементарной цепи; ii) нуклеотидной последовательности молекулы мРНК SLC39A5 в биологическом образце, при этом секвенированная часть содержит положение, соответствующее положению 1141 согласно SEQ ID NO: 11 или ее комплементарной цепи; и/или iii) нуклеотидной последовательности молекулы кДНК SLC39A5, полученной из мРНК в биологическом образце, при этом секвенированная часть содержит положение, соответствующее положению 1141 согласно SEQ ID NO: 18 или ее комплементарной цепи. Когда секвенированная часть молекулы нуклеиновой кислоты SLC39A5 в биологическом образце содержит: цитозин в положении, соответствующем положению 5604 согласно SEQ ID NO: 4, цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 11, или цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 18, тогда молекула нуклеиновой кислоты SLC39A5 в биологическом образце представляет собой вариантную молекулу нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5.
В некоторых вариантах осуществления стадия определения, стадия обнаружения или генотипирование включают в себя секвенирование по меньшей мере части: i) нуклеотидной последовательности молекулы геномной нуклеиновой кислоты SLC39A5 в биологическом образце, при этом секвенированная часть содержит положение, соответствующее положению 6899 согласно SEQ ID NO: 6 или ее комплементарной цепи; ii) нуклеотидной последовательности молекулы мРНК SLC39A5 в биологическом образце, при этом секвенированная часть содержит положение, соответствующее положению 1468 согласно SEQ ID NO: 13 или ее комплементарной цепи; и/или iii) нуклеотидной последовательности молекулы кДНК SLC39A5, полученной из мРНК в биологическом образце, при этом секвенированная часть содержит положение, соответствующее положению 1468 согласно SEQ ID NO: 20 или ее комплементарной цепи. Когда секвенированная часть молекулы нуклеиновой кислоты SLC39A5 в биологическом образце содержит: цитозин в положении, соответствующем положению 6899 согласно SEQ ID NO: 6, цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 13, или цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 20, тогда молекула нуклеиновой кислоты SLC39A5 в биологическом образце представляет собой вариантную молекулу нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5.
В некоторых вариантах осуществления стадия определения, стадия обнаружения или генотипирование включают в себя секвенирование по меньшей мере части: i) нуклеотидной последовательности молекулы геномной нуклеиновой кислоты SLC39A5 в биологическом образце, при этом секвенированная часть содержит положение, соответствующее положению 1353 согласно с SEQ ID NO:2 или SEQ ID NO:3 или их комплементарным цепям; ii) нуклеотидной последовательности молекулы мРНК SLC39A5 в биологическом образце, при этом секвенированная часть содержит положение, соответствующее положению 371 согласно SEQ ID NO:9 или SEQ ID NO:10, или их комплементарным цепям; и/или iii) нуклеотидной последовательности молекулы кДНК SLC39A5, полученной из мРНК в биологическом образце, при этом секвенированная часть содержит положение, соответствующее положению 371 согласно SEQ ID NO:16 или SEQ ID NO:17 или их комплементарным цепям. Когда секвенированная часть молекулы нуклеиновой кислоты SLC39A5 в биологическом образце содержит: аденин или гуанин в положении, соответствующем положению 1353 согласно SEQ ID NO: 2 или SEQ ID NO: 3, аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 9 или SEQ ID NO: 10, или аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 16 или SEQ ID NO: 17, тогда молекула нуклеиновой кислоты SLC39A5 в биологическом образце представляет собой вариантную молекулу нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5.
В некоторых вариантах осуществления стадия определения, стадия обнаружения или генотипирование включают в себя секвенирование по меньшей мере части: i) нуклеотидной последовательности молекулы геномной нуклеиновой кислоты SLC39A5 в биологическом образце, при этом секвенированная часть содержит положение, соответствующее положению 6352 согласно SEQ ID NO: 5 или ее комплементарной цепи; ii) нуклеотидной последовательности молекулы мРНК SLC39A5 в биологическом образце, при этом секвенированная часть содержит положение, соответствующее положению 1194 согласно SEQ ID NO: 12 или ее комплементарной цепи; и/или iii) нуклеотидной последовательности молекулы кДНК SLC39A5, полученной из мРНК в биологическом образце, при этом секвенированная часть содержит положение, соответствующее положению 1194 согласно SEQ ID NO: 19 или ее комплементарной цепи. Когда секвенированная часть молекулы нуклеиновой кислоты SLC39A5 в биологическом образце содержит: тимин в положении, соответствующем положению 6352 согласно SEQ ID NO: 5, урацил в положении, соответствующем положению 1194 согласно SEQ ID NO: 12, или тимин в положении, соответствующем положению 1194 согласно SEQ ID NO: 19, тогда молекула нуклеиновой кислоты SLC39A5 в биологическом образце представляет собой вариантную молекулу нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5.
В некоторых вариантах осуществления стадия определения, стадия обнаружения или генотипирование включают в себя секвенирование по меньшей мере части: i) нуклеотидной последовательности молекулы геномной нуклеиновой кислоты SLC39A5 в биологическом образце, при этом секвенированная часть содержит положение, соответствующее положению 5624 согласно SEQ ID NO: 7 или ее комплементарной цепи; ii) нуклеотидной последовательности молекулы мРНК SLC39A5 в биологическом образце, при этом секвенированная часть содержит положение, соответствующее положению 1161 согласно SEQ ID NO: 14 или ее комплементарной цепи; и/или iii) нуклеотидной последовательности молекулы кДНК SLC39A5, полученной из мРНК в биологическом образце, при этом секвенированная часть содержит положение, соответствующее положению 1161 согласно SEQ ID NO: 21 или ее комплементарной цепи. Когда секвенированная часть молекулы нуклеиновой кислоты SLC39A5 в биологическом образце содержит: тимин в положении, соответствующем положению 5624 согласно SEQ ID NO: 7, урацил в положении, соответствующем положению 1161 согласно SEQ ID NO: 14, или тимин в положении, соответствующем положению 1161 согласно SEQ ID NO: 21, тогда молекула нуклеиновой кислоты SLC39A5 в биологическом образце представляет собой вариантную молекулу нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5.
В некоторых вариантах осуществления стадия определения, стадия обнаружения или генотипирование включают: а) приведение биологического образца в контакт с праймером, гибридизующимся с частью нуклеотидной последовательности SLC39A5: i) молекулы геномной нуклеиновой кислоты, расположенной вблизи положения, соответствующего положению 5604 согласно SEQ ID NO: 4; ii) молекулы мРНК, расположенной вблизи положения, соответствующего положению 1141 согласно SEQ ID NO: 11; и/или iii) молекулы кДНК, расположенной вблизи положения, соответствующего положению 1141 согласно SEQ ID NO: 18; b) удлинение праймера по меньшей мере включительно до положения нуклеотидной последовательности SLC39A5: i) молекулы геномной нуклеиновой кислоты, соответствующего положению 5604 согласно SEQ ID NO: 4; ii) молекулы мРНК, соответствующего положению 1141 согласно SEQ ID NO: 11; и/или iii) молекулы кДНК, соответствующего положению 1141 согласно SEQ ID NO: 18; и c) определение того, содержит ли продукт удлинения праймера: i) тимин в положении, соответствующем положению 5604 согласно SEQ ID NO: 4; ii) урацил в положении, соответствующем положению 1141 согласно SEQ ID NO: 11; и/или iii) тимин в положении, соответствующем положению 1141 согласно SEQ ID NO: 18.
В некоторых вариантах осуществления стадия определения, стадия обнаружения или генотипирование включают: а) приведение биологического образца в контакт с праймером, гибридизующимся с частью нуклеотидной последовательности SLC39A5: i) молекулы геномной нуклеиновой кислоты, расположенной вблизи положения, соответствующего положению 5604 согласно SEQ ID NO: 6; ii) молекулы мРНК, расположенной вблизи положения, соответствующего положению 1468 согласно SEQ ID NO: 13; и/или iii) молекулы кДНК, расположенной вблизи положения, соответствующего положению 1468 согласно SEQ ID NO: 20; b) удлинение праймера по меньшей мере включительно до положения нуклеотидной последовательности SLC39A5: i) молекулы геномной нуклеиновой кислоты, соответствующего положению 6899 согласно SEQ ID NO: 6; ii) молекулы мРНК, соответствующего положению 1468 согласно SEQ ID NO: 13; и/или iii) молекулы кДНК, соответствующего положению 1468 согласно SEQ ID NO: 20; и c) определение того, содержит ли продукт удлинения праймера: i) тимин в положении, соответствующем положению 6899 согласно SEQ ID NO: 6; ii) урацил в положении, соответствующем положению 1468 согласно SEQ ID NO: 13; и/или iii) тимин в положении, соответствующем положению 1468 согласно SEQ ID NO: 20.
В некоторых вариантах осуществления стадия определения, стадия обнаружения или генотипирование включают: a) приведение биологического образца в контакт с праймером, гибридизующимся с частью нуклеотидной последовательности SLC39A5: i) молекулы геномной нуклеиновой кислоты, расположенной вблизи положения, соответствующего положению 1353 согласно SEQ ID NO: 2 или SEQ ID NO: 3; ii) молекулы мРНК, расположенной вблизи положения, соответствующего положению 371, согласно SEQ ID NO: 9 или SEQ ID NO: 10; и/или iii) молекулы кДНК, расположенной вблизи положения, соответствующего положению 371, согласно SEQ ID NO: 16 или SEQ ID NO: 17; b) удлинение праймера по меньшей мере включительно до положения нуклеотидной последовательности SLC39A5: i) молекулы геномной нуклеиновой кислоты, соответствующего положению 1353 согласно SEQ ID NO: 2 или SEQ ID NO: 3; ii) молекулы мРНК, соответствующего положению 371, согласно SEQ ID NO: 9 или SEQ ID NO: 10; и/или iii) молекулы кДНК, соответствующего положению 371 согласно SEQ ID NO: 16 или SEQ ID NO: 17; и c) определение того, содержит ли продукт удлинения праймера: i) аденин или гуанин в положении, соответствующем положению 1353, согласно SEQ ID NO: 2 или SEQ ID NO: 3; ii) аденин или гуанин в положении, соответствующем положению 371, согласно SEQ ID NO: 9 или SEQ ID NO: 10; и/или iii) аденин или гуанин в положении, соответствующем положению 371, согласно SEQ ID NO: 16 или SEQ ID NO: 17.
В некоторых вариантах осуществления стадия определения, стадия обнаружения или генотипирование включают: а) приведение биологического образца в контакт с праймером, гибридизующимся с частью нуклеотидной последовательности SLC39A5: i) молекулы геномной нуклеиновой кислоты, расположенной вблизи положения, соответствующего положению 6352 согласно SEQ ID NO: 5; ii) молекулы мРНК, расположенной вблизи положения, соответствующего положению 1194 согласно SEQ ID NO: 12; и/или iii) молекулы кДНК, расположенной вблизи положения, соответствующего положению 1194 согласно SEQ ID NO: 19; b) удлинение праймера по меньшей мере включительно до положения нуклеотидной последовательности SLC39A5: i) молекулы геномной нуклеиновой кислоты, соответствующего положению 6352 согласно SEQ ID NO: 5; ii) молекулы мРНК, соответствующего положению 1194 согласно SEQ ID NO: 12; и/или iii) молекулы кДНК, соответствующего положению 1194 согласно SEQ ID NO: 19; и c) определение того, содержит ли продукт удлинения праймера: i) тимин в положении, соответствующем положению 6352 согласно SEQ ID NO: 5; ii) урацил в положении, соответствующем положению 1194 согласно SEQ ID NO: 12; и/или iii) тимин в положении, соответствующем положению 1194 согласно SEQ ID NO: 19.
В некоторых вариантах осуществления стадия определения, стадия обнаружения или генотипирование включают: а) приведение биологического образца в контакт с праймером, гибридизующимся с частью нуклеотидной последовательности SLC39A5: i) молекулы геномной нуклеиновой кислоты, расположенной вблизи положения, соответствующего положению 5624 согласно SEQ ID NO: 7; ii) молекулы мРНК, расположенной вблизи положения, соответствующего положению 1161 согласно SEQ ID NO: 14; и/или iii) молекулы кДНК, расположенной вблизи положения, соответствующего положению 1161 согласно SEQ ID NO: 21; b) удлинение праймера по меньшей мере включительно до положения нуклеотидной последовательности SLC39A5: i) молекулы геномной нуклеиновой кислоты, соответствующего положению 5624 согласно SEQ ID NO: 7; ii) молекулы мРНК, соответствующего положению 1161 согласно SEQ ID NO: 14; и/или iii) молекулы кДНК, соответствующего положению 1161 согласно SEQ ID NO: 21; и c) определение того, содержит ли продукт удлинения праймера: i) тимин в положении, соответствующем положению 5624 согласно SEQ ID NO: 7; ii) урацил в положении, соответствующем положению 1161 согласно SEQ ID NO: 14; и/или iii) тимин в положении, соответствующем положению 1161 согласно SEQ ID NO: 21.
В некоторых вариантах осуществления анализ включает в себя секвенирование всей молекулы нуклеиновой кислоты. В некоторых вариантах осуществления анализируют только молекулу геномной нуклеиновой кислоты SLC39A5. В некоторых вариантах осуществления анализируют только мРНК SLC39A5. В некоторых вариантах осуществления анализируют только кДНК SLC39A5, полученную из мРНК SLC39A5.
В некоторых вариантах осуществления стадия определения, стадия обнаружения или генотипирование включают в себя: а) амплификацию по меньшей мере части молекулы нуклеиновой кислоты, которая кодирует полипептид SLC39A5 человека, при этом амплифицированная часть содержит: i) тимин в положении, соответствующем положению 5604 согласно SEQ ID NO: 4 или ее комплементарной цепи; ii) урацил в положении, соответствующем положению 1141 согласно SEQ ID NO:11 или ее комплементарной цепи; и/или iii) тимин в положении, соответствующем положению 1141 согласно SEQ ID NO: 18 или ее комплементарной цепи; b) мечение амплифицированной молекулы нуклеиновой кислоты обнаруживаемой меткой; c) приведение меченой молекулы нуклеиновой кислоты в контакт с подложкой, содержащей специфический в отношении изменения зонд, при этом специфический в отношении изменения зонд содержит нуклеотидную последовательность, которая в жестких условиях гибридизуется с последовательностью нуклеиновой кислоты амплифицированной молекулы нуклеиновой кислоты, содержащей: i) тимин в положении, соответствующем положению 5604 согласно SEQ ID NO: 4 или ее комплементарной цепи; ii) урацил в положении, соответствующем положению 1141 согласно SEQ ID NO: 11 или ее комплементарной цепи; и/или iii) тимин в положении, соответствующем положению 1141 согласно SEQ ID NO: 18 или ее комплементарной цепи; и d) обнаружение обнаруживаемой метки.
В некоторых вариантах осуществления стадия определения, стадия обнаружения или генотипирование включают в себя: а) амплификацию по меньшей мере части молекулы нуклеиновой кислоты, которая кодирует полипептид SLC39A5 человека, при этом амплифицированная часть содержит: i) тимин в положении, соответствующем положению 6899 согласно SEQ ID NO: 6 или ее комплементарной цепи; ii) урацил в положении, соответствующем положению 1468 согласно SEQ ID NO:13 или ее комплементарной цепи; и/или iii) тимин в положении, соответствующем положению 1468 согласно SEQ ID NO: 20 или ее комплементарной цепи; b) мечение амплифицированной молекулы нуклеиновой кислоты обнаруживаемой меткой; c) приведение меченой молекулы нуклеиновой кислоты в контакт с подложкой, содержащей специфический в отношении изменения зонд, при этом специфический в отношении изменения зонд содержит нуклеотидную последовательность, которая в жестких условиях гибридизуется с последовательностью нуклеиновой кислоты амплифицированной молекулы нуклеиновой кислоты, содержащей: i) тимин в положении, соответствующем положению 6899 согласно SEQ ID NO: 6 или ее комплементарной цепи; ii) урацил в положении, соответствующем положению 1468 согласно SEQ ID NO: 13 или ее комплементарной цепи; и/или iii) тимин в положении, соответствующем положению 1468 согласно SEQ ID NO: 20 или ее комплементарной цепи; и d) обнаружение обнаруживаемой метки.
В некоторых вариантах осуществления стадия определения, стадия обнаружения или генотипирования включает: a) амплификацию по меньшей мере части молекулы нуклеиновой кислоты, которая кодирует полипептид SLC39A5 человека, при этом амплифицированная часть содержит: i) аденин или гуанин в положении соответствующий положению 1353 согласно SEQ ID NO: 2 или SEQ ID NO: 3, или их комплементарным цепям; ii) аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 9 или SEQ ID NO: 10, или их комплементарным цепям; и/или iii) аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 16 или SEQ ID NO: 17, или их комплементарным цепям; b) мечение амплифицированной молекулы нуклеиновой кислоты обнаруживаемой меткой; c) приведение в контакт меченой молекулы нуклеиновой кислоты с подложкой, содержащей специфический в отношении изменения зонд, причем специфический в отношении изменения зонд содержит нуклеотидную последовательность, которая гибридизуется в жестких условиях с последовательностью нуклеиновой кислоты амплифицированной молекулы нуклеиновой кислоты, содержащей: i) аденин или гуанин в положении, соответствующем положению 1353 согласно SEQ ID NO: 2 или SEQ ID NO: 3, или их комплементарным цепям; ii) аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 9 или SEQ ID NO: 10, или их комплементарным цепям; и/или iii) аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 16 или SEQ ID NO: 17, или их комплементарным цепям; и d) обнаружение обнаруживаемой метки.
В некоторых вариантах осуществления стадия определения, стадия обнаружения или генотипирование включают в себя: а) амплификацию по меньшей мере части молекулы нуклеиновой кислоты, которая кодирует полипептид SLC39A5 человека, при этом амплифицированная часть содержит: i) тимин в положении, соответствующем положению 6352 согласно SEQ ID NO: 5 или ее комплементарной цепи; ii) урацил в положении, соответствующем положению 1194 согласно SEQ ID NO:12 или ее комплементарной цепи; и/или iii) тимин в положении, соответствующем положению 1194 согласно SEQ ID NO: 19 или ее комплементарной цепи; b) мечение амплифицированной молекулы нуклеиновой кислоты обнаруживаемой меткой; c) приведение меченой молекулы нуклеиновой кислоты в контакт с подложкой, содержащей специфический в отношении изменения зонд, при этом специфический в отношении изменения зонд содержит нуклеотидную последовательность, которая в жестких условиях гибридизуется с последовательностью нуклеиновой кислоты амплифицированной молекулы нуклеиновой кислоты, содержащей: i) тимин в положении, соответствующем положению 6352 согласно SEQ ID NO: 5 или ее комплементарной цепи; ii) урацил в положении, соответствующем положению 1194 согласно SEQ ID NO: 12 или ее комплементарной цепи; и/или iii) тимин в положении, соответствующем положению 1194 согласно SEQ ID NO: 19 или ее комплементарной цепи; и d) обнаружение обнаруживаемой метки.
В некоторых вариантах осуществления стадия определения, стадия обнаружения или генотипирование включают в себя: а) амплификацию по меньшей мере части молекулы нуклеиновой кислоты, которая кодирует полипептид SLC39A5 человека, при этом амплифицированная часть содержит: i) тимин в положении, соответствующем положению 5624 согласно SEQ ID NO: 7 или ее комплементарной цепи; ii) урацил в положении, соответствующем положению 1161 согласно SEQ ID NO:14 или ее комплементарной цепи; и/или iii) тимин в положении, соответствующем положению 1161 согласно SEQ ID NO: 21 или ее комплементарной цепи; b) мечение амплифицированной молекулы нуклеиновой кислоты обнаруживаемой меткой; c) приведение меченой молекулы нуклеиновой кислоты в контакт с подложкой, содержащей специфический в отношении изменения зонд, при этом специфический в отношении изменения зонд содержит нуклеотидную последовательность, которая в жестких условиях гибридизуется с последовательностью нуклеиновой кислоты амплифицированной молекулы нуклеиновой кислоты, содержащей: i) тимин в положении, соответствующем положению 5624 согласно SEQ ID NO: 7 или ее комплементарной цепи; ii) урацил в положении, соответствующем положению 1161 согласно SEQ ID NO: 14 или комплементарной ей нуклеотидной последовательностью; и/или iii) тимин в положении, соответствующем положению 1161 согласно SEQ ID NO: 21 или ее комплементарной цепи; и d) обнаружение обнаруживаемой метки.
В некоторых вариантах осуществления молекула нуклеиновой кислоты представляет собой мРНК, и стадия определения дополнительно включает в себя выполнение обратной транскрипции мРНК в кДНК до стадии амплификации.
В некоторых вариантах осуществления стадия определения, стадия обнаружения или генотипирование включает: приведение в контакт молекулы нуклеиновой кислоты в биологическом образце с специфическим в отношении изменения зондом, содержащим обнаруживаемую метку, при этом специфический в отношении изменения зонд содержит нуклеотидную последовательность, которая гибридизуется в жестких условиях с нуклеотидной последовательностью амплифицированной молекулы нуклеиновой кислоты, содержащей: i) цитозин в положении, соответствующем положению 5604 согласно SEQ ID NO: 4, или ее комплементарной цепи; ii) цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 11, или ее комплементарной цепи; и/или цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 18, или ее комплементарной цепи; и обнаружение обнаруживаемой метки.
В некоторых вариантах осуществления стадия определения, стадия обнаружения или генотипирование включает: приведение в контакт молекулы нуклеиновой кислоты в биологическом образце с специфическим в отношении изменения зондом, содержащим обнаруживаемую метку, при этом специфический в отношении изменения зонд содержит нуклеотидную последовательность, которая гибридизуется в жестких условиях с нуклеотидной последовательностью амплифицированной молекулы нуклеиновой кислоты, содержащей: i) цитозин в положении, соответствующем положению 6899 согласно SEQ ID NO: 6, или ее комплементарной цепи; ii) цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 13, или ее комплементарной цепи; и/или цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 20, или ее комплементарной цепи; и обнаружение обнаруживаемой метки.
В некоторых вариантах осуществления стадия определения, стадия обнаружения или генотипирование включает: приведение в контакт молекулы нуклеиновой кислоты в биологическом образце с специфическим в отношении изменения зондом, содержащим обнаруживаемую метку, при этом специфический в отношении изменения зонд содержит нуклеотидную последовательность, которая гибридизуется в жестких условиях с нуклеотидной последовательностью амплифицированной молекулы нуклеиновой кислоты, содержащей: i) аденин или гуанин в положении, соответствующем положению 1353 согласно SEQ ID NO: 2 или SEQ ID NO: 3, или их комплементарным цепям; ii) аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 9 или SEQ ID NO: 10, или их комплементарным цепям; и/или аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 16 или SEQ ID NO: 17, или их комплементарным цепям; и обнаружение обнаруживаемой метки.
В некоторых вариантах осуществления стадия определения, стадия обнаружения или генотипирование включает: приведение в контакт молекулы нуклеиновой кислоты в биологическом образце с специфическим в отношении изменения зондом, содержащим обнаруживаемую метку, при этом специфический в отношении изменения зонд содержит нуклеотидную последовательность, которая гибридизуется при жестких условиях для нуклеотидной последовательности амплифицированной молекулы нуклеиновой кислоты, содержащей: i) тимин в положении, соответствующем положению 6352 согласно SEQ ID NO: 5, или ее комплементарной цепи; ii) урацил в положении, соответствующем положению 1194 согласно SEQ ID NO: 12, или ее комплементарной цепи; и/или тимин в положении, соответствующем положению 1194 согласно SEQ ID NO: 19, или ее комплементарной цепи; и обнаружение обнаруживаемой метки.
В некоторых вариантах осуществления стадия определения, стадия обнаружения или генотипирование включает: приведение в контакт молекулы нуклеиновой кислоты в биологическом образце с специфическим в отношении изменения зондом, содержащим обнаруживаемую метку, при этом специфический в отношении изменения зонд содержит нуклеотидную последовательность, которая гибридизуется при жестких условиях для нуклеотидной последовательности амплифицированной молекулы нуклеиновой кислоты, содержащей: i) тимин в положении, соответствующем положению 5624 согласно SEQ ID NO: 7, или ее комплементарной цепи; ii) урацил в положении, соответствующем положению 1161 согласно SEQ ID NO: 14, или ее комплементарной цепи; и/или тимин в положении, соответствующем положению 1161 согласно SEQ ID NO: 21, или ее комплементарной цепи; и обнаружение обнаруживаемой метки.
Могут применяться методики специфической в отношении изменения полимеразной цепной реакции для обнаружения мутаций, таких как ОНП, в последовательности нуклеиновой кислоты. Могут применяться специфические в отношения изменения праймеры, поскольку ДНК-полимераза не будет удлинять нуклеотидный продукт при наличии несоответствия с матрицей.
В некоторых вариантах осуществления молекула нуклеиновой кислоты в образце представляет собой мРНК, и проводят обратную транскрипцию указанной мРНК в кДНК до стадии амплификации. В некоторых вариантах осуществления молекула нуклеиновой кислоты может присутствовать в клетке, полученной от субъекта-человека.
Вариантная молекула нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 может представлять собой любую молекулу нуклеиновой кислоты SLC39A5 (такую как, например, молекулу геномной нуклеиновой кислоты, молекулу мРНК или молекулу кДНК), кодирующую полипептид SLC39A5, имеющий частичную потерю функции, полную потерю функции, прогнозируемую частичную потерю функции или прогнозируемую полную потерю функции. Например, вариантная молекула нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 может представлять собой любую молекулу нуклеиновой кислоты, кодирующую SLC39A5 M304T, G413A, Y47Stop, R322Stop, или R311Stop. В некоторых вариантах осуществления вариантная молекула нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 кодирует SLC39A5 Y47Stop, R322Stop или R311Stop.
В некоторых вариантах осуществления анализ может включать приведение биологического образца в контакт с праймером или зондом, таким как специфический в отношении изменения праймер или специфический в отношении изменения зонд, которые специфически гибридизуются с вариантной геномной последовательностью SLC39A5, вариантной последовательностью мРНК или вариантной последовательностью кДНК, но не с соответствующей эталонной последовательностью SLC39A5 в жестких условиях, и определение того, произошла ли гибридизация.
В некоторых вариантах осуществления анализ включает в себя секвенирование РНК (РНК-секвенирование). В некоторых вариантах осуществления анализы также включают в себя выполнение обратной транскрипции мРНК в кДНК, например, с помощью полимеразной цепной реакции с обратной транскриптазой (ОТ-ПЦР).
В некоторых вариантах осуществления способы используют зонды и праймеры достаточной нуклеотидной длины для связывания с целевой нуклеотидной последовательностью и, в частности, для обнаружения и/или идентификации полинуклеотида, содержащего вариантную молекулу геномной нуклеиновой кислоты SLC39A5, вариантную молекулу мРНК или вариантную молекулу кДНК. Условия гибридизации или условия реакции могут определяться проводящим эксперимент специалистом для достижения данного результата. Нуклеотидная длина может быть любой длиной, достаточной для использования в выбранном способе обнаружения, включая любой анализ, описанный или приведенный в качестве примера в данном документе. Такие зонды и праймеры могут специфически гибридизоваться с целевой нуклеотидной последовательностью в условиях гибридизации высокой жесткости. Зонды и праймеры могут быть полностью идентичными последовательности смежных нуклеотидов в пределах целевой нуклеотидной последовательности, хотя с помощью традиционных способов можно конструировать зонды, отличающиеся от целевой нуклеотидной последовательности, но которые сохраняют способность специфическим образом выявлять и/или идентифицировать целевую нуклеотидную последовательность. Зонды и праймеры могут быть на около 80%, около 85%, около 90%, около 91%, около 92%, около 93%, около 94%, около 95%, около 96%, около 97%, около 98%, около 99% или на 100% идентичны или комплементарны нуклеотидной последовательности целевой молекулы нуклеиновой кислоты.
В некоторых вариантах осуществления для определения того, содержит ли молекула нуклеиновой кислоты SLC39A5 (молекула геномной нуклеиновой кислоты, молекула мРНК или молекула кДНК) или ее комплементарная цепь в биологическом образце нуклеотидную последовательность, содержащую цитозин в положении, соответствующем положению 5604 согласно SEQ ID NO: 4 (молекула геномной нуклеиновой кислоты), или цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 11 (молекула мРНК), или цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 18 (молекула кДНК), биологический образец можно подвергнуть способу амплификации с использованием пары праймеров, которая включает первый праймер, полученный из 5'-фланкирующей последовательности, смежной с цитозином в положении, соответствующем положению 5604 согласно SEQ ID NO: 4 , или цитозином в положении, соответствующем положению 1141 согласно SEQ ID NO: 11, или цитозином в положении, соответствующем положению 1141 согласно SEQ ID NO: 18, и второй праймер, полученный из 3'-фланкирующей последовательности, смежной с цитозином в положении, соответствующем положению 5604 согласно SEQ ID NO: 4, или цитозином в положении, соответствующем положению 1141 согласно SEQ ID NO: 11, или цитозином в положении, соответствующем положению 1141 согласно SEQ ID NO: 18, для получения ампликона, который указывает на присутствие SNP в положениях, кодирующих цитозин в положении, соответствующем положению 5604 согласно SEQ ID NO: 4, или цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 11, или цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 18. В некоторых вариантах осуществления длина ампликона может находиться в диапазоне от комбинированной длины пар праймеров плюс одна пара нуклеотидных оснований до любой длины ампликона, получаемой согласно протоколу ДНК-амплификации. Это расстояние может находиться в диапазоне от одной пары нуклеотидных оснований до граничного значения реакции амплификации или до около двадцати тысяч пар нуклеотидных оснований. Необязательно, пара праймеров фланкирует область, включающую положения, содержащие цитозин в положении, соответствующем положению 5604 согласно SEQ ID NO: 4, или цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 11, или цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 18, и по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более нуклеотидов на каждой стороне положений, включающих цитозин в положении, соответствующем положению 5604 согласно SEQ ID NO: 4, или цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 11, или цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 18.
В некоторых вариантах осуществления для определения того, содержит ли молекула нуклеиновой кислоты SLC39A5 (молекула геномной нуклеиновой кислоты, молекула мРНК или молекула кДНК) или ее комплементарная цепь в биологическом образце нуклеотидную последовательность, содержащую цитозин в положении, соответствующем положению 6899 согласно SEQ ID NO: 6 (молекула геномной нуклеиновой кислоты), или цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 13 (молекула мРНК), или цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 20 (молекула кДНК), биологический образец можно подвергнуть способу амплификации с использованием пары праймеров, которая включает первый праймер, полученный из 5'-фланкирующей последовательности, смежной с цитозином в положении, соответствующем положению 6899 согласно SEQ ID NO: 6 , или цитозином в положении, соответствующем положению 1468 согласно SEQ ID NO: 13, или цитозином в положении, соответствующем положению 1468 согласно SEQ ID NO: 20, и второй праймер, полученный из 3'-фланкирующей последовательности, смежной с цитозином в положении, соответствующем положению 6899 согласно SEQ ID NO: 6, или цитозином в положении, соответствующем положению 1468 согласно SEQ ID NO: 13, или цитозином в положении, соответствующем положению 1468 согласно SEQ ID NO: 20, для получения ампликона, который указывает на присутствие SNP в положениях, кодирующих цитозин в положении, соответствующем положению 6899 согласно SEQ ID NO: 6, или цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 13, или цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 20. В некоторых вариантах осуществления длина ампликона может находиться в диапазоне от комбинированной длины пар праймеров плюс одна пара нуклеотидных оснований до любой длины ампликона, получаемой согласно протоколу ДНК-амплификации. Это расстояние может находиться в диапазоне от одной пары нуклеотидных оснований до граничного значения реакции амплификации или до около двадцати тысяч пар нуклеотидных оснований. Необязательно, пара праймеров фланкирует область, включающую положения, содержащие цитозин в положении, соответствующем положению 6899 согласно SEQ ID NO: 6, или цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 13, или цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 20, и по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более нуклеотидов на каждой стороне положений, включающих цитозин в положении, соответствующем положению 6899 согласно SEQ ID NO: 6, или цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 13, или цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 20.
В некоторых вариантах осуществления для определения того, содержит ли молекула нуклеиновой кислоты SLC39A5 (молекула геномной нуклеиновой кислоты, молекула мРНК или молекула кДНК, полученная из молекулы мРНК) или ее комплементарная цепь в биологическом образце нуклеотидную последовательность, содержащую аденин или гуанин в положении, соответствующем положению 1353 согласно SEQ ID NO: 2 или SEQ ID NO: 3 (молекула геномной нуклеиновой кислоты), или аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 9 или SEQ ID NO: 10 (молекула мРНК), или аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 16 или SEQ ID NO: 17 (молекула кДНК), биологический образец можно подвергнуть методу амплификации с использованием пары праймеров, которая включает первый праймер, полученный из 5'-фланкирующей последовательности, смежной с аденином или гуанином в положении, соответствующем положению 1353 согласно SEQ ID NO: 2 или SEQ ID NO: 3, или аденином или гуанином в положении, соответствующем положению 371 согласно SEQ ID NO: 9 или SEQ ID NO: 10, или аденином или гуанином в положении, соответствующем положению 371 согласно SEQ ID NO: 16 или SEQ ID NO: 17, и второй праймер, полученный из 3'-фланкирующей последовательности, смежной с аденином или гуанином в положении, соответствующем положению 1353 согласно SEQ ID NO: 2 или SEQ ID NO: 3, или аденином или гуанином в положении, соответствующем положению 371 согласно SEQ ID NO: 9 или SEQ ID NO: 10, или аденином или гуанином в положении, соответствующем положению 371 согласно SEQ ID NO: 16 или SEQ ID NO: 17, для получения ампликона, который указывает на присутствие SNP в положениях, кодирующих аденин или гуанин в положении, соответствующем положению 1353 согласно SEQ ID NO: 2 или SEQ ID NO: 3, или аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 9 или SEQ ID NO: 10, или аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 16 или SEQ ID NO: 17. В некоторых вариантах осуществления длина ампликона может находиться в диапазоне от комбинированной длины пар праймеров плюс одна пара нуклеотидных оснований до любой длины ампликона, получаемой согласно протоколу ДНК-амплификации. Это расстояние может находиться в диапазоне от одной пары нуклеотидных оснований до граничного значения реакции амплификации или до около двадцати тысяч пар нуклеотидных оснований. Необязательно, пара праймеров фланкирует область, включающую положения, содержащие аденин или гуанин в положении, соответствующем положению 1353 согласно SEQ ID NO: 2 или SEQ ID NO: 3, или аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 9 или SEQ ID NO: 10, или аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 16 или SEQ ID NO: 17, и по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более нуклеотидов на каждой стороне положений, содержащих аденин или гуанин в положении, соответствующем положению 1353 согласно SEQ ID NO: 2 или SEQ ID NO: 3, или аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 9 или SEQ ID NO: 10, или аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 16 или SEQ ID NO: 17.
В некоторых вариантах осуществления для определения того, содержит ли молекула нуклеиновой кислоты SLC39A5 (молекула геномной нуклеиновой кислоты, молекула мРНК или молекула кДНК) или ее комплементарная цепь в биологическом образце нуклеотидную последовательность, содержащую тимин в положении, соответствующем положению 6352 согласно SEQ ID NO: 5 (молекула геномной нуклеиновой кислоты), или урацил в положении, соответствующем положению 1194 согласно SEQ ID NO: 12 (молекула мРНК), или тимин в положении, соответствующем положению 1194 согласно SEQ ID NO: 19 (молекула кДНК), биологический образец можно подвергнуть методу амплификации с использованием пары праймеров, которая включает первый праймер, полученный из 5'-фланкирующей последовательности, смежной с тимином в положении, соответствующем положению 6352 согласно SEQ ID NO: 5, или урацилом в положении, соответствующем положению 1194 согласно SEQ ID NO: 12, или тимин в положении, соответствующем положению 1194 согласно SEQ ID NO: 19, и второй праймер, полученный из 3'-фланкирующей последовательности, смежной с тимином в положении, соответствующем положению 6352 согласно SEQ ID NO: 5, или урацил в положении, соответствующем положению 1194 согласно SEQ ID NO: 12, или тимином в положении, соответствующем в положении 1194 согласно SEQ ID NO: 19 для получения ампликона, который указывает на присутствие SNP в положениях, кодирующих тимин в положении, соответствующем положению 6352 согласно SEQ ID NO: 5, или урацил в положении, соответствующем в положении 1194 согласно SEQ ID NO: 12 или тимин в положении, соответствующем положению 1194 согласно SEQ ID NO: 19. В некоторых вариантах осуществления длина ампликона может находиться в диапазоне от комбинированной длины пар праймеров плюс одна пара нуклеотидных оснований до любой длины ампликона, получаемой согласно протоколу ДНК-амплификации. Это расстояние может находиться в диапазоне от одной пары нуклеотидных оснований до граничного значения реакции амплификации или до около двадцати тысяч пар нуклеотидных оснований. Необязательно, пара праймеров фланкирует область, включающую положения, содержащие тимин в положении, соответствующем положению 6352 согласно SEQ ID NO: 5, или урацил в положении, соответствующем положению 1194 согласно SEQ ID NO: 12, или тимин в положении, соответствующем положению 1194 согласно SEQ ID NO: 19, и по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более нуклеотидов на каждой стороне положений, содержащих тимин на положение, соответствующее положению 6352 согласно SEQ ID NO: 5, или урацил в положении, соответствующем положению 1194 согласно SEQ ID NO: 12, или тимин в положении, соответствующем положению 1194 согласно SEQ ID NO: 19.
В некоторых вариантах осуществления для определения того, содержит ли молекула нуклеиновой кислоты SLC39A5 (молекула геномной нуклеиновой кислоты, молекула мРНК или молекула кДНК) или ее комплементарная цепь в биологическом образце нуклеотидную последовательность, содержащую тимин в положении, соответствующем положению 5624 согласно SEQ ID NO: 7 (молекула геномной нуклеиновой кислоты) или урацил в положении, соответствующем положению 1161 согласно SEQ ID NO: 14 (молекула мРНК), или тимин в положении, соответствующем положению 1161 согласно SEQ ID NO: 21 (молекула кДНК), биологический образец может быть подвергнут амплификации с использованием пары праймеров, которая включает первый праймер, полученный из 5'-фланкирующей последовательности, смежной с тимином в положении, соответствующем положению 5624 согласно SEQ ID NO: 7, или урацилом в положении, соответствующем положению 1161 согласно SEQ ID NO: 14, или тимином в положении, соответствующем положению 1161 согласно SEQ ID NO: 21, и второй праймер, полученный из 3'-фланкирующей последовательности, смежной с тимином в положении, соответствующем положению 5624 согласно SEQ ID NO: 7, или урацилом в положении, соответствующем положению 1161 согласно SEQ ID NO: 14, или тимином в положении, соответствующем положению 1161 согласно SEQ ID NO: 21, для получения ампликона, который указывает на присутствие SNP в положениях, кодирующих тимин в положении, соответствующем положению 5624 согласно SEQ ID NO: 7, или урацила в положении, соответствующем положению 1161 согласно SEQ ID NO: 14, или тимин в положении, соответствующем положению 1161 согласно SEQ ID NO: 21. В некоторых вариантах осуществления длина ампликона может находиться в диапазоне от комбинированной длины пар праймеров плюс одна пара нуклеотидных оснований до любой длины ампликона, получаемой согласно протоколу ДНК-амплификации. Это расстояние может находиться в диапазоне от одной пары нуклеотидных оснований до граничного значения реакции амплификации или до около двадцати тысяч пар нуклеотидных оснований. Необязательно, пара праймеров фланкирует область, включающую положения, содержащие тимин в положении, соответствующем положению 5624 согласно SEQ ID NO: 7, или урацил в положении, соответствующем положению 1161 согласно SEQ ID NO: 14, или тимин в положении, соответствующем положению 1161 согласно SEQ ID NO: 21, и по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более нуклеотидов на каждой стороне положений, включающих тимин в положении, соответствующем положению 5624 согласно SEQ ID NO: 7, или урацил в положении, соответствующем положению 1161 согласно SEQ ID NO: 14, или тимин в положении, соответствующем положению 1161 согласно SEQ ID NO: 21.
Похожие ампликоны могут быть сгенерированы из последовательностей мРНК и/или кДНК. Пары ПЦР-праймеров могут быть получены из известной последовательности, например, с помощью компьютерных программ, предназначенных для этой цели, таких как инструмент анализа ПЦР-праймеров в Vector NTI, версия 10 (Informax Inc., Бетесда, штат Мэриленд, США); PrimerSelect (DNASTAR Inc., Медисон, штат Висконсин, США); и Primer3 (версия 0.4.0.COPYRGT., 1991, Whitehead Institute for Biomedical Research, Кембридж, штат Массачусетс, США). Кроме того, последовательность можно оценивать визуально и вручную определять праймеры, используя известные руководства.
Иллюстративные примеры методик секвенирования нуклеиновых кислот включают в себя, но не ограничиваются ими, секвенирование с терминатором синтеза цепи (по Сэнгеру) и секвенирование с терминатором-красителем. Другие способы включают в себя способы гибридизации нуклеиновых кислот, отличные от секвенирования, включая применение меченных праймеров или зондов, направленных против очищенной ДНК, амплифицированной ДНК и фиксированных клеточных препаратов (флуоресцентная гибридизация in situ (FISH)). В некоторых способах целевую молекулу нуклеиновой кислоты можно амплифицировать до обнаружения или одновременно с ним. Иллюстративные примеры методик амплификации нуклеиновых кислот включают в себя, помимо прочего, полимеразную цепную реакцию (ПЦР), лигазную цепную реакцию (ligase chain reaction, LCR), амплификацию с замещением цепей (strand displacement amplification, SDA) и амплификацию на основании нуклеотидной последовательности (nucleic acid sequence based amplification, NASBA). Другие способы включают в себя, помимо прочего, лигазную цепную реакцию, амплификацию с замещением цепей и термофильную SDA (tSDA).
В методиках гибридизации могут применяться жесткие условия так, чтобы зонд или праймер специфически гибридизовался со своей мишенью. В некоторых вариантах осуществления полинуклеотидный праймер или зонд в жестких условиях будут гибридизоваться со своей целевой последовательностью в большей степени выявляемой, чем с другими, нецелевыми, последовательностями, например, по меньшей мере в 2 раза, по меньшей мере в 3 раза, по меньшей мере в 4 раза или в большее число раз превышая фон, включая превышение фона больше чем в 10 раз. Жесткие условия зависят от последовательности и будут разными в разных обстоятельствах.
Соответствующие условия жесткости, которые стимулируют гибридизацию ДНК, например, 6X хлорид натрия/цитрат натрия (SSC) при температуре около 45°C с последующей промывкой 2X SSC при температуре 50°C, являются известными или же их можно найти в Current Protocols in Molecular Biology, John Wiley & Sons, N.Y. (1989), 6.3.1-6.3.6. Как правило, жесткие условия для гибридизации и обнаружения будут таковыми, при которых концентрация соли составляет меньше чем около 1,5 M ионов Na+, как правило, это концентрации ионов Na+ (или других солей) от около 0,01 до около 1,0 M при pH от 7,0 до 8,3, а температура составляет по меньшей мере около 30°C для коротких зондов (например, от 10 до 50 нуклеотидов) и по меньшей мере около 60°C для более длинных зондов (например, больше чем 50 нуклеотидов). Жесткие условия также можно обеспечить путем добавления дестабилизирующих агентов, таких как формамид. Необязательно, буферы для промывки могут содержать от 0,1% до 1% ДСН. Длительность гибридизации в общем случае составляет меньше чем около 24 часа, обычно - от около 4 часов до около 12 часов. Длительность времени промывки будет составлять по меньшей мере такой промежуток времени, который необходим для достижения равновесия.
В настоящем изобретении также представлены молекулярные комплексы, содержащие любую из молекул нуклеиновой кислоты SLC39A5 (молекулы геномной нуклеиновой кислоты, молекулы мРНК или молекулы кДНК) или их комплементарные цепи, описанные в данном документе, и любые аллель-специфические праймеры или аллель-специфические зонды, описанные в данном документе. В некоторых вариантах осуществления молекулы нуклеиновой кислоты SLC39A5 (молекулы геномной нуклеиновой кислоты, молекулы мРНК или молекулы кДНК) или комплементарные им нуклеотидные последовательности в указанных молекулярных комплексах являются одноцепочечными. В некоторых вариантах осуществления молекула нуклеиновой кислоты SLC39A5 представляет собой любую из молекул геномных нуклеиновых кислот, описанных в данном документе. В некоторых вариантах осуществления молекула нуклеиновой кислоты SLC39A5 представляет собой любую из молекул мРНК, описанных в данном документе. В некоторых вариантах осуществления молекула нуклеиновой кислоты SLC39A5 представляет собой любую из молекул кДНК, описанных в данном документе. В некоторых вариантах осуществления молекулярный комплекс содержит любую из молекул нуклеиновой кислоты SLC39A5 (молекулы геномной нуклеиновой кислоты, молекулы мРНК или молекулы кДНК) или их комплементарные цепи, описанные в данном документе, и любой из аллель-специфичных праймеров, описанных в данном документе. В некоторых вариантах осуществления молекулярный комплекс содержит любую из молекул нуклеиновой кислоты SLC39A5 (молекулы геномной нуклеиновой кислоты, молекулы мРНК или молекулы кДНК) или их комплементарные цепи, описанные в данном документе, и любой из аллель-специфических зондов, описанных в данном документе. В некоторых вариантах осуществления комплексы дополнительно содержат полимеразу нечеловеческого происхождения.
В некоторых вариантах осуществления молекулярный комплекс содержит вариантную молекулу геномной нуклеиновой кислоты SLC39A5, содержащую нуклеотидную последовательность согласно SEQ ID NO: 4, и аллель-специфический праймер или аллель-специфический зонд, который гибридизуется с цитозином в его положении 5604. В некоторых вариантах осуществления молекулярный комплекс содержит вариантную молекулу мРНК SLC39A5, содержащую нуклеотидную последовательность согласно SEQ ID NO: 11, и аллель-специфический праймер или аллель-специфический зонд, который гибридизуется с цитозином в его положении 1141. В некоторых вариантах осуществления молекулярный комплекс содержит вариантную молекулу кДНК SLC39A5, содержащую нуклеотидную последовательность согласно SEQ ID NO: 18, и аллель-специфический праймер или аллель-специфический зонд, который гибридизуется с цитозином в его положении 1141.
В некоторых вариантах осуществления молекулярный комплекс содержит вариантную молекулу геномной нуклеиновой кислоты SLC39A5, содержащую нуклеотидную последовательность согласно SEQ ID NO: 6, и аллель-специфический праймер или аллель-специфический зонд, который гибридизуется с цитозином в его положении 6899. В некоторых вариантах осуществления молекулярный комплекс содержит вариантную молекулу мРНК SLC39A5, содержащую нуклеотидную последовательность согласно SEQ ID NO: 13, и аллель-специфический праймер или аллель-специфический зонд, который гибридизуется с цитозином в его положении 1468. В некоторых вариантах осуществления молекулярный комплекс содержит вариантную молекулу кДНК SLC39A5, содержащую нуклеотидную последовательность согласно SEQ ID NO: 20, и аллель-специфический праймер или аллель-специфический зонд, который гибридизуется с цитозином в его положении 1468.
В некоторых вариантах осуществления молекулярный комплекс содержит вариантную молекулу геномной нуклеиновой кислоты SLC39A5, содержащую нуклеотидную последовательность согласно SEQ ID NO: 2 или SEQ ID NO: 3, и аллель-специфический праймер или аллель-специфический зонд, который гибридизуется с аденином или гуанином в его положении 1353, соответственно. В некоторых вариантах осуществления молекулярный комплекс содержит вариантную молекулу мРНК SLC39A5, содержащую нуклеотидную последовательность согласно SEQ ID NO: 9 или SEQ ID NO: 10, и аллель-специфический праймер или аллель-специфический зонд, который гибридизуется с аденином или гуанином в его положении 371, соответственно. В некоторых вариантах осуществления молекулярный комплекс содержит вариантную молекулу кДНК SLC39A5, содержащую нуклеотидную последовательность согласно SEQ ID NO: 16 или SEQ ID NO: 17, и аллель-специфический праймер или аллель-специфический зонд, который гибридизуется с аденином или гуанином в его положении 371, соответственно.
В некоторых вариантах осуществления молекулярный комплекс содержит вариантную молекулу геномной нуклеиновой кислоты SLC39A5, содержащую нуклеотидную последовательность согласно SEQ ID NO: 5, и аллель-специфический праймер или аллель-специфический зонд, который гибридизуется с тимином в его положении 6352. В некоторых вариантах осуществления молекулярный комплекс содержит вариантную молекулу мРНК SLC39A5, содержащую нуклеотидную последовательность согласно SEQ ID NO: 12, и аллель-специфический праймер или аллель-специфический зонд, который гибридизуется с урацилом в его положении 1194. В некоторых вариантах осуществления молекулярный комплекс содержит вариантную молекулу кДНК SLC39A5, содержащую нуклеотидную последовательность согласно SEQ ID NO: 19, и аллель-специфический праймер или аллель-специфический зонд, который гибридизуется с тимином в его положении 1194.
В некоторых вариантах осуществления молекулярный комплекс содержит вариантную молекулу геномной нуклеиновой кислоты SLC39A5, содержащую нуклеотидную последовательность согласно SEQ ID NO: 7, и аллель-специфический праймер или аллель-специфический зонд, который гибридизуется с тимином в его положении 5624. В некоторых вариантах осуществления молекулярный комплекс содержит вариантную молекулу мРНК SLC39A5, содержащую нуклеотидную последовательность согласно SEQ ID NO: 14, и аллель-специфический праймер или аллель-специфический зонд, который гибридизуется с урацилом в его положении 1161. В некоторых вариантах осуществления молекулярный комплекс содержит вариантную молекулу кДНК SLC39A5, содержащую нуклеотидную последовательность согласно SEQ ID NO: 21, и аллель-специфический праймер или аллель-специфический зонд, который гибридизуется с тимином в его положении 1161.
В данном изобретении также представлены способы обнаружения присутствия полипептида SLC39A5 человека с прогнозируемой потерей функции, включающие в себя проведение анализа образца, полученного от субъекта-человека, для определения того, содержит ли полипептид SLC39A5 в субъекте одну или более вариаций, которые приводят к потере функции указанного полипептида (частичной или полной) или прогнозируемой потере функции (частичной или полной) указанного полипептида. В некоторых вариантах осуществления указанные способы обнаруживают присутствие SLC39A5 M304T, G413A, Y47Stop, R322Stop, или R311Stop. В некоторых вариантах осуществления способы обнаруживают присутствие SLC39A5 Y47Stop, R322Stop, или R311Stop.
В некоторых вариантах осуществления указанные способы включают в себя проведение анализа образца, полученного от субъекта-человека, для определения того, содержит ли полипептид SLC39A5 в указанном образце треонин в положении, соответствующем положению 304 согласно SEQ ID NO: 24. В некоторых вариантах осуществления указанные способы включают в себя проведение анализа образца, полученного от субъекта-человека, для определения того, содержит ли полипептид SLC39A5 в указанном образце аланин в положении, соответствующем положению 413 согласно SEQ ID NO: 26.
В некоторых вариантах осуществления способы включают выполнение анализа образца, полученного от субъекта-человека, чтобы определить, содержит ли образец усеченный вариант полипептида SLC39A5, оканчивающийся в положении, соответствующем положению 46 согласно SEQ ID NO: 23. В некоторых вариантах осуществления усеченный вариант полипептида SLC39A5 не имеет аминокислот в положениях, соответствующих положениям 47-540 согласно SEQ ID NO: 22. В некоторых вариантах осуществления усеченный вариант полипептида SLC39A5 содержит или состоит из SEQ ID NO: 23.
В некоторых вариантах осуществления способы включают выполнение анализа образца, полученного от субъекта-человека, чтобы определить, содержит ли образец усеченный вариант полипептида SLC39A5, оканчивающийся в положении, соответствующем положению 321 согласно SEQ ID NO: 25. В некоторых вариантах осуществления усеченный вариант полипептида SLC39A5 не имеет аминокислот в положениях, соответствующих положениям 322-540 согласно SEQ ID NO: 22. В некоторых вариантах осуществления усеченный вариант полипептида SLC39A5 содержит или состоит из SEQ ID NO: 25.
В некоторых вариантах осуществления способы включают выполнение анализа образца, полученного от субъекта-человека, чтобы определить, содержит ли образец усеченный вариант полипептида SLC39A5, оканчивающийся в положении, соответствующем положению 310 согласно SEQ ID NO: 27. В некоторых вариантах осуществления усеченный вариант полипептида SLC39A5 не имеет аминокислот в положениях, соответствующих положениям 311-540 согласно SEQ ID NO: 22. В некоторых вариантах осуществления усеченный вариант полипептида SLC39A5 содержит или состоит из SEQ ID NO: 27.
В некоторых вариантах осуществления этап обнаружения включает в себя секвенирование по меньшей мере части полипептида, которая содержит положение, соответствующее положению 304 согласно SEQ ID NO: 22 или SEQ ID NO: 24. В некоторых вариантах осуществления этап обнаружения включает в себя секвенирование по меньшей мере части полипептида, которая содержит положение, соответствующее положению 413 согласно SEQ ID NO: 22 или SEQ ID NO: 26. В некоторых вариантах осуществления стадия обнаружения включает в себя секвенирование всего полипептида.
В некоторых вариантах осуществления секвенированный полипептид SLC39A5 содержит или состоит из SEQ ID NO: 23. В некоторых вариантах осуществления секвенированный полипептид SLC39A5 состоит из SEQ ID NO: 23. В некоторых вариантах осуществления стадия обнаружения включает секвенирование по меньшей мере части полипептида SLC39A5, который может содержать положения, соответствующие любым положениям, которые являются С-концевыми по отношению к 46, согласно SEQ ID NO: 23. Если аминокислоты обнаруживаются в полипептиде SLC39A5 в положениях, соответствующих положениям 47-540 согласно SEQ ID NO: 22, то такой полипептид SLC39A5 является эталонным полипептидом SLC39A5. Отсутствие положений 47-540 согласно SEQ ID NO: 22 в полипептиде SLC39A5 указывает на то, что полипептид SLC39A5 оканчивается в положении 46 согласно SEQ ID NO: 23 и является полипептидом с прогнозируемой потерей функции SLC39A5. В некоторых вариантах осуществления стадия обнаружения включает в себя секвенирование всего полипептида.
В некоторых вариантах осуществления секвенированный полипептид SLC39A5 содержит или состоит из SEQ ID NO: 25. В некоторых вариантах осуществления секвенированный полипептид SLC39A5 состоит из SEQ ID NO: 25. В некоторых вариантах осуществления стадия обнаружения включает секвенирование по меньшей мере части полипептида SLC39A5, который может содержать положения, соответствующие любым положениям, которые являются С-концевыми по отношению к 321, согласно SEQ ID NO: 25. Если аминокислоты обнаруживаются в полипептиде SLC39A5 в положениях, соответствующих положениям 322-540 согласно SEQ ID NO: 22, то такой полипептид SLC39A5 является эталонным полипептидом SLC39A5. Отсутствие положений 322-540 согласно SEQ ID NO: 22 в полипептиде SLC39A5 указывает на то, что полипептид SLC39A5 оканчивается в положении 321 согласно SEQ ID NO: 25 и является полипептидом с прогнозируемой потерей функции SLC39A5. В некоторых вариантах осуществления стадия обнаружения включает в себя секвенирование всего полипептида.
В некоторых вариантах осуществления секвенированный полипептид SLC39A5 содержит или состоит из SEQ ID NO: 27. В некоторых вариантах осуществления секвенированный полипептид SLC39A5 состоит из SEQ ID NO: 27. В некоторых вариантах осуществления стадия обнаружения включает секвенирование по меньшей мере части полипептида SLC39A5, который может содержать положения, соответствующие любым положениям, которые являются С-концевыми по отношению к 310, согласно SEQ ID NO: 27. Если аминокислоты обнаруживаются в полипептиде SLC39A5 в положениях, соответствующих положениям 311-540 согласно SEQ ID NO: 22, то такой полипептид SLC39A5 является эталонным полипептидом SLC39A5. Отсутствие положений 311-540 согласно SEQ ID NO: 22 в полипептиде SLC39A5 указывает на то, что полипептид SLC39A5 оканчивается в положении 310 согласно SEQ ID NO: 27 и является полипептидом с прогнозируемой потерей функции SLC39A5. В некоторых вариантах осуществления стадия обнаружения включает в себя секвенирование всего полипептида.
В некоторых вариантах осуществления стадия обнаружения включает иммуноанализ для обнаружения присутствия полипептида, который имеет положение, соответствующее положению 304, согласно SEQ ID NO: 22 или SEQ ID NO: 24. В некоторых вариантах осуществления стадия обнаружения включает иммуноанализ для обнаружения присутствия полипептида, который имеет положение, соответствующее положению 413, согласно SEQ ID NO: 22 или SEQ ID NO: 26.
В некоторых вариантах осуществления стадия обнаружения включает иммуноанализ для обнаружения присутствия полипептида SLC39A5, который содержит или состоит из SEQ ID NO: 23. В некоторых вариантах осуществления полипептид SLC39A5 состоит из SEQ ID NO: 23. В некоторых вариантах осуществления стадия обнаружения включает обнаружение по меньшей мере части полипептида SLC39A5, который может иметь положения, соответствующие любым положениям, которые являются C-концевыми по отношению к 46 согласно SEQ ID NO: 23. Если аминокислоты обнаруживаются в полипептиде SLC39A5 в положениях, соответствующих положениям 47-540 согласно SEQ ID NO: 22, то такой полипептид SLC39A5 является эталонным полипептидом SLC39A5. Отсутствие обнаружения положений 47-540 согласно SEQ ID NO: 22 в полипептиде SLC39A5 указывает на то, что полипептид SLC39A5 оканчивается в положении 46 согласно SEQ ID NO: 23 и является полипептидом с прогнозируемой потерей функции SLC39A5.
В некоторых вариантах осуществления стадия обнаружения включает иммуноанализ для обнаружения присутствия полипептида SLC39A5, который содержит или состоит из SEQ ID NO: 25. В некоторых вариантах осуществления полипептид SLC39A5 состоит из SEQ ID NO: 25. В некоторых вариантах осуществления стадия обнаружения включает обнаружение по меньшей мере части полипептида SLC39A5, который может иметь положения, соответствующие любым положениям, которые являются C-концевыми по отношению к 321 согласно SEQ ID NO: 25. Если аминокислоты обнаруживаются в полипептиде SLC39A5 в положениях, соответствующих положениям 322-540 согласно SEQ ID NO: 22, то такой полипептид SLC39A5 является эталонным полипептидом SLC39A5. Отсутствие обнаружения положений 322-540 согласно SEQ ID NO: 22 в полипептиде SLC39A5 указывает на то, что полипептид SLC39A5 оканчивается в положении 321 согласно SEQ ID NO: 25 и является полипептидом с прогнозируемой потерей функции SLC39A5.
В некоторых вариантах осуществления стадия обнаружения включает иммуноанализ для обнаружения присутствия полипептида SLC39A5, который содержит или состоит из SEQ ID NO: 27. В некоторых вариантах осуществления полипептид SLC39A5 состоит из SEQ ID NO: 27. В некоторых вариантах осуществления стадия обнаружения включает обнаружение по меньшей мере части полипептида SLC39A5, который может иметь положения, соответствующие любым положениям, которые являются C-концевыми по отношению к 310 согласно SEQ ID NO: 27. Если аминокислоты обнаруживаются в полипептиде SLC39A5 в положениях, соответствующих положениям 311-540 согласно SEQ ID NO: 22, то такой полипептид SLC39A5 является эталонным полипептидом SLC39A5. Отсутствие обнаружения положений 311-540 согласно SEQ ID NO: 22 в полипептиде SLC39A5 указывает на то, что полипептид SLC39A5 оканчивается в положении 310 согласно SEQ ID NO: 27 и является полипептидом с прогнозируемой потерей функции SLC39A5.
В некоторых вариантах осуществления, когда субъект-человек не имеет полипептида с прогнозируемой потерей функции SLC39A5, тогда субъект-человек имеет высокий риск развития повышенного уровня глюкозы в сыворотке и/или гипергликемии; и когда субъект-человек имеет полипептид с прогнозируемой потерей функции SLC39A5, тогда у субъекта-человека снижается риск развития повышенного уровня глюкозы в сыворотке и/или гипергликемии.
Зонды и/или праймеры (включая специфические в отношении изменения зонды и специфические в отношении изменения праймеры), описанные в данном документе, содержат или состоят из от около 15 до около 100, от около 15 до около 35 нуклеотидов. В некоторых вариантах осуществления специфические в отношении изменения зонды и специфические в отношении изменения праймеры содержат ДНК. В некоторых вариантах осуществления указанные специфические в отношения изменения зонды и заменоспецифичные праймеры содержат РНК. В некоторых вариантах осуществления зонды и праймеры, описанные в данном документе (включая специфические в отношении изменения зонды и специфические в отношении изменения праймеры), имеют нуклеотидную последовательность, которая специфически гибридизируется с любой из молекул нуклеиновых кислот, описанных в данном документе, или их комплементарной цепью. В некоторых вариантах осуществления зонды и праймеры (включая специфические в отношении изменения зонды и специфические в отношении изменения праймеры) специфически гибридизируются с любой из молекул нуклеиновых кислот, описанных в данном документе, в жестких условиях. В контексте данного описания выражение «специфически гибридизируется» означает, что зонд или праймер (включает специфические в отношении изменения зонды и специфические в отношении изменения праймеры) не гибридизируется с последовательностью нуклеиновой кислоты, кодирующей молекулу эталонной геномной нуклеиновой кислоты SLC39A5, молекулу эталонной мРНК SLC39A5 и/или молекулу эталонной кДНК SLC39A5. В некоторых вариантах осуществления зонды (такие как, например, специфический в отношении изменения зонд) содержат метку. В некоторых вариантах осуществления указанная метка представляет собой флуоресцентную метку, радиоизотопную метку или биотин.
Нуклеотидная последовательность молекулы эталонной геномной нуклеиновой кислоты SLC39A5 указана в SEQ ID NO: 1. В отношении SEQ ID NO: 1, нуклеотид в положении 5604 представляет собой тимин. В отношении SEQ ID NO: 1, положение 6899 представляет собой гуанин. В отношении SEQ ID NO: 1, положение 1353 представляет собой цитозин, а положения кодона с 1351 по 1353 представляют собой кодон TAC. В отношении SEQ ID NO: 1, положение 6352 представляет собой цитозин, а положения кодона с 6352 по 6354 представляют собой кодон CGA. В отношении SEQ ID NO: 1, положение 5624 представляет собой цитозин, а положения кодона с 5624 по 5626 представляют собой кодон CGA.
Существует вариантная молекула геномной нуклеиновой кислоты SLC39A5, в которой тимин в положении 5604 заменен на цитозин. Нуклеотидная последовательность этой вариантной молекулы геномной нуклеиновой кислоты SLC39A5 представлена в SEQ ID NO: 4. Существует еще один вариант молекулы геномной нуклеиновой кислоты SLC39A5, в которой гуанин в положении 6899 заменен на цитозин. Нуклеотидная последовательность этой вариантной молекулы геномной нуклеиновой кислоты SLC39A5 представлена в SEQ ID NO: 6. Существует еще одна вариантная молекула геномной нуклеиновой кислоты SLC39A5, в которой цитозин в положении 1353 согласно SEQ ID NO: 1 заменен аденином или гуанином, а кодон TAC в положениях 1351-1353 согласно SEQ ID NO: 1 заменен на TAA или TAG. Нуклеотидная последовательность этой вариантной молекулы геномной нуклеиновой кислоты SLC39A5 представлена в SEQ ID NO: 2 или SEQ ID NO: 3. Существует еще одна вариантная молекула геномной нуклеиновой кислоты SLC39A5, в которой цитозин в положении 6352 согласно SEQ ID NO: 1 заменен на тимин, а кодон CGA в положениях от 6352 до 6354 согласно SEQ ID NO: 1 заменен на TGA. Нуклеотидная последовательность этой вариантной молекулы геномной нуклеиновой кислоты SLC39A5 представлена в SEQ ID NO: 5. Существует еще одна вариантная молекула геномной нуклеиновой кислоты SLC39A5, в которой цитозин в положении 5624 согласно SEQ ID NO: 1 заменен тимином, а кодон CGA в положениях 5624-5626 согласно SEQ ID NO: 1 заменен на TGA. Нуклеотидная последовательность этой вариантной молекулы геномной нуклеиновой кислоты SLC39A5 указана в SEQ ID NO: 7.
Нуклеотидная последовательность молекулы эталонной мРНК SLC39A5 указана в SEQ ID NO: 8. В отношении SEQ ID NO: 8, нуклеотид в положении 1,141 представляет собой урацил. В отношении SEQ ID NO: 8, положение 1468 представляет собой гуанин. В отношении SEQ ID NO: 8, положение 371 представляет собой цитозин, а положения кодона с 369 по 371 представляют собой кодон UAC. В отношении SEQ ID NO: 8, положение 1194 представляет собой цитозин, а положения кодона с 1194 по 1196 представляют собой кодон CGA. В отношении SEQ ID NO: 8, положение 1161 представляет собой цитозин, а положения кодона с 1161 по 1163 представляют собой кодон CGA.
Существует вариантная молекула мРНК SLC39A5, в которой урацил в положении 1141 заменен на цитозин. Нуклеотидная последовательность этой вариантной молекулы мРНК SLC39A5 указана в SEQ ID NO: 11. Существует еще одна вариантная молекула мРНК SLC39A5, в которой гуанин в положении 1468 заменен на цитозин. Нуклеотидная последовательность этой вариантной молекулы мРНК SLC39A5 указана в SEQ ID NO: 13. Существует еще одна вариантная молекула мРНК SLC39A5, в которой цитозин в положении 371 согласно SEQ ID NO: 8 заменен аденином или гуанином, а кодон UAC в положениях 369-371 согласно SEQ ID NO: 8 заменен на UAA или UAG. Нуклеотидная последовательность этой вариантной молекулы мРНК SLC39A5 указана в SEQ ID NO:9 или SEQ ID NO:10. Существует еще одна вариантная молекула мРНК SLC39A5, в которой цитозин в положении 1194 согласно SEQ ID NO: 8 заменен урацилом, а кодон CGA в положениях 1194-1196 согласно SEQ ID NO: 8 заменен на UGA. Нуклеотидная последовательность этой вариантной молекулы мРНК SLC39A5 указана в SEQ ID NO: 12. Существует еще одна вариантная молекула мРНК SLC39A5, в которой цитозин в положении 1161 согласно SEQ ID NO: 8 заменен урацилом, а кодон CGA в положениях 1161-1163 согласно SEQ ID NO: 8 заменен на UGA. Нуклеотидная последовательность этой вариантной молекулы мРНК SLC39A5 указана в SEQ ID NO: 14.
Нуклеотидная последовательность молекулы эталонной кДНК SLC39A5 приведена в SEQ ID NO: 15. В отношении SEQ ID NO: 15, положение 1141 представляет собой тимин. В отношении SEQ ID NO: 15, положение 1468 представляет собой гуанин. В отношении SEQ ID NO: 15, положение 371 представляет собой цитозин, а положения кодона с 369 по 371 представляют собой кодон TAC. В отношении SEQ ID NO: 15, положение 1194 представляет собой цитозин, а положения кодона с 1194 по 1196 представляют собой кодон CGA. В отношении SEQ ID NO: 15, положение 1161 представляет собой цитозин, а положения кодона с 1161 по 1163 представляют собой кодон CGA.
Существует вариантной молекулы кДНК SLC39A5, в которой тимин в положении 1141 заменен на цитозин. Нуклеотидная последовательность этой вариантной молекулы кДНК SLC39A5 указана в SEQ ID NO: 18. Существует еще одна вариантная молекула кДНК SLC39A5, в которой гуанин в положении 1468 заменен на цитозин. Нуклеотидная последовательность этой вариантной молекулы кДНК SLC39A5 указана в SEQ ID NO: 20. Существует еще одна вариантная молекула кДНК SLC39A5, в которой цитозин в положении 371 согласно SEQ ID NO: 15 заменен аденином или гуанином, а кодон TAC в положениях 369-371 согласно SEQ ID NO: 15 заменен на TAA или TAG. Нуклеотидная последовательность этой вариантной молекулы кДНК SLC39A5 указана в SEQ ID NO:16 или SEQ ID NO:17. Существует еще одна вариантная молекула кДНК SLC39A5, в которой цитозин в положении 1194 согласно SEQ ID NO: 15 заменен тимином, а кодон CGA в положениях 1194-1196 согласно SEQ ID NO: 15 заменен на TGA. Нуклеотидная последовательность этой вариантной молекулы кДНК SLC39A5 указана в SEQ ID NO: 19. Существует еще одна вариантная молекула кДНК SLC39A5, в которой цитозин в положении 1161 согласно SEQ ID NO: 15 заменен тимином, а кодон CGA в положениях 1161-1163 согласно SEQ ID NO: 15 заменен на TGA. Нуклеотидная последовательность этой вариантной молекулы кДНК SLC39A5 указана в SEQ ID NO: 21.
Аминокислотная последовательность эталонного полипептида SLC39A5 указана в SEQ ID NO: 22. В отношении SEQ ID NO: 22, эталонный полипептид SLC39A5 имеет длину 540 аминокислот. В отношении SEQ ID NO: 22, нуклеотид в положении 304 представляет собой метионин. В отношении SEQ ID NO: 22, нуклеотид в положении 413 представляет собой глицин. В отношении SEQ ID NO: 22, нуклеотид в положении 47 представляет собой тирозин. В отношении SEQ ID NO: 22, положение 322 представляет собой аргинин. В отношении SEQ ID NO: 22, положение 311 представляет собой аргинин.
Существует вариантный полипептид SLC39A5 (M304T или Met304Thr), аминокислотная последовательность которого указана в SEQ ID NO: 24. В отношении SEQ ID NO: 24, вариантный полипептид SLC39A5 имеет длину 540 аминокислот. Ссылаясь на SEQ ID NO: 24, нуклеотид в положении 304 представляет собой треонин. Существует еще один вариантный полипептид SLC39A5 (G413A или Gly413Ala), аминокислотная последовательность которого указана в SEQ ID NO: 26. В отношении SEQ ID NO: 26, вариантный полипептид SLC39A5 имеет длину 540 аминокислот. В отношении SEQ ID NO: 26, нуклеотид в положении 413 представляет собой аланин. Существует усеченный вариантный полипептид SLC39A5 (Y47Stop или Tyr47Stop), аминокислотная последовательность которого указана в SEQ ID NO: 23. В отношении SEQ ID NO: 23, вариантный полипептид SLC39A5 имеет длину 46 аминокислот. В отношении SEQ ID NO: 23, вариантный полипептид SLC39A5 усечен в положении 46 и не содержит аминокислот в положениях, соответствующих положениям 47-540 согласно SEQ ID NO: 22. Существует еще один усеченный вариантный полипептид SLC39A5 (R322Stop или Arg322Stop), аминокислотная последовательность которого указана в SEQ ID NO: 25. В отношении SEQ ID NO: 25, вариантный полипептид SLC39A5 имеет длину 321 аминокислот. В отношении SEQ ID NO: 25, вариантный полипептид SLC39A5 усечен в положении 321 и не содержит аминокислот в положениях, соответствующих положениям 322-540 согласно SEQ ID NO: 22. Существует еще один усеченный вариантный полипептид SLC39A5 (R311Stop или Arg311Stop), аминокислотная последовательность которого указана в SEQ ID NO: 27. В отношении SEQ ID NO: 27, вариантный полипептид SLC39A5 имеет длину 310 аминокислот. В отношении SEQ ID NO: 27, вариантный полипептид SLC39A5 усечен в положении 310 и не содержит аминокислот в положениях, соответствующих положениям 311-540 согласно SEQ ID NO: 22.
Нуклеотидные и аминокислотные последовательности, перечисленные в сопроводительном перечне последовательностей, приведены с использованием стандартных буквенных сокращений для нуклеотидных оснований и трехбуквенного кода для аминокислот. Нуклеотидные последовательности соответствуют стандартной системе с началом в 5’-конце последовательности, продолжаясь вперед (т. е. слева направо в каждом ряду) до 3’-конца. Продемонстрирована только одна цепь каждой нуклеотидной последовательности, но подразумевается, что комплементарная цепь включается посредством любой ссылки на отображаемую цепь. Аминокислотная последовательность следует стандартному соглашению: она начинается с аминоконца последовательности и продолжается вперед (то есть слева направо в каждой строке) к карбоксиконцу.
В контексте данного документа фраза «соответствующий» или ее грамматические вариации при использовании в контексте нумерации конкретного нуклеотида или нуклеотидной последовательности или положения относится к нумерации указанной эталонной последовательности, когда конкретный нуклеотид или нуклеотидная последовательность сравнивается с эталонной последовательностью (такой как, например, SEQ ID NO: 1, SEQ ID NO: 8 или SEQ ID NO: 15). Другими словами, номер остатка (такого как, например, нуклеотид или аминокислота) или положение остатка (такого как, например, нуклеотид или аминокислота) конкретного полимера обозначают относительно эталонной последовательности, а не по фактическому номеру положения остатка в конкретном нуклеотиде или нуклеотидной последовательности. Например, конкретная нуклеотидная последовательность может быть выровнена с эталонной последовательностью путем введения гэпов для оптимизации совпадения остатков между двумя последовательностями. В этих случаях, несмотря на наличие гэпов, нумерация остатка в конкретном нуклеотиде или нуклеотидной последовательности производится относительно эталонной последовательности, с которой он был выровнен.
Например, молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, причем нуклеотидная последовательность содержит цитозин в положении, соответствующем положению 5604 согласно SEQ ID NO: 4, означает, что если нуклеотидная последовательность молекулы геномной нуклеиновой кислоты SLC39A5 выровнена с последовательностью SEQ ID NO: 4, последовательность SLC39A5 имеет цитозиновый остаток в положении, которое соответствует положению 5604 согласно SEQ ID NO: 4. То же самое относится к молекулам мРНК, содержащим нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, при этом нуклеотидная последовательность содержит цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 11, и молекулам кДНК, содержащим нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, при этом нуклеотидная последовательность содержит цитозин в положении, соответствующем положению 1141, согласно SEQ ID NO: 18. Другими словами, эти фразы относятся к молекуле нуклеиновой кислоты, кодирующей полипептид SLC39A5, при этом молекула геномной нуклеиновой кислоты имеет нуклеотидную последовательность, которая содержит цитозиновый остаток, который гомологичен цитозиновому остатку в положении 5604 согласно SEQ ID NO: 4 (или при этом молекула мРНК имеет нуклеотидную последовательность, которая содержит цитозиновый остаток, который гомологичен цитозиновому остатку в положении 1141 согласно SEQ ID NO: 11, или при этом молекула кДНК имеет нуклеотидную последовательность, которая содержит цитозиновый остаток, гомологичный цитозиновому остатку в положении 1141 согласно SEQ ID NO: 18). В данном документе такая последовательность также называется «последовательностью SLC39A5 с изменением M304T» или «последовательность SLC39A5 с вариацией M304T», что относится к молекулам геномной нуклеиновой кислоты (или «последовательность SLC39A5 с изменением U1,141C» или «последовательность SLC39A5 с вариацией U1,141C», что относится к молекулам мРНК, и «последовательность SLC39A5 с изменением T1,141C» или «последовательность SLC39A5 с вариацией T1,141C», что относится к молекулам кДНК).
Как описано в данном документе, положение в молекуле геномной нуклеиновой кислоты SLC39A5, которое соответствует положению 5604 согласно SEQ ID NO: 4, например, может быть идентифицировано путем выполнения выравнивания последовательностей между нуклеотидной последовательностью конкретной молекулы нуклеиновой кислоты SLC39A5 и нуклеотидной последовательностью по SEQ ID NO: 4. Существует множество вычислительных алгоритмов, которые можно использовать для выполнения выравнивания последовательностей для идентификации положения нуклеотида, которое соответствует, например, положению 5604 в SEQ ID NO: 4. Например, выравнивания последовательностей можно выполнять с помощью алгоритма NCBI BLAST (Altschul et al., Nucleic Acids Res., 1997, 25, 3389-3402) или программного обеспечения CLUSTALW (Sievers and Higgins, Methods Mol. Biol., 2014, 1079, 105-116). При этом последовательности также можно выравнивать вручную.
В настоящем изобретении также представлены терапевтические агенты, которые лечат или ингибируют повышенный уровень глюкозы в сыворотке и/или гипергликемию, для применения в лечении повышенного уровня глюкозы в сыворотке и/или гипергликемии (или для применения при приготовлении лекарственного препарата для лечения повышенного уровня глюкозы в сыворотке и/или гипергликемии) у субъекта-человека, причем субъект-человек имеет: молекулу геномной нуклеиновой кислоты, имеющую нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, причем нуклеотидная последовательность содержит цитозин в положении, соответствующем положению 5604 согласно SEQ ID NO: 4 или ее комплементарной цепи; молекулу мРНК, имеющая нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, причем нуклеотидная последовательность содержит цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 11, или ее комплементарной цепи; молекулу кДНК, имеющую нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, причем нуклеотидная последовательность содержит цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 18, или ее комплементарной цепи; или полипептид SLC39A5, который содержит треонин в положении, соответствующем положению 304 согласно SEQ ID NO: 24. Терапевтические агенты, которые лечат или ингибируют повышенный уровень глюкозы в сыворотке и/или гипергликемию, могут быть любыми терапевтическими агентами, которые лечат или ингибируют повышенный уровень глюкозы в сыворотке и/или гипергликемию, описанные в данном документе.
В настоящем изобретении также представлены ингибиторы SLC39A5 для применения в лечении повышенного уровня глюкозы в сыворотке и/или гипергликемии (или для применения при приготовлении лекарственного препарата для лечения повышенного уровня глюкозы в сыворотке и/или гипергликемии) у субъекта-человека, причем субъект-человек имеет: молекулу геномной нуклеиновой кислоты, имеющую нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, причем нуклеотидная последовательность содержит цитозин в положении, соответствующем положению 5604 согласно SEQ ID NO: 4 или ее комплементарной цепи; молекулу мРНК, имеющая нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, причем нуклеотидная последовательность содержит цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 11, или ее комплементарной цепи; молекулу кДНК, имеющую нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, причем нуклеотидная последовательность содержит цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 18, или ее комплементарной цепи; или полипептид SLC39A5, который содержит треонин в положении, соответствующем положению 304 согласно SEQ ID NO: 24. Ингибиторы SLC39A5 могут представлять собой любые из ингибиторов SLC39A5, описанных в данном документе.
В некоторых вариантах осуществления субъект-человек имеет: молекулу геномной нуклеиновой кислоты, имеющую нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, причем нуклеотидная последовательность содержит цитозин в положении, соответствующем положению 6899 согласно SEQ ID NO: 6, или ее комплементарной цепи; молекулу мРНК, имеющую нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, причем нуклеотидная последовательность содержит цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 13, или ее комплементарной цепи; молекулу кДНК, имеющую нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, причем нуклеотидная последовательность содержит цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 20, или ее комплементарной цепи; или полипептид SLC39A5, который содержит аланин в положении, соответствующем положению 413 согласно SEQ ID NO: 26.
В некоторых вариантах осуществления субъект-человек имеет: молекулу геномной нуклеиновой кислоты, имеющую нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, причем нуклеотидная последовательность содержит аденин или гуанин в положении, соответствующем положению 1353 согласно SEQ ID NO: 2 или SEQ ID NO: 3 или их комплементарным цепям; молекулу мРНК, имеющую нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, при этом нуклеотидная последовательность содержит аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 9 или SEQ ID NO: 10, или их комплементарным цепям; молекулу кДНК, имеющую нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, при этом нуклеотидную последовательность содержит аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 16 или SEQ ID NO: 17, или их комплементарным цепям; или полипептид SLC39A5, который усечен в положении 46 согласно SEQ ID NO: 23 и не содержит аминокислот в положениях, соответствующих положениям 47-540 согласно SEQ ID NO: 22.
В некоторых вариантах осуществления субъект-человек имеет: молекулу геномной нуклеиновой кислоты, имеющую нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, при этом нуклеотидная последовательность содержит тимин в положении, соответствующем положению 6352 согласно SEQ ID NO: 5, или ее комплементарной цепи; молекулу мРНК, имеющую нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, при этом нуклеотидная последовательность содержит урацил в положении, соответствующем положению 1194 согласно SEQ ID NO: 12, или ее комплементарной цепи; молекулу кДНК, имеющую нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, при этом нуклеотидная последовательность содержит тимин в положении, соответствующем положению 1194 согласно SEQ ID NO: 19, или ее комплементарной цепи; или полипептид SLC39A5, который усечен в положении 321 согласно SEQ ID NO: 25 и не содержит аминокислот в положениях, соответствующих положениям 322-540 согласно SEQ ID NO: 22.
В некоторых вариантах осуществления субъект-человек имеет: молекулу геномной нуклеиновой кислоты, имеющую нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, при этом нуклеотидная последовательность содержит тимин в положении, соответствующем положению 5624 согласно SEQ ID NO: 7, или ее комплементарной цепи; молекулу мРНК, имеющую нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, при этом нуклеотидная последовательность содержит урацил в положении, соответствующем положению 1161 согласно SEQ ID NO: 14, или ее комплементарной цепи; молекулу кДНК, имеющую нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, при этом нуклеотидная последовательность содержит тимин в положении, соответствующем положению 1161 согласно SEQ ID NO: 21, или ее комплементарной цепи; или полипептид SLC39A5, который усечен в положении 310 согласно SEQ ID NO: 27 и не содержит аминокислот в положениях, соответствующих положениям 311-540 согласно SEQ ID NO: 22.
Все патентные документы, веб-сайты, другие публикации, учетные номера и т. п., цитируемые выше или ниже, включены в данный документ посредством ссылки в полном объеме и во всех отношениях в той же степени, как если бы для каждого отдельного пункта было специально и отдельно указано его включение посредством ссылки. Если с учетным номером в разное время связаны разные версии последовательности, подразумевается версия, связанная с номером доступа на момент действительной даты подачи данной заявки. Действительная дата подачи означает более раннюю фактическую дату подачи или дату подачи приоритетной заявки, ссылающейся на учетный номер, если это применимо. Аналогично, если разные версии публикации, веб-сайта и т. п. опубликованы в разное время, подразумевается версия, опубликованная ближе всего к действительной дате подачи заявки, если не указано иное. Любой признак, стадия, элемент, вариант осуществления или аспект данного изобретения можно использовать в комбинации в любым другим признаком, стадией, элементом, вариантом осуществления или аспектом, если явно не указано иное. Несмотря на то, что данное изобретение было достаточно подробно описано с помощью иллюстрации и примера в целях ясности и понимания, является очевидным, что определенные изменения и модификации могут быть реализованы в рамках объема прилагаемой формулы изобретения.
Следующие примеры приведены для более подробного описания вариантов осуществления. Они предназначены для иллюстрации, но не ограничения заявляемых вариантов реализации. Следующие примеры приведены для того, чтобы предоставить рядовым специалистам в данной области техники раскрытие и описание создания и оценки соединений, композиций, изделий, устройств и/или способов, описанных в данном документе, и предназначены исключительно для иллюстрации, но не для ограничения объема любых пунктов прилагаемой формулы изобретения. Были предприняты усилия в отношении обеспечения точности чисел (например, количества, температуры и т. д.), но некоторые ошибки и отклонения могут быть приняты во внимание. Если не указано иное, доли представляют собой массовые доли, температура выражена в°C или равна температуре окружающей среды, а давление находится на уровне атмосферного или около него.
Примеры
Пример 1. SLC39A5 локализуется на поверхности клетки и опосредует цинк-зависимые транскрипционные ответы
Ген SLC39A5 экспрессировали с использованием репортерной системы IRES-dsRED, трансфицированной в клетки, и экспрессию подтвердили. Через день после трансфекции клетки переносили в среду, не содержащую Zn, и через день подвергали перфузии буфером, содержащим (0-1 мМ) свободный Zn2+ с или без хелатора TREN/Zn-Pyr (проникающий в клетки, высокоаффинный тяжелый металл (Zn2+>Fe2+>Mn2+), который проявляют низкую аффинность к Mg2+ и Ca2+). Цинк-зависимые транскрипционные ответы контролировали по экспрессии репортерного гена люциферазы, управляемого металлочувствительным элементом (MRE). Результаты показали, что SLC35 необходим для опосредованной Zn2+ активации MRE.
Пример 2. Варианты усечения в SLC39A5 приводят к потере функции
Функциональность нескольких вариантов SLC39A5 (Y47X (Y47Stop), R311X (R311Stop), R322X (R322Stop) и M304T; таблица 2) была исследована с использованием опосредованной Zn2± активации MRE. Результаты (Фиг. 1A и 1B) демонстрируют, что варианты усечения проявляют полную потерю функции, в то время как замена метионина треонином в положении 304 белка SLC39A5 приводит к частичной потере функции.
Таблица 2. Варианты SLC39A5
Пример 3. Добавка цинка устраняет стеатоз печени и толерантность к глюкозе при индуцированном диетой ожирении
Четыре группы 6-недельных самцов мышей (по 16 на группу) получали либо нормальный корм, либо диету с высоким содержанием жиров с добавлением различных концентраций цинка в течение 4 или 6 недель (Фиг. 2А). Уровни цинка анализировали через 4 недели (Фиг. 2B и 2C) и через 6 недель (Фиг. 2D и 2E). Хотя не было значительного изменения уровней цинка в сыворотке (Фиг. 2B и 2D) или уровней цинка в печени через 4 недели (Фиг. 2C), было статистически значимое увеличение уровней цинка в печени через 6 недель (Фиг. 2E), которое коррелировало с уровнем цинка в рационе.
Внутривенные тесты толерантности к глюкозе (Фиг. 3A и 3C) показали, что увеличение концентрации цинка в рационе смягчает повышение уровня глюкозы в крови, опосредованное диетой с высоким содержанием жиров, и уменьшает площадь под кривой (Фиг. 3B и 3D), хотя этот эффект не был статистически значимым. Микроскопический анализ печени мышей показал, что добавление цинка к диете с высоким содержанием жиров предотвращает накопление жира в печени (Фиг. 4).
Пример 4: Потеря Slc39a5 приводит к умеренному снижению уровня глюкозы в крови натощак у самок мышей
Эффект гомологичного и гетерологичного нокаута SLC39A исследовали на самцах и самках мышей в возрасте 12 недель. Результаты демонстрируют, что статистически значимое снижение массы тела как у самцов (Фиг. 5D), так и у самок (Фиг. 5A) мышей с гомологичным нокаутом SLC39A. Гомологичный нокаут SLC39A также приводил к статистически значимому увеличению содержания цинка в сыворотке (Фиг. 5C) и цинка в печени (Фиг. 5F) как у самцов, так и у самок мышей. Однако только самки гомологичных мышей с нокаутом SLC39A показали статистически значимое снижение уровня глюкозы в крови (Фиг. 5B). Напротив, никаких статистически значимых изменений средних уровней глюкозы в крови не наблюдали после 14 недель диеты с высоким содержанием жиров (Фиг. 9A) или в уровнях инсулина в крови не натощак/терминального уровня после 146 недель диеты с высоким содержанием жиров (Фиг. 9B).
Пример 5. Потеря Slc39a5 приводит к повышенным уровням циркулирующего цинка.
Уровни циркулирующих цинка, глюкозы, лептина, инсулина и С-пептида исследовали у 31-недельных самцов и самок мышей, гомологичных по SLC39A, после 25 недель диеты с высоким содержанием жиров. Никаких статистически значимых изменений не наблюдали ни для каких параметров, за исключением уровней цинка в сыворотке (Фиг. 6A-F).
Пример 6. Потеря функции Slc39a5 устраняет гипергликемию у мышей с дефицитом рецепторов лептина (db/db, самки)
Массу тела, уровень глюкозы в крови натощак и сывороточный цинк исследовали у 31-недельных самцов и самок мышей с гомологичным нокаутом SLC39A, с нокаутом рецептора лептина (Lepr) или мышей с двойным нокаутом, получавших нормальный корм. В то время как все мыши показали увеличение массы тела и уровня глюкозы в крови натощак, одновременный нокаут SLC39A значительно изменил массу тела у самцов, но не у самок мышей (Фиг. 7A и 7D). В то же время одновременный нокаут SLC39A приводил к снижению уровня глюкозы в крови натощак у самок мышей, но не у самцов (Фиг. 7B и 7E). Нокаут по Lepr не оказывал влияния на увеличение содержания цинка в сыворотке в результате нокаута SLC39A (Фиг. 7C и 7F).
Пример 7. Потеря функции Slc39a5 устраняет гипергликемию у мышей с дефицитом рецепторов лептина (db/db, самки) с сопутствующим усилением кетогенеза
Массу тела, уровни глюкозы в крови натощак и уровни β-гидроксибутирата исследовали у 10-недельных самцов и самок мышей с гомологичным нокаутом SLC39A, с нокаутом по рецепторам лептина (Lepr) или мышей с двойным нокаутом, получавших нормальный корм. У всех мышей наблюдали увеличение массы тела и уровня глюкозы в крови натощак, и одновременный нокаут SLC39A не оказал значительного влияния на массу тела (Фиг. 8A и 8D). В то же время, нокаут SLC39A приводил к снижению уровня глюкозы в крови натощак у самок, но не у самцов мышей как с нокаутом Lepr, так и без него (Фиг. 8B и 8E). Как нокаут SLC39A, так и нокаут Lepr приводили к снижению уровней β-гидроксибутирата у самок мышей, но, что удивительно, когда оба гена были нокаутированы, этот эффект был устранен (Фиг. 8C).
Пример 8: Гетерозиготные по потере функции SLC39A5 имеют повышенное содержание цинка в сыворотке
Сравнительные значения нетрансформированных показателей для различных признаков у мышей дикого типа и мышей с нокаутом SLC39A5 показаны в таблице 3 и на Фиг. 10.
Таблица 3
Пример 9: Потеря SLC39A5 приводит к повышению уровня цинка в сыворотке и костях
Получение мышей с потерей функции Slc39a5:
Генетически сконструированная линей Slc39a5-/- мышей был создано с использованием технологии VelociGene®. Вкратце, эмбриональные стволовые клетки C57Bl/6NTac (ЭСК) были нацелены на удаление части локуса Slc39a5, начиная сразу после начала ATG и заканчивая 5 парами оснований перед 3'-концом кодирующего экзона 2. Эта область содержит сигнальный пептид Slc39a5 и большую часть N-концевого внеклеточного домена. Репортерный модуль lacZ был вставлен в рамку считывания с началом Slc39a5, за которым следовала кассета устойчивости к неомицину fLoxed для селекции ЭСК. Кассета устойчивости была удалена перед микроинъекцией с использованием технологии самоудаления. Клетки-мишени подвергали микроинъекции в 8-клеточные эмбрионы мышей-альбиносов Swiss Webster от Charles River Laboratories, в результате чего получали мыши F0 VelociMice®, которые на 100% происходили из клеток-мишеней. Впоследствии этих мышей размножали для получения гомозиготного потомства и содержали в виварии в течение всего периода. В качестве контроля использовали гетерозиготных Slc39a5-/+ мышей и однопометников C57Bl/6NTac дикого типа.
Потеря печеночной функции Slc39a5 у мышей на длительной диете с высоким содержанием жиров (HFD):
Мышей, гомозиготных по потере функции Slc39a5, и однопометников дикого типа содержали вместе в контролируемых условиях (12-часовой цикл свет/темнота, 22±1 °C, влажность 60-70%) и они получали ad libitum корм с высоким содержанием жиров (Test Diet, кат. № 9GWP), содержащий 35 мкг цинка/г, начиная с 6-недельного возраста. В этом исследовании использовали как самцов, так и самок мышей. На 40 неделе контрольной диеты с высоким содержанием жиров после ночного голодания (продолжительностью 16 часов) оценивали сывороточный и печеночный цинк, и АЛТ и АСТ. Отдельная когорта мышей C57BLK/6 дикого типа соответствующего возраста, содержавшаяся на нормальном корме (Lab Diet, каталожный № 5K52), содержащем 85 мкг цинка/г, была получена от Jackson Laboratories в качестве контроля. Анализы содержания цинка в сыворотке и печени проводили с использованием пламенной атомно-абсорбционной спектроскопии, как описано ниже. Уровни АЛТ и АСТ в сыворотке, а также другие показатели печени и липидов измеряли с помощью системы ADVIA Chemistry XPT (Siemens Healthineers). Для гистологии образцы эксплантированной печени фиксировали в 10% забуференном фосфатом формалинацетате при 4°C в течение ночи, тщательно промывали фосфатно-солевым буферным раствором и заливали парафином. Окрашивание гематоксилином и эозином проводили на парафиновых срезах толщиной 5 мкм с использованием стандартных методов гистохимии. Срезы получали с помощью объектива с 20-кратным или 40-кратным увеличением с использованием микроскопа EVOS FL Auto (Thermo Fisher Scientific).
Анализы на содержание цинка в сыворотке и тканях:
Все измерения содержания цинка проводили с использованием атомно-абсорбционного спектрометра Agilent Technologies 240 FS в пламенном режиме. Образцы сыворотки количественно разбавляли деионизированной водой и впоследствии анализировали. Для образцов сыворотки в качестве эталона использовали сыворотку со следовыми элементами Seronorm (L-2). Сначала ткани, кости и другие материалы расщепляли азотной кислотой. Образцы взвешивали и инкубировали в течение ночи при 85°C в азотной кислоте. На следующий день образцы охлаждали до комнатной температуры и количественно переносили в полистирольные пробирки с деионизированной водой. Впоследствии они были проанализированы. Для всех образцов ткани в качестве эталона использовали стандартный эталонный материал бычьей печени (SRM 1577c) из Национального института стандартов и технологий.
Печеночные и липидные показатели:
Анализы выполняли на Siemens ADVIA Chemistry XPT. Печеночный и липидный профиль включали следующие вещества: аланинаминотрансферазу (АЛТ, Siemens REF 03036926), аспартатаминотрансферазу (АСТ, Siemens REF 07499718), холестерин (хол., Siemens REF 10376501), холестерин ЛПВП прямой (DHDL, Siemens REF 07511947), холестерин ЛПНП прямой (DLDL, Siemens REF 09793248), неэтерифицированные жирные кислоты (НЭЖК, Wako 999-34691, 995-34791, 991-34891, 993-35191), триглицериды (ТГ, Siemens REF 10335892). Эти вещества при смешивании с образцом будут подвергаться окислительно-восстановительным реакциям, специфичным для представляющего интерес аналита, которые вызывают изменение цвета, пропорциональное концентрации анализируемого вещества (колориметрический анализ). Измеряли поглощение света на длине волны, специфичной для анализируемого вещества (от галогенного источника света), и определяли концентрацию. Каждый набор реагентов был откалиброван в соответствии с рекомендациями производителя, а образцы с известными значениями (многоуровневый контроль качества) измеряли ежедневно. Параметрам никогда не разрешали отклоняться от известных средних значений более чем на одно стандартное отклонение. Образцы, как правило, анализировали в неразбавленном виде, хотя их можно разбавить до 1,5x, не влияя на результаты. Образцы загружали в анализатор в микроцентрифужные пробирки объемом 0,6 мл, и анализатор выполнял смешивание всех реагентов, определял время анализа, оптическую плотность и концентрацию.
Гистология печени:
Для окрашивания гематоксилином и эозином неокрашенные микропрепараты депарафинизировали в ксилоле, а затем гидратировали через батарею спиртов до воды. Срезы окрашивали гематоксилином Карацци, промывали водопроводной водой и затем помещали в 95% этанол. Оттуда их поместили в раствор эозина-флоксина, затем пропустили через батарею спиртов до ксилола. После ксилола окрашенные микропрепараты накрывали покрывными стеклами и визуализировали. Для окрашивания по Массону неокрашенные микропрепараты депарафинизировали в ксилоле, гидратировали через градуированные спирты до воды и затем оставляли в растворе Буэна на ночь. Затем их тщательно промывали и переводили на гематоксилин Вейгерта. После гематоксилина микропрепараты промывали водой, затем помещали в раствор фуксина алой кислоты Бибриха. Микропрепараты снова ополаскивали водой перед переносом в раствор фосфорномолибденовой и фосфорновольфрамовой кислоты. Затем микропрепараты ополаскивали водой и помещали в анилиновый синий, последний раз промывали водой, а затем обезвоживали с помощью батареи спиртов и помещали в ксилол. После ксилола окрашенные микропрепараты накрывали покровным стеклом, как описано выше.
Результаты.
На Фиг. 11, 12 и 13 показаны уровни цинка в сыворотке, цинка в печени, аланинаминотрансферазы и аспартатаминотрансферазы у мышей с потерей функции Slc39a5 на 40-й неделе на диете с высоким содержанием жиров. Самки гомозиготных по потере функции мышей имели повышенные уровни цинка в сыворотке и печени по сравнению с мышами дикого типа на нормальном корме (NC) или диете с высоким содержанием жиров (HFD). У мышей самцов в этом возрасте различий не наблюдали. Кроме того, самки гомозиготных по потере функции мышей имели пониженные уровни аланинаминотрансферазы по сравнению с мышами дикого типа на нормальном корме (NC) или диете с высоким содержанием жиров (HFD). Никаких различий в уровнях аспартатаминотрансферазы между группами не наблюдали. Самцы гомозиготных по потере функции мышей имели повышенные уровни цинка в сыворотке по сравнению с мышами дикого типа на нормальном корме (NC) или диете с высоким содержанием жиров (HFD) через 40 недель. Не наблюдалось различий в уровнях цинка в печени, аланинаминотрансферазы и аспартатаминотрансферазы у самцов гомозиготных по потере функции мышей по сравнению с мышами дикого типа на нормальном корме (NC) или диете с высоким содержанием жиров (HFD). В соответствии с этими наблюдениями, у самок гомозиготных по потере функции мышей наблюдали резкое снижение накопления липидов в печени по сравнению с мышами дикого типа на нормальном корме (NC) или диете с высоким содержанием жиров (HFD) через 40 недель на основании окрашивания гематоксилином и эозином и окрашивания по Массону. Самцы гомозиготных по потере функции мышей также показали умеренное снижение накопления липидов в печени по сравнению с самцами однопометников дикого типа на нормальном питании (NC) или на диете с высоким содержанием жиров (HFD) через 40 недель на основании окрашивания гематоксилином и эозином и окрашивания по Массону.
Пример 10. Потеря SLC39A5 приводит к снижению триглицеридов в печени
Анализ печеночного β-гидроксибутирата:
Анализы выполняли с использованием набора для анализа β-гидроксибутирата (SIGMA MAK041). Эксплантированные образцы печени (10 мг/образец) гомогенизировали в 4 объемах холодного
буфера для анализа β-гидроксибутирата в соответствии с рекомендациями производителя. Гомогенизированные образцы центрифугировали при 13000 g в течение 10 минут при 4 °C, и полученный супернатант использовали для последующих анализов. В этом анализе концентрацию β-гидроксибутирата определяли сопряженной ферментативной реакцией, которая приводит к колориметрическому (450 нм) продукту, пропорциональному присутствующему β-гидроксибутирату.
Анализ печеночных триглицеридов:
Анализы выполняли с использованием набора для колориметрического анализа триглицеридов (Cayman 10010303). Эксплантированные образцы печени (400 мг/образец) гомогенизировали в 2 мл реагента для анализа на замену NP-40, содержащего ингибиторы протеаз. Гомогенизированные образцы центрифугировали при 10000 g в течение 10 минут при 4 °C, и полученный супернатант разбавляли по меньшей мере 1:5 с использованием реагента для анализа NP-40 для последующих анализов. Этот анализ включает ферментативный гидролиз триглицеридов липазой с образованием глицерина и свободных жирных кислот. Высвободившийся глицерин впоследствии измеряют колориметрической сопряженной ферментативной реакцией. Поглощение измеряли при 530-550 нм.
Результаты.
На Фиг. 14 показаны уровни триглицеридов и β-гидроксибутирата в печени у самок мышей с потерей функции Slc39a5 через 40 недель на диете с высоким содержанием жиров. Самки гомозиготных по потере функции мышей имели пониженный уровень триглицеридов в печени по сравнению с мышами дикого типа на нормальном корме (NC) или диете с высоким содержанием жиров (HFD). Кроме того, самки гомозиготных по потере функции мышей имели повышенные уровни β-гидроксибутирата в печени по сравнению с мышами дикого типа, которые получали нормальный корм (NC) или диету с высоким содержанием жиров (HFD).
Пример 11. Потеря SLC39A5 приводит к улучшению функции печени и гликемических показатели
Печеночные, липидные и гликемические показатели мышей, гомозиготных по потере функции Slc39a5 и рецептора лептина (Lepr):
Самок мышей, гомозиготных по потере функции Slc39a5 и Lepr, и контрольных однопометников (дикого типа, Slc39a5-/-, Lepr-/-) содержали вместе в контролируемых условиях (12-часовой цикл свет/темнота, 22±1°C, влажность 60-70%) и они получали ad-libitum обычный корм (PicoLab Rodent Diet 20, кат. № 5053), содержащий 87 мкг цинка/г. У мышей периодически проверяли состояние здоровья и кинетику роста. После ночного голодания (продолжительностью 16 часов) у мышей в возрасте 22 недель измеряли сывороточные уровни АЛТ и АСТ вместе с DLDL и глюкозой крови натощак. Уровень глюкозы в крови оценивали с помощью системы для мониторинга уровня глюкозы в крови AlphaTrak (Zoetis United States, Парсиппани, штат Нью-Джерси) путем отбора пробы крови из боковой хвостовой вены. Печеночные и липидные показатели измеряли с использованием Siemens ADVIA Chemistry XPT, как описано ранее. Пероральный тест толерантности к глюкозе проводили после ночного голодания (продолжительностью 16 часов) в возрасте 20 недель путем введения 2 г декстрозы/кг массы тела (Hospira Inc, NDC 0409-4902-34) через желудочный зонд. Уровень глюкозы в крови оценивали в определенные моменты времени (0, 15, 30, 60 и 120 минут) с помощью системы для мониторинга уровня глюкозы в крови AlphaTrak (Zoetis United States, Парсиппани, штат Нью-Джерси) путем отбора пробы крови из боковой хвостовой вены.
Результаты.
Самок мышей, гомозиготных по потере функции Slc39a5, скрещивали мышами с дефицитным по рецепторам лептина фоном (Lepr-/-) (обычно используемая модель гипергликемии, вызванной ожирением и диабетом II типа, на грызунах). Мыши с дефицитом рецепторов лептина были гипергликемическими и демонстрировали повышенные уровни липопротеинов низкой плотности в сыворотке. Кроме того, у этих мышей были повышенные уровни АЛТ и АСТ в сыворотке, что свидетельствует о нарушении функции печени в возрасте 22 недель. Потеря функции Slc39a5 у самок мышей с дефицитом рецепторов Lepr значительно снижала уровни глюкозы в крови натощак, сывороточного LDL-C, сывороточного АЛТ и АСТ, потенциально улучшая индуцированную ожирением метаболическую дисрегуляцию при дефиците рецепторов лептина (см. Фиг. 15 и 16). В соответствии с этими наблюдениями, самки мышей, гомозиготные по потере функции Slc39a5 и Lepr, продемонстрировали улучшенную толерантность к глюкозе при пероральной глюкозной нагрузке.
Пример 12: Потеря SLC39A5 приводит к активации печеночной АМФ-активируемой протеинкиназы
Анализы методом иммуноблоттинга:
Белок печени экстрагировали с использованием буфера RIPA (Cell signaling technology, кат. № 9806) с коктейлем ингибиторов протеаз и фосфатаз Halt (ThermoFisher Scientific, кат. № 78440). Пять микрограммов белков каждого образца разделяли в геле NuPAGE 4-12% Bis-Tris (Invitrogen, кат. № WG1403BOX) и переносили на нитроцеллюлозную мембрану с использованием Trans-Blot® Turbo™ Transfer System (BioRad). Блоттинг выполняли с использованием следующих антител Cell Signaling Technology: фосфо-AMPKα (Thr172) (Cell signaling technology, кат. № 2535), AMPKα (Cell signaling technology, кат. № 5831), фосфо-AMPKβ1 (Ser182) (Cell signaling technology, кат. № 4186), SCD1 (Cell signaling technology, кат. № 2794), фосфо-ацетил-КоА-карбоксилаза (Ser79) (Millipore Sigma, кат. № 07-303), ацетил-КоА-карбоксилаза 1 (Millipore Sigma, кат. № MABS830), β-актин (Sigma, кат. № 5441), кроличий IgG, конъюгированный с пероксидазой хрена (ПХ) (Cell signaling technology, кат. № 7074), и мышиный IgG, конъюгированный с ПХ (Cell signaling technology, кат. № 7076). Блоты проявляли с использованием субстрата SuperSignal West Femto Substrate (ThermoFisher Scientific, кат. № 34095). Сигналы регистрировали с помощью ImageQuant LAS4000 (GE Healthcare).
Результаты.
Со ссылкой на Фиг. 17, самки гомозиготных по потере функции мышей имели повышенную активацию AMPK в печени, что определяли по повышенным уровням pAMPKα/AMPKα по сравнению с мышами дикого типа, которые получали нормальный корм (NC) или диету с высоким содержанием жиров (HFD). Кроме того, повышенная активация AMPK у этих мышей приводила к повышенному фосфорилированию ацетил-coA-карбоксилазы (определяемому по повышенным уровням pACC/ACC) по сравнению с мышами дикого типа, который получали нормальный корм (NC) или диету с высоким содержанием жиров (HFD). Не наблюдалось различий в уровнях стеароил-КоА-десатуразы (SCD1), ключевого фермента, ограничивающего скорость образования мононенасыщенных жирных кислот, включая триглицериды.
Пример 13. Получение и применение моноклонального антитела к SLC39A5
Иммуногенный пептидный фрагмент SLC39A5 для инокуляции мышей (SEQ ID NO: 67) был выбран на основании гидрофильности аминокислотной последовательности (см. Фиг. 18). Мыши инокулировали иммуногенным фрагментом SLC39A5. Мышь умерщвляли и выделяли спленоциты. Спленоциты сливали с клетками-партнерами гибридомы. Успешно слитые клетки разбавляли и аликвоты разведения помещали в лунки микротитрационного планшета, где рост культуры продолжался. Клоны, продуцирующие антитела, идентифицировали путем анализа реактивности антитела в супернатанте с клетками HEK, сверхэкспрессирующими мышиный SLC39A5 (см. Фиг. 19), и клетками HEK, сверхэкспрессирующими SLC39A5 человека (см. Фиг. 20). Были размножены три положительных клона, которые были реактивными в отношении SLC39A5 как человека, так и мыши (см. 10D1, 10D4 и 11C1), и был выбран их препарат на основе моноклонального антитела.
Пример 14. Метаболическое фенотипирование мышей с потерей функции Slc39a5
Метаболическое фенотипирование:
Мышей, гомозиготных или гетерозиготных по потере функции Slc39a5, и однопометников дикого типа содержали вместе в контролируемой среде (12-часовой цикл свет/темнота, 22±1°C, влажность 60-70%)и они получали ad libitum диету с высоким содержанием жира и высоким содержанием фруктозы (Test Diet, кат. № 5WK9) или контрольной диетой (Test Diet, кат. № 58Y2), содержащей 35 мкг цинка/г, начиная с 10-недельного возраста. В этом исследовании использовали как самцов, так и самок мышей. Оценку содержания цинка в сыворотке крови, глюкозы в крови натощак, а также аланинаминотрансферазы (АЛТ) и аспартатаминотрансферазы (АСТ) (биомаркеры повреждения печени) в динамике проводили после ночного голодания (продолжительностью 16 часов). Уровень глюкозы в крови измеряли перед началом голодания. Анализ цинка в сыворотке и печени (в конечной точке) проводили с использованием пламенной атомно-абсорбционной спектроскопии, как описано ниже.
Мышей, гомозиготных по Slc39a5 и Lepr с потерей функции (Slc39a5-/-; Lepr-/-), и контрольных однопометников (дикий тип, Slc39a5-/-, Lepr-/-) содержали вместе в контролируемой среде (12-часовой цикл свет/темнота, 22±1°C, влажность 60-70%) и они получали ad-libitum обычный корм (PicoLab Rodent Diet 20, кат. № 5053), содержащий 87 мкг цинка/г. У мышей периодически проверяли состояние здоровья и кинетику роста. После ночного голодания (продолжительностью 16 часов) у мышей в возрасте 22 недель измеряли сывороточные уровни АЛТ и АСТ (биомаркеры повреждения печени) вместе с DLDL и глюкозой крови натощак. Уровень глюкозы в крови оценивали с помощью системы для мониторинга уровня глюкозы в крови AlphaTrak (Zoetis United States, Парсиппани, штат Нью-Джерси) путем отбора пробы крови из боковой хвостовой вены. Печеночные и липидные показатели измеряли с использованием Siemens ADVIA Chemistry XPT, как описано ниже.
Пероральный тест толерантности к глюкозе:
Пероральный тест толерантности к глюкозе проводили после ночного голодания (продолжительностью 16 часов) в возрасте 20 недель путем введения 2 г декстрозы/кг массы тела (Hospira Inc, NDC 0409-4902-34) через желудочный зонд. Уровень глюкозы в крови оценивали в определенные моменты времени (0, 15, 30, 60 и 120 минут) с помощью системы для мониторинга уровня глюкозы в крови AlphaTrak (Zoetis United States, Парсиппани, штат Нью-Джерси) путем отбора пробы крови из боковой хвостовой вены.
Печеночные и липидные показатели:
Все печеночные и липидные показатели измеряли с использованием системы ADVIA Chemistry XPT (Siemens Healthineers), биохимического анализатора, одобренного FDA, который мы обслуживаем и работаем в соответствии с рекомендациями Siemens. Печеночный и липидный профиль включают следующие вещества: аланинаминотрансферазу (АЛТ, Siemens REF 03036926), аспартатаминотрансферазу (АСТ, Siemens REF 07499718), холестерин (хол., Siemens REF 10376501), холестерин ЛПВП прямой (DHDL, Siemens REF 07511947), холестерин ЛПНП прямой (DLDL, Siemens REF 09793248), неэтерифицированные жирные кислоты (НЭЖК, Wako 999-34691, 995-34791, 991-34891, 993-35191), триглицериды (ТГ, Siemens REF 10335892). Эти вещества при смешивании с образцом подвергаются окислительно-восстановительным реакциям, специфичным для представляющего интерес аналита, которые вызывают изменение цвета, пропорциональное концентрации анализируемого вещества (колориметрический анализ). Измеряли поглощение света на длине волны, специфичной для анализируемого вещества (от галогенного источника света), и определяли концентрацию. Каждый набор реагентов был откалиброван соответствии с рекомендациями производителя, а образцы с известными значениями (многоуровневый контроль качества) измеряли ежедневно. Параметрам никогда не разрешали отклоняться от известных средних значений более чем на одно стандартное отклонение. Образцы, как правило, анализировали в неразбавленном виде, хотя их можно разбавить до 1,5x, не влияя на результаты. Образцы загружали в анализатор в микроцентрифужные пробирки объемом 0,6 мл, и анализатор выполнял смешивание всех реагентов, определял время анализа, оптическую плотность и концентрацию.
Количественное определение ионов металлов:
Все измерения содержания ионов проводили с использованием атомно-абсорбционного спектрометра Agilent Technologies 240 FS в пламенном режиме. Образцы сыворотки количественно разбавляли деионизированной водой и впоследствии анализировали. Для образцов сыворотки в качестве эталона использовали сыворотку со следовыми элементами Seronorm (L-2). Сначала ткани, кости и другие материалы расщепляли азотной кислотой. Образцы взвешивали и инкубировали в течение ночи при 85°C в азотной кислоте. На следующий день образцы охлаждали до комнатной температуры и количественно переносили в полистирольные пробирки с деионизированной водой. Впоследствии они были проанализированы. Для всех образцов ткани в качестве эталона использовали стандартный эталонный материал бычьей печени (SRM 1577c) из Национального института стандартов и технологий.
Гистология печени и иммуноблоттинг:
Образцы эксплантированной печени фиксировали в 10% забуференном фосфатом формалинацетате при 4°C в течение ночи, тщательно промывали фосфатно-солевым буферным раствором и заливали парафином. Для окрашивания гематоксилином и эозином неокрашенные парафиновые срезы толщиной 5 мкм депарафинизировали в ксилоле, а затем гидратировали через батарею спиртов до воды. Срезы окрашивали гематоксилином Карацци, промывали водопроводной водой и затем помещали в 95% этанол. Оттуда их поместили в раствор эозина-флоксина затем пропустили через батарею спиртов до ксилола. После ксилола окрашенные микропрепараты накрывали покровными стеклами и окрашивали и визуализировали с использованием объектива 20X или 40X с использованием сканера микропрепаратов Aperio AT2 (Leica Biosystems Inc.).
Белок печени экстрагировали с использованием буфера RIPA (Cell signaling technology, кат. № 9806) с коктейлем ингибиторов протеаз и фосфатаз Halt (ThermoFisher Scientific, кат. № 78440). Пять микрограммов белка каждого образца разделяли в геле NuPAGE 4-12% Bis-Tris (Invitrogen, кат. № WG1403BOX) и переносили на нитроцеллюлозную мембрану с использованием Trans-Blot® Turbo™ Transfer System (BioRad). Блоттинг выполняли с использованием следующих антител Cell Signaling Technology: фосфо-AMPK™ (Thr172) (Cell signaling technology, кат. № 2535), AMPKα (Cell signaling Technology, кат. № 5831), β-актин (Sigma, кат. № 5441), фосфо-AKT (Ser473) (Cell signaling technology, кат. № 4060), AKT (Cell signaling technology,, кат. № 9272), фосфо-LKB1 (Ser428) (Cell signaling technology, кат. № 3482), LKB1 (Cell signaling technology, кат. № 3050), кроличий IgG, конъюгированный с пероксидазой хрена (ПХ) (Cell signaling technology, кат. №7074), и мышиный IgG, конъюгированный с ПХ (Cell signaling technology, кат. №7076). Блоты проявляли с использованием субстрата SuperSignal West Femto Substrate (ThermoFisher Scientific, кат. № 34095). Сигналы регистрировали с помощью ImageQuant LAS4000 (GE Healthcare).
Результаты приведены на фигурах 21, 22, 23, 24A, 24B, 25A, 25B, 26A, 26B, 27, 28, 29, 30, 31A, и 31B.
Пример 15. Мутации с потерей функции в SLC39A5 связаны с повышением уровней циркулирующего цинка и снижением риска T2D
Полногеномное исследование ассоциаций, изучающее взаимосвязь между мутациями с потерей функции SLC39A5 и уровнями циркулирующего цинка, было проведено на европейской когорте биобанка GHSF145K IDT и европейской когорте GHSF145K VCRome. Оба исследования, а также метаанализ двух исследований показали значительную связь (см. Фиг. 32, верхняя таблица).
Полногеномное исследование ассоциаций, изучающее связь между мутациями с потерей функции SLC39A5 и диабетом II типа (T2D), было проведено на европейской когорте биобанка GHSF145K IDT, европейской когорте GHSF145K VCRome и на когорте британского биобанка из 150 тысяч участников. Метаанализ трех исследований продемонстрировал значительную связь (см. Фиг. 32, нижняя таблица).
Пример 16. Потеря SLC39A5 приводит к подавлению активности фосфатазы
Повышенные концентрации цинка подавляли активность как тирозинфосфатазы (см. Фиг. 33A), так и серин/треонинфосфатазы (см. Фиг. 33B). Приводит ли потеря SLC39A5 к подавлению активности фосфатазы из-за увеличения концентрации цинка, проверяли в анализе ex vivo. Потеря SLC39A5 привела к подавлению как тирозинфосфатазы, так и серин/треонинфосфатазы у самок (см. Фиг. 34A и 34B) и самцов (см. Фиг. 34C и 34D) мышей. Подавление не зависело от диеты, и добавление к диете с высоким содержанием жиров различных концентраций цинка не спасало от подавления.
Разнообразные модификации описанного объекта изобретения, в дополнение к описанным в данном документе, будут очевидны для специалистов в данной области техники из вышеизложенного описания. Такие модификации также входят в объем прилагаемой формулы изобретения. Каждая ссылка (включая, но не ограничиваясь ими, статьи в научных журналах, патенты США и других стран, публикации патентных заявок, публикации международных патентных заявок, учетные номера в генных банках и т. п.), указанная в данной заявке, включена в данный документ посредством ссылки в полном объеме и для всех целей.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Regeneron Pharmaceuticals, Inc.
<120> Лечение гипергликемии с помощью ингибиторов члена 5 семейства 39
транспортеров растворенных веществ (SLC39A5)
<130> 189238.02302 (3199) (10534WO01)
<150> 62/976 716
<151> 14.02.2020
<150> 62/818 811
<151> 15.03.2019
<160> 67
<170> PatentIn версии 3.5
<210> 1
<211> 7784
<212> ДНК
<213> homo sapienss
<400> 1
agctggaacc aagaaggttg tgtccccctt cctctgggtg tccttgtctc ctgctatcag 60
gtaatgccaa cctcaacccc ctggaccagt caccccgatc agactttgct tgcctgattt 120
taggccaggt cagacatcag aggagagccc agatccttgt ttcctctccc cccgcagggc 180
ttcccctttc ttggtcatcg atccctagag ctctggctct ttctcttctt ggggtgagaa 240
actgctaaga acagtttatt tcccatgcat gcatctgggc ttgccactga tctgcctttt 300
cccccctcct ccccaggtta gggacacctg ggtccaacct tcccaaggaa tatggggatg 360
ggggttggag atgaagttta gtgctagact gtaaggtagg tggggtggaa gtacatgagg 420
gaaagggcta aaatggtact aatggtgtta aggatagggt gaattattta agaggaaaaa 480
gactaggccc aggttctcct tagccatgtg gctttcccag ggcagagggt ggcccctccc 540
tacccagggg cccagcagag actgactttt gatccctacc ccagagacca gtgaaccatt 600
aactcctctc ttatgtgagc cttcacacac tggccccacc cctgaccccg ccccaaggca 660
ggtgggctag gagggggtgc atgtccatct cagccttcta tgtgacgtgg cctccgatcc 720
acctggacac ctggaggcta agcctggatt cccccttccc tgactcagga actgcttaac 780
gtctacagca aggcctaata ggggacctga ggtgacagct cttatgttgc cagtaggggt 840
gaggccctgg ggattgaggg gggataaaga ggtggggcaa agttgagggg tggggtttag 900
gggacaagga atggacggtc agctctggat gaagtatgag gagagctctg actcagggag 960
gtgctccagg aaccagcaaa caagaggctg ctcccgcagg aggcagtgtg aagggagaaa 1020
gaaggctgca gtaggggctg ctgctggact cggtggggag caggtgcaag gagctctggc 1080
tcccccatgg acctgagctg gagagcagag cgcagctcca gcccattcct cattcttcca 1140
gggcacagtc ctcaggatgt ttcggggaga ataggagcca gaacctgagc ccctaagcta 1200
ttcccctcac caatgatggg gtccccagtg agtcatctgc tggccggctt ctgtgtgtgg 1260
gtcgtcttgg gctgggtagg gggctcagtc cccaacctgg gccctgctga gcaggagcag 1320
aaccattacc tggcccagct gtttggcctg tacggcgaga atgggacgct gactgcaggg 1380
ggcttggcgc ggcttctcca cagcctgggg ctaggccgag ttcaggggct tcgcctggga 1440
cagcatgggc ctctgactgg acgggctgca tccccagctg cagacaattc cacacacagg 1500
tactgacccc ttcctccact ccacagggcc acatctccca ggtcctctca gtgcttgccc 1560
ccagttgcct cgttctggct tcctcacgag atccctggag ttacaaattc ttcagaaccg 1620
agctccttgg tatctcttca aaacctctca tgcttctatt gccttctctc tcttttcttg 1680
agactggggg tctcgctttg tcacccaggc taaagtgcag tgacacattc acggctcact 1740
gcaacctctg cttcccaggc tgaagccatc ctcccacctc agcctcctga gcagctggga 1800
ccataggcac acaccaccac agccggctaa ttttaaaaat tttttacaga gacaagggtt 1860
tcgctgtgtt gcccaggctg gtctcaaact cctgggctca gctcagcgat ctgcctgcct 1920
cagcttccca aagtgctggg actacagatg tgaactacca ccctagccct ccgttgcctt 1980
ctaattctct cctcctccaa atctctaagc ccttaaattt cttgctctta gtatcactgt 2040
tcagtgtctc tgggctgatt tggctccaaa ttcgtagact tcttttttct tttcttttct 2100
tttttttttt tttttttttt tgagacagag tctcgctctg tcgcccaggc tggagtgcag 2160
tggtgtgatc ttggctcact gtaacctctg cctccccggt tcaagcgatt ctcctgcctc 2220
ggcctcctga gtagctggga ttacaggcac acaccaccac gccgggctaa tttttgcaat 2280
tttagtagag acggggtttc accattttgg tcaggctggt ctcgaacttc caacctcagg 2340
tgatccaccc acctcagcct cccaaagtgc tgggattaca ggcgtgagcc accgtgccca 2400
gccattcgta gcccttttgg ttgtcgtcct tttttttctg tcccccccag tggcagaaaa 2460
tggacaactc acagatcttc ctaagaatga cattccatgg tttctgggtc ccaggatctc 2520
cagtcagtgg ctagtccccc cattccccct aaaatccctg ggagcctctc aaagcgggtt 2580
gatagagaac acaagggagg ctgacttgct gtctcatcca ttccaggcca cagaaccctg 2640
agctgagtgt ggatgtctgg gcagggatgc ctctgggtcc ctcagggtgg ggtgacctgg 2700
aagagtcaaa ggcccctcac ctaccccgtg ggccagcccc ctcgggcctg gacctccttc 2760
acaggcttct gttgctggac cactcattgg ctgaccacct gaatgaggat gtgagtctga 2820
cggtctctag aggggaagga gccatgggat tagatggcct gaaatgttta aataatcagt 2880
agttttttgt tttgttttgt ttttaaatcc caacgtggac caagcgtggt ggctcacgcc 2940
tgtaatccca acactttggg aggccgaggt gggtggatca cctgaggtca ggagttcgag 3000
accagcctgg ccaacatggt gaaaccccat ctctactaaa aaatacaaaa attagccggg 3060
tgtggtaaca ggtgtgtgta atcctagcta ctcaggaggc tgaggtgaga aaattgcttg 3120
aacttgggag gcagaggttg cagtgagcca agatggcacc atttgcactc cagcctgggc 3180
aacaagaggg agactctgtc tcaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaat 3240
agctgggcgt ggtggcacat gcctataatc ccagttactc ggaaggctga ggcaggaaaa 3300
tcacttgaac ccaggaggcg gagattgcag tcagccgaga ttgcaccact gcactccagc 3360
ctgggtaaca cagcgagact ctgtctcaaa aatgaaaata aaaaaaataa aaaaataaaa 3420
aaaaaatatc tcactgtggt cttaggggat gttatttcaa tagtgaacta tgttccctct 3480
gggatcagag caggtgagcc catatccaga gctccaagac tcagtttagg ggaatagatg 3540
gcaaagcaga gaatctagag aagcagccca gggtaggatc tggatggtca cctggagagg 3600
agacctgcag ggaatggatg gctgtcttca tccagaaaga cagagaatat attccactta 3660
caccagaggg cagacaaagc tgcctaaccc tgatggaggt ccagtgagtg cccattgcag 3720
gaagcattca agctgaggct ggatgaacat cgacagggct gttgagaggg agattagatg 3780
gcatttcagg gtcttttccc ttttaagatt ctggcatgga gagctctagt tttccaacca 3840
gcttcattta tcaaatcaac aaaatgattg aaatgatcag agtttgcagg gaagatgatg 3900
acaatgctca ctagcaccca gtttgcatca aattgaatac ctgcattgga ctgaatattc 3960
actaataata cacattgatt ataagtaccc ttggccctag tccccaaggt acctgccagt 4020
aggagcaaag gggaccctgg gagagaccca ggagtctatg caatggaagg acaggtgtta 4080
aatatatata tatatatttt tttgaggtag agtctgactc tgtcacccag gctggagtgc 4140
aatggcgtga tcttggctca ctgcaacctc cacctcctgg gttaaagcaa ttctcctgcc 4200
tcagcctccc gagtagctgg gattataggt gttcactact atccccagct aatttttttt 4260
tttttttttt gagatggagt ctcactctgt cgcccaggct ggagtgcact ggtgcaatct 4320
cggctcactg caacctctgc ctcctgggtt caagcgattc tcctgtctca gcctcctgag 4380
tagctgggat cacaggtgca cgccaccatg cccagctaat tttttgtatt ttagtagaga 4440
cagggtttca ccatgttgcc caggctggtc tcgaactcct gagctcaggc aatctaccca 4500
cctcagcctc ccaaagtgct gggattacag gcgtgagcca ccgcacccgg ctcatcccca 4560
gctaattttt gtatttttag tagagacagg gtttcactat gttggccagg ttggtctcaa 4620
actcctgacc tcagatgata cacccgcctg ggcctctcaa gggctgggat tataggtgtg 4680
agccactaca cctggccagg tgttaaagat ctgagtcata gttcctggtg attctccaat 4740
gtatgaccct caattctcca gtgtctgaac ggctcccagc tgctggtcaa ttttggcttg 4800
agccccgctg ctcctctgac ccctcgtcag tttgctctgc tgtgcccagc cctgctttat 4860
cagatcgaca gccgcgtctg catcggcgct ccggcccctg cacccccagg ggatctacta 4920
tctggtcagc aagtaggagt gggtggggga caccctgaat cctggaagtg gggcccatgc 4980
caaaaaggag gctcactggg gtcctgcctc tccttgtagt gttctctctg ctccacctta 5040
cgtgtgggac cctcctcttg ccctgaccta acttcagccc ctgattctcc ccagccctgc 5100
ttcagagtgc cctggcagtc ctgttgctca gcctcccttc tcccctatcc ctgctgctgc 5160
tgcggctcct gggacctcgt ctactacggc ccttgctggg cttcctgggg gccctggcgg 5220
tgggcactct ttgtggggat gcactgctac atctgctacc gcatgtatgt gaagcccctt 5280
ccttgtaccc ctggcctcca tggatctaag gtgtccccag ccataggaca tcccctccgc 5340
ctttccatca gctcccatat cctactccca gatcctggct tcagcccaca gctgccttct 5400
agtagagcat atgagcgaag gcttgccaca atccatgcaa ggggatgttg ttgggtatag 5460
gggcttccag agtctgccct gaccttctct ctgtcaggca caagaagggc ggcacgcagg 5520
acctggcgga ctaccagaga aggacctggg cccggggctg tcagtgctcg gaggcctctt 5580
cctgctcttt gtgctggaga acatgctggg gcttttgcgg caccgagggc tcaggccagt 5640
gagtgatacc cttttctcct ccttctgctg agaccagagt cccagtcaag aactgggcca 5700
ggccgggcgc ggtggctcac gcctgtaatc ccagcacttt gggagcccaa ggcgggcaga 5760
tcacaaggtt aggagttcga gtccagcctg accaacatgg tgaaaccctg tctctactaa 5820
aaatacaaaa attagctggg cgtggtggtg cgtgtctgta atcccagcta ctcaggaggc 5880
tgaggcagga gaatcgcttg acttgggagg tggaggttgc agcgagctaa gatggcacca 5940
ctgcactcca gcccaggtga cagagcgaga ctccatctca aaaacaacaa caacaacaac 6000
aaaactgggc caaaaagcca agagatgagg agcagtgtgt gctcctggat ctctgacatt 6060
tgcctggtgt gcaggaccta tcggctaaca gggagtgggt aggggctcct taagcacaga 6120
cccaggactt ctggccaaat ggcatcctat tctgagctca agtcaacaag aaacagaggg 6180
gaggtgccaa cttgggaaga aggtagaggc caaagaacat cccaggtgcc agaggtggaa 6240
ccaggtgttc atcttcccag cttgtggcct ggcttcccct tagtccctgg ctctgctgcc 6300
tcctccacca ggagggatgc cctcctattt cagagatgct gcaggcgaaa acgaaggaat 6360
ctcgaaacac gcaacttgga tccggagaat ggcagtggga tggcccttca gcccctacag 6420
gcagctccag gtgactagag gagaaaattt gaagagtagg ttccaagctc acagtcctta 6480
cttgcagcca ccaacactgt cctgtgcttc ttcccgcaga gccaggggct cagggccaga 6540
gggagaagaa cagccagcac ccaccagctc tggcccctcc tgggcaccaa ggccacagtc 6600
atgggcacca gggtggcact gatatcacgt ggatggtcct cctgggagat ggtctacaca 6660
acctcactga tgggctggcc ataggtgtga ggggtgggaa cggagggaag caggtccgag 6720
gggaggccag ggctcctagt tatcagctgg ggctaggaga gggccgtcag gaagatgggg 6780
agaggacggg aggaccacgg aacacaggaa cctgcttctg aggagacttt tcttctggac 6840
tgacaacttc cgaccctgct ggccccaggt gctgccttct ctgatggctt ctccagcggc 6900
ctcagtacca ccttagcggt cttctgccat gagctgcccc acgaactggg taggaatggc 6960
aggagcaggg tggggtggac tccagaaagg agatagctcc aaggggtaga gcttggaggc 7020
tggtgggtgg catggatgag gggcacccca gcttactccc tcccatcctg tcctctgtct 7080
ccaataggtg actttgccat gctgctccag tcagggctgt cctttcggcg gctgctgctg 7140
ctgagcctcg tgtctggagc cctgggattg gggggtgcag tcctgggggt ggggctcagc 7200
ctgggccctg tccccctcac tccctgggtg tttggggtca ctgctggggt cttcctctat 7260
gtggcccttg tggacatggt gagagatgtc gggtagagca gagaaatcaa gggcagtggg 7320
gaggcgggag tggagaggga ggtagcagtc cctccgcctc taccattagc tcctggaagg 7380
gcgtcagacc ataggcccgc aaaagtctga gaaacaaggg actaaggtgt ttgggtgggg 7440
gctgctgatg ctttctgaca ccattcctct ggagttgaga ggtcaggggc aaggccagaa 7500
tcctgacatc ctctttttct ttcagctacc agccctgctt cgtcctccgg agcccctgcc 7560
tacgccccat gtgctcctgc aggggctggg gctgctgctg gggggcggcc tcatgcttgc 7620
cataaccctg ctggaggagc ggctactgcc cgtgaccact gagggctgat ggggccagtg 7680
gaaaggggtc gggttgccct tccttccccc caaccacagg aatggaggcg ggacacaggg 7740
ccagtaggag caataggatt ttaataaaca gaacccatcc caaa 7784
<210> 2
<211> 7784
<212> ДНК
<213> homo sapienss
<400> 2
agctggaacc aagaaggttg tgtccccctt cctctgggtg tccttgtctc ctgctatcag 60
gtaatgccaa cctcaacccc ctggaccagt caccccgatc agactttgct tgcctgattt 120
taggccaggt cagacatcag aggagagccc agatccttgt ttcctctccc cccgcagggc 180
ttcccctttc ttggtcatcg atccctagag ctctggctct ttctcttctt ggggtgagaa 240
actgctaaga acagtttatt tcccatgcat gcatctgggc ttgccactga tctgcctttt 300
cccccctcct ccccaggtta gggacacctg ggtccaacct tcccaaggaa tatggggatg 360
ggggttggag atgaagttta gtgctagact gtaaggtagg tggggtggaa gtacatgagg 420
gaaagggcta aaatggtact aatggtgtta aggatagggt gaattattta agaggaaaaa 480
gactaggccc aggttctcct tagccatgtg gctttcccag ggcagagggt ggcccctccc 540
tacccagggg cccagcagag actgactttt gatccctacc ccagagacca gtgaaccatt 600
aactcctctc ttatgtgagc cttcacacac tggccccacc cctgaccccg ccccaaggca 660
ggtgggctag gagggggtgc atgtccatct cagccttcta tgtgacgtgg cctccgatcc 720
acctggacac ctggaggcta agcctggatt cccccttccc tgactcagga actgcttaac 780
gtctacagca aggcctaata ggggacctga ggtgacagct cttatgttgc cagtaggggt 840
gaggccctgg ggattgaggg gggataaaga ggtggggcaa agttgagggg tggggtttag 900
gggacaagga atggacggtc agctctggat gaagtatgag gagagctctg actcagggag 960
gtgctccagg aaccagcaaa caagaggctg ctcccgcagg aggcagtgtg aagggagaaa 1020
gaaggctgca gtaggggctg ctgctggact cggtggggag caggtgcaag gagctctggc 1080
tcccccatgg acctgagctg gagagcagag cgcagctcca gcccattcct cattcttcca 1140
gggcacagtc ctcaggatgt ttcggggaga ataggagcca gaacctgagc ccctaagcta 1200
ttcccctcac caatgatggg gtccccagtg agtcatctgc tggccggctt ctgtgtgtgg 1260
gtcgtcttgg gctgggtagg gggctcagtc cccaacctgg gccctgctga gcaggagcag 1320
aaccattacc tggcccagct gtttggcctg taaggcgaga atgggacgct gactgcaggg 1380
ggcttggcgc ggcttctcca cagcctgggg ctaggccgag ttcaggggct tcgcctggga 1440
cagcatgggc ctctgactgg acgggctgca tccccagctg cagacaattc cacacacagg 1500
tactgacccc ttcctccact ccacagggcc acatctccca ggtcctctca gtgcttgccc 1560
ccagttgcct cgttctggct tcctcacgag atccctggag ttacaaattc ttcagaaccg 1620
agctccttgg tatctcttca aaacctctca tgcttctatt gccttctctc tcttttcttg 1680
agactggggg tctcgctttg tcacccaggc taaagtgcag tgacacattc acggctcact 1740
gcaacctctg cttcccaggc tgaagccatc ctcccacctc agcctcctga gcagctggga 1800
ccataggcac acaccaccac agccggctaa ttttaaaaat tttttacaga gacaagggtt 1860
tcgctgtgtt gcccaggctg gtctcaaact cctgggctca gctcagcgat ctgcctgcct 1920
cagcttccca aagtgctggg actacagatg tgaactacca ccctagccct ccgttgcctt 1980
ctaattctct cctcctccaa atctctaagc ccttaaattt cttgctctta gtatcactgt 2040
tcagtgtctc tgggctgatt tggctccaaa ttcgtagact tcttttttct tttcttttct 2100
tttttttttt tttttttttt tgagacagag tctcgctctg tcgcccaggc tggagtgcag 2160
tggtgtgatc ttggctcact gtaacctctg cctccccggt tcaagcgatt ctcctgcctc 2220
ggcctcctga gtagctggga ttacaggcac acaccaccac gccgggctaa tttttgcaat 2280
tttagtagag acggggtttc accattttgg tcaggctggt ctcgaacttc caacctcagg 2340
tgatccaccc acctcagcct cccaaagtgc tgggattaca ggcgtgagcc accgtgccca 2400
gccattcgta gcccttttgg ttgtcgtcct tttttttctg tcccccccag tggcagaaaa 2460
tggacaactc acagatcttc ctaagaatga cattccatgg tttctgggtc ccaggatctc 2520
cagtcagtgg ctagtccccc cattccccct aaaatccctg ggagcctctc aaagcgggtt 2580
gatagagaac acaagggagg ctgacttgct gtctcatcca ttccaggcca cagaaccctg 2640
agctgagtgt ggatgtctgg gcagggatgc ctctgggtcc ctcagggtgg ggtgacctgg 2700
aagagtcaaa ggcccctcac ctaccccgtg ggccagcccc ctcgggcctg gacctccttc 2760
acaggcttct gttgctggac cactcattgg ctgaccacct gaatgaggat gtgagtctga 2820
cggtctctag aggggaagga gccatgggat tagatggcct gaaatgttta aataatcagt 2880
agttttttgt tttgttttgt ttttaaatcc caacgtggac caagcgtggt ggctcacgcc 2940
tgtaatccca acactttggg aggccgaggt gggtggatca cctgaggtca ggagttcgag 3000
accagcctgg ccaacatggt gaaaccccat ctctactaaa aaatacaaaa attagccggg 3060
tgtggtaaca ggtgtgtgta atcctagcta ctcaggaggc tgaggtgaga aaattgcttg 3120
aacttgggag gcagaggttg cagtgagcca agatggcacc atttgcactc cagcctgggc 3180
aacaagaggg agactctgtc tcaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaat 3240
agctgggcgt ggtggcacat gcctataatc ccagttactc ggaaggctga ggcaggaaaa 3300
tcacttgaac ccaggaggcg gagattgcag tcagccgaga ttgcaccact gcactccagc 3360
ctgggtaaca cagcgagact ctgtctcaaa aatgaaaata aaaaaaataa aaaaataaaa 3420
aaaaaatatc tcactgtggt cttaggggat gttatttcaa tagtgaacta tgttccctct 3480
gggatcagag caggtgagcc catatccaga gctccaagac tcagtttagg ggaatagatg 3540
gcaaagcaga gaatctagag aagcagccca gggtaggatc tggatggtca cctggagagg 3600
agacctgcag ggaatggatg gctgtcttca tccagaaaga cagagaatat attccactta 3660
caccagaggg cagacaaagc tgcctaaccc tgatggaggt ccagtgagtg cccattgcag 3720
gaagcattca agctgaggct ggatgaacat cgacagggct gttgagaggg agattagatg 3780
gcatttcagg gtcttttccc ttttaagatt ctggcatgga gagctctagt tttccaacca 3840
gcttcattta tcaaatcaac aaaatgattg aaatgatcag agtttgcagg gaagatgatg 3900
acaatgctca ctagcaccca gtttgcatca aattgaatac ctgcattgga ctgaatattc 3960
actaataata cacattgatt ataagtaccc ttggccctag tccccaaggt acctgccagt 4020
aggagcaaag gggaccctgg gagagaccca ggagtctatg caatggaagg acaggtgtta 4080
aatatatata tatatatttt tttgaggtag agtctgactc tgtcacccag gctggagtgc 4140
aatggcgtga tcttggctca ctgcaacctc cacctcctgg gttaaagcaa ttctcctgcc 4200
tcagcctccc gagtagctgg gattataggt gttcactact atccccagct aatttttttt 4260
tttttttttt gagatggagt ctcactctgt cgcccaggct ggagtgcact ggtgcaatct 4320
cggctcactg caacctctgc ctcctgggtt caagcgattc tcctgtctca gcctcctgag 4380
tagctgggat cacaggtgca cgccaccatg cccagctaat tttttgtatt ttagtagaga 4440
cagggtttca ccatgttgcc caggctggtc tcgaactcct gagctcaggc aatctaccca 4500
cctcagcctc ccaaagtgct gggattacag gcgtgagcca ccgcacccgg ctcatcccca 4560
gctaattttt gtatttttag tagagacagg gtttcactat gttggccagg ttggtctcaa 4620
actcctgacc tcagatgata cacccgcctg ggcctctcaa gggctgggat tataggtgtg 4680
agccactaca cctggccagg tgttaaagat ctgagtcata gttcctggtg attctccaat 4740
gtatgaccct caattctcca gtgtctgaac ggctcccagc tgctggtcaa ttttggcttg 4800
agccccgctg ctcctctgac ccctcgtcag tttgctctgc tgtgcccagc cctgctttat 4860
cagatcgaca gccgcgtctg catcggcgct ccggcccctg cacccccagg ggatctacta 4920
tctggtcagc aagtaggagt gggtggggga caccctgaat cctggaagtg gggcccatgc 4980
caaaaaggag gctcactggg gtcctgcctc tccttgtagt gttctctctg ctccacctta 5040
cgtgtgggac cctcctcttg ccctgaccta acttcagccc ctgattctcc ccagccctgc 5100
ttcagagtgc cctggcagtc ctgttgctca gcctcccttc tcccctatcc ctgctgctgc 5160
tgcggctcct gggacctcgt ctactacggc ccttgctggg cttcctgggg gccctggcgg 5220
tgggcactct ttgtggggat gcactgctac atctgctacc gcatgtatgt gaagcccctt 5280
ccttgtaccc ctggcctcca tggatctaag gtgtccccag ccataggaca tcccctccgc 5340
ctttccatca gctcccatat cctactccca gatcctggct tcagcccaca gctgccttct 5400
agtagagcat atgagcgaag gcttgccaca atccatgcaa ggggatgttg ttgggtatag 5460
gggcttccag agtctgccct gaccttctct ctgtcaggca caagaagggc ggcacgcagg 5520
acctggcgga ctaccagaga aggacctggg cccggggctg tcagtgctcg gaggcctctt 5580
cctgctcttt gtgctggaga acatgctggg gcttttgcgg caccgagggc tcaggccagt 5640
gagtgatacc cttttctcct ccttctgctg agaccagagt cccagtcaag aactgggcca 5700
ggccgggcgc ggtggctcac gcctgtaatc ccagcacttt gggagcccaa ggcgggcaga 5760
tcacaaggtt aggagttcga gtccagcctg accaacatgg tgaaaccctg tctctactaa 5820
aaatacaaaa attagctggg cgtggtggtg cgtgtctgta atcccagcta ctcaggaggc 5880
tgaggcagga gaatcgcttg acttgggagg tggaggttgc agcgagctaa gatggcacca 5940
ctgcactcca gcccaggtga cagagcgaga ctccatctca aaaacaacaa caacaacaac 6000
aaaactgggc caaaaagcca agagatgagg agcagtgtgt gctcctggat ctctgacatt 6060
tgcctggtgt gcaggaccta tcggctaaca gggagtgggt aggggctcct taagcacaga 6120
cccaggactt ctggccaaat ggcatcctat tctgagctca agtcaacaag aaacagaggg 6180
gaggtgccaa cttgggaaga aggtagaggc caaagaacat cccaggtgcc agaggtggaa 6240
ccaggtgttc atcttcccag cttgtggcct ggcttcccct tagtccctgg ctctgctgcc 6300
tcctccacca ggagggatgc cctcctattt cagagatgct gcaggcgaaa acgaaggaat 6360
ctcgaaacac gcaacttgga tccggagaat ggcagtggga tggcccttca gcccctacag 6420
gcagctccag gtgactagag gagaaaattt gaagagtagg ttccaagctc acagtcctta 6480
cttgcagcca ccaacactgt cctgtgcttc ttcccgcaga gccaggggct cagggccaga 6540
gggagaagaa cagccagcac ccaccagctc tggcccctcc tgggcaccaa ggccacagtc 6600
atgggcacca gggtggcact gatatcacgt ggatggtcct cctgggagat ggtctacaca 6660
acctcactga tgggctggcc ataggtgtga ggggtgggaa cggagggaag caggtccgag 6720
gggaggccag ggctcctagt tatcagctgg ggctaggaga gggccgtcag gaagatgggg 6780
agaggacggg aggaccacgg aacacaggaa cctgcttctg aggagacttt tcttctggac 6840
tgacaacttc cgaccctgct ggccccaggt gctgccttct ctgatggctt ctccagcggc 6900
ctcagtacca ccttagcggt cttctgccat gagctgcccc acgaactggg taggaatggc 6960
aggagcaggg tggggtggac tccagaaagg agatagctcc aaggggtaga gcttggaggc 7020
tggtgggtgg catggatgag gggcacccca gcttactccc tcccatcctg tcctctgtct 7080
ccaataggtg actttgccat gctgctccag tcagggctgt cctttcggcg gctgctgctg 7140
ctgagcctcg tgtctggagc cctgggattg gggggtgcag tcctgggggt ggggctcagc 7200
ctgggccctg tccccctcac tccctgggtg tttggggtca ctgctggggt cttcctctat 7260
gtggcccttg tggacatggt gagagatgtc gggtagagca gagaaatcaa gggcagtggg 7320
gaggcgggag tggagaggga ggtagcagtc cctccgcctc taccattagc tcctggaagg 7380
gcgtcagacc ataggcccgc aaaagtctga gaaacaaggg actaaggtgt ttgggtgggg 7440
gctgctgatg ctttctgaca ccattcctct ggagttgaga ggtcaggggc aaggccagaa 7500
tcctgacatc ctctttttct ttcagctacc agccctgctt cgtcctccgg agcccctgcc 7560
tacgccccat gtgctcctgc aggggctggg gctgctgctg gggggcggcc tcatgcttgc 7620
cataaccctg ctggaggagc ggctactgcc cgtgaccact gagggctgat ggggccagtg 7680
gaaaggggtc gggttgccct tccttccccc caaccacagg aatggaggcg ggacacaggg 7740
ccagtaggag caataggatt ttaataaaca gaacccatcc caaa 7784
<210> 3
<211> 7784
<212> ДНК
<213> homo sapiens
<400> 3
agctggaacc aagaaggttg tgtccccctt cctctgggtg tccttgtctc ctgctatcag 60
gtaatgccaa cctcaacccc ctggaccagt caccccgatc agactttgct tgcctgattt 120
taggccaggt cagacatcag aggagagccc agatccttgt ttcctctccc cccgcagggc 180
ttcccctttc ttggtcatcg atccctagag ctctggctct ttctcttctt ggggtgagaa 240
actgctaaga acagtttatt tcccatgcat gcatctgggc ttgccactga tctgcctttt 300
cccccctcct ccccaggtta gggacacctg ggtccaacct tcccaaggaa tatggggatg 360
ggggttggag atgaagttta gtgctagact gtaaggtagg tggggtggaa gtacatgagg 420
gaaagggcta aaatggtact aatggtgtta aggatagggt gaattattta agaggaaaaa 480
gactaggccc aggttctcct tagccatgtg gctttcccag ggcagagggt ggcccctccc 540
tacccagggg cccagcagag actgactttt gatccctacc ccagagacca gtgaaccatt 600
aactcctctc ttatgtgagc cttcacacac tggccccacc cctgaccccg ccccaaggca 660
ggtgggctag gagggggtgc atgtccatct cagccttcta tgtgacgtgg cctccgatcc 720
acctggacac ctggaggcta agcctggatt cccccttccc tgactcagga actgcttaac 780
gtctacagca aggcctaata ggggacctga ggtgacagct cttatgttgc cagtaggggt 840
gaggccctgg ggattgaggg gggataaaga ggtggggcaa agttgagggg tggggtttag 900
gggacaagga atggacggtc agctctggat gaagtatgag gagagctctg actcagggag 960
gtgctccagg aaccagcaaa caagaggctg ctcccgcagg aggcagtgtg aagggagaaa 1020
gaaggctgca gtaggggctg ctgctggact cggtggggag caggtgcaag gagctctggc 1080
tcccccatgg acctgagctg gagagcagag cgcagctcca gcccattcct cattcttcca 1140
gggcacagtc ctcaggatgt ttcggggaga ataggagcca gaacctgagc ccctaagcta 1200
ttcccctcac caatgatggg gtccccagtg agtcatctgc tggccggctt ctgtgtgtgg 1260
gtcgtcttgg gctgggtagg gggctcagtc cccaacctgg gccctgctga gcaggagcag 1320
aaccattacc tggcccagct gtttggcctg tagggcgaga atgggacgct gactgcaggg 1380
ggcttggcgc ggcttctcca cagcctgggg ctaggccgag ttcaggggct tcgcctggga 1440
cagcatgggc ctctgactgg acgggctgca tccccagctg cagacaattc cacacacagg 1500
tactgacccc ttcctccact ccacagggcc acatctccca ggtcctctca gtgcttgccc 1560
ccagttgcct cgttctggct tcctcacgag atccctggag ttacaaattc ttcagaaccg 1620
agctccttgg tatctcttca aaacctctca tgcttctatt gccttctctc tcttttcttg 1680
agactggggg tctcgctttg tcacccaggc taaagtgcag tgacacattc acggctcact 1740
gcaacctctg cttcccaggc tgaagccatc ctcccacctc agcctcctga gcagctggga 1800
ccataggcac acaccaccac agccggctaa ttttaaaaat tttttacaga gacaagggtt 1860
tcgctgtgtt gcccaggctg gtctcaaact cctgggctca gctcagcgat ctgcctgcct 1920
cagcttccca aagtgctggg actacagatg tgaactacca ccctagccct ccgttgcctt 1980
ctaattctct cctcctccaa atctctaagc ccttaaattt cttgctctta gtatcactgt 2040
tcagtgtctc tgggctgatt tggctccaaa ttcgtagact tcttttttct tttcttttct 2100
tttttttttt tttttttttt tgagacagag tctcgctctg tcgcccaggc tggagtgcag 2160
tggtgtgatc ttggctcact gtaacctctg cctccccggt tcaagcgatt ctcctgcctc 2220
ggcctcctga gtagctggga ttacaggcac acaccaccac gccgggctaa tttttgcaat 2280
tttagtagag acggggtttc accattttgg tcaggctggt ctcgaacttc caacctcagg 2340
tgatccaccc acctcagcct cccaaagtgc tgggattaca ggcgtgagcc accgtgccca 2400
gccattcgta gcccttttgg ttgtcgtcct tttttttctg tcccccccag tggcagaaaa 2460
tggacaactc acagatcttc ctaagaatga cattccatgg tttctgggtc ccaggatctc 2520
cagtcagtgg ctagtccccc cattccccct aaaatccctg ggagcctctc aaagcgggtt 2580
gatagagaac acaagggagg ctgacttgct gtctcatcca ttccaggcca cagaaccctg 2640
agctgagtgt ggatgtctgg gcagggatgc ctctgggtcc ctcagggtgg ggtgacctgg 2700
aagagtcaaa ggcccctcac ctaccccgtg ggccagcccc ctcgggcctg gacctccttc 2760
acaggcttct gttgctggac cactcattgg ctgaccacct gaatgaggat gtgagtctga 2820
cggtctctag aggggaagga gccatgggat tagatggcct gaaatgttta aataatcagt 2880
agttttttgt tttgttttgt ttttaaatcc caacgtggac caagcgtggt ggctcacgcc 2940
tgtaatccca acactttggg aggccgaggt gggtggatca cctgaggtca ggagttcgag 3000
accagcctgg ccaacatggt gaaaccccat ctctactaaa aaatacaaaa attagccggg 3060
tgtggtaaca ggtgtgtgta atcctagcta ctcaggaggc tgaggtgaga aaattgcttg 3120
aacttgggag gcagaggttg cagtgagcca agatggcacc atttgcactc cagcctgggc 3180
aacaagaggg agactctgtc tcaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaat 3240
agctgggcgt ggtggcacat gcctataatc ccagttactc ggaaggctga ggcaggaaaa 3300
tcacttgaac ccaggaggcg gagattgcag tcagccgaga ttgcaccact gcactccagc 3360
ctgggtaaca cagcgagact ctgtctcaaa aatgaaaata aaaaaaataa aaaaataaaa 3420
aaaaaatatc tcactgtggt cttaggggat gttatttcaa tagtgaacta tgttccctct 3480
gggatcagag caggtgagcc catatccaga gctccaagac tcagtttagg ggaatagatg 3540
gcaaagcaga gaatctagag aagcagccca gggtaggatc tggatggtca cctggagagg 3600
agacctgcag ggaatggatg gctgtcttca tccagaaaga cagagaatat attccactta 3660
caccagaggg cagacaaagc tgcctaaccc tgatggaggt ccagtgagtg cccattgcag 3720
gaagcattca agctgaggct ggatgaacat cgacagggct gttgagaggg agattagatg 3780
gcatttcagg gtcttttccc ttttaagatt ctggcatgga gagctctagt tttccaacca 3840
gcttcattta tcaaatcaac aaaatgattg aaatgatcag agtttgcagg gaagatgatg 3900
acaatgctca ctagcaccca gtttgcatca aattgaatac ctgcattgga ctgaatattc 3960
actaataata cacattgatt ataagtaccc ttggccctag tccccaaggt acctgccagt 4020
aggagcaaag gggaccctgg gagagaccca ggagtctatg caatggaagg acaggtgtta 4080
aatatatata tatatatttt tttgaggtag agtctgactc tgtcacccag gctggagtgc 4140
aatggcgtga tcttggctca ctgcaacctc cacctcctgg gttaaagcaa ttctcctgcc 4200
tcagcctccc gagtagctgg gattataggt gttcactact atccccagct aatttttttt 4260
tttttttttt gagatggagt ctcactctgt cgcccaggct ggagtgcact ggtgcaatct 4320
cggctcactg caacctctgc ctcctgggtt caagcgattc tcctgtctca gcctcctgag 4380
tagctgggat cacaggtgca cgccaccatg cccagctaat tttttgtatt ttagtagaga 4440
cagggtttca ccatgttgcc caggctggtc tcgaactcct gagctcaggc aatctaccca 4500
cctcagcctc ccaaagtgct gggattacag gcgtgagcca ccgcacccgg ctcatcccca 4560
gctaattttt gtatttttag tagagacagg gtttcactat gttggccagg ttggtctcaa 4620
actcctgacc tcagatgata cacccgcctg ggcctctcaa gggctgggat tataggtgtg 4680
agccactaca cctggccagg tgttaaagat ctgagtcata gttcctggtg attctccaat 4740
gtatgaccct caattctcca gtgtctgaac ggctcccagc tgctggtcaa ttttggcttg 4800
agccccgctg ctcctctgac ccctcgtcag tttgctctgc tgtgcccagc cctgctttat 4860
cagatcgaca gccgcgtctg catcggcgct ccggcccctg cacccccagg ggatctacta 4920
tctggtcagc aagtaggagt gggtggggga caccctgaat cctggaagtg gggcccatgc 4980
caaaaaggag gctcactggg gtcctgcctc tccttgtagt gttctctctg ctccacctta 5040
cgtgtgggac cctcctcttg ccctgaccta acttcagccc ctgattctcc ccagccctgc 5100
ttcagagtgc cctggcagtc ctgttgctca gcctcccttc tcccctatcc ctgctgctgc 5160
tgcggctcct gggacctcgt ctactacggc ccttgctggg cttcctgggg gccctggcgg 5220
tgggcactct ttgtggggat gcactgctac atctgctacc gcatgtatgt gaagcccctt 5280
ccttgtaccc ctggcctcca tggatctaag gtgtccccag ccataggaca tcccctccgc 5340
ctttccatca gctcccatat cctactccca gatcctggct tcagcccaca gctgccttct 5400
agtagagcat atgagcgaag gcttgccaca atccatgcaa ggggatgttg ttgggtatag 5460
gggcttccag agtctgccct gaccttctct ctgtcaggca caagaagggc ggcacgcagg 5520
acctggcgga ctaccagaga aggacctggg cccggggctg tcagtgctcg gaggcctctt 5580
cctgctcttt gtgctggaga acatgctggg gcttttgcgg caccgagggc tcaggccagt 5640
gagtgatacc cttttctcct ccttctgctg agaccagagt cccagtcaag aactgggcca 5700
ggccgggcgc ggtggctcac gcctgtaatc ccagcacttt gggagcccaa ggcgggcaga 5760
tcacaaggtt aggagttcga gtccagcctg accaacatgg tgaaaccctg tctctactaa 5820
aaatacaaaa attagctggg cgtggtggtg cgtgtctgta atcccagcta ctcaggaggc 5880
tgaggcagga gaatcgcttg acttgggagg tggaggttgc agcgagctaa gatggcacca 5940
ctgcactcca gcccaggtga cagagcgaga ctccatctca aaaacaacaa caacaacaac 6000
aaaactgggc caaaaagcca agagatgagg agcagtgtgt gctcctggat ctctgacatt 6060
tgcctggtgt gcaggaccta tcggctaaca gggagtgggt aggggctcct taagcacaga 6120
cccaggactt ctggccaaat ggcatcctat tctgagctca agtcaacaag aaacagaggg 6180
gaggtgccaa cttgggaaga aggtagaggc caaagaacat cccaggtgcc agaggtggaa 6240
ccaggtgttc atcttcccag cttgtggcct ggcttcccct tagtccctgg ctctgctgcc 6300
tcctccacca ggagggatgc cctcctattt cagagatgct gcaggcgaaa acgaaggaat 6360
ctcgaaacac gcaacttgga tccggagaat ggcagtggga tggcccttca gcccctacag 6420
gcagctccag gtgactagag gagaaaattt gaagagtagg ttccaagctc acagtcctta 6480
cttgcagcca ccaacactgt cctgtgcttc ttcccgcaga gccaggggct cagggccaga 6540
gggagaagaa cagccagcac ccaccagctc tggcccctcc tgggcaccaa ggccacagtc 6600
atgggcacca gggtggcact gatatcacgt ggatggtcct cctgggagat ggtctacaca 6660
acctcactga tgggctggcc ataggtgtga ggggtgggaa cggagggaag caggtccgag 6720
gggaggccag ggctcctagt tatcagctgg ggctaggaga gggccgtcag gaagatgggg 6780
agaggacggg aggaccacgg aacacaggaa cctgcttctg aggagacttt tcttctggac 6840
tgacaacttc cgaccctgct ggccccaggt gctgccttct ctgatggctt ctccagcggc 6900
ctcagtacca ccttagcggt cttctgccat gagctgcccc acgaactggg taggaatggc 6960
aggagcaggg tggggtggac tccagaaagg agatagctcc aaggggtaga gcttggaggc 7020
tggtgggtgg catggatgag gggcacccca gcttactccc tcccatcctg tcctctgtct 7080
ccaataggtg actttgccat gctgctccag tcagggctgt cctttcggcg gctgctgctg 7140
ctgagcctcg tgtctggagc cctgggattg gggggtgcag tcctgggggt ggggctcagc 7200
ctgggccctg tccccctcac tccctgggtg tttggggtca ctgctggggt cttcctctat 7260
gtggcccttg tggacatggt gagagatgtc gggtagagca gagaaatcaa gggcagtggg 7320
gaggcgggag tggagaggga ggtagcagtc cctccgcctc taccattagc tcctggaagg 7380
gcgtcagacc ataggcccgc aaaagtctga gaaacaaggg actaaggtgt ttgggtgggg 7440
gctgctgatg ctttctgaca ccattcctct ggagttgaga ggtcaggggc aaggccagaa 7500
tcctgacatc ctctttttct ttcagctacc agccctgctt cgtcctccgg agcccctgcc 7560
tacgccccat gtgctcctgc aggggctggg gctgctgctg gggggcggcc tcatgcttgc 7620
cataaccctg ctggaggagc ggctactgcc cgtgaccact gagggctgat ggggccagtg 7680
gaaaggggtc gggttgccct tccttccccc caaccacagg aatggaggcg ggacacaggg 7740
ccagtaggag caataggatt ttaataaaca gaacccatcc caaa 7784
<210> 4
<211> 7784
<212> ДНК
<213> homo sapiens
<400> 4
agctggaacc aagaaggttg tgtccccctt cctctgggtg tccttgtctc ctgctatcag 60
gtaatgccaa cctcaacccc ctggaccagt caccccgatc agactttgct tgcctgattt 120
taggccaggt cagacatcag aggagagccc agatccttgt ttcctctccc cccgcagggc 180
ttcccctttc ttggtcatcg atccctagag ctctggctct ttctcttctt ggggtgagaa 240
actgctaaga acagtttatt tcccatgcat gcatctgggc ttgccactga tctgcctttt 300
cccccctcct ccccaggtta gggacacctg ggtccaacct tcccaaggaa tatggggatg 360
ggggttggag atgaagttta gtgctagact gtaaggtagg tggggtggaa gtacatgagg 420
gaaagggcta aaatggtact aatggtgtta aggatagggt gaattattta agaggaaaaa 480
gactaggccc aggttctcct tagccatgtg gctttcccag ggcagagggt ggcccctccc 540
tacccagggg cccagcagag actgactttt gatccctacc ccagagacca gtgaaccatt 600
aactcctctc ttatgtgagc cttcacacac tggccccacc cctgaccccg ccccaaggca 660
ggtgggctag gagggggtgc atgtccatct cagccttcta tgtgacgtgg cctccgatcc 720
acctggacac ctggaggcta agcctggatt cccccttccc tgactcagga actgcttaac 780
gtctacagca aggcctaata ggggacctga ggtgacagct cttatgttgc cagtaggggt 840
gaggccctgg ggattgaggg gggataaaga ggtggggcaa agttgagggg tggggtttag 900
gggacaagga atggacggtc agctctggat gaagtatgag gagagctctg actcagggag 960
gtgctccagg aaccagcaaa caagaggctg ctcccgcagg aggcagtgtg aagggagaaa 1020
gaaggctgca gtaggggctg ctgctggact cggtggggag caggtgcaag gagctctggc 1080
tcccccatgg acctgagctg gagagcagag cgcagctcca gcccattcct cattcttcca 1140
gggcacagtc ctcaggatgt ttcggggaga ataggagcca gaacctgagc ccctaagcta 1200
ttcccctcac caatgatggg gtccccagtg agtcatctgc tggccggctt ctgtgtgtgg 1260
gtcgtcttgg gctgggtagg gggctcagtc cccaacctgg gccctgctga gcaggagcag 1320
aaccattacc tggcccagct gtttggcctg tacggcgaga atgggacgct gactgcaggg 1380
ggcttggcgc ggcttctcca cagcctgggg ctaggccgag ttcaggggct tcgcctggga 1440
cagcatgggc ctctgactgg acgggctgca tccccagctg cagacaattc cacacacagg 1500
tactgacccc ttcctccact ccacagggcc acatctccca ggtcctctca gtgcttgccc 1560
ccagttgcct cgttctggct tcctcacgag atccctggag ttacaaattc ttcagaaccg 1620
agctccttgg tatctcttca aaacctctca tgcttctatt gccttctctc tcttttcttg 1680
agactggggg tctcgctttg tcacccaggc taaagtgcag tgacacattc acggctcact 1740
gcaacctctg cttcccaggc tgaagccatc ctcccacctc agcctcctga gcagctggga 1800
ccataggcac acaccaccac agccggctaa ttttaaaaat tttttacaga gacaagggtt 1860
tcgctgtgtt gcccaggctg gtctcaaact cctgggctca gctcagcgat ctgcctgcct 1920
cagcttccca aagtgctggg actacagatg tgaactacca ccctagccct ccgttgcctt 1980
ctaattctct cctcctccaa atctctaagc ccttaaattt cttgctctta gtatcactgt 2040
tcagtgtctc tgggctgatt tggctccaaa ttcgtagact tcttttttct tttcttttct 2100
tttttttttt tttttttttt tgagacagag tctcgctctg tcgcccaggc tggagtgcag 2160
tggtgtgatc ttggctcact gtaacctctg cctccccggt tcaagcgatt ctcctgcctc 2220
ggcctcctga gtagctggga ttacaggcac acaccaccac gccgggctaa tttttgcaat 2280
tttagtagag acggggtttc accattttgg tcaggctggt ctcgaacttc caacctcagg 2340
tgatccaccc acctcagcct cccaaagtgc tgggattaca ggcgtgagcc accgtgccca 2400
gccattcgta gcccttttgg ttgtcgtcct tttttttctg tcccccccag tggcagaaaa 2460
tggacaactc acagatcttc ctaagaatga cattccatgg tttctgggtc ccaggatctc 2520
cagtcagtgg ctagtccccc cattccccct aaaatccctg ggagcctctc aaagcgggtt 2580
gatagagaac acaagggagg ctgacttgct gtctcatcca ttccaggcca cagaaccctg 2640
agctgagtgt ggatgtctgg gcagggatgc ctctgggtcc ctcagggtgg ggtgacctgg 2700
aagagtcaaa ggcccctcac ctaccccgtg ggccagcccc ctcgggcctg gacctccttc 2760
acaggcttct gttgctggac cactcattgg ctgaccacct gaatgaggat gtgagtctga 2820
cggtctctag aggggaagga gccatgggat tagatggcct gaaatgttta aataatcagt 2880
agttttttgt tttgttttgt ttttaaatcc caacgtggac caagcgtggt ggctcacgcc 2940
tgtaatccca acactttggg aggccgaggt gggtggatca cctgaggtca ggagttcgag 3000
accagcctgg ccaacatggt gaaaccccat ctctactaaa aaatacaaaa attagccggg 3060
tgtggtaaca ggtgtgtgta atcctagcta ctcaggaggc tgaggtgaga aaattgcttg 3120
aacttgggag gcagaggttg cagtgagcca agatggcacc atttgcactc cagcctgggc 3180
aacaagaggg agactctgtc tcaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaat 3240
agctgggcgt ggtggcacat gcctataatc ccagttactc ggaaggctga ggcaggaaaa 3300
tcacttgaac ccaggaggcg gagattgcag tcagccgaga ttgcaccact gcactccagc 3360
ctgggtaaca cagcgagact ctgtctcaaa aatgaaaata aaaaaaataa aaaaataaaa 3420
aaaaaatatc tcactgtggt cttaggggat gttatttcaa tagtgaacta tgttccctct 3480
gggatcagag caggtgagcc catatccaga gctccaagac tcagtttagg ggaatagatg 3540
gcaaagcaga gaatctagag aagcagccca gggtaggatc tggatggtca cctggagagg 3600
agacctgcag ggaatggatg gctgtcttca tccagaaaga cagagaatat attccactta 3660
caccagaggg cagacaaagc tgcctaaccc tgatggaggt ccagtgagtg cccattgcag 3720
gaagcattca agctgaggct ggatgaacat cgacagggct gttgagaggg agattagatg 3780
gcatttcagg gtcttttccc ttttaagatt ctggcatgga gagctctagt tttccaacca 3840
gcttcattta tcaaatcaac aaaatgattg aaatgatcag agtttgcagg gaagatgatg 3900
acaatgctca ctagcaccca gtttgcatca aattgaatac ctgcattgga ctgaatattc 3960
actaataata cacattgatt ataagtaccc ttggccctag tccccaaggt acctgccagt 4020
aggagcaaag gggaccctgg gagagaccca ggagtctatg caatggaagg acaggtgtta 4080
aatatatata tatatatttt tttgaggtag agtctgactc tgtcacccag gctggagtgc 4140
aatggcgtga tcttggctca ctgcaacctc cacctcctgg gttaaagcaa ttctcctgcc 4200
tcagcctccc gagtagctgg gattataggt gttcactact atccccagct aatttttttt 4260
tttttttttt gagatggagt ctcactctgt cgcccaggct ggagtgcact ggtgcaatct 4320
cggctcactg caacctctgc ctcctgggtt caagcgattc tcctgtctca gcctcctgag 4380
tagctgggat cacaggtgca cgccaccatg cccagctaat tttttgtatt ttagtagaga 4440
cagggtttca ccatgttgcc caggctggtc tcgaactcct gagctcaggc aatctaccca 4500
cctcagcctc ccaaagtgct gggattacag gcgtgagcca ccgcacccgg ctcatcccca 4560
gctaattttt gtatttttag tagagacagg gtttcactat gttggccagg ttggtctcaa 4620
actcctgacc tcagatgata cacccgcctg ggcctctcaa gggctgggat tataggtgtg 4680
agccactaca cctggccagg tgttaaagat ctgagtcata gttcctggtg attctccaat 4740
gtatgaccct caattctcca gtgtctgaac ggctcccagc tgctggtcaa ttttggcttg 4800
agccccgctg ctcctctgac ccctcgtcag tttgctctgc tgtgcccagc cctgctttat 4860
cagatcgaca gccgcgtctg catcggcgct ccggcccctg cacccccagg ggatctacta 4920
tctggtcagc aagtaggagt gggtggggga caccctgaat cctggaagtg gggcccatgc 4980
caaaaaggag gctcactggg gtcctgcctc tccttgtagt gttctctctg ctccacctta 5040
cgtgtgggac cctcctcttg ccctgaccta acttcagccc ctgattctcc ccagccctgc 5100
ttcagagtgc cctggcagtc ctgttgctca gcctcccttc tcccctatcc ctgctgctgc 5160
tgcggctcct gggacctcgt ctactacggc ccttgctggg cttcctgggg gccctggcgg 5220
tgggcactct ttgtggggat gcactgctac atctgctacc gcatgtatgt gaagcccctt 5280
ccttgtaccc ctggcctcca tggatctaag gtgtccccag ccataggaca tcccctccgc 5340
ctttccatca gctcccatat cctactccca gatcctggct tcagcccaca gctgccttct 5400
agtagagcat atgagcgaag gcttgccaca atccatgcaa ggggatgttg ttgggtatag 5460
gggcttccag agtctgccct gaccttctct ctgtcaggca caagaagggc ggcacgcagg 5520
acctggcgga ctaccagaga aggacctggg cccggggctg tcagtgctcg gaggcctctt 5580
cctgctcttt gtgctggaga acacgctggg gcttttgcgg caccgagggc tcaggccagt 5640
gagtgatacc cttttctcct ccttctgctg agaccagagt cccagtcaag aactgggcca 5700
ggccgggcgc ggtggctcac gcctgtaatc ccagcacttt gggagcccaa ggcgggcaga 5760
tcacaaggtt aggagttcga gtccagcctg accaacatgg tgaaaccctg tctctactaa 5820
aaatacaaaa attagctggg cgtggtggtg cgtgtctgta atcccagcta ctcaggaggc 5880
tgaggcagga gaatcgcttg acttgggagg tggaggttgc agcgagctaa gatggcacca 5940
ctgcactcca gcccaggtga cagagcgaga ctccatctca aaaacaacaa caacaacaac 6000
aaaactgggc caaaaagcca agagatgagg agcagtgtgt gctcctggat ctctgacatt 6060
tgcctggtgt gcaggaccta tcggctaaca gggagtgggt aggggctcct taagcacaga 6120
cccaggactt ctggccaaat ggcatcctat tctgagctca agtcaacaag aaacagaggg 6180
gaggtgccaa cttgggaaga aggtagaggc caaagaacat cccaggtgcc agaggtggaa 6240
ccaggtgttc atcttcccag cttgtggcct ggcttcccct tagtccctgg ctctgctgcc 6300
tcctccacca ggagggatgc cctcctattt cagagatgct gcaggcgaaa acgaaggaat 6360
ctcgaaacac gcaacttgga tccggagaat ggcagtggga tggcccttca gcccctacag 6420
gcagctccag gtgactagag gagaaaattt gaagagtagg ttccaagctc acagtcctta 6480
cttgcagcca ccaacactgt cctgtgcttc ttcccgcaga gccaggggct cagggccaga 6540
gggagaagaa cagccagcac ccaccagctc tggcccctcc tgggcaccaa ggccacagtc 6600
atgggcacca gggtggcact gatatcacgt ggatggtcct cctgggagat ggtctacaca 6660
acctcactga tgggctggcc ataggtgtga ggggtgggaa cggagggaag caggtccgag 6720
gggaggccag ggctcctagt tatcagctgg ggctaggaga gggccgtcag gaagatgggg 6780
agaggacggg aggaccacgg aacacaggaa cctgcttctg aggagacttt tcttctggac 6840
tgacaacttc cgaccctgct ggccccaggt gctgccttct ctgatggctt ctccagcggc 6900
ctcagtacca ccttagcggt cttctgccat gagctgcccc acgaactggg taggaatggc 6960
aggagcaggg tggggtggac tccagaaagg agatagctcc aaggggtaga gcttggaggc 7020
tggtgggtgg catggatgag gggcacccca gcttactccc tcccatcctg tcctctgtct 7080
ccaataggtg actttgccat gctgctccag tcagggctgt cctttcggcg gctgctgctg 7140
ctgagcctcg tgtctggagc cctgggattg gggggtgcag tcctgggggt ggggctcagc 7200
ctgggccctg tccccctcac tccctgggtg tttggggtca ctgctggggt cttcctctat 7260
gtggcccttg tggacatggt gagagatgtc gggtagagca gagaaatcaa gggcagtggg 7320
gaggcgggag tggagaggga ggtagcagtc cctccgcctc taccattagc tcctggaagg 7380
gcgtcagacc ataggcccgc aaaagtctga gaaacaaggg actaaggtgt ttgggtgggg 7440
gctgctgatg ctttctgaca ccattcctct ggagttgaga ggtcaggggc aaggccagaa 7500
tcctgacatc ctctttttct ttcagctacc agccctgctt cgtcctccgg agcccctgcc 7560
tacgccccat gtgctcctgc aggggctggg gctgctgctg gggggcggcc tcatgcttgc 7620
cataaccctg ctggaggagc ggctactgcc cgtgaccact gagggctgat ggggccagtg 7680
gaaaggggtc gggttgccct tccttccccc caaccacagg aatggaggcg ggacacaggg 7740
ccagtaggag caataggatt ttaataaaca gaacccatcc caaa 7784
<210> 5
<211> 7784
<212> ДНК
<213> homo sapiens
<400> 5
agctggaacc aagaaggttg tgtccccctt cctctgggtg tccttgtctc ctgctatcag 60
gtaatgccaa cctcaacccc ctggaccagt caccccgatc agactttgct tgcctgattt 120
taggccaggt cagacatcag aggagagccc agatccttgt ttcctctccc cccgcagggc 180
ttcccctttc ttggtcatcg atccctagag ctctggctct ttctcttctt ggggtgagaa 240
actgctaaga acagtttatt tcccatgcat gcatctgggc ttgccactga tctgcctttt 300
cccccctcct ccccaggtta gggacacctg ggtccaacct tcccaaggaa tatggggatg 360
ggggttggag atgaagttta gtgctagact gtaaggtagg tggggtggaa gtacatgagg 420
gaaagggcta aaatggtact aatggtgtta aggatagggt gaattattta agaggaaaaa 480
gactaggccc aggttctcct tagccatgtg gctttcccag ggcagagggt ggcccctccc 540
tacccagggg cccagcagag actgactttt gatccctacc ccagagacca gtgaaccatt 600
aactcctctc ttatgtgagc cttcacacac tggccccacc cctgaccccg ccccaaggca 660
ggtgggctag gagggggtgc atgtccatct cagccttcta tgtgacgtgg cctccgatcc 720
acctggacac ctggaggcta agcctggatt cccccttccc tgactcagga actgcttaac 780
gtctacagca aggcctaata ggggacctga ggtgacagct cttatgttgc cagtaggggt 840
gaggccctgg ggattgaggg gggataaaga ggtggggcaa agttgagggg tggggtttag 900
gggacaagga atggacggtc agctctggat gaagtatgag gagagctctg actcagggag 960
gtgctccagg aaccagcaaa caagaggctg ctcccgcagg aggcagtgtg aagggagaaa 1020
gaaggctgca gtaggggctg ctgctggact cggtggggag caggtgcaag gagctctggc 1080
tcccccatgg acctgagctg gagagcagag cgcagctcca gcccattcct cattcttcca 1140
gggcacagtc ctcaggatgt ttcggggaga ataggagcca gaacctgagc ccctaagcta 1200
ttcccctcac caatgatggg gtccccagtg agtcatctgc tggccggctt ctgtgtgtgg 1260
gtcgtcttgg gctgggtagg gggctcagtc cccaacctgg gccctgctga gcaggagcag 1320
aaccattacc tggcccagct gtttggcctg tacggcgaga atgggacgct gactgcaggg 1380
ggcttggcgc ggcttctcca cagcctgggg ctaggccgag ttcaggggct tcgcctggga 1440
cagcatgggc ctctgactgg acgggctgca tccccagctg cagacaattc cacacacagg 1500
tactgacccc ttcctccact ccacagggcc acatctccca ggtcctctca gtgcttgccc 1560
ccagttgcct cgttctggct tcctcacgag atccctggag ttacaaattc ttcagaaccg 1620
agctccttgg tatctcttca aaacctctca tgcttctatt gccttctctc tcttttcttg 1680
agactggggg tctcgctttg tcacccaggc taaagtgcag tgacacattc acggctcact 1740
gcaacctctg cttcccaggc tgaagccatc ctcccacctc agcctcctga gcagctggga 1800
ccataggcac acaccaccac agccggctaa ttttaaaaat tttttacaga gacaagggtt 1860
tcgctgtgtt gcccaggctg gtctcaaact cctgggctca gctcagcgat ctgcctgcct 1920
cagcttccca aagtgctggg actacagatg tgaactacca ccctagccct ccgttgcctt 1980
ctaattctct cctcctccaa atctctaagc ccttaaattt cttgctctta gtatcactgt 2040
tcagtgtctc tgggctgatt tggctccaaa ttcgtagact tcttttttct tttcttttct 2100
tttttttttt tttttttttt tgagacagag tctcgctctg tcgcccaggc tggagtgcag 2160
tggtgtgatc ttggctcact gtaacctctg cctccccggt tcaagcgatt ctcctgcctc 2220
ggcctcctga gtagctggga ttacaggcac acaccaccac gccgggctaa tttttgcaat 2280
tttagtagag acggggtttc accattttgg tcaggctggt ctcgaacttc caacctcagg 2340
tgatccaccc acctcagcct cccaaagtgc tgggattaca ggcgtgagcc accgtgccca 2400
gccattcgta gcccttttgg ttgtcgtcct tttttttctg tcccccccag tggcagaaaa 2460
tggacaactc acagatcttc ctaagaatga cattccatgg tttctgggtc ccaggatctc 2520
cagtcagtgg ctagtccccc cattccccct aaaatccctg ggagcctctc aaagcgggtt 2580
gatagagaac acaagggagg ctgacttgct gtctcatcca ttccaggcca cagaaccctg 2640
agctgagtgt ggatgtctgg gcagggatgc ctctgggtcc ctcagggtgg ggtgacctgg 2700
aagagtcaaa ggcccctcac ctaccccgtg ggccagcccc ctcgggcctg gacctccttc 2760
acaggcttct gttgctggac cactcattgg ctgaccacct gaatgaggat gtgagtctga 2820
cggtctctag aggggaagga gccatgggat tagatggcct gaaatgttta aataatcagt 2880
agttttttgt tttgttttgt ttttaaatcc caacgtggac caagcgtggt ggctcacgcc 2940
tgtaatccca acactttggg aggccgaggt gggtggatca cctgaggtca ggagttcgag 3000
accagcctgg ccaacatggt gaaaccccat ctctactaaa aaatacaaaa attagccggg 3060
tgtggtaaca ggtgtgtgta atcctagcta ctcaggaggc tgaggtgaga aaattgcttg 3120
aacttgggag gcagaggttg cagtgagcca agatggcacc atttgcactc cagcctgggc 3180
aacaagaggg agactctgtc tcaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaat 3240
agctgggcgt ggtggcacat gcctataatc ccagttactc ggaaggctga ggcaggaaaa 3300
tcacttgaac ccaggaggcg gagattgcag tcagccgaga ttgcaccact gcactccagc 3360
ctgggtaaca cagcgagact ctgtctcaaa aatgaaaata aaaaaaataa aaaaataaaa 3420
aaaaaatatc tcactgtggt cttaggggat gttatttcaa tagtgaacta tgttccctct 3480
gggatcagag caggtgagcc catatccaga gctccaagac tcagtttagg ggaatagatg 3540
gcaaagcaga gaatctagag aagcagccca gggtaggatc tggatggtca cctggagagg 3600
agacctgcag ggaatggatg gctgtcttca tccagaaaga cagagaatat attccactta 3660
caccagaggg cagacaaagc tgcctaaccc tgatggaggt ccagtgagtg cccattgcag 3720
gaagcattca agctgaggct ggatgaacat cgacagggct gttgagaggg agattagatg 3780
gcatttcagg gtcttttccc ttttaagatt ctggcatgga gagctctagt tttccaacca 3840
gcttcattta tcaaatcaac aaaatgattg aaatgatcag agtttgcagg gaagatgatg 3900
acaatgctca ctagcaccca gtttgcatca aattgaatac ctgcattgga ctgaatattc 3960
actaataata cacattgatt ataagtaccc ttggccctag tccccaaggt acctgccagt 4020
aggagcaaag gggaccctgg gagagaccca ggagtctatg caatggaagg acaggtgtta 4080
aatatatata tatatatttt tttgaggtag agtctgactc tgtcacccag gctggagtgc 4140
aatggcgtga tcttggctca ctgcaacctc cacctcctgg gttaaagcaa ttctcctgcc 4200
tcagcctccc gagtagctgg gattataggt gttcactact atccccagct aatttttttt 4260
tttttttttt gagatggagt ctcactctgt cgcccaggct ggagtgcact ggtgcaatct 4320
cggctcactg caacctctgc ctcctgggtt caagcgattc tcctgtctca gcctcctgag 4380
tagctgggat cacaggtgca cgccaccatg cccagctaat tttttgtatt ttagtagaga 4440
cagggtttca ccatgttgcc caggctggtc tcgaactcct gagctcaggc aatctaccca 4500
cctcagcctc ccaaagtgct gggattacag gcgtgagcca ccgcacccgg ctcatcccca 4560
gctaattttt gtatttttag tagagacagg gtttcactat gttggccagg ttggtctcaa 4620
actcctgacc tcagatgata cacccgcctg ggcctctcaa gggctgggat tataggtgtg 4680
agccactaca cctggccagg tgttaaagat ctgagtcata gttcctggtg attctccaat 4740
gtatgaccct caattctcca gtgtctgaac ggctcccagc tgctggtcaa ttttggcttg 4800
agccccgctg ctcctctgac ccctcgtcag tttgctctgc tgtgcccagc cctgctttat 4860
cagatcgaca gccgcgtctg catcggcgct ccggcccctg cacccccagg ggatctacta 4920
tctggtcagc aagtaggagt gggtggggga caccctgaat cctggaagtg gggcccatgc 4980
caaaaaggag gctcactggg gtcctgcctc tccttgtagt gttctctctg ctccacctta 5040
cgtgtgggac cctcctcttg ccctgaccta acttcagccc ctgattctcc ccagccctgc 5100
ttcagagtgc cctggcagtc ctgttgctca gcctcccttc tcccctatcc ctgctgctgc 5160
tgcggctcct gggacctcgt ctactacggc ccttgctggg cttcctgggg gccctggcgg 5220
tgggcactct ttgtggggat gcactgctac atctgctacc gcatgtatgt gaagcccctt 5280
ccttgtaccc ctggcctcca tggatctaag gtgtccccag ccataggaca tcccctccgc 5340
ctttccatca gctcccatat cctactccca gatcctggct tcagcccaca gctgccttct 5400
agtagagcat atgagcgaag gcttgccaca atccatgcaa ggggatgttg ttgggtatag 5460
gggcttccag agtctgccct gaccttctct ctgtcaggca caagaagggc ggcacgcagg 5520
acctggcgga ctaccagaga aggacctggg cccggggctg tcagtgctcg gaggcctctt 5580
cctgctcttt gtgctggaga acatgctggg gcttttgcgg caccgagggc tcaggccagt 5640
gagtgatacc cttttctcct ccttctgctg agaccagagt cccagtcaag aactgggcca 5700
ggccgggcgc ggtggctcac gcctgtaatc ccagcacttt gggagcccaa ggcgggcaga 5760
tcacaaggtt aggagttcga gtccagcctg accaacatgg tgaaaccctg tctctactaa 5820
aaatacaaaa attagctggg cgtggtggtg cgtgtctgta atcccagcta ctcaggaggc 5880
tgaggcagga gaatcgcttg acttgggagg tggaggttgc agcgagctaa gatggcacca 5940
ctgcactcca gcccaggtga cagagcgaga ctccatctca aaaacaacaa caacaacaac 6000
aaaactgggc caaaaagcca agagatgagg agcagtgtgt gctcctggat ctctgacatt 6060
tgcctggtgt gcaggaccta tcggctaaca gggagtgggt aggggctcct taagcacaga 6120
cccaggactt ctggccaaat ggcatcctat tctgagctca agtcaacaag aaacagaggg 6180
gaggtgccaa cttgggaaga aggtagaggc caaagaacat cccaggtgcc agaggtggaa 6240
ccaggtgttc atcttcccag cttgtggcct ggcttcccct tagtccctgg ctctgctgcc 6300
tcctccacca ggagggatgc cctcctattt cagagatgct gcaggcgaaa atgaaggaat 6360
ctcgaaacac gcaacttgga tccggagaat ggcagtggga tggcccttca gcccctacag 6420
gcagctccag gtgactagag gagaaaattt gaagagtagg ttccaagctc acagtcctta 6480
cttgcagcca ccaacactgt cctgtgcttc ttcccgcaga gccaggggct cagggccaga 6540
gggagaagaa cagccagcac ccaccagctc tggcccctcc tgggcaccaa ggccacagtc 6600
atgggcacca gggtggcact gatatcacgt ggatggtcct cctgggagat ggtctacaca 6660
acctcactga tgggctggcc ataggtgtga ggggtgggaa cggagggaag caggtccgag 6720
gggaggccag ggctcctagt tatcagctgg ggctaggaga gggccgtcag gaagatgggg 6780
agaggacggg aggaccacgg aacacaggaa cctgcttctg aggagacttt tcttctggac 6840
tgacaacttc cgaccctgct ggccccaggt gctgccttct ctgatggctt ctccagcggc 6900
ctcagtacca ccttagcggt cttctgccat gagctgcccc acgaactggg taggaatggc 6960
aggagcaggg tggggtggac tccagaaagg agatagctcc aaggggtaga gcttggaggc 7020
tggtgggtgg catggatgag gggcacccca gcttactccc tcccatcctg tcctctgtct 7080
ccaataggtg actttgccat gctgctccag tcagggctgt cctttcggcg gctgctgctg 7140
ctgagcctcg tgtctggagc cctgggattg gggggtgcag tcctgggggt ggggctcagc 7200
ctgggccctg tccccctcac tccctgggtg tttggggtca ctgctggggt cttcctctat 7260
gtggcccttg tggacatggt gagagatgtc gggtagagca gagaaatcaa gggcagtggg 7320
gaggcgggag tggagaggga ggtagcagtc cctccgcctc taccattagc tcctggaagg 7380
gcgtcagacc ataggcccgc aaaagtctga gaaacaaggg actaaggtgt ttgggtgggg 7440
gctgctgatg ctttctgaca ccattcctct ggagttgaga ggtcaggggc aaggccagaa 7500
tcctgacatc ctctttttct ttcagctacc agccctgctt cgtcctccgg agcccctgcc 7560
tacgccccat gtgctcctgc aggggctggg gctgctgctg gggggcggcc tcatgcttgc 7620
cataaccctg ctggaggagc ggctactgcc cgtgaccact gagggctgat ggggccagtg 7680
gaaaggggtc gggttgccct tccttccccc caaccacagg aatggaggcg ggacacaggg 7740
ccagtaggag caataggatt ttaataaaca gaacccatcc caaa 7784
<210> 6
<211> 7784
<212> ДНК
<213> homo sapiens
<400> 6
agctggaacc aagaaggttg tgtccccctt cctctgggtg tccttgtctc ctgctatcag 60
gtaatgccaa cctcaacccc ctggaccagt caccccgatc agactttgct tgcctgattt 120
taggccaggt cagacatcag aggagagccc agatccttgt ttcctctccc cccgcagggc 180
ttcccctttc ttggtcatcg atccctagag ctctggctct ttctcttctt ggggtgagaa 240
actgctaaga acagtttatt tcccatgcat gcatctgggc ttgccactga tctgcctttt 300
cccccctcct ccccaggtta gggacacctg ggtccaacct tcccaaggaa tatggggatg 360
ggggttggag atgaagttta gtgctagact gtaaggtagg tggggtggaa gtacatgagg 420
gaaagggcta aaatggtact aatggtgtta aggatagggt gaattattta agaggaaaaa 480
gactaggccc aggttctcct tagccatgtg gctttcccag ggcagagggt ggcccctccc 540
tacccagggg cccagcagag actgactttt gatccctacc ccagagacca gtgaaccatt 600
aactcctctc ttatgtgagc cttcacacac tggccccacc cctgaccccg ccccaaggca 660
ggtgggctag gagggggtgc atgtccatct cagccttcta tgtgacgtgg cctccgatcc 720
acctggacac ctggaggcta agcctggatt cccccttccc tgactcagga actgcttaac 780
gtctacagca aggcctaata ggggacctga ggtgacagct cttatgttgc cagtaggggt 840
gaggccctgg ggattgaggg gggataaaga ggtggggcaa agttgagggg tggggtttag 900
gggacaagga atggacggtc agctctggat gaagtatgag gagagctctg actcagggag 960
gtgctccagg aaccagcaaa caagaggctg ctcccgcagg aggcagtgtg aagggagaaa 1020
gaaggctgca gtaggggctg ctgctggact cggtggggag caggtgcaag gagctctggc 1080
tcccccatgg acctgagctg gagagcagag cgcagctcca gcccattcct cattcttcca 1140
gggcacagtc ctcaggatgt ttcggggaga ataggagcca gaacctgagc ccctaagcta 1200
ttcccctcac caatgatggg gtccccagtg agtcatctgc tggccggctt ctgtgtgtgg 1260
gtcgtcttgg gctgggtagg gggctcagtc cccaacctgg gccctgctga gcaggagcag 1320
aaccattacc tggcccagct gtttggcctg tacggcgaga atgggacgct gactgcaggg 1380
ggcttggcgc ggcttctcca cagcctgggg ctaggccgag ttcaggggct tcgcctggga 1440
cagcatgggc ctctgactgg acgggctgca tccccagctg cagacaattc cacacacagg 1500
tactgacccc ttcctccact ccacagggcc acatctccca ggtcctctca gtgcttgccc 1560
ccagttgcct cgttctggct tcctcacgag atccctggag ttacaaattc ttcagaaccg 1620
agctccttgg tatctcttca aaacctctca tgcttctatt gccttctctc tcttttcttg 1680
agactggggg tctcgctttg tcacccaggc taaagtgcag tgacacattc acggctcact 1740
gcaacctctg cttcccaggc tgaagccatc ctcccacctc agcctcctga gcagctggga 1800
ccataggcac acaccaccac agccggctaa ttttaaaaat tttttacaga gacaagggtt 1860
tcgctgtgtt gcccaggctg gtctcaaact cctgggctca gctcagcgat ctgcctgcct 1920
cagcttccca aagtgctggg actacagatg tgaactacca ccctagccct ccgttgcctt 1980
ctaattctct cctcctccaa atctctaagc ccttaaattt cttgctctta gtatcactgt 2040
tcagtgtctc tgggctgatt tggctccaaa ttcgtagact tcttttttct tttcttttct 2100
tttttttttt tttttttttt tgagacagag tctcgctctg tcgcccaggc tggagtgcag 2160
tggtgtgatc ttggctcact gtaacctctg cctccccggt tcaagcgatt ctcctgcctc 2220
ggcctcctga gtagctggga ttacaggcac acaccaccac gccgggctaa tttttgcaat 2280
tttagtagag acggggtttc accattttgg tcaggctggt ctcgaacttc caacctcagg 2340
tgatccaccc acctcagcct cccaaagtgc tgggattaca ggcgtgagcc accgtgccca 2400
gccattcgta gcccttttgg ttgtcgtcct tttttttctg tcccccccag tggcagaaaa 2460
tggacaactc acagatcttc ctaagaatga cattccatgg tttctgggtc ccaggatctc 2520
cagtcagtgg ctagtccccc cattccccct aaaatccctg ggagcctctc aaagcgggtt 2580
gatagagaac acaagggagg ctgacttgct gtctcatcca ttccaggcca cagaaccctg 2640
agctgagtgt ggatgtctgg gcagggatgc ctctgggtcc ctcagggtgg ggtgacctgg 2700
aagagtcaaa ggcccctcac ctaccccgtg ggccagcccc ctcgggcctg gacctccttc 2760
acaggcttct gttgctggac cactcattgg ctgaccacct gaatgaggat gtgagtctga 2820
cggtctctag aggggaagga gccatgggat tagatggcct gaaatgttta aataatcagt 2880
agttttttgt tttgttttgt ttttaaatcc caacgtggac caagcgtggt ggctcacgcc 2940
tgtaatccca acactttggg aggccgaggt gggtggatca cctgaggtca ggagttcgag 3000
accagcctgg ccaacatggt gaaaccccat ctctactaaa aaatacaaaa attagccggg 3060
tgtggtaaca ggtgtgtgta atcctagcta ctcaggaggc tgaggtgaga aaattgcttg 3120
aacttgggag gcagaggttg cagtgagcca agatggcacc atttgcactc cagcctgggc 3180
aacaagaggg agactctgtc tcaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaat 3240
agctgggcgt ggtggcacat gcctataatc ccagttactc ggaaggctga ggcaggaaaa 3300
tcacttgaac ccaggaggcg gagattgcag tcagccgaga ttgcaccact gcactccagc 3360
ctgggtaaca cagcgagact ctgtctcaaa aatgaaaata aaaaaaataa aaaaataaaa 3420
aaaaaatatc tcactgtggt cttaggggat gttatttcaa tagtgaacta tgttccctct 3480
gggatcagag caggtgagcc catatccaga gctccaagac tcagtttagg ggaatagatg 3540
gcaaagcaga gaatctagag aagcagccca gggtaggatc tggatggtca cctggagagg 3600
agacctgcag ggaatggatg gctgtcttca tccagaaaga cagagaatat attccactta 3660
caccagaggg cagacaaagc tgcctaaccc tgatggaggt ccagtgagtg cccattgcag 3720
gaagcattca agctgaggct ggatgaacat cgacagggct gttgagaggg agattagatg 3780
gcatttcagg gtcttttccc ttttaagatt ctggcatgga gagctctagt tttccaacca 3840
gcttcattta tcaaatcaac aaaatgattg aaatgatcag agtttgcagg gaagatgatg 3900
acaatgctca ctagcaccca gtttgcatca aattgaatac ctgcattgga ctgaatattc 3960
actaataata cacattgatt ataagtaccc ttggccctag tccccaaggt acctgccagt 4020
aggagcaaag gggaccctgg gagagaccca ggagtctatg caatggaagg acaggtgtta 4080
aatatatata tatatatttt tttgaggtag agtctgactc tgtcacccag gctggagtgc 4140
aatggcgtga tcttggctca ctgcaacctc cacctcctgg gttaaagcaa ttctcctgcc 4200
tcagcctccc gagtagctgg gattataggt gttcactact atccccagct aatttttttt 4260
tttttttttt gagatggagt ctcactctgt cgcccaggct ggagtgcact ggtgcaatct 4320
cggctcactg caacctctgc ctcctgggtt caagcgattc tcctgtctca gcctcctgag 4380
tagctgggat cacaggtgca cgccaccatg cccagctaat tttttgtatt ttagtagaga 4440
cagggtttca ccatgttgcc caggctggtc tcgaactcct gagctcaggc aatctaccca 4500
cctcagcctc ccaaagtgct gggattacag gcgtgagcca ccgcacccgg ctcatcccca 4560
gctaattttt gtatttttag tagagacagg gtttcactat gttggccagg ttggtctcaa 4620
actcctgacc tcagatgata cacccgcctg ggcctctcaa gggctgggat tataggtgtg 4680
agccactaca cctggccagg tgttaaagat ctgagtcata gttcctggtg attctccaat 4740
gtatgaccct caattctcca gtgtctgaac ggctcccagc tgctggtcaa ttttggcttg 4800
agccccgctg ctcctctgac ccctcgtcag tttgctctgc tgtgcccagc cctgctttat 4860
cagatcgaca gccgcgtctg catcggcgct ccggcccctg cacccccagg ggatctacta 4920
tctggtcagc aagtaggagt gggtggggga caccctgaat cctggaagtg gggcccatgc 4980
caaaaaggag gctcactggg gtcctgcctc tccttgtagt gttctctctg ctccacctta 5040
cgtgtgggac cctcctcttg ccctgaccta acttcagccc ctgattctcc ccagccctgc 5100
ttcagagtgc cctggcagtc ctgttgctca gcctcccttc tcccctatcc ctgctgctgc 5160
tgcggctcct gggacctcgt ctactacggc ccttgctggg cttcctgggg gccctggcgg 5220
tgggcactct ttgtggggat gcactgctac atctgctacc gcatgtatgt gaagcccctt 5280
ccttgtaccc ctggcctcca tggatctaag gtgtccccag ccataggaca tcccctccgc 5340
ctttccatca gctcccatat cctactccca gatcctggct tcagcccaca gctgccttct 5400
agtagagcat atgagcgaag gcttgccaca atccatgcaa ggggatgttg ttgggtatag 5460
gggcttccag agtctgccct gaccttctct ctgtcaggca caagaagggc ggcacgcagg 5520
acctggcgga ctaccagaga aggacctggg cccggggctg tcagtgctcg gaggcctctt 5580
cctgctcttt gtgctggaga acatgctggg gcttttgcgg caccgagggc tcaggccagt 5640
gagtgatacc cttttctcct ccttctgctg agaccagagt cccagtcaag aactgggcca 5700
ggccgggcgc ggtggctcac gcctgtaatc ccagcacttt gggagcccaa ggcgggcaga 5760
tcacaaggtt aggagttcga gtccagcctg accaacatgg tgaaaccctg tctctactaa 5820
aaatacaaaa attagctggg cgtggtggtg cgtgtctgta atcccagcta ctcaggaggc 5880
tgaggcagga gaatcgcttg acttgggagg tggaggttgc agcgagctaa gatggcacca 5940
ctgcactcca gcccaggtga cagagcgaga ctccatctca aaaacaacaa caacaacaac 6000
aaaactgggc caaaaagcca agagatgagg agcagtgtgt gctcctggat ctctgacatt 6060
tgcctggtgt gcaggaccta tcggctaaca gggagtgggt aggggctcct taagcacaga 6120
cccaggactt ctggccaaat ggcatcctat tctgagctca agtcaacaag aaacagaggg 6180
gaggtgccaa cttgggaaga aggtagaggc caaagaacat cccaggtgcc agaggtggaa 6240
ccaggtgttc atcttcccag cttgtggcct ggcttcccct tagtccctgg ctctgctgcc 6300
tcctccacca ggagggatgc cctcctattt cagagatgct gcaggcgaaa acgaaggaat 6360
ctcgaaacac gcaacttgga tccggagaat ggcagtggga tggcccttca gcccctacag 6420
gcagctccag gtgactagag gagaaaattt gaagagtagg ttccaagctc acagtcctta 6480
cttgcagcca ccaacactgt cctgtgcttc ttcccgcaga gccaggggct cagggccaga 6540
gggagaagaa cagccagcac ccaccagctc tggcccctcc tgggcaccaa ggccacagtc 6600
atgggcacca gggtggcact gatatcacgt ggatggtcct cctgggagat ggtctacaca 6660
acctcactga tgggctggcc ataggtgtga ggggtgggaa cggagggaag caggtccgag 6720
gggaggccag ggctcctagt tatcagctgg ggctaggaga gggccgtcag gaagatgggg 6780
agaggacggg aggaccacgg aacacaggaa cctgcttctg aggagacttt tcttctggac 6840
tgacaacttc cgaccctgct ggccccaggt gctgccttct ctgatggctt ctccagcgcc 6900
ctcagtacca ccttagcggt cttctgccat gagctgcccc acgaactggg taggaatggc 6960
aggagcaggg tggggtggac tccagaaagg agatagctcc aaggggtaga gcttggaggc 7020
tggtgggtgg catggatgag gggcacccca gcttactccc tcccatcctg tcctctgtct 7080
ccaataggtg actttgccat gctgctccag tcagggctgt cctttcggcg gctgctgctg 7140
ctgagcctcg tgtctggagc cctgggattg gggggtgcag tcctgggggt ggggctcagc 7200
ctgggccctg tccccctcac tccctgggtg tttggggtca ctgctggggt cttcctctat 7260
gtggcccttg tggacatggt gagagatgtc gggtagagca gagaaatcaa gggcagtggg 7320
gaggcgggag tggagaggga ggtagcagtc cctccgcctc taccattagc tcctggaagg 7380
gcgtcagacc ataggcccgc aaaagtctga gaaacaaggg actaaggtgt ttgggtgggg 7440
gctgctgatg ctttctgaca ccattcctct ggagttgaga ggtcaggggc aaggccagaa 7500
tcctgacatc ctctttttct ttcagctacc agccctgctt cgtcctccgg agcccctgcc 7560
tacgccccat gtgctcctgc aggggctggg gctgctgctg gggggcggcc tcatgcttgc 7620
cataaccctg ctggaggagc ggctactgcc cgtgaccact gagggctgat ggggccagtg 7680
gaaaggggtc gggttgccct tccttccccc caaccacagg aatggaggcg ggacacaggg 7740
ccagtaggag caataggatt ttaataaaca gaacccatcc caaa 7784
<210> 7
<211> 7784
<212> ДНК
<213> homo sapiens
<400> 7
agctggaacc aagaaggttg tgtccccctt cctctgggtg tccttgtctc ctgctatcag 60
gtaatgccaa cctcaacccc ctggaccagt caccccgatc agactttgct tgcctgattt 120
taggccaggt cagacatcag aggagagccc agatccttgt ttcctctccc cccgcagggc 180
ttcccctttc ttggtcatcg atccctagag ctctggctct ttctcttctt ggggtgagaa 240
actgctaaga acagtttatt tcccatgcat gcatctgggc ttgccactga tctgcctttt 300
cccccctcct ccccaggtta gggacacctg ggtccaacct tcccaaggaa tatggggatg 360
ggggttggag atgaagttta gtgctagact gtaaggtagg tggggtggaa gtacatgagg 420
gaaagggcta aaatggtact aatggtgtta aggatagggt gaattattta agaggaaaaa 480
gactaggccc aggttctcct tagccatgtg gctttcccag ggcagagggt ggcccctccc 540
tacccagggg cccagcagag actgactttt gatccctacc ccagagacca gtgaaccatt 600
aactcctctc ttatgtgagc cttcacacac tggccccacc cctgaccccg ccccaaggca 660
ggtgggctag gagggggtgc atgtccatct cagccttcta tgtgacgtgg cctccgatcc 720
acctggacac ctggaggcta agcctggatt cccccttccc tgactcagga actgcttaac 780
gtctacagca aggcctaata ggggacctga ggtgacagct cttatgttgc cagtaggggt 840
gaggccctgg ggattgaggg gggataaaga ggtggggcaa agttgagggg tggggtttag 900
gggacaagga atggacggtc agctctggat gaagtatgag gagagctctg actcagggag 960
gtgctccagg aaccagcaaa caagaggctg ctcccgcagg aggcagtgtg aagggagaaa 1020
gaaggctgca gtaggggctg ctgctggact cggtggggag caggtgcaag gagctctggc 1080
tcccccatgg acctgagctg gagagcagag cgcagctcca gcccattcct cattcttcca 1140
gggcacagtc ctcaggatgt ttcggggaga ataggagcca gaacctgagc ccctaagcta 1200
ttcccctcac caatgatggg gtccccagtg agtcatctgc tggccggctt ctgtgtgtgg 1260
gtcgtcttgg gctgggtagg gggctcagtc cccaacctgg gccctgctga gcaggagcag 1320
aaccattacc tggcccagct gtttggcctg tacggcgaga atgggacgct gactgcaggg 1380
ggcttggcgc ggcttctcca cagcctgggg ctaggccgag ttcaggggct tcgcctggga 1440
cagcatgggc ctctgactgg acgggctgca tccccagctg cagacaattc cacacacagg 1500
tactgacccc ttcctccact ccacagggcc acatctccca ggtcctctca gtgcttgccc 1560
ccagttgcct cgttctggct tcctcacgag atccctggag ttacaaattc ttcagaaccg 1620
agctccttgg tatctcttca aaacctctca tgcttctatt gccttctctc tcttttcttg 1680
agactggggg tctcgctttg tcacccaggc taaagtgcag tgacacattc acggctcact 1740
gcaacctctg cttcccaggc tgaagccatc ctcccacctc agcctcctga gcagctggga 1800
ccataggcac acaccaccac agccggctaa ttttaaaaat tttttacaga gacaagggtt 1860
tcgctgtgtt gcccaggctg gtctcaaact cctgggctca gctcagcgat ctgcctgcct 1920
cagcttccca aagtgctggg actacagatg tgaactacca ccctagccct ccgttgcctt 1980
ctaattctct cctcctccaa atctctaagc ccttaaattt cttgctctta gtatcactgt 2040
tcagtgtctc tgggctgatt tggctccaaa ttcgtagact tcttttttct tttcttttct 2100
tttttttttt tttttttttt tgagacagag tctcgctctg tcgcccaggc tggagtgcag 2160
tggtgtgatc ttggctcact gtaacctctg cctccccggt tcaagcgatt ctcctgcctc 2220
ggcctcctga gtagctggga ttacaggcac acaccaccac gccgggctaa tttttgcaat 2280
tttagtagag acggggtttc accattttgg tcaggctggt ctcgaacttc caacctcagg 2340
tgatccaccc acctcagcct cccaaagtgc tgggattaca ggcgtgagcc accgtgccca 2400
gccattcgta gcccttttgg ttgtcgtcct tttttttctg tcccccccag tggcagaaaa 2460
tggacaactc acagatcttc ctaagaatga cattccatgg tttctgggtc ccaggatctc 2520
cagtcagtgg ctagtccccc cattccccct aaaatccctg ggagcctctc aaagcgggtt 2580
gatagagaac acaagggagg ctgacttgct gtctcatcca ttccaggcca cagaaccctg 2640
agctgagtgt ggatgtctgg gcagggatgc ctctgggtcc ctcagggtgg ggtgacctgg 2700
aagagtcaaa ggcccctcac ctaccccgtg ggccagcccc ctcgggcctg gacctccttc 2760
acaggcttct gttgctggac cactcattgg ctgaccacct gaatgaggat gtgagtctga 2820
cggtctctag aggggaagga gccatgggat tagatggcct gaaatgttta aataatcagt 2880
agttttttgt tttgttttgt ttttaaatcc caacgtggac caagcgtggt ggctcacgcc 2940
tgtaatccca acactttggg aggccgaggt gggtggatca cctgaggtca ggagttcgag 3000
accagcctgg ccaacatggt gaaaccccat ctctactaaa aaatacaaaa attagccggg 3060
tgtggtaaca ggtgtgtgta atcctagcta ctcaggaggc tgaggtgaga aaattgcttg 3120
aacttgggag gcagaggttg cagtgagcca agatggcacc atttgcactc cagcctgggc 3180
aacaagaggg agactctgtc tcaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaat 3240
agctgggcgt ggtggcacat gcctataatc ccagttactc ggaaggctga ggcaggaaaa 3300
tcacttgaac ccaggaggcg gagattgcag tcagccgaga ttgcaccact gcactccagc 3360
ctgggtaaca cagcgagact ctgtctcaaa aatgaaaata aaaaaaataa aaaaataaaa 3420
aaaaaatatc tcactgtggt cttaggggat gttatttcaa tagtgaacta tgttccctct 3480
gggatcagag caggtgagcc catatccaga gctccaagac tcagtttagg ggaatagatg 3540
gcaaagcaga gaatctagag aagcagccca gggtaggatc tggatggtca cctggagagg 3600
agacctgcag ggaatggatg gctgtcttca tccagaaaga cagagaatat attccactta 3660
caccagaggg cagacaaagc tgcctaaccc tgatggaggt ccagtgagtg cccattgcag 3720
gaagcattca agctgaggct ggatgaacat cgacagggct gttgagaggg agattagatg 3780
gcatttcagg gtcttttccc ttttaagatt ctggcatgga gagctctagt tttccaacca 3840
gcttcattta tcaaatcaac aaaatgattg aaatgatcag agtttgcagg gaagatgatg 3900
acaatgctca ctagcaccca gtttgcatca aattgaatac ctgcattgga ctgaatattc 3960
actaataata cacattgatt ataagtaccc ttggccctag tccccaaggt acctgccagt 4020
aggagcaaag gggaccctgg gagagaccca ggagtctatg caatggaagg acaggtgtta 4080
aatatatata tatatatttt tttgaggtag agtctgactc tgtcacccag gctggagtgc 4140
aatggcgtga tcttggctca ctgcaacctc cacctcctgg gttaaagcaa ttctcctgcc 4200
tcagcctccc gagtagctgg gattataggt gttcactact atccccagct aatttttttt 4260
tttttttttt gagatggagt ctcactctgt cgcccaggct ggagtgcact ggtgcaatct 4320
cggctcactg caacctctgc ctcctgggtt caagcgattc tcctgtctca gcctcctgag 4380
tagctgggat cacaggtgca cgccaccatg cccagctaat tttttgtatt ttagtagaga 4440
cagggtttca ccatgttgcc caggctggtc tcgaactcct gagctcaggc aatctaccca 4500
cctcagcctc ccaaagtgct gggattacag gcgtgagcca ccgcacccgg ctcatcccca 4560
gctaattttt gtatttttag tagagacagg gtttcactat gttggccagg ttggtctcaa 4620
actcctgacc tcagatgata cacccgcctg ggcctctcaa gggctgggat tataggtgtg 4680
agccactaca cctggccagg tgttaaagat ctgagtcata gttcctggtg attctccaat 4740
gtatgaccct caattctcca gtgtctgaac ggctcccagc tgctggtcaa ttttggcttg 4800
agccccgctg ctcctctgac ccctcgtcag tttgctctgc tgtgcccagc cctgctttat 4860
cagatcgaca gccgcgtctg catcggcgct ccggcccctg cacccccagg ggatctacta 4920
tctggtcagc aagtaggagt gggtggggga caccctgaat cctggaagtg gggcccatgc 4980
caaaaaggag gctcactggg gtcctgcctc tccttgtagt gttctctctg ctccacctta 5040
cgtgtgggac cctcctcttg ccctgaccta acttcagccc ctgattctcc ccagccctgc 5100
ttcagagtgc cctggcagtc ctgttgctca gcctcccttc tcccctatcc ctgctgctgc 5160
tgcggctcct gggacctcgt ctactacggc ccttgctggg cttcctgggg gccctggcgg 5220
tgggcactct ttgtggggat gcactgctac atctgctacc gcatgtatgt gaagcccctt 5280
ccttgtaccc ctggcctcca tggatctaag gtgtccccag ccataggaca tcccctccgc 5340
ctttccatca gctcccatat cctactccca gatcctggct tcagcccaca gctgccttct 5400
agtagagcat atgagcgaag gcttgccaca atccatgcaa ggggatgttg ttgggtatag 5460
gggcttccag agtctgccct gaccttctct ctgtcaggca caagaagggc ggcacgcagg 5520
acctggcgga ctaccagaga aggacctggg cccggggctg tcagtgctcg gaggcctctt 5580
cctgctcttt gtgctggaga acatgctggg gcttttgcgg cactgagggc tcaggccagt 5640
gagtgatacc cttttctcct ccttctgctg agaccagagt cccagtcaag aactgggcca 5700
ggccgggcgc ggtggctcac gcctgtaatc ccagcacttt gggagcccaa ggcgggcaga 5760
tcacaaggtt aggagttcga gtccagcctg accaacatgg tgaaaccctg tctctactaa 5820
aaatacaaaa attagctggg cgtggtggtg cgtgtctgta atcccagcta ctcaggaggc 5880
tgaggcagga gaatcgcttg acttgggagg tggaggttgc agcgagctaa gatggcacca 5940
ctgcactcca gcccaggtga cagagcgaga ctccatctca aaaacaacaa caacaacaac 6000
aaaactgggc caaaaagcca agagatgagg agcagtgtgt gctcctggat ctctgacatt 6060
tgcctggtgt gcaggaccta tcggctaaca gggagtgggt aggggctcct taagcacaga 6120
cccaggactt ctggccaaat ggcatcctat tctgagctca agtcaacaag aaacagaggg 6180
gaggtgccaa cttgggaaga aggtagaggc caaagaacat cccaggtgcc agaggtggaa 6240
ccaggtgttc atcttcccag cttgtggcct ggcttcccct tagtccctgg ctctgctgcc 6300
tcctccacca ggagggatgc cctcctattt cagagatgct gcaggcgaaa acgaaggaat 6360
ctcgaaacac gcaacttgga tccggagaat ggcagtggga tggcccttca gcccctacag 6420
gcagctccag gtgactagag gagaaaattt gaagagtagg ttccaagctc acagtcctta 6480
cttgcagcca ccaacactgt cctgtgcttc ttcccgcaga gccaggggct cagggccaga 6540
gggagaagaa cagccagcac ccaccagctc tggcccctcc tgggcaccaa ggccacagtc 6600
atgggcacca gggtggcact gatatcacgt ggatggtcct cctgggagat ggtctacaca 6660
acctcactga tgggctggcc ataggtgtga ggggtgggaa cggagggaag caggtccgag 6720
gggaggccag ggctcctagt tatcagctgg ggctaggaga gggccgtcag gaagatgggg 6780
agaggacggg aggaccacgg aacacaggaa cctgcttctg aggagacttt tcttctggac 6840
tgacaacttc cgaccctgct ggccccaggt gctgccttct ctgatggctt ctccagcggc 6900
ctcagtacca ccttagcggt cttctgccat gagctgcccc acgaactggg taggaatggc 6960
aggagcaggg tggggtggac tccagaaagg agatagctcc aaggggtaga gcttggaggc 7020
tggtgggtgg catggatgag gggcacccca gcttactccc tcccatcctg tcctctgtct 7080
ccaataggtg actttgccat gctgctccag tcagggctgt cctttcggcg gctgctgctg 7140
ctgagcctcg tgtctggagc cctgggattg gggggtgcag tcctgggggt ggggctcagc 7200
ctgggccctg tccccctcac tccctgggtg tttggggtca ctgctggggt cttcctctat 7260
gtggcccttg tggacatggt gagagatgtc gggtagagca gagaaatcaa gggcagtggg 7320
gaggcgggag tggagaggga ggtagcagtc cctccgcctc taccattagc tcctggaagg 7380
gcgtcagacc ataggcccgc aaaagtctga gaaacaaggg actaaggtgt ttgggtgggg 7440
gctgctgatg ctttctgaca ccattcctct ggagttgaga ggtcaggggc aaggccagaa 7500
tcctgacatc ctctttttct ttcagctacc agccctgctt cgtcctccgg agcccctgcc 7560
tacgccccat gtgctcctgc aggggctggg gctgctgctg gggggcggcc tcatgcttgc 7620
cataaccctg ctggaggagc ggctactgcc cgtgaccact gagggctgat ggggccagtg 7680
gaaaggggtc gggttgccct tccttccccc caaccacagg aatggaggcg ggacacaggg 7740
ccagtaggag caataggatt ttaataaaca gaacccatcc caaa 7784
<210> 8
<211> 1968
<212> ДНК
<213> homo sapiens
<400> 8
agcuggaacc aagaagguug ugucccccuu ccucugggug uccuugucuc cugcuaucag 60
ggcuuccccu uucuugguca ucgaucccua gagcucuggc ucuuucucuu cuuggggaac 120
ugcuuaacgu cuacagcaag gccuaauagg ggaccugagg gcacaguccu caggauguuu 180
cggggagaau aggagccaga accugagccc cuaagcuauu ccccucacca augauggggu 240
ccccagugag ucaucugcug gccggcuucu gugugugggu cgucuugggc uggguagggg 300
gcucaguccc caaccugggc ccugcugagc aggagcagaa ccauuaccug gcccagcugu 360
uuggccugua cggcgagaau gggacgcuga cugcaggggg cuuggcgcgg cuucuccaca 420
gccuggggcu aggccgaguu caggggcuuc gccugggaca gcaugggccu cugacuggac 480
gggcugcauc cccagcugca gacaauucca cacacaggcc acagaacccu gagcugagug 540
uggaugucug ggcagggaug ccucuggguc ccucagggug gggugaccug gaagagucaa 600
aggccccuca ccuaccccgu gggccagccc ccucgggccu ggaccuccuu cacaggcuuc 660
uguugcugga ccacucauug gcugaccacc ugaaugagga uugucugaac ggcucccagc 720
ugcuggucaa uuuuggcuug agccccgcug cuccucugac cccucgucag uuugcucugc 780
ugugcccagc ccugcuuuau cagaucgaca gccgcgucug caucggcgcu ccggccccug 840
cacccccagg ggaucuacua ucugcccugc uucagagugc ccuggcaguc cuguugcuca 900
gccucccuuc uccccuaucc cugcugcugc ugcggcuccu gggaccucgu cuacuacggc 960
ccuugcuggg cuuccugggg gcccuggcgg ugggcacucu uuguggggau gcacugcuac 1020
aucugcuacc gcaugcacaa gaagggcggc acgcaggacc uggcggacua ccagagaagg 1080
accugggccc ggggcuguca gugcucggag gccucuuccu gcucuuugug cuggagaaca 1140
ugcuggggcu uuugcggcac cgagggcuca ggccaagaug cugcaggcga aaacgaagga 1200
aucucgaaac acgcaacuug gauccggaga auggcagugg gauggcccuu cagccccuac 1260
aggcagcucc agagccaggg gcucagggcc agagggagaa gaacagccag cacccaccag 1320
cucuggcccc uccugggcac caaggccaca gucaugggca ccaggguggc acugauauca 1380
cguggauggu ccuccuggga gauggucuac acaaccucac ugaugggcug gccauaggug 1440
cugccuucuc ugauggcuuc uccagcggcc ucaguaccac cuuagcgguc uucugccaug 1500
agcugcccca cgaacugggu gacuuugcca ugcugcucca gucagggcug uccuuucggc 1560
ggcugcugcu gcugagccuc gugucuggag cccugggauu ggggggugca guccuggggg 1620
uggggcucag ccugggcccu gucccccuca cucccugggu guuugggguc acugcugggg 1680
ucuuccucua uguggcccuu guggacaugc uaccagcccu gcuucguccu ccggagcccc 1740
ugccuacgcc ccaugugcuc cugcaggggc uggggcugcu gcuggggggc ggccucaugc 1800
uugccauaac ccugcuggag gagcggcuac ugcccgugac cacugagggc ugauggggcc 1860
aguggaaagg ggucggguug cccuuccuuc cccccaacca caggaaugga ggcgggacac 1920
agggccagua ggagcaauag gauuuuaaua aacagaaccc aucccaaa 1968
<210> 9
<211> 1968
<212> ДНК
<213> homo sapiens
<400> 9
agcuggaacc aagaagguug ugucccccuu ccucugggug uccuugucuc cugcuaucag 60
ggcuuccccu uucuugguca ucgaucccua gagcucuggc ucuuucucuu cuuggggaac 120
ugcuuaacgu cuacagcaag gccuaauagg ggaccugagg gcacaguccu caggauguuu 180
cggggagaau aggagccaga accugagccc cuaagcuauu ccccucacca augauggggu 240
ccccagugag ucaucugcug gccggcuucu gugugugggu cgucuugggc uggguagggg 300
gcucaguccc caaccugggc ccugcugagc aggagcagaa ccauuaccug gcccagcugu 360
uuggccugua aggcgagaau gggacgcuga cugcaggggg cuuggcgcgg cuucuccaca 420
gccuggggcu aggccgaguu caggggcuuc gccugggaca gcaugggccu cugacuggac 480
gggcugcauc cccagcugca gacaauucca cacacaggcc acagaacccu gagcugagug 540
uggaugucug ggcagggaug ccucuggguc ccucagggug gggugaccug gaagagucaa 600
aggccccuca ccuaccccgu gggccagccc ccucgggccu ggaccuccuu cacaggcuuc 660
uguugcugga ccacucauug gcugaccacc ugaaugagga uugucugaac ggcucccagc 720
ugcuggucaa uuuuggcuug agccccgcug cuccucugac cccucgucag uuugcucugc 780
ugugcccagc ccugcuuuau cagaucgaca gccgcgucug caucggcgcu ccggccccug 840
cacccccagg ggaucuacua ucugcccugc uucagagugc ccuggcaguc cuguugcuca 900
gccucccuuc uccccuaucc cugcugcugc ugcggcuccu gggaccucgu cuacuacggc 960
ccuugcuggg cuuccugggg gcccuggcgg ugggcacucu uuguggggau gcacugcuac 1020
aucugcuacc gcaugcacaa gaagggcggc acgcaggacc uggcggacua ccagagaagg 1080
accugggccc ggggcuguca gugcucggag gccucuuccu gcucuuugug cuggagaaca 1140
ugcuggggcu uuugcggcac cgagggcuca ggccaagaug cugcaggcga aaacgaagga 1200
aucucgaaac acgcaacuug gauccggaga auggcagugg gauggcccuu cagccccuac 1260
aggcagcucc agagccaggg gcucagggcc agagggagaa gaacagccag cacccaccag 1320
cucuggcccc uccugggcac caaggccaca gucaugggca ccaggguggc acugauauca 1380
cguggauggu ccuccuggga gauggucuac acaaccucac ugaugggcug gccauaggug 1440
cugccuucuc ugauggcuuc uccagcggcc ucaguaccac cuuagcgguc uucugccaug 1500
agcugcccca cgaacugggu gacuuugcca ugcugcucca gucagggcug uccuuucggc 1560
ggcugcugcu gcugagccuc gugucuggag cccugggauu ggggggugca guccuggggg 1620
uggggcucag ccugggcccu gucccccuca cucccugggu guuugggguc acugcugggg 1680
ucuuccucua uguggcccuu guggacaugc uaccagcccu gcuucguccu ccggagcccc 1740
ugccuacgcc ccaugugcuc cugcaggggc uggggcugcu gcuggggggc ggccucaugc 1800
uugccauaac ccugcuggag gagcggcuac ugcccgugac cacugagggc ugauggggcc 1860
aguggaaagg ggucggguug cccuuccuuc cccccaacca caggaaugga ggcgggacac 1920
agggccagua ggagcaauag gauuuuaaua aacagaaccc aucccaaa 1968
<210> 10
<211> 1968
<212> ДНК
<213> homo sapiens
<400> 10
agcuggaacc aagaagguug ugucccccuu ccucugggug uccuugucuc cugcuaucag 60
ggcuuccccu uucuugguca ucgaucccua gagcucuggc ucuuucucuu cuuggggaac 120
ugcuuaacgu cuacagcaag gccuaauagg ggaccugagg gcacaguccu caggauguuu 180
cggggagaau aggagccaga accugagccc cuaagcuauu ccccucacca augauggggu 240
ccccagugag ucaucugcug gccggcuucu gugugugggu cgucuugggc uggguagggg 300
gcucaguccc caaccugggc ccugcugagc aggagcagaa ccauuaccug gcccagcugu 360
uuggccugua gggcgagaau gggacgcuga cugcaggggg cuuggcgcgg cuucuccaca 420
gccuggggcu aggccgaguu caggggcuuc gccugggaca gcaugggccu cugacuggac 480
gggcugcauc cccagcugca gacaauucca cacacaggcc acagaacccu gagcugagug 540
uggaugucug ggcagggaug ccucuggguc ccucagggug gggugaccug gaagagucaa 600
aggccccuca ccuaccccgu gggccagccc ccucgggccu ggaccuccuu cacaggcuuc 660
uguugcugga ccacucauug gcugaccacc ugaaugagga uugucugaac ggcucccagc 720
ugcuggucaa uuuuggcuug agccccgcug cuccucugac cccucgucag uuugcucugc 780
ugugcccagc ccugcuuuau cagaucgaca gccgcgucug caucggcgcu ccggccccug 840
cacccccagg ggaucuacua ucugcccugc uucagagugc ccuggcaguc cuguugcuca 900
gccucccuuc uccccuaucc cugcugcugc ugcggcuccu gggaccucgu cuacuacggc 960
ccuugcuggg cuuccugggg gcccuggcgg ugggcacucu uuguggggau gcacugcuac 1020
aucugcuacc gcaugcacaa gaagggcggc acgcaggacc uggcggacua ccagagaagg 1080
accugggccc ggggcuguca gugcucggag gccucuuccu gcucuuugug cuggagaaca 1140
ugcuggggcu uuugcggcac cgagggcuca ggccaagaug cugcaggcga aaacgaagga 1200
aucucgaaac acgcaacuug gauccggaga auggcagugg gauggcccuu cagccccuac 1260
aggcagcucc agagccaggg gcucagggcc agagggagaa gaacagccag cacccaccag 1320
cucuggcccc uccugggcac caaggccaca gucaugggca ccaggguggc acugauauca 1380
cguggauggu ccuccuggga gauggucuac acaaccucac ugaugggcug gccauaggug 1440
cugccuucuc ugauggcuuc uccagcggcc ucaguaccac cuuagcgguc uucugccaug 1500
agcugcccca cgaacugggu gacuuugcca ugcugcucca gucagggcug uccuuucggc 1560
ggcugcugcu gcugagccuc gugucuggag cccugggauu ggggggugca guccuggggg 1620
uggggcucag ccugggcccu gucccccuca cucccugggu guuugggguc acugcugggg 1680
ucuuccucua uguggcccuu guggacaugc uaccagcccu gcuucguccu ccggagcccc 1740
ugccuacgcc ccaugugcuc cugcaggggc uggggcugcu gcuggggggc ggccucaugc 1800
uugccauaac ccugcuggag gagcggcuac ugcccgugac cacugagggc ugauggggcc 1860
aguggaaagg ggucggguug cccuuccuuc cccccaacca caggaaugga ggcgggacac 1920
agggccagua ggagcaauag gauuuuaaua aacagaaccc aucccaaa 1968
<210> 11
<211> 1968
<212> ДНК
<213> homo sapiens
<400> 11
agcuggaacc aagaagguug ugucccccuu ccucugggug uccuugucuc cugcuaucag 60
ggcuuccccu uucuugguca ucgaucccua gagcucuggc ucuuucucuu cuuggggaac 120
ugcuuaacgu cuacagcaag gccuaauagg ggaccugagg gcacaguccu caggauguuu 180
cggggagaau aggagccaga accugagccc cuaagcuauu ccccucacca augauggggu 240
ccccagugag ucaucugcug gccggcuucu gugugugggu cgucuugggc uggguagggg 300
gcucaguccc caaccugggc ccugcugagc aggagcagaa ccauuaccug gcccagcugu 360
uuggccugua cggcgagaau gggacgcuga cugcaggggg cuuggcgcgg cuucuccaca 420
gccuggggcu aggccgaguu caggggcuuc gccugggaca gcaugggccu cugacuggac 480
gggcugcauc cccagcugca gacaauucca cacacaggcc acagaacccu gagcugagug 540
uggaugucug ggcagggaug ccucuggguc ccucagggug gggugaccug gaagagucaa 600
aggccccuca ccuaccccgu gggccagccc ccucgggccu ggaccuccuu cacaggcuuc 660
uguugcugga ccacucauug gcugaccacc ugaaugagga uugucugaac ggcucccagc 720
ugcuggucaa uuuuggcuug agccccgcug cuccucugac cccucgucag uuugcucugc 780
ugugcccagc ccugcuuuau cagaucgaca gccgcgucug caucggcgcu ccggccccug 840
cacccccagg ggaucuacua ucugcccugc uucagagugc ccuggcaguc cuguugcuca 900
gccucccuuc uccccuaucc cugcugcugc ugcggcuccu gggaccucgu cuacuacggc 960
ccuugcuggg cuuccugggg gcccuggcgg ugggcacucu uuguggggau gcacugcuac 1020
aucugcuacc gcaugcacaa gaagggcggc acgcaggacc uggcggacua ccagagaagg 1080
accugggccc ggggcuguca gugcucggag gccucuuccu gcucuuugug cuggagaaca 1140
cgcuggggcu uuugcggcac cgagggcuca ggccaagaug cugcaggcga aaacgaagga 1200
aucucgaaac acgcaacuug gauccggaga auggcagugg gauggcccuu cagccccuac 1260
aggcagcucc agagccaggg gcucagggcc agagggagaa gaacagccag cacccaccag 1320
cucuggcccc uccugggcac caaggccaca gucaugggca ccaggguggc acugauauca 1380
cguggauggu ccuccuggga gauggucuac acaaccucac ugaugggcug gccauaggug 1440
cugccuucuc ugauggcuuc uccagcggcc ucaguaccac cuuagcgguc uucugccaug 1500
agcugcccca cgaacugggu gacuuugcca ugcugcucca gucagggcug uccuuucggc 1560
ggcugcugcu gcugagccuc gugucuggag cccugggauu ggggggugca guccuggggg 1620
uggggcucag ccugggcccu gucccccuca cucccugggu guuugggguc acugcugggg 1680
ucuuccucua uguggcccuu guggacaugc uaccagcccu gcuucguccu ccggagcccc 1740
ugccuacgcc ccaugugcuc cugcaggggc uggggcugcu gcuggggggc ggccucaugc 1800
uugccauaac ccugcuggag gagcggcuac ugcccgugac cacugagggc ugauggggcc 1860
aguggaaagg ggucggguug cccuuccuuc cccccaacca caggaaugga ggcgggacac 1920
agggccagua ggagcaauag gauuuuaaua aacagaaccc aucccaaa 1968
<210> 12
<211> 1968
<212> ДНК
<213> homo sapiens
<400> 12
agcuggaacc aagaagguug ugucccccuu ccucugggug uccuugucuc cugcuaucag 60
ggcuuccccu uucuugguca ucgaucccua gagcucuggc ucuuucucuu cuuggggaac 120
ugcuuaacgu cuacagcaag gccuaauagg ggaccugagg gcacaguccu caggauguuu 180
cggggagaau aggagccaga accugagccc cuaagcuauu ccccucacca augauggggu 240
ccccagugag ucaucugcug gccggcuucu gugugugggu cgucuugggc uggguagggg 300
gcucaguccc caaccugggc ccugcugagc aggagcagaa ccauuaccug gcccagcugu 360
uuggccugua cggcgagaau gggacgcuga cugcaggggg cuuggcgcgg cuucuccaca 420
gccuggggcu aggccgaguu caggggcuuc gccugggaca gcaugggccu cugacuggac 480
gggcugcauc cccagcugca gacaauucca cacacaggcc acagaacccu gagcugagug 540
uggaugucug ggcagggaug ccucuggguc ccucagggug gggugaccug gaagagucaa 600
aggccccuca ccuaccccgu gggccagccc ccucgggccu ggaccuccuu cacaggcuuc 660
uguugcugga ccacucauug gcugaccacc ugaaugagga uugucugaac ggcucccagc 720
ugcuggucaa uuuuggcuug agccccgcug cuccucugac cccucgucag uuugcucugc 780
ugugcccagc ccugcuuuau cagaucgaca gccgcgucug caucggcgcu ccggccccug 840
cacccccagg ggaucuacua ucugcccugc uucagagugc ccuggcaguc cuguugcuca 900
gccucccuuc uccccuaucc cugcugcugc ugcggcuccu gggaccucgu cuacuacggc 960
ccuugcuggg cuuccugggg gcccuggcgg ugggcacucu uuguggggau gcacugcuac 1020
aucugcuacc gcaugcacaa gaagggcggc acgcaggacc uggcggacua ccagagaagg 1080
accugggccc ggggcuguca gugcucggag gccucuuccu gcucuuugug cuggagaaca 1140
ugcuggggcu uuugcggcac cgagggcuca ggccaagaug cugcaggcga aaaugaagga 1200
aucucgaaac acgcaacuug gauccggaga auggcagugg gauggcccuu cagccccuac 1260
aggcagcucc agagccaggg gcucagggcc agagggagaa gaacagccag cacccaccag 1320
cucuggcccc uccugggcac caaggccaca gucaugggca ccaggguggc acugauauca 1380
cguggauggu ccuccuggga gauggucuac acaaccucac ugaugggcug gccauaggug 1440
cugccuucuc ugauggcuuc uccagcggcc ucaguaccac cuuagcgguc uucugccaug 1500
agcugcccca cgaacugggu gacuuugcca ugcugcucca gucagggcug uccuuucggc 1560
ggcugcugcu gcugagccuc gugucuggag cccugggauu ggggggugca guccuggggg 1620
uggggcucag ccugggcccu gucccccuca cucccugggu guuugggguc acugcugggg 1680
ucuuccucua uguggcccuu guggacaugc uaccagcccu gcuucguccu ccggagcccc 1740
ugccuacgcc ccaugugcuc cugcaggggc uggggcugcu gcuggggggc ggccucaugc 1800
uugccauaac ccugcuggag gagcggcuac ugcccgugac cacugagggc ugauggggcc 1860
aguggaaagg ggucggguug cccuuccuuc cccccaacca caggaaugga ggcgggacac 1920
agggccagua ggagcaauag gauuuuaaua aacagaaccc aucccaaa 1968
<210> 13
<211> 1968
<212> ДНК
<213> homo sapiens
<400> 13
agcuggaacc aagaagguug ugucccccuu ccucugggug uccuugucuc cugcuaucag 60
ggcuuccccu uucuugguca ucgaucccua gagcucuggc ucuuucucuu cuuggggaac 120
ugcuuaacgu cuacagcaag gccuaauagg ggaccugagg gcacaguccu caggauguuu 180
cggggagaau aggagccaga accugagccc cuaagcuauu ccccucacca augauggggu 240
ccccagugag ucaucugcug gccggcuucu gugugugggu cgucuugggc uggguagggg 300
gcucaguccc caaccugggc ccugcugagc aggagcagaa ccauuaccug gcccagcugu 360
uuggccugua cggcgagaau gggacgcuga cugcaggggg cuuggcgcgg cuucuccaca 420
gccuggggcu aggccgaguu caggggcuuc gccugggaca gcaugggccu cugacuggac 480
gggcugcauc cccagcugca gacaauucca cacacaggcc acagaacccu gagcugagug 540
uggaugucug ggcagggaug ccucuggguc ccucagggug gggugaccug gaagagucaa 600
aggccccuca ccuaccccgu gggccagccc ccucgggccu ggaccuccuu cacaggcuuc 660
uguugcugga ccacucauug gcugaccacc ugaaugagga uugucugaac ggcucccagc 720
ugcuggucaa uuuuggcuug agccccgcug cuccucugac cccucgucag uuugcucugc 780
ugugcccagc ccugcuuuau cagaucgaca gccgcgucug caucggcgcu ccggccccug 840
cacccccagg ggaucuacua ucugcccugc uucagagugc ccuggcaguc cuguugcuca 900
gccucccuuc uccccuaucc cugcugcugc ugcggcuccu gggaccucgu cuacuacggc 960
ccuugcuggg cuuccugggg gcccuggcgg ugggcacucu uuguggggau gcacugcuac 1020
aucugcuacc gcaugcacaa gaagggcggc acgcaggacc uggcggacua ccagagaagg 1080
accugggccc ggggcuguca gugcucggag gccucuuccu gcucuuugug cuggagaaca 1140
ugcuggggcu uuugcggcac cgagggcuca ggccaagaug cugcaggcga aaacgaagga 1200
aucucgaaac acgcaacuug gauccggaga auggcagugg gauggcccuu cagccccuac 1260
aggcagcucc agagccaggg gcucagggcc agagggagaa gaacagccag cacccaccag 1320
cucuggcccc uccugggcac caaggccaca gucaugggca ccaggguggc acugauauca 1380
cguggauggu ccuccuggga gauggucuac acaaccucac ugaugggcug gccauaggug 1440
cugccuucuc ugauggcuuc uccagcgccc ucaguaccac cuuagcgguc uucugccaug 1500
agcugcccca cgaacugggu gacuuugcca ugcugcucca gucagggcug uccuuucggc 1560
ggcugcugcu gcugagccuc gugucuggag cccugggauu ggggggugca guccuggggg 1620
uggggcucag ccugggcccu gucccccuca cucccugggu guuugggguc acugcugggg 1680
ucuuccucua uguggcccuu guggacaugc uaccagcccu gcuucguccu ccggagcccc 1740
ugccuacgcc ccaugugcuc cugcaggggc uggggcugcu gcuggggggc ggccucaugc 1800
uugccauaac ccugcuggag gagcggcuac ugcccgugac cacugagggc ugauggggcc 1860
aguggaaagg ggucggguug cccuuccuuc cccccaacca caggaaugga ggcgggacac 1920
agggccagua ggagcaauag gauuuuaaua aacagaaccc aucccaaa 1968
<210> 14
<211> 1968
<212> ДНК
<213> homo sapiens
<400> 14
agcuggaacc aagaagguug ugucccccuu ccucugggug uccuugucuc cugcuaucag 60
ggcuuccccu uucuugguca ucgaucccua gagcucuggc ucuuucucuu cuuggggaac 120
ugcuuaacgu cuacagcaag gccuaauagg ggaccugagg gcacaguccu caggauguuu 180
cggggagaau aggagccaga accugagccc cuaagcuauu ccccucacca augauggggu 240
ccccagugag ucaucugcug gccggcuucu gugugugggu cgucuugggc uggguagggg 300
gcucaguccc caaccugggc ccugcugagc aggagcagaa ccauuaccug gcccagcugu 360
uuggccugua cggcgagaau gggacgcuga cugcaggggg cuuggcgcgg cuucuccaca 420
gccuggggcu aggccgaguu caggggcuuc gccugggaca gcaugggccu cugacuggac 480
gggcugcauc cccagcugca gacaauucca cacacaggcc acagaacccu gagcugagug 540
uggaugucug ggcagggaug ccucuggguc ccucagggug gggugaccug gaagagucaa 600
aggccccuca ccuaccccgu gggccagccc ccucgggccu ggaccuccuu cacaggcuuc 660
uguugcugga ccacucauug gcugaccacc ugaaugagga uugucugaac ggcucccagc 720
ugcuggucaa uuuuggcuug agccccgcug cuccucugac cccucgucag uuugcucugc 780
ugugcccagc ccugcuuuau cagaucgaca gccgcgucug caucggcgcu ccggccccug 840
cacccccagg ggaucuacua ucugcccugc uucagagugc ccuggcaguc cuguugcuca 900
gccucccuuc uccccuaucc cugcugcugc ugcggcuccu gggaccucgu cuacuacggc 960
ccuugcuggg cuuccugggg gcccuggcgg ugggcacucu uuguggggau gcacugcuac 1020
aucugcuacc gcaugcacaa gaagggcggc acgcaggacc uggcggacua ccagagaagg 1080
accugggccc ggggcuguca gugcucggag gccucuuccu gcucuuugug cuggagaaca 1140
ugcuggggcu uuugcggcac ugagggcuca ggccaagaug cugcaggcga aaacgaagga 1200
aucucgaaac acgcaacuug gauccggaga auggcagugg gauggcccuu cagccccuac 1260
aggcagcucc agagccaggg gcucagggcc agagggagaa gaacagccag cacccaccag 1320
cucuggcccc uccugggcac caaggccaca gucaugggca ccaggguggc acugauauca 1380
cguggauggu ccuccuggga gauggucuac acaaccucac ugaugggcug gccauaggug 1440
cugccuucuc ugauggcuuc uccagcggcc ucaguaccac cuuagcgguc uucugccaug 1500
agcugcccca cgaacugggu gacuuugcca ugcugcucca gucagggcug uccuuucggc 1560
ggcugcugcu gcugagccuc gugucuggag cccugggauu ggggggugca guccuggggg 1620
uggggcucag ccugggcccu gucccccuca cucccugggu guuugggguc acugcugggg 1680
ucuuccucua uguggcccuu guggacaugc uaccagcccu gcuucguccu ccggagcccc 1740
ugccuacgcc ccaugugcuc cugcaggggc uggggcugcu gcuggggggc ggccucaugc 1800
uugccauaac ccugcuggag gagcggcuac ugcccgugac cacugagggc ugauggggcc 1860
aguggaaagg ggucggguug cccuuccuuc cccccaacca caggaaugga ggcgggacac 1920
agggccagua ggagcaauag gauuuuaaua aacagaaccc aucccaaa 1968
<210> 15
<211> 1968
<212> ДНК
<213> homo sapiens
<400> 15
agctggaacc aagaaggttg tgtccccctt cctctgggtg tccttgtctc ctgctatcag 60
ggcttcccct ttcttggtca tcgatcccta gagctctggc tctttctctt cttggggaac 120
tgcttaacgt ctacagcaag gcctaatagg ggacctgagg gcacagtcct caggatgttt 180
cggggagaat aggagccaga acctgagccc ctaagctatt cccctcacca atgatggggt 240
ccccagtgag tcatctgctg gccggcttct gtgtgtgggt cgtcttgggc tgggtagggg 300
gctcagtccc caacctgggc cctgctgagc aggagcagaa ccattacctg gcccagctgt 360
ttggcctgta cggcgagaat gggacgctga ctgcaggggg cttggcgcgg cttctccaca 420
gcctggggct aggccgagtt caggggcttc gcctgggaca gcatgggcct ctgactggac 480
gggctgcatc cccagctgca gacaattcca cacacaggcc acagaaccct gagctgagtg 540
tggatgtctg ggcagggatg cctctgggtc cctcagggtg gggtgacctg gaagagtcaa 600
aggcccctca cctaccccgt gggccagccc cctcgggcct ggacctcctt cacaggcttc 660
tgttgctgga ccactcattg gctgaccacc tgaatgagga ttgtctgaac ggctcccagc 720
tgctggtcaa ttttggcttg agccccgctg ctcctctgac ccctcgtcag tttgctctgc 780
tgtgcccagc cctgctttat cagatcgaca gccgcgtctg catcggcgct ccggcccctg 840
cacccccagg ggatctacta tctgccctgc ttcagagtgc cctggcagtc ctgttgctca 900
gcctcccttc tcccctatcc ctgctgctgc tgcggctcct gggacctcgt ctactacggc 960
ccttgctggg cttcctgggg gccctggcgg tgggcactct ttgtggggat gcactgctac 1020
atctgctacc gcatgcacaa gaagggcggc acgcaggacc tggcggacta ccagagaagg 1080
acctgggccc ggggctgtca gtgctcggag gcctcttcct gctctttgtg ctggagaaca 1140
tgctggggct tttgcggcac cgagggctca ggccaagatg ctgcaggcga aaacgaagga 1200
atctcgaaac acgcaacttg gatccggaga atggcagtgg gatggccctt cagcccctac 1260
aggcagctcc agagccaggg gctcagggcc agagggagaa gaacagccag cacccaccag 1320
ctctggcccc tcctgggcac caaggccaca gtcatgggca ccagggtggc actgatatca 1380
cgtggatggt cctcctggga gatggtctac acaacctcac tgatgggctg gccataggtg 1440
ctgccttctc tgatggcttc tccagcggcc tcagtaccac cttagcggtc ttctgccatg 1500
agctgcccca cgaactgggt gactttgcca tgctgctcca gtcagggctg tcctttcggc 1560
ggctgctgct gctgagcctc gtgtctggag ccctgggatt ggggggtgca gtcctggggg 1620
tggggctcag cctgggccct gtccccctca ctccctgggt gtttggggtc actgctgggg 1680
tcttcctcta tgtggccctt gtggacatgc taccagccct gcttcgtcct ccggagcccc 1740
tgcctacgcc ccatgtgctc ctgcaggggc tggggctgct gctggggggc ggcctcatgc 1800
ttgccataac cctgctggag gagcggctac tgcccgtgac cactgagggc tgatggggcc 1860
agtggaaagg ggtcgggttg cccttccttc cccccaacca caggaatgga ggcgggacac 1920
agggccagta ggagcaatag gattttaata aacagaaccc atcccaaa 1968
<210> 16
<211> 1968
<212> ДНК
<213> homo sapiens
<400> 16
agctggaacc aagaaggttg tgtccccctt cctctgggtg tccttgtctc ctgctatcag 60
ggcttcccct ttcttggtca tcgatcccta gagctctggc tctttctctt cttggggaac 120
tgcttaacgt ctacagcaag gcctaatagg ggacctgagg gcacagtcct caggatgttt 180
cggggagaat aggagccaga acctgagccc ctaagctatt cccctcacca atgatggggt 240
ccccagtgag tcatctgctg gccggcttct gtgtgtgggt cgtcttgggc tgggtagggg 300
gctcagtccc caacctgggc cctgctgagc aggagcagaa ccattacctg gcccagctgt 360
ttggcctgta aggcgagaat gggacgctga ctgcaggggg cttggcgcgg cttctccaca 420
gcctggggct aggccgagtt caggggcttc gcctgggaca gcatgggcct ctgactggac 480
gggctgcatc cccagctgca gacaattcca cacacaggcc acagaaccct gagctgagtg 540
tggatgtctg ggcagggatg cctctgggtc cctcagggtg gggtgacctg gaagagtcaa 600
aggcccctca cctaccccgt gggccagccc cctcgggcct ggacctcctt cacaggcttc 660
tgttgctgga ccactcattg gctgaccacc tgaatgagga ttgtctgaac ggctcccagc 720
tgctggtcaa ttttggcttg agccccgctg ctcctctgac ccctcgtcag tttgctctgc 780
tgtgcccagc cctgctttat cagatcgaca gccgcgtctg catcggcgct ccggcccctg 840
cacccccagg ggatctacta tctgccctgc ttcagagtgc cctggcagtc ctgttgctca 900
gcctcccttc tcccctatcc ctgctgctgc tgcggctcct gggacctcgt ctactacggc 960
ccttgctggg cttcctgggg gccctggcgg tgggcactct ttgtggggat gcactgctac 1020
atctgctacc gcatgcacaa gaagggcggc acgcaggacc tggcggacta ccagagaagg 1080
acctgggccc ggggctgtca gtgctcggag gcctcttcct gctctttgtg ctggagaaca 1140
tgctggggct tttgcggcac cgagggctca ggccaagatg ctgcaggcga aaacgaagga 1200
atctcgaaac acgcaacttg gatccggaga atggcagtgg gatggccctt cagcccctac 1260
aggcagctcc agagccaggg gctcagggcc agagggagaa gaacagccag cacccaccag 1320
ctctggcccc tcctgggcac caaggccaca gtcatgggca ccagggtggc actgatatca 1380
cgtggatggt cctcctggga gatggtctac acaacctcac tgatgggctg gccataggtg 1440
ctgccttctc tgatggcttc tccagcggcc tcagtaccac cttagcggtc ttctgccatg 1500
agctgcccca cgaactgggt gactttgcca tgctgctcca gtcagggctg tcctttcggc 1560
ggctgctgct gctgagcctc gtgtctggag ccctgggatt ggggggtgca gtcctggggg 1620
tggggctcag cctgggccct gtccccctca ctccctgggt gtttggggtc actgctgggg 1680
tcttcctcta tgtggccctt gtggacatgc taccagccct gcttcgtcct ccggagcccc 1740
tgcctacgcc ccatgtgctc ctgcaggggc tggggctgct gctggggggc ggcctcatgc 1800
ttgccataac cctgctggag gagcggctac tgcccgtgac cactgagggc tgatggggcc 1860
agtggaaagg ggtcgggttg cccttccttc cccccaacca caggaatgga ggcgggacac 1920
agggccagta ggagcaatag gattttaata aacagaaccc atcccaaa 1968
<210> 17
<211> 1968
<212> ДНК
<213> homo sapiens
<400> 17
agctggaacc aagaaggttg tgtccccctt cctctgggtg tccttgtctc ctgctatcag 60
ggcttcccct ttcttggtca tcgatcccta gagctctggc tctttctctt cttggggaac 120
tgcttaacgt ctacagcaag gcctaatagg ggacctgagg gcacagtcct caggatgttt 180
cggggagaat aggagccaga acctgagccc ctaagctatt cccctcacca atgatggggt 240
ccccagtgag tcatctgctg gccggcttct gtgtgtgggt cgtcttgggc tgggtagggg 300
gctcagtccc caacctgggc cctgctgagc aggagcagaa ccattacctg gcccagctgt 360
ttggcctgta gggcgagaat gggacgctga ctgcaggggg cttggcgcgg cttctccaca 420
gcctggggct aggccgagtt caggggcttc gcctgggaca gcatgggcct ctgactggac 480
gggctgcatc cccagctgca gacaattcca cacacaggcc acagaaccct gagctgagtg 540
tggatgtctg ggcagggatg cctctgggtc cctcagggtg gggtgacctg gaagagtcaa 600
aggcccctca cctaccccgt gggccagccc cctcgggcct ggacctcctt cacaggcttc 660
tgttgctgga ccactcattg gctgaccacc tgaatgagga ttgtctgaac ggctcccagc 720
tgctggtcaa ttttggcttg agccccgctg ctcctctgac ccctcgtcag tttgctctgc 780
tgtgcccagc cctgctttat cagatcgaca gccgcgtctg catcggcgct ccggcccctg 840
cacccccagg ggatctacta tctgccctgc ttcagagtgc cctggcagtc ctgttgctca 900
gcctcccttc tcccctatcc ctgctgctgc tgcggctcct gggacctcgt ctactacggc 960
ccttgctggg cttcctgggg gccctggcgg tgggcactct ttgtggggat gcactgctac 1020
atctgctacc gcatgcacaa gaagggcggc acgcaggacc tggcggacta ccagagaagg 1080
acctgggccc ggggctgtca gtgctcggag gcctcttcct gctctttgtg ctggagaaca 1140
tgctggggct tttgcggcac cgagggctca ggccaagatg ctgcaggcga aaacgaagga 1200
atctcgaaac acgcaacttg gatccggaga atggcagtgg gatggccctt cagcccctac 1260
aggcagctcc agagccaggg gctcagggcc agagggagaa gaacagccag cacccaccag 1320
ctctggcccc tcctgggcac caaggccaca gtcatgggca ccagggtggc actgatatca 1380
cgtggatggt cctcctggga gatggtctac acaacctcac tgatgggctg gccataggtg 1440
ctgccttctc tgatggcttc tccagcggcc tcagtaccac cttagcggtc ttctgccatg 1500
agctgcccca cgaactgggt gactttgcca tgctgctcca gtcagggctg tcctttcggc 1560
ggctgctgct gctgagcctc gtgtctggag ccctgggatt ggggggtgca gtcctggggg 1620
tggggctcag cctgggccct gtccccctca ctccctgggt gtttggggtc actgctgggg 1680
tcttcctcta tgtggccctt gtggacatgc taccagccct gcttcgtcct ccggagcccc 1740
tgcctacgcc ccatgtgctc ctgcaggggc tggggctgct gctggggggc ggcctcatgc 1800
ttgccataac cctgctggag gagcggctac tgcccgtgac cactgagggc tgatggggcc 1860
agtggaaagg ggtcgggttg cccttccttc cccccaacca caggaatgga ggcgggacac 1920
agggccagta ggagcaatag gattttaata aacagaaccc atcccaaa 1968
<210> 18
<211> 1968
<212> ДНК
<213> homo sapiens
<400> 18
agctggaacc aagaaggttg tgtccccctt cctctgggtg tccttgtctc ctgctatcag 60
ggcttcccct ttcttggtca tcgatcccta gagctctggc tctttctctt cttggggaac 120
tgcttaacgt ctacagcaag gcctaatagg ggacctgagg gcacagtcct caggatgttt 180
cggggagaat aggagccaga acctgagccc ctaagctatt cccctcacca atgatggggt 240
ccccagtgag tcatctgctg gccggcttct gtgtgtgggt cgtcttgggc tgggtagggg 300
gctcagtccc caacctgggc cctgctgagc aggagcagaa ccattacctg gcccagctgt 360
ttggcctgta cggcgagaat gggacgctga ctgcaggggg cttggcgcgg cttctccaca 420
gcctggggct aggccgagtt caggggcttc gcctgggaca gcatgggcct ctgactggac 480
gggctgcatc cccagctgca gacaattcca cacacaggcc acagaaccct gagctgagtg 540
tggatgtctg ggcagggatg cctctgggtc cctcagggtg gggtgacctg gaagagtcaa 600
aggcccctca cctaccccgt gggccagccc cctcgggcct ggacctcctt cacaggcttc 660
tgttgctgga ccactcattg gctgaccacc tgaatgagga ttgtctgaac ggctcccagc 720
tgctggtcaa ttttggcttg agccccgctg ctcctctgac ccctcgtcag tttgctctgc 780
tgtgcccagc cctgctttat cagatcgaca gccgcgtctg catcggcgct ccggcccctg 840
cacccccagg ggatctacta tctgccctgc ttcagagtgc cctggcagtc ctgttgctca 900
gcctcccttc tcccctatcc ctgctgctgc tgcggctcct gggacctcgt ctactacggc 960
ccttgctggg cttcctgggg gccctggcgg tgggcactct ttgtggggat gcactgctac 1020
atctgctacc gcatgcacaa gaagggcggc acgcaggacc tggcggacta ccagagaagg 1080
acctgggccc ggggctgtca gtgctcggag gcctcttcct gctctttgtg ctggagaaca 1140
cgctggggct tttgcggcac cgagggctca ggccaagatg ctgcaggcga aaacgaagga 1200
atctcgaaac acgcaacttg gatccggaga atggcagtgg gatggccctt cagcccctac 1260
aggcagctcc agagccaggg gctcagggcc agagggagaa gaacagccag cacccaccag 1320
ctctggcccc tcctgggcac caaggccaca gtcatgggca ccagggtggc actgatatca 1380
cgtggatggt cctcctggga gatggtctac acaacctcac tgatgggctg gccataggtg 1440
ctgccttctc tgatggcttc tccagcggcc tcagtaccac cttagcggtc ttctgccatg 1500
agctgcccca cgaactgggt gactttgcca tgctgctcca gtcagggctg tcctttcggc 1560
ggctgctgct gctgagcctc gtgtctggag ccctgggatt ggggggtgca gtcctggggg 1620
tggggctcag cctgggccct gtccccctca ctccctgggt gtttggggtc actgctgggg 1680
tcttcctcta tgtggccctt gtggacatgc taccagccct gcttcgtcct ccggagcccc 1740
tgcctacgcc ccatgtgctc ctgcaggggc tggggctgct gctggggggc ggcctcatgc 1800
ttgccataac cctgctggag gagcggctac tgcccgtgac cactgagggc tgatggggcc 1860
agtggaaagg ggtcgggttg cccttccttc cccccaacca caggaatgga ggcgggacac 1920
agggccagta ggagcaatag gattttaata aacagaaccc atcccaaa 1968
<210> 19
<211> 1968
<212> ДНК
<213> homo sapiens
<400> 19
agctggaacc aagaaggttg tgtccccctt cctctgggtg tccttgtctc ctgctatcag 60
ggcttcccct ttcttggtca tcgatcccta gagctctggc tctttctctt cttggggaac 120
tgcttaacgt ctacagcaag gcctaatagg ggacctgagg gcacagtcct caggatgttt 180
cggggagaat aggagccaga acctgagccc ctaagctatt cccctcacca atgatggggt 240
ccccagtgag tcatctgctg gccggcttct gtgtgtgggt cgtcttgggc tgggtagggg 300
gctcagtccc caacctgggc cctgctgagc aggagcagaa ccattacctg gcccagctgt 360
ttggcctgta cggcgagaat gggacgctga ctgcaggggg cttggcgcgg cttctccaca 420
gcctggggct aggccgagtt caggggcttc gcctgggaca gcatgggcct ctgactggac 480
gggctgcatc cccagctgca gacaattcca cacacaggcc acagaaccct gagctgagtg 540
tggatgtctg ggcagggatg cctctgggtc cctcagggtg gggtgacctg gaagagtcaa 600
aggcccctca cctaccccgt gggccagccc cctcgggcct ggacctcctt cacaggcttc 660
tgttgctgga ccactcattg gctgaccacc tgaatgagga ttgtctgaac ggctcccagc 720
tgctggtcaa ttttggcttg agccccgctg ctcctctgac ccctcgtcag tttgctctgc 780
tgtgcccagc cctgctttat cagatcgaca gccgcgtctg catcggcgct ccggcccctg 840
cacccccagg ggatctacta tctgccctgc ttcagagtgc cctggcagtc ctgttgctca 900
gcctcccttc tcccctatcc ctgctgctgc tgcggctcct gggacctcgt ctactacggc 960
ccttgctggg cttcctgggg gccctggcgg tgggcactct ttgtggggat gcactgctac 1020
atctgctacc gcatgcacaa gaagggcggc acgcaggacc tggcggacta ccagagaagg 1080
acctgggccc ggggctgtca gtgctcggag gcctcttcct gctctttgtg ctggagaaca 1140
tgctggggct tttgcggcac cgagggctca ggccaagatg ctgcaggcga aaatgaagga 1200
atctcgaaac acgcaacttg gatccggaga atggcagtgg gatggccctt cagcccctac 1260
aggcagctcc agagccaggg gctcagggcc agagggagaa gaacagccag cacccaccag 1320
ctctggcccc tcctgggcac caaggccaca gtcatgggca ccagggtggc actgatatca 1380
cgtggatggt cctcctggga gatggtctac acaacctcac tgatgggctg gccataggtg 1440
ctgccttctc tgatggcttc tccagcggcc tcagtaccac cttagcggtc ttctgccatg 1500
agctgcccca cgaactgggt gactttgcca tgctgctcca gtcagggctg tcctttcggc 1560
ggctgctgct gctgagcctc gtgtctggag ccctgggatt ggggggtgca gtcctggggg 1620
tggggctcag cctgggccct gtccccctca ctccctgggt gtttggggtc actgctgggg 1680
tcttcctcta tgtggccctt gtggacatgc taccagccct gcttcgtcct ccggagcccc 1740
tgcctacgcc ccatgtgctc ctgcaggggc tggggctgct gctggggggc ggcctcatgc 1800
ttgccataac cctgctggag gagcggctac tgcccgtgac cactgagggc tgatggggcc 1860
agtggaaagg ggtcgggttg cccttccttc cccccaacca caggaatgga ggcgggacac 1920
agggccagta ggagcaatag gattttaata aacagaaccc atcccaaa 1968
<210> 20
<211> 1968
<212> ДНК
<213> homo sapiens
<400> 20
agctggaacc aagaaggttg tgtccccctt cctctgggtg tccttgtctc ctgctatcag 60
ggcttcccct ttcttggtca tcgatcccta gagctctggc tctttctctt cttggggaac 120
tgcttaacgt ctacagcaag gcctaatagg ggacctgagg gcacagtcct caggatgttt 180
cggggagaat aggagccaga acctgagccc ctaagctatt cccctcacca atgatggggt 240
ccccagtgag tcatctgctg gccggcttct gtgtgtgggt cgtcttgggc tgggtagggg 300
gctcagtccc caacctgggc cctgctgagc aggagcagaa ccattacctg gcccagctgt 360
ttggcctgta cggcgagaat gggacgctga ctgcaggggg cttggcgcgg cttctccaca 420
gcctggggct aggccgagtt caggggcttc gcctgggaca gcatgggcct ctgactggac 480
gggctgcatc cccagctgca gacaattcca cacacaggcc acagaaccct gagctgagtg 540
tggatgtctg ggcagggatg cctctgggtc cctcagggtg gggtgacctg gaagagtcaa 600
aggcccctca cctaccccgt gggccagccc cctcgggcct ggacctcctt cacaggcttc 660
tgttgctgga ccactcattg gctgaccacc tgaatgagga ttgtctgaac ggctcccagc 720
tgctggtcaa ttttggcttg agccccgctg ctcctctgac ccctcgtcag tttgctctgc 780
tgtgcccagc cctgctttat cagatcgaca gccgcgtctg catcggcgct ccggcccctg 840
cacccccagg ggatctacta tctgccctgc ttcagagtgc cctggcagtc ctgttgctca 900
gcctcccttc tcccctatcc ctgctgctgc tgcggctcct gggacctcgt ctactacggc 960
ccttgctggg cttcctgggg gccctggcgg tgggcactct ttgtggggat gcactgctac 1020
atctgctacc gcatgcacaa gaagggcggc acgcaggacc tggcggacta ccagagaagg 1080
acctgggccc ggggctgtca gtgctcggag gcctcttcct gctctttgtg ctggagaaca 1140
tgctggggct tttgcggcac cgagggctca ggccaagatg ctgcaggcga aaacgaagga 1200
atctcgaaac acgcaacttg gatccggaga atggcagtgg gatggccctt cagcccctac 1260
aggcagctcc agagccaggg gctcagggcc agagggagaa gaacagccag cacccaccag 1320
ctctggcccc tcctgggcac caaggccaca gtcatgggca ccagggtggc actgatatca 1380
cgtggatggt cctcctggga gatggtctac acaacctcac tgatgggctg gccataggtg 1440
ctgccttctc tgatggcttc tccagcgccc tcagtaccac cttagcggtc ttctgccatg 1500
agctgcccca cgaactgggt gactttgcca tgctgctcca gtcagggctg tcctttcggc 1560
ggctgctgct gctgagcctc gtgtctggag ccctgggatt ggggggtgca gtcctggggg 1620
tggggctcag cctgggccct gtccccctca ctccctgggt gtttggggtc actgctgggg 1680
tcttcctcta tgtggccctt gtggacatgc taccagccct gcttcgtcct ccggagcccc 1740
tgcctacgcc ccatgtgctc ctgcaggggc tggggctgct gctggggggc ggcctcatgc 1800
ttgccataac cctgctggag gagcggctac tgcccgtgac cactgagggc tgatggggcc 1860
agtggaaagg ggtcgggttg cccttccttc cccccaacca caggaatgga ggcgggacac 1920
agggccagta ggagcaatag gattttaata aacagaaccc atcccaaa 1968
<210> 21
<211> 1968
<212> ДНК
<213> homo sapiens
<400> 21
agctggaacc aagaaggttg tgtccccctt cctctgggtg tccttgtctc ctgctatcag 60
ggcttcccct ttcttggtca tcgatcccta gagctctggc tctttctctt cttggggaac 120
tgcttaacgt ctacagcaag gcctaatagg ggacctgagg gcacagtcct caggatgttt 180
cggggagaat aggagccaga acctgagccc ctaagctatt cccctcacca atgatggggt 240
ccccagtgag tcatctgctg gccggcttct gtgtgtgggt cgtcttgggc tgggtagggg 300
gctcagtccc caacctgggc cctgctgagc aggagcagaa ccattacctg gcccagctgt 360
ttggcctgta cggcgagaat gggacgctga ctgcaggggg cttggcgcgg cttctccaca 420
gcctggggct aggccgagtt caggggcttc gcctgggaca gcatgggcct ctgactggac 480
gggctgcatc cccagctgca gacaattcca cacacaggcc acagaaccct gagctgagtg 540
tggatgtctg ggcagggatg cctctgggtc cctcagggtg gggtgacctg gaagagtcaa 600
aggcccctca cctaccccgt gggccagccc cctcgggcct ggacctcctt cacaggcttc 660
tgttgctgga ccactcattg gctgaccacc tgaatgagga ttgtctgaac ggctcccagc 720
tgctggtcaa ttttggcttg agccccgctg ctcctctgac ccctcgtcag tttgctctgc 780
tgtgcccagc cctgctttat cagatcgaca gccgcgtctg catcggcgct ccggcccctg 840
cacccccagg ggatctacta tctgccctgc ttcagagtgc cctggcagtc ctgttgctca 900
gcctcccttc tcccctatcc ctgctgctgc tgcggctcct gggacctcgt ctactacggc 960
ccttgctggg cttcctgggg gccctggcgg tgggcactct ttgtggggat gcactgctac 1020
atctgctacc gcatgcacaa gaagggcggc acgcaggacc tggcggacta ccagagaagg 1080
acctgggccc ggggctgtca gtgctcggag gcctcttcct gctctttgtg ctggagaaca 1140
tgctggggct tttgcggcac tgagggctca ggccaagatg ctgcaggcga aaacgaagga 1200
atctcgaaac acgcaacttg gatccggaga atggcagtgg gatggccctt cagcccctac 1260
aggcagctcc agagccaggg gctcagggcc agagggagaa gaacagccag cacccaccag 1320
ctctggcccc tcctgggcac caaggccaca gtcatgggca ccagggtggc actgatatca 1380
cgtggatggt cctcctggga gatggtctac acaacctcac tgatgggctg gccataggtg 1440
ctgccttctc tgatggcttc tccagcggcc tcagtaccac cttagcggtc ttctgccatg 1500
agctgcccca cgaactgggt gactttgcca tgctgctcca gtcagggctg tcctttcggc 1560
ggctgctgct gctgagcctc gtgtctggag ccctgggatt ggggggtgca gtcctggggg 1620
tggggctcag cctgggccct gtccccctca ctccctgggt gtttggggtc actgctgggg 1680
tcttcctcta tgtggccctt gtggacatgc taccagccct gcttcgtcct ccggagcccc 1740
tgcctacgcc ccatgtgctc ctgcaggggc tggggctgct gctggggggc ggcctcatgc 1800
ttgccataac cctgctggag gagcggctac tgcccgtgac cactgagggc tgatggggcc 1860
agtggaaagg ggtcgggttg cccttccttc cccccaacca caggaatgga ggcgggacac 1920
agggccagta ggagcaatag gattttaata aacagaaccc atcccaaa 1968
<210> 22
<211> 540
<212> БЕЛОК
<213> homo sapiens
<400> 22
Met Met Gly Ser Pro Val Ser His Leu Leu Ala Gly Phe Cys Val Trp
1 5 10 15
Val Val Leu Gly Trp Val Gly Gly Ser Val Pro Asn Leu Gly Pro Ala
20 25 30
Glu Gln Glu Gln Asn His Tyr Leu Ala Gln Leu Phe Gly Leu Tyr Gly
35 40 45
Glu Asn Gly Thr Leu Thr Ala Gly Gly Leu Ala Arg Leu Leu His Ser
50 55 60
Leu Gly Leu Gly Arg Val Gln Gly Leu Arg Leu Gly Gln His Gly Pro
65 70 75 80
Leu Thr Gly Arg Ala Ala Ser Pro Ala Ala Asp Asn Ser Thr His Arg
85 90 95
Pro Gln Asn Pro Glu Leu Ser Val Asp Val Trp Ala Gly Met Pro Leu
100 105 110
Gly Pro Ser Gly Trp Gly Asp Leu Glu Glu Ser Lys Ala Pro His Leu
115 120 125
Pro Arg Gly Pro Ala Pro Ser Gly Leu Asp Leu Leu His Arg Leu Leu
130 135 140
Leu Leu Asp His Ser Leu Ala Asp His Leu Asn Glu Asp Cys Leu Asn
145 150 155 160
Gly Ser Gln Leu Leu Val Asn Phe Gly Leu Ser Pro Ala Ala Pro Leu
165 170 175
Thr Pro Arg Gln Phe Ala Leu Leu Cys Pro Ala Leu Leu Tyr Gln Ile
180 185 190
Asp Ser Arg Val Cys Ile Gly Ala Pro Ala Pro Ala Pro Pro Gly Asp
195 200 205
Leu Leu Ser Ala Leu Leu Gln Ser Ala Leu Ala Val Leu Leu Leu Ser
210 215 220
Leu Pro Ser Pro Leu Ser Leu Leu Leu Leu Arg Leu Leu Gly Pro Arg
225 230 235 240
Leu Leu Arg Pro Leu Leu Gly Phe Leu Gly Ala Leu Ala Val Gly Thr
245 250 255
Leu Cys Gly Asp Ala Leu Leu His Leu Leu Pro His Ala Gln Glu Gly
260 265 270
Arg His Ala Gly Pro Gly Gly Leu Pro Glu Lys Asp Leu Gly Pro Gly
275 280 285
Leu Ser Val Leu Gly Gly Leu Phe Leu Leu Phe Val Leu Glu Asn Met
290 295 300
Leu Gly Leu Leu Arg His Arg Gly Leu Arg Pro Arg Cys Cys Arg Arg
305 310 315 320
Lys Arg Arg Asn Leu Glu Thr Arg Asn Leu Asp Pro Glu Asn Gly Ser
325 330 335
Gly Met Ala Leu Gln Pro Leu Gln Ala Ala Pro Glu Pro Gly Ala Gln
340 345 350
Gly Gln Arg Glu Lys Asn Ser Gln His Pro Pro Ala Leu Ala Pro Pro
355 360 365
Gly His Gln Gly His Ser His Gly His Gln Gly Gly Thr Asp Ile Thr
370 375 380
Trp Met Val Leu Leu Gly Asp Gly Leu His Asn Leu Thr Asp Gly Leu
385 390 395 400
Ala Ile Gly Ala Ala Phe Ser Asp Gly Phe Ser Ser Gly Leu Ser Thr
405 410 415
Thr Leu Ala Val Phe Cys His Glu Leu Pro His Glu Leu Gly Asp Phe
420 425 430
Ala Met Leu Leu Gln Ser Gly Leu Ser Phe Arg Arg Leu Leu Leu Leu
435 440 445
Ser Leu Val Ser Gly Ala Leu Gly Leu Gly Gly Ala Val Leu Gly Val
450 455 460
Gly Leu Ser Leu Gly Pro Val Pro Leu Thr Pro Trp Val Phe Gly Val
465 470 475 480
Thr Ala Gly Val Phe Leu Tyr Val Ala Leu Val Asp Met Leu Pro Ala
485 490 495
Leu Leu Arg Pro Pro Glu Pro Leu Pro Thr Pro His Val Leu Leu Gln
500 505 510
Gly Leu Gly Leu Leu Leu Gly Gly Gly Leu Met Leu Ala Ile Thr Leu
515 520 525
Leu Glu Glu Arg Leu Leu Pro Val Thr Thr Glu Gly
530 535 540
<210> 23
<211> 46
<212> БЕЛОК
<213> homo sapiens
<400> 23
Met Met Gly Ser Pro Val Ser His Leu Leu Ala Gly Phe Cys Val Trp
1 5 10 15
Val Val Leu Gly Trp Val Gly Gly Ser Val Pro Asn Leu Gly Pro Ala
20 25 30
Glu Gln Glu Gln Asn His Tyr Leu Ala Gln Leu Phe Gly Leu
35 40 45
<210> 24
<211> 540
<212> БЕЛОК
<213> homo sapiens
<400> 24
Met Met Gly Ser Pro Val Ser His Leu Leu Ala Gly Phe Cys Val Trp
1 5 10 15
Val Val Leu Gly Trp Val Gly Gly Ser Val Pro Asn Leu Gly Pro Ala
20 25 30
Glu Gln Glu Gln Asn His Tyr Leu Ala Gln Leu Phe Gly Leu Tyr Gly
35 40 45
Glu Asn Gly Thr Leu Thr Ala Gly Gly Leu Ala Arg Leu Leu His Ser
50 55 60
Leu Gly Leu Gly Arg Val Gln Gly Leu Arg Leu Gly Gln His Gly Pro
65 70 75 80
Leu Thr Gly Arg Ala Ala Ser Pro Ala Ala Asp Asn Ser Thr His Arg
85 90 95
Pro Gln Asn Pro Glu Leu Ser Val Asp Val Trp Ala Gly Met Pro Leu
100 105 110
Gly Pro Ser Gly Trp Gly Asp Leu Glu Glu Ser Lys Ala Pro His Leu
115 120 125
Pro Arg Gly Pro Ala Pro Ser Gly Leu Asp Leu Leu His Arg Leu Leu
130 135 140
Leu Leu Asp His Ser Leu Ala Asp His Leu Asn Glu Asp Cys Leu Asn
145 150 155 160
Gly Ser Gln Leu Leu Val Asn Phe Gly Leu Ser Pro Ala Ala Pro Leu
165 170 175
Thr Pro Arg Gln Phe Ala Leu Leu Cys Pro Ala Leu Leu Tyr Gln Ile
180 185 190
Asp Ser Arg Val Cys Ile Gly Ala Pro Ala Pro Ala Pro Pro Gly Asp
195 200 205
Leu Leu Ser Ala Leu Leu Gln Ser Ala Leu Ala Val Leu Leu Leu Ser
210 215 220
Leu Pro Ser Pro Leu Ser Leu Leu Leu Leu Arg Leu Leu Gly Pro Arg
225 230 235 240
Leu Leu Arg Pro Leu Leu Gly Phe Leu Gly Ala Leu Ala Val Gly Thr
245 250 255
Leu Cys Gly Asp Ala Leu Leu His Leu Leu Pro His Ala Gln Glu Gly
260 265 270
Arg His Ala Gly Pro Gly Gly Leu Pro Glu Lys Asp Leu Gly Pro Gly
275 280 285
Leu Ser Val Leu Gly Gly Leu Phe Leu Leu Phe Val Leu Glu Asn Thr
290 295 300
Leu Gly Leu Leu Arg His Arg Gly Leu Arg Pro Arg Cys Cys Arg Arg
305 310 315 320
Lys Arg Arg Asn Leu Glu Thr Arg Asn Leu Asp Pro Glu Asn Gly Ser
325 330 335
Gly Met Ala Leu Gln Pro Leu Gln Ala Ala Pro Glu Pro Gly Ala Gln
340 345 350
Gly Gln Arg Glu Lys Asn Ser Gln His Pro Pro Ala Leu Ala Pro Pro
355 360 365
Gly His Gln Gly His Ser His Gly His Gln Gly Gly Thr Asp Ile Thr
370 375 380
Trp Met Val Leu Leu Gly Asp Gly Leu His Asn Leu Thr Asp Gly Leu
385 390 395 400
Ala Ile Gly Ala Ala Phe Ser Asp Gly Phe Ser Ser Gly Leu Ser Thr
405 410 415
Thr Leu Ala Val Phe Cys His Glu Leu Pro His Glu Leu Gly Asp Phe
420 425 430
Ala Met Leu Leu Gln Ser Gly Leu Ser Phe Arg Arg Leu Leu Leu Leu
435 440 445
Ser Leu Val Ser Gly Ala Leu Gly Leu Gly Gly Ala Val Leu Gly Val
450 455 460
Gly Leu Ser Leu Gly Pro Val Pro Leu Thr Pro Trp Val Phe Gly Val
465 470 475 480
Thr Ala Gly Val Phe Leu Tyr Val Ala Leu Val Asp Met Leu Pro Ala
485 490 495
Leu Leu Arg Pro Pro Glu Pro Leu Pro Thr Pro His Val Leu Leu Gln
500 505 510
Gly Leu Gly Leu Leu Leu Gly Gly Gly Leu Met Leu Ala Ile Thr Leu
515 520 525
Leu Glu Glu Arg Leu Leu Pro Val Thr Thr Glu Gly
530 535 540
<210> 25
<211> 321
<212> БЕЛОК
<213> homo sapiens
<400> 25
Met Met Gly Ser Pro Val Ser His Leu Leu Ala Gly Phe Cys Val Trp
1 5 10 15
Val Val Leu Gly Trp Val Gly Gly Ser Val Pro Asn Leu Gly Pro Ala
20 25 30
Glu Gln Glu Gln Asn His Tyr Leu Ala Gln Leu Phe Gly Leu Tyr Gly
35 40 45
Glu Asn Gly Thr Leu Thr Ala Gly Gly Leu Ala Arg Leu Leu His Ser
50 55 60
Leu Gly Leu Gly Arg Val Gln Gly Leu Arg Leu Gly Gln His Gly Pro
65 70 75 80
Leu Thr Gly Arg Ala Ala Ser Pro Ala Ala Asp Asn Ser Thr His Arg
85 90 95
Pro Gln Asn Pro Glu Leu Ser Val Asp Val Trp Ala Gly Met Pro Leu
100 105 110
Gly Pro Ser Gly Trp Gly Asp Leu Glu Glu Ser Lys Ala Pro His Leu
115 120 125
Pro Arg Gly Pro Ala Pro Ser Gly Leu Asp Leu Leu His Arg Leu Leu
130 135 140
Leu Leu Asp His Ser Leu Ala Asp His Leu Asn Glu Asp Cys Leu Asn
145 150 155 160
Gly Ser Gln Leu Leu Val Asn Phe Gly Leu Ser Pro Ala Ala Pro Leu
165 170 175
Thr Pro Arg Gln Phe Ala Leu Leu Cys Pro Ala Leu Leu Tyr Gln Ile
180 185 190
Asp Ser Arg Val Cys Ile Gly Ala Pro Ala Pro Ala Pro Pro Gly Asp
195 200 205
Leu Leu Ser Ala Leu Leu Gln Ser Ala Leu Ala Val Leu Leu Leu Ser
210 215 220
Leu Pro Ser Pro Leu Ser Leu Leu Leu Leu Arg Leu Leu Gly Pro Arg
225 230 235 240
Leu Leu Arg Pro Leu Leu Gly Phe Leu Gly Ala Leu Ala Val Gly Thr
245 250 255
Leu Cys Gly Asp Ala Leu Leu His Leu Leu Pro His Ala Gln Glu Gly
260 265 270
Arg His Ala Gly Pro Gly Gly Leu Pro Glu Lys Asp Leu Gly Pro Gly
275 280 285
Leu Ser Val Leu Gly Gly Leu Phe Leu Leu Phe Val Leu Glu Asn Met
290 295 300
Leu Gly Leu Leu Arg His Arg Gly Leu Arg Pro Arg Cys Cys Arg Arg
305 310 315 320
Lys
<210> 26
<211> 540
<212> БЕЛОК
<213> homo sapiens
<400> 26
Met Met Gly Ser Pro Val Ser His Leu Leu Ala Gly Phe Cys Val Trp
1 5 10 15
Val Val Leu Gly Trp Val Gly Gly Ser Val Pro Asn Leu Gly Pro Ala
20 25 30
Glu Gln Glu Gln Asn His Tyr Leu Ala Gln Leu Phe Gly Leu Tyr Gly
35 40 45
Glu Asn Gly Thr Leu Thr Ala Gly Gly Leu Ala Arg Leu Leu His Ser
50 55 60
Leu Gly Leu Gly Arg Val Gln Gly Leu Arg Leu Gly Gln His Gly Pro
65 70 75 80
Leu Thr Gly Arg Ala Ala Ser Pro Ala Ala Asp Asn Ser Thr His Arg
85 90 95
Pro Gln Asn Pro Glu Leu Ser Val Asp Val Trp Ala Gly Met Pro Leu
100 105 110
Gly Pro Ser Gly Trp Gly Asp Leu Glu Glu Ser Lys Ala Pro His Leu
115 120 125
Pro Arg Gly Pro Ala Pro Ser Gly Leu Asp Leu Leu His Arg Leu Leu
130 135 140
Leu Leu Asp His Ser Leu Ala Asp His Leu Asn Glu Asp Cys Leu Asn
145 150 155 160
Gly Ser Gln Leu Leu Val Asn Phe Gly Leu Ser Pro Ala Ala Pro Leu
165 170 175
Thr Pro Arg Gln Phe Ala Leu Leu Cys Pro Ala Leu Leu Tyr Gln Ile
180 185 190
Asp Ser Arg Val Cys Ile Gly Ala Pro Ala Pro Ala Pro Pro Gly Asp
195 200 205
Leu Leu Ser Ala Leu Leu Gln Ser Ala Leu Ala Val Leu Leu Leu Ser
210 215 220
Leu Pro Ser Pro Leu Ser Leu Leu Leu Leu Arg Leu Leu Gly Pro Arg
225 230 235 240
Leu Leu Arg Pro Leu Leu Gly Phe Leu Gly Ala Leu Ala Val Gly Thr
245 250 255
Leu Cys Gly Asp Ala Leu Leu His Leu Leu Pro His Ala Gln Glu Gly
260 265 270
Arg His Ala Gly Pro Gly Gly Leu Pro Glu Lys Asp Leu Gly Pro Gly
275 280 285
Leu Ser Val Leu Gly Gly Leu Phe Leu Leu Phe Val Leu Glu Asn Met
290 295 300
Leu Gly Leu Leu Arg His Arg Gly Leu Arg Pro Arg Cys Cys Arg Arg
305 310 315 320
Lys Arg Arg Asn Leu Glu Thr Arg Asn Leu Asp Pro Glu Asn Gly Ser
325 330 335
Gly Met Ala Leu Gln Pro Leu Gln Ala Ala Pro Glu Pro Gly Ala Gln
340 345 350
Gly Gln Arg Glu Lys Asn Ser Gln His Pro Pro Ala Leu Ala Pro Pro
355 360 365
Gly His Gln Gly His Ser His Gly His Gln Gly Gly Thr Asp Ile Thr
370 375 380
Trp Met Val Leu Leu Gly Asp Gly Leu His Asn Leu Thr Asp Gly Leu
385 390 395 400
Ala Ile Gly Ala Ala Phe Ser Asp Gly Phe Ser Ser Ala Leu Ser Thr
405 410 415
Thr Leu Ala Val Phe Cys His Glu Leu Pro His Glu Leu Gly Asp Phe
420 425 430
Ala Met Leu Leu Gln Ser Gly Leu Ser Phe Arg Arg Leu Leu Leu Leu
435 440 445
Ser Leu Val Ser Gly Ala Leu Gly Leu Gly Gly Ala Val Leu Gly Val
450 455 460
Gly Leu Ser Leu Gly Pro Val Pro Leu Thr Pro Trp Val Phe Gly Val
465 470 475 480
Thr Ala Gly Val Phe Leu Tyr Val Ala Leu Val Asp Met Leu Pro Ala
485 490 495
Leu Leu Arg Pro Pro Glu Pro Leu Pro Thr Pro His Val Leu Leu Gln
500 505 510
Gly Leu Gly Leu Leu Leu Gly Gly Gly Leu Met Leu Ala Ile Thr Leu
515 520 525
Leu Glu Glu Arg Leu Leu Pro Val Thr Thr Glu Gly
530 535 540
<210> 27
<211> 310
<212> БЕЛОК
<213> homo sapiens
<400> 27
Met Met Gly Ser Pro Val Ser His Leu Leu Ala Gly Phe Cys Val Trp
1 5 10 15
Val Val Leu Gly Trp Val Gly Gly Ser Val Pro Asn Leu Gly Pro Ala
20 25 30
Glu Gln Glu Gln Asn His Tyr Leu Ala Gln Leu Phe Gly Leu Tyr Gly
35 40 45
Glu Asn Gly Thr Leu Thr Ala Gly Gly Leu Ala Arg Leu Leu His Ser
50 55 60
Leu Gly Leu Gly Arg Val Gln Gly Leu Arg Leu Gly Gln His Gly Pro
65 70 75 80
Leu Thr Gly Arg Ala Ala Ser Pro Ala Ala Asp Asn Ser Thr His Arg
85 90 95
Pro Gln Asn Pro Glu Leu Ser Val Asp Val Trp Ala Gly Met Pro Leu
100 105 110
Gly Pro Ser Gly Trp Gly Asp Leu Glu Glu Ser Lys Ala Pro His Leu
115 120 125
Pro Arg Gly Pro Ala Pro Ser Gly Leu Asp Leu Leu His Arg Leu Leu
130 135 140
Leu Leu Asp His Ser Leu Ala Asp His Leu Asn Glu Asp Cys Leu Asn
145 150 155 160
Gly Ser Gln Leu Leu Val Asn Phe Gly Leu Ser Pro Ala Ala Pro Leu
165 170 175
Thr Pro Arg Gln Phe Ala Leu Leu Cys Pro Ala Leu Leu Tyr Gln Ile
180 185 190
Asp Ser Arg Val Cys Ile Gly Ala Pro Ala Pro Ala Pro Pro Gly Asp
195 200 205
Leu Leu Ser Ala Leu Leu Gln Ser Ala Leu Ala Val Leu Leu Leu Ser
210 215 220
Leu Pro Ser Pro Leu Ser Leu Leu Leu Leu Arg Leu Leu Gly Pro Arg
225 230 235 240
Leu Leu Arg Pro Leu Leu Gly Phe Leu Gly Ala Leu Ala Val Gly Thr
245 250 255
Leu Cys Gly Asp Ala Leu Leu His Leu Leu Pro His Ala Gln Glu Gly
260 265 270
Arg His Ala Gly Pro Gly Gly Leu Pro Glu Lys Asp Leu Gly Pro Gly
275 280 285
Leu Ser Val Leu Gly Gly Leu Phe Leu Leu Phe Val Leu Glu Asn Met
290 295 300
Leu Gly Leu Leu Arg His
305 310
<210> 28
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 28
cgcaacttgg atccggagaa tgg 23
<210> 29
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 29
gaatctcgaa acacgcaact tgg 23
<210> 30
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 30
cgaaacacgc aacttggatc cgg 23
<210> 31
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 31
tggatccgga gaatggcagt ggg 23
<210> 32
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 32
aggcagctcc aggtgactag agg 23
<210> 33
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 33
gatggccctt cagcccctac agg 23
<210> 34
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 34
aaataggagg gcatccctcc tgg 23
<210> 35
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 35
ttggatccgg agaatggcag tgg 23
<210> 36
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 36
gtcacctgga gctgcctgta ggg 23
<210> 37
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 37
aattttctcc tctagtcacc tgg 23
<210> 38
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 38
tcacctggag ctgcctgtag ggg 23
<210> 39
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 39
tcctatttca gagatgctgc agg 23
<210> 40
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 40
tgcagcatct ctgaaatagg agg 23
<210> 41
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 41
gtgttcatct tcccagcttg tgg 23
<210> 42
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 42
tgaacacctg gttccacctc tgg 23
<210> 43
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 43
catcttccca gcttgtggcc tgg 23
<210> 44
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 44
taggagggca tccctcctgg tgg 23
<210> 45
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 45
gatgctgcag gcgaaaatga agg 23
<210> 46
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 46
aagctgggaa gatgaacacc tgg 23
<210> 47
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 47
gcagcatctc tgaaatagga ggg 23
<210> 48
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 48
cagcagagcc agggactaag ggg 23
<210> 49
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 49
gcctgcagca tctctgaaat agg 23
<210> 50
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 50
gccatcccac tgccattctc cgg 23
<210> 51
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 51
gggaagccag gccacaagct ggg 23
<210> 52
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 52
agctgcctgt aggggctgaa ggg 23
<210> 53
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 53
ggggaagcca ggccacaagc tgg 23
<210> 54
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 54
agtcacctgg agctgcctgt agg 23
<210> 55
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 55
gcagcagagc cagggactaa ggg 23
<210> 56
<211> 23
<212> ДНК
<213> искусственная последовательность
<220>
< 223> Последовательность распознавания направляющей РНК
<400> 56
cctggcttcc ccttagtccc tgg 23
<210> 57
<211> 351
<212> ДНК
<213> Mus musculus
<400> 57
caggtgcagc tgaaggagtc aggacctggc ctggtggcgc cctcacagag cctgtccatc 60
acatgcaccg tctcagggtt ctcattaacc ggctatgctg taaactgggt tcgccagcct 120
ccaggacagg ggctggagtg gctgggagtg atttggggtg atggaagaac agactataat 180
tcagttctca aatccagact gagcatcaac aaggacaact ccaagagcca agttttctta 240
aaaatgaaca gtctgcaaac tgatgacaca gccaggtact actgtgccag atttggtaac 300
tcctatgctc tggactactg gggtcaagga acctcagtca ccgtctcctc a 351
<210> 58
<211> 117
<212> БЕЛОК
<213> Mus musculus
<400> 58
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Gly Tyr
20 25 30
Ala Val Asn Trp Val Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Gly Asp Gly Arg Thr Asp Tyr Asn Ser Val Leu Lys
50 55 60
Ser Arg Leu Ser Ile Asn Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Arg Tyr Tyr Cys Ala
85 90 95
Arg Phe Gly Asn Ser Tyr Ala Leu Asp Tyr Trp Gly Gln Gly Thr Ser
100 105 110
Val Thr Val Ser Ser
115
<210> 59
<211> 336
<212> ДНК
<213> Mus musculus
<400> 59
gacattgtga tgtcacagtc tccatcctcc ctggctgtgt cagcaggaga gaaggtcact 60
atgagctgca aatccagtca gagtctgctc aacagtagaa cccgaaagaa ctacttggct 120
tggtaccagc agaaaccagg gcagtctcct aaactgctga tctactgggc atccactagg 180
gaatctgggg tccctgatcg cttcacaggc agtggatctg ggacagattt cactctcacc 240
atcagcagtg tgcaggctga agacctggca gtttattact gcaagcaatc ttataatctt 300
cacacgttcg gaggggggac caagctggaa ataaaa 336
<210> 60
<211> 112
<212> БЕЛОК
<213> Mus musculus
<400> 60
Asp Ile Val Met Ser Gln Ser Pro Ser Ser Leu Ala Val Ser Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Arg Thr Arg Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Ser Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Asn Leu His Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 61
<211> 9
<212> БЕЛОК
<213> mus musculus
<400> 61
Phe Ser Leu Thr Gly Tyr Ala Val Asn
1 5
<210> 62
<211> 13
<212> БЕЛОК
<213> mus musculus
<400> 62
Trp Leu Gly Val Ile Trp Gly Asp Gly Arg Thr Asp Tyr
1 5 10
<210> 63
<211> 11
<212> БЕЛОК
<213> mus musculus
<400> 63
Ala Arg Phe Gly Asn Ser Tyr Ala Leu Asp Tyr
1 5 10
<210> 64
<211> 14
<212> БЕЛОК
<213> mus musculus
<400> 64
Gln Ser Leu Leu Asn Ser Arg Thr Arg Lys Asn Tyr Leu Ala
1 5 10
<210> 65
<211> 11
<212> БЕЛОК
<213> mus musculus
<400> 65
Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser
1 5 10
<210> 66
<211> 7
<212> БЕЛОК
<213> mus musculus
<400> 66
Lys Gln Ser Tyr Asn Leu His
1 5
<210> 67
<211> 18
<212> БЕЛОК
<213> mus musculus
<400> 67
Gly Pro Ser Gly Trp Gly Asp Gln Glu Glu Ser Lys Ala Pro Asp Leu
1 5 10 15
His Gly
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ЛЕЧЕНИЕ РЕСПИРАТОРНЫХ НАРУШЕНИЙ С ПОМОЩЬЮ ИНГИБИТОРОВ АРАХИДОНАТ 15-ЛИПОКСИГЕНАЗЫ (ALOX15) | 2019 |
|
RU2799084C2 |
| ЛЕЧЕНИЕ ОФТАЛЬМОЛОГИЧЕСКИХ ПАТОЛОГИЧЕСКИХ СОСТОЯНИЙ ИНГИБИТОРАМИ АНГИОПОЭТИН-ПОДОБНОГО БЕЛКА 7 (ANGPTL7) | 2020 |
|
RU2812912C2 |
| ВАРИАНТЫ БЕЛКА, РОДСТВЕННОГО РЕЦЕПТОРУ ИНТЕРЛЕЙКИНА-1 И СОДЕРЖАЩЕГО ОДИНОЧНЫЙ ДОМЕН ИММУНОГЛОБУЛИНА (SIGIRR), И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2815068C2 |
| КОМПОНЕНТ 1 МЕХАНОЧУВСТВИТЕЛЬНОГО ИОННОГО КАНАЛА ПЬЕЗОТИПА (PIEZO1) И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2812362C2 |
| НОВЫЙ TOTIVIRUS РЫБ | 2020 |
|
RU2798051C2 |
| КОНСТРУКЦИИ ДНК-АНТИТЕЛ ДЛЯ ПРИМЕНЕНИЯ ПРОТИВ БОЛЕЗНИ ЛАЙМА | 2017 |
|
RU2813829C2 |
| МОЛЕКУЛЫ НУКЛЕИНОВЫХ КИСЛОТ ДЛЯ УМЕНЬШЕНИЯ УРОВНЯ мРНК PAPD5 ИЛИ PAPD7 ДЛЯ ЛЕЧЕНИЯ ИНФЕКЦИОННОГО ГЕПАТИТА В | 2017 |
|
RU2768699C2 |
| НОВЫЙ КОРОНАВИРУС РЫБ | 2020 |
|
RU2813731C2 |
| Кодон-оптимизированная нуклеиновая кислота, которая кодирует белок SMN1, и ее применение | 2020 |
|
RU2742837C1 |
| DLL3-НАЦЕЛИВАЮЩИЕ АНТИТЕЛА И ИХ ПРИМЕНЕНИЯ | 2020 |
|
RU2839959C2 |
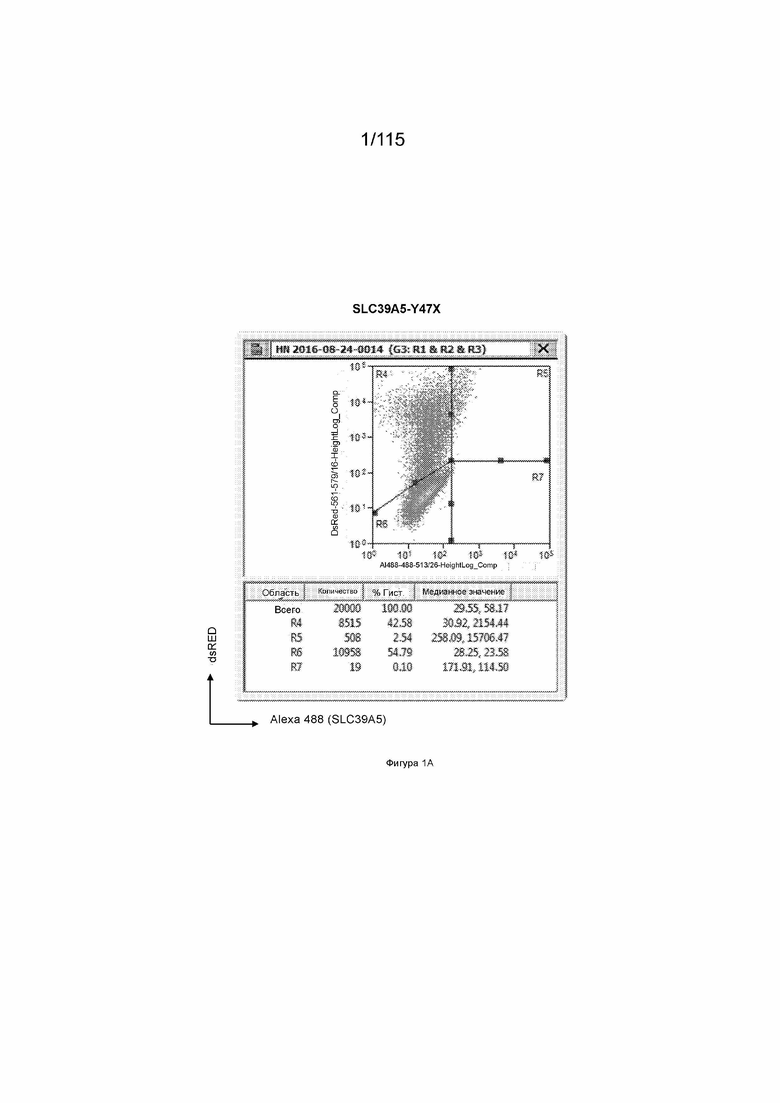
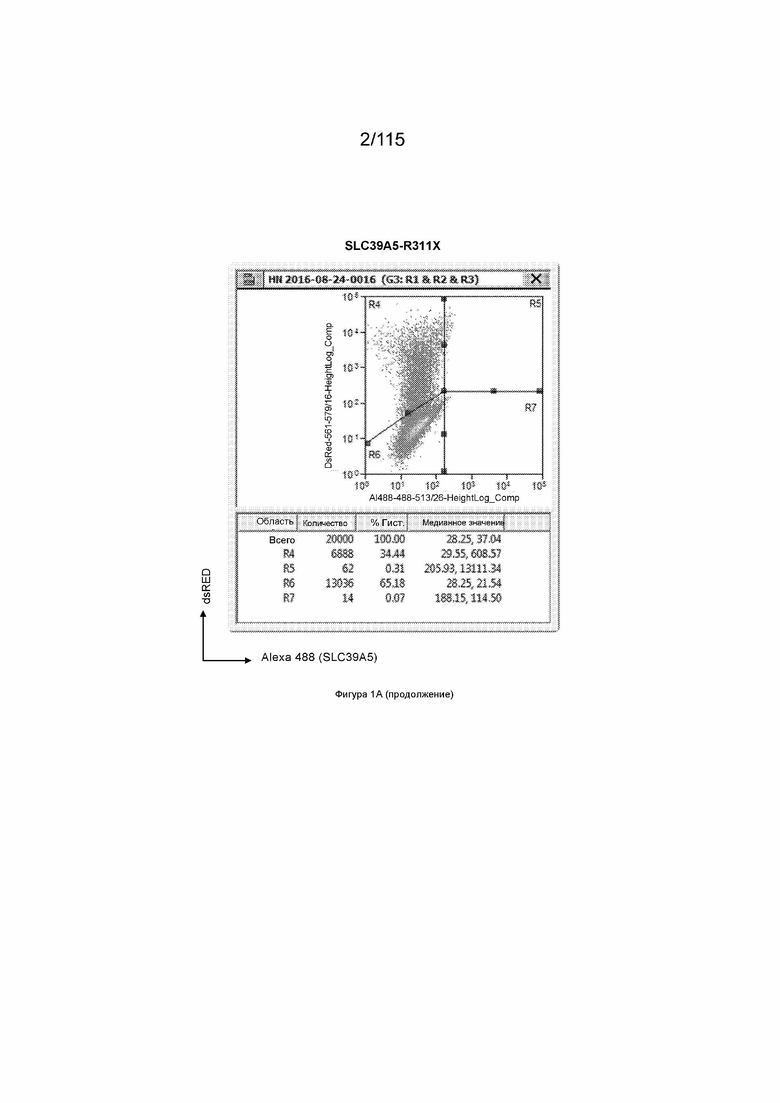
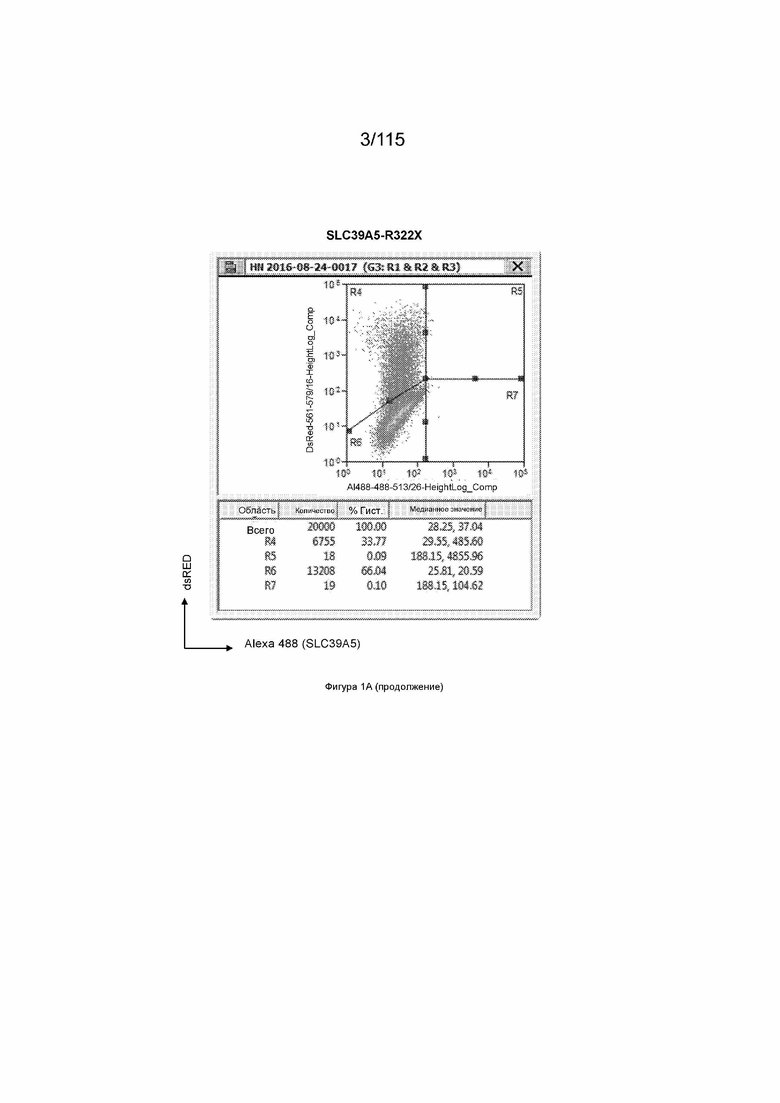
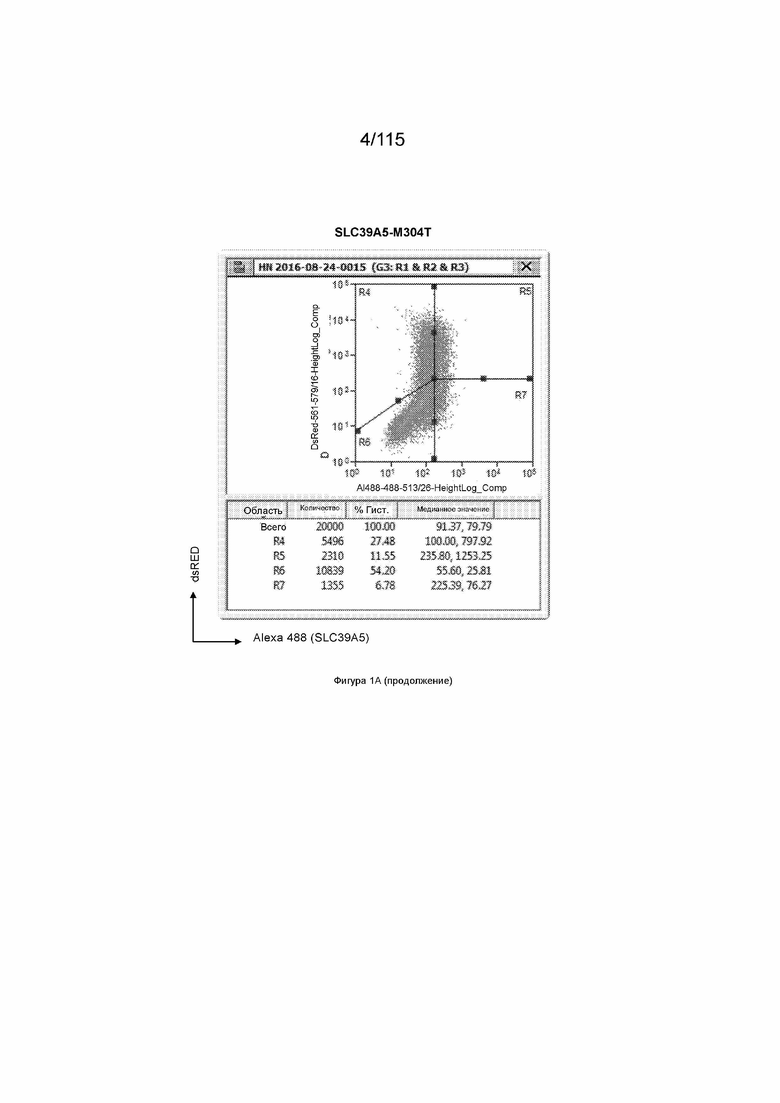
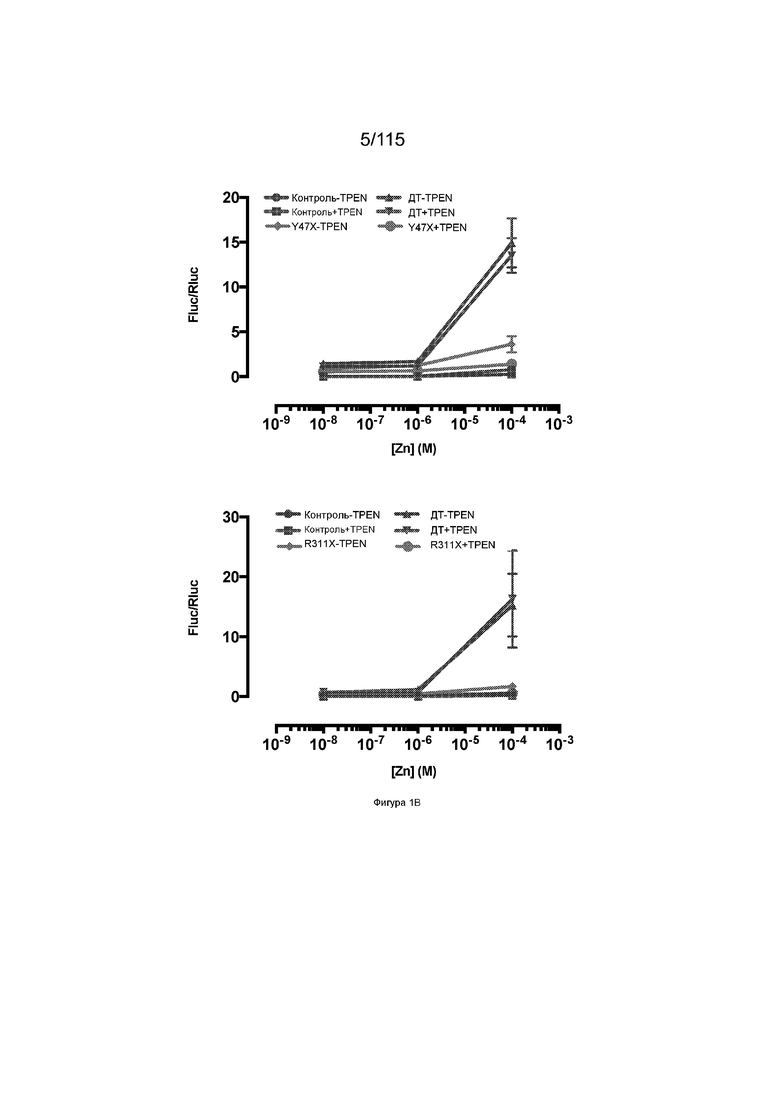
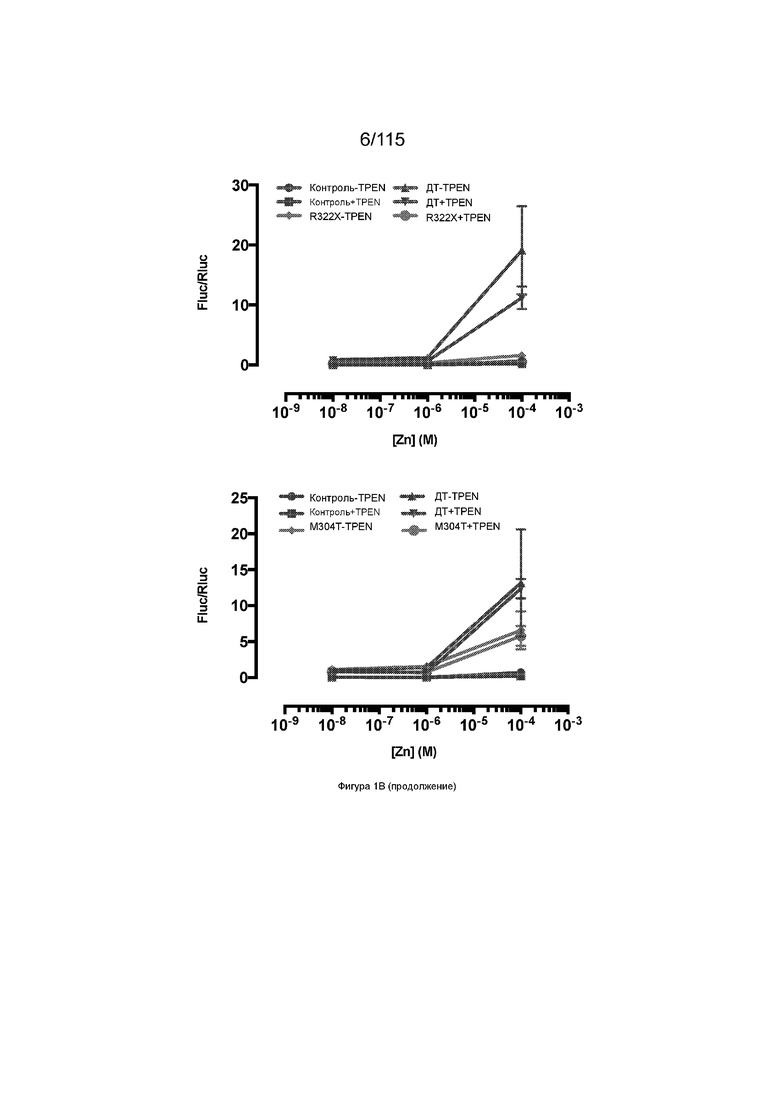
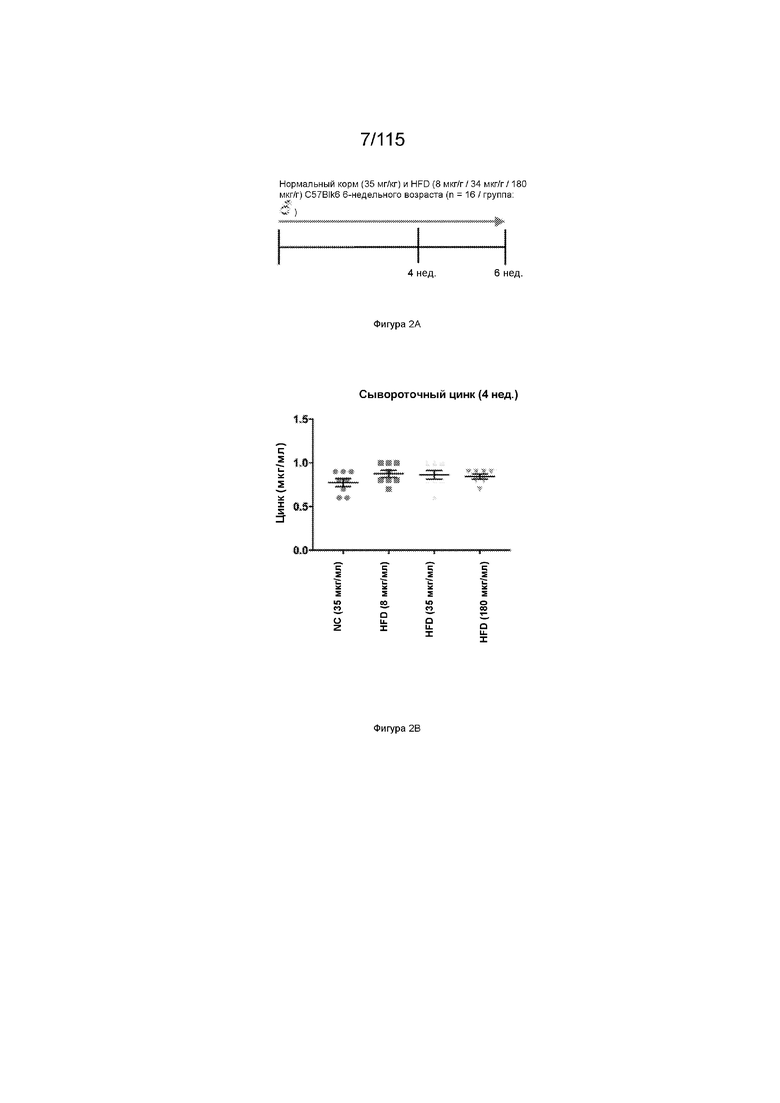
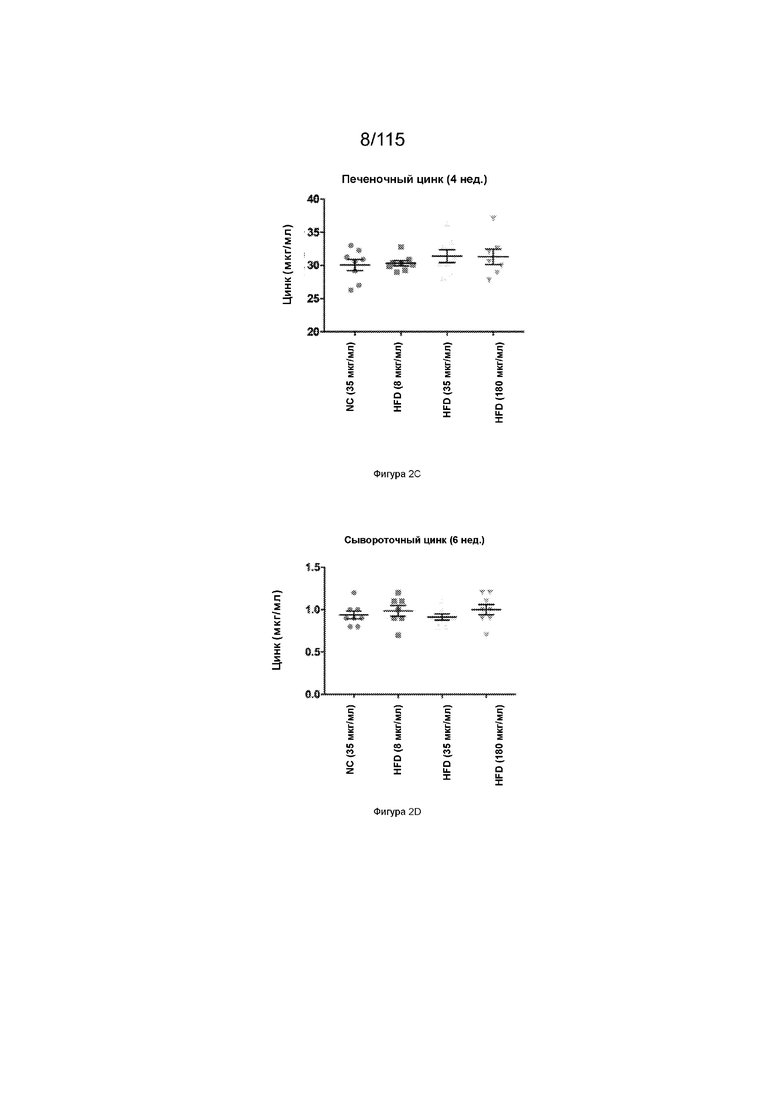
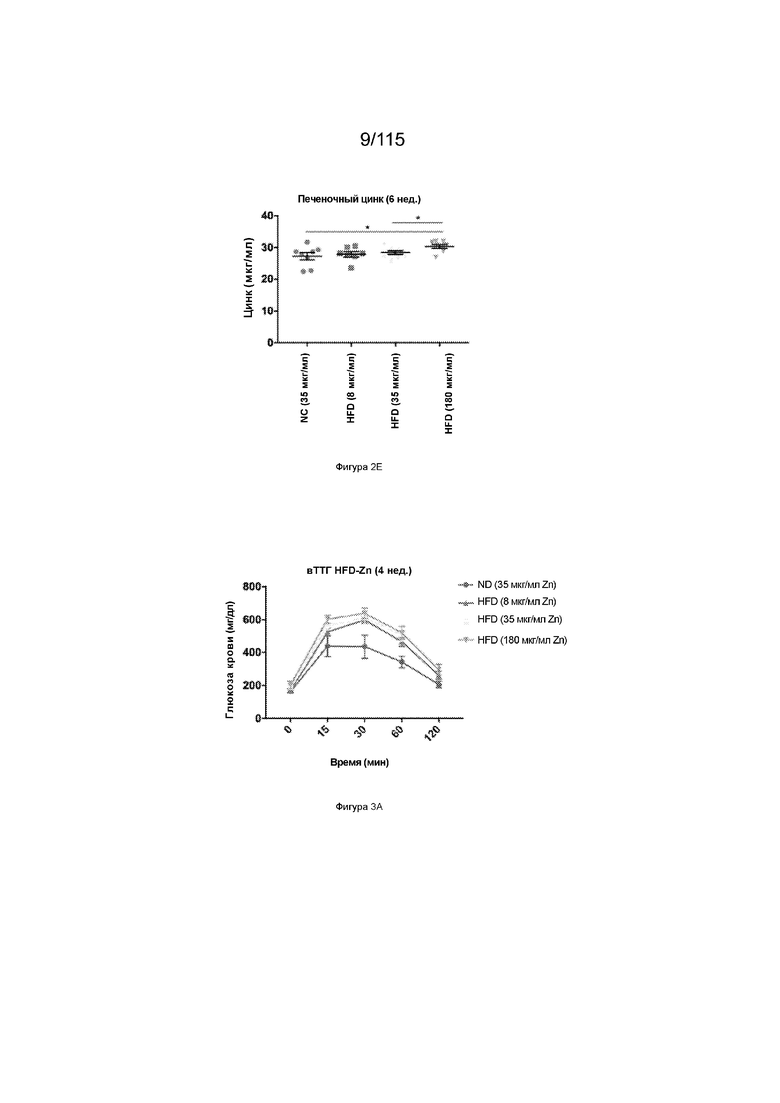
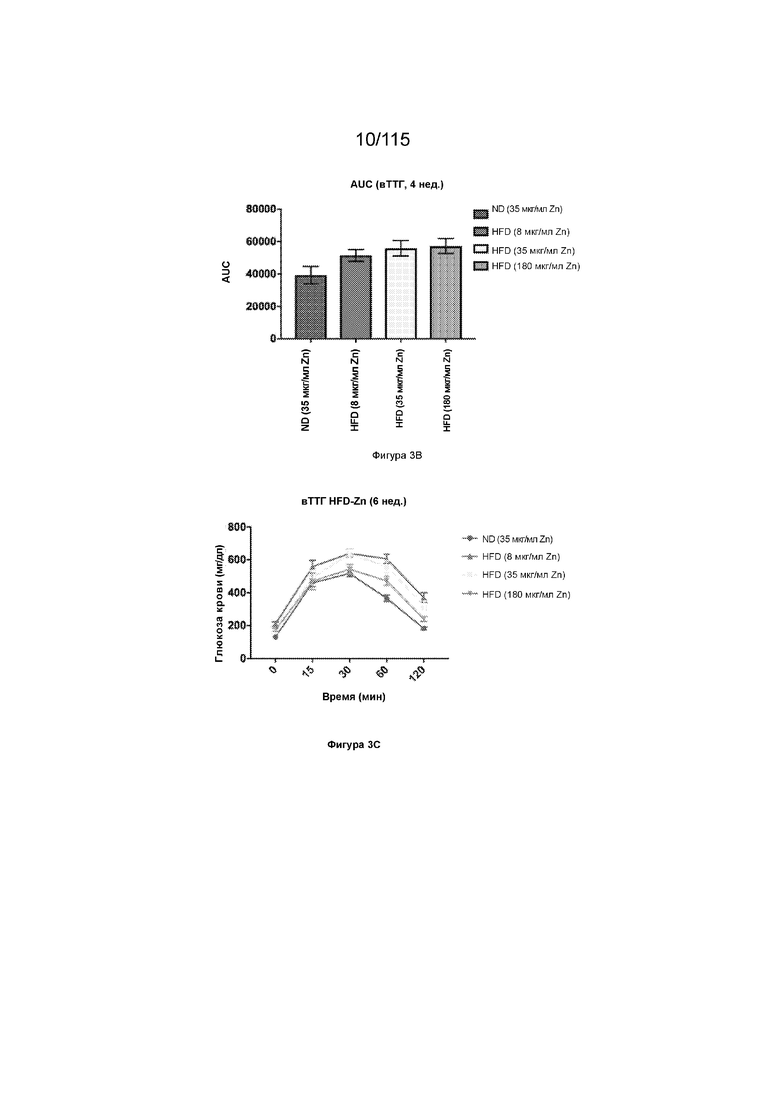
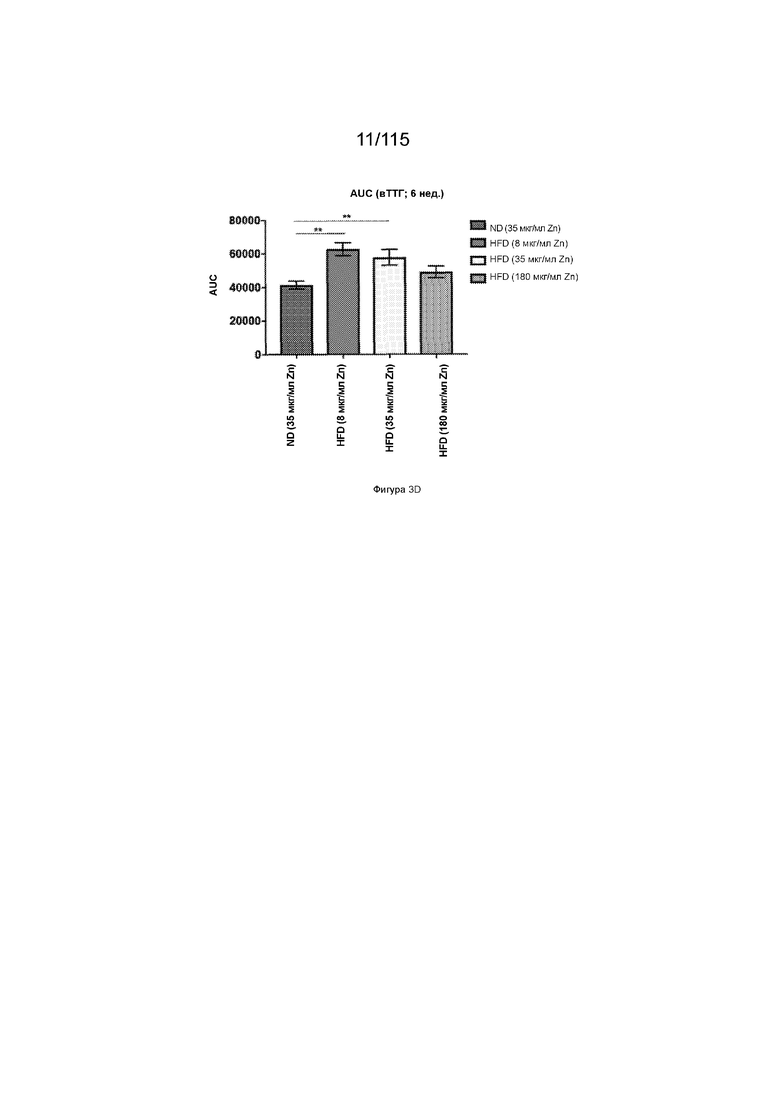
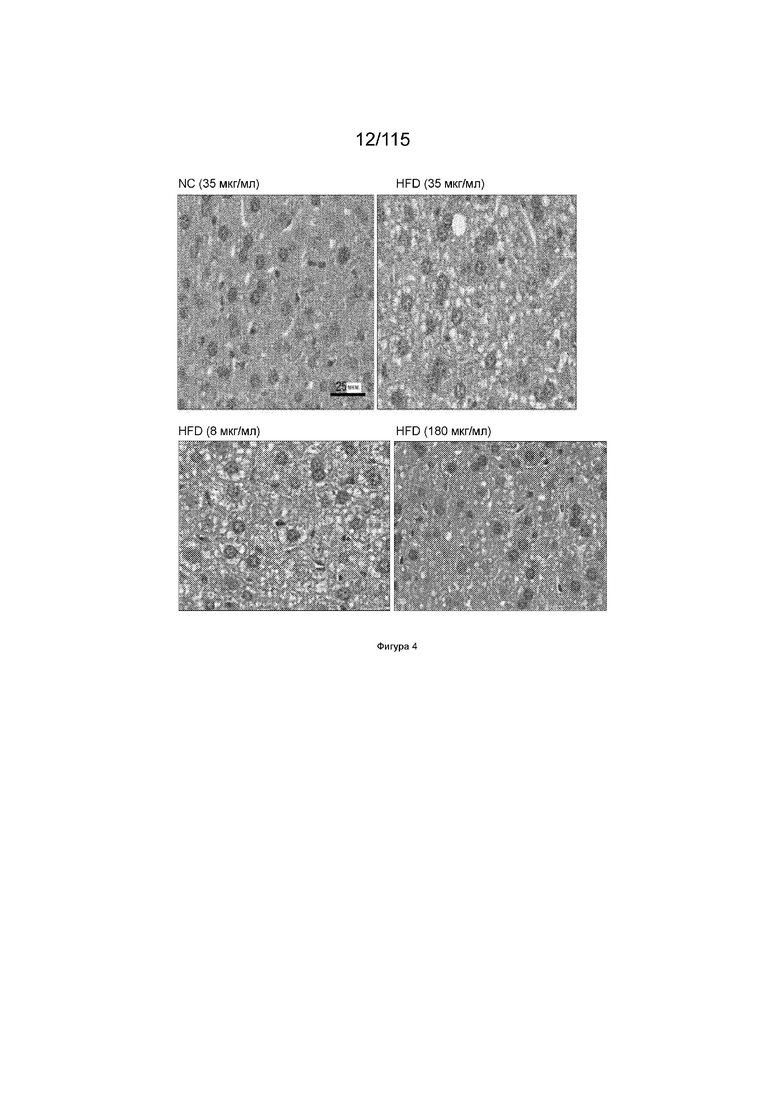
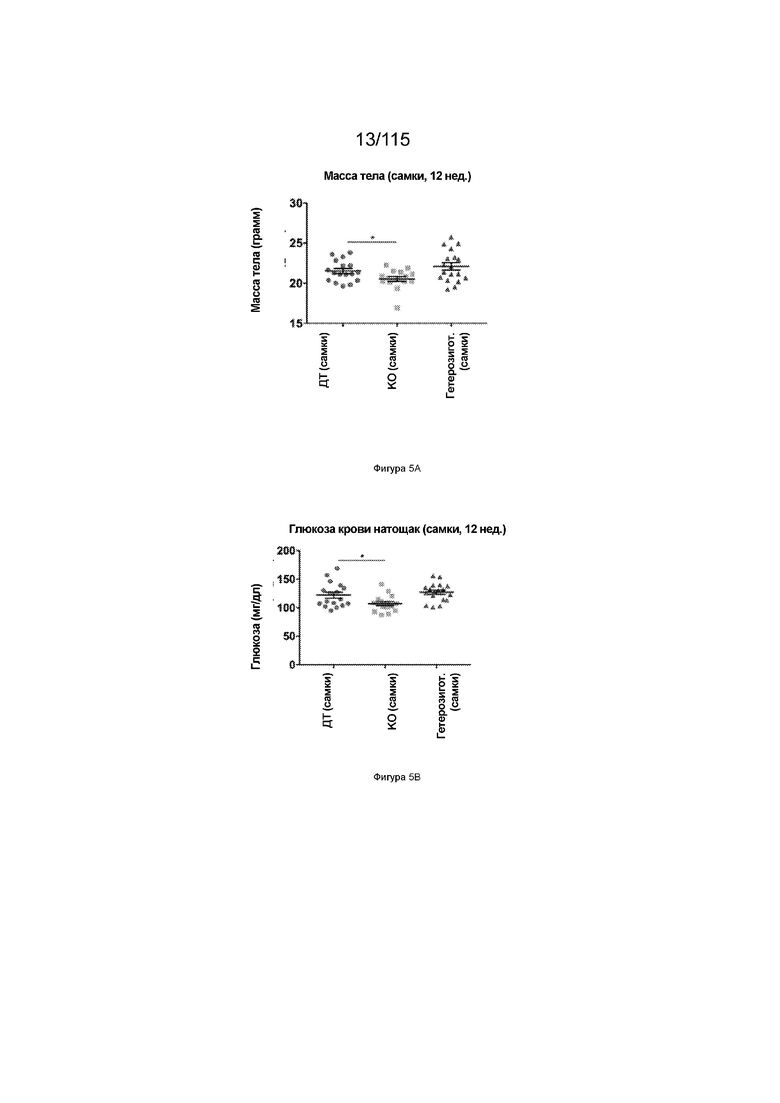
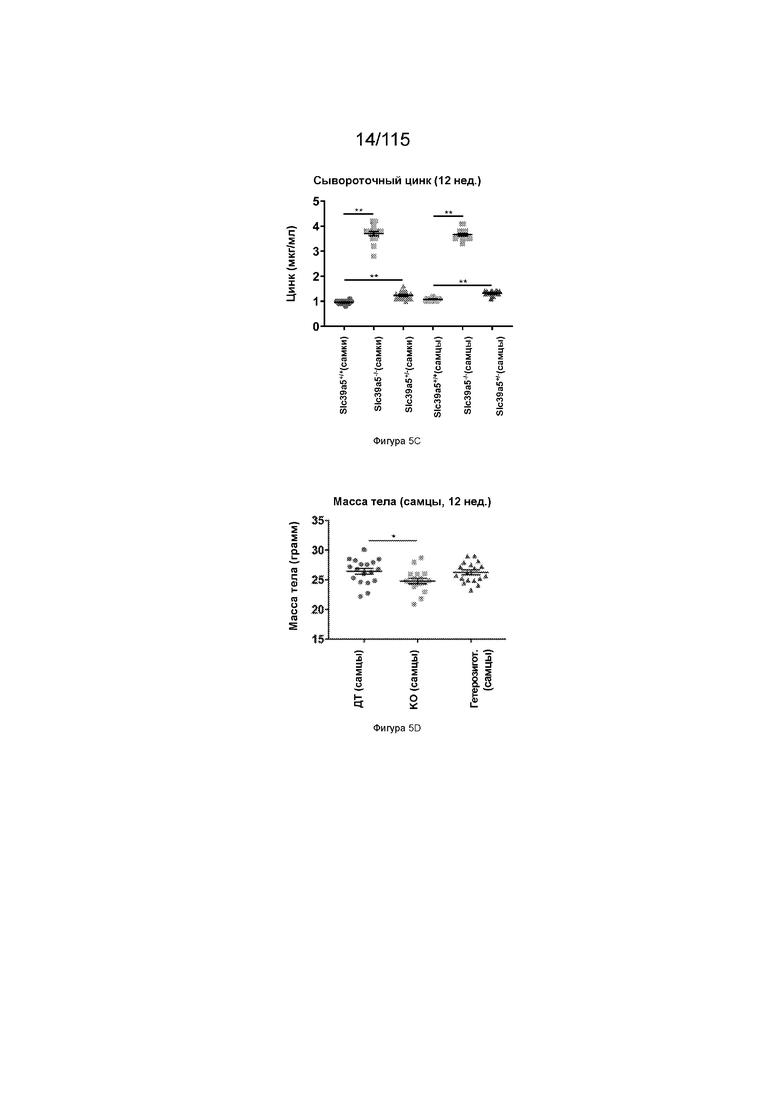
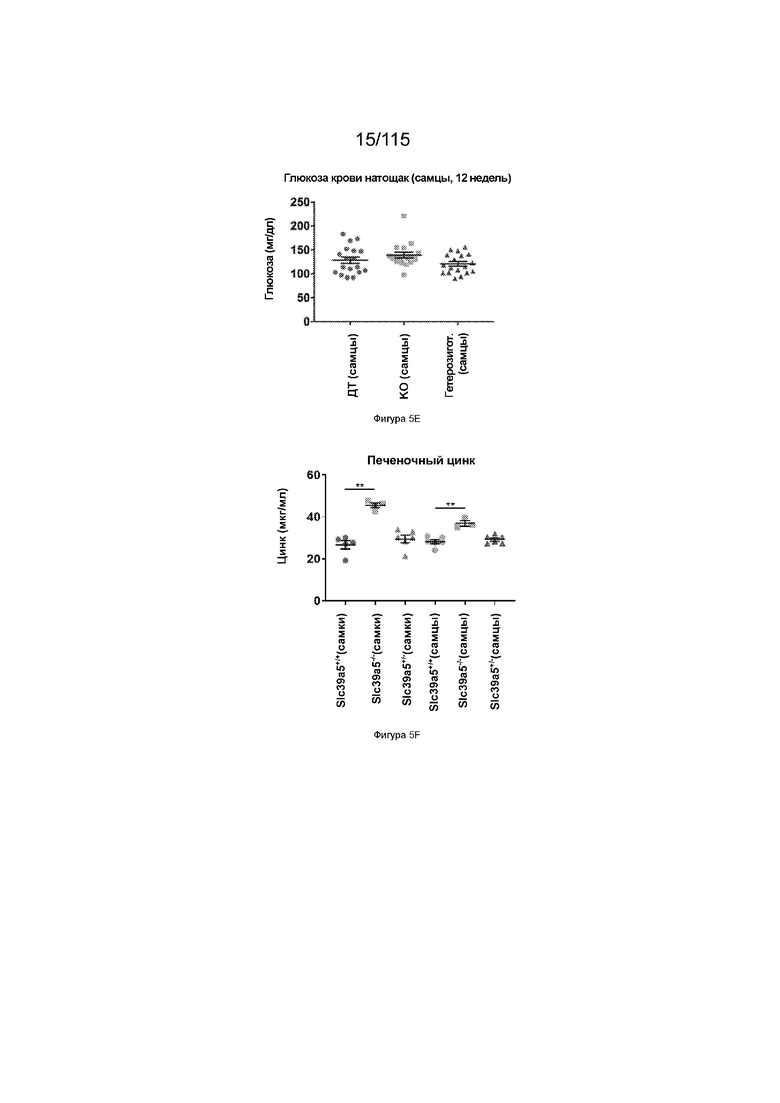
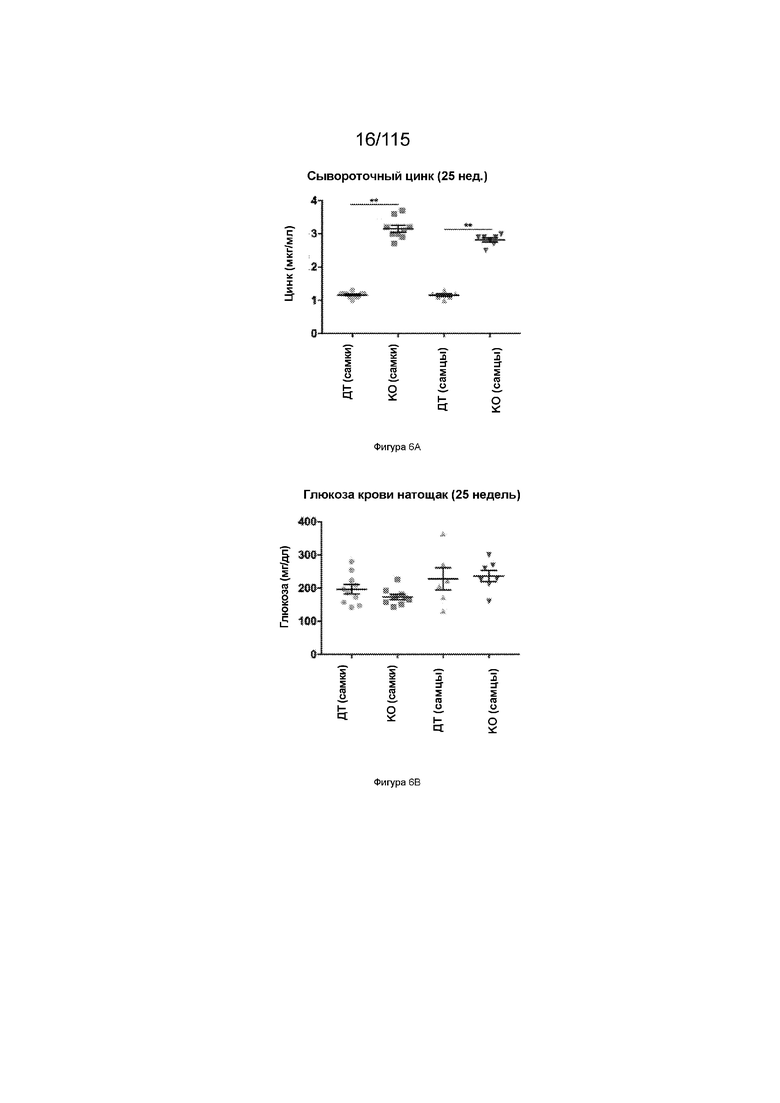
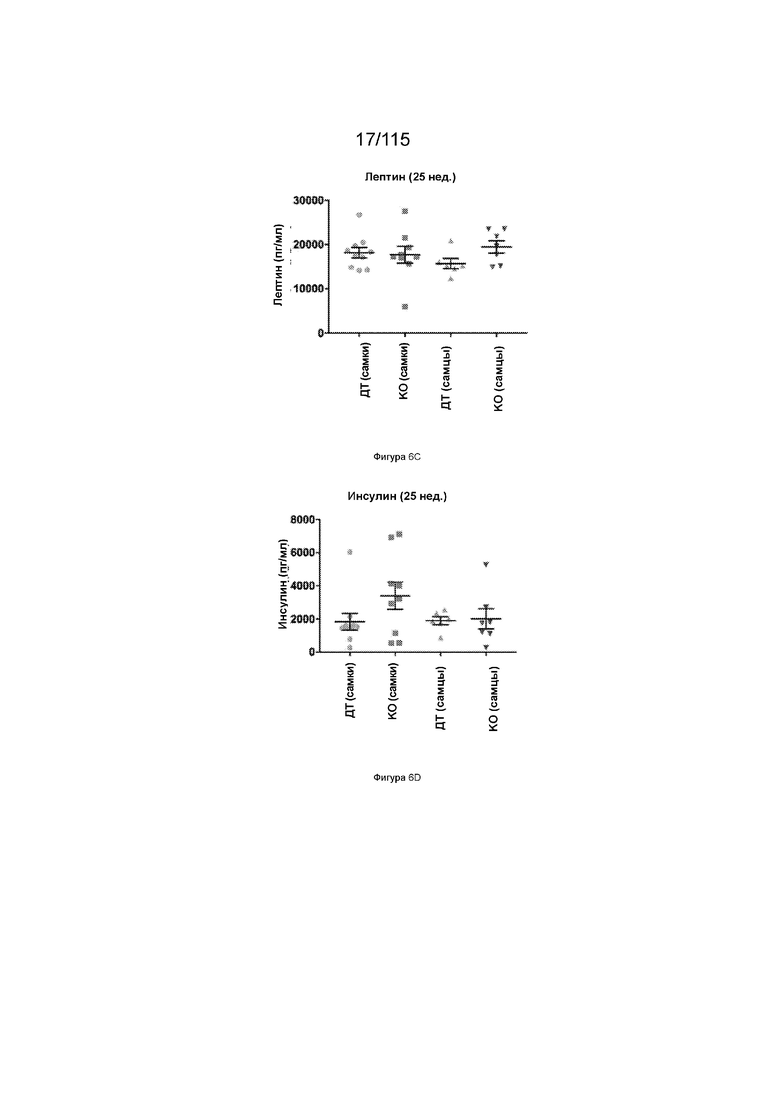
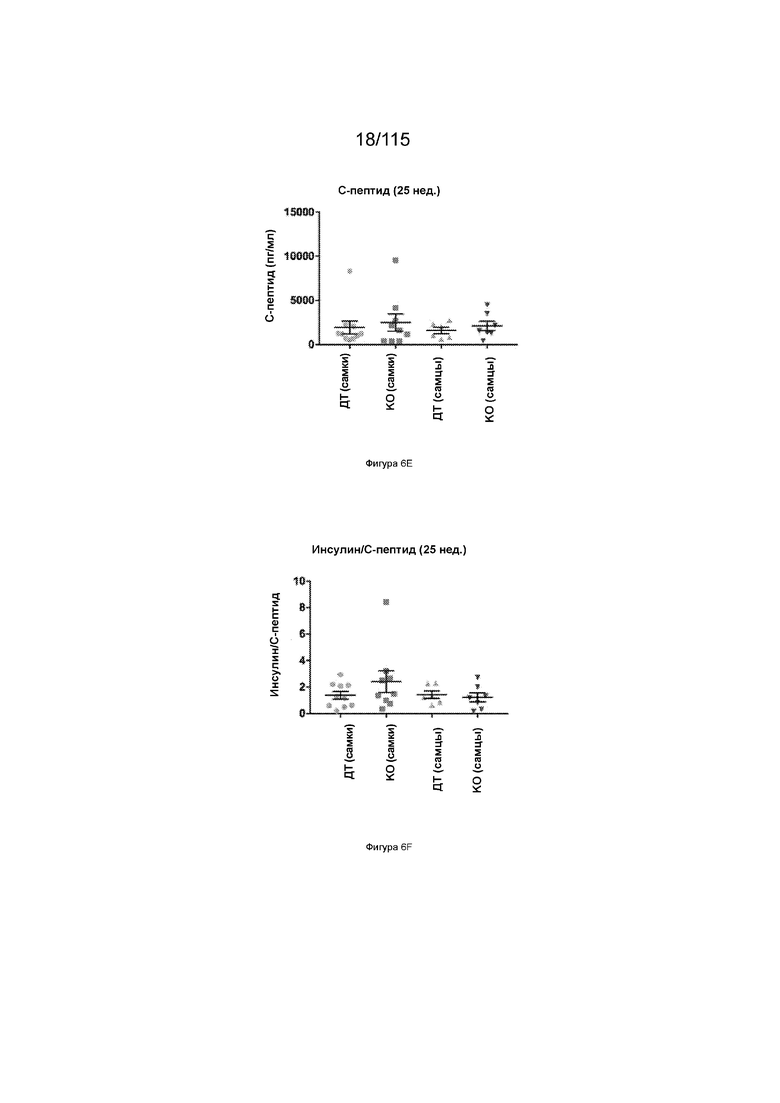
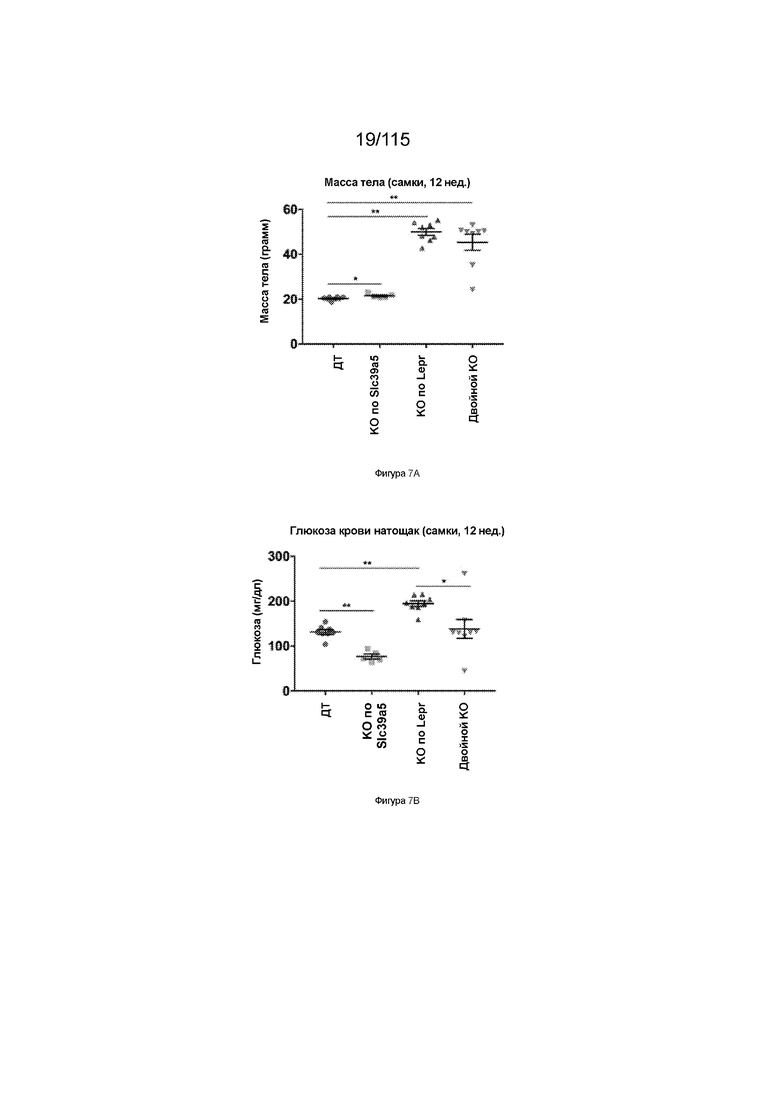
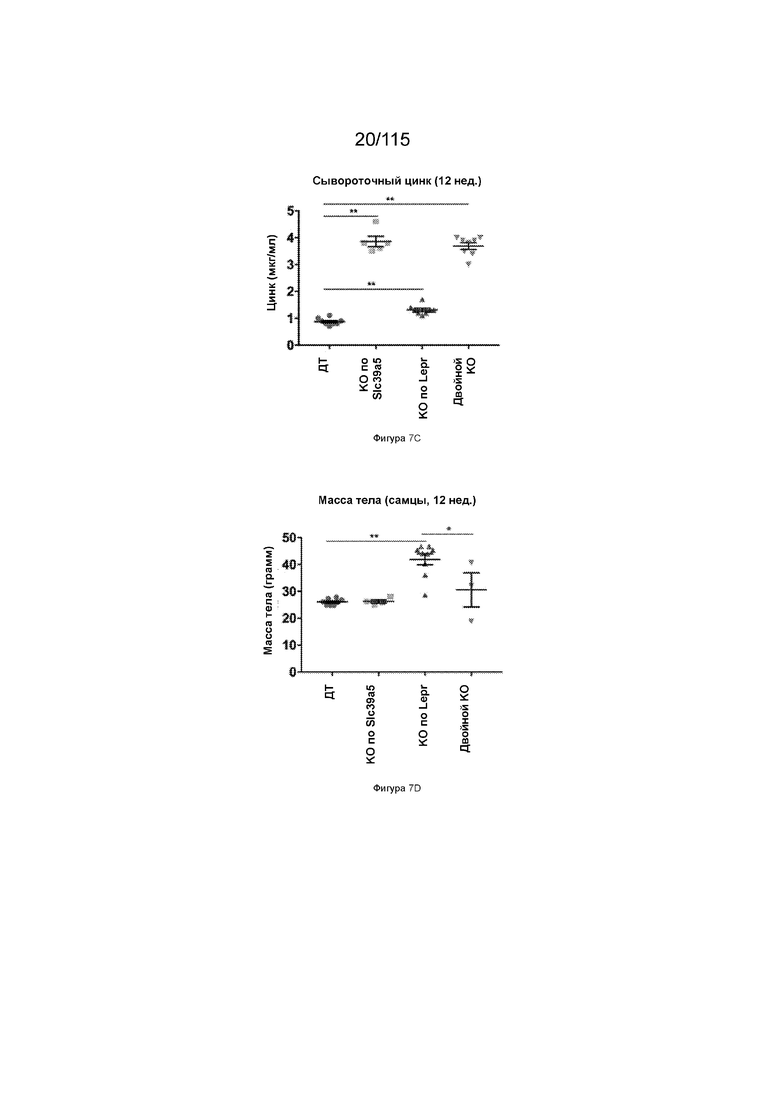
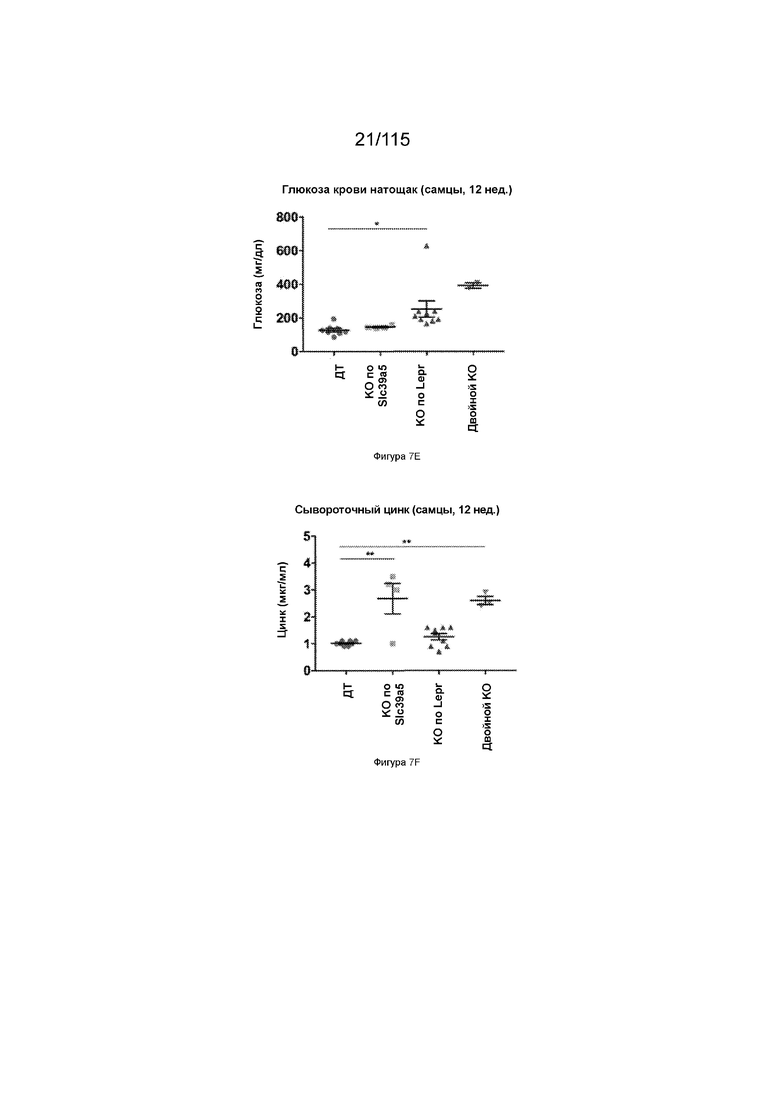
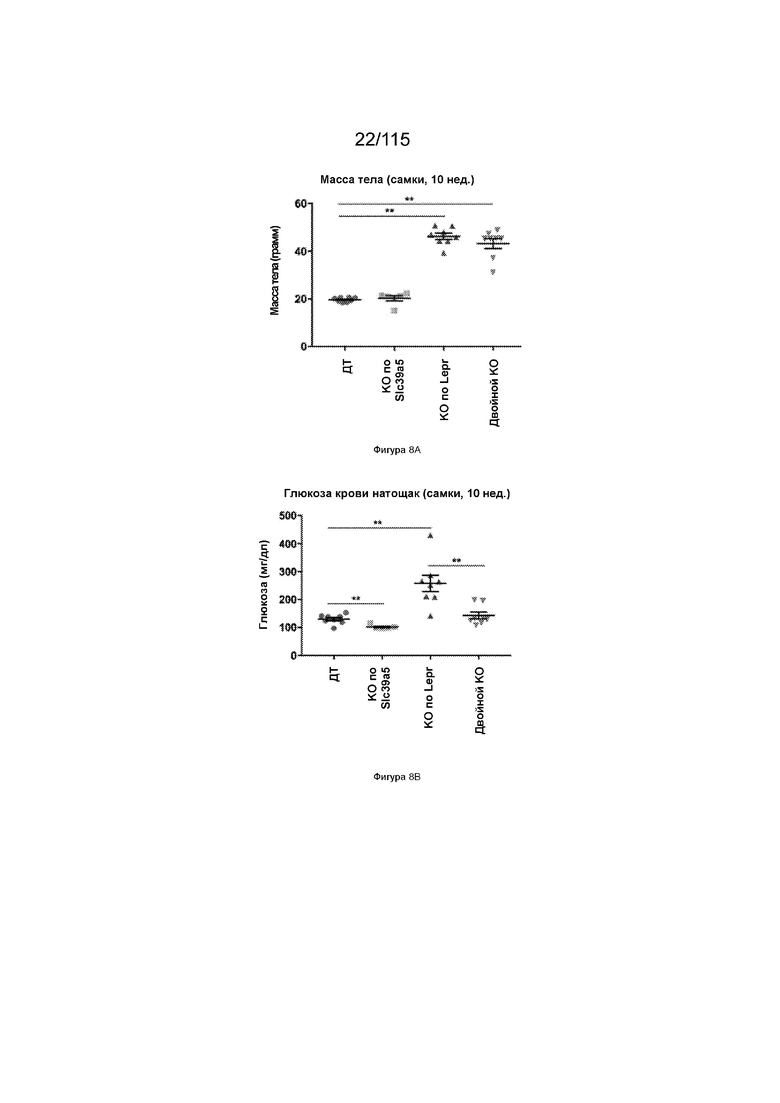
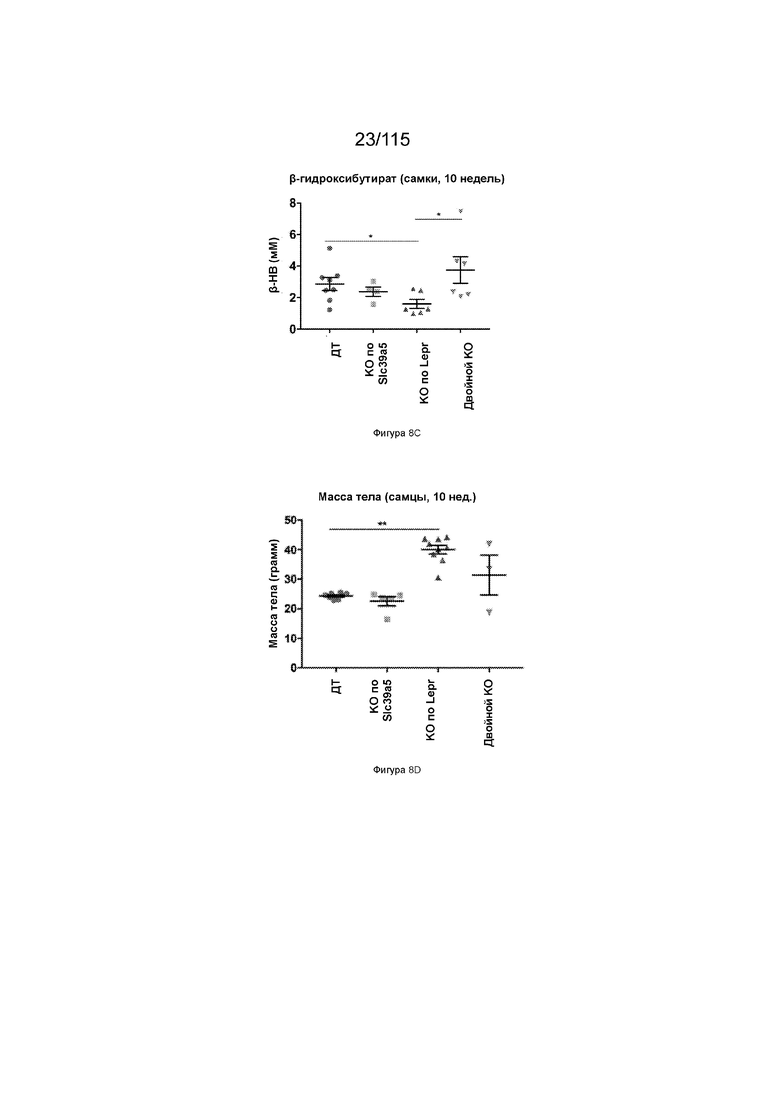
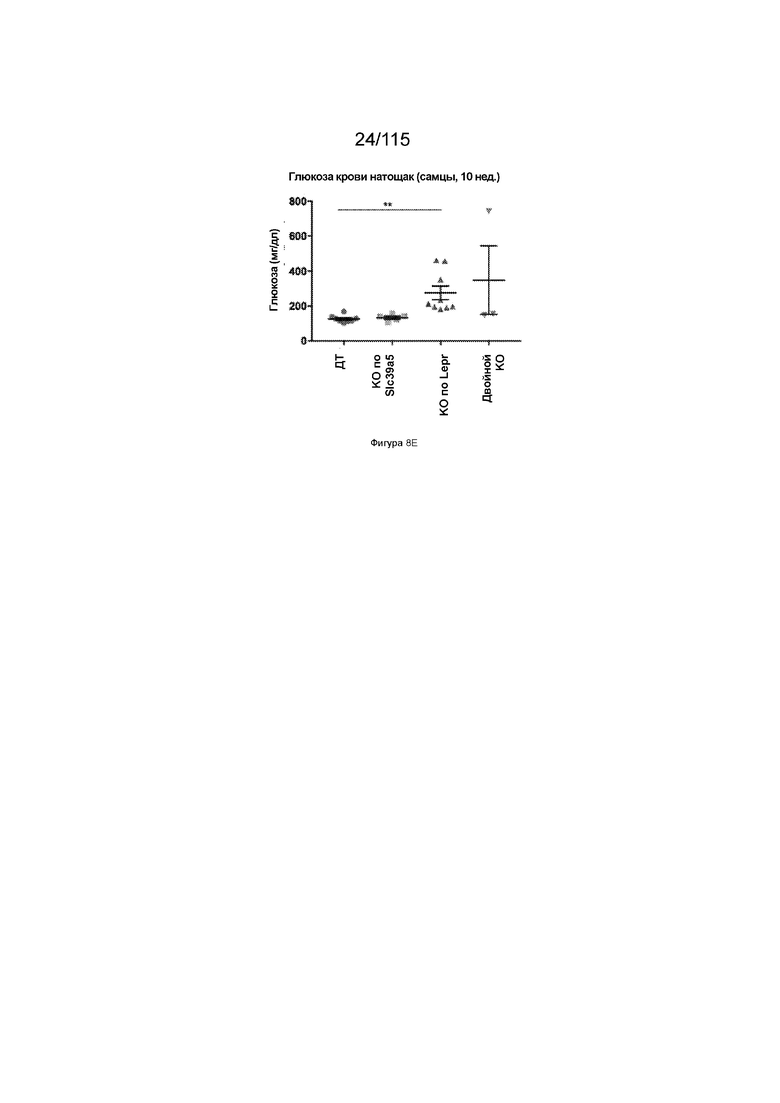
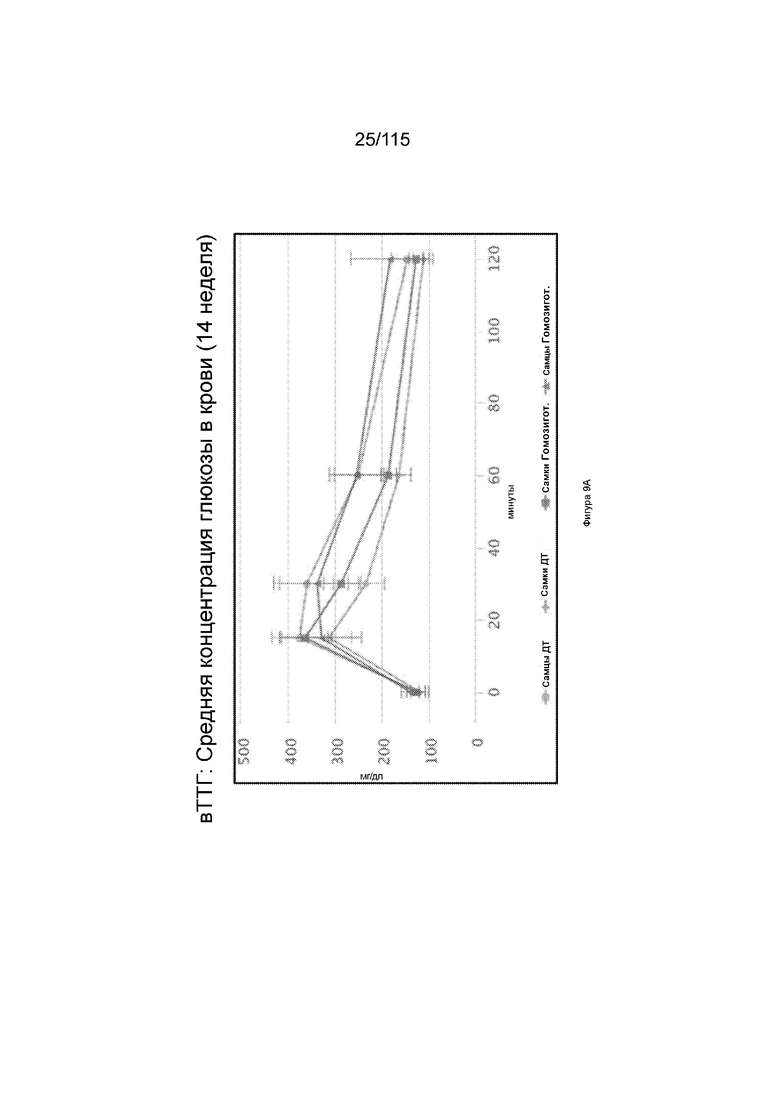

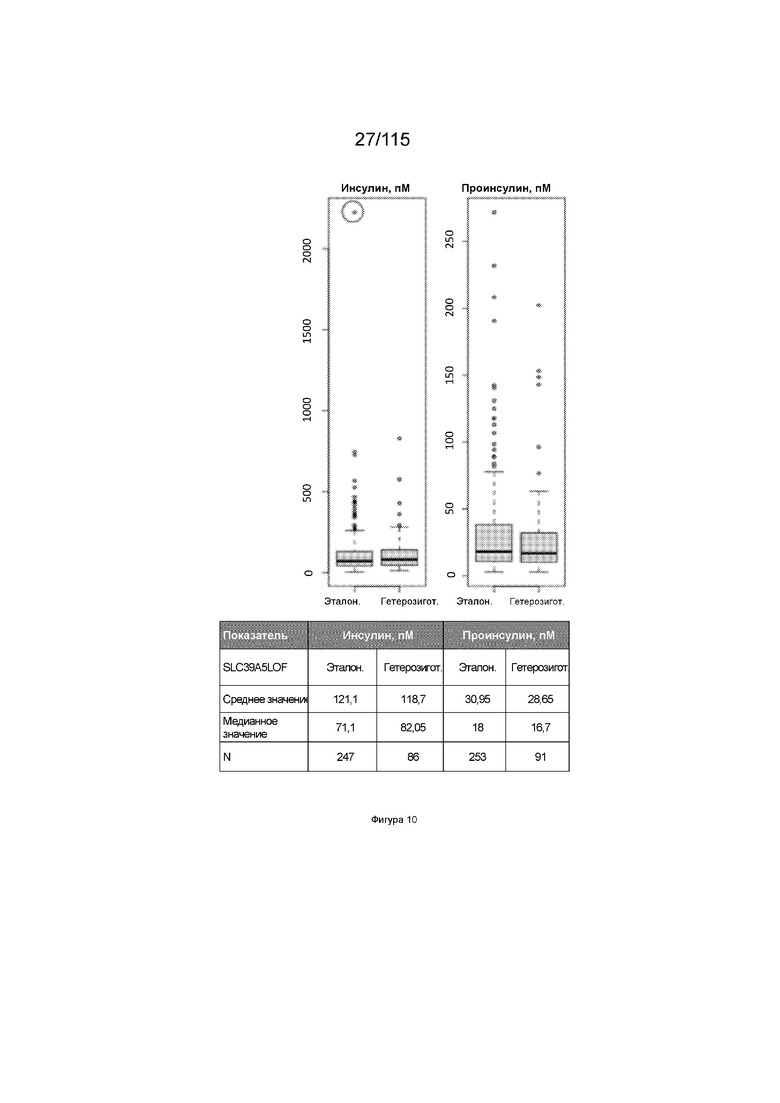
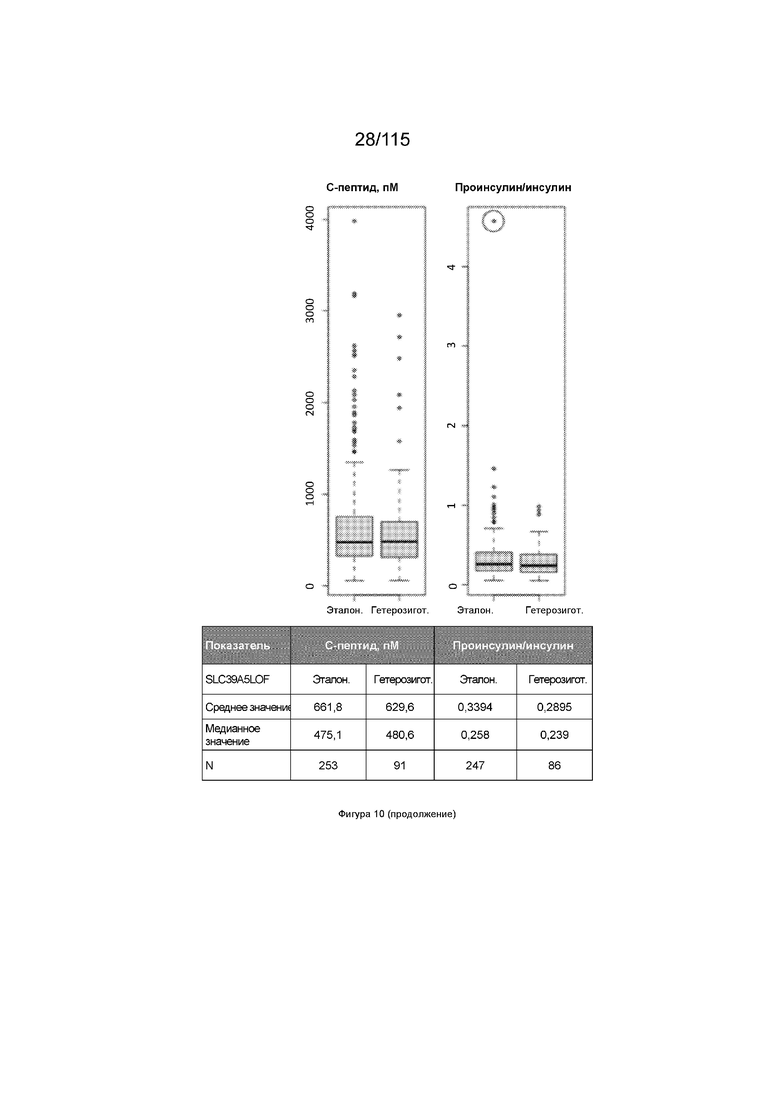
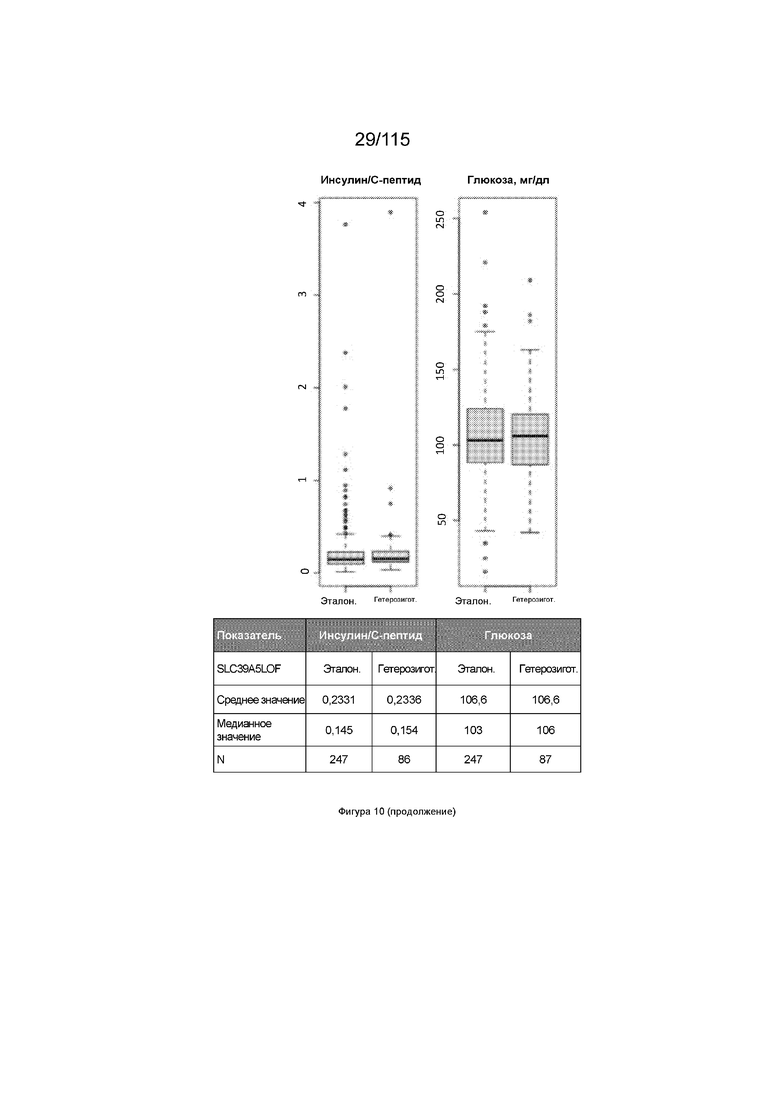
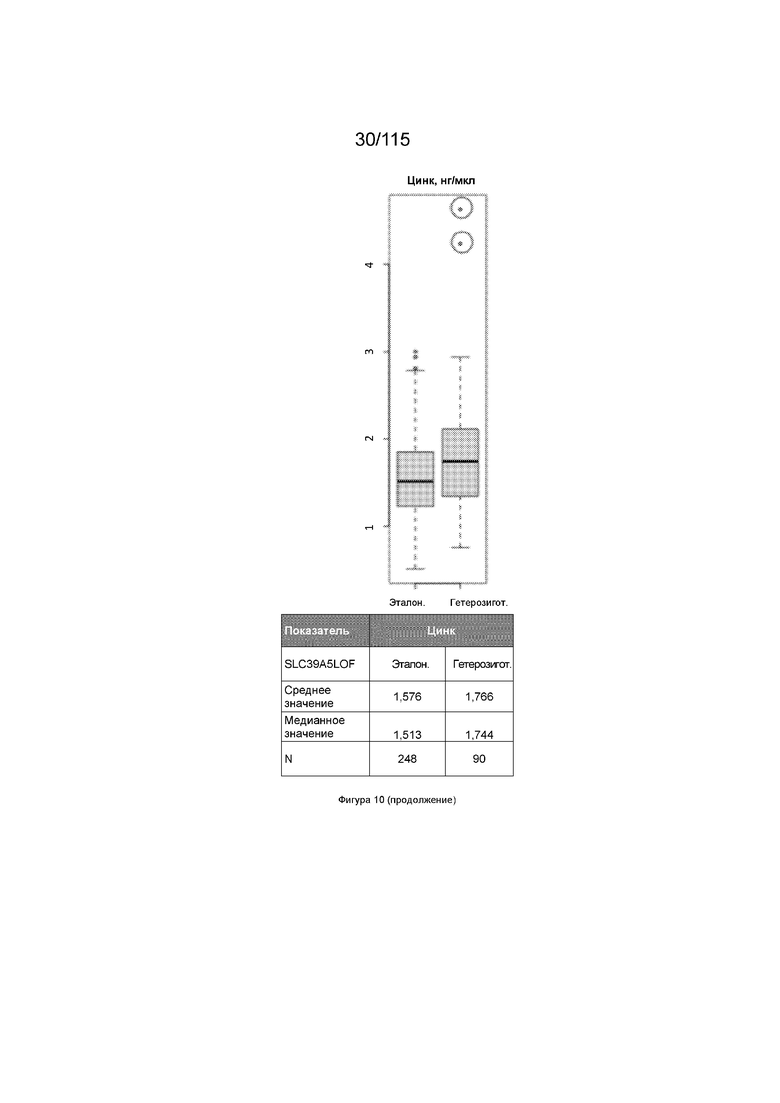
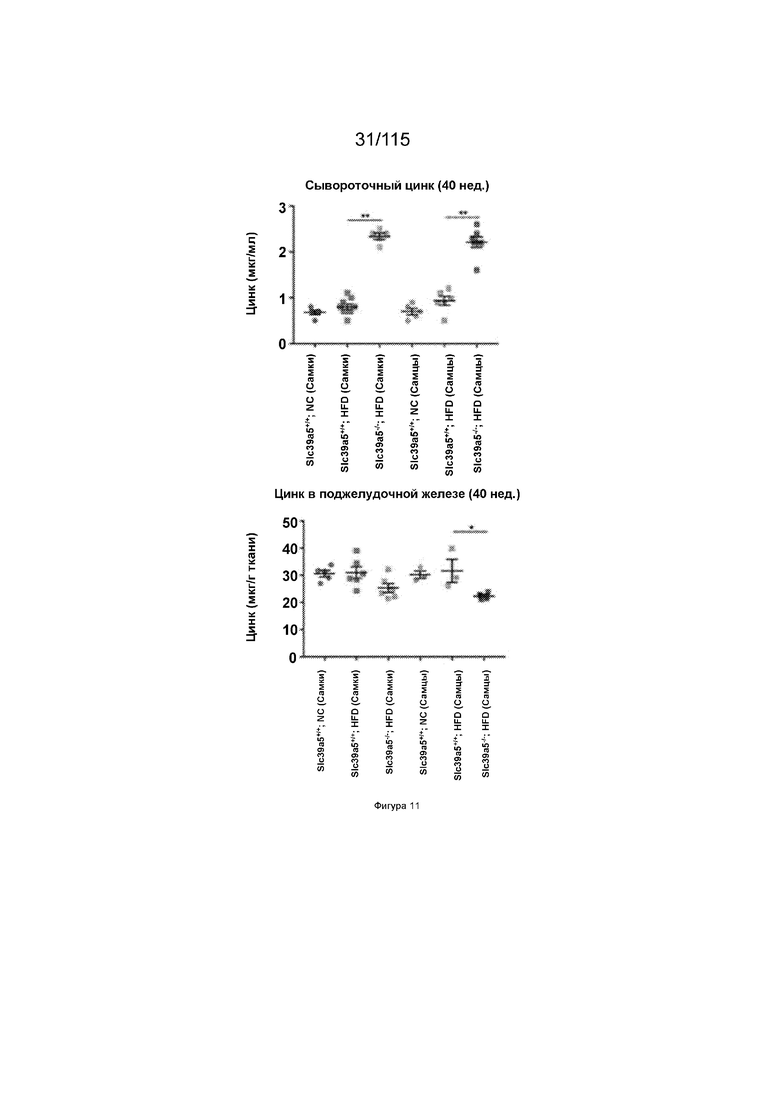
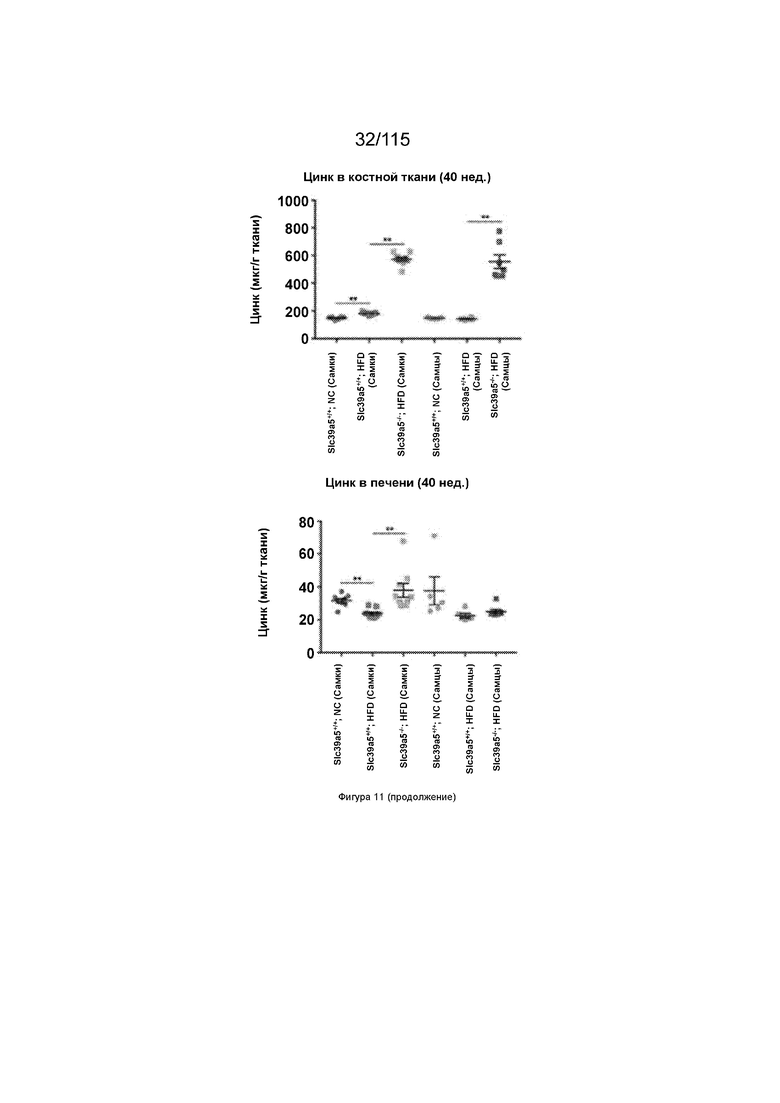
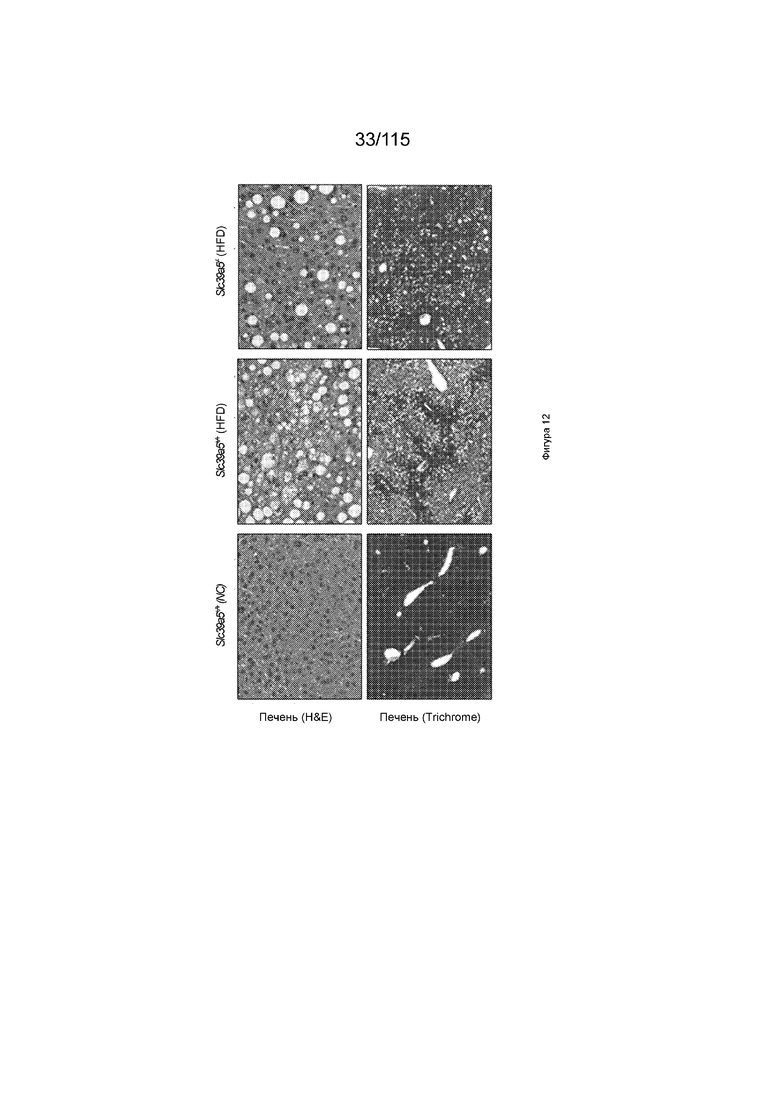
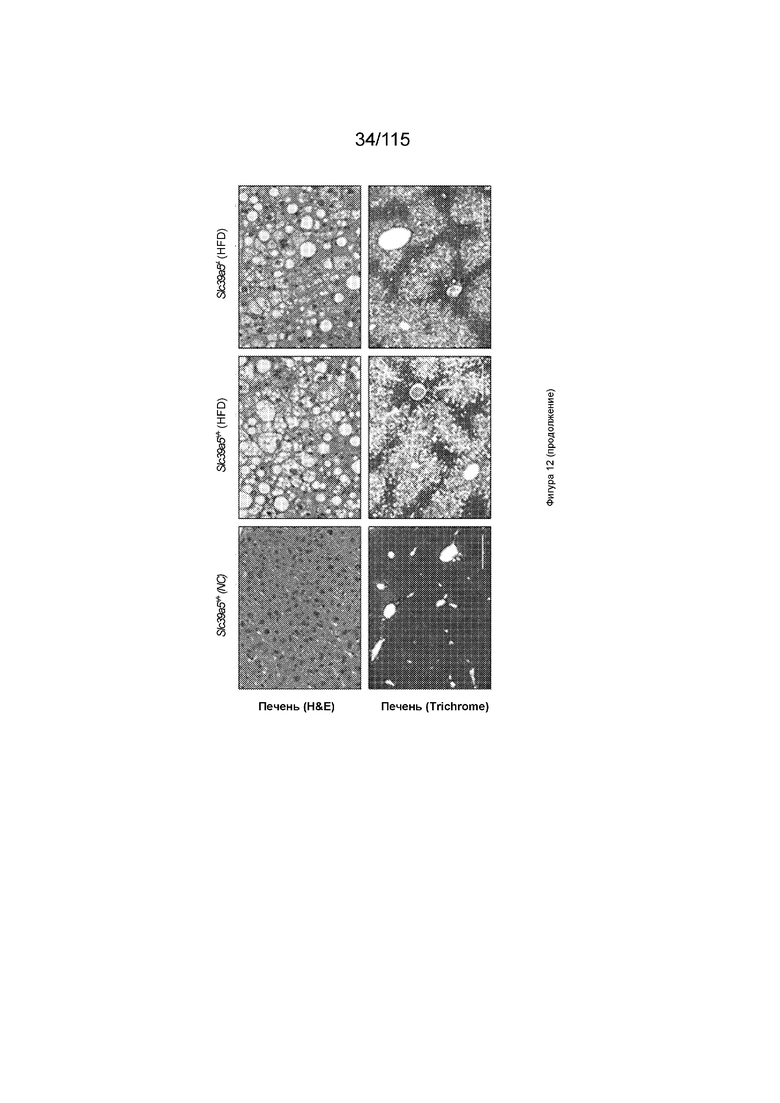
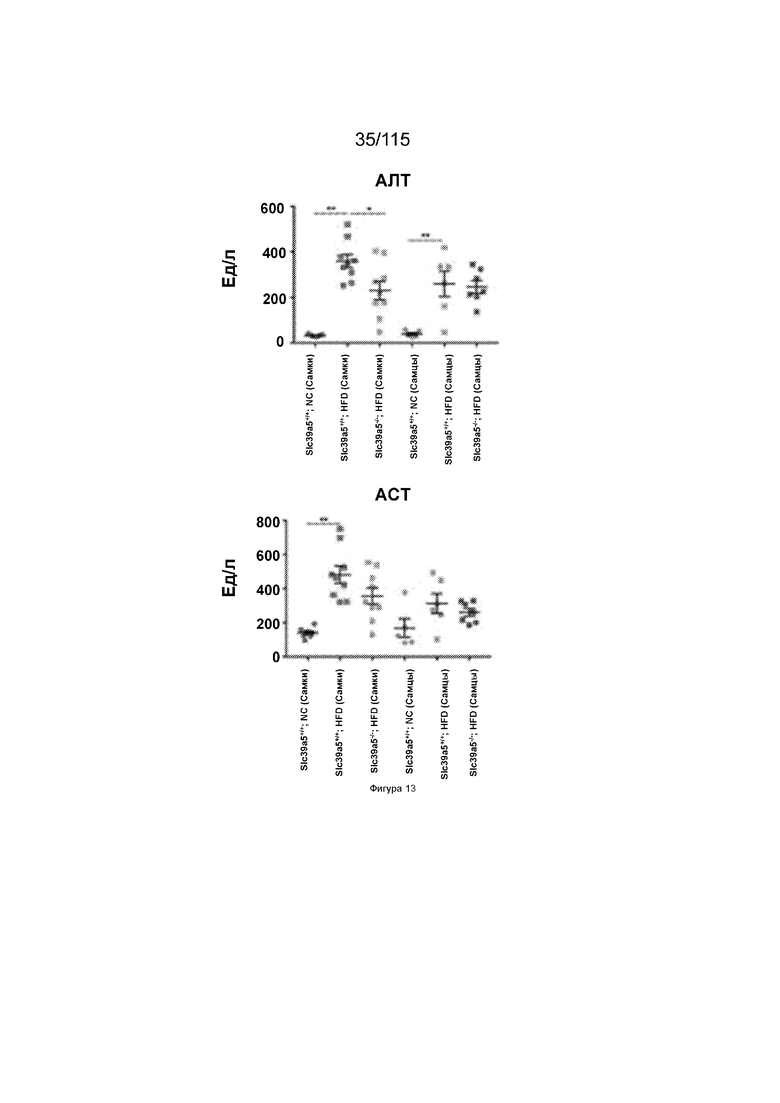


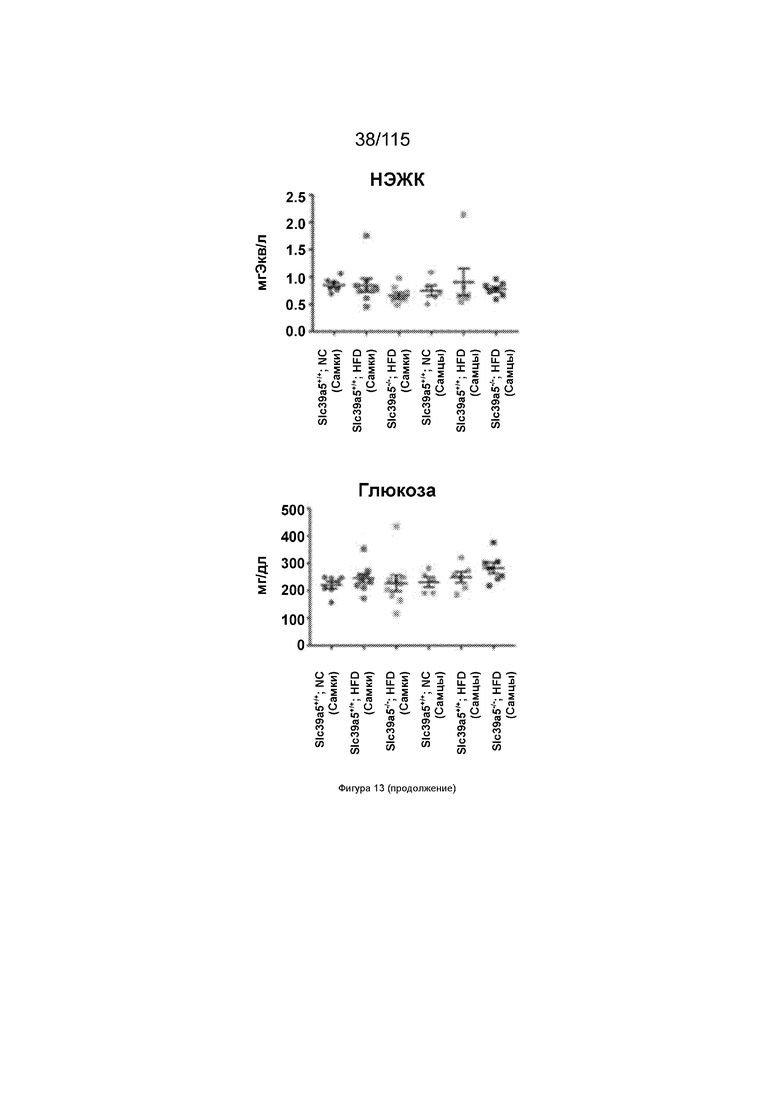
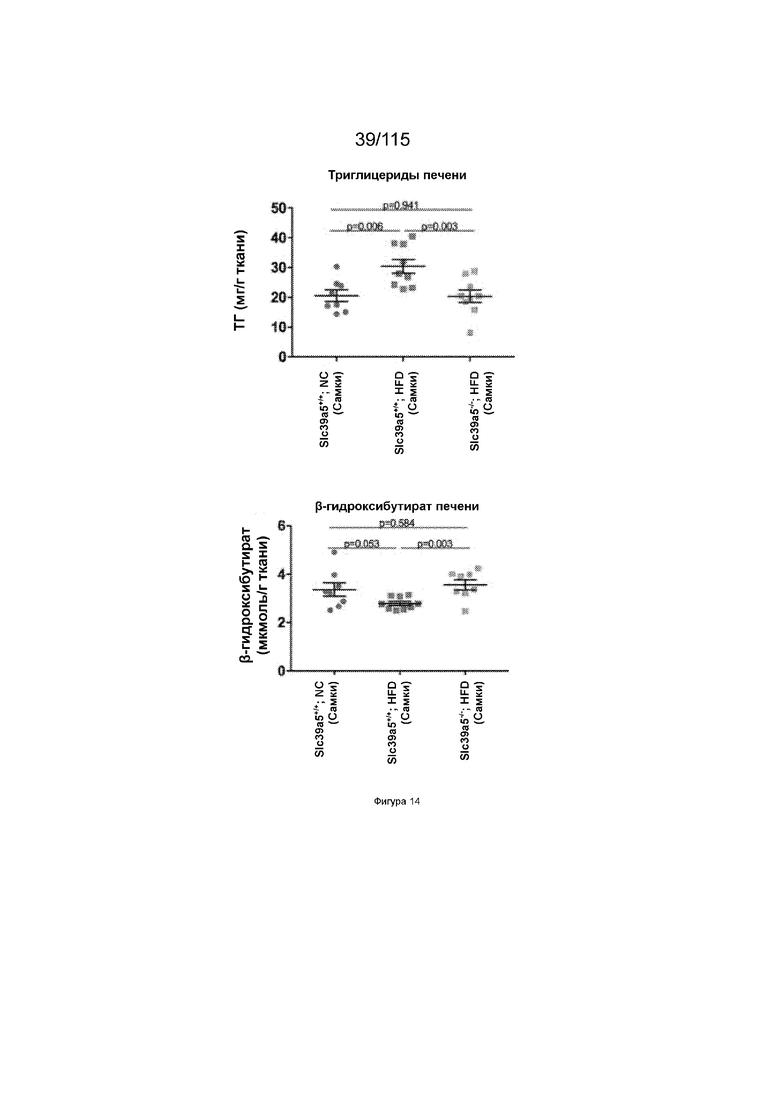
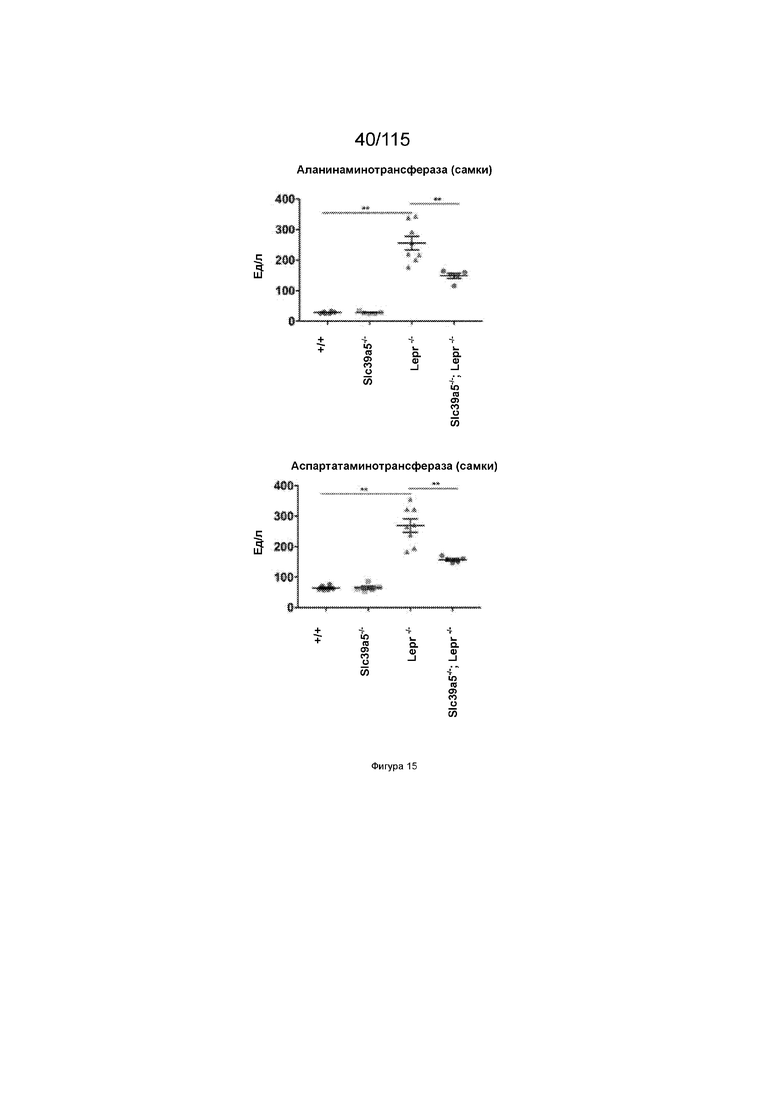

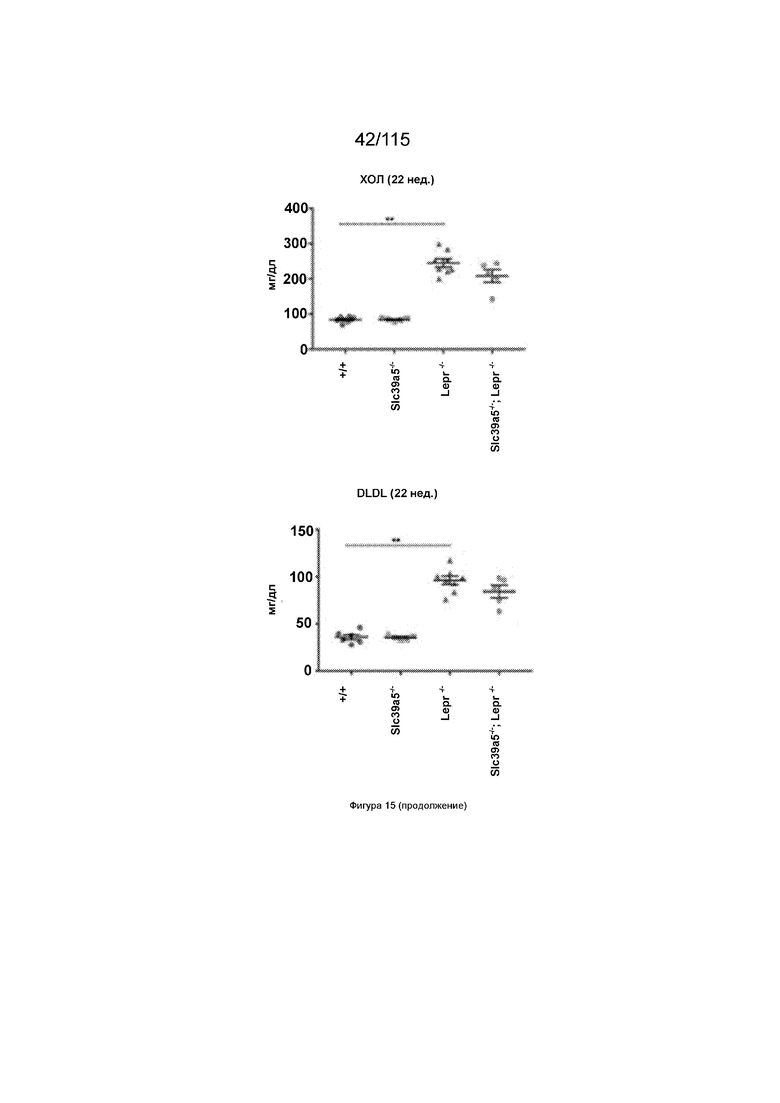
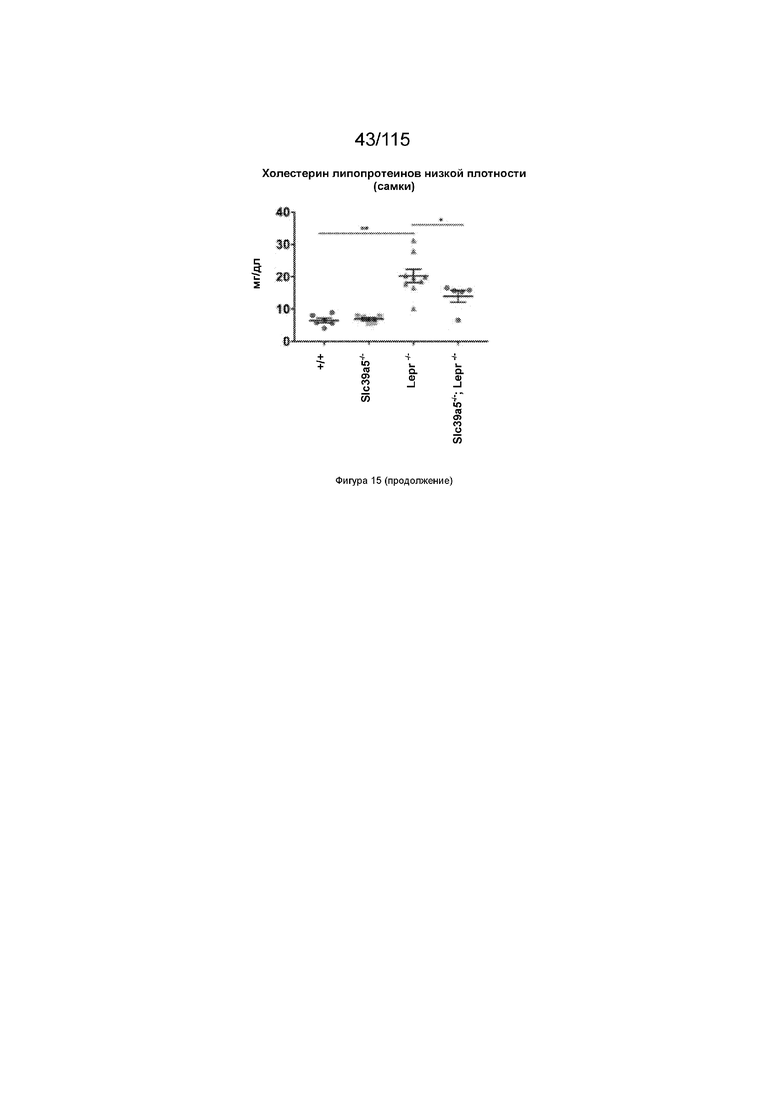
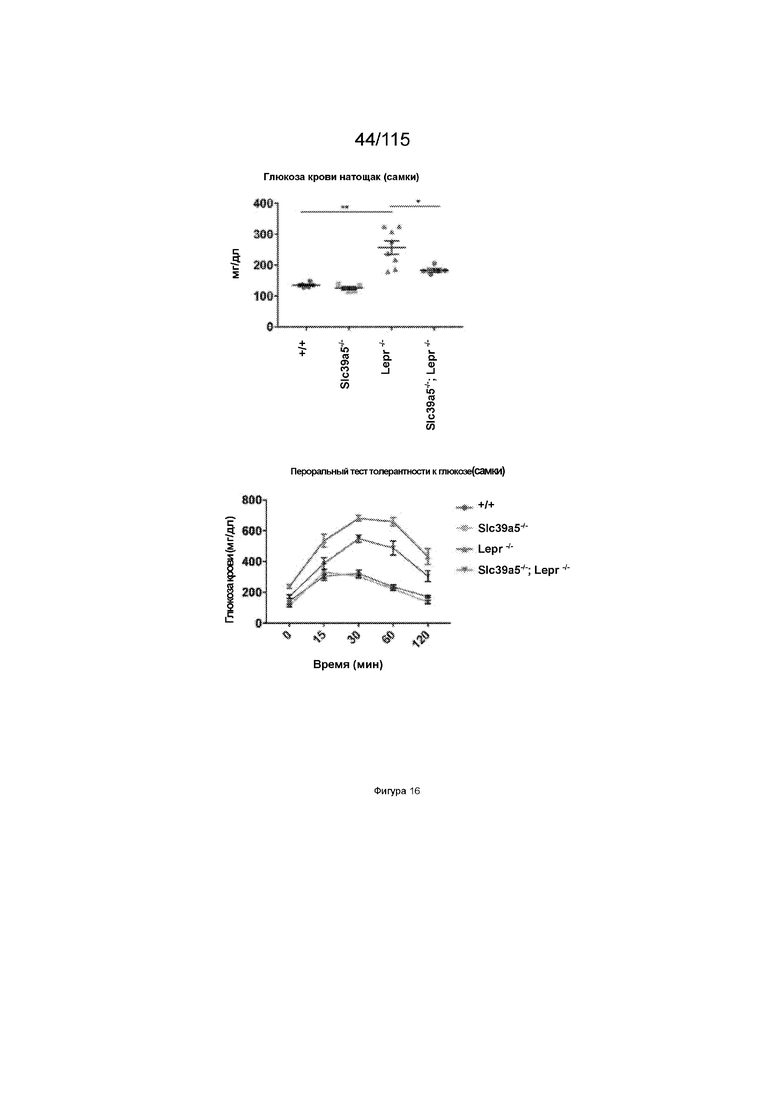
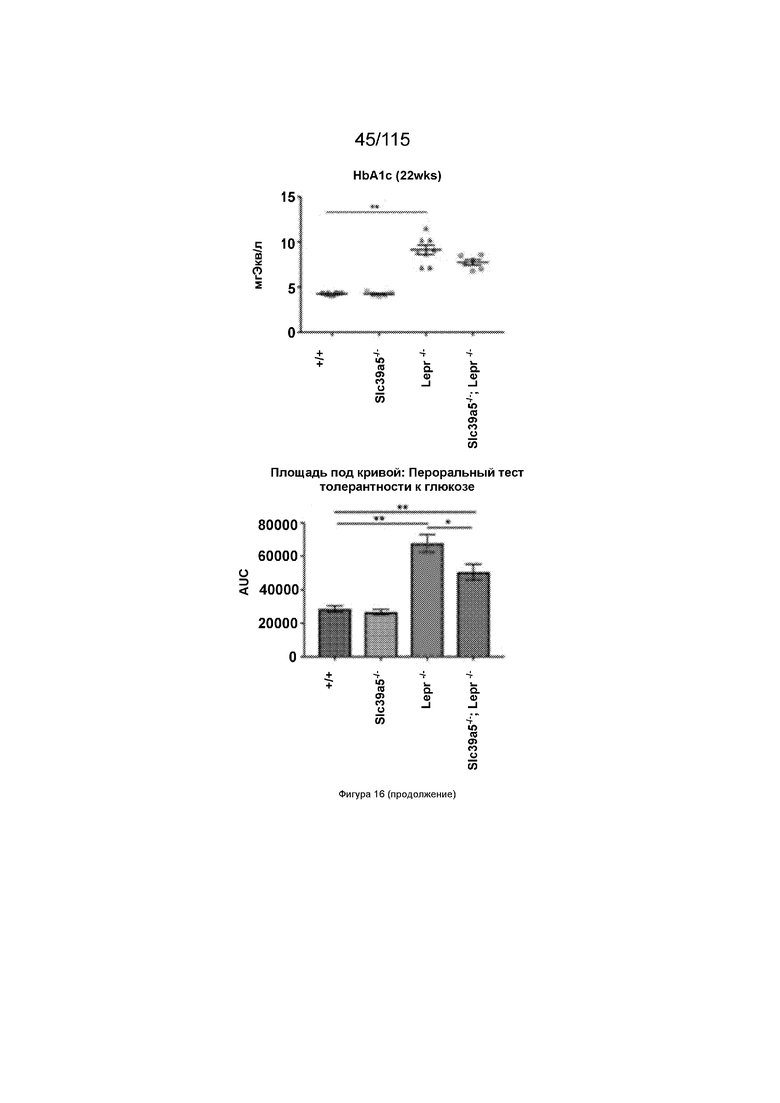

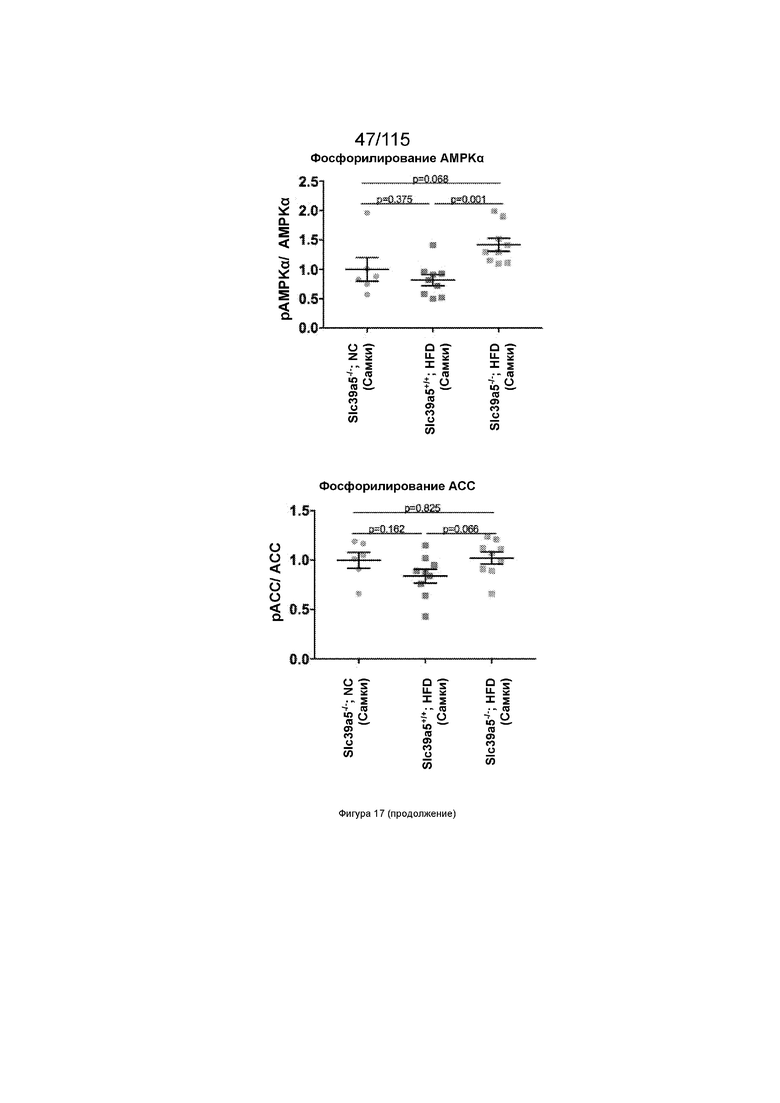
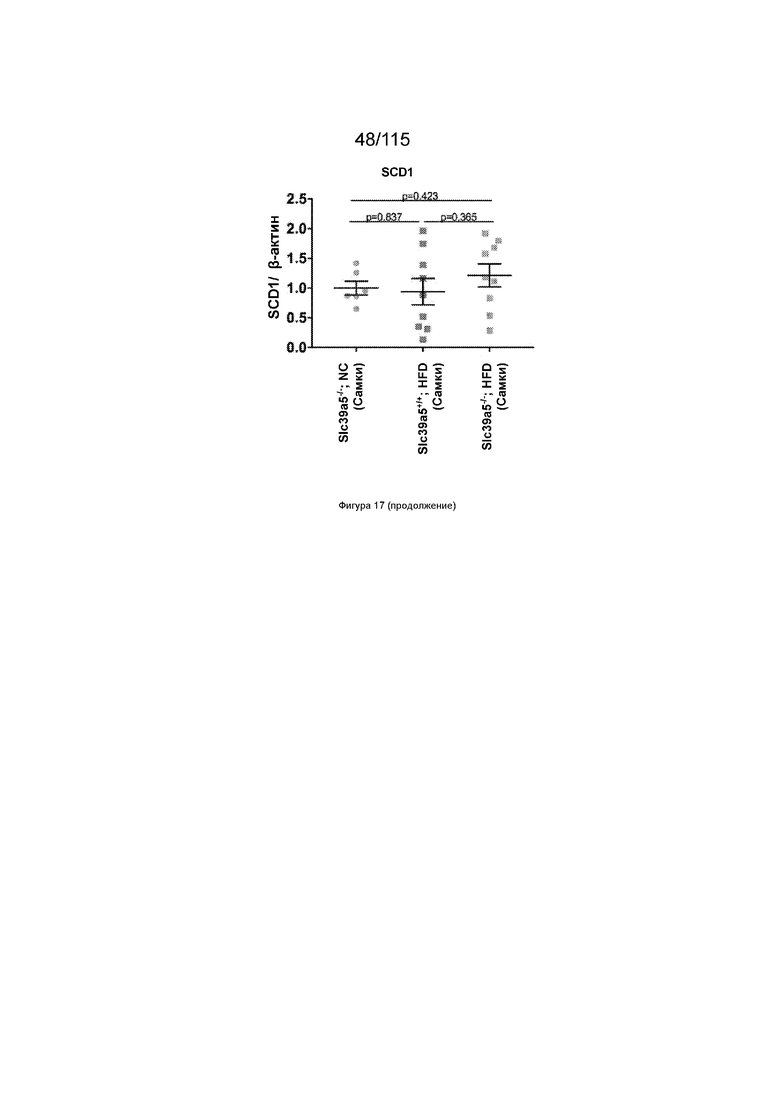
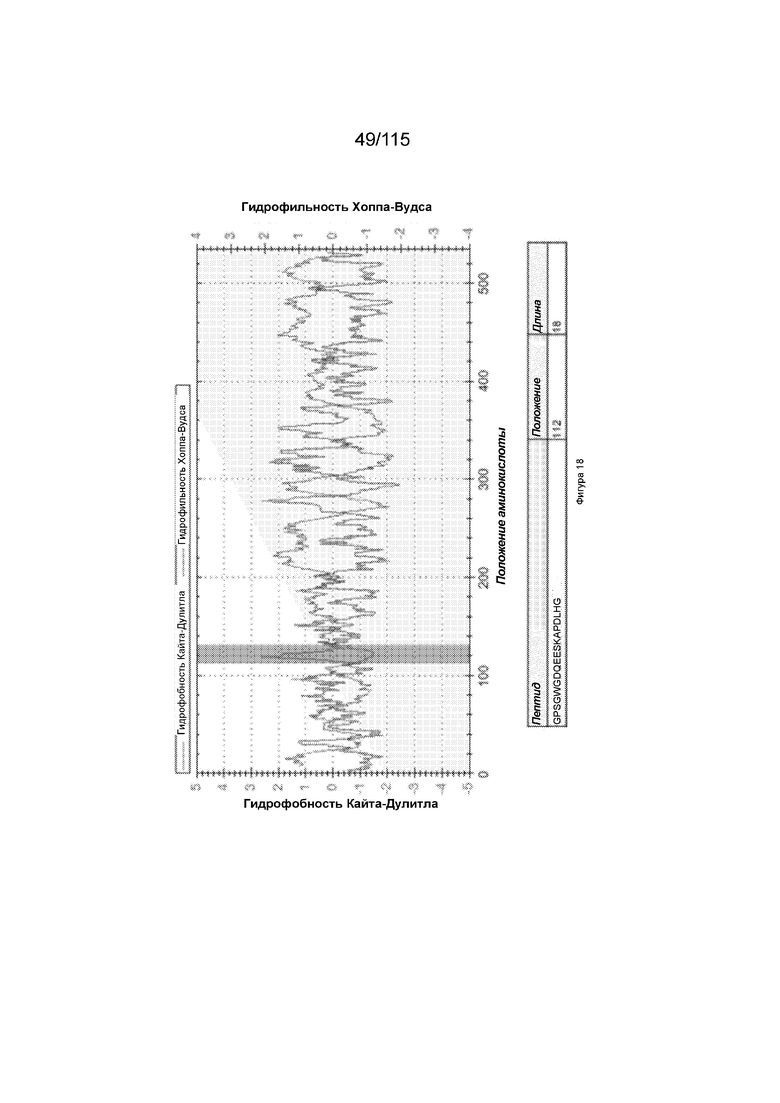


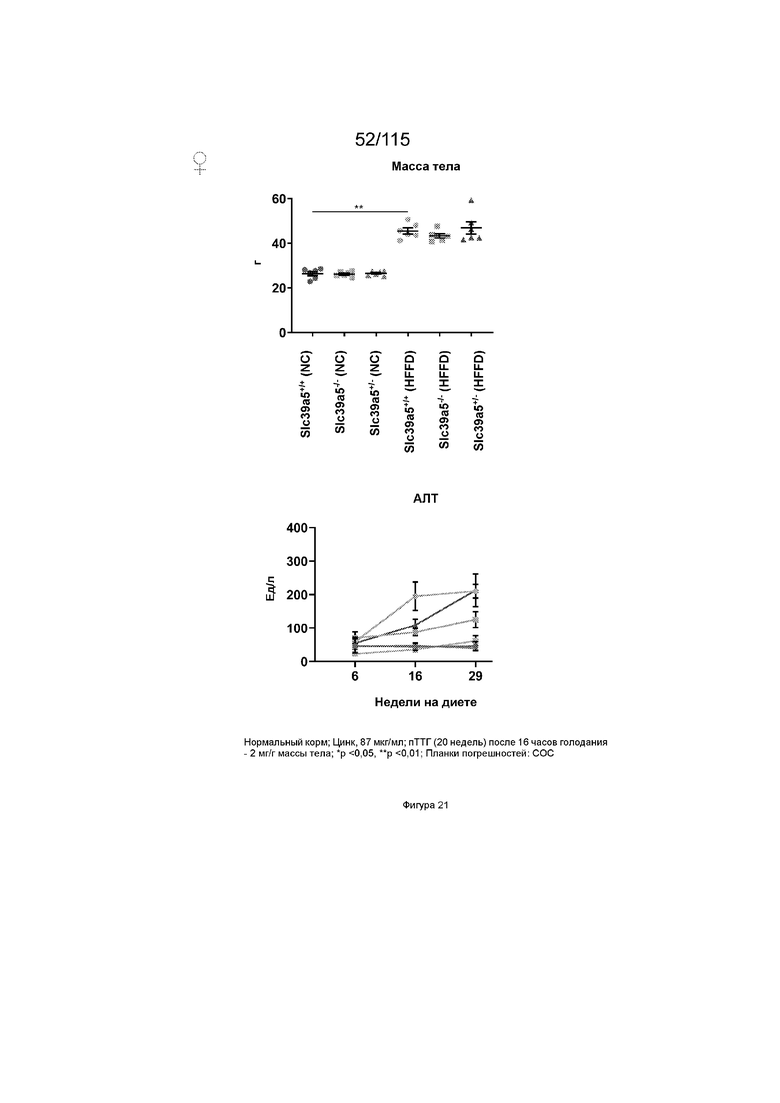
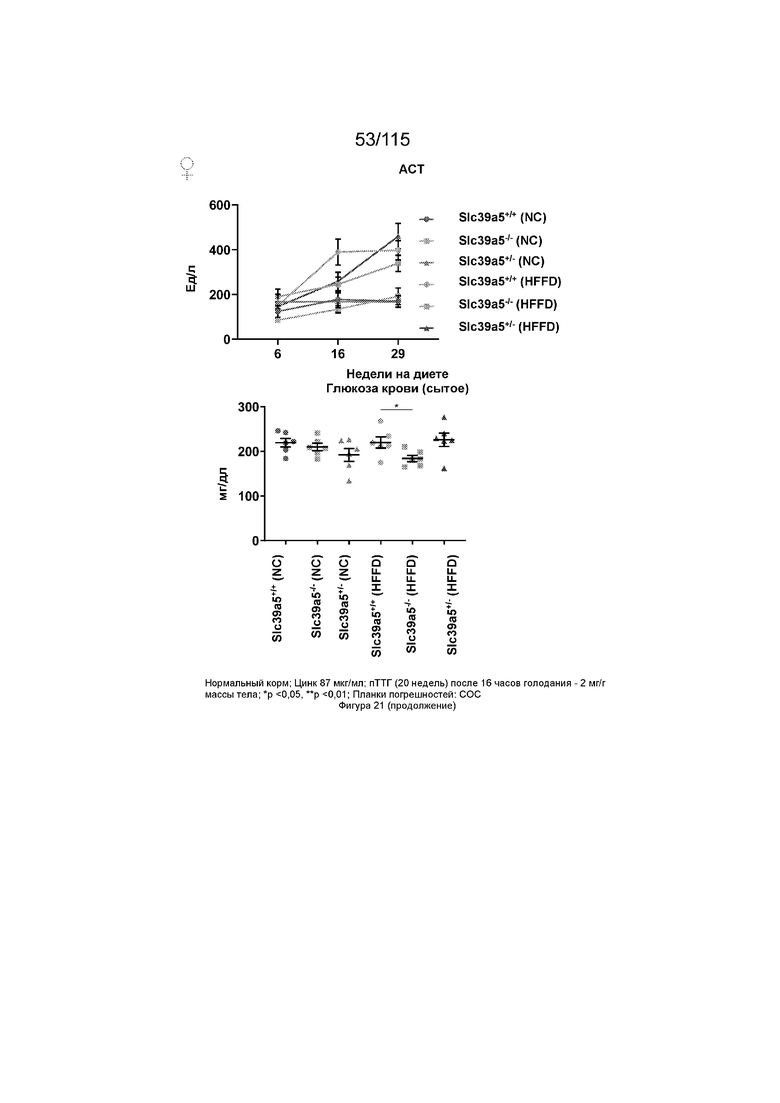

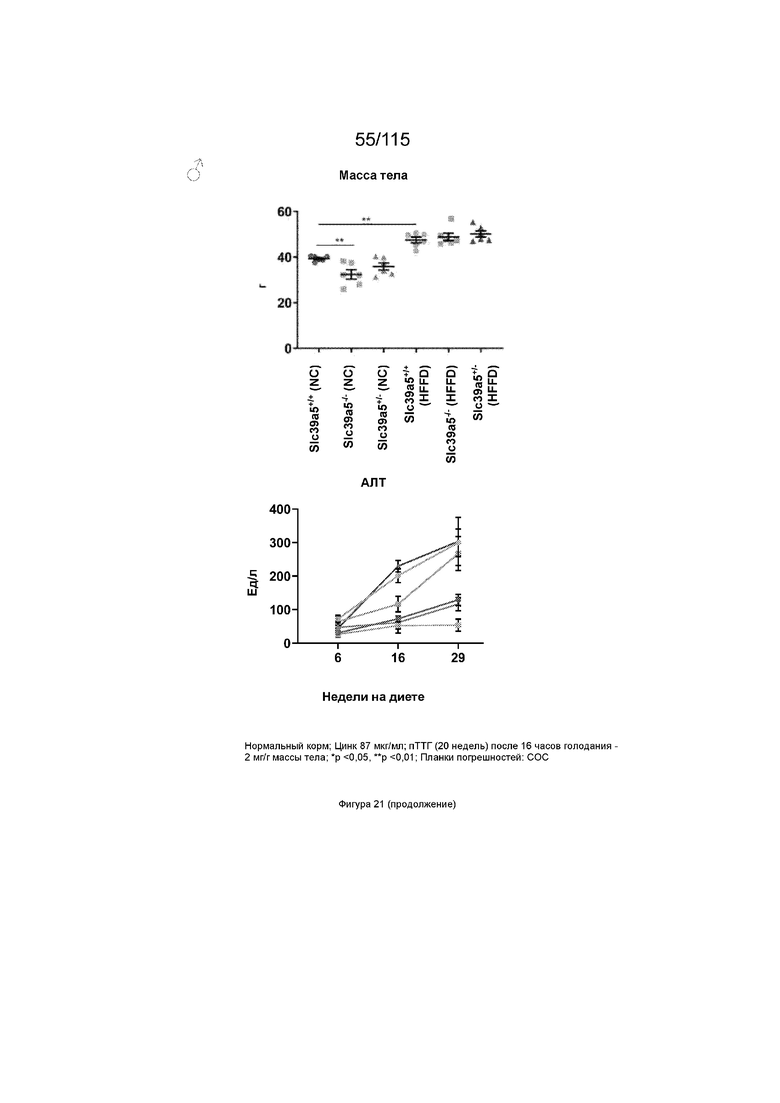
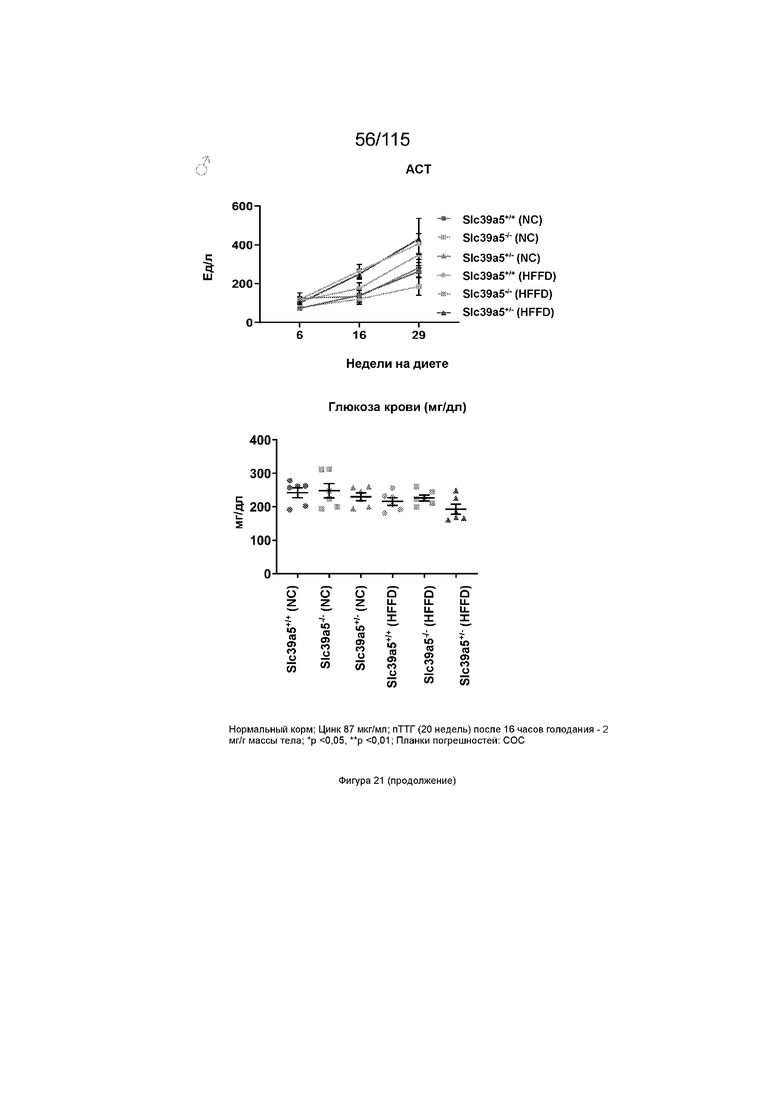
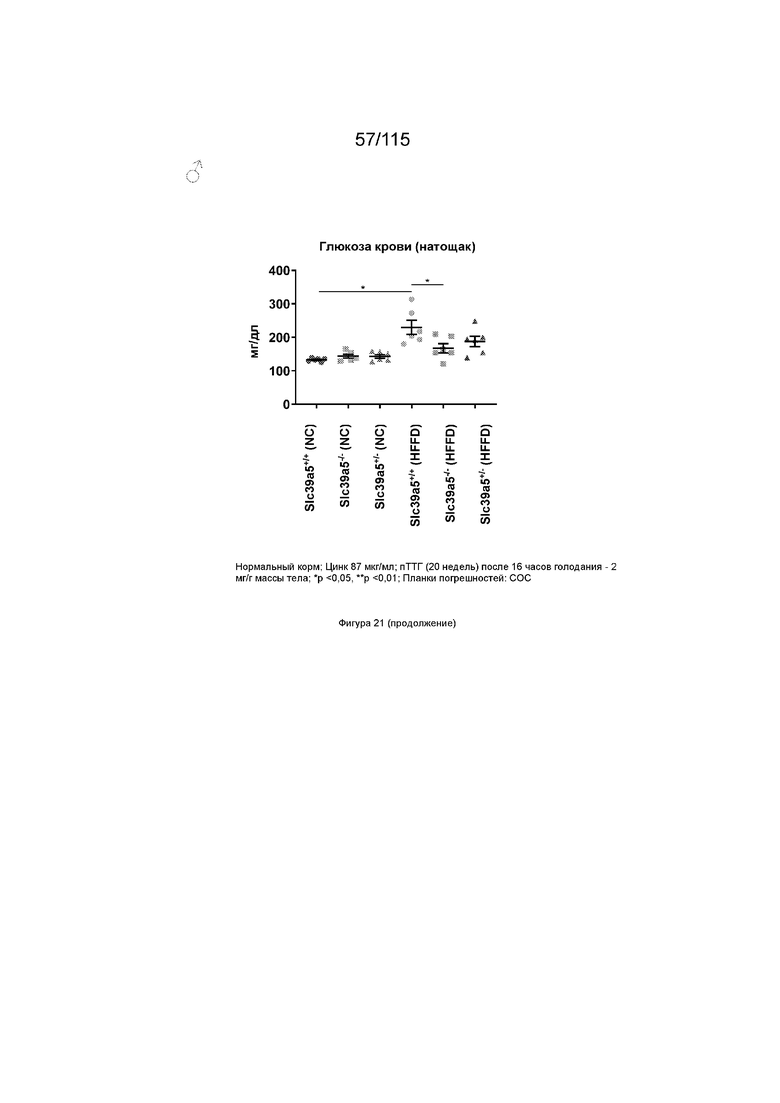
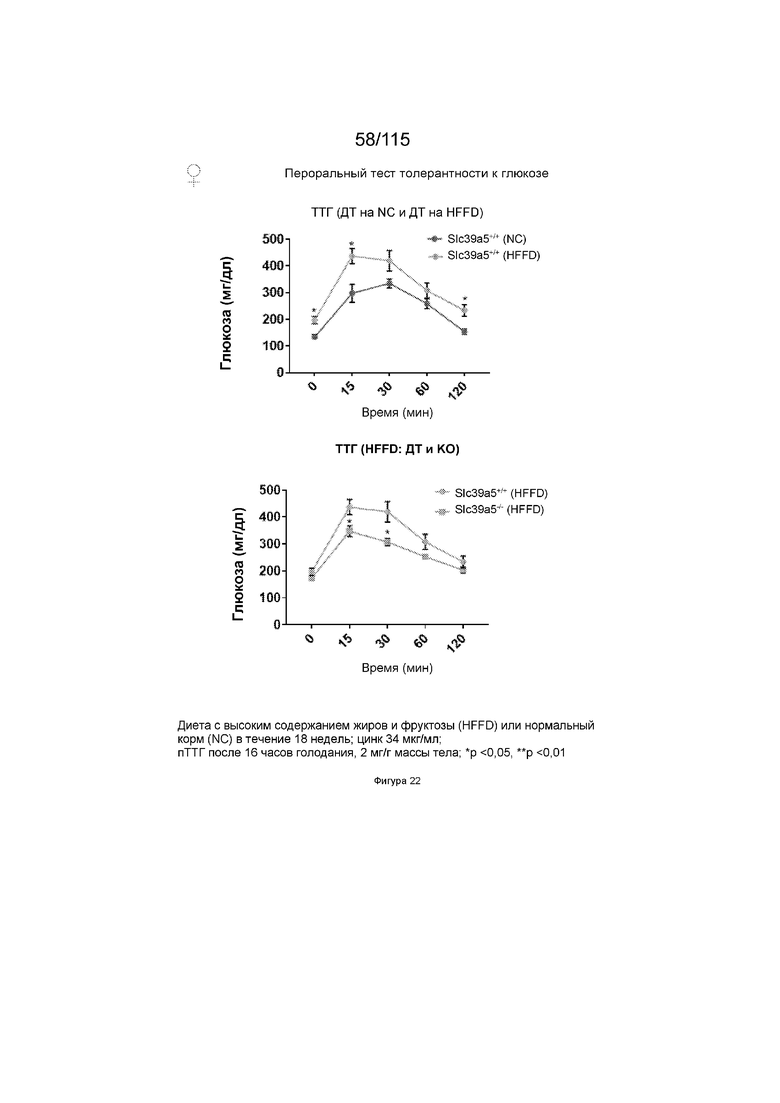
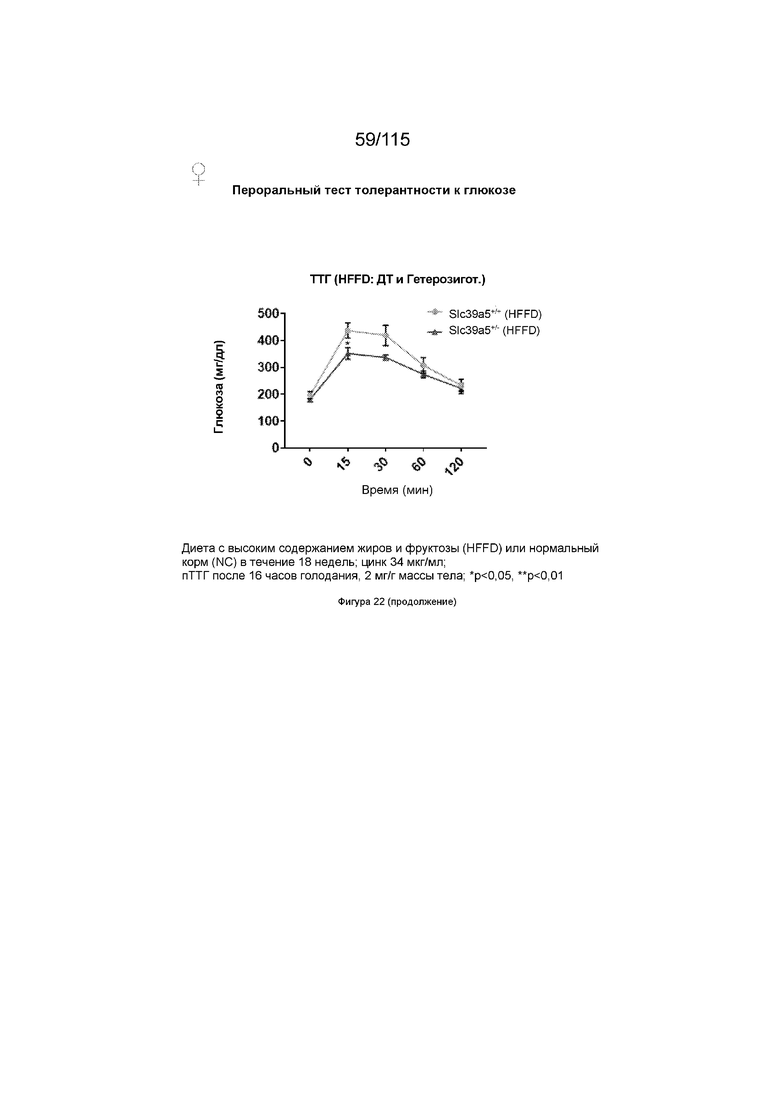
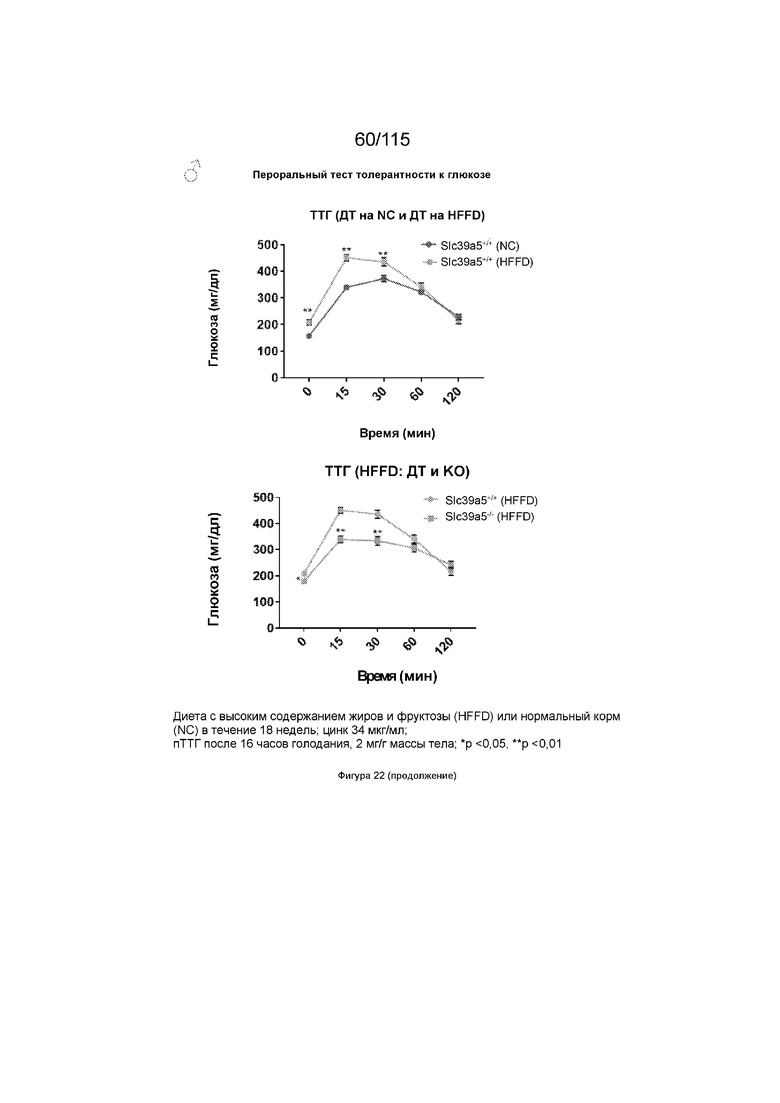
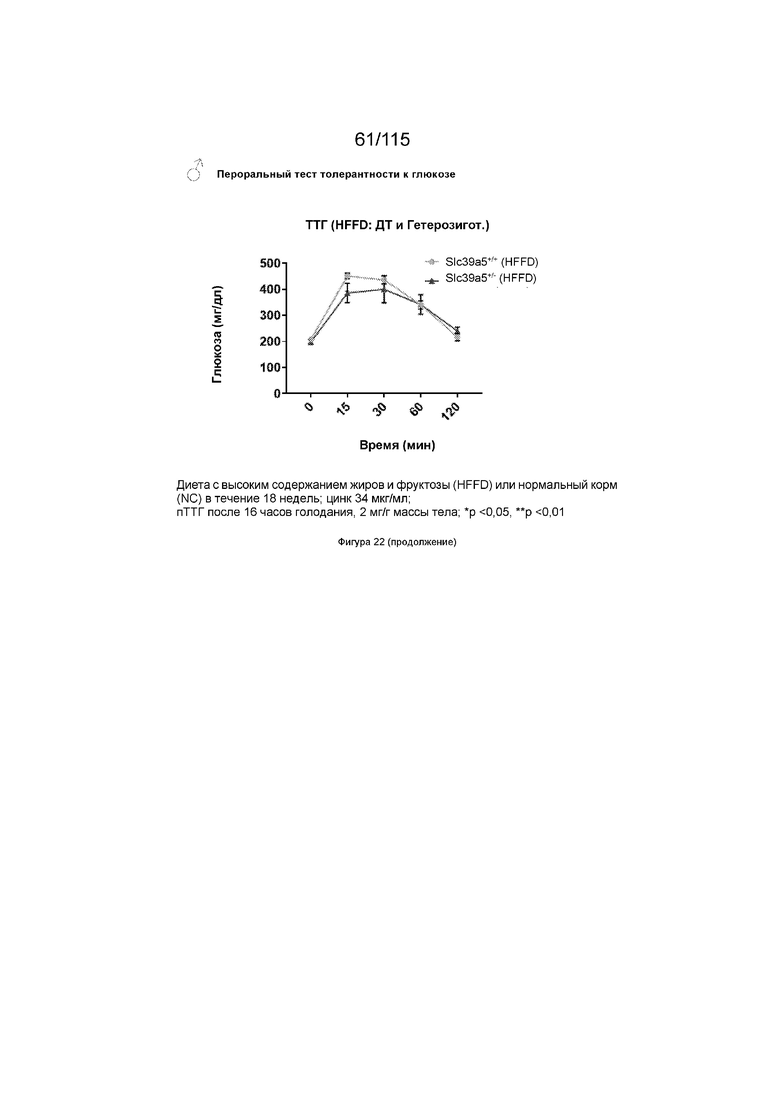

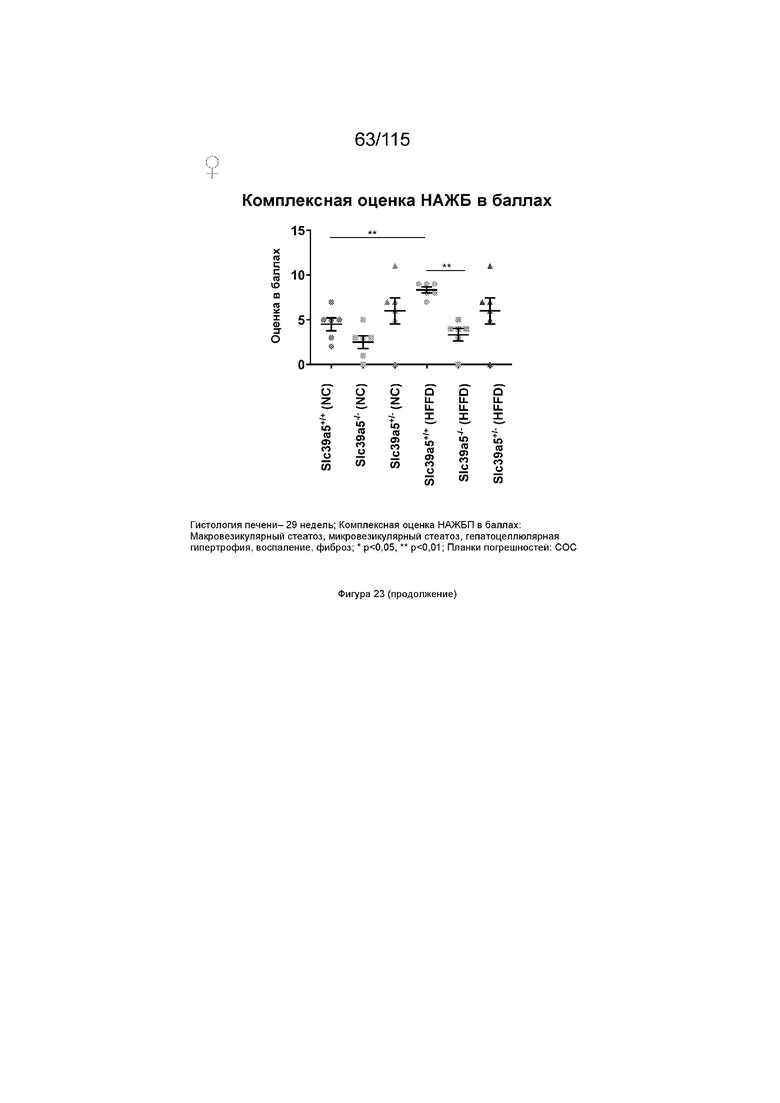
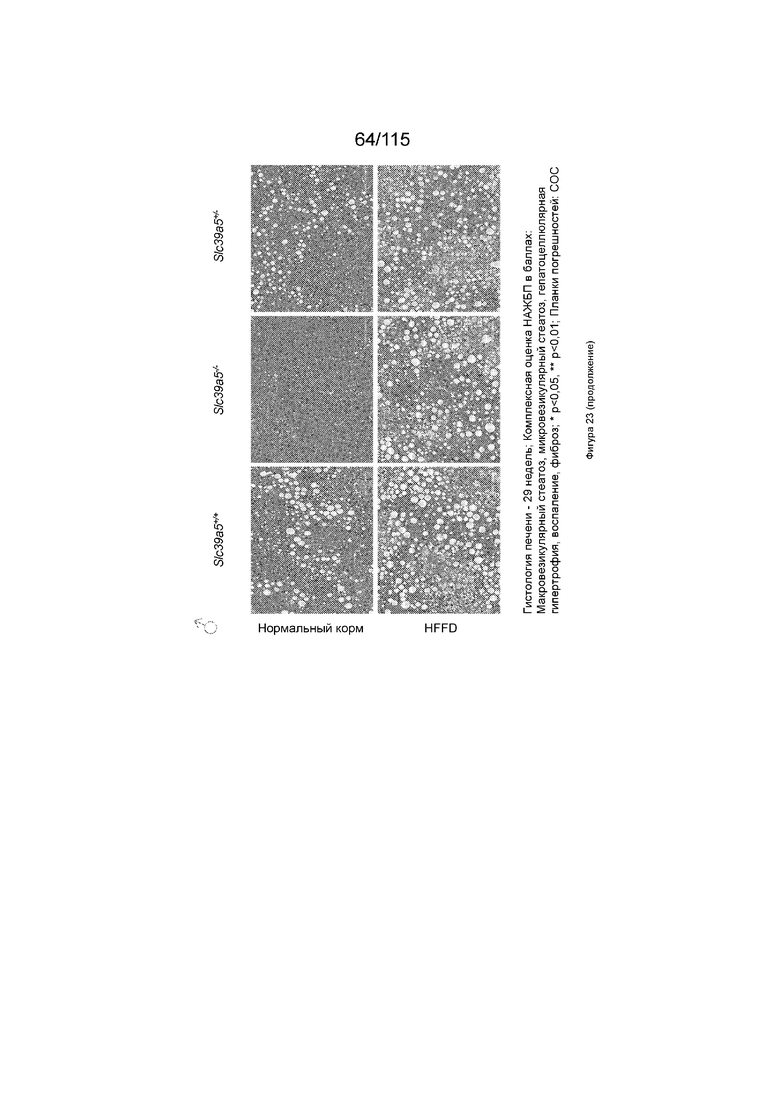
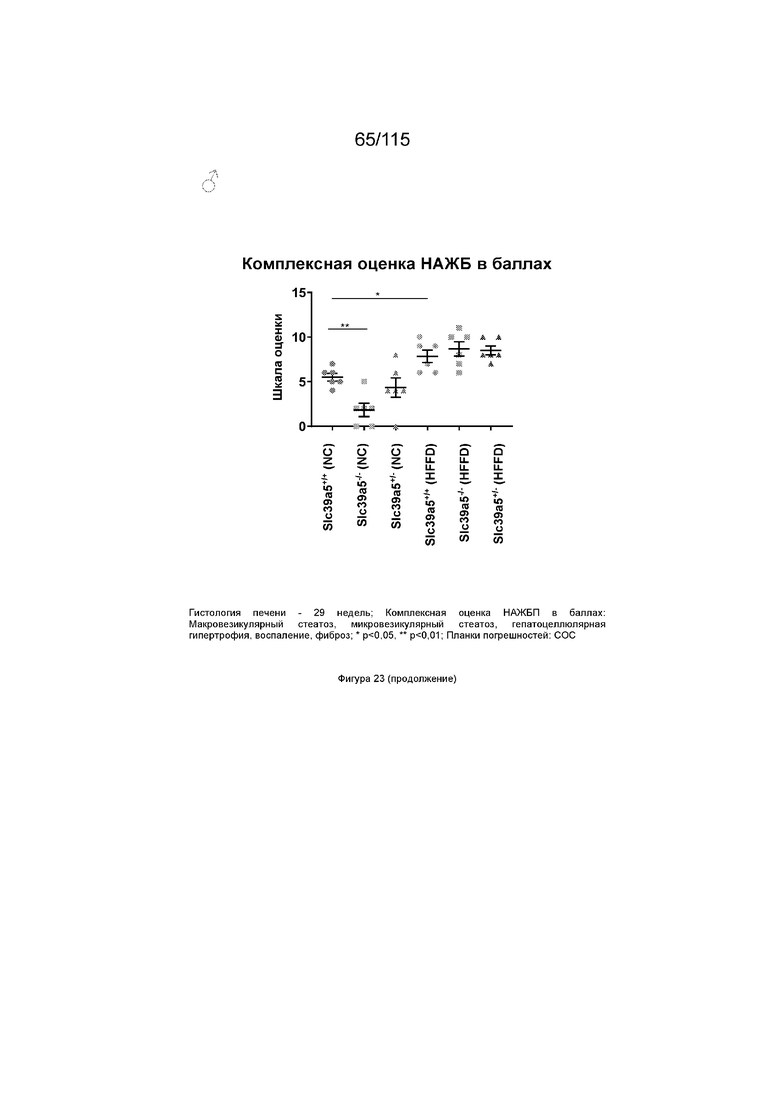


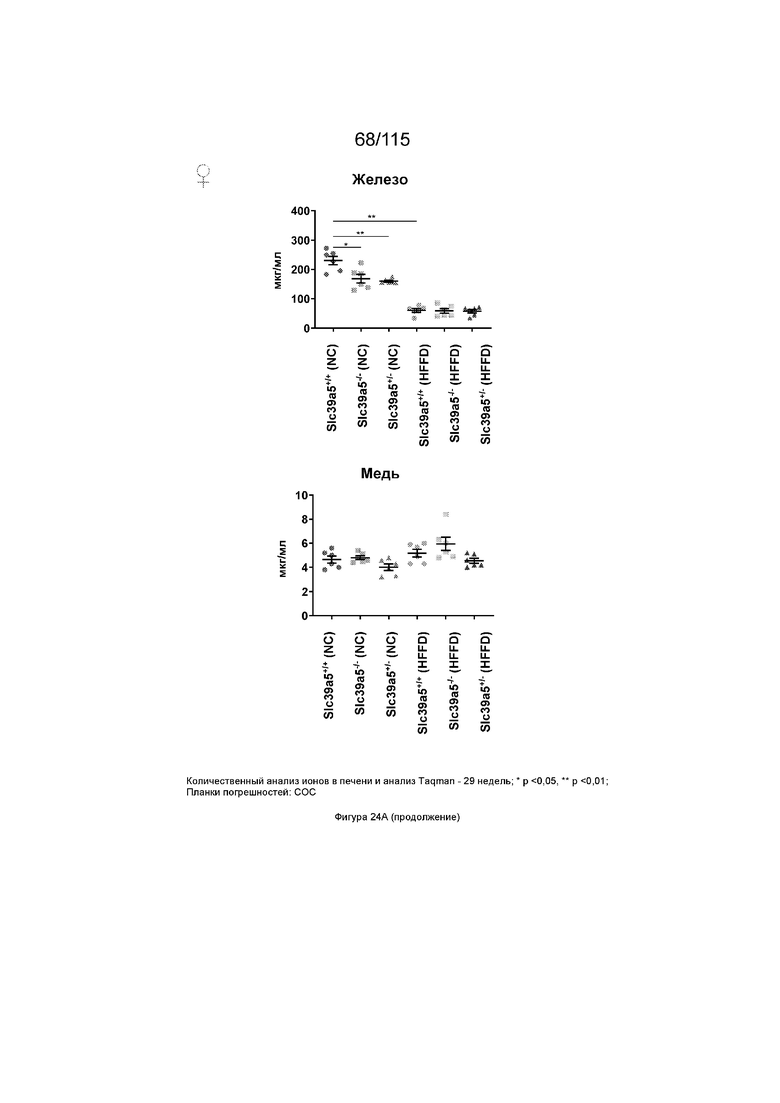
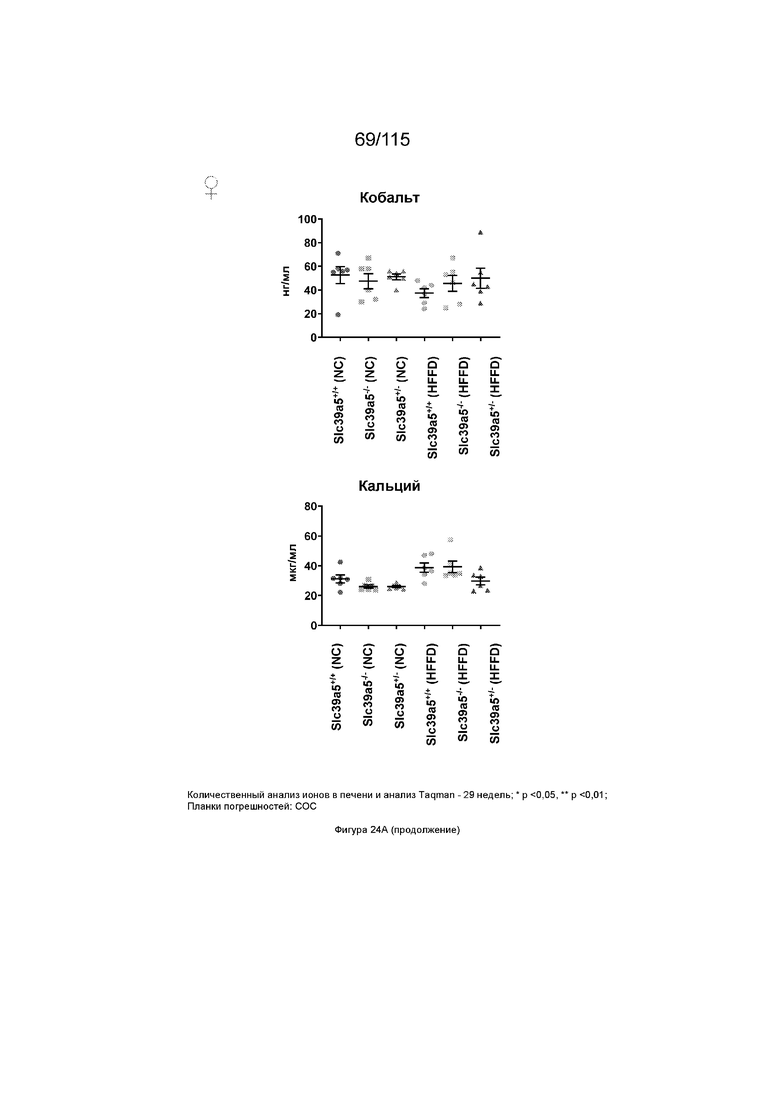
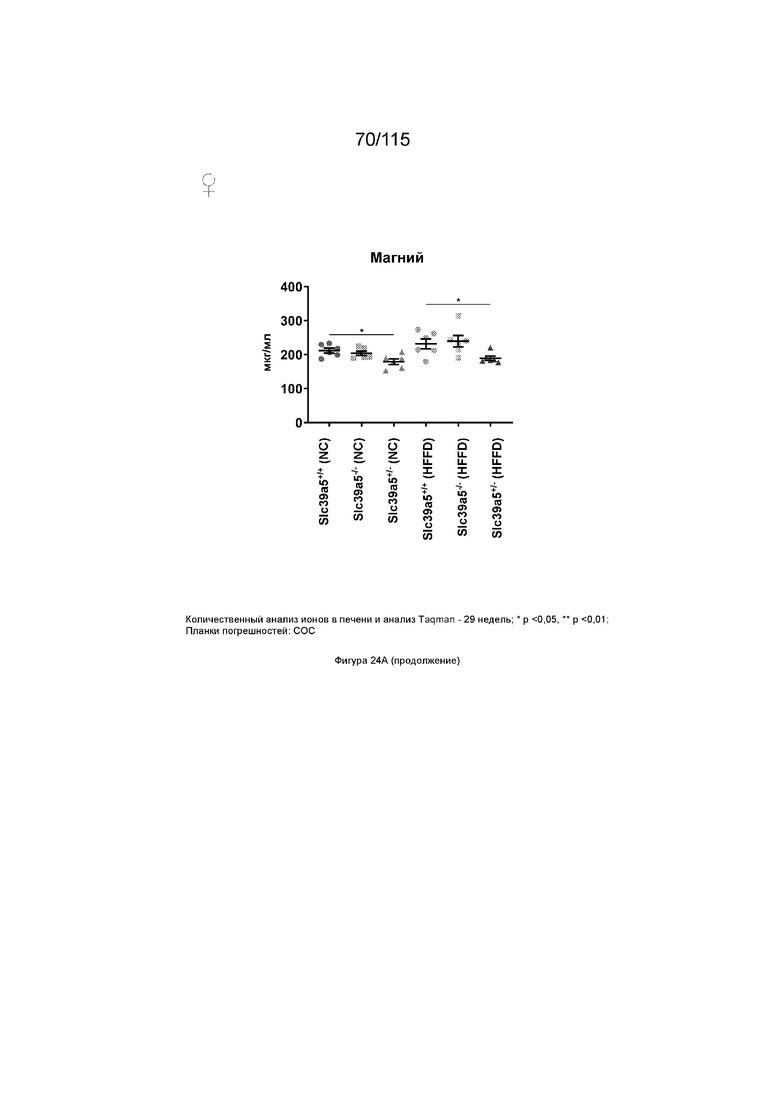
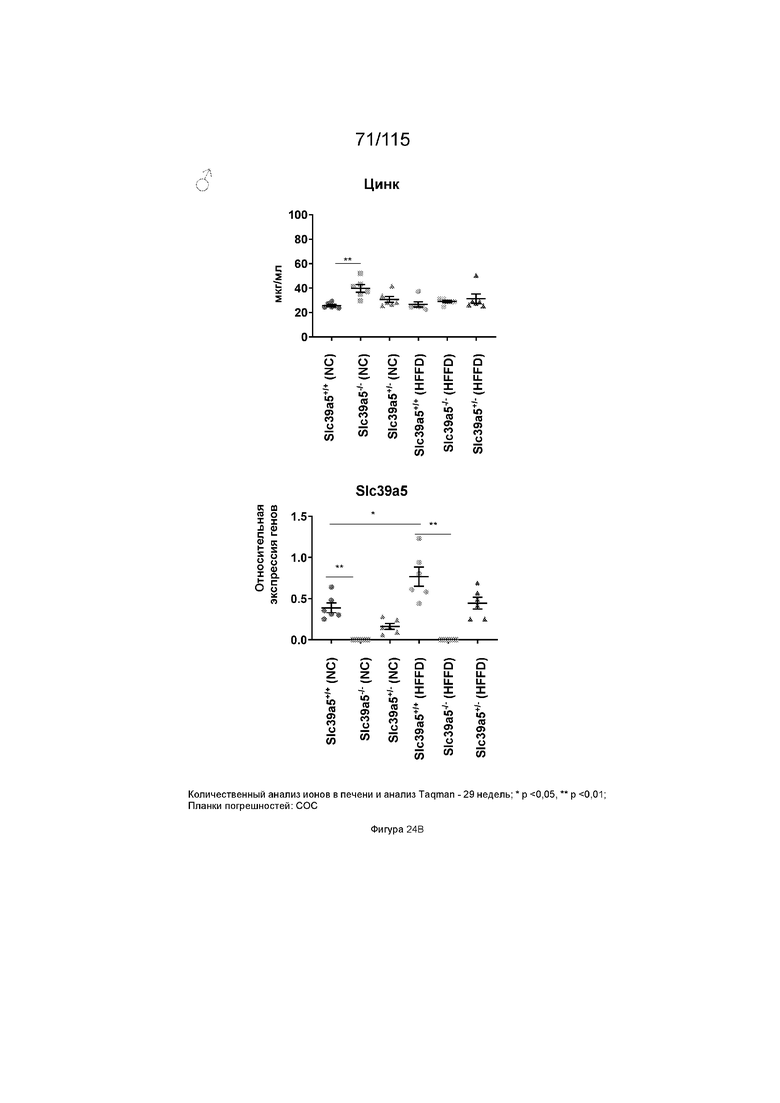

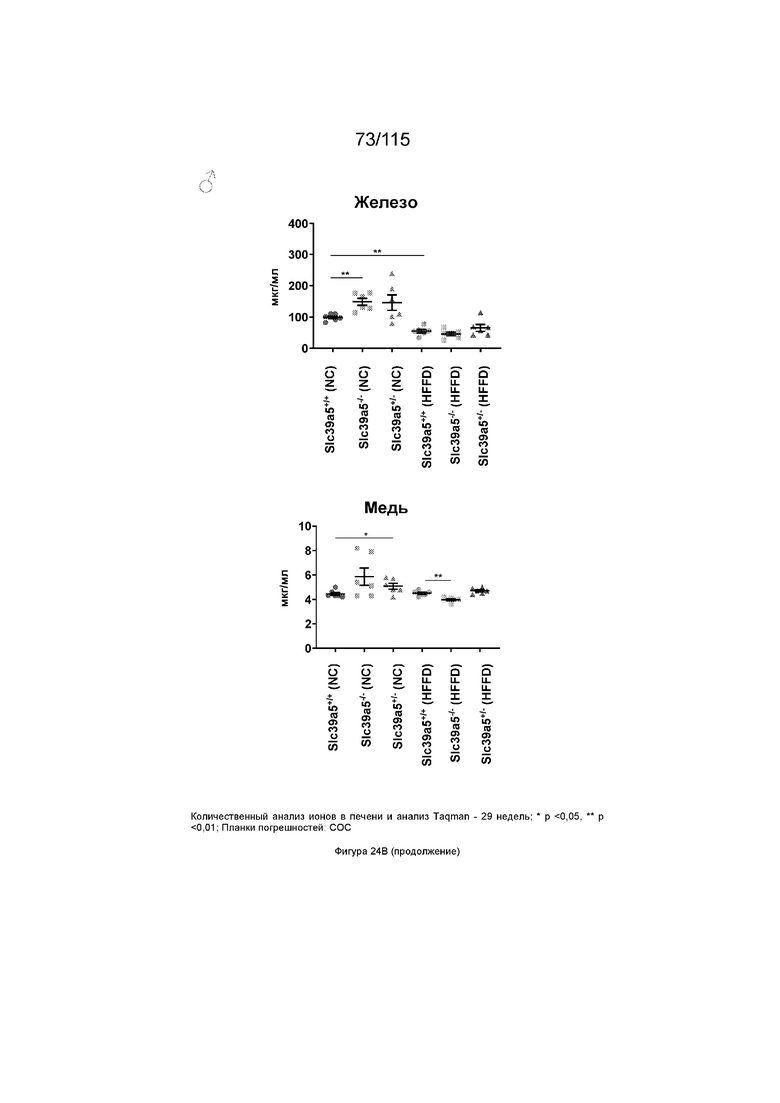
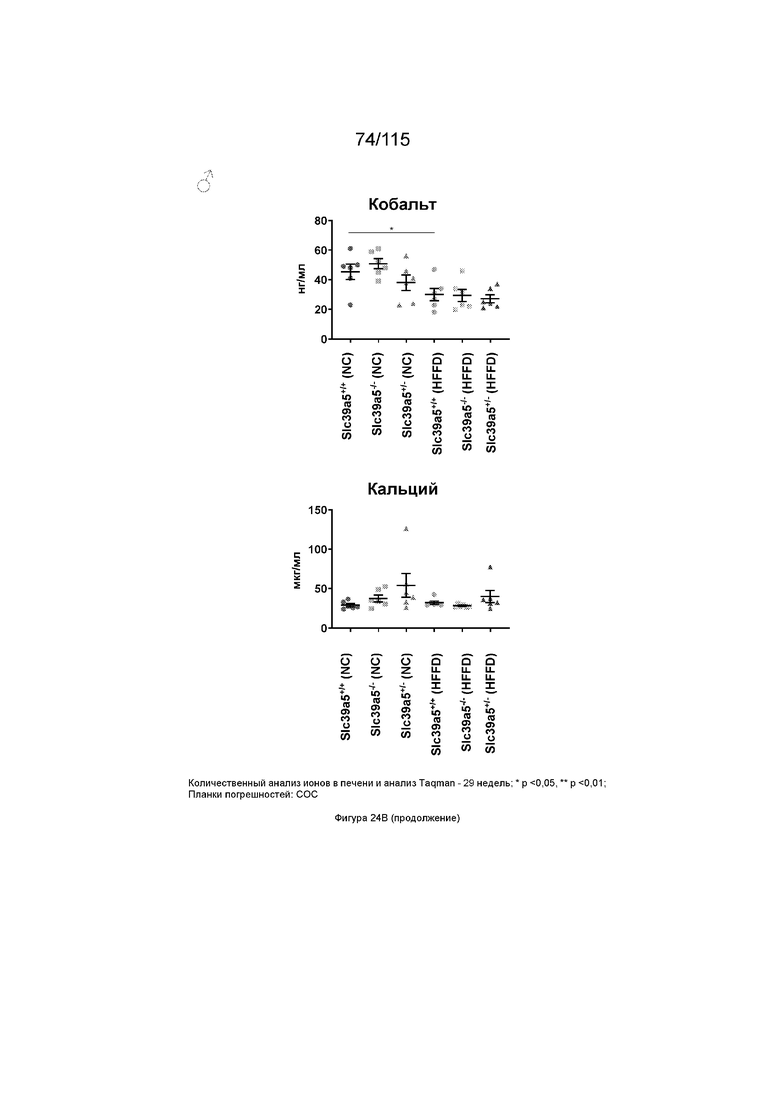






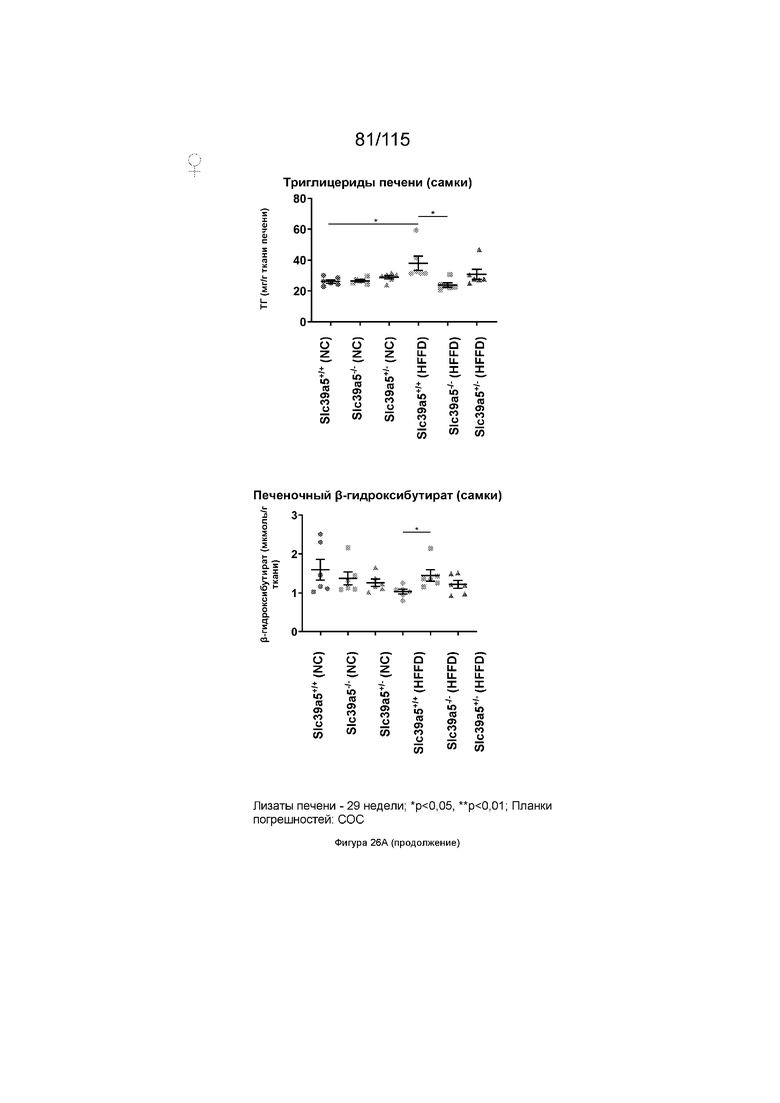
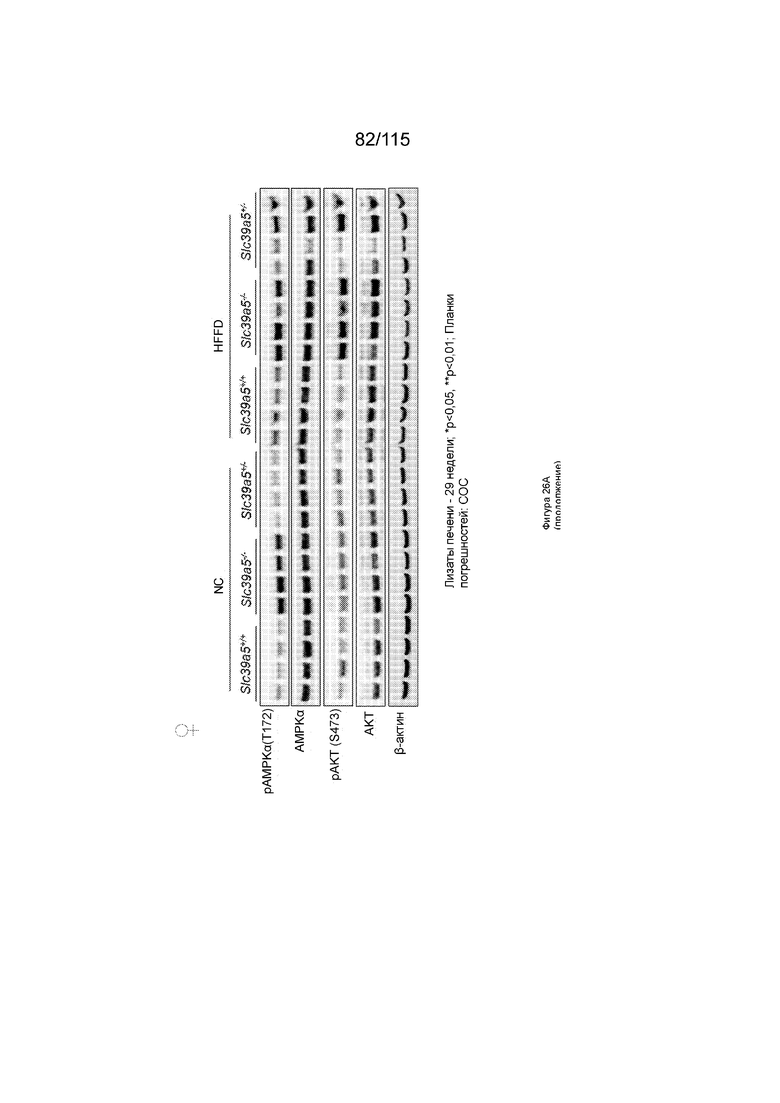
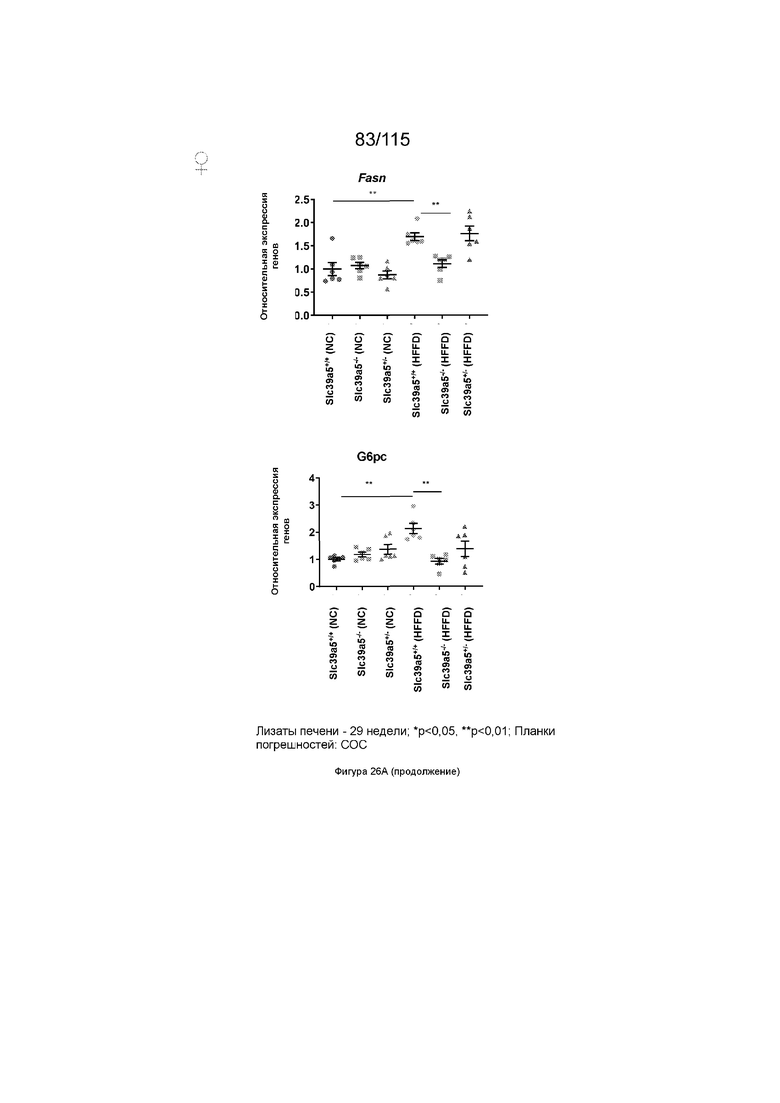

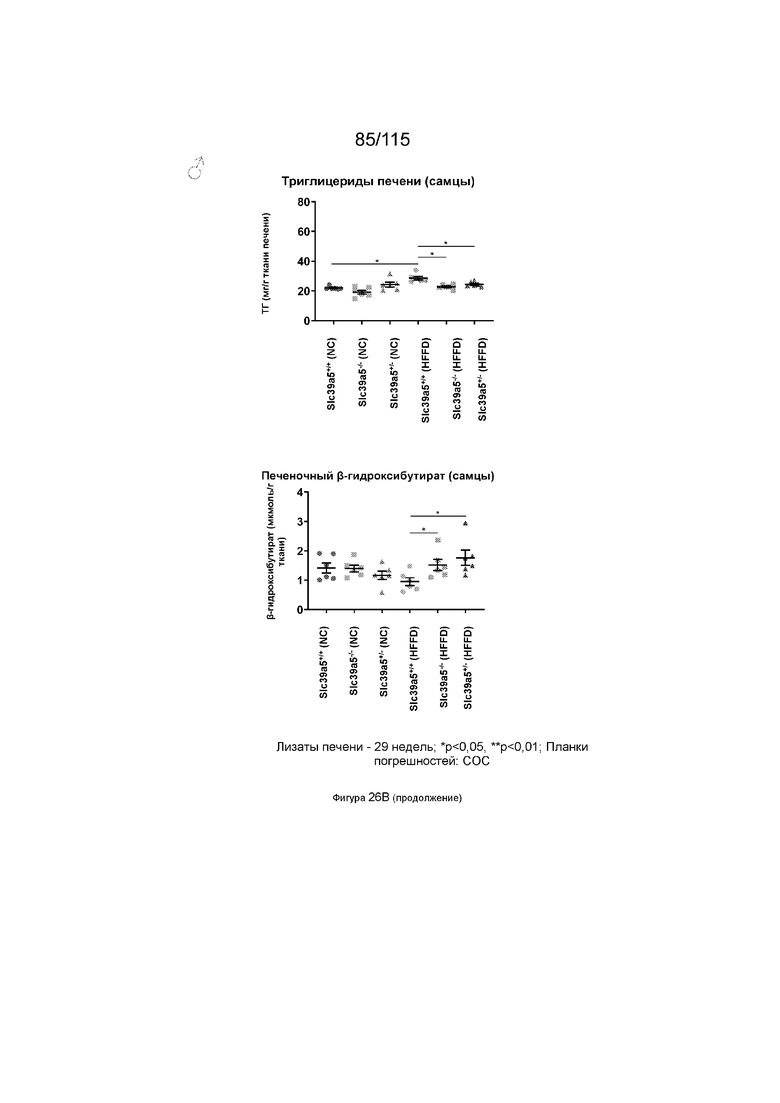

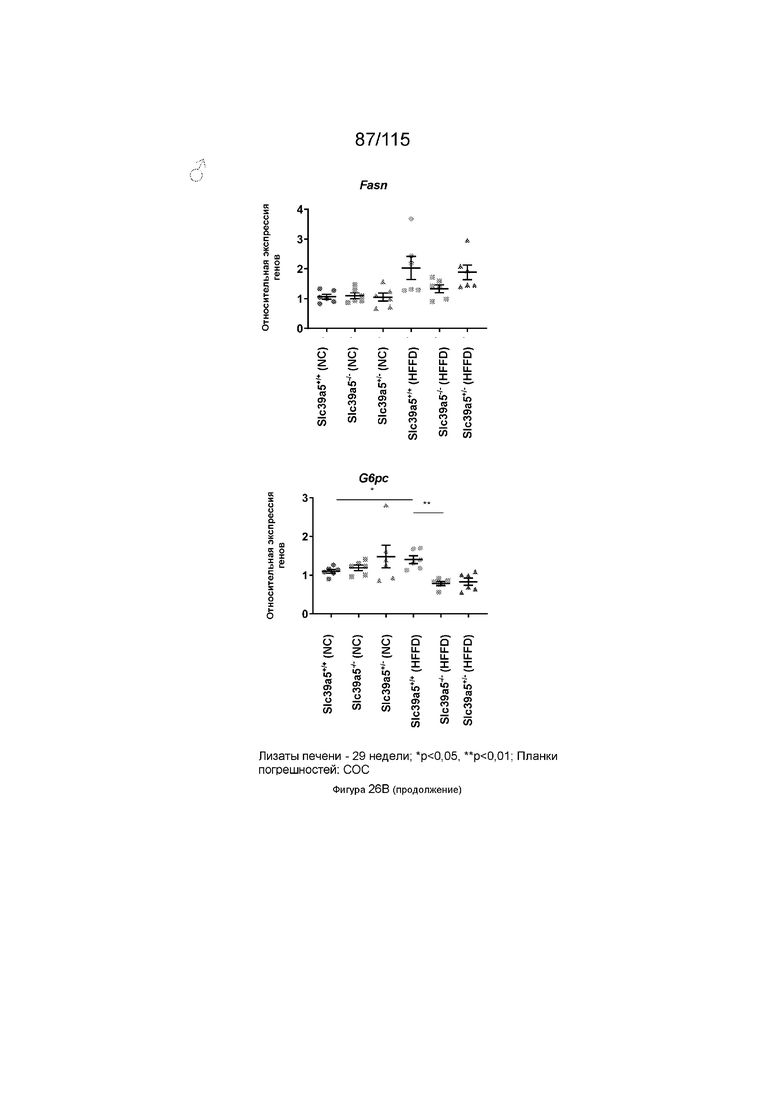
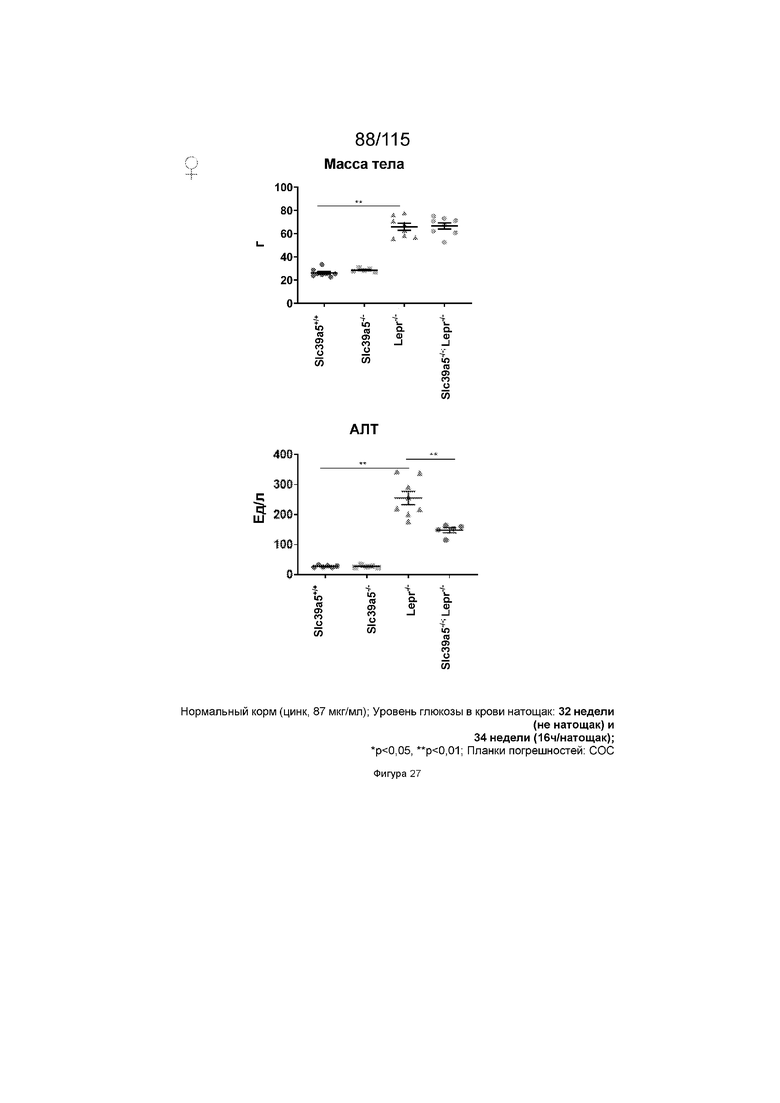


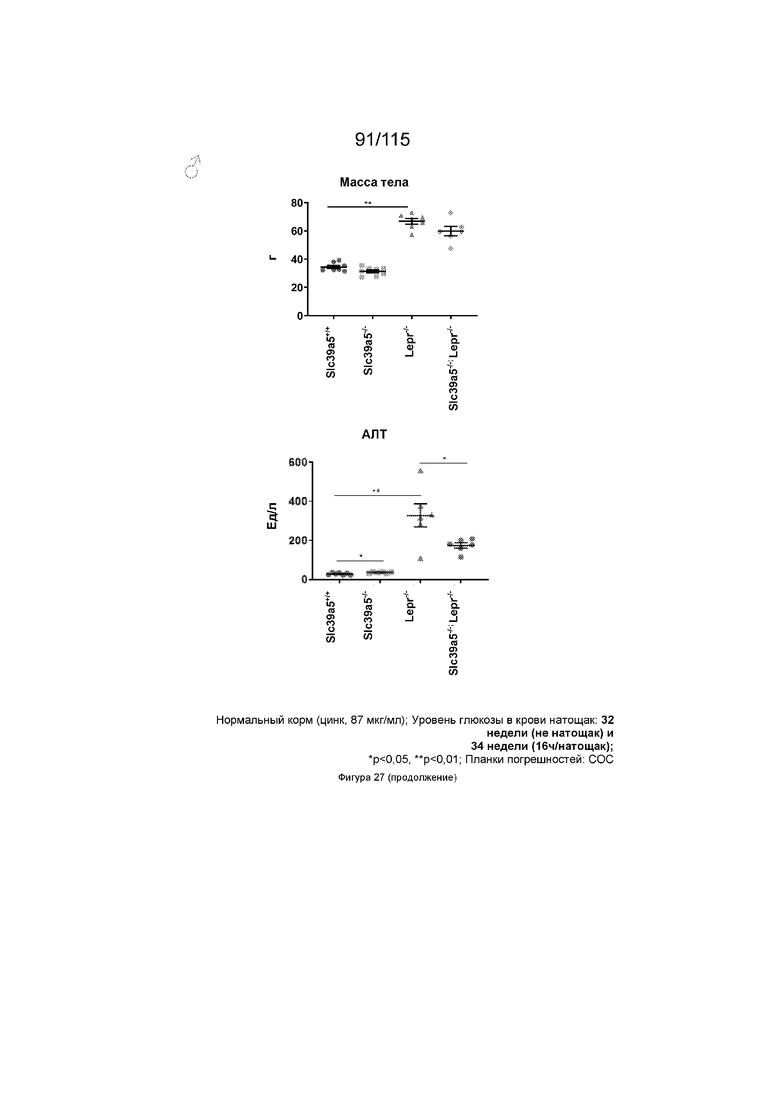


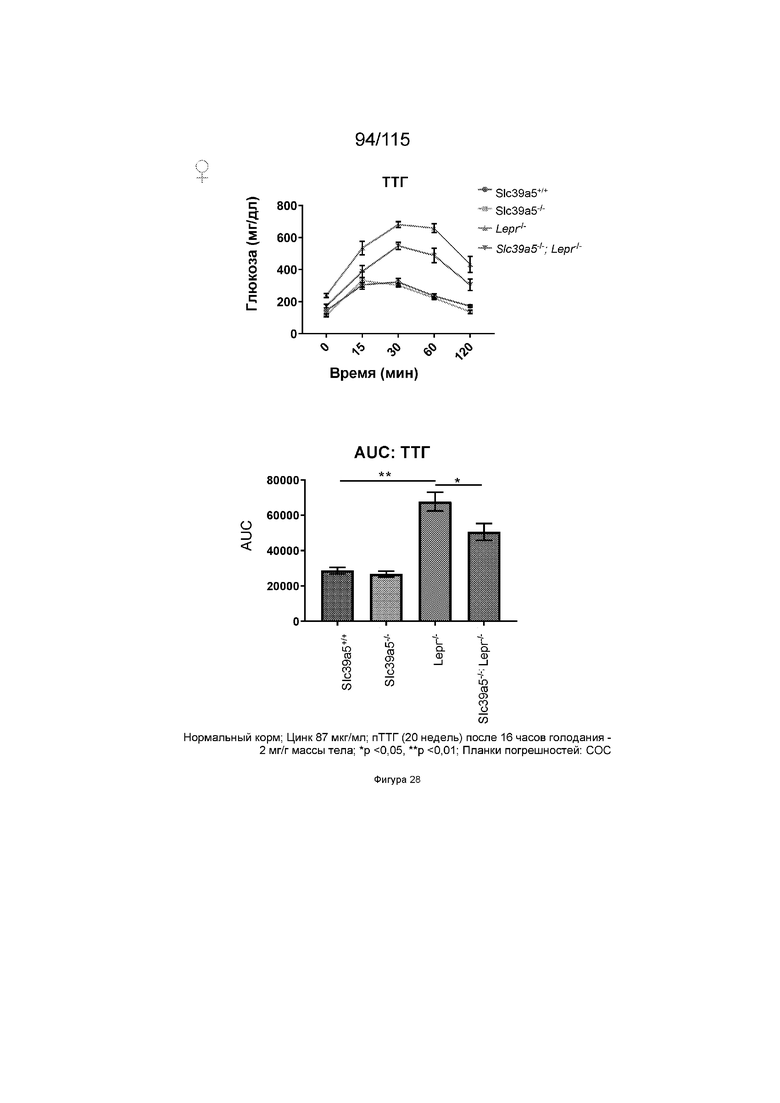
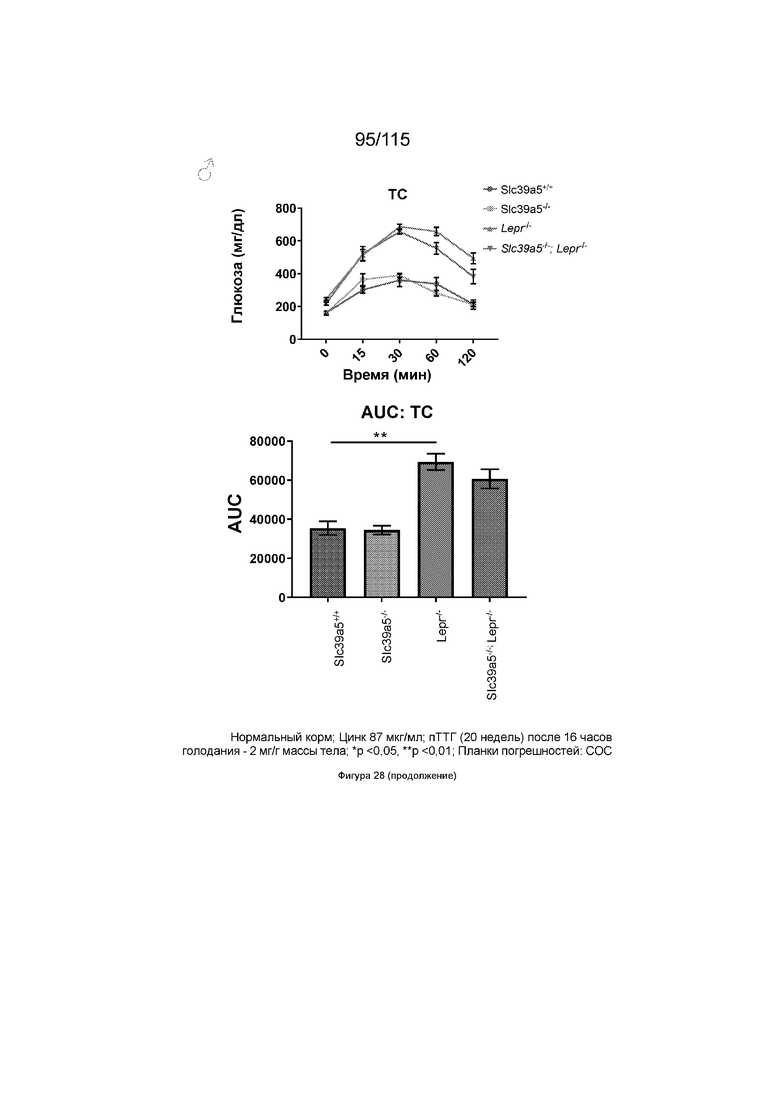
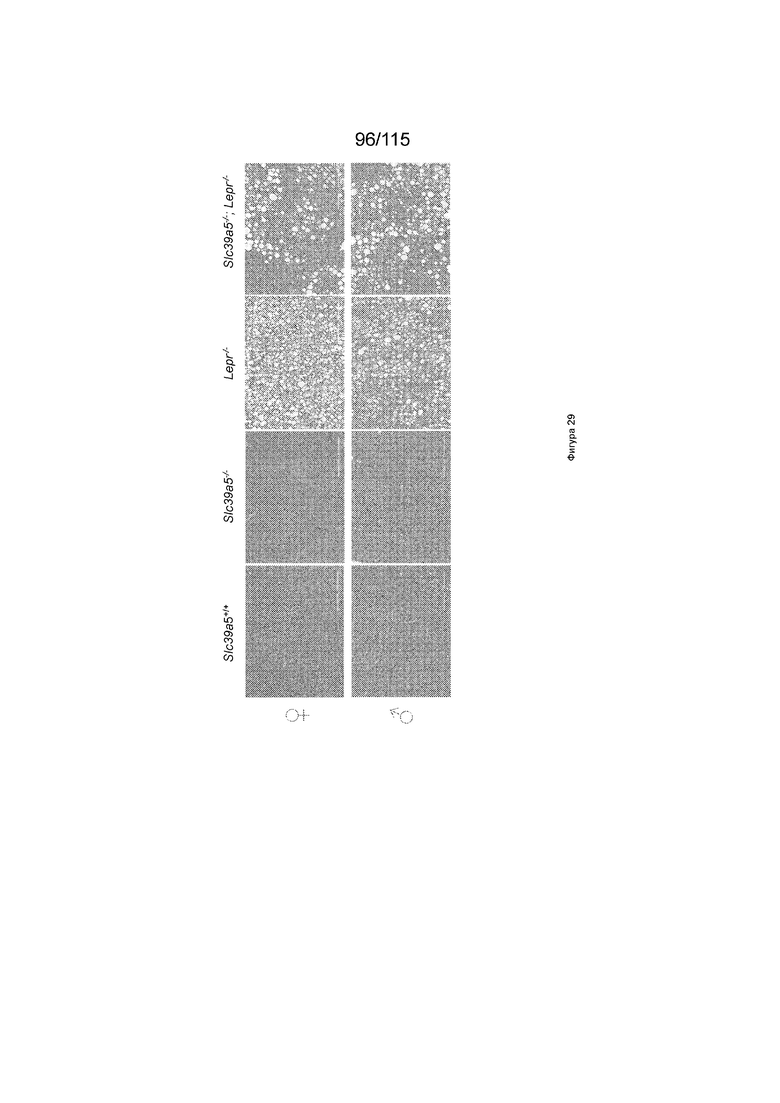
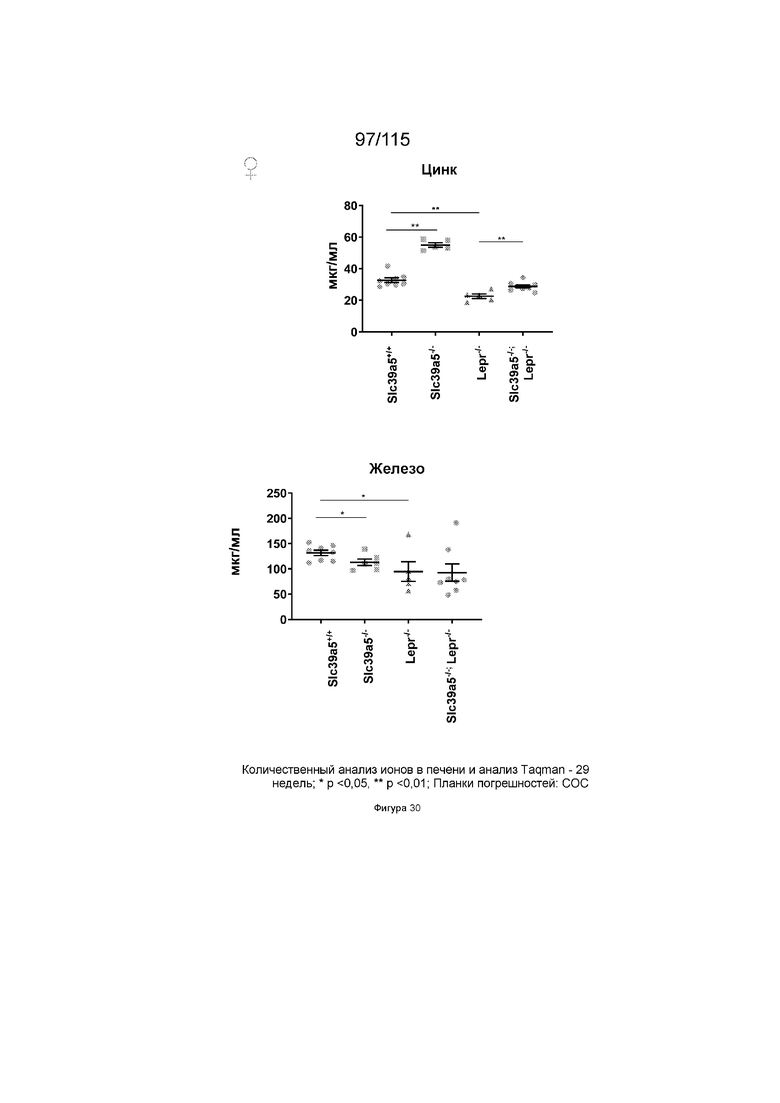
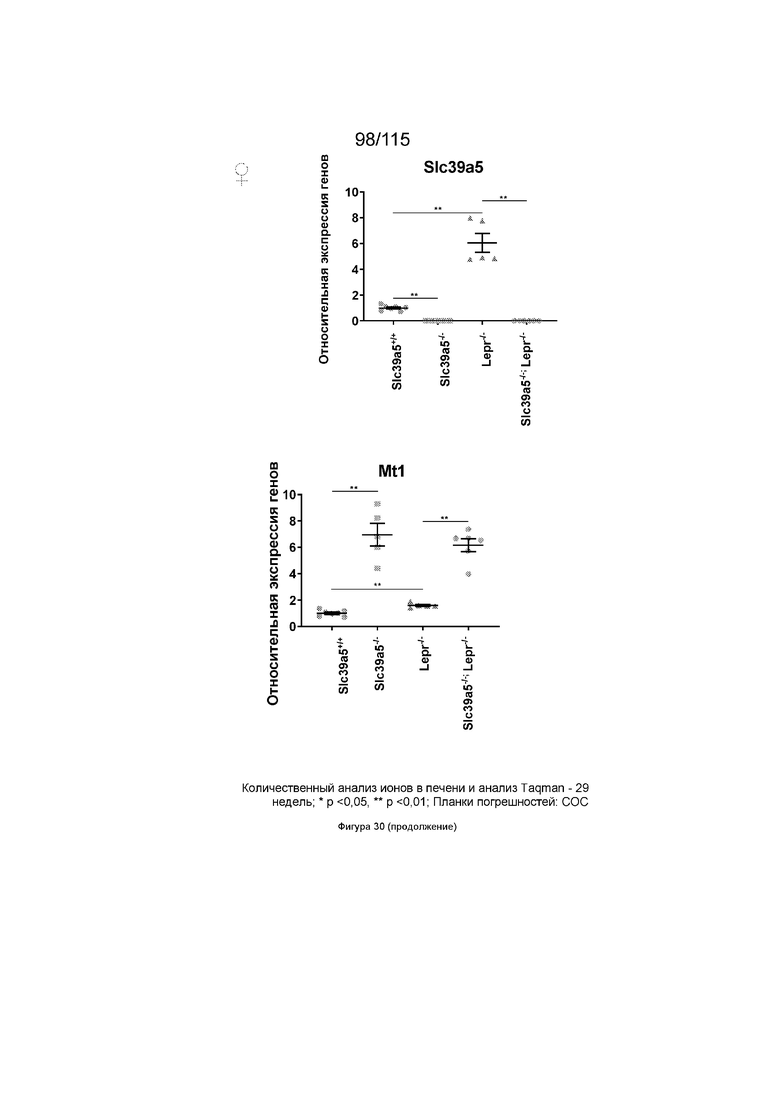
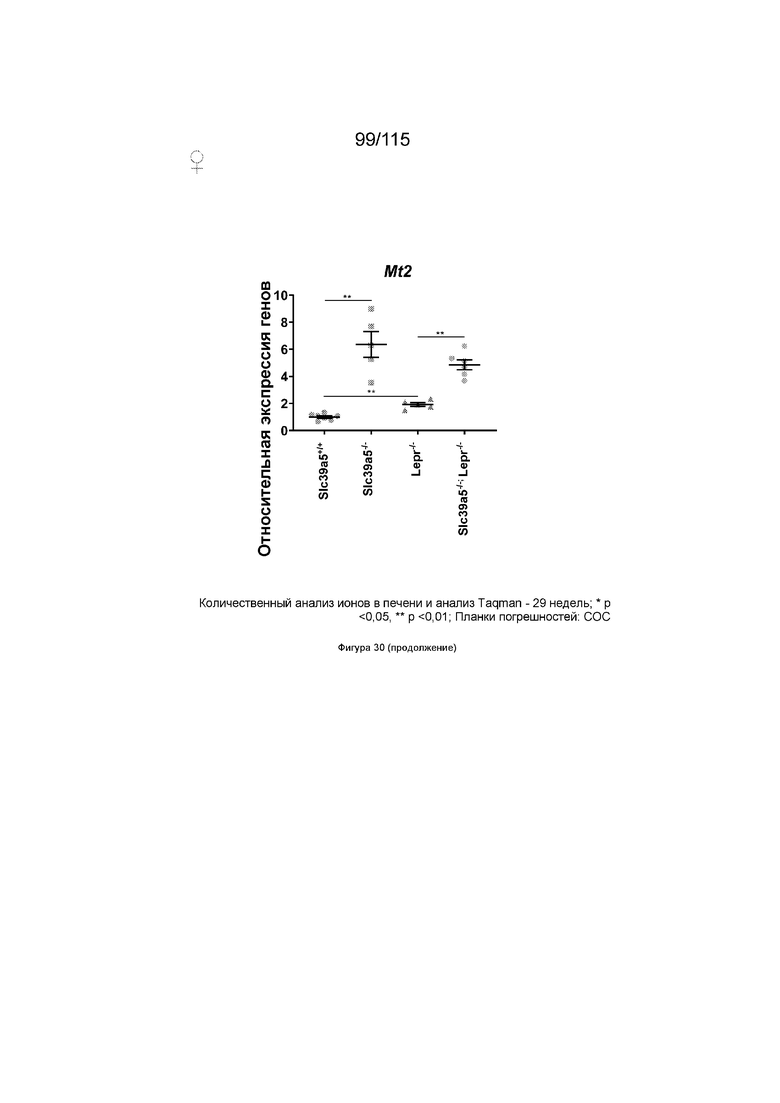
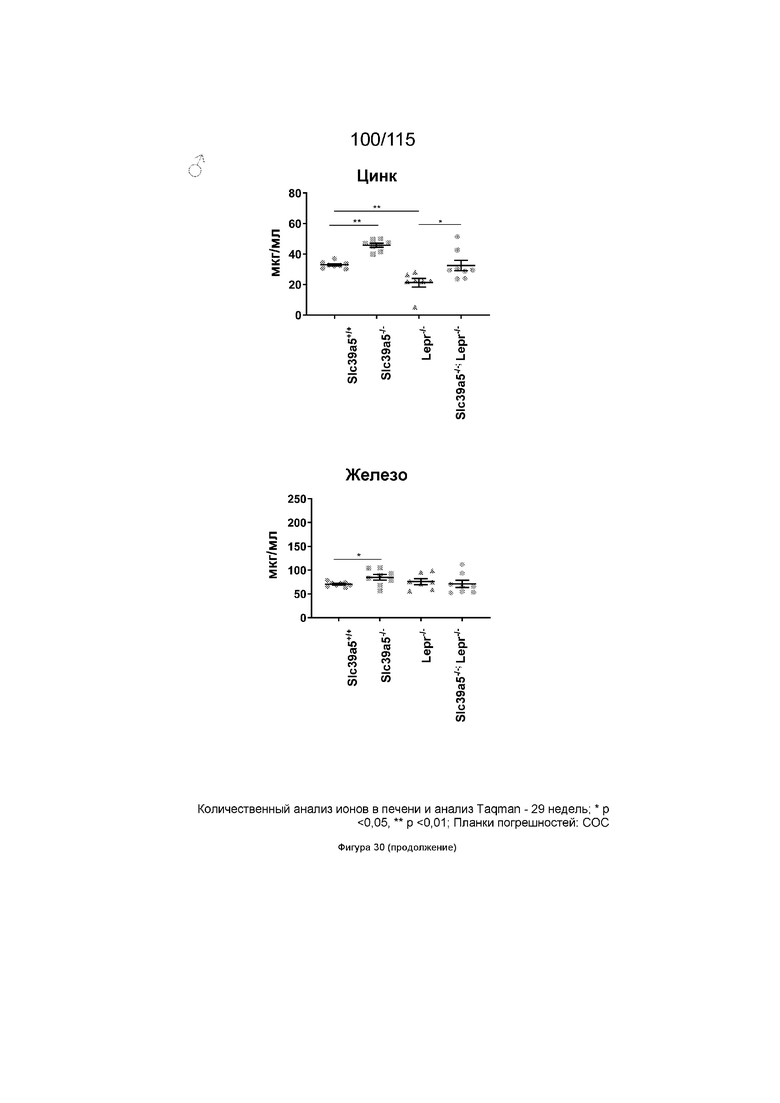
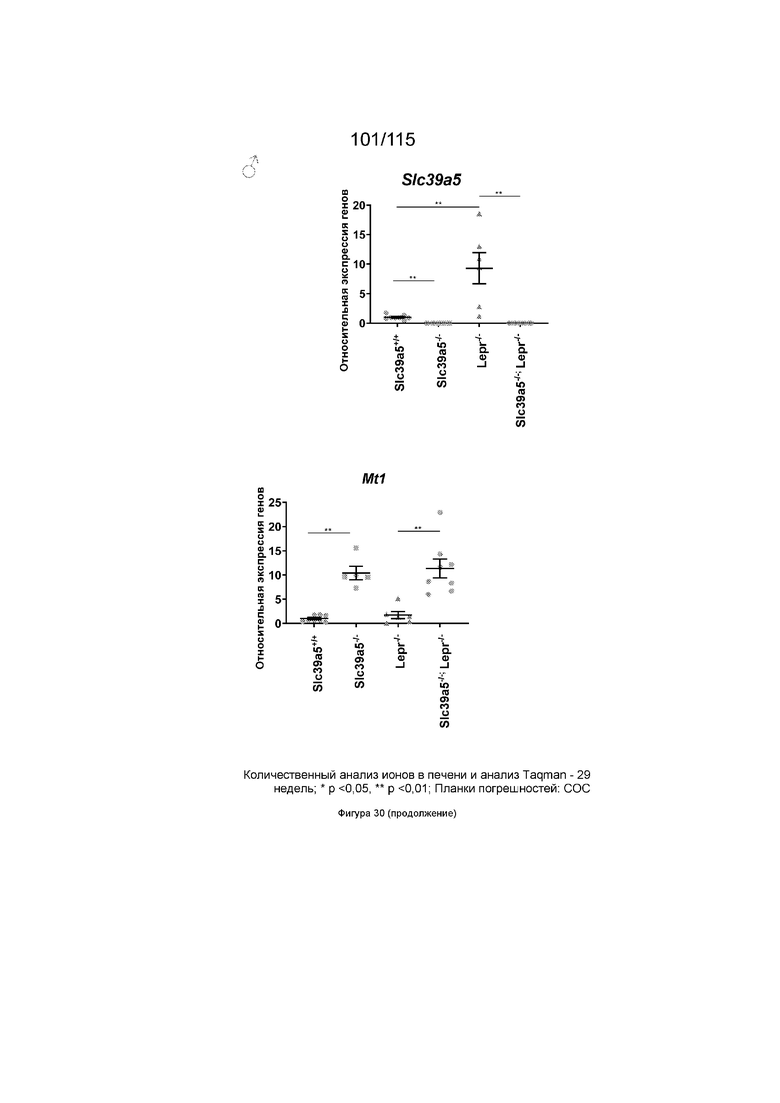


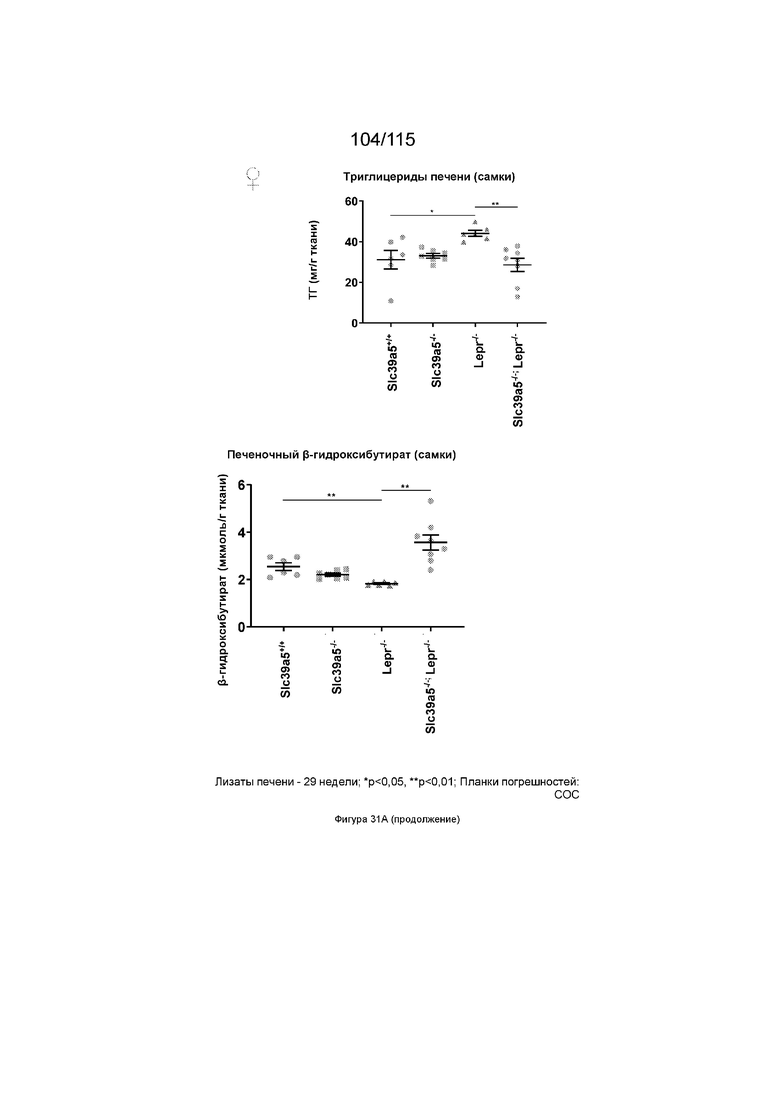
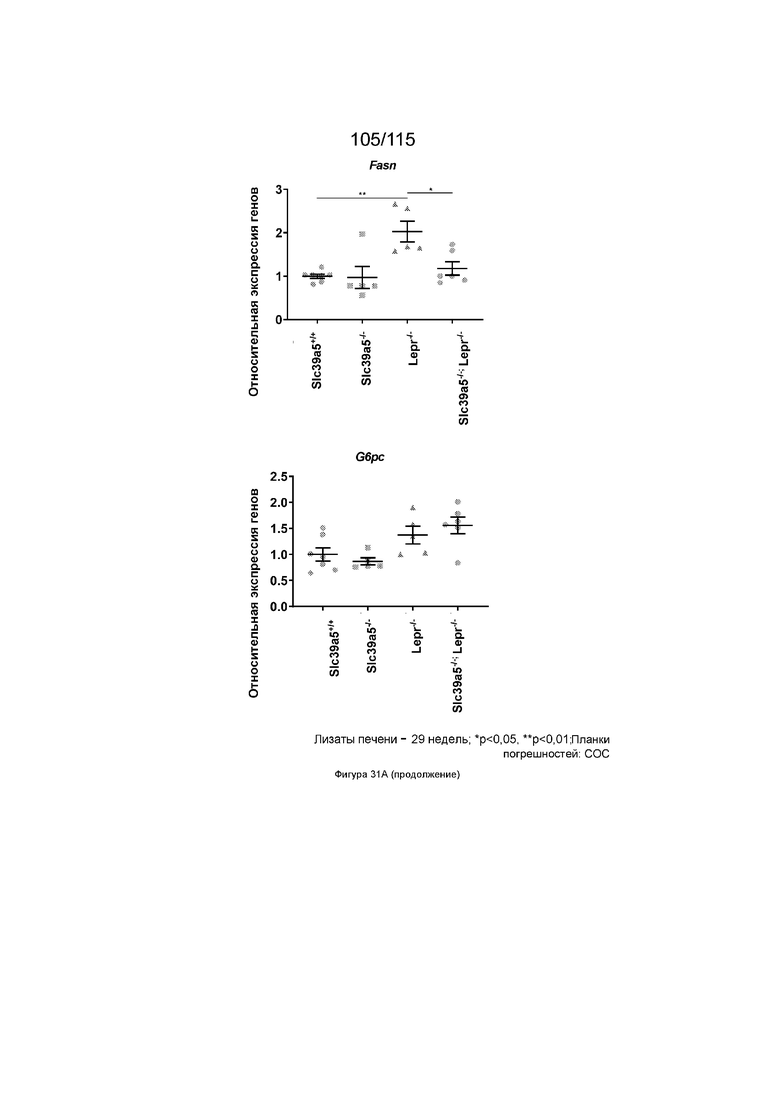

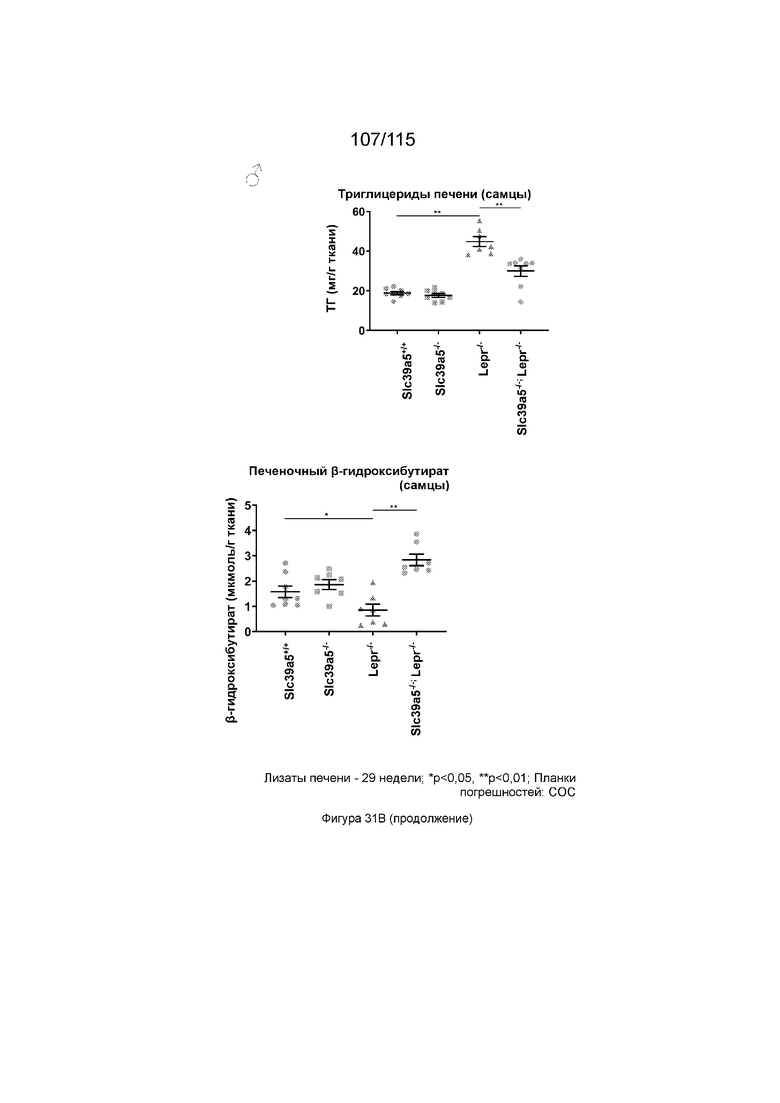
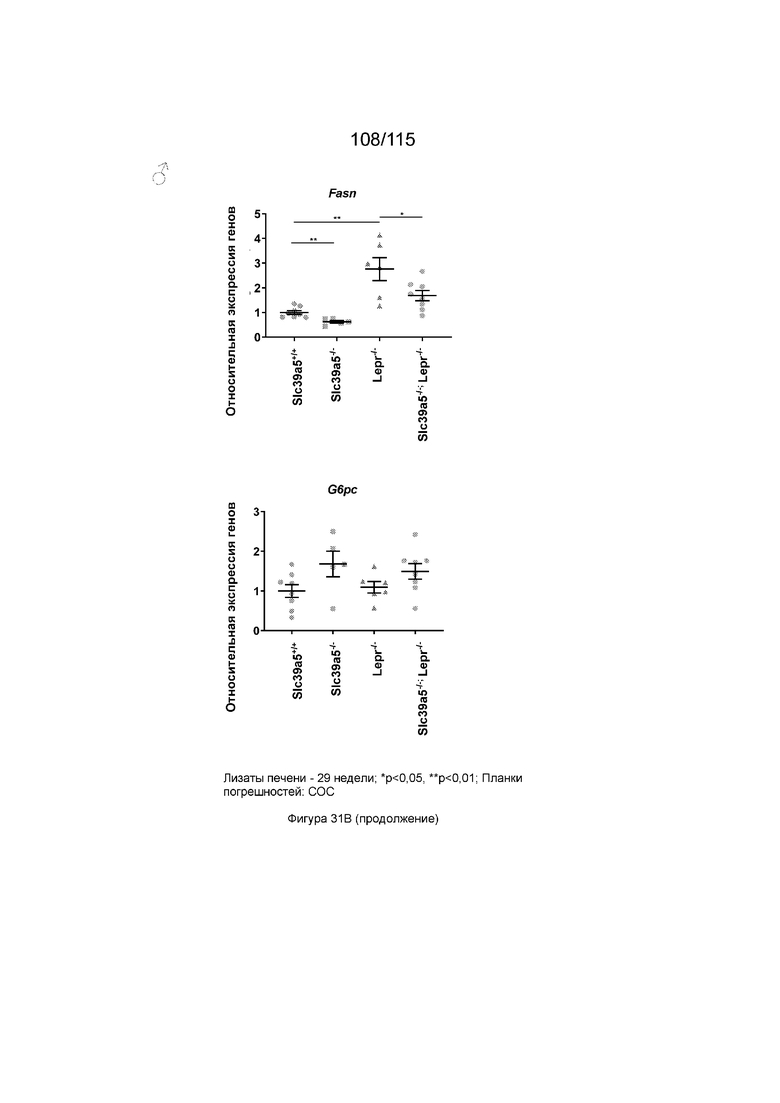

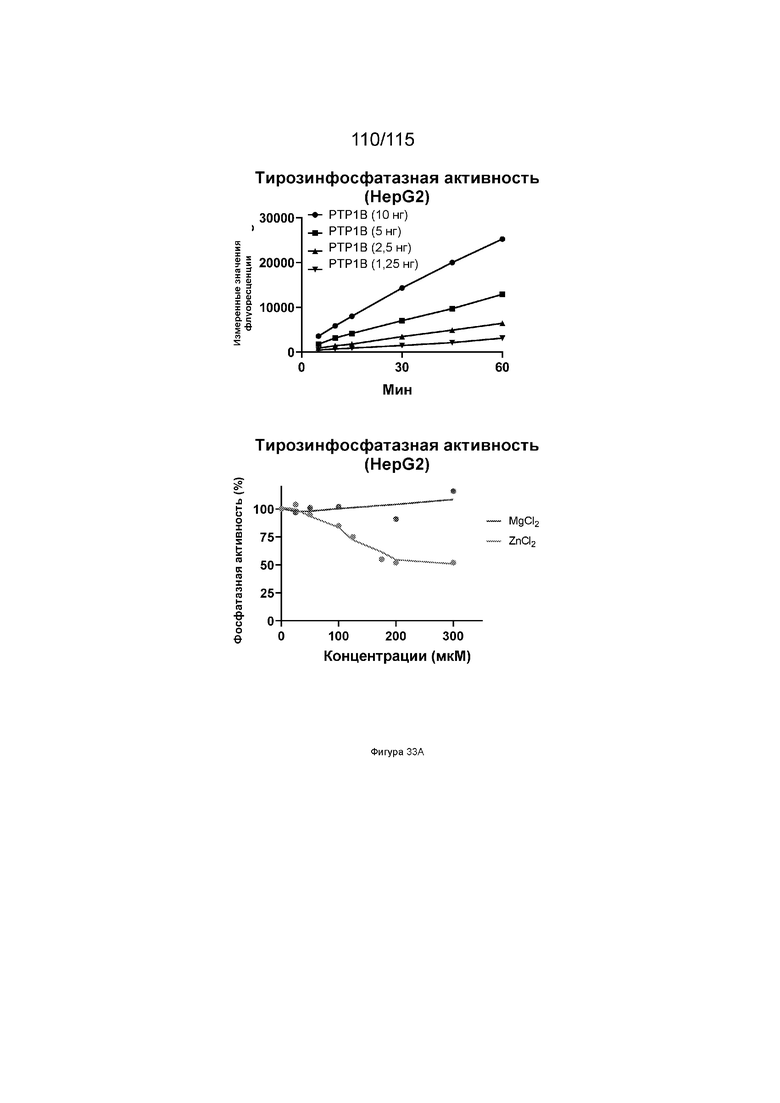
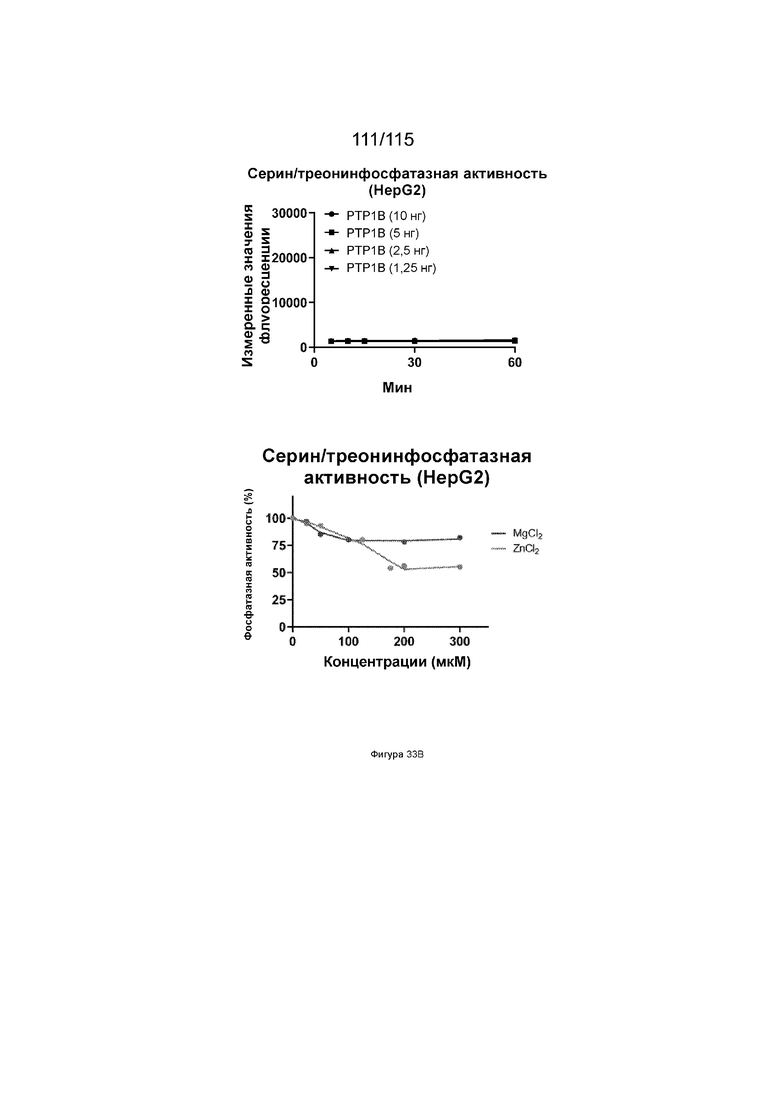
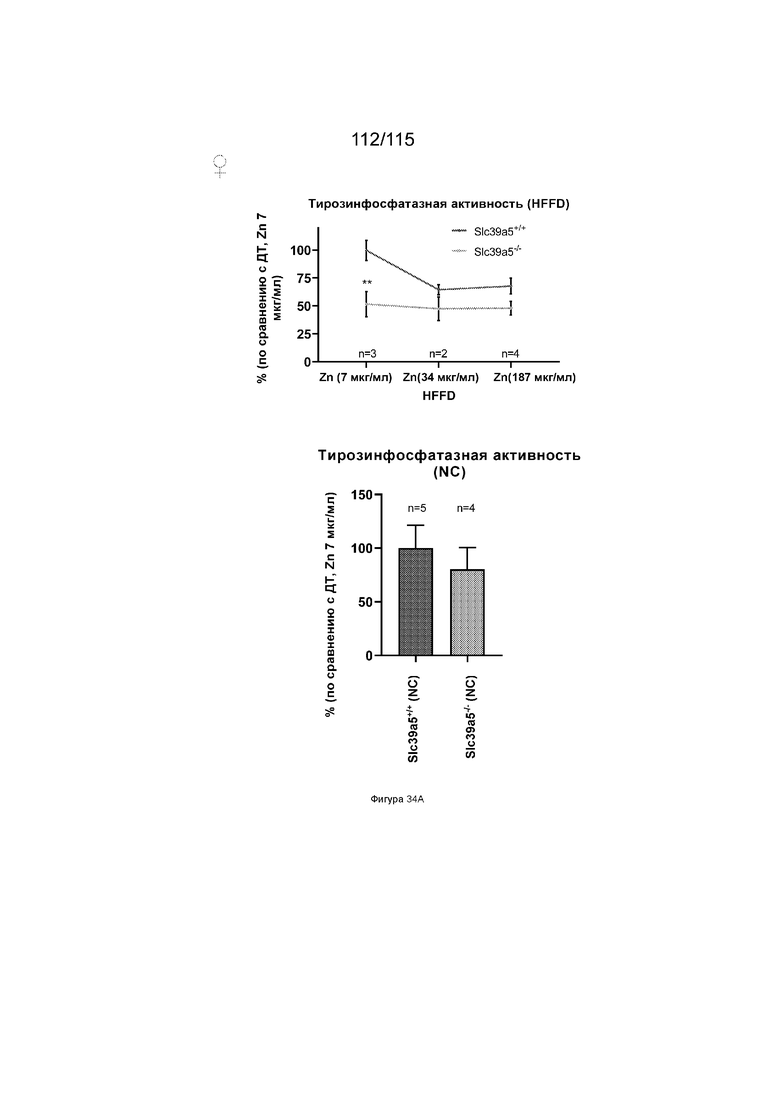
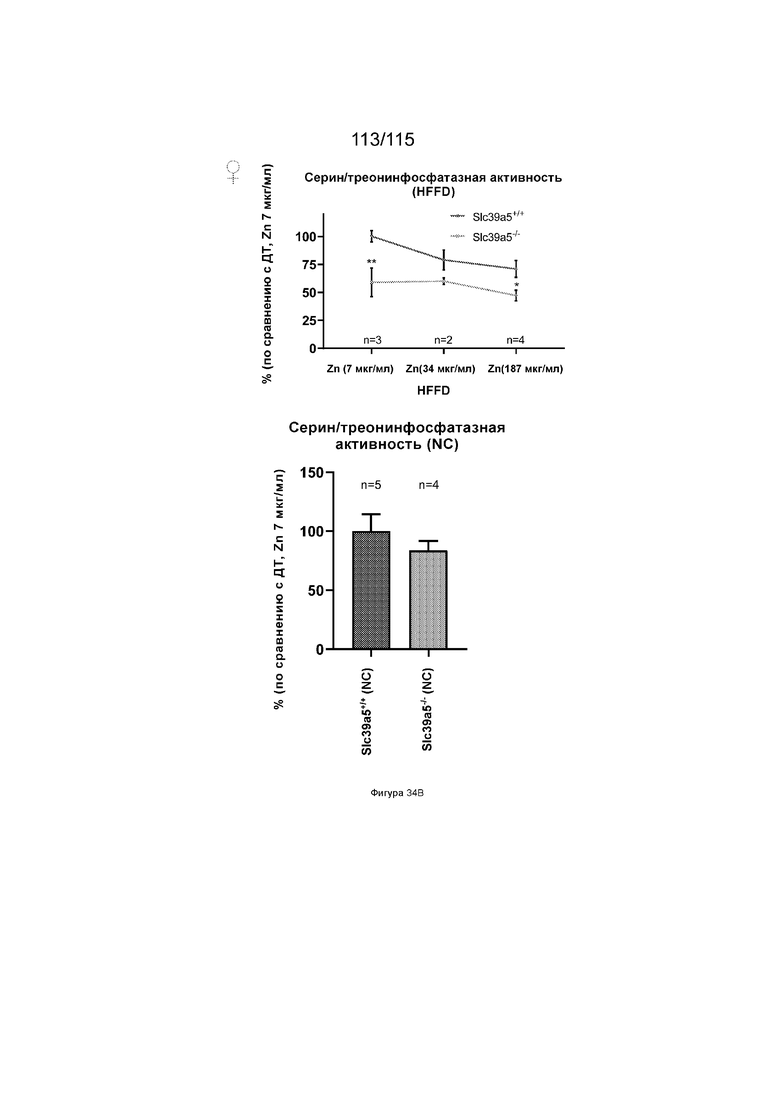
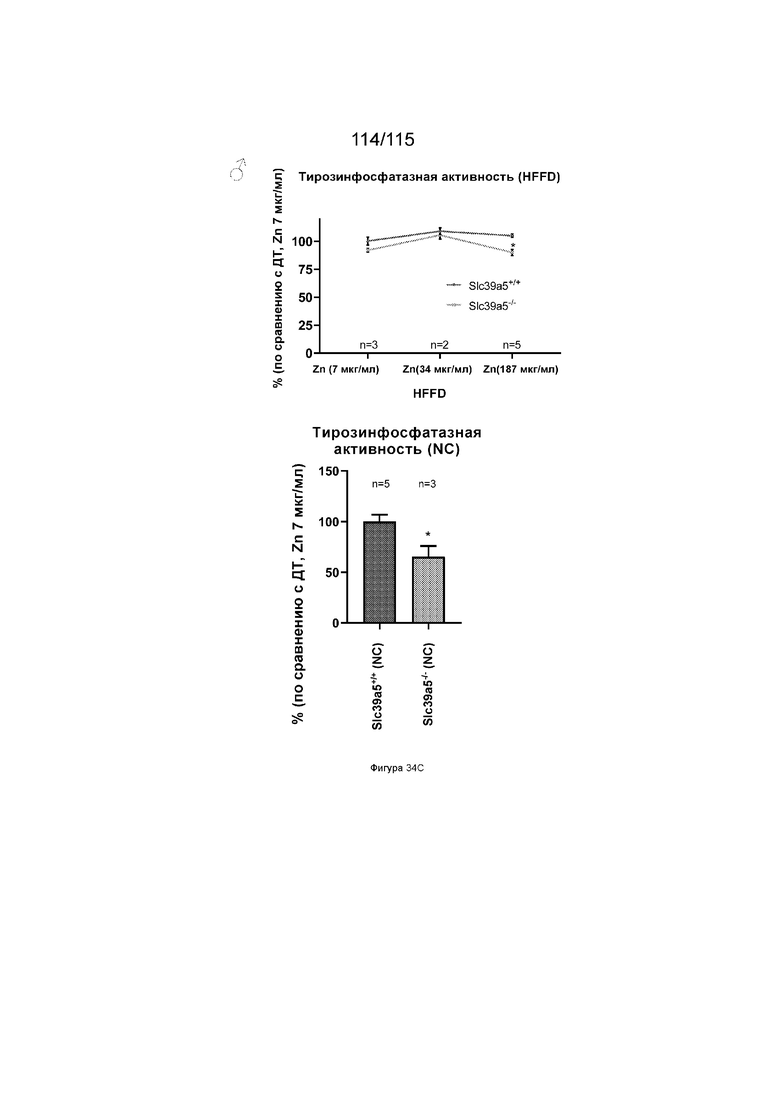
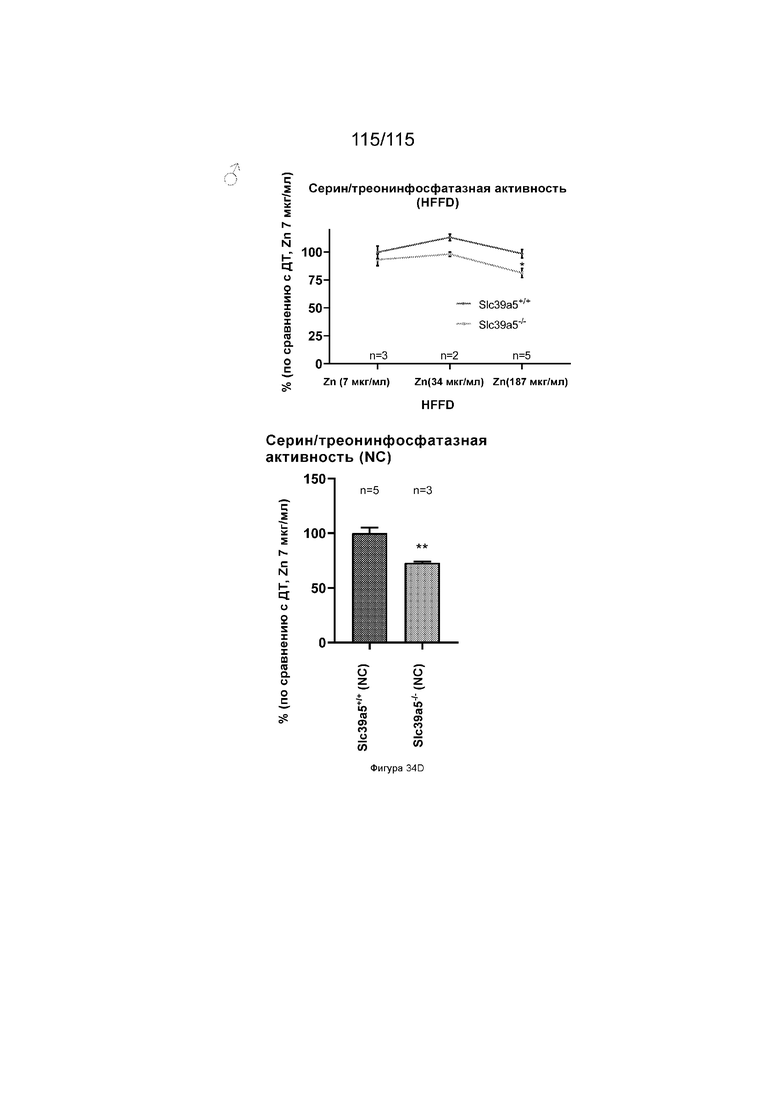
Группа изобретений относится к способам лечения субъекта-человека женского пола, имеющего толерантность к глюкозе, или субъекта-человека женского пола со стеатозом печени, где субъект является эталонным по SLC39A5 или гетерозиготным по вариантной молекуле нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5, а также к способам идентификации субъекта-человека женского пола, имеющего высокий риск толерантности к глюкозе или повышенный риск стеатоза печени. Способы лечения предусматривают применение терапевтического агента для лечения или ингибирования толерантости к глюкозе или ингибитора SLC39A5. Способы идентификации субъектов с высоким риском толерантности к глюкозе или повышенным риском стеатоза печени предусматривают определение присутствия или отсутствия вариантной молекулы нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5. Изобретения позволяют идентифицировать субъектов-людей, являющихся эталонными по SLC39A5 или гетерозиготными по варианту с прогнозируемой потерей функции SLC39A5, которые имеют высокий риск развития повышенного уровня глюкозы в сыворотке и стеатоза печени, так что субъектов из группы риска или субъектов с активным заболеванием можно лечить соответствующим образом. 10 н. и 39 з.п. ф-лы, 34 ил., 3 табл., 16 пр.
1. Способ лечения субъекта-человека женского пола, имеющего стеатоз печени, включающий введение субъекту ингибитора члена 5 семейства 39 транспортеров растворенных веществ (SLC39A5),
где указанный субъект является эталонным по SLC39A5 или гетерозиготным по вариантной молекуле нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5; и
где ингибитор SLC39A5 включает малую интерферирующую РНК (миРНК) или короткую шпилечную РНК (кшРНК), которые гибридизуются с мРНК SLC39A5.
2. Способ лечения субъекта-человека женского пола, имеющего толерантность к глюкозе, включающий введение субъекту ингибитора члена 5 семейства 39 транспортеров растворенных веществ (SLC39A5),
где указанный субъект является эталонным по SLC39A5 или гетерозиготным по вариантной молекуле нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5; и
где ингибитор SLC39A5 включает малую интерферирующую РНК (миРНК) или короткую шпилечную РНК (кшРНК), которые гибридизуются с мРНК SLC39A5.
3. Способ лечения субъекта-человека женского пола с помощью терапевтического средства, которое лечит или ингибирует стеатоз печени, где указанный субъект страдает стеатозом печени, где указанный способ включает стадии:
идентификации субъекта как требующего лечения посредством определения того, имеет ли субъект вариантную молекулу нуклеиновой кислоты с прогнозируемой потерей функции члена 5 семейства 39 транспортеров растворенных веществ (SLC39A5), кодирующую полипептид SLC39A5 человека, путем:
получения или осуществления получения биологического образца от субъекта; и
выполнения или осуществления выполнения генотипирования биологического образца для определения того, имеет ли субъект генотип, содержащий вариантную молекулу нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5; и
когда субъект является эталонным по SLC39A5, то введения или продолжения введения субъекту терапевтического средства, которое лечит или ингибирует стеатоз печени, в стандартной дозировке и введения субъекту ингибитора SLC39A5; и
когда субъект является гетерозиготным по вариантной молекуле нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5, то введения или продолжения введения субъекту терапевтического средства, которое лечит или ингибирует стеатоз печени, в количестве, которое является таким же или ниже чем стандартная дозировка, и введения субъекту ингибитора SLC39A5;
где присутствие генотипа, имеющего вариантную молекулу нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5, кодирующую полипептид SLC39A5 человека, указывает на то, что у субъекта снижен риск развития стеатоза печени; и
где ингибитор SLC39A5 включает малую интерферирующую РНК (миРНК) или короткую шпилечную РНК (кшРНК), которые гибридизуются с мРНК SLC39A5.
4. Способ идентификации субъекта-человека женского пола, имеющего повышенный риск стеатоза печени, включающий
определение или осуществление определения присутствия или отсутствия вариантной молекулы нуклеиновой кислоты с прогнозируемой потерей функции члена 5 семейства 39 транспортеров растворенных веществ (SLC39A5), кодирующей полипептид SLC39A5 человека, в биологическом образце, полученном от субъекта;
где:
когда указанный субъект-человек женского пола является эталонным по SLC39A5, тогда указанный субъект-человек женского пола имеет повышенный риск развития стеатоза печени; и
когда указанный субъект-человек женского пола является гетерозиготным по вариантной молекуле нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 или гомозиготным по вариантной молекуле нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5, тогда указанный субъект-человек женского пола имеет пониженный риск развития стеатоза печени.
5. Применение терапевтического средства для лечения или ингибирования стеатоза печени при лечении стеатоза печени у субъекта-человека женского пола, имеющего:
i) молекулу геномной нуклеиновой кислоты, имеющую нуклеотидную последовательность, кодирующую полипептид члена 5 семейства 39 транспортеров растворенных веществ (SLC39A5), где указанная нуклеотидная последовательность содержит: цитозин в положении, соответствующем положению 5604 согласно SEQ ID NO: 4 или ее комплементу; цитозин в положении, соответствующем положению 6899 согласно SEQ ID NO: 6 или ее комплементу; аденин или гуанин в положении, соответствующем положению 1353 согласно SEQ ID NO: 2 или SEQ ID NO: 3 или их комплементу; тимин в положении, соответствующем положению 6352 согласно SEQ ID NO: 5 или ее комплементу; или тимин в положении, соответствующем положению 5624 согласно SEQ ID NO: 7 или ее комплементу; или
ii) молекулу мРНК, имеющую нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, где указанная нуклеотидная последовательность содержит: цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 11 или ее комплементу; цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 13 или ее комплементу; аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 9 или SEQ ID NO: 10 или их комплементу; урацил в положении, соответствующем положению 1194 согласно SEQ ID NO: 12 или ее комплементу; или урацил в положении, соответствующем положению 1161 согласно SEQ ID NO: 14 или ее комплементу,
где указанное терапевтическое средство включает статин, агонист PPAR, гормон, агент на основе сульфонилмочевины, бигуанид, ингибитор α-глюкозидазы и/или агонист GLP-1.
6. Применение ингибитора члена 5 семейства 39 транспортеров растворенных веществ (SLC39A5) для лечения стеатоза печени у субъекта-человека женского пола, имеющего:
i) молекулу геномной нуклеиновой кислоты, имеющую нуклеотидную последовательность, кодирующую полипептид члена 5 семейства 39 транспортеров растворенных веществ (SLC39A5), где указанная нуклеотидная последовательность содержит: цитозин в положении, соответствующем положению 5604 согласно SEQ ID NO: 4 или ее комплементу; цитозин в положении, соответствующем положению 6899 согласно SEQ ID NO: 6 или ее комплементу; аденин или гуанин в положении, соответствующем положению 1353 согласно SEQ ID NO: 2 или SEQ ID NO: 3 или их комплементу; тимин в положении, соответствующем положению 6352 согласно SEQ ID NO: 5 или ее комплементу; или тимин в положении, соответствующем положению 5624 согласно SEQ ID NO: 7 или ее комплементу; или
ii) молекулу мРНК, имеющую нуклеотидную последовательность, кодирующую полипептид SLC39A5 человека, где указанная нуклеотидная последовательность содержит: цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 11 или ее комплементу; цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 13 или ее комплементу; аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 9 или SEQ ID NO: 10 или их комплементу; урацил в положении, соответствующем положению 1194 согласно SEQ ID NO: 12 или ее комплементу; или урацил в положении, соответствующем положению 1161 согласно SEQ ID NO: 14 или ее комплементу,
где ингибитор SLC39A5 включает малую интерферирующую РНК (миРНК) или короткую шпилечную РНК (кшРНК), которые гибридизуются с мРНК SLC39A5.
7. Способ по п. 1 или 2, где субъекту дополнительно вводят антитело к SLC39A5.
8. Способ по любому из пп. 1, 2 и 7, где субъекту дополнительно вводят цинк.
9. Способ по п. 1, где, когда субъект является эталонным по SLC39A5, указанному субъекту также вводят терапевтический агент, который нормализует или ингибирует стеатоз печени, в стандартной дозировке.
10. Способ по п. 1, где, когда субъект является эталонным по SLC39A5, указанному субъекту также вводят терапевтический агент, который нормализует или ингибирует толерантность к глюкозе, в стандартной дозировке.
11. Способ по п. 1, где, когда субъект является гетерозиготным по варианту с прогнозируемой потерей функции SLC39A5, указанному субъекту также вводят терапевтический агент, который нормализует или ингибирует стеатоз печени, в дозировке, которая является такой же или ниже стандартной дозировки.
12. Способ по п. 1, где, когда субъект является гетерозиготным по варианту с прогнозируемой потерей функции SLC39A5, указанному субъекту также вводят терапевтический агент, который нормализует или ингибирует толерантность к глюкозе, в дозировке, которая является такой же или ниже стандартной дозировки.
13. Способ по любому из пп. 1, 2 и 7-12, где вариантная молекула нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 представляет собой молекулу нуклеиновой кислоты, кодирующую SLC39A5 M304T, SLC39A5 G413A, SLC39A5 Y47Stop, SLC39A5 R322Stop или SLC39A5 R311Stop.
14. Способ по любому из пп. 1, 2 и 7-12, где вариантная молекула нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 представляет собой молекулу нуклеиновой кислоты, кодирующую SLC39A5 M304T, SLC39A5 Y47Stop, SLC39A5 R322Stop или SLC39A5 R311Stop.
15. Способ по п. 11 или 12, где вариантная молекула нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 представляет собой: i) молекулу геномной нуклеиновой кислоты, имеющую нуклеотидную последовательность, содержащую цитозин в положении, соответствующем положению 5604 согласно SEQ ID NO: 4; ii) молекулу мРНК, имеющую нуклеотидную последовательность, содержащую цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 11; iii) молекулу кДНК, полученную из молекулы мРНК, при этом молекула кДНК имеет нуклеотидную последовательность, содержащую цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 18; iv) молекулу геномной нуклеиновой кислоты, имеющую нуклеотидную последовательность, содержащую цитозин в положении, соответствующем положению 6899 согласно SEQ ID NO: 6; v) молекулу мРНК, имеющую нуклеотидную последовательность, содержащую цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 13; vi) молекулу кДНК, полученную из молекулы мРНК, при этом молекула кДНК имеет нуклеотидную последовательность, содержащую цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 20; vii) молекулу геномной нуклеиновой кислоты, имеющую нуклеотидную последовательность, содержащую аденин или гуанин в положении, соответствующем положению 1353, согласно SEQ ID NO: 2 или SEQ ID NO: 3; viii) молекулу мРНК, имеющую нуклеотидную последовательность, содержащую аденин или гуанин в положении, соответствующем положению 371, согласно SEQ ID NO: 9 или SEQ ID NO: 10; ix) молекулу кДНК, полученную из молекулы мРНК, при этом молекула кДНК имеет нуклеотидную последовательность, содержащую аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 16 или SEQ ID NO: 17; x) молекулу геномной нуклеиновой кислоты, имеющую нуклеотидную последовательность, содержащую тимин в положении, соответствующем положению 6352 согласно SEQ ID NO: 5; xi) молекулу мРНК, имеющую нуклеотидную последовательность, содержащую урацил в положении, соответствующем положению 1194 согласно SEQ ID NO: 12; xii) молекулу кДНК, полученную из молекулы мРНК, при этом молекула кДНК имеет нуклеотидную последовательность, содержащую тимин в положении, соответствующем положению 1194 согласно SEQ ID NO: 19; xiii) молекулу геномной нуклеиновой кислоты, имеющую нуклеотидную последовательность, содержащую тимин в положении, соответствующем положению 5624 согласно SEQ ID NO: 7; xiv) молекулу мРНК, имеющую нуклеотидную последовательность, содержащую урацил в положении, соответствующем положению 1161 согласно SEQ ID NO: 14; или xv) молекулу кДНК, полученную из молекулы мРНК, при этом молекула кДНК имеет нуклеотидную последовательность, содержащую тимин в положении, соответствующем положению 1161 согласно SEQ ID NO: 21.
16. Способ лечения субъекта-человека женского пола терапевтическим агентом, который нормализует или ингибирует толерантность к глюкозе, при этом способ включает стадии:
идентификации субъекта как требующего лечения посредством определения того, имеет ли субъект вариантную молекулу нуклеиновой кислоты с прогнозируемой потерей функции члена 5 семейства 39 транспортеров растворенных веществ (SLC39A5), кодирующую полипептид SLC39A5 человека, путем:
получения или осуществления получения биологического образца от субъекта; и
выполнения или осуществления выполнения анализа генотипирования биологического образца для определения того, имеет ли пациент генотип, содержащий вариантную молекулу нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5; и
когда субъект является эталонным по SLC39A5, то введения или продолжения введения субъекту терапевтического агента, который лечит или ингибирует толерантность к глюкозе, в стандартной дозировке и введения субъекту ингибитора SLC39A5; и
когда субъект является гетерозиготным по вариантной молекуле нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5, то введения или продолжения введения субъекту терапевтического агента, который нормализует или ингибирует толерантность к глюкозе, в количестве, которое является таким же или ниже чем стандартная дозировка, и введения субъекту ингибитора SLC39A5;
при этом присутствие генотипа, имеющего вариантную молекулу нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5, кодирующую полипептид SLC39A5 человека, указывает на то, что у субъекта снижен риск развития толерантности к глюкозе, и
где ингибитор SLC39A5 включает малую интерферирующую РНК (миРНК) или короткую шпилечную РНК (кшРНК), которые гибридизуются с мРНК SLC39A5.
17. Способ по п. 3, где субъект является эталонным по SLC39A5 и субъекту вводят или продолжают вводить терапевтический агент, который нормализует или ингибирует толерантность к глюкозе, в стандартной дозировке и вводят ингибитор SLC39A5.
18. Способ по п. 16, где субъект является эталонным по SLC39A5 и субъекту вводят или продолжают вводить терапевтический агент, который нормализует или ингибирует толерантность к глюкозе, в стандартной дозировке и вводят ингибитор SLC39A5.
19. Способ по п. 3, где субъект является гетерозиготным по вариантной молекуле нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 и указанному субъекту вводят или продолжают вводить терапевтический агент, который нормализует или ингибирует стеатоз печени, в количестве, которое является таким же или ниже чем стандартная дозировка, и вводят ингибитор SLC39A5.
20. Способ по п. 16, где субъект является гетерозиготным по вариантной молекуле нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 и указанному субъекту вводят или продолжают вводить терапевтический агент, который нормализует или ингибирует толерантность к глюкозе, в количестве, которое является таким же или ниже чем стандартная дозировка, и вводят ингибитор SLC39A5.
21. Способ по любому из пп. 3 и 16-20, где анализ генотипирования включает секвенирование по меньшей мере части нуклеотидной последовательности молекулы нуклеиновой кислоты SLC39A5 в биологическом образце, при этом секвенированная часть содержит положение, соответствующее положению варианта с прогнозируемой потерей функции, причем в случае обнаружения положения варианта с предполагаемой потерей функции молекула нуклеиновой кислоты SLC39A5 в биологическом образце представляет собой вариантную молекулу нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5.
22. Способ по любому из пп. 3 и 16-21, где генотипирование включает:
a) приведение биологического образца в контакт с праймером, гибридизующимся с частью нуклеотидной последовательности молекулы нуклеиновой кислоты SLC39A5, которая находится вблизи положения варианта с прогнозируемой потерей функции;
b) удлинение праймера по меньшей мере через положение варианта с прогнозируемой потерей функции; и
c) определение того, содержит ли продукт удлинения праймера вариантный нуклеотид в положении варианта с прогнозируемой потерей функции.
23. Способ по п. 21 или 22, где стадия обнаружения включает секвенирование всей молекулы нуклеиновой кислоты.
24. Способ по любому из пп. 3 и 16-19, где генотипирование включает:
а) амплификацию по меньшей мере части молекулы нуклеиновой кислоты SLC39A5, которая кодирует человеческий полипептид SLC39A5, при этом часть содержит положение варианта с прогнозируемой потерей функции;
b) мечение амплифицированной молекулы нуклеиновой кислоты обнаруживаемой меткой;
c) приведение меченой молекулы нуклеиновой кислоты в контакт с подложкой, содержащей специфический в отношении изменения зонд, причем специфический в отношении изменения зонд содержит нуклеотидную последовательность, которая в жестких условиях гибридизуется с положением варианта с прогнозируемой потерей функции; и
d) обнаружение обнаруживаемой метки.
25. Способ по п. 24, где молекула нуклеиновой кислоты в образце представляет собой мРНК и указанную мРНК обратно транскрибируют в кДНК перед стадией амплификации.
26. Способ по п. 24 или 25, где стадия обнаружения включает:
приведение молекулы нуклеиновой кислоты в биологическом образце в контакт со специфическим в отношении изменения зондом, содержащим обнаруживаемую метку, при этом специфический в отношении изменения зонд содержит нуклеотидную последовательность, которая в жестких условиях гибридизуется с положением варианта с прогнозируемой потерей функции; и
обнаружение обнаруживаемой метки.
27. Способ по любому из пп. 3 и 16-26, где вариантная молекула нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 представляет собой молекулу нуклеиновой кислоты, кодирующую SLC39A5 M304T, SLC39A5 G413A, SLC39A5 Y47Stop, SLC39A5 R322Stop или SLC39A5 R311Stop.
28. Способ по любому из пп. 3 и 16-26, где вариантная молекула нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 представляет собой молекулу нуклеиновой кислоты, кодирующую SLC39A5 M304T, SLC39A5 Y47Stop, SLC39A5 R322Stop или SLC39A5 R311Stop.
29. Способ по любому из пп. 3 и 16-28, где вариантная молекула нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 представляет собой: i) молекулу геномной нуклеиновой кислоты, имеющую нуклеотидную последовательность, содержащую цитозин в положении, соответствующем положению 5604 согласно SEQ ID NO: 4; ii) молекулу мРНК, имеющую нуклеотидную последовательность, содержащую цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 11; iii) молекулу кДНК, полученную из молекулы мРНК, при этом молекула кДНК имеет нуклеотидную последовательность, содержащую цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 18; iv) молекулу геномной нуклеиновой кислоты, имеющую нуклеотидную последовательность, содержащую цитозин в положении, соответствующем положению 6899 согласно SEQ ID NO: 6; v) молекулу мРНК, имеющую нуклеотидную последовательность, содержащую цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 13; vi) молекулу кДНК, полученную из молекулы мРНК, при этом молекула кДНК имеет нуклеотидную последовательность, содержащую цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 20; vii) молекулу геномной нуклеиновой кислоты, имеющую нуклеотидную последовательность, содержащую аденин или гуанин в положении, соответствующем положению 1353, согласно SEQ ID NO: 2 или SEQ ID NO: 3; viii) молекулу мРНК, имеющую нуклеотидную последовательность, содержащую аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 9 или SEQ ID NO: 10; ix) молекулу кДНК, полученную из молекулы мРНК, при этом молекула кДНК имеет нуклеотидную последовательность, содержащую аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 16 или SEQ ID NO: 17; x) молекулу геномной нуклеиновой кислоты, имеющую нуклеотидную последовательность, содержащую тимин в положении, соответствующем положению 6352 согласно SEQ ID NO: 5; xi) молекулу мРНК, имеющую нуклеотидную последовательность, содержащую урацил в положении, соответствующем положению 1194 согласно SEQ ID NO: 12; xii) молекулу кДНК, полученную из молекулы мРНК, при этом молекула кДНК имеет нуклеотидную последовательность, содержащую тимин в положении, соответствующем положению 1194 согласно SEQ ID NO: 19; xiii) молекулу геномной нуклеиновой кислоты, имеющую нуклеотидную последовательность, содержащую тимин в положении, соответствующем положению 5624 согласно SEQ ID NO: 7; xiv) молекулу мРНК, имеющую нуклеотидную последовательность, содержащую урацил в положении, соответствующем положению 1161 согласно SEQ ID NO: 14; или xv) молекулу кДНК, полученную из молекулы мРНК, при этом молекула кДНК имеет нуклеотидную последовательность, содержащую тимин в положении, соответствующем положению 1161 согласно SEQ ID NO: 21.
30. Способ по любому одному из пп. 3 и 16-29, где молекула нуклеиновой кислоты присутствует в клетке, полученной от субъекта-человека.
31. Способ по любому из пп. 3 и 16-30, где субъекту дополнительно вводят антитело к SLC39A5.
32. Способ идентификации субъекта-человека женского пола, имеющего повышенный риск толерантности к глюкозе, включающий
определение или осуществление определения наличия или отсутствия вариантной молекулы нуклеиновой кислоты с прогнозируемой потерей функции члена 5 семейства 39 транспортеров растворенных веществ (SLC39A5), кодирующей полипептид SLC39A5 человека, в биологическом образце, полученном от субъекта;
при этом
когда субъект-человек женского пола является эталонным по SLC39A5, то субъект-человек женского пола имеет повышенный риск развития толерантности к глюкозе; и
когда субъект-человек женского пола является гетерозиготным по вариантной молекуле нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 или гомозиготным по вариантной молекуле нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5, тогда субъект-человек женского пола имеет пониженный риск развития толерантности к глюкозе.
33. Способ по п. 4 или 32, где стадия определения включает секвенирование по меньшей мере части нуклеотидной последовательности молекулы нуклеиновой кислоты SLC39A5 в биологическом образце, при этом секвенированная часть содержит положение, соответствующее положению варианта с прогнозируемой потерей функции, причем в случае обнаружения положения варианта с предполагаемой потерей функции молекула нуклеиновой кислоты SLC39A5 в биологическом образце представляет собой вариантную молекулу нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5.
34. Способ по любому из пп. 4, 32 и 33, где стадия определения включает:
a) приведение биологического образца в контакт с праймером, гибридизующимся с частью нуклеотидной последовательности молекулы нуклеиновой кислоты SLC39A5, которая находится вблизи положения варианта с прогнозируемой потерей функции;
b) удлинение праймера по меньшей мере через положение варианта с прогнозируемой потерей функции; и
c) определение того, содержит ли продукт удлинения праймера вариантный нуклеотид в положении варианта с прогнозируемой потерей функции.
35. Способ по любому из пп. 4, 31 и 34, где стадия определения включает секвенирование всей молекулы нуклеиновой кислоты.
36. Способ по п. 31, где стадия определения включает:
а) амплификацию по меньшей мере части молекулы нуклеиновой кислоты SLC39A5, которая кодирует человеческий полипептид SLC39A5, при этом часть содержит положение варианта с прогнозируемой потерей функции;
b) мечение амплифицированной молекулы нуклеиновой кислоты обнаруживаемой меткой;
c) приведение меченой молекулы нуклеиновой кислоты в контакт с подложкой, содержащей специфический в отношении изменения зонд, причем специфический в отношении изменения зонд содержит нуклеотидную последовательность, которая в жестких условиях гибридизуется с положением варианта с прогнозируемой потерей функции; и
d) обнаружение обнаруживаемой метки.
37. Способ по п. 36, где молекула нуклеиновой кислоты в образце представляет собой мРНК и указанную мРНК обратно транскрибируют в кДНК перед стадией амплификации.
38. Способ по п. 36 или 37, где стадия определения включает:
приведение молекулы нуклеиновой кислоты в биологическом образце в контакт со специфическим в отношении изменения зондом, содержащим обнаруживаемую метку, при этом специфический в отношении изменения зонд содержит нуклеотидную последовательность, которая в жестких условиях гибридизуется с положением варианта с прогнозируемой потерей функции; и
обнаружение обнаруживаемой метки.
39. Способ по любому из пп. 4 и 32-38, где вариантная молекула нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 представляет собой молекулу нуклеиновой кислоты, кодирующую SLC39A5 M304T, SLC39A5 G413A, SLC39A5 Y47Stop, SLC39A5 R322Stop или SLC39A5 R311Stop.
40. Способ по любому из пп. 4 и 32-38, где вариантная молекула нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 представляет собой молекулу нуклеиновой кислоты, кодирующую SLC39A5 M304T, SLC39A5 Y47Stop, SLC39A5 R322Stop, SLC39A5 или R311Stop.
41. Способ по любому из пп. 4 и 32-40, где вариантная молекула нуклеиновой кислоты с прогнозируемой потерей функции SLC39A5 представляет собой: i) молекулу геномной нуклеиновой кислоты, имеющую нуклеотидную последовательность, содержащую цитозин в положении, соответствующем положению 5604 согласно SEQ ID NO: 4; ii) молекулу мРНК, имеющую нуклеотидную последовательность, содержащую цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 11; iii) молекулу кДНК, полученную из молекулы мРНК, при этом молекула кДНК имеет нуклеотидную последовательность, содержащую цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 18; iv) молекулу геномной нуклеиновой кислоты, имеющую нуклеотидную последовательность, содержащую цитозин в положении, соответствующем положению 6899 согласно SEQ ID NO: 6; v) молекулу мРНК, имеющую нуклеотидную последовательность, содержащую цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 13; vi) молекулу кДНК, полученную из молекулы мРНК, при этом молекула кДНК имеет нуклеотидную последовательность, содержащую цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 20; vii) молекулу геномной нуклеиновой кислоты, имеющую нуклеотидную последовательность, содержащую аденин или гуанин в положении, соответствующем положению 1353 согласно SEQ ID NO: 2 или SEQ ID NO: 3; viii) молекулу мРНК, имеющую нуклеотидную последовательность, содержащую аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 9 или SEQ ID NO: 10; ix) молекулу кДНК, полученную из молекулы мРНК, при этом молекула кДНК имеет нуклеотидную последовательность, содержащую аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 16 или SEQ ID NO: 17; x) молекулу геномной нуклеиновой кислоты, имеющую нуклеотидную последовательность, содержащую тимин в положении, соответствующем положению 6352 согласно SEQ ID NO: 5; xi) молекулу мРНК, имеющую нуклеотидную последовательность, содержащую урацил в положении, соответствующем положению 1194 согласно SEQ ID NO: 12; xii) молекулу кДНК, полученную из молекулы мРНК, при этом молекула кДНК имеет нуклеотидную последовательность, содержащую тимин в положении, соответствующем положению 1194 согласно SEQ ID NO: 19; xiii) молекулу геномной нуклеиновой кислоты, имеющую нуклеотидную последовательность, содержащую тимин в положении, соответствующем положению 5624 согласно SEQ ID NO: 7; xiv) молекулу мРНК, имеющую нуклеотидную последовательность, содержащую урацил в положении, соответствующем положению 1161 согласно SEQ ID NO: 14; или xv) молекулу кДНК, полученную из молекулы мРНК, при этом молекула кДНК имеет нуклеотидную последовательность, содержащую тимин в положении, соответствующем положению 1161 согласно SEQ ID NO: 21.
42. Способ по любому из пп. 4 и 32-41, где стадию определения выполняют in vitro.
43. Способ по любому из пп. 4 и 32-42, где субъект-человек женского пола является эталонным по SLC39A5 и указанному субъекту-человеку женского пола вводят терапевтическое средство, которое нормализует или ингибирует стеатоз печени, в стандартной дозировке и вводят ингибитор SLC39A5.
44. Способ по любому из пп. 4 и 32-42, где субъект-человек женского пола является эталонным по SLC39A5 и указанному субъекту-человеку женского пола вводят терапевтическое средство, которое нормализует или ингибирует толерантность к глюкозе, в стандартной дозировке и вводят ингибитор SLC39A5.
45. Способ по любому из пп. 4 и 32-42, где субъект-человек женского пола является гетерозиготным по варианту с прогнозируемой потерей функции SLC39A5 и указанному субъекту-человеку женского пола вводят терапевтическое средство, которое нормализует или ингибирует стеатоз печени, в количестве, которое является таким же или ниже количества стандартной дозировки, и вводят ингибитор SLC39A5.
46. Способ по любому из пп. 4 и 32-42, где субъект-человек женского пола является гетерозиготным по варианту с прогнозируемой потерей функции SLC39A5 и указанному субъекту-человеку женского пола вводят терапевтическое средство, которое нормализует или ингибирует толерантность к глюкозе, в количестве, которое является таким же или ниже количества стандартной дозировки, и вводят ингибитор SLC39A5.
47. Применение терапевтического агента для лечения или ингибирования толерантости к глюкозе в лечении толерантости к глюкозе у субъекта-человека женского пола, имеющего:
i) геномную молекулу нуклеиновой кислоты, имеющую нуклеотидную последовательность, кодирующую человеческий полипептид члена 5 семейства 39 транспортеров растворенных веществ (SLC39A5), при этом нуклеотидная последовательность содержит: цитозин в положении, соответствующем положению 5604 согласно SEQ ID NO: 4, или ее комплементарной цепи; цитозин в положении, соответствующем положению 6899 согласно SEQ ID NO: 6, или ее комплементарной цепи; аденин или гуанин в положении, соответствующем положению 1353 согласно SEQ ID NO: 2 или SEQ ID NO: 3, или их комплементарным цепям; тимин в положении, соответствующем положению 6352 согласно SEQ ID NO: 5, или ее комплементарной цепи; или тимин в положении, соответствующем положению 5624 согласно SEQ ID NO: 7, или ее комплементарной цепи; или
ii) молекулу мРНК, имеющую нуклеотидную последовательность, кодирующую человеческий полипептид SLC39A5, при этом нуклеотидная последовательность содержит: цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 11, или ее комплементарной цепи; цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 13, или ее комплементарной цепи; аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 9 или SEQ ID NO: 10, или их комплементарным цепям; урацил в положении, соответствующем положению 1194 согласно SEQ ID NO: 12, или ее комплементарной цепи; или урацил в положении, соответствующем положению 1161 согласно SEQ ID NO: 14, или ее комплементарной цепи, где указанный терапевтический агент включает статин, агонист PPAR, гормон, агент на основе сульфонилмочевины, бигуанид, ингибитор α-глюкозидазы и/или агонист GLP-1.
48. Применение ингибитора члена 5 семейства 39 транспортеров растворенных веществ (SLC39A5) в лечении толерантости к глюкозе у субъекта-человека женского пола, имеющего:
i) геномную молекулу нуклеиновой кислоты, имеющую нуклеотидную последовательность, кодирующую человеческий полипептид SLC39A5, при этом нуклеотидная последовательность содержит: цитозин в положении, соответствующем положению 5604 согласно SEQ ID NO: 4, или ее комплементарной цепи; цитозин в положении, соответствующем положению 6899 согласно SEQ ID NO: 6, или ее комплементарной цепи; аденин или гуанин в положении, соответствующем положению 1353 согласно SEQ ID NO: 2 или SEQ ID NO: 3, или их комплементарным цепям; тимин в положении, соответствующем положению 6352 согласно SEQ ID NO: 5, или ее комплементарной цепи; или тимин в положении, соответствующем положению 5624 согласно SEQ ID NO: 7, или ее комплементарной цепи; или
ii) молекулу мРНК, имеющую нуклеотидную последовательность, кодирующую человеческий полипептид SLC39A5, при этом нуклеотидная последовательность содержит: цитозин в положении, соответствующем положению 1141 согласно SEQ ID NO: 11, или ее комплементарной цепи; цитозин в положении, соответствующем положению 1468 согласно SEQ ID NO: 13, или ее комплементарной цепи; аденин или гуанин в положении, соответствующем положению 371 согласно SEQ ID NO: 9 или SEQ ID NO: 10, или их комплементарным цепям; урацил в положении, соответствующем положению 1194 согласно SEQ ID NO: 12, или ее комплементарной цепи; или урацил в положении, соответствующем положению 1161 согласно SEQ ID NO: 14, или ее комплементарной цепи, где ингибитор SLC39A5 включает малую интерферирующую РНК (миРНК) или короткую шпилечную РНК (кшРНК), которые гибридизуются с мРНК SLC39A5.
49. Применение по п. 48, где ингибитор SLC39A5 используют в комбинации с антителом к SLC39A5.
| LI QIAN ET AL | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| ONCOLOGY RESEARCH, 18 July 2016, v.24, no.3, p.205-214 | |||
| GUO HUI ET AL | |||
| Машина для изготовления проволочных гвоздей | 1922 |
|
SU39A1 |
| JOURNAL OF MEDICAL GENETICS, 2014, v.51, no.8, p.518-525 | |||
| US 6307080 B1, | |||
Авторы
Даты
2024-12-25—Публикация
2020-03-12—Подача