Область техники, к которой относится изобретение
Настоящее изобретение относится к области биомедицины и фармацевтической промышленности, в частности к фармацевтической композиции для лечения и предупреждения синдрома цитокинового шторма.
Эта композиция включает пептид, идентифицированный как SEQ ID NO: 1, и может быть использована для лечения острого респираторного дистресс-синдрома, синдрома активации макрофагов, респираторного сепсиса, лихорадки денге, печеночной энцефалопатии и перикардита, среди прочих заболеваний.
Предшествующий уровень техники
Среди лиц, инфицированных вирусом SARS-CoV-2, у которых развивается инфекционное заболевание Covid-19, описана подгруппа пациентов, у которых формируется состояние гипервоспаления. У этих пациентов описан «цитокиновый шторм», особенно связанный с интерлейкинами (IL), характеризующийся, среди прочего, повышением уровней IL-2, IL-17, IL-6, TNFα. Это состояние гипервоспаления приводит к смерти пациентов (Mehta, et al. (2020). The Lancet, 395: 1033-1034).
С другой стороны, в ретроспективном исследовании, включавшем 150 подтвержденных случаев Covid-19 в Ухане, Китай, было продемонстрировано значительное повышение концентрации ферритина у невыживших пациентов (1297,6 нг/мл) по сравнению с уровнями этого белка у пациентов, которые выжили (614 нг/мл) (Ruan et al. (2020). Intensive Care Med; https://doi.org/10.1007/s00134-020-05991-x).
У пациентов с Covid-19, находящихся в тяжелом и критическом состоянии, развивается острый респираторный дистресс-синдром. Этот синдром характеризуется наличием воспалительных явлений в альвеолах, которые расширяются за счет системного кровообращения организма. В ходе этого синдрома происходит вовлечение легочного эндотелия с повышенной проницаемостью сосудов и перемещением клеток и макромолекул в альвеолярное пространство, где они инактивируют легочный сурфактант, формируя типичные гиалиновые мембраны (Janz and Ware (2014). Clin Chest Med; 35: 685-96). Эпителиальный барьер также изменяется, и воспалительный ответ усугубляется с секрецией провоспалительных IL, таких как TNFα, IL-1β и IL-6, и других медиаторов воспаления с последовательной активацией нейтрофилов, моноцитов, макрофагов, и переносом этих молекул и клеток в альвеолярные пространства, увеличивая начальное вовлечение. Развитие этого гипервоспаления происходит при других заболеваниях, таких как респираторный сепсис, синдром активации макрофагов и сепсис у взрослых и новорожденных.
В настоящее время не существует эффективной терапии для пациентов с заболеванием Covid-19. Одобренные терапии используются для лечения других заболеваний, например введение моноклональных антител против IL-1 (анакинра), IL-6 (тоцилизумаб) и ингибиторов белка Янус-киназы. Однако эти лекарственные средства оказались неэффективными, а также являются иммунодепрессантами, поэтому использование этих терапий для лечения Covid-19 может привести к ухудшению общего состояния пациента, поскольку подтверждена персистенция вируса в течение заболевания, и даже после клинического выздоровления пациентов. Эффективного и безопасного лечения респираторного сепсиса, синдрома активации макрофагов, неонатального сепсиса, а также дыхательной недостаточности также не существует.
Поэтому представляет большой интерес получение лекарственных средств, эффективных для лечения гипервоспаления и характерного для этих патологий «цитокинового шторма».
Сущность изобретения
Настоящее изобретение решает проблему, указанную выше, путем предоставления фармацевтической композиции для лечения и профилактики синдрома цитокинового шторма, которая включает пептид, идентифицированный как SEQ ID NO: 1, в концентрации 1,8-3,6 мг/мл и сахарозу в концентрации 20-30 мг/мл, что неожиданно синергетически увеличивает биологическую активность указанного пептида, в дополнение к тому, что он является определяющим фактором для индукции регуляторных Т-клеток, которые контролируют степень воспаления. Композиция по изобретению способна уменьшать гипервоспаление, характерное для подгруппы пациентов с Covid-19, у которых заболевание прогрессирует до тяжелой стадии, характеризующейся респираторным дистресс-синдромом, как это происходит при респираторном сепсисе, синдроме активации макрофагов, а также сепсисе у новорожденных и взрослых. Введение пептида, идентифицированного как SEQ ID NO: 1, снижает уровень провоспалительных цитокинов у пациентов с заболеванием Covid-19, не вызывая иммуносупрессии или серьезных побочных эффектов или тех, которые связаны с пептидной терапией.
Пептид, идентифицированный как SEQ ID NO: 1, получен из области белка HSP60, состоящей из аминокислот с 83 по 109. HSP60 является высокоиммуногенным как у здоровых людей, так и у пациентов с аутоиммунными заболеваниями. Однако уровень антител и Т-клеток, которые может индуцировать этот белок, выше у пациентов с аутоиммунными заболеваниями (de Jong et al (2009). Arthritis Rheum. 7 (60): 1966-1976).
Этот белок обладает большой способностью стимулировать провоспалительную реактивность врожденной иммунной системы. Также было обнаружено, что HSP60 индуцирует экспрессию генов IL-12 и IL-15, цитокинов, вовлеченных в индукцию фенотипа Th1. Эти факты предполагают, что HSP60 действует как сигнал опасности для врожденной иммунной системы (Habich et al. (2005). J.Immunol. 3 (174): 1298-1305). С другой стороны, пептиды, полученные из HSP60, также могут представлять собой сигнал опасности (Quintana and Cohen (2011). Trends Immunol. 2 (32): 89-95).
Пептид SEQ ID NO: 1 содержит несколько перекрывающихся Т-клеточных эпитопов. Он увеличивает частоту Treg-клеток с CD4+CD25highFoxp3+ фенотипом в анализах ex vivo с мононуклеарными клетками периферической крови пациентов с ревматоидным артритом. Однако этого не происходит с клетками от здоровых доноров (Barbera et al (2016). Cell Stress. Chaperones 4 (21): 735-744).
В международных патентных заявках № PCT/CU2005/000008 и PCT/CU2009/000009 заявлен пептид, идентифицированный как SEQ ID NO: 1, и его применение для лечения ревматоидного артрита, болезни Крона, язвенного колита и сахарного диабета I типа, соответственно. Все эти патологии относятся к неинфекционным заболеваниям. Кроме того, в патентной заявке WO 2019/129315 описывается очень стабильная фармацевтическая композиция, содержащая пептид SEQ ID NO: 1, ее введение вызывает снижение антител против цитруллинированных пептидов и других параметров, тесно связанных с цитруллинированием белков.
Пептид, идентифицированный как SEQ ID NO: 1, получают путем химического синтеза. С использованием экспериментов, таких как описанные в настоящем изобретении, можно оценить те иммунологические механизмы, индуцированные пептидом, которые способствуют контролю гипервоспаления. Фармацевтическая композиция хорошо переносилась и имела высокий профиль безопасности без признаков иммуносупрессии. Ни у одного из пациентов не было выявлено серьезных нежелательных явлений.
Для целей настоящего изобретения под синдромом цитокинового шторма понимают повышение уровней провоспалительных цитокинов, когда достигаются концентрации, превышающие нормальные уровни. Этими провоспалительными цитокинами являются IL-6, TNFα, IL-1, IL-17 и другие. Это также относится к повышению уровней других цитокинов, таких как IL-10, IL-8 и IL-5. Также этот термин включает повышение уровней биомаркеров воспаления, таких как С-реактивный белок, фибриноген, D-димер, печеночные трансаминазы, лактатдегидрогеназа и ферритин. Повышение уровней этих молекул, связанное с цитокиновым штормом, происходит у пациентов, страдающих воспалительными патологиями, такими как: острая дыхательная недостаточность, синдром активации макрофагов, респираторный сепсис, лихорадка денге, печеночная энцефалопатия и перикардит. При клиническом обследовании у пациентов могут наблюдаться постоянная лихорадка, слабость, утомляемость и тошнота.
В другом аспекте изобретение раскрывает применение фармацевтической композиции, включающей пептид, идентифицированный как SEQ ID NO: 1, для получения лекарственного средства для лечения и профилактики синдрома цитокинового шторма. К удивлению, лечение композицией, включающей указанный пептид, позволяет отменить искусственную вентиляцию легких у пациентов с Covid-19, улучшить течение интерстициальной пневмонии, снизить уровень реагентов острой фазы воспаления между 24 и 48 часами и снизить уровень биомаркеров воспаления. Быстрое снижение уровня С-реактивного белка всего за 24 часа является неожиданным открытием. Ранее у пациентов с ревматоидным артритом, получавших лечение этим пептидом, не удавалось продемонстрировать значительное снижение С-реактивного белка. (Prada, et al (2018). J Clin Trials 1 (8): 1-11).
Настоящее изобретение демонстрирует способность пептида, идентифицированного как SEQ ID NO: 1, вводимого внутривенно, уменьшать дыхательную недостаточность, гипервоспаление, уровень реагентов острой фазы воспаления и провоспалительных цитокинов у пациентов с Covid-19. К удивлению, эти результаты были воспроизведены у пациентов с респираторным сепсисом, у которых наблюдался респираторный дистресс-синдром.
В конкретном примере фармацевтическую композицию, включающую пептид, идентифицированный как SEQ ID NO: 1, используют для получения лекарственного средства для лечения и профилактики синдрома цитокинового шторма, проявляющегося в виде острого респираторного дистресс-синдрома, синдрома активации макрофагов, респираторного сепсиса у взрослых или новорожденных, синдрома системного воспалительного ответа, венозной или артериальной тромбоэмболии, острого повышения уровней ферритина, тяжелого перикардита, острого повышения печеночных трансаминаз, вызывающего печеночную энцефалопатию, или заболевания, связанного с терапией Т-клетками с химерным антигенным рецептором. Патологии, которые лечат фармацевтической композицией, включающей пептид, идентифицированный как SEQ ID NO: 1, включают синдром цитокинового шторма, лежащий в основе синдрома системного воспалительного ответа, который возникает у пациентов после ожогов или тяжелых травм или при острых воспалительных заболеваниях. В одном варианте осуществления изобретения лекарственное средство вводят внутривенно.
В примере изобретения лекарственное средство применяют для лечения и профилактики синдрома цитокинового шторма, вызываемого инфекционным заболеванием. В конкретном варианте осуществления указанное инфекционное заболевание представляет собой Covid-19 или лихорадку денге.
Объектом настоящего изобретения является способ лечения или предупреждения синдрома цитокинового шторма, который включает введение пациенту, нуждающемуся в этом, фармацевтически эффективного количества фармацевтической композиции, включающей пептид, идентифицированный как SEQ ID NO: 1. В конкретном примере синдром цитокинового шторма проявляется в виде острого респираторного дистресс-синдрома, синдрома активации макрофагов, респираторного сепсиса у взрослых или новорожденных, синдрома системной воспалительной реакции, венозной или артериальной тромбоэмболии, острого повышения уровня ферритина, тяжелого перикардита, острого повышения печеночных трансаминаз, вызывающего печеночную энцефалопатию, или заболевания, связанного с терапией Т-клетками с химерным антигенным рецептором. Например, цитокиновый шторм (который лечат или предотвращают способом по изобретению) вызывается инфекционным заболеванием.
В качестве примера, способ по изобретению полезен для лечения инфекционного заболевания, такого как Covid-19 или лихорадка денге. В другом примере изобретения в указанном способе композицию вводят внутривенно.
Введение фармацевтической композиции, включающей пептид, идентифицированный как SEQ ID NO: 1, пациентам для индукции уменьшения событий, связанных с дыхательной недостаточностью. Это патологическое состояние вызывает у пациентов необходимость в:
• Кислородной терапии для поддержания насыщения кислородом (SO2) выше 93%
• Насыщении кислородом более чем на 3 процентных пункта или снижении парциального давления кислорода в артериальной крови (PaO2) более чем на 10% при стабильной фракции вдыхаемого кислорода (FiO2) за последние 24 часа
• Повышении FiO2 для поддержания стабильного уровня SO2 или другой потребности в искусственной вентиляции легких за последние 24 часа.
• Увеличении количества и/или размеров областей легочной консолидации.
Кроме того, введение композиции по изобретению полезно для лечения пациентов с инфекционным заболеванием Covid-19, когда указанные пациенты нуждаются в кислородной терапии не менее 6 л/мин плюс имеют одно из следующих состояний:
• Хрипы или прерывистая речь
• Частота дыхания более 22 вдохов/мин при кислородотерапии при 6 л/мин
• PaO2: менее 65 мм рт.ст.
• Ухудшение рентгенологической картины
• Повышение температуры до 39°C или выше
• Снижение исходных значений гемоглобина, тромбоцитов и лейкоцитов (гемоглобин ≤9,2 г/дл, лейкоциты ≤5000/мм3, тромбоциты ≤110000/мм
• Снижение оседания эритроцитов в отличие от С-реактивного белка, уровень которого повышен или не изменен.
• Повышение исходного уровня триглицеридов выше 3 ммоль/л
• Увеличение исходного значения ферритина от 500 нг/мл или абсолютное значение ферритина больше или равное 2000 нг/мл
• Уровень трансаминазы аспартатаминотрансферазы больше или равен 30 МЕд/л
• Повышение уровня D-димера
• Фибриноген менее 2,5 г/л
• Неврологические проявления
Композиция по изобретению также полезна для лечения пациентов с Covid-19, которые переходят в тяжелое состояние без необходимости в кислородотерапии, но у которых наблюдается повышение исходного значения ферритина от 500 нг/мл или абсолютное значение ферритина больше или равное 2000 нг/мл, при прогрессирующих рентгенологических признаках мультифокальной интерстициальной пневмонии.
Композиция по изобретению также полезна для лечения заболеваний, характеризующихся состоянием острого гипервоспаления, таких как заболевание, при котором развивается респираторный сепсис у взрослых или новорожденных; и при заболеваниях, при которых развивается респираторный дистресс-синдром, а также при указанном синдроме, вызванном механическими и физическими причинами.
Краткое описание чертежей
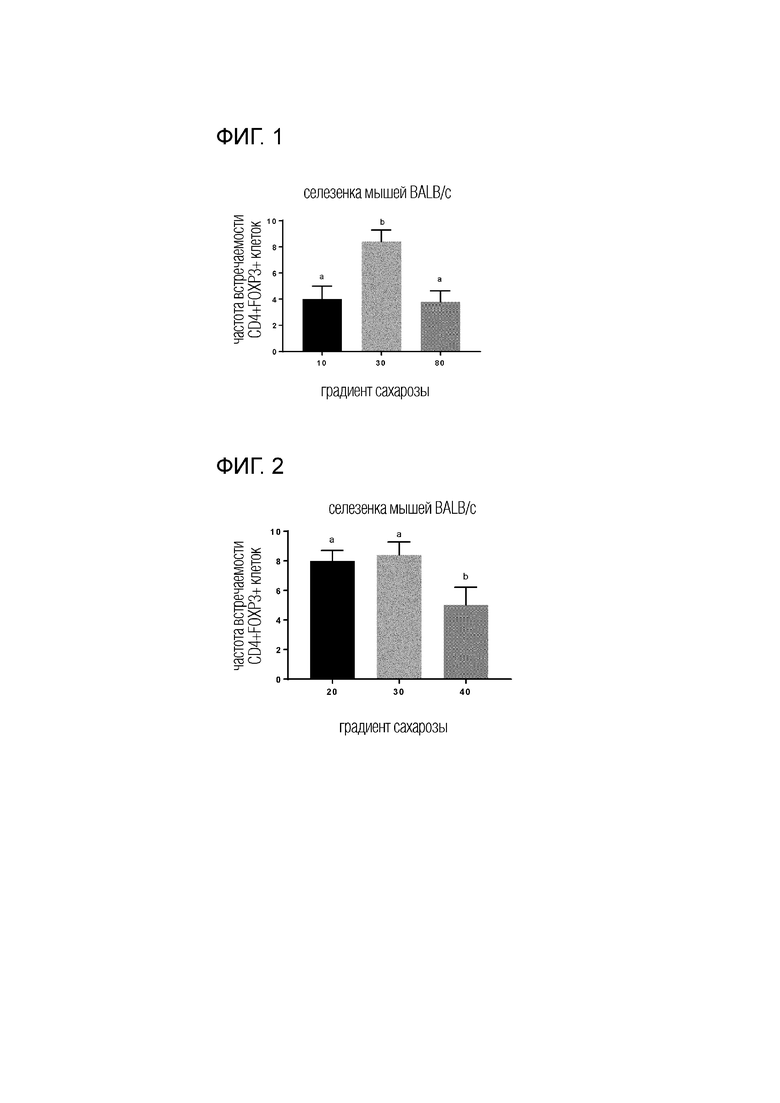
Фиг. 1. Частота Т-клеток, определенная методом проточной цитометрии, которые экспрессируют CD4+ Foxp3+ фенотип, выделенных из селезенки мышей BALB/c после инокуляции фармацевтической композицией пептида, идентифицированного как SEQ ID NO: 1, где сахароза была добавлена в концентрации 10 мг/мл (10), 30 мг/мл (30) и 80 мг/мл (80). Для анализа данных использовали статистические критерии Крускала-Уоллиса и Данна. Разные буквы означают статистически значимые различия (P <0,05).
Фиг. 2. Частота Т-клеток, определенная методом проточной цитометрии, которые экспрессируют CD4+ Foxp3+ фенотип, выделенных из селезенки мышей BALB/c после инокуляции фармацевтической композицией пептида, идентифицированного как SEQ ID NO: 1, где сахароза была добавлена в концентрации 20 мг/мл (20), 30 мг/мл (30) и 40 мг/мл (40). Для анализа данных использовали статистические критерии Крускала-Уоллиса и Данна. Разные буквы означают статистически значимые различия (P <0,05)
Подробное представление примеров/Примеры
Пример 1. Лечение пациентов с заболеванием Covid-19 фармацевтической композицией, включающей пептид, идентифицированный как SEQ ID NO: 1.
Это иллюстрируется на примере десяти пациентов, поступивших в отделение интенсивной терапии военного госпиталя Luis Dias Soto, с инфекционным заболеванием Covid-19. Эти пациенты получали медицинскую помощь в соответствии с протоколом, установленным Министерством здравоохранения Кубы для лечения этого заболевания. У этих пациентов развился острый респираторный дистресс-синдром, и в тот же день им была проведена искусственная вентиляция легких/вентиляция со сбросом давления в дыхательных путях (VAM APRV). После получения информированного согласия, установленного кубинским регулирующим органом и Комитетом по этике и наблюдению указанного госпиталя, пациенты получали фармацевтическую композицию, включающую пептид, идентифицированный как SEQ ID NO: 1. Указанный пептид был получен путем химического синтеза методом, хорошо известным в данной области техники.
Фармацевтическую композицию вводили внутривенно один раз каждые 12 часов. Восьми пациентам вводили 1 мг пептида на пациента при каждом применении. Пациенты с кодом 5 и 6 получали по 2 мг каждые 12 часов. Среди сопутствующих заболеваний у этих пациентов были онкологические заболевания. Демографические характеристики пациентов, а также дни VAM APRV и введения пептида отражены в Таблице 1.
Характеристики пациентов, получавших лечение фармацевтической композицией, включающей пептид, идентифицированный как SEQ ID NO: 1
HTA
ожирение курение
ожирение синдром
Кушинга
множественные узлы в щитовидной железе
опухоль надпочечников
рак мочевого пузыря
рак мочевого пузыря
Как видно из таблицы, у десяти пациентов с заболеванием Covid-19, получавших лечение пептидом, были факторы риска, предрасполагающие к тяжелому или критическому состоянию заболевания. Только у одного пациента не было сопутствующих заболеваний, но его преклонный возраст (80 лет) является фактором риска. В частности, этот пациент идентифицирован как не имеющий сопутствующих заболеваний. У 5 пациентов был тромбоз глубоких вен. Однако клиническое течение у десяти пациентов при введении пептида было благоприятным. К моменту экстубации острый респираторный дистресс-синдром считается устраненным. Эти результаты показывают, что лечение пептидом было эффективным при остром респираторном дистресс-синдроме. Исчезновение этого синдрома у пациентов совпало с их клиническим и рентгенологическим улучшением. У пациента с тромбозом глубоких вен также было благоприятное развитие. У этих пациентов не было никаких симптомов иммуносупрессии. До терапии у них была лимфопения, характерный признак пациентов с Covid-19. В результате лечения пептидом постепенно нормализовались уровни циркулирующих лимфоцитов.
В специальной литературе сообщается, что 85-90% пациентов с острым респираторным дистресс-синдромом не выживают. На Кубе среди пациентов с подтвержденным SAR-COV-2, перешедшим в критическую или тяжелую стадию, уровень летальности составил 68,6% у лиц, не получавших лечение фармацевтической композицией, которая включает пептид, идентифицированный как SEQ ID NO: 1. Напротив, уровень летальности составил 13,0% у критических или тяжелобольных пациентов с подтвержденным SAR-COV-2, которых лечили фармацевтической композицией, включающей пептид, идентифицированный как SEQ ID NO: 1.
Пример 2. Введение фармацевтической композиции, включающей пептид, идентифицированный как SEQ ID NO: 1, для предотвращения развития респираторного дистресс-синдрома.
У тяжелобольных и критически больных пациентов с Covid-19 развивается респираторный дистресс-синдром, который может привести к летальному исходу. К удивлению, введение фармацевтической композиции, включающей пептид, идентифицированный как SEQ ID NO: 1, предотвращало развитие острого респираторного дистресс-синдрома. Пептид вводили на ранней стадии, после появления первых признаков (прогрессирующие рентгенологические показатели мультифокальной интерстициальной пневмонии, повышенный ферритин (в 2 раза выше нормы), пульсоксиметрия: кислородная сатурация ниже 94). Таким образом, введение указанного пептида предотвращало необходимость в искусственной вентиляции легких. Таким образом удалось избежать вероятной эволюции до нозокомиального сепсиса.
Это продемонстрировано на примере 42-летней пациентки с заболеванием Covid-19, госпитализированной в палату интенсивного ухода госпиталя “Pedro Kouri” Института тропической медицины. Эта пациентка получила медицинскую помощь в соответствии с протоколом, установленным Министерством здравоохранения Кубы для лечения этого заболевания, но у нее возникла внезапная одышка с повышением температуры до 39°C и концентрацией ферритина 700 нг/мл. После получения информированного согласия фармацевтическую композицию, включающую пептид, идентифицированный как SEQ ID NO: 1, вводили внутривенно в дозе 1 мг каждые 12 часов. Через 2 часа исчезло состояние одышки и снизилась температура тела. У пациенки не развился острый респираторный дистресс-синдром, а концентрация ферритина снизилась ниже 500 нг/мл через 72 часа.
Кроме того, осуществляли лечение еще трех пациентов в тяжелом состоянии, демографические характеристики которых и сопутствующие заболевания представлены в Таблице 2. Эти пациенты были госпитализированы в отделение интенсивного ухода Центрального военного госпиталя Luis Dias Soto.
Возраст и сопутствующие заболевания тяжелобольных пациентов, получавших лечение фармацевтической композицией, включающей пептид, идентифицированный как SEQ ID NO: 1
Сахарный диабет
Ишемия сердца
Сахарный диабет
Ишемия сердца
У этих пациентов также были первые настораживающие признаки, такие как: устойчивая повышенная температура выше 38°C, одышка, требующая кислородотерапии с использованием маски или назальной вилки, чтобы поддерживать насыщение кислородом выше 93. У них также было учащенное дыхание с частотой более 25 вдохов в минуту, и им требовалась кислородотерапия при помощи маски или назальной вилки, чтобы поддерживать насыщение кислородом выше 93.
Введение фармацевтической композиции, содержащей пептид, идентифицированный как SEQ ID NO: 1, осуществляли внутривенно в дозе 1 мг каждые 24 часа. Через 2 часа после начала лечения исчезла одышка, снизилась температура тела. У пациентов не развился острый респираторный дистресс-синдром. Концентрация ферритина упала ниже 200 нг/мл через 72 часа.
Эти результаты демонстрируют, что лечение пациентов с заболеванием Covid-19 фармацевтической композицией, содержащей пептид, идентифицированный как SEQ ID NO: 1, до того, как у них разовьется острый респираторный дистресс-синдром, позволяет избежать использования искусственной вентиляции легких для этих пациентов.
Пример 3. Снижение уровня С-реактивного белка у пациентов с заболеванием Covid-19, получавших фармацевтическую композицию, включающую пептид, идентифицированный как SEQ ID NO: 1.
С-реактивный белок является одним из наиболее часто используемых маркеров воспалительных процессов; его считают одним из реагентов острой фазы воспаления. Фармацевтическую композицию, включающую пептид, идентифицированный как SEQ ID NO: 1, вводили внутривенно. Восемь из десяти пациентов с Covid-19, лечение которых описано в Примере 1, получали 1 мг пептида каждые 12 часов. Пациенты с кодом 5 и 6, у которых был рак среди сопутствующих заболеваний, получали по 2 мг пептида каждые 12 часов. Неожиданно, лечение пептидом SEQ ID NO: 1 заметно снижало уровни С-реактивного белка у пациентов, получавших лечение. Эти результаты представлены в Таблице 3.
Концентрация С-реактивного белка (мг/мл) у пациентов, получавших лечение пептидом, идентифицированным как SEQ ID NO: 1
Снижение С-реактивного белка при лечении этих пациентов является прямым указанием на то, что пептид SEQ ID NO: 1 уменьшает воспаление, и этот результат согласуется с исчезновением острого респираторного дистресс-синдрома, а также с клиническим и рентгенологическим улучшением состояния пациентов.
Результаты, полученные в этом исследовании, удивительны. В ходе клинического исследования у пациентов с ревматоидным артритом, получавших лечение тем же пептидом, не было обнаружено снижения этого реагента в острой фазе воспаления.
Пример 4. Снижение уровня провоспалительных цитокинов у пациентов с заболеванием Covid-19, получавших лечение фармацевтической композицией, включающей пептид, идентифицированный как SEQ ID NO: 1.
В этом исследовании уровни провоспалительных цитокинов IL-6, IL-17, IL-1, IFNγ и TNFα определяли у пациентов с заболеванием Covid-19, получавших композицию, включающую пептид, идентифицированный как SEQ ID NO: 1. Пациенты были в критическом состоянии. Лечение этих пациентов описано в Примере 1.
Указанные цитокины количественно определяли в сыворотке пациентов, обозначенных номерами 1, 2, 3, 4, 7 и 8, которые указаны в Таблице 1, Пример 1. Для определения цитокинов в образцах сыворотки вирус инактивировали при строгих мерах биобезопасности. Количественную оценку осуществляли непосредственно перед применением первой дозы пептида, а также через 48, 72 и 96 часов после начала лечения пептидом.
Все определения цитокинов осуществляли с использованием специфического для каждого из них ELISA (иммуноферментного анализа) в соответствии с рекомендациями изготовителя (Quantikine® R&D Systems, USA). Вкратце, в лунки добавляли 50 мкл указанного разбавителя для каждого цитокина, а затем 200 мкл стандартного раствора, образца или контроля. Планшет инкубировали в течение 2 ч при комнатной температуре, после чего содержимое каждой лунки удаляли. Затем осуществляли три промывки 1X промывочным раствором, в каждую лунку добавляли по 200 мкл конъюгированного антитела и инкубировали в течение 1 часа при комнатной температуре. Промывку повторяли и в каждую лунку добавляли по 200 мкл раствора субстрата. Планшет инкубировали в течение 20 мин при комнатной температуре и защищенным от света, в каждую лунку добавляли по 50 мкл стоп-раствора и определяли оптическую плотность при 450 нм в считывающем устройстве для микропланшетов (Thermo Scientific Multiskan Go, Finland). Второе считывание осуществляли при 570 нм, и полученные значения вычитали из показания при 450 нм, чтобы скорректировать оптические дефекты на планшете. Определение концентрации каждого цитокина осуществляли в трех повторах. Результаты, полученные для IL-6, представлены в Таблице 4.
Уровни цитокина IL-6 (пг/мл), обнаруженные у пациентов, получавших пептид
Как видно из таблицы, произошло снижение уровня цитокина IL-6, так как пациенты в критическом состоянии получали пептид SEQ ID NO: 1. Это цитокин, уровень которого заметно повышается при воспалительных процессах. Было описано, что у пациентов с болезнью Covid-19, которые переходят в тяжелую стадию, уровень этого цитокина повышен, в отличие от пациентов с легкими симптомами заболевания. Точно так же у этих пациентов было обнаружено снижение IL-17, IL-1, IFNγ и TNFα.
Эти результаты подтверждают, что лечение пептидом уменьшает гипервоспаление и цитокиновый шторм, развивающийся у пациентов с заболеванием Covid-19, переходящим в тяжелую стадию.
Пример 5. Лечение пациента с заболеванием Covid-19, у которого наблюдались высокие концентрации ферритина без дыхательной недостаточности, с использованием фармацевтической композиции, включающей пептид, идентифицированный как SEQ ID NO: 1.
Пациентка 66 лет, страдающая сахарным диабетом 2 типа, экзогенным ожирением, жировой болезнью печени 4 степени в анамнезе. Она была госпитализирована из-за диагноза COVID-19, у нее были симптомы, связанные с пищеварением, такие как диспепсия, тошнота, периодическая диарея, для лечения которых были показаны прокинетики и противорвотные средства. Кроме того, у пациентов наблюдались высокие концентрации ферритина, более 1500 нг/мл, и увеличение скорости оседания эритроцитов при падении гемоглобина.
Из-за этого клинического состояния специалисты назначили лечение фармацевтической композицией, которая включает пептид, идентифицированный как SEQ ID NO: 1, в дозе 1 мг каждые 12 часов. К удивлению, через 96 часов после начала лечения значения ферритина снизились до концентрации 350 нг/мл.
Лечение фармацевтической композицией, включающей пептид, идентифицированный как SEQ ID NO: 1, продолжалось еще 72 часа.
По окончании лечения концентрация ферритина нормализовалась, и у пациентки не было никаких симптомов.
Эти результаты показывают, что лечение фармацевтической композицией, включающей пептид, идентифицированный как SEQ ID NO: 1, способно снижать концентрацию ферритина, когда она повышается из-за вирусной инфекции.
Пример 6. Лечение пациента с перикардитом вирусной этиологии с использованием фармацевтической композиции, включающей пептид, идентифицированный как SEQ ID NO: 1.
Проходящему лечение пациенту было 48 лет, у него подтвердился Covid-19, и он был госпитализирован в военный госпиталь Holguin. Через два дня после госпитализации у пациента наблюдалось повышенная температуры 38°C и два стула с диареей, и был диагностирован перикардит как осложнение миокардита, вирусной этиологии (Covid-19), без гемодинамических нарушений. У пациента не было дыхательной недостаточности. Лечение начинали с фармацевтической композиции, включающей пептид, идентифицированный как SEQ ID NO: 1, в дозе 1 мг каждые 12 часов.
К удивлению, через 24 часа после начала лечения электрокардиограмма показала улучшение, а через 96 часов лечения пациент был бессимптомным со значительным клиническим улучшением. Эти результаты подтвердили, что фармацевтическая композиция, включающая пептид, идентифицированный как SEQ ID NO: 1, уменьшает воспаление, возникающее при таких патологиях, как перикардит на фоне миокардита, без гемодинамических нарушений вирусной этиологии.
Пример 7. Лечение пациента с Covid-19 и печеночной энцефалопатией с использованием фармацевтической композиции, включающей пептид, идентифицированный как SEQ ID NO: 1.
Пациентка 55 лет, европеоидной расы, с патологическим анамнезом артериальной гипертензии. Эта пациентка была госпитализирована в госпиталь Luis Diaz Soto, в изолятор службы внутренних болезней, с положительным результатом на коронавирус, вызывающий заболевание Covid-19. Поэтому она начала лечение от этого заболевания, согласно установленному в стране протоколу. При поступлении она была бессимптомной вплоть до десятого дня. Она сообщила, что в этот день у нее были эпизоды беспокойства или нервозности, связанные с высокими цифрами артериального давления (160/90 мм рт.ст.). Ее осмотрели специалисты в области психиатрии, и были сделаны дополнительные лабораторные анализы. У пациентки не было дыхательной недостаточности. Психиатр поставил диагноз: синдром беспокойства с элементами психопатического синдрома. На 11-е сутки у пациентки ухудшились клинические проявления, появились рвота, высокое артериальное давление, тенденция к тахикардии, без расслабления сфинктера, в связи с чем она была переведена в реанимационное отделение. Гемогазометрия показала наличие выраженной гипонатриемии (концентрация Na 105 ммоль/л). Компьютерная аксиальная томография не показала краниоэнцефалических изменений, а дополнительные тесты показали заметное повышение активности печеночных ферментов, а также лейкоцитоз. На основании этих результатов у пациентки была диагностирована печеночная энцефалопатия. Все гепатотоксические препараты были отменены у пациентки, внесены изменения в диету, продолжено постепенное замещение натрия и начато лечение фармацевтической композицией, которая включает пептид, идентифицированный как SEQ ID NO: 1, при 1 мг каждые 12 часов, внутривенно. Ежедневно осуществлялось клиническое наблюдение с дополнительными лабораторными исследованиями. К удивлению, через 72 часа после начала лечения фармацевтической композицией, которая включает пептид, идентифицированный как SEQ ID NO: 1, динамика была благоприятной, со снижением печеночных ферментов, прогрессивным снижением креатининкиназы и соединений азота в крови, а также нормализацией концентрации натрия. Через 96 часов после начала лечения клинические характеристики, соответствующие печеночной энцефалопатии, были полностью реверсированы, лечение фармацевтической композицией, включающей пептид, продолжалось еще три дня. Эти результаты подтвердили, что введение фармацевтической композиции, включающей пептид, идентифицированный как SEQ ID NO: 1, уменьшает воспаление, возникающее при таких патологиях, как печеночная энцефалопатия.
Пример 8. Лечение пациента с лихорадкой денге с использованием фармацевтической композиции, включающей пептид, идентифицированный как SEQ ID NO: 1.
Пациентка 19 лет, обратившаяся в госпиталь Luis Diaz Soto с жалобами на высокую температуру 38,5°C в течение более 72 часов и сильную голокраниальную головную боль. Кроме того, у пациентки была ретроокулярная боль, связанная с дискретной конъюнктивальной инъекцией. На основании этих симптомов пациентка была госпитализирована с подозрением на лихорадку денге. При медицинском осмотре у этой пациентки выявлены гипертермия 39,9°C, кровяное давление 90/60 мм рт.ст., тахикардия, умеренное похолодание конечностей. При осмотре кожных покровов врач обнаружил петехии в области предплечий и живота с положительной петлевой пробой. Пациентку лечили терапевтически с поддержкой объемом 30 мл/кг массы тела в течение 24 часов.
Через 24 часа после госпитализации у пациентки начались боли в животе и рвота. Дополнительные анализы показали лейкопению (общие количество лейкоцитов 2,9×109), скорость оседания эритроцитов 95 мм/ч, С-реактивный белок 150 мг/мл, лактатдегидрогеназа 918 Ед/л, глутамино-щавелевоуксусная трансаминаза 93 МЕд/л, глутаминово-пировиноградная трансаминаза 58 МЕд/л. УЗИ брюшной полости показало наличие свободной жидкости во всех четырех углах, умеренной интенсивности. Желчный пузырь имел утолщенные стенки и перивезикулярный отек, без литиаза. Были применены поддерживающие терапевтические меры для этой пациенки, которые включали кристаллоидные растворы из расчета 35-45 мл/кг массы тела в течение 24 часов.
Торпидная динамика пациентки и плохой ответ на терапевтические меры, основанные на возмещении жидкости, указали команде медиков на то, что у пациентки развился синдром активации макрофагов вследствие заражения вирусом, вызывающим лихорадку денге. Этот диагноз был подтвержден значениями лабораторных показателей, связанных с данным синдромом, ферритин: 1893 мг/л; фибриноген: 2,31 г/л; С-реактивный белок: 150 мг/мл; оседание эритроцитов: 53 мм/ч.
На основании этих результатов пациентка была переведена в отделение интенсивной терапии, и фармацевтическую композицию, содержащую пептид, идентифицированный как SEQ ID NO: 1, вводили внутривенно при 1 мг каждые 12 часов. Целью введения указанной композиции была модуляция иммунного ответа и, таким образом, контроль цитокинового шторма, который, согласно клиническим характеристикам и лабораторным параметрам, развивался у этой пациентки. Через 48 часов после начала лечения у пациентки наблюдалось заметное улучшение, так как исчезли боли в животе, артериальная гипотензия и похолодание конечностей. Пациентка начала принимать пищу. Через 72 часа продолжилось клинико-рентгенологическое улучшение состояния пациентки, поэтому частоту введения фармацевтической композиции, включающей пептид, уменьшили до 1 мг каждые 24 часа. После седьмого дня лечения пациентка была клинически и рентгенологически бессимптомной.
Инфицирование вирусом денге было подтверждено, так как IgM был положительным в серологическом тесте.
Все лабораторные показатели нормализовались, и пациентка была выписана из госпиталя.
Эти результаты являются подтверждением того, что изложено в предыдущих примерах, этот пример подтверждает, что фармацевтическая композиция, включающая пептид, идентифицированный как SEQ ID NO: 1, контролирует цитокиновый шторм, который может быть связан с гемофагоцитарным синдромом, который может быть связан с различными патологиями, такими как лихорадка денге, которые переходят в тяжелую стадию заболевания.
Пример 9. Эффекты концентрации сахарозы на фармакологическое потенциирование пептида SEQ ID NO: 1 для уменьшения воспаления.
Для того чтобы использовать пептид, идентифицированный как SEQ ID NO: 1, в качестве индуктора молекулярных механизмов, снижающих гипервоспаление у пациентов с COVID-19 и другими патологиями, авторы изобретения исследовали влияние сахара сахарозы на композицию в диапазоне концентраций, чтобы выбрать оптимальную концентрацию этого сахара, связанную с индукцией регуляторных Т-клеток, при внутривенном введении композиции. Для получения композиции использовали 1,8 мг/мл - 3,5 мг/мл пептида, идентифицированного как SEQ ID NO: 1, и его растворяли в натрий-ацетатном буфере, рН 4; к которому добавляли сахарозу в различных концентрациях, как описано ниже.
Самцов мышей линии BALB/c случайным образом разделяли на три группы по 10 мышей в каждой. Мышей, разделенных на группы, инокулировали внутривенно следующим образом:
- Группа 1: фармацевтическая композиция пептида, идентифицированного как SEQ ID NO: 1, где сахароза была добавлена в концентрации 10 мг/мл.
- Группа 2: фармацевтическая композиция пептида, идентифицированного как SEQ ID NO: 1, где сахароза была добавлена в концентрации 30 мг/мл.
- Группа 3: фармацевтическая композиция пептида, идентифицированного как SEQ ID NO: 1, где сахароза была добавлена в концентрации 80 мг/мл.
Через четыре дня мыши получили вторую дозу в идентичных условиях. 10 животных в группе умерщвляли на 8-й день после первой инокуляции. Клетки селезенки мышей предварительно инкубировали с Mab 2.4G2 (eBiosciences, USA) для блокирования неспецифического связывания с FC-рецепторами. Затем клетки метили в PBS, содержащем трехпроцентную телячью сыворотку и насыщающие количества следующих моноклональных антител (eBiosciences, USA): конъюгата APC-Cy7-анти-CD4 (клон RM4-5) и конъюгата APC-анти-CD25 (PC61). Транскрипционный фактор Foxp3 оценивали с использованием анти-Foxp3 mAb, конъюгированного с PE (FJK-16s; eBioscience, USA), следуя рекомендациям изготовителя. В качестве контроля использовали изотипически нерелевантное mAb (крысиное PE-Cy5 IgG2a; eBioscience, USA). Область, соответствующая лимфоцитам, обрамлена в соответствии с характеристиками их распределения на гистограммах проточной цитометрии, полученных на цитометре LSR-II™. Анализы осуществляли с использованием программы FlowJo® (Tree Star).
Как видно на этой Фиг. 1, у мышей, инокулированных композицией, содержащей пептид, идентифицированный как SEQ ID NO: 1, и сахарозу в концентрации 30 мг/мл, значительно увеличился процент регуляторных Т-клеток, что показывает синергетический эффект между этими компонентами композиции.
Чтобы определить, является ли сахароза в этой концентрации решающей для индукции частоты регуляторных Т-клеток, был осуществлен эксперимент в условиях, очень схожих с предыдущим экспериментом, но с сужением диапазона концентраций указанного сахара.
Мышей случайным образом разделяли на три группы по 10 мышей в каждой. Мышей, разделенных на группы, инокулировали внутривенно следующим образом:
- Группа 1: фармацевтическая композиция пептида, идентифицированного как SEQ ID NO: 1, где сахароза была добавлена в концентрации 20 мг/мл.
- Группа 2: фармацевтическая композиция пептида, идентифицированного как SEQ ID NO: 1, где сахароза была добавлена в концентрации 30 мг/мл.
- Группа 3: фармацевтическая композиция пептида, идентифицированного как SEQ ID NO: 1, где сахароза была добавлена в концентрации 40 мг/мл.
К удивлению, мыши, для обработки которых использовали эти концентрации сахарозы в пределах 20-40 мг/мл, показали значительное увеличение процента регуляторных Т-клеток по сравнению с группами, для обработки которых использовали концентрации 10-80 мг/мл в предыдущем эксперименте, при этом наблюдался синергетический эффект между компонентами композиции, демонстрируя больший эффект в группах мышей, обработанных фармацевтической композицией пептида, идентифицированного как SEQ ID NO: 1, где сахарозу добавляли в концентрациях 20 и 30 мг/мл (Фиг. 2).
Эти результаты позволяют сделать вывод о том, что добавление сахарозы в концентрациях в диапазоне 20-30 мг/мл является определяющим фактором для индукции регуляторных Т-клеток, которые контролируют степень воспаления, эта композиция, вводимая внутривенно, обладает способностью контролировать патологии, характеризующиеся гипервоспалением.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> CENTRO DE INGENIERIA GENETICA Y BIOTECNOLOGIA
<120> ПЕПТИД ДЛЯ ЛЕЧЕНИЯ СИДРОМА ЦИТОКИНОВОГО ШТОРМА.
<130> APL ANTIV
<140> CU 2020-0026
<141> 13.04.2020
<160> 1
<170> PatentIn Ver. 2.1
<210> 1
<211> 27
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Пептид
типа APL
<400> 1
Ser Ile Asp Leu Lys Asp Lys Tyr Lys Asn Ile Gly Ala Lys Leu Val
1 5 10 15
Gln Leu Val Ala Asn Asn Thr Asn Glu Glu Ala
20 25
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИИ АНТИТЕЛ К CD6 И СПОСОБЫ ЛЕЧЕНИЯ И СНИЖЕНИЯ НЕГАТИВНЫХ ПОСЛЕДСТВИЙ КОРОНАВИРУСА, ВКЛЮЧАЯ COVID-19 | 2021 |
|
RU2828013C1 |
| Способ клинико-лабораторного прогнозирования цитокинового шторма у пациента с установленным диагнозом "COVID-19" | 2023 |
|
RU2831060C1 |
| ВОДНАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ЛЕВИЛИМАБА И ЕЕ ПРИМЕНЕНИЕ | 2020 |
|
RU2745814C1 |
| ПРИМЕНЕНИЕ ПРОИЗВОДНОГО ГЛУТАРИМИДА ДЛЯ ТЕРАПИИ ЗАБОЛЕВАНИЙ, АССОЦИИРОВАННЫХ С АБЕРРАНТНОЙ АКТИВНОСТЬЮ ИНТЕРЛЕЙКИНА-6 | 2020 |
|
RU2774928C2 |
| Способ лечения больных с новой коронавирусной инфекцией COVID-19 при высокопоточной оксигенации | 2022 |
|
RU2787175C1 |
| ПРИМЕНЕНИЕ 1-[2-(1-МЕТИЛИМИДАЗОЛ-4-ИЛ)-ЭТИЛ]ПЕРГИДРОАЗИН-2,6-ДИОНА ДЛЯ ЛЕЧЕНИЯ COVID-19 | 2021 |
|
RU2823973C2 |
| Способ лечения коронавирусной инфекции | 2021 |
|
RU2751488C1 |
| Пептиды с противовирусной активностью | 2024 |
|
RU2834861C1 |
| Способ прогнозирования исхода острого заболевания, вызванного новой коронавирусной инфекцией COVID-19 | 2021 |
|
RU2766347C1 |
| Ингаляционный гексапептид для лечения респираторных заболеваний, связанных с интерлейкином-6 | 2020 |
|
RU2737799C1 |
Изобретение относится к области биотехнологии, в частности к фармацевтической композиции, включающей пептид типа APL, идентифицированный как SEQ ID NO: 1, в качестве ингибитора состояния гипервоспаления, характеризующегося повышением уровней цитокинов или интерлейкинов и молекул воспаления, которые увеличивают свою концентрацию до достижения состояния, определяемого как "цитокиновый шторм". Концентрации сахарозы в указанной композиции повышают биологическую активность пептида, облегчая его внутривенное применение. Указанный пептид в фармацевтической композиции полезен для получения лекарственного средства для лечения заболеваний, связанных с гипервоспалением, таких как Covid-19, лихорадка денге, синдром активации макрофагов, респираторный сепсис, и с терапиями Т-клетками с химерным антигенным рецептором, а также острым респираторным дистресс-синдромом. 2 н. и 9 з.п. ф-лы, 2 ил., 4 табл., 9 пр.
1. Фармацевтическая композиция для лечения или предупреждения синдрома цитокинового шторма, включающая фармацевтически эффективное количество пептида, идентифицированного как SEQ ID NO: 1, и фармацевтически приемлемый эксципиент, содержащая сахарозу в концентрации от 20 мг/мл до 30 мг/мл.
2. Фармацевтическая композиция по п. 1, где синдром цитокинового шторма проявляется в виде острого респираторного дистресс-синдрома, синдрома активации макрофагов, респираторного сепсиса у взрослых или новорожденных, синдрома системного воспалительного ответа, венозной или артериальной тромбоэмболии, острого повышения уровней ферритина, тяжелого перикардита, острого повышения печеночных трансаминаз, вызывающего печеночную энцефалопатию, или заболевания, связанного с терапиями Т-клетками с химерным антигенным рецептором.
3. Фармацевтическая композиция по п. 1, которую вводят внутривенным путем.
4. Фармацевтическая композиция по п. 1, где синдром цитокинового шторма вызван инфекционным заболеванием.
5. Фармацевтическая композиция по п. 4, где инфекционное заболевание представляет собой Covid-19 или лихорадку денге.
6. Фармацевтическая композиция по п. 5, включающая пептид, идентифицированный как SEQ ID NO: 1, в концентрации от 1,8 мг/мл до 3,6 мг/мл и сахарозу в концентрации от 20 мг/мл до 30 мг/мл.
7. Применение фармацевтической композиции, включающей пептид, идентифицированный как SEQ ID NO: 1, для лечения или предупреждения синдрома цитокинового шторма.
8. Применение по п. 7, где синдром цитокинового шторма проявляется в виде острого респираторного дистресс-синдрома, синдрома активации макрофагов, респираторного сепсиса у взрослых или новорожденных, синдрома системного воспалительного ответа, венозной или артериальной тромбоэмболии, острого повышения уровней ферритина, тяжелого перикардита, острого повышения печеночных трансаминаз, вызывающего печеночную энцефалопатию, или заболевания, связанного с терапиями Т-клетками с химерным антигенным рецептором.
9. Применение по п. 7, где композицию вводят внутривенным путем.
10. Применение по п. 8, где синдром цитокинового шторма вызван инфекционным заболеванием.
11. Применение по п. 10, где инфекционное заболевание представляет собой Covid-19 или лихорадку денге.
| WO 2019069307 A1, 11.04.2019 | |||
| US 2012035106 A1, 09.02.2012 | |||
| КОМБИНИРОВАННЫЙ ЛЕТАТЕЛЬНЫЙ АППАРАТ | 2014 |
|
RU2581110C1 |
| ТЮЛЯНДИНА Е.В | |||
| и др | |||
| Цитокиновый шторм: Особенности патогенеза, роль в развитии вирусной инфекции | |||
| Литературный обзор, Устойчивое развитие науки и образования, 2019, Номер 1, стр | |||
| Ножевой прибор к валичной кардочесальной машине | 1923 |
|
SU256A1 |
| CHOUSTERMAN B.G | |||
| et al | |||
| Cytokine storm and sepsis disease pathogenesis, | |||
Авторы
Даты
2025-02-05—Публикация
2021-04-12—Подача