Область техники
Изобретение относится к химии органических соединений, фармакологии и медицине и касается новых пептидов, характеризующихся противовирусной активностью, которые, в частности, могут использоваться для профилактики и лечения вирусных заболеваний у субъекта.
Уровень техники
Инфекционные заболевания, особенно вызванные вирусами, являются одним из важнейших факторов заболеваемости и смертности людей. Они составляют большую долю смертности и инвалидности во всем мире. Бремя вирусных заболеваний и расстройств иллюстрирует недавняя вспышка коронавирусной инфекции 2019 года (COVID-19). COVID-19 - это инфекционное респираторное заболевание, вызываемое штаммом вируса тяжелого острого респираторного синдрома коронавируса 2 (SARS-CoV-2), распространенными симптомами COVID-19 являются лихорадка, кашель и одышка. Несмотря на интенсивные контрмеры, принятые во всем мире, заболеваемость и смертность остаются высокими, и многие страны сталкиваются с новыми волнами инфекции. Вакцины являются важным инструментом в борьбе с COVID-19, но разработка противовирусных препаратов также является приоритетной задачей, особенно в связи с появлением вариантов, которые могут частично уклоняться от вакцин.
Известные противовирусные препараты оказались не способны в должной мере справиться с новой инфекцией - пандемией COVID-19. Поэтому в клинике остро необходим безопасный и эффективный препарат для профилактики и лечения новой коронавирусной инфекции. Исходя из того, что существующие противовирусные препараты имеют в большей или меньшей степени недостатки, создание противовирусных препаратов с лучшим лечебным эффектом является проблемой, требующей срочного решения в настоящее время. Важное значение имеет создание препаратов прямого противовирусного действия. В этой связи пептиды все чаще разрабатываются для использования в качестве терапевтических средств для лечения многих заболеваний.
Из уровня техники известно применение гексапептида даларгина в производстве лекарственных средств, предназначенных для лечения коронавирусной инфекции COVID-19 (RU2728939).
Из уровня техники также известны новые пептиды, которые могут блокировать связывающее взаимодействие нового коронавируса SARS-CoV-2 у млекопитающих, в частности, путем ингибирования взаимодействия между спайковым белком коронавирусов и рецептором ACE2 (US2024218020, US11667678, EP4333867).
Таким образом, попытки создания новых пептидных молекул с фармакологической активностью представляются целесообразными и актуальными.
Раскрытие изобретения
Задачей настоящего изобретения является разработка и создание новых эффективных противовирусных средств, перспективных для применения в клинической практике для терапии и/или профилактики инфекционных заболеваний, в частности, заболевания, вызванного SARS-CoV-2, например, простой инфекции (такой как лихорадка, кашель и/или боль в горле), пневмонии, острой или тяжелой респираторной инфекции, гипоксической дыхательной недостаточности, острого респираторного дистресс-синдрома, сепсиса или септического шока, в частности, COVID-19.
Техническим результатом изобретения является разработка и получение новых пептидных соединений, обладающих инфекционных действием и являющихся перспективными для применения в терапии противовирусных заболеваний, в частности, заболевания, вызванного SARS-CoV-2, например, простой инфекции (такой как лихорадка, кашель и/или боль в горле), пневмонии, острой или тяжелой респираторной инфекции, гипоксической дыхательной недостаточности, острого респираторного дистресс-синдрома, сепсиса или септического шока, в частности, COVID-19.
Указанный технический результат достигается посредством разработки и создания пептида с противовирусной активностью, имеющего последовательность SEQ ID NO: 1, 2, или 3, или его фармацевтически приемлемой соли. Более конкретно, пептиды по изобретению характеризуются противовирусной активностью в отношении коронавируса. В частных вариантах воплощения изобретения, коронавирус представляет собой SARS-CoV-2.
Настоящее изобретение также включает применение пептида по изобретению в качестве противовирусного средства. Более конкретно, применение пептида по изобретению в качестве противовирусного средства в отношении коронавируса. В частных вариантах воплощения изобретения, коронавирус представляет собой SARS-CoV-2.
Предметом настоящего изобретения также является применение пептида по изобретению для получения фармацевтической композиции с противовирусной активностью для лечения и/или профилактики инфекционного заболевания у субъекта. Более конкретно, фармацевтической композиции с противовирусной активностью в отношении коронавируса. В частных вариантах воплощения изобретения, коронавирус представляет собой SARS-CoV-2.
Предметом настоящего изобретения также является фармацевтическая композиция с противовирусной активностью для лечения и/или профилактики инфекционного заболевания у субъекта, содержащая эффективное количество пептида по изобретению или его фармацевтически приемлемой соли и по меньшей мере одно фармацевтически приемлемое вспомогательное вещество.
Более конкретно, фармацевтической композиции с противовирусной активностью в отношении коронавируса. В частных вариантах воплощения изобретения, коронавирус представляет собой SARS-CoV-2.
В частных вариантах воплощения изобретения заболевание представляет собой заболевание, вызванное SARS-CoV-2, например, простую инфекцию (такую как лихорадка, кашель и/или боль в горле), пневмонию, острую или тяжелую респираторную инфекцию, гипоксическую дыхательную недостаточность, острый респираторный дистресс-синдром, сепсис или септический шок, в частности, COVID-19.
В частных вариантах воплощения изобретения фармацевтически приемлемое вспомогательное вещество представляет собой носитель, наполнитель и/или растворитель.
В частных вариантах воплощения изобретения субъект представляет собой человека.
Настоящее изобретение также включает получение соединений (пептидов) по изобретению.
Настоящее изобретение также включает способ лечения и/или профилактики инфекционного заболевания у субъекта, посредством введения субъекту пептида по изобретению или фармацевтической композиции по изобретению. В частных вариантах воплощения изобретения заболевание представляет собой заболевание, вызванное коронавирусом, в том числе SARS-CoV-2, например, простую инфекцию (такую как лихорадка, кашель и/или боль в горле), пневмонию, острую или тяжелую респираторную инфекцию, гипоксическую дыхательную недостаточность, острый респираторный дистресс-синдром, сепсис или септический шок, в частности, COVID-19.
Настоящее изобретения также включает способ блокирования и/или ингибирования коронавируса, например, вируса SARS-CoV-2, в том числе варианта Delta B.1.617.2 или вариант Omicron BA.4/5, с помощью пептида по изобретению или фармацевтических композиций по изобретению.
Подробное раскрытие изобретения
Краткое описание чертежей
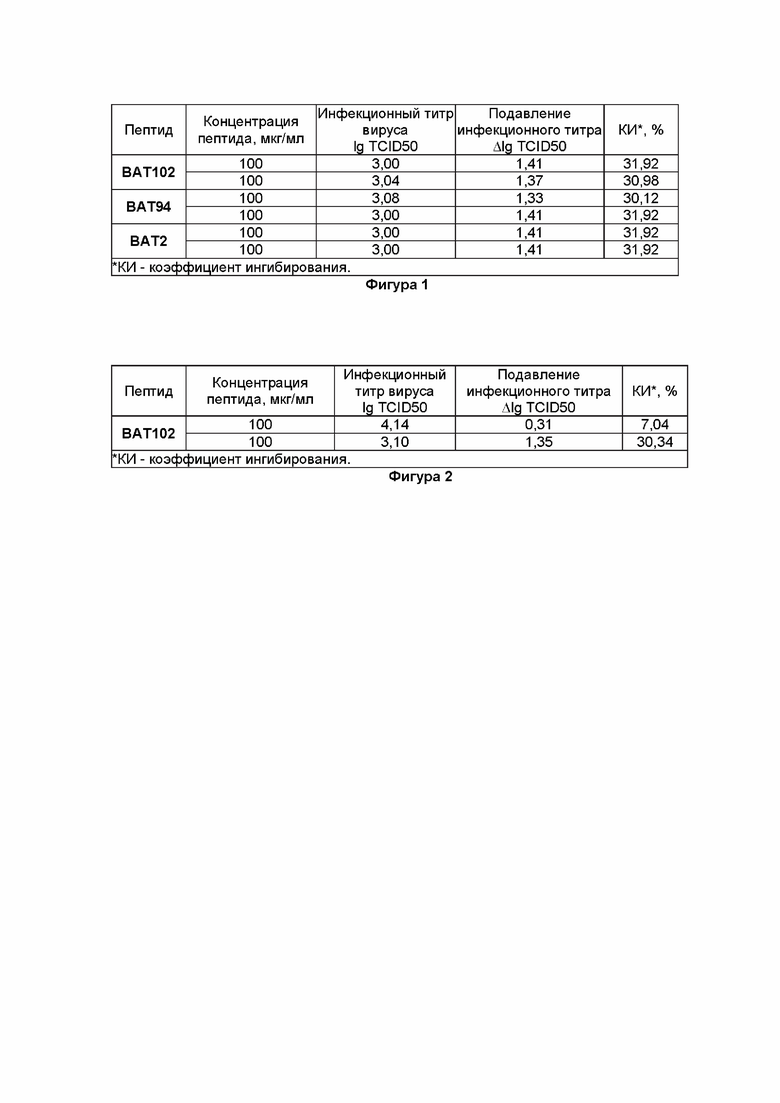
Фигура 1. Снижение инфекционного титра вируса SARS-CoV-2 (штамм СВ-534, вариант Delta B.1.617.2) при действии пептидов по изобретению при лечебной модельной схеме применения.
Фигура 2. Снижение инфекционного титра вируса SARS-CoV-2 (штамм СВ-657, вариант Omicron BA.4/5) при действии пептидов по изобретению при лечебной модельной схеме применения.
Определения и термины
Для лучшего понимания настоящего изобретения ниже приведены некоторые термины, использованные в настоящем описании изобретения. Следующие определения применяются в данном документе, если иное не указано явно.
В описании данного изобретения термины «включает» и «включающий» интерпретируются как означающие «включает, помимо всего прочего». Указанные термины не предназначены для того, чтобы их истолковывали как «состоит только из».
Термин «и/или» означает один, несколько или все перечисленные элементы.
Также здесь перечисление числовых диапазонов по конечным точкам включает все числа, входящие в этот диапазон.
Термин «необязательный» или «необязательно» или «опциональный» или «опционально», используемый в данном документе, означает, что описываемое впоследствии событие или обстоятельство может, но не обязательно, произойти, и что описание включает случаи, когда событие или обстоятельство происходит, и случаи, в которых оно не происходит.
Термин «аминокислота» относится и к природным аминокислотам (включая как L- аминокислоты, так и D- аминокислоты). Аминокислоты обозначают стандартными сокращениями: аргинин (Arg; R), лейцин (Leu; L), лизин (Lys; K), фенилаланин (Phe; F), триптофан (Trp; W), изолейцин (Ile; I), тирозин (Tyr; Y).
Соединения, составляющие суть данного изобретения, могут существовать в меченой радиоизотопом форме, т.е. указанные соединения могут содержать один или несколько атомов, чья атомная масса или массовое число отличается от атомной массы или массового числа наиболее распространенных природных изотопов. Радиоизотопы водорода, углерода, фосфора, хлора включают 3H, 14C, 32P, 35S, и 36Cl, соответственно. Соединения данного изобретения, которые содержат такие радиоизотопы и/или другие радиоизотопы других атомов, находятся в сфере настоящего изобретения. Тритиевые, т.е. 3H и углеродные, т.е. 14С радиоизотопы являются особенно предпочтительными благодаря простоте приготовления и обнаружения.
Соединения настоящего изобретения, меченые радиоактивными изотопами, могут быть получены с помощью методов, хорошо известных специалистам в данной области. Меченые соединения могут быть получены с помощью процедур, описанными здесь, простой заменой немеченых реагентов соответствующими мечеными реагентами.
Соединения настоящего изобретения могут существовать в свободной форме или, если требуется, в виде фармацевтически приемлемой соли или другого производного. Используемый здесь термин «фармацевтически приемлемая соль» относится к таким солям, которые, в рамках проведенного медицинского заключения, пригодны для использования в контакте с тканями человека и животных без излишней токсичности, раздражения, аллергической реакции и т.д., и отвечают разумному соотношению пользы и риска. Фармацевтически приемлемые соли аминов, карбоновых кислот, фосфонатов и другие типы соединений хорошо известны в медицине. Соли могут быть получены in situ в процессе выделения или очистки соединений изобретения, а также могут быть получены отдельно, путем взаимодействия свободной кислоты или свободного основания соединения изобретения с подходящим основанием или кислотой, соответственно. Примером фармацевтически приемлемых, нетоксичных солей кислот могут служить соли аминогруппы, образованные неорганическими кислотами, такими как соляная, бромоводородная, фосфорная, серная и хлорная кислоты, или органическими кислотами, такими как уксусная, щавелевая, малеиновая, винная, янтарная или малоновая кислоты, или полученные другими методами, используемыми в данной области, например, с помощью ионного обмена. К другим фармацевтически приемлемым солям относятся адипинат, альгинат, аскорбат, аспартат, бензолсульфонат, бензоат, бисульфат, борат, бутират, камфорат, камфорсульфонат, цитрат, циклопентанпропионат, диглюконат, додецилсульфат, этансульфонат, формиат, фумарат, глюкогептонат, глицерофосфат, глюконат, гемисульфат, гептанат, гексанат, гидройодид, 2-гидрокси-этансульфонат, лактобионат, лактат, лаурат, лаурил сульфат, малат, малеат, малонат, метансульфонат, 2-нафталинсульфонат, никотинат, нитрат, олеат, оксалат, пальмитат, памоат, пектинат, персульфат, 3-фенилпропионат, фосфат, пикрат, пивалат, пропионат, стеарат, сукцинат, сульфат, тартрат, тиоцианат, п-толуолсульфонат, ундеканат, валериат и подобные. Типичные соли щелочных и щелочноземельных металлов содержат натрий, литий, калий, кальций, магний и другие. Кроме того, фармацевтически приемлемые соли могут содержать, если требуется, нетоксичные катионы аммония, четвертичного аммония и амина, полученные с использованием таких противоионов, как галогениды, гидроксиды, карбоксилаты, сульфаты, фосфаты, нитраты, низшие алкилсульфонаты и арилсульфонаты.
Под «терапевтически эффективным количеством» подразумевается такое количество соединения, вводимого или доставляемого пациенту, при котором у пациента с наибольшей вероятностью проявится желаемая реакция на лечение инфекционных заболеваний, вызванных вирусной инфекцией, в частности, коронавирусом. Точное требуемое количество может меняться от субъекта к субъекту в зависимости от возраста, массы тела и общего состояния пациента, тяжести заболевания, методики введения препарата, комбинированного лечения с другими препаратами и т.п.
Под «профилактически эффективным количеством» подразумевается такое количество соединения, вводимого или доставляемого пациенту, при котором у пациента с наибольшей вероятностью проявится желаемая реакция на профилактику инфекционных заболеваний, вызванных вирусной инфекцией, в частности, коронавирусом. Точное требуемое количество может меняться от субъекта к субъекту в зависимости от возраста, массы тела и общего состояния пациента, методики введения препарата, комбинированной профилактики с другими препаратами и т.п. Для профилактического лечения терапевтически или профилактически эффективное количество представляет собой то количество, которое будет эффективно в предотвращении вирусной инфекции, в частности, вызванной SARS-CoV-2.
Термин «пациент» («субъект») охватывает все виды млекопитающих, предпочтительно человека, которые используют соединения в рамках данного изобретения как путем самостоятельного введения, так и/или введения пациенту другим лицом для лечения и/или профилактики заболевания или медицинского состояния.
Термины «лечение», «терапия» охватывают лечение патологических состояний у млекопитающих, предпочтительно у человека, и включают: а) блокирование (приостановку) течения заболевания, б) облегчение тяжести заболевания, т.е. индукцию регрессии заболевания.
Термин «профилактика», «предотвращение», «превентивная терапия» охватывает устранение факторов риска, а также профилактическое лечение субклинических стадий заболевания у человека, направленное на уменьшение вероятности возникновения клинических стадий заболевания. Пациенты для профилактической терапии отбираются на основе факторов, которые, на основании известных данных, влекут увеличение риска возникновения клинических стадий заболевания по сравнению с общим населением. К профилактической терапии относится а) первичная профилактика и б) вторичная профилактика. Первичная профилактика определяется как профилактическое лечение у пациентов, клиническая стадия заболевания у которых ещё не наступила. Вторичная профилактика - это предотвращение повторного наступления того же или близкого клинического состояния заболевания.
Термин «уменьшение риска» охватывает терапию, которая снижает частоту возникновения клинической стадии заболевания. Примерами уменьшения риска заболевания является первичная и вторичная профилактика заболевания.
Термин «противовирусное средство», как используется в настоящем документе, относится к соединению или комбинации соединений, способным к: (i) ингибированию, уменьшению или предотвращению проникновения вируса в клетку; (ii) ингибированию или уменьшению способности вируса вызывать инфекцию у субъекта; или (iii) ингибированию или уменьшению способности вируса размножаться или оставаться инфекционными в окружающей среде. Термин «противовирусное средство» также относится к соединениям, способным к уменьшению инфекционности или вирулентности вируса.
Специалисту в данной области техники будет понятно, что пептид, описанный в настоящем документе, может существовать и часто используется в виде своих фармацевтически приемлемых производных, таких как соли, пролекарства, метаболиты, сложные эфиры, простые эфиры, гидраты, полиморфы, сольваты, комплексы, энантиомеры или другие фармацевтически приемлемые производные. Поэтому предполагается, что ссылка на пептид, рассмотренный в настоящем документе, включает такие фармацевтически приемлемые соли, пролекарства, метаболиты, сложные эфиры, простые эфиры, гидраты, полиморфы, сольваты, комплексы, энантиомеры или любые другие их фармацевтически приемлемые производные.
Фармацевтические композиции
Изобретение также относится к фармацевтическим композициям, которые содержат пептид по изобретению (или про-лекарственную форму, фармацевтически приемлемую соль или другое фармацевтически приемлемое производное) и один или несколько фармацевтически приемлемых носителей, адъювантов, растворителей и/или наполнителей, таких, которые могут быть введены в организм пациента вместе с соединением, составляющим сущность этого изобретения, и которые не разрушают фармакологическую активность этого соединения, и нетоксичны при введении в дозах, достаточных для доставки терапевтического количества соединения.
Фармацевтические композиции, указанные в этом изобретении, содержат пептиды настоящего изобретения вместе с фармацевтически приемлемыми носителями, которые могут включать любые растворители (в частности, вода), разбавители, дисперсии или суспензии, поверхностно-активные вещества, изотонические агенты, загустители и эмульгаторы, консерванты, вяжущие вещества, смазки и т.д., подходящие для конкретной формы дозирования. Материалы, которые могут служить фармацевтическими приемлемыми носителями, включают, но не ограничены, моно - и олигосахариды, а также их производные; желатин; тальк; вспомогательные вещества, такие как масло какао и воск для суппозиториев; масла, такие как арахисовое, хлопковое, кунжутное, оливковое, кукурузное и соевое масло и другие; гликоли, такие как пропиленгликоль; сложные эфиры, такие как этилолеат и этиллаурат; агар; буферные вещества, такие как гидроксид магния и гидроксид алюминия; альгиновая кислота; депирогенизированная вода; изотонический раствор, раствор Рингера; спиртовые и фосфатные буферные растворы. Также в составе композиции могут быть другие нетоксичные совместимые смазочные вещества, такие как лаурилсульфат натрия и стеарат магния, а также красители, разделительные жидкости, пленочные агенты, подсластители, вкусовые добавки и ароматизаторы, консерванты и антиоксиданты.
Предметом настоящего изобретения являются также лекарственные формы - класс фармацевтических композиций, структура которых оптимизирована для определенного способа введения в организм в терапевтической эффективной дозе, например, для введения в организм внутривенно, перорально, внутримышечно, подкожно, ингаляционно, интраназально и сублингвально в рекомендуемых дозировках.
Лекарственные формы этого изобретения могут содержать структуры, полученные методами использования липосом, методами микрокапсулирования, способами получения наноформ лекарственного средства или другими способами, известными в фармацевтике.
Для введения парентеральным способом используются водные суспензии, изотонические физиологические растворы или стерильные растворы для инъекций, совместимые агенты которых содержат фармакологические, например, пропиленгликоль или бутиленгликоль.
В частных вариантах воплощения изобретения, композиции по изобретению могут включать пептид настоящего изобретения, конъюгированный с полиэтиленгликолем, а именно конъюгация N-конца пептида с полиэтиленгликолем (далее - ПЭГ) [ACS Appl. Mater. Interfaces 2020, 12, 41, 46991-47001; https://doi.org/10.1021/acsami.0c13492]. Существуют различные вариации ПЭГ - в зависимости от его молекулярной массы.
Данный подход позволяет снизить иммуногенность, увеличить растворимость и период полувыведения белковых препаратов [Pasut G. Pegylation of biological molecules and potential benefits: pharmacological properties of certolizumab pegol. BioDrugs. 2014;28 Suppl 1:S15-S23. Doi:10.1007/s40259-013-0064-z]. ПЭГ обладает высокой растворимостью в воде и многих органических растворителях, нетоксичен и неиммуногенен. ПЭГилирование биологически активных соединений позволяет повысить метаболическую стабильность за счет создания стерических затруднений, которые защищают молекулу от протеаз, и, таким образом, увеличить время циркуляции в условиях in vivo.
Методы терапевтического применения
Соединения настоящего изобретения является противовирусными агентами, и поэтому они являются полезными агентами для лечения и/или профилактики вирусной инфекции субъекта, в том числе инфекции, вызванной SARS-CoV-2.
В еще одном аспекте изобретение также относится к способам лечения или профилактики вирусной инфекции субъекта, включающим введение субъекту эффективного количества пептида по изобретению. Субъекты, подлежащие лечению, включают собак, кошек, лошадей, крупный рогатый скот, овец, свиней, домашнюю птицу, приматов (например, макак-резус и яванских макак, обезьян, мартышек, тамаринов, шимпанзе, макак), кроликов и грызунов (крыс, мышей, морских свинок и тому подобных). В одном варианте воплощения изобретения субъект представляет собой человека, и противовирусный пептид, согласно изобретению, может быть доставлен местно, интраназально и др. Противовирусный пептид может быть доставлен в форме капель, спрея, крема, геля, мази и тому подобных форм.
Соединение или композиции, описанные в настоящем документе, также могут быть использованы в целях профилактики. Соответственно, соединение или композиция могут быть введены субъекту, потенциально подверженному риску развития вирусной инфекции. Субъекты, подверженные риску развития вирусной инфекции, включают индивидуумов, подвергнутых воздействию определенного микроорганизма, принадлежащего к патогенным видам бактерий; индивидуумов с хроническими заболеваниями, в том числе с нарушениями иммунной системы, или индивидуумов старше 45 лет.
Описанные в данном изобретении противовирусные пептиды могут быть использованы для лечения или профилактики инфекционных заболеваний, вызванных SARS-CoV-2, например, простой инфекции (такой как лихорадка, кашель и/или боль в горле), пневмонии, острой или тяжелой респираторной инфекции, гипоксической дыхательной недостаточности, острого респираторного дистресс-синдрома, сепсиса или септического шока, в частности, COVID-19.
Для терапевтического применения соединения изобретения могут вводиться с помощью фармацевтической композиции в любой фармацевтической лекарственной форме любым способом введения. Лекарственные формы обычно включают фармацевтически приемлемый носитель, подходящий для выбранной конкретной лекарственной формы. В частности, соединение по изобретению может вводиться ежедневно в течение периода времени, необходимого для лечения и/или профилактики заболеваний, имеющих отношение к пациенту, включая курс терапии, длящийся дни, месяцы, годы Способы введения включают, но не ограничиваются внутривенно, внутримышечно, перорально, подкожно, ингаляционно, интраназально и сублингвально. Предпочтительным способом введения является внутривенный.
Изобретение также относится к фармацевтической композиции, содержащей ежедневную дозу указанного соединения в форме фиксированной единицы дозировки, и к комбинации, содержащей указанную фармацевтическую композицию или указанное соединение. В предпочтительном варианте осуществления указанную композицию для применения в соответствии с изобретением вводят один раз в день в дозировке 1 мг или более выбранного соединения по изобретению. Предпочтительная дозировка составляет 1-500 мг. Наиболее предпочтительная дозировка составляет 10-200 мг.
Один или несколько дополнительных фармакологически активных агентов могут вводиться в комбинации с пептидом по изобретению. Как правило, любые дополнительные одиночные или множественные активные агенты, отличные от соединений по изобретению, включая, но не ограничиваясь, другими противовирусными лекарственными средствами, могут использоваться в любой комбинации с соединением по изобретению в одной или отдельной лекарственной форме, позволяющей одновременное или последовательное терапевтическое действие активных агентов.
Осуществление изобретения
Несмотря на то, что изобретение описано со ссылкой на раскрываемые варианты воплощения, для специалистов в данной области должно быть очевидно, что конкретные подробно описанные эксперименты приведены лишь в целях иллюстрирования настоящего изобретения, и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения. Должно быть понятно, что возможно осуществление различных модификаций без отступления от сути настоящего изобретения.
Получение пептида по изобретению
Общие методики получения пептида по изобретению
Специалист в данной области техники может легко синтезировать пептид согласно изобретению. Стандартные способы получения синтетических пептидов хорошо известны в данной области техники. Пептид изобретения может быть синтезированы с помощью таких обычно используемых способов как t-BOC или FMOC защита альфа-аминогрупп. Оба способа включают ступенчатый синтез, при этом одна аминокислота добавляется на каждой стадии, начиная от карбоксильного конца пептида. Пептид изобретения также может быть синтезированы методами твердофазного синтеза пептидов, хорошо известными в данной области техники.
Помимо этого, пептид по изобретению может быть получены не только путем химического синтеза, но также с помощью применения биотехнологических методов: могут быть синтезированы нуклеотидные последовательности, кодирующие последовательность аминокислот заявленного пептида - данные нуклеотидные последовательности могут быть внедрены в клетки (с помощью векторов или нативных нуклеиновых кислот), и трансформированные таким образом клетки могут быть использованы для экспрессии заявленных пептидов. Указанные векторы и нуклеотидные последовательности могут быть введены в организм человека (и других живых организмов) для экспрессии заявленных пептидов непосредственно in vivo. Указанные методы также хорошо известны специалистам в данной области техники.
Синтез пептидов по изобретению
Пептиды по изобретению синтезированы методом твердофазного Fmoc-синтеза с помощью автоматического синтезатора JBMS-96-A (Jianbang Pharmacy Technology Co.,Ltd.). Пептиды были очищены (чистота >93%) с помощью высокоэффективной жидкостной хроматографии с обращенной фазой (табл.2).
Структуры пептидов по изобретению раскрыты в таблице 1 ниже.
Таблица 1. Примеры пептидов по изобретению.
ВЭЖХ пептидов по изобретению проводили на колонке Phenomenex Luna® 5 μm C18(2) (4.6*250mm*5 μm), элюируя 0,1% трифторуксусной кислоты в 100% воде (растворитель A) и 0,1% трифторуксусной кислоты в 100% ацетонитриле (растворитель B), при скорости потока 1 мл/мин.
Таблица 2. Данные ВЭЖХ и масс-спектроскопии для пептидов по изобретению.
обозначение
(по ВЭЖХ)
Заявленные пептиды могут быть включены в состав других крупных молекул (белков, пептидов, нуклеиновых кислот, углеводов, липидов, конъюгатов) без изменения их фармакологической активности или с целью придания им новых свойств. Кроме того, производные заявленных пептидов могут быть получены путем химической модификации концевых участков аминокислот.
Характеристика биологической активности
Изучение противовирусной активности пептидов на экспериментальной модели in vitro
Исследование противовирусного действия пептидов по изобретению проводили с использованием перевиваемой культуры клеток Vero 102 и двух штаммов вируса SARS-CoV-2 СВ-534 (вариант Delta B.1.617.2) и СВ-657 (вариант Omicron BA.4/5).
Клетки Vero 102 высевали в 96-луночные планшеты с посадочной концентрацией 1,2х104 в лунку. Трехсуточный монослой клеток заражали вируссодержащей жидкостью, расчетная доза вируса (MOI) составляла 0,01 TCID50/на 1 клетку (использовали штаммы вируса SARS-CoV-2 СВ-534 и СВ-657). Через два часа после заражения клеточных культур вируссодержащей жидкостью (лечебная модельная схема) в лунки планшета вносили растворы пептидов по изобретению, конечная концентрация пептидов в лунках планшета составляла 10 мкг/мл и 100 мкг/мл (каждое разведение пептидов тестировали в двух повторах). Жизнеспособность вируса проверяли при инфицировании контрольных лунок планшета (K+) (инфицировали 2 лунки планшета для каждого штамма вируса), цитопатическое действие пептидов (в концентрации 10 мкг/мл и 100 мкг/мл) оценивали при внесении препаратов в контрольные лунки (K0) (2 лунки планшета для каждого разведения пептидов), жизнеспособность монослоя клеток Vero 102 оценивали в контрольных лунках (K-).
В контрольные лунки (K+) вносили только вируссодержащую жидкость (MOI=0,01 TCID50/на 1 клетку). В контрольные лунки (K0) вносили только растворы пептидов (в концентрации 100 мкг/мл). В контрольные лунки (K-) вносили среду поддержки (до эквивалентного объема).
После внесения препаратов и постановки контролей клетки культивировали в течение 4 суток при 37°C в атмосфере CO2. На 4 сутки отмечали появление цитопатического действия (ЦПД)) в контрольных лунках (К+). На 4 сутки (после регистрации цитопатического действия) из лунок планшета отбирали аликвоты и замораживали при -70°С для последующего определения концентрации живых вирусных частиц и РНК вируса.
Концентрацию жизнеспособных вирусных частиц определяли методом титрования по ТЦД/50 на перевиваемой культуре клеток Vero 102, расчет концентрации вируса проводили по методу Спирмена-Кербера. Концентрацию РНК вируса SARS-CoV-2 определяли методом ПЦР в режиме реального времени. Для выделения РНК вируса применяли коммерческий набор реагентов «РибоПреп» (ФБУН ЦНИИЭ Роспотребнадзора, Россия) в соответствии с инструкцией производителя. Постановку амплификации с гибридизационно-флуоресцентной детекцией в режиме «реального времени» осуществляли с помощью тест-системы «АмплиСенс® SARS-CoV-2-IT» (ФБУН ЦНИИЭ Роспотребнадзора, Россия), в соответствии с инструкцией производителя на амплификаторе планшетного типа CFX96 (производство «Bio-Rad» США). Для определения количества РНК вируса SARS-CoV-2 использовали стандартные образцы с известной концентрацией РНК вируса (в геном-эквивалентах в 1 мл пробы супернатанта (геном-эквивалент/мл)).
Проводили сравнительный анализ падения инфекционного титра вирусов под действием пептидов по сравнению с контролем (K+). Падение инфекционного титра выражали в единицах (ΔlgTCID50). Также определяли коэффициент ингибирования цитопатического действия вируса (КИ) в процентах по стандартной формуле КИ = [(Ак - Ао) / Ак] х 100, где Ак - уровень накопления вируса при культивировании без внесения в питательную среду изучаемого средства (lg TCID50/мл) и Ао - уровень накопления вируса при культивировании с внесением в питательную среду и изучаемого средства (lg TCID50/мл).
Полученные результаты исследования представлены на фигурах 1-2.
Пептиды по изобретению (в том числе BAT102, BAT94, BAT2) в концентрации 100 мкг/мл обладали противовирусным действием в отношении штамма вируса SARS-CoV-2 СВ-534, вариант Delta B.1.617.2, приводили к снижению титра жизнеспособных вирусных частиц на 1,33-1,41 lg и снижению концентрации РНК вируса, коэффициент ингибирования составил 30,12-31,92 %.
Пептиды по изобретению (в том числе BAT102) в концентрации 100 мкг/мл обладали противовирусным действием в отношении штамма вируса SARS-CoV-2 СВ-657, вариант Omicron BA.4/5, приводили к снижению титра жизнеспособных вирусных частиц на 1,35 lg и снижению концентрации РНК вируса, коэффициент ингибирования составил 30,34 %.
Несмотря на то, что изобретение описано со ссылкой на раскрываемые варианты воплощения, для специалистов в данной области должно быть очевидно, что конкретные подробно описанные эксперименты приведены лишь в целях иллюстрирования настоящего изобретения, и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения. Должно быть понятно, что возможно осуществление различных модификаций без отступления от сути настоящего изобретения.
--->
<?xml version="1.0" encoding="UTF-8"?>
<!DOCTYPE ST26SequenceListing PUBLIC "-//WIPO//DTD Sequence Listing
1.3//EN" "ST26SequenceListing_V1_3.dtd">
<ST26SequenceListing dtdVersion="V1_3" fileName="4116365.xml"
softwareName="WIPO Sequence" softwareVersion="2.3.0"
productionDate="2024-07-16">
<ApplicationIdentification>
<IPOfficeCode>RU</IPOfficeCode>
<ApplicationNumberText></ApplicationNumberText>
<FilingDate></FilingDate>
</ApplicationIdentification>
<ApplicantFileReference>4116365</ApplicantFileReference>
<ApplicantName languageCode="ru">Общество с ограниченной
ответственностью «Альбоген»</ApplicantName>
<ApplicantNameLatin>Obshchestvo s ogranichennoj otvetstvennostyu
"AlboGene"</ApplicantNameLatin>
<InventionTitle languageCode="ru">Пептиды с противовирусной
активностью</InventionTitle>
<SequenceTotalQuantity>3</SequenceTotalQuantity>
<SequenceData sequenceIDNumber="1">
<INSDSeq>
<INSDSeq_length>8</INSDSeq_length>
<INSDSeq_moltype>AA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..8</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>protein</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q2">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>KLRKLIFR</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="2">
<INSDSeq>
<INSDSeq_length>9</INSDSeq_length>
<INSDSeq_moltype>AA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..9</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>protein</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q4">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>RYFLKRLLR</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="3">
<INSDSeq>
<INSDSeq_length>9</INSDSeq_length>
<INSDSeq_moltype>AA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..9</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>protein</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q6">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>RKWLLRLFK</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
</ST26SequenceListing>
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Противо-SARS-CoV-2 вирусное средство Антипровир | 2020 |
|
RU2738885C1 |
| ТЕРАПЕВТИЧЕСКИЙ АГЕНТ ПРОТИВ КОРОНАВИРУСА, ВКЛЮЧАЮЩИЙ ЭКСТРАКТ ELAEOCARPUS SYLVESTRIS | 2021 |
|
RU2780346C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ВИРУСНЫХ ЗАБОЛЕВАНИЙ | 2021 |
|
RU2780252C1 |
| Способ лечения коронавирусной инфекции, вызванной SARS-CoV-2 | 2021 |
|
RU2775966C1 |
| ПРИМЕНЕНИЕ ДАЛАРГИНА ДЛЯ ПРОИЗВОДСТВА СРЕДСТВ ЛЕЧЕНИЯ КОРОНАВИРУСНОЙ ИНФЕКЦИИ COVID-19 | 2020 |
|
RU2728939C1 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ ОСТРОГО РЕСПИРАТОРНОГО СИНДРОМА (SARS) | 2004 |
|
RU2411042C2 |
| ЛЕЧЕНИЕ КОРОНАВИРУСНОЙ ИНФЕКЦИИ | 2021 |
|
RU2837859C1 |
| ПРИМЕНЕНИЕ 2,4,5-ТРИЗАМЕЩЕННЫХ 1,2,4-ТРИАЗОЛОНОВ В ПРОТИВОВИРУСНОЙ ТЕРАПИИ | 2021 |
|
RU2820287C1 |
| СПОСОБЫ ЛЕЧЕНИЯ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ, ВЫЗВАННЫХ КОРОНАВИРУСОМ | 2021 |
|
RU2772701C1 |
| СПОСОБ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ КОРОНАВИРУСНОЙ И ДРУГИХ ОСТРЫХ РЕСПИРАТОРНЫХ ВИРУСНЫХ ИНФЕКЦИЙ | 2022 |
|
RU2794315C1 |
Изобретение относится к химии органических соединений, фармакологии и медицине и касается новых противовирусных пептидов. Заявленные пептиды характеризуются высокой противовирусной активностью и являются перспективными для применения в терапии инфекционных заболеваний у субъекта, вызванных вирусной инфекцией, в том числе заболеваний, вызванных SARS-CoV-2, например, простой инфекции (такой как лихорадка, кашель и/или боль в горле), пневмонии, острой или тяжелой респираторной инфекции, гипоксической дыхательной недостаточности, острого респираторного дистресс-синдрома, сепсиса или септического шока, в частности COVID-19. 3 н. и 6 з.п. ф-лы, 2 ил., 2 табл.
1. Пептид с противовирусной активностью или его фармацевтически приемлемая соль, имеющий последовательность, выбранную из последовательности SEQ ID NO: 1, 2, 3.
2. Применение пептида по п. 1 в качестве противовирусного средства.
3. Фармацевтическая композиция с противовирусной активностью для лечения и/или профилактики инфекционного заболевания у субъекта, вызванного вирусной инфекцией, содержащая эффективное количество пептида по п. 1 или его фармацевтически приемлемой соли и по меньшей мере одно фармацевтически приемлемое вспомогательное вещество.
4. Фармацевтическая композиция по п. 3, характеризующаяся тем, что фармацевтически приемлемое вспомогательное вещество представляет собой носитель, наполнитель и/или растворитель.
5. Фармацевтическая композиция по п. 3, характеризующаяся тем, что заболевание вызвано коронавирусом.
6. Фармацевтическая композиция по п. 5, характеризующаяся тем, что коронавирус представляет собой SARS-CoV-2.
7. Фармацевтическая композиция по п. 5, характеризующаяся тем, что заболевание представляет собой COVID-19.
8. Фармацевтическая композиция по п. 5, характеризующаяся тем, что заболевание представляет собой простую инфекцию, такую как лихорадка, кашель и/или боль в горле, пневмонию, острую или тяжелую респираторную инфекцию, гипоксическую дыхательную недостаточность, острый респираторный дистресс-синдром, сепсис или септический шок.
9. Фармацевтическая композиция по п. 3, характеризующаяся тем, что субъект представляет собой человека.
| US 20240218020 A1, 04.07.2024 | |||
| US 11667678 B2, 06.06.2023 | |||
| US 20230220010 A1, 13.07.2023 | |||
| WO 2022135622 A2, 30.06.2022 | |||
| CN 102295683 B, 31.12.2014 | |||
| АНТИБАКТЕРИАЛЬНЫЕ ПЕПТИДЫ | 2007 |
|
RU2468033C2 |
| WO 2021191851 A1, 30.09.2021. | |||
Авторы
Даты
2025-02-14—Публикация
2024-07-18—Подача