Приоритетная информация
Настоящая заявка испрашивает приоритет и преимущества заявки на патент № 202111485380.9, поданной в Национальное управление интеллектуальной собственности Китая 7 декабря 2021 г., содержание которой полностью включено в данный документ посредством ссылки.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к области антител и, в частности, к антителу, способному связываться с B7H6 или его антигенсвязывающим фрагментом, и его применению.
УРОВЕНЬ ТЕХНИКИ
NK-клетка является очень важным врожденным лимфоцитом в организме, который играет важную роль в антивирусной и противоопухолевой защите. NK-клетки экспрессируют на своей поверхности различные активирующие рецепторы, включая NKp30, NKG2D и т.д., а также распознают и связываются с лигандами, экспрессируемыми на поверхности опухолевой клетки. Эти лиганды кодируются собственными генами и экспрессируются на поверхности клеток в таких условиях, как злокачественная трансформация (опухоль) клеток.
NKp30 является важным рецептором, активирующим NK-клетки, который передает сигнал активации, способствующий уничтожению NK-клеткой опухоли после связывания с ее лигандом. B7H6 является единственным известным лигандом NKp30, экспрессируемым в виде мембранного белка. B7H6 высоко экспрессируется в различных опухолевых тканях, таких как меланома и рак печени, но не экспрессируется в нормальных тканях, и имеет опухолевую специфичность.
TGF-β и другие цитокины в микроокружении опухоли подавляют экспрессию NKp30 на поверхности NK-клетки, что приводит к неспособности NK-клеток применять взаимодействие NKp30-B7H6 для точного распознавания и уничтожения опухолей, что приводит к ускользанию опухоли от иммунного ответа. Следовательно, необходимо предоставить препарат на основе терапевтических антител, нацеленных на B7H6.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Цель настоящего изобретения состоит в том, чтобы преодолеть недостатки предшествующего уровня техники и представить антитело B7H6, способное связываться с B7H6 человека и макака и способствовать связыванию B7H6 с NKp30, а также его применение.
Антитело, представленное в настоящем изобретении, может стимулировать противораковую функцию NK-клеток, способствуя связыванию B7H6 с NKp30.
В одном аспекте настоящее изобретение представляет антитело или его антигенсвязывающий фрагмент, способный связывать B7H6, причем антитело или его антигенсвязывающий фрагмент включают CDR1 тяжелой цепи, CDR2 тяжелой цепи, CDR3 тяжелой цепи, CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи, при этом CDR1 тяжелой цепи включает по меньшей мере одну аминокислотную последовательность, выбранную из группы, состоящей из аминокислотной последовательности, как указано в SEQ ID NO: 1 и SEQ ID NO: 7, и аминокислотной последовательности в ее консервативной модифицированной форме;
CDR2 тяжелой цепи включает по меньшей мере одну аминокислотную последовательность, выбранную из группы, состоящей из аминокислотной последовательности, как указано в SEQ ID NO: 2 и SEQ ID NO: 8, и аминокислотной последовательности в ее консервативной модифицированной форме;
CDR3 тяжелой цепи включает по меньшей мере одну аминокислотную последовательность, выбранную из группы, состоящей из аминокислотной последовательности, как указано в SEQ ID NO: 3 и SEQ ID NO: 9, и аминокислотной последовательности в ее консервативной модифицированной форме;
CDR1 легкой цепи включает по меньшей мере одну аминокислотную последовательность, выбранную из группы, состоящей из аминокислотной последовательности, как указано в SEQ ID NO: 4 и SEQ ID NO: 10, и аминокислотной последовательности в ее консервативной модифицированной форме;
CDR2 легкой цепи включает по меньшей мере одну аминокислотную последовательность, выбранную из группы, состоящей из аминокислотной последовательности, как указано в SEQ ID NO: 5 и SEQ ID NO: 11, и аминокислотной последовательности в ее консервативной модифицированной форме; и
CDR3 легкой цепи включает по меньшей мере одну аминокислотную последовательность, выбранную из группы, состоящей из аминокислотной последовательности, как указано в SEQ ID NO: 6 и SEQ ID NO: 12, и аминокислотной последовательности в ее консервативной модифицированной форме.
В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент включают:
1) CDR1 тяжелой цепи, имеющую аминокислотную последовательность, как указано в SEQ ID NO: 1, CDR2 тяжелой цепи, имеющую аминокислотную последовательность, как указано в SEQ ID NO: 2, CDR3 тяжелой цепи, имеющую аминокислотную последовательность, как указано в SEQ ID NO: 3, CDR1 легкой цепи, имеющую аминокислотную последовательность, как указано в SEQ ID NO: 4, CDR2 легкой цепи, имеющую аминокислотную последовательность, как указано в SEQ ID NO: 5, CDR3 легкой цепи, имеющую аминокислотную последовательность, как указано в SEQ ID NO: 6; или
2) CDR1 тяжелой цепи, имеющую аминокислотную последовательность, как указано в SEQ ID NO: 7, CDR2 тяжелой цепи, имеющую аминокислотную последовательность, как указано в SEQ ID NO: 8, CDR3 тяжелой цепи, имеющую аминокислотную последовательность, как указано в SEQ ID NO: 9, CDR1 легкой цепи, имеющую аминокислотную последовательность, как указано в SEQ ID NO: 10, CDR2 легкой цепи, имеющую аминокислотную последовательность, как указано в SEQ ID NO: 11, CDR3 легкой цепи, имеющую аминокислотную последовательность, как указано в SEQ ID NO: 12.
В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент включают вариабельную область тяжелой цепи и вариабельную область легкой цепи, причем (i) вариабельная область тяжелой цепи включает аминокислотную последовательность, которая по меньшей мере на 80% гомологична по меньшей мере одной из аминокислотных последовательностей, как указано в SEQ ID NO: 13, SEQ ID NO: 15, SEQ ID NO: 17, SEQ ID NO: 19, и аминокислотную последовательность в ее консервативной модифицированной форме; и/или (ii) вариабельная область легкой цепи включает аминокислотную последовательность, которая по меньшей мере на 80% гомологична по меньшей мере одной из аминокислотных последовательностей, как указано в SEQ ID NO: 14, SEQ ID NO: 16, SEQ ID NO: 18, SEQ ID NO: 20, и аминокислотную последовательность в ее консервативной модифицированной форме.
В некоторых вариантах осуществления вариабельная область тяжелой цепи включает аминокислотную последовательность, которая по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% гомологична вариабельной области тяжелой цепи, выбранной из (i); причем вариабельная область легкой цепи включает аминокислотную последовательность, которая по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% гомологична вариабельной области легкой цепи, выбранной из (ii).
В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент включают:
1) аминокислотную последовательность вариабельной области тяжелой цепи, как указано в SEQ ID NO: 13, и аминокислотную последовательность вариабельной области легкой цепи, как указано в SEQ ID NO: 14;
2) аминокислотную последовательность вариабельной области тяжелой цепи, как указано в SEQ ID NO: 15, и аминокислотную последовательность вариабельной области легкой цепи, как указано в SEQ ID NO: 16;
3) аминокислотную последовательность вариабельной области тяжелой цепи, как указано в SEQ ID NO: 17, и аминокислотную последовательность вариабельной области легкой цепи, как указано в SEQ ID NO: 18; или
4) аминокислотную последовательность вариабельной области тяжелой цепи, как указано в SEQ ID NO: 19, и аминокислотную последовательность вариабельной области легкой цепи, как указано в SEQ ID NO: 20.
В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент включают:
1) аминокислотную последовательность тяжелой цепи, как указано в SEQ ID NO: 26, и аминокислотную последовательность легкой цепи, как указано в SEQ ID NO: 27;
2) аминокислотную последовательность тяжелой цепи, как указано в SEQ ID NO: 28, и аминокислотную последовательность легкой цепи, как указано в SEQ ID NO: 29;
3) аминокислотную последовательность тяжелой цепи, как указано в SEQ ID NO: 30, и аминокислотную последовательность легкой цепи, как указано в SEQ ID NO: 31; или
4) аминокислотную последовательность тяжелой цепи, как указано в SEQ ID NO: 32, и аминокислотную последовательность легкой цепи, как указано в SEQ ID NO: 33.
В некоторых вариантах осуществления выделенное антитело представляет собой IgG1, IgG2 или IgG4.
В некоторых вариантах осуществления антитело представляет собой моноклональное антитело, антитело мыши, химерное антитело, гуманизированное антитело, антитело, сконструированное человеком, антитело человека, Fv, одноцепочечное антитело (scFv), Fab, Fab', Fab'-SH или F(ab')2.
В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент способны связываться с аминокислотной последовательностью, как указано в SEQ ID NO: 21.
В другом аспекте настоящее изобретение представляет иммуноконъюгат, включающий терапевтическое средство и антитело или его антигенсвязывающий фрагмент, описанные выше, конъюгированные с терапевтическим средством.
В еще одном аспекте настоящее изобретение представляет композицию, включающую антитело или его антигенсвязывающий фрагмент, описанные выше, и/или иммуноконъюгат, описанный выше, и фармацевтически приемлемый носитель.
В еще одном аспекте настоящее изобретение представляет набор для обнаружения B7H6 в образце, набор включает антитело или его антигенсвязывающий фрагмент, описанные выше.
В еще одном аспекте настоящее изобретение представляет применение антитела или его антигенсвязывающего фрагмента, описанных выше, при получении реагента для обнаружения B7H6 в образце.
В еще одном аспекте настоящее изобретение представляет применение антитела или его антигенсвязывающего фрагмента, описанных выше, при получении лекарственного средства для предупреждения и/или лечения B7H6-опосредованного заболевания, причем B7H6-опосредованное заболевание представляет собой рак или инфекционное заболевание.
Необязательно, рак представляет собой по меньшей мере одно из рака легких, рака печени, рака яичников, рака шейки матки, рака кожи, рака мочевого пузыря, рака толстой кишки, рака молочной железы, глиомы, рака почек, рака желудка, рака пищевода, плоскоклеточного рака полости рта и рака головы и шеи.
В еще одном аспекте настоящее изобретение представляет нуклеиновую кислоту, включающую нуклеиновую кислоту, кодирующую антитело или его антигенсвязывающий фрагмент, описанные выше.
В дополнительном аспекте настоящее изобретение представляет рекомбинантный вектор или трансформант, включающий нуклеиновую кислоту, описанную выше.
В одном аспекте настоящее изобретение представляет рекомбинантную клетку, несущую нуклеиновую кислоту, экспрессирующую вектор или трансформант, описанный выше, или экспрессирующую антитело или его антигенсвязывающий фрагмент, описанный выше.
В другом аспекте настоящее изобретение представляет лекарственное средство, включающее антитело или его антигенсвязывающий фрагмент, иммуноконъюгат, композицию, лекарственное средство, нуклеиновую кислоту, рекомбинантный вектор или трансформант или рекомбинантную клетку, описанные выше.
В дополнительном аспекте настоящее изобретение представляет применение антитела или его антигенсвязывающего фрагмента, иммуноконъюгата, композиции, лекарственного средства, нуклеиновой кислоты, рекомбинантного вектора или трансформанта или рекомбинантной клетки, описанных выше, в лечении и/или предупреждении B7H6-опосредованного заболевания. Как описано выше, антитело или его антигенсвязывающий фрагмент способны эффективно связываться с B7H6, тем самым способствуя взаимодействию B7H6 с NKp30 и усиливая противораковую функцию NK-клеток, так что антитело или его антигенсвязывающий фрагмент и вещества, способные экспрессировать антитело или его антигенсвязывающий фрагмент в соответствующих условиях, могут эффективно предупреждать и/или лечить B7H6-опосредованное заболевание.
В другом аспекте настоящее изобретение представляет способ лечения и/или предупреждения B7H6-опосредованного заболевания. Согласно варианту осуществления настоящего изобретения способ включает введение субъекту по меньшей мере одного из 1) антитела или его антигенсвязывающего фрагмента, описанных выше; 2) иммуноконъюгата, описанного выше; 3) композиции, описанной выше; 4) лекарственного средства, описанного выше; 5) нуклеиновой кислоты, описанной выше; 6) рекомбинантного вектора или трансформанта, описанных выше; и 7) рекомбинантной клетки, описанной выше. Как описано выше, антитело или его антигенсвязывающий фрагмент могут эффективно связываться с B7H6, тем самым способствуя взаимодействию B7H6 с NKp30 и усиливая противораковую функцию NK-клеток, так что антитело или его антигенсвязывающий фрагмент и вещества, способные экспрессировать антитело или его антигенсвязывающий фрагмент в соответствующих условиях, или вещества, включающие антитело или его антигенсвязывающий фрагмент, могут эффективно предупреждать и/или лечить B7H6-опосредованное заболевание, и способ согласно варианту осуществления по настоящему изобретению может эффективно предупреждать и/или лечить B7H6-опосредованное заболевание.
В еще одном аспекте настоящее изобретение представляет способ диагностики наличия у субъекта B7H6-опосредованного заболевания. Согласно варианту осуществления настоящего изобретения способ включает обнаружение B7H6 в тестируемом образце с применением по меньшей мере одного из следующего: 1) антитела или его антигенсвязывающего фрагмента, описанных выше; 2) нуклеиновой кислоты, описанной выше; 3) рекомбинантного вектора или трансформанта, описанных выше; и 4) рекомбинантной клетки, описанной выше; и определение содержания B7H6 в тестируемом образце на основе результата обнаружения B7H6. Как описано ранее, антитело или антигенсвязывающий фрагмент согласно варианту осуществления настоящего изобретения способны эффективно связываться с B7H6, и, следовательно, антитело или антигенсвязывающий фрагмент можно применять для обнаружения B7H6, а B7H6 опосредует различные заболевания, и следовательно, наличие у субъекта B7H6-опосредованного заболевания можно определить на основе уровня B7H6, содержащегося в биологическом образце субъекта. Кроме того, вышеупомянутые вещества также можно применять для мониторинга содержания B7H6 в тестируемом образце субъекта, а именно, вышеупомянутые вещества также можно применять для определения стадии заболевания у субъекта, страдающего от B7H6-опосредованного заболевания, а также можно применять для прогноза B7H6-опосредованного заболевания.
В еще одном аспекте настоящее изобретение представляет применение по меньшей мере одного из следующего для диагностики наличия у субъекта B7H6-опосредованного заболевания: 1) антитела или его антигенсвязывающего фрагмента, описанных выше; 2) нуклеиновой кислоты, описанной выше; 3) рекомбинантного вектора или трансформанта, описанных выше; и 4) рекомбинантной клетки, описанной выше. Как описано ранее, антитело или антигенсвязывающий фрагмент согласно варианту осуществления настоящего изобретения способны эффективно связываться с B7H6, и, следовательно, антитело или антигенсвязывающий фрагмент можно применять для обнаружения B7H6, а B7H6 опосредует различные заболевания, и следовательно, наличие у субъекта B7H6-опосредованного заболевания можно определить на основе уровня B7H6, содержащегося в биологическом образце субъекта.
Согласно вышеуказанным техническим решениям настоящее изобретение представляет антитело к B7H6 или его антигенсвязывающий фрагмент, способный связываться с B7H6 человека и макака. Антитело или его антигенсвязывающий фрагмент по настоящему изобретению имеют по меньшей мере одно из следующих свойств: способны связываться с B7H6 человека и макака; способны стимулировать взаимодействию между B7H6 и NKp30; способны стимулировать противораковую функцию NK-клеток.
Дополнительные признаки и преимущества настоящего изобретения будут изложены в подробном описании, которое приведено ниже.
Дополнительные аспекты и преимущества настоящего изобретения будут частично изложены в последующем описании и частично станут очевидны из следующего описания или же они могут быть выявлены при практической реализации настоящего изобретения.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Вышеизложенные и/или дополнительные аспекты и преимущества настоящего изобретения станут очевидными и легко оценимы из следующего описания вариантов осуществления в сочетании с прилагаемыми графическими материалами, на которых:
прилагаемые графические материалы представлены для обеспечения дальнейшего понимания настоящего изобретения и являются частью описания. Графические материалы вместе с приведенными ниже конкретными вариантами осуществления применяются для пояснения настоящего изобретения, но не являются ограничением настоящего изобретения. В графических материалах:
ФИГ. 1 представляет собой график ИФА, показывающий связывание мышиного антитела B7H6 с B7H6 человека согласно конкретному варианту осуществления настоящего изобретения;
ФИГ. 2 представляет собой график, показывающий связывание мышиного антитела B7H6 с HL60-B7H6-клетками согласно конкретному варианту осуществления настоящего изобретения;
ФИГ. 3 представляет собой график ИФА, показывающий связывание гуманизированного антитела B7H6 с B7H6 человека согласно конкретному варианту осуществления настоящего изобретения;
ФИГ. 4 представляет собой график, показывающий связывание гуманизированного антитела B7H6 с HL60-B7H6-клетками согласно конкретному варианту осуществления настоящего изобретения;
ФИГ. 5 представляет собой график, показывающий связывание гуманизированного антитела B7H6 с B7H6-клетками CHO-K1-макака согласно конкретному варианту осуществления настоящего изобретения;
ФИГ. 6 представляет собой график ИФА, показывающий связывание гуманизированного антитела B7H6 с B7H6 макака согласно конкретному варианту осуществления настоящего изобретения;
ФИГ. 7 представляет собой график, показывающий влияние антитела B7H6 на стимулирование связывания рецептора NKp30 согласно конкретному варианту осуществления настоящего изобретения;
ФИГ. 8 представляет собой график, показывающий комплементзависимый цитотоксический эффект, опосредованный антителом B7H6, согласно конкретному варианту осуществления настоящего изобретения; и
ФИГ. 9 представляет собой график, показывающий эффект антитела B7H6 на стимулирование антагонистической опухоли острого миелолейкоза U-937 человека у голых мышей согласно конкретному варианту осуществления настоящего изобретения.
ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
Далее варианты осуществления настоящего изобретения будут описаны подробно, причем варианты осуществления проиллюстрированы в сопроводительных графических материалах. Варианты осуществления, описанные в качестве примера со ссылкой на прилагаемые графические материалы, являются примерными и предназначены для объяснения настоящего изобретения и не должны рассматриваться как ограничивающие настоящее изобретение.
Следует отметить, что термины «первый» и «второй» применяются только в описательных целях и не должны толковаться как указывающие или подразумевающие относительную важность или неявно указывающие на количество указанных технических характеристик. Таким образом, признак, определенный как «первый» или «второй», может явно или неявно включать в себя один или больше признаков. Кроме того, в описании настоящего изобретения, если не указано иное, значение «множество» равно двум или больше.
Далее конкретные варианты осуществления настоящего изобретения будут описаны подробно. Следует понимать, что конкретные варианты осуществления, описанные в данном документе, применяются только для иллюстрации и объяснения настоящего изобретения, а не для его ограничения.
Конечные точки диапазонов и любых значений, раскрытых в данном документе, не ограничиваются точным диапазоном или значением, и такие диапазоны или значения следует понимать как включающие значения, приближающие такие диапазоны или значения. Для числовых диапазонов конечные точки каждого диапазона и отдельные значения точек, а также отдельные значения точек можно комбинировать друг с другом для получения одного или больше новых числовых диапазонов, и такие числовые диапазоны следует рассматривать как конкретно раскрытые в данном документе.
Для облегчения понимания настоящего изобретения некоторые технические и научные термины определены ниже. Если это четко не указано где-либо в этом документе, все другие технические и научные термины, применяемые в данном документе, имеют значения, обычно понимаемые техническим персоналом в области техники, к которой относится настоящее изобретение. Аббревиатуры аминокислотных остатков представляют собой стандартные трехбуквенные и/или однобуквенные коды, применяемые в данной области техники для обозначения одной из 20, как правило, применяемых L-аминокислот.
В настоящем изобретении, если не указано иное, применяемый термин «антигенсвязывающий фрагмент», т.е. «фрагмент антитела», обычно относится к фрагменту антигенсвязывающего антитела и может включать часть интактного антитела, как правило, антигенсвязывающую или вариабельную область. Примеры фрагментов антител включают Fab, Fab’, F(ab’)2, Fv или scFv, диатело, линейное антитело, молекулы одноцепочечного антитела и т.д.
Термин «область, определяющая комплементарность», или «CDR», или «последовательность CDR» относится к аминокислотной последовательности, ответственной за связывание антигена в антителе, например, как правило, включает аминокислотные остатки около 23-34 (L1), 50-56 (L2) и 89-97 (L3) в вариабельной области легкой цепи, и 31-35B (H1), 50-65 (H2) и 95-102 (H3) в вариабельной области тяжелой цепи (Kabat et al. Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD.(1991)); и/или аминокислотные остатки из «гипервариабельных петель» (например, около 26-32 (LI), 50-52 (L2) и 91-96 (L3) в вариабельной области легкой цепи и 26-32 (H1) , 53-55 (H2) и 96-101 (H3) в вариабельной области тяжелой цепи (Chothia and Lesk J.Mol.Biol.196: 901-917 (1987)).
Термин «аминокислотная последовательность в консервативной модифицированной форме» относится к аминокислотной модификации, которая не оказывает существенного влияния или не изменяет характеристики связывания антитела, включающего аминокислотную последовательность, в том числе аминокислотные замены, дополнения и делеции. Модификации можно вводить в антитела настоящего изобретения стандартными методами, такими как сайт-направленный мутагенез и ПЦР-опосредованный мутагенез. Консервативная замена аминокислот относится к замене аминокислотных остатков на аминокислотные остатки с аналогичными боковыми цепями. Семейства аминокислотных остатков, имеющих сходные боковые цепи, были определены в данной области техники. Эти семейства включают аминокислоты с основными боковыми цепями, например, лизином, аргинином, гистидином, аминокислоты с кислыми боковыми цепями, например, аспаргиновой кислотой, глутаминовой кислотой, аминокислоты с незаряженными полярными боковыми цепями, например, глицином, аспарагином, глутамином, серином, треонином, тирозином, цистеином, триптофаном, аминокислоты с неполярными боковыми цепями, например, аланином, валином, лейцином, изолейцином, пролином, фенилаланином, метионином, аминокислоты с β-разветвленными боковыми цепями, например, треонином, валином, изолейцином, и аминокислоты с ароматическими боковыми цепями, например, тирозином, фенилаланином, триптофаном, гистидином. Таким образом, один или более аминокислотных остатков в CDR-области антитела настоящего изобретения можно заменить другими аминокислотными остатками из того же семейства боковых цепей, и измененное антитело можно проверить на сохранность функции с помощью функциональных анализов, описанных в данном документе. Предпочтительно количество консервативных модификаций не превышает одной или двух.
Что касается полипептидов, термин «(существенная) гомология» означает, что по меньшей мере около 80%, как правило, по меньшей мере от около 90% до 95% и более предпочтительно по меньшей мере от около 98% до 99,5% аминокислот двух полипептидов или их обозначенных последовательностей являются идентичными при оптимальном выравнивании и сравнении (при котором нуклеотиды вставляются или удаляются соответствующим образом).
% идентичности между двумя последовательностями варьируется в зависимости от количества идентичных положений, общих для последовательностей, когда последовательности оптимально выровнены (т.е. % гомологии = количество идентичных положений/общее количество положений × 100), где оптимальное выравнивание определяется с учетом количества пробелов, которые необходимо ввести, и длины каждого пробела для достижения оптимального выравнивания двух последовательностей. Сравнение последовательностей и определение процента идентичности между двумя последовательностями можно выполнить с помощью математических алгоритмов, как описано в неограничивающих примерах ниже.
Специалист в данной области техники может заменить, добавить и/или удалить одну или более (например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 или более) аминокислот в последовательности настоящего изобретения для получения варианта последовательности антитела или его функционального фрагмента без существенного влияния на активность антитела (с сохранением по меньшей мере 95% активности). Они считаются включенными в объем настоящего изобретения. Например, аминокислоты, имеющие сходные свойства, можно заменить в вариабельной области. Последовательность варианта настоящего изобретения может иметь по меньшей мере 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичности (или гомологии) с эталонной последовательностью. Идентичность последовательности, описанной в данном документе, можно измерить с помощью программного обеспечения для анализа последовательностей, например, компьютерной программы BLAST, применяющей параметры по умолчанию, в частности BLASTP или TBLASTN. Аминокислотные последовательности, упомянутые в данном документе, показаны от N-конца до С-конца.
Как описано ранее, антитело по настоящему изобретению может быть полноразмерным (например, антитела IgG1 или IgG4) или может включать только антигенсвязывающую часть (например, Fab, F(ab')2 или фрагмент scFv) или может быть модифицировано для влияния на функцию. Настоящее изобретение включает антитела к B7H6, имеющие модифицированный характер гликозилирования. В некоторых применениях может быть полезно внести модификации для удаления нежелательных сайтов гликозилирования или для устранения присутствия фукозных фрагментов в олигосахаридных цепях, например для усиления антителозависимой функции АКЗЦ. В других применениях можно выполнить модификации галактозилирования для изменения комплементзависимой цитотоксичности (КЗЦ).
Термин «функциональный фрагмент», применяемый в данном документе, относится, в частности, к частичному фрагменту антитела, например, Fv, scFv (sc означает одноцепочечный), Fab, F(ab')2, Fab', scFv-Fc фрагменту или диателу, или любому фрагменту, который должен быть способен увеличивать период полураспада путем химической модификации, например, с помощью добавления полиалкиленгликолей, например, полиэтиленгликоля («ПЭГилирование, ПЭГ») (называемые пегилированными фрагментами Fv-ПЭГ, scFv-ПЭГ, Fab-ПЭГ, F(ab')2-ПЭГ или Fab'-ПЭГ) («ПЭГ» означает полиэтиленгликоль) или путем встраивания в липосомы, причем указанные фрагменты обладают связывающей активностью B7H6. Предпочтительно, чтобы функциональный фрагмент состоял или содержал частичные последовательности вариабельной области тяжелой цепи или вариабельной области легкой цепи исходного антитела, достаточные для сохранения той же специфичности связывания и достаточной аффинности, что и исходное антитело. Предпочтительно, чтобы аффинность B7H6 составляла по меньшей мере 1/100 от аффинности исходного антитела, а в более предпочтительном варианте - по меньшей мере 1/10. Такие функциональные фрагменты будут включать минимум 5 аминокислот, предпочтительно 10, 15, 25, 50 и 100 смежных аминокислот последовательности антитела, из которой они получены.
Как описано выше, настоящее изобретение относится к антителу, способному связываться с B7H6 или его антигенсвязывающим фрагментом, причем антитело включает CDR1 тяжелой цепи, CDR2 тяжелой цепи и CDR3 тяжелой цепи; CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи.
Согласно настоящему изобретению антитело способно связываться с B7H6, в частности с аминокислотной последовательностью, как указано в SEQ ID NO: 21.
В предпочтительном варианте осуществления настоящего изобретения для дальнейшего улучшения биологической приемлемости антитела, его также можно гуманизировать, т.е. антитело представляет собой химерное или гуманизированное антитело. Термин «химерное антитело» относится к рекомбинантному антителу, полученному путем замены аминокислотной последовательности константной области моноклонального антитела одного вида (например, мыши) на константную область антитела другого вида (например, человека) с помощью технологии рекомбинантной ДНК. Термин «гуманизированное антитело» относится к рекомбинантному антителу, полученному путем полной замены константных и не-CDR (Fv каркасная область (FR)) аминокислотных последовательностей вариабельных областей моноклонального антитела одного вида (например, мыши) на константные и не-CDR аминокислотные последовательности вариабельных областей антитела другого вида (например, человека) с помощью технологии рекомбинантной ДНК. То есть, когда константная область антитела гуманизирована, оно называется химерным антителом, а если константная и не-CDR аминокислотные последовательности вариабельных областей гуманизированы, их называют гуманизированным антителом. Способы гуманизации могут быть реализованы со ссылкой на традиционные методы инженерии антител и не будут подробно описаны в данном документе.
Последовательность вариабельной области тяжелой цепи гуманизированного антитела, представленного в настоящем изобретении, как указано в SEQ ID NO: 17, и последовательность вариабельной области легкой цепи, как указано в SEQ ID NO: 18; альтернативно, последовательность вариабельной области тяжелой цепи, как указано в SEQ ID NO: 19, и последовательность вариабельной области легкой цепи такая, как указано в SEQ ID NO: 20.
Иммуноконъюгат, представленный в настоящем изобретении, включает терапевтическое средство и антитело или его антигенсвязывающий фрагмент, описанный выше, конъюгированный с терапевтическим средством. Способ, которым антитело или его антигенсвязывающий фрагмент конъюгируют с терапевтическим средством, может быть обычным.
Композиция, представленная в настоящем изобретении, включает антитело или его антигенсвязывающий фрагмент, описанный выше, и/или иммуноконъюгат, описанный выше, и фармацевтически приемлемый носитель. В некоторых вариантах осуществления композиция включает комбинации, которые разделены во времени и/или пространстве, при условии, что они могут работать вместе для достижения целей настоящего изобретения. Например, компоненты, содержащиеся в композиции, можно вводить субъектам целиком или по отдельности. Если компоненты, входящие в состав композиции, вводятся субъекту отдельно, отдельные компоненты могут вводиться субъекту одновременно или последовательно.
Термин «фармацевтически приемлемый» означает, что композицию можно вводить субъекту, не вызывая неблагоприятной физиологической реакции, которая препятствовала бы введению композиции. Например, «фармацевтически приемлемый носитель» относится к носителю, который можно применять для получения, как правило, безопасной, нетоксичной и желательной фармацевтической композиции. Предпочтительно примеры таких носителей или разбавителей включают, без ограничения, воду, физиологический раствор, раствор Рингера, декстрозу, маннит, глюкозу, лактозу, крахмал, стеарат магния, целлюлозу, карбонат магния, 0,3% глицерин, гиалуроновую кислоту, этанол, полиалкиленгликоли, такие как полипропиленгликоль, триглицериды, 5% сывороточный альбумин человека; также можно применять липосомы и неводные носители, такие как нелетучие масла.
Композицию по настоящему изобретению также можно вводить в комбинации друг с другом или в комбинации с одним или более другими терапевтическими соединениями, например, в комбинации с химиотерапевтическим средством. Таким образом, композиция может также содержать химиотерапевтическое средство. Антитело или его антигенсвязывающий фрагмент, или иммуноконъюгат настоящего изобретения можно также комбинировать со вторым терапевтическим средством, примерные средства которого включают, без ограничения, другие средства, ингибирующие активность B7H6 (включая другие антитела или их антигенсвязывающие фрагменты, пептидные ингибиторы, антагонисты малых молекул и т.д.) и/или средства, которые препятствуют передаче сигнала выше или ниже B7H6.
Обычно антитело или его антигенсвязывающий фрагмент вводили в эффективном количестве, то есть в количестве, достаточном для достижения желаемого терапевтического и/или профилактического эффекта, например, в количестве, которое приводит к предотвращению или облегчению симптомов, связанных с подлежащим лечению заболеванием, например, с заболеванием, связанным с B7H6. Эффективное количество композиции, вводимое субъекту, будет зависеть от типа и тяжести заболевания, а также от характеристик индивидуума, например, от общего состояния здоровья, возраста, пола, веса и переносимости лекарственных средств; оно также будет зависеть от тяжести и типа заболевания, а специалист в данной области техники сможет определить соответствующие дозировки в зависимости от таких факторов и т.д.
Набор для выявления B7H6 в образце согласно настоящему изобретению включает антитело или его антигенсвязывающий фрагмент, описанный выше. Образец может быть тканью пациента, страдающего от B7H6-опосредованного заболевания, в частности, отторжения трансплантата, аутоиммунного заболевания, инфекционного заболевания или рака, более предпочтительно пациента, страдающего по меньшей мере одним из рака легких, рака печени, рака яичников, рака шейки матки, рака кожи, рака мочевого пузыря, рака толстой кишки, рака молочной железы, глиомы, рака почки, рака желудка, рака пищевода, плоскоклеточного рака полости рта и рака головы и шеи. Набор также может включать реагенты, как правило, применяемые для обнаружения B7H6, например, растворы для нанесения покрытия и т.п.
В настоящем изобретении также представлено применение антитела или его антигенсвязывающего фрагмента, описанных выше, при получении реагента для обнаружения B7H6 в образце. Как упоминалось ранее, образец может быть тканью пациента, страдающего от B7H6-опосредованного заболевания, которое не описано подробно в данном документе. Антитело или его антигенсвязывающий фрагмент по настоящему изобретению имеет хорошую аффинность к B7H6 и способно эффективно обнаруживать B7H6 в образце.
В настоящем изобретении также представлено применение антитела или его антигенсвязывающего фрагмента, иммуноконъюгата, композиции, лекарственного средства, нуклеиновой кислоты, рекомбинантного вектора или трансформанта или рекомбинантной клетки при получении лекарственного средства для предупреждения и/или лечения B7H6-опосредованного заболевания. Предпочтительно, B7H6-опосредованное заболевание представляет собой отторжение трансплантата, аутоиммунное заболевание, инфекционное заболевание или рак. Более предпочтительно, рак представляет собой рак, экспрессирующий B7H6. Более предпочтительно, рак представляет собой по меньшей мере одно из рака легких, рака печени, рака яичников, рака шейки матки, рака кожи, рака мочевого пузыря, рака толстой кишки, рака молочной железы, глиомы, рака почек, рака желудка, рака пищевода, плоскоклеточного рака полости рта и рака головы и шеи. Более предпочтительно, инфекционное заболевание включает, без ограничения, инфекцию вируса ВИЧ и/или инфекцию вируса гепатита В.
Настоящее изобретение относится к лекарственному средству, включающему антитело или его антигенсвязывающий фрагмент, иммуноконъюгат, композицию, нуклеиновую кислоту, рекомбинантный вектор, трансформант или рекомбинантную клетку, описанные выше.
Согласно некоторым вариантам осуществления настоящего изобретения, лекарственное средство может включать по меньшей мере один из следующих дополнительных технических признаков.
Согласно некоторым вариантам осуществления настоящего изобретения, лекарственное средство включает фармацевтически приемлемый носитель и эффективное количество антитела или его антигенсвязывающего фрагмента, иммуноконъюгата, композиции, нуклеиновой кислоты, рекомбинантного вектора, трансформантной или рекомбинантной клетки.
Настоящее изобретение также относится к способу предупреждения и/или лечения B7H6-опосредованного заболевания (описанного выше), включающему: введение пациенту эффективного количества по меньшей мере одного из антитела или его антигенсвязывающего фрагмента, иммуноконъюгата, композиции, рекомбинантной клетки, нуклеиновой кислоты и лекарственного средства настоящего изобретения. Способ введения может быть пероральным, назальным, внутрикожным, подкожным, внутримышечным, внутривенным или внутрибрюшинным. Как было описано ранее, антитело или его антигенсвязывающий фрагмент способны эффективно связываться с B7H6, тем самым способствуя взаимодействию B7H6 с NKp30 и усиливая противораковую функцию NK-клеток. Таким образом антитело или его антигенсвязывающий фрагмент, вещества, способные экспрессировать антитело или его антигенсвязывающий фрагмент в соответствующих условиях, или вещества, включающие антитело или его антигенсвязывающий фрагмент, могут эффективно предупреждать и/или лечить B7H6-опосредованное заболевание, а способ согласно варианту осуществления настоящего изобретения может эффективно предупреждать и/или лечить B7H6-опосредованное заболевание.
Согласно некоторым конкретным вариантам осуществления настоящего изобретения способ может дополнительно включать по меньшей мере один из следующих дополнительных технических признаков.
Согласно конкретному варианту осуществления настоящего изобретения B7H6-опосредованное заболевание представляет собой рак или инфекционное заболевание.
Согласно конкретному варианту осуществления настоящего изобретения рак представляет собой по меньшей мере одно из рака легких, рака печени, рака яичников, рака шейки матки, рака кожи, рака мочевого пузыря, рака толстой кишки, рака молочной железы, глиомы, рака почек, рака желудка, рака пищевода, плоскоклеточного рака полости рта и рака головы и шеи.
В данном документе, «пациент» или «субъект» как правило относятся к млекопитающим, например, приматам и/или грызунам, в частности, людям или мышам.
Специалист в данной области техники может клонировать молекулу ДНК, кодирующую антитело или его антигенсвязывающий фрагмент по настоящему изобретению, в вектор, в частности вектор экспрессии, и трансформировать клетку-хозяина для получения антитела или его антигенсвязывающего фрагмента путем индуцирования экспрессии. Таким образом, настоящее изобретение также представляет (выделенную) нуклеиновую кислоту, кодирующую описанное выше антитело или его антигенсвязывающий фрагмент, а также рекомбинантный вектор и трансформант, содержащий его. Нуклеиновая кислота предпочтительно представляет собой кассету экспрессии, полученную с помощью средств генной инженерии.
Рекомбинантный вектор может относиться как к вектору клонирования, так и к вектору экспрессии, и может быть получен путем оперативного связывания нуклеиновой кислоты с коммерчески доступным вектором (например, плазмидой или вирусным вектором). Обычные плазмиды включают pSeTag2, PEE14, pMH3 и т.п.
Векторы экспрессии настоящего изобретения могут содержать последовательности ДНК, кодирующие вариабельную область тяжелой цепи, вариабельную область легкой цепи и/или константную область антитела. Однако можно также сконструировать два вектора экспрессии, один из которых содержит вариабельную и константную области тяжелой цепи, а другой содержит вариабельную и константную области легкой цепи, и трансфицировать клетки млекопитающих вместе. В предпочтительном варианте осуществления вектор экспрессии дополнительно включает промотор и последовательность ДНК, кодирующую сигнальный пептид секреции, и по меньшей мере один ген лекарственной устойчивости для скрининга.
Клетка-хозяин настоящего изобретения может быть прокариотической клеткой-хозяином, эукариотической клеткой-хозяином или бактериофагом. Прокариотической клеткой-хозяином может быть E. coli, Bacillus subtilis, Streptomyces или Proteus mirabilis, и т.д. Эукариотические клетки могут быть грибами, например Pichia pastoris, Saccharomyces cerevisiae, Schizosaccharomyces pombe, Trichoderma, клетками насекомых, например Mythimna separata, клетками растений, например, табака, клетками млекопитающих, например, BHK-клетками, CHO-клетками, COS-клетками, миеломными клетками и т.п. В некоторых вариантах осуществления клетки-хозяева по настоящему изобретению предпочтительно представляют собой клетки млекопитающих, более предпочтительно BHK-клетки, CHO-клетки, NSO-клетки или COS-клетки.
Настоящее изобретение относится к рекомбинантной клетке, несущей нуклеиновую кислоту, рекомбинантный вектор или трансформант или антитело или антигенсвязывающий фрагмент, описанные выше. Рекомбинантную клетку получали с помощью трансфекции или трансформации вектора экспрессии. Согласно варианту осуществления настоящего изобретения рекомбинантная клетка в подходящих условиях экспрессирует вышеупомянутое антитело на высоком уровне, причем антитело или его антигенсвязывающий фрагмент могут эффективно связываться с B7H6, и, кроме того, антитело или антигенсвязывающий фрагмент имеют хороший эффект в предупреждении и/или лечении B7H6-опосредованного заболевания.
Следует отметить, что рекомбинантная клетка по настоящему изобретению конкретно не ограничена и может представлять собой прокариотическую клетку, эукариотическую клетку или бактериофаг. Прокариотической клеткой может быть E. coli, Bacillus subtilis, Streptomyces или Proteus mirabilis и т.д. Эукариотические клетки могут быть грибами, например Pichia pastoris, Saccharomyces cerevisiae, Schizosaccharomyces pombe, Trichoderma, клетками насекомых, например Mythimna separata, клетками растений, например, табака, клетками млекопитающих, например, BHK-клетками, CHO-клетками, COS-клетками, миеломными клетками и т.п. В некоторых вариантах осуществления рекомбинантные клетки по настоящему изобретению предпочтительно представляют собой клетки млекопитающих, включая BHK-клетки, CHO-клетки, NSO-клетки или COS-клетки, и не включают зародышевые клетки животных, оплодотворенные яйцеклетки или эмбриональные стволовые клетки.
Следует отметить, что «подходящие условия», применяемые в описании настоящей заявки, означают условия, подходящие для экспрессии антитела или его антигенсвязывающего фрагмента, описанного в данном документе. Специалисты в данной области техники легко поймут, что условия, подходящие для экспрессии антитела или антигенсвязывающего фрагмента, включают, без ограничения, подходящие способы трансформации или трансфекции, подходящие условия трансформации или трансфекции, состояние здоровой клетки-хозяина, подходящую плотность клетки-хозяина, подходящую среду для культивирования клеток и подходящее время для культивирования клеток. «Подходящие условия» конкретно не ограничены, и специалист в данной области техники может оптимизировать оптимальные условия для экспрессии антитела или его антигенсвязывающего фрагмента в соответствии с конкретными лабораторными условиями.
Настоящее изобретение также относится к применению антитела или его антигенсвязывающего фрагмента, иммуноконъюгата, композиции, лекарственного средства, нуклеиновой кислоты, рекомбинантного вектора или трансформанта или рекомбинантной клетки, описанных выше, в лечении и/или предупреждении B7H6-опосредованного заболевания. Как описано выше, антитело или его антигенсвязывающий фрагмент могут эффективно связываться с B7H6, тем самым способствуя взаимодействию B7H6 с NKp30 и усиливая противораковую функцию NK-клеток, так что антитело или его антигенсвязывающий фрагмент и вещества, способные экспрессировать антитело или его антигенсвязывающий фрагмент в соответствующих условиях, могут эффективно предупреждать и/или лечить B7H6-опосредованное заболевание.
Согласно конкретному варианту осуществления настоящего изобретения, вышеупомянутое применение в лечении и/или предупреждении B7H6-опосредованного заболевания может дополнительно включать по меньшей мере один из следующих дополнительных технических признаков.
Согласно конкретному варианту осуществления настоящего изобретения B7H6-опосредованное заболевание представляет собой рак или инфекционное заболевание.
Согласно конкретному варианту осуществления настоящего изобретения рак представляет собой по меньшей мере одно из рака легких, рака печени, рака яичников, рака шейки матки, рака кожи, рака мочевого пузыря, рака толстой кишки, рака молочной железы, глиомы, рака почек, рака желудка, рака пищевода, плоскоклеточного рака полости рта и рака головы и шеи.
В еще одном аспекте настоящее изобретение представляет способ диагностики наличия у субъекта B7H6-опосредованного заболевания. Согласно конкретному варианту осуществления настоящего изобретения способ включает обнаружение B7H6 в тестируемом образце с применением по меньшей мере одного из следующего: 1) антитела или его антигенсвязывающего фрагмента, описанных выше; 2) нуклеиновой кислоты, описанной выше; 3) рекомбинантного вектора или трансформанта, описанных выше; и 4) рекомбинантной клетки, описанной выше; и определение содержания B7H6 в тестируемом образце на основе результата обнаружения B7H6. Как описано ранее, антитело или антигенсвязывающий фрагмент согласно варианту осуществления настоящего изобретения способны эффективно связываться с B7H6, и, следовательно, антитело или антигенсвязывающий фрагмент можно применять для обнаружения B7H6, а B7H6 опосредует различные заболевания, и следовательно, наличие у субъекта B7H6-опосредованного заболевания можно определить на основе уровня B7H6, содержащегося в биологическом образце субъекта. Кроме того, вышеупомянутые вещества также можно применять для мониторинга содержания B7H6 в тестируемом образце субъекта, а именно, вышеупомянутые вещества также можно применять для определения стадии заболевания у субъекта, страдающего от B7H6-опосредованного заболевания, а также можно применять для прогноза B7H6-опосредованного заболевания.
Согласно конкретному варианту осуществления настоящего изобретения, описанный выше способ может дополнительно включать по меньшей мере один из следующих дополнительных технических признаков.
Согласно конкретному варианту осуществления настоящего изобретения содержание B7H6 в тестируемом образце, которое не ниже минимального стандарта для заболевания, является показателем того, что тестируемый образец получен от пациента, страдающего от B7H6-опосредованного заболевания. Значение минимального стандарта можно определить путем сравнения, анализа и проверки разницы в содержании B7H6 в тестируемом образце, большого количества индивидуумов с B7H6-опосредованным заболеванием и большого количества здоровых индивидуумов.
Согласно конкретному варианту осуществления настоящего изобретения B7H6-опосредованное заболевание представляет собой рак или инфекционное заболевание.
Согласно конкретному варианту осуществления настоящего изобретения рак представляет собой по меньшей мере одно из рака легких, рака печени, рака яичников, рака шейки матки, рака кожи, рака мочевого пузыря, рака толстой кишки, рака молочной железы, глиомы, рака почек, рака желудка, рака пищевода, плоскоклеточного рака полости рта и рака головы и шеи.
Согласно конкретному варианту осуществления настоящего изобретения, тестируемый образец включает по меньшей мере одно из следующего: ткань, клетки, кровь, сыворотку, пот, кал и мочу.
В другом аспекте настоящее изобретение представляет применение по меньшей мере одного для диагностики наличия у субъекта B7H6-опосредованного заболевания: 1) антитела или его антигенсвязывающего фрагмента, описанных выше; 2) нуклеиновой кислоты, описанной выше; 3) рекомбинантного вектора или трансформанта, описанных выше; и 4) рекомбинантной клетки, описанной выше. Как описано ранее, антитело или антигенсвязывающий фрагмент согласно варианту осуществления настоящего изобретения способны эффективно связываться с B7H6, и, следовательно, антитело или антигенсвязывающий фрагмент можно применять для обнаружения B7H6, а B7H6 опосредует различные заболевания, и следовательно, наличие у субъекта B7H6-опосредованного заболевания можно определить на основе уровня B7H6, содержащегося в биологическом образце субъекта.
Согласно конкретному варианту осуществления настоящего изобретения, описанные выше применения могут дополнительно включать по меньшей мере один из следующих дополнительных технических признаков.
Согласно конкретному варианту осуществления настоящего изобретения B7H6-опосредованное заболевание представляет собой рак или инфекционное заболевание.
Согласно конкретному варианту осуществления настоящего изобретения рак представляет собой по меньшей мере одно из рака легких, рака печени, рака яичников, рака шейки матки, рака кожи, рака мочевого пузыря, рака толстой кишки, рака молочной железы, глиомы, рака почек, рака желудка, рака пищевода, плоскоклеточного рака полости рта и рака головы и шеи.
Описание последовательностей, включенных в настоящее изобретение, приведено в таблице 1.
Таблица 1. Список аминокислотных последовательностей
Нуклеиновая кислота, кодирующая тяжелые и/или легкие цепи антител настоящего изобретения в пределах объема настоящего изобретения, согласно аминокислотным последовательностям тяжелых и/или легких цепей, соответствует последовательностям нуклеиновых кислот, которые можно легко получить специалистам в данной области техники, как показано в таблице 2.
Таблица 2. Список нуклеотидных последовательностей
Далее настоящее изобретение будет описано подробно с помощью примеров. В примерах или тестовых примерах экспериментальные способы без указания конкретных условий проводили согласно обычным условиям.
Далее схема настоящего изобретения будет объяснена ниже в сочетании с примерами. Специалистам в данной области техники будет понятно, что следующие примеры применяются только для иллюстрации настоящего изобретения, и их не следует рассматривать как ограничивающие объем настоящего изобретения. Если в примерах не указаны конкретные методы или условия, их осуществляют в соответствии с методами или условиями, описанными в литературе в данной области техники или в соответствии со спецификацией продукта. Реагенты и инструменты, применяемые без указания производителя, являются обычными продуктами, которые можно приобрести коммерчески.
Пример 1. Получение антитела
Мышей Balb/c (9-недельного возраста, приобретенных в Shanghai SLAC, весом приблизительно 20 г) иммунизировали очищенным рекомбинантным Fc-слитым белком внеклеточной области B7H6 (B7H6-Fc) (Fc-слитым белком внеклеточной области B7H6, аминокислотная последовательность, как указано в SEQ ID NO: 22) в качестве антигена для получения мышиного моноклонального антитела к B7H6 человека.
Мышей трижды иммунизировали очищенным антигеном и полным адъювантом Фрейнда, а иммунные реакции обнаруживали после обескровливания через хвостовую вену. Сыворотку подвергали скринингу с помощью ИФА и проточной цитометрии для получения мышей с иммуноглобулином к B7H6 человека. Спленоциты мышей с самым высоким иммуноглобулином к B7H6 извлекали и сливали с клетками мышиной миеломы SP2/0 (ATCC NO. CRL-1581). Клетки слитой гибридомы подвергали скринингу на антитела для получения мышиных мАт.
Клетки-кандидаты гибридомы культивировали до получения общего количества 106. Клетки собирали с помощью центрифугирования при 800 об/мин в течение 10 мин, а суммарную РНК выделяли с помощью набора Trizol (Invitrogen). Суммарную РНК применяли в качестве шаблона для синтеза библиотеки кДНК (Invitrogen) с помощью обратной транскрипции, а кДНК применяли в качестве шаблона для амплификации соответствующей последовательности нуклеиновых кислот вариабельной области в клетках гибридомы с помощью ПЦР. Последовательности праймеров, применяемые в реакции ПЦР-амплификации, были комплементарны первой каркасной области вариабельной области антитела или области сигнального пептида и константной области (Larrick, J.W., et al., (1990) Scand. J. Immunol., 32, 121-128 и Coloma, J.J. et al., (1991) BioTechniques, 11, 152-156). В реакционную систему объемом 50 мкл добавляли 2 мкл кДНК, 5 мкл 10 × ПЦР-буфера, 2 мкл праймеров восходящего и нисходящего потоков (5 мкмоль), 2 мкл дНТФ, 1 мкл Taq-фермента (Takara, Ex Taq) и 38 мкл H2O соответственно. Предварительную денатурацию осуществляли в течение 5 мин при 95°С и процедуру вводили в температурный цикл для ПЦР-амплификации. Условия реакции включали: денатурацию при 94°С, 30 с, отжиг при 58°С, 45 с, удлинение при 72°С, 50 с, 32 цикла, затем удлинение при 72°С, 7 мин. После секвенирования продуктов амплификации получали последовательности вариабельных областей тяжелой и легкой цепи (включая последовательности аминокислот и последовательности нуклеиновых кислот) мышиного мАт.
Пример 2. ИФА-анализ связывания мышиного антитела B7H6
Анализ ИФА применяли для обнаружения характеристик связывания антитела B7H6. Fc-слитый белок внеклеточной области B7H6 (B7H6-Fc), описанный выше, наносили в 96-луночный планшет. Силу сигнала после добавления антитела применяли для определения характеристики связывания антитела и B7H6.
B7H6-Fc-слитый белок (аминокислотная последовательность, как указано в SEQ ID NO: 22) разводили до 1 мкг/мл с помощью буфера PBS, добавляли в 96-луночный планшет в объеме 100 мкл/лунку и оставляли на ночь при 4°С. Буферный раствор PBS отсасывали из 96-луночного планшета. Планшет промывали 6 раз буферным раствором PBST (рН 7,2, PBS, содержащий 0,1% Tween 20). Добавляли 200 мкл/лунку PBS/10% BSA и инкубировали при 37°C в течение 2 часов для блокирования. Блокирующий раствор удаляли. Планшет промывали 6 раз с помощью PBST 100 мкл/лунку тестируемого антитела B7H6 разводили до соответствующей концентрации в PBST/0,05% BSA и инкубировали при 37°C в течение 1 ч. Реакционную систему удаляли. Планшет промывали 6 раз с помощью PBST Вторичное антитело к мышиному антителу, меченное HRP (пероксидазой хрена), разводили с помощью PBST/0,05% BSA по 100 мкл/лунку и инкубировали в течение 1 часа при 37°C. Планшет промывали 6 раз с помощью PBST и добавляли 80 мкл/лунку ТМБ (тетраметилбензидин). После 3 минут инкубации при комнатной температуре добавляли 80 мкл/лунку 4М серной кислоты для остановки реакции. Поглощение при 450 мм считывали с помощью ридера для микропланшетов. Результаты (ФИГ. 1) показывают, что мышиные антитела 12F5 (SEQ ID NO: 26 и SEQ ID NO: 27) и 12G4 (SEQ ID NO: 28 и SEQ ID NO: 29) по настоящему изобретению способны связываться с B7H6.
Пример 3. Анализ проточной цитометрии на связывание мышиного антитела B7H6
Анализ проточной цитометрии применяли для обнаружения характеристик связывания антитела B7H6 и сверхэкспрессии белка B7H6 (HL60-B7H6, SEQ ID NO:21; SEQ ID NO:54) в HL60-клетках (ATCC NO: CCL-240). Вектор экспрессии представляет собой pLVX-EF1a-B7H6-IRES-ZsGreen, а силу сигнала после добавления антитела применяли для определения характеристик связывания антитела и B7H6.
HEK293T-клетки высевали в шестилуночный планшет из расчета 5×105 клеток на лунку и культивировали в течение ночи в среде DMEM без диатела. Среду перед трансфекцией удаляли и добавляли 1 мл свежей среды DMEM без диатела. pLVX-EF1a-B7H6-IRES-ZsGreen (кодирующую последовательность (SEQ ID NO: 54) белка B7H6 (SEQ ID NO: 21) вставляли между сайтами рестрикционной эндонуклеазы EcoRI и BamHI вектора pLVX-EF1a-IRES-ZsGreen1), pMD2G, psPAX2 (всего 3 мкг) в соотношении 2: 1: 1 к 200 мкл бессывороточной среды DMEM и добавляли 12 мкг полиэфиримида (PEI, polysciences Co. Ltd.). После тщательного перемешивания смесь выдерживали 16 мин. Затем всю жидкость добавляли в шестилуночный планшет, засеянный HEK293T-клетками. Через 6 ч культивирования среду удаляли и добавляли свежую полную среду DMEM. Через 48 ч после трансфекции супернатант клеточной культуры собирали и пропускали через фильтр 0,45 мкм (Millipore), чтобы получить супернатант вируса. Весь супернатант вируса добавляли в 6-луночный планшет, содержащий 1 × 104 HL60-клеток, добавляли полибрен (Sigma) в конечной концентрации 4 мкг/мл и инкубировали в течение 12 ч. Затем супернатант отбрасывали и добавляли свежую полную среду RPMI1640. В результате получали HL60-B7H6-клетки.
HL60-B7H6-клетки разводили до 2 × 106/мл с помощью PBS и добавляли в пробирку EP объемом 1,5 мл по 100 мкл на пробирку. Сыворотку козы в количестве 10 мкл/пробирку добавляли в пробирку и блокировали при 4°C в течение 30 мин. Антитело B7H6 добавляли в количестве 1 мкг/пробирку и инкубировали в течение 30 мин при 4°C. В пробирку EP добавляли 1 мл PBS и центрифугировали при 3500 об/мин при 4°C в течение 5 мин. Надосадочную жидкость отбрасывали, а осадок еще раз промывали PBS. После центрифугирования супернатант отбрасывали, а клетки ресуспендировали в 100 мкл/пробирку PBS и к нему добавляли 0,1 мкл/пробирку вторичного антитела козы к мышиному антителу (Invitrogen), меченного с помощью Alexa-647, и инкубировали при 4°С в условиях отсутствия света в течение 30 мин. Содержащий клетки осадок дважды промывали с помощью PBS, а супернатант отбрасывали после центрифугирования. Клетки ресуспендировали в 200 мкл/пробирку PBS и определяли с помощью проточной цитометрии. Результат такой, как показано на ФИГ. 2, дополнительно показывает, что мышиные антитела 12F5 (SEQ ID NO: 26 и SEQ ID NO: 27), 12G4 (SEQ ID NO: 28 и SEQ ID NO: 29) по настоящему изобретению могут связывать B7H6.
Пример 4. Эксперимент по гуманизации мышиных антител
С учетом последовательности вариабельной области легкой цепи и последовательности вариабельной области тяжелой цепи антитела B7H6, выбирали гуманизированную матрицу, которая лучше всего соответствует ее не-CDR-области. Область CDR мышиного антитела трансплантировали на выбранную гуманизированную матрицу для замены области CDR гуманизированной матрицы и получения гуманизированного антитела. Затем, основываясь на трехмерной структуре мышиного антитела, осуществляли обратные мутации на встроенных остатках, остатках, которые имеют прямое взаимодействие с CDR-областью, и остатках, которые оказывают важное влияние на конформацию VL и VH, чтобы получить гуманизированное антитело. Последовательность вариабельной области тяжелой цепи 12F5 гуманизированного антитела B7H6 такая, как указано в SEQ ID NO: 17, и последовательность вариабельной области легкой цепи такая, как указано в SEQ ID NO: 18, или последовательность вариабельной области тяжелой цепи 12G4 гуманизированного антитела B7H6 такая, как указано в SEQ ID NO: 19, и последовательность вариабельной области легкой цепи такая, как указано в SEQ ID NO: 20.
Пример 5. Анализ ИФА на связывание гуманизированного антитела B7H6
Анализ ИФА применяли для определения характеристик связывания гуманизированного антитела B7H6. Fc-слитый белок внеклеточной области B7H6 (B7H6-Fc), описанный выше, наносили в 96-луночный планшет. Силу сигнала после добавления антитела применяли для определения характеристик связывания антител и B7H6.
B7H6-Fc-слитый белок (аминокислотная последовательность, как указано в SEQ ID NO: 22) разводили до 1 мкг/мл с помощью буфера PBS, добавляли в 96-луночный планшет в объеме 100 мкл/лунку и оставляли на ночь при 4°С. Буферный раствор PBS отсасывали из 96-луночного планшета. Планшет промывали 6 раз буферным раствором PBST (рН 7,2, PBS, содержащий 0,1% Tween 20). Добавляли 200 мкл/лунку PBS/10% BSA и инкубировали при 37°C в течение 2 часов для блокирования. Блокирующий раствор удаляли. Планшет промывали 6 раз с помощью PBST Тестируемое антитело B7H6, разбавленное PBST/0,05% BSA до соответствующей концентрации, добавляли по 100 мкл/лунку и инкубировали при 37°C в течение 1 часа. Реакционную систему удаляли. Планшет промывали 6 раз с помощью PBST Мышиное вторичное антитело к IgG человека (Fab-специфическое) (Sigma), меченное HRP (пероксидазой хрена), разводили с помощью PBST/0,05% BSA по 100 мкл/лунку и инкубировали в течение 1 часа при 37°C. Планшет промывали 6 раз с помощью PBST и добавляли 80 мкл/лунку ТМБ (тетраметилбензидин). После 3 минут инкубации при комнатной температуре и добавляли 80 мкл/лунку 4М серной кислоты для остановки реакции. Поглощение при 450 мм считывали с помощью ридера для микропланшетов. Результаты (ФИГ. 3) показывают, что гуманизированные антитела h12F5 (SEQ ID NO: 30 и SEQ ID NO: 31), h12G4 (SEQ ID NO: 32 и SEQ ID NO: 33) по настоящему изобретению могут связывать B7H6.
Пример 6. Анализ проточной цитометрии на связывание гуманизированного антитела B7H6
Анализ проточной цитометрии применяли для обнаружения характеристик связывания антитела B7H6. Белок B7H6 (HL60-B7H6) сверхэкспрессировали в HL60-клетках (ATCC № CCL-240) (как показано в примере 3), а силу сигнала после добавления антитела применяли для определения характеристик связывания антитела и B7H6.
HL60-B7H6-клетки разводили до 2 × 106/мл с помощью PBS и добавляли в пробирку EP объемом 1,5 мл в объеме 100 мкл на пробирку. Туда добавляли 10 мкл/пробирку сыворотки мыши и блокировали при 4°C в течение 30 минут. Гуманизированное антитело B7H6 добавляли в количестве 1 мкг/пробирку и инкубировали в течение 30 мин при 4°C. В пробирку EP добавляли 1 мл PBS и центрифугировали при 3500 об/мин при 4°C в течение 5 мин. Надосадочную жидкость отбрасывали, а осадок еще раз промывали PBS. После центрифугирования супернатант отбрасывали. Клетки ресуспендировали в 100 мкл/пробирку PBS, к ним добавляли 1 мкл/пробирку меченного Alexa-647 мышиного вторичного антитела к IgG-Fc человека (Biolegend) и инкубировали при 4°C в условиях, исключающих свет, в течение 30 мин. Содержащий клетки осадок дважды промывали с помощью PBS, а супернатант отбрасывали после центрифугирования. Клетки ресуспендировали в 200 мкл/пробирку PBS и определяли с помощью проточной цитометрии. Результат такой, как показано на ФИГ. 4, дополнительно показывает, что гуманизированные антитела h12F5 (SEQ ID NO: 30 и SEQ ID NO: 31), h12G4 (SEQ ID NO: 32 и SEQ ID NO: 33) настоящего изобретения могут связываться с B7H6.
Пример 7. Анализ проточной цитометрии на связывание гуманизированного антитела B7H6
Анализ проточной цитометрии применяли для обнаружения характеристик связывания гуманизированного антитела B7H6. Белок B7H6 яванского макака (CHO-K1-макака-B7H6) сверхэкспрессировали в CHO-K1-клетках (ATCC № CCL-240). Силу сигнала после добавления антитела применяли для определения характеристик связывания антитела и B7H6 яванского макака.
HEK293T-клетки высевали в шестилуночный планшет из расчета 5×105 клеток/лунка и культивировали в течение ночи в среде DMEM без диатела. Среду перед трансфекцией удаляли и добавляли 1 мл свежей среды DMEM без диатела. pLVX-EF1a-cynoB7H6-IRES-ZsGreen (кодирующую последовательность (SEQ ID NO: 57) белка B7H6 макака (SEQ ID NO: 24) вставляли между сайтами рестрикционной эндонуклеазы EcoRI и BamHI вектора pLVX-EF1a-IRES-ZsGreen1), pMD2G, psPAX2 (всего 3 мкг) в соотношении 2: 1: 1 к 200 мкл бессывороточной среды DMEM и добавляли 12 мкг полиэфиримида (PEI, polysciences Co. Ltd.). После тщательного перемешивания смесь выдерживали 16 мин. Затем всю жидкость добавляли в шестилуночный планшет, засеянный HEK293T-клетками. Через 6 ч культивирования среду удаляли и добавляли свежую полную среду DMEM. Через 48 ч после трансфекции супернатант клеточной культуры собирали и пропускали через фильтр 0,45 мкм (Millipore), чтобы получить супернатант вируса. Весь супернатант вируса добавляли в 6-луночный планшет, содержащий 1 × 104 CHO-K1-клеток, добавляли полибрен (Sigma) в конечной концентрации 4 мкг/мл и культивировали в течение 12 ч. Затем супернатант отбрасывали и добавляли свежую полную среду RPMI1640. Полученные клетки представляли собой B7H6-клетки CHO-K1-макака.
B7H6-клетки CHO-K1-макака разводили до 2 × 106/мл с помощью PBS и добавляли в пробирку EP объемом 1,5 мл в объеме 100 мкл на пробирку. Туда добавляли 10 мкл/пробирку сыворотки мыши и блокировали при 4°C в течение 30 минут. Добавляли 1 мкг/пробирку гуманизированного антитела B7H6 и инкубировали в течение 30 минут при 4°C. В пробирку EP добавляли 1 мл PBS и центрифугировали при 3500 об/мин при 4°C в течение 5 мин. Надосадочную жидкость отбрасывали, а осадок еще раз промывали PBS. После центрифугирования супернатант отбрасывали. Клетки ресуспендировали в 100 мкл/пробирку PBS, к ним добавляли 1 мкл/пробирку меченного Alexa-647 мышиного вторичного антитела к IgG-Fc человека (Biolegend) и инкубировали при 4°C в месте, защищенном от света, в течение 30 мин. Содержащий клетки осадок дважды промывали с помощью PBS, а супернатант отбрасывали после центрифугирования. Клетки ресуспендировали в 200 мкл/пробирку PBS и определяли с помощью проточной цитометрии. Результат показан на ФИГ. 5, дополнительно демонстрирующий, что антитела h12F5, h12G4 по настоящему изобретению могут связываться с B7H6 макака.
Пример 8. Анализ ИФА на связывание гуманизированного антитела B7H6
Анализ ИФА применяли для определения характеристик связывания гуманизированного антитела B7H6. Внеклеточный Fc-слитый белок B7H6 яванского макака (cynoB7H6-Fc) наносили в 96-луночный планшет. Силу сигнала после добавления антитела применяли для определения характеристик связывания антитела и B7H6 макака.
Слитый белок cynoB7H6-Fc (аминокислотная последовательность, как указано в SEQ ID NO: 23) разводили до 1 мкг/мл с помощью буфера PBS, добавляли в 96-луночный планшет в объеме 100 мкл/лунку и оставляли на ночь при 4°С. Буферный раствор PBS отсасывали из 96-луночного планшета. Планшет промывали 6 раз буферным раствором PBST (рН 7,2, PBS, содержащий 0,1% Tween 20). Добавляли 200 мкл/лунку PBS/10% BSA и инкубировали при 37°C в течение 2 часов для блокирования. Блокирующий раствор удаляли. Планшет промывали 6 раз с помощью PBST Тестируемое антитело B7H6, которое разбавляли с помощью PBST/0,05% BSA до соответствующей концентрации, добавляли по 100 мкл/лунку и инкубировали при 37°C в течение 1 часа. Реакционную систему удаляли. Планшет промывали 6 раз с помощью PBST Мышиное вторичное антитело к IgG человека (Fab-специфическое) (Sigma), меченное HRP (пероксидазой хрена), разводили с помощью PBST/0,05% BSA по 100 мкл/лунку и инкубировали в течение 1 часа при 37°C. Планшет промывали 6 раз с помощью PBST и добавляли 80 мкл/лунку ТМБ (тетраметилбензидин). После 3 минут инкубации при комнатной температуре добавляли 80 мкл/лунку 4М серной кислоты для остановки реакции. Поглощение при 450 мм считывали с помощью ридера для микропланшетов. Результаты (ФИГ. 6) показывают, что гуманизированное антитело h12G4 по настоящему изобретению может связываться с B7H6 макака.
Пример 9. Аффинность связывания и кинетические эксперименты in vitro
Способ Biacore широко известен как объективный способ определения взаимной аффинности и кинетики связывания белков. Аффинность и кинетика связывания антитела B7H6 по настоящему изобретению анализировали и характеризировали с помощью Biacore T200.
Fc-слитый белок внеклеточного сегмента B7H6 (B7H6-Fc) ковалентно прикрепляли к чипу CM5 (GE) с помощью стандартных способов аминосочетания. Затем в каждом цикле вводили серию градиентов концентрации антитела B7H6, разведенного в PBS, и регенерировали 10 мМ раствором NaOH. Кинетику связывания антиген-антитело отслеживали в течение 3 минут, а кинетику диссоциации отслеживали в течение 10 минут, и полученные данные анализировали с помощью модели связывания 1: 1 (Ленгмюра) с помощью программного обеспечения GE BIAevaluation. Определенные таким образом значения KD составили 2,2 нМ для мышиного 12F5 и 0,15 нМ для мышиного 12G4.
Пример 10. Скрининг способности антитела способствовать связыванию B7H6 с NKp30.
Антитело B7H6 может стимулировать сигнальный путь B7H6 и его рецептор NKp30 путем связывания с внеклеточным доменом B7H6. Анализ проточной цитометрии применяли для обнаружения усиления связывания антитела B7H6 с рецептором NKp30.
HL60-B7H6-клетки (такие же, как указано выше) разбавляли с помощью PBS до 2 × 106/мл, добавляли в пробирку EP объемом 1,5 мл в объеме 100 мкл/пробирку, туда добавляли 10 мкл/пробирку сыворотки мыши и блокировали при 4°С в течение 30 мин. Fc-слитый белок внеклеточной области NKp30 (NKp30-Fc, SEQ ID NO: 25, экспрессированный в этой лаборатории) добавляли в дозе 4 мкг/пробирку и инкубировали в течение 30 минут при 4°C. Добавляли антитело B7H6 и инкубировали при 4°C в течение 30 мин. В пробирку EP добавляли 1 мл PBS и центрифугировали при 3500 об/мин при 4°C в течение 5 мин. Супернатант отбрасывали и осадок еще раз промывали с помощью PBS. После центрифугирования супернатант отбрасывали. Клетки ресуспендировали в 100 мкл/пробирку PBS, к ним добавляли 1 мкл/пробирку меченного 647 мышиного вторичного антитела к антителу человека (Biolegend) и инкубировали при 4°C в условиях, исключающих свет, в течение 30 мин. Содержащий клетки осадок дважды промывали с помощью PBS, а супернатант отбрасывали после центрифугирования. Клетки ресуспендировали в 200 мкл/пробирку PBS и определяли с помощью проточной цитометрии. Результаты показаны на ФИГ. 7. Как видно, мышиное антитело 12F5 настоящего изобретения может способствовать связыванию B7H6 с рецептором NKp30.
Пример 11. Определение комплемент-зависимой цитотоксичности
Анализ комплементзависимой цитотоксичности применяли для обнаружения эффекта уничтожения антитела B7H6 на опухолевые клетки. Среди них в качестве опухолевых клеток применяли HL60-B7H6-клетки.
(1) Опухолевые клетки ресуспендировали в бессывороточной среде RPMI-1640 и подсчитывали. Клетки разбавляли до 4× 105/мл в полной среде RPMI-1640. Разбавленные клетки добавляли в 96-луночный круглодонный планшет в объеме 25 мкл/лунку.
(2) Антитело B7H6 или контрольный мышиный IgG разводили в бессывороточной среде RPMI-1640 и добавляли разведенное антитело B7H6 или мышиный IgG в 96-луночный круглодонный планшет в объеме 25 мкл/лунку.
(3) Комплемент кролика (Cedarlane) растворяли в 1 мл сверхчистой воды, затем добавляли 1 мл бессывороточной культуральной среды RPMI-1640 и хорошо перемешивали как рабочий раствор. Рабочий раствор комплемента добавляли в 96-луночный круглодонный планшет в объеме 40 мкл/лунку. Клетки инкубировали при 37°C в течение 30 мин.
(4) Полную среду RPMI-1640 добавляли в 96-луночный круглодонный планшет в объеме 110 мкл/лунку, а 7-AAD (BD) добавляли в 96-луночный круглодонный планшет в объеме 1 мкл/лунку и хорошо перемешивали. Всю жидкость из лунки переносили в пробирку для проточной цитометрии и определяли с помощью проточного цитометра. Результаты показаны на ФИГ. 8. Как видно, мышиное антитело B7H6 12F5 настоящего изобретения имеет комплемент-зависимую цитотоксичность.
Пример 12. Антитело B7H6 стимулирует противораковую способность у мышей
Тест на эффективность in vivo применяли для выявления функции антитела B7H6 в стимулировании противораковой терапии у голых мышей. Среди них в качестве опухолевых клеток применяли клетки острого миелоидного лейкоза U-937 (АТСС № CRL-1953.2).
(1) Голым мышам подкожно имплантировали в правый бок 1,5× 106 клеток U-937 на мышь, а затем рандомизировали на группы.
(2) В дни 5, 7, 9, 11 и 13 мышам внутрибрюшинно делали инъекции 1 мг антитела на мышь.
(3) Объемы опухолей измеряли каждые 2 суток.
Результаты показаны на ФИГ. 9. Как видно, мышиное антитело 12F5 по настоящему изобретению имеет противораковую функцию.
Из приведенных выше результатов экспериментов видно, что антитело, полученное в соответствии с настоящим изобретением, способно связываться с B7H6 человека и макака; способствовать взаимодействию между B7H6 и NKp30; и способствовать противораковому действию у мышей.
Предпочтительные варианты осуществления настоящего изобретения были подробно описаны выше, но настоящее изобретение этим не ограничивается. В рамках изобретательской концепции возможен ряд простых вариантов изобретательского решения, включая любое другое подходящее сочетание отдельных признаков. Эти простые варианты и комбинации также следует рассматривать как раскрытые и как подпадающие под объем настоящего изобретения.
В описании данной спецификации описания со ссылкой на термины «один вариант осуществления», «некоторые варианты осуществления», «пример», «конкретные примеры» или «некоторые примеры» и т.д. означают, что конкретный признак, структура, материал или характеристика, описанные в связи с вариантом осуществления или примером, включены по меньшей мере в один вариант осуществления или пример настоящего изобретения. В настоящем описании схематические изображения вышеуказанных терминов не обязательно относятся к одному и тому же варианту осуществления или примеру. Кроме того, описанные конкретные признаки, структуры, материалы или характеристики могут быть скомбинированы любым подходящим образом в любом одном или более вариантах осуществления или примерах. Кроме того, специалисты в данной области техники могут интегрировать и комбинировать различные варианты осуществления или примеры, а также особенности различных вариантов осуществления или примеров, описанные в данной спецификации, не противореча друг другу.
Не смотря на то, что были показаны и описаны варианты осуществления настоящего изобретения, следует понимать, что описанные выше варианты осуществления являются иллюстративными и не должны рассматриваться как ограничивающие настоящее изобретение, и специалисты в данной области могут вносить изменения, модификации, замены и поправки в вышеупомянутые варианты осуществления, не выходя за рамки объема настоящего изобретения.
--->
<?xml version="1.0" encoding="utf-8"?>
<!DOCTYPE ST26SequenceListing PUBLIC "-//WIPO//DTD Sequence Listing
1.3//EN" "ST26SequenceListing_V1_3.dtd">
<ST26SequenceListing originalFreeTextLanguageCode="zh"
nonEnglishFreeTextLanguageCode="zh" dtdVersion="V1_3"
fileName="POI231537P-Sequence listing.xml" softwareName="WIPO
Sequence" softwareVersion="2.3.0" productionDate="2023-11-29">
<ApplicationIdentification>
<IPOfficeCode>CN</IPOfficeCode>
<ApplicationNumberText></ApplicationNumberText>
<FilingDate></FilingDate>
</ApplicationIdentification>
<ApplicantFileReference>HI5210687P</ApplicantFileReference>
<EarliestPriorityApplicationIdentification>
<IPOfficeCode>CN</IPOfficeCode>
<ApplicationNumberText>202111485380,9</ApplicationNumberText>
<FilingDate></FilingDate>
</EarliestPriorityApplicationIdentification>
<ApplicantName languageCode="en">HEFEI TG IMMUNOPHARMA CO.,
LTD.</ApplicantName>
<ApplicantNameLatin>HEFEI TG IMMUNOPHARMA CO.,
LTD.</ApplicantNameLatin>
<InventionTitle languageCode="en">АНТИТЕЛО B7H6 И ЕГО
ПРИМЕНЕНИЕ</InventionTitle>
<SequenceTotalQuantity>66</SequenceTotalQuantity>
<SequenceData sequenceIDNumber="1">
<INSDSeq>
<INSDSeq_length>8</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..8</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q1">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>GYTFTSYY</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="2">
<INSDSeq>
<INSDSeq_length>8</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..8</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q2">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>INPSNGGT</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="3">
<INSDSeq>
<INSDSeq_length>14</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..14</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q3">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>TRTLYYGNDWYFDV</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="4">
<INSDSeq>
<INSDSeq_length>5</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..5</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q4">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>SSVNY</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="5">
<INSDSeq>
<INSDSeq_length />
<INSDSeq_moltype />
<INSDSeq_division />
<INSDSeq_sequence>000</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="6">
<INSDSeq>
<INSDSeq_length>9</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..9</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q6">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>QQWSSNPVT</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="7">
<INSDSeq>
<INSDSeq_length>8</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..8</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q7">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>GYTFTDYN</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="8">
<INSDSeq>
<INSDSeq_length>8</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..8</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q8">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>INPNNGGT</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="9">
<INSDSeq>
<INSDSeq_length>13</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..13</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q9">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>ARSEVFYGNYADY</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="10">
<INSDSeq>
<INSDSeq_length>10</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..10</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q10">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>QSVDYDGDSY</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="11">
<INSDSeq>
<INSDSeq_length />
<INSDSeq_moltype />
<INSDSeq_division />
<INSDSeq_sequence>000</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="12">
<INSDSeq>
<INSDSeq_length>9</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..9</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q12">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>QQSKEDPRT</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="13">
<INSDSeq>
<INSDSeq_length>121</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..121</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q13">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>QVQLQQSGAELVKPGASVKLSCKASGYTFTSYYMYWVKQRPGQGLEWIG
EINPSNGGTNFNEKFKSKATLTVDKSSSTAYMQLSSLTSEDSAVYYCTRTLYYGNDWYFDVWGAGTTVTV
SS</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="14">
<INSDSeq>
<INSDSeq_length>106</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..106</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q14">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>QIVLTQSPAIMSASPGEKVTMTCSASSSVNYMHWYQQKSGTSPKRWIYD
TSKLASGVPARFSGSGSGTSYSLTISSMEAEDAATYYCQQWSSNPVTFGAGTKLELK</INSDSeq_seq
uence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="15">
<INSDSeq>
<INSDSeq_length>120</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..120</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q15">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>EVLLQQSGPEVVKPGASVKITCKASGYTFTDYNMDWVKQSHGKSLEWIG
DINPNNGGTLYNQKFRGRVTLIVDKSSSTAYMELRSLTSDDTAVYYCARSEVFYGNYADYWGQGTTLTVS
S</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="16">
<INSDSeq>
<INSDSeq_length>111</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..111</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q16">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>DIVLTQSPVSLAVPLGQRATISCKASQSVDYDGDSYMNWYQQKPGQPPK
LLIYAASTLHSGIPVRFSGSGSGTDFTLNIHPVEEEDAASYYCQQSKEDPRTFGGGTKLEIK</INSDSe
q_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="17">
<INSDSeq>
<INSDSeq_length>121</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..121</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q17">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>EVQLVQSGAEVKKPGASVKVSCKASGYTFTSYYMYWVRQAPGQGLEWIG
EINPSNGGTNFNEKFKSRVTLTVDKSISTAYMELSRLRSDDTAVYYCTRTLYYGNDWYFDVWGQGTTVTV
SS</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="18">
<INSDSeq>
<INSDSeq_length>106</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..106</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q18">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>EIVLTQSPDFQSVTPKEKVTITCSASSSVNYMHWYQQKPDQSPKRLIYD
TSKLASGVPSRFSGSGSGTDYTLTINSLEAEDAATYYCQQWSSNPVTFGQGTKLEIK</INSDSeq_seq
uence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="19">
<INSDSeq>
<INSDSeq_length>120</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..120</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q19">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>EVQLVQSGAEVKKPGASVKVSCKASGYTFTDYNMDWVRQAPGKGLEWIG
DINPNNGGTLYNQKFRGRVTLTVDKSISTAYMELSRLRSDDTAVYYCARSEVFYGNYADYWGQGTTVTVS
S</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="20">
<INSDSeq>
<INSDSeq_length>111</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..111</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q20">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>DIVLTQTPLSLSVTPGQPASISCKASQSVDYDGDSYMNWYLQKPGQPPQ
LLIYAASTLHSGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCQQSKEDPRTFGQGTKLEIK</INSDSe
q_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="21">
<INSDSeq>
<INSDSeq_length>454</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..454</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q21">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>MTWRAAASTCAALLILLWALTTEGDLKVEMMAGGTQITPLNDNVTIFCN
IFYSQPLNITSMGITWFWKSLTFDKEVKVFEFFGDHQEAFRPGAIVSPWRLKSGDASLRLPGIQLEEAGE
YRCEVVVTPLKAQGTVQLEVVASPASRLLLDQVGMKENEDKYMCESSGFYPEAINITWEKQTQKFPHPIE
ISEDVITGPTIKNMDGTFNVTSCLKLNSSQEDPGTVYQCVVRHASLHTPLRSNFTLTAARHSLSETEKTD
NFSIHWWPISFIGVGLVLLIVLIPWKKICNKSSSAYTPLKCILKHWNSFDTQTLKKEHLIFFCTRAWPSY
QLQDGEAWPPEGSVNINTIQQLDVFCRQEGKWSEVPYVQAFFALRDNPDLCQCCRIDPALLTVTSGKSID
DNSTKSEKQTPREHSDAVPDAPILPVSPIWEPPPATTSTTPVLSSQPPTLLLPLQ</INSDSeq_seque
nce>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="22">
<INSDSeq>
<INSDSeq_length>471</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..471</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q22">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>DLKVEMMAGGTQITPLNDNVTIFCNIFYSQPLNITSMGITWFWKSLTFD
KEVKVFEFFGDHQEAFRPGAIVSPWRLKSGDASLRLPGIQLEEAGEYRCEVVVTPLKAQGTVQLEVVASP
ASRLLLDQVGMKENEDKYMCESSGFYPEAINITWEKQTQKFPHPIEISEDVITGPTIKNMDGTFNVTSCL
KLNSSQEDPGTVYQCVVRHASLHTPLRSNFTLTAARHSLSETEKTDNFSLEPKSCDKTHTCPPCPAPELL
GGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSV
LTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPS
DIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSP
GK</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="23">
<INSDSeq>
<INSDSeq_length>466</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..466</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q23">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>DLKVEMMARGIQATRLNDSVTISCKVIYSQPLNITSMGITWFRKSLTLD
KEVKVFEFFGDHQKAFRPGANVSLWRLKSGDASLKLPGVQLEEAGEYRCEVVVTPLKAQGTVQLKVVASP
TSRLFQDQAVVKENEGKYMCESSRFYPKDINITWEKWTQKSPHHVVISENVITGPTIKNMDGTFNITSYL
KLNSSQEDPGTVYRCVIRHESLHTPVSIDFILTAPQQSLSEPEKTDPKSCDKTHTCPPCPAPELLGGPSV
FLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLH
QDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVE
WESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK</I
NSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="24">
<INSDSeq>
<INSDSeq_length>296</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..296</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q24">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>MAWRAASSACAAPLLLWCALMTAGDLKVEMMARGIQATRLNDSVTISCK
VIYSQPLNITSMGITWFRKSLTLDKEVKVFEFFGDHQKAFRPGANVSLWRLKSGDASLKLPGVQLEEAGE
YRCEVVVTPLKAQGTVQLKVVASPTSRLFQDQAVVKENEGKYMCESSRFYPKDINITWEKWTQKSPHHVV
ISENVITGPTIKNMDGTFNITSYLKLNSSQEDPGTVYRCVIRHESLHTPVSIDFILTAPQQSLSEPEKTD
IFSIYGWLFSFIAAGLILLIVLIHWKKVPLREEEGRN</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="25">
<INSDSeq>
<INSDSeq_length>356</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..356</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q25">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>WVSQPPEIRTLEGSSAFLPCSFNASQGRLAIGSVTWFRDEVVPGKEVRN
GTPEFRGRLAPLASSRFLHDHQAELHIRDVRGHDASIYVCRVEVLGLGVGTGNGTRLVVEKEHPQLGENL
YFQSLEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVD
GVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYT
LPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQG
NVFSCSVMHEALHNHYTQKSLSLSPGK</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="26">
<INSDSeq>
<INSDSeq_length>451</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..451</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q26">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>QVQLQQSGAELVKPGASVKLSCKASGYTFTSYYMYWVKQRPGQGLEWIG
EINPSNGGTNFNEKFKSKATLTVDKSSSTAYMQLSSLTSEDSAVYYCTRTLYYGNDWYFDVWGAGTTVTV
SSAKTTAPSVYPLAPVCGDTTGSSVTLGCLVKGYFPEPVTLTWNSGSLSSGVHTFPAVLQSDLYTLSSSV
TVTSSTWPSQSITCNVAHPASSTKVDKKIEPRGPTIKPCPPCKCPAPNLLGGPSVFIFPPKIKDVLMISL
SPIVTCVVVDVSEDDPDVQISWFVNNVEVHTAQTQTHREDYNSTLRVVSALPIQHQDWMSGKEFKCKVNN
KDLPAPIERTISKPKGSVRAPQVYVLPPPEEEMTKKQVTLTCMVTDFMPEDIYVEWTNNGKTELNYKNTE
PVLDSDGSYFMYSKLRVEKKNWVERNSYSCSVVHEGLHNHHTTKSFSRTPGK</INSDSeq_sequence
>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="27">
<INSDSeq>
<INSDSeq_length>213</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..213</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q27">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>QIVLTQSPAIMSASPGEKVTMTCSASSSVNYMHWYQQKSGTSPKRWIYD
TSKLASGVPARFSGSGSGTSYSLTISSMEAEDAATYYCQQWSSNPVTFGAGTKLELKRADAAPTVSIFPP
SSEQLTSGGASVVCFLNNFYPKDINVKWKIDGSERQNGVLNSWTDQDSKDSTYSMSSTLTLTKDEYERHN
SYTCEATHKTSTSPIVKSFNRNEC</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="28">
<INSDSeq>
<INSDSeq_length>450</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..450</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q28">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>EVLLQQSGPEVVKPGASVKITCKASGYTFTDYNMDWVKQSHGKSLEWIG
DINPNNGGTLYNQKFRGRVTLIVDKSSSTAYMELRSLTSDDTAVYYCARSEVFYGNYADYWGQGTTLTVS
SAKTTAPSVYPLAPVCGDTTGSSVTLGCLVKGYFPEPVTLTWNSGSLSSGVHTFPAVLQSDLYTLSSSVT
VTSSTWPSQSITCNVAHPASSTKVDKKIEPRGPTIKPCPPCKCPAPNLLGGPSVFIFPPKIKDVLMISLS
PIVTCVVVDVSEDDPDVQISWFVNNVEVHTAQTQTHREDYNSTLRVVSALPIQHQDWMSGKEFKCKVNNK
DLPAPIERTISKPKGSVRAPQVYVLPPPEEEMTKKQVTLTCMVTDFMPEDIYVEWTNNGKTELNYKNTEP
VLDSDGSYFMYSKLRVEKKNWVERNSYSCSVVHEGLHNHHTTKSFSRTPGK</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="29">
<INSDSeq>
<INSDSeq_length>218</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..218</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q29">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>DIVLTQSPVSLAVPLGQRATISCKASQSVDYDGDSYMNWYQQKPGQPPK
LLIYAASTLHSGIPVRFSGSGSGTDFTLNIHPVEEEDAASYYCQQSKEDPRTFGGGTKLEIKRADAAPTV
SIFPPSSEQLTSGGASVVCFLNNFYPKDINVKWKIDGSERQNGVLNSWTDQDSKDSTYSMSSTLTLTKDE
YERHNSYTCEATHKTSTSPIVKSFNRNEC</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="30">
<INSDSeq>
<INSDSeq_length>451</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..451</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q30">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>EVQLVQSGAEVKKPGASVKVSCKASGYTFTSYYMYWVRQAPGQGLEWIG
EINPSNGGTNFNEKFKSRVTLTVDKSISTAYMELSRLRSDDTAVYYCTRTLYYGNDWYFDVWGQGTTVTV
SSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSV
VTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISR
TPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSN
KALPAPIEKTISKAKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTP
PVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK</INSDSeq_sequence
>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="31">
<INSDSeq>
<INSDSeq_length>213</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..213</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q31">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>EIVLTQSPDFQSVTPKEKVTITCSASSSVNYMHWYQQKPDQSPKRLIYD
TSKLASGVPSRFSGSGSGTDYTLTINSLEAEDAATYYCQQWSSNPVTFGQGTKLEIKRTVAAPSVFIFPP
SDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHK
VYACEVTHQGLSSPVTKSFNRGEC</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="32">
<INSDSeq>
<INSDSeq_length>450</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..450</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q32">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>EVQLVQSGAEVKKPGASVKVSCKASGYTFTDYNMDWVRQAPGKGLEWIG
DINPNNGGTLYNQKFRGRVTLTVDKSISTAYMELSRLRSDDTAVYYCARSEVFYGNYADYWGQGTTVTVS
SASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVV
TVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRT
PEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNK
ALPAPIEKTISKAKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPP
VLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="33">
<INSDSeq>
<INSDSeq_length>218</INSDSeq_length>
<INSDSeq_moltype>АК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..218</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>белок</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q33">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>DIVLTQTPLSLSVTPGQPASISCKASQSVDYDGDSYMNWYLQKPGQPPQ
LLIYAASTLHSGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCQQSKEDPRTFGQGTKLEIKRTVAAPSV
FIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKAD
YEKHKVYACEVTHQGLSSPVTKSFNRGEC</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="34">
<INSDSeq>
<INSDSeq_length>24</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..24</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q34">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gggtacacatttaccagctactat</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="35">
<INSDSeq>
<INSDSeq_length>24</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..24</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q35">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>attaatccatctaacgggggaacc</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="36">
<INSDSeq>
<INSDSeq_length>42</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..42</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q36">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>actaggaccctgtattacggtaacgactggtatttcgatgtg</INSDS
eq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="37">
<INSDSeq>
<INSDSeq_length>15</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..15</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q37">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>tcttctgttaactat</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="38">
<INSDSeq>
<INSDSeq_length />
<INSDSeq_moltype />
<INSDSeq_division />
<INSDSeq_sequence>000</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="39">
<INSDSeq>
<INSDSeq_length>27</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..27</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q40">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>cagcaatggagcagtaatccagtcaca</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="40">
<INSDSeq>
<INSDSeq_length>24</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..24</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q41">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gggtacacatttacagactacaat</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="41">
<INSDSeq>
<INSDSeq_length>24</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..24</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q42">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>atcaatccaaacaatggcggtacc</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="42">
<INSDSeq>
<INSDSeq_length>39</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..39</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q43">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gctcgctctgaagtcttttatgggaattatgctgactac</INSDSeq_
sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="43">
<INSDSeq>
<INSDSeq_length>30</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..30</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q44">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>cagagcgtggactatgatggcgacagctat</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="44">
<INSDSeq>
<INSDSeq_length />
<INSDSeq_moltype />
<INSDSeq_division />
<INSDSeq_sequence>000</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="45">
<INSDSeq>
<INSDSeq_length>27</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..27</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q46">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>cagcagagcaaagaggatcctagaacc</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="46">
<INSDSeq>
<INSDSeq_length>363</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..363</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q47">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>caggtgcagttgcaacaatctggtgcagagctggtgaaacctggtgcat
cagtgaagctttcatgtaaagcttccgggtacacatttaccagctactatatgtactgggttaagcagcg
tcctggacagggtctggagtggatcggcgagattaatccatctaacgggggaaccaactttaacgaaaag
ttcaagtctaaggctacactgacagtcgataaatcctcatccaccgcctacatgcagctctcttctctga
cttcagaggacagcgccgtgtactactgcactaggaccctgtattacggtaacgactggtatttcgatgt
gtggggtgccggtacaacagtgaccgtgtcctca</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="47">
<INSDSeq>
<INSDSeq_length>318</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..318</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q48">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>caaatcgtgctgacccagtctccagcaataatgtccgcatctcctggtg
agaaagtgaccatgacttgttcagcttcctcttctgttaactatatgcactggtaccaacagaagtctgg
cacctccccaaagcggtggatttatgacacctccaagctggctagcggggtacccgcaaggttctccggt
tcaggcagcggcacttcttactccctgactattagctctatggaggcagaggatgccgctacctactatt
gccagcaatggagcagtaatccagtcacatttggggccggaaccaagctggagctgaag</INSDSeq_s
equence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="48">
<INSDSeq>
<INSDSeq_length>360</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..360</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q49">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gaagttctgcttcagcagtctggcccagaagttgttaagccaggagcct
ccgtgaaaattacttgcaaggcctccgggtacacatttacagactacaatatggactgggtgaagcagtc
ccatggaaagagtctggaatggatcggcgatatcaatccaaacaatggcggtaccctctataaccagaaa
tttcgcggacgtgtgaccttgatcgtcgacaaaagtagttctactgcctacatggagctgcgcagcctga
ctagtgacgacaccgccgtctactattgcgctcgctctgaagtcttttatgggaattatgctgactactg
gggccagggtaccactttgaccgtctccagt</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="49">
<INSDSeq>
<INSDSeq_length>333</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..333</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q50">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gacattgtgctgactcagagtcctgtaagtctggcagttcccctcggcc
aaagagctaccattagttgtaaggcttcccagagcgtggactatgatggcgacagctatatgaattggta
tcaacagaagccaggacagccacccaagctgctgatctacgccgcctccaccctgcattcaggtatccct
gtgcgattttctggtagtggctccggcacagatttcaccctgaatatccatccagttgaggaggaggatg
ctgcctcttactactgtcagcagagcaaagaggatcctagaaccttcggcggtggcactaagctggaaat
taag</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="50">
<INSDSeq>
<INSDSeq_length>363</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..363</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q51">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gaagttcaactggttcagagcggagctgaggtaaagaagccaggtgcca
gcgtgaaagttagttgcaaggcatccggatacactttcactagctattatatgtattgggtgcgacaggc
cccagggcaaggtttggagtggatcggagagatcaatccttcaaatggcggcacaaatttcaacgaaaag
ttcaaatctcgcgtgactctgacagtggacaagtccatctccacagcatatatggagctgagccggctta
gatccgatgacactgctgtctactattgtacaagaacactgtactatggcaacgactggtacttcgatgt
ctggggacaggggaccactgtgaccgtctccagt</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="51">
<INSDSeq>
<INSDSeq_length>318</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..318</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q52">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gaaatcgtgctgacccagagcccagatttccagagtgtcacaccaaagg
agaaggtaacaattacatgcagtgccagcagtagcgtgaactatatgcattggtatcagcagaaacccga
tcagtcccctaagcgactgatctacgatacctccaagctggccagcggtgttccaagtaggttctctggc
agcgggtctgggacagactacactctcactatcaactctctggaagctgaggatgctgctacttattatt
gccagcagtggagctcaaatcccgttacctttggccagggtaccaagctcgaaattaaa</INSDSeq_s
equence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="52">
<INSDSeq>
<INSDSeq_length>360</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..360</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q53">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gaagtgcagcttgtacagagtggagcagaggtcaagaaaccaggagctt
ccgtgaaggtgagctgcaaggcctccggctatacctttactgattacaacatggactgggtccgtcaggc
tcctggaaaaggactggagtggattggtgacattaatcctaataacggcggcacactttacaatcagaag
tttcgtggtagagttacactgactgtggataaatcaatcagcaccgcctatatggagctgtcccgactgc
ggtccgacgatactgcagtgtattactgcgccaggtcagaggtgttttacggtaactacgcagactattg
gggccaggggacaacagtgacagtcagcagc</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="53">
<INSDSeq>
<INSDSeq_length>333</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..333</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q54">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gacatagtattgacccagacaccattgtctttgagcgttaccccaggcc
agccagcttcaatatcttgcaaggcctctcagtccgtcgactatgatggcgattcctacatgaattggta
cctccaaaagccaggccaaccaccacagctgttgatttatgccgcttctacactccacagtggcgtgccc
gatcgattttcaggatccggctcagggaccgatttcacccttaagatttctcgagtggaagccgaggatg
tgggcgtgtattactgccagcagagcaaagaggatcctagaacttttggccagggaaccaagctggagat
taaa</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="54">
<INSDSeq>
<INSDSeq_length>1365</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..1365</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q55">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>atgacgtggagggctgccgcctccacgtgcgcggcgctcctgattctgc
tgtgggcgctgacgaccgaaggtgatctgaaagtagagatgatggcaggggggactcagatcacacccct
gaatgacaatgtcaccatattctgcaatatcttttattcccaacccctcaacatcacgtctatgggtatc
acctggttttggaagagtctgacgtttgacaaagaagtcaaagtctttgaattttttggagatcaccaag
aggcattccgacctggagccattgtgtctccatggaggctgaagagtggggacgcctcactgcggctgcc
tggaatccagctggaggaagcaggagagtaccgatgtgaggtggtggtcacccctctgaaggcacaggga
acagtccagcttgaagttgtggcttccccagccagcagattgttgctggatcaagtgggcatgaaagaga
atgaagacaaatatatgtgtgagtcaagtgggttctacccagaggctattaatataacatgggagaagca
gacccagaagtttccccatcccatagagatttctgaggatgtcatcactggtcccaccatcaagaatatg
gatggcacatttaatgtcactagctgcttgaagctgaactcctctcaggaagaccctgggactgtctacc
agtgtgtggtacggcatgcgtccttgcatacccccttgaggagcaactttaccctgactgctgctcggca
cagtctttctgaaactgagaagacagataatttttccattcattggtggcctatttcattcattggtgtt
ggactggttttattaattgttttgattccttggaaaaagatatgtaacaaatcatcttcagcctatactc
ctctcaagtgcattctgaaacactggaactcctttgacactcagactctgaagaaagagcacctcatatt
cttttgcactcgggcatggccgtcttaccagctgcaggatggggaggcttggcctcctgagggaagtgtt
aatattaatactattcaacaactagatgttttctgcagacaggagggcaaatggtccgaggttccttatg
tgcaagccttctttgccttgcgagacaacccagatctttgtcagtgttgtagaattgaccctgctctcct
aacagttacatcaggcaagtccatagatgataattccacaaagtctgagaaacaaacccctagggaacac
tcggatgcagttccggatgccccaatccttcctgtctcccctatctgggaacctcctccagccacaacat
caacaactccagttctatcctcccaacccccaactttactgttacccctacagtaa</INSDSeq_sequ
ence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="55">
<INSDSeq>
<INSDSeq_length>1413</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..1413</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q56">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gacctgaaggtggaaatgatggcagggggtactcagataacacctctca
atgataatgtcacaattttttgtaacatcttttactctcagccacttaatatcacctccatgggaatcac
ttggttttggaagtcattgaccttcgataaggaggtgaaggtatttgagtttttcggggaccaccaggaa
gctttccgaccaggagcaattgtgtccccttggcgcttgaagtctggcgacgccagcttgagacttcctg
gaatccaattggaggaagctggggagtacagatgtgaggttgtcgtgactcctctgaaagctcagggtac
cgtgcagttggaggttgtcgcctcacccgcttcccggcttctgctggaccaggttggaatgaaggagaac
gaagataagtatatgtgcgagagttccggattttatcccgaggccatcaacattacatgggagaaacaga
cccaaaagtttcctcaccccattgaaatcagcgaggatgtgattaccggacccaccattaaaaatatgga
tggcactttcaacgttacctcatgtttgaaattgaacagtagtcaggaagaccctggaacagtctatcag
tgcgtcgtgagacacgcatccctccatacacctctgcgttcaaacttcactctcactgccgccaggcata
gcctgagcgagaccgagaagaccgataacttctctctggagcctaagagctgcgacaagacccacacctg
tccaccctgtccagcccctgagctgctgggggggccctccgtgttccttttccctccaaaacccaaggac
accctgatgatctctagaacccccgaagtcacatgcgtggtggtagatgtctctcatgaggaccccgagg
tgaagttcaattggtacgtcgatggagtggaggtgcataacgccaagactaagcctagggaagagcagta
taattcaacctaccgcgtcgtgtctgtgctcaccgtgctgcatcaagactggctcaacggcaaagaatac
aagtgcaaggtctctaacaaggctctgcccgctcccatcgaaaagaccatctccaaggctaagggccaac
ccagggagccccaagtctacacactgcctccatcacgtgaagagatgactaaaaatcaagttagtttgac
ctgcttggttaagggcttctatccatctgatatagcagtcgaatgggagagcaacggccagcctgaaaac
aactacaagacaactccacccgtcttggactccgacggtagttttttcctgtactccaaactgaccgtgg
ataagagcagatggcagcagggcaacgtgttctcatgttccgtcatgcatgaagctctccacaaccacta
cacccagaagtctctgagtctctctcccggtaaa</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="56">
<INSDSeq>
<INSDSeq_length>1398</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..1398</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q57">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gatttgaaggtggagatgatggctcgaggaattcaggccaccagactca
acgacagcgtcacaatctcttgcaaagtgatctatagtcagcccctcaacataaccagtatgggaattac
ctggtttcgcaaatcactgactttggataaagaggttaaagtctttgaattttttggcgatcaccagaag
gccttcagacccggagcaaatgtgtccctgtggaggctgaagtctggcgacgctagcctgaaacttccag
gagttcagctcgaagaggccggcgagtacaggtgcgaagttgtagtaacccctctcaaagcacagggcac
cgttcagctgaaggtggtggcttcacctacttctagacttttccaggatcaggccgtggttaaggagaac
gagggcaaatatatgtgcgagtcctctcgtttttatcccaaagacatcaatatcacctgggagaaatgga
cacagaaatcacctcaccacgttgtaattagcgagaacgtgatcacaggccccacaataaagaacatgga
cggaactttcaatataacctcctacttgaagctgaactcctctcaagaagatcctggcactgtgtataga
tgtgtgattaggcacgagagcctccacacacccgtctctattgacttcatattgactgcaccacagcagt
ctctgtctgaaccagaaaagaccgatccaaaatcctgtgacaagactcatacatgtcctccttgtccagc
accagagctgcttggtggccctagcgtgttcctgttccctcccaagcctaaggacaccctgatgatttca
agaacccccgaggtgacttgtgtggtcgtggatgtgagccacgaggatcctgaagtcaaattcaattggt
acgttgatggcgtggaggtgcacaatgccaaaaccaagccacgagaggagcagtacaacagcacctacag
agtggtgtctgtgctgaccgtgttgcatcaggactggcttaatggaaaagaatacaagtgtaaggtctcc
aataaagctctccctgccccaatcgagaagactatctctaaggctaaaggacagccaagggaaccccagg
tttacacactgcccccaagccgagatgaattgacaaaaaatcaggtttccttgacctgcctggtgaaggg
tttctacccatctgatatcgccgttgagtgggagagcaatggacagcctgagaacaattacaaaacaacc
cctcctgtgttggatagtgatggcagcttctttctgtattctaagcttaccgtggataagtctagatggc
agcaaggaaatgtgttttcctgcagcgtaatgcacgaagcacttcataatcattatacacagaagtctct
ctctcttagcccagggaag</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="57">
<INSDSeq>
<INSDSeq_length>888</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..888</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q58">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>atggcatggagagctgcatcttccgcttgtgctgctcctttgcttctgt
ggtgtgctttgatgactgccggagacctgaaagtcgaaatgatggctagaggaatccaagctactcgcct
gaatgatagtgtgacaatctcatgtaaagtaatttattcccagcctttgaacatcacctctatgggcatt
acctggtttcgcaagagtctcaccctggataaagaggtaaaagtgttcgagttctttggagaccatcaaa
aagctttccgccctggagctaatgtgagcctttggcgcctgaagagtggagacgccagtctgaaattgcc
tggtgtgcagctcgaagaggctggtgaatataggtgcgaagtggtggtgactcctctgaaggctcagggg
accgtccagcttaaagtggtggccagtcctaccagtcgcctgtttcaggaccaggcagtggtcaaggaga
acgaaggtaaatatatgtgtgaatcttctcgtttctacccaaaggatattaatatcacctgggagaagtg
gacccaaaagagcccacaccatgtggtcatctcagagaatgtgatcaccggccccaccatcaagaatatg
gatggaactttcaatatcacatcttacctgaagctgaattcaagccaagaggatcctggaaccgtatata
ggtgcgtcatcagacatgagagcctccacacacccgtgagcatcgacttcattctgacagctccacagca
gagtctcagtgaacctgagaaaacagacattttttctatctatgggtggcttttttcttttatcgccgct
gggctgatcttgctgatcgtgctcatccactggaaaaaagtgccactgcgagaagaagaaggcagaaac<
/INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="58">
<INSDSeq>
<INSDSeq_length>1068</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..1068</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q59">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>tgggtgagtcaaccacctgagattagaactctggagggcagctctgcat
tcttgccatgctccttcaacgcaagtcaggggaggctggctatcggttccgtaacatggtttagggatga
ggtggtgccaggaaaagaagtgaggaacggaaccccagagttcagaggaagactggcccctctggcaagt
tcccgctttctgcatgatcaccaagccgaacttcacattcgcgacgtcagggggcacgacgcatctatat
acgtgtgcagagtggaggtgcttggtctgggtgtgggcaccggaaacggcactcgactcgtcgttgagaa
agagcatccacagctgggagaaaatctgtactttcagagcctcgaacctaagtcttgtgacaagacccat
acctgtcctccctgtcctgctcctgaactgttggggggcccctctgtgttcctgttccctccaaagccca
aggacacactgatgattagcaggacaccagaagtcacatgtgtcgtggttgatgtgtcccacgaggatcc
cgaggttaaatttaattggtatgtggacggtgttgaggtgcataacgccaagaccaagcctcgagaagag
cagtacaattccacttatagggtagtctccgtattgaccgtgctccatcaggactggctgaatggcaaag
agtacaaatgcaaggtctccaataaggcccttccagccccaattgaaaagactatttcaaaggccaaggg
gcaacccagagagcctcaggtgtatacacttcctccctcacgtgaggagatgacaaagaaccaagtgagt
ctgacatgtctcgtgaaaggcttttacccttcagacattgctgtggagtgggaaagcaacggccaacccg
agaacaactacaagaccacacctcccgtgctggacagcgatgggtctttctttctctacagcaagctgac
tgtggacaaaagtcgctggcagcaaggcaatgtcttcagctgctctgtgatgcacgaagccctccataat
cattatacccagaagtctctgagcctgagcccaggaaag</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="59">
<INSDSeq>
<INSDSeq_length>1353</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..1353</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q60">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>caggtgcagttgcaacaatctggtgcagagctggtgaaacctggtgcat
cagtgaagctttcatgtaaagcttccgggtacacatttaccagctactatatgtactgggttaagcagcg
tcctggacagggtctggagtggatcggcgagattaatccatctaacgggggaaccaactttaacgaaaag
ttcaagtctaaggctacactgacagtcgataaatcctcatccaccgcctacatgcagctctcttctctga
cttcagaggacagcgccgtgtactactgcactaggaccctgtattacggtaacgactggtatttcgatgt
gtggggtgccggtacaacagtgaccgtgtcctcagccaaaacaacagcccctagtgtatatccacttgcc
cctgtctgcggcgacactacagggtcttctgtgacactcgggtgtctggtcaaggggtatttccctgagc
cagtgaccctcacttggaactcaggctccctttctagcggcgtccacacatttccagccgtgcttcagtc
tgatctgtataccctgagcagcagcgtgaccgtcacctcctccacatggccttcacaaagcataacttgt
aatgtcgcccaccctgcctcatctaccaaagtcgacaagaagatcgagcctcgaggccccactatcaaac
cctgtccaccctgtaagtgccccgctccaaacttgctgggcggaccatccgttttcatcttccctccaaa
gatcaaagacgtgctgatgatttcactcagccctattgtcacttgtgtagtggtggacgtgtcagaagat
gatcctgacgtgcagatttcctggtttgtcaacaatgttgaggtgcatacagctcagacacagacccacc
gcgaagattataactctactttgagggtcgtttccgccctgccaattcagcaccaggactggatgtctgg
aaaggaattcaaatgtaaagtgaataataaggacctccccgctcccatcgaacggactatctctaagcct
aaagggagcgtacgagctcctcaggtgtatgtcctgccccccccagaggaagaaatgaccaagaaacagg
tgacccttacctgtatggttactgactttatgcctgaggacatctatgtagagtggaccaacaacgggaa
gactgagttgaactacaaaaacacagaacctgtgcttgatagtgatggttcttatttcatgtatagcaag
ctcagagtcgaaaaaaaaaactgggtggaacgcaattcttactcctgttccgtggtgcacgaggggttgc
acaatcaccacactacaaaaagcttcagtaggacccccggcaag</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="60">
<INSDSeq>
<INSDSeq_length>639</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..639</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q61">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>caaatcgtgctgacccagtctccagcaataatgtccgcatctcctggtg
agaaagtgaccatgacttgttcagcttcctcttctgttaactatatgcactggtaccaacagaagtctgg
cacctccccaaagcggtggatttatgacacctccaagctggctagcggggtacccgcaaggttctccggt
tcaggcagcggcacttcttactccctgactattagctctatggaggcagaggatgccgctacctactatt
gccagcaatggagcagtaatccagtcacatttggggccggaaccaagctggagctgaagcgagctgatgc
agctcccacagtatctatttttcctccatcttctgagcagctcacatctggtggggcctccgtggtctgc
ttcttgaataacttctatcctaaggacattaacgtgaaatggaagatcgacggatccgaacggcagaacg
gagtgcttaacagctggaccgaccaggatagtaaggattctacatattccatgtcttccaccctcacact
cacaaaggacgagtatgagagacacaacagctacacatgtgaagccactcacaaaacctccacatctcca
attgtgaagtcctttaataggaatgagtgt</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="61">
<INSDSeq>
<INSDSeq_length>1350</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..1350</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q62">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gaagttctgcttcagcagtctggcccagaagttgttaagccaggagcct
ccgtgaaaattacttgcaaggcctccgggtacacatttacagactacaatatggactgggtgaagcagtc
ccatggaaagagtctggaatggatcggcgatatcaatccaaacaatggcggtaccctctataaccagaaa
tttcgcggacgtgtgaccttgatcgtcgacaaaagtagttctactgcctacatggagctgcgcagcctga
ctagtgacgacaccgccgtctactattgcgctcgctctgaagtcttttatgggaattatgctgactactg
gggccagggtaccactttgaccgtctccagtgccaaaacaacagcccctagtgtatatccacttgcccct
gtctgcggcgacactacagggtcttctgtgacactcgggtgtctggtcaaggggtatttccctgagccag
tgaccctcacttggaactcaggctccctttctagcggcgtccacacatttccagccgtgcttcagtctga
tctgtataccctgagcagcagcgtgaccgtcacctcctccacatggccttcacaaagcataacttgtaat
gtcgcccaccctgcctcatctaccaaagtcgacaagaagatcgagcctcgaggccccactatcaaaccct
gtccaccctgtaagtgccccgctccaaacttgctgggcggaccatccgttttcatcttccctccaaagat
caaagacgtgctgatgatttcactcagccctattgtcacttgtgtagtggtggacgtgtcagaagatgat
cctgacgtgcagatttcctggtttgtcaacaatgttgaggtgcatacagctcagacacagacccaccgcg
aagattataactctactttgagggtcgtttccgccctgccaattcagcaccaggactggatgtctggaaa
ggaattcaaatgtaaagtgaataataaggacctccccgctcccatcgaacggactatctctaagcctaaa
gggagcgtacgagctcctcaggtgtatgtcctgccccccccagaggaagaaatgaccaagaaacaggtga
cccttacctgtatggttactgactttatgcctgaggacatctatgtagagtggaccaacaacgggaagac
tgagttgaactacaaaaacacagaacctgtgcttgatagtgatggttcttatttcatgtatagcaagctc
agagtcgaaaaaaaaaactgggtggaacgcaattcttactcctgttccgtggtgcacgaggggttgcaca
atcaccacactacaaaaagcttcagtaggacccccggcaag</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="62">
<INSDSeq>
<INSDSeq_length>654</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..654</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q63">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gacattgtgctgactcagagtcctgtaagtctggcagttcccctcggcc
aaagagctaccattagttgtaaggcttcccagagcgtggactatgatggcgacagctatatgaattggta
tcaacagaagccaggacagccacccaagctgctgatctacgccgcctccaccctgcattcaggtatccct
gtgcgattttctggtagtggctccggcacagatttcaccctgaatatccatccagttgaggaggaggatg
ctgcctcttactactgtcagcagagcaaagaggatcctagaaccttcggcggtggcactaagctggaaat
taagcgagctgatgcagctcccacagtatctatttttcctccatcttctgagcagctcacatctggtggg
gcctccgtggtctgcttcttgaataacttctatcctaaggacattaacgtgaaatggaagatcgacggat
ccgaacggcagaacggagtgcttaacagctggaccgaccaggatagtaaggattctacatattccatgtc
ttccaccctcacactcacaaaggacgagtatgagagacacaacagctacacatgtgaagccactcacaaa
acctccacatctccaattgtgaagtcctttaataggaatgagtgt</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="63">
<INSDSeq>
<INSDSeq_length>1353</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..1353</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q64">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gaagttcaactggttcagagcggagctgaggtaaagaagccaggtgcca
gcgtgaaagttagttgcaaggcatccggatacactttcactagctattatatgtattgggtgcgacaggc
cccagggcaaggtttggagtggatcggagagatcaatccttcaaatggcggcacaaatttcaacgaaaag
ttcaaatctcgcgtgactctgacagtggacaagtccatctccacagcatatatggagctgagccggctta
gatccgatgacactgctgtctactattgtacaagaacactgtactatggcaacgactggtacttcgatgt
ctggggacaggggaccactgtgaccgtctccagtgccagtacaaagggaccatctgtgtttcctctggca
ccttcatctaagagcacttctggtggtactgctgctctgggctgccttgtaaaggactatttcccagagc
ccgtgaccgtcagttggaattcaggcgcccttaccagcggggttcacactttcccagctgtgttgcagtc
ttcagggctttacagtctcagcagtgttgtcaccgtcccttcctcctcactgggcacccaaacctatatt
tgtaatgtcaaccataaaccaagtaacaccaaggtggacaagaaggtggagcccaagtcatgtgataaaa
ctcacacttgtccaccatgccctgctcccgaactgttgggcggacctagcgtgtttctctttccacccaa
accaaaggataccctgatgatcagcaggactcccgaggtgacttgtgtggtggttgacgtgtcccatgag
gatcctgaagtgaagttcaattggtacgtggacggcgtggaggttcataacgcaaagaccaagcccaggg
aagagcagtataactctacttaccgggtggtttcagtcttgactgtgttgcaccaggactggctgaatgg
aaaggagtataagtgtaaagtgagtaacaaagccctgccagctcccattgagaagacaatctcaaaagct
aagggtcagccccgcgaaccacaggtgtatacactcccaccctcccgcgaggagatgaccaaaaaccagg
tgtccctcacctgcctggtcaagggattttaccccagcgatattgctgtcgagtgggagtcaaacggtca
gcccgagaataattataaaactacccctcccgtgcttgacagcgatggatctttcttcctgtactcaaaa
ctgaccgtcgacaaatcccgatggcagcaaggtaacgtgttctcttgcagcgtaatgcacgaggctcttc
acaatcactatactcagaagtcactcagccttagtcctggaaag</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="64">
<INSDSeq>
<INSDSeq_length>639</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..639</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q65">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gaaatcgtgctgacccagagcccagatttccagagtgtcacaccaaagg
agaaggtaacaattacatgcagtgccagcagtagcgtgaactatatgcattggtatcagcagaaacccga
tcagtcccctaagcgactgatctacgatacctccaagctggccagcggtgttccaagtaggttctctggc
agcgggtctgggacagactacactctcactatcaactctctggaagctgaggatgctgctacttattatt
gccagcagtggagctcaaatcccgttacctttggccagggtaccaagctcgaaattaaacgtacagtcgc
agcacctagtgtcttcatctttcctccctctgacgagcagttgaagagcggaactgcaagcgtcgtttgc
ctcctgaacaatttctatccccgggaggctaaggtccagtggaaagtggataatgctctccagagcggta
actcacaagagtctgttaccgagcaggactccaaggattctacctatagtctgagctctaccctgacact
gtccaaggccgattacgagaaacacaaagtgtatgcctgcgaagtaacccaccagggcctgagttcccca
gtgaccaagtctttcaataggggggagtgt</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="65">
<INSDSeq>
<INSDSeq_length>1350</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..1350</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q66">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gaagtgcagcttgtacagagtggagcagaggtcaagaaaccaggagctt
ccgtgaaggtgagctgcaaggcctccggctatacctttactgattacaacatggactgggtccgtcaggc
tcctggaaaaggactggagtggattggtgacattaatcctaataacggcggcacactttacaatcagaag
tttcgtggtagagttacactgactgtggataaatcaatcagcaccgcctatatggagctgtcccgactgc
ggtccgacgatactgcagtgtattactgcgccaggtcagaggtgttttacggtaactacgcagactattg
gggccaggggacaacagtgacagtcagcagcgccagtacaaagggaccatctgtgtttcctctggcacct
tcatctaagagcacttctggtggtactgctgctctgggctgccttgtaaaggactatttcccagagcccg
tgaccgtcagttggaattcaggcgcccttaccagcggggttcacactttcccagctgtgttgcagtcttc
agggctttacagtctcagcagtgttgtcaccgtcccttcctcctcactgggcacccaaacctatatttgt
aatgtcaaccataaaccaagtaacaccaaggtggacaagaaggtggagcccaagtcatgtgataaaactc
acacttgtccaccatgccctgctcccgaactgttgggcggacctagcgtgtttctctttccacccaaacc
aaaggataccctgatgatcagcaggactcccgaggtgacttgtgtggtggttgacgtgtcccatgaggat
cctgaagtgaagttcaattggtacgtggacggcgtggaggttcataacgcaaagaccaagcccagggaag
agcagtataactctacttaccgggtggtttcagtcttgactgtgttgcaccaggactggctgaatggaaa
ggagtataagtgtaaagtgagtaacaaagccctgccagctcccattgagaagacaatctcaaaagctaag
ggtcagccccgcgaaccacaggtgtatacactcccaccctcccgcgaggagatgaccaaaaaccaggtgt
ccctcacctgcctggtcaagggattttaccccagcgatattgctgtcgagtgggagtcaaacggtcagcc
cgagaataattataaaactacccctcccgtgcttgacagcgatggatctttcttcctgtactcaaaactg
accgtcgacaaatcccgatggcagcaaggtaacgtgttctcttgcagcgtaatgcacgaggctcttcaca
atcactatactcagaagtcactcagccttagtcctggaaag</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="66">
<INSDSeq>
<INSDSeq_length>654</INSDSeq_length>
<INSDSeq_moltype>ДНК</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>источник</INSDFeature_key>
<INSDFeature_location>1..654</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>другая ДНК</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q67">
<INSDQualifier_name>организм</INSDQualifier_name>
<INSDQualifier_value>синтетическая
конструкция</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>gacatagtattgacccagacaccattgtctttgagcgttaccccaggcc
agccagcttcaatatcttgcaaggcctctcagtccgtcgactatgatggcgattcctacatgaattggta
cctccaaaagccaggccaaccaccacagctgttgatttatgccgcttctacactccacagtggcgtgccc
gatcgattttcaggatccggctcagggaccgatttcacccttaagatttctcgagtggaagccgaggatg
tgggcgtgtattactgccagcagagcaaagaggatcctagaacttttggccagggaaccaagctggagat
taaacgtacagtcgcagcacctagtgtcttcatctttcctccctctgacgagcagttgaagagcggaact
gcaagcgtcgtttgcctcctgaacaatttctatccccgggaggctaaggtccagtggaaagtggataatg
ctctccagagcggtaactcacaagagtctgttaccgagcaggactccaaggattctacctatagtctgag
ctctaccctgacactgtccaaggccgattacgagaaacacaaagtgtatgcctgcgaagtaacccaccag
ggcctgagttccccagtgaccaagtctttcaataggggggagtgt</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
</ST26SequenceListing>
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| БИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА И ИХ ПРИМЕНЕНИЯ | 2022 |
|
RU2821577C2 |
| АНТИТЕЛА ПРОТИВ ПРОПЕРДИНА И ИХ ПОЛУЧЕНИЕ | 2021 |
|
RU2830308C1 |
| Моноклональные антитела, специфичные к белку рустицианин, и использование антител для диагностики и лечения злокачественных новообразований | 2024 |
|
RU2823344C1 |
| АНТИТЕЛО ПРОТИВ ЛИГАНДА 1 ЗАПРОГРАММИРОВАННОЙ ГИБЕЛИ КЛЕТОК (PD-L1), ЕГО АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ И ИХ МЕДИЦИНСКОЕ ПРИМЕНЕНИЕ | 2016 |
|
RU2727914C2 |
| БЕЛОК СЛИЯНИЯ НАЦЕЛЕННОГО НА GPC3 АНТИТЕЛА И ИНТЕРФЕРОНА α И ЕГО ПРИМЕНЕНИЕ | 2022 |
|
RU2836245C2 |
| АНТИТЕЛО ПРОТИВ LAG-3, ЕГО АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ И ИХ ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2017 |
|
RU2757813C2 |
| АНТИТЕЛА ПРОТИВ БЕЛКА РЕЦЕПТОРА С-МЕТ | 2011 |
|
RU2608644C2 |
| Моноклональное антитело iC2 и его антигенсвязывающий фрагмент, селективно связывающие рецептор-связывающий домен Spike-белка вируса SARS-CoV-2, обладающие вируснейтрализующей активностью | 2023 |
|
RU2817697C1 |
| АНТИТЕЛО MICA С СОЗРЕВАНИЕМ АФФИННОСТИ И ЕГО ПРИМЕНЕНИЕ | 2024 |
|
RU2838565C1 |
| BCMA-СПЕЦИФИЧЕСКИЕ ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, СОДЕРЖАЩИЕ БЛОКАТОР ПЕРЕДАЧИ СИГНАЛА IL-6 | 2023 |
|
RU2828294C1 |
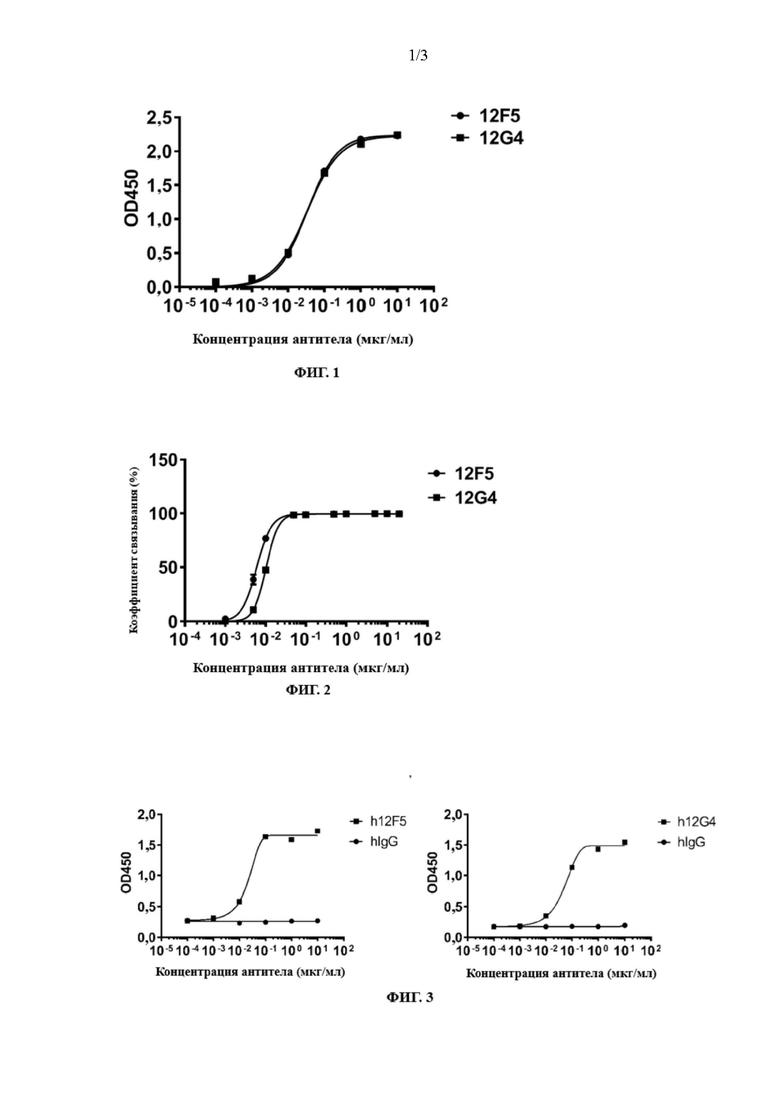
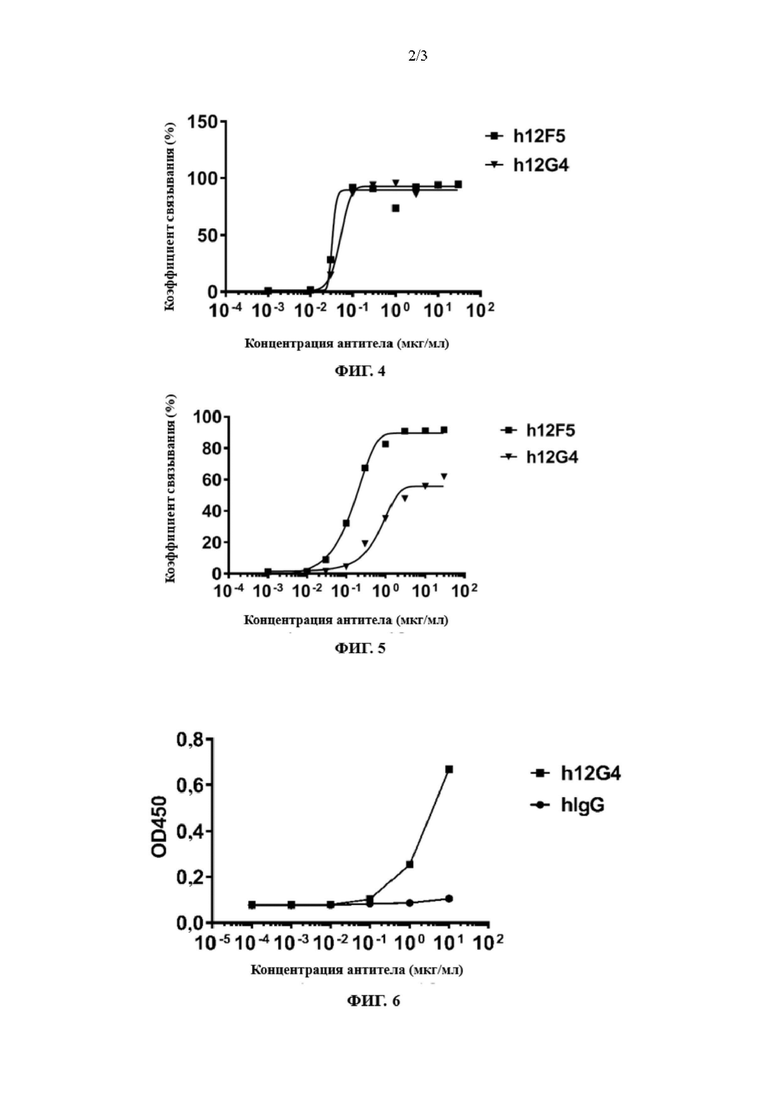
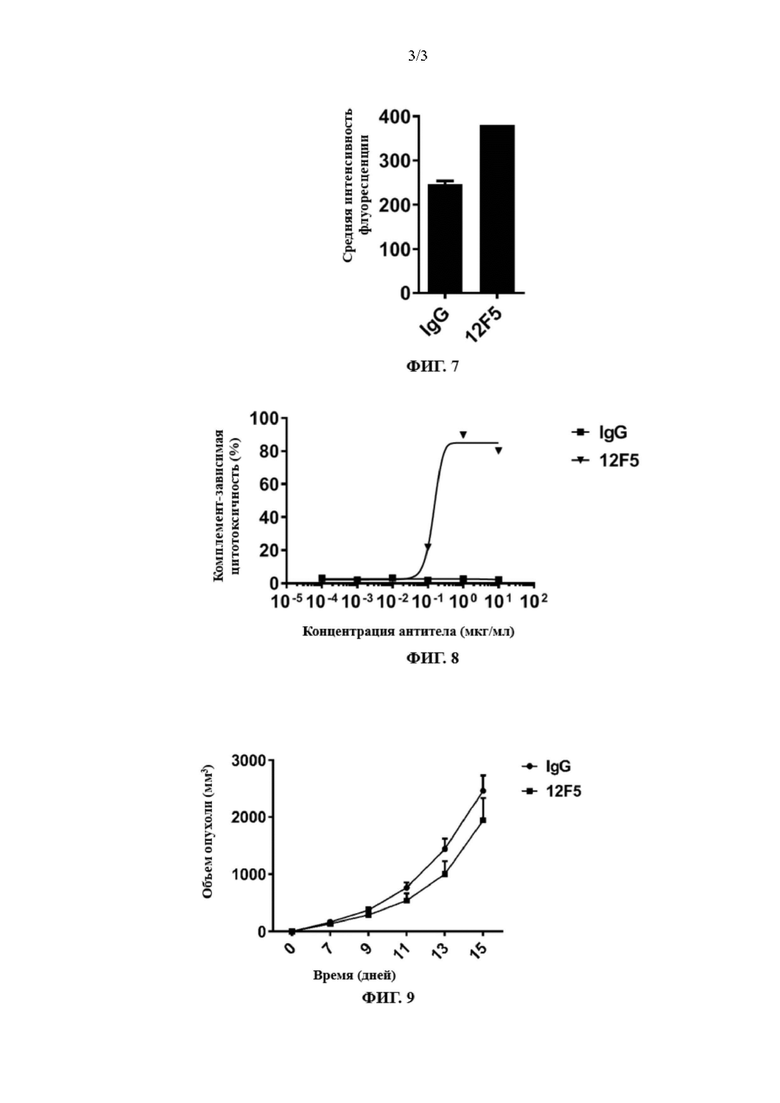
Изобретение относится к области биотехнологии. Предложены антитело или его антигенсвязывающий фрагмент, связывающиеся с B7H6, включающие их иммуноконъюгаты и фармацевтические композиции. Также предложены нуклеиновая кислота, кодирующая указанные антитело или его антигенсвязывающий фрагмент, и содержащие указанную нуклеиновую кислоту рекомбинантный вектор и рекомбинантная клетка для получения антитела или его антигенсвязывающего фрагмента. Кроме того, изобретение относится к применению антител и иммуноконъюгатов по изобретению для предупреждения или лечения B7H6-опосредованного заболевания, а также для диагностики наличия у субъекта B7H6-опосредованного заболевания. Антитело по настоящему изобретению способствует связыванию B7H6 с рецептором активации NK-клетки NKp30, стимулируя таким образом противораковую функцию NK-клеток. 13 н. и 13 з.п. ф-лы, 9 ил., 2 табл., 12 пр.
1. Антитело, способное связываться с B7H6, или его антигенсвязывающий фрагмент, причем антитело или его антигенсвязывающий фрагмент содержат:
1) CDR1 тяжелой цепи, имеющую аминокислотную последовательность, как указано в SEQ ID NO: 1, CDR2 тяжелой цепи, имеющую аминокислотную последовательность, как указано в SEQ ID NO: 2, CDR3 тяжелой цепи, имеющую аминокислотную последовательность, как указано в SEQ ID NO: 3, CDR1 легкой цепи, имеющую аминокислотную последовательность, как указано в SEQ ID NO: 4, CDR2 легкой цепи, имеющую аминокислотную последовательность, как указано в SEQ ID NO: 5, CDR3 легкой цепи, имеющую аминокислотную последовательность, как указано в SEQ ID NO: 6; или
2) CDR1 тяжелой цепи, имеющую аминокислотную последовательность, как указано в SEQ ID NO: 7, CDR2 тяжелой цепи, имеющую аминокислотную последовательность, как указано в SEQ ID NO: 8, CDR3 тяжелой цепи, имеющую аминокислотную последовательность, как указано в SEQ ID NO: 9, CDR1 легкой цепи, имеющую аминокислотную последовательность, как указано в SEQ ID NO: 10, CDR2 легкой цепи, имеющую аминокислотную последовательность, как указано в SEQ ID NO: 11, CDR3 легкой цепи, имеющую аминокислотную последовательность, как указано в SEQ ID NO: 12.
2. Антитело или его антигенсвязывающий фрагмент по п. 1, причем антитело или его антигенсвязывающий фрагмент содержат вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом (i) вариабельная область тяжелой цепи содержит аминокислотную последовательность, которая по меньшей мере на 80% гомологична по меньшей мере одной из аминокислотных последовательностей, как указано в SEQ ID NO: 13, SEQ ID NO: 15, SEQ ID NO: 17 и SEQ ID NO: 19, и аминокислотную последовательность в ее консервативной модифицированной форме; и/или (ii) вариабельная область легкой цепи содержит аминокислотную последовательность, которая по меньшей мере на 80% гомологична по меньшей мере одной из аминокислотных последовательностей, как указано в SEQ ID NO: 14, SEQ ID NO: 16, SEQ ID NO: 18 и SEQ ID NO: 20, и аминокислотную последовательность в ее консервативной модифицированной форме.
3. Антитело или его антигенсвязывающий фрагмент по п. 2, в котором вариабельная область тяжелой цепи содержит аминокислотную последовательность, которая по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% гомологична вариабельной области тяжелой цепи, выбранной из (i); при этом вариабельная область легкой цепи содержит аминокислотную последовательность, которая по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% гомологична вариабельной области легкой цепи, выбранной из (ii).
4. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-3, причем антитело или его антигенсвязывающий фрагмент содержат:
1) аминокислотную последовательность вариабельной области тяжелой цепи, как указано в SEQ ID NO: 13, и аминокислотную последовательность вариабельной области легкой цепи, как указано в SEQ ID NO: 14;
2) аминокислотную последовательность вариабельной области тяжелой цепи, как указано в SEQ ID NO: 15, и аминокислотную последовательность вариабельной области легкой цепи, как указано в SEQ ID NO: 16;
3) аминокислотную последовательность вариабельной области тяжелой цепи, как указано в SEQ ID NO: 17, и аминокислотную последовательность вариабельной области легкой цепи, как указано в SEQ ID NO: 18; или
4) аминокислотную последовательность вариабельной области тяжелой цепи, как указано в SEQ ID NO: 19, и аминокислотную последовательность вариабельной области легкой цепи, как указано в SEQ ID NO: 20.
5. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-4, причем антитело или его антигенсвязывающий фрагмент содержат:
1) аминокислотную последовательность тяжелой цепи, как указано в SEQ ID NO: 26, и аминокислотную последовательность легкой цепи, как указано в SEQ ID NO: 27;
2) аминокислотную последовательность тяжелой цепи, как указано в SEQ ID NO: 28, и аминокислотную последовательность легкой цепи, как указано в SEQ ID NO: 29;
3) аминокислотную последовательность тяжелой цепи, как указано в SEQ ID NO: 30, и аминокислотную последовательность легкой цепи, как указано в SEQ ID NO: 31; или
4) аминокислотную последовательность тяжелой цепи, как указано в SEQ ID NO: 32, и аминокислотную последовательность легкой цепи, как указано в SEQ ID NO: 33.
6. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-4, причем выделенное антитело представляет собой IgG1, IgG2 или IgG4.
7. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-4, причем антитело представляет собой моноклональное антитело, мышиное антитело, химерное антитело, гуманизированное антитело, антитело, сконструированное человеком, антитело человека, Fv, одноцепочечное антитело (scFv), Fab , Fab', Fab'-SH или F(ab')2.
8. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1-7, причем антитело или его антигенсвязывающий фрагмент способны связываться с аминокислотной последовательностью, как указано в SEQ ID NO: 21.
9. Иммуноконъюгат для предупреждения или лечения B7H6-опосредованного заболевания, содержащий терапевтическое средство и антитело или его антигенсвязывающий фрагмент по любому из пп. 1-8, конъюгированные с терапевтическим средством.
10. Композиция для предупреждения или лечения B7H6-опосредованного заболевания, содержащая антитело или его антигенсвязывающий фрагмент по любому из пп. 1-8 и/или иммуноконъюгат по п. 9 и фармацевтически приемлемый носитель.
11. Применение антитела или его антигенсвязывающего фрагмента по любому из пп. 1-8 при получении реагента для обнаружения B7H6 в образце.
12. Применение антитела или его антигенсвязывающего фрагмента по любому из пп. 1-8 при получении лекарственного средства для предупреждения или лечения B7H6-опосредованного заболевания, причем B7H6-опосредованное заболевание представляет собой рак или инфекционное заболевание.
13. Применение по п. 12, причем рак представляет собой по меньшей мере одно из рака легких, рака печени, рака яичников, рака шейки матки, рака кожи, рака мочевого пузыря, рака толстой кишки, рака молочной железы, глиомы, рака почек, рака желудка, рака пищевода, плоскоклеточного рака полости рта и рака головы и шеи.
14. Нуклеиновая кислота кодирующая антитело или его антигенсвязывающий фрагмент по любому из пп. 1-8.
15. Рекомбинантный вектор для получения антитела или его антигенсвязывающего фрагмента по любому из пп. 1-8, содержащий нуклеиновую кислоту по п. 14.
16. Рекомбинантная клетка для получения антитела или его антигенсвязывающего фрагмента по любому из пп. 1-8, несущая нуклеиновую кислоту по п. 14, рекомбинантный вектор по п. 15 или антитело или его антигенсвязывающий фрагмент по любому из пп. 1-8.
17. Лекарственное средство для предупреждения или лечения B7H6-опосредованного заболевания, содержащее антитело или его антигенсвязывающий фрагмент по любому из пп. 1-8, иммуноконъюгат по п. 9, композицию по п. 10.
18. Применение антитела или его антигенсвязывающего фрагмента по любому из пп. 1-8, иммуноконъюгата по п. 9, композиции по п. 10, лекарственного средства по п. 17 в лечении или предупреждении B7H6-опосредованного заболевания.
19. Применение по п. 18, причем B7H6-опосредованное заболевание представляет собой рак или инфекционное заболевание;
необязательно, рак представляет собой по меньшей мере одно из рака легких, рака печени, рака яичников, рака шейки матки, рака кожи, рака мочевого пузыря, рака толстой кишки, рака молочной железы, глиомы, рака почек, рака желудка, рака пищевода, плоскоклеточного рака полости рта и рака головы и шеи.
20. Способ лечения или предупреждения B7H6-опосредованного заболевания, включающий введение субъекту по меньшей мере одного из:
1) антитела или его антигенсвязывающего фрагмента по любому из пп. 1-8,
2) иммуноконъюгата по п. 9;
3) композиции по п. 10; и
4) лекарственного средства по п.17.
21. Способ по п. 20, причем B7H6-опосредованное заболевание представляет собой рак или инфекционное заболевание;
необязательно, рак представляет собой по меньшей мере одно из рака легких, рака печени, рака яичников, рака шейки матки, рака кожи, рака мочевого пузыря, рака толстой кишки, рака молочной железы, глиомы, рака почек, рака желудка, рака пищевода, плоскоклеточного рака полости рта и рака головы и шеи.
22. Способ диагностики наличия у субъекта B7H6-опосредованного заболевания, включающий:
обнаружение B7H6 в тестируемом образце с помощью
антитела или его антигенсвязывающего фрагмента по любому из пп. 1-8,
определение содержания B7H6 в тестируемом образце на основании результата обнаружения B7H6.
23. Способ по п. 22, в котором содержание B7H6 в тестируемом образце не ниже минимального стандарта для заболевания является показателем того, что тестируемый образец получен от пациента, имеющего B7H6-опосредованное заболевание.
24. Способ по п. 22, причем B7H6-опосредованное заболевание представляет собой рак или инфекционное заболевание;
необязательно, рак представляет собой по меньшей мере одно из рака легких, рака печени, рака яичников, рака шейки матки, рака кожи, рака мочевого пузыря, рака толстой кишки, рака молочной железы, глиомы, рака почек, рака желудка, рака пищевода, плоскоклеточного рака полости рта и рака головы и шеи.
25. Применение одного из следующего в диагностике наличия у субъекта B7H6-опосредованного заболевания:
антитела или его антигенсвязывающего фрагмента по любому из пп. 1-8.
26. Применение по п. 25, причем B7H6-опосредованное заболевание представляет собой рак или инфекционное заболевание;
необязательно, рак представляет собой по меньшей мере одно из рака легких, рака печени, рака яичников, рака шейки матки, рака кожи, рака мочевого пузыря, рака толстой кишки, рака молочной железы, глиомы, рака почек, рака желудка, рака пищевода, плоскоклеточного рака полости рта и рака головы и шеи.
| WO 2017181001 A1, 19.10.2017 | |||
| US 8822652 B2, 02.09.2014 | |||
| ШАПОВАЛ А.И | |||
| и др., Молекулы контроля иммунитета семейства В7 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
2025-02-14—Публикация
2022-12-07—Подача