Изобретение относится к области медицины, фармакологии и химико-фармацевтической промышленности, а именно, к новой аморфной форме [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата, а также включающей ее фармацевтической субстанции, фармацевтической композиции и лекарственному средству, которые проявляют профилактическую и/или терапевтическую противовирусную активность.
Одна из наиболее актуальных проблем современной медицины это борьба с вирусными инфекциями. По данным ВОЗ, ежегодно в мире от инфекционных болезней страдают 2 млрд человек и для 17 млн из них это причина смерти. Ежедневно в мире 50 тыс.летальных исходов обусловлены инфекционными болезнями, которые по-прежнему остаются в числе ведущих причин смертности и первой причиной преждевременной смерти [Брико Н.И., Миндлина А.Я., Полибин Р.В. Универсальность изменений в проявлениях эпидемического процесса антропонозных инфекций за последние десятилетия. Журнал микробиологии. 2015; 5: 12-20.].
Большую часть вирусов представляют собой вирусы, геном которых закодирован одноцепочечной нитью РНК и которые используют вирусную РНК-зависимую-РНК-полимеразу для своей репликации. Примерами таких вирусов являются вирус гриппа, коронавирус, пикорнавирус, аренавирус, флавивирус, буньявирус, филовирус, флебовирус, хантавирус, энтеровирус, тогавирус, калицивирус, респираторно-синцитиальный вирус, вирус парагриппа, риновирусы, метапневмовирусы, ротавирус или норавирус.
Препараты - аналоги нуклеозидов напрямую нацелены на блокировку активности РНК-зависимой-РНК-полимеразы и блокируют синтез вирусной цепи РНК для широкого спектра РНК-вирусов, включая семейство человеческих коронавирусов (Agostini, М. L., et al. Small-molecule antiviral beta-d-N (4)-hydroxycytidine inhibits a proofreading-intact coronavirus with a high genetic barrier to resistance.- 2019.- J. Virol. 93, e01348-19), вирусов гриппа (разных типов) (Toots, М., et al. Characterization of orally efficacious influenza drug with high resistance barrier in ferrets and human airway epithelia.- 2019.- Sci. Transl. Med. 11, eaax5866. doi: 10.1126/scitranslmed.aax5866), SARS-CoV-2, MERS-CoV (Kabinger F. et al. Mechanism of molnupiravir-induced SARS-CoV-2 mutagenesis // Nature structural & molecular biology. - 2021. - Т. 28. - №. 9. - С. 740-746.), венесуэльский конский вирус энцефалита (ВЭЭВ) (Urakova N, et al, β-d-N (4)-Hydroxycytidine Is a Potent Anti-alphavirus Compound That Induces a High Level of Mutations in the Viral Genome.- 2018.- J Virol 92. Painter GR, et al. The prophylactic and therapeutic activity of a broadly active ribonucleoside analog in a murine model of intranasal Venezuelan equine encephalitis virus infection.- 2019.- Antiviral Res 171:104597), вирус Эбола (Reynard, О., et al. Identification of a new ribonucleoside inhibitor of Ebola virus replication.- 2015.- Viruses 7, 6233-6240), норовирус (Costantini, V. P., et al. Antiviral activity of nucleoside analogues against norovirus.- 2012.- Antivir. Ther. 17, 981-991), респираторно-синцитиальных вирусов (Yoon, J. J., et al. Orally efficacious broad-spectrum ribonucleoside analog inhibitor of influenza and respiratory syncytial viruses.- 2018.- Antimicrob. Agents Chemother. 62, e00766-18), вирус Чикунгунья (Ehteshami, M., et al. Characterization of beta-d-N(4)-hydroxycytidine as a novel inhibitor of Chikungunya virus.- 2017.- Antimicrob. Agents Chemother. 61, e02395-16).
Вспышка SARS-CoV-2 по всему миру и связанные с ней последствия являются угрозой для общественного здравоохранения и экономики многих стран. Отсутствие специальной терапии против нового вируса и его высокая изменчивость требует создания новых лекарственных средств.
В рамках борьбы с новой инфекцией был разработан ряд профилактических вакцин, а также средств неспецифической терапии, облегчающих течение заболевания. Однако в дополнение к существующим средствам терапии необходимы специфические препараты, оказывающие непосредственное действие на вирус, приводящие к облегчению симптомов заболевания, ускоренному разрешению заболевания, блокированию передачи инфекции и уменьшению риска развития клинических осложнений.
Одним из перспективных аналогов нуклеозидов, проявляющим противовирусную активность, является [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноат, который характеризуется Формулой 1.
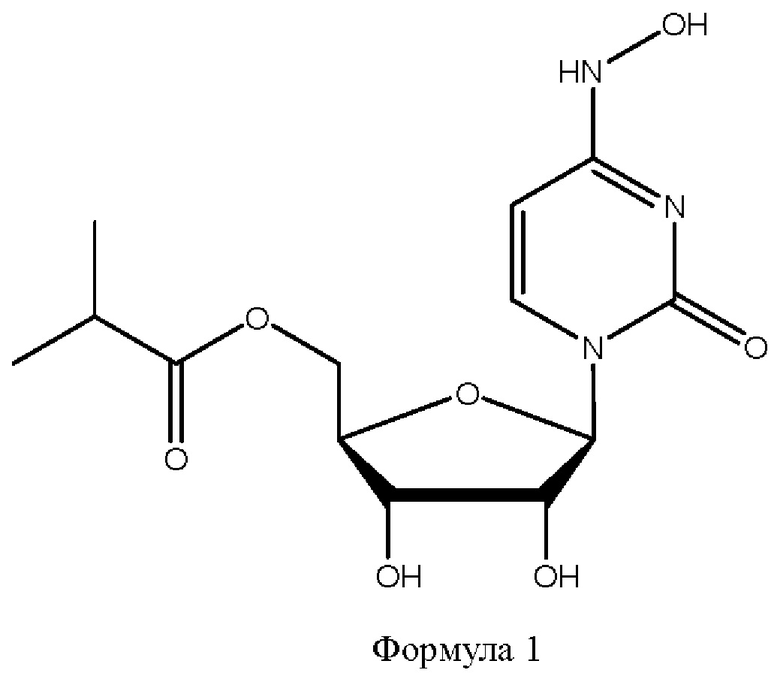
[(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноат - это синтетическое нуклеозидное производное N4-гидроксицитидина. Из уровня техники известна его высокая эффективность против вирусов гриппа и коронавирусов, включая SARS, MERS и SARS-CoV-2 [Mart Toots, et al. Quantitative efficacy paradigms of the influenza clinical drug candidate EIDD-2801 in the ferret model // Translational Research. - 2020. - T. 218. - C. 16-28]. Универсальный механизм действия [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата представляет собой специфичное действие на основополагающий фермент репликативного аппарата вируса, что предполагает широкий спектр противовирусной активности данного вещества.
При разработке лекарственных средств важно, чтобы вещество, которое является активным агентом, находилось в форме с удовлетворительными физико-химическими и технологическими свойствами. Это важно с точки зрения производства фармацевтических композиций, включающих активный агент.Вещество, которое является активным агентом, фармацевтические композиции и лекарственные средства, включающие его, должны обладать способностью эффективно храниться при самых различных условиях в течение значительных периодов времени, не проявляя значительного изменения физико-химических свойств активного агента (например, его химического состава, плотности, гигроскопичности, растворимости и сыпучести).
Открытие новых форм активного агента открывает возможности улучшения профиля физико-химических и технологических характеристик фармацевтического продукта (лекарственного средства). Это расширяет спектр активных агентов, которые специалист по разработке препаратов имеет в своем распоряжении при разработке нового лекарственного средства с улучшенными характеристиками.
Таким образом, в настоящее время имеется постоянная потребность в разработке других, улучшенных форм противовирусных агентов.
Фармацевтические субстанции в твердой форме могут существовать в кристаллическом или аморфном состоянии. Кристаллические формы вещества характеризуются наличием дальнего порядка, а аморфные его отсутствием. Строение вещества напрямую влияет на его свойства.
Метод порошковой рентгеновской дифрактометрии или качественный рентгенофазовый анализ позволяет идентифицировать количество форм твердого соединения и их строение, а именно: кристаллические, аморфные или их комбинации (смеси). Структурные исследования позволяют установить связь между структурой и свойствами твердых тел. Определение связи между структурой и свойствами вещества позволяет устанавливать рациональный контроль за технологическим процессом создания фармацевтических субстанций и лекарственных средств, раскрывать причины изменения этих свойств под действием того или иного фактора, дает возможность более осознанно управлять технологическим процессом создания фармацевтических субстанций, а также лекарственных средств их содержащих, и изменять его в нужном направлении.
В основе метода РФА лежит получение и последующий анализ картины, возникающей в результате дифракции рентгеновских лучей на электронной плотности атомов облучаемого твердого образца. Рентгеновские лучи это электромагнитные волны длинной приблизительно от 10 до 0,1 Å. Расстояния между атомами в пространстве кристаллической решетки твердых тел варьируют от единиц до нескольких сотен ангстрем, что и приводит к явлению дифракции.
Дифрагированный рентгеновский луч можно рассматривать как результат множественной интерференции от семейства плоскостей кристаллической решетки. Решетка представляет собой совокупность бесконечного числа параллельных атомных плоскостей, расположенных на равном расстоянии друг от друга. Отражение лучей будет происходить от всех атомных плоскостей (их серий), так как рентгеновский луч, в отличие от оптического излучения, проникает вглубь кристалла.
Дифракционная картина (профиль) - распределение интенсивности дифракции в зависимости от ее угла. Дифракционная картина является графиком зависимости интенсивности дифрагированного луча от значения 20 (или межплоскостного расстояния d) и может рассматриваться как «отпечатки пальцев данного кристаллического вещества», так как каждая кристаллическая форма определенного вещества всегда дает одинаковый набор дифракционных пиков, присущий только данной кристаллической форме (полиморфной модификации вещества).
При этом рентгенограмма смеси двух и более индивидуальных форм определенных веществ будет являться суперпозицией их дифракционных картин, то есть совмещением дифракционных картин индивидуальных веществ на одной дифрактограмме.
Дифрактограммы кристаллических форм представляют из себя отдельные, резко выраженные узкие линии (пики), в то время, как дифрактограммы аморфных форм представлены в виде широкого максимума (гало).
Несмотря на многообразие твердых форм фармацевтических субстанций (полиморфы, аморфы, сольваты, в частности, гидраты, соли, изомеры, сокристаллы и т.п.) дифракционные картины уникальны для каждой формы определенного вещества.
Различные формы одного и того же вещества могут обладать различными свойствами, такими, как растворимость, гигроскопичность, стабильность, размер и форма частиц, плотность, биодоступность, сыпучесть и т.д. Данные свойства тщательно исследуют и учитывают при приготовлении лекарственных средств. В частности, гигроскопичность влияет на стабильность лекарственной формы, а плохие показатели сыпучести и прессуемости затрудняют получение твердых лекарственных средств.
В последние годы ученые много времени уделяют изучению кристаллических и аморфных форм активных агентов из-за их большого различия в физико-химических свойствах. Иногда аморфные активные агенты предпочтительнее для разработки лекарственного средства и создания препарата. Однако, аморфные вещества обычно трудно получать из-за их метастабильного состояния, при этом они часто имеют другие недостатки, такие как плохая стабильность, агломерация частиц и плохая текучесть. Некоторые аморфные вещества склонны переходить в кристаллическую форму, что приводит к изменению фармацевтических и физико-химических свойств лекарственного средства, как в лучшую, так и в худшую сторону.
Таким образом, при разработке лекарственных средств необходимо устанавливать и учитывать особенности полиморфных и аморфных форм активных агентов. Они должны обладать способностью хорошо растворяться и храниться в течение длительных периодов времени, не проявляя значительного изменения физико-химических свойств.
Из уровня техники известно получение и структура двух кристаллических форм [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата (CN112778387, CN113307834).
В качестве ближайших аналогов авторы настоящего изобретения рассматривали кристаллические формы I и II [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата, которые проявляют противовирусную активность и раскрыты в документе CN113307834. Кристаллическая форма III [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата, заявленная в том же документе, не была использована в качестве ближайшего аналога так как она не была получена как таковая и для нее не раскрыт способ получения.
Таким образом, задачей настоящего изобретения являлась разработка стабильной при хранении, биодоступной аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата.
В результате исследований авторами настоящего изобретения была получена аморфная форма [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата. Исследования свойств аморфной формы [(2R,3S,4R,5R)-3,4-дигидроки-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата помимо улучшения стабильности по сравнению с его кристаллическими формами неожиданно продемонстрировали, что аморфная форма по настоящему изобретению практически не меняет показатели растворимости в процессе хранения, при этом отмечалось улучшение других физико-химических и технологических характеристик, таких как сыпучесть и уменьшение слеживаемости.
Таким образом, техническими результатами настоящего изобретения являются:
- увеличение продолжительности противовирусной активности и более длительный терапевтический эффект посредством использования аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-l-ил]оксолан-2-ил]метил-2-метилпропаноата;
- улучшение физико-химических и технологических свойств новой субстанции представляющей собой по существу аморфную форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению, фармацевтических композиций и лекарственных средств, которые ее содержат, в частности: повышение стабильности при хранении (в том числе в разных климатических зонах и фотостабильности) с сохранением показателей растворимости; уменьшение гигроскопичности; уменьшение слеживаемости в процессе хранения; улучшение прессуемости с сохранением хороших показателей сыпучести;
- расширение арсенала противовирусных средств, обладающих новыми фармакологическими, физико-химическими и технологическими свойствами без снижения терапевтической активности.
Ниже приведены определения терминов, которые используются в описании настоящего изобретения.
Если не указано иное, все технические и специальные термины, использованные в данном контексте, имеют общепринятое в данной области техники значение.
В контексте настоящего изобретения термин «фармацевтически приемлемый эксципиент» характеризует вещества неорганического или органического происхождения, используемые в процессе производства, изготовления лекарственных средств для придания им необходимых физико-химических свойств.
Термин «фармацевтическая композиция» в контексте настоящего изобретения обозначает композицию, включающую в себя терапевтически активный агент и, по меньшей мере, один из фармацевтически приемлемых и фармакологически совместимых эксципиентов, таких как, не ограничиваясь указанным, наполнителей, солюбилизаторов, растворителей, со-растворителей, антиоксидантов, буферных агентов, криопротекторов, разбавителей, консервантов, стабилизаторов, увлажнителей, эмульгаторов, лубрикантов, скользящих веществ, суспендирующих агентов, загустителей, связывающий агентов, подсластителей, отдушек, шипучих агентов, ароматизаторов, антибактериальных агентов, фунгицидов, регуляторов пролонгированной доставки, изотонических агентов, агентов, регулирующих рН, выбор и соотношение которых зависит от природы, назначения и дозировки терапевтически активного агента.
Неограничивающими примерами суспендирующих агентов являются этоксилированный, изостеариловый спирт, полиоксиэтилен, сорбитол и сорбитовый эфир, а также смеси этих веществ.
В качестве стабилизаторов могут быть использованы, не ограничиваясь указанным, маннитол, желатоза, микрокристаллическая целлюлоза, натриевая соль карбоксиметилцеллюлозы, поливинилпирролидон, коллоидный диоксид кремния, полисорбат-80, кроскармелоза натрия, натрия лаурилсульфат.
В качестве антиоксидантов в фармацевтической композиции могут быть использованы в том числе маннитол, аскорбиновая кислота, токоферол, 6-каротин, ликопин.
В качестве наполнителей в фармацевтической композиции могут быть использованы в том числе крахмал, глюкоза, сахароза, лактоза, магния окись, натрия хлорид, натрия гидрокарбонат, каолин, производные целлюлозы, кальция карбонат, декстрин, сорбит, кроскармеллоза натрия, гидроксипропилметилцеллюлоза, магния стеарат.
Защита фармацевтической композиции от действия микроорганизмов может быть обеспечена с помощью разнообразных антибактериальных и противогрибковых агентов, например, таких как сорбиновая кислота, парабены (метилпарабен, пропилпарабен, этилпарабен, бутилпарабен, изобутилпарабен, изопропилпарабен, бензилпарабен, гептилпарабен и их смеси), хлорбутанол и подобные им соединения.
В качестве изотонических агентов фармацевтическая композиция может включать, не ограничиваясь указанным, сахара, хлорид натрия, гидрокарбонат натрия и др. Пролонгированное действие фармацевтической композиции может быть обеспечено, не ограничиваясь указанным, с помощью агентов, замедляющих абсорбцию активного агента (например, гидрофильные и гидрофобные полимерные замедлители высвобождения).
Неограничивающими (иллюстративными) примерами подходящих наполнителей являются лактоза, различные типы крахмала, маннитол, микрокристаллическая целлюлоза, карбонат и фосфат кальция и др.
В качестве растворителей и разбавителей могут быть использованы, не ограничиваясь указанным, вода, пригодные для парентеральных форм органические сложные эфиры, этанол, полиспирты, а также их смеси. Примерами лубрикантов могут быть, не ограничиваясь указанным, стеарат магния или кальция, тальк, лаурилсульфат натрия, стеарилфумарат натрия. В качестве скользящих веществ могут выступать диоксид кремния, тальк, каолин, бентониты и др. Для регулирования рН могут быть использованы различные органические и неорганические кислоты или щелочи, такие как, не ограничиваясь указанным, соляная кислота, яблочная, аскорбиновая, лимонная, уксусная, янтарная, винная, фумаровая, молочная, аспарагиновая, глутаровая, глутаминовая, сорбиновая кислоты, гидроксид натрия и тд. Примерами диспергирующих агентов и распределяющих средств являются крахмал, альгиновая кислота и ее соли, силикаты.
Фармацевтическая композиция может быть введена животным и людям перорально, парентерально (внутрикожно, подкожно, внутримышечно, внутривенно, внутриартериально, в полости), сублингвально, местно, в том числе не ограничиваясь указанным, глазное, назальное введение и др., ректально в стандартной форме введения, в виде смеси с традиционными фармацевтическими носителями. Пригодные стандартные формы введения включают (без ограничения) пероральные формы: таблетки, капсулы, пеллеты, гранулы, порошки, растворы, растворы для распыления в полости рта и носа, сиропы, суспензии и др., пероральные: растворы, суспензии, эмульсии, концентраты для приготовления инъекционных и инфузионных лекарственных средств, аэрозоли и порошки для ингаляционного введения, пульмопорошки (порошки для распыления с помощью инхалера непосредственно в легкие), порошки и лиофилизаты для приготовления инъекционных и инфузионных лекарственных форм; ректальные: суппозитории, капсулы и др., глазные капли.
Термин «фармацевтически приемлемый» в контексте настоящего изобретения означает, что данное вещество или композиция, в отношении которых применяется этот термин, должны быть совместимы с точки зрения химии и/или токсикологии с другими ингредиентами, входящими в состав препарата, и безопасны для того, кого лечат этим веществом или композицией.
«Фармацевтически приемлемая соль» в контексте настоящего изобретения означает относительно безопасные и нетоксичные органические и неорганические соли кислот и оснований, заявленных в настоящем изобретении.
Термин «лекарственное средство» в контексте настоящего изобретения характеризует вещества или их комбинации, вступающие в контакт с организмом человека или животного, проникающие в органы, ткани организма человека или животного, применяемые для профилактики или лечения заболеваний. К лекарственным средствам относятся лекарственные препараты в виде готовых лекарственных форм, предназначенных для введения в организм животного или человека различными способами, например, не ограничиваясь указанным, перорально, сублингвально, местно, ректально, парентерально.
Выражение «находится в твердой форме» в данном контексте характеризует фармацевтические субстанции, фармацевтические композиции и лекарственные средства твердой, плотной или вязкой консистенции, при этом частицы активно взаимодействуют между собой, позволяя веществу сохранять свой размер и форму.
Термин «фармацевтическая субстанция» или «субстанция» в контексте настоящего изобретения означает технический продукт, представляющий собой по существу аморфную форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата или смесь его разных твердых форм, где по большей части присутствует аморфная форма по настоящему изобретению, синтетического или иного (биологического, биохимического, минерального, растительного, животного, микробного и прочего) происхождения, предназначенный для получения фармацевтических композиций и лекарственных средств, который в процессе производства лекарственного средства (препарата) становится активным агентом этого лекарственного средства и определяет его эффективность и физико-химические свойства. Такие вещества предназначены для проявления фармакологической активности или другого прямого эффекта при диагностике, лечении, облегчении симптомов или профилактики болезни.
Термин «содержащий», «содержит» в контексте настоящего изобретения означает, что указанные фармацевтические субстанции, фармацевтические композиции и лекарственные средства включают перечисленные компоненты, но не исключают включение других компонентов.
Термин «эффективное количество» в контексте настоящего изобретения означает количество вещества (а также комбинации веществ), которое при ведении субъекту для лечения или предотвращения заболевания, или по меньшей мере одного из клинических симптомов заболевания или нарушения является достаточным для воздействия - лечения и/или профилактики заболевания, нарушения или симптома. «Эффективное количество» определяется в зависимости от заболевания, нарушения и/или симптомов заболевания или нарушения, тяжести заболевания, нарушения и/или симптомов заболевания или нарушения, клинической картины и общего состояния здоровья пациента, а также от возраста и/или веса субъекта, которому необходимо такое лечение (профилактика).
Термин «дозировка», используемый здесь, характеризует содержание одного или нескольких активных агентов в количественном выражении на единицу дозы, или единицу объема, или единицу массы в соответствии с лекарственным средством либо для некоторых видов лекарственных средств количество высвобождаемого из лекарственного средства активного агента за единицу времени.
Термин «порошок», используемый здесь означает состояние вещества, при котором твердое вещество или вещества, входящие в его состав, находятся в свободной дисперсной системе без дисперсионной среды с дисперсионной фазой в виде твердых частиц различной формы.
«Порошковая рентгеновская дифракция» или «качественный рентгенофазовый анализ» - это аналитический метод, который позволяет качественно и количественно определять различные формы веществ в их смеси на основе анализа дифракционной картины, создаваемой при облучении исследуемого образца рентгеновскими лучами. Кристаллические вещества дают точные дифракционные максимумы, которые проявляются вблизи специфических углов, согласующихся с межплоскостными расстояниями кристаллической решетки. Напротив, аморфные вещества не обладают дальним порядком и дают уширенный пик в виде гало на дифракционной картине. Порошковая рентгеновская дифракция является самым эффективным методом для идентификации разного рода твердых форм вещества.
Термин «значение 2 тета» или «2θ», относится к положению пика на дифрактограмме исследуемого образца и представляет собой общепринятую единицу по оси абсцисс на дифракционных картинах. Рентгеновский луч падает на определенные плоскости кристаллических решеток под углом θ и отражается от них. При этом под углом 0 наблюдается дифракционный максимум для данного сорта плоскостей.
Используемый в тексте термины «примерно», «около» обозначает приблизительно плюс или минус десять процентов от указанной величины.
Термин «… представляющая собой по существу аморфную форму...» в контексте настоящего изобретения, характеризует субстанцию, которая имеет менее чем примерно 30 мас. % кристаллической формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата (в частности, менее 25 мас. %, менее 20 мас. %, менее 15 мас. %, менее 10 мас. %, менее 5 мас. %, менее 2 мас. %, менее 1 мас. % или не содержит кристаллическую форму вовсе). При этом общее содержание примесей в субстанции соответствует нормативной документации.
Термин «примеси» в контексте настоящего изобретения представляет собой любой компонент фармацевтической субстанции, который не является активным агентом. Показатель качества фармацевтической субстанции характеризует содержание в фармацевтической субстанции примесей, попавших в субстанцию в процессе ее синтеза, как производственных (технологические примеси), так и родственных, а также образующихся в ходе ее деградации при хранении, и выражающийся в процентах. Источником примесей могут являться используемые в синтезе исходных веществ реактивы, катализаторы, технологическое оборудование, остатки фильтрующих материалов, недостаточно очищенное исходное сырье, использующиеся для синтеза фармацевтических субстанций.
Термин «аморфная форма» в контексте настоящего изобретения означает твердое вещество, которое не обладает различимой кристаллической решеткой, и в котором отсутствует неограниченно повторяющаяся на больших расстояниях упорядоченность во взаимном расположении молекул в веществе, присущая кристаллам. В частности, аморфной называют форму, которая характеризуется широким максимумом (гало) и почти не демонстрирует резких пиков на рентгеновской дифрактограмме, однако при некоторых изменениях на фоне широкого максимума могут выявляться различимые пики.
Термин «широкий максимум (гало)» в контексте настоящего изобретения характеризует порошковую рентгенограмму аморфной формы вещества.
Термин «физико-химические свойства веществ» в контексте настоящего изобретения характеризует плотность, форму, размер и характер поверхности частиц, удельную поверхность частиц, силы адгезии (слипание на поверхности) и когезии (слипание частиц внутри тела), поверхностную активность, температуру плавления, растворимость, стабильность, реакционную способность веществ и тд.
Термин «технологические свойства веществ» в контексте настоящего изобретения характеризует объемную плотность, степень уплотнения, сыпучесть, влажность, фракционный состав, дисперсность, пористость, прессуемость веществ и др.
Поставленная задача решается, а заявленный технический результат достигается получением аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата.
Одним из вариантов воплощения изобретения является аморфная форма [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата, отличающаяся тем, что имеет на порошковой рентгенограмме дифракционный максимум в виде широкого гало.
Более предпочтительно аморфная форма [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению имеет на порошковой рентгенограмме дифракционный максимум в виде широкого гало в области 5-45° 2θ (±2°).
Более предпочтительно аморфная форма [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению имеет на порошковой рентгенограмме дифракционный максимум в виде широкого гало в области 10-40° 20 (±2°).
Более предпочтительно аморфная форма [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению имеет на порошковой рентгенограмме дифракционный максимум в виде широкого гало в области 13-30° 20 (±2°).
Более предпочтительно аморфная форма [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению имеет на порошковой рентгенограмме дифракционный максимум в виде широкого гало в области 17-27° 20 (±2°).
Более предпочтительно аморфная форма [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению имеет на порошковой рентгенограмме дифракционный максимум в виде широкого гало в области 19-26° 20 (±2°).
В предпочтительном варианте исполнения погрешность угла 2θ составляет ±0,2°.
Для получения аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению могут быть использованы следующие известные в уровне техники растворители, их дейтеропроизводные или их смеси: вода, аммиак, углеводороды, в том числе ароматические (пентан, ксилол, бензол, толуол и т.д.); сложные и простые эфиры (этилацетат, диэтиловый эфир, тетрагидрофуран, 1,4-диоксан, диметоксиэтан, краунэфиры и др.); спирты, в том числе многоатомные, в том числе фенолы (фенол, метанол, этанол, изопропанол, бутанол, этиленгликоль, пропиленгликоль, диэтиленгликоль и т.д.); кетоны (ацетон и т.д.); смеси углеводородов (керосин, бензин и т.д.); нитросоединения (нитрометан и т.д.); нитрилы (ацетонитрил и т.д.); амиды (диметилформамид, диметилацетамид и т.д.); циклические и ациклические тиолы; алкилгалогениды (дихлорметан, хлороформ, тетрахлорметан и т.д.); арилгалогениды (хлорбензол и т.д.); амины (триэтиламин и т.д.); петролейный эфир; сероуглерод; сульфоксиды (диметилсульфоксид и т.д.); карбонаты (пропиленкарбонат и т.д.); кислоты (муравьиная, уксусная и т.д.); гетероциклы (пиридин, морфолин, тиофен, пиррол, N-метил-2-пирролидон, имидазол и т.д.); оксиды (пропиленоксид); трет-бутилметиловый эфир; гексаметилфосфортриамид; силоксаны (гексаметилдисилоксан и т.д.), а также сверхкритические жидкости (диоксид углерода, вода, метан, этан, пропан, этилен, пропилен, метанол, этанол, ацетон, оксиды азота, оксид серы) или их смеси.
Аморфная форма [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению может быть введена в форме пролекарств. Пролекарство может включать ковалентно связанный носитель, который высвобождает активное исходное лекарственное средство при введении субъекту-млекопитающему. Пролекарства могут быть получены путем модификации функциональных групп, присутствующих в соединениях, таким образом, что модификации расщепляются, либо в ходе обычных манипуляций, либо in vivo, до исходных соединений. Пролекарства включают, например, соединения, в которых гидроксильная группа связана с любой группой, которая при введении субъекту расщепляется с образованием свободной гидроксильной группы. Примеры пролекарств включают, без ограничений, ацетатные, формиатные и бензоатные производные спиртовых функциональных групп в соединениях. Типичные пролекарства образуют активный метаболит путем превращения пролекарства гидролитическими ферментами, гидролиза амидов, лактамов, пептидов, сложных эфиров карбоновых кислот, эпоксидов или расщепления сложных эфиров неорганических кислот.
Поставленная задача решается, а заявленный технический результат также достигается созданием фармацевтической субстанции, содержащей вышеупомянутую аморфную форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата.
Одним из вариантов воплощения изобретения является вышеупомянутая фармацевтическая субстанция в форме порошка.
Одним из вариантов воплощения изобретения является фармацевтическая субстанция, содержащая аморфную форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению, отличающаяся тем, что дополнительно содержит кристаллическую форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата.
Более предпочтительно фармацевтическая субстанция, содержащая аморфную форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению, дополнительно содержит кристаллическую форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата в количестве менее 30 мас. %.
Более предпочтительно фармацевтическая субстанция, содержащая аморфную форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению, дополнительно содержит кристаллическую форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата в количестве менее 25 мас. %.
Более предпочтительно фармацевтическая субстанция, содержащая аморфную форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению, дополнительно содержит кристаллическую форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата в количестве менее 20 мас. %.
Более предпочтительно фармацевтическая субстанция, содержащая аморфную форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению, дополнительно содержит кристаллическую форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата в количестве менее 15 мас. %.
Более предпочтительно фармацевтическая субстанция, содержащая аморфную форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению, дополнительно содержит кристаллическую форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата в количестве менее 10 мас. %.
Более предпочтительно фармацевтическая субстанция, содержащая аморфную форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению, дополнительно содержит кристаллическую форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата в количестве менее 5 мас. %.
Более предпочтительно фармацевтическая субстанция, содержащая аморфную форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению, дополнительно содержит кристаллическую форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата в количестве менее 3 мас. %.
Более предпочтительно фармацевтическая субстанция, содержащая аморфную форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению, дополнительно содержит кристаллическую форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата в количестве менее 2 мас. %.
Более предпочтительно фармацевтическая субстанция, содержащая аморфную форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению, дополнительно содержит кристаллическую форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата в количестве менее 1,5 мас. %.
Более предпочтительно фармацевтическая субстанция, содержащая аморфную форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению, дополнительно содержит кристаллическую форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата в количестве менее 1,0 мас. %.
Более предпочтительно фармацевтическая субстанция, содержащая аморфную форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению, дополнительно содержит кристаллическую форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата в количестве менее 0,5 мас. %.
Более предпочтительно фармацевтическая субстанция, содержащая аморфную форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению, дополнительно содержит кристаллическую форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата в количестве менее 30 мас. %, но более 0,01 мас. %.
Более предпочтительно фармацевтическая субстанция, содержащая аморфную форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению, не содержит кристаллическую форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата.
Одним из вариантов воплощения изобретения является фармацевтическая субстанция, отличающаяся тем, что общее содержание примесей в ее составе не превышает 1 мас. % от массы фармацевтической субстанции.
Одним из вариантов воплощения изобретения является фармацевтическая субстанция, отличающаяся тем, что общее содержание примесей в ее составе менее 1 мас. %, но более 0,01 мас. % от массы фармацевтической субстанции.
Одним из вариантов воплощения изобретения является фармацевтическая субстанция, которая проявляет профилактическую и/или терапевтическую противовирусную активность.
Одним из вариантов воплощения изобретения является фармацевтическая субстанция для лечения и/или профилактики вирусных заболеваний, где вирус представляет собой РНК- содержащий вирус.
Одним из вариантов воплощения изобретения является фармацевтическая субстанция для лечения и/или профилактики вирусных заболеваний, где вирус представляет собой вирус, геном которого закодирован одноцепочечной смысловой (+)-нитью, а также антисмысловой (-)-нитью РНК и который использует вирусную РНК-зависимую-РНК-полимеразу для своей репликации.
Одним из вариантов воплощения изобретения является фармацевтическая субстанция для лечения и/или профилактики вирусных заболеваний, где вирус представляет собой высоковирулентный или низковирулентный вирус.
Одним из вариантов воплощения изобретения является фармацевтическая субстанция для лечения и/или профилактики вирусных заболеваний, где вирус представляет собой вирус гриппа, коронавирус, пикорнавирус, аренавирус, флавивирус, буньявирус, филовирус, флебовирус, хантавирус, энтеровирус, тогавирус, калицивирус, респираторно-синцитиальный вирус, вирус парагриппа, риновирусы, метапневмовирусы, тогавирус, ротавирус или норавирус.
Одним из вариантов воплощения изобретения является фармацевтическая субстанция для лечения и/или профилактики вирусных заболеваний, где вирус представляет собой вирус энцефалита, вирус Эбола, SARS-CoV, MERS-CoV, SARS-CoV-2 или Influenza А, В.
Одним из вариантов воплощения изобретения является фармацевтическая субстанция для лечения и/или профилактики вирусных заболеваний, где вирус представляет собой вирус гриппа А, включая штаммы A (H1N1), A (H1N1) pdm09, А (H1N2), A (H3N2), A (H2N2), A (H4N2), A (H7N2), свиной грипп типа А, птичий грипп типа А, включая высокопатогенные штаммы (в том числе, H5N1 и H7N9).
Поставленная задача решается, а заявленный технический результат также достигается получением фармацевтической композиции, проявляющей профилактическую и/или терапевтическую противовирусную активность, содержащей в терапевтически эффективном количестве фармацевтическую субстанцию по настоящему изобретению.
Поставленная задача решается, а заявленный технический результат также достигается получением фармацевтической композиции, проявляющей профилактическую и/или терапевтическую противовирусную активность, содержащей в терапевтически эффективном количестве аморфную форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению.
Поставленная задача решается, а заявленный технический результат также достигается получением фармацевтической композиции, проявляющей профилактическую и/или терапевтическую противовирусную активность, содержащей в терапевтически эффективном количестве аморфную форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению, и по меньшей мере, один фармацевтически приемлемый эксципиент.
Поставленная задача решается, а заявленный технический результат также достигается получением фармацевтической композиции, проявляющей профилактическую и/или терапевтическую противовирусную активность, содержащей в терапевтически эффективном количестве фармацевтическую субстанцию по настоящему изобретению и, по меньшей мере, один фармацевтически приемлемый эксципиент.
Поставленная задача решается, а заявленный технический результат также достигается получением фармацевтической композиции, проявляющей профилактическую и/или терапевтическую противовирусную активность, содержащей в терапевтически эффективном количестве фармацевтическую субстанцию аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению, и, по меньшей мере, один фармацевтически приемлемый эксципиент.
Поставленная задача решается, а заявленный технический результат также достигается получением фармацевтической композиции, проявляющей профилактическую и/или терапевтическую противовирусную активность, содержащей в терапевтически эффективном количестве фармацевтическую субстанцию, представляющую собой по существу аморфную форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению, и, по меньшей мере, один фармацевтически приемлемый эксципиент.
В некоторых вариантах осуществления фармацевтическую композицию согласно настоящему изобретению можно получить с помощью известных общепринятых способов в области фармацевтики.
Одним из вариантов воплощения изобретения является фармацевтическая композиция, в которой количество аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксо пиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата составляет от 20 до 6000 мг.
Более предпочтительно количество аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин- 1-ил]оксолан-2-ил]метил-2-метилпропаноата составляет от 20 до 5800 мг.
Более предпочтительно количество аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин- 1-ил]оксолан-2-ил]метил-2-метилпропаноата составляет от 20 до 5500 мг.
Более предпочтительно количество аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин- 1-ил]оксолан-2-ил]метил-2-метилпропаноата составляет от 20 до 5200 мг.
Более предпочтительно количество аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата составляет от 20 до 4900 мг.
Более предпочтительно количество аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата составляет от 20 до 4600 мг.
Более предпочтительно количество аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата составляет от 20 до 4300 мг.
Более предпочтительно количество аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата составляет от 20 до 4000 мг.
Более предпочтительно количество аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата составляет от 20 до 3700 мг.
Более предпочтительно количество аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин- 1-ил]оксолан-2-ил]метил-2-метилпропаноата составляет от 20 до 3400 мг.
Более предпочтительно количество аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин- 1-ил]оксолан-2-ил]метил-2-метилпропаноата составляет от 20 до 3100 мг.
Более предпочтительно количество аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин- 1-ил]оксолан-2-ил]метил-2-метилпропаноата составляет от 20 до 2800 мг.
Более предпочтительно количество аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата составляет от 20 до 2500 мг.
Более предпочтительно количество аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин- 1-ил]оксолан-2-ил]метил-2-метилпропаноата составляет от 20 до 2200 мг.
Более предпочтительно количество аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин- 1-ил]оксолан-2-ил]метил-2-метилпропаноата составляет от 20 до 1900 мг.
Более предпочтительно количество аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата составляет от 20 до 1600 мг.
Более предпочтительно количество аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин- 1-ил]оксолан-2-ил]метил-2-метилпропаноата составляет от 20 до 1300 мг.
Более предпочтительно количество аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин- 1-ил]оксолан-2-ил]метил-2-метилпропаноата составляет от 20 до 1000 мг.
Более предпочтительно количество аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата составляет от 20 до 700 мг.
Более предпочтительно количество аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата составляет от 20 до 400 мг.
Более предпочтительно количество аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин- 1-ил]оксолан-2-ил]метил-2-метилпропаноата составляет от 20 до 100 мг.
Одним из вариантов воплощения изобретения является фармацевтическая композиция, в которой фармацевтически приемлемые эксципиенты выбраны из группы, включающей формообразующие вещества, стабилизаторы, солюбилизаторы, растворители, увлажнители, лубриканты, скользящие вещества, загустители, подсластители, отдушки, ароматизаторы, фунгициды, регуляторы пролонгированной доставки, сорастворители, разбавители, наполнители, эмульгаторы, консерванты, антиоксид анты, буферные агенты, криопротекторы, регулирующие рН агенты, вещества для поддержания изотоничности или корригирующие вещества.
Одним из вариантов воплощения изобретения является фармацевтическая композиция, отличающаяся тем, что представляет собой твердую фармацевтическую композицию.
Одним из вариантов воплощения изобретения является фармацевтическая композиция для лечения и/или профилактики вирусных заболеваний, где вирус представляет собой РНК-содержащий вирус.
Одним из вариантов воплощения изобретения является фармацевтическая композиция для лечения и/или профилактики вирусных заболеваний, где вирус представляет собой вирус, геном которого закодирован одноцепочечной смысловой (+)-нитью, а также антисмысловой (-)-нитью РНК и который использует вирусную РНК-зависимую-РНК-полимеразу для своей репликации.
Более предпочтительно вирус по настоящему изобретению представляет собой вирус гриппа, коронавирус, пикорнавирус, аренавирус, флавивирус, буньявирус, филовирус, флебовирус, хантавирус, энтеровирус, тогавирус, калицивирус, респираторно-синцитиальный вирус, вирус парагриппа, риновирусы, метапневмовирусы, тогавирус, ротавирус или норавирус.
Более предпочтительно вирус по настоящему изобретению представляет собой высоковирулентный или низковирулентный вирус.
Более предпочтительно вирус по настоящему изобретению представляет собой вирус энцефалита, вирус Эбола, SARS-CoV, MERS-CoV, SARS-CoV-2 или Influenza А, В.
Более предпочтительно вирус гриппа по настоящему изобретению представляет собой, не ограничиваясь указанным, вирус гриппа А, включая штаммы A (H1N1), А (H1N1) pdm09, A (H1N2), A (H3N2), A (H2N2), A (H4N2), A (H7N2), свиной грипп типа А, птичий грипп типа А, включая высокопатогенные штаммы (в том числе, H5N1 и H7N9).
Фармацевтическая композиция наряду с фармацевтической субстанцией по настоящему изобретению может включать и другие фармацевтические субстанции, в том числе обладающие активностью, при условии, что они не вызывают нежелательных эффектов.
Поставленная задача решается, а заявленный технический результат достигается также созданием лекарственного средства, проявляющего профилактическую и/или терапевтическую активность, содержащее в терапевтически эффективном количестве фармацевтическую композицию по настоящему изобретению.
Поставленная задача решается, а заявленный технический результат достигается также созданием лекарственного средства, проявляющего профилактическую и/или терапевтическую активность, содержащее в терапевтически эффективном количестве фармацевтическую композицию по настоящему изобретению, включающую упомянутую фармацевтическую субстанцию по существу аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата.
Поставленная задача решается, а заявленный технический результат достигается также созданием лекарственного средства, проявляющего профилактическую и/или терапевтическую активность, содержащее в терапевтически эффективном количестве фармацевтическую композицию по настоящему изобретению, включающую упомянутую фармацевтическую субстанцию по настоящему изобретению, и по меньшей мере один дополнительный фармацевтически приемлемый эксципиент.
Одним из вариантов воплощения изобретения является лекарственное средство, представляющее собой твердое лекарственное средство.
Более предпочтительно твердое лекарственное средство по настоящему изобретению представляет собой, не ограничиваясь указанным, таблетку, капсулу, пеллету драже, гранулу, саше, порошок, лиофилизат.
Более предпочтительно твердое лекарственное средство по настоящему изобретению представляет собой, не ограничиваясь указанным, диспергируемую в полости рта таблетку, лиофилизированную таблетку, таблетку, покрытую оболочкой, буккальную таблетку, шипучую таблетку, таблетку с замедленным/прологрированным/ модифицированным высвобождением.
Лиофилизация (лиофильная сушка) представляет собой процесс удаления растворителя из замороженного материала путем возгонки (сублимации) кристаллов растворителя в условиях вакуума, т.е. превращения его в пар, минуя жидкую фазу. Лекарственное средство в форме лиофилизата полностью сохраняет свою фармакологическую активность.
Удаление растворителя при лиофилизациоиной сушке осуществляется главным образом за счет сублимации. Сублимация- это удаление растворителя из замороженного объекта без образования жидкой фазы, она проводится под вакуумом или значительно реже в инертном газе. Стадия замораживания является одной из определяющих стадий для получения качественного лекарственного средства в форме лиофилизата.
К вспомогательным фармацевтически приемлемым эксципиентам, используемым в лиофильно высушенных лекарственных средствах по настоящему изобретению, относятся: растворители, со-любилизаторы (ЭДТА, α-циклодекстрин и др.), наполнители (маннит, гли-цин, глюкоза, сахароза, лактоза, молоко и др.), консерванты (бензиловый спирт, этил- и метилпарагидроксибензоат и др.), регуляторы рН (буферные растворы, натрия гидроксид, хлористоводородная кислота), стабилизаторы, криопротекторы (декстран, желатин, гидроксиэтилкрахмал и др.).
В форме лиофилизатов по настоящему изобретению могут быть представлены как индивидуальные активные агенты, так и их смеси с фармацевтически приемлемыми эксципиентами.
Одним из вариантов воплощения изобретения является лекарственное средство, представляющее собой пероральное лекарственное средство.
Более предпочтительно пероральное лекарственное средство по настоящему изобретению представляет собой, не ограничиваясь указанным, таблетку, капсулу, пеллету, драже, гранулу, порошок, сироп или раствор.
Одним из вариантов воплощения изобретения является лекарственное средство, представляющее собой жидкое лекарственное средство.
Более предпочтительно жидкое лекарственное средство по настоящему изобретению представляет собой, не ограничиваясь указанным, раствор, концентрат для приготовления раствора, сироп, суспензию.
Одним из вариантов воплощения изобретения является лекарственное средство, представляющее собой паентеральное лекарственное средство.
Парентеральное введение лекарственных средств - это такие пути введения лекарственных средств в организм, при которых они минуют желудочно-кишечный тракт, в отличие от перорального способа применения лекарств. Парентеральные лекарственные средства- это стерильные препараты, предназначенные для введения путем инъекций, инфузий, ингаляций или имплантаций в организм человека или животного. К ним относятся растворы, эмульсии, суспензии, аэрозоли, порошки и таблетки для получения растворов и имплантации, порошки для ингаляций, лиофилизированные препараты для получения лекарственных форм, вводимых в организм парентерально (подкожно, внутримышечно, внутривенно, внутриартериально, в различные полости).
Парентеральные пути введения включают введение в ткани (внутрикожно, подкожно, внутримышечно, внутрикостно), в сосуды (внутривенно, внутриартериально, в лимфатические сосуды), в полости (в плевральную, брюшную, сердечную и суставную полости), в субарахноидальное пространство, а также ингаляционное, интраназальное и субконъюнктивальное введение.
Более предпочтительно парентеральное лекарственное средство представляет собой инфузионный раствор.
Более предпочтительно парентеральное лекарственное средство представляет собой инъекционный раствор.
Одним из вариантов воплощения изобретения является лекарственное средство, представляющее собой ингаляционное лекарственное средство.
Более предпочтительно ингаляционное лекарственное средство по настоящему изобретению представляет собой, не ограничиваясь указанным, аэрозоль, порошок или пульмопорошок.
Одним из вариантов воплощения изобретения является лекарственное средство, представляющее собой лекарственное средство для местного введения.
Под местным введением лекарственных средств понимается нанесение лекарственного препарата на слизистые оболочки (в т.ч. глазное, назальное, ректальное, вагинальное применение, нанесение на десны, слизистую оболочку полости рта и др.), а также введение в наружный слуховой проход.
Более предпочтительно местное лекарственное средство по настоящему изобретению представляет собой лекарственное средство для глазного, назального и ректального введения.
Одним из вариантов воплощения изобретения является лекарственное средство, представляющее собой ректальное лекарственное средство.
Более предпочтительно ректальное лекарственное средство по настоящему изобретению представляет собой, не ограничиваясь указанным, суппозитории или капсулы.
Одним из вариантов воплощения изобретения является лекарственное средство, в котором фармацевтически приемлемые эксципиенты выбраны из группы, включающей, не ограничиваясь указанным, формообразующие вещества, стабилизаторы, солюбилизаторы, растворители, увлажнители, лубриканты, скользящие вещества, загустители, подсластители, отдушки, ароматизаторы, фунгициды, регуляторы пролонгированной доставки, сорастворители, разбавители, наполнители, эмульгаторы, консерванты, антиоксид анты, буферные агенты, криопротекторы, регулирующие рН агенты, вещества для поддержания изотоничности или корригирующие вещества.
Более предпочтительно растворитель по настоящему изобретению представляет собой, не ограничиваясь указанным, физиологический раствор, инъекционную воду, апирогенную воду, дистиллированную воду, раствор Рингера или раствор глюкозы.
Поставленная задача решается, а заявленный технический результат достигается за счет применения аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению, для получения фармацевтической субстанции для лечения и/или профилактики вирусных заболеваний.
Поставленная задача решается, а заявленный технический результат достигается за счет применения фармацевтической субстанции аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению для получения фармацевтической композиции для лечения и/или профилактики вирусных заболеваний.
Поставленная задача решается, а заявленный технический результат достигается за счет применения фармацевтической композиции по настоящему изобретению для получения лекарственного средства для лечения и/или профилактики вирусных заболеваний.
Поставленная задача решается, а заявленный технический результат достигается за счет применения аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата и для лечения и/или профилактики вирусных заболеваний.
Поставленная задача решается, а заявленный технический результат достигается за счет применения аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата в составе фармацевтической субстанции, содержащейся в фармацевтической композиции для лечения и/или профилактики вирусных заболеваний.
Поставленная задача решается, а заявленный технический результат достигается за счет применения фармацевтической субстанции по настоящему изобретению в составе фармацевтической композиции для лечения и/или профилактики вирусных заболеваний.
Поставленная задача решается, а заявленный технический результат достигается за счет применения фармацевтической субстанции, представляющей собой по существу аморфную форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата, в составе фармацевтической композиции для лечения и/или профилактики вирусных заболеваний.
Поставленная задача решается, а заявленный технический результат достигается за счет применения фармацевтической композиции или лекарственного средства по настоящему изобретению для лечения и/или профилактики вирусных заболеваний.
Более предпочтительно вирусная инфекция по настоящему изобретению представляет собой вирус энцефалита, вирус Эбола, SARS-CoV, MERS-CoV, SARS-CoV-2 или Influenza А, В.
Далее приводятся примеры осуществления изобретения, которые иллюстрируют изобретение, но не охватывают все возможные варианты его осуществления и не ограничивают изобретение.
Специалисту в данной области понятно, что возможны и другие частные варианты осуществления изобретения.
Примеры
Пример 1. Способ получения аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата.
Рассчитанное количество исходного сырья [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата растворяли в смеси растворителей ацетонитрил/тетрагидрофуран (ТГФ)/ диметилсульфоксид (ДМСО) в объемных соотношениях в интервале 1:2:0,5-1:10:1,5 соответственно при температуре 20-30°С при перемешивании. Затем проводили ультразвуковую обработку смеси и добавляли толуол в количестве равном 10-15% от общего объема смеси. После чего смесь резко охлаждали до 0°С. Наблюдали образование белого аморфного осадка. Осадок фильтровали, сушили при пониженном давлении при 35°С.
Идентичность химической формулы аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата подтверждена методами ЯМР и элементным анализом.
1Н ЯМР (600 МГц, CD3OD): δ 6,94 (d, J=8,1 Гц, 1Н), 5,78 (d, J=4,6 Гц, Ш), 5,63 (d, J=8,2 Гц, 1Н), 4,25 (d, J=3,7 Гц, 2Н), 4,14 (t, J=5,0 Гц, 1Н), 4,10 (m, 2Н), 2,60 (m, 1H), 1,23 (d, J=7,2 Гц, 6Н); 13C NMR (75 МГц, CD3OD): δ 178,4, 151,8, 146,4, 132,1, 99,7, 90,8, 82,7, 74,7, 71,7, 65,3, 35,6, 27,5, 19,7, 19,5.
Элементный анализ C13H19N3O7: рассчитано С 47,42%, Н 5,82%, N 12,76%, О 34,01%; найдено С 47,54%, Н 5,90%, N 12,64%, О 33,94%.
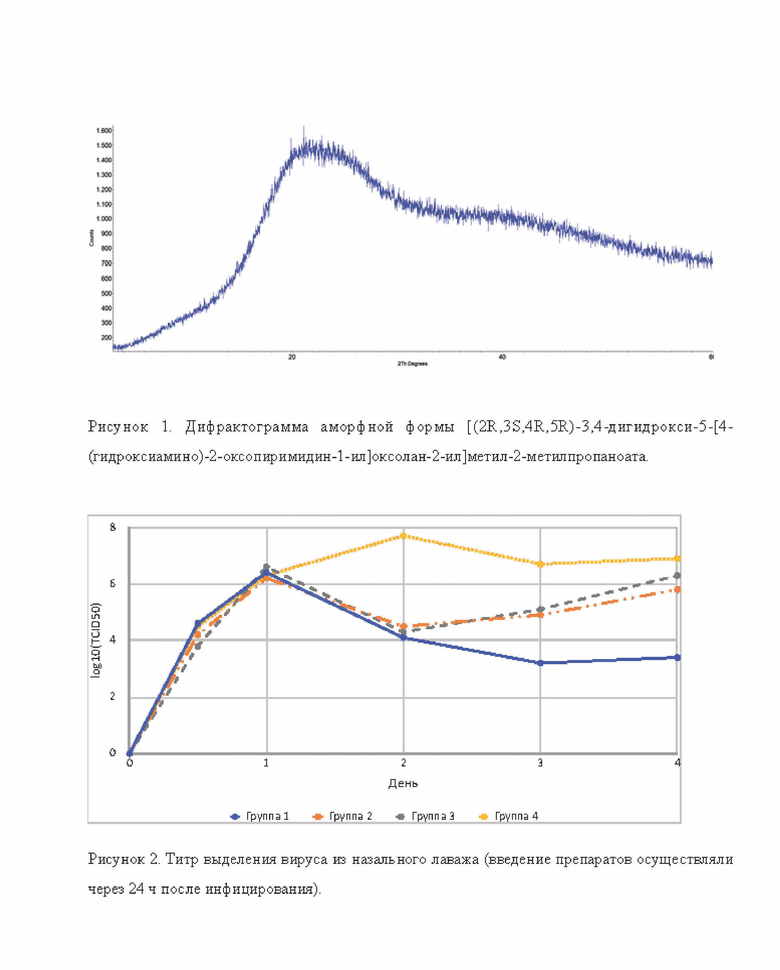
Картина порошковой рентгеновской дифракции аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-l-ил]оксолан-2-ил]метил-2-метилпропаноата была получена с помощью дифрактометра, оборудованного германиевым монохроматором и системой щелей для монохроматизации и фокусировки (λ[CuKα]=1,5406 Å), а также позиционно-чувствительным детектором с использованием геометрии на пропускание.
На дифрактограмме аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата наблюдали характерный дифракционный максимум в виде широкого гало в области 13-30° 29 (±2°) (рис. 1).
При этом в ряде экспериментов отмечались улучшенные характеристики новой аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по настоящему изобретению, в частности, улучшение стабильности с сохранением показателей растворимости и уменьшение гигроскопичности.
Пример 2. Получение лекарственных форм аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата.
2.1. Раствор
Заявленный раствор получали следующим способом: в снабженный примешивающим устройством и термостатирующей рубашкой аппарат для приготовления растворов помещали воду для инъекций и нагревали при непрерывном перемешивании до температуры 50-65°С, далее прибавляли рассчитанное количество маннитола и перемешивали до полного растворения. К полученному раствору прибавляли рассчитанное количество аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата и перемешивали при температуре 60-70°С до получения прозрачного раствора. Далее раствор доводили до объема 1000 мл водой для инъекций и фильтровали через мембранный фильтр 0,22 мкм.
2.2. Лиофилизат
Полученный в п. 2.1. Раствор подвергали лиофильной сушке. На выходе получали твердое лекарственное средство в виде лиофилизата аморфной формы [(2R,3S,4R,5R)-3,4-дигидр окси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата.
2.3. Таблетки
Для получения твердого лекарственного средства в форме таблетки, содержащего аморфную форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата в качестве активного агента в гранулятор последовательно загружали повидон, аморфную форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата и лактозы. Полученную смесь перемешивали мешалкой с последующим добавлением увлажнителя. Процесс перемешивания продолжали до полного внесения увлажнителя.
Полученную фармацевтическую композицию гранулировали с последующей сушкой гранул в установке кипящий слой. Далее гранулы калибровали через сито с размером ячеек 1 мм.
Для получения готовой фармацевтической композиции для таблетирования, полученный гранулят смешивали с кросповидоном и кремнием диоксидом коллоидным в гравиметрическом смесителе. Полученную фармацевтическую композицию опудривали стеаратом магния с последующим таблетированием на роторном таблетпрессе. Далее таблетки покрывали пленочной оболочкой.
Пример 3. Изучение терапевтической активности аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата.
Эксперимент проводили на 40 половозрелых мышах, которых содержали в стандартных условиях вивария, давали стерильный корм для грызунов и стерильную воду.
Моделирование вирусной инфекции у мышей проводили путем интраназального введения вирусных единиц высокопатогенного вируса H1N1 при анастезировании особей.
В ходе эксперимента ежедневно оценивали интегральные показатели (изменение веса животных) и оценивали клиническую симптоматику (лихорадка, слизистые выделения, уровень активности, дыхание).
Для проведения эксперимента животных разделили на четыре группы по 10 особей в каждой. Первой группе вводили [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноат в аморфной форме, полученной по примеру 1 настоящего изобретения. Вторая и третья группы получали лечение [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноатом в кристаллических формах I, II соответственно, полученных согласно методикам, описанным в источнике CN113307834. Четвертой группе (контроль) вводили микрокристаллическую целлюлозу.
Лечение начинали через 24 часа после инфицирования. Особям вводили по 800 мг (дозы представлены в пересчете на человека) [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата в описанных выше модификациях перорально при помощи зонда два раза в день в течение одного дня после инфицирования. Аналогично четвертая группа получала микрокристаллическую целлюлозу в виде суспензии через зонд 2 раза в день. Далее в ходе исследования ежедневно фиксировали вирусную нагрузку назального лаважа. Титры вируса определяли с помощью стандартного метода образования бляшек [Строганова, И.Я. Использование в вирусологии культуры клеток: метод, указания / И.Я. Строганова, А.А. Трухоненко; Краснояр. гос.аграр. ун-т. Красноярск, 2013. 48 с.]. Результаты измерений, усредненные по группам, представлены на рис. 2. Результаты эксперимента наглядно демонстрируют значительное снижение титра вируса в группах 1-3 уже на 2 день эксперимента, при этом отмечалось снижение лихорадки по сравнению с группой 4 (контроль). Спустя два дня после терапии (4 день эксперимента) в группе 1 сохранялся терапевтический эффект, при этом не фиксировалось существенное повышение температуры и снижение веса особей. Напротив, в группах 2-3 наблюдалось повышение вирусной нагрузки, сопровождающееся лихорадкой и уменьшением веса особей. Таким образом, новая аморфная форма [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата проявляет противовирусную активность, при этом наблюдается увеличение продолжительности терапевтического эффекта по сравнению с известными кристаллическими формами [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата. Такие свойства новой аморфной формы [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата позволяют использовать ее в дальнейших разработках различных лекарственных форм со сниженной дозировкой, что может улучшить профиль безопасности продукта.
Изобретение относится к области медицины, фармакологии и химико-фармацевтической промышленности, а именно к аморфной форме [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата, отличающейся тем, что имеет на порошковой рентгенограмме дифракционный максимум в виде одного широкого гало в области 10-30° 2θ (±2°). Изобретение относится к фармацевтической композиции, проявляющей профилактическую и/или терапевтическую противовирусную активность в отношении вирусов, геном которых закодирован одноцепочечной смысловой (+)-нитью, а также антисмысловой (-)-нитью РНК, и которые используют вирусную РНК-зависимую-РНК-полимеразу для своей репликации, содержащей в эффективном количестве аморфную форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата и по меньшей мере один фармацевтически приемлемый эксципиент. Также изобретение относится к лекарственному средству, проявляющему профилактическую и/или терапевтическую противовирусную активность в отношении вирусов, геном которых закодирован одноцепочечной смысловой (+)-нитью, а также антисмысловой (-)-нитью РНК, и которые используют вирусную РНК-зависимую-РНК-полимеразу для своей репликации, содержащее в эффективном количестве фармацевтическую композицию по изобретению. Технический результат - увеличение продолжительности противовирусной активности, а также улучшение физико-химических и технологических свойств аморфной формы [(2R,3R,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата. 4 н. и 9 з.п. ф-лы, 2 ил., 3 пр.
1. Аморфная форма [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата, отличающаяся тем, что имеет на порошковой рентгенограмме дифракционный максимум в виде одного широкого гало в области 10-30° 2θ (±2°).
2. Фармацевтическая композиция, проявляющая профилактическую и/или терапевтическую противовирусную активность в отношении вирусов, геном которых закодирован одноцепочечной смысловой (+)-нитью, а также антисмысловой (-)-нитью РНК, и которые используют вирусную РНК-зависимую-РНК-полимеразу для своей репликации, содержащая в эффективном количестве аморфную форму [(2R,3S,4R,5R)-3,4-дигидрокси-5-[4-(гидроксиамино)-2-оксопиримидин-1-ил]оксолан-2-ил]метил-2-метилпропаноата по п. 1, и по меньшей мере, один фармацевтически приемлемый эксципиент.
3. Фармацевтическая композиция по п. 2, отличающаяся тем, что фармацевтически приемлемые эксципиенты выбраны из группы, включающей формообразующие вещества, стабилизаторы, солюбилизаторы, растворители, увлажнители, лубриканты, скользящие вещества, загустители, подсластители, отдушки, ароматизаторы, фунгициды, регуляторы пролонгированной доставки, сорастворители, разбавители, наполнители, эмульгаторы, консерванты, антиоксиданты, буферные агенты, криопротекторы, регулирующие рН агенты, вещества для поддержания изотоничности или корригирующие вещества.
4. Фармацевтическая композиция по п. 2, отличающаяся тем, что представляет собой твердую фармацевтическую композицию.
5. Фармацевтическая композиция по п. 2, отличающаяся тем, что находится в форме порошка.
6. Фармацевтическая композиция по п. 2, где вирус представляет собой вирус энцефалита, вирус Эбола, SARS-CoV, MERS-CoV, SARS-CoV-2 или Influenza А, В.
7. Лекарственное средство, проявляющее профилактическую и/или терапевтическую противовирусную активность в отношении вирусов, геном которых закодирован одноцепочечной смысловой (+)-нитью, а также антисмысловой (-)-нитью РНК, и которые используют вирусную РНК-зависимую-РНК-полимеразу для своей репликации, содержащее в эффективном количестве фармацевтическую композицию по любому из пп. 2-6.
8. Лекарственное средство по п. 7, отличающееся тем, что представляет собой твердое лекарственное средство.
9. Лекарственное средство по п. 8, отличающееся тем, что представляет собой таблетку, капсулу, порошок, лиофилизат, саше, пеллету, гранулу.
10. Лекарственное средство по п. 9, отличающееся тем, что представляет собой диспергируемую в полости рта таблетку, лиофилизированную таблетку, таблетку, покрытую оболочкой.
11. Лекарственное средство по п. 7, отличающееся тем, что представляет собой пероральное лекарственное средство.
12. Применение фармацевтической композиции по любому из пп. 2-6 или лекарственного средства по любому из пп. 7-11 для лечения и/или профилактики вирусных заболеваний в отношении вирусов, геном которых закодирован одноцепочечной смысловой (+)-нитью, а также антисмысловой (-)-нитью РНК и которые используют вирусную РНК-зависимую-РНК-полимеразу для своей репликации.
13. Применение по п. 12, где вирусная инфекция представляет собой вирус энцефалита, вирус Эбола, SARS-CoV, MERS-CoV, SARS-CoV-2 или Influenza А, В.
| WO 2019113462 А1, 13.06.2019 | |||
| Toots M, и др.: "Quantitative efficacy paradigms of the influenza clinical drug candidate EIDD-2801 in the ferret model", Transl Res | |||
| Способ восстановления спиралей из вольфрамовой проволоки для электрических ламп накаливания, наполненных газом | 1924 |
|
SU2020A1 |
| Laitinen, Riikka et al | |||
| "Emerging trends in the stabilization of amorphous drugs." International journal of pharmaceutics | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| Разборное приспособление для накатки на рельсы сошедших с них колес подвижного состава | 1920 |
|
SU65A1 |
| НАНОАМОРФНАЯ ФОРМА (RS)-3-(4-АМИНО-1-ОКСО-1,3-ДИГИДРО-2Н-ИЗОИНДОЛ-2-ИЛ)ПИПЕРИДИН-2,6-ДИОН (ВАРИАНТЫ), СПОСОБ ЕЁ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ ИММУНОЛОГИЧЕСКИХ ИЛИ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2019 |
|
RU2723624C1 |
Авторы
Даты
2025-03-31—Публикация
2021-11-24—Подача