Область техники
Настоящее изобретение относится к молекулам антител, которые связывают мезотелин (MSLN). Указанные молекулы антител находят применение в лечении и диагностике заболеваний и нарушений, таких как рак.
Уровень техники
MSLN экспрессируется на относительно низких уровнях на мезотелиальных клетках, выстилающих плевру, брюшину и перикард (Hassan et al., 2005), у здоровых индивидуумов, но экспрессируется на высоком уровне в случае некоторых различных раковых заболеваний, включая мезотелиомы, плоскоклеточные карциномы, рак поджелудочной железы, рак легкого, желудка, молочной железы, эндометрия и яичников. Нормальная биологическая функция мезотелина неизвестна. В случае рака высокие уровни экспрессии MSLN коррелировали с неблагоприятным прогнозом при раке яичников, холангиокарциноме, аденокарциноме легкого и трижды негативном раке молочной железы. Ограниченная экспрессия MSLN на здоровых клетках в сравнении с высоким уровнем экспрессии на клетках опухоли делает его привлекательной мишенью для терапии с применением моноклональных антител (Hassan et al., 2016).
MSLN экспрессируется в виде белка-предшественника массой 69 кДа (628 аминокислот). Затем указанный белок-предшественник расщепляется под действием эндопротеазы фурина с высвобождением секретируемой N-концевой области, называемой мегакариоцит-потенцирующим фактором (MPF), в то время как зрелый белок MSLN массой 40 кДа остается присоединенным к клеточной мембране через гликозилфосфатидилинозитольный (GPI) линкер. Аминокислотная последовательность MSLN человека обладает 60% и 87% идентичностью аминокислотной последовательности ортологов MSLN мыши и яванского макака соответственно.
Мембраносвязанный зрелый MSLN отделяется от клеток в результате альтернативного сплайсинга за счет образования вариантов, в которых отсутствует последовательность, представляющая собой мембранный якорь, или протеазного расщепления под действием фермента, конвертирующего фактор некроза опухоли-α (TACE) (Sapede et al., 2008, Zhang et al., 2011). Растворимый отделенный MSLN детектируют в сыворотке крови у пациентов и в строме опухолей, включая злокачественную мезотелиому, рак яичников или высокометастатические раковые опухоли. FDA США одобрило измерение уровней растворимого MSLN в крови и экссудатах у пациентов, страдающих мезотелиомой, для мониторинга ответа пациентов на лечение и прогрессирования (Hollevoet et al., 2012, Creany et al., 2015).
Было разработано и протестировано в клинических исследованиях несколько видов терапии на основе антител, нацеленных на MSLN, преимущественно при мезотелиоме, раке поджелудочной железы и немелкоклеточном раке легкого (Hassan et al., 2016). Применяемые стратегии включают непосредственное уничтожение клеток опухоли путем применения антител к MSLN, таких как аматуксимаб, обладающих активностью в виде антителозависимой клеточноопосредованной цитотоксичности (АЗКЦ), а также путем применения конъюгатов антитело-лекарственное средство (ADC), таких как SS1P-PE38 и анетумаб-равтансин, содержащих антитело или фрагмент антитела, конъюгированный с токсином. Кроме того, Fv-фрагменты, связывающие MSLN, применяли в терапии Т-клетками с химерными антигенными рецепторами, а биспецифичные антитела, такие как ABBV-428, переходят из доклинических исследований на стадию клинических исследований.
Аматуксимаб представляет собой химерное моноклональное антитело (mAb) IgG1-каппа мыши, которое блокирует взаимодействие MSLN-MUC16 и действует на основе функции АЗКЦ для уничтожения клеток опухоли. Исследования I фазы продемонстрировали хороший профиль безопасности, но ограниченную клиническую эффективность при комбинировании с химиотерапией (гемцитабин или пеметрексед/цисплатин) с минимальным/отсутствующим увеличением выживаемости без прогрессирования при злокачественной мезотелиоме (NCT00738582, Hassan et al., 2014) и отсутствием общего ответа по сравнению с группой, получающей препарат сравнения, при раке поджелудочной железы (NCT00570713). SS1-PE-38 представляет собой рекомбинантный иммунотоксин, содержащий scFv к MSLN, присутствующий в аматуксимабе, связанный с ингибитором синтеза белка PE38. Несмотря на высокую противоопухолевую активность, наблюдаемую в исследованиях I фазы (частичный ответ 77% при комбинировании с химиотерапией, NCT01445392), клиническое применение SS1P ограничено иммуногенностью и дозолимитирующим синдромом пропотевания жидкости из сосудов. LMB-100, оптимизированный вариант SS1P-PE38 с пониженной иммуногенностью in vitro, в настоящее время тестируют в исследованиях I и II фаз отдельно и в комбинации с химиотерапией (NCT02798536, NCT02810418).
Нацеливание на MSLN чаще всего применяют для доставки цитотоксических лекарственных средств в клетки опухоли. Анетумаб-равтансин, IgG1 полностью человеческого происхождения, ковалентно связанный с антимитотическим агентом DM4, демонстрировал общую частоту ответа (ОЧО) 31% в исследованиях I фазы с раком яичников, первичным перитонеальным раком, раком фаллопиевой трубы и распространенной преимущественно эпителиоидной перитонеальной мезотелиомой (NCT01439152). При мезотелиоме анетумаб-равтансин продемонстрировал ОЧО 50% в комбинации с введением стандартных доз химиотерапии (NCT02639091). Как и другое лекарственное средство на основе ADC, RG7600, анетумаб-равтансин демонстрировал приемлемый профиль безопасности, но в этих исследованиях наблюдали дозолимитирующую токсичность, согласующуюся с той, о которой сообщали для соответствующих компонентов ADC. На сегодняшний день данные I фазы BMS86148 еще не доступны.
Таким образом, неконъюгированные антитела, нацеленные на MSLN, продемонстрировали благоприятные профили безопасности, но их терапевтическая эффективность была ограничена, тогда как ADC продемонстрировали более высокую противоопухолевую активность, но были связаны с дозолимитирующей токсичностью. С точки зрения безопасности у ADC может быть большее терапевтическое окно, чем у терапии иммунотоксинами (Zhao et al., 2016). Для ряда этих направленных на MSLN лекарственных средств на основе антител в настоящее время продолжаются клинические исследования II фазы, в которых указанное лекарственное средство комбинируют либо с химиотерапией, либо с ингибиторами иммунных контрольных точек, например, PD-1 или PD-L1. Также разрабатывают несколько биспецифичных молекул, предназначенных для вовлечения иммунной системы, включая ABBV-428, нацеленную на MSLN, а также костимулирующий белок CD40, привлекающий T-клетки MSLN-CD3-биспецифичный активатор (BITE) и MSLN-CD47-биспецифичную молекулу.
Сущность изобретения
Как описано выше, известно, что зрелый MSLN подобно другим опухолеассоциированным антигенам (TAA) отделяется от клеточной поверхности в результате ферментативного расщепления. Затем указанная отделенная/растворимая часть MSLN удаляется из области опухоли. Это представляет собой проблему для лекарственных средств, нацеленных на MSLN, поскольку указанная отделенная/растворимая часть может выступать в качестве «поглотителя» лекарственного средства и удалять лекарственное средство из области опухоли до того, как оно свяжется с опухолью.
Авторы настоящего изобретения провели обширную программу отбора для выделения молекул антител, которые связываются с более высокой аффинностью с иммобилизованным MSLN, чем с MSLN в растворе.
В настоящем описании термин «аффинность» может относиться к силе связывающего взаимодействия между молекулой антитела и распознаваемым антигеном, измеряемой по KD. Для специалиста понятно, что когда молекула антитела способна осуществлять множественные связывающие взаимодействия с антигеном (например, когда молекула антитела способна двухвалентно связывать антиген и, необязательно, указанный антиген является димерным), на аффинность, измеряемую по KD, может также влиять авидность, при этом термин «авидность» относится к общей прочности комплекса антитело-антиген.
В частности, полагают, что молекулы антител согласно настоящему изобретению связываются с MSLN с высокой авидностью и таким образом связывают MSLN сильнее, когда антитело способно связываться с двумя молекулами MSLN, как в случае, когда несколько копий указанного антигена иммобилизованы на поверхности, чем когда MSLN имеет форму мономера, как ожидают в случае с MSLN в растворе. Не желая быть связанными какой-либо теорией, соответственно, полагают, что молекулы антител согласно настоящему изобретению не будут оставаться связанными с отделенным MSLN в растворе in vivo из-за низкой аффинности антител к мономерному MSLN и, таким образом, не будут удаляться из области опухоли так быстро и, следовательно, будет больше времени для оказания терапевтического эффекта путем связывания MSLN на поверхности клеток опухоли. Ранее сообщали о предпочтительном нацеливании на мембраносвязанный MSLN, хотя рассматриваемые молекулы выделяли с применением подходов, отличных от применяемых авторами настоящего изобретения. В частности, существуют данные о предпочтительном нацеливании на мембраносвязанный MSLN посредством выделения молекул, нацеленных на другие области MSLN (Asgarov et al., 2017; Tang et al., 2013). Например, существуют данные об однодоменном (только вариабельный домен тяжелой цепи (VH)) антителе, слитом с Fc человека, SD1-Fc, которое нацелено на эпитоп, близкий к клеточной мембране, чтобы способствовать активности в виде комплементзависимой цитотоксичности (КЗЦ) (Tang et al., 2013). Однако неясно, насколько экспонированы такие эпитопы в условиях различных видов рака. Более того, также существуют данные о том, что привлекающий T-клетки MSLN-CD3-биспецифичный активатор (BITE) предпочтительно связывается с MSLN, связанным с клеткой. Однако ни одна из этих молекул не является полноразмерной молекулой IgG и ни одна из них не способна двухвалентно связываться с MSLN, поскольку обе демонстрируют одновалентное связывание с мишенью (через VH-домен в SD1-Fc или scFv в BITE).
Молекулы антител, выделенные авторами настоящего изобретения, связывают разные эпитопы/области на MSLN. Это понятно исходя из того факта, что некоторые молекулы антител способны блокировать связывание лиганда MUC16 с MSLN, тогда как другие - нет. Считают, что блокирование связывания MUC16 с MSLN является предпочтительным для ингибирования метастазирования раковых клеток, экспрессирующих MUC16, на поверхностях, экспрессирующи MSLN, в плевре и брюшине (Chen et al., 2013). Другие области связывания, расположенные ближе к клеточной мембране, могут способствовать АЗКЦ- или КЗЦ-активности.
Было показано, что молекулы антител к MSLN согласно настоящему изобретению обладают АЗКЦ-активностью и, соответственно, ожидают, что они найдут применение в лечении рака. В частности, было показано, что молекулы антител способны нацеливаться на клетки опухоли, содержащие MSLN на своей клеточной поверхности, и опосредовать уничтожение указанных клеток опухоли через АЗКЦ.
Молекулы антител согласно настоящему изобретению могут также подходить для получения ADC, содержащих молекулу антитела согласно настоящему изобретению и биоактивную молекулу, такую как токсин. Ожидают, что такие молекулы также найдут применение в лечении раковых опухолей, содержащих MSLN на своей клеточной поверхности, посредством направленной доставки биоактивной молекулы в клетку опухоли.
Авторы настоящего изобретения определили, что антитела к MSLN согласно настоящему изобретению можно применять для получения мультиспецифичных, например биспецифичных, молекул, которые связывают второй антиген в дополнение к MSLN. Предпочтительно, мультиспецифичная молекула двухвалентно связывает второй антиген. В частности, авторы настоящего изобретения получили молекулы антител к MSLN, содержащие дополнительный антигенсвязывающий сайт в каждом из CH3-доменов молекулы антитела, которые способны двухвалентно связывать второй антиген.
Указанный второй антиген, связываемый молекулой антитела, может представлять собой антиген иммунной клетки, такой как представитель суперсемейства рецепторов фактора некроза опухоли (TNFRSF). Для активации рецепторам фактора некроза опухоли (TNF) необходима кластеризация. В частности, первоначальное связывание лиганда рецептора TNF с рецептором инициирует цепочку событий, которая приводит к тримеризации рецептора TNF с последующей кластеризацией рецептора, активацией внутриклеточного пути передачи сигнала NFkB и последующей активации иммунных клеток. Соответственно, ожидают, что для эффективной активации рецептора TNFR терапевтическим агентом необходимо, чтобы несколько мономеров рецептора TNF были связаны друг с другом мостиковой связью способом, имитирующим тримерный лиганд. Для многих агонистических антител к рецептору TNF либо необходимо перекрестное связывание Fcγ-рецепторами для агонистической активности, либо они проявляют агонистическую активность в отсутствии перекрестного связывания. В обоих случаях указанная агонистическая активность антитела не ограничивается конкретной областью, поскольку Fcγ-рецепторы детектируют по всему организму человека.
Ожидают, что биспецифичные молекулы антител к MSLN, содержащие связывающие сайты в константном домене для антигена иммунных клеток, будут способны активировать указанный антиген иммунных клеток при определенных условиях в присутствии MSLN без необходимости, например, в перекрестном связывании, опосредованном Fcγ-рецепторами, необходимом для традиционных молекул антител. Полагают, что связывание молекул антител с MSLN будет вызывать перекрестное связывание молекул антител в области MSLN, что, в свою очередь, приведет к кластеризации и активации антигена иммунной клетки на поверхности иммунной клетки. Соответственно, ожидают, что агонистическая активность молекул антител будет зависеть от присутствия как антигена иммунной клетки, так и MSLN. Другими словами, ожидают, что агонистическая активность будет зависеть от определенных условий. Кроме того, полагают, что перекрестное связывание антител в присутствии MSLN способствует кластеризации антигена иммунной клетки, связанного через антигенсвязывающие сайты константного домена молекулы антитела. Поскольку MSLN представляет собой опухолевый антиген, соответственно ожидают, что молекулы антител будут способны активировать иммунные клетки способом, зависящим от заболевания, например в микроокружении опухоли. Ожидают, что такая прицельная активация иммунных клеток поможет избежать побочных эффектов, обусловленных неспецифичным воздействием. Авторы настоящего изобретения показали, что биспецифичные молекулы антител, содержащие связывающий сайт для MSLN и CD137, были способны ингибировать рост опухоли и увеличивать выживаемость в отсутствии связывания Fcγ-рецептора в модели опухоли у мышей.
Молекулы антител, содержащие связывающие сайты для MSLN в Fab и связывающие сайты в CH3 домене, специфичные в отношении второго антигена, двухвалентно связывают как MSLN, так и второй антиген. В случае, когда второй антиген является антигеном иммунной клетки, ожидают, что двухвалентное связывание обеих мишеней сделает мостиковую связь между иммунной клеткой, экспрессирующей указанный антиген иммунной клетки, и MSLN более стабильной и таким образом увеличит время, на протяжении которого иммунная клетка будет локализована в конкретной области, таком как микроокружение опухоли, и сможет действовать на заболевание, например, опухоль. Это отличается от подавляющего большинства традиционных форматов биспецифичных антител, которые являются гетеродимерными и одновалентно связывают каждый антиген-мишень через одну Fab-область. Ожидают, что такое одновалентное взаимодействие будет не только менее стабильным, но и во многих случаях недостаточным для индукции кластеризации антигенов иммунных клеток, таких как рецепторы TNF в первую очередь.
Еще одним свойством молекул антител к MSLN согласно настоящему изобретению, содержащих связывающие сайты в CH3-домене, специфичные в отношении второго антигена, является то, что оба антигенсвязывающих сайта для MSLN и второго антигена содержатся в самой структуре антитела. В частности, для указанных молекул антител нет необходимости в слиянии других белков с молекулой антитела через линкеры или другим способом для получения в результате молекулы, которая двухвалентно связывается с обеими мишенями. Это имеет ряд преимуществ. В частности, молекулы антител могут быть получены с применением способов, аналогичных тем, которые применяют для получения стандартных антител, поскольку они не содержат никаких дополнительных слитых областей. Также ожидают, что такая структура обеспечит повышенную стабильность антитела, поскольку линкеры могут со временем распадаться и приводить к гетерогенной популяции молекул антител. Те антитела в популяции, которые содержат только один слитый белок, могут не быть способны индуцировать условный агонизм в отношении антигенов иммунных клеток, таких как рецепторы TNF, так же эффективно, как антитела, содержащие два слитых белка. Расщепление/распад линкера может происходить до введения или после введения лекарственного средства пациенту (например, путем ферментативного расщепления или под действием pH пациента in vivo) и таким образом приводить к снижению его эффективности при циркуляции у пациента. Поскольку в молекулах антител линкеры отсутствуют, ожидают, что молекулы антител будут сохранять одинаковое количество связывающих сайтов как до, так и после введения. Более того, структура молекул антител также является предпочтительной с точки зрения иммуногенности молекул, поскольку введение слитых белков или линкеров, или того и другого может индуцировать иммуногенность при введении указанных молекул пациенту и приводить к снижению эффективности лекарственного средства.
Таким образом, согласно настоящему изобретению предложены:
[1] Молекула антитела, которая связывается с мезотелином (MSLN), при этом антигенсвязывающий сайт указанной молекулы антитела содержит определяющие комплементарность области (CDR) 1-6 антитела:
(i) FS28-256-271, указанные под SEQ ID NO 98, 73, 99, 20, 21 и 44 соответственно;
(ii) FS28-024-052, указанные под SEQ ID NO 10, 11, 41, 20, 21 и 22 соответственно;
(iii) FS28-256-021, указанные под SEQ ID NO 98, 73, 99, 20, 21 и 34 соответственно;
(iv) FS28-256-012, указанные под SEQ ID NO 98, 73, 99, 20, 21 и 25 соответственно;
(v) FS28-256-023, указанные под SEQ ID NO 101, 73, 103, 20, 21 и 34 соответственно;
(vi) FS28-256-024, указанные под SEQ ID NO 98, 73, 99, 20, 21 и 43 соответственно;
(vii) FS28-256-026, указанные под SEQ ID NO 101, 73, 103, 20, 21 и 43 соответственно;
(viii) FS28-256-027, указанные под SEQ ID NO 98, 73, 99, 20, 21 и 44 соответственно;
(ix) FS28-256-001, указанные под SEQ ID NO 85, 73, 75, 20, 21 и 34 соответственно;
(x) FS28-256-005, указанные под SEQ ID NO 85, 73, 75, 20, 21 и 43 соответственно;
(xi) FS28-256-014, указанные под SEQ ID NO 111, 73, 113, 20, 21 и 25 соответственно;
(xii) FS28-256-018, указанные под SEQ ID NO 101, 73, 103, 20, 21 и 25 соответственно;
(xiii) FS28-256, указанные под SEQ ID NO 71, 73, 75, 20, 21 и 25 соответственно;
(xiv) FS28-024-051, указанные под SEQ ID NO 10, 11, 32, 20, 21 и 22 соответственно;
(xv) FS28-024-053, указанные под SEQ ID NO 10, 11, 51, 20, 21 и 22 соответственно; или
(xvi) FS28-024, указанные под SEQ ID NO 10, 11, 12, 20, 21 и 22 соответственно; и
где последовательности CDR определены в соответствии со схемой нумерации ImMunoGeneTics (IMGT).
[2] Молекула антитела, которая связывается с MSLN, при этом антигенсвязывающий сайт указанной молекулы содержит CDR 1-6 антитела:
(i) FS28-256-271, указанные под SEQ ID NO 97, 182, 100, 23, 24 и 44 соответственно;
(ii) FS28-024-052, указанные под SEQ ID NO 13, 14, 42, 23, 24 и 22 соответственно;
(iii) FS28-256-021, указанные под SEQ ID NO 97, 74, 100, 23, 24 и 34 соответственно;
(iv) FS28-256-012, указанные под SEQ ID NO 97, 74, 100, 23, 24 и 25 соответственно;
(v) FS28-256-023, указанные под SEQ ID NO 102, 74, 104, 23, 24 и 34 соответственно;
(vi) FS28-256-024, указанные под SEQ ID NO 97, 74, 100, 23, 24 и 43 соответственно;
(vii) FS28-256-026, указанные под SEQ ID NO 102, 74, 104, 23, 24 и 43 соответственно;
(viii) FS28-256-027, указанные под SEQ ID NO 97, 74, 100, 23, 24 и 44 соответственно;
(ix) FS28-256-001, указанные под SEQ ID NO 86, 74, 76, 23, 24 и 34 соответственно;
(x) FS28-256-005, указанные под SEQ ID NO 86, 74, 76, 23, 24 и 43 соответственно;
(xi) FS28-256-014, указанные под SEQ ID NO 112, 74, 114, 23, 24 и 25 соответственно;
(xii) FS28-256-018, указанные под SEQ ID NO 102, 74, 104, 23, 24 и 25 соответственно;
(xiii) FS28-256, указанные под SEQ ID NO 72, 74, 76, 23, 24 и 25 соответственно;
(xiv) FS28-024-051, указанные под SEQ ID NO 13, 14, 33, 23, 24 и 22 соответственно;
(xv) FS28-024-053, указанные под SEQ ID NO 13, 14, 52, 23, 24 и 22 соответственно; или
(xvi) FS28-024, указанные под SEQ ID NO 13, 14, 15, 23, 24 и 22 соответственно; и
при этом указанные последовательности CDR определены в соответствии со схемой нумерации Кабата.
[3] Молекула антитела по п. [1] или п. [2], характеризующаяся тем, что указанная молекула антитела содержит вариабельный домен тяжелой цепи (VH) и/или вариабельный домен легкой цепи (VL), предпочтительно VH-домен и VL-домен.
[4] Молекула антитела по любому из пп. [1]-[3], характеризующаяся тем, что указанная молекула антитела содержит тяжелую цепь иммуноглобулина и/или легкую цепь иммуноглобулина, предпочтительно тяжелую цепь иммуноглобулина и легкую цепь иммуноглобулина.
[5] Молекула антитела по любому из пп. [3]-[4], характеризующаяся тем, что указанная молекула антитела содержит VH-домен и/или VL-домен, предпочтительно VH-домен и VL-домен, антитела:
(i) FS28-256-271, указанные под SEQ ID NO 180 и 56 соответственно;
(ii) FS28-024-052, указанные под SEQ ID NO 39 и 18 соответственно;
(iii) FS28-256-021, указанные под SEQ ID NO 109 и 93 соответственно;
(iv) FS28-256-012, указанные под SEQ ID NO 109 и 79 соответственно;
(v) FS28-256-023, указанные под SEQ ID NO 121 и 93 соответственно;
(vi) FS28-256-024, указанные под SEQ ID NO 109 и 53 соответственно;
(vii) FS28-256-026, указанные под SEQ ID NO 121 и 53 соответственно;
(viii) FS28-256-027, указанные под SEQ ID NO 109 и 56 соответственно;
(ix) FS28-256-001, указанные под SEQ ID NO 63 и 93 соответственно;
(x) FS28-256-005, указанные под SEQ ID NO 63 и 53 соответственно;
(xi) FS28-256-014, указанные под SEQ ID NO 115 и 79 соответственно;
(xii) FS28-256-018, указанные под SEQ ID NO 121 и 79 соответственно;
(xiii) FS28-256, указанные под SEQ ID NO 69 и 79 соответственно;
(xiv) FS28-024-051, указанные под SEQ ID NO 30 и 18 соответственно;
(xv) FS28-024-053, указанные под SEQ ID NO 49 и 18 соответственно; или
(xvi) FS28-024, указанные под SEQ ID NO 8 и 18 соответственно.
[6] Молекула антитела по любому из пп. [1]-[5], характеризующаяся тем, что указанная молекула антитела содержит тяжелую цепь [без LALA] и легкую цепь антитела:
(i) FS28-256-271, указанные под SEQ ID NO 176 и 95 соответственно;
(ii) FS28-024-052, указанные под SEQ ID NO 35 и 16 соответственно;
(iii) FS28-256-021, указанные под SEQ ID NO 105 и 83 соответственно;
(iv) FS28-256-012, указанные под SEQ ID NO 105 и 77 соответственно;
(v) FS28-256-023, указанные под SEQ ID NO 123 и 83 соответственно;
(vi) FS28-256-024, указанные под SEQ ID NO 105 и 90 соответственно;
(vii) FS28-256-026, указанные под SEQ ID NO 123 и 90 соответственно;
(viii) FS28-256-027, указанные под SEQ ID NO 105 и 95 соответственно;
(ix) FS28-256-001, указанные под SEQ ID NO 81 и 83 соответственно;
(x) FS28-256-005, указанные под SEQ ID NO 87 и 90 соответственно;
(xi) FS28-256-014, указанные под SEQ ID NO 117 и 77 соответственно;
(xii) FS28-256-018, указанные под SEQ ID NO 123 и 77 соответственно;
(xiii) FS28-256, указанные под SEQ ID NO 65 и 77 соответственно;
(xiv) FS28-024-051, указанные под SEQ ID NO 26 и 16 соответственно;
(xv) FS28-024-053, указанные под SEQ ID NO 45 и 16 соответственно; или
(xvi) FS28-024, указанные под SEQ ID NO 4 и 16 соответственно.
[7] Молекула антитела по любому из пп. [1]-[5], характеризующаяся тем, что указанная молекула антитела содержит тяжелую цепь [с LALA] и легкую цепь антитела:
(i) FS28-256-271, указанные под SEQ ID NO 178 и 95 соответственно;
(ii) FS28-024-052, указанные под SEQ ID NO 37 и 16 соответственно;
(iii) FS28-256-021, указанные под SEQ ID NO 107 и 83 соответственно;
(iv) FS28-256-012, указанные под SEQ ID NO 107 и 77 соответственно;
(v) FS28-256-023, указанные под SEQ ID NO 125 и 83 соответственно;
(vi) FS28-256-024, указанные под SEQ ID NO 107 и 90 соответственно;
(vii) FS28-256-026, указанные под SEQ ID NO 125 и 90 соответственно;
(viii) FS28-256-027, указанные под SEQ ID NO 107 и 95 соответственно;
(ix) FS28-256-001, указанные под SEQ ID NO 89 и 83 соответственно;
(x) FS28-256-005, указанные под SEQ ID NO 89 и 90 соответственно;
(xi) FS28-256-014, указанные под SEQ ID NO 119 и 77 соответственно;
(xii) FS28-256-018, указанные под SEQ ID NO 125 и 77 соответственно;
(xiii) FS28-256, указанные под SEQ ID NO 67 и 77 соответственно;
(xiv) FS28-024-051, указанные под SEQ ID NO 28 и 16 соответственно;
(xv) FS28-024-053, указанные под SEQ ID NO 47 и 16 соответственно; или
(xvi) FS28-024, указанные под SEQ ID NO 5 и 16 соответственно.
[8] Молекула антитела по любому из пп. [1]-[7], характеризующаяся тем, что указанная молекула антитела содержит CDR 1-6, VH-домен, VL-домен, легкую цепь и/или тяжелую цепь антитела FS28-256-271.
[9] Молекула антитела по любому из пп. [1]-[7], характеризующаяся тем, что указанная молекула антитела содержит CDR 1-6, VH-домен, VL-домен, легкую цепь и/или тяжелую цепь антитела FS28-024-052.
[10] Молекула антитела по любому из пп. [1]-[9], при этом MSLN представляет собой MSLN, связанный с клеточной поверхностью.
[11] Молекула антитела по п. [10], характеризующаяся тем, что указанная молекула антитела связывается с иммобилизованным MSLN с более высокой аффинностью, чем с MSLN в растворе.
[12] Молекула антитела по п. [11], характеризующаяся тем, что указанная молекула антитела связывается с иммобилизованным MSLN с аффинностью (kD), равной 8 нM, или с более высокой аффинностью.
[13] Молекула антитела по п. [11] или п. [12], характеризующаяся тем, что указанная молекула антитела связывается с MSLN в растворе с аффинностью (kD), равной 15 нM, или с более низкой аффинностью.
[14] Молекула антитела по любому из пп. [1]-[13], при этом MSLN представляет собой MSLN человека.
[15] Молекула антитела по п. [14], при этом MSLN состоит из или содержит последовательность, представленную в SEQ ID NO: 169.
[16] Молекула антитела по любому из пп. [1]-[13], при этом MSLN представляет собой MSLN яванского макака.
[17] Молекула антитела по п. [16], при этом MSLN состоит из или содержит последовательность, представленную в SEQ ID NO: 170.
[18] Молекула антитела по любому из пп. [1]-[17], характеризующаяся тем, что указанная молекула антитела содержит CDR 1-6, VH-домен, VL-домен, легкую цепь и/или тяжелую цепь антитела FS28-024-051, FS28-024-052, FS28-024-053 или FS28-024, и указанное антитело блокирует связывание MUC16 с MSLN.
[19] Молекула антитела по любому из пп. [1]-[17], характеризующаяся тем, что указанная молекула антитела содержит CDR 1-6, VH-домен, VL-домен, легкую цепь и/или тяжелую цепь антитела FS28-256-271, FS28-256-021, FS28-256-012, FS28-256-023, FS28-256-024, FS28-256-026 или FS28-256-027, FS28-256-001, FS28-256-005, FS28-256-014, FS28-256-018 или FS28-256, и указанное антитело не блокирует связывание MUC16 с MSLN.
[20] Молекула антитела по п. [18] или п. [19], при этом указанный MUC16 представляет собой MUC16 человека.
[21] Молекула антитела по любому из пп. [1]-[20], характеризующаяся тем, что указанная молекула антитела представляет собой молекулу мультиспецифичного антитела и содержит второй антигенсвязывающий сайт, который связывает второй антиген.
[22] Молекула антитела по п. [21], характеризующаяся тем, что молекула антитела представляет собой биспецифичную, триспецифичную или тетраспецифичную молекулу антитела.
[23] Молекула антитела по п. [22], характеризующаяся тем, что указанная молекула антитела представляет собой биспецифичную молекулу.
[24] Молекула антитела по любому из пп. [21]-[23], характеризующаяся тем, что второй антигенсвязывающий сайт расположен в константном домене указанной молекулы антитела.
[25] Молекула антитела по любому из пп. [21]-[24], при этом второй антиген представляет собой антиген иммунной клетки.
[26] Молекула антитела по п. [25], при этом указанный антиген иммунной клетки является представителем суперсемейства рецепторов фактора некроза опухоли (TNFRSF).
[27] Молекула антитела по п. [26], при этом указанный представитель TNFRSF представляет собой OX40 или CD137.
[28] Молекула антитела по любому из пп. [21]-[27], характеризующаяся тем, что второй антигенсвязывающий сайт содержит первую последовательность, вторую последовательность и/или третью последовательность, причем указанная первая последовательность, вторая последовательность и третья последовательность расположены в структурной петле AB, структурной петле CD и структурной петле EF константного домена соответственно.
[29] Молекула антитела по любому из пп. [24]-[28], характеризующаяся тем, что константный домен представляет собой CH3-домен.
[30] Молекула антитела по любому из пп. [26]-[29], характеризующаяся тем, что указанная молекула антитела способна активировать представителя TNFRSF на иммунной клетке в присутствии MSLN, связанного с поверхностью клетки опухоли.
[31] Молекула антитела по любому из пп. [26]-[30], характеризующаяся тем, что связывание указанной молекулы антитела с представителем TNFRSF и с MSLN, связанным с поверхностью клетки опухоли, вызывает кластеризацию указанного представителя TNFRSF на поверхности иммунной клетки.
[32] Молекула антитела по п. [30] или п. [31], при этом указанная иммунная клетка представляет собой
Т-клетку, B-клетку, естественную клетку-киллер (NK), естественную Т-клетку-киллер (NKT) или дендритную клетку (ДК).
[33] Молекула антитела по п. [32], при этом указанная иммунная клетка представляет собой T-клетку.
[34] Молекула антитела по любому из пп. [1]-[33], характеризующаяся тем, что указанная молекула антитела обладает или способна вызывать антителозависимую клеточноопосредованную цитотоксичность (АЗКЦ).
[35] Молекула антитела по любому из пп. [1]-[33], характеризующаяся тем, что указанная молекула антитела была модифицирована для уменьшения или устранения связывания CH2-домена молекулы антитела с одним или более Fcγ-рецепторами.
[36] Молекула антитела по любому из пп. [1]-[33] или п. [35], характеризующаяся тем, что указанная молекула антитела не связывается с Fcγ-рецепторами.
[37] Молекула антитела по п. [35] или п. [36], при этом указанный Fcγ-рецептор выбран из группы, состоящей из: FcγRI, FcγRIIa, FcγRIIb и FcγRIII.
[38] Конъюгат, содержащий молекулу антитела по любому из пп. [1]-[37] и биоактивную молекулу.
[39] Конъюгат, содержащий молекулу антитела по любому из пп. [1]-[37] и детектируемую метку.
[40] Молекула или молекулы нуклеиновой кислоты, кодирующие молекулу антитела по любому из пп. [1]-[37].
[41] Молекула (молекулы) нуклеиновой кислоты по п. [40], характеризующаяся тем, что указанная молекула (молекулы) нуклеиновой кислоты содержит (содержат) последовательность нуклеиновой кислоты для VH-домена и/или VL-домена антитела:
(i) FS28-256-271, представленную в SEQ ID NO 181 и 57 соответственно;
(ii) FS28-024-052, представленную в SEQ ID NO 40 и 19 соответственно;
(iii) FS28-256-021, представленную в SEQ ID NO 110 и 94 соответственно;
(iv) FS28-256-012, представленную в SEQ ID NO 110 и 80 соответственно;
(v) FS28-256-023, представленную в SEQ ID NO 122 и 94 соответственно;
(vi) FS28-256-024, представленную в SEQ ID NO 110 и 54 соответственно;
(vii) FS28-256-026, представленную в SEQ ID NO 122 и 54 соответственно;
(viii) FS28-256-027, представленную в SEQ ID NO 110 и 57 соответственно;
(ix) FS28-256-001, представленную в SEQ ID NO 64 и 94 соответственно;
(x) FS28-256-005, представленную в SEQ ID NO 64 и 54 соответственно;
(xi) FS28-256-014, представленную в SEQ ID NO 116 и 80 соответственно;
(xii) FS28-256-018, представленную в SEQ ID NO 122 и 80 соответственно;
(xiii) FS28-256, представленную в SEQ ID NO 70 и 80 соответственно;
(xiv) FS28-024-051, представленную в SEQ ID NO 31 и 19 соответственно;
(xv) FS28-024-053, представленную в SEQ ID NO 50 и 19 соответственно; или
(xvi) FS28-024, представленную в SEQ ID NO 9 и 19 соответственно.
[42] Молекула (молекулы) нуклеиновой кислоты по п. [40] или п. [41], характеризующаяся тем, что указанная молекула (молекулы) нуклеиновой кислоты содержит (содержат):
(i) последовательность нуклеиновой кислоты для тяжелой цепи антитела FS28-256-271, представленную в SEQ ID NO: 179 или 177, и/или последовательность нуклеиновой кислоты для легкой цепи антитела FS28-256-271, представленную в SEQ ID NO: 96;
(ii) последовательность нуклеиновой кислоты для тяжелой цепи антитела FS28-024-052, представленную в SEQ ID NO: 38 или 36, и/или последовательность нуклеиновой кислоты для легкой цепи антитела FS28-024-052, представленную в SEQ ID NO: 17;
(iii) последовательность нуклеиновой кислоты для тяжелой цепи антитела FS28-256-021, представленную в SEQ ID NO: 108 или 106, и/или последовательность нуклеиновой кислоты для легкой цепи антитела FS28-256-021, представленную в SEQ ID NO: 92;
(iv) последовательность нуклеиновой кислоты для тяжелой цепи антитела FS28-256-012, представленную в SEQ ID NO: 108 или 106, и/или последовательность нуклеиновой кислоты для легкой цепи антитела FS28-256-012, представленную в SEQ ID NO: 78;
(v) последовательность нуклеиновой кислоты для тяжелой цепи антитела FS28-256-023, представленную в SEQ ID NO: 126 или 124, и/или последовательность нуклеиновой кислоты для легкой цепи антитела FS28-256-023, представленную в SEQ ID NO: 92;
(vi) последовательность нуклеиновой кислоты для тяжелой цепи антитела FS28-256-024, представленную в SEQ ID NO: 108 или 106, и/или последовательность нуклеиновой кислоты для легкой цепи антитела FS28-256-024, представленную в SEQ ID NO: 91;
(vii) последовательность нуклеиновой кислоты для тяжелой цепи антитела FS28-256-026, представленную в SEQ ID NO: 126 или 124, и/или последовательность нуклеиновой кислоты для легкой цепи антитела FS28-256-026, представленную в SEQ ID NO: 91;
(viii) последовательность нуклеиновой кислоты для тяжелой цепи антитела FS28-256-027, представленную в SEQ ID NO: 108 или 106, и/или последовательность нуклеиновой кислоты для легкой цепи антитела FS28-256-027, представленную в SEQ ID NO: 96;
(ix) последовательность нуклеиновой кислоты для тяжелой цепи антитела FS28-256-001, представленную в SEQ ID NO: 84 или 82, и/или последовательность нуклеиновой кислоты для легкой цепи антитела FS28-256-001, представленную в SEQ ID NO: 92;
(x) последовательность нуклеиновой кислоты для тяжелой цепи антитела FS28-256-005, представленную в SEQ ID NO: 84 или 88, и/или последовательность нуклеиновой кислоты для легкой цепи антитела FS28-256-005, представленную в SEQ ID NO: 91;
(xi) последовательность нуклеиновой кислоты для тяжелой цепи антитела FS28-256-014, представленную в SEQ ID NO: 120 или 118, и/или последовательность нуклеиновой кислоты для легкой цепи антитела FS28-256-014, представленную в SEQ ID NO: 78;
(xii) последовательность нуклеиновой кислоты для тяжелой цепи антитела FS28-256-018, представленную в SEQ ID NO: 126 или 124, и/или последовательность нуклеиновой кислоты для легкой цепи антитела FS28-256-018, представленную в SEQ ID NO: 78;
(xiii) последовательность нуклеиновой кислоты для тяжелой цепи антитела FS28-256, представленную в SEQ ID NO: 68 или 66, и/или последовательность нуклеиновой кислоты для легкой цепи антитела FS28-256, представленную в SEQ ID NO: 78;
(xiv) последовательность нуклеиновой кислоты для тяжелой цепи антитела FS28-024-051, представленную в SEQ ID NO: 29 или 27, и/или последовательность нуклеиновой кислоты для легкой цепи антитела FS28-024-051, представленную в SEQ ID NO: 17;
(xv) последовательность нуклеиновой кислоты для тяжелой цепи антитела FS28-024-053, представленную в SEQ ID NO: 48 или 46, и/или последовательность нуклеиновой кислоты для легкой цепи антитела FS28-024-053, представленную в SEQ ID NO: 17; или
(xvi) последовательность нуклеиновой кислоты для тяжелой цепи антитела FS28-024, представленную в SEQ ID NO: 7 или 6, и/или последовательность нуклеиновой кислоты для легкой цепи антитела FS28-024, представленную в SEQ ID NO: 17.
[43] Вектор или векторы, содержащие молекулу или молекулы нуклеиновой кислоты по любому из пп. [40]-[42].
[44] Рекомбинантная клетка-хозяин, содержащая молекулу (молекулы) нуклеиновой кислоты по любому из пп. [40]-[42] или вектор (векторы) по п. [43].
[45] Способ получения молекулы антитела по любому из пп. [1]-[37], включающий культивирование рекомбинантной клетки-хозяина по п. [44] в условиях, позволяющих получать молекулу антитела.
[46] Способ по п. [45], дополнительно включающий выделение и/или очистку молекулы антитела.
[47] Фармацевтическая композиция, содержащая молекулу антитела или конъюгат антитела по любому из пп. [1]-[39] и фармацевтически приемлемое вспомогательное вещество.
[48] Молекула антитела или конъюгат антитела по любому из пп. [1]-[39] для применения в способе лечения рака у индивидуума.
[49] Способ лечения рака у индивидуума, включающий введение указанному индивидууму терапевтически эффективного количества молекулы антитела или конъюгата антитела по любому из пп. [1]-[39].
[50] Применение молекулы антитела или конъюгата антитела по любому из пп. [1]-[39] в получении лекарственного средства для лечения рака.
[51] Молекула антитела или конъюгат антитела для применения, способ или применение по любому из пп. [48]-[50], при этом клетки рака экспрессируют MSLN на клеточной поверхности.
[52] Молекула антитела или конъюгат антитела для применения, способ или применение по любому из пп. [48]-[50], при этом рак выбран из группы, состоящей из: мезотелиомы, рака поджелудочной железы, рака яичников и рака легкого.
[53] Молекула антитела или конъюгат антитела для применения по п. [48], при этом способ лечения включает введение указанной молекулы антитела или конъюгата антитела индивидууму в комбинации со вторым лекарственным средством.
[54] Способ по п. [49], характеризующийся тем, что указанный способ дополнительно включает введение индивидууму терапевтически эффективного количества второго лекарственного средства.
[55] Молекула антитела или конъюгат антитела по любому из пп. [1]-[37] или п. [39] для применения в способе детектирования, диагностики, прогнозирования или мониторинга прогноза рака у индивидуума.
[56] Способ детектирования, диагностики, прогнозирования или мониторинга прогноза рака у индивидуума, при этом указанный способ включает применение молекулы антитела или конъюгата антитела по любому из пп. [1]-[37] или п. [39].
[57] Применение молекулы антитела или конъюгата антитела по любому из пп. [1]-[37] или п. [39] в изготовлении диагностического продукта для детектирования, диагностики, прогнозирования или мониторинга прогноза рака у индивидуума.
[58] Набор для применения в способе детектирования, диагностики, прогнозирования или мониторинга прогноза рака у индивидуума, при этом указанный набор содержит молекулу антитела или конъюгат антитела по любому из пп. [1]-[37] или п. [39].
[59] Молекула антитела или конъюгат антитела для применения, способ, применение или набор по любому из пп. [55]-[58], при этом рак выбран из группы, состоящей из: мезотелиомы, рака поджелудочной железы, рака яичников и рака легкого.
Краткое описание фигур
На Фиг.1 показано связывание mAb к MSLN с клетками NCI-H226. Указанные mAb к MSLN человека FS28-024, FS28-026, FS28-091, FS28-185 и FS28-256 (все в LALA-формате IgG1) демонстрировали дозозависимое связывание с клетками NCI-H226. FS28-024, FS28-026 и FS28-091 демонстрировали высокую аффинность связывания в отношении MSLN клеточной поверхности с низкими наномолярными значениями EC50 подобно mAb к MSLN, SS1, положительного контроля. mAb FS28-185 и FS28-256 демонстрировали более слабое связывание с MSLN клеточной поверхности со значениями EC50 более 30 нМ и более низкими значениями Emax по сравнению с FS28-024, FS28-026 и FS28-091.
На Фиг.2 показана АЗКЦ-активность mAb² к MSLN. mAb² к MSLN человека, FS28-024-052 и FS28-256-271, а также антитело SS1 положительного контроля тестировали в LALA-формате hIgG1 (отсутствие эффекторной функции) и формате hIgG1 с компетентным по эффекторной функции остовом. Из тестируемых антител FS28-024-052 проявляло самую высокую АЗКЦ-активность, при этом FS28-256-271 проявляло АЗКЦ-активность, сопоставимую с контрольным антителом. Во всех случаях введение мутаций LALA в остов IgG1, как и ожидали, полностью устраняло любую АЗКЦ-активность.
На Фиг.3 показаны индивидуальные измерения объема опухоли в модели сингенной опухоли CT26.G10, которую лечили (A) G1-AA/HelD1.3 (контроль IgG1 человека), (B) FS22m-063-AA/HelD1.3 (Fcab к CD137 мыши в формате mAb2), (C) комбинацией FS22m-063-AA/HelD1.3 и G1-AA/FS28m-228-010 (Fcab к CD137 мыши плюс Fab к MSLN мыши), (D) FS22m-063-AA/FS28m-228-010 (mAb2 к CD137/MSLN мыши), (E) FS22m-063-AA/4420 (Fcab к CD137 мыши в формате mAb2) и (F) G1-AA/FS28m-228-010 (Fab к MSLN мыши). FS22m-063-AA/FS28m-228-010 демонстрировало сокращение роста опухоли по сравнению с изотипическим контролем, а также с другими группами лечения.
На Фиг.4 представлена кривая выживаемости Каплана-Мейера для модели сингенной опухоли CT26.G10, которую лечили G1-AA/HelD1.3 (контроль IgG), FS22m-063-AA/HelD1.3 (Fcab к CD137 мыши в формате mAb2), FS22m-063-AA/4420 (Fcab к CD137 мыши в формате mAb2), G1-AA/FS28m-228-010 (Fab к MSLN мыши), комбинацией FS22m-063-AA/HelD1.3 и G1-AA/FS28m-228-010 (Fcab к CD137 мыши плюс Fab к MSLN мыши) и FS22m-063-AA/FS28m-228-010 (mAb2 к CD137/MSLN мыши). Результаты показывают, что лечение FS22m-063-AA/FS28m-228-010 приводило к значительному увеличению выживаемости по сравнению с мышами, получавшими лечение изотипическим контролем или другими группами лечения.
Подробное описание
Настоящее изобретение относится к молекулам антител, которые связывают MSLN. Молекула антитела предпочтительно связывает MSLN человека, более предпочтительно MSLN человека и яванского макака. Молекула антитела согласно настоящему изобретению предпочтительно способна связываться с MSLN, экспрессируемым на поверхности клетки. Указанная клетка предпочтительно представляет собой клетку опухоли.
Молекула антитела предпочтительно специфично связывает MSLN. Термин «специфичный (специфический)» может относиться к ситуации, в которой молекула антитела не демонстрирует какого-либо значительного связывания с молекулами, отличными от ее партнера (партнеров) по специфичному связыванию, согласно настоящему изобретению - MSLN. Термин «специфичный (специфический)» также применим, когда молекула антитела специфична в отношении конкретных эпитопов, таких как эпитопы на MSLN, содержащихся в ряде антигенов, и в этом случае указанная молекула антитела способна связываться с различными антигенами, содержащими указанный эпитоп. Молекула антитела предпочтительно не связывается или не демонстрирует какого-либо значительного связывания с другими молекулами, вовлеченными в клеточную адгезию, такими как CEACAM-5, E-кадгерин, тромбомодулин и/или молекула клеточной адгезии эпителия (EpCAM).
Как описано в разделе «Уровень техники» выше, зрелый MSLN отделяется от клеток опухоли и удаляется из области опухоли. Этот отделенный MSLN может выступать в качестве «поглотителя» связывающих молекул к MSLN, которые после связывания с отделенным MSLN также удаляются из области опухоли. Для выбора (отбора) молекул, которые предпочтительно связываются с MSLN, присутствующим на поверхности клеток опухоли, авторы настоящего изобретения выбирали молекулы антител с высокой авидностью в отношении MSLN. В частности, авторы настоящего изобретения выбирали молекулы антител, которые связывались с иммобилизованным MSLN с более высокой аффинностью, чем с MSLN в растворе. Полагают, что молекулы антител, которые связываются с MSLN с высокой авидностью, предпочтительно связываются с MSLN, присутствующим на клетках опухоли, где, как ожидают, присутствуют нескольких копий MSLN и они доступны для двухвалентного связывания молекулой антитела, в отличие от мезотелина, отделенного от клеток опухоли, который, как ожидают, имеет форму мономера. Соответственно, не желая быть связанными какой-либо теорией молекулы антител согласно настоящему изобретению, как ожидают, будут медленнее удаляться из области опухоли и, следовательно, будут иметь большее временное окно для оказания терапевтического эффекта.
Молекула антитела предпочтительно связывается с иммобилизованным MSLN с более высокой аффинностью, чем с MSLN в растворе. Иммобилизованный MSLN может представлять собой MSLN, иммобилизованный на поверхности, такой как чип для применения в поверхностном плазмонном резонансе. В настоящем описании MSLN в растворе также называется растворимым MSLN и он не иммобилизован. Растворимый MSLN предпочтительно имеет форму мономера, т.е. представляет собой мономерный мезотелин.
Аффинность антитела к распознаваемому им антигену может быть выражена в виде равновесной константы диссоциации (KD), с которой указанное антитело связывает указанный антиген. Чем выше значение KD, тем ниже аффинность молекулы антитела к антигену.
Молекула антитела предпочтительно связывается с иммобилизованным MSLN с аффинностью (KD), равной по меньшей мере 9 нM, 8 нM, 7 нM или 6 нM, или с более высокой аффинностью. Предпочтительно, молекула антитела связывается с иммобилизованным MSLN с аффинностью (KD), равной по меньшей мере 7 нM, 6 нM, или с более высокой аффинностью.
Молекула антитела предпочтительно связывается с иммобилизованным MSLN с аффинностью (KD), равной 15 нM, или с более низкой аффинностью. Более предпочтительно, молекула антитела связывается с иммобилизованным MSLN с аффинностью (KD), равной 16 нM, 17 нM или 18 нM, или с более низкой аффинностью.
В предпочтительном варианте реализации молекула антитела связывает иммобилизованный MSLN с аффинностью (KD), равной 6 нМ, или с более высокой аффинностью и связывает MSLN в растворе с аффинностью (KD), равной 18 нМ, или с более низкой аффинностью.
Аффинность связывания молекулы антитела в отношении клеток, содержащих MSLN, связанный с поверхностью, может быть измерена путем определения концентрации указанной молекулы антитела, необходимой для достижения полумаксимального связывания (ЕС50) молекулы антитела с клетками. Подходящие способы определения концентрации молекулы антитела, необходимой для достижения полумаксимального связывания молекулы антитела с клетками, известны в этой области техники и описаны в примерах в настоящей заявке (см., например, Пример 4). Как описано выше, молекулы антител, на связывание которых с клетками опухоли, содержащими MSLN, связанный с поверхностью, не влияет или в меньшей степени влияет присутствие растворимого мезотелина, являются предпочтительными ввиду присутствия отделенного MSLN в окружении опухоли. Таким образом, в предпочтительном варианте реализации концентрация молекулы антитела, необходимая для достижения полумаксимального связывания (ЕС50) антитела с клетками (например, клетками опухоли), содержащими MSLN, связанный с поверхностью, в присутствии растворимого MSLN, менее чем в 20 раз, менее чем в 15 раз, менее чем в 10 раз, менее чем в 9 раз, менее чем в 8 раз, менее чем в 7 раз, менее чем в 6 раз, менее чем в 5 раз, менее чем в 4 раза или менее чем в 3 раза выше концентрации молекулы антитела, необходимой для достижения полумаксимального связывания (ЕС50) антитела с клетками в отсутствии растворимого MSLN.
Было показано, что присутствие растворимого MSLN в меньшей степени влияет на связывание молекул антител, которые не блокируют связывание MUC16 с MSLN, с клетками, содержащими MSLN, связанный с клетками. Таким образом, может быть предпочтительной молекула антитела, которая не способна или не блокирует связывание MUC16 с MSLN.
В качестве альтернативы, молекула антитела может блокировать связывание MUC16 с MSLN.
Иммобилизованный MSLN может иметь последовательность, представленную в SEQ ID NO: 169. MSLN в растворе может иметь последовательность, представленную в SEQ ID NO: 169.
Также было показано, что молекулы антител согласно настоящему изобретению связывают MSLN яванского макака. Полагают, что связывание с MSLN яванского макака, а также MSLN человека позволяет проводить исследования эффективности и токсичности молекулы антитела у яванских макак, которые могут предсказать эффективность и токсичность молекулы антитела у людей.
Молекула антитела может связываться с иммобилизованным MSLN человека и иммобилизованным MSLN яванского макака со схожей аффинностью. В дополнение к этому, молекула антитела может связываться с MSLN человека в растворе и MSLN яванского макака в растворе со схожей аффинностью. Полагают, что это позволяет убедиться в том, что исследования эффективности и токсичности, проводимые у яванских макак с применением молекулы антитела, предсказывают эффективность и токсичность молекулы антитела у людей.
Таким образом, в предпочтительном варианте реализации молекула антитела связывается с иммобилизованным MSLN яванского макака с аффинностью, которая не более чем в 10 раз, предпочтительно не более чем в 5 раз, более предпочтительно не более чем в 2 раза ниже или выше аффинности, с которой указанная молекула антитела связывает иммобилизованный MSLN человека. В дополнение к этому, молекула антитела предпочтительно связывается с MSLN яванского макака в растворе с аффинностью, которая не более чем в 10 раз, предпочтительно не более чем в 5 раз, более предпочтительно не более чем в 2 раза ниже или выше аффинности, с которой указанная молекула антитела связывает MSLN человека в растворе.
Аффинность связывания молекулы антитела в отношении распознаваемого антигена, такого как MSLN человека или яванского макака, может быть определена посредством поверхностного плазмонного резонанса (SPR), такого как, например, Biacore.
Молекула антитела может представлять собой химерную, гуманизированную молекулу антитела или молекулу антитела человека. Предпочтительно, молекула антитела представляет собой молекулу антитела человека.
Молекула антитела предпочтительно является моноклональной.
Молекула антитела может быть выделенной в том смысле, что она не содержит загрязняющих примесей, таких как антитела, способные связывать другие полипептиды, и/или компоненты сыворотки.
Молекула антитела может быть природной или частично, или полностью полученной путем синтеза. Например, молекула антитела может представлять собой рекомбинантную молекулу антитела.
Молекула антитела содержит один или более антигенсвязывающих сайтов на основе CDR для MSLN.
Молекула антитела может представлять собой иммуноглобулин или его антигенсвязывающий фрагмент. Например, молекула антитела может представлять собой молекулу IgG, IgA, IgE или IgM, предпочтительно молекулу IgG, такую как молекула IgG1, IgG2, IgG3 или IgG4, более предпочтительно молекулу IgG1 или IgG2, наиболее предпочтительно молекулу IgG1 или ее фрагмент. В предпочтительном варианте реализации молекула антитела представляет собой целую молекулу иммуноглобулина.
В других вариантах реализации молекула антитела может представлять собой антигенсвязывающий фрагмент, содержащий антигенсвязывающий сайт на основе CDR для MSLN. Например, указанный антигенсвязывающий фрагмент может представлять собой антигенсвязывающий фрагмент (Fab), IgGΔCH2, F(ab’)2, одноцепочечный Fab (scFab), стабилизированный дисульфидом вариабельный фрагмент (dsFv), одноцепочечный вариабельный фрагмент (scFv), (scFv)2, scFv-CH3 (миниантитело), scFv-Fc, scFv-молния (scFv-zipper), диатело, триатело, тетратело или однодоменное антитело (sdAb), такое как VHH-домен или нанотело. Предпочтительные антигенсвязывающие фрагменты содержат более одного антигенсвязывающего сайта на основе CDR для MSLN, т.е. они могут быть поливалентными. Таким образом, антигенсвязывающий фрагмент может предпочтительно представлять собой IgGΔ CH2, F(ab’)2, диатело, триатело или тетратело. (Brinkmann and Kontermann, (2017) и Powers et al, (2012))
Антитела и способы их конструирования и применения хорошо известны в этой области техники и описаны, например, в Holliger and Hudson, 2005. Можно использовать моноклональные и другие антитела и применять методы рекомбинантных ДНК для получения других антител или химерных молекул, которые сохраняют специфичность исходного антитела. Такие методы могут включать введение CDR-областей или вариабельных областей молекулы антитела в другую молекулу антитела (EP-A-184187, GB 2188638A и EP-A-239400).
Антигенсвязывающий сайт на основе CDR представляет собой антигенсвязывающий сайт в вариабельной области антитела. Антигенсвязывающий сайт на основе CDR может быть образован тремя CDR, такими как три CDR вариабельного домена легкой цепи (VL) или три CDR вариабельного домена тяжелой цепи (VH). Предпочтительно, антигенсвязывающий сайт на основе CDR образован шестью CDR: тремя CDR VL и тремя CDR VH. Вклад различных CDR в связывание антигена может варьироваться в разных антигенсвязывающих сайтах.
Три содержащиеся в VH-домене CDR антигенсвязывающего сайта могут быть расположены в пределах VH-домена иммуноглобулина, и три CDR VL-домена могут быть расположены в пределах VL-домена иммуноглобулина. Например, антигенсвязывающий сайт на основе CDR может быть расположен в вариабельной области антитела.
Молекула антитела содержит один или предпочтительно более одного, например, два антигенсвязывающих сайта на основе CDR для MSLN. Таким образом, молекула антитела может содержать один VH-домен и один VL-домен, но предпочтительно содержит два VH-домена и два VL-домена, т.е. две пары VH/VL-доменов, как, например, в случае встречающихся в природе молекул IgG.
Антигенсвязывающий сайт на основе CDR может содержать три CDR VH или три CDR VL, предпочтительно три CDR VH и три CDR VL антитела FS28-256-271, FS28-024-052, FS28-256-021, FS28-256-012, FS28-256-023, FS28-256-024, FS28-256-026, FS28-256-027, FS28-256-001, FS28-256-005, FS28-256-014, FS28-256-018, FS28-256, FS28-024-051, FS28-024-053 или FS28-024, предпочтительно антитела FS28-256-271 или FS28-024-052, наиболее предпочтительно антитела FS28-256-271.
Последовательности CDR могут быть легко определены по последовательностям VH- и VL-доменов молекулы антитела с применением рутинных методик. В настоящей заявке описаны последовательности VH- и VL-доменов антител FS28-256-271, FS28-024-052, FS28-256-021, FS28-256-012, FS28-256-023, FS28-256-024, FS28-256-026, FS28-256-027, FS28-256-001, FS28-256-005, FS28-256-014, FS28-256-018, FS28-256, FS28-024-051, FS28-024-053 и FS28-024, и по указанным последовательностям могут быть, таким образом, определены три CDR VH-домена и три CDR VL-домена указанных антител. Последовательности CDR могут быть, например, определены в соответствии с Kabat et al., 1991 или международной информационной системой ImMunoGeneTics (IMGT) (Lefranc et al., 2015).
Последовательности CDR1, CDR2 и CDR3 VH-домена молекулы антитела в соответствии с нумерацией IMGT могут представлять собой последовательности, расположенные в положениях 27-38, 56-65 и 105-117 VH-домена молекулы антитела соответственно.
Последовательности CDR1, CDR2 и CDR3 VH-домена молекулы антитела в соответствии с нумерацией Кабата могут представлять собой последовательности, расположенные в положениях 31-35, 50-65 и 95-102 VH-домена соответственно.
Последовательности CDR1, CDR2 и CDR3 VL-домена молекулы антитела в соответствии с нумерацией IMGT могут представлять собой последовательности, расположенные в положениях 27-38, 56-65 и 105-117 VL-домена соответственно.
Последовательности CDR1, CDR2 и CDR3 VL-домена молекулы антитела в соответствии с нумерацией Кабата могут представлять собой последовательности, расположенные в положениях 24-34, 50-56 и 89-97 VL-домена соответственно.
Например, последовательность CDR1, CDR2 и CDR3 VH-домена для:
(i) FS28-256-271 может быть такой, как представлена в SEQ ID NO 98, 73 и 99 соответственно;
(ii) FS28-024-052 может быть такой, как представлена в SEQ ID NO 10, 11 и 41 соответственно;
(iii) FS28-256-021 может быть такой, как представлена в SEQ ID NO 98, 73 и 99 соответственно;
(iv) FS28-256-012 может быть такой, как представлена в SEQ ID NO 98, 73 и 99 соответственно;
(v) FS28-256-023 может быть такой, как представлена в SEQ ID NO 101, 73 и 103 соответственно;
(vi) FS28-256-024 может быть такой, как представлена в SEQ ID NO 98, 73 и 99 соответственно;
(vii) FS28-256-026 может быть такой, как представлена в SEQ ID NO 101, 73 и 103 соответственно;
(viii) FS28-256-027 может быть такой, как представлена в SEQ ID NO 98, 73 и 99 соответственно;
(ix) FS28-256-001 может быть такой, как представлена в SEQ ID NO 85, 73 и 75 соответственно;
(x) FS28-256-005 может быть такой, как представлена в SEQ ID NO 85, 73 и 75 соответственно;
(xi) FS28-256-014 может быть такой, как представлена в SEQ ID NO 111, 73 и 113 соответственно;
(xii) FS28-256-018 может быть такой, как представлена в SEQ ID NO 101, 73 и 103 соответственно;
(xiii) FS28-256 может быть такой, как представлена в SEQ ID NO 71, 73 и 75 соответственно;
(xiv) FS28-024-051 может быть такой, как представлена в SEQ ID NO 10, 11 и 32 соответственно;
(xv) FS28-024-053 может быть такой, как представлена в SEQ ID NO 10, 11 и 51 соответственно; и
(xvi) FS28-024 может быть такой, как представлена в SEQ ID NO 10, 11 и 12 соответственно;
при этом указанные последовательности CDR определены в соответствии со схемой нумерации IMGT.
Последовательность CDR1, CDR2 и CDR3 VL-домена для:
(i) FS28-256-271 может быть такой, как представлена в SEQ ID NO 20, 21 и 44 соответственно;
(ii) FS28-024-052 может быть такой, как представлена в SEQ ID NO 20, 21 и 22 соответственно;
(iii) FS28-256-021 может быть такой, как представлена в SEQ ID NO 20, 21 и 34 соответственно;
(iv) FS28-256-012 может быть такой, как представлена в SEQ ID NO 20, 21 и 25 соответственно;
(v) FS28-256-023 может быть такой, как представлена в SEQ ID NO 20, 21 и 34 соответственно;
(vi) FS28-256-024 может быть такой, как представлена в SEQ ID NO 20, 21 и 43 соответственно;
(vii) FS28-256-026 может быть такой, как представлена в SEQ ID NO 20, 21 и 43 соответственно;
(viii) FS28-256-027 может быть такой, как представлена в SEQ ID NO 20, 21 и 44 соответственно;
(ix) FS28-256-001 может быть такой, как представлена в SEQ ID NO 20, 21 и 34 соответственно;
(x) FS28-256-005 может быть такой, как представлена в SEQ ID NO 20, 21 и 43 соответственно;
(xi) FS28-256-014 может быть такой, как представлена в SEQ ID NO 20, 21 и 25 соответственно;
(xii) FS28-256-018 может быть такой, как представлена в SEQ ID NO 20, 21 и 25 соответственно;
(xiii) FS28-256 может быть такой, как представлена в SEQ ID NO 20, 21 и 25 соответственно;
(xiv) FS28-024-051 может быть такой, как представлена в SEQ ID NO 20, 21 и 22 соответственно;
(xv) FS28-024-053 может быть такой, как представлена в SEQ ID NO 20, 21 и 22 соответственно; и
(xvi) FS28-024 может быть такой, как представлена в SEQ ID NO 20, 21 и 22 соответственно;
при этом указанные последовательности CDR определены в соответствии со схемой нумерации IMGT.
Например, последовательность CDR1, CDR2 и CDR3 VH-домена для:
(i) FS28-256-271 может быть такой, как представлена в SEQ ID NO 97, 182 и 100 соответственно;
(ii) FS28-024-052 может быть такой, как представлена в SEQ ID NO 13, 14 и 42 соответственно;
(iii) FS28-256-021 может быть такой, как представлена в SEQ ID NO 97, 74 и 100 соответственно;
(iv) FS28-256-012 может быть такой, как представлена в SEQ ID NO 97, 74 и 100 соответственно;
(v) FS28-256-023 может быть такой, как представлена в SEQ ID NO 102, 74 и 104 соответственно;
(vi) FS28-256-024 может быть такой, как представлена в SEQ ID NO 97, 74 и 100 соответственно;
(vii) FS28-256-026 может быть такой, как представлена в SEQ ID NO 102, 74 и 104 соответственно;
(viii) FS28-256-027 может быть такой, как представлена в SEQ ID NO 97, 74 и 100 соответственно;
(ix) FS28-256-001 может быть такой, как представлена в SEQ ID NO 86, 74 и 76 соответственно;
(x) FS28-256-005 может быть такой, как представлена в SEQ ID NO 86, 74 и 76 соответственно;
(xi) FS28-256-014 может быть такой, как представлена в SEQ ID NO 112, 74 и 114 соответственно;
(xii) FS28-256-018 может быть такой, как представлена в SEQ ID NO 102, 74 и 104 соответственно;
(xiii) FS28-256 может быть такой, как представлена в SEQ ID NO 72, 74 и 76 соответственно;
(xiv) FS28-024-051 может быть такой, как представлена в SEQ ID NO 13, 14 и 33 соответственно;
(xv) FS28-024-053 может быть такой, как представлена в SEQ ID NO 13, 14 и 52 соответственно; и
(xvi) FS28-024 может быть такой, как представлена в SEQ ID NO 13, 14 и 15 соответственно;
при этом указанные последовательности CDR определены в соответствии со схемой нумерации Кабата.
Последовательность CDR1, CDR2 и CDR3 VL-домена для:
(i) FS28-256-271 может быть такой, как представлена в SEQ ID NO 23, 24 и 44 соответственно;
(ii) FS28-024-052 может быть такой, как представлена в SEQ ID NO 23, 24 и 22 соответственно;
(iii) FS28-256-021 может быть такой, как представлена в SEQ ID NO 23, 24 и 34 соответственно;
(iv) FS28-256-012 может быть такой, как представлена в SEQ ID NO 23, 24 и 25 соответственно;
(v) FS28-256-023 может быть такой, как представлена в SEQ ID NO 23, 24 и 34 соответственно;
(vi) FS28-256-024 может быть такой, как представлена в SEQ ID NO 23, 24 и 43 соответственно;
(vii) FS28-256-026 может быть такой, как представлена в SEQ ID NO 23, 24 и 43 соответственно;
(viii) FS28-256-027 может быть такой, как представлена в SEQ ID NO 23, 24 и 44 соответственно;
(ix) FS28-256-001 может быть такой, как представлена в SEQ ID NO 23, 24 и 34 соответственно;
(x) FS28-256-005 может быть такой, как представлена в SEQ ID NO 23, 24 и 43 соответственно;
(xi) FS28-256-014 может быть такой, как представлена в SEQ ID NO 23, 24 и 25 соответственно;
(xii) FS28-256-018 может быть такой, как представлена в SEQ ID NO 23, 24 и 25 соответственно;
(xiii) FS28-256 может быть такой, как представлена в SEQ ID NO 23, 24 и 25 соответственно;
(xiv) FS28-024-051 может быть такой, как представлена в SEQ ID NO 23, 24 и 22 соответственно;
(xv) FS28-024-053 может быть такой, как представлена в SEQ ID NO 23, 24 и 22 соответственно; и
(xvi) FS28-024 может быть такой, как представлена в SEQ ID NO 23, 24 и 22 соответственно;
при этом указанные последовательности CDR определены в соответствии со схемой нумерации Кабата.
Антигенсвязывающий сайт на основе CDR может составлять VH- или VL-домены, предпочтительно VH- и VL-домены антитела FS28-256-271, FS28-024-052, FS28-256-021, FS28-256-012, FS28-256-023, FS28-256-024, FS28-256-026, FS28-256-027, FS28-256-001, FS28-256-005, FS28-256-014, FS28-256-018, FS28-256, FS28-024-051, FS28-024-053 или FS28-024, предпочтительно антитела FS28-256-271 или FS28-024-052, наиболее предпочтительно антитела FS28-256-271.
VH-домен антител FS28-256-271, FS28-024-052, FS28-256-021, FS28-256-012, FS28-256-023, FS28-256-024, FS28-256-026, FS28-256-027, FS28-256-001, FS28-256-005, FS28-256-014, FS28-256-018, FS28-256, FS28-024-051, FS28-024-053 и FS28-024 может иметь последовательность, представленную в SEQ ID NO 180, 39, 109, 109, 121, 109, 121, 109, 63, 63, 115, 121, 69, 30, 49 и 8 соответственно.
VL-домен антител FS28-256-271, FS28-024-052, FS28-256-021, FS28-256-012, FS28-256-023, FS28-256-024, FS28-256-026, FS28-256-027, FS28-256-001, FS28-256-005, FS28-256-014, FS28-256-018, FS28-256, FS28-024-051, FS28-024-053 и FS28-024 может иметь последовательность, представленную в SEQ ID NO 56, 18, 93, 79, 93, 53, 53, 56, 93, 53, 79, 79, 79, 18, 18 и 18 соответственно.
Молекула антитела может содержать тяжелую или легкую цепь, предпочтительно тяжелую и легкую цепь антитела FS28-256-271, FS28-024-052, FS28-256-021, FS28-256-012, FS28-256-023, FS28-256-024, FS28-256-026, FS28-256-027, FS28-256-001, FS28-256-005, FS28-256-014, FS28-256-018, FS28-256, FS28-024-051, FS28-024-053 или FS28-024, предпочтительно антитела FS28-256-271 или FS28-024-052, наиболее предпочтительно антитела FS28-256-271.
Тяжелая цепь (с мутацией LALA) антител FS28-256-271, FS28-024-052, FS28-256-021, FS28-256-012, FS28-256-023, FS28-256-024, FS28-256-026, FS28-256-027, FS28-256-001, FS28-256-005, FS28-256-014, FS28-256-018, FS28-256, FS28-024-051, FS28-024-053 и FS28-024 может иметь последовательность, представленную в SEQ ID NO 178, 37, 107, 107, 125, 107, 125, 107, 89, 89, 119, 125, 67, 28, 47, 5 соответственно.
Тяжелая цепь (без мутации LALA) антител FS28-256-271, FS28-024-052, FS28-256-021, FS28-256-012, FS28-256-023, FS28-256-024, FS28-256-026, FS28-256-027, FS28-256-001, FS28-256-005, FS28-256-014, FS28-256-018, FS28-256, FS28-024-051, FS28-024-053 и FS28-024 может иметь последовательность, представленную в SEQ ID NO 176, 35, 105, 105, 123, 105, 123, 105, 81, 87, 117, 123, 65, 26, 45 и 4 соответственно.
Легкая цепь антител FS28-256-271, FS28-024-052, FS28-256-021, FS28-256-012, FS28-256-023, FS28-256-024, FS28-256-026, FS28-256-027, FS28-256-001, FS28-256-005, FS28-256-014, FS28-256-018, FS28-256, FS28-024-051, FS28-024-053 и FS28-024 может иметь последовательность, представленную в SEQ ID NO 95, 16, 83, 77, 83, 90, 90, 95, 83, 90, 77, 77, 77, 16, 16 и 16 соответственно.
Молекула антитела может также содержать вариант CDR, VH-домена, VL-домена, последовательности тяжелой или легкой цепи, описанных в настоящей заявке. Подходящие варианты могут быть получены способами изменения или мутации и скрининга последовательностей. В предпочтительном варианте реализации молекула антитела, содержащая одну или более таких вариантных последовательностей, сохраняет одну или более функциональных характеристик исходной молекулы антитела, таких как специфичность связывания и/или аффинность связывания в отношении MSLN, предпочтительно MSLN человека и/или яванского макака. Например, молекула антитела, содержащая одну или более вариантных последовательностей, предпочтительно связывается с MSLN с такой же аффинностью или более высокой аффинностью по сравнению с (исходной) молекулой антитела. Исходная молекула антитела представляет собой молекулу антитела, которая не содержит замены (замен), делеции (делеций) и/или встраивания (встраиваний) аминокислоты, которые были включены в вариантную молекулу антитела.
Молекула антитела, содержащая CDR 1-6, VH-домен и/или тяжелую цепь антитела FS28-256-021, FS28-256-012, FS28-256-023, FS28-256-024, FS28-256-026, FS28-256-027, FS28-256-001, FS28-256-005, FS28-256-014, FS28-256-018 или FS28-256, может содержать замену аминокислоты в положении 55 или 57 VH-домена, при этом нумерация аминокислотных остатков соответствует схеме нумерации IMGT.
Например, молекула антитела может содержать CDR 1-6, VH-домен и/или тяжелую цепь антитела FS28-256-027, при этом указанная молекула антитела содержит замену аминокислоты в положении 55 VH-домена и нумерация аминокислотных остатков соответствует схеме нумерации IMGT.
Молекула антитела согласно настоящему изобретению может содержать VH-домен, VL-домен, тяжелую цепь или легкую цепь, которая обладает по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99%, по меньшей мере 99,1%, по меньшей мере 99,2%, по меньшей мере 99,3%, по меньшей мере 99,4%, по меньшей мере 99,5%, по меньшей мере 99,6%, по меньшей мере 99,7%, по меньшей мере 99,8% или по меньшей мере 99,9% идентичностью последовательности по отношению к VH-домену, VL-домену, тяжелой цепи или легкой цепи антитела FS28-256-271, FS28-024-052, FS28-256-021, FS28-256-012, FS28-256-023, FS28-256-024, FS28-256-026, FS28-256-027, FS28-256-001, FS28-256-005, FS28-256-014, FS28-256-018, FS28-256, FS28-024-051, FS28-024-053 или FS28-024, предпочтительно антитела FS28-256-271 или FS28-024-052, наиболее предпочтительно антитела FS28-256-271.
Идентичность последовательностей, как правило, определяют в соответствии с алгоритмом GAP (пакет программ Wisconsin GCG, Accelerys Inc, Сан-Диего, США). В GAP используют алгоритм Нидлмана-Вунша для выравнивания двух полных последовательностей с максимальным увеличением количества совпадений и сведением количества гэпов к минимуму. Как правило, используют параметры по умолчанию со штрафом за создание гэпа (gap creation penalty), равным 12, и штрафом за продление гэпа (gap extension penalty), равным 4. Применение GAP может быть предпочтительным, но можно применять и другие алгоритмы, например, BLAST (в котором используют способ Altschul et al., 1990, FASTA (в котором используют способ Пирсона-Липмана, 1988 г.) или алгоритм Смита-Уотермана (Смит и Уотерман, 1981 г.), или программу TBLASTN, Altschul et al., 1990 выше, как правило, с использованием параметров по умолчанию. В частности, можно применять алгоритм psi-Blast (Altschul et al., 1997).
Молекула антитела может содержать CDR1 VH, CDR2 VH, CDR3 VH, CDR1 VL, CDR2 VL и/или CDR3 VL, содержащую одно или более изменений аминокислотной последовательности (присоединение, делецию, замену и/или встраивание аминокислотного остатка), предпочтительно 3 изменения или меньше, 2 изменения или меньше, или 1 изменение относительно CDR1 VH, CDR2 VH, CDR3 VH, CDR1 VL, CDR2 VL и/или CDR3 VL антитела FS28-256-271, FS28-024-052, FS28-256-021, FS28-256-012, FS28-256-023, FS28-256-024, FS28-256-026, FS28-256-027, FS28-256-001, FS28-256-005, FS28-256-014, FS28-256-018, FS28-256, FS28-024-051, FS28-024-053 или FS28-024, предпочтительно антитела FS28-256-271 или FS28-024-052, наиболее предпочтительно антитела FS28-256-271.
Молекула антитела может содержать VH-домен, VL-домен, тяжелую цепь или легкую цепь, содержащую одно или более изменений аминокислотной последовательности (присоединение, делецию, замену и/или встраивание аминокислотного остатка), предпочтительно 20 изменений или меньше, 15 изменений или меньше, 10 изменений или меньше, 5 изменений или меньше, 4 изменения или меньше, 3 изменения или меньше, 2 изменения или меньше, или 1 изменение относительно VH-домена, VL-домена, тяжелой цепи или легкой цепи антитела FS28-256-271, FS28-024-052, FS28-256-021, FS28-256-012, FS28-256-023, FS28-256-024, FS28-256-026, FS28-256-027, FS28-256-001, FS28-256-005, FS28-256-014, FS28-256-018, FS28-256, FS28-024-051, FS28-024-053 или FS28-024, предпочтительно антитела FS28-256-271 или FS28-024-052, наиболее предпочтительно антитела FS28-256-271.
В частности, изменения аминокислотной последовательности могут быть расположены в одной или более каркасных областях молекул антител, например, в одной или более каркасных областях тяжелой и/или легкой цепи молекулы антитела.
В предпочтительных вариантах реализации, в которых одну или более аминокислот заменяют на другую аминокислоту, указанные замены могут представлять собой консервативные замены, например, в соответствии со следующей таблицей. В некоторых вариантах реализации аминокислоты в одной категории в среднем столбце заменяют друг на друга, т.е., например, неполярную аминокислоту заменяют на другую неполярную аминокислоту. В некоторых вариантах реализации аминокислоты в одной строке в крайнем правом столбце заменяют друг на друга.
В некоторых вариантах реализации замена (замены) может быть функционально консервативной. То есть в некоторых вариантах реализации замена может не влиять (или может по существу не влиять) на одно или более функциональных свойств (например, аффинность связывания) молекулы антитела, содержащей указанную замену, относительно эквивалентной молекулы антитела, не содержащей замены.
Тяжелая цепь молекулы антитела может необязательно содержать дополнительный остаток лизина (К) на непосредственном С-конце последовательности CH3-домена тяжелой цепи.
Известно, что CH2-домен связывается с Fcγ-рецепторами и комплементом. Связывание CH2-домена с Fcγ-рецепторами необходимо для антителозависимой клеточноопосредованной цитотоксичности (АЗКЦ), тогда как связывание с комплементом необходимо для комплементзависимой цитотоксичности (КЗЦ). В случае, когда молекулу антитела применяют в лечении рака и она не находится в форме ADC, ожидают, что АЗКЦ-активность будет приводить к уничтожению раковых клеток и поэтому ее следует предпочтительно сохранять. Однако, когда молекула антитела находится в форме ADC и конъюгирована с биоактивной молекулой, ожидают, что мутации для снижения или устранения АЗКЦ-активности, позволят избежать уничтожения раковых клеток-мишеней за счет АЗКЦ до доставки указанной биоактивной молекулы в клетку. Кроме того, ожидают, что мутации для снижения или устранения АЗКЦ- и/или КЗЦ-активности полезны в случае, когда молекула антитела содержит второй антигенсвязывающий сайт для антигена иммунной клетки, как описано в настоящей заявке, когда следует избегать АЗКЦ- и/или КЗЦ-опосредуемого уничтожения иммунных клеток, связанных молекулой антитела.
Таким образом, CH2-домен молекулы антитела может содержать одну или более мутаций, которые уменьшают или устраняют связывание CH2-домена с одним или более Fcγ-рецепторами, такими как FcγRI, FcγRlla, FcγRllb, FcγRIII, и/или с комплементом. Авторы настоящего изобретения допускают, что уменьшение или устранение связывания с Fcγ-рецепторами будет приводить к уменьшению или устранению АЗКЦ, опосредуемой молекулой антитела. Подобным образом, ожидают, что уменьшение или устранение связывания с комплементом будет приводить к уменьшению или устранению КЗЦ, опосредуемой молекулой антитела. В этой области техники известны мутации для уменьшения или устранения связывания CH2-домена с одним или более Fcγ-рецепторами и/или комплементом (Wang et al., 2018). Эти мутации включают «мутацию LALA», описанную в Bruhns et al., 2009 и Hezareh et al., 2001, которая включает замену остатков лейцина в положениях 1.3 и 1.2 CH2-домена на аланин (L1.3A и L1.2A). В качестве альтернативы, также известно, что получение a-гликозильных антител посредством мутации консервативного сайта N-связанного гликозилирования путем осуществления мутации: замены аспарагина (N) в положении 84.4 CH2-домена на аланин, глицин или глутамин (N84.4A, N84.4G или N84.4Q) снижает эффекторную функцию IgG1 (Wang et al., 2018). Также в качестве альтернативы, известно, что активацию комплемента (связывание C1q) и АЗКЦ снижают посредством мутации: замены пролина в положении 114 CH2-домена на аланин или глицин (P114A или P114G) (Idusogie et al., 2000; Klein et al., 2016). Эти мутации можно также комбинировать для получения молекул антител с еще бóльшим снижением или отсутствием АЗКЦ- или КЗЦ-активности.
Соответственно, молекула антитела может содержать CH2-домен, при этом указанный CH2-домен предпочтительно содержит:
(i) остатки аланина в положениях 1.3 и 1.2; и/или
(ii) аланин или глицин в положении 114; и/или
(iii) аланин, глутамин или глицин в положении 84.4;
при этом нумерация аминокислотных остатков соответствует схеме нумерации IMGT.
В предпочтительном варианте реализации молекула антитела содержит CH2-домен, при этом указанный CH2-домен содержит:
(i) остаток аланина в положении 1.3; и
(ii) остаток аланина в положении 1.2;
при этом нумерация аминокислотных остатков соответствует схеме нумерации IMGT.
Например, CH2-домен может содержать мутацию LALA и иметь последовательность, представленную в SEQ ID NO: 173.
В альтернативном предпочтительном варианте реализации молекула антитела содержит CH2-домен, при этом указанный CH2-домен содержит:
(i) остаток аланина в положении 1.3;
(ii) остаток аланина в положении 1.2; и
(iii) аланин в положении 114;
при этом нумерация аминокислотных остатков соответствует схеме нумерации IMGT.
Например, CH2-домен может содержать мутацию LALA-PA и иметь последовательность, представленную в SEQ ID NO: 174.
Также предусмотрена молекула антитела, которая содержит антигенсвязывающий сайт на основе CDR для MSLN и которая конкурирует с молекулой антитела, описанной в настоящей заявке, или которая связывается с тем же эпитопом на MSLN, что и молекула антитела, описанная в настоящей заявке. Способы определения конкуренции между двумя антителами за антиген известны в этой области техники. Например, конкуренция между двумя антителами за связывание с антигеном может быть определена посредством поверхностного плазмонного резонанса, например, с использованием устройства Biacore. Также известны методы картирования эпитопа, связываемого антителом.
Существуют данные о том, что N-концевая область MSLN взаимодействует с MUC16. По сообщениям, это взаимодействие может играть роль в адгезии раковых клеток.
Было показано, что молекулы антител демонстрируют диапазон активности в отношении связывания лиганда. Например, молекула антитела может быть способна блокировать или может не быть способна блокировать связывание MUC16 с MSLN. В качестве альтернативы, молекула антитела может быть способна усиливать связывание MUC16 с MSLN. Например, молекула антитела может содержать CDR 1-6, VH-домен, VL-домен, тяжелую цепь и/или легкую цепь антитела FS28-024-051, FS28-024-052, FS28-024-053 или FS28-024, или их вариант, при этом указанная молекула антитела блокирует связывание MUC16 с MSLN.
В предпочтительном варианте реализации молекула антитела не блокирует связывание MUC16 с MSLN. Например, молекула антитела может содержать CDR 1-6, VH-домен, VL-домен, тяжелую цепь и/или легкую цепь антитела FS28-256-271, FS28-256-021, FS28-256-012, FS28-256-023, FS28-256-024, FS28-256-026, FS28-256-027, FS28-256-001, FS28-256-005, FS28-256-014, FS28-256-018, FS28-256 или их вариант, при этом указанная молекула антитела не блокирует связывание MUC16 с MSLN.
Способы, подходящие для определения способности молекулы антитела блокировать связывание MUC16 с MSLN, известны в этой области техники и включают ELISA-анализы и анализы на основе клеток, например, анализ, в котором указанное антитело конкурирует за связывание с MUC16 за связывание с клетками, экспрессирующими MSLN, такими как клетки NCI-H226.
В предпочтительном варианте реализации молекула антитела может содержать один или более дополнительных антигенсвязывающих сайтов, которые связывают один или более дополнительных антигенов, в дополнение к антигенсвязывающему сайту на основе CDR для MSLN. Указанный один или более дополнительных антигенсвязывающих сайтов предпочтительно специфично связывают распознаваемые ими антигены.
Указанный один или более дополнительных антигенсвязывающих сайтов предпочтительно не связывают MSLN. Таким образом, молекула антитела может представлять собой мультиспецифичную, например, биспецифичную, триспецифичную или тетраспецифичную молекулу, предпочтительно биспецифичную молекулу. В предпочтительном варианте реализации молекула антитела способна одновременно связываться с MSLN и одним или более дополнительными антигенами.
Известно, что молекулы антител имеют модульную структуру, содержащую дискретные домены, которые можно комбинировать множеством различных способов для создания мультиспецифичных, например, биспецифичных, триспецифичных или тетраспецифичных форматов антител. Типичные мультиспецифичные форматы антител описаны, например, в Spiess et al. (2015) и Kontermann (2012). Молекулы антител согласно настоящему изобретению можно применять в таких мультиспецифичных форматах.
Например, молекула антитела согласно настоящему изобретению может представлять собой гетеродимерную молекулу антитела, такую как гетеродимерная целая молекула иммуноглобулина или ее фрагмент. В этом случае одна часть молекулы антитела будет содержать последовательность или последовательности, описанные в настоящей заявке. Например, в случае, когда молекула антитела согласно настоящему изобретению представляет собой биспецифичную гетеродимерную молекулу антитела, указанная молекула антитела может содержать тяжелую цепь и легкую цепь, описанные в настоящей заявке, спаренные с тяжелой цепью и легкой цепью, содержащими VH-домен и VL-домен соответственно, которые связывают антиген, отличный от MSLN, или дополнительно связываются с другим эпитопом на MSLN. Способы получения гетеродимерных антител известны в этой области техники и включают технологию «выступы-во-впадины» (knobs-into-holes, KIH), которая включает искусственное конструирование CH3-доменов молекулы антитела с получением либо «выступа», либо «впадины» для стимулирования гетеродимеризации цепи. В качестве альтернативы, гетеродимерные антитела могут быть получены путем введения пар зарядов в молекулу антитела, чтобы избежать гомодимеризации CH3-доменов за счет электростатического отталкивания и управлять гетеродимеризацией за счет электростатического притяжения. Примеры гетеродимерных форматов антител включают CrossMab, mAb-Fv, SEED-body и kih-IgG.
В качестве альтернативы, мультиспецифичная молекула антитела может содержать целую молекулу иммуноглобулина или ее фрагмент и дополнительный антигенсвязывающий фрагмент или фрагменты. Указанный антигенсвязывающий фрагмент может представлять собой, например, Fv, scFv или однодоменное антитело и может быть подвергнут слиянию с целой молекулой иммуноглобулина или ее фрагментом. Примеры мультиспецифичных молекул антител, содержащих дополнительные антигенсвязывающие фрагменты, слитые с целой молекулой иммуноглобулина, включают молекулы DVD-IgG, DVI-IgG, scFv4-IgG, IgG-scFv и scFv-IgG (Spiess et al., 2015; Фиг.1). Примеры мультиспецифичных молекул антител, содержащих дополнительные антигенсвязывающие фрагменты, слитые с фрагментом иммуноглобулина, включают молекулы BiTE, диатела и молекулы переориентирующихся антител с двойной аффинностью (DART) (Spiess et al., 2015; Фиг.1). Другие подходящие форматы будут понятны специалисту в этой области техники.
В предпочтительном варианте реализации молекула антитела содержит второй антигенсвязывающий сайт, который связывает второй антиген, при этом указанный второй антигенсвязывающий сайт расположен в константном домене молекулы антитела. Например, молекула антитела может представлять собой биспецифичное антитело mAb2 (™). Как указано в настоящем описании, биспецифичное антитело mAb2 представляет собой иммуноглобулин IgG, который содержит антигенсвязывающий сайт на основе CDR в каждой из вариабельных областей и по меньшей мере один антигенсвязывающий сайт в константном домене молекулы антитела.
В предпочтительном варианте реализации антитело представляет собой молекулу антитела, которая связывает MSLN и второй антиген, при этом указанная молекула антитела содержит:
(i) два антигенсвязывающих сайта на основе CDR для MSLN, каждый из которых образован VH-доменом иммуноглобулина и VL-доменом иммуноглобулина; и
(ii) два антигенсвязывающих сайта, которые связывают второй антиген, расположенные в двух CH3-доменах указанной молекулы антитела.
В более предпочтительном варианте реализации антитело представляет собой целую молекулу иммуноглобулина, например, целую молекулу IgG1, которая связывает MSLN и второй антиген, при этом указанная молекула антитела содержит:
(i) два антигенсвязывающих сайта на основе CDR для MSLN, каждый из которых образован VH-доменом иммуноглобулина и VL-доменом иммуноглобулина; и
(ii) два антигенсвязывающих сайта, которые связывают второй антиген, расположенные в двух CH3-доменах указанной молекулы антитела; и
при этом указанная молекула иммуноглобулина дополнительно содержит CH1-, CH2- и CL-домены.
Антигенсвязывающий сайт для второго антигена может быть расположен в любом константном домене молекулы антитела. Например, антигенсвязывающий сайт для второго антигена может быть расположен в одном или более из CH4-, CH3-, CH2-, CH1- или CL-доменов, предпочтительно в CH3- или CH2-домене, наиболее предпочтительно в CH3-домене.
Антигенсвязывающий сайт может состоять из одной или более, например, одной, двух, трех или более структурных петель константного домена молекулы антитела.
Указанные структурные петли константного домена антитела включают структурные петли AB, BC, CD, DE, EF и FG. Антигенсвязывающий сайт может содержать две или более структурных петель AB, BC, CD, DE, EF и FG константного домена, предпочтительно структурные петли AB и EF или структурные петли AB, CD и EF.
Положения структурных петель в константных доменах антител хорошо известны в этой области техники. Например, структурные петли CH3-домена расположены между положениями 10 и 19 (петля AB), 28 и 39 (петля BC), 42 и 79 (петля CD), 82 и 85 (петля DE), 91 и 102 (петля EF) и 106 и 117 (петля FG) CH3-домена, при этом остатки пронумерованы в соответствии со схемой нумерации IMGT. Можно легко определить расположение указанных положений структурных петель в других константных доменах.
Структурные петли константного домена могут содержать одну или более модификаций аминокислот для формирования антигенсвязывающего сайта для второго антигена. Одна или более модификаций аминокислот могут включать замены, присоединения или делеции аминокислот. Введение модификаций аминокислот в области структурных петель константных доменов антител для создания антигенсвязывающих сайтов для антигенов-мишеней хорошо известно в этой области техники и описано, например, в Wozniak-Knopp G et al., 2010, WO2006/072620 и WO2009/132876. Примеры связывающих сайтов в константных доменах приведены ниже.
В предпочтительном варианте реализации молекула антитела содержит одну или более модификаций аминокислот (замен, присоединений и/или делеций) в структурных петлях AB, CD и/или EF, предпочтительно структурных петлях AB и EF или структурных петлях AB, CD и EF. Например, молекула антитела может содержать одну или более модификаций аминокислот (замен, присоединений и/или делеций) в положениях 11-18, 43-78 и/или 92-101 CH3-домена, предпочтительно в положениях 11-18 и 92-101 или в положениях 11-18, 43-78 и 92-101 CH3-домена для получения антигенсвязывающего сайта для второго антигена, указанного в настоящей заявке. Более предпочтительно, молекула антитела содержит одну или более модификаций аминокислот (замен, присоединений и/или делеций) в положениях 12-18, с 45.1 по 78, с 92 по 94 и/или 97-98 CH3-домена, более предпочтительно в положениях 12-18, с 92 по 94 и 97-98 или в положениях 12-18, с 45.1 по 78, с 92 по 94 и 97-98 CH3-домена для получения антигенсвязывающего сайта для второго антигена, указанного в настоящей заявке. Немодифицированный CH3-домен предпочтительно содержит или состоит из последовательности, представленной в SEQ ID NO: 172. Нумерация остатков соответствует схеме нумерации IMGT.
Второй антиген, связываемый вторым антигенсвязывающим сайтом молекулы антитела, может представлять собой антиген иммунной клетки, предпочтительно представитель суперсемейства рецепторов фактора некроза опухоли (TNFRSF). Рецепторы TNFRSF представляют собой мембраносвязанные рецепторы цитокинов, которые содержат внеклеточный богатый цистеином домен, который связывает один или более лигандов суперсемейства факторов некроза опухолей (TNFSF).
Рецептор TNFRSF предпочтительно расположен на поверхности иммунной клетки, такой как Т-клетка, антигенпредставляющая клетка (АПК), NK-клетка и/или В-клетка, предпочтительно Т-клетка. После связывания лиганда TNFRSF рецепторы TNFRSF образуют кластеры на поверхности иммунной клетки, которые активируют иммунную клетку. Например, рецепторы TNFRSF, связанные лигандом, могут образовывать мультимеры, такие как тримеры, или кластеры мультимеров. Присутствие кластеров рецепторов TNFRSF, связанных лигандом, стимулирует внутриклеточные пути передачи сигнала, которые активируют иммунную клетку.
Не желая быть связанными какой-либо теорией полагают, что за счет вовлечения как MSLN на поверхности клетки опухоли, так и рецептора TNFRSF на поверхности иммунной клетки молекулы антител будут перекрестно связываться путем связывания с MSLN и таким образом управлять кластеризацией и активацией рецептора TNFRSF и, следовательно, активацией иммунной клетки (клеток). Другими словами, молекула антитела будет выступать в качестве агониста рецептора TNFRSF, когда обе мишени связаны. Затем активированные иммунные клетки могут инициировать, стимулировать или участвовать в иммунном ответе на рак, экспрессирующий MSLN, связанный с клеточной поверхностью. Обзор роли иммунной системы в распознавании и уничтожении раковых клеток проведен Chen and Mellman (2013).
Молекула антитела может быть перекрестно связана путем связывания с Fcγ-рецепторами, но это одновременно неэффективно и не может быть нацелено на конкретную область, например, очаг заболевания, поскольку клетки, экспрессирующие Fcγ-рецепторы, присутствуют по всему организму человека. Соответственно, в предпочтительном варианте реализации молекула антитела, содержащая второй антигенсвязывающий сайт для рецептора TNFRSF, содержит одну или мутаций для уменьшения или устранения связывания с одним или более Fcγ-рецепторами, как описано в настоящей заявке.
Авторы настоящего изобретения продемонстрировали с применением биспецифичных молекул, содержащих связывающие сайты как для MSLN, так и для рецептора TNFRSF, в частности молекул mAb2, содержащих два связывающих сайта в константном домене для рецептора TNFRSF и два антигенсвязывающих сайта на основе CDR для MSLN, что связывание молекулы антитела как с MSLN, так и с рецептором TNFRSF индуцирует или усиливает активацию Т-клеток.
Молекулу антитела, содержащую второй антигенсвязывающий сайт для рецептора TNFRSF, который активирует иммунные клетки, такие как Т-клетки, только при связывании с MSLN и рецептором TNFRSF, или активность в отношении активации иммунных клеток которого усиливается при связывании с MSLN и рецептором TNFRSF, также называют условным агонистом. Эта активность в отношении активации иммунных клеток не зависит от связывания молекулы антитела с Fcγ-рецепторами и/или внешними перекрестно связывающими агентами, такими как белок A или G, или вторичные антитела, и, следовательно, позволяет нацеливать условную агонистическую активность молекулы антитела на области, где присутствует как MSLN, так и TNFRSF. Поскольку MSLN представляет собой опухолевый антиген, молекула антитела может активировать иммунные клетки, такие как Т-клетки, избирательно в области опухоли, а не в каких-либо других областях организма у индивидуума.
Молекула антитела, активирующая иммунные клетки, такие как Т-клетки, только при связывании с MSLN и рецептором TNFRSF, может обладать повышенной активностью в отношении активации иммунных клеток по сравнению с молекулами антител, которые зависят от перекрестного связывания по другим механизмам, таким как внешние перекрестно связывающие агенты или перекрестное связывание через взаимодействие с Fcγ-рецептором. Поскольку активация рецептора TNFRSF более эффективна, активация иммунных клеток может быть достигнута при более низких концентрациях молекул антител, описанных в настоящей заявке, по сравнению с другими молекулами антител к TNFRSF.
В случае, когда молекула антитела согласно настоящему изобретению содержит второй антигенсвязывающий сайт для рецептора TNFRSF, присутствующего на Т-клетке, указанная молекула антитела предпочтительно индуцирует повышенную активацию иммунных клеток, таких как Т-клетки, когда молекула антитела перекрестно связана, например, через связывание с MSLN, по сравнению с тем, когда молекула антитела не является перекрестно связанной.
Способность молекулы антитела активировать Т-клетки может быть измерена с использованием анализа активации Т-клеток. После активации Т-клетки высвобождают IL-2. Соответственно, с помощью анализа активации Т-клеток можно измерять высвобождение IL-2 с определением уровня активации Т-клеток, индуцированной молекулой антитела.
Например, способность молекулы антитела активировать Т-клетки может быть определена путем измерения концентрации молекулы антитела, необходимой для достижения полумаксимального высвобождения IL-2 Т-клетками в анализе активации Т-клеток, когда указанная молекула антитела перекрестно связана. Ее также обозначают ЕС50 молекулы антитела. Более низкая EC50 указывает на то, что для достижения полумаксимального высвобождения IL-2 Т-клетками в анализе активации Т-клеток необходима более низкая концентрация молекулы антитела и, таким образом, на то, что указанная молекула антитела демонстрирует более высокую активность в отношении активации Т-клеток. Молекула антитела может быть перекрестно связана, например, с применением и антитела к CH2.
В дополнение к этому или в качестве альтернативы, способность молекулы антитела активировать Т-клетки может быть определена путем измерения максимальной концентрации IL-2, высвобождаемого Т-клетками в анализе активации Т-клеток в присутствии указанной молекулы антитела, при этом указанная молекула антитела перекрестно связана.
В предпочтительном варианте реализации молекула антитела (например, в формате mAb2, содержащем Fcab FS22-172-003), когда она перекрестно связана, например, через связывание с клетками NCI-H226, демонстрирует ЕС50 в анализе активации Т-клеток в пределах 50-кратного, 40-кратного, 30-кратного, 20-кратного, 10-кратного или 5-кратного значения ЕС50 FS22-172-003-AA/FS28-256-271 в этом же анализе, при этом FS22-172-003-AA/FS28-256-271 состоит из тяжелой цепи SEQ ID NO: 187 и легкой цепи SEQ ID NO: 188.
Например, молекула антитела, когда является перекрестно связанной, может демонстрировать EC50 в первичном анализе активации Т-клеток, составляющую 30 нМ или меньше, 25 нМ или меньше, 20 нМ или меньше, 14 нМ или меньше, 10 нМ или меньше, 5 нМ или меньше, 4 нМ или меньше, 3 нМ или меньше, 2 нМ или меньше, 1,5 нМ, 1 нМ или 0,5 нМ или меньше, предпочтительно 1,5 нМ или меньше, более предпочтительно 1 нМ, наиболее предпочтительно 0,5 нМ или меньше, когда является перекрестно связанной.
В дополнение к этому или в качестве альтернативы, способность молекулы антитела активировать Т-клетки может быть определена путем измерения максимальной концентрации IL-2, высвобождаемого Т-клетками в анализе активации Т-клеток в присутствии указанной перекрестно связанной молекулы антитела.
В предпочтительном варианте реализации максимальная концентрация IL-2, высвобождаемого Т-клетками в анализе активации Т-клеток в присутствии молекулы антитела (например, в формате mAb2, содержащем Fcab FS22-172-003), когда она перекрестно связана, например, через связывание с клетками NCI-H226, находится в пределах 20% или 10% от максимальной концентрации IL-2, высвобождаемого Т-клетками в присутствии FS22-172-003-AA/FS28-256-271 в этом же анализе, при этом FS22-172-003-AA/FS28-256-271 состоит из тяжелой цепи SEQ ID NO: 187 и легкой цепи SEQ ID NO: 188.
Например, указанный анализ Т-клеток может представлять собой анализ активации пан-Т-клеток или анализ активации CD8+ Т-клеток в зависимости от рецептора TNFRSF, связываемого вторым антигенсвязывающим сайтом. Например, анализ пан-Т-клеток подходит, когда рецептор TNFRSF представляет собой OX40, тогда как анализ CD8+ Т-клеток подходит, когда рецептор TNFRSF представляет собой CD137.
Например, анализ активации пан-Т-клеток может включать выделение мононуклеарных клеток периферической крови (МКПК) человека из лейкоцитарных фильтров. Способы выделения МКПК известны в этой области техники. Затем из МКПК могут быть выделены Т-клетки. Способы выделения Т-клеток из МКПК также известны в этой области техники.
Анализ активации Т-клеток может включать получение необходимого количества Т-клеток, например, в подходящей среде, такой как среда для Т-клеток. Необходимое количество Т-клеток получают в концентрации 1,0 × 106 клеток/мл. Затем Т-клетки стимулируют с использованием подходящего реагента для активации Т-клеток, который обеспечивает сигналы, необходимые для активации Т-клеток. Например, указанный реагент для активации Т-клеток может представлять собой реагент, содержащий CD3 и CD28, такой как гранулы, содержащие CD3 и CD28. Выделенные Т-клетки инкубируют в течение ночи совместно с реагентом для активации Т-клеток с активацией указанных Т-клеток. После этого активированные Т-клетки промывают с отделением Т-клеток от реагента для активации Т-клеток и ресуспендируют в среде для Т-клеток в подходящей концентрации, такой как 2,0 × 106 клеток/мл. Затем активированные Т-клетки добавляют в планшеты, покрытые антителом к CD3 человека.
Готовят подходящее разведение каждой тестируемой молекулы антитела и добавляют в лунки. Затем Т-клетки инкубируют при 37°C, 5% CO2 в течение 24 часов совместно с тестируемым антителом. Надосадочные жидкости собирают и анализируют с определением концентрации IL-2 в надосадочной жидкости. Способы определения концентрации IL-2 в растворе известны в этой области техники и описаны в примерах в настоящей заявке. Строят график зависимости концентрации IL-2 человека от логарифма концентрации молекулы антитела. Полученные кривые приводят в соответствие с использованием уравнения зависимости логарифма (агонист) и ответа.
Например, анализ активации CD8+ Т-клеток может включать выделение МКПК человека из лейкоцитарных фильтров. Способы выделения МКПК известны в этой области техники. Затем из МКПК могут быть выделены CD8+ Т-клетки. Способы выделения CD8+ Т-клеток из МКПК также известны в этой области техники.
Затем CD8+ Т-клетки добавляют в многолуночные планшеты, покрытые антителом к CD3 человека. Готовят подходящее разведение каждой тестируемой молекулы антитела и добавляют в лунки. Затем Т-клетки инкубируют при 37°C, 5% CO2 в течение 24 часов совместно с тестируемым антителом. Надосадочные жидкости собирают и анализируют с определением концентрации IL-2 в надосадочной жидкости. Способы определения концентрации IL-2 в растворе известны в этой области техники и описаны в примерах в настоящей заявке. Строят график зависимости концентрации IL-2 человека от логарифма концентрации молекулы антитела. Полученные кривые приводят в соответствие с использованием уравнения зависимости логарифма (агонист) и ответа.
Рецепторы TNFRSF включают CD27, CD40, EDA2R, EDAR, FAS, LTBR, RELT, TNFRSF1A, TNFRSF1B, TNFRSF4 (OX40), TNFRSF6B, TNFRSF8, TNFRSF9 (CD137), TNFRSF10A-10D, TNFRSF11A, TNFRSF11B, TNFRSF12A, TNFRSF13B, TNFRSF13C, TNFRSF14, TNFRSF17, TNFRSF18, TNFRSF19, TNFRSF21 и TNFRSF25.
В предпочтительном варианте реализации рецептор TNFRSF представляет собой TNFRSF4 (OX40).
В альтернативном предпочтительном варианте реализации рецептор TNFRSF представляет собой TNFRSF9 (CD137).
CD27 (TNFRSF7: ID гена 939) имеет эталонную аминокислотную последовательность NP_001233.1 и может кодироваться эталонной нуклеотидной последовательностью NM_001242.4. CD40 (TNFRSF5: ID гена 958) имеет эталонную аминокислотную последовательность NP_001241.1 и может кодироваться эталонной нуклеотидной последовательностью NM_001250.5. EDA2R (TNFRSF27: ID гена 60401) имеет эталонную аминокислотную последовательность NP_001186616.1 и может кодироваться эталонной нуклеотидной последовательностью NM_001199687.2. EDAR (ID гена 10913) имеет эталонную аминокислотную последовательность NP_071731.1 и может кодироваться эталонной нуклеотидной последовательностью NM_022336, 3. FAS (TNFRSF6: ID гена 355) имеет эталонную аминокислотную последовательность NP_000034.1 и может кодироваться эталонной нуклеотидной последовательностью NM_000043.5. LTBR (TNFRSF3: ID гена 4055) имеет эталонную аминокислотную последовательность NP_001257916.1 и может кодироваться эталонной нуклеотидной последовательностью NM_001270987.1. RELT (TNFRSF19L: ID гена 84957) имеет эталонную аминокислотную последовательность NP_116260.2 и может кодироваться эталонной нуклеотидной последовательностью NM_032871.3. TNFRSF1A (ID гена 7132) имеет эталонную аминокислотную последовательность NP_001056.1 и может кодироваться эталонной нуклеотидной последовательностью NM_001065.3. TNFRSF1B (ID гена 7133) имеет эталонную аминокислотную последовательность NP_001057.1 и может кодироваться эталонной нуклеотидной последовательностью NM_001066.2. TNFRSF4 (ID гена 7293) имеет эталонную аминокислотную последовательность NP_003318 и может кодироваться эталонной нуклеотидной последовательностью NM_003327. TNFRSF6B (ID гена 8771) имеет эталонную аминокислотную последовательность NP_003814.1 и может кодироваться эталонной нуклеотидной последовательностью NM_003823.3. TNFRSF8 (ID гена 943) имеет эталонную аминокислотную последовательность NP_001234.3 и может кодироваться эталонной нуклеотидной последовательностью NM_001243.4. TNFRSF9 (ID гена 3604) имеет эталонную аминокислотную последовательность NP_001552 и может кодироваться эталонной нуклеотидной последовательностью NM001561. TNFRSF10A (ID гена 8797) имеет эталонную аминокислотную последовательность NP_003835.3 и может кодироваться эталонной нуклеотидной последовательностью NM_003844.3. TNFRSF10B (ID гена 8795) имеет эталонную аминокислотную последовательность NP_003833.4 и может кодироваться эталонной нуклеотидной последовательностью NM_003842.4. TNFRSF10C (ID гена 8794) имеет эталонную аминокислотную последовательность NP_003832.2 и может кодироваться эталонной нуклеотидной последовательностью NM_003841.4. TNFRSF10D (ID гена 8793) имеет эталонную аминокислотную последовательность NP_003831.2 и может кодироваться эталонной нуклеотидной последовательностью NM_003840.4. TNFRSF11A (ID гена 8792) имеет эталонную аминокислотную последовательность XP_011524547.1 и может кодироваться эталонной нуклеотидной последовательностью XM_11526245.2. TNFRSF11B (ID гена 4982) имеет эталонную аминокислотную последовательность NP_002537.3 и может кодироваться эталонной нуклеотидной последовательностью NM_002546.3. TNFRSF12A (ID гена 51330) имеет эталонную аминокислотную последовательность NP_057723.1 и может кодироваться эталонной нуклеотидной последовательностью NM_016639.2. TNFRSF13B (ID гена 23495) имеет эталонную аминокислотную последовательность NP_0036584.1 и может кодироваться эталонной нуклеотидной последовательностью NM_012452.2. TNFRSF13C (ID гена 115650) имеет эталонную аминокислотную последовательность NP_443177.1 и может кодироваться эталонной нуклеотидной последовательностью NM_052945.3. TNFRSF14 (ID гена 8764) имеет эталонную аминокислотную последовательность NP_001284534.1 и может кодироваться эталонной нуклеотидной последовательностью NM_001297605.1. TNFRSF17 (ID гена 608) имеет эталонную аминокислотную последовательность NP_001183.2 и может кодироваться эталонной нуклеотидной последовательностью NM_001192.2. TNFRSF18 (ID гена 8784) имеет эталонную аминокислотную последовательность NP_004195.2 и может кодироваться эталонной нуклеотидной последовательностью NM_004186.1. TNFRSF19 (ID гена 55504) имеет эталонную аминокислотную последовательность NP_001191387.1 и может кодироваться эталонной нуклеотидной последовательностью NM_001204458.1. NFRSF21 (ID гена 27242) имеет эталонную аминокислотную последовательность NP_055267.1 и может кодироваться эталонной нуклеотидной последовательностью NM_014452.4. TNFRSF25 (DR3: ID гена 8718) связывается с лигандом TNFSF15 (TL1A) имеет эталонную аминокислотную последовательность NP_001034753.1 и может кодироваться эталонной нуклеотидной последовательностью NM_001039664.1.
В некоторых вариантах реализации молекула антитела может не содержать антигенсвязывающий сайт в константном домене, например, CH3-домене молекулы антитела. Например, молекула антитела может не содержать антигенсвязывающий сайт, который связывается с CD137, в константном домене, таком как CH3-домен, молекулы антитела. В частности, молекула антитела может не содержать антигенсвязывающий сайт для CD137 в константном домене молекулы антитела, где указанный антигенсвязывающий сайт содержит модификации в одной или более структурных петлях константного домена, такие как одна или более модификаций в структурных петлях AB, CD и/или EF константного домена. В конкретном варианте реализации молекула антитела может не содержать антигенсвязывающий сайт для CD137, расположенный в CH3-домене молекулы антитела, содержащий первую последовательность и вторую последовательность, расположенные в структурных петлях AB и EF указанного CH3-домена соответственно, причем указанная первая и вторая последовательности имеют последовательность, представленную в SEQ ID NO 198 и 199 соответственно [FS22-172-003]. Например, молекула антитела может не содержать последовательностей легкой и тяжелой цепи, представленных в SEQ ID NO: 200 и 201 [FS22-172-003-AA/FS28-256-271].
Молекула антитела может быть конъюгирована с биоактивной молекулой или детектируемой меткой. В этом случае молекула антитела может называться «конъюгатом». Такие конъюгаты находят применение в лечении и/или диагностике заболеваний, описанных в настоящей заявке.
Например, биоактивная молекула может представлять собой модулятор иммунной системы, такой как цитокин, предпочтительно цитокин человека. Например, указанный цитокин может представлять собой цитокин, который стимулирует активацию и/или пролиферацию Т-клеток. Примеры цитокинов для конъюгации с молекулой антитела включают IL-2, IL-10, IL-12, IL-15, IL-21, гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF) и IFN-гамма.
В качестве альтернативы, биоактивная молекула может представлять собой лигандную ловушку, такую как лигандная ловушка цитокина, например, TGF-бета или IL-6.
В качестве дополнительной альтернативы, биоактивная молекула может представлять собой лиганд, такой как CD137L, OX40L, TRAIL, CD40L, CD27L или GITRL.
В качестве дополнительной альтернативы, биоактивная молекула может представлять собой лекарственное средство, такое как ингибитор полимеризации тубулина (например, ауристатин), агент деполимеризации тубулина (например, майтансин), агент, индуцирующий разрыв цепи ДНК (например, калихеамицин), ДНК-алкилирующий агент (например, дуокармицин) или ингибитор РНК-полимеразы (такой как альфа-аманитин).
В качестве еще одной альтернативы, биоактивная молекула может представлять собой терапевтический радиоизотоп.
Радиоиммунотерапию применяют, например, в лечении рака. Терапевтические радиоизотопы, подходящие для радиоиммунотерапии, известны в этой области техники и включают иттрий-90, йод-131, висмут-213, астат-211, лютеций 177, рений-188, медь-67, актиний-225, йод-125.
Подходящие детектируемые метки, которые могут быть конъюгированы с молекулами антител, известны в этой области техники и включают радиоизотопы, такие как йод-125, йод-131, иттрий-90, индий-111 и технеций-99; флуорохромы, такие как флуоресцеин, родамин, фикоэритрин, техасский красный и производные цианиновых красителей, например Cy7 и Alexa750; хромогенные красители, такие как диаминобензидин; латексные гранулы; ферментные метки, такие как пероксидаза хрена; люминофорные или лазерные красители со спектрально выделенными характеристиками поглощения или эмиссии; и химические вещества, такие как биотин, которые можно детектировать через связывание с конкретным родственным детектируемым фрагментом, например меченым авидином.
Молекула антитела может быть конъюгирована с биоактивной молекулой или детектируемой меткой посредством любой подходящей ковалентной или нековалентной связи, такой как дисульфидная или пептидная связь. В случае, когда биоактивная молекула представляет собой цитокин, указанный цитокин может быть присоединен к молекуле антитела посредством пептидного линкера. Подходящие пептидные линкеры известны в этой области техники и их длина может составлять от 5 до 25, от 5 до 20, от 5 до 15, от 10 до 25, от 10 до 20 или от 10 до 15 аминокислот.
В некоторых вариантах реализации биоактивная молекула может быть конъюгирована с молекулой антитела посредством расщепляемого линкера. Указанный линкер может обеспечивать освобождение биоактивной молекулы от молекулы антитела в области, где происходит терапия. Линкеры могут включать амидные связи (например, пептидные линкеры), дисульфидные связи или гидразоны. Пептидные линкеры, например, могут расщепляться под действием сайт-специфических протеаз, дисульфидные связи могут расщепляться под воздействием восстановительной среды цитозоля, и гидразоны могут расщепляться в результате кислотного гидролиза.
Конъюгат может представлять собой слитый белок, содержащий молекулу антитела и биоактивную молекулу. В этом случае биоактивная молекула может быть конъюгирована с молекулой антитела посредством пептидного линкера или пептидной связи. В случае, когда молекула антитела представляет собой многоцепочечную молекулу, например, когда молекула антитела представляет собой или содержит Fcab, или представляет собой mAb2, биоактивная молекула может быть конъюгирована с одной или более цепями молекулы антитела. Например, биоактивная молекула может быть конъюгирована с одной или обеими тяжелыми цепями молекулы mAb2. Преимуществом слитых белков является то, что их легче получать и очищать, что облегчает получение вещества для клинического применения.
Согласно настоящему изобретению также предложена выделенная молекула или молекулы нуклеиновой кислоты, кодирующие молекулу антитела согласно настоящему изобретению. Специалисту не составит труда получить такие молекулы нуклеиновой кислоты с применением способов, хорошо известных в этой области техники.
Указанная молекула или молекулы нуклеиновой кислоты могут кодировать VH-домен и/или VL-домен, предпочтительно VH-домен и VL-домен: антитела FS28-256-271, FS28-024-052, FS28-256-021, FS28-256-012, FS28-256-023, FS28-256-024, FS28-256-026, FS28-256-027, FS28-256-001, FS28-256-005, FS28-256-014, FS28-256-018, FS28-256, FS28-024-051, FS28-024-053 или FS28-024, предпочтительно антитела FS28-256-271 или FS28-024-052, наиболее предпочтительно антитела FS28-256-271.
Например, молекула нуклеиновой кислоты, кодирующая VH-домен антитела FS28-256-271, FS28-024-052, FS28-256-021, FS28-256-012, FS28-256-023, FS28-256-024, FS28-256-026, FS28-256-027, FS28-256-001, FS28-256-005, FS28-256-014, FS28-256-018, FS28-256, FS28-024-051, FS28-024-053 и FS28-024, представлена в SEQ ID NO: 181, 40, 110, 110, 122, 110, 122, 110, 64, 64, 116, 122, 70, 31, 50 и 9 соответственно.
Молекула нуклеиновой кислоты, кодирующая VL-домен антитела FS28-256-271, FS28-024-052, FS28-256-021, FS28-256-012, FS28-256-023, FS28-256-024, FS28-256-026, FS28-256-027, FS28-256-001, FS28-256-005, FS28-256-014, FS28-256-018, FS28-256, FS28-024-051, FS28-024-053 и FS28-024, представлена в SEQ ID NO: 57, 19, 94, 80, 94, 54, 54, 57, 94, 54, 80, 80, 80, 19, 19 и 19 соответственно.
В предпочтительном варианте реализации молекула (молекулы) нуклеиновой кислоты кодирует тяжелую цепь и/или легкую цепь, предпочтительно тяжелую цепь и легкую цепь: антитела FS28-256-271, FS28-024-052, FS28-256-021, FS28-256-012, FS28-256-023, FS28-256-024, FS28-256-026, FS28-256-027, FS28-256-001, FS28-256-005, FS28-256-014, FS28-256-018, FS28-256, FS28-024-051, FS28-024-053 или FS28-024, предпочтительно антитела FS28-256-271 или FS28-024-052, наиболее предпочтительно антитела FS28-256-271.
Например, молекула нуклеиновой кислоты, кодирующая тяжелую цепь (с мутацией LALA) антитела FS28-256-271, FS28-024-052, FS28-256-021, FS28-256-012, FS28-256-023, FS28-256-024, FS28-256-026, FS28-256-027, FS28-256-001, FS28-256-005, FS28-256-014, FS28-256-018, FS28-256, FS28-024-051, FS28-024-053 и FS28-024, представлена в SEQ ID NO: 179, 38, 108, 108, 126, 108, 126, 108, 84, 84, 120, 126, 68, 29, 48 и 7 соответственно.
Например, молекула нуклеиновой кислоты, кодирующая тяжелую цепь (без мутации LALA) антитела FS28-256-271, FS28-024-052, FS28-256-021, FS28-256-012, FS28-256-023, FS28-256-024, FS28-256-026, FS28-256-027, FS28-256-001, FS28-256-005, FS28-256-014, FS28-256-018, FS28-256, FS28-024-051, FS28-024-053 и FS28-024, представлена в SEQ ID NO: 177, 36, 106, 106, 124, 106, 124, 106, 82, 88, 118, 124, 66, 27, 46 и 6 соответственно.
Молекула нуклеиновой кислоты, кодирующая легкую цепь антитела FS28-256-271, FS28-024-052, FS28-256-021, FS28-256-012, FS28-256-023, FS28-256-024, FS28-256-026, FS28-256-027, FS28-256-001, FS28-256-005, FS28-256-014, FS28-256-018, FS28-256, FS28-024-051, FS28-024-053 и FS28-024, представлена в SEQ ID NO: 96, 17, 92, 78, 92, 91, 91, 96, 92, 91, 78, 78, 78, 17, 17 и 17 соответственно.
В случае, когда нуклеиновая кислота кодирует VH- и VL-домен или тяжелую и легкую цепь молекулы антитела согласно настоящему изобретению, указанные два домена или цепи могут кодироваться двумя отдельными молекулами нуклеиновой кислоты.
Для экспрессии молекулы антитела согласно настоящему изобретению можно применять выделенную молекулу нуклеиновой кислоты. Нуклеиновая кислота, как правило, представлена в форме рекомбинантного вектора для экспрессии. Соответственно, согласно другому аспекту настоящего изобретения предложен вектор, содержащий нуклеиновую кислоту, описанную выше. Могут быть выбраны или сконструированы подходящие векторы, содержащие соответствующие регуляторные последовательности, включая промоторные последовательности, терминаторные фрагменты, последовательности полиаденилирования, энхансерные последовательности, маркерные гены и другие последовательности при необходимости. Предпочтительно, вектор содержит соответствующие регуляторные последовательности для управления экспрессией нуклеиновой кислоты в клетке-хозяине. Векторы могут представлять собой плазмиды, вирусные векторы, например, фаг или фагмиду при необходимости.
Молекула нуклеиновой кислоты или вектор, описанный в настоящей заявке, может быть введен в клетку-хозяина. Способы введения нуклеиновой кислоты или векторов в клетки-хозяева хорошо известны в этой области техники и можно применять любой подходящий способ. В этой области техники известен ряд клеток-хозяев, подходящих для получения рекомбинантных молекул антител, и он включает клетки-хозяева бактерий, дрожжей, насекомых или млекопитающих. Предпочтительная клетка-хозяин представляет собой клетку млекопитающего, такую как клетка CHO, NS0 или HEK, например, клетка HEK293.
В соответствии с другим аспектом настоящего изобретения предложен способ получения молекулы антитела согласно настоящему изобретению, включающий экспрессию нуклеиновой кислоты, кодирующей указанную молекулу антитела, в клетке-хозяине и необязательно выделение и/или очистку молекулы антитела, полученной таким образом. Способы культивирования клеток-хозяев хорошо известны в этой области техники. Указанный способ может дополнительно включать выделение и/или очистку молекулы антитела. Способы очистки рекомбинантных молекул антител хорошо известны в этой области техники и включают, например, ВЭЖХ, жидкостную хроматографию быстрого разрешения (FPLC) или аффинную хроматографию, например, с использованием белка A или белка L. В некоторых вариантах реализации очистку можно осуществлять с использованием аффинной метки на молекуле антитела. Способ может также включать введение молекулы антитела в состав фармацевтической композиции, необязательно совместно с фармацевтически приемлемым вспомогательным веществом или другим веществом, описанным ниже.
Как описано выше, MSLN экспрессируется на поверхности клеток опухоли, и высокие уровни экспрессии растворимого MSLN коррелировали с неблагоприятным прогнозом в случае некоторых раковых опухолей. Антитела к MSLN исследовали в качестве противораковых лекарственных средств. Эти антитела к MSLN либо индуцируют непосредственное уничтожение клеток за счет своей АЗКЦ-активности, либо их применяют в форме ADC.
Соответственно, ожидают, что молекулы антител, описанные в настоящей заявке, найдут применение в лечении рака. Соответственно, согласно родственным аспектам настоящего изобретения предложены:
(i) молекула антитела, описанная в настоящей заявке, для применения в способе лечения рака у индивидуума,
(ii) применение молекулы антитела, описанной в настоящей заявке, в изготовлении лекарственного средства для применения в лечении рака у индивидуума; и
(iv) способ лечения рака у индивидуума, при этом указанный способ включает введение указанному индивидууму терапевтически эффективного количества молекулы антитела, описанной в настоящей заявке.
Индивидуум может представлять собой пациента, предпочтительно пациента-человека.
Было показано, что молекулы антител согласно настоящему изобретению предпочтительно связываются с MSLN, присутствующим на поверхности раковой клетки, в сравнении с растворимым MSLN. Соответственно, рак, который лечат с применением молекулы антитела согласно настоящему изобретению, предпочтительно экспрессирует или, как определено, экспрессирует MSLN. Более предпочтительно, клетки рака, который лечат, содержат или, как определено, содержат MSLN на своей клеточной поверхности, т.е. содержат MSLN, связанный с клеточной поверхностью.
В случае, когда молекула антитела содержит второй антигенсвязывающий сайт для антигена иммунной клетки, такого как представитель TNFRSF, например, в константном домене молекулы антитела, рак предпочтительно содержит или, как определено, содержит лимфоциты, инфильтрирующие опухоль (TIL), которые экспрессируют указанного представителя TNFRSF. В частности, указанные TIL предпочтительно содержат или, как определено, содержат представителя TNFRSF на своей клеточной поверхности.
Способы определения присутствия антигена на клеточной поверхности известны в этой области техники и включают, например, проточную цитометрию.
Рак может представлять собой первичный или вторичный рак. Таким образом, молекулу антитела, описанную в настоящей заявке, можно применять в способе лечения рака у индивидуума, при этом указанный рак представляет собой первичную опухоль и/или метастаз опухоли.
Рак, который лечат с применением молекулы антитела согласно настоящему изобретению, может представлять собой солидный рак.
Рак может быть выбран из группы, состоящей из: мезотелиомы, рака поджелудочной железы, рака яичников, рака легкого (такого как мелкоклеточный рак легкого и немелкоклеточный рак легкого), рака пищевода, рака молочной железы, рака желудка, холангиокарциномы, рака толстой кишки, карциномы вилочковой железы, рака эндометрия, рака головы и шеи, саркомы (такой как двухфазная синовиальная саркома, саркома Капоши, остеогенная саркома, рабдомиосаркома или саркома мягких тканей), десмопластических мелкокруглоклеточных опухолей, лейкоза (такого как острый лимфоцитарный лейкоз, хронический лимфоцитарный лейкоз, острый гранулоцитарный лейкоз, хронический гранулоцитарный лейкоз, волосатоклеточный лейкоз или миелоидный лейкоз), рака коры надпочечников, рака мочевого пузыря, рака головного мозга, рака шейки матки, гиперплазии шейки матки, хориокарциномы яичка, эссенциального тромбоцитоза, урогенитальной карциномы, глиомы, глиобластомы, лимфомы (такой как болезнь Ходжкина или неходжкинская лимфома), злокачественной карциноидной опухоли, злокачественной гиперкальциемии, меланомы (также называемой злокачественной меланомой), злокачественной инсулиномы поджелудочной железы, медуллярной карциномы щитовидной железы, множественной миеломы, фунгоидного микоза, нейробластомы, истинной полицитемии, первичной карциномы головного мозга, первичной макроглобулинемии, рака предстательной железы, почечно-клеточного рака, рака кожи, плоскоклеточного рака, рака желудка, рака яичка, рака щитовидной железы и опухоли Вильмса.
Предпочтительно, рак выбран из группы, состоящей из: мезотелиомы, рака поджелудочной железы, рака яичников, рака легкого, рака пищевода, рака молочной железы, рака желудка, холангиокарциномы, рака толстой кишки, карциномы вилочковой железы, рака эндометрия, рака головы и шеи, двухфазных синовиальных сарком и десмопластических мелкокруглоклеточных опухолей.
Более предпочтительно, рак выбран из группы, состоящей из: мезотелиомы, рака поджелудочной железы, рака яичников и рака легкого.
Рак характеризуется аномальной пролиферацией злокачественных раковых клеток. При упоминании конкретного вида рака, такого как рак молочной железы, этот термин относится к аномальной пролиферации злокачественных клеток соответствующей ткани, такой как ткань молочной железы. Вторичная раковая опухоль, локализованная в молочной железе, но возникшая в результате аномальной пролиферации злокачественных клеток другой ткани, такой как ткань яичников, не является раком молочной железы, упомянутым в настоящем описании, а представляет собой рак яичников.
В случае рака лечение может включать подавление роста раковой опухоли, включая полную ремиссию по раку, и/или подавление метастазирования рака, а также предотвращение рецидива рака. Рост раковой опухоли, в целом, относится к любому из ряда показателей, которые указывают на переход раковой опухоли в более развитую форму. Таким образом, показатели для измерения подавления роста раковой опухоли включают уменьшение выживания раковых клеток, уменьшение объема или морфологии опухоли (например, определяемое с применением компьютерной томографии (КТ), ультразвуковой эхографии или другого метода визуализации), замедление роста опухоли, разрушение сосудистой сети опухоли, улучшение результатов кожного теста на гиперчувствительность замедленного типа, повышение активности противораковых иммунных клеток или других противораковых иммунных ответов и снижение уровней опухолеспецифических антигенов. Активация или усиление иммунных ответов на раковые опухоли у индивидуума может повышать способность указанного индивидуума противостоять росту раковой опухоли, в частности, росту раковой опухоли, уже имеющейся у субъекта, и/или снижать предрасположенность к росту раковой опухоли у указанного индивидуума.
Хотя молекулу антитела можно вводить отдельно, молекулы антител, как правило, вводят в форме фармацевтической композиции, которая может содержать по меньшей мере один компонент в дополнение к указанной молекуле антитела. Соответственно, согласно другому аспекту настоящего изобретения предложена фармацевтическая композиция, содержащая молекулу антитела, описанную в настоящей заявке. Также предложен способ, включающий введение молекулы антитела в состав фармацевтической композиции.
Фармацевтические композиции в дополнение к молекуле антитела могут содержать фармацевтически приемлемое вспомогательное вещество, носитель, буфер, стабилизатор или другие вещества, хорошо известные специалисту в этой области техники. В настоящем описании термин «фармацевтически приемлемый» относится к соединениям, веществам, композициям и/или лекарственным формам, которые с медицинской точки зрения подходят для применения в контакте с тканями субъекта (например, человека), не вызывая при этом чрезмерной токсичности, раздражения, аллергической реакции или другой проблемы или осложнения, при разумном соотношении польза/риск. Каждый носитель, вспомогательное вещество и т.д. должен быть также «приемлемым» в смысле совместимости с другими ингредиентами состава. Точная природа носителя или другого вещества будет зависеть от пути введения, который может представлять собой путь введения посредством инфузии, инъекции или другой подходящий путь, рассмотренный ниже.
Для парентерального, например подкожного или внутривенного введения, например путем инъекции, фармацевтическая композиция, содержащая молекулу антитела, может иметь форму парентерально приемлемого водного раствора, который не содержит пирогенных веществ и имеет подходящий рН, изотоничность и стабильность. Специалист в этой области техники может приготовить подходящие растворы с применением, например, изотонических носителей, таких как хлорид натрия для инъекций, раствор Рингера для инъекций, лактатный раствор Рингера для инъекций. При необходимости можно использовать консерванты, стабилизаторы, буферы, антиоксиданты и/или другие добавки, включая буферы, такие как фосфат, цитрат и другие органические кислоты; антиоксиданты, такие как аскорбиновая кислота и метионин; консерванты (такие как октадецилдиметилбензиламмония хлорид; гексаметония хлорид; бензалкония хлорид; бензетония хлорид; фенол; бутиловый или бензиловый спирт; алкилпарабены, такие как метил- или пропилпарабен; катехол; резорцин; циклогексанол; 3’-пентанол; и м-крезол); низкомолекулярные полипептиды; белки, такие как сывороточный альбумин, желатин или иммуноглобулины; гидрофильные полимеры, такие как поливинилпирролидон; аминокислоты, такие как глицин, глутамин, аспарагин, гистидин, аргинин или лизин; моносахариды, дисахариды и другие углеводы, включая глюкозу, маннозу или декстрины; хелатирующие агенты, такие как EDTA; сахара, такие как сахароза, маннитол, трегалоза или сорбитол; солеобразующие противоионы, такие как натрий; комплексы металлов (например, комплексы Zn-белок); и/или неионные поверхностно-активные вещества, такие как ТВИН™, ПЛЮРОНИК™ или полиэтиленгликоль (ПЭГ).
В некоторых вариантах реализации молекулы антител могут быть представлены в лиофилизированной форме для восстановления перед введением. Например, лиофилизированные молекулы антител могут быть восстановлены в стерильной воде и смешаны с физиологическим раствором перед введением индивидууму.
Введение можно осуществлять в «терапевтически эффективном количестве», которого достаточно для оказания индивидууму полезного эффекта. Фактическое вводимое количество и частота, и период действия введения будут зависеть от природы и тяжести того, что лечат, конкретного индивидуума, которого лечат, клинического состояния индивидуума, причины нарушения, места доставки композиции, типа молекулы антитела, способа введения, графика введения и других факторов, известных врачам. Назначение лечения, например, решения относительно дозы и т.д., находится в рамках ответственности врачей общей практики и других врачей, и может зависеть от тяжести симптомов и/или прогрессирования заболевания, которое лечат. Подходящие дозы молекул антител хорошо известны в это области техники (Ledermann et al., 1991; Bagshawe et al., 1991). Можно использовать конкретные дозы, которые как указано в настоящем описании или в Physician's Desk Reference (2003), подходят для вводимой молекулы антитела. Терапевтически эффективное количество или подходящая доза молекулы антитела может быть определена путем сравнения активности in vitro и активности in vivo в модели у животных. Известны методы экстраполяции эффективных доз у мышей и других тестируемых животных на людей. Точная доза будет зависеть от ряда факторов, включая размер и расположение области, подлежащей лечению, и точную природу молекулы антитела.
Типичная доза антитела находится в диапазоне от 100 мкг до 1 г для системного применения и от 1 мкг до 1 мг для топического применения. Может быть введена начальная более высокая загрузочная доза с последующим введением одной или больше более низких доз. Это доза для однократного лечения взрослого индивидуума, которую можно пропорционально корректировать для детей и младенцев, а также корректировать в случае других форматов антител пропорционально молекулярной массе.
Лечение можно повторять ежедневно, два раза в неделю, раз в неделю или раз в месяц на усмотрение врача. Схема лечения для индивидуума может зависеть от фармакокинетических и фармакодинамических свойств композиции антител, пути введения и природы состояния, которое лечат.
Лечение может быть периодическим, и период между введениями может составлять примерно две недели или больше, например, примерно три недели или больше, примерно четыре недели или больше, примерно один раз в месяц или больше, примерно пять недель или больше, или примерно шесть недель или больше. Например, лечение можно осуществлять каждые две-четыре недели или каждые четыре-восемь недель. Подходящие составы и пути введения описаны выше.
В случае лечения рака молекулу антитела, описанную в настоящей заявке, можно вводить индивидууму в комбинации с другой противораковой терапией или терапевтическим агентом, таким как противораковая терапия или терапевтический агент, который, как было продемонстрировано, подходит или, как ожидают, будет подходить для лечения рассматриваемого рака. Например, молекулу антитела можно вводить индивидууму в комбинации с химиотерапевтическим агентом, радиотерапией, иммунотерапевтическим агентом, противоопухолевой вакциной, онколитическим вирусом, терапией с применением адоптивного переноса клеток (ACT) (такой как адоптивная терапия NK-клетками или терапия Т-клетками с химерными антигенными рецепторами (CAR), аутологичными лимфоцитами, инфильтрирующими опухоль (TIL), или гамма/дельта-Т-клетками, или агентом для гормональной терапии.
Не желая быть связанными какой-либо теорией, полагают, что молекула антитела, описанная в настоящей заявке, при этом указанная молекула антитела содержит второй антигенсвязывающий сайт для антигена иммунных клеток, такого как рецептор TNFRSF, может выступать в качестве адъюванта в противораковой терапии. В частности, полагают, что введение молекулы антитела индивидууму в комбинации с химиотерапией и/или радиотерапией, или в комбинации с противоопухолевой вакциной, например, будет запускать более сильный иммунный ответ на рак, чем достигаемый в случае одной химиотерапии и/или радиотерапии, или в случае одной противоопухолевой вакцины.
Один или более химиотерапевтических агентов для введения в комбинации с молекулой антитела, описанной в настоящей заявке, могут быть выбраны из группы, состоящей из: таксанов, цитотоксических антибиотиков, ингибиторов тирозинкиназы, ингибиторов PARP, ингибиторов фермента B-Raf, ингибиторов MEK, ингибиторов c-MET, ингибиторов VEGFR, ингибиторов PDGFR, алкилирующих агентов, аналогов платины, аналогов нуклеозидов, антифолатов, производных талидомида, противоопухолевых химиотерапевтических агентов и других агентов. Таксаны включают доцетаксел, паклитаксел и наб-паклитаксел; цитотоксические антибиотики включают актиномицин, блеомицин и антрациклины, такие как доксорубицин, митоксантрон и валрубицин; ингибиторы тирозинкиназы включают эрлотиниб, гефитиниб, акситиниб, PLX3397, иматиниб, кобемитиниб и траметиниб; ингибиторы PARP включают пирапариб (piraparib); ингибиторы фермента B-Raf включают вемурафениб и дабрафениб; алкилирующие агенты включают дакарбазин, циклофосфамид и темозоломид; аналоги платины включают карбоплатин, цисплатин и оксалиплатин; аналоги нуклеозидов включают азацитидин, капецитабин, флударабин, фторурацил и гемцитабин; антифолаты включают метотрексат и пеметрексед. Другие химиотерапевтические агенты, подходящие для применения согласно настоящему изобретению, включают дефактиниб, энтиностат, эрибулин, иринотекан и винбластин.
Предпочтительные терапевтические агенты для введения совместно с молекулой антитела, описанной в настоящей заявке, представляют собой пентостатин, циклофосфамид, цисплатин, пеметрексед, паклитаксел, карбоплатин, гемцитабин, доксорубицин, винорелбин, доцетаксел или этопозид.
Радиотерапия для применения в комбинации с молекулой антитела, описанной в настоящей заявке, может представлять собой дистанционную радиотерапию (такую как радиотерапия с модулированной интенсивностью (IMRT), стереотаксическая радиотерапия тела (SBRT), радиотерапия под визуальным контролем (IGRT), интраоперационная радиотерапия (IORT), электронная терапия или электронно-лучевая терапия (EBT), поверхностная радиотерапия (SRT)) или внутреннюю радиотерапию (такую как брахитерапия, радиоизотопная или радионуклидная терапия, селективная внутренняя радиотерапия (SIRT)). Предпочтительно, радиотерапия представляет собой традиционную дистанционную радиотерапию, дистанционную радиационную терапию (EBRT), стереотаксическую радиотерапию или брахитерапию.
Иммунотерапевтический агент для введения в комбинации с молекулой антитела, описанной в настоящей заявке, может представлять собой терапевтическую молекулу антитела, нуклеиновую кислоту, цитокин или терапию на основе цитокинов. Например, терапевтическая молекула антитела может связываться с иммунорегуляторной молекулой, например, молекулой-ингибитором контрольных точек или иммуно-костимулирующей молекулой, рецептором врожденной иммунной системы или опухолевым антигеном, например, опухолевым антигеном клеточной поверхности или растворимым опухолевым антигеном. Примеры иммунорегуляторных молекул, с которыми может связываться терапевтическая молекула антитела, включают молекулы-ингибиторы контрольных точек, такие как CTLA-4, LAG-3, TIGIT, TIM-3, VISTA, PD-L1, PD-1 или KIR, иммуно-костимулирующие молекулы, такие как OX40, CD40, CD137, GITR, CD27 или ICOS, другие иммунорегуляторные молекулы, такие как CD47, CD73, CSF-1R, HVEM, TGFB или CSF-1. Примеры рецепторов врожденной иммунной системы, с которыми может связываться терапевтическая молекула антитела, включают TLR1, TLR2, TLR4, TLR5, TLR7, TLR9, RIG-I-подобные рецепторы (например, RIG-I и MDA-5) и STING.
Нуклеиновая кислота для введения в комбинации с молекулой антитела, описанной в настоящей заявке, может представлять собой малую интерферирующую РНК (ми-РНК).
Цитокины или терапия на основе цитокинов может быть выбрана из группы, состоящей из: IL-2, пролекарства конъюгированного IL-2, GM-CSF, IL-7, IL-12, IL-9, IL-15, IL-18, IL-21 и интерферона I типа.
Противоопухолевые вакцины для лечения рака как введены для клинического применения, так и подробно рассмотрены в научной литературе (например, Rosenberg, S. 2000). В основном включены стратегии, побуждающие иммунную систему отвечать на различные клеточные маркеры, экспрессируемые аутологичными или аллогенными раковыми клетками, путем применения этих клеток в качестве способа вакцинации, как совместно с гранулоцитарно-макрофагальным колониестимулирующим фактором (GM-CSF), так и без него. GM-CSF вызывает сильный ответ при представлении антигена и особенно хорошо действует при применении совместно с указанными стратегиями.
Химиотерапевтический агент, радиотерапия, иммунотерапевтический агент, противоопухолевая вакцина, онколитический вирус, ACT-терапия или агент для гормональной терапии предпочтительно представляют собой химиотерапевтический агент, радиотерапию, иммунотерапевтический агент, противоопухолевую вакцину, онколитический вирус, ACT-терапию или агент для гормональной терапии для рассматриваемого рака, т.е. химиотерапевтический агент, радиотерапию, иммунотерапевтический агент, противоопухолевую вакцину, онколитический вирус, ACT-терапию или агент для гормональной терапии, которые, как было показано, являются эффективными в лечении рассматриваемого рака. Специалист может выбрать подходящий химиотерапевтический агент, радиотерапию, иммунотерапевтический агент, противоопухолевую вакцину, онколитический вирус, ACT-терапию или агент для гормональной терапии, который, как было показано, эффективен в случае рассматриваемого рака.
Молекулы антител согласно настоящему изобретению могут подходить для детектирования MSLN, в частности, для детектирования иммобилизованного MSLN, такого как MSLN, связанный с клеточной поверхностью. Молекула антитела может быть конъюгирована с детектируемой меткой, как описано в иных местах настоящей заявки.
Таким образом, настоящее изобретение относится к применению молекулы антитела для детектирования присутствия иммобилизованного MSLN, предпочтительно присутствия клеток, содержащих MSLN на клеточной поверхности, в образце.
Также предложен способ детектирования MSLN in vitro, при этом указанный способ включает инкубацию молекулы антитела совместно с представляющим интерес образцом и детектирование связывания молекулы антитела с указанным образцом, где связывание антитела с образцом указывает на присутствие иммобилизованного MSLN. Связывание молекулы антитела с образцом можно детектировать, например, с использованием ELISA.
Предпочтительный вариант реализации настоящего изобретения относится к способу in vitro для детектирования клеток, содержащих MSLN на клеточной поверхности, при этом указанный способ включает инкубацию молекулы антитела совместно с представляющим интерес образцом клеток и определение связывания молекулы антитела с клетками, присутствующими в указанном образце, где связывание антитела с клетками, присутствующими в образце, указывает на присутствие клеток, содержащих MSLN на клеточной поверхности. Способы детектирования связывания молекулы антитела с клетками известны в этой области техники и включают ELISA-анализы и проточную цитометрию.
Молекулы антител согласно настоящему изобретению могут найти применение в детектировании, диагностике и/или прогнозировании рака. Указанный рак может представлять собой рак, который можно лечить молекулой антитела согласно настоящему изобретению, описанной в настоящей заявке.
Соответственно, согласно родственным аспектам настоящего изобретения предложены:
(i) молекула антитела, описанная в настоящей заявке, для применения в способе детектирования рака, диагностики рака, определения прогноза при раке или мониторинга прогноза при раке у индивидуума;
(ii) применение молекулы антитела, описанной в настоящей заявке, в изготовлении диагностического продукта для применения в детектировании рака, диагностике рака, определении прогноза при раке или мониторинге прогноза при раке;
(iii) способ детектирования рака, диагностики рака, определения прогноза при раке или мониторинга прогноза при раке у индивидуума с применением молекулы антитела, описанной в настоящей заявке; и
(iv) набор для применения в способе детектирования, диагностики, прогнозирования или мониторинга прогноза при раке у индивидуума, при этом указанный набор содержит молекулу антитела, описанную в настоящей заявке.
Способ может включать введение индивидууму молекулы антитела согласно настоящему изобретению и определение присутствия указанной молекулы антитела в области в организме индивидуума, где присутствие молекулы антитела в области в организме указывает на наличие опухоли, в частности на наличие опухоли, содержащей клетки, экспрессирующие MSLN на своей клеточной поверхности.
В предпочтительном варианте реализации способ включает определение присутствия клеток, экспрессирующих MSLN на своей клеточной поверхности, в образце, полученном от индивидуума, где присутствие клеток, экспрессирующих MSLN на своей клеточной поверхности, указывает на то, что указанного индивидуума есть рак.
В альтернативном предпочтительном варианте реализации способ включает определение присутствия клеток опухоли, экспрессирующих MSLN на своей клеточной поверхности, в образце опухоли, полученном от индивидуума, где присутствие клеток опухоли, экспрессирующих MSLN на своей клеточной поверхности, указывает на то, что указанный индивидуум имеет более неблагоприятный прогноз, такой как более высокий риск метастазирования рака, чем индивидуум с таким же раком, который не содержит клетки, экспрессирующие MSLN на своей клеточной поверхности.
Рак может представлять собой рак, указанный в настоящей заявке. Предпочтительно, рак выбран из группы, состоящей из: мезотелиомы, рака поджелудочной железы, рака яичников, рака легкого, рака пищевода, рака молочной железы, рака желудка, холангиокарциномы, рака толстой кишки, карциномы вилочковой железы, рака эндометрия, рака головы и шеи, двухфазных синовиальных сарком и десмопластических мелкокруглоклеточных опухолей. Более предпочтительно, рак выбран из группы, состоящей из: мезотелиомы, рака поджелудочной железы, рака яичников и рака легкого.
Другие аспекты и варианты реализации настоящего изобретения будут понятны специалисту в этой области техники в свете настоящего описания, включая следующие примеры экспериментов.
Полное содержание всех документов, упомянутых в настоящем описании, включено в настоящее описание посредством ссылки.
В настоящем описании «и/или» следует рассматривать как конкретное описание каждого из двух указанных признаков или компонентов вместе с другим или без него. Например, «А и/или В» следует рассматривать как конкретное описание каждого из: (i) A, (ii) B и (iii) A и B так, как если бы каждый был указан отдельно в настоящем описании.
Если в контексте не указано иное, описания и определения признаков, приведенные выше, не ограничиваются каким-либо конкретным аспектом или вариантом реализации настоящего изобретения и в равной степени применимы ко всем описанным аспектам и вариантам реализации.
Другие аспекты и варианты реализации настоящего изобретения предусматривают аспекты и варианты реализации, описанные выше, с заменой термина «содержащий (включающий)» на термин «состоящий из» или «по существу состоящий из», если в контексте не указано иное.
Некоторые аспекты и варианты реализации настоящего изобретения далее будут проиллюстрированы в качестве примера и со ссылкой на фигуры, описанные выше.
Примеры
Пример 1: выделение антител к MSLN человека: антигены, отбор и скрининг
Мезотелин представляет собой гликозилфосфатидилинозитол (GPI)-связанный гликопротеин, синтезируемый в виде предшественника массой 69 кДа и протеолитически процессируемый в NH2-концевую секретируемую форму массой 30 кДа (называемую мегакариоцит-потенцирующим фактором или MPF) и мембраносвязанный мезотелин (MSLN) массой 40 кДа. В сыворотке у пациентов детектируют растворимые формы MSLN, отделенные от поверхности клеток опухоли и образованные в результате альтернативного сплайсинга или под действием ферментов, превращающих фактор некроза опухоли-α (TACE), мембраносвязанного MSLN. Известно, что этот антиген, отделенный от опухоли, формирует «поглотитель», который может выступать в качестве ловушки для терапевтических антител (Lee et al, 2018), так что это необходимо преодолеть, чтобы позволить антителам связываться с MSLN на опухоли. Чтобы избежать этого эффекта поглощения авторы настоящего изобретения выделяли новые антитела к мезотелину, которые предпочтительно связывались с иммобилизованным MSLN относительно растворимого MSLN, с тем, чтобы это приводило к предпочтительному связыванию с мембраносвязанным MSLN, а не с растворимым MSLN. Для этого в отборе на основе фагового дисплея и последующем скрининге использовали различные формы антигенов MSLN.
1.1 Получение антигенов, представляющих собой мезотелин человека, яванского макака и мыши
Рекомбинантный биотинилированный антиген MSLN-His человека, обозначаемый «hMSLN-His Acro», в котором отсутствуют 18 С-концевых аминокислот, получали у Acrobiosystems (номер по каталогу MSN-H8223). Для максимального увеличения разнообразия связывающих агентов, выбранных по всему антигену, получали полноразмерный мономерный антиген MSLN человека и биотинилировали самостоятельно для отбора на основе фагового дисплея. Получали MSLN яванского макака и мыши, позволяющие выделять связывающие агенты, способные связываться с MSLN человека, а также яванского макака, а также выделять агенты, связывающие MSLN мыши, соответственно.
Вкратце, антигены MSLN получали путем клонирования ДНК, кодирующей MSLN человека (SEQ ID NO: 169) (hMSLN-His-Avi), яванского макака (SEQ ID NO: 170) (cMSLN-His-Avi) или мыши (SEQ ID NO: 171) (mMSLN-His-Avi) наряду с шестью С-концевыми остатками гистидина и последовательностью Avi, в модифицированные векторы pFUSE (Invivogen, номер по каталогу pfuse-mg2afc2) с использованием рестрикционных ферментов EcoRI-HF и BamHI-HF. Указанные векторы трансфицировали в клетки HEK293-6E (Национальный исследовательский совет Канады), и экспрессированный MSLN очищали с использованием колонки с никелем HisTrap™ excel (GE LifeSciences, 29048586). Каждый из указанных антигенов биотинилировали с использованием набора BirA biotin-biotin protein ligase reaction kit (Avidity LLC, BirA500) с получением мономерных антигенов MSLN, меченых одной молекулой биотина. В частности, от пяти до десяти мг антигена смешивали со смесью фермента BirA до молярного соотношения фермента и субстрата, составляющего 1:50. Затем добавляли дополнительные компоненты в соответствии с рекомендациями производителя, инкубировали в течение ночи при комнатной температуре, а затем рекомбинантный MSLN человека, яванского макака или мыши очищали с использованием колонки с никелем HisTrap™ excel (GE LifeSciences, 29048586) с удалением избытка свободного биотина.
Определяли биофизические свойства каждого антигена посредством анализа SEC-ВЭЖХ с определением того, присутствовали ли агрегаты, и посредством электрофореза в полиакриламидном геле (ПААГ) с подтверждением размера молекул. SEC-ВЭЖХ этих антигенов показала агрегацию менее 10%, и ПААГ подтвердил, что указанные антигены были мономерными. ELISA и поверхностный плазмонный резонанс (SPR) использовали для подтверждения того, что биотинилированные антигены MSLN могли связываться MSLN-специфичными антителами положительного контроля (SS1, см. раздел 1.3; Hassan et al 2002 и MOR6626, см. раздел 7.1, публикация патента № WO 2009/068204 A1). На основании этих данных все антигены считали подходящими для наивного отбора.
1.2 Отбор из фагмидных библиотек
Синтетические наивные фагмидные библиотеки, отображающие Fab-домен человека зародышевой линии с рандомизированными аминокислотами в CDR1, CDR2 и CDR3 (MSM Technologies), использовали для отбора с помощью антигенов MSLN, описанных в разделе 1.1.
Вначале отбирали библиотеки Fab в несколько подходов, каждый из трех или четырех циклов, с использованием частиц со стрептавидином (Streptavidin Dynabeads) (Thermo Fisher, 11205D), нейтравидина (Neutravidin) -связывающего белка, связанного с частицами Dynabeads (Thermo Fisher, 31000) или анти-His частиц Dynabeads (Thermo Fisher, 10103D) для выделения фага, связанного с биотинилированным MSLN-His-Avi человека, яванского макака или мыши, или hMSLN-His Acro. Подходы по отбору также осуществляли с использованием полноразмерных антигенов MSLN, полученных самостоятельно, в которых циклы отбора MSLN человека чередовали с антигеном MSLN яванского макака с целью выделения перекрестно реагирующих клонов человека и яванского макака. Также проводили отбор агентов, связывающих MSLN мыши (mMSLN-His 8604-MS R&D). Применяли стандартные методики отбора на основе фагового дисплея и методики выделения фага.
Для получения клонов, которые связываются с различными областями антигена MSLN, выбирали стратегию маскирования эпитопа с использованием антител к MSLN из подходов по первоначальному отбору, описанных выше. Вкратце, первый цикл отбора наивных библиотек Fab осуществляли с использованием биотинилированного MSLN-His-Avi человека в концентрации 500 нМ. Во 2 и 3 цикле фаговое связывание биотинилированного MSLN-His-Avi яванского макака в концентрации 500 нМ (2 цикл) или 100 нМ (3 цикл) тестировали в присутствии смеси наивных белков mAb к мезотелину, выделенных при первоначальном подходе по отбору (FS28-004, FS28-024, FS28-026, FS28-091 и FS28-97, 500 нM каждого mAb). Такой отбор на основе маскирования эпитопа приводил к снижению выходных титров, что указывает на то, что указанная стратегия отбора была действенной, поскольку идентифицировали меньшее количество связывающих агентов. Это позволило идентифицировать клоны (FS28-243, FS28-255 и FS28-256, см. раздел 2.1.3), нацеленные на дополнительные области MSLN, по сравнению с клонами из предыдущего подхода по отбору.
1.3 Скрининг для идентификации антител к MSLN
Примерно 2000 клонов, полученных в результате 3-го и 4-го циклов всего отбора, подвергали скринингу путем фагового ELISA на предмет связывания с 25 нМ иммобилизованным биотинилированным hMSLN-His Acro, полноразмерным биотинилированным MSLN-His-Avi человека или яванского макака, соответствующим антигену, используемому в цикле отбора. Планшеты со стрептавидином или планшеты c иммобилизованными несоответствующими биотинилированными His-мечеными антигенами включали в качестве отрицательных контролей. Отбирали клоны, демонстрировавшие сигнал связывания MSLN по меньшей мере в 4 раза более сильный, чем сигнал в случае отрицательных контролей, и секвенировали их вариабельные области, в результате чего идентифицировали 156 уникальных комбинаций последовательностей VH/VL, которые затем отбирали для экспрессии растворимой формы. Клоны отбирали в результате всех подходов по отбору, включая отбор на основе маскирования эпитопа. Для каждого клона VH и VL отдельно клонировали в вектор экспрессии pTT5 (Национальный исследовательский совет Канады), содержащий либо CH1-, CH2- (с мутацией LALA в CH2-домене (Bruhns et al., 2009; Hezareh et al., 2001) и CH3-домен, либо CL-домены соответственно. Полученные векторы pTT5-FS28 VH с мутацией LALA (AA) и pTT5-FS28 VL временно котрансфицировали в клетки HEK293-6E, и получали клоны в виде полных молекул IgG1. Антитела либо хранили в надосадочной жидкости, либо очищали на колонках mAb SelectSure с белком А и подвергали дальнейшему тестированию, как описано ниже. С применением этого же способа клонировали VH- и VL-области SS1 и антитела HelD1.3 к лизоциму белка куриного яйца и экспрессировали в LALA-формате IgG1 с получением G1-AA/SS1 (SEQ ID No 167 и 168) и G1-AA/HelD1.3 (SEQ ID No 165 и 166), служащих в качестве положительного и отрицательного контроля соответственно.
Пример 2: идентификация панели наивных mAb к MSLN
mAb к мезотелину имеют широкий спектр потенциального применения, включая их применение в качестве лекарственных средств, способных индуцировать АЗКЦ, в качестве средства для нацеливания на опухоль для доставки иммунотоксина, ADC и для получения биспецифичных антител, среди прочего. Желаемые характеристики mAb к мезотелину зависят от применения, и поэтому авторы настоящего изобретения решили идентифицировать панель mAb, которые связывались с мембраносвязанным MSLN человека и яванского макака с различной аффинностью, и которые могли быть нацелены на различные области MSLN. Для этого проводили ряд скрининговых анализов, включая ELISA, блокирующие анализы Biacore и связывание клеток, а также анализы, в которых сравнивали области связывания с MSLN.
2.1 Скрининг на предмет связывания с рекомбинантным MSLN
2.1.1 ELISA связывания
Надосадочные жидкости HEK293-6E, содержащие растворимые связывающие клоны к MSLN, или очищенные клоны, подвергали скринингу на предмет связывания с MSLN-His Acro человека, hMSLN-His-Avi и, в случае некоторых подходов, cMSLN-His-Avi путем ELISA. Вкратце, hMSLN-His Acro, hMSLN-His-Avi, cMSLN-His-Avi или несоответствующий His-меченый антиген наносили на планшеты maxisorp в концентрации 25 нМ на ночь при 4°C. На следующий день планшеты блокировали 300 мкл ФБР, содержащего 0,05% Твин20 и 2% молоко Marvel (сухое молоко Marvel). Надосадочные жидкости, содержащие mAb к MSLN, или очищенные белки инкубировали в течение 1 часа при комнатной температуре, и их связывание детектировали с помощью антитела к Fc-IgG человека, конъюгированного с пероксидазой хрена (HRP). Отбрасывали клоны, которые демонстрировали связывание с несоответствующим антигеном или не реагировали перекрестно с антигенами как человека, так и яванского макака. Кроме того, клоны, которые связывались с усеченным антигеном MSLN, hMSLN-His Acro, но не с полноразмерным антигеном MSLN, MSLN-His-Avi, также не использовали в дальнейшем, поскольку ожидали, что полноразмерный антиген будет больше соответствовать конформации антигена на клеточной поверхности клеток, экспрессирующих MSLN.
Мезотелин представляет собой гликопротеин, и его профиль гликозилирования может варьироваться в зависимости от вида и ткани. Чтобы убедиться в том, что антитела обладали специфичностью в отношении связывания с MSLN, связывающие клоны к MSLN также тестировали на предмет дифференциального связывания с гликозилированным и дегликозилированным MSLN. Биотинилированный hMSLN-His-Avi дегликозилировали с использованием фермента PNGase F (NEB, P0704L) в течение 24 часов при 37°C, очищали с использованием ультрацентрифужных фильтров Amicon (Millipore, UFC901024) и наносили на планшеты maxisorp в концентрации 25 нМ. ELISA-связывание уникальных mAb к мезотелину с MSLN детектировали с использованием антитела мыши к Fc-IgG-HRP (Sigma, A0170). Клоны, демонстрировавшие более чем 2-кратное ослабление сигнала связывания с дегликозилированным антигеном по сравнению с гликозилированным антигеном MSLN, исключали из панели наивных связывающих mAb к MSLN.
2.1.2 Скрининг BIAcore
MSLN-His-Avi человека иммобилизовали на проточной ячейке 2 на сенсорном чипе BIAcore CM5 серии S (GE Healthcare, BR100530) с использованием набора для иммобилизации по аминогруппе (GE Healthcare, BR10050) до приблизительно 200 единиц ответа (RU). Проточную ячейку 1 оставляли пустой для вычитания. Надосадочные жидкости HEK293-6E или очищенные белки доводили с помощью HBS-EP+ (GE Healthcare) до приблизительно 50 нМ mAb к MSLN на образец. Образцы вводили в проточную ячейку 1 и 2 в течение 2,5 минут со скоростью 30 мкл/мин, а затем оставляли диссоциировать в буфере HBS-EP в течение 2,5 минут. Регенерацию осуществляли путем введения 10 мМ глицина, pH 1,5 (GE Healthcare, BR100354) в течение 30 секунд со скоростью 30 мкл/мин. Данные, полученные после вычитания (проточная ячейка 2 - проточная ячейка 1), анализировали с применением программного обеспечения BIAevaluation 3.2 (GE Healthcare). Из 86 клонов, тестируемых в этом анализе из ELISA связывания, 39 клонов демонстрировали ответ связывания более 10 RU в случае 50 нМ и, соответственно, их отбирали для повторной экспрессии, очистки и дальнейшего скрининга.
2.1.3 Сортировка антител на основе области связываемого MSLN
Затем на основании данных ELISA и скрининга Biacore клоны тестировали в анализах с сортировкой, в которых связывание mAb с MSLN человека тестировали в присутствии другого mAb посредством биослойной интерферометрии (BLI) на Octet (ForteBio).
Вкратце, биотинилированный hMSLN-His-Avi (5 мкг/мл) связывали с покрытыми стрептавидином наконечниками (ForteBIO, 18-5020) в течение 5 минут. G1-AA/SS1 разводили до 200 нМ в 1x кинетическом буфере (FortéBIO, 18-1092) и оставляли связываться с hMSLN-His-Avi в течение 5 минут. Затем оценивали связывание смеси, содержащей 200 нМ тестируемого mAb и 200 нМ G1-AA/SS1, в течение 5 минут. Сравнивали со связыванием тестируемого mAb с hMSLN-His-Avi в отсутствии связанного G1-AA/SS1 с определением максимальной степени возможного связывания в отсутствии SS1 (т.е. когда не было конкуренции за связывание). Если бы оба антитела конкурировали за связывание с одной и той же областью MSLN, тестируемое антитело было бы неспособно связываться.
Эти эксперименты с сортировкой с использованием G1-AA/SS1 показали, что большинство (19 из 23) тестируемых антител линии FS28 были неспособны связывать MSLN в присутствии G1-AA/SS1 и, следовательно, им может быть приписано свойство связывать ту же область, что и G1-AA/SS1. Существуют данные о связыващем сайте для MSLN для антитела SS1 в формате Fab (Ma et al., 2012), и он определен как N-концевая область, содержащая аминокислоты с 7 по 64, которые также вовлечены в связывание MUC16. Тот факт, что большинство выделенных связывающих агентов к MSLN связывались с этой или подобной областью, позволяет предположить, что эти аминокислоты хорошо экспонированы в рекомбинантных антигенах. Идентифицировали четыре других клона FS28-185, FS28-243, FS28-255 и FS28-256, которые демонстрировали частичную конкуренцию или отсутствие конкуренции с G1-AA/SS1 за связывание с MSLN. Связывание этих клонов относительно друг друга показало, что эти клоны представляли собой две дополнительные независимые группы, т.е. были способны связываться еще с двумя другими областями MSLN. FS28-185, FS28-243 и FS28-255 относили к одной группе («группа 2»), тогда как FS28-256 относили к другой группе («группа 3»). Эти результаты показали, что отбор на основе маскирования эпитопа в разделе 1.2 был успешным, поскольку идентифицировали антитела, которые связывались с несколькими областями MSLN.
2.1.4 Аффинность
Для каждой группы, описанной в разделе 2.1.3, кинетику связывания определяли с применением того же способа, который описан в разделе 2.1.2, за исключением того, что MSLN-His-Avi человека или яванского макака иммобилизовали при 50 или 100 RU. Клоны тестировали в диапазоне концентраций от 81 нМ до 0,33 нМ в 3-кратных разведениях. Связывающие агенты ранжировали и выбирали лучшие из каждой группы: FS28-024, FS28-026 и FS28-091 - все из группы 1; FS28-185 из группы 2 и FS28-256 из группы 3. Было показано, что все эти клоны обладали перекрестной реактивностью с яванским макаком, но значения аффинности не рассчитывали в этих условиях тестирования. Значения аффинности отобранных антител приведены в Таблице 1, в которой показано, что значения аффинности, полученные при 50 RU иммобилизованного MSLN, были ниже значений при 100 RU иммобилизованного антигена MSLN, что демонстрирует усиление связывания при более высоких уровнях MSLN.
Таблица 1: аффинность наивных mAb к мезотелину в отношении иммобилизованного мезотелина человека
2.2 Анализы блокирования MUC16-MSLN
Существуют данные о том, что N-концевая область MSLN (аминокислоты 296-359) взаимодействует с гликопротеином MUC16, и это взаимодействие может играть роль в адгезии раковых клеток (Kaneko et al., 2009). Тестировали FS28-024, FS28-026, FS28-091, FS28-185 и FS28-256 на предмет их способности блокировать связывание MUC16 с мезотелином в анализе блокирования. Из литературы известно, что SS1 блокирует связывание MUC16 с MSLN (Ma et al., 2012). Как описано выше, авторы настоящего изобретения преобразовали его в формат G1-AA/SS1, ожидая, что это не будет влиять на его способность блокировать связывание MUC16. G1-AA/SS1 и контрольное антитело IgG1 (G1-AA/HelD1.3) включали в качестве положительного и отрицательного контроля соответственно.
Вкратце, рекомбинантный MUC16 человека (R&D Systems, 5809-MU-050) наносили на планшеты maxisorp в количестве 0,65 мкг/мл в 1x ФБР на ночь при 4°C. Планшеты 3 раза промывали 1xФБР и блокировали 300 мкл ФБР, содержащего 2% Твин20 и 2% молоко Marvel. mAb к MSLN в концентрации (от 0,23 нМ до 500 нМ, 3-кратные разведения) предварительно смешивали с биотинилированным антигеном hMSLN-His-Avi (конечная концентрация 2 мкг/мл) в объеме 100 мкл в течение 1 часа при комнатной температуре. После удаления блокирующего раствора в планшеты добавляли смесь mAb/MSLN и инкубировали в течение 1 часа при комнатной температуре. Планшеты 3 раза промывали ФБР-Т (1x ФБР и 0,05% Твин20) и инкубировали совместно со стрептавидин-HRP (Thermo Scientific, 21126, разведение 1:1000 в 1xФБР) в течение 1 часа при комнатной температуре. Наконец, планшеты промывали 3 раза ФБР-Т и 3 раза ФБР. MSLN, связанный с MUC16, визуализировали путем добавления 100 мкл TMB в течение 15 минут, а затем 100 мкл 1M раствора серной кислоты. Поглощение определяли при длине волны 450-630 нм (программное обеспечение Gen5, BioTek).
Таблица 2: активность наивных mAb к мезотелину в анализе блокирования MUC16-MSLN
IC50 (нM)
Клоны FS28-024, FS28-026 и FS28-091 из группы 1 демонстрировали дозозависимое блокирование взаимодействия MUC16-MSLN с IC50, составляющей 2,9 нМ, 5,2 нМ и 4,4 нМ соответственно (Таблица 2). Наблюдаемая блокирующая активность была схожа с блокирующей активностью G1-AA/SS1. FS28-256 не демонстрировал никакой блокирующей активности подобно G1-AA/HelD1.3 отрицательного контроля. Тогда как FS28-185 способствовал связыванию MUC16 с MSLN. Существуют данные об этом явлении (патент США 8911732 B2). Эти результаты согласовывались с данными сортировки в разделе 2.1.3 в том, что клоны, которые связывались с тремя разными областями MSLN, демонстрировали три разных типа поведения в анализе блокирования лиганда.
В заключение, результаты показывают, что отбирали панель клонов, которые связываются с 3 разными областями (группы) MSLN; связывание антител с одной из областей MSLN блокирует связывание MUC16 с MSLN, тогда как связывание антител с двумя другими областями - нет.
2.3 Специфичность
Ввиду присутствия разных областей MSLN, связываемых панелью антител, тестировали их специфичность в отношении связывания с MSLN. Специфичность FS28-024, FS28-026, FS28-091, FS28-185 и FS28-256 тестировали посредством ELISA путем сравнения связывания с MSLN со связыванием с другими молекулами, вовлеченными в клеточную адгезию, такими как CEACAM-5, E-кадгерин, тромбомодулин и EpCAM.
Использовали протокол, аналогичный описанному в разделе 1.2.1, в котором на планшеты maxisorp наносили 1 мкг/мл рекомбинантного MSLN-His-Avi человека, CEACAM-5-His-Fc человека (Sino Biological, 1077-H03H), E-кадгерина человека (R&D systems, 8505-EC), тромбомодулина человека (Peprotech, 100-58) или EpCAM-hFc человека (самостоятельного получения). Связывание mAb к MSLN, тестируемое в диапазоне концентраций от 0,02 до 1000 нМ (3-кратные разведения), детектировали с использованием антитела к Fab-HRP человека (Sigma, A0293). Положительные контроли для соответствующих молекул включали антитело к EpCAM человека (клон 2G8 из патента № US8236308 B2), антитело к CEACAM-5 (клон hMN15 из патента № US8771690 B2), антитело к Е-кадгерину человека, клон 180215 IgG2b мыши (R&D systems, MAB1838), антитело к тромбомодулину человека, IgG1 мыши, клон 501733 (R&D systems, MAB3947). Последние два детектировали с использованием антитела козы к Fc-HRP мыши (Sigma, A9309) в качестве вторичного mAb.
FS28-024, FS28-026, FS28-091 и FS28-185 связывались с MSLN-His-Avi человека (EC50 примерно 0,5 нМ и максимальный сигнал связывания 3), но не наблюдали связывания ни с одной из указанных молекул клеточной адгезии, тестируемого в концентрации до 1000 нМ. Как и ожидали, антитела положительного контроля связывались с соответствующими мишенями. Таким образом, антитела к MSLN демонстрировали высокий уровень специфичности.
2.4 Связывание с клеткой
Панель из пяти отобранных mAb к мезотелину анализировали на предмет связывания с эндогенным MSLN клеточной поверхности с использованием линии клеток рака легкого человека NCI-H226.
Вкратце, клетки NCI-H226 (ATCC CRL-5826) брали из колб для культивирования клеток Т175 с использованием Аккутазы (Accutase) StemPro (Gibco, A11105-01). Клетки центрифугировали при 1200 об/мин в течение 3 минут и ресуспендировали в ледяном буфере FACS, состоящем из фосфатного буферного раствора Дульбекко (Д-ФБР) (Life Technologies, 14190169) и 1% BSA (Sigma-Aldrich, A7906), в количестве 2х106 клеток/мл, и высевали по 50 мкл на лунку в 96-луночный планшет с V-образным дном (Costar, 3894). Все тестируемые mAb разводили в буфере FACS в 120 мкл в диапазоне концентраций 0,01-200 нМ (4-кратные разведения). Затем клетки NCI-H226 центрифугировали, удаляли надосадочную жидкость и клетки ресуспендировали в 100 мкл каждого разведения mAb, и инкубировали при 4°C в течение 45 минут. Клетки дважды промывали 150 мкл буфера FACS путем центрифугирования, ресуспендировали в 100 мкл, содержащих фрагмент F(ab′)2-R-фикоэритрин антитела козы к IgG (специфичного к γ-цепи) человека (Sigma, P8047), разведенный 1:1000 в буфере FACS, и инкубировали при 4°C в течение 45 минут. Клетки один раз промывали 150 мкл буфера FACS, а затем 150 мкл Д-ФБР, ресуспендировали в 150 мкл Д-ФБР, содержащего DAPI (Biotium, 40043) в соотношении 1:10000, и прочитывали на BDCantoII или iQue (Intellicyt). Данные анализировали с применением FlowJo v10 для определения среднего геометрического сигнала для PE для живых клеток в каждой лунке.
Данные связывания с клеткой (Таблица 3) показали, что все: FS28-024, FS28-026 и FS28-091 связывались с MSLN клеточной поверхности на NCI-H226 с EC50 в диапазоне от 0,62 до 1,22 нМ, как и G1-AA/SS1 положительного контроля. Для сравнения, FS28-185 и FS28-256 демонстрировали слабое связывание с EC50 более 30 нМ и низкий максимальный сигнал связывания (Emax). Типичный анализ связывания представлен на Фиг.1.
Таблица 3: связывание наивных mAb к мезотелину с раковыми клетками NCI-H226
2.5 Обобщенные результаты по методике наивного скрининга
Из 156 mAb, идентифицированных посредством первичного скрининга наивных фаговых библиотек, отбирали пять клонов mAb к MSLN человека (FS28-024, FS28-026, FS28-091, FS28-185 и FS28-256) на основе ряда скрининговых анализов, которые сначала подтвердили связывание с полноразмерным дегликозилированным рекомбинантным MSLN, а также способность связываться с MSLN яванского макака. Во-вторых, клоны группировали на основе различия области MSLN, которую они связывали (группы), и блокирующей активности в отношении MUC16, и из этих групп отбирали связывающие агенты с самой высокой аффинностью. Полученная панель клонов mAb: FS28-024, FS28-026, FS28-091, FS28-185 и FS28-256 связывала три разных области MSLN, один из указанных клонов (группа 1, включая FS28-024, FS28-026 и FS28-091) блокировал связывание MUC16 с MSLN in vitro. Панель из пяти mAb к MSLN демонстрировала специфичное связывание с MSLN, различную аффинность к рекомбинантному MSLN и MSLN клеточной поверхности, и ее отбирали для дальнейшего определения характеристик и/или оптимизации, как описано в Примерах 3 и 4 ниже.
Пример 3: созревание аффинности и оптимизация последовательностей наивных mAb к MSLN
3.1 Созревание аффинности для FS28-185 и FS28-256
По сравнению с FS28-024, FS28-026 и FS28-091, FS28-185 и FS28-256 демонстрировали более низкую аффинность как к рекомбинантному MSLN, так и к MSLN клеточной поверхности, и поэтому их подвергали созреванию аффинности.
3.1.1 Созревание аффинности и скрининг для FS28-185 и FS28-256
CDR3-области VH и VL подвергали созреванию аффинности параллельно в формате scFv путем рандомизации перекрывающихся кассет для пяти-шести аминокислот с использованием праймеров NNK. Области, рандомизированные для FS28-185, представляли собой G95-M100F VH и S91-A95 VL, и для FS28-256 они представляли собой Y95-L100B VH и S91-I96 VL (нумерация согласно Кабату). Перед созданием библиотеки осуществляли экономный мутагенез в потенциальных сайтах окисления метионина и деамидирования в CDR1- и CDR3-областях (за исключением библиотеки CDR3 VL FS28-256). Независимо создавали фагмидные библиотеки и их объединяли с получением одной библиотеки CDR3 VH и одной библиотеки CDR3 VL для каждого клона. Проводили два цикла отбора, как описано для подходов по наивному отбору, с использованием 20 нМ биотинилированного MSLN-His-Avi человека в 1 цикле и либо 20, либо 2 нМ MSLN-His-Avi яванского макака во 2 цикле. Затем тестировали растворимые scFv (одноточечная концентрация) на предмет связывания с линией клеток рака яичников OVCAR-3 (ATCC® HTB-161™). Клетки OVCAR-3 собирали с использованием Аккутазы StemPro (Gibco, A11105-01), центрифугировали при 1200 об/мин в течение 3 минут и ресуспендировали в буфере FACS (Д-ФБР, содержащий 2% BSA) в количестве 2х106 клеток/мл. 100 мкл клеток OVCAR-3 добавляли в 96-луночные планшеты с V-образным дном. Планшеты центрифугировали при 1200 об/мин в течение 3 минут и отбрасывали буфер. К клеткам добавляли 150 мкл scFv и инкубировали при 4°C в течение одного часа. В качестве контролей включали scFv исходных клонов FS28-185 и 256. После промывки клетки ресуспендировали в 100 мкл Penta His Alexa-Fluor 647 (Qiagen, 109-546-098) и промывали перед ресуспендированием в 100 мкл Д-ФБР, содержащего краситель Sytox Green Nucleic Acid Stain (Invitrogen S7020, разведение 1:10000). Образцы анализировали на iQue (Intellicyt Corporation, IQue Plus) и фиксировали среднее геометрическое для APC.
Как для FS28-185, так и для FS28-256 идентифицировали клоны с созревшей аффинностью, демонстрирующие улучшенное связывание с клетками OVCAR-3. На основе связывания клеток (MFI больше 850) и разнообразия последовательностей отбирали 10 клонов из наборов CDR3 VH FS28-256 и 9 из CDR3 VL. Из 38 клонов FS28-185 с созревшей аффинностью, тестируемых в этом анализе, 14 выбирали из наборов CDR3 VH и один из наборов CDR3 VL. Затем определяли характеристики отобранных клонов в формате биспецифичного антитела mAb2.
3.1.2 Получение mAb2 на основе FS28-185 и FS28-256
Для дальнейшего определения характеристик связывающих агентов к MSLN получали VH- или VL-область FS28-185 или FS28-256 с созревшей аффинностью, а также исходные клоны в формате mAb2. Полученные mAb2 представляли собой антитела IgG1, состоящие из CDR-областей либо клонов FS28-185 или FS28-256, либо полученных из них вариантов с созревшей аффинностью, мутации LALA в CH2-домене и связывающего сайта рецептора CD137 человека в CH3-домене. Эти молекулы mAb2 обозначали FS22-053-008-AA/FS28-185 (SEQ ID NO: 154 и 195) и FS22-053-008-AA/FS28-256 (SEQ ID NO: 156 и 77), и FS22-053-008-AA/FS28-256-x для потомства с созревшей аффинностью. Указанные mAb2 получали путем временной экспрессии в клетках HEK293-6E и, где указано, очищали с использованием колонок mAb SelectSuRe с белком А.
3.1.3 Скрининг аффинности для клонов FS28-185 и FS28-256 с созревшей аффинностью в отношении иммобилизованного MSLN
Затем связывание mAb2, содержащих области CDR-области с созревшей аффинностью, подвергали скринингу на предмет связывания с иммобилизованным MSLN-His-Avi человека и яванского макака посредством Biacore. Надосадочные жидкости HEK293-6E, содержащие клоны FS22-053-008-AA/FS28-185 и FS22-053-008-AA/FS28-256 с созревшей аффинностью, анализировали на предмет связывания с иммобилизованным MSLN при 200 RU, как описано в разделе 2.1.2. Тестировали две концентрации mAb2, т.е. 50 и 100 нМ, и связывание сравнивали со связыванием исходного антитела также в формате mAb2. Связывающие агенты ранжировали и шесть лучших связывающих агентов из каждой линии с перекрестной реактивностью с яванским макаком повторно экспрессировали, очищали и тестировали в анализах связывания клеток, как описано в разделе 3.1.4 ниже. Затем для линии FS28-256 клоны с улучшенной CDR3 VH перемешивали с клонами с улучшенными CDR3 VL с получением дополнительных девяти пар VH/VL, которые получали в виде mAb2 и также тестировали.
3.1.4 Связывание клеток в присутствии растворимого MSLN
Как описано выше в разделе 1, растворимый MSLN может действовать как ловушка для связывания любого антитела к MSLN. Поэтому клоны с созревшей аффинностью подвергали скринингу на предмет связывания с рекомбинантным MSLN и MSLN клеточной поверхности в присутствии и в отсутствии растворимого MSLN человека. Поскольку в растворимом отделенном MSLN отсутствуют либо 7, либо 13 C-концевых остатков (Zhang et al., 2011), в качестве миметика использовали коммерчески доступный антиген MSLN человека, MSLN-His Acro, в котором отсутствуют 18 C-концевых аминокислот. Этот антиген использовали в концентрации 20 нМ, которая примерно в 10-20 раз превышает уровень растворимого MSLN, который, как было установлено, имеет диагностическое значение для определения пациентов со злокачественной мезотелиомой и раком легкого как MSLN-положительных (Cui et al., 2014).
Анализы связывания клеток с использованием клеток OVCAR-3 выполняли аналогично анализам, описанным в разделе 2.4. Влияние присутствия растворимого MSLN тестировали путем предварительной инкубации антител в присутствии или в отсутствии растворимого MSLN перед смешиванием с клетками и определения того, влияла ли указанная предварительная инкубация на связывание с MSLN на клеточной поверхности. Клоны с созревшей аффинностью и исходные молекулы (все в формате mAb2, как описано выше) разводили в буфере FACS с получением 2x конечной концентрации в 96-луночном планшете с V-образным дном. Затем 60 мкл из каждой лунки добавляли либо в один буфер FACS, либо в буфер FACS, содержащий 60 мкл 40 нМ рекомбинантного hMSLN (R&D systems, 3265-MS-050) (с получением конечной концентрации, составляющей 20 нМ hMSLN), и предварительно инкубировали при комнатной температуре в течение 1 часа перед добавлением 100 мкл к клеткам. Связанное антитело детектировали с использованием антител козы к Fcγ человека, конъюгированных с Alexa-Fluor 488 (Jackson Immunoresearch, 109-546-098).
Для линии FS28-185 все клоны с созревшей аффинностью демонстрировали увеличение связывания с клетками OVCAR-3 (примерно в 7 раз по EC50) по сравнению со связыванием исходного клона. Однако это связывание уменьшалось в присутствии 20 нМ растворимого MSLN и приводило к повышению EC50 в 3-7 раз (с 1,6-1,8 нМ до приблизительно 5-7,8 нМ). Что касается линии FS28-256, отбирали пять клонов в качестве представителей этой линии, все из которых демонстрировали диапазон EC50, варьирующийся от 0,9 до 8,6 нМ. Наибольшее значение имеет то, что аффинность связывания сохранялась и наблюдали менее чем 2-кратное изменение связывания в присутствии 20 нМ растворимого MSLN по сравнению с тем, когда он отсутствовал. На основании этих данных клоны, отобранные для дальнейшего тестирования, включали FS28-256-012, FS28-256-021, FS28-256-023 и FS28-256-024.
3.2 Созревание аффинности для клона FS28-024 с применением стратегии NNK-мутагенеза (NNK walk strategy)
Тогда как FS28-024 связывался с MSLN человека с субнаномолярной аффинностью, его аффинность к MSLN яванского макака была примерно в 5 раз ниже (см. Пример 4, Таблицу 4). Для улучшения связывания с MSLN яванского макака применяли стратегию NNK-мутагенеза по пяти остаткам в CDR3-области VH.
Оптимизировали последовательность VH и VL FS28-024 в том же формате mAb2, который описан в разделе 3.1.2. Получали библиотеки на основе экономного мутагенеза путем изменения одного аминокислотного остатка за один раз из остатков RATLF (нумерация согласно Кабату: 95-99) в CDR3 VH, что приводило к получению всего пяти отдельных библиотек. Библиотеки получали с использованием кодонов NNK с низкой избыточностью, чтобы представить все возможные аминокислоты в положении, представляющем интерес. Разрабатывали прямые и обратные праймеры в соответствии с руководством из набора Quickchange Lightning Site-Directed Mutagenesis Kit (Agilent, 200518), который использовали для создания библиотек. Каждый мутант экспрессировали в малом масштабе в клетках HEK293-6E, и надосадочные жидкости подвергали скринингу посредством BIAcore на предмет сохранения или улучшения связывания с MSLN-His-Avi человека и яванского макака. Из 84 клонов, подвергнутых скринингу, малое число клонов сохранили связывание, большинство из них были с заменой остатка Т98. Четыре клона, FS28-024-51, FS28-024-52, FS28-024-53 и FS28-024-060, повторно экспрессировали, очищали и определяли их аффинность к MSLN человека и яванского макака. Только один клон, FS28-024-53, демонстрировал улучшение перекрестной реактивности с яванским макаком, которое обеспечивали одной мутацией T98V (нумерация согласно Кабату, см. Таблицу 4, Пример 4). Все четыре клона использовали в дальнейшем, поскольку они могли обеспечивать альтернативные последовательности и характеристики в зависимости от применения.
3.3 Обобщенные результаты по созреванию аффинности
В целом, стратегии созревания аффинности и оптимизации последовательностей для линий FS28-024, FS28-185 и FS28-256 были эффективными на основе дальнейшего расширения панели и увеличения разнообразия mAb к MSLN.
Пример 4: определение характеристик клонов к MSLN
4.1 Аффинность
Связывание отобранных клонов к MSLN в формате mAb2 с рекомбинантным антигеном MSLN-His-Avi человека и яванского макака измеряли посредством поверхностного плазмонного резонанса (SPR) с использованием устройства для обработки Biacore T200 (GE Healthcare). Как описано выше, было желательным более сильное связывание с иммобилизованным антигеном, чем с растворимым антигеном. Для оценки свойств связывания для клонов кинетику связывания с иммобилизованным антигеном MSLN определяли, как описано в разделе 2.1.2, и сравнивали с кинетикой, полученной, когда антигены MSLN в растворе связывались с захваченными клонами.
Для экспериментов с захватом осуществляли захват клонов в формате mAb2 с использованием сенсорного чипа BIAcore серии S с белком G (GE Healthcare, 29179315). mAb2, разведенные в буфере HBS-EP (GE Healthcare, BR100188), содержащем 900 мМ NaCl2 в количестве 1 мкг/мл, отдельно вводили в проточную ячейку 2, 3 и 4 со скоростью 30 мкл/мин с достижением ответа приблизительно 100 RU. Захват G1-AA/HelD1.3 осуществляли в проточную ячейку 1. Рекомбинантный mMSLN-His-Avi человека и яванского макака (раздел 1.1), разведенный в буфере HBS-EP, содержащем 900 мМ NaCl2, вводили в проточную ячейку 1, 2, 3 или 4 при необходимости, в диапазоне концентраций от 1000 нМ до 0,051 нМ с 3-кратными разведениями в течение 5 минут со скоростью 70 мкл/мин, а затем оставляли диссоциировать в буфере в течение 5 минут. Регенерацию осуществляли путем введения 10 мМ глицина, pH 1,5 (GE Healthcare, BR100354), и поверхностно-активного вещества P20 (GE Healthcare, BR-1000-54) в течение 20 секунд со скоростью 30 мкл/мин. Данные, полученные после вычитания (проточная ячейка 2 - проточная ячейка 1, проточная ячейка 3 - проточная ячейка 1 или проточная ячейка 4 - проточная ячейка 1), анализировали с применением программного обеспечения BIAevaluation 3.2 (GE Healthcare) для идентификации связывания с использованием модели связывания 1:1, локального Rmax и константой показателя преломления (RI) 0.
Таблица 4: значения аффинности к мезотелину человека, иммобилизованному и находящемуся в растворе, а также перекрестная реактивность с яванским макаком
иммобилизованный MSLN-His-Avi человека
*Аффинность FS28-026 к иммобилизованному MSLN, 100 RU, вероятно, переоценена, поскольку измерения скорости ассоциации выходят за пределы Biacore T200.
Кинетические данные продемонстрировали, что все тестируемые клоны за исключением FS28-024-060, обладали перекрестной реактивностью с MSLN-His-Avi яванского макака и проявляли аффинность к указанному антигену яванского макака в пределах 5-кратного значения аффинности к MSLN-His-Avi человека.
Кроме того, для каждой группы клонов, которые связывались с другой областью связывания MSLN, идентифицировали клоны, которые связывались с низкой наномолярной аффинностью с иммобилизованным MSLN-His-Avi человека.
Клоны потомства FS28-256 обладали более высокой аффинностью, чем соответствующие исходные антитела, что подтверждает то, что созревание аффинности для этих клонов было успешным. Все представляющие интерес клоны обладали более высокой аффинностью к иммобилизованному MSLN, чем к MSLN-His-Avi человека в растворе, характеристикой, которую количественно определяли путем вычисления кратности отличия KD в растворе от KD в случае иммобилизованного антигена (см. Таблицу 4). Таким образом, можно предложить гипотезу, что антитела к MSLN не связываются с высокой аффинностью с мишенью, о чем свидетельствует низкая аффинность связывания с растворимым MSLN, но, как полагают, сильнее связываются с иммобилизованным MSLN благодаря усиленным авидным взаимодействиям с иммобилизованным антигеном. Эта авидность, по-видимому, является антитело-специфичной.
4.2 Связывание с клетками NCI-H226 в присутствии растворимого MSLN
Затем все отобранные клоны, дополненные другими неперемешанными клонами FS28-256 с созревшей аффинностью (см. Таблицу 5), тестировали на предмет связывания с MSLN клеточной поверхности на клетках NCI-H226 в отсутствии и в присутствии 20 нМ MSLN. Применяемый способ был точно таким, как описано в разделе 3.1.4.
Определяли значения как EC50, так и Emax (Таблица 5).
Таблица 5: связывание клеток в отсутствии и в присутствии растворимого мезотелина
* Данные для FS28-185 получали на BD CantoII вместо iQue (Intellicyt), что обуславливает более низкие значения Emax из-за различий в напряжении PMT между устройствами
Данные продемонстрировали, что MSLN-связывающие Fab-области тестируемого mAb2 связывались с различной аффинностью с клетками NCI-H226 в диапазоне от 0,78 до более 16 нМ, при этом большинство клонов демонстрировали низкую наномолярную аффинность связывания клеток, согласующуюся с аффинностью, сообщаемой для рекомбинантного иммобилизованного MSLN. Ранжирование аффинности связывания клеток для наивных FS28-024, FS28-026, FS28-091, FS28-185 и FS28-256 также согласовывалось с данными ранжирования, полученными в формате mAb (Таблица 3, раздел 2.4). Представляющее интерес влияние 20 нМ рекомбинантного MSLN на аффинность связывания клеток было слабым с минимальным (менее чем 2,5-кратным) повышением ЕС50, наблюдаемым для большинства клонов. В частности, на аффинность связывания клеток для клонов, полученных из FS28-256, таких как FS28-256-001, FS28-256-005, FS28-256-012, FS28-256-014, FS28-256-018, FS28-256-023, FS28-256-024 и FS28-256-026, не влияло присутствие растворимого MSLN. Это показало, что даже в присутствии избытка растворимого MSLN большинство клонов предпочтительно связывались с мембраносвязанной формой MSLN.
Для клонов, полученных из FS28-024, наблюдали более переменное влияние растворимого MSLN с повышением EC50 в диапазоне от 3,4 до 17,6 раз.
Два клона с самой высокой аффинностью к рекомбинантному растворимому MSLN (см. Таблицу 4), т.е. FS28-024-060 и FS28-256-027 (для обоих нМ KD для MSLN-His-Avi в растворе представляет собой однозначное число), испытывали наибольшее влияние при связывании с клеткам в присутствии растворимого MSLN, что указывает на то, что на связывающие агенты с более высокой аффинностью с большей вероятностью влияет отделенный MSLN. Таким образом, повышение EC50 в присутствии растворимого MSLN менее предпочтительно, поскольку именно конечная EC50 в присутствии растворимого MSLN, как полагают, в наибольшей степени отражает аффинность mAb к этим клеткам опухоли у пациента. Фактическая необходимая аффинность антител к MSLN зависит от применения.
Пример 5: оптимизация последовательностей клонов FS28-256 с созревшей аффинностью
5.1 Оптимизация последовательностей клонов FS28-256 с созревшей аффинностью
Все клоны линии FS28-256 содержали потенциальный сайт N-связанного гликозилирования в CDR2 VH (нумерация в соответствии с IMGT: N55-X-S57, где X представляет собой любой остаток). Более того, FS28-256-001, FS28-256-021 и FS28-256-023 содержали потенциальный сайт деамидирования в CDR3-области VL в положении N116-T117 (нумерация IMGT). Подобно методике, описанной в разделе 3.2, применяли стратегию NNK-мутагенеза для идентификации замен аминокислот в клоне FS28-256-021, которая позволяет удалить эти потенциальные сайты гликозилирования и деамидирования. Сначала осуществляли мутацию остатка N55 в CDR2 VH и остатка N116 в CDR3 VL в соответствующих клонах, и мутанты подвергали скринингу на предмет сохранения и оптимизации связывания с MSLN человека и яванского макака. Для FS28-256-021 изменения остатка N116 в CDR3 VL приводили к утрате связывания антигена. Из изменений в CDR2 VH по N55 только четыре мутанта (N55A, N55H, N55S и N55T) сохраняли связывание с MSLN человека, хотя их связывание было слабее по сравнению с исходным клоном.
Поскольку было невозможно удалить потенциальный сайт деамидирования в CDR3 VL посредством мутации последовательности, выбирали альтернативные стратегии. Поскольку некоторые из остальных клонов с созревшей аффинностью, полученных из FS28-256, содержали такую же последовательность тяжелой цепи, что и FS28-256-021, но содержали другие последовательности легкой цепи, эти остальные клоны дополнительно исследовали. В частности, для тестирования выбирали FS28-256-027. Как описано ранее, FS28-256-027 демонстрировал более высокую аффинность к растворимому MSLN, чем FS28-256-021 (6,0 нМ, Таблица 4), что приводило к уменьшению связывания с MSLN, экспрессируемым на клеточной поверхности, в присутствии растворимого MSLN (Таблица 5) и, следовательно, тогда его не выбирали в качестве предпочтительного клона. Для исследования того, можно ли оптимизировать этот клон для связывания с MSLN, экспрессируемым на клеточной поверхности, мутации N55A, N55H, N55S или N55T, идентифицированные для клона FS28-256-021, вводили в тяжелую цепь FS28-256-027 и связывание 4 полученных клонов измеряли посредством SPR аналогично протоколу, применяемому в Примере 4.1, но с RU приблизительно 40 вместо 100 для связывания с иммобилизованным и находящимся в растворе MSLN. Результаты представлены в Таблице 6. Введение мутации N55T в FS28-256-027 позволило получить клон, FS28-256-274, который обладал гораздо более низкой аффинностью к иммобилизованному MSLN, чем другие клоны, и поэтому его дальше не использовали. Введение мутаций N55H и N55S в FS28-256-027 позволило получить клоны FS28-256-272 и FS28-256-273 соответственно, которые связывались с растворимым MSLN либо с более высокой, либо с сопоставимой аффинностью, что и с иммобилизованным MSLN. Следовательно, считали вероятным, что на связывание обоих этих клонов с MSLN, экспрессируемым на клеточной поверхности, будет отрицательно влиять присутствие растворимого MSLN. Введение мутации N55A в FS28-256-027, напротив, позволило получить клон FS28-256-271, который демонстрировал самую высокую аффинность к иммобилизованному MSLN из четырех тестируемых клонов и более слабое связывание с растворимым MSLN. Эти результаты показали, что удивительным образом мутация N55A в CDR2 VH исходного клона FS28-256-027 снижала аффинность связывания как с иммобилизованным, так и с растворимым MSLN, так что FS28-258-271 предпочтительно был нацелен на иммобилизованный MSLN, а не на растворимый MSLN. В соответствии с другими клонами, такими как FS28-256-021, которые связывались с KD на уровне 10 нМ или меньше с иммобилизованным MSLN и KD 10 нМ или больше с растворимым MSLN, ожидают, что на связывание FS28-258-271 с MSLN на клеточных поверхностях будет в меньшей степени влиять растворимый MSLN.
Таблица 6: значения аффинности к мезотелину человека, иммобилизованному и находящемуся в растворе
Для mAb² FS22-172-003-AA/FS28-256-271 перекрестную реактивность с яванским макаком определяли посредством SPR с использованием кинетического анализа для стационарного состояния. На чип CM5 (GE Healthcare BR-1005-30) наносили hMSLN-His-Avi или cMSLN-His-Avi при приблизительно 50RU в соответствии с инструкциями производителя. Вводили mAb² в диапазоне концентраций в серии трехкратных разведений, начиная с 243 нМ, со скоростью потока 10 мкл/мин. Время ассоциации составляло 1000 секунд до стационарного состояния, и время диссоциации составляло 30 секунд. Подвижный буфер представлял собой HBS-EP (GE Healthcare BR100188). Проточные ячейки регенерировали путем введения Глицина-HCl, pH 1,5, со скоростью потока 30 мкл/мин в течение 30 секунд. Данные анализировали путем использования двух эталонов и сравнения с проточной ячейкой, которую намеренно оставляли пустой (без нанесения на нее антигена). Модель аффинности в стационарном состоянии использовали для анализа кинетических данных с применением программного обеспечения BiaEvaluation, версия 3.2. Связывание с MSLN яванского макака было в пределах 3-кратного связывания с MSLN человека.
5.2 Активность в виде антителозависимой клеточноопосредованной цитотоксичности (АЗКЦ)
Для оценки эффекторной функции mAb к MLSN эти молекулы тестировали в анализе АЗКЦ in vitro. Для этого получали антитела FS28-256-271 и FS28-024-052 в формате IgG1 человека с мутациями LALA или без них (LALA или G1 соответственно).
Клетки Raji, экспрессирующие MSLN человека (клетки Raji.hMSLN), получали путем лентивирусной трансдукции с использованием системы Lenti-X HTX Packaging system (Takara, номер по каталогу 631253). Вектор экспрессии Lenti-X (pLVX) (Takara, номер по каталогу 631253), содержащий кДНК, кодирующую MLSN человека, котрансфицировали с использованием Lenti-X HTX Packaging Mix в линию клеток Lenti-X 293T (Takara, номер по каталогу 632180) с получением вируса. Затем трансдуцировали линию клеток Raji (ATCC® CCL-86™) этими лентивирусными векторами. Экспрессию MLSN человека на этих клетках подтверждали связыванием антитела положительного контроля G1/SS1 в течение 1 часа, а затем использовали флуоресцентно-меченое детекторное антитело к Fc человека (Stratech Scientific Ltd, номер по каталогу 109-546-098-JIR) для детектирования связывания клеток.
Использовали набор ADCC reporter bioassay kit (Promega, номер по каталогу G7010) в соответствии с протоколом производителя. Эффекторные клетки из указанного набора ADCC смешивали в соотношении 20:1 с клетками Raji.hMSLN. mAb² или контрольное антитело SS1 титровали на 96-луночном планшете и инкубировали при 37°C, 5% CO2 в течение 6 часов. Измеряли АЗКЦ-активность путем добавления субстрата люциферазы из набора Bio-Glo assay system kit (Promega, номер по каталогу G7941) в соответствии с инструкциями производителя. Строили график зависимости сигнала люминесценции от логарифма концентрации антитела, и полученные кривые приводили в соответствие с использованием уравнения зависимости логарифма (агонист) и ответа в GraphPad Prism. Результаты представлены на Фиг.2 и демонстрируют, что как FS28-256-271, так и FS28-024-052 были способны вызывать АЗКЦ-активность, когда были в формате IgG1 человека. Как и ожидали, АЗКЦ-активность утрачивалась, когда в hIgG1-остов этих антител вводили мутацию LALA. Эти данные демонстрируют, что антитела к MSLN, описанные в настоящей заявке, можно применять для индукции эффекторных функций для модуляции иммунных ответов.
5.3 Активность FS28-256-271 в первичных анализах Т-клеток
5.3.1 Активность FS28-256-271 в формате mAb² к OX40 in vitro в первичном анализе Т-клеток
Пан-Т-клетки выделяли из мононуклеарных клеток периферической крови (МКПК), полученных из лейкоцитарных фильтров, побочного продукта донорства тромбоцитов. Вкратце, содержимое лейкоцитарных фильтров промывали ФБР и наслаивали на градиент Фиколла (Ficoll) (GE Lifesciences, номер по каталогу 17144002). Выделяли МКПК путем центрифугирования и извлечения клеток, которые не проходили через градиент Фиколла. Затем МКПК промывали ФБР и оставшиеся эритроциты лизировали путем добавления 10 мл буфера для лизиса эритроцитов (eBioscience) в соответствии с инструкциями производителя. МКПК подсчитывали и ресуспендировали до 2,0 × 10^6 клеток/мл в среде для Т-клеток (среда RPMI (Life Technologies) с 10% FBS (Life Technologies), 1x пенициллином-стрептомицином (Life Technologies), пируватом натрия (Gibco), 10 мМ Hepes (Gibco), 2 мМ L-глутамином (Gibco) и 50 мкМ 2-меркаптоэтанолом (Gibco)).
Затем из МКПК выделяли Т-клетки с использованием набора для выделения пан-Т-клеток II (Pan T Cell Isolation Kit II) (Miltenyi Biotec Ltd) в соответствии с инструкциями производителя. Частицы Human T-Activator CD3/CD28 Dynabead (Invitrogen 111.32D) ресуспендировали путем перемешивания на вортексе. Частицы дважды промывали средой для Т-клеток (среда RPMI (Life Technologies) с 10% FBS (Life Technologies), 1x пенициллином-стрептомицином (Life Technologies), пируватом натрия (Gibco), 10 мМ Hepes (Gibco), 2 мМ L-глутамином (Gibco) и 50 мкМ 2-меркаптоэтанолом (Gibco)). Т-клетки в концентрации 1,0 x 106 клеток/мл в среде для Т-клеток стимулировали промытыми частицами Human T-Activator CD3/CD28 Dynabeads в соотношении клетки к частице 2:1 в колбе Т-25 (Sigma) и инкубировали в течение ночи при 37°C, 5% CO2 для активации Т-клеток. Активированные Т-клетки отмывали от частиц Dynabeads и ресуспендировали в среде для Т-клеток в концентрации 2,0 × 106 клеток/мл. На 96-луночные планшеты с плоским дном наносили антитело к CD3 человека путем инкубации с 2,5 мкг/мл антитела к CD3 человека (R&D Systems, клон UHCT1), разведенного в ФБР, в течение 2 часов при 37°C, 5% CO2, а затем дважды промывали ФБР. В указанные планшеты добавляли активированные Т-клетки в количестве 6 × 105 клеток/лунка. Добавляли клетки, экспрессирующие мезотелин, NCI-H226, в количестве 20000 клеток/лунка. В этом анализе тестировали mAb², содержащее Fcab к OX40, а также Fab FS28-256-271 к MSLN, вместе с контрольными антителами. Аналитические планшеты инкубировали при 37°C, 5% CO2 в течение 72 часов. Собирали надосадочные жидкости и измеряли высвобождение IL-2 путем ELISA-анализа IL-2 человека (Life Technologies, 88-7025-88). Строили график зависимости концентрации IL-2 человека (hIL-2) от логарифма концентрации антитела, и полученные кривые приводили в соответствие с использованием уравнения зависимости логарифма (агонист) и ответа в GraphPad Prism. Результаты представлены в Таблице 7 и они демонстрируют, что FS28-256-271 в формате mAb2 способен связываться с MSLN, экспрессируемым на клеточной поверхности, и перекрестно связывать антитело, так что связывающий сайт OX40 может связываться с OX40 и активировать его.
5.3.2 Активность FS28-256-271 в формате mAb² к CD137 в первичном анализе Т-клеток in vitro
Мононуклеарные клетки периферической крови (МКПК) получали, как описано в разделе 5.2. Выделяли CD8+ Т-клетки с использованием набора для выделения CD8+ Т-клеток II (CD8+ T cell isolation kit II) (Miltenyi Biotec Ltd, 130-096-495) в соответствии с инструкциями производителя. На 96-луночные планшеты с плоским дном для тканевых культур наносили 8 мкг/мл антитела к CD3 (клон UCHT1, R&D Systems, MAB100-SP) в ФБР на ночь при 4°C. Затем планшеты 3 раза промывали 200 мкл ФБР. Клетки NCI-H226 высевали по 2×104 клеток на лунку в покрытые антителом к CD3 (8 мкг/мл) 96-луночные планшеты с плоским дном в 100 мкл среды для культивирования Т-клеток (среда RPMI (Life Technologies, 61870-044) с 10% FBS (Life Technologies), 1X пенициллином-стрептомицином (Life Technologies, 15140122), 1 мМ пируватом натрия (Gibco, 11360-070), 10 мМ Hepes (Sigma-Aldrich, H0887), 2 мМ L-глутамином (Sigma-Aldrich, G7513) и 50 мкМ 2-меркаптоэтанолом (Gibco, M6250)). После адгезии клеток после 4 часов инкубации всю среду для культивирования Т-клеток удаляли и заменяли 50 мкл среды для культивирования Т-клеток, содержащей Т-клетки в концентрации 4,0 × 105 клеток/мл, в результате чего получали 2,0 × 104 клеток/лунка. Контрольные антитела или mAb², содержащие Fcab к CD137 и Fab FS28-256-271 к MSLN, разводили в среде для Т-клеток до 4× конечной концентрации, начиная с 60 нМ, и осуществляли серийные разведения 1:3 или 1:7. К клеткам добавляли 50 мкл антитела для титрования до общего объема образца 200 мкл и 1X концентрации антитела. Инкубировали образец при 37°C, 5% CO2 в течение 72 часов. Надосадочные жидкости собирали и анализировали с помощью набора V-PLEX IL-2 kit от Meso Scale Discovery (K151QQD-4) в соответствии с инструкциями производителя. Строили график зависимости концентрации IL-2 человека (hIL-2) от логарифма концентрации антитела, и полученные кривые приводили в соответствие с использованием уравнения зависимости логарифма (агонист) и ответа в GraphPad Prism. Результаты представлены в Таблице 7 и они демонстрируют, что FS28-256-271 в формате mAb2 способен связываться с MSLN на клеточной поверхности и перекрестно связывать антитело, так что связывающий сайт для CD137 может связываться с CD137 и активировать его.
5.3.3 Обобщенные результаты для клона FS28-256-271 к MSLN с оптимизированными последовательностями и его применение для управления агонизмом в отношении представителей TNFRSF
В Таблице 7 представлены результаты анализов Т-клеток, описанных в разделе 5.3.1 и 5.3.2, которые демонстрируют способность Fab к MSLN, таких как FS28-256-271, в формате mAb2 перекрестно связывать и активировать различные TNFSFR, такие как OX40- или CD137, для индукции агонизма в Т-клетках.
Таблица 7: анализ активации Т-клеток с применением FS28-256-271 в качестве мезотелин-связывающего Fab в формате mAb2 и с использованием клеток NCI-H226 для перекрестного связывания
Обобщенные результаты по выделению mAb к мезотелину человека (Примеры с 1 по 5)
Стратегии отбора на основе фагового дисплея и скрининга антител, направленные на выделение антител к MSLN человека, которые связываются с MSLN клеточной поверхности, позволили идентифицировать панель специфичных антител, связывающих мезотелин, с диапазоном аффинности, MUC16-MSLN-блокирующей активностью, группами на основе связывания областей MSLN и характеристиками связывания клеток. Благодаря выполненному каскаду скрининга большинство Fab, связывающих MSLN, независимо от того, тестировали ли их в формате mAb или mAb2, предпочтительно связывались с MSLN клеточной поверхности.
Пример 6: отбор и определение характеристик антител к MSLN мыши
6.1 Наивный отбор mAb к MSLN мыши
MSLN мыши и человека демонстрируют низкую аминокислотную идентичность (60%). Для обеспечения проведения исследований для подтверждения концепции (PoC) in vivo у мышей, авторы настоящего изобретения поставили перед собой задачу выделить mAb к MSLN мыши, обладающие свойствами, схожими со свойствами mAb к MSLN человека, описанных в Примере 1-5.
Использовали отбор на основе фагового дисплея с использованием синтетических наивных фагмидных библиотек, отображающих Fab-домен IgG1 зародышевой линии человека с рандомизацией по CDR1, CDR2 и CDR3 (MSM Technologies), для отбора с помощью биотинилированного MSLN-His-Avi мыши (SEQ ID NO 171, см. раздел 1.1), как описано в разделе 1.2. Проводили четыре цикла отбора со снижением концентраций биотинилированного mMSLN-His-Avi и, как и в случае отбора антител к MSLN человека, осуществляли стратегии маскирования эпитопа в последующем подходе. Более того, после первого цикла использования рекомбинантного антигена получали клетки HEK293-mMSLN, которые использовали во 2, 3 и 4 цикле.
Вкратце, последовательность MSLN мыши субклонировали в вектор pcDNA5/FRT/TO (Life Technologies, V652020), а затем котрансфицировали с плазмидой экспрессии рекомбиназы Flp, pOG44 (Life Technologies, V600520) в линии клеток Flp-In TREx 293 (Life Technologies, R78007). Клетки выращивали в среде DMEM, содержащей 10% FBS, 100 мкг/мл гигромицина B (Melford Laboratories Ltd, Z2475) и 15 мкг/мл бластицидина (Melford Laboratories Ltd, B1105), в течение 3-4 недель до образования колоний стабильно трансформированных клеток. Эти колонии амплифицировали в присутствии 1 мкг/мл доксициклина (Sigma Aldrich, D9891) и тестировали на предмет экспрессии MSLN с использованием антитела к MSLN мыши (LS Bio, LS-C179484).
Проводили скрининг всего 47 отдельных mAb из обогащенных популяций на предмет связывания антигена, и 45 уникальных положительно связывающих агентов субклонировали и экспрессировали в виде растворимых mAb в LALA-формате IgG1, как описано выше в Примере 1.3. Определяли характеристики mAb по специфичному связыванию с иммобилизованным mMSLN-His-Avi путем ELISA и ранжировали на основе аффинности к примерно 50 или 200 RU иммобилизованного mMSLN-His-Avi в кинетических экспериментах с применением анализа Biacore. В результате идентифицировали панель mAb, включая FS28m-194, FS28m-201, FS28m-209, FS28m-216, FS28m-228, FS28m-261 и FS28m-265, с аффинностью в диапазоне от 1 до 25 нМ. Кроме того, тестировали связывание с различными областями MSLN, как описано в разделе 2.1.3. В качестве положительного контроля использовали перекрестно реагирующее mAb мыши, G1-AA/MOR6626, полученное путем клонирования VH и VL клона MOR6626 (публикация патента № WO 2009/068204 A1). Большинство клонов, среди которых FS28m-228, не могли связываться с MSLN, уже связанным с MOR6626, тогда как другие, такие как FS28-194 или FS28-026, демонстрировали частичное или полное связывание соответственно. Таким образом, выделяли клоны, связывающиеся с разными областями (группы). Области MOR6626, связывающие MSLN, использовали для PoC-исследований in vivo (публикация патента № US 2017/0342169 A1). На основании полученных данных FS28m-228 может связываться с той же областью на MSLN, что и MOR6626.
6.2 Созревание аффинности для mAb к MSLN мыши
CDR3-области VH и VL FS28m-228 параллельно оптимизировали в формате scFv путем рандомизации перекрывающихся кассет для пяти аминокислот с использованием праймеров NNK, как описано в примере 3.1.1. Проводили два цикла отбора с использованием 50 нМ биотинилированного mMSLN-His-Avi в 1 цикле и 0,2 нМ mMSLN-His-Avi во 2 цикле. Для второго цикла также применяли давление отбора по скорости диссоциации путем добавления 1000-кратного избытка (200 нМ) mMSLN-His-Avi (небиотинилированного) и инкубации смеси антиген/фаг в течение 2,5 часов при комнатной температуре. Затем тестировали растворимые scFv (одноточечная концентрация) на предмет связывания с mMSLN-His-Avi с использованием Octet. Вкратце, сенсоры со стрептавидином (ForteBio, 18-5019) инкубировали совместно с mMSLN-His-Avi (10 мкг/мл) в течение 5 минут. Ассоциацию растворимого scFv, разведенного 10x кинетическим буфером до конечной концентрации 1х буфера (ForteBio, 18-1092), с mMSLN анализировали в течение 5 минут с последующим этапом диссоциации, составляющим 5 минут. По сравнению с исходным scFv FS28m-228 примерно 66 из 85 тестируемых клонов демонстрировали улучшенное связывание. Девять клонов использовали в дальнейшем для экспрессии в формате mAb2, комбинируя Fab-области с Fcab, который связывается с CD137 мыши, обозначаемым FS22-063-AA, с использованием того же метода клонирования и экспрессии, который описан (раздел 3.1.2). Полученные обозначенные mAb2 тестировали на предмет их аффинности связывания MSLN.
6.3 Аффинность связывания mAb2 к MSLN мыши в отношении иммобилизованного и растворимого MSLN мыши
Подобно агентам, связывающим MSLN человека, варианты с созревшей аффинностью, полученные из FS28m-228, тестировали на предмет связывания с иммобилизованным и растворимым MSLN с использованием Biacore. Методика связывания с иммобилизованным MSLN была аналогична методу, описанному в разделе 2.1.4, с использованием mMSLN-His-Avi, иммобилизованного при 50 RU. Для определения аффинности к растворимому MSLN осуществляли захват mAb2 через антитело к Fc человека. Вкратце, 25 мкг/мл антитела к IgG (Fc) человека (GE Healthcare, набор Human Antibody Capture Kit, BR100839) наносили на проточные ячейки 1, 2, 3 и 4 на сенсорном чипе CM5 Biacore (GE Healthcare, BR100530) с достижением конечного ответа приблизительно 750 RU. Клоны mAb2, разведенные в буфере HBS-EP (GE Healthcare, BR100188) в концентрации 50 нМ, отдельно вводили в проточную ячейку 2, 3 и 4 со скоростью 30 мкл/мин с достижением ответа приблизительно 100 RU. Рекомбинантные антигены mMSLN-His-Avi, разведенные в буфере HBS-EP, вводили в проточную ячейку 1, 2, 3 и 4 при необходимости в диапазоне концентраций от 243 нМ до 0,11 нМ с 3-кратными разведениями в течение 5 минут со скоростью 70 мкл/мин, а затем оставляли диссоциировать в буфере в течение 5 минут. Регенерацию осуществляли путем введения 3 М хлорида магния (GE Healthcare, набор Human Antibody Capture Kit, BR100839) в течение 30 секунд со скоростью 30 мкл/мин.
Кинетические данные аффинности в случае как иммобилизованного, так и находящегося в растворе антигена (Таблица 8) показали, что по сравнению с исходной Fab-областью FS28m-228 клоны с созревшей аффинностью демонстрировали улучшенное связывание с антигеном MSLN-His-Avi мыши. Более того, все клоны демонстрировали кинетику связывания с аффинностью к иммобилизованному MSLN, которая была выше, чем к растворимому MSLN, в различных соотношениях. Как и в случае клонов человека, описанных в разделах 4.1 и 5.1, полагали, что эти клоны будут демонстрировать более сильное связывание с мембраносвязанным MSLN, чем с растворимым отделенным MSLN благодаря усиленным авидным связывающим взаимодействиям. Таким образом, созревание аффинности для FS28m-228 позволило получить панель клонов с созревшей аффинностью, которые обладали повышенной аффинностью к MSLN мыши и все они связывались сильнее с иммобилизованным MSLN, чем с растворимым MSLN. Клон FS28m-228-010 выбирали в качестве предпочтительного клона, поскольку он обладал самой высокой аффинностью к иммобилизованному MSLN мыши и низкой аффинностью к MSLN мыши в растворе.
Таблица 8: значения аффинности к мезотелину человека, иммобилизованному и находящемуся в растворе
6.4 Обобщенные результаты по выделению mAb к мезотелину мыши
Стратегии отбора на основе фагового дисплея и скрининга антител позволили идентифицировать панель клонов, связывающих мезотелин мыши, с диапазоном значений аффинности, которые связываются с различными областями mMSLN. Подобно агентам, связывающим MSLN человека, указанные клоны демонстрировали характеристики связывания, способствующие связыванию с иммобилизованным mMSLN, а не с растворимым mMSLN, что делает их подходящими молекулами для изучения в PoC-исследованиях у мышей in vivo.
6.5 Эффективность mAb², содержащих mAb FS28m-228-010 к MSLN мыши
После демонстрации того, что mAb к MLSN изотипа hIgG1 были способны вызывать АЗКЦ-активность, было желательным показать, что mAb к MLSN были способны управлять MLSN-зависимым перекрестным связыванием in vivo в формате mAb2 к CD137.
Конструировали модель сингенной опухоли у мышей, экспрессирующую MSLN мыши. Клетки карциномы толстой кишки CT26 (ATCC, CRL-2638), экспрессирующие полноразмерный мезотелин мыши (SEQ ID NO: 171), получали путем липофекции (Липофектамин (Lipofectamine) 3000, Thermo Fisher Scientific, номер по каталогу L3000008) с использованием вектора pcDNA3.1 (+) (Thermo Fisher Scientific, номер по каталогу V79020). В соответствии с протоколом производителя клетки CT26 трансфицировали векторами pcDNA3.1, содержащими кДНК для MSLN мыши. Осуществляли стабильную трансфекцию с использованием генетицина в качестве селективного антибиотика (в количестве 600 мкг/мл) в полных средах (RPMI, 10% FBS). Экспрессию MSLN мыши на клетках CT26 подтверждали посредством проточной цитометрии путем использования антитела MOR6626 положительного контроля (WO 2009/068204 A1). В частности, клетки инкубировали совместно с антителом положительного контроля в течение 1 часа, а затем использовали флуоресцентно-меченое детекторное антитело к IgG человека (Stratech Scientific Ltd, номер по каталогу 109-546-098-JIR) для детектирования связывания клеток. Популяции клонов расширяли, а затем анализировали для определения относительных уровней экспрессии с применением такой же методики проточной цитометрии, после чего выбирали один клон и обозначали CT26.G10.
Рост опухоли CT26.G10 подтверждали in vivo. Самок мышей Balb/c (Charles River) в возрасте 8-10 недель микрочипировали и присваивали им уникальный идентификационный номер. Каждая когорта включала 17 мышей и каждое животное получало 1 × 105 клеток, вводимых подкожно в дорсальный левый бок в 100 мкл бессывороточной среды. Три раза в неделю проводили измерения объема опухоли с помощью штангенциркуля с определением самой длинной оси и самой короткой оси опухоли. Для расчета объема опухоли использовали следующую формулу:
Объем = L × S22
где L = самая длинная ось; S= самая короткая ось
Исследование прекращали, когда объем опухоли достигал конечной точки для эвтаназии из соображений гуманности в соответствии с Законом Соединенного Королевства о животных (научные процедуры) и Директивой ЕС EU86/609. По окончании исследования собирали ткани опухоли и экспрессию мембраносвязанного мезотелина подтверждали путем иммуногистохимического окрашивания в тканях опухоли, зафиксированных в формалине и залитый парафином (FFPE), следующим образом: 4 мкм срезы FFPE-ткани депарафинировали и извлекали антиген с использованием низкого pH 6,1 при 97°C (Dako PT Link), а затем перкосидазного блока и протеинового блока перед инкубацией совместно с первичным антителом к мезотелину (LifeSpan Biosciences, номер по каталогу LS-C407883) в концентрации 1 мкг/мл. Указанное антитело к мезотелину детектировали с использованием меченого полимера-HRP, конъюгированного со вторичным реагентом к иммуноглобулину кролика, и хромогенного анализа с использованием DAB (3,3'-диаминобензидин) (Dako EnVision+ System).
Для оценки антитела FS28m-228-010 тестировали in vivo следующие молекулы или комбинации: антитело FS28m-228-010 изотипа IgG1 человека с мутациями LALA (G1-AA/FS28m-228-010), два «ложных» mAb2 к CD137 (FS22m-063-AA/HelD1.3 и FS22m-063-AA/4420), комбинацию антитела FS28m-228-010 с ложным mAb2 к CD137 с мутациями LALA (G1-AA/FS28m-228-010 + FS22m-063-AA/HelD1.3), антитело человека изотипического контроля (G1-AA/HelD1.3) и, наконец, mAb² к CD137/MSLN (FS22m-063-AA/FS28m-228-010) с мутациями LALA (SEQ ID NO 196 и 197).
Самкам мышей Balb/c (Charles River), каждая из которых была в возрасте 8-10 недель и массой 20-25 г, давали одну неделю для акклиматизации перед началом исследования. Всех животных микрочипировали и присваивали им уникальный идентификационный номер. За исключением FS22m-063-AA/4420 (n=10 мышей), каждая когорта включала 20 мышей. Наращивали линию клеток карциномы толстой кишки CT26.G10 и создавали банки клеток. Каждое животное получало 1 × 105 клеток, вводимых подкожно в левый бок в 100 мкл бессывороточных сред. Каждую мышь, у которой не было опухоли через 12 дней после инокуляции клеток опухоли, исключали из исследования.
Готовили дозы 200 мкг каждого антитела (~10 мг/кг) и вводили мышам интраперитонеально (и/п) путем инъекции. Кроме того, оба G1-AA/FS28m-228-010 + FS22m-063-AA/HelD1.3 получали по 200 мкг на дозу каждое (~10 мг/кг) для группы комбинации. Мышам вводили дозы 200 мкл в 12, 14 и 16 дни (q2dx3) после инокуляции опухоли. Три раза в неделю проводили измерения объема опухоли с использованием штангенциркуля и осуществляли тщательный мониторинг мышей. Конечную точку исследования определяли по конечным точкам для эвтаназии из соображений гуманности на основе объема опухоли и состояния мышей.
Как показано на Фиг. 3, mAb2 FS22m-063-AA/FS28m-228-010 в значительной степени ингибировало рост опухоли по сравнению с изотипическим контролем G1-AA/HelD1.3. В Таблице 9 представлено попарное сравнение скоростей роста для всех групп лечения на протяжении всего исследования с использованием анализа смешанной модели, позволяющего сравнить все группы с изотипическим контролем G1-AA/HelD1.3.
Всех животных с опухолями, размер которых в конце исследования равен или меньше 62,5 мм3, считали полностью отвечающими животными (см. Таблицу 10). 35% животных, получавших лечение mAb2 к CD137/MSLN, полностью отвечали на лечение в конце исследования по сравнению с 0% в группах изотипического контроля G1-AA/HelD1.3, FS22m-063-AA/HelD1.3, FS22m-063-AA/4420 и комбинации FS22m-063-AA/HelD1.3 и G1-AA/FS28m-228-010.
Анализ выживаемости (Фиг.4 и Таблица 11) показал, что mAb2 FS22m-063-AA/FS28m-228-010 обуславливало значительное преимущество по выживаемости по сравнению с антителом G1-AA/HelD1.3, тогда как G1-AA/FS28m-228-010, FS22m-063-AA/HelD1.3 и FS22m-063-AA/4420 не демонстрировали преимущество по выживаемости. Более того, mAb2 FS22m-063-AA/FS28m-228-010 обеспечивало увеличение медианы выживаемости, составляющего 42,5 дня, по сравнению с G1-AA/HelD1.3 (29 дней), FS22m-063-AA/HelD1.3 (30 дней), FS22m-063-AA/4420 (29 дней), G1-AA/FS28m-228-010 (30 дней) и комбинацией FS22m-063-AA/HelD1.3 с G1-AA/FS28m-228-010 (29 дней).
Эти данные позволяют предположить, что перекрестное связывание mAb2 через MSLN способно управлять агонизмом в отношении CD137 в опухоли; действие биспецифичного антитела, которое превосходит нацеливание только на CD137 и/или MSLN (и даже в комбинации), что обеспечивает значительное увеличение выживаемости у мышей с опухолью. Само по себе mAb (G1-AA/FS28m-228-010) с мутацией LALA не проявляло внутренней активности в этом исследовании. Не желая быть связанными какой-либо теорией ожидают, что компетентный по эффекторной функции вариант антитела FS28m-228-010 (без мутации LALA) будет демонстрировать АЗКЦ-активность и противоопухолевую эффективность в соответствии с результатами in vitro, наблюдаемыми в разделе 5.2.
Таблица 9: результаты попарного сравнения роста опухоли с использованием анализа смешанной модели, позволяющего сравнить все группы с изотипическим контролем G1-AA/HelD1.3
NS - незначимый p≥0,05; **** - p-значение<0,0001; *** - p-значение 0,0001-0,001
Таблица 10: количество и процент мышей без опухоли (опухоли ≤ 62 мм3) к концу исследования в модели сингенной опухоли CT26.G10
FS22m-063-AA/HelD1.3, 10 мг/кг
Таблица 11: медиана выживаемости для животных, получавших лечение каждым соединением, и результаты попарного статистического анализа (с помощью лог-рангового критерия) в модели сингенной опухоли CT26.G10
FS22m-063-AA/HelD1.3, 10 мг/кг
NS - незначимый p≥0,05; **** - p-значение<0,0001
6.6 Механизм действия mAb2 к CD137/MSLN, содержащего mAb FS28m-228-010 к MLSN мыши
Для дальнейшего понимания фармакологии противоопухолевого ответа, наблюдаемого в случае FS22m-063-AA/FS28m-228-010, содержащего mAb FS28m-228-010 к MLSN мыши, исследовали механизм действия mAb2 к CD137/MSLN в модели MSLN-положительной сингенной опухоли.
Мышей подготавливали, как описано в Примере 6.5, и инокулировали линией клеток карциномы толстой кишки CT26.G10. Каждая когорта состояла из 20 мышей. Для сравнения также включали mAb2 FS22m-063-AA/FS28-228-010 (CD137/MSLN), изотипический контроль IgG1 человека (G1-AA/4420) и антитело-агонист к CD137 (клон 3H3; G1/3H3; Rickert et al., 2016). Все три антитела получали по 134 мкг на дозу (приблизительно 6,7 мг/кг для мыши массой 20 г) в Д-ФБР + 1 мМ аргинин + 0,05% Твин 80 и вводили мышам интраперитонеально (и/п) путем инъекции. Каждая мышь получала антитела путем одной интраперитонеальной инъекции 200 мкл в фиксированной дозе 134 мкг в 20 день после инокуляции опухоли. Три раза в неделю проводили измерения объема опухоли с использованием штангенциркуля, как описано в Примере 6.5, и осуществляли тщательный мониторинг мышей.
В 20 день после инокуляции опухоли проводили вскрытие шести мышей в группе через 24, 72, 144 и 192 часа после введения дозы. У мышей с опухолью CT26.G10, получавших лечение либо FS22m-063-AA/FS28-228-010, либо G1-AA/4420, либо G1/3H3, брали селезенку, кровь и опухолевую ткань для анализа. Все образцы исследовали на предмет избытка и пролиферации Т-клеток путем проточной цитометрии, поскольку известно, что маркеры активации и пролиферации Т-клеток являются нисходящими «эффектами» агонизма в отношении CD137 (Fisher et al., 2012). Кроме того, для детектирования и количественного определения экспрессии растворимого MSLN также брали сыворотку крови. Размельчали селезенку и опухолевую ткань до суспензии отдельных клеток стандартными механическими и ферментными способами, и один раз лизировали эритроциты в буфере для лизиса эритроцитов (Miltenyi Biotec Ltd., 130-094-183). Кровь собирали путем терминального кровопускания из сердца и половину собирали в EDTA-содержащие пробирки для анализа отдельных клеток путем проточной цитометрии, а половину крови собирали в пробирки с активатором свертывания/пробирки для сыворотки для анализа растворимого MSLN. Цельную кровь, собранную в EDTA-содержащие пробирки, три раза лизировали в буфере для лизиса эритроцитов (Miltenyi Biotec Ltd., 130-094-183) в соответствии с инструкциями производителя. Кровь, собранную в пробирки для сыворотки, делили на фракции путем центрифугирования и извлекали сыворотку для анализа растворимого MSLN.
Затем таким же образом обрабатывали единичные клетки селезенки, опухоли и крови, и клетки один раз промывали ФБР, образцы окрашивали фиксируемым красителем для оценки жизнеспособности (fixable viability dye) (eBioscience, 65-0865-14). Затем клетки окрашивали для оценки маркеров клеточной поверхности с помощью панели окрашивающих антител, представленной в Таблице 12 (почти все внутриклеточные маркеры, Ki67 и FoxP3), в присутствии Fc-блока (eBioscience, 16-0161-85, 1:25) в течение 45 минут при 4°C. Затем клетки фиксировали и пермеабилизировали с помощью набора для окрашивания FoxP3 eBioscience (eBioscience, 00-5523-00) в соответствии с инструкциями производителя. Клетки ресуспендировали в 100 мкл буфера для пермеабилизации с антителами - внутриклеточными маркерами Ki67 и FoxP3, и инкубировали в течение ночи при 4°C в темноте. Перед сбором данных на проточном цитометре BD Fortessa клетки один раз промывали буфером для пермеабилизации и ресуспендировали в 120 мкл ФБР, содержащего 0,5% BSA. Данные получали с применением программного обеспечения BD FACS Diva и анализировали с помощью FlowJo (V10) и Microsoft Excel. Эти данные демонстрируют избыток и пролиферацию CD8+ Т-клеток через 144 часа после введения дозы в процентах от исходной популяции.
Таблица 12: панель для проточной цитометрии
Как показано в Таблице 13, наблюдали увеличение процента CD8+ Т-клеток в опухоли через 144 часа после введения дозы G1/3H3 и mAb2 FS22m-063-AA/FS28-228-010 по сравнению с контрольной группой лечения (G1-AA/4420). Средний процент CD8+ Т-клеток в опухоли увеличивался с 32,1% (G1-AA/4420) до 56,1% для G1/3H3 и 58,4% для FS22m-063-AA/FS28m-228-010 через 144 часа после введения дозы.
Кроме того, также наблюдали увеличение количества CD8+ Т-клеток в крови и селезенке, но только в случае G1/3H3, по сравнению с контролем IgG1. В крови через 144 часа после введения дозы средний процент CD8+ Т-клеток увеличивался с 22,6% (G1-AA/4420) до 57,0% (G1/3H3), однако это увеличение не наблюдали в случае FS22m-063-AA/FS28m-228-010 (25,8%). Подобным образом в селезенке средний процент CD8+ Т-клеток увеличивался с 28,8% (G1-AA/4420) до 38,0% в случае G1/3H3, однако это увеличение не наблюдали в случае FS22m-063-AA/FS28m-228-010 (29%).
Это позволяет предположить, что mAb2 FS22m-063-AA/FS28m-228-010 увеличивает количество CD8+ Т-клеток специфично в опухоли, где экспрессируется MSLN, тогда как антитело, нацеленное на CD137, G1/3H3, также демонстрирует периферическое (кровь и селезенка) увеличение количества CD8+ Т-клеток.
Для определения, были ли какие-либо различия в пролиферации CD8+ T-клеток после введения дозы анализировали маркер пролиферации Ki67 на CD8+ T-клетках в опухоли, крови и селезенке. Как показано в Таблице 14, высокая доля CD8+ Т-клеток экспрессировала Ki67+ в контрольной группе (средняя экспрессия 75,1%), что позволяет предположить высокий уровень пролиферирующих CD8+ Т-клеток в опухоли в модели CT26.G10. Это может способствовать неясным различиям в экспрессии Ki67 на CD8+ Т-клетках между дозовыми группами в опухоли.
Для сравнения, наблюдали явное повышение экспрессии Ki67+ на CD8+ Т-клетках в крови и селезенке через 144 часа после введения дозы в случае G1/3H3 по сравнению с контролем IgG1. В крови, в то время как мыши, получавшие лечение изотипическим контролем, демонстрировали среднюю экспрессию Ki67+ на CD8+ Т-клетках, составляющую 10,4%, средняя экспрессия Ki67 на CD8+ Т-клетках после введения дозы в случае G1/3H3, как показано, составляла 86,3% через 144 часа после введения дозы. Для сравнения, это увеличение не наблюдали в крови для FS22m-063-AA/FS28m-228-010, когда среднюю экспрессию Ki67+ на CD8+ Т-клетках наблюдали на уровне 13,1% после введения дозы mAb2. Подобным образом в селезенке наблюдали среднюю экспрессию Ki67+ на уровне 36,1% CD8+ Т-клеток после введения дозы G1/3H3 по сравнению с 8,1%, наблюдаемыми после введения дозы в случае изотипического контроля, и 11,4%, наблюдаемыми в случае FS22m-063-AA/FS28m-228-010.
Таблица 13: средний процент CD8+ Т-клеток от общего количества CD3+ клеток в опухоли, крови и селезенке через 144 часа после введения дозы G1-AA/4420, G1/3H3 или FS22m-063-AA/FS28m-228-010. Данные показывают средний процент CD8+ Т-клеток от общего количества CD3+ Т-клеток ± стандартная ошибка среднего.
Таблица 14: средний процент Ki67, экспрессируемого на CD8+ Т-клетках в опухоли, крови и селезенке через 144 часа после введения дозы G1-AA/4420, G1/3H3 или FS22m-063-AA/FS28m-228-010. Данные показывают средний процент Ki67+ от общего количества CD8+ Т-клеток ± стандартная ошибка среднего.
В совокупности эти данные показывают, что mAb², содержащее mAb FS28m-228-010 к MLSN мыши, FS22m-063-AA/FS28m-228-010, опосредует опухолеспецифическое увеличение количества цитотоксических CD8+ Т-клеток в опухоли. Хотя это также наблюдали для G1/3H3, этот CD137-нацеленный агонист также способствует периферическому увеличению количества CD8+ Т-клеток в крови и селезенке. Более того, эти CD8+ Т-клетки также демонстрируют повышенную пролиферацию после введения дозы G1/3H3.
Перечень последовательностей
Аминокислотная последовательность тяжелой цепи исходного клона FS28-256, демонстрирующая «главную» последовательность CDR2, применимую к исходному клону и клонам с созревшей аффинностью FS28-256-001, FS28-256-005, FS28-256-012, FS28-256-014, FS28-256-018, FS28-256-021, FS28-256-023, FS28-256-024, FS28-256-026 и FS28-256-027. «X» с двойным подчеркиванием обозначают все потенциальные замены для устранения возможного N-связанного гликозилирования. Полученные клоны могут содержать либо одну или другую замену, либо обе.
SEQ ID NO: 1 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTETY MSWVRQAPGKGLEWVSX IXPTYSTT NYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARYNSYQGGLDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 2 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTETY MSWVRQAPGKGLEWVSX IXPTYSTT NYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARYNSYQGGLDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
Главная аминокислотная последовательность легкой цепи, применимая к клонам FS28-256-001, FS28-256-021 и FS28-256-023. «X» с двойным подчеркиванием обозначают все потенциальные замены для устранения возможного сайта деамидирования. Полученные клоны могут содержать либо одну или другую замену, либо обе.
SEQ ID NO: 3 Легкая цепь EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQHNQYPXXFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотные последовательности и последовательности кДНК для тяжелой цепи mAb FS28-024 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 4 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTLSYSS MSWVRQAPGKGLEWVSF ITPSTGYT HYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARRALTFDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 6 Тяжелая цепь, ДНК (без LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCCTCAGTTATTCTTCTATGTCATGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCTTTATTACTCCGTCTACTGGCTATACCCACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGACGGGCGCTGACGTTCGACTACTGGGGCCAGGGAACCTTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAACTGCTGGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 5 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTLSYSS MSWVRQAPGKGLEWVSF ITPSTGYT HYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARRALTFDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 7 Тяжелая цепь, ДНК (с LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCCTCAGTTATTCTTCTATGTCATGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCTTTATTACTCCGTCTACTGGCTATACCCACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGACGGGCGCTGACGTTCGACTACTGGGGCCAGGGAACCTTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAAGCTGCCGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 8 Вариабельный домен, а/к
EVQLLESGGGLVQPGGSLRLSCAAS GFTLSYSS MSWVRQAPGKGLEWVSF ITPSTGYT HYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARRALTFDY WGQGTLVTVSS
SEQ ID NO: 9 Вариабельный домен, ДНК
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCCTCAGTTATTCTTCTATGTCATGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCTTTATTACTCCGTCTACTGGCTATACCCACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGACGGGCGCTGACGTTCGACTACTGGGGCCAGGGAACCTTGGTCACCGTCTCGAGT
SEQ ID NO: 10 CDR1 (а/к) (IMGT) GFTLSYSS
SEQ ID NO: 13 CDR1 (а/к) (Кабат) YSSMS
SEQ ID NO: 11 CDR2 (а/к) (IMGT) ITPSTGYT
SEQ ID NO: 14 CDR2 (а/к) (Кабат) FITPSTGYTHYADSVKG
SEQ ID NO: 12 CDR3 (а/к) (IMGT) ARRALTFDY
SEQ ID NO: 15 CDR3 (а/к) (Кабат) RALTFDY
Аминокислотные последовательности и последовательности кДНК для легкой цепи mAb FS28-024 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 16 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQASSYPLT FGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
SEQ ID NO: 17 Легкая цепь, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAAGCTTCTTCTTATCCTCTCACGTTCGGCCAAGGGACCAAGGTGGAAATCAAACGTACTGTGGCCGCTCCTAGCGTGTTCATTTTTCCGCCATCCGACGAGCAGCTCAAGTCCGGCACCGCCTCCGTGGTCTGCCTGCTCAACAACTTCTACCCTCGCGAAGCTAAGGTCCAGTGGAAGGTCGACAATGCCCTGCAGTCCGGAAACTCGCAGGAAAGCGTGACTGAACAGGACTCCAAGGACTCCACCTATTCACTGTCCTCGACTCTGACCCTGAGCAAGGCGGATTACGAAAAGCACAAAGTGTACGCATGCGAAGTGACCCACCAGGGTCTTTCGTCCCCCGTGACCAAGAGCTTCAACAGAGGAGAGTGT
SEQ ID NO: 18 Вариабельный домен, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQASSYPLT FGQGTKVEIK
SEQ ID NO: 19 Вариабельный домен, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAAGCTTCTTCTTATCCTCTCACGTTCGGCCAAGGGACCAAGGTGGAAATCAAA
SEQ ID NO: 20 CDR1 (а/к) (IMGT) QSVSSSY
SEQ ID NO: 23 CDR1 (а/к) (Кабат) RASQSVSSSYLA
SEQ ID NO: 21 CDR2 (а/к) (IMGT) GAS
SEQ ID NO: 24 CDR2 (а/к) (Кабат) GASSRAT
SEQ ID NO: 22 CDR3 (а/к) (IMGT) QQASSYPLT
SEQ ID NO: 22 CDR3 (а/к) (Кабат) QQASSYPLT
Аминокислотные последовательности и последовательности кДНК для тяжелой цепи mAb FS28-024-051 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 26 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTLSYSS MSWVRQAPGKGLEWVSF ITPSTGYT HYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARRALIFDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 27 Тяжелая цепь, ДНК (без LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCCTCAGTTATTCTTCTATGTCATGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCTTTATTACTCCGTCTACTGGCTATACCCACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGACGGGCGCTGATTTTCGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAACTGCTGGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 28 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTLSYSS MSWVRQAPGKGLEWVSF ITPSTGYT HYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARRALIFDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 29 Тяжелая цепь, ДНК (с LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCCTCAGTTATTCTTCTATGTCATGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCTTTATTACTCCGTCTACTGGCTATACCCACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGACGGGCGCTGATTTTCGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAAGCTGCCGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 30 Вариабельный домен, а/к
EVQLLESGGGLVQPGGSLRLSCAAS GFTLSYSS MSWVRQAPGKGLEWVSF ITPSTGYT HYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARRALIFDY WGQGTLVTVSS
SEQ ID NO: 31 Вариабельный домен, ДНК
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCCTCAGTTATTCTTCTATGTCATGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCTTTATTACTCCGTCTACTGGCTATACCCACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGACGGGCGCTGATTTTCGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGT
SEQ ID NO: 10 CDR1 (а/к) (IMGT) GFTLSYSS
SEQ ID NO: 13 CDR1 (а/к) (Кабат) YSSMS
SEQ ID NO: 11 CDR2 (а/к) (IMGT) ITPSTGYT
SEQ ID NO: 14 CDR2 (а/к) (Кабат) FITPSTGYTHYADSVKG
SEQ ID NO: 32 CDR3 (а/к) (IMGT) ARRALIFDY
SEQ ID NO: 33 CDR3 (а/к) (Кабат) RALIFDY
Аминокислотные последовательности и последовательности кДНК для легкой цепи mAb FS28-024-051 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 16 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQASSYPLT FGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
SEQ ID NO: 17 Легкая цепь, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAAGCTTCTTCTTATCCTCTCACGTTCGGCCAAGGGACCAAGGTGGAAATCAAACGTACTGTGGCCGCTCCTAGCGTGTTCATTTTTCCGCCATCCGACGAGCAGCTCAAGTCCGGCACCGCCTCCGTGGTCTGCCTGCTCAACAACTTCTACCCTCGCGAAGCTAAGGTCCAGTGGAAGGTCGACAATGCCCTGCAGTCCGGAAACTCGCAGGAAAGCGTGACTGAACAGGACTCCAAGGACTCCACCTATTCACTGTCCTCGACTCTGACCCTGAGCAAGGCGGATTACGAAAAGCACAAAGTGTACGCATGCGAAGTGACCCACCAGGGTCTTTCGTCCCCCGTGACCAAGAGCTTCAACAGAGGAGAGTGT
SEQ ID NO: 18 Вариабельный домен, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQASSYPLT FGQGTKVEIK
SEQ ID NO: 19 Вариабельный домен, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAAGCTTCTTCTTATCCTCTCACGTTCGGCCAAGGGACCAAGGTGGAAATCAAA
SEQ ID NO: 20 CDR1 (а/к) (IMGT) QSVSSSY
SEQ ID NO: 23 CDR1 (а/к) (Кабат) RASQSVSSSYLA
SEQ ID NO: 21 CDR2 (а/к) (IMGT) GAS
SEQ ID NO: 24 CDR2 (а/к) (Кабат) GASSRAT
SEQ ID NO: 22 CDR3 (а/к) (IMGT) QQASSYPLT
SEQ ID NO: 22 CDR3 (а/к) (Кабат) QQASSYPLT
Аминокислотные последовательности и последовательности кДНК для тяжелой цепи mAb FS28-024-052 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 35 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTLSYSS MSWVRQAPGKGLEWVSF ITPSTGYT HYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARRALLFDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 36 Тяжелая цепь, ДНК (без LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCCTCAGTTATTCTTCTATGTCATGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCTTTATTACTCCGTCTACTGGCTATACCCACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGACGGGCGCTGCTTTTCGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGTCGGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAACTGCTGGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 37 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTLSYSS MSWVRQAPGKGLEWVSF ITPSTGYT HYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARRALLFDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 38 Тяжелая цепь, ДНК (с LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCCTCAGTTATTCTTCTATGTCATGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCTTTATTACTCCGTCTACTGGCTATACCCACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGACGGGCGCTGCTTTTCGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGTCGGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAAGCTGCCGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 39 Вариабельный домен, а/к
EVQLLESGGGLVQPGGSLRLSCAAS GFTLSYSS MSWVRQAPGKGLEWVSF ITPSTGYT HYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARRALLFDY WGQGTLVTVSS
SEQ ID NO: 40 Вариабельный домен, ДНК
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCCTCAGTTATTCTTCTATGTCATGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCTTTATTACTCCGTCTACTGGCTATACCCACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGACGGGCGCTGCTTTTCGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGTCG
SEQ ID NO: 10 CDR1 (а/к) (IMGT) GFTLSYSS
SEQ ID NO: 13 CDR1 (а/к) (Кабат) YSSMS
SEQ ID NO: 11 CDR2 (а/к) (IMGT) ITPSTGYT
SEQ ID NO: 14 CDR2 (а/к) (Кабат) FITPSTGYTHYADSVKG
SEQ ID NO: 41 CDR3 (а/к) (IMGT) ARRALLFDY
SEQ ID NO: 42 CDR3 (а/к) (Кабат) RALLFDY
Аминокислотные последовательности и последовательности кДНК для легкой цепи mAb FS28-024-052 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 16 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQASSYPLT FGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
SEQ ID NO: 17 Легкая цепь, ДНК
AAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAAGCTTCTTCTTATCCTCTCACGTTCGGCCAAGGGACCAAGGTGGAAATCAAACGTACTGTGGCCGCTCCTAGCGTGTTCATTTTTCCGCCATCCGACGAGCAGCTCAAGTCCGGCACCGCCTCCGTGGTCTGCCTGCTCAACAACTTCTACCCTCGCGAAGCTAAGGTCCAGTGGAAGGTCGACAATGCCCTGCAGTCCGGAAACTCGCAGGAAAGCGTGACTGAACAGGACTCCAAGGACTCCACCTATTCACTGTCCTCGACTCTGACCCTGAGCAAGGCGGATTACGAAAAGCACAAAGTGTACGCATGCGAAGTGACCCACCAGGGTCTTTCGTCCCCCGTGACCAAGAGCTTCAACAGAGGAGAGTGT
SEQ ID NO: 18 Вариабельный домен, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQASSYPLT FGQGTKVEIK
SEQ ID NO: 19 Вариабельный домен, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAAGCTTCTTCTTATCCTCTCACGTTCGGCCAAGGGACCAAGGTGGAAATCAAA
SEQ ID NO: 20 CDR1 (а/к) (IMGT) QSVSSSY
SEQ ID NO: 23 CDR1 (а/к) (Кабат) RASQSVSSSYLA
SEQ ID NO: 21 CDR2 (а/к) (IMGT) GAS
SEQ ID NO: 24 CDR2 (а/к) (Кабат) GASSRAT
SEQ ID NO: 22 CDR3 (а/к) (IMGT) QQASSYPLT
SEQ ID NO: 22 CDR3 (а/к) (Кабат) QQASSYPLT
Аминокислотные последовательности и последовательности кДНК для тяжелой цепи mAb FS28-024-053 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 45 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTLSYSS MSWVRQAPGKGLEWVSF ITPSTGYT HYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARRALVFDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 46 Тяжелая цепь, ДНК (без LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCCTCAGTTATTCTTCTATGTCATGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCTTTATTACTCCGTCTACTGGCTATACCCACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGACGGGCGCTGGTGTTCGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGTCGGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAACTGCTGGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 47 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTLSYSS MSWVRQAPGKGLEWVSF ITPSTGYT HYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARRALVFDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 48 Тяжелая цепь, ДНК (с LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCCTCAGTTATTCTTCTATGTCATGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCTTTATTACTCCGTCTACTGGCTATACCCACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGACGGGCGCTGGTGTTCGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGTCGGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAAGCTGCCGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 49 Вариабельный домен, а/к
EVQLLESGGGLVQPGGSLRLSCAAS GFTLSYSS MSWVRQAPGKGLEWVSF ITPSTGYT HYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARRALVFDY WGQGTLVTVSS
SEQ ID NO: 50 Вариабельный домен, ДНК
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCCTCAGTTATTCTTCTATGTCATGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCTTTATTACTCCGTCTACTGGCTATACCCACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGACGGGCGCTGGTGTTCGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGTCG
SEQ ID NO: 10 CDR1 (а/к) (IMGT) GFTLSYSS
SEQ ID NO: 13 CDR1 (а/к) (Кабат) YSSMS
SEQ ID NO: 11 CDR2 (а/к) (IMGT) ITPSTGYT
SEQ ID NO: 14 CDR2 (а/к) (Кабат) FITPSTGYTHYADSVKG
SEQ ID NO: 51 CDR3 (а/к) (IMGT) ARRALVFDY
SEQ ID NO: 52 CDR3 (а/к) (Кабат) RALVFDY
Аминокислотные последовательности и последовательности кДНК для легкой цепи mAb FS28-024-053 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 16 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQASSYPLT FGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
SEQ ID NO: 17 Легкая цепь, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAAGCTTCTTCTTATCCTCTCACGTTCGGCCAAGGGACCAAGGTGGAAATCAAACGTACTGTGGCCGCTCCTAGCGTGTTCATTTTTCCGCCATCCGACGAGCAGCTCAAGTCCGGCACCGCCTCCGTGGTCTGCCTGCTCAACAACTTCTACCCTCGCGAAGCTAAGGTCCAGTGGAAGGTCGACAATGCCCTGCAGTCCGGAAACTCGCAGGAAAGCGTGACTGAACAGGACTCCAAGGACTCCACCTATTCACTGTCCTCGACTCTGACCCTGAGCAAGGCGGATTACGAAAAGCACAAAGTGTACGCATGCGAAGTGACCCACCAGGGTCTTTCGTCCCCCGTGACCAAGAGCTTCAACAGAGGAGAGTGT
SEQ ID NO: 18 Вариабельный домен, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQASSYPLT FGQGTKVEIK
SEQ ID NO: 19 Вариабельный домен, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAAGCTTCTTCTTATCCTCTCACGTTCGGCCAAGGGACCAAGGTGGAAATCAAA
SEQ ID NO: 20 CDR1 (а/к) (IMGT) QSVSSSY
SEQ ID NO: 23 CDR1 (а/к) (Кабат) RASQSVSSSYLA
SEQ ID NO: 21 CDR2 (а/к) (IMGT) GAS
SEQ ID NO: 24 CDR2 (а/к) (Кабат) GASSRAT
SEQ ID NO: 22 CDR3 (а/к) (IMGT) QQASSYPLT
SEQ ID NO: 22 CDR3 (а/к) (Кабат) QQASSYPLT
Аминокислотные последовательности тяжелой и легкой цепи mAb FS28-024-060 (с LALA)
SEQ ID NO: 55 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTLSYSS MSWVRQAPGKGLEWVSF ITPSTGYT HYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARRALWFDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 16 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQASSYPLT FGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотные последовательности тяжелой и легкой цепи mAb FS28-026 (с LALA)
SEQ ID NO: 58 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFSNYA MTWVRQAPGKGLEWVSS ITPYYSKT DYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARNWYRFDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 59 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQYSSYPIT FGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотные последовательности тяжелой и легкой цепи mAb FS28-091 (с LALA)
SEQ ID NO: 60 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTNYA MSWVRQAPGKGLEWVSS IKPYDGNT YYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARNRWVFDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO 61 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQYSSSPFT FGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотные последовательности тяжелой и легкой цепи mAb FS28-185 (с LALA)
SEQ ID NO: 62 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTTSA MSWVRQAPGKGLEWVSR INPYEGET NYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARGWSIATYYKSAMDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 195 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQSSYSAPVT FGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотные последовательности и последовательности кДНК для тяжелой цепи mAb FS28-256 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 65 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTNTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARYNSYQGGLDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 66 Тяжелая цепь, ДНК (без LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTAACACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACTCTTACCAGGGTGGCTTGGACTACTGGGGCCAGGGAACCTTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAACTGCTGGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 67 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTNTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARYNSYQGGLDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 68 Тяжелая цепь, ДНК (с LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTAACACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACTCTTACCAGGGTGGCTTGGACTACTGGGGCCAGGGAACCTTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAAGCTGCCGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 69 Вариабельный домен, а/к
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTNTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARYNSYQGGLDY WGQGTLVTVSS
SEQ ID NO: 70 Вариабельный домен, ДНК
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTAACACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACTCTTACCAGGGTGGCTTGGACTACTGGGGCCAGGGAACCTTGGTCACCGTCTCGAGT
SEQ ID NO: 71 CDR1 (а/к) (IMGT) GFTFTNTY
SEQ ID NO: 72 CDR1 (а/к) (Кабат) NTYMS
SEQ ID NO: 73 CDR2 (а/к) (IMGT) ISPTYSTT
SEQ ID NO: 74 CDR2 (а/к) (Кабат) NISPTYSTTNYADSVKG
SEQ ID NO: 75 CDR3 (а/к) (IMGT) ARYNSYQGGLDY
SEQ ID NO: 76 CDR3 (а/к) (Кабат) YNSYQGGLDY
Аминокислотные последовательности и последовательности кДНК для легкой цепи mAb FS28-256 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 77 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQSYYYPIT FGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
SEQ ID NO: 78 Легкая цепь, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAATCTTATTATTATCCTATCACGTTCGGCCAAGGGACCAAGGTGGAAATCAAACGTACTGTGGCCGCTCCTAGCGTGTTCATTTTTCCGCCATCCGACGAGCAGCTCAAGTCCGGCACCGCCTCCGTGGTCTGCCTGCTCAACAACTTCTACCCTCGCGAAGCTAAGGTCCAGTGGAAGGTCGACAATGCCCTGCAGTCCGGAAACTCGCAGGAAAGCGTGACTGAACAGGACTCCAAGGACTCCACCTATTCACTGTCCTCGACTCTGACCCTGAGCAAGGCGGATTACGAAAAGCACAAAGTGTACGCATGCGAAGTGACCCACCAGGGTCTTTCGTCCCCCGTGACCAAGAGCTTCAACAGAGGAGAGTGT
SEQ ID NO: 79 Вариабельный домен, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQSYYYPIT FGQGTKVEIK
SEQ ID NO: 80 Вариабельный домен, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAATCTTATTATTATCCTATCACGTTCGGCCAAGGGACCAAGGTGGAAATCAAA
SEQ ID NO: 20 CDR1 (а/к) (IMGT) QSVSSSY
SEQ ID NO: 23 CDR1 (а/к) (Кабат) RASQSVSSSYLA
SEQ ID NO: 21 CDR2 (а/к) (IMGT) GAS
SEQ ID NO: 24 CDR2 (а/к) (Кабат) GASSRAT
SEQ ID NO: 25 CDR3 (а/к) (IMGT) QQSYYYPIT
SEQ ID NO: 25 CDR3 (а/к) (Кабат) QQSYYYPIT
Аминокислотные последовательности и последовательности кДНК для тяжелой цепи mAb FS28-256-001 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 81 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTETY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARYNSYQGGLDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 82 Тяжелая цепь, ДНК (без LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTGAGACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACTCTTACCAGGGTGGCTTGGACTACTGGGGCCAGGGAACCTTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAACTGCTGGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 89 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTETY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARYNSYQGGLDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 84 Тяжелая цепь, ДНК (с LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTGAGACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACTCTTACCAGGGTGGCTTGGACTACTGGGGCCAGGGAACCTTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAAGCTGCCGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 63 Вариабельный домен, а/к
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTETY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARYNSYQGGLDY WGQGTLVTVSS
SEQ ID NO: 64 Вариабельный домен, ДНК
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTGAGACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACTCTTACCAGGGTGGCTTGGACTACTGGGGCCAGGGAACCTTGGTCACCGTCTCGAGT
SEQ ID NO: 85 CDR1 (а/к) (IMGT) GFTFTETY
SEQ ID NO: 86 CDR1 (а/к) (Кабат) ETYMS
SEQ ID NO: 73 CDR2 (а/к) (IMGT) ISPTYSTT
SEQ ID NO: 74 CDR2 (а/к) (Кабат) NISPTYSTTNYADSVKG
SEQ ID NO: 75 CDR3 (а/к) (IMGT) ARYNSYQGGLDY
SEQ ID NO: 76 CDR3 (а/к) (Кабат) YNSYQGGLDY
Аминокислотные последовательности и последовательности кДНК для легкой цепи mAb FS28-256-001 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 83 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQHNQYPNT FGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
SEQ ID NO: 92 Легкая цепь, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAACATAATCAGTATCCGAATACGTTCGGCCAAGGGACCAAGGTGGAAATCAAACGTACTGTAGCAGCTCCTTCCGTGTTCATCTTTCCGCCCAGTGATGAGCAGCTGAAGTCAGGTACTGCTTCCGTGGTTTGCCTGCTCAACAACTTTTACCCCAGAGAAGCCAAAGTCCAGTGGAAAGTGGACAATGCGTTGCAAAGCGGGAACTCTCAGGAATCCGTCACAGAGCAGGACTCTAAGGACTCCACCTATAGCCTCTCTAGTACGCTGACACTGAGCAAAGCCGATTACGAGAAGCACAAGGTGTATGCCTGTGAGGTTACCCATCAAGGCCTTAGCTCACCAGTGACCAAGAGCTTCAATAGGGGAGAATGC
SEQ ID NO: 93 Вариабельный домен, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQHNQYPNT FGQGTKVEIK
SEQ ID NO: 94 Вариабельный домен, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAACATAATCAGTATCCGAATACGTTCGGCCAAGGGACCAAGGTGGAAATCAAA
SEQ ID NO: 20 CDR1 (а/к) (IMGT) QSVSSSY
SEQ ID NO: 23 CDR1 (а/к) (Кабат) RASQSVSSSYLA
SEQ ID NO: 21 CDR2 (а/к) (IMGT) GAS
SEQ ID NO: 24 CDR2 (а/к) (Кабат) GASSRAT
SEQ ID NO: 34 CDR3 (а/к) (IMGT) QQHNQYPNT
SEQ ID NO: 34 CDR3 (а/к) (Кабат) QQHNQYPNT
Аминокислотные последовательности и последовательности кДНК для тяжелой цепи mAb FS28-256-005 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 87 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTETY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARYNSYQGGLDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 88 Тяжелая цепь, ДНК (без LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTGAGACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACTCTTACCAGGGTGGCTTGGACTACTGGGGCCAGGGAACCTTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAACTGCTGGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 89 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTETY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARYNSYQGGLDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 84 Тяжелая цепь, ДНК (с LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTGAGACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACTCTTACCAGGGTGGCTTGGACTACTGGGGCCAGGGAACCTTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAAGCTGCCGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 63 Вариабельный домен, а/к
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTETY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARYNSYQGGLDY WGQGTLVTVSS
SEQ ID NO: 64 Вариабельный домен, ДНК
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTGAGACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACTCTTACCAGGGTGGCTTGGACTACTGGGGCCAGGGAACCTTGGTCACCGTCTCGAGT
SEQ ID NO: 85 CDR1 (а/к) (IMGT) GFTFTETY
SEQ ID NO: 86 CDR1 (а/к) (Кабат) ETYMS
SEQ ID NO: 73 CDR2 (а/к) (IMGT) ISPTYSTT
SEQ ID NO: 74 CDR2 (а/к) (Кабат) NISPTYSTTNYADSVKG
SEQ ID NO: 75 CDR3 (а/к) (IMGT) ARYNSYQGGLDY
SEQ ID NO: 76 CDR3 (а/к) (Кабат) YNSYQGGLDY
Аминокислотные последовательности и последовательности кДНК для легкой цепи mAb FS28-256-005 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 90 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQALGYPHT FGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
SEQ ID NO: 91 Легкая цепь, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAAGCTTTGGGTTATCCTCATACGTTCGGCCAAGGGACCAAGGTGGAAATCAAACGTACTGTAGCAGCTCCTTCCGTGTTCATCTTTCCGCCCAGTGATGAGCAGCTGAAGTCAGGTACTGCTTCCGTGGTTTGCCTGCTCAACAACTTTTACCCCAGAGAAGCCAAAGTCCAGTGGAAAGTGGACAATGCGTTGCAAAGCGGGAACTCTCAGGAATCCGTCACAGAGCAGGACTCTAAGGACTCCACCTATAGCCTCTCTAGTACGCTGACACTGAGCAAAGCCGATTACGAGAAGCACAAGGTGTATGCCTGTGAGGTTACCCATCAAGGCCTTAGCTCACCAGTGACCAAGAGCTTCAATAGGGGAGAATGC
SEQ ID NO: 53 Вариабельный домен, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQALGYPHT FGQGTKVEIK
SEQ ID NO: 54 Вариабельный домен, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAAGCTTTGGGTTATCCTCATACGTTCGGCCAAGGGACCAAGGTGGAAATCAAA
SEQ ID NO: 20 CDR1 (а/к) (IMGT) QSVSSSY
SEQ ID NO: 23 CDR1 (а/к) (Кабат) RASQSVSSSYLA
SEQ ID NO: 21 CDR2 (а/к) (IMGT) GAS
SEQ ID NO: 24 CDR2 (а/к) (Кабат) GASSRAT
SEQ ID NO: 43 CDR3 (а/к) (IMGT) QQALGYPHT
SEQ ID NO: 43 CDR3 (а/к) (Кабат) QQALGYPHT
Аминокислотные последовательности и последовательности кДНК для тяжелой цепи mAb FS28-256-012 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 105 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTHTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYC ARYNAYHAALDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 106 Тяжелая цепь, ДНК (без LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTCATACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAACAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCGTATCATGCTGCTCTGGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAACTGCTGGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 107 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTHTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYC ARYNAYHAALDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 108 Тяжелая цепь, ДНК (с LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTCATACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAACAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCGTATCATGCTGCTCTGGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAAGCTGCCGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 109 Вариабельный домен, а/к
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTHTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYC ARYNAYHAALDY WGQGTLVTVSS
SEQ ID NO: 110 Вариабельный домен, ДНК
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTCATACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAACAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCGTATCATGCTGCTCTGGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGT
SEQ ID NO: 98 CDR1 (а/к) (IMGT) GFTFTHTY
SEQ ID NO: 97 CDR1 (а/к) (Кабат) HTYMS
SEQ ID NO: 73 CDR2 (а/к) (IMGT) ISPTYSTT
SEQ ID NO: 74 CDR2 (а/к) (Кабат) NISPTYSTTNYADSVKG
SEQ ID NO: 99 CDR3 (а/к) (IMGT) ARYNAYHAALDY
SEQ ID NO: 100 CDR3 (а/к) (Кабат) YNAYHAALDY
Аминокислотные последовательности и последовательности кДНК для легкой цепи mAb FS28-256-012 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 77 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQSYYYPIT FGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
SEQ ID NO: 78 Легкая цепь, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAATCTTATTATTATCCTATCACGTTCGGCCAAGGGACCAAGGTGGAAATCAAACGTACTGTGGCCGCTCCTAGCGTGTTCATTTTTCCGCCATCCGACGAGCAGCTCAAGTCCGGCACCGCCTCCGTGGTCTGCCTGCTCAACAACTTCTACCCTCGCGAAGCTAAGGTCCAGTGGAAGGTCGACAATGCCCTGCAGTCCGGAAACTCGCAGGAAAGCGTGACTGAACAGGACTCCAAGGACTCCACCTATTCACTGTCCTCGACTCTGACCCTGAGCAAGGCGGATTACGAAAAGCACAAAGTGTACGCATGCGAAGTGACCCACCAGGGTCTTTCGTCCCCCGTGACCAAGAGCTTCAACAGAGGAGAGTGT
SEQ ID NO: 79 Вариабельный домен, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQSYYYPIT FGQGTKVEIK
SEQ ID NO: 80 Вариабельный домен, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAATCTTATTATTATCCTATCACGTTCGGCCAAGGGACCAAGGTGGAAATCAAA
SEQ ID NO: 20 CDR1 (а/к) (IMGT) QSVSSSY
SEQ ID NO: 23 CDR1 (а/к) (Кабат) RASQSVSSSYLA
SEQ ID NO: 21 CDR2 (а/к) (IMGT) GAS
SEQ ID NO: 24 CDR2 (а/к) (Кабат) GASSRAT
SEQ ID NO: 25 CDR3 (а/к) (IMGT) QQSYYYPIT
SEQ ID NO: 25 CDR3 (а/к) (Кабат) QQSYYYPIT
Аминокислотные последовательности и последовательности кДНК для тяжелой цепи mAb FS28-256-014 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 117 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTDTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARYNAYAAGLDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 118 Тяжелая цепь, ДНК (без LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTGATACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCGTATGCGGCGGGTCTTGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAACTGCTGGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 119 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTDTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARYNAYAAGLDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 120 Тяжелая цепь, ДНК (с LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTGATACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCGTATGCGGCGGGTCTTGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAAGCTGCCGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 115 Вариабельный домен, а/к
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTDTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARYNAYAAGLDY WGQGTLVTVSS
SEQ ID NO: 116 Вариабельный домен, ДНК
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTGATACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCGTATGCGGCGGGTCTTGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGT
SEQ ID NO: 111 CDR1 (а/к) (IMGT) GFTFTDTY
SEQ ID NO: 112 CDR1 (а/к) (Кабат) DTYMS
SEQ ID NO: 73 CDR2 (а/к) (IMGT) ISPTYSTT
SEQ ID NO: 74 CDR2 (а/к) (Кабат) NISPTYSTTNYADSVKG
SEQ ID NO: 113 CDR3 (а/к) (IMGT) ARYNAYAAGLDY
SEQ ID NO: 114 CDR3 (а/к) (Кабат) YNAYAAGLDY
Аминокислотные последовательности и последовательности кДНК для легкой цепи mAb FS28-256-014 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 77 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQSYYYPIT FGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
SEQ ID NO: 78 Легкая цепь, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAATCTTATTATTATCCTATCACGTTCGGCCAAGGGACCAAGGTGGAAATCAAACGTACTGTGGCCGCTCCTAGCGTGTTCATTTTTCCGCCATCCGACGAGCAGCTCAAGTCCGGCACCGCCTCCGTGGTCTGCCTGCTCAACAACTTCTACCCTCGCGAAGCTAAGGTCCAGTGGAAGGTCGACAATGCCCTGCAGTCCGGAAACTCGCAGGAAAGCGTGACTGAACAGGACTCCAAGGACTCCACCTATTCACTGTCCTCGACTCTGACCCTGAGCAAGGCGGATTACGAAAAGCACAAAGTGTACGCATGCGAAGTGACCCACCAGGGTCTTTCGTCCCCCGTGACCAAGAGCTTCAACAGAGGAGAGTGT
SEQ ID NO: 79 Вариабельный домен, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQSYYYPIT FGQGTKVEIK
SEQ ID NO: 80 Вариабельный домен, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAATCTTATTATTATCCTATCACGTTCGGCCAAGGGACCAAGGTGGAAATCAAA
SEQ ID NO: 20 CDR1 (а/к) (IMGT) QSVSSSY
SEQ ID NO: 23 CDR1 (а/к) (Кабат) RASQSVSSSYLA
SEQ ID NO: 21 CDR2 (а/к) (IMGT) GAS
SEQ ID NO: 24 CDR2 (а/к) (Кабат) GASSRAT
SEQ ID NO: 25 CDR3 (а/к) (IMGT) QQSYYYPIT
SEQ ID NO: 25 CDR3 (а/к) (Кабат) QQSYYYPIT
Аминокислотные последовательности и последовательности кДНК для тяжелой цепи mAb FS28-256-018 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 123 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTQTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARYNAYQIGLDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 124 Тяжелая цепь, ДНК (без LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTCAGACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCTTATCAGATTGGGTTGGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAACTGCTGGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 125 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTQTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARYNAYQIGLDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 126 Тяжелая цепь, ДНК (с LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTCAGACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCTTATCAGATTGGGTTGGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAAGCTGCCGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 121 Вариабельный домен, а/к
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTQTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARYNAYQIGLDY WGQGTLVTVSS
SEQ ID NO: 122 Вариабельный домен, ДНК
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTCAGACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCTTATCAGATTGGGTTGGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGT
SEQ ID NO: 101 CDR1 (а/к) (IMGT) GFTFTQTY
SEQ ID NO: 102 CDR1 (а/к) (Кабат) QTYMS
SEQ ID NO: 73 CDR2 (а/к) (IMGT) ISPTYSTT
SEQ ID NO: 74 CDR2 (а/к) (Кабат) NISPTYSTTNYADSVKG
SEQ ID NO: 103 CDR3 (а/к) (IMGT) ARYNAYQIGLDY
SEQ ID NO: 104 CDR3 (а/к) (Кабат) YNAYQIGLDY
Аминокислотные последовательности и последовательности кДНК для легкой цепи mAb FS28-256-018 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 77 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQSYYYPIT FGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
SEQ ID NO: 78 Легкая цепь, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAATCTTATTATTATCCTATCACGTTCGGCCAAGGGACCAAGGTGGAAATCAAACGTACTGTGGCCGCTCCTAGCGTGTTCATTTTTCCGCCATCCGACGAGCAGCTCAAGTCCGGCACCGCCTCCGTGGTCTGCCTGCTCAACAACTTCTACCCTCGCGAAGCTAAGGTCCAGTGGAAGGTCGACAATGCCCTGCAGTCCGGAAACTCGCAGGAAAGCGTGACTGAACAGGACTCCAAGGACTCCACCTATTCACTGTCCTCGACTCTGACCCTGAGCAAGGCGGATTACGAAAAGCACAAAGTGTACGCATGCGAAGTGACCCACCAGGGTCTTTCGTCCCCCGTGACCAAGAGCTTCAACAGAGGAGAGTGT
SEQ ID NO: 79 Вариабельный домен, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQSYYYPIT FGQGTKVEIK
SEQ ID NO: 80 Вариабельный домен, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAATCTTATTATTATCCTATCACGTTCGGCCAAGGGACCAAGGTGGAAATCAAA
SEQ ID NO: 20 CDR1 (а/к) (IMGT) QSVSSSY
SEQ ID NO: 23 CDR1 (а/к) (Кабат) RASQSVSSSYLA
SEQ ID NO: 21 CDR2 (а/к) (IMGT) GAS
SEQ ID NO: 24 CDR2 (а/к) (Кабат) GASSRAT
SEQ ID NO: 25 CDR3 (а/к) (IMGT) QQSYYYPIT
SEQ ID NO: 25 CDR3 (а/к) (Кабат) QQSYYYPIT
Аминокислотные последовательности и последовательности кДНК для тяжелой цепи mAb FS28-256-021 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 105 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTHTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYC ARYNAYHAALDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 106 Тяжелая цепь, ДНК (без LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTCATACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAACAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCGTATCATGCTGCTCTGGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAACTGCTGGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 107 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTHTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYC ARYNAYHAALDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 108 Тяжелая цепь, ДНК (с LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTCATACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAACAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCGTATCATGCTGCTCTGGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAAGCTGCCGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 109 Вариабельный домен, а/к
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTHTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYC ARYNAYHAALDY WGQGTLVTVSS
SEQ ID NO: 110 Вариабельный домен, ДНК
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTCATACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAACAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCGTATCATGCTGCTCTGGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGT
SEQ ID NO: 98 CDR1 (а/к) (IMGT) GFTFTHTY
SEQ ID NO: 97 CDR1 (а/к) (Кабат) HTYMS
SEQ ID NO: 73 CDR2 (а/к) (IMGT) ISPTYSTT
SEQ ID NO: 74 CDR2 (а/к) (Кабат) NISPTYSTTNYADSVKG
SEQ ID NO: 99 CDR3 (а/к) (IMGT) ARYNAYHAALDY
SEQ ID NO: 100 CDR3 (а/к) (Кабат) YNAYHAALDY
Аминокислотные последовательности и последовательности кДНК для легкой цепи mAb FS28-256-021 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 83 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQHNQYPNT FGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
SEQ ID NO: 92 Легкая цепь, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAACATAATCAGTATCCGAATACGTTCGGCCAAGGGACCAAGGTGGAAATCAAACGTACTGTAGCAGCTCCTTCCGTGTTCATCTTTCCGCCCAGTGATGAGCAGCTGAAGTCAGGTACTGCTTCCGTGGTTTGCCTGCTCAACAACTTTTACCCCAGAGAAGCCAAAGTCCAGTGGAAAGTGGACAATGCGTTGCAAAGCGGGAACTCTCAGGAATCCGTCACAGAGCAGGACTCTAAGGACTCCACCTATAGCCTCTCTAGTACGCTGACACTGAGCAAAGCCGATTACGAGAAGCACAAGGTGTATGCCTGTGAGGTTACCCATCAAGGCCTTAGCTCACCAGTGACCAAGAGCTTCAATAGGGGAGAATGC
SEQ ID NO: 93 Вариабельный домен, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQHNQYPNT FGQGTKVEIK
SEQ ID NO: 94 Вариабельный домен, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAACATAATCAGTATCCGAATACGTTCGGCCAAGGGACCAAGGTGGAAATCAAA
SEQ ID NO: 20 CDR1 (а/к) (IMGT) QSVSSSY
SEQ ID NO: 23 CDR1 (а/к) (Кабат) RASQSVSSSYLA
SEQ ID NO: 21 CDR2 (а/к) (IMGT) GAS
SEQ ID NO: 24 CDR2 (а/к) (Кабат) GASSRAT
SEQ ID NO: 34 CDR3 (а/к) (IMGT) QQHNQYPNT
SEQ ID NO: 34 CDR3 (а/к) (Кабат) QQHNQYPNT
Аминокислотные последовательности и последовательности кДНК для тяжелой цепи mAb FS28-256-023 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 123 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTQTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARYNAYQIGLDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 124 Тяжелая цепь, ДНК (без LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTCAGACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCTTATCAGATTGGGTTGGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAACTGCTGGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 125 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTQTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARYNAYQIGLDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 126 Тяжелая цепь, ДНК (с LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTCAGACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCTTATCAGATTGGGTTGGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAAGCTGCCGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 121 Вариабельный домен, а/к
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTQTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARYNAYQIGLDY WGQGTLVTVSS
SEQ ID NO: 122 Вариабельный домен, ДНК
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTCAGACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCTTATCAGATTGGGTTGGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGT
SEQ ID NO: 101 CDR1 (а/к) (IMGT) GFTFTQTY
SEQ ID NO: 102 CDR1 (а/к) (Кабат) QTYMS
SEQ ID NO: 73 CDR2 (а/к) (IMGT) ISPTYSTT
SEQ ID NO: 74 CDR2 (а/к) (Кабат) NISPTYSTTNYADSVKG
SEQ ID NO: 103 CDR3 (а/к) (IMGT) ARYNAYQIGLDY
SEQ ID NO: 104 CDR3 (а/к) (Кабат) YNAYQIGLDY
Аминокислотные последовательности и последовательности кДНК для тяжелой цепи mAb FS28-256-026 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 123 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTQTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARYNAYQIGLDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 124 Тяжелая цепь, ДНК (без LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTCAGACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCTTATCAGATTGGGTTGGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAACTGCTGGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 125 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTQTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARYNAYQIGLDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 126 Тяжелая цепь, ДНК (с LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTCAGACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCTTATCAGATTGGGTTGGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAAGCTGCCGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 121 Вариабельный домен, а/к
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTQTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYC ARYNAYQIGLDY WGQGTLVTVSS
SEQ ID NO: 122 Вариабельный домен, ДНК
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTCAGACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAGCAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCTTATCAGATTGGGTTGGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGT
SEQ ID NO: 101 CDR1 (а/к) (IMGT) GFTFTQTY
SEQ ID NO: 102 CDR1 (а/к) (Кабат) QTYMS
SEQ ID NO: 73 CDR2 (а/к) (IMGT) ISPTYSTT
SEQ ID NO: 74 CDR2 (а/к) (Кабат) NISPTYSTTNYADSVKG
SEQ ID NO: 103 CDR3 (а/к) (IMGT) ARYNAYQIGLDY
SEQ ID NO: 104 CDR3 (а/к) (Кабат) YNAYQIGLDY
Аминокислотные последовательности и последовательности кДНК для легкой цепи mAb FS28-256-023 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 83 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQHNQYPNT FGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
SEQ ID NO: 92 Легкая цепь, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAACATAATCAGTATCCGAATACGTTCGGCCAAGGGACCAAGGTGGAAATCAAACGTACTGTAGCAGCTCCTTCCGTGTTCATCTTTCCGCCCAGTGATGAGCAGCTGAAGTCAGGTACTGCTTCCGTGGTTTGCCTGCTCAACAACTTTTACCCCAGAGAAGCCAAAGTCCAGTGGAAAGTGGACAATGCGTTGCAAAGCGGGAACTCTCAGGAATCCGTCACAGAGCAGGACTCTAAGGACTCCACCTATAGCCTCTCTAGTACGCTGACACTGAGCAAAGCCGATTACGAGAAGCACAAGGTGTATGCCTGTGAGGTTACCCATCAAGGCCTTAGCTCACCAGTGACCAAGAGCTTCAATAGGGGAGAATGC
SEQ ID NO: 93 Вариабельный домен, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQHNQYPNT FGQGTKVEIK
SEQ ID NO: 94 Вариабельный домен, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAACATAATCAGTATCCGAATACGTTCGGCCAAGGGACCAAGGTGGAAATCAAA
SEQ ID NO: 20 CDR1 (а/к) (IMGT) QSVSSSY
SEQ ID NO: 23 CDR1 (а/к) (Кабат) RASQSVSSSYLA
SEQ ID NO: 21 CDR2 (а/к) (IMGT) GAS
SEQ ID NO: 24 CDR2 (а/к) (Кабат) GASSRAT
SEQ ID NO: 34 CDR3 (а/к) (IMGT) QQHNQYPNT
SEQ ID NO: 34 CDR3 (а/к) (Кабат) QQHNQYPNT
Аминокислотные последовательности и последовательности кДНК для тяжелой цепи mAb FS28-256-024 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 105 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTHTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYC ARYNAYHAALDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 106 Тяжелая цепь, ДНК (без LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTCATACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAACAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCGTATCATGCTGCTCTGGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAACTGCTGGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 107 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTHTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYC ARYNAYHAALDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 108 Тяжелая цепь, ДНК (с LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTCATACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAACAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCGTATCATGCTGCTCTGGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAAGCTGCCGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 109 Вариабельный домен, а/к
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTHTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYC ARYNAYHAALDY WGQGTLVTVSS
SEQ ID NO: 110 Вариабельный домен, ДНК
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTCATACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAACAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCGTATCATGCTGCTCTGGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGT
SEQ ID NO: 98 CDR1 (а/к) (IMGT) GFTFTHTY
SEQ ID NO: 97 CDR1 (а/к) (Кабат) HTYMS
SEQ ID NO: 73 CDR2 (а/к) (IMGT) ISPTYSTT
SEQ ID NO: 74 CDR2 (а/к) (Кабат) NISPTYSTTNYADSVKG
SEQ ID NO: 99 CDR3 (а/к) (IMGT) ARYNAYHAALDY
SEQ ID NO: 100 CDR3 (а/к) (Кабат) YNAYHAALDY
Аминокислотные последовательности и последовательности кДНК для легкой цепи mAb FS28-256-024 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 90 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQALGYPHT FGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
SEQ ID NO: 91 Легкая цепь, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAAGCTTTGGGTTATCCTCATACGTTCGGCCAAGGGACCAAGGTGGAAATCAAACGTACTGTAGCAGCTCCTTCCGTGTTCATCTTTCCGCCCAGTGATGAGCAGCTGAAGTCAGGTACTGCTTCCGTGGTTTGCCTGCTCAACAACTTTTACCCCAGAGAAGCCAAAGTCCAGTGGAAAGTGGACAATGCGTTGCAAAGCGGGAACTCTCAGGAATCCGTCACAGAGCAGGACTCTAAGGACTCCACCTATAGCCTCTCTAGTACGCTGACACTGAGCAAAGCCGATTACGAGAAGCACAAGGTGTATGCCTGTGAGGTTACCCATCAAGGCCTTAGCTCACCAGTGACCAAGAGCTTCAATAGGGGAGAATGC
SEQ ID NO: 53 Вариабельный домен, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQALGYPHT FGQGTKVEIK
SEQ ID NO: 54 Вариабельный домен, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAAGCTTTGGGTTATCCTCATACGTTCGGCCAAGGGACCAAGGTGGAAATCAAA
SEQ ID NO: 20 CDR1 (а/к) (IMGT) QSVSSSY
SEQ ID NO: 23 CDR1 (а/к) (Кабат) RASQSVSSSYLA
SEQ ID NO: 21 CDR2 (а/к) (IMGT) GAS
SEQ ID NO: 24 CDR2 (а/к) (Кабат) GASSRAT
SEQ ID NO: 43 CDR3 (а/к) (IMGT) QQALGYPHT
SEQ ID NO: 43 CDR3 (а/к) (Кабат) QQALGYPHT
Аминокислотные последовательности и последовательности кДНК для легкой цепи mAb FS28-256-026 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 90 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQALGYPHT FGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
SEQ ID NO: 91 Легкая цепь, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAAGCTTTGGGTTATCCTCATACGTTCGGCCAAGGGACCAAGGTGGAAATCAAACGTACTGTAGCAGCTCCTTCCGTGTTCATCTTTCCGCCCAGTGATGAGCAGCTGAAGTCAGGTACTGCTTCCGTGGTTTGCCTGCTCAACAACTTTTACCCCAGAGAAGCCAAAGTCCAGTGGAAAGTGGACAATGCGTTGCAAAGCGGGAACTCTCAGGAATCCGTCACAGAGCAGGACTCTAAGGACTCCACCTATAGCCTCTCTAGTACGCTGACACTGAGCAAAGCCGATTACGAGAAGCACAAGGTGTATGCCTGTGAGGTTACCCATCAAGGCCTTAGCTCACCAGTGACCAAGAGCTTCAATAGGGGAGAATGC
SEQ ID NO: 53 Вариабельный домен, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQALGYPHT FGQGTKVEIK
SEQ ID NO: 54 Вариабельный домен, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAAGCTTTGGGTTATCCTCATACGTTCGGCCAAGGGACCAAGGTGGAAATCAAA
SEQ ID NO: 20 CDR1 (а/к) (IMGT) QSVSSSY
SEQ ID NO: 23 CDR1 (а/к) (Кабат) RASQSVSSSYLA
SEQ ID NO: 21 CDR2 (а/к) (IMGT) GAS
SEQ ID NO: 24 CDR2 (а/к) (Кабат) GASSRAT
SEQ ID NO: 43 CDR3 (а/к) (IMGT) QQALGYPHT
SEQ ID NO: 43 CDR3 (а/к) (Кабат) QQALGYPHT
Аминокислотные последовательности и последовательности кДНК для тяжелой цепи mAb FS28-256-027 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 105 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTHTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYC ARYNAYHAALDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 106 Тяжелая цепь, ДНК (без LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTCATACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAACAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCGTATCATGCTGCTCTGGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAACTGCTGGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 107 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTHTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYC ARYNAYHAALDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 108 Тяжелая цепь, ДНК (с LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTCATACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAACAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCGTATCATGCTGCTCTGGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAAGCTGCCGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGACAGCCTCGAGAGCCTCAAGTGTACACCCTGCCTCCCTCTCGGGACGAGCTGACCAAGAACCAAGTCTCCCTGACCTGTCTGGTCAAGGGATTCTACCCATCGGATATCGCCGTGGAATGGGAAAGCAACGGACAGCCCGAGAACAACTACAAGACGACTCCGCCCGTGCTGGATTCCGACGGGAGCTTCTTCTTGTACTCCAAGCTGACCGTCGACAAGAGCAGATGGCAGCAGGGAAACGTGTTCTCCTGCTCCGTGATGCATGAGGCGCTGCACAACCACTACACTCAGAAGAGCTTGTCCCTGTCGCCCGGA
SEQ ID NO: 109 Вариабельный домен, а/к
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTHTY MSWVRQAPGKGLEWVSN ISPTYSTT NYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYC ARYNAYHAALDY WGQGTLVTVSS
SEQ ID NO: 110 Вариабельный домен, ДНК
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTCATACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCAATATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAACAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCGTATCATGCTGCTCTGGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGT
SEQ ID NO: 98 CDR1 (а/к) (IMGT) GFTFTHTY
SEQ ID NO: 97 CDR1 (а/к) (Кабат) HTYMS
SEQ ID NO: 73 CDR2 (а/к) (IMGT) ISPTYSTT
SEQ ID NO: 74 CDR2 (а/к) (Кабат) NISPTYSTTNYADSVKG
SEQ ID NO: 99 CDR3 (а/к) (IMGT) ARYNAYHAALDY
SEQ ID NO: 100 CDR3 (а/к) (Кабат) YNAYHAALDY
Аминокислотные последовательности и последовательности кДНК для легкой цепи mAb FS28-256-027 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 95 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQTVPYPYT FGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
SEQ ID NO: 96 Легкая цепь, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAAACTGTGCCGTATCCGTATACGTTCGGCCAAGGGACCAAGGTGGAAATCAAACGTACTGTGGCCGCTCCTAGCGTGTTCATTTTTCCGCCATCCGACGAGCAGCTCAAGTCCGGCACCGCCTCCGTGGTCTGCCTGCTCAACAACTTCTACCCTCGCGAAGCTAAGGTCCAGTGGAAGGTCGACAATGCCCTGCAGTCCGGAAACTCGCAGGAAAGCGTGACTGAACAGGACTCCAAGGACTCCACCTATTCACTGTCCTCGACTCTGACCCTGAGCAAGGCGGATTACGAAAAGCACAAAGTGTACGCATGCGAAGTGACCCACCAGGGTCTTTCGTCCCCCGTGACCAAGAGCTTCAACAGAGGAGAGTGT
SEQ ID NO: 56 Вариабельный домен, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQTVPYPYT FGQGTKVEIK
SEQ ID NO: 57 Вариабельный домен, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAAACTGTGCCGTATCCGTATACGTTCGGCCAAGGGACCAAGGTGGAAATCAAA
SEQ ID NO: 20 CDR1 (а/к) (IMGT) QSVSSSY
SEQ ID NO: 23 CDR1 (а/к) (Кабат) RASQSVSSSYLA
SEQ ID NO: 21 CDR2 (а/к) (IMGT) GAS
SEQ ID NO: 24 CDR2 (а/к) (Кабат) GASSRAT
SEQ ID NO: 44 CDR3 (а/к) (IMGT) QQTVPYPYT
SEQ ID NO: 44 CDR3 (а/к) (Кабат) QQTVPYPYT
SEQ ID NO: 175 Белок-предшественник MSLN человека cDNAAAGCTTGAATTCGCCGCCACCATGGCCCTGCCTACCGCTAGGCCTCTGCTCGGATCCTGCGGCACACCTGCCCTGGGAAGCCTCCTGTTCCTGCTGTTCTCCCTGGGCTGGGTGCAGCCCTCCAGAACACTGGCCGGCGAAACAGGACAAGAGGCTGCCCCTCTCGATGGCGTGCTCGCTAACCCCCCCAACATCAGCTCCCTGTCCCCTAGGCAGCTCCTGGGCTTTCCCTGTGCCGAGGTCAGCGGCCTCTCCACCGAGAGGGTGAGGGAGCTGGCTGTGGCCCTGGCTCAGAAGAACGTGAAACTGAGCACCGAGCAACTCAGGTGCCTGGCTCATAGGCTGTCCGAGCCCCCCGAGGATCTGGATGCCCTGCCTCTCGACCTGCTGCTGTTCCTGAACCCCGACGCTTTTAGCGGCCCCCAGGCCTGCACAAGGTTCTTCAGCAGAATCACCAAGGCCAACGTGGATCTGCTGCCCAGAGGCGCTCCCGAGAGGCAAAGACTGCTGCCCGCCGCTCTCGCCTGTTGGGGCGTCAGAGGATCCCTGCTGAGCGAGGCCGACGTGAGAGCCCTGGGCGGCCTGGCTTGTGATCTGCCCGGCAGGTTTGTCGCTGAGAGCGCCGAAGTGCTCCTGCCCAGACTGGTGAGCTGCCCTGGACCTCTGGACCAGGATCAACAGGAGGCCGCCAGAGCTGCTCTGCAGGGAGGAGGACCCCCCTACGGACCTCCTAGCACCTGGTCCGTGAGCACAATGGACGCCCTGAGAGGCCTGCTGCCTGTGCTGGGACAGCCCATCATTAGGAGCATTCCCCAGGGCATTGTGGCCGCCTGGAGACAGAGGAGCAGCAGGGACCCCTCCTGGAGGCAGCCTGAGAGAACAATCCTGAGGCCCAGATTCAGAAGAGAGGTGGAGAAAACCGCCTGCCCTAGCGGCAAGAAGGCCAGAGAGATTGACGAGAGCCTGATCTTCTATAAAAAGTGGGAGCTCGAAGCCTGCGTGGATGCTGCCCTGCTGGCCACACAGATGGACAGGGTGAACGCCATCCCCTTCACCTACGAGCAGCTGGACGTCCTGAAGCACAAGCTCGATGAGCTGTACCCCCAGGGCTACCCCGAGTCCGTGATTCAGCATCTCGGCTACCTGTTCCTGAAAATGAGCCCCGAAGACATCAGGAAGTGGAACGTGACAAGCCTGGAGACCCTCAAGGCCCTGCTGGAAGTGAACAAGGGACACGAGATGAGCCCCCAGGTGGCCACCCTCATCGACAGATTTGTGAAGGGAAGGGGACAGCTGGATAAGGACACCCTCGACACCCTGACCGCCTTCTACCCTGGATACCTCTGCAGCCTGTCCCCCGAAGAGCTGTCCAGCGTGCCTCCCTCCTCCATCTGGGCCGTCAGACCCCAGGATCTCGACACATGCGACCCCAGACAGCTGGATGTGCTGTACCCCAAGGCTAGGCTGGCCTTCCAGAACATGAACGGATCCGAATATTTCGTCAAAATCCAGAGCTTTCTGGGCGGAGCCCCCACAGAGGACCTCAAAGCCCTGAGCCAGCAGAACGTCAGCATGGACCTGGCCACCTTTATGAAACTGAGAACCGACGCCGTCCTCCCTCTGACAGTGGCCGAAGTGCAGAAGCTCCTGGGCCCCCATGTGGAAGGCCTGAAGGCCGAGGAGAGACACAGACCCGTGAGAGACTGGATTCTGAGGCAGAGGCAGGACGATCTGGATACCCTGGGCCTGGGACTGCAGGGCGGCATTCCTAACGGATACCTGGTCCTCGACCTGAGCATGCAGGAAGCCCTGAGCGGCACACCTTGTCTGCTGGGACCTGGCCCTGTCCTCACCGTGCTCGCTCTGCTGCTGGCTTCCACCCTCGCCTGATGAGCGGCCGC
Аминокислотные последовательности и последовательности кДНК для тяжелой цепи mAb FS28-256-271 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 176 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTHTY MSWVRQAPGKGLEWVSA ISPTYSTT NYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYC ARYNAYHAALDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 177 Тяжелая цепь, ДНК (без LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTCATACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCGCGATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAACAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCGTATCATGCTGCTCTGGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAACTGCTGGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGCCAGCCTCGAGAACCACAGGTGTACACCCTGCCCCCATCCCGGGATGAGCTGACCAAGAACCAGGTCAGCCTGACCTGCCTGGTCAAAGGCTTCTATCCCAGCGACATCGCCGTGGAGTGGGAGAGCAATGGGCAGCCGGAGAACAACTACAAGACCACGCCTCCCGTGCTGGACTCCGACGGATCCTTCTTCCTCTACAGCAAGCTCACCGTGGACAAGAGCAGGTGGCAGCAGGGGAACGTCTTCTCCTGCAGCGTGATGCATGAGGCTCTGCACAACCACTACACACAGAAGAGCCTCTCCCTGTCTCCGGGT
SEQ ID NO: 178 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTHTY MSWVRQAPGKGLEWVSA ISPTYSTT NYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYC ARYNAYHAALDY WGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 179 Тяжелая цепь, ДНК (с LALA)
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTCATACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCGCGATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAACAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCGTATCATGCTGCTCTGGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGTGCTAGCACTAAGGGCCCGTCGGTGTTCCCGCTGGCCCCATCGTCCAAGAGCACATCAGGGGGTACCGCCGCCCTGGGCTGCCTTGTGAAGGATTACTTTCCCGAGCCCGTCACAGTGTCCTGGAACAGCGGAGCCCTGACCTCCGGAGTGCATACTTTCCCGGCTGTGCTTCAGTCCTCTGGCCTGTACTCATTGTCCTCCGTGGTCACCGTCCCTTCGTCCTCCCTGGGCACCCAGACCTATATCTGTAATGTCAACCATAAGCCCTCGAACACCAAGGTCGACAAGAAGGTCGAGCCGAAGTCGTGCGACAAGACTCACACTTGCCCGCCTTGCCCAGCCCCGGAAGCTGCCGGTGGTCCTTCGGTGTTCCTCTTCCCGCCCAAGCCGAAGGATACCCTGATGATCTCACGGACCCCCGAAGTGACCTGTGTGGTGGTGGACGTGTCCCACGAGGACCCGGAAGTGAAATTCAATTGGTACGTGGATGGAGTGGAAGTGCACAACGCCAAGACCAAGCCACGGGAAGAACAGTACAACTCTACCTACCGCGTGGTGTCCGTGCTCACTGTGCTGCACCAAGACTGGCTGAACGGGAAGGAGTACAAGTGCAAAGTGTCCAACAAGGCGCTGCCTGCCCCAATTGAGAAAACTATCTCGAAAGCCAAGGGCCAGCCTCGAGAACCACAGGTGTACACCCTGCCCCCATCCCGGGATGAGCTGACCAAGAACCAGGTCAGCCTGACCTGCCTGGTCAAAGGCTTCTATCCCAGCGACATCGCCGTGGAGTGGGAGAGCAATGGGCAGCCGGAGAACAACTACAAGACCACGCCTCCCGTGCTGGACTCCGACGGATCCTTCTTCCTCTACAGCAAGCTCACCGTGGACAAGAGCAGGTGGCAGCAGGGGAACGTCTTCTCCTGCAGCGTGATGCATGAGGCTCTGCACAACCACTACACACAGAAGAGCCTCTCCCTGTCTCCGGGT
SEQ ID NO: 180 Вариабельный домен, а/к
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTHTY MSWVRQAPGKGLEWVSA ISPTYSTT NYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYC ARYNAYHAALDY WGQGTLVTVSS
SEQ ID NO: 181 Вариабельный домен, ДНК
GAAGTGCAACTGCTGGAGTCCGGTGGTGGTCTGGTACAGCCGGGTGGTTCTCTGCGTCTGAGTTGCGCGGCCAGTGGCTTTACCTTCACTCATACTTATATGAGCTGGGTGCGTCAGGCTCCGGGCAAAGGTCTGGAATGGGTTAGCGCGATTTCTCCGACTTATAGCACTACCAACTATGCGGATAGCGTGAAAGGCCGTTTTACCATTTCTCGCGACAACAACAAGAACACGCTGTACCTGCAGATGAACTCACTGCGTGCCGAAGATACGGCCGTGTATTACTGTGCGAGATACAACGCGTATCATGCTGCTCTGGACTACTGGGGCCAGGGAACCCTGGTCACCGTCTCGAGT
SEQ ID NO: 98 CDR1 (а/к) (IMGT) GFTFTHTY
SEQ ID NO: 97 CDR1 (а/к) (Кабат) HTYMS
SEQ ID NO: 73 CDR2 (а/к) (IMGT) ISPTYSTT
SEQ ID NO: 182 CDR2 (а/к) (Кабат) AISPTYSTTNYADSVKG
SEQ ID NO: 99 CDR3 (а/к) (IMGT) ARYNAYHAALDY
SEQ ID NO: 100 CDR3 (а/к) (Кабат) YNAYHAALDY
Аминокислотные последовательности и последовательности кДНК для легкой цепи mAb FS28-256-271 и ее вариабельного домена, и аминокислотная последовательность CDR-областей
SEQ ID NO: 95 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQTVPYPYT FGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
SEQ ID NO: 96 Легкая цепь, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAAACTGTGCCGTATCCGTATACGTTCGGCCAAGGGACCAAGGTGGAAATCAAACGTACTGTGGCCGCTCCTAGCGTGTTCATTTTTCCGCCATCCGACGAGCAGCTCAAGTCCGGCACCGCCTCCGTGGTCTGCCTGCTCAACAACTTCTACCCTCGCGAAGCTAAGGTCCAGTGGAAGGTCGACAATGCCCTGCAGTCCGGAAACTCGCAGGAAAGCGTGACTGAACAGGACTCCAAGGACTCCACCTATTCACTGTCCTCGACTCTGACCCTGAGCAAGGCGGATTACGAAAAGCACAAAGTGTACGCATGCGAAGTGACCCACCAGGGTCTTTCGTCCCCCGTGACCAAGAGCTTCAACAGAGGAGAGTGT
SEQ ID NO: 56 Вариабельный домен, а/к
EIVLTQSPGTLSLSPGERATLSCRAS QSVSSSY LAWYQQKPGQAPRLLIY GAS SRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYC QQTVPYPYT FGQGTKVEIK
SEQ ID NO: 57 Вариабельный домен, ДНК
GAAATTGTGCTGACCCAGTCTCCGGGCACGTTATCTCTGAGCCCTGGTGAGCGCGCCACTCTGTCATGCCGGGCTTCTCAAAGTGTTAGCAGTAGCTACCTGGCGTGGTATCAGCAAAAACCGGGCCAGGCCCCGCGTCTGCTGATTTACGGTGCATCCAGCCGTGCCACCGGCATTCCAGATCGTTTTTCCGGTAGTGGTTCTGGGACGGACTTCACTCTGACAATCTCACGCCTGGAACCGGAGGATTTTGCGGTGTATTACTGCCAGCAAACTGTGCCGTATCCGTATACGTTCGGCCAAGGGACCAAGGTGGAAATCAAA
SEQ ID NO: 20 CDR1 (а/к) (IMGT) QSVSSSY
SEQ ID NO: 23 CDR1 (а/к) (Кабат) RASQSVSSSYLA
SEQ ID NO: 21 CDR2 (а/к) (IMGT) GAS
SEQ ID NO: 24 CDR2 (а/к) (Кабат) GASSRAT
SEQ ID NO: 44 CDR3 (а/к) (IMGT) QQTVPYPYT
SEQ ID NO: 44 CDR3 (а/к) (Кабат) QQTVPYPYT
Аминокислотные последовательности тяжелой и легкой цепи mAb2 FS22-053-008/FS28-024
SEQ ID NO: 143 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTLSYSSMSWVRQAPGKGLEWVSFITPSTGYTHYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARRALTFDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 144 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTLSYSSMSWVRQAPGKGLEWVSFITPSTGYTHYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARRALTFDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 16 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQASSYPLTFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотная последовательность тяжелой и легкой цепи mAb2 FS22-053-008/FS28-024-051
SEQ ID NO: 145 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTLSYSSMSWVRQAPGKGLEWVSFITPSTGYTHYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARRALIFDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 146 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTLSYSSMSWVRQAPGKGLEWVSFITPSTGYTHYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARRALIFDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 16 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQASSYPLTFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотная последовательность тяжелой и легкой цепи mAb2 FS22-053-008/FS28-024-052
SEQ ID NO: 147 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTLSYSSMSWVRQAPGKGLEWVSFITPSTGYTHYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARRALLFDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 148 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTLSYSSMSWVRQAPGKGLEWVSFITPSTGYTHYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARRALLFDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 16 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQASSYPLTFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотная последовательность тяжелой и легкой цепи mAb2 FS22-053-008/FS28-024-053
SEQ ID NO: 149 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTLSYSSMSWVRQAPGKGLEWVSFITPSTGYTHYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARRALVFDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID BO: 150 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTLSYSSMSWVRQAPGKGLEWVSFITPSTGYTHYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARRALVFDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 16 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQASSYPLTFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотные последовательности тяжелой и легкой цепи mAb2 FS22-053-008-AA/FS28-024-060 (с LALA)
SEQ ID NO: 151 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTLSYSSMSWVRQAPGKGLEWVSFITPSTGYTHYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARRALWFDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 16 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQASSYPLTFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотные последовательности тяжелой и легкой цепи mAb2 FS22-053-008-AA/FS28-026 (с LALA)
SEQ ID NO: 152 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSNYAMTWVRQAPGKGLEWVSSITPYYSKTDYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARNWYRFDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 59 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQYSSYPITFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотные последовательности тяжелой и легкой цепи mAb2 FS22-053-008-AA/FS28-091 (с LALA)
SEQ ID NO: 153 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFTNYAMSWVRQAPGKGLEWVSSIKPYDGNTYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARNRWVFDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 61 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQYSSSPFTFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотные последовательности тяжелой и легкой цепи mAb2 FS22-053-008-AA/FS28-185 (с LALA)
SEQ ID NO: 154 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFTTSAMSWVRQAPGKGLEWVSRINPYEGETNYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARGWSIATYYKSAMDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 195 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQSSYSAPVTFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотные последовательности тяжелой и легкой цепи mAb2 FS22-053-008/FS28-256
SEQ ID NO: 155 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFTNTYMSWVRQAPGKGLEWVSNISPTYSTTNYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARYNSYQGGLDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 156 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFTNTYMSWVRQAPGKGLEWVSNISPTYSTTNYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARYNSYQGGLDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 77 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQSYYYPITFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотные последовательности и последовательности кДНК для тяжелой и легкой цепи mAb2 FS22-053-008/FS28-256-001
SEQ ID NO: 157 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFTETYMSWVRQAPGKGLEWVSNISPTYSTTNYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARYNSYQGGLDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 158 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFTETYMSWVRQAPGKGLEWVSNISPTYSTTNYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARYNSYQGGLDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 83 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQHNQYPNTFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотные последовательности и последовательности кДНК для тяжелой и легкой цепи mAb2 FS22-053-008/FS28-256-005
SEQ ID NO: 159 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFTETYMSWVRQAPGKGLEWVSNISPTYSTTNYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARYNSYQGGLDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 160 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFTETYMSWVRQAPGKGLEWVSNISPTYSTTNYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARYNSYQGGLDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 90 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQALGYPHTFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотные последовательности и последовательности кДНК для тяжелой и легкой цепи mAb2 FS22-053-008/FS28-256-012
SEQ ID NO: 127 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFTHTYMSWVRQAPGKGLEWVSNISPTYSTTNYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYCARYNAYHAALDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 128 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFTHTYMSWVRQAPGKGLEWVSNISPTYSTTNYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYCARYNAYHAALDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 77 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQSYYYPITFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотные последовательности и последовательности кДНК для тяжелой и легкой цепи mAb2 FS22-053-008/FS28-256-014
SEQ ID NO: 129 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFTDTYMSWVRQAPGKGLEWVSNISPTYSTTNYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARYNAYAAGLDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 130 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFTDTYMSWVRQAPGKGLEWVSNISPTYSTTNYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARYNAYAAGLDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 77 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQSYYYPITFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотные последовательности и последовательности кДНК для тяжелой и легкой цепи mAb2 FS22-053-008/FS28-256-018
SEQ ID NO: 131 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFTQTYMSWVRQAPGKGLEWVSNISPTYSTTNYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARYNAYQIGLDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 132 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFTQTYMSWVRQAPGKGLEWVSNISPTYSTTNYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARYNAYQIGLDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 77 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQSYYYPITFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотные последовательности и последовательности кДНК для тяжелой и легкой цепи mAb2 FS22-053-008/FS28-256-021
SEQ ID NO: 133 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFTHTYMSWVRQAPGKGLEWVSNISPTYSTTNYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYCARYNAYHAALDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 134 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFTHTYMSWVRQAPGKGLEWVSNISPTYSTTNYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYCARYNAYHAALDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 83 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQHNQYPNTFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотные последовательности и последовательности кДНК для тяжелой и легкой цепи mAb2 FS22-053-008/FS28-256-023
SEQ ID NO: 135 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFTQTYMSWVRQAPGKGLEWVSNISPTYSTTNYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARYNAYQIGLDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 136 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFTQTYMSWVRQAPGKGLEWVSNISPTYSTTNYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARYNAYQIGLDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 83 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQHNQYPNTFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотные последовательности и последовательности кДНК для тяжелой и легкой цепи mAb2 FS22-053-008/FS28-256-024
SEQ ID NO: 137 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFTHTYMSWVRQAPGKGLEWVSNISPTYSTTNYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYCARYNAYHAALDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 138 Тяжелая цепь, а/к (с LALA) EVQLLESGGGLVQPGGSLRLSCAASGFTFTHTYMSWVRQAPGKGLEWVSNISPTYSTTNYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYCARYNAYHAALDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 90 Легкая цепь, а/к EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQALGYPHTFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотные последовательности тяжелой и легкой цепи FS22-053-008/FS28-256-026
SEQ ID NO: 139 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFTQTYMSWVRQAPGKGLEWVSNISPTYSTTNYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARYNAYQIGLDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO:140 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFTQTYMSWVRQAPGKGLEWVSNISPTYSTTNYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARYNAYQIGLDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 90 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQALGYPHTFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотные последовательности тяжелой и легкой цепи mAb2 FS22-053-008/FS28-256-027
SEQ ID NO: 141 Тяжелая цепь, а/к (без LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFTHTYMSWVRQAPGKGLEWVSNISPTYSTTNYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYCARYNAYHAALDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 142 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFTHTYMSWVRQAPGKGLEWVSNISPTYSTTNYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYCARYNAYHAALDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELNPPYLFSNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDYWRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 95 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQTVPYPYTFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотные последовательности тяжелой и легкой цепи mAb2 FS22-172-003-AA/FS28-256-271
SEQ ID NO: 187 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFTHTYMSWVRQAPGKGLEWVSAISPTYSTTNYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYCARYNAYHAALDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELPYIIPPYNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVGADRWLEGNVFSCSVMHEALHNHYTQKSLSLSPGSEQ ID NO: 188 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQTVPYPYTFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотные последовательности тяжелой и легкой цепи mAb2 OX40 (FS20-022-049)/FS28-256-271
SEQ ID NO: 189 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFTHTYMSWVRQAPGKGLEWVSAISPTYSTTNYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYCARYNAYHAALDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDEYWDQEVSLTCLVKGFYPSDIAVEWESNGDEQFAYKTTPPVLDSDGSFFLYSKLTVDQYRWNPADYFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 190 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQTVPYPYTFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотные последовательности тяжелой и легкой цепи mAb FS28m-228 (с LALA)
SEQ ID NO: 161 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSTYFMVWVRQAPGKGLEWVSMISPKSSNTYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARWFTPARFDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 162 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQPFPFSFTFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотная последовательность тяжелой и легкой цепи mAb2 FS22-063-AA/FS28m-228 (с LALA)
SEQ ID NO: 163 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAASGFTFSTYFMVWVRQAPGKGLEWVSMISPKSSNTYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARWFTPARFDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDEPYWSYVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVMNYRWELGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 164 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQPFPFSFTFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотная последовательность тяжелой и легкой цепи mAb2 FS22m-063-AA/FS28m-228-010
SEQ ID NO: 196 Тяжелая цепь, а/к (с LALA) EVQLLESGGGLVQPGGSLRLSCAASGFTFSTYFMVWVRQAPGKGLEWVSMISPKSSNTYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARYHISPRFDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDEPYWSYVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVMNYRWELGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 197 Легкая цепь, а/к
EIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQPFPFSFTFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотная последовательность тяжелой и легкой цепи mAb2 FS22m-063-AA/HelD1.3 (с LALA)
SEQ ID NO: 191 Тяжелая цепь, а/к (с LALA)
QVQLQESGPGLVRPSQTLSLTCTVSGSTFSGYGVNWVRQPPGRGLEWIGMIWGDGNTDYNSALKSRVTMLVDTSKNQFSLRLSSVTAADTAVYYCARERDYRLDYWGQGSLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDEPYWSYVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVMNYRWELGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 192 Легкая цепь, а/к
DIQMTQSPASLSASVGETVTITCRASGNIHNYLAWYQQKQGKSPQLLVYNAKTLADGVPSRFSGSGSGTQYSLKINSLQPEDFGSYYCQHFWSTPRTFGGGTKLEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотная последовательность тяжелой и легкой цепи mAb2 FS22m-063-AA/4420 (с LALA)
SEQ ID NO: 193 Тяжелая цепь, а/к (с LALA)
EVKLDETGGGLVQPGRPMKLSCVASGFTFSDYWMNWVRQSPEKGLEWVAQIRNKPYNYETYYSDSVKGRFTISRDDSKSSVYLQMNNLRVEDMGIYYCTGSYYGMDYWGQGTSVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDEPYWSYVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVMNYRWELGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 194 Легкая цепь, а/к
DVVMTQTPLSLPVSLGDQASISCRSSQSLVHSNGNTYLRWYLQKPGQSPKVLIYKVSNRFSGVPDRFSGSGSGTDFTLKISRVEAEDLGVYFCSQSTHVPWTFGGGTKLEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотная последовательность тяжелой и легкой цепи mAb G1-AA/HelD1.3 (с LALA)
SEQ ID NO: 165 Тяжелая цепь, а/к (с LALA)
QVQLQESGPGLVRPSQTLSLTCTVSGSTFSGYGVNWVRQPPGRGLEWIGMIWGDGNTDYNSALKSRVTMLVDTSKNQFSLRLSSVTAADTAVYYCARERDYRLDYWGQGSLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 166 Легкая цепь, а/к
DIQMTQSPASLSASVGETVTITCRASGNIHNYLAWYQQKQGKSPQLLVYNAKTLADGVPSRFSGSGSGTQYSLKINSLQPEDFGSYYCQHFWSTPRTFGGGTKLEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Аминокислотная последовательность тяжелой и легкой цепи mAb G1-AA/SS1 (с LALA)
SEQ ID NO: 167 Тяжелая цепь (с LALA)
QVQLQQSGPELEKPGASVKISCKASGYSFTGYTMNWVKQSHGKSLEWIGLITPYNGASSYNQKFRGKATLTVDKSSSTAYMDLLSLTSEDSAVYFCARGGYDGRGFDYWGSGTPVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SEQ ID NO: 168 Легкая цепь
DIELTQSPAIMSASPGEKVTMTCSASSSVSYMHWYQQKSGTSPKRWIYDTSKLASGVPGRFSGSGSGNSYSLTISSVEAEDDATYYCQQWSKHPLTFGSGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
MSLN-His-Avi
Мезотелин (без MPF и С-конца) (показан)
His- и Avi-метки (не показаны)
SEQ ID NO: 169 Человек
EVEKTACPSGKKAREIDESLIFYKKWELEACVDAALLATQMDRVNAIPFTYEQLDVLKHKLDELYPQGYPESVIQHLGYLFLKMSPEDIRKWNVTSLETLKALLEVNKGHEMSPQVATLIDRFVKGRGQLDKDTLDTLTAFYPGYLCSLSPEELSSVPPSSIWAVRPQDLDTCDPRQLDVLYPKARLAFQNMNGSEYFVKIQSFLGGAPTEDLKALSQQNVSMDLATFMKLRTDAVLPLTVAEVQKLLGPHVEGLKAEERHRPVRDWILRQRQDDLDTLGLGLQGGIPNGYLVLDLSMQEALS
SEQ ID NO: 170 Яванский макак
DVERTTCPPEKEVHEIDESLIFYKKRELEACVDAALLAAQMDRVDAIPFTYEQLDVLKHKLDELYPQGYPESVIRHLGHLFLKMSPEDIRKWNVTSLETLKALLKVSKGHEMSAQVATLIDRVVVGRGQLDKDTADTLTAFCPGCLCSLSPERLSSVPPSIIGAVRPQDLDTCGPRQLDVLYPKARLAFQNMSGSEYFVKIRPFLGGAPTEDLKALSQQNVSMDLATFMKLRREAVLPLSVAEVQKLLGPHVEGLKVEEQHSPVRDWILKQRQDDLDTLGLGLQGGIPNGYLILDLSVREALS
SEQ ID NO: 171 Мышь
DAEQKACPPGKEPYKVDEDLIFYQNWELEACVDGTMLARQMDLVNEIPFTYEQLSIFKHKLDKTYPQGYPESLIQQLGHFFRYVSPEDIHQWNVTSPDTVKTLLKVSKGQKMNAQAIALVACYLRGGGQLDEDMVKALGDIPLSYLCDFSPQDLHSVPSSVMWLVGPQDLDKCSQRHLGLLYQKACSAFQNVSGLEYFEKIKTFLGGASVKDLRALSQHNVSMDIATFKRLQVDSLVGLSVAEVQKLLGPNIVDLKTEEDKSPVRDWLFRQHQKDLDRLGLGLQGGIPNGYLVLDFNVREAFS
Аминокислотная последовательность CH3-домена дикого типа
SEQ ID NO: 172
GQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
Аминокислотная последовательность CH2-домена, содержащего мутацию LALA (мутация LALA выделена жирным шрифтом и подчеркнута)
SEQ ID NO: 173
APEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAK
Аминокислотная последовательность CH2-домена, содержащего мутацию LALA-PA (мутация LALA-PA выделена жирным шрифтом и подчеркнута)
SEQ ID NO: 174
APEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALAAPIEKTISKAK
Аминокислотные последовательности структурных петель CH3-домена Fcab FS22-172-003
Первая последовательность FS22-172-003 - PYIIPPY (SEQ ID NO: 198)
Вторая последовательность FS22-172-003 - GADRWLE (SEQ ID NO: 199)
Аминокислотные последовательности и последовательности кДНК для легкой цепи FS22-172-003-AA/FS28-256-271
SEQ ID NO: 200 Легкая цепь, а/кEIVLTQSPGTLSLSPGERATLSCRASQSVSSSYLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQTVPYPYTFGQGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
SEQ ID NO: 201 Тяжелая цепь, а/к (с LALA)
EVQLLESGGGLVQPGGSLRLSCAAS GFTFTHTY MSWVRQAPGKGLEWVSA ISPTYSTT NYADSVKGRFTISRDNNKNTLYLQMNSLRAEDTAVYYC ARYNAYHAALDY WGQGTLVTVSS ASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCP APEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELPYIIPPYNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVGADRWLEGNVFSCSVMHEALHNHYTQKSLSLSPG
Ссылки
Полное содержание всех документов, упомянутых в настоящем описании, включено в настоящее описание посредством ссылки.
Altschul SF, Gish W, Miller W, Myers EW, Lipman DJ. Basic local alignment search tool. J. Mol. Biol. 215(3), 403-10 (1990).
Altschul SF, Madden TL, Schäffer AA, Zhang J, Zhang Z, Miller W, Lipman DJ. Gapped BLAST and PSI-BLAST: a new generation of protein database search programs. Nucleic Acids Res. 25(17), 3389-402 (1997).
Andrade VC, Vettore AL, Felix RS, Almeida MS, Carvalho F, Oliveira JS, Chauffaille ML, Andriolo A, Caballero OL, Zago MA, Colleoni GW. Prognostic impact of cancer/testis antigen expression in advanced stage multiple myeloma patients. Cancer Immun. 8, 2 (2008).
Asgarov K, Balland J, Tirole C, Bouard A, Mougey V, Ramos D, Barroso A, Zangiacomi V, Jary M, Kim S, Gonzalez-Pajuelo M, Royer B, de Haard H, Clark A, Wijdenes J and Borg C (2017). A new anti-mesothelin antibody targets selectively the membrane-associated form. Mabs 9:567-577.
Bagshawe KD, Sharma SK, Springer CJ, Antoniw P, Rogers GT, Burke PJ, Melton R. Antibody-enzyme conjugates can generate cytotoxic drugs from inactive precursors at tumor sites. Antibody, Immunoconjugates and Radiopharmaceuticals 4, 915-922 (1991).
Bhome R, Bullock MD, Al Saihati HA, Goh RW, Primrose JN, Sayan AE, Mirnezami AH. A top-down view of the tumor microenvironment: structure, cells and signaling. Front. Cel. Dev. Biol. 3, 33 (2015).
Brinkmann U, Kontermann RE. The making of bispecific antibodies. MAbs (9)2, 182-212 (2017)
Bruhns P, Iannascoli B, England P, Mancardi DA, Fernandez N, Jorieux S, Daëron M. Specificity and affinity of human Fcγ receptors and their polymorphic variants for human IgG subclasses. Blood 113(16), 3716-25 (2009).
Carter P, Smith L, Ryan M. Identification and validation of cell surface antigens for antibody targeting in oncology. Endocr. Relat. Cancer 11(4), 659-87 (2004).
Cheever MA, Allison JP, Ferris AS, Finn OJ, Hastings BM, Hecht TT, Mellman I, Prindiville SA, Viner JL, Weiner LM, Matrisian LM. Clin. Cancer Res. 15(17), 5323-37 (2009).
Chen SH, Hung WC, Wang P, Paul C, Konstantopoulos K (2013). Mesothelin binding to CA125/MUC16 promotes pancreatic cancer cell motility and invasion via MMP-7 activation. Sci Rep.3: 1870.
Chen DS, Mellman I. Oncology meets immunology: the cancer-immunity cycle. Immunity 39(1), 1-10 (2013).
Creaney J, Dick IM and Robinson BW (2015). Discovery of new biomarkers for malignant mesothelioma. Curr Pulmonol Rep. 4: 15-21.
Cui A, Jin X0G, Zhai K, Tong Z-H and Shi H-Z (2014). Diagnostic values of soluble mesothelin-related peptides for malignant pleural mesothelioma: updated meta-analysis. BMJ Open 4: e004145.
Grisshammer, R. and Nagai, K. (1995) Purification of overproduced proteins from E. coli cells In: DNA Cloning 2: Expression systems (Rickwood, D. and Hames, B.D., Eds.), The Practical Approach Series, pp. 59-92. IRL Press, Oxford University Press.
Gubin MM, Artyomov MN, Mardis ER, Schreiber RD. Tumor neoantigens: building a framework for personalized cancer immunotherapy. J. Clin. Invest. 125(9), 3413-21 (2015).
Gure AO, Chua R, Williamson B, Gonen M, Ferrera CA, Gnjatic S, Ritter G, Simpson AJ, Chen YT, Old LJ, Altorki NK. Cancer-testis genes are coordinately expressed and are markers of poor outcome in non-small cell lung cancer. Clin. Cancer Res. 11(22), 8055-62 (2005).
Hassan R, Kindler HL, Jahan T, Bazhenova L, Reck M, Thomas A, Pastan I, Parno J, O’Shannessy DJ, Fatato P, Maltzman JD and Wallin BA (2014). Phase II clinical trial of amatuximab, a chimeric antimesothelin antibody with pemetrexed and cisplatin in advanced unresectable pleural mesothelioma. Clin. Canc. Res. 20:5927-5936.
Hassan R, Kreitman RJ, Pastan I and Willingham MC (2005). Localization of mesothelin in epithelial ovarian cancer. Appl Immunohistochem Mol Morphol AIMM Off Publ Soc Appl Immunohistochem13:243-47;
Hassan R, Lerner MR, Benbrook D, Lightfoot SA, Brackett DJ, Wang QC and Pastan I (2002). Clin. Cancer Res.: 8: 3520-3526.
Hassan R, Thomas, A, Alewine, C, Le, DT, Jaffee, EM and Pastan I (2016). Mesothelin immunotherapy for cancer: ready for prime time? J. Clin. Onc. 34:4171-4180.
Hezareh M, Hessell AJ, Jensen RC, van de Winkel JG and Parren PW. Effector function activities of a panel of mutants of a broadly neutralizing antibody against human immunodeficiency virus type 1. J. Virol. 75(24), 12161-8 (2001).
Hezareh M, Hessell AJ, Jensen RC, van de Winkel JG, Parren PW. Effector function activities of a panel of mutants of a broadly neutralizing antibody against human immunodeficiency virus type 1. J. Virol. 75(24), 12161-8 (2001).
Hollevoet K, Reitsma JB, Creaney J, Grigoriu, BD, Robinson BW, Scherpereel A, Cristaudo A, Pass HI, Nackaerts K, Rodriques Portal JA, Schneider J, Muley, T, Di Serio F, Baas P, Tomasetti M, Rai AJ and van Meerbeeck JP. Serum mesothelin for diagnosing malignant pleural mesothelioma: an individual patient data meta-analysis. J Clin. Oncol. 30 (13),1541-1549 (2012).
Holliger P, Hudson PJ. Engineered antibody fragments and the rise of single domains. Nat. Biotechnol. 23(9), 1126-36 (2005).
Idusogie EE, Presta LG, Gazzano-Santoro H, Totpal K, Wong PY, Ultsch M, Meng YG, Mulkerrin MG. Mapping of the C1q binding site on rituxan, a chimeric antibody with a human IgG1 Fc. J. Immunol. 164(8), 4178-84 (2000).
Kabat EA, Wu TT, Perry HM, Gottesman KS, Foeller C. Sequences of Proteins of Immunological Interest, 5th ed. NIH Publication No. 91-3242. Washington, D.C.: U.S. Department of Health and Human Services (1991).
Kaneko O, Gong, L, Zhang, J, Hansen, JK, Hassan, R, Lee B and Ho M (2009). A binding domain on mesothelin for CA125/MUC16. J. Biol. Chem. 284: 3739-3749.
Klein C, Schaefer W, Regula JT. The use of CrossMAb technology for the generation of bi- and multispecific antibodies. MAbs 8(6), 1010-20 (2016).
Kontermann (2012). Dual targeting strategies with bispecific antibodies. MAbs 4(2):182-97.
Ledermann JA, Begent RH, Massof C, Kelly AM, Adam T, Bagshawe KD. A phase-I study of repeated therapy with radiolabelled antibody to carcinoembryonic antigen using intermittent or continuous administration of cyclosporin A to supress the immune response. Int. J. Cancer 47(5), 659-64 (1991).
Lee J-H, Kim H, Yao Z, Szajek L, Grasso L, Kim I and Paik C.H (2018). Tumour-Shed Antigen Affects Antibody Tumour Targeting: Comparison of Two 89Zr-Labeled Antibodies Directed against Shed or Nonshed Antigens”. Contrast Media and Molecular Imaging. ID: 2461257.
Lefranc MP, Giudicelli V, Duroux P, Jabado-Michaloud J, Folch G, Aouinti S, Carillon E, Duvergey H, Houles A, Paysan-Lafosse T, Hadi-Saljoqi S, Sasorith S, Lefranc G, Kossida S. IMGT®, the international ImMunoGeneTics information system® 25 years on. Nucleic Acids Res. 43(Database issue), D413-22 (2015).
Ma J, Tang WK, Esser L, Pastan I, Xia D. (2012). Recognition of mesothelin by the therapeutic antibody MORAb-009: structural and mechanistic insights. J Biol. Chem. 287: 33123-31.
Malarkannan S, Horng T, Shih PP, Schwab S, Shastri N. Presentation of out-of-frame peptide/MHC class I complexes by a novel translation initiation mechanism. Immunity 10(6), 681-90 (1999).
Napoletano C, Bellati F, Tarquini E, Tomao F, Taurino F, Spagnoli G, Rughetti A, Muzii L, Nuti M, Benedetti Panici P. MAGE-A and NY-ESO-1 expression in cervical cancer: prognostic factors and effects of chemotherapy. Am. J. Obstet. Gynecol. 198(1), 99.e1-99.e7 (2008).
Pearson WR, Lipman DJ. Improved tools for biological sequence comparison. Proc. Natl. Acad. Sci. U.S.A. 85(8), 2444-8 (1988).
Podojil JR, Miller SD. Potential targeting of B7-H4 for the treatment of cancer. Immunol. Rev. 276(1), 40-51 (2017).
Powers GA, Hudson PJ, Wheatcroft MP. Design and production of multimeric antibody fragments, focused on diabodies with enhanced clinical efficacy. Methods Mol. Biol. 907, 699-712 (2012)
Rickert KW, Grinberg L, Woods RM, Wilson S, Bowen MA, Baca M. Combining phage display with de novo protein sequencing for reverse engineering of monoclonal antibodies. MAbs, 2016;8(3):501-12
Rosenberg S. Development of Cancer Vaccines. ASCO Educational Book Spring: 60-62 (2000).
Sapede, C, Gauvrit A, Barbieux I, Padieu M, Cellerin L, Sagan C, Scherpereel A, Dabouis G, Gregoire M. Abberant splicing and protease involvement in mesothelin release from epithelioid mesothelioma cells. Canc. Sci 99(3): 590-594 (2008)
Scott AM, Renner C. Tumour Antigens Recognized by Antibodies. eLS (2001).
Simpson AJ, Cabellero OL, Jungbluth OL, Chen YT, Old LJ. Cancer/testis antigens, gametogenesis and cancer. Nat. Rev. Cancer 5(8), 615-25 (2005).
Smith TF, Waterman MS. Identification of common molecular subsequences. J. Mol. Biol. 147(1), 195-7 (1981).
Spiess, Zhai, Carter (2015). Alternative molecular formats and therapeutic applications for bispecific antibodies.
Molecular Immunology. 67:95-106.
Tai YT, Anderson KC. Targeting B-cell maturation antigen in multiple myeloma. Immunotherapy 7(11), 1187-99 (2015).
Tang Z, Feng, M, Gao, W, Chen W, Chaudhary, A, Croix, BS, Qian M, Dimitrov DS and Ho M, (2013). A human single-domain antibody elicits potent antitumor activity by targeting an epitope in mesothelin close to the cancer cell surface. Mol. Canc. Ther. 12:416-426.
Tinguely M, Jenni B, Knights A, Lopes B, Korol D, Rousson V, Curioni Fontecedro A, Cogliatti Bittermann AG, Schmid U, Dommann-Scherrer C, Maurer R, Renner C, Probst-Hensch NM, Moch H, Knuth A, Zippelius A. MAGE-C1/CT-7 expression in plasma cell myeloma: sub-cellular localization impacts on clinical outcome. Cancer Sci. 99(4), 720-5 (2008).
Tomasetti M, Rai AJ and van Meerbeeck JP (2012). Serum mesothelin for diagnosing malignant pleural mesothelioma: an individual patient data meta-analysis. J Clin. Oncol. 30:1541-1549.
Velazquez EF, Jungbluth AA, Yancovitz M, Gnjatic S, Adams S, O’Neill D, Zavilevich K, Albukh T, Christos P, Mazumdar M, Pavlick A, Polsky D, Shapiro R, Berman R, Spira J, Busam K, Osman I, Bhardwaj N. Expression of the cancer/testis antigen NY-ESO-1 in primary and metastatic malignant melanoma (MM) - correlation with prognostic factors. Cancer Immun. 7, 11 (2007).
Wang X, Mathieu M, Brezski RJ. IgG Fc engineering to modulate antibody effector functions. Protein Cell 9(1), 63-73 (2018).
Wozniak-Knopp G, Bartl S, Bauer A, Mostageer M, Woisetschläger M, Antes B, Ettl K, Kainer M, Weberhofer G, Wiederkum S, Himmler G, Mudde GC, Rüker F. Introducing antigen-binding sites in structural loops of immunoglobulin constant domains: Fc fragments with engineered HER2/neu-binding sites and antibody properties. Protein Eng. Des. Sel. 23(4), 289-97 (2010).
Zhang, Y, Chertov, O, Zhang, J, Hassan, R and Pastan I (2011). Cytotoxic activity of immunotoxin SS1P is modulated by TACE-dependent mesothelin shedding. Cancer Res. 71: 5915-5922.
Zhao XY, Subramanyam B, Sarapa N, Golfier S and Dinter H (2016). Novel antibody therapeutics targeting mesothelin in solid tumours. Clin. Cancer Drugs 3:76-86.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> F-STAR BETA LIMITED
<120> АНТИТЕЛА К МЕЗОТЕЛИНУ
<130> 007508377
<140> PCT/EP2019/068800
<141> 2019-07-12
<150> GB 1811415.7
<151> 2018-07-12
<160> 201
<170> PatentIn, версия 3.5
<210> 1
<211> 448
<212> Белок
<213> Искусственная последовательность
<220>
<223> FS28-256, тяжелая цепь (без LALA)
<220>
<221> MISC_FEATURE
<222> (50)..(50)
<223> Xaa обозначает все потенциальные замены для устранения возможного
N-связанного гликозилирования. Полученные клоны могут содержать
либо одну или другую замену, либо обе
<220>
<221> MISC_FEATURE
<222> (52)..(52)
<223> Xaa обозначает все потенциальные замены для устранения возможного
N-связанного гликозилирования. Полученные клоны могут содержать
либо одну или другую замену, либо обе
<400> 1
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Glu Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Xaa Ile Xaa Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ser Tyr Gln Gly Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 2
<211> 448
<212> Белок
<213> Искусственная последовательность
<220>
<223> FS28-256, тяжелая цепь (с LALA)
<220>
<221> MISC_FEATURE
<222> (50)..(50)
<223> Xaa обозначает все потенциальные замены для устранения возможного
N-связанного гликозилирования. Полученные клоны могут содержать
либо одну или другую замену, либо обе
<220>
<221> MISC_FEATURE
<222> (52)..(52)
<223> Xaa обозначает все потенциальные замены для устранения возможного
N-связанного гликозилирования. Полученные клоны могут содержать
либо одну или другую замену, либо обе
<400> 2
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Glu Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Xaa Ile Xaa Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ser Tyr Gln Gly Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 3
<211> 215
<212> Белок
<213> Искусственная последовательность
<220>
<223> FS28-256-001, FS28-256-021 и FS28-256-023, легкая цепь
<220>
<221> MISC_FEATURE
<222> (97)..(98)
<223> Xaa обозначает все потенциальные замены для устранения возможного
центра деамидирования. Полученные клоны могут содержать либо одну или
другую замену, либо обе
<400> 3
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln His Asn Gln Tyr Pro
85 90 95
Xaa Xaa Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 4
<211> 445
<212> Белок
<213> Искусственная последовательность
<220>
<223> тяжелая цепь mAb FS28-024 без LALA
<400> 4
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Tyr Ser
20 25 30
Ser Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Phe Ile Thr Pro Ser Thr Gly Tyr Thr His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Ala Leu Thr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 5
<211> 445
<212> Белок
<213> Искусственная последовательность
<220>
<223> тяжелая цепь mAb FS28-024 с LALA
<400> 5
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Tyr Ser
20 25 30
Ser Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Phe Ile Thr Pro Ser Thr Gly Tyr Thr His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Ala Leu Thr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 6
<211> 1335
<212> ДНК
<213> Искусственная последовательность
<220>
<223> тяжелая цепь mAb FS28-024 без LALA
<400> 6
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccctcagt tattcttcta tgtcatgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcttt attactccgt ctactggcta tacccactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acagcaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagacgggcg 300
ctgacgttcg actactgggg ccagggaacc ttggtcaccg tctcgagtgc tagcactaag 360
ggcccgtcgg tgttcccgct ggccccatcg tccaagagca catcaggggg taccgccgcc 420
ctgggctgcc ttgtgaagga ttactttccc gagcccgtca cagtgtcctg gaacagcgga 480
gccctgacct ccggagtgca tactttcccg gctgtgcttc agtcctctgg cctgtactca 540
ttgtcctccg tggtcaccgt cccttcgtcc tccctgggca cccagaccta tatctgtaat 600
gtcaaccata agccctcgaa caccaaggtc gacaagaagg tcgagccgaa gtcgtgcgac 660
aagactcaca cttgcccgcc ttgcccagcc ccggaactgc tgggtggtcc ttcggtgttc 720
ctcttcccgc ccaagccgaa ggataccctg atgatctcac ggacccccga agtgacctgt 780
gtggtggtgg acgtgtccca cgaggacccg gaagtgaaat tcaattggta cgtggatgga 840
gtggaagtgc acaacgccaa gaccaagcca cgggaagaac agtacaactc tacctaccgc 900
gtggtgtccg tgctcactgt gctgcaccaa gactggctga acgggaagga gtacaagtgc 960
aaagtgtcca acaaggcgct gcctgcccca attgagaaaa ctatctcgaa agccaaggga 1020
cagcctcgag agcctcaagt gtacaccctg cctccctctc gggacgagct gaccaagaac 1080
caagtctccc tgacctgtct ggtcaaggga ttctacccat cggatatcgc cgtggaatgg 1140
gaaagcaacg gacagcccga gaacaactac aagacgactc cgcccgtgct ggattccgac 1200
gggagcttct tcttgtactc caagctgacc gtcgacaaga gcagatggca gcagggaaac 1260
gtgttctcct gctccgtgat gcatgaggcg ctgcacaacc actacactca gaagagcttg 1320
tccctgtcgc ccgga 1335
<210> 7
<211> 1335
<212> ДНК
<213> Искусственная последовательность
<220>
<223> тяжелая цепь mAb FS28-024 с LALA
<400> 7
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccctcagt tattcttcta tgtcatgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcttt attactccgt ctactggcta tacccactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acagcaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagacgggcg 300
ctgacgttcg actactgggg ccagggaacc ttggtcaccg tctcgagtgc tagcactaag 360
ggcccgtcgg tgttcccgct ggccccatcg tccaagagca catcaggggg taccgccgcc 420
ctgggctgcc ttgtgaagga ttactttccc gagcccgtca cagtgtcctg gaacagcgga 480
gccctgacct ccggagtgca tactttcccg gctgtgcttc agtcctctgg cctgtactca 540
ttgtcctccg tggtcaccgt cccttcgtcc tccctgggca cccagaccta tatctgtaat 600
gtcaaccata agccctcgaa caccaaggtc gacaagaagg tcgagccgaa gtcgtgcgac 660
aagactcaca cttgcccgcc ttgcccagcc ccggaagctg ccggtggtcc ttcggtgttc 720
ctcttcccgc ccaagccgaa ggataccctg atgatctcac ggacccccga agtgacctgt 780
gtggtggtgg acgtgtccca cgaggacccg gaagtgaaat tcaattggta cgtggatgga 840
gtggaagtgc acaacgccaa gaccaagcca cgggaagaac agtacaactc tacctaccgc 900
gtggtgtccg tgctcactgt gctgcaccaa gactggctga acgggaagga gtacaagtgc 960
aaagtgtcca acaaggcgct gcctgcccca attgagaaaa ctatctcgaa agccaaggga 1020
cagcctcgag agcctcaagt gtacaccctg cctccctctc gggacgagct gaccaagaac 1080
caagtctccc tgacctgtct ggtcaaggga ttctacccat cggatatcgc cgtggaatgg 1140
gaaagcaacg gacagcccga gaacaactac aagacgactc cgcccgtgct ggattccgac 1200
gggagcttct tcttgtactc caagctgacc gtcgacaaga gcagatggca gcagggaaac 1260
gtgttctcct gctccgtgat gcatgaggcg ctgcacaacc actacactca gaagagcttg 1320
tccctgtcgc ccgga 1335
<210> 8
<211> 116
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024, вариабельный домен
<400> 8
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Tyr Ser
20 25 30
Ser Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Phe Ile Thr Pro Ser Thr Gly Tyr Thr His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Ala Leu Thr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 9
<211> 348
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-024, вариабельный домен
<400> 9
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccctcagt tattcttcta tgtcatgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcttt attactccgt ctactggcta tacccactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acagcaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagacgggcg 300
ctgacgttcg actactgggg ccagggaacc ttggtcaccg tctcgagt 348
<210> 10
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024, CDR1 (IMGT)
<400> 10
Gly Phe Thr Leu Ser Tyr Ser Ser
1 5
<210> 11
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024, CDR2 (IMGT)
<400> 11
Ile Thr Pro Ser Thr Gly Tyr Thr
1 5
<210> 12
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024, CDR3 (IMGT)
<400> 12
Ala Arg Arg Ala Leu Thr Phe Asp Tyr
1 5
<210> 13
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024, CDR1 (Кабат)
<400> 13
Tyr Ser Ser Met Ser
1 5
<210> 14
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024, CDR2 (Кабат)
<400> 14
Phe Ile Thr Pro Ser Thr Gly Tyr Thr His Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 15
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024, CDR3 (Кабат)
<400> 15
Arg Ala Leu Thr Phe Asp Tyr
1 5
<210> 16
<211> 215
<212> Белок
<213> Искусственная последовательность
<220>
<223> легкая цепь mAb FS28-024
<400> 16
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ala Ser Ser Tyr Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 17
<211> 645
<212> ДНК
<213> Искусственная последовательность
<220>
<223> легкая цепь mAb FS28-024
<400> 17
gaaattgtgc tgacccagtc tccgggcacg ttatctctga gccctggtga gcgcgccact 60
ctgtcatgcc gggcttctca aagtgttagc agtagctacc tggcgtggta tcagcaaaaa 120
ccgggccagg ccccgcgtct gctgatttac ggtgcatcca gccgtgccac cggcattcca 180
gatcgttttt ccggtagtgg ttctgggacg gacttcactc tgacaatctc acgcctggaa 240
ccggaggatt ttgcggtgta ttactgccag caagcttctt cttatcctct cacgttcggc 300
caagggacca aggtggaaat caaacgtact gtggccgctc ctagcgtgtt catttttccg 360
ccatccgacg agcagctcaa gtccggcacc gcctccgtgg tctgcctgct caacaacttc 420
taccctcgcg aagctaaggt ccagtggaag gtcgacaatg ccctgcagtc cggaaactcg 480
caggaaagcg tgactgaaca ggactccaag gactccacct attcactgtc ctcgactctg 540
accctgagca aggcggatta cgaaaagcac aaagtgtacg catgcgaagt gacccaccag 600
ggtctttcgt cccccgtgac caagagcttc aacagaggag agtgt 645
<210> 18
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> вариабельный домен mAb FS28-024
<400> 18
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ala Ser Ser Tyr Pro
85 90 95
Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 19
<211> 324
<212> ДНК
<213> Искусственная последовательность
<220>
<223> вариабельный домен mAb FS28-024
<400> 19
gaaattgtgc tgacccagtc tccgggcacg ttatctctga gccctggtga gcgcgccact 60
ctgtcatgcc gggcttctca aagtgttagc agtagctacc tggcgtggta tcagcaaaaa 120
ccgggccagg ccccgcgtct gctgatttac ggtgcatcca gccgtgccac cggcattcca 180
gatcgttttt ccggtagtgg ttctgggacg gacttcactc tgacaatctc acgcctggaa 240
ccggaggatt ttgcggtgta ttactgccag caagcttctt cttatcctct cacgttcggc 300
caagggacca aggtggaaat caaa 324
<210> 20
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024, CDR1 (IMGT)
<400> 20
Gln Ser Val Ser Ser Ser Tyr
1 5
<210> 21
<211> 3
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024, CDR2 (IMGT)
<400> 21
Gly Ala Ser
1
<210> 22
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024, CDR3 (IMGT)
<400> 22
Gln Gln Ala Ser Ser Tyr Pro Leu Thr
1 5
<210> 23
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024, CDR1 (Кабат)
<400> 23
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 24
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024, CDR2 (Кабат)
<400> 24
Gly Ala Ser Ser Arg Ala Thr
1 5
<210> 25
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256, CDR3 (IMGT)
<400> 25
Gln Gln Ser Tyr Tyr Tyr Pro Ile Thr
1 5
<210> 26
<211> 445
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024-051, тяжелая цепь без LALA
<400> 26
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Tyr Ser
20 25 30
Ser Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Phe Ile Thr Pro Ser Thr Gly Tyr Thr His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Ala Leu Ile Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 27
<211> 1335
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-024-051, тяжелая цепь без LALA
<400> 27
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccctcagt tattcttcta tgtcatgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcttt attactccgt ctactggcta tacccactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acagcaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagacgggcg 300
ctgattttcg actactgggg ccagggaacc ctggtcaccg tctcgagtgc tagcactaag 360
ggcccgtcgg tgttcccgct ggccccatcg tccaagagca catcaggggg taccgccgcc 420
ctgggctgcc ttgtgaagga ttactttccc gagcccgtca cagtgtcctg gaacagcgga 480
gccctgacct ccggagtgca tactttcccg gctgtgcttc agtcctctgg cctgtactca 540
ttgtcctccg tggtcaccgt cccttcgtcc tccctgggca cccagaccta tatctgtaat 600
gtcaaccata agccctcgaa caccaaggtc gacaagaagg tcgagccgaa gtcgtgcgac 660
aagactcaca cttgcccgcc ttgcccagcc ccggaactgc tgggtggtcc ttcggtgttc 720
ctcttcccgc ccaagccgaa ggataccctg atgatctcac ggacccccga agtgacctgt 780
gtggtggtgg acgtgtccca cgaggacccg gaagtgaaat tcaattggta cgtggatgga 840
gtggaagtgc acaacgccaa gaccaagcca cgggaagaac agtacaactc tacctaccgc 900
gtggtgtccg tgctcactgt gctgcaccaa gactggctga acgggaagga gtacaagtgc 960
aaagtgtcca acaaggcgct gcctgcccca attgagaaaa ctatctcgaa agccaaggga 1020
cagcctcgag agcctcaagt gtacaccctg cctccctctc gggacgagct gaccaagaac 1080
caagtctccc tgacctgtct ggtcaaggga ttctacccat cggatatcgc cgtggaatgg 1140
gaaagcaacg gacagcccga gaacaactac aagacgactc cgcccgtgct ggattccgac 1200
gggagcttct tcttgtactc caagctgacc gtcgacaaga gcagatggca gcagggaaac 1260
gtgttctcct gctccgtgat gcatgaggcg ctgcacaacc actacactca gaagagcttg 1320
tccctgtcgc ccgga 1335
<210> 28
<211> 445
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024-051, тяжелая цепь с LALA
<400> 28
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Tyr Ser
20 25 30
Ser Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Phe Ile Thr Pro Ser Thr Gly Tyr Thr His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Ala Leu Ile Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 29
<211> 1335
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-024-051, тяжелая цепь с LALA
<400> 29
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccctcagt tattcttcta tgtcatgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcttt attactccgt ctactggcta tacccactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acagcaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagacgggcg 300
ctgattttcg actactgggg ccagggaacc ctggtcaccg tctcgagtgc tagcactaag 360
ggcccgtcgg tgttcccgct ggccccatcg tccaagagca catcaggggg taccgccgcc 420
ctgggctgcc ttgtgaagga ttactttccc gagcccgtca cagtgtcctg gaacagcgga 480
gccctgacct ccggagtgca tactttcccg gctgtgcttc agtcctctgg cctgtactca 540
ttgtcctccg tggtcaccgt cccttcgtcc tccctgggca cccagaccta tatctgtaat 600
gtcaaccata agccctcgaa caccaaggtc gacaagaagg tcgagccgaa gtcgtgcgac 660
aagactcaca cttgcccgcc ttgcccagcc ccggaagctg ccggtggtcc ttcggtgttc 720
ctcttcccgc ccaagccgaa ggataccctg atgatctcac ggacccccga agtgacctgt 780
gtggtggtgg acgtgtccca cgaggacccg gaagtgaaat tcaattggta cgtggatgga 840
gtggaagtgc acaacgccaa gaccaagcca cgggaagaac agtacaactc tacctaccgc 900
gtggtgtccg tgctcactgt gctgcaccaa gactggctga acgggaagga gtacaagtgc 960
aaagtgtcca acaaggcgct gcctgcccca attgagaaaa ctatctcgaa agccaaggga 1020
cagcctcgag agcctcaagt gtacaccctg cctccctctc gggacgagct gaccaagaac 1080
caagtctccc tgacctgtct ggtcaaggga ttctacccat cggatatcgc cgtggaatgg 1140
gaaagcaacg gacagcccga gaacaactac aagacgactc cgcccgtgct ggattccgac 1200
gggagcttct tcttgtactc caagctgacc gtcgacaaga gcagatggca gcagggaaac 1260
gtgttctcct gctccgtgat gcatgaggcg ctgcacaacc actacactca gaagagcttg 1320
tccctgtcgc ccgga 1335
<210> 30
<211> 116
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024-051, вариабельный домен
<400> 30
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Tyr Ser
20 25 30
Ser Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Phe Ile Thr Pro Ser Thr Gly Tyr Thr His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Ala Leu Ile Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 31
<211> 348
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-024-051, вариабельный домен
<400> 31
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccctcagt tattcttcta tgtcatgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcttt attactccgt ctactggcta tacccactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acagcaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagacgggcg 300
ctgattttcg actactgggg ccagggaacc ctggtcaccg tctcgagt 348
<210> 32
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024-051, CDR3 (IMGT)
<400> 32
Ala Arg Arg Ala Leu Ile Phe Asp Tyr
1 5
<210> 33
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024-051, CDR3 (Кабат)
<400> 33
Arg Ala Leu Ile Phe Asp Tyr
1 5
<210> 34
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-001, CDR3 (IMGT) и (Кабат)
<400> 34
Gln Gln His Asn Gln Tyr Pro Asn Thr
1 5
<210> 35
<211> 445
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024-052, тяжелая цепь без LALA
<400> 35
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Tyr Ser
20 25 30
Ser Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Phe Ile Thr Pro Ser Thr Gly Tyr Thr His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Ala Leu Leu Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 36
<211> 1335
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-024-052, тяжелая цепь без LALA
<400> 36
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccctcagt tattcttcta tgtcatgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcttt attactccgt ctactggcta tacccactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acagcaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagacgggcg 300
ctgcttttcg actactgggg ccagggaacc ctggtcaccg tctcgtcggc tagcactaag 360
ggcccgtcgg tgttcccgct ggccccatcg tccaagagca catcaggggg taccgccgcc 420
ctgggctgcc ttgtgaagga ttactttccc gagcccgtca cagtgtcctg gaacagcgga 480
gccctgacct ccggagtgca tactttcccg gctgtgcttc agtcctctgg cctgtactca 540
ttgtcctccg tggtcaccgt cccttcgtcc tccctgggca cccagaccta tatctgtaat 600
gtcaaccata agccctcgaa caccaaggtc gacaagaagg tcgagccgaa gtcgtgcgac 660
aagactcaca cttgcccgcc ttgcccagcc ccggaactgc tgggtggtcc ttcggtgttc 720
ctcttcccgc ccaagccgaa ggataccctg atgatctcac ggacccccga agtgacctgt 780
gtggtggtgg acgtgtccca cgaggacccg gaagtgaaat tcaattggta cgtggatgga 840
gtggaagtgc acaacgccaa gaccaagcca cgggaagaac agtacaactc tacctaccgc 900
gtggtgtccg tgctcactgt gctgcaccaa gactggctga acgggaagga gtacaagtgc 960
aaagtgtcca acaaggcgct gcctgcccca attgagaaaa ctatctcgaa agccaaggga 1020
cagcctcgag agcctcaagt gtacaccctg cctccctctc gggacgagct gaccaagaac 1080
caagtctccc tgacctgtct ggtcaaggga ttctacccat cggatatcgc cgtggaatgg 1140
gaaagcaacg gacagcccga gaacaactac aagacgactc cgcccgtgct ggattccgac 1200
gggagcttct tcttgtactc caagctgacc gtcgacaaga gcagatggca gcagggaaac 1260
gtgttctcct gctccgtgat gcatgaggcg ctgcacaacc actacactca gaagagcttg 1320
tccctgtcgc ccgga 1335
<210> 37
<211> 445
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024-052, тяжелая цепь с LALA
<400> 37
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Tyr Ser
20 25 30
Ser Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Phe Ile Thr Pro Ser Thr Gly Tyr Thr His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Ala Leu Leu Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 38
<211> 1335
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-024-052, тяжелая цепь с LALA
<400> 38
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccctcagt tattcttcta tgtcatgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcttt attactccgt ctactggcta tacccactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acagcaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagacgggcg 300
ctgcttttcg actactgggg ccagggaacc ctggtcaccg tctcgtcggc tagcactaag 360
ggcccgtcgg tgttcccgct ggccccatcg tccaagagca catcaggggg taccgccgcc 420
ctgggctgcc ttgtgaagga ttactttccc gagcccgtca cagtgtcctg gaacagcgga 480
gccctgacct ccggagtgca tactttcccg gctgtgcttc agtcctctgg cctgtactca 540
ttgtcctccg tggtcaccgt cccttcgtcc tccctgggca cccagaccta tatctgtaat 600
gtcaaccata agccctcgaa caccaaggtc gacaagaagg tcgagccgaa gtcgtgcgac 660
aagactcaca cttgcccgcc ttgcccagcc ccggaagctg ccggtggtcc ttcggtgttc 720
ctcttcccgc ccaagccgaa ggataccctg atgatctcac ggacccccga agtgacctgt 780
gtggtggtgg acgtgtccca cgaggacccg gaagtgaaat tcaattggta cgtggatgga 840
gtggaagtgc acaacgccaa gaccaagcca cgggaagaac agtacaactc tacctaccgc 900
gtggtgtccg tgctcactgt gctgcaccaa gactggctga acgggaagga gtacaagtgc 960
aaagtgtcca acaaggcgct gcctgcccca attgagaaaa ctatctcgaa agccaaggga 1020
cagcctcgag agcctcaagt gtacaccctg cctccctctc gggacgagct gaccaagaac 1080
caagtctccc tgacctgtct ggtcaaggga ttctacccat cggatatcgc cgtggaatgg 1140
gaaagcaacg gacagcccga gaacaactac aagacgactc cgcccgtgct ggattccgac 1200
gggagcttct tcttgtactc caagctgacc gtcgacaaga gcagatggca gcagggaaac 1260
gtgttctcct gctccgtgat gcatgaggcg ctgcacaacc actacactca gaagagcttg 1320
tccctgtcgc ccgga 1335
<210> 39
<211> 116
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024-052, вариабельный домен
<400> 39
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Tyr Ser
20 25 30
Ser Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Phe Ile Thr Pro Ser Thr Gly Tyr Thr His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Ala Leu Leu Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 40
<211> 348
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-024-052, вариабельный домен
<400> 40
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccctcagt tattcttcta tgtcatgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcttt attactccgt ctactggcta tacccactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acagcaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagacgggcg 300
ctgcttttcg actactgggg ccagggaacc ctggtcaccg tctcgtcg 348
<210> 41
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024-052, CDR3 (IMGT)
<400> 41
Ala Arg Arg Ala Leu Leu Phe Asp Tyr
1 5
<210> 42
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024-052, CDR3 (Кабат)
<400> 42
Arg Ala Leu Leu Phe Asp Tyr
1 5
<210> 43
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-005, CDR3 (IMGT) и (Кабат)
<400> 43
Gln Gln Ala Leu Gly Tyr Pro His Thr
1 5
<210> 44
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-027, CDR3 (IMGT) и (Кабат)
<400> 44
Gln Gln Thr Val Pro Tyr Pro Tyr Thr
1 5
<210> 45
<211> 445
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024-053, тяжелая цепь без LALA
<400> 45
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Tyr Ser
20 25 30
Ser Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Phe Ile Thr Pro Ser Thr Gly Tyr Thr His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Ala Leu Val Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 46
<211> 1335
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-024-053, тяжелая цепь без LALA
<400> 46
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccctcagt tattcttcta tgtcatgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcttt attactccgt ctactggcta tacccactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acagcaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagacgggcg 300
ctggtgttcg actactgggg ccagggaacc ctggtcaccg tctcgtcggc tagcactaag 360
ggcccgtcgg tgttcccgct ggccccatcg tccaagagca catcaggggg taccgccgcc 420
ctgggctgcc ttgtgaagga ttactttccc gagcccgtca cagtgtcctg gaacagcgga 480
gccctgacct ccggagtgca tactttcccg gctgtgcttc agtcctctgg cctgtactca 540
ttgtcctccg tggtcaccgt cccttcgtcc tccctgggca cccagaccta tatctgtaat 600
gtcaaccata agccctcgaa caccaaggtc gacaagaagg tcgagccgaa gtcgtgcgac 660
aagactcaca cttgcccgcc ttgcccagcc ccggaactgc tgggtggtcc ttcggtgttc 720
ctcttcccgc ccaagccgaa ggataccctg atgatctcac ggacccccga agtgacctgt 780
gtggtggtgg acgtgtccca cgaggacccg gaagtgaaat tcaattggta cgtggatgga 840
gtggaagtgc acaacgccaa gaccaagcca cgggaagaac agtacaactc tacctaccgc 900
gtggtgtccg tgctcactgt gctgcaccaa gactggctga acgggaagga gtacaagtgc 960
aaagtgtcca acaaggcgct gcctgcccca attgagaaaa ctatctcgaa agccaaggga 1020
cagcctcgag agcctcaagt gtacaccctg cctccctctc gggacgagct gaccaagaac 1080
caagtctccc tgacctgtct ggtcaaggga ttctacccat cggatatcgc cgtggaatgg 1140
gaaagcaacg gacagcccga gaacaactac aagacgactc cgcccgtgct ggattccgac 1200
gggagcttct tcttgtactc caagctgacc gtcgacaaga gcagatggca gcagggaaac 1260
gtgttctcct gctccgtgat gcatgaggcg ctgcacaacc actacactca gaagagcttg 1320
tccctgtcgc ccgga 1335
<210> 47
<211> 445
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024-053, тяжелая цепь с LALA
<400> 47
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Tyr Ser
20 25 30
Ser Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Phe Ile Thr Pro Ser Thr Gly Tyr Thr His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Ala Leu Val Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 48
<211> 1335
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-024-053, тяжелая цепь с LALA
<400> 48
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccctcagt tattcttcta tgtcatgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcttt attactccgt ctactggcta tacccactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acagcaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagacgggcg 300
ctggtgttcg actactgggg ccagggaacc ctggtcaccg tctcgtcggc tagcactaag 360
ggcccgtcgg tgttcccgct ggccccatcg tccaagagca catcaggggg taccgccgcc 420
ctgggctgcc ttgtgaagga ttactttccc gagcccgtca cagtgtcctg gaacagcgga 480
gccctgacct ccggagtgca tactttcccg gctgtgcttc agtcctctgg cctgtactca 540
ttgtcctccg tggtcaccgt cccttcgtcc tccctgggca cccagaccta tatctgtaat 600
gtcaaccata agccctcgaa caccaaggtc gacaagaagg tcgagccgaa gtcgtgcgac 660
aagactcaca cttgcccgcc ttgcccagcc ccggaagctg ccggtggtcc ttcggtgttc 720
ctcttcccgc ccaagccgaa ggataccctg atgatctcac ggacccccga agtgacctgt 780
gtggtggtgg acgtgtccca cgaggacccg gaagtgaaat tcaattggta cgtggatgga 840
gtggaagtgc acaacgccaa gaccaagcca cgggaagaac agtacaactc tacctaccgc 900
gtggtgtccg tgctcactgt gctgcaccaa gactggctga acgggaagga gtacaagtgc 960
aaagtgtcca acaaggcgct gcctgcccca attgagaaaa ctatctcgaa agccaaggga 1020
cagcctcgag agcctcaagt gtacaccctg cctccctctc gggacgagct gaccaagaac 1080
caagtctccc tgacctgtct ggtcaaggga ttctacccat cggatatcgc cgtggaatgg 1140
gaaagcaacg gacagcccga gaacaactac aagacgactc cgcccgtgct ggattccgac 1200
gggagcttct tcttgtactc caagctgacc gtcgacaaga gcagatggca gcagggaaac 1260
gtgttctcct gctccgtgat gcatgaggcg ctgcacaacc actacactca gaagagcttg 1320
tccctgtcgc ccgga 1335
<210> 49
<211> 116
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024-053, вариабельный домен
<400> 49
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Tyr Ser
20 25 30
Ser Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Phe Ile Thr Pro Ser Thr Gly Tyr Thr His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Ala Leu Val Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 50
<211> 348
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-024-053, вариабельный домен
<400> 50
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccctcagt tattcttcta tgtcatgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcttt attactccgt ctactggcta tacccactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acagcaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagacgggcg 300
ctggtgttcg actactgggg ccagggaacc ctggtcaccg tctcgtcg 348
<210> 51
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024-053, CDR3 (IMGT)
<400> 51
Ala Arg Arg Ala Leu Val Phe Asp Tyr
1 5
<210> 52
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024-053, CDR3 (Кабат)
<400> 52
Arg Ala Leu Val Phe Asp Tyr
1 5
<210> 53
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-005, вариабельный домен
<400> 53
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ala Leu Gly Tyr Pro
85 90 95
His Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 54
<211> 324
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-005, вариабельный домен
<400> 54
gaaattgtgc tgacccagtc tccgggcacg ttatctctga gccctggtga gcgcgccact 60
ctgtcatgcc gggcttctca aagtgttagc agtagctacc tggcgtggta tcagcaaaaa 120
ccgggccagg ccccgcgtct gctgatttac ggtgcatcca gccgtgccac cggcattcca 180
gatcgttttt ccggtagtgg ttctgggacg gacttcactc tgacaatctc acgcctggaa 240
ccggaggatt ttgcggtgta ttactgccag caagctttgg gttatcctca tacgttcggc 300
caagggacca aggtggaaat caaa 324
<210> 55
<211> 445
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-024-060, тяжелая цепь с LALA
<400> 55
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Tyr Ser
20 25 30
Ser Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Phe Ile Thr Pro Ser Thr Gly Tyr Thr His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Ala Leu Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 56
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-027, вариабельный домен
<400> 56
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Thr Val Pro Tyr Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 57
<211> 324
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-027, вариабельный домен
<400> 57
gaaattgtgc tgacccagtc tccgggcacg ttatctctga gccctggtga gcgcgccact 60
ctgtcatgcc gggcttctca aagtgttagc agtagctacc tggcgtggta tcagcaaaaa 120
ccgggccagg ccccgcgtct gctgatttac ggtgcatcca gccgtgccac cggcattcca 180
gatcgttttt ccggtagtgg ttctgggacg gacttcactc tgacaatctc acgcctggaa 240
ccggaggatt ttgcggtgta ttactgccag caaactgtgc cgtatccgta tacgttcggc 300
caagggacca aggtggaaat caaa 324
<210> 58
<211> 445
<212> Белок
<213> Искусственная последовательность
<220>
<223> тяжелая цепь mAb FS28-026 (с LALA)
<400> 58
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Thr Pro Tyr Tyr Ser Lys Thr Asp Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Trp Tyr Arg Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 59
<211> 215
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-026, легкая цепь
<400> 59
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Ser Ser Tyr Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 60
<211> 445
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-091, тяжелая цепь с LALA
<400> 60
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asn Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Lys Pro Tyr Asp Gly Asn Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Arg Trp Val Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 61
<211> 215
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-091, легкая цепь
<400> 61
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Ser Ser Ser Pro
85 90 95
Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 62
<211> 452
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-185, тяжелая цепь с LALA
<400> 62
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Thr Ser
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Arg Ile Asn Pro Tyr Glu Gly Glu Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Trp Ser Ile Ala Thr Tyr Tyr Lys Ser Ala Met Asp Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
195 200 205
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
210 215 220
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala
225 230 235 240
Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
260 265 270
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
275 280 285
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
305 310 315 320
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
325 330 335
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
340 345 350
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
355 360 365
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
370 375 380
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
385 390 395 400
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
405 410 415
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
420 425 430
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
435 440 445
Leu Ser Pro Gly
450
<210> 63
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-001, вариабельный домен
<400> 63
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Glu Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ser Tyr Gln Gly Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 64
<211> 357
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-001, вариабельный домен
<400> 64
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccttcact gagacttata tgagctgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcaat atttctccga cttatagcac taccaactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acagcaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagatacaac 300
tcttaccagg gtggcttgga ctactggggc cagggaacct tggtcaccgt ctcgagt 357
<210> 65
<211> 448
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256, тяжелая цепь без LALA
<400> 65
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asn Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ser Tyr Gln Gly Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 66
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256, тяжелая цепь без LALA
<400> 66
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccttcact aacacttata tgagctgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcaat atttctccga cttatagcac taccaactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acagcaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagatacaac 300
tcttaccagg gtggcttgga ctactggggc cagggaacct tggtcaccgt ctcgagtgct 360
agcactaagg gcccgtcggt gttcccgctg gccccatcgt ccaagagcac atcagggggt 420
accgccgccc tgggctgcct tgtgaaggat tactttcccg agcccgtcac agtgtcctgg 480
aacagcggag ccctgacctc cggagtgcat actttcccgg ctgtgcttca gtcctctggc 540
ctgtactcat tgtcctccgt ggtcaccgtc ccttcgtcct ccctgggcac ccagacctat 600
atctgtaatg tcaaccataa gccctcgaac accaaggtcg acaagaaggt cgagccgaag 660
tcgtgcgaca agactcacac ttgcccgcct tgcccagccc cggaactgct gggtggtcct 720
tcggtgttcc tcttcccgcc caagccgaag gataccctga tgatctcacg gacccccgaa 780
gtgacctgtg tggtggtgga cgtgtcccac gaggacccgg aagtgaaatt caattggtac 840
gtggatggag tggaagtgca caacgccaag accaagccac gggaagaaca gtacaactct 900
acctaccgcg tggtgtccgt gctcactgtg ctgcaccaag actggctgaa cgggaaggag 960
tacaagtgca aagtgtccaa caaggcgctg cctgccccaa ttgagaaaac tatctcgaaa 1020
gccaagggac agcctcgaga gcctcaagtg tacaccctgc ctccctctcg ggacgagctg 1080
accaagaacc aagtctccct gacctgtctg gtcaagggat tctacccatc ggatatcgcc 1140
gtggaatggg aaagcaacgg acagcccgag aacaactaca agacgactcc gcccgtgctg 1200
gattccgacg ggagcttctt cttgtactcc aagctgaccg tcgacaagag cagatggcag 1260
cagggaaacg tgttctcctg ctccgtgatg catgaggcgc tgcacaacca ctacactcag 1320
aagagcttgt ccctgtcgcc cgga 1344
<210> 67
<211> 448
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256, тяжелая цепь с LALA
<400> 67
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asn Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ser Tyr Gln Gly Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 68
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256, тяжелая цепь с LALA
<400> 68
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccttcact aacacttata tgagctgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcaat atttctccga cttatagcac taccaactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acagcaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagatacaac 300
tcttaccagg gtggcttgga ctactggggc cagggaacct tggtcaccgt ctcgagtgct 360
agcactaagg gcccgtcggt gttcccgctg gccccatcgt ccaagagcac atcagggggt 420
accgccgccc tgggctgcct tgtgaaggat tactttcccg agcccgtcac agtgtcctgg 480
aacagcggag ccctgacctc cggagtgcat actttcccgg ctgtgcttca gtcctctggc 540
ctgtactcat tgtcctccgt ggtcaccgtc ccttcgtcct ccctgggcac ccagacctat 600
atctgtaatg tcaaccataa gccctcgaac accaaggtcg acaagaaggt cgagccgaag 660
tcgtgcgaca agactcacac ttgcccgcct tgcccagccc cggaagctgc cggtggtcct 720
tcggtgttcc tcttcccgcc caagccgaag gataccctga tgatctcacg gacccccgaa 780
gtgacctgtg tggtggtgga cgtgtcccac gaggacccgg aagtgaaatt caattggtac 840
gtggatggag tggaagtgca caacgccaag accaagccac gggaagaaca gtacaactct 900
acctaccgcg tggtgtccgt gctcactgtg ctgcaccaag actggctgaa cgggaaggag 960
tacaagtgca aagtgtccaa caaggcgctg cctgccccaa ttgagaaaac tatctcgaaa 1020
gccaagggac agcctcgaga gcctcaagtg tacaccctgc ctccctctcg ggacgagctg 1080
accaagaacc aagtctccct gacctgtctg gtcaagggat tctacccatc ggatatcgcc 1140
gtggaatggg aaagcaacgg acagcccgag aacaactaca agacgactcc gcccgtgctg 1200
gattccgacg ggagcttctt cttgtactcc aagctgaccg tcgacaagag cagatggcag 1260
cagggaaacg tgttctcctg ctccgtgatg catgaggcgc tgcacaacca ctacactcag 1320
aagagcttgt ccctgtcgcc cgga 1344
<210> 69
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256, вариабельный домен
<400> 69
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asn Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ser Tyr Gln Gly Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 70
<211> 357
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256, вариабельный домен
<400> 70
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccttcact aacacttata tgagctgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcaat atttctccga cttatagcac taccaactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acagcaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagatacaac 300
tcttaccagg gtggcttgga ctactggggc cagggaacct tggtcaccgt ctcgagt 357
<210> 71
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256, CDR1 (IMGT)
<400> 71
Gly Phe Thr Phe Thr Asn Thr Tyr
1 5
<210> 72
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256, CDR1 (Кабат)
<400> 72
Asn Thr Tyr Met Ser
1 5
<210> 73
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256, CDR2 (IMGT)
<400> 73
Ile Ser Pro Thr Tyr Ser Thr Thr
1 5
<210> 74
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256, CDR2 (Кабат)
<400> 74
Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 75
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256, CDR3 (IMGT)
<400> 75
Ala Arg Tyr Asn Ser Tyr Gln Gly Gly Leu Asp Tyr
1 5 10
<210> 76
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256, CDR3 (Кабат)
<400> 76
Tyr Asn Ser Tyr Gln Gly Gly Leu Asp Tyr
1 5 10
<210> 77
<211> 215
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256, легкая цепь
<400> 77
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Tyr Tyr Tyr Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 78
<211> 645
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256, легкая цепь
<400> 78
gaaattgtgc tgacccagtc tccgggcacg ttatctctga gccctggtga gcgcgccact 60
ctgtcatgcc gggcttctca aagtgttagc agtagctacc tggcgtggta tcagcaaaaa 120
ccgggccagg ccccgcgtct gctgatttac ggtgcatcca gccgtgccac cggcattcca 180
gatcgttttt ccggtagtgg ttctgggacg gacttcactc tgacaatctc acgcctggaa 240
ccggaggatt ttgcggtgta ttactgccag caatcttatt attatcctat cacgttcggc 300
caagggacca aggtggaaat caaacgtact gtggccgctc ctagcgtgtt catttttccg 360
ccatccgacg agcagctcaa gtccggcacc gcctccgtgg tctgcctgct caacaacttc 420
taccctcgcg aagctaaggt ccagtggaag gtcgacaatg ccctgcagtc cggaaactcg 480
caggaaagcg tgactgaaca ggactccaag gactccacct attcactgtc ctcgactctg 540
accctgagca aggcggatta cgaaaagcac aaagtgtacg catgcgaagt gacccaccag 600
ggtctttcgt cccccgtgac caagagcttc aacagaggag agtgt 645
<210> 79
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256, вариабельный домен
<400> 79
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Tyr Tyr Tyr Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 80
<211> 324
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256, вариабельный домен
<400> 80
gaaattgtgc tgacccagtc tccgggcacg ttatctctga gccctggtga gcgcgccact 60
ctgtcatgcc gggcttctca aagtgttagc agtagctacc tggcgtggta tcagcaaaaa 120
ccgggccagg ccccgcgtct gctgatttac ggtgcatcca gccgtgccac cggcattcca 180
gatcgttttt ccggtagtgg ttctgggacg gacttcactc tgacaatctc acgcctggaa 240
ccggaggatt ttgcggtgta ttactgccag caatcttatt attatcctat cacgttcggc 300
caagggacca aggtggaaat caaa 324
<210> 81
<211> 448
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-001, тяжелая цепь без LALA
<400> 81
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Glu Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ser Tyr Gln Gly Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 82
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-001, тяжелая цепь без LALA
<400> 82
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccttcact gagacttata tgagctgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcaat atttctccga cttatagcac taccaactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acagcaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagatacaac 300
tcttaccagg gtggcttgga ctactggggc cagggaacct tggtcaccgt ctcgagtgct 360
agcactaagg gcccgtcggt gttcccgctg gccccatcgt ccaagagcac atcagggggt 420
accgccgccc tgggctgcct tgtgaaggat tactttcccg agcccgtcac agtgtcctgg 480
aacagcggag ccctgacctc cggagtgcat actttcccgg ctgtgcttca gtcctctggc 540
ctgtactcat tgtcctccgt ggtcaccgtc ccttcgtcct ccctgggcac ccagacctat 600
atctgtaatg tcaaccataa gccctcgaac accaaggtcg acaagaaggt cgagccgaag 660
tcgtgcgaca agactcacac ttgcccgcct tgcccagccc cggaactgct gggtggtcct 720
tcggtgttcc tcttcccgcc caagccgaag gataccctga tgatctcacg gacccccgaa 780
gtgacctgtg tggtggtgga cgtgtcccac gaggacccgg aagtgaaatt caattggtac 840
gtggatggag tggaagtgca caacgccaag accaagccac gggaagaaca gtacaactct 900
acctaccgcg tggtgtccgt gctcactgtg ctgcaccaag actggctgaa cgggaaggag 960
tacaagtgca aagtgtccaa caaggcgctg cctgccccaa ttgagaaaac tatctcgaaa 1020
gccaagggac agcctcgaga gcctcaagtg tacaccctgc ctccctctcg ggacgagctg 1080
accaagaacc aagtctccct gacctgtctg gtcaagggat tctacccatc ggatatcgcc 1140
gtggaatggg aaagcaacgg acagcccgag aacaactaca agacgactcc gcccgtgctg 1200
gattccgacg ggagcttctt cttgtactcc aagctgaccg tcgacaagag cagatggcag 1260
cagggaaacg tgttctcctg ctccgtgatg catgaggcgc tgcacaacca ctacactcag 1320
aagagcttgt ccctgtcgcc cgga 1344
<210> 83
<211> 215
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-001, легкая цепь
<400> 83
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln His Asn Gln Tyr Pro
85 90 95
Asn Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 84
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-001, тяжелая цепь с LALA
<400> 84
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccttcact gagacttata tgagctgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcaat atttctccga cttatagcac taccaactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acagcaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagatacaac 300
tcttaccagg gtggcttgga ctactggggc cagggaacct tggtcaccgt ctcgagtgct 360
agcactaagg gcccgtcggt gttcccgctg gccccatcgt ccaagagcac atcagggggt 420
accgccgccc tgggctgcct tgtgaaggat tactttcccg agcccgtcac agtgtcctgg 480
aacagcggag ccctgacctc cggagtgcat actttcccgg ctgtgcttca gtcctctggc 540
ctgtactcat tgtcctccgt ggtcaccgtc ccttcgtcct ccctgggcac ccagacctat 600
atctgtaatg tcaaccataa gccctcgaac accaaggtcg acaagaaggt cgagccgaag 660
tcgtgcgaca agactcacac ttgcccgcct tgcccagccc cggaagctgc cggtggtcct 720
tcggtgttcc tcttcccgcc caagccgaag gataccctga tgatctcacg gacccccgaa 780
gtgacctgtg tggtggtgga cgtgtcccac gaggacccgg aagtgaaatt caattggtac 840
gtggatggag tggaagtgca caacgccaag accaagccac gggaagaaca gtacaactct 900
acctaccgcg tggtgtccgt gctcactgtg ctgcaccaag actggctgaa cgggaaggag 960
tacaagtgca aagtgtccaa caaggcgctg cctgccccaa ttgagaaaac tatctcgaaa 1020
gccaagggac agcctcgaga gcctcaagtg tacaccctgc ctccctctcg ggacgagctg 1080
accaagaacc aagtctccct gacctgtctg gtcaagggat tctacccatc ggatatcgcc 1140
gtggaatggg aaagcaacgg acagcccgag aacaactaca agacgactcc gcccgtgctg 1200
gattccgacg ggagcttctt cttgtactcc aagctgaccg tcgacaagag cagatggcag 1260
cagggaaacg tgttctcctg ctccgtgatg catgaggcgc tgcacaacca ctacactcag 1320
aagagcttgt ccctgtcgcc cgga 1344
<210> 85
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-001, CDR1 (IMGT)
<400> 85
Gly Phe Thr Phe Thr Glu Thr Tyr
1 5
<210> 86
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-001, CDR1 (Кабат)
<400> 86
Glu Thr Tyr Met Ser
1 5
<210> 87
<211> 448
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-005, тяжелая цепь без LALA
<400> 87
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Glu Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ser Tyr Gln Gly Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 88
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-005, тяжелая цепь без LALA
<400> 88
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccttcact gagacttata tgagctgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcaat atttctccga cttatagcac taccaactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acagcaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagatacaac 300
tcttaccagg gtggcttgga ctactggggc cagggaacct tggtcaccgt ctcgagtgct 360
agcactaagg gcccgtcggt gttcccgctg gccccatcgt ccaagagcac atcagggggt 420
accgccgccc tgggctgcct tgtgaaggat tactttcccg agcccgtcac agtgtcctgg 480
aacagcggag ccctgacctc cggagtgcat actttcccgg ctgtgcttca gtcctctggc 540
ctgtactcat tgtcctccgt ggtcaccgtc ccttcgtcct ccctgggcac ccagacctat 600
atctgtaatg tcaaccataa gccctcgaac accaaggtcg acaagaaggt cgagccgaag 660
tcgtgcgaca agactcacac ttgcccgcct tgcccagccc cggaactgct gggtggtcct 720
tcggtgttcc tcttcccgcc caagccgaag gataccctga tgatctcacg gacccccgaa 780
gtgacctgtg tggtggtgga cgtgtcccac gaggacccgg aagtgaaatt caattggtac 840
gtggatggag tggaagtgca caacgccaag accaagccac gggaagaaca gtacaactct 900
acctaccgcg tggtgtccgt gctcactgtg ctgcaccaag actggctgaa cgggaaggag 960
tacaagtgca aagtgtccaa caaggcgctg cctgccccaa ttgagaaaac tatctcgaaa 1020
gccaagggac agcctcgaga gcctcaagtg tacaccctgc ctccctctcg ggacgagctg 1080
accaagaacc aagtctccct gacctgtctg gtcaagggat tctacccatc ggatatcgcc 1140
gtggaatggg aaagcaacgg acagcccgag aacaactaca agacgactcc gcccgtgctg 1200
gattccgacg ggagcttctt cttgtactcc aagctgaccg tcgacaagag cagatggcag 1260
cagggaaacg tgttctcctg ctccgtgatg catgaggcgc tgcacaacca ctacactcag 1320
aagagcttgt ccctgtcgcc cgga 1344
<210> 89
<211> 448
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-005, тяжелая цепь с LALA
<400> 89
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Glu Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ser Tyr Gln Gly Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 90
<211> 215
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-005, легкая цепь
<400> 90
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ala Leu Gly Tyr Pro
85 90 95
His Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 91
<211> 645
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-005, легкая цепь
<400> 91
gaaattgtgc tgacccagtc tccgggcacg ttatctctga gccctggtga gcgcgccact 60
ctgtcatgcc gggcttctca aagtgttagc agtagctacc tggcgtggta tcagcaaaaa 120
ccgggccagg ccccgcgtct gctgatttac ggtgcatcca gccgtgccac cggcattcca 180
gatcgttttt ccggtagtgg ttctgggacg gacttcactc tgacaatctc acgcctggaa 240
ccggaggatt ttgcggtgta ttactgccag caagctttgg gttatcctca tacgttcggc 300
caagggacca aggtggaaat caaacgtact gtagcagctc cttccgtgtt catctttccg 360
cccagtgatg agcagctgaa gtcaggtact gcttccgtgg tttgcctgct caacaacttt 420
taccccagag aagccaaagt ccagtggaaa gtggacaatg cgttgcaaag cgggaactct 480
caggaatccg tcacagagca ggactctaag gactccacct atagcctctc tagtacgctg 540
acactgagca aagccgatta cgagaagcac aaggtgtatg cctgtgaggt tacccatcaa 600
ggccttagct caccagtgac caagagcttc aataggggag aatgc 645
<210> 92
<211> 645
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-021, легкая цепь
<400> 92
gaaattgtgc tgacccagtc tccgggcacg ttatctctga gccctggtga gcgcgccact 60
ctgtcatgcc gggcttctca aagtgttagc agtagctacc tggcgtggta tcagcaaaaa 120
ccgggccagg ccccgcgtct gctgatttac ggtgcatcca gccgtgccac cggcattcca 180
gatcgttttt ccggtagtgg ttctgggacg gacttcactc tgacaatctc acgcctggaa 240
ccggaggatt ttgcggtgta ttactgccag caacataatc agtatccgaa tacgttcggc 300
caagggacca aggtggaaat caaacgtact gtagcagctc cttccgtgtt catctttccg 360
cccagtgatg agcagctgaa gtcaggtact gcttccgtgg tttgcctgct caacaacttt 420
taccccagag aagccaaagt ccagtggaaa gtggacaatg cgttgcaaag cgggaactct 480
caggaatccg tcacagagca ggactctaag gactccacct atagcctctc tagtacgctg 540
acactgagca aagccgatta cgagaagcac aaggtgtatg cctgtgaggt tacccatcaa 600
ggccttagct caccagtgac caagagcttc aataggggag aatgc 645
<210> 93
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-021, вариабельный домен
<400> 93
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln His Asn Gln Tyr Pro
85 90 95
Asn Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 94
<211> 324
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-021, вариабельный домен
<400> 94
gaaattgtgc tgacccagtc tccgggcacg ttatctctga gccctggtga gcgcgccact 60
ctgtcatgcc gggcttctca aagtgttagc agtagctacc tggcgtggta tcagcaaaaa 120
ccgggccagg ccccgcgtct gctgatttac ggtgcatcca gccgtgccac cggcattcca 180
gatcgttttt ccggtagtgg ttctgggacg gacttcactc tgacaatctc acgcctggaa 240
ccggaggatt ttgcggtgta ttactgccag caacataatc agtatccgaa tacgttcggc 300
caagggacca aggtggaaat caaa 324
<210> 95
<211> 215
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-027, легкая цепь
<400> 95
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Thr Val Pro Tyr Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 96
<211> 645
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-027, легкая цепь
<400> 96
gaaattgtgc tgacccagtc tccgggcacg ttatctctga gccctggtga gcgcgccact 60
ctgtcatgcc gggcttctca aagtgttagc agtagctacc tggcgtggta tcagcaaaaa 120
ccgggccagg ccccgcgtct gctgatttac ggtgcatcca gccgtgccac cggcattcca 180
gatcgttttt ccggtagtgg ttctgggacg gacttcactc tgacaatctc acgcctggaa 240
ccggaggatt ttgcggtgta ttactgccag caaactgtgc cgtatccgta tacgttcggc 300
caagggacca aggtggaaat caaacgtact gtggccgctc ctagcgtgtt catttttccg 360
ccatccgacg agcagctcaa gtccggcacc gcctccgtgg tctgcctgct caacaacttc 420
taccctcgcg aagctaaggt ccagtggaag gtcgacaatg ccctgcagtc cggaaactcg 480
caggaaagcg tgactgaaca ggactccaag gactccacct attcactgtc ctcgactctg 540
accctgagca aggcggatta cgaaaagcac aaagtgtacg catgcgaagt gacccaccag 600
ggtctttcgt cccccgtgac caagagcttc aacagaggag agtgt 645
<210> 97
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-271, CDR1 (Кабат)
<400> 97
His Thr Tyr Met Ser
1 5
<210> 98
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-271, CDR1 (IMGT)
<400> 98
Gly Phe Thr Phe Thr His Thr Tyr
1 5
<210> 99
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-271, CDR3 (IMGT)
<400> 99
Ala Arg Tyr Asn Ala Tyr His Ala Ala Leu Asp Tyr
1 5 10
<210> 100
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-271, CDR3 (Кабат)
<400> 100
Tyr Asn Ala Tyr His Ala Ala Leu Asp Tyr
1 5 10
<210> 101
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-018, CDR1 (IMGT)
<400> 101
Gly Phe Thr Phe Thr Gln Thr Tyr
1 5
<210> 102
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-018, CDR1 (Кабат)
<400> 102
Gln Thr Tyr Met Ser
1 5
<210> 103
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-018, CDR3 (IMGT)
<400> 103
Ala Arg Tyr Asn Ala Tyr Gln Ile Gly Leu Asp Tyr
1 5 10
<210> 104
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-018, CDR3 (Кабат)
<400> 104
Tyr Asn Ala Tyr Gln Ile Gly Leu Asp Tyr
1 5 10
<210> 105
<211> 448
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-021, тяжелая цепь без LALA
<400> 105
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr His Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Asn Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr His Ala Ala Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 106
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-021, тяжелая цепь без LALA
<400> 106
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccttcact catacttata tgagctgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcaat atttctccga cttatagcac taccaactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acaacaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagatacaac 300
gcgtatcatg ctgctctgga ctactggggc cagggaaccc tggtcaccgt ctcgagtgct 360
agcactaagg gcccgtcggt gttcccgctg gccccatcgt ccaagagcac atcagggggt 420
accgccgccc tgggctgcct tgtgaaggat tactttcccg agcccgtcac agtgtcctgg 480
aacagcggag ccctgacctc cggagtgcat actttcccgg ctgtgcttca gtcctctggc 540
ctgtactcat tgtcctccgt ggtcaccgtc ccttcgtcct ccctgggcac ccagacctat 600
atctgtaatg tcaaccataa gccctcgaac accaaggtcg acaagaaggt cgagccgaag 660
tcgtgcgaca agactcacac ttgcccgcct tgcccagccc cggaactgct gggtggtcct 720
tcggtgttcc tcttcccgcc caagccgaag gataccctga tgatctcacg gacccccgaa 780
gtgacctgtg tggtggtgga cgtgtcccac gaggacccgg aagtgaaatt caattggtac 840
gtggatggag tggaagtgca caacgccaag accaagccac gggaagaaca gtacaactct 900
acctaccgcg tggtgtccgt gctcactgtg ctgcaccaag actggctgaa cgggaaggag 960
tacaagtgca aagtgtccaa caaggcgctg cctgccccaa ttgagaaaac tatctcgaaa 1020
gccaagggac agcctcgaga gcctcaagtg tacaccctgc ctccctctcg ggacgagctg 1080
accaagaacc aagtctccct gacctgtctg gtcaagggat tctacccatc ggatatcgcc 1140
gtggaatggg aaagcaacgg acagcccgag aacaactaca agacgactcc gcccgtgctg 1200
gattccgacg ggagcttctt cttgtactcc aagctgaccg tcgacaagag cagatggcag 1260
cagggaaacg tgttctcctg ctccgtgatg catgaggcgc tgcacaacca ctacactcag 1320
aagagcttgt ccctgtcgcc cgga 1344
<210> 107
<211> 448
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-021, тяжелая цепь с LALA
<400> 107
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr His Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Asn Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr His Ala Ala Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 108
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-021, тяжелая цепь с LALA
<400> 108
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccttcact catacttata tgagctgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcaat atttctccga cttatagcac taccaactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acaacaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagatacaac 300
gcgtatcatg ctgctctgga ctactggggc cagggaaccc tggtcaccgt ctcgagtgct 360
agcactaagg gcccgtcggt gttcccgctg gccccatcgt ccaagagcac atcagggggt 420
accgccgccc tgggctgcct tgtgaaggat tactttcccg agcccgtcac agtgtcctgg 480
aacagcggag ccctgacctc cggagtgcat actttcccgg ctgtgcttca gtcctctggc 540
ctgtactcat tgtcctccgt ggtcaccgtc ccttcgtcct ccctgggcac ccagacctat 600
atctgtaatg tcaaccataa gccctcgaac accaaggtcg acaagaaggt cgagccgaag 660
tcgtgcgaca agactcacac ttgcccgcct tgcccagccc cggaagctgc cggtggtcct 720
tcggtgttcc tcttcccgcc caagccgaag gataccctga tgatctcacg gacccccgaa 780
gtgacctgtg tggtggtgga cgtgtcccac gaggacccgg aagtgaaatt caattggtac 840
gtggatggag tggaagtgca caacgccaag accaagccac gggaagaaca gtacaactct 900
acctaccgcg tggtgtccgt gctcactgtg ctgcaccaag actggctgaa cgggaaggag 960
tacaagtgca aagtgtccaa caaggcgctg cctgccccaa ttgagaaaac tatctcgaaa 1020
gccaagggac agcctcgaga gcctcaagtg tacaccctgc ctccctctcg ggacgagctg 1080
accaagaacc aagtctccct gacctgtctg gtcaagggat tctacccatc ggatatcgcc 1140
gtggaatggg aaagcaacgg acagcccgag aacaactaca agacgactcc gcccgtgctg 1200
gattccgacg ggagcttctt cttgtactcc aagctgaccg tcgacaagag cagatggcag 1260
cagggaaacg tgttctcctg ctccgtgatg catgaggcgc tgcacaacca ctacactcag 1320
aagagcttgt ccctgtcgcc cgga 1344
<210> 109
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-021, вариабельный домен
<400> 109
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr His Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Asn Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr His Ala Ala Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 110
<211> 357
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-021, вариабельный домен
<400> 110
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccttcact catacttata tgagctgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcaat atttctccga cttatagcac taccaactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acaacaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagatacaac 300
gcgtatcatg ctgctctgga ctactggggc cagggaaccc tggtcaccgt ctcgagt 357
<210> 111
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-014, CDR1 (IMGT)
<400> 111
Gly Phe Thr Phe Thr Asp Thr Tyr
1 5
<210> 112
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-014, CDR1 (Кабат)
<400> 112
Asp Thr Tyr Met Ser
1 5
<210> 113
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-014, CDR3 (IMGT)
<400> 113
Ala Arg Tyr Asn Ala Tyr Ala Ala Gly Leu Asp Tyr
1 5 10
<210> 114
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-014, CDR3 (Кабат)
<400> 114
Tyr Asn Ala Tyr Ala Ala Gly Leu Asp Tyr
1 5 10
<210> 115
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-014, вариабельный домен
<400> 115
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr Ala Ala Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 116
<211> 357
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-014, вариабельный домен
<400> 116
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccttcact gatacttata tgagctgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcaat atttctccga cttatagcac taccaactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acagcaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagatacaac 300
gcgtatgcgg cgggtcttga ctactggggc cagggaaccc tggtcaccgt ctcgagt 357
<210> 117
<211> 448
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-014, тяжелая цепь без LALA
<400> 117
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr Ala Ala Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 118
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-014, тяжелая цепь без LALA
<400> 118
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccttcact gatacttata tgagctgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcaat atttctccga cttatagcac taccaactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acagcaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagatacaac 300
gcgtatgcgg cgggtcttga ctactggggc cagggaaccc tggtcaccgt ctcgagtgct 360
agcactaagg gcccgtcggt gttcccgctg gccccatcgt ccaagagcac atcagggggt 420
accgccgccc tgggctgcct tgtgaaggat tactttcccg agcccgtcac agtgtcctgg 480
aacagcggag ccctgacctc cggagtgcat actttcccgg ctgtgcttca gtcctctggc 540
ctgtactcat tgtcctccgt ggtcaccgtc ccttcgtcct ccctgggcac ccagacctat 600
atctgtaatg tcaaccataa gccctcgaac accaaggtcg acaagaaggt cgagccgaag 660
tcgtgcgaca agactcacac ttgcccgcct tgcccagccc cggaactgct gggtggtcct 720
tcggtgttcc tcttcccgcc caagccgaag gataccctga tgatctcacg gacccccgaa 780
gtgacctgtg tggtggtgga cgtgtcccac gaggacccgg aagtgaaatt caattggtac 840
gtggatggag tggaagtgca caacgccaag accaagccac gggaagaaca gtacaactct 900
acctaccgcg tggtgtccgt gctcactgtg ctgcaccaag actggctgaa cgggaaggag 960
tacaagtgca aagtgtccaa caaggcgctg cctgccccaa ttgagaaaac tatctcgaaa 1020
gccaagggac agcctcgaga gcctcaagtg tacaccctgc ctccctctcg ggacgagctg 1080
accaagaacc aagtctccct gacctgtctg gtcaagggat tctacccatc ggatatcgcc 1140
gtggaatggg aaagcaacgg acagcccgag aacaactaca agacgactcc gcccgtgctg 1200
gattccgacg ggagcttctt cttgtactcc aagctgaccg tcgacaagag cagatggcag 1260
cagggaaacg tgttctcctg ctccgtgatg catgaggcgc tgcacaacca ctacactcag 1320
aagagcttgt ccctgtcgcc cgga 1344
<210> 119
<211> 448
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-014, тяжелая цепь с LALA
<400> 119
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr Ala Ala Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 120
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-014, тяжелая цепь с LALA
<400> 120
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccttcact gatacttata tgagctgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcaat atttctccga cttatagcac taccaactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acagcaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagatacaac 300
gcgtatgcgg cgggtcttga ctactggggc cagggaaccc tggtcaccgt ctcgagtgct 360
agcactaagg gcccgtcggt gttcccgctg gccccatcgt ccaagagcac atcagggggt 420
accgccgccc tgggctgcct tgtgaaggat tactttcccg agcccgtcac agtgtcctgg 480
aacagcggag ccctgacctc cggagtgcat actttcccgg ctgtgcttca gtcctctggc 540
ctgtactcat tgtcctccgt ggtcaccgtc ccttcgtcct ccctgggcac ccagacctat 600
atctgtaatg tcaaccataa gccctcgaac accaaggtcg acaagaaggt cgagccgaag 660
tcgtgcgaca agactcacac ttgcccgcct tgcccagccc cggaagctgc cggtggtcct 720
tcggtgttcc tcttcccgcc caagccgaag gataccctga tgatctcacg gacccccgaa 780
gtgacctgtg tggtggtgga cgtgtcccac gaggacccgg aagtgaaatt caattggtac 840
gtggatggag tggaagtgca caacgccaag accaagccac gggaagaaca gtacaactct 900
acctaccgcg tggtgtccgt gctcactgtg ctgcaccaag actggctgaa cgggaaggag 960
tacaagtgca aagtgtccaa caaggcgctg cctgccccaa ttgagaaaac tatctcgaaa 1020
gccaagggac agcctcgaga gcctcaagtg tacaccctgc ctccctctcg ggacgagctg 1080
accaagaacc aagtctccct gacctgtctg gtcaagggat tctacccatc ggatatcgcc 1140
gtggaatggg aaagcaacgg acagcccgag aacaactaca agacgactcc gcccgtgctg 1200
gattccgacg ggagcttctt cttgtactcc aagctgaccg tcgacaagag cagatggcag 1260
cagggaaacg tgttctcctg ctccgtgatg catgaggcgc tgcacaacca ctacactcag 1320
aagagcttgt ccctgtcgcc cgga 1344
<210> 121
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-018, вариабельный домен
<400> 121
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Gln Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr Gln Ile Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 122
<211> 357
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-018, вариабельный домен
<400> 122
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccttcact cagacttata tgagctgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcaat atttctccga cttatagcac taccaactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acagcaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagatacaac 300
gcttatcaga ttgggttgga ctactggggc cagggaaccc tggtcaccgt ctcgagt 357
<210> 123
<211> 448
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-023, тяжелая цепь без LALA
<400> 123
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Gln Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr Gln Ile Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 124
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-023, тяжелая цепь без LALA
<400> 124
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccttcact cagacttata tgagctgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcaat atttctccga cttatagcac taccaactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acagcaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagatacaac 300
gcttatcaga ttgggttgga ctactggggc cagggaaccc tggtcaccgt ctcgagtgct 360
agcactaagg gcccgtcggt gttcccgctg gccccatcgt ccaagagcac atcagggggt 420
accgccgccc tgggctgcct tgtgaaggat tactttcccg agcccgtcac agtgtcctgg 480
aacagcggag ccctgacctc cggagtgcat actttcccgg ctgtgcttca gtcctctggc 540
ctgtactcat tgtcctccgt ggtcaccgtc ccttcgtcct ccctgggcac ccagacctat 600
atctgtaatg tcaaccataa gccctcgaac accaaggtcg acaagaaggt cgagccgaag 660
tcgtgcgaca agactcacac ttgcccgcct tgcccagccc cggaactgct gggtggtcct 720
tcggtgttcc tcttcccgcc caagccgaag gataccctga tgatctcacg gacccccgaa 780
gtgacctgtg tggtggtgga cgtgtcccac gaggacccgg aagtgaaatt caattggtac 840
gtggatggag tggaagtgca caacgccaag accaagccac gggaagaaca gtacaactct 900
acctaccgcg tggtgtccgt gctcactgtg ctgcaccaag actggctgaa cgggaaggag 960
tacaagtgca aagtgtccaa caaggcgctg cctgccccaa ttgagaaaac tatctcgaaa 1020
gccaagggac agcctcgaga gcctcaagtg tacaccctgc ctccctctcg ggacgagctg 1080
accaagaacc aagtctccct gacctgtctg gtcaagggat tctacccatc ggatatcgcc 1140
gtggaatggg aaagcaacgg acagcccgag aacaactaca agacgactcc gcccgtgctg 1200
gattccgacg ggagcttctt cttgtactcc aagctgaccg tcgacaagag cagatggcag 1260
cagggaaacg tgttctcctg ctccgtgatg catgaggcgc tgcacaacca ctacactcag 1320
aagagcttgt ccctgtcgcc cgga 1344
<210> 125
<211> 448
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-023, тяжелая цепь с LALA
<400> 125
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Gln Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr Gln Ile Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 126
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-023, тяжелая цепь с LALA
<400> 126
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccttcact cagacttata tgagctgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcaat atttctccga cttatagcac taccaactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acagcaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagatacaac 300
gcttatcaga ttgggttgga ctactggggc cagggaaccc tggtcaccgt ctcgagtgct 360
agcactaagg gcccgtcggt gttcccgctg gccccatcgt ccaagagcac atcagggggt 420
accgccgccc tgggctgcct tgtgaaggat tactttcccg agcccgtcac agtgtcctgg 480
aacagcggag ccctgacctc cggagtgcat actttcccgg ctgtgcttca gtcctctggc 540
ctgtactcat tgtcctccgt ggtcaccgtc ccttcgtcct ccctgggcac ccagacctat 600
atctgtaatg tcaaccataa gccctcgaac accaaggtcg acaagaaggt cgagccgaag 660
tcgtgcgaca agactcacac ttgcccgcct tgcccagccc cggaagctgc cggtggtcct 720
tcggtgttcc tcttcccgcc caagccgaag gataccctga tgatctcacg gacccccgaa 780
gtgacctgtg tggtggtgga cgtgtcccac gaggacccgg aagtgaaatt caattggtac 840
gtggatggag tggaagtgca caacgccaag accaagccac gggaagaaca gtacaactct 900
acctaccgcg tggtgtccgt gctcactgtg ctgcaccaag actggctgaa cgggaaggag 960
tacaagtgca aagtgtccaa caaggcgctg cctgccccaa ttgagaaaac tatctcgaaa 1020
gccaagggac agcctcgaga gcctcaagtg tacaccctgc ctccctctcg ggacgagctg 1080
accaagaacc aagtctccct gacctgtctg gtcaagggat tctacccatc ggatatcgcc 1140
gtggaatggg aaagcaacgg acagcccgag aacaactaca agacgactcc gcccgtgctg 1200
gattccgacg ggagcttctt cttgtactcc aagctgaccg tcgacaagag cagatggcag 1260
cagggaaacg tgttctcctg ctccgtgatg catgaggcgc tgcacaacca ctacactcag 1320
aagagcttgt ccctgtcgcc cgga 1344
<210> 127
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-256-012, тяжелая цепь без LALA
<400> 127
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr His Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Asn Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr His Ala Ala Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly
450
<210> 128
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-256-012, тяжелая цепь с LALA
<400> 128
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr His Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Asn Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr His Ala Ala Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly
450
<210> 129
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-256-014, тяжелая цепь без LALA
<400> 129
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr Ala Ala Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly
450
<210> 130
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-256-014, тяжелая цепь с LALA
<400> 130
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asp Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr Ala Ala Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly
450
<210> 131
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-256-018, тяжелая цепь без LALA
<400> 131
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Gln Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr Gln Ile Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly
450
<210> 132
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-256-018, тяжелая цепь с LALA
<400> 132
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Gln Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr Gln Ile Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly
450
<210> 133
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-256-021, тяжелая цепь без LALA
<400> 133
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr His Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Asn Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr His Ala Ala Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly
450
<210> 134
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-256-021, тяжелая цепь с LALA
<400> 134
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr His Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Asn Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr His Ala Ala Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly
450
<210> 135
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-256-023, тяжелая цепь без LALA
<400> 135
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Gln Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr Gln Ile Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly
450
<210> 136
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-256-023, тяжелая цепь с LALA
<400> 136
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Gln Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr Gln Ile Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly
450
<210> 137
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-256-024, тяжелая цепь без LALA
<400> 137
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr His Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Asn Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr His Ala Ala Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly
450
<210> 138
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-256-024, тяжелая цепь с LALA
<400> 138
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr His Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Asn Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr His Ala Ala Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly
450
<210> 139
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<223> FS22-053-008/FS28-256-026, тяжелая цепь без LALA
<400> 139
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Gln Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr Gln Ile Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly
450
<210> 140
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<223> FS22-053-008/FS28-256-026, тяжелая цепь без LALA
<400> 140
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Gln Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr Gln Ile Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly
450
<210> 141
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-256-027, тяжелая цепь без LALA
<400> 141
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr His Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Asn Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr His Ala Ala Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly
450
<210> 142
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-256-027, тяжелая цепь с LALA
<400> 142
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr His Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Asn Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr His Ala Ala Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly
450
<210> 143
<211> 450
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-024, тяжелая цепь без LALA
<400> 143
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Tyr Ser
20 25 30
Ser Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Phe Ile Thr Pro Ser Thr Gly Tyr Thr His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Ala Leu Thr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly
450
<210> 144
<211> 450
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-024, тяжелая цепь с LALA
<400> 144
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Tyr Ser
20 25 30
Ser Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Phe Ile Thr Pro Ser Thr Gly Tyr Thr His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Ala Leu Thr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly
450
<210> 145
<211> 450
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-024-051, тяжелая цепь без LALA
<400> 145
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Tyr Ser
20 25 30
Ser Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Phe Ile Thr Pro Ser Thr Gly Tyr Thr His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Ala Leu Ile Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly
450
<210> 146
<211> 450
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-024-051, тяжелая цепь с LALA
<400> 146
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Tyr Ser
20 25 30
Ser Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Phe Ile Thr Pro Ser Thr Gly Tyr Thr His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Ala Leu Ile Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly
450
<210> 147
<211> 450
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-024-052, тяжелая цепь (без LALA)
<400> 147
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Tyr Ser
20 25 30
Ser Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Phe Ile Thr Pro Ser Thr Gly Tyr Thr His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Ala Leu Leu Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly
450
<210> 148
<211> 450
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-024-052, тяжелая цепь (с LALA)
<400> 148
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Tyr Ser
20 25 30
Ser Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Phe Ile Thr Pro Ser Thr Gly Tyr Thr His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Ala Leu Leu Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly
450
<210> 149
<211> 450
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-024-053, тяжелая цепь без LALA
<400> 149
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Tyr Ser
20 25 30
Ser Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Phe Ile Thr Pro Ser Thr Gly Tyr Thr His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Ala Leu Val Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly
450
<210> 150
<211> 450
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-024-053, тяжелая цепь с LALA
<400> 150
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Tyr Ser
20 25 30
Ser Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Phe Ile Thr Pro Ser Thr Gly Tyr Thr His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Ala Leu Val Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly
450
<210> 151
<211> 450
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008-AA/FS28-024-060, тяжелая цепь с LALA
<400> 151
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Tyr Ser
20 25 30
Ser Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Phe Ile Thr Pro Ser Thr Gly Tyr Thr His Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Ala Leu Trp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly
450
<210> 152
<211> 450
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008-AA/FS28-026, тяжелая цепь с LALA
<400> 152
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Thr Pro Tyr Tyr Ser Lys Thr Asp Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Trp Tyr Arg Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly
450
<210> 153
<211> 450
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008-AA/FS28-091, тяжелая цепь с LALA
<400> 153
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asn Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Lys Pro Tyr Asp Gly Asn Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asn Arg Trp Val Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly
450
<210> 154
<211> 457
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008-AA/FS28-185, тяжелая цепь с LALA
<400> 154
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Thr Ser
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Arg Ile Asn Pro Tyr Glu Gly Glu Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Trp Ser Ile Ala Thr Tyr Tyr Lys Ser Ala Met Asp Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
195 200 205
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
210 215 220
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala
225 230 235 240
Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
260 265 270
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
275 280 285
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
305 310 315 320
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
325 330 335
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
340 345 350
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Asn Pro Pro Tyr
355 360 365
Leu Phe Ser Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
370 375 380
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
385 390 395 400
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
405 410 415
Leu Tyr Ser Lys Leu Thr Val Asp Tyr Trp Arg Trp Leu Glu Gly Asn
420 425 430
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
435 440 445
Gln Lys Ser Leu Ser Leu Ser Pro Gly
450 455
<210> 155
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-256, тяжелая цепь без LALA
<400> 155
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asn Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ser Tyr Gln Gly Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly
450
<210> 156
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-256, тяжелая цепь с LALA
<400> 156
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Asn Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ser Tyr Gln Gly Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly
450
<210> 157
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-256-001, тяжелая цепь без LALA
<400> 157
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Glu Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ser Tyr Gln Gly Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly
450
<210> 158
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-256-001, тяжелая цепь с LALA
<400> 158
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Glu Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ser Tyr Gln Gly Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly
450
<210> 159
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-256-005, тяжелая цепь без LALA
<400> 159
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Glu Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ser Tyr Gln Gly Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly
450
<210> 160
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-053-008/FS28-256-005, тяжелая цепь с LALA
<400> 160
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr Glu Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Asn Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ser Tyr Gln Gly Gly Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Asn Pro Pro Tyr Leu Phe Ser Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Tyr Trp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly
450
<210> 161
<211> 447
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28m-228 (с LALA), тяжелая цепь
<400> 161
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Phe Met Val Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Met Ile Ser Pro Lys Ser Ser Asn Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Trp Phe Thr Pro Ala Arg Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
260 265 270
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
340 345 350
Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys
355 360 365
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
405 410 415
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 162
<211> 215
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28m-228, легкая цепь
<400> 162
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Pro Phe Pro Phe Ser
85 90 95
Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 163
<211> 447
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-063-AA/FS28m-228, тяжелая цепь с LALA
<400> 163
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Phe Met Val Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Met Ile Ser Pro Lys Ser Ser Asn Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Trp Phe Thr Pro Ala Arg Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
260 265 270
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
340 345 350
Pro Pro Ser Arg Asp Glu Pro Tyr Trp Ser Tyr Val Ser Leu Thr Cys
355 360 365
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Met Asn Tyr
405 410 415
Arg Trp Glu Leu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 164
<211> 215
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-063-AA/FS28m-228, легкая цепь
<400> 164
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Pro Phe Pro Phe Ser
85 90 95
Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 165
<211> 445
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb G1-AA/HelD1.3, тяжелая цепь с LALA
<400> 165
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Arg Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Ser Thr Phe Ser Gly Tyr
20 25 30
Gly Val Asn Trp Val Arg Gln Pro Pro Gly Arg Gly Leu Glu Trp Ile
35 40 45
Gly Met Ile Trp Gly Asp Gly Asn Thr Asp Tyr Asn Ser Ala Leu Lys
50 55 60
Ser Arg Val Thr Met Leu Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Glu Arg Asp Tyr Arg Leu Asp Tyr Trp Gly Gln Gly Ser Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 166
<211> 214
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb G1-AA/HelD1.3, легкая цепь
<400> 166
Asp Ile Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Glu Thr Val Thr Ile Thr Cys Arg Ala Ser Gly Asn Ile His Asn Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Gln Gly Lys Ser Pro Gln Leu Leu Val
35 40 45
Tyr Asn Ala Lys Thr Leu Ala Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Gln Tyr Ser Leu Lys Ile Asn Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Gly Ser Tyr Tyr Cys Gln His Phe Trp Ser Thr Pro Arg
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 167
<211> 448
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb G1-AA/SS1 (с LALA), тяжелая цепь
<400> 167
Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Glu Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Thr Met Asn Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Leu Ile Thr Pro Tyr Asn Gly Ala Ser Ser Tyr Asn Gln Lys Phe
50 55 60
Arg Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Asp Leu Leu Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Arg Gly Gly Tyr Asp Gly Arg Gly Phe Asp Tyr Trp Gly Ser Gly
100 105 110
Thr Pro Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 168
<211> 213
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb G1-AA/SS1, легкая цепь
<400> 168
Asp Ile Glu Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Gly Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Asn Ser Tyr Ser Leu Thr Ile Ser Ser Val Glu Ala Glu
65 70 75 80
Asp Asp Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Lys His Pro Leu Thr
85 90 95
Phe Gly Ser Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 169
<211> 303
<212> Белок
<213> MSLN-His-Avi Homo sapiens
<400> 169
Glu Val Glu Lys Thr Ala Cys Pro Ser Gly Lys Lys Ala Arg Glu Ile
1 5 10 15
Asp Glu Ser Leu Ile Phe Tyr Lys Lys Trp Glu Leu Glu Ala Cys Val
20 25 30
Asp Ala Ala Leu Leu Ala Thr Gln Met Asp Arg Val Asn Ala Ile Pro
35 40 45
Phe Thr Tyr Glu Gln Leu Asp Val Leu Lys His Lys Leu Asp Glu Leu
50 55 60
Tyr Pro Gln Gly Tyr Pro Glu Ser Val Ile Gln His Leu Gly Tyr Leu
65 70 75 80
Phe Leu Lys Met Ser Pro Glu Asp Ile Arg Lys Trp Asn Val Thr Ser
85 90 95
Leu Glu Thr Leu Lys Ala Leu Leu Glu Val Asn Lys Gly His Glu Met
100 105 110
Ser Pro Gln Val Ala Thr Leu Ile Asp Arg Phe Val Lys Gly Arg Gly
115 120 125
Gln Leu Asp Lys Asp Thr Leu Asp Thr Leu Thr Ala Phe Tyr Pro Gly
130 135 140
Tyr Leu Cys Ser Leu Ser Pro Glu Glu Leu Ser Ser Val Pro Pro Ser
145 150 155 160
Ser Ile Trp Ala Val Arg Pro Gln Asp Leu Asp Thr Cys Asp Pro Arg
165 170 175
Gln Leu Asp Val Leu Tyr Pro Lys Ala Arg Leu Ala Phe Gln Asn Met
180 185 190
Asn Gly Ser Glu Tyr Phe Val Lys Ile Gln Ser Phe Leu Gly Gly Ala
195 200 205
Pro Thr Glu Asp Leu Lys Ala Leu Ser Gln Gln Asn Val Ser Met Asp
210 215 220
Leu Ala Thr Phe Met Lys Leu Arg Thr Asp Ala Val Leu Pro Leu Thr
225 230 235 240
Val Ala Glu Val Gln Lys Leu Leu Gly Pro His Val Glu Gly Leu Lys
245 250 255
Ala Glu Glu Arg His Arg Pro Val Arg Asp Trp Ile Leu Arg Gln Arg
260 265 270
Gln Asp Asp Leu Asp Thr Leu Gly Leu Gly Leu Gln Gly Gly Ile Pro
275 280 285
Asn Gly Tyr Leu Val Leu Asp Leu Ser Met Gln Glu Ala Leu Ser
290 295 300
<210> 170
<211> 303
<212> Белок
<213> MSLN-His-Avi яванского макака
<400> 170
Asp Val Glu Arg Thr Thr Cys Pro Pro Glu Lys Glu Val His Glu Ile
1 5 10 15
Asp Glu Ser Leu Ile Phe Tyr Lys Lys Arg Glu Leu Glu Ala Cys Val
20 25 30
Asp Ala Ala Leu Leu Ala Ala Gln Met Asp Arg Val Asp Ala Ile Pro
35 40 45
Phe Thr Tyr Glu Gln Leu Asp Val Leu Lys His Lys Leu Asp Glu Leu
50 55 60
Tyr Pro Gln Gly Tyr Pro Glu Ser Val Ile Arg His Leu Gly His Leu
65 70 75 80
Phe Leu Lys Met Ser Pro Glu Asp Ile Arg Lys Trp Asn Val Thr Ser
85 90 95
Leu Glu Thr Leu Lys Ala Leu Leu Lys Val Ser Lys Gly His Glu Met
100 105 110
Ser Ala Gln Val Ala Thr Leu Ile Asp Arg Val Val Val Gly Arg Gly
115 120 125
Gln Leu Asp Lys Asp Thr Ala Asp Thr Leu Thr Ala Phe Cys Pro Gly
130 135 140
Cys Leu Cys Ser Leu Ser Pro Glu Arg Leu Ser Ser Val Pro Pro Ser
145 150 155 160
Ile Ile Gly Ala Val Arg Pro Gln Asp Leu Asp Thr Cys Gly Pro Arg
165 170 175
Gln Leu Asp Val Leu Tyr Pro Lys Ala Arg Leu Ala Phe Gln Asn Met
180 185 190
Ser Gly Ser Glu Tyr Phe Val Lys Ile Arg Pro Phe Leu Gly Gly Ala
195 200 205
Pro Thr Glu Asp Leu Lys Ala Leu Ser Gln Gln Asn Val Ser Met Asp
210 215 220
Leu Ala Thr Phe Met Lys Leu Arg Arg Glu Ala Val Leu Pro Leu Ser
225 230 235 240
Val Ala Glu Val Gln Lys Leu Leu Gly Pro His Val Glu Gly Leu Lys
245 250 255
Val Glu Glu Gln His Ser Pro Val Arg Asp Trp Ile Leu Lys Gln Arg
260 265 270
Gln Asp Asp Leu Asp Thr Leu Gly Leu Gly Leu Gln Gly Gly Ile Pro
275 280 285
Asn Gly Tyr Leu Ile Leu Asp Leu Ser Val Arg Glu Ala Leu Ser
290 295 300
<210> 171
<211> 303
<212> Белок
<213> MSLN-His-Avi мыши
<400> 171
Asp Ala Glu Gln Lys Ala Cys Pro Pro Gly Lys Glu Pro Tyr Lys Val
1 5 10 15
Asp Glu Asp Leu Ile Phe Tyr Gln Asn Trp Glu Leu Glu Ala Cys Val
20 25 30
Asp Gly Thr Met Leu Ala Arg Gln Met Asp Leu Val Asn Glu Ile Pro
35 40 45
Phe Thr Tyr Glu Gln Leu Ser Ile Phe Lys His Lys Leu Asp Lys Thr
50 55 60
Tyr Pro Gln Gly Tyr Pro Glu Ser Leu Ile Gln Gln Leu Gly His Phe
65 70 75 80
Phe Arg Tyr Val Ser Pro Glu Asp Ile His Gln Trp Asn Val Thr Ser
85 90 95
Pro Asp Thr Val Lys Thr Leu Leu Lys Val Ser Lys Gly Gln Lys Met
100 105 110
Asn Ala Gln Ala Ile Ala Leu Val Ala Cys Tyr Leu Arg Gly Gly Gly
115 120 125
Gln Leu Asp Glu Asp Met Val Lys Ala Leu Gly Asp Ile Pro Leu Ser
130 135 140
Tyr Leu Cys Asp Phe Ser Pro Gln Asp Leu His Ser Val Pro Ser Ser
145 150 155 160
Val Met Trp Leu Val Gly Pro Gln Asp Leu Asp Lys Cys Ser Gln Arg
165 170 175
His Leu Gly Leu Leu Tyr Gln Lys Ala Cys Ser Ala Phe Gln Asn Val
180 185 190
Ser Gly Leu Glu Tyr Phe Glu Lys Ile Lys Thr Phe Leu Gly Gly Ala
195 200 205
Ser Val Lys Asp Leu Arg Ala Leu Ser Gln His Asn Val Ser Met Asp
210 215 220
Ile Ala Thr Phe Lys Arg Leu Gln Val Asp Ser Leu Val Gly Leu Ser
225 230 235 240
Val Ala Glu Val Gln Lys Leu Leu Gly Pro Asn Ile Val Asp Leu Lys
245 250 255
Thr Glu Glu Asp Lys Ser Pro Val Arg Asp Trp Leu Phe Arg Gln His
260 265 270
Gln Lys Asp Leu Asp Arg Leu Gly Leu Gly Leu Gln Gly Gly Ile Pro
275 280 285
Asn Gly Tyr Leu Val Leu Asp Phe Asn Val Arg Glu Ala Phe Ser
290 295 300
<210> 172
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> CH3-домен дикого типа
<400> 172
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp
1 5 10 15
Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
20 25 30
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
35 40 45
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
50 55 60
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
65 70 75 80
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
85 90 95
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
100 105
<210> 173
<211> 110
<212> Белок
<213> Искусственная последовательность
<220>
<223> CH2-домен, содержащий мутацию LALA
<400> 173
Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
100 105 110
<210> 174
<211> 110
<212> Белок
<213> Искусственная последовательность
<220>
<223> CH2-домен, содержащий мутацию LALA-PA
<400> 174
Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Ala Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
100 105 110
<210> 175
<211> 1901
<212> ДНК
<213> Белок-предшественник MSLN Homo sapiens
<400> 175
aagcttgaat tcgccgccac catggccctg cctaccgcta ggcctctgct cggatcctgc 60
ggcacacctg ccctgggaag cctcctgttc ctgctgttct ccctgggctg ggtgcagccc 120
tccagaacac tggccggcga aacaggacaa gaggctgccc ctctcgatgg cgtgctcgct 180
aaccccccca acatcagctc cctgtcccct aggcagctcc tgggctttcc ctgtgccgag 240
gtcagcggcc tctccaccga gagggtgagg gagctggctg tggccctggc tcagaagaac 300
gtgaaactga gcaccgagca actcaggtgc ctggctcata ggctgtccga gccccccgag 360
gatctggatg ccctgcctct cgacctgctg ctgttcctga accccgacgc ttttagcggc 420
ccccaggcct gcacaaggtt cttcagcaga atcaccaagg ccaacgtgga tctgctgccc 480
agaggcgctc ccgagaggca aagactgctg cccgccgctc tcgcctgttg gggcgtcaga 540
ggatccctgc tgagcgaggc cgacgtgaga gccctgggcg gcctggcttg tgatctgccc 600
ggcaggtttg tcgctgagag cgccgaagtg ctcctgccca gactggtgag ctgccctgga 660
cctctggacc aggatcaaca ggaggccgcc agagctgctc tgcagggagg aggacccccc 720
tacggacctc ctagcacctg gtccgtgagc acaatggacg ccctgagagg cctgctgcct 780
gtgctgggac agcccatcat taggagcatt ccccagggca ttgtggccgc ctggagacag 840
aggagcagca gggacccctc ctggaggcag cctgagagaa caatcctgag gcccagattc 900
agaagagagg tggagaaaac cgcctgccct agcggcaaga aggccagaga gattgacgag 960
agcctgatct tctataaaaa gtgggagctc gaagcctgcg tggatgctgc cctgctggcc 1020
acacagatgg acagggtgaa cgccatcccc ttcacctacg agcagctgga cgtcctgaag 1080
cacaagctcg atgagctgta cccccagggc taccccgagt ccgtgattca gcatctcggc 1140
tacctgttcc tgaaaatgag ccccgaagac atcaggaagt ggaacgtgac aagcctggag 1200
accctcaagg ccctgctgga agtgaacaag ggacacgaga tgagccccca ggtggccacc 1260
ctcatcgaca gatttgtgaa gggaagggga cagctggata aggacaccct cgacaccctg 1320
accgccttct accctggata cctctgcagc ctgtcccccg aagagctgtc cagcgtgcct 1380
ccctcctcca tctgggccgt cagaccccag gatctcgaca catgcgaccc cagacagctg 1440
gatgtgctgt accccaaggc taggctggcc ttccagaaca tgaacggatc cgaatatttc 1500
gtcaaaatcc agagctttct gggcggagcc cccacagagg acctcaaagc cctgagccag 1560
cagaacgtca gcatggacct ggccaccttt atgaaactga gaaccgacgc cgtcctccct 1620
ctgacagtgg ccgaagtgca gaagctcctg ggcccccatg tggaaggcct gaaggccgag 1680
gagagacaca gacccgtgag agactggatt ctgaggcaga ggcaggacga tctggatacc 1740
ctgggcctgg gactgcaggg cggcattcct aacggatacc tggtcctcga cctgagcatg 1800
caggaagccc tgagcggcac accttgtctg ctgggacctg gccctgtcct caccgtgctc 1860
gctctgctgc tggcttccac cctcgcctga tgagcggccg c 1901
<210> 176
<211> 448
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-271, тяжелая цепь без LALA
<400> 176
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr His Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Asn Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr His Ala Ala Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 177
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-271, тяжелая цепь без LALA
<400> 177
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccttcact catacttata tgagctgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcgcg atttctccga cttatagcac taccaactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acaacaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagatacaac 300
gcgtatcatg ctgctctgga ctactggggc cagggaaccc tggtcaccgt ctcgagtgct 360
agcactaagg gcccgtcggt gttcccgctg gccccatcgt ccaagagcac atcagggggt 420
accgccgccc tgggctgcct tgtgaaggat tactttcccg agcccgtcac agtgtcctgg 480
aacagcggag ccctgacctc cggagtgcat actttcccgg ctgtgcttca gtcctctggc 540
ctgtactcat tgtcctccgt ggtcaccgtc ccttcgtcct ccctgggcac ccagacctat 600
atctgtaatg tcaaccataa gccctcgaac accaaggtcg acaagaaggt cgagccgaag 660
tcgtgcgaca agactcacac ttgcccgcct tgcccagccc cggaactgct gggtggtcct 720
tcggtgttcc tcttcccgcc caagccgaag gataccctga tgatctcacg gacccccgaa 780
gtgacctgtg tggtggtgga cgtgtcccac gaggacccgg aagtgaaatt caattggtac 840
gtggatggag tggaagtgca caacgccaag accaagccac gggaagaaca gtacaactct 900
acctaccgcg tggtgtccgt gctcactgtg ctgcaccaag actggctgaa cgggaaggag 960
tacaagtgca aagtgtccaa caaggcgctg cctgccccaa ttgagaaaac tatctcgaaa 1020
gccaagggcc agcctcgaga accacaggtg tacaccctgc ccccatcccg ggatgagctg 1080
accaagaacc aggtcagcct gacctgcctg gtcaaaggct tctatcccag cgacatcgcc 1140
gtggagtggg agagcaatgg gcagccggag aacaactaca agaccacgcc tcccgtgctg 1200
gactccgacg gatccttctt cctctacagc aagctcaccg tggacaagag caggtggcag 1260
caggggaacg tcttctcctg cagcgtgatg catgaggctc tgcacaacca ctacacacag 1320
aagagcctct ccctgtctcc gggt 1344
<210> 178
<211> 448
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-271, тяжелая цепь с LALA
<400> 178
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr His Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Asn Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr His Ala Ala Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 179
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-271, тяжелая цепь с LALA
<400> 179
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccttcact catacttata tgagctgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcgcg atttctccga cttatagcac taccaactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acaacaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagatacaac 300
gcgtatcatg ctgctctgga ctactggggc cagggaaccc tggtcaccgt ctcgagtgct 360
agcactaagg gcccgtcggt gttcccgctg gccccatcgt ccaagagcac atcagggggt 420
accgccgccc tgggctgcct tgtgaaggat tactttcccg agcccgtcac agtgtcctgg 480
aacagcggag ccctgacctc cggagtgcat actttcccgg ctgtgcttca gtcctctggc 540
ctgtactcat tgtcctccgt ggtcaccgtc ccttcgtcct ccctgggcac ccagacctat 600
atctgtaatg tcaaccataa gccctcgaac accaaggtcg acaagaaggt cgagccgaag 660
tcgtgcgaca agactcacac ttgcccgcct tgcccagccc cggaagctgc cggtggtcct 720
tcggtgttcc tcttcccgcc caagccgaag gataccctga tgatctcacg gacccccgaa 780
gtgacctgtg tggtggtgga cgtgtcccac gaggacccgg aagtgaaatt caattggtac 840
gtggatggag tggaagtgca caacgccaag accaagccac gggaagaaca gtacaactct 900
acctaccgcg tggtgtccgt gctcactgtg ctgcaccaag actggctgaa cgggaaggag 960
tacaagtgca aagtgtccaa caaggcgctg cctgccccaa ttgagaaaac tatctcgaaa 1020
gccaagggcc agcctcgaga accacaggtg tacaccctgc ccccatcccg ggatgagctg 1080
accaagaacc aggtcagcct gacctgcctg gtcaaaggct tctatcccag cgacatcgcc 1140
gtggagtggg agagcaatgg gcagccggag aacaactaca agaccacgcc tcccgtgctg 1200
gactccgacg gatccttctt cctctacagc aagctcaccg tggacaagag caggtggcag 1260
caggggaacg tcttctcctg cagcgtgatg catgaggctc tgcacaacca ctacacacag 1320
aagagcctct ccctgtctcc gggt 1344
<210> 180
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-271, вариабельный домен
<400> 180
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr His Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Asn Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr His Ala Ala Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 181
<211> 357
<212> ДНК
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-271, вариабельный домен
<400> 181
gaagtgcaac tgctggagtc cggtggtggt ctggtacagc cgggtggttc tctgcgtctg 60
agttgcgcgg ccagtggctt taccttcact catacttata tgagctgggt gcgtcaggct 120
ccgggcaaag gtctggaatg ggttagcgcg atttctccga cttatagcac taccaactat 180
gcggatagcg tgaaaggccg ttttaccatt tctcgcgaca acaacaagaa cacgctgtac 240
ctgcagatga actcactgcg tgccgaagat acggccgtgt attactgtgc gagatacaac 300
gcgtatcatg ctgctctgga ctactggggc cagggaaccc tggtcaccgt ctcgagt 357
<210> 182
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-256-271, CDR2 (Кабат)
<400> 182
Ala Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 183
<400> 183
000
<210> 184
<400> 184
000
<210> 185
<400> 185
000
<210> 186
<400> 186
000
<210> 187
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-172-003-AA/FS28-256-271, тяжелая цепь с LALA
<400> 187
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr His Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Asn Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr His Ala Ala Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Pro Tyr Ile Ile Pro Pro Tyr Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Gly Ala Asp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly
450
<210> 188
<211> 215
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22-172-003-AA/FS28-256-271, легкая цепь
<400> 188
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Thr Val Pro Tyr Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 189
<211> 448
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 (FS20-022-049)/FS28-256-271 к OX40, тяжелая цепь с LALA
<400> 189
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr His Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Asn Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr His Ala Ala Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Tyr Trp Asp Gln Glu Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Asp Glu Gln Phe Ala Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Gln
405 410 415
Tyr Arg Trp Asn Pro Ala Asp Tyr Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 190
<211> 215
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 (FS20-022-049)/FS28-256-271 к OX40, легкая цепь
<400> 190
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Thr Val Pro Tyr Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 191
<211> 445
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22m-063-AA/HelD1.3, тяжелая цепь с LALA
<400> 191
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Arg Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Ser Thr Phe Ser Gly Tyr
20 25 30
Gly Val Asn Trp Val Arg Gln Pro Pro Gly Arg Gly Leu Glu Trp Ile
35 40 45
Gly Met Ile Trp Gly Asp Gly Asn Thr Asp Tyr Asn Ser Ala Leu Lys
50 55 60
Ser Arg Val Thr Met Leu Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Glu Arg Asp Tyr Arg Leu Asp Tyr Trp Gly Gln Gly Ser Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Pro Tyr Trp Ser Tyr Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Met Asn Tyr Arg Trp
405 410 415
Glu Leu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 192
<211> 214
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22m-063-AA/HelD1.3, легкая цепь
<400> 192
Asp Ile Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Glu Thr Val Thr Ile Thr Cys Arg Ala Ser Gly Asn Ile His Asn Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Gln Gly Lys Ser Pro Gln Leu Leu Val
35 40 45
Tyr Asn Ala Lys Thr Leu Ala Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Gln Tyr Ser Leu Lys Ile Asn Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Gly Ser Tyr Tyr Cys Gln His Phe Trp Ser Thr Pro Arg
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 193
<211> 447
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22m-063-AA/4420, тяжелая цепь с LALA
<400> 193
Glu Val Lys Leu Asp Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Pro Met Lys Leu Ser Cys Val Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ser Pro Glu Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Arg Asn Lys Pro Tyr Asn Tyr Glu Thr Tyr Tyr Ser Asp
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Ser
65 70 75 80
Val Tyr Leu Gln Met Asn Asn Leu Arg Val Glu Asp Met Gly Ile Tyr
85 90 95
Tyr Cys Thr Gly Ser Tyr Tyr Gly Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Ser Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
260 265 270
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
340 345 350
Pro Pro Ser Arg Asp Glu Pro Tyr Trp Ser Tyr Val Ser Leu Thr Cys
355 360 365
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Met Asn Tyr
405 410 415
Arg Trp Glu Leu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 194
<211> 219
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22m-063-AA/4420, легкая цепь
<400> 194
Asp Val Val Met Thr Gln Thr Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu Arg Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Lys Val Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Phe Cys Ser Gln Ser
85 90 95
Thr His Val Pro Trp Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 195
<211> 216
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb FS28-185, легкая цепь
<400> 195
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Ser Tyr Ser Ala
85 90 95
Pro Val Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val
100 105 110
Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys
115 120 125
Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg
130 135 140
Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn
145 150 155 160
Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser
165 170 175
Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys
180 185 190
Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr
195 200 205
Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 196
<211> 447
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22m-063-AA/FS28m-228-010, тяжелая цепь с LALA
<400> 196
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Phe Met Val Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Met Ile Ser Pro Lys Ser Ser Asn Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr His Ile Ser Pro Arg Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
115 120 125
Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly
130 135 140
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
145 150 155 160
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
165 170 175
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
180 185 190
Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser
195 200 205
Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr
210 215 220
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser
225 230 235 240
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
245 250 255
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
260 265 270
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
275 280 285
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
290 295 300
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
305 310 315 320
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
325 330 335
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
340 345 350
Pro Pro Ser Arg Asp Glu Pro Tyr Trp Ser Tyr Val Ser Leu Thr Cys
355 360 365
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
370 375 380
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
385 390 395 400
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Met Asn Tyr
405 410 415
Arg Trp Glu Leu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
420 425 430
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 197
<211> 215
<212> Белок
<213> Искусственная последовательность
<220>
<223> mAb2 FS22m-063-AA/FS28m-228-010, легкая цепь
<400> 197
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Pro Phe Pro Phe Ser
85 90 95
Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 198
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> Последовательность структурной петли CH3-домена Fcab FS22-172-003
<400> 198
Pro Tyr Ile Ile Pro Pro Tyr
1 5
<210> 199
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> Последовательность структурной петли CH3-домена Fcab FS22-172-003
<400> 199
Gly Ala Asp Arg Trp Leu Glu
1 5
<210> 200
<211> 217
<212> Белок
<213> Искусственная последовательность
<220>
<223> FS22-172-003-AA/FS28-256-271, легкая цепь
<400> 200
Ala Ala Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser
1 5 10 15
Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser
20 25 30
Ser Ser Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg
35 40 45
Leu Leu Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg
50 55 60
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg
65 70 75 80
Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Thr Val Pro
85 90 95
Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr
100 105 110
Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu
115 120 125
Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro
130 135 140
Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly
145 150 155 160
Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr
165 170 175
Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His
180 185 190
Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val
195 200 205
Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 201
<211> 453
<212> Белок
<213> Искусственная последовательность
<220>
<223> FS22-172-003-AA/FS28-256-271, тяжелая цепь с LALA
<400> 201
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Thr His Thr
20 25 30
Tyr Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Pro Thr Tyr Ser Thr Thr Asn Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Asn Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Asn Ala Tyr His Ala Ala Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Pro Tyr Ile Ile Pro Pro Tyr Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Gly Ala Asp Arg Trp Leu Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro Gly
450
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| МОЛЕКУЛЫ, СВЯЗЫВАЮЩИЕ МЕЗОТЕЛИН И CD137 | 2019 |
|
RU2815066C2 |
| КОНЪЮГИРОВАННЫЕ ЧЕРЕЗ CYS80 ИММУНОГЛОБУЛИНЫ | 2016 |
|
RU2756101C2 |
| ПРОТИВОРАКОВЫЕ ВАКЦИНЫ | 2017 |
|
RU2718663C2 |
| ПОЛНОСТЬЮ ЧЕЛОВЕЧЕСКИЕ АНТИТЕЛА К МЕЗОТЕЛИНУ И ИММУННЫЕ ЭФФЕКТОРНЫЕ КЛЕТКИ, НАЦЕЛЕННЫЕ НА МЕЗОТЕЛИН | 2016 |
|
RU2748281C2 |
| АНТИТЕЛА К РЕЦЕПТОРУ IL4 ДЛЯ ПРИМЕНЕНИЯ В ВЕТЕРИНАРИИ | 2019 |
|
RU2837141C2 |
| КОНСТРУКЦИИ СЛИТОГО БЕЛКА ДЛЯ ЗАБОЛЕВАНИЯ, СВЯЗАННОГО С КОМПЛЕМЕНТОМ | 2019 |
|
RU2824402C2 |
| УЛУЧШЕННЫЕ АНТИГЕНСВЯЗЫВАЮЩИЕ РЕЦЕПТОРЫ | 2018 |
|
RU2825816C2 |
| АНТИ-IL31 АНТИТЕЛА ДЛЯ ПРИМЕНЕНИЯ В ВЕТЕРИНАРИИ | 2020 |
|
RU2835543C1 |
| ХИМЕРНЫЕ РЕЦЕПТОРЫ АНТИГЕНА ПРОТИВ МЕЗОТЕЛИНА ЧЕЛОВЕКА И ИХ ПРИМЕНЕНИЕ | 2014 |
|
RU2714902C2 |
| СЛИТЫЙ БЕЛОК, ВКЛЮЧАЮЩИЙ IL-12 И АНТИТЕЛО ПРОТИВ FAP, И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2831612C1 |
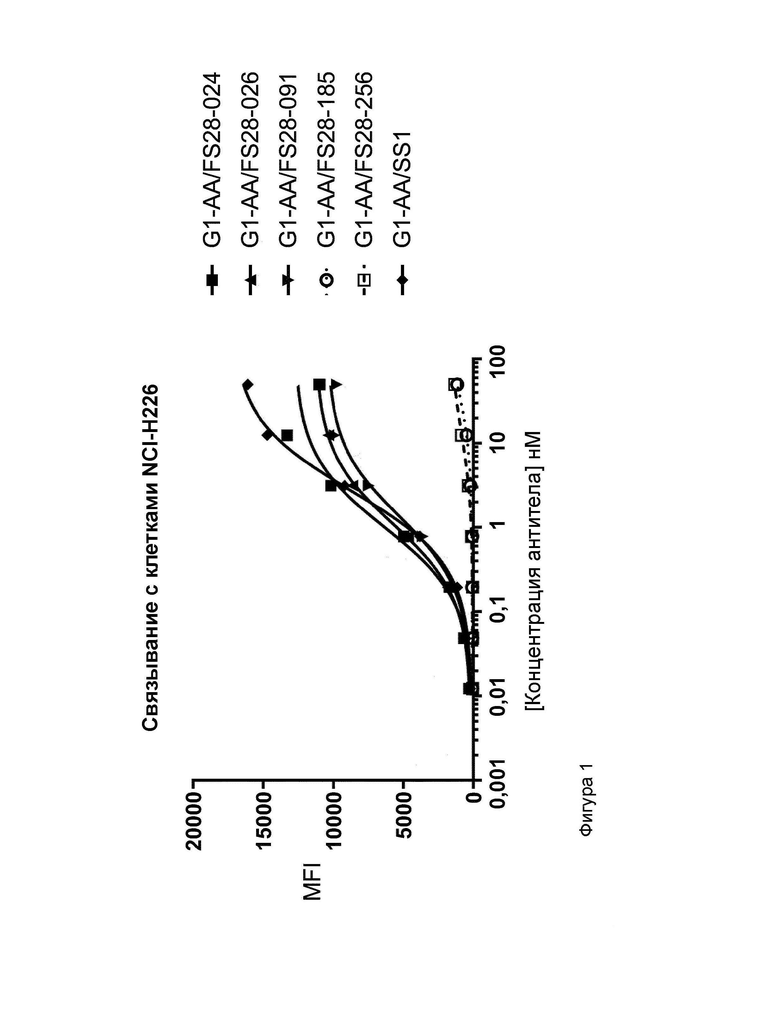
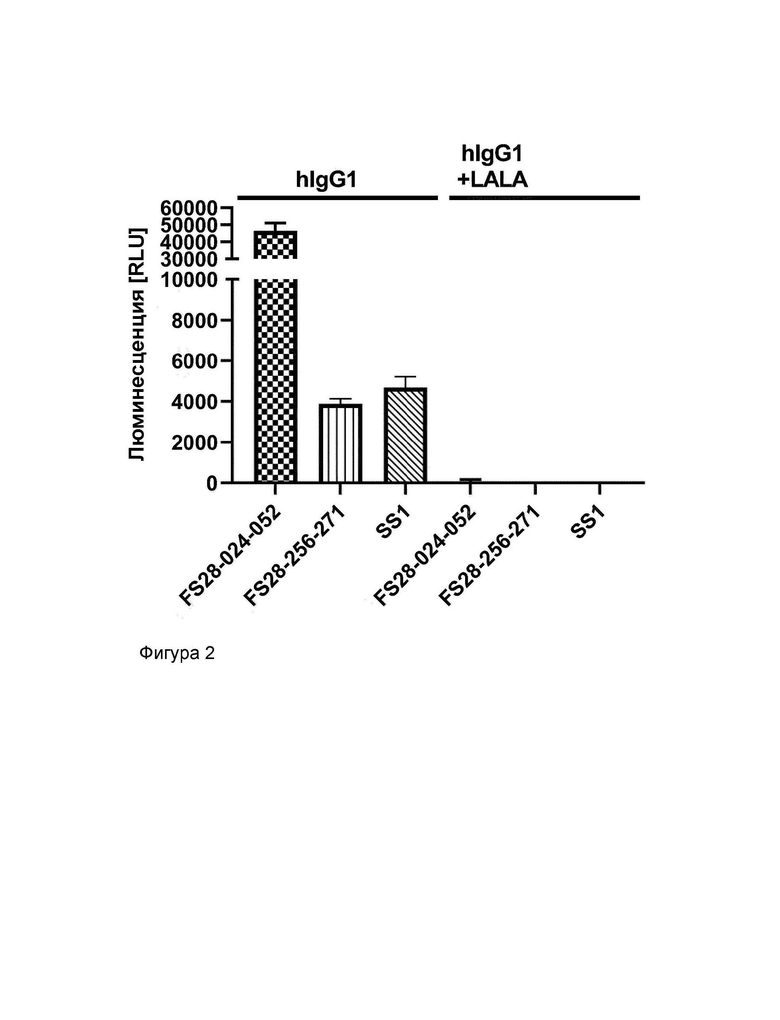
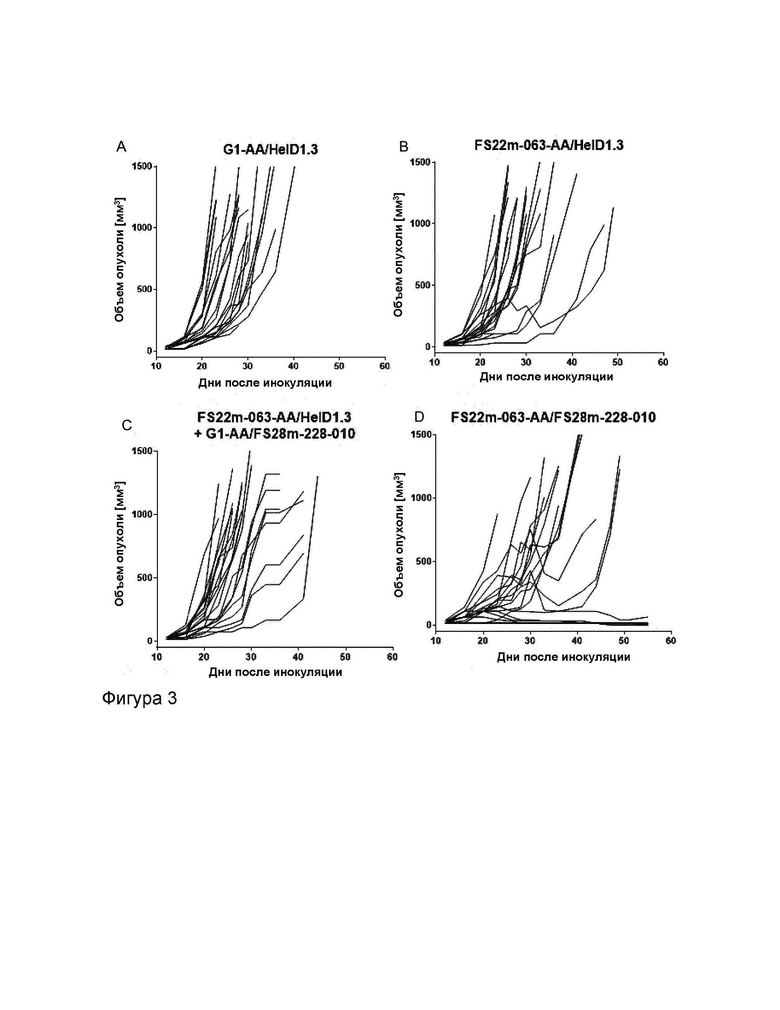
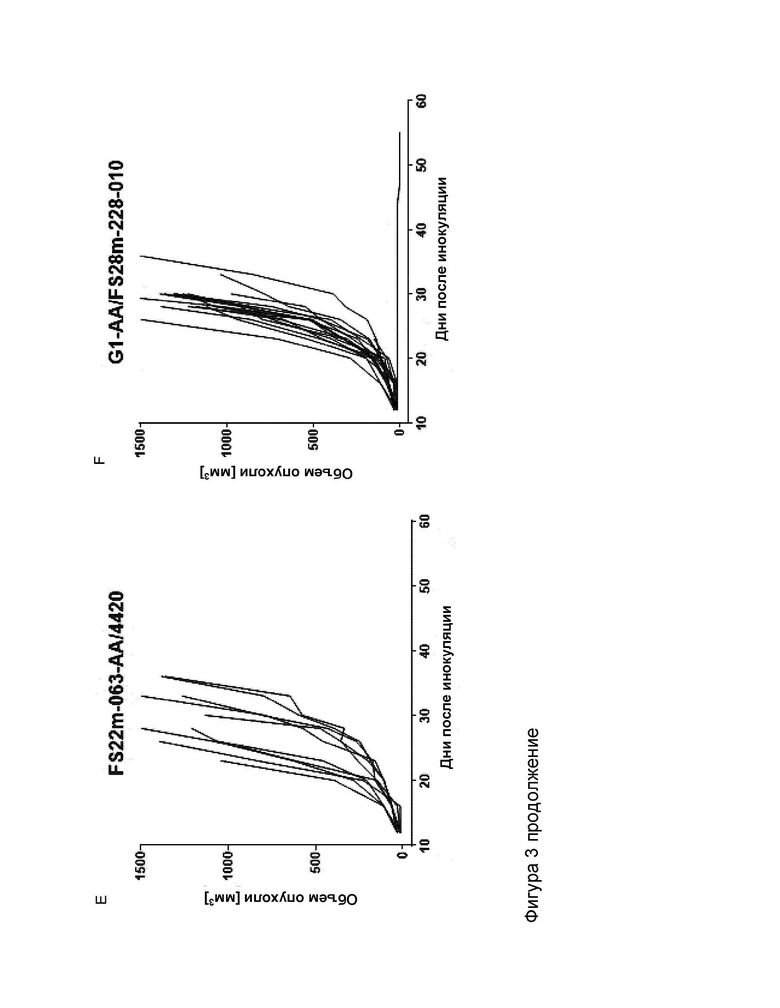
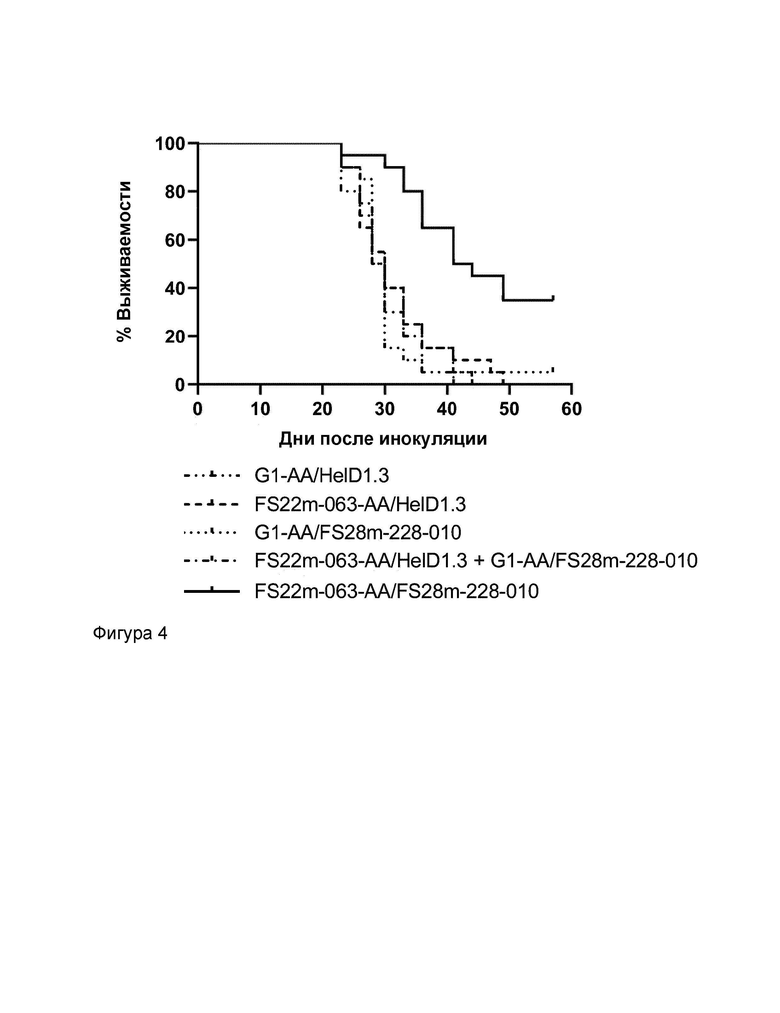
Изобретение относится к области биотехнологии, а именно к молекуле антитела, которая связывает мезотелин (MSLN), к молекуле мультиспецифичного антитела, которая специфична к MSLN и к представителю суперсемейства рецепторов фактора некроза опухоли (TNFRSF), а также к способам их получения. Также раскрыты конъюгат, содержащий вышеуказанное антитело, а также фармацевтическая композиция, содержащая вышеуказанное антитело, молекулу или конъюгат. Изобретение также относится к молекуле нуклеиновой кислоты, кодирующей антитело, которая связывает MSLN, к молекуле нуклеиновой кислоты, кодирующей молекулу мультиспецифичного антитела, к молекуле нуклеиновой кислоты, кодирующей домены вышеуказанных антител, а также к вектору и клетке-хозяину, их содержащим. Изобретение эффективно для лечения рака, причем клетки указанного рака экспрессируют MSLN на своей клеточной поверхности. 21 н. и 12 з.п. ф-лы, 4 ил., 14 табл., 6 пр.
1. Молекула антитела, которая связывает мезотелин (MSLN), при этом сайт, связывающий антиген MSLN, указанной молекулы антитела содержит последовательности VH CDR1, VH CDR2, VH CDR3, VL CDR1, VL CDR2 и VL CDR3:
(i) согласно SEQ ID NO: 98, 73, 99, 20, 21 и 44, соответственно;
(ii) согласно SEQ ID NO: 10, 11, 41, 20, 21 и 22, соответственно;
(iii) согласно SEQ ID NO: 98, 73, 99, 20, 21 и 34, соответственно;
(iv) согласно SEQ ID NO: 98, 73, 99, 20, 21 и 25, соответственно;
(v) согласно SEQ ID NO: 101, 73, 103, 20, 21 и 34, соответственно;
(vi) согласно SEQ ID NO: 98, 73, 99, 20, 21 и 43, соответственно;
(vii) согласно SEQ ID NO: 101, 73, 103, 20, 21 и 43, соответственно;
(viii) согласно SEQ ID NO: 85, 73, 75, 20, 21 и 34, соответственно;
(ix) согласно SEQ ID NO: 85, 73, 75, 20, 21 и 43, соответственно;
(x) согласно SEQ ID NO: 111, 73, 113, 20, 21 и 25, соответственно;
(xi) согласно SEQ ID NO: 101, 73, 103, 20, 21 и 25, соответственно;
(xii) согласно SEQ ID NO: 71, 73, 75, 20, 21 и 25, соответственно;
(xiii) согласно SEQ ID NO: 10, 11, 32, 20, 21 и 22, соответственно;
(xiv) согласно SEQ ID NO: 10, 11, 51, 20, 21 и 22, соответственно; или
(xv) согласно SEQ ID NO: 10, 11, 12, 20, 21 и 22, соответственно; и
при этом указанные последовательности CDR определены в соответствии со схемой нумерации ImMunoGeneTics (IMGT); и/или
указанный антигенсвязывающий сайт указанной молекулы антитела содержит последовательности VH CDR1, VH CDR2, VH CDR3, VL CDR1, VL CDR2 и VL CDR3:
(i) согласно SEQ ID NO: 97, 182, 100, 23, 24 и 44, соответственно;
(ii) согласно SEQ ID NO: 13, 14, 42, 23, 24 и 22, соответственно;
(iii) согласно SEQ ID NO: 97, 74, 100, 23, 24 и 34, соответственно;
(iv) согласно SEQ ID NO: 97, 74, 100, 23, 24 и 25, соответственно;
(v) согласно SEQ ID NO: 102, 74, 104, 23, 24 и 34, соответственно;
(vi) согласно SEQ ID NO: 97, 74, 100, 23, 24 и 43, соответственно;
(vii) согласно SEQ ID NO: 102, 74, 104, 23, 24 и 43, соответственно;
(viii) согласно SEQ ID NO: 97, 74, 100, 23, 24 и 44, соответственно;
(ix) согласно SEQ ID NO: 86, 74, 76, 23, 24 и 34, соответственно;
(x) согласно SEQ ID NO: 86, 74, 76, 23, 24 и 43, соответственно;
(xi) согласно SEQ ID NO: 112, 74, 114, 23, 24 и 25, соответственно;
(xii) согласно SEQ ID NO: 102, 74, 104, 23, 24 и 25, соответственно;
(xiii) согласно SEQ ID NO: 72, 74, 76, 23, 24 и 25, соответственно;
(xiv) согласно SEQ ID NO: 13, 14, 33, 23, 24 и 22, соответственно;
(xv) согласно SEQ ID NO: 13, 14, 52, 23, 24 и 22, соответственно; или
(xvi) согласно SEQ ID NO: 13, 14, 15, 23, 24 и 22, соответственно, и
при этом указанные последовательности CDR определены в соответствии со схемой нумерации Кабата.
2. Молекула антитела по п. 1, содержащая вариабельный домен тяжелой цепи (VH) и вариабельный домен легкой цепи (VL):
(i) согласно SEQ ID NO: 180 и 56 соответственно;
(ii) согласно SEQ ID NO: 39 и 18 соответственно;
(iii) согласно SEQ ID NO: 109 и 93 соответственно;
(iv) согласно SEQ ID NO: 109 и 79 соответственно;
(v) согласно SEQ ID NO: 121 и 93 соответственно;
(vi) согласно SEQ ID NO: 109 и 53 соответственно;
(vii) согласно SEQ ID NO: 121 и 53 соответственно;
(viii) согласно SEQ ID NO: 109 и 56 соответственно;
(ix) согласно SEQ ID NO: 63 и 93 соответственно;
(x) согласно SEQ ID NO: 63 и 53 соответственно;
(xi) согласно SEQ ID NO: 115 и 79 соответственно;
(xii) согласно SEQ ID NO: 121 и 79 соответственно;
(xiii) согласно SEQ ID NO: 69 и 79 соответственно;
(xiv) согласно SEQ ID NO: 30 и 18 соответственно;
(xv) согласно SEQ ID NO: 49 и 18 соответственно; или
(xvi) согласно SEQ ID NO: 8 и 18 соответственно.
3. Молекула антитела по п. 1, отличающаяся тем, что указанный антигенсвязывающий сайт указанной молекулы антитела содержит VH CDR1, VH CDR2, VH CDR3, VL CDR1, VL CDR2 и VL CDR3, определённые согласно схеме нумерации IMGT, согласно SEQ ID NO: 98, 73, 99, 20, 21 и 44 соответственно и/или VH CDR1, VH CDR2, VH CDR3, VL CDR1, VL CDR2 и VL CDR3, определённые согласно схеме нумерации Кабата, согласно SEQ ID NO: 97, 182, 100, 23, 24 и 44 соответственно.
4. Молекула антитела по п. 2, содержащая домен VH и домен VL согласно SEQ ID NO: 180 и 56 соответственно.
5. Молекула антитела по любому из предыдущих пунктов, отличающаяся тем, что указанная молекула антитела содержит тяжелую цепь и легкую цепь согласно SEQ ID NO: 178 и 95 соответственно, причем CH3-домен в тяжелой цепи необязательно содержит остаток лизина (К) непосредственно на С-конце последовательности CH3-домена.
6. Молекула антитела по п. 1, отличающаяся тем, что указанный антигенсвязывающий сайт указанной молекулы антитела содержит VH CDR1, VH CDR2, VH CDR3, VL CDR1, VL CDR2 и VL CDR3, определённые согласно схеме нумерации IMGT, согласно SEQ ID NO: 10, 11, 41, 20, 21 и 22 соответственно и/или VH CDR1, VH CDR2, VH CDR3, VL CDR1, VL CDR2 и VL CDR3, определённые согласно схеме нумерации Кабата, согласно SEQ ID NO: 13, 14, 42, 23, 24 и 22 соответственно.
7. Молекула антитела по п. 2, содержащая домен VH и домен VL согласно SEQ ID NO: 39 и 18 соответственно.
8. Молекула антитела по любому из пп. 1, 2, 6 или 7, отличающаяся тем, что указанная молекула антитела содержит тяжелую цепь и легкую цепь согласно SEQ ID NO: 37 и 16 соответственно, причем CH3-домен в тяжелой цепи необязательно содержит остаток лизина (К) непосредственно на С-конце последовательности CH3-домена.
9. Молекула мультиспецифичного антитела, которое специфично к MSLN и к представителю суперсемейства рецепторов фактора некроза опухоли (TNFRSF), содержащая сайт, связывающий антиген MSLN, или домен VH и домен VL молекулы антитела по любому из пп. 1-8, причем указанная молекула мультиспецифичного антитела содержит второй антигенсвязывающий сайт, связывающий TNFRSF, при этом указанный второй антигенсвязывающий сайт расположен в константном домене указанной молекулы мультиспецифичного антитела и необязательно указанный константный домен представляет собой CH3-домен.
10. Молекула мультиспецифичного антитела по п. 9, отличающаяся тем, что указанный представитель TNFRSF представляет собой CD137 или OX40.
11. Молекула мультиспецифичного антитела по п. 9 или 10, отличающаяся тем, что указанный представитель TNFRSF представляет собой CD137.
12. Молекула мультиспецифичного антитела по любому из пп. 9-11, отличающаяся тем, что указанный второй антигенсвязывающий сайт содержит структурные петли AB, CD и EF указанного константного домена, причём указанные структурные петли AB и EF или структурные петли AB, CD и EF содержат одну или более модификаций аминокислот.
13. Молекула мультиспецифичного антитела по любому из пп. 9-12, отличающаяся тем, что указанная молекула антитела способна активировать иммунную клетку в присутствии MSLN, при этом необязательно указанная иммунная клетка представляет собой Т-клетку, B-клетку, естественную клетку-киллер (NK), естественную Т-клетку-киллер (NKT) или дендритную клетку (ДК).
14. Молекула антитела по любому из пп. 1-8 или молекула мультиспецифичного антитела по любому из пп. 9-13, отличающаяся тем, что:
(i) указанная молекула антитела была модифицирована для уменьшения или устранения связывания CH2-домена указанной молекулы антитела с одним или более Fcγ-рецепторами; и/или
(ii) указанная молекула антитела не связывается с одним или более Fcγ-рецепторами.
15. Конъюгат, содержащий (i) молекулу антитела по любому из пп. 1-8 или молекулу мультиспецифичного антитела по любому из пп. 9-13 и (ii) биоактивную молекулу, для лечения рака, причем клетки указанного рака экспрессируют MSLN на своей клеточной поверхности.
16. Молекула нуклеиновой кислоты, кодирующая молекулу антитела по любому из пп. 1-8 или 14.
17. Молекула нуклеиновой кислоты, кодирующая молекулу мультиспецифичного антитела по любому из пп. 9-14.
18. Молекула нуклеиновой кислоты, кодирующая домен VH молекулы антитела по любому из пп. 1-8 или 14.
19. Молекула нуклеиновой кислоты, кодирующая домен VL молекулы антитела по любому из пп. 1-8 или 14.
20. Молекула нуклеиновой кислоты, кодирующая домен VH молекулы мультиспецифичного антитела по любому из пп. 9-14.
21. Молекула нуклеиновой кислоты, кодирующая домен VL молекулы мультиспецифичного антитела по любому из пп. 9-14.
22. Вектор, содержащий молекулу нуклеиновой кислоты по п. 16 или молекулы нуклеиновой кислоты по пп. 18 и 19, для экспрессии домена VH и домена VL молекулы антитела по любому из пп. 1-8 или 14 в клетке-хозяине, причем указанные домен VH и домен VL имеют следующие последовательности:
(i) SEQ ID NO: 180 и 56, соответственно;
(ii) SEQ ID NO: 39 и 18, соответственно;
(iii) SEQ ID NO: 109 и 93, соответственно;
(iv) SEQ ID NO: 109 и 79, соответственно;
(v) SEQ ID NO: 121 и 93, соответственно;
(vi) SEQ ID NO: 109 и 53, соответственно;
(vii) SEQ ID NO: 121 и 53, соответственно;
(viii) SEQ ID NO: 109 и 56, соответственно;
(ix) SEQ ID NO: 63 и 93, соответственно;
(x) SEQ ID NO: 63 и 53, соответственно;
(xi) SEQ ID NO: 115 и 79, соответственно;
(xii) SEQ ID NO: 121 и 79, соответственно;
(xiii) SEQ ID NO: 69 и 79, соответственно;
(xiv) SEQ ID NO: 30 и 18, соответственно;
(xv) SEQ ID NO: 49 и 18, соответственно; или
(xvi) SEQ ID NO: 8 и 18, соответственно.
23. Вектор, содержащий молекулу нуклеиновой кислоты по п. 18 для экспрессии домена VH молекулы антитела по любому из пп. 1-8 или 14 в клетке-хозяине.
24. Вектор, содержащий молекулу нуклеиновой кислоты по п. 19 для экспрессии домена VL молекулы антитела по любому из пп. 1-8 или 14 в клетке-хозяине.
25. Вектор, содержащий молекулу нуклеиновой кислоты по п. 17 или молекулы нуклеиновой кислоты по пп. 20 и 21, для экспрессии домена VH и домена VL молекулы мультиспецифичного антитела по любому из пп. 9-14 в клетке-хозяине, причем указанные домен VH и домен VL имеют следующие последовательности:
(i) SEQ ID NO: 180 и 56, соответственно;
(ii) SEQ ID NO: 39 и 18, соответственно;
(iii) SEQ ID NO: 109 и 93, соответственно;
(iv) SEQ ID NO: 109 и 79, соответственно;
(v) SEQ ID NO: 121 и 93, соответственно;
(vi) SEQ ID NO: 109 и 53, соответственно;
(vii) SEQ ID NO: 121 и 53, соответственно;
(viii) SEQ ID NO: 109 и 56, соответственно;
(ix) SEQ ID NO: 63 и 93, соответственно;
(x) SEQ ID NO: 63 и 53, соответственно;
(xi) SEQ ID NO: 115 и 79, соответственно;
(xii) SEQ ID NO: 121 и 79, соответственно;
(xiii) SEQ ID NO: 69 и 79, соответственно;
(xiv) SEQ ID NO: 30 и 18, соответственно;
(xv) SEQ ID NO: 49 и 18, соответственно; или
(xvi) SEQ ID NO: 8 и 18, соответственно.
26. Вектор, содержащий молекулу нуклеиновой кислоты по п. 20, для экспрессии домена VH молекулы мультиспецифичного антитела по любому из пп. 9-14 в клетке-хозяине.
27. Вектор, содержащий молекулу нуклеиновой кислоты по п. 21, для экспрессии домена VL молекулы мультиспецифичного антитела по любому из пп. 9-14 в клетке-хозяине.
28. Рекомбинантная клетка-хозяин, содержащая молекулу нуклеиновой кислоты по п. 16, молекулы нуклеиновой кислоты по пп. 18 и 19, вектор по п. 22 или векторы по пп. 23 и 24, для получения молекулы антитела по любому из пп. 1-8 или 14, причем указанные домен VH и домен VL молекулы антитела имеют следующие последовательности:
(i) SEQ ID NO: 180 и 56, соответственно;
(ii) SEQ ID NO: 39 и 18, соответственно;
(iii) SEQ ID NO: 109 и 93, соответственно;
(iv) SEQ ID NO: 109 и 79, соответственно;
(v) SEQ ID NO: 121 и 93, соответственно;
(vi) SEQ ID NO: 109 и 53, соответственно;
(vii) SEQ ID NO: 121 и 53, соответственно;
(viii) SEQ ID NO: 109 и 56, соответственно;
(ix) SEQ ID NO: 63 и 93, соответственно;
(x) SEQ ID NO: 63 и 53, соответственно;
(xi) SEQ ID NO: 115 и 79, соответственно;
(xii) SEQ ID NO: 121 и 79, соответственно;
(xiii) SEQ ID NO: 69 и 79, соответственно;
(xiv) SEQ ID NO: 30 и 18, соответственно;
(xv) SEQ ID NO: 49 и 18, соответственно; или
(xvi) SEQ ID NO: 8 и 18, соответственно.
29. Рекомбинантная клетка-хозяин, содержащая молекулу нуклеиновой кислоты по п. 17, молекулы нуклеиновой кислоты по пп. 20 и 21, вектор по п. 25 или векторы по пп. 26 и 27, для получения молекулы мультиспецифичного антитела по любому из пп. 9-14, причем указанные домен VH и домен VL молекулы мультиспецифичного антитела имеют следующие последовательности:
(i) SEQ ID NO: 180 и 56, соответственно;
(ii) SEQ ID NO: 39 и 18, соответственно;
(iii) SEQ ID NO: 109 и 93, соответственно;
(iv) SEQ ID NO: 109 и 79, соответственно;
(v) SEQ ID NO: 121 и 93, соответственно;
(vi) SEQ ID NO: 109 и 53, соответственно;
(vii) SEQ ID NO: 121 и 53, соответственно;
(viii) SEQ ID NO: 109 и 56, соответственно;
(ix) SEQ ID NO: 63 и 93, соответственно;
(x) SEQ ID NO: 63 и 53, соответственно;
(xi) SEQ ID NO: 115 и 79, соответственно;
(xii) SEQ ID NO: 121 и 79, соответственно;
(xiii) SEQ ID NO: 69 и 79, соответственно;
(xiv) SEQ ID NO: 30 и 18, соответственно;
(xv) SEQ ID NO: 49 и 18, соответственно; или
(xvi) SEQ ID NO: 8 и 18, соответственно.
30. Способ получения молекулы антитела по любому из пп. 1-8 или 14, включающий культивирование рекомбинантной клетки-хозяина по п. 28 в условиях, обеспечивающих получение указанной молекулы антитела, дополнительно включающий выделение и необязательно очистку указанной молекулы антитела.
31. Способ получения молекулы мультиспецифичного антитела по любому из пп. 9-14, включающий культивирование рекомбинантной клетки-хозяина по п. 29 в условиях, обеспечивающих получение указанной молекулы мультиспецифичного антитела, дополнительно включающий выделение и необязательно очистку указанной молекулы мультиспецифичного антитела.
32. Фармацевтическая композиция, содержащая в терапевтически эффективном количестве молекулу антитела по любому из пп. 1-8 или 14, молекулу мультиспецифичного антитела по любому из пп. 9-14 или конъюгат по п. 15 и фармацевтически приемлемое вспомогательное вещество, для лечения рака, причем клетки указанного рака экспрессируют MSLN на своей клеточной поверхности.
33. Применение молекулы антитела по любому из пп. 1-8 или 14, молекулы мультиспецифичного антитела по любому из пп. 9-14 или конъюгата молекулы антитела или конъюгата молекулы мультиспецифичного антитела по п. 15 для лечения рака у индивидуума, причем клетки указанного рака экспрессируют MSLN на своей клеточной поверхности.
| WO 2017052241 A1, 30.03.2017 | |||
| KAMAL ASGAROV et al., A new anti-mesothelin antibody targets selectively the membrane-associated form, MABS, 2017, VOL | |||
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| RAFFIT HASSAN et al., Phase II clinical trial of amatuximab, a chimeric anti-mesothelin antibody with pemetrexed and cisplatin in advanced unresectable pleural mesothelioma, Clin | |||
Авторы
Даты
2025-04-01—Публикация
2019-07-12—Подача