Изобретение относится к химико-фармацевтической промышленности, а именно к способу количественного определения флавоноидов в плодах и настойке боярышника, может быть использовано при экспертизе лекарственных средств, содержащих боярышник по показателю «Количественное определение».
Востребованность лекарственного растительного препарата «Боярышника плоды» в цельном и измельченном виде и «Боярышника настойка» подтверждает актуальность задачи совершенствования стандартизации в соответствии с современными требованиями по действующим веществам плодов боярышника, в частности флавоноидам, в области фитохимического анализа, фармакологического действия. В соответствии с Государственной Фармакопеей РФ стандартизация указанных лекарственных растительных средств проводится методом дифференциальной спектрофотометрии по сумме флавоноидов в пересчете на гиперозид. Нормы содержания действующих веществ составляют «не менее 0,04%» в плодах боярышника и «не менее 0,003%» в настойке боярышника. Методика основана на определении комплекса полифенольных соединений в спиртовых экстрактах боярышника с алюминия хлоридом по удельному показателю поглощения. К недостаткам данной методики можно отнести низкую селективность, невозможность раздельно определять компоненты действующих веществ и меньшую точность, так как не предусмотрено использование стандартного образца в аналогичных условиях испытания.
Из уровня техники известны и другие способы определения флавоноидов боярышника. Например, известен способ количественного определения суммы флавоноидов в листьях боярышника кроваво-красного (патент РФ № 2669162, дата приоритета 26.12.2017, МПК G01 N21/59, G01 N33/48, A61 K36/734), который включает в себя получение водно-спиртового извлечения из листьев боярышника путем экстракции 1 г измельченных листьев этиловым спиртом и определение суммы флавоноидов методом дифференциальной спектрофотометрии. Экстракцию сырья осуществляют однократно, а в качестве экстрагента используют этиловый спирт в концентрации 70%. Количественное определение суммы флавоноидов проводят при длине волны 392 нм в пересчете на 2ʺ-O-рамнозид витексина. Содержание суммы флавоноидов в пересчете на 2ʺ-O-рамнозид витексина и абсолютно сухое сырье рассчитывают по формуле
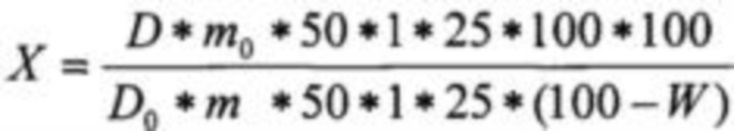 , где D - оптическая плотность испытуемого раствора; Do - оптическая плотность раствора стандартного образца 2ʺ-O-рамнозид витексина; m - масса сырья, г; mo - масса стандартного образца 2ʺ-O-рамнозид витексина, г; W - потеря в массе при высушивании в процентах. Однако предложенный способ недостаточно селективен, позволяет оценить только суммарное содержание целевой группы биологически активных веществ и вследствие этого приводит к завышению получаемых результатов.
, где D - оптическая плотность испытуемого раствора; Do - оптическая плотность раствора стандартного образца 2ʺ-O-рамнозид витексина; m - масса сырья, г; mo - масса стандартного образца 2ʺ-O-рамнозид витексина, г; W - потеря в массе при высушивании в процентах. Однако предложенный способ недостаточно селективен, позволяет оценить только суммарное содержание целевой группы биологически активных веществ и вследствие этого приводит к завышению получаемых результатов.
Наиболее близким аналогом выбран способ определения флавоноидов боярышника в лекарственных формах методом высокоэффективной жидкостной хроматографии в пересчет на рутин («Определение флавоноидов боярышника в лекарственных формах методом высокоэффективной жидкостной хроматографии», Салахов А.И., Гармонов С.Ю., Прикладная химия и химическая технология), которая включает растворение 20 таблеток навески в 10 мл метанола в мерной колбе объемом 25 мл при нагревании до 60°С, параллельно готовят раствор рабочего стандартного раствора (РСО), оба раствора обрабатывают ультразвуком 10 мин, добавляют 5 мл воды, доводят до метки 0,02 М фосфатным буферным раствором и фильтруют через гидрофобный мембранный фильтр, далее хроматографируют испытуемый раствор и раствор РСО (оптимальная длина волны предложена авторами - 354 нм), получая хроматограммы каждого раствора, рассчитывают количество каждого компонента в анализируемых таблетках по формуле:
Хк = (Sk mст mс)/(Sсп mн), где
Хк - количество компонента;
Sk и Sсп - средние значения площадей пиков определяемых компонентов на хроматограммах испытуемого раствора и раствора РСО соответственно;
mст mс и mн - масса стандарта определяемого вещества в растворе РСО, средняя масса таблетки и масса навески растертых таблеток, взятой для приготовления испытуемого раствора соответственно в граммах. Недостатками приведенного способа определения флавоноидов боярышника можно отметить неполную экстракцию и невысокий выход целевых действующих веществ, что приводит к снижению точности количественного расчета флавоноидов в исследуемой пробе.
Технической задачей, решаемой изобретением, является создание селективного способа, позволяющего достоверно оценить содержание флавоноидов в плодах и настойке боярышника по показателю «Количественное определение».
Техническим результатом применения предложенного авторами способа является повышение выхода целевых действующих веществ и точности определения флавоноидов в плодах и настойке боярышника.
Технический результат достигается способом количественного определения флавоноидов в плодах и настойке боярышника, включает этап проведения пробоподготовки, этап проведения хроматографирования исследуемой пробы методом ВЭЖХ и этап расчета флавоноидов в исследуемой пробе плодах или настойке боярышника, при этом на этапе пробоподготовки проводят кислотный гидролиз 25% раствором хлористоводородной кислоты исследуемой пробы при нагревании на водяной бане при температуре 85°С в течение 60 мин, далее осуществляют хроматографирование испытуемого раствора и 0,005%-ного стандартного раствора кверцетина в метаноле в условиях изократического элюирования, рассчитывают количественное содержание суммы флавоноидов в пересчете на гиперозид методом внешнего стандарта, при этом количественное определение (Х) в плодах боярышника (1) и настойке боярышника (2) вычисляют по формулам (1)-(2) соответственно:
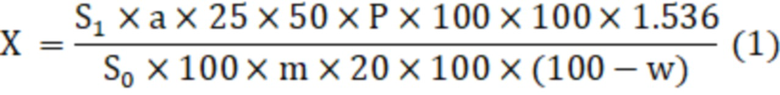
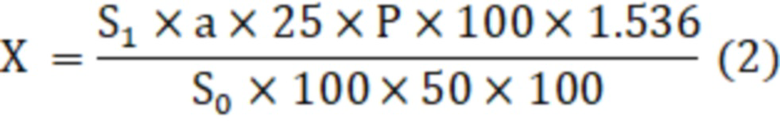
Х - содержание суммы флавоноидов в пересчете на гиперозид в препарате, %;
S0 - площадь пика кверцетина на хроматограмме раствора стандартного образца;
S1 - площадь пика кверцетина на хроматограмме испытуемого раствора;
a - навеска стандартного образца кверцетина, г;
m - навеска препарата (плодов боярышника), г;
w - влажность препарата (плодов боярышника), %;
Р - содержание действующего вещества в стандартном образце кверцетина, %;
1,536 - коэффициент пересчета кверцетина на гиперозид, равный отношению молекулярных масс гиперозида и кверцетина (464,38/302,24).
Пример 1. Осуществление способа количественного определения флавоноидов в плодах и настойке боярышника
Способ количественного определения флавоноидов в плодах и настойке боярышника включает этапы: пробоподготовки, проведения хроматографирования методом ВЭЖХ и этап расчета флавоноидов в исследуемой пробе плодах или настойки боярышника.
Этап пробоподготовки для определения флавоноидов в плодах боярышника включает помещение пробы 10 г точной навески препарата боярышника плоды, измельченного до размера частиц 2 мм в аппарат непрерывной экстракции (аппарат Сокслета) соединенной с колбой, содержащей 250 мл метанола и экстракцию испытуемой пробы непрерывно в течение 5 ч. Охлаждают и выпаривают под вакуумом растворитель из экстракта до 15 мл. Полученный раствор количественно переносят в мерную колбу вместимостью 25 мл и доводят метанолом до метки. 20,0 мл полученного раствора переносят в колбу с обратным холодильником, добавляют 2 мл 25 % хлористоводородной кислоты и нагревают на водяной бане при 85°С в течение 60 мин. Охлаждают, содержимое колбы количественно переносят в мерную колбу вместимостью 50 мл, доводят метанолом до метки, перемешивают. Фильтруют через мембранный фильтр 0,45 мкм, CHROMAFIL Xtra PET-45/25.
Этап пробоподготовки для определения флавоноидов в настойке боярышника включает помещение пробы 50 мл настойки боярышника в колбу со шлифом вместимостью 250 мл, добавление 5 мл кислоты хлористоводородной разведенной 25% и нагревание с обратным холодильником на водяной бане при температуре 85 С в течение 60 мин. После охлаждения до комнатной температуры содержимое колбы упаривают под вакуумом приблизительно до 10 мл. Полученный раствор количественно переносят в мерную колбу вместимостью 25 мл и доводят метанолом до метки.
Авторами предложен способ кислотного гидролиза флавоноидов в плодах боярышника и настойке боярышника до их агликона - кверцетина в среде хлористоводородной кислоты 25% при нагревании до 85°С в течение 60 мин. Это позволяет использовать только один стандартный образец - кверцетин. Для пересчета полученного значения на гиперозид, основной флавоноид боярышника с доказанной эффективностью, в формуле расчета используется коэффициент, равный отношению молекулярных масс гиперозида и кверцетина.
Предлагаемые авторами условия пробоподготовки способствуют полноте высвобождения определяемых действующих веществ из плодов боярышника и настойки боярышника, что повышает точность определения.
Хроматографирование проводили на обращеннофазовой колонке Gemini C18 с октадецилсилилсиликагельным сорбентом, размер колонки 250×4,6 мм, размер частиц 5 мкм. Детектировали при длине волны 370 нм с помощью спектрофотометрического детектора. Скорость потока составляла 1,5 мл/мин, температура колонки 25°С, объем вводимой пробы 10 мкл. Подвижная фаза состояла из смеси метанола, воды и кислоты фосфорной в объемном соотношении 100:100:1. Концентрацию испытуемого вещества определяли методом внешнего стандарта. В качестве стандартного раствора использовали 0,5 мг/мл раствор кверцетина в метаноле. Время удерживания пика кверцетина в описанных условиях составляло около 10 мин.
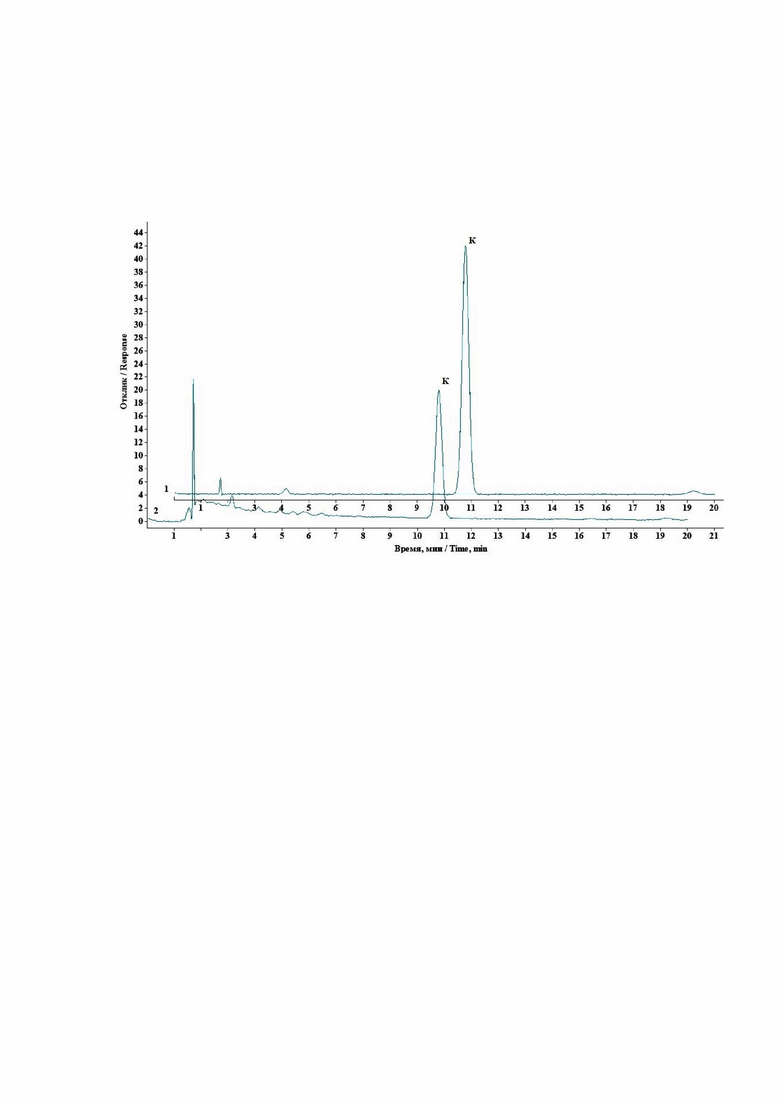
На чертеже представлены типичные хроматограммы испытуемого раствора (2) и стандартного образца кверцетина (1) представлены; К - пик, соответствующий кверцетину.
Оценка пригодности хроматографической системы по хроматограмме стандартного образца удовлетворяет требованиям ОФС.1.2.1.2.0001 «Хроматография» ГФ XV (значение асимметрии пика кверцетина - 1,02; эффективность колонки по пику кверцетина - 7652 теоретических тарелок; относительное стандартное отклонение площади пика кверцетина для 6 определений - 0,59%).
Содержание суммы флавоноидов в пересчете на гиперозид составило 0,024 %, RSD = 1,80 % (образец 1), 0,043%, RSD = 0,21 % (образец 2) и 0,021%, RSD = 1,92 % (образец 3).
Разработанный способ количественного определения суммы флавоноидов в пересчете на гиперозид был также адаптирован для препарата «Боярышника настойка». Пробоподготовка заключалась в проведении кислотного гидролиза, концентрировании пробы и хроматографировании полученного испытуемого раствора в условиях, описанных для боярышника плодов. Содержание суммы флавоноидов в пересчете на гиперозид в настойке боярышника составило 0,02 %, RSD = 1,57%.
Пример 2. Количественное определение суммы флавоноидов в пересчете на гиперозид в плодах боярышника заявляемым способом
Для приготовления испытуемого раствора около 10,05677 г / 9,15416 г / 10014,21 (точная навеска) предварительно измельченных до размера частиц 2 мм плодов боярышника (влажность сырья, w = 6,48%), помещают в аппарат непрерывной экстракции (аппарат Сокслета), соединенный с колбой, содержащей 250 мл метанола, экстрагируют испытуемый образец в течение 5 ч. Охлаждают и выпаривают под вакуумом растворитель из экстракта до 15 мл. Полученный раствор количественно переносят в мерную колбу вместимостью 25 мл и доводят метанолом до метки. 20,0 мл полученного раствора переносят в колбу с обратным холодильником, добавляют 2 мл 25 % кислоты хлористоводородной и нагревают на водяной бане при 85°С в течении 60 мин. Охлаждают, содержимое колбы количественно переносят в мерную колбу вместимостью 50 мл, доводят метанолом до метки, перемешивают. Фильтруют через мембранный фильтр 0,45 мкм, CHROMAFIL Xtra PET-45/25.
Для приготовления стандартного раствора около 5,380 мг / 5,680 мг (точная навеска) кверцетина (чистота стандарта Р = 81,7%) помещают в мерную колбу 100 мл, доводят до метки метанолом.
Хроматографирование проводят на обращенно-фазовой колонке Gemini C18, размер колонки 250×4,6 мм, размер частиц 5 мкм. Детектирование осуществляли с помощью спектрофотометрического детектора при длине волны 370 нм. Скорость потока - 1,5 мл/мин, температура колонки - 25°С, объем вводимой пробы - 10 мкл. Подвижная фаза состояла из смеси метанола, воды и кислоты фосфорной в объемном соотношении 100:100:1.
Количественное определение (Х) в плодах боярышника вычисляли по формуле:
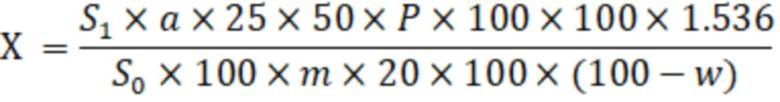
Содержание суммы флавоноидов в пересчете на гиперозид в плодах боярышника составило 0,02370 %, RSD = 0,18 %.
Пример 2. Количественное определение суммы флавоноидов в пересчете на гиперозид в настойке боярышника заявляемым способом
Для приготовления испытуемого раствора 50,0 мл настойки боярышника помещали в колбу со шлифом вместимостью 250 мл, добавляли 5 мл кислоты хлористоводородной разведенной 25% и нагревали с обратным холодильником на водяной бане при температуре 85 С в течение 60 мин. После охлаждения до комнатной температуры содержимое колбы упаривали под вакуумом приблизительно до 10 мл. Полученный раствор количественно переносили в мерную колбу вместимостью 25 мл и доводили метанолом до метки.
Для приготовления стандартного раствора около 6,000 мг / 5,950 мг (точная навеска) кверцетина (чистота стандарта Р = 81,7%) помещают в мерную колбу 100 мл, доводят до метки метанолом.
Хроматографирование проводят на обращенно-фазовой колонке Gemini C18, размер колонки 250×4,6 мм, размер частиц 5 мкм. Детектирование осуществляли с помощью спектрофотометрического детектора при длине волны 370 нм. Скорость потока - 1,5 мл/мин, температура колонки - 25°С, объем вводимой пробы - 10 мкл. Подвижная фаза состояла из смеси метанола, воды и кислоты фосфорной в объемном соотношении 100:100:1.
Количественное определение (Х) в настойке боярышника вычисляли по формуле:
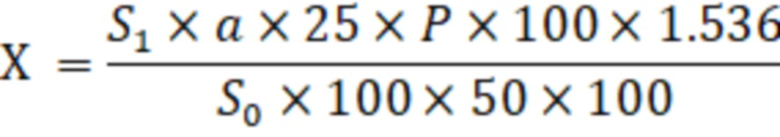
Содержание суммы флавоноидов в пересчете на гиперозид в настойке боярышника составило 0,01895 %, RSD = 1,57%.
Пример 3. Оценка специфичности, линейности, повторяемости, внутрилабораторной прецизионности способа количественного определения флавоноидов в плодах и настойке боярышника
В рамках валидационных исследований была проведена оценка специфичности, линейности, повторяемости, внутрилабораторной прецизионности.
Оценку линейности проводили по стандартному раствору кверцетина. Условия регистрации хроматограмм приведены выше. Полученные данные статистически обрабатывали и строили график зависимости аналитического сигнала от концентрации определяемого вещества в анализируемой пробе в пределах аналитической области методики от 30 % до 200 %. Зависимость содержания действующих веществ в испытуемом образце (мг/мл) от площади пика кверцетина описывалась уравнением y = 16135х + 7,9127. Квадрат коэффициента корреляции (r2) составил 0,9999 (критерий линейности ⋅≥0,99), что подтверждает линейность в рассматриваемом диапазоне.
Прецизионность оценивалась для 6 определений для испытуемых растворов со 100% содержанием определяемого вещества с помощью валидированных программ статистической обработки экспериментальных данных Microsoft Excel с вычислением граничных значений доверительного интервала среднего результата и определением ошибки единичного определения.
Таблица. Результаты валидации аналитической методики количественного определения суммы флавоноидов в пересчете на гиперозид
y = bx + a
Коэффициент корреляции
|r| ≥ 0,99
y = 16135х + 7,9127
Коэффициент корреляции
r2 = 0,9999
|r| > 0,99
область
Повторяемость
Внутрилабораторная прецизионность
Полученное значение критерия Фишера, вычисленное по результатам проведения испытаний разными исполнителями на разном оборудовании, должно быть меньше табличного значения
F = S12/S22
F ≤ Fтабл.
Determination
Results %
S = 0,0003; RSD = 1,32 %
Доверительный интервал
(Р = 95%, a = 0,05) ± 0,0003
Оборудование 1
Оборудование 2
Fтабл.(0,05; 2; 2) = 19,00
F < Fтабл.
Таблица составлена авторами по данным проведенных исследований.
Примечание. RSD - относительное стандартное отклонение; t (0,95; n-2) - коэффициент Стьюдента; F, Fтабл. - критерий Фишера полученный и табличный соответственно; S1, S2 - стандартное отклонение; Р = 95% - доверительная вероятность, a = 0,05 - уровень значимости.
В ходе проведения валидации способа получены результаты, соответствующие критериям приемлемости (табл. 3). Разработанный авторами способ количественного определения флавоноидов в пересчете на гиперозид в плодах боярышника позволяет получать достоверные, воспроизводимые результаты, повысить выход целевых действующих веществ и точности определения флавоноидов в плодах и настойке боярышника.
Пример 4. Предлагаемый авторами способ более точный, в таблице 2 приведены данные, полученные экспериментальным путем при применении условий пробоподготовки по способу прототипу и по способу, предлагаемому авторами
Таблица 2
Таким образом, разработанный авторами способ количественного определения флавоноидов в плодах боярышника и настойке боярышника позволяет повысить выход целевых действующих веществ и точность определения флавоноидов в плодах и настойке боярышника.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения суммы сесквитерпеновых кислот в пересчете на валереновую кислоту методом ВЭЖХ в лекарственных средствах | 2020 |
|
RU2744231C1 |
| Способ количественного определения аскорбиновой кислоты в лекарственных растительных препаратах | 2023 |
|
RU2801885C1 |
| Способ количественного определения конваллятоксина в лекарственных препаратах, содержащих сердечные гликозиды ландыша | 2024 |
|
RU2837486C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ НАРЦИССИНА В ЦВЕТКАХ КАЛЕНДУЛЫ ЛЕКАРСТВЕННОЙ | 2015 |
|
RU2599016C1 |
| Способ получения лекарственного средства "Боярышника плодов настойка" | 2021 |
|
RU2772208C1 |
| Способ количественного определения папаверина гидрохлорида и его родственных примесей в лекарственных средствах | 2021 |
|
RU2772608C1 |
| Способ определения флавоноидов в траве горца перечного и траве горца птичьего | 2024 |
|
RU2839147C1 |
| Способ определения арбутина в листьях толокнянки | 2023 |
|
RU2802173C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ГИПОТЕНЗИВНОЙ АКТИВНОСТЬЮ | 2000 |
|
RU2182487C2 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО АДАПТОГЕННОЙ АКТИВНОСТЬЮ | 1997 |
|
RU2135198C1 |
Изобретение относится к аналитической химии и может быть использовано в фармацевтической промышленности. Способ количественного определения флавоноидов в плодах и настойке боярышника включает этап проведения пробоподготовки, этап проведения хроматографирования исследуемой пробы методом ВЭЖХ и этап расчета флавоноидов в исследуемой пробе: плодах или настойке боярышника. На этапе пробоподготовки проводят кислотный гидролиз 25% раствором хлористоводородной кислоты исследуемой пробы при нагревании на водяной бане при температуре 85°С в течение 60 мин, далее осуществляют хроматографирование испытуемого раствора и 0.005%-ного стандартного раствора кверцетина в метаноле в условиях изократического элюирования, рассчитывают количественное содержание суммы флавоноидов в пересчете на гиперозид методом внешнего стандарта. Техническим результатом является повышение точности определения флавоноидов в плодах и настойке боярышника. 1 ил., 2 табл.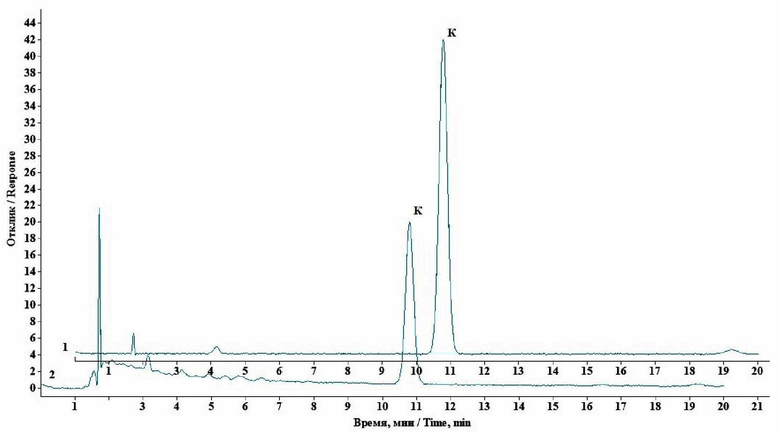
Способ количественного определения флавоноидов в плодах и настойке боярышника, включающий этап проведения пробоподготовки, этап проведения хроматографирования исследуемой пробы методом ВЭЖХ и этап расчета флавоноидов в исследуемой пробе: плодах или настойке боярышника, при этом на этапе пробоподготовки проводят кислотный гидролиз 25% раствором хлористоводородной кислоты исследуемой пробы при нагревании на водяной бане при температуре 85°С в течение 60 мин, далее осуществляют хроматографирование испытуемого раствора и 0.005%-ного стандартного раствора кверцетина в метаноле в условиях изократического элюирования, рассчитывают количественное содержание суммы флавоноидов в пересчете на гиперозид методом внешнего стандарта, при этом количественное определение (Х) в плодах боярышника (1) и настойке боярышника (2) вычисляют по формулам (1)-(2) соответственно:
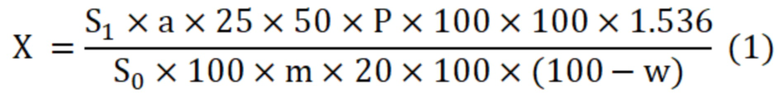
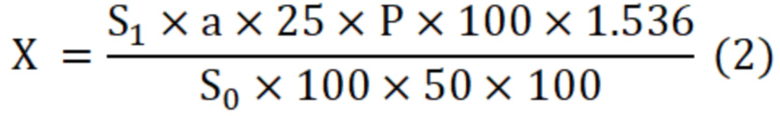 ,
,
где: Х – содержание суммы флавоноидов в пересчете на гиперозид в препарате, %,
S0 – площадь пика кверцетина на хроматограмме раствора стандартного образца,
S1 – площадь пика кверцетина на хроматограмме испытуемого раствора;
a – навеска стандартного образца кверцетина, г,
m – навеска препарата (плодов боярышника), г,
w – влажность препарата (плодов боярышника), %,
Р – содержание действующего вещества в стандартном образце кверцетина, %.
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СУММЫ ФЛАВОНОИДОВ В ЛИСТЬЯХ ТОПОЛЯ ЧЕРНОГО | 2018 |
|
RU2701726C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СУММЫ ФЛАВОНОИДОВ В ПЛОДАХ БОЯРЫШНИКА МЯГКОВАТОГО | 2018 |
|
RU2695760C1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ФЛАВОНОИДОВ В ЖЕЛЧЕГОННОМ СБОРЕ № 3 | 2014 |
|
RU2554780C1 |
Авторы
Даты
2025-04-11—Публикация
2024-10-22—Подача