Область техники
Группа изобретений относится к области медицины и биомедицинской инженерии и может быть использована в аппаратах гемодиализа для очистки крови. Рассматривается возможность очистки крови, содержащей молекулы различных метаболитов, отличающихся размером, в том числе при почечной недостаточности.
Уровень техники
Известен способ производства полупроницаемых мембран для очистки водных биологических жидкостей, в частности для очищения экстракорпоральной крови посредством гемодиализа (RU 2108144, МПК: A61M 1/18, опубл. 10.04.1998). Мембраны предпочтительно имеют форму полых волокон. Изготавливают их из гидрофильного полимерного материала, предпочтительно ацетата целлюлозы. Мембраны имеют следующие характеристики: коэффициент ультрафильтрации (Kuf) от 15 до 55 мл/ч • мм рт.ст. • м2, коэффициент массопередачи для мочевины (Kov (мочевина)) не менее 38 × 10-3 см/мин и отношение Kov (мочевина)/Kuf не менее 2,5 × 10-3. Полые волокна таких мембран, пригодных для гемодиализа, имеют диаметр внутреннего канала от 175 до 210 мкм и толщину стенок от 10 до 35 мкм. В соответствии с описанными методами изготовления мембран расплав, содержащий от 32 до 40 мас.% ацетата целлюлозы, от 5 до 10 мас.% глицерина и от 50 до 65 мас.% полиэтиленгликоля, экструдируют, получая полые волокна; волокна охлаждают, подвергают холодной вытяжке, отмывают водой и репластифицируют раствором глицерина.
К недостаткам мембран на основе целлюлозы относят более низкую биосовместимость по сравнению с синтетическими в контакте с кровью.
Известен гемодиафильтровальный/гемофильтровальный картридж, образованный первой ступенью гемодиафильтрации, и второй ступенью гемофильтрации, при этом обе ступени расположены в одном картридже. Картридж содержит отдельный корпус, например цилиндрический, в котором расположена внутренняя разделительная стенка, разделяющая корпус на первое и второе отделения, первое из которых связано с первой ступенью фильтрации, а второе - со второй ступенью фильтрации. Картридж имеет впускные и выпускные патрубки для крови и диазизата. Первая ступень фильтрации сообщается с впуском для крови, а вторая ступень фильтрации - с выпуском для крови. Следовательно, гемодиафильтровальный/гемофильтровальный картридж осуществляет диафильтрацию и гемофильтрацию в отдельном корпусе путем размещения в первом отделении первых фильтрующих элементов (первого пучка полых волокон), а во втором отделении - вторых фильтрующих элементов (второго пучка полых волокон). Таким образом, предлагаемый картридж своим внешним видом схож с обычным диализатором за исключением того, что патрубки для диализата расположены на противоположных сторонах картриджа. Впускной и выпускной патрубки для крови предпочтительно расположены на первом торце картриджа или вблизи него. Впуск и выпуск для крови могут быть выполнены в виде двух отдельных крышек или в виде одной крышки, разделенной внутренней стенкой или уплотнением, которая (которое) разделяет указанные фильтрующие элементы, первые и вторые, на первую ступень гемодиафильтрации и вторую ступень гемофильтрации (см. патенты RU 2292225, МПК: A61M 1/16, опубл. 27.01.2007).
Известно устройство для очистки крови, содержащее мембрану, выполненную из полых волокон, в которых иммобилизованы молекулы лектина внутри пористой внешней части мембраны (RU 2353399, МПК: A61M 1/16, опубл. 27.01.2006). Устройство включает в себя множество каналов полых волокон ультрафильтрационнной мембраны, которые образуют фильтрационную камеру. Впускное отверстие и отверстие для выходящего потока сообщаются с фильтрационной камерой. Ультрафильтрационная мембрана является предпочтительно анизотропной мембраной с плотной или удерживающей стороной, обращенной к току крови. Мембрана традиционно сформирована из любых типов полимеров, известных в уровне техники, например полисульфона, полиэфирсульфона, полиамидов, полиимидов, ацетата целлюлозы и полиакриламида. Предпочтительно мембрана обладает порами диаметром 200-500 нм. Мембраны предпочтительно имеют внутренний диаметр 0,3 мм и внешний диаметр 0,5 мм. При работе устройства раствор, содержащий лектины, загружается в устройство через отверстие. Лектинам предоставляется возможность иммобилизироваться на внешней стороне мембраны. Несвязанные лектины могут быть собраны из отверстия 50 посредством промывания солевым раствором или другими растворами.
Недостатком данного устройства является недостаточная удельная площадь рабочей поверхности мембраны, что отсутствует в мембране, модифицированной наночастицами (Ст. Мельниковой в Нефрологии).
Наиболее близким аналогом является устройство для очистки крови в аппарате «исскуственная почка». Устройство содержит цилиндрический корпус с впускными и выпускными патрубками, съемные крышки на его торцах, закрепленную в нем полуволоконную мембрану. Материал мембраны представляет собой сополимер, включающий гидрофобное звено и гидрофильное звено, причем в качестве гидрофобного полимера может быть использован полимер, выбранный из группы, состоящей из полимера на основе полисульфона, полиметакрилата, полиакрилата, полиэфира или полистирола, а в качестве гидрофильного звена выступает звено винилового эфира алкилкарбоновой кислоты или винилпирролидона (RU 2748752, МПК: B01D 71/00, опубл. 31.05.2021).
Недостатком данной мембраны является недостаточная удельная площадь рабочей поверхности мембраны.
Раскрытие сущности изобретения
Техническая проблема, на решение которой направлены изобретения, заключается в разработке для изменения проницаемости мембран нового перспективного композиционного материала с применением биосовместимых наноматериалов для аппарата «искусственная почка» и способа его изготовления.
Технический результат заключается в повышении рабочей поверхности половолоконных мембран из полисульфона при снижении временных затрат на проведение процедуры гемодиализа при повышении её качества, повышении проницаемости и сорбции мембран в рамках диффузионных процессов гемодиализа.
Технический результат достигается тем, что в гемодиализаторе, включающем цилиндрический корпус с впускными и выпускными патрубками, съемные крышки с патрубками на его торцах, вблизи которых к корпусу закреплена половолоконная мембрана заливкой из полиуретана, плотно прилегающая к нему и волокнам из полисульфона, согласно изобретению, внутренняя поверхность волокон модифицирована наночастицами бемита размером 30 нм - 100 нм. Длина волокон мембраны составляет 150 мм, а их внутренний диаметр 200 мкм.
Технический результат достигается тем, что способ изготовления половолоконной мембраны для гемодиализатора, включает приготовление в емкости состава из 1,5% - 5% раствора поверхностно-активного вещества (ПАВ) в дистиллированной воде и наночастиц бемита размером 30 нм - 100 нм, помещение емкости в ультразвуковую ванну и воздействие ультразвуком на компоненты состава в течение 10 минут при рабочей частоте колебаний преобразователей 35±2 кГц для получения суспензии, размещение гемодиализатора нижней частью со снятыми колпачками вертикально в емкости с суспензией и при той же рабочей частоте пропитку волокон суспензией сначала с одной его стороны, а затем - с другой методом ультразвукового капиллярного эффекта, после чего гемодиализатор сушат в сушильном шкафу. Сушку гемодиализатора осуществляют в течение 3 часов при 100-120°С.
Краткое описание чертежей
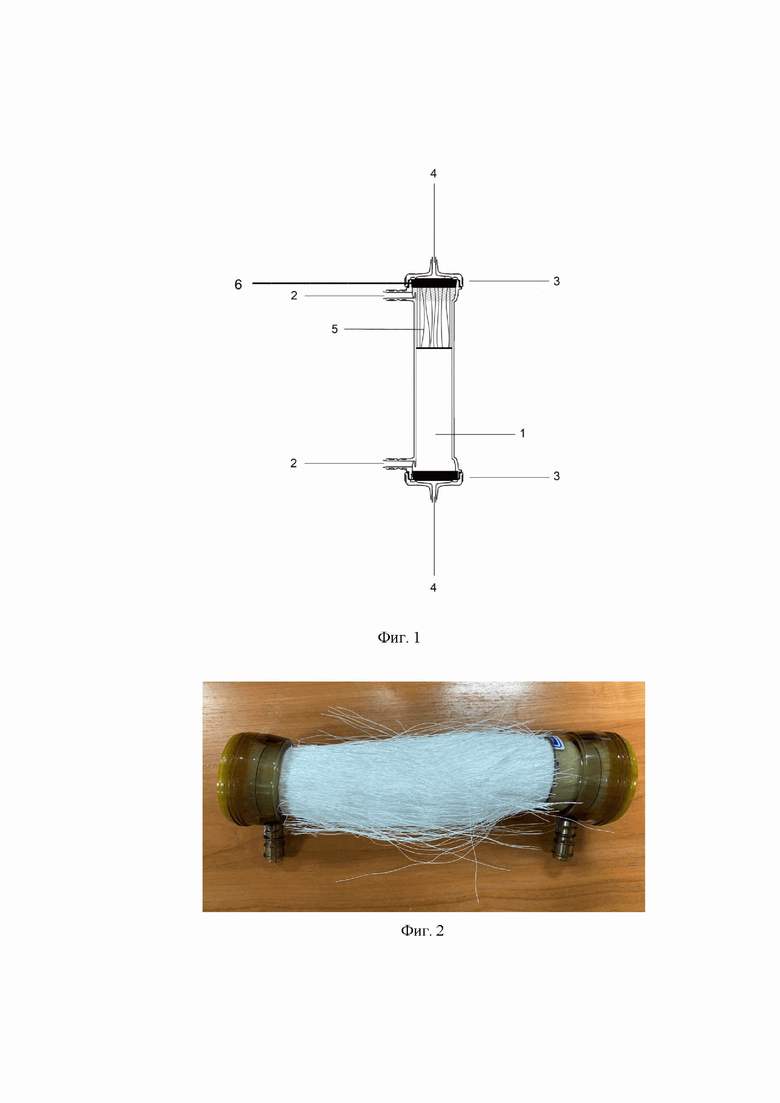
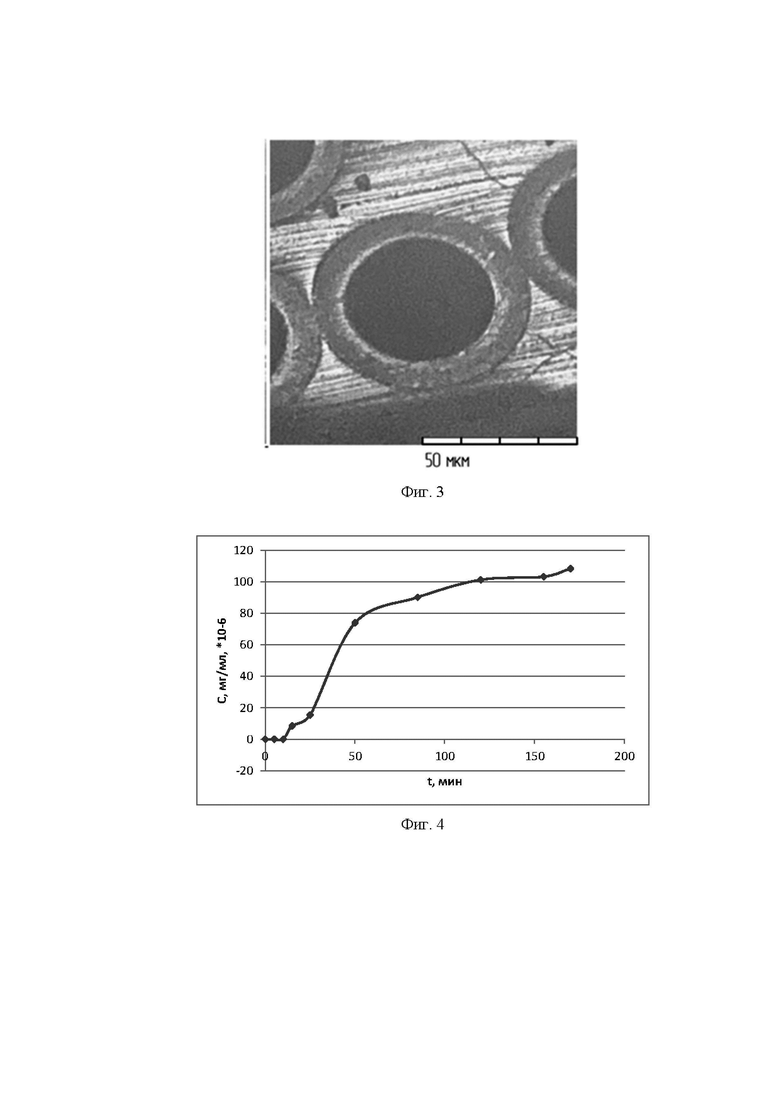
Изобретения поясняются чертежами, где на фиг. 1 приведен общий вид гемодиализатора в разрезе; на фиг. 2 - фото гемодиализатора при срезанном корпусе, со снятыми крышками и мембраной, которая внутри волокон модифицирована наночастицами бемита; на фиг. 3 приведена структура мембраны (вид с торца): приведены ассиметричные полые волокна из полисульфона, модифицированного наночастицами бемита, в заливке из полиуретана, при увеличении 130× (частиц не видно при данном увеличении); на фиг. 4 - динамическая кривая массопереноса эозина через мембранну, модифицированную наночастицами бемита в дистиллированную воду.
Осуществление изобретения
Заявляемое устройство содержит (фиг. 1) цилиндрический корпус 1 с патрубками для ввода и вывода воды 2. Корпус снабжен съемными крышками 3 с патрубками для ввода венозной крови и вывода очищенной крови 4. Вблизи торцов к корпусу прикреплена половолоконная мембрана из полисульфоновых полых волокон 5 заливкой из полиуретана 6, плотно прилегающей к нему и волокнам (фиг. 2, 3). При этом внутренняя поверхность волокон модифицирована наночастицами бемита размером 30 нм - 100 нм. Получить эффективное увеличение удельной площади поверхности мембраны можно только с применением наночастиц. Частицы размером менее 30 нм получить очень сложно, а при размерах более 100 нм они не относятся к наночастицам.
Использовали наиболее распространённые в диализной терапии ассиметричные мембраны, которые имели неоднородное строение по толщине полого волокна. Внутренний тонкий слой (толщиной ~15 мкм) обладал более плотной структурой. Он определял проницаемость волокна для веществ с различной молекулярной массой, а поддерживающий его поверхностный слой с рыхлой структурой (толщиной ~25 мкм) составлял основную толщину стенки волокна. В биологии и медицине в качестве ПАВ широко применяется полиэтиленгликоль (ПЭГ-200, ПЭГ-400). Высокий интерес к нему проявляется в том числе в виду высокой био- и гемосовместимости. Полимер не растворяется, а лишь набухает в воде и водных системах, создавая сетчатые гидрогели с определённой проницаемостью по отношению к различным по размеру частицам. Проницаемость связана с размером пор в гидрогелях, являющихся контейнерами для диспергированных наночастиц. В качестве наночастиц выбран биосовместимый наноматериал - бемит (AlOOH), обладающий положительным зарядом. Он, аналогично алундовой керамике, относится к биоинертным биосовместимым материалам для придания бактерицидных свойств покрытиям из гидроксиапатита на дентальных имплантатах и волокнистым сорбционным материалам в диализе.
Способ изготовления мембраны заключается в следующем. Сначала приготавливают раствор ПАВ в дистиллированной воде, добавляют наночастицы бемита, емкость с этим составом помещают в ультразвуковую ванну и подвергают ультразвуковому воздействию состав для получения суспензии наночастиц, представляющую собой взвесь наночастиц в растворе. Пропитывают волокна суспензией методом ультразвукового капиллярного эффекта и сушат гемодиализатор в сушильном шкафу.
Экспериментальную работу выполняли на диализаторе фирмы Fresenius Medical Care с мембраной из полисульфоновых полых волокон. Рассчитанное необходимое количество суспензии 200 мл для пропитки полых волокон готовили следующим образом. Исходный состав для суспензии готовили на основе дисцилированной воды, наночастиц бемита AlOOH и ПАВ ПЭГ-400. Готовили несколько составов разной концентрации в интервале 1,5% - 5%: 1,5%, 2,5% и 5% ПАВ в дисцилированной воде, к которым добавляли 8 г просушенного при 200°С в течение двух часов и измельченного в керамической ступе бемита (что составило 8% от веса полисульфоновых волокон). ПАВ проникает между частицами агломератов и снижает поверхностное натяжение, что приводит к диспергированию. Обычно вводят не более 5% ПАВ в растворы. Наночастицы бемита размером ~30 нм при хранении слипаются в агломераты, в нашем случае размером ~6 мкм. Поэтому, при изготовлении суспензии для пропитки волокон агломераты бемита в ней диспергировали воздействием ультразвука.
Отработку процесса диспергирования наночастиц бемита (наличие ПАВ, время воздействия ультразвуком) и оценка возможного времени пропитки выполняли путем анализа седиментации частиц бемита (0,1 г) в дистиллированной воде, в 2,5 % растворе ПАВ ПЭГ-400 в дистиллированной воде (по 10 мл воды в каждом растворе) и с применением ультразвукового воздействия на суспензию с ПАВ ПЭГ-400. Результаты Седиментация частиц бемита приведены в табл. 1.
Таблица 1
Подготовленные составы помещали в ультразвуковую ванну УЗУМИ-2 и воздействовали на них ультразвуком в течение 10 мин при частоте колебаний преобразователей 35±2 кГц. Осуществляли экспресс контроль наличия агломератов наночастиц бемита в суспензии с помощью автоматизированного анализатора АПГМ-6 или оптического микроскопа МИМ-7. Стеклянной палочкой каплю суспензии наносили тонким слоем в виде вуали на стекло, сушили и контролировали размеры редких сгустков. Они не должны превышать размер 3 мкм, чтобы снизить до минимума возможность эмболии сосудов и отрицательного воздействия на организм биосовместимых наночастиц бемита в случае попадания их в кровь при возможном отрыве наночастиц от мембраны, хотя теоретически такая вероятность ничтожно мала. Сопоставление размеров биосовместимых наночастиц (они не должны превышать 100 нм) с размерами элементов крови (диаметр эритроцитов 8 мкм, лейкоцитов 20 мкм, тромбоцитов 2-5 мкм) показывает реальную возможность их использования при очистке крови в контакте с кровотоком. При наличии более крупных сгустков дополнительно воздействовали на суспензию ультразвуком в течение 10 минут.
Пропитку волокон гемодиализатора осуществляли на картридже после удаления части корпуса при снятых крышках. Помещали картридж гемодиализатора с закрепленной в корпусе мембраной вертикально в полученную суспензию. Волокна под действием ультразвукового капиллярного эффекта пропитывали суспензией в течение 5 мин. Полноту (глубину) пропитки контролировали по объёму жидкости в волокнах, предварительно рассчитав необходимое её количество для пропитки по геометрическим размерам волокон. Пропитку волокон длиной 250 мм выполняли в два этапа. Мембрана после первого этапа пропитки заполнилась только на 1/3. Поэтому заканчивали пропитку оставшейся суспензией с другой стороны картриджа гемодиализатора методом закапывания с помощью шприца, что было длительно (2 часа) и неудобно. Изменили длину мембраны до 150 мм. Уменьшение длины мембраны позволило сократить время пропитки с 2 часов до 10 мин. Это стало возможным в результате выполнения второго этапа пропитки методом ультразвукового капиллярного эффекта с другой стороны картриджа в течение 5 минут. Капиллярные явления происходят мгновенно, поэтому выполнять пропитку более 5 минут нецелесообразно. Для обеспечения постоянства объема мембраны (пропускаемой жидкости) увеличивается диаметр гемодиализатора при той же плотности укладки волокон и увеличении их числа. Если волокна пропитались не на всю глубину, то заканчивали пропитку оставшейся суспензией с другой стороны диализатора методом ультразвукового капиллярного эффекта в течение 5 мин, аналогично вышеописанному. После этого картридж с волокнами помещали в сушильный шкаф SPT-200 и сушили до постоянного веса, который, исключая вес самого картриджа, был равен весу введённого бемита.
Для модифицирования мембраны использовали наночастицы бемита размером порядка 30-100 нм. Расположение наночастиц на внутренней поверхности волокон позволило значительно увеличить удельную площадь рабочей поверхности мембраны.
В соответствии с формулой для удельной площади поверхности S:
S=6/Dч,
чем мельче размер частицы Dч, тем она больше. Таким образом, сгруппированные на внутренней поверхности волокон наночастицы, значительно повышают и активируют рабочую поверхность мембраны. Полученная конструкция может использоваться для очистки крови.
Известно, что частицы крови имеют отрицательный заряд, поэтому тестовые испытания проницаемости полученной мембраны проводили на тестовом метаболите - водном растворе эозина, представляющего собой анионный краситель. При открытых крышках закапывали тестовый раствор с концентрацией 500 мг/л сверху с помощью шприца в волокна картриджа, помещенного вертикально в емкость с дистиллированной водой. Контролировали проницаемость раствора эозина через мембрану в дистиллированную воду по концентрации эозина в дистилированной воде в емкости в зависимости от времени фотоколориметрическим методом (фиг. 4). Процесс пропитки волокон полисульфона суспензией на основе положительно заряженных наночастиц бемита не приводит к закупориванию пор в мембране и обеспечивает качественный процесс гемодиализа. Создание электроположительного заряда на внутренней поверхности волокон наиболее эффективно отразится на адсорбции веществ крови, имеющих отрицательный заряд (например, фосфатов), и последующем массопереносе через мембрану. Положительно заряженные наночастицы бемита хорошо смачиваются водой и за счет наличия положительного заряда, они осуществляют электростатическое притяжение отрицательных элементов крови, что, по-видимому, и привело к повышению адсорбции и проницаемости через мембрану анионов эозина. Обнаружена слабая диффузия эозина через мембрану из полисульфона в диализаторе с немодифицированной мембранной. Через 60 мин концентрация исследуемого раствора не превышала 13,65*10-6 мг/мл и мало изменялась с увеличением времени диализа. На динамической кривой массопереноса молекул эозина из волокон, внутренняя поверхность которых покрыта наночастицами бемита, имеется участок нулевых концентраций. Полученные через ~15 мин результаты свидетельствуют о возрастании скорости массопереноса молекул эозина через мембрану в диализирующую дистиллированную воду и достижении значений концентрации 113*10-6 мг/мл. Таким образом, эффективность фильтрации увеличена примерно в 8 раз. Интенсивный процесс диффузии анионов эозина через волокна из модифицированного полисульфона свидетельствует о том, что не происходит закупоривания пор в мембране в процессе осаждения положительно заряженных наночастиц бемита на внутренней поверхности волокон. Это обеспечивает качественный процесс гемодиализа. Заявляемая конструкция обеспечивала проникновение пропитывающей суспензии внутрь волокон и отсутствие попадания ее на их поверхность.
После пропитки суспензией волокна сушили в сушильном шкафу до постоянного веса.
Время сушки, определенное по изменению веса после полной пропитки волокон мембраны при сушке в сушильном шкафу при температуре 100°С, приведено в таблице 2.
Таблица 2
п/п
Полисульфон разлагается при температуре около 300°С, а бемит - 257°С. Температура сушки в интервале 100-120°С соответствует значению температуры отжига ~0,5 от температуры плавления (Tотж = ~0,5 Тпл), которая является температурой активации диффузионного процесса в материалах. Поэтому длительный процесс сушки способствует припеканию наночастиц к поверхности волокон. В процессе работы не было замечено отделения наночастиц от волокон мембраны.
Сушки волокон в интервале 100-120°С можно одновременно рассматривать как стерилизацию паром, часто применяемую в технологиях изготовления гемодиализаторов.
Применение наночастиц в мембранах приведёт к сокращению затрат времени на проведение процедуры при повышении качества гемодиализа.
| название | год | авторы | номер документа |
|---|---|---|---|
| Сорбционно-бактерицидный материал из нетканого полимерного волокнистого материала, способ диализа жидких сред | 2023 |
|
RU2835016C2 |
| ПОЛОВОЛОКОННЫЙ МЕМБРАННЫЙ ОЧИСТИТЕЛЬ КРОВИ | 2022 |
|
RU2835528C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕМБРАН ДЛЯ УЛЬТРАФИЛЬТРАЦИИ ВОДНЫХ СРЕД | 2018 |
|
RU2689595C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ВНУТРИКОСТНЫХ ИМПЛАНТАТОВ С АНТИМИКРОБНЫМ ЭФФЕКТОМ | 2013 |
|
RU2512714C1 |
| Способ напыления биосовместимого покрытия модифицированного компонентом с низкой температурой разложения | 2018 |
|
RU2684283C1 |
| МОДУЛЬ ПОЛОВОЛОКОННЫХ МЕМБРАН И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2005 |
|
RU2369429C2 |
| АЦЕТАТЦЕЛЛЮЛОЗНАЯ ПОЛУПРОНИЦАЕМАЯ МЕМБРАНА В ВИДЕ ПОЛОГО ВОЛОКНА, СПОСОБ ИЗГОТОВЛЕНИЯ ПОЛОВОЛОКОННОЙ ПОЛУПРОНИЦАЕМОЙ АЦЕТАТЦЕЛЛЮЛОЗНОЙ МЕМБРАНЫ, ГЕМОДИАЛИЗАТОР И ПРИБОР ДЛЯ ОБРАБОТКИ ЭКСТРАКОРПОРАЛЬНОЙ КРОВИ | 1993 |
|
RU2108144C1 |
| Способ получения микро-мезопористых наноматериалов на основе складчатых нанолистов оксигидроксида алюминия и материал, полученный данным способом | 2017 |
|
RU2674952C1 |
| Способ получения мембраны из полисульфона для фильтрации водных сред | 2022 |
|
RU2808876C1 |
| ПОЛОВОЛОКОННОЕ МЕМБРАННОЕ УСТРОЙСТВО ДЛЯ ОЧИСТКИ КРОВИ | 2015 |
|
RU2682761C2 |
Группа изобретений относится к медицинской технике. Гемодиализатор включает цилиндрический корпус с впускными и выпускными патрубками, съемные крышки с патрубками на его торцах, для ввода венозной и вывода очищенной крови, и половолоконную мембрану, выполненную из полисульфоновых полых волокон, закрепленную к корпусу посредством заливки из полиуретана, плотно прилегающей к корпусу и полисульфоновым полым волокнам. Использована половолоконная мембрана, изготовленная способом по п.3. Внутренняя поверхность полисульфоновых полых волокон половолоконной мембраны модифицирована наночастицами бемита размером 30-100 нм. Раскрыт способ изготовления половолоконной мембраны для гемодиализатора. В емкости готовят 1,5% - 5% раствор поверхностно-активного вещества (ПАВ) в дистиллированной воде. Получают состав для пропитки, добавляя в раствор ПАВ наночастицы бемита размером 30 нм - 100 нм. Емкость с составом для пропитки помещают в ультразвуковую ванну и подвергают воздействию в течение 10 минут при рабочей частоте колебаний 35±2 кГц для получения суспензии. Гемодиализатор со снятыми крышками вертикально размещают в емкости с суспензией, при той же рабочей частоте методом ультразвукового капиллярного эффекта пропитывают волокна и сушат в сушильном шкафу. Технический результат состоит в увеличении рабочей поверхности половолоконных мембран. 2 н. и 3 з.п. ф-лы, 4 ил., 2 табл.
1. Гемодиализатор, включающий цилиндрический корпус с впускными и выпускными патрубками, съемные крышки с патрубками на его торцах, для ввода венозной и вывода очищенной крови, и половолоконную мембрану, выполненную из полисульфоновых полых волокон, закрепленную к корпусу посредством заливки из полиуретана, плотно прилегающей к корпусу и полисульфоновым полым волокнам, отличающийся тем, что использована половолоконная мембрана, изготовленная способом по п.3, причем внутренняя поверхность полисульфоновых полых волокон половолоконной мембраны модифицирована наночастицами бемита размером 30-100 нм.
2. Гемодиализатор по п.1, отличающийся тем, что длина волокон половолоконной мембраны составляет 150 мм, а их внутренний диаметр 200 мкм.
3. Способ изготовления половолоконной мембраны для гемодиализатора по п.1, согласно которому в емкости готовят 1,5% - 5% раствор поверхностно-активного вещества (ПАВ) в дистиллированной воде, получают состав для пропитки, добавляя в раствор ПАВ наночастицы бемита размером 30 нм - 100 нм, емкость с составом для пропитки помещают в ультразвуковую ванну и подвергают воздействию в течение 10 минут при рабочей частоте колебаний 35±2 кГц для получения суспензии, гемодиализатор со снятыми крышками вертикально размещают в емкости с суспензией, при той же рабочей частоте методом ультразвукового капиллярного эффекта пропитывают волокна и сушат в сушильном шкафу.
4. Способ по п.3, отличающийся тем, что гемодиализатор со снятыми крышками переворачивают и повторяют пропитку.
5. Способ по п.3, отличающийся тем, что гемодиализатор сушат в течение 3 часов при 100-120°С.
Авторы
Даты
2025-05-19—Публикация
2024-10-18—Подача