Изобретение относится к области медицины, а именно диагностике инвазивности злокачественных новообразований. Изобретение основано на применении 70 кДа белка теплового шока (БТШ). Данные белки в малом количестве синтезируются в любых ядерных клетках внутри разнообразных органелл. В некоторых случаях в покоящихся клетках БТШ могут составлять до 2% от всех белков [Craig, E. A., Is hsp70 the cellular thermometer? / E.A. Craig, C.A. Gross // Trends in biochemical sciences. - 1991. - №16. - p. 135-140.]. Характерная черта для БТШ - значительное повышение экспрессии при стрессовом воздействии на клетку. Таким образом, синтез БТШ - это распространенный среди эукариотов неспецифичный ответ клеток на стресс [Евдокимовская, Ю.В., Секреция белков теплового шока опухолевыми клетками человека in vitro / Ю.В. Евдокимовская и др. // Международный научно-исследовательский журнал.- 2013. - 13].
Важная особенность шаперонов БТШ 70 - присутствие на мембране клеток злокачественных новообразований [Shevtsov M, Balogi Z, Khachatryan W, Gao H, Vígh L, Multhoff G. Membrane-Associated Heat Shock Proteins in Oncology: From Basic Research to New Theranostic Targets. Cells. 2020 May 20;9(5):1263. doi: 10.3390/cells9051263. 5]. Мембранная форма шаперонов в виде гомо- и гетеродимеров БТШ в комплексе с факторами обмена нуклеотидов и другими компонентами шаперонного цикла - характерная черта опухолевых клеток [Murphy, M. E., The hsp70 family and cancer. / M. E. Murphy // Carcinogenesis. - 2013. - №34.6. - p. 1181-1188.]. Новообразования отличаются по составу и уровню экспрессии шаперонов, что делает БТШ важным маркером для таргетной диагностики и терапии.
На сегодняшний день известен ряд способов определения инвазивного потенциала злокачественных новообразований.
Из источника [Крахмаль Н.В. и др. Морфологические и молекулярно-генетические проявления опухолевой инвазии при раке молочной железы, под ред. В.М. Перельмутера, М.В. Завьяловой. - Томск: Изд-во Том. ун-та, 2017. - 128 с. - 2017] известно, что в пределах одного злокачественного новообразования клетки могут одновременно двигаться как коллективно, так и индивидуально. При этом переход от коллективной миграции к индивидуальной представляет собой важнейший этап на пути повышения инвазивного и метастатического потенциала злокачественных новообразований. Одиночные опухолевые клетки отделяются от многоклеточных опухолевых структур и приобретают более выраженную способность к инвазии, интравазии и трансмиграции через эндотелий. Следовательно, выявление индивидуально двигающихся клеток в опухоли говорит о повышенном инвазивном потенциале опухоли.
Из источников [Albini A. et al. A rapid in vitro assay for quantitating the invasive potential of tumor cells //Cancer research. - 1987. - Т. 47. - №. 12. - С. 3239-3245.], [Chen H. C. Boyden chamber assay //Cell migration: developmental methods and protocols. - 2005. - С. 15-22.] известен такой метод оценки инвазивного потенциала клеточных культур in vitro, как камера Бойдена. Камеры Бойдена являются наиболее широко применяемым методом анализа инвазивного потенциала и представляют из себя полую пластиковую камеру, закрытую с одного конца пористой мембраной с диаметром пор 8 мкм. Эта камера помещается внутрь большей по объёму камеры, которая может содержать культуральную среду и/или хемоаттрактанты. Клетки помещают внутрь меньшей камеры и позволяют им мигрировать через поры на другую сторону мембраны. Инвазивные клетки (злокачественные и незлокачественные) способны проникать через 8-микронные поры мембраны. Затем мигрировавшие на другую сторону мембраны клетки окрашивают и подсчитывают. Из существующих на рынке решений, использующих эту технологию, можно упомянуть Transwell®, EZCell™ Cell Invasion Assay, Corning® BioCoat™ Matrigel® Invasion Chamber, BD BioCoat™ Matrigel™ invasion Chamber.
Из источника [Китаева К.В., Ризванов А.А., Соловьева В.В. Современные методы доклинического скрининга противоопухолевых препаратов с применением тест-систем на основе клеток. // Ученые записки Казанского университета. Серия Естественные науки. - 2021. - Т. 163. - №.2. - С. 155-176] известен такой метод оценки инвазивного потенциала клеточных культур in vitro, как применение микрофлюидных систем. Они позволяют проводить исследования в малых объемах жидкости, что позволяет снизить влияние внешних факторов на результаты экспериментов. Из существующих на рынке решений, использующих эту технологию, можно упомянуть Millicell® μ-Migration Assay Kit.
Общим недостатком вышеуказанных методов является то, что для их применения необходима специальная посуда, и сложная, дорогостоящая аппаратуры, что затрудняет применение таких методов в клинической практике.
Помимо этого, на точность данных методов влияет то, что образцы биопсии могут содержать и другие типы подвижных клеток, помимо опухолевых. Из источников [Chen P.-Y., Wei W.-F., Wu H.-Z., Fan L.-S., Wang W. Cancer-Associated Fibroblast Heterogeneity: A Factor That Cannot Be Ignored in Immune Microenvironment Remodeling. Front. Immunol. 2021;12:2760. doi: 10.3389/fimmu.2021.671595.] и [Gilson P., Merlin J. L., Harlé A. Deciphering tumour heterogeneity: From tissue to liquid biopsy // Cancers. - 2022. - Т. 14. - №. 6. - С. 1384] известно, что это могут быть опухоль-ассоциированные фибробласты, наличие которых не вносит вклада в инвазивный потенциал злокачественного новообразования.
Поэтому необходим метод, позволяющий дифференцировать подвижные клетки на высокоинвазивные (опухолевые, одиночные, подвижные) и невысокоинвазивные (опухоль-ассоциированных фибробластов).
Задачей, решаемой авторами, являлось создание более точного простого и дешевого способа оценки инвазивного потенциала злокачественных новообразований.
Задача решается за счет применения мишенного пептида, содержащего последовательность аминокислот SEQ ID NO: 1 TKDNNLLGRFELSGRGD (далее - пептид TKD-RGD).
Краткое описание фигур
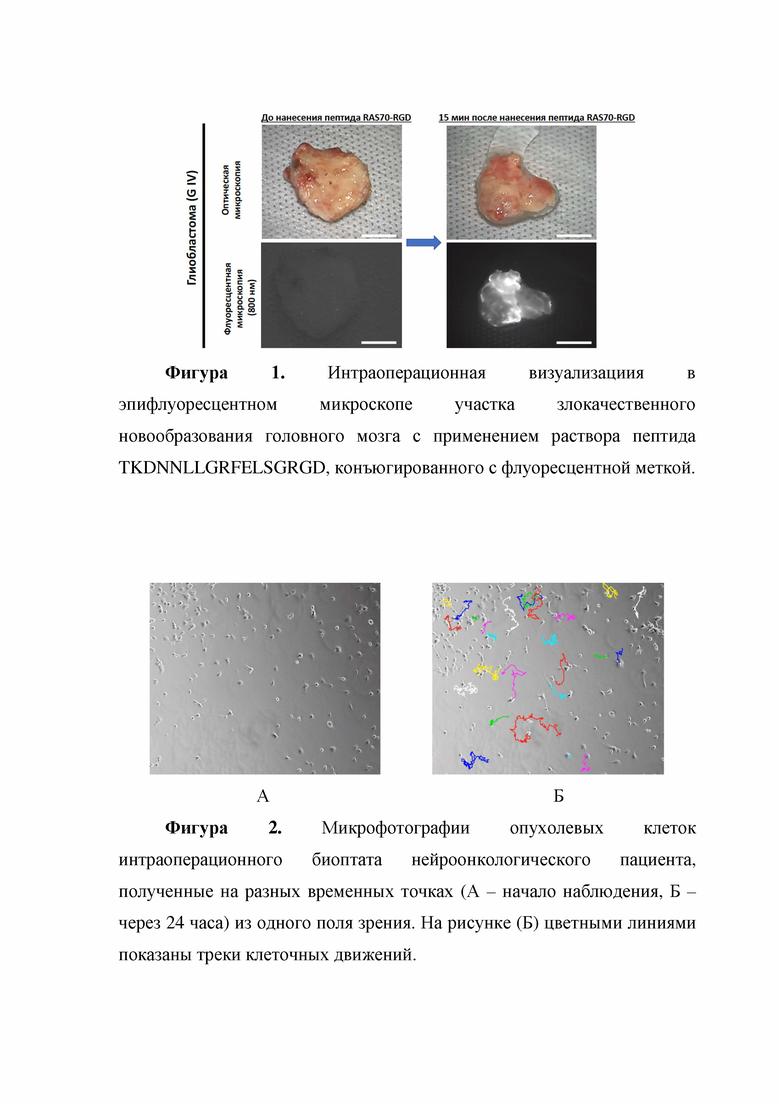
На Фиг. 1 представлена интраоперационная визуализациия в эпифлуоресцентном микроскопе участка злокачественного новообразования головного мозга с применением раствора пептида SEQ ID NO: 1 (TKDNNLLGRFELSGRGD), конъюгированного с флуоресцентной меткой.
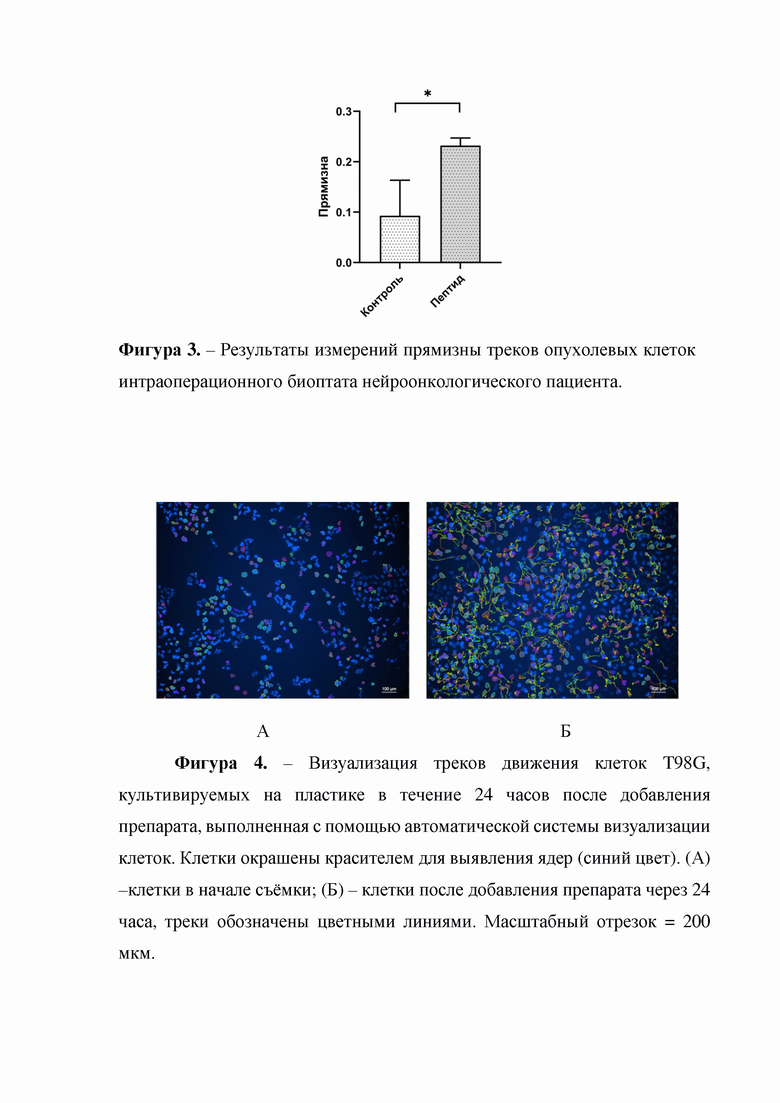
На Фиг. 2 представлены микрофотографии опухолевых клеток интраоперационного биоптата нейроонкологического пациента, полученные на разных временных точках (А - начало наблюдения, Б - через 24 часа) из одного поля зрения. На рисунке (Б) цветными линиями показаны треки клеточных движений.
На Фиг. 3 Представлены результаты измерений прямизны треков опухолевых клеток интраоперационного биоптата нейроонкологического пациента.
На Фиг. 4 представлена визуализация треков движения клеток T98G, культивируемых на пластике в течение 24 часов после добавления препарата, выполненная с помощью автоматической системы визуализации клеток. Клетки окрашены красителем для выявления ядер (синий цвет). (А) - клетки в начале съёмки; (Б) - клетки после добавления препарата через 24 часа, треки обозначены цветными линиями. Масштабный отрезок = 200 мкм.
На Фиг. 5 представлены результаты измерений прямизны треков клеток глиобластомы линии T98G.
На Фиг. 6 представлена визуализация треков движения клеток M-FetMSC, культивируемых на пластике в течение 24 часов после добавления препарата. Клетки окрашены красителем для выявления ядер (синий цвет).
(А) - клетки в начале съёмки; (Б) - клетки через 24 часа, треки обозначены цветными линиями. Масштабный отрезок = 200 мкм.
На Фиг. 7 представлены результаты измерений прямизны треков мезенхимных стволовых клеток человека линии FetMSC. Представлены средние значения и стандартные отклонения. ns - результат выполнения теста Манна-Уитни: достоверных отличий не обнаружено (U = 420).
Сущность изобретения.
Пептид, содержащий последовательность аминокислот SEQ ID NO: 1 (TKDNNLLGRFELSGRGD), способный избирательно накапливаться в клетках злокачественных новообразований и изменять прямизну треков движений высокоинвазивных опухолевых клеток.
Способ оценки инвазивного потенциала злокачественных новообразований, заключающийся в том, что клетки злокачественного новообразования делят на две группы: первую группу обрабатывают пептидом содержащим последовательность аминокислот SEQ ID NO: 1 (TKDNNLLGRFELSGRGD), вторую группу обрабатывают физиологическим раствором, после чего регистрируют треки движения клеток двух групп, а затем сравнивают прямизну полученных треков: если прямизна треков движения клеток двух групп различается, то принимают решение о причислении тестируемых клеток к разряду высокоинвазивных.
Способ осуществляется следующим образом. Кусочки удаленного злокачественного новообразования культивируют в инкубаторе в пластиковых планшетах, покрытых, для улучшения адгезии, белками внеклеточного матрикса. Клетки мигрируют и спонтанно формируют сфероиды. Полученные сфероиды делят на контрольную и опытную группы. Обе группы культивируют на способствующих адгезии белковых субстратах.
К опытной группе сфероидов добавляют раствор пептида TKD-RGD в физиологическом растворе, к контрольной группе добавляют равный объём физиологического раствора. Культуральную посуду со сфероидами помещают в программно-аппаратный комплекс для прижизненной визуализации и анализа параметров клеток, после чего каждые 15 минут в течение 24 часов производят микрофотографирование клеток.
Затем регистрируют X и Y координаты треков клеточных движений с помощью анализа изображений покадровой съёмки. По полученным наборам координат вычисляют прямизну треков как отношение евклидова расстояния к длине пути по следующим формулам:
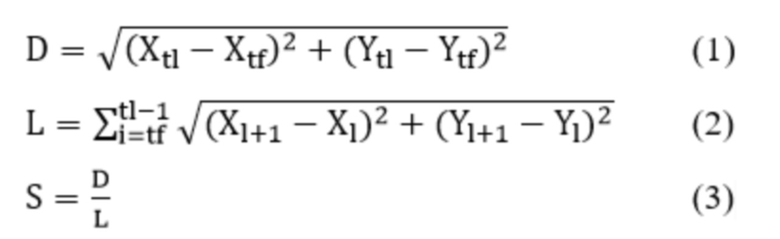
где:
S - прямизна трека,
D - расстояние между начальной и конечной точками трека,
L - длина трека,
tl - первый индекс времени трека,
tf - последний индекс времени трека.
Таким образом, прямизна треков является признаком, измеренным количественно для двух независимых выборок: для контрольной группы клеток (обработанной физиологическим раствором) и опытной группы клеток (обработанной пептидом TKD-RGD).
Затем сравнивают прямизну треков клеток контрольной и опытной групп с помощью U-критерия Манна-Уитни с уровнем значимости 0,05. Из источников [Mann H. B., Whitney D. R. On a test of whether one of two random variables is stochastically larger than the other. // Annals of Mathematical Statistics. - 1947. - № 18. - P. 50-60], [Гублер Е. В., Генкин А. А. Применение непараметрических критериев статистики в медико- биологических исследованиях. - Л., 1973], [Крамер Г. Математические методы статистики, 2 изд., пер. с англ., М., 1975.] известен U-критерий Манна-Уитни - статистический критерий, используемый для оценки различий между двумя независимыми выборками по уровню какого-либо признака, измеренного количественно. Критические значения критерия U- Манна-Уитни для уровня значимости 0,05 представлены в источнике [Большев Л. Н., Смирнов Н. В., Таблицы математической статистики, 2 изд., М., 1968]
Если полученное значение U-критерия меньше или равно критическому значению, то признается наличие значимого различия между уровнем признака (прямизна трека) в контрольной и опытной группах, и принимается решение о причислении тестируемых злокачественных новообразований к разряду высокоинвазивных.
Примеры
Пример 1
Из нейрохирургического отделения Российского научно-исследовательского нейрохирургического института им. проф. А.Л. Поленова (г. Санкт-Петербург) в ходе удаления злокачественного новообразования головного мозга получили образец опухолевого интраоперационного биоптата нейроонкологического пациента (Фигура 1). Из детектированного участка вырезали кусочек злокачественного новообразования размером около 0,5 мм3, положили в чашку Петри диметром 3 см и накрыли предметным стеклом. Клетки культивировали при 37 °C (5 % CO2, влажность 90 %) в присутствии 10 % фетальной бычьей сыворотки в питательной среде DMEM/F12 (Gibco, США), дополненной 1 % GlutaMAX (Gibco, США), 0,5 % 1 М раствором HEPES (Sigma, США), 2 % B27 supplement minus vitamin A (Gibco, США), recombinant human EGF (SCI store, Россия) и bFGF (SCI store, Россия) в рабочей концентрации 20 нг/мл. Из кусочка начали радиально мигрировать клетки, которые самопроизвольно сформировали сфероиды. Для оценки скорости миграции клеток полученные сфероиды высевали на 24-луночные пластиковые планшеты, лунки которых покрывали, для улучшения адгезии, белком внеклеточного матрикса фибриногеном.
Клетки злокачественного новообразования, посеянные на фибриноген, разделили на две группы: первой группе сменили среду на содержащую пептид SEQ ID NO: 1 (TKDNNLLGRFELSGRGD) (10 мкг/мл), второй группе сменили среду на содержащую равный объем физиологического раствора.
С использованием покадровой съемки произвели анализ движения 30 клеток в каждой группе. Для регистрации движения отдельных клеток использовали настольную систему цитометрии Image ExFluorer LCI (Южная Корея), представляющую из себя программно-аппаратный комплекс для прижизненной визуализации и анализа параметров клеток. В эту систему помещали 24-луночные пластиковые планшеты с клетками. Изображения получали с помощью лазера 405 нм и освещения в светлом поле с использованием сухого объектива 20×. Выбирали поле зрения в лунках с клетками контрольной и опытной групп, затем производили микрофотографирование полей зрения каждые 15 минут в течение 24 часов. На полученных изображениях выявили популяцию активно движущихся клеток. Треки движения этих клеток регистрировали как наборы их X-Y координат. Для получения X-Y координат отмечали середину ядра движущейся клетки на каждом изображении. Примеры полученных треков представлены на Фигуре 2.
В процессе анализа треков были получены значения D и L. Рассчитали прямизну треков S (по формуле 3). Результаты представлены в Таблице 1 и на Фигуре 3.
Для выявления различий между контрольной и опытной группами в программе GraphPad Prism версии 9.4.1 вычислили U-критерий Манна-Уитни, который оказался равен 206. Для двух выборок, содержащих по 30 элементов, и уровня значимости 0,05 критическое значение критерия U-Манна-Уитни равно 317. Поскольку 206 меньше чем 317, то было принято решение о причислении тестируемых клеток к разряду высокоинвазивных, а исследуемый образец оценили, как злокачественное новообразование с высоким инвазивным потенциалом.
Пример 2
Клетки линии T98G получили в ЦКП «Коллекция культур клеток позвоночных» (Институт цитологии РАН, Санкт-Петербург). Клетки культивировали при 37 °C (5 % CO2, влажность 90 %) в ростовой среде, содержащей 90 % среды DMEM/F12 и 10 % фетальной бычьей сыворотки. Микробиологический анализ подтвердил отсутствие бактериального, грибкового или микоплазменного загрязнения культивированной линии. Далее провели операции согласно Примеру 1. Визуализация полученных треков представлена на Фигуре 4.
В процессе анализа треков были получены значения D и L. Рассчитали прямизну треков S. Результаты представлены в Таблице 2 и на Фигуре 5. Для выявления различий между контрольной и опытной группами в программе GraphPad Prism версии 9.4.1 вычислили U-критерий Манна-Уитни, который оказался равен 253. Поскольку 253 меньше, чем 317, то было принято решение о причислении тестируемых клеток к разряду высокоинвазивных, а исследуемый образец оценили, как культуру клеток с высоким инвазивным потенциалом.
Пример 3
Клетки линии M-FetMSC получили в ЦКП «Коллекция культур клеток позвоночных» (Институт цитологии РАН, Санкт-Петербург).
Провели операции согласно Примеру 1. Визуализация полученных треков представлена на Фигуре 6.
В процессе анализа треков были получены значения D, L. Рассчитали прямизну треков S. Результаты представлены в Таблице 1 и на Фиг. (2). Для выявления различий между контрольной и опытной группами в программе GraphPad Prism версии 9.4.1 вычислили U-критерий Манна-Уитни, который оказался равен 420. Поскольку 420 больше, чем 317, то было принято решение о не причислении тестируемых клеток к разряду высокоинвазивных, а исследуемый образец оценили, как культуру клеток без высокого инвазивного потенциала.
Таким образом, вышеприведённые примеры показывают, что создан точный, простой, и дешевый способ оценки инвазивного потенциала злокачественных новообразований.
Таблица 1. Значения параметров D, L, S опухолевых клеток интраоперационного биоптата нейроонкологического пациента, двигающихся в течение 24 часов.
Таблица 2. Значения параметров D, L, S клеток линии T98G, двигающихся в течение 24 часов.
Таблица 3. Значения параметров D, L, S клеток линии M-FetMSC, двигающихся в течение 24 часов.
--->
<?xml version="1.0" encoding="UTF-8"?>
<!DOCTYPE ST26SequenceListing PUBLIC "-//WIPO//DTD Sequence Listing
1.3//EN" "ST26SequenceListing_V1_3.dtd">
<ST26SequenceListing dtdVersion="V1_3" fileName="1-TRACK.xml"
softwareName="WIPO Sequence" softwareVersion="2.3.0"
productionDate="2024-03-01">
<ApplicationIdentification>
<IPOfficeCode>RU</IPOfficeCode>
<ApplicationNumberText>2023127706</ApplicationNumberText>
<FilingDate>2023-10-27</FilingDate>
</ApplicationIdentification>
<ApplicantFileReference>1-TR</ApplicantFileReference>
<ApplicantName languageCode="ru">Федеральное государственное
бюджетное учреждение "Национальный медицинский исследовательский
центр имени В.А. Алмазова" Министерства здравоохранения
Российской Федерации (ФГБУ "НМИЦ им. В.А. Алмазова"
Минздрава России)</ApplicantName>
<ApplicantNameLatin>Federal State Budgetary Institution
"Almazov National Medical Research Centre" of the Ministry
of Health of the Russian Federation</ApplicantNameLatin>
<InventionTitle languageCode="ru">Мишенный пептид и способ его
применения для оценки инвазивного потенциала злокачественных
новообразований</InventionTitle>
<SequenceTotalQuantity>1</SequenceTotalQuantity>
<SequenceData sequenceIDNumber="1">
<INSDSeq>
<INSDSeq_length>17</INSDSeq_length>
<INSDSeq_moltype>AA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..17</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>protein</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q2">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
<INSDFeature>
<INSDFeature_key>ACT_SITE</INSDFeature_key>
<INSDFeature_location><1..>17</INSDFeature_location>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>TKDNNLLGRFELSGRGD</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
</ST26SequenceListing>
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ выявления туморогенных клеток в первичной культуре фибробластов человека | 2021 |
|
RU2792061C1 |
| СПОСОБ ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2004 |
|
RU2271831C1 |
| Способ культивирования и исследования гетерогенной культуры опухолевых клеток и устройство для его осуществления | 2024 |
|
RU2837629C1 |
| Комплексное антиангиогенное и гипоксия-ориентированное противоопухолевое средство | 2022 |
|
RU2804771C1 |
| ПОЛИМЕРНЫЕ НАНОЧАСТИЦЫ, ПОКРЫТЫЕ ОКСИДОМ МАГНИТНОГО МЕТАЛЛА, И ИХ ПРИМЕНЕНИЕ | 2008 |
|
RU2472530C2 |
| ХИМЕРНЫЙ ПЕПТИД ДЛЯ ЛЕЧЕНИЯ ЭПИТЕЛИАЛЬНЫХ И МЕЗЕНХИМАЛЬНЫХ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ | 2008 |
|
RU2369402C1 |
| АНАЛОГИ ЖИРНЫХ КИСЛОТ ДЛЯ ЛЕЧЕНИЯ РАКА | 2001 |
|
RU2283105C2 |
| Способ определения метастатического потенциала опухолевых новообразований | 2022 |
|
RU2802213C1 |
| ЦИКЛИЧЕСКИЕ ПЕПТИДЫ С АНТИНЕОПЛАСТИЧЕСКОЙ И АНТИАНГИОНЕННОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2603286C2 |
| АНТИТЕЛА, СПЕЦИФИЧНЫЕ К АЛЬФА-ЭНОЛАЗЕ, И СПОСОБЫ ПРИМЕНЕНИЯ В ПРОТИВООПУХОЛЕВОЙ ТЕРАПИИ | 2013 |
|
RU2656153C1 |

Группа изобретений относится к пептиду, содержащему последовательность аминокислот TKDNNLLGRFELSGRGD, способному избирательно накапливаться в клетках злокачественных новообразований и изменять прямизну треков движений высокоинвазивных опухолевых клеток, и также относится к способу оценки инвазивного потенциала злокачественных новообразований, отличающемуся тем, что клетки злокачественного новообразования делят на две группы: первую группу обрабатывают пептидом, содержащим последовательность аминокислот TKDNNLLGRFELSGRGD, вторую группу обрабатывают физиологическим раствором, после чего обе группы помещают в программно-аппаратный комплекс для прижизненной визуализации и анализа параметров клеток, после чего каждые 15 минут в течение 24 часов производят микрофотографирование клеток, затем регистрируют X и Y координаты треков движения клеток двух групп с помощью анализа изображений покадровой съёмки, и по полученным наборам координат вычисляют прямизну треков движения клеток как отношение евклидова расстояния к длине пути по следующим формулам:
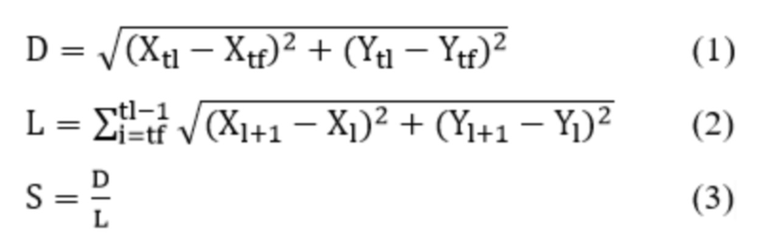
где: S - прямизна трека, D - расстояние между начальной и конечной точками трека, L - длина трека, tl - первый индекс времени трека, tf - последний индекс времени трека, а затем сравнивают прямизну полученных треков: если прямизна треков движения клеток двух групп различается, то принимают решение о причислении тестируемых клеток к разряду высокоинвазивных. Группа изобретений обеспечивает создание более точного простого и дешевого способа оценки инвазивного потенциала злокачественных новообразований. 2 н.п. ф-лы, 6 ил., 3 табл., 3 пр.
1. Пептид, содержащий последовательность аминокислот TKDNNLLGRFELSGRGD, способный избирательно накапливаться в клетках злокачественных новообразований и изменять прямизну треков движений высокоинвазивных опухолевых клеток.
2. Способ оценки инвазивного потенциала злокачественных новообразований, отличающийся тем, что клетки злокачественного новообразования делят на две группы: первую группу обрабатывают пептидом, содержащим последовательность аминокислот TKDNNLLGRFELSGRGD, вторую группу обрабатывают физиологическим раствором, после чего обе группы помещают в программно-аппаратный комплекс для прижизненной визуализации и анализа параметров клеток, после чего каждые 15 минут в течение 24 часов производят микрофотографирование клеток, затем регистрируют X и Y координаты треков движения клеток двух групп с помощью анализа изображений покадровой съёмки, и по полученным наборам координат вычисляют прямизну треков движения клеток как отношение евклидова расстояния к длине пути по следующим формулам:
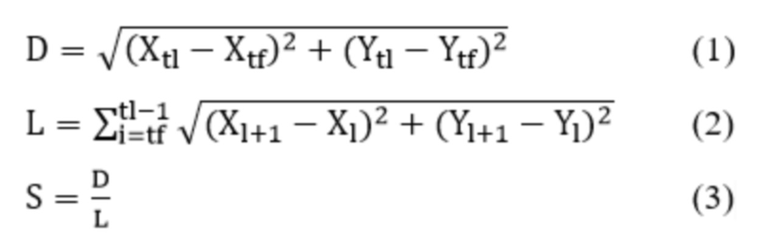
где:
S - прямизна трека,
D - расстояние между начальной и конечной точками трека,
L - длина трека,
tl - первый индекс времени трека,
tf - последний индекс времени трека,
а затем сравнивают прямизну полученных треков: если прямизна треков движения клеток двух групп различается, то принимают решение о причислении тестируемых клеток к разряду высокоинвазивных.
| ПОЛИРОВАЛЬНЫЙ БАРАБАН | 1964 |
|
SU222656A1 |
| WO 2018219980 A1, 06.12.2018 | |||
| US 2005079516 A1, 14.04.2005. | |||
Авторы
Даты
2025-05-21—Публикация
2023-10-27—Подача