Изобретение относится к области химии полимеров и химикофармацевтической промыдпенности, а именно к способу получения иммобилизованного фибринолизина, обладающего пролонгированной тромболитической активностью. Оибринолизин широко применяют вмедицине -в качестве тромболитическог препарата при терапии таких заболева ний как инфаркт миокарда, тромбозы, тромбоэмболии легочных артерий. Препарат вводят внутривенно в течение нескольких дней. Однако терапия фиб ринолизином осложняется следующими обстоятельствами. Во-первых, фибрино лизин не обладает субстратной специфичностью. Он гидролизирует не только фибрин, но и другие белки: фибриноген, казеин и некоторые белки свер тываюцей системы крови. Во-вторых, применение фибринолизина может вызывать не только повыиение фибринолитической активности, но активацию свертывающей системы, в результате чего возможно повторное возникновени тромбов. В-третьих, как и все фермен тные препараты, фибринолизин быстро инактивируется в физиологических условиях под действием рН, температуры эндогенных протеаз и природных ин-, гибиторов и быстро выводится из кровотока, что приводит к необходимости введения больших доз фе1рмента в течв ние продолжительного времени. При этом безуспешным оказалось лечение больных со значительными размерами тромбов, а также с низкими антикоагуляитными показателями крови. В нас оящее время известно, что во многих случаях связывание ферментов с растворимыми биосовместимыми полимерами позволяет получать препараты, обладающие по сравнению с нативными ферментами, более высокой стабильностью по отношению к различным .инактивирующим воздействиям, замедленным выведением из организма и пониженной аитигенностью. Известен способ получения иммобилизованного .фибринолизина путем ковалентного связывания фибринолизина с сополимером этилена- и мапеинового ангидрида С ЗНедостатком этого способа является несовместимость иммобилизованного фибринолизина с тканями живого организма, поскольку сополимер этилена с малеиновым ангидридом не являетсябиоразлагаемым.
Наиболее близким к изобретению по технической сущности и достигаемым результатам является способ получений иммобилизованного фибринолизина путем ковапентного связЕлвания фибринолизиНД с альдегидсодержащим полисахаридом 5 при рН 8,0-9,5 при 8-30 С f 2 .
В качестве .альдегидсодержащего полисахарида используют апьдегидсефадекс и ковалентное связывание приво.-10 дят в фосфатном буфере в течение нескольких, часов.
Недостатком этого способа является нерастворимость иммобилизованного фиб ринолизина в воде и водных растворах,
Целью изобретения является получе- 15 ние водорастворимых препаратов иммобилизованного фибринолизина.
Цель достигается тем, что в способе иммобилизованного фибринолизина путем ковалентного связывания фибри- 20 .нолизкна с альдегидсодержащим полисахаридом при рН 8,0-9,5 при в качестве альдегидсодержащего полисахарида используют диальдегидцекстран с молекулярной массэй 20000-110000, 25 а иммобилизованный фибринолизин дополнительно восстанавливают боргидридом натрия..
Исходный диальгеддекстран получают окислением декстрана йодной кисло- зо той или ее натриевой солью. Иммобилизованный фибринолизин отделяет от избытка минеральных солей деминерализацией на мембранах, в частности деализом против воды. Раствор полученного лс препарата лиофилизируют.
Продукт полностьй сохраняет биологическую активность.
Пример 1. Раствор 1 г диальдегиддекстрана с молекулярной массой 20000 в 20 мл дистиллированной воды смешивают со 110 мл 0,2 М содового раствора (рН 9,5) и к раствору добавляют при легком перемешивании 6,5 г фибринолизина.
Реакционную смесь в объеме 130 мл 5 выдерживают при рН 9,5 при 30°С 1 ч, затем охлаждают до lOtfC и добавляют 40 мл 0,5%-ного раствора боргидрида натрия в содовом буфере с рН 8,5, охлажденного до 10±1°С. Реакцию восста-50 новления проводят 30 мин при рН 8,59,0.
Раствор иммобилизованного фибринолизина разливают в целлофановые мешки) два мешка по 85 мп и диализуют при 55 емпературе 6t2°C против 17 л дистилированной воды в течение 24 ч. Диаизованный раствор иммобилизованного ибринолизина разбавляют апирогенной одой до 350-мл, пропускаютчерез
терильный фильтр (диаметр пор ,22 мкм) и высушивают лиофильно.
Выход препарата составляет 2275мг. дельная фибринолитическая активность авна 21,2 ед/мг препарата общей активностью 47230 ад., что составляет 31,0% от исходного. Полученный продукт представляет собой пористую массу белого цвета без запаха, без вкуса. Препарат гигроскопичен, растворим в воде и в 0,9%-нрм изотоническом растворе натрия хлорида, практически нерастворим в 95%-иом спирте, эфире, хлороформе.
Пример 2. Раствор 8 г диальдегиддекстрана с молекулярной массой 110000 в 150 мл дистиллированной води смешивают с 425 мп содового буферного раствора с рН 8,0. Полученный раствор смешивают с раствором нативного фибринолизина, приготовляемого растворением 45 г фибринолизина в 425 мл дистиллированной воды.
Реакционную смесь в объеме 1000 глл выдерживают при температуре 8, 40 мин и добавляют 310 мл охлажденного до температуры 6±2°С раствора боргидрида натрия, получаемого растворением 1,5 г боргидрида натрия в 310 мл 0,1 М содового буферного раствора с рН 8,5. Реакцию восстановления прово,цят 30 мин. Затем раствор иммобилизованного фибринолизина ставят на днаЛИЗ против дистиллированной воды в соотношении диализуемый раствор: вода 1 : 150 на 24 ч при и высушивают лиофильно. Выход препарат составляет 12,5 ГС удельной активностью 24 ед/мг и общей активностью 300000 ед что составляет 30% от исходного.
Полученный продукт представляет собой порошок с желтоватым оттенком без запаха, без вкуса. Препарат гигроскопичен, легко растворим в- воде и 0,9%-ном изотоническом растворе натрия хлорида практически нераствоРИМ в 95%-ном спирте,эфире , хлороформе .
Изучение специфического (тромболитического) действия иммобилизованного фибринолизина проводят на моделях тромбозов яремНой вены кролика и бедренной вены или артерии собаки. У указанных выше животных формируют тромбы размером от 1 до 2,5 см, полностью облитерирующие просвет кровеносного сосуда. Введение испытуемого препарата на фоне гепарина начинают через 1 ч после образования тромба.
Дозу препарата (от 400 до 4000 ед на кг веса) растворяют в физиологическом растворе для кроликов в 2030 мл, а для собак в 50-100 мл и вводят.шприцем на протяжении 20 мин внутривенно струйно, а не по инструкции по применению фибринолизина (внугривенно - капельным методом со скоростью 10-12 капель в лшнуту).
Динамику образования и лизиса тромба наблюдают визуально и пальпаторно на протяжении 6 ч опыта через одни, двое и трое суток. Ангиограф11ю
И флюометрию проводят до начала лечения и через сутки послевведения препарата.
Результаты изучения тромболитической активности иммобилизованного фибринолизина представлены в табл.1.
Таблица


| название | год | авторы | номер документа |
|---|---|---|---|
| Стабилизированная стрептокиназа,обладающая тромболитической активностью | 1979 |
|
SU822551A1 |
| Стабилизированная урокиназа,обладающая тромболитической активностью,и способ ее получения | 1979 |
|
SU1022988A1 |
| Урокиназа,иммобилизированная на фибриногене | 1983 |
|
SU1128601A1 |
| Способ получения модифицированной урокиназы | 1981 |
|
SU1037683A1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ТРОМБОЛИТИЧЕСКИМИ, ПРОТИВОВОСПАЛИТЕЛЬНЫМИ И ЦИТОПРОТЕКТИВНЫМИ СВОЙСТВАМИ | 2001 |
|
RU2213557C2 |
| Способ иммобилизации фермента субтилизиноподобная протеиназа, продуцируемого штаммом бактерии рода Bacillus вида Bacillus sp. 7Р/3-19, на инструменте | 2017 |
|
RU2663128C1 |
| Способ получения иммобилизованного плазминогена | 1980 |
|
SU979508A1 |
| ФРАГМЕНТ ДНК, КОДИРУЮЩИЙ ПОЛИПЕПТИД К2Р СО СВОЙСТВАМИ АКТИВАТОРА ПЛАЗМИНОГЕНА, ПОЛИПЕПТИД К2Р СО СВОЙСТВАМИ АКТИВАТОРА ПЛАЗМИНОГЕНА, РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК РА27.3, КОДИРУЮЩАЯ ПОЛИПЕПТИД К2Р СО СВОЙСТВАМИ АКТИВАТОРА ПЛАЗМИНОГЕНА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ФИБРИНОЛИТИЧЕСКОЙ АКТИВНОСТЬЮ | 1990 |
|
RU2107094C1 |
| ФЕРМЕНТНЫЙ ПРЕПАРАТ ТРОМБОЛИТИЧЕСКОГО И ФИБРИНОЛИТИЧЕСКОГО ДЕЙСТВИЯ ИЗ БАЗИДИАЛЬНОГО ГРИБА РОДА Coprinus | 2010 |
|
RU2435848C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ТРОМБОЛИТИЧЕСКИМ И ФИБРИНОЛИТИЧЕСКИМ ДЕЙСТВИЕМ | 2002 |
|
RU2216348C1 |

Фибринолизин
2 1 Фибринолизин
Иммо били 3 ованный фибриИз экспериментальных данных следует, что лечение фибринолизином кроликов не дает тромболитического эффекта во всех случаях применения минимальной лечебной дозы (800 ед/кг). При этом наблюдается кровоточивость, патологические изменения в третьей фазе свертывания крови, падение содержания фибриногена в первые часы введения до О. Увеличение дозы до 4000 ед/мЛ вызывают гибель животного от фибринолизина. В отличие от нативного фибринолизина лечение иммобилизованным фибринолизином более эф фективно даже при применении минималь ной терапевтической дозы в 400 ед/кг Кроме того, фибринолитическое действие иммобилизованного фибринолизина наблюдается длительное время - до
Лизиса нет Лизис полный Лизиса нет
1 1 1 Лизис полный . Лизис полный
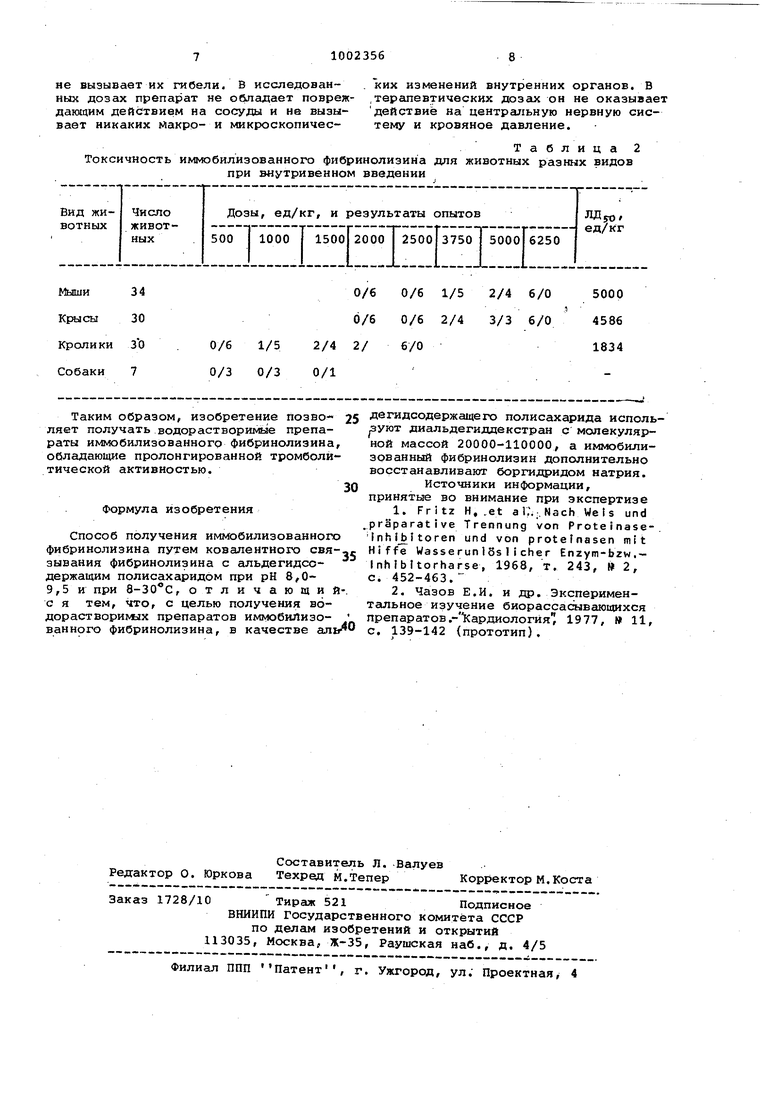
Лизис полный (погиб от кровотечения) двух суток после введения. Препарат не вызывает резких изменений в третьей фазе свертывания крови. и в связи с этим лечение не сопровождается кровотечением. Токсичность иммобилизованного фиб-ринолизина в острых опытах изучают на белых мышах, крысах, кроликах и собаках (см. табл.2). Полученные резуль- таты показывают, что ЛД различньлх партий иммобилизованного фибринолизина колеблется в сравнительно небольших пределах от 5000 До 6000 ед/кг. Токсичность иммобилизованного фибринолизина оказалась сходной с токсичностью нативного фибринолизина. Однократное введение животным иммобилизованного фибринолизина в дозах, в 4-5 раз превышающих терапевтическую.
не вызывает их гибели. В исследованных дозах препарат не обладает повреждающим действием на сосуды и не вызывает никаких Макро- и микроскопичесТоксичность иммобилизованнохх) фибринолизина при внутривенном введении Таким образом, изобретение позволяет получать водорастворимае препараты иммобилизованного фибринолизина, обладающие пролонгированной тромболйтической активностью. Формула изобретения Способ получения иммобилизованного фибринолизина путем ковалентного связывания фибринолизина с альдегидсодержащим полисахаридом при рН 8,09,5 и при , отличающий с я тем, что, с целью получения водорастворимых препаратов илпуюбиЛизованного фибринолизина, в качестве аль
изменений внутренних органов. В .терапевтических дозс1Х он не оказывает действие на центральную нервную систему и кровяное давление. Таблица 2 для животных разных видов дегидсодержащего полисахарида используют диальдегиддекстран с молекулярной массой 20000-110000, а иммобилизованный фибринолизин дополнительно восстанавливают боргидридом натрия. Источники информации, принятые во внимание при экспертизе 1.Fritz Н, .et а i;, . Nach We ts und preparative Trennung von Proteinase-. Inhi Itoren und von protefnasen mit Hiffe Wasserunlos1icher Enzym-bzw,- tnhfbftorharse, 1968, т. 243, 2, с. 452-463. 2.Чазов Е.И. и др. Экспериментальное изучение биорассасывающихся препаратов .- Кардиология 1977, 11, с. 139-142 (прототип).
Авторы
Даты
1983-03-07—Публикация
1980-12-31—Подача