СП
:
о
Изобретение относится к синтезу новых органических соединений, а именно производных фталимидинов общей формулы I
.«
.с- itfe Rp
, гЗе х-н, CHj.ci
которые могут найти применение как мономеры для получения термостойких полимеров,
По химической структуре к предлагаемым производным фталимидинов наиболее близок N-этил-З-хлор-3фенилфталимидин fll формулы
/О
Особенности строения этого соединения (наличие в положении 3 фенильного заместителя) не позволяют его использовать в качестве мономера (псевдохлорангидрида) для синтеза полигетероариленов нового типа, которые служат основой для изготовления термостойких материалов
С точки зрения аналогов по назначению наиболее близкими к предлагаемым производным- фталимидинов являются хлорангидриды, полученные на основе биядерных монокарбоновых кислот (4-карбоксидифенилоксид и 4-карбоксидифенил), применяемые при синтезе полимеров - поликтонов 2.
Однако указанные поликетоны име ряд существенных недостатксда. Они легко кристаллизуются и характеризуются относительно высокой температурой плавления (450°С,),, Кроме того, они имеют низкие температуры стеклования (от 154 до 185°С;) Недостатком их являб;тся также растворимость. Они растворяются в ограниченном числе растворителей (в концентрированной серной кислоте и о-хлорфеноле).
Цель изобретения - изыскание фталимидинов, используемых в качестве мономеров для синтеза полимеров с повьвденной растворимостью и теплостойкостью..
Предлагаются производные фталимидинов общей формулы 1 как мономеры для синтеза термостойких полимзров,
Производные фталимидинов (псевдохлорангидриды) формулы 1 получают конденсацией производных фталимидинов (псевдокислот) общей формулы
1Q
15
го
с хлористым тионилом при комнатной температуре при весовом соотноше5нии 1-:2,4.
Доказательством структуры полученных соединений является наличие в ИК-спектрах полосы поглощения валентных колебаний СвО фталимидиЦ
0 новой группировки при 1712-1718
Пример 1. 2-Фенил-З-хлор3- (п-дифенил)фталимидин,
В токе сухого инертного газа к.10,0 г (0,0265 моль)2-фенил-З5окси-3- (ii-дифенил) фталимидгг на прибавляют при комнатной температуре 15 мл хлористого тионила. По истечении 5-10 мин реакция, заканчивается и непрореагировавший хлористый тионил отгоняется в течение 30-60
0 60 мин в вакууме при комнатной температур.ев Затем вещество досушивают в течение 20-30 мин при 6070°С . После трехкратной перекристаллизации из бензола вещество
5 промывают петролейнымti эфиром и сушат в вакууме при 95®С 5 с Полученный псевдохлорангидрид - белое кристаллическое вещество, т.пл. 148-150 С, Выход 7,8 г (74,4% тео0рии).
Найдено, %: С 78,93 И 4,50 Ч 3,36 СР 8,21. .
CjgHfgNOCa.
Вычислено,%: С 78,88 Н 4,55
5 W 3,53 се 8,9,7, :
Пример 2.. 2- (И- Фолил) 3-хлор-З- (п-дифенил) фталимиди:н. ;
В токе сухого инертного газа к 2,9 г (0,0074 моль) 2- «-толил )03-окси-З-(П-дифенил)фталимидина прибавляют при комнатной температуре б мл хлористого тионилаи Далее, как в примере А, Полученный псевдохлорангидрид - белое кристадлическое вещество, зв ДПв 156-158 С
5
Выход 2,2 г (73,3% от теории)
Найдено,%: С 79,17; Н 4,81 J 3,39; се 8,13.
С27НздКОСе
Вычислено,% С 79,12; Н 4,88; N 3,41; се 8,66,
Пример 3,. 2-(м-Толил)-3хлор-3- (п -дифенил) -фталимндин,
В токе сухого инертного газа к 5,0 г (0,0127 моль) 2-(м-толил)3-окси-З-(h-Дифенил)фталимидина прибавляют 7,5 мл хлористого тионил. Далее, как в примере 1 Полученный псевдохлорангидрид белое кристаллическое вещество, т ПЛ1 154-155 С. Выход. 3,4 г (66,3% теории).
Найдено,%: С 79,10; Н 4,80; 3,35; се 8,51.
Qj-fH jNOCe.
Вычислено,%: С 79,12; Н 4,88; Н 3,41; Ct 8,66.
Пример 4, 2-(п-Хлорфенил3-хлор-З-(п-дифених фталнмидин.
В токе сухого инертного газа к 2,6 г (0/0063 моль) 2-(П-хлорфенил).-3-окси-З- (П-дифенил)фт.алимдина прибавляют 5 мл хлористого тионила. Далее, как в примере 1. Полученный псевдохлорангидрид белое кристаллическое вещество, .T.ivi, 153-155 С. Выход 1,7 г (62,9% теории)
Найдено,%: С 72,58; Н 3,90; М 3,78; се 16,41.
Cj(,H,7MOCe
ВычисленоДС 72,55;.Н 3,95 N 3,25; се 16,55.
Пример 5. 2-Фенил-З-хлор3-(4-феноксифенил)фталимидин
В токе сухого инертного газа к 2,6 г (0,0066 моль) 2-фенил-3окси-3-(4-феноксифенил)фталимидина прибавляют 5,0 мл хлористого тионида. Далее, как в примере Дв Полученный псевдохлорангидрид бледно-желтое вещество, двГШе :4548 С. Выход 2,13 г (79,0% теории
Найдено, %: С 75,95 Н 4,43; М 3,31; а 8,58.
Ся-Н,а .
Вычислено, %: С 75,82; Н 4,37; N 3,40; се 8,63.
Пример б Пример 64 2-Фенил-З-хлор(флуоренил)фталимидин.
В токе сухого инертного газа к 2,0 г (0,00514 моль) 2-фенил-Зокси-3-(флуоренил)фталимидина прибавляют 4,0 мл хлористого тионила Далее, как в примере 1, Полученны продукт - белое кристаллическое вещество, т, Щ1, 165-167 с . Выход 1,4 г (71,5% теории;).
Найдено,%: С 83,14; Н5,03 Ч 3,32.
мосе.
Вычислено,%: С 83,07; Н 5,12; М 3,58.
Пример 7, Получение полимера на основе мономера (псевдохлорангидрида)-2-фенил-З-хлор-З(П-дифенил)-фталймидина.
В токе сухого инертного газа в колбу, снабженную гидравлическим затвором и мешалкой, вносят 0,494 (0,00129 моль) 2-фенил-З-хлор-З(П-дифенил)фталимидина, 0,64 мл нитробензола и 0,42 г (0,0032 моль хлористого алюмини я. Синтез проводят при 100°С в течение 15 ч . По окончании синтеза реакционную массу охлаждают до температуры -«60°С, добавляют хлороформ для полного растворения реакционной массы и высаживают в этиловый спирт. Выпавший осадок отфильтровывают, промывют несколько раз этиловым спиртом, ацетоном и сушат при 10 ч. Полученный продукт переосаждают повторно аналогичным образом, суша при 2 ч, затем в вакууме при 100°С 10 ч.Получают 0,4 Г (94,0% теории) плимера с приведенной вязкостью 0,46 дл/г, измеренной в растворе полимера в хлороформе при .
Найдено, %: С 85,41; Н 4,50; Ц 3,47.
(С2бНпМО)„.
Вычислено,% С 86,90; Н 4,73; К 3,88.
Температура размягчения полимер 530°:С„ :
Пример 8, Получение полимра.
В токе сухого инертного газа в колбу, снабженную гидравлическим затвором и мешалкой, вносят 0,494 (0,001249 моль) 2-фенил-3-хлор-2(tt-дифенил)фталимидина, 0,64 мл нитробензола и. 0,42 г (0,0032 моль хлористого алюминия.. Реакционную массу пepeмeшIiвaют приюо СВ течение 15 ч . По окончании синтеза реакционную массу охлаждают до , добавляют хлороформ до полно го растворения реакционной массы и высаживают в этиловый спирт Выпавший осадок отфильтровывают, промывают несколько раз этиловым спиртом, ацетоном и сушат при .10 чt Полученный продукт переосажда.ю повторно аналогичным образом
80 С
и сушат при
затем в вакууме
100 -при
10 ч..
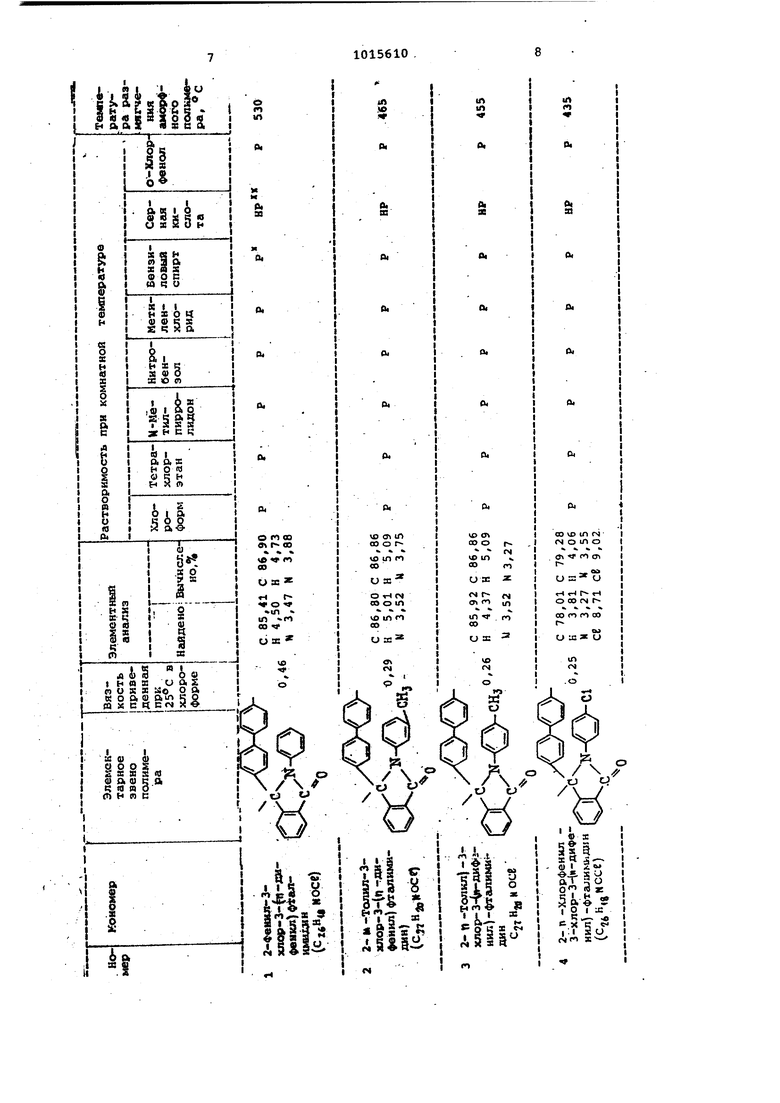
Получают 0,4 г (91%теории) поли60 мера с приведенной вязгкостью TI 0,46 дл/г, измеренной в растворе полимера в хлороформе при - Темлература размягчения 530°С . Прочность на разрыв 800 кгс/см , относитель65 ное удлинение при разрыве 10 %. .Подтверждением структуры синтезированного полимера являются данные элементногО|анализа. Найдено,%: С 85,41 Я 4,50; N 3,47. Вычислено,%: С 86,90; Н4,73; N 3,83. Молекулярный йес синтезированных полимеров согласно данным приведенн вязкости (1пр ОГ 0,25 до 0,43 дл/г), измеренной,в растворе полимера в хлороформе при 25°С, равен 30-50 ты Полученные на основе псевдохлорангидридов полигетероарилены имеют ряд преимуществ перед описанными в литературе поликетонами. Синтезированные полимеры хорсядо растворимы, имеют аморфную структуру ев отличие от поликетонов, име ющих кристаллическую структуру и низкую температуру стеклования (154-185°С)3 и высокую температуру размягчения (до 530°С), что позволя ет широко применять их в:; качестве термостойких материалов Такие преимущества полигетероарилемов обусловлены сочетанием в их макромолекулах фталимидиновых группировок и полиядерннх ароматических структур. Так, температуры размягчения амо 1полигетероариленов, т, е их температуры стеклования (поскольку у жесткоцепных полимеров нет высокоэластического состояния. и температуры их размягчения и стеклования практически совпадают) во всех случаях (т. е,, у полимеров , полученных из всех исходных соединений) намного рыше (430-530 С, см. таблицу, температуры стеклЬвания поликетона (154-185 С). Температуры размягчения полигетероариленов даже выше температуры размягчения кристаллического поликетона (т,пл,. ) Наиболее убедительную информацию о большей теплостойкости (т, е,способности работать под нагрузкой при более высокихтемпературах;) полученных полигетероариленов по сравнению с поликетоном на основе ri -феноксибендоилхлорида дает именно.сравнение температур стеклования (размягчение (аморфных фаз, величина которых Зсшисит ОТ;гибкости макромолекул (. Поскольку потер я полимерами технической прочности при больших нагрузках определяет прежде всего размягчение их ;аморфных фаз, то изделия из предлагаемь1Х полигетероариленов будут способны работать под большими нагрузками в Области значительно более высоких температур. ..
о ЧГ 00 (Ч ч ч
«njft со
OS г- м г
(О(Ч г4
«, Н 1Л Ч
в
ояс
«п
«
«
о
sS2
о «
пда г rt ш Г-г
00
t-l 1в
о тЧ о
VP ГЛ 00
ия
ш «п




| название | год | авторы | номер документа |
|---|---|---|---|
| Производные фталимидинов в качестве промежуточных соединений для синтеза мономеров,используемых при получении термостойких полимеров | 1981 |
|
SU1012575A1 |
| Способ получения полигетероариленов с фталимидиновыми группами | 1981 |
|
SU966093A1 |
| 2-[4'-(2", 6"-ДИМЕТИЛФЕНОКСИ)БЕНЗОИЛ]БЕНЗОЙНАЯ КИСЛОТА И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2016 |
|
RU2621343C1 |
| ПСЕВДОХЛОРАНГИДРИД 2-[4'-(2",6"-ДИМЕТИЛФЕНОКСИ)БЕНЗОИЛ]БЕНЗОЙНОЙ КИСЛОТЫ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2016 |
|
RU2625157C1 |
| Полигетероарилены для изготовления термостойких материалов и способ их получения | 1977 |
|
SU734989A1 |
| ТЕРМОСТОЙКИЙ ПОЛИАРИЛЕНФТАЛИД И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2016 |
|
RU2625158C1 |
| Способ получения 9-замещенных 2,3-дигидроимидазо /1,2-а/ бензимидазола или их солей | 1981 |
|
SU952847A1 |
| Способ получения производных арилалкиламина ил их солей | 1976 |
|
SU620209A3 |
| Способ получения 9-замещенных 2,3-дигидроимидазо [1,2-а] бензимидазола или их солей | 1981 |
|
SU952848A1 |
| Способ получения ароматических политиоэфиров | 1985 |
|
SU1321728A1 |
Производные фталимидинов общей формулы X - н, сн, се . как мономеры для синтеза термостойких полимерор... :
А
я
ш
си
ё
04
а.
&
Ж
а.
ш
ftt
а
р
CW
г I
.:
I i
Аморфна структура полигетероарйленов в сочетании с особенностями их химического строения обеспечивает им прекрасную растворимость в органических растворителях, Так, полигетероарилены хорошо раство|ряются в хлорированных растворителях (хлороформе, тетрахлорэтане, метиленхлориде,о-хлорфеноле), апротонных амидных растворителях (N,Hдиметилформамиде,.Н,Ы -.диметилце -амиде, К - метилпирролид6не , а также в нитробензоле, бензилрвом спирте в отличие от поликетонов, которые ра.створяются в ограниченном числе растворителей - о-хлорфеноле и концентрированной серной
кислоте Особенностью полигетерог/ ариленов является, то, что они растворяются (в отличие от поликегонов) в низкокипящих растворителях таких,как хлороформ, Такая раствори мость в сочетании с исключительно высокой теплостойкостью открывает широкие возможности для формовгшия из растворов этих полимеров различных изделий, в том числе и прозрачных пленок (прозрачность благодаря; аморфной; структуре)k Формование же из раствора поликетона изделий крайне сложно из-за его плохой растворимости, а получение прозрачных пленок осложняет его склонность к кристаллизация :
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ термической обработки холоднокатаной электротехнической анизотропной стали | 1988 |
|
SU1520116A1 |
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
Авторы
Даты
1983-12-23—Публикация
1981-04-09—Подача