0 IsD
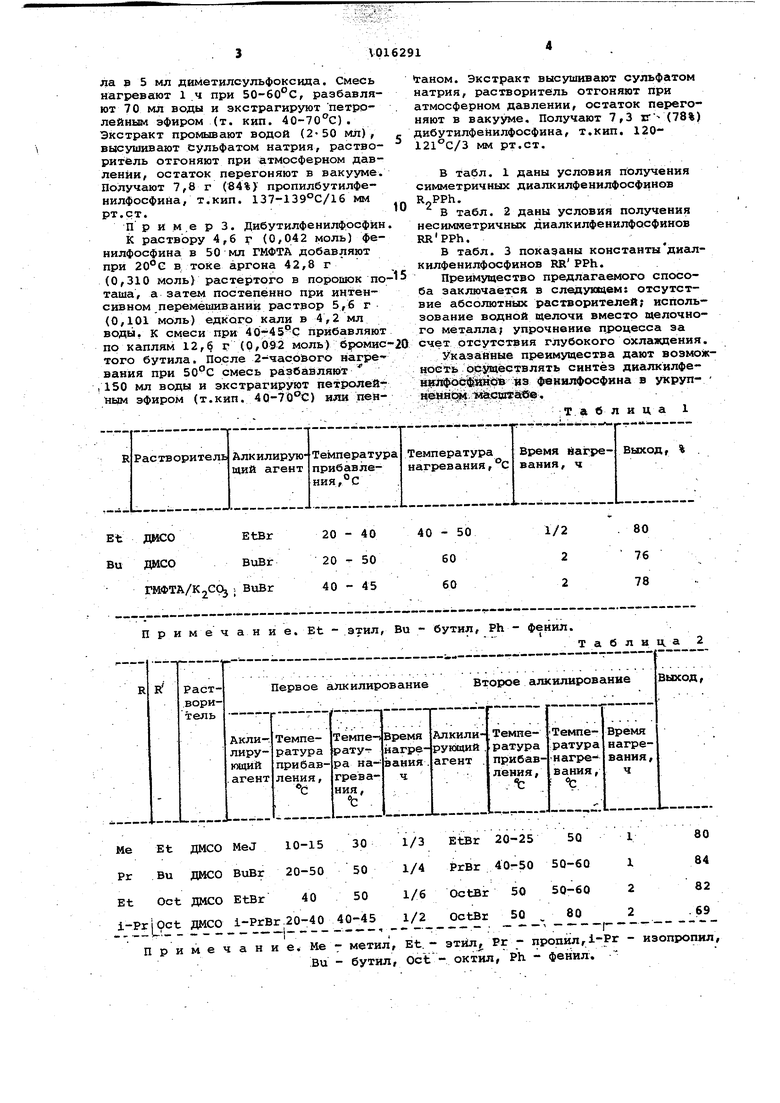
CD Изобретение относится к химии фос форорганических соединений с С-Р связью, а именно к усовершенствованному способу получения диалкилфенилфосфинов, которые нашли широкое применение в качестве составной части комплексов, являющихся катализаторами процессов циклизации и полимеризации олефинов, ацетилена и его производных, альдегидов, а: также процес сов формилирования и гидроформилирования. Третичные фосфины используются для повышения чувствительности фотографических эмульсий, а также в качестве Стабилизаторов полимерных материалов, ингибиторов коррозии. Известен способ получения третичных фосфинов обработкой первичных или вторичных фосфинов калием или натрием в атмосфере инертного газа в жидком аммиаке при низких температурах или в среде ароматических угле водородов йри кипении реакционной смеси (1. Наиболее близким к изобретению по технической сущности и достигаемому результату является способ получения диалкилфенилфосфинов, который заключается в том, что фенилфосфин обраба тывают натрием в жидком аммиаке в ат мосфере инертного газа, алкилируют образуйацийся фосфид натрия алкилгало генидом с последующей повторной обра боткой вторичного Фосфина натрием в . жидком аммиаке и алкилированием алкилфенилфосфида иатрия га:лоидным алкиЯом в среде эфира. Реакцию проводят при -70 С/выход продукта 74% 2 К недостаткам известного способа относятся необходимость использования щелочного металла/ жидкого аммиа ка и абсолютного огнеопасного раство рителя, а также проведение процесса при глубоком охлаждении i Целью изобретения является упроще ние процесса. Поставленная цель достигается тем что согласно способу получения, диалкилфенилфосфинов обработкой фенилФос фина Щелочным агентом в среде раство рителя в атмосфере инертного газа с . последующим алкилированием образующе гося фосфида щелочного металла алкил галогенидом, в качестве щелочного агента используют концентрированный .водный раствор щелочи, в качестве растворителя - биполярный апротонный растворитель, обработку фенилфосфина щелочью ведут при комнатной температуре и а.пкилирование фосфида щелочног э металла - при 30-80 С. Причем в качестве биполярного ап-. ротонного растворителя желательно использовать диметилсульфоксид (ДМСО Кроме того/ в качестве .биполярного апротонного растворителя используют гексаметапол (ГМФТА) и обработку фенилфосфина концентрированным водным раствором щелочи ведут в присутствии безводного поташа. Исходный фенилфосфин и промежуточно образующиеся алкилфенилфосфины являются слабыми Н-кислотами, поэтому для получения их солей - фосфидов используют сильные основания (щелочные металлы или литий- и магнийорганические соединения) в инертных растворителях или в ЖИДКОМ: аммиаке. Растворители должны быть безводными, таккак фосфиды легко гидролизуются водой. Преимущество ДМСО как растворителя заключается в том, что его использование дает возможность для получения фосфидов применять в качестве основания водную щелочь, так как в. этом растворителе фенилфосфин и алкилфенилфосфины являются более сильными кислотами, чем вода, и поэтому их соли (фосфиды) не гидролизуются или слабо гидролизируются в этих условиях. ДМСО является наилучшим растворителем. Вследствие наличия в реакционной смеси довольно значительного количества воды (два эквивалента щелочного раствора), другие биполярные апротонные растворители менее эффективны (второе алкилирование проходит не полностью), хотя в ГМФТА удается добиться положительного результата при введении в систему поташа в качестве водоотнимающего агента. Пример. Диэтилфенилфосфин. К раствору 6,6 г (0,060 моль) фенилфосфина в 70 мл диметилсульфоксида добавляют в токе аргона 5,3 г (0,132 моль), едкого натра в 6 мл воды, а затем при 20-30°С прибавляют по каплям.при перемешивании 14,4 г (0,132 моль) бромистого этила в 10 мл диметилсульфоксида. После получасового нагревания при 40-50 с реакционную смесь разбавляют 100 .мл воды и экстрагируют петролейным эфиром (т,кип. 40-70 С) . Экстракт промывают водой (2-50 мл), высушивают сульфатом натрия, растворитель отгоняют при атмосферном давлении, остаток перегоняют в вакууме. Выход диэтилфенилфосфина 8,0 г (80%), т.кип. 10510б°С/17 мм рт. ст. П р им е р 2. Пропилбутилфенил- . фосфин. К раствору 4,9 г (0,045 моль) фенилфосфина в 45 мл диметилсульфоксида добавляют в токе аргона 6,0 г (0,107 моль) едкого к.али в 4 мл воды, а затем при прибавляют по каплям при перемешивании 6,1 г (0,045 моль) бромистого бутила в 5 мл диметилсульфоксида. После 15-минутного нагревания при 50°С к смеси при 40-50°С прибавляют по каплям 5,5 г (0,045 моль) бромистого пропила в 5 мл диметилсульфоксида. Смесь нагревают 1 ч при 50-60°С, разбавляют 70 мл воды и экстрагируют петролейным эфиром (т. кип. 40-70°С). Экстракт промывают водой (250 мл), высушивают сульфатом натрия, растворитель отгоняют при атмосферном давлении, остаток перегоняют в вакууме. Получают 7,8 г (84%) пропилбутилфенилфосфина, т.кип. 137-139°С/16 мм рт.ст. П р и м.е р 3. Дибутилфенилфрсфйн К раствору 4,6 г 0,042 моль) фенилфосфина в 50 мл ГМФТА добавляют при в токе аргона 4 2,8 г (0,310 моль) растёртого в порошок по таша, а затем постепенно при интенсивном перемешивании растрор 5,6 Г(0,101 моль) едкого кали в 4,2 мл воды, к смеси при прибавляют по каплям 12,6 г (0,092 моль) бромис того бутила. После 2-часОвого нагре вания при 50°С смесь разбавляют ,150 мл воды и экстрагируют ретролей-ным эфиром (т.кип. 4 0-7 ) или пен ганом. Экстракт высушивают сульфатом натрия, растворитель отгоняют при атмосферном давлении, остаток перегоняют в вакууме. Получают 7,3 (78%) дибутилфенилфосфина, т.кип. 120121°С/3 мм рт.ст. В табл. 1 даны условия получения симметричных диалкилфенилфосфинов . В табл. 2 даны условия получения несимметричных диалкилфенилфосфииов RRPPh. В табл. 3 показаны константыдиалкилфенилфосфинов RR PPh. Преимущество предлагаемого способа заключается в следующем: отсутствие абсолютных растворителей; использование водной щелочи вместо щелочного металла; упрочнение процесса за счет отсутствия глубокого охлаждения. Указанные преимущества дают возможность осуществлять синтез диалкилфеиилФос цщет вз Фенилфосфина в укруп- неявок 1иёсшта&в, таблица 1
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения вторичных алкилфенилфосфинов | 1982 |
|
SU1016294A1 |
| Способ получения диалкилфенил(алкилдифенил)фосфинов | 1982 |
|
SU1016293A1 |
| Способ получения @ -дифенилфосфинокарбоновых кислот | 1982 |
|
SU1016292A1 |
| Способ получения трис(2-фенилэтил)фосфиноксида | 1990 |
|
SU1759841A1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-АЛКОКСИКАРБОНИЛМЕТИЛПИРРОЛИДОНОВ-2 | 1992 |
|
RU2032668C1 |
| СПОСОБ ПОЛУЧЕНИЯ 5-(2-ОКСИФЕНОКСИМЕТИЛ)-1,2,4-ОКСАДИАЗОЛОВ | 1983 |
|
SU1139129A1 |
| Способ получения @ , @ -ненасыщенных кетонов | 1982 |
|
SU1098210A1 |
| Способ получения дивинилтеллурида | 1977 |
|
SU660974A1 |
| Способ получения натриевых солей сн-кислот | 1980 |
|
SU910638A1 |
| Способ получения -алкилированных органических соединений | 1971 |
|
SU667547A1 |
1. СПОСОБ ПОЛУЧЕНИЯ ДИАЛКИЛФЕНИЛФОСФИНОВ обработкой фенилфрсфина щелочным агентом в среде растворителя в атмосфере инертного таза с последующим алкилирЬванием образующего- / ся фосфида «целочного металла алкилга- , логенидом,о т л и ч а ю щ и и с я тем, что, с целью упрощения процесса, в качестве щелочного агента используют концентрированный водный раствор щелочи, в качестве растворителя - биполярный апротонный растворитель, обработку фенилфосфина щелочью ведут при комнатной температуре и алкилирование фосфида щелочного металла - при 30-80 С. 2.Способ поп, 1, отличающийся тем, что в качестве биполярного апротонного растворителя используют диметилсульфоксид. 3.Способ по п. I, о т л и ч а ю -„ щ и и с я тем, что в качестве бипо- s лярного апротонного растворителя иссл пользуют гексаметапол и обработку фе нилфосфнна концентрированным водным раствором щелочи ведут в присутствии безводного поташа.
П р и меч аи и e.Et - этил, Ей - бутил, П р и м е ч а н и е. Me - метил, Et. Би - бутил, Oct Ph - фенил. Таблица этил,, Рг - пропил, 1-Рг - иэопропил, - октил, Ph - фенил. Et 95-97 (18) 1,55560,958151,03 50,40 Et Et 105-106 (18) 1,54600,945855,65 Pr Bu 137-139 (16) 1,5285 0,9216 69,65
Bu 120-121 (3) 1,52300,913874,32 73,49
Bu Et Oct 122-125 (1) 1,51620,907483,36 i-Pr Oct 148-149 (2) 1,5127 0,9032 87,94
Получено MejEt PPhlc т.пл. 149 - . Литературные данные:
Найдено4 %: С 77,3; 76,9 Н 11,0; 11,2; Р 11,7; 11,4. С„. ВычислейО, %: С 77,2; Н 11,1; Р 11,7.
Таблица 3
83 (0,2) 1,5249 0,9115
1,5160 0,9062
т.пл. 148,5 - . 96-97 (15) 1,5555 0,9603 55,02 108-109 (20) 1,5460 0,9445 68,87 127-130 (10) 82,73 132-134 (1) 87,35
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| СПОСОБ ПОЛУЧЕНИЯ НЕКУРИТЕЛЬНОГО ИЗДЕЛИЯ ИЗ МАХОРКИ | 2010 |
|
RU2437595C1 |
| Прибор для периодического прерывания электрической цепи в случае ее перегрузки | 1921 |
|
SU260A1 |
| Станок для изготовления деревянных ниточных катушек | 1925 |
|
SU1948A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Harmon R.E., Parsons J.L., Gupta S.К | |||
| Synthesis of Trichlorotris | |||
Авторы
Даты
1983-05-07—Публикация
1982-01-22—Подача